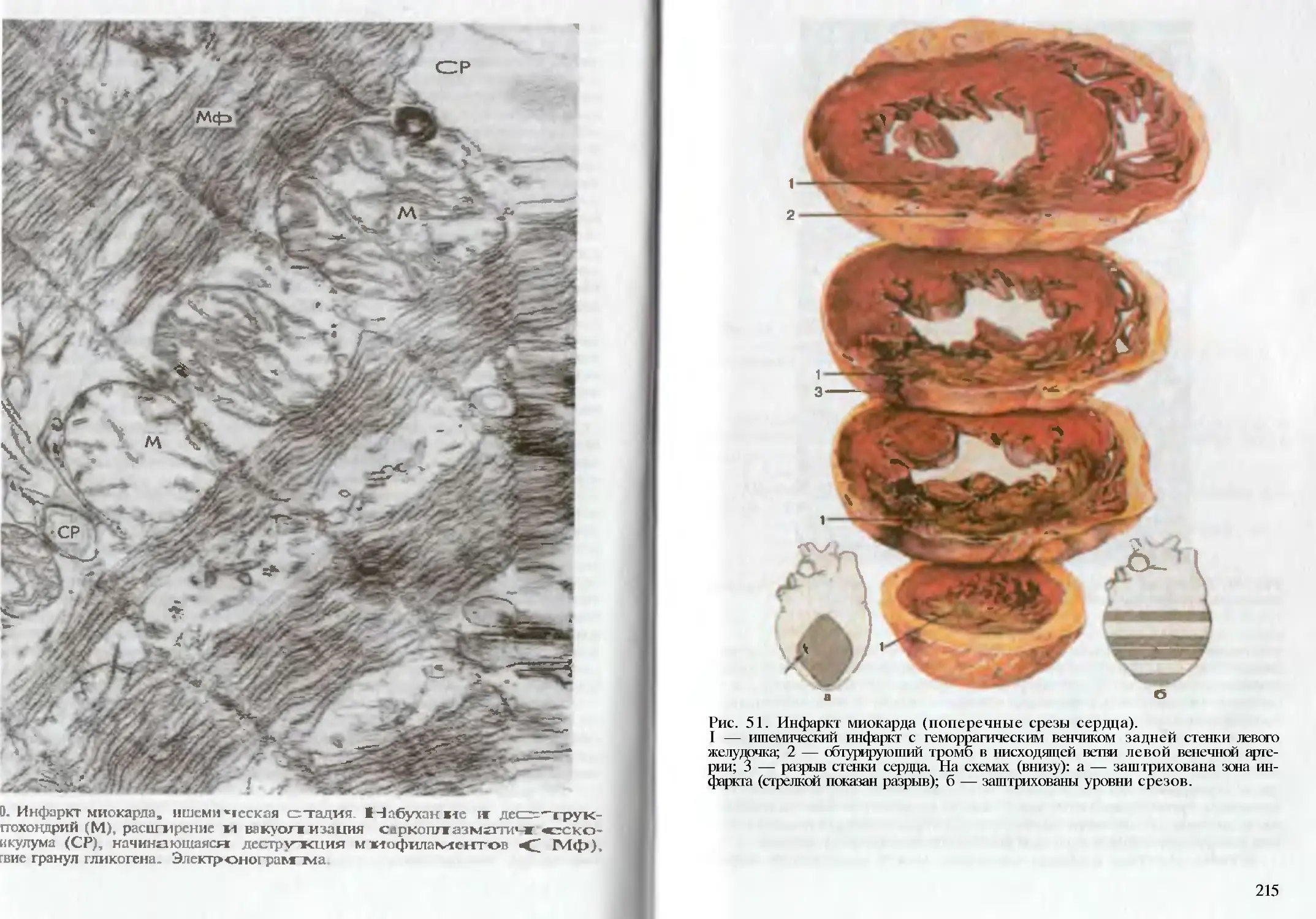
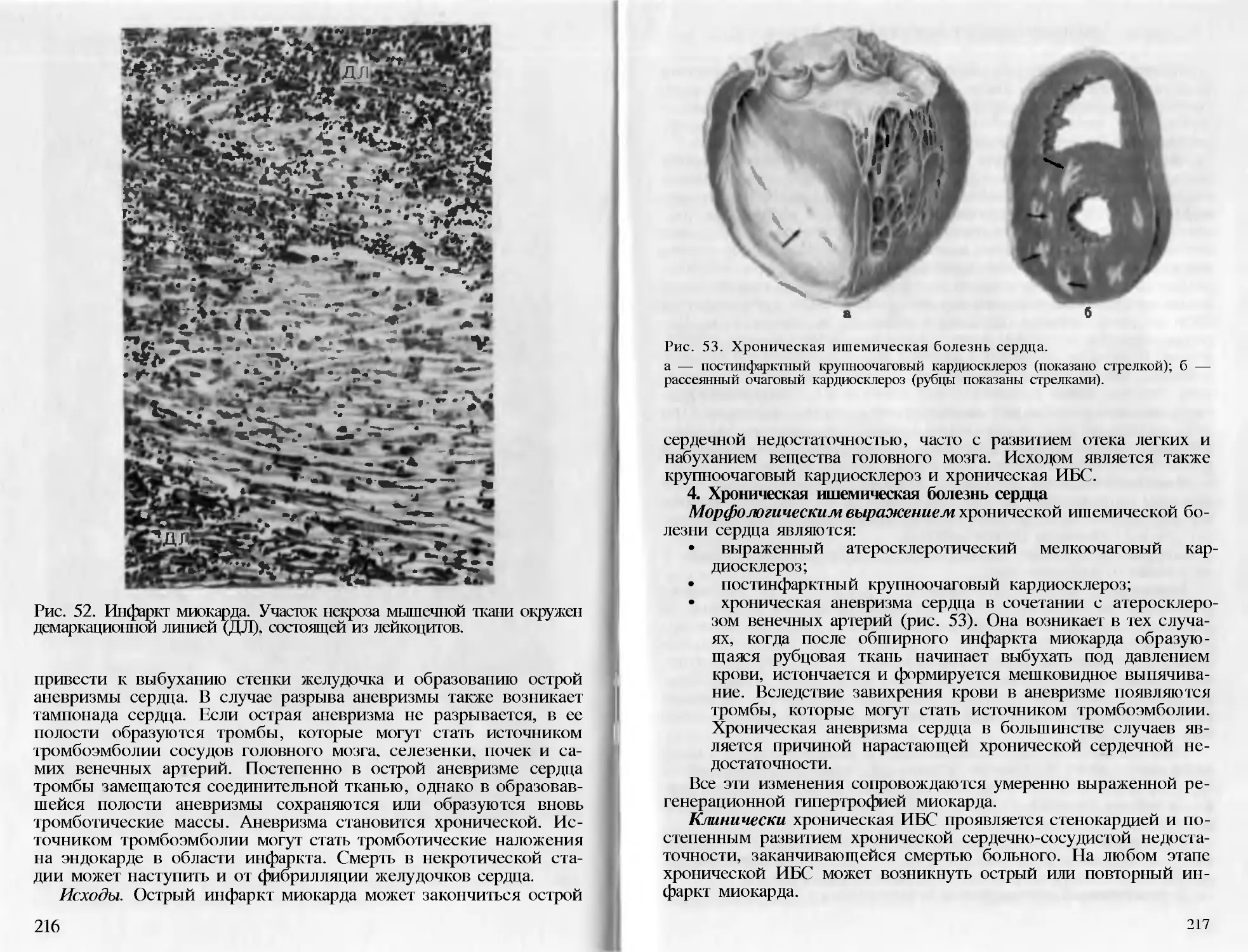
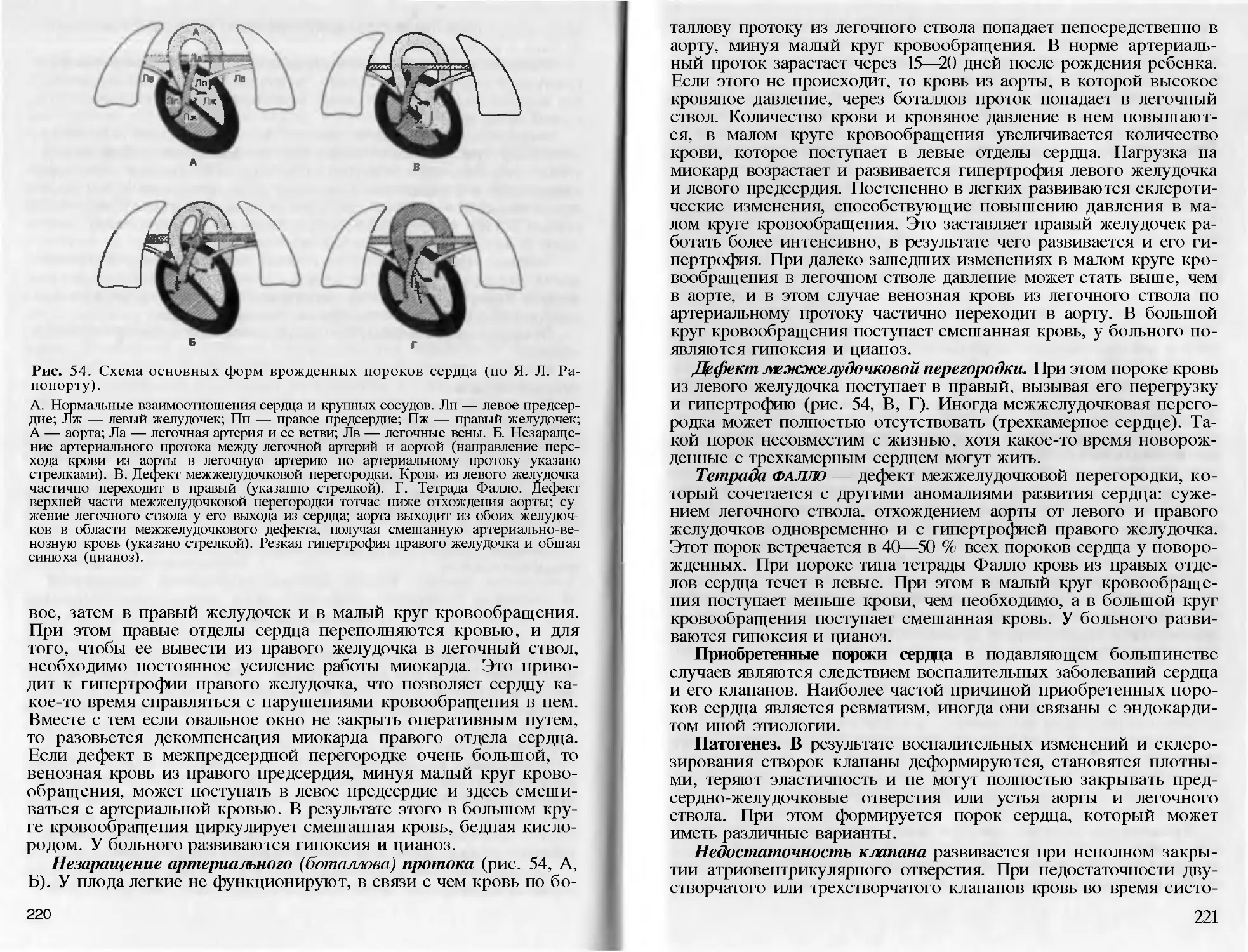
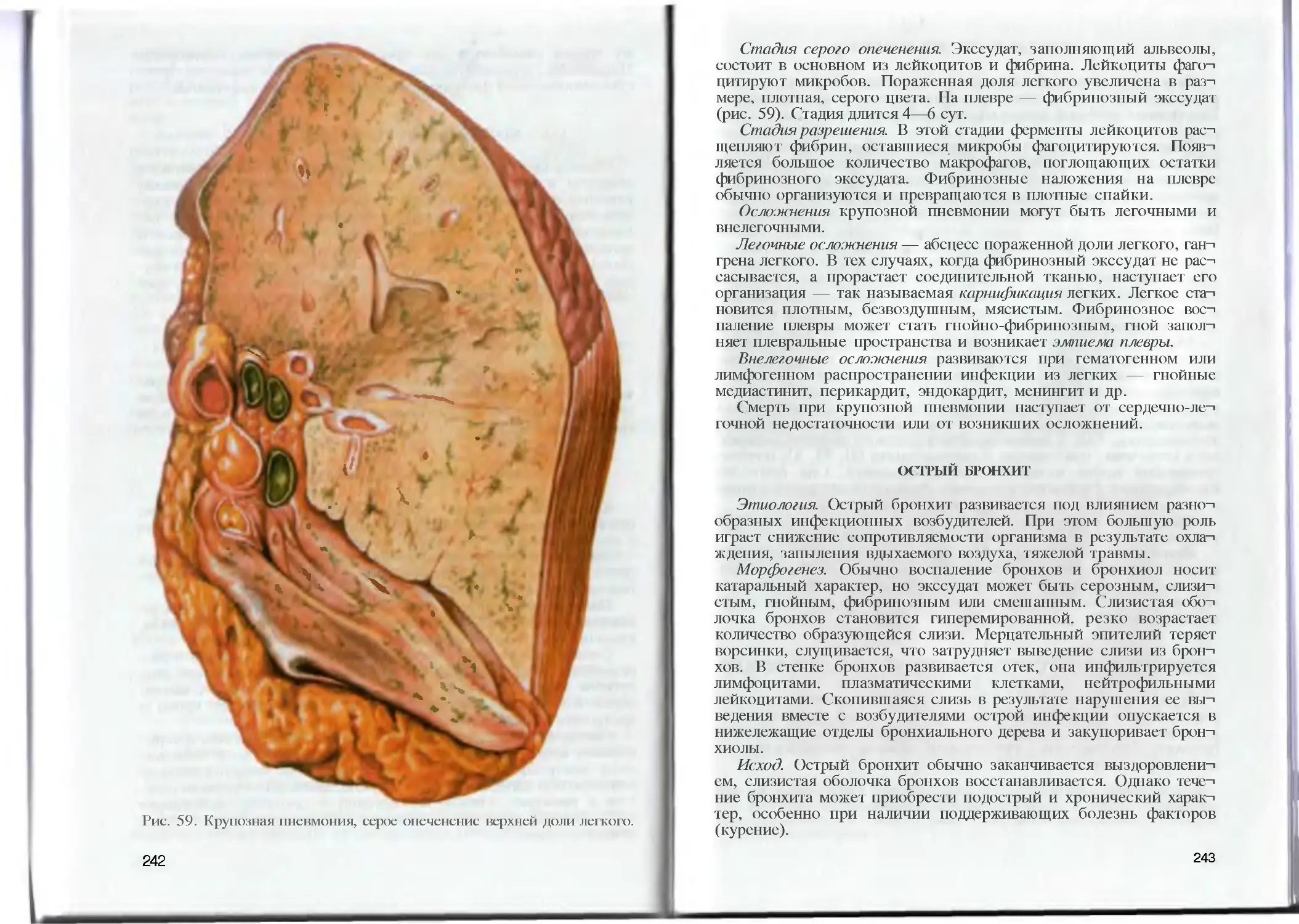
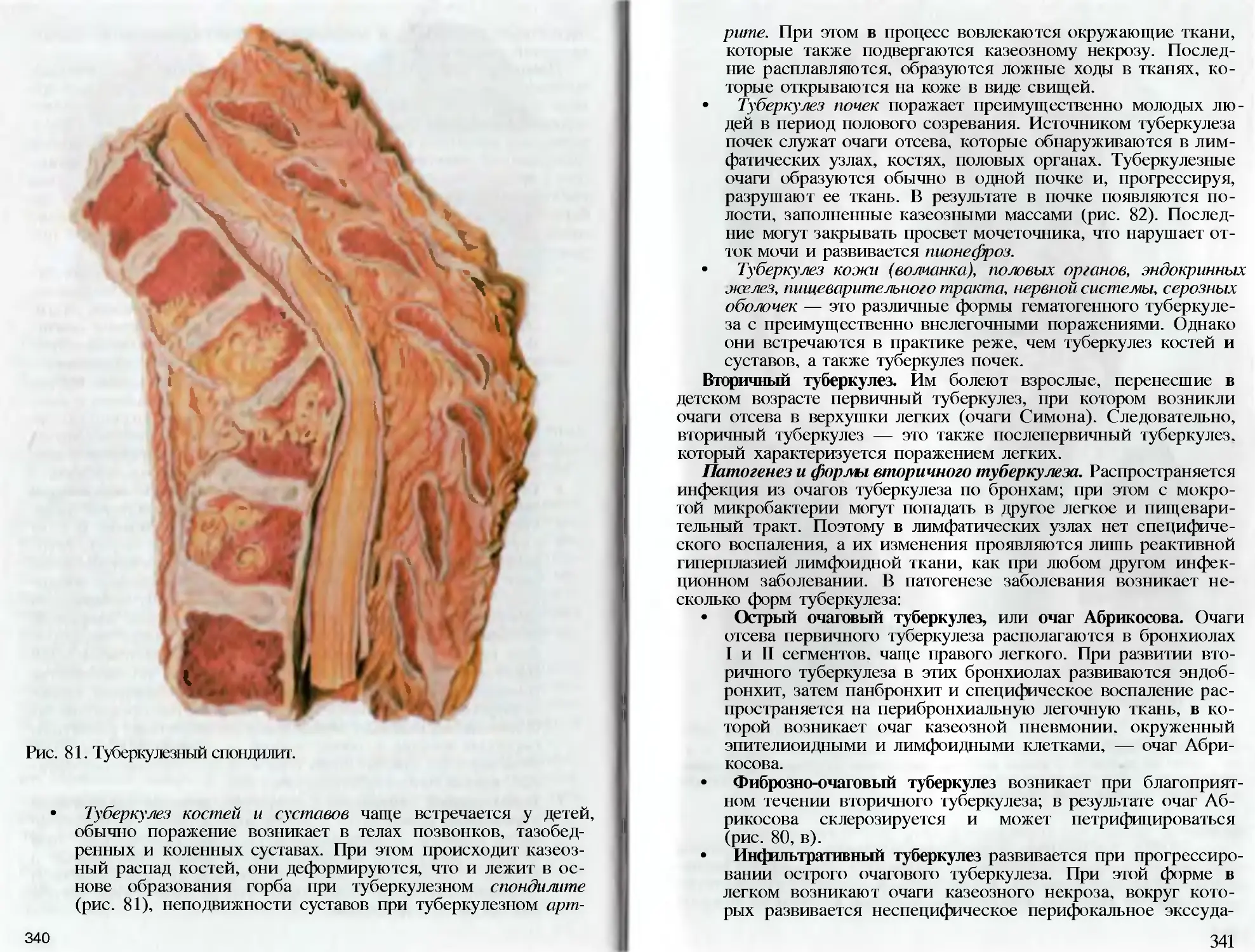
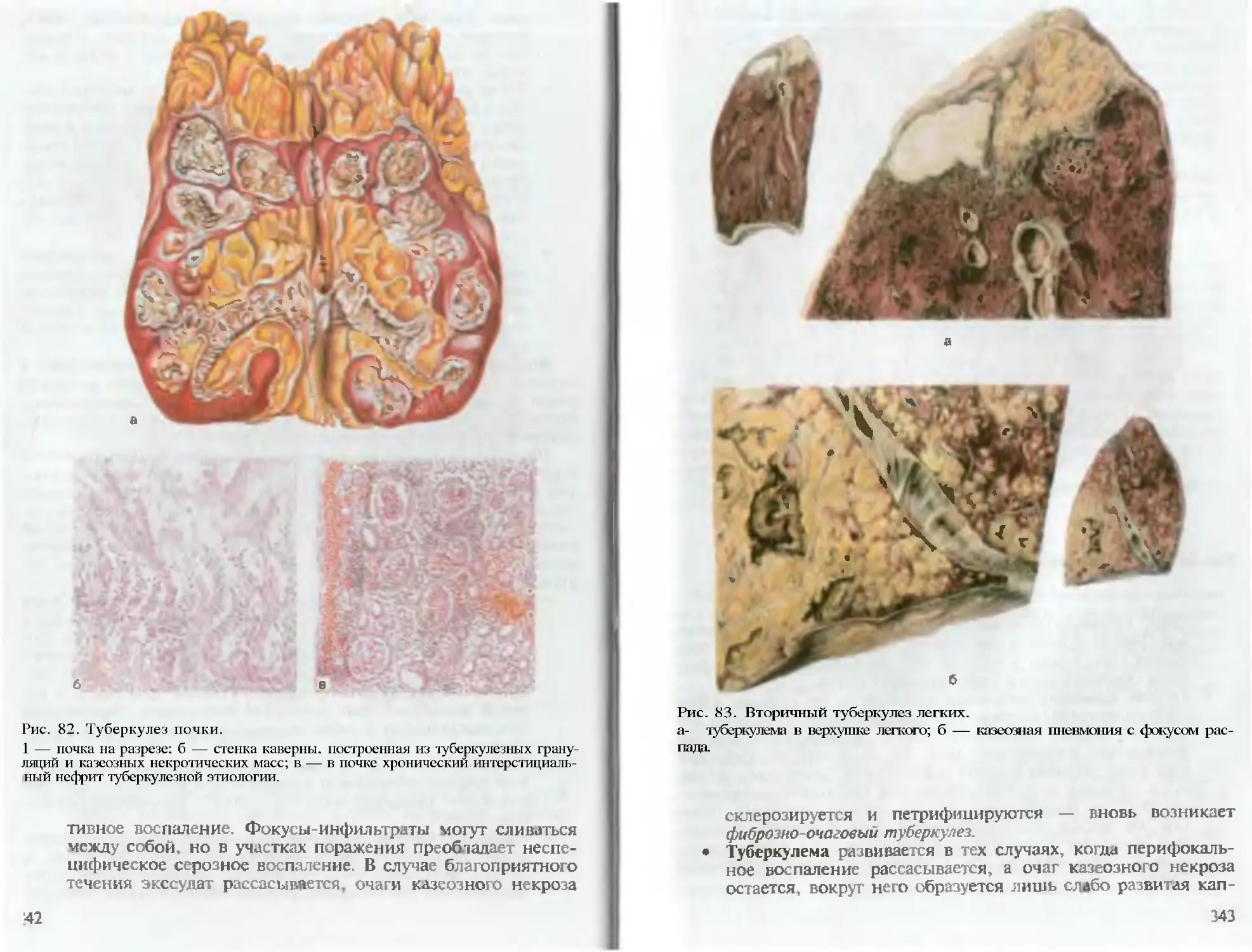
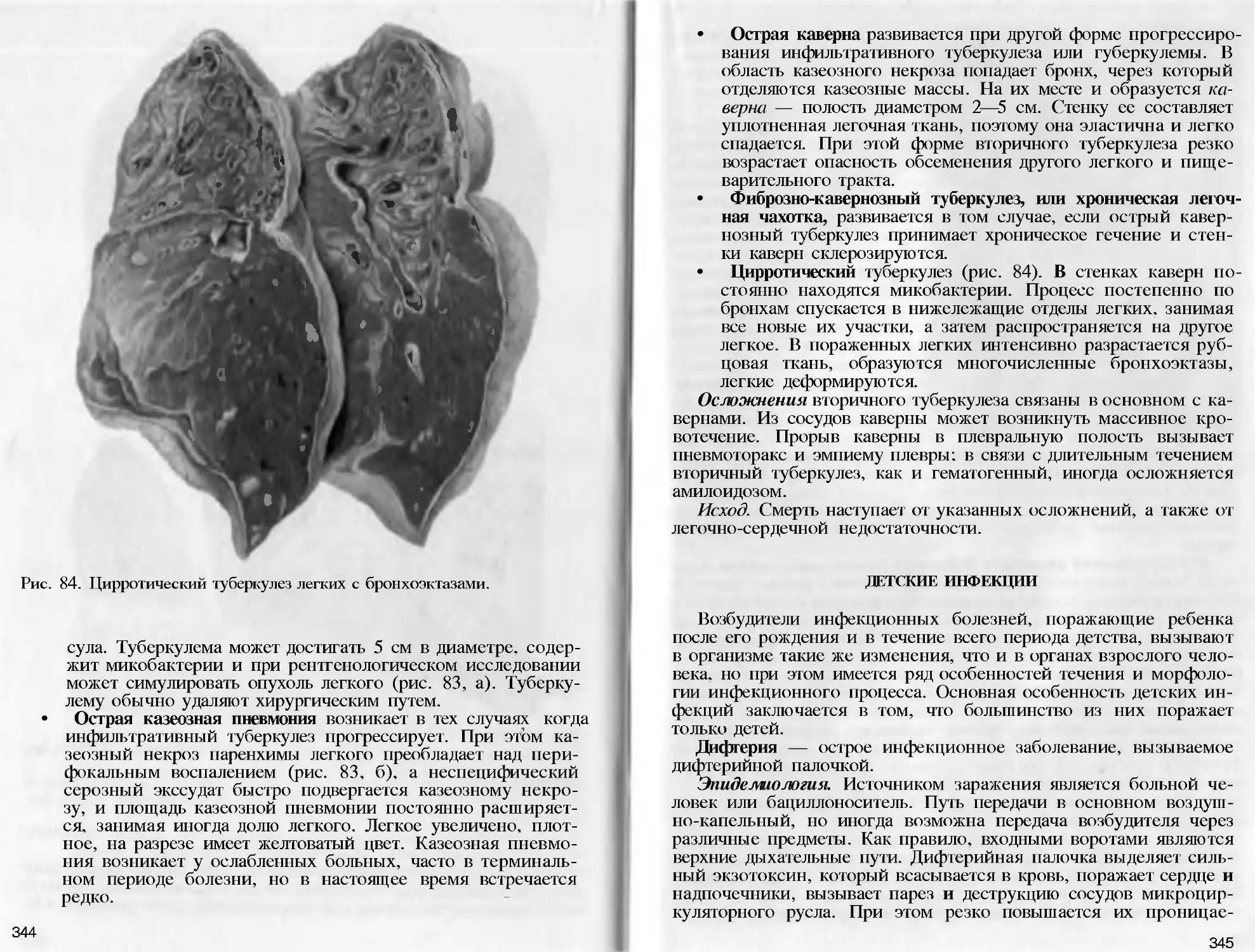
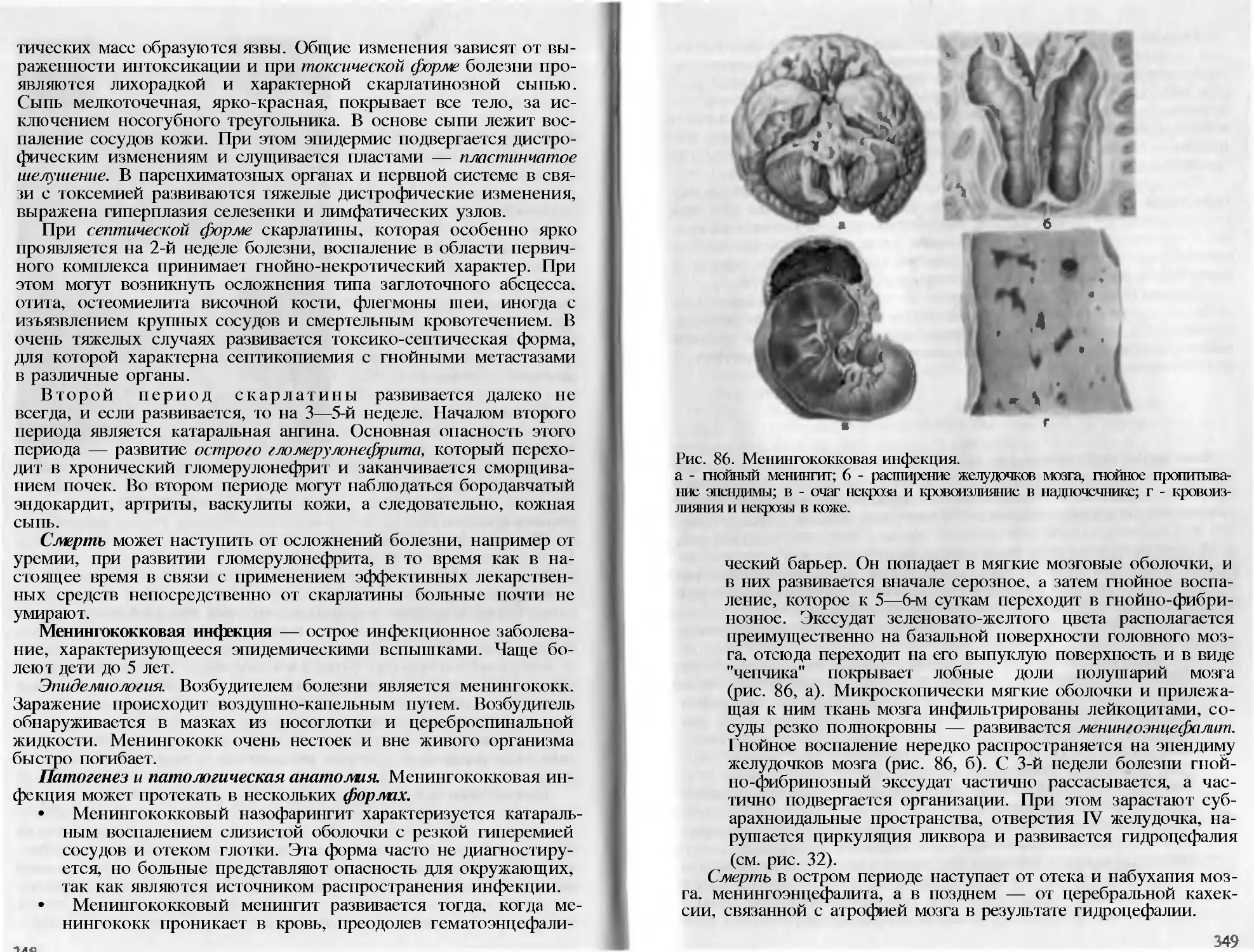
Author: Пауков В.С. Литвицкий П.Ф.
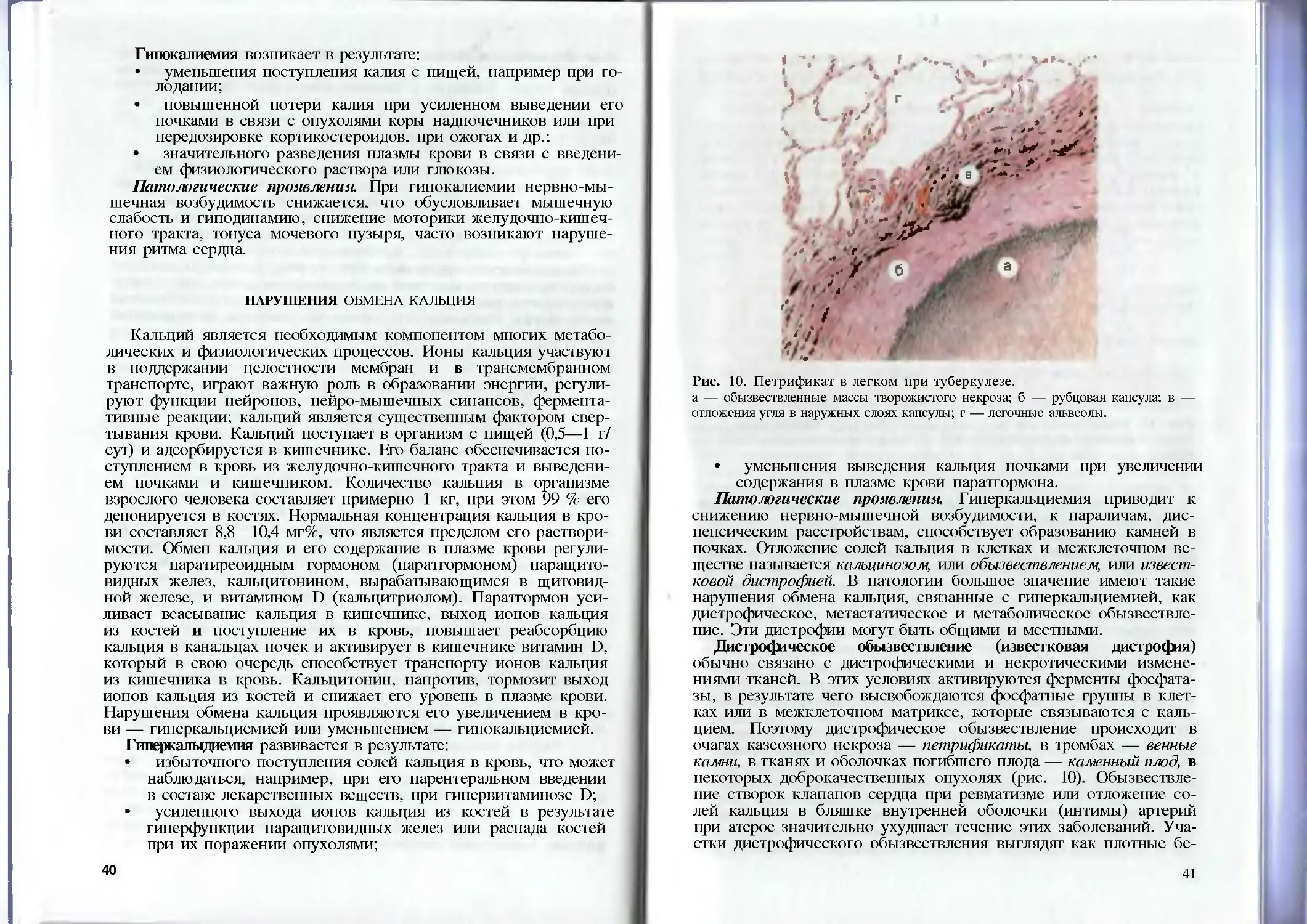
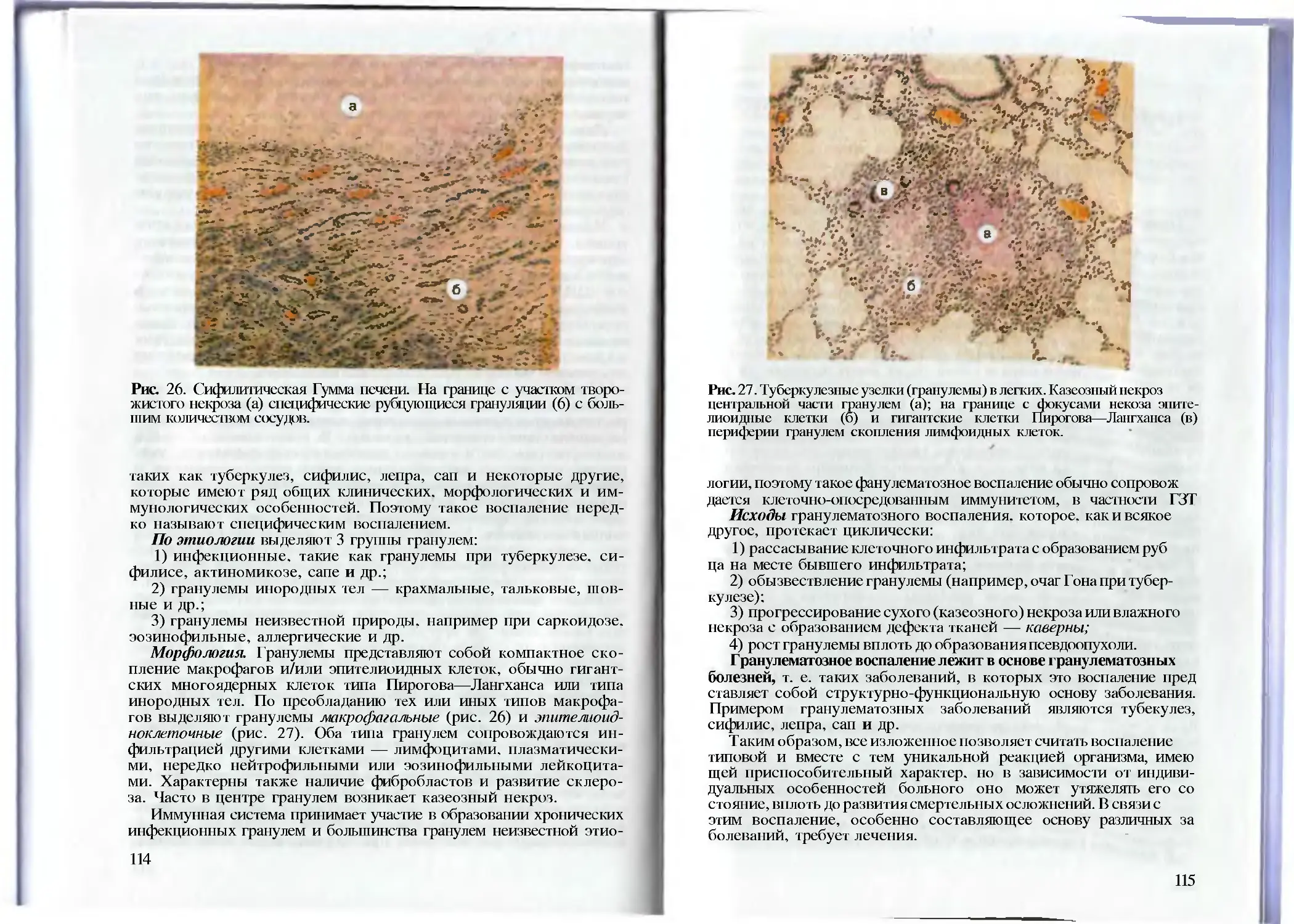
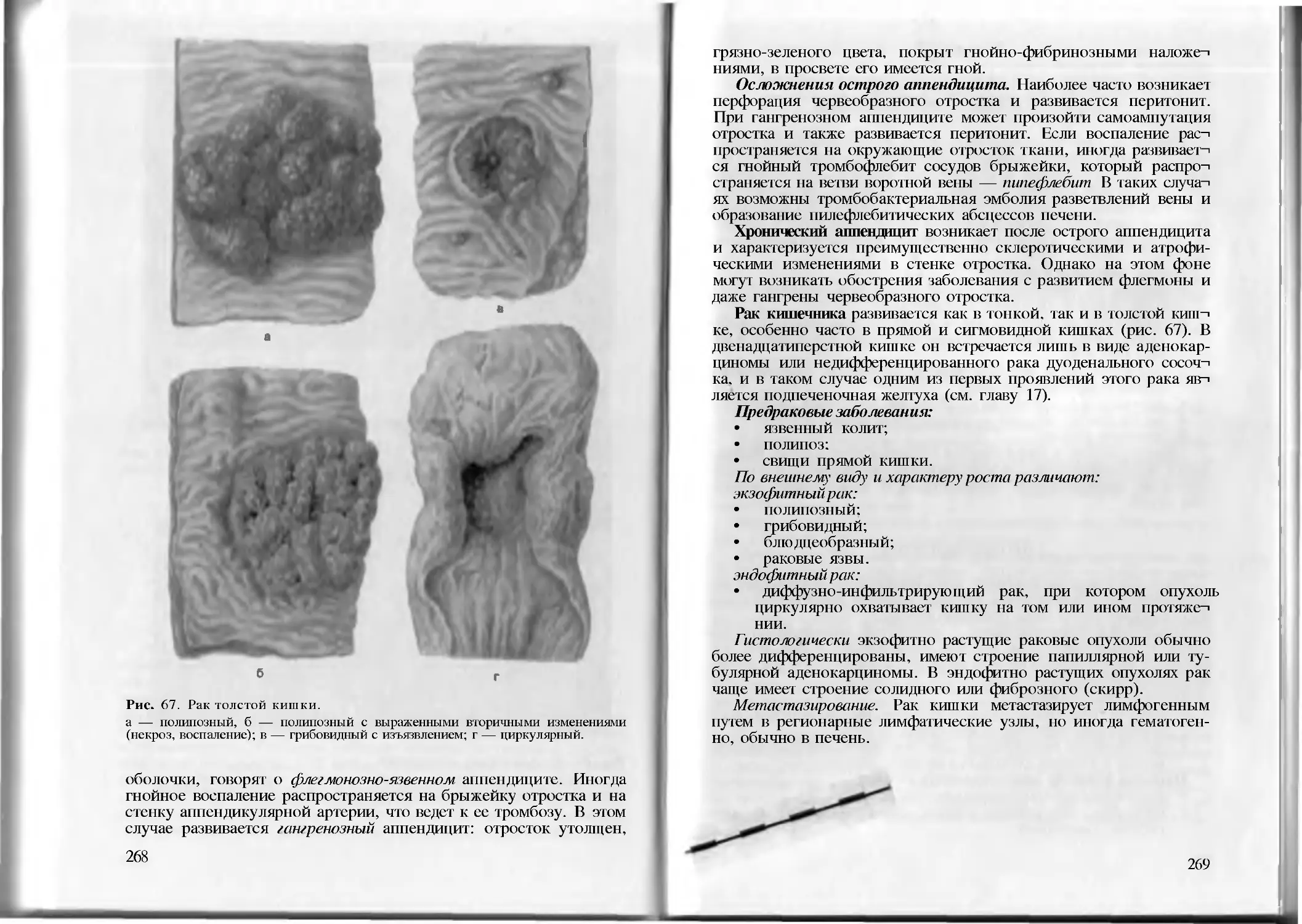
Tags: медицина патология дистрофии
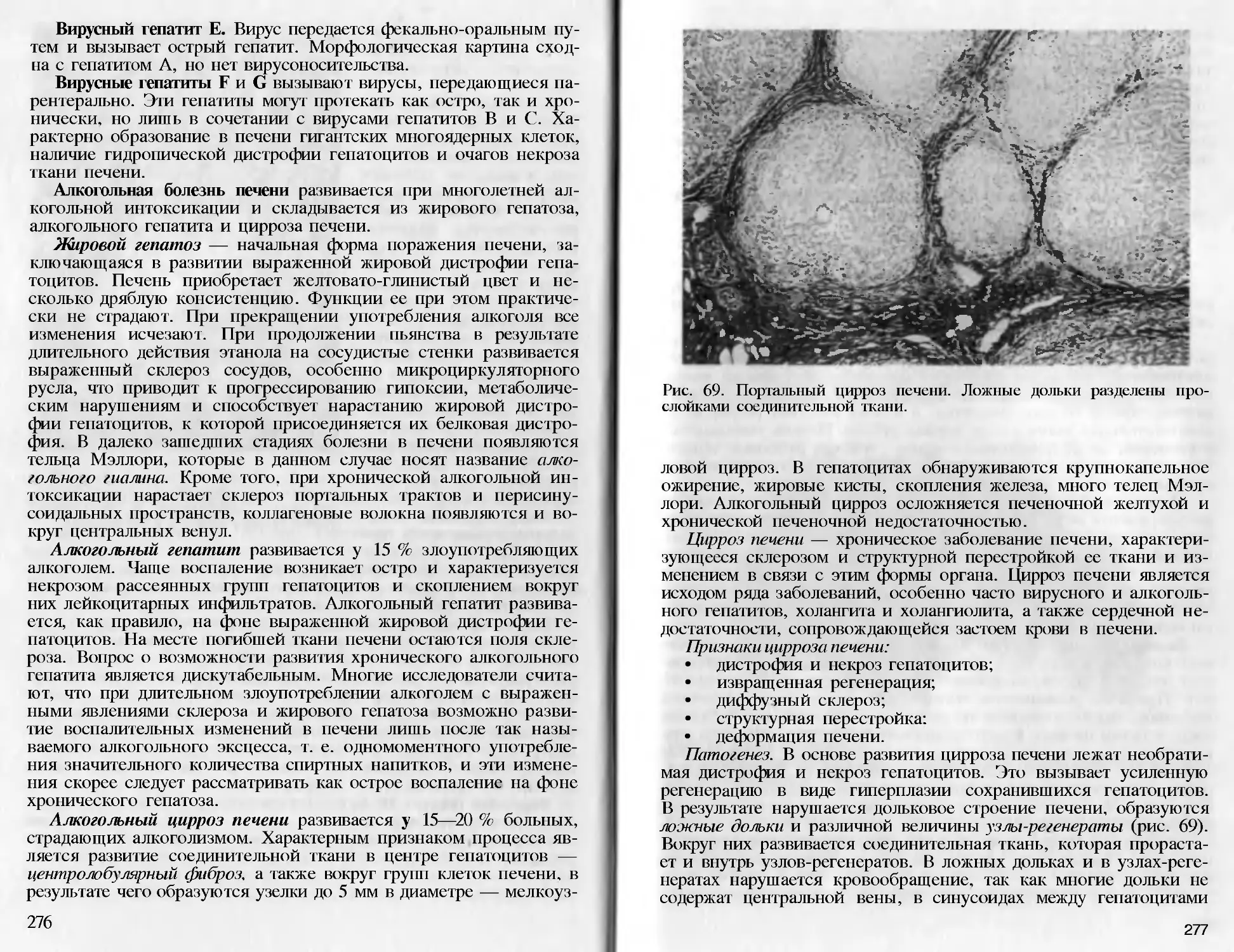
ISBN: 5-225-04860-9
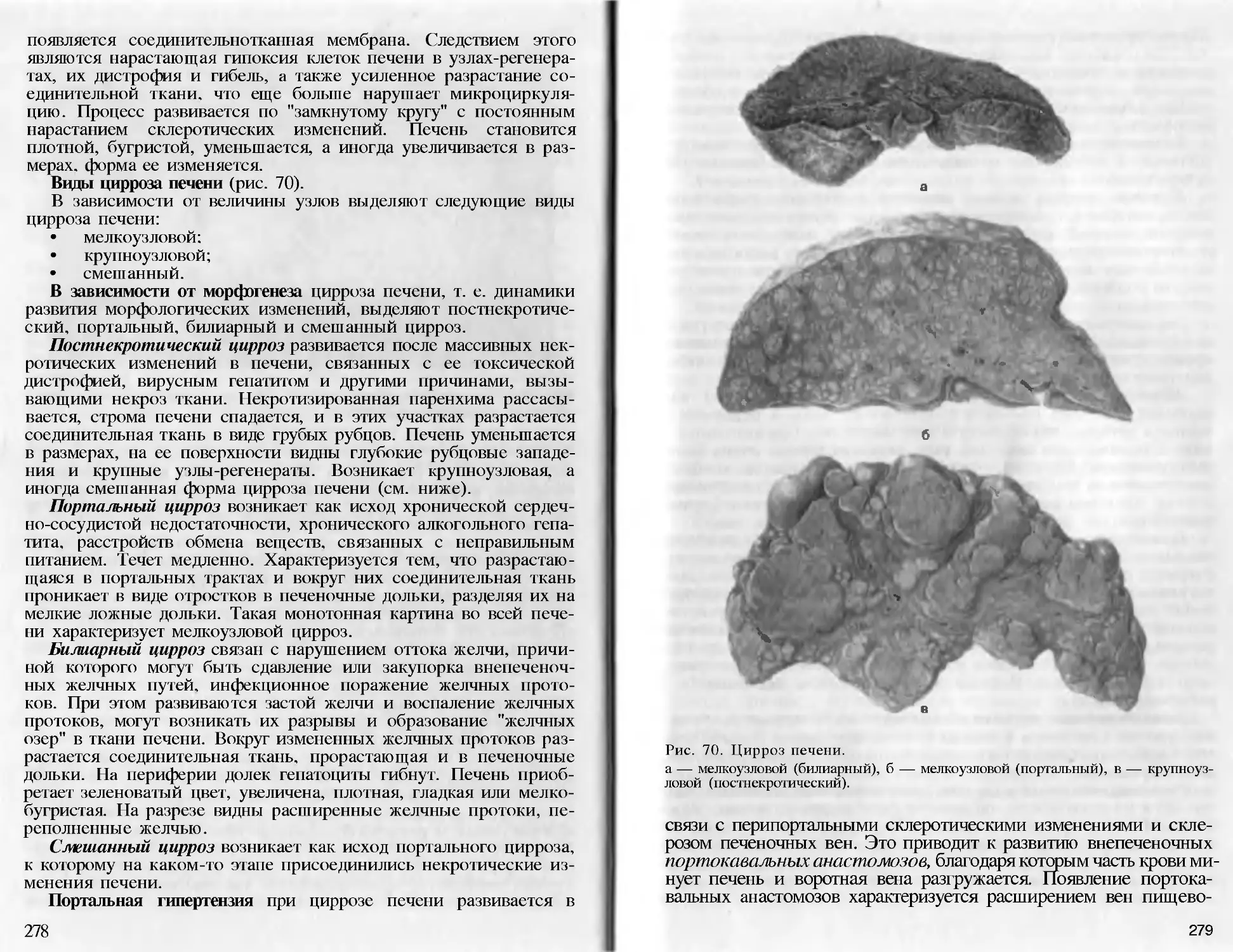
Year: 2004
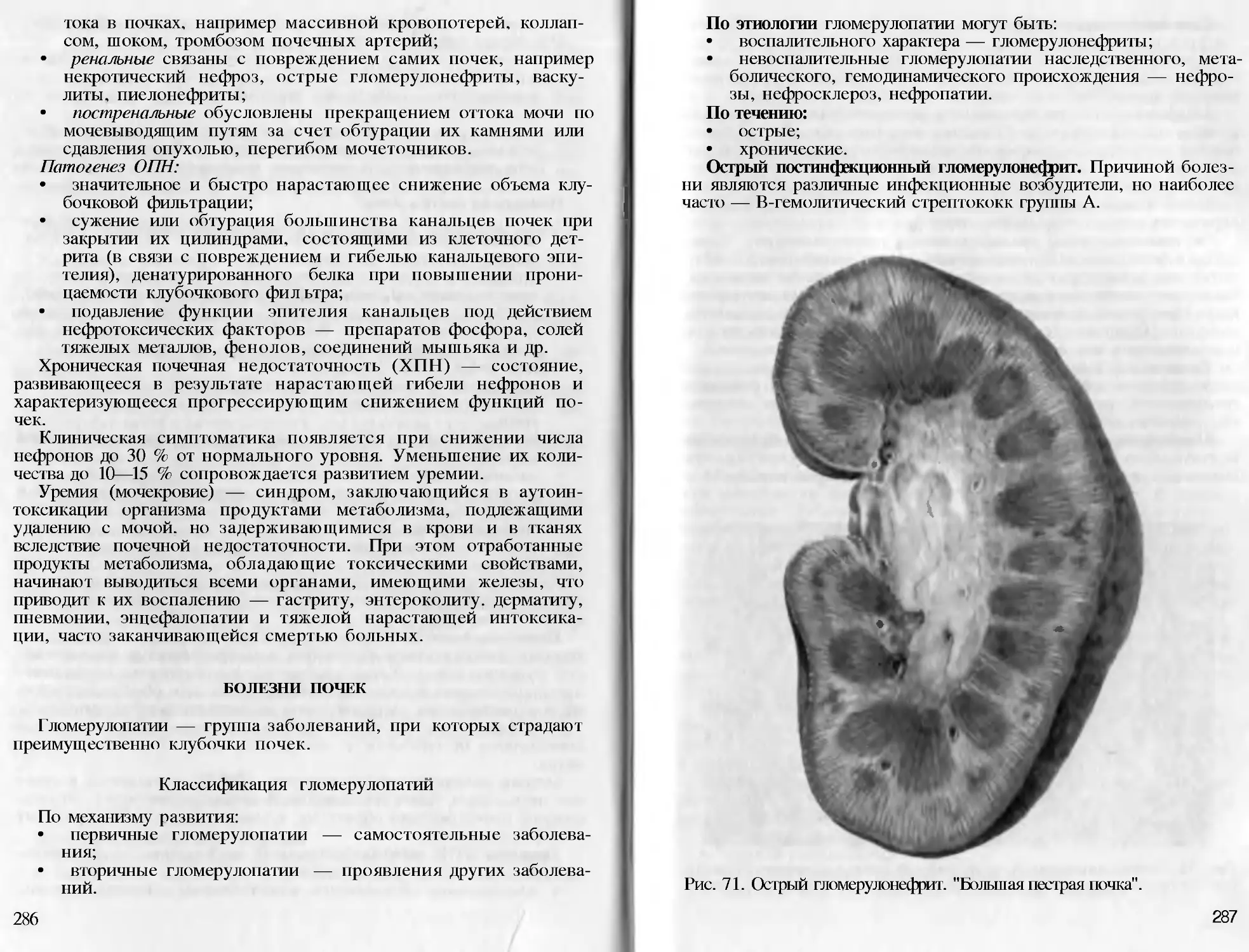
Text
Рецензенты: Е. А. Демуров — докт. мед. наук, профессор
кафедры патофизиологии Российского уни-
верситета Дружбы народов;
О. Д Мишнев — профессор, зав. кафедрой
патологической анатомии Российского госу-
дарственного медицинского университета
Пауков В. С, Литвнцкий П. Ф.
Патология: Учебник. — М.: Медицина, 2004. — 400 с:
илл. (Учеб. лит. для учащихся медицинских училищ и
колледжей). - ISBN 5-225-04860-9
В учебнике объединен материал двух дисциплин — патологической
анатомии и патологической физиологии. Учебник состоит из трех час-
тей: основы общей патологии, основы частной патологии, болезни
орофациальной области. Рассматриваются причины возникновения,
механизмы развития и завершения патологических процессов и болез-
ней. Особое внимание уделяется защитно-приспособительным и ком-
пенсаторным реакциям организма.
Для учащихся медицинских училищ, колледжей, лицеев и специа-
лизированных медицинских классов средних школ.
Пауков В. С,
Литвнцкий П. Ф., 2004
ОГЛАВЛЕНИЕ
Предисловие. .7
Введение. . .9
Часть I.
ОСНОВЫ ОБЩЕЙ ПАТОЛОГИИ
Глава 1. Повреждение.......................... . .14
Общая характеристика дистрофий, их виды. .14
Механизмы развития дистрофий .15
Паренхиматозные дистрофии .15
Углеводные дистрофии................................ .24
Стромально-сосудистые дистрофии. .26
Смешанные дистрофии................................. .33
Нарушения минерального обмена .38
Нарушения водного обмена, отек . .44
Апоптоз и некроз. . .47
Глава 2. Нарушения кислотно-щелочного равновесия. 54
Показатели кислотно-щелочного равновесия 54
Глава 3. Гипоксия. ... 57
Типы гипоксии 58
Структурно-функциональные расстройства при гипок-
сии. ... .60
Адаптивные реакции при гипоксии. 62
Глава 4. Нарушения теплового баланса организма .63
Гипертермические состояния и их виды. 64
Гипотермические состояния .69
Глава 5. Нарушения кровообращения и лимфообращения .... 71
Виды расстройств кровообращения .72
Нарушения реологических свойств крови. .81
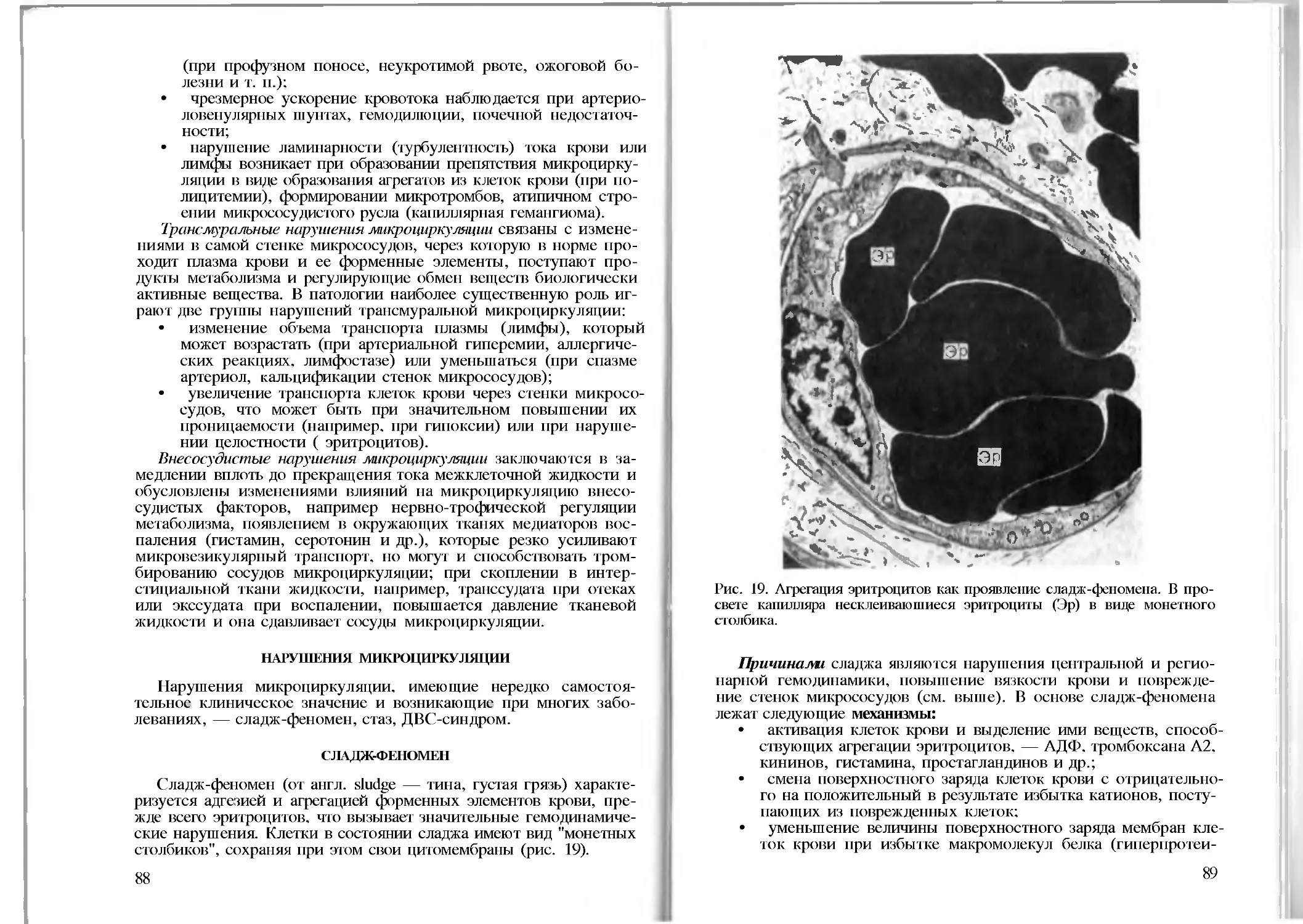
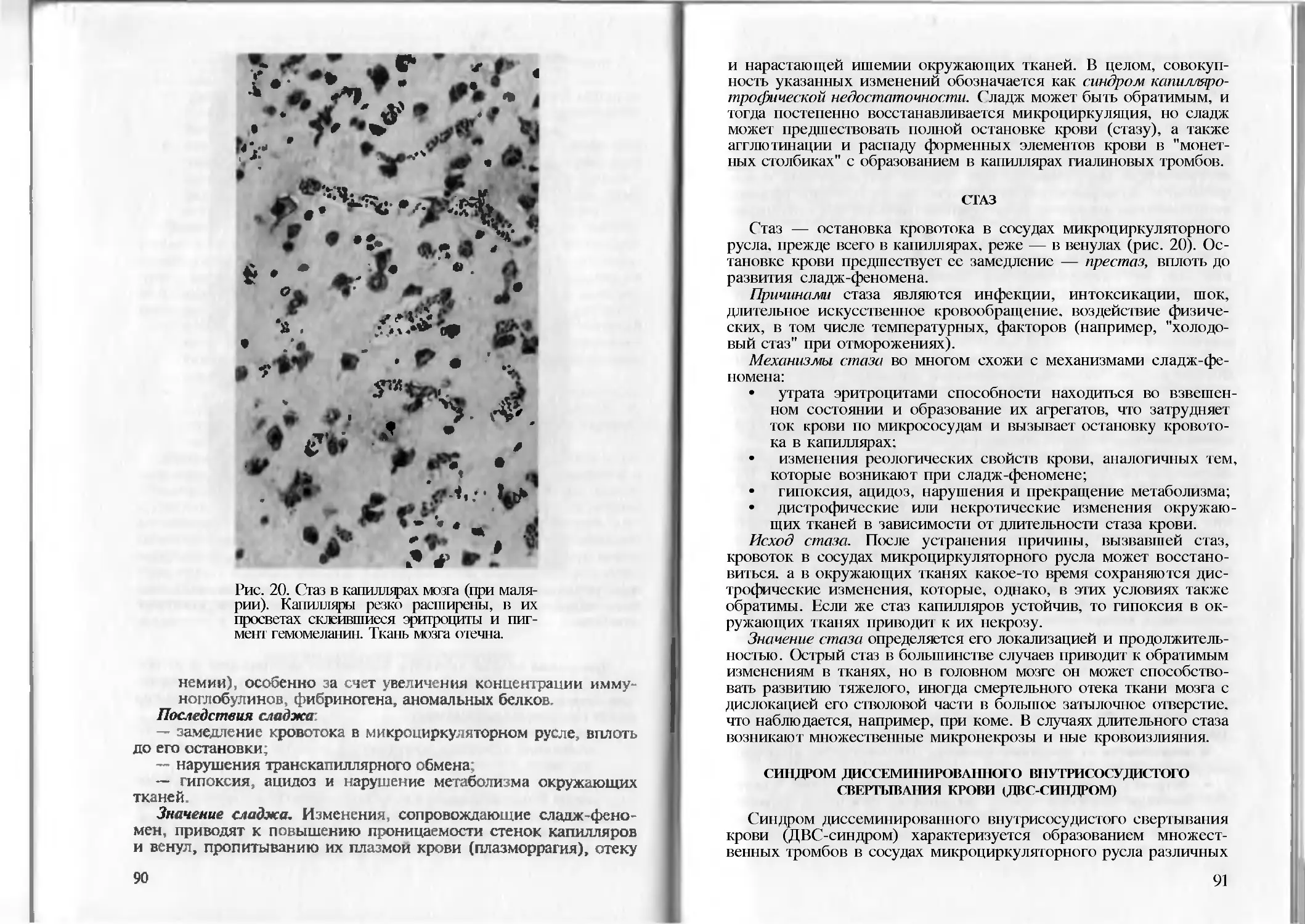
Нарушения микроциркуляции........................... .87
Нарушения проницаемости стенок сосудов. .93
Нарушения лимфообращения .95
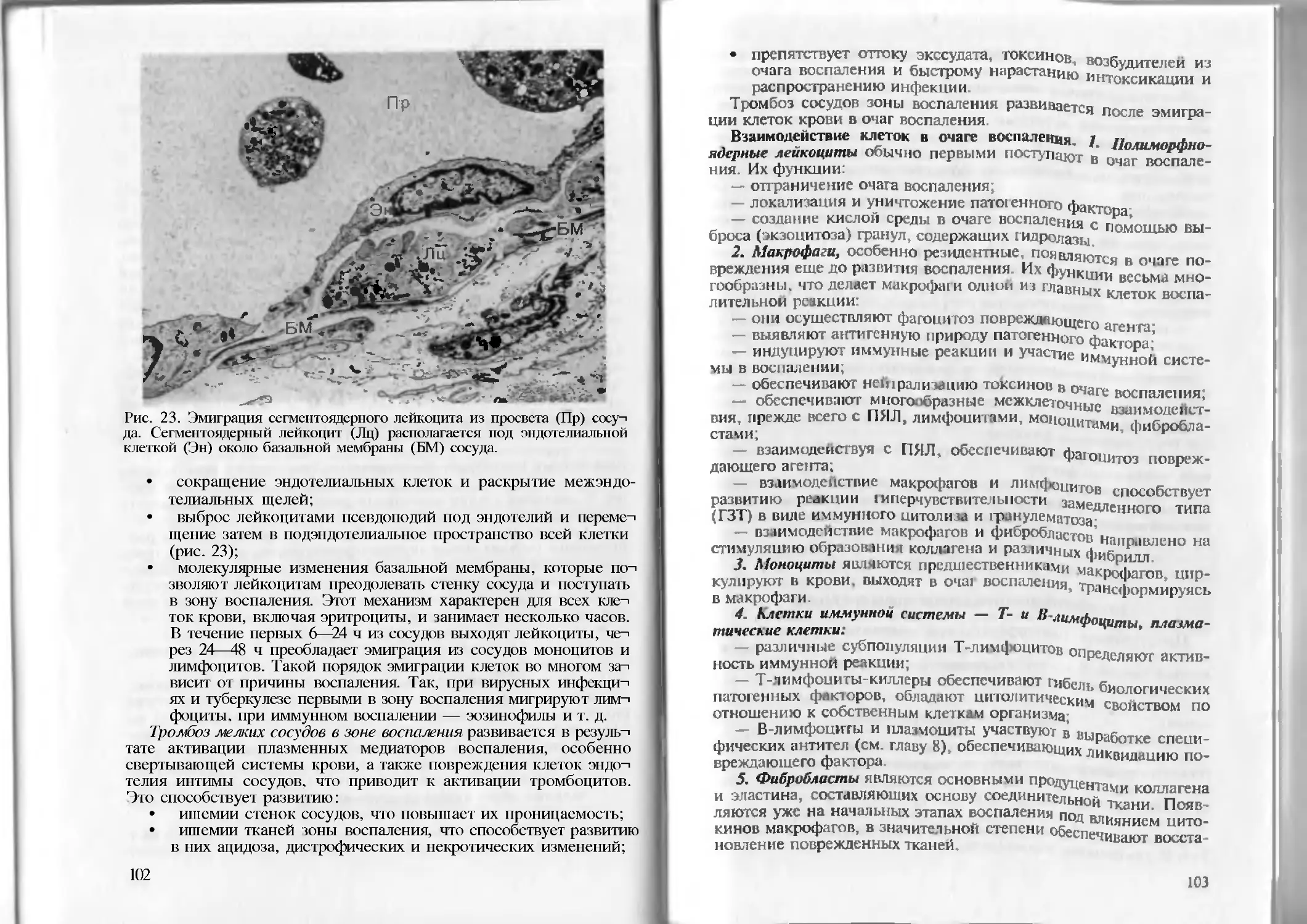
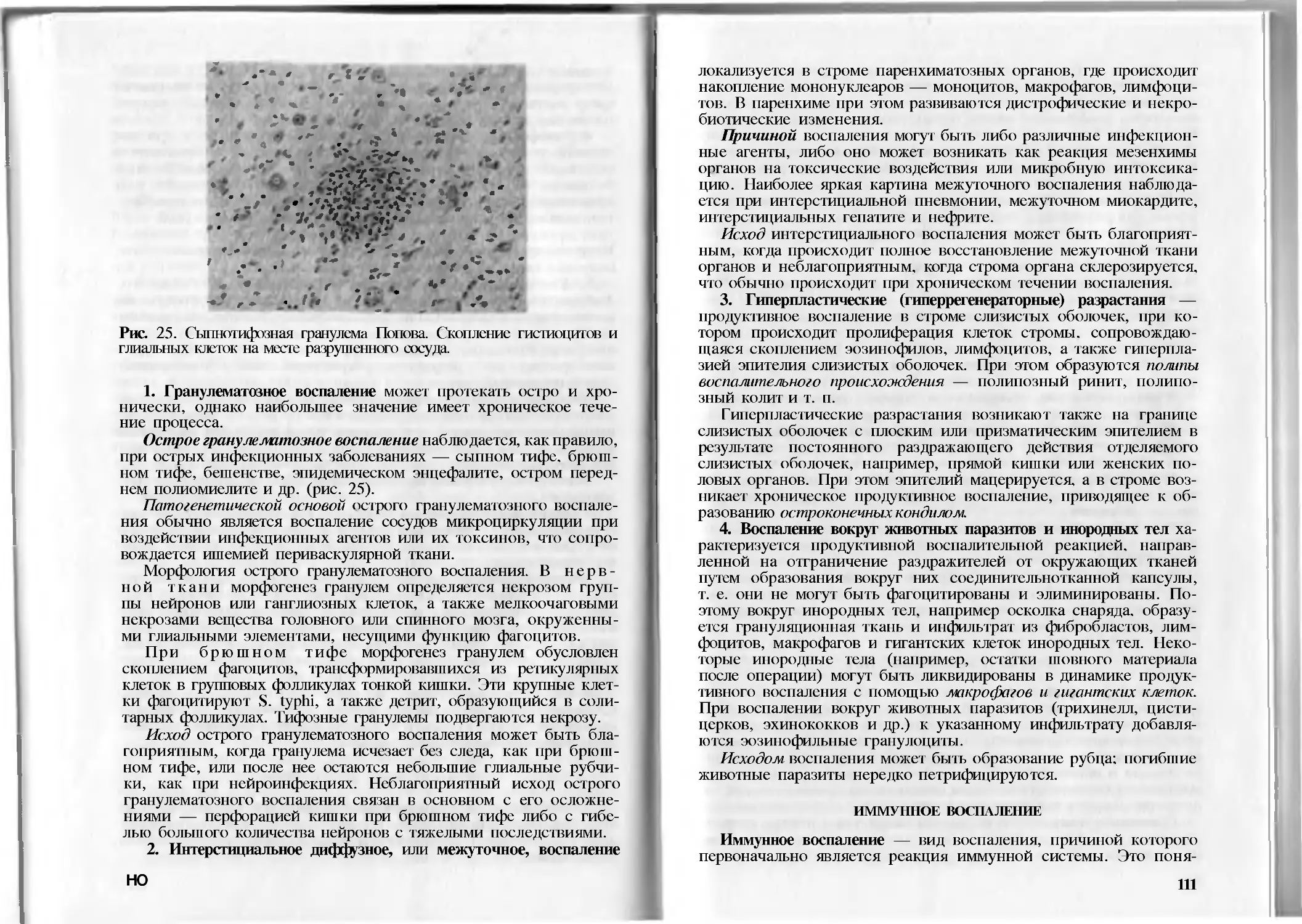
Глава 6. Воспаление......................................... .96
Общая характеристика воспаления . . .96
Патофизиология и морфология воспаления .100
Формы острого воспаления .105
Глава 7. Приспособительные и компенсаторные процессы .... 116
Характеристика понятий............................. .116
Виды приспособления и компенсации. . .117
Механизмы компенсации функций при болезнях . . . 124
Адаптационный процесс. ... .127
Компенсация и декомпенсация нарушенных функций 130
Глава 8. Иммунопатологические процессы.... .132
Общая характеристика иммунной системы............132
Типовые формы иммунопатологических процессов 134
Аллергические реакции .138
Глава 9. Значение факторов окружающей среды и реактивности
организма в патологии.................... .146
Основные группы повреждающих факторов. .146
Значение условий в возникновении болезней .148
Значение реактивности организма в возникновении и
развитии болезней................................148
Роль наследственности в патологии .150
Глава 10. Опухоли......................................... .153
Общая характеристика опухолей ..........153
Строение опухолей . .153
Рост опухолей ... .156
Виды опухолей . .157
Предопухолевые процессы..........................159
Причины и механизмы возникновения опухолей — он-
когенез. ........................................160
Особенности развития опухолей ...................162
Классификация опухолей .163
Эпителиальные опухоли ...........................163
Мезенхимальные опухоли...........................168
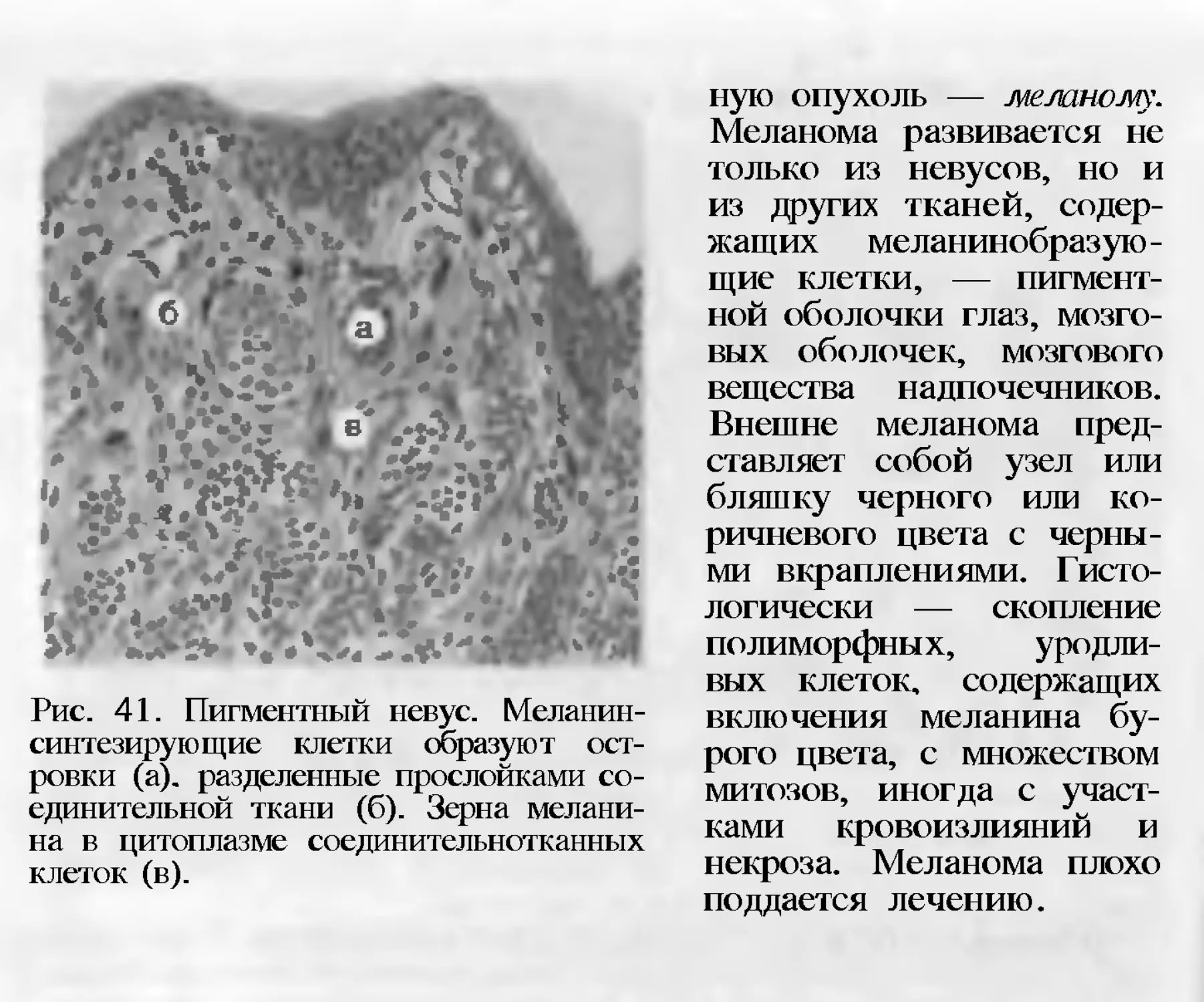
Опухоли меланинобразующей ткани .171
Часть II.
ОСНОВЫ ЧАСТНОЙ ПАТОЛОГИИ
Глава 11. Введение в нозологию. .173
Основные понятия нозологии .173
Этиология . .175
Патогенез........... . . . . . . .176
Исходы болезней ..................................177
Номенклатура и классификация болезней.............178
Глава 12. Болезни системы крови .181
Функции системы крови .181
Морфология кроветворения..........................182
Нарушения объема циркулирующей крови. .183
Патология системы эритроцитов. . . . .185
Патология системы лейкоцитов.................... 189
Опухоли системы крови, или гемобластозы. . .191
Глава 13. Болезни сердечно-сосудистой системы. .198
Патология системы кровообращения .198
Патология сердечной деятельности . . . .199
Болезни сердечно-сосудистой системы............. .202
Болезни сосудов...................................222
Глава 14. Ревматические болезни. .225
Ревматизм............... . . . .226
Ревматоидный артрит. ... . ... 232
Системная красная волчанка 234
Системная склеродермия 235
Узелковый периартериит. ... .237
Дерматомиозит. 237
Глава 15. Болезни системы дыхания............................238
Болезни системы дыхания............................241
Хронические неспецифические болезни легких .... 244
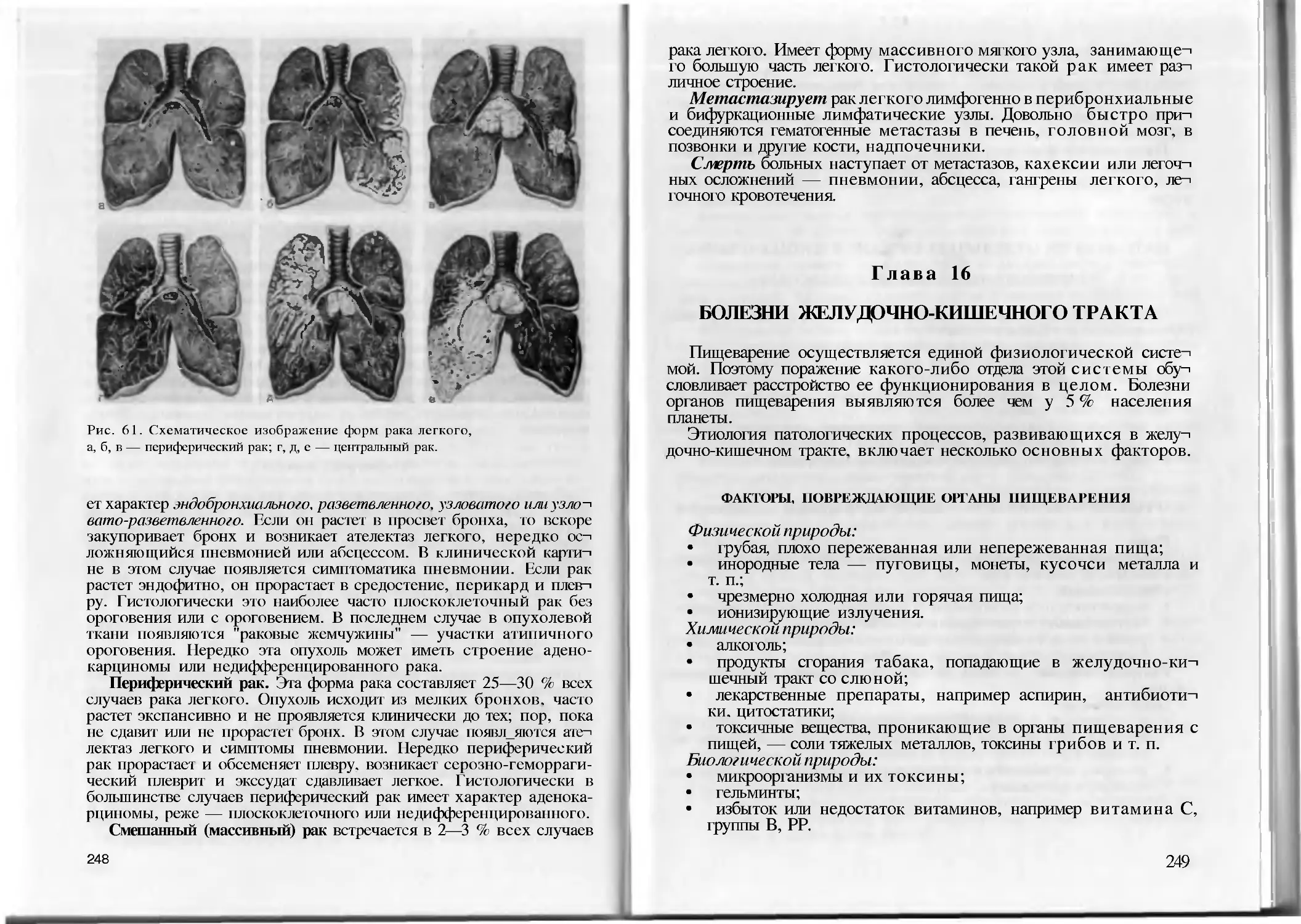
Глава 16. Болезни желудочно-кишечного тракта. . . . .249
Патология отдельных органов пищеварения . 250
Глава 17. Болезни печени, желчного пузыря и поджелудочной же-
лезы........................ 270
Глава 18. Болезни почек. ................................... 283
Глава 19. Болезни эндокринной системы....................... 297
Общая патология эндокринной системы. .298
Болезни эндокринной системы. . .... 299
Глава 20. Болезни нервной системы.......................... .311
Типовые формы патологии нервной системы. .312
Заболевания нервной системы........................316
Глава 21. Инфекционные болезни..............................320
Классификация инфекционных болезней .321
Общая характеристика инфекционных болезней 322
Глава 22. Болезни периода беременности .357
Глава 23. Экстремальные состояния...........................361
Коллапс............................................362
Шок.........................363
Кома...............................................366
Глава 24. Профессиональные болезни 368
Пневмокониозы......................................368
Профессиональные болезни, возникающие при дейст-
вии физических факторов.......... . . , . .370
Глава 25. Смерть, реанимация и болезни оживленного организма 372
Смерть. . . ... .372
Реанимация.........................................374
Болезни оживленного организма......................376
ВВЕДЕНИЕ
ПРЕДМЕТ, ЗАДАЧИ И МЕТОДЫ ПАТОЛОГИИ
Патология — фундаментальная наука, изучающая закономер-
ности возникновения, развития и завершения болезней. Предме-
том ее исследования является больной организм. Как учебная
дисциплина патология основывается на синтезе двух наук: пато-
логической физиологии и патологической анатомии.
Методы, используемые в патологии. Для познания и объясне-
ния сущности патологических процессов и болезней патология
использует данные:
• клинического обследования больных;
• морфологического изучения прижизненно взятых участков
тканей больного организма;
• результаты исследования трупов;
• моделирование болезней.
Патология включает два раздела — общую и частную патоло-
гию.
Общая патология изучает типовые (стереотипные) патологиче-
ские процессы, лежащие в основе болезней, — дистрофию, нек-
роз, атрофию, нарушения крово- и лимфообращения, воспале-
ние, аллергию, лихорадку, гипоксию, а также приспособительные
и компенсаторные реакции, шок. стресс и опухоли.
Частная патология изучает конкретные болезни, причины и
механизмы их развития, проявления, осложнения и исход отдель-
ных заболеваний.
Патология является теорией медицины, так как именно она по-
зволяет раскрыть сущность болезни, выявить ее функциональные
и структурные проявления, указать направление поиска принци-
пов профилактики и лечения болезней.
Для решения стоящих перед ней задач патология использует
два подхода:
патофизиологический, который позволяет изучить расстройства
в организме на разных этапах развития отдельных патологических
процессов и болезней в целом:
патоморфологический, который, с помощью разнообразных со-
временных морфологических методов, дает возможность исследо-
вать нарушения структуры органов и тканей во время болезни,
при выздоровлении или гибели организма.
Вместе с тем единство и взаимообусловленность функции и
структуры в норме и при патологии стирают грань между этими
двумя подходами, и они по существу лишь дополняют друг дру-
га. Так, патофизиология в настоящее время широко использует
для анализа патологических процессов морфологические мето-
ды. Патологическая анатомия в свою очередь располагает мето-
9
дами, позволяющими оценивать функцию поврежденных струк->
тур.
Патологическая анатомия использует несколько методов. К ним
относятся биопсия, вскрытие трупов и эксперименты на живот-"
пых.
Биопсия — прижизненное исследование кусочков тканей и срп
ганов больного. Высокое техническое оснащение современной
клинической медицины позволяет получить фрагмент ткани
(биоптат) практически любого органа человека. Анализируя с по-л
мощью микроскопа и других методов изменения, обнаруженные
в биоптате, патологоанатом устанавливает прижизненный клиниче->
ский диагноз заболевания. Результаты исследования биопсийного
материала позволяют выявить болезнь на самых ранних этапах ее
развития, когда еще отсутствуют четкие клинические симптомы
заболевания. Это дает возможность рано начать лечение и служит
залогом благоприятного исхода болезни. В ряде случаев только
патологоанатом может установить правильный диагноз (напри->
мер, точно определить характер опухоли).
Вскрытие (аутопсия) трупов умерших больных проводится
для выяснения тех изменений в органах и тканях, которые были
вызваны болезнью, а также для установления причины смерти;
по результатам вскрытия составляется патологоанатомический
диагноз.
Эксперименты на животных широко используются для изуче-i
ния морфологических изменений в органах и тканях в процессе
болезни, от самых ранних ее проявлений до завершения, а также
с целью оценки эффективности различных методов лечения.
Патофизиология — фундаментальная дисциплина, и поэтому
моделирование (в том числе на животных) болезней, близких к
заболеваниям человека, является ее ведущим методом. Экспери->
мент позволяет вскрыть сущность предболезненных состояний и
самых ранних стадий заболевания, что не всегда удается в клини->
ке. С помощью экспериментальных моделей исследуют механизм
мы развития болезней, оценивают разные способы их лечения,
находят пути управления течением заболевания (эксперименталь->
пая терапия), разрабатывают проблемы диагностики и профилак->
тики болезней. Любое лекарственное или нелекарственное сред-i
ство, прежде чем оно будет использовано в клинике, проходит
испытание на животных.
История патологии. Возникновение патологии и выделение ее
в качестве самостоятельной науки относятся к первой половине
XIX в., когда благодаря развитию химии, биологии, физиологии,
хирургии, терапии и морфологии для нее была подготовлена со->
ответствую щая основа.
Первая в России кафедра патологической анатомии и патоло->
гической физиологии была организована в 1849 г. в Московском
университете известным терапевтом А. И. Полуниным. Он пер->
вым понял необходимость сопоставления проявлений болезни,
имевшихся при жизни больного, с изменениями, которые выяв-
10
лялись при вскрытии трупов. А. И. Полунин — основоположник
клинико-анатомического направления, которое стало характерной
чертой отечественной медицины. Идеи А. И. Полунина продол-"
жали и развивали его многочисленные ученики и последователи.
Среди них и создатель Московской школы патологоанатомов, ав-i
тор первого в России учебника по патологической анатомии
проф. М. Н. Никифоров. Учениками М. Н. Никифорова были
академики А. И. Абрикосов и И. В. Давыдовский. Развивая идеи,
заложенные А. И. Полуниным и М. Н. Никифоровым, А. И. Аб->
рикосов создал принципы отечественной патологической анато-i
мии и внес большой вклад в разработку многих проблем общей и
частной патологии. И. В. Давыдовский доказал закономерности
развития патологических процессов и болезней; ему принадлежат
крупные исследования в области общей патологии, патологии во->
енного времени. Учеником М. Н. Никифорова был профессор
М. А. Скворцов — признанный основоположник детской патоло-"
гической анатомии.
Преемником идей Московской школы патологоанатомов стал
ученик А. И. Абрикосова — академик А. И. Струков. С его име->
нем связаны разработки патоморфологии туберкулеза, ревматичек
ских болезней, патологии микроциркуляции, воспаления, а также
введение в патологическую анатомию новых методов исследова-"
ния — гистохимии, гистоферментохимии, электронной микроскоп
пии, придавших ей функциональную направленность. Современ-"
ный этап развития патологической анатомии характеризуется появ->
лением молекулярной патологии, изучающей болезни на молеку-"
лярном уровне, обеспечивающим межклеточные отношения. Это
направление в нашей стране возглавляет академик М. А. Пальцев.
Параллельно с патологической анатомией развивалась и пято-"
логическая физиология. В 1849 г. тот же профессор А. И. Полу-"
нин стал основателем кафедры патологической физиологии в
Московском университете. В этот период эксперимент на живот-"
ных уже прочно вошел в арсенал методов научного исследования.
Фундаментом для развития патологической физиологии явились
исследования физиологов И. М. Сеченова, И. П. Павлова,
Н. Е. Введенского, терапевта С. П. Боткина.
В создании кафедр общей и экспериментальной патологии
(патологической физиологии) в России большая заслуга принад-"
лежит выдающемуся физиологу, ученику И. М. Сеченова —
проф. В. В. Пашутину. Его научные исследования были сосредо-"
точены на механизмах нарушения обмена веществ, голодании и
патологии эндокринной системы. Крупный вклад в развитие об-"
щей патологии внесли отечественные патофизиологи профессора
А. Б. Фохт, А. А. Богомолец, Н. Н. Аничков, С. С. Халатов, А. Д.
Сперанский. Н. Н. Сиротинин. которые разрабатывали различ-"
ные аспекты проблем реактивности, старения, патологии эндок-"
ринной системы. Н. Н. Аничков и С. С. Халатов создали первую
экспериментальную модель атеросклероза и многое сделали для
понимания механизмов его развития.
11
Большой вклад в развитие патологии внесли крупные зарубеж->
ные физиологи и морфологи — К. Бернар. В. Кеннон. К. Роки-
танский, Р. Вирхов, Г. Селье. Так, известный физиолог XIX века
К. Бернар является основоположником экспериментально-фи->
энологического направления в патологии и учения о постоянстве
внутренней среды организма — гомеостазе. Крупнейший немец-1
кий патолог Р. Вирхов — основатель учения о клеточной патоло->
гии. Клеточная теория патологии стала мощным стимулом для
изучения и систематизации клеточных, а позднее субклеточных
механизмов развития болезни. Широкую известность и распро->
странение получили исследования Г. Селье, показавшего важную
роль нейроэндокринной системы в формировании приспособив
тельных реакций и расстройств жизнедеятельности. Он является
основоположником учения о стрессе.
В настоящее время патология имеет в своем арсенале большой
комплекс современных физиологических и морфологических ме->
тодов исследования. Изучение патологических процессов и бел
лезней проводится на организменном, органном, клеточном, суСН
клеточном и молекулярном уровнях. Использование современных
методических подходов позволило вскрыть ряд важных для меди-1
цины общебиологических закономерностей. Основополагающие
ми среди них являются представление о типовых, или стереотипе
пых, реакциях; учение о гомеостазе; представление о том, что в
основе всех патологических процессов лежат физиологические
реакции; гетерогенность.
Представление о типовых, или стереотипных, реакциях, т. е. об
относительно небольшом наборе ответов организма на изменения
окружающего мира и внутренней среды, распространяется на все
и физиологические, и патологические процессы. Стереотипные
реакции проявляются на всех уровнях организации живой мате->
рии. На молекулярном уровне набор стереотипных реакций оикл
сительно невелик, на уровне внутриклеточных структур их не-"
сколько больше (например, в митохондриях могут происходить
набухание, потеря матрикса, разрушение крист, разрыв наружной
мембраны); на уровне клетки — секвестрация (отделение части
клетки), дифференцировка, деление, созревание. Различные с<л
четания стереотипных реакций на уровне внутриклеточных
структур, клеток, тканей и органов в условиях патологии состав-!
ляют специфику общепатологических процессов, а на уровне систем
и всего организма — картину болезни.
Учение о гомеостазе — совокупности типовых реакций, состав-!
ляющих относительное постоянство состава крови, метаболизма,
температуры тела, артериального давления, иными словами — по~>
стоянства внутренней среды. Эти же реакции определяют ответы
организма на патогенные воздействия.
В основе всех патологических процессов лежат физиологиче->
ские реакции, и никаких других, особых реакций, появляющихся
только при развитии патологии, не существует. Ответные реак->
ции организма на действие раздражителя в пределах параметров
12
гомеостаза являются нормальными, физиологическими. Но если
в ответ на действие раздражителя нарушаются структурно-функ-ч
циональные основы гомеостаза, те же самые реакции становятся
патологическими. Они могут вызвать гибель не только отдельных
частей организма, но и его смерть. Так, способность крови свер->
тываться в норме — действительно защитная физиологическая
реакция, предупреждающая смерть от кровотечения при повреж->
дениях. Но та же реакция в определенных неблагоприятных усло-ч
виях приводит к образованию тромба, закрывающего просвет со->
суда, что вызывает повреждение тканей организма (например,
инфаркт миокарда). Воспалительный процесс в норме направлен
на защиту организма от патогенных раздражителей, но при опре-ч
деленных условиях он может вызвать летальный (смертельный)
исход.
Гетерогенность — еще одна важная биологическая закономер->
ность. Органы функционируют на протяжении многих десятков
лет потому, что в каждый данный момент функционально актива
на не вся ткань органа, а только ее определенная часть. Функ->
ционирующие структуры разрушаются, для их восстановления
требуются время, энергетические и пластические затраты. Пока
идет процесс восстановления разрушившихся структур, функция
органа осуществляется другими структурами, которые в свою оче-ч
редь тоже разрушаются. Все это в норме создает структурно-
функциональную мозаичность органов и тканей, которая называ-ч
ется гетерогенностью. Она выявляется на всех уровнях жизнедея-ч
тельности: даже отдельная митохондрия не функционирует в
клетке одновременно всей своей структурой. Явление гетероген->
пости создает функциональный (жизненный) резерв организма.
Исчезновение гетерогенности структур клеток и тканей является
плохим прогностическим признаком, указывающим на истоще-ч
ние резервных возможностей организма.
Знание указанных биологических закономерностей позволяет
правильно понять болезнь, оценить состояние больного и провоз
дить целенаправленное лечение.
Часть I
ОСНОВЫ ОБЩЕЙ ПАТОЛОГИИ
Глава 1
ПОВРЕЖДЕНИЕ
Повреждение, или альтерация, — это изменение клеток, меж->
клеточного вещества или тканей, сопровождающееся нарушением
функции органов. Повреждения могут быть представлены одним
из трех процессов: дистрофия, некроз и апоптоз.
ОБЩАЯ ХАРАКТЕРИСТИКА ДИСТРОФИЙ, ИХ ВИДЫ
Дистрофия — патологический процесс, отражающий наруше->
ние обмена веществ (метаболизма) в организме. В основе дистро->
фий лежит расстройство трофики, т. е. комплекса механизмов,
обеспечивающих обмен веществ и сохранность структуры клеток
и тканей. Регуляция трофики осуществляется на следующих уров->
нях:
• центральная нервная система (ЦНС);
• нейроэндокринная система;
• система транспорта метаболитов (кровяное и лимфатиче->
ское, в том числе микроциркуляторное, русло);
• клетка;
• геном.
Нарушения или повреждения, возникающие на каждом из
этих уровней, приводят в итоге к изменению функции ферментов
(ферментопатии) и к развитию дистрофий. В зависимости от кп
го, на каком уровне нарушена регуляция метаболизма и что яви->
лось причиной ферментопатии, дистрофии разделяют на приоб->
ретенные и врожденные (болезни накопления, или тезаурисмо-
зы), развивающиеся у новорожденных и у детей раннего возраста
в результате генетического дефекта.
Морфологически дистрофии выражаются в следующих вариант
тах накопления продуктов обмена веществ:
• встречающихся в норме и в типичных для определенного
вещества структурах, но в избыточном количестве;
• накопление веществ, встречающихся в норме, но в нетипич->
ных для них структурах;
• появление веществ, не встречающихся в норме.
14
Виды дистрофий
В зависимости от преобладания .метаболического повреждения
в тех или иных структурах тканей выделяют следующие виды
дистрофий:
• паренхиматозные (клеточные), развивающиеся преимущем
ственно в клетках паренхиматозных органов;
• стромально-сосудистые (мезенхимальные), происходящие
преимущественно в строме органов (межклеточном матрик-
се) и в стенках сосудов;
• смешанные, развивающиеся как в клетках органов, так и в
межклеточном матриксе.
В зависимости от нарушениятого или иного вида метаболизма
дистрофии делят на:
• белковые (диспротеинозы);
• жировые (липидозы);
• углеводные;
• минеральные;
• нарушения водного обмена.
МЕХАНИЗМЫ РАЗВИТИЯ ДИСТРОФИЙ
Инфильтрация, при которой с кровью поступают в клетку или
в межклеточный матрикс свойственные им продукты метаболизм
ма, но в большем количестве, чем в норме.
Извращенный синтез, при котором в клетках или в межклеточм
ном матриксе образуются не свойственные этим клеткам и тканям
(аномальные) вещества.
Трансформация, при которой вместо продуктов одного вида
обмена образуются вещества, свойственные другому виду метабо~>
лизма.
Декомпозиция, или фанероз, при которой дистрофия развивает-"
ся в результате распада сложных химических соединений, состав-"
ляющих клеточные или межклеточные структуры.
В зависимости от степени метаболического повреждения дисм
трофии могут быть обратимыми и необратимыми.
ПАРЕНХИМАТОЗНЫЕ ДИСТРОФИИ
В зависимости от вида нарушенного обмена веществ паренхим
матозные дистрофии могут быть белковыми, жировыми и углем
водными.
Белковые дистрофии (диспротеинозы) связаны с нарушениями
обмена белка. Белок является одним из основных компонентов
клеток и тканей организма. Его масса составляет примерно 45 %
от массы тела, при этом 2/3 белка входят в состав костей скелета,
мышц и кожи, а 7з — внутренних органов. Обмен белка отлича-
15
ется высокой интенсивностью — за 24 ч обновляется около 1 г/кг
белка организма. Цикл полной замены молекул белка составляет
130-160 сут.
Белок обладает следующими основными функциями:
• информационная — белок является носителем специфичен
ских признаков клеток и тканей организма, в том числе ан-"
тигенных;
• рецепторная, так как белок — необходимый компонент ре->
цепторов клеток;
• ферментная — многие белки регулируют метаболические
процессы;
• структурная, в связи с тем что большинство белков являют-"
ся компонентами структур — от молекулярных до тканевых
и органных.
Белок в организме не депонируется, и поэтому при его дефи-"
ците мобилизуются белки мышц, кожи, внутренних органов.
Интегральным показателем общего уровня белкового обмена
является азотистый баланс, т. е. суточная разница между азотом,
поступающим в организм с пищей, и количеством его. выделяв-"
мым с мочой и калом.
Выделяют следующие виды азотистого баланса:
• нулевой, когда количества поступающего и выводимого
азота совпадают;
• положительный, в том случае, если количество поступаю-"
щего в организм азота выше, чем количество выводимого;
• отрицательный, когда количество поступающего в организм
азота меньше, чем выводимого.
Типовые нарушения белкового обмена заключаются в несоот-"
ветствии количества и состава белка, поступающего в организм,
потребностям в нем.
Оптимальное количество белка, которое должно поступать в
организм с пищей в течение суток, составляет 1,5—2,5 г на 1 кг
массы тела.
Виды несоответствия количества и состава белка потребно~>
стяморганизли:
• недостаток поступления белка в организм;
• избыток поступления или образования белка в организме;
• нарушение аминокислотного состава потребляемого белка.
Основные проявления дефицита белка в организме:
• снижение массы тела;
• понижение содержания белка в крови — гипопротеинемия;
• отеки;
• отрицательный азотистый баланс (на 15—25 % ниже нормы);
• иммунодефицитные состояния в результате нарушения об-"
разевания лимфоцитов;
• задержка физического и умственного развития.
Избыток поступления или образования белка в организме
• Основные причины:
— переедание;
16
— несбалансированная диета с длительным употреблением
большого количества белков.
• Проявления:
— положительный азотистый баланс;
— повышенное содержание белка в крови — гиперпротеинемия;
— диспепсические расстройства.
Расстройства метаболизма аминокислот существенно изменяют
обмен белков. При этом расстраиваются практически все другие
виды метаболизма — нуклеиновых кислот, липидов, витаминов,
углеводов, электролитов и жидкости.
Интегративным параметром белкового обмена в организме яв->
ляется содержание небелкового — остаточного азота крови. Его
нормальная концентрация в крови составляет 14,3—28,5 с/<
ммоль/л.
ПРИОБРЕТЕННЫЕ ПАРЕНХИМАТОЗНЫЕ БЕЛКОВЫЕ ДИСТРОФИИ
Зернистая дистрофия, или ранняя стадия дистрофии, обычно
развивается в клетках сердца, печени и почек при гиперфункции
этих органов, сопровождающейся распадом усиленно функцио->
пирующих внутриклеточных структур, нередко также при инток->
сикации организма. При этом органы становятся тусклыми,
дряблыми. Повреждения клеток заключаются в набухании внуг-i
риклеточных структур и распаде их мембран. Высвобождающийся
белок, а также белок цитоплазмы клеток подвергается поверхно->
стной денатурации, уплотняется и приобретает вид мелких зерен,
а цитоплазма клеток становится набухшей, мутноватой и зерни->
стой (рис. 1). Эта дистрофия обратима, и при прекращении дей->
ствия повреждающего фактора структура и функции клеток вос->
станавливаются.
Гиалиново-капельная дистрофия развивается как более глубо-i
кое повреждение клеток, связанное с коагуляцией белка, кото->
рый, уплотняясь, приобретает форму светлых капель, напоми->
нающих гиалиновый хрящ. Она развивается наиболее часто в
почках, реже в печени и сердце. Так, при заболеваниях, сопрово->
ждающихся повышенной проницаемостью почечного фильтра
(гломерулонефрит, нефротический синдром, сахарный диабет,
амилоидоз почек и др.), в первичной моче резко повышается со->
держание белка (протеинурия), который реабсорбируется эпите->
лием почечных канальцев. Однако клетки эпителия не способны
утилизировать такое большое количество белка, он скапливается
в их цитоплазме, образует крупные агрегаты, в которых и подверг
гается коагуляции. Это состояние белка необратимо, поэтому
эпителиальные клетки, цитоплазма которых перегружена коагу->
лированным белком, гибнут и слущиваются в просвет канальцев,
образуя гиалиновые цилиндры. В печени гиалиново-капельная
дистрофия гепатоцитов развивается при хронической алкоголь->
ной интоксикации, хроническом застое желчи, билиарном цир-
17
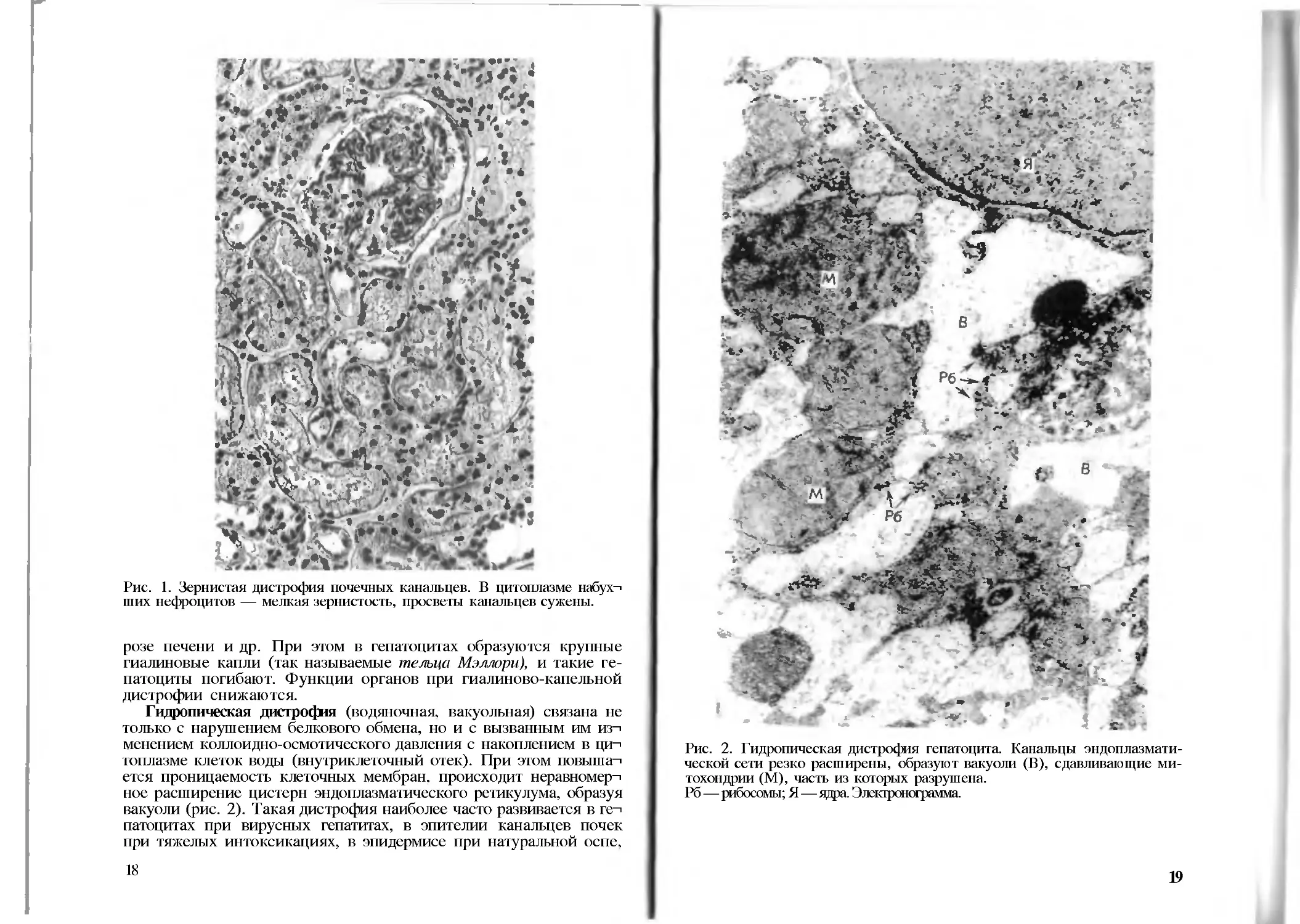
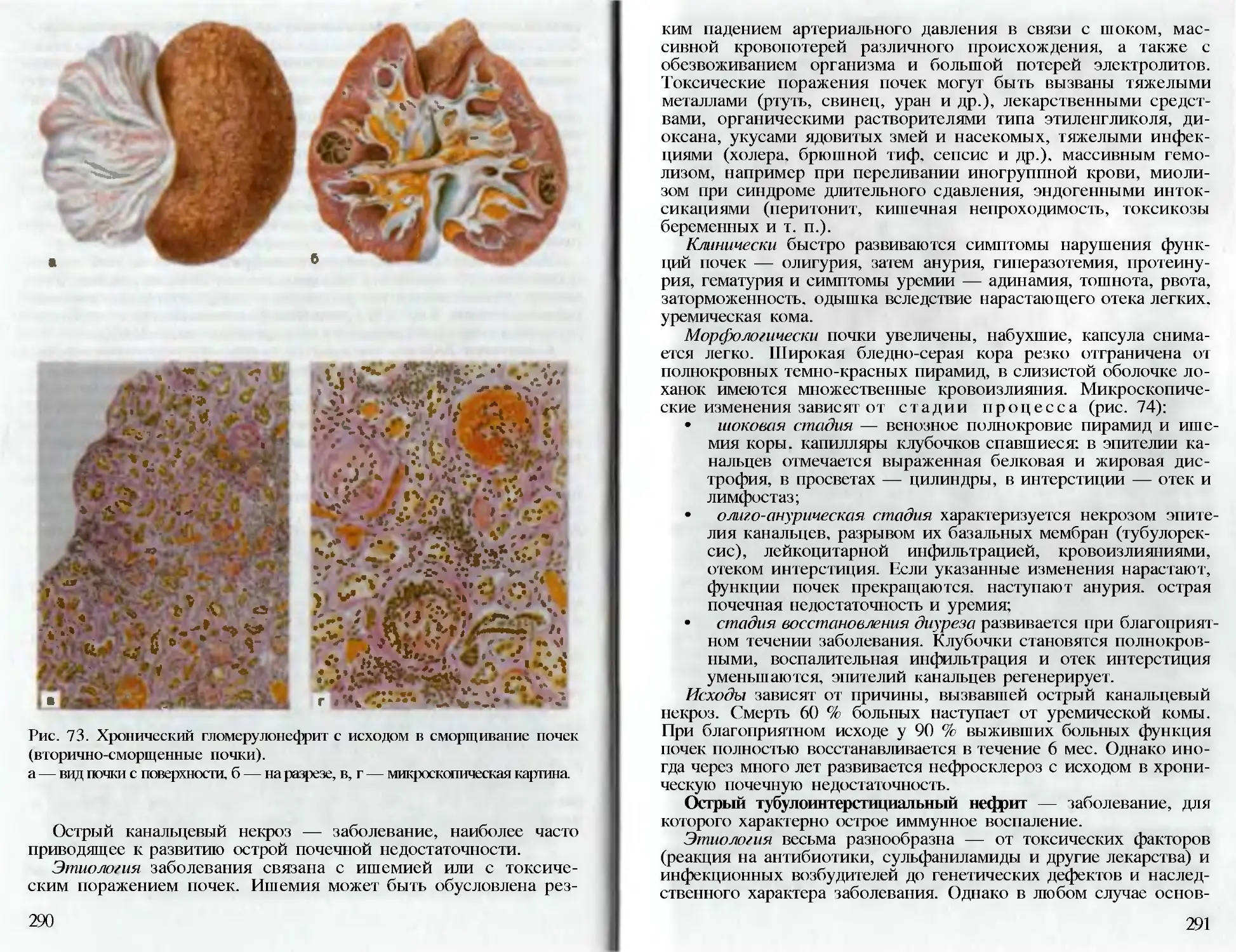
Рис. 1. Зернистая дистрофия почечных канальцев. В цитоплазме набух-'
ших нефроцитов — мелкая зернистость, просветы канальцев сужены.
розе печени и др. При этом в гепатоцитах образуются крупные
гиалиновые капли (так называемые тельца Мэллори), и такие ге-
патоциты погибают. Функции органов при гиалиново-капельной
дистрофии снижаются.
Гидропическая дистрофия (водяночная, вакуольная) связана не
только с нарушением белкового обмена, но и с вызванным им из->
менением коллоидно-осмотического давления с накоплением в ци-'
топлазме клеток воды (внутриклеточный отек). При этом повыша->
ется проницаемость клеточных мембран, происходит неравномер->
ное расширение цистерн эндоплазматического ретикулума, образуя
вакуоли (рис. 2). Такая дистрофия наиболее часто развивается в re-i
патоцитах при вирусных гепатитах, в эпителии канальцев почек
при тяжелых интоксикациях, в эпидермисе при натуральной оспе.
18
Рис. 2. Гидропическая дистрофия гепатоцита. Канальцы эндоплазмати-
ческой сети резко расширены, образуют вакуоли (В), сдавливающие ми-
тохондрии (М), часть из которых разрушена.
Рб—рибосомы; Я—ядра. Электронограмма.
19
в эпителии кишечника при холере и некоторых энтеритах. В этих
условиях активизируются ферменты лизосом — гидролазы, которые
разрушают органеллы клеток, в том числе мембраны цистерн эндо-
плазматического ретикулума. Последние разрываются, вакуоли
сливаются между собой, образуя одну большую вакуоль, смещаю-!
щую ядро и остатки органелл на периферию клетки. В этом случае
гидропическая дистрофия носит название баллонной. При этом
гибнет клеточное ядро и развивается колликвационный некроз
клетки. Макроскопически органы при гидропической дистрофии
изменены незначительно, но функция их снижается отчетливо.
Роговая дистрофия характеризуется избыточным образованием
рогового вещества в многослойном плоском эпителии {гиперкера~<
тоз) или образованием кератина в многослойном плоском неоро-
говевающем эпителии или в слизистых оболочках {лейкоплакия').
Эта дистрофия развивается при хроническом воспалении или при
некоторых авитаминозах и носит очаговый характер. У детей из->
редка встречается врожденная роговая дистрофия — ихтиоз. Она
проявляется образованием на коже роговых пластин, напоминаю-!
щих рыбью чешую, и нередко сочетается с другими пороками
развития — "рыбьим ртом", выворотом век, недоразвитием ушных
раковин и обычно заканчивается смертью. Роговая дистрофия и
ихтиоз, как правило, необратимы.
ВРОЖДЕННЫЕ ПАРЕНХИМАТОЗНЫЕ ДИСПРОТЕИНОЗЫ
Врожденные паренхиматозные белковые дистрофии связаны с
ферментопатиями, наследуемыми по аутосомно-рецессивному
типу и приводящими к нарушению всасывания тех или иных
аминокислот, а также связанного с ними синтеза клеточных бел->
ков. При этом развивается ряд синдромов:
• синдром мальабсорбции, или недостаточного всасывания
аминокислот, в частности метионина, в кишечнике, что
приводит к поносам, истощению, судорогам, одышке. умст->
венной отсталости, депигментации кожи и волос;
• наследственная цистинурия, являющаяся результатом пару-!
шения реабсорбции цистина, а также аргинина и лизина в
канальцах почек, что приводит к развитию у грудных детей
почечнокаменной болезни, связанной с выпадением плохо
растворимых цистиновых кристаллов и нередко осложняю-!
щейся пиелонефритом;
• фенилкетонурия (фенилпировиноградная олигофрения), вы->
званная отсутствием фермента фенилаланин-4-гидроксила-
зы, что приводит к накоплению фенилаланина и фенилпи-
ровинограднй кислоты, выявляемой в моче. При этом у
грудных детей развиваются прогрессирующее слабоумие
(олигофрения), поражение периферических нервов. депиг->
ментации глаз, волос и кожи, а также своеобразные кожные
заболевания;
20
цистиноз, тирозиноз и другие редко встречающиеся болезни
накопления.
ЖИРОВЫЕ ДИСТРОФИИ (ЛИПИДОЗЫ)
Жировые дистрофии связаны с избыточным накоплением в
цитоплазме паренхиматозных клеток липидов (нейтральных жи->
ров, триглицеридов, фосфолипидов, холестерина), либо с появле->
нием их в тех клетках, где они в норме не встречаются, либо с
появлением в цитоплазме клеток липидов аномального состава.
Потребность человека в жирах составляет 80—100 г в сутки.
Основные функции липидов в организме:
• структурная — липиды составляют основу клеточных мем->
бран;
• регулирующая;
• энергообеспечивающая, поскольку липиды являются одним
из главных источников энергии.
В зависимости от клинических проявлений выделяют:
• липидозы;
• ожирение;
• истощение.
Причинами приобретенных липидозов наиболее часто служат
гипоксия и различные интоксикации. Поэтому жировые дистро->
фии являются компонентом заболеваний, сопровождающихся ки->
слородным голоданием. — ишемической болезни сердца. гипер->
тонической болезни, пороков сердца, хронических заболеваний
легких (бронхоэктатическая болезнь, туберкулез, эмфизема лег->
ких). приводящих к развитию легочно-сердечной недостаточно-!
сти. Кроме того, жировую дистрофию вызывают различные ин->
фекции и интоксикации, которые сопровождаются как гипокси->
ей, так и блокадой токсинами ферментов, катализирующих в
клетках метаболизм липидов. Липидозы иногда могут быть связа->
ны с недостатком витаминов и некоторых аминокислот.
В патологии наибольшее значение имеют жировые дистрофии
миокарда, печени и почек.
Жировая дистрофия миокарда развивается путем декомпозиции
жиробелковых комплексов мембран внутриклеточных структур, а
также в результате инфильтрации кардиомиоцитов липидами.
Вне зависимости от механизма дистрофии в клетках миокарда
иначале появляются мелкие включения жира (пылевидное ожире->
ние), затем они сливаются в капли (мелкокапельное ожирение),
которые постепенно заполняют всю саркоплазму и могут приво-
дить к гибели клеток (рис. 3). Макроскопически полости сердца
I к растянуты, миокард дряблый, тусклый, глинистого виданаразре-
Иногда на эндокарде трабекул и папиллярных мышц видны
желтоватые поперечные полоски, соответствующие расположе->
нию венул и напоминающие шкуру тигра. Поэтому такое сердце
называется "тигровым" (рис. 4). Указанная морфология характер-
21
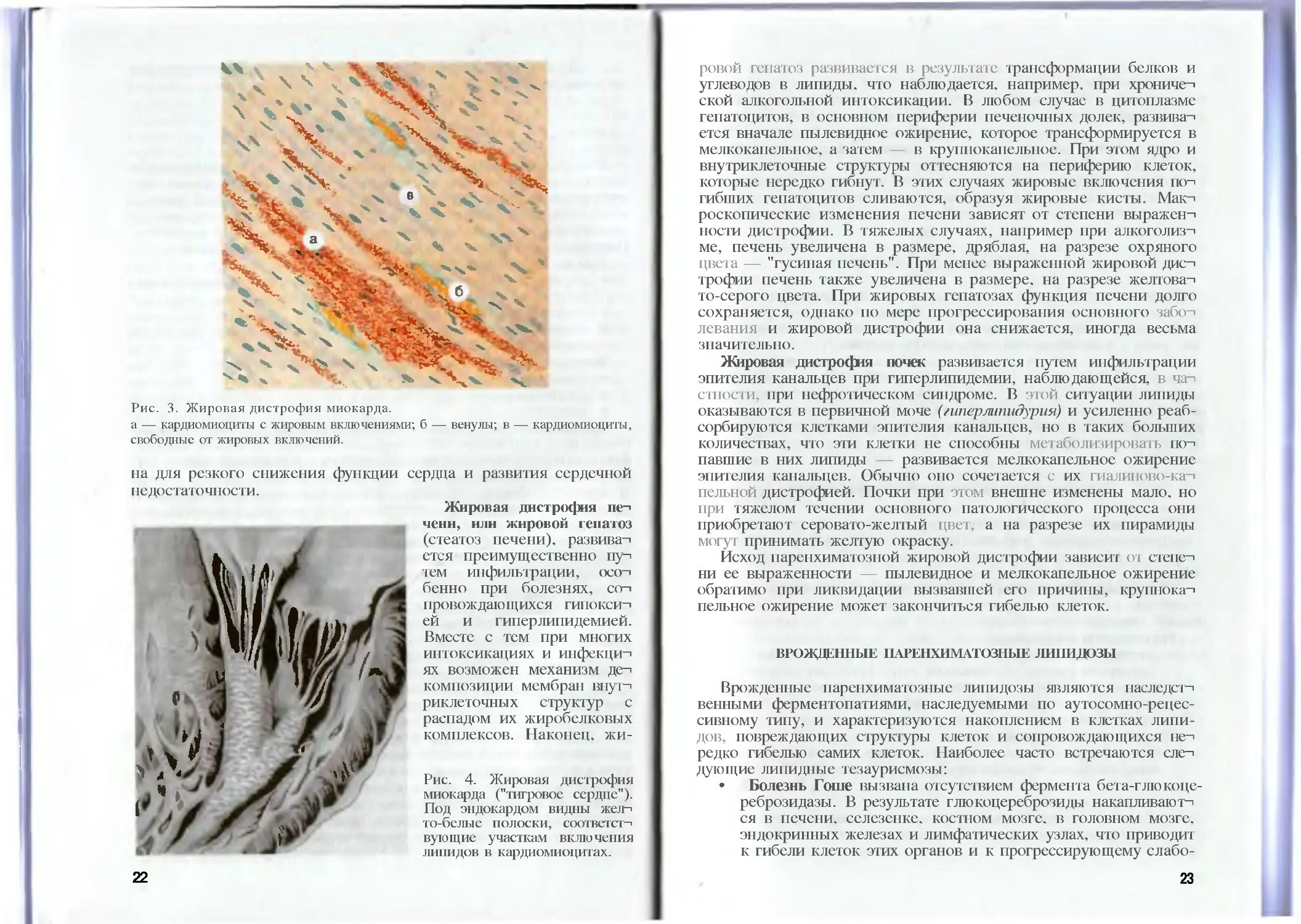
Рис. 3. Жировая дистрофия миокарда.
а — кардиомиоциты с жировым включениями; б — венулы; в — кардиомиоциты,
свободные от жировых включений.
на для резкого снижения функции сердца и развития сердечной
недостаточности.
Жировая дистрофия не-'
чени, или жировой гепатоз
(стеатоз печени), развива->
ется преимущественно пул
тем инфильтрации, осо->
бенно при болезнях, со-ч
провождающихся гипокси->
ей и гиперлипидемией.
Вместе с тем при многих
интоксикациях и инфекции
ях возможен механизм де->
композиции мембран внуг-i
риклеточных структур с
распадом их жиробелковых
комплексов. Наконец, жи-
Рис. 4. Жировая дистрофия
миокарда ("тигровое сердце").
Под эндокардом видны жел->
то-белые полоски, соответст-i
вующие участкам включения
липидов в кардиомиоцитах.
22
ровой гепатоз развивается в результате трансформации белков и
углеводов в липиды, что наблюдается, например, при хроничем
ской алкогольной интоксикации. В любом случае в цитоплазме
гепатоцитов, в основном периферии печеночных долек, развива-'
ется вначале пылевидное ожирение, которое трансформируется в
мелкокапельное, а затем — в крупнокапельное. При этом ядро и
внутриклеточные структуры оттесняются на периферию клеток,
которые нередко гибнут. В этих случаях жировые включения псп
гибших гепатоцитов сливаются, образуя жировые кисты. Макм
роскопические изменения печени зависят от степени выражен^
пости дистрофии. В тяжелых случаях, например при алкоголизм
ме, печень увеличена в размере, дряблая, на разрезе охряного
цвета — "гусиная печень". При менее выраженной жировой дисм
трофии печень также увеличена в размере, на разрезе желтовам
то-серого цвета. При жировых гепатозах функция печени долго
сохраняется, однако по мере прогрессирования основного забом
левания и жировой дистрофии она снижается, иногда весьма
значительно.
Жировая дистрофия почек развивается путем инфильтрации
эпителия канальцев при гиперлипидемии, наблюдающейся, в чам
стности, при нефротическом синдроме. В этой ситуации липиды
оказываются в первичной моче (гиперлипидурия) и усиленно реаб-
сорбируются клетками эпителия канальцев, но в таких больших
количествах, что эти клетки не способны метаболизировать пом
павшие в них липиды — развивается мелкокапельное ожирение
эпителия канальцев. Обычно оно сочетается с их гиалиново-кам
пельной дистрофией. Почки при этом внешне изменены мало, но
при тяжелом течении основного патологического процесса они
приобретают серовато-желтый цвет, а на разрезе их пирамиды
могут принимать желтую окраску.
Исход паренхиматозной жировой дистрофии зависит от степем
ни ее выраженности — пылевидное и мелкокапельное ожирение
обратимо при ликвидации вызвавшей его причины, крупнокам
пельное ожирение может закончиться гибелью клеток.
ВРОЖДЕННЫЕ ПАРЕНХИМАТОЗНЫЕ ЛИПИДОЗЫ
Врожденные паренхиматозные липидозы являются наследстм
венными ферментопатиями, наследуемыми по аутосомно-рецес-
сивному типу, и характеризуются накоплением в клетках липи-
дов, повреждающих структуры клеток и сопровождающихся нем
редко гибелью самих клеток. Наиболее часто встречаются слем
дующие липидные тезаурисмозы:
• Болезнь Гоше вызвана отсутствием фермента бета-глюкоце-
реброзидазы. В результате глюкоцереброзиды накапливаютм
ся в печени, селезенке, костном мозге, в головном мозге,
эндокринных железах и лимфатических узлах, что приводит
к гибели клеток этих органов и к прогрессирующему слабо-
23
умию, увеличению массы печени, селезенки и истощению
(кахексии).
• Болезнь Нимана—Пика развивается при отсутствии фермента
сфингомиелиназы, расщепляющей сфингомиелин, входящий
в состав многих тканей, но особенно нервной ткани. У боль->
пых детей он накапливается в клетках большинства органов
и при этом происходит увеличение массы печени и селезень
ки (гепато- и спленомегалия), отставание в психическом раз->
витии, появляются неврологическая симптоматика, гипото-л
ния, истощение. Дети погибают в возрасте 2—3 лет.
УГЛЕВОДНЫЕ ДИСТРОФИИ
Углеводные дистрофии связаны с накоплением в клетках бел-
ково-полисахаридных комплексов (гликоген, гликопротеины),
либо с образованием этих веществ в тех клетках, где их нет в нор->
ме, либо с изменением их химического состава.
Углеводы — обязательный и наиболее значительный компо->
пент пищи. В сутки человек потребляет 400—600 г различных уг->
леводов. Они являются необходимым элементом метаболизма,
важным компонентом структуры клеток и межклеточного веще->
ства и одним из главных источников энергии для обеспечения
жизнедеятельности организма.
ПРИОБРЕТЕННЫЕ УГЛЕВОДНЫЕ ДИСТРОФИИ
Гипогликемии — состояния, характеризующиеся снижением
содержания глюкозы в крови ниже 65 мг%, или 3,58 ммоль/л. В
норме уровень глюкозы крови натощак колеблется в диапазоне
65—ПО мг%, или 3,58—6,05 ммоль/л.
Причинами гипогликемии являются заболевания печени — xpo-i
нические гепатиты, циррозы печени, ее жировая дистрофия, а
также длительное голодание.
Результаты заболеваний:
• нарушение транспорта глюкозы из крови в гепатоциты,
снижение уровня образования в них гликогенеза и в связи с
этим отсутствие депонированного гликогена;
• торможение процесса образования гликогена и транспорта
глюкозы из гепатоцитов в кровь.
Последствия гипогликемии
• Гипогликемический синдром — стойкое снижение содержа->
ния глюкозы в крови ниже нормы (до 60—50 мг%, или
3,3—2,5 ммоль/л), приводящее к расстройству жизнедея->
тельности организма.
• Гипогликемическая кома — состояние, характеризующееся:
— падением концентрации глюкозы в крови ниже 40—30 мг%,
или 2.0—1.5 ммоль/л);
24
— потерей сознания;
— опасными для жизни расстройствами функций организма.
Гипергликемии — состояния, характеризующиеся увеличением
содержания глюкозы в крови выше нормы (более 120 мг%, или
6,05 ммоль/л натощак).
Причины гипергликемии
• патология эндокринной системы, сопровождающаяся из->
бытком гормонов, стимулирующих поступление углеводов в
кровь (глюкагона, глюкокортикоидов, катехоламинов, ти-
реоидных гормонов, соматотропного гормона) либо псдос-
татком инсулина или снижением его эффективности;
• нейро- и психогенные расстройства, например реактивные
психозы, стресс-реакции и подобные им состояния, харак->
теризующиеся активацией органов эндокринной системы;
• переедание, прежде всего длительное избыточное потребле->
ние кондитерских изделий;
• заболевания печени, при которых гепатоциты теряют спо->
собность трансформировать глюкозу в гликоген.
Последствия
• Гипергликемический синдром — состояние сопровождающее-'
ся значительным увеличением содержания глюкозы в крови
выше нормы (до 190—210 мг%, 10,5—11,5 ммоль/л и более),
приводящее к расстройствам жизнедеятельности организма.
• Гипергликемическая кома, характеризующаяся потерей соз->
нания, снижением или утратой рефлексов, расстройствами
дыхания и кровообращения, нередко заканчивающаяся
смертью больного.
Наиболее часто гипергликемия наблюдается при сахарном
диабете, развивающемся в результате абсолютной или относи-'
тельной инсулиновой недостаточности (см. главу 19).
НАСЛЕДСТВЕННЫЕ УГЛЕВОДНЫЕ ДИСТРОФИИ (ГЛИКОГЕНОЗЫ)
Гликогенозы — типовая форма патологии углеводного обмена
наследственного генеза, характеризующаяся накоплением глико-'
гена в клетках, что обусловливает нарушение жизнедеятельности
организма.
Главная причина — наследуемая или врожденная аномалия re-i
нов, кодирующих синтез ферментов расщепления (реже — обра->
зования) гликогена. Наследуются по аутосомно-рецессивному ти-i
пу. Выделяют более 10 типов гликогенозов. Среди них наиболее
часто встречаются болезни Гирке. Помпе, фетальный муковисци-
доз, а также болезни Форбса—Кори, Андерсена, Мак-Ардла.
Болезнь Гирке возникает при отсутствии фермента глюкозо-6-
фосфатазы, что приводит к накоплению гликогена в клетках пе-"
чени и почек, но к отсутствию углеводов в крови. Это сопровожу
дается вторичным гипофизарным ожирением. Большинство детей
погибают от ацидотической комы.
25
Болезнь Помпе связана с отсутствием кислой альфа- 1,4-глюко-
зидазы в лизосомах, что приводит к накоплению гликогена в
сердце, поперечнополосатых и гладких мышцах, в том числе в
межреберных, диафрагмальных, в мышцах языка, пищевода, же->
лудка и т. п. Дети погибают в раннем возрасте от сердечной или
дыхательной недостаточности.
Остальным муковисцидоз — заболевание, связанное с геноти-
пической ферментопатией. приводящей к нарушению обмена му-
коидов, входящих в секрет многих желез. В результате секрет же->
лез становится вязким и густым, выводится с трудом, что привод
дит к растяжению желез, превращению их в кисты, особенно в
поджелудочной железе, слизистых оболочках желудочно-кишеч->
него тракта и дыхательных путей, слюнных, потовых, слезных
железах и др. При этом в легких часто развиваются ателектазы с
развитием пневмонии и бронхоэктазов. Смерть наиболее часто
наступает от легочно-сердечной недостаточности.
СТРОМАЛЬНО-СОСУДИСТЫЕ ДИСТРОФИИ
Стромально-сосудистые, или мезенхимальные, дистрофии pan
виваются в тканях, производных мезенхимы, в первую очередь в
интерстициальной соединительной ткани, составляющей строму
органов и стенки сосудов. Она состоит из коллагеновых. эластич->
ных и ретикулиновых волокон, внеклеточного матрикса, пред-"
ставленного гликозаминогликанами; фибробластов, продуцирую^
щих такие белки, как коллаген и эластин; гистиоцитов. В интер->
стициальной соединительной ткани располагаются кровеносные
и лимфатические сосуды микроциркуляторного русла, нервные
окончания, рециркулирующие лимфоциты и резидентные макрос
фаги. В зависимости от вида нарушения обмена веществ cipin
мально-сосудистые дистрофии делят на белковые (диспротеино-
зы), жировые (липидозы) и углеводные.
БЕЛКОВЫЕ СТРОМАЛЬНО-СОСУДИСТЫЕ ДИСТРОФИИ
Белковые стромально-сосудистые дистрофии (диспротеинозы)
включают следующие виды нарушения белкового обмена: муко-
идное набухание, фибриноидное набухание (фибриноид), гиали-
ноз и амилоидоз.
Мукоидное набухание. Его причиной могут быть инфекционно-
аллергические заболевания, в том числе ревматические болезни,
атеросклероз, гипертоническая болезнь и др. Основным механизм
мом развития является инфильтрация.
Морфология. Дистрофия характеризуется поверхностной и обра->
тимой дезорганизацией соединительной ткани в строме органов и в
стенках сосудов за счет накопления и перераспределения гликоза-
миногликанов, главным образом гиалуроновой кислоты. Гликоза-
26
Рис. 5. Мукоидное набухание клапана сердца (ревматический эндокар-"
дит). В клапане сердца (а) и париетальном эндокарде (б) — резкая мета-
хромазия. Умеренная лимфогистиоцитарная инфильтрация ткани клала-"
на. Окраска толуидиновым синим.
миногликаны обладают гидрофильными свойствами, и их накопле-"
ние в строме органов и в стенках сосудов ведет к повышению сосу-"
диетой проницаемости, выходу в ткани мелкодисперсных белков
плазмы крови и гликопротеинов. При этом происходит лишь пабу-"
хание, но не разрушение коллагеновых волокон и внеклеточного
матрикса. Однако коллагеновые волокна теряют устойчивость к
коллагеназе и приобретают способность при окраске толуидине-"
вым синим изменять голубой цвет на сиреневый (рис. 5). Это явле-"
ние называется метахромазией и указывает на развитие мукоидного
набухания, не имеющего клинической симптоматики. Наиболее
хорошо метахромазия выражена в стенках артерий, эндокарде, кла-"
панах сердца, синовиальных оболочках. При этом органы внешне
не изменены, функция их снижена незначительно.
Фибриноидное набухание. Фибриноид является следующей
стадией развития стромально-сосудистой дистрофии.
Механизмы фибриноида — декомпозиция и инфильтрация.
Морфология: глубокая и необратимая дезорганизация соедини-"
тельной ткани стромы органов и стенок сосудов. Усиливается вы-"
ход из сосудов плазмы, плазменных белков, причем не только мел-"
кодисперсных, но и таких крупнодисперсных, как фибриноген, ко-"
торый в соединительной ткани превращается в фибрин. Происхо-"
дит накопление фибрина, гликозаминогликанов и других белков
между фазами коллагеновых волокон, во внеклеточном матриксе и
в стенках сосудов. В результате этого они вначале резко набухают и
возникает фибриноидное набухание, а затем разрушаются. Остатки
коллагеновых и эластических волокон вместе с набухшим и резко
измененным внеклеточным матриксом превращаются в гомоген-"
ную, рыхлую, бесструктурную массу. Развивается фибриноидный
некроз (рис. 6). Функция органов при этом отчетливо страдает,
27
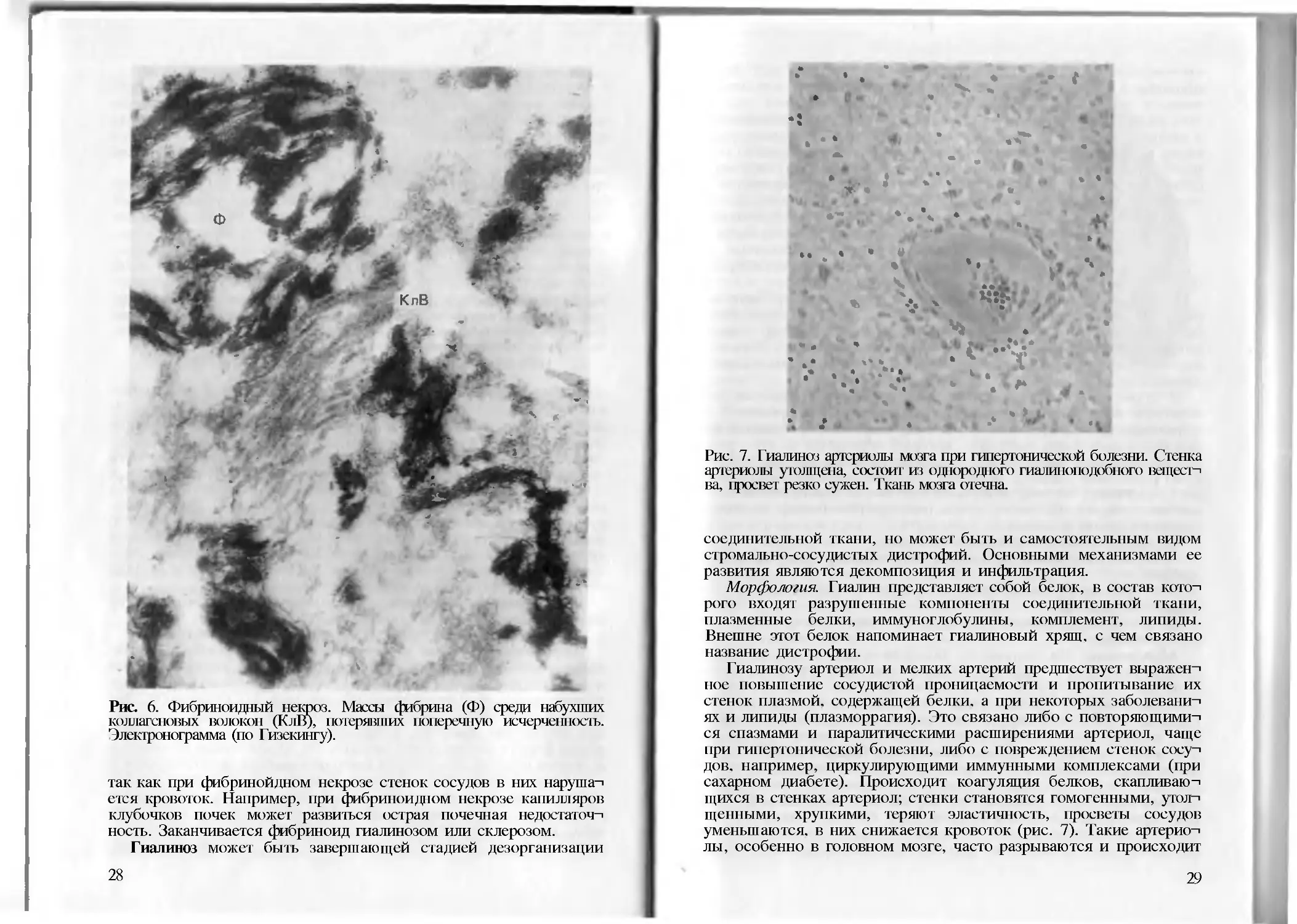
Рис. 6. Фибриноидный некроз. Массы фибрина (Ф) среди набухших
коллагеновых волокон (КлВ), потерявших поперечную исчерченность.
Электронограмма (по Гизекингу).
так как при фибринойдном некрозе стенок сосудов в них нарушав
ется кровоток. Например, при фибриноидном некрозе капилляров
клубочков почек может развиться острая почечная недостаточ->
ность. Заканчивается фибриноид гиалинозом или склерозом.
Гиалиноз может быть завершающей стадией дезорганизации
28
Рис. 7. Гиалиназ артериолы мозга при гипертонической болезни. Стенка
артериолы утолщена, состоит из однородного гиалиноподобного вещесг-i
ва, просвет резко сужен. Ткань мозга отечна.
соединительной ткани, но может быть и самостоятельным видом
стромально-сосудистых дистрофий. Основными механизмами ее
развития являются декомпозиция и инфильтрация.
Морфология. Гиалин представляет собой белок, в состав кото->
рого входят разрушенные компоненты соединительной ткани,
плазменные белки, иммуноглобулины, комплемент, липиды.
Внешне этот белок напоминает гиалиновый хрящ, с чем связано
название дистрофии.
Гиалинозу артериол и мелких артерий предшествует выражен-'
ное повышение сосудистой проницаемости и пропитывание их
стенок плазмой, содержащей белки, а при некоторых заболевание
ях и липиды (плазморрагия). Это связано либо с повторяющими->
ся спазмами и паралитическими расширениями артериол, чаще
при гипертонической болезни, либо с повреждением стенок сосу
дов. например, циркулирующими иммунными комплексами (при
сахарном диабете). Происходит коагуляция белков, скапливаю^
щихся в стенках артериол; стенки становятся гомогенными, угол-'
щенными, хрупкими, теряют эластичность, просветы сосудов
уменьшаются, в них снижается кровоток (рис. 7). Такие артериое
лы, особенно в головном мозге, часто разрываются и происходит
29
кровоизлияние в мозг. Гиалиноз артериол почечных клубочков
приводит к их гибели, склерозу и сморщиванию почек, что может
явиться причиной почечной недостаточности. Местный гиали-
ноз, развивающийся в створках клапанов сердца при ревматизме
в исходе фибриноидных изменений соединительной ткани, при-
водит к склерозу, деформации створок клапанов и развитию по-
рока сердца. Таким образом, гиалиноз значительно нарушает
функции органов. Вместе с тем местный гиалиноз встречается у
пожилых людей как проявление инволютивных изменений.
• Вцщ>1 гиалиноза — гиалиноз сосудов и гиалиноз собственно со-
единительной ткани. По распространенности он может быть:
— местным, например в клапанах сердца при ревматизме;
— системным, например в стенках всех артериол при гиперто-
нической болезни.
Амилоидоз — стромально-сосудистый диспротеиноз. характе-
ризующийся отложением в межуточной ткани, на базальных мем-
бранах слизистых оболочек и сосудов плотного вещества — ами-
лоида, состоящего на 96 % из аномального белка и на 4 % из по-
лисахаридов. Механизмом образования амилоида является извра-
щенный синтез.
В норме этот белок у человека не встречается. Накопления
амилоида в строме органов приводят к атрофии их паренхимы и
функциональной недостаточности. Существует много биохимиче-
ски различных форм амилоида, который образуется из его пред-
шественников в фибробластоподобных клетках (амилоидобла-
стах) различных органов. Амилоид обладает слабыми антигенны-
ми свойствами, поэтому иммунная система не реагирует на него
как на чужеродный белок, что и позволяет амилоиду накапли-
ваться в органах и тканях.
По происхождению амилоид может быть:
— первичным (идиопатическим, т. е. невыясненного происхо-
ждения);
— вторичным, развивающимся в результате различных хрони-
ческих заболеваний.
По распространенности различают амилоидоз местный и гене-
рализованный.
Морфология. На основании биохимических и клинических
данных выделяют 14 типов амилоида, связанных с извращенным
синтезом иммуноглобулинов, секрета эндокринных желез, сыво-
роточных белков и др. Амилоидоз развивается почти во всех ор-
ганах и тканях, за исключением костной и хрящевой. Поражен-
ные амилоидозом органы увеличиваются в размерах, становятся
плотными, на разрезе имеют сальный вид. Нанесение на поверх-
ность разреза таких органов растворов йода и соляной кислоты
вызывает синее окрашивание ткани. На микроскопических срезах
органов амилоид выявляется при окраске конго красным (конго-
рот), приобретая кирпично-красный цвет. Особенно часто амило-
ид откладывается в строме и сосудах селезенки, почек, печени и
надпочечников. В селезенке амилоид вначале появляется в лим-
30
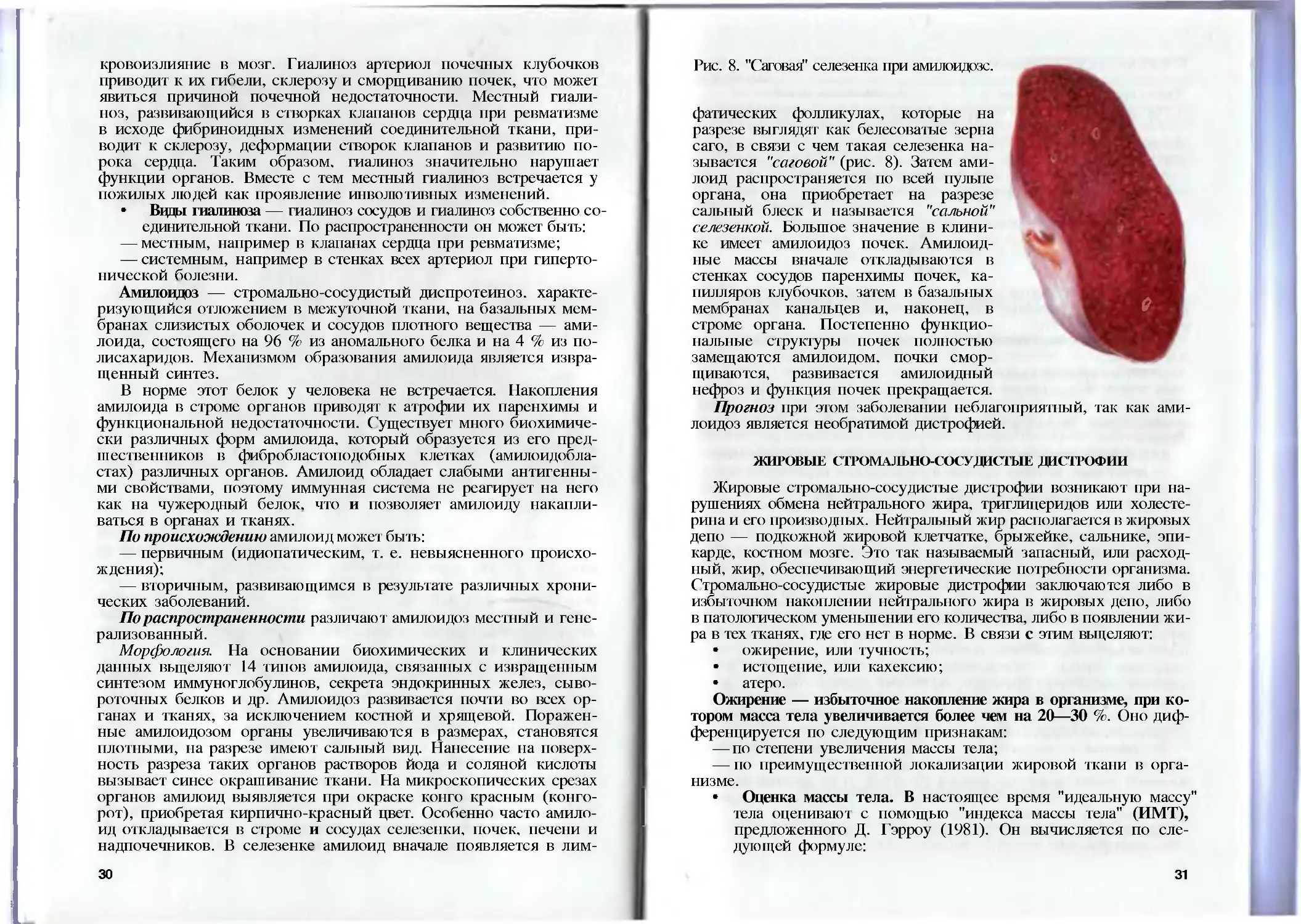
Рис. 8. "Саговая" селезенка при амилоидозе,
фатических фолликулах, которые на
разрезе выглядят как белесоватые зерна
саго, в связи с чем такая селезенка на-
зывается "саговой" (рис. 8). Затем ами-
лоид распространяется по всей пульпе
органа, она приобретает на разрезе
сальный блеск и называется "сальной"
селезенкой. Большое значение в клини-
ке имеет амилоидоз почек. Амилоид-
ные массы вначале откладываются в
стенках сосудов паренхимы почек, ка-
пилляров клубочков, затем в базальных
мембранах канальцев и, наконец, в
строме органа. Постепенно функцио-
нальные структуры почек полностью
замещаются амилоидом, почки смор-
щиваются, развивается амилоидный
нефроз и функция почек прекращается.
Прогноз при этом заболевании неблагоприятный, так как ами-
лоидоз является необратимой дистрофией.
ЖИРОВЫЕ СТРОМАЛЬНО-СОСУДИСТЫЕ ДИСТРОФИИ
Жировые стромально-сосудистые дистрофии возникают при на-
рушениях обмена нейтрального жира, триглицеридов или холесте-
рина и его производных. Нейтральный жир располагается в жировых
депо — подкожной жировой клетчатке, брыжейке, сальнике, эпи-
карде, костном мозге. Это так называемый запасный, или расход-
ный, жир, обеспечивающий энергетические потребности организма.
Стромально-сосудистые жировые дистрофии заключаются либо в
избыточном накоплении нейтрального жира в жировых депо, либо
в патологическом уменьшении его количества, либо в появлении жи-
ра в тех тканях, где его нет в норме. В связи с этим выделяют:
• ожирение, или тучность;
• истощение, или кахексию;
• атеро.
Ожирение — избыточное накопление жира в организме, при ко-
тором масса тела увеличивается более чем на 20—30 %. Оно диф-
ференцируется по следующим признакам:
— по степени увеличения массы тела;
— по преимущественной локализации жировой ткани в орга-
низме.
• Оценка массы тела, В настоящее время "идеальную массу"
тела оценивают с помощью "индекса массы тела" (ИМТ),
предложенного Д. Гэрроу (1981). Он вычисляется по сле-
дующей формуле:
31
Таблица 1. Степень увеличения массы тела, в кг/м2 (норма 18,5—24,9)
Индекс массы тела (Тепень Описательная оценка
25-29.29 I Повышенная масса тела ("степень завис- ти окружающих")
30-39,9 I] Тучность ("степень улыбки окружающих")
>40 III Болезненная тучность ("степень сочувст- вия окружающих")
ИМТ = масса тела (кг) (КГ/М)
рост (м)
Масса тела считается нормальной при ИМТ в диапазоне 18,5—
24,9. Большие значения ИМТ свидетельствуют об избыточной
массе тела (табл. 1).
• По преимущественной локализации жировой ткани выде-
ляю!:
— общее (равномерное) ожирение;
— местное ожирение — женский тип, при котором избыток
подкожного жира преимущественно в области бедер и ягодиц;
мужской тип, характеризующийся накоплением жира в области
живота.
• По происхождению выделяют следующие виды ожирения:
— первичное, которое является результатом нарушений нейро-
эндокринной регуляции жирового обмена и развивается при ряде
заболеваний ЦНС, сопровождающихся нейроэндокринными на-
рушениями — травма или опухоль головного мозга, энцефалит,
поражения гипофиза и других желез внутренней секреции;
— вторичное, причиной которого могут быть избыточная кало-
рийность пищи, пониженный уровень энергозатрат организма,
что зависит от физической активности и образа жизни, индиви-
дуальные особенности обмена веществ (в том числе липидов).
Алиментарное ожирение имеет наибольшее значение среди вто-
ричных мезенхимальных липидозов, связано с избыточным пита-
нием и малоподвижным образом жизни. При этом развивается
ожирение сердца с отложением жира под эпикардом и между
пучками мышечных волокон, особенно правых отделов сердца.
Сдавленные жировой тканью мышечные волокна атрофируются,
истончаются, функция миокарда снижается, иногда происходит
разрыв стенки правого желудочка сердца.
Истощение — патологическое снижение массы жировой ткани.
Индекс массы тела падает до 20 кг/м и ниже. При этом дефицит
жировой ткани может составлять 20—25 % от ее нормального ко-
личества. Если масса тела снижается на 50 % и более по сравне-
нию с нормой, то говорят о кахексии.
Причины истощения и кахексии:
— голодание;
32
— низкая калорийность пищи, не восполняющая энергозатрат
организма;
— злокачественные опухоли.
Морфология. При истощении и особенно при кахексии почти
полностью исчезает жир из жировых депо, при этом кожа смор-
щивается, подкожная клетчатка, большой и малый сальники,
брыжейка приобретают охряно-желтый цвет за счет концентра-
ции в них пигментов (красящих веществ) — липохромов^ Все орга-
ны резко уменьшаются в размерах, приобретают бурый цвет, не-
редко покрываются слизью.
Атеро — заболевание, в развитии которого большую роль игра-
ет нарушение обмена холестерина и его производных (см. главу
13).
УГЛЕВОДНЫЕ СТРОМАЛЬНО-СОСУДИСТЫЕ ДИСТРОФИИ
Углеводные стромально-сосудистые дистрофии связаны в ос-
новном с нарушением обмена глюко протеинов и проявляются
развитием в соединительной ткани, хрящах, в жировой клетчатке
густой слизеподобной массы. Это так называемая слизистая дис-
трофия, обусловленная нарушениями функций эндокринных же-
лез. Такая дистрофия развивается, например, при микседеме —
заболевании, связанном с недостаточностью функции щитовидной
железы. Ослизнение тканей может наблюдаться и при кахексии.
СМЕШАННЫЕ ДИСТРОФИИ
Смешанные дистрофии характеризуются нарушениями обмена
веществ, которые проявляются одновременно в клетках и во вне-
клеточном матриксе. Смешанные дистрофии являются следстви-
ем нарушения обмена сложных белков и минералов.
Сложные белки — соединения, состоящие из белка и связан-
ного с ним вещества небелковой природы. Выделяют следующие
сложные белки:
— хромопротеины — соединения, в которых белок связан с
красящими веществами — пигментами;
— нуклеопротеины — комплекс белка и нуклеиновых кислот;
— липопротеины — соединения белка и липидов;
— глюко протеины — соединения белка и углеводов.
Нарушения минерального обмена связаны с нарушениями мета-
болизма солей и их ионов.
СМЕШАННЫЕ БЕЛКОВЫЕ ДИСТРОФИИ
Смешанные белковые дистрофии характеризуются нарушения-
ми обмена сложных белков, главным образом нарушениями ме-
33
таболизма хромопротеинов, или эндогенных пигментов. Выделяют
три группы хромо протеинов:
• гемоглобиногенные пигменты;
• протеиногенные (тирозиновые) пигменты;
• липидогенные пигменты.
Патогенез нарушений обмена пигментов может заключаться в
изменении их количества
— увеличении, уменьшении или в полном отсутствии;
— распространенности (местные или общие);
— появлении аномальных пигментов, не встречающихся в норме.
Нарушения обмена гемоглобиногенных пигментов, связанных с
обменом гемоглобина. Физиологические функции этих пигментов
заключаются в транспорте и депонировании кислорода и железа,
в транспорте углекислого газа, электронов и др.
В организме постоянно происходит гемолиз (распад) эритро-
цитов, в результате чего их красящее вещество — гемоглобин —
распадается на белок — глобин, и протопорфирин железа — гем.
Железо либо сохраняется в геме, либо покидает его. Таким обра-
зом, уже в норме появляются две группы гемоглобиногенных
пигментов: железосодержащие и не содержащие железа.
Железо, вышедшее из гема, соединяется с цитоплазмой клеток
ретикулоэндотелиальной системы (РЭС) и макрофагов, образуя
четыре пигмента, два из которых возникают только в условиях па-
тологии:
• гемосидерин — образуется как в норме, так и в условиях па-
тологии;
• ферритин — образуется как в норме, так и в условиях пато-
логии;
• солянокислый гематин — образуется при желудочных кро-
вотечениях;
• малярийный пигмент (гемомеланин) — образуется при ма-
лярии.
Гем. лишенный железа, образует три пигмента:
билирубин;
стеркобилин;
уробилин.
Патогенез. В условиях патологии (при некоторых инфекциях,
интоксикациях, переливании несовместимой крови, анемиях, пе-
реохлаждении организма, при ожоговой болезни и др.) резко уси-
ливается внутрисосудистый гемолиз эритроцитов и в избытке об-
разуются гемоглобиногенные пигменты. Гемоглобин захватывает-
ся эндотелиальными клетками интимы сосудов, ретикулярными
клетками, гистиоцитами селезенки, печени, костного мозга, лим-
фатических узлов, макрофагами и эпителиальными клетками лег-
ких. почек. В этих клетках гем соединяется с мукополисахарида-
ми цитоплазмы и образуются гемосидерин и ферритин. Эти пиг-
менты придают органам ржаво-коричневую окраску, что характе-
ризует общий (распространенный) гемосидероз.
Если разрушение эритроцитов происходит после их выхода из
34
сосудов, например при кровоизлияниях в ткани, возникает мест-
ный гемосидероз. При этом гемосидерин захватывается в основном
макрофагами, в которых образуются гемосидерин и ферритин, и та-
кие макрофаги называются сидерофагами. Они выявляются в тка-
нях с помощью реакции Перлса — реакции образования берлинской
лазури (железосинеродистой соли трехвалентного железа), при ко-
торой все клетки и внеклеточные скопления гемосидерина, а также
других гемоглобиногенных пигментов, содержащих железо, окра-
шиваются в голубой цвет. В клинике большое значение имеет ме-
стный гемосидероз легких — так называемая бурая индурация легких.
В условиях патологии могут появляться еще два железосодер-
жащих гемоглобиногенных пигмента, не встречающихся в норме:
—солянокислый гематин;
— малярийный пигмент.
Солянокислый гематин имеет бурый цвет и образуется в желуд-
ке при соединении соляной кислоты желудочного сока с гемогло-
бином при желудочных кровотечениях, которые могут возникать
при язвенной болезни желудка, эрозивных гастритах, распаде
опухолей желудка. При этом возникает рвота "кофейной гущей"
из-за содержания в рвотных массах солянокислого гематина. Ма-
лярийный пигмент (гемомеланин) появляется в циркулирующей
крови при распаде эритроцитов, пораженных малярийным плаз-
модием. Гемомеланин захватывается клетками РЭС, в результате
чего ткани селезенки, печени, костного и головного мозга, мозго-
вых оболочек, лимфатических узлов приобретают пепельную ок-
раску. Развивается распространенный гемосидероз.
В физиологических условиях при распаде эритроцитов и потере
гемом железа в результате сложных биохимических реакций в пе-
чени образуется не содержащий железа пигмент билирубин, вхо-
дящий в состав желчи и придающий ей желтовато-зеленый цвет.
Попадая вместе с желчью в кишечник, под влиянием ферментов
кишечного сока билирубин превращается в стеркобилин и окра-
шивает каловые массы, а попадая вместе с кровью в почки и затем
в мочу, превращается в уробилин, обусловливающий ее окраску.
При нарушении образования билирубина в печени или при
нарушении его выделения из нее билирубин накапливается в
крови и окрашивает все ткани в желтый цвет. Развивается жел-
туха (см. главу 17).
НАРУШЕНИЯ ОБМЕНА ПРОТЕИНОГЕННЫХ ПИГМЕНТОВ
Основными функциями протеиногенных пигментов являются ре-
цепция света, защита от ультрафиолетового излучения, синтез и де-
понирование биологически активных веществ. Наибольшее значе-
ние в патологии имеют следующие протеиногенные пигменты: ме-
ланин, пигмент гранул энтерохромаффинных клеток, адренохром.
Меланин — пигмент коричнево-черного цвета, образующийся
при окислении тирозина в клетках-меланобластах при участии
фермента тирозиназы. Обмен меланина регулируется вегетатив-
35
нои нервной системой, гипо-
физом, надпочечниками, по-
ловыми железами. В норме
меланин содержится в радуж-
ке глаз, волосах, коже, пище-
варительном тракте, твердой
мозговой оболочке, обуслов-
ливая их окраску. При избы-
точном ультрафиолетовом
облучении меланин накапли-
вается в коже, придавая ей
коричневый оттенок, назы-
ваемый загаром.
Патогенез. Патологическое
усиление образования мела-
нина называется меланозом,
который может быть общим и
местным. Общий меланоз
развивается в коже при кахек-
Рис. 9. Меланодермия и пигмента- си!?’ тяжелых авитаминозах,
ция слизистой оболочки полости туберкулезном или опухоле-
рта при аддисоновой болезни. ,!ом поражении надпочечни-
ков. В последнем случае раз-
вивается бронзовая, или адди-
сонова, болезнь, при которой кожные покровы приобретают брон-
зовый оттенок (рис. 9). К местным меланозам относятся так назы-
ваемые родимые пятна, или невусы, на коже. Из невусных клеток
может развиться злокачественная опухоль — меланома.
Наследственное отсутствие меланина — альбинизм характери-
зуется отсутствием пигмента в коже, волосах, радужке глаз. Люди
и животные, страдающие альбинизмом, называются альбиносами —
у них очень белая кожа, белые волосы, а радужки глаз красные.
Локальное отсутствие меланина в виде разной формы очагов мо-
жет наблюдаться после воспалительных заболеваний кожи и но-
сит название лейкодерма.
Пигмент гранул энтерохромаффинных клеток, входящих в со-
став APUD-системы, или диффузной эндокринной системы орга-
низма, участвует в образовании биологически активных веществ —
серотонина, гастрина и др.
Адренохром — темно-коричневый пигмент клеток мозгового
вещества надпочечников, образуется при окислении адреналина.
Опухоли из этих клеток называются феохромоцитомами и имеют
своеобразную клиническую картину.
НАРУШЕНИЯ ОБМЕНА ЛИПИДОГЕННЫХ ПИГМЕНТОВ
Среди липидогенных пигментов основное значение имеет ли-
пофусцин и его разновидности — гемофусцин, цероид, липохро-
мы. Липофусцин представляет собой сложное соединение, в ко-
36
тором преобладают жиры; он образуется в клетках печени, серд-
ца, почек, скелетных мышц, симпатических ганглиев в виде мел-
ких золотисто-коричневых гранул. Внутриклеточные скопления
липофусцина не оказывают влияния на функции клеток: этот
пигмент накапливается в них при старении организма, при исто-
щающих заболеваниях — алиментарной и опухолевой кахексии,
гнойно-резорбтивной лихорадке, некоторых инфекциях. Поэтому
липофусцин иногда называют "пигментом старения", или "пиг-
ментом изнашивания". Избыточное накопление липофусцина в
клетках называется липофусцинозом.
НАРУШЕНИЯ ОБМЕНА НУКЛЕОПРОТЕИНОВ
Нуклеопротеины — вещества, состоящие из белка, соединен-
ного либо с нуклеиновыми кислотами, либо с пуриновыми осно-
ваниями. Наибольшее значение в патологии нуклеопротеинов
имеют дезоксирибонуклеиновая кислота (ДНК), рибонуклеино-
вая кислота (РНК) и пуриновые основания.
ДНК является основой хромосом и содержится в клеточном
ядре, а РНК — переносчик генетической информации и распола-
гается в ядрышках и цитоплазме клеток. При распаде нуклеопро-
теинов, помимо белка и ряда других соединений, образуются пу-
риновые основания, превращающиеся в мочевую кислоту, кото-
рая выделяется с мочой. При заболеваниях, сопровождающихся
интенсивным распадом ядер клеток (гнойные воспалительные
процессы, лейкозы и др.), возрастает содержание мочевой кисло-
ты в крови — гиперурикемня и как следствие в моче — гиперурику-
рия. На содержание в организме и метаболизм мочевой кислоты
оказывает влияние богатая пуринами пища — мясо, яйца, икра.
При нарушениях обмена нуклеопротеинов может развиться ряд
заболеваний, среди которых наибольшее значение имеет подагра.
Подагра, В развитии заболевания определенную роль играет
наследственная предрасположенность, а также употребление пи-
щи, содержащей большое количество животных белков.
Патогенез. Болезнь заключается в повышенном образовании
солей мочевой кислоты, что проявляется гиперурикемией и ги-
перурикурией. При этом периодически происходит выпадение
кристаллов мочекислого натрия в синовиальных оболочках и хря-
щах мелких суставов, в основном пальцев рук и ног, но могут по-
ражаться и голеностопные, и коленные суставы, сухожилия
мышц, хрящи ушных раковин.
Морфология. Ткани в области выпадения кристаллов некроти-
шруются, что сопровождается резкой болью. Вокруг очагов нек-
роза и скоплений кристаллов мочекислых солей развивается про-
дуктивное воспаление, завершающееся образованием рубцовой
соединительной ткани. Повторяющиеся атаки подагры приводят
к массивному развитию соединительной ткани и формированию
так называемых подагрических шишек (tophi unci). При этом
происходит деформация суставов. В почках кристаллы мочевой
37
кислоты накапливаются в канальцах и собирательных трубках, в
ответ на это развивается хроническое воспаление и атрофия по-
чечной ткани — подагрические почки.
НАРУШЕНИЯ МИНЕРАЛЬНОГО ОБМЕНА
Соли и их ионы принимают участие практически во всех видах
обмена веществ, поэтому без них невозможны течение физиоло-
гических процессов и поддержание гомеостаза. Они определяют
осмотическое давление крови и ее объем, регулируют распределе-
ние жидкости между клетками и внеклеточной средой, участвуют
в поддержании кислотно-основного состояния, обеспечивают
проницаемость мембран, образование энергии в клетках, работу
мышц, функционирование нервных клеток и многие другие про-
цессы. Расстройства минерального обмена возникают в результа-
те изменения поступления солей в организм, при нарушении их
выведения, а также при изменении распределения ионов между
клетками и внеклеточной средой. Поэтому расстройство мине-
рального обмена является либо причиной, либо важным звеном
патогенеза заболевания, либо осложнением или исходом многих
болезней. Наибольшее значение в жизнедеятельности организма
имеют соли натрия, калия и кальция.
НАРУШЕНИЕ ОБМЕНА НАТРИЯ
Натрий составляет 90 % всех внеклеточных катионов, его су-
точная потребность определяется в 10—12 г, поэтому натрий спе-
циально включают в пищевой рацион в виде поваренной соли.
Важнейшей функцией натрия является регулирование осмотиче-
ского давления плазмы крови. Он постоянно выводится с мочой,
потом и другими экскретами, что требует его непрерывного вос-
полнения. Нарушение обмена натрия проявляется либо увеличе-
нием его концентрации в крови (гипернатриемия), либо умень-
шением (гипонатриемия).
Гипернатриемия развивается в результате:
• избыточного поступления в организм хлорида натрия, на-
пример с соленой пищей;
• задержки выведения натрия, обычно при заболеваниях по-
чек или надпочечников;
• обезвоживания организма при неукротимой рвоте, поносах
(например, при холере) или в связи с избыточным выделе-
нием мочи (полиурии) при гломерулонефритах;
• ограниченного поступления в организм при отсутствии
питьевой воды;
• сгущения крови в силу различных причин.
Патологические проявления гипернатриемии могут заключаться
в повышении нервно-мышечной возбудимости и развитии судо-
рог вследствие повышения чувствительности сосудов к прессор-
38
ным веществам; в результате гипернатриемии может повышаться
артериальное давление; увеличение осмотического давления
плазмы крови, связанное с повышенным содержанием ионов на-
трия, приводит к поступлению воды из клеток в кровь, к увели-
чению объема циркулирующей крови и соответственно — к по-
вышению нагрузки на сердце.
Гипонатриемия возникает в результате:
• дефицита натрия в пище, например при бессолевой диете;
• повышенной потери натрия с мочой, потом или кишечным
соком в результате, например, недостаточного образования
альдостерона и уменьшения в связи с этим его реабсорбции
в канальцах нефрона, при сильном потоотделении, наруше-
ниях функции почек, при тяжелом поносе.
Патологические проявления. Для гипонатриемии характерны
снижение нервно-мышечной возбудимости и появление мышеч-
ной слабости, развитие тахикардии и гипотонии, диспепсические
расстройства. Снижение осмотического давления плазмы крови
приводит к усиленному поступлению воды из сосудов в ткани и
развитию отеков.
НАРУШЕНИЯ ОБМЕНА КАЛИЯ
Калий участвует в регуляции процессов возбуждения и тормо-
жения в нервной системе, в синтезе гликогена и белков, обмене
натрия, способствует диурезу, снижая чувствительность почечных
канальцев к антидиуретическому гормону; введение калия стиму-
лирует выведение из организма натрия и, следовательно, воды.
В норме человек потребляет в среднем 3 г калия в сутки. Око-
ло 90 % этого иона поступает в клетки, 9 % содержится в интер-
стициальной жидкости и около 0,4 % — в плазме крови. Регуля-
ция обмена калия, как и натрия, осуществляется минералокорти-
коидами, прежде всего альдостероном. Нарушения обмена калия
проявляются двумя состояниями: повышением его концентрации
в плазме крови — гиперкалиемия, или снижением содержания ка-
лия в крови — гипокалиемия.
Гиперкалиемия развивается при:
• избыточном поступлении в организм с пищей или лекарст-
венными препаратами (бромид калия, хлорид калия и др.);
• снижении выделения калия почками при почечной недос-
таточности;
• повышении выхода калия из клеток в кровь в результате
распада клеток, например при ожогах, травме, тяжелой ги-
поксии, гемолизе эритроцитов и др.
Патологические проявления. Гиперкалиемия приводит к вре-
менному повышению, а затем падению нервно-мышечной возбу-
димости, к нарушению чувствительности. Характерны снижение
артериального давления и частоты сердечных сокращений, боли в
области живота, обусловленные спастическим сокращением мышц
желудка, кишечника и желчного пузыря.
39
Гипокалиемия возникает в результате:
• уменьшения поступления калия с пищей, например при го-
лодании;
• повышенной потери калия при усиленном выведении его
почками в связи с опухолями коры надпочечников или при
передозировке кортикостероидов, при ожогах и др.;
• значительного разведения плазмы крови в связи с введени-
ем физиологического раствора или глюкозы.
Патологические проявления. При гипокалиемии нервно-мы-
шечная возбудимость снижается, что обусловливает мышечную
слабость и гиподинамию, снижение моторики желудочно-кишеч-
ного тракта, тонуса мочевого пузыря, часто возникают наруше-
ния ритма сердца.
НАРУШЕНИЯ ОБМЕНА КАЛЬЦИЯ
Кальций является необходимым компонентом многих метабо-
лических и физиологических процессов. Ионы кальция участвуют
в поддержании целостности мембран и в трансмембранном
транспорте, играют важную роль в образовании энергии, регули-
руют функции нейронов, нейро-мышечных синапсов, фермента-
тивные реакции; кальций является существенным фактором свер-
тывания крови. Кальций поступает в организм с пищей (0,5—1 г/
сут) и адсорбируется в кишечнике. Его баланс обеспечивается по-
ступлением в кровь из желудочно-кишечного тракта и выведени-
ем почками и кишечником. Количество кальция в организме
взрослого человека составляет примерно 1 кг, при этом 99 % его
депонируется в костях. Нормальная концентрация кальция в кро-
ви составляет 8,8—10,4 мг%, что является пределом его раствори-
мости. Обмен кальция и его содержание в плазме крови регули-
руются паратиреоидным гормоном (паратгормоном) паращито-
видных желез, кальцитонином, вырабатывающимся в щитовид-
ной железе, и витамином D (кальцитриолом). Паратгормон уси-
ливает всасывание кальция в кишечнике, выход ионов кальция
из костей и поступление их в кровь, повышает реабсорбцию
кальция в канальцах почек и активирует в кишечнике витамин D,
который в свою очередь способствует транспорту ионов кальция
из кишечника в кровь. Кальцитонин, напротив, тормозит выход
ионов кальция из костей и снижает его уровень в плазме крови.
Нарушения обмена кальция проявляются его увеличением в кро-
ви — гиперкальциемией или уменьшением — гипокальциемией.
Гиперкалыдиемия развивается в результате:
• избыточного поступления солей кальция в кровь, что может
наблюдаться, например, при его парентеральном введении
в составе лекарственных веществ, при гипервитаминозе D;
• усиленного выхода ионов кальция из костей в результате
гиперфункции паращитовидных желез или распада костей
при их поражении опухолями;
40
Рис. 10. Петрификат в легком при туберкулезе.
а — обызвествленные массы творожистого некроза; б — рубцовая капсула; в —
отложения угля в наружных слоях капсулы; г — легочные альвеолы.
• уменьшения выведения кальция почками при увеличении
содержания в плазме крови паратгормона.
Патологические проявления. Гиперкальциемия приводит к
снижению нервно-мышечной возбудимости, к параличам, дис-
пепсическим расстройствам, способствует образованию камней в
почках. Отложение солей кальция в клетках и межклеточном ве-
ществе называется кальцинозом, или обызвествлением, или извест-
ковой дистрофией. В патологии большое значение имеют такие
нарушения обмена кальция, связанные с гиперкальциемией, как
дистрофическое, метастатическое и метаболическое обызвествле-
ние. Эти дистрофии могут быть общими и местными.
Дистрофическое обызвествление (известковая дистрофия)
обычно связано с дистрофическими и некротическими измене-
ниями тканей. В этих условиях активируются ферменты фосфата-
зы, в результате чего высвобождаются фосфатные группы в клет-
ках или в межклеточном матриксе, которые связываются с каль-
цием. Поэтому дистрофическое обызвествление происходит в
очагах казеозного некроза — петрификаты, в тромбах — венные
камни, в тканях и оболочках погибшего плода — каменный плод, в
некоторых доброкачественных опухолях (рис. 10). Обызвествле-
ние створок клапанов сердца при ревматизме или отложение со-
лей кальция в бляшке внутренней оболочки (интимы) артерий
при атерое значительно ухудшает течение этих заболеваний. Уча-
стки дистрофического обызвествления выглядят как плотные бе-
41
a
Рис. 11. Метастатическое обызвествление миокарда. Инкрустированные
солями кальция мышечные волокна (а) среди неизмененного миокарда
(б).
лесоватые очаги, с трудом разрезаются ножом, вокруг них разрас-
тается соединительная ткань.
Метастатическое обызвествление наблюдается при гиперкаль-
циемии в результате поступления солей кальция из их депо в кос-
тях и переноса в различные органы и ткани. Такое нарушение об-
мена кальция может быть связано, например, с гипервитамино-
зом D, гиперфункцией паращитовидных желез при развитии в
них опухоли, при деструкции костей в связи с остеомиелитом
или злокачественными опухолями. При этом кальций выпадает
прежде всего в интерстиции слизистой оболочки желудка, в стро-
ме почек, легких, миокарда, в стенках вен и артерий (рис. 11).
Все эти ткани при функционировании ощелачиваются. Посколь-
ку соли кальция, хорошо растворимые в кислой среде, в щелоч-
ной среде не растворяются, они выпадают в ткани этих органов
из перенасыщенного раствора плазмы, который характерен для
гиперкальциемии. Этому могут способствовать заболевания по-
чек, при которых они теряют способность выводить фосфор, по-
ступающий в кровь, образуя с кальцием нерастворимое соедине-
ние. Гиперкальциемия возникает и при поражениях толстой
кишки и потере ею способности выводить кальций из организма.
Соли кальция, выпавшие в межклеточное вещество, вызывают
воспалительную реакцию с появлением гигантских клеток и раз-
42
растанием вокруг кальцинатов соединительной ткани. При этом
функции органов снижаются незначительно, а их внешний вид
не изменяется.
Метаболическое обызвествление (кальцифилаксия) — недоста-
точно изученная дистрофия, которую связывают с нестойкостью
буферных систем крови. Наблюдается она чаще у больных с хро-
нической почечной или печеночной недостаточностью. При этом
может повышаться чувствительность кровеносных сосудов к
кальцию. Происходит обызвествление средней оболочки артерий
кожи, подкожной клетчатки, что вызывает воспаление этих сосу-
дов. их тромбоз и некроз окружающей ткани. В коже появляются
очаги некроза, воспаления и изъязвления. Возможно также обыз-
вествление аорты.
Гипокальциемия развивается в результате:
• снижения уровня паратгормона в плазме крови, что тормо-
зит выход кальция из костей, стимулирует его выделение
почками и развивается при гипопаратиреозе;
• гиповитаминоза D, который приводит к снижению всасы-
вания кальция в кишечнике;
• гиперсекреции кальцитонина, который является антагони-
стом паратгормона;
• заболеваний кишечника, сопровождающихся снижением
всасывания кальция.
Патологические проявления. Гипокальциемия приводит к рез-
кому повышению нервно-мышечной возбудимости и развитию
судорог (тетания). Спастические сокращения могут распростра-
няться на межреберные мышцы и диафрагму, вызывая спазм го-
лосовой щели, бронхоспазм и удушение — гасфиксию. При не-
достатке витамина D в детском возрасте развивается рахит. Ги-
покальциемия может сопровождаться снижением свертываемости
крови и кровоточивостью тканей, способствовать заболеваниям
зубов из-за нарушения кальцификации дентина и ряду других па-
тологических процессов.
ОБРАЗОВАНИЕ КАМНЕЙ
Образование камней, или конкрементов, происходит на фоне
нарушений минерального и других видов обмена веществ. Они
образуются в полых органах или в выводных протоках. Наиболь-
шее значение в патологии имеют камни желчного пузыря, желч-
ных протоков и мочевыводящих путей.
Камни желчного пузыря и желчных протоков состоят из извес-
ти. холестерина и пигмента билирубина, имеют округлую или
граненную (фасетчатую) форму, составляют морфологическую
основу желчнокаменной болезни.
Камни мочевых путей (почек, мочеточников и мочевого пузы-
ря) состоят из солей мочевой кислоты (ураты), фосфора и каль-
ция (фосфаты), щавелевой кислоты и кальция (оксалаты) и др.,
43
имеют отростчатую форму в почках, округлую — в мочевом пузы-
ре, являются морфологической основой мочекаменной болезни.
Местные изменения (нарушение секреции, застой секрета,
воспаление) также имеют значение для образования камней. При
этом возникает какая-либо органическая основа для камнеобра-
зования в виде скоплений слизи, слущенного эпителия, на кото-
рую выпадают те или иные соли.
Значение камнеобразования в патологии велико. Так, при мо-
чекаменной болезни камни могут способствовать воспалению по-
чек (пиелонефрит) либо, закрывая мочеточник, препятствовать
оттоку мочи, что приводит к развитию гидронефроза и гибели
почки. Камни желчного пузыря и червеобразного отростка спо-
собствуют хроническому течению воспаления этих органов и мо-
гут вызвать перфорацию их стенки с развитием воспаления брю-
шины — перитонита. При обтурации камнем общего желчного
протока развивается подпеченочная желтуха.
НАРУШЕНИЯ ВОДНОГО ОБМЕНА. ОТЕК
Вода является самым распространенным веществом в живой
природе. Общее содержание ее в организме человека составляет
от 50 до 80 % от массы тела. Вода организма находится в разных
состояниях и структурных пространствах.
Внутриклеточная (или интрацеллюлярная) вода составляет в
среднем 31 % от массы тела. т. е. примерно 24 л, и находится в
двух основных состояниях: связанном с цитоплазмой и свободном.
Внеклеточная (или экстрацеллюлярная) жидкость составляет в
среднем 22 % от общей массы тела, т. е. примерно 15 л, и входит
в состав:
• плазмы крови, в которой вода составляет в среднем около
4 % массы тела, или 2—2,5 л;
• межклеточной (или интерстициальной) жидкости, которая
составляет в среднем 18 % от массы тела. т. е. примерно
12 л;
• "трансцеллюлярной" жидкости, вырабатываемой клетками.
Она выделяется в различные пространства организма, обра-
зуя:
— цереброспинальную (спинномозговую) жидкость;
— синовиальную жидкость, содержащуюся в полостях суставов;
— желудочный и кишечный сок;
— жидкость полостей капсул клубочков и канальцев почек
(первичная моча);
— жидкость серозных полостей (плевральной, перикарда,
брюшной и др.);
— влагу камер глаза.
Водный баланс представляет собой уравновешивание трех
процессов:
• поступления воды в организм с пищей и питьем;
44
• образование в процессе обмена веществ так называемой эн-
догенной воды;
• выделения воды из организма.
Нарушения водного баланса. Все разновидности нарушений
водного обмена называются дисгидриями (dys — нарушение и
греч. hydor — вода, жидкость). В зависимости от изменения об-
щего количества воды в организме дисгидрии разделяют на две
группы: гипо- и гипергидратация.
ГИПОГИДРАТАЦИЯ
Гипогидратация (обезвоживание, дегидратация) — уменьше-
ние количества жидкости в организме. Гипогидратация характе-
ризуется преобладанием потерь воды над ее поступлением в орга-
низм и обозначается как отрицательный водный баланс. Его при-
чинами могут быть:
• недостаточное поступление воды в организм, что наблюда-
ется при водном голодании, некоторых инфекционных и
психических болезнях, при нарушении проходимости пи-
щевода в результате его ожога или роста опухоли;
• повышенная потеря воды организмом, что наблюдается при
полиурии, неукротимой рвоте, хронических поносах, мас-
сивной кровопотере, продолжительном и значительном по-
тоотделении и др.;
• эксикоз, или высыхание, — крайняя степень гипогидратации.
ГИПЕРГИДРАТАЦИЯ
Гипергидратация — увеличение количества жидкости в орга-
низме, характеризуется преобладанием поступления воды в орга-
низм в сравнении с ее выведением и обозначается как положи-
тельный водный баланс. Его причинами могут быть:
• избыточное поступление жидкости в организм, например
при обильном питье воды, массивном введении растворов
внутривенно или в клизмах;
• повышенная задержка жидкости в организме, например
при гиперпродукции антидиуретического гормона при опу-
холи аденогипофиза или при почечной недостаточности,
при недостаточности кровообращения с развитием отеков;
• отек — одна из наиболее частых форм нарушения водного
баланса организма, характеризующаяся накоплением избытка
жидкости в межклеточных пространствах или полостях тела.
Отечная жидкость может иметь различный состав и конси-
стенцию и представлена в виде:
• транссудата — бедной белком (менее 2 %) жидкости;
• слизи, представляющей собой смесь из воды и коллоидов
межуточной ткани. В патологии характеризует слизистый
отек, или микседему, развивающуюся при гипофункции щи-
товидной железы и ее гормонов.
45
В зависимости от участка тела, в котором скапливается отеч-
ная жидкость, выделяют анасарку и водянку.
Анасарка — отек подкожной клетчатки.
Водянка — скопление транссудата в полостях тела:
• асцит — накопление транссудата в брюшной полости;
• гидроторакс — накопление транссудата в грудной полости;
• гидроперикард — избыток жидкости в перикарде;
• гидроцеле — накопление транссудата между листками се-
розной оболочки яичка;
• гидроцефалия — избыток жидкости в желудочках мозга.
В зависимости от распространенности отек может быть мест-
ным (например, в ткани или органе в области воспаления или ал-
лергической реакции) или общим — накопление избытка жидко-
сти во всех органах и тканях, например гипопротеинемический
отек при нефротическом синдроме.
В зависимости от скорости развития выделяют:
• молниеносный отек, который развивается в течение не-
скольких секунд после воздействия патогенного фактора,
например после укуса насекомых или ядовитых змей;
• острый отек — развивается в пределах 1-го часа после дей-
ствия причинного фактора, например отек легких при ост-
ром инфаркте миокарда;
• хронический отек — формируется в течение нескольких су-
ток или недель, например нефротический отек, отек при
голодании.
Основные патогенетические факторы отека
Гидродинамический фактор характеризуется увеличением эф-
фективного гидростатического давления, например при повыше-
нии венозного давления общего, что наблюдается при недоста-
точности сердца в связи со снижением его сократительной и на-
сосной функций, или местного, который является результатом
обтурации венозных сосудов тромбом или эмболом либо сдавле-
ния вен опухолью, рубцом, отечной тканью, или при увеличении
объема циркулирующей крови.
Лимфогенный фактор возникает при затруднении оттока лим-
фы от тканей вследствие либо механического препятствия, либо
ее избыточного образования.
Онкотический фактор, для которого характерно снижение он-
котического давления крови или увеличение его в межклеточной
жидкости.
Осмотический фактор связан либо с повышением осмоляль-
ности интерстициальной жидкости, либо со снижением осмо-
ляльности плазмы крови, либо с сочетанием того и другого, на-
пример, при парентеральном введении больших объемов рас-
творов.
Мелбраногенный фактор характеризуется существенным по-
вышением проницаемости стенок сосудов микроциркуляторного
46
русла для воды, мелко- и крупномолекулярных белков, что может
быть результатом гипоксии, значительного ацидоза и др.
Последствия отеков:
• механическое сдавление тканей и органов;
• нарушение обмена веществ между кровью и клетками, что
способствует развитию дистрофий:
• разрастание соединительной ткани с развитием а;
• нарушения кислотно-основного равновесия в связи с рас-
стройством обмена веществ.
АПОПТОЗ И НЕКРОЗ
Завершающим этапом повреждений тканей организма являет-
ся их гибель. Однако сами повреждения связаны не только с па-
тологическими процессами, возникающими в организме, но и со
старением функционирующих биологических структур. Вместе с
тем механизмы гибели клеток и тканей в условиях нормы и в ус-
ловиях патологии значительно отличаются друг от друга и имеют
разное морфологическое выражение.
АПОПТОЗ
Апоптоз — физиологическая гибель клеток в живом организме.
Общая характеристика. Все ткани организма имеют свой срок
жизни, после истечения которого и прекращения функции они
должны погибнуть и на их месте появляются новые, аналогичные
погибшим, клетки и ткани. Сроки жизни у разных живых струк-
тур различны. Они определены в их геноме, т. е. генетически за-
программированы. Поэтому апоптоз является генетически запро-
граммированной гибелью клеток. Это важнейший физиологиче-
ский процесс, позволяющий организму постоянно сохранять
функции своих структур на определенном уровне. Кроме того, в
процессе образования новых клеток и внеклеточных структур
возникают генетические ошибки, происходят мутации и появля-
ются клетки, отличающиеся от клеток организма. Они должны
быть немедленно уничтожены, и их гибель также осуществляется
с помощью апоптоза, который является и механизмом генетиче-
ского контроля синтеза веществ и клеток организма. Таким обра-
зом, апоптоз как физиологический процесс протекает непрерыв-
но на протяжении всей жизни человека, и биологический смысл
его заключается в поддержании постоянства клеток и тканей ор-
ганизма, т. е. тканевого гомеостаза. С помощью апоптоза проис-
ходит инволюция органов и тканей после завершения ими своих
физиологических функций, например атрофия вилочковой желе-
зы после окончания формирования иммунной системы, атрофия
половой системы женщин после завершения детородной функ-
ции, атрофия органов и тканей при старении человека и др.
Вместе с тем апоптоз может развиваться и в условиях патоло-
47
гии — в тех случаях, когда повреждающие факторы действуют на
гены, контролирующие включение программы апоптоза. Обычно
это происходит с помощью определенных веществ — цитокинов,
различных факторов роста, гормонов, активизирующихся при за-
болеваниях и функционирующих на молекулярном уровне. Эту
особенность апоптоза нередко пытаются использовать в клинике.
Например, в онкологии постоянно идет поиск возможностей сти-
мулировать апоптоз в злокачественных опухолях с тем, чтобы ак-
тивизировать распад опухолевых клеток, и это весьма перспек-
тивный путь онкотерапии.
Морфология апоптоза. Апоптоз развивается в отдельных клет-
ках, которые вначале теряют контакты с соседними клетками, за-
тем уменьшаются в размерах, в их ядрах конденсируется хрома-
тин. ядра становятся изрезанными, плотными и фрагментируют-
ся на отдельные глыбки. Одновременно происходит распад цито-
плазмы, в которой сохраняются в конденсированной форме внут-
риклеточные структуры. В результате клетка распадается на апоп-
тозные тельца, каждое из которых окружено мембраной. Апоп-
тозные тельца очень быстро поглощаются окружающими клетка-
ми, иногда макрофагами. Однако в ответ на апоптоз никогда не
развивается воспалительная реакция и на месте погибших клеток
воспроизводятся клетки той же ткани. Следует подчеркнуть, что
апоптозу подвергаются лишь клетки, но не ткани в целом.
НЕКРОЗ
Некроз — гибель клеток и тканей в результате патологических
воздействий.
Причины некроза разнообразны, однако их можно объединить
в пять групп:
1) травлитический некроз, который является результатом пря-
мого действия на ткань физических или химических факторов
(механических, температурных, радиационных, кислот, щелочей
и др.);
2) токсический некроз развивается при действии на ткани ток-
сических факторов бактериальной или иной природы;
3) трофоневротический некроз, который связан с нарушениями
иннервации тканей при заболеваниях центральной или перифе-
рической нервной системы;
4) аллергический некроз — следствие иммунных реакций не-
медленной или замедленной гиперчувствительности;
5) сосудистый некроз, обусловленный прекращением циркуля-
ции крови в артериях, реже — в венах.
По консистенции мертвых масс некроз может быть коагуляци-
онным, казеозным и колликвационным.
Коагуляционный (плотный) некроз возникает при коагуляции
распавшегося белка, обычно в мышечных тканях и в большинст-
ве внутренних органов.
Разновидностью коагуляционного некроза является казеозный
48
(творожистый) некроз, массы которого имеют замазкообразную
консистенцию; развивается при некоторых видах воспаления.
Колликвационный некроз развивается в тканях, богатых жидко-
стью, например в головном мозге.
По механизму действия фактора, вызвавшего некроз, выделяют:
• прямой некроз, который возникает при непосредственном
действии на ткань причины, вызывающей ее гибель, —
травма, токсины, высокая или низкая температура и т. п.;
• непрямой некроз, когда причина гибели ткани связана с на-
рушениями функций сосудов, нервов или с аллергическими
реакциями.
Некрозу предшествует период умирания, он никогда не возни-
кает мгновенно. Период умирания может быть длительным или
быстрым. В этот период в клетках и во внеклеточном матриксе
развиваются изменения, представляющие собой тот или иной вид
дистрофии, чаще белковый. Эти изменения называются некробио-
зом, или парабиозом. Функции клеток и органов при этом ослабе-
вают и прекращаются, но на начальных этапах процесса они мо-
гут восстановиться, если ликвидирована причина, вызвавшая
некробиоз. Если же причина продолжает действовать, дистрофия
становится необратимой, некробиоз переходит в некроз и какие-
либо функции прекращаются. Некротизированные ткани под
действием гидролитических ферментов подвергаются разложе-
нию — аутолизу. В области очага некроза развивается воспаление
как ответная реакция организма на гибель его части.
Морфология некроза зависит от его причины, но общим явля-
ется изменение цвета некротизированной ткани и ее консистен-
ции. Цвет некротических масс зависит от наличия примесей кро-
ви и различных пигментов. Мертвая ткань бывает белой или жел-
товатой, нередко окружена красно-бурым венчиком. При гнило-
стном расплавлении мертвая ткань издает характерный дурной
запах. Микроскопические признаки некроза складываются из не-
обратимых изменений ядер и цитоплазмы клеток. В период некро-
биоза клетки теряют воду, поэтому при некрозе ядра сморщива-
ются и уплотняются — развивается кариопикноз. Затем нуклеино-
вые кислоты в виде отдельных глыбок выходят из ядра в цито-
плазму клетки — происходит распад ядра — кариорексис. Нако-
нец, ядерное вещество растворяется — наступает кариолизис. Ис-
чезновение клеточных ядер — один из основных признаков нек-
роза. Та же динамика гибели наблюдается в цитоплазме, в кото-
рой развиваются плазморексис и плазмолиз. Наконец, растворяется
вся клетка — происходит цитолиз.
При некрозе интерстициальной и сосудистой тканей экстра-
целлюлярный матрикс набухает и расплавляется, волокнистые
структуры подвергаются фибриноидному некрозу и уплотняются.
Образовавшиеся некротические массы носят название некротиче-
ский детрит. Вокруг очага некроза, отграничивая его от живых
тканей, развивается демаркационная линия, представляющая собой
зону воспаления. Эта линия имеет большое значение в хирурги-
49
ческой практике, так как указывает на возможные пределы иссе-
чения погибших тканей или уровень ампутации конечности.
Исходы некроза. Благоприятный, при котором происхо-
дит ферментативное расплавление некротизированных тканей,
после чего они подвергаются организации, т. е. замещению де-
фекта соединительной тканью, обычно с образованием рубца,
или инкапсуляции, т. е. отграничению некротизированного уча-
стка соединительной тканью. При этом нередко некротизирован-
ные массы подвергаются петрификации. На месте колликвацион-
ного некроза образуется полость — киста.
Неблагоприятный, когда некроз ткани или органа закан-
чивается смертью больного, например инфаркт миокарда или нек-
роз поджелудочной железы. Кроме того, некротизированные ткани
могут подвергаться гнойному расплавлению, при котором токси-
чные продукты некроза и аутолиза всасываются в кровь, развивает-
ся интоксикация, которая также может привести к смерти.
Клинико-морфологические формы некроза. В зависимости от
локализации и особенностей некроза выделяют его следующие
клинико-морфологические формы.
Гангрена — некроз тканей, соприкасающихся с внешней сре-
дой. При этом железо гемоглобина, находящегося в некротизиро-
ванных тканях, соединяется с сероводородом воздуха и образует-
ся сульфид железа, придающий некротизированным тканям чер-
ный цвет. Гангрена развивается в коже, конечностях, кишечнике,
легких, влагалище, матке и т. д. Имеется несколько разновидно-
стей гангрены (рис. 12):
• сухая гангрена развивается в тканях с малым содержанием
жидкости, при этом ткани могут подвергаться мумифика-
ции. Она характерна для конечностей, возникает на разных
участках тела при их отморожении, ожогах, при тяжелых
инфекциях;
• влажная гангрена обычно развивается в тканях, богатых жид-
костью, поэтому встречается в легких, матке, кишечнике. У
ослабленных детей, страдающих корью или скарлатиной,
иногда развивается влажная гангрена щеки — нома;
• анаэробная, или газовая, гангрена возникает при тяжелых,
обычно массивных ранениях или травмах конечностей при
попадании в рану бактерий — анаэробов. В некротизиро-
ванных мышцах развивается коагуляционный некроз, они
становятся грязно-серыми, при надавливании из них выде-
ляются пузырьки газа.
Пролежень имеет трофоневротическое происхождение, возни-
кает на участках кожи, подкожной клетчатки или слизистых обо-
лочек. подвергающихся давлению у ослабленных больных, стра-
дающих онкологическими, сердечно-сосудистыми и некоторыми
инфекционными заболеваниями. Пролежни могут возникать в
области крестца, ягодиц, пяточных костей, а также в трахее или
гортани от давления трахеостомической трубки после операции
трахеостомии.
50
Рис. 12. Гангрена. Влажная гангрена кожи бедра (а) и стопы (б); сухая
гангрена стопы (в), предплечья и кисти (г).
Секвестр — участок омертвевшей ткани, свободно распола-
гающийся среди живых тканей, обычно сопровождающийся
гнойным воспалением. Особенно часто секвестром является нек-
ротизированный фрагмент кости при остеомиелите.
51
Рис. 13. Инфаркт.
а — белые (ишемические) инфаркты селезенки; б — красные (геморрагические)
инфаркты легкого; в — микроскопическая картина геморрагического инфаркта
легкого; г — ишемические инфаркты почки; д — микроскопическая картина ише-
мического инфаркта почки. Участки некроза тканей показаны стрелками.
Инфаркт — некроз ткани внутренних органов, развивающий-
ся в результате острого нарушения кровообращения в них при
тромбозе, эмболии, длительном спазме артерий. Наиболее ярки-
ми примерами этого вида некроза являются инфаркты миокарда,
52
головного мозга, легких, почек, селезенки (рис. 13). Инфаркты
различают по форме и цвету, что зависит от особенностей органа
и архитектоники его сосудистой системы:
• по форме
— клиновидная;
— неправильная.
• по цвету
— белый;
— красный;
— белый с геморрагическим венчиком.
Сравнительная характеристика апоптоза и некроза
Отличия апоптоза от некроза связаны с различиями в их рас-
пространенности, генетических, биохимических, морфологиче-
ских и клинических проявлениях:
апоптоз — физиологический вид смерти, некроз возника-
ет в условиях патологии;
апоптоз генетически запрограммирован, некроз развива-
ется под воздействием различных повреждающих причин и не
связан с геномом клетки;
апоптоз распространяется только на отдельные клетки,
некроз развивается на территории ткани и даже целого ор-
гана;
апоптоз не сопровождается дистрофическими изменениями
клеток, некрозу предшествует дистрофия, имеющая характер
некробиоза;
апоптоз не сопровождается воспалением, вокруг некро-
за обязательно развивается воспалительная реакция;
апоптоз заканчивается фагоцитозом апоптозных телец со-
седними клетками, некроз заканчивается аутолизом погибшей
ткани;
после апоптоза восстанавливаются клетки, аналогичные
погибшим, на месте некроза обычно разрастается рубцовая со-
единительная ткань;
апоптоз не сопровождается активацией внутриклеточных
гидролитических ферментов, некроз развивается с помощью
гидролаз;
апоптоз не имеет клинических проявлений, некроз со-
провождается выраженной клинической симптоматикой.
Апоптоз и некроз — два разных варианта гибели клеток и тка-
ней в живом организме, хотя некоторые патогенные факторы,
способные оказывать воздействие на генетический код, могут вы-
зывать апоптоз. Однако при этом апоптоз все-таки остается фи-
зиологическим механизмом смерти, но активизирующимся в ус-
ловиях определенной патологии.
Все описанные изменения — дистрофии, апоптоз и некроз —
носят характер типовых (или стереотипных) реакций, которыми
организм отвечает на различные воздействия, и те или иные их
сочетания возникают при любых болезнях, что необходимо учи-
тывать при назначении лечения.
53
Глава 2
НАРУШЕНИЯ КИСЛОТНО-ЩЕЛОЧНОГО
РАВНОВЕСИЯ
Кислотно-щелочное равновесие (КЩР) — определенное соот-
ношение активных масс водородных и гидроксильных ионов.
Концентрация ионов водорода [Н+] в клетках и биологических
жидкостях является одним из важных факторов обеспечения го-
меостаза, так как величина [Н+] во внеклеточной жидкости суще-
ственно влияет на многие жизненно важные свойства:
• активность ферментов;
• физико-химическое и структурное состояние мембран;
• способность гемоглобина связывать кислород;
• чувствительность рецепторов к биологически активным ве-
ществам;
• возбудимость и проводимость нервных структур и ряд дру-
гих.
Отклонение ионов водорода от оптимального диапазона обу-
словливает нарушения метаболизма и функций клеток тканей и ор-
ганов (вплоть до их гибели). Сдвиг показателя pH в диапазоне
±0,1 обусловливает расстройства дыхания и кровообращения; в
диапазоне ±0,3 — потерю сознания, нарушение гемодинамики и
вентиляции легких; в диапазоне ±0,4 и более — чреват гибелью
организма.
Концентрация ионов водорода в биологических жидкостях оп-
ределяет их КЩР.
pH жидких сред организма зависит от содержания в них орга-
нических и неорганических кислот и оснований (щелочей). Ус-
ловно за норму принята величина pH 7.39.
Кислота — вещество, которое в растворе является донором
протонов.
Щелочь (основание) — вещество, являющееся в растворе ак-
цептором протонов.
ПОКАЗАТЕЛИ КИСЛОТНО-ЩЕЛОЧНОГО РАВНОВЕСИЯ
Оценка КЩР и его изменений проводится с учетом нормаль-
ного диапазона его основных показателей, которые исследуют
именно в плазме крови (табл. 2).
МЕХАНИЗМЫ УСТРАНЕНИЯ СДВИГОВ КЩР
В эволюции сформировались системные, хорошо интегриро-
ванные механизмы регуляции КЩР в норме и устранения сдви-
гов его при развитии патологии. В норме в организме образуются
почти в 20 раз больше кислых продуктов, чем основных. В связи
54
Таблица 2. Показатели кислотно-щелочного равновесия (сводные дан-
ные)
№ п/п Показатели Значения в системе СИ Значения в обычно исполь- зуемых единицах
1 2 Основн pH — артериальная кровь — венозная кровь — капиллярная кровь рсо2а ые 7,34-7,43 7,35-7,45 4,3-6,0 кПа 33—46 мм
3 4 5 1 Стандартный бикарбонат плазмы 22—26 ммоль/л крови (SB — Standart Bicarbonate) Буферные основания капилляр- 44—53 ммоль/л ной крови (ВВ — Buffer Base) Избыток основания капиллярной -3,4 + 2,5 крови (BE — Base Excess) ммоль/л Дополнительные Кетоновые тела крови (КТ) рг. ст. 0,5-2,5 мг%
2 3 I 4 1 _1 Молочная кислота крови (МК) Титруемая кислотность суточной мочи Аммиак суточной мочи (NH+~) 20—40 ммоль/л 10—107 ммоль/л (20—50 ммоль/л) 6,16 мг%
с этим в нем преобладают системы, обеспечивающие нейтрализа-
цию, выведение и секрецию избытка соединений с кислыми
свойствами. К этим системам относятся химические буферные
системы и физиологические механизмы.
Химические буферные системы представлены в основном би-
карбонатным, фосфатным, белковым и гемоглобиновым буфера-
ми. Эти буферные системы начинают действовать сразу же при
увеличении или снижении [Н+]. Буферы крови, например, спо-
собны устранить умеренные сдвиги КЩР в течение 10—40 с.
Физиологические механизмы. Наряду с мощными и быстродей-
ствующими химическими системами в организме функциониру-
ют органные механизмы компенсации и устранения сдвигов
КЩР. Для их реализации и достижения необходимого эффекта
требуется больше времени — от нескольких минут до нескольких
часов. К наиболее эффективным механизмам регуляции КЩР от-
носят процессы, протекающие в легких, почках, печени и желу-
дочно-кишечном тракте.
ТИПОВЫЕ ФОРМЫ НАРУШЕНИЙ КЩР
Типовые формы нарушений КЩР дифференцируют по не-
скольким критериям.
55
По направленности изменения pH выделяют две типовые фор-
мы нарушений КЩР: ацидоз и алкалоз.
Ацидоз характеризуется избытком в организме кислот. В кро-
ви наблюдается повышение [Н+] и уменьшение pH ниже нормы.
Алкалоз характеризуется избытком в организме щелочей.
Причины расстройств КЩР. Эндогенные (внутренние) причины
изменений КЩР являются наиболее частыми и значимыми в
клинической практике. Как к ацидозам, так и к алкалозам ведут
расстройства функций сердечно-сосудистой, дыхательной и пи-
щеварительной систем, почек, печени, системы крови, наруше-
ния обмена веществ в органах и тканях.
Экзогенные (внешние) причины нарушений КЩР заключаются,
как правило, в избыточном поступлении в организм веществ ки-
слого или щелочного характера. Чаще всего это:
• лекарственные препараты, которые образуют в процессе их
распада ионы водорода (например, салицилаты; растворы
для искусственного питания, содержащие кислые вещества:
NPI4CI, аргинин — НС1, лизин — НО и др.);
• токсичные вещества, например метанол, этиленгликоль, со-
ляная кислота;
• продукты питания. Так, использование продуктов, содержа-
щих соляную кислоту, сопровождается поступлением в меж-
клеточную жидкость и кровь НС1, диссоциирующей на ионы
Н+ и СП. Потребление в большом количестве щелочных ми-
неральных вод, молока может обусловить развитие алкалоза.
По степени компенсированности изменения КЩР выделяют
компенсированные и некомпенсированными нарушения КЩР.
Компенсированными сдвигали КЩР являются такие, при кото-
рых pH крови не отклоняется за пределы диапазона нормы: 7,35—
7,45. При этом за "среднюю" ("нейтральную") величину условно
принимают 7,39. В связи с этим отклонения pH в диапазонах:
• 7,38—7,35 обозначают как компенсированный ацидоз,
• 7,40—7,45 — как компенсированный алкалоз.
Некомпенсированными нарушениями КЩР называют такие,
при которых pH крови выходит за диапазон нормы:
• при pH 7,34 и ниже говорят о некомпенсированном аци-
дозе;
• при pH 7.46 и выше — о некомпенсированном алкалозе.
По причинам и механизмам развития нарушения КЩР диффе-
ренцируют на газовые, негазовые и смешанные, или комбиниро-
ванные, нарушения КЩР.
Газовые, или респираторные, расстройства КЩР характеризу-
ются первичным изменением содержания в организме С02 и как
следствие — изменением концентрации угольной кислоты в соот-
ношении [НС03]/[Н2С03].
При газовом ацидозе знаменатель соотношения (т. е. концен-
трация угольной кислоты) увеличивается, при газовом алкалозе —
уменьшается.
Негазовые, или нереспираторные, нарушения КЩР характери-
56
зуются первичным изменением содержания гидрокарбоната в со-
отношении [HC03J/[H2C03J.
При негазовых ацидозах числитель соотношения (т. е. концен-
трация гидрокарбонатов) уменьшается, а при негазовых алкало-
зах — увеличивается.
Причины нарушений КЩР:
• расстройства обмена веществ;
• нарушения экскреции кислых и основных соединений поч-
ками;
• потеря кишечного сока;
• потеря желудочного сока;
• введение в организм экзогенных кислот или оснований.
Вцпы негазовых нарушений КЩР обусловливают развитие
следующих расстройств:
Метаболические расстройства КЩР развиваются в результате
нарушения обмена веществ, ведущего к накоплению в организме
избытка либо кислых либо основных валентностей.
Выделительные формы нарушений КЩР являются следствием
избыточной потери или задержки в организме кислых веществ
или оснований. Это обусловлено нарушениями функции почек
или желудочно-кишечного тракта.
Экзогенные расстройства КЩР развиваются в результате попа-
дания в организм веществ с кислыми или щелочными свойства-
ми, например при избыточном употреблении продуктов питания
или жидкостей, содержащих лимонную, яблочную, салициловую
и другие кислоты или щелочи; при применении лекарств, вклю-
чающих кислые или основные вещества, и т. п.
Глава 3
ГИПОКСИЯ
Одним из обязательных условий жизни организма является
непрерывное образование и потребление им энергии. Она расхо-
дуется на обеспечение метаболизма, на сохранение и обновление
структурных элементов органов и тканей, а также на осуществле-
ние их функции. Недостаток энергии в организме приводит к су-
щественным нарушениям обмена веществ, морфологическим из-
менениям и нарушениям функций, а нередко — к гибели органа
и даже организма. В основе дефицита энергии лежит гипоксия.
Гипоксия — типовой патологический процесс, характеризую-
щийся как правило снижением содержания кислорода в клетках
и тканях. Развивается в результате недостаточности биологиче-
ского окисления и является основой нарушений энергетического
обеспечения функций и синтетических процессов организма.
57
типы гипоксии
В зависимости от причин и особенностей механизмов развития
выделяют следующие типы:
1. Экзогенный:
— гипобарический;
— нормобарический.
2. Респираторный (дыхательный).
3. Циркуляторный (сердечно-сосудистый).
4. Гемический (кровяной).
5. Тканевый (первично-тканевый).
6. Перегрузочный (гипоксия нагрузки).
7. Субстратный.
8. Смешанный.
В зависимости от распространенности в организме гипоксия
может быть общей или местной (при ишемии, стазе или веноз-
ной гиперемии отдельных органов и тканей).
В зависимости от тяжести течения выделяют легкую, умеренную,
тяжелую и критическую гипоксию, чреватую гибелью организма.
В зависимости от скорости возникновения и длительности тече-
ния гипоксия может быть:
• молниеносной — возникает в течение нескольких десятков
секунд и нередко завершается смертью;
• острой — возникает в течение нескольких минут и может
длиться несколько суток;
• хронической — возникает медленно, длится несколько не-
дель, месяцев, лет.
ХАРАКТЕРИСТИКА ОТДЕЛЬНЫХ ТИПОВ ГИПОКСИИ
Экзогенный тип
Причина: уменьшение парциального давления кислорода Р02 во
вдыхаемом воздухе, что наблюдается при высоком подъеме в го-
ры ("горная" болезнь) или при разгерметизации летательных ап-
паратов ("высотная" болезнь), а также при нахождении людей в
замкнутых помещениях малого объема, при работах в шахтах, ко-
лодцах. в подводных лодках.
Основные патогенные факторы:
• гипоксемия (снижение содержания кислорода в крови);
• гипокапния (снижение содержания С02), которая развивается
в результате увеличения частоты и глубины дыханий и приво-
дит к снижению возбудимости дыхательного и сердечно-сосу-
дистого центров головного мозга, что усугубляет гипоксию.
Респираторный (дыхательный) тип
Причина: недостаточность газообмена в легких при дыхании,
что может быть обусловлено снижением альвеолярной вентиля-
58
ции или затруднением диффузии кислорода в легких и может на-
блюдаться при эмфиземе легких, пневмое.
Основные патогенные факторы:
• артериальная гипоксемия, например при пневмое, гиперто-
нии малого круга кровообращения и др.;
• гиперкапния, т. е. увеличение содержания С02;
• гипоксемия и гиперкапния характерны и для асфиксии —
удушения (прекращения дыхания).
Циркуляторный (сердечно-сосудистый) тип
Причина: нарушение кровообращения, приводящее к недоста-
точному кровоснабжению органов и тканей, что наблюдается при
массивной кровопотере, обезвоживании организма, нарушениях
функции сердца и сосудов, аллергических реакциях, нарушениях
электролитного баланса и др.
Основной патогенетический фактор — гипоксемия венозной
крови, так как в связи с ее медленным протеканием в капиллярах
происходит интенсивное поглощение кислорода, сочетающееся с
увеличением артериовенозной разницы по кислороду.
Гемический (кровяной) тип
Причина: снижение эффективной кислородной емкости крови.
Наблюдается при анемиях, нарушении способности гемоглобина
связывать, транспортировать и отдавать кислород в тканях (на-
пример, при отравлении угарным газом или при гипербарической
оксигенации).
Основной патогенетический фактор — снижение объемного
содержания кислорода в артериальной крови, а также падение
напряжения и содержания кислорода в венозной крови.
Тканевый тип
Причины:
• нарушение способности клеток поглощать кислород;
• уменьшение эффективности биологического окисления в
результате разобщения окисления и фосфорилирования.
Развивается при угнетении ферментов биологического окисле-
ния, например при отравлении цианидами, воздействии ионизи-
рующего излучения и др.
Основное патогенетическое звено — недостаточность биологи-
ческого окисления и как следствие дефицит энергии в клетках.
При этом отмечаются нормальное содержание и напряжение ки-
слорода в артериальной крови, повышение их в венозной крови,
снижение артериовенозной разницы по кислороду.
59
Перегрузочный тип
Причина: чрезмерная или длительная гиперфункция какого-
либо органа или ткани. Чаще это наблюдается при тяжелой фи-
зической работе.
Основные патогенетические звенья:
• значительная венозная гипоксемия;
• гиперкапния.
Субстратный тип
Причина: первичный дефицит субстратов окисления, как пра-
вило. глюкозы. Так. прекращение поступления глюкозы в голов-
ной мозг уже через 5—8 мин ведет к дистрофическим изменени-
ям и гибели нейронов.
Основной патогенетический фактор — дефицит энергии в
форме АТФ и недостаточное энергоснабжение клеток.
Смешанный тип
Причина: действие факторов, обусловливающих включение
различных типов гипоксии. По существу любая тяжелая гипок-
сия, особенно длительно текущая, является смешанной.
СТРУКТУРНО-ФУНКЦИОНАЛЬНЫЕ РАССТРОЙСТВА
ПРИ ГИПОКСИИ
Нарушения обмена веществ и энергии выявляются уже на на-
чальном этапе гипоксии и характеризуются:
1. Снижением эффективности тканевого дыхания и как следст-
вие — уменьшением образования и содержания в клетках энер-
гии в форме АТФ и креатинфосфата.
2. Активацией гликолиза и снижением в тканях содержания
гликогена. В ответ на это из жировых депо организма мобилизу-
ются липиды — другой источник образования энергии. В крови
развивается гиперлипидемия, а во внутренних органах — жировая
дистрофия.
3. Увеличением уровня молочной и пировиноградной кислот в
тканях и крови, что приводит к метаболическому ацидозу. Это
тормозит интенсивность реакций гликолиза, окислительных и
энергозависимых процессов в клетках, в том числе ресинтеза гли-
когена из молочной кислоты, что еще более угнетает гликолиз и
способствует нарастанию ацидоза, т. е. гипоксия развивается по
принципу "порочного круга".
4. Активацией процессов липолиза и появлением жировой дис-
трофии органов и тканей.
60
5. Дисбалансом электролитов — обычно увеличением в интер-
стициальной жидкости и крови ионов калия, в клетках — натрия
и кальция.
6. Расстройством функции нервной системы, что проявляется:
• нарушением процессов мышления;
• психомоторным возбуждением, немотивированным поведе-
нием;
• нарушением и потерей сознания, что обусловлено высокой
чувствительностью нейронов к дефициту кислорода и энер-
гии. При тяжелой гипоксии уже через 5—7 мин выявляются
признаки необратимой дистрофии и деструкции нейронов.
7. Нарушениями кровообращения и кровоснабжения тканей и
органов, что выражается:
• снижением сократительной функции сердца и уменьшени-
ем сердечного выброса крови;
• недостаточным кровоснабжением тканей и органов, что
усугубляет степень гипоксии в них;
• нарушением ритма сердца, вплоть до фибрилляции миокар-
да предсердий и желудочков;
• прогрессирующим снижением артериального давления
вплоть до коллапса и расстройств микроциркуляции.
8. Расстройства внешнего дыхания характеризуются увеличени-
ем объема дыхания на начальной стадии гипоксии и нарушения-
ми частоты, ритма и амплитуды дыхательных движений в терми-
нальном периоде. При нарастании длительности и тяжести ги-
поксии период дискоординированного дыхания сменяется прехо-
дящей остановкой его. последующим развитием периодического
дыхания (Биота, Куссмауля, Чейна—Стокса), а затем его прекра-
щением. Это является результатом нарушения функций нейронов
дыхательного центра.
МОРФОЛОГИЯ гипоксии
Гипоксия является важнейшим звеном очень многих патоло-
гических процессов и болезней, а развиваясь в финале любых за-
болеваний, она накладывает свой отпечаток на картину болезни.
Однако течение гипоксии может быть различным, и поэтому как
острая, так и хроническая гипоксия имеют свои морфологиче-
ские особенности.
Острая гипоксия, которая характеризуется быстрым наруше-
ниями в тканях окислительно-восстановительных процессов, на-
растанием гликолиза, закислением цитоплазмы клеток и внекле-
точного матрикса, приводит к повышению проницаемости мем-
бран лизосом, выходу гидролаз, разрушающих внутриклеточные
структуры. Кроме того, гипоксия активирует перекисное окисле-
ние липидов, появляются свободнорадикальные перекисные со-
единения, которые разрушают мембраны клеток. В физиологиче-
ских условиях в процессе обмена веществ постоянно возникает
61
легкая степень гипоксии клеток, стромы, стенок капилляров и
артериол. Это является сигналом к повышению проницаемости
стенок сосудов и поступлению в клетки продуктов метаболизма и
кислорода. Поэтому острая гипоксия, возникающая в условиях
патологии, всегда характеризуется повышением проницаемости
стенок артериол, венул и капилляров, что сопровождается плаз-
моррагией и развитием периваскулярных отеков. Резко выражен-
ная и относительно длительная гипоксия приводит к развитию
фибриноидного некроза стенок сосудов. В таких сосудах крово-
ток прекращается, что усиливает ишемию стенки и происходит
диапедез эритроцитов с развитием периваскулярных кровоизлия-
ний. Поэтому, например, при острой сердечной недостаточности,
которая характеризуется быстрым развитием гипоксии, плазма
крови из легочных капилляров поступает в альвеолы и возникает
острый отек легких. Острая гипоксия мозга приводит к перива-
скулярному отеку и набуханию ткани мозга с вклинением его
стволовой части в большое затылочное отверстие и развитием ко-
мы, приводящей к смерти.
Хроническая гипоксия сопровождается долговременной пере-
стройкой обмена веществ, включением комплекса компенсатор-
ных и приспособительных реакций, например гиперплазией кост-
ного мозга для увеличения образования эритроцитов. В паренхи-
матозных органах развивается и прогрессирует жировая дистро-
фия и атрофия. Кроме того, гипоксия стимулирует в организме
фибробластическую реакцию, активизируются фибробласты, в
результате чего параллельно с атрофией функциональной ткани
нарастают склеротические изменения органов. На определенном
этапе развития заболевания изменения, обусловленные гипокси-
ей, способствуют снижению функции органов и тканей с разви-
тием их декомпенсации.
АДАПТИВНЫЕ РЕАКЦИИ ПРИ ГИПОКСИИ
При гипоксии в организме активируются приспособительные
и компенсаторные реакции, направленные на ее предотвращение,
устранение или снижение степени выраженности. Эти реакции
включаются уже на начальном этапе гипоксии — их обозначают
как экстренные, или срочные, в последующем (при длительной
гипоксии) они сменяются более сложными приспособительными
процессами — долговременными.
Механизмы срочной адаптации активируются сразу при возник-
новении гипоксии в связи с недостаточностью энергетического
обеспечения клеток. К числу основных механизмов относятся
системы транспорта кислорода и субстратов обмена веществ, а
также тканевого метаболизма.
Дыхательная система реагирует увеличением альвеолярной
вентиляции за счет углубления, учащения дыхания и мобилизации
резервных альвеол. Одновременно усиливается легочный кровоток.
62
Сердечно-сосудистая система. Активация ее функции в виде
увеличения сердечного выброса крови и изменения тонуса сосу-
дов обеспечивает возрастание объема циркулирующей крови (за
счет опорожнения кровяных депо), венозного возврата, а также
перераспределением кровотока между различными органами. Все
это направлено на преимущественное кровоснабжение мозга,
сердца и печени. Этот феномен обозначают как "централизация"
кровотока.
Система крови. В ней происходят изменения свойств гемогло-
бина. что обеспечивает насыщение крови кислородом в легких
даже при значительном его дефиците и более полное отщепление
кислорода в тканях.
Адаптивные реакции на уровне тканей характеризуются ослаб-
лением функции органов, обмена веществ и пластических про-
цессов в них, увеличением сопряженности окисления и фосфори-
лирования, усилением анаэробного синтеза АТФ за счет актива-
ции гликолиза. В целом это снижает расход кислорода и субстра-
тов обмена веществ.
Механизмы долговременной адаптации формируются посте-
пенно в процессе хронической гипоксии, продолжаются на всем
ее протяжении и даже в течение некоторого времени после ее
прекращения. Именно эти реакции обеспечивают жизнедеятель-
ность организма в условиях гипоксии при хронической недоста-
точности кровообращения, нарушении дыхательной функции
легких, длительных анемических состояниях. К основным меха-
низмам долговременной адаптации при хронической гипоксии
относят:
• стойкое увеличение диффузионной поверхности легочных
альвеол;
• более эффективную корреляцию легочной вентиляции и
кровотока;
• компенсаторную гипертрофию миокарда;
• гиперплазию костного мозга и увеличенное содержание ге-
моглобина в крови.
Глава 4
НАРУШЕНИЯ ТЕПЛОВОГО БАЛАНСА ОРГАНИЗМА
Температура тела является одним из важных параметров го-
меостаза. Оптимум температуры организма — необходимое усло-
вие эффективного протекания реакций метаболизма, пластиче-
ских процессов и обновления структур, функционирования орга-
нов, тканей, физиологических систем и деятельности организма в
целом. Благодаря активному поддержанию необходимого диапа-
63
Схема 1
зона температуры внутренней среды организм обладает стабиль-
ным уровнем жизнедеятельности в оптимальных условиях суще-
ствования и эффективным приспособлением к их изменениям,
включая экстремальные воздействия.
Действие различных факторов может привести к изменению
теплового баланса организма, что проявляется либо гипертерми-
ческими, либо гипотермическими состояниями (схема 1). Гипер-
термические состояния характеризуются повышением, а гипотер-
мические — понижением температуры тела, соответственно выше
и ниже нормы. Чаще эти отклонения носят временный, обрати-
мый характер (например, при лихорадке и гипертермических ре-
акциях). Однако если патогенный агент обладает высоким повре-
ждающим действием, а адаптивные механизмы организма недос-
таточны, то указанные состояния могут перейти гомеостатиче-
ский порог и даже обусловить смерть человека.
ГИПЕРТЕРМИЧЕСКИЕ СОСТОЯНИЯ И ИХ ВИДЫ
ГИПЕРТЕРМИЯ
Гипертермия, или перегревание организма, — типовая форма
расстройства теплового обмена, возникающая в результате дейст-
вия высокой температуры окружающей среды или нарушения
процессов теплоотдачи организма. Она характеризуется срывом
механизмов теплорегуляции и проявляется повышением темпера-
туры тела выше нормы.
Причины гипертермии:
• высокая температура окружающей среды;
64
• факторы, препятствующие теплоотдаче, что сопровождается
увеличением образования доли так называемой свободной
энергии, выделяющейся в виде тепла;
• влияние разобщителей процессов окисления и фосфорили-
рования в митохондриях клеток, что может быть следст-
вием:
— первичного расстройства механизмов терморегуляции, на-
пример при кровоизлиянии в область гипоталамуса, участвующе-
го в регуляции температурного режима организма;
— нарушения процессов отдачи тепла в окружающую среду,
например у тучных людей, при ношении влагонепроницаемой
одежды или высокой влажности воздуха.
Эти факторы могут действовать содружественно и повышать
возможность возникновения гипотермии.
Важными условиями, способствующими развитию гипертер-
мии, являются:
• факторы, снижающие эффективность процессов теплоотда-
чи — значительная влажность воздуха, воздухе- и влагоне-
проницаемая одежда;
• воздействия, повышающие активность реакций теплопро-
дукции, например интенсивная мышечная работа;
• возраст — гипертермия легче развивается у детей и стари-
ков, у которых понижена эффективность системы терморе-
гуляции;
• некоторые заболевания — гипертоническая болезнь, сер-
дечная недостаточность, гипертиреоз, ожирение, вегетосо-
судистая дистония.
Механизмы развития гипертермии. Различают две стадии ги-
пертермии — компенсации (адаптации) и декомпенсации (деа-
даптации) механизмов терморегуляции организма.
Стадия компенсации характеризуется активацией экстренных
механизмов адаптации организма к перегреванию. Эти механизмы
направлены на увеличение теплоотдачи и снижение теплопродук-
ции. В результате температура тела хотя и повышается, однако ос-
тается в пределах верхней границы нормального диапазона.
Стадия декомпенсации характеризуется срывом и неэффектив-
ностью как центральных, так и местных механизмов терморегуля-
ции. Это обусловливает нарушение температурного гемостаза ор-
ганизма, что является главным звеном патогенеза стадии.
Интенсивность и степень декомпенсации механизмов теплорегу-
ляции определяются многими факторами. Ведущее значение среди
них имеют два:
• скорость и величина повышения температуры окружающей
среды — чем они выше, тем быстрее и сильнее нарастают
расстройства жизнедеятельности организма;
• тренированность организма повторяющимися эпизодами
высокой внешней температуры. При повторном воздейст-
вии на организм умеренно повышенной температуры рези-
стентность к ней возрастает. Это обеспечивается формиро-
65
ванием состояния адаптации к перегреванию. Такое состоя-
ние характеризуется активацией системных и местных ме-
ханизмов "терморезистентности".
Критической температурой тела, обусловливающей гибель орга-
низма, является 42—44 "С. Смерть может наступить и при более
низкой температуре. Это определяется тем, что при гипертермии
организм подвергается действию не только чрезмерной темпера-
туры, но и других факторов, вторично формирующихся в орга-
низме: некомпенсированных сдвигов pH, изменений содержания
ионов и жидкости; накопления избытка токсичных продуктов об-
мена веществ; последствий недостаточной функции органов и
физиологических систем — сердечно-сосудистой, внешнего дыха-
ния, крови, почек, печени и др.
ТЕПЛОВОЙ УДАР
Тепловой удар — форма гипертермии, характеризующаяся бы-
стрым развитием жизненно опасного уровня температуры тела,
который составляет 42—43 °C. Он является следствием быстрого
истощения и срыва приспособительных процессов, характерных
для стадии компенсации гипертермии.
Причинами дезадаптации могут быть:
• действие теплового фактора высокой интенсивности;
• низкая эффективность механизмов адаптации организма к
повышенной температуре внешней среды. В связи с этим
перегревание после кратковременной стадии компенсации
быстро приводит к срыву механизмов терморегуляции орга-
низма и интенсивному нарастанию температуры тела. Сле-
довательно, тепловой удар — это гипертермия с непродол-
жительной стадией компенсации, быстро переходящая в
стадию декомпенсации.
Смерть человека при тепловом ударе обычно является резуль-
татом:
• сердечной недостаточности;
• остановки дыхания;
• острой прогрессирующей интоксикации, развивающейся в
связи с почечной недостаточностью и нарушением обмена
веществ.
СОЛНЕЧНЫЙ УДДР
Причина: прямое воздействие энергии солнечного излучения
на организм, преимущественно на голову. Наибольшее патоген-
ное действие наряду с другими оказывает радиационное тепло,
которое прогревает одновременно и поверхностные, и глубокие
ткани организма. Кроме того, инфракрасное излучение интен-
сивно прогревает и ткань головного мозга, в котором располага-
66
ются нейроны центра терморегуляции. В связи с этим солнеч-
ный удар развивается быстротечно и чреват смертельным ис-
ходом.
Патогенез солнечного удара представляет собой комбинацию
механизмов гипертермии и собственно солнечного удара, кото-
рый включает:
• нарастающую артериальную и венозную гиперемию голов-
ного мозга;
• увеличение образования цереброспинальной жидкости и
избыточное наполнение ею мягкой мозговой оболочки, что
вызывает набухание и сдавление вещества головного мозга.
В свою очередь венозная гиперемия приводит к плазморра-
гии, отеку, гипоксии и множественным диапедезным кро-
воизлияниям в ткани мозга, в том числе в регионе ядер
центра терморегуляции. Это обусловливает нарушение его
функции по регуляции теплоотдачи и в целом по поддержа-
нию температурного гомеостаза.
ЛИХОРАДКА
Лихорадка — типовая терморегуляторная реакция организма
на действие пирогенного фактора, характеризующаяся динамиче-
ской перестройкой функции системы терморегуляции и времен-
ным повышением температуры тела выше нормы вне зависимо-
сти от температуры внешней среды. Лихорадка отличается от дру-
гих гипертермических состояний сохранением механизмов термо-
регуляции на всех этапах ее развития.
Причины.
Пирогены — вещества, вызывающие повышение темпера-
туры тела.
По происхождению пирогены дифференцируют на две катего-
рии: инфекционные (бактерии, вирусы, риккетсии, грибки) и не-
инфекционные.
По биохимической структуре они чаще всего являются белка-
ми. жирами, реже нуклеиновыми кислотами или нуклеопротеи-
нами, стероидными веществами.
Условия развития лихорадки:
• состояние реактивности организма;
• особенности пирогенов.
Механизм развития лихорадки включает три категории взаимо-
связанных процессов:
• регулирующих уровень теплового баланса организма в связи
с образованием в нем пирогенных веществ;
• изменений, развивающихся под влиянием повышенной
температуры тела;
• реакций, формирующихся в связи с повреждающим дейст-
вием факторов, вызывающих лихорадку.
Эти процессы имеют двоякий характер: в основном — адап-
67
тивный, но в случае превышения физиологических параметров —
повреждающий.
Лихорадочная реакция — динамичный, стадийный процесс.
В нем условно выделяют три стадии.
• Стадия подъема температуры тела характеризуется накопле-
нием в организме дополнительного количества тепла за
счет преобладания теплопродукции по сравнению с реак-
циями теплоотдачи.
• Стадия сохранения температуры тела на повышенном уров-
не проявляется относительной сбалансированностью тепло-
продукции и теплоотдачи. Однако баланс этих двух процес-
сов достигается уже на уровне, существенно превышающем
"долихорадочный". Именно это и поддерживает температуру
тела на повышенном (по сравнению с долихорадочным пе-
риодом) уровне: интенсивная теплопродукция уравновеши-
вается эквивалентной ей теплоотдачей.
В этой стадии лихорадки выделяют несколько степеней повы-
шениятелтературытела:
• слабую, или субфебрильную (от 36,7 до 38 °C);
• умеренную, или "фебрильную" (в диапазоне 38—39 °C);
• высокую, или пиретическую (39—-41 °C);
• чрезмерную, или гиперпиретическую (выше 41 °C).
Температура внешней среды не оказывает существенного
влияния на развитие лихорадки и динамику температуры тела
при ней, так как при развитии лихорадки система терморегуля-
ции организма не расстраивается. Она динамично перестраивает-
ся, активируется и работает на более высоком функциональном
уровне.
• Стадия снижения температуры тела до нормального диапазо-
на характеризуется постепенным снижением продукции
лейкоцитарных пирогенных пептидов. Причиной этого яв-
ляется прекращение действия "первичного" пирогена, что
связано с уничтожением микроорганизмов или с ликвида-
цией неинфекционных пирогенных веществ.
Выделяют два варианта снижения температуры на Ш стадии
лихорадки: постепенное, или литическое, и быстрое, или крити-
ческое.
Значение лихорадки. Учитывая, что в эволюции лихорадка
сформировалась как типовая, стереотипная реакция, у каждого
человека она сопровождается как адаптивными (преимуществен-
но), так и, при определенных условиях, патогенными эффектами.
Основные адаптивные эффекты лихорадки:
• прямые и опосредованные бактериостатические и бактери-
цидные эффекты;
• усиление специфических и неспецифических механизмов
системы иммунобиологического надзора;
• активация неспецифической стресс-реакции как компонен-
та общего адаптационного процесса. Изменения в организ-
ме, развивающиеся в ходе реализации стресса, с одной сто-
68
роны, активируют или потенцируют ряд неспецифических
и специфических реакций системы иммунобиологического
надзора, а с другой — способствуют изменению пластиче-
ских процессов, функции органов и их физиологических
систем, участвующих в формировании лихорадочной реак-
ции.
Наиболее значимые патогенные эффекты лихорадки:
1. Повреждающее действие на организм высокой (особенно
чрезмерной) температуры (см. выше "Гипертермия").
2. Патогенные эффекты причин, вызывающих развитие лихо-
радки: микробные эндо- и экзотоксины; чужеродные белки и
другие соединения, способные вызывать иммунопатологичекие
процессы (аллергию, иммунодефицита, болезни иммунной ауто-
агрессии) и др.
3. Функциональная перегрузка органов и физиологических сис-
тем, непосредственно включающихся в механизм развития лихо-
радки (сердечно-сосудистой, дыхания, печени и др.). Например,
при значительном повышении температуры тела, а также при ее
критическом падении могут развиться коллапс, обморок или сер-
дечная недостаточность.
4. Расстройство функций органов и систем, непосредственно не
участвующих в реализации лихорадочной реакции, например сис-
темы пищеварения, что характеризуется снижением аппетита, на-
рушением пищеварения, похуданием больного; нервной системы,
сопровождающееся головной болью, иногда судорогами и галлю-
цинациями, нарушением рефлексов и др.
ГИПОТЕРМИЧЕСКИЕ СОСТОЯНИЯ
К гипотермическим состояниям относят:
• гипотермию;
управляемую (искусственную) гипотермию, или медицинскую
гибернацию.
ГИПОТЕРМИЯ
Гипотермия — типовая форма расстройства теплового обмена
организма, возникающая в результате действия на него низкой
температуры внешней среды или значительного снижения тепло-
продукции в нем и характеризующаяся нарушением механизмов
теплорегуляции, что проявляется снижением температуры тела
ниже нормы.
Причины гипотермии:
• низкая температура внешней среды;
• параличи мышц или уменьшение их массы, например при
атрофии в результате кровоизлияния в мозг;
• крайняя степень истощения организма.
69
Условия, способствующие возникновению гипотермии:
• повышенная влажность воздуха;
• увеличение скорости движения воздуха (ветер);
• влажная или мокрая одежда;
• попадание в холодную воду, что сопровождается быстрым
охлаждением организма, поскольку вода примерно в 4 раза
более теплоемка и в среднем в 25 раз более теплопроводна,
чем воздух. В связи с этим замерзание в воде может наблю-
даться при сравнительно высокой температуре.
Индивидуальная резистентность организма к охлаждению зна-
чительно снижается под действием длительного голодания, физи-
ческого переутомления, алкогольного опьянения, а также при
различных заболеваниях, травмах и экстремальных состояниях.
Механизмы гипотермии. Развитие гипотермии — процесс ста-
дийный. В основе ее формирования лежат более или менее дли-
тельное перенапряжение и срыв механизмов терморегуляции ор-
ганизма. В связи с этим выделяют две стадии гипотермии.
1. Стадия компенсации характеризуется активацией экстрен-
ных адаптивных механизмов, направленных на уменьшение теп-
лоотдачи и увеличение теплопродукции. К числу этих механиз-
мов относятся:
• изменение поведения, направленное на "уход" от воздейст-
вия холода;
• снижение эффективности процессов теплоотдачи;
• активация процессов теплопродукции;
• "включение" стрессорной реакции.
Благодаря комплексу указанных изменений температура тела
хотя и понижается, но еще не выходит за рамки нижней границы
нормы. Температурный гомеостаз организма сохраняется.
2. Стадия декомпенсации процессов терморегуляции организма
является результатом срыва центральных механизмов регуляции
теплового обмена. На этой стадии температура тела падает ниже
нормального уровня и продолжает снижаться. Температурный го-
меостаз организма нарушается.
При нарастании действия охлаждающего фактора наступает
замерзание и смерть организма. Непосредственными причинами
смерти при глубокой гипотермии являются прекращение сердеч-
ной деятельности и остановка дыхания.
Медицинская гипотермия
Управляемая, или медицинская, гипотермия — метод управ-
ляемого снижения температуры тела или его части с целью
уменьшения интенсивности обмена веществ, уровня функций
тканей, органов, физиологических систем и повышения их устой-
чивости к гипоксии. Управляемая гипотермия используется в ме-
дицине в двух разновидностях: общей и местной.
Общая управляемая гипотермия применяется при выполнении
70
операции в условиях значительного снижения или даже времен-
ного прекращения кровообращения. Этот метод применяется при
операциях на так называемых сухих органах: сердце, головном
мозге, легких, крупных сосудах, при использовании искусствен-
ного кровообращения.
Локальная управляемая гипотермия отдельных органов или
тканей (головного мозга, печени и др.) используется при необхо-
димости проведения оперативных вмешательств или других ма-
нипуляций на этих органах для коррекции кровотока, пластиче-
ских процессов и других целей.
Глава 5
НАРУШЕНИЯ КРОВООБРАЩЕНИЯ
И ЛИМФООБРАЩЕНИЯ
Кровообращение условно разделяют на центральное и перифе-
рическое.
Центральное кровообращение, осуществляясь на уровне сердца
и крупных сосудов, обеспечивает:
• поддержание системного давления крови;
• направление движения крови из артериального русла в ве
нозное и далее — в сердце;
• демпфирование (амортизацию) систолических и диастоли
ческих колебаний артериального давления при выбросе
крови из желудочков сердца для обеспечения равномерного
кровотока.
Периферическое (регионарное) кровообращение осуществляется
в сосудах органов и тканей. К нему относится кровообращение в
сосудах микроциркуляторного русла, которое включает:
• артериолы;
• прекапилляры;
• капилляры;
• посткапилляры;
• венулы;
• артериоловенулярные шунты.
Микроциркуляторное русло обеспечивает доставку крови к
тканям, транскапиллярный обмен субстратами метаболизма, ки-
слородом. углекислым газом, а также транспорт крови от тканей.
Артериоловенозные шунты определяют объем крови, притекаю-
щей к капиллярам. При закрытии этих шунтов кровь из артериол
поступает в капилляры, а при открытии — в венулы, минуя ка-
пилляры.
Лимфатическая система структурно и функционально объеди-
нена с системой кровообращения и обеспечивает лимфообразую-
71
щую, дренажную, барьерную, дезинтоксикационную, кровообра-
зующую функции и включает:
• лимфатические органы — лимфатические узлы, лимфатиче-
ские фолликулы, миндалины, селезенку;
• лимфатические транспортные пути — капилляры, микро- и
макрососуды, синусы, которые имеют адренергическую ин-
нервацию. общую с кровеносными сосудами.
Все компоненты системы кровообращения тесно связаны между
собой, и расстройство деятельности одного из них, например
центрального, приводит к изменениям и периферического, и
микроциркуляторного кровообращения. С другой стороны, рас-
стройства системы микроциркуляции могут стать причиной или
усугублять нарушения функции сердца или крупных сосудов. При
этом большую роль в патологии играет тесная интеграция крове-
носной системы с лимфатической, которая по существу также со-
ставляет систему микроциркуляции. Лимфа образуется в лимфа-
тических капиллярах из тканевой жидкости и по лимфатическим
сосудам транспортируется в венозную систему. При этом 80—
90 % тканевого фильтрата оттекает в венозное, а 10—20 % — в
лимфатическое русло. Отток лимфы и венозной крови обеспечи-
вается одними и теми же механизмами — присасывающим дейст-
вием сердца, грудной клетки, диафрагмы и работой мышц.
ВИДЫ РАССТРОЙСТВ КРОВООБРАЩЕНИЯ
Выделяют нарушения центрального и периферического крово-
обращения.
Патология центрального кровообращения обусловлена главным
образом нарушениями функций сердца или тока крови в крупных
сосудах — аорте, нижней и верхней полых венах, легочном стволе,
легочных венах. При этом возникает недостаточность кровообра-
щения, которая сопровождается изменениями периферического
кровообращения, в том числе и микроциркуляции. В результате
органы и ткани не получают достаточного количества кислорода и
других метаболитов, из них не удаляются токсичные продукты ме-
таболизма. Причиной этих нарушений может быть либо нарушение
функции сердца, либо снижение сосудистого тонуса—гипотония.
Патология периферического (регионарного) кровообращения,
включая нарушения микроциркуляции, проявляются в трех ос-
новных формах:
1) нарушения кровонаполнения (артериальное полнокровие и
малокровие, венозное полнокровие);
2) нарушения реологических свойств крови (тромбоз, эмболия,
стаз, ДВС-синдром);
3) нарушения проницаемости стенок сосудов (кровотечения,
кровоизлияния, плазморрагия).
Полнокровие сосудов (гиперемия) может быть артериальным и
венозным. Каждое из них в свою очередь может быть:
72
по течению — острым и хроническим;
по распространенности — местным и общим.
ПОЛНОКРОВИЕ
Артериальное полнокровие (гиперемия) обусловлено увеличени-
ем притока крови в систему микроциркуляции при нормальном
ее оттоке по венам, что проявляется расширением артериол, по-
вышением внутрисосудистого давления и местной температуры
тканей.
Причиной общей артериальной гиперемии может быть увеличе-
ние объема циркулирующей крови (плетора) или количества
эритроцитов (эритремия); местной артериальной гиперемии —
различные физические (температурные), химические (щелочи,
кислоты), биологические (инфекционной и неинфекционной
природы) факторы, воспаление, а также нарушение иннервации
(ангионевротическая гиперемия) и психогенные воздействия: на-
пример, слово может привести к артериальной гиперемии лица и
шеи, проявляющейся "краской стыда или гнева".
Механизмы развития артериального полнокровия:
• нейрогенный механизм связан с преобладанием парасимпа-
тических эффектов на артериолы и капилляры над симпа-
тическими влияниями, что наблюдается, например, при
травме, сдавлении опухолью или воспалении регионарных
парасимпатических ганглиев, а также симпатических ганг-
лиев или нервных окончаний;
• гуморальный механизм обусловлен увеличением либо уровня
биологически активных веществ с сосудорасширяющим
действием (кининов, простагландинов, серотонина), либо
повышением чувствительности к ним стенок артериол (в
частности, к ионам внеклеточного калия);
• нейромиопаралитический механизм заключается в истоще-
нии запасов катехоламинов в симпатических нервных окон-
чаниях или в снижении тонуса мышечных волокон в стен-
ках артериол, что может быть вызвано длительным физиче-
ским воздействием (например, при применении грелок,
горчичников, медицинских банок), изменениями баромет-
рического давления и др.
Вицы артериального полнокровия. Физиологическая артериаль-
ная гиперемия возникает при интенсивном функционировании
органа, например в работающих мышцах, беременной матке, в
стенке желудка после приема пищи. Она обеспечивает усиленное
поступление в ткани кислорода и питательных веществ и способ-
ствует удалению продуктов их распада.
Патологическая артериальная гиперемия не связана с усилени-
ем функции органа, развивается при воспалении, нарушениях
иннервации органов, травмах тканей, эндокринных заболеваниях,
значительном повышении артериального давления и др. При
73
Рис. 14. Полнокровие сосудов.
а — артериальная гиперемия; б — венозная гиперемия: расширение и переполне-
ние кровью вен бедра и голени.
этом стенки артериол могут разрываться и возникает кровотече-
ние или кровоизлияние в ткани.
Признаки артериального полнокровия. При артериальной гипере-
мии увеличивается пульсация артерий, меняется микроциркулятор-
ное русло — расширяются артериолы, раскрываются резервные ка-
пилляры, в них увеличивается скорость кровотока, повышается
кровяное давление. Гиперемия хорошо видна на поверхности кожи
(рис. 14, а). При артериальной гиперемии отмечаются:
• увеличение числа и диаметра артериальных сосудов;
• покраснение органа, ткани или их участков;
• повышение температуры тканей в области их гиперемии;
• увеличение объема и напряжения (тургора) органа или тка-
ни в связи с увеличением их кровонаполнения;
• увеличение лимфообразования и лимфооттока, что обуслов-
лено повышением перфузионного давления в сосудах мик-
роциркуляции.
Венозное полнокровие (гиперемия) обусловлено затруднением
оттока крови по венам при нормальном ее притоке по артериям,
что приводит к увеличению кровонаполнения органа или ткани.
Причиной венозного полнокровия является препятствие оттоку
74
крови в результате закрытия просвета вены тромбом или эмболом,
при сдавлении вен опухолью, рубцом, жгутом, при врожденном
недоразвитии эластического каркаса стенок вен или их клапанного
аппарата, а также при развитии сердечной недостаточности.
Признаки венозного полнокровия:
• цианоз, т. е. синюшный оттенок слизистых оболочек, кожи,
ногтей и органов из-за увеличения в них количества веноз-
ной крови, бедной кислородом;
• снижение температуры тканей вследствие падения в них ин-
тенсивности обмена веществ;
• отек тканей, развивающийся в результате гипоксии (кисло-
родного голодания) тканей стенок сосудов микроциркуля-
торного русла, повышения их проницаемости и выхода в
окружающую ткань плазмы крови;
• увеличение объема органов и тканей из-за скопления в них
венозной крови и отека.
Местное венозное полнокровие имеет значение в патологии
главным образом в связи с развивающимся при этом острым оте-
ком тканей в том или ином регионе тела, а также с возможно-
стью возникновения инфаркта селезенки при тромбозе селезе-
ночной вены. При хроническом местном венозном (застойном)
полнокровии в органе активизируется образование фибробласта-
ми коллагена и в строме разрастается соединительная ткань —
развивается органа.
Общее венозное полнокровие имеет большое значение в пато-
логии, возникает при различных заболеваниях и может иметь тя-
желые последствия.
Острое общее венозное полнокровие чаще развивается при ост-
рой сердечной недостаточности (острый инфаркт миокарда, ост-
рый миокардит), а также в атмосфере с низким содержанием ки-
слорода (например, при разгерметизации кабины самолета, высо-
ко в горах, при недостаточном поступлении кислорода из аква-
ланга при подводных работах и т. п.). При этом в тканях быстро
нарастают гипоксия и ацидоз (закисление), повышается сосуди-
стая проницаемость, появляется и прогрессирует отек, часто со-
провождающийся периваскулярными кровоизлияниями.
Хроническое общее венозное полнокровие обычно развивается при
хронических заболеваниях сердца, заканчивающихся хронической
сердечной недостаточностью (хроническая ишемическая болезнь
сердца, пороки сердца, кардиомиопатии). Помимо всех тех изме-
нений, которые характеризуют острую венозную гиперемию, при
хроническом венозном полнокровии постепенно развиваются атро-
фия паренхимы органов и их стромы, в результате чего происхо-
дит уплотнение (индурация) органов и тканей. Кроме того, хрони-
ческий отек и плазморрагия вызывают перегрузку лимфатической
системы и развитие ее недостаточности. Формируется капиллярно-
трофическая недостаточность, которая характеризуется:
• ом микрососудов, уменьшением их просветов и уменьшением
количества капилляров, что обусловливает уменьшение кро-
75
вотока по капиллярам, транскапиллярный обмен веществ и
нарастание кислородного голодания;
• преобразованием истинных капилляров в емкостные (депони-
рующие), в которых эритроциты располагаются не в один, а
в несколько рядов, капилляры резко расширяются и пре-
вращаются в венулы, стенки их теряют тонус, что приводит
к еще большему расширению капилляров и венул и усили-
вает венозную гиперемию. При этом количество истинных
капилляров снижается, артериальная кровь попадает в ве-
нозную систему по коллатералям (обходным сосудам), что
способствует нарастанию гипоксических и метаболических
изменений в тканях.
Характерные извинения в органах и тканях, которые развива-
ются при хроническом общем венозном полнокровии.
• В коже и подкожной клетчатке, особенно нижних конечно-
стей, происходит расширение венозных сосудов, отек кожи
и подкожной клетчатки (анасарка), атрофия кожи, застой
лимфы в лимфатических сосудах (лимфостаз). На фоне хро-
нического венозного полнокровия часто развиваются тро-
фические язвы голеней и стоп (рис. 14, б).
• В легких длительный венозный застой имеет особое значе-
ние в связи с тем, что он развивается при хронической сер-
дечной недостаточности (см. главу 13). При этом в легоч-
ных венах, впадающих в левое предсердие, развивается за-
стой крови, что способствует прогрессирующей гипоксии.
При этом повышается проницаемость стенок сосудов и из
венул и капилляров в окружающую ткань выходит сначала
плазма крови, а затем и эритроциты. Последние захватыва-
ются макрофагами, в которых гемоглобин превращается в
гемосидерин и ферритин, а макрофаги получают название
сидерофагов. Часть макрофагов альвеол, загруженных гемо-
сидерином, попадает в бронхи и вместе с мокротой выво-
дится из организма. В мокроте они называются "клетками
сердечных пороков". Часть сидерофагов распадается в строме
легких, чему способствует нарастающая недостаточность
лимфатических сосудов, перегруженных отечной жидко-
стью, сидерофагами и гемосидерином. Постепенно развива-
ется застой лимфы. Прогрессирующие гипоксия и застой
лимфы являются стимулами для активизации системы фиб-
робластов в ткани легких и интенсивного образования ими
коллагена. Нарастает склероз легких, они становятся плот-
ными, развивается их индурация (от лат. durum — плотный).
При этом гемосидерин, образующий скопления в строме и
в альвеолах и характеризующий местный гемосидероз, при-
дает легким бурый цвет и развивается бурая индурация лег-
ких — необратимое состояние, значительно ухудшающее те-
чение хронической сердечной недостаточности и общее со-
стояние больного (рис. 15).
• В печени хроническая венозная обычно также является
76
Рис. 15. Хроническое венозное полнокровие легких (бурая индурация
легких). Сосуды межальвеолярных перегородок расширены (а); в строме
легкого и в просвете альвеол — сидсрофаги (б); часть альвеол заполнена
отечной жидкостью (в); межальвеолярные перегородки утолщены и скле-
розированы (г).
следствием хронической сердечной недостаточности и де-
компенсации сердца. При этом застой крови вначале про-
исходит в нижней полой вене, затем в венах печени и в
центральных венах печеночных долек. Центральные вены
расширяются, через их стенки выходит плазма крови и
эритроциты и в центре долек атрофируются гепатоциты. На
периферии дольки гепатоциты подвергаются жировой дис-
трофии и ткань печени на разрезе становится пестрой, на-
поминающей мускатный орех — на желто-коричневом фоне
отчетливо видны красные точки в центрах долек. Такая
картина носит название "мускатной печени"(рис. 16).
• Селезенка при венозном застое увеличивается в размерах
{застойная спленомегалия), становится синюшной и плотной
(цианотическая индурация селезенки), на разрезе не дает со-
скоба пульпы, ее фолликулы атрофичны, а красная пульпа
склерозирована.
МАЛОКРОВИЕ
Артериальное малокровие, или ишемия, — уменьшение крове-
наполнения органа или ткани, обусловленное либо снижением
притока к ним крови по артериям, либо значительным увеличе-
77
Рис. 16. Хроническое венозное полнокровие печени (мускатная печень).
В центре долек центральные вены и синусоиды резко расширены, пол-
нокровны (а), печеночные клетки атрофичны (б), в области кровоизлия-
нии (в) разрушены. По периферии долек печеночные балки сохранены
(г), перисинусоидальные пространства расширены (д).
нием потребности тканей в кислороде и субстратах метаболизма,
что приводит к несоответствию между потребностями тканей в
кровоснабжении и возможностями артериального кровотока. В
зависимости от причин и механизмов развития ишемии выделяют
пять разновидностей артериального малокровия: ангиоспастиче-
ское. обтурационное, компрессионное, в результате острого пере-
распределения крови и дисфункциональное.
Ангиоспастическое малокровие обусловлено спазмом артерий
вследствие увеличения содержания в тканях веществ, вызываю-
щих спазм сосудов (например, ангиотензин, вазопрессин, катехо-
ламины и т. п.), или повышением чувствительности к ним стенок
артериол (при увеличении содержания в них ионов кальция или
натрия), а также при преобладании симпатико-адреналовых
влияний над парасимпатическими (стресс, стенокардия, аппенди-
кулярная колика).
Обтурационное малокровие развивается при полном или час-
тичном закрытии просвета артерии тромбом, эмболом (при ост-
ром малокровии) или атеросклеротической бляшкой (при хрони-
ческой ишемии).
Компрессионное малокровие возникает при остром или хрони-
ческом сдавлении сосуда извне — жгутом, опухолью, отечной
тканью и т. п.
Малокровие в результате острого перераспределения крови на-
78
блюдается при быстром притоке крови в ранее ишемизированные
ткани. Например, при быстром удалении асцитической жидко-
сти, сдавливавшей сосуды брюшной полости, в эту область уст-
ремляется кровь и возникает ишемия сосудов головного мозга.
Дисфункциональное малокровие является следствием значи-
тельного повышения тканями расхода кислорода и субстратов ме-
таболизма при резкой интенсификации функции органа, напри-
мер ишемия миокарда при внезапной интенсивной нагрузке на
сердце (бег, поднятие тяжестей, тяжелая физическая работа),
ишемия мышц голени у пожилых людей при быстрой ходьбе и
т. п. Обычно этот вид ишемии возникает при сужении просвета
снабжающей артерии атеросклеротической бляшкой.
По характеру течения ишемия может быть острой и хрониче-
ской.
Признаки ишемии:
• побледнение ткани и органа из-за снижения их кровена-
полнения и числа функционирующих капилляров;
• снижение пульсации артерий и уменьшение их диаметра в
результате уменьшения их диастолического наполнения
кровью и падения артериального давления;
• понижение температуры ишемизированной ткани вследст-
вие уменьшения притока теплой артериальной крови и сни-
жения интенсивности метаболизма в ишемизированном ре-
гионе;
• замедление тока крови по микрососудам вплоть до ее оста-
новки;
• снижение лимфообразования в результате падения перфу-
зионного давления в сосудах микроциркуляции.
Последствия и значение ишемии. Кислородное голодание тка-
ней (гипоксия) является главным патогенным фактором ишемии.
Развивающиеся при этом изменения связаны с продолжительно-
стью и тяжестью гипоксии, чувствительностью к ней органов и
наличием коллатерального кровообращения в ишемизированной
ткани. Наиболее чувствительны к гипоксии головной мозг, почки
и миокард, в меньшей степени — легкие и печень, в то время как
соединительная, костная и хрящевая ткани отличаются макси-
мальной устойчивостью к недостатку кислорода.
Ишемия способствует распаду в клетках макроэргических со-
единений — креатинфосфата и АТФ, что компенсаторно активи-
зирует бескислородный (анаэробный) путь окисления и образова-
ния энергии — анаэробный гликолиз. Следствием этого является
накопление в тканях недоокисленных продуктов метаболизма,
что приводит к ацидозу тканей, усилению перекисного окисле-
ния липидов, стимуляции гидролитических ферментов лизосом и
в итоге — к распаду мембран клеток и внутриклеточных структур.
Возникающий энергетический дефицит способствует, кроме того,
накоплению в клетках ионов кальция, активизирующих ряд фер-
ментов, которые также приводят клетки к гибели.
Функциональное состояние органа имеет большое значение при
79
Рис. 17. Схема развития коллатерального кровообращения и образования
инфарктов (по Я. Л. Рапопорту).
а — схема достаточных коллатералей: артерия (1) разделялся на три ветви, из ко-
торых одна (2) закупорена; питаемая ею область получает достаточное количество
крови по коллатералям (3 и 4); б — схема концевых артерии: артерия (1) разделя-
ется на три ветви, не имеющие артериальных соединении, а только капиллярные;
закут ю]жа одной ветви (2) лишает соответствующую часть капилляров (3) снабже-
ния кровью (белый инфаркт); в — схема недостаточных коллатералей при гемор-
рагическом инфаркте: 1 — артерия, разделяющая на три ветви; Z — просвет сред-
ней артерии закупорен; 3 — окольный артериальный сосуд, по которому протека-
ет кровь, заливающая участок, снабжаемый артерией (1), но недостаточный для
питания тканей; 4 — вена.
ишемии: чем интенсивнее он функционирует, тем больше нужда-
ется в притоке артериальной крови и тем чувствительнее к мало-
кровию .
Скорость развития ишемии играет решающую роль: если арте-
риальное малокровие возникает остро, в тканях развиваются дис-
трофические и некротические изменения; если же ишемия носит
хронический, медленно прогрессирующий характер, то в ишеми-
зированных органах и тканях нарастают атрофические и склеро-
тические процессы. При этом в тканях обычно успевают сформи-
роваться коллатерали, снижающие степень гипоксии.
Коллатеральное кровообращение иногда приобретает опреде-
ляющее значение в возможных исходах ишемии. Коллатеральное,
или обходное, кровообращение представлено сетью мелких сосу-
дов, соединяющих более крупные артерии и вены. Коллатераль-
ные сосуды имеются в норме, но они находятся в спавшемся со-
стоянии, так как потребности тканей в кровоснабжении обеспе-
чиваются магистральными сосудами. Коллатерали начинают про-
водить кровь либо в условиях резко возросшей функции органа,
либо при возникновении препятствия току крови по магистраль-
ному сосуду. В этих случаях раскрываются имеющиеся капилля-
ры и начинают образовываться новые, от скорости их образова-
ния зависит уровень компенсации ишемии и ее исход. Однако в
некоторых органах, таких как сердце, головной мозг, почки, кол-
латерали развиты слабо, поэтому при закрытии просвета магист-
ральной артерии коллатеральное кровообращение часто не спо-
80
собно компенсировать ишемию и развивается некроз тканей этих
органов. Вместе с тем в подкожной клетчатке, кишечнике и саль-
нике сеть коллатеральных сосудов в норме развита хорошо, что
нередко позволяет этим органам и тканям справиться с ишемией.
В остальных органах имеются коллатерали промежуточного типа,
которые лишь частично позволяют компенсировать артериальное
малокровие (рис. 17).
Значение ишемии заключается в снижении функций ишемизи-
рованных органов, которое, однако, может быть обратимым, если
ишемия продолжалась относительно недолго и в тканях разви-
лись лишь обратимые дистрофические изменения. В случаях мед-
ленно нарастающей ишемии в организме успевают развиться
компенсаторные и приспособительные процессы, позволяющие в
какой-то степени восполнить функцию ишемизированного орга-
на. Если же в ишемизированных органах развиваются некротиче-
ские изменения с утратой их функций, то это может приводить к
тяжелой инвалидности и смерти.
НАРУШЕНИЯ РЕОЛОГИЧЕСКИХ СВОЙСТВ КРОВИ
Эти нарушения проявляются такими патологическими процес-
сами. как тромбоз, эмболия, стаз, сладж. ДВС-синдром.
Тромбоз — процесс прижизненного свертывания крови в про-
свете сосуда или в полостях сердца. Свертывание крови является
важнейшей физиологической реакцией, препятствующей смер-
тельной потере крови при повреждениях сосудов, и если эта ре-
акция отсутствует, развивается опасное для жизни заболевание —
гемофилия. Вместе с тем при повышении свертываемости крови в
просвете сосуда образуются свертки крови — тромбы, препятст-
вующие кровотоку, что становится причиной тяжелых патологи-
ческих процессов в организме, вплоть до наступления смерти.
Наиболее часто тромбы развиваются у больных в послеопераци-
онном периоде, у людей, находящихся на длительном постельном
режиме, при хронической сердечно-сосудистой недостаточности,
сопровождающейся общим венозным застоем, при атеросклерозе,
злокачественных опухолях, у беременных, у старых людей.
Причины тромбоза делят на местные и общие.
Местные причины — повреждение стенки сосуда, начиная от
слущивания эндотелия и заканчивая ее разрывом; замедление и
нарушения кровотока в виде возникающих завихрений крови при
наличии препятствия ее току, например атеросклеротической
бляшки, варикозного расширения или аневризмы стенки сосуда.
Общие причины — нарушение соотношения между свертываю-
щей и противосвертывающей системами крови в результате уве-
личения концентрации или активности свертывающих факторов
— прокоагулянтов (тромбопластинов, тромбина, фибриногена
и др.) либо снижения концентрации или активности антикоагу-
лянтов (например, гепарина, фибринолитических веществ), а так-
81
же повышения вязкости крови, например, в связи с увеличением
количества ее форменных элементов, особенно тромбоцитов и
эритроцитов (при некоторых системных заболеваниях крови).
Стадии образования тромба. Выделяют 4 стадии тромбообразо-
вания.
1-я — стадия агглютинации тромбоцитов (сосудисто-тромбоци-
тарная), начинается уже при повреждении эндотелиоцитов инти-
мы и характеризуется адгезией (прилипанием) тромбоцитов к об-
наженной базальной мембране сосуда, чему способствует появле-
ние определенных факторов свертывания — фибронектина, фак-
тора Виллебрандта и др. Из разрушающихся тромбоцитов выде-
ляется тромбоксан А2 — фактор, суживающий просвет сосуда, за-
медляющий кровоток и способствующий выбросу тромбоцитами
серотонина, гистамина и тромбоцитарного фактора роста. Под
влиянием этих факторов запускается каскад свертывающих реак-
ций, в том числе и образование тромбина, который вызывает раз-
витие следующей стадии.
2-я — стадия коагуляции фибриногена (плазменная), характе-
ризуется трансформацией фибриногена в нити фибрина, которые
образуют рыхлый сверток и в нем (как в сети) задерживаются
форменные элементы и компоненты плазмы крови с развитием
последующих стадий.
3-я — стадия агглютинации эритроцитов. Она связана с тем,
что эритроциты должны передвигаться в потоке крови, а если
они останавливаются, то склеиваются (агглютинируют). При
этом выделяются факторы, вызывающие ретракцию (сжатие) об-
разовавшегося рыхлого тромба.
4-я — стадия преципитации плазменных белков. В результате
ретракции из образовавшегося сгустка отжимается жидкость, бел-
ки плазмы и белки из распавшихся форменных элементов крови
подвергаются преципитации, сверток уплотняется и превращает-
ся в тромб, который закрывает дефект стенки сосуда или сердца,
но может закрыть и весь просвет сосуда, прекратив тем самым
кровоток.
Морфология тромба. В зависимости от особенностей и скоро-
сти образования тромбы могут иметь различный состав, строение
и внешний вид. Выделяют следующие виды тромбов:
белый тролб, состоящий из тромбоцитов, фибрина и лейкоци-
тов, образуется медленно при быстром кровотоке, обычно в арте-
риях, между трабекулами эндокарда, на створках клапанов
сердца;
красный тролб, в состав которого входят эритроциты, тромбо-
циты и фибрин, возникает быстро в сосудах с медленным током
крови, обычно в венах;
слешанный тролб включает в себя тромбоциты, эритроциты,
фибрин, лейкоциты и встречается в любых отделах кровеносного
русла, в том числе в полостях сердца и в аневризмах артерий;
гиалиновые тролбы, состоящие из преципитированных белков
плазмы и агглютинированных форменных элементов крови, об-
82
разующих гомогенную, бесструктурную массу; они обычно мно-
жественные, формируются только в сосудах микроциркуляции
при шоке, ожоговой болезни, ДВС-синдроме, тяжелой интокси-
кации и т. п.
Структура тромба. Макроскопически в тромбе определяется
небольшая, тесно связанная со стенкой сосуда головка тромба, по
строению соответствующая белому тромбу, тело - обычно сме-
шанный тромб и рыхло прикрепленный к интиме хвост тромба,
как правило, красный тромб. В области хвоста тромб может от-
рываться, что служит причиной тромбоэмболии.
По отношению к просвету сосуда выделяют:
• пристеночные тромбы, обычно белые или смешанные, не
закрывают целиком просвет сосуда, хвост их растет против
тока крови;
• обтурирующие тромбы, как правило, красные, полностью
закрывающие просвет сосуда, хвост их чаще растет по току
крови.
По течению выделяют:
• локализованный (стационарный) тромб, который не увели-
чивается в размерах и подвергается замещению соедини-
тельной тканью - организации
• прогрессирующий тромб, который увеличивается в разме-
рах с различной скоростью, его длина иногда может дости-
гать нескольких десятков сантиметров.
^Исходы тромбоза принято подразделять на благоприятные и
неблагоприятные.
К благоприятным исходам относят организацию тром-
ба, которая начинается уже на 5-6-й день после его образования
и заканчивается замещением тромботических масс соединитель-
ной тканью. В ряде случаев организация тромба сопровождается
его канализацией, т. е. образованием щелей, через которые в ка-
кой-то степени осуществляется кровоток, и васкуляризацией, ко-
гда образовавшиеся каналы покрываются эндотелием, превраща-
ясь в сосуды, через которые частично восстанавливается крово-
ток, обычно через 5-6 нед после тромбоза. Возможно обызвеств-
ление тромбов (образование флеболитов).
Неблагоприятные исходы: тромбоэмболия, возникаю-
щая при отрыве тромба или его части, и септическое (гнойное)
расплавление тромба при попадании в тромботические массы
гноеродных бактерий.
Значение тромбоза определяется быстротой образования тром-
ба, его локализацией и степенью сужения сосуда. Так, мелкие
тромбы в венах малого таза сами по себе не вызывают каких-ли-
бо патологических изменений в тканях, но, оторвавшись, могут
превратиться в тромбоэмболы. Пристеночные тромбы, незначи-
тельно суживающие просветы даже крупных сосудов, могут не
нарушать в них гемодинамику и способствовать развитию колла-
терального кровообращения. Обтурирующие тромбы артерий яв-
ляются причиной ишемии, заканчивающейся инфарктом или ган-
83
греной органов. Тромбоз вен (флеботромбоз) нижних конечностей
способствует развитию трофических язв голеней, кроме того,
тромбы могут стать источником эмболии. Шаровидный тромб, об-
разующийся при отрыве от эндокарда левого предсердия, перио-
дически закрывая атриовентрикулярное отверстие, нарушает цен-
тральную гемодинамику, в связи с чем больной теряет сознание.
Прогрессирующие септические тромбы, подвергающиеся гнойно-
му расплавлению, могут способствовать генерализации гнойного
процесса.
Эмболия — циркуляция в крови или лимфе не встречающихся
в норме частиц (эмболов) и закупорка ими просвета сосудов
(рис. 18).
По происхождению выделяют экзо- и эндогенные эмболии.
При экзогенных эмболиях эмболы попадают в сосудистое руло
из окружающей среды. Различают воздушную, газовую эмболию
и эмболию инородными телами.
Воздушная эмболия происходит при попадании воздуха через
поврежденные крупные вены шеи (имеющие отрицательное дав-
ление по отношению к атмосферному), через зияющие после от-
торжения плаценты вены матки, при введении воздуха с лекарст-
венными препаратами с помощью шприца или капельницы, при
пневмотораксе (попадании воздуха в плевральные полости). Воз-
душные эмболы обтурируют капилляры легких, головного мозга;
воздушные пузыри, скапливающиеся в правых отделах сердца,
придают имеющейся в них крови пенистый вид.
Газовая эмболия развивается при быстрой декомпрессии (у во-
долазов при быстром подъеме с глубины, при разгерметизации
кабины самолета, барокамеры), приводящей к высвобождению из
крови азота. Газовые эмболы поражают различные органы, в том
числе головной и спинной мозг, вызывая кессонную болезнь.
Эмболия инородными телами возникает при попадании в трав-
мированные крупные сосуды частиц инородных предметов — ме-
дицинских катетеров, осколков ампул, кусочков одежды или ос-
колков пуль и снарядов при огнестрельных ранениях.
При эндогенных эмболиях эмболами являются собственные
ткани организма: тромбоэмболия, жировая, тканевая и микроб-
ная эмболия.
Тромбоэмболия развивается при отрыве тромба или его части и
является наиболее частой эмболией. Ее источником могут быть
тромбы любой локализации — артерий, вен. полостей и створок
клапанов сердца. Самой распространенной является тромбоэмбо-
лия легочной артерии, возникающая обычно у больных в после-
операционном периоде, при варикозном расширении вен нижних
конечностей, тромбофлебите или флеботромбозе у больных, стра-
дающих сердечно-сосудистой недостаточностью, онкологически-
ми заболеваниями. При этом тромбоэмболы попадают в легоч-
ный ствол или легочные артерии из вен нижних конечностей,
жировой клетчатки малого таза, иногда из печеночных вен. ниж-
ней и верхней полых вен или правых отделов сердца с пристеноч-
84
Рис. 18. Схема направления движения эмболов (по Я. Л. Рапопорту). Из
венозной системы эмболы заносятся в правую половину сердца, а оттуда
в легочный ствол и легкие (область распространения эмболов из веноз-
ной сети заштрихована). Из левых отделов сердца эмболы заносятся по
артериям в разные органы (указано стрелками).
85
ними тромбами, что, как правило, заканчивается смертью. Меха-
низм смерти связан с пульмоно-коронарным рефлексом, который
возникает при ударе тромбоэмбола в рефлексогенную зону, рас-
положенную в интиме области разветвления легочного ствола.
При этом остро возникает спазм сосудов сердца, легких, а также
бронхов и наступает остановка сердца. Определенную роль играет
и закрытие тромбоэмболом просвета легочного ствола. Мелкие
тромбоэмболы могут проходить легочный ствол и обтурировать
мелкие ветви легочной артерии, вызывая инфаркты легких. В
случае массивной тромбоэмболии мелких ветвей легочных арте-
рий может развиться острое падение артериального давления —
коллапс. Оторвавшиеся тромбы створок клапанов или пристеноч-
ные тромбы эндокарда, образующиеся при эндокардитах, ин-
фаркте миокарда, в хронической аневризме сердца, с током кро-
ви попадают по большому кругу кровообращения в различные
органы, вызывая тромбоэмболический синдром.
Жировая эмболия возникает при переломах трубчатых костей,
размозжении подкожной жировой клетчатки при травмах, при
ошибочном введении в кровяное русло масляных лекарственных
растворов. Жировые эмболы закупоривают мелкие ветви легоч-
ных артерий, причем если обтурировано больше 2/з этих сосудов,
то может развиться острая правожелудочковая недостаточность,
что, однако, бывает очень редко. Чаще жировая эмболия легких
вызывает пневмонию в пораженных участках.
Тканевая эмболия является результатом разрушения тканей
при заболеваниях и травмах, например эмболия опухолевыми
клетками, лежащая в основе формирования метастазов опухоли,
эмболия околоплодными водами у родильниц, разрушенными
тканями у новорожденных с тяжелыми родовыми травмами.
Микробная эмболия возникает при закупорке сосудов скопле-
ниями бактерий, грибов, простейшими и животными паразитами
(например, альвеококками). Этот вид эмболии, чаще наблюдается
при гнойном расплавлении тромба, особенно при септикопиемии.
По механизму распространения выделяют эмболии большого и
малого круга кровообращения, орто- и ретроградную, парадок-
сальную (рис. 18).
Эмболии большого круга кровообращения — эмбол из левых от-
делов сердца, аорты или других крупных артерий, перемещаясь
по току крови, обтурирует органные артерии, в результате чего в
этих органах возникают инфаркты или гангрена. Эмболы, обра-
зующиеся в венах большого круга кровообращения, по току кро-
ви обтурируют либо воротную вену, либо попадают в правые от-
делы сердца и оттуда — в малый круг кровообращения.
При эмболии милого круга кровообращения эмбол из правых от-
делов сердца проходит в малый круг кровообращения, вызывая
либо эмболию легочного ствола, ведущую к остановке сердца,
либо инфаркты легких.
При ортоградной эмболии эмбол перемещается по току крови
или лимфы — наиболее частый вид эмболии.
86
Ретроградная эмболия характеризуется движением эмбола про-
тив тока или лимфы и возникает обычно при эмболии тяжелыми
инородными телами или при ретроградном лимфогенном мета-
стазировании рака желудка.
Парадоксальная эмболия развивается при проникновении эм-
бола из венозного отдела большого круга кровообращения в арте-
риальный отдел, минуя легкие. Это редкий вид эмболии, которая
наблюдается при незаращении межжелудочковой или межпред-
сердной перегородки в сердце (например, при незаращении
овального окна), при артериовенозных анастомозах, прежде всего
при открытом артериальном (боталловом) протоке или при трав-
матическом образовании артериовенозного соустья.
Значение эмболии определяется ее видом, распространенно-
стью и локализацией. Особенно опасны эмболии головного моз-
га, сердца, легочного ствола, часто заканчивающиеся смертью
больного, тогда как поражение почек, печени, селезенки, скелет-
ных мышц имеет меньшее значение. Однако в любом случае эм-
болия кровеносных сосудов приводит к нарушению кровообра-
щения в тканях, вызывает их ишемию и некроз. Эмболия лимфа-
тических сосудов, особенно нижних конечностей, может приво-
дить к лимфатическому отеку тканей, их склерозу и снижению
функции органа, например значительное увеличение размеров
нижней конечности при слоновости.
НАРУШЕНИЯ МИКРОЦИРКУЛЯЦИИ
Причины расстройств микроциркуляции:
• нарушения центрального и регионарного кровообращения —
развиваются при сердечной недостаточности, артериальной
и венозной гиперемии, при ишемии;
• изменения вязкости и объема крови (лимфы) — наблюдают-
ся при уменьшении объема жидкости в плазме (гипогидра-
тация), увеличении количества форменных элементов (по-
лицитемия) или белков плазмы, агрегации и агглютинации
клеток крови;
• гемодилюция, или разжижение крови, — возникает в резуль-
тате значительного поступления тканевой жидкости в кровь
(гипергидратация), снижения общего числа форменных эле-
ментов крови (панцитопения), уменьшения содержания бел-
ков плазмы (гипопротеинемия).
По локализации первично возникающих нарушений расстрой-
ства микроциркуляции разделяют на внутрисосудистые, трансму-
ральные и внесосудистые.
Внутрисосудистые нарушения микроциркуляции проявляются
следующим образом:
• замедление, вплоть до прекращения (стаза), тока крови или
лимфы наиболее часто возникает при сердечной недоста-
точности, ишемии, венозной гиперемии, сгущении крови
87
(при профузном поносе, неукротимой рвоте, ожоговой бо-
лезни и т. п.);
• чрезмерное ускорение кровотока наблюдается при артерио-
ловенулярных шунтах, гемодилюции, почечной недостаточ-
ности;
• нарушение ламинарности (турбулентность) тока крови или
лимфы возникает при образовании препятствия микроцирку-
ляции в виде образования агрегатов из клеток крови (при по-
лицитемии), формировании микротромбов, атипичном стро-
ении микрососудистого русла (капиллярная гемангиома).
Трансмуральные нарушения микроциркуляции связаны с измене-
ниями в самой стенке микрососудов, через которую в норме про-
ходит плазма крови и ее форменные элементы, поступают про-
дукты метаболизма и регулирующие обмен веществ биологически
активные вещества. В патологии наиболее существенную роль иг-
рают две группы нарушений трансмуральной микроциркуляции:
• изменение объема транспорта плазмы (лимфы), который
может возрастать (при артериальной гиперемии, аллергиче-
ских реакциях, лимфостазе) или уменьшаться (при спазме
артериол, кальцификации стенок микрососудов);
• увеличение транспорта клеток крови через стенки микросо-
судов, что может быть при значительном повышении их
проницаемости (например, при гипоксии) или при наруше-
нии целостности ( эритроцитов).
Внесосудистые нарушения микроциркуляции заключаются в за-
медлении вплоть до прекращения тока межклеточной жидкости и
обусловлены изменениями влияний на микроциркуляцию внесо-
судистых факторов, например нервно-трофической регуляции
метаболизма, появлением в окружающих тканях медиаторов вос-
паления (гистамин, серотонин и др.), которые резко усиливают
микровезикулярный транспорт, но могут и способствовать тром-
бированию сосудов микроциркуляции; при скоплении в интер-
стициальной ткани жидкости, например, транссудата при отеках
или экссудата при воспалении, повышается давление тканевой
жидкости и она сдавливает сосуды микроциркуляции.
НАРУШЕНИЯ МИКРОЦИРКУЛЯЦИИ
Нарушения микроциркуляции, имеющие нередко самостоя-
тельное клиническое значение и возникающие при многих забо-
леваниях, — сладж-феномен, стаз, ДВС-синдром.
СЛАДЖ-ФЕНОМЕН
Сладж-феномен (от англ, sludge — тина, густая грязь) характе-
ризуется адгезией и агрегацией форменных элементов крови, пре-
жде всего эритроцитов, что вызывает значительные гемодинамиче-
ские нарушения. Клетки в состоянии сладжа имеют вид "монетных
столбиков", сохраняя при этом свои цитомембраны (рис. 19).
88
Рис. 19. Агрегация эритроцитов как проявление сладж-феномена. В про-
свете капилляра несклеиваюшиеся эритроциты (Эр) в виде монетного
столбика.
Причинили сладжа являются нарушения центральной и регио-
нарной гемодинамики, повышение вязкости крови и поврежде-
ние стенок микрососудов (см. выше). В основе сладж-феномена
лежат следующие механизмы:
• активация клеток крови и выделение ими веществ, способ-
ствующих агрегации эритроцитов. — АДФ. тромбоксана А2.
кининов, гистамина, простагландинов и др.;
• смена поверхностного заряда клеток крови с отрицательно-
го на положительный в результате избытка катионов, посту-
пающих из поврежденных клеток;
• уменьшение величины поверхностного заряда мембран кле-
ток крови при избытке макромолекул белка (гиперпротеи-
89
Рис. 20. Стаз в капиллярах мозга (при маля-
рии). Капилляры резко расширены, в их
просветах склеившиеся эритроциты и пиг-
мент гемомеланин. Ткань мозга отечна.
немии), особенно за счет увеличения концентрации имму-
ноглобулинов, фибриногена, аномальных белков.
Последствия сладжа:
— замедление кровотока в микроциркуляторном русле, вплоть
до его остановки;
— нарушения транскапиллярного обмена;
— гипоксия, ацидоз и нарушение метаболи ма окружающих
тканей.
Значение сладжа. Изменения, сопровождающие сладж-фено-
мен, приводят к повышению проницаемости стенок капилляров
и венул, пропитыванию их плазмой крови (плазморрагия), отеку
90
и нарастающей ишемии окружающих тканей. В целом, совокуп-
ность указанных изменений обозначается как синдром капилляро-
трофической недостаточности. Сладж может быть обратимым, и
тогда постепенно восстанавливается микроциркуляция, но сладж
может предшествовать полной остановке крови (стазу), а также
агглютинации и распаду форменных элементов крови в "монет-
ных столбиках" с образованием в капиллярах гиалиновых тромбов.
СТАЗ
Стаз — остановка кровотока в сосудах микроциркуляторного
русла, прежде всего в капиллярах, реже — в венулах (рис. 20). Ос-
тановке крови предшествует ее замедление — престаз, вплоть до
развития сладж-феномена.
Причинами стаза являются инфекции, интоксикации, шок,
длительное искусственное кровообращение, воздействие физиче-
ских, в том числе температурных, факторов (например, "холодо-
вый стаз" при отморожениях).
Механизмы стаза во многом схожи с механизмами сладж-фе-
номена:
• утрата эритроцитами способности находиться во взвешен-
ном состоянии и образование их агрегатов, что затрудняет
ток крови по микрососудам и вызывает остановку кровото-
ка в капиллярах;
• изменения реологических свойств крови, аналогичных тем,
которые возникают при сладж-феномене;
• гипоксия, ацидоз, нарушения и прекращение метаболизма;
• дистрофические или некротические изменения окружаю-
щих тканей в зависимости от длительности стаза крови.
Исход стаза. После устранения причины, вызвавшей стаз,
кровоток в сосудах микроциркуляторного русла может восстано-
виться. а в окружающих тканях какое-то время сохраняются дис-
трофические изменения, которые, однако, в этих условиях также
обратимы. Если же стаз капилляров устойчив, то гипоксия в ок-
ружающих тканях приводит к их некрозу.
Значение стаза определяется его локализацией и продолжитель-
ностью. Острый стаз в большинстве случаев приводит к обратимым
изменениям в тканях, но в головном мозге он может способство-
вать развитию тяжелого, иногда смертельного отека ткани мозга с
дислокацией его стволовой части в большое затылочное отверстие,
что наблюдается, например, при коме. В случаях длительного стаза
возникают множественные микронекрозы и ные кровоизлияния.
СИНДРОМ ДИССЕМИНИРОВАННОГО ВНУТРИСОСУДИСТОГО
СВЕРТЫВАНИЯ КРОВИ (ДВС-СИНДРОМ)
Синдром диссеминированного внутрисосудистого свертывания
крови (ДВС-синдром) характеризуется образованием множест-
венных тромбов в сосудах микроциркуляторного русла различных
91
органов и тканей вследствие активации факторов свертывания
крови и развивающимся в связи с этим их дефицитом, что приво-
дит к усилению фибринолиза, падению свертываемости крови и
многочисленным кровоизлияниям. ДВС-синдром часто развива-
ется при шоке любого происхождения (травматическом, анафи-
лактическом, геморрагическом, кардиальном и др.), при перели-
вании несовместимой крови, злокачественных опухолях, после
хирургических вмешательств, при тяжелой интоксикации и ин-
фекции, в акушерской патологии, при трансплантации органов,
использовании аппаратов искусственной почки и искусственного
кровообращения и др.
В своем развитии ДВС-синдром проходит 4 стадии.
1-я стадия — гиперкоагуляции и тромбообразования — характе-
ризуется внутрисосудистой агрегацией форменных элементов,
диссеминированным (т. е. во многих микрососудах одновремен-
но) свертыванием крови и формированием множественных тром-
бов в микрососудах разных органов и тканей. Эта стадия длится
всего 8—10 мин.
2-я стадия — нарастающая коагулопатия потребления, особен-
ностью которой является значительное снижение числа тромбо-
цитов и уровня фибриногена, израсходованных на образование
тромбов в предыдущей стадии. Поэтому свертываемость крови
снижается и в результате развивается геморрагический диатез, т. е.
множественные мелкие кровоизлияния.
3-я стадия — глубокой гипокоагуляции и активации фибриноли-
за, которая наступает через 2—8 ч от начала ДВС-синдрома. На-
звание стадии говорит о том, что в этом периоде практически
прекращаются процессы свертывания крови вследствие истоще-
ния всех свертывающих факторов и одновременно резко активи-
зируются процессы фибринолиза (т. е. растворения фибрина,
тромбов). Поэтому возникает полная несвертываемость крови,
развиваются кровотечения и множественные кровоизлияния.
4-я стадия — восстановительная, или остаточных проявлений,
заключается в дистрофических, некротических и геморрагических
изменениях тканей многих органов. При этом примерно в 50 %
случаев может наступить полиорганная недостаточность (почеч-
ная, печеночная, надпочечниковая, легочная, сердечная), приво-
дящая больных к смерти. При благоприятном исходе заболевания
наступает восстановление поврежденных тканей и восстанавлива-
ются функции органов.
В зависимости от распространенности выделяют варианты
ДВС-синдрома: генерализованный и местный.
В зависимости от продолжительности ДВС-синдрома выделяют
следующие формы:
• острую (от нескольких часов до нескольких суток), проте-
кающую наиболее тяжело, развивается при шоке, характе-
ризуется генерализованным некротическим и геморрагиче-
ским поражением органов с развитием полиорганной не-
достаточности;
92
• подострую (от нескольких дней до недели), развивается ча-
ще при поздних гестозах, лейкозах, злокачественных опухо-
лях. характеризуется локальными или мозаичными тромбо-
геморрагическими повреждениями тканей;
• хроническую (несколько недель и даже месяцев), которая
чаще развивается при аутоиммунных заболеваниях, дли-
тельной интоксикации, при злокачественных опухолях; у
больных отмечаются обычно локальные или мигрирующие
изменения в органах с развитием их медленно прогресси-
рующей недостаточности.
Патологическая анатомия ДВС-синдрома заключается в обра-
зовании в капиллярах и венулах множественных микротромбов,
как правило, состоящих из фибрина, стаза в капиллярах, крово-
излияний, дистрофических и некротических изменений в различ-
ных органах.
НАРУШЕНИЯ ПРОНИЦАЕМОСТИ СТЕНОК СОСУДОВ
При повреждении стенок сосудов или полостей сердца, а также
при повышении сосудистой проницаемости вытекает содержащая-
ся в сосудах или в сердце кровь. Исходя из особенностей и послед-
ствий кровопотери выделяют кровотечение и кровоизлияние.
Кровотечение (haemorrhagia) — выход крови за пределы сосу-
дистого русла или сердца в окружающую среду (наружное крово-
течение), а также в полости тела или в просвет полого органа
(внутреннее кровотечение). Примером наружного кровотечения
являются кровотечение из полости матки (метроррагия), из ки-
шечника (мелена), кровотечения при травмах конечностей или
тканей поверхности тела. Внутренними являются кровотечения в
полость перикарда (гемоперикард), в полости грудной клетки (ге-
моторакс), в брюшную полость (гемоперитонеум).
По источнику кровотечения выделяют:
• артериальное;
• венозное;
• артериально-венозное (смешанное);
• капиллярное;
• паренхиматозное кровотечение (капиллярное из паренхима-
тозных органов);
• сердечное кровотечение.
Кровоизлияние — частный вид кровотечения, при котором вы-
шедшая из сосудов кровь накапливается в окружающих тканях.
Выделяют 4 разновидности кровоизлияния:
• гематома — кровоизлияние, при котором в тканях образует-
ся полость, заполненная кровью;
• кровоподтек — плоское кровоизлияние в коже, подкожной
клетчатке, слизистых оболочках;
• геморрагическое пропитывание (имбибиция) — диффузное
кровоизлияние без четких границ;
93
Рис. 21. Эмиграция эритроцитов (Эр) и сегментоядерных лейкоцитов
(Лц) через стыки эндотелиальных клеток (Эн) из просвета сосудов в ок-
ружающую ткань.
• петехии — точечные кровоизлияния в коже, слизистых и
серозных оболочках и под капсулами внутренних органов.
Механизмы развития кровотечений и кровоизлияний:
• разрыв сосуда или стенки сердца (haemorrhagia per rexin) при
травме, некрозе (инфаркте), аневризме;
• разъедание стенки сосуда (haemorrhagia per diabrosin), что
происходит при воспалении ткани или при злокачествен-
ном росте, например в дне язвы желудка или в опухоли,
при прорастании ворсинами хориона сосудов маточной тру-
бы при внематочной беременности и др.;
• диапедез (haemorrhagia per diapedesin, от греч. dia — через,
pedao — скачу) характеризуется выходом крови из сосуда в
результате повышения проницаемости его стенки без нару-
шения ее целостности. Это один из наиболее частых меха-
низмов кровоизлияния наблюдается при гипоксии, инток-
сикациях, инфекциях, различных коагулопатиях, геморра-
гических диатезах, при гипертоническом кризе, гемофилии
и др. (рис. 21).
Исход кровоизлияния может быть благоприятным, когда излив-
шаяся кровь рассасывается, как, например, при кровоподтеке,
или организовывается, что бывает при гематомах, но может быть
и неблагоприятным, если кровоизлияние происходит в жизненно
94
важные органы — головной мозг, надпочечники. В этом случае
больной может погибнуть или становится инвалидом.
Значение кровотечения обусловлено его видом, выраженно-
стью и продолжительностью. Так, больной может погибнуть при
небольшом кровоизлиянии в область ствола головного мозга и
при острой массивной артериальной кровопотере. Вместе с тем
повторяющиеся в течение длительного времени, но небольшие
кровотечения, например при геморрое или из язвы желудка, обу-
словливают лишь развитие постгеморрагической анемии, сопро-
вождающейся жировой дистрофией паренхиматозных органов.
Большое значение имеет скорость кровотечения — быстрая кро-
вопотеря даже относительно небольших объемов крови (300—
350 мл) приводит больного к смерти, в то время как потеря зна-
чительно больших объемов крови, но на протяжении длительного
времени (маточные или геморроидальные кровотечения) не вы-
зывает тяжелых осложнений, так как в организме успевают раз-
виться компенсаторные процессы.
НАРУШЕНИЯ ЛИМФООБРАЩЕНИЯ
Патологические изменения функций лимфатической системы
тесно связаны с нарушениями кровообращения и усугубляют воз-
никающие при этом изменения в тканях. Среди нарушений лим-
фообращения основную роль играют лимфатическая недостаточ-
ность и лимфостаз.
ЛИМФАТИЧЕСКАЯ НЕДОСТАТОЧНОСТЬ
Лимфатическая недостаточность — состояние при котором ин-
тенсивность образования лимфы превышает способность лимфа-
тических сосудов транспортировать ее в венозную систему. Выде-
ляют следующие виды недостаточности лимфатической системы:
механическую, динамическую и резорбционную.
При механической недостаточности возникает органическое
или функциональное препятствие току лимфы, что происходит
при закупорке лимфатических сосудов опухолевыми клетками,
сидерофагами, сдавлении лимфатических путей опухолью, а так-
же при венозном застое.
Динамическая недостаточность наблюдается при несоответст-
вии между количеством тканевой жидкости и возможностями
лимфатических путей для ее отведения, что имеет место при зна-
чительном повышении проницаемости кровеносных сосудов в
связи с воспалением, аллергическими реакциями, при выражен-
ных отеках тканей.
Резорбционная недостаточность обусловлена уменьшением
проницаемости стенок лимфатических капилляров или измене-
нием дисперсных свойств тканевых белков.
95
ЛИМФОСТАЗ
Лимфостаз — остановка тока лимфы, что происходит при не-
достаточности лимфатической системы вне зависимости от меха-
низма ее развития. Выделяют общий и регионарный лимфостаз.
Общий лимфостаз возникает при общем венозном застое, так
как при этом уменьшается перепад давления между кровью и
лимфой — один из главных факторов, определяющих отток лим-
фы из лимфатических сосудов в венозную систему.
Регионарный лимфостаз развивается при местной венозной ги-
перемии, при закупорке регионарных лимфатических сосудов или
при сдавлении их опухолью.
Последствием лимфостаза является лимфатический отек —
лимфедема. Длительный застой лимфы способствует активации
фибробластов и разрастанию соединительной ткани, что приво-
дит к склерозу органов. Лимфатический отек и склероз тканей
вызывают стойкое увеличение объема органа либо той или иной
части тела — нижних конечностей, половых органов и др., и раз-
вивается заболевание, которое называется слоновостью.
Глава 6
ВОСПАЛЕНИЕ
ОБЩАЯ ХАРАКТЕРИСТИКА ВОСПАЛЕНИЯ
Воспаление — сложная местная реакция организма на повреж->
дение, направленная на уничтожение повреждающего фактора и
восстановление поврежденных тканей, которая проявляется ха->
рактерными изменениями в микроциркуляторном русле и соеди->
нительной ткани.
Признаки воспаления были известны еще древним врачам, ко->
торые считали, что его характеризуют 5 симптомов: краснота (ru-
bor), опухоль тканей (tumor), жар (calor), боль (dolor) и наруше->
ние функций (functio laesa). Для обозначения воспаления к назвав
нию органа, в котором оно развивается, прибавляют окончание
"ит": кардит — воспаление сердца, нефрит — воспаление почки,
гепатит — воспаление печени и т. д.
Биологический смысл воспаления заключается в отграничении
и ликвидации очага повреждения и вызвавших его патогенных
факторов, а также в восстановлении гомеостаза.
Воспаление характеризуется следующими особенностями.
Воспаление — это защитно-приспособительная реакция, воз->
никшая в ходе эволюции. Благодаря воспалению происходит сти->
муляция многих систем организма, он избавляется от инфекци-
96
онного или другого повреждающего фактора; обычно в исходе
воспаления возникает иммунитет и устанавливаются новые взаи->
моотношения с окружающей средой. В результате не только ор->
дельные люди, но и человечество, как биологический вид, при->
спосабливается к изменениям того мира, в котором оно живет, —
атмосферы, экологии, микромира и т. д. Однако у конкретного
человека воспаление иногда может привести к тяжелым осложне->
ниям, вплоть до смерти больного, так как на течение воспали->
тельного процесса влияют особенности реактивности организма
этого человека — его возраст, состояние защитных систем и т. п.
Поэтому воспаление нередко требует медицинского вмешательства.
Воспаление — типовой общепатологический процесс, которым
организм отвечает на самые различные воздействия, поэтому оно
имеет место при большинстве заболеваний и сочетается с други->
ми реакциями.
Воспаление может быть самостоятельным заболеванием в тех
случаях, когда оно составляет основу болезни (например, крупоз->
ной пневмонии, остеомиелита, гнойного лептоменингита и др.).
В этих случаях воспаление имеет все признаки заболевания, т. е.
специфическую причину, своеобразный механизм течения, ос->
ложнения и исходы, что требует целенаправленного лечения.
Воспаление и иммунитет. Между воспалением и иммунитетом
существует как прямая, так и обратная связь, так как оба процесс
са направлены на "очищение" внутренней среды организма от чу->
жеродного фактора или измененного "своего" с последующим ор->
торжением чужеродного фактора и ликвидацией последствий по->
вреждения. В процессе воспаления формируются иммунные ре->
акции, а сам иммунный ответ реализуется через воспаление и от
выраженности иммунного ответа организма зависит течение вос->
паления. Если иммунные средства защиты эффективны. воспале->
ние может вообще не развиться. При возникновении иммунных
реакций гиперчувствительности (см. главу 8) воспаление стано->
вится их морфологическим проявлением — развивается иммун->
ное воспаление (см. ниже).
Для развития воспаления, помимо повреждающего фактора,
необходимо сочетание различных биологически активных ве->
ществ, определенных клеток, межклеточных и клеточно-матрикс-
ных отношений, развитие местных изменений тканей и общих
изменений организма.
Воспаление — это сложный комплекс процессов, который скла->
дывается из трех взаимосвязанных реакций — альтерации (повре->
ждения), экссудации и полиферации. Отсутствие хотя бы одной из
этих трех составляющих реакций не позволяет говорить о воспа->
лении.
Альтерация — повреждение тканей, при котором возникают
разнообразные изменения клеточных и внеклеточных компонен->
тов в месте действия повреждающего фактора.
Экссудация — поступление в очаг воспаления экссудата, т. е.
богатой белком жидкости, содержащей форменные элементы
97
крови, в зависимости от количества которых образуются различи
ные экссудаты.
Промферация — размножение клеток и формирование внекле->
точного матрикса, направленных на восстановление поврежден^
ных тканей.
Необходимым условием развития этих реакций является нали->
чие медиаторов воспаления. Медиаторы воспаления — биологичек
ски активные вещества, обеспечивающие химические и молекуляр->
ные связи между процессами, протекающими в очаге воспаления и
без которых развитие воспалительного процесса невозможно.
Выделяют 2 группы медиаторов воспаления:
Клеточные (или тканевые) медиаторы воспаления, с помощью
которых включается сосудистая реакция и обеспечивается экссу->
дация. Эти медиаторы продуцируются клетками и тканями, осо->
бенно лаброцитами (тучными клетками), базофильными и эози-
нофильными гранулоцитами, моноцитами, макрофагами, лимфо->
цитами, клетками APUD-системы и др. Важнейшими клеточные
ми медиаторами воспаления являются:
• биогенные амины, особенно гистамин и серотонин. вызы->
вающие острую дилатацию (расширение) сосудов микро-
циркуляторного русла, что повышает сосудистую проницаем
мость, способствует отеку ткани, усиливает слизеобразова-
ние и сокращение гладкой мускулатуры;
• кислые липиды, образующиеся при повреждении клеток и
тканей и сами являющиеся источником тканевых медиатор
ров воспаления;
• медленно регулирующая субстанция анафилаксии увеличива->
ет сосудистую проницаемость;
• эозинофильный хемотаксический фактор А повышает сосу
дистую проницаемость и выход в очаг воспаления эозино-
филов;
• фактор активации тромбоцитов стимулирует тромбоциты и
их многогранные функции;
• простагландины обладают широким спектром действия, в
том числе повреждают сосуды микроциркуляции. повыша->
ют их проницаемость, усиливают хемотаксис, способствуют
пролиферации фибробластов.
Плазменные медиаторы воспаления образуются в результате ак->
тивации под влиянием повреждающего фактора и клеточных ме->
диаторов воспаления трех плазменных систем — системы компле~>
мента, системы плазмша (каллекриин-кининовой системы) и
свертывающей системы крови. Все компоненты этих систем нахо-ч
дятся в крови в виде предшественников и начинают функциони->
ровать только под влиянием определенных активаторов.
• Медиаторами кининовой системы являются брадикинин и
калликреин. Брадикинин усиливает сосудистую проницаем
мость, вызывает чувство боли, обладает гипотензивным
свойством. Калликреин осуществляет хемотаксис лейкоцит
тов и активирует фактор Хагемана, включая, таким обра-
98
зом, в воспалительный процесс системы свертывания крови
и фибринолиза.
• Фактор Хагемана, ключевой компонент системы свертывав
ния крови, инициирует свертываемость крови, активирует
другие плазменные медиаторы воспаления, повышает про->
ницаемость сосудов, усиливает миграцию нейтрофильных
лейкоцитов и агрегацию тромбоцитов.
• Система комплемента состоит из группы специальных белков
плазмы крови, вызывающих лизис бактерий и клеток, ком-"
поненты комплемента СЗЬ и С5Ь повышают проницаемость
сосудов, усиливают движение к очагу воспаления полиморф-"
но-ядерных лейкоцитов (ПЯЛ), моноцитов и макрофагов.
Реактанты острой фазы — биологически активные белковые
вещества, благодаря которым в воспаление включаются не только
система микроциркуляции и иммунная система, но и другие сис->
темы организма, в том числе эндокринная и нервная. Среди ре-
актантов острой фазы наибольшее значение имеют:
С-реактивный белок, концентрация которого в крови увеличи-"
вается при воспалении в 100—1000 раз, активирует цитолитиче-
скую активность Т-лимфоцитов-киллеров, замедляет агрегацию
тромбоцитов;
интерлейкин-1 (ИЛ-1), влияет на активность многих клеток
очага воспаления, особенно Т-лимфоцитов, ПЯЛ, стимулирует
синтез простагландинов и простациклинов в эндотелиальных
клетках, способствует гемостазу в очаге воспаления;
Т-кининоген является предшественником плазменных медиаторов
воспаления — кининов, ингибирует (-цистеиновые протеиназы.
Таким образом, в очаге воспаления возникает гамма очень
сложных процессов, которые не могут долго протекать автоном-"
но, не являясь сигналом для включения различных систем орга->
низма. Такими сигналами являются накопление и циркуляция в
крови биологически активных веществ, кининов, компонентов
комплемента, простагландинов, интерферона и др. В результате
этого в воспаление вовлекаются система кроветворения, иммун->
пая, эндокринная, нервная системы, т. е. организм в целом. По-1
этому в широком плане воспаление следует рассматривать как
местное проявление общей реакции организма.
Воспаление обычно сопровождает интоксикация. Она связана
не только с самим воспалением, но и с особенностями повреж->
дающего фактора, прежде всего инфекционного агента. По мере
увеличения площади повреждения и выраженности альтерации
усиливается всасывание токсичных продуктов и нарастает интою
сикация, которая угнетает различные защитные системы организм
ма — иммунокомпетентную, кроветворную, макрофагальную
и др. Интоксикация часто оказывает определяющее влияние на
течение и характер воспаления. С этим в первую очередь связана
недостаточная эффективность воспаления, например, при остром
разлитом перитоните, ожоговой болезни, травматической болезни
и многих хронических инфекционных заболеваниях.
99
ПАТОФИЗИОЛОГИЯ И МОРФОЛОГИЯ ВОСПАЛЕНИЯ
В своем развитии воспаление проходит 3 стадии, последова->
тельность которых и определяет течение всего процесса.
СТАЛИЯ АЛЬТЕРАЦИИ
А. Стадия альтерации (повреждения) — начальная, пусковая
стадия воспаления, характеризующаяся повреждением тканей.
В этой стадии развивается хелюаттракция, т. е. привлечение к
очагу повреждения клеток, продуцирующих медиаторы воспале->
ния, необходимые для включения в процесс сосудистой реакции.
Хемоаттрактанты — вещества, определяющие направление дви->
жения клеток в тканях. Они продуцируются микробами, клетка->
ми, тканями, содержатся в крови. Непосредственно после повре->
ждения из тканей выделяются такие хемоаттрактанты, как просе-
ринэстераза, тромбин, кинин, а при повреждении сосудов —
фибриноген, активированные компоненты комплемента.
В результате совокупной хемоаттракции в зоне повреждения
возникает первичная кооперация клеток, продуцирующих медиато-i
ры воспаления, — скопление лаброцитов, базофильных и эозино-
фильных гранулоцитов, моноцитов, клеток APUD-системы и др.
Только находясь в очаге повреждения, эти клетки обеспечивают
выброс тканевых медиаторов и начало воспаления.
В результате действия тканевых медиаторов воспаления в зоне
повреждения происходят следующие процессы:
• повышается проницаемость сосудов микроциркуляторного
русла;
• в соединительной ткани развиваются биохимические изме->
нения приводящие к задержке в тканях воды и к набуханию
внеклеточного матрикса;
• инициальная активация плазменных медиаторов воспале->
ния под влиянием повреждающего фактора и тканевых ме->
диаторов;
• развитие дистрофических и некротических изменений тка->
ней в зоне повреждения;
• высвобождающиеся из клеточных лизосом и активирую->
щиеся в очаге воспаления гидролазы (протеазы, липазы,
фосфолипазы, эластазы, коллагеназы) и другие ферменты
играют существенную роль в развитии повреждений клеток
и неклеточных структур;
• нарушения функций, как специфических — того органа, в
котором возникла альтерация, так и неспецифических —
терморегуляции, местного иммунитета и др.
СТАДИЯ ЭКССУДАЦИИ
Б. Стадия экссудации наступает в разные сроки вслед за по->
вреждением тканей в ответ на действие клеточных и особенно
100
Рис. 22. Краевое состояние сегментоядерного лейкоцита (Лц).
плазменных медиаторов воспаления, образующихся при акгива->
ции кининовой, комплементарной и свертывающей систем кро->
ви. В динамике стадии экссудации различают 2 этапа: плазмати->
ческая экссудация и клеточная инфильтрация.
Плазматическая экссудация обусловлена первоначальным рас->
ширением сосудов микроциркуляторного русла, усилением при->
тока крови к очагу воспаления (активная ), что приводит к повы->
шению гидростатического давления в сосудах. Активная способ^
ствует развитию оксигенации очага воспаления, в результате чего
возникают следующие процессы:
• образование активных форм кислорода;
• приток гуморальных факторов защиты — комплемента,
фибронектина, пропердина и др.;
• приток ПЯЛ, моноцитов, тромбоцитов и других клеток крови.
Клеточная инфильтрация — поступление в зону воспаления
различных клеток, прежде всего клеток крови, что связано с за->
медлением кровотока в венулах (пассивная ) и действием медиа->
торов воспаления. При этом развиваются следующие процессы:
• лейкоциты перемещаются на периферию осевого потока крови;
• катионы плазмы крови Са2+, Мп и Mg2+ снимают отрицав
тельный заряд клеток эндотелия и лейкоцитов и лейкоциты
прилипают к стенке сосуда (адгезия лейкоцитов);
• возникает краевое состояние лейкоцитов, т. е. остановка их у
стенки сосудов (рис. 22);
101
Рис. 23. Эмиграция сегментоядерного лейкоцита из просвета (Пр) сосу->
да. Сегментоядерный лейкоцит (Лц) располагается под эндотелиальной
клеткой (Эн) около базальной мембраны (БМ) сосуда.
• сокращение эндотелиальных клеток и раскрытие межэндо-
телиальных щелей;
• выброс лейкоцитами псевдоподий под эндотелий и переме->
щение затем в подэндотелиальное пространство всей клетки
(рис. 23);
• молекулярные изменения базальной мембраны, которые no-i
зволяют лейкоцитам преодолевать стенку сосуда и поступать
в зону воспаления. Этот механизм характерен для всех кле-i
ток крови, включая эритроциты, и занимает несколько часов.
В течение первых 6—24 ч из сосудов выходят лейкоциты, че->
рез 24—48 ч преобладает эмиграция из сосудов моноцитов и
лимфоцитов. Такой порядок эмиграции клеток во многом за->
висит от причины воспаления. Так, при вирусных инфекции
ях и туберкулезе первыми в зону воспаления мигрируют лим->
фоциты. при иммунном воспалении — эозинофилы и т. д.
Тромбоз мелких сосудов в зоне воспаления развивается в резуль-ч
тате активации плазменных медиаторов воспаления, особенно
свертывающей системы крови, а также повреждения клеток эндо->
телия интимы сосудов, что приводит к активации тромбоцитов.
Это способствует развитию:
• ишемии стенок сосудов, что повышает их проницаемость;
• ишемии тканей зоны воспаления, что способствует развитию
в них ацидоза, дистрофических и некротических изменений;
102
• препятствует оттоку экссудата, токсинов т «
очага воспаления и быстрому нарастанию и пок^кашп^и
распространению инфекции (оксикации и
Т] омбоз сосудов зоны воспаления развивается лиспе эмигпя
ции клеток крови в очаг воспаления после эмигра-
Взаимоденствие клеток в очаге воспаления j п .
ядсрные лейкоциты обычно первыми поступав т в ПоЛиморФно~
ния. Их функции: очаг воспале-
— отграничение очага воспаления;
— локализация и уничтожение патогенного факта
— создание кислой среды в очаге воспаления с п’
броса (экзоцитоза) гранул, содержащих гидролазы Помощью вы~
2. Макрофаги, особенно резидентные, поЯадяютс
вреждения еще до развития воспаления. Их Фунг,™,
гообразны. что делает макрофаги одной из главных ^^XSna"
лительнои реакции: клеток воспа-
— они осуществляют фагоцитоз повреждающего а
— выявляют антигенную природу патогенного dnJeHTa’
- индуцируют иммунные реакции и участие иммганой смете
мы в воспалении; муннои смете
— обеспечивают неГпрализацию токсинов в очаге
— обеспечивают многообразные межклеточн.,.1 воспалс,|»я;
вия, прежде всего с ПЯЛ, лимфоцитами, моцОии
стами; пиитами фибробла-
- взаимодействуя с ПЯЛ, обеспечивают фагоШ1тоз повоеж
дающего агента; «митоз повреж-
взаимодеиствие макрофагов и лимфоцн cnocoEk.TRVeT
развитию реакции гиперчувствителвнести замел г, ’
(ГЗТ) в виде иммунного цитолиза и 1ранулематоза- ецного тапа
- взаимодействие макрофагов и ФибробЛастов’
стимуляцию образования коллагена и различных фиб Н° На
3. Моноциты являются предшественниками v' 1
купируют в крови, выходят в оча! воспаления r™.?aroD цир‘
в макрофаги. * ТраРеформируясь
4. Клетки иммунной системы — Т- и П-Лил,Л„„
тические клетки: ^Фоциты, плазма-
- различные субпопуляции Т-лимЦюцитов определяют акти1!
ность иммунной реакции; наделяют актив-
— Т-яимфониты-киллеры обеспечивают гибел> би
патогенных факторов, обладают цитолитическим ” 1огических
отношению к собственным клеткам организма свойством по
— В-лимфоциты и плазмоциты участвуют в
фических антител (см. главу 8), обеспечивающих работке спе11И'
вреждающего фактора мквидацию по-
5. Фибробласты являются основными продуцентя
и эластина, составляющих основу соединительной 'И кол^гена
ляются уже на начальных этапах воспаления под rL? ™' Ояв~
кинов макрофагов, в значительной степени обегл^,. нием цито‘
новление поврежденных тканей. и аю восста-
103
6. Другие клетки (эозинофилы, эритроциты), появление кото-
рых зависит от причины воспаления.
Все эти клетки, а также внеклеточный матрикс, компоненты
соединительной ткани взаимодействуют между собой благодаря
многочисленным активным веществам, определяющим клеточ-
ную и внеклеточную рецепцию — цитокинам и факторам роста.
Реагируя с рецепторами клеток и внеклеточного матрикса, они
активируют или ингибируют функции клеток, участвующих в
воспалении.
Лимфомикрососудистая система участвует в воспалении син-
хронно с гемомикроциркуляторным руслом. При выраженной
инфильтрации клеток и пропотевании плазмы крови в области
венулярного звена микроциркуляторного русла вскоре в процесс
вовлекаются корни "ультрациркуляторной" системы интерстици-
альной ткани — интерстициальные каналы. В результате в зоне
воспаления происходит:
— нарушение кроветканевого баланса;
— изменение внесосудистой циркуляции тканевой жидкости;
— возникновение отека и набухания ткани;
— развивается лимфостаз. в результате чего лимфатические
капилляры переполняются лимфой. Она выходит в окружающие
ткани и возникает острый лимфатический отек.
Некроз тканей является важным компонентом воспаления, так
как несет несколько функций:
— в очаге некроза вместе с гибнущими тканями должен погиб-
нуть патогенный фактор;
— при определенной массе некротизированных тканей появ-
ляются биологически активные вещества, включающие различ-
ные интегративные механизмы регуляции воспаления, в том чис-
ле и реактанты острой фазы, и систему фибробластов;
— способствует активации иммунной системы, которая регу-
лирует утилизацию измененных "своих" тканей.
ПРОДУКТИВНАЯ (ПРОЛИФЕРАТИВНАЯ) СТАДИЯ
Продуктивная (пролиферативная) стадия завершает острое
воспаление и обеспечивает репарацию (восстановление) повреж-
денных тканей. В эту стадию происходят следующие процессы:
— уменьшается воспаленной ткани;
— снижается интенсивность эмиграции форменных элементов
крови;
— уменьшается количество лейкоцитов в зоне воспаления;
— очаг воспаления постепенно заполняют макрофаги гемато-
генного происхождения, которые выделяют интерлейкины — хе-
моаттрактанты для фибробластов и стимулирующие, кроме того,
новообразование сосудов;
— происходит размножение в очаге воспаления фибробластов:
— скопление в очаге воспаления клеток иммунной системы —
Т- и В-лимфоцитов, плазмоцитов;
104
— образование воспалительного инфильтрата — скопление ука-
занных клеток при резком уменьшении жидкой части экссудата;
— активация анаболических процессов — интенсивности син-
теза ДНК и РНК, основного вещества и фибриллярных структур
соединительной ткани;
— "очищение" поля воспаления за счет активации гидролаз
лизосом моноцитов, макрофагов, гистиоцитов и других клеток;
— пролиферация эндотелиоцитов сохранившихся сосудов и
образование новых сосудов;
— формирование грануляционной ткани после ликвидации
некротического детрита.
Грануляционная ткань — незрелая соединительная ткань, харак-
теризующаяся скоплением клеток воспалительного инфильтрата и
особой архитектоникой вновь образованных сосудов, растущих вер-
тикально до поверхности повреждения, а затем вновь опускающихся
в глубину. Участок поворота сосудов выглядит как гранула, что и да-
ло название ткани. По мере очищения очага воспаления от некро-
тических масс грануляционная ткань заполняет всю зону поврежде-
ния. Она обладает большой резорбционной способностью, но в то
же время представляет собой барьер для возбудителей воспаления.
Воспалительный процесс заканчивается созреванием грануля-
ций и образованием зрелой соединительной ткани.
ФОРМЫ ОСТРОГО ВОСПАЛЕНИЯ
Клинико-анатомические формы воспаления определяются по
преобладанию в его динамике либо экссудации, либо пролифера-
ции над другими реакциями, составляющими воспаление. В зави-
симости от этого выделяют:
• экссудативное воспаление;
• продуктивное (или пролиферативное) воспаление.
По течению различают:
• острое воспаление — длится не более 4—6 нед;
• хроническое воспаление — длится более 6 нед, вплоть до
нескольких месяцев и лет.
По патогенетической специфике выделяют:
• обычное (банальное) воспаление;
• иммунное воспаление.
ЭКССУДАТИВНОЕ ВОСПАЛЕНИЕ
Экссудативное воспаление характеризуется образованием экс-
судатов, состав которых определяется главным образом:
• причиной воспаления;
• ответной реакцией организма на повреждающий фактор и
его особенности;
• экссудат определяет и название формы экссудативного вос-
паления.
105
1. Серозное воспаление характеризуется образованием серозно-
го экссудата — мутноватой жидкости, содержащей до 2—2 5 %
белка и небольшое количество клеточных элементов — лейкоци-
тов, лимфоцитов, слущенных эпителиальных клеток.
Причинили серозного воспаления являются:
• действие физических и химических факторов (например,
отслоение эпидермиса с образованием пузыря при ожоге);
• действие токсинов и ядов, вызывающих резкую плазморра-
гию (например, пустулы на коже при натуральной оспе);
• выраженная интоксикация, сопровождающаяся гиперрёак-
тивностью организма, что вызывает серозное воспаление в
строме паренхиматозных органов — так называемое межу-
точное воспаление.
Локализация серозного воспаления — слизистые и серозные
оболочки, кожа, интерстициальная ткань, клубочки почек, пери-
синусоидальные пространства печени.
Исход обычно благоприятный — экссудат рассасывается и
структура поврежденных тканей восстанавливается. Неблагопри-
ятный исход связан с осложнениями серозного воспаления’ на-
пример, серозный экссудат в мягких мозговых оболочках (сероз-
ный лептоменингит) может сдавливать головной мозг, серозное
пропитывание альвеолярных септ легких является одной из при-
чин острой дыхательной недостаточности. Иногда после серозно-
го воспаления в паренхиматозных органах развивается диффузный
склероз их стромы.
2. Фибринозное воспаление характеризуется образованием фиб-
ринозного экссудата, содержащего, помимо лейкоцитов, моноци-
тов, макрофагов, распадающихся клеток воспаленной ткани,
большое количество фибриногена, который выпадает в виде
свертков фибрина. Поэтому в фибринозном экссудате содержа-
ние белка составляет 2,5—5 %.
Причинили фибринозного воспаления может быть разнообраз-
ная микробная флора: токсигенные коринебактерии дифтерии,
различные кокки, микобактерии туберкулеза, некоторые шигел-
лы — возбудители дизентерии, эндогенные и экзогенные токси-
ческие факторы и др.
Локализация фибринозного воспаления — слизистые и сероз-
ные оболочки.
Морфогенез. Экссудации предшествует некроз ткани и агрегация
тромбоцитов в очаге воспаления. Фибринозный экссудат пропиты-
вает мертвые ткани, образуя светло-серую пленку, под которой
располагаются микробы, выделяющие токсины. Толщина пленки
определяется глубиной некроза, а сама глубина некроза зависит от
структуры эпителиальных или серозных покровов и особенностей
подлежащей соединительной ткани. Поэтому в зависимости от глу-
бины некроза и толщины фибринозной пленки выделяют 2 вида
фибринозного воспаления: крупозное и дифтеритическое.
Крупозное воспаление в виде тонкой, легко снимающейся фиб-
ринозной пленки развивается на однослойном эпителиальном по-
106
Рис 24. Фибринозное воспаление. Дифге-
ритическая ангина, крупозный ларингит и
трахеит.
крове слизистых или серозных оболо-
чек, расположенных на тонкой плот-
ной соединительнотканной основе.
После снятия фибринозной пленки не
образуется дефекта подлежащих тканей.
Крупозное воспаление развивается на
слизистой оболочке трахеи и бронхов,
на эпителиальной выстилке альвеол,
на поверхности плевры, брюшины, пе-
рикарда при фибринозном трахеите и
бронхите, крупозной пневмонии, пери-
тоните, перикардите и т. п. (рис. 24).
Дифтеритическое воспаление, раз-
вивающееся на поверхностях, выстлан-
ных плоским или переходным эпите-
лием, а также другими видами эпите-
лия, расположенными на рыхлой и -
широкой соединительнотканной осно-
ве. Такая структура ткани обычно спо-
собствует развитию глубокого некроза
и образованию толстой, трудно сни-
мающейся фибринозной пленки, после удаления которой остают-
ся язвы. Дифтеритическое воспаление развивается в зеве, на сли-
зистых оболочках пищевода, желудка, кишечника, матки и влага-
лища, мочевого пузыря, в ранах кожи и слизистых оболочек.
Исход фибринозного воспаления может быть благоприятным:
при крупозном воспалении слизистых оболочек фибринозные
пленки расплавляются под влиянием гидролаз лейкоцитов и на
их месте восстанавливается исходная ткань. Дифтеритическое
воспаление заканчивается образованием язв, которые иногда мо-
гут заживать с образованием рубцов. Неблагоприятным исходом
фибринозного воспаления является организация фибринозного
экссудата, образование спаек и шварт между листками серозных
полостей вплоть до их облитерации, например полости перикар-
да, плевральных полостей.
3. Гнойное воспаление характеризуется образованием гнойного
экссудата, который представляет собой сливкообразную массу,
состоящую из детрита тканей очага воспаления, дистрофически
измененных клеток, микробов, большого количества форменных
элементов крови, основную массу которых составляют живые и
погибшие лейкоциты, а также лимфоцитов, моноцитов, макрофа-
гов, часто эозинофильных гранулоцитов. Содержание белка в
гное составляет 3—7 %. pH гноя 5.6—6.9. Гной имеет специфиче-
ский запах, синевато-зеленоватую окраску с различными оттен-
ками. Гнойный экссудат обладает рядом качеств, определяющих
107
биологическую значимость гнойного воспаления; содержит раз-
личные ферменты, в том числе протеазы, расщепляющие погиб-
шие структуры, поэтому в очаге воспаления характерен лизис
тканей; содержит наряду с лейкоцитами, способными фагоцити-
ровать и убивать микробы, различные бактерицидные факторы —
иммуноглобулины, компоненты комплемента, белки и др. Поэто-
му гной задерживает рост бактерий и уничтожает их. Через 8—
12 ч лейкоциты гноя погибают, превращаясь в "гнойные тельца".
Причиной гнойного воспаления являются гноеродные микро-
бы — стафилококки, стрептококки, гонококки, брюшнотифозная
палочка и др.
Локализация гнойного воспаления — любые ткани организма и
все органы.
Формы гнойного воспаления. Абсцесс — отграниченное гнойное
воспаление, сопровождающееся образованием полости, заполненной
гнойным экссудатом. Полость ограничена пиогенной капсулой —
грануляционной тканью, через сосуды которой поступают лейко-
циты. При хроническом течении абсцесса в пиогенной мембране
образуются два слоя: внутренний, состоящий из грануляционной
ткани, и наружный, образующийся в результате созревания грану-
ляционной ткани в зрелую соединительную ткань. Абсцесс обычно
заканчивается опорожнением и выходом гноя на поверхность тела,
в полые органы или полости через свищ — канал, выстланный гра-
нуляционной тканью или эпителием, соединяющий абсцесс с по-
верхностью тела или с его полостями. После прорыва гноя полость
абсцесса рубцуется. Изредка абсцесс подвергается инкапсуляции.
Флегмона — неотграниченное, диффузное гнойное воспале-
ние, при котором гнойный экссудат пропитывает и расслаивает
ткани. Флегмона обычно образуется в подкожной жировой клет-
чатке, межмышечных прослойках и т. п. Флегмона может быть
мягкой, если преобладает лизис некротизированных тканей, и
твердой, когда во флегмоне возникает коагуляционный некроз
тканей, которые постепенно отторгаются. В некоторых случаях
гной может стекать под влиянием силы тяжести в нижележащие
отделы по ходу мышечно-сухожильных влагалищ, нервно-сосуди-
стых пучков, жировых прослоек и образовывать вторичные, так
называемые холодные абсцессы, или натечники. Флегмонозное
воспаление может распространяться на сосуды, вызывая тромбоз
артерий и вен (тромбофлебиты, тромбартерииты, лимфангииты).
Заживление флегмоны начинается с ее ограничения с последую-
щим образованием грубого рубца.
Элпиели — гнойное воспаление полостей тела или полых ор-
ганов. Причиной эмпиемы являются как гнойные очаги в сосед-
них органах (например, абсцесс легкого и эмпиема плевральной
полости), так и нарушение оттока гноя при гнойном воспалении
полых органов — желчного пузыря, червеобразного отростка, ма-
точной трубы и т. д. При длительном течении эмпиемы происхо-
дит облитерация полого органа или полости.
Гнойная рана — особая форма гнойного воспаления, которая
108
возникает либо вследствие нагноения травматической, в том чис-
ле хирургической, раны, либо в результате вскрытия во внешнюю
среду очага гнойного воспаления и образования раневой поверх-
ности, покрытой гнойным экссудатом.
4. Гнилостное, или ихорозное, воспаление развивается при по-
падании гнилостной микрофлоры в очаг гнойного воспаления с
выраженным некрозом тканей. Обычно возникает у ослабленных
больных с обширными, длительно не заживающими ранами или
хроническими абсцессами. При этом гнойный экссудат приобре-
тает особо неприятный запах гниения. В морфологической кар-
тине превалирует некроз тканей без склонности к отграничению.
Некротизированные ткани превращаются в зловонную массу, что
сопровождается нарастающей интоксикацией.
5. Геморрагическое воспаление является формой серозного,
фибринозного или гнойного воспаления и характеризуется особо
высокой проницаемостью сосудов микроциркуляции, диапедезом
эритроцитов и их примесью к уже имеющемуся экссудату (сероз-
но-геморрагическое, гнойно-геморрагическое воспаление). При-
месь эритроцитов в результате превращений гемоглобина придает
экссудату черный цвет.
Причиной геморрагического воспаления обычно является очень
высокая интоксикация, сопровождающаяся резким повышением
проницаемости сосудов, что наблюдается, в частности, при таких
инфекциях, как чума, сибирская язва, при многих вирусных ин-
фекциях, натуральной оспе, при тяжелых формах гриппа и др.
Исход геморрагического воспаления обычно зависит от его
этиологии.
6. Катаральное воспаление развивается на слизистых оболочках
и характеризуется примесью слизи к любому экссудату, поэтому
оно, как и геморрагическое, не является самостоятельной фор-
мой воспаления.
Причиной катарального воспаления могут быть различные ин-
фекции. продукты нарушенного метаболизма, аллергические раз-
дражители, термические и химические факторы. Например, при
аллергическом рините слизь примешивается к серозному экссуда-
ту (катаральный ринит), нередко наблюдается гнойный катар
слизистой оболочки трахеи и бронхов (гнойно-катаральный тра-
хеит или бронхит) и т. п.
Исход. Острое катаральное воспаление продолжается 2—3 нед
и, заканчиваясь, не оставляет следов. Хроническое катаральное
воспаление может привести к атрофическим или гипертрофиче-
ским изменениям слизистой оболочки.
ПРОДУКТИВНОЕ ВОСПАЛЕНИЕ
Продуктивное (пролиферативное) воспаление характеризуется
преобладанием пролиферации клеточных элементов над экссуда-
цией и альтерацией. Выделяют 4 основные формы продуктивного
воспаления:
109
Рис 25. Сыпнотифозная гранулема Попова. Скопление гистиоцитов и
глиальных клеток на месте разрушенного сосуда.
1. Гранулематозное воспаление может протекать остро и хро-
нически, однако наибольшее значение имеет хроническое тече-
ние процесса.
Острое гранулематозное воспаление наблюдается, как правило,
при острых инфекционных заболеваниях — сыпном тифе, брюш-
ном тифе, бешенстве, эпидемическом энцефалите, остром перед-
нем полиомиелите и др. (рис. 25).
Патогенетической основой острого гранулематозного воспале-
ния обычно является воспаление сосудов микроциркуляции при
воздействии инфекционных агентов или их токсинов, что сопро-
вождается ишемией периваскулярной ткани.
Морфология острого гранулематозного воспаления. В нерв-
ной ткани морфогенез гранулем определяется некрозом груп-
пы нейронов или ганглиозных клеток, а также мелкоочаговыми
некрозами вещества головного или спинного мозга, окруженны-
ми глиальными элементами, несущими функцию фагоцитов.
При брюшном тифе морфогенез гранулем обусловлен
скоплением фагоцитов, трансформировавшихся из ретикулярных
клеток в групповых фолликулах тонкой кишки. Эти крупные клет-
ки фагоцитируют S. typhi, а также детрит, образующийся в соли-
тарных фолликулах. Тифозные гранулемы подвергаются некрозу.
Исход острого гранулематозного воспаления может быть бла-
гоприятным, когда гранулема исчезает без следа, как при брюш-
ном тифе, или после нее остаются небольшие глиальные рубчи-
ки, как при нейроинфекциях. Неблагоприятный исход острого
гранулематозного воспаления связан в основном с его осложне-
ниями — перфорацией кишки при брюшном тифе либо с гибе-
лью большого количества нейронов с тяжелыми последствиями.
2. Интерстициальное диффузное, или межуточное, воспаление
НО
локализуется в строме паренхиматозных органов, где происходит
накопление мононуклеаров — моноцитов, макрофагов, лимфоци-
тов. В паренхиме при этом развиваются дистрофические и некро-
биотические изменения.
Причиной воспаления могут быть либо различные инфекцион-
ные агенты, либо оно может возникать как реакция мезенхимы
органов на токсические воздействия или микробную интоксика-
цию. Наиболее яркая картина межуточного воспаления наблюда-
ется при интерстициальной пневмонии, межуточном миокардите,
интерстициальных гепатите и нефрите.
Исход интерстициального воспаления может быть благоприят-
ным, когда происходит полное восстановление межуточной ткани
органов и неблагоприятным, когда строма органа склерозируется,
что обычно происходит при хроническом течении воспаления.
3. Гиперпластические (гиперрегенераторные) разрастания —
продуктивное воспаление в строме слизистых оболочек, при ко-
тором происходит пролиферация клеток стромы, сопровождаю-
щаяся скоплением эозинофилов, лимфоцитов, а также гиперпла-
зией эпителия слизистых оболочек. При этом образуются полипы
воспалипельного происхождения — полипозный ринит, полипо-
зный колит и т. п.
Гиперпластические разрастания возникают также на границе
слизистых оболочек с плоским или призматическим эпителием в
результате постоянного раздражающего действия отделяемого
слизистых оболочек, например, прямой кишки или женских по-
ловых органов. При этом эпителий мацерируется, а в строме воз-
никает хроническое продуктивное воспаление, приводящее к об-
разованию остроконечных кондилом
4. Воспаление вокруг животных паразитов и инородных тел ха-
рактеризуется продуктивной воспалительной реакцией, направ-
ленной на отграничение раздражителей от окружающих тканей
путем образования вокруг них соединительнотканной капсулы,
т. е. они не могут быть фагоцитированы и элиминированы. По-
этому вокруг инородных тел. например осколка снаряда, образу-
ется грануляционная ткань и инфильтрат из фибробластов, лим-
фоцитов, макрофагов и гигантских клеток инородных тел. Неко-
торые инородные тела (например, остатки шовного материала
после операции) могут быть ликвидированы в динамике продук-
тивного воспаления с помощью макрофагов и гигантских клеток.
При воспалении вокруг животных паразитов (трихинелл, цисти-
церков, эхинококков и др.) к указанному инфильтрату добавля-
ются эозинофильные гранулоциты.
Исходом воспаления может быть образование рубца: погибшие
животные паразиты нередко петрифицируются.
ИММУННОЕ ВОСПАЛЕНИЕ
Иммунное воспаление — вид воспаления, причиной которого
первоначально является реакция иммунной системы. Это поня-
111
тие ввел А. И. Струков (1979), который показал, что морфологи-
ческой основой реакций ггтерчувствительности немедленного ти-
па (анафилаксия, феномен Артюса и др.), а также гиперчувстви-
тельности замедленного типа (туберкулиновая реакция) является
воспаление. В связи с этим и пусковым механизмом такого вос-
паления становится повреждение тканей иммунными комплекса-
ми антиген—антитело, компонентами комплемента и ряда медиа-
торов иммунитета.
При реакции гиперчувствительности немедленного типа эти
изменения развиваются в определенной последовательности:
1) образование иммунных комплексов антиген—антитело в
просветах венул:
2) связывание этих комплексов с комплементом;
3) хемотаксическое действие иммунных комплексов на ПЯЛ и
скопление их около вен и капилляров;
4) фагоцитоз и переваривание иммунных комплексов лейко-
цитами;
5) повреждение иммунными комплексами и лизосомами лейко-
цитов стенок сосудов, с развитием в них фибриноидного некроза,
периваскулярных кровоизлияний и отека окружающих тканей.
В результате в зоне иммунного воспаления развивается экссуда-
тивно-некротическаяреакиияс серозно-геморрагическим экссудатом.
При реакции гиперчувствительности замедленного типа, кото-
рая развивается в ответ на находящийся в тканях антиген, после-
довательность процессов несколько иная:
1) Т-лимфоциты и макрофаги выселяются в ткань, находят ан-
тиген и уничтожают его, разрушая при этом и ткани, в которых
находится антиген;
2) в зоне воспаления скапливается лимфомакрофагальный ин-
фильтрат, нередко с гигантскими клетками и небольшим количе-
ством ПЯЛ;
3) изменения микроциркуляторного русла выражены слабо;
4) это иммунное воспаление протекает по типу продуктивно-
го, чаще всего гранулематозного, иногда межуточного и характе-
ризуется затяжным течением.
ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ
Хроническое воспаление — патологический процесс, характери-
зующийся персистенцией патологического фактора, развитием в
связи с этим иммунологической недостаточности, что обусловливает
своеобразие морфологических изменений тканей в области воспале-
ния, течение процесса по принципу порочного круга, затруднение
репарации и восстановления гомеостаза. По существу хроническое
воспаление является проявлением возникшего дефекта в системе за-
щиты организма к изменившимся условиям его существования.
Причиной хронического воспаления является в первую очередь
постоянное действие (персистенция) повреждающего фактора,
которое может быть связано как с особенностями этого фактора
112
(например, устойчивость против гидролаз лейкоцитов), так и с
недостаточностью механизмов воспаления самого организма (па-
тологией лейкоцитов, угнетением хемотаксиса, нарушением ин-
нервации тканей или их аутоиммунизацией и т. п.).
Патогенез. Персистенция раздражителя постоянно стимулирует
иммунную систему, что приводит к ее срыву и появлению на оп-
ределенном этапе воспаления комплекса иммунопатологических
процессов, прежде всего появление и нарастание иммунодефицита,
иногда также к аутоиммунизации тканей, и этот комплекс уже сам
обусловливает хронизацию воспалительного процесса.
У больных развивается лимфоцитопатия, в том числе снижается
уровень Т-хелперов и Т-супрессоров, нарушается их соотношение,
одновременно повышается уровень образования антител, увеличи-
вается концентрация в крови циркулирующих иммунных комплек-
сов (ЦИК), комплемента, что приводит к повреждению сосудов
микроциркуляции и развитию васкулитов. При этом снижается
способность организма к выведению иммунных комплексов. Пада-
ет также способность лейкоцитов к хемотаксису из-за накопления
в крови продуктов распада клеток, микробов, токсинов, иммунных
комплексов, особенно при обострении воспаления.
Морфогенез. Зона хронического воспаления обычно заполнена
грануляционной тканью со сниженным числом капилляров. Ха-
рактерны продуктивные васкулиты, а при обострении процесса
васкулиты носят гнойный характер. В грануляционной ткани
множественные очаги некроза, лимфоцитарный инфильтрат, уме-
ренное количество нейтрофильных лейкоцитов, макрофагов и
фибробластов, содержатся также иммуноглобулины. В очагах хро-
нического воспаления нередко обнаруживаются микробы, но при
этом остается сниженным количество лейкоцитов и их бактери-
цидная активность. Нарушены также и регенераторные процес-
сы — мало эластических волокон, в формирующейся соедини-
тельной ткани преобладает нестойкий коллаген Ш типа, мало кол-
лагена IV типа, необходимого для построения базальных мембран.
Общим признаком хронического воспаления является наруше-
ние циклического течения процесса в виде постоянного наслаива-
ния одной стадии на другую, прежде всего стадий альтерации и
экссудации на стадию пролиферации. Это ведет к постоянным
рецидивам и обострениям воспаления и невозможности репара-
ции поврежденных тканей и восстановления гомеостаза.
Этиология процесса, особенности структуры и функции орга-
на, в котором развивается воспаление, реактивность и другие
факторы накладывают отпечаток на течение и морфологию хро-
нического воспаления. Поэтому клинические и морфологические
проявления хронического воспаления разнообразны.
Хроническое гранулематозное воспаление развивается в тех слу-
чаях, когда организм не может уничтожить патогенный агент, но
в то же время имеет возможность ограничить его распростране-
ние, локализовать в определенных участках органов и тканей.
Наиболее часто оно возникает при инфекционных заболеваниях,
113
a
Рис 26. Сифилитическая Гумма печени. На границе с участком творо-
жистого некроза (а) специфические рубцующиеся грануляции (6) с боль-
шим количеством сосудов.
таких как туберкулез, сифилис, лепра, сап и некоторые другие,
которые имеют ряд общих клинических, морфологических и им-
мунологических особенностей. Поэтому такое воспаление неред-
ко называют специфическим воспалением.
По этиологии выделяют 3 группы гранулем:
1) инфекционные, такие как гранулемы при туберкулезе, си-
филисе, актиномикозе, сапе и др.;
2) гранулемы инородных тел — крахмальные, тальковые, шов-
ные и др.;
3) гранулемы неизвестной природы, например при саркоидозе,
эозинофильные, аллергические и др.
Морфология. Гранулемы представляют собой компактное ско-
пление макрофагов и/или эпителиоидных клеток, обычно гигант-
ских многоядерных клеток типа Пирогова—Лангханса или типа
инородных тел. По преобладанию тех или иных типов макрофа-
гов выделяют гранулемы макрофагальные (рис. 26) и эпителиоид-
ноклеточные (рис. 27). Оба типа гранулем сопровождаются ин-
фильтрацией другими клетками — лимфоцитами, плазматически-
ми, нередко нейтрофильными или эозинофильными лейкоцита-
ми. Характерны также наличие фибробластов и развитие склеро-
за. Часто в центре гранулем возникает казеозный некроз.
Иммунная система принимает участие в образовании хронических
инфекционных гранулем и большинства гранулем неизвестной этио-
114
Рис. 27. Туберкулезные узелки (гранулемы) в легких. Казеозный некроз
центральной части гранулем (а); на границе с фокусами некоза эпите-
лиоидные клетки (б) и гигантские клетки Пирогова—Лангханса (в)
периферии гранулем скопления лимфоидных клеток.
логии, поэтому такое фанулематозное воспаление обычно сопровож
дается клеточно-опосредованным иммунитетом, в частности ГЗТ
Исходы гранулематозного воспаления, которое, как и всякое
другое, протекает циклически:
1) рассасывание клеточного инфильтрата с образованием руб
ца на месте бывшего инфильтрата;
2) обызвествление гранулемы (например, очаг Гона при тубер-
кулезе):
3) прогрессирование сухого (казеозного) некроза или влажного
некроза с образованием дефекта тканей — каверны;
4) рост гранулемы вплоть до образования псевдоопухоли.
Гранулематозное воспаление лежит в основе гранулематозных
болезней, т. е. таких заболеваний, в которых это воспаление пред
ставляет собой структурно-функциональную основу заболевания.
Примером гранулематозных заболеваний являются тубекулез,
сифилис, лепра, сап и др.
Таким образом, все изложенное позволяет считать воспаление
типовой и вместе с тем уникальной реакцией организма, имею
щей приспособительный характер, но в зависимости от индиви-
дуальных особенностей больного оно может утяжелять его со
стояние, вплоть до развития смертельных осложнений. В связи с
этим воспаление, особенно составляющее основу различных за
болеваний, требует лечения.
115
Глава 7
ПРИСПОСОБИТЕЛЬНЫЕ И КОМПЕНСАТОРНЫЕ
ПРОЦЕССЫ
ХАРАКТЕРИСТИКА ПОНЯТИЙ
Приспособление — широкое биологическое понятие, вклю-
чающее филогенез, онтогенез, эволюцию, наследственность и
все формы регуляции функций организма как в нормальных ус-
ловиях, так и при патологии. Сама жизнь есть непрерывное
приспособление, или адаптация, индивидуума к постоянно ме-
няющимся условиям внешней среды. И от того, насколько вы-
ражена приспособительная способность людей к меняющимся
условиям внешнего мира, зависит адаптация к нему человечест-
ва как биологического вида, состоящего из индивидуумов. За
миллиарды лет жизни на Земле постоянно менялись и меняют-
ся условия внешнего мира и сотни тысяч видов вымерли, не су-
мев приспособиться к новым условиям существования. Однако
и сейчас имеются некоторые виды животных, существующие
уже сотни миллионов лет благодаря, очевидно, их необычайным
приспособительным способностям. Таким образом, приспособ-
ление — это понятие, в основном характеризующее возможно-
сти биологического вида. т. е. комплекс постоянно саморегули-
рующихся процессов, возникающих в организмах вида и позво-
ляющих этому виду приспособиться к меняющимся условиям
существования и выжить в этих условиях, а также возможности
индивидуумов, образующих вид.
Приспособительные реакции проявляются как в условиях здоро-
вья, так и в условиях болезни. Так, с помощью реактивности —
важнейшего механизма приспособления, присущего всем пред-
ставителям животного мира, организм адаптируется к внешней
среде, сохраняя гомеостаз, характерный для представителей дан-
ного вида, и вместе с тем изменения реактивности и гомеостаза
являются звеньями патогенеза любой болезни.
Болезнь — явление индивидуальное, и, следовательно, у кон-
кретного больного видовые приспособительные реакции прелом-
ляются через его индивидуальные особенности, связанные имен-
но с его реактивностью, возрастом, полом, условиями жизни
и др. Поэтому проблема приспособления является не только био-
логической. но и медицинской проблемой патологии.
Приспособление необходимо в ситуациях:
• когда в результате заболевания или возрастных изменений
возникает либо патологическое напряжение функций орга-
на или системы органов;
• когда происходит снижение или извращение этих функций.
В динамике болезни приспособительные реакции больного на-
116
правлены на восстановление гомеостаза и адаптацию к новым ус-
ловиям жизни, жизни после болезни.
Гомеостатические реакции — это реакции всего организма, на-
правленные на поддержание динамического постоянства его
внутренней среды, и поэтому все физиологические и общепато-
логические реакции (нарушения кровообращения, дистрофии,
воспаление и др.) являются реакциями приспособительными, на-
правленными на восстановление гомеостаза.
Биологический смысл приспособления заключается в адаптации
к изменившимся условиям жизни, связанным как с внешним ми-
ром, так и с внутренней средой организма и при этом не обяза-
тельно с восстановлением функций его органов в полном объеме.
Компенсация — совокупность реакций организма, возникаю-
щих при повреждениях или болезнях и направленных на восста-
новление нарушенных функций. Ее характеризуют несколько ос-
новных положений.
1. Компенсация — одна из важнейших форм приспособления,
развивающихся в условиях патологии, т. е. при болезнях, и, следо-
вательно, она носит индивидуальный характер, ибо болезнью за-
болевает конкретный человек.
2. Компенсаторные реакции — это область медицины, область
патологии, и этим они отличаются от видовых приспособитель-
ных реакций, которые обеспечивают жизнь организма и в норме,
и при патологии.
3. Компенсация нарушенных функций направлена на сохранение
жизни, а следовательно, также является приспособлением, но
возникающим лишь в том случае, если организм терпит ущерб.
4. Компенсаторные реакции более узкие, чем приспособитель-
ные и соотносятся с ними как часть с целым.
5. Каждый человек обладает собственными реакциями, но од-
новременно как представитель биологического вида он имеет и
видовые приспособительные реакции. Во время болезни на восста-
новление гомеостаза, на выздоровление направлены и те. и дру-
гие реакции, и их трудно разделить. Поэтому в клинике их часто
обозначаю т как компенсаторно-приспособительные реакции.
Однако эти понятия не идентичны, ибо приспособление часто
развивается в физиологических условиях, и именно приспособи-
тельные реакции позволяют не заболеть и исключают необходи-
мость развития компенсаторных реакций организма.
ВИДЫ ПРИСПОСОБЛЕНИЯ И КОМПЕНСАЦИИ
Приспособительные реакции постоянно протекают в физиоло-
гических условиях в связи с функционированием органов и рас-
ходованием при этом их морфологических структур, возрастными
изменениями человека, воздействием внешней среды и измене-
ниями внутренней среды организма или в связи с длительным
повышением функции органов в физиологических пределах. Вы-
117
деляют 3 основные формы приспособительных и компенсатор-
ных реакций: регенерацию, атрофию, гипертрофию.
РЕГЕНЕРАЦИЯ
Регенерация — это восстановление организмом тканей, кле-
ток, внутриклеточных структур, погибших или поврежденных ли-
бо в результате их физиологического функционирования, либо
вследствие патологического воздействия. Без регенерации сама
жизнь невозможна и поэтому регенерация протекает в организме
непрерывно. Она контролируется и регулируется различными
системами организма:
• гуморальным!, обеспечивающими регенерацию на внутри-
клеточном, клеточном уровнях и на уровне ткани. С помо-
щью большого количества цитокинов, факторов роста, вы-
деляемых макрофагами, тромбоцитами, фибробластами и др.;
• иммунной системой, с помощью лимфоцитов контролирую-
щей "регенерационную информацию", обеспечивающую ан-
тигенное единство регенерирующих структур, без которой не
может быть регуляции трофики и полноценной регенерации;
• нервной системой;
• очень важную роль играет так называемый функциональный
запрос, т. е. тот необходимый для жизни уровень функций,
который должен быть обеспечен соответствующими морфо-
логическими структурами, степенью и особенностями их
метаболизма, уровнем биоэнергетики и т. д.
Выделяют три основных вида регенерации:
• физиологическая регенерация, обеспечивающая восстановле-
ние на всех уровнях структур, погибших в процессе жизне-
деятельности;
• репаративная регенерация, развивающаяся при болезнях;
• патологическая регенерация, или дисрегенерация.
В зависимости от особенностей структуры и функций регенери-
рующих тканей регенерация в разных органах протекает неодина-
ково:
• регенерация происходит в основном за счет вновь образую-
щихся клеток при гибели клеток пограничных тканей, таких
как кожа, слизистые оболочки, а также кроветворной, лим-
фатической систем, костей (рис. 28);
• регенерация как путем образования новых клеток взамен по-
гибших, так и в результате восстановления, внутриклеточных
структур при сохранении клетки в целом протекает в пече-
ни, почках, вегетативной нервной системе и в большинстве
других органов;
• регенерация только за счет восстановления внутриклеточ-
ных структур, при которой клетки не перестают функцио-
нировать, происходит в сердце и головном мозге, требую-
щих одновременного и синхронного функционирования
множества клеток.
118
Рис. 28. Периостальная мозоль, сме-
щенные отломки костей.
Эти принципы регенерации раз-
личных тканей сохраняется как в
норме, так и в условиях патологии.
Регенерация тканей, утраченных
при болезнях протекает в двух фор-
мах: либо репаративной, либо пато-
логической.
Репаративная регенерация (от
слова "репарация" — восстановле-
ние) восстановление утраченного в
результате патологических процес-
сов. В зависимости от степени вос-
становления тканей выделяют:
• реституцию — восстановле-
ние ткани, идентичной утра-
ченной, и при этом не оста-
ется следов бывшего повреж-
дения;
• субституцию, характеризую-
щуюся образованием рубца
на месте повреждения.
В патологии преобладает субсти-
туция, при этом образованию рубца
предшествует возникновение и созревание грануляционной ткани.
Эта ткань уникальна и универсальна, так как репарация в боль-
шинстве органов происходит именно с ее участием (см. главу 6).
Конечным этапом развития грануляционной ткани является об-
разование соединительнотканного рубца — наиболее прочной,
быстрее других образующейся ткани, позволяющей в кратчайшие
сроки ликвидировать повреждение. Рубец не несет специфиче-
ской функции, но этого и не надо, так как функцию орган вос-
становит за счет других приспособительных и компенсаторных
процессов, прежде всего таких, как гипертрофия (рис. 31).
Патологическаярегенерация, или дисрегенерация, характеризу-
ется образованием ткани, не полностью соответствующей утра-
ченной, и при этом функция регенерирующей ткани не восста-
навливается или извращается. В основе дисрегенерации лежит
срыв адаптации организма к патологическим воздействиям в ре-
зультате полома физиологической регуляции реакций приспособ-
ления. Причин такого полома может быть много, например изме-
нение реактивности организма, развитие иммунного дефицита,
нарушения межклеточных взаимоотношений, что в свою очередь
может приводить к неполноценности хемотаксиса, нарушению
функций макрофагов и т. п. Выделяют три варианта дисрегене-
рации:
119
Рис. 29. Гидроцефалия.
1) гипорегенерация — восстановление утраченных тканей идет
очень медленно или совсем останавливается, например при тро-
фических язвах, пролежнях;
2) гиперрегенерация — ткань регенерирует избыточно, функция
органа при этом часто страдает (например, образование келоид-
ного рубца в области бывшей раны);
3) метаплазия — переход одного вида ткани в другой, но род-
ственный ей гистогенетинески. При этом, естественно, функция
утраченной ткани не восстанавливается. Примером метаплазии
является развитие в области повреждения слизистой оболочки
бронха вместо мерцательного эпителия многослойного плоского
ороговевающего эпителия или трансформация соединительной
ткани в кость. Проявлением дисрегенерации являются и хрони-
120
Рис. 30. Компенсаторная гипертрофия миокарда. Гиперплазия митохонд-
рий кардиомиоцита. Митохондрии (М) образуют большие скопления меж-
ду миофибриллами (Мф). Часть митохондрий в состоянии деструкции.
Л — липиды; Лз — лизосомы; СР — саркоплазматический ретикулум. Электроно-
грамма.
121
Рис. 31. Рубец (Рц) в мышце сердца после перенесенного инфаркта мио-
карда (крупноочаговый кардиосклероз).
ческие воспалительные процессы, не заканчивающиеся восста-
новлением утраченной ткани и соответствующих функций ор-
гана.
АТРОФИЯ
Атрофия — это уменьшение объема морфологических структур
органа и ткани, сопровождающееся снижением или полной утра-
той их функций. При этом уменьшается объем функциональных
клеток, в них становится меньше внутриклеточных органелл, не-
редко накапливается липофусцин — так называемая бурая атро-
фия. В большинстве случаев атрофия — процесс обратимый.
Виды атрофии:
• физиологическая, с помощью которой организм приспосаб-
ливается к меняющимся условиям своей жизни. Так, в оп-
ределенном возрасте происходит атрофия вилочковой желе-
зы, яичников и молочных желез у женщин, сперматогенно-
го эпителия яичек у мужчин; в старости в связи со сниже-
нием уровня обмена веществ и выключением многих функ-
ций организма наступает атрофия всего тела человека (стар-
ческая, или инволюционная кахексия);
• патологическая, с помощью которой организм приспосабли-
вается к изменениям, вызванным различными болезнями;
• общая, связанная, например, со старческим возрастом —
инволюционная кахексия (или истощение), но может являть-
ся и проявлением болезни — патологическая кахексия, раз-
вивающаяся при голодании — алиментарное истощение,
при различных заболеваниях головного мозга — церебраль-
ная, гипофизарная, посттравматическая кахексия, злокаче-
ственных опухолях и т. п.;
• местная — атрофия органа (тимуса, почки, яичников и
т. п.).
В медицине наибольшее значение имеет патологическая атро-
фия. Исходя из причины, вызвавшей такую атрофию, выделяют
следующие ее виды:
• дисфункциональная (атрофия от бездеятельности) развивает-
ся в результате отсутствия функции (например, атрофия
мышц конечности при переломе ее кости);
• атрофия от давления — атрофия ткани мозга вследствие
давления спинномозговой жидкости, скапливающейся в
желудочках мозга при гидроцефалии и т. п. (рис. 29);
• атрофия вследствие недостаточного кровоснабжения (атро-
фия почки при стенозе почечной артерии атеросклеротиче-
ской бляшкой);
• нейротрофическая атрофия, возникающая при нарушении
иннервации ткани (атрофия скелетных мышц в результате
разрушения моторных нейронов при полиомиелите спин-
ного мозга);
• атрофия от действия повреждающих (химических или фи-
зических) факторов (например, атрофия костного мозга
при действии лучевой энергии).
При атрофии клеток строма органа обычно сохраняет свой
объем и при этом нередко подвергается склерозированию.
ГИПЕРТРОФИЯ
Гипертрофия — увеличение объема функционирующей ткани —
форма приспособления и компенсации, возникающая при дли-
тельном повышении нагрузки на орган или систему органов.
В основе гипертрофии лежит гиперплазия — увеличение количе-
ства клеток, внутриклеточных структур, компонентов стромы,
количества сосудов. Так, за счет гиперплазии крист митохондрий
может развиваться гипертрофия этих органелл ("гигантские" ми-
тохондрии); гиперплазия внутриклеточных структур обеспечивает
гипертрофию клеток, а гиперплазия последних лежит в основе
гипертрофии органа.
Вместе с тем масса таких высокоспециализированных органов,
как сердце и ЦНС, увеличивается только за счет гипертрофии
уже существующих клеток, так как новые кардиомиоциты и ней-
роциты не образуются. В основе их гипертрофии также лежит ги-
перплазия внутриклеточных структур, и в этом, несомненно, про-
является биологическая целесообразность приспособления и ком-
пенсации (рис. 30). Эти органы отличаются чрезвычайной слож-
ностью структурно-функциональной организации (автоматизм
сократимости кардиомиоцитов, огромное количество разнообраз-
122
123
ных связей нейрона с другими структурами и т. п.)- Кроме того, в
процессе дифференцирования вновь образованной клетки она не
функционирует; например, в мышце сердца это может прервать
функцию "миокардиального синцития", что нарушит проводи-
мость и автоматизм сокращения всего миокарда и вызовет арит-
мию. Очевидно, и для ЦНС значительно целесообразнее сохране-
ние функций за счет гипертрофии уже имеющегося нейрона с его
сложной системой регуляции, чем образование новой нервной
клетки и восстановление ее связей с другими нервными структу-
рами. В других органах, таких как печень или почки, также обла-
дающих очень сложными функциями, увеличение массы ткани
тем не менее происходит как за счет гиперплазии клеток, так и в
результате их гипертрофии, и в основе последней также лежит
гиперплазия внутриклеточных структур.
Таким образом, универсальным механизмом гипертрофии явля-
ется гиперплазия внутриклеточных структур, а механизмы ги-
пертрофии разных органов зависят от их структурно-функцио-
нальных особенностей.
Гипертрофия поддерживается гиперфункцией органа, но вме-
сте с тем это процесс обратимый — гипертрофия исчезает при
ликвидации причины, вызвавшей эту гиперфункцию.
Виды гипертрофии:
• физиологическая гипертрофия развивается у здоровых лю-
дей как приспособительная реакция на повышенную
функцию тех или иных органов, например увеличение со-
ответствующих групп скелетных мышц или сердца при за-
нятии спортом, увеличение массы тела матки при бере-
менности и др.;
• компенсаторная (рабочая) гипертрофия появляется при бо-
лезнях и является компенсаторной реакцией, позволяющей
сохранить функцию органов в условиях патологии.
МЕХАНИЗМЫ КОМПЕНСАЦИИ ФУНКЦИЙ
ПРИ БОЛЕЗНЯХ
Эти механизмы принципиально не отличаются от механизмов
приспособления. Все многообразие изменений поврежденных ор-
ганов и тканей организма при болезнях направлено на сохране-
ние их функций.
Она развивается при длительной гиперфункции органа. При
этом увеличивается вся масса функционирующей ткани, но сама
эта ткань не поражена патологическим процессом (например, ги-
пертрофия миокарда при артериальной гипертонии).
Регенерационная гипертрофия развивается в сохранившихся
тканях поврежденного органа и компенсирует утрату его части.
Такая гипертрофия развивается при крупноочаговом кардиоскле-
розе после инфаркта миокарда в сохранившейся мышечной ткани
сердца, в сохранившейся ткани почки при нефросклерозе и т. п.
124
Рис. 32. Железисто-кистозная гиперплазия слизистой оболочки матки.
Железы извиты, просветы некоторых из них кистозно расширены (б),
строма богата клетками (в).
Викарная (залкстительная) гипертрофия развивается в сохра-
нившемся парном органе при гибели или удалении одного из
них. При викарной гипертрофии сохранившийся орган берет на
себя функцию утраченного.
Патологическая гипертрофия — это увеличение объема и мас-
сы органа, которое не является компенсаторной реакцией, так
как не только не компенсирует утраченную функцию, но нередко
извращает ее. Патологическая гипертрофия сама служит проявле-
нием болезни и требует лечения. Примером такой гипертрофии
являются:
нейрогуморальная гипертрофия, возникающая при нарушении
функции эндокринных желез: акромегалия при гиперфункции
передней доли гипофиза, железистая гиперплазия эндометрия
при дисфункции яичников (рис. 32). И акромегалия, и желези-
стая гиперплазия эндометрия не несут в себе ни приспособитель-
ного, ни компенсаторного смысла, а являются симптомами забо-
леваний, по поводу которых необходимо лечение;
гипертрофические разрастания тканей в области длительно те-
кущих воспалительных процессов или увеличение объема тканей
в области нарушенного лимфообращения (например, слоновость
нижней конечности) также не имеют компенсаторного значения,
ибо никоим образом не компенсируют нарушенную функцию то-
го органа, в котором они развиваются.
Ложная гипертрофия возникает на месте атрофирующейся
функциональной ткани или органа, которая замещается разрас-
тающейся жировой клетчаткой и соединительной тканью, что
125
также никакого отношения ни к гипертрофии, ни к компенсатор-
ным реакциям не имеет.
Стадии компенсаторных процессов. Одной из важнейших осо-
бенностей компенсаторных реакций является их стадийный (фа-
зовый) характер. В их динамике выделяют 3 стадии.
1-я стадия — стадия становления компенсаторных процессов,
или аварийная стадия, характеризуется тем. что при развитии лю -
бого заболевания в органах резко повышается нагрузка на струк-
туры, несущие специфическую функцию органа, что требует аде-
кватного увеличения метаболизма и энергетического обеспече-
ния. Это вынуждает имеющиеся в клетках митохондрии резко по-
вышать образование энергии. Но гиперфункция митохондрий со-
провождается усиленным разрушением их крист, что не позволя-
ет увеличить образование энергии до необходимого уровня. Воз-
никает энергетический дефицит, являющийся основой этой стадии.
Это объясняется тем, что без энергии, без энергетического обес-
печения невозможен ни один процесс в организме, без этого нет
метаболизма, так как без энергии не работают трансмембранные
помпы, не могут обеспечиваться градиенты тока электролитов и
жидкостей, невозможен синтез веществ, необходимых для восста-
новления разрушающихся в результате гиперфункции морфоло-
гических структур, и т. д. Степень эффективности компенсатор-
ных и приспособительных процессов в период энергетического
дефицита и инициальной гиперфункции ультраструктур клеток и
является так называемым функциональным резервом каждого боль-
ного, от которого зависят течение и исход болезни.
2-я стадия — стадия относительно устойчивой компенсации —
характеризуется гиперплазией внутриклеточных структур, обеспе-
чивающих гипертрофию и гиперплазию клеток. Значительно воз-
растают биосинтетические процессы в клетках и резко снижается
энергетический дефицит. Однако если не ликвидирована причи-
на, вызвавшая гиперфункцию органа, т. е. если болезнь приобре-
тает хроническое течение, то сохраняется гиперфункция ультра-
структур клеток, требующая высокого энергетического обеспече-
ния. Однако основная часть образующейся в митохондриях энер-
гии расходуется на обеспечение функции органа и меньшая — на
восстановление самих себя. И коль скоро нагрузка на орган не
снижается, а функция его поддерживается необходимой для этого
энергией, то постепенно количество энергии, необходимой для
ресинтеза ультраструктур падает. В результате постоянно восста-
навливается несколько меньше крист митохондрий, чем необхо-
димо. А это значит, что на имеющиеся кристы падает и та нагруз-
ка, которую должны были бы нести недостающие кристы. Тем
самым не только поддерживается, но и постепенно нарастает
энергетический дефицит гиперфункционирующих клеток, зако-
номерно вызывающий гиперфункцию, а следовательно, и уско-
ренный распад внутриклеточных структур, в том числе и мито-
хондрий. Поэтому в стадию относительно устойчивой компенса-
ции возникает порочный круг, и это объясняет причину неизбеж-
126
ной декомпенсации, которая наступает раньше или позже, если
не ликвидирована болезнь, вызвавшая необходимость включения
компенсаторных и приспособительных процессов.
3-я стадия — стадия декомпенсации — характеризуется про-
грессирующим преобладанием процессов распада внутриклеточ-
ных структур над их ресинтезом. В патологически измененном
органе постоянно функционируют и. следовательно, разрушаются
почти все клетки, и в результате этого они теряют возможность
восстанавливаться, ибо для репарации должны на определенное
время перестать функционировать. Нарастает гипоксия тканей
даже при достаточном поступлении кислорода, так как уменьша-
ется количество полноценных внутриклеточных структур, способ-
ных его утилизировать. Меняется метаболизм, развиваются дис-
трофические процессы, прежде всего жировая дистрофия, нарас-
тает ацидоз, способствующий повышению проницаемости мем-
бран лизосом и поступлению гидролаз в цитоплазму. Кроме того,
все меньше восстанавливаются и распадающиеся в результате ги-
перфункции митохондрии, что ведет к прогрессирующему умень-
шению образования энергии, особенно необходимой для ресин-
теза всех гиперфункционирующих структур. Это заставляет де-
фектные ультраструктуры еще интенсивнее функционировать,
чтобы поддержать функцию органа. Наконец, деструкция внутри-
клеточных структур достигает такой степени, а энергетический
дефицит вырастает до такого уровня, когда обеспечение специ-
фической функции становится невозможным. Наступает энерге-
тическое истощение и развивается декомпенсация.
Компенсаторные и приспособительные реакции, как явление
одного биологического плана, основываются на определенных
биологических закономерностях. Прежде всего следует подчерк-
нуть, что в их основе лежат нормальные физиологические реак-
ции. Это объясняется тем, что функции являются производными
от деятельности клеток различных органов и тканей, а новые ти-
пы клеток в организме ни при каких условиях не образуются.
Поэтому не могут появиться и никакие новые, необычные функ-
ции, и при формировании защитных реакций в ответ на внешние
воздействия организм может лишь варьировать комбинации из
стереотипного набора своих функций. Таким образом, следует го-
ворить не о принципиальных качественных отличиях приспосо-
бительных и компенсаторных реакций организма от его нормаль-
ных реакций, а лишь об их своеобразии, связанном с патологиче-
скими, т. е. чрезвычайными, воздействиями на человека.
АДАПТАЦИОННЫЙ ПРОЦЕСС
В процессе жизни человек постоянно подвергается чрезвычай-
ным воздействиям, на которые он реагирует своими защитными
механизмами, прежде всего приспособительными реакциями.
В большинстве таких ситуаций благодаря адаптационному про-
127
цессу организму удается "уйти" от действия раздражителя, т. е.
сохранить параметры гомеостаза. Однако при действии чрезвы-
чайного раздражителя, которым могут быть физические, химиче-
ские, биологические, психические и другие факторы, развивается
стресс-синдром, представление о котором было сформулировано
Г. Селье в 1935 г.
СТРЕСС-СИНДРОМ
Стресс (от англ, stress — напряжение) — генерализованная, не-
специфическая реакция организма, возникающая под действием
различных факторов внешней или внутренней среды необычного
характера, силы или длительности. Стресс характеризуется ста-
дийными неспецифическими изменениям в организме: активаци-
ей защитных процессов и повышением его общей резистентности
с возможным последующим снижением ее и развитием патологи-
ческих процессов.
Механизм стресс-реакции
Стресс-реакция сформировалась в эволюции как одно из зако-
номерных звеньев механизма приспособления.
Воздействие любого чрезвычайного фактора вызывает в орга-
низме два взаимосвязанных процесса:
• мобилизацию его физиологических и формирование функцио-
нальных систем, обеспечивающих специфическую адаптацию
именно к данному фактору (холоду, гипоксии, физической на-
грузке, дефициту субстрата метаболизма, токсину и др.);
• активацию стандартных, неспецифических описанных вы-
ше реакций, развивающихся при воздействии любого не-
обычного для организма воздействия. Эти реакции и со-
ставляют сущность процесса, обозначаемого как собственно
стресс, или стресс-реакция.
В процессе развития стресс-реакции выделяют три стадии.
1-я стадия стресса — общая реакция тревоги. Ее пусковыми
факторами являются:
• воздействие на организм чрезвычайного фактора, нарушаю-
щего гомеостаз (боль, холод, гипоксия, психическая тревога
и др.);
• отклонение от нормального диапазона различных парамет-
ров гомеостаза (р02, pH, рост, АД, массы циркулирующей
крови, температуры тела и др.);
• активация симпатико-адреналовой, гипоталамо-гипофизар-
но-надпочечниковой системы, щитовидной, поджелудочной
и других желез внутренней секреции, что обусловливает бы-
струю мобилизацию комплекса различных адаптивных ме-
ханизмов, в первую очередь компенсаторных и восстанови-
тельных.
Эти механизмы обеспечивают:
128
— "ускользание" организма от действия повреждающего факто-
ра, возможный уход его от экстремальных условий существования;
— формирование повышенной устойчивости к повреждающе-
му фактору;
— необходимый уровень функционирования организма даже в
условиях продолжающегося чрезвычайного воздействия.
2-ястадиястресса—повышение общей сопротивляемости орга-
низма к стрессорнымвоздействиям В динамике 2-й стадии стресса
нормализуются функционирование органов и их систем, интенсив-
ность обмена веществ, уровни гормонов и субстратов метаболизма.
В основе указанных изменений лежат гиперплазия и гипертрофия
структурных элементов тканей и органов. Они обеспечивают раз-
витие повышенной резистентности организма — желез внутренней
секреции, сердца, печени, кроветворных органов.
3-я стадия стресса — истощение. Эта стадия стресса возника-
ет в том случае, если продолжает действовать фактор, вызываю-
щий стресс. Она характеризуется расстройством механизмов
нервной и гуморальной регуляции, доминированием катаболиче-
ских процессов, развитием энергетического истощения и наруше-
нием их функционирования. В конечном итоге снижаются общая
резистентность и приспособляемость организма, нарушается его
жизнедеятельность.
При очень длительном, сильном, а также повторном стрессе
развиваются два закономерных феномена:
— снижается эффективность системы иммунобиологического
надзора;
— облегчается экспрессия отдельных клеточных генов. В связи
с этим активируется синтез нуклеиновых кислот и белков. Соче-
тание этих двух феноменов может создать благоприятные условия
для экспрессии онкогенов и развития опухолей (см. главу 10).
ВИДЬ! СТРЕСС-РЕАКЦИИ
1, Адаптивная, Если активация функций органов и их систем у
человека в условиях действия стрессорного агента предотвращает
отклонение параметров гомеостаза за пределы нормального диа-
пазона, а стрессорный фактор характеризуется умеренной силой
и относительно непродолжительным воздействием, то может
сформироваться состояние повышенной резистентности организ-
ма к нему, т. е. приспособление. В подобных случаях стресс име-
ет адаптивное значение, и такую стресс-реакцию обозначают как
адаптивную. Она нередко возникает при тренировке человека к
какому-либо экстремальному воздействию (физической нагрузке,
гипо- или гипербарии, гипоксии и т. д.).
2, Патогенная возникает при чрезмерном длительном или час-
том повторном воздействии сильного стрессорного агента на орга-
низм, вызывающего нарушение его гомеостаза, может привести к
значительным расстройствам жизнедеятельности и развитию экс-
тремального (коллапс, шок, кома) состояния или даже к смерти.
129
КОМПЕНСАЦИЯ И ДЕКОМПЕНСАЦИЯ
НАРУШЕННЫХ ФУНКЦИЙ
Жизнь человека зависит от способности адекватно реагировать
на бесчисленные воздействия внешней и внутренней среды. Эту
способность обозначают как надежность биологических систем.
Надежность биологических систем — это способность организ-
ма противостоять различным повреиедающим воздействия. В осно-
ве этого лежат приспособительные и компенсаторные реакции,
обеспечивающие сохранение гомеостаза как в процессе нормаль-
ной жизнедеятельности, так и при различных болезнях.
Надежность биологических систем может проявляться в стой-
кой невосприимчивости к инфекционным агентам (иммунитет), в
способности нейтрализовать действие даже сильных ядов (деток-
сикация), в исключительной выносливости организма по отно-
шению к физическим нагрузкам, колебаниям уровня кислорода
во вдыхаемом воздухе, сильным перепадам температуры окру-
жающей среды и т. п. Во всех этих случаях в действие включают-
ся различные системы организма, усиливают свою работу разные
ткани и клеточные элементы, продуцируются разнообразные био-
логически активные вещества. Но при почти бесконечном разно-
образии этих ответов организма на действие факторов окружаю-
щей или внутренней среды все они основываются на использова-
нии относительно небольшого количества регуляторных механиз-
мов и структурных реакций. Эти реакции являются типовыми,
или стереотипными, не только потому, что с их помощью орга-
низм приспосабливается ко всему разнообразию физиологиче-
ских и патогенных факторов, но и в связи с тем, что все они в
одинаковой степени свойственны и стереотипны в своих прояв-
лениях для всех уровней организации: молекулярного (генетиче-
ского, биохимического), ультраструктурного, клеточного, ткане-
вого, органного, системного. В целостном организме, в котором
все взаимосвязано, взаимообусловлено, все взаимодействует и
практически нет каких-то строго изолированных реакций, интен-
сификация приспособительных и компенсаторных процессов в
том или ином органе обязательно сопрягается с такими же реак-
циями в ряде других органов и систем. В целом это способствует
повышению мощности и эффективности ответа всего организма
на определенное воздействие. Например, благоприятное влияние
физической тренировки связано с усилением функции не только
непосредственно ответственной за это мышечной системы, но и с
оптимизацией ее связей с респираторной, гемодинамической и
другими системами организма.
КОМПЕНСАЦИЯ И ВЫЗДОРОВЛЕНИЕ
На практике очень важно понимание принципиальной разни-
цы между состоянием высокой компенсации патологических из-
менений при той или иной болезни, с одной стороны, и процес-
130
сом выздоровления от нее — с другой. И в том, и в другом случае
человек чувствует себя одинаково хорошо и окружающим кажет-
ся вполне здоровым. Однако даже при полной компенсации на-
рушенных функций он остается больным и болезнь продолжает
прогрессировать, морфологические изменения органов непрерыв-
но нарастают. И лишь благодаря крайнему напряжению компен-
саторных реакций болезнь клинически не проявляется и нередко
уже тяжелобольной человек продолжает считаться практически
здоровым. Только когда начинают истощаться компенсаторные
реакции и их уже не хватает для нейтрализации деструктивных
изменений, тогда появляются первые клинические симптомы бо-
лезни, ошибочно расцениваемые как начало болезни. На самом
же деле уже имеет место декомпенсация морфологических струк-
тур и нарушение функции, т. е. несостоятельность компенсатор-
ных реакций. Особенно трагично то, что состояние декомпенса-
ции нередко начинает проявляться тогда, когда болезнь уже дале-
ко заходит в своем развитии и больной нередко становится инку-
рабельным.
Различие между процессами выздоровления и компенсации со-
стоит в том, что выздоровление обычно сопровождается ликви-
дацией некоторых из тех изменений, которые в динамике забо-
левания появились как компенсаторные. Например, нарушения
гемодинамики при врожденных и приобретенных пороках кла-
панов сердца компенсируются гипертрофией миокарда и нарас-
тающей параллельно с ней гиперплазией его стромы и сосудов.
Гипертрофия мышцы сердца позволяет организму существовать
в условиях нарушенной гемодинамики. После устранения поро-
ка сердца и восстановления кровообращения все морфологиче-
ские и функциональные изменения должны быть ликвидирова-
ны. Поэтому возможность обратимости компенсаторных изме-
нений — гипертрофии миокарда и гиперплазии его стромы по-
сле того, как больше нечего компенсировать, чрезвычайно важ-
на, так как сохранение увеличенной массы мышцы сердца не
может дать уже ничего, кроме опасности декомпенсации гипер-
трофированного миокарда. Так же нормализуется строение ги-
пертрофированной стенки сосудов после устранения причины
некоторых видов симптоматического повышения артериального
давления, восстанавливается масса почки после удаления стено-
зирующей атеросклеротической бляшки из почечной артерии
и т. д.
Вместе с тем любой компенсаторный процесс не может про-
должаться бесконечно, и если сохраняется вызвавшая его причи-
на, то продолжающаяся на всех уровнях гиперфункция повреж-
денных систем, т. е. их высокое и длительное напряжение, обяза-
тельно заканчивается срывом компенсации и развитием деком-
пенсации. В ее основе лежат дистрофические изменения клеток,
связанные в первую очередь с нарастающей гипоксией из-за не-
адекватного разрушения митохондрий при их гиперфункции и
прогрессирующим энергетическим дефицитом, переходящим в
131
энергетическое истощение. Постепенно разрушение внутрикле-
точных структур достигает такой степени, что развиваются некро-
биотические изменения клеток, приводящие их к гибели. При
этом следует подчеркнуть, что если в декомпенсации клетки ос-
новную роль играют внутриклеточные процессы, то в развитии
декомпенсации органа наряду с этим не меньшее значение имеет
и состояние общерегуляторных механизмов работы этого органа в
системе целостного организма.
Однако неизбежный финал всякого компенсаторно-приспосо-
бительного процесса при сохраняющемся заболевании в виде де-
компенсации органа вовсе не снижает значения этого процесса
как важнейшей защитной реакции, позволяющей человеку пол-
ноценно жить порой в течение десятков лет, позволяет оказывать
ему медицинскую помощь, нередко радикальную, а в большинст-
ве случаев создает возможность полностью избавить человека от
болезни.
Глава 8
ИММУНОПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
ОБЩАЯ ХАРАКТЕРИСТИКА ИММУННОЙ СИСТЕМЫ
Иммуногенная реактивность — ответ организма на антигенный
стимул. Материальным субстратом иммуногенной реактивности
является иммунная, или иммунокомпетентная, система (ИКС).
Иммунная система представляет собой совокупность органов,
тканей и клеток, обеспечивающих биохимическую, структурную
и функциональную однородность и индивидуальность организма
путем обнаружения, уничтожения и удаления (элиминации) из
него чужеродных антигенов.
Эволюционно иммунная система сформировалась как меха-
низм контроля за однородным и индивидуальным антигенным
составом организма. В основе этого механизма лежит способ-
ность клеток иммунной системы отличать собственные клетки и
белковые соединения от чужеродных. Обнаружение последних
сопровождается инактивацией, разрушением и элиминацией их
из организма.
Антиген — вещество экзо- или эндогенного происхождения,
вызывающее иммунную реакцию, которая заключается в выра-
ботке иммунных антител и лимфоцитов, их взаимодействии с ан-
тигеном, сопровождающимся его инактивацией и элиминацией.
Виды антигенов. Антигены разделяют на несколько групп в за-
висимости от их биохимической структуры, происхождения, пути
попадания в организм и других критериев.
132
По биохимической структуре антигены делят на два вида:
1) белки и белоксодержащие соединения; 2) небелковые соедине-
ния — гаптены, к которым относятся полисахариды, липиды, не-
которые синтетические полимеры, неорганические вещества (со-
единения йода, брома, висмута), лекарственные средства. Сами
по себе гаптены неиммуногенны. Однако после их соединения с
белками или клетками организма они приобретают способность
вызывать иммунные реакции.
По происхождению антигены делят на экзо- и эндогенные.
Экзогенные антигены составляют большую часть антигенов:
• инфекционно-паразитарного происхождения (антигены ви-
русов, риккетсий, бактерий, паразитов);
• неинфекционного происхождения (чужеродные белки и бе-
локсодержащие соединения, гаптены, входящие в состав
пыли, пищевых продуктов, пыльцы растений, ряда лекарст-
венных веществ).
Эндогенные антигены также подразделяют на:
• инфекционные и/или паразитарные (белковые компоненты
микробов, "заселяющих" миндалины, кишечник, слизистые
оболочки рта, дыхательных путей);
• неинфекционные, которые образуются при повреждении
собственных белков, при конъюгации гаптенов с белками
клеток и биологических жидкостей организма, при мутациях
в геноме клеток или при выработке ими аномальных белков.
Иммунная система представлена тремя субсистемами клеток: А,
В и Т.
Субсистему А-клеток составляют мононуклеарные клетки —
моноциты, тканевые макрофаги и некоторые другие. Эти клетки
обладают высокой способностью обнаруживать чужеродные анти-
гены. поглощать их. выявлять их молекулярную структуру, пере-
давать информацию о них Т- и В-лимфоцитам.
Субсистели В-клеток состоит из различных клонов В-лимфо-
цитов. При первом контакте антигена с В-лимфоцитами часть их
превращается в плазматические, антителопродуцирующие клетки,
а часть — в долгоживущие, рециркулирующие клетки иммунной па-
мяти. Повторный контакт этих клеток с тем же антигеном сопро-
вождается массированной бласттрансформацией лимфоцитов па-
мяти и трансформацией их в плазматические клетки, вырабаты-
вающие специфические иммуноглобулины — антитела. У человека
выделяют 5 основных классов иммуноглобулинов: А, Е, G, М, D.
Субсистели Т-клеток представлена различными клонами Т-
лимфоцитов. Их пролиферация и созревание происходят в основ-
ном с участием вилочковой железы (тимуса), с чем связано их
обозначение: Т-лимфоциты, т. е. тимусзависимые. Первый кон-
такт Т-клеток с антигеном сопровождается их дифференцировкой
в зрелые, долгоживущие лимфоциты различных субполяций.
включая клетки памяти. При повторном контакте с тем же анти-
геном клетки памяти превращаются в специфические Т-лимфо-
циты различных клонов.
133
В субсистемах Т- и В-лимфоцитов имеются "исполнительные"
клетки:
• плазматические, продуцирующие иммуноглобулины:
• Тл — киллеры (убийцы), разрушающие клетки и ткани, не-
сущие чужеродный антиген;
• Тл-хелперы, т. е. помощники;
• Тл-супрессоры, т. е. сдерживающие. Они влияют на проли-
ферацию и дифференцировку других лимфоцитов.
Иммунный ответ организуется клетками всех субсистем ИКС,
сопровождается развитием разнообразных иммунопатологических
состояний, реализующихся через воспаление. Инициальным эта-
пом иммунной реакции является распознавание антигена: если
он чужероден для организма, информация о нем передается эф-
ферентным клеткам ИКС.
ТИПОВЫЕ ФОРМЫ ИММУНОПАТОЛОГИЧЕСКИХ
ПРОЦЕССОВ
Иммунопатологические процессы — это реакции организма,
развивающиеся в результате нарушений иммунитета. В большин-
стве случаев они являются следствием дефекта или истощения
одного или нескольких механизмов, необходимых для обеспече-
ния эффективного иммунного ответа.
ВИДЫ ИММУНОПАТОЛОГИЧЕСКИХ ПРОЦЕССОВ
По происхождению:
Первичные (наследственные, врожденные). Они являются ре-
зультатом генетического дефекта, обусловливающего нарушения
процессов пролиферации, дифференцировки и функционирова-
ния клеток А-, В- или Т-лимфк щитов иммунной системы.
Вторичные (приобретенные в постнатальном периоде онтоге-
неза). Развиваются под влиянием повреждающих факторов фи-
зического характера (например, высокой дозы рентгеновского
излучения), химического (например, действия цитостатических
агентов) или биологического (например, значительного повы-
шения уровня в крови глюкокортикоидов, повреждения клеток
иммунной системы при вирусной или бактериальной инфек-
ции).
По механизмам развития:
• Обусловленные отсутствием или значительным уменьшени-
ем количества А-клеток, различных популяций В- или
Т-лимфоцитов, в связи с подавлением процессов их деле-
ния, созревания или в связи с усиленным разрушением.
• Обусловленные нарушением дифференцировки, макрофа-
гов, Т- и В-лимфоцитов, а также их кооперации в результа-
те изменения количества в организме Т- и В-лимфоцитов-
134
регуляторов (увеличение числа "супрессоров", уменьшение
"хелперов") или биологически активных веществ (кортико-
стероидов. интерлейкинов, гормонов и др.).
По преимущественному повреждению клеток различных иммун-
ных субсистем:
• "В-зависимые"("гуморальные");
• "Т-зависимые" ("клеточные");
• "A-зависимые" ("фагоцитарные", "мононуклеарные").
• Комбинированные.
Характеристика отдельных иммунопатологических процессов
Выделяют несколько основных групп типовых расстройств
иммунитета: иммунодефицитные состояния (ИДС), патологиче-
скую толерантность, реакцию "трансплантат против хозяина",
аллергические реакции, состояния иммунной аутоагрессии (схе-
ма 2).
Иммунодефицитные состояния
Иммунодефицитные состояния (или иммунодефициты) характе-
ризуются значительным снижением активности или неспособно-
стью организма к эффективному осуществлению реакций клеточ-
ного или гуморального иммунитета. Они проявляются высокой
склонностью организма к развитию инфекционных, паразитар-
ных, опухолевых и аллергических заболеваний.
Главным звеном патогенеза иммунодефицитов является блока-
да процессов деления и/или созревания клеток А-, Т- или В-суб-
систем ИКС либо деления и дифференцировки их клеток-пред-
шественников.
Примером иммунодефицитного состояния может служить син-
дром ретикулярной дискинезии. Она характеризуется значитель-
ным уменьшением в костном мозге количества стволовых гемо-
поэтических клеток и блокадой созревания из них лимфю- и мо-
ноцитов с развитием дефицита клеток А-, В- и Т-субсистем. Па-
Схема 2
135
циенты, страдающие этим синдромом, погибают вскоре после ро-
ждения от различных инфекций или злокачественных опухолей.
Нарушения в субсистеме А-клеток проявляются расстройством
фагоцитоза, процессов "переработки" и представления антигена
лимфоцитам.
Расстройства деления и созревания В- или Т-лимфоцитов обу-
словливают нарушение реакций гуморального и клеточного им-
мунитета. В связи с этим у больных часто наблюдаются вирус-
ные, бактериальные и грибковые инфекции, заболеваемость но-
вообразованиями увеличивается более чем в 100 раз.
Виды иммунодефицитных состояний
Синдром приобретенного иммунодефицита (СПИД) является
одним из наиболее ярких иммунодефицитных состояний. Впер-
вые описан в научной литературе в 1981 г. Однако ретроспектив-
ный анализ свидетельствует о том, что СПИД поражал людей и
ранее. Первые случаи синдрома были зарегистрированы в США,
Африке, на Гаити. В последние годы установлено, что каждые
12—14 мес число зарегистрированных случаев заболевания удваи-
вается. Наибольшее распространение СПИД имеет среди гомо- и
бисексуальных мужчин; наркоманов, вводящих наркотики внут-
ривенно и пользующихся "коллективными" шприцами; реципи-
ентов гемотрансфузий (больные анемиями); детей, родители ко-
торых больны СПИДом.
Возбудителем СПИДа является вирус, который обозначают
как ВИЧ — вирус иммунодефицита человека или ЛАВ — лимфа-
денопатический вирус. Он относится к группе ретровирусов под-
семейства лентивирусов. Ретровирусы содержат однонитчатую
линейную РНК и фермент ревертазу. Репликация вирусной нук-
леиновой кислоты идет через стадию синтеза двунитчатой ДНК
на матрице РНК, т. е. как бы обратным путем (отсюда название
фермента — ревертаза и группы вирусов — ретровирусы).
Попав в организм, возбудитель СПИДа внедряется в клетки,
содержащие рецептор Т4, к которому вирусы высокоспецифичны.
Наиболее богаты такими рецепторами Т-лимфоциты-хелперы.
Однако, помимо этих клеток, вирус способен внедряться также и
в моноциты, тканевые макрофаги, клетки глии, нейроны. В ядро
клетки-мишени проникает ДНК-копия с РНК вируса, которая
внедряется в клеточный геном. Вирус обнаруживается в крови, в
ткани слюнных желез, предстательной железы, яичек. Через 6—
8 нед (реже через 8—9 мес) после инфицирования организма в
крови появляются антитела к ВИЧ. С этого момента инфициро-
вание организма может быть выявлено современными методами.
Действие ВИЧ на клетки организма приводит к их лизису и
уменьшению их числа. В наибольшей мере это относится к Т-
лимфоцитам-хелперам. Именно поэтому развивается лимфопе-
ния. Одновременно примерно на 80—90 % снижаются количество
136
и функциональная активность Т-лимфоцитов-киллеров. Число В-
лимфоцитов, как правило, остается в пределах нормы, но функ-
циональная активность их снижена.
Количество макрофагов и других А-клеток не изменяется, од-
нако нарушаются хемотаксис и внутриклеточное переваривание
чужеродных агентов. Нарушается также механизм представления
макрофагом антигена Т- и В-лимфоцитам. Эти изменения созда-
ют предрасположенность больных СПИДом к инфекциям, лим-
форетикулярным опухолям — к саркоме Капоши.
В лимфатических узлах больных СПИДом выявляется гипер-
плазия фолликулов, в основном за счет увеличения количества Т-
супрессоров. Содержание Т-хелперов значительно снижено. В ти-
мусе обнаруживается атрофия эпителиальных и уменьшение чис-
ла лимфоидных клеток. Таким образом, СПИД представляет со-
бой вариант комбинированного иммунодефицитного состояния.
ТоЛэрантнэсть
Толерантность (от лат. tolerantia — переносимость, терпи-
мость) — состояние, характеризующееся "терпимостью", т. е. от-
сутствием реакции иммунной системы на чужеродные антигены.
При этом состоянии в иммунной системе нарушена выработка
иммунных лимфоцитов, либо клетки иммунной системы не выра-
батывают антител, либо не реализуется эфферентное звено имму-
нитета — уничтожение и элиминация носителя чужеродной анти-
генной информации.
Толерантность может быть подразделена на три разновидно-
сти: физиологическую, патологическую и индуцированную.
Основные механизмы патологической толерантности:
• отсутствие, недостаточное количество или нарушение
функции клеток иммунной системы, т. е. иммунодефицит-
ное состояние;
Физиологическаятолерантностъ—терпимость иммунной сис-
темы антигенов собственных белков организма. При этом те кло-
ны иммунных клеток, которые в период эмбрионального разви-
тия подвергаются массированному воздействию антигенов собст-
венных белков, гибнут и выводятся из организма.
Одной из форм физиологической толерантности является изо-
ляционная толерантность. Она распространяется на антигены
клеток тканей, изолированных от иммунокомпетентной системы
структурно-физиологическими барьерами. К ним относятся ткань
головного мозга, хрусталик глаза, яички, щитовидная железа.
Патологическая толерантность. В этом случае речь идет о
"терпимости" иммунной системой чужеродных антигенов, чаще
всего бактерий, вирусов, многоклеточных паразитов, клеток зло-
качественных опухолей или трансплантата.
• повышение активности Т- и В-лимфоцитов-супрессоров,
которые тормозят созревание "эффекторных" клеток им-
137
мунной системы — Т-лимфоцитов-киллеров и плазматиче-
ских клеток;
• угнетение или блокада реакций клеточного иммунитета на
антиген.
Это происходит тогда, когда специфические иммуноглобули-
ны, взаимодействуя с антигенами клеток не способны инактиви-
ровать их. Антигенные детерминанты клеток закрываются ("экра-
нируются") этими "недееспособными" антителами или комплек-
сами "антиген—антитело". Т-лимфоциты-киллеры в таком случае
не способны обнаружить "экранированную" чужеродную клетку.
Индуцированная толерантность (искусственная, лечебная)
достигается с помощью воздействий, целенаправленно подавляю-
щих активность иммунных клеток, таких как ионизирующее из-
лучение, высокие дозы цитостатиков, иммунодепрессанты. Они
вызывают лизис, торможение или блокаду деления и созревания
клеток иммунной системы. Индуцированную толерантность в ме-
дицине используют с целью повышения успеха трансплантации
органов и тканей, лечения аллергических реакций.
Реакция "трансплантантат против хозяина" (РТПХ)
Реакция развивается в случае трансплантации реципиенту
большой массы тканей донора, содержащих иммунные клетки
(например, костного мозга или лейкоцитной массы). Течение
РТПХ усугубляется при пониженной активности иммунной сис-
темы "хозяина" (например, при воздействии ионизирующего из-
лучения. иммунодепрессантов). РТПХ характеризуется поражени-
ем органов и тканей иммунокомпетентной системы реципиента,
а также повреждением кожи, желудочно-кишечного тракта (осо-
бенно в зоне расположения групповых лимфатических фоллику-
лов — пейеровых бляшек), печени.
Клинико-морфологические проявленияРТПХ заключаю тсяв раз-
витии некротических и дистрофических поражений указанных
органов, лимфопении, анемии, тромбоцитопении, диспепсиче-
ских расстройств (тошнота, рвота, диарея), увеличении печени. У
взрослых описанное состояние обозначают термином "гомологи-
ческая болезнь" (следствие гомотрансплантации клеток иммун-
ной системы), у новорожденных — как "рант-болезнь" — болезнь
малого роста (в связи с нарушением физического развития ребен-
ка, которому имплантировали ткань, содержащую клетки иммун-
ной системы).
АЛЛЕРГИЧЕСКИЕ РЕАКЦИИ
Аллергия — одна из форм иммунопатологических процессов,
характеризующихся повышением чувствительности организма к
повторным воздействиям аллергенов. Проявляется аллергия, в от-
138
личие от иммунитета, повреждением собственных тканей орга-
низма и снижением эффективности его адаптивных реакций. Это
нередко приводит к тому, что носитель чужеродного антигена не
разрушается до конца или не элиминируется из организма. Вме-
сте с тем в целом аллергия, так же как и иммунитет, способствует
поддержанию антигенной индивидуальности и однородности ор-
ганизма путем удаления из него чужеродных агентов-аллергенов.
Аллергические реакции встречаются у 10—20 % населения.
Одной из причин широкой распространенности аллергии счита-
ются "химизация" жизни современного человека, прием некото-
рых лекарственных препаратов, а также иногда профилактиче-
ские прививки.
Аллергия формируется под воздействием аллергенов — агентов
антигенной или гаптенной природы, а также некоторых физиче-
ских факторов (высокой или низкой температуры, ультрафиоле-
тового и ионизирующего излучений и др.).
Виды аллергенов
По происхождению:
Экзогенные аллергены:
• пищевые (алиментарные), к которым относятся многие
продукты питания (например, шоколад, яйца, молоко, раз-
личные ягоды);
• лекарственные аллергены. Широкое применение лекарст-
венных препаратов (особенно антибиотиков, вакцин) при-
вело к сенсибилизации (повышенной чувствительности)
миллионов людей, развитию у них аллергических осложне-
ний и заболеваний (отеков, кожного зуда, крапивницы,
анафилактического шока и др.);
• пыльцевые аллергены. Пыльца многих растений, представ-
ляющая собой комплекс белков с углеводами или пигмен-
тами пыльцы, вызывает аллергическое заболевание — пол-
линоз. характеризующийся преимущественным поражением
дыхательных путей и слизистой оболочки глаз;
• пылевые аллергены вызывают аллергическое поражение
преимущественно органов дыхания. (Бытовая пыль имеет
сложный состав. В нее входят остатки органических ве-
ществ животного, растительного, микробного происхожде-
ния, синтетических тканей, пластмасс, а также неорганиче-
ские соединения. Одним из наиболее активных действую-
щих начал домашней пыли являются микроскопические
клещи. Производственная пыль приобретает антигенность
за счет бактериального и особенно грибкового заражения, а
также примесей пестицидов, гербицидов, минеральных ве-
ществ. частиц насекомых и др.);
• эпидермальные аллергены (роговые чешуйки кожи, перьев
птиц, частицы шерсти животных и т. п.);
139
• бытовые химические соединения (различные красители,
стиральные порошки, кремы, косметические средства, дез-
одоранты и др.);
• сывороточные аллергены — препараты крови животных и
человека, содержащие антитела, которые нередко использу-
ются для диагностики, лечения и профилактики различных
заболеваний;
• инфекционно-паразитарные аллергены — различные мик-
роорганизмы, вирусы, грибы, паразиты и т. д.;
• физические факторы (высокая или низкая температура, из-
лучения с различной длиной волны и др.).
Эндогенные аллергены. К ним относятся компоненты клеток и
тканей собственного организма (белки, полипептиды, крупномо-
лекулярные полисахариды, липополисахариды), приобретающие
аллергенные свойства в результате:
• действия физических, химических, инфекционных и других
факторов экзогенного происхождения, приводящего к обра-
зованию в организме человека денатурированных белков
или комплексов белков организма с экзогенными аллерге-
нами (гаптенами), чаще всего с липидами, нуклеиновыми
кислотами, многими лекарственными препаратами;
• повреждения клеток, становящихся мишенями для иммун-
ной системы (например, клетки, на которых фиксируется
гаптен).
По путям проникновения аллергенов в организм:
• респираторные, т. е. проникающие через дыхательные пу-
ти. Так проникают пыльца, пыль, аэрозоли, эпидермаль-
ные аллергены, некоторые лекарственные препараты и
т. д.;
• алиментарные, т. е. проникающие через пищеварительный
тракт. Пищевые аллергены вызывают аллергические забо-
левания не только органов пищеварения, но также и дыха-
ния (аллергический ринит, бронхиальную астму), кожи и
слизистых оболочек (крапивницу, аллергическую экзему и
т. Д-);
• "контактные" (через кожу и слизистые оболочки). Таким
способом могут проникать различные низкомолекулярные
вещества или местно применяемые лекарственные средства
(например, мази, содержащие антибиотики), красители,
древесные смолы, кремы и др.);
• парентеральные — обычно внутривенное введение препара-
тов крови, лекарственных препаратов, а также яды насеко-
мых — пчел, комаров и др., попадающих в кровоток;
• трансплацентарные (некоторые лекарственные средства, на-
пример антибиотики, белковые препараты и др.).
140
ВИДЬ! АЛЛЕРГИЧЕСКИХ РЕАКЦИЙ
В зависимости от вида клеток иммунной системы, принимаю-
щих участие в развитии аллергии, условно различают В-лимфо-
цитзависимые (гуморальные, иммуноглобулиновые) и Т-лимфо-
цитзависимые ("клеточные") аллергические реакции.
К группе В-лимфоцитзависилых относят такие формы аллер-
гии. в механизмах которых ведущую роль играют продуцируемые
В-лимфоцитами циркулирующие в крови гуморальные антитела,
принадлежащие к различным классам иммуноглобулинов — IgE,
IgG, IgM. В-лимфоцитзависимые иммуноглобулиновые реакции
гиперчувствительности могут быть "перенесены" от сенсибилизи-
рованного организма в другой с помощью сыворотки, содержа-
щей эти аллергические антитела, что называется "пассивным пере-
носом аллергии ".
К группе Т-лимфоцитзависимых относят аллергические реак-
ции, в патогенезе которых ведущая роль принадлежит Т-лимфо-
цитам и продуцируемым ими биологически активным вещест-
вам — лимфокинам. Последние выполняют роль посредников
(медиаторов) в механизмах аллергии. Причинами развития таких
реакций могут быть антигены чужеродных тканей и клеток, низ-
комолекулярные химические соединения, в том числе некоторые
местно применяемые лекарственные средства (например, анти-
биотики), антигены микроорганизмов.
Состояние аллергии этого типа может быть "пассивно" перене-
сено от больного человека здоровому сенсибилизированными
лимфоцитами или "экстрактом" из таких клеток, например при
переливании крови или введении сывороточных препаратов.
В зависимости от скорости развития морфологических измене-
ний и клинических проявлений после повторного действия на
сенсибилизированный организма антигена (его называют "разре-
шающим") аллергические реакции (реакции гиперчувствительно-
сти) делят на три типа:
— реакции гиперчувствительности немедленного типа;
— реакции гиперчувствительности позднего, или отсроченно-
го, типа;
— реакции гиперчувствительности замедленного типа.
Реакции гиперчувствительности немедленного типа проявля-
ются сразу или через несколько минут после повторного контакта
организма с аллергеном (например, аллергический ринит, конъ-
юнктивит. анафилактический шок).
Реакции гиперчувствительности позднего типа выявляются че-
рез несколько часов (но не позднее 5—6 ч) после контакта с раз-
решающим антигеном (например, гемолитическая анемия аллер-
гического генеза, некоторые разновидности сывороточной бо-
лезни).
Реакция гиперчувствительности замедленного типа регистри-
руются обычно через несколько часов или, чаще, суток после по-
вторного "разрешающего" воздействия аллергена на сенсибилизи-
141
рованный организм (например, туберкулиновая реакция или кон-
тактный дерматит).
В зависимости от особенностей механизмов развития реакции
гиперчувствительности немедленного и позднего типов развива-
ются в результате взаимодействия антигена с антителами сенси-
билизированного организма — иммуноглобулинами. Реакция ги-
перчувствительности замедленного типа реализуется в основном
с участием сенсибилизированных клеток — Т-лимфоцитов, их
лимфокинов, а также макрофагов. Однако в патогенезе аллерги-
ческих реакций участвуют механизмы, как правило, не одного, а.
возможно, всех типов гиперчувствительности. И поэтому боль-
шинство болезней и реакций аллергического генеза являются
комбинированными по своему механизму.
СТАДО! И МЕХАНИЗМЫ РАЗВИТИЯ АЛЛЕРГИЧЕСКИХ РЕАКЦИЙ
В развитии аллергии выделяют три стадии: I — иммуногенная
(или сенсибилизации); II — патохимическая (образование, акти-
вация и реализация эффектов медиаторов аллергии) и Ш — кли-
нико-морфологическая (морфологические проявления аллергиче-
ской реакции).
I. Иммуногенная стадия начинается с момента первого контак-
та аллергена с клетками иммунной системы и заключается в ини-
циации аллергической реакции: развивается состояние сенсибили-
зации, т. е. повышенной чувствительности организма к данному
антигену (аллергену). В этот период образуются специфические
антитела или сенсибилизированные (активированные) лимфоци-
ты к определенному антигену и накоплению их преимущественно
в определенной ткани.
По механизму формирования различают активную и пассив-
ную сенсибилизацию.
Активная сенсибилизация развивается при попадании в орга-
низм даже минимальных количеств антигена. Пассивная сенсиби-
лизация формируется после введения реципиенту сыворотки кро-
ви, содержащей специфические, сенсибилизирующие гумораль-
ные антитела, или цельной крови, содержащей лимфоциты от ак-
тивно сенсибилизированного донора.
II. Патохимическая стадия. После взаимодействия образовав-
шихся специфических антител или сенсибилизированных лим-
фоцитов с антигеном начинаются патохимические изменения в
организме. В реакциях гиперчувствительности немедленного и
позднего типов образование комплекса антиген—антитело в
сенсибилизированном организме вызывает активацию клеточ-
ных и сывороточных протеолитических и липолитических фер-
ментов, высвобождение клетками крови и тканей медиаторов
воспаления.
При развитии аллергических реакций гиперчувствительности
замедленного типа патохимическая стадия характеризуется акти-
142
вацией синтеза и высвобождением лимфокинов сенсибилизиро-
ванными лимфоцитами.
III. Клинико-морфологическая стадия. Образующиеся при ал-
лергизации организма гуморальные антитела и Т-лимфоциты-
киллеры, взаимодействуя со свободным либо фиксированным на
клетках и неклеточных структурах антигеном, вызывают прямое
или опосредованное (через соответствующие медиаторы аллер-
гии) повреждение клеток и тканей.
Для аллергии немедленного и отсроченного типов характерно
быстрое развитие местных морфологических изменений вплоть
до некроза тканей, а иногда и общих нарушений, включая разви-
тие шока. К наиболее значительным изменениям такого рода от-
носятся:
• вазомоторные реакции (местные и системные), приводящие
к различным изменениям кровяного давления, регионарно-
го кровообращения, микроциркуляции, развитию плазмор-
рагии и фибриноидного некроза стенок сосудов;
• повышение проницаемости стенок сосудов, нередко сопро-
вождающееся диапедезом эритроцитов и ведущее к разви-
тию отеков, волдырей и кровоизлияний;
• спастические сокращения гладких мышечных клеток брон-
хиол, кишечника и других органов, что проявляется асфик-
сией. диспепсическими расстройствами (рвотой, диареей,
болями в животе) и т. д.;
• раздражение нервных рецепторов (в основном биогенными
аминами и кининами), приводящее к развитию чувства бо-
ли. зуда, жжения и т. п.
Структурно-функциональные повреждения при реакции ги-
перчувствительности замедленного типа связаны с развитием
вначале экссудативного воспаления, которое сменяется продук-
тивным воспалением с выраженной мононуклеарной инфильт-
рацией тканей. При персистенции антигена макрофаги транс-
формируются в эпителиоидные клетки с образованием грану-
лем.
ХАРАКТЕРИСТИКА ОТДЕЛЬНЫХ ВИДОВ АЛЛЕРГИЧЕСКИХ РЕАКЦИЙ
Анафилактический шок развивается у человека в ответ на внут-
ривенное введение антигена, к которому организм хозяина был
предварительно сенсибилизирован. Таким антигеном являются
чужеродные белки, например антисыворотки, гормоны, фермен-
ты. производные витамина В । препараты из группы пеницилли-
на, причем даже в минимальных дозах.
Развитие анафилактического шока связано с активацией IgE,
который через ряд сложных реакций вызывает дегрануляцию туч-
ных клеток и базофилов с выбросом медиаторов анафилаксии —
гистамина, лейкотриенов, факторов активации тромбоцитов
(ФАТ), фактора некроза опухолей (ФИО) и др. В результате раз-
143
вития спазма гладких мышц бронхов, желудочно-кишечного
тракта нарушается дыхание, появляются боли в животе, рвота,
понос. Резко повышается проницаемость сосудов с развитием
отека слизистых оболочек, особенно легких, усилением секреции
слизи. Появляется кожный зуд, крапивница. В финале развивает-
ся коллапс и наступает потеря сознания. Смерть может наступить
в течение получаса при явлениях асфиксии, тяжелого поражения
почек, печени, желудочно-кишечного тракта, сердца.
Острая крапивница и отек Квинке — проявления местной
анафилаксии или атопической аллергии. Около 10 % населения
страдает от местной анафилаксии, возникающей в ответ на по-
падание в организм аллергенов — пыльцы растений, перхоти
животных, домашней пыли и т. п. При этом значительно повы-
шается проницаемость сосудистых стенок с развитием отеков,
появлением мучительного кожного зуда, тошноты, болей в жи-
воте. иногда рвоты, озноба. При отеке Квинке в результате бы-
стро нарастающего отека области шеи и лица появляются на-
пряжение тканей, увеличение размеров губ, век, носа, ушей,
языка. Наступает отек слизистой оболочки трахеи, особенно в
области голосовых связок, появляется осиплость голоса и раз-
вивается асфиксия. Иногда отек распространяется на слизистые
оболочки органов пищеварительного тракта с нарушением гло-
тания и развитием острой кишечной непроходимости. Возмо-
жен отек мозга.
Острая сывороточная болезнь возникает после многократных
введений чужеродной сыворотки крови при пассивной иммуниза-
ции. При этом в крови образуются иммунные комплексы анти-
ген—антитело, которые, осаждаясь в различных тканях, вызыва-
ют воспалительные реакции. Появляются лихорадка, кожный зуд,
озноб, головная боль, потливость. Иногда развиваются тошнота,
рвота, боль в животе, перемежающиеся боли в суставах. Нарас-
тающее острое воспаление сосудов, поврежденных циркулирую-
щими иммунными комплексами (некротизирующий васкулит),
проявляется появлением кожных высыпаний, поражением почеч-
ных клубочков. Продолжительность заболевания от нескольких
дней до 2—3 нед.
Феномен Артюса может развиваться у больного через 4—10 ч
после повторного введения в то же место лекарственных препара-
тов ("ягодичные реакции"). В области инъекций развивается экс-
судативно-некротическая реакция в виде некроза тканей, сопро-
вождающегося выраженным отеком, гиперемией кожи, резкой
болезненностью, кожным зудом. В основе феномена лежит экссу-
дативно-некротическая реакция в виде фибриноидного некроза
стенок сосудов, что может сопровождаться тромбозом или крово-
излиянием.
Аллергические заболевания, развивающиеся по механизму ги-
перчувствительности замедленного типа (клеточно-опосредованно-
го). Эти заболевания вызывают специфически сенсибилизиро-
ванные Т-лимфоциты, прежде всего СД4 и СД8 (т. е. Т-лимфо-
144
циты-супрессоры и Т-лимфоциты-киллеры). Это основной тип
иммунного ответа на внутриклеточные микробные агенты, осо-
бенно микобактерии туберкулеза, а также на многие вирусы, гри-
бы, простейшие, паразиты. Примером такой реакции служит ре-
акция на внутрикожно введенный туберкулин — компонент стен-
ки микобактерии туберкулеза. У пациента, уже сенсибилизиро-
ванного микобактерией туберкулеза, через 8—12 ч возникает по-
краснение и уплотнение в месте введения туберкулина, а пик ре-
акции наступает через 24—72 ч, когда в дерме и подкожной клет-
чатке накапливаются мононуклеарные клетки, преимущественно
вокруг венул, образуя периваскулярные манжетки. При этом пре-
обладают Т-лимфоциты (СД4). В зоне инъекции может разви-
ваться некроз.
Болезни иммунной аутоагрессии (БИА), или аутоиммунные бо-
лезни. К ним относят нарушения жизнедеятельности организма,
вызванные развитием иммунопатологических реакций, направ-
ленных против собственных клеток и неклеточных структур.
Сущность этих заболеваний заключается в потере клетками и
тканями организма аутотолерантности.
Конкретные причины и механизмы отдельных аутоиммунных
заболеваний сложны и еще недостаточно изучены. К числу наибо-
лее исследованных механизмов происхождения БИА относят:
• БИА обусловленные патологическими изменениями в сис-
теме иммунобиологического надзора (мутацией пролифери-
рующих иммуноцитов, расстройством оптимального соот-
ношения количества или активности Т-, В-лимфоцитов-
сугрессоров и Т-лимфоцитов-хелперов, отменой невоспри-
имчивости Т-лимфоцитов к аутоантигенам, антигеннеспе-
цифической поликлональной активацией лимфоцитов);
• БИА вызванные патологическими изменениями вне систе-
мы иммунобиологического надзора [отсутствием естествен-
ной толерантности к собственным антигенным структурам,
изменением антигенов организма, мутацией (изменением)
генома отдельных клеток организма, внедрением экзоген-
ных антигенов, сходных с собственными антигенами].
БОЛЕЗНИ ИММУННОЙ АУТОАГРЕССИИ
В зависимости от доминирующего механизма развития выде-
ляют:
— болезни иммунной аутоагрессии, развивающиеся в основ-
ном с участием иммуноглобулинов, например тиреоидит Хаши-
мото, гемолитическая анемия, тромбоцитопения, лейкопения,
системная красная волчанка;
— аутоиммунные болезни, развивающиеся в основном с уча-
стием Т-киллеров, например отдельные разновидности полимио-
зита и синдрома Шегрена;
— аутоиммунные болезни, развивающиеся с участием обоих
145
звеньев иммунного ответа, например синдром Шегрена, при ко-
тором происходит поражение слезных, слюнных, слизистых и др.
желез, проявляющийся поражением глаз (сухой кератоконъюнк-
тивит), слизистой оболочки рта (ксеростомия); склеродермия;
дермато- и полимиозит.
В зависимости от числа пораженных органов различают моно-
органные (или органоспецифические аутоиммунные болезни) и
полиорганные БИА (сип.: системные, генерализованные).
При люноорганных БИА аутоагрессивные Т-киллеры или спе-
цифические антитела взаимодействуют с антигенными структура-
ми только одного органа.
Примерами являются тиреоидит Хашимото и анемия Аддисо-
на—Бирмера (пернициозная). При тиреоидите Хашимото имму-
ноглобулины (антитела) строго специфичны по отношению к ан-
тигену — белку щитовидной железы тиреоглобулину. В результате
этого взаимодействия гибнет функциональная ткань щитовидной
железы.
В случае анемии Аддисона—Бирмера в крови выявляются ау-
тоагрессивные иммуноглобулины к измененному внутреннему
фактору Касла — гастромукопротеину, образующемуся в слизи-
стой оболочке желудка и являющемуся важнейшем звеном регу-
ляции гемопоэза.
При полиорганных БИА действие аутоиммунных Т-киллеров и
антител направлено против антигенных структур многих органов
и тканей организма.
Причины: наличие у них сходного антигена, низкая специ-
фичность аутоагрессивных Т-лимфоцитов и антител. Примером
может служить системная красная волчанка, при которой аутоим-
муноглобулины (аутоантитела) взаимодействуют с определенны-
ми антигенами ядер и цитоплазмы клеток многих тканей и орга-
нов, в том числе полиморфно-ядерных лейкоцитов.
Глава 9
ЗНАЧЕНИЕ ФАКТОРОВ ОКРУЖАЮЩЕЙ СРЕДЫ
И РЕАКТИВНОСТИ ОРГАНИЗМА В ПАТОЛОГИИ
ОСНОВНЫЕ ГРУППЫ ПОВРЕЖДАЮЩИХ ФАКТОРОВ
Каждая болезнь имеет свою причину, без которой она не мо-
жет возникнуть и которая обусловливает признаки, характерные
для данной болезни. В качестве причин болезней выступают мно-
гочисленные факторы окружающей и внутренней среды организ-
ма — патогенные факторы.
146
Виды патогенных факторов
1. По происхождению:
• экзогенные, например чрезмерно высокая или низкая темпе-
ратура воздуха; воздействие электрического тока, механиче-
ские воздействия: микробы, находящиеся в продуктах пита-
ния или воздухе;
• эндогенные, например избыток или недостаток гормонов
или ферментов; высокий уровень свободных радикалов и
перекисей органических веществ; отложения в тканях солей
кальция.
В свою очередь экзо- и эндогенные патогенные факторы могут
быть:
• инфекционными (различные микроорганизмы — бактерии,
вирусы риккетсии, грибы, прионы);
• неинфекционнылм (например, чужеродные белки, попавшие
в кровь; продукты поврежденных тканей и др.; воздействие
пламени, холодной воды, кислоты, щелочи).
2. По природе:
физические факторы, например проникающая радиация, воз-
действие низкой или высокой температуры, электрического тока;
увеличение или снижение барометрического давления и др.;
химические факторы, например кислоты, щелочи, лекарствен-
ные препараты в избыточной дозе; пестициды; недостаток или
избыток кислорода в тканях; органические растворители; продук-
ты обмена веществ, которые в норме выводятся из организма —
аммиак и его соединения, фенолы;
биологические агенты, например микроорганизмы или чуже-
родные белки, попавшие в кровь.
Причиной заболеваний являются также дефекты генетическо-
го аппарата, реализующие свое патогенное действие через пер-
вичные нарушения метаболизма.
Важно, что даже обычный фактор среды может стать чрезвы-
чайным в связи с чрезмерной длительностью воздействия на ор-
ганизм или нарушением естественных биоритмов (длительное
звуковое раздражение или полная тишина; одиночество, пребы-
вание в темноте, вибрация, гипокинезия, запыленность воздуха,
хроническая нервно-психическая перегрузка и т. п.).
Особое место занимают индифферентные воздействия, в том
числе не материального, а информационного характера, ранее со-
четавшиеся с действием на организм какого-либо патогенного
фактора. Такие воздействия могут, иногда даже после однократ-
ного сочетания, сами стать патогенными. Механизм условного
патогенного рефлекса лежит, например, в основе возникновения
тошноты при виде пищи, однажды вызвавшей рвоту в связи с ее
недоброкачественностью. Подобный механизм может лежать в
основе приступов стенокардии или бронхиальной астмы и др.
147
ЗНАЧЕНИЕ УСЛОВИЙ В ВОЗНИКНОВЕНИИ БОЛЕЗНЕЙ
Один и тот же патогенный фактор может приводить к раз-
личным результатам в зависимости от условий, в которых про-
исходит его взаимодействие с организмом. Под условиями по-
нимают какие-либо обстоятельства или воздействия, которые
сами по себе не могут вызвать заболевания, но ослабляют, уси-
ливают или модифицируют действие этиологических факторов.
Так, высокая температура воздуха при низкой влажности может
не вызвать каких-либо расстройств жизнедеятельности, а в ус-
ловиях высокой влажности стать для организма чрезмерной и
привести к гипертермии или тепловому удару. При этом очевид-
но, что сама по себе высокая влажность не может вызвать теп-
лового удара.
Знание причин и условий (в совокупности их обозначают тер-
мином "этиология") возникновения болезни или патологического
процесса позволяет сформулировать принципы этиотропного ле-
чения и профилактики. К ним относятся:
• установление этиологического фактора, его устранение, ос-
лабление патогенных свойств или ограждение организма от
его воздействия;
• выявление условий, влияющих на патогенный эффект при-
чинного фактора, и их изменение в благоприятном для ор-
ганизма направлении.
ЗНАЧЕНИЕ РЕАКТИВНОСТИ ОРГАНИЗМА
В ВОЗНИКНОВЕНИИ И РАЗВИТИИ БОЛЕЗНЕЙ
Наряду с особенностями этиологических факторов большое
значение имеют свойства самого организма, подвергающегося па-
тогенному воздействию, — его реактивность — свойство организ-
ма определенным образом реагировать на воздействие факторов
внешней и внутренней среды изменениями жизнедеятельности.
ВИДЬ! РЕАКТИВНОСТИ
В зависимости от биологических свойств организма выделяют
видовую, групповую и индивидуальную реактивность.
Видовая реактивность определяется особенностями вида, к ко-
торому принадлежит животное (например, атеросклероз наблюда-
ется у людей, но не выявляется у кроликов: у животных, в отли-
чие от человека, также не развивается сифилис и другие венери-
ческие болезни).
Групповая реактивность. В ней выделяют:
• возрастную реактивность (например, дети в большой мере,
чем взрослые, подвержены инфекционным заболеваниям в
связи с незрелостью их иммунной системы);
148
• половую реактивность, которая характеризуется, в частно-
сти, разной устойчивостью мужчин и женщин к кровопоте-
ре (у женщин она выше), физической нагрузке (выше у
мужчин):
• конституциональную реактивность (относительно стабиль-
ные морфофункциональные особенности организма, обу-
словленные наследственностью и длительным влиянием
факторов окружающей среды). Например, так называемые
"астеники", в отличие от "нормостеников", менее устойчивы
к сильным и длительным физическим и психическим на-
грузкам.
Индивидуальная реактивность определяется наследуемой гене-
тической информацией и индивидуальной изменчивостью орга-
низма. В отличие от первых двух категорий индивидуальная реак-
тивность организма может быть физиологической и патологиче-
ской. Последнее проявляется, например, развитием у отдельных
людей аллергических реакций на факторы, которые у других та-
кого ответа не вызывают.
В зависимости от степени специфичности ответа организма раз-
личают специфическую и неспецифическую реактивность.
Специфическаяреактивностъ — например, развитие иммунно-
го ответа на антигенное воздействие; неспецифическая реактив-
ность — такая как активация фагоцитарной реакции лейкоцитов
при их контакте с бактериями, вирусами, паразитами.
В зависимости от выраженности реакции организма на воздей-
ствие:
• нормергическая реактивность выражается количественно и
качественно адекватной реакций на воздействие патогенно-
го фактора;
• гиперергическая реактивность проявляется чрезмерной ре-
акцией на раздражитель, например развитием анафилакти-
ческого шока на повторное попадание в кровь антигена;
• гипергическая реактивность характеризуется неадекватной,
слабой реакцией на воздействие, например неэффективным
иммунным ответом на чужеродный антиген при развитии
иммунодефицитного состояния.
В зависимости от природы патогенного фактора, вызывающего
ответ организма, выделяют неиммуногенную и иммуногенную ре-
активность.
Неимлуногенная реактивность характеризуется изменениями
жизнедеятельности организма, вызванными воздействием различ-
ных факторов психического, химического или биологического ха-
рактера, не обладающих антигенными свойствами.
Иммуногенная реактивность проявляется изменениями жиз-
недеятельности организма, обусловленными антигенными факто-
рами.
В зависимости от биологической значимости ответа организма
выделяют физиологическую и патологическую реактивность.
Физиологическая реактивность представляет собой ответ, аде-
149
кватныи характеру и интенсивности воздействия, а также играет
адаптивную роль (примером может служить одна из разновидно-
стей иммуногенной реактивности — иммунитет).
Патологическая реактивность неадекватна воздействию по
выраженности или характеру изменения реакция организма, со-
провождается снижением его адаптивных возможностей (пример:
аллергические реакции).
Реактивность — динамичное, постоянно меняющееся свойство
организма. Это свойство можно изменять целенаправленно с це-
лью повышения устойчивости организма к действию различных
патогенных факторов.
Факторы реактивности организма в значительной мере опре-
деляют другое важное его свойство — резистентность — устойчи-
вость организма, его отдельных органов или тканей к воздействию
определенных факторов внешней и внутренней среды (например, ги-
поксии, холоду или токсинам).
РОЛЬ НАСЛЕДСТВЕННОСТИ В ПАТОЛОГИИ
Наследственность — свойство организмов сохранять и обеспе-
чивать передачу морфофункциональных признаков потомкам, а
также программировать особенности их индивидуального разви-
тия в конкретных условиях окружающей среды. Отсюда следует,
что состояния здоровья и болезни — результат взаимодействия
наследственных и средовых факторов.
В отличие от этого изменчивость — свойство организмов при-
обретать новые морфофункциональные признаки и особенности
индивидуального развития, отличающиеся от родительских. Но-
вые признаки могут служить основой для эволюции вида при ус-
ловии их наследования. Часть изменчивости проявляется только
изменением самого признака; другая часть затрагивает генетиче-
ский аппарат.
ПРИЧИНЫ НАСЛЕДСТВЕННОЙ ПАТОЛОГИИ
Инициальным ("стартовым") звеном механизма наследствен-
ных форм патологии являются мутации — нарушения структуры
генов, хромосом или изменения их числа. Причинами мутаций
могут быть различные факторы физической, химической, биоло-
гической природы — мутагены.
Физические мутагены:
• ионизирующие излучения (например, альфа-, бета-, гамма-
рентгеновское, нейтронное);
• ультрафиолетовое излучение;
• чрезмерно высокая или низкая температура внешней среды
Химические мутагены — самая многочисленная группа. К ним
относятся:
150
• сильные окислители или восстановители (например, нитра-
ты. нитриты, активные формы кислорода);
• пестициды (например, гербициды, фунгициды);
• некоторые пищевые добавки (например, ароматические уг-
леводороды);
• продукты переработки нефти;
• лекарственные препараты (например, цитостатики, ртутьсо-
держащие средства, иммунодепрессанты) и другие химиче-
ские соединения.
Биологические мутагены:
• вирусы;
• антигены некоторых микробов.
ВИДЫ МУТАЦИЙ
По причине:
• спонтанные — возникают под влиянием естественных му-
тагенов экзо- или эндогенного происхождения, без специ-
ального (целенаправленного) вмешательства человека.
Спонтанные мутации возникают, например, в результате
действия химических веществ, образующихся в процессе
обмена веществ, воздействия естественного фона радиа-
ции или ультрафиолетового излучения; ошибок реплика-
ции ит. д.;
• индуцированные — вызваны случайным или умышленным
воздействием факторов внешней или внутренней среды.
По биологическому значению:
• патогенные — вызывают развитие патологии;
• нейтральные — не влияют на жизнедеятельность организма
(например, мутации, вызывающие веснушки, изменение
цвета волос, радужки глаз);
• благоприятные — повышают жизнедеятельность организма
или вида (например, темная окраска кожных покровов у
жителей африканского континента).
По уровню ("масштабу") изменения генетического материала:
• генные (сип.: точковые) мутации — любые изменения мо-
лекулярной структуры ДНК, которые приводят к развитию
генных болезней. Эти мутации проявляются признаками
нарушений метаболизма в организме. Например, гемофи-
лии, которые характеризуются дефектом факторов сверты-
вающей системы крови, что проявляется повышенной кро-
воточивостью и кровоизлияниями в ткани.
В зависимости от типа наследования генные болезни разделяют
на несколько групп.
Аутосомно-доминантные. Патогенный доминантный ген, на-
ходящийся в одной из хромосом, закономерно проявляется ка-
кой-либо формой патологии, например полипозом толстого ки-
шечника или семейной гиперхолестеринемией.
151
Аутосомно-рецессивные. Патогенный ген проявляет свои свой-
ства при условии его нахождения в обеих хромосомах, получен-
ных от матери и отца. Примеры: фенилкетонурия, гемофилии,
гликогенозы.
Доминантные, сцепленные с Х-хромосомой. Патогенный ген
находится в Х-хромосоме, вызывает патологию чаще у женщин,
например рахит, устойчивый к лечению препаратами витамина D,
Рецессивные, сцепленные с Х-хромосомой (патогенный ген на-
ходится в Х-хромосоме). Заболевания поражают почти исключи-
тельно лиц мужского пола, а матери являются обязательными но-
сителями патогенного гена, например дальтонизм.
Голандрические, или сцепленные с Y-хромисомюй. Патогенный
ген локализован в Y-хромосоме, а признак передается только от
отца сыновьям, например мужское бесплодие в связи с азооспер-
мией.
Митохондриальные. У человека ДНК содержится и в митохон-
дриях. Мутация ее генов приводит к "митохондриальным болез-
ням": атрофии зрительного нерва, эпилепсии, кардиомиопатии.
Хромосомные мутации (сип.: аберрации). Характеризуются из-
менением структуры отдельных хромосом. При этом обычно не
меняется последовательность нуклеотидов в генах. Однако изме-
нение числа или положения генов может обусловить генетиче-
ский "дисбаланс", что приводит к нарушению нормального разви-
тия организма. Например, хронический миелолейкоз является
следствием утраты участка хромосомы 21-й пары. Удвоение уча-
стка короткого плеча 9-й пары хромосом приводит к развитию
множественных пороков развития, включая микроцефалию, за-
держку физического, психического и интеллектуального разви-
тия.
Геномные мутации характеризуются изменением числа хромо-
сом. К числу наиболее частых геномных мутаций относятся три-
сомия и моносомия.
Трисомия — наличие трех гомологичных хромосом в кариотипе
(например, по 21-й паре, что обусловливает развитие синдрома
Дауна; по 18-й паре — синдрома Эдвардса; по 13-й паре — син-
дрома Патау; по половым хромосомам: синдромы полисемии —
XXX, XXY, XYY).
Моносомия — наличие только одной из двух гомологичных
хромосом. При моносомии по любой из аутосом в подавляющем
большинстве случаев нормальное развитие эмбриона невоз-
можно.
Глава 10
ОПУХОЛИ
ОБЩАЯ ХАРАКТЕРИСТИКА ОПУХОЛЕЙ
Опухоль (тумор, бластома, новообразование, неоплазма) — па-
тологический процесс, в основе которого лежит безграничное и
нерегулируемое размножение клеток с потерей их способности к
дифференцировке. Наука, изучающая причины, механизмы раз-
вития, виды, морфологию и клинику опухолей, а также их по-
следствия, называется онкологией. В отличие от всех других видов
размножения клеток (при воспалении, репаративной регенера-
ции, гипертрофии и т. п.) опухолевый рост не имеет никакого
приспособительного или компенсаторного смысла. Это чисто па-
тологический процесс, который существует столько же времени,
сколько и жизнь на Земле. При этом нет такого живого организ-
ма, в котором не могла бы возникнуть опухоль. Она может разви-
ваться у всех животных, птиц, рыб, насекомых, одноклеточных
растений. Однако наиболее часто опухоли встречаются у людей,
являясь второй среди основных причин смерти.
Эпидемиология опухолей. Одновременно не менее 6 млн чело-
век в мире страдают опухолями, ежегодно около 2 млн из них по-
гибают. В течение года регистрируется примерно 2 млн новых
случаев опухолевых заболеваний. Рост заболеваемости и смертно-
сти от опухолей наблюдается во всех странах мира и во всех воз-
растных группах, но особенно после 50 лет, при этом мужчины
заболевают в 1,5 раза чаще женщин. В структуре заболеваемости
мужчин с 1981 г. ведущее место занимает рак легкого, желудка и
толстой кишки, а у женщин — рак молочной железы, матки и
толстой кишки. Онкологическая заболеваемость зависит от раз-
личных факторов — географических (она различается в разных
странах и регионах), условий труда, быта, экологии, питания на-
селения. В определенной степени рост заболеваемости новообра-
зованиями связан с увеличением продолжительности жизни, по-
скольку у пожилых и старых людей опухоли развиваются чаще. В
России на рубеже XX и XXI веков количество больных злокачест-
венными новообразованиями составляло 303,3 на 100 000 человек
(т. е. около 1 500 000), и в течение года 36,2 % из них умирали.
СТРОЕНИЕ ОПУХОЛЕЙ
Опухоли чрезвычайно многообразны, они развиваются во всех
тканях и органах, могут быть доброкачественными и злокачест-
венными; кроме того, имеются опухоли, занимающие как бы про-
межуточное положение между доброкачественными и злокачест-
153
венными — "пограничные опухоли". Вместе с тем у всех опухолей
есть общие признаки.
Опухоли могут иметь разнообразную форму — либо в виде уз-
лов различной величины и консистенции, либо диффузно, без
видимых границ, прорастают в окружающие ткани. Опухолевая
ткань может подвергаться некрозу, гиалинозу. обызвествлению.
Опухоль нередко разрушает сосуды, вследствие чего возникают
кровотечения.
Любая опухоль состоит из паренхимы (клеток) и стромы (вне-
клеточного матрикса, включающего строму, сосуды микроцирку-
ляции и нервные окончания). В зависимости от преобладания па-
ренхимы или стромы опухоль может быть мягкой или плотной.
Строма и паренхима новообразования отличаются от нормальных
структур тканей, из которых оно возникло. Это отличие опухоли
от исходной ткани называется атипизмом, или анаплазией. Раз-
личают морфологический, биохимический, иммунологический и
функциональный атипизм.
Морфологический атипизм складывается из двух видов: ткане-
вого и клеточного.
Тканевый атипизм характеризуется нарушением взаимоотно-
шений различных элементов исходной ткани. Например, добро-
качественная опухоль кожи папиллома (рис. 33) отличается от
нормальной кожи нарушением взаимоотношения эпидермиса и
дермы: в одних участках эпидермис глубоко и неравномерно по-
гружается в дерму, в других — фрагменты дермы локализуются в
эпидермисе. Количество слоев клеток эпидермиса в разных уча-
стках опухоли различно. Однако сами клетки имеют обычное
строение.
Клеточный атипизм заключается в патологических измене-
ниях клеток паренхимы опухоли, при которых они теряют спо-
собность к созреванию и дифференцировке. Клетка останавли-
вается обычно на ранних стадиях дифференцировки, нередко
уподобляясь эмбриональным клеткам. Это состояние называет-
ся анаплазией: опухолевые клетки имеют разные величину и
форму, ядра увеличиваются в размерах, имеют уродливый вид,
занимают большую часть цитоплазмы клетки, в них увеличива-
ется количество хроматина и ядрышек, постоянно возникают
неправильные митозы. Атипичными становятся и внутриклеточ-
ные структуры: митохондрии приобретают уродливую форму, в
них уменьшается количество крист, эндоплазматическая сеть
неравномерно расширяется, в цитоплазме увеличивается коли-
чество рибосом, лизосом, различных включений. Чем больше
выражен клеточный атипизм, чем больше клетки опухоли отли-
чаются от клеток нормальной ткани, тем злокачественнее опу-
холь, тяжелее ее прогноз. И наоборот, чем более высокой степе-
ни дифференцировки достигли клетки новообразования, чем
больше они имеют сходства с исходной тканью, тем доброкаче-
ственнее течение опухоли.
Биохимический атипизм отражает изменения метаболизма опу-
154
Рис. 33. Папиллома кожи.
холей, который лежит в основе ее безудержного роста. Изменя-
ются все виды обмена веществ, но наиболее характерны измене-
ния углеводного и энергетического метаболизма, результатом ко-
торых является усиление в 10—30 раз анаэробного гликолиза и
ослабление тканевого дыхания. Возникающий при этом ацидоз
неблагоприятно отражается на кислотно-основном состоянии
крови и других тканей. В опухоли синтез белка и нуклеиновых
кислот преобладает над их распадом. Опухолевая ткань активно
поглощает аминокислоты, конкурируя с нормальными тканями, в
ней происходят как количественные, так и качественные измене-
ния белков, нарушается синтез липидов. Опухоль усиленно по-
глощает воду, накапливает ионы калия, способствующего проли-
ферации клеток. При этом снижается концентрация кальция, в
155
результате чего ослабевают межклеточные связи, что способству-
ет инфильтрирующему росту и метастазированию опухоли.
Иммунологический атипизм заключается в том. что клетки опу-
холи отличаются от нормальных своей антигенной структурой.
Существует точка зрения, что опухолевый процесс, особенно
прогрессирование опухоли, происходит только в случае угнетения
иммунной системы организма, что практически всегда наблюда-
ется у онкологических больных. Однако это угнетение в значи-
тельной степени обеспечивается антигенами опухоли.
Функциональный атипизм возникает в результате развития в
опухолях морфологического, биохимического и иммунологиче-
ского атипизма. Он проявляется изменениями функций, харак-
терных для нормальных клеток исходной ткани. В одних случаях,
например при гормонопродуцирующих опухолях эндокринных
желез, специфическая функция их клеток увеличена при отсутст-
вии повышенной потребности организма в гормонах. В других
случаях из-за остановки созревания клеток опухоли они прекра-
щают свою специфическую деятельность. Так, при опухолях кро-
ветворной ткани незрелые клетки миелоидного и моноцитарного
рядов теряют функцию фагоцитоза и поэтому не участвуют в
формировании иммунной защиты организма против опухоли. В ре-
зультате у онкологических больных обычно развивается иммун-
ный дефицит, что способствует возникновению инфекционных
осложнений. Нередко опухолевые клетки начинают выполнять не
характерную для них, извращенную функцию: например, клетки
коллоидного рака желудка продуцируют слизь, специфическую
для кишечника, клетки плазмоцитомы (аналоги плазматических
клеток) при миеломной болезни продуцируют необычные белки —
парапротеины и т. д.
Атипизм опухолей распространяется как на их клетки, так и
на строму, которая возникает вместе с атипичным ростом опухо-
левых клеток.
РОСТ ОПУХОЛЕЙ
Рост опухолей является определяющим признаком опухоли,
ибо он характеризуется беспредельностью и автономностью. Это
означает, что опухоль не подвержена регулирующим влияниям
организма и растет без остановки так долго, как долго будет про-
должаться жизнь человека, у которого она возникла.
ВИДЫ ОПУХОЛЕВОГО РОСТА
Экспансивный рост характеризуется тем, что опухоль растет
как бы "сама из себя". Ее клетки, размножаясь, не выходят за
пределы опухоли, которая, увеличиваясь в объеме, отодвигает ок
ружающие ткани, подвергающиеся атрофии и замещению соеди
156
нительной тканью. В результате вокруг опухоли образуется капсу-
ла и опухолевый узел имеет четкие границы. Такой рост характе-
рен для доброкачественных новообразований.
Инфильтрирующий, или инвазивный, рост заключается в диф-
фузной инфильтрации, врастании опухолевых клеток в окружаю-
щие ткани и их разрушении. При этом очень трудно определить
границы опухоли. Она врастает в кровеносные и лимфатические
сосуды, ее клетки проникают в кровоток или лимфоток и перено-
сятся в другие органы и участки тела. Этот рост характеризует
злокачественные опухоли.
Экзофитный рост наблюдается только в полых органах (желу-
док, кишечник, бронх и др.) и характеризуется распространением
опухоли преимущественно в просвет органа.
Эндофитный рост также происходит в полых органах, но при
этом опухоль растет преимущественно в толщу стенки.
Уницентрический рост характеризуется возникновением опу-
холи в одном участке ткани и соответственно одним опухолевым
узлом.
Мультицентрический рост означает возникновение опухолей
одновременно в нескольких участках органа или ткани.
ВИДЫ ОПУХОЛЕЙ
Различают доброкачественные и злокачественные опухоли.
Доброкачественные опухоли состоят из зрелых дифференциро-
ванных клеток и поэтому близки к исходной ткани. В них нет
клеточного атипизма, но наблюдается тканевый атипизм Напри-
мер, опухоль из гладкомышечной ткани — миома (рис. 34) состо-
ит из пучков мышц, имеющих разную толщину, идущих в разных
направлениях, образующих многочисленные завихрения, причем
в одних участках больше мышечных клеток, в других — стромы.
Те же изменения наблюдаются и в самой строме. Нередко в опу-
холи появляются очаги гиалиноза или обызвествления, что ука-
зывает на качественные изменения ее белков. Доброкачественные
опухоли растут медленно, обладают экспансивным ростом, оттес-
няя окружающие ткани. Они не дают метастазов, не оказывают
общего отрицательного влияния на организм.
Вместе с тем при определенной локализации морфологически
доброкачественные опухоли могут клинически протекать злокаче-
ственно. Так, доброкачественная опухоль твердой мозговой обо-
лочки, увеличиваясь в размерах, сдавливает головной мозг, что
приводит к смерти больного. Кроме того, доброкачественные
опухоли могут озлокачествлятъся, или малинизироваться, т. е.
приобретать характер злокачественной опухоли.
Злокачественные опухоли характеризует ряд признаков: кле-
точный и тканевый атипизм. инфильтрирующий (инвазивный)
рост, метастазирование, рецидивирование и общее влияние опу-
холи на организм.
157
Рис. 34. Лейомиома. Пучки гладких мышечных клеток различной тол-
щины, расположены неравномерно.
Клеточный и тканевой а/иииизл/заключается в том, что опухоль
состоит из незрелых, малодифференцированных, анаплазирован-
ных клеток и атипичной стромы. Степень атипизма может быть
различной — от относительно невысокой, когда клетки напомина-
ют исходную ткань, до резко выраженной, когда клетки опухоли
похожи на эмбриональные и по их виду невозможно узнать даже
ткань, из которой возникло новообразование. Поэтому по степени
люфологического атипизма злокачественные опухоли могут быть:
• высокодифференцированными (например, плоскоклеточ-
ный рак, аденокарцинома);
• низкодифференцированными (например, мелкоклеточный
рак, слизистый рак).
Инфильтрирующий (инвазивный) рост не позволяет точно оп-
ределить границы опухоли. Благодаря инвазии опухолевых клеток
и разрушению окружающих тканей опухоль может прорастать в
кровеносные и лимфатические сосуды, что является условием ме-
тастазирования.
Метастазирование — процесс переноса клеток опухоли или их
комплексов с током лимфы или крови в другие органы и разви-
тие в них вторичных опухолевых узлов. Имеется несколько путей
переноса клеток опухоли:
• лимфогенное метастазирование характеризуется переносом
клеток опухоли по лимфатическим путям и развивается
преимущественно при раке;
158
• гематогенное метастазирование осуществляется по крове-
носному руслу, и этим путем метастазируют преимущест-
венно саркомы;
• периневральное метастазирование наблюдается в основном
при опухолях нервной системы, когда клетки опухоли рас-
пространяются по периневральным пространствам;
• контактное метастазирование возникает при распростране-
нии опухолевых клеток по контактирующим друг с другом
слизистым или серозным оболочкам (листки плевры, ниж-
няя и верхняя губы и др.), при этом опухоль с одной слизи-
стой или серозной оболочки перемещается на другую;
• смешанное метастазирование характеризуется наличием не-
скольких путей переноса опухолевых клеток. Например,
при раке желудка вначале развивается лимфогенное мета-
стазирование в регионарные лимфатические узлы, а по ме-
ре прогрессирования опухоли возникают и гематогенные
метастазы в печень и другие органы. При этом, если опу-
холь прорастает стенку желудка и начинает контактировать
с брюшиной, появляются контактные метастазы — карци-
номатоз брюшины.
Рецидивирование — повторное развитие опухоли в том месте,
где она была удалена хирургическим путем или с помощью луче-
вой терапии. Причиной рецидива являются сохранившиеся опу-
холевые клетки. Рецидивировать могут иногда после удаления не-
которые доброкачественные опухоли.
Общее влияние опухоли на организм обусловлено нарушением
обмена веществ вследствие необычных рефлекторных воздейст-
вий из опухоли, усиленным поглощением ею из нормальных тка-
ней глюкозы, аминокислот, витаминов, липидов, угнетением
окислительно-восстановительных процессов. У больных развива-
ются анемия, гипоксия, они быстро худеют вплоть до кахексии,
или истощения. Этому могут способствовать вторичные измене-
ния самой опухоли (некроз ее ткани) и интоксикация организма
продуктами распада.
ПРЕДОПУХОЛЕВЫЕ ПРОЦЕССЫ
Любой опухоли предшествуют какие-либо другие заболевания,
как правило, связанные с непрерывно повторяющимися процес-
сами повреждения тканей и постоянно текущими в связи с этим
репаративными реакциями. Вероятно, непрерывное напряжение
регенерации, метаболизма, синтеза новых клеточных и внекле-
точных структур приводит к полому механизмов этих процессов,
что проявляется в ряде их изменений, являющихся как бы проме-
жуточными между нормой и опухолью. К предопухолевым забо-
леваниям относятся:
• хронические воспалительные процессы, такие как хронический
бронхит, хронический колит, хронический холецистит и др.;
159
• метаплазия — изменения структуры и функции клеток, от-
носящихся к одному тканевому ростку. Метаплазия, как
правило, развивается в слизистых оболочках в результате
хронического воспаления. Примером может служить мета-
плазия клеток слизистой оболочки желудка, теряющих
свою функцию и начинающих секретировать кишечную
слизь, что указывает на глубокие повреждения механизмов
репарации;
• дисплазия — потеря репаративным процессом физиологиче-
ского характера и приобретение клетками все увеличивающе-
гося количества признаков атипизма. Выделяют три степени
дисплазии, причем первые две обратимы при интенсивном
лечении; третья степень весьма незначительно отличается от
опухолевого атипизма, поэтому в практике к тяжелой дис-
плазии относятся как к начальным формам рака.
ПРИЧИНЫ И МЕХАНИЗМЫ ВОЗНИКНОВЕНИЯ
ОПУХОЛЕЙ - ОНКОГЕНЕЗ
В настоящее время раскрыто очень много фактов, позволяю-
щих проследить условия и механизмы возникновения опухолей, и
все же пока еще нельзя считать, что точно известны причины их
развития. Однако на основе данных, особенно полученных в по-
следние годы благодаря достижениям молекулярной патологии,
можно с высокой степенью вероятности говорить об этих при-
чинах.
Причиной развития опухолей являются изменения молекулы
ДНК в геноме клетки под влиянием разнообразных канцерогенов —
факторов, способных вызывать генетические мутации. При этом
условием, способствующим реализации действия канцерогенов,
является снижение эффективности противоопухолевой защиты,
осуществляющейся также на генетическом уровне — с помощью
антионкогенов Р53, Rb. Выделяют 3 группы канцерогенов: хими-
ческие, физические и вирусные.
Химические канцерогены. По данным ВОЗ. более 75 % случаев
злокачественных опухолей человека вызвано воздействием хими-
ческих факторов внешней среды. К возникновению опухолей
приводят преимущественно продукты сгорания табака (примерно
40 %); химические агенты, входящие в состав пищи (25—30 %), и
соединения, используемые в различных сферах производства
(около 10 %). Известно более 1500 химических соединений, обла-
дающих канцерогенным эффектом. Из них не менее 20 опреде-
ленно являются причиной опухолей у человека. Наиболее опас-
ные канцерогены относятся к нескольким классам химических
веществ.
Корганическимхимическим канцерогенам относятся:
• полициклические ароматические углероды — 3,4-бензпи-
рен, 20-метилхолантрен, диметилбензантрацен (ежегодно в
160
атмосферу промышленных городов выбрасываются сотни
тонн этих и подобных им веществ);
• гетероциклические ароматические углеводороды — дибенз-
акридин. дибензкарбазол и др.;
• ароматические амины и амиды — 2-нафтиламин, бензидин
и др.;
• органические вещества с канцерогенной активностью —
эпоксиды, пластмассы, уретан, четыреххлористый углерод,
хлорэтиламины и др.
Неорганические канцерогены могут иметь экзо- и эндогенное
происхождение.
Экзогенные соединения попадают в организм из окружающей
среды — хроматы, кобальт, окись бериллия, мышьяк, асбест и
ряд других.
Эндогенные соединения образуются в организме в результате
модификации продуктов нормального обмена веществ. Такими
потенциально канцерогеннымии веществами являются метаболи-
ты желчных кислот, эстрогенов, некоторых аминокислот (тирози-
на, триптофана), липопероксидные соединения.
Физические канцерогены. К физическим канцерогенам отно-
сятся:
• радиоактивное излучение веществ, содержащих 32Р, 131I, 90Sr
и др.;
• рентгеновское излучение;
• ультрафиолетовое излучение в избыточной дозе.
У подвергшихся воздействию радиации во время аварий на
атомных реакторах, а также при бомбардировке Хиросимы и На-
гасаки онкологическая заболеваемость намного выше, чем в об-
щей популяции.
ЭТАПЫ ХИМИЧЕСКОГО И ФИЗИЧЕСКОГО КАНЦЕРОГЕНЕЗА
Сами по себе канцерогенные вещества не вызывают опухоле-
вого роста, поэтому их называют проканцерогенами или преканце-
рогеналш. В организме они подвергаются физико-химическим
превращениям, в результате которых становятся истинными, ко-
нечными канцерогенами. Именно такие канцерогены вызывают
изменения в геноме нормальной клетки, ведущие к ее трансфор-
мации в опухолевую.
Этапы канцерогенеза складываются из двух взаимосвязанных
процессов: инициации и промоции.
На этапе инициации происходит взаимодействие канцерогена с
участками ДНК, содержащими гены, контролирующие деление и
созревание клетки. Такие участки называются протоонкогенными.
Инициированная клетка становится илшортализованной, т. е. бес-
смертной.
На этапе пролюции осуществляется экспрессия онкогена и пре-
вращение нормальной клетки в опухолевую и формирование но-
вообразования.
161
Канцерогены биологической природы. К биологическим канце-
рогенам относят онкогенные вирусы. По типу вирусной нуклеи-
новой кислоты их подразделяют на ДНК-co держащие и РНК-со-
держащие.
• ДНК-содержищие вирусы. Гены ДНК-онковирусов способ-
ны непосредственно внедряться в геном клетки-мишени.
Участок ДНК-онковируса (онкоген), интегрированный с
клеточным геномом, может осуществить опухолевую транс-
формацию клетки. К ДНК-содержащим онковирусам отно-
сят некоторые аденовирусы, паповавирусы и герпесвирусы,
такие как вирус Эпштейна—Барр (вызывающие развитие
лимфом), вирусы гепатита В и С.
• РНК-содержащие вирусы — ретровирусы. Интеграция ви-
русных РНК-генов в клеточный геном происходит не непо-
средственно, а после образования их ДНК-копий с помо-
щью фермента ревертазы.
ЭТАПЫ ВИРУСНОГО КАНЦЕРОГЕНЕЗА
• проникновение онкогенного вируса в клетку;
• включение вирусного онкогена в геном клетки;
• экспрессия онкогена;
• превращение нормальной клетки в опухолевую;
• образование опухолевого узла.
ОПУХОЛЕВАЯ ТРАНСФОРМАЦИЯ КЛЕТОК
Трансформация нормальной генетической программы в про-
грамму формирования опухолевого атипизма происходит на уров-
не клетки. В основе опухолевой трансформации лежат стойкие
изменения ДНК. При этом программа опухолевого роста стано-
вится программой клетки, закодированной в ее геноме. Единый
конечный результат действия канцерогенов различной природы
(химической, биологической, физической) на клетки и их опухо-
левая трансформация обеспечиваются нарушением взаимодейст-
вия в клеточном геноме онкогенов и антионкогенов.
ОСОБЕННОСТИ РАЗВИТИЯ ОПУХОЛЕЙ
В динамике онкогенеза злокачественных опухолей от клетки
до опухолевой ткани можно выделить несколько этапов:
• пролиферация клеток на ограниченном участке ткани; на
этом этапе морфологический атипизм еще не проявляется;
• дисплазия клеток, характеризующаяся постепенным накоп-
лением признаков атипии;
• carcinoma in situ (рак на месте) — скопление атипичных опу-
холевых клеток, еще не обладающих опухолевым ростом;
• инфильтрирующий, или инвазивный, рост опухолевой ткани;
162
• опухолевая прогрессия — нарастание злокачественности в ди-
намике онкогенеза. Это явление связано с тем, что по мере
развития опухоли на ее клетки действуют различные факто-
ры, угнетающие их рост. При этом часть клеток погибает, а
выживают и продолжают размножаться наиболее жизнеспо-
собные. Именно они оказываются наиболее злокачествен-
ными и передают свои свойства потомкам, которые в свою
очередь подвергаются селекции, становясь все более злока-
чественными.
КЛАССИФИКАЦИЯ ОПУХОЛЕЙ
Опухоли классифицируют исходя из их принадлежности к оп-
ределенной ткани. По этому принципу выделяют 7 групп опухо-
лей, в каждой из которых есть доброкачественные и злокачест-
венные формы.
1. Эпителиальные опухоли без специфической локализации.
2. Опухоли экзо- и эндокринных желез и специфических эпи-
телиальных покровов.
3. Мягкотканные опухоли.
4. Опухоли меланинобразующей ткани.
5. Опухоли нервной системы и оболочек мозга.
6. Гемобластомы.
7. Тератомы (дисэмбриональные опухоли).
Название опухоли складывается из двух частей — наименова-
ния тканей и окончания "ома". Например, опухоль кости — ос-
теома, жировой ткани — липома, сосудистой ткани — ангиома,
железистой ткани — аденома. Злокачественные опухоли из эпите-
лия носят название рак (канцер, карцинома), а злокачественные
опухоли из мезенхимы называются саркомами, однако в названии
указывается вид мезенхимальной ткани — остеосаркома, миосар-
кома, ангиосаркома, фибросаркома и т. п.
ЭПИТЕЛИАЛЬНЫЕ ОПУХОЛИ
Опухоли из эпителия могут быть доброкачественными и зло-
качественными.
ДОБРОКАЧЕСТВЕННЫЕ ЭПИТЕЛИАЛЬНЫЕ ОПУХОЛИ
Доброкачественные эпителиальные опухоли могут исходить из
покровного эпителия и называются папилломы, и из железистого
эпителия — аденомы. И те, и другие имеют паренхиму и строму и
характеризуются только тканевым атипизмом.
Папилломы (см. рис. 33) возникают из плоского или переход-
ного эпителия — в коже, слизистых оболочках глотки, голосовых
связок, мочевого пузыря, мочеточников и лоханок почек и др.
163
Они имеют вид сосочков или цветной капусты, могут быть еди-
ничными или множественными, иногда имеют ножку. Тканевый
атипизм проявляется в нарушении одной из основных особенно-
стей любого эпителия — комплексности, т. е. определенного рас-
положения клеток, а также полярности, т. е. нарушения базально-
го и апикального краев клеток, но при этом сохраняется базаль-
ная мембрана — важнейший признак экспансивного, а не инва-
зивного роста.
Течение папиллом из разных видов покровного эпителия раз-
лично. Если папилломы кожи (бородавки) растут медленно и не
доставляют особых беспокойств человеку, то папилломы голосо-
вых связок нередко рецидивируют после удаления, а папилломы
мочевого пузыря часто изъязвляются, что приводит к кровотече-
нию и появлению крови в моче (гематурия). Любая папиллома
может малигнизироваться, превращаясь в рак.
Аденома может возникать везде, где есть железистый эпите-
лий, — в молочной, щитовидной и других железах, в слизистых
оболочках желудка, кишечника, бронхов, матки и т. д. Она обла-
дает экспансивным ростом и имеет вид узла, хорошо отграничен-
ного от окружающей ткани. Аденома слизистой оболочки, имею-
щая ножку, называется аденоматозным полипом Аденома, в кото-
рой преобладает паренхима, имеет мягкую консистенцию и назы-
вается простой аденомой. Если преобладает строма, опухоль плот-
ная и называется фиброаденомой. Фиброаденомы особенно часто
возникают в молочных железах (рис. 35).
Тканевый атипизм аденом проявляется в том, что их желези-
стые структуры имеют различные размеры и форму, эпителий
может разрастаться и ветвиться в виде сосочков, иногда в виде
трабекул. Нередко железистые образования в аденоме не имеют
выводных протоков, поэтому вырабатывающийся секрет растяги-
вает железы и вся опухоль оказывается состоящей из полостей —
кист, заполненных жидким или слизистым содержимым. Такая
аденома называется цистаденомой. Чаще всего они возникают в
яичниках и иногда достигают огромных размеров. Аденомы эн-
докринных желез имеют обычно повышенную функцию, что про-
является эндокринными нарушениями. Аденомы могут малигни-
зироваться, переходя в рак (аденокарциномы).
ЗЛОКАЧЕСТВЕННЫЕ ЭПИТЕЛИАЛЬНЫЕ ОПУХОЛИ
Рак может развиваться в любом органе, где имеется эпители-
альная ткань, и является самой распространенной формой злока-
чественных опухолей. Ему свойственны все признаки злокачест-
венности. Раку, как и другим злокачественным новообразовани-
ям, предшествуют предраковые процессы. На каком-то этапе их
развития клетки приобретают признаки анаплазии и начинают
размножаться. В них отчетливо выражен клеточный атипизм. по-
вышена митотическая активность, много неправильных митозов.
Однако все это происходит в пределах эпителиального пласта и
164
Рис. 35. Интраканаликулярная фиброаденома молочной железы. Желе-
зистые образования опухоли (а) сжаты пучками стромы (б).
не распространяется за базальную мембранную мембрану, т. е.
еще нет инвазивного роста опухоли. Такая, самая начальная,
форма рака называется "рак на месте", ил( carcinoma in situ
(рис. 36). Ранняя диагностика прединвазивного рака позволяет
своевременно провести соответствующее, обычно хирургическое,
лечение с благоприятным прогнозом.
Большинство других форм рака макроскопически имеет форму
узла с нечеткими границами, сливающимися с окружающей тка-
нью. Иногда раковая опухоль диффузно прорастает орган, который
при этом уплотняется, стенки полых органов становятся толще, а
просвет полости уменьшается. Нередко раковая опухоль изъязв-
ляется, в связи с чем могут возникать кровотечения. По степени
снижения признаков зрелости выделяют несколько форм рака.
Плоскоклеточный рак развивается в коже и слизистых оболоч-
ках. покрытых плоским эпителием: в полости рта, пищеводе, вла-
галище, шейке матки и т. д. В зависимости от типа плоского' эпи-
телия имеются два вида плоскоклеточного рака — ороговевающий
и неороговевающий. Эти опухоли относятся к дифференцирован-
ным формам рака. Эпителиальные клетки имеют все признаки
клеточного атипизма. Инфильтрирующий рост сопровождается
нарушением полярности и комплексности клеток, а также разру-
шением базальной мембраны. Опухоль состоит из тяжей плоского
эпителия, инфильтрирующего подлежащие ткани, образуя ком-
плексы и скопления. При плоскоклеточном ороговевающем раке
165
Рис. 36. Carcinoma in situ шейки матки.
a — слой покровного эпителия слизистой оболочки утолщен, его клетки поли-
морфны, атипичны, ядра гиперхромны, много митозов; б — базальная мембрана
сохранена; в — подлежащая соединительная ткань; г — кровеносные сосуды.
атипичные клетки эпидермиса располагаются концентрически,
сохраняя способность к ороговению. Такие ороговевшие гнезда
раковых клеток называются "раковыми жемчужинами" (рис. 37).
Плоскоклеточный рак может развиваться и на слизистых обо-
лочках, покрытых призматическим или цилиндрическим эпите-
лием, но только в том случае, если в результате хронического па-
тологического процесса произошла его метаплазия в многослой-
ный плоский эпителий. Плоскоклеточный рак растет относитель-
но медленно и довольно поздно дает лимфогенные метастазы.
Лденокарцинома — железистый рак, возникающий в органах,
имеющих железы. Аденокарцинома включает несколько морфо-
логических разновидностей, часть из которых относится к диф-
ференцированным, а часть — к недифференцированным формам
рака. Атипичные опухолевые клетки формируют железистые
структуры различной величины и формы без базальной мембра-
ны и выводных протоков. В клетках паренхимы опухоли выраже-
на гиперхромия ядер, много неправильных митозов, имеется так-
же атипизм стромы (рис. 38). Железистые комплексы врастают в
окружающую ткань, ничем от нее не отграничиваясь, разрушают
лимфатические сосуды, просветы которых заполняются раковыми
клетками. Это создает условия для лимфогенного метастазирова-
ния аденокарциномы, которое развивается относительно поздно.
166
Рис. 37. Плоскоклеточный ороговевающий рак легкого. РЖ — "раковые
жемчужины".
Солидный рак. При этой форме опухоли раковые клетки обра-
зуют компактные, бессистемно расположенные группы, разделен-
ные прослойками стромы. Солидный рак относится к недиффе-
ренцированным формам рака, в нем выражена клеточная и тка-
невая анаплазия. Опухоль быстро инфильтрирует окружающие
ткани и рано дает метастазы.
Мелкоклеточный рак — форма крайне недифференцированно-
го рака, состоящего из мелких, круглых, гиперхромным клеток,
напоминающих лимфоциты. Нередко только благодаря примене-
нию специальных методов исследования можно установить при-
надлежность этих клеток к эпителиальным. Иногда опухолевые
клетки несколько вытягиваются и приобретают сходство с зерна-
167
Рис. 38. Аденокарцинома желудка.
а — железистые образования опухоли: б — митозы в раковых клетках.
ми овса (овсяно-клеточный рак), иногда они становятся крупны-
ми (крупноклеточный рак). Опухоль крайне злокачественная, бы-
стро растет и рано дает обширные лимфо- и гематогенные мета-
стазы.
МЕЗЕНХИМАЛЬНЫЕ ОПУХОЛИ
Из мезенхимы развиваются соединительная, жировая, мышеч-
ная ткани, кровеносные и лимфатические сосуды, синовиальные
оболочки, хрящи и кости. В каждой из этих тканей могут возни-
кать доброкачественные и злокачественные опухоли (рис. 39).
Среди мезенхимальных опухолей важное значение имеет группа
опухолей мягких тканей, жировой ткани и группа первичных
опухолей костей, встречающих наиболее часто.
ОПУХОЛИ МЯГКИХ ТКАНЕЙ
Доброкачественные мезенхимальные опухоли, К ним относятся
фиброма, миома, гемангиомы, липома.
Фиброма развивается из зрелой волокнистой соединительной
168
Рис. 39. Мезенхимальные опухоли.
а — твердая фиброма подкожной клетчатки;
б — мягкая фиброма кожи; в — множест-
венные лейомиомы матки; г — фибросарко-
ма мягких тканей плеча.
ткани. Она встречается везде, где есть соединительная ткань, а
следовательно, в любых органах, но чаще в коже, молочной желе-
зе, матке. Фиброма характеризуется тканевым атипизмом, кото-
рый проявляется неправильным, хаотичным расположением во-
локон соединительной ткани, неравномерным распределением
сосудов. Опухоль растет экспансивно, имеет капсулу. В зависи-
мости от преобладания стромы или паренхимы фиброма может
быть плотной или мягкой. Значение фибромы зависит от ее лока-
лизации — фиброма кожи не доставляет особых беспокойств
больному, а фиброма в спинномозговом канале может вызвать
тяжелые нарушения нервной деятельности.
Миома — опухоль из мышечной ткани. В соответствии с двумя
видами мышц и миомы имеют два варианта: возникающие из
гладких мышц называются лейомиомами, а из поперечнополоса-
тых — рабдомиомами. Тканевый атипизм заключается в неодина-
ковой толщине мышечных пучков, идущих в разных направлени-
ях и образующих завихрения. Опухоли, в которых сильно развита
строма, называют фибро-
миомами. Лейомиомы наи-
более часто встречаются в
матке, где достигают ино-
гда значительных разме-
ров. Рабдомиома — более
редкая опухоль, может
возникать в мышцах язы-
ка, в миокарде и в других
органах, содержащих ис-
черченную мышечную
ткань.
Гемангиомы — группа
опухолей из сосудов. В за-
висимости от того, из ка-
ких сосудов возникает
опухолевый рост, различа-
ют капиллярную, веноз-
ную и кавернозную геман-
гиомы. Капиллярная геман-
гиома обычно бывает вро-
жденной, локализуется в
коже в виде багровых пя-
тен с неровной поверхно-
стью. Венозная ангиома со-
стоит из сосудистых по-
лостей. напоминающих
вены. Кавернозная геман-
гиома также состоит из со-
судистых полостей разной
величины и формы, со
стенками неодинаковой
169
Рис. 40. Дифференцированная фибросаркома.
толщины. В сосудистых полостях нередко образуются тромбы.
При травме кавернозная гемангиома может давать обильное кро-
вотечение. Венозная и кавернозная ангиомы встречаются наибо-
лее часто в печени, мышцах, иногда в костях и головном мозге.
Липома — опухоль из жировой ткани, растет экспансивно в
виде одного или множественных узлов, обычно имеет капсулу.
Чаще располагается в подкожной жировой клетчатке, но может
возникать везде, где имеется жировая ткань. Иногда липома дос-
тигает очень больших размеров.
Злокачественные мезенхимальные опухоли. Эти опухоли имеют
общее название саркомы и на разрезе напоминают рыбье мясо.
Они развиваются из тех же тканей (производных мезенхимы), что
и доброкачественные мезенхимальные опухоли. Для них харак-
терны выраженный клеточный и тканевый атипизм, а также ге-
матогенное метастазирование, вследствие чего метастазы появля-
ются довольно быстро и отличаются распространенностью. По-
этому саркомы протекут очень злокачественно. Выделяют не-
сколько видов сарком мягких тканей: фибросаркома, липосарко-
ма, миосаркомы, ангиосаркома.
Фибросаркома возникает из волокнистой соединительной тка-
ни, имеет вид узла с нечеткими границами, инфильтрирует окру-
жающие ткани. Она состоит из атипичных фибробластоподобных
круглых или полиморфных клеток и незрелых коллагеновых во-
локон (рис. 40). Фибросаркома обычно возникает на плече, бедре
и в мягких тканях других частей тела. Отличается выраженной
злокачественностью.
170
1
Липосаркома развивается из незрелых жировых клеток (липо-
цитов) и липобластов. Она может достигать больших размеров и
долго не давать метастазов. Опухоль встречается относительно
редко.
Миосаркомы в зависимости от вида мышечной ткани подраз-
деляют на лейомиосаркомы и рабдомиосаркомы. Клетки этих опухо-
лей крайне атипичны и полиморфны, нередко полностью утрачи-
вают сходство с мышечной тканью, в связи с чем определение
исходной ткани возможно только с помощью электронного мик-
роскопа.
Ангиосаркома — злокачественная опухоль сосудистого проис-
хождения. Состоит из атипичных эндотелиоцитов и перицитов.
Отличается высокой злокачественностью и рано дает гематоген-
ные метастазы.
ПЕРВИЧНЫЕ ОПУХОЛИ КОСТЕЙ
Доброкачественные опухоли костей. Хондрома — опухоль из
гиалинового хряща, растет в виде плотного узла или узлов в об-
ласти суставов кистей, стоп, позвонков, таза. Гистологически со-
стоит из беспорядочного расположенных клеток гиалинового
хряща, заключенных в основное вещество.
Остеома возникает в костях, чаще в костях черепа. Гистологи-
чески состоит из беспорядочно расположенных костных балок,
между которыми разрастается соединительная ткань. Среди ос-
теом особое место занимает "гигантоклеточная опухоль" (доброка-
чественная остеобластома), в состав которой входят многоядер-
ные гигантские клетки. Ее особенность заключается в том. что
она разрушает кость, но не дает метастазов.
Злокачественные опухоли костей. Остеосаркома возникает в
костях, часто после их травмы. Состоит из атипичных остеобла-
стов с большим количеством неправильных митозов. Опухоль бы-
стро разрушает кость, прорастает в окружающие ткани, дает мно-
жественные гематогенные метастазы, особенно в печень и легкие.
Пораженное метастазами легкое имеет вид "булыжной мостовой".
Хондросаркома состоит из атипичных хрящевых клеток, ткань
ее нередко ослизняется и некротизируется. Хондросаркома растет
относительно медленно и метастазируется позже, чем другие сар-
комы.
ОПУХОЛИ МЕЛАНИНОБРАЗУЮЩЕЙ ТКАНИ
Меланинобразующая ткань является разновидностью нервной
ткани и включает клетки меланобласты и меланоциты, содержа-
щие пигмент меланин. Эти клетки образуют опухолеподобные
доброкачественные образования — невусы (рис. 41). Их травмати-
зация нередко вызывает трансформацию невуса в злокачествен-
171
Рис. 41. Пигментный невус. Меланин-
синтезирующие клетки образуют ост-
ровки (а), разделенные прослойками со-
единительной ткани (б). Зерна мелани-
на в цитоплазме соединительнотканных
клеток (в).
ную опухоль — меланому.
Меланома развивается не
только из невусов, но и
из других тканей, содер-
жащих меланинобразую-
щие клетки, — пигмент-
ной оболочки глаз, мозго-
вых оболочек, мозгового
вещества надпочечников.
Внешне меланома пред-
ставляет собой узел или
бляшку черного или ко-
ричневого цвета с черны-
ми вкраплениями. Гисто-
логически — скопление
полиморфных, уродли-
вых клеток, содержащих
включения меланина бу-
рого цвета, с множеством
митозов, иногда с участ-
ками кровоизлияний и
некроза. Меланома плохо
поддается лечению.
Часть II
ОСНОВЫ ЧАСТНОЙ ПАТОЛОГИИ
Глава 11
введение В НОЗОЛОГИЮ
Нозология — учение о болезнях (от греч. nosos — болезнь и
logos — учение). Нозология включает еледующие вопросы:
• биологические и медицинские основы болезней;
• этиологию, т. е. причины и условия возникновения бел
лезни;
• патогенез, или механизмы развития болезни;
• морфогенез — морфологические изменения в динамике за-i
болевания;
• осложнения болезни;
• исходы заболевания;
• номенклатуру и классификацию болезней;
• правила составления диагноза;
• патоморфоз, т. е. изменчивость болезней;
• ошибки медицинских работников.
В соответствии с нозологией выделяют нозологические едини-i
цы, или конкретные болезни.
ОСНОВНЫЕ ПОНЯТИЯ нозологии
Болезнь — это жизнь, нарушенная в своем течении поврежде-i
нием структуры и функции организма под влиянием внешних и
внутренних факторов; болезнь характеризуется снижением при-i
способляемости к среде и ограничением свободы жизнедеятель-i
пости больного. Таким образом, понятие "болезнь" обязательно
подразумевает нарушение взаимодействия организма с внешней
средой и полом гомеостаза.
Фундаментальные положения, которыми характеризуется люп
бая болезнь:
• болезнь, как и здоровье, одна из форм жизни;
• болезнь — это общее страдание организма;
• для возникновения болезни необходимо определенное со-п
четание факторов внешней и внутренней среды;
• в возникновении и течении болезни важнейшая роль при-i
надлежит компенсаторным и приспособительным реакциям
организма;
173
• любая болезнь сопровождается морфологическими измене-^
ниями в органах и тканях, что определяется единством
структуры и функции.
Периоды (стадии) болезни. В большинстве случаев, хотя и не
всегда, можно выделить несколько периодов (или стадий) разви->
тия болезни:
• латентный период, т. е. скрытый, — клинически никак не
проявляющийся этап заболевания, который длится от мо->
мента воздействия патогенного фактора до первых призна-i
ков болезни;
• продромальный период (или стадия предвестников), характер
ризующийся появлением первых неспецифических призна-i
ков болезни в виде недомогания, утомляемости, раздражи^
тельности, головной боли, болезненности в суставах и
мышцах ит. и.;
• период выраженной болезни (или стадия разгара) — этап за->
болевания, характеризующийся появлением специфических
признаков конкретной болезни;
• период исходов болезни, которые могут быть благоприятны-'
ми, когда наступает выздоровление, или неблагоприятны-'
ми, если болезнь заканчивается инвалидизацией больного
или его смертью.
Патологический процесс — закономерно возникающая в орга->
низме последовательность реакций на повреждение, вызванное
патогенным фактором, и характеризующаяся нарушением жизне-'
деятельности. Патологический процесс является компонентом
болезни, но при этом он может быть местным и протекать в пре-"
делах одного органа или ткани, в то время как болезнь — это об->
щее страдание организма.
Патологическое состояние — устойчивое отклонение от нор-'
мы, имеющее отрицательное значение для организма. Для патсп
логического состояния характерно длительное, нередко пожиз^
пенное течение. Примером таких состояний могут быть деформа->
ция створок клапанов сердца после перенесенного эндокардита,
состояние после потери глазного яблока или удаления одной из
почек, части легкого или кишечника, различные аномалии разви-п
тия (косолапость, расщепление верхней губы или твердого неба и
т. и.).
Патологическая реакция — неадекватный ответ организма или
отдельных органов на действие обычных или патогенных раздра->
жителей. Примером таких реакций могут быть патологические
рефлексы — спазм венечных артерий сердца с развитием приступ
па стенокардии при прохождении камня через общий желчный
проток, разнообразные аллергические реакции как неадекватный
ответ на действие обычных для большинства людей веществ.
174
этиология
Этиология — учение о причинах и условиях возникновения
болезней. Вопрос о том, что является причиной болезней, — это
кардинальный вопрос медицины, на который человечество пыта->
ется ответить на протяжении всей своей истории. Учение об
этиологии болезней прошло несколько этапов, пока не стали по->
нятными несколько основных закономерностей возникновения
болезней:
• без причины не лижет быть болезни. Однако одной причин
ны недостаточно для того, чтобы началась болезнь: причина
болезни, или патогенный фактор, может быть нейтрализо->
вана благодаря защитным системам организма, его реактив^
ности, иммунной системе и др. Примером могут служить
эпидемии инфекционных заболеваний, когда среди людей,
находящихся в одинаковых условиях, часть заболевает, а
другие остаются здоровыми;
• для того чтобы причина вызвала болезнь, необходимы соот~>
ветствующие условия, в которых приспособляемость орга-ч
низма становится недостаточной. При этом условия жизни
составляет внешняя среда — социальная, географическая,
биологические, физические и другие окружающие факторы,
и внутренняя среда, т. е. условия, которые складываются в
самом организме под влиянием наследственных, конститу->
циональных и других факторов;
• специфика болезни, т. е. характерные для нее клиническая
картина и морфологические изменения определяются причин
ной болезни (патогенным фактором). Именно патогенный
фактор, обладающий специфическими особенностями, вы->
зывает закономерный ответ организма в виде характерных
признаков болезни — симптомов и синдромов, т. е. группы
симптомов, совокупность которых определяет специфику
заболевания.
Таким образом, этиология — это не просто причина болезни, а
учение о сложных процессах взаимодействия организма человека с
причиной болезни и о комплексе дополнительных условий, в кото->
рых эти взаимодействия реализуются,
В практической деятельности используется более узкое толко->
вание понятия "этиология" — как причины и условия возникнем
вения конкретной болезни, что на основании соответствующей
симптоматики позволяет поставить диагноз и проводить лечение,
направленное в первую очередь на ликвидацию патогенного фак->
тора, т. е. причины этого заболевания.
Причины многих болезней, например большинства инфекции
онных, эндокринных или травматических заболеваний, известны.
Вместе с тем имеется много болезней, этиология которых не ус->
тановлена — психические заболевания, злокачественные опухоли,
атеросклероз, сепсис и др., что, однако, не исключает их успеш->
него лечения путем воздействия не на этиологию, а на опреде-
175
ленные механизмы развития таких болезней. Так, хорошо извест-"
ны клиническая картина, морфология, течение и исходы аппен-"
дицита. Ежегодно в мире удаляют сотни тысяч червеобразных от-"
ростков, однако этиология аппендицита до сих пор не установле-"
на. Неизвестна этиология рака, но многие формы этого заболева-"
ния успешно лечат во всем мире.
ПАТОГЕНЕЗ
Патогенез — учение об общих закономерностях и механизмах
развития, течения и исхода патологических процессов и болез-"
ней. Проблема патогенеза тесно связана с проблемой этиологии и
также имеет широкое толкование, как учение об общих законе-"
мерностях развития болезней вообще, и узкое понятие — как ме->
ханизм развития конкретной болезни или патологического про-"
цесса. Если этиология отвечает на вопрос, почему возникло забо->
левание, то патогенез отвечает на вопрос, как оно возникло. Па-"
тогенез учитывает прежде всего роль факторов внутренней среды
организма. В отличие от этиологических факторов, определяемых
преимущественно внешней средой и поэтому характеризующихся
изменчивостью в зависимости от множества условий, патогенети-"
ческие факторы отличаются известным постоянством, как и все
наследственно закрепленные физиологические механизмы. Это
создает устойчивость и стереотипность реакций организма на
различные воздействия. Так, рак может быть вызван самыми pan
нообразными химическими и физическими канцерогенами, что
указывает на множество этиологических факторов и единый па-"
тогенетический механизм. Вместе с тем один и тот же канцероген
у одного человека вызывает рак, а у другого не вызывает. Это гсп
ворит о том, что этиологическое значение тех или иных факторов
внешней среды определяется факторами патогенетическими, ко-"
торым принадлежит решающая роль. Однако разделить этиоло-"
гию и патогенез нельзя, они взаимосвязаны, и понять их роль
можно, только рассматривая причину болезни и механизмы ее
развития в неразрывном единстве.
Морфогенез — совокупность механизмов развития морфологи-"
ческих изменений в динамике болезни или патологического про-"
цесса. Морфогенез неотделим от патогенеза, они находятся в
диалектическом единстве, развиваются параллельно друг другу, и
чем глубже и тяжелее морфологические изменения органов и тка->
ней, тем тяжелее течение болезни, т. е. ее патогенез. Суть любой
болезни заключается в том. что она вызывает изменения в струк->
туре органов и тканей. Эти изменения обусловливают определен-"
ные нарушения функций поврежденных органов, что проявляется
в появлении симптомов и синдромов болезни. Выздоровление
подразумевает не только уничтожение патогенного фактора, но и
исчезновение механизмов развития болезни, чему соответствует
репарация, заживление тех морфологических повреждений, кото-
176
рые были вызваны патогенным фактором и лежали в основе наз
рушений функций органов и систем, что проявлялось клиничез
ской картиной болезни.
Биологический смысл патогенеза заключается в том, чтобы с
помощью имеющихся у организма физиологических и патологиз
ческих реакций ликвидировать причину болезни и вернуть физ
зиологические константы, составляющие гомеостаз, т. е. вернуть
состояние здоровья. Поэтому важнейшая особенность патогенез
за — его гомеостатическая направленность. Знание закономерно-'
стей патогенеза, стереотипности его ответов на различные поврез
ждения позволяет проводить патогенетическую терапию, не зная
этиологию заболевания. Так, до конца неизвестна причина сахарз
него диабета, но хорошо изучены механизмы, морфология и диз
намика метаболических нарушений при этом страдании, что поз
зволяет успешно проводить патогенетическое лечение болезни.
Вместе с тем стереотипный ответ организма на различные возз
действия нередко проявляется в появлении одинаковых симптоз
мов, но характеризующих разные заболевания. Например, гипер-
тензия (повышение артериального давления) может быть проявз
лением гипертонической болезни как самостоятельного заболева-'
ния. но может быть и симптомом поражения почек, атеросклероз
за или опухоли надпочечника (феохромоцитомы) или сахарного
диабета. И искусство диагностики заключается в умении распоз
знать болезнь при симптомах и синдромах, сходных с проявлез
ниями других заболеваний.
ИСХОДЫ БОЛЕЗНЕЙ
Каждая болезнь имеет исход. Он может быть:
• благоприятным, когда уничтожается патогенный этиологиз
ческий фактор, ликвидируются морфологические и функз
циональные последствия заболевания и восстанавливается
гомеостаз;
• неблагоприятным, или летальным, когда болезнь заканчиваз
ется смертью больного.
Болезнь может закончиться инвалидизацией больного, когда в
результате заболевания возникает структурно-функциональный
дефект, требующий постоянного лечения. В динамике заболеваз
ния может возникать рецидив — повторное появление симптомов
болезни после их устранения, причем рецидивы могут быть неодз
некратными. В таком случае говорят о рецидивирующем течении
болезни.
Ремиссия — временное ослабление или устранение симптомов
болезни, но не излечение от нее. Смерть — прекращение жизнез
деятельности организма, о котором свидетельствует остановка
сердца.
Имеются два вида смерти, которые являются этапами умираз
ния: клиническая и биологическая смерть.
177
Клиническая смерть — это терминальное состояние, характер
ризующееся отсутствием признаков жизни, но из которого чело->
века можно вывести с помощью реанимационных мероприятий.
Длительность клинической смерти составляет 5—7 мин. Это то
время, в течение которого нервные клетки головного мозга со->
храняют жизнеспособность.
Биологическая смерть наступает вслед за клинической смер->
тью и характеризуется необратимым прекращением всех функций
организма, включая обмен веществ.
Танатогенез — механизм и динамика наступления смерти.
НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ БОЛЕЗНЕЙ
Номенклатура и классификация болезней является важнейшей
частью нозологии.
Медицинская номенклатура — перечень согласованных назвав
ний болезней и причин смерти.
Медицинская классификация — группировка нозологических
единиц (болезней) и причин смерти для достижения определен-'
ных целей — унифицированного написания диагноза, медицин^
ской статистики заболеваемости и смертности и др.
Международная классификация болезней (МКБ) составляется
Всемирной организацией здравоохранения (ВОЗ), которая посто-i
янно дополняет классификацию и номенклатуру болезней по ме->
ре изменения знаний о них или в связи с появлением новых за->
болеваний. Комитет экспертов ВОЗ периодически анализирует
все изменения, которые произошли в понимании этиологии и
патогенеза за 6—8 лет, и вносит соответствующие изменения в
МКБ. Это называется пересмотром. В настоящее время весь мир
пользуется МКБ 10-го пересмотра (1993 г.). Медицинские диаг->
нозы должны соответствовать номенклатуре и классификации бел
лезней ВОЗ, даже если порой они не совпадают с национальны-'
ми представлениями о какой-либо болезни. Такая унификация
необходима для того, чтобы всемирное здравоохранение могло
иметь четкое представление о медицинской ситуации в мире и
при необходимости оказывать специальную помощь тем или
иным странам, разрабатывать и проводить профилактические ме->
роприятия регионального или континентального масштаба, а так->
же готовить квалифицированные медицинские кадры для разных
стран.
МКБ-10 состоит из 3 томов, два из которых имеют техниче—'
ское значение, а третий представляет собой алфавитный указа-'
тель, в котором приводятся термины или ключевые слова, обо-i
значающие название болезни, травмы, синдрома, подлежащие
специальному и унифицированному кодированию. Для этого су
ществуют буквенно-цифровые кодовые номера, для которых npe->
дусмотрены 25 букв латинского алфавита и четырехзначные ко->
ды, в которых последняя цифра ставится после точки. Каждой
178
букве соответствуют до 100 трехзначных цифр. Все болезни, пере->
численные в МКБ-10. разделены на 21 класс, в каждом из кото->
рых болезни объединены в семейства по родственным признакам.
Основной принцип рубрикации — нозологический, т. е. учитываю-!
щий этиологию, патогенез и исходы болезней. Например, класс
I — "Инфекционные и паразитарные болезни" (шифруется по ко->
ду А00—В99), или класс II — "Новообразования". И хотя в этом
классе не всегда известны точные причины болезней, но раскрыт
ты многие этиологические факторы, патогенез опухолей и их ис->
ходы. МКБ создает иерархическую систему приоритетов болезней
при написании диагнозов, основанную на единых для всего мира
принципах.
Диагноз — медицинское заключение о состоянии здоровья об->
следуемого, об имеющимся заболевании или о причине смерти,
выраженное в терминах, предусмотренных принятыми классифи->
нациями и номенклатурой болезней. Это базовый документ для
всей последующей медицинской документации. Имеется не->
сколько разновидностей диагноза — предварительный и оконча->
тельный, гистологический и анатомический, ретроспективный и
судебно-медицинский и др. Однако в клинической медицине ос->
новное значение имеют клинический и патологоанатомический
диагнозы. Оба этих диагноза составляются по одинаковому прин-i
ципу, что позволяет их сравнивать, а сравнение клинического и
патологоанатомического диагнозов дает возможность выявить
ошибки клинической диагностики, их причины, а также правиль->
ность лечения больного.
Основополагающим принципом составления диагноза является
наличие в нем трех главных рубрик — основное заболевание, ос->
ложнения основного заболевания и сопутствующие заболевания.
При этом основное заболевание обычно представляет собой но->
зологическую единицу и по нему проводится кодирование болез->
ни или причины смерти в соответствии с МКБ.
В клиническом диагнозе основное заболевание — это состояние,
по поводу которого проводилось лечение или обследование во
время обращения больного за медицинской помощью. В патоло-
гоанатомическом диагнозе основное заболевание — это то заболев
вание, которое само по себе или через свои осложнения явилось
причиной смерти больного.
Осложнение — это заболевание, патогенетически связанное с
основным заболеванием и утяжеляющее его течение.
Однако далеко не всегда удается всю патологию, имеющуюся у
больного, уложить в одно основное заболевание, и для того, чтсп
бы описать в диагнозе такую ситуацию, вводится рубрика комби~>
нированного основного заболевания, позволяющая назвать несколь-!
ко основных заболеваний, которые привели больного к смерти.
Конкурирующие заболевания — два или более заболеваний, ка->
ждое из которых само по себе или через свои осложнения могло
привести больного к смерти. Например, рак желудка IV стадии с
множественными метастазами и выраженной кахексией и одно-
179
временно острый инфаркт миокарда. Невозможно точно устано-ч
вить, какая из этих болезней привела больного к смерти, они
конкурируют между собой в танатогенезе.
Сочетанные заболевания — это болезни с разными этиологией
и патогенезом, каждая из которых в отдельности не является при-ч
чиной смерти, но, совпадая по времени развития и взаимно отя->
гощая друг друга, они приводят больного к смерти. Например, у
пожилой женщины перелом шейки бедра и очагово-сливная за->
стойкая пневмония в заднебазальных отделах левого легкого. Ка->
ждое из этих заболеваний в отдельности не является смертель->
ным, но их сочетание, особенно у пожилой пациентки, явилось
причиной смерти.
Фоновые заболевания — болезни, создающие неблагоприятный
фон для течения основного заболевания. Например, у больного
основным заболеванием является острый инфаркт миокарда, а
неблагоприятным фоном для него — выраженный атеросклероз с
преимущественным поражением сосудов сердца.
После составления патологоанатомического диагноза обяза->
тельно проводится сличение его с клиническим диагнозом. Это
делается для того, чтобы вместе с лечащим врачом окончательно
уяснить этиологию, патогенез и морфогенез болезни у конкрегп
него больного. Такой совместный анализ — большая и повсе->
дневная школа и для клинициста, и для патологоанатома, так как
именно на вскрытии можно увидеть, оценить и уточнить, какие
изменения и в каких органах возникли в результате заболевания,
ибо в прозектуре, по выражению К. Рокитанского, "мертвые учат
живых". Кроме того, сличение диагнозов позволяет оценить уро-1
вень диагностической и лечебной работы больницы или поли->
клиники — большое количество совпадений клинического и па->
тологоанатомического диагнозов говорит о хорошей работе боль->
ницы и высоком профессионализме ее персонала. И наоборот,
большое количество диагностических ошибок, каждая из которых
может повлечь за собой неправильное лечение больного, говорит
о недостаточном уровне профессиональной подготовки медицин^
ского персонала или о недостаточных диагностических возмож->
ностях лечебного учреждения в связи с отсутствием необходимого
оборудования.
Очень важной и сложной проблемой являются заболевания
или осложнения болезней, связанные с действием медицинского
персонала, так называемые ятрогении.
Ятрогении — это любые неблагоприятные последствия профи->
лактических. диагностических или лечебных вмешательств либо
процедур, которые приводят к нарушениям функций организма,
инвалидизации или к смерти больного. Ятрогении делят на меди->
цинские ошибки и медицинские проступки или преступления.
Следует заметить, что медицинское преступление может быть ус->
тановлено только судом.
Медицинская ошибка — это добросовестное заблуждение ме->
дицинского работника при исполнении им своих профессиональ-
но
ных обязанностей и поэтому не являющееся проступком или пре->
ступлением. Медицинская ошибка не является результатом халат-"
него отношения к своим обязанностям, невежества или зло->
умышленного действия. Она не может быть предусмотрена или
предотвращена медицинским работником вследствие его недоста->
точного профессионального опыта, из-за отсутствия необходим
мых лабораторных возможностей или соответствующей аппаратур
ры. Например, при катетеризации подключичной артерии иногда
разрушается катетер и его кусочки становятся эмболами, вызы->
вающими тяжелые последствия или даже смерть больного. Это
ятрогения, но она не является следствием халатности медицин^
ского работника.
Медицинское преступление — нанесение вреда здоровью или
смерть больного в результате ненадлежащего или халатного ис->
полнения медицинским работником своих профессиональных
обязанностей. Например, операционная сестра не зафиксировала
салфетку в брюшной полости и не пересчитала салфетки после
операции. В результате у больного развился перитонит и он умер.
Это медицинское преступление. Либо медицинская сестра по ха->
латности ввела больному не то лекарство, которое было назначе->
но врачом, и это нанесло вред больному, или быстро ввела стро-ч
фантин и больной умер, хотя медсестра обязана знать особенное
сти введения этого препарата.
Ятрогении сопровождают работу медицинского персонала, они
чаще представляют собой технические ошибки, однако их оценка
производится отдельно в каждом конкретном случае либо кол->
лективом больницы, либо следствием и судом.
Таким образом, учение о нозологии является тем стержнем
медицинской науки и практики, без которого не может быть по->
нимания сущности болезней, принципов их лечения, а также
взаимодействия медицинского сообщества.
Глава 12
БОЛЕЗНИ СИСТЕМЫ КРОВИ
ФУНКЦИИ СИСТЕМЫ КРОВИ
Система крови включает:
• органы и ткани кроветворения, или гемопоэта, в которых
созревают форменные элементы крови;
• периферическую кровь, которая включает циркулирующую
и депонированную в органах и тканях фракции;
• органы кроворазрушения
181
Система крови является внутренней средой организма и одной
из его интегрирующих систем. Кровь выполняет многочисленные
функции — дыхания, обмена веществ, экскреции, терморегуля-
ции, поддержания водно-электролитного баланса. Она осуществ-
ляет защитные и регуляторные функции благодаря наличию в
ней фагоцитов, различных антител, биологически активных ве-
ществ, гормонов. На процессы кроветворения влияют многие
факторы. Важное значение имеют особые вещества, регулирую-
щие пролиферацию и созревание клеток крови, — гемопоэтины,
но общее регулирующее влияние оказывает нервная система. Все
многочисленные функции крови направлены на поддержание го-
меостаза.
Картина периферической крови и костного мозга позволяет
судить о функциях многих систем организма. При этом наиболее
полное представление о состоянии самой кроветворной системы
можно получить, лишь исследуя костный мозг. Для этого специ-
альной иглой (трепаном) проводят пункцию грудины или гребня
подвздошной кости и получают костномозговую ткань, которую
затем исследуют под микроскопом.
МОРФОЛОГИЯ КРОВЕТВОРЕНИЯ
Все форменные элементы крови в нормальных условиях обра-
зуются в красном костном мозге плоских костей — грудины, ре-
бер, костей таза, позвонков. В трубчатых костях взрослого чело-
века костный мозг представлен в основном жировой тканью и
имеет желтый цвет. У детей в трубчатых костях происходит кро-
ветворение, поэтому костный мозг красный.
Морфогенез кроветворения. Родоначальником всех клеток кро-
ви является стволовая кроветворная клетка костного мозга, кото-
рая трансформируется в клетки-предшественники, морфологиче-
ски неотличимые друг от друга, но дающие начало миело- и лим-
фопоэзу (рис. 42). Эти процессы регулируются гемопоэтинами,
среди которых выделяют эритро-. лейко- и тромбоцитопоэтины.
В зависимости от преобладания тех или иных поэтинов усилива-
ется миелопоэз и клетки-предшественники начинают трансфор-
мироваться в бластные формы миелоцитарного, эритроцитарного
и тромбоцитарного ростков крови. При стимуляции лимфопоэза
начинается созревание лимфоцитарного, а также моноцитарного
ростков крови. Таким образом происходит развитие зрелых кле-
точных форм — Т- и В-лимфоцитов, моноцитов, базофилов, эо-
зинофилов, нейтрофилов, эритроцитов и тромбоцитов.
На разных этапах гемопоэза в результате патологических воз-
действий могут возникать нарушения созревания кроветворных
клеток и развиваются болезни крови. Кроме того, на многие па-
тологические процессы, возникающие в организме, система кро-
ви реагирует изменением своего клеточного состава и других па-
раметров.
182
НАРУШЕНИЯ ОБЪЕМА ЦИРКУЛИРУЮЩЕЙ КРОВИ
При различных болезнях и
меняться общий объем крови,
патологических процессах может
а также соотношение ее формен-
Обсщя
хвли-лрадиюстввммщ
«««ЛОИВМ (КОе-ГЭММ)
II
Стволовая клопа
КОЕ-МГцЭ
Общи
лоти пр«ШМСТМ>Н1ц|
лммфопом*
кОЕ-ГЗ
Клета-
предшест
КОЕтунюй
клетки
КОЕ-ЭО КОЕ Г КОЕ-Э
кое-гм
Клетке
прОДшяст
Т лыыфо
цитоа
(лрв-Т)
:-М
ХОЕ6
IN
Нейтрофила КО&Э
КОЕ МГЦ
Монобласт
Эритробласт
проносиаоцит
Промрноцит
Палокгждярныо
Рипжулоцмг
Нормоцит
базофильный
Эрзмяо
фильный
ммллсбмст
Нормоцит
оксифильный
срмоцит
оынхрома
ТОфиЛМЫЙ
Промята
карноцит
»*м I
миелоблест '
Т лиыфофгг 8-л-»фоц <г
Биофиль-
шй
ьмиобшл
Т-лммфобто
В лшфобмст
Т-лролнмфоциг
В ГфОЛИМфОЦ Л
Моноцит
Т лимфоцит
Эйаинофил
биофил
М»гш-
рюцит
Зр>ггроцхг
Некрофил Тромбоцит
цитре
(npo-Bj
рноблает
В- имыунрбласт
Плезмобпст
ПрОЛЛИМОфСГ
ЮТО
СОвДИ»Ы-
тельной
ткани
КОСТНОГО
мака
сало
звнкм
Ммлснжты
Сегмвнпл^цврныа
Макрофеп*
смМфепЕ
брюши-w плееры
чеша
узлов
состжЛ
TYMt
Мрянэй
смстекы
Рис. 42. Схема кроветворения (по И. Л. Черткову и А. И. Воробьеву).
183
ных элементов и плазмы. Выделяют 2 основные группы наруше-
ний объема крови:
• гиперволемии — состояния, характеризующиеся увеличением
общего объема крови и. обычно, изменением гематокрита:
• гиповолемии — состояния, характеризующиеся уменьшени-
ем общего объема крови и сочетающегося со снижением
или увеличением гематокрита.
ГИПЕРВОЛЕМИИ
Видщ:
• Норлюцителическаягиперволемия — состояние, проявляю-
щееся эквивалентным увеличением объема форменных эле-
ментов и жидкой части циркулирующей крови. Гематокрит
остается в пределах нормы. Такое состояние возникает, на-
пример. при переливании большого количества (не менее
2 л) крови.
• Олигоцителическая гиперволемия — состояние, характери-
зующееся увеличением общего объема крови вследствие
возрастания главным образом объема плазмы. Показатель
гематокрита при этом ниже нормы. Такая гиперволемия
появляется при введении большого количества физиологи-
ческого раствора или кровезаменителей, а также при недос-
таточности выделительной функции почек.
• Полицителическая гиперволемия — состояние, проявляю-
щееся увеличением общего объема крови вследствие пре-
имущественного повышения числа ее форменных элемен-
тов, в первую очередь эритроцитов. При этом гематокрит
становится выше нормы. Наиболее часто такое явление на-
блюдается при длительной гипоксии, стимулирующей вы-
ход эритроцитов из костного мозга в кровь, например у жи-
телей высокогорья, на определенных этапах патогенеза ряда
заболеваний легких и сердца.
ГИПОВОЛЕМИИ
Виды:
• Норлюцителическая гиповолемия — состояние, проявляю-
щееся уменьшением общего объема крови при сохранении
гематокрита в пределах нормы, что наблюдается сразу после
кровопотери.
• Олигоцителическая гиповолемия характеризуется уменьше-
нием общего объема крови с преимущественным снижени-
ем количества ее форменных элементов. Гематокрит при
этом ниже нормы. Наблюдается также после кровопотери,
но в более поздние сроки, когда из межклеточного про-
странства в сосуды поступает тканевая жидкость. В этом
случае объем циркулирующей крови начинает возрастать, а
количество эритроцитов остается на низком уровне.
184
Полщителшческая гиповолемия — состояние, при котором
снижение общего объема крови обусловлено в основном
уменьшением объема плазмы. Показатель гематокрита при
этом выше нормы. Такое сгущение крови наблюдается при
потере жидкости после обширных ожогов, при гипертермии
с массивным потоотделением, холере, характеризующейся
неукротимой рвотой и поносом. Сгущение крови способст-
вует также образованию тромбов, а уменьшение общего
объема крови нередко приводит к сердечной недостаточ-
ности.
ПАТОЛОГИЯ СИСТЕМЫ ЭРИТРОЦИТОВ
Анемии, или малокровие, — снижение общего количества ге-
моглобина в организме и, как правило, гематокрита. В большин-
стве случаев анемии сопровождаются эритропенией — снижени-
ем количества эритроцитов в единице объема крови ниже нормы
(менее 3 • 109/л у женщин и 4 • 109/л у мужчин). Исключением яв-
ляются железодефицитная анемия и талассемия, при которых ко-
личество эритроцитов может быть нормальным или даже увели-
ченным.
Значение анемии для организма определяется прежде всего
уменьшением кислородной емкости крови и развитием гипоксии,
с которой связаны основные симптомы расстройств жизнедея-
тельности этих больных.
Виды анемий:
• вследствие кровопотери — постгеморрагические;
• вследствие нарушенного кровообразования —дефицитные;
• вследствие повышенного кроворазрушения — гемолитиче-
ские.
По течению анемии могут быть острыми и хроническими.
По изменениям структуры эритроцитов при анемиях выделяют:
• анизоцитоз, который характеризуется разной формой эрит-
роцитов;
• пойкилоцитоз — характеризуется разными размерами эрит-
роцитов.
При анемиях изменяется цветной показатель — содержание
гемоглобина в эритроцитах, который в норме равен 1. При ане-
миях он может быть:
• больше 1 (гиперхромная анемия);
• меньше 1 (гипохромная анемия).
АНЕМИИ ВСЛЕДСТВИЕ КРОВОПОТЕРИ (ПОСТГЕМОРРАГИЧЕСКИЕ)
Эти анемии всегда вторичны, так как возникают в результате
болезней или ранений.
Острая постгеморрагическая анемия возникает при острой кро-
вопотере. например из сосудов дна язвы желудка, при разрыве
185
маточной трубы в случае трубной беременности, из легочных ка-
верн при туберкулезе и т. п. (внутреннее кровотечение) или из
поврежденных сосудов при ранениях конечностей, шеи и других
частей тела (наружное кровотечение).
Механизмы развития острых постгеморрагических состояний.
На начальном этапе кровопотери в большей или меньшей мере
снижается объем циркулирующей крови и развивается гиповоле-
мия. В связи с этим уменьшается приток венозной крови к серд-
цу. его ударный и минутный выброс. Это обусловливает падение
уровня артериального давления и ослабление сердечной деятель-
ности. В результате уменьшается транспорт кислорода и субстра-
тов метаболизма из крови к клеткам, а от последних — углеки-
слого газа и отработанных продуктов обмена веществ. Развивает-
ся гипоксия, которая во многом определяет исход кровопотери.
Крайняя степень указанных расстройств в организме обозначает-
ся как постгеморратический шок.
Морфология. Проявлениями острой анемии являются бледность
кожных покровов и малокровие внутренних органов. В связи с рез-
ким уменьшением оксигенации тканей повышается выработка эри-
тропоэтина, стимулирующего эритропоэз. В костном мозге при
этом происходит значительное увеличение числа клеток эритроид-
ного ряда и костный мозг приобретает малиновый цвет. В селезен-
ке, лимфатических узлах, периваскулярной ткани появляются оча-
ги внекостномозгового, или экстрамедуллярного, кроветворения.
Нормализация показателей периферической крови после воспол-
нения кровопотери наступает примерно через 48—72 ч.
Нарушение гемодинамики и снижение интенсивности биоло-
гического окисления в клетках обусловливают включение адап-
тивных механизмов:
• активацию тромбообразования;
• реакции сердечно-сосудистой компенсации кровопотери в
виде сужения просвета мелких сосудов и выброса крови из
депо;
• повышение сердечного выброса;
• поддержание объема циркулирующей крови за счет поступ-
ления в сосуды жидкости из интерстиция.
Хроническая постгеморрагическая анемия возникает при значи-
тельной кровопотере вследствие повторяющихся кровотечений,
например из геморроидальных вен, при маточных кровотечениях
и т. п. Такая кровопотеря приводит к хронической гипоксии тка-
ней и нарушению в них обмена веществ.
Морфология. Хроническая гипоксия способствует развитию
жировой дистрофии паренхиматозных органов. Желтый костный
мозг трансформируется в красный, так как усиливаются эритро-
и миелопоэз. В печени, селезенке, лимфатических узлах могут
появляться очаги экстрамедуллярного кроветворения. Вместе с
тем при длительно повторяющихся и выраженных ковопотерях
может наступить гипо- и аплазия кроветворной ткани, что указы-
вает на истощение гемопоэза.
186
АНЕМИИ ВСЛЕДСТВИЕ НАРУШЕННОГО КРОВООБРАЗОВАНИЯ
(ДЕФИЦИТНЫЕ)
Эти анемии являются следствием недостатка ряда веществ, не-
обходимых для нормального гемопоэза — железа, витамина Bi2)
фолиевой кислоты и др. Среди них наибольшее значение имеет
злокачественная анемия Аддисона—Бирмера, в основе которой
лежит дефицит витамина В,2 и фолиевой кислоты.
В,2-дефицитная, или фолиеводефицитная, анемия. Этиология
анемии связана с дефицитом витамина В,2 и фолиевой кислоты,
которая регулирует нормальный гемопоэз в костном мозге. Одна-
ко для активации фолиевой кислоты необходимо, чтобы посту-
пающий с пищей витамт В12 (внешний фактор) соединился с об-
разующимся в желудке белком — гастромукопротеином {внутрен-
ний фактор), который вырабатывается добавочными клетками
желез слизистой оболочки желудка. Вместе они образуют ком-
плекс, который называется антианемическим фактором Затем
этот комплекс поступает в печень и активирует фолиевую кисло-
ту, а та в свою очередь стимулирует эритропоэз по эритробла-
стичскому типу. Если же развивается аутоиммунный гастрит и
появляются антитела к добавочным клеткам или гастромукопро-
теину, которые уничтожают эти клетки или внутренний фактор,
то в слизистой оболочке желудка не всасывается витамин Bi2 и не
образуется гастромукопротеин. Такая же ситуация возникает при
высокой резекции желудка по поводу опухоли или язвенного
процесса.
Патогенез. В результате атрофии слизистой оболочки желудка
аутоиммунного характера возникает дефицит фолиевой кислоты
и витамина Bi2. Нарушается эритропоэз и вместо эритроцитов об-
разуются их предшественники — крупные мегалобласты, которые
появляются в периферической крови. Однако мегалобласты быст-
ро разрушаются, развиваются анемия и общий гемосидероз. Кро-
ме того, при дефиците витамина Bi2 нарушается образование
миелина в оболочках нервных стволов, что нарушает их функ-
цию.
Патологическая анатомия. У больных отмечаются бледность
кожных покровов, водянистая кровь, точечные кровоизлияния,
из-за атрофии слизистой оболочки языка он приобретает мали-
новую окраску (гунтеровский голоссит), характерны атрофиче-
ский гастрит, уплотнение и увеличение печени из-за жировой
дистрофии и гемосидероза, связанных с гипоксией и с усилен-
ным разрушением мегалобластов. В спинном мозге — распад
осевых цилиндров в задних и боковых столбах и очаги размяг-
чения ткани мозга (фуникулярный миелоз), что сопровождается
тяжелой неврологической симптоматикой. Костный мозг пло-
ских и трубчатых костей красный, напоминает малиновое желе.
В селезенке и лимфатических узлах очаги экстрамедуллярного
кроветворения.
Течение заболевания прогрессирующее, с периодами ремиссии
187
и обострения. Лечение анемии препаратами фолиевой кислоты и
витамина Bi2 привело к тому, что больные перестали умирать от
этого заболевания.
АНЕМИИ ВСЛЕДСТВИЕ ПОВЫШЕННОГО КРОВОРАЗРУШЕНИЯ -
ГЕМОЛИТИЧЕСКИЕ
Для этих анемий характерно преобладание процесса разруше-
ния эритроцитов (гемолиз) над их образованием. Продолжитель-
ность жизни эритроцитов при этом снижена и не превышает 90—
100 дней.
Виды гемолитических анемий
По происхождению гемолитические анемии делят на приобре-
тенные (вторичные) и врожденные или наследственные.
Приобретенные гемолитические анемии могут быть вызваны
многочисленными факторами. Этиология этих анемий связана с
действием факторов физического, химического и биологического,
в том числе аутоиммунного, характера, особенно при дефиците
веществ, стабилизирующих мембраны эритроцитов, например а-
токоферола. Наибольшее значение имеют так называемые гемо-
литические яды химического (соединения мышьяка, свинца, фос-
фора и др.) и биологического происхождения. Среди последних
— яды грибов, различные токсичные вещества, образующиеся в
организме при тяжелых ожогах, инфекционные болезни (напри-
мер, малярия, возвратный тиф), переливание крови, несовмести-
мой по группе или резус-фактору.
Патогенез. Гемолиз эритроцитов может происходить внутри
сосудов и за их пределами. При этом распадается гемоглобин и
из гема синтезируются два пигмента — гемосидерин и билиру-
бин. Поэтому гемолитические анемии обычно сопровождаются
развитием общего гемосидероза и желтухи. Кроме того, эритро-
пения и распад гемоглобина приводят к появлению выраженной
гипоксии, сопровождающейся жировой дистрофией паренхима-
тозных органов.
Морфология гемолитических анемий характеризуется развити-
ем гиперпластических процессов в костном мозге, в связи с чем
он приобретает малиновый цвет, появлением очагов экстрамедул-
лярного кроветворения, выраженной желтухой кожных покровов
и внутренних органов, гемосидерозом и жировой дистрофией пе-
чени, сердца и почек.
Гемолитическая болезнь новорожденных является примером
приобретенных гемолитических анемий и имеет большое значе-
ние в акушерской и педиатрической практике. В ее основе лежит
иммунный конфликт между матерью и плодом по резус-фактору,
который обладает антигенными свойствами. Этот фактор впервые
был обнаружен в эритроцитах обезьян макак резусов и имеется у
80—85 % людей. Если мать резус-отрицательна, т. е. не имеет ре-
зус-фактора, а плод резус-положительный, то в организме матери
188
Рис. 43. Серповидно-клеточная ане-
мия. Эритроциты серповидной фор-
мы. Электронограмма.
образуются антитела против
эритроцитов плода и у него воз-
никает внутрисосудистый гемо-
лиз эритроцитов. При этом плод
может погибнуть на 5—7-м меся-
це беременности, а у новорож-
денных развивается гемолитиче-
ская анемия, сопровождающаяся
малокровием и жировой дистро-
фией внутренних органов, выра-
женной желтухой и гемосиде-
розом.
Наследственные, или врожденные, гемолитические анемии свя-
заны с каким-либо генетическим дефектом структуры мембран,
ферментов или гемоглобина. Этот дефект передается по наслед-
ству.
Виды: врожденные гемолитические анемии в зависимости от
генетического дефекта могут быть обусловлены мембранопатия-
ми, ферментопатиями, гемоглобинопатиями.
Патогенез всех врожденных гемолитических анем ий в основ-
ном сходен — в результате того или иного генетического дефекта
либо разрушается мембрана эритроцитов, а сами эритроциты
уменьшаются в размерах и могут принимать сферическую форму
(микросфероиитоз), либо повышается проницаемость мембраны и
эритроциты увеличиваются в размерах за счет поступления избы-
точного количества жидкости, либо нарушается синтез гемогло-
бина (гемоглобинозы) и образуются эритроциты неправильной
формы, содержащие быстро распадающийся гемоглобин, причем
удерживающий кислород (талассемия, серповидно-клеточная ане-
мия и др.) (рис. 43).
Морфология врожденных гемолитических анемий мало отлича-
ется от изменений при вторичных гемолитических анемиях, за
исключением размеров и формы эритроцитов. Также характерны
выраженный внутрисосудистый гемолиз, гипоксия, гемосидероз,
жировая дистрофия паренхиматозных органов, гиперплазия кро-
ветворной ткани, возможны очаги экстрамедуллярного кроветво-
рения, гепато- и спленомегалия.
ПАТОЛОГИЯ СИСТЕМЫ ЛЕЙКОЦИТОВ
В крови здорового человека в условиях покоя натощак содер-
жится 4* 109/л лейкоцитов. Много лейкоцитов находится в тка-
нях, где они участвуют в иммунном контроле.
189
ТИПОВЫЕ ИЗМЕНЕНИЯ
Типовые изменения количества лейкоцитов в единице объема
крови характеризуются либо их снижением — лейкопении, либо
увеличением — лейкоцитозы, что, как правило, является реакци-
ей системы лейкоцитов, развивающейся при болезнях и патоло-
гических состояниях. Поэтому излечение болезни приводит к
нормализации лейкоцитарной формулы.
Лейкопения — уменьшение количества лейкоцитов в единице
объема крови ниже нормы, обычно менее 4* 109/л. Она возникает
в результате угнетения белого ростка системы гемопоэза, при
усиленном разрушении лейкоцитов или при перераспределении
крови между кровеносным руслом и депо крови, что наблюдает-
ся, например, при шоке.
Значение лейкопении заключается в ослаблении защитных сил
организма и повышении его восприимчивости к различным ин-
фекционным возбудителям.
Виды лейкопений по происхождению:
• первичные лейкопении (врожденные или наследственные)
связаны с различными генетическими дефектами в системе
кроветворения на разных этапах лейкопоэза;
• вторичные лейкопении возникают при действии на организм
различных факторов — физических (ионизирующие излуче-
ния и т. п.), химических (бензол, инсектициды, цитостати-
ки, сульфаниламиды, барбитураты и др.), продуктов мета-
болизма или компонентов различных возбудителей болезней.
Лейкоцитарная формула — соотношение различных видов
циркулирующих лейкоцитов. Если увеличивается количество мо-
лодых форм нейтрофилов (палочкоядерных, метамиелоцитов,
миелоцитов, промиелоцитов), расположенных в левой части лей-
коцитарной формулы, говорят о сдвиге формулы влево, что ука-
зывает на усиление пролиферации клеток миелоцитарного ряда.
В правой части формулы располагаются зрелые формы этих кле-
ток. Излечение болезни приводит к нормализации лейкоцитар-
ной формулы. Уменьшение нормального числа лейкоцитов в лей-
коцитарной формуле указывает на снижение регенераторных воз-
можностей миелоидной ткани.
Патогенез лейкопений отражает нарушение или угнетение про-
цесса лейкопоэза, а также чрезмерное разрушение лейкоцитов в
циркулирующей крови или в органах гемопоэза, перераспределе-
ние лейкоцитов в сосудистом русле, возможна также потеря лей-
коцитов организмом. При этом вследствие угнетения регенера-
ции лейкопоэтической ткани на начальных этапах лейкопении
снижается количество молодых форм нейтрофилов, а увеличение
их молодых форм (т. е. сдвиг лейкоцитарной формулы влево)
указывает на прекращение повреждающего действия и активацию
лейкопоэза. Возможно также появление анизоцитоза и пойкило-
цитоза лейкоцитов.
Лейкоцитоз — увеличение количества лейкоцитов в единице
190
объема крови выше 4 • 109/л. Он может быть физиологическим,
адаптивным, патологическим или носить форму пейкемоидной
реакции.
Физиологический лейкоцитоз возникает у здоровьк людей в свя-
зи с перераспределением крови во время пищеварения, при фи-
зической работе.
Адаптивный лейкоцитоз развивается при заболеваниях, особен-
но характеризующихся воспалением. При этом количество лейко-
цитов может увеличиваться до 40- 109/л.
Патологический лейкоцитоз отражает опухолевуи природу лей-
коцитоза и характеризует лейкоз.
Лейкемоидная реакция — повышение общего чиста лейкоцитов
периферической крови более 40- 109/л с появлением их незрелых
форм (промиелоцитов, миелобластов), что делает лейкоцитоз по-
хожим на лейкоз.
Виды лейкоцитоза связаны с увеличением тех или иных форм
лейкоцитов:
базофильный — увеличение количества базофилов, встречается
редко, в основном при некоторых лейкозах;
.юзинофтльный — проявляется увеличением количества эозино-
филов и характерен для хронического воспаления, заболеваний,
вызванных паразитами (аскаридоз, эхинококкоз, трихинеллез и
т. п.), а также как проявление аллергии (бронхиальная астма);
нейтрофильный — наиболее частый вид лейкоцитоза. Характе-
рен для гнойного и других видов экссудативного воспаления, а
также для асептического воспаления (например, инфаркт мио-
карда), развивается при кровопотере и др. При этом обычно на-
блюдается сдвиг лейкоцитарной формулы влево;
лимфоцитарный — развивается при некоторых хронических
инфекционных заболеваниях, таких как туберкулез, бруцеллез
и др., а также может быть в норме у детей раннего возраста;
моноцитарный — появляется при некоторых протозойных (ма-
лярия, лейшманиоз) и вирусных инфекциях (инфекционный мо-
нонуклеоз, краснуха).
Агранулоцитоз — отсутствие или значительное снижение абсо-
лютного числа всех видов зернистых гранулоцитов (лейкоцитов) —
нейтрофилов, эозинофилов, базофилов. Агранулоштоз, как пра-
вило, сочетается с лейкопенией.
ОПУХОЛИ СИСТЕМЫ КРОВИ, ИЛИ ГЕМОБЛАСТОЗЫ
Гемобластозы — опухолевые заболевания кроветворной и лим-
фатической ткани. Они подразделяются на системные заболева-
ния — лейкозы, и регионарные — злокачественные ли мфо мы, или
гематосаркомы. При лейкозах первично поражается костный
мозг и опухолевые клетки обнаруживаются в крови (лейкемия), а
при лимфомах в терминальной стадии наступает обширное мета-
стазирование со вторичным поражением костного мозга. По рас-
193
пространенности гемобластозы занимают 5-е место среди всех
опухолей человека. У детей первых 5 лет жизни на их долю при-
ходится 30 % случаев онкологических заболеваний.
Этиология гемобластом принципиально не отличается от при-
чин, вызывающих другие опухоли (см. главу 10) — это различные
мутагенные факторы экзо- и эндогенного происхождения, дейст-
вующие на стволовые и полустволовые клетки-предшественницы.
Большое значение в возникновении гемобластозов имеет наслед-
ственный фактор.
Патогенез. Множество этиологических факторов воздействуют
на геном стволовых и полустволовых клеток, приводя к их злока-
чественной трансформации. Поэтому геном является так назы-
ваемым узким местом, через которое мутагены воздействуют на
протоонкогены и антионкогены, превращая их в клеточные онко-
гены, что приводит к появлению опухоли. Развитие гемобласто-
зов начинается с малигнизации одной стволовой или полустволо-
вой клетки, дающей пул опухолевых клеток. Следовательно, все
гемобластозы имеют моноклоновое происхождение, и все после-
дующие опухолевые клетки развиваются из первоначально мути-
ровавшей клетки и относятся к одному клону. Кроме малигниза-
ции на уровне стволовых и полустволовых клеток-предшествен-
ниц, развивается еще блок дифференцировки в пуле опухолевых
клеток и они теряют способность к созреванию.
ЛЕЙКОЗЫ
Лейкозы — системные опухолевые заболевания, возникающие
из кроветворных клеток с поражением костного мозга. Заболевае-
мость лейкозами колеблется от 3 до 10 на 100 000 населения.
Мужчины болеют в 1,5 раза чаще женщин. Острые лейкозы чаще
наблюдаются в возрасте от 10 до 18 лет, а хронические — у людей
старше 40 лет.
Морфогенез. При лейкозах опухолевая ткань первоначально
разрастается на территории костного мозга и постепенно подав-
ляет и вытесняет нормальные ростки кроветворения. Поэтому у
больных лейкозом развиваются анемия, тромбоците»-, лимфоци-
те)-, гранулоцитопения, что приводит к повышенной кровоточи-
вости, кровоизлияниям, снижению иммунитета и присоединени-
ем инфекционных заболеваний. Метастазирование при лейкозах
заключается в появлении лейкозных инфильтратов в печени, се-
лезенке, лимфатических узлах, стенках сосудов и др. Обтурация
сосудов опухолевыми клетками приводит к развитию инфарктов
органов и язвенно-некротическим осложнениям.
Классификация лейкозов основана на 5 признаках этих заболе-
ваний.
1. По степени дифференцировки опухолевых клеток выделяют
недифференцированные, властные и цитарные лейкозы.
При высоком уровне блока дифференцировки клетки опухо-
ли напоминают недифференцированные и бластные формы ге-
192
мопоэза. Такие лейкозы протекают остро и очень злокачест-
венно.
При остановке дифференцирования на уровне процитарных и
цитарных клеток-предшественниц лейкозы протекают хрониче-
ски и менее злокачественно.
2. По цитогенетическому признаку острые лейкозы подразделя-
ют на лимфобластный, миелобластный, монобластный, эритро-
миелобластный, мегакариобластный, недифференцированный.
Хронические лейкозы делят на лейкозы миелоцитарного проис-
хождения (хронический миелоцитарный, хронический нейтро-
фильный, хронический эозинофильный и др.), лимфоцитарного
(хронический лимфолейкоз и парапротеинемические лейкозы —
миеломная болезнь, первичная макроглобулинемия Вальденстре-
ма и др.) и моноцитарного — хронический моноцитарный лей-
коз, гистиоцитоз X.
3. По иммунному фенотипу опухолевых клеток: на основании
выявления маркеров их антигенов.
4. По общему количеству лейкоцитов в периферической крови
выделяют лейкозы:
лейкемические — десятки и сотни тысяч лейкоцитов в 1
мкл крови, в том числе бласты;
сублейкемические — число лейкоцитов крови составля-
ет 25—50 • 109/л, включая бластные формы;
лейкопенические — количество лейкоцитов в перифери-
ческой крови ниже нормы, но есть бласты;
алейкемические — количество лейкоците» в крови мень-
ше нормы и отсутствуют бластные формы.
5. По характеру течения выделяют:
— острые лейкозы (они же недифференцированные и бластные);
— хронические лейкозы (цитарные).
Острые лейкозы развиваются из всех ростков морфологически
недифференцируемых кроветворных клеток-предшественниц.
Длительность течения заболевания составляет 2—18 мес, при ус-
пешном лечении ремиссии могут длиться до 5—8 лет.
Морфогенез. Различные формы острых лейкозе» имеют стерео-
типные морфологические проявления. Они заклинаются в разви-
тии лейкозной инфильтрации костного мозга атипичными клет-
ками ранних стадий гемопоэза (рис. 44). Ввиду недифференциро-
ванное™ этих клеток их цитогенетическую принадлежность мож-
но выявить лишь с помощью цитохимических и иммуногистохи-
мических методов. Костный мозг трубчатых костей становится
красным, при некоторых острых лейкозах он приобретает зелено-
ватый цвет, свойственный гною, — пиоибный костный мозг. При
этом происходит вытеснение нормальных клеток гемопоэза опу-
холевыми клетками. В периферической крови и в костном мозге
имеются только бластные и зрелые формы клеток, но отсутству-
ют их промежуточные формы. Такая картина крви называется
"лейкелшческий провал". Лейкозные инфильтраты обнаруживаются
в лимфатических узлах, селезенке и печени, что приводит к уве-
193
Рис. 44. Костный мозг при
остром лимфобластном лейко-
зе. Ткань мозга состоит в ос-
новном из лимфобластов (а),
просветы сосудов заполнены
теми же клетками (б).
личению этих органов —
спленомегалии, гепатомега-
лии. Лейкозная инфильтра-
ция слизистой оболочки
полости рта и ткани минда-
лин осложняется некроти-
ческим гингивитом, тон-
зиллитом, некротической
ангиной, а при инфильтра-
ции оболочек мозга развивается лейкозный менингит. Подавле-
ние эритроцитарного ростка приводит к нарастающей гипоксии и
жировой дистрофии паренхиматозных органов. В результате
тромбоцитопении, поражения печени и стенок сосудов у больных
развивается геморрагический синдром вплоть до кровоизлияний
в мозг и смертельных желудочно-кишечных кровотечений. На
этом фоне иногда присоединяется сепсис, приводящий больных
к смерти (рис. 45).
Наиболее часто, особен-
но у детей, встречается ост-
рый лимфобластный лейкоз,
связанный с опухолевой
трансформацией предшест-
венников Т- и В-лимфоци-
тов, и острый миелобласт-
ный лейкоз, которым чаще
страдают взрослые, обу-
словленный опухолевой
пролиферацией клеток-
предшественниц миелоид-
ного ряда.
Рис. 45. Острый лейкоз,
а — лейкозная инфильтрация пе-
чени (показано стрелками); б —
некроз миндалины (некротическая
ангина); в — лейкозная инфильт-
рация почек; г — множественные
кровоизлияния в эпикарде и эндо-
карде; д — лейкозная инфильтра-
ция костного мозга (пиоидный ко-
стный мозг), истончение корти-
кального слоя бедренной кости
(показано стрелкой).
194
Рис. 46. Печень при хрониче-
ском миелолейкозе. Разраста-
ние клеток миелоидного рода
(а) по ходу синусоидов.
Хронические лейкозы те-
кут более 4 лет, при успеш-
ном лечении ремиссии забо-
левания могут продолжаться
20 лет и более. Хронические
лейкозы отличаются от ост-
рых цитарной дифференци-
ровкой опухолевых клеток
и более длительным тече-
нием, которое имеет опре-
деленные стадии:
• моноклоновая стадия характеризуется присутствием только
одного клона опухолевых клеток, течет годами, относитель-
но доброкачественно;
• поликлоновая стадия, или властный криз, связана с появле-
нием вторичных опухолевых клонов, характеризуется быст-
рым злокачественным течением, и 80 % больных погибают
именно в этой стадии.
Морфогенез. Лейкозные инфильтраты разрастаются в костном
мозге, печени, селезенке, почках, в лимфатических узлах, бры-
жейке кишечника, нередко в средостении, в связи с чем эти орга-
ны и ткани резко увеличиваются в размерах и могут сдавливать
соседние органы (рис. 46). Особенно выражена спленомегалия
(масса селезенки достигает 6—8 кг) и гепатомегалия (масса пече-
ни 5—6 кг). В сосудах образуются лейкозные тромбы, которые
могут привести к развитию ишемических инфарктов, чаще в се-
лезенке и почках. В крови нарастает количество нейтрофильных
лейкоцитов или лимфоцитов, много переходных клеточных форм.
Выражена анемия, тромбоцитопения, значительная иммуноде-
прессия и предрасположенность к инфекционным осложнениям,
от которых больные нередко погибают. Костный мозг серо-крас-
ный. Жировая дистрофия паренхиматозных органов придает им
серо-желтую окраску.
Доброкачественное течение сменяется бластным кризом. При
этом в крови быстро нарастает количество бластных форм — мие-
ло-, эритро-, лимфо-, мегакариобластов и др. Общее число лейко-
цитов периферической крови может достигать несколько миллио-
нов в 1 мкл. Властный криз служит причиной смерти больных.
ПАРАПРОТЕИНЕМИЧЕСКИЕ ЛЕЙКОЗЫ
Парапротеинемические лейкозы характеризуются способно-
стью опухолевых клеток синтезировать однородные иммуногло-
булины или их фрагменты — парапротеины. При этом опухоле-
195
вые клетки представляют собой атипичные плазмоциты и поэто-
му сохраняют способность в извращенной форме синтезировать
атипичные иммуноглобулины.
Миеломная болезнь (плазмоцитома) — хронический лейкоз,
наиболее часто встречающийся среди парапротеинемических ге-
мобластозов. Возникает в основном у взрослых и при современ-
ных методах лечения может продолжаться 4—5 лет. В основе бо-
лезни лежит опухолевое разрастание в костном мозге атипичных
плазмоцитов, получивших название миеломных клеток. Они син-
тезируют парапротеины, которые обнаруживаются в крови и моче
больных. По характеру и распространенности опухолевого ин-
фильтрата в костном мозге выделяют узловатую и диффузную
формы болезни.
При узловатой форлк плазмоцитома образует опухолевые узлы
в костном мозге, обычно плоских костей (свода черепа, ребер, та-
за) и позвонков. Лейкозная инфильтрация сопровождается раз-
жижением кости или ее пазушным рассасыванием (остеолизис и
остеопороз) с образованием правильной формы округлых дефек-
тов, которые на рентгенограмме выглядят как гладкостенные
пробоины. Пазушное рассасывание обусловливает выход кальция
из костей и развитие гиперкальциемии с появлением множест-
венных известковых метастазов в мышцах и паренхиматозных ор-
ганах. Кроме того, возникают патологические переломы костей.
При генерализованной фор лк миеломной болезни разрастание
миеломных клеток происходит, помимо костного мозга, в селе-
зенке, лимфатических узлах, печени, почках и других внутренних
органах.
Морфогенез. В периферической крови обнаруживаются ано-
мальные иммунные белки (парапротеины), в том числе мелко-
дисперсный белок Бенс-Джонса, который легко проходит через
почечный фильтр и выявляется в моче. В связи с большой кон-
центрацией белка Бенс-Джонса развивается парапротеинемиче-
ский нефроз. Кроме того, в связи с нарушениями нормального
синтеза иммунопротеинов плазмоцитома часто осложняется раз-
витием амилоидоза с поражением почек. Поэтому причиной
смерти этих больных нередко является уремия. Из-за резкого уг-
нетения функции иммунной системы к основному заболеванию
может присоединяться вторичная инфекция, которая также слу-
жит причиной смерти больных миеломной болезнью.
ЗЛОКАЧЕСТВЕННЫЕ ЛИМФОМЫ (ГЕМАТОСАРКОМЫ)
Злокачественные лимфомы (гематосаркомы) — регионарные
злокачественные опухоли лимфоидной ткани, имеющие моно-
клоновое происхождение. Лимфомы развиваются из незрелых
форм лимфоцитов и поражают лимфатическую ткань какой-либо
одной области, однако в терминальной стадии заболеваний воз-
можна генерализация опухолевого процесса с развитием метаста-
зов в костный мозг.
196
Этиология. Причины возникновения злокачественных лим-
фом в принципе не отличаются от причин, вызывающих опухоли
другого происхождения. Вместе с тем доказано, что часть лим-
фом. так же как и некоторые другие лейкозы, имеет вирусное
происхождение. Не исключена и наследственная предрасполо-
женность к заболеванию. Трансформация нормальных гемопо-
этических клеток в опухолевые происходит в результате измене-
ний в геноме, вследствие чего нормальная генетическая програм-
ма гемопоэза изменяется в направлении опухолевого атипизма.
Классификация лимфом.
Поклинико-люрфол)гическимособенностялс
— лимфогранулематоз, или болезнь Ходжкина;
— неходжкинские лимфомы.
По источнику роста (цитогенезу):
— В-лимфоцитарные;
—Т-лимфоцитарные.
По степени дифференцировки опухолевых клеток:
— низкой злокачественности;
— умеренной злокачественности;
— высокой злокачественности.
Лимфогранулематоз (болезнь Ходжкина) описан в 1832 г. анг-
лийским врачом Т. Ходжкиным. Частота заболевания составляет
3 случая на 100 000 населения, или 1 % всех злокачественных но-
вообразований. Опухоль поражает лимфатические узлы обычно
одной области — шейные, медиастинальные, забрюшинные, реже
подмышечные или паховые.
Морфогенез. Пораженные лимфатические узлы увеличиваются
в размерах, сливаются между собой и образуют крупные пакеты.
В начале заболевания лимфатические узлы мягкие, на разрезе ро-
зового цвета. По мере прогрессирования лимфомы в них развива-
ются некротические, а затем склеротические изменения, в связи
с чем лимфатические узлы уплотняются, на разрезе выглядят су-
ховатыми и пестрыми. В своем развитии лимфогранулематоз про-
ходит несколько стадий — от изолированного поражения группы
лимфатических узлов до генерализованного поражения внутрен-
них органов с подавлением лимфоидной ткани и замещением ее
полями склероза.
При микроскопическом исследовании опухоль состоит из поли-
морфных опухолевых клеток лимфоцитарного ряда, среди которых
имеются характерные гигантские клетки с лопастным ядром и уз-
ким ободком цитоплазмы — клетки Березовского—Штернберга. Эти
клетки служат диагностическим признаком лимфогранулематоза.
Кроме того, характерны клетки Ходжкина — крупные клетки с
большим светлым ядром и темным ядрышком. Нередко в финале
заболевания оно приобретает генерализованный характер с пора-
жением многих внутренних органов — желудка, легких, печени,
кожи. При вскрытии умерших от лимфогранулематоза особенно
демонстративно выглядит селезенка — она увеличена в размерах,
плотная, на разрезе красная с множественными бело-желтыми оча-
197
гами некроза и склероза, что придает ей сходство с особым видом
гранита — порфиром (порфировая селезенка).
Неходжкинские лимфомы. Это группа злокачественных опухо-
лей из недифференцированных и бластных форм В- и Т-клеток
лимфатической ткани. Диагноз этих заболеваний требует обяза-
тельного морфологического и иммуногистохимического исследо-
вания биоптатов лимфатичесих узлов.
Глава 13
БОЛЕЗНИ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ
ПАТОЛОГИЯ СИСТЕМЫ КРОВООБРАЩЕНИЯ
Система кровообращения является одной из интегрирующих
систем организма. В норме она оптимально обеспечивает потреб-
ности органов и тканей в кровоснабжении. При этом уровень
системного кровообращения определяется:
• деятельностью сердца;
• тонусом сосудов:
• состоянием крови — величиной ее общей и циркулирую-
щей массы, а также реологическими свойствами.
Нарушения функции сердца, сосудистого тонуса или измене-
ния в системе крови могут привести к недостаточности кровооб-
ращения — состоянию, при котором система кровообращения не
обеспечивает потребности тканей и органов в доставке к ним с
кровью кислорода и субстратов метаболизма, а также транспорт
от тканей углекислоты и метаболитов.
Основные причины недостаточности кровообращения:
• патология сердца;
• нарушения тонуса стенок кровеносных сосудов;
• изменения массы циркулирующей крови и/или ее реологи-
ческих свойств.
По остроте развития и характеру течения выделяют острую и
хроническую недостаточность кровообращения.
Острая недостаточность кровообращения развивается в течение
часов или суток. Наиболее частыми причинами ее могут быть:
• острый инфаркт миокарда;
• некоторые виды аритмии;
• шок;
• острая кровопотеря.
Хроническая недостаточность кровообращения развивается на
протяжении нескольких месяцев или лет и причинами ее явля-
ются:
• хронические воспалительные заболевания сердца;
198
• кардиосклероз:
• пороки сердца;
• гипер- и гипотензивные состояния;
• анемии.
По выраженности признаков недостаточности кровообращения
выделяют 3 ее стадии. При I стадии признаки недостаточности
кровообращения (одышка, сердцебиение, венозный застой) от-
сутствуют в покое и выявляются лишь при физической нагрузке.
При II стадии указанные и другие признаки недостаточности
кровообращения обнаруживаются как в покое, гак и особенно
при физической нагрузке. При III стадии наблюдаются значи-
тельные нарушения сердечной деятельности и гемодинамики в
покое, а также развитие выраженных дистрофических и структур-
ных изменений в органах и тканях.
ПАТОЛОГИЯ СЕРДЕЧНОЙ ДЕЯТЕЛЬНОСХИ
Основную часть различных патологических процессов, пора-
жающих сердце, составляют три группы типовых форм патоло-
гии: коронарная недостаточность, аритмии и сердечная недоста-
точность.
1. Коронарная недостаточность характеризуется превышением
потребности миокарда в кислороде и субстратах метаболизма над
их притоком по коронарным артериям.
Виды коронарной недостаточности:
• обратимые (транзиторные) нарушения коронарного крово-
тока; к ним относится стенокардия, характеризующаяся
сильной сжимающей болью в области грудины, возникаю-
щей вследствие ишемии миокарда;
• необратимое прекращение кровотока или длительное зна-
чительное уменьшение притока крови по коронарным арте-
риям, что завершается, как правило, инфарктом миокарда.
Механизмы повреждения сердца при коронарной недостаточно-
сти.
Недостаток кислорода и субстратов обмена веществ в миокар-
де при коронарной недостаточности (стенокардии, инфаркте
миокарда) обусловливает развитие ряда общих, типовых механиз-
мов повреждения миокарда:
• расстройство процессов энергетического обеспечения кар-
диомиоцитов;
• повреждение их мембран и ферментов;
• дисбаланс ионов и жидкости;
• расстройство механизмов регуляции сердечной деятельно-
сти.
Изменение основных функций сердца при коронарной недос-
таточности заключается прежде всего в нарушениях его сократи-
тельной деятельности, показателем чего является снижение удар-
ного и сердечного выбросов.
199
2. Аритмии — патологическое состояние, обусловленное нару-
шением ритма сердца. Они характеризуются изменением частоты
и периодичности генерации импульсов возбуждения или последо-
вательности возбуждения предсердий и желудочков. Аритмии яв-
ляются осложнением многих заболеваний сердечно-сосудистой
системы и главной причиной внезапной смерти при сердечной
патологии.
Виды аритмий, их этиология и патогенез. Аритмии являются
следствием нарушения одного, двух или трех основных свойств
сердечной мышцы: автоматизма, проводимости и возбудимости.
Аритмии в результате нарушения автоматизма, т. е. способ-
ности ткани сердца генерировать потенциал действия ("импульс
возбуждения"). Эти аритмии проявляются изменением частоты и
регулярности генерации сердцем импульсов, могут проявляться в
виде тахикардии и брадикардии.
Аритмии в результате нарушения способности клеток сердца
проводить импульс возбуждения. Выделяют следующие виды на-
рушений проводимости:
• замедление или блокада проведения;
• ускорение проведения.
Аритмии в результате нарушений возбудимости сердечной
ткани. Возбудимость — свойство клеток воспринимать
действие раздражителя и реагировать на него реакцией возбуж-
дения. К таким аритмиям относятся экстрасистолия, пароксиз-
мальная тахикардия и фибрилляция (мерцание) предсердий или
желудочков.
Экстрасистола — внеочередной, преждевременный импульс,
вызывающий сокращение всего сердца или его отделов. При этом
правильная последовательность сердечных сокращений наруша-
ется.
Пароксизмальная тахикардия — приступообразное, внезапное
увеличение частоты импульсации правильного ритма. При этом
частота эктопических импульсов составляет от 160 до 220 в минуту.
Фибрилляция (мерцание) предсердий или желудочков представля-
ет собой нерегулярную, беспорядочную электрическую актив-
ность предсердий и желудочков, сопровождающуюся прекраще-
нием эффективной насосной функции сердца.
3. Сердечная недостаточность — синдром, развивающийся при
многих болезнях, поражающих различные органы и ткани. При
этом сердце не обеспечивает их потребности в кровоснабжении,
адекватном их функции.
Этиология сердечной недостаточности связана в основном с
двумя группами причин: непосредственным повреждением сердца —
травма, воспаление оболочек сердца, длительная ишемия, ин-
фаркт миокарда, токсические повреждения сердечной мышцы
и др., или функциональной перегрузкой сердца в результате:
• увеличения объема крови, притекающей к сердцу и повы-
шающей давление в его желудочках при гиперволемии, по-
лицитемии, пороках сердца;
200
• возникающего сопротивления изгнанию крови из желудоч-
ков в аорту и легочную артерию, что происходит при арте-
риальной гипертензии любого генеза и некоторых пороках
сердца.
Виды сердечной недостаточности (схема 3). По преимуществен-
но пораженном отделу сердца:
левожелудочковая, которая развивается в результате поврежде-
ния или перегрузки миокарда левого желудочка;
правожелудочковая, которая обычно является результатом пе-
регрузки миокарда правого желудочка, например при хрониче-
ских обструктивных заболеваниях легких — бронхоэктазах, брон-
хиальной астме, эмфиземе легких, пневмосклерозе и т. п.
По скорости развития:
Острая (минуты, часы). Является результатом ранения сердца,
острого инфаркта миокарда, эмболии легочного ствола, гиперто-
нического криза, острого токсического миокардита и т. п.
Хроническая (месяцы, годы). Является следствием хронической
артериальной гипертензии, хронической дыхательной недостаточ-
ности, длительной анемии, хронических пороков сердца.
Нарушения функции сердца и центральной гемодинамики. Сни-
жение силы и скорости сокращения, а также расслабления мио-
карда при сердечной недостаточности проявляется изменением
показателей функции сердца, центральной и периферической ге-
модинамики. К. числу основных среди них относятся:
• уменьшение ударного и минутного выброса сердца, которое
развивается в результате депрессии сократительной функ-
ции миокарда;
• увеличение остаточного систолического объема крови в по-
лостях желудочков сердца, что является следствием непол-
ной систолы;
С хема 3
201
• повышение конечного диастолического давления в желу-
дочках сердца. Обусловлено увеличением количества крови,
скапливающейся в их полостях, нарушением расслабления
миокарда, растяжением полостей сердца вследствие увели-
чения в них конечного диастолического объема крови;
• повышение давления кроззи в тех венозных сосудах и сер-
дечных полостях, откуда поступает кровь в пораженные от-
делы сердца. Так, при левожелудочковой сердечной недос-
таточности повышается давление в левом предсердии, ма-
лом круге кровообращения и правом желудочке. При пра-
вожелудочковой сердечной недостаточности давление уве-
личивается в правом предсердии и в венах большого круга
кровообращения;
• снижение скорости систолического сокращения и диасто-
лического расслабления миокарда. Проявляется главным
образом увеличением длительности периода изометрическо-
го напряжения и систолы сердца в целом.
БОЛЕЗНИ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ
Группу заболеваний сердечно-сосудистой системы составляют
такие распространенные болезни, как атеросклероз, гипертониче-
ская болезнь, ишемическая болезнь сердца, воспалительные забо-
левания сердца и его пороки, а. также заболевания сосудов. При
этом атеросклероз, гипертоническая болезнь и ишемическая бо-
лезнь сердца (ЙБС) характеризуются во всем мире наибольшей
заболеваемостью и смертностью, хотя это относительно "моло-
дые" болезни и свое значение они приобрели лишь в начале XX
века. И. В. Давыдовский называл их "болезнями цивилизации",
обусловленными неспособностью человека адаптироваться к бы-
стро прогрессирующей урбанизации и связанными с ней измене-
ниями образа жизни людей, постоянными стрессовыми влияния-
ми, нарушениями экологии и другими особенностями "цивилизо-
ванного общества".
В этиологии и патогенезе атеросклероза и гипертонической
болезни много общего. Вместе с тем ИБС. которая: сейчас рас-
сматривается как самостоятельное заболевание, по существу яв-
ляется кардиальной формой атеросклероза и гипертонической
болезни. Однако в связи с тем, что основная смертность связана
именно с инфарктом миокарда, который и составляет суть ИБС.
по решению ВОЗ, она приобрел а статус самостоятельной нозоло-
гической единицы.
АТЕРОСКЛЕРОЗ
Атеросклероз — хроническое заболевание крупных и средних
артерий (эластического и мьшечно-эластического типа), свя-
занное с нарушением в основном жирового и белкового обмена.
202
Это заболевание чрезвычайно распространено во всеги мире, так
как признаки атеросклероза обнаруживаются у всех людей стар-
ше 30—35 лет, хотя они выражены в разной степени. Для атеро-
склероза характерны очаговые отложения в стенках крупных ар-
терий липидов и белков, вокруг которых разрастается соедини-
тельная ткань, в результате чего образуется атеросклеротическая
бляшка.
Этиология атеросклероза до конца не раскрыта, хотя обще-
признано, что это полиэтиологическое заболевание, обусловлен-
ное сочетанием изменений жиро-белкового обмена и поврежде-
нием эндотелия интимы артерий. Причины обменных наруше-
ний, как и повреждающие эндотелий факторы, могут быть раз-
личными, но широкие эпидемиологические исследования атеро-
склероза позволили выделить наиболее значимые влияния, кото-
рые получили название факторов риска. К ним относятся:
• возраст, так как увеличение частоты и выраженности ате-
росклероза с возрастом не вызывает сомнений;
• пол — у мужчин заболевание развивается раньше, чем у
женщин, и протекает тяжелее, чаще возникают осложне-
ния;
• наследственность — доказано существование генетически
обусловленных форм заболевания;
• гиперлипидемия (гиперхолестеринемия) — ведущий фактор
риска, обусловленный преобладанием в крови липопротеи-
нов низкой плотности над липопротеинам и высокой плотно-
сти, что связано в первую очередь с особенностями питания;
• артериальная гипертензия, которая приводит к повышению
проницаемости сосудистых стенок, в том числе и для липо-
протеинов, а также к повреждению эндотелия интимы;
• стрессовые ситуации — важнейший фактор риска, так как
они приводят к психоэмоциональному перенапряжению,
являющемуся причиной нарушений нейроэндокринной ре-
гуляции жиро-белкового обмена и вазомоторных рас-
стройств;
• курение — атеросклероз у курильщиков развивается в 2 раза
интенсивнее и встречается в 2 раза чаще, чем у некурящих;
• гормональные факторы, так как большинство гормонов
влияет на нарушения жиро-белкового обмена, что особенно
проявляется при сахарном диабете и гипотиреозе. К этим
факторам риска близки пероральные контрацептивы, при
условии употребления их более 5 лет;
• ожирение и гиподинамия способствуют нарушению жиро-
белкового обмена и накоплению в крови липопротеинов
низкой плотности.
Пато- и морфогенез атеросклероза складывается из нескольких
стадий (рис. 47).
Долипидная стадия характеризуется появлением в интиме арте-
рий жиро-белковых комплексов в таких количествах, которые
еще нельзя увидеть невооруженным глазом и при этом нет еще
203
Рис. 47. Атеросклероз аорты,
а — жировые пятна и полоски (окраска
Суданом III); б — фиброзные бляшки с
изъязвлением; в — фиброзные бляшки; г
— изъязвленные фиброзные бляшки и
кальциноз; д — фиброзные бляшки, изъ-
язвление, кальциноз, тромбы.
атеросклеротических бля-
шек.
Стадия липоидоза отра-
жает накопление в интиме
сосудов жиро-белковых
комплексов, которые стано-
вятся видны в виде жировых
пятен и полосок желтого
цвета. Под микроскопом
определяются бесструктур-
ные жиро-белковые массы,
вокруг которых располага-
ются макрофаги, фибробла-
сты и лимфоциты.
Стадия липосклероза раз-
вивается в результате раз-
растания соединительной
ткани вокруг жиро-белко-
вых масс и образуется фиб-
розная бляшка, которая на-
чинает возвышаться над по-
верхностью интимы. Над
бляшкой интима склерози-
руется — образуется по-
крышка бляшки, которая мо-
жет гиалинизироваться.
Фиброзные бляшки являют-
ся основной формой атеро-
склеротического поражения
сосудов. Они располагают-
ся в местах наибольшего ге-
модинамического воздейст-
вия на стенку артерии — в
области ветвления и изги-
бов сосудов.
Стадия осложненных пораженийвключает три процесса: атеро-
матоз, изъязвление и кальциноз.
Атероматоз характеризуется распадом жиро-белковых масс
в центре бляшки с образованием аморфного кашицеобразного
детрита, содержащего остатки коллагеновых и эластических воло-
кон стенки сосуда, кристаллы холестерина, подвергшиеся омыле-
нию жиры, коагулированные белки. Средняя оболочка сосуда под
бляшкой нередко атрофируется.
Изъязвлению нередко предшествует кровоизлияние в
бляшку. При этом покрышка бляшки разрывается и атероматоз-
ные массы выпадают в просвет сосуда. Бляшка представляет со-
бой атероматозную язву, которая прикрывается тромботическими
массами.
Кальциноз завершает морфогенез атеросклеротической
204
бляшки и характеризуется выпадением в ней солей кальция. Про-
исходит обызвествление, или петрификация, бляшки, которая
приобретает каменистую плотность.
Течение атеросклероза волнообразное. При пропрессировании
заболевания нарастает липоидоз интимы, при стихании болезни
вокруг бляшек усиливается разрастание соединительной ткани и
отложение в них солей кальция.
Клинико-морфологические формы атеросклероза. Проявления
атеросклероза зависят от того, какие артерии большие поражены.
Для клинической практики наибольшее значение имеет атеро-
склеротическое поражение аорты, венечных артерий сердца, арте-
рий мозга и артерий конечностей, преимущественно» низкних.
Атеросклероз аорты — наиболее частая локализация атероскле-
ротических изменений, которые здесь и наиболее выражены.
Обычно бляшки образуются в области отхождения от аорты более
мелких сосудов. Больше поражаются дуга и брюшной отдел аор-
ты, где располагаются крупные и мелкие бляшки. Когда бляшки
достигают стадий изъязвления и атерокальциноза, в местах их
расположения возникают нарушения кровотока и образуются
пристеночные тромбы. Отрываясь, они превращаются в тромбо-
эмболы, закупоривают артерии селезенки, почек и других орга-
нов, вызывая инфаркты. Изъязвление атероослеротической
бляшки и разрушение в связи с этим эластических волокон стен-
ки аорты могут способствовать образованию аневризмы — мешко-
видного выпячивания стенки сосуда, заполненно го кровью и
тромботическими массами. Разрыв аневризмы приводит к быст-
рой массивной кровопотере и скоропостижной смерти.
Атеросклероз артерий мозга, или церебральная форма, харак-
терна для пожилых и старых больных. При значительном стено-
зе просвета артерий атеросклеротическими бляшками головной
мозг постоянно испытывает кислородное голодание; и постепен-
но атрофируется. У таких больных развивается атеросклеротиче-
ское слабоумие. Если просвет одной из мозговых артерий пол-
ностью закрывается тромбом, возникает ишемический инфаркт
мозга в виде очагов его серого размягчения. Пораженные атеро-
склерозом мозговые артерии становятся хрупкими и могут раз-
рываться. Возникает кровоизлияние — геморрагический инсульт,
при котором соответствующий участок ткани мозга гибнет. Те-
чение геморрагического инсульта зависит от его локализации и
массивности. Если кровоизлияние произошло в области дна IV
желудочка или излившаяся кровь прорвалась в боковые желу-
дочки мозга, то наступает быстрая смерть. При ишемическом
инфаркте, а также при небольших геморрагических инсультах,
не приведших больного к смерти, погибшая ткань мозга посте-
пенно рассасывается и на ее месте образуется полость, содержа-
щая жидкость, — киста мозга. Ишемический инфаркт и гемор-
рагический инсульт мозга сопровождаются неврологическими
нарушениями. У выживших больных развивается паралич, не-
редко страдает речь и появляются другие расстрой отв а. При со-
205
ответствующем лечении со временем возможно восстановление
части утраченных функций ЦНС.
Атеросклероз сосудов нижних конечностей также чаще встреча-
ется в пожилом возрасте. При значительном сужении просвета
артерий голеней или стоп атеросклеротическими бляшками ткани
нижних конечностей подвергаются ишемии. При повышении на-
грузки на мышцы конечностей, например при ходьбе, в них по-
является боль, и больные вынуждены останавливаться. Этот сим-
птом носит название перемежающаяся хромота. Кроме того, от-
мечаются похолодание и атрофия тканей конечностей. Если про-
свет стенозированных артерий полностью закрывается бляшкой,
тромбом или эмболом, у больных развивается атеросклеротиче-
ская гангрена.
В клинической картине атеросклероза может наиболее ярко
выступать поражение почечных и кишечных артерий, однако эти
формы болезни встречаются реже.
ГИПЕРТОНИЧЕСКАЯ БОЛЕЗНЬ
Гипертоническая болезнь — хроническое заболевание, харак-
теризующееся длительным и стойким повышением артериаль-
ного давления (АД) — систолического выше 140 мм рт. ст. и
диастолического — выше 90 мм рт. ст. Мужчины болеют не-
сколько чаще женщин. Заболевание обычно начинается в 35—45
лет и прогрессирует до 55—58 лет, после чего АД часто стабили-
зируется на повышенных значениях. Иногда стойкое и быстро
нарастающее повышение АД развивается у лиц молодого воз-
раста.
Этиология. В основе гипертонической болезни лежит сочета-
ние 3 факторов:
• хронического психоэмоционального перенапряжения:
• наследственного дефекта клеточных мембран, приводящего
к нарушению обмена ионов Са2+ и Na2+;
• генетически обусловленного дефекта почечно-объемного
механизма регуляции артериального давления.
Факторы риска:
• генетические факторы не вызывают сомнения, так как ги-
пертоническая болезнь часто носит семейный характер;
• повторяющийся эмоциональный стресс;
• рацион питания с большим потреблением поваренной соли;
• гормональные факторы — усиление прессорных влияний ги-
поталамо-гипофизарной системы, избыточное выделение ка-
техоламинов и активация ренин-ангиотензиновой системы;
• почечный фактор;
• тучность;
• курение;
• гиподинамия, малоподвижный образ жизни.
Пато- и морфогенез. Гипертоническая болезнь характеризует-
ся стадийным развитием.
206
Транзиторная, или доклиническая, стадия характеризуется пе-
риодическими подъемами АД. Они обусловлены спазмом арте-
риол, во время которого стенка самого сосуда испытывает ки-
слородное голодание, вызывающее в ней дистрофические изме-
нения. В результате повышается проницаемость стенок арте-
риол. Они пропитываются плазмой крови (плазморрагия), кото-
рая выходит и за пределы сосудов, обусловливая периваскуляр-
ный отек.
После нормализации уровня АД и восстановления микро-
циркуляции плазма крови из стенок артериол и периваскуляр-
ных пространств удаляется в лимфатическую систему, а попав-
шие в стенки сосудов вместе с плазмой белки крови преципити-
руют. В связи с повторяющимся повышением нагрузки на сердце
развивается умеренная компенсаторная гипертрофия левого же-
лудочка. Если в транзиторной стадии ликвидировать условия, вы-
зывающие психоэмоциональное перенапряжение, и провести со-
ответствующее лечение, начинающуюся гипертоническую бо-
лезнь можно излечить, так как в этой стадии еще отсутствуют не-
обратимые морфологические изменения.
Сосудистая стадия клинически характеризуется стойким по-
вышением АД. Это объясняется глубокими нарушениями регу-
ляции сосудистой системы и ее морфологическими изменения-
ми. Переход транзиторного повышения АД в устойчивое связан
с действием нескольких нейроэндокринных механизмов, среди
которых наибольшее значение имеют рефлекторный, почечный,
сосудистый, мембранный и эндокринный. Часто повторяющие-
ся подъемы АД приводят к снижению чувствительности бароре-
цепторов дуги аорты, которые в норме обеспечивают ослабле-
ние активности симпатико-адреналовой системы и понижение
АД. Усиление влияния этой системы регуляции и спазм арте-
риол почек стимулируют выработку фермента ренина. Послед-
ний приводит к образованию в плазме крови ангиотензина, ко-
торый стабилизирует АД на высоком уровне. Кроме того, ан-
гиотензин усиливает образование и выход из коркового вещест-
ва надпочечников минералокортикоидов, которые еще более
повышают АД и также способствуют его стабилизации на высо-
ком уровне.
Повторяющиеся с нарастающей частотой спазмы артериол,
усиливающаяся плазморрагия и возрастающее количество преци-
питированных белковых масс в их стенках приводят к гиалинозу,
или партериолосклерозу. Стенки артериол уплотняются, теряют
эластичность, значительно увеличивается их толщина и соответ-
ственно уменьшается просвет сосудов.
Постоянное высокое АД значительно повышает нагрузку, па-
дающую на сердце, в результате чего развивается его компенса-
торная гипертрофия (рис. 48, б). При этом масса сердца достигает
600—800 г. Постоянное высокое АД увеличивает нагрузку и на
крупные артерии, в результате чего атрофируются мышечные
клетки и эластические волокна их стенок теряют эластичность. В
207
сочетании с изменениями биохимического состава крови, >накоп-
лением в ней холестерина и крупном юл скуля рных белков созда-
ются предпосылки для развития атерооклерот'ического поражения
крупных артерий. Причем выраженность этих изменений значи-
тельно больше, чем при атеросклерозе, не сопровождающемся
повышением АД.
Стадия изменений органов. Изменен ия в оржганах носят вторич-
ный характер. Их выраженность, а также клинические проявле-
ния зависят от степени повреждения артериол и артерий, а. также
от осложнений, связанных с этими изменениями. В основе хро-
нических изменении органов лежат нарушен нс их кровообЗраще-
ния, нарастающее кислородное голодание и обусловленными им
склероз органа со снижением функции .
В течении гипертонической болезни! важнейшее значени <? име-
ет гипертонический криз, т. е. резкое и длительное повыше!* не АД
в связи со спазмом артериол. Гипертонический криз имеет свое
морфологическое выражение: спазм артериол, плазморратия и
фибриноидный некроз их стенок, периваскулярные диапещезн ые
кровоизлияния. Эти изменения, возникающие в таких ор>танах,
как головной мозг, сердце, почки, нередко приводят больных к
смерти. Криз может возникнуть на любом этапе развития LTinep-
тонической болезни. Частые кризы характеризуют злокачествен-
ное течение заболевания, встречающееся обычно у лиц моттодого
возраста.
Осложнения гипертонической болезни, проявляющиеся спаз-
мом, тромбозом артериол и артерий илги их разрывом, приводят к
инфарктам или кровоизлияниям в органах, которые обычно яв-
ляются причиной смерти.
Клинико-морфологические формы гипертонической бодпезни.
В зависимости от преобладания поражения гс=х или иных органов
выделяют сердечную, мозговую и почечную клин и ко-морфологи-
ческие формы гипертонической болезни.
Сердечная форма, как и сердечная форма атеросклероз в, со-
ставляет сущность ишемической болезни сердкда и рассматр зевает-
ся как самостоятельное заболевание.
Мозговая, или церебральная, форма — одна из наиболее частых
форм гипертонической болезни. Обычно она связана с раз(л»ывом
гнали визированного сосуда и развитием массивного кровоизлия-
ния в мозг (геморрагический инсульт) по типу гематомы (рис. 48,
а). Прорыв крови в желудочки мозга всегда заканчивается смер-
тью больного. Ишемические инфаркты мозга также могут е*<>зн и-
кать при гипертонической болезни, хотя значительно реже, чем
при атеросклерозе. Их развитие связано с тромбозом или спаз-
мом атеросклеротически измененных средних мозговых ар>терпи
или артерий основания мозга
Почечная форма. При хроническом, течении гипертонической
болезни развивается артеориолосклерютический нефросклероз,
связанный с гиалинозом приносящих артер>иол. Умены_пение
притока крови приводит к атрофии и гихшнозу соответствуйющих
208
в
Рис. 48. Гипертоническая болезнь.
а — кровоизлияние в левом полушарии головного мозга; б — гипертрофия мио-
карда левого желудочка сердца; в — первично-сморщенная почка (артериолоскле-
ротический нефросклероз).
209
Рис. 49. Артериолосклеротический нефросклероз. .Гиалинизированный
(ГК) и атрофирующийся (АК) клубочки.
клубочков. Их функцию выполняют сохранившиеся клубочки,
которые подвергаются гипертрофии. Поэтому поверхность почек
приобретает зернистый вид: гиалинизированные клубочки и ат-
рофированные, склерозированные, нефроны западают, а гипер-
трофированные клубочки выступают над поверхностью почек
(рис. 48, в, 49). Постепенно склеротические процессы начинают
преобладать и развиваются первично-сморщенные почки. При
этом нарастает хроническая почечная недостаточность, которая
завершается уремией.
Симптоматические гипертонии (гипертензии). Гипертензией на-
зывают повышение АД вторичного характера — симптом при раз-
личных заболеваниях почек, желез внутренней секреции, сосудов.
Если удается ликвидировать основное заболевание, исчезает и ги-
210
пертензия. Так, после удаления опухоли надпочечника — феохро-
моцитомы. сопровождающейся значительной гипертензией, нор-
мализуется и АД. Поэтому гипертоническую болезнь следует от-
личать от симптоматических гипертензий.
ИШЕМИЧЕСКАЯ БОЛЕЗНЬ СЕРДЦА (ИБС)
Ишемическая, или коронарная, болезнь сердца — группа забо-
леваний, обусловленных абсолютной или относительной недоста-
точностью коронарного кровообращения, что проявляется несо-
ответствием между потребностью миокарда в кислороде и его
доставкой к мышце сердца. В 95 % случаев ИБС обусловлена ате-
росклерозом коронарных артерий. Именно ИБС выступает как
основная причина смертности населения. Скрытая (доклиниче-
ская) ИБС обнаруживается у 4—6 % людей старше 35 лет. Еже-
годно в мире регистрируется более 5 млн больных. И Б С и более
500 тыс из них умирает. Мужчины заболевают раньше женщин,
однако после 70 лет мужчины и женщины болеют ИБС одинако-
во часто.
Формы ишемической болезни сердца. Выделяют 4 формы забо-
левания:
• внезапная коронарная смерть, наступающая из-за остановки
сердца у человека, за 6 ч до этого не предъявлявшего жалоб
на сердце;
• стенокардия — форма ИБС, характеризующаяся приступа-
ми загрудинной боли с изменениями на ЭКГ, но без появ-
ления характерных ферментов в крови;
• инфаркт миокарда — острый очаговый ишемический (цир-
куляторный) некроз сердечной мышцы, развивающийся
вследствие внезапного нарушения коронарного кровообра-
щения;
• кардиосклероз — хроническая ишемическая болезнь сердца
(ХИБС) — исход стенокардии или инфаркта миокарда; на
основе кардиосклероза может сформироваться хроническая
аневризма сердца.
Течение ишемической болезни может быть острым и хрониче-
ским. Поэтому выделяют острую ИБС (стенокардия, внезапная
коронарная смерть, инфаркт миокарда) и хроническую ИБС (кар-
диосклероз во всех его проявлениях).
Факторы риска те же, что при атеросклерозе и гипертониче-
ской болезни.
Этиология ИБС принципиально та же, что и этиология атеро-
склероза и гипертонической болезни. Более 90% больных ИБС
страдают стенозирующим атеросклерозом коронарных артерий со
степенью сужения хотя бы одной из них до 75 % и выше. При
этом не может быть обеспечен кровоток, адекватный даже не-
большой физической нагрузке.
211
Патогенез различных форм ИБС
Развитие различных видов острой ИБС связан с острым нару-
шением коронарного кровообращения, что ведет к ишемическо-
му повреждению мышцы сердца. Степень этих повреждений за-
висит от длительности ишемии.
1. Стенокардия характеризуется обратимой ишемией миокарда,
связанной со стенозирующим коронаросклерозом, и является
клинической формой всех видов ИБС. Для нее характерны при-
ступы сдавливающих болей и чувство жжения в левой половине
грудной клетки с иррадиацией в левую руку, область лопатки,
шею, нижнюю челюсть. Приступы возникают при физической
нагрузке, эмоциональном стрессе и т. п. и купируются приемом
сосудорасширяющих средств. Если смерть наступает во время
приступа стенокардии, длившегося 3—5 и даже 30 мин, морфоло-
гические изменения в миокарде можно обнаружить только с по-
мощью специальных методик, так как макроскопически сердце
не изменено.
2. Внезапная коронарная смерть связана с тем, что при острой
ишемии в миокарде уже через 5—10 мин после приступа могут
образовываться аритмогенные субстанции — вещества, вызываю-
щие электрическую нестабильность сердца и создающие предпо-
сылки для фибрилляции его желудочков. На вскрытии умерших
вследствие фибрилляции миокарда сердце дряблое, с расширен-
ной полостью левого желудочка. Микроскопически выражена
фрагментация мышечных волокон.
3. Инфаркт миокарда.
Этиология острого инфаркта миокарда связана с внезапным
прекращением коронарного кровотока либо из-за обтурации ко-
ронарной артерии тромбом или эмболом, либо в результате д л и -
тельного спазма атеросклеротически измененной венечной арте-
рии.
Патогенез инфаркта миокарда в значительной степени опреде-
ляется тем. что сохранившиеся просветы трех коронарных арте-
рий в сумме составляют лишь 34 % от средней нормы, в то время
как "критическая сумма" этих просветов должна быть не менее
35 %, поскольку даже при этом общий кровоток в коронарных
артериях падает до минимально допустимого уровня.
В динамике инфаркта миокарда выделяют 3 стадии, каждая из
которых характеризуется своими морфологическими особенно-
стями.
Ишемическая стадия, или стадия ишемической (дистрофии,
развивается в первые 18—24 ч после закупорки венечной артерии
тромбом. Макроскопические изменения миокарда в этой стадии
не видны. При микроскопическом исследовании наблюдаются
дистрофические изменения мышечных волокон в виде их фраг-
ментации, утраты поперечной исчерченности, строма миокарда
отечна. Выражены расстройства микроциркуляции в виде стазов
и сладжей в капиллярах и венулах, имеются диапедезмые крово-
212
излияния. В участках ишемии отсутствуют гликоген и окисли-
тельно-восстановительные ферменты. При электронно-микроско-
пическом изучении кардиомиоцитов из участка ишемии миокар-
да в них обнаруживаются набухание и деструкция митохондрий,
исчезновение гранул гликогена, отек саркоплазмы, пересокраще-
ние миофиламентов (рис. 50). Эти изменения связаны с гипокси-
ей, электролитным дисбалансом и прекращением обмена веществ
в участках ишемии миокарда. В непораженных ишемией отделах
миокарда в этот период развиваются нарушения микроциркуля-
ции и отек стромы.
Смерть в ишемической стадии наступает от кардиогенного шо-
ка, фибрилляции желудочков или остановки сердца ('асистпо-шя).
Некротическая стадия инфаркта миокарда развивается в кон-
це первых суток после приступа стенокардии. На вскрытии в об-
ласти инфаркта нередко наблюдается фибринозный перикардит.
На разрезе мышцы сердца хорошо видны желтоватые, неправиль-
ной формы очаги некроза миокарда, окруженные красной поло-
сой гиперемированных сосудов и кровоизлияний — ишемиче-
ский инфаркте геморрагическим венчиком (рис. 51). При гисто-
логическом исследовании обнаруживаются очаги некроза мышеч-
ной ткани, ограниченные от непораженного миокарда демаркаци-
онной (пограничной) линией, представленной зоной лейкоцитар-
ной инфильтрации и гиперемированных сосудов (рис. 52).
Вне участков инфаркта в этот период развиваются нарушения
микроциркуляций, выраженные дистрофические изменения кар-
диомиоцитов, деструкция многих митохондрий одновременно с
увеличением их количества и объема.
Стадия организации инфаркта миокарда начинается тотчас по-
сле развития некроза. Лейкоциты и макрофаги очищают поле
воспаления от некротических масс. В демаркационной зоне появ-
ляются фибробласты, продуцирующие коллаген. Очаг некроза за-
мещается вначале грануляционной тканью, которая в течение
примерно 4 нед созревает в грубоволокнистую соединительную
ткань. Происходит организация инфаркта миокарда, и на его
месте остается рубец (см. рис. 30). Возникает крупноочаговый
кардиосклероз. В этот период миокард вокруг рубца и миокард
всех остальных отделов сердца, особенно левого желудочка, под-
вергается регенерационной гипертрофии. Это позволяет посте-
пенно нормализовать функцию сердца.
Таким образом, острый инфаркт миокарда длится 4 нед. Если
за этот период у больного возникает новый инфаркт миокарда, то
он называется рецидивирующим Если новый инфаркт миокарда
развился спустя 4 нед или более после первого инфаркта, то он
называется повторным
Осложнения могут возникать уже в некротической стадии. Так,
участок некроза подвергается расплавлению — миомаляции, в ре-
зультате чего может произойти разрыв стенки миокарда в области
инфаркта, заполнение кровью полости перикарда — тампонада
сердца, ведущая к скоропостижной смерти. Миомаляция может
213
). Инфаркт миокарда, и теми веская стадия Набухание и деструк-
гтохондрий И), расширение ч вакуолизация саркогитазмити1-» «тс ко-
нсул ума (СР), начинающаяся деструкция м иофиламентов 1Мф).
вне гранул гликогена* Электроногракгтиа.
Рис. 51. Инфаркт миокарда (поперечные срезы сердца).
I — ишемический инфаркт с геморрагическим венчиком задней стенки левого
желудочка; 2 — тотурируюший тромб в нисходящей ветви левой венечной арте-
рии; 3 — разрыв стенки сердца. На схемах (внизу): а — заштрихована зона ин-
фаркта (стрелкой показан разрыв); б — заштрихованы уровни срезов.
215
Рис. 52. Инфаркт миокарда. Участок некроза мышечной ткани окружен
демаркационной линией (ДЛ). состоящей из лейкоцитов.
привести к выбуханию стенки желудочка и образованию острой
аневризмы сердца. В случае разрыва аневризмы также возникает
тампонада сердца. Если острая аневризма не разрывается, в ее
полости образуются тромбы, которые могут стать источником
тромбоэмболии сосудов головного мозга, селезенки, почек и са-
мих венечных артерий. Постепенно в острой аневризме сердца
тромбы замещаются соединительной тканью, однако в образовав-
шейся полости аневризмы сохраняются или образуются вновь
тромботические массы. Аневризма становится хронической. Ис-
точником тромбоэмболии могут стать тромботические наложения
на эндокарде в области инфаркта. Смерть в некротической ста-
дии может наступить и от фибрилляции желудочков сердца.
Исходы. Острый инфаркт миокарда может закончиться острой
216
Рис. 53. Хроническая ишемическая болезнь сердца.
а — постинфарктный крупноочаговый кардиосклероз (показано стрелкой); б —
рассеянный очаговый кардиосклероз (рубцы показаны стрелками).
сердечной недостаточностью, часто с развитием отека легких и
набуханием вещества головного мозга. Исходом является также
крупноочаговый кардиосклероз и хроническая ИБС.
4. Хроническая ишемическая болезнь сердца
Морфологическим выражением хронической ишемической бо-
лезни сердца являются:
• выраженный атеросклеротический мелкоочаговый кар-
диосклероз;
• постинфарктный крупноочаговый кардиосклероз;
• хроническая аневризма сердца в сочетании с атеросклеро-
зом венечных артерий (рис. 53). Она возникает в тех случа-
ях, когда после обширного инфаркта миокарда образую-
щаяся рубцовая ткань начинает выбухать под давлением
крови, истончается и формируется мешковидное выпячива-
ние. Вследствие завихрения крови в аневризме появляются
тромбы, которые могут стать источником тромбоэмболии.
Хроническая аневризма сердца в большинстве случаев яв-
ляется причиной нарастающей хронической сердечной не-
достаточности.
Все эти изменения сопровождаются умеренно выраженной ре-
генерационной гипертрофией миокарда.
Клинически хроническая ИБС проявляется стенокардией и по-
степенным развитием хронической сердечно-сосудистой недоста-
точности, заканчивающейся смертью больного. На любом этапе
хронической ИБС может возникнуть острый или повторный ин-
фаркт миокарда.
217
ВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ СЕРДЦА
Причинами воспаления сердца являются различные инфекции
и интоксикации. Воспалительный процесс может поражать одну
из оболочек сердца или всю его стенку. Воспаление эндокарда —
эндокардит, воспаление миокарда — миокардит, перикарда — пе-
рикардит, а воспаление всех оболочек сердца — панкардит.
Эндокардит. Воспаление эндокарда обычно распространяется
только на определенную его часть, покрывающую либо клапаны
сердца, либо их хорды, либо стенки полостей сердца. При эндо-
кардите наблюдается сочетание характерных для воспаления про-
цессов — альтерации, экссудации и пролиферации. Наибольшее
значение в клинике имеет клапанный эндокардит. Чаще других
поражается двустворчатый клапан, несколько реже — аорталь-
ный, довольно редко возникает воспаление клапанов правой поло-
вины сердца. Альтерации подвергаются либо только поверхностные
слои клапана, либо он поражается целиком, на всю глубину. Не-
редко альтерация клапана ведет к его изъязвлению и даже перфо-
рации. В области деструкции клапана обычно образуются тромбо-
тические массы (тромбоэндокардит) в виде бородавок или поли-
пов. Экссудативные изменения заключаются в пропитывании кла-
пана плазмой крови и инфильтрации его клетками экссудата. При
этом клапан набухает и становится толще. Продуктивная фаза вос-
паления заканчивается склерозом, утолщением, деформацией и
срастанием створок клапана, что ведет к пороку сердца.
Эндокардит резко осложняет течение того заболевания, при
котором он развился, так как при этом тяжело страдает функция
сердца. Кроме того, тромботические наложения на клапанах мо-
гут стать источником тромбоэмболии.
Исходом клапанных эндокардитов являются пороки сердца и
сердечная недостаточность.
Миокардит. Воспаление мышцы сердца обычно осложняет
различные заболевания, не являясь самостоятельной болезнью. В
развитии миокардита важное значение имеет инфекционное по-
ражение мышцы сердца вирусами, риккетсиями, бактериями, ко-
торые достигают миокарда с током крови, т. е. гематогенным пу-
тем. Миокардиты протекают остро или хронически. В зависимо-
сти от преобладания той или иной фазы воспаление миокарда
может быть альтеративным, экссудативным, продуктивным (про-
лиферативным).
При остром течении экссудативный и продуктивный миокар-
диты могут стать причиной острой сердечной недостаточности.
При хроническом течении они приводят к диффузному кар-
диосклерозу, который в свою очередь может обусловить развитие
хронической сердечной недостаточности.
Перикардит. Воспаление наружной оболочки сердца возникает
как осложнение других болезней и протекает либо в форме экссу-
дативного, либо хронического слипчивого перикардита.
Экссудативный перикардит в зависимости от характера экссу-
218
дата может быть серозным, фибринозным, гнойным, геморраги-
ческим и смешанным.
Серозный перикардит характеризуется накоплением в полости
перикарда серозного экссудата, который нередко рассасывается
без особых последствий в случае благоприятного исхода основно-
го заболевания.
Фибринозный перикардит развивается чаще при интоксикациях,
например при уремии, а также при инфаркте миокарда, ревма-
тизме, туберкулезе и ряде других болезней. В полости перикарда
скапливается фибринозный экссудат и на поверхности его лист-
ков появляются свертки фибрина в виде волосков ("волосатое
сердце"). При организации фибринозного экссудата между лист-
ками перикарда образуются плотные спайки.
Гнойный перикардит наиболее часто возникает как осложнение
воспалительных процессов в рядом расположенных органах —
легких, плевре, средостении, лимфатических узлах средостения, с
которых воспаление распространяется на перикард.
Геморрагический перикардит развивается при метастазах рака в
сердце.
Исходом острых экссудативных перикардитов может быть ос-
тановка сердца.
Хронический слипчивый перикардит характеризуется экссуда-
тивно-продуктивным воспалением, нередко развивается при ту-
беркулезе и ревматизме. При этом виде перикардита экссудат не
рассасывается, а подвергается организации. В результате между
листками перикарда образуются спайки, затем полость перикарда
полностью зарастает, склерозируется, сдавливая сердце. Нередко
в рубцовую ткань откладываются соли кальция и развивается
"панцирное сердце".
Исходом такого перикардита является хроническая сердечная
недостаточность.
ПОРОКИ СЕРДЦА
Пороки сердца являются частой патологией, обычно подлежа-
щей только хирургическому лечению. Суть пороков сердца заклю-
чается в изменении строения его отдельных частей или отходящих
от сердца крупных сосудов. Это сопровождается нарушением сер-
дечной функции и общими расстройствами кровообращения. По-
роки сердца могут быть врожденными и приобретенными.
Врожденные пороки сердца являются следствием нарушений эм-
брионального развития, связанного либо с генетическими измене-
ниями эмбриогенеза, либо с болезнями, перенесенными плодом в
этот период (рис. 54). Наиболее часто среди этой группы пороков
сердца встречаются незаращение овального окна, артериального
протока, межжелудочковой перегородки и тетрада Фалло.
Незаращение овального окна. Через это отверстие в межпред-
сердной перегородке кровь из левого предсердия поступает в пра-
219
Рис. 54. Схема основных форм врожденных пороков сердца (по Я. Л. Ра-
попорту).
А. Нормальные взаимоотношения сердца и крупных сосудов. Лп — левое предсер-
дие; Лж — левый желудочек; Пп — правое предсердие; Пж — правый желудочек;
А — аорта; Ла — легочная артерия и ее ветви; Лв — легочные вены. Б. Незараще-
ние артериального протока между легочной артерий и аортой (направление пере-
хода крови из аорты в легочную артерию по артериальному протоку указано
стрелками). В. Дефект межжелудочковой перегородки. Кровь из левого желудочка
частично переходит в правый (указанно стрелкой). Г. Тетрада Фалло. Дефект
верхней части межжелудочковой перегородки тотчас ниже отхождения аорты; су-
жение легочного ствола у его выхода из сердца; аорта выходит из обоих желудоч-
ков в области межжелудочкового дефекта, получая смешанную артериально-ве-
нозную кровь (указано стрелкой). Резкая гипертрофия правого желудочка и общая
синюха (цианоз).
вое, затем в правый желудочек и в малый круг кровообращения.
При этом правые отделы сердца переполняются кровью, и для
того, чтобы ее вывести из правого желудочка в легочный ствол,
необходимо постоянное усиление работы миокарда. Это приво-
дит к гипертрофии правого желудочка, что позволяет сердцу ка-
кое-то время справляться с нарушениями кровообращения в нем.
Вместе с тем если овальное окно не закрыть оперативным путем,
то разовьется декомпенсация миокарда правого отдела сердца.
Если дефект в межпредсердной перегородке очень большой, то
венозная кровь из правого предсердия, минуя малый круг крово-
обращения, может поступать в левое предсердие и здесь смеши-
ваться с артериальной кровью. В результате этого в большом кру-
ге кровообращения циркулирует смешанная кровь, бедная кисло-
родом. У больного развиваются гипоксия и цианоз.
Незаращение артериального (боталлова) протока (рис. 54, А,
Б). У плода легкие не функционируют, в связи с чем кровь по бо-
220
таллову протоку из легочного ствола попадает непосредственно в
аорту, минуя малый круг кровообращения. В норме артериаль-
ный проток зарастает через 15—20 дней после рождения ребенка.
Если этого не происходит, то кровь из аорты, в которой высокое
кровяное давление, через боталлов проток попадает в легочный
ствол. Количество крови и кровяное давление в нем повышают-
ся, в малом круге кровообращения увеличивается количество
крови, которое поступает в левые отделы сердца. Нагрузка на
миокард возрастает и развивается гипертрофия левого желудочка
и левого предсердия. Постепенно в легких развиваются склероти-
ческие изменения, способствующие повышению давления в ма-
лом круге кровообращения. Это заставляет правый желудочек ра-
ботать более интенсивно, в результате чего развивается и его ги-
пертрофия. При далеко зашедших изменениях в малом круге кро-
вообращения в легочном стволе давление может стать выше, чем
в аорте, и в этом случае венозная кровь из легочного ствола по
артериальному протоку частично переходит в аорту. В большой
круг кровообращения поступает смешанная кровь, у больного по-
являются гипоксия и цианоз.
Дефект .межжелудочковой перегородки. При этом пороке кровь
из левого желудочка поступает в правый, вызывая его перегрузку
и гипертрофию (рис. 54, В, Г). Иногда межжелудочковая перего-
родка может полностью отсутствовать (трехкамерное сердце). Та-
кой порок несовместим с жизнью, хотя какое-то время новорож-
денные с трехкамерным сердцем могут жить.
Тетрада ФАЛЛО — дефект межжелудочковой перегородки, ко-
торый сочетается с другими аномалиями развития сердца: суже-
нием легочного ствола, отхождением аорты от левого и правого
желудочков одновременно и с гипертрофией правого желудочка.
Этот порок встречается в 40—50 % всех пороков сердца у новоро-
жденных. При пороке типа тетрады Фалло кровь из правых отде-
лов сердца течет в левые. При этом в малый круг кровообраще-
ния поступает меньше крови, чем необходимо, а в большой круг
кровообращения поступает смешанная кровь. У больного разви-
ваются гипоксия и цианоз.
Приобретенные пороки сердца в подавляющем большинстве
случаев являются следствием воспалительных заболеваний сердца
и его клапанов. Наиболее частой причиной приобретенных поро-
ков сердца является ревматизм, иногда они связаны с эндокарди-
том иной этиологии.
Патогенез. В результате воспалительных изменений и склеро-
зирования створок клапаны деформируются, становятся плотны-
ми, теряют эластичность и не могут полностью закрывать пред-
сердно-желудочковые отверстия или устья аоргы и легочного
ствола. При этом формируется порок сердца, который может
иметь различные варианты.
Недостаточность клапана развивается при неполном закры-
тии атриовентрикулярного отверстия. При недостаточности дву-
створчатого или трехстворчатого клапанов кровь во время систо-
221
лы поступает не только в аорту или легочный ствол, но и обратно
в предсердия. Если же имеется недостаточность клапанов аорты
или легочной артерии, то во время диастолы кровь частично по-
ступает назад в желудочки сердца.
Стеноз, или сужение отверстий, между предсердием и желу-
дочками развивается не только при воспалении и склерозирова-
нии клапанов сердца, но и при частичном сращении их створок.
При этом атриовентрикулярное отверстие или устье легочной ар-
терии либо отверстие конуса аорты становятся меньше.
Комбинированный порок сердца возникает при сочетании стеноза
предсердно-желудочкового отверстия и недостаточности клапанов.
Это наиболее частый вид приобретенных пороков сердца. При
комбинированном пороке двустворчатого или трехстворчатого кла-
пана увеличенный объем крови во время диастолы не может посту-
пить в желудочек без дополнительного усилия миокарда предсер-
дия, а во время систолы кровь частично возвращается из желудоч-
ка в предсердие, которое переполняется кровью. Для того чтобы не
возникло перерастяжение полости предсердия, а также чтобы обес-
печить поступление необходимого объема крови в сосудистое рус-
ло, компенсаторно повышается сила сокращения миокарда пред-
сердия и желудочка, в результате чего развивается его гипертро-
фия. Однако постоянное переполнение кровью, например, левого
предсердия при стенозе предсердно-желудочкового отверстия и не-
достаточности двустворчатого клапана приводит к тому, что кровь
из легочных вен не может полностью поступить в левое предсер-
дие. Возникает застой крови в малом круге кровообращения, а это
затрудняет поступление венозной крови из правого желудочка в ле-
гочную артерию. Чтобы преодолеть повышенное кровяное давле-
ние в малом круге кровообращения, сила сокращения миокарда
правого желудочка повышается и мышца сердца также гипертро-
фируется. Развивается компенсаторная (рабочая) гипертрофия сердца.
Исходом приобретенных пороков сердца, если дефект клапа-
нов не ликвидирован хирургическим путем, является хроническая
сердечная недостаточность и декомпенсация сердца, развиваю-
щаяся через определенное время, исчисляемое обычно годами
или десятилетиями.
БОЛЕЗНИ СОСУДОВ
Заболевания сосудов могут быть врожденными и приобретен-
ными.
ВРОЖДЕННЫЕ БОЛЕЗНИ СОСУДОВ
Врожденные болезни сосудов носят характер пороков разви-
тия, среди которых наибольшее значение имеют врожденные
аневризмы, коарктация аорты, гипоплазия артерий и атрезия вен.
Врожденные аневризмы — очаговые выпячивания сосудистой
222
стенки, вызванные дефектом ее строения и гемодинамической
нагрузкой. Аневризмы имеют вид небольших мешотчатых образо-
ваний, иногда множественных, размером до 1,5 см. Среди них
особенно опасны аневризмы внутримозговых артерий, так как их
разрыв приводит к субарахноидальному или внутримозговому
кровоизлиянию. Причинами аневризм являются врожденное от-
сутствие в стенке сосудов гладкомышечных клеток и дефект эла-
стических мембран. Образованию аневризм способствует артери-
альная гипертензия.
Коарктация аорты — врожденное сужение аорты, обычно в
области перехода дуги в нисходящую часть. Порок проявляется
резким повышением артериального давления на верхних конеч-
ностях и снижением его на нижних конечностях с ослаблением
там пульсации. При этом развиваются гипертрофия левой поло-
вины сердца и коллатеральное кровообращение через системы
внутренней грудной и межреберных артерий.
Гипоплазия артерий характеризуется недоразвитием этих сосу-
дов, в том числе аорты, при этом гипоплазия коронарных арте-
рий может лежать в основе внезапной сердечной смерти.
Атрезия вен — редкий порок развития, заключающийся во
врожденном отсутствии определенных вен. Наибольшее значение
имеет атрезия печеночных вен, что проявляется тяжелыми нару-
шениями структуры и функции печени (синдром Бадда—Киари).
Приобретенные болезни сосудов весьма распространены, осо-
бенно при атеросклерозе и гипертонической болезни. Клиниче-
ское значение имеют также облитерирующий эндартериит, при-
обретенные аневризмы, васкулиты.
Облитерирующий эндартериит — заболевание артерий в ос-
новном нижних конечностей, характеризующееся утолщением
интимы с сужением просвета сосудов вплоть до его облитерации.
Это состояние проявляется тяжелой, прогрессирующей гипокси-
ей ткани с исходом в гангрену. Причина заболевания не установ-
лена, однако среди факторов риска важнейшее значение имеют
курение и артериальная гипертензия. В патогенезе страдания оп-
ределенную роль играют повышение активности симпатико-адре-
наловой системы и аутоиммунные процессы.
ПРИОБРЕТЕННЫЕ АНЕВРИЗМЫ
Приобретенные аневризмы — локальное расширение просвета
кровеносных сосудов вследствие патологических изменений сосу-
дистой стенки. Они могут иметь мешковидную или цилиндриче-
скую форму. Причинами этих аневризм могут быть повреждения
сосудистой стенки атеросклеретической, сифилитической или
травматической природы. Чаще аневризмы встречаются в аорте,
реже в других артериях.
Атеросклеротические аневризмы, как правило, развиваются в
поврежденной атеросклеротическим процессом аорте с преобла-
данием осложненных изменений, обычно после 65—75 лет, чаще
223
у мужчин. Причиной служит разрушение мышечно-эластического
каркаса сердечной оболочки аорты атероматозными бляшками.
Типичная локализация — брюшной отдел аорты. В аневризме об-
разуются тромботические массы, служащие источником тромбо-
эмболии.
Осложнения — разрыв аневризмы с развитием смертельного
кровотечения, а также тромбоэмболия артерий нижних конечно-
стей с последующей гангреной.
Сифилитические аневризмы—следствие сифилитического мез-
аортита, характеризующегося разрушением мышечно-эластиче-
ского каркаса средней оболочки стенки аорты, как правило, в об-
ласти восходящего отдела дуги и грудной ее части. Чаще эти
аневризмы наблюдаются у мужчин, могут достигать 15—20 см в
диаметре. При длительном существовании аневризма оказывает
давление на прилежащие тела позвонков и ребра, вызывая их ат-
рофию. Клинические симптомы связаны со сдавлением прилежа-
щих органов и проявляются дыхательной недостаточностью, дис-
фагией из-за сдавления пищевода, постоянным кашлем в связи
со сдавлением возвратного нерва, болевым синдромом, деком-
пенсацией сердечной деятельности.
Васкулиты — большая и неоднородная группа заболеваний со-
судов воспалительного характера. Васкулиты характеризуются об-
разованием инфильтрата в стенке сосудов и в периваскулярной
ткани, повреждением и слущиванием эндотелия, потерей сосуда-
ми тонуса и гиперемией в остром периоде, склерозом стенки и
нередко облитерацией просвета при хроническом течении.
Васкулиты подразделяют на системные, или первичные, и вто-
ричные. Первичные васкулиты составляют большую группу болез-
ней, носят распространенный характер и имеют самостоятельное
значение. Вторичные васкулиты развиваются при многих заболе-
ваниях и будут описаны в соответствующих главах.
Болезни вен представлены в основном флебитом — воспалени-
ем вен, тромбофлебитом — флебитом, осложненным тромбозом,
флеботромбозом — тромбозом вен без их предшествующего вос-
паления, и варикозным расширением вен.
Флебит, тромбофлебит и флеботромбоз. Флебит обычно явля-
ется следствием инфицирования венозной стенки, он может ос-
ложнять острые инфекционные заболевания. Иногда флебит раз-
вивается вследствие травмы вены или ее химического поражения.
При воспалении вены обычно повреждается эндотелий, что ведет к
потере его фибринолитической функции и образованию в этом
участке тромба. Возникает тромбофлебит. Он проявляется боле-
вым симптомом, отеком тканей дистальнее окклюзии, цианозом и
покраснением кожи. В остром периоде тромбофлебит может ос-
ложниться тромбоэмболией. При длительном хроническом течении
тромботические массы подвергаются организации, однако тром-
бофлебит и флеботромбоз магистральных вен могут служить при-
чиной развития трофических язв, обычно нижних конечностей.
Варикозное расширение вен — аномальное расширение, извили-
224
стость и удлинение вен, возникающее в условиях повышенного
внутривенозного давления. Предрасполагающим фактором явля-
ется врожденная или приобретенная неполноценность венозной
стенки и ее истончение. Одновременно компенсаторно рядом
возникают очаги гипертрофии гладкомышечных клеток и скле-
роз. Чаще поражаются вены нижних конечностей, геморроидаль-
ные вены и вены нижнего отдела пищевода при блокаде в них ве-
нозного оттока. Участки расширения вен могут иметь узловатую,
аневризмоподобную, веретеновидную форму. Нередко варикоз
сочетается с тромбозом вены.
Варикозное расширение вен нижних конечностей — наиболее рас-
пространенная форма венозной патологии. Встречается преимуще-
ственно у женщин после 50 лет. Повышение внутривенозного дав-
ления может быть связано с профессиональной деятельностью и
образом жизни (с беременностью, работа стоя, перенос тяжестей и
т. п.). Поражаются преимущественно поверхностные вены, клини-
чески болезнь проявляется отеком конечностей, трофическими на-
рушениями кожи с развитием дерматита и язв.
Варикозное расширение геморроидальных вен — также распро-
страненная форма патологии. Предрасполагающими факторами
являются запоры, беременность, иногда портальная гипертензия.
Варикоз развивается в нижнем геморроидальном сплетении с
формированием наружных узлов или в верхнем сплетении с обра-
зованием внутренних узлов. Узлы обычно тромбируются, выбуха-
ют в просвет кишки, травмируются, подвергаются воспалению и
изъязвлению с развитием кровотечения.
Варикозное расширение вен пищевода развивается при порталь-
ной гипертензии, обычно связанной с циррозом печени, или при
сдавлении опухолью портального тракта. Это происходит вследст-
вие того, что вены пищевода шунтируют кровь из портальной
системы в кавальную. В варикозных венах происходят истонче-
ние стенки, воспаление и образование эрозий. Разрыв стенки ва-
рикозной вены пищевода приводит к тяжелому, нередко смер-
тельному, кровотечению.
Глава 14
РЕВМАТИЧЕСКИЕ БОЛЕЗНИ
Ревматические болезни — группа заболеваний, характеризую-
щаяся системным поражением соединительной ткани и сосудов,
обусловленным в основном иммунными нарушениями. Для этих бо-
лезней характерно образование антител к белкам собственных
тканей организма (аутоантигенам), в результате чего ревматиче-
ские болезни протекают по типу замкнутого порочного круга —
225
чем больше антитела разрушают собственные ткани, тем больше
образуется аутоантигенов, и этот порочный круг пока еще разо->
рвать не удается.
Общими признаками всей группы болезней являются:
• хронический инфекционный очаг;
• нарушения иммунного гомеостаза в виде реакций гиперчув-
ствительности немедленного и замедленного типов;
• системное поражение соединительной ткани;
• генерализованный васкулит;
• хроническое волнообразное течение с обострениями и ре-
миссиями.
Группа ревматических болезней включает:
• ревматизм;
• ревматоидный артрит;
• системную красную волчанку;
• системную склеродермию;
• узелковый периартериит;
• дерматомиозит;
• синдром Шегрена;
• анкилозирующий спондилоартрит.
Морфологической основой всей группы ревматических болезней
служит системная прогрессирующая дезорганизация соединительной
ткани, которая складывается из 4 фаз: мукоидного набухания,
фибриноидных изменений, воспалительных клеточных реакций и
склероза (см. также в главе 1 "Стромально-сосудистые дистро->
фии"). Несмотря на наличие общих характерных изменений, воз->
пикающих в патогенезе всех болезней этой группы, клинико-мор-
фологические особенности каждой из ревматических болезней обу
словлены преимущественным поражением того или иного органа.
РЕВМАТИЗМ
Ревматизм — инфекционно-аллергическое заболевание, кото-i
рое характеризуется дезорганизацией всей системы соединитель-!
ной ткани аутоиммунной природы с преимущественным пораже->
нием сердца и сосудов. Острый ревматизм, или ревматизм в ак->
тивной фазе, обозначают термином "острая ревматическая лихо-i
радка". Ревматизм обусловливает значительную временную и
стойкую утрату трудоспособности больных, что определяет соци->
альную значимость этого заболевания.
Эпидемиология. Ревматизм регистрируется во всех странах ми->
ра. однако заболеваемость в разных государствах колеблется от 5
до 100 случаев в год на 100 000 населения. В России она состав-!
ляет 3 на 1000 жителей, однако колеблется в различных регионах
страны.
Течение ревматизма может быть острым, подострым, затяжным
и латентным. Продолжительность ревматической атаки от не->
скольких недель до 6 мес.
226
Этиология ревматизма связана с р-гемолитическим стрепто->
кокком группы А, который вызывает ангину или фарингит, не->
редко текущие хронически, что создает сенсибилизацию организм
ма. Стрептококки образуют ряд ферментов и веществ, обладают
щих патогенным действием на клетки и внеклеточный матрикс
организма-хозяина. Вместе с тем, поскольку ревматизм развива->
ется лишь у 1—-3 % людей, инфицированных стрептококком,
предполагают генетическую предрасположенность к этому забо->
леванию. Так, установлено более частое развитие ревматизма в
семьях, в которых кто-то из родителей болен ревматической ли->
хорадкой: выявлен риск развития заболевания у лодей с группа-^
ми крови А(П), В(Ш). Вспышки ревматизма связывают также с
возможными мутациями в геноме стрептококков.
Патогенез заболевания нельзя считать полностью изученным.
Болезнь обычно начинается в возрасте 7— 15 лет. изредка — в 4—
5 лет. В 20 % случаев первая атака ревматизма развивается в ютп
шеском или более старшем возрасте. При этом существенное зна->
чение имеет антигенное сходство (мимикрия) между соматиче->
скими фрагментами стрептококков и антигенами сарколеммы
кардиомиоцитов, а также между М-протеином клеточной стенки
бактерии и антигенами стромы миокарда и соединительной ткани
клапанов сердца и суставов. Поэтому персистирующая стрепто->
кокковая инфекция, вызывающая сенсибилизацию организма,
может привести к образованию иммунного ответа не только на
антигены стрептококка, но и на антигены собственной соедини-!
тельной ткани, прежде всего сердца. Это индуцирует аутоимму-
низацию с развитием реакций гиперчувствительности немедлен-!
него и замедленного типов. В крови появляются перекрестно-
реагирующие антитела с образованием циркулирующих иммун->
пых комплексов и фиксацией их на базальной мембране сосудов
микроциркуляторного русла. Возникает реакция гиперчувстви->
тельности немедленного типа (ГНТ), для которой характерна
морфология острого иммунного воспаления в виде экссудативно-
некротического васкулита. Активируется комплемент, а его хемо-
таксические компоненты привлекают лейкоциты и макрофаги.
Микробные антигены переносятся макрофагами на Т-лимфоци-
ты-хелперы, ответственные за иммунологическую память, и из->
вращают ее. Одновременно макрофаги вырабатывают ряд цито-
кинов. вызывающих пролиферацию В-лимфоцитов, ответствен-!
пых за образование антител. Постепенно реакция ГНТ сменяется
реакцией гиперчувствительности замедленного типа (ГЗТ), развит
вается склероз сосудов и периваскулярной соединительной тка->
ни. в том числе сердца и суставов. Таким образом, изменения
при ревматизме и его хроническое волнообразное течение опре->
деляются развитием и периодической сменой реакций ГНТ и
ГЗТ. В результате участия в процессе иммунных реакций для всех
форм ревматизма характерны гиперплазия и плазмоклеточная
трансформация лимфоидной ткани, а также полисерозиты.
227
Рис. 55. Ревматическая гранулема Ашоффа— Талалаева в строме миокар-'
да. Гранулема состоит из гистиоцитов с базофильной цитоплазмой (а), в
центре гранулемы — очаг фибриноидного некроза соединительной ткани
(б).
Морфогенез ревматизма характеризуется прогрессирующей
системной дезорганизацией соединительной ткани и изменения-!
ми сосудов микроциркуляторного русла, наиболее выраженными
в строме и клапанах сердца. Стадия мукоидного набухания и фиб-
риноидных изменений является морфологическим выражением ре->
акций ГНТ. Клеточная воспалительная реакция проявляется вос->
новном образованием специфических гранулем Ашоффа—Тала-
лаева, названных в честь описавших их авторов (рис. 55). Гранул
лема при ревматизме формируется в ответ на фибриноидный
некроз стенки сосуда микроциркуляторного русла и околососуди->
стой соединительной ткани. Назначение ревматической грануле-!
мы заключается в фагоцитозе некротических масс, содержащих
остатки иммунных комплексов. Гранулема имеет определенную
динамику, отражающую реакцию иммунокомпетентной системы.
Вокруг очага фибриноидного некроза появляются крупные мак->
рофаги с базофильной цитоплазмой и круглыми или овальными
ядрами с центральным расположением хроматина ("совиный
глаз"), иногда встречаются многоядерные гистиоциты. Ревматичек
ская гранулема при этом называется "цветущей". В дальнейшем
реакции ГНТ сменяются на реакции ГЗТ, в гранулеме появляютл
ся фибробласты, количество фибриноидного детрита уменыпает-
228
ся ("увядающая" гранулема). Затем фибриноид полностью расса->
сывается и область гранулемы склерозируется ("рубцующаяся”гра~>
нулема). Ревматические гранулемы появляются также в суставных
сумках, апоневрозах, перитонзиллярной соединительной ткани, в
строме других органов.
Клинико-морфологические формы ревматизма выделяют на ос->
новании преимущественного поражения того или иного органа.
Различают кардиоваскулярную, полиартритическую, церебраль->
ную и нодозную формы. Это деление условно, так как при ревма->
тизме поражение сердца встречается всегда.
Кардиоваскулярная форма заболевания развивается чаще дру-1
гих форм. При этом всегда имеет место ревматический эндокар ->
дит. При поражении эндокарда и миокарда развиваетсяревмапш~>
ческий кардит, или ревмокардит. При сочетанием поражении эн->
докарда, миокарда и перикарда говорят о ревметическом панкар-
дите.
Эндокардит — воспаление эндокарда — чаще всего развивает^
ся в клапанном аппарате сердца (клапанный эндокардит). В про-"
цесс могут быть вовлечены сухожильные хорды — хордальный
эндокардит, а также пристеночный эндокард предсердий или же->
лудочков — пристеночный (париетальный) эндокардит. Наиболее
часто поражаются створки митрального клапана (65—70 % ревмо->
кардитов). На 2-м месте по частоте комбинированное поражение
створок митрального и аортального клапанов (25 %), на 3-м мес->
те — аортального клапана. Изменения трехстворчатого клапана
встречаются значительно реже, и исключительно редко возника->
ют поражения клапана легочного ствола. Выделяют 4 вида свя-i
занных между собой морфологических изменений клапанов серд->
ца: диффузный эндокардит (вальвулит), острый бородавчатый,
фибропластический и возвратно-бородавчатый эндокардит.
Диффузный эндокардит (вальвулит) характеризуй
ется мукоидным набуханием и умеренными фибриноидными из->
менениями соединительной ткани створок клапана без поврежде-i
ния эндотелия, что обусловливает отсутствие на них наложений
тромботических масс. Исходом вальвулита является склероз ство->
рок клапана, иногда при рано начатом и адекватном лечении
процесс обратим. Сходные изменения, заканчивающиеся склероз
зом, могут развиваться в сухожильных хордах.
Острый бородавчатый эндокардит протекает с бсп
лее выраженными фибриноидными изменениями, клеточной ре->
акцией и вовлечением в процесс эндотелия клапанов. При этом
образуются мелкие (1—2 мм) тромбы, которые располагаются по
замыкающему краю створок в виде бородавок серого цвета.
Фибропластический эндокардит развивается из
двух предыдущих форм эндокардита и характеризуется усиленные
ми процессами склероза створок клапанов и их деформацией.
Возвратно-бородавчатый эндокардит возникает
при повторных атаках ревматизма на фоне склероза, гиалиноза и
деформаций створок клапанов. При этом дезорганизация соеди-
229
нительнои ткани происходит как в предсуществующеи строме,
так и в уже склерозированных тромботических бородавках. В ре-<
зультате на уже склерозированные тромботические массы откла->
дываются новые массы фибрина, которые при затихании процесс
са также склерозируются.
Осложнения. Острый бородавчатый и возвратно-бородавчатый
эндокардиты могут осложняться тромбоэмболией сосудов боль->
шого или малого круга кровообращения. Следствием таких тром-i
боэмболии являются инфаркты селезенки, почек, головного моз->
га, миокарда, сетчатки глаза, иногда легких, изредка гангрена
кишки или нижних конечностей.
В исходе эндокардита развиваются склероз, гиалиноз и дефор->
мация створок клапанов. Часто они срастаются друг с другом, не->
редко развиваются склероз и петрификация фиброзного кольца.
Атриовентрикулярное отверстие обычно резко сужено, имеет вид
"рыбьего рта" — формируется порок сердца. Сухожильные хорды
также утолщены, укорочены и спаяны друг с другом.
Миокардит — воспаление миокарда; как правило, протекает в
форме ревмокардита, т. е. сочетания эндокардита и миокардита.
Миокардит встречается в двух основных формах: узелковый (гра-
нулематозный) и диффузный межуточный экссудативный мио->
кардит.
Узелковый (гранулематозный) миокардит хал
рактеризуется образованием ревматических гранулем в перива-
скулярной ткани стромы миокарда, особенно в ушке левого пред-"
сердия, стенке левого желудочка сердца, в межжелудочковой пе->
регородке и в сосочковых мышцах. Гранулемы могут быть в раз->
ных фазах развития. Кардиомиоциты находятся в состоянии бел-"
ковой или жировой дистрофии. В исходе узелкового миокардита
развивается диффузный мелкоочаговый кардиосклероз.
Диффузный межуточный экссудативный мио->
кардит развивается у детей. Макроскопически полости сердца
резко расширены, миокард дряблый, тусклый. Микроскопически
сосуды полнокровные, интерстиций миокарда пропитан сероз->
ным экссудатом, инфильтрирован лимфоцитами, гистиоцитами,
полиморфно-ядерными лейкоцитами. Мышечные волокна разво-
локняются, в кардиомиоцитах выражены дистрофические изме-i
нения. Клинически проявляется тяжелой сердечно-сосудистой
недостаточностью. В исходе развивается диффузный кардио-i
склероз.
Перикардит характеризуется серозно-фибринозным и фибри->
нозным воспалением перикарда, причем наложения фибрина из-
за сокращений сердца напоминают волосы, и поэтому такое
сердце называют "волосатым" (рис. 56). При организации фибри->
нозного экссудата образуются спайки и полость перикарда обли-
терируется. Иногда происходит обызвествление образовавшейся
соединительной ткани — возникает "панцирное сердце".
Ревматические васкулиты имеют генерализованный характер и
обнаруживаются постоянно. Наиболее характерно поражение со-
230
Рис. 56. Фибринозный перикардит
(при ревматизме): а — на эпикарде
рыхлые наложения фибринозного
экссудата; б — подлежащие ткани
полнокровны, отечны, инфильтри->
рованы лейкоцитами.
в виде муфт, появлением се->
судов микроциркуляторного pyc-i
ла. В артериях и артериолах —
фибриноидные изменения сте-i
нок, тромбоз; в капиллярах —
пролиферация и слущивание эн->
дотелия, муфты из пролифери-
рующих адвентициальных кле->
ток.
В исходе ревматических васку-
литов наблюдается склероз со->
судов.
Полиартритическая форма
ревматизма характеризуется по->
ражением крупных суставов с
развитием очагов дезорганиза->
ции в синовиальной оболочке
(синовит), васкулитов с гипере->
мией сосудов, периваскулярны-
ми лимфоидными инфильтратами
розного и серозно-фибринозного выпота в суставной полости.
Суставной хрящ в процесс не вовлекается, поэгому деформация
суставов при ревматизме не происходит.
Нодозная (узловатая) форма характеризуется появлением под
кожей на разгибательной стороне крупных суставов, по ходу по->
звоночника, в фасциях, апоневрозах, сухожилиях узелков и узлов,
состоящих из очага фибриноидного некроза, окруженного ин->
фильтратом из лимфоцитов, макрофагов. В исходе на месте узел->
ков формируются рубчики. Для этой формы характерно и пора->
жение сердца.
Церебральная форма называется малой хореей. В головном
мозге обнаруживают артерииты, микроглиальные узелки, дистро->
фические изменения нервных клеток, изредка очаги кровоизлия-i
ний. Эти изменения сопровождаются мышечной слабостью, на->
рушением координации движений. Поражение других органов и
систем не выражено.
Осложнения. При атаке ревматизма в процесс могут вовлекать-!
сявсе органы и системы. Возможно развитие инфекционного эн->
докардита, ревматической пневмонии, ревматического очагового
или диффузного гломерулонефрита, полисерозитов с развитием
спаечных процессов в полостях перикарда, плевры, брюшины,
очагов восковидного некроза в скелетных мышцах, кольцевидной
эритемы или сыпи на коже, дистрофических и атрофических из-
231
менений эндокринных желез, а также тромбоэмболического син->
дрома.
Исходы ревматизма связаны с поражением сердечно-сосуди->
стой системы. Атака ревматизма может сопровождаться острой
сердечно-сосудистой недостаточностью и аритмиями. При сфор->
мированных сердечных пороках и ревматическом кардиосклерозе
развивается хроническая сердечно-сосудистая недостаточность.
РЕВМАТОИДНЫЙ АРТРИТ
Ревматоидный артрит — хроническое аутоиммунное заболева->
ние, основу которого составляет системная дезорганизация с<п
единительной ткани с прогрессирующим поражением в основном
периферических суставов, с развитием продуктивного синовита,
деструкции суставного хряща с последующей деформацией и ан->
килозом суставов.
Эпидемиология. Распространенность ревматоидного артрита
среди взрослого населения составляет от 0,6 до 1,3 %. Заболеваем
мость среди женщин примерно в 3 раза выше, чем среди мужчин.
С возрастом риск развития заболевания возрастает.
Этиология болезни неизвестна. Предполагают роль различных
возбудителей, но наибольшее значение придают вирусу Эпштей-
на—Барр, поскольку обнаружена антигенная мимикрия между
вирусом, коллагеном II типа синовиальной ткани, что может вы->
зывать аутоиммунный ответ к коллагену II типа. Показано также,
что у больных ревматоидным артритом имеется более высокий
титр антител к белкам микобактерий, и установлено, что антигем
ны этих микобактерий способны вызывать пролиферацию Т-лим-
фоцитов в синовиальной оболочке сустава. Кроме того, доказана
генетическая предрасположенность к ревматоидному артриту.
Патогенез ревматоидного артрита до конца не изучен. Очевидм
но, стимулом для заболевания является микробный фактор, котом
рый персистирует в сенсибилизированном организме. При этом
вызванный им иммунный ответ направлен против антигенов этих
неустановленных возбудителей, но в силу антигенной мимикрии —
и на собственные антигены, что вызывает аутоагрессию и хроним
ческое воспаление. При этом важнейшую роль играют Т-лимфо-
циты-хелперы, которые инициируют развитие синовита. Они
продуцируют многочисленные цитокины, вызывающие активам
цию и пролиферацию макрофагов, В-лимфоцитов, эндотелиаль-
ных клеток капилляров синовиальной оболочки, синовиоцитов.
Кроме того, при ревматоидном артрите выявляются разнообрази
ные аутоантитела, часть которых выступает в роли аутоантигенов,
а другая часть — в роли аутоантител. Они взаимодействуют друг с
другом, поддерживая тем самым воспаление в суставе.
Морфогенез. Ревматоидный артрит протекает в 3 стадии, при
этом основные морфологические изменения обнаруживают в суем
тавах и во всей системе соединительной ткани.
232
В первой стадии, которая может продолжаться несколько лет, в
синовиальной оболочке происходят мукоидные и фибриноидные
изменения, она становится отечной, полнокровной, с очагами
кровоизлияний. В полости сустава накапливается серозный вы->
пот. Часть ворсин синовиальной оболочки, подвергшихся фибри-
ноидному некрозу, образует плотные слепки — "рисовые тельца".
На ранней стадии выражены капилляриты, пролиферативно-нек-
ротические васкулиты главным образом мелких венул и артериол,
в стенках сосудов — фибриноид и иммунные комплексы. Изме->
нения суставного хряща в этой стадии не выражены.
Во второй стадии синовита происходит выраженная про л ифе->
рация синовиоцитов, отмечается гипертрофия ворсинок. Строма
инфильтрирована лимфоцитами, плазматическими клетками. На
поверхности синовиальной оболочки обнаруживаются наложения
фибрина, способствующего пролиферации фибробластов. Сосуды
в состоянии продуктивного воспаления. На суставных концах
костей формируется грануляционная ткань, которая в виде пласта
(паннуса) наползает на хрящ и врастает в него и в синовиальную
оболочку. Хрящ под паннусом истончается, в нем появляются
глубокие трещины, участки обызвествления. Затем происходит
замещение хряща фиброзной тканью и костью. Паннус резко су
живает суставную полость, что обусловливает развитие тугопо-
движности сустава, могут развиваться вывихи или подвывихи.
Характерна наружная девиация пораженных суставов, особенно
кистей рук — "плавники люрэюа". В суставных концах костей на->
растает остеопороз, возможны переломы. Между остатками кост->
ной ткани разрастается грануляционная и фиброзная ткань с оча->
гами фибриноидного некроза, инфильтрацией лимфоцитами и
плазматическими клетками. Одновременно происходит восста->
новление костной ткани, результатом чего являются анкилозы
суставов.
В третьей стадии, которая может развиваться через 15—
30 лет, формируются фиброзно-костные анкилозы, обусловли->
вающие прогрессирующую обездвиженность больного. Однако
процессы дезорганизации тканей суставов продолжаются и на
этой стадии.
Внесуставные висцеральные проявления ревматоидного артрита
наблюдаются у 20—25 % больных и характеризуются образование
ем во многих органах и тканях, но чаще — в коже и синовиалье
ной оболочке суставов ревматоидных узлов диаметром от 0,5 до
3 см. На разрезе они состоят из крошащихся серо-желтых масс,
окруженных фиброзной капсулой. В основе формирования узлов
лежат аутоиммунные реакции, проявляющиеся процессами дезе
организации соединительной ткани, продуктивным воспалением
и генерализованным васкулитом. В структурах иммунной систее
мы — гиперплазия лимфатических узлов, селезенки, плазмоцитоз
костного мозга. Поражение сердца при ревматоидном артрите
проявляется в виде перикардита, миокардита, эндокардита, реве
матоидных узлов, кардиосклероза. Нередки полисерозит, пораже-
233
ния почек, а также амилоидоз. В легких — фиброзирующий аль-
веолит, ревматоидные узлы, плеврит с исходом в фиброз плевры.
Часто отмечается атрофия скелетных мышц.
Осложнения — подвывихи и вывихи мелких суставов, обусловь
ленные фиброзными и костными анкилозами, переломы костей,
анемия.
Исходом является хроническая почечная недостаточность. обу->
словленная амилоидозом, или смерть от присоединения вторич->
ной инфекции.
СИСТЕМНАЯ КРАСНАЯ ВОЛЧАНКА
Системная красная волчанка (СКВ) — заболевание системы
соединительной ткани, обусловленное аутоиммунными наруше->
ниями, характеризующееся преимущественным поражением по->
чек, серозных оболочек, кожи и суставов.
Эпидемиология. Частота СКВ колеблется от 4 до 250 случаев на
100 000 населения в год. В 70 % случаев болезнь начинается в
возрасте 14—25 лет. Соотношение заболевших женщин и мужчин
в среднем 9:1.
Этиология заболевания не установлена. Предполагается роль
вирусов, на что указывает наличие у больных маркеров вирусной
инфекции и антител к вирусам кори, краснухи, парагриппа. Вме->
сте с тем выявленная у заболевших СКВ бактериальная сенсиби->
лизация, наличие очагов хронической инфекции, частые ангины
легли в основу концепции бактериального генеза болезни. Уста->
новлена также наследственная предрасположенность к СКВ. Шин
рокая распространенность заболевания среди женщин детородно^
го возраста указывает на роль гормональных влияний в патогене->
зе страдания.
Патогенез. В основе развития заболевания лежат полом регу-
ляторных механизмов апоптоза и дефекты механизмов, обеспечив
вающих толерантность к собственным антигенам. Нарушение
процессов выведения апоптозных тел сопровождается накопление
ем аутоантигенов на мембранах апоптоматозных телец, что может
стимулировать аутоиммунизацию. Важнейшее значение имеет ак->
тивация В-лимфоцитов с образованием аутоантител против собе
ственной ядерной ДНК различных клеток, которая, таким обрае
зом, выступает в качестве аутоантигена. Антинуклеарные антитее
ла (АНАТ), относящиеся к IgG, носят название волчаночного фак~>
тора. Кроме того, аутоантигенами могут быть полипептиды ядере
пых РНК, некоторые растворимые антигены цитоплазмы клеток,
коллаген, мембранные антигены нейронов и клеток крови, вклюе
чая эритроциты, лимфоциты, нейтрофилы.
Большинство висцеральных поражений при СКВ связано с
циркуляцией и отложением иммунных комплексов в базальных
мембранах сосудов микроциркуляции и соединительнотканной
строме, где они вызывают иммунное воспаление.
234
Рис. 57. Системная красная волчанка.
Волчаночная клетка (показано стрелкой).
Морфогенез. Изменен
ния при СКВ носят ге-1
нерализованный харак-i
тер с поражением мно->
гих органов. Микроско-i
пическая картина имеет
ряд особенностей, no-i
зволяющих поставить
диагноз. Наиболее ха->
рактерные изменения
возникают в микрососу->
дах в виде васкулитов и
в соединительной ткани,
где развиваются явле->
ния ее дезорганизации.
Кроме того, отмечается
межуточное воспаление
в строме всех органов с
характерными для иммунного воспаления лимфомакрофагальны-
ми и плазмоцитарными инфильтратами. Все это является морфо->
логическим выражением гиперчувствительности немедленного и
замедленного типов. Во всех органах гибнут ядра клеток, и такие
клетки фагоцитируются нейтрофильными лейкоцитами и макрос
фагами, приобретая характерный вид (рис. 57). Они называются
волчаночными клеткам! (или LE-клеткам!). Очень характерно
развитие вокруг кисточковых артерий селезенки соединительной
ткани в виде колец — луковичный склероз. Кроме того, в органах
иммунной системы, в интерстициальной ткани внутренних орга->
нов, вокруг мелких сосудов отмечаются скопления лимфоцитов и
плазматических клеток, продуцирующих антитела.
Особенно часто поражаются кожа и почки. На коже щек и
скул появляются гиперемированные участки, соединенные поло->
сой на переносице — так называемая фигура бабочки. В почках
развивается иммунное воспаление — волчаночный нефрит, кото-i
рый завершается сморщиванием почек и уремией. У некоторых
больных возникает абактериальный бородавчатый эндокардит
клапанов сердца. Суставы также поражаются при СКВ, но не на->
столько сильно, чтобы развилась их деформация.
Причиной смерти больных СКВ наиболее часто является по->
чечная недостаточность.
СИСТЕМНАЯ СКЛЕРОДЕРМИЯ
Системная склеродермия (системный склероз) — хроническое
ревматическое заболевание с преимущественным поражением ко->
жи. опорно-двигательного аппарата и внутренних органов. харак->
теризующимся прогрессирующим склерозом дермы, стромы орга->
нов и сосудов.
235
Эпидемиология. Заболеваемость системной склеродермией с<п
ставляет 2.7—12 случаев на 1 000 000 населения в год. В возрасте
30—50 лет женщины болеют чаще мужчин в соотношении 7:1.
У детей заболевание встречается очень редко, болеют чаще девоч->
ки (соотношение 3:1).
Этиология заболевания не установлена. Одним из предпола-i
гаемых этиологических факторов является цитомегаловирус. В no-i
следнее время этиологическое значение придают эмбриональным
клеткам, которые преодолевают плацентарный барьер во время
беременности и циркулируют в материнском кровеносном русле
или фиксируются в тканях различных органов. Эти клетки-химе->
ры имеют иную генетическую структуру и, персистируя в орга->
низме больных системной склеродермией, могут участвовать в
патогенезе заболевания, индуцируя хроническую иммунную реак->
цию по типу "трансплантат против хозяина". Очевидно, имеет
значение и генетическая предрасположенность, а также воздейст-i
вие химических агентов, травмы, вибрации, охлаждения, с после->
дующим развитием иммунных реакций.
Патогенез. Неизвестный этиологический фактор запускает
иммунный ответ, ведущий к системной дезорганизации соедини->
тельной ткани, повреждению сосудистой стенки и активации
фибробластов, что в итоге обусловливает выраженный склероз
кожи и внутренних органов.
Морфогенез. В коже и внутренних органах последовательно
развиваются стадии дезорганизации соединительной ткани с не-"
резкой клеточной воспалительной реакцией и исходом в скле->
роз и гиалиноз. Может развиваться кальциноз кожи, преимуще->
ственно в области пальцев рук и вокруг суставов. В заключи^
тельной фазе в результате склероза и стягивания тканей лицо
приобретает маскообразность, пальцы становятся похожими на
птичью лапу, выражены трофические нарушения — изъязвлен
ния, гнойники, вплоть до самоампутации пальцев, облысение.
Развивается полиартрит с поражением мелких суставов кистей.
В легких развивается диффузный интерстициальный пневмо-
фиброз, сопровождающийся легочной гипертензией. Поражен
ние почек отмечается у 75 % больных системной склеродермии
ей. Важнейшее значение имеет склеродермическая микроангиопа-
тия почек с поражением преимущественно междольковых арте->
рий, в которых развиваются мукоидное набухание и фибрино-
идный некроз стенок и тромбоз их просветов, вследствие чего
развиваются инфаркты почек и острая почечная недостаточ->
ность ("истинная склеродермическая почка"). В результате про-"
дуктивного васкулита сосудов сердца нарастают кардиосклероз,
склероз париетального и клапанного эндокарда, сухожильных
хорд с формированием склеродерлшческого порока сердца. Харак->
терны также стриктуры пищевода, пептические язвы и метя его
эпителия. Нарушения моторики, склероз и атрофия слизистой
оболочки развиваются и в других органах желудочно-кишечного
тракта.
236
Исход. У больных системной склеродермией развивается уре->
мия, сердечно-сосудистая или сердечно-легочная недостаточ->
ность и др.
УЗЕЛКОВЫЙ ПЕРИАРТЕРИИТ
Узелковый периартериит — ревматическое заболевание. харак->
теризующееся системным васкулитом с некрозом стенок средних
и мелких артерий.
Эпидеми)логия. Ежегодно регистрируется 0,2—1 новый случай
узелкового периартериита на 1 000 000 населения. Среди мужчин
заболевание встречается несколько чаще, чем среди женщин (2:1).
Этиология не установлена. Определенное значение в развитии
заболевания придают вирусу гепатита В, меньшее значение — ви->
русу гепатита С. Отмечена связь между развитием узелкового пе->
риартериита и инфекцией, вызванной цитомегаловлрусом, парво-
вирусом В19, вирусом иммунодефицита человека (ВИЧ). В каче->
стве предрасполагающих факторов рассматриваются стрептококк
ковая инфекция, лекарственные препараты (сульфаниламиды и
антибиотики), яды, вакцинации, роды.
Патогенез. Основная роль принадлежит иммунокомплексному
механизму поражения сосудов. В последние годы определенное
значение придается клеточным иммунным реакциям.
Морфогенез. Характерный патоморфологический признак —
сегментарные фибриноидные некрозы артерий мышечного типа
мелкого и среднего калибра в месте ветвления или бифуркации
сосудов вследствие отложений здесь иммунных комплексов. В оср->
рой стадии развивается выраженная инфильтрация всех слоев со->
судистой стенки нейтрофилами, эозинофилами, макрофагами, что
вызывает четкообразные "узелковые" утолщения сосудов. В мес->
тах фибриноидного некроза появляются разрывы и мелкие анев->
ризмы. Просвет пораженных сосудов обычно закрывается тром->
бом, в дальнейшем развивается склероз с муфтообразным утол->
щением стенки в области поражения и окклюзией просвета сосуда.
Осложнения: профузные кровотечения вследствие разрыва со-ч
суда, перитонит в результате перфорации пораженной язвенно-
некротическим процессом кишки.
Исход без лечения неблагоприятный, летальность составляет
75—90 %. Наиболее частой причиной смерти является почечная
недостаточность.
ДЕРМАТОМИОЗИТ
Дерматомиозит — ревматическое заболевание, основным кли-
нико-морфологическим проявлением которого является систем->
пая дезорганизация соединительной ткани, поражение попереч->
нополосатой и гладкой мускулатуры, а также кожи.
237
Этиология заболевания до конца не изучена. Предполагается
роль вирусов Коксаки В, пикорнавирусов, бактериальных, пара->
зитарных инфекций, некоторых лекарственных препаратов. Су
щественную роль в развитии заболевания играют генетические
факторы.
Патогенез. Точный механизм развития аутоиммунизации при
дерматомиозите еще неизвестен. Предполагается значение анти->
генной мимикрии неуточненных инфекционных агентов и ауто-
антигенов. При этом почти у 90 % больных в сыворотке крови
обнаруживается широкий спектр аутоантител, направленных про->
тив собственных цитоплазматических белков, в том числе и мио-
зитспецифических. При дерматомиозите, вероятно, основной ми->
шенью антител и комплемента становятся интрафасциальные ка->
пилляры, в которых образуются депозиты, предшествующие вос->
палительной инфильтрации. Предполагается, что поражение
мышц при дерматомиазите связано с развитием Т-клеточной ци-
тотоксичности против мышечных клеток, экспрессирующих ауто-
антигены.
Морфогенез. Характерные изменения обнаруживаются в попе->
речнополосатых мышцах и в коже. Макроскопически мышцы
отечные, бледно-желтого цвета с участками каменистой плотно->
сти вследствие очагового кальциноза. Микроскопически вокруг
мелких сосудов в перимизии выявляются инфильтраты, преиму->
щественно из В-лимфоцитов, плазматических клеток и Т-лимфо-
цитов-хелперов. Характерно развитие перифасцикулярной атро->
фии мышечных волокон. В коже выявляются продуктивные и
продуктивно-некротические васкулиты дермы с периваскулярной
лимфоцитарной инфильтрацией.
Исходом заболевания является грубый склероз кожи и подкож->
ной клетчатки в сочетании с атрофией мышц.
В основе остальных заболеваний группы ревматических болез-i
ней также лежат процессы системной дезорганизации соедини->
тельной ткани и сосудов аутоиммунной природы, но они имеют
меньшее значение в клинике.
Глава 15
БОЛЕЗНИ СИСТЕМЫ ДЫХАНИЯ
Газообмен кислорода и углекислого газа в организме происхо->
дит при участии систем кровообращения и дыхания.
Система дыхания включает:
• дыхательные пути;
• паренхиму легких, где происходит газообмен с помощью
системы кровообращения;
238
• грудную клетку, в том числе ее костно-хрящевой каркас и
нервно-мышечную систему:
• нервные центры регуляции дыхания.
Система дыхания обеспечивает:
• обмен кислорода и углекислого газа в альвеолах — альвеол
лярную вентиляцию;
• кровообращение легких, включая альвеолы;
• диффузию кислорода и углекислого газа через альвеолока-
пиллярную мембрану, или аэрогематическлй барьер.
Расстройства функционирования системы дькания могут при->
вести к дыхательной недостаточности — состоянию», характери^
зующемуся развитием гипоксии и гиперкапнии в результате нару->
шения газообменной функции легких.
НАРУШЕНИЯ ОБМЕНА КИСЛОРОДА И УГЛЕКИСЛОГО ГАЗА
В АЛЬВЕОЛАХ ЛЕГКИХ
Эти нарушения включают гипо- и гипервенгиляцию легких,
гипертензию в сосудах малого круга кровообращения.
Гиповентиляция альвеол воздухом характеризуется падением
объема вентиляции альвеол за единицу времени, ниже необходим
мого организму.
Причинами могут быть:
• снижение проходимости дыхательных путей для воздуха из-
за обструкции (закрытия) просветов бронхов опухолью,
рвотными массами, западающим языком при коме. нарко->
зе, слизью, кровью или в результате спазма бронхиол, на->
пример при приступе бронхиальной астмы, и др.;
• снижение степени расправления легких при очагово-слив-
ной пневмонии, опухолях паренхимы легких, склерозе ле->
точной ткани, а также при сдавлении грудкой клетки тяже->
лыми предметами, например при завалах землей, при плев->
рите, скоплении в плевральных полостях крови, экссудата,
транссудата, воздуха;
• нарушение механизмов регуляции дыхания на уровне дыха->
тельного центра или его афферентных и эфферентных пу
тей, что наблюдается при травме продолговатого мозга,
сдавлении головного мозга при его отеке или воспалении,
кровоизлияниях в вещество мозга, опухоли продолговатого
мозга, при острой выраженной гипоксии различного генеза
и др.
Проявления заключаются в появлении патологического дыха->
ния — апнейстического, дыхания Биота, Чейна—Стокса, Кус-
смауля (рис. 58).
Атеистическое дыхание (от греч. apnoia— отсутствие дыхания)
— временные остановки дыхания, характеризующиеся удлинена
ным вдохом и коротким выдохом.
Дыхание Биота проявляется непродолжительными периодами
239
Биот*
ГуТГМГ)1М
Рис. 58. Типы патологического ды-1
хания.
интенсивных дыхательных дви->
жений (как правило 4—6), че->
ре дующихся с периодами ain
ноэ в течение нескольких ce-i
кунд.
Дыхание Чейна—Стокса хал
рактеризуется нарастающим
увеличением частоты и глубин
ны дыхательных движений с
последующим их прогресси->
рующим снижением и разви->
тием периодов апноэ ддитель->
ностью 5—20 с.
Дыхание Кусслюуля прояв-ч
ляется редкими неглубокими
вдохами и шумными выдохам
ми с последующим периодом
апноэ.
Гипервентиляция легких характеризуется превышением венти->
ляции легких за единицу времени в сравнении с необходимой ор->
ганизму.
Причинам! могут быть неадекватная искусственная вентиля->
ция легких, например при сотрясениях, кровоизлияниях, внутре-
черепных опухолях и др.
РАССТРОЙСТВА КРОВООБРАЩЕНИЯ В ЛЕГКИХ
Причины:
• нарушения тока крови в сосудах малого и большого круга
кровообращения;
• нарушения перфузии легких при гипертензии в сосудах ма->
лого круга кровообращения и при нарушении оттока крови
из легких как результат гипертонической болезни. митраль->
него порока сердца, пневмосклероза и др.
Гипотензия в сосудах малого круга кровообращения характерна
зуется стойким снижением в них давления крови.
Причины:
• пороки сердца с шунтированием крови "справа налево" и
"сбросом" венозной крови в артериальную систему, напри->
мер при тетраде Фалло, недостаточности клапанов легочной
артерии;
• гиповолемии различного генеза, например при длительной
диарее, шоковых состояниях, в результате хронической
кровопотери ит. п.;
• системная артериальная гипотензия, например при коллапс
се или коме.
Дыхательная недостаточность — патологическое состояние, при
котором система дыхания не обеспечивает необходимого организ-
240
му уровня газообмена, что проявляется развитием гипоксемии.
Причинами гиперкапнии являются все указанныевыше расстрой-"
ства газообменной функции легких и внелегочныхм нарушений.
БОЛЕЗНИ СИСТЕМЫ ДЫХАНИИ
Органы системы дыхания имеют непосредственный контакт с
воздухом и в связи с этим постоянно подвераются прямому
влиянию патогенных факторов окружающей среди. К ним в пер-"
вую очередь относятся вирусы и бактерии, многочисленные хи->
мические и физические раздражители, поступающие в органы
дыхания вместе с воздухом. Эти факторы вызывает болезни ды->
хательных путей, среди которых наиболее часто встречаются ост-"
рые воспалительные заболевания трахеи, бронхов и легких, хро-"
нические неспецифические болезни легких и рак легкого.
ОСТРЫЕ ВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ БРОНХоВ И ЛЕГКИХ
Острые воспалительные заболевания бронхов и ле гких пора-"
жают различные звенья системы дыхания. Наибольшее значение
среди них имеют крупозная пневмония, бронхит и очаговая
бронхопневмония.
КРУПОЗНАЯ ПНЕВМОНИЯ
Крупозная пневмония — острое инфекционное заболевание,
проявляющееся воспалением одной или нескольких долей легких
с обязательным вовлечением в процесс плевры.
Этиология. Возбудителями являются пневмококки различных
типов, которые проявляют свое действие в предвари тел ьно сенси-"
билизированном им:и и ослабленном организме.
Пато- и морфогенез. В развитии крупозной пневмонии, прозе-"
кающей в течение 9—11 дней, выделяют четыре стадии: прилива,
красного опеченения, серого опеченения и разрешения.
Стадия прилива характеризуется серозным воспалением и раз-"
вивается в ответ на размножение микробов в пораженной доле
легкого. В этот период резко повышается проницаемость калил-"
ляров и венул и в паренхему легких выходят плазма крови и
эритроциты. Длительность стадии — около 1 сут.
Стадия красного опеченения характеризуется развитием фибри-"
нозного крупозного воспаления. Альвеолы всей доли заполня-"
ются эритроцитами, к ним примешиваются полинуклеарные
лейкоциты и выпадают нити фибрина. Доля легкого увеличива-"
ется в размерах, становится красной и плотной, напоминает
ткань печени (отсюда и название "опеченение") - Эта стадия
длится 2—3 дня.
241
Рис. 59. Крупозная пневмония, серое опеченснис верхней доли легкого.
242
Стадия серого опеченения. Экссудат, заполняющий альвеолы,
состоит в основном из лейкоцитов и фибрина. Лейкоциты фаго->
цитируют микробов. Пораженная доля легкого увеличена в раз->
мере, плотная, серого цвета. На плевре — фибринозный экссудат
(рис. 59). Стадия длится 4—6 сут.
Стадия разрешения. В этой стадии ферменты лейкоцитов рас-'
щепляют фибрин, оставшиеся микробы фагоцитируются. Появ->
ляется большое количество макрофагов, поглощающих остатки
фибринозного экссудата. Фибринозные наложения на плевре
обычно организуются и превращаются в плотные спайки.
Осложнения крупозной пневмонии могут быть легочными и
внелегочными.
Легочные осложнения — абсцесс пораженной доли легкого, ган->
грена легкого. В тех случаях, когда фибринозный экссудат не рас-'
сасывается, а прорастает соединительной тканью, наступает его
организация — так называемая карнификация легких. Легкое ста->
новится плотным, безвоздушным, мясистым. Фибринозное вос->
паление плевры может стать гнойно-фибринозным, гной запол-i
няет плевральные пространства и возникает эмшема плевры.
Внелегочные осложнения развиваются при гематогенном или
лимфогенном распространении инфекции из легких — гнойные
медиастинит, перикардит, эндокардит, менингит и др.
Смерть при крупозной пневмонии наступает от сердечно-ле-'
точной недостаточности или от возникших осложнений.
ОСТРЫЙ БРОНХИТ
Этиология. Острый бронхит развивается под влиянием разно-'
образных инфекционных возбудителей. При этом большую роль
играет снижение сопротивляемости организма в результате охла->
ждения, запыления вдыхаемого воздуха, тяжелой травмы.
Морфогенез. Обычно воспаление бронхов и бронхиол носит
катаральный характер, но экссудат может быть серозным, слизи->
стым, гнойным, фибринозным или смешанным. Слизистая обо->
лочка бронхов становится гиперемированной. резко возрастает
количество образующейся слизи. Мерцательный эпителий теряет
ворсинки, слущивается, что затрудняет выведение слизи из брон->
хов. В стенке бронхов развивается отек, она инфильтрируется
лимфоцитами, плазматическими клетками, нейтрофильными
лейкоцитами. Скопившаяся слизь в результате нарушения ее вы->
ведения вместе с возбудителями острой инфекции опускается в
нижележащие отделы бронхиального дерева и закупоривает брон->
хиолы.
Исход. Острый бронхит обычно заканчивается выздоровлени-'
ем, слизистая оболочка бронхов восстанавливается. Однако тече-'
ние бронхита может приобрести подострый и хронический харак->
тер, особенно при наличии поддерживающих болезнь факторов
(курение).
243
ОЧАГОВАЯ БРОНХОПНЕВМОНИЯ
Этиология. Очаговая пневмония (бронхопневмония) — ост-
ровозникающее воспаление ткани легких, связанное с бронхитом.
Причинами очаговой пневмонии обычно являются микробы, ви->
русы, грибы.
Патогенез. Воспалительный процесс с бронхов распростра->
няется на участок прилежащей легочной паренхимы. Иногда
очаговая пневмония возникает первично, но при этом в процесс
вовлекается и расположенный в зоне воспаления бронх. В зави~<
симости от размеров очага воспаления бронхопневмония может
быть:
• альвеолярной;
• ацинозной;
• дольковой;
• сливной дольковой;
• сегментарной;
• межуточной.
Морфология. Очаги воспаления наиболее часто развиваются в
задненижних сегментах легких. Они разных размеров, плотнова->
тые. выступают над поверхностью разреза легких в виде очагов
серо-красного цвета. Экссудат носит серозный, иногда серозно-
геморрагический характер. В зависимости от возраста больных
имеются некоторые особенности локализации и течения брон->
хопневмонии. Так. у маленьких детей очаги воспаления возникав
ют в сегментах, прилежащих к позвоночнику (II, VI, X), поэтому
пневмония носит название паравертебральной. Она протекает
благоприятно. Напротив, у больных старше 50 лет рассасывание
очагов воспаления происходит относительно медленно.
Осложнения: карнификация фокусов воспаления, их гнойное
расплавление и образование абсцессов, иногда плеврит.
Исход чаще благоприятный. Смерть наступает в тех случаях,
когда очаги воспаления приобретают множественный и распро->
страненный характер. В этой ситуации факторами, определяющи->
ми состояние больного, становятся дыхательная гипоксия и ин->
токсикация.
ХРОНИЧЕСКИЕ НЕСПЕЦИФИЧЕСКИЕ БОЛЕЗНИ ЛЕГКИХ
Группу хронических неспецифических заболеваний легких со->
ставляют несколько болезней дыхательных путей, развитие кото->
рых тесно связано между собой. К ним относятся хронический
бронхит, бронхоэктазы, хронический абсцесс, пневмосклероз и
эмфизема легких.
244
ХРОНИЧЕСКИЙ БРОНХИТ
Этиология. Хронический бронхит развивается как исход затя->
нувшегося острого бронхита. Его причинами могут быть возбуди->
тели инфекций, а также длительное раздражение бронхов физи->
ческими и химическими веществами.
Пато- и морфогенез. Характерно диффузное поражение всего
бронхиального дерева. При этом экссудативное (катарально-сли-
зистое, катарально-гнойное) воспаление с течением времени при->
обретает в основном продуктивный характер. Слизистая оболочка
бронхов при хроническом бронхите гиперемирована, все слои
стенки бронха инфильтрированы лимфоцитами, нейтрофильны-
ми лейкоцитами, макрофагами. Эпителий постепенно слущивает-
ся. железы атрофируются, нередко происходит метаплазия мерца->
тельного эпителия в многослойный плоский. Длительно текущее
воспаление в стенке бронха приводит к дистрофии мышечных
волокон и нервных окончаний, атрофии и гибели эластического
каркаса. В результате этих изменений снижается перистальтика
бронха, и он не может выполнять свою дренажную функцию,
т. е. выводить слизь, экссудат. Слизисто-гнойный экссудат за->
стаивается в бронхах, содержащиеся в нем микробы поддержива->
ют воспаление. Склероз сосудов и нарушение кровоснабжения
бронха обусловливают гипоксию его стенки, что активирует фиб-
робласты, и нарастает склероз. Стенки бронха неравномерно рас->
ширяются, образуя полости в виде мешков или цилиндров -
Рис. 60. Хронический гнойный бронхит с образованием бронхоэктазов,
а — просвет бронха неравномерно расширен; б — некроз и гнойное расплавление
слизистой оболочки; в — инфильтрация стенки бронха лейкоцитами; г — склероз
перибронхиальной ткани.
245
бронхоэктазы. Этому способствуют и кашлевые толчки. В бронхо-
эктазах скапливается гнойный экссудат, постоянно поддержи^
вающий воспаление стенки бронха. Развивается грануляционная
ткань, которая, разрастаясь в виде полипа, может резко суживать
или полностью закрывать просвет бронха, что приводит к ателек->
тазу участка легкого (рис. 60). Кроме того, в воспалительный
процесс вовлекается прилежащая к бронху легочная ткань — воз->
никает очаговая бронхопневмония. Ее хроническое течение спо->
собствует развитию склероза в фокусе воспаления, что также
приводит к растяжению и деформации бронха. Бронхоэктазы ста->
новятся множественными, обычно содержат гнойный экссудат.
Выстилающий их эпителий часто подвергается метаплазии в мно->
гослойный плоский. Обострение воспаления в стенке бронхоэк-
тазов способствует появлению новых очагов пневмонии, а затем
новых полей склероза ткани легких.
ЭМФИЗЕМА ЛЕГКИХ
Пато- и морфогенез. Эмфизема легких нарастает одновремен->
но с прогрессированием склероза и характеризуется увеличением
объема альвеол и содержащегося в них воздуха. Довольно долгое
время она имеет компенсаторное значение, так как возникает во->
круг безвоздушных очагов воспаления, ателектазов, участков
склероза паренхимы легких. С течением времени легочная ткань
в очагах эмфиземы теряет эластические свойства, межальвеоляр->
ные перегородки разрываются или склерозируются, что увеличив
вает общий объем склеротических изменений в легких. Развива->
ется пневмосклероз, который сопровождается повышением арте->
риального давления в малом круге кровообращения. Оно опреде->
ляет постоянное повышение нагрузки на правые отделы сердца, в
результате чего они гипертрофируются и развивается "легочное
сердце".
БРОНХОЭКТАТИЧЕСКАЯ БОЛЕЗНЬ
Бронхоэктатическая болезнь характеризуется сочетанием
бронхоэктазов, пневмосклероза, гипертонии малого круга крово->
обращения и "легочного сердца". Она течет с частыми обостре->
ниями воспаления и соответственно увеличением объема склеро->
за легочной ткани. Постепенно склеротические изменения при->
водят к деформации легких, и тогда говорят о пневлюциррозе.
Осложнения, В динамике развития хронических неспецифиче->
ских болезней легких могут появляться различные осложнения:
• метаплазия эпителия бронхов и бронхоэктазов (нередко да->
ет начало раку бронхов);
• кровотечение из сосудов стенки бронхоэктаза;
• абсцесс легкого;
246
• вторичный амилоидоз, развивающийся на фоне длительно
текущего гнойного воспаления в бронхах и в паренхиме
легких.
Исход. Смерть больных, страдающих хроническими неспецифи->
ческими заболеваниями легких с развитием пневмоцирроза и "ле-i
точного сердца", наступает от хронической легочно-сердечной не-"
достаточности. К смерти могут привести также кровотечение из со->
судов бронхоэктаза, амилоидоз внутренних органов, рак легкого,
развившийся на фоне хронического бронхита или бронхоэктазов.
РАК ЛЕГКОГО
Статистические исследования показывают, что в последние
десятилетия во всем мире быстро увеличивается заболеваемость
раком легкого. Помимо факторов, с которыми связывают вообще
развитие онкологических заболеваний, для возникновения рака
легкого особое значение имеет запыление легких, особенно ньи
лью, содержащей канцерогенные вещества. Чрезвычайно боль->
шую роль в возникновении рака легкого играет курение. Отмече->
но, что среди больных этим заболеванием 90 % составляют ку
рилыцики. В качестве предраковых состояний следует назвать
метаплазию эпителия бронхов при хроническом бронхите и брон-
хоэктазах.
Формы рака легкого
В зависимости от источника роста опухоли выделяют бронхо-
генный и альвеолярный рак. Бронхогенный рак — наиболее частая
форма, при которой опухоль развивается из эпителия бронхов.
Источником альвеолярного рака может служить эпителий альвеол
легких.
В зависимости от локализации опухоли выделяют (рис. 61):
• прикорневой (центральный) рак, исходящий из стволового,
долевого и начальной части сегментарного бронхов;
• периферический рак, исходящий из более мелких ветвей
бронха, бронхиол и альвеолярного эпителия:
• смешанный (массивный) рак.
По отношению к просвету бронха опухоль может расти: эк-
зофитно (в просвет бронха) и эндофитно (в толщу стенки бронха).
В зависимости от морфологических особенностей выделяют:
• плоскоклеточный ороговевающий рак;
• плоскоклеточный неороговевающий рак;
• аденокарциному;
• недифференцированный рак.
Прикорневой (центральный) рак встречается наиболее часто
(наблюдается в 65—70 % всех случаев рака легкого). Возникает в
слизистой оболочке бронха в виде бляшек или узелка. В дальней->
шем опухоль может расти экзо- или эндофитно, и рак приобрета-
247
Рис. 61. Схематическое изображение форм рака легкого,
а, б, в — периферический рак; г, д, е — центральный рак.
ет характер эндобронхиального, разветвленного, узловатого илиузло->
вато-разветвленного. Если он растет в просвет бронха, то вскоре
закупоривает бронх и возникает ателектаз легкого, нередко ос->
ложняющийся пневмонией или абсцессом. В клинической карти->
не в этом случае появляется симптоматика пневмонии. Если рак
растет эндофитно, он прорастает в средостение, перикард и плев->
ру. Гистологически это наиболее часто плоскоклеточный рак без
ороговения или с ороговением. В последнем случае в опухолевой
ткани появляются "раковые жемчужины" — участки атипичного
ороговения. Нередко эта опухоль может иметь строение адено-
карциномы или недифференцированного рака.
Периферический рак. Эта форма рака составляет 25—30 % всех
случаев рака легкого. Опухоль исходит из мелких бронхов, часто
растет экспансивно и не проявляется клинически до тех; пор, пока
не сдавит или не прорастет бронх. В этом случае появл_яются ате->
лектаз легкого и симптомы пневмонии. Нередко периферический
рак прорастает и обсеменяет плевру, возникает серозно-геморраги-
ческий плеврит и экссудат сдавливает легкое. Гистологически в
большинстве случаев периферический рак имеет характер аденока-
рциномы, реже — плоскоклеточного или недифференцированного.
Смешанный (массивный) рак встречается в 2—3 % всех случаев
248
рака легкого. Имеет форму массивного мягкого узла, занимающее
го большую часть легкого. Гистологически такой рак имеет раз-,
личное строение.
Метастазирует рак легкого лимфогенно в перибронхиальные
и бифуркационные лимфатические узлы. Довольно быстро при-i
соединяются гематогенные метастазы в печень, головной мозг, в
позвонки и другие кости, надпочечники.
Смерть больных наступает от метастазов, кахексии или легоч-i
ных осложнений — пневмонии, абсцесса, гангрены легкого, ле-,
точного кровотечения.
Глава 16
БОЛЕЗНИ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА
Пищеварение осуществляется единой физиологической систе-i
мой. Поэтому поражение какого-либо отдела этой системы обу-i
словливает расстройство ее функционирования в целом. Болезни
органов пищеварения выявляются более чем у 5 % населения
планеты.
Этиология патологических процессов, развивающихся в желу->
дочно-кишечном тракте, включает несколько основных факторов.
ФАКТОРЫ, ПОВРЕЖДАЮЩИЕ ОРГАНЫ ПИЩЕВАРЕНИЯ
Физической природы:
• грубая, плохо пережеванная или непережеванная пища;
• инородные тела — пуговицы, монеты, кусочен металла и
т. п.;
• чрезмерно холодная или горячая пища;
• ионизирующие излучения.
Химической природы:
• алкоголь;
• продукты сгорания табака, попадающие в желудочно-ки-i
шейный тракт со слюной;
• лекарственные препараты, например аспирин, антибиоти-i
ки. цитостатики;
• токсичные вещества, проникающие в органы пищеварения с
пищей, — соли тяжелых металлов, токсины грибов и т. п.
Биологической природы:
• микроорганизмы и их токсины;
• гельминты;
• избыток или недостаток витаминов, например витамина С,
группы В, РР.
249
Расстройства механизмов нейрогуморальной регуляции — дефи->
цит или избыток биогенных аминов — серотонина, меланина,
гормонов, простагландинов, пептидов (например, гастрина), из->
быточные или недостаточные эффекты симпатической или пара->
симпатической системы (при неврозах, затянувшихся стресс-ре->
акциях и т. п.).
Патогенные факторы, связанные с поражением других физио->
логических систем, например фибринозный гастроэнтерит и ко->
лит при уремии, развивающейся в исходе почечной недостаточ->
ности.
ПАТОЛОГИЯ ОТДЕЛЬНЫХ ОРГАНОВ ПИЩЕВАРЕНИЯ
НАРУШЕНИЯ ПИЩЕВАРЕНИЯ В ПОЛОСТИ РТА
Основными причинами этой патологии могут быть нарушения
пережевывания пищи в результате:
• воспалительных заболеваний полости рта;
• недостатка зубов;
• травмы челюстей;
• нарушения иннервации жевательной мускулатуры.
Возможные последствия:
• механическое повреждение слизистой оболочки желудка
плохо пережеванной пищей;
• нарушение желудочной секреции и моторики.
НАРУШЕНИЯ ОБРАЗОВАНИЯ И ВЫДЕЛЕНИЯ СЛЮНЫ - САЛИВАЦИИ
Виды:
Гипосаливация вплоть до прекращения образования и выделе->
ния слюны в полость рта.
Последствия:
• недостаточное смачивание и набухание пищевого комка;
• затруднения пережевывания и глотания пищи;
• развитие воспалительных заболеваний полости рта — десен
(гингивит), языка (глоссит), зубов.
Гиперсаливация — повышенное образование и выделение
слюны.
Последствия:
• разведение и ощелачивание желудочного сока избытком
слюны, что снижает его пептическую и бактерицидную ак->
тивность;
• ускорение эвакуации желудочного содержимого в двенадца->
типерстную кишку.
250
БОЛЕЗНИ ПОЛОСТИ РТА
Ангина, или тонзиллит, — заболевание, которое характеризует-"
ся воспалением лимфоидной ткани глотки и небных миндалин.
Причиной развития различных видов ангин являются стрепто-i
кокки, стафилококки, аденовирусы. Важное значение при этом
имеют сенсибилизация организма и охлаждение тела.
Течение ангин может быть острым и хроническим.
В зависимости от особенностей воспаления выделяют несколь->
ко видов острых ангин.
Катаральная ангина характеризуется гиперемией миндалин и
небных дужек, их отеком, серозно-слизистым (катаральным) экс-"
судатом.
Лакунарная ангина, при которой к катаральному экссудату
примешивается значительное количество лейкоцитов и спущен-"
него эпителия. Экссудат накапливается в лакунах и виден на по-"
верхности отечных миндалин в виде желтых пятен.
Фибринозная ангина характеризуется дифтеригическим воспа-"
лением. при котором фибринозная пленка покрывает слизистую
оболочку миндалин. Эта ангина возникает при дифтерии.
Фолликулярная ангина отличается гнойным расплавлением
фолликулов миндалин и их резким отеком.
Флегмонозная ангина, при которой гнойное воспаление неред-"
ко переходит на окружающие ткани. Миндалины отечны, резко
увеличены в размерах, полнокровны.
Некротическая ангина характеризуется некрозом слизистой
оболочки миндалин с образованием язв и кровоизлияний.
Гангренозная ангина может быть осложнением некротической
и проявляется распадом миндалин.
Некротическая и гангренозная ангины возникают при скарла-"
гине и острых лейкозах.
Хроническая ангина развивается в результате неоднократных
рецидивов острой ангины. Для нее характерны гиперплазия и
склероз лимфоидной ткани миндалин, их капсулы, иногда изъ-"
язвления.
Осложнения ангины связаны с переходом воспаления на окру-"
жающие ткани и развитием перитонзиллярного или заглоточного
абсцесса, флегмоны клетчатки зева. Рецидивирующие ангины
способствуют развитию ревматизма и гломерулонефрита.
ПАТОЛОГИЯ ПИЩЕВОДА
Нарушения функций пищевода характеризуются:
• затруднением движения пищи по пищеводу;
• забросом содержимого желудка в пищевод с развитием га-
строэзофагального рефлюкса, для которого характерны орп
рыжка, срыгивание, или регургитация, изжога, аспирация
пищи в дыхательные пути.
251
Отрыжка — неконтролируемое выделение газов или неболь->
шого количества пищи из желудка в пищевод и полость рта.
Срыгивание, или регургитация, — непроизвольный заброс части
желудочного содержимого в полость рта, реже — носа.
Изжога — ощущение жжения в эпигастральной области. Явля->
ется результатом заброса кислого содержимого желудка в пище->
вод.
БОЛЕЗНИ ПИЩЕВОДА
Эзофагит — воспаление слизистой оболочки пищевода. Тече->
ние может быть острым и хроническим.
Причинами острого эзофагита являются действия химических,
термических и механических факторов, а также ряда возбудите->
лей инфекции (дифтерии, скарлатины и др.).
Морфология. Для острого эзофагита характерны различные ви->
ды экссудативного воспаления, в связи с чем он может быть ка~*
таральным, фибринозным, флегмонозным, гангренозным, а также яз~<
венным. Наиболее часто возникают химические ожоги пищевода,
после чего некротизированная слизистая оболочка отделяется в
виде слепка пищевода и не восстанавливается, а в пищеводе об->
разуются рубцы, резко суживающие его просвет.
Причинами хронического эзофагита являются постоянные раз->
дражения пищевода алкоголем, горячей пищей, продуктами куре->
ния табака и другими раздражающими веществами. Он может
развиваться и в результате нарушения кровообращения в пищевод
де при застойных явлениях в нем, обусловленных хронической
сердечной недостаточностью, циррозом печени и портальной ги-
пертензией.
Морфология. При хроническом эзофагите слущивается эпите->
лий пищевода, происходит его метаплазия в ороговевающий мно->
гослойный плоский (лейкоплакия), склероз стенки.
Рак пищевода составляет 11 — 12 % всех случаев заболевания
раком.
Морфогенез. Опухоль развивается обычно в средней трети пи->
щевода и циркулярно прорастает его стенку, сдавливая просвет, —
кольцевидный рак. Нередко заболевание имеет форму раковой язвы
с плотными краями, расположенной вдоль пищевода. Гистологии
чески рак пищевода имеет строение плоскоклеточного рака с
ороговением или без ороговения. Если рак развивается из желез
пищевода, он имеет характер аденокарциномы.
Метастазирует рак пищевода лимфогенным путем в регионар->
ные лимфатические узлы.
Осложнения связаны с прорастанием в окружающие органы —
средостение, трахею, легкие, плевру, при этом могут возникать
гнойные воспалительные процессы в этих органах, от которых и
наступает смерть больных.
252
ПАТОЛОГИЯ ЖЕЛУДКА
Основными функциями желудка является переваривание пи->
щи. которое включает частичное расщепление компонентов пи->
щевого комка. Это происходит под влиянием желудочного сока,
главными компонентами которого являются протеолитические
ферменты — пепсины, а также соляная кислота и слизь. Пепси-i
ны разрыхляют пищу и расщепляют белки. Соляная кислота ак->
тивирует пепсины, вызывает денатурацию и нгбухание белков.
Слизь предупреждает повреждение стенки желудка пищевым
комком и желудочным соком.
Нарушения пищеварения в желудке. В основе этих нарушений
лежат расстройства функций желудка.
Расстройства секреторной функции, которые обусловливают
несоответствие уровня секреции различных компонентов желу-i
дочного сока потребностям в них для норматьного пищева-i
рения:
• нарушение динамики секреции желудочного сока во вре->
мени;
• увеличение, уменьшение объема желудочного сока или его
отсутствие:
• нарушение образования соляной кислоты с повышением, по->
нижением или отсутствием кислотности желудочного сока;
• увеличение, снижение или прекращение образования и сек->
рении пепсина;
• ахилия — полное прекращение секреции в желудке. Возни-п
кает при атрофическом гастрите, раке желухка, заболевание
ях эндокринной системы. При отсутствии соляной кислоты
уменьшается секреторная активность поджелудочной желе-1
зы, ускоряется эвакуация пищи из желудса, усиливаются
процессы гниения пищи в кишечнике.
Нарушения .моторной функции
Вцпщ этих нарушений:
• нарушения тонуса мышц стенки желудка в виде его избы-1
точного повышения (гипертонус), чрезмерного снижения
(гипотонус) или отсутствия (атония);
• расстройства тонуса сфинктеров желудка в виде его сниже-i
ния, что обусловливает зияние кардиального или пилориче-
ского сфинктера, либо в виде повышения тонуса и спазма
мышц сфинктеров, приводящего к кардиоспазму или пило-
роспазму;
• нарушения перистальтики стенки желудка: ускорение ее —
гиперкинез, замедление — гипокинез;
• ускорение или замедление эвакуации пищи из желудка, что
приводит к:
— синдрому быстрого насыщения при снижении тонуса и мо->
торики антрального отдела желудка;
— изжоге — жжению в области нижней части пищевода в pe-i
зультате снижения тонуса кардиального сфинктера желудка, ниж-
253
него сфинктера пищевода и заброса в него кислого желудочного
содержимого;
— рвоте — непроизвольному рефлекторному акту, характери->
зующемуся выбросом содержимого желудка наружу через пище-'
вод, глотку и полость рта.
БОЛЕЗНИ ЖЕЛУДКА
Основными заболеваниями желудка являются гастрит, язвсн-i
ная болезнь и рак.
Гастрит — воспаление слизистой оболочки желудка. Выделяют
острый и хронический гастрит, однако эти понятия означают не
столько время течения процесса, сколько морфологические изме-i
нения в желудке.
Острый гастрит
Причинили острого гастрита могут быть:
• алиментарные факторы — недоброкачественная, грубая или
острая пища;
• химические раздражители — алкоголь, кислоты, щелочи,
некоторые лекарственные вещества;
• инфекционные агенты — Helicobacter pylori, стрептококки,
стафилококки, сальмонеллы и др.;
• острые расстройства кровообращения при шоке, стрессе,
сердечной недостаточности и др.
Классификация острого гастрита
По локализации:
• диффузный;
• очаговый (фундальный, антральный, пилородуоденальный).
По характеру воспаления:
• катаральный гастрит, который характеризуется гипе-i
ремией и утолщением слизистой оболочки, гиперсекрецией
слизи, иногда эрозиями. В этом случае говорят об эрозивном
гастрите. Микроскопически наблюдаются дистрофия и слу-
щивание поверхностного эпителия, серозно-слизистый экс->
судат, сосудов, отек, диапедезные кровоизлияния;
• фибринозный гастрит отличается тем, что на по-"
верхности утолщенной слизистой оболочки образуется фиб->
ринозная пленка серо-желтого цвета. В зависимости от глу—>
бины некроза слизистой оболочки фибринозный гастрит
может быть крупозным или дифтеритическим;
• гнойный (флегмонозный) гастрит — редкая
форма острого гастрита, которая осложняет травмы, язвы
или изъязвленный рак желудка. Характеризуется резким
утолщением стенки, сглаживанием и огрубением складок,
гнойными наложениями на слизистой оболочке. Микроскоп
пически определяются диффузная лейкоцитарная инфильт-i
рация всех слоев стенки желудка, некроз и кровоизлияния в
слизистой оболочке;
254
• некротический (коррозиеный) гастрит—ред-<
кая форма, возникает при химических ожогах слизистой
оболочки желудка и характеризуется ее некрозом. При огп
торжении некротических масс образуются язвы.
Осложнениями эрозивного и некротического гастрита могут
быть кровотечения, перфорация стенки желудка. При флегмоноз-
ном гастрите возникают медиастинит, поддиафрагмальный абс->
цесс, абсцесс печени, гнойный плеврит.
Исходы. Катаральный гастрит обычно заканчивается выздоров-i
лением; при воспалении, вызванном инфекцией, возможен пере-,
ход в хроническую форму.
Хронический гастрит — заболевание, которое характеризуется
хроническим воспалением слизистой оболочки желудка, наруше-,
нием регенерации и морфофункциональной перестройкой эпите-i
лия с развитием атрофии желез и секреторной недостаточности,
лежащими в основе расстройств пищеварения. Ведущим призна-i
ком хронического гастрита является дисрегенерация — нарушение
обновленияклеток эпителия Хронический гастрит составляет 80—
85 % всех болезней желудка.
Этиология хронического гастрита связана с длительным дейст-i
вием экзо- и эндогенных факторов:
• инфекций, в первую очередь Helicobacter pylori, на долю
которого приходится 70—90 % всех случаев хронического
гастрита;
• химических (алкоголь, аутоинтоксикации и др.);
• нейроэндокринных и др.
Классификация хронического гастрита:
• хронический поверхностный гасхрит;
• хронический атрофический гастрит;
• хронический хеликобактерный гастрит;
• хронический аутоиммунный гастрит;
• особые формы хронического гастрита — хи-,
мический, радиационный, лимфоцитарный и др.
Патогенез заболевания при различных видах хронического га-,
стрита неодинаков.
Морфогенез. При хроническом поверхностном гастрите отсуг-i
ствует атрофия слизистой оболочки, желудочные ямки выражены
плохо, железы не изменены, характерна диффузная лимфоэози-
нофильная инфильтрация, незначительный фиброз стромы.
Хронический атрофический гастрит характеризуется низким
покровно-ямочным эпителием, редукцией желудочных ямок,
уменьшением количества и размеров желез, дистрофическими и
нередко метапластическими изменениями железистого эпителия,
диффузной лимфоэозинофильной и гистиоцитарной инфильтра-1
цией, фиброзом стромы.
П1)и хроническом хеликобактерном гастрите ведущую роль иг-,
рает Helicobacter pylori, который поражает преимущественно ан-
тральный отдел желудка. Возбудитель попадает в желудок через
рот и располагается под слоем слизи, защищающей его от дейст-
255
вия желудочного сока. Основным свойством бактерии является
синтез уреазы — фермента, расщепляющего мочевину с образовав
нием аммиака. Аммиак сдвигает pH в щелочную сторону и пару-!
шает регуляцию секреции соляной кислоты. Несмотря на возни-!
кающую гипергастринемию, происходит стимуляция секреции
НС1, что приводит к гиперацидному синдрому. Морфологическая
картина характеризуется атрофией и нарушением созревания по-
кровно-ямочного и железистого эпителия, выраженной лимфо-
плазмоцитарной и эозинофильной инфильтрацией слизистой
оболочки и собственной пластинки с образованием лимфоидных
фолликулов.
Хронический аутоиммунный гастрит. Его патогенез обусловлен
образованием антител к париетальным клеткам желез фундально-
го отдела желудка, эндокринным клеткам слизистой оболочки, а
также к гастромукопротеину (внутреннему фактору), которые ста->
новятся аутоантигенами. В фундальном отделе желудка отмечает-!
ся выраженная инфильтрация В-лимфоцитами и Т-хелперами,
резко возрастает количество IgG-плазмоцитов. Быстро прогресси-!
руют атрофические изменения слизистой оболочки, особенно у
больных старше 50 лет.
Среди особых форм хронических гастритов наибольшее значе-!
ние имеет гипертрофический гастрит, который характеризуется
образованием гигантских складок слизистой оболочки, похожих
на извилины головного мозга. Толщина слизистой оболочки дос->
тигает 5—6 см. Ямки длинные, заполнены слизью. Эпителий же->
лез уплощен, как правило, развивается его кишечная метаплазия.
В железах часто отсутствуют главные и париетальные клетки, что
приводит к снижению секреции соляной кислоты.
Осложнения. Атрофический и гипертрофический гастриты мо->
гут осложняться образованием полипов, иногда язв. Кроме того,
атрофический и хеликобактерный гастриты являются пре дракой
выми процессами.
Исход поверхностного и хеликобактерного гастритов при соот->
ветствующем лечении благоприятный. Терапия других форм хро->
нических гастритов приводит лишь к замедлению их развития.
Язвенная болезнь — хроническое заболевание, клиническим и
морфологическим выражением которого является рецидивирую-!
щая язва желудка или двенадцатиперстной кишки. Поэтому раз->
дичают язвенную болезнь желудка и язвенную болезнь двенадца-!
типерстной кишки, которые несколько отличаются друг от друга
в основном по патогенезу и исходам. Язвенной болезнью страда-!
ют преимущественно мужчины в возрасте 50 лет и старше. Язвы
двенадцатиперстной кишки встречаются в 3 раза чаще жслу-!
дочных.
Этиология язвенной болезни связана в основном с Helico-
bacter pylori и с общими изменениями, возникающие в организме
и способствующими повреждающему действию этого микроорга-!
низма. Определенные штаммы Helicobacter pylori обладают высо->
кой адгезией к клеткам поверхностного эпителия и вызывают вы-
256
раженную нейтрофильную инфильтрацию слизистой оболочки,
что приводит к ее повреждению. Кроме того, образуемая бакте->
риями уреаза синтезирует аммиак, который высокотоксичен для
эпителия слизистой оболочки и также вызывает ее деструкцию.
При этом нарушаются микроциркуляция и трофика тканей в об->
ласти некротических изменений эпителиоцитов. Помимо этого,
указанные бактерии способствуют резкому повышгнию образовав
ния гастрина в крови и соляной кислоты в желудке.
Общие изменения, возникающие в организме я способствую-"
щие повреждающему действию Helicobacter pylori:
• психоэмоциональные перенапряжения, которым подверга-"
ется современный человек (стрессовые состояния нарушают
координирующие влияния коры головного мозга на под-"
корковые центры);
• нарушения эндокринных влияний в результаге расстройства
деятельности гипоталамо-гипофизарной и гипофизарно-ад-
реналовой систем;
• усиление влияния блуждающих нервов, что совместно с из-"
бытком кортикостероидов повышает активность кислотно-
пептического фактора желудочного сока и моторную функ->
цию желудка и двенадцатиперстной кишки;
• снижение эффективности образования слизистого барьера;
• нарушения микроциркуляции и нарастание гипоксии.
Среди других факторов, способствующих образованию язвы,
важное значение имеют лекарства типа аспирина, алкоголь. куре->
ние, которые не только сами повреждают слизистую оболочку, но
и влияют на секрецию соляной кислоты и гастрина, на микро-"
циркуляцию и трофику желудка.
Морфогенез. Основным выражением язвенной болезни являет-"
ся хроническая рецидивирующая язва, которая в своем развитии
проходит стадии эрозии и острой язвы. Наиболее частая локали-"
зация язвы желудка — малая кривизна в антральном или пилори-
ческом отделе, а также в теле желудка, в области перехода в ан-
тральный отдел. Это объясняется тем, что малая кривизна, как
"пищевая дорожка", легко травмируется, ее слизистая оболочка
выделяет наиболее активный сок, эрозии и острые язвы этой об-"
ласти плохо эпителизируются. Под влиянием желудочного сока
некроз захватывает не только слизистую оболочку, но и распро-"
страняется на подлежащие слои стенки желудка и эрозия превра-"
щается в острую пептическую язву. Постепенно острая язва ста-"
новится хронической и может достигать 5—6 см в диаметре, про-"
пикая на различную глубину (рис. 62). Края хронической язвы
приподняты в виде валиков, плотные. Край язвы, обращенный ко
входу в желудок, подрытый, край, обращенный к привратнику —
пологий. Дном язвы служат рубцовая соединительная ткань и об-"
рывки мышечной ткани. Стенки сосудов толстые, склерозирован-
ные, просветы их сужены.
При обострении язвенной болезни в дне язвы появляется
гнойно-некротический экссудат, в окружающей рубцовой ткани
257
Рис. 62. Хроническая язва желудка.
и в склерозированных стенках сосудов — фибриноидный некроз.
За счет нарастающего некроза язва углубляется и расширяется, а
в результате разъедания стенки сосудов может возникнуть их раз->
рыв и кровотечение. Постепенно на месте некротизированных
тканей развивается грануляционная ткань, которая созревает в
грубую соединительную ткань. Края язвы становятся очень плот-i
ными, омозолелыми, в стенках и в дне язвы выражены разраста->
ние соединительной ткани, склероз сосудов, что нарушает крово->
снабжение стенки желудка, а также образование слизистого барь->
ера. Такая язва называется каллезной.
При язвенной болезни двенадцатиперстной кишки язва обычно
располагается в луковице и лишь иногда локализуется ниже ее.
Множественные язвы двенадцатиперстной кишки встречаются не
очень часто и располагаются на передней и задней стенках луко->
вицы друг против друга — "целующиеся язвы".
При заживлении язвы дефект ткани возмещается образовани->
ем рубца, а на поверхности разрастается измененный эпителий, в
области бывшей язвы железы отсутствуют.
Осложнения язвенной болезни. К их числу относятся кровотече->
ние. перфорация, пенетрация. флегмона желудка, грубый рубец,
хлоргидропеническая уремия.
Кровотечение из некротизированного сосуда сопровождается
рвотой "кофейной гущей" из-за образования в желудке соляно->
кислого гематина (см. главу 1). Каловые массы становятся дегте->
образными из-за большого содержания в них крови. Кровяни->
стый стул носит название "мелена ".
258
Перфорация, или прободение, стенки желудка или двенадцати-!
перстной кишки приводит к острому разлитому перитониту —
гнойно-фибринозному воспалению брюшины.
Пенетрация — осложнение, при котором перфоративное отвер->
стие открывается в том месте, где в результате воспаления про->
изошло спаяние желудка с рядом расположенными органами —
поджелудочной железой, поперечной ободочной кишкой, печенью,
желчным пузырем. Пенетрация сопровождается перевариванием
желудочным соком тканей прилежащего органа и его воспалением.
Грубый рубец может образовываться на месге язвы при ее за->
живлении.
Хлор гидропоническая уремия сопровождается судорогами, развит
вается в том случае, если рубец резко деформирует желудок, при-!
вратник, двенадцатиперстную кишку, почти полностью закрывая
выход из желудка. В этом случае желудок растягивается пищевы-!
ми массами, у больных возникает неукротимая рвота, при кото->
рой организм теряет хлориды. Каллезная язва желудка может
стать источником развития рака.
Рак желудка наблюдается более чем в 60 % всех опухолевых
заболеваний. Смертность при этом составляет 5 % от общей
смертности населения. Эта болезнь чаще возникает у людей в
возрасте 40—70 лет; мужчины болеют примерно в 2 раза чаще
женщин. Развитию рака желудка обычно предшествуют предра->
ковые заболевания, такие как полипоз желудка, хронический га->
стрит, хроническая язва желудка.
Формы рака желудка в зависимости от внешнего вида и харак->
тера роста:
• бляшковидный имеет форму небольшой плотной, белесова->
той бляшки, располагается в слизистом и подслизистом
слоях (рис. 63, а). Течет бессимптомно, ему обычно пред->
шествует carcinoma in situ. Растет преимущественно экзо-
фитно и предшествует полипозному раку;
• полиполный имеет вид небольшого узла на ножке (рис. 63,
б), растет преимущественно экзофитно. Иногда развивается
из полипа (малигнизированный полип);
• грибовидный, или фунгозный, представляет собой бугристый
узел на широком основании (рис. 63, в). Грибовидный рак
— это дальнейшее развитие полипозного, так как они име->
ют одинаковое гистологическое строение:
• изъязвленные формы рака встречаются в половине всех ра->
ков желудка:
— первично-изъязвленный рак (рис. 64, а) развивается при изъ->
язвлении бляшковидного рака, гистологически обычно низко-
дифференцированный; протекает очень злокачественно, дает об->
ширные метастазы. Клинически очень похож на язвенную бо->
лезнь желудка, в чем состоит коварство этого рака;
— блюдцеобразный рак, или рак-язва, возникает при некрозе и
изъязвлении полипозного или грибовидного рака и при этом на->
поминает блюдце (рис. 64, б);
259
Рис. 63. Формы рака желудка.
а — бляшковидный, б — полипозный, в — грибовидный, г — диффузный.
— язва-рак развивается из хронической язвы (рис. 64, в);
— диффузный, или тотальный, рак растет преимущественно
эндофитно (рис. 64, г), поражая все отделы желудка и все слои
его стенки, которые становятся малоподвижными, складки тол->
стые, неравномерные, полость желудка уменьшается, напоминая
трубку.
По гистологическому строению выделяют:
аденокарцинолу, или железистый, рак, который имеет не->
сколько вариантов строения и является относительно дифферент
цированной опухолью (см. главу 10). Обычно составляет структур
ру бляшковидного, полипозного и фундального рака;
Недифференцированные формы рака:
• солидный, представляющий собой плотные скопления ати-
пичных клеток с хорошо развитой стромой;
• слизистый, или перстневидно-клеточный, рак — весьма зло-
качественная опухоль, клетки которой продуцируют ати-i
пичную слизь, которая отодвигает ядро на периферию клет->
ки и становится при этом похожей на перстень;
260
Рис. 64. Формы изъязвленного
рака желудка.
а — первично-язвенный, б — блюд-
цеобразный, в — язва-рак.
• скирр — опухоль С б)ОЛЬ-1
шим количеством стро-
мы и относительно не->
большим количеством
резко атипичных кле-i
ток, часто с ослизнени-
ем. Рак отличается вы-п
сокой степенью злока-п
чественности.
Редкие формы рака описа->
ны в специальных руково->
дствах. К ним относятся плос~>
коклеточный и железисто-
плоскоклеточный рак.
Метастазирование рака же->
лудка осуществляется преиму-i
щественно лимфогенным ну
тем, прежде всего в регионар-i
ные лимфатические узлы, а по
мере их разрушения появляют-i
ся отдаленные метастазы в раз->
личные органы. При раке же->
лудка может происходить рет~>
роградное лимфогенное метаста
зирование, когда эмбол из рако->
вых клеток продвигается про-"
тив тока лимфы и, попадая в
определенные органы, дает ме->
тастазы, носящие имя описав-i
ших их авторов:
• рак Крукенберга — рер->
роградные лимфогенные
метастазы в яичники;
• метастаз Шнитцлера —
ретроградный метастаз в
параректальную клет->
чатку;
• метастаз Вирхова — ретроградный метастаз в левые над-i
ключичные лимфатические узлы.
Наличие ретроградных метастазов говорит о запущенности
опухолевого процесса. Кроме того, рак Крукенберга и метастаз
Шнитцлера могут быть приняты за самостоятельные опухоли co-i
ответственно яичников или прямой кишки.
Гематогенные метастазы обычно развиваются после лимфоген-
261
ных и поражают печень, реже — легкие, почки, надпочечники,
поджелудочную железу, кости.
Осложнения рака желудка:
• кровотечение при некрозе и изъязвлении опухоли;
• воспаление стенки желудка с развитием его флегмоны;
• прорастание опухоли в близлежащие органы — поджелудоч->
ную железу, поперечную ободочную кишку, большой и ма->
лый сальники, брюшину с развитием соответствующей сим->
птоматики.
Исход рака желудка при рано проведенном и радикальном
оперативном лечении может быть благоприятным у большинства
больных. В остальных случаях удается только продлить им жизнь.
ПАТОЛОГИЯ КИШЕЧНИКА
Расстройства пищеварения в кишечнике связаны с нарушение
ем его основных функций — переваривающей, всасывательной,
моторной, барьерной.
Расстройства переваривающей функции кишечника обусловли->
вают:
• нарушение полостного пищеварения, т. е. переваривания в
полости кишечника;
• расстройства пристеночного пищеварения, которое проте->
кает на поверхности мембран микроворсинок с участием
гидролитических ферментов.
Расстройства всасывательной функции кишечника, основными
причинами которого могут быть:
• дефекты полостного и мембранного пищеварения;
• ускорение эвакуации кишечного содержимого, например
при поносах;
• атрофия ворсинок слизистой оболочки кишечника после
хронических энтеритов и колитов;
• резекция большого фрагмента кишечника, например при
кишечной непроходимости;
• расстройства крово- и лимфообращения в стенке кишечни->
ка при атеросклерозе брыжеечных и кишечных артерий, за->
вороте кишки и т. п.
Нарушение .моторной функции кишечника. В норме кишечник
обеспечивает перемешивание и перемещение пищи от двенадца->
типерстной кишки к прямой. Двигательная функция кишечника
может расстраиваться в разной степени и форме.
Понос, или диарея, — учащенный (более 3 раз в сутки) стул
жидкой консистенции, сочетающийся с усилением моторики ки->
шечника.
Запор — длительная задержка стула или затруднение опорож->
нения кишечника. Наблюдается у 25—30 % людей, особенно в
возрасте после 70 лет.
Нарушение барьерно-защитной функции кишечника. В норме
262
стенка кишечника является механическим и физико-химическим
защитным барьером для кишечной флоры и токсичных веществ,
образующихся при переваривании пищи, выделяемых микроба^
ми. попадающих в кишечник через рот. и т. и. Микроворсинки и
гликокаликс образуют микропористую структуру, непроницаемую
для микробов, которая обеспечивает стерилизацию переваренных
продуктов питания при всасывании их в тонком кишечнике.
В условиях патологии нарушение структуры и функции энте-
роцитов, их микроворсинок, а также ферментов может разрушить
защитный барьер. Это в свою очередь приводит к инфицировав
нию организма, развитию интоксикации, расстройству процесса
пищеварения и жизнедеятельности организма в целом.
БОЛЕЗНИ КИШЕЧНИКА
Среди заболеваний кишечника основное клиническое значе->
ние имеют воспалительные и опухолевые процессы. Воспаление
тонкой кишки называется энтеритом, толстой кишки — колитом,
всех отделов кишки — энтероколитом.
Энтерит. В зависимости от локализации процесса в тонкой
кишке выделяют:
• воспаление двенадцатиперстной кишки — дуоденит;
• воспаление тощей кишки — еюнит;
• воспаление подвздошной кишки — илеит.
Течение энтерита может быть острым и хроническим.
Острый энтерит. Его этиология:
• инфекции (бутулизм, сальмонеллез, холера, брюшной тиф,
вирусные инфекции и т. и.);
• отравления ядами, ядовитыми грибами и т. и.
Виды и морфология острого энтерита наиболее часто развива-ч
ется катаральный энтерит. Слизистая и подслизистая оболочки
пропитываются слизисто-серозным экссудатом. При этом проис-
ходят дистрофия эпителия и его слущивание, увеличивается ко->
личество бокаловидных клеток, продуцирующих слизь, иногда
появляются эрозии.
Фибринозный энтерит сопровождается некрозом слизистой
оболочки (крупозный энтерит) или слизистого, подслизистого и
мышечного слоев стенки (дифгеритический энтерит); при оттор-i
жении фибринозного экссудата в кишке образуются язвы.
Гнойный энтерит встречается реже и характеризуется пропиты^
ванием стенки кишки гнойным экссудатом.
Некротически-язвенный энтерит, при котором некрозу и изъ->
язвлению подвергаются либо только солитарные фолликулы (при
брюшном тифе), либо язвенные дефекты слизистой оболочки
имеют распространенный характер (при гриппе, сепсисе).
Вне зависимости от характера воспаления отмечается гипер->
плазия лимфатического аппарата кишки и лимфатических узлов
брыжейки.
263
Исход. Обычно острый энтерит заканчивается восстановление
ем слизистой оболочки кишки после выздоровления от основное
го заболевания, но может принять хроническое течение.
Хронический энтерит. Этиология заболевания — инфекции,
интоксикации, применение некоторых лекарственных средств,
длительные погрешности в пище, нарушения обмена веществ.
Морфогенез. В основе хронического энтерита лежит наруше->
ние процессов регенерации эпителия. Вначале развивается хро->
нический энтерит без атрофии слизистой оболочки. Воспалитель->
ный инфильтрат расположен в слизистой и подслизистой оболоч->
ках, а иногда достигает мышечного слоя. Основные изменения
развиваются в ворсинках — в них выражена вакуольная дистро->
фия, они укорачиваются, спаиваются между собой, в них снижав
ется ферментативная активность. Постепенно энтерит без атро-i
фии переходит в хронический атрофический энтерит, который
является следующей стадией хронического энтерита. Она харак->
теризуется еще большей деформацией, укорочением, вакуольной
дистрофией ворсинок, кистозным расширением крипт. Слизистая
оболочка выглядит атрофичной, ферментативная активность тии
телия еще больше снижается, а иногда извращается, что препят-i
ствует пристеночному пищеварению.
Осложнения тяжелого хронического энтерита — анемия, ави->
таминоз. остеопороз.
Колит — воспаление толстой кишки, которое может развит
ваться в каком-либо одном ее отделе: тифлит, трансверзит, сиг-
моидит, проктит.
По течению колит может быть острым и хроническим.
Острый колит. Этиология заболевания:
• инфекции (дизентерия, брюшной тиф, туберкулез и др.);
• интоксикации (уремия, отравление сулемой или лекарств
венными средствами и т. п.).
Виды и .морфология острого колита:
• катаральный колит, при котором воспаление распространяв
ется на слизистую и подслизистую оболочки, в серозном
экссудате много слизи;
• фибринозный колит, возникающий при дизентерии, может
быть крупозным и дифтеритическим;
• флегмонозный колит характеризуется гнойным экссудатом,
деструктивными изменениями стенки кишки, тяжелой ин->
токсикацией;
• некротический колит, при котором омертвение ткани рас->
пространяется на слизистый и подслизистый слои кишки;
• язвенный колит, возникающий при отторжении некротиче->
ских масс, после чего образуются язвы, достигающие ино->
гда серозной оболочки кишки.
Осложнения:
• кровотечения, особенно из язв;
• перфорация язвы с развитием перитонита;
• парапроктит — воспаление клетчатки вокруг прямой киш-
264
ки, нередко сопровождается образованием параректальных
свищей.
Исход. Острый колит обычно проходит при выздоровлении от
основного заболевания.
Хронический колит. Морфогенез. По механизму развития хро->
нический колит также является в основном процессом, развиваю
щимся в результате нарушения регенерации эпителия, но при
этом выражены и воспалительные изменения. Поэтому кишка
выглядит красной, гиперемированной, с кровоизлияниями, отме->
чаются слущивание эпителия, увеличение количества бокаловид->
пых клеток, укорочение крипт. Лимфоциты, эозинофилы, плаз->
матические клетки, нейтрофильные лейкоциты инфильтрируют
стенку кишки вплоть до мышечного слоя. Первоначально возни->
кающий колит без атрофии слизистой оболочки постепенно сме->
няется атрофическим колитом и заканчивается склерозом слизи->
стой оболочки, что приводит к прекращению ее функции. Хро->
нический колит может сопровождаться нарушением минерально^
го обмена, изредка возникает авитаминоз.
Неспецифический язвенный колит — заболевание, причина ко->
торого не выяснена. Чаще болеют молодые женщины. Считают,
что в возникновении этого заболевания ведущую роль играет ал->
лергия. связанная с кишечной флорой и аутоиммунизацией. Бо->
лезнь течет остро и хронически.
Острый иеснсцифический язвенный колит характеризуется по->
ражением отдельных участков либо всей толстой кишки. Веду-i
щим признаком является воспаление стенки кишки с образовав
нием очагов некроза слизистой оболочки и множественных язв
(рис. 65). При этом в язвах сохраняются островки слизистой обо->
лочки, напоминающие полипы. Язвы проникают в мышечный
слой, где наблюдаются фибриноидные изменения интерстициаль-
ной ткани, стенок сосудов и кровоизлияния. В части язв избы->
точно разрастаются грануляционная ткань и покровный эпите->
лий, образуя полиповидные выросты. В стенке кишки имеется
диффузный воспалительный инфильтрат.
Осложнения. При остром течении заболевания возможны пер->
форация стенки кишки в области язв и кровотечения.
Хронический неспецифический язвенный колит характеризуется
продуктивной воспалительной реакцией и склеротическими из->
менениями стенки кишки. Происходит рубцевание язв, но рубцы
почти не покрываются эпителием, который разрастается вокруг
рубцов, образуя псевдополипы. Стенка кишки становится толстой,
теряет эластичность, просвет кишки диффузно или сегментарно
суживается. В криптах нередко развиваются абсцессы (крипт-абс-
цессы). Сосуды склерозируются, просветы их уменьшаются или
полностью зарастают, что поддерживает гипоксическое состояние
тканей кишечника.
Аппендицит — воспаление червеобразного отростка слепой киш->
ки. Это широко распространенное заболевание неясной этиологии.
По течению аппендицит может быть острым и хроническим.
265
Рис. 65. Неспецифический язвенный колит. Множественные язвы и кро->
воизлияния в стенке кишки.
Острый аппендицит имеет следующие морфологические фор->
мы. которые являются и фазами воспаления:
• простой;
• поверхностный;
• деструктивный, который имеет несколько стадий:
— флегмонозный;
— флегмонозно-язвенный.
• гангренозный.
Морфогенез. В течение нескольких часов от начала приступа
возникает простой . для которого характерны нарушения крово->
обращения в стенке отростка — стаз в капиллярах, сосудов, отек,
иногда периваскулярные кровоизлияния. Затем развивается се->
розное воспаление и появляется участок деструкции слизистой
оболочки — первичный аффект. Он знаменует развитие острого
поверхностного а. Отросток набухает, становится тусклым, сосуды
оболочки полнокровны. К концу суток развивается деструктив-'
ный , который имеет несколько стадий. Воспаление приобретает
гнойный характер, экссудат диффузно инфильтрирует всю тол->
щину стенки отростка. Такой аппендицит называется флегмоноз-
ным (рис. 66). Если при этом происходит изъязвление слизистой
266
Рис. 66. Флегмонозный аппендицит.
а — гнойный экссудат диффузно пропитывает все слои стенки червеобразного от-i
ростка. Слизистая оболочка некротизирована; б — то же, большое увеличение.
267
б
Рис. 67. Рак толстой кишки.
а — полипозный, б — полипозный с выраженными вторичными изменениями
(некроз, воспаление); в — грибовидный с изъязвлением; г — циркулярный.
оболочки, говорят о флегмонозно-язвенном аппендиците. Иногда
гнойное воспаление распространяется на брыжейку отростка и на
стенку аппендикулярной артерии, что ведет к ее тромбозу. В этом
случае развивается гангренозный аппендицит: отросток утолщен,
268
грязно-зеленого цвета, покрыт гнойно-фибринозными наложе-"
ниями, в просвете его имеется гной.
Осложнения острого аппендицита. Наиболее часто возникает
перфорация червеобразного отростка и развивается перитонит.
При гангренозном аппендиците может произойти самоампутация
отростка и также развивается перитонит. Если воспаление рас->
пространяется на окружающие отросток ткани, иногда развивает-"
ся гнойный тромбофлебит сосудов брыжейки, который распро->
страняется на ветви воротной вены — пипефлебит В таких случае
ях возможны тромбобактериальная эмболия разветвлений вены и
образование пилефлебитических абсцессов печени.
Хронический аппендицит возникает после острого аппендицита
и характеризуется преимущественно склеротическими и атрофи-
ческими изменениями в стенке отростка. Однако на этом фоне
могут возникать обострения заболевания с развитием флегмоны и
даже гангрены червеобразного отростка.
Рак кишечника развивается как в тонкой, так и в толстой киш-"
ке, особенно часто в прямой и сигмовидной кишках (рис. 67). В
двенадцатиперстной кишке он встречается лишь в виде аденокар-
циномы или недифференцированного рака дуоденального сосоч->
ка. и в таком случае одним из первых проявлений этого рака яв->
ляется подпеченочная желтуха (см. главу 17).
Предраковые заболевания:
• язвенный колит;
• полипоз;
• свищи прямой кишки.
По внешнему виду и характеру роста различают:
экзофитный рак:
• полипозный;
• грибовидный;
• блюдцеобразный;
• раковые язвы.
эндофитный рак:
• диффузно-инфильтрирующий рак, при котором опухоль
циркулярно охватывает кишку на том или ином протяже-"
НИИ.
Гистологически экзофитно растущие раковые опухоли обычно
более дифференцированы, имеют строение папиллярной или ту-
булярной аденокарциномы. В эндофитно растущих опухолях рак
чаще имеет строение солидного или фиброзного (скирр).
Метастазирование. Рак кишки метастазирует лимфогенным
путем в регионарные лимфатические узлы, но иногда гематоген-
но, обычно в печень.
269
Глава 17
БОЛЕЗНИ ПЕЧЕНИ, ЖЕЛЧНОГО ПУЗЫРЯ
И ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
Печень — один из основных органов, обеспечивающих гомео-
стаз организма путем участия в реализации большинства его ме-
таболических процессов. К ее наиболее значительным функциям
относятся обмен веществ, участие в пищеварении, дезинтоксика-
ция токсичных веществ, поступающих из желудочно-кишечного
тракта, а также попадающих в организм извне, участие в процес-
се кроветворения и реакциях системы иммунобиологического
надзора.
Печень участвует в обмене:
• белков — гепатоциты синтезируют все альбумины, Уз
а-глобулинов, половину О=В-глобулинов;
• липидов и липопротеинов — в гепатоцитах образуются ли-
попротеины низкой и высокой плотности, холестерин и ке-
тоновые тела;
• углеводов — в клетках печени протекают гликогенолиз,
гликогенез, глюконеогенез;
• витаминов А, группы В, С, D, К, РР, фолиевой кислоты;
• минеральных веществ — железа, меди, хрома и др.;
• желчных кислот.
Участие печени в пищеварении осуществляется путем образо-
вания желчных кислот, способствующих эмульгации, расщепле-
нию и всасыванию жиров, витаминов A, D, Е, К, а также актива-
ции липаз.
ПАТОЛОГИЯ ПЕЧЕНИ
Патология печени наиболее ярко проявляется в развитии пе-
ченочной недостаточности и желтухи, которые являются исходом
или осложнением многих болезней печени.
Печеночная недостаточность — состояние, характеризующееся
стойким снижением или полным выпадением одной или не-
скольких функций печени, что приводит к нарушению жизнедея-
тельности организма.
По течению различают:
• острую печеночную недостаточность, развивающуюся в те-
чение нескольких часов или суток;
• хроническую печеночную недостаточность, которая форми-
руется в течение нескольких месяцев или лет.
Причины развития недостаточности печени:
• дистрофии печени различного генеза;
• гепатиты — воспаление печени, вызванное вирусами, мик-
робами, токсинами;
270
• циррозы печени — хронически протекающие патологиче-
ские процессы в печени, характеризующиеся прогресси-
рующим повреждением и гибелью гепатоцитов и развитием
соединительной ткани, замещающей паренхиму;
• паразитарные поражения, например альвеококкоз, эхино-
коккоз ит. п.;
• опухоли печени;
• нарушения кровообращения в печени, особенно сопровож-
дающиеся развитием портальной гипертензии — стойкого
повышения кровяного давления в сосудах системы ворот-
ной вены выше 6 мм рт. ст.
Проявления печеночной недостаточности:
• расстройства обмена веществ — белков, липидов, углево-
дов, витаминов, минеральных веществ;
• нарушение функций печени — дезинтоксикационной, анти-
микробной, кроветворной, желчеобразования и желчевыде-
ления.
Финалом прогрессирующей печеночной недостаточности яв-
ляется печеночная кома, которая характеризуется:
• утратой сознания;
• подавлением или значительным снижением выраженности
рефлексов;
• расстройствами жизнедеятельности организма, включая на-
рушения дыхания и кровообращения.
Желтуха — синдром, характеризующийся избыточным содер-
жанием билирубина в крови и интерстициальной жидкости, в
связи с чем происходит желтушное окрашивание кожи, склер,
слизистых оболочек и мочи. Многие формы патологии печени
сопровождаются желтухой.
Вцды желтух: печеночная (или паренхиматозная): надпеченоч-
ная, или гемолитическая; и подпеченочная.
Печеночная, или паренхиматозная, желтуха может быть вы-
звана первичным повреждением гепатоцитов инфекционными
агентами (вирусами, бактериями, плазмодиями и др.) или гепато-
токсическими факторами (например, высокими дозами этанола,
токсинами грибов, гепатотропными ядами и т. п.), а также цир-
розом печени. Возникающие некротические изменения ткани пе-
чени сопровождаются расстройством желчеобразования и желче-
выведения, а также признаками печеночной недостаточности.
При этом желчь из разрушенных гепатоцитов и желчных капил-
ляров попадает в кровь через кровеносные и лимфатические ка-
пилляры.
Надпеченочная, или гемолитическая, желтуха обусловлена
повышенным поступлением в плазму крови неконъюгированно-
го билирубина. Это наблюдается при значительном внутри- или
внесосудистом гемолизе, при гемолитических анемиях, гемоли-
зе эритроцитов и их предшественников в костном мозге, при
образовании избытка непрямого билирубина в обширных гема-
томах.
271
Основные проявления гемолитической желтухи: анемия, били-
рубинемия. гемоглобинурия и билирубинурия. увеличение в кро-
ви уровня непрямого билирубина, признаки печеночной недоста-
точности.
Подпеченочная желтуха. Ее причиной является стойкое нару-
шение выведения желчи по желчным капиллярам при внутрипе-
ченочном холестазе, по внутрипеченочным, пузырному или об-
щему желчным протокам, при обтурации желчевыводящих путей
камнями и опухолями, а также при сдавлении желчных путей из-
вне, например опухолью головки поджелудочной железы или
большого дуоденального сосочка, Рубцовыми изменениями ткани
вокруг желчевыводящих путей, увеличенными лимфатическими
узлами и т. п.
Основные проявления подпеченочной желтухи: желтушное ок-
рашивание склер, кожи и слизистых оболочек, зуд кожи, что обу-
словлено раздражением нервных окончаний желчными кислота-
ми, билирубинурия, развитие ахолии (отсутствие желчи в кишеч-
ном тракте, обесцвечивание кала). Ахолия обусловливает наруше-
ние полостного и мембранного пищеварения, дисбактериоз, ки-
шечную аутоинфекцию и интоксикацию в результате отсутствия
бактерицидного действия желчи.
БОЛЕЗНИ ПЕЧЕНИ
Болезни печени разнообразны, однако их можно объединить в
несколько групп в зависимости от этиологии и характера морфо-
логических изменений — гепатозы, гепатиты, циррозы и опухоли.
Гепатозы — группа заболеваний печени, в основе которых ле-
жат дистрофические и некротические изменения ее паренхимы.
Гепатозы могут протекать остро и хронически.
Острые гепатозы. Массивный прогрессирующий некроз печени,
клинически характеризуется синдромом печеночной недостаточ-
ности.
Причиной заболевания являются экзогенные токсические воз-
действия (отравления гепатотропными ядами, некоторыми гри-
бами, недоброкачественной пищей, химическими веществами)
и эндогенные токсические влияния — токсикоз беременных, тире-
отоксикоз и др. При этом токсичные вещества непосредственно
воздействуют на гепатоциты, в основном центральных отделов
долек.
Морфогенез болезни характеризуется прогрессирующим некро-
зом паренхимы, обычно заканчивающимся развитием печеноч-
ной недостаточности. Заболевание протекает в течение 3 нед и
проходит стадии желтой и красной атрофии печени.
• Стадия желтой атрофии печени. Вначале печень
несколько увеличивается в объеме, становится дряблой и
приобретает ярко-желтую окраску из-за скопления в гепа-
тоцитах липидов и билирубина, затем развивается некроз
272
ткани и к концу 2-й недели печень начинает уменьшаться в
размерах.
• Стадия красной атрофии печени. Некротиче-
ский детрит рассасывается макрофагами, а строма печени
спадается. При этом синусоиды переполнены кровью. Пе-
чень резко уменьшается в размерах, становится дряблой и
красной. Это происходит к концу 3-й недели болезни.
Осложнения. По мере развития заболевания возникают парен-
химатозная желтуха, множественные кровоизлияния в коже, сли-
зистых и серозных оболочках, тяжелые дистрофические и некро-
тические изменения в почках, поджелудочной железе, сердце,
нервной системе.
Исходы. Больные умирают от прогрессирующей печеночной
или почечно-печеночной недостаточности (гепаторенальный син-
дром). Если больные выживают, то процесс может приобрести за-
тяжное течение, на месте некротизированной ткани развивается
рубцовая соединительная ткань — формируется постнекротиче-
ский цирроз печени.
Хронические гепатозы. В этой группе болезней печени наибо-
лее часто развивается жировой гепатоз.
Жировой гепатоз характеризуется выраженной жировой дис-
трофией и некрозом гепатоцитов, а также хроническим течением.
Причины — интоксикация, в том числе алкогольная, гипоксия,
особенно при хроническом венозном застое, связанном с сердеч-
но-сосудистой недостаточностью, кахексия различного генеза.
Исходы. В большинстве случаев гепатозы обратимы при пре-
кращении интоксикации или гипоксии. При длительном дейст-
вии повреждающих факторов возможно развитие цирроза печени.
Гепатиты — группа воспалительных заболеваний печени, кото-
рые характеризуются дистрофическими и некротическими изме-
нениями гепатоцитов и воспалительной инфильтрацией стромы
органа.
По течению выделяют острый и хронический гепатит.
Острый гепатит может быть экссудативным и продуктивным.
Наиболее часто развивается серозный экссудативный гепатит, на-
пример при тиреотоксикозе. Экссудат пропитывает строму пече-
ни и диффузно инфильтрирует портальные тракты. Может разви-
ваться и гнойный абсцедирующий гепатит (пилефлебитические
абсцессы). Острый продуктивный гепатит характеризуется лим-
фогистиоцитарной и нейтрофильной инфильтрацией портальных
трактов, дистрофией и некробиозом гепатоцитов и пролифераци-
ей звездчатых эндотелиоцитов (клеток Купфера). Острые гепати-
ты, как правило, заканчиваются благополучно, ткань печени ре-
генерирует, однако при некоторых вирусных гепатитах возможна
хронизация заболевания.
Хронический гепатит обычно развивается как исход острого.
При этом печень увеличена в размерах, плотная, на разрезе имеет
пестрый вид. Для хронического гепатита характерны диффузная
воспалительная инфильтрация портальных трактов, вакуольная или
273
жировая дистрофия гепатоцитов, возможен прогрессирующий оча-
говый некроз ткани печени и нарастающий склероз органа.
По современной классификации различают:
• хронический неактивный гепатит, при котором воспаление
не выходит за пределы портальных трактов. В них развива-
ется лимфогистиоцитарная инфильтрация, без выраженного
фиброза. Клинически такой гепатит часто течет бессим-
птомно.
• хронический активный гепатит — воспаление печени, выхо-
дящее за пределы портальной зоны, с развитием своеобраз-
ного некроза печеночных долек, фиброза и нередко цирро-
за печени. Печень при этом увеличивается в размерах, на
коже появляются сосудистые "звездочки" и развивается дос-
таточно яркая клиническая симптоматика.
Осложнениями хронического гепатита являются печеночная
недостаточность и портальная гипертензия.
Вцпщ гепатитов. Вирусные гепатиты — одно из наиболее рас-
пространенных в настоящее время заболеваний печени. Это свя-
зано с общим увеличением вирусных болезней, с широким рас-
пространением гемотрансфузий, а также с ростом количества
наркоманов, которые, вводя внутривенно наркотики, как прави-
ло, используют один и тот же нестерильный шприц.
Этиология. Вирусный гепатит развивается, когда организм ин-
фицируют гепатотропные вирусы — в подавляющем большинстве
случаев это вирусы гепатитов А, В, С, D, Е, F, G и значительно
реже другие вирусы, поражающие печень при виремии — цитоме-
галовирус, вирус герпеса и др. Вирусные гепатиты могут проте-
кать остро, в том числе молниеносно, и хронически.
Вирусный гепатит А обычно протекает остро. Заболевание
впервые описал крупнейший отечественный терапевт С. П. Бот-
кин, и ранее вирусный гепатит А называли болезнью Боткина.
Путь передачи возбудителя — фекально-оральный, т. е. через за-
грязненные продукты питания, грязные руки. Проникая в орга-
низм, вирус попадает в лимфатические узлы кишечника, затем в
кровь и с кровью — в печень. В зависимости от реакции иммун-
ной системы развивается или не развивается некроз гепатоцитов.
При высокой степени иммунной защиты вирус локализуется в
пределах портальных трактов, в клетках печени происходят лишь
дистрофические изменения без тяжелых расстройств ее функций
и развивается безжелпушная форма болезни. Если вирусу удается
достичь гепатоцитов, он вызывает их баллонную дистрофию, нек-
роз и развивается печеночная желпуха (рис. 68). Печень увеличи-
вается в размерах, становится красной из-за гиперемии сосудов и
отека стромы. В некротизированных гепатоцитах наблюдается
коагуляционный некроз, и такие гепатоциты называются тельца-
ми Каунсильмена. В портальных трактах и синусоидах нарастает
лимфогистиоцитарная инфильтрация. Одновременно начинаются
процессы регенерации, которые приводят к восстановлению па-
ренхимы печени, но гепатит А может закончиться и циррозом пе-
274
чени. После перенесен-
ного заболевания иногда
сохраняется вирусоноси-
тельство.
Вирусный гепатит В.
Вирус попадает в орга-
низм парентерально, в
том числе половым пу-
тем, и вызывает как ост-
рый, так и хронический
гепатит. Основным мар-
кером вируса является
HBs-антиген (HBsAg)
крови и образующиеся к
нему антитела. Гепатит
чаще протекает хрониче-
ски и примерно у 10 %
больных заканчивается
печеночной недостаточ-
ностью. Вирус гепатита В.
локализуясь в гепатоци-
тах, не оказывает на них
прямого цитопатического
действия, но гепатоциты
погибают в результате
разрушения их антитела-
ми против HBsAg.
Морфологически вос-
паление проявляется вы-
раженной лимфомакро-
Рис. 68. Вирусный гепатит. Баллонная
дистрофия гепатоцитов. Лимфогистио-
цитарный инфильтрат в портальном
тракте (вверху слева) и в синусоидах.
фагальной инфильтрацией портальных трактов, гидропической и
баллонной дистрофией гепатоцитов с появлением пелец Мэллори —
гепатоцитов в состоянии гиалиново-капельной дистрофии.
Вирусный гепатит С вызывает соответствующий вирус, также
попадающий в организм преимущественно с кровью и являю-
щийся причиной около 90 % посттрансфузионньх гепатитов. Ха-
рактеризуется выраженной лимфомоноцитарной и плазмоклеточ-
ной инфильтрацией портальных трактов с образованием лимфо-
идных фолликулов, наличием своеобразных некрозов гепатоци-
тов, связанных с действием антител, гидропической и жировой
дистрофией гепатоцитов и поражением внутрипеченочных желч-
ных протоков. У большинства больных развивается хронический
гепатит, а у трети из них — цирроз печени.
Вирусный гепатит D. Вирус гепатита D проникает в организм
главным образом парентерально, однако для развития гепатита
необходимо его сочетание с вирусом гепатита В, что значительно
ухудшает течение процесса, вызывая более тяжелые морфологи-
ческие изменения. Поэтому гепатит D часто заканчивается разви-
тием цирроза печени и печеночной недостаточности.
275
Вирусный гепатит Е. Вирус передается фекально-оральным пу-
тем и вызывает острый гепатит. Морфологическая картина сход-
на с гепатитом А, но нет вирусоносительства.
Вирусные гепатиты F и G вызывают вирусы, передающиеся па-
рентерально. Эти гепатиты могут протекать как остро, так и хро-
нически, но лишь в сочетании с вирусами гепатитов В и С. Ха-
рактерно образование в печени гигантских многоядерных клеток,
наличие гидропической дистрофии гепатоцитов и очагов некроза
ткани печени.
Алкогольная болезнь печени развивается при многолетней ал-
когольной интоксикации и складывается из жирового гепатоза,
алкогольного гепатита и цирроза печени.
Жировой гепатоз — начальная форма поражения печени, за-
ключающаяся в развитии выраженной жировой дистрофии гепа-
тоцитов. Печень приобретает желтовато-глинистый цвет и не-
сколько дряблую консистенцию. Функции ее при этом практиче-
ски не страдают. При прекращении употребления алкоголя все
изменения исчезают. При продолжении пьянства в результате
длительного действия этанола на сосудистые стенки развивается
выраженный склероз сосудов, особенно микроциркуляторного
русла, что приводит к прогрессированию гипоксии, метаболиче-
ским нарушениям и способствует нарастанию жировой дистро-
фии гепатоцитов, к которой присоединяется их белковая дистро-
фия. В далеко зашедших стадиях болезни в печени появляются
тельца Мэллори, которые в данном случае носят название алко-
гольного гиалина. Кроме того, при хронической алкогольной ин-
токсикации нарастает склероз портальных трактов и перисину-
соидальных пространств, коллагеновые волокна появляются и во-
круг центральных венул.
Алкогольный гепатит развивается у 15 % злоупотребляющих
алкоголем. Чаще воспаление возникает остро и характеризуется
некрозом рассеянных групп гепатоцитов и скоплением вокруг
них лейкоцитарных инфильтратов. Алкогольный гепатит развива-
ется, как правило, на фоне выраженной жировой дистрофии ге-
патоцитов. На месте погибшей ткани печени остаются поля скле-
роза. Вопрос о возможности развития хронического алкогольного
гепатита является дискутабельным. Многие исследователи счита-
ют, что при длительном злоупотреблении алкоголем с выражен-
ными явлениями склероза и жирового гепатоза возможно разви-
тие воспалительных изменений в печени лишь после так назы-
ваемого алкогольного эксцесса, т. е. одномоментного употребле-
ния значительного количества спиртных напитков, и эти измене-
ния скорее следует рассматривать как острое воспаление на фоне
хронического гепатоза.
Алкогольный цирроз печени развивается у 15—20 % больных,
страдающих алкоголизмом. Характерным признаком процесса яв-
ляется развитие соединительной ткани в центре гепатоцитов —
центролобулярный фиброз, а также вокруг групп клеток печени, в
результате чего образуются узелки до 5 мм в диаметре — мелкоуз-
276
Рис. 69. Портальный цирроз печени. Ложные дольки разделены про-
слойками соединительной ткани.
ловой цирроз. В гепатоцитах обнаруживаются крупнокапельное
ожирение, жировые кисты, скопления железа, много телец Мэл-
лори. Алкогольный цирроз осложняется печеночной желтухой и
хронической печеночной недостаточностью.
Цирроз печени — хроническое заболевание печени, характери-
зующееся склерозом и структурной перестройкой ее ткани и из-
менением в связи с этим формы органа. Цирроз печени является
исходом ряда заболеваний, особенно часто вирусного и алкоголь-
ного гепатитов, холангита и холангиолита, а также сердечной не-
достаточности, сопровождающейся застоем крови в печени.
Признаки цирроза печени:
• дистрофия и некроз гепатоцитов;
• извращенная регенерация;
• диффузный склероз;
• структурная перестройка:
• деформация печени.
Патогенез. В основе развития цирроза печени лежат необрати-
мая дистрофия и некроз гепатоцитов. Это вызывает усиленную
регенерацию в виде гиперплазии сохранившихся гепатоцитов.
В результате нарушается дольковое строение печени, образуются
ложные дольки и различной величины узлы-регенераты (рис. 69).
Вокруг них развивается соединительная ткань, которая прораста-
ет и внутрь узлов-регенератов. В ложных дольках и в узлах-реге-
нератах нарушается кровообращение, так как многие дольки не
содержат центральной вены, в синусоидах между гепатоцитами
277
появляется соединительнотканная мембрана. Следствием этого
являются нарастающая гипоксия клеток печени в узлах-регенера-
тах, их дистрофия и гибель, а также усиленное разрастание со-
единительной ткани, что еще больше нарушает микроциркуля-
цию. Процесс развивается по "замкнутому кругу" с постоянным
нарастанием склеротических изменений. Печень становится
плотной, бугристой, уменьшается, а иногда увеличивается в раз-
мерах. форма ее изменяется.
Вцдщ цирроза печени (рис. 70).
В зависимости от величины узлов выделяют следующие виды
цирроза печени:
• мелкоузловой;
• крупноузловой;
• смешанный.
В зависимости от морфогенеза цирроза печени, т. е. динамики
развития морфологических изменений, выделяют постнекротиче-
ский, портальный, билиарный и смешанный цирроз.
Постнекротический цирроз развивается после массивных нек-
ротических изменений в печени, связанных с ее токсической
дистрофией, вирусным гепатитом и другими причинами, вызы-
вающими некроз ткани. Некротизированная паренхима рассасы-
вается, строма печени спадается, и в этих участках разрастается
соединительная ткань в виде грубых рубцов. Печень уменьшается
в размерах, на ее поверхности видны глубокие рубцовые западе-
ния и крупные узлы-регенераты. Возникает крупноузловая, а
иногда смешанная форма цирроза печени (см. ниже).
Портальный цирроз возникает как исход хронической сердеч-
но-сосудистой недостаточности, хронического алкогольного гепа-
тита, расстройств обмена веществ, связанных с неправильным
питанием. Течет медленно. Характеризуется тем, что разрастаю-
щаяся в портальных трактах и вокруг них соединительная ткань
проникает в виде отростков в печеночные дольки, разделяя их на
мелкие ложные дольки. Такая монотонная картина во всей пече-
ни характеризует мелкоузловой цирроз.
Билиарный цирроз связан с нарушением оттока желчи, причи-
ной которого могут быть сдавление или закупорка внепеченоч-
ных желчных путей, инфекционное поражение желчных прото-
ков. При этом развиваются застой желчи и воспаление желчных
протоков, могут возникать их разрывы и образование "желчных
озер" в ткани печени. Вокруг измененных желчных протоков раз-
растается соединительная ткань, прорастающая и в печеночные
дольки. На периферии долек гепатоциты гибнут. Печень приоб-
ретает зеленоватый цвет, увеличена, плотная, гладкая или мелко-
бугристая. На разрезе видны расширенные желчные протоки, пе-
реполненные желчью.
Слушанный цирроз возникает как исход портального цирроза,
к которому на каком-то этапе присоединились некротические из-
менения печени.
Портальная гипертензия при циррозе печени развивается в
278
Рис. 70. Цирроз печени.
а — мелкоузловой (билиарный), б — мелкоузловой (портальный), в — крупноуз-
ловой (постнекротический).
связи с перипортальными склеротическими изменениями и скле-
розом печеночных вен. Это приводит к развитию внепеченочных
портокавальных анастомозов, благодаря которым часть крови ми-
нует печень и воротная вена разгружается. Появление портока-
вальных анастомозов характеризуется расширением вен пищево-
279
да, желудка, геморроидальных вен и вен передней брюшной стен-
ки. Как следствие портальной гипертонии и нарушений кровооб-
ращения в портальной системе в брюшную полость поступает
жидкость — развивается асцит. Живот увеличивается в объеме,
иногда в брюшной полости скапливается до 7—10 л асцитической
жидкости.
Осложнения. Расширенные вены нередко разрываются, что
приводит к массивному кровотечению, от которого больные мо-
гут погибнуть.
Исходом цирроза печени является печеночная недостаточ-
ность, которая сопровождается желтухой и множественными кро-
воизлияниями. В почках возможны тяжелые изменения, вплоть
до некроза эпителия канальцев, обусловливающего развитие гепа-
торенального синдрома, который также может стать причиной
смерти больных. В цирротически измененной печени может раз-
виться рак.
Опухоли печени в основном развиваются из гепатоцитов и
эпителия желчных протоков. Они бывают доброкачественными и
злокачественными. Из числа доброкачественных опухолей наибо-
лее часто встречаются аденомы и гемангиомы.
Аденомы развиваются из гепатоцитов (гепатоаденомы) или
эпителия желчных протоков (холангиоаденомы), в основном у
женщин детородного возраста. Растут медленно, бессимптомно, в
виде ограниченного капсулой узла, достигая иногда очень боль-
ших размеров. Характеризуются тканевым атипизмом, который
заключается в том, что гепатоциты не формируют печеночную
дольку. Аденомы могут подвергаться малигнизации, трансформи-
руясь в рак.
Гемангиомы развиваются из венозных сосудов. Это наиболее
частые доброкачественные опухоли печени, имеющие вид мелко-
бугристого, иногда гладкого узла синюшно-красного цвета, дос-
тигающего 5—7 см в диаметре. Микроскопически представляет
собой кавернозную гемангиому, тканевый атипизм которой за-
ключается в образовании содержащих кровь сосудистых полостей
разной величины и формы, со стенками разной толщины на раз-
личных участках. Возможен разрыв гемангиомы с внутрибрюш-
ным кровотечением. Изредка малигнизируется, превращаясь в
ангиосаркому.
Злокачественные опухоли развиваются из гепатоцитов, эпите-
лия желчных протоков и иногда из мезенхимальных тканей пече-
ни. Выделяют гепатоцеллюлярный и холангиоцеллюлярный рак,
ангиосаркому.
Гепатоцеллюлярный рак, или злокачественная гепатома, раз-
вивается из гепатоцитов, обычно на фоне цирроза печени. Муж-
чины болеют в 2 раза чаще женщин. Характерен инвазивный рост
с тенденцией к прорастанию в воротную и полую вены, а также в
диафрагму. Выражен клеточный атипизм. клетки имеют различ-
ную форму и размеры, содержат атипичные гиперхромные ядра,
наблюдаются неправильные митозы. В большинстве случаев
280
клетки опухоли расположены в виде трабекул, но могут образо-
вывать псевдожелезы и секретировать желчь.
Метастазирует гепатоцеллюлярная карцинома в портальные
лимфатические узлы, позже появляются гематогенные метастазы
в легкие, поджелудочную железу, головной мозг, кости, надпо-
чечники. У больных развиваются слабость, гепатомегалия, боль в
правом подреберье, затем нарастают асцит, желтуха, кахексия.
Прогноз неблагоприятный.
Холангиоцеллюлярный рак исходит из эпителия желчных прото-
ков. обладает инфильтрирующим ростом, преимущественно по
ходу желчных путей, прорастая в ткань печени, что обусловливает
развитие желтухи. Микроскопически рак представлен небольши-
ми клетками кубической формы с гиперхромными атипичными
ядрами, клетки образуют железистоподобные структуры. В опухо-
ли много стромы. Прогноз неблагоприятный.
Ангиосаркома имеет типичное строение в виде сосудистых ла-
кун разной формы и размеров, выстланных атипичными эндоте-
лиоцитами и перицитами, с множественным тромбозом, очагами
некроза ткани опухоли и кровоизлияниями. Характерны обшир-
ные гематогенные метастазы. Прогноз неблагоприятный.
БОЛЕЗНИ ЖЕЛЧНОГО ПУЗЫРЯ
Болезни желчного пузыря связаны либо с образованием в нем
камней, либо с воспалением его стенок, либо с развитием опу-
холи.
Камни желчного пузыря нередко образуются как проявление
различных метаболических нарушений, в первую очередь мине-
рального обмена. Нередко наличие камней в желчном пузыре не
сопровождается клинической симптоматикой. Однако, попадая в
пузырный проток, они затрудняют выход желчи из желчного пу-
зыря, что приводит к его водянке. Если камень обтурирует общий
желчный проток, то развивается подпеченочная желтуха. Иногда
камень является причиной пролежня стенки желчного пузыря с
развитием перитонита.
Воспаление желчного пузыря, или холецистит, вызывают раз-
личные причины, но очень часто связано с наличием камней в
желчном пузыре. Может протекать как остро, так и хронически.
Острый холецистит носит характер серозного, но нередко
гнойного (флегмонозный холецистит) и гангренозного. При обту-
рации пузырного протока камнем развивается эмпиема желчного
пузыря. Воспаление может распространяться на желчные протоки
с развитием холангита и холангиолита.
Хронический холецистит возникает в исходе острого. При этом
в стенке желчного пузыря наряду с умеренно выраженной лим-
фоидной инфильтрацией наблюдаются атрофия слизистой обо-
лочки, иногда и мышечного слоя, сочетающаяся со склерозом
стромы пузыря.
281
Желчнокаменная болезнь, или калькулезный холецистит, воз-
никает при травме камнем стенки желчного пузыря, в связи с
чем в ней появляется воспаление и развивается клиническая сим-
птоматика, что позволяет говорить о болезни. Обычно заболева-
ние протекает хронически с периодическими обострениями. При
остром калькулезном холецистите в стенке пузыря развивается
серозное, фибринозное, изредка гнойное воспаление. Хрониче-
ский калькулезный холецистит характеризуется в основном атро-
фическими и склеротическими изменениями стенки желчного
пузыря.
Опухоли желчного пузыря. Наиболее часто встречается аденома
и рак желчного пузыря.
Адена ли возникает из эпителия слизистой оболочки. При этом
тканевый атипизм проявляется в очаговой пролиферации эпите-
лиальных клеток с образованием желез разной величины и фор-
мы, стромы обычно мало.
Рак желчного пузыря наиболее часто развивается на фоне хро-
нического калькулезного холецистита. Гистологически он имеет
строение аденокарциномы, локализуется в области шейки или
дна желчного пузыря. Прогрессируя, он может распространяться
по внутрипеченочным желчным протокам. Метастазирует лимфо-
генным путем.
БОЛЕЗНИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
Болезни поджелудочной железы в основном связаны с воспа-
лительными или опухолевыми процессами в ней.
Панкреатит — воспаление поджелудочной железы, может
иметь острое или хроническое течение.
Острый панкреатит развивается при отравлении алкоголем,
переедании, при нарушении оттока панкреатического сока и др.
Морфологически проявляется в появлении очагов некроза, кро-
воизлияний, отека, иногда очагов нагноения. Если преобладают
некротические и геморрагические изменения, что характерно для
алкогольного поражения поджелудочной железы, то развивается
геморрагический панкреонекроз, который без экстренного хирурги-
ческого вмешательства заканчивается смертью.
Хронический панкреатит может быть следствием инфекций,
интоксикаций, прежде всего алкогольной, болезней желудка, пе-
чени, желчного пузыря, может развиваться после острого пан-
креатита. Преобладают атрофические и склеротические измене-
ния ткани железы в сочетании с регенерацией ацинозных клеток
и образованием регенераторных аденом. Склеротические измене-
ния могут вести к стенозу протоков и образованию кист. В скле-
розированные участки нередко выпадают соли кальция. Железа
уменьшается и становится очень плотной. Возможно развитие са-
харного диабета.
Рак поджелудочной железы чаще обнаруживается в ее головке,
282
но может возникать и в теле, и в хвосте. Обычно гистологически
это аденокарцинома, развивающаяся из эпителия протоков. Рас-
тет инфильтрирующим ростом, но в головке железы нередко име-
ет вид плотного узла, сдавливающего и прорастающего проток
поджелудочной железы и общий желчный проток. Это приводит
к панкреатиту, холангиту и развитию подпеченочной желтухи.
Смерть наступает от истощения, метастазов рака или присоеди-
нившейся пневмонии.
Глава 18
БОЛЕЗНИ ПОЧЕК
К числу важнейших почечных функций относятся:
• мочеобразование и мочевыделение:
• поддержание жизненно важных параметров — кислотно-ос-
новного состояния, осмоляльности крови, уровня артери-
ального давления и др.;
• регуляция гемопоэза посредством синтеза эритропоэтинов.
ПАТОЛОГИЯ ПОЧЕК И МОЧЕВЫВОДЯЩИХ ПУТЕЙ
Патологию почек вызывают первичные и вторичные причины.
Первичные, или наследственные, формы патологии обусловле-
ны изменениями генетической информации, что приводит к на-
рушению синтеза ферментов (ферментопатии), клеточных мем-
бран (мелбранопатии), структуры почек. Проявлением врожден-
ной патологии являются, например, поликистоз почек, семейная
дисплазия почек, почечный несахарный диабет, аминоацидурия,
фосфатурия и др.
Вторичные, или приобретенные, причины: инфекции (бакте-
рии, вирусы, риккетсии), химические (сулема, ртуть), физические
(переохлаждение, травма), иммунопатологические факторы.
Этиологические факторы реализуются на преренальном. ре-
нальном и постренальном уровнях:
Преренальные факторы:
• нервно-психические расстройства, состояния, сочетающие-
ся с сильной болью (рефлекторная болевая анурия);
• эндокринопатии, например, сочетающиеся с избытком или
недостатком АДГ, альдостерона, тиреоидных гормонов, ин-
сулина, катехоламинов и т. п.;
• расстройства кровообращения в виде гипотензивных (кол-
лапс, артериальная гипотензия и др.) и гипертензивных со-
стояний.
283
Ренальные факторы:
• прямое повреждение ткани почек инфекционными возбу-
дителями (например, при пиелонефрите);
• нарушение кровообращения непосредственно в почках,
особенно ишемия — при атеросклерозе, тромбозе или
тромбоэмболии.
Постренальные факторы, нарушающие отток мочи по моче-
выводящим путям, что сопровождается повышением внутрипо-
чечного давления (сдавление или обтурация мочевыводящих пу-
тей камнями, опухолями, перегибы мочеточника и т. п.).
Общие механизмы возникновения и развития патологии почек
Нарушения мочеобразования почками являются результатом
расстройств процессов фильтрации, реабсорбции и экскреции.
Расстройства фильтрации плазмы крови в клубочках могут быть
обусловлены снижением или увеличением объема фильтрации
плазмы крови.
Снижение объели фильтрации плазлы крови происходит в ре-
зультате:
• понижения фильтрационного давления в клубочках при
коллапсе, артериальной гипотензии, ишемии почек, за-
держке мочи в мочеточниках или мочевом пузыре;
• уменьшения площади клубочкового фильтра при некрозе
части почки или склерозе клубочков при хронических гло-
мерулонефритах;
• снижения проницаемости мембран клубочков вследствие их
склероза, например при сахарном диабете или амилоидозе.
Увеличение объели фильтрации плазлыкрови обусловлено:
• повышением фильтрационного давления в клубочках, на-
пример под влиянием избытка катехоламинов при феохро-
моцитоме или ангиотензина при ишемии почек;
• увеличением проницаемости клубочкового фильтра, напри-
мер при воспалении в клубочках или в строме.
Снижение канальцевой реабсорбции может быть следствием:
• генетических дефектов ряда ферментов эпителия канальцев;
• гиалиново-капельной дистрофии эпителия канальцев.
Нарушение процессов экскреции эпителием канальцев ионов ка-
лия, водорода, ряда метаболитов, экзогенных веществ может на-
блюдаться при гломерулонефритах, пиелонефрите, ишемии по-
чек.
ПРОЯВЛЕНИЯ ПАТОЛОГИИ ПОЧЕК
Изменения показателей диуреза:
• полиурия — выделение за сутки более 2000—2500 мл мочи;
• олигурия — выделение в течение суток менее 500—300 мл
мочи;
284
• анурия — прекращение поступления мочи в мочевой пузырь.
Изменения плотности мочи:
• гиперстенурия — увеличение плотности мочи выше нормы —
более 1029—1030;
• гипостенурия — снижение плотности мочи ниже нормы —
менее 1009;
• изостенурия — мало меняющаяся в течение суток относи-
тельная плотность мочи, что свидетельствует об уменьше-
нии эффективности процесса реабсорбции в канальцах и
снижении концентрационной способности почек.
Изменения состав мочи:
• увеличение или уменьшение по сравнению с нормой содер-
жания нормальных компонентов мочи — глюкозы, ионов,
воды, азотистых соединений;
• появление в моче отсутствующих в норме компонентов —
эритроцитов (ия), лейкоцитов (пиурия), белка (протеинурия),
аминокислот (аминоацидурия), осадка солей, цилиндров
(слепков канальцев из белка, клеток крови, эпителия ка-
нальцев. клеточного детрита).
Общие нефрогенные синдромы:
• гиперволемия, например при олигурии;
• гигю волемия, например в результате хронической поли-
урии;
• азотемия, или уремия, — повышение уровня небелкового
азота в крови;
• гипопротеинемия — снижение уровня белка в крови;
• диспротеинемия — нарушение нормального соотношения
отдельных фракций белка в крови;
• гиперлипопротеинемия;
• почечная артериальная гипертензия;
• почечные отеки.
Характер отклонений определяется конкретным заболеванием
почек и нарушением процессов фильтрации, реабсорбции, экс-
креции и секреции в них.
Почечная недостаточность — синдром, развивающийся в ре-
зультате значительного снижения или прекращения выделитель-
ной функции почек. Характеризуется прогрессирующим увеличе-
нием содержания в крови продуктов азотистого обмена (азотеми-
ей) и нарастающим расстройством жизнедеятельности организма.
Выделяют острую и хроническую почечную недостаточность в
зависимости от скорости ее возникновения и дальнейшего раз-
вития.
Острая почечная недостаточность (ОПН) развивается в тече-
ние нескольких часов или дней и быстро прогрессирует. Это со-
стояние потенциально обратимо, однако нередко ОПН приводит
к смерти больных.
Причины ОПН условно разделяют на 3 группы — пререналь-
ные, ренальные и постренальные:
• преренальные обусловлены значительным снижением крово-
тока в почках, например массивной кровопотерей, коллап-
сом, шоком, тромбозом почечных артерий;
• ренальные связаны с повреждением самих почек, например
некротический нефроз, острые гломерулонефриты, васку-
литы, пиелонефриты;
• постренальные обусловлены прекращением оттока мочи по
мочевыводящим путям за счет обтурации их камнями или
сдавления опухолью, перегибом мочеточников.
Патогенез ОПН:
• значительное и быстро нарастающее снижение объема клу-
бочковой фильтрации;
• сужение или обтурация большинства канальцев почек при
закрытии их цилиндрами, состоящими из клеточного дет-
рита (в связи с повреждением и гибелью канальцевого эпи-
телия), денатурированного белка при повышении прони-
цаемости клубочкового фи л ьтра;
• подавление функции эпителия канальцев под действием
нефротоксических факторов — препаратов фосфора, солей
тяжелых металлов, фенолов, соединений мышьяка и др.
Хроническая почечная недостаточность (ХПН) — состояние,
развивающееся в результате нарастающей гибели нефронов и
характеризующееся прогрессирующим снижением функций по-
чек.
Клиническая симптоматика появляется при снижении числа
нефронов до 30 % от нормального уровня. Уменьшение их коли-
чества до 10—15 % сопровождается развитием уремии.
Уремия (мочекровие) — синдром, заключающийся в аутоин-
токсикации организма продуктами метаболизма, подлежащими
удалению с мочой, но задерживающимися в крови и в тканях
вследствие почечной недостаточности. При этом отработанные
продукты метаболизма, обладающие токсическими свойствами,
начинают выводиться всеми органами, имеющими железы, что
приводит к их воспалению — гастриту, энтероколиту, дерматиту,
пневмонии, энцефалопатии и тяжелой нарастающей интоксика-
ции, часто заканчивающейся смертью больных.
БОЛЕЗНИ ПОЧЕК
Гломерулопатии — группа заболеваний, при которых страдают
преимущественно клубочки почек.
Классификация гломерулопатий
По механизму развития:
• первичные гломерулопатии — самостоятельные заболева-
ния;
• вторичные гломерулопатии — проявления других заболева-
ний.
286
По этиологии гломерулопатии могут быть:
• воспалительного характера — гломерулонефриты;
• невоспалительные гломерулопатии наследственного, мета-
болического, гемодинамического происхождения — нефро-
зы, нефросклероз, нефропатии.
По течению:
• острые;
• хронические.
Острый постинфекционный гломерулонефрит. Причиной болез-
ни являются различные инфекционные возбудители, но наиболее
часто — В-гемолитический стрептококк группы А.
Рис. 71. Острый гломерулонефрит. "Большая пестрая почка".
287
Клинически характеризуется внезапным началом с развитием
нефритического синдрома, который складывается из ге-
матурии, уменьшения скорости клубочковой фильтрации и оли-
гурии, протеинурии, повышения уровня мочевины и креатинина
в крови, артериальной гипертензии и отеков.
Морфология. Почки увеличены в размерах, с мелким красным
крапом на поверхности ("большая пестрая почка"), клубочки
отечны и увеличены, выражена пролиферация эндотелия вплоть
до закрытия просвета клубочковых капилляров, отек и лимфоид-
ная инфильтрация стромы почек (рис. 71),
Исход благоприятный, возникшие изменения подвергаются
обратному развитию примерно через 8 нед.
Экстракапиллярный пролиферативный гломерулонефрит. Этио-
логия в большинстве случаев остается неизвестной, однако часто
этот гломерулонефрит развивается при системных заболеваниях,
таких как системная красная волчанка, системная склеродермия
и др. При этом в базальных мембранах клубочков откладываются
иммунные депозиты, состоящие из различных иммунных белков
и компонентов комплемента.
Клинически болезнь характеризуется быстрым прогрессирова-
нием склероза клубочков почек, злокачественной артериальной
гипертензией, протеинурией, нарастающими отеками и олигури-
ей, переходящей в анурию и уремию.
Морфология весьма характерна и заключается в образовании
полулуний из клеток в полостях капсул клубочков (рис. 72). Они
возникают в результате разрыва стенок капилляров клубочков и
Рис. 72. Экстракапиллярный продуктивный гломерулонефрит. "Полулу-
ние" из пролиферирующих клеток нефротелия капсулы клубочка почки.
288
выхода в полость капсулы моноцитов, превращающихся в макро-
фаги, фибрина, иммунных комплексов. К ним добавляются эпи-
телиальные клетки капсул клубочков. В остром периоде почки
увеличены в размерах, дряблые, кора широкая, красная, сливает-
ся с пирамидами — "большая красная почка". Образовавшиеся
полулуния сдавливают капилляры клубочков, в результате чего
вначале уменьшается, а затем прекращается образование первич-
ной мочи. По мере прогрессирования заболевания клубочки
склерозируются, в строме нарастают отек, лимфоидно-макрофа-
гальная инфильтрация и склероз — развивается нефроцирроз.
Исход неблагоприятный, довольно быстро развивается вто-
рично-сморщенная почка и хроническая почечная недостаточ-
ность.
Мезангиокапиллярный гломерулонефрит. Причина этого ауто-
иммунного заболевания в большинстве случаев неизвестна. Воз-
можно, что аутоиммунизация связана с инфицированностью ви-
русами гепатита В и С. В крови больных выявляются аутоантите-
ла, а также циркулирующие иммунные комплексы (ЦИК).
Клинически болезнь начинается остро, но течет хронически,
характеризуется снижением скорости клубочковой фильтрации и
развитием нефротического синдрома — тяжелой протеинурии, в
связи с чем нарастает гипопротеинемия и диспротеинемия,
так как почки выделяют в основном альбумины. Из-за гипопро-
теинемии падает онкотическое давление в плазме крови и разви-
ваются отеки.
Морфология. Почки плотные, бледные, при длительном тече-
нии заболевания постепенно уменьшаются в размерах. В начале
заболевания клубочки увеличены, в базальных мембранах капил-
ляров клубочков откладываются иммунные депозиты, что приво-
дит к повреждению и прогрессирующему склерозу этих мембран.
Происходит гиперплазия эндотелия с резким сужением или пол-
ным закрытием просветов капилляров, увеличивается количество
мезангиальных клеток, нарастают макрофагальная инфильтрация
и постепенный склероз клубочков.
Исход неблагоприятный, процесс неуклонно прогрессирует и
заканчивается нефроциррозом, развивается вторично-сморщен-
ная почка и больные погибают от хронической почечной недос-
таточности (рис. 73).
Гломерулопатии невоспалительного генеза, такие как амилоид-
ная нефропатия, гломерулопатия при гипертонической болезни и
артериальных гипертензиях, при инфаркте почки и т. п. описаны
в соответствующих главах учебника.
Тубулоинтерстициальные поражения — группа заболеваний, ха-
рактеризующихся преимущественным поражением канальцев и
интерстициальной ткани почек.
По течению выделяют:
• острый канальцевый некроз;
• острый тубулоинтерстициальный нефрит:
• хронический тубулоинтерстициальный нефрит.
289
Рис. 73. Хронический гломерулонефрит с исходом в сморщивание почек
(вторично-сморщенные почки).
а — вид почки с поверхности, б — на разрезе, в, г — микроскопическая картина.
Острый канальцевый некроз — заболевание, наиболее часто
приводящее к развитию острой почечной недостаточности.
Этиология заболевания связана с ишемией или с токсиче-
ским поражением почек. Ишемия может быть обусловлена рез-
290
ким падением артериального давления в связи с шоком, мас-
сивной кровопотерей различного происхождения, а также с
обезвоживанием организма и большой потерей электролитов.
Токсические поражения почек могут быть вызваны тяжелыми
металлами (ртуть, свинец, уран и др.), лекарственными средст-
вами, органическими растворителями типа этиленгликоля, ди-
оксана, укусами ядовитых змей и насекомых, тяжелыми инфек-
циями (холера, брюшной тиф. сепсис и др.), массивным гемо-
лизом, например при переливании иногруппной крови, миоли-
зом при синдроме длительного сдавления, эндогенными инток-
сикациями (перитонит, кишечная непроходимость, токсикозы
беременных и т. п.).
Клинически быстро развиваются симптомы нарушения функ-
ций почек — олигурия, затем анурия, гиперазотемия, протеину-
рия, гематурия и симптомы уремии — адинамия, тошнота, рвота,
заторможенность, одышка вследствие нарастающего отека легких,
уремическая кома.
Морфологически почки увеличены, набухшие, капсула снима-
ется легко. Широкая бледно-серая кора резко отграничена от
полнокровных темно-красных пирамид, в слизистой оболочке ло-
ханок имеются множественные кровоизлияния. Микроскопиче-
ские изменения зависят от стадии процесса (рис. 74):
• шоковая стадия — венозное полнокровие пирамид и ише-
мия коры, капилляры клубочков спавшиеся: в эпителии ка-
нальцев отмечается выраженная белковая и жировая дис-
трофия, в просветах — цилиндры, в интерстиции — отек и
лимфостаз;
• олиго-анурическая стадия характеризуется некрозом эпите-
лия канальцев, разрывом их базальных мембран (тубулорек-
сис), лейкоцитарной инфильтрацией, кровоизлияниями,
отеком интерстиция. Если указанные изменения нарастают,
функции почек прекращаются, наступают анурия, острая
почечная недостаточность и уремия;
• стадия восстановления диуреза развивается при благоприят-
ном течении заболевания. Клубочки становятся полнокров-
ными, воспалительная инфильтрация и отек интерстиция
уменьшаются, эпителий канальцев регенерирует.
Исходы зависят от причины, вызвавшей острый канальцевый
некроз. Смерть 60 % больных наступает от уремической комы.
При благоприятном исходе у 90 % выживших больных функция
почек полностью восстанавливается в течение 6 мес. Однако ино-
гда через много лет развивается нефросклероз с исходом в хрони-
ческую почечную недостаточность.
Острый тубулоинтерстициальный нефрит — заболевание, для
которого характерно острое иммунное воспаление.
Этиология весьма разнообразна — от токсических факторов
(реакция на антибиотики, сульфаниламиды и другие лекарства) и
инфекционных возбудителей до генетических дефектов и наслед-
ственного характера заболевания. Однако в любом случае основ-
291
Рис. 74. Некротический нефроз.
а — корковое вещество желтого цвета, интермедиарная зона и пирамиды резко
полнокровны; б — полнокровие и отек пирамид; в — некроз эпителия почечных
канальцев.
ную роль играют иммунопатологические механизмы, и при этом
обнаруживаются антитела к базальным мембранам канальцев или
отложения в них иммунных комплексов.
Клинически заболевание обычно проявляется реакцией гипер-
292
чувствительности с развитием высокой лихорадки, гематурией,
умеренной протеинурией, нередко с кожной сыпью.
Морфология. Почки увеличены в размерах, отечны, в межуточ-
ной ткани обнаруживаются отек и лимфоплазмоцитарная ин-
фильтрация с небольшим количеством нейтрофилов. Затем в
процесс быстро вовлекаются канальцы, эпителий которых некро-
тизируется, слущивается в просветы с образованием цилиндров.
В базальных мембранах канальцев имеются отложения иммунных
комплексов.
Исходы зависят от причины заболевания и длительности ее
воздействия. Например, лекарственный тубулоинтерстициаль-
ный нефрит может закончиться благополучно после отмены
препарата, но возможно и развитие острой почечной недоста-
точности.
Хронический интерстициальный нефрит иногда развивается в
исходе острого, но обычно является самостоятельным первичным
заболеванием.
Причиной болезни могут быть бактериальные инфекции, обту-
рация мочевыводящих путей, нефропатия, вызванная некоторы-
ми анальгетиками, радиационные повреждения и др.
Морфология: прогрессирующий диффузный интерстициальный
фиброз с атрофией канальцев почек и клеточной, в основном
лимфоцитарной, инфильтрацией.
Исходом является нефросклероз, выраженный в различной
степени. При тяжелом склеротическом поражении почек возмож-
но развитие хронической почечной недостаточности.
Пиелонефрит — заболевание, характеризующееся воспалением
в почечной лоханке, чашечках и строме почки. Бывает одно- и
двусторонним.
По течению выделяют острый и хронический пиелонефрит.
Острый пиелонефрит. Его этиология связана в первую очередь
с различной инфекцией — кишечной палочкой, протеем, стреп-
тококком и др. Имеют значение также снижение реактивности
организма, вызванное, например, переохлаждением, и местные
факторы в виде нарушения оттока мочи, например в связи с ги-
перплазией предстательной железы у мужчин или опущением
матки у женщин.
Патогенез пиелонефрита в значительной степени определяется
путями проникновения инфекции в почки. Выделяют следующие
пути:
• восходящий (урогенный), который может быть вызван нали-
чием возбудителей инфекции в моче, дискинезией мочеточ-
ников, затруднением оттока мочи и др.;
• гематогенный — при инфекционных заболеваниях, сопрово-
ждающихся бактериемией или виремией;
• лимфогенный — при воспалении толстой кишки и половых
органов.
Клинически острый пиелонефрит характеризуется болезненно-
стью в области поясницы, лихорадкой, недомоганием, лейкоци-
293
тозом крови и мочи, цилинд-
рурией.
Морфология. Почка увели-
чена, полнокровна, капсула
ее снимается легко. Лоханка
и чашечка расширены, за-
полнены мутной мочой, сли-
зистая оболочка их тусклая, с
кровоизлияниями. В парен-
химе почки очаги кровоиз-
лияний чередуются с участ-
ками нагноений, что придает
ей пестрый вид, под капсу-
лой могут быть мелкие абс-
цессы. В межуточной ткани
всех слоев почки — отек,
множественные кровоизлия-
ния, лейкоцитарные ин-
фильтраты с образованием
абсцессов, особенно в корко-
вом веществе. Гной и бакте-
рии проникают в канальцы.
Осложнения. При слиянии
мелких абсцессов может об-
разоваться карбункул почки,
при прорыве гноя из абсцес-
сов в лоханку развивается
пионефроз, при распростране-
Рис. 75. Хронический пиелонефрит —
"щитовидная почка".
нии гноя на капсулу почки и паранефральную клетчатку возника-
ют перинефрит и паранефрит. В тяжелых случаях возможны нек-
роз верхушек сосочков пирамид — папиллонекроз, и острая почеч-
ная недостаточность. Иногда возникает сепсис, а также метаста-
тическое распространение инфекции и гноя в кости, оболочки
головного мозга, эндокард и др.
Исход обычно благоприятный, но при развитии осложнений
возможно наступление смерти.
Хронический пиелонефрит обычно является следствием неизле-
ченного острого пиелонефрита, иногда острая фаза заболевания
остается незамеченной. Болезнь чаще развивается в детском воз-
расте, особенно у девочек.
Клиническая картина заболевания может быть не выражена.
Часто основным симптомом обострения хронического пиелонеф-
рита является необъяснимая лихорадка, при одностороннем про-
цессе — тупая постоянная боль в поясничной области на стороне
пораженной почки, а также артериальная гипертензия. В анали-
зах крови и мочи — лейкоцитоз. Течение длительное, рецидиви-
рующее.
Морфология характеризуется прогрессирующим воспалением и
склерозом чашечно-лоханочной системы. Прогрессирует склероз
294
ткани почки на фоне атрофии канальцев, множественных очагов
воспалительной инфильтрации и микроабсцессов. Нарастают
склероз и гиалиноз клубочков. Просветы сохранившихся каналь-
цев резко и неравномерно расширены и заполнены веществом,
напоминающим коллоид (рис. 75). По строению почка становит-
ся похожей на щитовидную железу ("щитовидная почка"). Посте-
пенно почки уменьшаются в размерах и деформируются, поверх-
ность их становится крупнобугристой, капсула снимается с тру-
дом, развивается нефроцирроз.
Осложнения заключаются в возможности развития нефроген-
ной гипертонии; из-за потерь почками кальция и фосфатов воз-
можен вторичный гиперпаратиреоидизм.
Исходы хронического пиелонефрита зависят от длительности
его течения, одностороннего или двусторонего воспаления почек,
тяжести поражения почечных структур, от особенностей микро-
флоры. Полное выздоровление возможно только при раннем и
интенсивном лечении. Значительно чаще развиваются вторично-
сморщенная почка и хроническая почечная недостаточность, за-
канчивающаяся уремией.
Мочекаменная болезнь, или нефролитиаз, заключается в обра-
зовании в мочевых путях камней, формирующихся из составных
частей мочи. Заболевание течет хронически, можег быть как од-
носторонним, так и двусторонним. Чаще болеют мужчины, пре-
имущественно в возрасте 20-—40 лет.
Причины болезни подразделяют на:
• общие — наследственные и приобретенные нарушения ми-
нерального обмена и кислотно-щелочного равновесия, пре-
обладание в пище углеводов и белков, недостаток витамина
А. нарушения регуляции обмена веществ (например, при
гиперпаратиреозе);
• местные — замедление почечного кровотока и застой мочи,
воспаление в мочевых путях, тубулопатии (оксалатурия,
фосфатурия и т. п.), повышение в моче концентрации со-
лей, изменение ее pH и коллоидного равновесия.
Клиническая картина. Камни в почках могут длительное время
не проявляться клинически, однако они могут повреждать слизи-
стую оболочку лоханки, вызывая ее воспаление. Тогда появляют-
ся гематурия и пиурия. Типичны также почечные колики, возни-
кающие при продвижении камней в мочеточник, — резкая боль в
пояснице и нарушения мочевыделения. По составу различают
камни уратные, оксалатные, фосфатные, холестериновые и др.
Механизмы их образования описаны в главе 1.
Морфология заболевания зависит от локализации камней, их
величины, длительности процесса, наличия инфекции и других
факторов. Если камни расположены в лоханке, то она расширя-
ется, отток мочи нарушается, в паренхиме почки развиваются ат-
рофические и склеротические изменения, часто сопровождаю-
щиеся ее воспалением. Иногда воспаление распространяется на
паранефральную клетчатку — паранефрит. При обтурации кам-
295
нем просвета мочеточника нарушается отток мочи, она растяги-
вает лоханку и при длительном течении развивается гидронефроз —
атрофия паренхимы почки, которая превращается в большую по-
лость, окруженную склерозированной капсулой и заполненную
мочей.
Осложнения: пролежни и перфорация мочеточника, пионеф-
роз, пиелонефрит, уросепсис.
Исход при своевременном оперативном вмешательстве может
быть благоприятным, хотя нередко развиваются рецидивы болез-
ни. При двустороннем поражении почек и без хирургического
вмешательства заболевание может завершиться развитием хрони-
ческой почечной недостаточности и уремией. Смерть может на-
ступить и от осложнений.
Опухоли почек, как и других органов и тканей, разделяют на
доброкачественные и злокачественные, эпителиальные и мезен-
химальные.
Аденома — наиболее часто встречающаяся доброкачественная
опухоль почки. Развивается из эпителия канальцев, растет мед-
ленно, может достигать размеров самой почки, не дает метаста-
зов.
Гипернефроидный, или почечно-клеточный, рак — злокачест-
венная опухоль из канальцевого эпителия, самая распространен-
ная злокачественная опухоль почек у взрослых. Мужчины болеют
в 2 раза чаще женщин. Факторами риска считают тучность, дли-
тельный контакт с асбестом, наследственную кистозную болезнь
почек, длительный гемодиализ.
Клиническая картина. В большинстве случаев при развитии
почечно-клеточного рака у больных появляются боли в пояснице,
гематурия, реже — артериальная гипертензия, пиурия, похудание,
гиперкальциемия.
Морфология Опухоль имеет вид дольчатого узла, мягкой кон-
систенции, желтого цвета, часто с очагами некрозов и кровоиз-
лияний. Растет инфильтративно, прорастая капсулу почки, ло-
ханку, врастает в почечную вену и по венам может достигать пра-
вого предсердия ("опухолевые тромбы"). Микроскопически состо-
ит из полигональных опухолевых клеток с многочисленными ати-
пичными митозами. Опухолевые клетки образуют альвеолы и
дольки, железистые и сосочковые структуры с небольшим коли-
чеством стромы. Опухоль быстро метастазирует в регионарные
лимфатические узлы, нередко в противоположную почку. Рано
возникают гематогенные метастазы в легкие, кости, печень, над-
почечник, головной мозг.
Прогноз. При отсутствии метастазов 5-летняя выживаемость
после лечения составляет 45—70 %. При инвазии в почечную ве-
ну и метастазах в регионарные лимфатические узлы 5-летняя вы-
живаемость после лечения снижается до 15—20 %.
Нефробластома (опухоль Вильмса) — злокачественная опухоль
почки смешанного строения, состоящая из мезенхимальных и
эпителиальных эмбриональных элементов. В основном опухоль
296
развивается у детей 3—4 лет и составляет около 30 % всех злока-
чественных новообразований детского возраста, но иногда она
возникает и у взрослых. В развитии нефробластомы большое зна-
чение придают наследственной предрасположенности.
Клиническая картина. Опухоль может протекать бессимптомно
и обнаруживается случайно при пальпации в виде безболезненно-
го узла. В поздних стадиях заболевания наблюдаются резкое уве-
личение и асимметрия живота из-за болезненной опухоли, сдав-
ливающей соседние органы. В моче обнаруживаются лейкоциты,
отмечаются гематурия и протеинурия.
Морфология. Опухоль имеет вид узла, окруженного остатками
почечной ткани, на разрезе серовато-белого цвета, с очагами све-
жих и старых кровоизлияний. Микроскопически опухоль очень
полиморфна — состоит из атипичных недифференцированных
клеток разной формы, эмбрионального характера. В зависимости
от преобладания различных вариантов атипичных эмбриональных
клеток выделяют высоко-, средне- и низкозлокачественную фор-
мы опухоли Вильмса.
Прогноз после оперативного лечения у детей младше 2 лет бла-
гоприятнее, чем у больных более старшего возраста. При прорас-
тании опухоли за пределы капсулы почки прогноз неблагоприят-
ным даже после удаления нефробластомы.
Глава 19
БОЛЕЗНИ ЭНДОКРИННОЙ СИСТЕМЫ
Эндокринная система — совокупность специфических эндок-
ринных желез (желез внутренней секреции) и эндокринных кле-
ток. Она включает:
• гипофиз;
• эпифиз (шишковидная железа);
• щитовидную железу;
• околощитовидные железы;
• надпочечники;
• APUD-систему, или диффузную систему, образованную гор-
мональными клетками, рассеянными в различных органах и
тканях организма — эндокринные клетки желудочно-кишеч-
ного тракта, продуцирующие гастрин, глюкагон, соматоста-
тин и др.; интерстициальные клетки почек, вырабатываю-
щие, например, простагландин Е2, эритропоэтин, и анало-
гичные эндокринные клетки некоторых других органов.
Эндокринная клетка — клетка, синтезирующая и выделяющая
гормон в жидкие среды организма — кровь, лимфу, межклеточ-
ную жидкость, ликвор.
297
Гормон — биологически активное вещество, циркулирующее
в жидких средах организма и оказывающее специфическое
влияние на определенные клетки-мишени. Химическая структу-
ра гормонов различна. Большинство из них является пептидами
(белками), стероидными веществами, аминами, простагланди-
нами.
Клетка-мишень для гормона — это клетка, специфически взаи-
модействующая при помощи рецептора с гормоном и отвечаю-
щая на это изменением своей жизнедеятельности и функции.
ОБЩАЯ ПАТОЛОГИЯ ЭНДОКРИННОЙ СИСТЕМЫ
Нарушения деятельности эндокринных желез проявляются в
двух основных формах: гиперфункции (избыточной функции) и
гипофункции (недостаточной функции).
Основными начальными звеньями патогенеза эндокринных
расстройств могут быть центрогенные, первичные железистые и
постжелезистые нарушения.
Центрогенные расстройства обусловлены нарушением меха-
низмов нейрогуморальной регуляции желез внутренней секреции
на уровне головного мозга и гипоталамо-гипофизарного ком-
плекса. Причинами этих нарушений могут быть повреждения
ткани мозга в результате кровоизлияния, роста опухолей, дейст-
вия токсинов и инфекционных агентов, затянувшихся стресс-ре-
акций, психоз и др.
Последствиями повреждения головного мозга и гипоталамо-
гипофизарной системы являются нарушение образования нейро-
гормонов гипоталамуса и гормонов гипофиза, а также расстрой-
ства функций эндокринных желез, деятельность которых регули-
руется этими гормонами. Так, например, нервно-психическая
травма может привести к нарушению деятельности ЦНС, что
обусловливает избыточную функцию щитовидной железы и раз-
витие тиреотоксикоза.
Первичные железистые нарушения вызваны расстройствами
биосинтеза или выделения гормонов периферическими эндок-
ринными железами в результате уменьшения или увеличения
массы железы и соответственно уровня гормона в крови.
Причинами этих нарушений могут быть опухоли эндокринных
желез, в результате чего синтезируется избыточное количество
гормона, атрофия железистой ткани, в том числе и возрастная
инволюция, что сопровождается снижением гормональных влия-
ний, а также дефицит субстратов синтеза гормонов, например йо-
да, требующегося для образования тиреоидных гормонов, или не-
достаточный уровень биосинтеза гормонов.
Первичные железистые нарушения по принципу обратной
связи могут оказывать влияние на функцию коры головного моз-
га и гипоталамо-гипофизарную систему. Так, снижение функции
щитовидной железы (например, наследственный гипотиреоз)
298
приводит к нарушению деятельности ЦНС и развитию слабоумия
(тиреопривный кретинизм).
Постжелезистые расстройства обусловлены нарушениями
транспорта гормонов их рецепции, т. е. нарушением взаимодей-
ствия гормона со специфическим рецептором клетки и ткани и
метаболизма гормонов, что заключается в нарушении их биохи-
мических реакций, взаимодействия и деструкции.
БОЛЕЗНИ ЭНДОКРИННОЙ СИСТЕМЫ
ЗАБОЛЕВАНИЯ ГИПОФИЗА
Гипофиз — инкреторный орган, связывающий нервную и эн-
докринную системы, обеспечивая единство нейрогуморальной
регуляции организма. Гипофиз состоит из аденогипофиза и ней-
рогипофиза.
Основные функции гипофиза. Аденогипофиз продуцирует гор-
моны:
• фоллитропин (ранее его называли фолликулостимулирую-
щим гормоном, ФСГ);
• лютропин (ранее — лютеинизирующий гормон, ЛГ);
• пролактин (ранее — лютеомамматропный гормон, ЛТГ);
• кортикотропин (ранее — адренокортикотропный гормон,
АКТГ);
• тиреотропин (ранее — тиреотропный гормон. ТТГ) и ряд
других гормонов.
Нейрогипофиз выделяет в кровь два гормона: антидиуретиче-
ский и окситоцин.
Антидиуретический гормон (АДГ), или аргинин-вазопрессин,
усиливает реабсорбцию воды в почечных канальцах, а в высоких
концентрациях вызывает сокращения артериол клубочков и по-
вышение в них артериального давления.
Окситоцин регулирует физиологические процессы в женской
половой системе, увеличивает сократительную функцию беремен-
ной матки.
БОЛЕЗНИ, СВЯЗАННЫЕ С ГИПЕРФУНКЦИЕЙ АДЕНОГИПОФИЗА
Гиперпитуигаризм — избыток содержания или эффектов одно-
го или нескольких гормонов аденогипофиза.
Причины. В большинстве случаев гиперпитуитаризм является
результатом опухоли аденогипофиза или его повреждения при
интоксикациях и инфекциях.
Гипофизарный гигантизм проявляется чрезмерным увеличени-
ем роста и внутренних органов. При этом рост обычно выше
200 см у мужчин и 190 см у женщин, величина и масса внутрен-
них органов не соответствуют размерам тела, чаше органы также
299
Рис. 76. Акромегалия. Справа — здоровый, слева — больной акромега-
лией.
увеличены, реже — относительно уменьшены по сравнению со
значительным ростом. В связи с этим возможно развитие функ-
циональной недостаточности сердца и печени. Как правило, на-
блюдается гипергликемия, нередко сахарный диабет; отмечается
недоразвитие половых органов (гипогенитализм). нередко бес-
плодие; психические расстройства — эмоциональная неустойчи-
вость, раздражительность, нарушения сна, снижение умственной
работоспособности, психастения.
Акромегалия — заболевание, при котором диспропорциональ-
но увеличиваются размеры отдельных частей тела (чаще — кистей
рук, стоп), черты лица становятся грубыми за счет увеличения
нижней челюсти, носа, надбровных дуг, скул (рис. 76). Эти изме-
нения сочетаются с нарушениями жизнедеятельности организма
и постепенным развитием полиорганной недостаточности.
Синдром преждевременного полового развития — состояние, ха-
рактеризующееся ускоренным развитием половых желез, появле-
нием вторичных половых признаков, в некоторых случаях — на-
ступлением половой зрелости у девочек до 8-летнего, у мальчи-
ков до 9-летнего возраста, которая, однако, сопровождается пси-
хическим недоразвитием.
Гипофизарный гиперкорпщизм (болезнь Иценко—Кушинга) воз-
никает при избыточной продукции кортикотропина, что приво-
дит к гиперфункции коркового вещества надпочечников. Клини-
300
чески болезнь Иценко—Кушинга проявляется ожирением, тро-
фическими изменениями кожи, артериальной гипертензией, раз-
витием кардиомиопатии, остеопороза, нарушением половой функ-
ции, гиперпигментацией кожи, психическими нарушениями.
БОЛЕЗНИ, СВЯЗАННЫЕ С ГИПОФУНКЦИЕЙ АДЕНОГИПОФИЗА
Гипопитуитаризм — недостаточность содержания гормонов ги-
пофиза.
Причины. Гипофункция аденогипофиза может развиваться по-
сле перенесенного менингита или энцефалита, нарушения крово-
обращения в гипофизе (тромбоз, эмболия, кровоизлияние), че-
репно-мозговой травмы с повреждением основания черепа, а так-
же в результате белкового голодания.
Гипофункция аденогипофиза может проявляться гипофизарной
кахексией, гипофизарной карликовостью и гипофизарным гипо-
гонадизмом.
Гипофизарная кахексия развивается при тотальной гипофунк-
ции аденогипофиза, проявляющейся снижением образования
практически всех гормонов, что приводит к нарушению всех ви-
дов обмена веществ и прогрессирующему истощению.
Гипофизарная карликовость, или гипофизарный нанизм, раз-
вивается в случае недостаточности соматотропина и характеризу-
ется прогрессирующим отставанием в росте и массе тела (к пе-
риоду завершения формирования организма рост обычно не пре-
вышает ПО см у женщин и 130 см у мужчин), старческим видом
лица (морщины, сухая и дряблая кожа), недоразвитием половых
желез и вторичных половых признаков в сочетании с первичным
бесплодием. Интеллект в большинстве случаев не нарушен, одна-
ко нередко выявляются признаки снижения умственной работо-
способности и памяти.
Гипофизарный развивается при недостатке поло-
вых гормонов, обусловленном гипофункцией аденогипофиза. Он
проявляется:
• у мужчин — евнухоидизмом, для которого характерны недо-
развитие яичек и наружных половых органов, слабовыра-
женные вторичные половые признаки, высокий (женопо-
добный) тембр голоса, бесплодие, развитие женоподобной
фигуры, ожирение;
• у женщин — женским инфантилизмом, сопровождающимся
недоразвитием молочных желез, поздним началом менст-
руаций, нарушением менструального цикла вплоть до аме-
нореи, бесплодием, астеническим телосложением, эмоцио-
нальной неустойчивостью.
Гипофункция нейрогипофиза может возникать в результате
развития в нем опухоли, воспалительных процессов, травм, что
проявляется несахарным диабетом вследствие снижения образо-
вания АДГ. Для этого заболевания характерно выделение боль-
301
того количества мочи (от 4 до 40 л/сут) при ее низкой относи-
тельной плотности. Потеря воды и повышение осмотического
давления плазмы крови сопровождаются неукротимой жаждой
(полидипсией), вследствие которой больные в большом количест-
ве пьют воду.
БОЛЕЗНИ НАДПОЧЕЧНИКОВ
Надпочечники — парные эндокринные железы, расположен-
ные у верхних полюсов почек и состоящие из коркового (коры) и
мозгового вещества.
Основные функции надпочечников. В коре надпочечников син-
тезируется 3 группы стероидных гормонов: глюкокортикоиды,
минералокортикоиды и половые стероиды.
Глюкокортикоиды оказывают влияние на углеводный обмен,
обладают противовоспалительным действием и снижают актив-
ность иммунной системы.
Минералокортикоиды (у человека в основном альдостерон) ре-
гулируют обмен электролитов, прежде всего ионов натрия и ка-
лия.
Половые стероиды (андрогены и эстрогены) определяют разви-
тие вторичных половых признаков, а также стимулируют синтез
нуклеиновых кислот и белка.
Болезни, обусловленные гиперфункцией коры надпочечников
(гиперкортицизм), связаны с повышением содержания в крови
кортикостероидов и проявляется гиперальдостеронизмом и син-
дромом Иценко—Кушинга.
Гиперальдостеронизм обычно связан с развитием альдостеро-
мы — опухоли коркового вещества надпочечников. Характерны
задержка натрия в плазме и гипернатриемия. Повышается арте-
риальное давление, появляются аритмии сердца.
СиндромИценко—Кушинга развивается, как правило, при опу-
холи коркового вещества надпочечника, что сопровождается из-
бытком глюкокортикоидов. Характерно ожирение с отложением
жира на лице, шее, в области верхнего плечевого пояса. У боль-
ных повышаются артериальное давление и уровень глюкозы в
крови, часто повышена температура тела. Вследствие угнетения
иммунной системы снижается устойчивость к инфекциям. У
мальчиков ускорено и не соответствует возрасту развитие вторич-
ных половых признаков, но первичные половые признаки и по-
ведение отстают в развитии. У девочек появляются черты муж-
ского телосложения.
Болезни, обусловленные гипофункцией коры надпочечников,
или надпочечниковой недостаточностью. В зависимости от мас-
штаба поражения надпочечников выделяют 2 разновидности над-
почечниковой недостаточности: тотальную и парциальную.
Тотальнаянадпочечниковаянедостаточность обусловлена де-
фицитом всех гормонов коры надпочечника — глюко-, минерало-
302
кортикоидов и андрогенных стероидов. При этом отмечается
нормальный уровень катехоламинов, продуцирующихся мозго-
вым веществом надпочечников.
Парциальная надпочечниковаянедостаточность—недостаточ-
ность какого-либо одного класса гормонов коры надпочечников,
чаще всего — минерало- или глюкокортикоидов.
В зависимости от характера течения выделяют острую и хро-
ническую тотальную недостаточность коры надпочечников.
Острая тотальная недостаточность коры надпочечников. Ее
причины:
• Прекращение введения в организм кортикостероидов после
длительного их применения с лечебной целью. Развиваю-
щееся при этом состояние обозначают как синдром отмены
кортикостероидов или ятрогенную надпочечниковую недоста-
точность. Обусловлена продолжительным угнетением
функции гипоталамо-гипофизарно-надпочечниковой систе-
мы и атрофией коры надпочечников.
• Повреждение коры обоих надпочечников, например при
падении с большой высоты, двустороннем кровоизлиянии в
ее ткань при тромбогеморратическом синдроме, молние-
носно протекающем сепсисе.
• Удаление надпочечника, пораженного гормонопродуцирую-
щей опухолью. Однако недостаточность развивается только
при гипо- или атрофии коркового вещества второго надпо-
чечника.
Проявления:
• острая гипотензия:
• нарастающая недостаточность кровообращения, обуслов-
ленная острой сердечной недостаточностью, снижением то-
нуса мышц артериальных сосудов, уменьшением массы
циркулирующей крови в связи с ее депонированием. Как
правило, острая тяжелая недостаточность кровообращения
является причиной смерти большинства больных.
Хроническая тотальная недостаточность коры надпочечников
(болезнь Аддисона). Основной причиной служит разрушение ткани
коры надпочечников в результате иммунной аутоагрессии, тубер-
кулезного поражения, метастазов опухолей, амилоидоза.
Проявлениях
• мышечная слабость, утомляемость:
• артериальная гипотензия;
• полиурия;
• гипогидратация организма и гемоконцентрация в результате
снижения объема жидкости в сосудистом русле, приводя-
щего к гиповолемии;
• гипогликемия;
• гиперпигментация кожи и слизистых оболочек вследствие
повышения секреции аденогипофизом АКТГ и меланоци-
тостимулирующего гормона, так как оба гормона стимули-
руют образование меланина. Характерна для первичной
303
надпочечниковой недостаточности, при которой гипофиз
не поражен.
Болезни, обусловленные гиперфункцией мозгового вещества
надпочечников. Причины: опухоли из хромаффинных клеток моз-
гового вещества — доброкачественные (феохромоцитомы) и реже
злокачественные (феохромобластомы). Феохромоцитомы выраба-
тывают избыток катехоламинов, в основном норадреналина.
Проявления гиперкатехо лалине лии:
• артериальная гипертензия;
• острые гипотензивные реакции с кратковременной потерей
сознания в результате ишемии мозга (обморок), развиваю-
щиеся на фоне артериальной гипертензии, бледность, пот-
ливость, мышечная слабость, утомляемость;
• катехоламиновые гипертензивные кризы — периоды значи-
тельного повышения уровня артериального давления (сис-
толического до 200 мм рт. ст. и выше);
• нарушения ритма сердца в виде синусовой тахикардии и
экстрасистолии;
• гипергликемия и гиперлипидемия.
Недостаточность уровня или эффектов катехоламинов надпо-
чечников как самостоятельная форма патологии не наблюдается,
что обусловлено парностью надпочечников и их высокими ком-
пенсаторно-приспособительными возможностями.
БОЛЕЗНИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
Щитовидная железа является компонентом системы гипотала-
мус—гипофиз—щитовидная железа. Паренхима щитовидной же-
лезы состоит из трех видов клеток: А-, В- и С-клеток.
• А-клетки, или фолликулярные, вырабатывают йодсодержа-
щие гормоны. Они составляют большую часть массы же-
лезы.
• В-клетки продуцируют биогенные амины (например, серо-
тонин).
• С-клетки синтезируют гормон кальцитонин и некоторые
другие пептиды.
Структурной единицей щитовидной железы является фолли-
кул — полость, выстланная А- и С-клетками и заполненная кол-
лоидом.
Щитовидная железа вырабатывает йодсодержащие и пептид-
ные гормоны, регулирующие физическое, психическое и половое
развитие организма.
Йодсодержащие гормоны — трийодтиронин и тироксин. Рецеп-
торы тиреоидных гормонов имеются практически у всех клеток
организма.
Пептидные гормоны (кальцитонин, катакальцин и др.) синтези-
руются С-клетками. Увеличение содержания кальцитонина в кро-
ви происходит при опухолях щитовидной железы и при почечной
304
Рис. 77. Зоб.
недостаточности, сопровождающейся нарушением реабсорбции
кальция в канальцах почек.
Многочисленные заболевания щитовидной железы, характери-
зующиеся изменением уровня или эффектов йодсодержащих гор-
монов, объединяют в две группы: гипертиреозы и гипотиреозы.
Гипертиреозы, или тиреотоксикоз, характеризуются избытком
эффектов йодсодержащих гормонов в организме. При развитии
гипотиреозов наблюдается недостаточность эффектов этих гормо-
нов.
Заболевания щитовидной железы, сопровождающиеся гиперти-
реозом, Эти болезни возникают при нарушении деятельности са-
мой железы или в результате расстройства функций гипофиза или
гипоталамуса. Наибольшее значение среди этих болезней имеют
зоб (струма) и опухоли.
Зоб (струма) — узловатое или диффузное разрастание ткани
щитовидной железы (рис. 77).
Вцды зоба. По распространенности:
• эндемический зоб, причиной которого является недостаток
йода в воде и пище в некоторых регионах (в нашей стране
ряд районов Урала и Сибири);
305
• спорадический зоб, возникающий у жителей неэндемиче-
ских районов.
По .морфологии:
• диффузный зоб. характеризующийся равномерным разрас-
танием ткани железы;
• узловатый зоб, при котором разрастающаяся ткань железы
образует плотные узловатые образования различной вели-
чины ;
• коллоидный зоб, который отличается накоплением в фол-
ликулах коллоида;
• паренхиматозный зоб, который характеризуется разрастани-
ем эпителия фолликулов при почти полном отсутствии кол-
лоида.
Диффузный токсический зоб (базедова болезнь) составляет бо-
лее 80 % случаев гипертиреоза. Встречается обычно после 20—
50 лет. женщины болеют в 5—7 раз чаще мужчин.
Причины:
• наследственная предрасположенность;
• повторяющиеся психические травмы (стресс), вызывающие
активацию гипоталамуса и симпатико-адреналовой систе-
мы, что приводит к интенсивному образованию гормонов
щитовидной железы.
Патогенез. Начальным звеном патогенеза является наследуе-
мый генетический дефект лимфоцитов, обусловливающий синтез
плазматическими клетками большого количества "аутоагрессив-
ных" иммуноглобулинов. Особенность этих иммуноглобулинов
заключается в способности специфически взаимодействовать с
рецепторами для ТТГ на А-клетках эпителия фолликулов, стиму-
лировать образование и инкрецию ими в кровь трийодтиронина,
избыточное количество которого вызывает гипертиреоз или даже
тиреотоксикоз. Чем больше аутоагрессивных иммуноглобулинов
в крови, тем тяжелее тиреотоксикоз, характеризующийся значи-
тельным изменением обмена веществ: повышением уровня окис-
лительных процессов, основного обмена и температуры тела, что
приводит к резкому повышению чувствительности организма к
гипоксии. Усиливается распад гликогена, белков и жиров, возни-
кает гипергликемия, нарушается водный обмен.
Морфология. Зоб обычно диффузный, иногда узловатый. Гис-
тологически он характеризуется сосочковыми разрастаниями
эпителия фолликулов и лимфоплазмоцитарной инфильтрацией
стромы. В фолликулах очень мало коллоида.
Вследствие нарушения водного обмена в мышце сердца разви-
вается вакуольная дистрофия, сердце увеличивается в размерах; в
печени наблюдается серозный отек и в последующем — склероз;
нередки дистрофические изменения нервной ткани, в том числе
головного мозга (тиреотоксический энцефалит). Нарушения дея-
тельности нервной системы и мышц обусловлены возникающим
дефицитом АТФ, истощением в мышцах запаса гликогена и дру-
гими расстройствами обмена веществ.
306
Клиническая картина. У больных появляется характерная
триада — зоб, пучеглазие (экзофтальм) и тахикардия. Больные ху-
деют, они легко возбудимы, беспокойны; характерны быстрая
смена настроения, суетливость, утомляемость, дрожание пальцев
рук, повышение рефлексов. Тахикардия связана с активацией
симпатико-адреналовой системы. У больных отмечаются одышка,
повышение систолического артериального давления, полиурия.
Гипотиреоцдные состояния (гипотиреозы) характеризуются не-
достаточностью эффектов йодсодержащих гормонов в организме.
Встречаются у ОД—1 % населения, в том числе у новорожденных.
Причины. Различные этиологические факторы могут вызывать
гипотиреоз, действуя либо непосредственно на щитовидную же-
лезу, гипофиз, гипоталамические центры, либо снижая чувстви-
тельность клеток-мишеней к тиреоидным гормонам.
К числу наиболее часто встречающихся заболеваний, в основе
которых лежит гипотиреоз, относятся кретинизм и микседема.
Кретинизм — форма гипотиреоза, наблюдающаяся у новорож-
денных и в раннем детском возрасте.
Патогенез болезни связан с дефицитом гормонов трийодтиро-
нина и тироксина.
Основные проявления: отставание детей раннего возраста в фи-
зическом и умственном развитии. У больных карликовый рост,
грубые черты лица, что обусловлено отечностью мягких тканей;
большой язык, который часто не вмещается во рту; широкий
плоский "квадратный" нос с западением его спинки; далеко рас-
ставленные друг от друга глаза; большой живот, нередко с нали-
чием пупочной грыжи, что свидетельствует о слабости мускула-
туры.
Микседема — тяжелая форма гипотиреоза, развивающаяся,
как правило, у взрослых, а также у детей старшего возраста. Ха-
рактерным признаком микседемы является отек кожи и подкож-
ной клетчатки, при котором после надавливания на ткань не об-
разуется ямка (слизистый отек).
Причиной микседемы является недостаточность эффектов ти-
реоидных гормонов в результате первичного поражения щитовид-
ной железы (в 90 % случаев), реже — вторичного (травма, хирур-
гическое удаление большей части железы, воспаление, введение
препаратов, нарушающих синтез гормонов, дефицит йода и др.),
а также при нарушении функции аденогипофиза и гипоталамуса.
Патогенез. Существо характерного для болезни слизистого
отека состоит в накоплении воды не только во внеклеточной, но
и во внутриклеточной среде вследствие изменения свойств бел-
ков кожи и подкожной жировой клетчатки. При недостатке гор-
монов щитовидной железы происходит превращение белков в му-
циноподобное вещество, имеющее высокую гидрофильность.
Развитию отека способствует задержка воды в организме вследст-
вие усиления ее реабсорбции в почечных канальцах при недос-
татке тиреоидных гормонов.
У больных снижены частота сердечных сокращений и систо-
307
лическое артериальное давление. Окислительные процессы ос-
лаблены, понижены основной обмен и температура тела. Умень-
шается распад гликогена, белков и жиров; в крови отмечается ги-
погликемия. Усиливается и ускоряется развитие атеросклероза и
коронарной недостаточности вследствие ослабления распада жи-
ров, особенно холестерина.
Клиническая картина. Характерны внешний вид и поведение
больного: одутловатое лицо, сухая, холодная на ощупь кожа, при-
пухшие веки, суженные глазные щели. Типичны вялость, апатия,
сонливость, отсутствие интереса к окружающему, ослабление па-
мяти. Мышечный тонус снижен, ослаблены рефлексы, больные
быстро утомляются. Все эти изменения связаны с ослаблением
возбудительных процессов в ЦИС и нарушением обмена веществ.
Исход. Исходом микседемы, крайне тяжелым, нередко смер-
тельным, является гипотиреоидная, или микседематозная, кома.
Она может быть конечным этапом любой разновидности гипоти-
реоза при его неадекватном лечении или у нелеченых больных.
БОЛЕЗНИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
Поджелудочная железа выполняет, помимо экскреторной,
важную инкреторную функцию, обеспечивающую нормальное те-
чение обмена веществ в тканях. В а-клетках поджелудочной же-
лезы вырабатывается гормон глюкагон, а в р-клетках островкового
аппарата — инсулин.
• Инсулин усиленно вырабатывается при увеличении уровня
глюкозы в крови,- повышает утилизацию глюкозы тканями
и одновременно увеличивает запас источников энергии в
форме гликогена и жиров. Инсулин обеспечивает активный
процесс транспорта глюкозы из внеклеточной среды в клет-
ку. В самой клетке он повышает активность важного фер-
мента гексокиназы, в результате чего из глюкозы образуется
глюкозо-6-фосфат. Именно в этой форме глюкоза вступает
в различные метаболические превращения в клетке. Инсу-
лин стимулирует синтез гликогена и тормозит его распад,
повышая запас гликогена в тканях, прежде всего в печени и
мышцах.
• Глюкагон относится к группе контринсулярных гормонов:
стимулирует распад гликогена, тормозит его синтез и вызы-
вает гипергликемию.
Болезни, сопровождающиеся гиперфункцией островкового
аппарата поджелудочной железы
Повышение уровня инсулина в организме возникает при гор-
монопродуцирующей опухоли р-клеток поджелудочной железы —
инсуломе; при передозировке инсулина, используемого для лече-
ния сахарного диабета; при некоторых опухолях мозга. Это со-
308
стояние проявляется гипогликемией, вплоть до развития гипогли-
кемической комы.
Выделяют абсолютную и относительную недостаточность ост-
ровкового аппарата. При абсолютной недостаточности поджелу-
дочная железа не вырабатывает или вырабатывает мало инсулина.
В организме возникает дефицит этого гормона. При относитель-
ной недостаточности количество вырабатываемого инсулина яв-
ляется нормальным.
Сахарный диабет — хроническое заболевание, обусловленное
абсолютной или относительной инсулиновой недостаточностью,
приводящей к нарушению всех видов обмена веществ (прежде
всего углеводного, проявляющегося в гипергликемии), пораже-
нию сосудов (ангиопатии), нервной системы (нейропатии) и па-
тологическим изменениям в различных органах и тканях. Са-
харным диабетом в мире страдают свыше 200 млн человек, при-
чем наблюдается постоянная тенденция роста заболеваемости
на 6—10 %, особенно в промышленно развитых странах. В Рос-
сии за последние 15 лет количество больных сахарным диабетом
увеличилось в 2 раза и в некоторых регионах достигает 4 % от
всего населения, а среди людей старше 70 лет даже превышает
10%.
Классификация сахарного диабета.
• Сахарный диабет Imuna — инсулинозависимый, развивает-
ся в основном у детей и подростков (юношеский диабет) и
обусловлен гибелью р-клеток островков Лангерганса.
• Сахарный диабет II типа — инсулиннезависимый, развива-
ется у взрослых, чаще после 40 лет, и обусловлен как не-
достаточной функцией р-клеток. так и инсулиновой рези-
стентностью (невосприимчивостью к инсулину) тканей.
Причины болезни: наследственная неполноценность р-клеток
островков, нередко также склеротические изменения в поджелу-
дочной железе, развивающиеся по мере старения человека, ино-
гда — психическая травма. Развитию сахарного диабета может
способствовать неумеренное потребление углеводов. Существен-
ное значение может иметь изменение антигенных свойств инсу-
лина при его нормальной физиологической активности. В этом
случае в организме образуются антитела, связывающие инсулин и
предупреждающие его поступление в ткань. Важное значение мо-
жет иметь увеличение инактивации инсулина под влиянием фер-
мента инсулиназы, которая активируется СТГ гипофиза.
Сахарный диабет может возникать при значительном увеличе-
нии гормонов, снижающих действие инсулина и вызывающих ги-
пергликемию. При длительном избытке контринсулярных гормо-
нов относительная недостаточность инсулина может перейти в
абсолютную вследствие истощения р-клеток островкового аппа-
рата под влиянием гипергликемии.
Патогенез. Характерным для сахарного диабета является по-
вышение уровня глюкозы в крови (гипергликемия), которое мо-
жет доходить до 22 ммоль/л и более при норме 4,2—6,4 ммоль/л.
309
Гипергликемия обусловлена нарушением поступления глюкозы в
клетки, ослаблением использования ее тканями, снижением син-
теза и увеличением распада гликогена и усилением синтеза глю-
козы из белков и жиров. В нормальных условиях в почечных ка-
нальцах происходит полная реабсорбция глюкозы в кровь. Мак-
симальная концентрация глюкозы в плазме крови и первичной
моче, при которой она полностью реабсорбируется, составляет
10,0—11,1 ммоль/л. При концентрации выше этого уровня (порог
выведения для глюкозы) избыток ее выделяется с мочой. Это яв-
ление носит название "глюкозурия". Глюкозурия связана не только
с гипергликемией, но также и со снижением почечного порога
выведения, так как процесс реабсорбции глюкозы может проис-
ходить нормально только при превращении ее в эпителии почеч-
ных канальцев в глюкозо-6-фосфат. При сахарном диабете этот
процесс нарушается. В связи с усиленным распадом жиров обра-
зуются кетокислоты; при накоплении их в крови у больных раз-
вивается гиперкетонемия. Характерным для сахарного диабета
является также увеличение в крови уровня холестерина.
Гипергликемия приводит к повышению осмотического давле-
ния плазмы крови, что в свою очередь вызывает потерю тканями
воды (дегидратация); это сопровождается жаждой, увеличением
потребления воды и соответственно полиурией. Повышение
уровня глюкозы во вторичной моче и ее осмотического давления
снижает реабсорбцию воды в канальцах, вследствие чего возрас-
тает диурез. Гиперкетонемия способствует возникновению ацидо-
за и вызывает интоксикацию организма.
Патологическая анатомия. Морфологические изменения при
сахарном диабете представлены достаточно ярко. Поджелудочная
железа несколько уменьшена в размерах, склерозирована. Часть
островкового аппарата атрофируется и склерозируется, сохранив-
шиеся островки подвергаются гипертрофии.
Патология сосудов связана с нарушением углеводного, белко-
вого и жирового обмена. В крупных артериях развиваются атеро-
склеротические изменения, а в сосудах микроциркуляторного русла
возникают повреждения их базальных мембран, пролиферация
эндотелия и перителия. Все эти изменения заканчиваются скле-
розом сосудов всего микроциркуляторного русла — микроангиопа-
тия. Она приводит к поражению головного мозга, пищеваритель-
ного тракта, сетчатки глаз, периферической нервной системы.
Наиболее глубокие изменения микроангиопатия вызывает в поч-
ках. Вследствие повреждения базальных мембран и повышенной
проницаемости капилляров клубочков на капиллярных петлях
выпадает фибрин, что приводит к гиалинозу клубочков. Развива-
ется диабетический гломерулосклероз. Клинически он характеризу-
ется протеинуриеи, отеками, артериальной гипертензией. Печень
при сахарном диабете увеличена в размерах, в гепатоцитах отсут-
ствует гликоген, развивается их жировая дистрофия. Инфильтра-
ция липидами отмечается также в селезенке, лимфатических
узлах.
310
Варианты течения и осложнения сахарного диабета. У людей
разного возраста сахарный диабет имеет особенности и протекает
по-разному. У лиц молодого возраста заболевание характеризуется
злокачественным течением, у стариков — относительно доброка-
чественным. При сахарном диабете возникают разнообразные ос-
ложнения. Возможно развитие диабетической комы. Диабетиче-
ский гломерулосклероз осложняет сахарный диабет развитием
уремии. В результате макроангиопатии могут возникать тромбоз
сосудов конечностей и гангрена. Снижение сопротивляемости ор-
ганизма часто проявляется активацией гнойной инфекции в виде
фурункулов, пиодермии, пневмонии, иногда сепсиса. Указанные
осложнения сахарного диабета являются наиболее частыми при-
чинами смерти больных.
Глава 20
БОЛЕЗНИ НЕРВНОЙ СИСТЕМЫ
Заболевания нервной системы могут вызывать экзо- и эндо-
генные причины.
Экзогенными причинами являются:
• физические (механическая травма, ионизирующее излуче-
ние и т. п.);
• химические (ядохимикаты, фармакологические вещества, в
том числе наркотики, различные токсины и т. п.);
• биологические (нейротропные вирусы, микробы и их ток-
сины);
• психогенные (стресс и другие психотравмирующие ситуа-
ции).
Эндогенные причины:
• патология тканей, органов и физиологических систем орга-
низма, приводящая к расстройствам крово- и лимфообра-
щения в головном и спинном мозге;
• патологические влияния гормонов, нейромедиаторов и дру-
гих биологически активных веществ;
• гипо- и гипертермические состояния.
Основные механизмы повреждениянервной системы. Патогене-
тическую основу большинства форм нарушений нервной деятель-
ности составляют расстройства генерации и проведения передачи
импульсов возбуждения нейронами в результате:
• нарушения биосинтеза медиаторов — норадреналина, дофа-
мина. серотонина, ацетилхолина и др.;
• нарушения транспорта медиаторов по аксонам, обусловлен-
ного дефицитом некоторых витаминов, интоксикацией, от-
равлением нейротропными ядами и др.;
ЗП
• нарушения взаимодействия медиатора со специфическими
рецепторами клеток и внеклеточных структур.
ТИПОВЫЕ ФОРМЫ ПАТОЛОГИИ НЕРВНОЙ СИСТЕМЫ
Типовые формы патологии нервной системы могут проявлять-
ся в зависимости от преимущественного расстройства движений,
нарушения чувствительности, расстройства трофики, нарушений
высшей нервной деятельности.
НЕЙРОГЕННЫЕ РАССТРОЙСТВА ДВИЖЕНИЙ
Нейрогенные расстройства движений характеризуются патоло-
гическими изменениями количества движений, их темпа и коор-
динации:
Гипокинезии — уменьшение объема и скорости произвольных
движений. Они могут проявляться в виде:
• пареза — уменьшения объема и силы движений;
• паралича — полного отсутствия движений.
В зависимости от распространенности расстройств движений
выделяют:
• моноплегии — паралич одной конечности;
• параплегии — паралич обеих рук или ног;
• гемиплегии — паралич одной половины тела;
• тетраплегии — паралич рук и ног.
Гиперкинезии — увеличение непроизвольных движений.
Гиподинамии — снижение двигательной активности и силы
мышечных сокращений при движении.
Атаксии — нарушение координации движений.
НАРУШЕНИЯ ЧУВСТВИТЕЛЬНОСТИ. БОЛЬ
Нейрогенные нарушения любой чувствительности имеют в
своей основе повреждение соматосенсорного анализатора.
Все виды чувствительности формируются при раздражении ре-
цепторов кожи, слизистых оболочек, мышц, суставов и сухожи-
лий, о чем информация передается в ЦНС.
Формы расстройств чувствительности. В зависимости от вида
нарушений чувствительности выделяют:
• расстройство контактных видов чувствительности — так-
тильной. болевой, температурной при повреждении рецеп-
торов кожи и слизистых оболочек;
• расстройство дистантных видов чувствительности — зри-
тельной, слуховой, обоняния в результате поражений соот-
ветственно глазного или слухового анализатора, слизистой
оболочки носа.
312
В зависимости от нарушения восприятия интенсивности ощуще-
ния выделяют:
• гипестезию — снижение, или анестезию (полную потерю)
чувствительности;
• гиперестезию — повышение чувствительности к действию
раздражителя.
Причины нарушений восприятия ощущений:
• повышение чувствительности рецепторов, что наблюдается
при повреждении или заболеваниях кожи и слизистых обо-
лочек, например при ранах, ожогах, опоясывающем герпесе
и т. п.;
• повышение возбудимости нейронов сенсорных полей коры
головного мозга, гиппокампа, что отмечается при неврозах,
некоторых психических расстройствах, энцефалитах.
В зависимости от нарушения адекватности ощущения вызвавшему
его раздражителю. Эти расстройства называются дизестезиями.
Вцлщ дизестезий:
• термалгия — восприятие холодового и теплового воздейст-
вия как болевого;
• полиестезия — ощущение действия множества раздражите-
лей при воздействии одного реального фактора (например,
ощущение жжения, покалывания и давления при уколе ко-
жи иглой);
• аллодиния — восприятие неболевого воздействия как боле-
вого;
• гиперпатия — чрезмерная боль, возникающая при действии
различных раздражителей, в том числе неболевых (напри-
мер, поглаживание), сочетающаяся с потерей чувства точ-
ной локализации их действия;
• парестезия — тактильные неболевые, но необычные по ха-
рактеру ощущения в виде чувства онемения, одеревенения,
ползания "мурашек", покалывания. Возникают без явного
раздражителя.
Наиболее частые причины дизестезий:
• ишемия тканей;
• охлаждение тканей;
• патологические процессы, поражающие задние корешки
спинного мозга (например, спинная сухотка — поздняя
форма нейросифилиса).
Механизмы расстройств чувствительности. На уровне рецепторов:
• повышение или снижение порога чувствительности рецеп-
торов в силу различных причин;
• увеличение или уменьшение количества рецепторов при
ишемии или дистрофии клеток.
На уровне проводящих путей — торможение или полный блок
проведения импульса возбуждения. Развивается при повреждении:
• нервных стволов — при травмах, интоксикациях, гиповита-
минозах. сахарном диабете, инфекциях, аллергических ау-
тоиммунных процессах;
313
• задних корешков и задних рогов спинного мозга, что харак-
теризуется болями, парестезиями и сопровождается рас-
стройством кожной чувствительности по сегментарному ти-
пу в виде образования "полос нарушений" — круговых на
туловище и продольных на конечностях;
• боковых столбов спинного мозга, что приводит к выпаде-
нию болевой и температурной чувствительности на проти-
воположной от места поражения стороне.
На уровне центральных структур сенсорной системы:
• изменение порога чувствительности нейронов;
• нарушение формирования ощущений при действии либо
при отсутствии раздражителя.
Боль — особый вид чувствительности, возникающий под дей-
ствием патогенного раздражителя и характеризующийся неприят-
ным ощущением, а также, возможно, существенными изменения-
ми в организме, вплоть до нарушения жизнедеятельности и
смерти.
Значение боли: сигнальное и патогенное.
Сигнальное: ощущение боли вызывают различные агенты, об-
ладающие реальной или потенциальной опасностью повредить
организм. Поэтому болевой сигнал обеспечивает:
• мобилизацию организма для защиты от патогенного агента,
активацию фагоцитоза, изменение центрального и перифе-
рического кровообращения и т. п. Важной является защит-
ная поведенческая реакция на боль, направленная либо на
"уход" от действия повреждающего фактора, либо на его ли-
квидацию — отдергивание руки, извлечение инородного те-
ла и т. п.;
• ограничение функций органа или организма в целом; на-
пример, резкое болевое ощущение при инфаркте миокарда
сопровождается страхом смерти. Это заставляет больного
значительно ограничить двигательную активность, что в
свою очередь существенно снижает гемодинамическую на-
грузку на поврежденное сердце.
Патогенное. Боль нередко является причиной или компонен-
том патогенеза различных болезней и болезненных состояний.
Например, боль в результате травмы может вызвать шок; боль
при воспалении нервных стволов обусловливает нарушение
функции органов; развитие общих реакций организма — повы-
шение или снижение артериального давления, нарушение функ-
ции сердца, почек, легких и других органов.
Причины. Боль вызывают различные факторы:
• физические (например, механическая травма, повышенная
или пониженная температура, электрический ток);
• химические (например, действие на кожу или слизистые
оболочки сильных кислот, щелочей, накопление в ткани
солей кальция или калия);
• биологические (например, высокая концентрация медиато-
ров воспаления — кининов, гистамина, серотонина).
314
Механизмы формирования боли.
Рецепторы — свободные нервные окончания, способные вос-
принимать воздействия различных агентов как болевые, а также
специализированные рецепторы восприятия боли — ноцицепторы.
Нейрохимические механизмы активации ноцицепторов. Раздра-
жители. вызывающие боль, высвобождают из поврежденных кле-
ток ряд веществ (их нередко называют медиаторами боли), дейст-
вующих на ноцицепторы. Среди этих веществ основное значение
имеют биогенные амины (гистамин).
Проводящие пути:
• афферентные проводники боли, проникают в спинной мозг
через задние корешки и контактируют с нейронами задних
рогов;
• проводящие пути спинного мозга;
• нейроны таламуса, гипоталамуса, миндалевидного ком-
плекса. Эти структуры обусловливают системный ответ
организма на болевой стимул, включающий вегетативный,
двигательный, эмоциональный и поведенческий компо-
ненты.
Центральные нервные структуры. Целостное ощущение боли
формируется одновременным участием корковых и подкорковых
структур, воспринимающих импульсацию боли. В коре мозга
происходит отбор информации о болевом воздействии и форми-
рование целенаправленного "болевого поведения" для устранения
источника боли или уменьшения ее степени.
Клинически выделяют три разновидности боли:
• таламическая боль, которая характеризуется преходящими
эпизодами сильных, изнуряющих болей и болью, сочетаю-
щейся с вегетативными, двигательными и психоэмоцио-
нальными расстройствами;
• фантомная боль, которая ощущается в отсутствующей части
тела, чаще всего в ампутированных конечностях;
• каузалгия — приступообразно усиливающаяся жгучая боль в
области поврежденных нервных стволов, особенно трой-
ничного, лицевого, языкоглоточного и седалищного нервов.
Антиноцицептивная система образуется механизмами, контро-
лирующими чувство боли, и включает нейрогенные и гумораль-
ные механизмы. Нейрогенные механизмы обеспечиваются им-
пульсацией специальных нейронов головного мозга, которые тор-
мозят поток восходящей болевой информации к подкорковым и
корковым структурам. Гуморальные механизмы представлены ря-
дом биохимических систем, способных вырабатывать вещества,
подавляющие формирование боли. Нейрогенные и гуморальные
механизмы тесно взаимодействуют друг с другом и способны бло-
кировать болевую импульсацию на всех уровнях ноцицептивной
системы — от рецепторов до ее центральных структур.
Реакция организма на боль проявляется как адаптивными, так
и патогенными изменениями в организме и включает психоэмо-
циональный, вегетативный и двигательный компоненты.
315
Психоэмоциональный компонент. Кора головного мозга транс-
формирует боль в тягостное, неприятное ощущение. Боль — сиг-
нал повреждения организма, в связи с чем чувство боли всегда
носит негативный психоэмоциональный характер.
Вегетативный компонент. Боль является одной из причин
стресса, в связи с которым происходит активация нервной и эн-
докринной систем, дыхания, кровообращения, системы иммуно-
биологического надзора и других, направленных на ликвидацию
повреждающего фактора.
Двигательный компонент включает как непроизвольную реак-
цию на болевое воздействие (отдергивание конечности), так и це-
ленаправленное устранение болевого фактора, например горячего
предмета.
ЗАБОЛЕВАНИЯ НЕРВНОЙ СИСТЕМЫ
СОСУДИСТЫЕ ЗАБОЛЕВАНИЯ
Острое нарушение мозгового кровообращения по ишемическому
типу, или инфаркт мозга, — очаг некроза ткани мозга, возникаю-
щий вследствие острого прекращения его кровоснабжения.
Этиология. Причиной острого нарушения кровоснабжения
ткани мозга может быть атеросклероз магистральных артерий
шеи и основания мозга, гипертоническая болезнь, тромбоэмбо-
лия. жировая или воздушная эмболия, а также спазм артерий го-
ловного мозга.
Морфология. Очаг некроза наиболее часто локализуется в об-
ласти больших полушарий, реже — в стволе мозга. При благопри-
ятном течении заболевания выделяют 3 стадии течения инфаркта:
• некротическая стадия, в которой формируется зона некроза
ткани, по периферии которой располагаются нервные клет-
ки с признаками выраженных ишемических повреждений;
• репаративная стадия, которая характеризуется формирова-
нием новых капилляров по периферии зоны некроза и ми-
грацией в эту зону макрофагов и астроцитов, лизирующих
некротизированную ткань;
• стадия организации, в которой происходит активная проли-
ферация астроцитов и фибробластов. Организовавшийся
инфаркт мозга представляет собой полость с уплотненными
стенками.
Исход. В острой стадии инфаркта мозга смерть наступает от
обширного некроза либо от выраженного отека ткани мозга. На
стадиях организации и репарации смерть может наступить от ос-
ложнений — пневмонии, тромбоэмболии легочной артерии, вто-
ричных (реперфузионных) кровоизлияний в зону инфаркта.
Острое нарушение мозгового кровообращения по геморрагиче-
скому типу — очаг кровоизлияния в ткань головного мозга, обыч-
но с образованием гематомы.
316
Этиологическими факторами являются гипертоническая бо-
лезнь, разрыв аневризмы сосудов мозга, травма головного мозга
и др.
Морфология. Кровоизлияние чаще локализуется в области
больших полушарий, реже в области моста и крайне редко —
мозжечка. Выделяют два вида кровоизлияний:
• кровоизлияние по типу гематомы — представляет собой по-
лость, заполненную свертками крови. Стенки полости про-
питаны кровью, при благоприятном исходе в них скаплива-
ются сидерофаги, что придает образовавшейся кисте ржа-
вый вид;
• кровоизлияние по типу гемюррагического пропитывания —
характеризуется образованием в веществе мозга множества
мелких сливающихся очагов кровоизлияний без формиро-
вания полости.
Исход. При обширных кровоизлияниях смерть наступает
вследствие разрушения обширных участков мозга, отека мозга
или проникновения крови в желудочки мозга с их гемотампона-
дой. При благоприятном исходе обычно сохраняются нарушения
различных функций — двигательной, речевой и др.
Дегенеративные заболевания ЦНС — группа разнообразных за-
болеваний головного и спинного мозга, которые характеризуются
дистрофией и прогрессирующей атрофией нейронов и аксонов.
Среди них наибольшее значение в настоящее время имеет бо-
лезнь Альцгеймера.
Болезнь Альцгеймера — наиболее частая причина прогресси-
рующего слабоумия, составляет примерно 70 % от всех случаев
дегенеративных заболеваний нервной системы. У лиц моложе 60
лет частота возникновения заболевания составляет 2 случая на
100 000 жителей, а у лиц старше 60 лет — 127 случаев на 100 000
человек.
Этиология неизвестна, но у многих больных прослеживается
наследуемый характер заболевания. Некоторые специалисты вы-
сказывают предположение о связи болезни Альцгеймера с ами-
лоидозом.
Морфология характеризуется диффузной атрофией коры голов-
ного мозга с истончением борозд, углублением извилин и резким
истончением коры. Отмечается также выраженное расширение
боковых желудочков. Микроскопически в нейронах коры обнару-
живаются тонковолокнистые скопления и мелкие эозинофильные
включения, вакуольная дистрофия нейронов лимбической систе-
мы, а также хаотические скопления поврежденных аксонов, в
центре которых выявляется амилоид. Количество сохранившихся
нервных клеток не превышает 35 %. В сосудах мозга и его оболо-
чек — амилоидные отложения.
Исход. Заболевание обычно проходит несколько стадий, длит-
ся 7—10 лет и заканчивается полным слабоумием. Больные при-
кованы к постели и умирают часто от застойной бронхопневмо-
нии.
317
Болезнь Паркинсона — заболевание, проявляющееся в основ-
ном различными видами мышечной ригидности (скованности) и
тремором.
Этиология. Различают идиопатическую болезнь Паркинсона,
причина которой неизвестна, и паркинсонизм, когда клинические
проявления возникают вторично, на фоне перенесенной травмы,
инфекций, интоксикаций, сосудистых поражений и др.
Патогенез заболевания связан с уменьшением количества ней-
ронов в черном веществе и других областях мозга с уменьшением
уровня дофамина и метионин-энкефалина, преобладанием дейст-
вия холинергической системы.
Паркинсонизм — неврологический синдром, характеризую-
щийся тремором, скованностью движений, семенящей походкой,
согбенным положением тела, маскообразным лицом. Часто эти
явления сочетаются с нарушением обоняния. Возможно посте-
пенное развитие слабоумия.
Морфология заключается в атрофии пигментированных ядер
ствола мозга (черная субстанция) и уменьшении количества ней-
ронов в этой и других областях. В самих нейронах определяются
округлые включения. Характерно разрастание глии.
Исход при соответствующем медикаментозном или хирургиче-
ском лечении может быть благоприятным.
ТРАВМАТИЧЕСКИЕ ПОРАЖЕНИЯ ГОЛОВНОГО МОЗГА
К ним относятся сотрясение мозга, ушиб мозга, эпидуральная
и субдуральная гематомы.
Сотрясение мозга имеет достаточно яркую клинику, однако
морфологические изменения при этом выявляются только на
ультраструктурном уровне.
Ушиб мозга характеризуется повреждением ткани мозга,
обычно на стороне, противоположной приложению силы. Очаг
ушиба располагается в основном в коре и представляет собой
участок некроза ткани мозга с геморрагическим пропитыва-
нием.
Эпидуральная гематома — очаговое кровоизлияние между ко-
стью и наружным листком твердой мозговой оболочки, обычно
возникающее после сильного удара. Объем кровоизлияния боль-
ше 75 мл расценивается как смертельный.
Исход может быть благоприятным при своевременном оказа-
нии медицинской помощи, хотя послеоперационная летальность
составляет 10—15 %. Основной причиной смерти при этой травме
является отек и набухание головного мозга с вклинением и
ущемлением ствола в большом затылочном отверстии.
Субдуральная гематома — скопление крови между внутренним
листком твердой мозговой оболочки и паутинной оболочкой.
Причинами чаще являются падение с высоты собственного
роста, травма с ускорением, например при падении в результате
318
толчка, спортивная травма. Наиболее типичный механизм — раз-
рыв вен, проходящих в субдуральном пространстве. Перелом кос-
тей черепа наблюдается в 60 % случаев.
Морфология. Преимущественная локализация — лобно-темен-
ная область, у детей 80 % субдуральных гематом — двусторонние.
Излившаяся кровь напоминает "кровавое желе", объем свыше 100
мл считается смертельным. Иногда небольшие субдуральные ге-
матомы могут протекать бессимптомно и заканчиваться организа-
цией образовавшегося сгустка крови.
ОПУХОЛИ НЕРВНОЙ СИСТЕМЫ
Опухоли нервной системы — многочисленная группа новооб-
разований. Их строение и развитие зависят от вида нервной тка-
ни, которая дала начало опухолевому росту. Опухоли нервной
системы могут быть доброкачественными и злокачественными.
Однако новообразования, локализующиеся в головном и спин-
ном мозге, вне зависимости от морфологического строения вызыва-
ют тяжелые расстройства функций ЦНС и поэтому опасны для
жизни. Если не удалить даже доброкачественную опухоль, распо-
ложенную в полости черепа, то рано или поздно она сдавит мозг
и приведет к смерти больного. Злокачественные опухоли имеют,
кроме того, еще одну особенность — они метастазируют только
в пределах головного или спинного мозга.
Классификация опухолей нервной системы зависит от того, ка-
кие клетки явились источником опухолевого роста. Новообразо-
вания нервной ткани подразделяют на опухоли:
• центральной нервной системы;
• оболочек мозга;
• вегетативной нервной системы;
• периферической нервной системы.
Опухоли ЦНС подразделяют на нейроэктодермальные, нейро-
нальные и развивающиеся из низкодифференцированных и эм-
бриональных клеток нервной системы.
Нейроэктодермальные опухоли возникают на разных этапах
развития клеток глии и нейронов. Поэтому среди этих опухолей
выделяют глиомы — развивающиеся из различных видов глии:
• астроцитарной — астроцитомы и глиобластома;
• олигодендроглии — олигодендроглиома и злокачественная
олигодендроглиома;
• эпендимы и хориоидного эпителия — доброкачественные
(эпендимомы и хориоидпапиллома), злокачественные (ана-
пластическая эпендимома и хориоидкарцинома).
Нейрональные опухоли—развиваю щиеся из нервных клеток:
• ганглионеврома (доброкачественная);
• ганглионейробластома (злокачественная).
Опухоли, развивающиеся из низкодифференцированных и эм-
бриональных клеток нервной системы, только злокачественные.
319
низкодифференцированные опухоли — медуллобластома и глиоб-
ластома.
Менингососудистые опухоли развиваются в оболочках мозга.
Их разделяют на доброкачественные (менингиома и арахноидэн-
дотелиома) и злокачественные (менингеальные саркомы).
Опухоли вегетативной нервной системы развиваются в основ-
ном из ганглиозных клеток симпатических ганглиев, и в зависи-
мости от зрелости клеток здесь возникают доброкачественная —
ганглионеврома и злокачественные — симпатобластома и ганг-
лионейробластома.
Опухоли периферической нервной системы развиваются из
шванновских оболочек нервов, которые дают начало доброкаче-
ственным опухолям — неврилеммоме, или невриноме, и нейро-
фиброме. Нейрофибромы могут иметь множественный, систем-
ный характер как проявления болезни Реклингхаузена. Среди зло-
качественных опухолей наиболее часто встречается злокачествен-
ная неврилеммома.
Морфология почти всех указанных опухолей выявляется в ос-
новном под микроскопом. Однако приведенная классификация
помогает понять генез опухолей центральной, вегетативной и пе-
риферической нервной системы, которые в целом составляют
группу почти из 100 типов опухолей, и каждая из них имеет свои
морфологические и клинические особенности. Вместе с тем в
опухолях нервной ткани имеют место все те закономерности доб-
рокачественного и злокачественного роста, которые вообще при-
сущи опухолям (см. главу 10).
Глава 21
ИНФЕКЦИОННЫЕ БОЛЕЗНИ
Инфекционные болезни по распространению во всем мире за-
нимают третье место после болезней сердечно-сосудистой систе-
мы и опухолей. В различных странах распространены разные ин-
фекции, и на заболеваемость ими большое влияние оказывают
социальные условия жизни населения. Чем выше социальный и
культурный уровень населения, организация профилактической и
лечебной помощи, санитарного просвещения, тем меньше рас-
пространенность инфекционных заболеваний и смертность от
них.
Инфекционные болезни по существу отражают меняющиеся
взаимоотношения между микро- и макроорганизмами. В обыч-
ных условиях в разных органах человека и животных живет ог-
ромное количество микробов, с которыми установились симби-
онтные отношения, т. е. такие отношения, когда эти микроорга-
320
низмы не только не вызывают заболевания, но и способствуют
физиологическим функциям, например функции пищеварения.
Больше того, уничтожение таких микробов с помощью лекарств
приводит к возникновению тяжелых заболеваний — дисбактерио-
зов. Симбионтные отношения могут складываться по-разному,
что находит отражение в классификациях инфекционных болез-
ней.
КЛАССИФИКАЦИЯ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ
В зависимости от особенностей отношений между человеком и
микроорганизмом различают антропонозы, антропозоонозы и
биоценозы.
Антропонозы — инфекционные заболевания, свойственные
только человеку (например, сыпной тиф).
Антропозоонозы — инфекционные заболевания, которыми бо-
леют и люди, и животные (сибирская язва, бруцеллез и др.).
Биоценозы — инфекции, которые характеризуются тем, что для
их возникновения необходим промежуточный хозяин (так, на-
пример, возникает заболевание малярией). Поэтому биоценозы
могут развиваться лишь в тех местах, в которых они находят про-
межуточного хозяина.
КЛАССИФИКАЦИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ В ЗАВИСИМОСТИ
ОТ ЭТИОЛОГИИ
Очевидно, что для возникновения инфекционного заболева-
ния необходим определенный возбудитель, поэтому по этиологи-
ческому признаку все инфекции можно разделить на:
• вирусные;
• риккетсиозы;
• бактериальные;
• грибковые;
• протозойные;
• паразитарные.
По характеру заражения инфекции могут быть:
• эндогенными, если возбудители постоянно живут в орга-
низме и становятся патогенными в результате нарушений
симбионтных отношений с хозяином;
• экзогенными, если их возбудители попадают в организм из
окружающей среды.
МЕХАНИЗМЫ ПЕРЕДАЧИ ИНФЕКЦИИ
• фекально-оральный (через рот), который характерен для
кишечных инфекций;
321
воздушно-капельный, приводящий к развитию инфекций
дыхательных путей;
через кровососущих членистоногих передаются "кровяные
инфекции";
инфекции наружных покровов, клетчатки и мышц тела,
при которых возбудитель болезни попадает в организм в ре-
зультате травм;
инфекции, возникающие при смешанных механизмах пере-
дачи.
КЛАССИФИКАЦИЯ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ В ЗАВИСИМОСТИ
ОТ ОСОБЕННОСТЕЙ АДМ Н АЦИИ ВОЗБУДИТЕЛЕЙ К ТКАНЯМ
Эти особенности определяют клинико-морфологические про-
явления инфекционных болезней, по которым они группируются.
Выделяют инфекционные заболевания с преимущественным по-
ражением:
• кожных покровов, слизистых оболочек, клетчатки и мышц;
• дыхательных путей;
• пищеварительного тракта;
• нервной системы;
• сердечно-сосудистой системы;
• системы крови;
• мочеполовых путей.
ОБЩАЯ ХАРАКТЕРИСТИКА ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ
Имеются несколько важных общих положений, характеризую-
щих любое инфекционное заболевание. Каждая инфекционная бо-
лезнь имеет:
• своего специфического возбудителя;
• входные ворота, через которые возбудитель попадает в орга-
низм. Они характерны для каждого определенного вида
возбудителей;
• первичный аффект — участок ткани в области входных во-
рот, в котором возбудитель начинает повреждать ткань, что
вызывает воспаление;
• лимфангит — воспаление лимфатических сосудов, по кото-
рым возбудители, их токсины, остатки распавшейся ткани
отводятся от первичного аффекта в регионарный лимфати-
ческий узел;
• лимфаденит — воспаление лимфатического узла, регионар-
ного по отношению к первичному аффекту.
Инфекционный комплекс — триада повреждений, которую со-
ставляет первичный аффект, лимфангит и лимфаденит. Из инфек-
ционного комплекса инфекция может распространяться:
• лимфогенно;
322
• гематогенно;
• по тканевым и органным каналам (интраканаликулярно);
• периневрально;
• по контакту.
Генерализации инфекции способствует любой путь, но осо-
бенно первые два.
Заразность инфекционных болезней определяется наличием
возбудителя и путей передачи инфекции.
Каждая инфекционная болезнь проявляется:
• специфическими местными изменениями, характерными
для конкретной болезни, например язвы в толстой кишке
при дизентерии, своеобразное воспаление в стенках арте-
риол и капилляров при сыпном тифе;
• общими изменениями, характерными для большинства ин-
фекционных заболеваний и не зависящими от определен-
ного возбудителя. — кожными высыпаниями, гиперплазией
клеток лимфатических узлов и селезенки, дистрофией па-
ренхиматозных органов и др.
Реактивность и иммунитет при инфекционных болезнях. Разви-
тие инфекционных болезней, их патогенез и морфогенез, ослож-
нения и исходы зависят не столько от возбудителя, сколько от
реактивности макроорганизма. В ответ на проникновение любой
инфекции в органах иммунной системы образуются антитела, на-
правленные против антигенов возбудителей. Циркулирующие в
крови антимикробные антитела образуют комплекс с антигенами
возбудителей и комплементом, в результате чего возбудители
уничтожаются, а в организме возникает послеинфекционный гу-
моральный иммунитет. Вместе с тем проникновение возбудителя
вызывает сенсибилизацию организма, которая при повторном по-
явлении инфекта проявляется аллергией. Возникают реакции ги-
перчувствительности немедленного или замедленного типа, отра-
жающие различное проявление реактивности организма и обу-
словливающие появление общих изменений при инфекциях.
Общие изменения отражают морфологию аллергии в виде гипер-
плазии лимфатических узлов и селезенки, увеличения печени, со-
судистой реакции в виде васкулитов, фибриноидных некрозов, ге-
моррагии, сыпей и дистрофических изменений паренхиматозных
органов. Могут возникать различные осложнения, связанные в
значительной степени с морфологическими изменениями в тканях
и органах, развивающимися при гиперчувствительности немедлен-
ного и замедленного типа. Однако организм может локализовать
инфекцию, что и проявляется образованием первичного инфекци-
онного комплекса, появлением местных изменений, характерных
для конкретного заболевания и позволяющих отличить его от других
инфекционных болезней. Формируется повышенная устойчивость
организма к инфекции, отражающая зарождение иммунитета. В
дальнейшем на фоне нарастающего иммунитета развиваются репа-
ративные процессы и наступает выздоровление.
Вместе с тем иногда быстро истощаются реактивные свойства
323
организма, при этом приспособительные реакции оказываются
недостаточными и организм становится по существу беззащит-
ным. В этих случаях появляются некрозы, нагноения, микробы
обнаруживаются в большом количестве во всех тканях, т. е. раз-
виваются осложнения, связанные с резким снижением реактив-
ности организма.
Цикличность течения инфекционных болезней. Выделяют три
периода течения инфекционных болезней: инкубационный, про-
дромальный и период основных проявлений болезни.
Во время инкубационного, или латентного (скрытого), периода
возбудитель попадает в организм, проходит в нем определенные
циклы своего развития, размножается, в результате чего наступа-
ет сенсибилизация организма.
Продромальный период связан с нарастающей аллергией и появ-
лением общих реакций организма, проявляющихся в виде недо-
могания, слабости, головной боли, отсутствия аппетита, устало-
сти после сна. В этот период определить конкретное заболевание
еще нельзя.
Период основных проявлений болезни складывается из трех фаз:
• нарастания симптомов болезни;
• разгара болезни;
• исходов заболевания.
Исходами инфекционных болезней могут быть выздоровление,
остаточные явления осложнений болезни, хроническое течение
заболевания, бациллоносительство, смерть.
Патолюрфоз (изменение панорамы болезней). За последние 50
лет в большинстве стран мира заметно снизилось количество ин-
фекционных заболеваний. Некоторые из них, например натураль-
ная оспа, полностью ликвидированы во всем мире. Резко снизи-
лась заболеваемость такими болезнями, как полиомиелит, скарла-
тина, дифтерия и др. Многие инфекционные болезни под влияни-
ем эффективной лекарственной терапии и своевременных мер про-
филактики стали протекать гораздо благоприятнее, с меньшим ко-
личеством осложнений. Вместе с тем на земном шаре сохраняются
очаги холеры, чумы, желтой лихорадки, других инфекционных бо-
лезней, которые могут периодически давать вспышки, распростра-
няясь внутри страны в виде эпидемий или по всему миру — панде-
мий. Кроме этого, появились новые, особенно вирусные инфек-
ции, например синдром приобретенного иммунного дефицита
(СПИД), ряд своеобразных геморрагических лихорадок и др.
Инфекционных болезней очень много, поэтому приводим
описание лишь наиболее часто встречающихся и тяжело проте-
кающих.
ВИРУСНЫЕ БОЛЕЗНИ
Вирусы адаптированы к определенным клеткам организма.
Они проникают в них благодаря тому, что имеют на своей по-
верхности специальные "ферменты проникновения", которые
324
контактируют с рецепторами наружной мембраны определенной
клетки. При попадании вируса в клетку покрывающие его белки —
капсомеры разрушаются клеточными ферментами и высвобожда-
ется вирусная нуклеиновая кислота. Она проникает в клеточные
ультраструктуры, в ядро и вызывает изменение белкового обмена
клетки и гиперфункцию ее ультраструктур. При этом образуются
новые белки, имеющие те особенности, которые придает им ви-
русная нуклеиновая кислота. Таким образом, вирус "заставляет"
клетку работать на себя, обеспечивая собственную репродукцию.
Клетка перестает выполнять свою специфическую функцию, в
ней нарастает белковая дистрофия, затем она некротизируется, а
образовавшиеся в ней вирусы, оказавшись свободными, проника-
ют в другие клетки организма, поражая все большее их количест-
во. Этот общий принцип действия вирусов в зависимости от их
специфики может иметь и некоторые особенности. Для вирусных
заболеваний характерны все указанные выше общие признаки
инфекционных болезней.
Грипп — острое вирусное заболевание, относящееся к группе
антропонозов.
Этиология. Возбудителем болезни является группа вирусов,
которые морфологически сходны между собой, но отличаются
антигенной структурой и не дают перекрестного иммунитета. Ис-
точником заражения является больной человек. Для гриппа ха-
рактерны массовые эпидемии.
Эпидемиология. Вирус гриппа передается воздушно-капельным
путем, он попадает в клетки эпителия слизистой оболочки верх-
них дыхательных путей, затем проникает в кровоток — возникает
«премия. Токсин вируса оказывает повреждающее действие на со-
суды микроциркуляторного русла, повышая их проницаемость.
Одновременно вирус гриппа контактирует с иммунной системой,
а затем вновь скапливается в клетках эпителия верхних дыхатель-
ных путей. Вирусы фагоцитируются нейтрофильными лейкоцита-
ми. но последние их не уничтожают, напротив — вирусы сами уг-
нетают функцию лейкоцитов. Поэтому при гриппе нередко акти-
визируется вторичная инфекция и возникают связанные с ней
осложнения.
Патогенез и патологическая анатомия. По клиническому тече-
нию выделяют легкую, средней тяжести и тяжелую формы гриппа.
Легкая форма. После внедрения вируса в клетки эпителия
слизистых оболочек носа, зева, гортани у больных возникает ка-
таральное воспаление верхних дыхательных путей. Оно проявляет-
ся гиперемией сосудов слизистых оболочек, усиленным образова-
нием слизи, белковой дистрофией, гибелью и слущиванием кле-
ток мерцательного эпителия, в которых происходит репродукция
вируса. Легкая форма гриппа продолжается 5—6 дней и заканчи-
вается выздоровлением.
Грипп средней тяжести характеризуется распространением
воспаления на трахею, бронхи, бронхиолы и легкие, причем в
слизистых оболочках возникают очаги некроза. В эпителиальных
325
клетках бронхиального дерева и в клетках альвеолярного эпите-
лия содержатся вирусы гриппа. В легких возникают фокусы
бронхопневмонии и очаги ателектаза, которые также подвергают-
ся воспалению и могут стать источником затянувшейся хрониче-
ской пневмонии. Эта форма гриппа особенно тяжело протекает у
маленьких детей, стариков и больных сердечно-сосудистыми за-
болеваниями. Она может закончиться смертью от сердечной не-
достаточности.
Тяжелая форма гриппа имеет две разновидности:
• грипп с преобладанием явлений интоксикации организма,
которая может быть выражена настолько резко, что боль-
ные погибают на 4—6-й день болезни. На вскрытии опреде-
ляется резкое полнокровие верхних дыхательных путей,
бронхов и легких. В обоих легких имеются очаги ателекта-
зов и ацинозной пневмонии. В головном мозге и во внут-
ренних органах обнаруживаются кровоизлияния.
• Грипп с легочными осложнениями развивается при присое-
динении бактериальной инфекции, чаще стафилококковой.
На фоне выраженной интоксикации организма в дыхатель-
ных путях возникает фибринозно-гелюррагическое воспаление
с глубокими некрозами стенки бронхов. Это способствует
образованию острых бронхоэктазов. Скопление экссудата в
бронхах ведет к развитию ателектазов в легких и очаговой
бронхопневмонии. Присоединение бактериальной инфек-
ции нередко приводит к возникновению некрозов и абсцес-
сов в участках пневмонии, кровоизлияний в окружающие
ткани. Легкие увеличиваются в объеме, имеют пестрый
вид— "большие пестрые легкие ".
Осложнения и исходы. Интоксикация и поражение сосудистого
русла могут явиться причиной осложнений и смерти. Так, в па-
ренхиматозных органах развиваются выраженные дистрофиче-
ские изменения, причем дистрофия и некробиоз интрамуральных
нервных ганглиев сердца могут вызвать его остановку. Стаз, пе-
рикапиллярные диапедезные кровоизлияния и гиалиновые тром-
бы в капиллярах головного мозга становятся причиной его отека,
вклинения миндалин мозжечка в большое затылочное отверстие
и смерти больных. Иногда развивается энцефалит, от которого
также больные умирают.
Аденовирусная инфекция — острое инфекционное заболевание,
при котором попадающий в организм ДНК-содержащий аденови-
рус вызывает воспаление дыхательных путей, лимфоидной ткани
зева и глотки. Иногда поражаются кишечник и конъюнктива глаз.
Эпидемиология. Инфекция передается воздушно-капельным пу-
тем. Аденовирусы проникают в ядра клеток эпителия слизистой
оболочки, где размножаются. В результате клетки погибают и воз-
никает возможность для генерализации инфекции. Выход вирусов
из погибших клеток сопровождается явлениями интоксикации.
Патогенез и патологическая анатомия. Болезнь протекает в
легкой или тяжелой форме.
326
• При легкой форме обычно развиваются катаральные
ринит, ларингит и трахеобронхит, иногда фарингит. Неред-
ко к ним присоединяется острый конъюнктивит. Слизистая
оболочка при этом гиперемирована, инфильтрирована се-
розным экссудатом, в котором видны аденовирусные клет-
ки, т. е. погибшие и слущенные клетки эпителия. Они уве-
личены в размерах, в крупных ядрах содержатся вирусные,
а в цитоплазме — фуксинофильные включения. У малень-
ких детей аденовирусная инфекция нередко протекает в
форме пневмонии.
• Тяжелая форма заболевания развивается при генера-
лизации инфекции. Вирус поражает клетки различных
внутренних органов и головного мозга. При этом резко на-
растает интоксикация организма и снижается его сопротив-
ляемость. Создается благоприятный фон для присоедине-
ния вторичной бактериальной инфекции, вызывающей ан-
гину. отит, синуситы, пневмонию и т. д.. причем нередко
катаральный характер воспаления сменяется гнойным.
Исход. Осложнения аденовирусной инфекции — пневмонии,
менингит, миокардит — могут привести к смерти больного.
Полиомиелит — острое вирусное заболевание с преимущест-
венным поражением передних рогов спинного мозга.
Эпидемиология. Заражение происходит алиментарным путем.
Вирус размножается в глоточных миндалинах, пейеровых бляшках,
в лимфатических узлах. Затем он проникает в кровь и в дальней-
шем фиксируется либо в лимфатическом аппарате пищеваритель-
ного тракта (в 99 % случаев), либо в двигательных нейронах перед-
них рогов спинного мозга (в 1 % случаев). Там вирус размножает-
ся, вызывая тяжелую белковую дистрофию клеток. При их гибели
вирус выделяется и поражает другие двигательные нейроны.
Патогенез и патологическая анатомия полиомиелита склады-
ваются из нескольких стадий.
Предпаралитическая стадия характеризуется нарушением кро-
вообращения в спинном мозге, дистрофией и некробиозом двига-
тельных нейронов передних рогов спинного мозга и гибелью час-
ти из них. Процесс не ограничивается передними рогами спин-
ного мозга, а распространяется на двигательные нейроны продол-
говатого мозга, ретикулярной формации, среднего мозга, проме-
жуточного мозга и передних центральных извилин. Вместе с тем
изменения в этих отделах мозга выражены меньше, чем в спин-
ном мозге.
Паралитическая стадия характеризуется очаговым некрозом
вещества спинного мозга, выраженной реакцией глии вокруг по-
гибших нейронов и лейкоцитарной инфильтрацией ткани и обо-
лочек мозга. В этот период у больных полиомиелитом развивают-
ся тяжелые параличи, нередко и дыхательный мускулатуры.
Восстановительная стадия, а затем стадия остаточных явлений
развиваются в том случае, если больной не погибает от дыхатель-
ной недостаточности. На месте очагов некроза в спинном мозге
327
образуются кисты, а на месте погибших групп нейронов — гли-
альные рубчики.
При полиомиелите в миндалинах, групповых и солитарных
фолликулах, лимфатических узлах отмечается гиперплазия лим-
фоидных клеток. В легких возникают очаги коллапса и наруше-
ния кровообращения; в сердце — дистрофия кардиомиоцитов и
межуточный миокардит; в скелетной мускулатуре, особенно ко-
нечностей и дыхательных мышц, — явления нейрогенной атро-
фии. На фоне изменений в легких развивается пневмония. В свя-
зи с повреждением спинного мозга возникают параличи и кон-
трактуры конечностей. В остром периоде больные могут погиб-
нуть от дыхательной недостаточности.
Энцефалит — воспаление головного мозга. Энцефалит может
быть вызван вирусами, риккетсиями, бактериями, паразитами, но
может иметь и неинфекционное происхождение.
Весенне-летний клещевой энцефалит имеет наибольшее значе-
ние среди различных энцефалитов.
Эпидемиология. Это биоциноз, вызываемый нейротропным ви-
русом и передающийся кровососущими клещами от животных-
носителей человеку. Входными воротами для нейротропного ви-
руса являются кровеносные сосуды кожи. При укусе клеща вирус
попадает в кровь, а затем в паренхиматозные органы и головной
мозг. В этих органах он размножается и непрерывно поступает в
кровь, контактирует со стенкой сосудов микроциркуляторного
русла, обусловливая их повышенную проницаемость. Вместе с
плазмой крови вирус выходит из сосудов и вследствие нейро-
тропности поражает нервные клетки мозга.
Клиническая картина. Энцефалит обычно протекает остро, из-
редка — хронически. Продромальный период короткий. В перио-
де разгара развиваются лихорадка до 38 °C, глубокая сонливость,
иногда доходящая до комы, появляются глазодвигательные рас-
стройства — двоение в глазах, расходящееся косоглазие и другие
симптомы. Острый период продолжается от нескольких суток до
нескольких недель. В этот период больные могут погибнуть от
комы.
Патологическая анатомия. Макроскопическое изменение
мозга при вирусном энцефалите заключается в диффузном или
очаговом полнокровии его сосудов, появлении мелких кровоиз-
лияний в сером и белом веществе, некотором его набухании. Бо-
лее специфична микроскопическая картина энцефалита. Она ха-
рактеризуется множественными васкулитами сосудов мозга и
мягких мозговых оболочек со скоплением вокруг сосудов ин-
фильтратов из лимфоцитов, макрофагов, нейтрофильных лейко-
цитов. В нервных клетках возникают дистрофические, некробио-
тические и некротические процессы, в результате которых клетки
погибают в определенных участках мозга либо группами по всей
его ткани. Гибель нервных клеток обусловливает пролиферацию
глии: вокруг погибших клеток, а также вокруг очагов воспаления
сосудов образуются узелки (гранулемы).
328
Исход. В ряде случаев энцефалит заканчивается благополучно,
часто после выздоровления сохраняются остаточные явления в
виде головной боли, периодической рвоты и других симптомов.
Нередко после эпидемического энцефалита остаются стойкие па-
раличи мышц плечевого пояса и развивается эпилепсия.
РИККЕТСИОЗЫ
Риккетсиями называют микроорганизмы, занимающие проме-
жуточное положение между вирусами и бактериями. Как и виру-
сы, риккетсии являются внутриклеточными паразитами. Они
внедряются и размножаются в эндотелиоцитах сосудов. Носите-
лями риккетсии являются кровососущие членистоногие (вши,
блохи, клещи), а также некоторые дикие и домашние животные.
Современная классификация выделяет 10 групп риккетсиозов,
однако наибольшее значение в патологии имеет эпидемический
сыпной тиф.
Эпидемический сыпной тиф — острое инфекционное заболева-
ние, протекающее с выраженными явлениями интоксикации
ЦНС. В начале века оно носило характер эпидемий, в настоящее
время встречается в виде спорадических случаев.
Этиология. Возбудителем эпидемического сыпного тифа явля-
ется риккетсия Провацека.
Эпиделшология. Источником инфекции служит больной чело-
век, а переносит риккетсии от больного к здоровому платяная
вошь, которая кусает здорового человека, одновременно выделяя
зараженные риккетсиями фекалии. При расчесе места укуса фе-
калии втираются в кожу и риккетсии попадают в кровь, а затем
проникают в эндотелий сосудов.
Патогенез. Токсин риккетсии Провацека оказывает повреж-
дающее действие в первую очередь на нервную систему и сосуды.
Инкубационный период продолжается 10—12 дней, после чего
появляются продромы и начинается лихорадочный период, или
разгар болезни. Он характеризуется повреждением и параличом
сосудов микроциркуляторного русла во всех органах, но особенно
в головном мозге.
Внедрение риккетсии и размножение их в эндотелии микросо-
судов обусловливают развитие васкулитов. На коже васкулиты
проявляются в виде сыпи, появляющейся на 3—5-й день болезни.
Особенно опасны васкулиты, возникающие в ЦНС, в частности в
продолговатом мозге. На 2—3-й день заболевания в связи с пора-
жением продолговатого мозга может нарушаться дыхание. Пора-
жение симпатической нервной системы и надпочечников обу-
словливает падение артериального давления, нарушается функ-
ция сердца и может развиться острая сердечная недостаточность.
Сочетание васкулитов и расстройств нервной трофики приводит
к возникновению пролежней, особенно в участках тела, которые
подвергаются даже незначительному давлению — в области лопа-
329
ток, крестца, пяток. Развиваются некрозы кожи пальцев под
кольцами и перстнями, кончика носа, мочки уха.
Патологическая анатомия. На вскрытии умерших каких-либо
характерных для сыпного тифа изменений обнаружить не удает-
ся. Вся патологическая анатомия этого заболевания выявляется
под микроскопом. Наблюдается воспаление артериол, прекапил-
ляров и капилляров. Происходят набухание, слущивание эндоте-
лия и образование тромбов в сосудах. Постепенно нарастает про-
лиферация эндотелия и перицитов, вокруг сосудов появляются
лимфоциты. В стенке сосудов может развиться фибриноидный
некроз, и она разрушается. В итоге возникает сыпнотифозный де-
структивно-пролиферативный эндотромбоваскулит, при котором
сам сосуд теряет очертания. Эти явления развиваются не на всем
протяжении сосуда, а лишь в отдельных его участках, которые
приобретают вид узелков — сыпнотифозные гранулемы Попова (по
имени автора, впервые их описавшего). Гранулемы Попова обна-
руживаются почти во всех органах. В головном мозге образование
гранулем Попова, а также описанных выше других изменений
микроциркуляции приводит к некрозу нервных клеток, пролифе-
рации нейроглии, а весь комплекс морфологических изменений
обозначается как сыпнотифозный энцефалит. В сердце развивает-
ся межуточный миокардит. В крупных сосудах появляются очаги
некроза эндотелия, что способствует образованию пристеночных
тромбов и развитию инфарктов в головном мозге, сетчатке глаз и
других органах.
Исход. У леченых больных исход в большинстве случаев, осо-
бенно у детей, благоприятный. Однако смерть при сыпном тифе
может наступить от острой сердечно-сосудистой недостаточности.
БОЛЕЗНИ, ВЫЗЫВАЕМЫЕ БАКТЕРИЯМИ
Брюшной тиф — острое инфекционное заболевание, относя-
щееся к группе антропонозов и вызываемое тифозной сальмонел-
лой.
Эпидемиология. Источником заболевания является больной че-
ловек или бациллоноситель, в выделениях которого (кал, моча,
пот) содержатся брюшнотифозные бактерии. Заражение происхо-
дит при попадании возбудителей с загрязненными, плохо вымы-
тыми продуктами питания в рот, а затем в пищеварительный
тракт (фекально-оральный путь заражения).
Патогенез и патологическая анатомия Инкубационный пери-
од продолжается около 2 нед. В нижнем отделе тонкой кишки
бактерии начинают размножаться, выделяя эндотоксины. Затем
по лимфатическим сосудам они поступают в групповые и соли-
тарные фолликулы кишки и в регионарные лимфатические узлы.
Дальнейшая инкубация сальмонелл обусловливает стадийное раз-
витие брюшного тифа (рис. 78).
1-я стадия — стадия мозговидного набухания солитарных фолли-
330
Рис. 78. Брюшной тиф.
а — мозговидное набухание групповых и солитарных фолликулов, б — некроз со-
литарных фолликулов и образование грязных язв, в — чистые язвы.
кулов — развивается в ответ на первый контакт с возбудителем,
на который организм отвечает нормергической реакцией. Они
увеличиваются, выступают над поверхностью кишки, в них появ-
ляются борозды, напоминающие извилины мозга. Это происхо-
дит за счет гиперплазии ретикулярных клеток групповых и соли-
тарных фолликулов, которые вытесняют лимфоциты и фагоцити-
руют брюшнотифозные палочки. Такие клетки называются
брюшнотифозными клетками, они образуют брюшнотифозные
гранулемы. Эта стадия продолжается 1 нед. В это время бактерии
из лимфатических путей попадают в кровь. Возникает бактерие-
мия. Контакт бактерий с сосудами обусловливает их воспаление
и появление на 7—11-й день болезни сыпи — брюшнотифозной
экзантемы. С кровью бактерии проникают во все ткани, контак-
тируют с органами иммунной системы, а также вновь попадают в
солитарные фолликулы. Это вызывает их сенсибилизацию, нарас-
тание аллергии и начало становления иммунитета. В этот период,
т. е. на 2-й неделе заболевания, в крови появляются антитела к
брюшнотифозной сальмонелле и ее можно высеять из крови, по-
та, кала, мочи; больной становится особенно заразен. В желчных
путях бактерии усиленно размножаются и с желчью вновь посту-
пают в кишку, в третий раз контактируя с солитарными фоллику-
лами, и развивается вторая стадия.
2-я стадия — стадия некроза солитарных фолликулов. Она раз-
331
вивается на 2-й неделе болезни. Это гиперергическая реакция,
являющаяся реакцией сенсибилизированного организма на раз-
решающее воздействие.
3-я стадия — стадия грязных язв — развивается на 3-й неделе
заболевания. В этот период некротизированная ткань начинает
частично отторгаться.
4-я стадия — стадия чистых язв — развивается на 4-й неделе и
характеризуется полным отторжением некротизированной ткани
солитарных фолликулов. Язвы имеют ровные края, дном служит
мышечный слой стенки кишки.
5-я стадия — стадия заживления — совпадает с 5-й неделей и
характеризуется заживлением язв, причем происходит полное
восстановление тканей кишки и солитарных фолликулов.
Циклические проявления болезни, помимо изменений в тон-
кой кишке, отмечаются и в других органах. В лимфатических уз-
лах брыжейки, так же как и в солитарных фолликулах, происхо-
дит гиперплазия ретикулярных клеток и образование брюшноти-
фозных гранулем. Селезенка резко увеличивается в размерах, на-
растает гиперплазия ее красной пульпы, которая на разрезе дает
обильный соскоб. В паренхиматозных органах наблюдаются вы-
раженные дистрофические изменения.
Осложнения. Среди кишечных осложнений наиболее опасны
возникающие во 2, 3 и 4-й стадиях болезни кишечные кровотече-
ния, а также прободение язв и развитие разлитого перитонита.
Среди других осложнений наибольшее значение имеют очаговая
пневмония нижних долей легких, гнойный перихондрит гортани
и развитие пролежней у входа в пищевод, восковидный некроз
прямых мышц живота, гнойный остеомиелит.
Исход в большинстве случаев благоприятный, больные выздо-
равливают. Смерть больных наступает, как правило, от осложне-
ний брюшного тифа — кровотечений, перитонита, пневмонии.
Дизентерия, или шигеллез, — острое инфекционное заболева-
ние, характеризующееся поражением толстой кишки. Она вызы-
вается бактериями — шигеллами, единственным резервуаром ко-
торых является человек.
Эпидемиология. Путь передачи фекально-оральный. Возбудите-
ли попадают в организм с пищей или водой и размножаются в
эпителии слизистой оболочки толстой кишки. Проникая в клетки
эпителия, шигеллы становятся недоступными действию лейкоци-
тов, антител, антибиотиков. В эпителиальных клетках шигеллы
размножаются, при этом клетки гибнут, слущиваются в просвет
кишки, и шигеллы инфицируют содержимое кишки. Эндотоксин
погибших шигелл оказывает повреждающее действие на крове-
носные сосуды и нервные ганглии кишки. Внутриэпителиальное
существование шигелл и действие их токсина определяют различ-
ный характер воспаления кишки в разные стадии дизентерии
(рис. 79).
Патогенез и патологическая анатомия.
1-я стадия — катаральный колит, болезни продолжается 2—3
332
a
Рис. 79. Изменения толстой кишки при дизентерии.
а — катаральный колит; б — фибринозный колит, начало образования язв; в —
заживление язв, полипозные разрастания слизистой оболочки; г — рубцовые из-
менения в кишке.
дня, в прямой и сигмовидной кишках развивается катаральное
воспаление. Слизистая оболочка гиперемирована, отечна, ин-
фильтрирована лейкоцитами, имеются кровоизлияния, усиленно
продуцируется слизь, мышечный слой стенки кишки спазмиро-
ван.
2-я стадия — дифтеритический колит, длится 5—10 дней. Вос-
паление кишки приобретает характер фибринозного, чаще дифте-
ритического. На слизистой оболочке образуется фибринозная
пленка зелено-коричневого цвета. Под микроскопом виден нек-
роз слизистой оболочки и подслизистого слоя, иногда распро-
страняющийся и на мышечный слой стенки кишки. Некротизи-
рованная ткань пропитана фибринозным экссудатом, по краям
некроза слизистая оболочка инфильтрирована лейкоцитами, име-
ются кровоизлияния. Тяжелым дистрофическим и некробиотиче-
ским изменениям подвергаются нервные сплетения стенки
кишки.
3-я стадия — язвенный колит, наступает на 10—12-и день бо-
лезни, когда фибринозно-некротическая ткань отторгается. Язвы
имеют неправильную форму и различную глубину.
4-я стадия — стадия заживления язв, развивается на 3—4-й не-
деле заболевания. На их месте образуется грануляционная ткань,
333
на которую из краев язв наползает регенерирующий эпителии.
Если язвы были неглубокими и небольшими, возможна полная
регенерация стенки кишки. В случае глубоких обширных язв
полной регенерации не наступает, в стенке кишки образуются
рубцы, суживающие ее просвет.
У детей дизентерия имеет некоторые .морфологические особен-
ности, связанные с выраженным развитием лимфатического ап-
парата прямой и сигмовидной кишок. На фоне катарального вос-
паления происходит гиперплазия солитарных фолликулов, они
увеличиваются в размерах и выступают над поверхностью слизи-
стой оболочки кишки. Затем фолликулы подвергаются некрозу и
гнойному расплавлению — возникает фолликулярно-язвенный ко-
лит.
Общие изменения при дизентерии проявляются гиперплазией
лимфатических узлов и селезенки, жировой дистрофией паренхи-
матозных органов, некрозом эпителия канальцев почек. В связи с
участием толстой кишки в минеральном обмене при дизентерии
нередко развиваются его нарушения, что проявляется появлением
известковых метастазов.
Хроническая дизентерия развивается в результате очень вялого
течения дизентерийного язвенного колита. Язвы заживают плохо,
появляются полипозные разрастания слизистой оболочки вблизи
язв. Не все инфекционисты рассматривают указанные изменения
как хроническую дизентерию, считают их постдизентерийным
колитом.
Осложнения при дизентерии связаны с кишечным кровотече-
нием и прободением язв. Если при этом перфоративное отвер-
стие небольшое (микроперфорация), возникает парапроктит, ко-
торый может дать начало перитониту. При попадании в язвы
кишки гнойной флоры развивается флегмона кишки, а иногда
гангрена. Встречаются и другие осложнения дизентерии.
Исход благоприятный, однако иногда от осложнений заболева-
ния может наступить смерть.
Холера — острейшее инфекционное заболевание из группы
антропонозов, характеризующееся преимущественным поражени-
ем тонкой кишки и желудка. Холера относится к разряду каран-
тинных инфекций. Это чрезвычайно контагиозная болезнь, и за-
болеваемость ею имеет характер эпидемий и пандемий. Возбуди-
телями холеры являются вибрион азиатской холеры и вибрион
Эль-Тор.
Эпидемиология Резервуаром для возбудителя служит вода, а
источником заражения — больной человек. Заражение происхо-
дит при употреблении воды, содержащей вибрионы. Последние
находят оптимальные условия в тонкой кишке, где размножаются
и выделяют экзотоксин (холероген).
Патогенез и патологическаяанатомия
1-й период болезни — холерный энтерит развивается под дейст-
вием экзотоксина. Энтерит носит серозный или серозно-геморра-
гический характер. Слизистая оболочка кишки гиперемирована, с
334
небольшими, но иногда многочисленными кровоизлияниями.
Экзотоксин обусловливает секрецию клетками кишечного эпите-
лия большого количества изотонической жидкости, и при этом
она не всасывается обратно из просвета кишки. Клинически у
больного неожиданно начинается и не прекращается понос. Со-
держимое кишечника водянистое, без цвета и запаха, содержит
огромное количество вибрионов, имеет вид "рисового отвара",
так как в нем плавают мелкие комочки слизи и слущенные эпи-
телиальные клетки.
2-й период болезни — холерный гастроэнтерит развивается к
концу первых суток и характеризуется прогрессированием энтерита
и присоединением серозно-геморрагического гастрита. У больно-
го развивается неукротимая рвота. С поносом и рвотой больные
теряют до 30 л жидкости в сутки, обезвоживаются, наступают
сгущение крови и падение сердечной деятельности, понижается
температура тела.
3-й период — алгидный, который характеризуется эксикозом
(высыханием) больных и понижением температуры их тела. В тон-
кой кишке сохраняются признаки серозно-геморрагического эн-
терита, но появляются очаги некроза слизистой оболочки, ин-
фильтрация стенки кишки нейтрофильными лейкоцитами, лим-
фоцитами, плазматическими клетками. Петли кишки растянуты
жидкостью, тяжелые. Серозная оболочка кишечника сухая, с то-
чечными кровоизлияниями, между петлями кишечника имеется
прозрачная, тянущаяся слизь. В алгидном периоде обычно насту-
пает смерть больных.
Труп умершего от холеры имеет специфические особенности,
определяемые эксикозом. Трупное окоченение наступает быстро,
выражено очень сильно и держится несколько дней. Из-за силь-
ного и стойкого сокращения мышц возникает характерная "поза
гладиатора". Кожа сухая, морщинистая, на ладонях сморщена
("руки прачки"). Все ткани трупа сухие, в венах — густая темная
кровь. Селезенка уменьшена в размерах, в миокарде и печени яв-
ления паренхиматозной дистрофии, иногда мелкие очаги некро-
за. В почках — некроз эпителия канальцев главных отделов неф-
ронов. чем объясняется иногда развивающаяся у больных холе-
рой острая почечная недостаточность.
Специфические осложнения холеры проявляются холерным ти-
фоидом, когда в ответ на повторное попадание вибрионов в тол-
стой кишке развивается дифтеритическое воспаление. В почках
при этом может возникнуть подострый экстракапиллярный гло-
мерулонефрит или некроз эпителия канальцев. Этим объясняется
развитие уремии при холерном тифоиде. Постхолерная уремия
может быть обусловлена и появлением очагов некроза в корко-
вом веществе почек.
Исход. Смерть больных наступает в алгидном периоде от обез-
воживания, холерной комы, интоксикации, уремии. При своевре-
менном лечении большинство больных, особенно холерой, вы-
званной вибрионом Эль-Тор, выживают.
335
Туберкулез — хроническое инфекционное заболевание из
группы антропозоонозов, характеризующееся развитием в орга-
нах специфического воспаления. Это заболевание не теряет сво-
его значения, так как больные ом составляют I % всего населе-
ния Земли, а в современной России заболеваемость приближает-
ся к эпидемии. Возбудителем болезни являются микобактерии ту-
беркулеза, открытые Р. Кохом. Различают четыре типа возбудите-
лей туберкулеза, но для человека патогенными являются только
два — человеческий и бычий.
Эпидемиология. Микобактерии попадают в организм обычно
вместе с вдыхаемым воздухом и проникают в легкие. Значительно
реже они оказываются в пищеварительном тракте (при употреб-
лении зараженного молока). Крайне редко заражение происходит
через плаценту или поврежденную кожу. Наиболее часто мико-
бактерии попадают в легкие, но при этом далеко не всегда они
вызывают заболевание. Нередко микобактерии обусловливают
развитие в легком специфического воспаления, но без каких-ли-
бо других проявлений болезни. Это состояние называется инфи-
цированностъю туберкулезом. Если же имеются клиника болезни
и своеобразные морфологические изменения в тканях, можно го-
ворить о заболевании туберкулезом.
Микобактерии, попавшие во внутренние органы, вызывают
различные морфологические реакции, связанные с сенсибилиза-
цией организма и становлением иммунитета. Наиболее характер-
ны реакции гиперчувствительности замедленного типа. Различают
три основных вида туберкулеза — первичный, гематогенный и
вторичный.
Первичный туберкулез развивается в основном у детей при
первом попадании микобактерии в организм. В 95 % случаев за-
ражение происходит аэрогенным путем.
Патогенез и патологическая анатомия. С вдыхаемым воздухом
возбудитель попадает в Ш, УШ или X сегмент легких. В этих сег-
ментах, особенно часто в Ш сегменте правого легкого, возникает
небольшой очаг экссудативного воспаления, который быстро
подвергается казеозному некрозу, и вокруг него появляются се-
розный отек и лимфоцитарная инфильтрация. Возникает первич-
ный туберкулезный аффект. Очень быстро специфическое воспа-
ление распространяется на прилежащие к первичному аффекту
лимфатические сосуды (лимфангит) и регионарные лимфатиче-
ские узлы корня легкого, в которых развивается казеозный нек-
роз (лимфаденит). Появляется первичный туберкулезный комплекс.
При алиментарном заражении туберкулезный комплекс возника-
ет в кишечнике.
В дальнейшем в зависимости от состояния больного, его реак-
тивности и ряда других факторов течение туберкулеза может быть
различным — затухание первичного туберкулеза; прогрессирова-
ние первичного туберкулеза с генерализацией процесса; хрониче-
ское течение первичного туберкулеза.
При затухании первичного туберкулеза экссудативные явления
336
стихают, вокруг первичного туберкулезного аффекта появляются
вал из эпителиоидных и лимфоидных клеток, а затем соедини-
тельнотканная капсула. В казеозные некротические массы откла-
дываются соли кальция, и первичный аффект петрифицируется.
Такой заживший первичный очаг называется очагом Гона. Лим-
фатические сосуды и лимфатические узлы также склерозируются,
в последних откладывается известь и возникают петрификаты.
Однако в очаге Гона на протяжении десятков лет сохраняются
микобактерии туберкулеза, и этим поддерживается нестерильный
туберкулезный иммунитет. После 40 лет очаги Гона обнаружива-
ются почти у всех людей. Такое течение первичного туберкулеза
следует считать благоприятным.
Фор.мыпрогрессированияпервичного туберкулеза. При недоста-
точной резистентности организма происходит прогрессирование
первичного туберкулеза, и этот процесс может протекать в четы-
рех формах.
• Гематогенная генерализация первичного туберкулеза возни-
кает при раннем попадании микобактерии в ток крови из
первичного аффекта и диссеминации (распространении)
инфекции по организму. При этом в различных органах об-
разуются туберкулезные бугорки от очень мелких, просо-
видных, до более крупных диаметром 3—4 мм. Первая фор-
ма называется милиарным туберкулезом, вторая — крупно-
очаговым туберкулезом. При гематогенной генерализации
туберкулез может протекать очень бурно с симптоматикой
поражения тех органов, куда попали микобактерии туберку-
леза. например оболочек мозга, в которых развивается ту-
беркулезный менингит. Нередко эта форма первичного ту-
беркулеза может затихать, но в органах сохраняются очаги
отсева туберкулеза, которые при неблагоприятных условиях
могут обусловить новую вспышку заболевания.
• Лимфожелезистая генерализация первичного туберкулеза ха-
рактеризуется вовлечением в процесс бронхиальных, би-
фуркационных, под- и надключичных лимфатических уз-
лов. в которых развивается специфическое воспаление с ка-
зеозным некрозом (рис. 80, а). Особенно тяжело протекает
туберкулезный лимфаденит, когда увеличенные лимфатиче-
ские узлы сдавливают трахею и бронхи, что ведет к разви-
тию ателектазов легких. Нередко процесс с бронхов распро-
страняется на клетчатку средостения и поражает нервные
стволы, проходящие в средостении сосуды, иногда в про-
цесс вовлекается пищевод.
• Рост первичного аффекта — наиболее тяжелая форма про-
грессирования первичного туберкулеза. При этом специфи-
ческое воспаление распространяется на прилежащие к пер-
вичному аффекту участки легочной паренхимы, возникает
первичная лобарная или тотальная казеозная пневмония
• Смешанная форма прогрессирования первичного туберкулеза
может развиваться как исход всех других форм прогресси-
337
Рис. 80. Туберкулез легких.
а — первичный туберкулезный комплекс с лимфожелезистым прогрессированием;
б — милиарный туберкулез легких; в — фиброзно-очаговый туберкулез легких.
рования при снижении защитных сил организма. При этом
обнаруживаются казеозная пневмония, расплавление пора-
женных лимфатических узлов и многочисленные туберку-
лезные бугорки в обоих легких.
Исходы первичного туберкулеза. Исходы прогрессирующего
первичного туберкулеза зависят от возраста больного, сопротив-
ляемости организма и степени распространенности процесса. У де-
тей эта форма туберкулеза течет особенно тяжело. Смерть боль-
ных наступает от генерализации процесса и туберкулезного ме-
нингита. При благоприятном течении и применении соответст-
вующих лечебных мероприятий экссудативная воспалительная
реакция сменяется продуктивной, очаги туберкулеза склерозиру-
ются и петрифицируются.
При хроническом течении первичного туберкулеза первичный
аффект инкапсулируется, а процесс течет в лимфожелезистом ап-
парате волнообразно: вспышки болезни сменяются ремиссиями.
В то время как в одних лимфатических узлах процесс затихает, в
других он начинается.
Иногда туберкулезный процесс в лимфатических узлах затиха-
ет, казеозные массы в них склерозируются и петрифицируются,
но прогрессирует первичный аффект. Казеозные массы в нем
размягчаются, на их месте образуются полости — первичные легоч-
ные каверны.
Гематогенный туберкулез развивается через несколько лет по-
сле перенесенного первичного туберкулеза, поэтому он носит
еще название послепервичный туберкулез. Он возникает на фоне
повышенной чувствительности к туберкулину людей, перенесших
338
первичный туберкулез и сохраняющих иммунитет против тубер-
кулезной микобактерии.
Патогенез и формы гематогенного туберкулеза. Гематогенный
туберкулез возникает из очагов отсева, попавших в различные ор-
ганы в период первичного туберкулеза или туберкулезной инфи-
цированное™. Эти очаги многие годы могут не проявлять себя, а
затем под влиянием неблагоприятных факторов и сохранившейся
повышенной реактивности в них возникает экссудативная реак-
ция и начинается гематогенный туберкулез. Выделяют три формы
гематогенного туберкулеза — генерализованный гематогенный ту-
беркулез; гематогенный туберкулез с преимущественным пораже-
нием легких; гематогенный туберкулез с преимущественным по-
ражением внутренних органов.
• Генерализованный гематогенный туберкулез — наиболее тя-
желая форма, при которой в большинстве органов появля-
ются туберкулезные бугорки и мелкие некротические очаги.
Эту форму еще называют острейший туберкулезный сепсис.
В других случаях во всех органах развиваются мелкие про-
совидные продуктивные бугорки — это острый общий мили-
арный туберкулез. Иногда возникает крупноочаговый тубер-
кулез, при котором очаги специфического воспаления дости-
гают в диаметре 1 см. При любой форме гематогенного ту-
беркулеза необходимо найти первичный очаг. Обычно это не
вполне заживший очаг отсева первичного туберкулеза в лег-
ких, костях, кишечнике при зажившем первичном аффекте.
• Гематогенный туберкулез с преимущественным поражением
легких развивается в обоих легких и характеризуется нали-
чием множественных мелких белесоватых бугорков. В этом
случае говорят о милиарном туберкулезе (рис. 80, б), кото-
рый может протекать остро и хронически. При остром тече-
нии туберкулеза нередко возникает туберкулезный менин-
гит. При хроническом течении этой формы туберкулеза
происходит рубцевание бугорков, развиваются эмфизема
легких и пневмосклероз, в связи с чем возникает гипертро-
фия правых отделов сердца. Хронический крупноочаговый
гематогенный туберкулез легких (в клинике он называется
гематогенно-диссеминированный легочный туберкулез) харак-
теризуется образованием преимущественно продуктивных
бугорков, зеркальным поражением обоих легких, развитием
округлых каверн в обоих легких и пневмосклероза. При
этом имеется внелегочный очаг отсева — в половых орга-
нах, костях или лимфатических узлах.
• Гематогенный туберкулез с преимущественным внелегочным
поражением развивается в различных органах, но особенно
часто в костях и мочеполовой системе. Источником этой
формы туберкулеза являются очаги отсева, занесенные в
органы в период первичного туберкулеза или туберкулезной
инфицированности. Эта форма туберкулеза имеет острое
или хроническое течение.
339
Рис. 81. Туберкулезный спондилит.
Туберкулез костей и суставов чаще встречается у детей,
обычно поражение возникает в телах позвонков, тазобед-
ренных и коленных суставах. При этом происходит казеоз-
ный распад костей, они деформируются, что и лежит в ос-
нове образования горба при туберкулезном спондилите
(рис. 81), неподвижности суставов при туберкулезном арт-
340
рите. При этом в процесс вовлекаются окружающие ткани,
которые также подвергаются казеозному некрозу. Послед-
ние расплавляются, образуются ложные ходы в тканях, ко-
торые открываются на коже в виде свищей.
• Туберкулез почек поражает преимущественно молодых лю-
дей в период полового созревания. Источником туберкулеза
почек служат очаги отсева, которые обнаруживаются в лим-
фатических узлах, костях, половых органах. Туберкулезные
очаги образуются обычно в одной почке и, прогрессируя,
разрушают ее ткань. В результате в почке появляются по-
лости, заполненные казеозными массами (рис. 82). Послед-
ние могут закрывать просвет мочеточника, что нарушает от-
ток мочи и развивается пионефроз.
• Туберкулез кожи (волчанка), половых органов, эндокринных
желез, пищеварительного тракта, нервной системы, серозных
оболочек — это различные формы гематогенного туберкуле-
за с преимущественно внелегочными поражениями. Однако
они встречаются в практике реже, чем туберкулез костей и
суставов, а также туберкулез почек.
Вторичный туберкулез. Им болеют взрослые, перенесшие в
детском возрасте первичный туберкулез, при котором возникли
очаги отсева в верхушки легких (очаги Симона). Следовательно,
вторичный туберкулез — это также послепервичный туберкулез,
который характеризуется поражением легких.
Патогенез и формы вторичного туберкулеза. Распространяется
инфекция из очагов туберкулеза по бронхам; при этом с мокро-
той микробактерии могут попадать в другое легкое и пищевари-
тельный тракт. Поэтому в лимфатических узлах нет специфиче-
ского воспаления, а их изменения проявляются лишь реактивной
гиперплазией лимфоидной ткани, как при любом другом инфек-
ционном заболевании. В патогенезе заболевания возникает не-
сколько форм туберкулеза:
• Острый очаговый туберкулез, или очаг Абрикосова. Очаги
отсева первичного туберкулеза располагаются в бронхиолах
I и II сегментов, чаще правого легкого. При развитии вто-
ричного туберкулеза в этих бронхиолах развиваются эндоб-
ронхит, затем панбронхит и специфическое воспаление рас-
пространяется на перибронхиальную легочную ткань, в ко-
торой возникает очаг казеозной пневмонии, окруженный
эпителиоидными и лимфоидными клетками, — очаг Абри-
косова.
• Фиброзно-очаговый туберкулез возникает при благоприят-
ном течении вторичного туберкулеза; в результате очаг Аб-
рикосова склерозируется и может петрифицироваться
(рис. 80, в).
• Инфильтративный туберкулез развивается при прогрессиро-
вании острого очагового туберкулеза. При этой форме в
легком возникают очаги казеозного некроза, вокруг кото-
рых развивается неспецифическое перифокальное экссуда-
341
Рис. 82. Туберкулез почки.
1 — почка на разрезе: б — стенка каверны, построенная из туберкулезных грану-
ляций и казеозных некротических масс; в — в почке хронический интерстициаль-
ный нефрит туберкулезной этиологии.
тивное воспаление. Фокусы-инфильтраты могут сливаться
между собой, но в участках поражения прео&ладает неспе-
цифическое серозное воспаление. В случае благоприятного
течения экссудат рассасывается, очаги казеозного некроза
'42
a
Рис. 83. Вторичный туберкулез легких.
а- туберкулема в верхушке легкого; б — казеозная пневмония с фокусом рас-
пада.
склерозируется и петрифицируются — вновь возникает
фиброзно-очаговый туберкулез.
• Туберкулема развивается в тех случаях, когда перифокаль-
ное воспаление рассасывается, а очаг казеозного некроза
остается, вокруг него образуется лишь слабо развитая кап-
343
Рис. 84. Цирротический туберкулез легких с бронхоэктазами.
сула. Туберкулема может достигать 5 см в диаметре, содер-
жит микобактерии и при рентгенологическом исследовании
может симулировать опухоль легкого (рис. 83, а). Туберку-
лему обычно удаляют хирургическим путем.
Острая казеозная пневмония возникает в тех случаях когда
инфильтративный туберкулез прогрессирует. При этом ка-
зеозный некроз паренхимы легкого преобладает над пери-
фокальным воспалением (рис. 83, б), а неспецифический
серозный экссудат быстро подвергается казеозному некро-
зу, и площадь казеозной пневмонии постоянно расширяет-
ся, занимая иногда долю легкого. Легкое увеличено, плот-
ное, на разрезе имеет желтоватый цвет. Казеозная пневмо-
ния возникает у ослабленных больных, часто в терминаль-
ном периоде болезни, но в настоящее время встречается
редко.
344
• Острая каверна развивается при другой форме прогрессиро-
вания инфильтративного туберкулеза или туберкулемы. В
область казеозного некроза попадает бронх, через который
отделяются казеозные массы. На их месте и образуется ка-
верна — полость диаметром 2—5 см. Стенку ее составляет
уплотненная легочная ткань, поэтому она эластична и легко
спадается. При этой форме вторичного туберкулеза резко
возрастает опасность обсеменения другого легкого и пище-
варительного тракта.
• Фиброзно-кавернозный туберкулез, или хроническая легоч-
ная чахотка, развивается в том случае, если острый кавер-
нозный туберкулез принимает хроническое течение и стен-
ки каверн склерозируются.
• Цирротический туберкулез (рис. 84). В стенках каверн по-
стоянно находятся микобактерии. Процесс постепенно по
бронхам спускается в нижележащие отделы легких, занимая
все новые их участки, а затем распространяется на другое
легкое. В пораженных легких интенсивно разрастается руб-
цовая ткань, образуются многочисленные бронхоэктазы,
легкие деформируются.
Осложнения вторичного туберкулеза связаны в основном с ка-
вернами. Из сосудов каверны может возникнуть массивное кро-
вотечение. Прорыв каверны в плевральную полость вызывает
пневмоторакс и эмпиему плевры; в связи с длительным течением
вторичный туберкулез, как и гематогенный, иногда осложняется
амилоидозом.
Исход. Смерть наступает от указанных осложнений, а также от
легочно-сердечной недостаточности.
ДЕТСКИЕ ИНФЕКЦИИ
Возбудители инфекционных болезней, поражающие ребенка
после его рождения и в течение всего периода детства, вызывают
в организме такие же изменения, что и в органах взрослого чело-
века. но при этом имеется ряд особенностей течения и морфоло-
гии инфекционного процесса. Основная особенность детских ин-
фекций заключается в том, что большинство из них поражает
только детей.
Дифтерия — острое инфекционное заболевание, вызываемое
дифтерийной палочкой.
Эпидемиология. Источником заражения является больной че-
ловек или бациллоноситель. Путь передачи в основном воздуш-
но-капельный, но иногда возможна передача возбудителя через
различные предметы. Как правило, входными воротами являются
верхние дыхательные пути. Дифтерийная палочка выделяет силь-
ный экзотоксин, который всасывается в кровь, поражает сердце и
надпочечники, вызывает парез и деструкцию сосудов микроцир-
куляторного русла. При этом резко повышается их проницае-
345
мость, в окружающие ткани поступают фибриноген, превращаю-
щийся в фибрин, а также клетки крови, в том числе лейкоциты.
Клинико-морфологические (формы:
• дифтерия зева и миндалин;
• дифтерия дыхательных путей.
Патологическая анатолия дифтерии зева и миндалин. В связи
с тем что зев и верхний отдел гортани выстланы многослойным
плоским эпителием, здесь развивается дифтеритическое воспале-
ние. Зев и миндалины покрывает плотная белесоватая пленка,
под которой ткани некротизированы, пропитаны фибринозным
экссудатом с примесью лейкоцитов. Резко выражены отек окру-
жающих тканей, а также интоксикация организма. Она связана с
тем, что фибринозная пленка, содержащая микробы, долго не от-
торгается, что способствует всасыванию экзотоксина. В регио-
нарных лимфатических узлах возникают очаги некроза и крово-
излияний. В сердце развивается токсический межуточный миокар-
дит. Появляется жировая дистрофия кардиомиоцитов, миокард
становится дряблым, полости сердца расширяются.
Нередко возникает паренхиматозный неврит с распадом мие-
лина. Поражаются языкоглоточные, блуждающий, симпатиче-
ский и диафрагмальный нервы. Изменения нервной ткани посте-
пенно нарастают, и через 13—2 мес от начала заболевания может
возникнуть паралич мягкого неба, диафрагмы и сердца. В надпочеч-
никах появляются очаговые некрозы и кровоизлияния, в почках —
некротический нефроз (см. рис. 75), в селезенке нарастает гипер-
плазия фолликулов.
Смерть может наступить в начале 2-й недели заболевания от
раннего паралича сердца или через 15—2 мес от позднего паралича
сердца.
Патологическая анатолия дифтерии дыхательных путей. При
этой форме развивается крупозное воспаление гортани, трахеи и
бронхов (см. рис. 24). Ниже голосовых связок слизистая оболочка
дыхательных путей выстлана призматическим и цилиндрическим
эпителием, выделяющим много слизи. Поэтому образующаяся
здесь фибринозная пленка легко отделяется, экзотоксин почти не
всасывается и общие токсические явления выражены слабее.
Крупозное воспаление гортани при дифтерии называется истин-
ным крупом. Дифтеритическая пленка легко отторгается и при
этом может закупоривать трахею, вследствие чего возникает ас-
фиксия. Воспалительный процесс иногда спускается в мелкие
бронхи и бронхиолы, что сопровождается развитием бронхопнев-
монии и абсцессов легких.
Смерть больных наступает от асфиксии, интоксикации и от
указанных осложнений.
Скарлатина — острое инфекционное заболевание, вызываемое
р-гемолитическим стрептококком группы А и характеризующееся
воспалением зева и типичной сыпью. Обычно болеют дети до
16 лет, иногда — взрослые.
Эпидемиология Заражение происходит воздушно-капельным
346
путем от больного скар-
латиной. Входными во-
ротами инфекции явля-
ются зев и миндалины,
где возникает первич-
ный скарлатинозный аф-
фект. В развитии болезни
решающее значение име-
ет повышенная чувстви-
тельность человека к
стрептококку. Из вход-
ных ворот стрептококк
проникает в регионарные
лимфатические узлы, вы-
зывая лимфангит и лим-
фаденит, которые в соче-
тании с первичным аф-
-е ктом образуют инфек-
ционный комплекс. Из
лимфатических путей
возбудитель попадает в
кровь, происходит его ге-
матогенная диссемина-
ция, сопровождающаяся
токсемией, поражением
нервной системы и внут-
Рис. 85. Скарлатина. Острый некротиче-
ский тонзиллит и резкое полнокровие
зева (по А. В. Цинзсрлингу).
ренних органов.
Формы скарлатины.
По степени тяжести выделяют:
• легкую форму;
• форму средней тяжести;
• тяжелую форму скарлатины, которая может быть токсиче-
ской, септической, токсико-септической.
Патогенез. Течение скарлатины характеризуют два периода.
Первый период болезни занимает 7—9 дней и харак-
теризуется аллергизацией организма, связанной с образованием
антитоксических антител при бактериемии. В результате токсе-
мии и распада микробных тел в крови на 3—5-й неделе болезни
может возникнуть аутоиммунный процесс, являющийся выраже-
нием аллергии, при котором развивается поражение ряда внут-
ренних органов.
Патологическая анатомия. Первый период скарлатины сопро-
вождается катаральной ангиной с резким полнокровием минда-
лин зева — "пылающий зев". Она сменяется характерной для
скарлатины некротической ангиной, что способствует распро-
странению стрептококков в тканях (рис. 85). Некрозы могут раз-
виваться в мягком небе, глотке, слуховой трубе, а оттуда перехо-
дить на среднее ухо; с шейных лимфатических узлов некроз ино-
гда распространяется на клетчатку шеи. При отторжении некро-
347
тических масс образуются язвы. Общие изменения зависят от вы-
раженности интоксикации и при токсической форме болезни про-
являются лихорадкой и характерной скарлатинозной сыпью.
Сыпь мелкоточечная, ярко-красная, покрывает все тело, за ис-
ключением носогубного треугольника. В основе сыпи лежит вос-
паление сосудов кожи. При этом эпидермис подвергается дистро-
фическим изменениям и слущивается пластами — пластинчатое
шелушение. В паренхиматозных органах и нервной системе в свя-
зи с токсемией развиваются тяжелые дистрофические изменения,
выражена гиперплазия селезенки и лимфатических узлов.
При септической форме скарлатины, которая особенно ярко
проявляется на 2-й неделе болезни, воспаление в области первич-
ного комплекса принимает гнойно-некротический характер. При
этом могут возникнуть осложнения типа заглоточного абсцесса,
отита, остеомиелита височной кости, флегмоны шеи, иногда с
изъязвлением крупных сосудов и смертельным кровотечением. В
очень тяжелых случаях развивается токсико-септическая форма,
для которой характерна септикопиемия с гнойными метастазами
в различные органы.
Второй период скарлатины развивается далеко не
всегда, и если развивается, то на 3—5-й неделе. Началом второго
периода является катаральная ангина. Основная опасность этого
периода — развитие острого гломерулонефрита, который перехо-
дит в хронический гломерулонефрит и заканчивается сморщива-
нием почек. Во втором периоде могут наблюдаться бородавчатый
эндокардит, артриты, васкулиты кожи, а следовательно, кожная
сыпь.
Смерть может наступить от осложнений болезни, например от
уремии, при развитии гломерулонефрита, в то время как в на-
стоящее время в связи с применением эффективных лекарствен-
ных средств непосредственно от скарлатины больные почти не
умирают.
Менингококковая инфекция — острое инфекционное заболева-
ние, характеризующееся эпидемическими вспышками. Чаще бо-
леют дети до 5 лет.
Эпидемиология. Возбудителем болезни является менингококк.
Заражение происходит воздушно-капельным путем. Возбудитель
обнаруживается в мазках из носоглотки и цереброспинальной
жидкости. Менингококк очень нестоек и вне живого организма
быстро погибает.
Патогенез и патологическая анатомия Менингококковая ин-
фекция может протекать в нескольких формах.
• Менингококковый назофарингит характеризуется катараль-
ным воспалением слизистой оболочки с резкой гиперемией
сосудов и отеком глотки. Эта форма часто не диагностиру-
ется, но больные представляют опасность для окружающих,
так как являются источником распространения инфекции.
• Менингококковый менингит развивается тогда, когда ме-
нингококк проникает в кровь, преодолев гематоэнцефали-
Рис. 86. Менингококковая инфекция.
а - гнойный менингит; 6 - расширение желудочков мозга, гнойное пропитыва-
ние эпендимы; в - очаг некроза и кровоизлияние в надпочечнике; г - кровоиз-
лияния и некрозы в коже.
ческий барьер. Он попадает в мягкие мозговые оболочки, и
в них развивается вначале серозное, а затем гнойное воспа-
ление, которое к 5—6-м суткам переходит в гнойно-фибри-
нозное. Экссудат зеленовато-желтого цвета располагается
преимущественно на базальной поверхности головного моз-
га. отсюда переходит на его выпуклую поверхность и в виде
"чепчика" покрывает лобные доли полушарий мозга
(рис. 86, а). Микроскопически мягкие оболочки и прилежа-
щая к ним ткань мозга инфильтрированы лейкоцитами, со-
суды резко полнокровны — развивается менингоэнцефалит.
Гнойное воспаление нередко распространяется на эпендиму
желудочков мозга (рис. 86, б). С 3-й недели болезни гной-
но-фибринозный экссудат частично рассасывается, а час-
тично подвергается организации. При этом зарастают суб-
арахноидальные пространства, отверстия IV желудочка, на-
рушается циркуляция ликвора и развивается гидроцефалия
(см. рис. 32).
Смерть в остром периоде наступает от отека и набухания моз-
га. менингоэнцефалита, а в позднем — от церебральной кахек-
сии, связанной с атрофией мозга в результате гидроцефалии.
349
Менингококковый сепсис возникает при изменении реактивно-
сти организма. При этом поражаются все сосуды микроциркуля-
торного русла. Иногда в кровотоке происходит интенсивный рас-
пад лейкоцитов, содержащих микробы. Менингококки и освобо-
ждающийся гистамин приводят к бактериальному шоку и парезу
микроциркуляторного русла. Развивается молниеносная форма ме-
нингококкемии. при которой больные погибают через 1—2 сут
после начала болезни.
При других вариантах течения менингококковый сепсис харак-
теризуется геморрагической кожной сыпью, поражением суставов
и сосудистой оболочки глаз. В надпочечниках развиваются некро-
зы и кровоизлияния, что приводит к их острой недостаточности
(рис. 86, в). В почках иногда возникает некротический нефроз. В
коже также развиваются кровоизлияния и некрозы (рис. 86, г).
Смерть больных при этом варианте течения болезни наступает
либо от острой надпочечной недостаточности, либо от уремии,
связанной с некротическим нефрозом. При длительном течении
менингококкемии больные умирают от гнойного менингита и
септикопиемии.
СЕПСИС
Сепсис — инфекционное нециклическое заболевание, возни-
кающее в условиях нарушенной реактивности организма при
проникновении из местного очага инфекции в кровеносное русло
различных микроорганизмов и их токсинов. Важно подчеркнуть,
что это инфекционное заболевание связано именно с нарушенной,
а не просто измененной реактивностью организма. На сепсис не
распространяются все те закономерности, которые характерны
для других инфекций. Выделяют несколько особенностей, которые
принципиально отличают сепсис от других инфекций.
1-я особенность сепсиса — бактериологическая — заключается в
следующем:
• не существует какого-то специфического возбудителя сеп-
сиса. Это страдание полиэтиологическое и может быть вы-
звано практически любыми микроорганизмами или пато-
генными грибами, что отличает сепсис от всех других ин-
фекций, при которых имеется специфический возбудитель;
• вне зависимости от того, каким возбудителем вызван сеп-
сис, он всегда тенет одинаково — именно как сепсис, т. е.
особенность инфекта не накладывает отпечаток на ответ
организма при сепсисе;
• сепсис не имеет специфического морфологического субстра-
та, который возникает при любой другой инфекции;
• сепсис возникает нередко уже после заживления первичного
очага, в то время как при всех других инфекционных забо-
леваниях изменения органов и тканей развиваются в тече-
ние болезни и исчезают после выздоровления;
• сепсис зависит от предсуществующих болезней и почти
всегда появляется в динамике какого-то другого инфекци-
онного заболевания или местного воспалительного про-
цесса.
2-я особенность сепсиса — эпидемиологическая:
• сепсис, в отличие от других инфекционных болезней, не за-
разен;
• сепсис не удается воспроизвести в эксперименте в отличие
от других инфекций;
• вне зависимости от формы сепсиса и характера возбудителя
клиника заболевания всегда одинакова.
3-я особенность сепсиса — иммунологическая:
• при сепсисе нет выраженного иммунитета и поэтому нет и
цикличности течения, в то время как все другие инфекции
характеризуются четкой цикличностью течения процесса,
связанной с образованием иммунитета;
• из-за отсутствия иммунитета при сепсисе резко затруднена
репарация поврежденных тканей, в связи с чем болезнь либо
заканчивается смертью, либо выздоровление протекает дос-
таточно долго;
• после излечения от сепсиса не остается иммунитета.
Все эти особенности говорят о том, что для развития сепсиса
необходима особая реактивность организма, и поэтому сепсис —
это особая форма реагирования макроорганизма на самые разно-
образные инфекционные возбудители. Эта особая реактивность от-
ражает своеобразную, необычную аллергию и, следовательно, своеоб-
разную гиперергию, не наблюдающуюся при других инфекцион-
ных заболеваниях.
Патогенез сепсиса далеко не всегда понятен. Возможно, что
особой реактивностью организм отвечает не на микроб, а на ток-
сины любых микробов. А токсины довольно быстро угнетают им-
мунную систему. При этом возможно нарушение ее реакции на ан-
тигенную стимуляцию, которая вначале запаздывает из-за полома
восприятия сигнала об антигенной структуре токсинов, а потом
уже оказывается недостаточной в силу угнетения токсинами самой
иммунной системы при быстро нарастающей интоксикации.
Формы течения сепсиса:
• молниеносная, при которой смерть наступает в течение
первых суток болезни;
• острая, которая длится до 3 сут;
• хроническая, которая может длиться годами.
Клинико-морфологические особенности. Общие изменения при
сепсисе складываются из 3 основных морфологических процес-
сов — воспалительных, дистрофических и гиперпластических,
причем последние развиваются в органах иммуногенеза. Все они
отражают как высокую интоксикацию, так и своеобразную гипе-
рергическую реакцию, развивающуюся при сепсисе.
— это очаг гнойного воспаления. котой5Дй
является аналогом первичного аффекта, возникающего при
других инфекциях;
• лимфангит и регионарный лимфаденит, как правило, гнойно-
го характера;
• септический гнойный тромбофлебит, который при гнойном
расплавлении тромба обусловливает бактериальную эмбо-
лию и тромбоэмболию с развитием во внутренних органах
абсцессов и инфарктов и тем самым — гематогенную гене-
рализацию инфекции;
• входные ворота, где в большинстве случаев локализуется
септический очаг.
Виды сепсиса в зависимости от входных ворот:
• терапевтический, или параинфекционный сепсис, который
развивается в ходе или после других инфекций или неин-
фекционных болезней;
• хирургический, или раневой (в том числе послеоперационный)
сепсис, когда входными воротами является рана, особенно
после удаления гнойного очага. К этой группе относят и
своеобразный ожоговый сепсис:
• маточный, или гинекологический, сепсис, источник которого
находится в матке или в ее придатках;
• пупочный сепсис, при котором источник сепсиса локализу-
ется в области культи пуповины;
• тонзиллогенный сепсис, при котором септический очаг рас-
полагается в миндалинах;
• одонтогенный сепсис, связанный с кариесом зубов, особенно
осложняющимся флегмоной;
• отогенный сепсис, возникающий при остром или хрониче-
ском гнойном отите;
• урогенный сепсис, при котором септический очаг располага-
ется в почках или в мочевых путях;
• криптогенный сепсис, который характеризуется клиникой и
морфологией сепсиса, но при этом ни его источник, ни
входные ворота неизвестны.
Клинико-морфологические формы сепсиса. В зависимости от
выраженности и своеобразия аллергии, соотношения местных и
общих изменений, наличия или отсутствия гноя, а также дли-
тельности течения заболевания выделяют:
• септицемию;
• септикопиемию;
• бактериальный (септический) эндокардит;
• хронический сепсис.
Септицемия — форма сепсиса, при которой нет специфиче-
ской морфологической картины, нет гноя и септических гной-
ных метастазов, но чрезвычайно ярко выражена гиперергиче-
ская реакция организма. Характерно молниеносное или острое
течение, в большинстве случаев больные умирают через 1—3
сут, и отчасти поэтому не успевают развиться отчетливые мор-
фологические изменения. Обычно имеется септический очаг,
352
хотя иногда его не удается обнаружить, и тогда говорят о крип-
тогенном сепсисе.
Патологическая анатолия септицемии в первую очередь отра-
жает сильнейшую интоксикацию и гиперергию и складывается из
микроциркуляторных нарушений, иммунологических реакций ги-
перчувствительности и дистрофических изменений. Наблюдается
гемолиз эритроцитов, обычно выражен геморрагический син-
дром, обусловленный васкулитами с фибриноидным некрозом
стенок сосудов, межуточное воспаление различных органов, ги-
потония. У умерших от септицемии на вскрытии часто обнаружи-
ваются ДВС-синдром. шоковые почки с ишемизированной корой
и гиперемированным мозговым веществом, шоковые легкие со
сливающимися множественными кровоизлияниями, в печени на-
блюдаются очаги лобулярного некроза и холестаз, в паренхима-
тозных органах — жировая дистрофия.
Септикопиемия — форма сепсиса, которая рассматривается как
генерализованная инфекция. Она характеризуется наличием в об-
ласти входных ворот септического очага в виде локального гной-
ного воспаления, сопровождающегося гнойными лимфангитом и
лимфаденитом, а также гнойным тромбофлебитом с метастазиро-
ванием гноя, что обусловливает генерализацию процесса (рис. 87,
а, б). Вместе с тем микробы определяются лишь в 74 посевов
крови. Наиболее часто септикопиемия развивается после крими-
нального аборта, оперативных вмешательств, осложнившихся на-
гноением, при других заболеваниях, характеризующихся наличи-
ем гнойного очага. Септикопиемия — это также необычная ал-
лергия. но выраженная не столь бурно, как при септицемии.
Клиническая картина в основном обусловлена изменениями,
связанными с гнойными метастазами, с развитием абсцессов и
"септических" инфарктов в разных органах — в почках (эмболи-
ческий гнойный нефрит), печени, в костном мозге (гнойный
остеомиелит), легких (нагноившиеся инфаркты) и др. Может
развиваться острый септический полипозно-язвенный эндокар-
дит с наличием гноя на эндокарде клапанов сердца. Характерна
спленомегалия, при которой масса селезенки достигает 500—
600 г. Такая большая селезенка с напряженной капсулой, даю-
щая на разрезе обильный соскоб пульпы, называется септиче-
ской селезенкой (рис. 87, в). Умеренная гиперплазия и выражен-
ная миелоидная метаплазия отмечаются и в лимфатических уз-
лах, развивается гиперплазия костного мозга плоских и трубча-
тых костей.
Осложнения септикопиемии — эмпиема плевры, гнойный пе-
ритонит, гнойный паранефрит. Острый септический полипозно-
язвенный эндокардит становится причиной тромбоэмболического
синдрома с развитием инфарктов в различных органах.
Септический (бактериальный) эндокардит — форма сепсиса,
при которой входными воротами служит клапанный аппарат
сердца и септический очаг локализуется на створках сердечных
клапанов. Примерно в 70 % случаев этой форме сепсиса предше-
353
Рис. 87. Сепсис.
а — септический эндометрит; б — септические нагноившиеся инфаркты легких.
ствует ревматическое поражение клапанов сердца, а в 5 % наблю-
дений первичный септический очаг локализуется на створках
клапанов, уже измененных в результате атеросклероза или других
неревматических заболеваний, в том числе врожденных пороков
сердца. Однако в 25 % наблюдений септический бактериальный
эндокардит развивается на интактных клапанах. Эта форма эндо-
кардита называется болезнью Черногубова.
Выделяют факторы риска бактериального эндокардита. Среди
них сенсибилизация лекарствами, различные вмешательства на
сердце и сосудах (внутрисосудистые и внутрисердечные катетеры,
искусственные клапаны и т. п.), а также хронические наркома-
нии, токсикомании и хроническая алкогольная интоксикация.
Выраженность аллергической реакции в первую очередь опреде-
ляет и формы течения септического эндокардита:
• острую, текущую около 2 нед и встречающуюся редко;
• подострую, которая может длиться до 3 мес и встречается
значительно чаще, чем острая форма;
• хроническую, длящуюся месяцами и годами. Эту форму не-
редко называют затяжным септическим эндокардитом, а
также sepsis lenta; она является преобладающей формой сеп-
тического эндокардита.
Патогенез и морфогенез. Локализация поражения клапанов
при бактериальном септическом эндокардите достаточно харак-
терна и обычно отличается от ревматических пороков сердца. В
40 % случаев поражается митральный клапан, в 30 % — аорталь-
354
Рис. 87. Продолжение.
в - септическая селезенка, обильный соскоб пульпы; г - полипозно-язвенныи
эндокардит аортального клапана при бактериальном септическом эндокардите.
355
ный, в 20 % наблюдений страдает трехстворчатый клапан, и в
10 % имеет место сочетанное поражение аортального и митраль-
ного клапанов. Механизмы развития процесса связаны с образо-
ванием циркулирующих иммунных комплексов из антигенов воз-
будителей, антител к ним и комплемента. Их циркуляция обу-
словливает развитие реакций гиперчувствительности с достаточно
характерной морфологией в виде тетрады повреждений — кла-
панного эндокардита, воспаления сосудов, поражения почек и
селезенки, к которым добавляются изменения, обусловленные
тромбоэмболическим синдромом.
Патологическая анатолия бактериального септического эн-
докардита, как и при других инфекциях, складывается из мест-
ных и общих изменений. Местные изменения развиваются в
септическом очаге, т. е. на створках клапанов сердца. Здесь на-
блюдаются колонии микробов и возникают очаги некроза, ко-
торые быстро изъязвляются, вокруг них возникает лимфоги-
стиоцитарная и макрофагальная инфильтрация, но без нейтро-
фильных лейкоцитов. На язвенных дефектах клапанов образу-
ются массивные тромботические наложения в виде полипов
(рис. 87, г), которые легко крошатся, нередко обызвествляются
и довольно быстро организуются, что усугубляет существующие
изменения клапанов или приводят к образованию пороков
сердца при болезни Черногубова. Прогрессирующие язвенные
дефекты створок клапанов сопровождаются образованием их
аневризм, а нередко и перфорацией створки. Иногда происхо-
дит отрыв створки клапана с развитием острой сердечной не-
достаточности. Тромботические наложения на клапанах сердца
являются источником развития тромбоэмболического синдрома.
При этом в разных органах образуются инфаркты, однако, не-
смотря на наличие в тромбоэмболах гноеродной инфекции, эти
инфаркты не нагнаиваются.
Общие изменения заключаются в поражении сосудистой сис-
темы, в основном микроциркуляторного русла, характеризуются
развитием васкулитов и геморрагического синдрома — множест-
венных петехиальных кровоизлияний в коже и подкожной клет-
чатке. в слизистых и серозных оболочках, в конъюнктиве глаз.
В почках развивается иммунокомплексный диффузный гломеру-
лонефрит, нередко сочетающийся с инфарктами почек и рубцами
после них. Селезенка резко увеличена в размере, капсула ее на-
пряжена, при разрезе пульпа малинового цвета, дает обильный
соскоб (септическая селезенка), часто в ней обнаруживаются ин-
фаркты и рубцы после них. Циркулирующие иммунные комплек-
сы нередко оседают на синовиальных оболочках, способствуя
развитию артритов. Характерным признаком септического эндо-
кардита являются также утолщения ногтевых фаланг пальцев
рук— "барабанные палочки ". В паренхиматозных органах развива-
ются жировая и белковая дистрофии.
Затяжной септический эндокардит следует считать хрониосеп-
сисом, хотя имеется точка зрения, что хрониосепсис — это так
356
называемая гнойно-резорбтивная лихорадка, которая характеризу-
ется наличием незаживающего гнойного очага. Однако в настоя-
щее время большинство специалистов считают, что это другая
болезнь, хотя и похожая на хронически текущий сепсис.
Глава 22
БОЛЕЗНИ ПЕРИОДА БЕРЕМЕННОСТИ
В период беременности в организме женщины значительно
изменяется нервная и гормональная регуляция обмена веществ и
физиологических функций. Развитие плода сопровождается обра-
зованием сложных взаимосвязей его с материнским организмом.
Все эти особенности могут быть своеобразным фоном, на кото-
ром возникают заболевания, связанные с беременностью. Среди
них наибольшее значение имеют гестоз, эклампсия, внематочная
беременность, трофобластическая болезнь.
ГЕСТОЗ
Гестоз — синдром, возникающий после 20 нед беременности и
включающий развитие гипертензии в сочетании с протеинурией и
отеками Чаще развивается у женщин, особенно первородящих
моложе 18 и старше 35 лет и страдающих гипертонией, заболева-
ниями почек, сахарным диабетом. Гестоз вызывает задержку раз-
вития и раннюю гибель плода.
Этиология и патогенез. Этиология неизвестна. Основное звено
патогенеза — снижение маточно-плацентарного кровотока и раз-
витие ишемии плаценты. В результате нарушается миграция тро-
фобласта и задерживаются соответствующие беременности изме-
нения спиральных артерий.
Морфология. Какой-либо специфической морфологической
картины нет. Плацента несколько увеличена в размерах, в ней
обнаруживаются обширные инфаркты, иногда ретроплацентар-
ные гематомы. Много мелких ворсин хориона с множественными
синцитиальными узелками, слабо выражены фетальные капилля-
ры. Происходят сужение и облитерация артерий в столовых вор-
синах. имеются очаги фибриноидного некроза маточных спи-
ральных артерий, макрофагальные инфильтраты.
Эклампсия — одно из тяжелых и опасных заболеваний периода
беременности, возникающее в ее второй половине, в родах и в
послеродовом периоде.
Этиология эклампсии окончательно не установлена. Считают,
что в некоторых случаях организм беременной женщины сенси-
357
билизируется белками плода и последа. Вероятно, в возникнове-
нии эклампсии определенное значение имеют и эндокринные на-
рушения. которые могут появляться при беременности.
Клиническая картина. Заболевание проявляется судорогами,
потерей сознания, недостаточностью функций печени и почек,
выражением чего являются желтуха и отеки.
Патологическая анатолия При вскрытии умерших от эклам-
псии отмечаются увеличение и пестрота печени. На разрезе она
дряблая, глинистого вида, с многочисленными очагами кровоиз-
лияний и некрозов. В гепатоцитах выражена белковая и жировая
дистрофия. Мелкие сосуды полнокровны, нередко отмечается
фибриноидный некроз их стенок с образованием тромбов в про-
светах, преимущественно капилляров и венул.
Почки увеличены, дряблые, довольно часто развивается нек-
роз их коркового слоя. В стенках приносящих артериол и капил-
ляров клубочков нередко видны участки фибриноидного некроза,
а в просвете клубочков — эмболы, состоящие из клеток последа.
В эпителии канальцев обнаруживаются дистрофические и некро-
тические изменения со слущиванием клеток эпителия в просветы
канальцев и образованием цилиндров. В строме почек — множе-
ственные кровоизлияния. Такие же кровоизлияния, как правило,
обнаруживаются в серозных оболочках, головном мозге, сердце,
легких.
Смерть беременных обычно наступает от почечно-печеночной
недостаточности, а также кровоизлияний в мозг.
ВНЕМАТОЧНАЯ БЕРЕМЕННОСТЬ
Внематочная беременность — нередкая патология первой поло-
вины беременности. При этом плод может развиваться в маточ-
ной трубе (трубная беременность), яичнике (яичниковая беремен-
ность) и брюшной полости (брюшинная беременность).
Причиной внематочной беременности обычно являются дефор-
мация маточных труб и сужение их просвета в результате перене-
сенных воспалительных процессов. Измененные маточные трубы
не могут обеспечить продвижение в полость матки оплодотворен-
ной яйцеклетки, она задерживается в трубе и имплантируется в
ее стенку. Иногда оплодотворенная яйцеклетка выпадает из ма-
точной трубы и имплантируется в яичник, брюшину или другие
органы брюшной полости.
Морфология. При трубной беременности в слизистой оболочке
маточной трубы развивается децидуальная ткань, ворсинчатая
оболочка плода (рис. 88). Ворсины хориона проникают в стенку
маточной трубы, способствуя ее разрыву. Матка при внематочной
беременности также несколько увеличивается в размерах, в эндо-
метрии появляются нерезко выраженные децидуальные измене-
ния. На 5—10-й неделе беременности обычно возникает кровоте-
чение, плод погибает и выпадает в просвет трубы. Развивается не-
358
Рис. 88. Трубная беременность. В полости маточной трубы видны свет-
лые ворсины хориона (ВХ), участки децидуальной ткани (ДТ).
полный трубный аборт. Если погибший плод вместе с оболочками
выпадает через фимбриальный конец трубы в брюшную полость,
то возникает полный трубный аборт.
Обычно при трубной беременности развивается разрыв маточ-
ной трубы, сопровождающийся массивным кровотечением в
брюшную полость, что приводит к развитию коллапса. Изредка
при разрыве маточной трубы погибший плод может выпасть в
брюшную полость, где он мумифицируется — "бумажный плод" —
или пропитывается солями кальция — "каменный плод".
Слкрть может наступить от коллапса в связи с острой крово-
потерей.
Самопроизвольное прерывание беременности включает несколь-
ко понятий:
• самопроизвольный аборт, или выкидыш, — самопроизволь-
ное прерывание беременности в срок до 14 нед после зача-
тия:
• поздний аборт — самопроизвольное прерывание беремен-
ности в срок от 14 до 28 нед;
• преждевременные роды — самопроизвольное прерывание
беременности в срок от 28 до 39 нед.
Причинами самопроизвольного прерывания беременности
обычно являются гибель плода при патологических изменениях
эндометрия, не позволяющих осуществиться полноценной им-
плантации плодного яйца, а также наличие опухоли матки, обыч-
359
но миомы. Иногда причиной выкидыша или преждевременных
родов может стать психическая травма.
Морфология. При самопроизвольном прерывании беременно-
сти или сразу после нее производят выскабливание полости мат-
ки. При гистологическом исследовании в скобах определяются
фрагменты плодного яйца в виде обрывков плодных оболочек,
ворсины хориона и децидуальная ткань.
ГЕСТАЦИОННАЯ ТРОФОБЛАСТИЧЕСКАЯ БОЛЕЗНЬ
Гестационная трофобластическая болезнь — общий термин,
который объединяет три патологических процесса: пузырный за-
нос, хориокарциному и трофобластическую опухоль плацентар-
ного ложа.
1. Пузырный занос возникает в связи с оплодотворением яйце-
клетки с утраченным или инактивированным ядром. Продукт за-
чатия является для матери полным аллотрансплантатом. Риск пу-
зырного заноса минимальный при беременности в возрасте 20—
35 лет. У подростков моложе 15 лет этот риск в 20 раз выше, у
женщин старше 50 лет риск развития повторного пузырного за-
носа в 200 раз выше, чем для 20—35-летних. Риск развития по-
вторного пузырного заноса в 20—40 раз выше, чем риск первого
пузырного заноса.
Морфология. В плаценте ворсины хориона превращаются в
мелкие и средней величины кисты, напоминающие гроздья вино-
града, причем пузырьки могут самопроизвольно отторгаться.
Плод при пузырном заносе погибает. Одновременно происходит
пролиферация эпителия и синцития ворсин хориона. Иногда эта
пролиферация выражена чрезвычайно интенсивно и ворсины хо-
риона прорастают в стенку матки, в ее вены, вены таза. Это инва-
зивный (злокачественный) пузырный занос. Кисты отрываются от
ворсин, превращаются в эмболы, имеющие форму пузырей, и с
током крови попадают в легкие, вызывая эмболию ветвей легоч-
ной артерии.
2. Хориокарцинома — злокачественная опухоль трофобласта,
встречается нечасто, преимущественно у молодых беременных
женщин. Опухоль развивается после пузырного заноса, аборта или
трубной беременности из трофобласта, лишена ворсин хориона.
Морфология. Опухоль имеет вид мягкого губчатого узла, распо-
ложенного в миомитрии, на разрезе пестрая из-за чередования в
ней очагов некроза и кровоизлияний. Микроскопически опухоль
состоит из атипичных клеток Лангханса и синцития, прорастаю-
щих стенку матки. В опухоли почти нет стромы. Хориокарцинома
метастазирует гематогенно, в первую очередь в легкие.
Прогноз. Несмотря на злокачественное течение хориокарцино-
мы, применение химиотерапии способствует излечению более
80 % больных, в том числе при наличии метастазов.
3. Трофобластическая опухоль плацентарного ложа проявляется
360
инфильтрацией эндометрия и миометрия преимущественно клет-
ками трофобласта и синцитиотрофобластическими клетками.
Развитию опухоли предшествуют роды или аборт. В большинстве
случаев это доброкачественная опухоль, но в 10 % случаев может
иметь злокачественное течение.
Морфология. Опухоль представляет собой узел с кровоизлия-
ниями. Наблюдается тенденция к инвазивному росту клеток опу-
холи. особенно к прорастанию в сосуды. Обычно наблюдаются
обширные очаги некроза ткани опухоли и кровоизлияний, что
может служить признаком неблагоприятного течения заболева-
ния.
РОДОВАЯ ИНФЕКЦИЯ МАТКИ
Острый эндометрит — тяжело текущее воспаление эндометрия,
вызываемое микробной инфекцией: стрептококками, стафило-
кокками, кишечной палочкой. Он может развиваться до родов, в
родах и в послеродовом периоде. Причиной эндометрита иногда
является инфекционное заболевание, которое перенесла женщи-
на во второй половине беременности. Порой эндометрит возни-
кает как следствие нарушения правил асептики, в том числе и в
родовспомогательных учреждениях.
Септический эндометрит наиболее опасен. Воспаление при
этом имеет дифтеритический, гнойный или гнилостный характер.
Эндометрий приобретает грязно-серый цвет. Инфекция распро-
страняется по лимфатическим путям и венам, что способствует
развитию сепсиса. Нередко в воспаление вовлекается мышечная
оболочка матки (метрит), а также серозная ее оболочка (перимет-
рит) и брюшина — развивается перитонит.
Слкрть в случае гнойного эндометрита и сепсиса наступает от
резкой интоксикации организма.
Глава 23
ЭКСТРЕМАЛЬНЫЕ СОСТОЯНИЯ
Экстремальные состояния — это состояния, вызванные такими
патогенными факторами, которые оказывают на организм пре-
дельное. нередко разрушительное воздействие.
Вцдщ экстремальных состояний. К числу наиболее клинически
значимых экстремальных состояний относят:
• коллапс;
• шок;
• кому.
361
Экстремальные факторы. Человек может подвергаться воздей-
ствию факторов чрезвычайной силы, продолжительности и не-
обычного характера. Эти факторы могут быть экзогенными и эн-
догенными.
Экзогенные воздействия — резкие и значительные колебания
атмосферного давления, содержания кислорода во вдыхаемом
воздухе, механические травмы, электрический ток, дефицит про-
дуктов питания и воды, переохлаждение или перегревание, ин-
фекции. интоксикации и многие другие.
Эндогенные факторы — состояния, значительно нарушающие
жизнедеятельность организма — тяжелые болезни и осложнения.
Действия экстремальных факторов приводят к развитию одно-
го из двух состояний:
• экстренной адаптации к экстремальному фактору, которая
характеризуется предельным напряжением адаптивных ме-
ханизмов организма, что позволяет сохранить его функции.
После прекращения действия чрезвычайного фактора со-
стояние организма нормализуется;
• критического, или неотложного, состояния, которое характе-
ризуется чреватыми смертью расстройствами жизнедеятель-
ности организма и проявляется предельной активацией и
последующим истощением адаптивных механизмов, грубы-
ми расстройствами функций органов и физиологических
систем и требует неотложной врачебной помощи.
КОЛЛАПС
Коллапс — остро развивающаяся сосудистая недостаточность,
возникающая в результате значительного падения тонуса сосудов
и уменьшения объема циркулирующей крови. Коллапс характе-
ризуется недостаточностью кровообращения, первичной цирку-
ляторной гипоксией, расстройством функций тканей, органов и
систем.
Непосредственной причиной коллапса является значительно
большая емкость сосудистого русла по сравнению с объемом
циркулирующей в нем крови. Это может быть результатом:
• снижения величины выброса крови из левого желудочка
сердца в сосудистое русло, что происходит при острой сер-
дечной недостаточности, вызываемой инфарктом миокарда,
выраженной аритмией, эмболией сосудов системы легочной
артерии, при быстром вставании из положения лежа или
сидя;
• уменьшения массы циркулирующей крови при остром мас-
сивном кровотечении, быстром значительном обезвожива-
нии организма (при профузном поносе, массивном потоот-
делении, неукротимой рвоте), потере большого объема
плазмы крови при обширных ожогах, а также при перерас-
пределении крови с депонированием значительного ее ко-
362
личества в венозных сосудах, кровеносных синусах и ка-
пиллярах, например при шоке или гравитационных пере-
грузках;
• снижения общего периферического сосудистого сопротив-
ления из-за падения тонуса стенок артериол или снижения
их ответа на воздействие вазопрессорных веществ (катехо-
ламинов, вазопрессина и др.)- Такие изменения наблюдают-
ся при тяжелых инфекциях, интоксикациях, гипертермии,
гипотиреозе, надпочечниковой недостаточности и др.
Обморок — внезапная кратковременная потеря сознания, при-
чиной которой является острая гипоксия мозга, возникающая как
следствие коллапса. При восстановлении сознания пациенты бы-
стро ориентируются в окружающих событиях и случившемся с
ними.
Вцлщ коллапса. В соответствии с тремя категориями этиологи-
ческих факторов выделяют и три основные группы коллапса: кар-
диогенный, вазодилатационный и гиповолемический. В практи-
ческой медицине выделяют постгеморрагический, инфекцион-
ный, токсический, радиационный, панкреатический, ортостати-
ческий, гипокапнический и другие виды коллапса.
Морфология коллапса характеризуется бледностью кожных по-
кровов, сухостью слизистых оболочек, венозным полнокровием
печени, почек, селезенки, жидкой темной кровью, малокровием
полостей сердца, жировой дистрофией паренхиматозных органов,
отсутствием отека легких.
ШОК
Шок — крайне тяжелое состояние организма, возникающее
под действием сверхсильных, экстремальных факторов, характе-
ризующееся прогрессирующим расстройством жизнедеятельности
организма, в результате нарастающего нарушения функций нерв-
ной, эндокринной, сердечно-сосудистой и других жизненно важ-
ных систем. Без проведения экстренных врачебных мероприятий
шок приводит к смерти.
Этиология. Шок вызывается экстремальными факторами
большой силы, разрушающими структуры тканей и органов. Наи-
более частыми причинами шока являются:
• различные травмы;
• массивная кровопотеря;
• переливание несовместимой крови;
• попадание в организм аллергенов;
• острая ишемия или некроз органов — сердца, почек, пече-
ни и др.
Виды шока. В соответствии с причинами выделяют следующие
виды шока:
• травматический (раневой);
• ожоговый;
363
• посттрансфузионный:
• аллергический (анафилактический);
• кардиогенный;
• токсический;
• психогенный (психический).
В зависимости от тяжести течения шок подразделяют на:
• шок I степени (легкий);
• шок II степени (средней тяжести);
• шок III степени (тяжелый).
Патогенез шока складывается из двух стадий.
Адаптивная, или колтенсаторная, стадия развивается сразу по-
сле воздействия чрезвычайного повреждающего фактора, когда
активируются неспецифические адаптивные реакции.
Вторая стадия шока — стадия дезадаптации, или декомпенса-
ции, развивается, если адаптивные процессы оказываются недос-
таточными, и характеризуется:
• истощением и срывом адаптивных реакций организма;
• прогрессирующим снижением эффективности нейроэндок-
ринной регуляции;
• развитием нарастающей недостаточности органов и систем.
ОСОБЕННОСТИ НЕКОТОРЫХ ВИДОВ ШОКА
Травматический шок. Причина — массивное повреждение орга-
нов, мягких тканей и костей, в основном механического характе-
ра. Как правило, травма тканей сочетается с кровопотерей и неред-
ко инфицированием раны.
Патогенез и проявления. Травматический шок характеризуется
значительной болевой афферентацией в связи с повреждением
находящихся в тканях нервных стволов, узлов и сплетений. Его
патогенез складывается из двух указанных выше стадий — ком-
пенсации, которая коррелирует с масштабом и степенью травмы,
и декомпенсации.
Исход. Нарушения в организме при отсутствии врачебной по-
мощи усиливают друг друга и могут привести к смерти.
Ожоговый шок. Причина — обширный ожог кожи (более 25 %
ее поверхности) II или III степени.
Патогенез и проявления. Основные звенья механизма ожогово-
го и травматического шока сходны. Вместе с тем ожоговый шок
имеет ряд особенностей. К числу наиболее важных следует отне-
сти следующие:
• значительная болевая афферентация от обожженой кожи и
мягких тканей;
• сравнительно короткая стадия компенсации, часто перехо-
дящая в стадию декомпенсации еще до оказания первой
врачебной помощи;
• выраженная дегидратация организма в результате массив-
ной потери плазмы крови;
364
• сгущение крови, расстройства микроциркуляции, развитие
феномена сладжа. тромбообразования;
• выраженная интоксикация организма продуктами денатура-
ции белка и протеолиза, избытком биологически активных
веществ, образующихся при повреждении тканей (кининов,
биогенных аминов, полипептидов, ионов и др.), а также эк-
зо- и эндотоксинами микробов;
• частое поражение почек, обусловленное нарушением их
кровоснабжения и массированным гемолизом эритроцитов;
• прогрессирующее угнетение иммунной системы и ауто-
агрессия вследствие интоксикации организма.
Анафилактический (аллергический) шок. Причины — действие
различных аллергенов. Наиболее часто это:
• лекарственные средства, вводимые парентерально — содер-
жащие белок сыворотки и вакцины, а также цельная кровь;
препараты, играющие роль гаптенов, — многие антибиоти-
ки, препараты йода, брома и др.;
• иногруппная кровь или ее компоненты, вводимые паренте-
рально;
• яды насекомых, птиц и животных, попадающие в организм.
Патогенез. Для анафилактического шока характерно интен-
сивное начало, обычно быстропреходящая стадия компенсации и
прогрессирующая декомпенсация.
Морфология шока. Помимо травм, ожогов, отеков, которые
вызывают шок, в организме развивается морфологическая карти-
на шока. Она складывается из развития ДВС-синдрома, "шоко-
вых почек", "шоковых легких" и гипоксических изменений.
ДВС-синдром, когда просветы сосудов микроциркуляторного
русла, в первую очередь капилляров и венул, почек, легких, серд-
ца, головного мозга и других органов закрываются фибриновыми
тромбами. При этом резко нарушается микроциркуляторное кро-
вообращение и развивается острая гипоксия, сопровождающаяся
резким повышением сосудистой проницаемости и развитием ост-
рого отека органов, в том числе головного мозга и легких.
Развитие "шоковых почек" является компенсаторной реакцией
на нарушение кровообращения и падение артериального давле-
ния. При этом рефлекторно происходит сброс крови из коры по-
чек в мозговое вещество и возникает острая ишемия юкстагломе-
рулярного аппарата клубочков почек, в кровь поступает ренин и
другие гипертензивные вещества. Они вызывают спазм артериол
и повышение артериального давления, что необходимо для
уменьшения степени гипоксии и обеспечения функции сердца и
головного мозга. Почки при этом имеют характерный вид —
светло-желтая ишемизированная кора и темно-красное, перепол-
ненное кровью мозговое вещество. Однако если ишемия коры
почек продолжается достаточно долго, то кора некритизируется,
развиваются некротический невроз, уремия, от которой больные
и погибают.
Развитие "шоковых легких" отражает динамику ДВС-синдрома
365
в легких, где выявляются фибриновые тромбы большого количе-
ства легочных капилляров, периваскулярные кровоизлияния в
ткани легких, ателектазы и развитие дистресс-синдрома.
Гипоксические изменения, которые вызывают резкую жиро-
вую дистрофию паренхиматозных органов, сохраняются и в пери-
од реконвалесценции (выздоровления).
КОМА
Кома — крайне тяжелое состояние организма, возникающее в
результате действия различных повреждающих факторов и харак-
теризующееся глубоким угнетением нервной деятельности, поте-
рей сознания, гипо- и арефлексией, недостаточностью функций
органов и систем организма.
Причинами комы являются следующие факторы.
Экзогенные факторы чрезвычайной силы или токсичности. К.
ним относятся:
• травмирующие факторы, как правило, головной мозг;
• термические воздействия — перегревание, солнечный удар,
переохлаждение и т. п.;
• значительные колебания барометрического давления;
• токсины — алкоголь и его суррогаты, этиленгликоль, ток-
сические дозы наркотиков, седативных средств, барбитура-
тов и др.;
• инфекционные агенты — вирусы, микробы, особенно воз-
будители малярии, сыпного и брюшного тифа;
• экзогенная гипоксия и аноксия.
Эндогенные факторы, которые возникают при неблагоприят-
ном течении различных болезней и болезненных состояний, —
ишемия, инсульт, опухоль мозга, дыхательная недостаточность,
патология системы крови, печеночная и почечная недостаточ-
ность и др.
Вцды комы. По происхождению комы дифференцируют на:
• эндогенные, обусловленные патологическими процессами в
организме;
• экзогенные, вызванные патогенными агентами внешней
среды;
• первичные, или церебральные, развивающиеся в результате
непосредственного повреждения мозга;
• вторичные, обусловленные нарушением функции органов и
тканей, вторично приводящими к альтерации мозга, напри-
мер кома при сахарном диабете, уремии, печеночной недос-
таточности и т. п.
Патогенез колы. Вне зависимости от специфики вызвавших
коматозные состояния причин механизм их развития включает
несколько общих ключевых звеньев:
• гипоксию и нарушение процессов энергообеспечения клеток;
• интоксикацию веществами, попавшими в организм извне
366
Таблицa 3. Общие проявления .
’Нтозных состоянии
Органы и системы Измененные функции
Нервная и эн- докринная CMC- Расстройство и Гипо-, арсфлекстц р ° н ния ДоГ " бИ 1Огичсски активных веществ и их эф-
темы
Ссрдсчно-сосу- Сердечная недост^
листая система Аритмии шесть
Легкие Артериальная гигь^ КЬтЬлфнс троф^нз,,я- коллапс ^чческая недостаточность
Дыхательная нсдо^^^
Система крови Депонирование к^
и гемостаза Изменение вязкое Тромбогеморрагиь„ ₽ови к веский синдром
[) очень Печеночная недо^ гаточность
Почки Почечная недостд^,^^
Пищеваритель- ная система ГНОСТЬ волостного и мембранного пищева- JUHp-Хттл_л. Кишечная аугоину.„ . ? ^оксикация, аутоинфекция
кчеиочиоН недостаточно*": на"'м'ме₽ при почечной или
к"“ото““^вного состоят., КМ пршяою. -
иЦИДОЗу
• дисбаланс ионов и жидкосТи.
. нарушение алекгрофи3и^о-чсских ссов в клетках
Указанные расстройства раз^ я во п
по в большей мере они выражеь., „ .,„ога ы
1 ‘ чц в мозге. Именно по /тому обя-
зательным признаком комы явдв&г„„ ___„„ ' у
1 чется потеря сознания
Степень тяжести комы оп1к ' специально* шкале,
оценшшющеи в баллах степень р Выделяю!
три степени тяжести комы: r
• тяжелую, с ремыюп упхчвд смертельного исхода;
' Расстройствами фуйкйй» утро-
• легкую, обратимую
Общие проявления коматозн^ состоянии приведены в табл 3.
Они обусловлены главным обра нарушениРем функций нерв-
ной, сердечно-сосудистой, пищеВЧр^ной сис-
тем, печени, почек, а также сисТе щ ь
Глава 24
ПРОФЕССИОНАЛЬНЫЕ БОЛЕЗНИ
Профессиональные болезни — заболевания, связанные с воз-
действием на организм вредных факторов производства в процес-
се трудовой деятельности человека. В зависимости от влияния тех
или иных факторов выделяют несколько групп профессиональ-
ных болезней, однако в повседневной практике наибольшее зна-
чение имеют профессиональные болезни, вызываемые промыш-
ленной пылью, а также заболевания, возникающие от воздейст-
вия физических факторов, с которыми сталкивается человек на
производстве.
ПНЕВМОКОНИОЗЫ
Пневмокониозы — "пылевые" болезни. Они характеризуются
развитием в легких склеротических изменений, обусловленных
попаданием в дыхательные пути промышленной пыли — мель-
чайших частиц твердых веществ, проникающих в глубокие отде-
лы легочной паренхимы. Пневмокониозы вызывают частицы
кремния, асбеста, красного железняка, алюминия, бериллия,
угольная пыль и продукты других производств, однако наиболь-
шее значение по своей практической значимости имеют силикоз,
силикатоз и антракоз.
Силикоз вызывается длительным вдыханием пыли, содержа-
щей свободную двуокись кремния.
Патогенез. Попадая в паренхиму легкого, кристаллы кремния
растворяются, в результате чего образуется кремниевая кислота,
повреждающая легочную ткань и вызывающая развитие фиброз-
ного процесса в виде узелков или диффузного разрастания соеди-
нительной ткани.
Морфология. Исходя из патогенеза выделяют две формы сили-
коза: узелковую и диффузно-склеротическую.
Узелковая форма, при которой в альвеолах и альвеолярных хо-
дах, на месте лимфатических сосудов образуется большое количе-
ство силикотических узелков и узлов различной величины и фор-
мы. Иногда они сливаются в крупные узлы, занимающие значи-
тельную часть доли легкого. Типичные силикотические узелки
построены из концентрически или вихреобразно расположенных
волокон соединительной ткани (рис. 89). Макрофаги межальвео-
лярных перегородок фагоцитируют частицы пыли и превращают-
ся в кониофаги. С течением времени вследствие тяжелых измене-
ний в кровеносных сосудах и нервном аппарате легких в центре
крупных силикотических узелков происходит распад соедини-
тельной ткани и образуются силикотические каверны.
Диффузно-склеротическая форма характеризуется разрастанием
368
Рис. 89. Силикоз легких.
а — силикотические узелки с концентрическим расположением коллагеновых
пучков; б — силикотические узелки с вихреобразным расположением пучков.
соединительной ткани в межальвеолярных перегородках, вокруг
сосудов и бронхов. В легких развивается эмфизема, а в бронхах —
воспалительные изменения и бронхоэктазы.
При обеих формах силикоза легкие увеличиваются в объеме,
становятся плотными, в слизистых оболочках носа, гортани, тра-
хеи развиваются атрофические и склеротические изменения.
Правые отделы сердца гипертрофируются. Нередко к силикозу
присоединяется туберкулез, развивается силикотуберкулез.
Исход. Силикоз течет хронически, и лишь изредка встречается
его острая форма, характеризующаяся быстрым прогрессировани-
ем болезни, приводящей больных к смерти через 1—2 года.
Силикатозы вызываются пылью, содержащей не свободную
окись кремния, а ее силикаты, в которых она находится в связан-
ном состоянии с алюминием, магнием, кальцием, железом и т. п.
Все силикаты могут вызывать силикатозы, но наибольшее значе-
ние среди них имеет асбестоз.
Асбестоз возникает при запылении легких асбестовой пылью —
силикатом магния. Течет болезнь хронически, клинически харак-
теризуется нарастающей одышкой и легочно-сердечной недоста-
точностью.
Морфология. В легких отмечается диффузное разрастание со-
единительной ткани в межальвеолярных перегородках, вокруг со-
судов и бронхов. В тяжелых случаях просветы альвеол настолько
уменьшаются, что их почти не видно. В разросшейся соедини-
369
тельной ткани много пыли и асбестовых телец, представляющих
собой мельчайшие образования в виде палочек с утолщениями на
концах. В бронхах и бронхиолах развиваются явления хрониче-
ского серозного, иногда гнойного бронхита, бронхоэктазы. Лим-
фатические узлы легких содержат много асбестовой пыли, плот-
ные, увеличены в размерах. У рабочих асбестовой промышленно-
сти на пальцах рук, ног, подошвах, ладонях могут возникать оча-
ги гиперкератоза, содержащие асбестовые тельца и гигантские
клетки инородных тел (асбестовые бородавки).
Исход. Смерть больных асбестозом наступает от присоединяю-
щейся пневмонии, эмфиземы легких, легочно-сердечной недоста-
точности.
Антракоз — пневмокониоз, вызываемый длительным вдыхани-
ем угольной пыли. Считают, что повреждающее действие на ле-
гочную ткань оказываю! не угольные частицы, а кремниевая ки-
слота, содержание которой в разных углях неодинаковое.
Морфология. Угольная пыль откладывается во всей паренхиме
легких, но особенно много ее накапливается вокруг сосудов, брон-
хов, в межальвеолярных перегородках. Здесь же развивается соеди-
нительная ткань. Пыль фагоцитируется гистиоцитами межальвео-
лярных перегородок — "пылевыми клетками". При слиянии очагов
запыления возникают антракотические узлы. При диффузном ан-
тракотическом пневмосклерозе значительные участки легких ока-
зываются безвоздушными, плотными, аспидо-черного цвета — это
аспидная, или антракотическая, индурация легких. Для антракоза
характерны хронический бронхит и рецидивирующая очаговая
пневмония, а также склероз и зарастание просвета сосудов.
Осложнения. Вследствие расстройства кровообращения в ан-
тракотических узлах иногда возникают очаги некроза с последую-
щим распадом — образуются каверны с черными стенками и с
черным крошащимся содержимым. Возникает кровохарканье. Эта
форма антракоза называется черной чахоткой.
Исход. Больные умирают от рецидивирующей хронической
пневмонии, черной чахотки, от легочно-сердечной недостаточности.
ПРОФЕССИОНАЛЬНЫЕ БОЛЕЗНИ, ВОЗНИКАЮЩИЕ
ПРИ ДЕЙСТВИИ ФИЗИЧЕСКИХ ФАКТОРОВ
Основные положения, касающиеся патогенного действия фак-
торов окружающей среды, изложены в главе 3. Среди таких тяже-
лых профессиональных заболеваний, как кессонная болезнь, виб-
рационная болезнь, болезней, связанных с действием производст-
венного шума, электромагнитных волн, радиочастот и др., особое
значение имеет лучевая болезнь, возникающая при действии на
организм ионизирующих излучений.
370
ЛУЧЕВАЯ БОЛЕЗНЬ
Патогенез. Среди многих изменений, обусловленных повреж-
дающим действием ионизирующего излучения, следует отметить
угнетение ферментных систем организма, что ведет к резкому на-
рушению обмена веществ, прекращению митотического деления
клеток и, следовательно, нарушению процессов регенерации по-
врежденных тканей. Особенно чувствительными к ионизирующе-
му излучению органы, репарация в которых осуществляется за
счет клеточной регенерации, — органы кроветворения, половые
железы, кожа и эпителий пищеварительного тракта. Различают
острую и хроническую лучевую болезнь.
Острая лучевая болезнь
Пато- и морфогенез. Острая лучевая болезнь проявляется
главным образом угнетением кроветворной системы. В костном
мозге быстро прогрессирует опустошение кроветворной ткани,
т. е. исчезают ее клеточные элементы, развиваются анемия, лей-
копения, лимфоцитопения и тромбоцитопения. В лимфатиче-
ских узлах, селезенке, лимфоидных образованиях пищевари-
тельного тракта гибнут лейкоциты и угнетается их новообразо-
вание. У больных появляется геморрагический синдром в виде
множественных кровоизлияний в органах. Они связаны с отсут-
ствием тромбоцитов и тяжелыми структурными изменениями
стенок сосудов микроциркуляторного русла, что приводит к
резкому повышению их проницаемости. Многочисленные ге-
моррагии пищеварительного тракта иногда обусловливают мас-
сивные желудочно-кишечные кровотечения. В слизистой обо-
лочке желудка и кишечника образуются эрозии и множествен-
ные изъязвления.
В связи с гибелью лимфоцитов возникает угнетение иммун-
ной системы. В этих условиях активируется собственная микро-
флора больных. В картине болезни ярко проявляются аутоин-
фекционные процессы, особенно в пищеварительном тракте, в
виде гангренозного стоматита, глоссита, ангины и энтероколи-
та. При этом, несмотря на наличие некроза и большого количе-
ства микробов в тканях, лейкоцитарная реакция не возникает,
грануляционная ткань не образуется. В коже появляются дли-
тельно незаживающие язвы также без воспалительной реакции.
В легких на фоне кровоизлияний и очагов некроза развиваются
тяжелая алейкоцитарная пневмония и микробизм. Очень тяже-
лые повреждения появляются в половых железах и гипофизе. У
мужчин подавляется сперматогенез; в гипофизе некробиотиче-
ским изменениям подвергаются базофильные клетки. Характер-
ным признаком является выпадение волос, вплоть до полного
облысения.
Исход. Смерть больных от острой лучевой болезни при боль-
371
ших дозах облучения наступает от комы, анемии, кровоизлияний
в жизненно важные органы, массивных внутренних кровотече-
ний, а также от присоединившейся инфекции.
Хроническая лучевая болезнь
Пато- и морфогенез. Хроническая лучевая болезнь в зависимо-
сти от тяжести поражения кроветворной системы протекает раз-
нообразно. Она развивается либо в исходе острой лучевой болез-
ни вследствие остаточных изменений в связи с ослабленной реге-
нерацией кроветворной ткани, либо в результате повторных воз-
действий малых доз радиации. Хроническая лучевая болезнь мо-
жет проявляться апластической анемией и лейкопенией.
Осложнения хронической лучевой болезни связаны с актива-
цией аутоинфекций, кровоизлияниями. При действии ионизи-
рующего излучения в связи с извращением процессов регенера-
ции в кроветворной ткани, появлением недифференцированных
и несозревающих кроветворных клеток нередко развиваются лей-
козы. Хроническая лучевая болезнь приводит к возникновению
опухолей кожи, костей и других органов.
Исход хронической лучевой болезни без лечения неблагопри-
ятный. Смерть наступает от присоединившихся инфекций и дру-
гих осложнений. При интенсивной терапии жизнь больных мо-
жет быть сохранена.
Глава 25
СМЕРТЬ, РЕАНИМАЦИЯ
И БОЛЕЗНИ ОЖИВЛЕННОГО ОРГАНИЗМА
СМЕРТЬ
Смерть — прекращение жизни, которое характеризуется утра-
той всех функций организма.
Терминальные состояния — это состояния, предшествующие
смерти. Они представляют собой конечные этапы жизни, погра-
ничные между жизнью и смертью.
К терминальным состояниям относятся все стадии умирания:
агония, клиническая смерть и биологическая смерть.
Агония — период, когда артериальное давление прогрессирую-
ще снижается, уменьшается частота сердечных сокращений,
пульс становится редким, сознание затемнено. В дальнейшем
снижается тонус мускулатуры, расслабляются сфинктеры, возни-
кают непроизвольное мочеиспускание и выделение кала. В ре-
зультате застоя крови в легких повышается проницаемость сосу-
372
дов малого круга кровообращения, нарастает отек легких и дыха-
ние становится клокочущим, хриплым. Из-за тяжелой гипоксии
и угнетения дыхательного центра появляется атональное дыхание,
угасают рефлексы, в частности реакция зрачков на свет. В даль-
нейшем развивается клиническая смерть.
Клиническая смерть — обратимый этап умирания, для которо-
го характерна остановка дыхания и кровообращения, но сохране-
ние в течение некоторого времени возможности восстановления
жизни. Этот этап умирания длится 5—6 мин, в течение которых
сохраняется жизнеспособность мозга. При медленном умирании
клинической смерти предшествует агония.
Биологическая смерть — необратимый этап умирания, насту-
пающий за клинической смертью и характеризующийся прекра-
щением обмена веществ в мозге, а затем и в других органах, в
тканях которых развиваются необратимые, несовместимые с жиз-
нью изменения.
ВИДЫ СМЕРТИ
Естественная смерть наступает в старости от физиологического
угасания метаболизма и прекращения функций организма.
Насильственная смерть является результатом несчастных слу-
чаев (травма, отравление), убийства и самоубийства.
Патологическая смерть, или смерть от болезней, возникает в
результате несовместимых с жизнью изменений в организме:
• внезапная, или скоропостижная, смерть — вариант патоло-
гической смерти, наступающей неожиданно на фоне кажу-
щегося здоровья при скрыто протекающих патологических
процессах. Причиной внезапной смерти обычно являются
инсульт, инфаркт миокарда, кардиомиопатии, массивное
кровотечение из аорты при разрыве ее аневризмы и т. п.
Трансплантация — пересадка органов и тканей умершего жи-
вым людям. Эта возможность основана на том, что после наступ-
ления биологической смерти некоторое время сохраняется жиз-
недеятельность органов и в связи с этим возможность восстанов-
ления их функции. Вопросами трансплантации органов и тканей
занимается медицинская наука — трансплантология.
Биологическая смерть
Патологическая анатолия. Биологическая смерть проявляется
рядом признаков. К ним относятся охлаждение трупа, трупное
высыхание, трупные гипостазы, трупные пятна, трупное окочене-
ние, посмертный аутолиз и трупное разложение, гниение тканей
и трупное разложение.
Охлаждение трупа до температуры окружающей среды начина-
ется спустя некоторое время после остановки дыхания и кровооб-
373
ращения. Это происходит в связи с прекращением обмена ве-
ществ, образования энергии и тепла.
Трупное высыхание начинается в результате отдачи влаги в ок-
ружающую среду. При этом мутнеет роговица глаз, на коже появ-
ляются желто-бурые "пергаментные" пятна.
Трупные гипостазы — багрово-фиолетовые пятна, исчезающие
при надавливании, развиваются через 3—5 ч в результате пере-
распределения крови: левые камеры сердца запустевают, а в его
правых камерах образуются блестящие гладкие свертки крови
красного или желтого цвета. Артерии также запустевают, а вены
нижележащих частей тела переполняются кровью.
Трупные пятна развиваются в результате посмертного гемолиза
эритроцитов: плазма крови, содержащая гемоглобин, выходит из
вен и пропитывает ткани, после чего трупные гипостазы уже не
исчезают при надавливании.
Трупное окоченение начинается через 2—6 ч после смерти. Оно
появляется в мышцах лица и. постепенно распространяясь на
мышцы туловища и нижних конечностей, через 24—32 ч захваты-
вает всю мускулатуру. Мышцы становятся очень плотными, теря-
ют растяжимость и эластичность. Скорость и характер трупного
окоченения зависят от различных причин — температуры окру-
жающей среды, характера болезни и состояния больных перед
смертью. Так, у истощенных, ослабленных болезнью умерших, а
также у маленьких детей трупное окоченение может быть выра-
жено слабо. У недоношенных плодов трупное окоченение вообще
не развивается. После смерти от некоторых инфекционных бо-
лезней (столбняк, холера) трупное окоченение развивается быст-
ро и выражено очень резко. Через 2—3 сут трупное окоченение
исчезает.
Посмертный аутолиз и трупное разложение развиваются в по-
гибших тканях трупа. Эти изменения раньше возникают в орга-
нах, содержащих много протеолитических ферментов, — в пече-
ни, поджелудочной железе, желудке.
Гниение тканей обусловлено гнилостными процессами в ре-
зультате разложения бактерий кишечника в тканях трупа. Они
расплавляются, приобретают грязно-зеленую окраску и зловон-
ный запах.
Трупное разложение характеризуется тем, что образующиеся в
результате гниения газы пропитывают ткани трупа, накапливают-
ся в полостях. Труп раздувается, иногда до огромных размеров.
РЕАНИМАЦИЯ
Реанимация — восстановление жизненно важных функций ор-
ганизма. Реаниматология — наука об оживлении организма.
Опыты по оживлению организма проводились уже давно
И. И. Бахметьевым, Ф. А. Андреевым, С. И. Чечулиным, С. С. Брю-
хоненко и др. Они заложили основы реаниматологии, которая в
374
настоящее время достигла больших успехов. В мире живут и
трудятся многие тысячи людей, перенесших клиническую
смерть. Реанимация оказалась возможной потому, что специ-
альные мероприятия стали применять максимально рано — в
период агонии или в первые минуты клинической смерти, а
также в связи с применением высокоэффективных способов
оживления.
Методы реанимации. При остановке сердца и дыхания на ста-
дии клинической смерти немедленно применяют комплекс меро-
приятий, направленных на восстановление угасающих или угас-
ших жизненных функций организма. К ним относятся массаж
сердца, электрическая дефибрилляция, электрическая стимуля-
ция, применение лекарственных препаратов.
Массаж сердца может быть непрямым (через грудную клетку)
и прямым — при вскрытой грудной клетке. Массаж сердца на-
правлен на восстановление его функции и кровотока в мозге.
Электрическая дефибрилляция используется в том случае, если
у больного применение реанимационных мероприятий началось
во время фибрилляции сердца. Это часто нормализует ритм серд-
ца и сердечную деятельность.
Электрическая стимуляция сердца (кардиостимуляция) приме-
няется для стимуляции остановленного сердца.
Лекарственные препараты, например адреналин или хлорид
кальция, внутриартериальное введение крови также используют
для стимуляции остановленного сердца.
Интенсивная терапия — система мероприятий, направленных
на предупреждение расстройств или восстановление разнообраз-
ных функций организма при угрозе жизни человека. Современ-
ная реанимация — это не только временное замещение и восста-
новление жизненно важных функций организма, но и последую-
щего управления ими до того момента, пока не восстановится
полностью собственная регуляция функций. Для этой цели до
возникновения клинической смерти, во время оживления и после
него (постреанимационный период) применяют приемы интен-
сивной терапии. Интенсивная терапия проводится в специализи-
рованных отделениях больниц — отделениях реанимации и интен-
сивной терапии. Здесь осуществляется непрерывная регистрация
состояния кровообращения и дыхания на специальных установ-
ках — мониторах, а также постоянный контроль жизненно важ-
ных показателей гомеостаза. В комплекс интенсивного лечения
входят:
• инфузионная терапия — введение в сосуды больного крови,
электролитов и т. п., направленное на восстановление объе-
ма циркулирующей крови, нормализацию гомеостаза и вос-
становление микроциркуляции;
• искусственное питание — больным парентерально вводят
изотонический раствор глюкозы, аминокислоты, белковые
гидролизаты, витамины;
• детоксикация при наличии интоксикации организма;
375
• очищение крови (гемодиализ, гемосорбция) и лимфы (лим-
фосорбция);
• гипербарическая оксигенация — дыхание кислородом под
повышенным барометрическим давлением. Она рассчитана
на насыщение плазмы крови кислородом и устранение ги-
поксии тканей.
Осложнения во время реанимации и после нее возникают в ре-
зультате крайне высокой чувствительности мозга к кислородному
голоданию, а также обусловлены сложностью применения реани-
мационных методов.
БОЛЕЗНИ ОЖИВЛЕННОГО ОРГАНИЗМА
Постреанимационная болезнь. Возникающие в постреанимаци-
онном периоде нарушения функций органов и тканей наслаива-
ются на проявления основной болезни, вызвавшей клиническую
смерть. При этом постреанимационные нарушения нередко вы-
ражены более интенсивно, чем изменения, связанные с основ-
ным заболеванием. Такие расстройства проявляются преимущест-
венным поражением той или иной физиологической системы в
виде определенных синдромов.
Аноксическая энцефалопатия — повреждение головного мозга
вследствие тяжелого кислородного голодания — одна из основ-
ных причин гибели больных в постреанимационном периоде. В
основе этого поражения мозга лежат его отек и набухание, возни-
кающие вследствие гипоксии, повышения проницаемости сосу-
дов и выхода жидкости из сосудов в ткань мозга. Возникают рас-
пространенные ишемические повреждения головного мозга, за-
канчивающиеся гибелью нейронов и распадом волокон белого
вещества. Эти нарушения развиваются преимущественно в коре
большого мозга и мозжечке. Тяжелые повреждения коры приво-
дят к резкому угнетению, а в дальнейшем и к выпадению ее
функций — децеребрации. Это состояние называется "мозговой
смертью", ибо необратимая децеребрация при работающем сердце
означает гибель человека как социального существа, так как толь-
ко функции головного мозга определяют психическую деятель-
ность и индивидуальность человека. Наряду с этим децеребрация
обычно заканчивается прекращением дыхания.
Если при сохраненной сердечной деятельности происходит ос-
тановка дыхания и длительное время используется искусственная
вентиляция легких, могут развиваться еще более глубокие повре-
ждения головного мозга — "респираторный мозг". Наблюдается
смещение мозга в результате его деформации при отеке и набуха-
нии, образование очагов распада нервной ткани. Возможен также
частичный некроз ткани мозга, чаще всего это симметричный
некроз подкорковых образований. В крайне тяжелых случаях воз-
никает некроз всего головного мозга. Вещество его приобретает
характер бесструктурной полужидкой массы, заключенной в моз-
376
говые оболочки. Рефлекторная деятельность ЦИС отсутствует,
нет собственного дыхания, исчезает биоэлектрическая активность
мозга. Мозговой кровоток резко нарушен или полнос тью выклю-
чен, хотя сердечная деятельность может сохраняться длительное
время. В конечном итоге наступает остановка сс| пи. Необрати-
мая децеребрация, а тем более тотальный некроз i о то иного мозга
несовместимы с жизнью.
Сердечно-легочный синдром часто возникает после реапимлнин
даже при отсутствии тяжелых поражений мозга Он прояизяси и
недостаточностью функции сердца и легких. Поражения eep'iiiu в
постреанимационном периоде связаны с белковой и жировой
дистрофией миокарда, гибелью групп кардиомиоциюв >ш р.п
стройства возникают вследствие гипоксии миокарда и ею пере
трузки из-за нарушения кровообращения в малом круге I цинк
сия ткани легких в пострсанимапионном периоде обуслов ит! i 1
нарушения микроциркуляции, развитие тромбозов, а гслек и юн
На этом фоне вследствие длительного применения искусе гвеннои
вентиляции легких в них нередко развиваются бронхопневмония,
абсцессы и др. Закупорка мелких бронхов слизью и клеточным
детритом, повреждение ал ьвео.т я рно-капиллярных мембран,
бронхопневмония приводят к недостаточности газообмен нои
функции легких.
Печеночно-почечный синдром возникает в постреанимацион-
ный период вместе с аноксической энцефалопатией и сердечно-
легочным синдромом, усугубляя их течение. Недостаточность
функции печени и почек развивается в результате расстройств
кровообращения. Наблюдаются застой крови в системе воротной
вены, диффузная белковая и жировая дистрофия гепатоцитов,
очаги некроза в печени наряду с резким нарушением микроцир-
куляции. В почках возникают ишемия и очаги некроза. Особенно
тяжелые расстройства функции почек наблюдаются при распаде
большой массы скелетных мышц, который появляется при уми-
рании и оживлении организма вследствие нарушения микроцир-
куляции и связанного с этим некроза мышц спины, плечевого
пояса, ягодиц и бедер. Расплавление мышечных клеток (миолиз)
приводит к появлению в плазме крови белка мышц — миоглоби-
на и выделению его почками. В результате этого возникает заку-
порка канальцев этим белком, некротизированным эпителием ка-
нальцев и нарушается выделительная функция почек (миоглоби-
нурийный нефроз). Недостаточность печени и почек способству-
ет накоплению в крови токсичных продуктов обмена веществ, из-
менению КЩР и ионного равновесия, белкового состава крови,
что усугубляет течение энцефалопатии и сердечно-легочной не-
достаточности.
Желудочно-кишечный синдром в постреанимационном периоде
встречается реже, чем другие расстройства. Вследствие наруше-
ния общего кровообращения, застоя крови в портальной системе
и расстройств микроциркуляции в желудке и двенадцатиперстной
кишке могут возникать кровоточащие эрозии и язвы. Возможно
377
прободение язвы желудка или кишечника с развитием гнойного
перитонита. В последние годы в постреанимационном периоде в
тонкой кишке все чаще обнаруживаются обширные некрозы с ге-
моррагическим пропитыванием, в основе которых лежит тромбоз
венул, распространяющийся на крупные сосуды, вплоть до ворот-
ной вены.
В последние годы число осложнений реанимации и постреа-
нимационного периода значительно снизилось. Это стало воз-
можным в результате распространения опыта реаниматологов,
проведения интенсивной терапии специалистами высокой квали-
фикации, совершенствования реанимационных мероприятий.
ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ
Абсцесс 108
— натечник 108
— холодный 108
Агранулоцитоз 191
Адаптация 116
Адгезия 82
Аденома 164
Аденогипофиз, гиперфункция 299
— гипофункция 301
Акромегалия 300
Алкалоз 56
Аллергены 139
Аллергическая реакция 141
----стадия иммунная 142
----патохимическая 142
----патофизиологическая 143
Аллергические антитела 141
Аллергия 138
— виды 141
----анафилаксия 143
----атопия 144
----аутоаллергия
----бактериальная 139
----контактная 140
Альтерация 97
Анаплазия 154
Анасарка 46
Ангина 251
Аневризма 222
Аномалия лица, расщелины 379
— заячья губа 379
— волчья пасть 379
— сквозная губы и неба 379
Артериолосклероз 207
Анизоцитоз 185
Анкилоз 232
Антракоз 370
Апноэ 240
Апоптоз 47
Аппендицит 265
Аритмии 200
Аррозия
Артрит ревматоидный 232
Аспирация 251
Асфиксия 43
Асцит 46
Атеросклероз 202
— аорты 205
— артерий мозга 205
— сосудов нижних конечностей 206
— стадии 204
Атипизм 154
Атрофия 122
Аутоинтоксикация кишечника 255
394
Ацидоз 56
Барьер аэрогематический 239
— диффузия газов, нарушение 239
Беременность внематочная 358
— прерывание самопроизвольное 359
Болезнь(и) базедова 306
— бронхоэктатическая 246
— вирусные 324
— гипертоническая 206
---криз 208
---стадии 207
---формы 208
— гипофиза 299
— желез(ы) поджелудочной 308
---щитовидной 304
---эндокринных 299
— зубов 380
— инфекционные 322
---вызываемые бактериями 330
---детские 345
---классификация 321
— кишечные 263
— легких хронические
неспецифические 244
— лучевая 371
— мочекаменная 295
— организма оживленного 376
— органов полости рта 388
— период инкубационный 324
---продромальный 324
---разгара 324
---реконвалисценции 324
— пищевода 252
— при беременности 357
— профессиональные 368
— пузыря желчного 281
— ревматические 225
— сердца 218
— системы дыхания 238, 238
---зубочелюстной 379
Водянка 46
Гемолитическая болезнь новорож-
денных 188
Гепатит(ы) 273
— алкогольный 276
— вирусный 274
Гематурия 164
Гематома 93
Гемоглобинозы 189
Гемобластоз 191
Гемосидерин 34
Гемолиз 34
Гемосидероз 34
Гепатозы 272
Гепатомегалия 194
Гиалиноз 28
Гидролазы 20
Гингивит 388
Гиперволемия 184
Гипергидратация 45
Гиперкапния 59
Гиперемия артериальная 73
— венозная 74
Гиперкалиемия 39
Гиперкальииемия 40
Гиперкинезы 312
Гипернатриемия 38
Гиперплазия 123
Гиперпноэ 240
Гиперстенурия 285
Гипертермия 64
Гипертрофия 123
— викарная 125
— истинная 124
— компенсаторная рабочая 124
— нейрогуморальная 125
— регенерационная 124
Гиповолемия 184
Гипогидратаиия 45
Гипокалиемия 40
Гипокальциемия 43
Гипоксия 57
— нарушения 60, 62
— реакции компенсаторно-
приспособительные 62
— типы 58
Гипоксемия 58
Гипонатриемия 39
Гипостенурия 285
Гипотермия 69
Гломерулонефрит 286
Глоссит 389
— функции, расстройства, изжога
-------отрыжка
-------рак
-------рвота
-------тошнота
Диапедез 94
Дилатация 98
Дисгидрия 45
Детрит 49
Демаркация 49
Дисплазия 160
Желчь, выделение, нарушения
Здоровье, определение 173
Зубы, опухоли доброкачественные
390
-------злокачественные 390
Изостенурия 285
Инкапсуляция 50
Инсульт 205
Интерстиций
Инфаркт миокарда 212
Инфекция аденовирусная 326
— матки родовая 361
— менингококковая 348
Инфильтрат 105
Ишемическая болезнь сердца 211
Ишемия 77
Камнеобразование 43
Канцерогены 160
Капилляры легочные, перфузия,
нарушение 240
Кардит 96
Кариес 380
Катар 109
Кахексия 32
Киста 50
Кишечник, болезни 263
— рак 269
— функции 262
— нарушения 262
Кишка двенадцатиперстная, болезнь
язвенная 256
Колит 264
Коллапс 362
Кома 366
— диабетическая 366
— печеночная 366
— причины 366
— уремическая 366
Компенсация 117
Кондилома 111
Кроветворение, морфология 182
Кровообращение, нарушения
Кровопотеря 183
---энергетического
— объема циркулирующей крови
—работы сердца
— состояния кислотно-основного
-------алкалоз
-------ацидоз
— терморегуляции
Малигнизация 192
Мацерация
Медиаторы 98
Метастазирование 158
Микросфероцитоз 189
Микседема 307
Миамалиция
Морфогенез 173
Наследственность 150
Натечник 108
Недостаточность печеночная 270
- почечная 285
- сердечная 200
395
Некроз 48
— исходы 50
— признаки 49
— причины 48
— формы 50
Неороз некротический 291
Нефросклсроз 291
Нозология 173
Облитерация 223
Одышка 239
Окружающая среда, действие
факторов биологических 147
--------—физических 147
---------химических 147
-----и организм, взаимодействие 146
Онкогены 162
Опухоли 153
— возникновение, теория вирусно-
генетическая
-------полиэтиологическая
-------физико-химическая
— доброкачественные 157
— злокачественные 157
— классификация 163
— костей первичные 171
-------доброкачественные 171
------------остеома 171
------------хондрома 171
-------злокачественные 171
---------остеосаркома 171
---------хондросаркома 171
— челюстных 391
— мезенхимальные 168
-----доброкачественные 168
-------гемангиома 169
-------липома 169
-------миома 170
— эзофагит 252
— функции, расстройства
Плазморрагия 90
Пневмокониозы 368
Пневмония крупозная 241
Повреждение(я) 14
Пойкилоцитоз 185
Полиартрит ревматический 231
Полиомиелит 327
Полип 111
Полиурия 284
Полицитемия 87
Пороки сердца 219
Почка(и), болезни 283
— искусственная 92
— функция, нарушения 284
Приспособление 116
Пролежни 50
Пролиферация 98
Протоонкогены 161
Процессы иммунопатологические
132
Пузырь желчный, болезни 281
Пульпа, дистрофия 382
— атрофия 383
— некроз 383
Пульпит 383
Рана гнойная 108
Реактивность 148
Реакции компенсаторные
и приспособительные 117
---при гипоксии 62
Реанимация, методы 375
Ревматизм 226
Ревмокардит 229
Регенерация 118
Регургитация 252
Резистентность 150
Резорбция 95
Ремиссия 187
Репарация 104
Рецидив 177
Риккстсиозы 329
Ринит 327
Саливация 250
Свищ 108
Склероз 28
Спайка 219
Спленомегалия 194
Талассемия 185
Тампонада 213
Терморегуляция, нарушения 64
Тиф брюшной 330
— сыпной эпидемический 329
Толерантность иммунная 137
Тонзилит
Тромбоз 81
Тромбоэмболия 83
Туберкулез 336
Удар солнечный 66
Уремия 285
Урикемия 37
Урикурия 37
Уробилин 34
Фагоцитоз 136
Флегмона 108
Хемоаттракция 100
Холера 334
Хорея 231
Хромата 206
— перемежающаяся 206
Цианоз 75
Челюстно-лицевая область 379
— болезни 379
— лица 379
396
— зубов 380
Чувствительность болевая, виды 312
---расстройства нейрогенные 312
Шок 363
— анафилактический 365
— гемотрансфузионный
— ожоговый 364
— травматический 364
Эзофагит 252
Эклампсия 357
Экзоцитоз 103
Эксикоз 45
Экссудат 97
Экссудация 97
Элиминация 132
Эмболия 84
— воздушная 84
— газовая 84
— жировая 86
— клеточная 86
— микробная 86
Эмпиема 108
Эмфизема легких 246
Эндокардит 218
Энтерит 263
Энцефалит 328
Энцефалопатия анокхическая 376
Эритропения 185
Эритропоэз 186
Эрозия 254
Эпилепсия 329
Язык, рак 393