Author: Арзамасцев А.П. Раменская Г.В. Роднонова Г.М. Кузменова Н.И. Петухов А.Е.
Tags: здравоохранение медицинские науки медицина фармакология токсикология
ISBN: 978-5-9704-1144-5
Year: 2010
Г.В. Раменская,
Г.М. Родионова,
Н.И. Кузнецова,
А.Е. ПетуховТСХ-СКРИНИНГТОКСИКОЛОГИЧЕСКИ
ЗНАЧИМЫХ СОЕДИНЕНИЙ,
ИЗОЛИРУЕМЫХ
ЭКСТРАКЦИЕЙ И СОРБЦИЕЙУЧЕБНОЕ ПОСОБИЕПод редакцией
академика РАМН,
профессора
А.П. АрзамасцеваИЗДАТЕЛЬСКАЯ ГРУППА«ГЭОТАР-Медиа»
ББК 52.Я4я73-1. фармацевтической химии с курсом
Лвп)(н-кнй коллектив: сотрудники кафйОР Ф- Сеченои; Лрзамаснев Александр
дологической химии ММА имен ^ Раменская Галина Владиславою«,
П^вич. акал. РАМН Михайловна, канл. фирм. наук, лоц.;Й2Е»у«. «*: — “„ *—*" ~отделом химико-токсикологических и су-
Реиензенты: д-р ферм. на> . ^е’ ных Исследований Российского центра судеб-
дебно-химнческих научн ^надз0„ £д/ Соломатин; канд. фарм. наук.“да"™»ко-токснколоп,ч;ско,1 лабораторией Наркологическом кл„„„-
Жйшшы № 17 Департамента нравоохранения г. Москвы А.В. Смирное.Т80 ТСХ-скрининг токсикологически значимых соединений, изолируемых экс¬
тракцией и сорбцией . учеб. пособие для самостоят. подгот. студентов, обучаю¬
щихся по специальности «Фармация» — 060108 / Г. В. Раменская [и др.) ; под
ред. А. П. Арзамасцева. — М. : ГЭОТАР-Медиа, 2010. — 240 с. : ил.978-5-9704-1144-5Учебное пособие посвящено ТСХ-скринингу отдельных групп токсикологически
значимых веществ. В пособии представлены теоретические основы ТСХ и рассмо¬
трен ТСХ-скрининг наркотических анальгетиков, производных 1,4-бензодиазепина,
фенотиазина. барбитуровой кислоты, пиразола, ароматических кислот, кокаина, кан-
набиноидов, фенялакиламинов и галлюциногенов в рамках действующей программы
по курсу токсикологической химии [раздел 3 «Химико-токсикологический анализ
(судебно-химическии) на группу веществ, изолируемых экстракцией и сорбцией. Ле¬
карственные средства»] 2003 г. В пособии содержится нормативная документация
о наркотических средствах и психотропных веществах, перечисленных в официаль¬
ном Перечне средств и веществ, утвержденном Правительством Российской Федера¬
ции. а также Запрещенный список ВАДА.Пособие предназначено для студентов медицинских и фармацевтических вузов
В п^То * ТГе аСПИраНТ0В и "Р-одавателей. Вовд! обсу^аемые
сулебно-мйицинской экслеотизы ЭКСПертов сУдебн°-химических отделений бюро
ми токсикологической химии И Лруп,х спеииалис'тов, занимающихся проблема-УДК (54:615)(075.8)
ББК 52.84я73-1группа 'ГЭОТАР-Медиак Воспроизведение
’ ’Ш ООО Издательская группТ.ГЭОГАР^Т * 6Ы'ПЬ устеленыпис'***"ого разрешения ООО “ “* ЦМОг° иШния *ИхЬтелюиы группа .ГЭОТАР-Медиа.? ЙЯ"*“ авк,Р°в. 2008ООО Иддательска!ООО Иадательссш
оформление. 2010
СОДЕРЖАНИЕСписок сокращений еВведение £Глава 1. Нормативная документация 91.1. Федеральный закон «О наркотических средствахн психотропных веществах» 131.2. Основные понятия, используемые в сфере борьбыс незаконным оборотом наркотических средств, психотропных
веществ и их прекурсоров 141.3. Перечень наркотических средств, психотропных веществ
и их прекурсоров, подлежащих контролюв Российской Федерации 18Глава 2. Основные направления метаболизма токсикологически
значимых веществ 22Глава 3. Скрининговые методы определения токсикологическизначимых веществ 34Глава 4. ТСХ-скрининг токсикантов 364.1. Области применения 364.2. Объекты тонкослойного хроматографического скрининга 364.3. Преданалитическая подготовка объектов 374.4. Характеристика биологических объектов и методы
изолирования 39Глава 5. Теоретические основы тонкослойной хроматографии 515.1. Сорбенты 525.2. Системы растворителей 535.3. Нанесение образца и хроматографирование 555.4. Идентификация веществ методом тонкослойной
хроматографии 605.5. Детектирование 615.6. Направленный и ненаправленный ТСХ-скрининг 665.7. Количественное определение 715.8. Воспроизводимость результатов исследования 775.9. Представление результатов экспертизы 77Глава 6. Применение ТСХ-скрининга на примере использованиясистемы Тох1-ЬаЬ
V 'сдельных “^«ких %Uulw^^"^^^ки'-п'рои^миыомолфина;:;;;;;^ „^иГ^^^ю^ПЫ^МСЛШи »и era «Р^“‘Гсреде™ ГРУ""“ феитаиила 7.1.2.2. Наркоти'чаи > ^ фу„„ы фенциклидина 7 1.2.3. Наркотичики * _ производные других7.13. Наркотические анальгетики рс химических структур 7.1.3.!. Метадон 7 I 3 2 7.2. Производные 1.4-бенюдиазепина 227.3. Производные феиотиазина... 327.4. Производные барбитуровой кислоты 377.5. Кокаин ^7.6. Каннабиноиды 7.7. Фенил ал киламины 1607.7.1. Эфедрин и его производные 1617.7.2. Мескалин и его структурные аналоги 1647.7.3. Амфетамин и его структурные аналоги 1697.7.4. Метилендиоксипроизводные амфетамина 1757.7.5. Химико-токсикологический анализ фенилалкиламинов ... 1797.8. Галлюциногены 1827.8.1. ЛСД 1827.8.2. Триптамин и его структурные аналоги 188Глава 8. Контрольные вопросы, тестовые задания и ситуационные
задачи 194Контрольные вопросы 104Тестовые задания ’’ ’ ’ ,о^Ситуационные задачи 204ЛитератураПриложения 215
СПИСОК СОКРАЩЕНИЙ!! YiV*AI,A> " Нссми{нюс •"пиопиигмюе «тмтство
выс<>1а,,ффе*»и*мая «идкосткм хромэтшрцфия
В М < X высоко«ффсктинная тонкослойная хроматограф««I АХ f а к>'жидкостная иромлпмрафкя
I X I а «оная хромапиряфияI \ М< I а юная хромапирафмм/масс-спсктромсфияАЖ ) - жн.1 ко - жидкостная жстракпия
И К - инфракрасный (например, спектр)ИФА - иммунофсрментныи анализ
И ХА - иммунохроматографический шали!J1C ~ лекарственное средствоМККН - Международный комитет по контролю наркотиков
МИН - международное непатентованное название
НС — наркотическое средство
Г1В - психотропное веществоОМОСО - отделение медицинского освидетельствования на состояниеопьяненияПеречень - Перечень наркотических средств, психотропных веществ и их
прекурсоров, подлежащих контролю в РФ
Г1ККН - Постоянный комитет по контролю наркотиков РФ
Г1ФИА - поляризационный флюоресцентный иммуноанализ
САР — стимуляторы амфетаминового ряда
СХА — судебно-химический анализ
СХЭ - судебно-химическая экспертиза
ТСХ - тонкослойная хромапмрафия,ТФЭ - твердофазная экстракцияУФ - ультрафиолетовый (например, спектр)ФСКН РФ - Федеральная служба по контролю за оборотом наркотиков РФФЭК - фотоэлектроколориметрияХТА - химико-токсикологический анализХТЛ - химико-токсикологическая лабораторияЦНС — центральная нервная системаDEA — Управление по борьбе с распространением наркотиков, США
(Drug Enforcement Administration)DP - дискриминирующая силаRf (Rf) — отношение фронтов (ratio of fronts)T, _ - период полувьшеденияUNDCP - Проект Организации Объединенных наций по контролю нар¬
котиков (United Nations Drug Control Project)Vd — объем распределения
Введениеотмечается увеличение числа отравле-
За последние в0 всех странах мира. Ставится дажен„й химическими вешестам« слоЖИвшейся в современном че-вопрос О -ксическои ейСЯ, с одной стороны, в накопле-„овеческом обществе количества веществ, способныхНИИ В окружающей среде причиной отравлений, в отдельныхпри определенных услови ' ^ И( с другой стороны, в росте не-случаях заканчивающее тх средСтв (НС), психотропныхЭЭКОННОГО ^карственных средств (ЛС),веществ (ПВ) и друг Законом «О наркотических сред-В соответствии с федермьнь^^ (Собрание 3аконодательства рфтН,"Га 219) утвержден Перечень НС, ПВ и нх прекурсоров,
™даши* контролю в РФ (Постановление Правительства РФ от30.06.1998 г. № 681).В последнее время наркомания распространяется в нашей стране
большими темпами. Количество лиц, употребляющих НС, согласно дан¬
ным Минздравсоцразвития РФ за последние два года, составляет 5 млн
человек, подавляющее большинство которых — молодые люди в возрас¬
те до 30 лет.Отличительной чертой современного оборота наркотиков в Рос¬
сии является расширение их ассортимента, поскольку импортируются
многочисленные ЛС, обладающие одурманивающим действием в до¬
зах, превышающих терапевтические. Кроме того, увеличивается доля
незаконно производимых наркотических препаратов с высоким со¬
держанием действующего начала. Усиливается нелегальный оборот
наркотиков.Злоупотребления НС и ПВ наблюдаются также среди спортсме-
С Э™п ®семиРное антидопинговое агентство (ВАДА)
разоешенныуЛИ,СУеТ рещенный Список субстанций и методов, не
внесоревнователкнИСГЮЛЬЗОВаНИЯ КЗК В соРевновательный, так и во£Г„ЛяГИ ПеРИ0ДЫ ,см' Приложение 2).чие медицинского освилр*' 6орь6ы * наркоманией является проведе-новления факта употоеГптТЫ",СТВОВаНИЯ подозРеваемых с целью уста-
Улотребления наркотика с помощью лабораторного
Введение7исследовании биологических проб. Результат такого исследования во
многом зависит от сроков, прошедших со времени последнего приемачеловеком НС.Клини веская диагностика острых отравлений, проявляющихся, как
правило, в течение первых 24 ч, требует наличия экспрессных, про-
С1ЫХ по технике выполнения и достоверных методов исследования.Аналитическая служба, осуществляющая химико-токсиколо-
гический анализ (ХТА) наркотических и других одурманивающих ве¬
ществ — один из важнейших инструментов государства в борьбе с
наркоманией.Клинико-токсикологические исследования осуществляются на базе
лабораторий Республиканского центра по лечению острых отравлений
(НИИ им. Н.В. Склифосовского), а также региональных информаци¬
онных центров и центров по лечению острых отравлений.Судебно-химическая экспертиза (СХЭ) биоматериала на нали¬
чие индивидуальных Л С и их комбинаций, НС и ПВ, вызывающих
около 6 % зафиксированных смертельных отравлений, представляет
значительную трудность, что обусловлено их многочисленностью и
разнообразием химического строения ЛС, НС и ПВ (алкалоиды и их
синтетические аналоги; производные 1,4-бензодиазепина, барбитуро¬
вой кислоты, фенотиазина, фенилалкиламина, экгонина; тетрагидро-
каннабинол и продукты его метаболизма).Увеличение номенклатуры лекарственных препаратов, комбиниро¬
вание интоксикации, процессы метаболизма их в организме и трупе,
ограниченное количество объектов, поступающих на исследование,
определяют необходимость внедрения в СХЭ и ХТА высокочувстви¬
тельных и специфичных методов анализа.Достоверные результаты медико-криминалистических исследова¬
ний вещественных доказательств с места преступления на наличие
токсикантов являются важной составляющей уголовного расследова¬
ния.В области спорта, согласно Списку, проводят допинг-контроль на
запрещенные субстанции: анаболические агенты, гормоны и связанные
с ними субстанции, р,-адреномиметики, агенты с антиэстроген ной
активностью, диуретики и другие маскирующие вещества, на запре¬
щенные вещества: стимуляторы, наркотики, каннабиноиды, глюко¬
кортикостероиды; на вещества, запрещенные в отдельных видах спорта.алкоголь и р-блокаторы.ВАДА постоянно совершенствует методы обнаружения субстанций,
их метаболитов и маркеров в биожидкостях, взятых у спортсменов.
■-'“«дение
Глава 1НОРМАТИВНАЯ ДОКУМЕНТАЦИЯДля контроля за легальным использованием и борьбы с неза¬
конным оборотом наркотиков в Российской Федерации преду¬
смотрена система административно-правовых и законодательных
актов. В зависимости от степени воздействия конкретного веще¬
ства на организм человека и масштабов влияния, оказываемого
на общество его незаконным оборотом, меры контроля за ним
могут предусматривать полное запрещение на территории России
его производства, оборота и применения у людей или введение
ограничений на его оборот. Принятие решения о соответствую¬
щем контроле и уровень такого контроля предусматривает рас¬
смотрение трех аспектов: медицинского, социального и юридического,
которые тесно взаимосвязаны между собой, и в правовом аспекте
обязывают признавать средство наркотическим только при нали¬
чии всех трех критериев.Медицинский аспект проблемы незаконного оборота наркоти¬
ков состоит в том, что рассматриваемое средство или вещество
должно оказывать на организм человека специфическое воздей¬
ствие одного из трех типов: стимулирующее, седативное либо гал¬
люциногенное, обусловливающее их немедицинское потребление, и
развитие у людей зависимости от этого вещества.Согласно существующим в настоящее время официальным диаг¬
ностическим системам, например диагностической системе вы¬
явления психических заболеваний и расстройств Американской
психиатрической ассоциации (American Psychiatrical Association,
АРА), злоупотребление химическим веществом определяется как
«неправильное употребление химического вещества, ведущее к
ухудшению состояния или заболеванию, требующему клиническо¬
го лечения, о чем свидетельствует один или более признаков из
приведенных ниже.
Глава 1дяшеества— химического вещества, приво-огме употребление и социальные обязатель-\Ти^""»*ЯОСТ" ,ЫГ“Гж'чашнее хозяйство.
шее к неви ть или вести д еского вещества в ситуа-“ Сод^схое У"^""„апример при вождении автомо-пгия это опасно ДЛЯ *ИЗ и 0ПЬянения.виля или работе на сганхе ° связа„„ые с употребле-з Периодические "Р»^““ть| 33 противоправные действия, со¬
пле« вешества. например арго вешества.„ершенные под влиянием химического вещества, не-4. Продолжительное '1' ые соянальные или межличност-
смотря на "да"Я""“„“ыеили обостряемые приемом ЭТОГО веще-ства». „,—гпй системе, зависимостью от химиче-По той же диагност ное употребление химическо-
скош «шеетаа считается «неправ^ьн У яния ^ за6от
схКоГлГн1, о чем свидетельствуют три
™ Шеею нижеперечисленных признаков, зафиксированных вдвенадцатимесячный период.I. Толерантность, определяемая любым способом из приведен¬
ных ниже:а) потребность в значительном увеличении количества прини¬
маемого вешества для достижения интоксикации или желае¬
мого эффекта;б) ослабление действия одинакового количества вещества при
продолжительном приеме.2. Абстиненция проявляющаяся любым способом из приведен¬
ных ниже.а) характерный абстинентный синдром, связанный с употребле¬
нием данного вещества;б) прием данного (или близкородственного) вещества для об-
летония или предупреждения абстинентных симптомов.еетаах или в“",,астый и “ й»"ь„,их коли-исано врачом *** ",МШ)'1|*и7е',ьшно периода, чем пред-??»"Р:стг:чгтгисн::гаые ,юпытки "(ккрагн,ь нли—^--р™ггггигг^г;мпир^г
Нормативная документация11нис больших расстояний), на использование химического веще¬
ства (например, непрерывное курение) или на восстановление ор¬
ганизма после употребления химического вещества.6. Полное или частичное прекращение занятий, связанных с об¬
щественной или профессиональной деятельностью, а также дея¬
тельностью, направленной на отдых.7. Продолжительное употребление вещества, несмотря на осо¬
знаваемые постоянные или регулярные физиологические или
психические проблемы, вызываемые или обостряемые таким упо¬
треблением (например, постоянный прием кокаина во время де¬
прессии, несмотря на осознание того, что депрессия вызвана кока¬
ином; или продолжительная алкоголизация организма, несмотря
на осознание того, что из-за нее открылась язва).Уже приведенные выше симптомы наркомании дают четкое
представление о таких понятиях, как синдром психической зависи¬
мости (психический комфорт при интоксикации) и синдром фи¬
зической зависимости (потеря контроля над дозой, абстинентный
синдром, физический комфорт при интоксикации).Под психической зависимостью понимается состояние, при ко¬
тором ЛС вызывает чувство удовлетворения, психического подъ¬
ема и которое требует периодически возобновляемого или посто¬
янного введения ЛС для того, чтобы испытать удовольствие или
избежать дискомфорта.Физической зависимостью обозначается состояние, которое про¬
является интенсивными физическими расстройствами (вплоть до
смертельного исхода), когда прекращается введение соответствую¬
щего ЛС. Это синдром абстиненции, или лишения. При абстинен¬
ции резко выражены вегетативные нарушения: сердцебиение, пот¬
ливость, тахикардия. В костях и мышцах появляются мучительно
болезненные, мозжащие, тянущие боли («ломка»). Больным овла¬
девает сильное беспокойство, сопровождающееся криками, стона¬
ми. Появляются судороги (парестезия) конечностей. Отмечаются
потеря аппетита, тошнота, рвота, понос, боли в животе, упорная
бессонница. Обман, подкуп, ложь, воровство — все пускается в
ход с целью раздобыть наркотик или что-либо его заменяющее.Таким образом, наркотическое опьянение представляет собой
состояние, возникающее после приема НС, включающее опре
деленные психические и соматические симптомы. Психическая
реакция на наркотическое опьянение выражается в шфориии. >й
Глава 112_ — ' . проявлений, психических и.«ртся ИЗ эмоииональн _ наркотиков (стимулято-вескихоиушений Диогены, обусловливает свойпу седативные ереРШ Эйфории. „„.„мании состоит в том. что немедицин-Социальный аспект наркома тва пр„обретает социальноское применение средствазначимые масштабы. оборота НС на территории РоссииНа увеличение незакон" йствие ряд факторов: геополитическое
и стран СНГвыпалнение регионом функции комму-
положение. определяют Азиатско-Т ихоокеанским регио-никаш1оиного моста мемуАзие^^А организации таможенного
„ом и Западной Европой, сложност Р ^ qSSÄSSÄU- и связанное с ним сни-Же™ли™»йНчер“овГемснното оборота НС в России яв¬
ляется расширение их ассортимента за счет появления многочис-
ленных легальных медицинских препаратов и интенсификации
контрабандных поставок. При этом увеличивается доля незаконно
производимых наркотических препаратов с высоким содержанием
действующего начала.Особое место в сфере незаконного оборота НС занимают тран¬
зитные перевозки их через территорию России в страны Европы.
Статистика правоохранительных органов свидетельствует о резком
увеличении активности международных наркокартелей в данной
области.Юридический аспект наркомании выражается в требовании при¬
знания (на основе вышеуказанных предпосылок) соответствующей
инстанцией (Министерство здравоохранения и социального раз-!™,ГЙСК0Й ®едерации и ДР) определенного средства нар¬
котическим и включения его в Список НС.действи™вямнн1!!,МЯ HJ ,ер|,итории Российской Федерации все™K0»^Z"4“™,He3aKOHHb'Mo6opoTOM Ha»K°-tob. К их числу nTHrv ar V рядом законодательных докумен-
и Гражданский кодексы Рос^0Л0ВНЬ|^ Уголовно-процессуальный
коны Российской ФедераиииИ пСК°Й Федерации' Федеральные за-
сийской Федерации, а гакжр п 0становлсния Правительства Рос-
<*ктвуюишх ведомств (МВЛ м HopviafMBHb,x документов соот-
<МВД, Министерства здравоохранения и
Нормативная документация13социального развития, Министерства экономического развитияи торговли. Таможенного комитета и др.).1.1. ФЕДЕРАЛЬНЫЙ ЗАКОН
«О НАРКОТИЧЕСКИХ СРЕДСТВАХ
И ПСИХОТРОПНЫХ ВЕЩЕСТВАХ»Федеральный закон «О наркотических средствах и психотроп¬
ных веществах» № 73-Ф3 вступил в действие 14 апреля 1998 г.С его принятием российское законодательство о наркотиках
стало соответствовать основным принципам трех международных
конвенций, принятых Организацией Объединенных наций (ООН):
Единой Конвенции о наркотических средствах (1961 г.), Конвен¬
ции о психотропных веществах (1971 г.) и Конвенции ООН о
борьбе против незаконного оборота наркотических средств и пси¬
хотропных веществ (1988 г.).Федеральный закон состоит из 8 глав, включающих 61 статью.Глава I. Общие положения (ст. 1 - ст. 5).Глава И. Организационные основы деятельности в сфере обо¬
рота наркотических средств, психотропных веществ и в области
противодействия их незаконному обороту (ст. 6 - ст. 8).Глава III. Особенности лицензионной деятельности, связан¬
ной с оборотом наркотических средств и психотропных веществ
(ст. 9 — ст. 13).Глава IV. Условия осуществления отдельных видов деятельно¬
сти, связанных с оборотом наркотических средств, психотропных
веществ и их прекурсоров (ст. 14 — ст. 30).Глава V. Использование наркотических средств и психотроп¬
ных веществ (ст. 31 — ст. 39).Глава VI. Противодействие незаконному обороту наркотических
средств, психотропных веществ и их прекурсоров (ст. 40 — ст. 53).Глава VII. Наркологическая помощь больным наркоманией
(ст. 54 — ст. 57).Глава VIII. Заключительные положения (ст. 58 — ст. 61).
1.2. ОСНОВНЫЕ ПОНЯ ворьБыИСПОЛЬЗУЕМЫ оворотомС НЕЗАКОННЫнаркотических сгадПСИХОТРОПНЫХВЕШЕСи ИХ ПРЕКУРСОРОВ« ^ **есгк не.иконный оборот которых
В РФ чо даононге^пн Эгоескялс-с* * >2- -я-л*«. а такжелес*и>ек* * . АЖ- л также *х -^»лречры;^ ' _ 1ГО ^щества синтегаческого »им
дв^ня« "р^р*™. р«-: " ч ,.• < .Гкжч«» шгкоп.чл-к,.у срехп. пси-
X » иажжжшн* контролю вФыкиаи* * ооогктешш с тлюмгетьспюи РФ.
у,И_--,чг.шч1Уч»у«< ЛЧ«СЛ1УМ РФ. ? ТО* ЧИСЛС Елино»1 Конвенциио :>**с-яг*ааи срсжгакх 1%1 т. НС — это фармакологически
ж-!-я у— у естествен ного кли синтетического пронс-и*х5еч:.> шго^е ,:гг гсоорсг>'5ноч действии способно изменять
эваехлие ■ 8осцригп*е (хим. а при повторном применении —
зш&;х;-ь гкюичгекхто *нди физическлу* зависимость и развитие
кафмшшяЕПашутушик кякто (ПВ> — это велесгва синтетического
ла* есггстк - -ого гтрожпозцеьЧч. препарат*«. природные матери¬
алы иикченньк *-.Перечень наркотических средств, психотроп-
<аа кжетз « их щ^глреоров. подлежащих контролю в РФ* в со-
^техта* > зш>*\тезьгт»м РФ. международными договорами
Звгс* Ьонкшшей о психотропных веществах 1971 Г.в чеч состоят различия меаах НС и ПВ.КШЛГП! К игегоР“и психотропных
ПкКН , - в ^и""ом 00 ««прано ндркотаковКдЖЮщхм о 310 9ещл'ш мз Списков Н и 111ешье* : Г"™* 1971 г- В соответствии соеттощщо. цятетщ*** м ^^лествах 1971 г. соогвет-* " «В.ИЮТСЯ С1ел>кчцне
|*г?ш 11?!Iнормативная документ;' ^ ,к<ооностъ вещества формировать зависимость от него и
окалывать стимллирующ« или депрессивное воздействие на ЦНС
человека. вы ыпл.я галлюцинацию или нарушение моторной функ¬
ции пнх> мышления. л»«ад повеления, либо восприятия, либо ка-
строения; или обусловливать такие же злоупотребления и врезные
последствия, ка». н какое-либо вещество, включенное в Списки
ПВ конвенции 1971 г.* Достаточные свидетельства тою. что имеет место иди сулцс-
С'^>СТ »гроягность зиоупотребления данным веществом, которое
представляет иди может представлять угрюзу хтя здоровья насе-
еннч и создавать социальные проблемы. что лает основания ддя
осу-цествлення мсжду народного контроля за таким веществом.Прекурсоры — это вещества, часто ислозьзуемые при производ¬
стве. изготовлении, переработке НС и ПВ. вжлюченные в «Перечень
наркотических средств, психотропных веществ и их прекурсоров,
подлежащих контролю в РФ» в соответствии с законодательством
РФ. международными договорами РФ. в том числе Конвенцией
ООН о борьбе с незаконным оборотом НС и ПВ 19$^ г.Сильноленствуюшие вещества — вещества синтетического или
природного происхождения, в том числе растения, включенные в
Слисок сильнодействующих веществ, утвержденный ПккНЯдовитые вещества — вещества растительного, животного и ми¬
нерального происхождения иди продукты химического синтеза,
вкаченные в Список ядовитых веществ, утвержденный ПккН.
н способные при воздействии на живой организм вызвать остро:
пт хроническое отравление или смерть.В отличие от »Перечня наркотических средств н психотропных
веществ и их прекурсоров* Списки сильнодействующих и ядо¬
витых веществ формируются и издаются ПккН ежегодно Они
сформированы на основе части Списка 1\ конвенции о ПВ И71 г.
и Таблиц I и 2 конвенции ООН о борьбе с незаконным оборотом
НС и ПВ г. В эго списки включены также вещества, в отно¬
шении которых имеются данные о фактах здоу потребления ими.Одурманивающие вещества — средств, лающие одурманивав¬
ший эффект, в частности изменяющие психику м поведение, и не
входящие в Списки НС и ПВ.к таким веществам ПккН относит: смесь клофедина и алкоголя
в любом процентном соотношении. смесь димедрола с алкоголем,
барбнтх ра го-ад когольную смесь, хлороформ, эфир, год\ч\л. хлор.*-
Глава 1— с алкоголем, закись азота, ксе-доксиламинасукпинитвсмес содсржаших алкалоиды тро-™ спиртовые экстракты риетеи , ^ отнесены экстракты из
„аиовой ФУЛПЫ. К ™™"И”1тит „щшт. Атра МЫоппа, Нуо5-
расений Вашга^гтотт^ ^ фстатт, содержащие
сутшщег. &оро1,с а!горо,т^ ^ производным тропана -В основном алкалоиды, отнис н сап0НИны и стероидныеатропин, скоползмин, з такж^очетаниях.гликоалкалоиды в различи а в 0б0рот или хранить их -Пускать одурманивающие веуголовно ненаказуемое асянЖ' статья 23, где упоминается дан-
й УК РФ имеется только одна статьи и, /
ная категория вешеств: «Лицо, совершившее преступление в со-
“Гьянения, вызванном употреблением алкоголя, нарко¬
тических средств или других одурманивающих веществ, подлежитуголовной ответственности».Однако смеси алкоголя с клофелином, барбитуратами и диме¬
дролом применяются не для достижения состояния опьянения, а,
как правило, с криминальной целью, для приведения человека в
беспомощное состояние и совершения в отношении него какого-
либо корыстно-насильственного преступления (грабеж, изнасило¬
вание и др.).Аналоги наркотических средств и психотропных веществ — это
запрещенные для оборота вещества синтетического или естествен¬
ного происхождения, не включенные в Перечень НС и ПВ и их
прекурсоров; химическая структура и свойства аналогов сходны
с химической структурой и свойствами НС и ПВ, психоактивное
действие которых они воспроизводят.л„“ГнТ изготош|ение> приобретение, хранение, перевозка
ша4 „Гка^аГГР0ПНЫХ- сильнодейетвующих и ядовитых ве-
с I января 1997 г со°тветствии с УК РФ, вступившим в силуста НС, Других факторов, влияют количе-находя' "~«::йг£гк===:
17ниях. В Сводную таблицу включены также большие объемы сильно¬
действующих веществ, что соответствует требованиям УК РФ.Ниже приводится, каковы небольшие, крупные и особо круп¬
ные размеры количеств НС, психотропных и сильнодействующих
веществ с точки зрения закона.Небольшой размер количеств НС или ПВ — это количество НС
или ПВ, выраженное в общепринятых единицах объема, массы,
нахождение которого в незаконном хранении или обороте пред¬
ставляет опасность для здоровья одного человека в случае немеди¬
цинского употребления.Крупный размер количеств наркотических средств или психотроп¬
ных веществ — это количество НС или ПВ, выраженное в обще¬
принятых единицах объема, массы, нахождение которого в неза¬
конном хранении или обороте представляет опасность для здоровья
нескольких лиц в случае немедицинского употребления.Особо крупный размер наркотических средств или психотропных
веществ — это количество НС или ПВ, выраженное в общеприня¬
тых единицах объема, массы, нахождение которого в незаконном
хранении или обороте представляет особую опасность для здоровья
нескольких лиц в случае немедицинского употребления.Крупный размер количеств сильнодействующих веществ — это
количество таковых, выраженное в общепринятых единицах изме¬
рения объема, массы, нахождение которого в незаконном обороте
представляет повышенную опасность для здоровья человека.Крупный размер количеств запрещенных к возделыванию рас¬
тений, содержащих наркотические вещества, — это выраженное в
общепринятых единицах массы количество запрещенных к воз¬
делыванию растений, содержащих наркотические вещества, не¬
законное культивирование которых представляет повышенную
общественную опасность.
Глава 1НАРКОТИЧЕСКИХ СРЕДСТВ,18^Гз ПЕРЕЧЕНЬ ВЕЩЕСТВ"Курсоров, подлежащих
и ИХ ПРЕз росСИЙСКОЙ ФЕДЕРАЦИИКОНТРОЛЮ психотропных веществ и их«Перечень наркотических сред ^ россИЙСКОЙ федерации» (да-поекурсоров, подлежащих контр верЖден Постановлением^Перечень. с*., приложение 0. рт ^ от зо июш |998 года
Правительства Россиис прекурсоров.И включает 4 Списка ми ф заПреШен в соответствииСписок НС и договорами РФ (Список I).с законодательством р<ри* £ „ пв не использующиеся в ме-
Список I составляют 153 НС и 8 по,ДИТперечень^НС включены: гашиш, героин, каннабис, кокаино¬
вый ^Глиа кока, маковая солома, мескалин, метадон, морфин
Г^мил. опий, плоловое тело любого вида грибов^ содержа¬
щих псилоцибин и (или) псюкшин, экгонин, эфедрон, МДА и др.К ПВ Списка I относят: дексамфетамин, катин, катинон, ле-
вамфетамин, меклоквалон, метаквалон, 4-метиламинорекс и ме¬
ти.лфенидат.Необходимо отметить, что в Список 1 включены (или могут
быть включены): изомеры НС и ПВ в тех случаях, когда существо¬
вание таких изомеров возможно в рамках данного химического
обозначения; эфиры сложные и простые НС и ПВ, перечисленных
в данном Списке; соли всех НС и ПВ, перечисленных в данном
Списке, если существование таких солей возможно; все смеси, с
содержанием НС и ПВ данного Списка, независимо от количества
последних.Список НС и ПВ, оборот которых в РФ ограничен и в отношении
которых >станавливаются меры контроля в соответствии с законода¬
тельством РФ и международными договорами РФ (Список II)но пГ^ГаШМЮГ45 НС и 9 ПВ. используемых в медицине,
лл» чс,ок^ “аН"ОМ "рименении представляющих опасностьЧИН и комбиии^мпт^'п 4 Л0Г0 <-писка Относятся: амфета-«шис; бупренорфии, глкп^„л^оксиХГРаТЫ' СГ° °°ДеР',н°ксирон); кодеин, кокаина
Нормативная документациягидрохлорид, морфина гидрохлорид, морфина сульфат, омнопон,
просидол, пиритрамид (дипидолор), сомбревин, фентанил, этил-
морфина гидрохлорид и др.В Список 11 включены лекарственные формы, содержащие нар¬
котические средства: свечи тилидина с разными дозировками и
следующие таблетки, содержащие кодеин или его соли.1. Таблетки алнагона (кодеина фосфата 20 мг, кофеина 80 мг,
фенобарбитала 20 мг, кислоты ацетилсалициловой 20 мг).2. Габлетки, включающие кодеина камфосульфоната 0,025 г,
сульфагваякола калия 0,100 г, густого экстракта гринделии
0,017 г.3. Таблетки кодеина 0,03 г + парацетамола 0,500 г.4. Таблетки кодеина фосфата 0,015 г + сахара 0,25 г.5. Таблетки кодеина 0,01 г, или 0,015 г + сахара 0,25 г.6. Таблетки кодеина 0,015 г + натрия гидрокарбоната 0,25 г.7. Таблетки кодтерпина (кодеина 0,015 г + натрия гидрокарбо¬
ната 0,25 г + терпингидрата 0,25 г).8. Таблетки от кашля (трава термопсиса в порошке 0,01 г (0,02 г),
кодеина 0,02 г (0,01 г), натрия гидрокарбоната 0,2 г, корня
солодки в порошке 0,2 г).В перечень ПВ Списка II включены: амобарбитал (барбамил),
амфепрамон, кетамин, кетамина гидрохлорид (калипсол, кеталар),
фенметразин, фентермин, этаминал натрия, хальцион (триазолам)
и таблетки следующего состава: барбамил — 0,15 г + бромизовал —0,15 г.Кроме того, в Список II могут быть включены соли всех НС и
ПВ, перечисленных в данном Списке, если существование таких
солей возможно.Список ПВ, оборот которых в РФ ограничен и в отношении ко¬
торых допускается исключение некоторых мер контроля в соответ¬
ствии с законодательством РФ и международными договорами РФ
(Список III).В Список III входят ПВ, применяемые в медицинских целях,
но представляющие определенную опасность при их бесконтроль¬
ном применении. Список III включает 17 веществ: аминорекс,
апрофен, бензфетамин, галотан, декстрометорфан, левамфетамин,
лефетамин, мазиндол, мефенорекс, натрия оксибутират и другие
соли оксимасляной кислоты, пентобарбитал, пипрадрол, гарен,
фендиметразин, фенпропорекс, ципепрол, этил амфетамин. Кроме
Глава 1III worvr входить соли веществ, перечисленных в
ГОГО- 8 Списке "ели ошествование такихсолей возможно,
данном оборот которых в РФ ограничен и в отноше-Список ^^Я^нмкш:я меры контроля в соответствии с зако-
РФ и «жд-каролными договорами РФ (Список IV).?ШГ£ви.очает 26 вешеств неорганической и органиче¬
ской природы, используемых для изготовления НС и П В. В табл. I
представлен перечень прекурсоров, а также наименования НС и
ПВ для изготоатения которых они используются.Данный Перечень периодически пересматривается и корректи¬
руется соответствующими органами и структурами путем исклю¬
чения и добаатения НС, ПВ и их прекурсоров.Таким образом, всего в Перечень и все приведенные выше спи¬
ски входит около 300 индивиду'альных химических соединений, а
также все возможные их соли, простые и сложные эфиры, при¬
родные и искусственные смеси, содержащие эти вещества, более
10 видов высших растений и грибов, их части, а также продукты
их кустарной и промышленной переработки.Разнообразие видов и форм контролируемых веществ, а также
действия производителей зелья, направленные на маскировку и
сокрытие своей продукции, обусловливают специфические аспек¬
ты криминалистического обеспечения этих противозаконных ви
дов деятельности.Н?7пв' СПИСОК ПреКурсоров- используемых для изготовленияНиммкжаюе прекурсораНС и ПВ, для изготовления которых
используется прекурсорI Аипирнд уксусной кислотыМетаквалон, героин’ Актраикловая кислота4-метиламинорекс, метаквалон^-аигтшгграикловая кислотаМетаквалон! ЛистонРастворитель при изготовлении многих НС
и ПВ ^первитина. ЛСД, кокаина, героина и
ТА.)i И «сафрщМДА илфгимиом кислое’N игг*' «феерии “ |ПсрвнгинЛСДстелимом
Нормативная документацияОкончание табл. 13.4-метилендиоксифенил-2-пропанонМДА, МДМАМетилэтилкетон (2-бутанон)эастворитель при изготовлении многих НС (
и ПВНорпсевдоэфедринНоркатинонПерманганат калияМеткатинонПиперональПроизводные амфетаминаПиперидинФенциклидин и те ной и клинПсевдоэфедрин'ПервитинСафролМДЕАСерная кислота (за исключением
ее солей)Реактив при изготовлении многих НС и ПВ 1Соляная кислота (за исключением
ее солей)Реактив при изготовлении многих НС и ПВ |ТолуолРастворитель при изготовлении многих НС
и ПВФенил уксусная кислотаМДА и его производныеФенилпропаноламин*Кати нон. меткатинон1 -фенил-2-пропанонАмфетаминЭргометрин (эргоновин)*ЛСДЭрготамин'ЛСДЭтиловый эфирРастворитель при изготоатении многих НС
и ПВЭфедрин"Меткатинон' Данное вещество включено в список вместе с соответствующими салями, еслиобразование таких солей возможно.
Глава 2ПГНОВНЫЕ НАПРАВЛЕНИЯогьемлемой частью выведения ток-
Метаболизм является Ионизированные и полярныесических вешеств "3 °^к правило, в неизмененной форме, а
вЫтоПли „ной степени подвергаются гидрофобные(То«иГвсшесш органической природы, попадая в орга¬
низм претерпевают самые разнообразные превращения. Чаще все-го образуются гидрофильные метаболиты наряду с метаболитами,
которые практически не отличаются от нативных веществ по сво¬
им кислотно-основным и гидрофильно-гидрофобным свойствам.
Некоторые ядовитые и сильнодействующие вещества, особенно
интенсивно подвергающиеся метаболизму, не всегда обнаружи¬
ваются при ХТА. Вследствие этого выделение, идентификация и
количественное определение метаболитов токсических веществ с
известными параметрами порой становятся доказательствами от¬
равления нативными веществами.Биотрансформация протекает чаще всего в две фазы.В первой фазе биотрансформации (метаболическая трансфор¬
мация) происходит химическая перестройка структуры токсиче-
СЫН веществ путем биохимических процессов окисления, восста-
вТ„Т;ГТИЗа С 06разованИ(:м функциональных групп.ямоаей™^сХНихФвешеЦИИ ' (конъюгация> ~ «за-
«ой трансформации с ™ ИЛИ продУктов их метаболиче-
соединениями с образованиСТВеНН° солержащимися в организмепрс^ествуГ^ГГоГй ГЪЮГ0В 0бЬ,ЧНО коньюгациинекоторые токсические вещества *1Л Ж0ТрансФ°РмаЦии- Однако
НОИ« кислоты и др., мо, ера ,/1*.™™- аР°«а™ческие карбо-У ступать во вторую фазу био-
Основные направления метаболизма.23трансформации и, наоборот, реакциям первой фазы (например,
гидролизу) подвергаются конъюгаты.Большинство токсических веществ метаболизируется в печени,
в органеллах гепатоцитов: гиалоплазме, микросомах, митохондри¬
ях, содержащих ряд ферментных систем. Эти системы обладают
большой мощностью и невысокой субстратной специфичностью;
под их действием метаболизируются самые разнообразные ток¬
сические вещества, независимо от их химической структуры и
свойств. В метаболизме токсических веществ определенную роль
играют также ферменты кишечника, легких, почек, плаценты,
крови и некоторых других тканей.Различают микросомальные и немикросомальные ферментные
системы, катализирующие различные биохимические реакции.
Реакции окисления катализируют оксидазы (альдегидоксидазы,
аминооксидазы, М- и Б-оксидазы), гидроксилазы, дегидрогеназы
(алкоголь-, альдегид-, сукцинатдегидрогеназы), деалкилазы и др.
Процессы восстановления катализируются редуктазами: альдегид-,
нитро-, азоредуктазами и др. Гидролизуются токсические веще¬
ства под действием эстераз, амилаз, сульфатаз, глюкуронидаз и др.
Конъюгация токсических веществ происходит главным обра¬
зом при участии трансфераз: глюкуронил-, сульфо-, глутатион-,
Ы-ацетил-, метилтрансферазы и некоторых других ферментов, на¬
пример глицинацилазы. Некоторые ядовитые и сильнодействую¬
щие вещества (например, фенобарбитал, дифенин, карбамазепин,
изониазид, бензпирен и др.) способны индуцировать (активиро¬
вать) метаболизирующие системы, в частности цитохром Р-450-
содержащие ферменты. В результате увеличивается скорость
метаболизма и выведения других ядовитых и сильнодействующих
веществ, уменьшается токсичность как самого индуктора, так и
прочих токсических соединений. Иные вещества (например, сте¬
роиды), наоборот, могут ингибировать ферменты.Изучение теоретических и практических вопросов метаболизма
ядовитых и сильнодействующих веществ при ХТА позволяет сфор¬
мулировать некоторые положения:• Определить токсические вещества возможно по их метабо¬
литам и продуктам гидролиза. Например, основными ме¬
таболитами, позволяющими идентифицировать алкалоид
аконитин, являются бензоилаконин и аконин; амидопирин
4-аминоантипирин и 4-ацетиламиноантипирин; изониашд
Глава 2янетилизониаэкд, изоникотиновая и
„ салюзид - ™РазичН^ГИТОТьность и специфичность об-
опиановая кислоты. Чувств 0дных фенотиаэина по„аружения некоторых " _ фенотиазину с помощьюпродукту ихщелочного ги^зфИОЛетоВой (УФ) спектрофо-
реакции окрашивания и > ю с таковыми обнаружениями
тометрии выше• метаболитом героина яиляет-ГГоа:Гморфин(б-МЛМ, . — ^фЗГифенциклидином уст.нанди-
вают по анализу мочи на наличие метаболита 5 N (1-фе-Г«огексин)-аминовалериановой кислоты; трамадолом -по его метаболитам О- и ^дезметилированным соединени¬
ям Одним из вариантов ХТА при отравлении производны¬
ми 1,4-бензодиазепина является обнаружение и определение
продуктов их кислотного гидролиза — бензофенонов.. Метаболиты некоторых токсических веществ более устойчивы
и в объектах исследования сохраняются реакционноспособ¬
ными дольше, чем нативные соединения. Например, в био¬
логическом материале, содержащем диазепам, через год после
захоронения были обнаружены его метаболиты — бензофено-
ны. Алкилдифенольные соединения практически сразу мета-
болизируют, и в трупном материале обнаруживаются только
их метаболиты.• Токсичность метаболитов неодинакова. В результате метабо¬
лизма образуются, как правило, менее токсичные соединения,
однако такие биотрансформации, как бензонал -> фенобар-
битал, метафос -» метаксон, кодеин -> норкодеин, ртуть ->и нек«торые другие, приводят к появлению мета-
болитов более токсичных, чем нативные вещества:™"°“е.НИ1ИЮТНОШения концентраций нативных веществРЯДе СЛуЧаеВ Дает возм°жность определить
Хроническое отраш1енияРТИ ^ ДИ^еренциР°вать острое иС глюкуроновой кислотой 05 ~ конъюгирование
куроннда И морфин-6-глюкУгх>ииРа30паНИеМ М0РФин-3-глю-
10 морфина и связанного » Соо™ошение свободно-морфии-б-глюкуронида) в крови с,Густа'^-3 'люкУронида иус/я I з ч после приема
Основные направления метаболизма... 25препарата изменяется от 1:20 до 1:28, при этом морфин-
3-глюкуронида образуется примерно в 7 раз больше, чем
морфи н-6-гл юкуронида.В табл. 2 представлены некоторые общие пути метаболизма ток¬
сикологически значимых веществ органической природы и приве¬
дены примеры ядовитых и сильнодействующих веществ, наиболее
часто встречающихся в химико-токсикологической практике.Таблица 2. Основные пути метаболизма токсических веществОсновнойбиохимическийпроцессБиотрансформацияПримерыгоксических веществ1-я фаза биотрансформации1. Окисление
1.1. С-окислениеобразованиеспиртов[О]я - СН3 ► Я - сн2он10]к, -сн2- ►К1-СН-Я2он\мфетамии, барби-
гураты, имипрамин,
кетамин, ЛСД, ме¬
пробамат, метилен-
диоксиамфетамин,
фентанил, флура-
зепамю^хгЛСД, ТГК, трамал,
фенциклидинонГексенал<К- <К-1,4-бензодиазепины
Глава 226Продаїжение табл. 2Основно*(І|Ю\ІГЧІГ?ЄСКИМ^фооессОбрАЗОВІНИСД^'Ч4ЛП<ЧЄСКН\іидрокс и произ¬
водныхБиогрзи*сфорМ!ШИЯПримеры
токсических веществгде \ — бензол, бензольный цикл, фе-
нилышй радикал. ароматический гете¬
роцикл и др.образованиеальаепиовг~г
оосшованнеКАТОНОВ^>н окисли¬
тельной іеза-
^ИЗШро&ІНИНАмнтриптилин. ам¬
фетамин. атропин,
имиттрамин, кокаин,
лндоканн. ЛСД,
метадон, метамфе-
тамин. мефенитоин.
салициловая кисло¬
та. стрихнин, фена¬
цетин. фенобарби¬
тал. фенотиазины.
хинин, хлорпротик-
сен. эфедринМезапамЭфедр ннХлорпроти ксен^.-СН-мня-с=о Амфетамин, метиI ^МИ|- Я.-те нджжеиамфета -! мин
Основные направления метаболизма.27Продолжение табл. 2
Глава 228 — -— Продолжение табл. 2ОсновнойбиохимическийПроцессБиотрансформацияПримерытоксических веществ"—н ОV /О 1 //1 // N— Q
/N| 2 чгн [G| ^ 2 он/ з -nДемоксепам— ZJТФенциклидинн1 [О]R—СН — N—СН (-NH ) -■-» R-CTОНМоно- и бисдезме-
тильные производ¬
ные димедрола1.2. С-окисление уходящей частицы1.2.1 ДеалкилированиеС-деал копиро¬
ваниеN-деалкилиро¬
вание-С-А.к^-(:н—нБарбитал/ОD _г^ [О] .ОГЧнГ^ R-<OHМетадонj°uАминазин, ими-
прамин, лидокаин,
ЛСД, просилол,
нонахлазин, трамал.
фонтанил. флура*
зонам
направления метаболизма... Осн£!^^^— ' ,"" Продолжение табл. *^ОСНОВНОЙбиохимическимБиотрансформацияПримерытоксических веществМ.деметилиро-ваниесн, н1 [О] 1 [01
Я—и—сн,—►Я N сн,—►Я >Ш2Амидопирин, амина¬
зин, амитриптилин,
атропин, бензоилэк-
гонин, верапамил,
гексенал, диазепам,
димедрол, ими-
прамин, кетамин,
кодеин, кокаэти-
лен, кофеин, ЛСД,
мезапам, метадон,
метадол, метамфе-
тамин, метилен-
диоксиамфетамин,
морфин, оксикодон,
теофиллин, тиори-
дазин, трамал, фен-
танил, хлордиазепо-
ксид, эфедринО-деалкилиро-вание[О]Я-О-АІк —► я—ОНКодеин, оксикодон,
папаверин, проси-
дол, тебаин, трамал,
фенацетин1.3.1Ч-окислениеМ-гидрокси-лирование[О]Я—N112 —► Я—ЫНОНАмфетамин, фена¬
цетин[О]Я,->Ш —► я-ы-он
1 1 1
я, я2Этаминал-натрийобразование
N-оксидовг, ' [О]я,—N —*- я —N —»-Оі 1
я3 я,Амитриптилин,
диметилфенамин.
имипрамин, мета-
дон, фенотиазины
(ли метил алкильные
производные)_____)Ч [О] )Чн—оАнабазин, морфин,
трамал ,
зоГлава 2Продолжение табл. 2і З- І "лро.тІ про,аш 4ировМетаболиты, содер¬
жащие N-оксидные
Фуппы, хлордиазе-
покеид,-онДионин, кодеин, фе¬
нацетин
Основные направления метаболизма.31Основнойбиохимическийпроцесссложных эфировПродолжение табл. 21>ио трансформацииПримеры
токсических веществбензодиазепи-новамидовглюкуронидово - ион,-ОНАтропин, ацетилса¬
лициловая кислота,
ацетил морфин,
бенюилэкгонин,
героин, дикаин,
кокаин, новокаин,
пирстроидыЧ_У [Н,0| **ч
С—N Производные
1,4-бен зодиазепиновЫННовокаинамидОН|Н10] .0 Я-С^ +С1исОНОСЛис ОН|Н,0|Я—0-С1ис —► Я-ОН + С1исОН|Н,0|И-N4-01110—2—+ И - N14, + 01ис0Н|Н,0|И —Б-СПис—*—*■ Я-БН + С1исОНГлюкурониды токси-1
чсских веществ и их
метаболитоворганическихсульфатовИ-О-БО-Н Я-ОН + Н^ОКонъюгаты феноловорганическихфосфатовОН1Н О]я—-о—Р—о —г—► И-ОН + Н,РОПсилоцибин1Ч-ацилпроиз-водных|Н,0| //и.-ын-с-а,—2^ н,—мн.) к, счЛидокаинОоно =с— к ооБензонал
Глава 2Продолжение табл. 2в миСН.ШОН
К\Н — NN МН-СНк он К^„_оснБензойная кислота,
нитрофураны, са-
лиииловая кислота,
цианиды и др.Аминозепам, амино-
ангинирин, новока¬
ин, новокаинамидНорморфинМорфин, жюнин
Основные направления метаболизма... 33Окончание таб/1. 2ОсновнойбиохимическийпроцессБио трансформацияПримеры
токсических веществс сульфатом[5042 ]Я-ОН И—0—50,НМорфин, парацета¬
мол, салициламид,
фенолыОбозначения: СИ не ОН — глюкуроновая кислота; К — алифатический, алицикличе-
ский или ароматический радикалы; ТГК — теграгидроканнабинол.
Глава 3СКРИНИНГОВЫЕ МЕТОДЫ
ОПРЕДЕЛЕНИЯ ТОКСИКОЛОГИЧЕСКИ
ОП ад ЗНАЧИМЫХ ВЕЩЕСТВаналитическая практика располагает много-
В настояшее время анали токсикологически важных ве-,именными методами определенияшеств. мртолов для скрининга токсикантовВыбор аналитичеш ^ короткий промежуток времени
определяется целью анали максимума положительных^ГиГГ—Тдавными параметрами анализа,С^^Мот^."jSk-"п^еивание, отбор) - система
методических приемов, позволяюших выбрать научно обоснован¬
ную последовательность операций, в результате которых поэтапно
«отсеиваются» (определяются) группы соединений и отдельные
вещества. Скрининг используется при анализе многокомпонент¬
ных смесей, а также при ненаправленном анализе — анализе на
неизвестное вещество и группу веществ. Хроматографический
скрининг преследует цель отобрать, отсеять часть веществ, чтобы
сузить круг исследования и сократить время анализа.В зависимости от поставленной задачи исследования различают:• ненаправленный скрининг, т.е. определение химической
гр\ппы токсикантов, а затем установление конкретного ядо¬
витого вещества;• напраазенный скрининг, т.е. определение токсиканта из из-
вестного химического класса.поляризационный фчу^'уж*1*рментный анализ - ИФА,^^Фич^ПГиГ-ТмГ' " ПФИА' ИММУ‘
Скрининговые методы определения... 352. Оптические (спектроскопия в УФ-области).3. Хроматографические (тонкослойная хроматография — ТСХ).В настоящее время наиболее часто при химико-токсикологичес¬
ком анализе токсикологически важных веществ в процессе скри¬
нинговых исследований используются ИХА на тест-полосках,
ПФИА и ИФА. Современные иммунохимические методы отли¬
чаются высокой чувствительностью, простотой и экспрессностью
исполнения, одновременно позволяют анализировать большое
число проб, не требуя дополнительной или специальной очистки
пробы или концентрирования, а поэтому удобны для скрининг-
диагностики. При получении положительного результата, т.е. когда
концентрация вещества превышает пороговую, требуется провести
дальнейшее исследование образца мочи подтверждающими аль¬
тернативными методами. При отрицательном результате не нужно
проведения дальнейшего исследования на данное анализируемое
соединение или группу веществ.Из оптических методов, основанных на зависимости спек¬
тральных характеристик от природы растворителя, pH сре¬
ды и других факторов, для скрининга наиболее подходит
УФ-спектрофотометрия. Однако применение метода непосред¬
ственно к экстрактам, полученным из биологического материала,
весьма проблематично, в связи с чем большинство исследований
комбинируют УФ-спектрофотометрию с хроматографией.В течение последних лет хроматография стала одним из наи¬
более эффективных методов, определяющих методологию скри¬
нинга токсикологически важных веществ. Наиболее доступная для
химико-токсикологических лабораторий ТСХ — хроматография в
тонком слое сорбента. Она проста по технике проведения иссле¬
дований и привлекательна низкой стоимостью необходимых для
работы реактивов.Наряду с ТСХ для скрининга широко применяются методы
газовой хроматографии (ГХ) и высокоэффективной жидкостной
хроматографии (ВЭЖХ).
Г лава 4
«„.скрининг токсикантов„„..нге токсичных веществ следу».
Пг, тех ИР" "р.И"вь,сокая специфичность, быстро-шк »р.ши»чуктвиге1ьн«ть очис1ха от «экстрактивныхГанаГт просто« »“ '""^сдружмифизико-х чеекимивешсств, ВОЗМОЖНОСТЬ сметодами.4.1. ОБЛАСТИ ПРИМЕНЕНИЯТСХ-скринннг испа«)отпри лровед^ (эка]ресс диагностика
диагностические иссдедования в нарко-логии);2) судебно-химических исследовании,3) допингового контроля;4) медико-криминалистических исследовании.4.2. ОБЪЕКТЫ ТОНКОСЛОЙНОГО
ХРОМАТОГРАФИЧЕСКОГО СКРИНИНГАОбъектами ТСХ-скрининга являются:1) биологические жидкости (кровь, моча, слюна, желчь, спин¬
номозговая жидкость, промывные воды желудка);2) биологический материал (внутренние органы и ткани);3) вещественные доказательства: остатки порошка, таблеток,
ампул, капсул и других лекарственных форм; образцы рас-(шлштмГ°гтМатериала’ инь,е вещественные доказательства
(шприцы, пищевые продукты и пр.).
ТСХ-с»римимг токсикантов374.3. ПРЕДАИАЛИТИЧЕСКАЯ ПОДГОТОВКА
ОБЪЕКТОВРезультаты ТСХ-скринига каждой группы объектов во многом
мнисят от преланалитичсской техники обработки обрата. В згой
сия т. несмотря на специфику кажлого объекта, необходимо учесть
некоторые общие положения1. На нежащий огбор пробы Этот лап исследования может
быть существенно осложнен вследствие стремления испытуемых
лиц исказить или скрыть факты наличия контролируемых веществ
в исследуемом биологическом объекте. К числу возможных дей¬
ствий такого рода, например при анализе мочи, можно отнести
следующие: подмену образна «холостой* пробой мочи: разбавле¬
ние пробы мочи; подмену пробы мочи разбавленным чаем, пивом;
добавление в мочу средств бытовой химии.2. Условия отбора и хранения пробы. Условия отбора пробы ре¬
гламентирует Приказ М3 РФ № 161 от 24.04.03 г. В соответствии
с ним с целью обнаружения и количественного определения ядо¬
витых веществ изымают и направляют на судебно-химическое ис¬
следование различные внутренние органы, кровь и мочу с учетом
природы предполагаемого яда и путей введения его в организм,
распределения, путей и скорости выведения, длительности тече¬
ния интоксикации и лечебных мероприятий. Направляют также
рвотные массы, первые порции промывных вод, остатки лекар¬
ственных и химических веществ, пищи, напитков и другие объ¬
екты. Внутренние органы и биологические жидкости забирают в
количествах, достаточных для проведения судебно-химического
исследования, но с учетом того, что одна треть материала должна
остаться в архиве для возможных повторных анализов. Каждый
орган, кровь или мочу помещают в отдельные чистые и сухие сте¬
клянные банки. Использование металлической или керамической
посуды запрещается. Банки герметически закрывают, на них на¬
клеивают этикетки с необходимыми записями и помещают в опе¬
чатанный полиэтиленовый пакет или контейнер, который немед¬
ленно отсылают на исследование.Для успеха анализа огромное значение имеет правильное хра¬
нение пробы в промежутке времени между ее отбором и обра¬
боткой. Наиболее предпочтительны при этом условия глубокого
замораживания при температурах от —20 до —56 °С.
При подготовке органов „
„Я пробы К )КГ^~ . необходимо разрушить целост.
Пм,^‘ в п<Р»>'ю » <чет чего значи™ьно по-тканей К ан ^еточНых «.тр. •H0CTbT1Ci 2ьективность экстр N П0М0ШЬЮ ножниц до размераrSZZu''«н0 с песком-стсклом ил" «мя-„s^?nvK«Pacn,paH^^тмогенязагоров ИЛИ современных вь,.
Гс помошьк. ножевых го“ праксов. Возможна обработка“коскоростньи »Тви» - *‘„Р««уль>тм»ук0»'- опредедения лекарственных, нарко-
4 Метол экстр**11*1 1PVTHX веществ органической природы
„„еских. ®л1ШГО"Ы'2подГОтовки обычно используют жидко-
„етоаом тех Д1Я "l**» ЖЭ) твердофазную экстракцию
жидкостную экстрами v жжэ остается самым распростра-
(ТФЭ). На сс1тан™мения анализируемых веществ из биообъек-
ненным Приемом вьи • постепенно переходят на ТФЭ.го"5“™,“*Гзшген1.Ых и эндогенных вешеств. влияющих на ре-
Jn™ га-скрннянп. Химико-аналитическое исследование
6 ,отогаческвх объектов в значительной степени осложняется на¬
личием в пробе различных экзогенных и эндогенных соединений,
зачастую не имеющих отношения к соединениям, являющимся
целью химико-аналитического определения, а в других случаях -■ПЛМ'^ЛТОРиииН п U1JVHI<клс1.Iкппым I. пяти.Так, например, на распределение токсических продуктов в ор-
_лнзме человека ечияют такие факторы, как особенности метабо¬
лизма, активность ферментов, объем кровотока; возраст, пол и вес
обследуемого субъекта; наличие в организме экзогенных веществ
(кофеин, никотин, алкоголь. ЛС); характер пищи, употреблявшей¬
ся субъектом в течение ближайших часов перед отбором пробы.При анализе также важно, подвергся ли биоматериал путри-
фикации (гниению), так как от этого напрямую зависит методи¬
ка изолирования токсических веществ. В процессе путрификации
идет рапожение высокомолекулярных соединений под влиянием0КЙС!ГТ ЭНЗИМ0В (декаРб°ксилнрование, дезаминирование,
образованию Ле^килирование и ДР), что приводит, например, ксП**туреканмизируТмымТ'г аМ"Н°В' вЯИЗКИХ "° химической"“Я. пря исеяедовании „ос«мс%гТ° экспеРиментальнымдан-
материала, подвепгаит^г^ ,(“Х-скрининга биологического
^«.«шееЛГ Г ГНИЛ0СТН0МУ разложению в течение
Решающих скрииигу в эфирных и хлороформных
ТСХ-скрининг токсикантов39экстрактах, не обнаруживалось, но допускалось предположениео наличии таких биогенных аминов, как кадаверин, путресцин и
гриптамин в хлороформных экстрактах. При исследовании по схе¬
ме ГСХ-скрининга биологического материала, подвергавшегося
гнилостному разложению в течение 4 нсд, в эфирных и хлоро-
формных экстрактах обнаруживался целый ряд соэкстрактивных
веществ, мешающих проведению ТСХ-скрининга без предвари¬
тельной очистки органических экстрактов.Ниже приводятся характеристики основных объектов биоло¬
гического характера, которые используются для анализа методом
ТСХ-скрининга.4.4. ХАРАКТЕРИСТИКА БИОЛОГИЧЕСКИХ
ОБЪЕКТОВ И МЕТОДЫ ИЗОЛИРОВАНИЯМоча — наиболее распространенный и простой объект для
предварительного ТСХ-скрининга веществ, имеющих наибольшее
токсикологическое значение.Существенным преимуществом ее использования как биообъ¬
екта является то, что проба мочи для исследования обычно может
быть получена в достаточном количестве, а концентрация психо¬
активных веществ или их метаболитов в ней, как правило, доста¬
точно высокая.Важный показатель — значение pH мочи, которое может ме¬
няться. Повышение pH со временем происходит из-за действия
бактериальной флоры, выделяющей аммиак. Действие бактерий
замедляют добавлением таких бактериостатических средств, как
фторид натрия или борная кислота, однако надо учитывать их
дальнейшее участие в экстракции и образовании фона. Наилуч¬
ший способ стабилизации значения pH — хранение мочи в замо¬
роженном виде.Моча содержит незначительное количество белковых компо¬
нентов. что весьма облегчает выделение и дальнейший анализ кон¬
тролируемых веществ. С другой стороны, многие группы НС и ПВ
(опиаты, каннабиноиды), а также их метаболиты присутствуют в
моче в виде конъюгатов с глкжуроновой кислотой по гидроксиль¬
ным или аминным группам. Поэтому во многих случаях первич¬
ный этап при исследовании мочи — щелочной, кислотный или
ферментативный гидролиз конъюгатов.
41/- яизкомолекуляР-:н-ые- кислоты), небольшие коли-Т(^^о^тОВ’ ПИГМеНТ0В' °КРаШИВа,ОЩ^мочу” желтый ,м6ода „очи включает различные опера-Хлана™™ческая °Т^\,Я экстракции органическим раство.
шш: прямого коииенФ^ уения или сорбции на твердо«
р^ем, хроматограф«® значимые вешества экстрагируются изсорбенте. Токсикологимочи согласно схеме .ей может быть подвергнута цельная
Кровь. Обработке экс Рт^а ^ ана,пизе проб крови следует
кровь, плазма или сы £ руемЫх веществ в крови достаточ-
иметь в виду: уровен пр0Текания интенсивных биохи-ГвГГа^еГ количественное содержаниеГсиГских вешеств в артериальной и венозной крови, в крови
живых людей и трупов.Если для предотвращения свертывания крови использовались
антикоагулянты, например гепарин, то необходимо учитывать,Образец (5-20 мл)+ НС1дорН = 2-3,
экстракция эфиром,
центрифугирование|ирганическая Фаза!Фильтрование через безводный
N82804, упаривание досуха
Остаток 1 (вещества кислого
и нейтрального характера)родная Фаза)+ №Н4ОН до pH = 9-10,
экстракция хлороформом,
центрифугирование,, —Остаток 2 (вещества основного
и слабоосновного характера)Схема I. Изолирование веществ из мочи и слюны |оодная фаз:-ГанИе чеРез безводный2 4| Упаривание досуха
ТСХ-скрининг токсикантов41что гепарин вытесняет жирные кислоты из мест их связывания с
альбумином. Это влияет на увеличение связывания токсических
вешеств с белками, а также на переход жирных кислот в органиче¬
ский растворитель при экстракции.Для уменьшения энзиматической активности кровь рекоменду¬
ют хранить в холодильнике в замороженном виде. Хранение био¬
объектов в стеклянной таре способствует связыванию полярных
веществ стенками посуды (свободные гидроксильные группы) за
счет образования водородных связей. Это явление важно учиты¬
вать при анализе следовых количеств контролируемых вешеств.
Альтернатива — использование посуды из полипропилена или
тефлона, однако в таком случае необходимо считаться с загрязне¬
нием пробы мономерами смолы.Изолирование токсических веществ из крови живых лиц пред¬
ставлено на схеме 2.ЦентрифугированиеПлазма или сыворотка+ НСІ до pH = 2-3,
экстракция эфиром,
центрифугирование|Органическая фаза]| Водная фаза)Фильтрование через безводный
№2304, упаривание досуха+ 1ЧН4ОН до pH = 9-10,
экстракция хлороформом,
центрифугированиеОстаток 1 (вещества кислого
и нейтрального характера)[Органическая фаза] [Водная фаза|Фильтрование через безводный
Ыа2504, упаривание досухаОстаток 2 (вещества основного
и слабоосновного характера)Схема 2. Изолирование веществ из крови живых лиц, промывных вод,желчи
Имеет немаловажное значение, взята ли проба крови у
мм или V груш, так как со временем в крот трупа лРОИс^ог°
разрушение эритроцитов, в результате чего стали» иснтриф ^Ит
вания не дает положительных результатов. Методика изолир0и"Ро'
токсических веществ из трупной крови представлена на схем о ****
Слюна - продукт секреции желез ротовой полости. Слюн
лательно собирать из ротовой полости ватными тампонами ^
рые потом отжимают в пробирку. При отборе слюны другим К°Т°~
собами возможно обильное пенообразование. Этот биооб ^ Сг>0'
составу менее сложен, чем кровь или моча, причем изве ЪСКт по
шествует прямая зависимость между содержанием анали СТН°: СУ'
вещества в крови и его концентрацией в слюне. Все рек "^е^°Го
относительно консервации и хранения различных проГ°Х1еНДа^иИ
ные выше, касаются и проб слюны, которая, как и кп ' ИЗЛ°ЖеИ~
высокой ферментативной активностью. Токсически^’ °блаДает
изолируются из слюны согласно схеме I.*ие соелиненИя[образец!Г+НС1до pH = 2-3,I Центрифугирование
IЦентрифугат/ЭкстРакция эфиромЦентрифугирование
ТСХ-скрининг токсикантов 43Желчь в химико-аналитической практике встречается реже.Она является продуктом секреторной деятельности печени, желч¬
ного пузыря и двенадцатиперстной кишки. Эта жидкость содержит
большое количество воды, эндогенных веществ, подобных тем, ко¬
торые находят в крови, плазме и сыворотке, а также желчные кис¬
лоты и пигменты. Значения pH желчи могут находиться в интер¬
вале ог 6,7 до 8,3, следовательно, необходимо контролировать pH в
ходе пробоподготовки. Желчь содержит довольно большое количе¬
ство холестерина, поэтому для его удаления пробу рекомендуется
центрифугировать при низких скоростях (1000—1500 об/мин).При экстракции из желчи желчные кислоты образуют стойкую
эмульсию, и для разделения фаз необходим длительный период
центрифугирования. Поскольку большинство токсических веществ
выделяется из желчи в виде конъюгата с глюкуроновой кислотой,
желчь перед процедурой изолирования подвергают гидролизу.Экстракты из желчи часто окрашены, однако предварительное
осаждение белков спиртовыми растворами несколько осветляет
пробы.Вследствие липофильного характера большинства эндогенных
веществ желчи, экстракты обусловливают значительный фон, осо¬
бенно при использовании неполярных растворителей. Желчь экс¬
трагируется согласно схеме 2.Печень представляет собой центральный орган химического
гомеостаза. Вследствие многообразия функций, выполняемых в
организме печенью, в экстрактах из тканей этого органа, как пра¬
вило, присутствует большое количество экзогенных и эндогенных
веществ, включая продукты белкового (самый разнообразный бе¬
лок и продукты его метаболизма вплоть до аммиака и мочевины),
жирового (метаболиты стероидов, полупродукты синтеза нейтраль¬
ных, фосфо- и гликолипидов, холестерина) и углеводного (про¬
межуточные продукты синтеза гликогена, реакций цикла Кребса,
окислительного фосфорилирования) обмена.Разрушение гемоглобина приводит к образованию открытых
тетрапирролов — желчных пигментов. Образовавшиеся в резуль¬
тате ферментативного расщепления билирубины (билирубин и
биливердин) выводятся с желчью в виде глюкуронидов. Бактерии
кишечника восстанавливают билирубин до бесцветных структур,
которые на воздухе окисляются, становясь желто-коричневыми,
придавая окраску фекалиям и моче (стеркобилин и уробилин).
Глава 4та отличается высоким содер-44 этот вид биоо6?* ‘ ипидов, СТерИНОв И лр. Изтин» прежде всего «рсIV метаболизма белковых
ниемлилид® тканях МО3™ "Пекулярные пептиды, некото-присугствуюши^ ^ет11ТЪ низком^йствами Из стеринов в зна_кШеСТ’„иТобл»“а10ТО"Иам“ется холестерин (0,25 0,3% в сухомр“с",Гколичеетве содержится в нервной ткани,чкге"'«Г Болыие *ег0 * В мелом в мозговой ткани содержание“ГГо’вГом^стве В - тве 0 9 д0 |-4%1 а в белом
особенно в ОВД ^ в сером вешеыо»,ГГ"от 4,0 ДО 5,3%. необходимо учитывать, что хо-“ При экстрами из дан в органических веществ (хло-
леетерол хорошо раствор» то ацетон) „ водереформ, диэтиловь1изФ'Р'на6ухает образуя стоикую эмульсию,
„„ нерастворим, НО .Л ать огромное количество воды, пре-вследствие чего може, удр Поэтому становится очевидной не-
вышаюшееегомассу в о экстракцией) удаления ли-Гв:"Г;ТбЬ;т0пРеждс всего разрущення комплекса
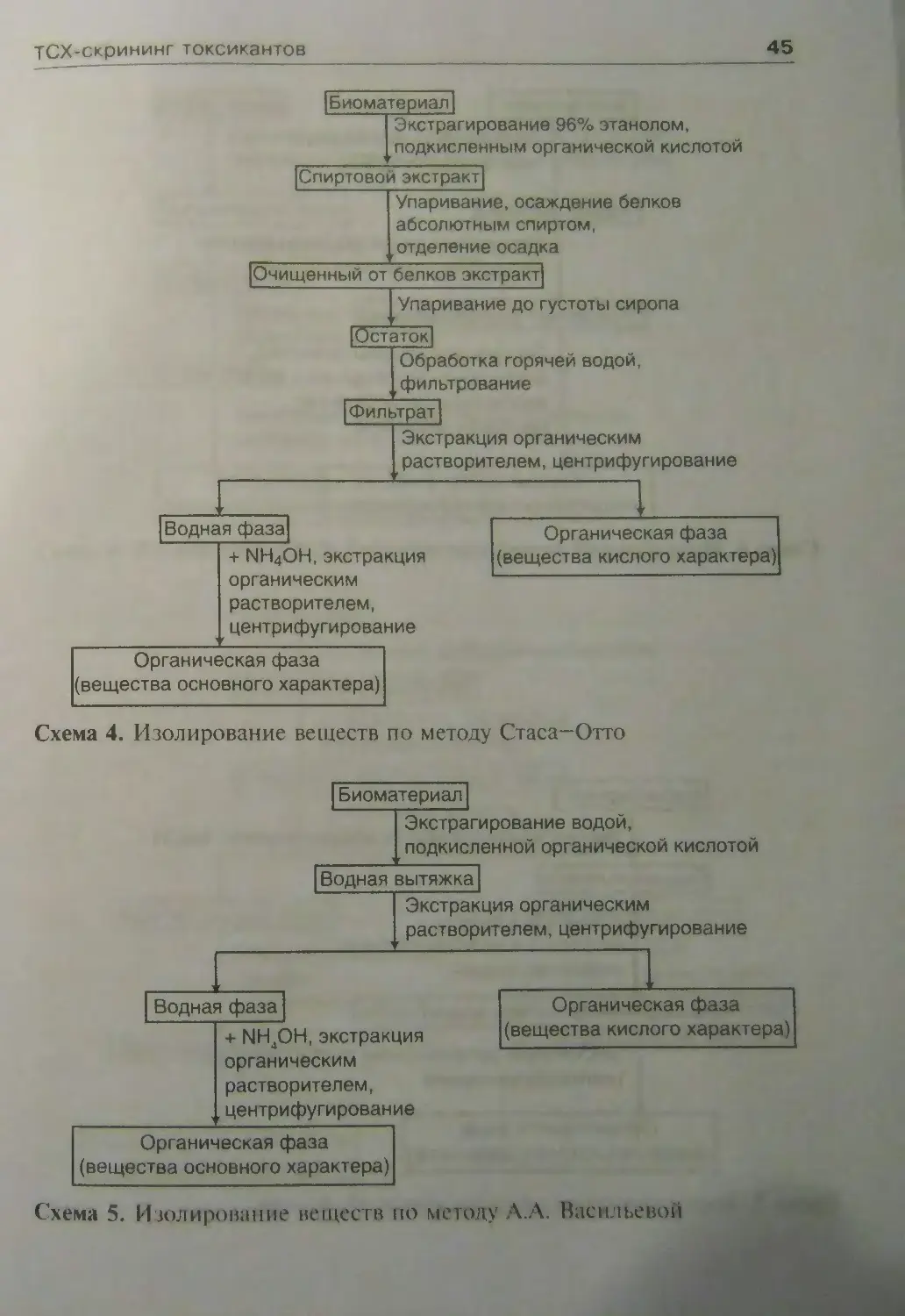
ТГоргаГГЗдаХГвешества изолируются мето-лами Стаса-Огго (схема 4), А.А. Васильевой (схема 5), В.Ф. Кра¬
маренко (схема 6), П. Валова (схема 7), Грусц-Харди (схема 8)
и с помощью ацетона (схема 9).Волосы, легко доступные для отбора, являются консервативной
средой, способной в течение длительного времени сохранять вво¬
димые в организм органические и неорганические токсикологиче¬
ски значимые вещества, в том числе и наркотики.Установлено, что в волосах наркоманов в течение длительного
времени сохраняются и могут быть обнаружены многочисленные
наркотические вещества и соединения, вызывающие гоксикома-
г и ,',екарственнУю зависимость (опиаты, каннабиноиды, кока-
ны;^ГаИН,ФеНЦИЮ1ИДИНИДР )- вешества, зафиксирован-
отдаяенные спп^аСТУШИХ Н3 голове и на теле> выявляются даже в
соединения сохраняй"11 °Кончания их пРиема. При этом данные
*«« ЙСеГм “ ' В0Л0Сах' не подвергаются метабо-
Обычно скорость роста
1 см В месяи. Оценивая п.т г °1(>С На голове составляет примерноі ределение токсичных веществ по длине
ТСХ-скрининг токсикантов45| Биоматериал!Экстрагирование 96% этанолом,
подкисленным органической кислотой|Спиртовой экстракт]Упаривание, осаждение белков
абсолютным спиртом,
г отделение осадка
|Очищенный от белков экстракт}Упаривание до густоты сиропа
|Остаток|Обработка горячей водой,
фильтрование
| Фильтрат!Экстракция органическим
растворителем, центрифугирование| Водная фаза|+ ЫН4ОН, экстракция
органическим
растворителем,
центрифугированиеОрганическая фаза
(вещества кислого характера)Органическая фаза
(вещества основного характера)Схема 4. Изолирование веществ по методу Стаса—ОттоСхема 5. Изолирование веществ по методу А.А. Васильевой
46Гкиоматериал]=7Драгирование водой,/ подкисленной н2ьи4[Водная вытяжка]Насыщение раствора электролитом
(Ш4)2504, отделение осадкаЭкстракция эфиром (очистка),добавление N801-1 до pH = 8,5-9экстракция хлороформом,центрифугированиеОрганическая фаза(вещества основного характера)Схема 6. Изолирование веществ по методу В.Ф. КрамаренкоІБноматерияп! ЭкстРагирование1§одная іводой, подщелаченной N804[Очищен,ОрГ;**М>4 + Н&0Лог*^еео^Дянойб^е,«ИГ^^а:ГКИМ Зрителем^сгващР<*ньан*ческаяЦелогоФаза5аРакпера)Вс,ХіЄсті■Тв ПоП. Вг•ІІІОЦЦ
ТСХ-скрининг токсикантов47| Биоматериал 1Растирание с кристаллическим (МН^ЭОд и НС1,
экстрагирование смесью спирта и хлороформаОрганическая фазаУпаривание[Сухой остаток]Обработка горячей водой,
фильтрование[Фильтрат!Экстракция органическим растворителем,
центрифугированиеОрганическая фаза
(вещества кислого характера)Схема 8. Изолирование веществ по методу Грусц—ХардиI Биоматериал 1Экстракция нейтральным ацетоном| Ацетоновое извлечение |0,5М НС1 (1:1), экстракция
н-гексаном (очистка)| Очищенная ацетоно-водная фаза|Экстракция эфиром,
центрифугирование| Ацетоно-водная фаза |+ 1\1Н4ОН, экстракция
эфиром,центрифугирование
| Эфирное извлечение)тех,элюированиеИсследование на вещества
основного характераI Эфирное извлечение!тех,элюированиеИсследование на вещества
кислого характераСхема 9. Изолирование веществ с помощью ацетона
проследить характер посту-
' 'Тяе 6'8 см' “тугих токсических веществ на
„ри их ^ V шшкотиков и „Понятно, что по прошествии„ро«*ении6 *“ времени анализ вде нарко™коо.столь ллительн»г зультато» на построены Из белкового ком-дагь„оло*нтель осы.восновио ТЬ поступаюшие в орга_Ногти, как И собны зад Р ненИя. Однако сохраня-гг^я-г-г?“ • —ются они В в® вещества содержатся в во-^Гтоксиколотиче^^ниентрациях (10- г); исполь-“ , ногтях в »‘"“^„Проведении ТСХ-скрининга нецеле-
пияние таких объектов при Р в аналитиЧескои практикесообразно. При МСТ0ДЫ’ ГХ’ ГХ'МС’применяют такие высокому«ВЭЖХ. Уемых средств из вещественных доказа-Изолирование контрол ру ^ анализИруемого образца (расти-
тельств напрямую завис амгтуЛьные растворы и др.).ге Солержаш^наркотических средств в исследуемых образцах „0-
*ет «аткя в очень широких пределах - от 100% в чистых
Гпаштах ло лолей процента в сильно разбавденных образцах
наркотиков кустарного приготовления иди в препаратах, являю-
шихся предметом «уличной» торговли. Кроме того, при анализе
таких образцов следует иметь в виду, что на результаты исследова¬
ния могут оказывать влияние красители, специально добавляемые
в препараты, или окрашенные вещества — компоненты раститель¬
ного сырья.В тех случаях, когда подлежащий исследованию образец твер¬
дых вешеств представляет собой единичную упаковку, ее содер¬
жимое тщательно перемешивают для достижения возможно более
полной однородности состава (при необходимости с предваритель¬
ным измельчением). Из однородного материала отбирают на ис-
слелование 2 3 пробы по 5-15 мг. При анализе капсулированных
ТСХ-скрининг токсикантов 49Часть габлетки измельчают, смешивают с одинаковым коли-
чеством безводного сульфата натрия и растворяют в И) мл воды.В жидкость из шприца или ампулы объемом 0,5—1 мл добавляют
иоду, чтобы общий объем составлял 10 мл. Полученные образцы
исследуют по схеме 10.Часть растительного сырья измельчают (или растирают в ступ¬
ке), заливают 10 мл воды, подкисленной соляной кислотой до
pH — 2—3, и настаивают в течение 0,5—1 часа. По истечении ука¬
занного времени солянокислый раствор отделяют фильтрованием.
К фильтрату добавляют раствор гидроксида аммония до pH = 9—10
и далее исследуют, как указано на схеме 11.Образец (10 мл)+ НСІ до pH = 2-3,
экстракция эфиром|Органическая фаза)| Водная фаза|Фильтрование через безводный
Ма2304, упаривание досухаОстаток 1 (вещества кислого
и нейтрального характера)ш+ 1ЧН4ОН дорН= 9-10,
экстракция хлороформом,
центрифугированиеганическаяфаза)ІВодная фаза)Фильтрование через безводный
Ма2504, упаривание досухаОстаток 2 (вещества основного
и слабоосновного характера)Схема 10. Изолирование веществ из вещественных доказательств
[Р^иё5і^^вание водой,подкисленной НСІ(воднаявытяжка]Экстракция органическим растворителем,центрифугирование+ Ж4ОН, экстракция
органическим растворителем,
центрифугированиеОрганическая фаза
(вещества кислого характера)Органическая фаза
(вещества основного характера)Схема 11. Изолирование вешеств из растительного материала
Глава 5ТЕОРЕТИЧЕСКИЕ ОСНОВЫ
ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИТонкослойная хроматография — один из скрининговых мето¬
дов качественного и количественного определения токсических
веществ.Хроматография в тонком слое, предложенная в 1938 г. совет¬
скими учеными Н.А. Измайловым и М.С. Шрайбером, занимает в
настоящее время важное место в ХТА благодаря своей экспресс-
ности, воспроизводимости, простоте и низкой стоимости анализа.Как аналитический метод ТСХ широко используется для очист¬
ки экстрактов от мешающих веществ, подтверждения результатов
ХТА, проведенного другими методами, для скрининга токсических
веществ в объектах природного, полусинтетического и синтетиче¬
ского происхождения, а также с успехом сочетается с инструмен¬
тальными методами.Метод ТСХ относится к плоскостным видам хроматографии,
поскольку слой сорбента закреплен на плоской поверхности (этот
вид хроматографии еще называют планарной). Хроматографиче¬
ское разделение обусловлено переносом компонентов подвижной
фазы вдоль слоя неподвижной фазы с различными скоростями в
соответствии с коэффициентами распределения разделяемых ве¬
ществ между двумя фазами.Роль подвижной фазы выполняет смесь растворителей, непод¬
вижной фазой являются сорбенты на пластинке, а для обнаруже¬
ния токсических веществ на хроматограмме используются химиче¬
ские реагенты и УФ-свет.Эффективность хроматографического разделения широкого
круга токсических веществ обусловлена прежде всего выбором
сорбента, подвижной фазы, детектирующего реагента, техникой
исследования и стандартизацией условий хроматографического
анализа.
Глава 5ТСХ очень широкое„ . удоматографин- широкий круг— ' 1В планаР"01 1 ' щдач и. главное, возмож-Д^^^шьюанал^^ зо проб на одной хромато-
^и°^*«^'чили ме,од> ~
графической п. „азработаны приемы, позво-распроетранен „„ хх столетия оы- Р ТСХ Оказалость '^оГино анализа до 30-лившие ЗН ечить разделени ^ 15_20 мин При ЭТОмГГонентов анализируемых составЛять нанограммовые^ины опрелеляемые ^овни отдельныхГ'понентов - Ф«,оф“;МОВ“евсрш^ствованнь1х модификаций
в целом эффективность у ста таковую ее классических
ТСХ более чем на порядс> н говорить 0 формировании ново-вариантов. Это дало возкк ^ высокоэффективной тонкослойной
го аналитического' стала результатом ряда усовершен-Г1вГ "о'^ски вьпекаюших из обших положений теориивысокоэффективной хроматографии.Наиболее важные из этих усовершенствовании:1) применение адсорбентов с оптимальными характеристика¬
ми, аналогичными требованиям высокоэффективном колоноч¬
ной жидкостной хроматографии (малый размер зерна 3 5 мкм,
однородность размеров зерен — разброс размеров не более 10%;
низкое сопротивление массопередаче; тщательное кондициониро¬
вание);2) улучшенные способы нанесения проб, обеспечивающие
очень малые значения начальной ширины хроматографических
зон (пятен);3) усовершенствованные способы подвода элюента, исключаю¬
щие неравномерности его продвижения в слое сорбента;4) применение усовершенствованного оборудования для полу¬
чения хроматограмм и их количественной обработки.олее подробно рассмотрены особенности метода ТСХ.5.1. СОРБЕНТЫстеклянной или плаети!ль«3^ЮТ шРеплениые на металлической,
и подложке слои сорбента. В качестве
Теоретические основы тонкослойной хроматографии 53последнего применяются силикагели различного зернения, обра-
боганные или не ооработанные реактивами, для осуществления
как прямого, так и обрашеннофазното вариантов хроматографии,
а также целлюлозу, окись алюминия, кизсльгель, сефадекс, полиа¬
мид и некоторые другие материалы. Характеристики некоторых
сорбентов для ТСХ представлены в табл. 3.Таблица 3. Сорбенты для ТСХ и их характеристикиСорбентОбласть примененияПримечанияСиликагельРазделение неполярных ве¬
ществ; выделение веществ,
обладающих основными
свойствамиРекомендуется использовать
элюенты с основными свой¬
ствамиОксид алюминияРазделение слабополярных
основных веществПоверхность сорбента силь¬
но полярнаяМодифициро¬
ванный силикагельРазделение полярных ве¬
ществ в условиях обращен -
нофазовой хроматографииПоверхность покрыта хими¬
чески связанными углеводо¬
родными группамиПолиамидРазделение веществ, образу¬
ющих с амидными группами
сорбента водородные связиЭлюирующие свойства
растворителей возрастают
в ряду: вода < метанол <
ацетон < формамид < диме¬
тил формамидИногда к сорбентам добавляют флуоресцентный индикатор.
Для закрепления адсорбционного слоя применяют гипс, крахмал,
агар-агар и другие связующие материалы. В настоящее время при
анализе в основном используют готовые пластинки отечественного
или импортного производства, такие как «Сорбфил», «Силуфол»,
«Армсорб», «Мерк».Обычно в практике ХТА применяют пластины размером 5x5,10x10 или 20x20 см.5.2. СИСТЕМЫ РАСТВОРИТЕЛЕЙПри выборе систем растворителей пользуются элюотропными
рядами с учетом свойств разделяемых веществ и применяемых
сорбентов. Существуют элюотропные ряды для данного сороента,
облегчающие в какой-то мере выбор растворителя для осущест¬
вления ТСХ. В таком ряду растворители расположены в порядке
увеличения их элюирующей способности и возрастания их по¬
лярности (диэлектрической проницаемости): гексан, гептан, ци-
Глава 554 — лл-лерод, бензол, хлороформ, диэти-четыреххлористыи ут г нацеТОН, этанол, метанол, вОДа
КЛ0ГСКСаАда этилацетат, пИр Систсму растворителем, используе-
ЛовыиЭ£Рирмй ряд по Шталю). ^ подбирают, смешивая два рае-
"МВИ*Н0Й элюотропного ряда. Меняя раство.;^с„,кч°анс™ получить подвижную с^мь^ГсвоГтва“^ описано множество хромато-В настоящее время в литер ^ необхоДимо объективно и на-графических систем' “лежно уметь ИХ й системы ддя каждой конкретнойВыбор наиболее эфф№_ цели исследования.задачи зависит от поста» тографических систем решатьДля оценки сносов' токсических веществ используютпоставленную задгдчу р (0Р). Расчет ОР производитсярасчет «дискриминирующей силь Vпо формуле:2 МВР АМЛГГ~0 ’
где М- число сходных пар; И- общее число определяемых ве¬
ществ. А ,Величина О? существует в пределах от 0 до 1, поэтому чембольше значение ИР, тем более эффективна данная система рас¬
творителей для анализа исследуемых соединений.Отсюда следует, что наилучшая система растворителей обеспе¬
чивает хорошее распределение пятен по всей пластинке для наи¬
более важных веществ.С точки зрения гидродинамики потока для ТСХ с подачей под¬
вижной фазы за счет капиллярных сил более выгодно применять
растворители с высоким поверхностным натяжением и по возмож¬
ности с малой вязкостью. Такими наилучшими растворителями
являются ацетонитрил, ацетон, вода, диэтиловый эфир. Именно
эти растворители используются в настоящее время в ТСХ в каче¬
стве подвижных фаз наиболее часто.непосп1лгт1рРаСТВ°РИТеЛеЙ смешивают в требуемых соотношениях
перемешикани«0 Гел применением при помощи интенсивного
ригелей возможна нек070рь,х слУчаях при смешивании раство-
избыточной вол! I ГУ‘ИСНИе Раствора вследствие присутствия
графическую камеру с«|!!^ученную смесь выливают в хромато-и дно которой проложены фильтро-
Теоретические основы тонкослойной хроматографии 55вольной бумагой. Если в конкретной методике нет специального
разъяснения, то камеру герметично закрывают крышкой и остав¬
ляют на и,Ь ч для установления равновесия. Обычно для каждой
новой пластинки іотовят новую порцию системы. Допускается
временное хранение системы в посуде с притергой пробкой.Хроматографические системы подбираются таким обратом,
чтобы получаемые с их помощью результаты были максимально
эффективны, воспроизводимы от опыта к опыту в разных лабора¬
ториях.Однако Комитет по токсикологическому анализу Международ¬
ной ассоциации судебных токсикологов рекомендует ряд систем
для проведения ТСХ-скрининга в качестве стандартных (точнее,предпочтительных):На вещества основного характера• ТА: метанол - 25% аммиак (100:1,5).• ТВ: циклогексан — толуол - диэтиламин (75:15:10).• ТС: хлороформ - метанол (90:10).• TL: ацетон.• ТАЕ: метанол.• TAF: метанол — н-бутанол (60:40).На вещества кислого и нейтрального характера• TD: хлороформ - ацетон (80:20).• ТЕ: этилацетат — метанол - 25% аммиак (85:10:5).• TF: этилацетат.• TAD: хлороформ - метанол (90:10).На вещества кислого, нейтрального и основного характера• TAJ: хлороформ — этанол (90:10).• ТАК: хлороформ — циклогексан - ледяная уксусная кислота
(40:40:20).• TAL: хлороформ — метанол — пропионовая кислота (72:18:10).5.3. НАНЕСЕНИЕ ОБРАЗЦА
И ХРОМАТОГРАФИРОВАНИЕПластинку подготавливают, отмечая линию старта на расстоя¬
нии не менее 1 см от нижнего края. Отмечают также и границу,
которую при хроматографировании должен достичь фронт подвиж¬
ной фазы. Как правило, границу намечают в 1-1,5 см от противо-
Глава 55® На пластинках с достаточно прочно„„ложного края линии можно без особого труда про.
Лепленными слоями -и; . Необходимо ЛИШЬ ирослс.
£ега мягким П»Ф-'“\МСЬ поверхность слоя сорбента.
ЗКП.М тем. чтобы не наруш |іодлсжаших хроматографическомуОбычно пробы веШ^т1Графическую пластинку в виде раз_
анализу, наносят на хром«>Гщем раств0рителе возможно мень-
бавленных растворов в - что предотвращает чрезмер-шей полярности (шшрими^ пятна в подобном случае вещество
ное расплывание старті і выхода из капилляра. Однакосорбируется на анализируемый образец растворитсяследует иметь в1ВИД1. полностью, то плохо растворимыеВ неполярном Ра^7Хе^стриРо»аТЬ не удастся, и данные о со-
—Гб^г недостоверны. Обычно на практике применяют
меганоГьные растворы стандартов, а полученные после пробопод-
готовки экстракты растворяют в хлороформе.В качестве метчиков (свидетелей) используют чистые
субстанции-стандарты анализируемых веществ. При отсутствии
стандартов метчики можно приготовить из соответствующих ле¬
карственных препаратов путем обработки соответствующими ор¬
ганическими растворителями измельченных таблеток, инъекцион¬
ных лекарственных форм и т. д.Анализируемые растворы — точки А, В на рис. 1 — осторож¬
но. чтобы не повредить поверхность слоя адсорбента, наносят
на пластину с использованием капилляров или микрошприцов в
несколько приемов, обращая внимание на размеры получаемого
пятна. Размер пятна не должен превышать 3 мм в диаметре во
избежание бокового размывания. Одновременно на пластину на¬
носят эталонные (согласно утвержденным методикам) растворыи -.'т . М А ,к11кии (ЮЧКИ С, Э). Расстояние между точками на-
неиния должно быть не менее I см.
онные ск>йстм°М выпа,нении операции нанесения проб сорбци-чо,уі н—«ю*™ м
"ри выполнении операции ^анс "<”ЛУ’а' !1оэтому Рекомендуется
ные тонкослойные пластинки ия Пр° на высокоэффектив-
иионного слоя стеКЛИМЫ ш мПикРывать основную часть сорб-
стинкой Часто такая пласти МЄТа'ии'ІССКОЙ или пластиковой пла¬
фоном для нанесения большом,'*°ЖСТ 0ДН(>нРеменно служить ша-
Теоретичес кио основы гонкослойной хроматографииРис. 1. Разметка хроматографической пластинки и нанесение образцовВ различных публикациях описаны полностью или частично
автоматизированные устройства для нанесения большого числа
проб, выпускаемые приборостроительными фирмами (рис. 2, см.цв. вклейку).В ряде случаев перед выполнением хроматографического раз¬
деления проводят специальные операции по дополнительному
сжатию зон уже нанесенных проб. Этим достигается наилучшее
разделение компонентов пробы и увеличивается чувствительность
метода, так как после обработки хроматограммы детектирующими
реагентами вещества на пластинке проявляются в виде узких по¬
лос. а не в виде пятен.Для получения сильно сжатых начальных юн применют спе¬
циальные пластинки, имеющие, кроме основного ра иимяющего
сорбционного СЛОЯ силикагеля, ДОПОЛНИТеЛЬНуЮ ПОЛОСА и І ІЮ.ІЄС
Глава 558 — вблизи стартового края. В про-Л ял сорбента (кизельгуру лые пятна нанесенных проб
ИНЄРТНпоматографии исхОДНЫ!1ои ^стижении ими границы слоя
допевают сильное сжатИЄ ^ едное хроматографирование и
^ дивного м»Р^<пзагем продвигаются далее в форме«С^^^Т^оТпластинку помешают в равномерно
■ После нанесения образно» ^ наполненную подвиж-
насыщенную ^отТОГР2„ВМЖНОй фазы, помещенной в хромато-
ной фазой. КолИчесТВОпяСечитывается таким образом, чтобы при
графическую камеру. Р< хроматографии уровень ее соот-восходяшем вариант^юРпластиНы не более чем на 5 мм.
ветствовал погружению использование отдельной хро-хорошей "Р"ыС,"”^дой конкретной разделительной
ГеЖ —Рмос™ быстрой смены системы растворите-
лей^самеру просушивают, промывают 10 мл этанола, снова сушат,
мтем промышнот той системой растворителей, применение кото-
рой планируется.После помещения пластинки в хроматографическую камеру
растворитель движется по ней под действием капиллярных сил,
пока не достигнет линии финиша, после чего пластинку вынима¬
ют и сушат.Когда система растворителей достигнет линии фронта, пла¬
стинку вынимают из камеры и сушат до полного удаления следов
растворителей. Для этих целей можно использовать фен или по¬
местить пластинку в сушильный шкаф.Нанесение экстрактов по схеме ТСХ-скрининга проводят в три
точки - А, В и С (рис. 3)После хроматографирования зону А обрабатывают общими реа¬
гентами дія веществ кислого, нейтрального и слабоосновного ха-Щ хТрактераТрТ 5Г)ЄНТаМИ ВЄЩЄСТВ °СНОВНОГ° ”нилииа 'ИСТНЬ1Х реагентов: Раствора ва-серной и азотной киглт смеси концентрированнойсерной кислоты (см рис ’5ГИЯ >ихр0мата И концентРиР°ваннойв штатов в зонах А илини» полтвердлающих тесло» и кшит-'''“ И’ 3°Н“ С для "Р°"сде_И количественного определении.
Теоретические основы тонкослойной хроматографии59тов3она53она43она3она3она1АвсРис. 4. Схема последовательного обнаружения веществ кислого, нсйтра и>-
ного и слабоосновного характера
Реактив Марки:
H2SO4 + HN03 (1:1)
К2СГ2О7 + HgSQ4qoc FeClj
,уф-свет-
20 °С, ЗОРкс. 5. Схема последовательного обнаружения веществ основного и ела-
боосновного характераГ лава 55.4. ИДЕНТИФИКАЦИЯ ВЕЩЕСТВМЕТОДОМ тонкослойной
ХРОМАТОГРАФИИОсновной качественной характеристикой в ТСХ является вели¬
чина Rf (Ratio of fronts), которая представляет собой отношение
расстояний, пройденных исследуемым веществом и подвижной
фазой:го кшестС™ЯНп1°Т линии старта ло Центра пятна исследуемо- —- *—■от приролы сорбент “«гла < |. Величина R) зависитороенга. толшины слоя, способа нанесения пробы
Теоретические основы тонкослойной хроматографии 61и размера пятна, качества и природы растворителей, влажности
атмосферы, температуры и ряда других факторов.Для снижения влияния на величину Я/ факторов, вызванных
условиями проведения эксперимента, используют относительную
величину Лг, которая представляет собой отношение значения Я/
исследуемого вещества к значению Я/' стандарта:где /у — отношение расстояний, пройденных исследуемым веще¬
ством и подвижной фазой; Я/' — отношение расстояний, пройден¬
ных стандартом и подвижной фазой.5.5. ДЕТЕКТИРОВАНИЕПервоначальный этап при исследовании полученной хромато¬
граммы — идентификация хроматографических зон по свечению в
УФ-свете. их обработка одним химическим реагентом или последо¬
вательно несколькими реагентами в соответствии с утвержденными
методиками. После обработки реагентами отмечают положение и
окраску хроматографических зон.При проведении направленного ТСХ-скрининга веществ, при¬
надлежащих к известной группе химических соединений, исполь¬
зуют частные реагенты (табл. 4).Таблица 4. Состав реактивов и получаемая с их помощью окраска хтя
визуализации хроматографических зонНазваниереактиваМетодика приготовления
реактиваОсобенностипримененияОкрашиваниеFPN-реак-тив250 мг хлорида железа
(III) растворяют в 15 мл
60% раствора хлорной
кислоты. 35 мл 70% азот¬
ной кислоты и 100 мл
дистиллированной водыКрасное или
коричневато-красное
окрашивание соот¬
ветствует фенотыа-
зинамРаствор
йода
в йодиде
калия5% раствор йода в смеси
10% раствора йодида ка¬
лия, дистиллированной
воды и 2 н раствора ук¬
сусной кислотыРеактив хтя обнару¬
жения и.1ли«ш<кч>
Продолжение табл. 4и*-— —рованной СОЛЯ^НаИСЛ°
средственно перед обраОсобенностипримененияОкрашиваниеНазваниереактиварастворнингидринаПосле опрыски¬
вания пластинку
нагревают при
100 °С в течение
5 минфиолетовая, розо¬
вая или пурпурная
окраска соответствует
первичным аминам.
Желтая окраска
пятен — вторичным
аминамботкои мастип /тГпПурпурные цветаРастворхлорида10 г хлорида железа (
растворяют в 100 мл дис¬
тиллированной водыдают фенольные сое¬
диненияРеактивВан-Урка1 г л-диметиламино-
бензальдегида растворяют
в 90 мл этанола и 10 мл
концентрированной со¬
ляной кислоты
Реактив готовится непо¬
средственно перед обра¬
боткой пластинПосле опрыски¬
вания пластинку
нагревают при
100 °С в течение
5 минМногие вещества
дают розовую окраску
ПрО* для ЛСД —0,05 мгРеактив
Драге н-
дорфаРеактивйодплатина-Раствор 1. 2 г висмута
нитрата основного рас¬
творяют в 25 мл ледяной
уксусной кислоты и
100 мл дистиллированной
воды.Раствор 2. 40 г калия
йодида в 100 мл дистил¬
лированной воды.Реактив готовят путем
смешивания растворов
И 2 (по 10 мл каждого)
м мл ледяной уксусной
кислоты и 100 мл воды£7™готовят раз °загтйг.После опрыски¬
вания пластинку
нагревают при
100°С в течение
5 мин. Удаление
желтого фона
реактива про¬
изводится
опрыскиванием
пластинки 10%
раствором сер¬
ной кислоты споследующимнагреваниемЖелтая, оранжевая,
крас но-оранжевая,
кирпично-красная,
коричнево-оранжевая
окраска соответствует
соединениям,со¬
держащим третичный
атом азотата подкис.ленныйМосле опрыски¬
вания пластинку
нагревают ад,С в течение
' МинПурпурная или с раз-
личными оттенками
окраска соответствует
не 1 вер) ичныч *ммма*;алкалоиды, перми***И нгорнчмые яммиылам г разную окряску1 1 * 1 па!
^■^.иргкие основы тонкослойнойхроматографии Продолжение табл. 4НазваниереактиваРеактивМанделинаРеактивМаркиМетодика приготовления
реактиваРастворяют 1,62 г вана-
дата аммония в 125 мл
концентрированной сер¬
ной кислоты, охлаждают
и приливают раствор к
125 мл ледяной дистил¬
лированной воды; перед
употреблением реактив
разбавляют в 10 раз дис¬
тиллированной водойДобавляют 2 мл 36% рас¬
твора формальдегида к
100 мл концентрирован¬
ной серной кислоты
Реактив готовят непо¬
средственно перед обра¬
боткой пластинОсобенностипримененияПосле опрыски¬
вания пластинку
нагревают при
110 °С в течение3 минНаносится ка¬
пел ьно или ме¬
тодом макания
пластинки
в реактивОкрашиваниеАлкалоиды и фенолыобнаруживаются с
пределом обнаруже¬
ния 0,25-2,5 мкг в
пятнеЧерное или пурпур¬
ное окрашивание мо¬
жет соответствовать
опиатамРеактивМекке1 г селеновой кислоты
растворяют в 100 мл кон¬
центрированной серной
кислотыРеактив для обнару¬
жения алкалоидовРеактивМунье2 мл реактива
Драгендорфа, 0,1 г аскор¬
биновой кислоты, 0,1 мл
уксусной кислоты и 8 мл
дистиллированной водыАлкалоиды и тре¬
тичные амины дают
светло-оранжевое
окрашивание; окра¬
шиваются липиды,
ненасыщенные сте¬
роиды и другие ве¬
ществаРеактивФредеРеактив
Эрлиха
модифици¬
рованныйНасыщенный раствор
молибдата натрия или ка¬
лия в концентрированной
серной кислоте
Реактив готовят непо¬
средственно перед обра¬
боткой пластин1 г л-диметиламино-
бензальдегида растворяют
в 10 мл метанола и 10 мл
концентрированной
ортофосфорной кислоты
(плотность 1,75 г/мл)
Реактив готовят непо¬
средственно перед обра
боткой пластинРеактив для обнару¬
жения алкалоидовКрасная окраска со¬
ответствует фенци¬
клидину; темно-синее
окрашивание харак¬
терно для индолов
Продолжение табл.Няз»аииерсакі ивареактивпрочногочерного Крастворхлорнойкислоты,содержащей
3% нитрита
натрияметодик» прип.го*-еНИ"реактива ^■ Г- "!оряют°в ' Н)0НМ^л»°-Реск тии гопичч"” "1"'средств»« перед Ф<>(ютко^иас^ 7^Т51% раствор
хлорной кислоты
раствор 2. 0,5 г натрия
нитрита растворяют
в НЮ мл дистиллирован¬
ной водыРеактив готовят путем
смешивания раствора / и
‘ в соотношении 97:3Раствор
сульфата
ртути (II)Раствор
Дифенил-
карбазонаРаствор
прочного
с»него ББРеактив
ФУРфураля5 г желтой окиси ртути
растворяют в 100 мл дис¬
тиллированной воды,
добавляют 20 мл кон¬
центрированной серной
кислоты, охлаждают и
доводят до 250 мл дис-
пшированной водой01 г днФенилкарбазона«ЮТ в,00 мл Ио.5 мгР^'творяют В наёк,! ББ
иом раствор, капк КН'кадия (40%) ЫрбонатаУед™т«1н2'7”''\непо'
Г‘Г,Ра'РасП1^рТТГ
£аля сМеШиваЛ фуРФу-
^иетона ают с 98 Мл
аств0р 2 лТрированн(ШМл к°нцен-ОсобенностипримененияРеактив исполь¬
зуется спустя
1 ч после сме¬
шивания исхо¬
дных растворовПрименяется
только в сочета¬
нии с раствором
сульфата ртути
(II)Рабатывакуг
Двором 1 аОкрашиваниеАмфетамины и фе-
нилалкиламины про¬
являются пятнами
коричнево-розового
цвета на светло-
коричневом фонеРазличное окрашива¬
ние производных фе-
нотиазина, тиоксанте-
на, 1,4-бензодиазепинаБелые пятна на сером
фоне соответствуют
барбитуратамКрасно-фиолетовые,
сине-фиолетовые
пятна соответствуют
барбитуратамКрасная, фиолетово¬
красная окраска со¬
ответствует каннабн-
ноидам°т пурпурного до
СИНе-ЧерНОГО ЦНС1Я
скрашиваются не ко
5Х)Рые всщссгна нейтрального характер*-Л.—*
тонкослойной хроматографии65Окончание табл. 4 — — 1НазваниереактиваМетодика приготовления
реактиваОсобенностипримененияОкрашиваниерастворванилина1 г ванилина растворя¬
ют в 100 мл метилового
спирта, добавляют 2 мл
концентрированной сер¬
ной кислотыЖелтое окрашивание
соответствует мепро¬
баматуРеактивПрохазкиСмешивают 35% раствор
формальдегида с 25%
раствором соляной кис¬
лоты и этанолом в соот¬
ношении 1:1:2
Реактив готовят непо¬
средственно перед обра¬
боткой шастинОкраска усили¬
вается после об¬
работки царской
водкой (смесь
концентриро¬
ванной азотной
и соляной кис¬
лот в соотноше¬
нии 1:3)Индольные соеди¬
нения; при дневном
свете зоны окрашены
в разные цвета; в
УФ-свете они флюо¬
ресцируют
ПрО*-10 нгРеактивы для проведения реакции Браттона-МаршалаРаствор
нитрита на¬
трия (А)0,1 г натрия нитрита рас¬
творяют в 100 мл дистил¬
лированной воды
Реактив готовят непо¬
средственно перед обра¬
боткой пластинПластинку
поочередно об¬
рабатывают рас¬
творами А, В и
С; после каждой
обработки пла¬
стину высуши¬
ваютБензофеноны 1,4-
бензодиазепина даютрозовое, красное
окрашиваниеРастворсульфаматааммония(В)0,5 г сульфамата аммония
растворяют в 100 мл дис¬
тиллированной водыРаствор
N-0-
нафтил-
этилендиа-
мина (С)* Пг,П 0,1 г Ы-а-нафтил-
этилендиамина растворя¬
ют в 100 мл дистиллиро¬
ванной водыТак, при исследовании на вещества оснпянпгп
стины можно обрабатывать реактивами 1 Актера пла-характера — 57 16-18- нейтпя На вещества кислогоактив прочный синий кк Г Р НОГ° характеРа ~ 7-12, 19. Ре-
каннабиноидов. спользуется только для обнаруженияЗрительного ТСХЖскриниТ[Г я1П° СХеМе ненапРавленного прсд-ного количества химических ГГ«! °ПРеДеЛеНиеРасходовании экстракта. ' ПРИ Минимальном
И— ,.н0 обоснованный выбор схемы по-П ,я этого используют « о6шефупповых реагентов в одной
слеловательното "^Параллельную зону используют для о6.хроматофафигентами. _работки частными РеагеНТименеНИя общих реагентов для обнару,
Последовательность пр' ого и слабоосновного характеражения вешеств кислого рис 4) 3ону б обрабатываютв зоне А представлена ванилина) для определения ме-частным реагентом (1% Растворобамата. ппмменения общих реагентов для обнару.Последовательное ь^мененб00сн0вн0г0 в ^ Рукия веществ ос^ ^ ^ 5) 3ону Б используют для примене-в зоне А
частным ■
проба мата.Последов и слабоосноьниі w оипс Ажения веществ 0CH°BHÜ сч 3ону Б используют для примене-
представлена вь,ше (СМ, Р осят На пластинку капельно):ШЯ. реактив Марки - обнаружение морфина, кодеина, дионина,. ГьТиаае"вТины* H;S04 и HNO, (1:1) - обнаруже-ние димедрола;• кристаллы К2Ст,07 и концентрированная H2S04 — обнаруже¬
ние стрихнина.5.6. НАПРАВЛЕННЫЙ
И НЕНАПРАВЛЕННЫЙ ТСХ-СКРИНИНГВнелабораторная оценка эффективности разделения токсиче¬
ских вешеств системами растворителей на различных сорбентах
была использована для разработки схемы ТСХ-скрининга.Методологической основой ТСХ-скрининга является сочетание
общих систем растворителей, хроматографирование в которых по¬
зволяет разделить токсические вещества на группы с частными си¬
стемами растворителей, определяющими конкретный токсикант.-истема ненаправленного ТСХ-скрининга токсических веществвключает два этапа.раствооитряр^^и4еск^ разделение веществ в общей системе
Минированного п)Наружение исследуемых соединений путем ком-
Rf что Позволяет устанЄНИЯ 0бЩИХ реагентов’ измерение значения
ленному химическому массу ПрИнадлежность вещества к опреде-творитеяей, о^аружени(ЖС ВСЩ^СТВ в частных системах рас-снсцифическими и чувствительными
Теоретические основы тонкослойной хроматографии 67реагентами, определение неизвестного токсического вещества,
элюирование последнего с целью дальнейшего проведения под¬
тверждающего анализа и количественного определения.Ненаправленный ТСХ-скрининг ряда веществ кислого, ней¬
трального, слабоосновного и основного характера представлен на
схеме 12.I Объект!ТГИзолирование органическим растворителемЭлюированиеЭфиром при pH = 2 (веществаХлороформом при pH = 10кислого, нейтрального и(вещества слабоосновного ислабоосновного характера)основного характера)Хроматографирование вХроматографирование вобщей системеобщей системерастворителейрастворителейПоследовательноеПоследовательноеобнаружение веществобнаружение веществобщими реагентамиобщими реагентамиХроматографирование в
частных системах
растворителейЭлюированиеГХроматографирование в
частных системах
растворителейОбнаружение веществ
частными реагентамиЭлюированиеОбнаружение веществ
частными реагентамиЭлюированиеПодтверждающие методы
(качественный анализ)Количественное
определениеСхема 12. Схема предварительного ненаправленного ТСХ-скрининга
^ппявленный ТСХ-скрининг веществслабоосновного характера
I эта" извлечения (pH = 2) в общей системе рас.Исследование эфирного и сорбент - силикагель КСК.хлороформ - аието„ .„.„еств на хроматографические зоныРаспределение вещес_^ АнальгинАцетилсалициловая кисло сСалициловая кислота —.Мепробамат
Бензойная кислота
Антипирин
АмидопиринКофеин ФенобарбиталБарбиталНитразепамБарбамилЭтаминал натрияЦиклобарбиталБензонал
Диазепам
Ноксирон
Бутадион 0,00-0,020,19-0,250,31-0,410,57-0,83Обнаружение: УФ-свет -> HgS04 + 0,1% раствор дифенилкар-
базона -> 1 °С -> 10% раствор РеС13 —> реактив Драгендорфа -> ре¬
акция Браттона-Маршала; обнаружение мепробамата — 1% раствор
ванилина в метаноле*.Элюирование: 1-3-я зоны — метанол; 4—5-я зоны — ацетон.II этапИсследование злюата в частных системах растворителей | Система растворителейСорбентРеагент0,00 0,02 1. Хлороформ - ацетон (9:1)
2 Бута нол - этанол - 25%| аммиак (5:1:1;Силикагель
КСК забуфе-
ренный 0,1 н
КН80,10 % РеС13ииіи ііриїотоплении рсагенн іотражена в іаГ.л 4.
Теоретическиеосновы^онкос^ной хроматографии69К,Система растворителейСорбентРеагент0,11-0.12Ацетон - бензол - ледяная
уксусная кислота (45:5:1)СиликагельКСК1% раствор ванилина
в метаноле; 10 %
РеС1,0,19-0,25Ацетон - циклогексан (5:1)Окись алюми¬
ния (основная)10 % ЯсСІ,;
реактив Драгенлорфа0,31-0,41Хлороформ - н-бутанол -
25% аммиак (70:40:5)Силикагель
КСК забуфе-
ренный 0,1 Нн,во,Нц504 + 0,1% рас¬
твор дифенилкар-
базона; реактив
Драгендорфа0,57-0,831. Этилацетат2. Бензол - этанол - 25%
аммиак (95:15:5)СиликагельКСК+ 0,1% рас¬
твор дифенилкар-
базоиа; реактив
1 Драгендорфа1III этапИсследование элюата подтверждающими методами (ГХ, ГХ-МС,
ВЭЖХ) и проведение количественного определения.Предварительный ненаправленный ТСХ-скрининг веществ
основного и слабоосновного характераI этапИсследование хлороформного извлечения (pH = 10) в общей
системе растворителей ацетон-хлороформ-25 % аммиак-диоксан
(5:45:2,5:47,5); сорбент - силикагель КСК.Распределение веществ на хроматографические зоныВещества»гПахикарпинМорфинАтропинЭфедрин0 12-0,36ХининСтрихнинКодеинДионинЭтилморфин —ТрифлуоперазинМежептил0,50-0,58АнтипиринКофеинСкополамин
ПрометзэинДимедр0'1т"ОридазинИмипрам””Хюрпр°маПромел0-1НитратамХлорпроге^ІТизерцин
Папаверин
диазепам
КокаинII этапИсследование элюата в частных системах растворителейк!Система растворителейСорбентРеагент0,12-0,361. Хлороформ - диэтиламин
(9:1)2. Бензол - этилацетат -
диэтиламин (7:2:1)СиликагельКСКУФ-свет;реактив Драгендорфа0.50-0,58Хлороформ - ацетон (5:1)Окись алюми¬
ния (нейтраль¬
ная)10% раствор РеС1
57% раствор НС104и
0,5% раствор Ыа^2(97:3);реактив Драгендорфа0,63-0.831. Хлороформ - этанол
(29:1)2 Гептан - ацетон (5:1)Окись алюми¬
ния (основная)То же0,87-0,98Циклогексан - ацетон (5:1)Окись алюми¬
ния (основная)То же• *5=»«, в табл 4
Теоретические основы тонкослойной хроматографии 71III этап.“Г иодтверждающими методами <ГХ, ГХ-МС,
в ЗЛХ) и проведение количественного определенияС истема направленного предварительного ТСХ-скринингаИК:Г:^:.~Н'К ’КСТракта в «Роматографичкких параме-
грач (сорбент, система растворителей, детектирующий реагент),
характерных для анализируемого класса токсических веществ.И ре }\льглге направленного скрининга устанавливают неиз¬
вестные токсические вещества (совпадение величины ЯГ и окраски
пятна с веществом-стандартом), затем пятно элюируют и проводят
подтверждающий анализ и количественное определение.5.7. КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕВсе способы количественной оценки хроматограмм можно
условно подразделить на две группы.1. Способы количественной оценки непосредственно на хромато¬
графической пластинке без экстрагирования разделенных токсикан¬
тов.Визуальный метод сравнения окрашенных пятен разделенных
веществ с окрашенными пятнами стандартов, хроматографируе¬
мых на той же пластинке.Фотографические методы: хроматограммы, даюшие при иден¬
тификации в результате опрыскивания реагентами контрастные
пятна с неизменяюшейся окраской, можно объективно оценить,
используя зависимость площади пятна от концентрации вещества
на хроматограмме, графическим или алгебраическим путем.Фотоденситометрическое (от лат. (1епзИаз — плотность) опреде¬
ление после окраски исследуемых веществ на хроматограмме с по¬
мощью специальных инструментальных методов.Радиоавтографические методы определения меченых исследуе¬
мых веществ на хроматограммах с помощью специальных прибо¬
ров (например, счетчиков Гейгера и др.).2. Способы количественной оценки хроматограмм после элюиро¬
вания исследуемых соединений с хроматографической пластинки.Для количественной оценки изучаемых соединений после их
элюирования с хроматографической пластинки в дальнейшем ис¬
пользуют все известные химические или физико-химические ме¬
тоды определения концентрации полученного элюата.
Глава 572 _ ' " количественной оценки хромате-всерялом при"ЄущТ^»" °*» не-ИМ положится мет0Д сравн бласти концентраций име-ется ВИЗвешества и плошадью пя^на нные ^ законе Пурду о ^Фотографические ^“^концентрации нанесенных на хро-висим^и между логарифмом еств и корнем квадратным измиографическую пласТ^ннЫх зон, применяются ограниченноплошали полученных окрашу ния ПЛОщади образующихсяплощади получепп" 0Г0В связи с трудностью
пятен- п.рства на хроматографической пластинке опре-£—■^ = я X о X е,мм2- а - наибольший радиус, мм; в -
где П - плошадь пятна, мм , онаименьший радиус, мм.для определения массы вещества в пятне используют уравне-ние:а/Т— 1 л,8И,= ,8Г- + лЯтыгде й/— масса пятна раствора пробы, мг; А — площадь пятна рас¬
твора пробы, мм2; № - масса пятна стандартного раствора, мг;
А - площадь пятна стандартного раствора, мм2; Лц — площадь
пятна разбавленного раствора пробы, мм2; */ — коэффициент раз¬
бавления.Немаловажное значение имеет соотношение концентраций ре¬
актива и определяемого вещества, неодинаковое в центре и у края
хроматографического пятна, из-за чего ход реакции может быть
различным. Кроме того, сам слой часто окрашивается реактивом,
и возникает необходимость учета фона.Ленситометрический способ количественной оценки исследуе-
сгинкГжп!!-?'^ непосрсдствсино на хроматографической пла¬
тою способа 1("°!ИХ ВЬ|,исперечисленных недостатков. В основе• и) имерение интенсивности отраженного или
Теоретические основы тонкослойной хроматографии 73поглощенного света в ультрафиолетовой или видимой областяхспектра.Денситометр состоит из осветительной камеры, цветной видео-
ил и фотокамеры, платы ввода изображения, компьютера, монитора,
принтера и программного обеспечения (рис. 6., см. ив. вклейку).Освети гельная камера представляет собой металлический кор¬
пус. На днище корпуса устанавливается предметный столик, на
нем крепится исследуемая пластинка. В верхней части корпуса
установлены УФ-лампы с длинами волн 254 и 365 нм и лампы
дневного света.Изображение хроматограммы, видимое в дневном и УФ-свете,
с помощью видеокамеры через плату ввода изображения переда¬
ется на компьютер, записывается и затем обрабатывается по про¬
грамме.Денситометр производит расчет видеоизображения ТСХ-плас-
тины с построением хроматограммы (аналоговой кривой) по от¬
клонению яркости фона пластины с последующим нахождением
пиков на этой кривой и определением их площади.Количественную обработку пятна в денситометрии проводят по
двум характеристикам: по площади пятна и по его «объему» в про¬
странстве, при этом в качестве третьей координаты используют
яркость (интенсивность окраски) пятна (рис. 7).Приблизительныйцентр пятна V зРис. 7. Вид пространственного распределения яркости в области пятна.
А - значение уровня яркости точки пятна; Вм - значение уровня яркости
точки на базовой поверхности; V - объем пятна; 8 - площадь пятна
Г лава 574 . 'пр0«вести два вида количественны«Денситометр позв
ваетегов. „ „имизируемых веществ в смеси прово-I Расчет содержания анал ^ ^ представляет выраженное в
дится методом пР°СТОИп^11Ди/высоть. каждого отдельного пика
процентах отношение шкшмд / в треке (ориентировочныйК сумме площадей/высотрасчет). прмгества в пробе производится мето-2. Расчет ^нцент^ киТметодом внешнего стандарта). По
дом абсолютной кали Р оенному мя известных количеств
калибровочному граф У. нной площади пятна искомоговещества (стандартов», и рассчш д ^ ^ГМГ-—пробь'’находят концентрацию вещс-ства. ,На точность анализа влияет ряд факторов.В частности, необходимо, чтобы: а) размеры стартовых пятен
были одинаковыми (по этой причине концентрации растворов
не должны заметно различаться); б) микропипетки для нанесе¬
ния экстрактов и стандартов были точно откалиброваны; в) давле¬
ние паров в камере для хроматографирования было постоянным;
г) применяемые растворители обеспечивали четкое разделение
соединений; д) реактивы для обработки хроматографической пла¬
стинки обеспечивали четкое контрастирование пятен; е) опрыски¬
вание реактивами было равномерным; ж) разделение стандартных
растворов и растворов проб проводилось одновременно.Ниже приведена методика количественного определения мор¬
фина, кодеина, тебаина, наркотина и папаверина в опии методом
денситометрии.пы п!Г0 300 МГ 0ПИЯ помещают в мерную колбу на 100 мл (если
вапитс™^ исслед°ва”ие в виДе твердого вещества, его пред-
лГн^Гвают лоЛЬ,ипЮТ)- Ш В К°Лбу добавл™т 50 мл метано-30 мин, перемешивГИс^рВжимоеИЛЮТ ПРИ ЭТ°Й ТеМПературе
охлаждают доводят пп к,» Далее содержимое колбыполученного экстракта отб^™ метанолом и Дают отстояться. Из
Досуха. Сухой осадок растворяют 7^ °6ЪШШ 3 мл и Упаривают
носят на пластину НРТ1 Гр , метанола и по 10 мкл на-
^ Фирмы «Мегск» (Германия?» 8Шса Се| МЕКСК 60|,ластину наносят 4 повтопа см. Одновременноповтора пробы и 5 калибровочных образно,.
Теоретические основы тонкослойной хроматографии 75компонентов опия. Хроматофафирование проводят в системах спробегом растворителя не менее 8 см.1. Толуол - ацетон - этанол - 25 % аммиак (45:45:7:3).2. Хлороформ - ацетон - этанол - 25 % аммиак (20:20:3:1).3. Толуол - диэгиламин - этанол (9:1:1).После удаления остатков растворителя пластину денситоме-
трируют при 280 нм на приборе «ТЬС^СА^ЕЯ III* фирмы
«С АМАО* ([ермания). В табл. 5 представлены максимумы отра¬
жения и значения КГ основных компонентов опия. Следует отме¬
тить, что в зависимости от использованной системы максимумы
отражения веществ могут незначительно изменяться в пределах
ошибки ± 4 нм.Таблица 5. Максимумы отражения и значения К, компонентов опияВеществоМаксимумы шражения, нмЗначения Л,» системахХ\Х2)3Х4Х5№ 1№2№3Героин207280312--0,38--Г идрокодон208218293--0,140,340,47Гидрокотарнин217225320--0,58--Дигидрокодеин212222245293-0,090,260,43Кодеин216226295--0,190,270,45Криптопин208218295245-0,510,760,63Меконин217225320--0,73--Морфин219229297--0,090,150,20Наркотин217225322--0,700,780,67Оксикодон209218292--0,530,740,63Папаверин2392492912113350,580,720,60Тебаин286296216236-0,300,470,64Этилморфин217226295--0,190,380.46На рис. 8 представлен спектр отражения кодеина, полученный
после хроматографирования в системе № 2.
лРис. 8. Спектр отражения кодеина, выделенного с помощью системы
№ 2 из образца героинаПриведенная выше методика может с успехом применяться для
количественного определения действующего начала в героине. На
рис. 9 приведена денситограмма 5 мг/мл метанольного раствора
героина, полученная при сканировании пластины при 280 нм по¬
сле разделения в системе № 2.
Теоретические основы тонкослойной хроматографии77В результате проведенного исследования в данном образце уста¬
новлено присутствие 46,6 ± 1,6% диацетилморфина, 29,8 ± 2,0%
наркотина и 2,6 ± 0,4% папаверина. Результаты денситометриче-
ского определения этих веществ совпали в пределах 5 % ошибки
с результатами газохроматографического исследования, проведен¬
ного по утвержденной ПККН методике.5.8. ВОСПРОИЗВОДИМОСТЬ
РЕЗУЛЬТАТОВ ИССЛЕДОВАНИЯВоспроизводимость результатов исследования методом ТСХ
определяют следующие факторы.1. Инструментальное обеспечение эксперимента: конструкция
используемой хроматографической камеры; способ ее герметиза¬
ции; условия насыщения камеры парами растворителей и т. д.2. Свойства хроматографической системы: тип и способ хими¬
ческой обработки использованного сорбента, величина его зерне¬
ния, толщина слоя, тип подложки, на которую он нанесен, вид
и количество внесенных в адсорбент вспомогательных веществ,
таких как связующие компоненты и флуоресцирующие вещества,
метод активации сорбента, например выдерживание при повышен¬
ной температуре, способ обработки пластинки импрегнирующими
буферами, щелочами и кислотами, а также веществами, модифи¬
цирующими свойства сорбента.3. Методические подходы к нанесению пробы и проведению
хроматографирования: способ нанесения образца на пластинку и
используемое при этом устройство, размеры начальной зоны хро¬
матографирования, полярность растворителя, использованного
для нанесения образца, и его количество, продолжительность ис¬
следования и величина пробега растворителя, его состав и чистота,
температура и влажность окружающей среды в момент проведения
исследования.5.9. ПРЕДСТАВЛЕНИЕ РЕЗУЛЬТАТОВ
ЭКСПЕРТИЗЫЭкспертное заключение о полученных предварительных ре¬
зультатах ТСХ-скрининга должно содержать подробное описание
Глава 5условий проведения эксперимента (хроматографические пластин-
п мм&нТналичие или отсутствие индикатора в его составеиспользсшнное связующее вещество, ТИП ПОДЛОЖКИ для адсор.’
&нта фирма-изготовитель, проведенная спсииальная обработка
пластин перед исследованием, например высушивание их при По.
вышенной температуре или импрегнированис кислотой, шелочью
или буфером. Если применяются готовые пластинки (Силуф0/,
Сорбфил, Мегск), то в этом случае достаточно привести данное
мячнание полностью. Далее идет описание использованных систем— ^.„гтненного и количественного£и"вуфером[_!?1ИтоТэтом” случае достаточно привести данноеназвание полностью. Далее ил иВДСпенн0Г<) и количественногорастворителей с Укамниео ,,ирования (вертикальный [обычно
состава, способа хром «к ч- юй или многомерный), а так-
опуекаегся), гоР"зон.т^оимёр проволилось ли хроматографиро-
*е особых приемов ( Р И1И при п0вышенн0й температуре).В описание дамы обработки хроматографических пластин входятс«"* использованных реактивах - их полном качествен¬
ном и количественном составе, последовательности проведения
ZnoB обработки, и* интенсивности и продолжительности. Особо
отмечается интенсивность и окраска хроматографических тон ис-
стедусмых веществ после обработки каждым реактивом, а также
величин а их RrЗаключение об обнаружении токсического вешества методом
ТСХ-скрининга лелают на основании совпадения величины R(
метчика и анализируемого объекта, а также интенсивности окра¬
ски пятен при обработке химическими реактивами.Данные ТСХ-скрининга подтверждают результатами исполь¬
зования аналитических методов, основанных на других физико¬
химических принципах.ТСХ-скрининг имеет отрицательное химико-токсикологическое
значение, т, е. при получении отрицательных результатов дальней¬
шее исследование другими методами не проводится, а в отноше-'x"Pajlja Делается заключение о том, что он не
Р токсикологически значимых веществ.
Глава 6ПРИМЕНЕНИЕ ТСХ-СКРИНИНГА
НА ПРИМЕРЕ ИСПОЛЬЗОВАНИЯ
СИСТЕМЫ TOXI-LABПеред специалистами, работающими в области XTА, стоит за¬
дача экспрессного и в то же время однозначного определения ши¬
рокого круга биологически активных вешеств в биообъектах, ха¬
рактеризующихся различными биохимическими свойствами.Стандартизация хроматографических параметров метода ТСХ
позволяет выявлять в биологических объектах присутствие не¬
скольких сотен токсикологически значимых вешеств и их метабо¬
литов.В настоящее время одним из примеров лаборатории, сочетаю¬
щей пробоподготовку объектов с последующим определением ток¬
сикологически значимых вешеств и их метаболитов методом ТСХ,
является система Toxi-Lab, выпускаемая фирмой Varian (США).Комплексная лаборатория Toxi-Lab позволяет идентифициро¬
вать токсикологически значимые вещества кислого, нейтрального
и основного характера из групп опиатов, каннабиноидов, беню-
диазепинов, барбитуратов, фенотиазинов, а также галлюциногены
и кокаин.Система Toxi-Lab содержит полный набор всего необходимого
для проведения пробоподготовки с последующим определением
наркотических веществ методом ТСХ. Система включает обору¬
дование для извлечения, концентрирования и обнаружения более
чем 700 токсикологически значимых веществ и их метаболитов.
Процедура анализа состоит из нескольких стадий (экстракция;
концентрирование; нанесение пробы на пластинку; хроматогра¬
фическая разгонка, или разделение; детектирование; идентифика¬
ция).В набор (рис. 10, см. цв. вклейку) входят хроматографические
камеры, аппликаторы, термовоздушный фен, камера с УФ-лампой,
приспособления для проявления хроматограмм, пластинки для
Глава 680 " диски, содержащие определен-ТСХ и специальные ста^Р™“ наркот„ческих веществ („о*Г-шчествоодного ИЛИ неско/ прилагаются методики, злю-
выбор\ пользователя). К^елеНия наркотиков. Такие системыенты документация для определ ^ и ^ определсния целевь(хмогут служить как для скриниШ амфетамины и др.).аналитов (каннабиноиды. опи значИМых веществ из мочи осу-
Экстракиия ТОКСИК0Л°Г', ^пе„иальных патентованных устройств
шествляется с применением дофазной экстракции.ДЛЯ жидко-жидкостнои кт у токсикантов проводят на спе-
Кониентрирование выл\ ^ того же матерИала, что и хро-циальные диски, вь,п^ Пеоенос сконцентрированной пробы
матографическая плас• остинку осуществляют с помо-
(лиска) на хроматографическую пда^ ^ вставляют всТо?одТеао?ае^сЬтНия пластинки на линии старта. Кроме того, на
,™нн старта помешают лиск с нанесенными стандартными об-разиами наркотических веществ.Хроматографическое разделение проводят в специальных сте¬
клянных камерах.В качестве подвижной фазы используют смесь органических
растворителей, предназначенных для конкретной группы (или
груш) наркотических веществ.Детектирование осуществляют путем последовательной обра¬
ботки хроматограммы специфическими реагентами.Идентификация компонентов проводится по совокупности ве¬
личины ЯГ и цвета пятна на различных стадиях детектирования,
путем сравнения со стандартным образцом (рис. 11, см. цв. вклей¬
ку). Если величина Я/или окраска пятна не совпадает с величиной
Я/ или окраской пятна стандарта, то необходимо воспользоваться
компендиумом наркотиков (рис. 12, см. цв. вклейку), в котором
для каждого значения ЯГ приведены возможные наркотические ве-
шества и их метаболиты, а также окраска пятен этих соединений
на каждой стадии детектирования.ты^истеГто™ьФУПП ВСШеСТВ Существуют следующие комплек-"я быстрого опре-рассчитанная на 100 ? нейтральной природы,нений и 100 определений неитральных и основных соеди-Рекомендуется для забои- >ар |*туРатов и Других кислых Езеществ.- Для лабораторий с низким и средним пробопото-
применение ТСХ-скрининга.81ком. Количество определений зависит от числа входящих в набор
компонентов (экстракционных пробирок, хроматографических
пластинок, дисков для концентрирования).Экстракция осуществляется в специальных экстракционных
пробирках, наполненных органической фазой и высаливающим
реагентом, к которым добавляется определенное количество мочи
или плазмы (жидко-жидкостная экстракция). Экстракционные
пробирки кш-1 иЬе А маркируются желтым цветом и используют¬
ся для извлечения органических оснований и некоторых веществ
нейтрального характера. Экстракционные пробирки Тох1-ТиЬе В
маркируются красным цветом и используются для извлечения ор¬
ганических веществ кислого характера и некоторых нейтральных
веществ (рис. 13, см. цв. вклейку).Концентрирование осуществляется на специальные диски, вы¬
полненные из того же материала, что и хроматографическая пла¬
стинка. Диски помещают в концентрационные колпачки, в кото¬
рые переносят органическую фазу (см. рис. 13, см. цв. вклейку),
после чего органический растворитель упаривают до тех пор, пока
диски не высохнут. Далее диск с концентрированной пробой за¬
прессовывают в пластинку при помощи препаровальной иглы (см.
рис. 13, см. цв. вклейку).Хроматографирование производится в специальных стеклянных
камерах. В качестве подвижной фазы используется смесь раство¬
рителей, указанная в методике. Подвижная фаза А применяется
для разделения веществ основного и нейтрального характера на
хроматографических пластинках А, в которые запрессовываются
диски, полученные после концентрирования органической фазы
из экстракционных пробирок ТохьТиЬе А. Соответственно под¬
вижная фаза В служит для разделения веществ кислого и некото¬
рых веществ нейтрального характера на хроматографических пла¬
стинках В, в которые запрессовываются диски, полученные после
концентрирования органической фазы из экстракционных проби¬
рок ТохьТиЬе В.Состав подвижной фазы А: этилацетат — метанол — вода
(87:3:1’5)- .Состав подвижной фазы В: дихлорметан этилацетат (60.40).В каждую подвижную фазу добавляют необходимое количество
30% аммиака, которое указано на этикетках склянок для хранения
хроматографических пластинок.
Лыппвяния контролируют, отслеживая пере-
Проиессхроматографирив пластинки оставляют в камерахмешение розовых пятен мар еров не поднимутся на высотудо тех пор, пока розовые г После заверШения процесса9.5 см (пР”близитеЛаЬНп°пястинк„ высушивают до удаления запаха
^„™е?1Тс™орителей и аммиака и начинают процесс детек-™ Детектирование производится последовательным проявлением
*ши реагентами и просмотром пластинки в УФ-облаети(рис. 14 и 15, см. цв. вклейку).Таким образом, система Toxi-Lab АВ является универсальнойсистемой для ТСХ-скрининга токсикологически значимых ве¬
ществ, так как позволяет определить в пробе вещества кислого,основного и нейтрального характера.Наряду с системой Toxi-Lab АВ существуют системы для опре¬
деления либо только веществ основного и нейтрального характера
(Toxi-Lab A-Plus), либо для определения только веществ кислого и
нейтрального характера (Toxi-Lab В-Plus).Системы Toxi-Lab A-Plus и Toxi-Lab B-Plus рассчитаны на ла¬
боратории с высоким пробопотоком. Каждый комплект включает
одиннадцатиканальные пластины — 10 каналов для проб и канал
для стандарта (в системе Toxi-Lab АВ вухканальные пластинки),
а также соответствующий набор стандартных дисков, систем для
пробоподготовки и референсных образцов для анализа токсиколо¬
гически значимых соединений.^гуКаННабИН0ИЛЫ невозможно выявить с помощью общей
ТСХ'скрининга to образцов мочи необходим щелочнойфГ Где~ГнФИР!ВаНИе Т0В0ДЯТ в Частнь,х подвижных
лиза биопроб на эту rnvn специ^ичными Реагентами), для ана-
необходима иная мегоГи™ У то*сикологически значимых веществ
ния (подробнее см. ниже) ПР° °П0ДГ0Т0ВКИ и хРоматографирова-ком^ектаТя^праеТелеГиТ1бОТаНа с“стема Toxi-Lab ТНС II -
Рагидроканнабиноевой кислот^?1™ метаболитов Д9-тет-
ЛЛпТ рассчитан на 100 определений^ ™ УР°Вне ~15 нг/мл- Ком*То>' р'тнс в^юТа^Гть лГоеСТВа П° сисгеме скрининга• I пароли,(шелочной,кстРа«сция/кониентрирование.
Применение ТСХ-скрининга...• Перенос пробы на хроматографическую пластинку.• Хроматографирование.• Детектирование.На лапе гидролиза мочу помещают в одноразовые тестовые
пробирки, промаркированные в соответствии с номером образца
(рис. 16, см. цв. вклейку), одновременно готовят контрольный об¬
разец (добавляют 200 мкл концентрата Toxi-Control ТНС к 6 мл
деионизированной воды или мочи, не содержащей наркотиков),
далее в каждую пробирку добавляют реагент для щелочного гидро¬
лиза, а через некоторое время пробы подкисляют ледяной уксус¬
ной кислотой. После подкисления образец мочи пропускают через
экстракционный картридж SPEC-C18-I (рис. 16, см. цв. вклейку).
Картридж содержит экстракционный диск с химически модифи¬
цированным сорбентом на основе силикагеля, который удерживает
метаболиты каннабиноидов в процессе, известном как твердофаз¬
ная экстракция. Диск высушивают и помещают на хроматографи¬
ческую пластинку (рис. 16, см. цв. вклейку).В качестве подвижной фазы для хроматографирования исполь¬
зуется система растворителей: н-гептан — ацетон — ледяная ук¬
сусная кислота (50:50:1). Пластинку вынимают из камеры, когда
цветной маркер пройдет 4 см (2-3 мин). Пластинку высушивают
до исчезновения запаха органических растворителей.Детектирование проводится в 3 этапа.1. Реагент Toxi-Dip ТНС-1 — раствор прочного синего ББ (Fast
Blue ВВ).2. Реагент Toxi-Dip ТНС-2 — диэтиламин. Под воздействием
диэтиламина каннабиноиды на стандартном и контрольном кана¬
лах должны немедленно образовывать красно-розовые пятна (при¬
близительно 5 мм) на желтом фоне. Через 10—15 с желтый фон
исчезает, и красное пятно становится более интенсивным. Все¬
ми остальными окрашенными зонами, которые не совпадают со
стандартом и контрольным образцом, на этой стадии можно пре¬
небречь.3. Реагент НС1 — пары соляной кислоты. Красно-розовые пятна
каннабиноидов, помещенные в пары НС1, переходят в пурпурные
на бледно-желтом фоне (рис. 17, см. цв. вклейку).Если пурпурное пятно появляется на канале пробы, но не со¬
впадает с пятнами стандартного и контрольного образца, получен¬
ными на стадии 1, проба считается отрицательной и обозначав к я
как «не детектирующаяся».
Глава 684 «ьикании опиатов и увеличения по-Для более надежной ^ПОДГОТОВКИ необходимо вклю-рога» обнаружения на этапе пр в (так как соед„„ения"„ть стадию кислотного гидрол конъюг„рованных метабо-этой группы выводятся с мочойлитов). опиатов рекомендуется использовать на-Поэтому ДЛЯ анализа ОЛИ ^ ПОЗВоляюшую определять вГче^н.^лис,си'ЭХ“аНЬХр°жёния неизвестного вещества по системескрининга^Toxi-Lab Ltd Opiate включает следующие этапы.• Гидролиз (кислотный).• Экстракцию.• Элюирование.• Концентрирование.• Перенос диска на хроматографическую пластинку.• Хроматографическое разделение.• Детектирование.Гидролиз производится в специальных тестовых пробирках,
предварительно пронумерованных в соответствии с номером про¬
бы (рис. 18, см. цв. вклейку). В качестве гидролизующего реагента
используют ледяную уксусную кислоту. После кислотного гидро¬
лиза образец мочи пропускают через экстракционный картридж
SPEC Ltd MP3 (рис. 18, см. цв. вклейку), в который добавляют
промывочный буфер (метанол - ледяная уксусная кислота 100:0,6),
и аспирируют. Затем каждый картридж дважды промывают элюи-
руюшим реагентом (этилацетат — 30% аммиак 98:2). Далее необхо¬
димое количество чистых дисков Toxi-Discs Ltd Blank О помещаютваКуГUт WТрЭаЦHfc'HНЫе алюминиевые колпачки, в которые перели-
высохнст к аК ТОЛЬК0 диски в концентрационных колпачках
Mici ^тыlaiumm зкстРакционный колпачок добавляют по 100высыхан^дисков^Пои "еремешива|от и упаривают до полногоиглы диски пе-пластинку. ^ніачков на хроматографическуюВ качестве подвижной rtv
пользуется система раствооитеприТ* хроматогРаФирования ис-дихлормсган — метанол (95:5).
Применение ТСХ-скрининга... 85Перед началом хроматографирования (не ранее, чем за 15 с)
к подвижной фазе добавляют необходимое количество 30% раство¬
ра аммиака, указанное на упаковке с хроматографическими пла¬
стинками. Пластинку вынимают, когда цветной маркер (розового
ивета) пройдет фронт 10 см (около 10 мин) на канале стандарта.
Пластинку высушивают до полного удаления запаха органических
растворителей.Для детектирования используют реактив Toxi-Dip А-2 — кон¬
центрированную серную кислоту (95-98%). На рис. 19 представле¬
на пластинка Toxi-Lab Ltd Opiate после детектирования.В настоящее время система Toxi-Lab благодаря своей надежно¬
сти, экспрессности и чувствительности находит все большее при¬
менение в следующих областях:• Судебной экспертизе — для определения наркотических ве¬
ществ и их метаболитов в пробах посмертной мочи и мочи
живых людей, а также определения следов наркотических
веществ в пробах питьевой воды.• Ветеринарии — для определения допинга в моче лошадей на
лошадиных бегах.• Медицине скорой помощи — для экстренного определения
причин интоксикации для правильного выбора последующе¬
го лечения.
Глава 7ТСХ-СКРИНИНГ ОТДЕЛЬНЫХ ГРУПП
ТОКСИЧЕСКИХ ВЕЩЕСТВгпмитета по контролю наркоти-^КК№Мкеес^.еХюшие наркотики подразделяют по ха-
ков (мккш, все J c 3 больших класса: седативные,рактеру их воздействия на UHL на j wnстимуляторы и галлюциногены.1 Г*Р1ЯТИЯНЫ6.. Собственно наркотики (опиаты и опиоиды): героин, мор¬
фин. опий, синтетические и полусинтетические вещества с
морфиноподобным типом действия.• Седативно-снотворные препараты: барбитураты, бензодиа-
зепины.2. Стимуляторы.• Кокаин.• Стимуляторы амфетаминового ряда (САР).3. Галлюциногены.• ЛСД, мескалин, псилоцин, псилоцибин.• Препараты конопли.Наибольшую опасность представляют наркотики, относящиеся
к опийной группе.7.1. НАРКОТИЧЕСКИЕ АНАЛЬГЕТИКИНазвание «опиаты* обозначает группу физиологически актив-
~ алкал°ид°в, выделяемых из опия, затвердевшего
И3 Надрезов' вделанных на зрелых
девает на воздухе °г/^ apaverютпУегит). Млечный сок затвер-ставляющий собой aZlyucZZT’ ^ °ПИЙ'Шреи’ прея‘шаров и других вешестн « ' липияов' смол, нж~алкаломлов (10-20* обшей массыГнГ^ солеРжаший болсе 50ы). Наиболее важные алкалоиды
ТСХ-скрининг отдельных групп токсических веществ 87опия — морфин, кодеин, папаверин и тебаин. Два первых алка¬
лоида применяются в качестве ЛС, но в то же время используются
и как наркотические средства. Папаверин наркотическими свой¬
ствами не обладает, но широко распространен как лекарство. Те¬
баин эго в основном сырье для получения других лекарственных
препаратов.Кроме названных веществ, в состав опия входит большое число
минорных алкалоидов, содержащихся в количествах порядка де¬
сятых долей процента. Среди них наиболее значимы следующие
соединения: нарцеин, неопин (А-кодеин), протопин, порфирок-
син, криптопин, псевдоморфин, лауданозин.Путем относительно несложной химической обработки извле¬
каемого из опия морфина получают ряд его производных, среди
которых имеются соединения с очень высокой наркотической ак¬
тивностью. Эти вещества называют полусинтетическими опиата¬
ми. Наиболее известным и распространенным среди них является
3,6-диацетилморфин — героин.Существует также целый ряд веществ, отличающихся по струк¬
туре молекул от морфина, но оказывающих сходное, более силь¬
ное физиологическое действие. Эти вещества принято называть
опиоидами. К ним относятся фенциклидин, метадон, фентанил,
кетамин, бупренорфин.Препараты опийной группы используют в медицине в качестве
анальгетиков для купирования болевых ощущений, подавления
кашля и лечения диареи.Особое влияние наркотических анальгетиков на ЦНС, вызы¬
вающее эйфорию, и развивающаяся толерантность (ослабление
действия при повторном применении, требующее все больших доз
для достижения эффекта) приводят к возникновению физической
и психической зависимости у потребителей. Данной особенностью
опиатов объясняются ограниченность их медицинского примене¬
ния и мотивы немедицинского использования.7.1.1. Наркотические анальгетики —
производные морфинаПроизводные алкалоидов опия в соответствии с их химическим
строением подразделяют на четыре группы (табл. 6).
Глава 788алкалоидов опия » соответствии с „х строс-ниемГруппаСодержаниеСтруктура молекулыПредставителиМорфина3-23Фенантреновый циклМорфинКодеинТебаинПсевдоморфинНеопинПапаверина0,5-1,3БензилизохинолиновыйциклПапаверинЛауданозинНаркотина2-8фталилизохино-
линовый циклНаркотинНарцеинПротопинаМалоеАзециновый циклПротопинКриптопинКзк видно из табл. 6, морфин является основным алкалоидом
опия, поэтому он служит стандартом для оценки других алкалои¬
дов.К началу XIX в. опий повсеместно продавался легально в виде
различных лекарственных препаратов, а выделенный в 1803 г. не¬
мецким аптекарем Сетюрнером из опия морфин еще долгое время
использовался в качестве основного обезболивающего средства.
Синтезировать морфин удалось лишь в 1952 г. после установле¬
ния его химической структуры. Однако из-за высокой стоимости
синтеза морфин и сейчас продолжают получать из опия. В 1874 г.
английским химиком Райтом был синтезирован из морфина геро¬
ин, а уже в 1898 г. фармацевтическая компания «Bayer» начала его
производство в качестве ЛС.Параллельно шло немедицинское «освоение» опия, морфина и
героина; от приема внутрь и курения люди переходили к инъекци-
поп«*п1^гв1 ,К0Ниу *** началу XX в. стали очевидны тяжелейшие
не lern I Jü™ УМ0Т ЛСНИЯ опиатов- Юридическое преследование
Г„ГГ“еНИЯ И пр0дажи опиатов в США привело к
с подпольным пигг?К>ЛЬЗ°ВаНИЯ героина в 1924 г. С тех пор борьба
к'ванных странах росграиением ,еР°ина ведется во всех цивили-Аистралия, Китай Т(тел(1ьоли^слями 01|ия являются Индия,Пакистан Иран},'(Ого Boc.rwL ^ияТл. H<’C1.OKa «Афганистан,,ия (Лаос, Ьирма), Мексика.
ТСХ-скрининг отдельных групп токсических веществ 89Только четверть всего объема производимого опия используется
для медицинских целей.И настоящее время в РФ опий и героин запрещены к произ¬
воле! ну, распространению и употреблению и внесены в Список I
Перечня. Некоторые опиаты, например морфин, кодеин, относят
к разрешенным J1C, используемым под определенным контролем
при соответствующих медицинских показаниях (Список И).Криминальные торговцы морфин разного качества называют
Morph, White, Stuff, Miss, Emma. В тайных «лабораториях» путем
ацетилирования морфина уксусным ангидридом получают героин.
Содержание героина в уличных препаратах, именуемых Smack,
Junk, Horse, «Феррари», «белая смерть», варьирует в достаточно ши¬
роких пределах (от 20 до 80-90%). Наиболее частыми примесями
являются 3- и 6-моноацетилморфин (1 — 15%) — продукты непол¬
ного ацетилирования морфина или частичного гидролиза диаце-
тилморфина, ацетилкодеин (2-5%) и др. В зависимости от количе¬
ства производственных примесей или пищевых красителей героин
может различаться по агрегатному состоянию (высокодисперсный
порошок или гранулы) и цвету (от белого до темно-коричневого).
Особо чистый вид героина в виде белой пудры называют «белым
китайцем». Героин, приготовленный непосредственно из опия без
сколько-нибудь серьезной очистки, распространяют под назва¬
ниями «черная смола» (Black Таг), «мексиканский коричневый»
(Mexican Brown), «грязь» (Mud).В табл. 7 представлены производные морфинана, которые, со¬
гласно Федеральному закону «О наркотических средствах и психо¬
тропных веществах», являются НС Списка 1 и Списка II Перечня.Таблица 7. Список наркотических средств, относящихся к группе морфи¬
нанаНаркотическое средствоСписок ПеречияАцетилкодеин1Ацетилированный опий1Ацстилгидрокодеин 1 Ацеторфин 1Бсгпил морфин _1 ероин (диацетилморфин) 1
тгх-скрининг отдельных групп токсических веществ 9}Окончание modi 7Наркотическое средствоСписок ПеречняГраиеморфанI^ — — ’ ' "■ ""1 Тебакон1 !фолъкодннI {Экстракт маковой сатомы (концентрат маковойсоломы)1 ЭторфннБупренорфнн»-Дигкдрокоденни 1 Кодеин11 1 Кодеина фосфатIIКодеин N-окись11МорфинИМорфина гидрохлоридIIМорфина сульфатIIМорфидонг11ОмнопонИ 1ТебаинИЭтидморфин <11 — JЭли морфина гидрохлорид11Структура некоторых опиатов представлена на рис. 20 и в табл 8
1*1R,—О'20. Общая формула опиатовсн.
92Глава 7Таблица 8. Стр^Р^ ОНВеществоИ,МорфинКпприНОНОСН3онООГероинIIн,с—с—Н3С Сфизико-химические свойстваПо своим физико-химическим свойствам опиаты представляют
собой типичные аминоспирты. В химико-аналитической практи¬
ке приходится встречаться с представителями этой группы как в
форме оснований, так и в форме солей (гидрохлоридов, сульфатов,
ацетатов, фосфатов). Все опиаты растворимы в воде и в этиловом
спирте. Они плавятся (чаще всего с разложением) при 200—208 °С
и способны возгоняться, образуя аэрозоли, что и определяет воз¬
можность их введения в организм путем курения.У основных опиатов весьма характерные УФ- и ИК-спектры,
обусловливающие четкие сигналы в масс-спектрах.Токсикокинетика и биотрансформацияПри внутривенном введении морфина максимальный фармако¬
логический эффект достигается через несколько минут, при под¬
кожном и внутримышечном введении — через 15 мин. В дальней¬
шем содержание морфина в крови резко падает. Морфин выводится
из организма в основном с мочой в течение 36~48 ч (табл. 9).
До 80 % морфина может выделяться в течение первых 8— 10 ч после
введения, причем только менее 3 % — в неизмененном виде. Через
72 80 ч в моче удается определить лишь следы морфина (даже
при исследовании наиболее чувствительными методами). Однако
определенная часть наркотика фиксируется в волосах и ногтях.ри приеме морфина внутрь в моче обнаруживаются в основ-
ГЛ1глюкУР°нов°й и серной кислотами, причем
больше и °В ^моРФИН~3~ и морфин-6-глюкурониды) значительно
нГ монп1?ЛЬфаТНЫХ к°™тов. К тому же из двух изомер-
свойствами нЛГяНИДОВ моРФин-3-глюкуронид наркотическими
тельную активнпгтк т"7, * м°Рфин- 6 -глюкуронид проявляет значи-количества норморфинХеГ13)°бНаРУЖИВа,ОТМ НеЗНаЧИТеЛЬНЫ<'
ТСХ-скрининготДельных групп токсических веществТаблица 9. Фармакокинетические параметры некоторых опиатовВеществорКаТУ2, чВыведение
в неизме¬
ненном виде,%Ус1,
л/кгСвязывание
с белками плазмы
крови, %Морфин8,09,92-333-520-35Кодеин8,23-46-82,5-3,57-25Диацетилморфин7,60,2-0,50Н.д.Н.д.Примечание. Н.д. — нет данных.Конъюгаты с глюкуроновой кислотойНОНОНОо^-сн.Н3СС0'II
оо6-МАММорфини-нНорморфиннс,с\^.Н3ССО^^^
^ ГероинКонъюгаты с глюкуроновой кислотой
Схема 13. Метаболизм опиатов
Глава 7начальный период выведения кодеина в моче обнаруживают-п начальпшп ———г-. .ся в основном конъюгаты кодеина, спустя 20-40 ч их заменяютконъюгаты морфина.Героин при внутривенном введении быстро (3 7 мин) мета-
болизируется до 6-моноацетилморфина (6-МАМ), который далее
медленно деацетилируется до морфина в течение нескольких ча¬
сов (см. схем)' 13). Вследствие высокой липидной растворимости
героин (в отличие от морфина) легко преодолевает гематоэнцефа-
лический барьер, что и обусловливает его мощное наркотическое
действие. Далее морфин относительно медленно превращается в
глюкурониды. Для доказательства употребления героина необхо¬
димо идентифицировать его метаболит 6-МАМ (табл. 10), так как
другие опиаты его не образуют.Таблица 10. Содержание основных метаболитов морфина, героина и ко-
леина в моче (в процентах от введенной дозы)МорфинМорфинГероинКодеинI ^°РФиН-3-ГЛЮКУРОНИЛ2-125-70,1-1| Морфин-б-глюкуронид
і Морфин-З-сульфат
| Кодеин Л(одсин-6-)люкурони.-,: Лиаііетилморфцц65-750,3-3550-6014-165-131-25-Ю5-1732-46^•фморфин0,2-І,7!Н<5>морфин К(^Г0,5-1,5
3-5
ТСХ-скрининг отдельных групп токсических веществ 95При внутривенном введении героина образующийся 6-МАМ
регистрируется в плазме крови в течение 1—2 ч, а свободный мор¬
фин 10—12 ч. В моче лиц, употребляющих героин, 6-МАМ ре¬
гистрируется в течение 6—8 ч, а морфин — 48 ч и более. В случае
смерти потерпевших от передозировки героина диацетилморфин,
как правило, не идентифицируется в крови, но обнаруживается в
моче в концентрациях до 90 нг/мл.Таким образом, токсикокинетические данные позволяют сде¬
лать следующие выводы. Присутствие в моче исключительно мор¬
фина и его конъюгатов указывает на употребление чистого препа¬
рата морфина или на злоупотребление героином одним или двумя
днями ранее. Наличие в моче морфина, кодеина и их конъюгатов
одновременно может свидетельствовать о медицинском использо¬
вании препаратов кодеина (в этом случае концентрация морфина
ниже, чем кодеина). Употребление кодеина в терапевтических до¬
зах дает возможность обнаруживать свободный морфин или коде¬
ин только в течение нескольких часов после введения наркотика в
организм, хотя другие метаболиты могут быть обнаружены спустя2—3 дня после введения.Следует иметь в виду: если люди едят пищу, содержащую мак,
в их моче наряду с морфином и кодеином обнаруживается теба-
ин, что служит отличительным признаком пищевого поступления
данных веществ в организм. При использовании лекарственных
препаратов, содержащих морфин или кодеин, а также при неле¬
гальном приеме указанных наркотиков тебаин в моче и в плазме
крови не обнаруживается.Химико-токсикологический анализУчитывая, что в неизмененном виде опиаты выделяются с мо¬
чой в очень небольших количествах, перед проведением предва¬
рительного ТСХ-скрининга мочу подвергают солянокислому или
ферментативному гидролизу для разрушения конъюгатов, повы¬
шая концентрацию нативных соединений. Кислотный гидролиз
более надежен и эффективен, чем ферментативный, но приводит
к разрушению 6-МАМ, поэтому при идентификации 6-МАМ (для
установления факта употребления героина) гидролиз проб мочи
не проводят. Опиаты экстрагируют из мочи смесью хлороформ
изопропанол (9:1) при pH = 9 10 по схеме 1, из крови — по схе¬
мам 2 и 3, из органов и тканей — по схемам 4—6 и 9.
этичного атома азота практически у всех опиатов
Шлвчие тоетачно юзыожиьм использование для их идеи.
„ ИХ метаболитов да |Х рсакт11В0„: реактива Драгендорфатификации обшеал в0[х) цвета|, подкисленного раствора
(морфин - пят Р _ пятн0 гемно-синего цвета), реактива
Машкина (морфин - пятно фиолетового цвета), реактива фреде,
каетта Мекке реактива Мунье. Морфин, как целевой метаболит
опиатов, можно обнаружить на хроматограмме частными реатен-
та ми. Так, за счет наличия в молекуле морфина фенольного ги¬
дроксила обработка хроматограммы раствором железа (III) хлори¬
да приводит к появлению пятна сине-фиолетового цвета. Реакцию
образования арил метанового красителя с реактивом Марки осу¬
ществляют на хроматограмме капельно (пятно сине-фиолетового
цвета). Окраска пятен опиатов и их метаболитов при обработке
хроматограммы различными реагентами отражена в табл. 11.Папаверин имеет собственную голубоватую флуоресценцию в
УФ-свете при Я = 365 нм.При проведении ТСХ-скрининга на опиаты в качестве подвиж¬
ной фазы используют следующие системы растворителей.Общие• ТА: метанол - 25% раствор аммиака (100:1,5).• ТВ: циклогексан - толуол - диэтиламин (75:15:10).• ТС: хлороформ — метанол (9:1).• ТЕ; этилаиетат - этанол - 25% раствор аммиака (85-10 5)• TL: ацетон. '• ТАЕ: метанол.• ТАР: метанол - //-бутанол (60:40).• TAJ: хлороформ - этанол (90:10).(Ш0:20)РОФ°РМ "иклогексан ~ ледяная уксусная кислота
4acniHh * ^ РМ ML ГаНОЛ ~ пР°пионовая кислота (72:18:10).Бен^"6™^; ™этиламин (5:4:1).4) ЬлуГ^:~_- «тиламин (7;2.,}6» метанол - аммиака (20:20:3:|)-
f20 40:1 2) ’ ~ Ш раствор аммиака - „ода
ТСХ-скрининг отдельных групп токсических веществ97Таблица 11. Окрашивание опиатов и их метаболитов различными реакти¬
вамиВеществоРеактив МаркиРеактивМаиделинаРеактивДраге ндорфаРеактив МеккеРеактив МуиьеРеактивФредеПодкисленныййодплатинатГероин1Н.д.15836 -> 114Морфин6 —» 111159 -> 231 -> И2Кодеин181573856-МАМ1Н.д.157313Н.д.Ацетилкодеин1Н.д.15736 -> 14Н.д.Тебаин441510310Н.д.Папаверин61215739Н.д.Коды окрашивания: 1 — фиолетовое; 2 — синее; 3 — оранжевое; 4 — фио-
летово-коричневое; 5 — фиолетово-серое; 6 — пурпурное; 7 — темно¬
зеленое; 8 — светло-зеленое; 9 — зеленое; 10 — коричневое; 11 — серое;12 — коричнево-зеленое; 13 — желто-зеленое; 14 — палевое; 15 —
кирпично-красное; Н.д. — нет данных.В табл. 12, 13 приведены значения Rf некоторых опиатов и их
метаболитов на пластинках с силикагелем G («Merck», Германия).На рис. 21 (см. цв. вклейку) представлена хроматографическая
пластинка Toxi-Lab типа А (система Toxi-Lab AB) на различных
стадиях детектирования (см. главу 6). Для хроматографирования
использовался экстракт из мочи лица, употреблявшего героин.Таблица 12. Значения И,, некоторых опиатов и их метаболитов в обших
системах растворителейВеществоСистемы растворителей, R,ТАТВТСТЕTLТАЕTAFTAJТАКTALГероин0,470,150,380,65Н.д.0,26Нл.Нд.Ил.Нл.Морфин0,370,000,120,370,010,180,230,000.000,15Кодеин0,330,060,180,350,030,200,220,100,000,266-МАМ0,460,060,190,44Н.д.Н.д.Н.д.олз0,020.5. ]
ВешествоТАТВТССиетеТЕмы расТІ0.12гворитеТАЕ0,26кгп чТАР0.25ТАЛ0,32ТАК0,05ТАЬ0,61Адети-1 ко¬0.440.230,43деинТебаинПапаверин0,450.610.240.080,370.651)А5~~0.69 1о^оГ-0,470,230,740,320,740,220,660,110,080,760,93Примечание. Н.д. — нет данных.Таблица 13. Значения Я,, некоторых опиатов и их метаболитов в частнь
пагтнппителейСистемы растворителей, И,Вещество123456ГероинН.д.Н.д.0,650,49Н.д.Н.д.Морфин0,080,080,030,020,370,46Кодеин0.360,150,380,250,620,666-МАМН.д.Н.д.0,460,47Н.д.Н.д.Алетил кодеинН.д.Н.д.0,690,75Н.д.Н.д.Тебаин0,640,380,690,45Н.д.Н.д.Папаверин0,670,770,730,86Н.д.Н.д.Примечание. Н.Д.— нет данных.Для подтверждающего исследования используют ГХ, ВЭЖХ,
ГХ-МС, спектральные методы.7.1.2. Наркотические анальгетики — производные
фенилпиперидинаВ течение многих десятков лет исследователями ведутся поиски
новых анальгетиков, у которых отсутствуют недостатки, характер¬
ные для морфина: развитие толерантности и пристрастия. Подоб¬
ные изыскания, связанные прежде всего с модификацией структуры
морфина, привели к внедрению в медицинскую практику таких ле¬
карственных препаратов, как пентазоцин, нубаин и др.Однако Гххпее активные вещества, в основе которых — фенил-
пи периди новая система, присутствующая в структуре того же мор¬
фина получены синтетическим путем. Синтезированы ЛС, при¬
ТСХ-скрининг отдельных групп токсических веществ99меняющиеся в нашей стране и за рубежом: меперидин, промедол,п рос идол и др.Дальнейшие поиски препаратов с аналыезируюшим действием
привели к синтезу фентанила и его структурных аналогов, по ак¬
тивности во много раз превышающих морфин.В настоящее время производные фенилпиперидина можно
условно разделить на 3 группы:• тримеперидин (промедол) и его структурные аналоги;• фентанил и его производные;• фенциклидин и его структурные аналоги.7.1.2.1. Наркотические средства группы промедола
и его структурных аналоговОсновными представителями этой группы наркотических
анальгетиков являются тримеперидин (промедол), феноперидин и
петидин (демерол, меперидин). Их структурные формулы пред¬
ставлены на рис. 22.н5с2ПетидинФеноперидинТримеперидинРис. 22. Структурные формулы петидина, феноперидина и тримеиеридиш
100)0 ____ В 1931 г. впервые синтезирован петидин. Это первый опиоид,
полученный синтетическим путем, но по своей активности и ПО
продолжительности действия он примерно в 8 раз уступает морфи¬
ну. Чуть позднее синтезирован промедол, оказавшийся в несколь¬
ко раз сильнее петидина. Существует несколько стерео-изомеров
промедола, но фармакологической активностью обладает толькоу-изомер. ппп.имр тпимепепилиняомедола, ПЧ у-изомер.В табл. 14 представлены НС — производные тримеперидина,
которые, согласно Федеральному закону «О наркотических сред¬
ствах и психотропных веществах», являются НС Списка I и Спи¬
ска II Перечня.Таблица 14. Список ни - НССписок ПеречняТримеперидин (промедол) IIПросидолIIПетидинIПетидина промежуточный продукт А
(4-циано-1 -метил-4-фенилпиперидин)IМетил фенидат1ПипрадролIIДифеноксилатIIРеазек (дифеноксилата гидрохлорид)IIПиритрамидIIАнилэридинIКетобемидонIФеноперидинIПиминодинIМППП (1-метил-4-фенил-4-пиперидинол
пропионат, эфир)IБезитрамилIФизико-химические свойстваПетидин-основание — маслянистая жидкость, которая медленно
кристаллизуется. Петидина гидрохлорид — белый кристаллический
порошок, Тм - 186-1% °С. Хорошо растворим в воде, растворим в
хлороформе, этаноле 1:20, практически нерастворим в эфире.
ТСХ-скрининг отдельных групп токсических веществ101Промедол — белый кристаллический порошок. Хорошо раство¬
рим в воде и хлороформе, растворим в этаноле, практически не¬
растворим в эфире. Водные растворы имеют pH = 4,5—6.Феноперидин — белый кристаллический порошок с Тпл = 200—
202 °С. Растворим в воде 1:50, в 90% спирте 1:10 и 1:3 — в хлоро¬
форме.У основных представителей этой группы характерные УФ- и
ИК-спектры и соответственно характерные сигналы в масс-спектрах.Токсикокинетика и биотрансформацияПосле орального применения петидина максимум концентра¬
ции в крови наблюдается спустя 1,3 ч. Около 7% введенной дозы
выводится с мочой в неизмененном виде вместе с 17% норпе-
тидина (схема 14). При кислых значениях pH мочи эти показа-СН3ПртитшнНорпетидинСН3Норпетидиновая кислотаПетидиновая кислотаКонъюгацияСхема 14. Метаболизм петидина
Глава 7и 27% соответственно; при щелочных
тели изменяются до ^а®, соответственно. Петидиновая и нор-
значениях - 0,6% и 3,6» ^ и 23% соответственно,
петидиновая кислоты выв д аКТИВНОСТИ петидина и обычно
Норпетидин обладает по^ разовых приемов, но мо-в плазме крови не обн^е^0Гпотреблении. Норпетидин в 2-3
жет выявляться при хро янтиконвульсантную активность,раза более токсичени пр^ незначительные количества Ы-оксид-,
В моче присутству илметаболитов петидина.^МеЕизм промедола и метаболизм феноперидина аналогич¬
ны мегаболиму петидина - происходит М-деадкилирование и об-
риоважте соответствующих кислот, которые выводятся с мочой в
конъютированном виде. Неизмененного вещества выходит менее5% от введенной дозы.В табл. 15 приведены основные фармакокинетические параме¬
тры производных группы тримеперидина.ірия г ;Таблица 15. Фармакокинетические параметры структурных аналогов
медолапро-ВеществорКаТ/г, ЧВыведение
в неизме¬
ненном виде,%ул,л/кгСвязывание
с белками
плазмы крови,%Тримеперидин(промедол)8,061,5-33-5Н.д.50Петидин8,582-573,7-4,264Феноперидин8,280,8-1,23-5Н.д.Н.д.Примечание. Н.д. — нет данных.
Химико-токсикологический анализ ііхм»VI папалгмПромедол и его структурные аналоги изолируются из биосред
органическими растворителями (хлорированными и алифатиче-('т!!.|У1ЛЄВОЛОРОДаіМИ^ При = ^ по СХеме 1 (из МОЧИ итканей) П° СХЄМаМ и ^из КР°ВИ)> схемам 4-6 и 9 (из органов иныхн:Го:0Г1и;г ГиГмазту пр°мед°ла и ег° ^труктур-пользование лпо ? метаболитов делает возможным ис-Для опрыскивания ^ленти^икации °бщеалкалоидных реактивов.подкисленного йодплатината* пе*™ ° у(І"ехом применять раствор, реакіивьі Марки и Драгендорфа.
тсх-скрининг отдельных групп токсических веществ 103Окраска пятен петидина, промедола и феноперидина при обра¬
ботке хроматофаммы различными реагентами отражена в табл. 16.Таблица 16. Окрашивание пятен петидина, промедола и феноперидинаразличными реактивамиВеществоРеакгмв МаркиРеактив ДрагенлорфаокрашиваниеПетилинКоричневоеКирпично-красноеПромедолКрасно-фиолетовоеКирпично-красноеФеноперилинСлабо-коричневоеКирпично-красноеПри проведении ТСХ-скрининга на промедол и его структурные
аналоги в качестве подвижной фазы используют следующие систе¬
мы растворителей.Общие• ТА: метанол — 25% раствор аммиака (100:1,5).• ТВ: циклогексан - толуол — диэтиламин (75:15:10).• ТС: хлороформ - метанол (9:1).• ТЕ: этилацетат — метанол — 25% раствор аммиака (85:10:5).• ТЬ: ацетон.• ТАЕ: метанол.• ТАР: метанол — и-бутанол (60:40).Для хроматографирования также возможно применение систе¬
мы гексан — ацетон — 25 % раствор аммиака (10:10:1).В табл. 17 приведены значения Л, промедола и его структурных
аналогов на пластинках с силикагелем в («Мегск», Германия).Таблица 17. Значения промедола, петидина, феноперидинаВеществоСистемы растворителей, Я,ТАТВТСТЕтъТАЕТАЕПромедол0,580,410,41Н.д.0,17Нл.Н.д.Петидин0,520,370,340,600,110,340,40Феноперидин0,710,260,640,760,580,700,82Примечание. Н.д. — нет данных.
в качестве подтверждающих методов при анализе промедола
и его структурных аналогов возможно использование ПС, ВЭЖХ,
ГХ/МС, спектральных методов.7.1.2.2. Наркотические средства группы фентанилаВ настоящее время применяется более 12 гомологов фента¬
нила. Так, эффективность действия фентанила, суфентанила,3-метилфентанила превосходит таковую у морфина в 200, 2000,
6000 раз соответственно.Фентанил (рис. 23) в клинической практике используется с 1963
г. для местной анестезии, снятия острых болей при инфаркте мио¬
карда, стенокардии. На черном рынке появился с 1991 г. как за¬
менитель героина. Его эффективная доза составляет 0,025—0,1 мг,
продолжительность действия — не более 30 мин. Минимальная ле¬
тальная доза — 2 мг. Алфентанил отличается еще более коротким
действием — 10 мин.ФентанилНзС^43-метил фентанилсн,ОСН3АлфентанилРис. 23. Структурные формулы фентанила, 3-метилфентанила и апфен-ганила
ТСХ-скрининг отдельных групп токсических веществ105Аналог фентанила - 3-метилфентанил (см. рис. 23) в медицине
не применяется. Янляется одним из наиболее активных аналогов
фентанила, встречающихся в незаконном обороте. Представляет со¬
бой смесь цис- и транс-изомеров в соотношении 80:20. Цис-изомер
в 6000 раї активнее морфина, транс-мюмср по активности пример¬
но равен героину. Минимальная летальная доза — 250 мкг.В іабл. 18 приведены структурные аналоги фентанила, вклю¬
ченные в Перечень.I аблица 18. Наркотические средства, относящиеся к группе фентанилаНаркотическое средствоСписок ПеречняАльфа-мет ил фентанилIАл ьфа-метилтиофентанилIАцетил-альфа-метилфентанилIБета-гид рокси-3-метнл фентанил1Бета-гид роксифентанил1З-МетилтиофентанилI3- МетилфентанилIя-флуорофентанилIТиофентанил1Ал фентанилИСуфентанилIIФентанилIIФизико-химические свойстваФентанил и 3-метилфентанил — кристаллические порошки с
Тпл = 83—85 °С у фентанила и 135—140 °С — у алфентанила. Плохо
растворимы в воде, хорошо — в органических растворителях, за ис¬
ключением эфира. Окраска образцов фентанила может изменяться
от чисто белой («Persian White») до беловатой или светло-бежевой
(«China White», «Synthetic Heroin»), светло- и темно-коричневой
(«Mexican Brown»). Коричневый цвет придает лактоза, которая при
нагревании подвергается карамелизации. Текстура образцов также
различна — от легкого и тонкого порошка до более рыхлою, по¬
хожего на сухое молоко.Фентанил и его структурные аналоги имеют характерные мак¬
симумы поглощения в УФ- и ИК-спектрах.
Глава 7106Токсикокинетика ибиотрансформац^ растворяются в липидах, поэ-Производные фситанил ^» меМбранный барьер и эффек-ТОМулегхо и быстро прео^ют^ Рведення После внугри_тмвно всасываются при бысТпо исчезают из кровяного русла
венной инъекции ^“^“^изма. Более 90% дозы фента-
и распределяются п течение 5 мин. Быстрое распределе-ннла выводится из - ^ авной причиной короткой продолжитель¬
на Латвия и чрезвычайно низкой (субнанограммовые уровни)
концентрации в крови и других биожидкостях.Фен^ил примерно на 80% связан с белками плазмы крови
(табл. 19). Время его полужизни в плазме (Т1/2), по данным различ¬
ных исследователей, изменяется в широких пределах: от 1,5 до 6 ч.
Такие вариации, вероятно, связаны с внугрипеченочнои рецирку¬
ляцией, возрастом и физиологическим статусом пациента.Таблица 19. Фармакокинетические параметры структурных аналогов про-ГВеществорКаТа, чВыведение
в неизме¬
ненном
виде, %Уё,л/кгСвязывание
с белками
плазмы
крови, %Фентанил9,11,5-610-202-480Алфентанил6,51,515-200,5-190Суфентанил8,22,515-20285Все аналоги фентанила быстро метаболизируются по идентич¬
ному механизму, образуя около 10 более полярных метаболитов,
фармакологически неактивных (схема 15). Основное направле¬
ние процесса - отщепление фенилалкильного заместителя азо¬
та пиперидина: >4-деалкилирование до норметаболитов. Менее
значительные направления включают гидроксилирование пипе-
сРиИ—0 кольца или пропиониловой боковой цепи. Гидрок-
глюкуронидов МСТа °ЛИ7Ы далее конъюгируются с образованием8 ч и около°70-80^ ТГ0И Л03Ы (^)ентанила выводится в первые
92-98% — и вилр° Г 1<ИЫ ^лиминиРУется за 72 ч, при этомФаКТ ТЙКЖе об^—ает
ТСХ-скрининг отдельных групп токсических веществСхема 15. Метаболизм фентанилаКонцентрации фентанила в моче при медицинском и нелегаль¬
ном применении значительно не различаются и, как правило, не
выходят за предел 100 нг/мл.Химико-токсикологический анализИз-за довольно низких уровней фентанила и его структурных
аналогов в биологических объектах, использование для анализа
метода ТСХ нецелесообразно, хотя этот метод можно использовать
для обнаружения фентанила в вещественных доказательствах, из
которых фентанил и его аналоги изолируются по схемам 10 и 11.Хроматографирование проводят в следующих системах раство¬
рителей.
Глава 7108Общие паствор аммиака (100:1,5).. ТА: метанол - 25* |ЖЯ»ор_ ламин (75:15:10).• ТВ: циклогексан толуо. ТС: хлороформ - метанол, , ор аммиака (85:10:5).• ТЕ: этилаиетат - метанол• TL: ацетон.• ТАЕ: метанол. /£л.лп\• ТАР: метанол - «-буганол (6<). )■• TAJ- хлороформ — этанол (90.1U).!^Zp<xj»PM - циклогексан - ледяная уксусная кислота. ТА^мороформ - метанол - пропионовая кислота
(72:18:10).Частные• Гексан - толуол - триэтиламин (15:10:2).В табл. 20 приведены значения R,. фентанила и алфентанила на
пластинках с силикагелем G («Merck», Германия).Таблица 20. Значения Rf фентанила и алфентанилаВеществоСистемы растворителей, RfТАТВТСТЕTLТАЕTAFTAJТАКTALФентанил0,700,430,740,780,580,700,770,590,080,84АлфентанилН.д.0,16Н.д.0,72Н.д.0,78Н.д.Н.д.Н.д.Н.д.Примечание. Н.д. — нет данных.Для детектирования пластинку обрабатывают подкисленным
раствором йодплатината.Подтверждение присутствия фентанила и его структурных ана-
ГХ/МС ВЭЛоТ* ВОЗМОЖНО при применении методов ИФА, ГХ,7.1.2.3. Наркотические средства группы фенциклидинапре^ра!И;ыГим^СР) ВПервые синтезирован в 1956 г. в США как
пу|» внедрен в ЛГИНОГО наркоза и под наименованием «Бег-
угнетает сердечно ж“скую практи,сУ- В отличие от опиатов он не
РДЄІНО СОСУДИСТОЙ деятельности или дыхания. Однако
ТСХ-скрининг отдельных групп токсических веществ 109в процессе клинического применения были выявлены токсические
побочные эффекты, такие как постоперационные галлюцинации,
возбуждение, ментальные расстройства и депрессивные состояния.
Поэтому, несмотря на хорошие терапевтические свойства, препарат
исключили из клинической практики. После непродолжительного
применения в ветеринарии в 1960-е годы под названием «Semylan»
с 1979 г. производство лекарства остановили, PCP изъяли из обра¬
щения и запретили для использования. В настоящее время фенци¬
клидин и его структурные аналоги находятся под международным
контролем и включены в Списки 1 и II Перечня (табл. 21).Таблица 21. Наркотические средства, относящиеся к группе фенцикли¬
динаНаркотическое средствоАббревиатураСписок ПеречняФенциклидинPCPIТеноциклидинTCPIРолициклидинРСРу1ЭтициклидинPCEIКетаминКЕТИКетамина гидрохлорид
(калипсол, кеталар)КЕТIIТилИДИН-IIКетамин структурно и фармакологически близок к фенцикли¬
дину (рис. 24). Используется в медицине с 1972 г. в качестве сред¬
ства для наркоза и обезболивания при операциях. Широко приме-Рис. 24. Структурные формулы фенциклидина и кетамина
курения, или ингаляций через нос. Жидкие формы для внутривен¬
ного введения встречаются реже.Основной способ потребления PCP курение (около 73%).
Для него обычно используют смеси PCP с растительным материа¬
лом: марихуаной, табаком, листьями мяты. Для орального введе¬
ния или вдыхания также часто используются смеси PCP с другими
наркотическими средствами: кокаином, опиатами, амфетаминами.
Зарегистрировано более 30 содержащих фенциклидин смесей, на¬
ходящихся в нелегальном обороте.Физико-химические свойства
Фенциклидин основание — белый кристаллический порошок с
Тщ, = 46-46,5 °С. Растворим в хлороформе, эфире, бензоле. Фен¬
циклидина гидрохлорид — белый кристаллический порошок с
Тпл ~ 233—235 С. Растворим 1:6 в воде, 1:7 — в этаноле и 1:2 — в
хлороформе, очень плохо растворим в эфире.Кетамина гидрохлорид — белый кристаллический порошок с
„ , - 2 263 С. Растворим 1:4 в воде, 1:14 — в этаноле и Гб — в
—иГ° РЗСТВОРИМ В ХЛ0Р°Ф0Рме> практически нераство-Токсикокинетика и биотрансформацияНачало действия фенциклидина при
ильном приеме уличной дозы 1-3 мг на
ТСХ-скриминг отдельных групп токсических веществ111кровообращения, что отражено в большой величине объема рас¬
пределения. 6,2 л/кг (габл. 22). Биодоступность PCP составляет
50—90%. Однако при курении фенциклидина из-за пиролитиче¬
ского расщепления до I -фенил-циклогексена, ацегилпиперидина
и пиперидина в организм вводится только около 30% исходной
дозы.Кетамин, как и фенциклидин, отличается большим сродством к
липидам и в основном накапливается в головном мозге и печени,
но в отличие от PCP имеет меньшую продолжительность действия,около 2 ч.Таблица 22. Фармакокинетические параметры фенциклидина и кетаминаВеществорКаТ/2, чВыведение
в неизме¬
ненном виде,%Vd,л/кгСвязывание
с белками
плазмы крови,%Фенциклидин9,17-4830-505,3-7,565Кетамин7,53-42420-50Основные направления метаболизма фенциклидина в орга¬
низме человека — окислительное гидроксилирование циклогек¬
санового и пиперидинового колец с образованием биологически
активных соединений (схема 16). Гидроксилированные метабо¬
литы далее конъюгируются с образованием глюкуронидов и суль¬
фатов.Фенциклидин обнаруживается в моче после приема разовой
дозы в сроки до 7 дней, при хроническом употреблении до 20дней.Кегамин выводится из организма преимущественно с мочой,
причем около 90% введенной дозы — в течение 72 ч. Примерно 2%
выходит в неизмененном виде, а остальное — в виде фармакологи¬
чески активных метаболитов: норкетамина — около 2% и дегидро-
оксиноркетамина — около 16% (схема 17). Метаболиты выводятся
с мочой в основном в виде конъюгатов с глюкуроновой кислотой
(около 80%).
1 -(1 -фенилциклогексил)-4-гидроксшшперидин5-(1-фенилциклогексиламино)-
валериановая кислотаНО4-фенил-4-пиперидиноциклогексанолСхема 16. Метаболизм фенциклидинаКонъюгацияФенциклидинОШ-СН,КетаминЫН-аоынаНоркетаминIДс I хдроокс И моркг Гй м мнГидроксилирование и конъюгаиия
Схема 17. Метаболизм кетам и на
тографическую пластинкуРис. 6. Вид оборудования для денситометрии
Pec. 13. Ten:-Lar \t 31-71T г—> іш ■ ас*хірд і - зв^гэвшшнвк *а®-
згчи : зжреезв&ъъавж іясіі г дроуазас^іфиг і итча адосянге і
Рис. 14. Вид пластинок А на каждом этапе детектирования (на примере
циталогірама (А) и его метаболита (а): 1 - реактив А-1 — пары 37% рас¬
твора формальдегида; реактив А-2 - концентрированная серная кислота
(95-98%); 2 - реактив Н,0 - вода; 3 - просмотр пластинки в УФ-свете;
4 - реактив А-3 - модифицированный реактив Драгендорфа
ис. 15. Вид пластинок В на каждом этапе детектирования: I - реактив
раствор дифенилкарбазона в дихлорметане; реактив В-2 - раствор
нитрата серебра; реактив В-3 - раствор сульфата ргути; 2 - просмотр
пластинки в УФ-свеге
в гРис. 16. Тохі-ЬаЬ ТНС: тестовые пробирки (а), экстракционный картридж
(б), вакуумный экстрактор (в), запрессовывание диска в хроматографиче¬
скую пластинку (г)
ТНС IIРис. 17. Вид хроматографической пластинки Тохі-І-аЬ-ТНС после детек-
гирования: Б — контрольный образец; пробы І, 2, 3, 5, 7, 8, 10 — положи¬
тельныеРис. 18. Toxi-Lab Ltd Opiate: тестовые пробирки (а); экстракционный ка-
тридж (б); вакуумный экстрактор (в); перенос чистых дисков в концен¬
трационные колпачки (г); перенос элюента (д); запрессовывание диска в
хроматографическую пластинку (е)
МОРФИН НОРМОРФИНР»С. 19. Вил хроматографической пластинки Toxi-Lab Ltd Opiate после
детектирования
Рис. 27. Вид хроматографической пластинки Toxi-Lab типа А на различи.\а — метаболиты флуразепамаb — метаболит флуразепама (N-1-дезалкнл-З-підроксифлуразепам)
(Политы фснотиаэина— і:1іА А* А * *КГ 0.00-0.45Рис. 35. Вид хроматографической пластинки Тохі-ЬаЬ типа А на различ¬
ных стадиях детектирования
Рис. 39. Вил хроматографической пластинки ТохьЬаЬ типа А на различных стадиях детектирован
Рис. 40. Внешний вид растения СаппаЫх зай\'а /..ТНС11ВИН * I * > < I * г I » иРис. 42. Вид хроматографической пластинки ТохМаЬ-ТНС после детек¬
тирования
Рис. 47. Внешний вид кактуса Lophophora williamsii
А — эфедрин / псевдоэфедринRi 0.14
д \'СГи<Ч"ит мотамфстамина (амфетамин)
' мстмфетамин♦*♦I*ИГ 0.32Рис. 53. Вид хроматографической пластинки ТохьЬаЬ типа А на различных стадиях цитированияРис. 54. Вид хроматографической пластинки Кш-ЬаЬ типа А на различных сгапых к кчащ
- . Фармацевтическая хи;Под ред. А.П. АрзамасцеваОтличительные особенности640 с., 2008 г.• Учебное пособие разработано кочвом кафедры фармацевтическом химии
ММА им. И М Сеченова и соответству¬
ет примерной программе по дисциплине]
фармацевтическая химия для специаль-|
мости — «Фармация*. Рассмотрены
методы оценки качества лекарственна
средств, в том числе современные ф»1
ю>-химичес*ие (ИК- и
ЯМР-спектроскопия. хромат
методы - ФЭЖХ. ГЖХ. ТСХ и др.),
же особенности количественного
применительно к индивидуальным
твам и лекарственным формам,
современные тенденции в развитж^^^Н
цеб-п»чес*.ого анал*<за.® предназначено студентам фарчин^^Н|Н
О« вузов и фармацевтических1^а*ультетов,
аслирвнтзм >• ’ровизорак»
ТСХ-скрининг отдельных групп токсических веществ 113Химико- токсикологический анализДля выделения фенциклидина из биожидкостей возможно при¬
менение метода прямой экстракции различными органическими
растворителями в щелочной среде (pH = 9—10) по схеме 1. из кро¬
ви по схемам 2 и 3, по схемам 4—6 и 9 — из органов и тканей.Так как фенциклидин выводится с мочой в виде конъюгиро¬
ванных метаболитов, для его изолирования из чючи целесообразно
применять кислотный или ферментативный гидролиз с последую¬
щей жидко-жидкостной экстракцией.Изолирование кетамина из биологического материала прово¬
дится аналогично таковому фенциклидина.Метод ТСХ рекомендован главным образом для исследования
вещественных доказательств.Хроматографирование проводят в следующих системах раство¬
рителей.Общие• ТА: метанол - 25Яг раствор аммиака (100:1,5).• ТВ: циклогексан - толуол - диэтиламин (75:15:10).• ТС: хлороформ — метанол (9:1).• ТЕ. этил ацетат - метанол - 25% раствор аммиака (85:10:5).• ТАЕ: метанол.• ТА1_: хлороформ — метанол — пропионовая кислота (~2:18:10).В табл. 23 приведены значения II, фенциклидина и кетамина на
пластинках с силикагелем С («Мегск*. Германия).Для детектирования пластинку обрабатывают подкисленным
раствором йод платината либо реактивом Эрлиха (фенциклидиндает красную окраску пятна).Таблица 23. Значения И, фенциклидина и кетамина1 ВеществоСистемы растворителей. КТАТВТСТЕТАЕТАЬ1 Фенциклидин0.5*)0,730350.!у40.230.48[ Кетам и н0,630.3?0,63о.*>0.680,4?Для подтверждения присутствия фенциклидина и кетамина в
биообъектах возможно применение методов ИФА. ГХ. ГХМС .
ВЭЖХ.
Глава 7ГГГнаокотические анальгетики - производные
^ химических структур7 1.3.1. Метадон' метадон (6-димггаламино4,4-дифенид-3-гешанон) яааяется син-
„ГГ Гидом и. отличаясь от морфина по химическом слрук-
тетическим с III фИС 25), оказывает на человекаво многом сходное действие.Метадон синтезирован во время
Второй мировой войны как заме¬
нитель морфина, причем в отличие
от морфина, метадон эффективен
при оральном применении.Метадон имеет высокое срод¬
ство к р-опиоидным рецепторам и
с 1963 г. применялся (а в некоторых
странах до сих пор применяется)
Рис. 25. Структурная формула Д™ лечения больных с опиатной
метадона зависимостью. Чтобы предупре¬дить развитие физической зависи¬
мости, дозировку при лечении поддерживают на одном уровне или
непрерывно >'меньшают. Кроме того, метадон дает значительный
наркотический эффект, ведущий к злоупотреблениям, и его рас¬
пределение должно тщательно контролироваться. В нашей стране
метадон запрещен для использования в клинической практике.Лекарственное средство метадон является рацематом, т.е. смесью
1:1 двух оптических изомеров (1-метадона и 1-метадона. 1-метадон
фармакологически активен, (1-метадон в 25—50 раз менее активен.
У оптических изомеров метадона различные фармакокинетические
и фармакодинамические параметры. Данные, имеющиеся в лите¬
ратуре. относятся в основном к рацемическому метадону.В Перечень включено 16 производных метадона, приведенныхв табл. 24.Метадон вводят внутривенно, внутримышечно, подкожно и
принимают внутрь (орально). Обычная оральная доза составляет
и 1 1 10 1еток- Но при заместительной терапии доза мо-
«ма уГГЬ МГ В сутки; Метадон, нелегально продаваемыйисточник;» *лошадка*» СМПеь), обычно добывают из легальногоисточника - больниц и клиник.
ТСХ-скрининг отдельных групп токсических веществ115физико-химические свойства_ Метадон-основание - белый кристаллический порошок с
пл • аств°рим в воде (48,5 мг/л). Метадона гидрюхлорид —бесцветные кристаллы или белый кристаллический порошок с
Тпя " С Растворимость (1г/100 мл): спирт — 8, хлороформ — 3,
практически нерастворим в воде и глицерине.Таблица 24. Наркотические средства, относящиеся к группе метадонаНаркотическое средствоСписок ПеречняАльфа-метадол1Альфа-ацетилметадол1АцетилметадолIБета-метадол1Бета-ацетилметадол1ДипипанонIИзометадонIМетадонIб-метадонI1-метадонIМетадона промежуточный продукт
(4-циано-2-диметиламино-4.4-дифенилбутан)IНорациметадолIНорметадон1НорпипанонIФенадонIДекстропропоксифен11Токсикокинетика и биотрансформацияПик концентрации в плазме достигается спустя 2—4 ч после
орального приема и 0,5— 1 ч при внутримышечном введении. Время
полувыведения из плазмы крови при кислых значениях pH мочи
около 20 ч, при щелочных — около 40 ч у одного и того же человека
(табл. 25). Метадон довольно быстро выходит из системы крово¬
обращения и локализуется в тканях: печени, легких, почках, селе¬
зенке. Небольшая часть достигает мозга.
116 Таблица 25. Фармакокинетические параметры метадона
ї I Выведение |~~ВеществоМетадонрКа9,0ТА, чВыведение
В неизмененномвиде, %30-35\Л,л/кгСвязывание с
белками плазмы
крови, %4-587Метаболизм метадона происходит главным образом в пече¬
ни. Основные направления биотрансформации (схема 18): от¬
щепление метильной группы от атома азота с последующей
циклизацией до основного метаболита ЭДДП (2-этилиден-1,5-
диметил-3,3-дифенилпирролидин) и 2-го метаболита ЭМДП
(2-этил-5-метил-3,3-дифенил-1 -пирролин). В результате других
процессов метаболизма образуются еще по крайней мере 9 ме¬
таболитов. Наиболее важные из таких процессов: гидроксилиро-
вание метадона и обоих метаболитов в пара-положение фениль-
тгх-скрининг отдельных групп токсических веществ 117ного кольца, окисление метадона до метадола с последующим
N -деметилированием. Окислительное дезалкилирование метадона
ведет к образованию кислотного метаболита, который далее под¬
вергается циклизации в кето-проиэводное пирролидина. Неконъю-
тированные соединения составляют около 75% выведенной дозы.
Основной метаболит метадона - ЭДЦП - образует два оптиче¬
ских изомера. сЬЭДДП и 1-ЭДДП. Все основные метаболиты фар¬
макологически неактивны.Химико-токсикологический анализМетадон изолируется из биожидкостей методом прямой экс¬
тракции иди после кислотного гидролиза органическими раство¬
рителями из щелочной среды (pH = 9— 10) по схеме 1. Для выделе¬
ния метадона из внутренних органов предпочтение следует отдать
методу Стаса-Отто (см. схему 4) с экстракцией препарата хлоро¬
формом при pH = 9-10.При проведении ТСХ-скрининга на метадон хроматографиро¬
вание проводят в следующих системах растворителей.Общие• ТА: метанол — 25% раствор аммиака (100:1,5).• ТВ: циклогексан — толуол - диэтиламин (75:15:10).• ТС: хлороформ — метанол (9:1).• ТЕ: этилацетат — метанол — 25% раствор аммиака (85:10:5).• ТЬ: ацетон.• ТАЕ: метанол.• ТАР: метанол — н-бутанол (60:40).• ТАЗ: хлороформ — этанол (90:10).• ТАК: хлороформ - циклогексан - ледяная уксусная кислота
(40:40:20).• ТАЬ: хлороформ — метанол — пропионовая кислота (72.18.10).
В табл. 26 приведены значения Яг метадона на пластинках ссиликагелем О («Мегск», Германия).Таблица 26. Значения Я. метадонаСистемы растворителей, Я,ВеществоТАТВТСТЕтьТАЕТАРТАЗТАКТАЬМетадон0,480,590,200,770,270,160,600,080,000,45
118 — л тястннках осуществляется реактивом
Детекция метадона н ^ переходящее в голубое окрашн-Манделина. который д* с __ ^^.оранжевое окрашивание;
вание: ярко-малиновое окрашивание.с ЗН:",,ЗС на Метадон
возможно использование ГХ. ГХ/МС.7 1 3.2. Трамадол
' Тромадса. рациональное название: 2-(еЧ(диметиламино)ме-
тилМ-кИ3-метоксифенил)-ииклогексан-1 -(а)-ол (рис. 26). пред-
стааляет собой синтетический опиоид со свойствами агониста-
антапжиста, анальгетик центрального действия средней силы,
подобный кодеину. Широко и эффективно применяется для обе¬
зболивания в терапии и хирургии.Лекарственное средство представляет собой гидрохлорид осно¬
вания трамадола и производится несколькими фармацевтическими
компаниями под разными названиями, но самым распространен¬
ным в РФ является «Трамал*. изготовляемый по лицензии фирмы
«Грюненталь* (Германия), в которой был синтезирован, исследо¬
ван и выпушен на мировой рынок препарат для терапевтического
использования.На ранних стадиях изучения трамадола. когда был установлен
опноиднын механизм анальгетического действия (трамадол обла¬
дает селективностью к ц-опиондным рецепторам), его относили
к опиондным анальгетикам. Однако дальнейшие исследования и
опыт применения в клинической практике показали низкий уровень
побочных эффектов опиатного типа (к которым относятся прежде
всего ос ;золение функции дыхания, проявления эйфории, разви¬
тие лекарственной зависимости и толерантности) при приеме тера¬
певтических ООО мг) и даже трехкратных терапевтических (300 мг)ОН
ТСХ-скрининг отдельных групп токсических веществ 119доз трамадола по сравнению с таковыми при употреблении экви¬
валентных по анальгетическому действию доз морфина. Специ¬
альные эксперименты показали: трамадол не продуцирует морфи-
ноподобныи эффект, имеет низкую наркотическую активность и
не может служить заменой морфина при опийной наркомании для
лиц с низкими или умеренными уровнями опиатной зависимости
(по крайней мере в дозах до 300 мг). В отношении ингибирования
р-опиоидного связывания кодеин в 10 раз, метадон — в 1000 раз,
а морфин — в 6000 раз активнее трамадола. Для продуцирования
морфиноподобных эффектов у толерантных субъектов требуются
более высокие дозы последнего.По принятой в настоящее время классификации трамадол не
есть наркотик, но отнесен к сильнодействующим средствам. Тра¬
мадол также не включен в списки Перечня.Тем не менее существуют указания на немедицинское исполь¬
зование трамадола лицами с опиатной зависимостью в дозах, зна¬
чительно превышающих терапевтические. В подобном случае на¬
блюдается большое количество побочных эффектов, в том числе и
развитие пристрастия к препарату.Трамадш может существовать в виде двух стереоизомеров:1) 2-(г)-[(диметнламино)метил]-1-(еНЗ-метокснфенилЫшклогек-
сан-1-(а)-ол: 2) 2-( д)-[(диметиламино)метил]-1-(*)-( 3-метоксифе-
нил)-циклогексан-1-(в)-од. Они отличаются взаимным расположе¬
нием заместителей, каждый из которых обладает различной аналь-
гетической активностью. Стереоизомер 1 имеет большую фарма¬
кологическую активность, что объясняется соответствием этой
стру ктуры пространственной структуре морфина. В лекарственных
препаратах содержание менее активного стереоиэомера обычно не
превышает 1-2%. В свою очередь каждый из стереоизомеров пред¬
ставляет собой рацемическую (1:1) смесь двух оптических изоме¬
ров: с1- и 1- энантиомеров.Физико-химические свойстваТрамадол — белый или белый со слегка желтоватым оттенком
кристаллический порошок с Тг! = 179—182 С. Легко растворим в
воде, этаноле, хлороформе, практически нерастворим в эфире.Токсикокинетикв и биотрансформацияАнальгезирутощее действие при оральном приеме терапевт нче
ской дозы 100 мг трамадола наступает через 30—60 мин, при вну-
120Глава 7три вен ном введении - через 15-30 мин и сохраняется 5-6 ч. При
повторных приемах трамадола наблюдается кумулирование самого
трамадола и его метаболитов в плазме.Кинетика выведения описывается двухкамерной моделью
с временем «полужизни» в плазме Т/г = 4,3-6,7 ч (табл. 27)
для самого трамадола и около 9 ч для активного метаболита
(О-деметилированного трамадола).Таблица 27. Фармакокинетические параметры трамадолаВеществорКаТ/з, чВыведение
в неизме¬
ненном виде,%V«!, л/кгСвязывание
с белками
плазмы крови,%Трамадол9,44,3-6,727-332,6-2,975Трамадол интенсивно метаболизируется в организме и образует
несколько метаболитов в результате последовательного отщепле¬
ния метильной группы от атомов кислорода и азота и присоеди¬
нения гидроксильного радикала к циклогексановому фрагменту
(схема 19).Метаболиты, содержащие гидроксильную группу, далее конъю¬
гируются (вторая фаза метаболизма).Наиболее важным метаболитом является продукт О-деме-
тилирования трамадола. Он активен фармакологически, отличает¬
ся большим сродством к опиатным рецепторам, чем сам трамадол,
и превосходит его по анальгетической активности в 2—4 раза.Более 90% введенной в организм дозы трамадола экскретирует-
ся почками в течение 3 дней: в виде неизмененного трамадола —
около 30%, в виде свободного и связанного О-деметилтрамадола —
около 20%, в виде нортрамадола — около 17% и около 20% в виде
свободного и конъюгированного М,0-деметилнортрамадола и дру¬
гих метаболитов.Химико- токсикологический анализТрамадол и; биожидкостей изолируется методом прямой экс-
'фиром или хлороформом при pH = 8-9
И .бишкш.-й! "0СЛС кислотного ™ДРОЛИэа при pH = 10-11.
мГГхЙ,:Г~ Стаса—Отто (см. схему 4).ил н с 1слу|01ли* ''ИМК на 'Памалол хроматографирование прово-
в следующих системах растворителей: I
N.О-МТБ ПТР (АГТ)МТБ — метаболит; ПТР - продукт термического разложения.
Схема 19. Биотрансформация трамадолаТ( X ( криниш отдельных групп токсических веществ
ОСНзО-МТБснгКГ
снСНг^СN-N15ОН-ТРМмГ'сн,СН,-^СН3СН,ТрамадолМ,Ы,0-МТБОбщие• ТЕ: этилацетат — метанол - 25% раствор аммиака (85:10:5).• ТАЕ: метанол.Частные• Д и эти л оный эфир ~ этанол — 25% раствор аммиака (6:3:1)В табл. 28 приведены значения ^ трамадола на пластинках с
силикагелем О («Мегск», Германия).
I пае«) 7122Таблица 28. ЗначВешссшо'Грамаддя( МС 11‘МЫ ряс 1 ворм ГС1СИ. 11ТАЕ0,78 „0.30 „ьыи^гких пластинок осуществляется вПроявление М>ома1хпраф ^ МандслиНа, а та1СЖе 0,5% рас-уф-свете Реакт‘,,а .„‘тоне. При проявлении пластинок реак-
твором нингидри * е „бработки последним обмыть'^По^^а^^нных Р^твором нинги-дрина. наблюдается сине-голубое окрашивание.На рис. 27 (см. цв. вклейку) представлена хроматографическая
пластинка ТохМаЬ типа А (система ТохьЬаЬ АВ) на различных
стадиях детектирования (см. главу 6). Для хроматографирования
использовался экстракт из мочи лица, употреблявшего 1рамадол.В качестве подтверждающих методов при анализе на метадон
возможно использование ГХ, ГХ/МС, ВЭЖХ.7.2. ПРОИЗВОДНЫЕ
1,4-БЕНЗОДИАЗЕПИНАИз числа транквилизаторов бензодиазепины остаются непре¬
взойденными по активности, спектру терапевтического действия
и малой токсичности. Более того, с каждым годом перечень бен-
зодиазепинов, обладающих физиологической активностью, непре¬
рывно расширяется как за счет производных 1,4-бензодиазепина
(правильнее бензо-1,4-диазепина), так и благодаря синтезу и вне¬
дрению в клиническую практику производных 1,5-бензодиазепина
и ДЗ-бензодиазепина.Бензодиазепины представляют собой обширную группу биоло-
более Г«паК:ИВ11ЫХ соединени^’ в составе которой насчитывается
веществ о*:ГН01ШНИЙ лекаРственнь,х препаратов и более 2000
в1! ГЩИХ седативными свойствамижит 5-арил- М-бенч^ ‘1роизвод/НЬ1Х бензодиазегжна (рис. 28) ле-кольцо соединено аЗСПИН ^табл- 29), в котором бензольноении 5 обычно имеется ГЖСМИИ 6' 7 с •'^-диазепином. В положе-
имеется фенильный радикал.
ТСХ скрининг отдельных групп токсических веществ 123Рис. 28. Общая формула крон людных 1,4-бем юдиазсиина(аблица 29. Общая формула и структура некоторых наиболее распростра¬
ненных бензолиазепинов1,4-бен юдиа к’иинк,К,Оксазспам (нозспам)ИоннаДиазепам (сибазон)сн,ниаНитразеламиннN0,ФсназеламинС1ВгГидазепам? 1
—СН2—с— гчн— N42нВтМедазепам (мезапам)*сн,ннаХлордиазепоксид (хлозспнд)**нннС!* Вместо С=0 в положении 2 стоит группа СН „** Вместо С=0 в положении 2 стоит группа С-Г^ЬНСН,), в положении 4стоит N->0. двойная связь М(=СГНа 8-й специальной сессии в феврале 1984 года Комиссия по
наркотическим средствам ООН решила поставить под междуна¬
родный контроль 33 производных бензодиазепина.Физико-химические свойстваПроизводные 1,4-бензодиазепина — белые кристаллические по¬
рошки (за исключением нитразепама, отличающегося наличием в
молекуле нитрогруппы и имеющего светло-желту ю окраску с зеле¬
новатым оттенком).
Глава 7124 '„ I 4 бензодиазепина являются слабыми основани-
Производныс 1.4 |,4-6ензодиазепина — это амфо-ями. 1,2-дигидрокси Р леамидНой группы). Производныелить, (за счет наличия в м^екулеамид и щелочной1,4-бензодиазепина склонны к гидрат >СР Основания производных 1,4-бензодиазепина плохо растворимы
, в^е в то же время они достаточно хорошо растворяются в ор-Га А^ияп^дных 1,4-бензодиазепина в УФ-области из-меняется в зависимости от pH их растворов.. В кислой среде изменение происходит за счет протонирова¬
ния атома азота положения 1 или 4.• В щелочной среде возможно изменение хромофорной систе¬
мы (увеличение сопряжения за счет лактим-лактамной тау¬
томерии азометиновой связи в положении 1, 2).Это свойство лежит в основе идентификации соединений дан¬
ной группы по электронным спектрам поглощения.В УФ-спектра\ производных 1,4-бензодиазепина наблюдаются
три максимума поглощения при 200-215, 220-240 и 290—330 нм.
Две первые полосы отвечают возбуждению ароматических хромо¬
форов, а третью полосу связывают с колебательным возбуждением
азометиновой группы.Токсикокинетика и биотрансформацияВ организме человека бензодиазепины накапливаются в жиро¬
вых тканях и из них выделяются в кровь. Это обеспечивает полу-
период их выведения от 8 до 40 ч (табл. 30). Из организма до 60%
бензодиазепинов выделяется с мочой, часто в форме конъюгатов
с глюкуроновой кислотой, а остальное — через пищеварительный
тракт.Метаболические трансформации бензодиазепинов включают
дечетилирование метилам и ногрупп, окисление по углероду и об¬
разование конъюгатов с глюкуроновой кислотой по гидроксиль-
ФУ те ) с г Нитрогруппа в нитразепаме восстанавливается
КИ^::ТГ,11Ы' П0 которой далее образуется амид с уксусной
“ В,,ро,1ессс метаб°лических превращений те-бромный аналог Г гГ™ В положении 1 и превращается в
Лейне при атоме с ПИДа |,рсменно может протекать окис-
^^нием -куронида по
ТСХ-скрининг отдельных групп токсических веществ125с6н5Оксазепам
(3-гид роксипроизводное)Схема 20. Метаболизм диазепама,мсн3с6н5С6Н5ХлозепидС6Н5Дезметил хлордиазепоксидОксазепамС*н5Демокселам
Схема 21. Мегаболи $м хиозепила
126Глава 7Схема 22. Метаболизм оксазепама<■«. И. Метабол ти
ТСХ-скрининг отдельных групп токсических веществ 127Схема 24. Метаболизм гидазепама
128 Таблица 30. Фармакокинетические параметры некоторых бензодиазепи-нов1,4-бензодиазепинОксазепам (нозспам)рКа1.7; И.6Т/2, ч4-1520—96Выведение
в неизме¬
ненном виде,%Менее 10
Менее 10V«!,мг/кг0,5-20,7Связывание
с белками
плазмы
крови, %9598Диазепам (сибазон)НитразепамХлордиазепоксид3,4
3,2; Ю,5
4,621-285-3015Менее 1.2,1
0,3-0,68596Химико-токсикологический анализВ зависимости от преобладания кислотных или основных
свойств у представителей производных 1,4-бензодиазепина, они
могут обнаруживаться либо в экстрактах из кислого извлечения,
либо в экстрактах из щелочного извлечения. Вследствие этого в
каждом отдельном случае для их изолирования из биологических
объектов возможно применение какой-либо из схем, указанных
выше.Учитывая особенности химического строения производных1,4-бензодиазепина, для их идентификации используют реакции
окисления, гидролитического расщепления с последующим опре¬
делением продуктов гидролиза, а также осадочные реактивы.ТСХ-скрининг производных 1,4-бензодиазепина проводят:• по нативным соединениям;• по продуктам гидролиза — аминобензофенонам.Для обнаружения нативных соединений и их метаболитов на хро-
маклрафической пластинке используют реактивы, дающие различ¬
ные окраски.1еактив Драгендорфа образует оранжевые или желто¬
оранжевые пятна.• РРЫКмя^тмЫ*!гЙ0ДП1аТИНат обРазУет пятна темного цвета." Дггхроматографической
нитрированной соляной ™ Ш1асгинки раствором кон-
соляной кислоты (кислотный гидролиз).
ТСХ-скрининг отдельных групп токсических веществ129• Термостатирование закрытой покровным стеклом пластинки
в течение 30 мин при 120 °С (образование аминобензофено-нов).. Проведение реакции Братгона-Маршала (реакция образова¬
ния азокрасителя).При кислотном гидролизе разрыву подвергаются амидная и
азометиновая группы 1,4-бензодиазепинов (рис. 29). Продуктами
гидролиза являются аминобензофеноны и аминохинолоны.ОIIно—С я,\/Ан^ нРис. 29. Кислотный гидролиз производных 1,4-бензодиазепинаМетод ТСХ предусматривает не только разделение аминобензо-
фенонов, но и их обнаружение по собственной окраске и харак¬
терной флуоресценции в УФ-свете.В табл. 31 приведены основные бензодиазепины и соответству¬
ющие им продукты кислотного гидролиза — аминобензофеноны.После проведения кислотного гидролиза и охлаждения пластин¬
ки ее опрыскивают 0,1% раствором №М02, через 2 мин — 0,5%
раствором сульфамата аммония и в заключение 0,1% раствором
М-а-нафтилэтилендиамина (рис. 30).Таблица 31. Основные бензодиазепины и соответствующие им аминобензо¬
феноныБензодиазепиныПродукт гидролиза — аминобензофеноннаименованиесокращенное на іваниеОксазепам2-амино-5-хлорбензофенонАХ БХлордиазепокеид2-амино-5-хлорбензофенонАХБДиазепам2-метиламино-5-хлорбензофенонМАХ Б
Глава 7Окончание табл. „?/БензодиазепиныПродукт пиролиза ами
наименованиенобензофенон
сокращенное название
АН БНитразепамФеназепам2-амино-5-бром-2'-хлорбензо-фенонАБХБМедазепам?-м«тиламино-5-хлорбензофснонМАХ БСульфамат аммониясн,-сн2-сн2Азо краситель
(красно-фиолетового цвета)Р*С. 30. Проведение реакции Браттона-Маршалачест^пТ^ Скрини,нге на производные 1,4-бензодиазепина в ка-
рителей вижнои Фазы используют следующие системы раство-Общие• ТН ГН°Л ~ 25% раств°Р «ммиака (100:1,5).• ТС: хлорХтм” ' Т°ЛУ°Л ~ ди зтиламин (75:15:10).хлоР°форм - метанол (90:10).
ТСХ-скрининг отдельных групп токсических веществ131• TD: хлороформ - ацетон (80:20).• ТЕ. этилацетат — метанол — 25% раствор аммиака (85:10:5).• TF: этилацетат.• TL: ацетон.• ТАЕ: метанол.• TAF: метанол - м-бутанол (60:40).• TAJ: хлороформ - этанол (90:10).• ТАК. хлороформ — циклогексан — ледяная уксусная кислота(40:40:20).• TAL: хлороформ — метанол — пропионовая кислота (72:18:10).Частные• Гексан - метанол - ацетон (15:3:1).• Бензол - ацетон - этанол (8:1:1).• Гексан - ацетон (3:2).• Бензол — изопропанол — 25% раствор аммиака (85:15:1)В табл. 32 приведены значения R, некоторых бензодиазепинов
на пластинках с силикагелем G («Merck*, Германия).Таблица 32. Значения Rf некоторых бензодиазепиновВеществоСистемы растворителей, R,ТАТВТСTDТЕTFTLТАЕТАКTAJТАКTALДиазепам0,750,270,730,580,760,490,590,820,850,670,480.%Ннтразе-пам0,670,410,740,540,780,400,620,790,830.700,120,95Оксазепам0,560,000,400.220,450,350.510,820,910.470,470,89Хлозепид0,620,020,500,100520,110,220,760,770.480,020.79Медазепам0,680,000,360,350,640.460.550,900,860,530,520,92В табл. 33 приведены значения и цвета окраски пятен некото¬
рых бензофенонов после проведения реакции Браттона-Маршала
на пластинках с силикагелем в («Мегск», Германия) в системе ТВ.Таблица 33. Значения Я,, и окраска пятен некоторых бензофеноновБензофенонОкраскаАХ Б0,27ФиолетовыйМАХ Б0,52ЖелтоватыйАН Б0,15Красно-фиолетовый
Глава 7132представлена хроматографическая
На рис. 31А (система Тох(-1.аЬ АВ) на различных
пластинка Тох1-ьао ш для хроматографированиястадиях Детектирования (см^ употреблявшего флуразе_использовался экстрактпам , „п оКГ,ейку) представлена хроматографическаяпластинка Тох -иЬ типа В (система Тсш-ЬаЬ АВ) на различных
стадиях детектирования. Для хроматографирования использовался
=,*„ мочи лииа, употреблявшего хдордиазепоксид.В качестве методов, подтверждающих результаты ТСХ скри¬
нинга производных 1,4-бензодиазепина, используют методы
УФ-спектрофотометрии, ИК-спектрометрии, а с целью количе¬
ственного определения — ГХ, ВЭЖХ, ГХ/МС.7.3. ПРОИЗВОДНЫЕ ФЕНОТИАЗИНАНейролептические средства (нейролептики) составляют одну
из главных групп современных психотропных препаратов. Лекар¬
ственные средства группы фенотиазина используются как анти¬
депрессанты, транквилизаторы, антигистаминные и антиангиналь-ные средства.История создания первого антипсихотического средства —
хлорпромазина — начинается с 30-х годов XX в., когда среди про¬
изводных фенотиазина искали антигистаминные препараты. Об¬
наружилось, что ряд из них оказывает также нейролептическое и
антипсихотическое действие, а ацилпроизводные фенотиазина —
антиаритмическое действие.Структура токсикологически значимых фенотиазинов (рис 33)
приведена в табл. 34.блица 34. Структура юксикологически значимых фенотиазиновФенотиазиик,К,Хлориромаэин(аминазин)СН3 N СН2—СН2—СН2—сн3С1ЛевомспромамнСНз—1\|-сн2-СН-СН2—
СН3 сн3-о-сн.
Окончание табл. 34ТСХ-скрининг отдельных групп токсических веществ 13ВОкончание табл. 34Фснотиа зинДипразинСНз-^Н—
Н3С^ СНзнТиоридазини—\СН3-Б-СНзТрифлуоперазин(трифтазин)-СР,Промазин (пропазин)сн3—у—сн2-сн2-сн2—СН3нРис. 33. Общая формула производных фенотиазинаНейролептики группы фенотиазина подразделяются на три
класса в зависимости от вида заместителя Я,:• аминопропильного ряда (аминазин, пропазин, тизерцин, ле-
вомепромазин);• пиперидинового ряда (тиоридазин);• пи перазинового ряда (трифтазин).
134Глава 7Олнако для них всех характерно наличие в молекуле фрагмента
.с-с С-Ы - структуры, определяющей нейролептическое дей-ствие.физико-химические свойстваПо физическим свойствам производные фенотиазина представ¬
ляют собой белые (или со слабым желтоватым, сероватым, кремо¬
вым оттенком) кристаллические вещества.При взаимодействии с кислотами фенотиазины образуют соли,
они легко растворимы в воде, спирте, хлороформе, но практически
нерастворимы в эфире и бензоле. Основания фенотиазинов, липо-
фильные вещества, нерастворимы в воде, но растворимы в спирте,
эфире, хлороформе, этилацетате.Абсорбция производных фенотиазина в УФ-области спектра
характеризуется наличием двух максимумов при 250—260 нм и
300-315 нм.Сульфоксиды фенотиазинов (что отличает их от нативных со¬
единений) имеют четыре максимума в УФ-области: при 230, 265,
285, 400 нм.Токсикокинетика и биотрансформация
Фенотиазины хорошо растворяются в органических веществах.
Их липофильный характер способствует депонированию в жиро¬
вых тканях, что определяет длительный период их выведения из
организма (табл. 35).Таблица 35. Фармакокинетические параметры некоторых фенотиазиновФенотиазинрКаТ/2, ЧВыведение
в неизме¬
ненном виде,%Vd,мг/кгСвязывание
с белками
плазмыХлорпромаэин(аминазин)9.315-30Менее 12195-98ЛевомелромазинДинрачин9,29,116-7810-15Менее 1
2-3301397-99Т иоридаэин, Грифлуоперамн|^триф!а 1ин)9,58,12 ?|
ГУ» I 1Менее 1
Менее 115-19Н.д.99Н.д.Примечание. Н.д. - и<п9,411'ЛИП20-31Менее 116-1995-98
ТСХ-скрининг отдельных групп токсических веществ135Производные фенотиазина являются химически очень лабиль¬
ными соединениями и в организме человека подвергаются био-
трансформаиии. На первой ее стадии происходит окисление ато¬
ма серы с образованием различных продуктов сульфооксиления
(рис. 34), М-деметилирования, гидроксилирования, окисления.Радикальные реакции окисления одинаково легко осуществля¬
ются как в растворах производных фенотиазина, так и в живом
организме.На второй стадии биотрансформации происходит конъюгация сглюкуроновой кислотой.Химико-токсикологический анализПоскольку фенотиазины являются веществами основного ха¬
рактера, их изолируют из биологических объектов, используя схе¬
му I (для мочи и слюны), схемы 2, 3 (для крови), схемы 4-6 и 9
(для органов и тканей).Для обнаружения производных фенотиазина и их метаболитов
в ТСХ-скрининге используют реактивы, окислители.• РР1М-реактив образует пятна с окраской от розовой до сине¬
фиолетовой.Г*2Сульфоксид (8-оксид)Сульфон (Б,8-диоксид)
Рис. 34. Реакции сульфоокисления фенотиазинов
Глава 7136. <7* гиствор »торной кислота, содержащей три процента 0,5%
рктаора нитр'т натрия - пятна с окраской от розовой д„зелено- голубой.. Подкисленный йод платинат дает окраску пятен от желтой до
серо-зеленой.. Спиртовой раствор концентрированной серной кислоты (9:1)
обеспечивает пятна различной окраски.При проведении ТСХ-скрининга на производные фенотиазина
в качестве подвижной фазы используют следующие системы рас¬
творителей.Общие• ТА: метанол - 25% раствор аммиака (100:1,5).• ТВ. циклогексан - толуол - диэтиламин (75:15:10).• ТС: хлороформ — метанол (90:10).• ТЕ: этилацетат - метанол - 25% раствор аммиака (85:10:5).• TL: аиетон.• ТАЕ: метанол.• TAF: метанол - «-бутанол (60:40).• TAJ: хлороформ - этанол (90:10).• TAL: хлороформ - метанол - пропионовая кислота (72:18:10)
Частные1) Бензол - диоксан - 25% раствор аммиака (60:35:5).2) Этилацетат - ацетон - 25% раствор аммиака (50-45-4)
в этаноле 1:1. v '3,,«Х’ЫТН ~этанол"25Ж раствор аммиака(47,5:4^2.5). ,с10р0^>0*)м ~ ацетон - 25% раствор аммиакаВ табл. 36 приведены значения Я,- некоторых фенотиазинов
пластинках с силикагелем в («Мегск», Германия).Таблица 36. Значения Я, некоторых фенотиазиновI наI Хлорнроыа )ин|Лс>ОМС»^РМ«ДНН
[Дмлрямн
ТСХ-скрининг отдельных групп токсических веществ 137Окончание табл. 36ВеществоСистемы растворителей, ^ТАТВТСТЕтьТАЕТАРтиТАЬТиоридазин0,480,420,300,670.130,200.550.090.51Трифлуоперазин0,530,330,300,550,080,300,29Н.д.Н.д.Промази н0,440,380,300,62О.П0.180.350,060,41Примечание. Н.д. — нет данных.На рис. 35 (см. цв. вклейку) представлена хроматографическая
пластинка Тох^ЬаЬ типа А (система ТохьЬаЬ АВ) на различных
стадиях детектирования (см. главу 6). Для хроматографирования
использовался экстракт из мочи лица, употреблявшего производ¬
ные фенотиазина.В качестве подтверждающих методов при анализе на фенотиа-
зины возможно использование методов УФ-спектрофотометрии,
ИК-спектрометрии, ГХ, ВЭЖХ, ГХ/МС.7.4. ПРОИЗВОДНЫЕ БАРБИТУРОВОЙкислотыЭта обширная группа химических соединений насчитывает бо¬
лее 2500 различных веществ, различающихся по своему строению и
фармакологическому действию. Более 60 из них широко применя¬
лись в медицине. В настоящее время в развитых странах использу¬
ется 20—25 наименований барбитуратов. Широко распространены
их комбинированные ЛС в смеси с другими веществами, таки¬
ми как кофеин, ацетилсалициловая кислота, теофиллин, кодеин.
В незаконном обороте наркотиков нередко находят барбитураты в
смеси с героином, кокаином, амфетаминами, а также алкоголем.Практически все представители этой группы соединений являют¬
ся депрессантами ЦНС. В медицинской практике многие из них ис¬
пользуются как седативно-снотворные средства.Являясь производными барбитуровой кислоты (рис. 36), в за¬
висимости от природы радикала (табл. 37), барбитураты оказывают
более или менее длительное действие в пределах от 15 20 мин до
!~2 дней и более.
RОРис. 36. Обшая формула производных барбитуровой
кислотыТаблица 37. Структура токсикологически значимых барбитуратовБарбитуратRБарбитал-С2Н51 Фенобарбитал-с6н5Циклобарбитал!-о:■j Барбамил-СН2-СН,-СН(СН3)2Этаминал-СН(СН3)-С3Н7В соответствии с Конвенцией ООН о психотропных веществах
1971 г.. под международным контролем находятся 12 барбитуратов:
аллобарбитал, амобарбитал (барбамил), барбитал, бутабарбитал,
буталбитал, ииклобарбитал, метилфенобарбитал, пентобарбитал,
фенобарбитал, секбутабарбитал, секобарбитал, винилбитал. Бар¬
бамил и этаминал натрия также включены в Список II, а пенто¬
барбитал — в Список III Перечня.Физико-химические свойстваБарбитураты представляют собой белые кристаллические по¬
рошки без запаха. Кислотные формы практически нерастворимы
или малорастворимы в воде (например, барбамил). Натриевые соли
'■»Р“*м>р<1!ов легко растворимы в воде. Барбитураты растворимы
или умеренно растворимы в эфире, этаноле (фенобарбитал легко
растворим в ланоле) и хлороформе (барбитал — мало, фенобарби-rt.w иио*- ^ш,ие и спиртовые растворы кислотных формбарбитуратов имеют кислую реакцию среды.
ТСХ-скрининг отдельных групп токсических веществ139Кислотные формы барбитуратов хорошо растворяются в вод¬
ных растворах щелочей с образованием солей, что определяет их
быстрое всасывание в желудочно-кишечном тракте.УФ-спектры большинства производных барбитуровой кислоты
схожи, они не имеют заметного поглощения в области 200-300 нм
при кислых и нейтральных значениях pH, но имеют два максиму¬
ма поглощения при щелочных значениях pH, которые характери¬
зуют поглощения ионизированных форм первой (238-240 нм) и
второй (254—256 нм) ступени диссоциации.Токсикокинетика и биотрансформацияВсе барбитураты быстро всасываются после орального введе¬
ния (биодоступность 90—100%). Из организма они выводятся с
мочой в самых разнообразных формах как в неизмененном виде,
так и в виде метаболитов. Барбитураты пролонгированного дей¬
ствия (например, фенобарбитал) экскретируются в значительных
количествах в неизмененном виде (табл. 38), а остаточные уровни
их могут быть зафиксированы в течение 15-16 дней. Барбитура¬
ты средней продолжительности действия (например, этаминал на¬
трия) интенсивно метаболизируют, и в виде исходного соединения
выделяются в очень небольших количествах.Таблица 38. Фармакокинетические параметры некоторых барбитуратовБарбитуратрКаТ/г, чВыведение
в неизме¬
ненном виде,%Уй,мг/кгСвязывание
с белками
плазмы крови,%Барбитал7,848-7290-950,52Фенобарбитал7,350-15025-350,550Циклобарбитал7,68-172-60,570Барбамил7,98-401-3140-60Этаминал815-48100,7-160-70Фенобарбитал выводится с мочой в форме исходного К-глю-
копиранозида формы и в форме конъюгата с глюкуроновой кис¬
лотой его метаболита 4-оксифенобарбитала (схема 25). Основное
направление метаболизма барбамила и этаминала натрия - окис-
Глава 74-гидроксифенобарбитал-глюкуронидСхема 25. Метаболизм фенобарбиталаление З'-углеродного атома алкильного заместителя до оксипро-
изводных, далее до кетофуппы и затем до карбоксильной группы.
Возможно также окисление до М-оксипроизводных по азотным
атомам цикла (схемы 26, 27). Сходным образом циклобарбитал
окисляется до З'-кетоциклобарбитала (схема 28).Химико-токсикологический анализИ і биологических жидкостей (кровь, моча, слюна) барбитура-
п.1 жсфаіируются различными органическими растворителями
(ли лиловый *фир, хлористый метилен, хлороформ и др.) при сла¬
ні II,К шачениях pH без предварительного гидролиза образцовх< мы > )• И юлирование барбитуратов из биологического ма¬
териала проводят по схемам 5 и 7.
ТСХ-скрининг отдельных групп токсических веществн141З'-гидроксипроизводноеЫ-глюкуронидСхема 26. Метаболизм барбамилаДля идентификации производных барбитуровой кислоты
(!МН-кислоты) и их метаболитов в ТСХ-скрининге используетсяследующее.• Реакция комплексообразования с солями ртути. Для уси¬
ления окраски образующихся комплексов пластинку опры¬
скивают раствором дифенилкарбазона. Пятна барбитуратов
имеют окраску от синего до фиолетового цвета.• 1% раствор кобальта нитрата в этаноле. Розовая окраска со¬
ответствует 5,5-дизамещенным барбитуратам, зеленая — серо¬
содержащим барбитуратам, слабо-розовая — бромосодержа¬
щим и 1,5,5-тризамещенным барбитуратам. Данный тест
имеет очень низкую чувствительность, поэтому почти не ис¬
пользуется в практике лабораторий.При проведении ТСХ-скрининга на производные барбитуровой
кислоты в качестве подвижной фазы применяют следующие систе¬
мы растворителей.
Глава 7О СНзЭтаминал натрияN - гндроксипроизводноесн—сн->—с—сн3
І IО СНз онЗ'-гидроксипроизводноеО СН3 ОЗ'-оксопроизводноесн-сн2-с-онО СН3 О
З'-карбоксипроизводноеСхема 27. Метаболизм этаминала натрияСм*“ М Мста6о*изм ииклобарбизала
ТСХ-скрининг отдельных групп токсических веществ 143Общие• TD: хлороформ - ацетон (80:20).• ТЕ: этилацетат — метанол — 25% раствор аммиака (85:10:5).• TF: этилацетат.• TAD: хлороформ - метанол (90:10).• ТАЕ: метанол.Частные• Изопропанол — хлороформ — 25% раствор аммиака (9:9:2).В табл. 39 приведены значения Rf некоторых барбитуратов на
пластинках с силикагелем G («Мегск», Германия).Таблица 39. Значения Rr некоторых барбитуратовВеществоСистемы растворителей, R,TDТЕTFТАЕTAD1Барбитал0,410,320,610,840,570,51Фенобарбитал0,470,280,650,850,530,38Циклобарбитал0,500,400,640.880,580,59Барбамил0,520,440,660,880,580,74Этаминал0,550,450,660,900,590,76На рис. 37 (см. цв. вклейку) представлена хроматографическая
пластинка Toxi-Lab типа В (система Toxi-Lab АВ) на различных
стадиях детектирования (см. главу 6). На хроматограмме видны
пятна веществ-метчиков производных барбитуровой кислоты.В качестве методов, подтверждающих результаты ТСХ-скри-
нинга производных барбитуровой кислоты используют методы
УФ-спектрофотометрии, ИК-спектрометрии, а с целью количе¬
ственного определения — ГХ, ВЭЖХ, ГХ/МС.7.5. КОКАИНКокаин является алкалоидом, который получают из сухих ли¬
стьев кокаинового куста (Erythroxylon coca), содержащих 1—2%
данного алкалоида. Кокаиновый куст растет в диком виде только
в Колумбии, Боливии и Перу. В настоящее время кустарник куль¬
тивируют в других странах. Кокаин добывают также путем синтеза
из экгонина.
Глава 7144НС-О-СНзо-с-с6н5оIIВ медицине кокаин — эффек¬
тивный местный анестетик; во
время соревнований спортсме¬
нов — запрещенный стимулятор
ЦНС; введенный путем инъекций
или ингаляций — наркотик, вы-Рис 38 Структурная формула ко- зывающий эйфорию и возбужде-
каина ние ЦНС.По химической структуре кокаин - дважды сложный эфир
спиртокислоты экгонина, метилового спирта и бензойной кислоты
(рис. 38), обладает слабыми основными свойствами.В подпольной практике препараты кокаина распространяютсяв следующих формах.• Паста коки (Basuko, Bazooka) — дешевый продукт, получае¬
мый на начальных стадиях производства кокаина при экстрак¬
ции из листьев коки. Это обычно сырой желтоватый порошок
с содержанием кокаина от 40 до 90%. Пасту коки используют
при курении, часто в смеси с табаком или марихуаной.• Кокаин (Coke, Snow) — кокаина гидрохлорид с содержанием
основного вещества от 80 до 90%. Для нелегальной продажи в
кокаин добавляют до 12—75 % неконтролируемых синтетиче¬
ских местных анестетиков (лидокаин, прокаин) или углеводы
(маннитол, лактозу, глюкозу, крахмал). Внешний вид нелегаль¬
ных образцов кокаина при этом практически не меняется.• Кокаин-основание («крэк», Crack, Коек) получают кустарно
из кокаина гидрохлорида при нагревании с водой и бикар¬
бонатом натрия для удаления хлорид-ионов. Свое название
«крэк* получил из-за того, что при нагревании остаток би¬
карбоната натрия часто вызывает потрескивание. «Крэк» в
основном курят, так как его температура плавления состав¬
ляет ) С. При курении или ингаляции чеэез tov6kv паоы
ТСХ-скрининг отдельных групп токсических веществется стимулятором с коротким, от 8 до 10 мин, и чрезвычай¬
но интенсивным эффектом. После этого наступают сильное
нервное возбуждение и депрессия. Героин, проявляя седа¬
тивное действие, длящееся до 4 ч, противодействует депрес¬
сии, вызываемой кокаином. Настроение потребителя «спид-
болла» меняется быстро и непредсказуемо.В Перечень включены 5 НС, перечисленных в табл. 40.Таблица 40. Наркотические средства, получаемые из куста кокиНаркотические средстваСписок ПеречняКокаиновый кустIЛист кокаIЭкгонин, его сложные эфиры и производные, кото¬
рые могут быть превращены в экгонин и кокаинIКокаинIIКокаина гидрохлоридIIфизико-химические свойстваКокаин основание — белые кристаллы с Тпл = 98 °С. Растворим
в воде (1:600), этаноле (1:6,5), хлороформе (1:0,7) и эфире (1:3,5),
хорошо растворим в ацетоне и этилацетате.Кокаина гидрохлорид — бесцветные кристаллы или белый кри¬
сталлический порошок, гигроскопичен. Плавится при Т = 195 °С
с разложением. Растворим в воде (1:0,4), хлороформе (1:12,5), эта¬
ноле, ацетоне и глицерине; практически нерастворим в эфире.Токси коки нети ка и биотрансформацияПри курении и внутривенном введении кокаин легко всасы¬
вается. Пик концентрации в плазме достигается быстро и через
очень короткое время снижается. Длительность максимальных
психотропных и физиологических эффектов также очень мала, по
субъективным данным, эйфорию ощущают при курении в тече
ние 20 мин. Интраназальное и оральное применение дают сходные
концентрационные профили в плазме. Однако при »1 играна кип
ном введении действие наступает быстрее, а его пра1^1 ^
ность доходит до 60—90 мин. Оральный способ приме не
теризуется медленным развитием эффектов и
слабой их интенсивностью. Основные фармако с
раметры кокаина приведены в габл. 41.
глава 7|СТИческие параметры кокаинаТаблица 41. Фарм*ВеществоЖОМ'"1-рКаТ/2, чВыведение
в неизме¬
ненном виде,%V«!,мг/кг0,7-1,541-3Кокаин8,6Связывание
с белками
плазмы крови% ^Н.д.Примечание. Н.д.нет данныхКокаин быстро метаболизируется в плазме и печени в про-
иессах Ферментативного гидролиза (с участием холинэстеразь,
плазмы)- ло метилэкгонина; неэнзимного гидролиза - до беи-
зоилэкгонииа; К-деметилирования - до норкокаина. Кроме того,
образуются минорные метаболиты кокаина: экгонин, норкокаин.
В присутствии этанола можно обнаружить кокаэтилен, норкока-
этилен, этиловый эфир экгонина (схема 29).Распределение кокаина и его метаболитов имеет специфиче¬
ские особенности. Кокаин и норкокаин — липофильные соедине¬
ния, легко преодолевают гематоэнцефалический и плацентарный
барьеры. В высоких концентрациях кокаин накапливается в жи¬
ровых депо. Метаболиты кокаина — бензоилэкгонин и экгонин —
высокополярные соединения, не способные преодолевать гемато¬
энцефалический барьер по крайней мере в фармакологически зна¬
чимых концентрациях.Подкожная жировая клетчатка и ороговевшие частички кожи
людей, в течение 40 нед употреблявших кокаин, также содержат
небольшие количества наркотика. Относительно высокое со-
держание кокаина в мозге, а также стабильность такого уровняхимии™*1 позволяют использовать мозговую ткань при судебно¬
химическом анализе.отобраннойппглг1КаИН продолжает активно метаболизировать в
'Крид в качестве консерада°бУ ^ ШЛЛтЯ добаш,яют натРия
Хитко-гокикологический анализМИШАМВПМлшъшмм!К0Каии ии>лируют ири pH = 9-Юшей »кстра/ируюшей сп<»( гРас1В0рителями (по схемам I и2)Луч-Нм»|ропанал (3:1). Жосн>ю обладает смесь хлороформ —
тсх-скрининг отдельных групп токсических веществ147Н3С^Норкокаин ОкогольЯас-о-сн2Пиролиз
окаина-гидрохлоридіКарбометоксициклогептатриен(изомеры)Нз<^н/ о^-с6н!Кокаэтилен О/"о-с-едII Ангидроэкгонин-О метиловый эфир (АЭМЭ)Кокаинс-онМетилэкгонино-^-ад
оБензоилэкгонинСхема 29. Биотрансформация кокаинаВыделение кокаина и его метаболитов из биотканей проводят
подкисленным спиртом (метод Стаса-Отто, схема 4) и подкислен¬
ной водой (методы А.А. Васильевой и В.Ф. Крамаренко, схемы5 и 6).
148 В качестве реагентов для обнаружения кокаина и его метабоди.Т0в на ЯРК° °Ранжевые,пятна;. реактив Драгендорф . йодплатината; КОкаин образует пятно
. подкисленный Pfт Р иты _ от пурпурного до синего.пурпурного цвета, а кокаин в качестве подвиж-при проведении ТС^“РИНиИеНсистемь, растворителей.НОЙ фазы используют следующие ст..^тГмеганол - 25% раствор аммиака
. ТВ: циклогексан - толуол - диэтиламин (75.15.10).• ТС‘ хлороформ - метанол (90:10).. ТЕ: этилацетат - метанол - 25% раствор аммиака (85:10:5).• TL: ацетон.• ТАЕ: метанол.• TAF: метанол - «-бутанол (60:40).• TAI: хлороформ - этанол (90:10).• TAL: хлороформ ~ метанол - пропионовая кислота
(72:18:10).Частные• Гексан - толуол - диэтиламин (65:20:5).• Метанол - диэтиламин (95:5).• //-Бутанол - уксусная кислота ледяная - вода (35:3:10).В габл. 42 приведены значения Rf кокаина и его метаболитов на
пластинках с силикагелем G («Merck», Германия).Габлица 42. Значения R, кокаина и его метаболитовЖЧЖИИПримечание Н д _нет /шнных.
ТСХ-скрининг отдельных групп токсических веществ 149На рис. 39 (см. цв. вклейку) представлена хроматографическая
пластинка Toxi-Lab типа А (система Toxi-Lab АВ) на различных
стадиях детектирования (см. главу 6). Для хроматографирования
использовался экстракт из мочи лица, употреблявшего кокаин.В качестве методов, подтверждающих результаты ТСХ-скри-
нинга кокаина и его метаболитов возможно применение
уф-спсктрофотометрии, ИК-спектрометрии, а с целью количе¬
ственного определения — ГХ, ВЭЖХ, ГХ/МС.7.6. КАННАБИНОИДЫВ эту группу НС входят препараты, приготавливаемые из раз-
личных частей конопли. Конопля (Cannabis sativa L.) представляет
собой однолетний древовидный куст, достигающий 3~4 м в высо¬
ту. Имеет характерное нечетное количество (5, 7, 9) листьев с за¬
зубренными краями (рис. 40, см. цв. вклейку). В период цветения
на черешках верхних листьев выделяется смолистое вещество, ко¬
торое защищает растение от солнца (так называемая смолка). Про¬
израстает в диком виде в условиях жаркого и умеренного климата.
Наряду с этим каннабис (конопля) культивируется и используется
для получения пеньки, пакли, масла, семян и наркотиков.Растение каннабис известно людям уже несколько тысячеле¬
тий. Еще в рукописных источниках XV в. говорится о применении
в китайской фармакопее смолы каннабиса в качестве анестетика.В медицинских и культовых целях его использовали в Индии, за¬
тем в странах Среднего Востока и Северной Африки. В Европе и
США каннабис стал популярным с XIX в. как лекарственное и
психоактивное средство — о нем много писали и изучали его воз¬
действие на организм человека.Конец XIX и начало XX вв. характеризуются ростом популяр¬
ности марихуаны и значительным увеличением ее продаж. Однако
в 1930 г. федеральные органы США по борьбе с распространением
наркотиков добились принятия закона, запрещающего не только
выращивание конопли и свободную торговлю ею, но и употребле¬
ние изготавливаемых из нее препаратов. Несмотря на заявления
административных органов, научных институтов и организаций,
накопивших достаточно фактов негативного медицинскою и со¬
циального влияния наркотика, в обществе долгое время сохрани
лось устойчивое мнение о безопасности использовании марихуаны
й о социальной ее приемлемости.и отсутствии привыкания к ^ ья и фактическое разреше-Игнорирование опасности ^ и видеоПродУкции привелиние популяризовать марихуа у данного наркотика среди аме-
к повсеместному распростририканских подростков- ы ^ молодеЖной среде в США при-Пик употребления мар поУледуюшие Г()ДЫ отношение Обществашелся на 1960 19/и гг. 0бРазом изменилось. Миф о безвред-
к этой проблеме кореннь б0ЛЬШИНСТВ0 исследователей утвер-
ности «травки» рзсссялс . а и в более низкой степелились во мнении, Ч™ Р физическую зависимость, всени обусловливает психическу^и^еское пристрастие и оказывать
же способна вызь ментальНые, эмоциональные и физиче-
с^ефункции1Организма. Дискуссия о легализации препаратов из
марихуаны с целью использования в медицине в качестве лекар¬
ственных средств и в качестве «легкого» наркотика для наркоманов
продолжается, несмотря на серьезность выдвигаемого аргумента о
наличии опасности перехода к «тяжелым» наркотикам - героину
или кокаину.В США до 1942 г. препараты конопли были разрешены в ка¬
честве Л С, входили в Фармакопею и продавались в аптеках. До
1992 г. в США марихуана числилась в Списке №2, что означало
возможность ограниченного ее использования в медицинских це¬
лях (в основном для предотвращения тошноты и рвоты у больных
СПИДом, при онкологических заболеваниях, при радиоактивном
облучении). С 1992 г. только основной психоактивный ингредиент
марихуаны — Д9-ТГК, легально производимый в США, разрешен в
некоторых странах (США и Германия) к применению в медицине
под контролем медицинского персонала, в основном для лечения
глаукомы и токсикоза у онкологических больных, прошедших курс
химиотерапии (препараты «Дронабиол» и «Набинол»).В Нидерландах и Испании не преследуется законом выращива¬
ние небольшого количества конопли для собственных нужд.азличают следующие препараты, получаемые из конопли: ма-
^^На'гашиш и гашишное масло. В настоящее время каннабис,
тер полУчаемые из него, а также их основное «действую-
Список I каиш. ^-идроканнабинол (все его изомеры) входят в
рсчня (таб I 41|>ШИИ И соответствУЮЩий ему Список I Пе-(в том чис к и I ,Т° <ммачает ™пРет на использование в любых
ТОМ желе и в медицинских) целях.
ТСХ-скрининг отдельных групп токсических веществ151Таблица 43. Наркотические средства, получаемые из марихуаныНаркотические средстваСписок ПеречняГашиш (анаша, смола каннабиса)IКаннабис (марихуана)1Масло каннабиса (гашишное масло)1Тетрагидроканнабинол (все изомеры)IСогласно заключению ПККН, «марихуана — приготовленная
смесь высушенных или невысушенных верхушек с листьями и
остатками стебля любых сортов конопли без центрального стебля».
Единая Конвенция ООН о НС 1961 г. термин каннабис трактует
так: «Верхушки растения конопли с цветами или плодами (за ис¬
ключением семян и листьев, если они не сопровождаются верхуш¬
ками), из которых не была извлечена смола, каким бы названием
они не были обозначены».После высушивания марихуана содержит более 400 компонен¬
тов. При курении в результате пиролитических превращений они
трансформируются в 2000 химических веществ. Более 70 из 400
компонентов марихуаны составляют группу каннабиноидов, био¬
логически активных веществ особого строения, встречающихся
исключительно в растении каннабис. Основной компонент, от¬
вечающий за психоактивные свойства марихуаны (рис. 41), транс-
дельта-9-тетрагидро-каннабинол (А9-ТГК). Однако суммарный эф¬
фект марихуаны определяется всеми активными каннабиноидами.
д8_ТГК (см. рис. 41), содержание которого гораздо ниже такового
Д9-ТГК (по некоторым данным Д8-ТГК в свежесобранном материа¬
ле вообще отсутствует), столь же активен, как и Д9-ТГК. Каннаби-
нол (см. рис. 41) в 10 раз менее активен, чем Д9-ТГК, каннабидиол
не обладает психоактивными свойствами.Содержание Д9-ТГК, как и других каннабиноидов, зависит
от вида растения и региона его произрастания. В американских
сортах конопли доля Д9-ТГК составляет менее 0,5%, в конопле,
произрастающей в Колумбии, Мексике, на Ямайке — от 0,5 до
7%. В конопле из Юго-Восточной Азии содержание Д9-ТГК до¬
ходит до 20%.Минорные компоненты, такие как каннабидиварин, каннабих-
ромин, каннабиварин, бутиловые аналоги ДЧ-ТГК, содержатся в
марихуане в разных соотношениях в зависимости от вида сырья.
Рис. 41. Структурные формулы каннабидиол, каннабинол, ДХ-ТГК, АЧ-ТГКПомимо каннабиноидов, в состав марихуаны входит множество
веществ других классов: терпены, стероиды, углеводы, фенолы, кар¬
боновые кислоты, азотсодержащие соединения, алкалоиды и др.Согласно заключению ПККН, «гашиш — специально приготов¬
ленная смесь отдельной смолы, пыльцы растения каннабис или
смесь, приготовленная путем обработки (измельчением, прессова¬
нием и т. д.) верхушек растения каннабис с различными наполни¬
телями, независимо от того, какая форма была придана смеси —
таблетки, пилюли, спрессованные плитки, пасты и др.». Термин
«гашиш» включает термин «смола каннабиса», который согласно
определению Единой конвенции ООН о НС 1961 г. обозначает
•отделенную смолу, неочищенную или очищенную, полученную
из растения каннабис*..1|я отделения частей растения, содержащих смолу, раститель¬
ный материал подвергают механическому воздействию, напри-р ыо( о твердую поверхность, после чего полученный матери-
ТСХ-скрининг отдельных групп токсических веществ 153ал просеивают и прессуют. При просеивании макроскопические
признаки конопли фактически разрушаются, однако сохраняются
многие микроскопические признаки растения.При втором способе получения плодоносящие и цветущие
верхушки растения растирают по резиновому полотну или между
ладонями, иногда раздавливают ногами. Затем смолу собирают с
подложки острым предметом. Иногда выделение смолы каннаби¬
са осуществляют с применением температурной обработки смесей
растительного материала и воды.Содержание основного психоактивного вещества (Д9-ТГК) со¬
ставляет от 2 до 10%, хотя в последнее время нередки случаи изъя¬
тия этого наркотика с содержанием ДЧ-ТТК до 40%. В зависимости
от условий получения цвет наркотика различается от светло-
зеленого до темно-коричневого, почти черного. Запах характерен
для НС, получаемых из конопли.Согласно заключению ПККН, «гашишное масло — наркотиче¬
ское средство, получаемое из частей любых видов и сортов ко¬
нопли путем извлечения (экстракции) различными растворителя¬
ми или жирами (может встречаться в виде растворов или вязкой
массы); экстракты и настойки каннабиса». Согласно определению
Многоязычного словаря по НС и ПВ, находящимся под между¬
народным контролем (ШОСР, ООН, 1993), масло каннабиса —
«концентрат каннабиса, полученный путем экстрагирования кан¬
набиса или смолы каннабиса и обычно содержащий растительное
масло». Понятия «масло каннабиса» и «гашишное масло» совпа¬
дают и обозначают экстракт, полученный из марихуаны или га¬
шиша. Это НС встречается в виде растворов или густой вязкой
массы и употребляется путем курения после нанесения на различ¬
ные растительные объекты, например на табак. Гашишное масло
часто получают в виде экстракта марихуаны или гашиша в молоке.
К маслу каннабиса относятся продукты, получаемые прожарива¬
нием марихуаны или гашиша в растительном или животном жире
или масле. Гашишное масло содержит от 10 до 60% Д^-ТПС.Способы употребления продуктов, получаемых из конопли,
следующие.• Курение. Для него используют сигареты с марихуаной или
обычные табачные сигареты с добавкой гашиша или неболь¬
шого количества гашишного масла. Иногда курят с помощью
особых стеклянных трубок. Распространено также вдыхание
Глава 7154„аров масла, нагреваемого в пламени на алюминиевой фольгеили на лезвии ножа^ ^ ^ виде заварКи или добавки к пище.. Оральное потре ^ на оргаНизм человека как стиму-Марихуана мож ^ воздействие, дополняемое при болееГГЛоз^юниногенными Эффектами.Физико-химические свойстваа9 тгкг И л8 ТГК - маслянистые жидкости, их температуры
плавления - 210 и 213 -С соответственно. Все каннабиноиды хо-
мшо растворимы в спирте и ацетоне ограниченно растворимы
ГГлГ"нРы* растворителях (хлороформ и диэтиловыи эфир)
и малорастворимы в воде. Спиртовые растворы Д -ТГК и Д«-ТГК
поглощают уф-иалучение с длинами волн 283, 276 и _78 нм.Токсикокинетика и биотрансформацияПри курении каннабиноиды быстро (за несколько минут) вса¬
сываются. При этом возрастает количество физиологически актив¬
ных компонентов каннабинола и Д9-ТГК вследствие разложения
каннабидиола. При пероральном введении из-за плохой всасы¬
ваемости в желудочно-кишечном тракте концентрация Д9-ТГК в
крови нарастает медленно, достигая максимальных значений через
1,5-2 ч.Кинетика выведения из плазмы описывается согласно моде¬
ли двухфазного элиминирования: «быстрое», в течение примерно
40 мин, и «медленное» — до 24 ч. Максимум психологического
эффекта соответствует максимальной концентрации в крови. Уро¬
вень ТА Д9-ТГК в плазме при «быстрой» и «медленной» фазе —3-4,5 мин и около 20 ч соответственно.Обладая липофильными свойствами, после поступления в ор¬
ганизм ДУ-ТГК быстро покидает кровяное русло, распределяясь в
тканях, богатых липидами: жировых отложениях, мозге, легких.
Объем распределения 10 л/кг (табл. 44). Детектируемые количе¬
ства Л -ТГК в жировых отложениях организма, взятых методом
иопсии у хронических курильщиков марихуаны, обнаруживают-
М-^Гнг/г 166 ^ НеД после последнего курения и составляют
ТСХ-скрининг отдельных групп токсических веществ 155Таблица 44. Фармакокинетические параметры Д9-ТГКВеществорКаТ/г, чВыведение
в неизме¬
ненном виде,%V«!,мг/кгСвязывание
с белками
плазмы крови,%ДЧ-ТГК10,615-57;72-240Менее 14-1465-70Кумулированный Д'-ТГК медленно возвращается в систему
кровообращения и может быть определен высокочувствительными
методами в крови в течение нескольких часов, а в моче — спустя7—10 дней после выкуривания одной сигареты. При регулярном
курении 2 сигарет в неделю в течение 6 мес следовые количества
д9-ТГК порой обнаруживаются через несколько недель после пре¬
кращения курения.В организме человека основной путь метаболизма Д9-ТГК —
быстрое окисление углерода аллильной группы энзимной систе¬
мой печеночного цитохрома Р450 до первичного психоактивного
короткоживущего 11-гидрокси-дельта-9-тетрагидроканнабинола
(11-гидрокси-Д9-ТГК), который далее под действием алкогольдеги-
дрогеназы окисляется в конечный биологически неактивный про¬
дукт: 11-нор-дел ьта-9-тетрагидроканнабинол-9-карбоновую ки¬
слоту (Д9-ТГК-СООН). Начальный продукт биотрансформации
11-гидрокси-Д9-ТГК обладает равной с Д9-ТГК активностью. Пи¬
ковая концентрация 11-гидрокси-Д9-ТГК в плазме гораздо ниже,
чем исходного Д9-ТГК.Гидроксилированные и карбоксилированные метаболиты да¬
лее на 75—80% конъюгируются в соответствующие глюкурониды
и сульфаты (схема 30).Содержание неизмененного Д9-ТГК в продуктах, выводимых
мочой, составляет менее 1 % дозы. При приеме 30 мг ДЧ-ТГК за 6 ч
экскретируется в мочу 0,005% дозы неизмененного Д4-ТГК (сред¬
нее для четырех образцов); 15—20% дозы выводится в виде кислых
метаболитов. Остальное количество кумулируется в организме и
медленно экскретируется в течение следующих нескольких дней.
За 5 дней выводится 80—90% введенной дозы, причем из ни\ толь¬
ко 20% с мочой и 65% с каловыми массами.Основной продукт выделения (около 65%) неактивный ме¬
таболит Д9-ТГК-СООН в виде моноглюкуронида и, возможно, дн-
Глава 7156
ТСХ-скрининг отдельных групп токсических веществ 157глюкуронида, хотя по некоторым данным, фенольная группа Д9-
ТГК-СООН конъюгированию не подвергается.8(5,11-дигидрокси-Дч-ТГК поступает в мочу в течение примерно
24 ч после момента курения и может служить маркером недавнего
потребления марихуаны. Максимум концентрации отмечается че¬
рез 1-4 ч, потом она снижается до 10-20 нг/мл за 4-6 ч.Присутствие следовых количеств каннабинола в моче объ¬
ясняется его образованием из Д9-ТГК при курении в результате
термического превращения. Кроме того, каннабинол может пере¬
ходить в мочу как компонент каннабиса. Второй важный компо¬
нент, входящий в состав растения — не обладающий психической
активностью каннабидиол; он широко метаболизируется, образуя
многочисленные гидрокси- и карбоксипроизводные каннабидиола
и внося вклад в метаболизм.Таким образом, с мочой выводятся следующие метаболиты.
Основной метаболит: Д9-ТГК-СООН-глюкуронид (Д9-ТГК-СООН-
диглюкуронид). В меньшем количестве выделяются: Д9-ТГК-СООН
свободный; 11тидрокси-Д9-ТГК-глюкуронид и 11-гидрокси-Д9-
ТГК свободный; 8(3-гидрокси-Д9-ТГК; 8(3,11-дигидрокси-Д9-ТГК-
глюкуронид и 8(3,11 -дигидрокси-Д9-ТГК свободный; Д9-ТГК-
глюкуронид и Д9-ТГК свободный. Биологической активностью
обладают 11-гидрокси-Д9-ТГК и 8(}-гидрокси-Д9-ТГК.В следовых количествах обнаруживаются: каннабинол; каннаби¬
диол.На основании полученных при анализе мочи данных в общем
случае нет возможности установить, когда имел место «сеанс» при¬
ема ТГК-содержащих продуктов. Можно лишь сделать некоторые
ориентировочные выводы относительно времени и интенсивности
их употребления.Слюна по некоторым критериям является лучшей биологиче¬
ской матрицей для судебно-химического анализа при доказатель¬
стве факта недавнего потребления марихуаны. Отбор слюны осу¬
ществляется просто и быстро, исключается возможность инвазии.
Концентрации активных веществ в слюне после приема обычных
доз Д9-ТГК достигают 1000 нг/мл, т.е. значительно превосходят ве¬
личины, выявляемые в крови, и, кроме того, коррелируют с дина¬
микой психотропных эффектов, в отличие от содержания данных
каннабиноидов в моче, поте и волосах. Через 3—4 ч концентрация
ДЧ-ТГК в слюне уменьшается примерно до 50 нг/мл.
отдельная
ны\ выше Глава 7158употребления продуктов каннабиса
Для доказательства а • правильно определять основной
на основе ан^изаг^н чем сам л*-ТГК. из-за возможности за-
иетабспнт Л'-1« к-'- • пассивного курения (когда некурящий
трязнення юте «ж* ,м0;, замкнутом пространстве одиовре-
находится в невенпч > куряшими. и длительность сеан-менно с одним иди нсс^ы-имирр^ | ч)
са курения составляет по меныжХ№»ю-тс*сикопопгчесп<н анм*3Пои исследовании биообъектов на каннабниоиды необходима
Г^подготовка. отлична» от любой из схем. приведен-КшЛ'к I мл крови добавляют I мл 7,5* раствора гидроксида
аммония и 3 мл смеси лиэтиловый эфир к-пентан ( :П. далее
сиееь встряхивают в течение 2-3 мин. После центрифугирования
надоеалоютю жидкость переносят в стеклянную емкость, пред¬
варительно промытую метанолом (во избежание сорбции канна-
бнноиаов) и выпаривают в токе азота Полненный осадок иселе-дуется методом ТСХ.Моча. 10 мл мочи смешивают с 0.5 мл 50% раствора гидрок¬
сида натрия и смесь гидролизуют в течение 20 мин при 60 С. По
охлаждении к гидролиза ту добавляют концентрированною соля-
нмо кисютл до pH = 2. и жидкость экстрагируют смесью гексан
- этилацетат (7:1). Органический слой отделяют и упаривают в
токе азота. Остаток исследуют методом ТСХ.Слюна. Отбирают 3 мл слюны. Полость рта промывают 50 мл
'01г раствора этилового спирта, насыщенного хлоридом натрия
(чтобы не глотали). Слюн> и смыв объединяют и экстрагируют
10 мл этиллиетата в течение 5 мин. Слой органического раство¬
рителя отделяют и фильтруют через 1.5 г безводного сульфата на¬
трия Фильтрат испаряют в токе азота и исследуют методом ТСХ.Внутренние органы. Внутренние органы гомогенизируют, сме¬
шивают с 50^ раствором трмхлоруксусной кислоты; смесь цен¬
трифугируют при 3000 об/мин в течение 5 мин. Надосадочную
жидкость экстрагируют в течение 10 мин 20 мл смеси хлороформ-
июпропанод (4:1) или л-бугилхлорид - изопропанол (4:1) или
^Г08ЫЙ ~ « пентан (9:1). После отделения слой орга-
ТС\^КОГ° РЗСТВ°^ителн УпаРивают досуха и исследуют методом
ТСХ скрининг отдельных групп токсических веществ 159Поскольку волосы нецелесообразно исследовать методом ТСХ
(концентрации каннабиноидов в них ниже порога чувствительности
метода), то рассматривать пробоподготовку на них мы не будем.Во і можно также использование метода ТСХ при анализе об¬
разцов вещественных доказательствОбнаружение пятен осущестлзяют в УФ-свете (при испозьзова-
нии пластинок с флуоресцирующим индикатором), а также путем
опрыскивания щелочным раствором красителя прочного синего Б
(пли ВБ) (Fast Blue В or ВВ). Каннабидиол образует пятна оран¬
жевого цвета, каннабинол — красно-фиолетового цвета. Л"-ТГК —
красного цвета. Л^-ТГК-СООН — красно-фиозетового цвета.Для анализа каннабиноидов методом ТСХ испозьзуют следую¬
щие системы растворителей.Общие• ТА: метанол - 25<* раствор аммиака (100:1,5).• ТЕ: этилацетат - метанол — 25ЯЕ- раствор аммиака (85:10:5).• TAJ: хлороформ - этаноз (90:10).• ТАК: хлороформ - циклогексан — ледяная уксусная кислота
(4:4:2).• TAL: хлороформ — меганоз - пропионовая кислота (72:18 10).Частные• Тазуаз.• Ксилол — гексан - диэтнламнн (25:10:1).• Пегролейный эфир — диэтиловый эфир (4:1).• Ацетон — гептан — ледяная уксусная кислота (30:22:0.5).• Гексан — нэобутанол - ледяная уксусная кислота (90:9:1).В табл. 45 приведены значения R. некоторых каннабиноидов на
пластинках с силикагелем G («Merck*. Германия).Таблица 45. Значения R, некоторых каннабиноидовВеществоСистемы растворителей. R,ТАТЕTAJТАКTAL•23 !■—н4 I5У-ТГК0.110.310.000.010.310,300.290.66Нл.НлКаннабинол0,940.95о.*)0,77о.ч:0.520.200.55НлНлКаннабндмоло.*»0,950.SS0.7 6о.*»?0.05О.Зб0,7bНл.Нл.Д4-ТГК-СООННл.Нл.Нл.Нд.Нл.НлНлНл.0.620,*Примечание. Нл. - нет данных.
Глава 7160я, пи Г 42 (см ив. вклейку) представлена хроматографическая
пластинка Toxi-Lab-THC (система Toxi-Lab-THC) после детекти-
™вания (см главу 6). Для хроматографирования использовались
жгоакты из образцов мочи лиц, употреблявших марихуану.В качестве подтверждающих методов можно использовать ГЖХ,
ВЭЖХ, ГХ/МС, УФ- И ИК-спектрометрию.7.7. ФЕНИЛАЛКИЛАМИНЫВ эту группу входят вещества, различные по химическому стро¬
ению, фармакологическому действию и источникам получения.Вещества данного класса являются стимуляторами ЦНС, имеют
свойства активизировать психическую деятельность, устранять фи¬
зическую и психическую усталость. В некоторых случаях это J1C,
используемые в практике для лечения депрессивных состояний,
нарколепсии (непреодолимого желания спать), для преодоления
усталости, контролирования массы тела и снижения аппетита, а
также лечения гипокинезии у детей.Общее действие фенилалкиламинов на организм выражается в
проявлении физической активности и бодрости, повышении ум¬
ственной работоспособности, уменьшении аппетита, сонливости,
усталости и улучшении настроения. Вместе с тем проявляются раз¬
дражительность, беспокойство, неадекватные реакции, бессонни¬
ца. Обязательная реакция — расширение зрачков. Характер, дли¬
тельность и сила симптомов определяются структурой вещества и
дозой.Стимуляторы действуют на нейротрансмиттеры — звенья, от¬
ветственные за передачу сигнала от клетки к клетке. Их влияние
на работу мозга обусловлено механизмами, различными для раз¬
ных препаратов. В основе действия лежит стимулирование высво-
ждения катехоламинов (норадреналина, серотонина, дофамина)
и торможение их обратного захвата."Грашение приема стимуляторов после длительного при¬
яв 1ении .^10Жет вызвать синдром отмены, что выражается в про-
неско НКГ состояния и глубокой депрессии, длящейсятаки yxv/iiuеHM«dГ1 d 1Ии’ усталости. Появляются и нарастают при-
скольких месяшм ьои|рия'ия и п°тери ориентации. В течение не-
нленции. Н НС проходят состояния тревоги и суицидальные
ТСХ-скрининг отдельных групп токсических веществ 1617.7.1. Эфедрин и его производныеЭфедрин, в химическом отношении представляющий собой
2-метиламино-1-фенил-пропанол-1, является алкалоидом, содер¬
жащимся в различных видах эфедры (Ephedra L.). Помимо эфе¬
дрина (эритро-изомер), трава эфедры содержит трео-изомер ал¬
калоид псевдоэфедрин (рис. 43), норэфедрин, норпсевдоэфедрин,
метилэфедрин, метилпсевдоэфедрин. Каждый из них представляет
собой рацемат и состоит из двух оптических антиподов: лево- и
правовращающего.Более 5000 лет назад в древнем Китае растение «ма хуанг» —
Ephedra vulgaris (рис. 44, см. цв. вклейку) - применялось в качестве
противокашлевого и потогонного средства.Эфедрин получают извлечением из слегка подщелоченного
мелкоизмельченного растительного сырья органическими раство¬
рителями или подкисленной водой. Разделение эфедрина и псев¬
доэфедрина основано на различной растворимости их оксалатов в
спирте. Сокращение запасов дикорастущего сырья, всевозрастаю¬
щие потребности в препарате, а также низкое содержание алка¬
лоида в различных видах эфедры побудило химиков к разработке
синтетических методов получения эфедрина.Эфедрон («белое», «джеф», «марцефаль») (см. рис. 43) — нарко¬
тическое средство, дающее более сильный стимулирующий эффект,
чем эфедрин (вызывает галлюцинации, быстро формирует психи¬
ческую зависимость). Эфедрон получают кустарным способом из
эфедрина путем окисления гидроксильной группы в молекуле эфе¬
дрина до карбонильной. Реакция проводится в уксуснокислой средесн3 дат°1 ^СН, ОН .1нЭфедрин Эфедрон ПсешюэфедрннРис. 43. Структурные формулы эфедрина, эфедрон а и псевдоэфедрина
162 при температуре 50-60 °С, при этом в качестве окислителя исполь¬
зуется перманганат калия.Эфедрин, псевдоэфедрин и их соли включены в С писок сильно-действующих веществ (Список №1) ПККН и Список IV Перечня
(табл. 46).Таблица 46. Соединения, относящиеся к группе эфедрина и его произво-Глава 7ДНЫ.\ Наркотические средстваСписок ПеречняЭфелрин IVПсеадоэфедрин IVКустарно изготоштенные препараты из эфедрина или из пре
паратов. содержащих эфедрин IКустарно изготовленные препараты из псевдоэфедрина или
из препаратов, содержащих псевдоэфедринIЫ-метилэфедрон1Норпсевдоэфедрин (катин. фенилпропаноламин)I. IVКатинон (норэфедрон)IЭфедрон (метилкатинон)IАмфепрамонIIАмфепрамон относится к группе анорексигенных средств.
Входит в состав пакетов, применяемых в курсовом лечении по
программе снижения веса «Медислим» (иногда они именуют¬
ся «Тайские таблетки» для похудания) и включенных в Список
№1 сильнодействующих веществ ПККН. Кроме амфепрамона, в
«Тайских таблетках* могут содержаться диазепам, фенфлюрамин
и фентермин.Из соединений, указанных в табл. 46. особое значение имеет ка-
тин, или норпсевдоэфедрин, фенилпропаноламин (рис. 45). Катин -
это алкалоид, выделенный из свежих молодых побегов растения
ката съедобного (СшИа Ыи1Ь), произрастающего в Центральной и
Восточной Африке. С древних времен листья этого растения ис-
подьювались в культовых обрядах, а арабский врач Наджиб Ад-
Дин предлагал листьями кустарника ката лечить депрессии. Зеле¬
ные листья при пероральном применении вызывают эйфорию и
галлюцинации. Кроме катина, из листьев ката выделяют алкалоид
катннон (см рис. 45) и эфедрой. Основные поставщики ката —
Сомали. Йемен. Эфиопия, Нигерия.
ТСХ-скрининг отдельных групп токсических веществ163Рис. 45. Структурные формулы катина и катинонаКатин и катинон относятся к психотропным веществам Списка
I Перечня. Кроме того, катин и комбинированные ЛС на его осно¬
ве включены ПККН в Список сильнодействующих веществ.физико-химические свойстваЭфедрин-основание (полугидрат) представляет собой бесцвет¬
ные кристаллы или белый кристаллический порошок, который
разлагается под действием света. Тпл = 40 °С. Растворим в воде
(1:20) и этаноле (менее 1:1), а в хлороформе и эфире растворяется
с образованием эмульсии по причине отделения воды. Эфедрина
гидрохлорид — бесцветные кристаллы или белый кристаллический
порошок 0^ = 217—220 °С. Растворим в воде (1:4), этаноле (1:14),
малорастворим в хлороформе, практически нерастворим в эфире.Эфедрон - белый порошок или бесцветные кристаллы с
Тп1 = 182—184 °С. Растворим в соляной кислоте с образованием
гидрохлорида. Представляет собой кристаллы в спиртовом ацетоне
сТ = 176-177 °С.плКатин - бесцветные кристаллы с Т11л = 77—78 °С, растворимые
в этаноле, хлороформе, эфире и разбавленных кислотах; практи¬
чески нерастворимы в воде. Катина гидрохлорид — бесцветные
кристаллы с Тш| = 180—181 °С, растворимы в воде и практически
нерастворимы в органических веществах.Все представители данной группы обладают оптической актив¬
ностью и имеют характерные спектры в ИК- и УФ-области.Токси коки нети ка и биотрансформацияПри оральном применении эфедрин быстро абсорбируется,
максимальная концентрация в крови достигается через 1 ч. При
приеме 10 добровольцами по 22 мг эфедрина гидрохлорида перо¬
рально его концентрация в крови составила в среднем 0,0Ь (0,04
0,14) мг/л; Р/г — около 8 ч (табл. 47).
Глава 7164Таблиця 47. Фармакокинетические параметры лфелрина и его „рои,вод-ных ВеществорКаТА, чВыведение
в неизме¬
ненном виде,%V«!,мг/кгСвязывание
с белками
плазмы крови,%9.63-1655-75Н.д.Н.д.9,83-16902-3Н.д.7,154-715-20Н.Д.Н.д.9,4340Н.д.Н.д.Катинон82,7-6Н.д.Н.д.Н.д.Примечание. Н.д. — нет данных.В организме человека эфедрин метаболизируется путем
N - д е м ети л и ро ва н и я до норэфедрина и путем окислительного деа-
минирования, за которым следует конъюгация (схема 31).Кумулируется в печени, легких, почках. Около 90% введенной
дозы выводится с мочой в течение 24 ч, причем около 55~75%
в неизмененном виде, 8—20% — в виде норэфедрина и 4—13% —
в виде дезаминированных метаболитов, таких как бензойная и
гиппуровая кислоты.Псевдоэфедрин выводится из организма в основном в неиз¬
мененном виде (около 90%) и лишь незначительная часть (око¬
ло 1%) - как основной метаболит норпсевдоэфедрин (катин)
(схема 32). Эфедрон метаболизируется до норэфедрина и норпсев-
доэфедрина (схема 33). Метаболизм катинона аналогичен метабо¬
лизму эфедрина (см. схему 31).Химико-токсикологический анализ
См. соответствующий раздел ниже.7.7.2. Мескалин и его структурные аналогиГаллюциногенный алкалоид мескалин (рис. 46) впервые выде-мпИ В г 1 Иі кактУса нейот - ЬорИорИога \villiamsii (рис. 47, см.\отстающего в Северной Мексике. Южноамери-псіиішнтІІІИги использовали мескалинсодержащие кактусы приКолумбом Т РЯЛаХ 13 несколько веков до открытия Америки(псиом и їй і'! ЯО,° 1,рименяли настои из нарезанных колечками
(пейот; и подсушенных кактусов.
ТСХ-скрининг отдельных групп токсических веществ165ФснилацетонЭфедринНорофедрин4-гидроксиэфедрин 4-гидроксинорэфедринССхема 31. Биотрансформация эфедрина
Глава 7166н— у'НПсевдоэфедрин
Схема 32. Биотрансформация псевдоэфедринаНорпсевдоэфедрнннНорпсевдоэфедрнн
Сша 33. Биотрансформаиия эфедрона
ТСХ-скрининг отдельных групп токсических веществ 167Рис. 46. Структурная формула мескалина НЗсоКроме мескалина, кактусы данного вила содержат еще два нар¬
котически активных алкалоида: пейотин и лофофорин.Учитывая фармакологические свойства мескалина, малодоступ¬
ность кактуса и низкое содержание в нем наркотического средства,
многие исследователи пытались соединить воедино свойства ме¬
скалина и амфетамина посредством введения в молекулу амфета¬
мина метоксигрупп, меняя их положения и количество. В табл. 48
представлены структурные аналоги мескалина, являющиеся нар¬
котическими средствами и включенные в Список I Перечня.Таблица 48. Соединения, относящиеся к группе мескалина и его произ¬
водныхНСХимическое названиеСписокПеречняМескалин3,4.5-триметокси-фенилэтиламинIТМАD.L -3.4.5-триметокси-альфа-метил-фенилэтиламин1ПМА4-метокс и-ал ьфа-метил -фе н ил этилам и нIДМАD.L -2.5-диметокси-альфа-метил-фенилэтмламинIСТП* (ДОМ)2-амино-1 -(2,5-диметокси-4-метил )-фенилпропанIДОЭТD.L -2,5-диметокси-4-этиламфетачинI2С-В (ДОБ)D.L -2,5-диметокси-4-бром-амфетаминIДОХD. L -2,5 -диметокси -4-хлорамфетамин1* СТП (STP) расшифровывается как «Serenity, Tranquility, Peace*, т.е.
«безмятежность, спокойствие, мир*.Физико-химические свойстваМескалин-основание представляет собой бесцветные кристал¬
лы, которые имеют способность поглощать из воздуха углекислый
Глава 7168 т _ ^_зб °С Умеренно растворим в воде, растворим в хло-
реформе и этаноле' практически нерастворим в эфире и петролей-Н0МЭеск£ина гидрохлорид - игольчатые кристаллы сТ„=181 -С
Хорошо растворим в воде и спирте.Токсикокинетика и биотрансформацияГаллюциногенные эффекты мескалина в 4000 раз слабее тако¬
вых ЛСД. Применяется перорально, путем курения или внутривен¬
но. Действие развивается через 30—60 мин после приема и длится4-6 ч.Быстро абсорбируется после орального приема. При при¬
еме внутрь мескалина в дозе 5—10 мг/кг через 30—45 мин на¬
блюдаются озноб, тошнота, головная боль, возбуждение, су¬
етливость. яркие иллюзии и галлюцинации (нередко в виде
окрашенных картин, ландшафтов). Одновременно меняется
восприятие положения тела, теряется ощущение пространства
и времени. Концентрации в плазме через 2 и 7 ч после перо-
рального приема составляют 3,8 мг/л и 1,7 мг/л соответственно-
Р/г - около 8 ч (табл. 49).Таблица 49. Фармакокинетические параметры мескалинаВеществорКаТа, чВыведение
в неизме¬
ненном виде,%V«!,мг/кгСвязывание с
белками плазмы
крови, %Мескалин9,66-1250-60Н.д.Н.д.Примечание. Н.д. - нет данных.Разовая пероральная доза мескалина выводится с мочой
за 24 ч на 90%. В неизмененном виде выходит до 65% введен¬
ной дозы, остальное количество — в виде основного метабо¬
лита - 3.4,5-триметоксифенилуксусной кислоты (27—30%),
\'-ацетил-3,4-диметокси-5-гидроксифенетиламина (около 5%) иМ-ацетилмескалина (0,1%) (метаболизм мескалина отражен на
схеме 34).Химию-токсикологический анализ
См. соответствующий раздел ниже.
ТСХ-скрининг отдельных групп токсических веществ 169ІЧ-ацетилмескалин МескалинОСН33,4,5-три мето кс ифе н ил-
уксусная кислота
/ОСН3М-ацетнл-3,4-диметокси-
5 - гидроксифе нетилами нОСН3
ОСН33,4,5-триметоксибензойнаякислотаСхема 34. Метаболизм мескалина7.7.3. Амфетамин и его структурные аналогиАмфетамин и его структурные аналоги относятся к синтетиче¬
ским фенилалкиламинам, которые составляют значительную часть
НС в незаконном обороте на территории РФ.Амфетамин (рацемат ё,1-аль¬
фа-метилфенилэтиламин), струк- Н2і>
турная формула которого пред- ^ л=\ СНі
ставлена на рис. 48, широко и
давно применяется как в терапии
(под торговыми названиями фе¬
намин и бензедрин), так И с не- рИс. 48. Структурная формула ам
медицинскими целями. Амфета- фетамина
Глава 7170 1Я87 г как аналог эфедрина и сразу получил
мин синтезирован в 1во/ . ингаляционНое средство для рас-широкое РаслРостранен”,ти П0И лечении бронхиальной астмы,
ширения бронхов, в частности ^ к т1 г и с ^Психоактивные своист в качестве стимулятора ЦНС. Од-пор началось его исп>’-|ь г0 наблюдения были сделаны вы-нако в результате почти 30-летнего н, н кроме ^воды о Ф°1’мировани последствия длительного и регулярного
стали очевидными тяжелы вероятноСти мозговых кро-вИоС™ГИповь,шение давления крови, аритмии, а также пара-
„”ы'психозы,- Эта информация потребовала резкого огра-
ГГия и контроля лекарственного применения амфетамина.
Амфетамин в качестве стимулятора используется различными
категориями людей в различных ситуациях, требующих длитель-
ной физической и умственной работоспособности (молодыми
людьми на дискотеках, водителями грузовиков в дальних поезд¬
ках для ночного бодрствования, спортсменами). Известно, что во
время Второй мировой войны солдаты обоих фронтов принимали
амфетамин как средство против усталости.Метамфетамин (рацемат (1,1-Ы-альфа-диметилфенилэтиламин)
представлен на рис. 49. Лекарственное средство (первитин), раз¬
решенное в США, представляет собой с!-изомер метамфетамина.
Препарат используется с 1919 г. в качестве аналептика при алкоголь¬
ной или наркотической интоксикации (для преодоления состояния
ступора), во время хирургических операций для поддержания кро¬
вяного давления при анестезии. В настоящее время основная сфера
применения метамфетамина как лекарственного препарата в стра¬
нах, где он зарегистрирован, - лечение детской гипоактивности с
расстройством внимания.В настоящее время наряду с амфетамином и метамфетамином
на территории РФ с теми же целями используется ряд соединений,полученных путем модифика¬
ции структуры амфетамина и
метамфетамина в результате за¬
мещения водорода в бензоль¬
ном кольце (дезопимон) или в
аминогруппе (этиламфетамин и
Рис. 49. Структурная формула ме- ® табл. 50 приведены НС и' ^ ,мина психотропные вещества, являю-
TCX-скрининг отдельных групп токсических веществ 171щиеся производными амфетамина и включенные в Списки I, II иIII Перечня.Таблица 50. Перечень НС и Г!В, являющихся производными амфетаминаНазваниеСписок ПеречняАмфетаминIIЛсвамфетаминIIЛевометамфетаминIМетамфетаминIДексамфетаминIN-диметиламфетаминIЭтиламфетаминIIIБензфетамин ’IIIФентерминIIФенпропорексIIIФенатинIОсновное количество препаратов, приведенных в табл. 50, по¬
ступает в нелегальную продажу из подпольных лабораторий, неко¬
торая часть — из легальных источников в виде фармацевтическихсредств.В нелегальную продажу амфетамин (Bennies, White cross) и ме-
тамфетамин поступают в различной дозировке и формах: амфета¬
мин в основном в виде таблеток (иногда в виде капсул, сиропов и
эликсиров); метамфетамин (Speed, Crank, «Мент», «Винт») в виде
порошка (реже встречаются таблетки).Как правило, чистота продукта, синтезированного в подполь¬
ной лаборатории, составляет 90—99%. Однако для продажи содер¬
жание основного компонента доводится до 40% или менее путем
добавления углеводов (глюкозы, лактозы, крахмала), магния суль¬
фата, а также эфедрина.В 1985 г. на нелегальном рынке наркотиков на Гавайях впервые
было отмечено появление новой формы метамфетамина для куре¬
ния, которая представляла собой кристаллический метамфетамин,
по внешнему виду сходный с кусочками кристаллической соли и
получивший поэтому уличное название «!се» («лед»). Очень быстро
«лед» распространился по остальным странам мира, но вплоть до
_ Глава 7172 и» воспринят к;)к всеобщая проблема, а рас-
1987 г. этот фаю не бы _ е явление. Из-за легкости получения
сматривался лишь как г юго привыкания «лед» приводит к
слишком большой дозы ^ ^ «Крэк».летальному исходу даже чащ. ^ ^.ЭНантномер метамфетамина
«Лед» это чни ь * ’ усл0ВИй синтеза получают «лед»тХГкГства "о чистоте и эффективности средства судят ио
еТда' Бесцветным и прозрачный «дед» - это «водная., иди
«гидратная», форма, он быстро сгорает, образуя молочно-белый
1™ток Желты.' «лев» - «жирная», или «масляная», форма, он
Пеннее сгорает, образуя коричневый или черный остаток.
В отличие от марихуаны или «крэка», «лед» не имеет запаха и не
дает запаха при курении (одна из причин роста его популярности).
Другой причиной популярности является то, что «лед» дает долгий
аффект, длящийся до 14 ч, в то время как, например, воздействие
«крэка» продолжается всего несколько минут.Таблетки амфетамина принимают внутрь орально. Порошко¬
образный амфетамин и метамфетамин вдыхают через нос или в
виде раствора вводят внутривенно, «лед» курят.Для амфетаминов характерна «циклическая» форма примене¬
ния. После инъекции или «сеанса» курения ощущается короткий,
но очень сильный эффект, всплеск ощущений, длящийся несколь¬
ко минут. После спада эффекта, несмотря на то, что концентрация
стимулятора в крови все еще достаточно высока, вводится следую¬
щая доза, затем следующая и г. д. Например, ритм цикла может
быть таким: инъекции производятся каждые 50-60 мин в течение2-3 дней, затем следует период отказа от наркотика (6-10 ч), уга¬
сание симптомов и сон в течение I—2 сут.1аким образом, злоупотребление амфетаминами, подобно эпи-
лемии распространилось по странам Европы, Северной Америки
и Азии. Однако в Европе запрещенное производство амфетамина
превышает производство метамфетамина, а в Северной Америке
более популярен метамфетамин.Физико химические свойствесобой ч а Г/Г"’ ,1М(^)Сгамин и метамФетамин представляютж~ с т — 200 -с-минеральных кистою .• пг, рмом 11 ■’Фиром. Растворимы в
Ш1 °6рм<-«анием соответствующих солей.
ТСХ-скрининг отдельных групп токсических веществ173Амфетамина фосфат — белый кристаллический порошок, раз¬
лагающийся при Г = 300 “С. Очень хорошо растворим в воде, пло¬
хо растворим в этаноле, практически нерастворим в хлороформе,
бензоле и эфире.Амфетамина сульфат — белый кристаллический порошок с ТШ1
выше 300 С (с разложением). Растворим в воде (1:9) и этаноле
(1:515), практически нерастворим в хлороформе и эфире.Метамфетамина гидрохлорид — белые кристаллы или белый
кристаллический порошок с ТМ1 = 170—175 °С. Растворим в воде
(1:2), этаноле (1:4), хлороформе (1:5), практически нерастворим в
эфире.Вещества обладают оптической активностью, причем изомеры
отличаются формой кристаллов, Т|п, растворимостью.УФ-спектры амфетаминов в водно-кислой среде имеют харак¬
терную для бензольного кольца полосу поглощения.Токсикокинетика и биотрансформацияПосле орального применения амфетамины быстро всасывают¬
ся в желудочно-кишечном тракте и распределяются по органам и
тканям. Действие наступает через 5-15 мин, при внутривенном
введении — через 30 с. При курении метамфетамина максимальная
концентрация в крови устанавливается через 7 мин после начала
курения.Обычная оральная или интраназальная доза амфетамина для
использования с немедицинскими целями равна 5-15 мг, доза ам¬
фетамина для внутривенного введения — 20-40 мг.Период полувыведения амфетаминов из плазмы составляет8—12 ч (табл. 51). В зависимости от pH мочи эта величина может
меняться: от 8 ч (7—14 ч) при кислых и до 22 ч (18—34 ч) при ще¬
лочных значениях.Таблица 51. Фармакокинетические параметры амфетамина и метамфета¬
минаВеществорКаТУз, чВыведение
в неизме¬
ненном виде,%\а.мг/кгСвязывание
с бедками
плазмы крови.%Амфетамин9.87-10743-416-40Метамфетамин10,18-12434-710-20
174 - —_£лава7Амфетамины распределяются по всему организму. Хотя При
физиологических значениях pH соединения ионизированы, ОНи
легко преодолевают гематоэнцефалическии барьер и после вну¬
тривенного введения достигают головного мозга через несколько^Основной процесс биотрансформации амфетамина в организме
человека - дезаминирование, менее выражены гидроксилирова-
ние ароматического цикла, |3-гидроксилирование и N-окисление.
Основной процесс биотрансформации метамфетамина —
Т^-деметилирование (схема 35). Гидроксилированные метаболиты
далее конъюгируются с глюкуроновой и серной кислотами.Химико-токсикологический анализ
См. соответствующий раздел 7.7.5.а тон,сг^НМСН3 ^ 'ОН
4-гилроксиметамфетаминNH24-гидроко ггаминМетамфетаминщ« гилр.жсинорзфелрин 0НЛшнонГ липли• '■'»ши Ьснюймаи кислота* V«« 35. Ьишрансформааии амфетамина и метамфетаминаонI фенил-2-пропанол
ТСХ-скрининг отдельных групп токсических веществ 1757.7.4. Метилендиоксипроизводные амфетаминаВ последние годы среди синтетических НС широкое распро¬
странение получили 3,4- и 4,5-метилендиоксипроизводные ам¬
фетамина (рис. 50). Эта группа НС была получена вследствие
модификации структуры амфетамина посредством введения заме¬
стителей в бензольное кольцо и боковую алкиламинную группи¬
ровку (табл. 52).Таблица 52. Структура некоторых метилендиоксипроизводных амфетами¬
наМетилендиоксипроизводные амфетаминаR.*43,4-метилендиоксиамфетамин (МДА)ннн3,4-метилендиоксиметамфетамин (МДМА)ннсн,Г^-этил-3,4-метилендиоксиамфетамин (МДЕА)ннС2Н5М,М-диметил-3,4-метилендиоксиамфетамин (МДДМА)нсн,сн,1-(3,4-метилендиоксифенил)-2-бутамин (БДБ)сн,ннМ-метил-1-(3,4-метилендиоксифенил)-2-бутамин(МБДБ)сн3сн,нЫ-гидрокси-3,4-метилендиоксиамфетамин(N-OH-МДА)н....нонМетилендиоксиамфетамин («Love drug») снтезирован в 1910 г.
и является родоначальником метилендиоксипроизводных амфета¬
мина. Синтезированный в 1914 г. МДМА (известный под улич¬
ными названиями Ecstasy, Adam, «Экстази») некоторое время
использовался в психиатрии в качестве средства, снижающего бес¬
покойство и придающего пациенту эмоциональную открытость.
Отсутствие информации о тяжелых побочных эффектах и привы¬
кании, свойственных другим подобным средствам, обусловило его
популярность и невозможность социального противодействия рас-Рис. 50. Общая формула метилендиоксипроизводных амфетамина
близких ДРУ^и /V—ис./л ных соединений как угрозу общественному здоровью и объявить
их средствами, запрещенными к применению.ЛЛ - X В настоящее время метилендиоксипроизводные амфетамина
получили широкое распространение во многих странах, включая
РФ, из-за их способности вызывать легкую эйфорию и особое пси¬
хическое состояние, проявляющееся в расширении и обострении
эмоционального воспрятия, возрастания силы эмоций и ощущений
(в том числе и при половом акте). Эти свойства обеспечивают особую
привлекательность метилендиоксипроизводных амфетамина в моло¬
дежной среде, на вечеринках и дискотеках. Причем эмоциональные
воздействия не сопровождаются галлюциногенными проявлениями.
Галлюциногенный эффект развивается при употреблении МДА в вы¬
соких дозах, в незначительной степени свойственен МДМА и не ха¬
рактерен для МБДБ, т.е. МБДБ — «чистый» энтактоген.После спада основных проявлений влияния указанных нарко-
гиков ра;виьается сонливость, спутанность сознания и нарушение
координации. ""Уфивенное введение.
ТСХ-скрининг отдельных групп токсических веществ177В настоящее время все метилендиоксипроизводные амфетами¬
на запрещены для употребления и введены в Список I Конвенции
ООН и Список I «Перечня наркотических средств, психотропных
веществ и их прекурсоров, подлежащих контролю в РоссийскойФедерации».физико-химические свойстваВ виде оснований метилендиоксипроизводные амфетамина
представляют собой маслянистые жидкости, в виде гидрохлори¬
дов — белые или белые со слегка желтоватым оттенком кристал¬
лические порошки с характерными Тпл. Легко растворимы в по¬
лярных растворителях и практически нерастворимы в хлороформе
и эфире. Метилендиоксипроизводные амфетамина обладают опти¬
ческой активностью и имеют характерные области поглощения в
УФ- и ИК-спектрах.Токсикокинетика и биотрансформацияФармакологический эффект метилендиоксипроизводных ам¬
фетамина проявляется через 30—45 мин после орального приема,
достигает максимума через 1 — 1,5 ч и продолжается от 3 до 10 ч.
Последействие может продолжаться в течение нескольких дней.
Период «полужизни» МДМА в плазме ТУ2 = 7,6 ч (табл. 53). После
приема внутрь соединения быстро всасываются и обнаруживаются
в плазме лишь через 15—30 мин после применения.Таблица 53. Фармакокинетические параметры МДА и МДМАВеществорКаТ/г, ЧВыведение
в неизме¬
ненном виде, %Уё,мг/кгСвязывание с
белками плазмы
крови, %МДА9,7Н.д.Н.д.Н.д.Н.д.МДМА10,36-865Н.д.65Примечание. Н.д. - нет данных.Биотрансформация метилендиоксипроизводных амфетамина
протекает в основном как два перекрывающихся процесса. Пер¬
вый не затрагивает циклический заместитель и включает дезал-
килирование азота боковой цепи (метаболит I), окислительное
дезаминирование (метаболит V), гидроксилирование ароматиче¬
ского кольца (метаболит VI). Второй процесс идет с окислени-
ем метилендиокси-заместителя и образованием соответствуЮщИх
3.4-метокси- и/или гидроксизамешенных фенилалкиламинов (Ме_
таболиты 11-1У)- Аналогичный процесс проходит с участием мета¬
болитов I и V. Гидроксилированные метаболиты далее конъюгиру¬
ются с образованием глюкуронидов и сульфатов (схема 36).Основные метаболиты МДМА и МДЕА 4-гидрокси-З-меток-
си-производные (III на схеме). Деалкилированный метаболит МДд
образуется в меньшем количестве.у МДМАН}н&Г' / н^Ксн3XI соон XII XIIIСхема 36. Метаболизм метилендиоксипроизводных амфетамина.I метиленлиоксиамфетамин (МДА); II - 3,4-дигидроксиметамфетамин;
III ^гидрокси-З-метоксиметамфетамин (ГММА); IV - З-гидрокси-4-
метоксимпамфстачин; V - 3,4-метилендиоксифенил-2-пропанон; VI —
г и «роки МДМА; VII и-метиллофамин; VIII — 3-метокси-а-метилдо-
фамим. IX 3.4 джилроксифенилаипон (ДГФА); X — 4-гилрокси-З-
мс 11 жсифеиил и рома нон - 2 (ГМФА); XI. XII, XIII - 3,4-замешенные гип-
яуроеш кислоты; IV и VI - исроитные метаболиты
ТСХ-скрининг отдельных групп токсических веществ179Продукты окислительного дезаминирования — 4-гидрокси-3-метоксифенилацетон (ГМФА, метаболит X), 3,4-дигидрокси-
фенилаиетон (ДГФА, метаболит IX) и 3,4-метилендиоксифенил-
пропанон-2 (метаболит V) — образуются в следовых количествах.МБДБ и БДБ претерпевают аналогичную биотрансформацию.
Однако МДА, МДМА и МДЕА образуют 3,4-замешенные бензой¬
ные кислоты, вступающие далее в реакцию конъюгации с глици¬
ном с образованием соответствующих гиппуровых кислот (метабо¬
литы X—XII). Подобный метаболизм МБДБ и БДБ не установлен.Значительная часть принятого МДМА выводится в виде ис¬
ходного соединения (до 65% от принятой дозы в течение 20 ч) и
основного метаболита ГММА. На долю деалкилированного мета¬
болита МДА приходится 7% дозы.Так, отношение количества деметилированного метаболита
МДА при употреблении МДМА к содержанию родительского со¬
единения не превышает 0,15. В случае потребления МДЕА коли¬
чество деалкилированного метаболита МДА в моче в период 1—4 ч
после применения также не превышает 10—15 % от количества ис¬
ходного соединения. На основании этих количественных соотно¬
шений предложено проводить ориентировочное дифференцирова¬
ние потребления МДА в смеси с аналогами (МДМА и/или МДЕА)
от его образования в качестве метаболита. При более высоком со¬
держании МДА по сравнению с таковым МДМА или МДЕА мож¬
но предполагать совместное употребление группы родственных
соединений. Те же рекомендации высказываются относительно
МБДБ и БДБ, поскольку последний, являясь деалкилированным
метаболитом МБДБ, может также употребляться самостоятельно.Химико-токсикологический анализСм. соответствующий раздел 7.7.5.7.7.5. Химико-токсикологический анализ
фенилалкиламиновИз биологических жидкостей фенилалкиламины изолируют при
pH = 9-11 различными органическими растворителями (по схемам
1 и 2 а), но, согласно данным литературы, лучшей экстрагирующей
способностью обладает смесь хлороформ — н-бутанол (9:1).Выделение фенилалкиламинов из биотканей проводят подкис¬
ленным спиртом по методу Стаса-Отго (схема 4) и подкисленной
180 —-— й и з ф Крамаренко (схемы 5 и 6)а пп методам АЛ-Васильев жидкостной экстракции ам0„™мальиь,ми условиями ^ являются щеЛочная реакция; Гимнов ИЗ биосред И 6ИО в качестве экстрагента хлори-
„еды (pH =9-12) И использ «-бутилхлорида, дихлорме-^ВаВН“„рт™нГл°и°™лоД эфира, этилаиетата. бутилацетата.ииоогеюана, бензола и упариваиия органической фазыв конечный экстрактт ‘ соляной кислоты в метаноле (9:1) во
добавляют 1-2 капли расгеу пр0ИЗВ0ДНЫх при выпаривании.избежание потерь легкие у бнаружения фениладкиламинов иВ качестве Реаген™в при проведении ТСХ-скрининга ис-
их метаболитов на пластинке прТрГГв ДраГлорфа (оранжево-коричневые иятна на желтом. Реактив Марки (пятна различной окраски, например: меска-
лин - желтая, МДМА - синяя, амфетамин - коричневая,
метамфетамин - грязно-зеленая).• Реактив нингидрина (фиолетовая, розовая пурпурная окрас¬
ка - первичные амины; желтая окраска - вторичные амины).. Реактив Прочного черного К (пятна от розовой до пурпурно¬
фиолетовой окраски на светло-коричневом фоне).• Подкисленный раствор йодплатината (пятна различной окра¬
ски).При проведении ТСХ-скрининга на фенилалкиламины в ка¬
честве подвижной фазы используют следующие системы раство¬
рителей.рителейОбщиеиощие• ТА: метанол - 25 % раствор аммиака (100:1,5).• ТВ: циклогексан - толуол - диэтиламин (75:15:10).• ТС: хлороформ - метанол (90:10).• ТЕ. этилацетат - метанол - 25 % раствор аммиака (85:10:5).• IЬ: ацетон.• ТАЕ: метанол.• ТАЯ: метанол - «-бутанол (60:40).! ТАК ХЛ°РО(*ЮРМ ~ этанол (90:Ю).(4:4 2) ,г>0(^орм циклогексан - ледяная уксусная кислотаТАЬ хлороформ - метанол - пропионовая кислота (72:18:10).
ТСХ-скрининг отдельных групп токсических веществ181В табл. 54 приведены значения Кг отдельных представителей
фенилалкиламинов на пластинках с силикагелем О («Мегск», Гер¬
мания).Таблица 54. Значения Rf отдельных представителей фенилалкиламиновВеществоСистемы растворителей, R,ТАТВТСТЕTLТАЕTAFTAJТАКTALЭфедрин0,300,050,050,250,010,100,640,000,010,29Псевдоэфедрин0,330,540,040,170,630,09Н.д.0,000,010,30Катин0,420,250,05Н.д.Н.д.Н.д.Н.д.Н.д.Н.д.Н.д.Мескалин0,200,030,100,240,120,060,630,020,090,51Амфетамин0,430,200,090,430,180,120,75Н.д.Н.д.Н.д.Метамфетамин0,310,280,130,420,050,090,630,000,030,45МДА0,390,180,120,420,170,100,76Н.д.Н.д.Н.д.МДМА0,330,24Н.д.0,39Н.д.0,08Н.д.0,030,170,57Примечание. Н.д. — нет данных.На рис. 52 (см. цв. вклейку) представлена хроматографиче¬
ская пластинка Toxi-Lab типа А (система Toxi-Lab AB) на различ¬
ных стадиях детектирования (см. главу 6). Для хроматографирова¬
ния использовался экстракт из мочи лица, употреблявшего смесь
эфедрина и псевдоэфедрина. На рис. 53 (см. цв. вклейку) пред¬
ставлена хроматографическая пластинка Toxi-Lab типа А (система
Toxi-Lab AB) на различных стадиях детектирования (см. главу 6).
Для хроматографирования использовался экстракт из мочи лица,
употреблявшего метамфетамин. На рис. 54 (см. цв. вклейку) пред¬
ставлена хроматографическая пластинка Toxi-Lab типа А (система
Toxi-Lab AB) на различных стадиях детектирования (см. главу 6).
Для хроматографирования использовался экстракт из мочи лица,
употреблявшего МДА.В качестве методов, подтверждающих результаты ТСХ-скри-
нинга фенилалкиламинов и их метаболитов возможно применение
УФ-спектрофотометрии, ИК-спектрометрии, а с целью количе¬
ственного определения — ГХ, ВЭЖХ, ГХ/МС.
182 — rJ^Z7.8. ГАЛЛЮЦИНОГЕНЫГаллюциногены - вещества, вызывающие нарушения в воспри¬
ятии реального мира, особенно световых сигналов, запаха, вкуса,
а также искажения в оценке пространства (направления, расстоя¬
ния) и времени. Под воздействием галлюциногенов иногда про¬
исходит визуализация цвета и звука, по субъективным отзывам,
можно «слышать цвет» и «видеть звуки». Большие дозы вызываютвизуальные галлюцинации и видения.Обшей чертой галлюциногенов является их способность изме¬
нять настроение и характер мышления. Они возбуждают ЦНС, а
в результате происходит сдвиг сознания, обычно выражающийся
эйфорией, но иногда сильной депрессией или агрессией. Самое
опасное следствие применения галлюциногенов — нарушение спо¬
собности логически рассуждать, ведущее к неадекватным решени¬
ям и несчастным случаям. Иногда депрессия и «деперсонализа¬
ция* столь велики, что заканчиваются самоубийством.В течение долгого времени после выведения из организма дан¬
ных НС могут ощущаться «возвратные вспышки» (flashbacks) —
небольшие повторения психоделических эффектов, таких как ин¬
тенсификация цветового восприятия, наблюдение передвижения
фиксированных объектов, путаница в идентификации предметов.Наиболее распространенными галлюциногенами являются
ЛСД, мескалин, псилоцин и псилоцибин, фенциклидин.7:8.1. лсдЛСД - чрезвычайно сильный галлюциноген, который был осо¬
бенно популярен в 60-х годах XX в. и вновь обретает популярность
сейчас. Его получают из лизергиновой кислоты, вещества, добы¬
ваемого из спорыньи (Беса/е сотиШт), гриба, паразитирующего
на хпаковых растениях, являющегося источником эргоалкалоидов,
многие из которых применяются в качестве ЛС.Впервые ЛСД был синтезирован в 1938 г., и в течение многих
лет из-за чрезвычайно высокой эффективности его применяли при
изучении механизма ментальных расстройств.[ аллюциногенные свойства синтетического ЛСД случайно от¬
крыл швсйпарский химик Альберт Хоффман в 1943 г. при изуче¬
нии и рои 1нодных эргота. Среди 25 соединений, исследованных
ТСХ-скрининг отдельных групп токсических веществ 183Хоффманом, только d-диэтиламид лизергиновой кислоты обладалгаллюциногенной активностью.,В ПОСЛС сигматического изучения клинических эф¬фектов ЛСД в психиатрической клинике Цюрихского университе¬
та, Л С «Delysid» (Sandoz), представляющее собой ЛСД в виде тар-
трата, было выпущено на фармацевтический рынок. Последующие
годы характеризовались повсеместным распространением ЛСД в
США и Европе в качестве ЛС в психиатрии, затем последовали
спад интереса и полное прекращение клинического использова¬
ния ЛСД в начале 1970-х годов.Начало употребления ЛСД как наркотика приходится на сере¬
дину XX в. Уже к 1966 г. около 4 млн американцев пробовали этот
препарат. Общественное мнение вначале было терпимо к ЛСД и
позволило возникнуть культу его поклонников во главе с бывшим
психиатром Гарвардского университета доктором Тимоти Лири,
уволенным за эксперименты с грибами и наркотиками. В куль¬
туре движения хиппи ЛСД играл ключевую роль. Однако по мере
знакомства с последствиями приема ЛСД общественное мнение и
контролирующие организации стали решительно бороться за его
запрещение, и в 1966 г. США объявили производство, распростра¬
нение и употребление ЛСД вне закона. В Великобритании ЛСД
запретили в 1971 г.В настоящее время на территории РФ ЛСД, как и другие про¬
изводные лизергиновой кислоты, запрещены и включены в списки
I и IV Перечня (табл. 55).Таблица 55. Перечень НС и ПВ, получаемых из грибов рода PsylocybeНазваниеСписок ПеречняЛизергиновая кислота и ее производные1d-Лизергид (ЛСД, ЛСД-25)1Лизергиновая кислотаIVЭргометрин (эргоновин)IVЭрготаминIVПо химической структуре ЛСД - М,1Ч-диэтиламиМ-лизер-
гиновой кислоты (рис. 55) — аналог серотонина. Известно. ЛСД
сильный антагонист 5-НТ2-рецепторов, однако полностью меха¬
низм его действия не изучен.
Глава 1184Рис. 55. Структурная формула
N.N-ли этиламила-(1-лизерг ино¬
кой кислотыВ молекуле ЛИ iepi иновои кис¬
лоты имеются два хиральиых
центра у атомов С, и Ск, потому
возможно образование четырех
стереоизомеров. Из них един¬
ственное активное соединение —
tl-ЛСД, в молекуле которого со¬
держится экваториальная Сх-
амид-ная группа. Изомер, со¬
держащий С8-амидную группу в
аксиальном положении и назы¬
ваемый изо-ЛСД, неактивен.Синтез ЛСД в подпольных лабо¬
раториях осуществляют обычно на
основе лизергиновой кислоты или
алкалоидов эргота. Лизергиновую
кислоту получают из эргометрина
или тартрата эрготамина.Все эти методы дают «сырой» продукт, содержащий большие
количества неактивного изо-ЛСД и другие побочные составляю¬
щие. Как правило, формы ЛСД, продаваемые на улице, содержат
значительные количества изо-ЛСД.Когда ЛСД (называемый на слэше Acid, Blotter Acid, Microdot)
впервые появился в нелегальной продаже, он применялся обыч¬
но в виде разнообразных субстратов, получаемых при добавлении
капли раствора ЛСД к различным сорбирующим материалам. Наи¬
более часто распространяемые носители: кубики сахара, марки,
кусочки фильтровальной бумаги, фармакологически инертные по¬
рошки, которыми затем наполняются пустые желатиновые капсу¬
лы. Г.ще существуют так называемые пирамидки (window panes):
для их получения ЛСД вводят в желатиновую матрицу, и затвер¬
девший желатин режуг на маленькие кусочки.В 1970-е годы таблетированные формы ЛСД разных разме¬
ров и окраски были наиболее распространенными. Содержание
sun В та,ле1|<ах мялось в очень широком интервале (от 20 до
| их/) и , ia Iрулности получения гомогенного порошка для та-
м—ИИЯ ();|ИН »»типов, превалирующий в настоящее вре-п гк* л стан ля ‘)М _р ы м к е и называемый микродог («microdot»),
I се >я круглые таблетки ггримерно 1,6 мм в диа¬
ТГХ-<■ крининг отдельных групп токсических веществ185метре, характери зующиеся постоянной дозировкой 50—100 мк!ЛСД и таблетке.ХО-е годы XX в. характеризуются повсеместным распростране¬
нием имнрегнированных бумажных форм (гак называемых «ма¬
рок»). В отличие от ранее принятого способа их приготовления (до
сих пор встречающегося в некоторых странах), когда небольшое
количество раствора ЛСД капельным способом наносилось на бу¬
магу, новый способ приготовления бумажных дозированных форм
состоит в погружении листов подготовленной бумаги в раствор
ЛСД, что гарантирует получение наиболее однородною продукта.
Обычно уги листы перфорируются на квадраты (около 5 мм2), со¬
держащие типичную дозу 30—50 мкг ЛСД. На поверхность листов
наносятся разнообразные рисунки - от абстрактных картинок до
анимационных фигурок.При приеме 10—15 мкг ЛСД через несколько минут начинаются
изменения в настроении, эмопиях, появляется смех, иногда крик.
Возникают эйфория, изменения в восприятии окружающего, по¬
являются зрительные и тактильные, реже слуховые галлюцинации.
Через 30—90 мин развиваются субъективные эффекты, продолжаю¬
щиеся 8-12 ч. ЛСД способен вызывать возвратные галлюпинации
даже спустя 6 мес с момента последнего употребления.Социальные последствия употребления ЛСД представляют со¬
бой основную проблему, связанную с его распространением. Вы¬
зываемые ЛСД психологические и психические нарушения ведут
не только к асоциальному поведению, но и провоцируют действия
и поступки, причиняющие вред непосредственно личности и даже
заканчивающиеся смертью.Физико-химические свойстваЛСД представляет собой бесцветный кристаллический порошок
с Тмл = 80—85 °С, хорошо растворимый в воде.Токсикокинетика и биотрансформацияЛСД быстро всасывается и распределяется по организ¬
му, легко преодолевая гематоэнцефалический барьер и дости¬
гая мозга. Время «полужизни» в плазме — 3,6 ч (табл. 56). Дли¬
тельность действия — 8—12 ч. Уровни ЛСД в плазме и моче
в течение нескольких часов после приема разовой дозы — око¬
ло 1 нг/мл. Максимальная концентрация в плазме после прм
ма орально 1 мкг/кг ЛСД достигается через I ч и в интервале до
186Глава 73 ч составляет 1,7-1,87 нг/мл. Затем концентрация резко снижает¬
ся- через 6 ч - до 1,1 нг/мл, через 24 ч - до 0,2 нг/мл. Пик кон¬
центрации в плазме после употребления дозы 2 мкг/кг составляет
4-6 нг/мл в течение I ч.Таблица 56. Фармакокинетические параметры ЛСДВеществорКаТА, чВыведение
в неизмененном
виде, %Vd,мг/кгСвязывание
с белками
плазмы крови, %лсд7,52,9-5,1Менее 10,390ЛСД быстро метаболизируется и выводится. Менее 1% дозы
обнаруживается в моче в виде неизмененного соединения. Мета¬
болизм ЛСД в организме человека полностью не изучен, основные
сведения получены за счет экспериментов с животными или экс¬
периментов in vitro с микросомами печени человека.Основной продукт превращения ЛСД in vitro: этиламид лизер-
гиновой кислоты (ЛАЭ) и его эпимер - изо-ЛАЭ. При метаболиз¬
ме ЛСД в организме человека (в отличие от опытов in vitro) ЛАЭ
образуется в незначительных количествах, а основными продук¬
тами биотрансформации являются: N-деметилированное произво¬
дное - нор-ЛСД и его эпимер; 2-оксо-ЛСД и 2-оксо-З-гидрокси
ЛСД; 12-, 13- и 14-гидрокси-ЛСД, которые выводятся с мочой в
виде конъюгатов (схема 37).
ТСХ-скрининг отдельных групп токсических веществ 187Ввиду низкой величины Ус1 ЛСД и его метаболиты практически
не накапливаются в органах и тканях. Содержание ЛСД в волосах
также очень мало и составляет пикограммовые количества.Химико-токсикологический анализИз-за низких концентраций ЛСД и его метаболитов в биологи¬
ческих жидкостях метод ТСХ при анализе образцов биообъектов
нецелесообразен. Для этих целей используют высокочувствитель¬
ные методы анализа, такие как ИФА, ВЭЖХ, ГХ и ГХ-МС.Применение ГСХ-скрининга возможно при анализе веществен¬
ных доказательств (марок, микродот и др.). ЛСД из вещественных
доказательств изолируют по схеме 10.При проведении ТСХ-скрининга на ЛСД в качестве подвижной
фазы используют следующие системы растворителей.Общие• ТА: метанол — 25% раствор аммиака (100:1,5).• ТВ: циклогексан — толуол - диэтиламин (75:15:10).• ТС: хлороформ — метанол (90:10).• ТЭ: хлороформ - ацетон (8:2).• ТЕ: этилацетат — метанол - 25% раствор аммиака (85:10:5).• ТЬ: ацетон.• ТАЕ: метанол.• ТАР: метанол — «-бутанол (60:40).• ТАЛ: хлороформ — этанол (90:10).• ТАК: хлороформ — циклогексан — ледяная уксусная кислота(4:4:2).• ТАЬ: хлороформ — метанол - пропионовая кислота (72:18:10).В табл. 57 приведены значения Я, ЛСД на пластинках с силика¬
гелем в («Мегск», Германия).Таблица 57. Значения Я, ЛСДВеществоСистемы растворителей, її,ТАТВтсТЭТЕтьТАЕТАЕТАЛТАКТАЬлсд0,600,030,390,030,560,240,600,590,330,020,59Для детектирования ЛСД на хроматографической пластинке
возможно применение следующих реактивов.• Реактив Марки (серое окрашивание).• Реактив Ван-Урка (синее окрашивание).
Глава 7Ш — —. реактив Эрлиха (темно-синее окрашивание).• Реактив Прохазки.• Реактив Лрагендорфл.. Реактив йодплатината.Кроме того. ЛСД порой обнаруживается на хроматографиче¬
ских атастинках по яркой флуоресценции при 254 и 365 нх..7.8.2. Триптамин и его структурные аналогиЭта группа наркотических веществ Списка 1 Перечня представ¬
лена тремя соединениями - N. N - д и ме тил гр» I п там ином (ДМТ).
N.N -диэтаттрмптамином (ДЭТ> и этриптамином (рис. 56).ДМТ и егс> производные широко распространены в животном
и растительном мире, но могут быть получены и синтетическим
путемОни малоэффективны, если их оральный npnexi не комбини¬
руется с приемом других веществ, снижающих скорость их мета¬
болизма. Используются интраназально. nyrext курения и парен¬
терального введения в дозах от 50 до 100 мг. Продолжительность
действия, подобного ЛСД. составляет 45—60 мин. Эффективность
ЛЭТ намного меньше, чем ДМТ. Концентрация эндогенного ДМТ
в плазме крови человека составляет х»енее чем 0,001 мкг/мл.Псилоцин и псилоцибин (рис. 57) имеют в своей основе струк¬
туру ДМТ Грибы рода Psilocybe использовались с древних BpexieH
в культовых обрчдах для достижения галлюциногенного эффекта.
В 1958 г швейцарский ученый А. Гофман выделил вещество из
грибов PsiJocybe тсасапа, названное им псилоцибином.СН-,СН;VVN.N-л>NНДКЛШтиаэпс:н.с:н,ЛТШММНнЭтрингаминvs (ДМТ'-
ТСХ-скрининг отдельных групп токсически* веществ189ОНПснлоцнні4-г*цроксн-ДМ'ПОНО—Р—онПсилоинбмн
1 сложный эфир 4-пироксн-ДМТ
и ортефхфорной кислоты)Рис. 57. Структурные формулы пенлоиинл и псилоцибинаВ химическом отношении псилоцибин (4-фосфорилокси-
диметидтриптамнн) яаляется сложным эфиром фосфорной кислоты
и 4-окснднметнлтриптамина. Позднее было установлено наличие
в грибах рода РзіїосуЬе еше одною алкалоида с галлюциногенным
действием, названного псилоцином.В Список 1 Перечня включены 3 НС. получаемых из грибов
рода РхЦосуЬе (табл. 58).Таблица 58. Перечень наркотических средств н психотропных веществ,получаемых из грибов рода Р&кхуЬеНіжинеСписок ПеречняПлодовое тело (любая часть) любого вида грибов,
содержащих псилоцибин и (или) псилоиннIПсилоцибинПсилоцииРод ЬіІосуЬе. насчитывающий приблизительно 20 видов, ши¬
роко распространен по всем континентам В России встречают¬
ся 3 вида пснлоцнбинсодержащих грибов — Ла/счт/ч* А'тИапсыш
(Ленинградская область. Дальний Восток и др.). ІпосуЬс сі>г\\іаІіпа
(Центральна и Южная Россия) и Рапаеоіт зиЫмкеапа (Централь¬
ная Россия, Сибирь).Пси лоцибинсодержашие грибы имеют непривлекательного ни и
плодовые тела, и грибники их обычно не соб и раю і как несъедоо
Глава 7живаюшими неприятный вкус, а водные растворы внугривенно.Под влиянием псилоцибинсодержащих грибов восприятие ста¬
новится необычайно ярким и интенсивным, цвета кажутся бога¬
че. музыка более эмоциональной и глубокой, а запахи и вкусовые
ошушения обострены. Обычными явлениями считаются синесте¬
зии. цвета могут слышаться, а звуки видеться. Возникают также
расстройства положения тела и восприятия времени и простран¬
ства. Галлюцинации могут быть как зрительными, так и слухо¬
выми Чаше всего отмечаются зрительные галлюцинации в виде
геометрических форм и цифр.Физико-химические свойстваПсилоиин представляет собой белые кристаллы с Т = 173-
176 С, растворимые в этаноле и разбавленной уксусной кислоте,
очень плохо растворимые в воде. В водных растворах нестабилен,
особенно если у них щелочная реакция среды.Псилоцибин представляет собой белые кристаллы. Плавится
при Т , - 185-195 С с разложением. Растворим в кипящей воде
), кипящем меганоле (1:120) и разбавленной уксусной кисло¬
те Практически нерастворим в хлороформе и бензоле.Тсхсикокинетика и биотрансформациянике Наркотический эффект возникаетI V) К иПсилоиин и псилоцибин хорошо всасываютсяываются в тонком кишеч-
через 0,5-1 ч и длится отакокинетические парамс-
ТСХ-скрининг отдельных групп токсических веществ191Таблица 59. Фармакокинетические параметры псилоцина и псилоцибинаВеществорКаТ/2, чВыведение 1
в неизменен¬
ном виде, %V«!,мг/кгСвязывание с
белками плазмы
крови,%Псилоцин10Н.д.Н.д.Н.д.Н.д.Псилоцибин9,41,8-4,5Н.д.2,5-5Н.д.Примечание. Н.д. — нет данных.Биотрансформация псилоцибина начинается в ЖКТ под дей¬
ствием щелочной фосфатазы и неспецифических эстераз слизи¬
стой оболочки кишечника. В молекуле псилоцибина расщепляет¬
ся сложноэфирная связь с фосфорной кислотой. Далее псилоцин
подвергается деметилированию, последовательному дезаминиро¬
ванию и окислению до 4-гидрокси-З-уксусной кислоты. Выводит¬
ся псилоцин главным образом в виде глюкуронидов (схема 38).-О-глюкуронидСхема 38. Схема биотрансформации псилоцина и псилоцибинаНО—Р—ОННПсилоцибин
Химико-токсикологический анализБиожидкости. 10 мл крови (плазмы) или мочи экстрагируют
ъиожадкис дихлорметана (или хлороформа)шптиесью дихлорэтан -^дихлорметан ,1:1) по схемам , и 2.Внутренние органы. Определение пндольных алкалоидов из вну¬
тренних органов методом ТСХ следует считать нецелесообразным
из-за очень малых концентраций определяемых веществ. При про-
ведении ТСХ-скрининга на псилоцин и псилоцибин в качестве
подвижной фазы используют следующие системы растворителей.Общие• ТА: метанол — 25% раствор аммиака (100.1,5).• ТВ: циклогексан - толуол - диэтиламин (75:15:10).• ТС: хлороформ - метанол (90:10).• ТЕ: этилацетат ~ метанол — 25% раствор аммиака (85:10:5).• ТЬ: ацетон.• ТАЕ: метанол.• ТАР: метанол - и-бутанол (60:40).Частные• Метанол - ледяная уксусная кислота — вода (15:2:3).• и-Бутанол - ледяная уксусная кислота - вода (12:3:5).В табл. 60 приведены значения Лг псилоцина и псилоцибина на
пластинках с силикагелем в («Мегск», Германия).Таблица 60. Значения Яг псилоцина и псилоцибинаВеществоСистемы растворителей, Я.Ь ТАТВТСТЕтьТАЕТАЕ12Псилоцин0,390,050,090,470,090,140,480,460,55Псилоцибин0,050,00Н.д.0,000,000,800,010,280,40Примечание. Н.д. - нет данных.їси ,!ГИВ ^аи'^Рка ПРИ обработке хроматографической пластин-
синей тС"СИЛОЦИНОМ И псилоцибином окраску от пурпурной до
йолп птиня-т- во,можно применение для детектирования реактива
и рсакіива Прохазки. При обработке пластинок ре-
ТСХ-скрининг отдельных групп токсических веществ193активом Эрлиха наблюдается розовое окрашивание, переходящеев фиолетовое.На рис. 59 (см. цв. вклейку) представлена хроматографическая
пластинка Toxi-Lab типа А (система Toxi-Lab AB) на различных
стадиях детектирования (см. главу 6). Для хроматографирования
использовался экстракт из мочи лица, употреблявшего псилоцин-
и псилоцибинсодержащие грибы.В качестве методов, подтверждающих результаты ТСХ-скри-
нинга псилоцина и псилоцибина возможно применение
УФ-спектрофотометрии, ИК-спектрометрии, а с целью количе¬
ственного определения — ГХ, ВЭЖХ, ГХ/МС.
Глава 8КОНТРОЛЬНЫЕ ВОПРОСЫ,
ТЕСТОВЫЕ ЗАДАНИЯ
И СИТУАЦИОННЫЕ ЗАДАЧИКОНТРОЛЬНЫЕ ВОПРОСЫ1. Рассмотрение каких аспектов предусматривает принятие ре-
шения об отнесении средства к наркотическим и введении кон¬
троля над ним? Расшифруйте каждый из них.2. Дайте определение понятиям: «наркотическое средство»,
«психотропное вещество», «прекурсор», «сильнодействующее ве¬
щество», «ядовитое вещество», «одурманивающее вещество».3. Каким нормативным документом утвержден «Перечень нар¬
котических средств, психотропных веществ и их прекурсоров, под¬
лежащих контролю в Российской Федерации»? Из каких Списков
состоит этот документ? Назовите каждый из Списков, приведите
примеры веществ, включенных в него.4. Приведите примеры скрининговых методов определения ток¬
сикологически значимых соединений. Дайте краткую характери¬
стику каждого из них.5. Дайте определение понятиям: «скрининг», «направленный
скрининг», «ненаправленный скрининг». Приведите общую схему
ненаправленного скрининга.6. Дайте характеристику моче и слюне как биологическим объ¬
ектам. Приведите схему изолирования токсикологически значи¬
мых соединений из мочи и слюны.7. Дайте характеристику крови как биологическому объекту.
Приведите схему изолирования токсикологически значимых соеди¬
нений из крови.8. Дайге характеристику желчи как биологическому объекту,
риведите схему изолирования токсикологически значимых соеди¬
нении из желчи.
Контрольные вопросы, тестовые задания И ситуационные задачи 1959. Дайте характеристику тканям мозга как биологическому объ¬
екту. Приведите схему изолирования токсикологически значимых
соединении но методу Стаса-Отто и методу В.Ф. Крамаренко.К). Данте характеристику печени как биологическому объекту.
Приведите схему изолирования токсикологически значимых сое¬
динении по методу п. Валова и методу Грусц-Харди.11. Каковы особенности изолирования контролируемых средств
из пешее I венных доказательств и растительного сырья? Приведите
схемы изолирования.12. Укажите основные требования, предъявляемые к скринин¬
говым методам.13. Дайте характеристику каждого из сорбентов в ТСХ.14. Каковы системы растворителей в ТСХ? На чем основан вы¬
бор растворителей для каждой системы? Дайте определение поня¬
тию «дискриминирующая сила», приведите расчетную формулу.15. Дайте определение величин И.г и Яч. Укажите факторы, вли¬
яющие на воспроизводимость16. Назовите реагенты, используемые для обнаружения на хро¬
матограмме токсикантов кислого, нейтрального и слабоосновного
характера.17. Назовите реагенты, используемые для обнаружения на хро¬
матограмме токсикантов основного и слабоосновного характера.18. Назовите способы количественной оценки хроматограмм.
Дайте краткую характеристику каждого способа.19. На чем основан денситометрический способ количественной
оценки хроматограмм? Какие факторы влияют на точность прове¬
денного анализа?20. Расскажите о применении системы ТохьЬаЬ в ТСХ-скри-
нинге. Дайте характеристику комплектам системы ТохьЬаЬ. На¬
зовите области применения системы Тох1-ЬаЬ.21. Каковы основные направления метаболизма токсикологи¬
чески значимых веществ? Приведите примеры метаболизма токси¬
кологически значимых соединений в организме человека (в виде
схем).22. Перечислите подтверждающие методы исследования токси¬
кантов по результатам ТСХ-скрининга.
ТЕСТОВЫЕ ЗАДАНИЯВыберите один или несколько правильных ответов.1. Каким приказом .Министерства здравоохранения СССР регламен¬
тируется перечень токсикологических вешеств, подлежащих судебно-
химическому исследованию в лаборатории бюро судебно-медицинской
экспертизы при проведении обшего анализа?1) N° 161 от 24.04.2003.2) 460 от 29.12.2000.3) № 1021 от 25.12.1973.2. В каком документе приведен перечень НС, ПВ и их прекурсоров,
подлежащих контролю в РФ?1) Федеральный закон *0 наркотических средствах и психо¬
тропных веществах» от 10.12.1997.2) Постановление Правительства РФ № 681 от 30.06.1998.3) Приказ М3 РФ № 289 от 05.10.1998.3. Укажите источник, в котором перечислены субстанции и методы,
запрещенные к использованию спортсменом в соревновательный и
несоревновательный периоды.1) Всемирное .Антидопинговое Агентство.2) Всемирный Антидопинговый Кодекс.3) Запрещенный список. Международный стандарт.4. Основными треоованнями. предъявляемыми к скрининговым мето¬
дам. являются:1) экспрессностъ;2) воспроизводимость;3) чувствительность;4) специфичность;5) точность.5. Для предварительного скрининга в ХТА применяют методы:1) иммунологические;2) ГЖХ:3) ВЭЖХ;4) ГХ-МС;
Контрольные вопросы, тестовые -«г,^ 1айания * г-*туациоммые задачи 1976. Наиболее информативными объектами скгшииит| > сердие; «ютами скрининга являются:2) кровь;3) моча:4) сальник:5) волосы.7. Объектами пя скрининга методом ТСХ чоггг быть:1) ткани мозга;2) соскоб со слизистой оболочки внутренней поверхностишски.3) минеральная вода;4) ногти:5)таблетки.8. Производные барбитуровой кислоты (фенобарбитал. этаминал,
оарбамил. барбитал) в наибольшей степени изолируются из тканейорганов следующими методами:1) Стаса—Отто;2)А.А. Васильевой;3; В.Ф. Крамаренко;4) водой, подкисленной серной кислотой, с последующим вы¬
делением методом гель-проникаюшей хроматографии.5) П. Валова.9. К веществам, экстрагируемым хлороформом при pH = 9—10, от¬
носят:1) кодеин:2) хинин;3) аспирин;4) анальгин;5) тебаин.10. Е.М. Саломатин рекомендует проводить изолирование спиртом,
подкисленным до pH = 2_3 раствором щавелевой кислоты, с после¬
дующей экстракцией оснований эфиром при pH = 13 и ре экстракцией0.5 М раствором серной кислоты следующих токсикантов.1) аминазина;2) фенобарбитала;3) стрихнина:4) дипразина;5) морфина.
Глава 8198 11. Хроматографическими параметрами, определяющими метододо-
гию ТСХ-скрининга токсикантов, являются.1) сорбенты;2) система растворителей;3) хроматографическая камера,4) подложка;5) детектирующие реагенты.12. Расположите растворители в порядке увеличения их элюирующей
способности (полярности).1) бензол;2)гексан;3) диэтиловый эфир;4) метанол;5) этилацетат.13. Идентификацию токсикантов методом ТСХ проводят по величине:1) индекса удерживания;2) коэффициента удерживания (Яг);3) коэффициента емкости;4) ширины основания пика;5) предела обнаружения.14. На воспроизводимость величины влияют:1) конструкция камеры;2) количество нанесенного токсиканта;3) толщина слоя сорбента;4) наличие соэкстрактивных веществ;5) температура окружающей среды.15. Расчет величины для конкретного токсиканта используют
с целью:1) стандартизации условий хроматографирования;2) увеличения чувствительности метода;3) получения точных результатов;4) снижения влияния факторов, обусловленных условиями ис¬
следования;5) количественного определения.16. Принцип ТСХ-скрининга токсикантов основан на:) хромагографировании в общих системах растворителей;2) сочетании общих и частных систем растворителей;> мослсловагелыюм обнаружении детектирующими реагентами;
4 параллельном использовании химических реагентов;Р< < >н>флфировании в частных системах растворителей.
Контрольные вопросы, тестовые задания и ситуационные задачи 19917. Эфирные жстракты (pH = 2) содержат следующие группы токси¬
кантов:1) производные 1,4-бензодиазепина.2) производные фен ил ал килам ина;3) производные барбитуровой кислоты;4) производные пиразолона;5) производные фенотиазина.18. Найдите соответствия.Реагент для обнаружения на пластинке1) Реактив Марки.2) Раствор РеС13.3) Н§504 + дифенилкарбазон.4) Реактив Драгендорфа.5) Реактив Браттона-Маршала.19. Найдите соответствия:Реагент для обнаружения на пластинке1) Реактив Драгендорфа.2) Раствор нингидрина.3) НС104 и 0,5% раствора №М02(97:3).4) К2Сг207 + Н2804 (концентрированная).5) УФ-свет.20. Наркотические вещества не метаболизируют в следующем био¬
логическом объекте.1) слюна;2) кровь;3) волосы;4) ткани мозга;5) моча.21. Экстракты из следующего биологического объекта имеют харак¬
терную окраску.1) моча;2) легкие;3) желчь;4) кусочки кожи;5) надпочечники.ТоксикантA. Анальгин.Б. Фенобарбитал.B. Кодеин.Г. Кофеин.Д. Нитразепам.ТоксикантA. Эфедрин.Б. Папаверин.B. Хинин.Г. Стрихнин.Д. Хлорпромазин.
200Г лава 822 Обнаружение производных фенотиазина раствором хлорной кис¬
лоты, содержащей три процента 0,5% раствора натрия нитрита, обу¬
словлено:1) наличием третичного ароматического игома <) юта,2) гидролитическим разложением;3) способностью к окислению;4) основными свойствами;5) наличием карбамияной группы.23. Обнаружение производных 1,4-бензодиазепииа по реакции
Браттона—Маршала обусловлено:1) наличием ковалентно-связанного галогена;2) гидролитическим разложением;3) способностью к окислению;4) образованием аминобензофенона;5) основными свойствами.24. Детектирование каннабиноидов проводят с помощью:1) ре актива Марки;2) реактива Фреде;3) раствора Прочною синего Б;4) раствора нингидрина;5) РР/Ч-реактива.25. Детектирование ЛСД (диэтиламид-(|-лизергиновой кислоты) про¬
водят с иомошью:1) ре актива Драгендорфа;2; реактива Лрохазки;3) раствора Прочного синего ЬБ;4) реактива Ван-Урка;5; реактива Эрлиха.сотрпжя!и1аЮ1,и,МИ ме70дами *СХ-скрининга растительного сы-
" иаРк,г,и ><=ские вещества, являются:хромогенные реакции*2) ГХ-МС;3) ИФА;4) биологические тесты;5) холииэстсразная проба.
Конфольныс иоп{,оо,| кчлоиые падания и сигуждонные чадачи 20127. Количественное определение триникличееких антидепрессантов,
элюированных по схеме I СХ-скрининга, проводят методами:1) жоракпионно-фотометрическим-2) 11ФИА;3) ГЖХ;4) В *ЖХ;5) Къельдаля.28. Для количественного определения токсикологических вешеств ие-
носредс'1 венно на хроманнрамме используют методы:1) визуальный;2) радиоавтографический;3) фотоэлектроколориметрический;4) фотоденситометрический;5) спсктрофогометрический.29. Денситометрический мегод количественного определения токси¬
кологических веществ основан на измерении:1) интенсивности люминесценции;2) интенсивности отраженного или поглощенного света в
УФ-области или видимой области спектра;3) поглощения монохроматического излучения атомами опреде¬
ляемого вещества в газовой фазе после атомизапии вещества;4) показателей светопреломления;5) величины оптического вращения угла вращения плоскости
поляризации света оптически активными веществами.30. Количественная оценка токсикологически значимых веществ по¬
сле элюировании с хроматограммы возможна с применением:1) титриметрии;2) ионообменной хроматографии;3) флуориме грии;4) фотоэлектроколориметрии;5) полярографии.31. Система Тох1-ЬаЬ (Уапап) идентифицирует токсикологически
значимые вещества из групп:1) опиатов;2) пестицидов;3) каннабиноидов;4) сульфаниламидов;5) барбитуратов.
202Глава 832. Укажите последовательность операций ТСХ-скрининга наркоти¬
ческих веществ с помощью системы ТохЬЬаЬ (Уапап):1) хроматографическое разделение;2) нанесение пробы на пластинку;3) экстракция;4) детектирование;5) концентрирование.33. Концентрирование выделенных из объекта токсикантов в системе
ТохЬЬаЬ (Уапап) осуществляется на:1) фильтровальную бумагу;2) диски из того же материала, что и хроматографическая пла¬
стинка;3) индикаторную бумагу;4) бумажные диски;5) пластинки силуфола.34. Идентификация токсиканта в системе ТохьЬаЬ (Уапап) прово¬
дится по сравнению с величиной Иг и цветом пятна обнаруженного
вещества:1)с величиной и цветом пятна вещества, приведенного в
Компедиуме наркотиков;2) величиной Яги цветом пятна вещества, найденного в Интер¬
нете;3) величиной Я,- и цветом пятна стандартного образца, нанесен¬
ного на ту же хроматографическую пластинку;4) величиной и цветом пятна вещества, выписанного из на¬
учного журнала;5) величиной Я, стандартного образца.35. Проведение предварительного гидролиза по системе Тох1-ЬаЬ
( апап) увеличивает надежность и порог обнаружения в моче токси¬
кантов из групп:П барбитуратов;2) каннабиноидов;3) опиатов;4) фенотиазинов;5) фенилалкиламинов.
Контрольные вопросы, тестовые задания и ситуационные задачи 20336. Экспрессность, надежность и чувствительность системы ТохьЬаЬ
(Уапап) — основа для ее применения:1) в ветеринарии;2) допинг-контроле;3) судебной экспертизе;4) клинической токсикологии;5) экологической экспертизе.Ответы1. 3.2. 2.3. 3.4. 1, 3,4.5. 1, 5.6. 2, 3.7. 1, 3, 5.8. 1, 4, 5.9. 1, 2, 5.10. 1, 4.11. 1, 2, 5.12. 2 -> 1 -> 3 -> 5 -> 4.13. 2.14. 1,2, 3,4, 5.15. 4.16. 2, 3.17. 1, 3, 4.18. 1 - В; 2 - А; 3 - Б; 4- В,Г, Д; 5 - Д.19. 1 - А, Б, В, Г; 2 - А; 3
Д; 4 - Г; 5 - В.20. 3.21. 3.22. 3.23. 2, 4.24. 3.25. 1, 2, 4, 5.26. 1, 2, 3.27. I, 2, 3, 4.28. I, 2, 4.29. 2.30. 4.31. 1, 3, 5.32. 3, 5, 2, 1, 4.33. 2.34. 3.35. 2, 3.36. 1, 2, 3, 4, 5.
Глава 8204 СИТУАЦИОННЫЕ ЗАДАЧИСитуационная задача № 1На ХТА доставлены: кровь, моча, промывные водь, жедудка, во-Л° Обстоятельства деда. Стюардесса, обслуживающая рейс Кабуд -
Москва, обратила внимание на оживленное поведение, интенсив¬
ную жестикуляцию, повышенную речевую активность пассажира N.
При его движении по проходу самолета наблюдалось резкое на¬
рушение координации и создание конфликтных ситуаций с дру¬
гими пассажирами. Обшаясь с пассажиром Ы, стюардесса отме¬
тила смазанную речь, бледность лица и суженные зрачки, о чем
поставила в известность командира экипажа. После приземления
лайнера наркологическая служба таможни предложила пассажиру
N пройти рентгенографию и мануальное обследование.Информация. В ходе освидетельствования установлено следую¬
щее. Обследование полостей тела и естественных отверстий не
дало результатов. В процессе рентгенографического исследования
в желудке пассажира N было обнаружено несколько предметов, по
форме напоминающих контейнеры, один из которых поврежден.При проведении ТСХ-скрининга хлороформного экстракта (pH
= 9-10), полученного из мочи в общей системе растворителей ТС
хлороформ - метанол (9:1), установлено наличие пятен со зна¬
чением Яп = 0,12, = 0,19, Яп = 0,35 кирпично-красного цвета
после детектирования реактивом Драгендорфа.При исследовании в частной системе растворителей № 4 после
обработки пластинки реактивом Марки проявились пятна фиоле¬
тового цвета со значением Я(| = 0,02, = 0,47, Я = 0,25Характерные особенности поведения', результата ре’нтгеногра-
скрининга позволили сделать заключение: пассажир N
ми7жД,"еТ1?М ,человек> перевозящий упаковки с наркотика-
Состояние задеРжанного резко ухудшилось, потре-
цГ,Г 1ГИРУРГИЧеСКОе вмеша™ьство - энтеротомия
ных бГо^“ ПР0ВеС™ ХТА на НС в доставлен¬ной в конце <раздела ° с'' 2 П провес™ по схеме. представлен-
Контрольные вопросы, тестовые задания и ситуационные задачи205Ситуационная задача № 2На СХЭ доставлены внутренние органы (желудок с содержи¬
мым, печень, почки, сердце, легкие, головной мозг, селезенка),кровь, моча, волосы трупа.Оосгоятельства дела. В одном из общежитий Сингапура нашли
26-летнюю китаянку, лежавшую в кровати без движения. След¬
ствием установлено, что умершая работала в ночном клубе, где
предлагала таблетки «Экстази* посетителям.Информация. Посмертное обследование трупа не выявило при¬
знаков насильственной смерти. В легких обнаружили умеренный
отек с геморрагией на срезе. Каких-либо других морфологических
изменений со стороны сердца, печени и почек не отмечено. Полу¬
ченные извлечения из внутренних органов и биологических жид¬
костей исследовали по схеме ТСХ-скрининга токсикологически
значимых веществ основного характера методом одномерной вос¬
ходящей хроматографии на пластинках с силикагелем О фирмы
«Мегск». В качестве подвижной фазы использовали общую систему
растворителей ТЕ этилацетат - метанол - 25% аммиак (85:10:5).
При обработке реактивом Марки проявилось пятно синего цвета
сЯ, = 0,39.Цель исследования: провести СХЭ доставленных биообъектов
на наличие токсиканта из группы НС и ПВ.Решение ситуационной задачи провести по схеме, представлен¬
ной в конце раздела, с. 211.Ситуационная задача № 3На ХТА доставлены: кровь, моча.Обстоятельства дела. Молодая женщина несколько раз будила
своего 4-летнего сына, спавшего уже более 10 ч, однако он никак
не просыпался. Наступил вечер, затем утро следующего дня, но ре¬
бенок продолжал спать. Наблюдая за малышом, мать обнаружила
непроизвольные ритмические двухфазные (с быстрой и медленной
фазой) движения глазных яблок и периодическую остановку взгля¬
да. Встревоженная женщина спросила у старшей дочери, где они
были с братом накануне и что делали. Девочка рассказала, она ви¬
дела брата около клуба, собиравшим окурки сигарет и жующим их.
Мать срочно вызвала врача, госпитализировавшего ребенка.
206 1ЛЭВ^8Информация: результаты осмотра в клинике тяжелое угне¬
тение ЦНС, апноэ, судороги, миоз, необычное положение тела.
Исследование биологических жидкостей по схеме ТСХ-скрининга
показало наличие токсиканта из группы наркотических анальгети¬
ков - производных фенилпиперидина. При хроматографировании
пластинки в системе растворителей ТА метанол — 25% аммиак
(100:1,5) и дальнейшем проявлении пластинки реактивом Эрлиха
проявилось пятно красного цвета (R, = 0,59).Известно, что в конце 1950-х годов крупная фармацевтическая
компания «Park-Davis» выпустила данный препарат в качестве
седативного и анальгезирующего средства. Предполагалось, что
в отличие от других анестетиков, препарат не угнетает дыхание
и сердечную деятельность. Однако у пациентов, которым препа¬
рат давали при анестезии, развивались дистрофия и возбуждение.
Средство изъяли с фармацевтического рынка, и сегодня офици¬
ально используют только в ветеринарии, а нелегально — как НС.Данное соединение легко синтезируется из недорогих веществ.
Его продают в качестве наркотика (вместо марихуаны, меска¬
лина, псилоцибина) или фальсификата других НС. Наркоманы
Сан-Франциско назвали препарат РСР от «РеаСе Pili» («мирная
таблетка»).Цель исследования: провести ХТА доставленных биообъектов на
наличие токсиканта.Решение ситуационной задачи провести по схеме, представлен¬
ной в конце раздела, с. 211.Ситуационная задача № 4На СХЭ доставлены: внутренние органы трупа, кровь, моча,
рвотные массы пострадавших, боевые снаряды с газом.Обстоятельства дела. В одном из административных офисов сто¬
лицы Сомали Могадишо произошел террористический акт. В зда-
f и работало около 1000 сотрудников, ворвались вооруженные
представители самопровозглашенного образования «Пунтланд».
еррфисгы гребовали освободить из тюрем членов своей орга-
",'1ИИ- держанных за похищение кораблей в территориальных
1 1И ,ьи,жмиков согнали в зал для заседаний, а тер-
н-хкп м к ,ожились в одной из прилегающих комнат. Через
ас<ж н ,аж‘ раздались глухие взрывы, и в течение по-i и»м itMi-i.kr.irаСЬ стрельба и* а|1Томатов, сопровождающаяся запу-
’иаентриронанного аэрозоля с «веселящим газом».
Контрольные вопросы, тестовые задания и ситуационные задачи 207Многократные попытки полиции города освободить заложников
увенчались успехом только через 56 ч.В результате террористического акта 153 заложника погибли.
Оставшимся в живых с поражениями разной степени тяжести ока¬
зали неотложную токсико-терапевтическую помощь в специализи¬
рованных лечебных учреждениях.Информация. Действию ядовитого аэрозоля в условиях невенти-
лируемой аудитории способствовали гипоксия, гиподинамия, от¬
сутствие воды, продуктов питания и канализации.В процессе транспортировки в автобусах люди были без созна¬
ния, в положении полулежа или полусидя, с запрокинутой голо¬
вой. Такое положение приводит к западанию языка, захлебыванию
рвотными массами и прекращению дыхания.ТСХ-скрининг биообъектов на наличие токсиканта показал,
что основным компонентом аэрозоля является производное пи¬
перидина, которое выпускается в спиртовом растворе в виде соли
лимонной кислоты в ампулах по 10 мл. Через 2—3 мин после вве¬
дения оказывает сильное анальгезирующее действие на протяже¬
нии 15—30 мин. Применяют для премедикации, вводного нарко¬
за, послеоперационной анестезии и нейролептоаналгезии в дозах
200—600 мкг. В более высокой дозе (50—100 мкг/кг) используют
для операций на открытом сердце.Болевая чувствительность подавляется почти полностью, что
объясняется легким проникновением вещества через гематоэнце-
фалический барьер. Концентрация в тканях головного мозга в 10
раз превышает его концентрацию в крови.Профессор B.C. Галкин в своих работах показал: скорость и
величина усвоения НС рецептивным полем легких идентичны та¬
ковым при внутреннем пути введения.Цель исследования: провести СХЭ внутренних органов трупа,
биологических жидкостей, вещественных доказательств на нали¬
чие психотропных средств и наркотических веществ.Решение ситуационной задачи провести по схеме, представлен¬
ной в конце раздела, с. 211.Ситуационная задача № 5На ХТА доставлены: кровь, моча.Обстоятельства дела. Бывший зоолог и охотовед после выходана пенсию устроился сторожем в коттедже.
Глава 8208 АППМ когда хозяева отсутствовали, он услышал
Однажды вечер . ^ доча- сторож обошел участок, од¬
носторонний шу • о6наружил. Через полчаса услышал звук от-
нако посторон комнате появились два мужчины и началикрываюшегося окна^В ком^ ^ сторож снял ^ ^о^нГье Ружье и выстрелил. Один из грабителей упал на пол,
Грои успел выскочить в окно. При попытке подняться мужчина
почувствовал уменьшение тонуса мыши в восходящем направле¬
нии нижние конечности - туловище - руки - голова; ослабление
тонуса разгибателей, затем сгибателей.В области бедра появилась кровь, состояние характеризовалось
спутанностью сознания, тяжелым головокружением, затруднением
дыхания, замедленным сердцебиением.Сторож решил вызвать скорую помощь. Приехавшим врач за¬
фиксировал аритмию, пониженное АД, обильное ^прекращаю¬
щееся кровотечение.Информация. Работая в одном из охотничьих хозяйств, сторож
имел опыт использования микстовых пуль, начиненных физио¬
химикатами, дающих эффект, подобный таковому яда кураре.
Поражение микстовыми пулями временно парализует скелетную
мускулатуру животных, функцию зрительного и слухового анали¬
заторов. Характерными признаками ингредиента пули являются
сонливость, нистагм, диплопия.ТСХ-скрининг биообъектов на наличие токсиканта показал,
что микстовая пуля, ранившая грабителя, содержит миорелаксант
центрального действия. При хроматографическом исследовании
экстракта на наличие токсикантов кислого, нейтрального и сла¬
боосновного характера по схеме ТСХ-скрининга в общей системе
растворителей хлороформ - ацетон (9:1) в зоне Б при обработке 1%
раствором ванилина обнаружено пятно желтого цвета с = 0,11.
Затем пятно элюировали метанолом и далее исследовали в частной
системе растворителей ацетон — бензол — ледяная уксусная кис¬
лота (45:5:1).Цель исследования: провести ХТА представленных объектов на
наличие неизвестного токсиканта.Решение ситуационной задачи провести по схеме, представлен¬
ной в конце раздела, с. 211.
Контрольные вопросы^ тестовые задания и ситуационные задачи209Ситуационная задача № 6На X IЛ доставлены: кровь, моча, кусочки сахара.Обстоятельства дела. 17-летний юноша пошел с друзьями на
рок-концерт леюндарной рок-группы «13th Floor Elevator» из Те¬
хаса, руководимой Роки Эриксоном. Во время перерыва молодые
люди пили прохладительные напитки, бросая в стакан кусочки
сахара. Во втором отделении молодой человек сообщил своей де¬
вушке. музыку он «видит» в форме изменчивых цветовых полос,
концертный зал приобрел искаженный вид, стены наклонились.
Музыканты превратились в маленькие фигуры уродцев, а их ин¬
струменты перемещаются в пространстве, оставляя хвост (след).
Испуганная девушка доставила юношу в отделение неотложной
помощи.Информация. Врач констатировал у юноши нарушение психи¬
ческого статуса. Известно, что подобное состояние, а также воз¬
буждение наблюдаются при инфекционных заболеваниях (менин¬
гите и энцефалите), метаболических расстройствах (гипертермии),
электролитных нарушениях, гипер- или гипотиреозе, а также пси¬
хических заболеваниях. Сотрудники ФСКН изъяли в качестве ве¬
щественных доказательств кусочки сахара. У пациента взяли про¬
бы мочи и крови для определения концентрации глюкозы (для
исключения гипогликемии), а также проведения исследования на
наличие НС и ПВ.При ТСХ-скрининге кусочков сахара обнаружилось пятно си¬
ней окраски (Rf = 0,33) после обработки хроматографической пла¬
стинки реактивом Ван-Урка. В качестве подвижной фазы исполь¬
зовалась общая система растворителей TAJ хлороформ — метанол
(90:10).Сим патомиметическая симптоматика токсиканта возникает
уже через 5— 10 мин. Она включает мидриаз, тахикардию и воз¬
буждение. Галлюцинации и психические изменения наблюдаются
спустя 30-60 мин. Как правило, человек погибает не в результате
фармакологического эффекта токсиканта, а из-за обусловленных
делириозным состоянием поступков (самоповреждения, травмы,
депрессии и самоубийства).Цель исследования: провести ХТА доставленных биообъектов и
вещественных доказательств на наличие токсиканта.Решение ситуационной задачи провести по схеме, представлен¬
ной в конце раздела, с. 211.
210Глава 8Ситуационная задача № 7На ХТА доставлены: кровь, моча, таблеткиОбстоятельства дела. Пожилой мужчина, прошедшии повтор¬
ный курс химиотерапии, вернулся из клиники домой. Несмотря
на внимание и заботу близких, больной чувствовал слабость, го¬
ловокружение и, что больше всего беспокоило домашних, отсут¬
ствие аппетита. Больного навестил сын, предложивший принять
таблетки для улучшения аппетита. На следующий день мужчина не
смог сконцентрировать внимание на разговоре с женой, правильно
оценить, на каком расстоянии находятся окружающие предметы,
чувствовал полную беззаботность и приятную расслабленность; у
него усилились зрительные и слуховые восприятия. На следующий
день мужчину' госпитализировали.Информация. Действующее вещество, входящее в состав табле¬
ток. включено в Список I Перечня. В США и Германии разреше¬
ны к медицинскому применению (под контролем медицинского
персонала, при наличии соответствующих показаний) препараты,
содержащие это вещество.ТСХ-скрининг проводили сначала в общей системе растворите¬
лей ТА метанол — 25% аммиак (100:1,5), а затем в частной: ацетон —
гептан - ледяная уксусная кислота (30:22:0,5). Детектирование
осуществляли реактивом прочного синего ББ. На хроматограмме
проявились пятна с различным значением Я,-оранжевого, красного
и красно-фиолетового цвета.Цель исследования: провести ХТА доставленных биообъектов и
вещественных доказательств на наличие токсиканта.Решение ситуационной задачи провести по схеме, представлен¬
ной в конце раздела, с. 211.Ситуационная задача № 8На ХТА доставлены: моча.ГИмТГЛЛЬСТВа ДеЛа* На стаиионаРном посту ДПС сотрудник
по полосе ^:^аВТОМОбИЛЬ марки «Дули», который двигался
движения по полосеРаЗН°’ С ОТКЛОнением от основной траекторииУ водите!« неалеТи^п док^,ентов на машину инспектор отметил
:,бСТаН0ИКе повеДение: молодой человек
’ пальцы РУК дрожали, он периодически
Контрольные вопросы, тестовые задания и ситуационные задачи211почесывал нос, речь его была смазана. При проверке алкометром
в выдыхаемом парнем воздухе алкоголя не обнаружилось. Подо¬
зревая водителя в употреблении наркотиков, инспектор составил
протокол для направления мужчины на медицинское освидетель¬
ствование на наличие состояния опьянения.В отделении медицинского освидетельствования на состояние
опьянения (ОМОСО) врач-психиатр на основании клинических
признаков опьянения установил состояние опьянения. У водителя
взяли мочу для дальнейшего ее направления на исследование в
химико-токсикологическую лабораторию.Информация. При ТСХ-скрининге в обшей системе ТА мета¬
нол — 25% аммиак (100:1,5) обнаружены пятна от пурпурной до
синей окраски после обработки подкисленным раствором йодпла-
тината (11п = 0,65; Яп= 0,17; 0,65).Выявленное НС (как и кустарник, из которого его получают)
включено в Список I Перечня.Цель исследования: провести ХТА представленных на эксперти¬
зу биообъектов на наличие токсиканта.Решение ситуационной задачи провести по схеме, представлен¬
ной ниже.Схема решения ситуационной задачиПри решении ситуационных задач приведите схему ХТА пред¬
ставленных на экспертизу биообъектов и/или вещественных до¬
казательств с указанием:• законов, приказов, регламентирующих правовые основы го¬
сударственной политики в сфере оборота и употребления НС
и ПВ;• названия токсиканта (международное непатентованное назва¬
ние - МНН — рациональное и уличное);• принадлежности к Перечню или к Запрещенному спискуВАДА;• химической формулы токсиканта;• физико-химических свойств токсиканта;• оптимального биообъекта скрининга с учетом физико¬
химических свойств;• фармакокинетических параметров токсиканта;• биотрансформации токсиканта в организме;
212Глава 8• способов пробоподготовки биообъектов и метода изолиро¬
вания токсиканта с использованием его физико-химических
свойств;• схемы ТСХ-скрининга (сорбент, общая и частная системы
растворителей, детектирующие реагенты);• подтверждающих методов исследования;• методов количественного определения;• результатов химико-токсикологического исследования.
ЛИТЕРАТУРАI Беликов В.Г. Фармацевтическая химия: в 2 ч: учебное пособие. - 4-е
и», псрсраб. и доп. М.: МЕДпресс-информ, 2007. - 624 с2. Бешуев Е.С., Бабаханян Р.В., Куклин В.Н. Современные проблемы
химико-токсикологического анализа наркотических средств и психотроп¬
ных веществ. - СПб.: НИ ИХ СПбГУ, 2003. - 135 с.3. Веселовская Н.В., Коваленко А.Е. Наркотики: пособие для работни¬
ков химико-токсикологических и судебно-химических лабораторий - М •
Триада X, 2000. - 206 с.4. Веселовская Н.В., Коваленко А.Е. и др. Наркотики. Свойства, дей¬
ствие, фармакокинетика, метаболизм. - М.: Нарконет, 2002. - 232 с.5. Карташов В.А., Чернова J1.B. Практикум по токсикологической хи¬
мии. - Майкоп: ООО «Аякс», 2004. - 182 с.6. Карташов В.А., Чернова Л.В. Химико-токсикологический анализ:
в 2 ч. / ч. 1. Выделение токсических веществ из биологических объектов. —
Майкоп: ООО «Качество», 2008. - 188 с.7. Кирхер Ю. Тонкослойная хроматография: в 2 т.: пер. с англ. — М.:
МИР, 1981.8. Кодекс РФ об административных правонарушениях от 30 декабря
2001 г. № 195-ФЗ (с последующими изменениями и дополнениями).9. Основы аналитической токсикологии / Р.Дж. Фланаган, P.A. Брей-
туэйт, С.С. Браун и др. - Женева: ВОС, 1997. - 363 с.10. Приказ по Министерству здравоохранения СССР № 1021 от 25
декабря 1973 г. «О введении нового перечня токсикологических веществ,
подлежащих судебно-химическому исследованию в лабораториях бюро
судебно-медицинской экспертизы».11. Постановление правительства РФ от 30 июня 1998 г. № 681 «Об
утверждении перечня наркотических средств, психотропных веществ и их
прекурсоров, подлежащих контролю в Российской Федерации» (с после¬
дующими изменениями и дополнениями).12. Постановление правительства РФ от 29 декабря 2007 г. № 964 «Об
утверждении списков сильнодействующих и ядовитых веществ для целей
статьи 234 и других статей Уголовного Кодекса Российской Федерации, а
также крупного размера сильнодействующих веществ для целей статьи 234
Уголовного Кодекса Российской Федерации».13. Приказ М3 РФ от 5 октября 1998 г. № 289 «Об аналитической
диагностике наркотических средств, психотропных и других токсическихвеществ в организме человека».14. Приказ М3 РФ от 14 июля 2003 г. № 308 «О медицинском ос ни
детельствовании на состояние опьянения* (с изменениями от 7 сентября2004 г.).
214Литература15. Родионова Г.М. Разработка системы ХТС-скрининга лекарственных
вешеств применительно к судебно-химическому анализу / Г.М. Родионо¬
ва- Дис. ... канд. фармац. наук. - М., 1977. - > 76 с.16. Руденко Б.А., Коваленко А.Е., Галузин К.А. и др. Химико-аналитическое
определение наркотических и допинговых средств. М.. Нарконет,
2007. - 367 с.17. Симонов Е.А., Найденова Л. Ф., Ворнаков С.А. Наркотические сред¬
ства и психотропные вещества, контролируемые на территории Россий¬
ской Федерации / Под ред. В.В. Рогозина. — М: Ibterlab, 2003. — 411 с.18. Симонов Е.А. Методические рекомендации по использованию мето¬
да тонкослойной хроматографии при исследовании наркотических средств
и психотропных веществ / Под ред. В.Ю. Владимирова. — М.: ЭКУ Фе¬
деральная служба РФ по контролю за оборотом наркотических средств и
психотропных веществ, 2004. — 30 с.19. Смирнов A.B., Крылова Е.Н., Кислун Ю.В. и др. Новый метод пробо-
подготовки для обнаружения наркотических веществ в моче // Микроэле¬
менты в медицине. — 2005. — №6 — С. 94—99.20. Смирнов A.B., Крылова Е.Н., Шуляк Ю.А. Особенности химико¬
токсикологического анализа наркотических и сильнодействующих ве¬
ществ в условиях специализированной лаборатории Наркологической
клинической больницы №17 // Биологические аспекты наркологии. —
2006. - №6. - С. 32-40.21. Уголовный Кодекс РФ от 19 июня 1996 г. № 63-Ф3 (с последующи¬
ми изменениями и дополнениями).22. Уголовно-Процессуальный Кодекс РФ от 18 декабря 2001 г.
№ 174-ФЗ (с последующими изменениями и дополнениями).23. Федеральный закон от 8 января 1998 г. № З-ФЗ «О наркотических
средствах и психотропных веществах».24. Федеральный закон от 31 мая 2001 г. № 73-Ф3 «О государственной«ТУлГбряТоШгГ“™ ‘ Р°ССИЙСК0Й ФеДераиИИ» <с«ж - &сГяГолаН2Ш™ЧеСКаЯ ХИМИЯ 8 2 т. - 2-е1%^-Х508МсаТ°ФаФИ>1 ‘ Т°тИХ СЛ°ЯХ ' ПоД ред' Э' Ш™я - М.: МИР,
289с7' ШвайКОт МД Токсикол°гическая химия. - М.: Медицина, 1975. -
СМ ЕС. Analysis of Dreg and Poisons. - London: Pharm. Press, 2004. -nHHio«uePuen^'dOPm8Corarol ni/ (Официальный сайт ФГУП «Антидо-’I Н..РР-^^Г^;%ГЬНЫЙ СЭЙТ KOMnaH™ Varian, Inc.)."О горолу Москве), ^ ,0Фи'1иальный сайт ФСКН. Управление
ПРИЛОЖЕНИЯПриложение 1ПРАВИТЕЛЬСТВО РОССИЙСКОЙ ФЕДЕРАЦИИ
ПОСТАНОВЛЕНИЕ от 30 июня 1998 г. № 681ОБ УТВЕРЖДЕНИИ ПЕРЕЧНЯ НАРКОТИЧЕСКИХ СРЕДСТВ,
ПСИХОТРОПНЫХ ВЕЩЕСТВ И ИХ ПРЕКУРСОРОВ,
ПОДЛЕЖАЩИХ КОНТРОЛЮ В РОССИЙСКОЙ ФЕДЕРАЦИИ
В соответствии с Федеральным законом «О наркотических
средствах и психотропных веществах» (Собрание законодательства
Российской Федерации, 1998, № 2, ст. 219) Правительство Россий¬
ской Федерации постановляет:Утвердить прилагаемый перечень наркотических средств, пси¬
хотропных веществ и их прекурсоров, подлежащих контролю в
Российской Федерации.Установить, что внесение изменений и дополнений в указан¬
ный перечень осуществляется по представлению Министерства
здравоохранения Российской Федерации совместно с Министер¬
ством внутренних дел Российской Федерации.Председатель Правительства Российской ФедерацииС. КИРИЕНКОУтвержден Постановлением Правительства Российской Федерацииот 30 июня 1998 г. № 681ПЕРЕЧЕНЬ НАРКОТИЧЕСКИХ СРЕДСТВ, ПСИХОТРОПНЫХ
ВЕЩЕСТВ И ИХ ПРЕКУРСОРОВ, ПОДЛЕЖАЩИХ
КОНТРОЛЮ В РОССИЙСКОЙ ФЕДЕРАЦИИ
Список наркотических средств и психотропных веществ, оборот ко¬
торых в Российской Федерации запрещен в соответствии с законо¬
дательством Российской Федерации и международными договорами
Российской Федерации (Список I)Наркотические средства• Аллилпродин• Альфамепродин
216• .Альфаметадол• Альфа-метилфентанил• Альфа-метилтиофентанил• Альфапродин• Альфацетилметадол• Анилэридин• Ацетил-альфаметилфентанил• Ацетилгидрокодеин• Аиетилированный опий• Ацетилкодеин• Аиетилметадол• Аиеторфин• БДБ (Ь-[3,4-метилендиоксифенил]-2-бутанамин)• Безитрамид• Бензетидин• Бензилморфин• Бета-гидрокси-З-метилфентанил• Бета-гидроксифентанил• Бетамепродин• Бетаметадол• Бетапродин• Бетацетилметадол• Гашиш (анаша, смола каннабиса)• Героин (диацетилморфин)• Гидрокодон• Гидрокодона фосфат• М-гидрокси-МДА• Гидроморфинол• Г идроморфон• Дезоморфин• Диамлромид—^.„лдмфетамин• Димепгептанол• Димстилтиамбутен1ЯНОН
Приложение 1217ДифеноксинДиэтилтиамбутенДМА (с1, 1.^-2,5-диметокси-альфа-метил-фенил-этиламин)ДМГП (диметилгептилпиран)ДМТ (диметилтриптамин)ДОБ (с1, Ь-2,5-диметокси-4-бром-амфетамин)ДОХ (с1, Ь-2,5-диметокси-4-хлор-амфетамин)ДОЭТ (с1, Ь-2,5-диметокси-4-этил-амфетамин)ДротебанолДЭТ (N,N-диэтилтpиптaмин)Изометадон
Каннабис (марихуана)КатКетобемидон
Клонитазен
Кодоксим
Кокаиновый кустКустарно изготовленные препараты из эфедрина или из пре¬
паратов, содержащих эфедринКустарно изготовленные препараты из псевдоэфедрина илииз препаратов, содержащих псевдоэфедринЛевометорфанЛевоморамидЛеворфанол (леморан)ЛевофенацилморфанЛизергиновая кислота и ее производныес!-Лизергид (ЛСД, ЛСД-25)Лист кока
Маковая соломаМасло каннабиса (гашишное масло)МБДБ (Ы-Метил- 1-[3,4-метилендиоксифенил]-2-бутанамин)
МДА (тенамфетамин)МДМА ((1, Ь-3,4-метилендиокси-М-альфа-диметил-фенил-
этиламин)3-Моноацетил морфин6-МоноацетилморфинМескалинМетадонс1-Метадон
Приложение218 • L-Метадон продукт (4-циано-2-диметиламино-. Метадона промежуточный проду* v
4.4-дифенил бутан)• Метазоцин• Метамфетамин• Метилдезорфин• Метилд и гидроморфин• 3-метилтиофентанил• 3-метилфентанил• N-метилэфедрон• Метопон• Мирофин• Млечный сок разных видов мака, не являющегося опийным
или масличным маком, но содержащего алкалоиды мака,
включенные в списки НС и ПВ• ММДА (2-метокси-альфа-4-метил-4,5-(метилендиокси)-фене-
тиламин)• Морамида, промежуточный продукт (2-метил-3-морфолин-1,1 -дифенил-пропан-карбоновая кислота)• Морферидин• Морфин метилбромид• Морфин-1Ч-окись• МППП [ 1 -метил-4-фенил-4-пиперидинол пропионат (эфир)]• Никодикодин• Никокодин• Никоморфин• Норациметадол• Норкодеин• Норлеворфанол• Норметадон• Норморфин• Норпипанон• Оксикодон (текодин)• Оксиморфон^ ного илиТмасли5ногоемакаИНСКИЙ) ~ СВернУвшийся сок опий'• Орипавин МЗК (растение вида Papaver somniferum L)• Пара-флуорофентанил (пара-фгорфентанил)
219ПарагексилГ1ЕПАП |Ь-фенэтил-4-фенил-4-пиперидинол ацетат (эфир)]ПетидинПетидина промежуточный продукт А (4-циано-1-метил-4-фе-
нилпиперидин)ПиминодинПлодовое тело (любая часть) любого вида грибов, содержащих
псилоцибин и (или) Г1СИЛОЦИН
П МА (4-метокси-альфа-метилфенилэтиламин)ПрогептазинПроперидинПропирамПсилоцибинПсилоцинРацеметорфанРацеморамидРацеморфанРолициклидин2С-В (4-бром-2,5-диметоксифенетиламин)СТП (ДОМ) [2-амино-1-(2,5-диметокси-4-метил)фенилпро-
пан]ТебаконТеноциклидинТетрагидроканнабинол (все изомеры)ТиофентанилТМА (с1, Ь-3,4,5-триметокси-альфа-метилфенил-амин)ФенадоксонФенадонФеназоцинФенампромидФенатинФенциклидинФеноморфанФеноперидинФолькодинФуретидинЭкгонин, его сложные эфиры и производные, которые могут
быть Превращены в экгонин и кокаин
. Экстракт маковой соломы (концентрат маковой соломы)
Приложения220 ^ rJ т м чтил-альфа-метил-3,4-(метиленди-
. N-ЭТИЛ-МДА [d. L-N-этилокси)-фе-нетиламил]• Этилметилтиамбутен• Этиииклидин• Этоксеридин• Этонитазен• Эторфин• Этриптамин• Эфедрой (меткатинон)Психотропные вещества• Дексамфетамин• Катин (d-норпсевдоэфедрин). Катинон (L-альфа-аминопропиофенон)• Левамфетамин• Меклоквалон• Метаквалон• 4-метиламинорекс• Метилфенидат (риталин)• Изомеры (если таковые определенно не исключены) НС и
ПВ, перечисленных в данном списке (в тех случаях, когда
существование таких изомеров возможно в рамках данного
химического обозначения)• Эфиры перечисленных в данном списке НС и ПВ, сложные
и простые• Соли всех НС и ПВ, перечисленных в данном списке, если
существование таких солей возможно• Все смеси, в состав которых входят НС и ПВ данного списка,
независимо от их количестваСписок НС и ПВ, оборот которых в Российской Федерации ограни¬
чен и в отношении которых устанавливаются меры контроля в соот-
мчствии с законодательством Российской Федерации и международ¬
ными договорами Российской Федерации (Список II)Наркотические средства• р Амимопропиофенон (РАРР) и его оптические изомеры (ан¬
тидот против цианидов)• Альфентанил,,^аМИН ^,снамин^ и комбинированные лекарственные
(кпараты, содержащие фенамин (амфетамин)
Приложение 1221• Бупренорфин• Глютетимид (Ноксирон)• Декстроморамид• Декстропропоксифен (ибупроксирон, проксивон, спазмо-проксивон)• Дигидрокодеин• Дифеноксилат• Кодеин• Кодеина фосфат• Кокаин• Кокаина гидрохлорид• Кодеин N-окись• Морфин• Морфина гидрохлорид• Морфина сульфат• Морфилонг• Омнопон• Пентазоцин• Проперидин• Пропирам• Просидол• Пиритрамид (дипидолор)• Реазек• Свечи тилидина в разных дозировках• Сомбревин• Суфентанил• Таблетки алнагона (кодеина фосфата 20 мг, кофеина 80 мг,
фенобарбитала 20 мг, кислоты ацетилсалициловой 20 мг)• Таблетки (кодеина камфосульфоната 0,025 г, сульфагваякола
калия 0,100 г, густого экстракта гринделии 0,017 г)• Таблетки кодеина 0,03 г + парацетамола 0,500 г• Таблетки кодеина фосфата 0,015 г + сахара 0,25 г• Таблетки кодеина 0,01 г, 0,015 г + сахара 0,25 г• Таблетки кодеина 0,015 г + натрия гидрокарбоната 0,25 г• Таблетки кодтерпина (кодеина 0,015 г + натрия гидрокарбо¬
ната 0,25 г + терпингидрата 0,25 г)• Таблетки от кашля. Состав: травы термопсиса в порошке0,01 г (0,02 г), кодеина - 0,02 г (0,01 г), натрия гидрокарбона¬
та — 0,2 г, корня солодки в порошке - 0,2 г
224 .ПоВДОжвНВД!'ГГ":%сп,к^„,еТС. ка все средства и вещества, указанные .
^ГГсре^не. как бы фирменными названиями (синонимами)и и обозначались.' Коитікуіь распространяется также на препараты, содержащие сред,
сш, и вешества. указанные в настоящем перечне, независимо от их №.
іичества и наличия нейтральных компонентов (подл, крахмал, сахап
бмкірбонат натрия, гапьк и т.п.). В отношении комбинированных Ле_
мч гвенных препаратов, содержащих, кроме основного контролируемо¬
го нешества, дру гие фармакологически акжвные компоненты, контроль
устанавливается в индивидуальном порядке путем включения данного
комбинированного лекарственного препарата в соответствующий список
настояшего перечня.3. Транзит через территорию Российской Федерации НС, ПВ и их пре¬
курсоров. включенных в настоящий перечень, запрещается.
Приложение 2225Приложение 2ЗАПРЕЩЕННЫЙ СПИСОК 2007
ВСЕМИРНЫЙ АНТИДОПИНГОВЫЙ КОДЕКСВступил в силу с 1 января 2008Использование любых препаратов должно быть ограничено и
оправдано по медицинским показаниямСУБСТАНЦИИ И МЕТОДЫ, ЗАПРЕЩЕННЫЕ ВСЕ ВРЕМЯ
(КАК В СОРЕВНОВАТЕЛЬНЫЙ,ТАК И ВО ВНЕСОРЕВНОВАТЕЛЬНЫЙ ПЕРИОД)ЗАПРЕЩЕННЫЕ СУБСТАНЦИИSI. АНАБОЛИЧЕСКИЕ АГЕНТЫПрименение анаболических агентов запрещено.1. Анаболические андрогенные стероиды (AAS)а) Экзогенные* AAS, включая• 19-норандростендион (эст-4-ен-3,17-дион)• 1-андростендиол (5а-андроет-1-ен-Зр,^-диол)• 1 -андростендион (5а-андрост-1-ен-3,17-дион)• 1-тестостерон (17ß-niapoKCii-5a-aaapoeT-l-eH-3-oH)• 4-гидрокситестостерон (4,17ß-flnniapoKcnatupocT-4-eH-3-oH)• боландиол (19-норандростендиол)• боластерол• болденон• болдион (андроста-1,4-диен-З,17-дион)• гестринон• даназол (17а-этинил-17р-гидроксиандрост-4-ено(2,3-с1|изок-сазол)• дегидрохлорметилтестостерон (4-хлоро-17р-гидрокси-17а-ме-
тиландроста-1,4-диен-З-он)• дезокеимегилтеетостерон ( 17а-метил-5а-андрост-2-ен-17ß-ai)• дростанолон• калюете рои• клостебол• местанолон* «Экюгснныс» субстанции - w субстанции, которые не мотуг ныриоатнатичорганизмом.
Приложения226 .* =е™ён (17ß-nmpoKCH-17а-метиландроста-1,4-диен-З-он)• метасгерон1 (2а, 17а-диметил-5аандростан-3-он-17р-ол).* Mcmi-T-тестостерон (17р-шдрокси-17а-метил-5«-анлрост-1 -ен-3-он) . п ,. метилдиенолон (17р-гидрокси-17а-метилэстра-4,9-диен-3-он)• метилнортестостерон (17р-гидрокси-17а-метилэстр 4-ен-З-он)• метилтестостерон• метилтриенолон (17р~гидрокси-17а-метилэстра-4,9,11 -триен-
3-он)• миболерон• нандролон• норболетон• норклостебол• норэтандролон• оксаболон• оксандролон• оксиместерон• оксиметолон• простанозол ([3,2-с]пиразол-5а-этиоаллохолан-17р-тетрагид-
рогшранол)• станозолол• стенболон• тетрагидрогестринон (18а-гомо-прегна-4,9,11 -триен-17р-ол-
3-он)•тренболон• флюоксиместерон• формеболон• фуразабол (173-гидрокси-17а-метил-5а-андростано[2,3-с1-
фуразан)• хинболон (квинболон)этилэстренат (19-нор- 17а-прегн-4-ен-17-ол) и другие суб-логичЛ-^0 СХОЛ* ХИМИЧеск°й структурой или схожими био¬
логическими эффектамиб) Эндогенные* AAS• аил росте ндиол (андрост-5-ен-Зр,17р-диол)• Эндогенные. субстанции - /то субстанции
ганмшом у^станции, которые могут вырабатываться ор-
Приложение 2227• андростендион (андрост-4-ен-3,17-дион)• дигидротестостерон (17р-гидрокси-5а-андростан-3-он)• прастерон (дигидроэпиандростерон, ЭНЕА)• тестостеронМетаболиты и изомеры• 19-норандростерон• 19-норетиохоланолон• За-гидрокси-5а-андростан-17-он• 3(3-гидрокси-5а-андростан-17-он• 4-андростендиол (андрост-4-ен-Зр,17р-диол)• 5а-андростан-За,17а-диол• 5а-андростан-За,17р-диол• 5а-андростан-Зр,17а-диол• 5а-андростан-Зр,17(3-диол• 5-андростендион (андрост-5-ен-3,17-дион)• андрост-4-ен-За,17а-диол• андрост-4-ен-За,17р-диол• андрост-4-ен-Зр,17а-диол• андрост-5-ен-За, 17а-диол• андрост-5-ен-За,17р-диол• андрост-5-ен-3[},17а-диол• эпи-дигидротестостеронЕсли какая-либо из указанных выше запрещенных субстанций мо¬
жет вырабатываться организмом естественным образом, проба будет
считаться содержащей такие запрещенные субстанции в тех случаях,
когда концентрация запрещенных субстанций или концентрация их
метаболитов либо маркеров и/или их соответствующих соотноше¬
ний в пробах спортсмена отклоняется от верхних и нижних зна¬
чений норм, являющихся обычными для людей, и вряд ли может
соответствовать обычному уровню эндогенной выработки данных
веществ организмом. Проба не считается содержащей запрещенной
субстанции, если спортсмен приведет подкрепленные свидетельства¬
ми доказательства того, что ненормальная концентрация запрещен¬
ной субстанции или ее метаболитов либо маркеров и/или их соответ¬
ствующих соотношений в пробе спортсмена может быть обусловлена
его патологическим или особым физиологическим состоянием.Во всех случаях и при любых концентрациях лаборатория со¬
общает о неблагоприятном результате aнaJluзa. если, основываясь
на любом надежном методе анализа (например, 1ЯМБ), она может
доказать: запрещенная субстанция имеет экзогенное происхожде¬
ние. В таких случаях дальнейшее расследование не проводится.
Приложения228I то уоовень субстанции не превышает обыч-
Если сообщается, ч™ ^ые аналИтические методы (например,
ного для людей, И над происхождения субстанции, но1RMS) не выявляют^нпвания предполагать (такие как сравнение
имеются серьезные ос ие запрещенной субстанции, ан-стероидных провести расследование - про-тидопинговая Ч тестирований или провести дополни-верить данные пред щ ^ 8ЫЯВИТЬ, вызван ли такой результатанализа физиологическим или патологическим состоянием спор.
ГГГже он является следствием экзогенного происхожде-НИКоХла1ГраториГсообшает о соотношении Т/Е более чем
четыре к одному, а надежные методы анализа (ндпример, IRMS)
не выявили экзогенного происхождения субстанции, может быть
проведено дальнейшее расследование — проверка данных преды¬
дущих тестирований или проведение дополнительных с целью
определить, вызван ли такой результат анализа физиологическим
или патологическим состоянием спортсмена или же он является
следствием экзогенного происхождения запрещенной субстанции.
Если лаборатория сообщает, что дополнительные надежные мето¬
ды анализа (например, IRMS) выявили экзогенное происхождение
запрещенной субстанции, никаких дальнейших расследований боль¬
ше не требуется, проба считается содержащей данную запрещен¬
ную субстанцию. Когда дополнительные надежные аналитические
методы (например, IRMS) не применялись, а результаты мини¬
мум трех предыдущих тестирований недоступны, соответствую¬
щая антидопинговая организация должна определить продольный
профиль спортсмена путем минимум трехкратного тестирования
без предупреждения в течение трех последующих месяцев. Если
продольный профиль спортсмена, определенный с помощью даль¬
нейших тестирований, не является физиологически нормальным,
результат тестирования считается положительным.В крайне редких случаях в моче может содержаться болденон
эндогенного происхождения в очень низких концентрациях (не-
<-ю.п,ко нанограммов на миллилитр). Если лаборатория сообщает
■*' i> if. и применение любых надежных аналитических ме-
cvfJ^ m?ПРИМСР» IRMS) не выявляет экзогенного происхождения
пгх ш*пь-1ИИ МОЖСГ ^)ЫГЬ проведено дальнейшее расследование •"
полните и МГХ1ьиУ|11Их тестирований или проведение ДО-( 1 11 лополнительные надежные аналитические
Приложение 2методы (например, IRMS) не применялись, соответствующая
антидопинговая организация должна определить продольный про¬
филь спортсмена путем как минимум трехкратного тестирования
без предупреждения в течение трех последующих месяцев. Если
продольный профиль спортсмена, определенный с помощью даль¬
нейших тестирований, не является физиологически нормальным,
результат тестирования считается положительным.Если лаборатория сообщает об обнаружении 19-норандростерона,
результат тестирования будет считаться положительным, т.е. само по
себе обнаружение данной субстанции — научно обоснованное под¬
тверждение экзогенного происхождения запрещенной субстанции.В таких случаях нет нужды проводить дальнейшее расследование.В случае отказа спортсмена сотрудничать с лицами, проводящи¬
ми расследования, проба спортсмена будет считаться содержащей
запрещенную субстанцию.2. Другие анаболические агенты (список не является исчерпывающим)• зеранол• зилпатерол• кленбутерол• тиболонS2. ГОРМОНЫ И СВЯЗАННЫЕ С НИМИ СУБСТАНЦИИЗапрещены нижеперечисленные субстанции, в том числе дру¬
гие субстанции со схожей химической структурой или схожими
биологическими эффектами, а также их рилизинг-факторы.• Эритропоэтин (ЭПО).• Гормон роста (hGH), инсулиноподобные факторы роста (на¬
пример, ИФР-1).Запрещены механические факторы роста (МФР) и другие суб¬
станции, способствующие росту мышечной массы.• Гонадотропины (ЛГ, ХГЧ) запрещены только мужчинам.• Инсулин.• Кортикотропины.Если спортсмен не докажет, что концентрация вызвана физио¬
логическим или патологическим состоянием, проба будет считать¬
ся содержащей какую-либо из перечисленных в списке запрещен¬
ных субстанций при концентрации запрещенной субстанции или ее
метаболитов либо маркеров и/или их соответствующих соотноше¬
ний, превышающей норму, являющуюся обычной для людей, и
вряд ли соответствующей обычному уровню эндогенной выработ¬
ки данного вещества организмом.
Приложения230 Если лаборатория сообщает, основываясь на надежном аналити¬
ческом методе, что запрещенная субстанция имеет экзо!енное про¬
исхождение, проба считается содержащей запрещенную субстанцию
и объявляется о неблагоприятном результате анализа. ^Наличие других субстанций со схожей химической структурой
или схожими биологическими эффектами, диагностических мар¬
керов или рилизинг-факторов, перечисленных в списке выше гор¬
монов или какой-либо другой субстанции экзогенного характера
считается неблагоприятным результатом анализа.S3. БЕТА-2 АГОНИСТЫЗапрещены все бета-2 агонисты, включая их D- и L- изомеры.
Исключение составляют формотерол, сальбутамол, сальметерол
и тербуталин, вводимые путем ингаляции. Такое их применение
требует оформления сокращенной формы запроса на терапевтиче¬
ское использование.Безотносительно к тому, получил ли спортсмен право на тера¬
певтическое использование (сокращенный процесс), при установ¬
лении лабораторией факта, что концентрация сальбутамола (сво¬
бодного плюс глюкуронида) превышает 1000 нг/мл, это считается
неблагоприятным результатом анализа, за исключением случаев,
когда спортсмен сможет доказать: данный результат есть следствие
терапевтического использования ингаляций сальбутамола.54. АГЕНТЫ С АНТИЭСТРОГЕНОВОЙ АКТИВНОСТЬЮ
Запрещены следующие классы антиэстрогеновых субстанций.1. Ингибиторы ароматазы, включая анастрозол, летрозол, ами-
ноглютетимид, экземестан, форместан, тестолактон и др.2. Избирательные модуляторы эстрогеновых рецепторов (SERMs),
в том числе ралоксифен, тамоксифен, торемифен и др.Другие антиэстрогеновые компоненты, в том числе кломи-фен, циклофенил, фулвестрант и др.55. ДИУРЕТИКИ И ДРУГИЕ МАСКИРУЮЩИЕ ВЕЩЕСТВА
Маскирующие агенты запрещены. Они включают-• диуретики*;степиrts°^U альФа'РедУктазы (например, финастерид, дута-ST"“ "mMU (на"РимеР. альбумин, декстрин,
|идрокси/гил крахмал);• иробснецид;шпре,неншх Станций не лей-
нтш tu. панции. УРГП пороговым или сувпоро-
Приложение 2 231• И другие,с>'бстани“и со схожей химической
структурой или схожими биологическими ЭффектамиДиуретики включают:• амилорид;• ацетазоламид;• буметанид;• индапамид;• канренон;• метолазон;• спиронолактон;• тиазиды (например, бендрофлюметиазид, хлоротиазид, ги-
дрохлоротиазид) триамтерен;• фуросемид;• хлорталидон;• этакриническую кислоту, а также другие вещества со схожей
химической структурой или схожими биологическими эффек¬
тами (за исключением дросперинона, который не является за¬
прещенным).ЗАПРЕЩЕННЫЕ МЕТОДЫМ1. УСИЛЕНИЕ ПЕРЕНОСА КИСЛОРОДАЗапрещены следующие методы.А. Кровяной допинг, в том числе использование аутологиче¬
ских, гомологических или гетерологических продуктов крови или
клеток крови любого происхождения.Б. Искусственное повышение способности крови поглощать,
транспортировать и доставлять кислород, например с помощью
перфторирования или использования эфапроксирала (1181*13) и
модифицированных продуктов на основе гемоглобина (например,
заменители крови на основе гемоглобина, гемоглобиновые про¬
дукты в микрокапсулах).М2. ХИМИЧЕСКИЕ И ФИЗИЧЕСКИЕ МАНИПУЛЯЦИИЗапрещено следующее.Фальсификации или попытки фальсификации с целью наруше¬
ния целостности и подлинности проб, взятых при допинг-контроле.
Это может включать, например, внутривенную катетеризацию,подмену мочи и др.Внутривенные инфузии (за исключением случаев, когда они
необходимы по медицинским показаниям).
Припожения23243. ГЕННЫЙ ДОПИНГЗапрещено нетерапевтическое испапыовлние четок. генов,
генных цементов или мод>ляиий генной экспрессии, которые
способны улучшать спортивные результаты.ВЕЩЕСТВА II МЕТОДЫ, ЗАПРЬ1ЦКННЫЕ
НА СОРЕВНОВАНИЯХ
В дополнение к категориям. перечисленным в пунктах 81-85 и
М1-МЗ. во время соревнований запрещены следующие категории.
ЗАПРЕЩЕННЫЕ ВЕЩЕСТВА.40 СТИМУЛЯТОРЫВсе стимуляторы, включая оба их оптических изомера (Э- и
Ы. если шковые имеются, запрещены. Исключение составляет
имидазол. применяемый местно. а также стимуляторы, вктючен-
ные в Прсярамм> мониторинга 200'*.Стимуляторы.• адрафнннл• адреналин**• амифеназол• амфепрамон• амфетамин• амфетамин ил• бензфетамин• бромантан• гегггаминол• -зи метил амфетамин• июмстегттен• карфедон• катин***• ообенюрекс• кокаин• кролропамил• ?евметамфетамин■ ГНюгрм«> ммогтершо» 2«П инючсны _-* А следующие с>«сганции. не являющие—, .^»ишилп, ш«.офеин фснм.г<фрмн. фенмлпролдтиаммн. пмпри-< » прешрагл ш место« вместеши или хгш местного" в11 Фимю>опгксш>. разрешен»ев шмашптльио*). ест его содержание » моче
мшимлтр
Приложение 2 233• мезокарб• меклофеноксат• метамфетамин (D-)• метилендиоксиамфетамин• метилендиоксиметамфетамин• метилфенидат• мет ил эфедрин*• мефенорекс• мефентермин• модафинил• никетамнд• норфенефрин• норфенфлюрамин• окснлофрин• октопамин• ортетамин• парагидроксиамфетамин• пемолин• пролинтан• пропилгекседрин• n-метил амфетамин• ротетамнд• сслегидин• сибутрамин• стрихнин• туаминогептан• фампрофазон• фенбутразат• фендиметразин• 4-фенилперацетам (карфедон)• фенетиллин• фенкамин• фенкамфамин• фенметразин• фенпрометамнн• фенпропорекс• фентермин• фенфлюрамин• фурфенорекс* “КЪсдрмн и метил эфелрмн ««решены (проб* считает*:* п»мажителы*>й». еегм со¬
держание КАЖДОГО МЛ МН\ В моче превыииет -Kv-rrw MHkpOrpiWW'.'« MJ мичдмдитр
Приложения234• циклазодон• этамиван• этиламфетамингва со схожей структурой или схож и-в7. НАРКОТИКИЗапрещены следующие наркотики.• бупренорфин• гилроморфин• декстроморамид• диаморфин (героин)• метадон• морфин• оксикодон• оксиморфон• пентазоцин• петидин• фентанил и его производныеN8. КАННАБИНОИДЫЗапрещены канпабиноиды (например, марихуана, гашиш).Ь9. ГЛЮКОКОРТИКОСТЕРОИДЫОральное, ректальное, внутривенное или внутримышечное вве¬
дение глюкокортикосгероидов запрещено. Их применение требует
разрешения на терапевтическое использование./Іія приема их лруїими способами (такими как интраартику-
лирные, периаргикулярные, околосухожильные, эпидуральные и
ннугрикожные иньекции и ингаляции) требуется заявка на тера¬
певтическое использование в сокращенной форме.Местные препараты, наносимые на кожу (в гом числе ионтофо-
р< » и фонофорез), десны, нерианальные, а также капли в уши, нос
и паза не млрешены, и для их применения не требуется оформ-
Iі ним разрешения на терапевтическое использование.РІ. АЛКОГОЛЬ< ііирі іл анод) в нижеперечисленных видах спорта запрещен> и» н і соревнованиях. Обнаруживается он путем анализа ды-ВКЩЕСТВА, *А1ІРЕЩЕНIIЫЕ
В ОТДЕЛЬНЫХ ВИДАХ СПОР! Асчитается положительной), если со
< ип. микрогриммов на миллилитр.
Приложение 2235хания и/или крови. Пороговые концентрации (гематологические
объемы), принятые за критерий в конкретной федерации, указаныв скобках.Аэронавтика (FAI) (0,20 г/л)Стрельба из лука (FITA, I PC) (010 г/л)Автоспорт (FIA) (0,10 г/л)Петанк (CMSB, IPC) (0,10 г/л)Каратэ (WKF) (0,10 г/л)Современное пятиборье (UIPM) (0,10 г/л)для дисциплин, включающих стрельбу
Мотоспорт (FIM) (о,ю г/л)Водномоторный спорт (UIM) (0 30 г/л)Р2. БЕТА- БЛ О КАТО Р ЫЕсли не указано иного, бета-блокаторы запрещены в следую¬
щих видах спорта только на соревнованиях.Аэронавтика (FAI)Стрельба из лука (FITA, IPC) (также запрещены вне соревно¬
ваний)Автоспорт (FIA)Бильярдный спорт (WCBS)Бобслей (FIBT)Петанк (CMSB, IPC)Бридж (FMB)Керлинг (WCF)Гимнастика (FIG)Мотоспорт (FIM)Современное пятиборье (UIPM) для дисциплин, включающих
стрельбуБоулинг (FIQ)Парусный спорт (ISAF) (только в матчевых гонках)Стрельба (ISSF, IPC) (также запрещены вне соревнований)
Лыжный спорт/сноуборд (FIS) (прыжки на лыжах с трамплина,
фристайл, сноуборд)Борьба (FILA)К бета-блокаторам относятся (список не является исчерпываю¬
щим):• альпрснолол• атенолол• ацебутолол• бстаксолол
Приложения236 • бисопролол• бунолол• карведиол• картеолол• лабеталол• левобунолол• метипранолол• метопролол• надолол• окспренолол• пиндолол• пропанолол• соталол• тимолол• целипролол• эсмололОСОБЫЕ СУБСТАНЦИИК «особым субстанциям»* относятся следующие.• Все бета-2 агонисты в виде ингаляций, за исключением саль-
бутамола (свободного или с глюкуронидом) в концентрации
более 1000 нг/мл и кленбутерола.• Пробенецид.• Катин, кропропамид, кротетамид, эфедрин, этамиван, фам¬
профазон, гептаминол, изометептен, левметамфетамин, ме¬
клофеноксат, р-метиламфетамин, метилэфедрин, никетамид,
норфенефрин, октопамин, оксилофрин, фенпрометамин,
пропилгекседрин, селегилин, сибутрамин, туаминогептан и
любые другие стимуляторы, не указанные конкретно в раз¬
деле Б6, но попадающие под условия, изложенные в данном
разделе.• Каннабиноиды.• Все глюкокортикостероиды.• Алкоголь.• Все бета-блокаторы.Л ии\{н т, с пш ке могут специально обозначаться особые субстанции, употребле-
'л"тш Р““»отрываться как непреднамеренное ввиду их общедоступности
пи нии лч<,иМ,"ит' ти ЫХ шко^ности влиять на спортивные результаты». Нару-» / мсм/г ИИ"ЖЫХ м,м,,и ' |! '»улыатс использования лих субстанций может- [»ними санкциями, если будет установлено, что •...спортсмен ис-
1ННуН> с^тонцию не Оля улучшения своих спортивных результатов...».
Приложение 3 237Приложение 3ПРИКАЗПо Министерству здравоохранения СССРг МоСКва № 1021 25 декабря 1973 г.О введении нового перечня токсикологических веществ,
подлежащих судебно-химическому исследованию в лабораториях бюро
судебно-медицинской экспертизыПри судебно-медицинском исследовании трупов нередко возника¬
ют вопросы, связанные с установлением отравления. В этих случаях в
судебно-медицинские лаборатории направляются различные объекты
исследования, преимущественно внутренние органы из трупа и био¬
логические жидкости.В отдельных случаях лечебные учреждения могут направлять в
судебно-медицинские лаборатории рвотные массы, промывные воды,
мочу, кровь и остатки лекарственных веществ.Судебно-химический анализ объектов исследования производит¬
ся на основании: постановления органов дознания, следствия, про¬
куратуры; определения суда, письменного направления судебно-
медицинского эксперта; письменного направления руководителя
лечебного учреждения с визой начальника бюро судебно-медицинской
экспертизы.В постановлении (определении) или направлении должна быть
точно сформулирована цель исследования, в соответствии с которой
выполняется судебно-химический анализ на указанное конкретное
вещество или группу веществ.При отсутствии достаточных данных (определенной клинической
и секционной картины, обстоятельств дела и т. д.) перед экспертом-
химиком может быть, в порядке исключения, поставлен вопрос о про¬
ведении общего анализа.Номенклатура веществ, на которые производятся судебно¬
химические исследования, в последние годы значительно расши¬
рилась. Перечень исследуемых веществ, приведенный в «Прави¬
лах судебно-химической экспертизы вещественных доказательств в
судебно-химических отделениях судебно-медицинских лабораторий
органов здравоохранения», утвержденных в 1956 г., не отражает насто¬
ящего положения и не способствует составлению экспертом-химиком
Приложения238пМН1 анализа направленных ему биологи-объективно обоснованного плана аналических объектов. ПРИКАЗЫВАЮ:в связи с изложенным, вие НОВЫЙ «Перечень токсикологиче-
Утверлить и ввести д дебно.химическому исследованию в ла-
ских веществ, п0^с^и медицинской экспертизы органов здраво-
бораториях бюро> суд‘ Считать утратившими силу §§ 54 и 55охранения» (см. при;’ экспертизы вещественных доказательств«Правил судебно-хим судебно-медицинских лабораторий;^Го“ГРГе;ГЛДр»еннЬ,х , лекабря ,956 т. Министер-
ством здравоохранения СССР.Заместитель Министра
Е. НовиковаПриложениек приказу по Министерству здравоохранения СССР
№ 1021 от 25 декабря 1973 г.ПЕРЕЧЕНЬтоксикологических веществ, подлежащих
судебно-химическому исследованию в лабораториях бюро
судебно-медицинской экспертизыI Группы веществ, на которые должны производиться исследова¬
ния при общем анализе.1.1. Вещества, изолируемые с водяным паром:
синильная кислога и ее соединения, метиловый, этиловый, пропи-
ловый. бутиловый, амиловый спирты, формальдегид, хлороформ, хло-
ралгидрат, четыреххлористый углерод, дихлорэтан, фенол, крезолы.1.2 Вещества, изолируемые минерализацией:
ртугь. мышьяк, таллий, кадмий, свинец, барий, медь, марганец,
хром, цинк, сурьма, серебро, висмут.I Оринические вещества, изолируемые подкисленной водой или
подкисленным спиртом, другими органическими растворителями:
м іиі.іі '(кгнобарбигал, барбамил, эта ми нал, циклобарбитал, гсксо-
ь і!! ' *-нкжал» морфин, кодеин, дионин, героин, гидрокодон, папа-
п-пи» ' ’ Л^СТриянин’атР°пии’ •'иосциамин, скополамин, кокаин,
•• Г а5ИМ иикотии’ аминазин, дипразин, ти зернин, мажеп-имижн и его аналоги, карбофос, метафос, метил этил-
Приложение З239гиофос, меіилнитрофос, трихлорметафос-3, метил меркаптофос, фосфа-
мид, фталофос, фозапон, бутифос, хлорофос, октаметил, севин.2. Вещества, на которые расширяют общий анализ в зависимости
от клинической и секционной картины, результатов гистологического
и гистохимического исследований, особенностей течения химических
реакций и т. д.2.1. Вещества, изолируемые с водяным паром:тетраэтилсвинец, чтилен гликоль, ацетон, нитро- и динитробензо¬
лы, анилин, бензол, ксилол, толуол, бензин, керосин.2.2. Вещества, изолируемые минерализацией:селен, теллур, олово, железо, молибден, бериллий, никель, кобальт,
литий, ванадий.2.3. Вещества, изолируемые подкисленной водой и подкисленным
спиртом, другими органическими растворителями:салициловая, ацетилсалициловая, бензойная кислоты, производ¬
ные барбитуровой и тиобарбигуровой кислот, не указанные в п. 1.3;
сантонин; феликс-флороглюциды: мепробамат; триоксазин; мидо-
калм; ноксирон; новокаин, дикаин, лидокаин; амидопирин, анальгин,
антипирин, бугадион; ареколин, бруцин, кониин; кофеин; хинин,
хинидин; резерпин; галантамин, секуринин; эфедрин; пилокарпин;
платифиллин, саррацин; аконитин, вератрин; прозерин, хингамин;
игіразид, тубазид, фтивазид, ИНГА-17; производные фенотиазиново-
го ряда, не отмеченные в п. 1.3; элениум, нитразепам, седуксен; кар-
бахолин, декаметонин, димедрол, гексамидин; строфантины К и Г,
лантозиды, олеандрин, дигитоксин, дигоксин; фосфорорганические
соединения, не отмеченные в п. 1.3; ДДТ, гексахлоран, 2, 4-Д, по-
лихлорпинен, гептахлор; зоокумарин; альфа-нафтилтиомочевина, ан¬
табус, тиурам; ДНОК, ртутьорганические соединения.2.4. Вещества, изолируемые диализом:азотная кислота, нитраты, нитриты, серная, соляная, уксусная, му¬
равьиная, щавелевая и другие кислоты, едкие кали и натр, гидроокись
аммония.2.5. Вещества, изолируемые специальными методами:фосфид цинка; соли фтористоводородной, кремнефтористой, хлор¬
ной кислот; йод, бром; окись углерода.Главный судебно-медицинский эксперт М3 СССР,
Заслуженный деятель науки РСФСР,
профессор В.И. Прозоровский
Учебное пособи»* посвящено ТСХ-скри
ним)у отдельных групп токсикологичес¬
ки значимых веществ. И пособии пред
с мм /и* мы теоретические основы К X и
раї смотрен ГСХ-скринині наркотических
.1Н.111Ы Є1ИКОВ, прои зводных 1,4-бен зоди-
аіепина, фенотиазина, барбитуровой кис-
лоты. пира юла, ароматических кислої, ко¬
каина. каннабиноидов, фенилакиламинов
и галлюциногенов в рамках действующей
программы по курсу токсикологической
химии (раздел 3 «Химико-токсикологи-
ческий анализ (судебно-химический) на
группу веществ, изолируемых экстракци¬
ей и сорбцией. Лекарственные средства»)
2003 г. В пособии содержится норматив¬
ная документация о наркотических средс¬
твах и психотропных веществах, перечис¬
ленных в официальном Перечне средств
и веществ, утвержденном Правительством
Российской Федерации, а также Запре¬
щенный список ВАДА.Пособие предназначено для студентов
медицинских и фармацевтических вузов
и факультетов, обучающихся по специаль¬
ности «Фармация» 060108 по дисципли¬
не «токсикологическая химия», а также для
аспирантов и преподавателей. Для само¬
стоятельной подготовки студентов по дан¬
ной іеме приведены контрольные вопросы,
тестовые задания и ситуационные задачи.Вопросы, обсуждаемые в пособии, могут
заинтересовать экспертов судебно-хими¬
ческих отделений бюро судебно-медицин-
скои экспертизы и других специалистов,
занимающихся проблемами токсикологи¬
ческой химии.Нормативная документацияОсновные направления
метаболизматоксикологически значимых
веществСкрининговые
методы определения
токсикологически значимых
веществТСХ-скрининг токсикантовТеоретические основы
тонкослойной хроматографииПрименение ТСХ-скрининга
на примере использования
системы ТохМаЬТСХ-скрининг отдельных
групп токсических веществКонтрольные вопросы,
тестовые задания
и ситуационные задачи‘»78 :> ‘>-4*1 І III >■'9 765970 А 1 1445