Author: Сулимон В.А. Благова О.В.
Tags: патология сердечно-сосудистой системы сердечно-сосудистые заболевания внутренние болезни медицина
ISBN: 978-5-9704-2
Year: 2012
Text
КЛИНИЧЕСКИЕ
РАЗБОРЫВ ФАКУЛЬТЕТСКОЙ
ТЕРАПЕВТИЧЕСКОЙ
КЛИНИКЕ
им. В.Н. ВИНОГРАДОВАРЕДКИЕ И ДИАГНОСТИЧЕСКИ ТРУДНЫЕ
ЗАБОЛЕВАНИЯ В КЛИНИКЕ ВНУТРЕННИХ БОЛЕЗНЕЙПод редакцией В.А. Сулимова, О.В. Благовой>»L-a:.>sv
УДК 616.1/9
ББК 54.1
К49К49 Клинические разборы в Факультетской терапевттеской клинике им. В.Н. Виноградова. Редкие и
диагностически трудные заболевания в клинике внутренних болезней / Под ред. В. А. Сули мова,
О.В. Благовой. — М. ; ГЭОТАР-Мелиа, 2012. — 688 с.ISBN 978-5-9704-2.^13-4Книга представляет собой сборник клинических разборов, проходивших в Факультетской
терапевтической клинике им. В.Н.Виноградова на протяжении последних лет. Каждая из
33 глав состоит из подробного описания клинического сл\'чая, ихтожения современного ч^еоре-
тического маіериа;іа, который привлекался врачами в процессе постановки диагноза, опре-
леления тактики и оценки результатов лечения, а также из комментариев {нередко полемичных)
сотрудников клиники и приглашенных специалистов (нефрологов, гемагологов, кардиохирурі ов,
генеіиков и др.).Клинические разборы отражают все традиционные направления работы клиники
(пульмонология, кардиология, гастроэнтерология, ревматология, отчасти гематология). Вместе
с тем они объединены единством подхода к больному, который, по ГА. Захарьину, подразумевав і
вдосіижение связи всех яЕпений данного болезненного строяПрелстаяпялось важным сохра¬
нить все нюансы диагностического поиска. Многие из представленных в книге случаев
уникалыш; но и при относительно нередких заболеваниях индивидуализация особенностей
пациента делает разборы интересными и поучительными. Особенностями разборов в целом
стали заметное преобладание инфекционной, иммунной и генетической патологии и широкое
использование прижизненной морфологической диагностики.Издание адресовано студентам старших курсов, начинаюміим врачам, интернам и клини¬
цистам различных специальностей.УДК 616.1/9
ББК 54.1Права т данное издание принадлежат ООО Издательская группа «ГЭОТАР-Медиа». Воспроизведение
и распространение в каком бы то ни быпо виде части или целого издания не могут быть осуществлены
без письменного разрешения ООО Издательская группа «ГЭОТАР-Медиа».© Коллектив авторов, 2012© ООО Издательская группа «ГЭОТАР-Медиа», 2012
© ООО Издачельская ipvnna «ГЗОТАР-Медиа»,
ISBN 978-5-9704-2313-4 офоркшение, 2012 '
СОДЕРЖАНИЕАвторский коллектив 6Список сокращений 11Лабораторные показатели и их нормальные значения,используемые в данной книге 14Предисловие 15ПУЛЬМОНОЛОГИЯ 18Глава 1. Идиопатические интерстициальные пневмонии;
современный подход к диагностике, трудности лечения
при наличии сопутствующей патологии. С.И. Овчареяко,ЕЛ. Сон, В.А. Капустина 18Глава 2. Криптогенная организующаяся пневмония — относительно
благоприятный вариант интерстициального заболевания легких.И.В. Чичкова, КС. Щедрина 38Глава 3. Необычный вариант поражения легких при системной
красной волчанке. Н.Д. Саркисова, О.В. Благова, А.В. Иедоступ,Н.В. Петухова, А,В. Родионов, ЕМ. Шилов 48Глава 4, Лимфангиолейомиоматоз: клиническая, и[іструментальная,
морфологическая диагностика, подходы к лечению. С.И. Овчаренко,ЕЛ. Сон 74Глава 5. Саркоидоз с затяжным лабораторным дебютом и высокойиммунологической активностью. И.В. Чичкова, И.С. Щедрина 97Глава 6. Дифференциальная диагностика легочных эозинофилий;
от бронхиальной астмы к синдрому Черджа—Стросс. С.И. Овчаренко,И.В. Чичкова, И.В. Морозова, И.С. Щедрина, В..А. Капустина 109КАРДИОЛОГИЯ 123Глава 7. Комбинированное использование интервенционных методоіі
в лечении рефрактерной желудочковой тахикардии у пациента с
постинфарктным кардиосклерозом. СЛ. Термосесов, В.А. Сулимое,Д.В. Кузьменков, ИЛ. Новикова, Д.А. Царегородцев, И.Л. Ильич,Р.Ш. Гарипов, М.Ю. Гиляров, С.С. Васюков, А.В. Добровольский 123Глава 8. Артериальная гипертония и цереброваскулярная патология:
патогенетическая связь и подходы к лечению. И.Д. Саркисова,О.В. Благова, А.В. Иедоступ, Л.Ю. Стойда, А.Ю. Зайцев,В.Е. Смирнов 137Глава 9. Псевдоклапанный вариант инфекционно-иммунного миокардитаили ревмокардит? Н.Д. Саркисова, О.В. Благова, А.В. Иедоступ 149Глава 10. Миокардит с выраженными иммунными проявлениями и
нефропатией — трудности нозологической диагностики.О.В. Благова, А.В. Иедоступ, Е.М. Шилов 170Глава П. Фульминантный миокардит: диагноз, этиология, лечение,
прогноз, И.А, Новикова, М.Ю. Гиляров, А.В. Седов, Д.А. Парфенов,Н.В. Гагарина, Е.С. Белышева, В.П. Седов, А.Л. Сыркин 190
Клинические разборы.Глава 12. От «идиопатической» мерцательной аритмии
к постановке иозологического диагноза. О.В. Благова,Л.В. Иедоступ, Е.А. Коган, В.А. Сулимое 206Глава 13. Миокардиальный васкулит; путь к диагнозу, клинические
варианты, попытки патогенетической терапии..4.Я Иедоступ,О.В. Благова, Е.А. Коган, В.А. Сулимое, И.В. Чичкова,И.С. Щедрина 230Глава 14. Генера.лизованный саркоидоз с преимущественным
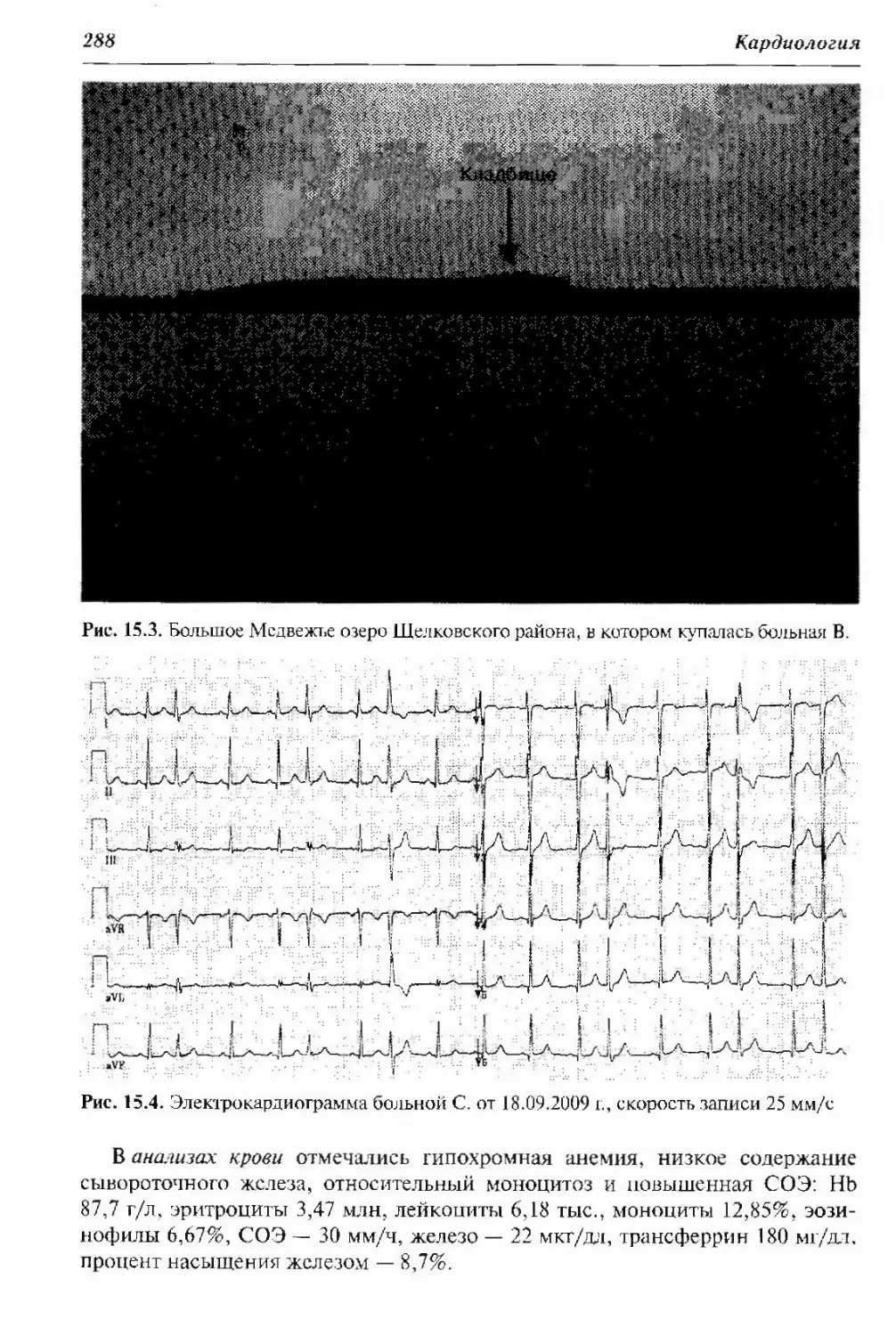
поражением сердца: верификация диагноза и терапин.Д.А. Иванова, А.В. Иедоступ, ДА. Царегородцев, С.Е. Борисов,С.П. Паша 267Глава 15. Тяжелый инфекционный эндокардит крайне
редкой этиологии у больной с врожденным иммунодефицитом:
особенности диагностики и лечение. А.В. Вахляев, Л.И. Катков,А.П. Нестеров, И.А. Новикова, Р,С. Овчинников, В.П. Седов,А.Л. Сыркин 285Глава 16. Болезнь Лайма: успешное лечение острого перикардита на
основе точного ;^тиологического диагноза. Дй. Герок, С.А. Сучкова,A.П. Нестеров, М.Ю. Гиляров, ИЛ. Новикова, А.Л. Сыркин 308Глава 17. Длительное течение нераспознанного констриктивиого
перикардита и псевдоапевризмы левого желудочка у больногос истинной иостинфарктной аиевризмой. А.В. Иедоступ,И.С. Морозова, М.П. Троицкая, О.В. Благова, И.В. Гагарина,B.И. Седов 322Глава 18, Подклапанный стеноз легочной артерии — врожденный
порок или кардномиопатия? А.В. Иедоступ, О.В. Благова,Г.М. Иапакин, В.А. Капустина 339Глава 19. «Идиопатическая» трикуспидальная недостаточность и
«немое» предсердие — новый генетический синдром (предсердная
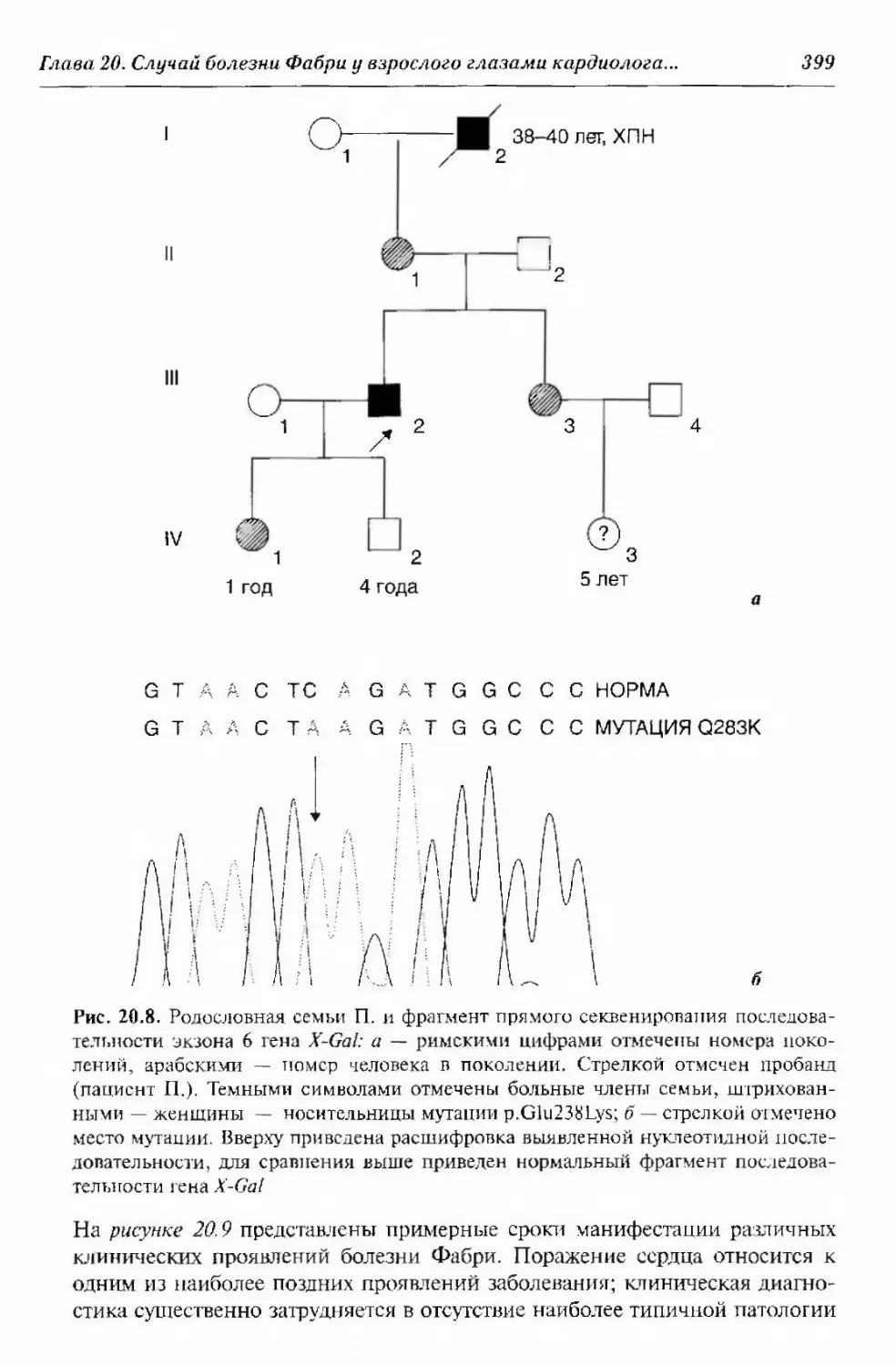
кардиомиопатия с нарушением проводимости). О.В. Благова,R.B. Заклязьминская, AS. Иедоступ 362Глава 20, Случай болезни Фабри у взрослого глазами кардиолога,
морфолога и генетика (три ступени к диагнозу), О.В. Благова,Е.В. Заклязьманская, А.В. Иедоступ, Е.А. Коган, Г.М, И а паки н 389Глава 21. Лритмогенная дисплазии правого желудочка
(правожелудочковая кардиомиопатия): полиморфизм клинических
проявлений. О.В. Благова, А.В. Иедоступ, И.С. Морозова,Е.А. Коган, И.В. Гагарина, В.И. Седов, Е.В. Заклязьманская,Ю.В. Фролова, С.Л. Дземешкевич 403Глава 22, Амилоидоз сердца — рутинный диагноз? С,И. Овчаренко,A.В. Иедоступ, В.И. Седов, Е.А. Сон, ЕЛ. Окишева, О.В. Благова,B.А. Варшавский, Е.А. Коган, В.И. Маколкин 442Глава 23, Первичные злокачественные опухоли сердца (опыті ерапевтов). О.В. Благова, И.Д. Саркисова, А.В. Иедоступ,C.Л. Дземешкевич, В.Е. Синицын, И.В. Гагарина, В.И. Седов 464
СодержаниеГлава 24. Успешное лечение массивного тромбоза нижней полой
вены с нефротическим синдромом и хроиической двусторонней
тромбоэмболией ветвей легочной артерии у пациента с генетически
обусловленной тромбофилией. О.В. Благова, С.Л. Дземешкевич,H.J7. Козловская, А.В. Йедоступ, И.Д- Саркисова, 8,11. Седов,Ю.В. Фролова, В.В. Раскин,- А.С. Дземешкевт, Е.С. Мершина,В.Е. Синицын, Е.М. Шилов, EJO. Еорностаева 512СИСТЕМНЫЕ ЗАБОЛЕВАНИЯ 535Глава 25. Тяжелая легочная гипертензия как результат сочетания
двух редких заболеваний: системной склеродермии и саркоидоза.И.Д. Саркисова, О.В. Благова, А Я. Недоступ 535Глава 26. Гранулсматоз Вегенера у больной с длительным анамнезом
ХОБЛ; путь к диагнозу и специфическая терапия. И.В. Чичкова,И.С. Щедрина 557Глава 27. Трудности постановки нозологического диагноза при
констриктивном полисерозите. О.В. Благова, Д.А. Царегородцев,А,В. Недоступ, Л1Я. Троицкая, B.EI. Седов, И.В. Петухова 567Глава 28. Случай длительного течения синдрома Фслти: особенности
диагностики и терапевтической тактики. Н.В. Петухова,Н.М. Михлина, Е.В. Сокол 592Глава 29,1 Іеобьічііьій вариант течения висцерального туберкулеза
с рефрактерной анемией. Н.Д. Саркисова, О.В. Благова,А.В. Недоступ, Е.А, Лукина, ДЛ Сапооісников 606ГЕЛиТОЛОГИЯ ‘ 636Глава 30. Анемии хронических заболеваний: современные
представления о патогенезе и подходы к лечению. Е.А. Лукина,А.В. Недоступ, О.В. Благова 636Глава 31. Впервые выявленная множественная миелома в сочетании
с тяжелой трикуснидалыюй регургитацией. Е,С. Родионова,ВЛ. Осадчая, Д.А. Царегородцев, В.В. Самойленко 654ГАСТРОЭНТЕРОЛОГИЯ 665Глава 32. Вторичный полимиозит как первое клиническое проявлениеопухоли кишечника. Н.В. Чичкова, И.С. /Цедрина 665Глава 33. Особенности лечения хронического вирусного гепатита R
у больных с циррозом иечеми. В.М. Махов, JLH, Угрюмова 676
АВТОРСКИМ КОЛЛЕКТИВБелышева Елена Семеновна — заведующая межклиническим кабинетом
магнитно-резонансной томографии отдела лучевой диагностики Первого
МГМУ им. И.М. Сеченова, канд. мед. наук.Благова Ольга Владимировна — доцент кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед. наук.Борисов Сергей Евгеньевич — заместитель директора по научно-клинической
работе Московского городского научно-практического центра борьбы с тубер¬
кулезом Департамента здравоохранения г. Москвы, профессор, д-р мед. наук.Варшавский Владитір Анатольевич — профессор кафедры патологической
анатомии Первого МГМУ им. И.М. Сеченова, д-р мед. наук.Васюков Сергей Сергеевич — ассистент кафедры факультетской тера¬
пии № 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, врач-
электрофизиолог межклинического рентгенодиагностического отделения
ангиографии отдела лучевой диагностики Первого МГМУ им. И.М. Сеченова,
канд. мед. наук.Вахляев Антон Викторович — врач отделения интенсивной терапии и реани¬
мации Клиники кардиологии Первого МГМУ им. И.М. Сеченова.Гагарина Нина Владимировна — врач отделения компьютерной томографии
УКВ № 1 отдела лучевой диагностики Первого МГМУ им. И.М. Сеченова,
канд. мед. наук.Оірипов Рустэм Шамильевич — врач-электрофизиолог отделения хирургиче¬
ского лечения сложных нарушений ритма сердца и электрокардиостимуляции
Московского НИИ педиатрии и детской хирургии.Герок Дарья Викторовна — аспирант кафедры профилактической и неотлож¬
ной кардиологии ФППО Первого МГМУ им. И.М. Сеченова.Гиляров Михаил Юрьевич — заведующий отделением интенсивной терапии
и реанимации кітиники кардиологии, доцент кафедры профилактической и
неотложной кардиологии ФППО Первого МГМУ им. И.М. Сеченова, д-р мед.
наук.Горностаева Екатерина Юрьевна — врач нефрологического отделения клини¬
ки нефрологии, внутренних и профессиональных болезней им. Е.М. Тареева,
канд. мед. наук.Дземешкевич Сергей Леонидович — директор Российского научного центра
хирургии им. акад. Б.В. Петровского РАМН, профессор, д-р мед. наук.Дземешкевич Андрей Сергеевич — кардиохирург, научный сотрудник отделе¬
ния хирургического лечения дисфункций миокарда и сердечной недостаточ¬
ности РНЦХ им. акад. Б.В. Петровского РАМН.Добровольский Алексей Владимирович — доцент кафедры профилактиче¬
ской и неотложной кардиологии ФППО Первого МГМУ им. И.М. Сеченова,
канд. мед. наук.Зайцев Александр Юрьевич — врач межклинического рентгенодиагности-
чсского отделения ангиографии отдела лучевой диагностики Первого МГМУ
им. И.М. Сеченова, канд. мед. наук.
Авторский коллективЗаклязьминская Елена Валерьевна — заведующая лабораторией медицин¬
ской генетики РНЦХ им. акад. Б.В. Петровского РАМН, д-р мед. наук.Иванова Диана Александровна — научный сотрудник Московского город¬
ского научио-практического центра борьбы с туберкулезом Департамента здра¬
воохранения г. Москвы, канд. мед. наук.Ильич Илья Леонидович — кардиохирург, врач отделения хирург№іеско-
го лечения сложных нарушений ритма сердца и :^лектрокардиостимуляции
Московского НИИ педиатрии и детской хирургии и межклинического рент-
гснодиагностического отделения ангиофафии отдела лучевой диаіностики
Первого МГМУ им. И. М. Сеченова.Капустина Валентина Андреевна — ассистент кафедры факультетской тера¬
пии № I лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед.
наук.Катков Андрей Ильич — кардиохирург, врач отделения кардиохи¬
рургии клиники сердечно-сосудистой и общей хирургии Первого МГМУ
им. И.М. Сеченова, канд. мед. наук.Коган Евгения Алексавдровна — профессор кафедры патологической анато¬
мии Первого МГМУ им. И.М. Сеченова, д-р мед. наук.Козловская Наталия Львовна — профессор кафедры нефрологии и гемодиа¬
лиза ФППО Первого МГМУ им. И.М. Сеченова, д-р мед, наук.Кузьменков Дмитрий Викторович — врач межклинического рентгенодиаг¬
ностического отделения аніиофафии отдела лучевой диагностики Первого
МГМУ им. И.М. Сеченова, канд. мед. наук.Лукина Елена Алексеевна — профессор Гематологического научного центра
РАМН, д-р мед. наук.Маколкин Владимир Иванович — почетный заведующий кафедрой факуль¬
тетской терапии № 1 лечебного факультета Первого МГМУ им. И.М. Сеченова,
директор Факультетской терапевтической клиники им. В.П. Виноірадова в
Ї977-2004 гг., член-корр. РАМН, профессор, д-р мед. наук.Махов Валерий Михайлович — профессор кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, научный руково¬
дитель отделения гастроэнтерологии ФТК им. В.Н. Виноградова, д-р мед. наук.Мершина Елена Александровна — врач Центра лу^іевой диагностики Лечебно¬
реабилитационного центра Росздрава, канд. мед. наук.Михлина Нина Михайловна — врач-ревматолог Центра суставной боли
УКБ № 1 Первого МГМУ им. И.М. Сеченова, кагщ, мед. наук.Морозова Наталия Владимировна — врач терапевтического отделения
Факультетской терапевтической клиники им. В.Н. Виноградова Первого
МГМУ им. И.М. Сеченова, канд. мед. наук.Морозова Наталия Сергеевна — доцент кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед. наук.Недоступ Алексавдр Викторович — профессор кафедры факультетской тера¬
пии № 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, научный
руководитель отделения кардиологии ФТК им. В.Н. Виїюфадова, д-р мед,
наук.
S Клинические разборы...Нестеров Алексей Петрович — врач отделения интенсивной терапии и реа¬
нимации клиники кардиологии Первого МГМУ им. И.М. Сеченова, канд. мед.
наук.Новикова Нина Александровна ~ профессор кафедры профилактической и
неотложной кардиологии ФППО Первого МГМУ им. И. М. Сеченова, научный
руководитель отделения реанимации и интенсивной терапии клиники карди¬
ологии, д-р мед. наук.Овчаренко Светлана Ивановва — профессор кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-р мед. на>тс.Овчинников Роман Сергеевич — кардиохирург, врач отделения кардиохи¬
рургии клиники сердечно-сосудистой и общей хирургии Первого МГМУ им.
И.М. Сеченова, канд. мед. наук.Окишева Елена Андреевна — ассистент кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед. наук.Осадчая Вера Анатольевна — врач терапевтического отделения Факуль¬
тетской терапевтической клиники им. В.П. Винофадова Первого МГМУ им.
И.М. Сеченова.Папакин Геннадий Матвеевич — врач отделения кардиологии Факультетской
терапевтической клиники им. В.П. Виноградова Первого МГМУ им. И.М. Се¬
ченова.Парфенов Дмитрий Александрович — врач отделения интенсивной терапии и
реанимации клиники кардиологии Первого МГМУ им. И.М. Сеченова, канд.
мед. наук.Паша Сергей Платонович — заведующий межклиническим радионуклидным
диагностическим отделением отдела лучевой диагностики Первого МГМУ
им. И.М. Сеченова, канд. мед. наук.Петухова Наталия Владимировна — заведующая лечебно-диагностическим
отделением Центра суставной боли Первого МГМУ им. И.М. Сеченова
(до 2009 г. — зав. артрологическим отделением ФТКим. В.Н. Виноградова)Раскнн Владимир Вячеславович — кардиохирург, старший научный сотруд¬
ник отделения хирургического лечения дисфункций миокарда и сердечной
недостаточности РНЦХим. акад. Б,В. Петровского РАМН, канд. мед. наук.Родионов Антон Владимирович — доцент кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, врач-терапевт
клинико-диагностического отделения У КБ № 1, канд. мед. наук.Родионова Екатерина Сергеевна — клинический интерн (в 2008—2009 гг.)
кафедры факультетской гсрапии № 1 лечебного факультета Первого МГМУ
им. И.М. Сеченова.Самойленко Валерий Вячеславович — ассистент кафедры факультетской
терапии № 1 лечебного факультета Первого МГМУ им. И.М, Сеченова (до
2010 г.), канд. мед. наук,Сапожников Дмитрий Леонидович — врач хирургического отделения № 3
Факультетской хирургической клиники им, Н.Н. Бурденко Первого МГМУ
им. И.М, Сеченова.
Авторский коллектив 9Саркисова Наталия Донатовна — заведующая отделением кардиологии
Факультетской терапевтической клиники им. В.Н. Виноградова, канд. мед.
наук.Седов Всеволод Парисович — профессор кафедры лучевой диагностики и
лучевой терапии Первого М ГМ У им. И. М. Сеченова, врач отделения функтщ-
ональной диагностики клиники кардиологии, д-р мед. наук.Седов Алексей Всеволодович — врач отделения кардиологии Факультетской
терапевтической клиники и.м. В.Н. Виноградова Первого МГМУ им. И.М. Сече¬
нова.Синицын Валентин Евгеньевич — руководитель Центра лучевой диагностики
Лечебно-реабилитационного центра Росздрава, профессор, д-р мед. наук.Смирнов Василий Евгеньевич — врач межхлинического ангиографичсского
отделения ММА им. И.М. Сеченова (до 2006 г).Сокол Евгения Владимировна — клинический ординатор (в 2007—2009 гг.)
кафедры факультетской терапии № 1 лечебного факультета Первого МГМУ
им. И.М. Сеченова.Сон Елена Алексеевна — ассистент кафедры факультетской терапии № ]
лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед. наук.Стойда Алексей Юрьевич — врач межклинического рентгенодиагностиче¬
ского отделения ангиографии отдела лучевой диагностики Первого МГМУ им.
И.М. Сеченова, канд. мед. наук.Сулимов Виталий Андреевич — заведующий кафедрой факультетской тера¬
пии № 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, директор
Факультетской терапевтической клиники им. В.Н. Виноградова, профессор,
д-р мед, наук.Сучкова Светлана Александровна — врач кардиологического отделения
для больных инфарктом миокарда клиники кардиологии Первого МГМУ им.
И.М. Сеченова.Сыркин Абрам Львович — заведующий кафедрой профилактической и неот¬
ложной кардиологии ФППО Первого МГМУ им. И.М. Сеченова, директор
клиники кардиологии, член-корр. РАЕН, профессор, д-р мед. наук.Термосесов Сергей і^турович — хирург-аритмолог, заведуютций отделением
хирургического лечения сложных нарушений ритма сердца и элекгрокардио¬
стимуляции Московского НИИ педиатрии и детской )шрургии.Троицкая Мария Павловна — аспирант кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова.Угрюмова Лшщя Николаевна — заведующая отделеш^ем гастроэнтерологии
Факультетской терапевтической клиники им. В.Н. Виноградова, канд. мед. паук.Фролова Юлия Валерьевна — ведущий на\^ный сотрудник отделения хирур¬
гического лечения дисфункций миокарда и сердечной недостаточности РНЦХ
им. акад. Б.В. Петровского РАМН, канд. мед. наук.Царегородцев Дмитрий Александрович — доцент кафедры факультетской
терапии № 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, врач
межклинического решгенодиагностического отделения ангиографии отдела
л^-чевой диагностики Первого МГМУ им. И.М. Сеченова, канд. мед. наук.
10 Клинические разборы...Чичкова Наталия Васильевна -- доцент кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед. наук.Шилов Евгений Михайлович — заведующий кафедрой нефрологии и гемо¬
диализа ФППО Первого МГМУ им. И.М. Сеченова, профессор, д-р мед. наук.Щедрина Ирина Сергеевна — врач терапевтического отделения Факуль¬
тетской терапевтической клиники и.м. В.Н. Виноградова Первого МГМУ
им. И.М. Сеченова, канд. мед. наук.
список СОКРАЩЕНИЙлее (American College of Cardiology) — Американский колледж кардиологии
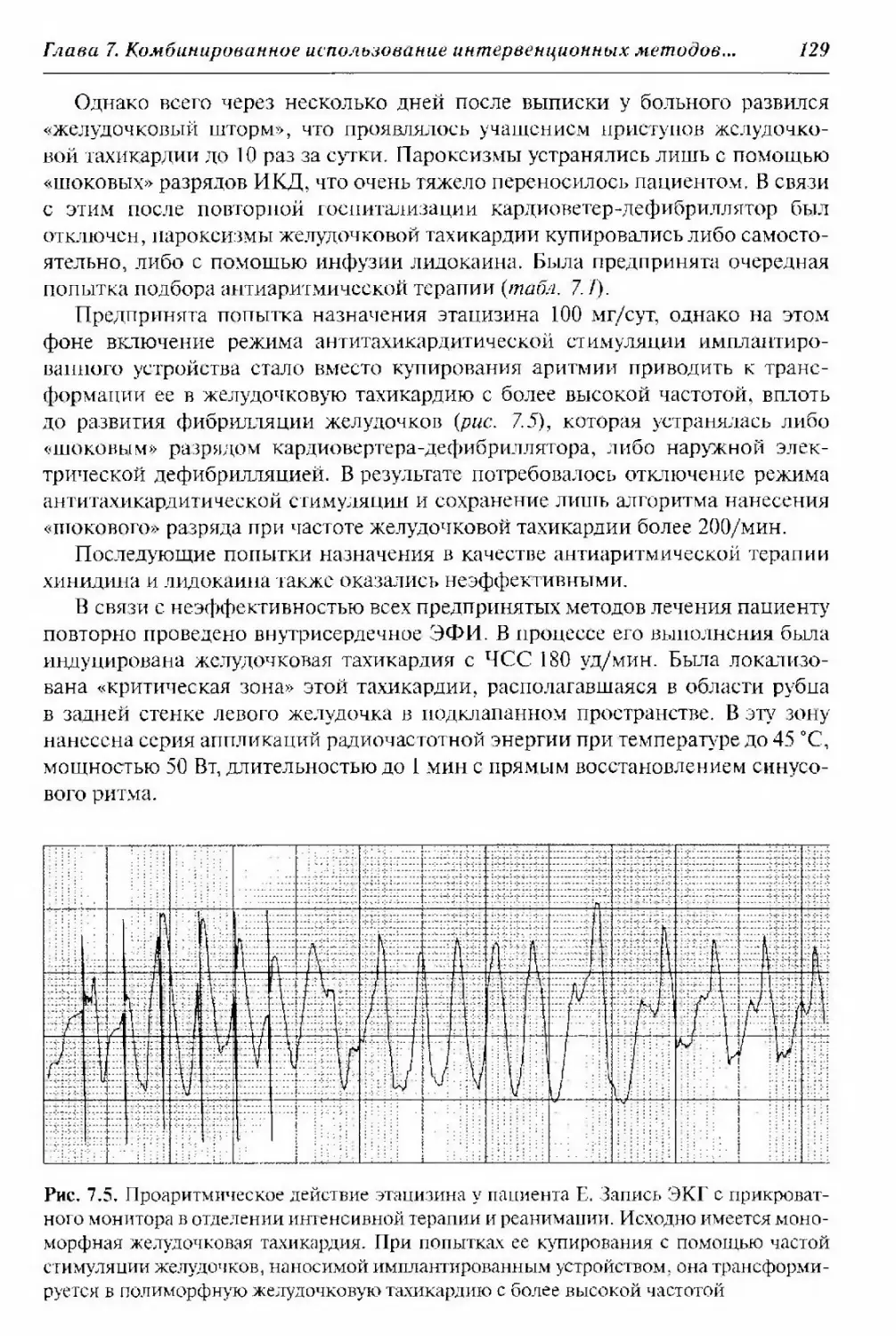
ANCA — антитела к цитоплазме нейтрофилов
cANCA — цитоплазматические антитела к цитоплазме нейтрофилов
Dla^j — диффузионная емкость легких, измеренная в единицах концентрации гемогло¬
бинаDj_co ~ диффузионная емкость легких для СО (монооксила углерода)DMT-1, Nramp-1 (natural resistance-associated macrophage protein) — белок-транспортер
G-CSF — гранулоцитарный колониестимулирующий фактор
GM-CSF — гранулоцитарно-макрофагшіьньїй колониестимулирующий фактор
ISS (International Staging System) — международная система определения стадии забо¬
леванияNYHA — Нью-Йоркская ассоциация сердечных заболеванийpANCA — перинуклеарные антитела к цитоплазме нейтрофиловRW — реакция ВассерманаSaOj — сатурация (насыщение) крови кислородомSpOj — насыщенность крови кислородомVTI — velocity time integral (линейный интеграл кровотока)у-ГТ — гамма-глутамилтрансферазаАаРО^ — альвеолярно-артериолярный фадиентАВ — aTpHOBeHTpHKyj'iHpHb^(aH)АДПЖ — аритмогенная дисплазия правого желудочкаАКА — антикератиновые антителаАД — артериальное давлениеАЛТ — аланинаминотрансферазаАМА — антитела к митохондриямАНА — антинуклеарные антителаАНФ — антинуклеарный факторАНЦА — антитела к цитоплазме нейтрофиловАПФ — ангиотензинпреврашающий ферментACT — аспартатаминотрансферазаАФП — альфа-фетопротеинАЦЦП — антитела к циклическому цитруллинированному пептидуАЧТВ — активированное частичное тромбопластиновое времяБАЛ — бронхоальвеолярньтй лаважВГВ — вирус гепатита ВВИЧ — вирус иммунодефицита человекаВОЗ — Всемирная организация здравоохраненияВОПЖ — выводной отдел правого желудочкаВПГ — вирус простого герпесаВС — внезапная смертьГКМП — гипертрофическая кардиомиопатияГКС — глюкокортикостероидыГЛЖ — гипертрофия левого желудочка
12 Клинические разборы.ДДЛА — диастолическое давление в легочной артерии
дзет — диффузные заболевания соединительной ткани
ДИ — доверительный интервалДИП — десквамативная интерстициальная пневмонияДМ — дерматомиозитДНК — дезоксирибон>'клеиновая кислотаЖЕЛ — жизненная емкость легкихЖНР — желудочковые нарушения ритмаЖТ — желудочковая тахикардияЖЭ — желудочковая экстрасистолияЗС — задняя стенкаИБС — ишемическая болезнь сердцаИКД — имплантируемый кардиовертер-дефибршыяторИИП — идиопатическая интерстициальная пневмонияИЛФ — идиопатический легочный фиброзИМТ — индекс массы телаИФН-а — интерферон-альфаИЭ — инфекционный эндокардитКА — коэффициент атерогенностиКДО — конечный диастолический объемКДР — конечный диастолический размерКИ — кислородный индексКОП — криптогенная организчтощаяся пневмонияКСО — конечный систолический объемКСР — конечный систолический размерКТ — компьютерная томографияКФ — клубочковая фильтрацияКФК — креатининфосфокиназаЛА — легочная артерияЛАМ — лимфангиолейомиоматозЛАМ-ТС — лимфангаолейомиоматоз, сочетанный с т>’берозным склерозом
ЛДГ — лактатдегидрогеназа
ЛЖ — левый желудочеклип — лимфоцитарная интерстициальная пневмония
ЛП — левое предсердиеЛПВП, ЛПВП-хс — липопротеины высокой плотностиЛПНП, ЛПНП-хс — липопротеины низкой плотностиЛПОНП, ЛПОНП-хс — липопротеины очень низкой плотностиМА — мерцательная аритмияМВ-КФК — МВ-фракция креатининфосфокиназыМЖП — межжелудочкова;! перегородкаММ — множественная миеломаМНО — международное нормализованное отношениеМОС — максимальная объемная скоростьМРТ — магнитно-резонансная томофафия
Список сокращений 13MCKT — \і>''льтиспиральная компьютерная томография
НИГТ — неспецифическая интерстициальная пневмония
ОЖСС — общая железосвязывающая способность сыворотки
ОИП — острая интерстициальная пневмония
ОР — относительный рискОФВ, — объем форсированного выдоха за одн>’ секунду
ПЖ — правый желудочек
ПЗР — передне-задний размер
ПИ — протромбиновый индекс
ПМ — полимиозитПНУЛ — предсердный натрийуретический пептид
ПЦР — полимеразная цепная реакцияРБ-ИЗЛ — респираторный бронхиолит, ассоциированный с ИЗЛ
РИБТ — реакция иммобилизации бледных трепонем
РИФ — реакция иммунофлюоресценцииРКФМ-тест ~ тест на растворимые комплексы фибрин-мономераРФ — ревматоидный факторРЧА — радиочастотная аблацияСДЛА — систолическое давление в легочной артерииСКВ — системная красная волчанкаСОЭ — скорость оседания эритроцитовСПИД — синдром приобретенного иммунодефицитаСРВ — С-реактивный белоктЗС — толщина задней стенкитЗСІЖ — толщина задней стенки левого желудочкатМЖП — толщина межжелудочковой перегородкитПЖ — толщина правого желудочкаТПО — тиреоидная пероксидазатРНК-синтетаза — синтетаза транспортной рибонуклеиновой кислотыТТГ — тиреотропный гормонТЭЛА — тромбоэмболия легочной артерииУЗИ — ультразвуковое исследованиеУЗ — ультразвуковойУО — ударный объемФВ — фракция выбросаФВД — функция внешнего дыханияФЖ — фибрилляция жел>^дочковФЖЕЛ — фактическая жизненная емкость легкихФНО — фактор некроза опухолейХГВ — хронический гепатит ВХСН — хроническая сердечная недостаточностьЦИК — циркулирующие ик1мунные комплексыЦМВ — цитомегаловирусЦП — цирроз печениЧСС — частота сердечных сокращений
14Клинические разборы.ШИК-реактщя — исследование с использованием шифф-йодной кислотыШФ — щелочная фосфатазаЭГДС — эзофагогастродуоденоскопияЭКГ — электрокардиограммаЭКС — злекірокардиости.муляторЭМГ — электромиографияЭОС — электрическая ось сердцаЭхоКГ — эхокардиографияЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ И ИХ НОРМАЛЬНЫЕ
ЗНАЧЕНИЯ, ИСПОЛЬЗУЕМЫЕ В ДАННОЙ КНИГЕПоказательНорма (в единицах СИ)Норма (в других единицах)Триглицериды0,57-2,28 ммоль/л50—150 мг/дяОбщий холестерин3,88-6,47 ммоль/л150-250 мг/длЛВП0,7-2,3 ммоль/л35-75 мг/длЛНП2,6-4,2 ммоль/л100-160 мг/длЛОНП0,114-0,342 ммоль/л10-30 мг/длКоэффициент атерогенности1,2-4,21,2-4,2Альбітиіиновая фракция■54,8-66,8%Альфа-1 -глобулршы—3,7-7,8%Лльфа-2-глобулины—5,2-10,7%Бета-глобулины_8,6-13,7%Гамма-глобулины—10,7-19,3%Обший белок57-82 г/л6,0-8,0 г/длАльбумин32-48 г/л3,5-5,0 г/длКреатинин44—115 мкмоль/л0,7-1,4 мг/длГлюкоза4Д-5,9 ммоль/л60-100 мг/длАзот мочевины3,2-8,2 ммоль/л10-20 мг/длМочевая кислота148,75-416,5 мкмоль/л2,5-7,0 мг/длОбщий билирубин5,0-21,0 мкмоль/л0,2-1,0 мг/длПрямой билирубин0-5,0 мкмоль/л0-0,2 мг/длНепрямой билирубин0-16,0 мкмоль/л0—0,8 мг/длНатрий135-145 мэкв/л—Калий3,5-5,0 мэкв/л—Железо8,0-30,0 мкмоль/л40—160 мкг/длЩелочная фосфатаза0-115 ед/л—Гамма-ГТ0-55 ед/л—ACT0-40 ед/л_АЛТ0-40 ед/л—КФК38-174 ед/л—МВ-КФК0-25 ед/л—
ПРЕДИСЛОВИЕДорогие коллеги — читатели этой книги!Перед вами сборник клинических разборов, составленный сотрудника¬
ми Факультетской терапевтической клиники им. В,Н. Виноградова Первого
Московского государственного медицинского университета им, И.М. Сеченова
(прежде — Первого Московского медицинского института. Московской меди¬
цинской академии, а до того — медицинского факультета Императорского
московского университета) — старейшей терапевтической клиники России.
Идея единой терапевтической клиники, которая вынашивалась нашими пред¬
шественниками, продолжает жить, несмотря на неизбежную и стремитель¬
ную специализацию во всех областях внутренней медицины. Как писал
ГА.Захарьин, «что было бы и с преподаванием, и с наукой, если бы существо¬
вали лишь специальные кяиники, если бы не было такой, которая имела бы
главной целью достижение связи всех явлений данного болезненного строя.
Такой клиникой была и всегда будет клиника внутренних болезней», И такая
клиника с'фоится не просто на взаимодействии узких специалистов — это
изначально единый подход к больному.Мы ііадеемся, что в этом сборнике (хотя мы и не ставили такой задачи
специально) нашли отражение все особенности Факультетской терапии —
клиники, кафедры, школы. Здесь студенты не только изучают определенный
круг нозологий — они впервые учатся клиническому мышлению и тому, как
вести диагностический поиск. В далеко не студенческих случаях, вошедших в
сборник, именно следование мудровско-захарьинскому методу обследования
больного (с подробнейшим сбором анамнеза, который ничем невозможно
заменить) вело врачей к постановке «трудньп^ диагнозов». Мы считали важ¬
ным сохранить для читателя все этапы и нюансы диагностического поиска,
предельно очерчивая индивидуальность каждого случая, все трудности, сомне-
ния и ошибки. Широко — и в тесной взаимосвязи с вопросами, которые ставит
конкретная клиническая ситуация — привлекаются и анализируются данные
современной медицинской литературы. «Больной — книга, книга — больной»
(Е.М.Тареев) — в этом принципе вся суть клинической работы.Клиника не только учебное заведение. Традиционно сюда направляют
сложных, непонятных пациентов. Больному, который попал в Факультетскую
терапию, диагноз должен быть поставлен. Некоторая часть представленных
наблюдений уникальна (принцип «частые болезни встречаются часто, ред¬
кие — редко» верен, но не означает, что редких болезней не бывает совсем;
опыт показывает, что частота постановки редких диагнозов зависит от готов¬
ности к этому врача). Принимая пациентов с неустановленным диагнозом не
только из районных поликлиник, но и из центральных институтов страны,
мы много раз убеждались в том, что единый подход к больному оказывается
16 Клинические разборы...важнее, чем глубокие, но узкоспециализированные знания. «Специалист
подобен флюсу — полнота его одностороння», — говорил Е.М. Тареев. К сожа¬
лению, существует разрыв между «первичным звеном» медицинской помощи
и высокоспециа.шзированными учреждениями. Наша клиника — мы надеем¬
ся — отчасти заполняет эту нишу.В то же время практически в каждом из представленных клинических
наблюдений к диагностике и, особенно, к лечению привлекались высоко¬
классные специалисты. Мы не просто открыты для взаимодействия — сегод¬
ня мы не видим возможности полноценно помочь больному без участия
«узких» специалистов, поскольку при современном уровне медицины уже
невозможно одинаково хорошо владеть методами лечения в разных областях
внутренней медицины (зачастую — даже в рамках одной терапевтической
специальности). Завершив обследование и лечение в клинике, значительная
часть больных была направлена в дружественные нам учреждения, в том числе
и на хирургическое лечение. Так должно быть. Вместе с тем интервенцион¬
ные методы лечения прочно вошли в практику работы самой Факультетской
клиники.Клиника носит имя В.Н. Виноградова. Мы имеем еще возможность сиро-
сить тех, кто непосредственно работал с Владимиром Никитичем: что было для
него главным? — «Всё для больного». Этому учатся с первых шагов в клинике.
Сделать все возможное и не сделать лишнего. Лечить — когда нельзя не лечить.
Помогать че.м можем — когда :^ффсктивного лечения нет. Ставить диагноз — не
ради диагноза, не из научного или «академического» интереса. В обсуждении
многих из представленных в сборнике больных встает вопрос: как си.ттьно мы
можем рисковать в стреАшении разобраться до конца? Ответ зависит только от
того, насколько это может помочь больному. И все же почти в половине случа¬
ев была проведена морфологическая верификация диагноза.Несмотря ііа совершенствование инструментальной диагностики, про¬
цент диагностических ошибок (по данным патологоанатомов) остается неиз¬
менным. Все сложнее бывает разобраться с данными УЗИ, КТ, МРТ, дать им
однозначную, верную интерпретацию, избежать субъективности. Сколько
раз мы получали противоположные заключения от разных параклинических
специалистов! Значение прижизненной морфологической диагностики только
растет — в кардиологии, пульмонологии, гастроэнтерологии, ревматологии.
В работе клиники за последние годы это стало одной из очевидных тенден¬
ций — необходимость получить «кусочек болезни», построить лечение на
камне морфологических данных вытекает из того, что все более агрессивной
становится терапия: показания к ней должны быть абсолютными. Заметное
преобладание иммуно-воспалительной, инфекционной и генетической пато¬
логии — сше одна особенность этого сборника, которая отражает реальную
ситуацию в современной клинике внутренних болезней.Наконец, для нас этот сборник — бесценное собрание историй болез¬
ней наших пациентов, каждый из которых нам дорог и по-своему уникален.
Это наш опыт, с каждым из этих больных мы немного росли и одновре¬
менно понимали всю бесконечную сложность и разнообразие клинической
Предисловие 17медицины. М.Я. Мулров писал, поручая свой клинический архив ученикам:
«Сие сокровииіс для меня дороже всей моей библиотеки. Печатаые книги
везде можно найти, а историй болезни нигде. В 1812 г. все книги, состав¬
лявшие мое богатство и ученую роскошь, оставались здесь на расхищение
неприятелю, но сей архив везде был со мною; ибо от больных приобретают¬
ся книги и цельте библиотеки». Тот архив сохранить не удалось, но оста-шсь
«ІСтинические лекции» Г.А. Захарьина, Л.Е. Голубинина, уже совсем недавние
работы М,П. Кончаловского, Д.Д. Плетнева, В.Н. Виноградова. Перечитывая
их, понимаешь: по большому счет>; в клинической работе ничего не меняется.
Мы надеемся, что у студента и молодого врача, только начинаютцего свой
путь в медицине, эта книга пробудит вкус к ежедневной и далеко не рутинной
врачебной работе, а в опытном клиницисте найдет заинтересованного и сочув¬
ствующего читателя.
ПУЛЬМОНОЛОГИЯГлава 1ИДИОПАТИЧЕСКИЕ ИНТЕРСТИЦИАЛЬНЫЕ
ПНЕВМОНИИ: СОВРЕМЕННЫЙ ПОДХОД
К ДИАГНОСТИКЕ, ТРУДНОСТИ ЛЕЧЕНИЯ ПРИ
НАЛИЧИИ СОПУТСТВУЮЩЕЙ ПАТОЛОГИИС,И. Овчаренко, ЕЛ. Сон, В.А. КапустинаСовременные исследования проблемы интерстициальных заболеваний лег¬
ких носят мулътидисциплинарный характер и базируются, наряду с анализом
кяинической картины, на изучении данных компьютерной томографии (КТ)
высокого разрешения в сопоставлении с данными морфологического исследо¬
вания ткани легкого. Внедрение результатов этих исследований в клиническую
практику позволяет назначать дифференцированную терапию и определять
прогноз у конкретного больного.приводим клиническое наблюдение, которое иллюстрирует НС только
возможности современных методов диагностики, но и сложности в терапии
интерстициальных заболеваний легких у пожилых больнык с сопутствующей
патологией (в первую очередь кардиальной),Больная К,, 75 лет, неоднократно наблюдалась в терапевтическом отделении
Факультетской терапевтической клиники им. В.Н. Виноградова. При первом
поступлении в KjjHHHKy fi декабре 2007 п предъявляла жалобы:— на выраженную одышку при минимальной физической нагрузке и в
покое, сопровождающуюся сердцебиением;— повышение АД максимально до 200/100 мм рт.ст., сопровождающееся
болями в затылке (адаптирована к АД 130 и 80 мм рт.ст.);— эпизоды перебоев в работе сердца, возниюювенис которых ни с чем не
связывала;— головокружение и пошатьцзание при ходьбе;— ощущение утренней скованности в мелких суставах кистей, длящейся
до получаса.Анамнез заболевания (рис. /.}): с 45 лет отмечает подъемы АД максимально
до 200/100 мм рт.ст.; длительное время постоянной антигипертензивной тера¬
пии не получала, с 60 лет принимает комбинацию антигипертензивных пре¬
паратов различных групп с некоторым положительным :>ффскюм. Примерно15 лет назад (в возрасте 60 лет) отметила появление болезненности в правом
Глава 1. Идиопатические интерстициальные пневмонии...191;160ЭКГБПНПГ
БПВЛНПГ
АВ ІСТ.ЭСДиагнозПодагра/Рис. 1.1. Анамнез заболевания больной К., 75 леттазобедренном суставе, по поводу чего находилась на стационарном лечении с
диагнозом «коксартроз», внутрисуставно вводился кеналог с эффектом.В начале 1997 г (в возрасте 65 лет) впервые появилось ощущение скован¬
ности, болей и припухання в мелких суставах кистей и коленных суставах.
Находилась на стационарном лечении в ГКБ № 5, состояние было расценено
как подагра, однако с учетом повышенного титра ревматоидного фактора
(РФ) (1:160) проводилась дифференциальная диагностика с ревматоидным
артритом. Лечи^іась нестероидными противовоспалительными препаратами с
эффектом. Медицинская документация отсутствует В это же время впервые
отметила появление небольшой одышки при физической нагрузке, на которую
особого внимания не обратила (так как связывала ее с возрастом и избыточной
массой тела),В 2002 г. (в возрасте 69 лет) на ЭКГ были зафиксированы блокада правой
ножки пучка Гиса, блокада передней ветви левой ножки пучка Гиса, атрио¬
вентрикулярная блокада 1 степени, экстрасистолия (?), по поводу чего был
назначен аллапинин в дозе 25 мг/сут^ которьгй пациентка npHHHMBjia вплоть
до госпитализации в Факультетскую терапевтическую юшнику. Все это время
постепенно продолжала нарастать одышка, которая с 2002 г стала возникать
при бытовых физических нагрузках. Терапевтом по месту жительства это бьшо
20 Пульмонологиярасценено как проявление застойной сердечной недостаточности у больной
69 лет с выявленными изменениями на ЭКГ.Значительное ух>'дшение состояния — с февраля 2007 г., когда больная
вновь отметила появление отечности и покраснение коленных суставов, лечи¬
лась в/м инъекциями нестероидных противовоспалительных препаратов с
хорошим эффектом, с этого же времени значительно наросла одышка, которая
стала беспокоить при минимальных физических нафузках и в покое, что резко
изменило качество жизни больной. Рентгенологическое исследование легких
длительное время не проводилось, с вышеописанными жалобами больная
поступила в Факультетск>то терапевтическую клинику в декабре 2007 г.При поступлении: состояние средней тяжести. Обращала на себя внимание
повьппенная масса тела больной [рост 165 см, вес 93 кг, индекс массы тела
(ИМТ) 35,5 кг/м^]. Визуально суставы не изменены, объем движений в них
сохранен. ЧД 24 в минуту. Основные изменения бьти выявлены при аускуль¬
тации в легких: высл>тш[ивались нежная крепитация в базальных отделах обоих
легких на большом пространстве, единичные с>^ие свистящие хрипы на фор¬
сированном выдохе. Тоны сердца приглушены, шумов нет. Частота сердечных
сокращений (ЧСС) 96 ударов в минуту, частая экстрасистолия. АД 160/90 мм
рт.ст. Живот увеличен за счет жировой клетчатки, при пальпации мягкий, без¬
болезненный во всех отделах, жидкости нет. Печень, селезенка не увеличены,В клиническом анализе крови, кроме некоторого снижения тромбоцитов
(160 тыс.), патологии не выявлено. В повторных анализах крови число тромбоци¬
тов в пределах нормы. В биохимическом аншіизе крови — шперлипидемия 4 типа
[триглицериды 213 мг/л^'1 при норме 50—150, общ. холестерин 123 мг/дл, ЛПВП
42 мг/дл, ЛПНП 38,1 мг/дл, ЛПОНП 42,6 мг/дл при норме 10—30, коэффици¬
ент атерогенности (КА) 1,93], в остальном без патологии. Обращало на себя
внимание повышение уровня С-реактивного белка (СРВ) (-Ы-++), а также РФ
(+++-І-) и незначительное увелі^чение титра антинуклеарного фактора (1:40,
свечение гомогенное). Австралийский антиген и антитела к вирусу гепатита С
не обнаружены.В первом анализе мочи отмечалось увеличение уровня лейкоцитов до 5-7
в п/зр, в анализе мочи по Нечипорснко — 0,125%о белка в первой порции,
лейкоциты 4750 и 3000 в 1 мл в 1-й и 2-й порциях, эритроциты — 250 и 20000
соответственно.в К.1ИНИКЄ урологии им. P.M. Фрониггейна было проведено УЗИ почек, при
котором выявлен конкремент в чаше^гке левой почки, микрогематурия бьша
расценена как проявление почечно-каменной болезни, было рекомендовано
динамическое наблюдение за больной.На ЭКГ (рис. 1.2) регистрировались частая желудочковая экстрасистолия
по типу аллоритмии (бигеминия), АВ-блокада I степени (PQ 0,22 с), полная
блокада правой ножки пучка Гиса, блокада передней ветви левой ножки пучка
Гиса.При суточном мониторировании ЭКГ по Холтеру выявлено: PQ днем до 0,22 с,
ЧСС днем 55-12/мин (ср. 86/мин), ЧСС ночью 42—84/мин (ср. 50/мин),
около 2 тыс. наджелудочковьЕХ экстрасистол, а также около 2 тыс. политопных
Глава 1. Идиопатические интерстициальные пневмонии.21 !f^/K 1^ I^S ift'riiaРис. 1.2. Электрокардиограмма больной К. (скорость записи 25 мм/с)желудочковых экстрасистол (в TO\f числе куплеты, триплеты) и 2 пробежки
неустойчивой желудочковой тахикардии из 4-5 комплексов.в связи с наличием частой желудочковой экстрасистолии в качестве антиа-
ритмического препарата бы.а выбран соталол в дозе 80 мт/суг. При повторном
мониторировании ЭКГ, проведенном на фоне приема препарата, отмечалась
положительная динамика в виде урежения ЧСС днем до 43-91/мин (ср. ЧСС
53/мин), в ночные часы — до 33—57/мин (ср. ЧСС 40/мин), уменьшения числа
как наджелудочковых (до 500), так и желудочковых (до 395) экстрасистол;
отсутствовали пробежки желудочковой тахикардии.При ЭхоКГ — аорта 3,5 см, уплотнена, левое предсердие 4,9 см (N до 4,0),
объем 70 мл (N до 65 мл), правое предсердие 4,5x3,4 см (N 4,5x3,5), левый
желудочек не расширен (КДО 83 мл, КСО 30 мл), толщина МЖП 1,5 см, ЗСЛЖ1,2 см (N до 1,1), ФВ 63%. Правый желудочек не расширен, толщина его стен¬
ки 0,6-0,7 см (N до 0,5). Аортальный клапан; створки уплотнены, амшіитуда
раскрытия не уменьшена (2,1 см при N >1,5), скорость кровотока 101 см/с
(N 80-160). Митральный клапан; подвижность створок не ограничена, регур-
гитации нет, трансмитральный поток: Е = 3,5 см/с, А 7,5 см/с, Е/А 0,5.
Заключение: гипертрофия обоих желудочков. Умеренно выраженная дилатация
левого предсердия. Клапанный аппарат без грубой патологии. Признаки уме¬
ренно выраженной легочной гипертензии. Нар>тііений локальной и глобальной
22ПульмонологияРис. 1.3. Рентгенография органов грудной
клетки больной К. (прямая проекция)сократимости левого желудочка не
выявлено.При УЗИ органов брюшной полос¬
ти печень не увеличена, контуры
ровные, четкие, паренхима неодно¬
родной структуры за счет множе¬
ственных гиперэхогснных вклю¬
чений по ходу внутрипеченочных
желчньге протоков, средней степе¬
ни эхогенности, сосудистый рису¬
нок «смазан», внутрипеченочные
желчные протоки не расширены;
воротная вена до 6,5 мм, кровоток
гепатопетатьный, фазный; желчный
пузъфъ удален. Вышшены кисты в обеих почках — справа одна размерами до
72x58 мм, слева две кисты размерами 41х23мм и 11 мм в диаметре.П ри рентгенологическом исследовании органов грудной клетки ірис. 1.3) обра¬
щали на себя внимание снижение прозрачности легочного фона, выражен¬
ное уп.10тнение интерстиция, мелкоячеистая деформация легочного рисунка
по типу «сотового легкого^» в базальных отделах с обеих сторон. Выявлена
воздутлная булла в верхнем сегменте левого легкого 5,5 см в диаметре.
Рентгенологическая картина не позволяла исключить фиброзирующий аль-
веолит.В связи с выявленными изменениями проведена компьютерная томогра¬
фия органов грудной клетки (рис. 1.4), при которой более четко бьыа видна
перестройка легочного рисунка за счет интерстициального фиброза преиму¬
щественно в субплевральных отделах обоих легких, что соответствовало
КТ-признакам фиброзируюшего атьвеолита.При исследовании функции внешнего дыхания (ФВД) отмечены как выраженные
рестрикгивные изменения в виде значительного снижения жизненной емкости
легких (1720 мл:, 56% от нормы), так и обструктивные — снижение ОФБ, (62%),
причем рестриктивные изменения преоб.аадали над обструкгивными. Отмечено
снижение сатурации кислорода до 90%. Реакция на атровент бьиіа выражена слабо
(OOBj увеличился до 69%; MOQj 126%, МОС.^^ 62%, МОС.^ 41%, ОФВуФЖЕЛ
75% при исходньг( показателях 114%, 48%, 27%, 69%). Бодиплетизмография (рис.1.5) еще раз подчеркнула преимущественные изменения по рестриктивному типу
(значительно снижены общая емкость легких и остаточный объем).Таким образом, клиническая и инструментальная картина соответствовала
фиброзируюЕцему альвеолиту, природу которого необходимо было уточнить,
в первую очередь требовалось ответить на вопрос, является ли данный фибро¬
зирующий алъвеолит проявлением поражения легких в рамках диффузных
заболеваний соединительной ткани (наиболее вероятно, ревматоидного артри¬
та) или он является самостоятельным заболеванием.в связи с имеющимся суставным синдромом была проведена рентгеногра¬
фия суставов кистей, при которой признаков ревматоидного артрита выявлено
Глава L Идиопатические интерстициальные пневмонии...23Ш'Шкшь -Рис* 1.4. Компьютерная томография легких больной К.ПотокРис. 1.5. Бодиплетизмотрафия больной К,НС бьыо (определялись диффузный остеопороз с кистовидной перестройкой,
краевые костные разрастания в области суставных поверхностей и незначи¬
тельное сужение суставных щелей дистальных мсжфаланговых суставов, 5-я
пястная кость правой кисти несколько укорочена и утолщена). На рентгено¬
граммах коленньа суставов определялись диффузный остеопороз, значительное
заострение межмыщелковых возвьппений обоих коленных суставов и неболь¬
шие краевые костные разрастания в области суставных поверхностей.Больная была проконсультирована заведующей отделением патологии суста¬
вов и соединительной ткани Факультетской терапевтической клиники Н.В. Пету¬
ховой, которая также отвергла наличие у больной ревматоидного артрита.С учетом возраста, в котором началось заболевание, его течения, преобла¬
дания одыпгки над кашлем, отсутствия других явных причин фиброзирующего
альвеолита мы остановились на диагнозе идиопатического фиброзирующего
альвеолита.
24 ПульмонологияЗаключительный диагноз был сформу^тирован следующим образом; идио-
патический фиброзируюший альвеол ит. Булла левого легкого с лока^чизацией
в S3. Дыхательная недостаточность IT степени. ИБС: атеросклеротический
кардиосклероз с нарушениями ритма и проводимости сердца: суправентри-
кулярная экстрасистолия, частая желудочковая экстрасистолия, полная бло¬
када правой ножки пучка Гиса, блокада передней ветви левой ножю-! пучка
Гиса, АВ блокада I степени. Атеросклероз аорты, коронарных и церебраль¬
ных артерий. Гипертоническая болезнь ТІ стадии, 3 степени повышения
АД, высокого риска. Дисциркуляторная эннефа.аопатия смешанного генеза.
Экзогенно-конституциональное ожирение 3-й степени. Гиперлипидемия 4-го
типа. Остеоартроз с преимуш,ественным поражением шейно-грудного отдела
позвоночника, мелких суставов кистей рук, коленных суставов. Кисты ночек.Выписана из клиники с рекомендациями продолжить прием следуюпіих пре¬
паратов: атровент по 2 вд. 4 р/сут, флуи\туцил і200—1800 мг/сут, сиднофарм2 мг по 1 таб. 2 р/сут (у, в), соталекс 160 мг по V4 таб. 2 р/сут (у, в), рснитек 10 мг
по 1 таб. >пгром и Уг таб. вечером, арифон-ретард 1,5 мг по 1 таб. утром, тромбо-
АСС 100 мг по 1 таб. на ночь, к,чоназепам 2 мг ло ’А таб. на ночь, коаксил 12,5 мг
по 1 таб. 2 р/сут. ГТрием флуимутдила в высоких дозах был рекомендован в каче¬
стве антиоксидантной терапии.С учетом необходимости морфологической верификации диагноза для
определения дальнейшей тактики лечения больная была проконсультирована
в Национальном медико-хирургическом центре им. Н.И. Пирогова профес¬
сором Ю.А. Аблицовым, который принял решение о необходимости провести
видеоторакоскопическую биопсию легкою.Однако с умістом низких вентиляционных показателей и невозможности
отключения левого легкого из вентиляции от выполнения вилеоторакоскопи-
ческой биопсии решено было воздержаться, и 20.02.2008 г. в Национальном
мсдико-хирургичсском центре им. Н.И. Пирогова больной были проведены
резекция легкого из миниторакотомного дост>тта с целью морфологического
исследования и буллэктомия.Патологоанатомичсская служба Национального медико-хирургического
центра им. Н.И. Пирогова дала следующее гистологическое заключение: бронхи
расширены, деформированы, эпителий мерцательный, вокруг бронхов —
плотные лимфоидные инфильтраты. Межа-1ьвеолярныс перегородки скле-
розированы, резко утолщены, содержат слабовыраженньте очаговые лимфо¬
идные инфильтраты, пучки гладкой мускулатуры и артерии, большей частью
перестроенные по замыкательному типу. Большинство альвеол в состоянии
эмфизематозного вздутия. Изредка встречаются гиалиновые массы в просветах
альвеол.Учитывая, что гистологическое зак^тючение носило лишь описатель¬
ный характер, те же микропрепараты были повторно проконсультированы
на кафедре патологической анатомии ММА им. И.М. Сеченова (Первого
МГМУ им. И.М. Сеченова) профессором Е.А. Коган. Заключение: диффе>
ренциальный диагноз необходимо проводить между фиброзирующим альвеоли-
том (обьиной интерстициальной пневмонией) на стадии «сотового легкого*»
Глава 1. Идиопатические интерстициальные пневмонии.., 25и лимфангиолейомиоматозом легкого на стадии «сотового легкого»-. Учитывая
своеобразный характер кистозных изменений в «сотовом легком» с выражен¬
ным гладкомышечным компонентом, а также отсутствие миофибробластиче-
ских фокусов, следует думать о наличии у больной лимфангиолейомиоматоза
легкого на стадии «сотового легкого» с очаговым аденоматозом и фокусами
вторичного протеиноза. Для уточнения диагноза бьшо рекомендовано про¬
ведение иммуногистохими*іеской реакции с антителами против рецепторов
к эстрогену и прогестерону НМВ45.С нашей точки зрения, диагноз лимфангиолейомиоматоза вызьгеал боль¬
шие сомнения, поскольку данное заболевание преилсущественно возникает
у женщин фертильного возраста. Однако рекомендации были выполнены:
микропрспаратьт были исследованы в НИИ пульмонологии, в лаборатории
профессора А.Л. Черняева профессором М.В. Самсоновой — реакция с НМВ45
отрицательная.Таким образом, окончательным диагнозом являлся фиброзирующий альвеолит.На представленных фотографиях микропрепаратов {рис. 1.6, а, см. цветную
вклейку) видны нарушения структуры легочной ткани: сохраненные альвеолы
полностью отсутствуют, определяются лишь фрагменты утолщенных разо¬
рванных межа^іьвеолярньїх перегородок и формирующиеся соты. Легочная
паренхима замещена разрастающимися коллагеновьтми волокнами с формиро¬
ванием зон фиброза (бледно-розовый цвет); определяются гладко-мышечные
волокна (более темная окраска).При 100-кратном увеличении [рис. 1.6, 6, см. цветную вклейку) видны тон¬
костенные вновь образованные сосуды в полях фиброза (признак ангаонеоге-
неза), в отличие от сосудов из русла легочного ствола, где имеются признаки
легочной гипертензии. Отчетливо видны мышечные разрастания, лимфоцитар¬
ная инфильтрация, которая является микроскопическим маркером активности
воспаления. При окраске по Ван Гизону {рис. 1.6, в, см. цветную вклейку) мышцы
окрашены в желтый цвет, а соединительная ткань сохранила розовую окраску.Заключение, выданное в НИИ пульмонологии, звучало следующим обра¬
зом: идиопатический фиброзирующий альвеолит (обычная интерстициальная
пневмония) с микро- и макросотовой дегенерацией и мышечным циррозом.
Признаки артериальной легочной гипертензии.Больная повторно поступила в Факультетскую терапевтическую клинику
для выбора тактики лечения фиброзируюшего альвсолита.На момент повторной госпитализации сатурация кислорода составляла
63—80%, Проводилась малопоточная многочасовая кислородотерапия, назна¬
чался флуимупил. Причем, согласно последним рекомендациям, в течение3 нед препарат вводился через небулайзер в дозе 600 мг/с>т, в дальнейшем — по
1200—1800 мг/сут внутрь (в зависимости от переносимости).Несмотря на формирование сотового легкого, по данным .морофологиче-
ского исследования имелись также признаки выраженной активности воспа¬
лительного процесса, в связи с чем была предпринята попытка терапии глю¬
кокортикостероидами (метипред 24 мг/сут с постепенным снижением дозы до16 мг/сут). Одновременно с этим для уменьшения побочных эффектов терапии
26 Пульмонологияначат прием препаратов калия (паиангин 3 таб./суг) и калыщя (кальций-актив1 таб./сут). Пациентка продолжала получать антигипсртензивную и антиарит-
мичсскуго терапию.Учитывая наличие у больной нарушений сердечного ритма и проводимо¬
сти, было проведено контрольное суточное мониторирование ЭКГ по Холтеру
(на фоне продолжающейся терапии соталолом в прежней дозе 80 мг/сут), при
котором ЧСС днем составила 45-63/мин (ср. ЧСС 59/мин), ЧСС ночью 29—63/
мин (ср, 37/мин), выявлены более 3 тыс. наджелудочковых и 1230 желудоч¬
ковых экстрасиситол, а также 2 пробежки желудочковой тахикардии из 5—6
комплексов, 94 паузы более 2 с.Пациентка была проконсультирована специалистами Факультетской тера¬
певтической клиники, занимающимися лечением нарушений ритма сердца
(доцентом Д.А. Царегородцевым); в связи с тем, что у больной имеются нару¬
шения атриовентрикулярной и внутрижелудочковой проводимости (гюлная
блокада правой ножки пучка Гиса, передней ветви левой ножки пучка Гиса,
преходящая А В блокада 1 степени) в сочетании с дисфункцией синусового узла
(синдром слабости синусового узла с эпизодами брадикардии до 30/мин), и
необходимостью проведения антиаритмїтческой терапии по поводу желудочко¬
вых нарушений ритма, есть все показания для имплантации постоянного двух¬
камерного частотно-адаптивного электрокардиостищлятора.С учетом изменений, которые претерпела к этому времени классификация
интерстии>тальных болезней легких, диагноз больной на данном этапе наблю¬
дения звучал следующим образом: идиопатический легочный фиброз, леченный
системными глюкокортикостероидами на стадии сотового легкого. Буллезная
эмфизема. Состояние после буллэктомии (22.02.2008 г.). Ограниченный пнев¬
моторакс. Дыхательная недостаточность И1 степени.29.12.2008 г. больная повторно поступила в Факультетскую терапевтическую
клинику для динамического наблюдения и имплантации элекгрокардиостиму-
лятора.При поступлении: состояние средней тяжести, температура тела 36,5°С.
При аускультациги над легкими выслушивается жесткое дыхание, ослабленное,
проводится во все отделы, над нижними отделами обоих легких по-прежнему
выслуцпгвается нежная крепитация. ЧД 22 в минуту. Тоны сердца приглушены,
аритмртчные, сохраняется экстрасистолия. Сердечных шумов нет. ЧСС около 98
в минуту. АД 150/100 мм рт.ст При поступлении больная жаловалась на боли в
области поясничного отдела позвоночника при перемене положения тела, при
осмотре отмечена болезненность при пальпации пояснично-крестцового отдела
позвоіючника.На фоне приема глюкокортикостероидов и оксигенотерапии сатурация
кислорода выросла и составила 93%.При лабораторном исследовании получены следующие данные: в общем ана¬
лизе крови без отклонений от нормы. В биохимическом анализе крови отме¬
чается некоторое увелшіение ЩФ (115 ед/л при норме 32—92) и у-ГТ (114 ед/л
при норме 0—55) при нормальном уровне билирубина, а также повышение
уровня азота мочевины (9,0 ммоль/л при норме 3,2—8,2) и мочевой кислоты
Глава h Идиопатические интерстициальные пневмонии... 27(508,8 мкмоль/л при норме 148,8—416,5). Остальные показатели, включая креа-
тинин (1,11 мг/дл), калий (5,0 мэкв/л), в пределах нормы. В липидном спектре
изменений не произошло.в общем анализе мочи обращали на себя внимание лейкоцитурия (8—14 в п/зр.),
связанная с мочевой инфекцией, по поводу которой был назначен курс терапии
5-НОК, и эритроцитурия (5-10 в п/зр.), связажая с мочекаменной болез?п>ю.По данным КТ органов грудной клетки, картина оставалась прежней, отри¬
цательной динамики по сравнению с предыдущей госпитализацией не отме¬
чено: состояние после атипичной резекции левого легкого. В верхней доле
левого легкого булла размером 39x32 мм. Выраженный мелкосетчатый фиброз
в субплевральных отделах легких с формированием тракционных бронхо- и
бронхиолоэктазов. В средостении визуализируются лимфатические узлы ниж¬
ней паратрахеальной фуппы размером до 10 мм. В перикарде слева по задней
поверхности небольшое количество жидкости.Учитывая жалобы больной на боли в области поясничного отдела позво¬
ночника, было выполнено рентгенологическое исследование, которое выявило
снижение высоты тела и небольшую клиновидную деформацию позвонка
(компрессионный перелом). Пациентка была проконсультирована ортопедом-
травматологом С.А.Сергиенко, рекомендовавшим курсовой прием нестеро¬
идных противовоспалительных препаратов (мовалис 15 мг в/м, кетанов н/н),
терапию миокальциком, препаратами кальция, ношение корсета «ленинград¬
ского типа», спать на жесткой кровати; проведение денситометрии костей и
биохимического анализа крови на содержание Са^^ в плазме крови.Однако по техническим причинам имплантировать электрокардиости¬
мулятор в Факультетской терапевтической клинике не удалось. Для выпол¬
нения этой операции больная была переведена в Московский городской
центр хирургического лечения нарушений ритма сердца, где 28.01.2009 т. ей
был имплантирован двухкамерный частотно-адаптивный кардиостимуля¬
тор. Через сутки после операции отмечены повышение температуры тела
до 38,0 “С, нарастание одышки. Был назначен антибиотик цефтриаксон в
большой дозе (3 г/сут), который относится к условно нефротоксичным анти¬
биотикам. На фоне проводимой терапии одышка уменьшилась, температура
тела нормализовалась, цефтриаксон был заменен на амоксиклав. При рент¬
генологическом исследовании органов грудной клетки свежих очаговых и
инфильтративных изменений выявлено не бьыо, антибиотик был отменен.
Несмотря на постоянную терапию лазиксом в дозе 80 мг/сут, больная отмети¬
ла постепенное снижение диуреза.06.02.2008 г. была вновь переведена в Факультетскую терапевтическую
клинику для подбора антиаритмической терапии и дальнейшего лечения. При
поступлении состояние ее было средней тяжести, температура нормальная,
при аускультации сохранялась крепитация над нижними отделами легких.
Выраженная одышка, ЧД до 24 в минуту, отмечалось снижение сатурации кис¬
лорода до 90%. ЧСС 75 в минуту. Отмечалось снижение АД до 110/70 мм ртст.В течение последующих дней у больной периодически отмечалось усштение
одышки, снижение диуреза до 350-400 мл в сутки (при офашменном объеме
2S Пульмонологиявводимой жидкости — от 900 до 1100 мл в день), что расцениватось как нарас¬
тание сердечной недостаточности и требовало >’величения дозы диуретиков.
Одновременно было отмечено небольшое повышение уровня креатинина плазмы
крови до 1,7 мг/д.1, азота мочевины до 15,5 ммо-ть/л и снижение уровня калия до3,9 мэкв/л. Ситуация бьиа расценена как эпизод преренальной почечной недо¬
статочности вследствие гиповолемии, обусловленный водно-электролитны\ги
нарушениями на фоне тяжелой соматической патологии и лекарственной тера¬
пии. После в/в введения физиологического раствора и увеличения объема потре¬
бляемой жидкости были отмечены увеличение диуреза до 1000 мл/сут, нормачи-
зация уровня креатинина (1,14 мг/дл) и калия (4,3 мэкв/л) плазмы крови.Выполненная в последующем проба Реберга показала выраженное сниже¬
ние уровня клубочковой фильтрации, которая составила 30 мл/мин, а реаб-
сорбщю ~ 97,7%. Такое снижение фильтрационной способности почек делало
необходимым дальнейшее наблюдение больной совместно как пульмоноло¬
гом, так и нефрологом, а также исключение всех возможных факторов риска
гипотонии, дегидратации и нефротоксичности.На фоне терапии соталолом в дозе 160 мг/сут было выполнено суточное
мониторирование ЭКГ по Хо.лтеру: синусовый ритм, работа ЭКС в режиме
DDD с ЧСС 60 в минуту, сокращения от ЭКС составляют более 90%. Количество
суцравентрикулярных экстрасистол — не более 1000.При выписке рекомендованы обильное питье до 1500—1600 мл/сут в течение
нескольких дней, соб.тюдение диеты, оксигенотерапия, прием метипреда в дозе
8 мг/сут с постепенным снижением дозы до 4 мг/сут, плаквенила 200 мг/сут в
качестве противовоспалительной терапии, соталекса 160 мг/сут, омеза 20 мг/сут,
миакальцика и кальция ДЗ никомед в связи с нарастающим остеопорозом.
Гипотензивная терапия была сведена к приему нормодипина и арифона-ретард
по требованию. Рекомендована сахароснижающая терапия глюринормом,
назначен аллопуринол для профилактики развития острой мочекислой блока¬
ды. На фоне соблюдения всех рекомендаций состояние пациентки в дальней¬
шем оставалось стабильным, эпизодов олигоурии не было.Мы попытались оценить результат длительной системной терапии глюко-
кортикостероидами у больной с идиопатическим легочным фиброзом, учиты¬
вая развившиеся на фоне терапии осложнения — стероидный сахарный диабет
и компрессионный перелом XII грудного позвонка.Д.1Я этого была использована таблица, рекомендованная Американским
торакальным и Европейским респираторным обществами в 2000 г. {табл. 1.1).
Состояние больных на фоне терапии оценивается по 5 критериям: клиниче¬
ские проявления, картина при КТ легких, жизненная емкость легких (ЖЕЛ),
респираторная способность легких, атьвеолярно-артериолярный градиент.Из трех возможных вариантов реакция больной на терапию была расценена
нами как стабилизация процесса, поскольку прогрессирование одышки пре¬
кратилось, КТ легких в течение 1,5 года наблюдения больной без динамики
{табл. 1.2). Отмечался прирост ЖЕЛ более чем на 10%. Диффузионная спо¬
собность легких и альвеолярно-артериолярный градиент не оценивались по
техническим причинам.
Глава 1. Идиопатические интерстициальные пневмонии...29Таблица 1.1Оценка ответа на терапию у больных интерстициальным легочным фиброзомПараметрыУлучшениеСтабилизацияУхудшениеСимптомыУменьшение одышки и
кашляНет измененийУвеличение одышки и
кашляRh-графия, КТУменьшение измененийНет измененийУвеличение измененийЖЕЛУвеличение >10%Изменения +10%Уменьшение > 10%Увеличение >15%Изменения ±15%Уменьшение > 15%AaPOjУменьшение > 10 мм
рт.ст.Изменения +10 мм
рт.ст.Увеличение > 10 мм
рт.стОценка эффективности терапии у больной К.Таблица 12ПараметрыГоспитализацияI(декабрь 2007 г.)
исходноII(май 2008 г.)
до ГКСIII(декабрь 2008 г.)
на фоне ГКСIV(февраль 2009 г.)Симптомы++++++++Re/KT легкихБез диналїикиЖЕЛ (% к N)56475455SaO,9067-879390-95ИНТЕРСТИЦИАЛЬНЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХСовременная югассификация интерстициальных заболеваний легких, пред¬
ложенная Американским торакальным и Европейским респираторным обще¬
ствами в 2000 г., представлена на рис. 1.7. Она включает интерстициальные
заболевания легких известной этиологии (поражения легких при систем¬
ных заболеваниях соединительной ткани, таких как ревматоидный артрит и
системная склеродермия, лекарственные поражения, одним из самым распро¬
страненных среди которых является амиодароновое легкое), гранулематозные
поражения (саркоидоз), а также редкие нозологические формы, такие как
лимфангиолейомиоматоз и гистиоцитоз X.Идиопатические интерстициальные пневмонии (ИИП) также относятся
к группе интерстициа1ьных заболеваний легких и включают в себя 7 заболе¬
ваний: идиопатический легочный фиброз (ИЛФ) и так называемые другие
ИИП (не-ИЛФ) — десквамативная ИП (ДИП), острая ИП (ОИП), неспеии-
фическая ИП (КИП), респираторный бронхиолит, ассоциированный с ИЗЛ
(РБ-ИЗЛ), криптогенная организующаяся пневмония (КОП), лимфоцитарная
ИП (ЛИП).Следует отметить, что в настоящее время в медицинской литературе суще¬
ствует некоторая терминологическая путаница как в формулировке диагноза
ИИП, так и в употреблении понятия «интерстициа^іьная пневмония».Термин «идиопатические интерстициальные пневмонии^» объединяет груп¬
пу сходных по клинической картине заболеваний, дифференцировать которые
зоПульмонологияРис. 1.7. Классификация интерстициальных заболеваний легкихмежду собой можно только на основании результатов морфологического иссле¬
дования. Ранее все эти заболевания объединяли в диагноз «идиопатический
фиброзирующий альвеолит^ (ИФА), который очень метко отражал сущность
патологического процесса и на долгие годы прочно укоренился не только в
пульмонологии, но и в терапии в целом. В дальнейшем, при выявлении неод¬
нородности этой группы в связи с разграничением 7 разных морфологических
типов ИИП и соответствующих им нозологических форм, термин «ИФА»
решено было применять только по отношению к ИЛФ, который соответствует
морфологической форме обычной интерстициальной пневмонии.Интерстициальной пневмонией принято называть пневмонии, вызванные
«атипичными возбудителями», такими как хламидии, легионеллы и др., кото¬
рые, будучи внутриклеточными паразитами, вызывают пневмонии с преиму¬
щественным поражением интерстиция легких с минимальным скоплением
экссудата в полости альвеол и при рентгенографии легких нередко бывают
рентгенонегативными. Выявить наличие такой интерстициальной пневмонии
в большинстве случаев можно с помощью компьютерной томографии. Кроме
этого, сам термин «пневмония» применяется к острым инфекционным заболе¬
ваниям легочной паренхимы. ИИП в большинстве случаев являются хрониче¬
скими заболеваниями идиопатической, а не инфекционной природы. В связи
с этим более корректным по отношению к ИИП считается употребление тер¬
мина «пневмонитьт».ИИП — группа заболеваний неизвестной этиологии, клинически харак¬
теризующаяся прогрессирующей одышкой и кашлем, чаще непродуктив¬
ным. При аускультации обычно выслушивается крепитация разной степени
Глава L Идиопатические интерстициальные пневмонии...31выраженности — от нежной до типичного «целлофанового треска». При рент¬
генографии или КТ легких выявляются диффузные двусторонние изменения.
Присієм КТ высокого разрешения позволяет дифференцировать рентгенологи¬
ческий симптом «матового стекла», свидетельствующий, как правило, о преоб¬
ладании воспалительного процесса, от симптома «ретикулярного или сетчатого
фиброза», чтоявляеіся маркером наличия соединительной ткани. Исследование
функциональной способности легких позволяет выявить рестриктивные вен¬
тиляционные нарушения (снижение легочных объемов), снижение диффу¬
зионной способности легких, расширение альвеоло-артериального градиента
(АаРОз).В соответствии с клинико-патологической классификацией Американского
іораісального и Европейского респираторного обществ 2000 г. клинический
диагноз ИИП устанавливается на основании морфологической картины био-
птата легкого {табл. 1.3).Так, морфологическая картина обычной интерстициальной пневмонии
соответствует клиническому диагнозу ИЛФ/ИФА. Гистологический вариант
неспеиифической интерстициальной пневмонии (НИТТ) и лимфоцитарной
интерстициальной пневмонии (ЛИП) соответствует одноименным клиниче¬
ским формулировкам диагноза. При морфологическом диагнозе макрофагаль-
ной ИП клинический диагноз должен формулироваться как десквамагивная
ИП (ДИП). В случае выявления гистологической картины респираторного
бронхиолита диагноз формулируется как респираторный бронхиолит, ассо¬
циированный с ИЗЛ (РБ-ИЗЛ). И, наконец, в случае гистологической картины
диффузного атьвеолярного повреждения клиницист вправе сформулировать
диагноз как острая ИП, или болезнь Хаммана-Рича.Итак, каждому морфологическому типу ИИП соответствует определен¬
ная гистологическая картина {табл. 1.4), При обычной интерстициальнойТаблица 1.3Соответствие клинических и гистологических вариантов различных иднопатическихинтерстициальных пневмонийГЬстологический вариантКлинический диагнозОбычная интерстициальная пневмо¬
нияИдиоиатический легочный фиброзНсспецифическая итттерстициальная
пневмонияНеспеиифическая интсрстициальная пнев¬
монияОрганизующаяся пневмонияКрипгогенна>: организующаяся пневмонияДиффузное альвеолярное повреждениеОстрая интерстициальная иневмонияРеспираторный бронхиолитРеспираторный бронхиолит, ассоциирован¬
ный с ИЗЛМакрофагальна>х интерстициальная
пневмонияДесквамативная интсрстициальная пневмо¬
нияЛ имфоцитарная интерститшаїьная
пневмонияЛимфотщтарная интерстициальная пневмо¬
ния
32ПульмонологияТаблица J.4Клинико-морфологическая классификация идиолатических
интерстициа.1ьных пневмонийМорфологический тип и клинический
диагноз ИИППтстологическая картинаИдиопатический легочный фиброз =
ДФА (обычная итттерстициальная пнев¬
мония)Нар>тііение архитектуры легких, фиброз с
«сотовыми» изменениями, фокусы фибро-
бластоп. Неоднородность данных измсне-
ний в биоптатс (временная гетерогенность)Нсспеиифическая ИП (т?еспецифиче-
ская интерстициальная пневмония)Вариабельное интерстициальное вос¬
паление и фиброз, однородность данных
изменений в биоптате, фибробластичсские
фокусы отсутствуют или очетгь редкиКринтогенная организ\тошаяся пнев¬
мония (организ>тощаяся пневмония)Легочная архитектоника сохранена, пят¬
нистое распространение полипопидной
грануляциотшой ткани в дистальных возду¬
хоносных ГГУТЯХОстрая ИП = болезнь Хаммана—Рича
(диффузное альвеолярное поврежде¬
ние)Диффузный процесс, уголшение альвео¬
лярных перегородок, организация альвеол,
гиалиновые мембраны РБ-ИЗЛ (респираторный бропхиолит)Бронхо центричная аккл'муляция альвеоляр¬
ных макрофагов, минимальное воспаление
и фиброз ДИП (макрофагальная интерстициаль¬
ная птгевмония)Равномерное поражение паренхимы легких,
альвеолярные макрофаги в просвете алт^пе-
ол, минимальное поражение интерстицияЛИП (лимфоциіарнаяинтерстициаль¬
ная пневмония)Выраженная лимфоцитарная инфильтрация
интерстиция часто ассоциирована с пери-
бронхиальными лимфоидными фоллтткула-
ми (фолликулярный бронхиолит) пневмонии выявляют нарушение архитектоники легких, фиброз с «сото¬
выми» изменениями, фокусы фибробластов. Отличительной особенностью
этой нневмонии является неоднородность данных изменений в биоптате
(временная гетерогенность). Для неспецифической интерстициальной пнев-
монии свойственно выявление вариабельного интерстициального воспсшения
и фиброза, при этом фибробластические фокусы либо отсутствуют, либо край¬
не редки. В отличие от обьгчной интерстициальной пневмонии, обращает на
себя внимание однородность данных изменений в биоптате. Лимфоцитарная
интерстициальная пневмония названа так благодаря тому, что для нее харак¬
терна выраженная лимфоцитарная инфильтрация интерстициальной ткани.
Кроме лимфоцитарной инфи^іьтрации, при этой пневмонии в биоптатс часто
выявляют перибронхишіьньїе лимфоидные фолликулы, так называемый фол¬
ликулярный бронхиолит. в случае, когда при микроскопическом исс.ттедовании
обнаруживают диффузное утолщение альвеолярных перегородок, образование
гиалиновых мембран, а также организацию альвеол, речь идет о диффузном
альвеолярном повреждении или об острой интерстициальной пневмонии
(болезни Хаммана—Рича).
Глава 1, Идиопатические интерстициальные пневмонии... 33При организующейся пневмонии на фоне сохранной легочной архитек¬
тоники выявляется пятнистое распространение полиповидной грануляци¬
онной ткани преимутцествснно в дистальных отделах воздухоносных путей.
Десквамативная интерстициальная пневмония традиционно называется
так потому, что для нее характерны скопления альвеолярных макрофагов в
полостях альвеол, ранее ошибочно принимавшиеся за десквамированные
клетки альвеолярного эпителия. Кроме того, для гистологической картины
ДИП характерно равномерное незначительное повреждение интерстиция.
При РБ-ИЗЛ обычно выяв.1яется бронхоцентри^шая аккумуляция альвеоляр¬
ных макрофагов в сочетании с минимальным воспалением и фиброзом.ИЛФ — одна из наиболее часто встречающихся и, следовательно, наибо¬
лее изученных ИИП. Согласительной комиссией ATS/ERS были предложены
клинико-рентгенологические критерии вероятного диагноза ИЛФ (специфич¬
ность 97%, чувствительность 62%, Raghu et.al.). Критерии разделены на две
группы: большие и малые.К большим критериям относятся; 1) исключение других ИЗЛ, вызванных
известными причинами (лекарства, экзогенные факторы, диффузные заболе¬
вания соединительной ткаьш); 2) рестриктивные изменения ФВД и нарушение
газообмена; 3) двусторонние изменения в базальных отделах легких по типу
«матового стекла» по данным КТ высокого разрешения; 4) по данным транс¬
бронхиальной биопсии или бронхоальвеолярного лаважа (БАЛ) нет признаков,
свидетельствующих об альтернативном диагнозе.Малые критерии включают: 1) возраст более 50 лет; 2) незаметное, постепен¬
ное появление диспноэ при физической нагрузке; 3) длительность заболевания
более 3 мес; 4) ипспираторную крепитацию в базальных отделах легких.Вероятность ИЛФ считается достаточно высокой, если имеются четыре
больших и хотя бы три малых критерия.Вопрос лечения ИЛФ на сегодняшний день является одним из краеуголь¬
ных камней терапии интерстициальных болезней легких. Следует отметить,
что на современном уровне развития внутренней медицины нет эффективных
методов лечения ИЛФ, способных улучшить выживаемость и качество жизни
больных. Тем не менее имеются данные об эффективности некоторьк схем
патогенетической терапии этого заболевания. Под эффективностью лечения
ИЛФ следует понимать не увеличение продолжительности и качества жизни, а
возможіюсть торможения прогрессирования заболевания.Учитывая гистологическую времени^ гетерогенность, т.е. одновременное
наличие в препарате зон активного воспа.тения и зон уже сформировавшего
фиброза (что создаст типичную картину «сотового легкого» и так метко было
отражено в названии «фиброзирующий альвеолит»), проводится противовос¬
палительная и антифиброзная терапия. В качестве противовоспалительной
терапии рекомендуются три схемы с использованием глюкокортикостероидов
(ГКС) и цитостатических препаратов: ГКС, ГКС + азатиоприн и ГКС + цикло-
фосфамид. В качестве препаратов, подавляющих прогрессирование фиброза,
используются 0-пеници.аяамин, колхицин, интерферон-у-1Ь и пирфенидон.
Кроме того, имеются данные об эффективности длительного приема больших
34 Пульмонологиядоз N-aucTJHLmHCTeMHa (препарат флуимуцил-600) в качестве антиоксидант¬
ного препарата. К сожалению, для пациентов с ИЛФ до сих пор не потеряла
актуальности трансплантация легких, и именно среди этой фуппы больных,
ожидающих операцию, смертность остается наиболее высокой.Все рекомендуемые ATS/ERS схемы противовоспалительной терапии
включают назначение ГКС. Принимая во внимание возможные побочные
эффекты кортикостероидной терапии, средний возраст больных ИЛФ, а также
отсутствие данных об увеличении их продолжительности и качества жизни на
фоне лечения, необходимо оценивать существующие показания и противопо¬
казания к проведению противовоспалительной терапии. По уже имеющимся
данным, ГКС оказываются эффективными лишь у 15—20% больных ИЛФ.
Предикторами успешности терапии ГКС являются женский пол, возраст моло¬
же 50 лет, изменения при КТ высокого разрешения по типу «матового стекла»,
а не ретикулярного фиброза и содержание лимфоцитов более 25% в жидкости
БАЛ. Предикторами того, чю риск развития побочньоі эффектов от терапии
ГКС будет превышать ожидаемую пользу, считаются возраст старше 70 лет,
наличие ожирения (ИМТ > 35 кг/м^), остеопороза и сахарного диабета.Сегодня наиболее радикальным способом терапии ИЛФ остается транс¬
плантация легких. Как уже было сказано, самая высокая легальность среди
пациентов, ожидающих трансплантацию, отмечается именно в группе больных
ИЛФ, а 3-летняя выживаемость этих больных после трансплантации легких
составляет около 60%. Показаниями к трансплантации легких у больных
ИЛФ считаются диспноэ ПІ-IV (NYHLA), гипоксемия при физической нагруз¬
ке, снижение ЖЕЛ менее 60—70% и снижение DLco менее 50%. В качестве
противопоказаний можно назвать пожилой возраст и быстрое прогрессирова¬
ние заболевания. В настоящее время в связи с неудовлетворенностью врачей
результатами консервативного лечения ИЛФ продолжается активный поиск
новых способов воздействия на две основные составляющие идиопатического
фиброзирующего альвеолита — воспаление и фиброз. В связи с этим изучается
возможность использования босентана, ингибиторов АПФ, циклоспорина,
этанерсепта, иматиниба, фактора роста кератиноцитов, микофенолата мофе-
тила, рапамицина, а также ловастатина и др. (табл. 7.5).Оценивать эффективность терапии ИЛФ на сегодняшний момент представ¬
ляется возможньші только по «суррогатным точкам», отражающим преимуще¬
ственно функциональную способность легких, и по рентгенологической кар¬
тине. Для этого используют 5 критериев (см. табл. 1.1): динамику симптомов,
проявляющихся в основном одышкой, ЖЕЛ, DLco и АаРО,, а также изменения
при рентгенологическом исследовании (рентгенография или КТ). В зависи¬
мости от направления и степени их изменений состояние расценивается как
улучшение, ухудшение или стабилизация. Средняя выживаемость больных
ИЛФ колеблется от 2,9 до 5,0 лет, при этом прогноз течения заболевания
бывает лучше у женщин, лиц более молодого возраста, с анамнезом заболева¬
ния менее 1 года и меньшей выраженностью фиброза по данным биопсии и
КТ высокого разрешения, а также у пациентов, ответивших на терапию ГКС
в течение 3 мес.
Глава /, Идиопатические интерстициальные пневмонии...35Таблица 1.5Перспективы развития медикаментозной терапии
интерстициального легочного фиброзаПрепаратОбоснованнеБосентан — антагонист рецепто¬
ров эндотелина А и ВЭндотелии-1 обладает вазоактивным, митогенным
и иммуномодудяторным эффектами; повышает
прод>'кцию TGF-P и независимо стимулирует
фибробластьтКаптоприл, лозартанАнгиотензин-П активирует пролиферацию
фибробластов.Ингибирование АПФ предотвраищет апоптоз аль¬
веолярного эпителия.Уменьшают фиброз легких in vivoЦиклоспоринИнгибирует Т-лимфоиитыЭтанерсепт — антагонист TNF-aTNF-a — цитокин с митогенным эффектом на
фибробластьт и синтез коллагенаИматиниб — ингибитор проте-
интирозиновых киназПодавляет пролиферацию опухолевых и мсзеттхи-
мальных клеток, в том числе фибробластовРепифермин — фактор роста
кератиноиитовИндуцирует нормальттую (ингибирует аномаль¬
ную) пролиферацию альвеолоцитов И типаЛовастагинБлокирует формирование грануляционной ткани
путем HHAjTaOTH апоитоза фибробластовСиролимусИммуносуцрессивный препарат с антапролифера-
тивными свойствамиМикофенолата мофетил
(CeUCept)Нар\тиает функцию лимфоцитов путем блокиро¬
вания биосинтеза пуринов через ингибирование
фермента инозин-монофосфат-дегидрогеназыВ структуре причин смерти больных ИЛФ преобладает дыхательная недо-статочность, которая составляет 39%. Второе место занимают сердечно¬
сосудистые заболевания, удельный вес которых 27%. Рак легких развивается у
10% пациентов с ИЛФ. По 3% приходится на смерть от ТЭЛА и сопутствующих
легочных инфекций. И почти одна пятая часть больных погибает от других
причин, составляющих 18%.Комментарий С.И. Овчаренко — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукОсновные дели представления данного клиническою наблюдения следую¬
щие.1. Показать, что с более широким распространением метода морфологиче¬
ской верификации диагноза в пульмонологии, особенно в группе больных с
интерстициальными заболеваниями легких, произошел существенный про¬
рыв. Так, выделено семь основных морфологических типов идиопатических
интерстициальных пневмоний. Произошла попытка «привязать» каждый из
них к определенной клинической форме (правда, этот процесс находится
только у истоков и требует дальнейшего развития и совершенствования).
36Пульмонология2. Подчеркнуть, что термин «идиопатический фиброзирующий альвеолит»
теперь соответствует термину «идиопатический легочный фиброз» (ИФЛ),
ему морфологически соответствует обьиная интерстициальная пневмония,
что и вьтяатено у данной пациентки.3. Показать, что уже по данным тщательно собранного анамнеза можно
из этой обширной группы идиопатических интерстипиальных пневмо¬
ний выделить вариант идиопатического легочного фиброза (идиопати-
ческого фиброзирующего альвеолита). Основные дифференциально-
диагностические критерии, предложенные сотрудниками клиники им.
Е.М. Тареева, приведены в табл. 1.6. Практргчески все основные признаки
ИФЛ выявлены у нашей больной.Не совсем нонятным остается наличие у больной бронхообструктивного
синдрома. По данным литературы {табл. 1. 7), бронхообструктивньгй син¬
дром развивается при ИЛФ в случае сочетания его с вирусной инфекци¬
ей. Унашей папиентки вируса гепатита В и С не выявлено, а на цитомегало-
вирус и вирус Эпт1ггейна-Барр, мы, к сожалению, ее не обследовали.И самый главный вопрос: надо ли бьию с учетом всего объема данных,
полученных у нашей больной, назначать глюкокортикостероиды (памятуя о
том, что у больной развились на этом фоне стероидный сахарный диабет и
перелом XII грудного позвонка)? Возвращаясь в прошлое, отвечаем на негоТаблица 1.6Дифференциальный диагноз идиопатического легочного фиброза и интерстициальных
пневмоний (клиника им. £.М. Тареева, 2004 г.)Клинический признакИЛФ (п = 65)ИИП (пнсвмониты, п = 87)Начало болезниЧаще хроническоеОстрое или хроническоеВозраст50,9 ± 3,454,3 ± 5,4Одышка, баллы52,5Кашель65 (100%)87 (100%)Кровохарканье6(9%)5 (5,7%)Боли в грудной клетке, ощущение
грудобрюшной преграды65(100%)19(21%)Потеря массы тела65 (74%)44 (51%)«Барабанные палочки» и «часовые
стекла»57 (88%)43 (50%)Легочная гиперіензия41 (63%)27 (32%)Синдром Рейнс2(3%)8(9%)Мышечно-суставные боли3(4%)И (12%)Цианоз65 (100%)27 (31%)ПрогнозНеблагоприятныйОтносительно благопри¬
ятныйПродолжительность заболеванияОт 5 мес до 4 летБолее 4,5 лет
Глава і. Идиопатические интерстициальные пневмонии.37утвердительно, уровень глюкозы держится на нормальных значениях путем
соблюдения диеты и приема таблетированных сахароснижающих препара¬
тов. Перелом мог развиться и самостоятельно у тучной пожилой больной с
выраженным остеопорозом. Но у больной почти за полтора года динамиче¬
ского наблюдения не ухудшились фзгнкциональные показатели (по сравне¬
нию с теми значениями, которые были до назначения глюкокортикостеро¬
идов), а даже несколько улучшились. Дома она передвигается по квартире,
частично себя обслуживает. Динамическое наблюдение за больной про¬
должается. Когда у нашей пациентки началась болезнь, точно ответить не
можем, но считаем, что с того времени, когда у нее наросла одышка — она
уже была проявлением этой болезни.Таблица /.7Частота обнаружения маркеров вирусной инфекции у больных иднопатическим
фиброзирующим альвеолитомЪт инфекцииЧисло обследо¬
ванных больныхИсследуемыйматериалП ол ожите л ьныи
результатСравнение с
контролемГепатит В152Кровь9(5%)<0,05Гепатит С76Кровь8(10,5%)<0,05Вирус Эпштейна-Барр79Кровь14(17,7%)<0,05Цитомегаловирус79Кровь6 (7,6%)<0,05
Глава 2КРИПТОГЕННАЯ ОРГАНИЗУЮЩАЯСЯ
ПНЕВМОНИЯ — ОТНОСИТЕЛЬНО БЛАГОПРИЯТНЫЙ
ВАРИАНТ ИНТЕРСТИЦИАЛЬНОГО ЗАБОЛЕВАНИЯ
ЛЕГКИХН.В. Чичкова, И.С. ЩедринаВажность точной дифференциальной диагностики в группе интерсти¬
циальных заболеваний легких, о которых шла речь в предыдущей главе,
подчеркивает следующее клиническое наблюдение. При сходстве возраста,
жалоб, клинической картины с таковыми у больной, представленной в главе 1,
тералия, ответ па нее и прогноз заболевания оказались несколько иными, что
стало возможным благодаря проведению морфологического исследования лег¬
кого. Как и в первом случае, даже при наличии биоптатов легких диагноз бьш
поставлен не сразу, наряду с морфолог№іескими использовался весь комплекс
клинико-инстр>тііЄнтальньіх данных. Вопросы длительной терапии различных
вариантов интерстициальных заболеваний легких остаются недостаточно раз-
работагшыми, в связи с чем собственный опыт лечеиия и длительного наблю¬
дения за такими больными представ-іяется особенно ценным.Больная И., 68 лет, поступила в отделение общей терапии Факультетской
терапевтической клиники им. В.Н. Виноградова 10.02,2010 г. с жсиюбами на
слабость, повышение температуры тела до субфебрильных цифр, присту¬
пообразный непродуктивный кашель, боли при дыхании в левой половине
ірудной клетки, дистанционные хрипы, одышку при небольшой физической
нагрузке.Анамнез жизни без особенностей. Профессиональных вредностей не имела.Из анамнеза заболевания известно {рис. 2.1), что с 2006 г наблюдается в
Факультетской терапевтической клинике им. В.Н, Виноградова в связи с гипер¬
тонической болезнью ТТ стадии, 3 степени повышения АД, высокой степени
риска. Во время госпитализации в 2006 г. больной была подобрана адекватная
гипотензивная терапия следующими препаратами: аккупро 20 мг/сут, конкор
5 мг/сут, арифон-ретард 1,5 мг/сут. В последующие годы АД находилось, как
правило, на оптимальном уровне.Ухудшение состояния отметила 12.01,2009 г., когда вскоре после контакта с
больным респираторной вирусной инфекцией и переохлаждения появились
слабость, сухой приступообразным кашель, температура тела повысилась до
субфебрильных цифр, возникли боли при дыхании в левой половине грудной
юіетки; вскоре появились дистанционные хрипы, одышка при умеренной
физической нагрузке. Недлительно принимала антибиотик ципролет без
эффекта. При рентгенографии, выполненной в амбулаторных условиях, бьша
Глава 2. Криптогенная организующаяся пневмония...3904.200907.200910.2009 01.2010 02.2010ЛечениеПульс-терапия:
преднизолон
500-700 мг/сут.
иГКС 1000 мкг/сут.Метипред 4 мг/сут
Плаквенил 400 мг/сут,
иГКС 1000 мкг/сутРис. 2.1. Анамнез заболевания больной И., 68 летвьывлена инфильтрация в ншкней доле левого легкого, в связи с чем была
госпитализирована в Факультетскую терапевтическую клинику им. В.Н. Вино¬
градова 23.01.2009 гПри поступлении состояние было расценено как удовлетворительное. ИМТ
30 кг/м‘. Кожные покровы обычной окраски. Периферические лимфоузлы не
увслртчены. Отеков нет. ЧД до 20 в минуту. В легких дькание ослаблено слева
ниже угла лопатки, крепитация в базальных отделах, преимущественно слева.
При форсированном дыхании появлялись сухие свистящие хрртпы. Границы
сердца не расширены, тоны не изменены, шумов нет. ЧСС 72 в минуту. АД
130/80 мм рт.ст. Живот безболезненный, мягкий. Печень не увеличена, край не
пштьпируется.В анализах крови обращало на себя внимание лишь небольшое увеличение
СОЭ до 24 мм/ч и повышение СРБ до 1,25 мг/дл. НЬ 122 г/л, эритроциты
3,7 млн, ЦП 0,97, лейкоциты 5,3 тыс., нейтроциты 63%, лимфоциты 27%, моно¬
циты 3,7%, эозиноциты 4,1%, базофилы 0,8%, тромбоциты 228 тыс. Общий
белок 67,7 г%, альбумин 39,9 г%, креатинии 0,99 мг%, глюкоза 5,2 ммоль/л,
общий билирубин 14.2 мкмоль/л, у-ГТ 26 ед/л, ACT 46 ед/л, АЛТ 34 ед/л.На ЭКГ без существенной патологии. При ЭхоКГ — левый желудочек не
увеличен (КДР 4,7 см, КДО 82 мл, КСО 33 мл), левое предсердие 37 мл, тМЖП1,0 см, тЗС 1,0 см, тПЖ 0,35 см, ФВ 60%. Диастолическая функция нарушена
Е/А=0,6, правый желудочек 2,1 см, тПЖ 0,4 см, ПП 36 мл. НПБ не расширена,
коллабирует после глубокого вдоха более чем на 50%, Уплотнение фиброз¬
ных колец MHTpajTbHoro и аортального клапанов. Стенки аорты уплотнены.
Жидкости в полости перикарда нет.При анализе рентгенограмм органов грудной клетки было сделано заключение
о наличии инфильтрации в нижней доле левого легкого с реакцией корня лег¬
кого. Участки уплотнения легочной ткани определялись и в язычковых сегмен¬
тах левого легкого. Корень правого легкого структурен. Плевральные синусы
40Пульмонологиясвободны. Таким образом, рентгенологическая картина не противорсчи^ш диа¬
гнозу «полисегментарная пневмония», в связи с чем была начата антибактери¬
альная терапия (клафоран 3,0 г в сутки в/в и клацид 1000 мг/суг peras).На фоне проводимой терапии в течение 3-4 последующих дней отмечалось
улучшение состояния в виде нормаїизации температуры, уменьшения кашля,
отсутствия болей при дыхании в левой половине грудной клетки, однако сохра¬
нялись одышка, аускультативные изменения в легких (крепитация и признаки
бронхообструкпии).При исследовании ФВД были выявлены снижение ЖЕЛ (51%, после иііга-
лядии сальбутамола — 55%), OOBj (61%, после инга-іяции — 67%), скоростных
потоков на уровне дистальных бронхов (MOC^j 55%, после ингаляции — 64%)
при нормальном значении ОФВуФЖЕЛ (85%), что свидетельствовало о пре¬
обладании рестриктивных изменений. Показатель оксигенации — на нижней
границе нормы (SatOj 94%).Через неделю от начала антибактериальной терапии была проведена МСКТ
органов грудной клетки (рис. 22): в 3, 6,10-м сегментах правого легкого, язычко¬
вых сегментах левого легкого определялись перибронховаскулярные инфиль¬
траты неправильной формы, неоднородной структуры. Во всех отделах обоих
легких, преимущественно субплевралыю, выявлялись инфильтраты округлой
формы с гиподенсным ободком. Визуализированы просветы крупных бронхов
до уровня сегментов. Структуры средостения, корней легких дифференциро¬
ваны. в нижней паратрахеальной и бифуркационной областях определялись
немногочисленные лимфоузлы до 12 мм в поперечнике.Таким образом, были выделены следующие синдромы:• прогрессирующая одышка;• аускультативные изменения в легких (крепитация);• смешанные нарушения легочной венти^іяции (снижение ЖЕЛ и OФB^);• изменения КТ-картины легких.Полученные в процессе обследования данные заставили расширить
диагностический поиск (в сравнении с исходным диагнозом пневмонии).
Рассматривались следующие состояния:Рис. 2.2. КТ легких больной И. от января 2009 г. (поясненггя п тексте)
Глава 2. Криптогенная организующаяся пневмония.,, 411) полисегментарная пневмония, вызванная атипичным возбудителем;2) грибковое поражение легких;3) туберкулезное поражение легких;4) интерстициа^чьная пневмония, а именно криптогенная организующаяся
пневмония;5) саркоидоз;6) бронхоальвеолярный рак.Поэтому, наряду с проведением антибактериальной и противогрибковой
терапии (авелокс 400 мг в/в капельно и микосист 100 мл в/в капелъно), было
продолжено обследование, направленное на исключение и,іи подтверждение
вышеуказанных причин поражения легочной ткани.В первую очередь для уточнения состояния бронхов и получения материала для
дальнейших исследований проведена бронхоскопия: слизистая o6oj[04Ka трахеи и
бронхов была незначительно отечна и гиперемирована. На слизистой оболочке
среднедолевого бронха и обоих верхнедолевых бронхов имелись ограниченные
участки белесоватых студенистых наложений. Получены смывы и соскоб из верх¬
недолевого бронха; биопсию из измененною участка провести не удатось.Цитологи^геское исследование бронхиального смыва; клетки пролифери¬
рующего бронхиального зіштелия, лейкоциты.Микробиологическое исследование бронхиального смыва (выполнено в
различных учреждениях): не обнаружен рост грибов, получен рост неспетщфи-
чсской условно-патогенной микрофлоры.Консультация в НИИ фтизиопульмонологни: дифференпиаін>ную диагно¬
стику следует проводить между микозом, бронхо-альвеолярным раком, эози¬
нофильными инфильтратами; менее вероятен неактивный туберкулез.Люминесцентная микроскопия и иммунологические исследования бронхи¬
ального смыва на туберкулез (определение антител к микобактериям методом
ИФА; определение ДНК микобактерий методом ПЦР; гамма-интерфероновый
тест) дали отрицательный результатПовторные консультации в Центре глубоких микозов; нельзя иск^іючить
пневмомикоз (аспергилло\ту).Серологическое исследование крови на антигены аспергилл и кандид —
результат отрицательный.За время пребывания в клинике, наряду с уменьшением кашля, норма.'іи-
зацией температуры тела, нарастали явления дыхательной недостаточности и
выраженность бронхообструкции.Проведение повторной КТ легких (рис. 2.J) на фоне терапии авелоксом
и микосистом подтвердило отсутствие положительной рентгенологической
динамики: сохранялись перибронхиальные и субплевральные инфильтраты
во всех отделах обоих легких. Было высказано предположение о соответствии
эп'их изменений картине криптогенной организующейся пневмонии, которая
включает следующие КТ-признаки;• единичные или множественные легочные инфи^тьтраты;• преимуществе НПО периферическое (субплсвральное) расположение
инфильтратов;
42Пульмонология• очаговые или диффузные изменения по типу «матовых стекол»;• очаги (1-10 мм в диаметре);• утолщение бронхишіьной стенки и/или бронхоэктазы;• сетчатые и линейные тени;• отсутствие выраженного фиброза.В процессе обследования не нашли подтверждение прежде всего бактери¬
альная пневмония, грибковое поражение легких, а также туберкулез легких.
Другие состояния (интерстициальная пневмония, саркоидоз легких, бронхо¬
альвеолярный рак) требовали морфологической верификации. Единственным
методом точной постановки диагноза являлась биопсия легкого. 01.04.2009 г
больная бьша госпитализирована в Национальный медико-хирургический
центр им, Н.И. Пирогова для проведения видеоторакоскопической биопсии
легкого.При ревизии во время операции легочная ткань изменена, резко уплотне¬
на, ригидна при инструментальной пальпации. В толше ткани определяются
множественные плотные инфшіьтратьт. Учитывая ригидность легочной ткани,
выполнение видеоторакоскопической резекции легкого было признано невоз¬
можным. Произведена микроторакотомия, выполнены атипичные резекции
средней и нижней долей правого легкого.Морфологами Национального медико-хирургического центра им. Н.И. Пи¬
рогова было сделано заключение об алъвеолите, перенесенном респираторном
дистресс-синдроме И.ТИ исходе интерстициальной пневмонии. Препараты были
исследованы в НИИ фтизиоиульмонологии: данные за туберкулез и бронхоаль¬
веолярный рак отсутствуют, выявленные изменения соответствуют интерстици-
а.1ьной болезни легких. Однако данные заключения не позволяли сделать выводо клинико-морфологическом варианте интерстициальной болезни легких.Препараты были исследованы также зав. отделом narojmrnH Инститчта
пульмонологии профессором А.Л.Черняевым: фибробластические фокусы
в стенках альвеол, очаговые разрастания грануляционной ткани в альвео¬
лах и стенках бронхиол, очаговыеРис. 2.3. КТ леї ккгх больной И. от февраля
2009 г. (пояснения в тексте)бронхиолоэктазы, в части бронхи¬
ол — слизь с лимфоцитами и макро¬
фагами. Очаговый дистел ектаз,
гипертрофия замыкательных пла¬
стинок входа в альвеолы. В просвете
и стенках бронхиол лимфоидные
инфилыраты. Пролиферация avibBe-
олоцитов II типа. Периваскулярные
лимфоидные инфильтраты. Группы
ветвей легочной артерии с пролифе¬
рацией интимы, сужением просве¬
тов и периваскулярным разраста¬
нием фиброзной ткани в виде муфт.
Дано заключение: облитерируюший
бронхиол ит с организующейся
Глава 2. Криптогенная организующаяся пневмония... 43пневмонией, местами фолликулярный бронхиолит, продуктивный васкулит
с эозинофилами мелких артериол, бронхиолоэктазы, признаки артериальной
легочной гипертензии.Данное гистологическое заключение соответствовато криптогенной орга¬
низующейся пневмонии, патоморфологическая картина которой включает:• полиповидные массы, фануляционную ткань, заполняющие респиратор¬
ные бронхиолы;• вовлечение в продесс альвеолярных ходов и альвеол;• воспалительные клетки в бронхоальвеолярной стенке и перибронхиаль-
ных областях;• пенящиеся макрофаги в альвеолярных пространствах;• гиперплазию II типа пневмоцитов;• инфильтрацию мононуклеарами альвеолярного интерстиция;• отсутствие сотовой трансформации и тяжелого фиброза.Вскоре после получения результатов морфологического исследования боль¬
ная была повторно госпитализирована в Факультетскую терапевтическую
клинику им. В.Н, Виноградова с диагнозом: интерстициальная болезнь лег¬
ких; криптогенная организующаяся пневмония. Дыхательная недостаточностьII степени. Гипертоническая болезнь ТІ стадии, 3 степени повышения АД,
высокой степени риска. Атеросклероз аорты. Начато лечение: пульс-терапия
преднизолоном (І000 мг/сут в течение 3 дней) с последующим приемом 4 мг
метипреда и 400 мг плаквенила в сочетании с ингаляционными кортикосте¬
роидами. Данный вариант лечения (а именно терапия низкими дозами глюко¬
кортикостероидами) казался нам предпочтительнее в связи с наличием факто¬
ров риска развития осложнений стероидной терапии; избыточной массы тела,
артериальной гипертензии, эрозивного гастрита (выявленного при повторной
госпитализации).В результате проводимой терапии состояние существенно улучшилось:
постепенно уменьшилась одышка вплоть до полного ее отсутствия, не беспо¬
коил кашель. При контрольной КТ легких отмечена положительная динамика
в виде у\іеньшения количества инфильтратов (рис. 2.4). В дальнейшем паци¬
ентка продолжала принимать метипред 4 мг 1 таб. в день, плаквенил 200 мг2 таб. в день, ингаляционные глюкокортикостероиды (суммарно 1000 мкг
фликсотида в сутки).Во время планового обследования в январе 2010 г при очередной КТ легких
отмечалась существенная положительная динамика; отсутствие участков пери-
бронхиалъной инфильтрации и консолидации с формированием в этих зонах
линейных участков фиброза и плевральных сращений (рис. 25). Однако в пер¬
вых числах февраля после стрессовой ситуации у больной вновь повысилась
температура тела до фебрильных цифр, появились и стали нарастать одышка,
дистанционные хрипы, малопродуктивный кашель. При аускультации вновь
выслушивались крепитация и признаки бронхообструкции, при КТ легких —
появление участков инфильтрации и утолщения интерстиция, зоны повыше¬
ния плотности по типу «матового стекла» (рис. 2.6), в связи с чем больная бьша
госпитализирована в клинику.
44ПульмонологияРис. 2.4. КТ легких больной И. от июня
2009 г. (пояснения в тексте)Рис. 2.5. КТ легких больной И, от января
2010 г. (пояснения в тексте)В анализах крови вновь отмечено увеличение СОЭ до 23 мм/ч; при ЭхоКГ
обращало на себя внимание появление признаков небольшой легочной гипер¬
тензии. При оценке ФВД и по данным бодиплетизмографии — вентиляцион¬
ные нарушения по рестриктивному типу, снижение ЖЕЛ (56%), умеренное
увеличение общего бронхиального сопротивления. Показатели оксигенации
крови на нижней границе нормы (SatO^ 94%). При исследовании диффузион¬
ной способности легких показатель умеренно снижен (54%). При посту¬
плении была увеличена доза кортикостероидов (20 мг метипреда), продолжена
терапия плаквенилом 400 мг/сут, беродуалом 15 кап. 4 раза в день через небу-
лайзер, фликсотидом 1000 мкг/сут, в результате чего отмечено клиническое
улучшение — уменьшение одышки и каш.чя.Криптогенная организующаяся пневмония — клинический диагноз, кото¬
рый соответствует одному из морфологических вариантов идиопатических
интерстициальных пневмоний — организующейся пневмонии (см. табл.1.4, глава 1). В 1983 г. А. Davison
впервые описал клинико-морфоло¬
гический синдром неизвестной эти¬
ологии с поражением бронхиол и
вовлечением в воспалительный про¬
цесс альвеол. Синонимами крипто¬
генной организующейся пневмонии
являются облитерирующий бронхи-
олит с организующейся пневмонией
(термин предложил G. Еріег в 1985
г.) или пролиферативный бронхио-
лит. Криптогенная организующая¬
ся пневмония рассматривается как
клинико-морфологический син¬
дром, характеризующийся особыми
морфологическими признаками:Рис, 2.6. КТ легких больной И. от февраля
2010 г. (пояснения в тексте)
Глава 2. Криптогенная организующаяся пневмония... 45- поражением респираторных бронхиол и альвеол {рис. 2.7, а, см. цветную
вклейку);- развитием хронического воспаления вокруг альвеолы;- альвеолярным поражением (организующейся пневмонией), которое
всегда преобладает над поражением бронхиол (бронхиолитом).В 70% случаев криптогенная организующаяся пневмония является идио-
патическим заболеванием (этиология ее остается неизвестной), однако в 30%
случаев заболевание развивается в рамках:• посттрансплантационных осложнений (после пересадки легких, комплек¬
са сердце—легкие, костного мозга);• диффузных заболеваний соединительной ткани (ревматоидный артрит,
системная красная волчанка, системная склеродермия, синдром Шенгрена);• инфекций {Mycoplasma pneumonia, цитомегаловирус, аденовирус, ВИЧ
и др.);• лекарственного поражения (амиодарон, D-пеницилламин, препараты
золота, сульфаса-іазин);• рааличных интоксикаций (оксиды серы, азота, фосген и др.);• осложнений лучевой терапии;• синдрома Стивенса-Джонсона.Распространенность криптогенной организующейся пневмонии неиз¬
вестна; половых различий нет, средний возраст начала заболевания состав¬
ляет 55—60 лет. Начальным патогенетическим звеном при криптогенной
организующейся пневмонии является некроз бронхиолярного эпителия с
обнажением базальной мембраны и активацией регуляторных пептидов,
иммунных факторов. Следствием этого становятся разрастания грану¬
ляционной ткани внутри ацинуса (тельца Масона) и развитие умеренно
выраженного интерстициального фиброза. Наиболее типичными клиниче¬
скими проявлениями криптогенной организующейся пневмонии являются
кашель (встречается у 90% больных) и одышка (у 80%); несколько реже
встречаются слабость, лихорадка (у 60%), потеря массы тела и миалгии
(у 50%).При аускультации легких выявляются конечно-инспираторная крепитация,
реже — сухие свистящие хрипы вместе с крепитацией; характерны лейкоцитоз
периферической крови (у 50% больных), повыщение СОЭ и С-реактивного
белка (у 70-80%). При исследовании ФВД выявляется рестриктивный тип
нарушений дыхания (снижение ЖЕЛ, ФЖЕЛ, индекса Тиффно), и лишь у
20% больных — снижение ОФВ,, выраженное снижение DLco. У 80% имеется
гипоксемия в покое и при физической нагрузке. Рентгенологически выявля¬
ются пятнистые двусторонние плотные очаги периферической консолидации
легочной ткани субплевральной локализации, по данным КТ легких инфиль¬
траты локализованы субплевратьно в 60% случаев, размер их может варьиро¬
вать от 2 см до долевого поражения, описана миграция легочных инфильтра¬
тов, чаще от нижних отделов к верхним; реже выявляются центролобулярные
узелки, линейные тени и шчевратіьньїй выпот; синдром «матового стекла» при¬
сутствует не всегда (50%).
46 ПульмонологияПри цитологическом исследовании бронхиального смыва, как правило,
обнаруживают высокий лимфоцитоз (>25%), может быть повышено количе¬
ство нейтрофилов и эозинофилов, могут встречаться пенистые макрофаги,
тучные и плазматические клетки. Трансбронхиальная биопсия может выявить
характерные для криптогенной организующейся пневмонии гистологические
признаки, однако не позволяет достоверно поставить диагноз — для морфо¬
логической верификации диагноза рекомендуется проведение открытой или
торакоскопической биопсии легких. Морфологической основой криптогенной
организующейся пневмонии является продуктивное воспаление с повреж¬
дением эпителия, разрастанием в респираторных бронхиолах и альвеолах
грануляционной, а затем соединительной ткани, образование телеп Массона
{рис. 2.7, б, см. цветную вклейку).Выделены следующие клинические варианты течения криптогенной орга¬
низующейся пневмонии:• типичная;• острая быстропрогрессирующая (фульминантная);• фиброзирующая;• очаговая.Для типичной криптогенной организующейся пневмонии характерны
быстрый ответ на лечение, волнообразное течение (рецидивы развиваются
как спонтанно, непрогнозируемо, так и при лечении низкими дозами глю¬
кокортикостероидов либо при снижении их дозы) и хороший прогноз (50%
спонтанная ремиссия, 50% частичная ремиссия). Современные рекомен¬
дации по лечению этого варианта интерстициальных пневмоний основаны
преимущественно на мнении экспертов (уровень доказательности С) и
подразумевают двухэтапное лечение: пульс-терапию метилпреднизолоном
500—1000 мг в/в в первые 3 дня с последующим назначением преднизолона в
суточной дозе 1—1,5 мг/кг на срок 3 мес) с постепенным снижением дозы и
терапию преднизолоном 20 мг/сут с дальнейшим снижением его дозы и отме¬
ной через 6-12 мес. Одновременно назначается симптоматическая терапия:
ингаляционные глюкокортикостероиды, р^-^гонисты длительного действия,
N-ацетилцистеин по 600 мг 2 раза в сутки длительно. Клинический эффект
наблюдается уже через 48 ч от начала терапии, рентгенологический эффект
оценивается через 3 мес.В нашем случае точная морфологическая верификация диагноза позво¬
лила начать активную терапию, которая оказалась достаточно эффективной:
отмечено как к,тиническое, так и рентгенологическое улучшение. Вместе
с тем нежелательным было назначение полной дозы преднизолона на дли¬
тельный срок. Развитие обострения заболевания можно расценивать как
результат не только перенесенного больной стресса, но и «мягкого» режима
терапии; повторное использование пульс-терапии для купирования обо¬
стрения представляется нам наиболее оправданным режимом лечения в этой
ситуации.
Глава 2. Криптогенная организующаяся пневмония... 47ЛИТЕРАТУРАВеялс А.У,, Хирани Н. Интерстациалъные заболевания легких: клинические
рекомендации Британского торакального общества совместно с Торакальным
обществом Австралии и Новой Зеландии и Ирландским торакальным обще¬
ством // Пульмонология. — 2009. — № 4. — С. 7-12.CordierJ.F., Loire R., BruneJ. Idiopathic bronchiolitis obliterans organizing pneu¬
monia. Definition of characteristic clinical profiles in a series of 16 patients // Chest.
1989; 96(5): 999-1004.Davison A.G., Haslam P.L., CorrinB. et al. Interstitial lung disease and asthma in
hard-metal workers: bronchoalveolar (avage, ultrastructural, and analytical findings
and results of bronchial provocation tests // Thorax. І983; 38(2):119-128.
Глава ЗНЕОБЫЧНЫЙ ВАРИАНТ ПОРАЖЕНИЯ ЛЕГКИХ
ПРИ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКЕИ.Д. Саркисова, О.В. Благова, А.В, Іїедоступ,
Н.В. Петухова, АЯ, Родионов, Е.М. ШиловНаряду с классическим, легко узнаваемым клиническим «образом» системной
красной волчанки (СКВ) хорошо известны ее многочисленные «маски» (нефро-
логическая, гематологическая и др.), которые нередко создают определенные
трудности в диагностике этого заболевания. Специфическое (не обусловленное
сопутствующей бронхолегочной инфекцией) поражение легких, как правило,
лишь сопутствует более ярким и опасным проявлениям волчанки и крайне редко
вь[ходит на первый план, определяя тяжесть состояния больного и прогноз забо¬
левания. Если в первых двух главах ре^Пз шла об идиопатических интерстициаль¬
ных заболеваниях легких, то в данной главе будут подробно рассмо грены вариан¬
ты интерстициального поражения легких в рамках системных заболеваний.Больной К., 26 лет, поступил в отделение кардиологии Факультетской
терапевтической клиники им. В.Н. Виноградова 3.04.2007 г. с жалобами на
ежедневные подъемы температуры до 37,6-39,6“С, обычно сопровождающи¬
еся ^гувством жара, реже ознобом, потливостью, на выраженную одышку при
небольших физических нафузках и в покое, на кашель с отхождснием светлой
мокроты, ноюшие боли в нижних отделах грудной клетки, усиливающиеся при
їздохе, ощущение умеренной скованности практ№іески во всех суставах, выра¬
женную общую слабость, потерю в весе 7 кг, выпадение волос.Анамнез жизни: отец 52 лет, мать 49 лет и брат 21 года здоровы. Родился в
Казахстане, постоянно жил в г. Чебоксары, в настоящее время живет и рабо¬
тает в Московской области менеджером. С 21 года курил по 1 пачке сигарет в
день, за месяц до поступления в клинику бросил курение. В детстве — частые
ОРВИ, ангины (последняя — в возрасте 17 лет). В 5-летнем возрасте — аннен-
дэктомия, в 11 лет — черепно-мозговая травма. С детства страдал стомаї и-
том, проводилось местное лечение, в юности наблюдался по поводу вегето-
сосудистой дистонии (отмечались нечастые подъемы АД до 140/80 мм рт.ст.).
Аллергологический анамнез не отягощен.Анамнез заболевания {рис. 3,1): весной 2006 г. развился короткий эпизод
болей и скованности практически во всех суставах (преимущественно ~ в
суставах нижних конечностей), что не сопровождалось их внешними изме-
ііениями; эпизод купировался самостоятельно в течение нескольких дней, к
врачу не обращался. В дальнейшем чувствовал себя удовлетворительно, сохра-
ня.ттись периодические малой нтенсивньте боли в суставах, В октябре—ноябре
2006 г. вновь возникли интенсивные боли во всех суставах (мелких суставах
Глава 3. Необычный вариант поражения легких...49весна 2006 10-12.200602.2007 03.2007боли и скованность
в суставахлихорадкаодышка39 "С
37 "Скашель с мокротой
выпадение волосСОЭ, мм/члечение20^комплемент
АНФ 1 ; 320
АТ к ДНК 1 : 40
46-73анемия до 83 г/л
протеинурия до 3,3%антибиотикиаспирин, грязи
(санаторий
«Славянск»)Рис. 3.1. Анамнез заболевания больного К., 26 леткистей и стоп, лучезапястных, локтевых, коленньгк, тазобедренных, в спине),
сопровождавшиеся покраснением кожи над суставами, припуханием, скован¬
ностью (при ходьбе хромал), Тогда же отметил появление субфебрильной лихо¬
радки. Обратился в больницу, где в анализе крови отмечено повышение СОЭ
до 20 мм/ч. Состояние расценено как переуто^іение, больной направлен на
санаторно-курортное лечение (без дополнительного обследования). Во второй
половине декабря лечился в санатории на Украине, где был проведен курс гря¬
зелечения; принимал аспирин. Состояние субъективно несколько у.тучгаилось,
купировались отечность и гиперемия суставов (однако малоинтенсивные боли
сохранялись), контроль температуры тела прекратил. В санатории (до начала
лечения) проведено обследование — выявлено умеренное увеличение СОЭ,
изменения на рентгенограммах кистей отсутствовали.С февраля 2007 т. состояние заметно ухудшилось: возобновились боли
практически во всех суставах, но в большей степени в mcjIKHX суставах кистей
и стоп, чувство скованности, более выраженное в вечернее время, впервые
появились и стали нарастать одышка, боли и чувство тяжести за груди¬
ной, периодически — чувство жара (темиерат>ру не измерял), небольшой
кашель с отхождением незначительного количества слизистой мокроты, уси¬
лилась слабость, головокружение. Снизился аппетит, потерял в весе около 7 кг.
Самостоятельно передвигается с большим трудом. 9.03.2007 г. был госпитали¬
зирован в одну из городских больниц Московской области. При поступлении
50 Пульмонологиясостояние расценивалось как тяжелое, выявлены лихорадка до 38-39,6 'С,
выпот в обеих плевральных полостях, тахикардия до 110/мин, нарастагошая
анемия (НЬ до 83 г/л), увеличение СОЭ до 46-73 мм/ч. При иммунологиче¬
ском исследовании крови, выполненном в НИИ ревматологии, обращали на
себя внимание выраженное снижение комплемента (до 20 при норме не ниже
70), наличие криоглобулинов (+), небольшое повышение титра антител к ДНК
(40 ед. при норме до 20) и РФ (1:20), а также АНФ в тшрс 1:320. Уровень ЦИК
оставался нормальным (93 ед. при норме до 130). Отмечались выраженные
изменения в анализах мочи: протеинурия от 0,3 до 3,3%о, умеренная лейко-
цитурия, эритроцитурия, что в сочетании с колебаниями уровня креатинина
расценивалось как нефрит. При посеве мочи получен рост гемолитического
стрептококка. При посеве крови роста микрофлоры не получено, в мазке из
зева высеял ся эпидермальный стрептококк. По данным Эхо КГ определялись
минимальное снижение сократительной функции миокарда (ФВ левого желу¬
дочка 50%), легочная рсгургитация П степени; камеры сердца расширены не
были. При одном из ЭхоКГ исследований не исключалось появление вегета¬
ций на клапане (на каком — не уточнялось). Трижды проводились безуспеш¬
ные попытки получить плевральный пунктат. В связи с эпизодом падения НЬ
до 86 г/л проведена ЭГДС, существенных изменений не выявлено.С учетом полученных данных проводился дифференциальный диагноз между
системной красной волчанкой и инфекционным эндокардитом. Проводилась
парентеральная антибактериальная терапия без существенного эффекта (тем¬
пература не была ниже субфебрильной): цефтриаксои 2,0 г/сут в течение 8 дней
в/в, абактал 800 мг/сут в течение 3 дней, амикацин 1,5 г/сут в течение 3 дней,
нолицин 800 мг/сут 2 раза в день, а также терапия мовалисом в/м, верошпиро-
ном 50 Ml в сутки, лазиксом, низоралом, омезом, альмагелем.Со слов больного, на фойе терапии стали CHjibHO вьптадать волосы (до лече¬
ния этого не замечал). Однократно в связи с развитием артеришіьной гипо¬
тонии парентерально вводился преднизолон (доза неизвестна) — в этот день
отмечена нормализация температуры тела.Повышение температуры обьгшо сопровождалось ч^твством жара, однократ¬
но отметил развитие выраженного озноба, иногда наблюдалась потливость по
ночам. Кроме того, беспокошш зудящая эритематозно-папулезная (по описа¬
нию больного) сыпь на коже спины и нижних конечностей. На фоне терапии в
полости рта было отмечено развитие кандидоза. В целом состояние оставалось
без существенной динамики, продолжала нарастать одытпка. С 28—29.04.2007 г.
усилился кашель с отделением большого количества слизистой мокроты, на
этом фоне наросла одышка, температура колебалась в пределах 38—39,4 “С.
Диагноз оставался не ясным. Для дальнейшего обследования и лечения посту¬
пил в Факультетскую терапевтическую клинику им. В.Н, Виноградова.При поступлении в клинику: состояние тяжелое. Температура тела 38,5 "С,
масса — 65 кг, рост 174 см. Кожные покровы и слизистая оболочка рото¬
вой полости чистые, кожа умеренно бледная, горячая, повышенной влаж¬
ности, волосы легко выпадают. Область суставов не изменена. Отеков нет.
Периферические лимфоузлы не увеличены. ЧД до 30 в минуту. В акте дыхания
Глава <?. Необычный вариант поражения легких... 51активно участвуют межреберные мышцы. Одышка нарастает при минималь¬
ных движениях, разговоре. Дыхание ослаблено, плохо проводится в базальные
отделы с обеих сторон (ниже уровня 8 ребра по лопаточной линии)» справа над
диафрагмой — крепитация, сухих хрипов нет. Границы сердца не изменены,
ЧСС до 120/мин, ритм правильный, тоны ясные, шумов нет. АД 120 и 70 мм
рт.ст, (в дальнейшем отмечалось повышение АД до 140—150 и 80—90 мм рт.ст.).
Живот мягкий, безболезненный. Печень на 2 см выступает из-под края ребер¬
ной дуги, селезенка не увеличена.В общих анализах крови (от 04.04 и 16.04.2007 г.) обращали на себя внима¬
ние анемия с ретикулоцитозом (реакция Кумбса отрицательная), лейкоцитоз с
лимфопенией: НЬ 83,5 г/л, эритроциты 3,2-3,0 млн, ретикулоциты 22—33%о,
цветовой показатель 0,79—0,87, лейкоциты 9,1—9,6 тыс., нейтрофилы 77,4-
71,0%, лимфоциты 17,0-22,9%, эозинофилы 0,5-0,4%, моноциты 5,0—5,9%,
базофилы 0,4-0,1%, тромбоциты 412-261 тыс., СОЭ 64-60 мм/ч.В биохимических анализах крови от 04,10 и 23.04.2007 г. выявлены гипопро-
теинемия с гипоальбуминемией при нормальном уровне креатинина: общий
белок 4,6-5,3—4,6 г/дл, альбумин 2,1-2,4—2,3 г/дл, глюкоза 83 мі’/дл, креати-
нин 1,1—1,0—0,6 мг/дл, азот мочевины 36—25—20 мг/дл, мочевая кислота 6,8—
5,1—5,1 мг/дл, обцщй билирубші 0,3—0,3—0,6 мг/дл, ACT 34—71—28 сд/л, АЛТ
44-81-59 ед/л, гамма-ГТ 101-178-140 ед/л (норма до 55), ШФ 121-92 ед/л,
Na" 138—139—143 мэкв/л, 4,8—4,5—4,2 мэкв/л, железо 24—177—94 мкг/лд,
трансферрин 148-133 мг/дл, % насыщения железом 11,5-94,4%.Липидный спектр от 04.04—10.04.2007 г.: триглицериды 269—641 мг/дл,
общ. холестерин 248-307 мг/дл, ЛПВП-хс 56 мг/дл (норма 35-75), ЛПНП-хс138,2 мг/дл (норма 100-160), ЛПОНП-хс 53,8-128,2 мг/дл (норма 10-30),
КА 3,43 (1,2—4,2). Гиперлипидемия 4-го типа.Электрофорез белков (04.04—10.04.2007 г): альбулган 42,0-46,5% (норма
54,7-68,7), альфа-1 5,2-4,2% (норма 3,7-7,8), альфа-2 29,6-21,6% (норма 5,2-
10,7), бета 12,1—13,4% (норма 8,6-13,7), гамма 11,1-14,3% (норма 10,7—19,3).Иммунологическое исследование крови; HBsAg, HCVAb, RW, антитела
к ВИЧ отрицательны. Имм)чюглобулины: А— 175 мг/дл (норма 50-300),
М — 120 мг/дл (норма 40-200), G — 1400 мг/дл (норма 600-2000). РФ (кач.)
отрицателен, антистрептолизин-О О МЕ/мл (0-125), СРВ 8,11 мг/дл (0-0,8).
Комплемент 27,7 гем.ед. (норма 20-40). LE клетки единичные в препарате.
АТ к ДНК (нат.) отриц. АНФ 1:40. Криоглобулины отрицательны. Антитела к
кардиолипину IgM 3,52 МЕ/л (0-26), IgG 2,18 МЕ/л (0-23).Коагулофамма: АЧТВ 1,11 (нет данных за наличие волчаночного антикоагу¬
лянта), ПИ 111%, фибриноген 4,06 т/л, РКФМ 0,620 (0,350-0,470). Активация
плазменного звена гемостаза.Гормоны щитовидной железы в пределах нормы.При 3-кратном посеве крови роста микрофлоры не получено.Прокальцитонин крови в пределах нормы.Общий анализ мочи от 04.04-16.04.2007 г.: рН-5-5, уд. вес — 1015-1023, про¬
зрачность неполная, сахара, ацеї ина їТЯіТїїелок Oj67(]^2j4jp0 %cl желч. пигм. —эритроциты —OTp., уробилин — норма, леійк^ї^і^^—
52Пульмонология15—20/ 8—12 в п/зр., цилиндры зернистые 001 отс. в п/зр., гиалиновых цилин¬
дров нет, слизь — немного, бактерии — умеренное количество.Нарастала суточная иротеинурия: 630 мг, 1700 мг, 3225 мг (от 07.05.2007 г.).Анализ мочи по Нечипорснко от 19.04.2007 г.: pH 7, белка 2Л00%о, лейкоцитов
30 ООО, эритроцитов 46 250. При посеве мочи роста микрофлоры не выявлено.Проба Ребергц от 18.04.2007 г.; конц. индекс 82,6, фильтрация 75 \иі/мин,
реабсорбция 98,8%.ЭКГ при постутении {рис. 3.2): ритм синусовый, ЧСС 87 в минуту, ЭОС
расположена нормально. R в otb.V.+S в отв. V, 43 мм. PQ 0,14 с, QRS 0,09 с,
QT 356 мс. Снижение амплитуды зубиов Т в отв. V^—V^. Минимальный подъем
сегмента ST и двухфазный Т в отведении V,.ЭхоКГ. камеры сердца не расширены: КДР левого желудочка 5,3 см (норма до5,5), левое предсердие 3,1 см, правое предсердие не увеличено, правый желудочек
2,6 см (до 2,6 см). Толщина стенок: МЖП 1,1 см (N до 1,0), ЗСЛЖ 1,2 см (до 1,1).
Давление в легочной артерии 26 .мм рт.ст. Характер движения стенок не изменен.
Общая сократительная функция не нарушена, ФВ 68%. Клапанный аппарат и
стенки аорты не изменены. Максимальный фадиент на аортальном клапане8,9 мм рт.ст. Трикуспидштьная рег>ргитапия 1 степени. В полости перикарда
определяется умерешюе коли'іество избыточной жидкости (до 150—170 мл).Чреспищеводнан ЭхоКГ: створки клапанов сердца тонкие, подвижные, без
дополнительных эхопозитивных образований.При УЗИ органов брюшной полости: печень не увеличена, контуры ровные,
паренхима однородной структуры, обычной эхогенности, селезенка 133x45 мм.1—■».€« — Рис. 3.2. Злекірокардиограліма больного К.
Глава 3. Необычный вариант поражения легких...53Почки нормальных размеров, обычно расположены, с ровными контурами,
дилатацрш ЧЛС и теней конкрементов не выявлено. Область надпочечников не
изменена. Асцита не выявлено.ФВДпри поступлении: ЖЕЛ - 39%, ОФВ, - 35%, МОС„ - 39%, MOCj, -
22%, МОС^з — 17%, ОФВуФЖЕЛ — 73%. Бронхиальная обструкпия резко
выражена, резкие вентиляционные нарушения рестриктивного типа.Общий анализ мокроты: характер — слизисто-гнойная, цвет — бело-серый,
лейкоциты 30—60—90 в поле зрения, в скоплении до негусто-густо, эритроциты001 в поле зрения, макрофаги — много, эпите.чий цилиндршіеский — немного,
плоский — умеренное количество, спирали Куршмана и кристахім Шарко—
Лейдена не найдены, эозинофилы ед. в препарате, атипичные клетки не най¬
дены. БК — не найдены, кокки, палочки — немного.Рентгенография грудной клетки от 03.04.2007 г. (рис. 3.3): в обеих плевраль¬
ных полостях жидкость до переднего отрезка 4 ребра, которая пращевидно
поднимается вверх. Судить о состоянии легочной ткани за жидкостью не
представляется возможным. Отмечается небольшое понижение воздушности
легочной ткани в средних отделах легкого, вероятно, за счет жидкости в плев¬
ральном синусе. В других отделах легкие без свежих очаговых и инфильтратив-
ньгх изменений. Корни легких структурны. Диафрагма за жидкостью не видна,
междолевые плевры утолщены. Сердце горизонтально расположено, несколь¬
ко расширено влево, аорта рентгенологически не изменена.Таким образом, диагноз сепсиса и инфекционного эндокардита был окон¬
чательно отвергнут на основании отсутствия вегетаций на клапанах сердца,
отрицательного посева крови и нормального уровня прокальцитонина, а также
клинической картины в целом. Сочетание типичных клинических и имму¬
нологических признаков (достаточно хорошо переносимая лихорадка непра¬
вильного типа, которая чаще не сопровождается потами, ознобами и устой¬
чива к антибактериальной терапии, потеря массы гела, алопеция, достаточно
вероятный афтозный стоматит — хотя больной считает стоматит привычным
заболеванием; на момент поступления в клинику его признаки отсутствовали,
возможно — дерматит, хотя он мог
носить аллергический характер,
интенсивные артралгии и поли¬
артрит в дебюте болезни, поли¬
серозит — двусторонний плеврит
с небольшим количеством выпо¬
та, перикардит, перитонит — при
КТ выявлялись признаки асцита,
нефрит с признаками нефрити¬
ческого синдрома и нарастающей
вплоть до нефротического син¬
дрома протеинурией, гемолитиче¬
ская анемия с ретикулопитозом,
небольшая лимфопения, выражен¬
ное увеличение СОЭ, СРБ, АНФРис. 3.3. Рентгенография органоп грудной
клетки больного К., прямая проекция (пояс¬
нения в тексте)
54Пульмонологияв титре до 1:320, LE-клетки, снижение комплемента и увеличение титра
антител к ДНК по данным анамнеза), что составляло не менее 6 критериев
Американской ревматологической ассоциации, позволяло расценивать забо¬
левание как системную красную волчанку.Однако причины выраженной одышки, которая выходила на первый план в
к^тинической картине и определяла т5скесть состояния больного, оставались
неясны. Наиболее очевидным было наличие двустороннего плеврита, но
количество жидкости в полостях было не настолько велико и нарастало не
так быстро, чтобы считать плеврит главной причиной одышки. Можно было
думать о наличии лего^шой гипертензии, связанной с васкулитом или анти-
фосфолипидным синдромом (анализы в этот момент еще не были получены),
однако признаки перегрузки правых отделов сердца отсутствовали, при ЭхоКГ
определялось нормальное давление в легочной артерии (26 мм рт.ст.). Другой
вероятной причиной одышки мог бьггь миокардит с развитием сердечной
недостаточности, но никаких признаков миокардита (расширения границ
сердца, ритма галопа, нарушений ритма и проводимости, снижения ФВ, изме¬
нений зубца 7) у больного не было, отсутствовали отеки, акроцианоз, похоло¬
дание конечностей. Дыхательная мускулатура работала интенсивно, и думать о
ее поражении (миозите) тоже не приходилось.Анемия сама по себе была довольно умеренной и нарастала постепенно, что
также не позволяло считать ее единственной причиной одышки. Оставалось
предполагать поражение легочной паренхимы, которая при рентгенографии
была плохо видна за жидкостью в плевральных полостях. Гнойный характер
мокроты и влажные хрипы справа заставляли думать о возможности неспец-
иф№іеской пневмонии. Вполне возможным было также развитие туберкулеза
легких, хотя характерные ночные поты у больного отсутствовали. Несмотря на
отсутствие легочной гипертензии, нельзя было полностью исключить тром¬
боэмболию мелких ветвей легочной артерии, связанную с возможным анти-
фосфолипидным синдромом. Наконец, интерстициальное поражение легких в
рамках СКВ (волчаночный пневмонит, в том числе острый люпус-пневмонит)
могло усугубить действие других причин одышки.с целью оценки состояния
паренхимы легких и выяснения
причин выраженной одышки была
выполнена КТ легких.КТ органов грудной клетки от
04.04.2007 г. {рис. 3.4): в обоих легких
определяется диффузное равномер¬
ное повышение плотности легоч¬
ной паренхимы по типу «матового
стекла». На этом фоне определя¬
ются множественные воздушные
кисты размерами от 4 до 12 мм и
единичные субплевральньте буллы
размером до 17 мм. Сосудистый иРис. 3.4. КТ органов грудной клетки боль¬
ною К. (пояснения п тексте)
Глава 3. Необычный вариант поражения легких.55Рис. 3.5. КТ-картина поражения легких
при лимфангиолейомиоматозе (поясне¬
ния в тексте)интерстициа.'1ьный рисунок не изме¬
нен. В базальных отделах обоих лег¬
ких— участки консолидапии легоч¬
ной паренхимы и участки фиброза. В
плевральной полости с обеих сторон —
осумкованная, частично организован¬
ная жидкость с толщиной слоя до 20
мм. Трахея и крупные бронхи сво¬
бодно проходимы, не деформирова¬
ны. Лимфатические узлы средостения
не увеличены. Аорта, легочный ствол
и их ветви не расширены. В пери¬
карде определяются следы жидкости,
в брюшной полости под диафрагмой также определяется жидкость. Селезенка
не увеличена. Заключение: изменения легких могут быть расценены как гисти-
оцитоз. Однако, учитывая клинические и рентгенологические данные, картина
остается неясной. Рекомендуется биопсия легкого. Нельзя исключїггь левосто¬
роннюю нижнедолевую пневмонию. Гидроторакс. Асцит.Выявленные в легких изменения были настолько нетипичны для волчанки
(не говоря уже о кистах, отсутствовало собственно поражение интерстипия),
что заставляли думать о двух возможностях: либо мы столкнулись с псрвич^шім
иммунным заболеванием легких, которое протекает с выраженными систем¬
ными проявлениями, либо имеет место вторая болезнь — самостоятельное
поражение легких у больного с СКВ. Предпочтительнее бьшо объяснить все
проявления в рамках одной болезни.По мнению рентгенологов, КТ-картина в наибольшей степени соответ-
ствова.іа диагнозу лимфангиолейомиоматоза (рис. 3.5, разрастание гладко¬
мышечных волокон в интерстиции легких с деструкцией альвеол), для диф¬
фузной формы которого характерны микрокистозные образования на фоне
сетчатого рисунка. Однако заболеванием страдают исключительно женщины
детородного возраста, при этом обострение болезни зависит от менструаль¬
ного цикла.Уже менее вероятным пред¬
ставлялось наличие гистиоцитоза
X (рис. 5.6), который был вынесен
в заключение. Гистиоципгоз X (или
эозинофильная гранулема) — забо¬
левание неизвестной этиологии,
для которого характерно образова¬
ние гистиоцитарных инфильтратов
в легких и других органах (в том
числе в костях, почках, глазнице и
др.); гистиоциты отличаются раз¬
ной степенью злокачественности.В легких, помимо гранулем, могутРис. 3.6. КТ-картина поражения легких при
гистиоцитозе X (пояснения в тексте)
56 Пульмонологияобнаруживаться микрокровоиз.гияния и тонкостенные кисты; у половины
больных со временем развивается пневмоторакс; лимфоаденопатия не харак¬
терна. Поражение почек проявляется выраженной протеинурией, прогресси¬
рующей почечной недостаточностью. Возможны неспецифичсские имму^н-
ные сдвиги в крови. Диагноз ставится с помощью исследования лаважной
жидкости или биопсии легкого (по обнаружению гистиоцитов с Х-тельцами
и клеток Лангсрганса), однако биопсия угрожает развитием пневмоторакса.
Препаратами выбора являются кортикостероиды.От других редких заболеваний (таких как альвеолярный протеиноз легких,
альвеолярный микролитиаз, первичный бронхолегочный амилоидоз) гистио-
цитоз отличается именно ранним появлением тонкостей ньсс кист в легких;
и все-таю1 клиническая картина в нашем случае полностью не укладывалась
в диагноз гистиоцитоза X — ему противоречили нехарактерные системные
проявления (артрит» полисерозит, стоматит, алопеция, нефрит с выраженной
гематурией, высокий титр АНФ в анамнезе); было трудно предполагать также
одновременное развитие волчанки и гистиоцитоза.Диагнозу саркоидоза полностью противоречило отсутствие внутрифудной
лимфоаденопатии. Сочетание нефрита и кист в легких заставляло думать о
синдроме Гудпасчера, микроскопическом полиартериите или гранулематозе
Вегенера, однако для этих заболеваний характерно образование полостей рас¬
пада в легких с кровохарканьем, а не тонкостенньгх кист; выраженные систем¬
ные поражения характерны лишь для гранулематоза Вегенера, но на этой
стадии, как правило, присутствует и поражение верхних дыхательных путей.
Туберкулез может развиваться и на фоне волчанки, однако он не даст таких
тонкостенных кист без всякого содержимого, без кровохарканья и без увеличе¬
ния внутригрудных лимфоузлов. То же самое можно сказать о деструктивных
пневмониях, в частности пневмопистной. Двукратное отсутствие антител
к ВИЧ вообще делало диагноз пнев.моцистной пневмонии маловероятным.Наконец, врожденные кисты в легких и буллезная эмфизема дают совер¬
шенно иную рентгенологическую картину и не протекают столь бурно (даже в
сочетании с волчанкой).Таким образом, найти вторую (легочную) болезнь или объяснить всю кли¬
ническую картину одним заболеванием не удавалось; перед нами стоял вопрос
о проведении открытой биопсии легкого, с другой стороны, заболевание
носило отчетливо иммунный характер (гнойная мокрота отражала все-таки
неспецифическую инфекцию). Данных за сепсис не было. Все это делало воз¬
можным назначение кортикостероидов под прикрытием антибиотиков без
четкой морфологической верификации диагноза.Кроме того, необходимо было еще раз проанализировать все возможные
варианты поражения легких в рамках СКВ. И здесь неоценимую роль сыфа-
ло обнаружение в Интернете описания чрезвычайно редкого (единственного)
клинического случая — сочетания СКВ с так называемым лимфоцитарным
интерститшальным пневмонитом (рис. 3.7), на поздних этапах которого у боль¬
ной развились множественные тонкостенные кисты в легких. КТ-картина на
четвертом году наблюдения у этой больной была практит^іески идентична тому,
Глава 3. Необычный вариант поражения легких.57Рис. 3.7. КТ органов грудной клетки больной СКВ (из статьи M.S. Filipek и соавт.):
а — 1998 г.5 симптом «матовою стекла» и хорошо различимые цептролобулярные узел¬
ки с отдельными ПОЛЯМИ слшшия; б— 1999 г., нарастание изменений по тииу «мато¬
вого стекла», множественные участки консолидации и отдельные маленькие кисты;
в — 2002 г., диффузные изменения по типу «матового стекла» и драматическое нарас¬
тание размеров кистс чем мы столкнулись у нашего пациента. К ранее диагностированной волчанке
уже на фоне терапии у больной присоединилась одышка, в легких бьига выяштсны
сначала узелки в сочетании с симптомом «матового стекла». Через год появились
ма^тенькие кисты, а еще через 3 года размер этих кист драматически увеличился.
Описание подобного случая позволило нам окончательно утвердиться в диагнозе
СКВ; был проведен консилиум и начата стероиддіая терапия в сочетании с анти¬
биотиками.Диагноз был сформулирован следующим образом: системная красная вол¬
чанка под острого течения с ;шхорадкой, поражением слизистых оболочек
(афтозный стоматит), суставов (полиартрит, артралгии), серозных оболочек
(плеврит, перикардит, перитонит?), легких (лимфоцитарный интерстициаль¬
ный пневмонит), почек (активный волчаночный нефрит с нефритическим и
нефротическим синдромами), системы крови (гемолитическая анемия, лим-
фопения), трофическими расстройствами (алопеция), III степени активности.
Левосторонняя нижнедолевая пневмония.Проводилась терапия: ингаляции увлажненного кислорода, с 05.04.2007 г. —
преднизолон 40 мг/сут (доза выбрана с учетом наличия неспсцифической
легочной инфекции), с 18.04 по 20.04 — сочетанная пульс-терапия {преднизо¬
лон 1000 мг 3 раза, циклофосфан 1000 мг однократно); в/в капельно 10% р-р
альбумина 100 мл № 8 (в связи с появлением отеков голеней), цефтриаксон
(отменен после первого вливания в связи с аллергической реакцией в виде
гиперемии лица, нарастания одышки), авелокс 400 мг в/в один раз в сутки в
течение 10 дней, метрогил 500 мг в/в капельно 2 раза в день в течение 10 дней,
58 Пульмонологиядифлюкан 50 мг в день в течение 7 дней, далее нистатин 500 тыс. Ед 4 раза в
день, халиксол 30 мг 3 раза в день, метопролол 50 мг в день, омез 20 мг на ночь.В результате лечения состояние заметно улучшилось: одышка полностью
купирова.іась (поднимался на 4—5-й этаж в обычном темпе), сохранялись
лишь болевые ошуш,ения в нижних отделах грудной клетки (в дальнейшем
практически полностью исчезли), на третий день кортикостероидной терапии
нормализовалась температура тела (сохранялись вечерние под:ъемы темпера¬
туры до 37,1 '’С, которые прекратились после пульс-терапии), практически
прекратились боли в суставах, на фоне терапии метопрололом нормализо¬
валось артериальное давление (110-120/70-80 мм рт.ст.), хрипы в легких
не выслушивались; уровень гемоглобина повысился до 115 г/л, СОЭ снизи¬
лась до 17 мм/ч, сохранялся небольшой ретикулоцитоз, остальные показатели
общего анализа крови нормализова-тись, несколько повысился уровень альбу¬
мина (до 2,9 г%). При контрольном определении ФВД ЖЕЛ 61%, ОФВ, 49%,
МОС25 ^0^53 26%, МОС^^ 68%.По данным контрольной КТ легких отмечена вьфаженная положительная
динамика: повышение воздушности легочной ткани, уменьшение размеров
кист, исчезновение выпота в плевральных полостях, уменьшение размера
фиброза в нижней доле левого легкого.Однако признаки активности нефрита сохранялись (в анализе по
Нечипоренко от 2 мая — после к>'рса в/в вливаний альбумина — в трех порци¬
ях: pH 6,5; белок І0,5%о, 7,4%с, 8,7%о, лейкоциты 45250, 28500, 5000, эритро¬
циты 88750, 45000, 40000), в связи с чем 04.05 больной был проконсультирован
на кафедре нефрологии ММА им, И.М, Сеченова: диагноз тот же, поражение
почек протекает по типу активного волчаночного нефрита с нефритическим и
нефротическим синдромами. Целесообразно продолжить выбранный протокол
лечения, увеличив дозу преднизолона до 50 мг/сут с проведением повторных
сочетанных пульсов (преднизолон 500 мг х 3 раза + циклофосфан 800-1 ООО мг)
с интервалами от 2 до 4 нед.С 04.05 доза преднизолона (в связи с сохраняющейся активностью нефри¬
та) увеличена до 50 мг/сут; 7-9 мая проведена повторная сочетанная пульс-
терапия (преднизолон 500 мг х 3 + циклофосфан 1000 мг). Проба Реберга от
07.05: креатинин крови 0,7 мг/дл, креатинин мочи 68,0 мг/дл, фильтрация
105 мл/мш1, реабсорбция 99,0%.Необходимо подробно остановиться на необычном для СКВ варианте
поражения ЛЄГКТІХ, который был диагностирован у нашего больного, — лимфо¬
цитарном интерстициальном ігаевмоните (или пневмонии — в данном случае эти
термины используются в литературе как синонимы).Поражение легких при диффузных заболеваниях соединительной ткани
встречается довольііо часто, но в основном это касается системной склеро¬
дермии (при которой пневмосклероз является одним из критериев диагноза),
дермато/полимиозтгга (до трети пациентов имеют легочные симптомы), ревма¬
тоидного артрита и синдрома Шегрена. Для СКВ легочная патология гораздо
менее характерна (в дебюте заболевания менее 5% больных имеют клиниче¬
ские или рентгенологические признаки поражения легких).
Глава 3. Необычный вариант поражения легких.,. 59Прежде чем говорить о лимфоцитарном интерстициальном пневмоните,
кратко остановимся на том, как развивалось представление ревматологов о
поражении легких при диффузных болезнях соедішительной ткани в течение
последних 50 лет. В качестве точки отсчета возьмем одну из самых первых совет¬
ских монографий по коллагеновым болезням, написанную А.И. Нестеровым
и Я.А. Сигидиным в 1966 г. Авторы описывают следующие известные на тот
момент формы поражения легких.1. Плеврит, который встречается при ревматоі-щном артрите, ревматизме
(ревматизм входил в тройку основных причин выпотного перикардита, но и
плеврит развивался достаточно часто).2. Острая ревматическая пневмония — поражение легких, которого мы
сегодня практически не видим, как не видим и острого ревматизма. Между
тем именно о ревматизме С.П. Боткин сказал: <хМожет открыться пневмония
совершенно любого характера и дающая любое предсказание...». Это была именно
иммунная пневмония с выраженным отеком альвеол, которая не поддавалась
лечению антибиотиками и поддавалась противоревматической терапии. За
рубежом эту форму неинфекционного воспаления альвеол стали называть
пневмонитом.3. Хроническая интерстициальная пневмония, которая, в отличие от острой,
не только протекает длительно, но и заканчивается фиброзом. Ее описывали при
ревматоидном артрите, СКВ. В частности, патоморфологи отмечали при волчан¬
ке важное отличие от обычных интерстициальных пневмоний -- преобладание в
инфильтратах мазмоцитов; описаны не только типичные для СКВ гиалиновые
тромбы в капиллярах, фибриноидные изменения сосудов, утолщение, отек и
некроз альвеол, но и связанный с сосудистыми поражениями распад легочной
ткани, образование полостей (при этом выраженный пневмофиброз редок).4. Легочный васкулит — преимущественно при СКВ, реже при ревматоид¬
ном артрите (преобладает картина легочной гипертензии),К другим формам поражения легких при диффузных заболеваниях соеди¬
нительной ткани относили базальный пневмосклероз (типичен для ревматоид¬
ного артрита, системной склеродермии), «сотовое легкое», иногда с развитием
пневмоторакса (те же заболевания), характерные для волчанки дисковидные
ателектазы; описывались также тонкостенные каверны (сосудистого генеза)
при СКВ (преимущественно при морфологическом исследовании).Сегодня интерстициальные поражения легких при диффузных заболе¬
ваниях соединительной ткани рассматриваются как особая этиологическая
группа интерстициальных заболеваний легких. Морфологические варианты
хронического интерстициального поражения легких у больных с диффузными
заболеваниями соединительной ткани намного разнообразнее, чем это счита¬
лось раньше. Наиболее часто встречается так называемая обычная интерстици¬
альная пневмония (ОИП), которая характеризуется воспалением и фиброзом
в стенках альвеол. Именно этот — наиболее частый — вариант труднее всего
поддается лечению и может приводить к развитию «сотового легкого». Другие
варианты — более редкие — намного лучше отвечают на терапию кортикосте¬
роидами и цитостатиками (циклофосфаном, азатиоприном, метотрексатом).
60 ПульмонологияК ним отаосятся десквамативная интерстициальная пневмония (ДИП, при
диффузных заболеваниях соединительной ткани встречается довольно редко),
неспецифическая (НИП), лимфоцитарная (ЛИП), организующаяся пнев¬
мония с облитерирующим бронхиолитом (ОПОБ). При острых поражениях
легочного интерстиция в рамках диффузной альвеолярной геморрагии мор¬
фологически выявляют так называемое острое альвеолярное повреждение и
диффузную альвеолярную геморрагию (ДАТ) с капилляритом или без него.Острое альвео.іярное повреждение при диффузных заболеваниях соеди¬
нительной ткани встречается почти исключительно при волчанке (изредка —
при дерматомиозите) и напоминает обычную пневмонию (чаще двусторон¬
нюю) преимущественно в базальных отделах; при КТ легких определяется
сочетание изменений по типу «матового стекла» и выраженной консолидации;
на этом фоне могут выявляться бронхоэкгазы. Выделяют три фазы острой
интерстициальной пневмонии: экссудативную, организующуюся и фиброз¬
ную. Морфологически характерны утолщение межальвеолярных перегородок
и высокая активность воспаления и склероза, формирование гиалиновых
мембран, капиллярит; при этом собственно интерстипиальный фиброз отсут¬
ствует.Диффузная альвеолярная геморрагия (ДАТ) протекает, как правило, остро
(хотя возможно и хроническое течение), среди диффузных заболеваний соеди¬
нительной ткани альвеолярная геморрагия встречается, главным образом,
при СКВ (является одним из морфологических вариантов острого люпус-
пневмонита), реже — при дермато/полимиозите или смещанном заболевании
соединительной ткани (болезни Шарпа), которую Е.М. Тареев, как известно,
не признавал. Для СКВ особенно характерен вариант диффузной альвеоляр¬
ной геморрагии с легочным капилляритом, который встречается также при
системных васкулитах (гранулематозе Вегенера, микроскогшческом полиар¬
териите, синдроме Черджа-Стросс), синдроме Гудпасчера, геморрагическом
васкулите, смешанной криоглобулинемии, синдроме Бехчета. Отличительным
клиническим симптомом, наряду с одышкой, является кровохарканье.
Рентгенологически основным признаком являются неоднородные диффузные
инфильтраты с заполненными воздушными пространствами, обусловленные
кровотечением в альвеолы, морфологически — нейтрофи-іьная инфильтрация
легочных капилляров и альвеолярных перегородок с последующей геморраги¬
ей и неспецифическим фиброзом шіьвеолярной стенки.Обычная интерстициальная пневмония встречается главным образом при
ревматоидном артрите, системной склеродермии, дермато/полимиозите и
СКВ. Это основной (до 90%) морфологический вариант при фиброзирующем
альвеолите; наиболее характерным рентгенологическим признаком является
сетчатый рисунок легкого преимущественно в субплевральных и базальных
отделах (вплоть до формирования картины сотового легкого). Возможно уве¬
личение лимфатических узлов средостения; основным отличием от других
форм интерстициа-іьной пневмонии является отсутствие симптома «матового
стекла«>. Гистологически, наряду с зонами интерстициального фиброза, встре¬
чаются и признаки воспаления (с участием мононуклеаров, гранулоцитов,
Глава З, Необычный вариант поражения легких... 61плазмоцитов), а также участки нормальной легочной паренхимы — характерна
гетерогенность картины.Десквамативная пневмония отличается от обычной наличием большого
количества альвеолярных макрофагов в полости альвеол (что отражается в
появлении изменений по типу «матового стекла» преимущественно в базаль¬
ных отделах) и значительно менее выраженным фиброзом; при диффузных
заболеваниях соединительной ткани встречается редко (иногда может лежать в
основе острого люпус-пневмонита), иногда приводит к формированию брон-
хоэктазов, множественных кист в ткани легкого.Неспецифическая интерстициальная пневмония встречается практически
при всех диффузных заболеваниях соединительной ткани, вк.іючая СКВ, и
отличается от обычной интерстициальной пневмонии появлением воспаления
по типу «матового стекла» при меньшей выраженности фиброзных изменений;
возможно формирование сотового легкого и увеличение внутригрудных лим¬
фоузлов, развитие бронхоэктазов.Организующаяся пневмония с облитсрир>тощим бронхиолитом (ОПОБ)
встречается преим)тцественно при ревматоидном артрите и дерматомиозите,
морфологически проявляется интраальвеолярной организацией и фиброзом,
который распространяется на дистальные бронхиолы и вызывает их фиброз
(облитерирующий бронхиолит). Диагноз организующейся пневмонии с обли-
терирующим бронхиолитом ставится при одновременном наличии очагов
консолидации легочной ткани, полей фиброза, линейных участков уплотнения
(радиальных или субплевральных) с воспалением по типу «матового стекла» и
центролобулярными узелками.Облитерирующий бронхиолит и другие поражения бронхиального дере¬
ва (панбронхиолит, бронхоэктазы) также для волчанки нехарактерны, они
встречаются при ревматовдном артрите и синдроме Шегрена. При КТ легких
выявляются мозаично ослабленный (особенно на вьщохе) рисунок в соче¬
тании с расщиреннъши (во всяком случае не суженными) сегментарными
и субсегментарными бронхами с утолщенными стенками (бронхоэктазы),
центролобулярными и перибронхиальными узелками с участками «матового
стекла» (фолликулярный панбронхиолит) или изменениями по типу «дерева
в почках» при панбронхиолите. Прямым гистологическим признаком облите-
рирующего бронхиолита является концентрическая фиброзная облитерация
терминальных и респираторных бронхиол. Доказана роль Д-пеницилламина
в развитии облитерируюшего бронхиолита, однако он может развиваться и
самостоятельно.Лимфоцитарный интерстициальный пневмонит (или пневмония, ЛИП)
описан у больных с синдромом Шефена, ревматоидным артритом и СКВ,
Рентгенологически лимфоцитарный интерстициальный пневмонит проявля¬
ется сочетанием изменений по типу «матового стекла» с утолщением интерло-
булярных перегородок, центролобулярными или субплевральньтми узелками
и тонкостенными кистами; кисты обычно многочисленны и не превышают
в диаметре 3 см; при синдроме Шегрена возможно появление кальцини¬
рованных депозитов амилоида. Гистологически вокруг бронхиол выяв,чяют
62ПульмонологияТаблица 3.1Дифференциальная диагностика различных вариантов интерстициального поражения
легких при диффузных заболеваниях соединительной ткани на основании данныхКТ легкихItiliн в-1SкsisS § §|МІёовой¥11И 23 «
X 2* 1
Д g.1§Опеее.ю4)1Острая интерстици¬Диффузное++++++ + +альная пневмонияОбычная интерсти¬Периф., базально+++-ь++циальная пневмониясубплевральноДесквамативнаяНижние доли,+-1-4-+++интерстициальнаяпериферияпневмонияНеспепифическаяСубплеврально-ь-ь+++++интерстициальнаяпневмонияОблитерирующийДревовидно++ +++++ + +бронхиолиторганизующаясяСубплеврально++++ + +пневмонияперибронхиатьноЛимфоцитарныйДиффузно+ + +++++++интерстициальныйпневмонитдиффузную лимфоцитарную инфильтрацию (Т-лимфоциты, плазмоциты),
которая и дает картину «матового стекла»; могут обнаруживаться гистиоциты
и гигантские многоядерные клетки. Характер инфильтрации аналогичен тому,
что обнаруживают при синдроме Шегрена в слюнных железах. Появление ами¬
лоида у части больных становится закономерным результатом лимфопролифе-
рации. Как показано Е.А. Коган, Б.М. Корневым и Е.Н. Поповой, отложения
белковых масс при ЛИП могут носить псевдоамилоидный характер (на самом
деле они представляют собой им\іуноглобулиньі, вырабатываемые плазмоци-
тами). Патофизиология образования кист не вполне ясна — предполагают, что
перибронхиолярная инфильтрация приводит к частичной обструкции бронхи¬
ол с формированием клапанного эффекта (симптом воздушной ловушки); во
всяком случае клеточной инфильтрации в стенках кист не находили.В табл. 3.1 суммированы основные рентгенологические признаки различ¬
ных морфологических вариантов интерстициального поражения легких при
диффузных заболеваниях соединительной ткани. Поскольку клинически не
всегда удается отделить лишь острые варианты от хронических, для точной диа¬
гностики того или иного варианта пневмонита данная таблица весьма актуаль¬
на. В частности, из нее видно, что те кисты, которые были вьывлены у нашего
Глава 3. Необычный вариант поражения легких,..63Клинико-рентгенологические формы поражения легких при СКВТаблица 3:2Форма поражения легкихЧастотаПлеврит25%Острый люпус-пне вменит (острое альвеолярное повреждение, диффузная
альвеолярная геморрагия, десквамативная интерстициальная, организую¬
щаяся пневмони>1, лимфоцитарный интерстициальный пневмонит)1,3%Хронический интерстициальный пневмонит (неспеиифическая, реже
обычная интерститщатьная пневмония, лимфоцитарный интерстициаль¬
ный пневмонит)),9%ОблитерирующиЙ бронхиолит (крайне редко — с амилоидозом)Высокое стояние диафрагмы (диафрагматит, спайки)Дисковидные ателектазыФиброзв рамках антифосфолиііидного синдрома;
тромбоэмболии (тромбозы) лешчных артерий;
микрососудистые тромбозы;
легочная гипертензия;
диффузная альвеолярная і-еморрагия;
респираторный дисіресс-синдром взрослых1,9%•>15,3%1,9%??Банальная инфекция19,1%Туберкулезбольного в сочетании с изменениями по типу «матового стекла», принципиаль¬
но могут встречаться только при лимфоцитарном интерстициальном пневмо¬
ните и десквамативной интерстициальной пневмонии, но для десквамативной
интерстициальной пневмонии кисты гораздо менее характерны, и сам этот
вариант практически не встречается при СКВ. Во всяком слу^ше дескваматив¬
ная пневмония с кистами при СКВ в доступной нам литературе не описана.Остановимся на том, какие клинико-рентгенологические формы пораже¬
ния легких известны при СКВ и какие морфологические вариантьт им соответ¬
ствуют. Надо сказать, что в целом поражение легких длительно (до нескольких
лет!) может быть единственным проявлением болезни; при развернутой карти¬
не болезни легочные симптомы встречаются у 40—90% больных, чаще симме¬
тричны. Наиболее частым поражением дыхательной системы при СКВ являет¬
ся плеврит — обычно двусторонний, с небольшим количеством жидкости, он
нередко подвергается спонтанному рассасыванию с образованием спаек.Поражение легких встречается примерно у трети больных СКВ
{табл. 3.2), при этом смертность в 7 раз выше, чем у больных СКВ без пора¬
жения легких (7 и 1% соответственно). Поражение легких может протекать
в острой форме (так называемый острый люпус-пневмонит): тяжелейшая
одышка, не соответствующая размерам поражения, цианоз, кашель, реже —
кровохарканье; заболевают преимущественно лица до 40 лет. Хотя самому
пожилому пациенту, у которого описано развитие острого волчаночно-
го пневмонита, было 92 года. Недавно было отмечено большое сходство
64 Пульмонологияклинической картины острого люпус-пнсвмонита с ретровирусной ати¬
пичной пневомнией (SARS-синдромом). Примерно у половины больных с
острым люпус-пневмонигом он развивается в самом дебюте заболевания,
может осложняться отеком легких, у больных с антифосфолипидным
синдромом — приводит к развитию дистресс-синдрома (хотя значительно
чаще причиной респираторного дистресс-синдрома становится инфекция);
около трети таких больных нуждаются в искусственной вентиляции легких,
смертность достигает 50% и выше.Рентгенологическая картина напоминает обычную пневмонию (острое аль¬
веолярное повреждение); заболевание протекает лабильно, быстро распростра¬
няется, имеет блуждающий характер. Нередко развивается диффузная альвео¬
лярная геморрагия (преобладают мелкие кровотечения, которые бывает трудно
диагностировать), и гораздо реже при остром люпус-пневмоните выявляются
десквамативная интерстициальная пневмония, организующаяся пневмония
И.Ш лимфоцитарный интерстициальный пневмонит.В нашем случае одышка нарастаїа в течение месяца, не было блуждающих
легочных инфильтратов, кровохарканья (необязательного, впрочем) и призна¬
ков отека легкоі'о, которые отличают острый люпус-пневмонит.Хронический интерстициальный пневмонит вообще мало характерен для
СКВ; он может развиваться из острого люпус-пнсвмонита, либо сам со време¬
нем разворачивается в острый пневмонит. Клинически проявляется одышкой,
катітлсм с трудноотделяемой мокротой, плевральными болями, скудными
сухими и влсіжньїми хрипами, усилением легочного рисунка и фиброзом
базальных отделов. Болеют также преи\іуіцественно лица до 40 лет. Гомоі енное
помутнение средних и базальных отделов легких по типу «матового стекла»
характерно для ранних с гадий и отражает отек интерстиция вследствие повы¬
шенной сосудистой проницаемости. Гистологической основой хронического
люп>'с-гшевмонита является чаще всего неспецифическая, реже обычная или
лимфоцитарная интерстициальная пневмония. На поздних стадиях выявляется
умеренный фиброз с сетчатым рисунком.Развитие обстрл^ивных поражений дыхательных путей (облитерирующего
бронхиолита) при волчанке возможно, но мало характерно. В единичных слу¬
чаях при облитерирующем бронхиолите у пациентов с СКВ находили в ткани
легкого амилоид. Рентгенологически (без клинических проявлений) могут
обнаруживаться дисковидные ателектазы, высокое стояние диафрагмы (вслед¬
ствие диафрагматита и образования плевральных спаек). При этом иннерва¬
ция остается сохранной. В результате развиваются ателектаз и фиброз легкого
на пораженной стороне — синдром «сморщенного легкого» с развитием значи-
тельнь(х нарушений по рестриктивному типу.Особая группа легочных осложнений связана с налившем антител к фосфо¬
липидам — у таких больных возможно развитие тромбозов легочных артерий,
в том числе мелких, легочной гипертензии (вообще не характерной для СКВ),
диффузной альвеолярной геморрагии. Неспецифическая инфекция присоеди¬
няется чаще всего на фоне иммуносупрессии; наиболее серьезным вариантом
является развитие стероидного туберкулеза.
Глава <3. Необычный вариант поражения легких,,. 65При анализе клинической картины СКВ более чем у 500 больных установ¬
лена частота развития различных легочных проявлений: плеврит встретился
у 25% больных, острый люпус-пневмоннт (с инфильтратами в нижних долях)
без летальных исходов — у 1,3%, диффузная легочная геморрагия — почти в
2%, причем летальность составила 66% (по литературным данным, она коле¬
блется в пределах 50—60% и во многом обусловлена вторичной инфекцией),
тромбоэмболии — гакже примерно у 2%, хронический интерстициальный
пневмонит— у 6%. После плеврита наиболее частыми легочньши проявле¬
ниями оказались легочная гипертензия (около 15% больных) и различные
инфекпии (19%).Лимфоцитарный интерстициальный пневмонит впервые описан в 1966 г.
Первое сообщение о возможности образования множественных кист при лим¬
фоцитарном интерстициальном пневмоните было сделано в 1994 г. Несмотря
на то, что морфологически это состояние удается достаточно четко отграни¬
чить от других вариантов интерстициального поражения легких и клинически
лимфоцитарный интерстициальный пневмонит имеет довольно характерные
проявления (кашель, одышка, похудание, слабость), идиопатическая лимфо-
цитарная пнеВіМОния как самостоятельный клинический случай встречается
редко (нам встретилось описание лишь у больного с двусторонней транс¬
плантацией легких). Иногда лимфоцитарный интерстициальный пневмонит
описывают как вариант поражения легких при собственно интерстициальных
болезнях легких: саркоидозе, альвеолярном микролигиазе и, особенно часто,
экзогенном аллергическом, или, как его называют теперь, гиперсенситивном,
пневмоните — примерно в 20% случаев у таких больных выявляются мелкие
кисты в легких (что является проявлением именно лимфоцитарного пневмо-
нита). Но чаще он встречается как легочное проявление внелегочных и систем¬
ных болезней (табл. 3.3).Уже бьию сказано о том, что из фуппы диффузіїьіх заболеваний соеди¬
нительной ткани лимфоцитарный интерстициальный пневмонит чаще всего
выявляется при синдроме Шегрена — зти случаи составляют до трети всех
слу^іаев лимфоцитарного интерстициального пневмонита среди взрослых.
При этом частота развития лимфоцитарного интерстициального пневмонита
у больных с синдромом Шегрена составляет всего около 1% — можно судить,
насколько редким состоянием является сам лимфоцитарный интерстицихіь-
ный пневмонит. Характер лимфоплазмоцитарной инфильтрации в легких при
этом очень сходен с инфильтрацией экзокринных желез в рамках сиіідрома
Шегрена, т.е. лимфоцитарный интерстициальный пневмонит можно рассма¬
тривать как проявление более распространенной формы болезни Шегрена.
Описано сочетание синдрома Шегрена с лимфогщтарным интерстициальным
пневмонитом, на фоне которого в легких выявлены типичные саркоидные
гранулемы без казеоза. При ревматоидном ар ірите лимфоцитарный іінтерсти-
ииальный пневмонит встречается реже, и чрезвычайно редко он описывается
в рамках СКВ без признаков сухого синдрома. Имеется также описание лим¬
фоцитарного интерстициатьного пневмоііита при ювенильном рев.м:атоидном
артрите.
66ПульмонологияТаблица 3.3Этиология лимфоцитарного интерстициального пневмоиитаГ)}улпа заболеваний, при которых встречается
ЛИПЗаболевания, при которых встречается
ЛИПЛимфоцитарный интерстициальный пневмо¬
нит в рамках других интерстициальных болез¬
ней легкихГиперсенситивный пневмонит (экзо¬
генный аллергический альвеолит)
СаркоидозАльвеолярный микролитиазДиффузные заболевания соединительной
тканиСиндром Шегрена
Ревматоидіїьтй артрит
Системная красная волчанкаЛимфопролиферативные заболеванияПсевдолимфома
Болезнь Кастельмана
Лимфомы легкого
Внелегочные лимфомы (ходжкин-
ские и неходжкинские)Болезнь Вальдетістрема, другие пара¬
протеинемииГипогаммаглобулинемии (врожден¬
ные и приобретенные)АмилоидозВирусная инфекцияВИЧ-инфекция (диффузный
инфильтративный лимфоцитоз)
Вирус Эпштейна-Барр
HTLV-1Цитомегаловируе?Эндокринные заболевания имм>’нного харак¬
тераАутоиммунный тиреоидит
МиастенияПернициозная (В,^ — дефицитная) анемияАутоиммунные заболевания печениАутоиммунный гепатит
Первичный билиарный ииррозЛекарственное поражениеФлекаинидРеакция отторжения трансплантатттаТраттсплантаиия костіюго мозга,
легкихНа втором месте по частоте причин лимфоцитарного интерстициаль¬
ного пнсвмонита стоят различные лимфопролиферативные заболевания:
псевдолимфома (болезнь Кастельмана), лимфомы легочной и внелегоч-
ной локализации, различные парапротеинемии, гипотаммаглобулинемии,
а также амилоидоз, представляющий собой результат патологической
трансформации плазмоцитов, которые начинают синтезировать аномаль¬
ный белок амилоид. Кальцинированные отложения амилоида иногда
находят и при лимфоцитарном интерстициальном пневмоните у больных
с синдромом Шегрена. Лимфоцитарный интерстициальный пневмонит
рассматривают как первый этап лимфопролифераиии (ее доброкаче¬
ственный вариант). При проведении дифференциального диагноза между
Глава 3. Необычный вариант поражения легких.., 67лимфоцитарным интерстициальным пневмонитом и злокачественными
лимфомами выявление кист в легких играет очень большое значение:
при лимфоцитарном интерстициальном пневмоните они встречаются
очень часто (82%), а при лимфомах — очень редко (2%). У пациентов с
лимфомами, напротив, значительно чаще обнаруживают крупные (боль¬
ше 1 см) узелки и участки консолидации в легких. Однако окончательно
удостовериться в отсутствии малигнизации при лимфоцитарном интер¬
стициальном пневмоните можно только с помощью биопсии, при болезни
Вальденстрема описаны случаи дебюта заболевания в виде лимфоцитарно¬
го интерстициального пневмонита, и лишь через несколько лет развива¬
лась типичная картина заболевания.Третьей по значимости причиной лимфоцитарного интерстициального
пневмонита является ВИЧ-инфекция (у детей она выходит на первое место).
Инфильтрацию ткани слюнных желез, легких, почек, щитовидной железы
и желудочно-кишечного тракта Т-лимфоцитами (CD-8) при ВИЧ называют
синдромом диффузного инфильтративного лимфоцитоза (D1LS), который
отличается от синдрома Шегрена большим спектром органных поражений и
меньшей вовлеченностью слюнных желез. На фоне активной противовирус¬
ной терапии частота выявления DILS достоверно снижается. Картина лим¬
фоцитарного интерстициального пневмонита может быть настолько сходна
с пневмоцистной пневмонией, что для дифференциального диагноза требу¬
ется проведение биопсии. Именно в случае ВИЧ-инфицированных наиболее
активно обсуждается роль вирусной инфекции в этиопатогенезе лимфоци¬
тарного интерстициального пневмонита; показано высокое содержание ДНК
вируса Эпштейна—Барр в легких у таких больнььх. Описано развитие лимфо¬
цитарного интерстициального пневмонита у больных с инфекцией вирусом
Эпштейна-Барр и без ВИЧ, а также у лиц, инфицированных человеческим
Т-лимфотропным вирусом HTLV-1, у которых одновременно может развивать¬
ся и типичный синдром Шегрена. Имеется также описание случая цитомегало-
вирусного пневмонита у больной СКВ, причем рентгенологически выявлялись
множественные полости в легких (морфологическое исследование у данного
больного не проводилось, но можно предполагать, что речь идет именно о
лимфоцитарном интерстициальном пневмоните).Реже поражение легких по типу лимфоцитарного интерстициального пнев¬
монита описывают при различных аутоиммунных болезнях, например при
аутоиммунном тиреоидите. При хроническом активном гепатите (преиму¬
щественно аутоиммунном) или первичном билиарном циррозе лимфоцитар¬
ный интерстициальный пневмонит развивается как результат генерализации
иммунного процесса.От момента появления симптомов до постановки диагноза лимфоцитарного
интерстициального пневмонита (что требует, как правило, биопсии легкого)
проходит в среднем 2 года, и не всегда сразу удается установить, в рамках како¬
го заболевания развился лимфоцитарный интерстициальный пневмонит. Чаще
всего в подобных случаях речь идет о лимфопролиферативных заболеваниях,
отчетливые признаки которых проявляются позднее.
6S ПульмонологияНам удалось найти 6 случаев лимфоцитарного интерстициального пневмо-
нита при системной красной волчанке: в двух из них у больных с СКВ диагно¬
стирован также синдром Шсгрена; диагноз ЛИП поставлен морфологически;
лишь в одном случае из 6 лимфоцитарный интерстициальный пневмонит
проявлялся множественными кистами на КТ легких — именно это описание
и позволило нам расценить выявленные при КТ легких кисты как проявление
лимфоцитарного интерстициального пневмонита в рамках СКВ. В двух случа¬
ях в ткани легкого был выявлен вирусный геном (вирусы герпеса, Эпштейна-
Барр).Описан случай спонтанного пневмоторакса у больной с высокой активно¬
стью волчанки, которому предшествовало поражение легких по типу интерсти-
циа^іьного пневмонита и легочных геморрагий, однако о характере пневмонита
и наличии легочных кист не сообщается. В другом случае у женщины 21 года
развился острый интерстициальный пневмонит с множественными «балло¬
нами» на рентгенограммах; морфологическое исследование не провоїщлось,
через 2 мес больная погибла от выраженного легочного фиброза.Необходимо сказать несколько слов о том, какое место лимфоцитарный
интерстициальный нневмонит занимает в структуре лимфопролифератив-
ных заболеваний с вовлечением легочной паренхимы. Лимфоциты, которые
инфильтрируют легочный интерстиций при иневмоните, имеют в значитель¬
ной степени леїочное происхождение; они в норме содержатся в бронхо¬
ассоциированной лимфоидной ткани, которую сокращенно называют БАЛТ.
Поэтому лимфоцитарный интерстициальный пневмонит рассматривают не
только как аутоиммунное поражение легких, но и как определенную степень
активации собственной иммунной системы легких в ответ на какой-либо фак¬
тор. При 1-й степени активации БАЛТ (фоллику^лярная лимфоидная гипер¬
плазия) формируется плазмоцитарная гранулема. Датсе развивается узловая
гиперплазия БАЛТ (псевдолимфома), затем — лимфоцитарный интерстици¬
альный пневмонит, который представляет собой множественную, мультифо¬
кальную лимфоидную гиперплазию БАЛТ; лимфопролиферативные синдромы
после трансплантации включают не только лимфоцитарный интерстициаль¬
ный пневмонит, но и более выраженную пролиферацию; наконец, могут раз¬
виваться лимфоматоидный гранулематоз (процесс с внутрисосудистым рас¬
пространением, в этиологии которого доказана роль вируса Эпштейна—Барр) и
собственно бронхогенная лимфома. Включенностью лимфоцитарного интер¬
стициального пневмонита в этот ряд обусловлена возможность его прогресси¬
рования в бронхогенн>то лимфолїу.Нам каза.'1ось целесообразным представить определенный алгоритм,
согласно которому клиницист может поставить диагноз лимфоцитарного
интерстициального пневмонита (при каком бы заболевании он ни был запо¬
дозрен) (рис. 3.^. Относительно неспецифические клинические признаки
(кашель, одышка, общая слабость, рестриктивно-обструктивные изменения
по данным ФВД) и отсутствие специфичных изменений при рентгеногра¬
фии становятся основанием для проведения КТ органов грудной клетки.
Если при этом выявляется сочетание симптомов, в определенной степени
Глава З, Необычный вариант поражения легких...69Рис. 3.8. Алгоритм диагностики лимфоцитарной интерстидиалт.ной пневмонииспецифичное для лимфоиитарного интерстиииальлого пнсвмонита («мато¬
вое стекло», узелки, кисты), то дальнейший диагностический поиск зави¬
сит от того, какое заболевание подозревается (или уже диагностировано)
у данного больного. Если есть основания подозревать заболевание, кото¬
рым может сопровождаться лимфоцитарный интерстициальный пневмонит,
необходимо целенаправленно подтверждать или исключать именно этот
вариант интерстициального поражения легких. При наличии на КТ легких
кист в первую очередь необходимо провести дифференциальный диагноз с
десквамативной интерстициальной пневмонией, а также с другими причи¬
нами кист. При отсутствии кист ситуация и проще, и сложнее: необходимо
дифференцировать лимфоцитарный интерстициа.1ьный пневмонит с дру¬
гими вариантами интерстициальной пневмонии. С этой целью может быть
использован бронхоальвеолярный лаваж, но методом верификации диагноза
остается биопсия легкого.Больших исследований по лечению и исходам лимфоцитарного интерсти¬
циального пневмонита нет, что связано с редкостью и полиэтиологичностью
этого состояния. Однако в целом сообщается об эффективности высоких
(реже — средних) доз кортикостероидов (в сравнении, например, с таким
морфологическим вариантом, как обычная интерстициа^іьная пневмония).
Кортикостероиды являются препаратами выбора. В случаях их неэффектив¬
ности с успехом используются и цитостатики (состояние требует активной
иммуносутірессивной терапии), Имеются единичные сообщения об успешном
применении в/в вливаний гамма-глобулина, плазмафереза.
70 ПульмонологияРентгенологические признаки лимфоцитарного интерстициального пнев-
монита могут почти полностью регрессировать, трансформироваться в фиброз
либо оставаться неизменными на фоне клинического улучшения. Описаны
прогрессирование лимфоцитарного интерстициального пневмонита (при син¬
дроме Шегрена) в злокачественную лимфому, а также развитие аденокарцино¬
мы легкого на фоне лимфоцитарного интерстициального пневмонита. Оценить
летальность именно от лимфоцитарного интерстициального пневмонита очень
сложно: сообщается о смертности 25% при диффузном инфи^іьтративном лим¬
фоцитарном синдроме (у больных с ВИЧ и другими вирусными инфекциями),
при других вариантах лимфоцитарного интерстициального пневмонита четких
данных нет.В нашем слу^іае стремление к постановке точного «легочного» диагноза
диктовалось в первую очередь необходимостью объяснить необычную выра¬
женность одышки, причем удалось это сделать в рамках СКВ.Комментарий Н.В. Петуховой — заведующей лечебно-диагностическим отделе¬
нием Центра суставной боли Первого МГМУ им. И. М. СеченоваВ данном слу^ше можно выделить несколько особенностей. Это мужская
волчанка, которая, как известно, встречается существенно реже (соотно¬
шение женщин и мужчин у взрослых 9:1, но у детей лишь 2:1) и протекает
тяжелее, что мы и видим в нашем слу^іае. Поражение легких действительно
очень необычно. Нам приходилось видеть такую одышку при СКВ, но
это были фактически терминальные больные с поражением всех органов
и систем, на вскрытии у них находили почти все описанные варианты
поражения легких: и респираторный дистресс-синдром на фоне массив¬
ной инфекции, и тромбоэмболии, и альвеолярную геморрагию. В данном
случае это был как будто сохранный молодой человек, который так тяже¬
ло задыхался. Нас не оставляли опасения, что мы имеем дело в первую
очередь с тяжелой неспецифической инфекцией; опыт одновременного
назначения кортикостероидов и антибиотиков у таких больных обычно
оказывается успешным. На сегодняшний день тяжесть состояния больного
определяет уже нефрит. Идея проведения биопсии почки кажется очень
своевременной — важно не столько определение морфологического вари¬
анта гломерулонефрита, сколько соотношение процессов воспаления и
фиброза. При выраженном фиброзе высокие дозы цитостатиков не должны
применяться.Нефрит может длительное время протекать латентно. Но мы надеемся, что
в данном случае давность его все же не так велика и в биоптатах фиброз не
будет преобладать над воспалением, т.е. сохраняется мишень для воздей¬
ствия иммуносупрессивной терапии. Еще необходимо сказать о том, что
диафрагматит при волчанке — это не миф. Мы наблюдали молодую боль¬
ную, у которой в результате диафрагматита диафрагма справа поднималась
до уровня 3-4-го ребра (рентгенологически), в результате стероидной тера¬
пии диафрагма опустилась и ушла одышка.
Глава З, Необычный вариант поражения легких... 71Комментарий С.И. Овчаренко — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукХочется сказать о том, что сейчас, при наличии компьютерных баз данных,
реальным стал такой поиск сходных случаев, который был проведен по поводу
данного больного, и это действительно помогло поставить диагноз по анато-
гии с очень редким описанием лимфоцитарного интерстициального пневмо-
нига с кистами у больной СКВ. Что касается использования бронхоальвео¬
лярного лавіїжа, то он дает лишь картину лимфоцитоза, которая совершенно
неспеїхифична тя лимфощггарного интерстициального шіевмонита, поэтому
действительно методом диагностики яатяется (не в этом конкретном случае)
биопсия легкого. А вьщеление описанных морфологических вариантов интер¬
стициального поражения легких имеет клинический смысл — мы по-разному
относимся к десквамативной пневмонии, организующейся пневмонии и т.д.ЛИТЕРАТУРАБегларян Л.Г., Потекаева М.А. В кн.; Коллагеновыс болезни и ревматизм. —
М., 1962.-С. 45.Коган Е.Л., Попова Е.Н., Секамова С,М., Корнев Б.М. Природапсевдоамилоидных
масс при лимфоцитарном пневмоните //Архив патологии. — 1995, 57(4):84—86.Нестеров Л.И,, Сигидин Я.А. Клиника колотагеновых болезней. — М.;
Мединина, 1966. — 482 с.Парсонз П.Э., Хеффнер Д.Э. Секреты пульмонологии / Под ред.О.Ф. Колодкиной. — М.; МЕДпресс-информ, 2004. — 647 с.Ahamed М. F., Giampitri Е.А., Л1 ShamyA. Pulmonary amyloidosis in a patient with
lymphocytic interstitial pneumonia // Aim Saudi Med. 2007; 27(l):40-44.Basu D., Williams F.M., Ahn C. W,, Reveille J.D. Changing spectrum of the diffuse
infiltrative lymphocytosis syndrome // Arthritis Rheum. 2006; 55(3):466-472.Benisch B., Peison B. The association of lymphocytic interstitiall pneumonia and
systemic lupus erythematosus, // Mt Sinai J. Med. 1979; 46: 398—401.Berentsen s., MykingA.O., Andreassen AH. [Pulmonary changes as primary mani¬
festations in Waldenstrom macroglobulinemia] [Article in Norwegian] j j Tidsskr Nor
Laegeforen. 1997;117(9):1270-1271.Carrington C.B., Liebow A.A. Lymphocytic interstial pneumonitis // Am. J. Path.
1966; 48: 36a.Filipek M.S., Thompson M.E., Wang P.L. etai Lymphocytic interstitial pneumoni¬
tis in a patient with systemic lupus erythematosus: radiographic and high-resolution
CTfmdings //J. Thorac. Imaging. 2004;19(3):200-203.Fishback N., Koss M. Update on lymphoid interstitial pneumonitis 11 Curr. Opin.
Puhn Med. 1996; 2(5):429-433.Hayasaka S., Fujino N., Yoshinaga T. et al. [Primary Sjogren’s syndrome with
lymphocytic interstitial pneumonia and pulmonary multiple cystic lesions] [Article in
Japanese] Nihon Kokyuki Gakkai Zasshi. 1999; 37(10):802—806.
72 ПульмонологияHonda О., Johkoh Т., Ichikado К. et ai Differential diagnosis of lymphocytic
interstitial pneumonia and malignant lymphoma on high-resolution CT j IAJR. Am,
J. Roentgenol. 1999; 173(l):71-74.Ichikawa Y., Kinoshita М., Koga T. et al Lung cyst formation in lymphocytic
interstitial pneumonia: CT features // J. Comput. Assist. Tomogr. 1994; 18(5):745-
748.Ikeda K., Ishibashi Г., Noji H. et al. A 92-ycar-old man with systemic lupus erythe¬
matosus who developed acute lupus pneumonitis // J. Rheumatol. 2000; 27(1):234-
237.Imaging. European respiratoiy monograph. \bl. 9, Monograph 30, Dec 2004/ Ed.
by A. Bankier, P. A. Gevenois. P. 176-194.Interstitial lung disease. European respiratory monograph. Vol. 5, Monograph 14,
Aug 2000/ Ed. by D.Olivieri and R.M. du Bois.Itescu S. Diffuse infiltrative lymphocytosis syndrome in children and adults infect¬
ed with HIV-1: a model of rheumatic illness caused by acquired viral infection // Am.
J. Reprod. Immunol. 1992; 28(3-4):247-250.Kamholz S., Sher A., Bartand P. et al. Sjogren’s syndrome: severe upper airways
obstruction due to primary malignant tracheal lymphoma developing during suc¬
cessful treatment of lymphocytic interstitial pneumonitis // J. Rheumatol. 1987;
14(3):588-594.Kerbourc’h J.F., Cledes J., Garre M. et al. [Fatal acute pncumonopathies in dis¬
seminated lupus erythematosus] [Article in French] 11 Rev. Pneumol. Clin. 1988;
44(1):6-13.Khardori R., Eagleton L.E., Soler N.G. et al. Lymphocytic interstitial pneumonitis
in autoimmune thyroid disease //Am. J, Med. 1991; 90(5):649-652.Koss M.N. Pulmonary lymphoid disorders // Semin. Diagn. Pathol. 1995;
12(2):158-171.Koulaouzidis A., Karagiamidis A., Prados S. et al. Lymphocytic interstitial pneu¬
monitis (LlP)-the liver and the lung // Ann. Hepatol. 2006; 5(3): 170-171.Lois М., Roman J,, Holland Ж, Agudelo C. Coexisting Sjogren's syndrome and
sarcoidosis in the lung j j Semin. Arthritis. Rheum. 1998; 28(l):31-40.Marenco J. L., Sanchez-Burson J., Ruiz Campos / etat. Pulmonary amyloidosis and
unusual lung involvement in SLE // Clin. Rheumatol. 1994; 13(3):525-527.Min J.K., Hong Y.S., Park S.H. et al. Bronchiohtis obliterans organizing pneu¬
monia as an initial manifestation in patients with systemic lupus erythematosus //
J. Rheumatol. 1997; 24(ll):2254-2257.Mok C.C., Ying K.Y. Lupus pneumonitis or severe acute respiratory syndrome? //
Lupus. 2004;13(7):549-553.Najjar М., SiddiquiA.K., RossoffL., Cohen R.L Cavitary'lung masses in SLE patients:
an unusual manifestation of CMVinfection// Eur. Respir J. 2004; 24(l):182-184.Nishizaka Y., Oda Y. [A ca.se of systemic lupus erjthematosus associated with
Sjogren’s syndrome diagnosed by lung localization] [Article in Japanese] // Nihon.
Kyobu Shikkan Gakkai Zasshi. 1992; 30(4):689-694.Okada F., Ando Y., Yoshttake S. et at. Pulmonary CT findings in 320 carriers of
human T-lymphotropic virus type 1 // Radiology 2006; 240(2):559—564.
Глава 3. Необычный вариант поражения легких... 73Ratjen F.A., Schoenfelcl В., Wiesemann H.G. Pulmonary alveolar microlithiasis
and lymphocytic interstitial pneumonitis in a ten year old girl // Eur. Respir. J, 1992;
5(10):I283-1285.Shen М., Wang K, Xu W.B, et al. [Pleuropulmonary manifestations of sys¬
temic lupus erythematosus] [Article in Chinese] Zhonghua Yi Xue Za Zhi. 2005;
85(4S):3392-3395.Silva C.L, ChurgA., Muller N.L. Hypersensitivity pneumonitis: spectrum of high-
rcsolution CT and pathologic findings //AJR. Am. J. Roentgenol. 2007; 188(2);334-
344.Silva C.L, Flint J.D., Levy R.D., Muller N.L. Diffuse lung cysts in lymphoid inter¬
stitial pneumonia; high-resolution CT and pathologic findings // J. Thorac. Imaging.
2006; 21(3):24l-244.Tokuyasu H., Watanabe E., Okazaki R. et al. Sjogren’s Syndrome with Multiple
Bullae Caused by Lymphocytic Interstitial Pneumonia. Lung. 2007; 185(3): 187-188.Totani.Y, Demura Y., Atneshima S. et al. [A case of lymphocytic interstitial pneu¬
monia with Sjogren’s syndrome and systemic lupus erythematosus in which human
herpes virus-6 infection was the suspected pathogen] [Article in Japanese] // Nihon
Kokyiiki Gakkai Zasshi. 2001; 39(10):763~769.Uziel Y., Hen B., Cordoba M, Wolach B. Lymphocytic interstitial pneumonitis
preceding polyarticular juvenile rheumatoid arthritis // Clin. Exp. Rheumatol. 1998;
16(5):617-619.Yen J.H., Tsai W.C., Ou T.T. et al. Systemic lupus erythematosus complicated by
recurrent spontaneous pneumothorax — a case report // Kaohsiung. J. Med. Sci.
2001; 17(10):540-544.Yood R.A., Steigman DM,, Gill L.R. Lymphocytic interstitial pneumonitis in a
patient with systemic lupus erythematosus // Lupus, 1995; 4(2); 161-І63.Yum H.K, Kim E.S., Ok K.S. et al. Lymphocytic interstitial pneumonitis associated
with Epstein—Barr virus in Systemic Lupus Erythematosus and Sjogren’s Syndrome.
Complete remission with corticosteriod and cyclophosphamide // Korean J. Intern,
Med. 2002; 17(3); 198-203.
Глава 4ЛИМФАНГИОЛЕЙОМИОМАТОЗ: КЛИНИЧЕСКАЯ,
ИНСТРУМЕНТАЛЬНАЯ, МОРФОЛОГИЧЕСКАЯ
ДИАГНОСТИКА, ПОДХОДЫ К ЛЕЧЕНИЮС.И. Овчаренко, ЕА. СонПродолжая тему необычных, в частности «кистозных», иорсіжений легких,
выявление которых стало возможным благодаря применению компьютерной
томографии высокого разрешения, мы представляем случай тяжелого диф¬
фузного поражения легких со своеобразным патогенезом — лимфангиолейо-
миоматоза, который манифестировал постепенно нараставшей одышкой и в
течение длительного времени расценивался как хронический обструктивный
бронхит; отсутствие факторов риска бронхита в сочетании с резко выраженной
бронхиальной обструкцией и характерными изменениями на рентгенограммах
легких стали основанием для проведения КТ; диагноз лимфангиолейомиомато-
за бьш подтвержден морфологически. Подробно обсуждаются вопросы этиоло¬
гии, патогенеза, диагностики и лечения этого не столь уж редкого заболевания,
в финальной стадии которого помочь может только трансплантация легких.Больная Г., 62 лет, поступила в терапевтическое отделение Факультетской
терапевтической клиники им. В.Н. Виноградова 18.03.2008 г. с жалобами на
одышку при физической нагрузке, периодически возникающее ощущение
затрудненного дыхания, что сопровождается учащенным сердцебиением.Из семейного анамнеза: мать у\терла в преклонном возрасте, страда^ша артери-
aju>Hoft гипертензией; об отце данных нет; сын 33 лет — здоров. Анамнез жизни:
патщснтка в детстве росла и развивалась нормально, имеет высшее образова¬
ние, инженер-металлург, профессиональных вредностей не было. С 2002 г. по
настоящее время работает бухгалтером. Курила в 1965-1971 гг. по 1-2 сигареты
вдень (ИКЧ — 0,3-0,6 пачка/лет). Менопауза с 50 лет. В 1980 г. диагностирован
полип шейки матки, в 1982 г проведено оперативное лечение по этому поводу;
наблюдается у гинеколога, последний осмогр в 2007 г. В 1971, 1978 гг. — секто¬
ральная резекция по поводу фиброаденомы левой молочной железы. На при¬
менение цефтриаксона отмечала развитие крапивницы.Анамнез заболевания {рис. 4.1): с 2000 г. обратила внимание на появление
умеренно выраженной одышки при физической нагрузке, которая к 2005 г.
стала носить более выраженный характер. На фоне простудных заболеваний
(1-2 раза в год) отмечала появление кашля с отделением мокроты зеленовато¬
го цвета, что сопровождалось повышением температуры тела до 37,1 “С. Редко
прибегала к приему антибиотиков, их прием был эффективным.В 2005 г, проводилось амбулаторное обследование, по результатам которого
был поставлен диагноз хронического бронхита, рекомендовано применение
Глава 4. Лимфангиолейомиоматоз: клиническая, инструментальная...75Жалобы2000 г.2005 г.2006 г.2008 г.январь февральМарт
2008 г.ОдышкаПовышениетемпературытелаПокашлива¬ниеДиагнозХроническийбронхитЛечениеДАИ(название не
помнит)Хроническийобструк-тивныйбронхитФорадил
12 мкг 2 р/д,
беклазон2 р/д (дози¬
ровку не
помнит),
теопек37,2-fОРВИ,пневмо-ния(?)Цефтри-аксонХОБЛСеретид
25/250
мкг/д 2 р/дГОспитАЛи3АцияРис. 4.1. Анамнез больной Г., 62 годадозированного ингалятора, название которого больная не помнит. Применение
в течение месяца дозированного ингалятора не улучшило самочувствия, само¬
стоятельно прекратила им пользоваться. В 2006 г. в связи с сохраняющейся
одышкой повторно обратилась к пульмонологу в другое лечебное учреждение,
где состояние также трактуется как хронический обструктивний бронхит. По
рекомендации врача начала прием теопека, ингаляции форадила в сочетании
с беклазоном 2 раза в день (дозу препаратов не знает), что также принципи¬
ально не изменило самочувствия, а в дальнейшем отметила появление ночных
судорог после ингаляции форадила и тошноту, которую пациентка связывает с
приемом беклазона, в связи с чем препараты были отменены.Ухудшение самочувствия с января 2008 г, когда на фоне ОРВИ отметила
усиление одьішгаї, субфебрильную температуру тела. Учасжовьш врачом не
исключалась пневмония. Проводилась терапия цефтриаксоном по 1 г 2 раза в
день в/м Б течение 10 дней, на фоне чего появилась крапивница. Температура
т«ла нормализовалась, при проведении рентгенологического исследования
легких инфильтративных изменений не выявлено, клинический анализ крови
в пределах нормы, но сохранялась одышка при физической нагрузке. В февра¬
ле 2008 г. рекомендован прием серетида 2 раза в день, самочувствие несколько
улучшилось. Госпитализирована в Факультетскую терапевтическую клинику им.
В.Н. Виноградова с вышеуказанными жалобами для обследования и лечения.При осмотре состояние относительно удовлетворительное. Рост 173 см, вес
63 кг. Кожные покровы обычной окраски и влажности. Обе половины грудной
76Пульмонологияклетки в акте дыхания участвуют равномерно. Пальпация грудной клетки без¬
болезненна, Голосовое дрожание не изменено. В легких хрипы не выслушива¬
ются, ЧД 16 в минуту. Тоны сердца ритмичные, ЧСС 72 уд/мин, АД І25 и 80 мм
рт.ст. Живот мягкий, безболезненный при пальпации, печень и селезенка не
увеличены. Щитовидная железа пальпаторно не увеличена. Неврологический
статус без особенностей.В клиническом анализе крови без отклонений от нормы: НЬ 137,3 г/л, эритро¬
циты 4,5 млн, ЦП 0,92; лейкоциты 4,7 тыс., нейтрофилы 44,9%, лимфоциты
44,7%, моноциты 7,9%, эозинофилы 1,9%, базофилы 0,5%, СОЭ 4 мм/ч, тром¬
боциты — 266 тыс.В биохимическом анализе крови также без отклонений от нормы.Диспротеинемии не выявлено, СРБ 0,1 мг/дл (норма 0-0,8), антитела к
ВИЧ не обнаружены, реакция Вассермана отрицательная. Маркеры вирусов
гепатита В и С не выявлены.В обшем анализе мочи и кала без изменений.На ЭКГ {рис. 4.2) ритм синусовый, признаков гипертрофии желудочков нет,
определяется Р «pulmonale» во II и в III стандартных отведениях.У больной, имеющей индекс Kj-pnmero человека 0,3—0,6 пачка/лет и с
1975 г. не курящей, не имеющей профессиональных вредностей, при отсут¬
ствии аускультативных признаков бронхообструкции, по результатам оценки
ФВД бьыи определены выраженные обструктивные нарушения на всех уров¬
нях бронхиального дерева с резким нарушением модифицированного индек¬
са Тифно (36%), с небольшой положительной реакцией на атровент (43%):- ;s«? f S9 SSFrrr^; f r-4 с 1 .ЗЇ W« 40»a 248 S9-» ',Рис. 4.2. Электрокардиогралша больной Г. Скорость записи 25 мм/с. Пояснения в тексте
Глава 4. Лимфангиолейомиоматоз: клиническая, инструментальная... 77ЖЕЛ 81%, ОФВ, 44% (после ингаляции атровента 53%), MOCj^ 20% (25%),
МОС5015% (18%), МОС^з 17% (20%).По данным ЭхоКГ, размеры камер сердца не изменены. МЖП 0,9 см,
ЗС 0,9 см, Піобальная сократительная функция ЛЖ не нарушена, ФВ 58 %.
Диастолическая функция не нарушена: Е/А 1,1. Митральный клапан: систоли¬
ческий прогиб створок до фиброзного кольца, митральной регургитации нет.
Аортальный клапан: умеренное уплотнение створок, аортальной регургитации
нет. Трикуспидальный клапан не изменен, трикуспидальной регургитации нет.
Признаков легочной гипертензии нет. Стенки аорты уплотнены. Жидкости в
полости перикарда нет.При рентгенологическом исследовании легких {рис. 4,3) обраш,ало на себя вни¬
мание значительное диффузное усиление легочного рисунка за счет интерсти¬
циального компонента, в верхних отделах деформация по ячеистому типу. Эти
изменения, а также результаты оценки ФВД послужили основанием для про¬
ведения КТ органов грудной клетки. Получено следуюш;ее заключение: легочная
ткань без свежих очаговььх и инфильтративных изменений. С обеих сторон по
всем легочным по.тям визуализируются множественные тонкостенные кисты
различных размеров до 22,7 мм, практически замещающие .тегочную ткань
{рис. 4.4). Жидкость в плевральных полостях не определяется. Структуры сре¬
достения и корней легких дифференцированы. Признаков лимфоаденопатии
не выявлено. Кальциноз коронарных артерий. Заключение: изменения расце¬
ниваются как признаки лимфангиолейомиоматоза.В связи с тем, что лимфангиолейомиоматоз может быть проявлением дру¬
гого патологического состояния, а именно туберозного склероза, в план обсле¬
дования бьши включены ЭхоКГ с целью исключения рабдомиомы сердца;
УЗИ органов брюшной полости с целью исключения лейомиом забрюшинногоРис. 4.3. Рентгенография органов грудной клетки, прямая и боковая проекции (пояс¬
нения в тексте)
78ПульмонологияРис. 4.4. Компьютерные томограммы органов грудной клетки (пояснения в тексте)пространства, печени; УЗИ малого таза с целью исключения фибромиомы
матки; консультации окулиста, дерматолога.От проведения КТ головного мозга было решено воздержаться ввиду отсут¬
ствия в анамнезе приступов эпилепсии, а также умственной отсталости, что
характерно для туберозного склероза.Кроме этого, учитывая поликистозное поражение легких, в дифференци-
ально-диагностический поиск включали гистиоцитоз X (прогрессирующее
формирование ячеистого легкого с последующим образованием булл и реци¬
дивирующим пневмотораксом, одна из форм заболевания характеризуется
на поздней стадии развития сочетанием эозинофильной гранулемы черепа,
экзофтальма, сахарного диабета). Несмотря на то, что гистиоцитоз встречается
преимущественно у курящих мужчин, нами было проведено рентгенологиче¬
ское исследование костей черепа: деструктивных изменений в костях не выявле¬
но. Турецкое седло в размерах не увеличено: 11x8 мм.Больная осмотрена дерматологом: лицевые ангиофибромы, щагреневые
бляшки, участки гипопигментации, характерные для туберозного склероза, не
выявлены. Консультирована окулистом с целью исключения астроцитарных
гамартом сетчатки — изменений не обнаружено.При рентгенологическом исследовании придаточных пазух носа патологии не
выявлено. При проведении УЗИ органов брюшной полости изменений со сторо¬
ны печени, желчного пузыря, поджелудочной железы, селезенки не выявлено.
Забрюшинные лимфатические узлы не визуализируются. В нижнем полюсе
левой почки обнаружена ангиомиолипома 7 мм в диаметре; справа — интра-
паренхиматозная киста 10x4 мм; чашечно-лоханочная система не расширена;
область надпочечников не изменена.По данным УЗИ малого таза: мочевой пузырь — конт>'ры и стенки не изме¬
нены, содержимое однородное, внутрипросветных образований не вьювлено.
Тело матки отклонено кпереди, имеются эхо-признаки двурогой матки, кон¬
туры матки неровные, миометрий неоднороден за счет наличия нескольких
субсерозных и интерстициальных узлов миомы размером от 10 до 14 мм и каль-
цинатов размером 2-6 мм. Полость матки не деформирована, толщина эндо¬
метрия в двух рогах — до 2,7 мм. Правый яичник 22x12 мм, фолликулярный
аппарат отсутствует, строма аваскулярна. Левый яичник 2бх 12 мм, с единичной
инклюзионной кистой до 3 мм, строма аваскулярна. Скоплений свободной
Глава 4. Лимфангиолейомиоматоз: клиническая, инструментальная... 79жидкости, патологических объемных образований в малом тазу не выявлено.
Заключение: двурогая матка. Миома матки небольших размеров.На основании данных, полученных в процессе обследования, был постав¬
лен предположительный диагноз: лимфангиолейомиоматоз легких (?), диф¬
фузная форма. Киста правой почки. Ангиомиолипома левой почки. Миома
матки малых размеров.В клинике проводилась терапия: беродуал по 2 вд. 3 раза в день, фликсотид
250 мкг по I вд. 2 раза в день с последуюпі;ей отменой, халиксол 30 мг по 1 т.3 раза в день (с последующей отменой препарата), лечебная физкультура.При выписке рекомендовано проведение биопсии легкого для уточнения диа¬
гноза, которая выполнена 11.04.2008 г в Национальном медико-хирургическом
центре им. Н.И. Пирогова профессором Ю.А. Аблицовым. При видеоторако¬
скопии: в плевральной полости выпота нет, спаек нет. Ткань легкого уплот¬
нена, ригидна при инструментальной пальпации. В паренхиме легкого выяв¬
лены множественные воздушные кисты во всех отделах до 2,5 см в диаметре.
Произведена атипичная резекция 5-го и 8-го сегментов легкого.В лаборатории патологшіеской анатомии НИИ пульмонологии дано сле-
дуюшее заключение по гистологическому исследованию: в препаратах ткань
легких с отдельными полостями больших размеров, части^шо выстланных
однорядным эпителием. В стенках части полостей периваскулярно, в стенках
венул, терминальных бронхиол, в висцеральной плевре образования ова-чьной
и неправильной формы в виде узелков, состоящих из пролиферирующих, ино¬
гда дис'грофичньтх миоцитов, при окраске по Ван Гизону — в части узелков
разрастания коллагеновых волокон, в отдельных — фиброзная ткань полно¬
стью замещает пролиферирующие миоциты. Стенки, окружающие эти участки
альвеол, тонкие, обычного строения. В части полостей альвеол скопление
макрофагов и сидерофагов. Стенки мелких сосудов — со слабо выраженной
гипертрофией мышечного слоя, полнокровие сосудов. Иммуногистохимическое
исследование: умеренное положительное окрашивание антителами к НМВ45,
слабоположительная реакция на рецепторы к эстрогену (менее 10% клеток,
слабое окрашивание ядер), отрицательная реакция к прогестерону. Заключение:
лимфангиолейомиоматоз с формированием кистозных полостей и частичным
фиброзом мышечных узелков.Таким образом, морфологическое и иммуногистохимическое исследование
позволило нам утвердиться в диагнозе', лимфaнгиoлeйo^tиoмaтoз, диффузная
форма.Лимфангиолейомиоматоз (ЛАМ) — редкое заболевание с поражением легких
и лимфатической системы, встречающееся почти исключительно у женщин и
развивающееся обычно до наступления менопаузы. Морфологическим марке¬
ром лимфангиолейомиоматоза является обнаружение в іюраженньгх органах
специфических для этого заболевания лимфангиолейомиоматозных клеток.
Морфологическим субстратом болезни является мультифокальная узловая
пролиферация специфических лимфангиолейомиоматозных клеток, преиму¬
щественно располагающаяся по ходу лимфатических сосудов и в лимфатиче¬
ских узлах, сочетающаяся в легких с кистозной перестройкой его паренхимы.
80 ПульмонологияКлиническая картина лимфангиолейомиоматоза складывается из легочных
и внелегочных проявлений. легочным относится прогрессирующая кистозная
перестройка паренхимы легких с развитием рецидивирующих пневмоторак¬
сов, хилезного плеврального выпота и формированием в исходе заболевания
дыхательной недостаточности. Среди внелегочных проявлений болезни наи¬
более часто встречаются лимфоаденопатия, расширенные и утолщенные лим¬
фатические сосуды, образующие целые кистозные конгломераты и поэтому
называемые лимфангиолейомиомами, хилезный асцит и ангиомиолипомы.Выделяются два варианта лимфангиолейомиоматоза — спорадический и соче¬
танный с туберозным склерозом (ТС). Спорадический лимфангиолейомиоматоз
и лимфангиолейомиоматоз, сочетанный с туберозным склерозом (ЛАМ-ТС),
морфо;югически неразличимы. Впервые спорадический лимфангиолейомиома¬
тоз был оииеан в 1937 г. Распространенность спорадического лимфангиолейо¬
миоматоза состашіяет 1-2 случая на 1 млн взрослых женшин или 1 случай на 400
тыс. взрослых женишн. Распространенность же лимфангиолейомиоматоза среди
взрослых женщин, больных туберозным склерозом, составляет 30-40%.іуберозньїй склероз — генетически детерминированное заболевание, наслед>'е-
мое по аутосомно-доминантному типу и относящееся к группе нейроэктодермаль¬
ных нарушений. Учитывая мультисистемность поражений при туберозном скле¬
розе, это заболевание также принято называть туберозно-склерозным комплексом
{tuberoiLs sclerosis complex — TSC). Туберозный склероз, или болезнь Бурневилля—
Прингля— аутосомно-доминантное заболевание, относящееся к факоматозам
(системным наследственным дисплазиям, связаннъгл с нарушением заютадкрт
эктодермального зародышевого листка) и характеризующееся комбинированны¬
ми оп>'холевидными поражениями кожи, головного мозга, глазных яблок, сердца,
почек и легких, кроме туберозного склероза, к группе факоматозов относятся ней-
рофиброматоз, или болезнь Реклингхаузена, синдром Стержа-Всбера и болезнь
Гиппеля—Лнгндау. Учитывая, что распространенность туберозного склероза, по
разным данным, колеблется и составляет от 1 случая на 30 тыс. взрослого насе¬
ления до 1 случая на 150 тыс. взрослого населения, по самым приблизительным
подсчетам лимфангиолейомиоматоз, сочеганный с туберозным склерозом, встре¬
чается примерно в 3—17 раз чаще, чем спорадический лимфангиолейомиоматоз.
Поэтому вполне закономерно, что самое первое описание этого заболевания в
1918 г бьио посвящено именно лимфангиояейомиоматозу у больного с тубероз¬
ным склерозом, т.е. лимфангиолейомиоматозу, ассоциированному с ту-берозным
склерозом, который значительно чаше встречается в популяции. Однако, несмо¬
тря на то, что почти треть шщиентов, страдающих туберозным склерозом, имеют
рентгенологические признаки лимфангаолейомиоматоза легких, выявленные
первый раз при КТ высокого разрешения, только у 2—3% из них в дальнейшем
развивается симптоматика лимфангиолейомиоматоза.Учитывая имеющиеся описания случаев, помимо Европы, из Юго-Восточ-
ной Азии, Японии и Северной Америки, можно говорить о том, что лимфан¬
гиолейомиоматоз поражает все этнические группы населения Земли.Этиология и патогенез лимфангиолейомиоматоза до конца неизвест¬
ны, однако, принимая во внимание большую распространенность этого
Глава 4. Лимфангиолейомиоматоз: клиническая, инструментальная,.. 81заболевания среди лиц, страдающих туберозным склерозом, возникает мысль
об их этиологическом и/или патогенетическом сходстве. На родство лимфан-
гиолейомиоматоза и туберозного склероза указывает наличие инактивир>тощих
\іутаций в одних и тех же генах — генах туберозного склероза; TSC1 и TSC2,
причем мутации в этих генах имеют место как при лимфангиолейомиоматозе,
ассоциированном с туберозным склерозом, гак и при спорадическом лимфан¬
гиолейомиоматозе. Однако если туберозный склероз является наследственным
заболеванием и наследуется по аутосомно-доминантному типу, в связи с чем
;иія него характерна равная вероятность встречаемости как у мужчин, так и
у женщин, то для спорадического лимфангиолейомиоматоза характерно то,
что болеют только женщины и не описаны случаи передачи заболевания «по
наследству» — от матери к дочери.Гены TSC1 и TSC2 по сути своей являются генами-супрессорами опухоле¬
вого роста и кодируют синтез белков гамартина и туберина соответственно.
В свою очередь, гамартин-тубериновый комплекс подавляет избыточный
клеточный рост через мишени для рапамипина М;іекопитающих — niTOR
{mammalian target of rapamycin). Мутации в генах TSCl іл 7’5'C2 приводяї к сни¬
жению нормальной активности гаматрин-туберинового комплекса и, следо¬
вательно, к уменьщению контроля над пролиферацией клеток, рост которых
контролируется посредством этого механизма. Для спорадического лимфан¬
гиолейомиоматоза более характерна мутация в гене TSC2, которая была выяв¬
лена в клетках пациенток, полученных из легких, крови и мочи и хилезной
плевральной жидкости. Тем не менее мутация гена TSC1 также была описана
у больных спорадическим лиімфангиолейомиоматозом. Таким образом, пато¬
генез лимфангиолейомиоматоза сходен с патогенезом туберознош склероза;
вследствие мутации генов TSC1 и TSC2 имеет место нар>ттісние регуляции пути
метаболизма mTOR. Результатом этого является образование популяции лим-
фангиолейомиоматозных к.іеток.При микроскопическом исследовании лимфангиолейомиоматозные клет¬
ки достаточно вариабельны, но на сегодняшний день по внешнему виду
выделяют как минимум две их субпонуляции: незрелые гладкомышечные и
энителиоидные, а также множество промежуточных форм. Предшественники,
а следователыю, и гистологическая принадлежность лимфангиолейомиома-
тозных клеток, неизвестны, поскольку, с одной стороны, они экспрессируют
гладкомышечный актин, характерный для миоцрггов гладких мышц, а с дру¬
гой стороны, они экспрессируют бе.лок премеланоцита, который выявляется
посредством положительной реакции с НМВ-45 (моноклональными анти¬
телами Human Melanoma Black-45) и содержат премеланосомы — маркеры
дифференцттровки меланоцитов. Представительство маркеров меланоцитов
может наводить на мысль об их происхождении из нервного фебня, поэтому
лимфангиолейомиоматозные клетки, внешне напоминающие эпителиальные,
хотя и не имеющие с ними более ничего общего, классифицируются как иери-
васкулярные энителиоидные клетки.Принимая во внимание тот факт, что основным патогенетическим механиз¬
мом прогрессирования лимфангиолейомиоматоза является бесконтрольная
82 Пульмонологиямультифокальная узловая пролиферация лимфангиолейомиоматозных клеток,
а также «генетическая» общность лимфангиолсйомиоматоза с туберозным скле¬
розом — гамартомным, т.е. «опухолевоподобным^> заболеванием, совершенно
естественно возникает мысль об определенном родстве лимфангиолейомиома-
тоза с опухолевыми процессами. Классическими признаками «злокачественно¬
сти» являются: 1) наличие автономно пролиферирующего бессмертного клона
клеток, эволюционирующего в сторону независимости контроля от организма,
2) способность к инвазивному росту и 3) метастазирование.Сопоставляя эти критерии, характеризующие злокачественные новооб¬
разования, с имеюш^тмися на сегодняшний день данными, полученными при
наблюдении за пациентами с лимфангиолейомиоматозом, можно выявить
определенные сходства по всем ірем пунктам.1 Морфологическим субстратом лимфангиолейомиоматоза яаіяегся оггухоле-
воподобный рост лимфангиолейомиоматозных клеток, до некоторой степени
бесконтрольный. Лимфангиолейомиоматозные клетки, подобно клеткам мно¬
гих злокачествен! 1ЫХ опухолей, экспрессируют сосудистый эндотелиальный
ростовой фактор D (Vascular Endothelial Growth Factor-D - VEGF-D), блаїо-
даря которому поддерживается ангиогенез в узлах, образованных лимфангио-
лейомиоматозными клетками.2. В пользу «инвазивности» роста лимфангиолейомиоматозных клеток свиде¬
тельствует повышенное содержание в них сывороточного ответного фактора
(Serum Response Factor — SRF) и матриксных металлопротсиназ (ММП). SRF
увеличивает экспрессию ММП 2-го (коллагеназа IV) и 14-го (мембраносвя¬
занная ММП) типов, содержание которых при лимфангиолейомиоматозе
повышается. Как известно, степень инвазивного роста и метастазирования
опухолевых клеток определяется их способностью расщеплять компоненты
экстрацеллюлярного матрикса, такие как базальные мембраны и компоненты
межтканевой стромы (коллаген, эластин, ламинин и т.д.), что достигается с
помощью повышенного синтеза ММП. В отличие от многих протеолитиче-
ских ферментов, способных расщеплять отдельные компоненты ЭКС'ГрацеЛЛЮ-
яярного матрикса, ММП разрушают все его структуры, что и позволяет опухо¬
левым клеткам внедряться на территорию других тканей. Кроме того, наряду
с увеличением экспрессии ММП при лимфангиолейомиоматозе отмечается
снижение уровня тканевых ингибиторов ММП 3-го типа (TIMP-3). Однако
следует отметить, что повышение уровня ММП было выявлено и при других
иятерстициальных заболеваниях легких, таких как идиопатический легочный
фиброз и саркоидоз.3. В пользу теории <^доброкачественного метастазирования» лимфангиолейо¬
миоматоза свидетельствует тот факт, что лимфангиолейомиоматозные клетки
биоптата легких и клетки ангиомиолипомы почки у пациентки с лимфан-
гиолейомиомагозом имели общую мутацию, а следовательно, и общее про¬
исхождение. Широко известен случай рецидива лимфангиолейомиоматоза
в донорском легком после трансплантации. Кроме того, клетки с мутацией
в гене TSC2 были выделены из крови и мочи, а также хилезной плевральной
жидкости больных. Тем не менее следует отметить, что параллельно теории
Глава 4, Лимфангиолейомиоматоэ: клиническая, инструментальная... 83«доброкачественного метастазирования» все перечисленные выше факты
некоторыми исследователями трактуются в рамках гипотезы о том, что пред¬
шественники лимфангиолейомиоматозных клеток представлены и циркулиру¬
ют в кровообращении.Наряду с вышеизложенным, в соответствии с накопленными на сегодняш¬
ний день фактами, в этиологии и прогрессировании лимфангиолейомиоматоза
определенную роль, вероятно, ифают женскис половые гормоны, которые
регулируют транскрипцию многих генов, а также могут играть роль стимула в
пролиферации и миграции лимфангиолейомиоматозных клеток в другие орга¬
ны и ткани. В пользу этого предположения свидетельствуют перечисленные
ниже факты.Заболевание развивается почти исключительно у женщин детородного воз¬
раста, и почти всегда симптоматика дебютирует до наступления менопаузы.
Первые симптомы заболевания появляются, как правило, после 30 лег, а сред¬
ний возраст на момент постановки диагноза обычно составляет 41—43 года.
После наступления менопаузы заболевали в основном те женщины, которые
находились на заместительной терапии эстрогенами.Дебют и обострения заболевания могут быть спровоцированы беремен¬
ностью и лечением эстрогенами, а после наступления менопаузы или уда¬
ления яичников в ряде случаев профессированис заболевания замедляется.
Пневмоторакс более часто развивается во время беременности.Примерно в половине случаев при проведении иммуногистохимическою
исследования на лимфангиолейомиоматозных клетках BbiHBjmjiHCb поверх¬
ностные PRs (прогестероновые) и ERs (эстрогсновые) рецепторы, что также
свидетельствует в пользу гормональной обусловленности заболевания. По дан¬
ным отечественных авторов, экспрессия лимфангиолейомиоматозных клеток
PRs и ERs была выявлена в 80% случаев.Резюмируя вышеизложенное, следует подчеркнуть, что лимфангиолейоми-
оматоз поражает почти исключительно женщин, на сегодняшний день в лите¬
ратуре представлены описания только пяти случаев лимфангиолейомиоматоза
у мужчин, которые имели гистологическое подтверждение диагноза. В трех из
них речь шла о сочетании лимфангиолейомиоматоза с туберозным склерозом,
поскольку имел место диагноз достоверного или вероятного туберозного скле¬
роза. В одном случае описывался мезентериальный лимфангиолейомиоматоэ,
диагностировашіьій у мужчины с синдромом Кляйнфельтера; и лишь в одном
сообщении было описание случая лимфангиолейомиоматоза у мужчины с нор¬
мальным кариотипом и без явных генетических доказательств ТС.Таким образом, на основании приведенных выше данных можно говорить
о том, что в патогенезе и прогрессировании лимфангиолейомиоматоза важное
значение придается популяции лимфангиолейомиоматозных клеток, которые
обладают фенотипом, способным к бесконтрольному росту, экспрессии гормо¬
нальных рецепторов, протеаз и факторов роста, включая сосудистый эндотели¬
альный фактор роста, и характеризуются метастатическим поведением.Пролиферация лимфангиолейомиоматозных клеток имеет место в основ¬
ном в паренхиме легких и лимфатической системе. В легких изменения носят
Н4 Пульмонологиядиффузный характер и проявляются мультифокальной узловой пролифера¬
цией лимфангиолейомиоматозных клеток, которая сочетается с кистозной
перестройкой паренхимы, связана с пролиферацией лимфатических сосудов и
обычно располагается вокруг них, а также подплеврально — и в альвеолярных
септах. Кроме этого, при морфологическом исследовании ткани легких описа¬
ны расширенные лимфатические протоки преимущественно в а^іевре и обра¬
зование осевых (располагающихся вдоль оси туловища) лимфангиолейомиом
лимфатических сосудов грудной клетки. Следствием таких изменений являют¬
ся клинические симптомы и синдромы, составляющие легочные проявления
заболевания и доминирующие в его клинической картине. Самым частым
проявлением поражения легких при лимфангиолейомиоматозе, по данным 10
наиболее крупных обзоров, является одышка, встречающаяся в 87% случаев
и иногда ассоциированная со стридорозным дыханием. Вероятно, одышка
является следствием нарушения диффузионной способности легких (DL^^y),
которая у 82% пациентов снижается уже на начальньїх стадиях болезни и/или
бронхообструкции, поскольку даже при нетяжелом течении лимфангиолейо-
миоматоза сниженный показатель ОФВ^ имеют 58% больных.У 65% больных лимфангиолейомиоматозом в течение болезни развивается
пневмоторакс, причем у 4% из них он бывает двусторонним и достаточно часто
рецидивирующим. При этом обращает на себя внимание, что пневмоторакс
у бо.ттьных лимфангиолейомиоматозом чаше развивается во время беремен¬
ности. Около 51% больных лимфангиолейомиоматозом предъявляют жалобы
на кашель, как правило, сухой, но на более поздних стадиях болезни было
отмечено присоединение выделения мокроты и учащение повторных респи¬
раторных инфекций. Характерной особенностью лимфангиолейомиоматоза
является частое развитие хилезного плеврального выпота, который выявля¬
ется у 28% больных лимфангиолейомиоматозом, в то время как по частоте
встречаемости в общей структуре выпота в плевральную полость хилоторакс
занимает одно из последних мест. Частое развитие хилоторакса в клинической
картине лимфашиолейомиоматоза при столь редком его развитии вследствие
других заболеваний позволило отнести его к критериям диагностики этого
заболевания. Он является следствием обструкции лимфангиолейомиоматоз-
ными клетками лимфатических сосудов грудной клетки — грудного протока,
лимфатических сосудов плевры или средостения, поэтому после аспирации
жидкости из плевральной полости хилоторакс при лимфангиолейомиоматозе
имеет тенденцию быстро рецидивировать. У 22% лиц, страдающих лимфанги¬
олейомиоматозом, встречается кровохарканье как следствие обструкции лим-
фангиолейомиоматозными клетками легочных капилляров, а у 7% — хилофтиз
как проявление нарушения проходимости капилляров легких.Внелегочные проявления лимфангиолейомиоматоза включают поражение
лимфатической системы (лимфангиолейомиомы и лимфоаденопатия), ангио-
миолипомы и менингаомы.Особенно характерным для лимфангиолейомиоматоза является поражение
в основном крупных осевых лимфатических сосудов брюшной полости, таза
и ретроперитонеального просіранства, которые становятся утолщенными и
Глава 4. Лимфангиолейомиоматоз: клиническая, инструментальная.,. 85расширенными, а в некоторых случаях могут закупориваться лимфангиолсйо-
миоматозными клетками. Наиболее специфично образование лимфангио-
лейомиом — скопление кистозно увеличенных и расширенных лимфатических
сосудов, которое выявляется у 21% пациентов. Разрыв лимфаіииолейомиом в3 0% случаев приводит к образованию хилезного асцита. При схожих измене¬
ниях в лимфатических сосудах мочевого пузыря появляется хилурия. Также
имеются описания хилоперикарда, хотя отмечается, что он редко бывает кли¬
нически значимым.У 40% пациентов с лимфангиолейомиоматозом выявляется лимфоадено-
патия с преимущественным поражением ретроперитонеалънььх, реже тазовых
лимфатических узлов, а также лимфатігческих узлов, находящихся позади
места прикрепления ножек диафрагмы — ретрокруралъных. Как увеличенные
конгломераты лимфатических узлов, гак и лимфангиолейомиомы могут при¬
водить к появлению малоспецифичной симптоматики со стороны брюшной
полости. Клиническими проявлениями лимфоаденопатрш брюшной полости
и таза обычно являются наличие пальпируемых образований, ощущение дис¬
комфорта в брюшной полости, метеоризм, парестезии и отеки ног. К несколько
более специфичным проявлениям относятся синдромы сдавления внутренних
органов, особенно когда тазовые конгломераты сдавливают мочевой пузырь.
Однако следует отметить, что эти симптомы не только малоспецифичны, но и
встречаются у небольшого количества пациентов. Так, из 21% больные, имев¬
ших ангиомиолипомы, симптоматика со стороны брюшной полости наблюда¬
лась в 45%, т.е, менее чем у половины.Достаточно часто у больных лимфангиолейомиоматозом выявляются
ангиомиолипомы — доброкачественные опухоли, состоящие из гладко¬
мышечных лимфангиолейомиоматозных клеток, кровеносных сосудов и
жира. Ангиомиолипомы имеют место более чем у 50% пациентов со спо¬
радическим лимфангиолейомиоматозом и выявляются в 69—80% случаев у
больных туберозным склерозом, а среди лиц, страдающих лимфангиолейо¬
миоматозом, ассоциированным с туберозным склерозом, ангиомиолипомы
имеют место почти у всех пациентов. Учитывая столь частое распростране¬
ние ангиомиолипом почек при лимфангиолейомиоматозе и генетическое
единство лимфангиолейомиоматозных клеток легких и почек, их выявление
у пациентов с характерными для лимфангиолейомиоматоза данными ком¬
пьютерной томографии легких является одним из возможных вариантов
достоверной диагностики лимфангиолейомиоматоза. При спорадическом
лимфангиолейомиоматозе ангиомиолипомы обычно выявляются в почках,
единичные, менее 1,5 см в диаметре, как правило, асимптомные, тогда как
при сочетании лимфангиолейомиоматоза с туберозным склерозом ангиоми¬
олипомы часто большие, множественные, двусторонние и кроме почек могут
поражать другие органы (печень, селезенка, средостение). Опухоли более4 см, особенно имеющие аневризматические сосуды, склонны к кровоточи¬
вости, проявляющейся как гематурия и гемоперитонеум. Одновременно с
этим как при спорадическом, так и при лимфангиолейомиоматозе, ассоци¬
ированном с туберозным склерозом, кроме ангиомиолипом, в почках могут
86 Пульмонологиябыть выявлены и злокачественные новообразования: почечноклеточная кар¬
цинома и недавно описанный у этих больных карциномоподобный вариант
ангиомиолипомы.Последним внелегочным проявлением лимфангиолейомиоматоза можно
считать менингиому, однако, принимая во внимание значительно меньшую
ес частоту возникновения по сравнению с другими указанными выше про¬
явлениями болезни, более правильно говорить об ассоциации менингиомы с
лимфангиолейомиоматозом. У больных лимфангиолейодшоматозом как спо¬
радическим, так и ассоциированным с туберозным склерозом имеется повы¬
шенный риск развития менингиомы. При проведении магнитно-резонансной
томографии головною мозга 250 пациентам с лимфангиолейомиоматозом у
3,6% (9 человек) была выявлена менингиома, причем у 3 пациентов менингио-
ма сопровождалась соответствующими симптомами. Поскольку в популяции в
целом риск развития менингиомы составляет 0,005%, очевидно, что у больных
лимфалгиолейомиохматозом эта опухоль встречается гораздо чаще — 3,6% про¬
тив 0,005%.Несмотря на HajiH4He в клинической картине лимфангиолейомиоматоза
столь демонстративных, необычных и редко встречающихся в рутинной вра¬
чебной практике признаков, как хилезный выпот, рецидивирующие пневмо¬
тораксы, наличие лимфангиолейомиом, ангиомиолипом почек и менингиом,
возникающих почти исключительно у молодьгх женщин, диагностика этого
заболевания представляет большие трудности, связанные не только с невысо¬
кой распространенностью заболевания и невысокой осведо\шенностью врачей
общей практики, но и с отсутствием до недавнего временит четко сформули¬
рованных диагностических критериев лимфангиолейомиоматоза. В декабре
2009 г. рабочей группой Европейского респираторного общества впервые были
опубликованы клинические рекомендации по диагностике и лечению лимфан¬
гиолейомиоматоза .Диагностические критерии лимфauгиoлeй0lvшoмaтoзaДостоверный лимфангиолейомиоматоз«Характерные для лимфангиолейомиоматоза легких» или «совместимые
с лимфангиолейомиоматозом легких» данные компьютерной томографии и
биопсии легких, соответствующие морфологическим критериям для лимфан¬
гиолейомиоматоза.Или«Характерные для лимфангиолейомиоматоза легких» данные КТ и любой из
следующих признаков:ангиомиолипома (почки);хилезный выпот в фудной или брюшной полости;лимфангиолейомиома или поражение лимфоузлов, характерное для лим¬
фангиолейомиоматоза;определенный или возможный туберозный склероз.Вероятный лимфангиолейомиоматоз«Характерные для лимфангиолейомиоматоза легких» данные компьютер¬
ной томографии и клиническая картина.
Глава 4. Лимфангиолейомиоматоз: клиническая, инструментальная... 87Или«Совместимые с лимфангиолейомїтоматозом легких» данные КТ и любой
из следрэщих признаков: ангиомиолипома почкп, хилезный выпот в грудной
или брюпіной полости.Сомнительный лимфангиолейомиоматоз«Характерные для лимфангиолейомиоматоза легких» или «совместимые с
лимфангиолейомиоматозом легких» данные КТ.По степени специфичности для лимфангиолейомиоматоза рентгенологиче¬
ские критерии подразделены на «характерные для лимфангиолейомиоматоза
легких» и «совместимые с лимфангиолейомиоматозом легких».Характерные для лимфангиолейомиоматоза легких данные КТ вюіючают
множественные тонкостенные круглые хорошо дифференцируемые воздуш¬
ные кисты при сохранном или увеличенном объеме легких без других значи¬
мых поражений, нет признаков других интерстициальных болезней легких, за
исключением маленьких узелков, которые наиболее часто при проведении КТ
легких являются проявлением мультифокальной микроузловой гиперплазии
пневмоцитов у пациентов с туберозным склерозом (как без, так и в сочетании
с лимфангиолейомиоматозом).К совместимым с лимфангиолейомиоматозом легких изменениям, выявляе¬
мым при КТ, относят наличие только небольшого количества (от 2 до 10) таких
кист размером до 30 мм в диаметре при соблюдении прочих перечисленных
выше условий.Из оценки диагностической значимости существующих критериев следует,
что самыми информативными исследованиями в диагностике лимфангиолейо¬
миоматоза являются компьютерная томография легких высокого разрешения
и морфологическое исследование ткани легкого, поскольку для этих методов
разработаны наиболее достоверные критерии. Сочетание положительных
результатов обоих этих исследований позволяет убедительно диагностировать
лимфангиолейомиоматоз.По данным большинства имеюш,ихся на сегодняшний день исследований,
к «золотому стандарту» диагностики относят морфологическое исследование
биоптата ткани легкого {рис. 4.5, см. цветную вклейку). Критериями диагноза
служат одновременное присутствие множественных мелких воздушных кист
и наличие мультифокальной узловой пролиферации двух основных видов
лимфангиолейомиоматозных клеток— незрелых гладкомышечных и пери-
васкулярных эпителиоидньгх клеток. Целесообразно проведение дополни¬
тельного иммуногистохимического исследования для вьывления экспрессии
а-гладкомышечного актина и НМВ-45, особенно в случаях трансбронхиаль¬
ного метода получения образца ткани легкого. Полезным может бьггь опреде¬
ление рецепторов к эстрогену и прогестерону.Тем не менее диагноз может быть верифицирован и без проведения биоп¬
сии, с помошью убедительных данных, полученных при помощи КТ легких
в сочетании с соответствующей клинической картиной; большое значение
придается как легочным, так и внелегочным клиническим проявлениям забо¬
левания.
ПульмонологияПосле постановки диагаоза необходимо оценить риск возникнове¬
ния ннсвмоюракса, накопления хилезного выпота и развития кровотечения
из ангиомиолипом почек: пациенты должны быть хоропто осведомлены о воз¬
можных симптомах и необходимости аксірс иного поиска медицинской помоши
в случаях их поямения. Дебют пневмоторакса, кровотечения и хилезною выпо¬
та может быть связан с бсрсмснностью и приемом эстрогенов и,'1и спровоциро¬
ван ими. Пациенткам, страдаютцим лимфангиолейомиомаюзом, целесообразно
разъяснять возможные осложнения беременности, рекомендовать воздержи¬
ваться от нее, а также избегать терапии эстрогенсодсржащими препаратами.Некоторую осторожность пациентам с лимфангиолейомиоматозом и нерс-
несенньпк! пневмотораксом следует соблюдать в отношении совершения авиа¬
перелетов. Данных о повышенном риске развития пневмоторакса у больных
лимфангиолейомиоматозом при авиаперелетах нет, но имеготся сведения о
развитии головокружения и гипоксемии, особенно у лиц с нарушениями функ¬
ции дыхания: лиц с развернутой стадией болезни следует оценить на предмет
необходимости кислородной поддержки в течение полета.Консервативное лечение при развитии пневмоторакса (наблюдение, плев¬
ральная пункция, установка дренажной трубки) у больных лимфангиолей¬
омиоматозом сопровождается рецидивом пневмоторакса в 2/3 всех случаев.
Радикальные хирургические методы лечения включают плевродез с видеотора-
коскопическим пособием, плевральную абразию, плеврэктомию и буллзкто-
мию. При развитии хилоторакса рекомендуется назначение безжировой диеты,
а при значительном объеме плеврального выпота используют различные про¬
цедуры, выбор которых хирург определяет индивидуально в каждой ситуации:
торакоцентез, плевродез посредством инстилляции ск.'іерозирующих веществ
или париетальной плеврэктомии, торакотомия с перевязкой грудного протока
и ішевроперитонеальное шунтирование.Индикаторами риска кровотечений из ангаолтоолипом считают размер опухо¬
ли более 4 см и наличие расширенных сосудов с аневризмами > 5 мм. Д.чя больных
с ангаомиолипомами болсс 4 см требуется выполнение дважды в год УЗИ почек, с
тем чтобы иметь возможность своевременного проведения ангиографии с после¬
дующим обсуждением радикального лечения (резекция или эмболизация) аш ио-
миолипомы не только при остром кровотечении, но и профилактически.Кроме наблюдения за пациентами, в настоящее время ведутся актив¬
ные поиски методов лечения, направленных на улучшение качества жизни,
стабилизацию заболевания и предотвращение профессирования необрати¬
мых изменений, приводящих пациентов к инва-тидизации и необходимости
трансіь'іантации легких. Наиболее исследованными являются патогенетиче¬
ские медикаментозные методы, включающие применение бронходилататоров,
ингаляционных глюкокортикостероидов, прогестерона, анти^строгенных пре¬
паратов и ингибиторов m-TOR.В связи с тем, что у 20-24% пациентов с лимфангиолейомиоматозом выяв¬
лен положительный ответ при проведении бронходилатационного теста, инга¬
ляционные бронходилататоры следует назначать пациентам с лимфангиолей¬
омиоматозом и обструкцией воздушного потока, отвечающим на применение
Глава 4. Лимфангиолейомиоматоз: клиническая, инструментальная,,, 89ингаляционных бронходилататоров. Принимая во внимание отсутствие дан¬
ных, подтверждающих эффективность ингаїящионньїх глюкокортикостерои-
дов при лимфангиолейомиоматозе, несмотря на теоретически обоснованное и
допустимое воздействие этой лекарственной группы на воспаление воздушных
путей в виде броігіхиолита, имеющееся при лимфангиолейомиоматозе, назна¬
чение кортикостероидов не вошло в клинические рекомендации.Патогенетически обоснованное применение прогестерона при терапии
лимфангиолсйомиоматоза в исследованиях не продемонстрировало досто¬
верного клинического эффекта, в связи с чем прогестерон не должен рутин¬
но назначаться таким больным. Только в случае быстрого проірессирования
падения показателей функции легких лечение прогестероном допустимо при
динамическом контроле ОФВ, и диффузионной способности легких (ОЦо)
каждые 3 мес в течение одною года и с отменой препарата при отсутствии
положительной динамики по истечении этого срока.Среди других антиэстрогенных методов лечения исследовались оофорэкто-
мия, тамоксифен и трипторелин — агонист гонадотропин-релизинг-фактора.
Доказательства эффективности этих методов отсутствуют (для терапии трипто-
рслином, кроме того, выявлена ассоциация с редукцией минеральной костной
плотности). Гормональные методы лечения, кроме прогестерона, не следует
использовать при лимфангиолейохмиоматозе.Поскольку мутации в генах TSCJ и TSC2 ассоциированы с активацией
m-TOR-пути, вполне обоснованным представляется назначение шігибиторов
m-TOR — сиролимуса и эверолимуса. Результаты двух исследований по оценке
их эффективности неоднозначны и требуют дальнейшего изучения: пока тера¬
пию сиролимусом рекомендуют в рамках будущих клинических исследований
или при быстропрогрессирующем течении, под пристальным динамическим
наблюдением. В финале встает вопрос о трансплантации легких, показаниями
к которой являются 1П или ТУ функциональный класс по N YHA с гипоксемией
в 1ЮК0Є, тяжелое нарушение легочной функции и снижение дееспособности.
Эксперты рекомендуют своевременно вюіючать пациентов с лимфангиолейо-
миоматозом в программы по легочной реабилитации и проводить иротиво-
гриптюзнутю и ішевмококков>то вакцинацию.Комментарий С. И. Овчареыко — профессора кафедры фаі^льтетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукВ заключение слелует обрати!ь внимание на ряд особенностей представлен¬
ного клинического случая.Известно, что лимфані'иолейомиоматоз поражает практически исключитель¬
но женщин детородного возраста, обьпно между 20 и 40 годами. У нашей же
пациентки заболевание развилось достаточно поздно: в возрасте около 60 лет
появились первые симптомы заболевания. В мировой литературе есть описа¬
ние двух случаев лимфангиолсйомиоматоза у женщин в период менопаузы,
при этом отмечалось более благоприятное течение болезни, что характерно
и для нашей пациентки. У нее при таком большом колігіестве тонкостенных
кист разли^[ных размеров, выявленных при КТ и практически замещающих
90 Пульмонологиялегочную ткань, очень скромная клиническая картина: беспокоит лишь
одышка при физической нагрузке, больная сохраняет работоспособность.
Вопрос о применении контрацептивов нашей больной совершенно право¬
мочен. Известно, что лимфангиолейомиоматоз в ряде случаев возникает на
фоне применения препаратов, содержаших эстрогены, применяемые в виде
пероральной контрацепции, а также для лечения остеопороза или бесплодия,
что подтверждает важную роль эстрогенов в развитии лимфангиолсйомио-
матоза.Данная демонстрация на клиническом разборе не первая. Уже в 2004 т. мы
с Н.В. Петуховой и К.К. Осадчим представляли больную 47-ми лет, у кото¬
рой заболевание npoTCKajio тяжело. Она поступила в отделение патолоіии
суставов с диагнозом «системная красная вол^шнка*, по поводу чего при¬
нимала преднизолон, но в ходе обследования этот диагноз не подтвердился.
Клиницистами обсуждался диагноз фиброзирующего альвеолита, но после
анализа результатов биопсии легких, вьтолненной в Национальном медико¬
хирургическом центре им. Н.И. Пирогова, был поставлен диагноз лимфан-
гиолейомиоматоза легких и бьша начата терапия медроксипрогестероном в
дозе 450 мкг.Необходимо подчеркнуть, что в настоящее время, вероятно, с развитием
современных методов диагностики, лимфангиолейомиоматоз дисігностируют
не гак уж редко, хотя клинические проявления его могут быть самыми раз¬
нообразными. Отсюда следует, что диагноз лимфангиолейомиоматоза можно
заподозрить по данным КТ легких, а верифицировать — по результатам мор¬
фологического исследования биоптата (а в ряде случаев при использовании
гистохимических методов).Нашу больную мы передали под наб.іюдение НИИ пульмонологии в Москве,
где концентрируются все пациентки с лимфангиолейомиоматозом. В США
даже создано общество больных лимфангиолейомиоматозом, и все больные
мира, страдаюшде этой болезнью, могут связаться друг с другом с помощью
Интернета. Прогноз при лимфангиолейомиоматозе изучен мало. Средняя
продолжительность жизни составляет 4,5—5 лет. К настоящему моменту
появились сообщения о продолжительности ЖИЗІІИ около 10 лет от начала
заболевания. Описан даже случай спонтанного регресса заболевания (я очень
сомневаюсь в этом случае в диагнозе лимфангиолейомиоматоза). К сожа¬
лению, из-за редкости болезни и малого количества исследований трудно
судить о влиянии терапии на прогноз больных лимфангиолейомиоматозом.ЛИТЕРАТУРААбе.іев Г.И,, Эрайзер Т. Р. На пути к пониманию природы рака // Биохимия. —
2008. - № 73(5). - С. 605-618.Каменева М.Ю., Двораковская И.В,, Новикова Л.Н., Баранова О. П., Илька-
вин М.М. Лейомиоматоз легких (Морфофункциональное исследование). —
2007. - С. 86-95.
Глава 4, Лимфангиолейомиоматоз: клиническая, инструментальная,,, 91Клітко Е,В., Кондакова И.В., Чойнзонов Е,Л. Матриксные металлопротеина-
зы в онкогенезе // Сиб. онкол. журнач. ~ 2003. — № 2. — С. 63—70.Перепечин В., Стеблянская О,, Черняев Л. и др. Диффузный лимфангиолейо¬
миоматоз легких // врач. — 2008. — № 2. — С. 6-11.Респираторная медицина: Руководство / Под ред. А.Г. Чучалина. — М.,
2007.Almoosa K.F,, Ryu J.H., Mendez J- et al. Management of Pneumothorax in
Lymphangioleiomyomatosis: Effects on Recurrence and Lung Transplantation
Complications //Chest. 2006; 129(5):1274—1281.Aubry M.-C., Myers J.L., Ryu J.H. et al. Pulmonary lymphangioleiomyomatosis in
a man //Am. J, Respir. Crit. Care Med. 2000; 162:749—752.Avila N.A., BechtieJ., Dwyer A. J. etal Lymphangioleiomyomatosis: CT of Diurnal
\^riation of Lymph angioleiomyomas // Radiology. 2001; 221(2):415-421.Avila N.A., Dwyer A.J., Rabel A. et al Sporadic lymphangioleiomyomatosis and
tuberous sclerosis complex with lymphangioleiomyomatosis: comparison of CT fea¬
tures // Radiology. 2007; 242:277-285.Avila N.A., Dwyer A. J., Rabel A., DeCastro R.M., MossJ. CT of pleural abnormalities
in lymphangioleiomyomatosis and comparison of pleural findings after different types
of pleurodesis // AJR American Journal of Roentgenology 2006; 186(4): 1007-1012.Avila N.A., Kelly J.A., Chu S.C. etal. Lymphangioleiomyomatosis: abdominopelvic
CT and US findings // Radiology 2000; 216(1): 147-153.Bernstein S.М., Newell J.D., Adamczyk D. et al. How common are renal angiomyo-
lipomas in patients with pulmonary lymphangioleiomyomatosis? j I Am. J. Respir
Crit. Care Med. 1995; 152:2138-2143.Bissler J.J., McCormack F.X., Young L.R., Elwing J.M., Chuck G., Leonard J.M.,
Schmithorst V.J., Laor Т., Brody A.S., Bean J,, Salisbury S., Franz D.N. Sirolimus for
Angiomyolipoma in Tuberous Sclerosis Complex or Lymphangioleiomyomatosis // N.
Engl. J. Med. 2008; 358(2);140-151.Bonetti F., Chiodera P.L., Pea M. et al Transbronchial biopsy in lymphangi¬
oleiomyomatosis of the lung. HMB'45 for diagnosis 11 Am. J. Surg. Pathol. 1993;
17(11):1092-И02.BrunelHA., Catalini G., Fianchini A. Pregnancy exacerbating unsuspected medias¬
tinal lymphangioleiomyomatosis and chylothorax // Int. J. Gynaecol. Obstet. 1996;
52(3):289-290.Carrington C.B., Cugell D.IV., Gaensler E.A, et al. Lymphangioleiomyomatosis.
Physiologic-pathologic-radiologic correlations // Am. Rev. Respir. Dis. 1977;
ll6(6):977-995.Carsillo Т., Astrinidis A., Henske E.P. Mutations in the tuberous sclerosis complex
gene TSC2 are a cause of sporadic pulmonary lymphangioleiomyomatosis // Proc.
Natl. Acad. Sci USA. 2000; 97(ll):6085-6090.Castro М., Shepherd C. W., Gomez M,R. et al. Pulmonaiy tuberous sclerosis j I Chest
1995;107:189-195. Tuberous sclerosis.Christodoulou М., Ris H.-B., Pezzetta E. Video-assisted right supradiaphragmatic
thoracic duct ligation for non-traumatic recurrent chylothorax // Eur J. Cardiotho-
rac. Surg. 2006; 29(5):810-814.
92 ПульмонологияChu S.C., Horiba К., lisuki J. et aL Comprehensive evaluation of 35 patients with
l>Tnphangloleiomyomatosis//Chest. 1999; 115:1041-1052.Clements D., Chang W.Y.C., Johnson S.R. Lyraphangioleiomyomatosis // Eur.
Respir. Mon. 2009:46; 176-207.Cohen M.M., Pollock-BarZiv S., Johnson S.R. Emerging clinical picture of
lymphangioleiomyomatosis // Thorax. 2005;60:875-879.Corrin B., Liehow A.A., Friedman PJ. Pulmonary lymphangioleiomyomatosis //
Am. J. of Pathology. 1975; 79:348-382.Crooks D., Pacheco-Rodriguez G., DeCastro R. et ai. Molecular and genetic analysis
of disseminated neoplastic cells in lymphangioleiomyomatosis j I Proc. Natl. Acad. Sci
USA. 2004; 101:17462-17467.Davies D,M., Johnson S.R., Tattersfield Л.Е., Kingswood J.C., CoxJ.A., McCartney
D.L., Doyle Т., Elmslie F., Saggar A., de Vries PJ., Sampson J.R. Sirolimus Therapy in
Tuberous Sclerosis or Sporadic Lymphangioleiomyomatosis // N. Engl. J. Med. 2008;
358(2);200-203.Druelle S., Aubry P., Levi-Valensi P. [Pulmonaiy lymphangiomyomatosis: a 3-year
foUowup of medroxyprogesterone acetate therapy. Apropos of a casej j I Rev. Pneumol.
Clin. 1995;51(5):284-287.European Respirator>' Society guidelines for the diagnosis and management of
lymphangioleiomyomatosis // Eur. Respir. J. 2010; 35:14-26.Fwalt D.H., Sheffield E., Sparagana S.P. et ai Renal lesion growth in children with
tuberous sclerosis complex // J. of Urology. 1998; 160(1): 141—145.Fiore M.G., Sanguedolce F, Lolli I. etal. Abdominal lymphangioleiomyomatosis in
a man with Klinefelter syndrome: the first reported case // Ann, Diagn. Pathol. 2005;
9:96-100.Franz D.N., Brody A., Meyer C. et aL Mutational and radiographic analysis of
pulmonary disease consistent with lymphangioleiomyomatosis and micronodular
pneumocyte hyperplasia in women with tuberous sclerosis // Am. J. Respir. Crit. Care
Med, 2001; 164(4):661-668.Fujimoto М., Ohara N., Sasaki И., Funakoshi Т., Morita H., Deguchi М., Мато Т.
Prcgnancy complicated with pulmonary lymphangioleiomyomatosis: case report j j
Clinical & Experimental Obstetrics & Gynecology. 2005; 32(3): 199-200.Glassherg M.K., Elliot SJ., Fritz J. et al Activation of the Estrogen Receptor
contributes to the Progression of Pulmonary Lymphangioleiomyomatosis via MMP-
induced Cell Invasiveness //J. Clin. Endocrinol. Metab. 2008.Goncharova Е.Л., Goncharov D.A., Eszterhas A. et al. Tuberin Regulates p70S6
Kinase Activation and Ribosomal Protein S6 Phosphorj^lation. A role for the TSC2
tumor suppressor gene in pulmonary lymphangioleiomyomatosis (LAM) // J. Biol.
Chem. 2002; 277(34): 30958-30967.Gray S,, Carrington C., Comog J. Lymphangioleiomyomatosis: report of case with
ureteral involvement andchyluria//Cancer. 1975; 35:490-498.Hancock E., Tomkins S., Sampson J. et al. Lymphangioleiomyomatosis and
tuberous sclerosis// Respir. Med. 2002; 96:7-13.Harari S., Cassandra R., Chiodini J., Taveira-DaSilva A.M., Moss J, Effect
of a Gonadotrophin-Releasing Hormone Analogue on Lung Function in
Lymphangioleiomyomatosis // Chest. 2008; 133(2): 448-454.
Глава 4. Лимфангиолейомиоматоз: клиническая, инструментальная... 93Hayashida М., Seyama К., Inoue Y. et al. The epidemiology of lymphangioleio-
myomatosis in Japan: a nationwide cross-sectional study of presenting features and
prognostic factors // Respirology. 2007; 12:523—530.Henry M. Т., К. McMahoi, MackarelA. J. etal Matrix metalloproteinasesand inhibitor
of metalloproteinase-1 in sarcoidosis and IPF11 Eur, Respir. J. 2002; 20:1220-1227.Henske E.P. Metastasis of benign tumor cells in tuberous sclerosis complex //
Genes, Chromosomes Cancer. 2003; 38:376-381.Hirama М., Atsura R., Mitani K. et al. Lymphangioleiomyomatosis diagnosed by
immunocytochemical and genetic analysis of lymphangioleiomyomatosis cell clusters
found in chylous pleural effusion I j Intern. Med. 2007; 46: 1593-1596.John R. W. Yates. Tuberous sclerosis // European Journal of Human Genetics.
2006; 14(10):1065-1073.Johnson S. Rare diseases. 1. Lymphangioleiomyomatosis: clinical features,
management and basic mechanisms // Thorax. 1999; 54(3):254—264.Johnson S.R., Taffersfield A.E. Clinical experience of lymphangioleiomyomatosis in
the UK // Thorax. 2000; 55(12):1052-1057.JohnsonS.R., Decline inlung functioninlymphangioleiomyomatosis:relation to menopause and progesterone treatment // Am. J, Resr. Crit. Care Med.
1999; 160 (2):628-633.Karbowniczek М., Astrinidis A., Balsara B.R. et al. Recurrent lymphangioleio¬
myomatosis after transplantation: genetic analyses reveal a metastatic mechanism j I
Am. J. Respir. Crit. Care Med. 2003; 167:976-982.L'Hostis H., Deminiere C., Ferriere J.M. et al. Renal angiomyolipoma:
clinicopathologic, immunohistochemical, and follow-up study of 46 cases // Am. J.
Surg. Pathol. 1999; 23:1011-1020.Lazor R., Valeyre D., Lacronique J. et at. Low initial KCO predicts rapid FEVl
decline in puknonary lymphangioleiomyomatosis // Respir Med. 2004; 98(6):536—541.Lemaitre L. , Robert Y., DubruUe F. et al Renal angiomyolipoma: growth followed
up with CT and/or US 11 Radiology. 1995; 197(3):598-602.Logan R.F., Fawcett I. W. Oophorectomy forpulmonary lymphangioleiomyomatosis:
a case report I j Br. J. Dis. Chest. 1985; 79:98-100.Lutembacher R. Dyesmbryomes metatypiques des reinds; carcinosc submallairc
aigue du puomon avec emphseme generalise et double pneumothorax [Atypical kidney
dysembryomas: acute submiliary carcinomatosis of the lung with emphysema and
double pneumothorax] //Arm Med. 1918; 5:435-450.Mascarenhas R., McLaughlin P. Haemorrhage from angiomyolipoma of kidney
during pregnancy - a diagnostic dilemma 11 Irish Medical Journal. 2001; 94(3):83—84.Matsui K., Beasley M.B., Nelson W.K. et al. Prognostic significance of pulmonar\’
lymphangioleiomyomatosis histologic score //Am, J. Surg. Pathol. 2001; 25(4):479—484.Matsui K., Takeda K., Yu Z.X. et al. Downregulation of estrogen and progestorone
receptors in the abnormal smooth muscle cells in pulmonary lymphangioleiomyomatosis
following therapy An immunohistochemical stud // Am. J. Respir. Crit. Care Med.
2000; 161(3 Pt 1): 1002-1009.Matsui K, Takeda K., Yu Z.X. etal. Role for activation of matrix metalloproteinases
in the pathogenesis of pulmonary lymphangioleiomyomatosis // Arch. Pathol. Lab.
Med. 2000; 124:267-275.
94 ПульмонологияMatsuiK., TatsuguchiA., Valencia J. etai. Extrapulmonaiylymphangioleiomyomatosis
(LAM); clinicopathologic features in 22 cases // Hum. Pathol. 2000; 31(10): 1242-
1248.Matsumoto Y., Horiba K., Usuki J. etal. Markers of cell proliferation and expression
of melanosomal antigen in lymphangioleiomyomatosis // Am. J. Respir. Cell Мої.
BioL 1999; 21(3):327-336.Maziak D.E., Kesten S., Rappaport D.S. et al. Extrathoracic angiomyolipomas in
lymphangioleiomyomatosis // Eur. Respir, J. 1996; 9:402-405.McLoughlin L., Thomas G., Hasan K. Pregnancy and lymphangioleiomyomatosis:
anaesthetic management // International Journal of Obstetric Anesthesia. 2003;
12(l):40-44.Miyake М., Tateishi U., Maeda T, etal. Pulmonary lymphangioleiomyomatosis in a
male patient with tuberous sclerosis complex // Radiat Med. 2005; 23:525-527.Morales J.P., Georganas М., Khan M.S., Dasgupta P., Reidy J.F. Embolization of
a bleeding renal angiomyolipoma in pregnancy: case report and review. [Review] [21
refs] // Cardiovascular & Interventional Radiology 2005; 28(2):265-268,Morimoto N., Hirasaki S., Kamei Т., Horiike A., Miyatake K, Ogita Y., Nakano H.
Pulmonary lymphangiomyomatosis (LAM) developing chylothorax // Intern. Med.
2000; 39(9):738-74LMoss J., Avili N,A., Barnes P.M. et al. Prevalence and clinical characteristics of
lymphangioleiomyomatosis (LAM) in patients with tuberous sclerosis complex // Am.
J. Respir. Crit. Care Med. 2001; 164 (4): 669-671.MossJ., DeCastro R., Patronas N.J. etal. Meningiomas in lymphangioleiomyoma¬
tosis //JAMA. 2001; 286(15):1879-1881.O'Callaghan F.J., Noakes M.J., Martyn C.N. etal. An epidemiological study of renal
pathology in tuberous sclerosis complex // BJU International 2004; 94(6):853—857.Oh Y.M., Mo E.K., Jang S.H. et al Pulmonary lymphangioleiomyomatosis in
Korea j I Thorax, 1999; 54:618-621.Osborne J.P, Fryer A., Webb D. Epidemiology of Tuberous Sclerosis // Annals of
the New York Academy of Sciences. 1991; 615:125-128.Pan C, Chung М., Ng K. at al Constant allelic alteration on chromosome 16p
(TSC2 gene) in perivascular epithelioid cell tumor (PEComa): genetic evidence for
the relationship of PEComa with angiomyolipoma //J. Pathol. 2008; 214:387-393.Pea М., Bonetti F, Zamboni G. et al. Clear cell tumor and angiomyolipoma // Am.
J. Surg. Pathol. 1991; 15:199-202.Peh W.C., Law S., Fok M, et al. Case report: lymphangioleiomyomatosis with
spontaneous peritoneal rupture // Br. J. Radiol. 1994; 67(798):605-608.Pollock-BarZiv S., Cohen M.M., Downey G.P., Johnson S.R., Sullivan E., McCormack
F.X. Air travel in women with lymphangioleiomyomatosis // Thorax. 2007; 62(2): 176-
180.RaftJ., LalotJ.M., MeistelmanC., LongroisD. [Renal angiomyolipoma rupture during
pregnancy], [French] // Gynecologie, Obstetrique & Fertilite. 2006; 34(10):917-919.Rakowski S.K., Winterkom E.B., Paul E. et al Renal manifestations of tuberous
sclerosis complex: Incidence, prognosis, and predictive factors // Kidney International.
2006;70(10):1777-1782.
Глава 4. Лимфангиолейомиоматоз: клиническая, инструментальная.,, 95Roach E.S., Di Mario F.J., Kandt R.S. et al. Tuberous Sclerosis Consensus
Conference; recommendations for diagnostic evaluation. National Tuberous Sclerosis
Association //J. of Child Neurology. 1999; 14(6) :401-407.Ryu J.H., Doerr C.H., Fisher S.D. et al. Chylothorax in lyrnphangioleiomyomato-
sis//Chest. 2003; 123:623-627.Ryu J.H., Moss Beck G.J. et al. The NHLBI Lymphangioleiomyomatosis
Registry; Characteristics of 230 Patients at Enrollment // Am. J. Respir. Crit. Care
Med. 2006; 173(1): 105-111.Sato Т., Seyama K., Fujii H. et al. Mutation analysis of TSCl and TSC2 genes
in Japanese patients with pulmonary lymphangioleiomyomatosis // J. Hum. Genet.
2002; 47(l):20-28.Schiavina M,, DiScioscio V., Contini P. etal Pulmonary lymphangioleiomyomatosis
in a karyotypically normal man without tuberous sclerosis complex // Am. J. Respir.
Crit. Care Med. 2007; 176:96-98.Seyama K., Kumasaka Т., Souma S. etal. Vascular endothelial growth factor-D in
increased in serum of patients with lymphangioleiomyomatosis // Lymphat. Res. Biol.
2006; 4:143-152.Sinclar W., Wright J.L., Churg A, Lymphangioleiomyomatosis presenting in
postmenopausal women // Thorax. 1985; 40:75—76.Steiner M.S., Goldman S.М., Fishman E.K. et al. The natural history of renal
angiomyolipoma//J. Urol. 1993; 150:1782-1786.Storm D.W., Mowad J,J. Conservative management of a bleeding renal
angiomyolipoma in pregnancy // Obstetrics & Gynecology 2006; 107(2 Pt 2);490—
492.Sullivan EJ. Lymphangioleiomyomatosis: a review // Chest. 1998; 114(6): 1689-
1703.Svendsen T.L., Viskum K., Hansborg N., Thorpe S.М., Nielsen N.C.
Pulmonary lymphangioleiomyomatosis: a case of progesterone receptor positive
lymphangioleiomyomatosis treated with medroxyprogesterone, oophorectomy and
tamoxifen // Br. J. Dis. Chest. 1984; 78(3):264-271.Taveira-DaSilva A.M., Hedin C., Stylianou M.P., Travis W.D., Matsui K,,
Ferrans V.J., Moss J. Reversible Airflow Obstruction, Proliferation of Abnormal
Smooth Muscle Cells, and Impairment of Gas Exchange as Predictors of Outcome in
Lymphangioleiomyomatosis //Am. J. Respii. Crit. Care Med. 2001; 164(6): 1072-1076.Taveira-DaSilva A.M., Stylianou M.P., Hedin C.J. et al. Decline in Lung Function
in Patients With Lymphangioleiomyomatosis Treated With or Without Progesterone j j
Chest. 2004; 126(6): 1867-1874.Taylor J.R., Ryu J., Colby TV., Raffin Т.Л. Lymphangioleiomyomatosis. Clinical
coursc in 32 patients // N. Engl. J. Med. 1990; 323(18): 1254-1260.TomasienA., Greenberg M.S., Rumerman H. Tamoxifen for lymphangioleiomyoma¬
tosis 11 N. Engl. J. Med. 1982; 306:745-746.Urbun T, Lozor R., Lacronique J. et al. Pulmonary lymphangioleiomyomatosis.
A study of 69 pacients. Group d'Etudes et de Recherche sur les Maladies “Oфhelines”
Pulmonaires (GERM “0”P) [Study and research group on orphan lung disease] //
Medicine (Baltimore), 1999; 78 (5):321-337.
96 Пульмонологияvan BaaU.G., Smits N.J., Keeman J.N. etai The evolution of renal angiomyolipomas
in patients with tuberous sclerosis complex. Icomment] // J. of Urology, 1994;
152(l):35-38.von Stossel E. Uber musckulare Cirrhose der lunge [Muscular cirrhosis of the lungj.
Beitr Klin Tuberk. 1937; 90:432-442.Warren S,E., Lee D., Martin V., Messink W. Pulmonary lyrriphangiomyomatosis
causing bilateral pneumothorax during pregnancy // Annals of Thoracic Surgery.
2000: 55(4): 998-1000.Warth A, Herpel £., Schmahl A. et al. Mediastinal angiomyolipomas in a male
patient aflTected by tuberous sclerosis // Eur Respir J. 2008; 31: 678-680.Wojcik P., Otto Т., Jagiello R., Komarow L, Zaremba J., Drygalska-Pozoranska A.,
Chudanski M. Use ofpleuro-peritoneal shunt in the treatment of chronic chylothorax//
Pncumonol. Alergol. Pol. 1998; 66:473—479.Yamakado K., Tanaka N., Nakagawa Т., Kobayashi S., Yanagawa М., Takeda K.
Renal angiomyolipoma: relationships between tumor size, aneurysm formation, and
rupture // Radiology. 2002; 225(1):78—82.Yockey C.C., Riepe.RE., Ryan K. Pulmonary lymphangioleiomyomatosis
complicated by pregnancy// Kans Med. 1986; 87(10):277-278, 293.Zanella A., Toppan P., Nitti D., Use M, Pulmonary l>Tnphangioleiomyomatosis:
a case report in postmenopausal woman treated with pleurodesis and progesterone
(medroxyprogesterone acetate) //Tumori, 1996; 82(Г):96-98.Zhe X., Schitger L Combined smooth muscle and melanocytic differentiation in
lymphangioleiomyomatosis //J. Histochem C>tochem. 2004; 52(12): 1537-1542.Zhe X., Yang Y., Jakkaraju S. et al. Tissue inhibitor of metalloproteinasc-3
downregulation in lymphangioleiomyomatosis: potential consequence of abnormal
serum response factor expression // Am. J. Respir, Cell Moll Biol. 2003; 28:504—511.
а б вРис. 1.6. Биоптаты легких больной К.: а, б — окраска гематоксилином-эозином, в — окра¬
ска по Ван Гизону (пояснения в тексте)Альвеолярные ■
ходы ^ Альвеолярные мешочкиТерминальная
бронхиолаДыхательные (респи¬
раторные) бронхиолы_ Альвеолы
Межальвео-
лярные
перего¬
родки
Сообщение
альвео¬
лярного
мешочка с
альвеоляр¬
ным
ходомАцинусРис. 2.7. Морфология криптогенной организующейся пневмонии; а — строение дис¬
тального отдела респираторного тракта; б— гистологическая картина криптогенной
организующейся пневмонии, окраска гематоксилином-эозином (стрелками обозначе¬
но альвеолярное поражение по типу организующейся пневмонии)Рис. 4.5. Гистологические изменения в легких при лимфангиолейомиоматозе (поясне¬
ния в тексте) (http;//medumver.com/medical/pulmonologia)
Рис. 5.7. Саркоидные гранулемы в ткани легкого. Окраска гематоксилином-эозином
(пояснения в тексте)Полость носа
и околоносовые
пазухиБронхо¬легочнаясистемаПочкиСосудистоеруслоцнси периферические
нервыСердцеЖелудочно-кишечныйтрактКожаРис. 6.1. Поражение различных органов и систем при синдроме Черджа-Стросс
► 1-1-f-ReMapAblation >127 Points-211 msVolume: 228.34 RAO: 35“ Caudal: 14° Swivel:174°Рис. 7.3. Изохрональная карта возбуждения в левом желудочке сердца у пациента Е.,
75 лет, построенная на фоне левожелудочковой тахикардии. Красный цвет соответ¬
ствует наиболее раннему возбуждению ЛЖ, фиолетовый — наиболее позднему Серым
цветом маркированы зоны рубцовых изменений. Коричневые точки — места нанесения
аппликаций РЧ-энергии в критических зонах петель ре-ентриРис. 12.3. Биоптат субэндокардиального
участка свободной стенки правого желу¬
дочка. Окраска гематоксилином-эозином,
большое увеличение. Стрелками обозначе¬
ны единичный нейтрофил (сверху) и лим-
фогистиоцитарная инфильтрация в стенке
сосуда (снизу)Рис. 12.4. Биоптат субэндокардиально¬
го участка верхушки правого желудочка.
Окраска по Ван Гизону, малое увеличение.
Стрелками обозначены зоны выраженно¬
го интерстициального фиброза
Рис. 12.5. Биоптат субэндокардиально-
го участка верхушки правого желудочка.
Окраска гематоксилином-эозином, боль¬
шое увеличение. Участок липоматоза и
лимфо-гистиоцитарная инфильтрация в
интерстиции.Рис. 12.6. Биоптат субэндокардиального
участка свободной стенки правого желу¬
дочка. Окраска гематоксилином-эозином,
малое увеличение. Миокард окрашен
неравномерно — более бледные участки
соответствуют зонам некроза кардиомио-
цитов (одна из них обозначена стрелкой)Рис. 12.7. Биоптат субэндокардиального
участка свободной стенки правого желу¬
дочка. Окраска гематоксилином-эозином,
большое увеличение. Некроз кардиомио-
цитов (показан стрелкой)Рис. 12.8. Биоптат субэндокардиального
участка свободной стенки правого желу¬
дочка. Окраска гематоксилином-эозином,
большое увеличение. Некроз кардиомио-
цитовРис. 12.9. Биоптат субэндокардиального
участка базальных отделов правого желу¬
дочка. Окраска по Ван Гизону, большое
увеличение. Фиброз эндотелия (показан
стрелками)Рис. 12.10. Биоптат субэндокардиального
участка базальных отделов правого желу¬
дочка. Окраска гематоксилином-эозином,
большое увеличение. Продуктивный капил-
лярит со стенозированием просвета сосудов
и микротромбозом (правая стрелка)
Рис. 12.11. Биоптат субэндокардиального
участка базальных отделов правого желу¬
дочка. Окраска гематоксилином-эозином,
большое увеличение. Продуктивный
капилляритРис. 13.5. Биоптат субэндокардиального
участка межжелудочковой перегородки
больного С. Окраска гематоксилином-
эозином, большое увеличение. Склероз и
утолщение эндокардаРис. 13.6. Биоптат субэндокардиального участка верхушки правого желудочка больно¬
го С. Окраска гематоксилином-эозином, большое увеличение. Слева — гипертрофия
отдельных ядер, исчезновение поперечной исчерченности кардиомиоцитов, единичные
лимфогистиоцитарные элементы в интерстиции. Справа — продуктивный капилляритРис. 13.7. Биоптат субэндокардиального участка свободной стенки правого желудочка
больного С. Окраска гематоксилином-эозином, большое увеличение. Продуктивный
заскулит с облитерацией просвета сосуда, межуточные лимфогистиоцитарные инфиль¬
траты
Рис. 13.17. Биоптаты правого желудочка больной Г. (а-г). Окраска гематоксилином-
эозином, большое увеличение. Пояснения в текстеРис. 14.4. Сцинтиграфия миокарда больного Т. Пояснения в тексте
Рис. 14.5. MCKT органов грудной клетки больного Т. Пояснения в тексте. Стрелками
обозначены увеличенные внутригрудные лимфоузлыРис. 14.8. Феномен обратного перераспределения, выявляемый при последовательном
проведении сцинтиграфии миокарда в покое (левый рисунок) и с нагрузкой (правый
рисунок). Пояснения в тексте
Рис. 15.6. Трансаортальная экспозиция
передней створки митрального клапа¬
на (интраоперационная фотография).
Стрелкой обозначена перфорация перед¬
ней створки митрального клапанаРис. 15.8. Конверсия трансаортального
доступа к аортомитральной занавеске в
биатриальный доступ (интраопераци¬
онная фотография). Стрелкой указаны
головки папиллярных мышц с неохорда¬
ми из PTFE-нитей GoreTex CV5Рис. 15.10. Микропрепараты створок аортального (слева) и митрального (справа) клапа¬
нов. Окраска гематоксилином-эозином. Пояснение в тексте
Рис. 15.14. Цитохимическое исследование нейтрофилов на миелопероксидазу. Слева
положительный контроль (гранулы, содержащие миелопероксидазу, окрашены в корич¬
невый цвет). Справа кровь пациентки В., проба отрицательная (полное отсутствие гра¬
нул, содержащих миелопероксидазу)Рис. 16.6. Боррелии при микроскопическом исследовании
Рис. 16.7. Клещ Ixodes scapularis — переносчик боррелиоза. Слева — женская, мужская
особь и нимфа, справа — нимфа и «сытая» нимфаРис. 16.8. Мигрирующая эритема (Erythema
migrans) — начальное проявление борре-
лиозаРис. 17.4. Мультиспиральная компьютерная томография сердца с в/в контрастирова¬
нием. Слева — первичное изображение, справа — трехмерная реконструкция в цвете.
Стрелками показана псевдоаневризма левого желудочка. Участки кальцинирования
перикарда имеют интенсивную белую окраску
а о вРис. 17.7. Псевдоаневризма у больного, 59 лет, из работы N. Dobrilovic и соавт. (2007).
Компьютерная томограмма {а), интраоперационный снимок {б) и гистологическое
исследование стенки псевдоаневризмы {в), при котором в стенке аневризмы не выявле¬
но мышечной ткани. Пояснения в текстеРис. 19.6. Структура коннексинов. Пояснения в тексте
^ Д' ■ V < 'eU, ,,^ >* Л; \. ^ЧЛ«'. V * ^ --i' -s>sз*-**'■' 'i' »»v*«'*I» ''’'^’-^i■-Рис. 19.7. Результаты интраоперационной биопсии правого предсердия больной С.:
а — окраска гематоксилином-эозином; б-г — иммуногистохимическое исследование
на а-актин, десмин и виментин; д—е — электронная микроскопия. Пояснения в текстеРис. 20.6. Эндомиокардиальная биопсия больного П. Слева — окраска гематоксилином-
эозином, справа — ШИК-реакция. Пояснения в тексте
IРис. 20.7. Характерные внешние признаки болезни. Сверху — периферическая ангио¬
патия, ампутация фаланги, снизу — кератоангиомы в областях поясницы, нижней трети
живота, ягодичной, паховойРис. 21.6. Аутопсия правого (верхний ряд и левая половина нижнего ряда) и левого (пра¬
вая половина нижнего ряда) желудочков сердца больной Е., 22 лет. Пояснения в тексте
Herpes Simplex Virus Type 1 (HSV-1) ОБНАРУЖЕНО
Herpes Simplex Virus Type 2 (HSV-2) не выявлено
Human Herpesvirus (HHV-6) ОБНАРУЖЕНО ^4,І,■с:J»вS.'г' Л*■І, .. иVHerpes Simplex Virus Type 1 (HSV-1) не выявлено
Herpes Simplex Virus Type 2 (HSV-2) не выявлено
Human Herpesvirus (HHV-6) ОБНАРУЖЕНОРис. 21.11. Аутопсия левого (верхний ряд) и правого (нижний ряд) желудочков сердца
больного Ч., 40 лет. Пояснения в текстеs ■' , V "r ? V' "3 ГШV " T, 'Рис. 22.6. Эндомиокардиальная биопсия больного Ш. (участки межжелудочковой
перегородки и свободной стенки правого желудочка): а, б, г — окраска гематокси¬
лином-эозином: кардиомиоциты имеют более интенсивную розовую окраску, между
ними — светлая гиалиноподобная ткань (амилоид), плотно окутывающая мышечные
волокна; в — два скопления неокрашенных клеток — очаги липоматоза; г — видны
пустоты (результат лизиса кардиомиоцитов?), сохранившие внешнюю оболочку (т.е.
перимизий); д — окраска по Ван Гизону; в центре сосуд с утолщенными стенками, не
окрасившимися в фиолетовый цвет (цвет фиброза), как и нижележащие кардиомиоци¬
ты; д-и — окраска конго красным: отложения амилоида окрашены красным цветом, в
том числе в стенке сосуда (с сужением его просвета); наряду с периретикулярным нельзя
исключить внутриклеточное отложение амилоида
Рис. 23.18. Эндобронхиальные биоптаты опухоли больного Е.: а, б — гистологическое
исследование (окраска гематоксилином-эозином); в — цитологическое исследование.
Фотографии препаратов сделаны проф. Е.А. Коган
Рис. 23.19. Морфологическая и инструментальная диагностика первичной лимфомы
сердца: а — лимфома передней створки митрального клапана пересаженного сердца
(Jung A.J. et. al., 1997); б — макроскопическая картина лимфомы с поражением правых
отделов сердца (Fujita Y. et. al., 2009); в — макропрепарат сердца, пораженного лим-
фомой (инфильтративный рост опухоли, Skalidis E.I. et. al., 1999); г — ангиография:
лимфома с поражением правого желудочка и развитием сужения трикуспидального кла¬
пана (Tada Н. et. al., 1998); — MPT, режим ТІ: гипоинтенсивность сигнала от опухоли
(указана стрелками); е — МРТ, контрастирование гадолинием: участок ненакопления
гадолиния в зоне опухоли (указан стрелками) (Ryu S.J. et. al., 2001)
Рис. 24.4. Компьютерные томограммы больного Г., 23 лет, до операции. Верхний ряд;
компьютерные томограммы органов грудной клетки с внутривенным контрастирова¬
нием; слева — дефекты контрастирования ветвей легочной артерии (показаны стрел¬
ками), справа — выраженное снижение перфузии легких, особенно в нижней доле
левого легкого (КТ сосудов легких, выполненная в Лечебно-реабилитационном цен¬
тре Росздрава). Нижний ряд: компьютерные томограммы органов брюшной полости.
Реконструкция; стрелками показан протяженный тромб нижней полой вены с участка¬
ми кальцификации (справа)Рис. 24.5. Удаленные в результате тромбэндартерэктомии тромбированные «слепки»
легочных артерий. Из работы Jamieson S.W. и соавт. (2008)
Рис. 25.4. Изменения кистей больной Ю. Пояснения в текстеРис. 26.4. Антитела к цитоплазме нейтрофилов (ANCA): цитоплазматические (слева),
перинуклеарные (справа). В центре — схема участия ANCA в патологическом иммун¬
ном воспаленииРис. 27.2. Геморрагическая сыпь при повторной госпитализации в Факультетскую тера¬
певтическую клинику им. В.Н. Виноградова
СГ’Є сіШ-Рис. 30.6. Шизоты в мазке периферической крови (указаны стрелками)Рис. 31.4. Миелоидная кардиомиопатия вследствие инфильтрации миокарда легки¬
ми цепями иммуноглобулинов (Nakamura М. et. al., 2002). Слева — эхокардиограмма
пациента (утолщение стеноклевого желудочка). В центре — биоптат миокарда, окраска
конго красным (конго-положительного материала не выявлено. Справа — биоптат
миокарда, иммуногистохимическое исследование на легкие цепи иммуноглобулинов
(указаны стрелками)
Глава 5САРКОИДОЗ С ЗАТЯЖНЫМ ЛАБОРАТОРНЫМ
ДЕБЮТОМ И ВЫСОКОЙ ИММУНОЛОГИЧЕСКОЙ
АКТИВНОСТЬЮН.В. Чичкова, И.С. ЩедринаПредставленный в данной главе клинический случай интересен прежде
всего в связи с необычностью растянувшегося почти на 5 лет лабораторного
дебюта заболевания с яркой иммунной окраской, диагноз которого, несмо¬
тря на наличие убедительных морфологических данных и положительного
эффекта специфической терапии, все еще расценивается лишь как наиболее
вероятный.Больная К., 58 лет, впервые поступила в терапевтическое отделение
Факультетской терапевтической клиники Иім, В.Н. Виноградова в 2002 г. с
жалобами на общую слабость.Анамнез жизни без особенностей. Отмечалась аллергическая реакция на
сумамед в виде крапивницы.Из анамнеза заболевания {рис. 5.1) известно, что в 2000 г. впервые при случай¬
ном обследовании выявлено увеличение СОЭ до 29 мм/ч. С 2002 г. наблюдается20002002 2003 2004 10.2005 12.2005-01.2006СлабостьСОЭКашель,одышкаЛихорадка
1дМ мг/дл
IgG мг/длГ ипер-
протеинемия9,4 мг%Лечение Тиреоидэктомия Авелокс, амиксинРис. 5.1. Анамнез заболевания больной К., 58 лет (ло 2006 г.)
98 Пульмонологияв Факультетской терапевтической клинике им. В,Н. Винофадова, куда была
госпитализирована в связи с появлением астенических жалоб.При поступлении состояние было расценено как удовлетворительное.
Кожные покровы и видимые слизистые оболочки обычной окраски. Лимфоузлы
не увел№1ены. Число дыханий 16 в минуту. Дыхание везикулярное, хрипов нет.
Гранины сердца не расширены, юны не изменены. ЧСС 80 ударов в минуту. АД
120/80 мм рт.ст. Живот безболезненный, печень и селезенка не увеличены.В анааизах крови обращало на себя внимание увеличение СОЭ до 35 мм/ч,
были выявлены антитела к кардиолипину (Ig М 102 МЕ/мл, IgG 33,5 МЕ/мл),
повышение титра АНФ (1:80), антикардиолипиновый тест на сифилис ++++.
Было проведено тщательное обследование, в процессе которого выявлены
многоузловой эутиреоидный зоб (произведена нункция щитовидной железы,
цитологически — коллоидный зоб), формируюпщйся полип субкардиального
отдела желудка. Среди возможных состояний, объясняющих данные лаборатор¬
ные изменения, обсуждался диагноз первичного антифосфолипидного синдро¬
ма. Бьто рекомендовано хирургическое лечение многоузлового зоба, а также
динами^іеское наблюдение в связи с выявленными лабораторными данными.В 2003 г. произведена тиреоидэктомия, с этою времени получает замести¬
тельную терапию L-тироксином. После операции сохранялись асгенические
жалобы. При следующей госпитализации в Факультетскую терапевтическую
клинику им. В.Н. Виноградова в августе 2003 г выяштены увели^іение СОЭ до
46 мм/ч, умеренная гипохромная анемия, а также повышение уровня общего
белка до 90 г/л, IgM до 228 мг%, IgG до 2400 мг%, что потребовало дальней¬
шего более детального обследования. Был проведен онкопоиск, включавший
УЗИ органов брюшной полости, ЭГДС, маммофафию. Произведена биопсия
обнаруженного полипа желудка. С целью исключения гемобластоза проведены
стернальная пункция, рентгенография плоских костей. Все вышеперетаслен-
ные исследования не выявили каких-либо патологических изменений. Было
рекомендовано динамическое наблюдение.За время последующего наблюдения отмечалось дальнейшее увеличение
СОЭ (до 66 мм/ч), анемия и тромбоцитопения, гиперпротеинемия до 100 г/л,
а также высокий уровень иммуноглобулинов крови, антител к кардиолипину.
Впервые было выявлено также повьппение pANCA. Полученные данные обо¬
значили следующие направления диагностического поиска.1. Онкологическое заболевание как источник вышеуказанных изменений.2. Парапротеинемический гемобластоз, на что указывали существенное уве¬
личение СОЭ, гиперпротеинемия, поликлональная гаммапатия.3. Дебют системного васкулита или диффузного заболеваїїия соединитель¬
ной ткани.Онкопоиск включал проведение КТ органов брюшной полости и грудной
клетки, ЭГДС, колоноскопию, маммографию, гинекологическое обследова¬
ние, МРТ головного мозга. Проведенные обследования не выявили причину
лабораторных изменений.Гематологическое обследование было проведено в Гематологическом науч¬
ном центре РАМН и включало:
Глава 5. Саркоидоз с затяжным лабораторным дебютом... 99иммунохиминеское исследование белков сыворотки крови — подтверждена
поликлональная выраженная гипергаммаглобулинемия с высоким уровнем
ЦИК;трепанобиопсию костного мозга — кроветворная ткань представлена тремя
ростками гемопоэза в умеренном количестве на всех стадиях созревания.
Видны мелкие труппы лимфоцитов, диффузно рассеянные плазматические
клетки. Встречаются единичные белковые фолликуляты.По мнению гематологов, полученные результаты исключали парапротеи-
немический гемобластоз, изменения костного мозга могли расцениваться как
вторичные. Подобное гематологическое обследование было повторно проведе¬
но в 2005 г. и имело сходные результаты.Столь выраженные лабораторные изменения [стойкое увеличение СОЭ,
гипергаммаглобулинемия до 43 отн%, повышение IgG до 3000 мг%, положи¬
тельный антикардиолипиновый тест на сифилис, вновь выявленный высокий
уровет РФ (1530 МЕ/мл) и АНФ (1:40), значимое повышение pANCAJ не
позволяли исключить дебют диффузного заболевания соединительной ткани или
системного васкулита. В то же время отсутствовали критерии, необходимые
для достоверной постановки конкретного нозологи^іеского диагноза. На дан¬
ном этапе имели место лишь лабораторные изменения, не дающие представле¬
ния о характере заболевания: больная предъявляла лишь астенические жалобы,
которые могли быть связаны и с имевшимся у нее первичным гипотиреозом.Следующий этап развития болезни следует отнести к 2005 г. Летом этою
года больная отметила появление малопродуктивного приступообразного
кашля, несколько позже — выделения из носа гнойного характера, повыше¬
ние температуры тела до фебрильных цифр. По поводу предполагаемого гай¬
морита проводилась терапия пероральными цефалоспоринами с некоторым
эффектом. В связи с сохраняющимся кашлем в сентябре 2005 г іюступила в
Факультетскую терапевтическую клинику им. В.Н. Виноградова для обследо¬
вания и динамического наблюдения.При осмотре обращало на себя внимание лишь жесткое дыхание, неболь¬
шое количество басовых хрипов. Проведенное лабораторное обследование
выявило дальнейший рост СОЭ до 73 мм/ч, сохранение умеренной анемии,
тромбоцитопении, гиперпротеинемии, повышения уровня иммуноглобулинов
М (до 600 мг%) и G (до 6340 мг%).По результатам оценки ФВД выявлялись умеренные признаки бронхооб-
струкцим. Характер мокроты расценивался как слизисто-гнойный. С учетом
вновь появившейся легочной симптоматики была проведена КТ органов груд¬
ной клетки. Впервые за время наблюдения были выявлены изменения: отме¬
чено появление зон сетчатого фиброза и уплотнения легочной ткани по типу
«матового стекла*> субплеврально в разных отделах легких, больше в базальных
отделах левого легкого.Больная была осмотрена оториноларингологом', атрофические изменения
слизистой оболочки носа могли рассматриваться в рамках системного васку¬
лита. Учитывая данную клинико-рентгенологическую картину, измененрія
со стороны ЛОР-органов, выявлявшееся ранее повышение титра pANCA,
і 00 Пульмонологиябольная была направлена на консультацию к профессору Е.Н. Семенковой,
по мнению которой убедительных данных в пользу системного васкули-
та недостаточно: отсутствуют поражение почек, характерные изменения
слизистой оболочки носа, поражение нервной системы, эозинофилия.
Обсуждался первичный амилоидоз легких как причина данных изменений
паренхимы легких. Были выполнены биопсия подкожно-жировой клетчат¬
ки передней брготпной стенки, препараты удаленной шитовидной железы
окрашены на амилоид. Проведенные морфологические исследования также
не дали положительных результатов: амилоид в исследуемых тканях не был
выявлен.Для уточнения характера поражения легких обсуждалось проведение биоп¬
сии легочной ткани. Однако эта манипуляция не была проведена в связи со
значительным ухудшением состояния больной, которое наступило 20,12.2005 г.
Вскоре после контакта с больными респираторной вирусной инфекцией у паци¬
ентки повысилась температура тела до фебрильных цифр, появились малопро¬
дуктивный кашель, боль в грудной клетке при дыхании, одышка. В дальнейшем
состояние !ірогрессивно ухудшалось, нарастала одышка. При рентгенологиче¬
ском исследовании была выявлена картина двусторонней пневмонии, в связи с
чем больная была госпитализирована в Факультетскую терапевтическую клини¬
ку им. В. Н. Виноградова.При поступлении в клинику состояние расценивалось как тяжелое, отме¬
чалась выраженная одышка до 36 в минуту, влажные разнокалиберные
хрипы практически над всей поверхностью легких, ЧСС 110 ударов в минуту,
АД 100/60 мм рт.ст.В анализах крови выявля,1ись умеренный нейтрофильный лейкоцитоз, уве¬
личение СОЭ до 69 мм/ч, нормохромная анемия. Характер мокроты лейкоци¬
тарный. В посеве мокроты обнаружен рост Str. рпеит.. Sir. gr. viridans в диагно¬
стически значимых титрах.При проведении МСКТ легких органов грудной клетки (рис. 5.2): в задних
отделах обоих легких (6, 9, 10-й сегменты) определялись зоны пониженной
воздушности легочной ткани типа «матового стекла». В субплевральных отде¬
лах тех же сегментов — участки консолидации неправильной формы. Во 2, 3 и
8-м сегментах правого легкого и язычковых сегментах левого легкого опреде¬
лялись участки «матового стекла» без четких границ, В верхушках обоих легких
имелись участки фиброза. Стенки бронхов утолщены, В правой верхней пара-
трахеальной и трахеобронхиальной областях — увеличенные лимфатические
узлы.Были начаты терапия авелоксом в/в капельно, амиксином, оксигенация,
инфузионная и бронхолитическая терапия. В связи с тяжестью состояния,
тяжелой дыхательной недостаточностью (SatOj 82%) больная была переведена
в отделение интенсивной терапии и реанимации. В результате проводимой
антибактериальной, противовирусной, инфузионной терапии, оксигенотера-
пии состояние значительно улучшилось, температура тела нормализовалась,
купировались явления дыхательной недостаточности. Была выполнена МСКТ
легких в динамике: отмечено повьппение воздушности легочной ткани во всех
Глава 5. Саркоидоз с затяжным лабораторным дебютом...101Рис. 5.2. КТ легких больной К. от 2005 г (пояснения в тексте)отделах, уменьшение >’частков «матового стекла» и участков консолидации,
формирование фиброза в 6, 9, 10-м сетоентах обоих легких, небольшие участ¬
ки консолидации в 10-х сегментах легких, уменьшение размеров лимфоузлов
средостения.Дифференциальный диагноз проводился между двусторонней полисег-
ментарной пневмонией и интерстициальной пневмонией. С учетом эпиде¬
миологического анамнеза, высевания из мокроты возможного возбудителя
заболевания, эффективности проведенной антибактериальной терапии, рент¬
генологического регресса выявленных изменений более вероятным пред¬
ставлялся диагноз двусторонней полисегментарной пневмонии. В то же время
нельзя бььто не учитывать предшествуюшее развитие болезни, недавнее появ¬
ление изменений легочной ткани, что могло быть очередной стадией развития
интерстициальной болезни легких.В дальнейшем больная оставалась под наблюдением. Сохранялись сла¬
бость, одышка при умеренной физической нагрузке, малопродуктивный
кашель. При проведении МСКТлегких, выполненной в марте 2006 г. {рис. 5.3),
отмечена отрицательная динамика в виде увеличения зон «матового сіхік-та» и
повышения их плотности, появления слева, в области диафрагмальной іьтев-
ры, округлого мягкотканного образования размером 13x13 мм.Из всего многообразия форм интерстициальных болезней легких в круг
дифференциального диагноза у нашей больной могли быть включены следую¬
щие состояния,Саркоидоз— в его пользу свидетельствовали юшнические проявления
(кашель, одышка), характер изменения паренхимы легких («матовое стекло»,
очаговые тени, фиброз), внутригрудная лимфоаденопатия. В то же время для
саркоидоза не характерны затяжной лабораторный дебют (на протяжении3 лет), столь выраженная иммунная активность, отсутствие четкой рентгено¬
логической стадийности.
W2ПульмонологияРис. 5.3. КТ легких больной К. от марта 2006 г.
(поясненш! В тексте)криптогенная организующаяся
пневмония — для нее также харак¬
терны кашель, одышка, лихорад¬
ка, увеличение СОЭ в сочетании
с изменениями по типу «матового
стекла» и участками консолидации
и столь же не типичны длительный
лабораторный дебют и выраженные
иммунные сдвиги.Лимфоцитарная интерстициаль¬
ная пневмония — этому диагнозу
до некоторой степени противоре¬
чило обнаружение локальных теней
и фиброза при выполнении КТ лег¬
ких, однако высокая иммунологи¬
ческая активность и затяжное тече¬
ние как раз достаточно типичны для
этого варианта интерстициального
поражения легких.После стабилизации состояния больной 28.04,2006 г. в Национальном меди-
ко-хирургическом центре им. Н.И. Пирогова была выполнена видеоторако¬
скопия с атипичной резекцией 8 и 10-го сегментов правого легкого. При реви¬
зии ткань легкого резко >таотцена, ригидна при инструментальной пальпации.
Лимфоузлы в средостении не увеличены.При морфологическом исаіедоваиии биоптатов легкого (кафедра патологи¬
ческой анатомии ММА им. И.М. Сеченова, профессор Е.А. Коган) выявлены
ятутсния альвеолита с выраженной лимфоплазматической и макрофагальной
инфшіьтрацией легочного интерстиция со скоплением макрофагов, гигантских
многоядерных клеток типа Пирогова—Лангханса, инородных тел, лимфоцитов
в просветах альвеол и со склерозом альвеолярных перегородок. В зоне воспа¬
лительного инфильтрата — картина продуктивного васкулита мелких сосудов.
Легочная ткань также содержит множество саркоидных гранулем из эпители-
оидных клеток, гигантских многоядерных клеток типа Пирогова-Лангханса
и лимфоцитов. По периферии гранулем имеется незначительный фиброз.
Явления выраженного хронического обструктивного панбронхита и бронхио-
лита с воспалительной лимфогистиоцитарной и плазмаклеточной инфильтра¬
цией. Имеются также признаки развивающейся легочной гипертензии.Препараты были также исследованы в патологоанатомическом отделении
НИИ онкологии им. П.А. Герцена: диагностирован продуктивный воспали¬
тельный процесс с наличием гигантских многоядерных клеток, лимфоштаз-
мацитарной и гистиоцитарной инфильтрацией, микроскопический альвеолит,
бронхиолит. Опухолевого роста не обнаружено. Больная была также обследова¬
на в НИИ фтизиопз'льмонологии, диагноз туберкулеза исключен.Данный клинический случай имеет ряд особенностей. Прежде всего
его отличает затяжной лабораторный дебют с высокой иммунологической
Глава 5, Саркоидоз с затяжным лабораторным дебютом..103напряженностью, іірсдіттествуюший клиническим проявлениям болезни почти
за 5 лет. Кроме того, следует отметить многообразие рентгенологических про¬
явлений (v^MaTOBbie стекла», консолидация, сетчатый фиброз) и их сравнитель¬
но быструю трансформацию. В то же время по совокупности данных и прежде
всего на основании морфологической картины в биоптатах легких наиболее
вероятным представлялся диагноз саркоидоза легких.Больная была ііаиравлсна в Кшнику терапии и профессиональных заболеваний
им. Е.М. Тареева, куда была госпитализирована впервые летом 2006 г. (рис. 5.4)
с жалобами на одышку при умеренной физической нагрузке, кашель с мокро¬
той слизистого характера, слабость. При аускультации выслушивалось жесткое
дыхание, хрипы отсутствовали. В анализах крови СОЭ 65 мм/ч, общий белок
до 11,7 г/дл, повышение уровня IgM до 460 мг/дл, IgG до 5900 мг/дл, резко
положительный РФ, повышение уровня антител к кардиолипину.На основании имеющихся морфологических данных, клинической картины
состояние было расценено как саркоидоз хронического течения с поражением
легких. В качестве базисной терапии был назначен плаквенил 400 мг/сут в соче¬
тании с витамином Е. Однако данная терапия не бьта достаточно эффективной,
сохранялись астенические жалобы, дыхательная недостаточность. При повтор¬
ной госпита^тизации в клинику им. Е.М. Тареева в сентябре—октябре 2006 г.
сохраня;1ись увеличение СОЭ, анемия, гиперпротеинемия, поликлональная
гаммапатия. При проведении КТ легких отмечались утолщение и деформация
интерстиция в субплевральных отделах легких, наиболее выраженные в средней
доле правого легкого и язычковых сегментах левого легкого. Полученіїьіе резуль¬
таты Дсии основанинс говорить о высокой степени активности саркоидоза.05.200606.200610.200603.200703.2008СлабостьСОЭКашель,одышкаСухость слизи¬
стых оболочек,
увеличение
слюнных желез.IgM мг/дл
IgG мг/длГ ипер-протеинемияЛечение17 мм/ч16 мм/ч65 мм/ч50 мм/ч4 460 Л575217210594046001460138011,7 мг%10,5 мг% 7,3 мг%7,5 мг%Плаквенил Метипред 12 мг/с Метипред 4 мг/с +
800 мг/сут + Плаквенил 200 мг/с Плаквенил 400 мг/сРис. 5.4. Ана\гнез больной К., 58 лет, после 2006 г.
104ПульмонологияВ это же время отмечено появление сухости слизистых оболочек глаз, уве¬
личение околоушных желез, при лабораторном исследовании были выявлены
антитела к экстрагируемым ядерным антигенам SS-A, SS-B, что не позволило
полностью исключить синдром Шефена как в рамках саркоидоза, так и в каче¬
стве самостоятслыюго заболевания. Высокая активность саркоидоза, появ-
ЛС1ШЄ синдрома Шсгрена дали основание для назначения кортикосшроидов
внутрь (метипред 12 мг/сут в сочетании с плаквснилом 200 мг/сут), которые
оказали значимый клинический и лабораторный эффект: уменьшились одъттп-
ка, кашель, значительно снизились СОЭ (до 17 мм/ч), уровень общего белка
[до 73 г/л РФ (27,6 МЕ/мл), TgG 1400 мг/дл], отмечено отчетливое улучшение
состояния легочной ткани поданным КТ {рис. 5.5).Таким образом, рабочим диагнозом, основанным прежде всего на результа¬
тах морфологического исследования, являлся саркоидоз хронического течения
высокой степени активности с поражением легких, леченный глюкокортико¬
стероидами; синдром Шегрена (сухой ксратоконъюнктивит, увеличение око¬
лоушных желез).Саркоидоз — мультисистемный относительно доброкачественный гранулс-
матоз неизвестной этиологии, характеризующийся скоплением активирован¬
ных Т-лимфоцитов и мононуклеарных фагоцитов, образованием несекрети-
руюших эпителиодноклеточных неказеозных гранулем в различных органах.
История изучения саркоидоза насчитывает более 130 лет.• В 1877 г Дж. Хатчинсон описал первый случай саркоидоза — больного с
пятнами на коже, которые постепенно развивались в течение 2 лет симме-
тршшо на ногах и руках.• В 1889 г Э. Бенье описал пациента с увеличенными лимфатическими узла¬
ми и пурпурно-фиолетовым опуханием носа, эрозией носовой полости и
серовато-синим опуханием ушей и пальцев {lupus pemio — «ознобленная
волчанка»).• В 1899 п Ц. Бек обнаружил сочетание кожных проявлений болезни с пора¬
жением глаз, легких, костей, селезенки; на основании морфологического
изучения кожи прехтожил термин саркоидоз, образованный от слов sar--
cos — мясо и eidos — вид («подобный мясу»).• В 1941 г. А. Квейм предложил
проведение специальной кожной
пробы с целью дифференциальной
диагностики между туберкулезом и
саркоидозом — внутрикожное вве¬
дение суспензии саркоидных лим¬
фоузлов вызывает образование мел¬
ких узелков (проба Квейма).• В 1946 г. С, Лефгрен описал соче¬
тание узловатой эритемы, двусторон¬
ней лимфаденопатии, полиартрита
и лихорадки как раннее проявление
саркоидоза.Рис. 5.5. КТ легких больной К. от февраля
2008 г. (пояснения в тексте)
Глава 5. Саркоидоз с затяжным лабораторным дебютом... 105• В 1958 г. К. Вурм предложил выделять стадии саркоидоза на основании
рентгенологических изменений в легких и внутригрудньтх лимфоузлов.• в 1987 г была создана Всемирная ассоциация саркоидоза и других грану¬
лематозных болезней — WASOG.• В 1999 г. было принято последнее соглашение по диагностике и лечению
саркоидоза.Саркоидоз называют «великим имитатором», «болезнью-хамелеоном».
Неполный список клинических симптомов и синдромов, которые могут встре¬
чаться при саркоидозс, вк.іючает лихорадку, астенический синдром, потерю
массы тела, узловатую эритему, артралгии/артриты, сухой синдром, лимфа-
дснопатию, гепатомегалию, спленомегалию, миопатию/миозит. Наиболее
типично при саркоидозе развитие поражения легких (у 90% больных), лимфа-
денопатии (в 75-90% случаев выявляется увеличение прикорневых и паратра-
хеальных, реже ~ периферических лимфоузлов), неспецифических симптомов
(сухой кашель, одышка, боли в трудной клетке, как исключение — плевраль¬
ный выпот). Рентгенологические стадии не отражают хронологической после¬
довательности развития саркоидоза, но коррелируют с вероятностью того или
иного исхода болезни.Стадия О — изменения обнаруживаются при проведении КТ высокою раз¬
решения.Стадия 1 — двустороннее увеличение лимфоузлов корней легких и средосте¬
ния (возможна спонтанная регрессия в 55-90% случаев).Стадия Н — двусторонняя лимфаденопатия + изменения в легких, которые
могут быть очаговыми, сетчатыми или по типу «матового стекла» {рис. 5.6, а).Стадия III — отсутствует лимфаденопагия; изменения легких, которые
могут быть очаговыми, сетчатыми или по типу «матового стекла», признаки
фиброза {рис. 5.6,6).Ст адия rv — фиброзные изменения в виде «сотового легкого», уменьшение
объема легочной ткани за счет фиброза {рис. 5.6, в, г).На I стадии процесса в биоптатах легких вьшвляегся лимфоцитарный альве-
олит; на И стадии развивается фанулсматозное воспаление {рис. 5.7, см. цвет¬
ную вклейку) — выявляются саркоидные гранулемы, состоящие из скоплений
макрофагов, лимфоцитов, эпителиоидньтх клеток и гигантских многоядерных
клеток типа Пирогова-Лангханса. Гранулемы располагаются по ходу бронхо¬
сосудистого пучка, в стенках легочной артерии, вдоль лимфатических сосудов,
что доказывает иммунный характер восп^шения.Разнообразие клинической картины саркоидоза обус;ювлено его внслсгоч-
ными проявлениями: поражением кожи (узловатая эритема, «ознобленная вол¬
чанка», бляшки, папулы и др., встречается в 25% случаев), глаз (25% — иридо-
циюшт, острый передний увеит), печени (до 80% поданным морфологнгческого
исследования, клинически часто протекает бессимптомно), сердца (5-10%),
нервной системы (5—10% — полинейропатия, схшнальные синдромы), почек
(40% по данным морфологического исследования, клинически не более чем
у 10% — саркоидный тубулоинтерстициальный нефрит), мышечно-суставным
синдромом (25-39%).
Ї06ПульмонологияРис. 5.6. Рентгенологические стадии саркоилоза: а — П стация; б — ТП стадия; в и г — IV
стадия (пояснения п тексте)Особые сложности в диагностике саркоидоза возникают при развитии его
относительно редких клинических прояштений:1) саркоидного поражения кожи: подкожного саркоида Дарье—Русси (гра¬
нулематозных узлов в подкожно-жировой клетчатке с расположением иреиму-
шественно на лиие, в области глаз и на щеках); алопеции; обширных полей
инфильтративных бляшек; феномена «оживших» рубпов; изменений кожи,
схожих с псориазом;2) гранулематозного васкулита легочных сосудов с развитием легочной
гипертензии и легочного сердца (развивается в 1—4% случаев, протекает бес¬
симптомно до появления значимой легочной гипертензии); при этом признаки
системного васкулита отсутствуют;3) поражения верхних дыхательных путей (встречается в 5% случаев):
выраженной заложенности носа, не поддающейся лечению деконгестантами
и назальными стероидами; перфорацией носовой перегородки, а также раз-
рутпсния хряш:ей с формированием «седловидного носа»; поражения гораани и
голосовых связок (осиплость, стридорозное дыхание, синдром ночного апноэ);
увеличения миндачин, макроглоссии в сочетании с лихорадкой, не поддаю¬
щихся лечению антибактериальными препаратами;4) поражения глаз: неврита зрительного нерва или ретинита с быстропро¬
грессирующей слепотой; синдрома Хеерфордта как варианта острого саркоидоза
(лихорадки, иридоииклита, увеличения околоушных желез, поражения лип;еюю
нерва);
Глава 5. Саркоидоз с затяжным лабораторным дебютом,.. 1075) поражения желудочно-кишечного тракта: гранулематозного гепатита
(лихорадки, гепатомегалии, в отсутствие лечения — быстрого развития цир¬
роза с тяжелой портальной гипертензией); эзофагита с упорной дисфагией,
диспепсией и абдоминальной боли по ходу тонкого и толстого кишечника,
аппендицита;6) поражения сердца: нарушений ритма и проводимости; поражения кла¬
панного аппарата с развитием недостаточности митрального, аортального,
TpHKycnHna-ibHoro клапанов и клапана легочной артерии; тяжелой сердечной
недостаточности при диффузном поражении миокарда; сухого и выпотного
перикардита;7) гематологических синдромов — поликлональной гипергаммаглобулине-
мии {возможно также снижение уровня гаммаглобулинов с развитием имму¬
нодефицита); панцитопении при отсутствии спленомегалии и гиперспленизма
(обусловлена гранулематозным поражением костного мозга); хронической
периферической лимфааенопатии;8) поражения эндокринной системы: дисфункции гипоталамо-гипофизар-
ной системы с развитием несахарного диабета; узлового поражения щитовид¬
ной железы с нарушением функции; тиреоидита; первичной надпочечниковой
недостаточности;9) поражения мочеполовой системы: у мужчин — острого эпидидимоорхи-
та, увеличения яичек; у женщин — дисменореи, опухолевьЕс поражений матки
и яичников (редко клинически значимые).Саркоидоз — иммунное заболевание, патогенетическое лечение которо¬
го состоит в назначений иммуносупрессивной терапии. Однако постановка
достоверного диагноза саркоидоза далеко не всегда означает необходимость в
проведении специфической терапии, поскольку течение заболевания вариа¬
бельно, нередко оно имеет тенденцию к спонтанной ремиссии, в частности,
патогенетическая терапия не назначается при:• остром саркоидозе (вариант Лефгрена);• впервые выявленном саркоидозе I и 11 стадий;• бессимптомном саркоидозе, не прогрессирующем при динамическом
наблюдении.Показаниями к назначению патогенетической терапии при саркоидозе
являются:• признаки дыхательной недостаточности, особенно профессирующей;• прогрессирование внутригрудных изменений, II и ПТ стадии саркоидоза;• внелегочные проявления саркоидоза, в особенности впервые появившие¬
ся или прогрессирующие;• поражение почек;• поражение сердца;• поражение центральной нервной системы.Основой патогенетической терапии саркоидоза яатяются глюкокортико¬
стероиды, которые применяются с 1950 г.; длительность лечения составляет
не менее 6 мес, преднизолон назначается в начальной дозе 40 мг/сут с ее мед¬
ленным постепенным снижением до 5 мг/сут. Эффективность ингаляционных
108 Пульмонологиякортикостероидов доказана лишь в сочетании с пероральными в отношении
симптоматической терапии кашля. Топическое использование кортикостерои¬
дов возможно также при поражении кожи, глаз.При генерализованном саркоидозе, в особенности с поражением централь¬
ной нервной системы, глаз, кожи, при наличии резистентности к кортикосте¬
роидам дополнительно назначают цитотоксические препараты (метотрексат,
азатиоприн, циклофосфамид), которые применяются с 1968 г Длительность
терапии также составляет не менее 6 мес.Производные 4-аминохинолина используют в качестве иммунодепрессив-
ной терапии для лечения кожного саркоидоза или в комбинации с кортикосте¬
роидами; доказанная эффективность не превышает 50%.Наконец, антибиотики тетрациклинового ряда (доксициклин, миноци-
клин) используют в лечении хронического кожного саркоидоза; они обладают
бактерицидным эффектом в отношении Propionibacterium acnes — предполагае¬
мого бактериального агента при саркоидозе.Перспективы в лечении саркоидоза связаны с применением биологических
препаратов: моноклональных антител к ФНО-а (инфликсимаб; использу¬
ется при рефрактерном к стероидам саркоидозе с выраженными органными
нарушениями), а также пентоксифиллина (подавляет выработку питокинов,
в частности ФНО-а, альвеолярными макрофагами; эффективен при остром
саркоидозе в сочетании с кортикостероидами; назначается в дозе 25 мг/кт в
течение 6 мес). Сообшается также об использовании для лечения саркоидоза
талидомида — антииитокинового препарата, обладающего выраженным тера¬
тогенным эффектом и не зарегистрированного в РФ.В нашем сл>^ае, несмотря на отсутствие выраженных системных прояв¬
лений (за исключением синдрома Шегрена), терапия плаквенилом оказалась
недостаточной, потребовалось назначение кортикостероидов, что обуслов¬
лено, по-видимому, высокой лабораторной активностью болезни. Вместе с
тем отчетливый клинический эффект оказала небольшая доза метипреда, что
позволяет прогнозировать относительно благоприятное течение болезни.
Глава 6ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ЛЕГОЧНЫХ
ЭОЗИНОФИЛИЙ: ОТ БРОНХИАЛЬНОЙ АСТМЫ
К СИНДРОМУ ЧЕРДЖА-СТРОССС.И. Овчаренко, И.В. Чичкова, И.В. Морозова,И£, Щедрина, В Л. КапустинаВ данной главе, завершающей раздел «Пульмонология», будут рассмотрены
еще два клинических наблюдения, при которых ведущим клиническим про¬
явлением системного заболевания (АНЦА-ассоциированного васкулита) стало
поражение легких. Путь к диагнозу в представленных случаях был непростым:
заболевание дебютировало картиной типичной бронхиальной астмы, и лищь
высокая эозинофилия в сочетании с системными проявлениями заставила
проводить расщиренный диагностический поиск. Рассматриваются вопро¬
сы дифференциальной диагностики эозинофилий, в том числе с поражением
легких, клиническая картина, диагностика и дифференциальная диагностика
эозинофильного ангиита (синдрома Черджа-Стросс); обсуждаются современ¬
ные возможности специфической терапии.Эозинофилия — увеличение уровня эозинофилов в крови — встречается в
клинической практике врачей многих специальностей, но наиболее часто в
практике пульмонологов, аллергологов и инфекционистов. Круг болезней и
состояний, при которых встречается эозинофилия, довольно обширен и разно¬
образен, Количество эозинофилов в нормальном мазке крови составляет 1-5%
от общего числа лейкоцитов или в абсолютном исчислении 120—250 эозино¬
филов в 1 мкл крови, при числе эозинофилов 500-1500 клеток в 1 мкл крови
констатируют легкую эозинофилию, при 1500-5000 — умеренную гиперэози-
нофилию, при количестве >1500 говорят о выраженной гиперэозинофилии,
которая встречается редко.В зависимости от уровня иммуноглобу.чина Е (IgE) в периферической крови
эозинофилии делят на реактивные, сопровождающиеся повыщением уровня IgE,
и клональные, при которых уровень IgE, как правило, остается нормальным.Около четверти случаев реактивных эозинофилий вызваны паразитарными
инвазиями (трихинеллез, стронгиловдозы, анкилостомоз, аскаридоз, токсока-
роз и др.), грибковыми заболеваниями и ретровирусной инфекцией, но наибо¬
лее частой причиной реактивной эозинофилии являются аллергические забо¬
левания, в первую очередь болезни дыхательных путей (аллергический ринит,
бронхиальная астма) и кожи (крапивница, атопический дерматит). Системные
васкулиты также могут протекать с повышением уровня IgE. Кроме того, реак¬
тивные эозинофилии возникают при иммунодефицитных состояниях, неопла¬
стических процессах (опухолях толстой кишки, легких, молочных желез).
но ПульмонологияЮюнальные эозинофилии развиваются при гематологических заболеваниях:
димфогранулематозах, лимфо- и миелопролиферативных состояниях, в том
числе при гиперэозинофильном идиопатическом синдроме. Эозинофилия при
данных состояниях обусловлена прямой или опосредованной пролиферацией
кроветворных клеток.Причины эозинофилии• Аллергические заболевания (аллергический ринит, бронхиальная астма,атопический дерматит, лекарственная аллергия).• Инфекции:— глистные инвазии (филяриозы, эхинококкоз, трихинеллез, токсокароз,
стронгилоидоз, аскаридоз и др.);— системные микозы (в том числе бронхолегочный аспергиллоз);— туберкулез.• Онкологические заболевания:— злокачественные новообразования внутренних органов;— лимфопролиферативные заболевания (лимфомы, острый лимфобласт¬
ный лейкоз, болезнь тяжелых цепей);— миелопролиферативные заболевания (эозинофильный лейкоз, хрони¬
ческий миелолейкоз);— гистиоцитозы.• Заболевания соединетельной ткани:— васкулиты [аллергический гранулематозный ангиит (синдром Черджа—
Стросс), гиперсенситивный васкулит];— ревматоидный артрит;— эозинофильный фасциит.• Другие заболевания и состояния (болезнь Аддисона, хронический гемоди¬
ализ, лучевые поражения).• Идиопатическая гиперзозинофилия,У взрослых наиболее частой причиной умеренной эозинофилии является
реакция на лекарственный препарат (пенициллины, цефалоспорины, нитро-
фураны, противогрибковые и противотуберкулезные средства, нестероидные
противовоспалительные препараты, психотропные препараты). В последнее
время много внимания уделяется эозинофилиям, вызванным приемом пре¬
паратов, применение которых обычно сопровождается снижением уровня
эозинофилов: кромогликата натрия, кортикостероидов.В отдельную групггу выделяют легочные эозинофилии, отличительной чер¬
той которых являются эозинофильные инфильтраты легких; условно их делят
на первичные и вторичные. К группе первичных (идиопатических) легочных
эозинофилий относят простую, острую и хроническую эозинофильные пнев¬
монии, идиопатический гиперэозинофильный синдром и синдром Черджа—
Стросс.простая эозинофильная пневмония, или синдром Леффлера — относитель¬
но легко протекающее заболевание с минимальными проявлениями брон¬
холегочного синдрома и благоприятным прогнозом. Основной причиной ее
развития являются паразитарные заболевания. Кроме того, описаны простые
Глава 6. Дифференциальная диагностика легочных эозинофилий... 1Иэозинофильные пневмонии, развившиеся после приема некоторых лекар¬
ственных препаратов. Чаще всего лечение не требуется (достаточно провести
дегельминтизацию или отменить лекарственный препарат, который вызвал
заболевание).Острая эозинофильная пневмония отличается более тяжелым течением,
быстрым развитием гипоксемии, острой дыхательной недостаточности.
Легочные инфильтраты локализуются преимущественно в верхних отделах
легких, инфильтрация часто затрагивает плевру, что может сопровождаться
накоплением экссудата в п-певральных: полостях. Несмотря на невысокое коли¬
чество эозинофилов в периферической крови, в бронхоальвеолярной жидко¬
сти их количество резко увеличено (>40%). при назначении кортикостероидов
прогноз благоприятный.Хроническая эозинофильная пневмония протекает не так остро, может длиться
неделями и даже месяпцами. Заболевание протекает с кащлем, одьппкой, лихорад¬
кой, потерей массы тела, анемией, гепатомегалией и диффузной полиаденопатией.
Помимо высокой эозинофилии периферической крови, отмечается эозинофилия
бронхоальвеолярного лаважа. У большинства больных обнаруживается феномен
«матового стекла», легочные инфильтраты локализукугся преим>тцественно в
области верхушек легких и ближе к периферии, самостоятельно инфильтраты раз¬
решаются редко. Заболевание хорошо поддается лечению кортикостероидами.Диагноз тдиопатический гиперэозинофильный синдром» ставится при
наличии эозинофилии периферической крови, сохраняющейся более 6 мес,
когда исключены и паразитарные инфекции, и аллергические заболева¬
ния. Клиническая картина проявляется кашлем, повышением температуры,
неспецифическими симптомами. На этом этапе проводится лишь динамиче¬
ское наблюдение за больными. В более поздних стадиях поражается костный
мозг, сердечно-сосудистая и нервная система, селезенка. Прогностически
неблагоприятным является поражение сердца в связи с развитием эндокарди¬
та, некрозов миокарда, фиброза миокарда с дальнейшим переходом в рестрик¬
тивную кардиомиопатию, с образованием внутрисердечных тромбов. Основой
терапии при полиорганном поражении являются стероиды.Синдром Черджа—Стросс проявляется приступами бронхиальной астмы,
синуситами и обтцими симптомами (повышением температуры, похуданием,
повышенной утомляемостью, слабостью). Поражаются сосуды кожи, серд¬
ца, центральной нервной системы, почек. Американская ревматологическая
ассоциация в 1990 г. определила критерии диагноза синдрома Черджа—Стросс.
Диагаоз синдрома Черджа-Стросс является достоверным при наличии по
крайней мере четырех из шести перечисленных критериев:1) бронхиальной астмы;2) эозинофилии периферической крови >10%;3) эозинофильных легочных инфильтратов;4) параназального синусита;5) множественных мононевритов или полинейропатии;6) гистологических признаков васкулита с присутствием эозинофилов
в тканях.
112 ПульмонологияЗаболевание хорошо поддается лечению кортикостероидами.К группе вторичных легочных эозинофилий относят аллергический брон¬
холегочный аспергиллез, тропическую легочную эозинофилию.Аллергический бронхолегочный аспергиллез — это своего рода бронхиаль¬
ная астма с синдромом гипсрэозинофилии и высоким содержанием IgE.
Но заболевание протекает с повышением температуры, кашлем с мокротой
грязно-серого, коричневого цвета. Характерными являются бронхоэктазы цен¬
трального типа (проксимальные). Гиперэозинофилия выявляется как в пери¬
ферической крови, так и в мокроте. Причиной заболевания яв;іястся колони¬
зация на слизистой оболочке трахеи и бронхов Aspergillus fumigatus, поэтому в
постановке диагноза большую роль играет выявление колоний этих грибов в
мокроте, определение в крови специфических антител к антигену аспергилл.
Лечение проводится кортикостероидами и другими противоастматичсскими
препаратами.Тропическую легочную эозинофилию вызывают микрофилярии Wuchereria
bancrofti, Brugia malayi. Характеризуется она тяжелыми приступами по типу
бронхиальной астмы, вплоть до астматического статуса, лихорадкой, кашлем с
трудноотделяемой слизистой мокротой, ноюшими, иногда приступообразны¬
ми болями в животе без четкой локализации, периферической лимфаденопа-
тией, кожной сыпью, полиартралгиями, спленомегалией. Важными являются
очаговые инфильтративные, часто диссеминированные (милиарные) изме¬
нения в легких и высокая, «ошеломляющая» эозинофилия периферической
крови (60—80%), высокое содержание в крови IgE вместе с высоким титром
антифилярийных аитител. Хороший ответ на лечение антигельминтными пре¬
паратами подтверждает диагноз.Приводим клинические наблюдения, свидетельствующие о сложности диф¬
ференциальной диагностики легочных эозинофилий.Больная Ч., 57 лет, москвичка, преподаватель по образованию, поступила
в терапевтическое отделение Факультетской терапевтической клиники им.
В.Н. Виноградова 07.09.2004 г с жалобами на ощущение заложенности в груд¬
ной клетке, затрудненное дыхание, покапыивание, одышку при физической
нагрузке, головные боли, потливость по типу приливов, общую слабость.Из анамнеза жизни известно, что по роду своей деятельности больная часто
контактирует с мелкодисперсной пылью дерева, парами пластика, масел. Не
курит, дома содержит собаку С 11 лет страдает миіренью, периодически при¬
нимает анальгетические препараты. Перенесла несколько операций: в 26 лет —
тонзиллэктомию в связи с часто повторяющимися ангинами, в 53 года — амп>'-
тацию матки и левого яичника из-за миомы матки и кисты левого яичника.Из анамнеза заболевания известно, что в 15 лет обратила внимание на
периодически возникающий приступообразный кашель, заложенность носа.
Состояние расденивалось как хронический фарингит, аллергический ринит.
Со временем стала отмечать появление затрудненного дыхания на фоне
острого респираторного заболевания, пользовалась теопеком, теотардом с
кратковременным положительным эффектом. С 53 лет на фоне затрудненного
дьосания стала отмечать подъемы АД до 140 и 90 мм ртст. В связи с очередным
Глава 6. Дифференциальная диагностика легочных эозинофилий... ИЗухудшением состояния на фоне острого респираторного заболевания, про¬
являющимся возникновением какшя с трудноотделясмой вязкой мокротой,
присоединением одышки при физической нагрузке, и с у^іетом неэффектив¬
ности начатой антибактериальной терапии в 2000 г. бьша госпитализирована в
Факультетскую терапевтическую клинику им. В.Н. Виноградова.При обследовании обращено внимание на увеличение уровня эозинофилов
крови до 23%, небольшое повышение уровня IgE (до 161 МБ/мл). Проводилось
серологическое исследование крови на грибы, паразиты, получены отрицатель¬
ные результаты. Состояние трактовалось как бронхиальная астма инфекдионно-
зависимая с атопическими реакциями средней степени тяжести, гиисрэозино-
фиішя неясного генеза, была подобрана ингатяционная терапия оксисом 4,5 мкг2 раза в сутки, пульмикортом-турбухаїером 200 мкг 2 вдоха 2 раза в сутки. В тече¬
ние последующих ipex лет продолжалось лечение в виде приема комбинирован¬
ного препарата симбикорт 160/4,5 мкг в режиме гибкого дозирования, состояние
больной оставалось относительно удовлетворительным.С мая 2004 г. на фоне острого респираторного заболевания отмстила появ¬
ление першения в горле, затрудненного дыхания, одышки при физической
нагрузке, затем появились ощущения распирания в подчелюстной области
с обеих сторон, отек языка, сопровождавшийся затруднением речи. Больная
обследовалась амбулаторно; в анализах крови было отмечено увеличение
эозинофилов до 50% при нормальной СОЭ. При выполнении КТ органов
фудной клетки обнаружены медиастинальная лимфаденопатия, легочные
инфильтраты. Было высказано предположение об эозинофильной пневмонии.
При УЗИ подчелюстной области выявлено сушествеинос увеличение в раз¬
мерах подчелюсгных слюнных xcjje3, что трактова-юсь в рамках системного
поражения внутренних органов, возможно, эозинофильного характера. Начат
прием метипреда в дозе 24 мт/сут с положительным эффектом; уменыиение
в размерах подчелюстных лимфатических узлов, уменьшение одышки, при
повторных анаїизах крови было отмечено уменьшение эозинофилии до 9%,
по данным КТ органов грудной клетки — уменьшение количества и размеров
легочнь[х инфильтратов.Через 10 дней после постепенной отмены метипреда и на фоне переохлаж¬
дения вновь отметила ощущение заложенности в грудной клетке, появление
одышки при физической нагрузке, покашливание, присоединилась потли¬
вость, в связи с чем в сентябре 2004 г была госпитализирована в Факультетскую
терапевтическую клинику им. В.Н. Виноградова.При nocmyrvieHuu состояние относительно удовлетворительное. Кожные
покровы бледные, чистые. Рост 169 см, масса тела 80 кг (ИМТ 2Н кг/м-).
Периферические лимфатические узлы не увсішченьї. Умеренно увеличены
подчелюстные слюнные железы. Дыхание через нос затруднено. Перкуторный
звук над легкими ясный легочный. При аускультации легких дыхание жест¬
кое, при форсированном выдохе рассеянные свистящие и жужжащие хрипы.
Частота дыхания 16 в минуту. Тоны сердца ясные, ритмичные, на верхушке
короткий систолический шум, ЧСС 84 уд/мин, АД 120/70 мм рт.ст. Живот мяг¬
кий, при пальпации безболезненный. Печень, селезенка не увеличены.
1І4 ПульмонологияЬлабораторных данных обращали на себя внимание лейкоцитоз до 16 тыс.,
эозинофилия до 55% (абсолютное число эозинофилов 9317 в мкл), повы¬
шение СОЭ до 30 мм/ч при нормальном уровне гемоглобина и тромбоцитов.
Повышен уровень IgE до 1204,6 МЕ/мл, РФ положительный (++). В анализе
мочи выявлен белок 0,030%о. В анализе кала без особенностей, гельминты и
яйца глистов не выявлены.Таким образом, у больной с бронхиальной астмой, аллергическим ринитом,
гиперэозинофилией, эозинофильными инфильтратами легких в анамнезе,
которые поддавались терапии системными кортикостероидами, вновь отме¬
чена гилерэозинофилия, сопровождаюшаяся резким повышением уровня IgE
крови. Имеющийся лейкоцитоз мог быть объяснен приемом кортикостерои-
лов, но причина повышения СОЭ оставалась неясной.Учитывая эпидемиологический анамнез (наличие в квартире собаки), эози-
нофилию крови, повышение в крови TgE, в первую очередь встал вопрос о воз¬
можном наличии грибкового поражения, не исключалась возможность парази¬
тарной инвазии. Больная была проконсультирована в Институте паразитологии.
При исследовании крови антитела к токсокарам не обнаружены. Паразитарное
заболевание было исключено. Патогенные фибът также не были обнаружены.При КТ органов грудной клетки определялись множественные участки
понижения воздушности типа «матового стекла» во всех отделах, участки кон¬
солидации неправильной формы в УП1, IX сегментах правого легкого, V111 сег¬
менте левого легкого, единичные очаги 5 мм в диаметре в 1П сегменте правого
легкого, IX, X сегментах левого легкого, расширение корней легких за счет
увеличения лшмфатических узлов средостения. Учитывая аллергический ринит
в анамнезе, было выполнено рентгенологическое исследование придаточных
пазух носа: выявлено понижение прозрачности и подушкообразное утолщение
слизистой оболочки верхнечелюстных пазух.С целью исключения неопластического образования, при котором возмож¬
ны реактивные эозинофилии, бьы начат онкопоиск. Проведено УЗИ органов
брюшной полости (выявлены конкременты желчного пузыря до 4 мм в диаме¬
тре), УЗИ гениталий, УЗИ щитовидной железы, при исследовании патологии
не выявлено. От исследования кишечника пациентка категорически отказа¬
лась. Несмотря на повышенный уровень IgE, для иск^тючсния іемоб;гастоза
бьша проведена стернальная пункция. В миелограмме кол^гчество эозинофилов
увеличено до 36%, ускорено созревание нейтрофилов, эритропоэз нормо-
бластический, найдены мегакариоциты. Данных в пользу эозинофильного
лейкоза получено не было. Учитывая умеренно увеличенные внутригрудные
лимфатические узлы, с гематологами была обсуждена вероятность лимфоіра-
нулематоза, однако в связи с отсутствием периферической лимфаденопатии,
характерных изменений в миелофамме данный диагноз был отвергнут. От про¬
ведения трепанобионсии пациентка отказалась. Таким образом, убедительных
данных в пользу неопластического образования получено не было.Учитывая повышенные цифры артериального давления, больная была про¬
консультирована окулистом. Получены данные за гипертоническую ангиопа¬
тию сетчатки.
Глава 6. Дифференциальная диагностика легочных эозинофилий... 115Постепенно отвергая одну за другой причины гиперэозинофилии, врачи
склонялись в пользу системного заболевания. Поскольку болезнь нашей
пациентки началась с аллергического ринита, вскоре присоединились симпто¬
мы брониальной астмы, в анамнезе на фоне гиперэозинофилии отмечались
легочные инфильтраты, ушедшие на терапии системными кортикостероидами,
высказано предположение о синдроме Черджа-Стросс — первичном систем¬
ном васкулите. Учитывая, что у 67% больных при штлергическом гранулематозс
(синоним синдрома Черджа—Стросс) в крови выявляются антинейтрофильиые
антитела, у пациентки были взяты анализы крови на pANCA, Данные антитела
отсутствовали, что, однако, не противоречило основному диагнозуБыла начата терапия метипредом 24 мг/сут перорально и продолжена
терапия симбикортом 160/4,5 мкг. В результате лечения быстро исчезли кти-
нические признаки бронхмаяьной обструкции, уменьшилась эозинофилия
периферической крови до 9%, СОЭ снизиыась до 24 мм/ч. Также отмечена
положительная динамика по данным КТ органов грудной клетки: уменьшение
количества и размеров участков пониженной воздушности легких типа «матово¬
го стекпа*>, уменьшение размеров участков консолидации в VIT1 сегментах обоих
легких с формированием фиброза, однако сохранялось увеличение лимфоузлов
средостения и корней легких, в относительно удовлетворительном состоянии
больная была выписана, динамическое наблюдение было продолжено.Через месяц в анализах крови: лейкоцитов 8,8 тыс., эозинофилов 2% (абсо¬
лютное число 176 в 1 мкл), СОЭ 7 мм/ч. Поданным КТ органов грудной клет¬
ки сохраняется ли.мфаденопатия медиастинальных лимфоузлов, размеры их
уменьшились до 11 мм в поперечнике, у^шстки консолидации и пониженной
воздушности не определялись.Характерная клиническая картина, результаты обследования, хороший
ответ на лечение системными стероидами позволили сформулировать клиниче¬
ский диагноз следующим образом: гиперэозинофилъный аигиит типа Черджа-
Стросс (аллергический риносинусит, гиперэозинофилия, бронхиальная астма,
эозинофильные инфильтраты); диффузный пневмосклероз; гипертоническая
болезнь II стадии, 1 степени повышения артериального давления, среднего
риска; атеросклероз аорты; дисциркуляторная энцефалопатия смешанного
генеза; мигрень; желчнокаменная болезнь вне обострения.Приведенное динамическое клиническое наблюдение с этапной оценкой
течения заболевания демонстрирует типичное течение синдрома Черджа-
Стросс, что и позволило поставить диагноз, несмотря на отсутствие морфоло¬
гического подтверждения (в основе заболевания лежит аллергический некро-
тизирующий ангиит с экстраваскулярным гранулематозом и эозинофильными
инфильтратами тканей).Впервые заболевание было описано в 1951 г. J. Churge и L. Strauss и вклю¬
чено в рубрику узелкового периартериита с бронхиальной астмой, эозинофи-
лией и системными васкулитами. И только в 1992 г. синдром Черджа-Стросс
был выделен в отдельную группу — васкулитьт с поражением сосудов мелкого
калибра. Заболевание встречается нечасто, точных статистических данных нет.
В среднем оно диагностируется у 6—8 человек на 1 миллион населения. Дебют
lie Пульмонологияero происходит в среднем в 44 года. Причина аллергического фанулематоза до
сих пор неизвестна; существуют несколько теорий на этот счет;• вирусная теория (ассоциация с вирусами гепатита В и С, ВИЧ 1 типа);• бактериальная теория;• концепция, основанная на факте повышенной продукции антинейтро-
филъных цитоплазматических аутоантитсл (ANCA— antineutrophil cyto¬
plasmic autoantibodies), которые рассматриваются в качестве биологиче¬
ских маркеров васкулитов;• генетическая предрасположенность к формированию воспалительных
реакций сосудов, протекающих с участием ANCA.Одной из главных черт синдрома является бронхиапьная астма, симптомы
коюрой возникают задолго до васкулита, что и объясняет частоту диагноза
«бронхтгальная астма» у этих больных. Временной интервал между возникшими
симптомами бронхиальной астмы и васкулита составляет в среднем три года.
С появлением признаков системного васкулита степень тяжести астмы может
уменьшиться. Другими ранними симптомами являются аллергический ринит,
полипозные разрастания слизистой оболочки носа (табя. 6.1). Следующая
фаза болезни характеризуется повышенным содержанием эозинофилов в пери¬
ферической крови и их миграцией в ткани с формированием эозинофильной
инфшіьірации легких и желудочно-кишечного тракта. Последняя фаза харак¬
теризуется развитием васкулита, полиорганностью поражения. Чаще вовлека¬
ются кожа, нервная система, сердце и почки {рис. 6.1, см. цветную вклейку).Таблица 6.1Фазы заболеваний при синдроме Черджа-СтроссФазаКлинические проявленияАллергическая фазаКлинически — эозинофилия крови в сочетании с
проявлениями аллергических заболеваний: ринитом,
полинозом, астмой и др.Фаза эозинофильной
инфильтрации тканейКлинически — эозинофилия крови, тяжелые при-
ст>тты бронхиальной астмы, летучие эозинофильные
инфильтраты легких, эозинофильный гастроэнтеритФаза развития паскулитаРазвернутая картина системного васк>'литаПравильный диагноз в начальной стадии заболевания нередко поставить
трудно, так как довольно часто бронхиальная астма сочетается с риносинусо-
патиями. Заподозрить аллергический гранулематоз следует тогда, когда у боль¬
ного бронхиальной астмой с аллергическим ринитом или риносинусопатией
начинает расти эозинофилия периферической крови (более 800 эозинофилов
в 1 мкл крови) и возникают другие симптомы заболевания (моно- или поли¬
нейропатия, но чаще легочные инфильтраты — быстро проходящие одно- или
двусторонние инфильтративные изменения), круг дифференциальной диагно¬
стики различен в зависимости от фазы заболевания (табл. 6.2).Первой линией терапии являются системные кортикостероиды. Начальная
доза достаточно большая и составляет 1 мг/кг в сутки преднизолона внутрь
в течение 1 месяца с послед>тощим быстрым снижением дозы. Курс терапии
рассчитан на срок до одного года. При полиорганном поражении проводится
Глава 6. Дифференциальная диагностика легочных эозинофилий... 117Таблица 6.2Дифференциальная диагностика на разных этапах синдрома Черджа—СтроссФазаЗаболевания, с которыми необходимо проводить
дифференциальную диагностику Аллергическая фазаАллергический бронхолегочш>ш аспергиллез
СаркоидозФаза эозинофильной
инфильтрации тканейПаразитарные инвазииХроническая зозинофи.іьна>і пневмонияГиперэозинофильный синдром Фаза развития васкулитаГранулематоз Вегенера
Узелковый периартериитпульс-терапия преднизолоном (внутривенно 1 г метилпреднизолона в течение3 дней, с последующим пероральным приемом 40—60 мг преднизолона и мед¬
ленным снижением дозы), проводятся повторные исследования перифериче¬
ской крови и контролируются уровни эозинофилов, СОЭ, Стойкая клиниче¬
ская ремиссия и позитивные лабораторные показатели позволяют перейти на
альтернирующую схему приема кортикостероидов, В случаях тяжелого некро-
тизируюшего васкулита добаатяют циклофосфамид из расчета 2 мг/кг в сутки в
течение 1 года. При тяжелых обострениях возможно проведение плазмафереза.Следующее наблюдение характеризуется более развернутой клинической
картиной с выраженными изменениями внутренних органов и рядом сопут¬
ствующих заболеваний, что выну-ждало включать в крут дифференциально¬
диагностического поиска большее количество заболеваний и требовало боль¬
ших сроков для постановки диагноза синдрома Черджа—Стросс.Больной С., 80 лет, поступил в Факультетскую терапевтическую клинику им.
В.Н. Виноградова 01.02.2004 п с жалобами на приступы экспираторного удушья
с частотой до 6 раз в сутки, кашель с мокротой слизистого характера, одышку
при умеренной физической нагрузке, заложенность носа, повышение АД мак¬
симально до 170 и 100 мм ртхт.Из анамнеза жизни известно, что в течение длительного времени страдал
язвенной болезнью двенадцатиперстной кишки с редкими обострениями, в
возрасте 70 лет был оперирован по поводу доброкачественной гиперплазии
предстательной железы. В остальном в семейном анамнезе и в анамнезе жизни
без особенностей.Из анамнеза заболевания известно {рис. 6.2), что осенью 2002 г. обратил
внимание на прогрессирующее похудашіе. В январе 2003 г отметил появление
лихорадки с максимальными подъемами до 38 С, сопровождающейся озно¬
бом и потливостью при снижении температуры; появртлись также выраженная
слабость, заложенность носа, по поводу чего поступил в Клинику болезней
уха, горла, носа ММА им. И.М.Сеченова. После проведенного обследования
бьш диагностирован аллергический риносинусит, назначено соответствующее
лечение. Однако в связи с выявленными гипохромной анемией, эозинофилией
крови и увеличением СОЭ, сохраняющейся лихорадкой, выраженным астени¬
ческим синдромом был переведен в Факультетскую терапевтическую клинику
им. В.Н. Виноградова.
ІІ8ПульмонологияСнижение
массы телаАстеническийсиндромЗаложенностьносаПриступыудушьяАртериальнаягипертензияЛихорадкаЭозинофилиякрови33%АнемияУвеличениеСОЭ3,8 мг%Креатинин —Осень 01.2003 03.2003 01.20042002 02.2003 06.2003 02.2004Рис. 6.2, Анамнез больного С., 80 летПри постутгении обращали на себя внимание бледность кожных покро¬
вов и видимых слизистых оболочек, отеки голеней и стоп, при аускультации
легких выслушивалось везикулярное дыхание, незвонкие мелкопузырчатые
хрипы над базаіьньїми отделами. Вдоль левого края грудины сердца — мягкий
систолический игум. АД 110 и 80 мм рт.ст. При пальпации живота определялась
умеренная гепатомегалия.В лабораторных данных обращали на себя внимание лейкоцитоз до 12,3 тыс.,
зозинофи-чия до 15% (абсолютное число эозинофилов 1845 в мкл), повыщение
СОЭ до 40 мм/ч, снижение уровня гемоглобина до 95^2 г/дл, сывороточного
железа до 2 мкг/дл, повышение креатинина до 1,5 мг/л, снижение уровня
общего белка до 5 г/дл. В иммунологическом анализе крови уровень IgE был
в пределах нормы (56,8 МЕ/мл), СРБ слабоположительный. В анализе мочи
микрогематурия, цилиндрурия, невысокая протеинурия (суточная экскреция
белка составляла 100 мг).Таким образом, наличие у больного выраженных астенических жалоб,
лихорадки, анемии, гиперэозинофилии, повышения СОЭ не позволяло оста¬
новиться на каком-либо определенном заболевании и делало необходимым
включить в круг диагностического поиска паразитарную инвазию, туберку¬
лез, инфекционный эндокардит, онкологическое заболевание, гемобластоз и,
наконец, системный васкулит.
Глава 6. Дифференциальная диагностика легочных »озинофилий,„ І19Учитывая фебрильную лихорадку, сопровождаютцуюся ночной потливо¬
стью, выраженной слабостью, увеличение СОЭ, лейкоцитоз крови, не исклю¬
чалась возможность развития инфекционного эндокардита. Было проведено
исследование крови на стерильность (рост микрофлоры выявлен не был). Для
выявления вегетаций на клапанах сердца проведена чреспищеводная ЭхоКГ
(вегетации не обнаружены). Кроме того, был исключен туберкулез легких
[ДНК микобактерий туберкулеза методом полимеразной цепной реакции
(ГЩР) в бронхиальном смыве не найдены, антитела к микобактериям туберку¬
леза Б сыворотке крови также не обнаружены].Для исключения гемобластоза была выполнена стернальная пункция, В мие-
лограмме вьтяатсны небольшое увеличение количества плазматических клеток
(до 2,6%), ускорение созревания нейтрофилов, увеличение количества эозино-
филов (до 14,9%), нормобластический эритропоэз состашшл 13,3%. Данных в
пользу эозинофильного лейкоза не получено.В связи с гиперэозинофилией крови, анемией, похуданием, лихорадкой для
исключения паразитарного заболевания больной был обследован в НИИ парази¬
тологии и тропической медицины. В анализе кала яйца гельминтов обнаружены
не бьиіи. При исследовании крови выявлен высокий титр антител к токсокарам
(1:1600), однако, по мнению паразитологов, наливше токсокароза было мало¬
вероятным, поскольку нехарактерными для этого заболевания являются ане¬
мия, повышение СОЭ, изменения мочевого осадка. В динамике проводилось
повторное исследование крови на антитела к токсокарам — результаты отрица¬
тельные. Таким образом, паразитарное заболевание бьиіо исключено.Для исключения неопластического процесса проведен обширный онко¬
поиск, включавший ЭГДС (выявлена рубцовая деформация луковицы две¬
надцатиперстной кишки), бронхоскопию с последующим изучением цитоло-
птческого состава смывов из бронхиального дерева (патологическая флора и
мицелии грибов НС обнаружены), урологическое обследование (PSA 1,9 нг/мл,
ультразвуковые признаки хроїшческого простатита), УЗИ шитовидной желе¬
зы — злокачественное образование не найдено. При колоноскопии выявлен
полипоз толстого кишечника, проведены биопсия полипов и исследование
слизистой оболочки прямой кишки на амшюид. Атипичные клетки и ами^юад
обнаружены не были,Проводилась КТ органов фудной и брюшной полостей. При КТ органов
грудной клетки (рис. 6.3) в верхней доле правого легкого в субішевральном отде¬
ле 111 сегмента и парамедиастинально определялось вуалеоподобное уплот¬
нение легочной ткани по типу «матового стекла». Пневматизация и васкуля-
ризация паренхимы остальных отделов бьыи не изменены, лимфадснопатия
не выявлена. Учитывая гиперэозинофилию крови, обнаруженные изменения
оказались сходны с эозинофильными инфильтратами с локализацией в верх¬
ней доле правого легкого.Обращала на себя внимание желудочковая экстрасистолия, расцененная
как проявление атеросклеротического кардиосклероза, в связи с чем были
назначены р-адреноблокаторы (метопролол 50 мг/сут). С целью коррекции
железодефицитной анемии — препараты железа. В связи с гипоальбуминемией
120ПульмонологияРис. 6.3. Компьютерттые томогра\шьт органов грултюй клетки (02.04.2004 г.)проводились внутривенные инфузии альбумина. У больного исчезла лихорад¬
ка, уменьшилась слабость, однако продолжала беспокоить заложенность носа.
В анализах крови сохранялись гиперэозинофилия (до 21%), повышение СОЭ
(до 55 мм/ч), креатинина до 1,6 мг/д,1, суточная протсинурия составляла 170 мг.
Проведенное обследование не позволяло выяснить причину повышения уров¬
ня эозинофилов крови. Больной был выписан с клиническим диагнозом: желе¬
зодефицитная анемия; полипоз толстого кишечника; гиперэозинофилия неяс¬
ного генеза; ИБС (атеросклеротнгческий кардиосклероз с нарушениями ритма,
желудочковая экстрасистолия). Атеросклероз аорты, коронарных артерий;
язвенная болезнь двенадиатиперстной кишки в стадии ремиссии.После выписки из стационара пациент продолжал наблюдаться
в Факультетской терапевтической кіинике им. В.Н. Виноградова. Весной2003 г. было выявлено нарастание уровня эозинофилов до 35%, креатинина
крови до 3,5 мг/дл. Летом 2003 г. отметил появление приступов затрудненного
дыхания. В течение полугода состояние прогрессивно ухудшалось: участились
приступы удушья, присоединрілась одышка. Амбулаторно была начата терапия
ингаляционными кортикостероидами, однако в связи с ее неэффективностью
в феврале 2004 г. больной вновь бьы госпитализирован в Факультетскую тера¬
певтическую клинику им. В.Н. Винофадова.При поступлении состояние средней тяжести. Кожные покровы чистые.
Дыхание через нос затруднено. При аускультации легких выслупгивается
жесткое дыхание, большое количество свистящих хрипов. Частота дыхания
22 в минуту. Тоны сердца ритмичные. АД 150 и 90 мм рт.ст.В лабораторных данных обраш^ает на себя внимание эозинофилия до 11 %
(абсолютное число эозинофилов 636 в мюі) при нормальном количестве лейко¬
цитов, повышение СОЭ до 47 мм/ч, гемоглобин 107 мг/л, креатинин 3,9 мг/дл.
В общем анализе мочи микрогематурия, протеинурия (суточная протеипурия
составила 200 мг). В общем анализе мокроты большое количество эозинофи¬
лов и кристаллов Шарко-Лейдена. При бодиплетизмографии — признаки
обструкции дистальных бронхов. Совокупность вышеизложенных данных сви¬
детельствует о наличии у больного бронхиальной астмы. Состояние улучши¬
лось после назначения небулайзерной терапии бронходилататорами (атровент)
и кортикостероидами (суспензия пульмикорта 3 мг/сут).При анализе клинической картины были вьшелены следующие основные
клинические и лабораторные синдромы', синусит, бронхиальная астма, легочный
Глава 6, Дифференциальная диагностика легочных эозинофилий... 121инфильтрат, хроническая почечная недостаточность, гиперэозинофилия
крови. Подобное сочетание синдромов и течение заболевания (постепенное
развитие от лихорадки, синусита и выраженной астении до бронхиальной
астмы, а затем и поражения внутренних органов) характерно для системного
васкулита с поражением сосудов мелкого калибра — аллергического грануле-
матоза или синдрома Черджа—Стросс. Для подтверждения этого заболевания
бьто проведено исследование крови на антитела к цитоплазме нейтрофилов.
Обнаружены p-ANCA в титре 1:40, характерные д.'гя синдрома Черджа-Стросс
(c-ANCA обнаружены не были).Характерная клиническая картина, этапность развития заболевания,
результаты обследования позволили сформулировать клинический диагноз как
аллергический гранулематозный ангиит Черджа—Стросс с поражением почек
(ХПН Г стадии, артериальная гипертензия) и легких (бронхиальная астма).
Полипозный риносинусит ИБС: атеросклеротический кардиосклероз с нару¬
шениями ритма и проводимости — желудочковая экстрасистолия, аїриовен-
трикулярная блокада 1 степени. Атеросклероз аорты, коронарных артерий.
Язвенная болезнь двенадцатиперстной кишки в стадии ремиссии.Учитывая прогрессирующий характер поражения почек и высокий риск
осложнений, от применения больших доз преднизолона решено бьшо отка¬
заться, начато лечение ииклофосфаном 300 мг в неделю в сочетании с варфа-
рином. Больной был выписан в удошіетворительном состоянии, продолжено
динамическое наблюдение.Последняя госпитализация больного в Факультетскую терапевтическую
клинику им. В.Н. Виноградова в октябре 2004 г. была связана с возобнов¬
лением приступов удушья, постоянной одышкой, мокротой слизистого
характера, повышением цифр АД до 180 и 100 мм рт.ст. В обшем анализе
крови отмечался нормальный уровень эозинофилов (1%), повышение СОЭ
до 30 мм/ч. В биохимическом анализе крови уровень креатинина составлял2,9 мг/дл. С целью стабилизации состояния усилена иммуносуцрессивная
терапия (доза метипреда увеличена до 20 мг/сут per os. циклофосфан 100
мг через день, суспензия пульмикорта через небулайзер в дозе 2 ліг/сут).
С целью коррекции артериальной гипертензии были назначены б локатор
медленных кальциевых каналов (лацидипин 4 мг/сут) и вазодилататор (сид-
нофарм 6 мг/с>'т). На фоне комбинированной терапии достигнуто исчез¬
новение признаков бронхообструкции, нормализация цифр АД (120—130 и
80 мм рт.ст.), снижение СОЭ до 12 мм/ч, креатинина до 2,7 мг/дл. Пациент
выписан на поддерживаюш^ей иммуносупрессивной и антигипертензивной
терапии.Таким образом, клинические наблюдения демонстрируют сложность
постановки диагноза «синдром Черджа-Стросс». Учитывая достаточтто рас¬
пространенность легочных эозинофилий, необходима настороженность при
возникновении легочных инфильтратов у больных бронхиа.чьной астмой с
аллергическіш ринитом или риносинусопатией в сочетании с высокой эози-
нофилией периферической крови.
/22 ПульмонологияЛИТЕРАТУРАЛнаев Э.Х. Эозинофилы и эозинофилии. Атмосфера // Пульмонология и
аллергология. — 2002; 3.Ершов В.И., Соколова И.Я., Бочкарникова О,В. Большая эозинофилия и ток-
сокароз // Актуальные вопросы медицины (сборник научных трудов)/ Под ред.
академика РАМН, проф. Л.И.Ольбинской. — М., 2003. — С. 264-276.Чучалин А. Г. Актуальные вопросы диагностики в пульмонологии //
Терапевтический архив. — 2001; 8:28.Чуча,шн Л.Г. Гиперэозинофи^тия при заболеваниях органов дыхания //
Терапевтический архив. — 2003; 3:5.Чучалин А. Г, Первичные системные и легочные васкулиты // Терапевтический
архив. — 2002; 3:5.Юдин Л А., Курбачева О. М., Полетаева Т. А., Азеркович В. И. Дифференциаль¬
ная диагностика бронхиальной астмы и синдрома Черджа—Стросс //
Пульмонология. — 2003; 1: 115-117.Masi Л.Т., Hunder G.G., Lie J.T. et ai. The American College of Rheumatology
1990 criteria for the classification of Churg-Strauss syndrome (allergic granulomatosis
and angiitis) I I Arthritis Rheumatology, — 1990; 33; 1094-1100.Matthew Conron, Huw L.C. Beynon. Churg-Strauss syndrome // Thorax. — 2000;
55: 870-877.Nath Imre, StrekMary E., LeffAlan R. Chuig-Strauss syndrome //Lancet. — 2003;
361:587-594.
КАРДИОЛОГИЯГлава 7КОМБИНИРОВАННОЕ ИСПОЛЬЗОВАНИЕ
ИНТЕРВЕНЦИОННЫХ МЕТОДОВ В ЛЕЧЕНИИ
РЕФРАКТЕРНОЙ ЖЕЛУДОЧКОВОЙ ТАХИКАРДИИ
У ПАЦИЕНТА С ПОСТИНФАРКТНЫМ
КАРДИОСКЛЕРОЗОМС А. Термосесов, В.Л. Сулимое, Д. В. Кузьменков,НА. Новикова, ДА, Царегородцев, И.Л. Ильич,Р.Ш. Гарипов, М.Ю. Гиляров, С.С. Васюков,А.В. ДобровольскийДиагноз ишемической болезни сердца (ИБС), как, наверное, никакой дру¬
гой в кардиологии, позволяют достаточно уверенно ставить инструментальные
методы исследования, но задача профилактики ИБС, ее осложнений и, тем
более, лечения до сего дня далека от разрешения. В лечении пациентов с ИБС»
осложненной желудочковыми нарушениями ритма, используются, наряду
с комплексной медикаментозной терапией, различные способы реваскуля-
ризации миокарда, имплантация кардиовертеров-дефибрилляторов (ИКД),
радиочастотная катетерная аблация (РЧА) аритмогенных зон и петель ре-ентри
в желудочках сердца, хирургическое лечение (аневризмэктомия, различные
реконструктивные операции и др.). Данное клиническое наблюдение пред¬
ставляет интерес с точки зрения успешного применения у больного ИБС с
угрожающими жизни аритмиями всего арсена,іа современных интервенцион¬
ных методов диагностики и лечения. Необходимо подчеркнуть, что все этапы
интервенционного лечения осушествлялись в терапевтической клинике, где
лечащий врач одновременно являлся и интервенционным кардиологом, прово¬
дились неоднократное перепрограммирование имплантированного устройства
и подбор антиаритмической терапии в зависимости от динамично менявшейся
клинической ситуации. Представляется оптимальной и последовательность
использования различных методов у нашего больного. Данное наблюдение
особенно ярко демонстрирует прогресс медицины со времен ГА. Захарьина
и Б.П. Образцова и в то же время наводит на мысль о неизбежньк потерях на
этом пути к дифференцированному высокотехнологичному лечению, требую¬
щему от врача глубокой специализации.
І24 КардиологияБольной Е., 75 лет, госпитализирован в клинику с жалобами на эпизоды
частого ритмичного сердцебиения, сопровождающиеся головокружением и
резкой слабостью.Из анамнеза известно: в возрасте 49 лет на фоне полного здоровья впервые
возник пароксизм тахикардии [по данным выписного эпикриза, на ЭКГ реги¬
стрировалась суправентрикулярная тахикардия с блокадой правой ножки пучка
Гиса (ПНПГ) и частотой сердечных сокращений (ЧСС) 180/мин; ЭКГ не пре-
доставлерпії]. В последующем подобные пароксизмы возникали в течение двух
лет около 10 раз, купировались внутривенным введением новокаинамида. Как
правило, пароксизмы сопровождались повышением артериального давления
(АД) до 200/100 мм рт.ст. и давящими болями за грудиной умеренной интенсив¬
ности. В течение последующих 10 лет приступы не повторялись. Периодически
беспокоили перебои в работе сердца, при суточном мониторировании ЭКГ
регистрировалась частая желудочковая экстрасистолия. Постоянно принимал
обзидан 40 мг/с>т. До 2000 г. чувствовал себя хорошо, физические нагрузки
переносил удовлетворительно.В те^іение последних 6 лет периодически стал отмечать повышение АД макси-
мштъно до 160—170/100 мм ртхт. В 2000 г. при интенсивной физической нагрузке
возникли давящие боли за грудиной, продолжавшиеся около 30 мин, прошед¬
шие самостоятельно, После этого обследовался в стационаре, диагностически
значимого повышения кардиоспецифических ферментов не отмечалось, но
при ЭхоКГ выявляли гипокинезы заднебоковой стенки левого желудочка (ЛЖ),
С этого времени подобные прист>'пы длительностью 3—5 мин стали возникать
при выходе на улицу в морозную погоду, при ходьбе в гору, подъеме тяжестей.
Постоянно принимал теветен 600 мг/сут, триампур 1 таб./сут, зокор 10 мг/сут,
обзидан 40 мг/сут, тромбо-АСС 100 мг/сут, нитросорбид по необходимости.
В 2003 г развился типичный пароксизм тахикардии, который был купирован
внутривенным введением новокаинамида. Следующий приступ тахикардии с
ЧСС 180—200/мин возник 10.04,2006 г., сопровождался интенсивными давя¬
щими болями за грудиной, одышкой, обильным потоотделением. После купи¬
рования приступа, продолжавшегося около часа, на ЭКГ сохранялась блокада
ножки пучка Гиса (какой — больной не помнит, ЭКГ не предоставлены), в связи
с чем был госпитализирован в стационар по месту жительства.В приемном отделении вновь появились ангинозные боли и развился при¬
ступ тахикардии с широкими комплексами QRS по типу полной блокады
правой ножки пучка Гиса с ЧСС 120 в минуту {рис. 7,1), сменявшейся другой
тахикардией с широкими комплексами QRS и с ЧСС 200 в минуту {рис. 7.2).
Попытки купирования лидокаином, кордароном — без эффекта. Синусовый
ритм восстановлен с помощью электроимпульсной терапии (ЭИТ). 14.04.2006 г.
повторно развился пароксизм тахикардии с широкими комплексами QRS и с
ЧСС 200 в минуту, больной потерял сознание. Пароксизм был купирован элек¬
троимпульсной терапией. Вне приступов на ЭКГ отрицательной динамики по
сравнению с ЭКГ от 2005 г. не отмечалось, но при ЭхоКГ появились новые
зоны гипо-/акинезии в области передней, нижней, боковой стенок. В анализе
крови выявлено повышение МВ-фракции креатинфосфокиназы. Состояние
Глава 7. Комбинированное использование интервенционных методов.125Рис. 7.1, Пароксизмальная тахикардия с широким комшіексом QRS и морфологаей
полной блокады правой ножки пучка Гиса, зарегистрированная у пациента Е., 75 лет, в
приемном отделенииJj!;..; .. V.• Рис. 7,2. Второй вариант тахикардии с широким комплексом QRS у пациента Е., 75 лет,
зарегистрированной в приемном отделении стационара по месту жительстварасценено как повторный инфаркт миокарда от 10.04.06 г., осложненный
желудочковой тахикардией (ЖТ). На фоне терапии гепарином, атенололом 50
мг/сут, кардикетом 60 мг/сут, предукталом, престариумом, приступов стено¬
кардии не было, пароксизмы желудочковой тахикардии не рецидивировали.
С 20.04.2006 по 15.05.2005 г. пациент находился на лечении в Клинике кардио¬
логии ММА имени И.М, Сеченова. По данным перфузионной сщштиграфии
миокарда в покое, подтвержден диагноз повторного инфаркта миокарда ниж¬
небоковой стенки левого желудочка (вероятно, инфаркт миокарда был спрово¬
цирован пароксизмом тахикардии с ЧСС 200 в минуту).
126 КардиологияПациенту проведена коронароангиография: сбалансированный тип кровос¬
набжения сердца. Ствол левой коронарной артерии не изменен. Передняя
межжелудочковая артерия без признаков гемодинамически значимых сте¬
нозов. Огибающая артерия малого диаметра (1,5 мм). Окклюзирована в
проксимальной части. В средней трети правой коронарной артерии выявлен
70% осложненный стеноз.Проводилось лечение тромбо-АССом 100 мг/сут, плавиксом 75 мг/сут,
кордароном 200 мг/сут, конкором 2,5 мг/сут, кардикетом 80 мг/сут, крестором
10 мг/сут, омезом 20 мг/сут.Повторная госпитализация — для проведения баллонной ангиопластики и
стентирования правой коронарной артерии.При поступлении состояние относительно удовлетворительное. Кожные
покровы обычной окраски. Отеков нет. В легких дыхание везикулярное, хрипы
ІІЄ выслушиваются, Частота дыхания 16 в минуту. Тоны сердца ритмичные,
ЧСС 74 в минуту, АД 140 и 75 мм рт.ст. Шумы на сонных артериях не выслу¬
шиваются. Пульсация периферических артерий сохранена. Живот мягкий,
безболезненный. Печень не увеличена.В анализах крови существенных отклонений от нормы не выявлено.При ЭхоКТ: аорта умеренно уплотнена, левое предсердие 4,2 см, ЛЖ не рас¬
ширен, толщина стенки 1,3 см, ФВ левого желудочка 52%. Локальная сократи¬
мость левого желудочка не нарушена. Правые камеры не изменены. Створки
аортального и митрального клапанов уплотнены. Регургитация на митральном
клапане I—II степени. Признаков легочной гипертензии нет. Нарушение диа¬
столической функции I типа.24.05.2006 г выполнены баллонная ангиопластика и стентирование правой
коронарной артерии стентом Cypher 3,5x33 мм. В ходе процедуры у пациента
развился пароксизм желудочковой тахикардии с 4СС 120 в минуту. Попытки
купирования лидокаином и кордароном — без эффекта. Синусовый ритм
восстановлен электрической кардиоверсией. В течение суток после ангио¬
пластики состояние оставалось удовлетворительным, однако в дальнейшем
приступы желудочковой тахикардии рецидивировали ежедневно, синусовый
ритм восстанавливался лишь после повторных электрических кардиоверсий.
Попытки увеличения дозы кордарона до 600—800 мг/сут, его комбинации с
Р-адреноблокаторами эффекта не имели и сопровождались появлением выра¬
женной синусовой брадикардии, эпизодов узлового ритма, В связи с неэф¬
фективностью антиаритмической терапии, рецидивированием устойчивой
желудочковой тахикардии 08.06.2006 г выполнено инвазивное внутрисердечное
электрофизиологическое исследование (ЭФИ).Внутрисердечное ЭФИ, для проведения которого использоватасъ система
нефлюороскопического электрофизиологического картирования С arto ХР
(Biosense Webster, Jonson&Jonson, США), начато на фоне очередного парок¬
сизма желудочковой тахикардии с ЧСС 115/мин. Во время исследования
периодически отмечалась трансформация исходной тахикардии в желудоч¬
ковую тахикардию другой морфологии с ЧСС 160 уд/мин. На фоне желу¬
дочковой тахикардии построена карта последовательности распространения
Глава 7. Комбинированное использование интервенционных методов...127возбуждения по левому желудочку (изохрональная карта). Была определена
«критическая зона» желудочковой тахикардии в области рубца заднебоковой
стенки левого желудочка. В эту зону нанесена серия аппликаций радиочастот¬
ной энергии при температуре до 45 "С, мощностью 50 Вт, длительностью до1 мин с прямым восстановлением синусового ритма.После окончания РЧА было проведено повторное ЭФИ и вновь была инду¬
цирована желудочковая тахикардия с ЧСС 100/мин, имевшая другую морфо¬
логию. «Критическая зона» этой тахикардии располагалась в той же области
заднебоковой стенки левого желудочка. В эту же зону повторно была нанесена
серия аппликаций радиочастотной энергии, что привело к купированию желу¬
дочковой тахикардии (рис. 7.3 на цветной вклейке, 7.4).При контрольном ЭФИ с использованием различных режимов программи¬
рованной стимуляции левого желудочка тахисистолических нарутиений ритма
индуцировано не бьшо.При проведении программированной стимуляции из правого желудочка
тремя экстрастимулами (600—260/260/280 мс) индуцирована фибрил.-іяция
желудочков, купированная разрядом наружного дефибриллятора 220 Дж.
С учетом сохраняющегося высокого риска внезапной сердечной смерти у дан¬
ного больного вторым этапом оперативного вмешательства явилась имплан¬
тация кардиовертера-дефибриллятора MAXIM О DR 7278 (Medtronic, США).
Желудочковый электрод с одной шоковой спиралью (активная фиксация)
фиксирован в области верхушки правого желудочка, предсердный элек¬
трод (пассивная фиксация) установлен в области ушка правого предсердия.
В ходе тестирования кapдиoвepтepa-дeфибpилJTятopa протоколом «шок на Т»Рис. 7.4. Прямое восстановление синусового ритма в ходе радиочастотной аблации в
«критической зоне» желудочковой тахикардии у пациента £,,75 лет
128Кардиологияиндуцирована фибри-тляиия желудочков, купированная ра:ірядом кардиовер-
тсра-дсфибриллятора мощностью і 5 Дж.Несмотря на то, что в ходе контрольного ЭФИ желудочковая тахикардия не
была индуцирована, в раннем послеоперационном периоде она рецидивиро¬
вала вновь. ЧСС при этом составляла 110/мин. Попытки купирования желу¬
дочковой тахикардии кардиовертером-дефибриллятором с помощью режима
антитахикардитической стимуляции бьши неэффективны, синусовый ритм
восстанавливался только после «шокового» разряда. К терапии добавлен сота-
лол 160 мг/сут в сочетании с метопрололом 50 мг/суг. На этом фоне в течение
7 дней пароксизмы не рецидивировали. Пациент выписан из стационара.Таблица 7.1Программирование имплантированного кардиовертера-дефибриллятора в зависимости
от проводимой антиаритмической терапии у пациента Е., 75 летДата10.07.0612.07.0614.07.0616.07.0620.07.0621,07.0625.07-01.08.06Антиарит-мичсскаятерапияСоталске
160 мг/л,
метопро-
лол50 мг/дЛидокаинЭтаиизин
100 мг/лХиііидин
600-800
мг/д,
обзидан
60 мг/дЛндо-каинРЧА,
затем
соталол
160
мг/д,
обзидан
60 мг/дКорда-
рон 800
мг/д, +
600 мг/д
в/вЦикл ЖХ
мс550-570540-570400-240540-570540-500570-620,сменаморфо¬логии620Частота
прист\'пов
в с>тки9414Непре-рывтторециди¬вирую¬щаяНепре¬рывнорециди¬вирую¬щаяДо 10Непре¬рывнорециди¬вирую¬щаяРежимыикдBurst84%Ramp91%Ramp+75%-69%-66%CV(10 Дж)Burst 75%Ramp75%Ramp+72%-66%-63%Ramp75%-63%Ramp+72%-66%-63%СУ(ІОДж)CV
при
ЧСС >
200/минBurst75%,затемRamp66%Ramp66%Ramp66%Эффек-типньгйрежимCVRamp72%CVBurst
75% (npWHOMрежиме)Burst75%,затемRamp66%Ramp66%
Глава 7. Комбинированное использование интервенционных методов..129Однако всего через несколько дней после выписки у больного развился
«желудочковый шторм», что проявлялось учащением приступов желудочко¬
вой тахикардии до 10 раз за сутки. Пароксизмы устранялись лишь с помощью
«шоковых» разрядов ИКД, что очень тяжело переносилось пациентом, В связи
с этим после повторной госпитализации кардиоветер-лефибриллятор был
отключен, пароксизмы желудочковой тахикардии купировались либо самосто¬
ятельно, либо с помощью инфузии лидокаина. Была предпринята очередная
попытка подбора алтиаритмической терапии {табл. 7.1).Предпринята попытка назначения этацизина 100 мг/сут, однако на этом
фоне включение режима антитахикардитической стимуляции имплантиро¬
ванного устройства стало вместо купирования аритмии приводить к транс¬
формации ее в желудочков>то тахикардию с более высокой частотой, вплоть
до развития фибрилляции желудочков {рис. 7.5), которая устраня^тась либо
«шоковым» разрядом кардиовертера-дефибриллятора, либо наружной элек¬
трической дефибрилляцией. В результате потребовалось отключение режима
антитахикардитической стимуляции и сохранение лишь алгоритма нанесения
«ТІТОКОВОГО» разряда при частоте желудочковой тахикардии более 200/мин.Последуюш;ие попытки назначения в качестве антиаритмической терапии
хинидина и лидокаина также оказались неэффективными.В связи с неэффективностью всех предпринятых методов лечения пациенту
повторно проведено внутрисердечное ЭФИ. в процессе его выполнения была
индуцирована желудочковая тахикардия с ЧСС 180 уд/мин. Была локализо¬
вана «критическая зона» этой тахикардии, располагавшаяся в области рубыа
в задней стенке левого желудочка в подюіапанном пространстве. В эту зону
нанесена серия аппликаций радиочастотной энергии при температуре до 45 °С,
мощностью 50 Вт, длительностью до 1 мин с прямым восстановлением синусо¬
вого ритма.Рис. 7.5. Проаритмическое действие этацизина у пакиента Е. Запись ЭКГ с прикроват¬
ного монитора в отделении интенсивной терапии и реанимации. Исходно имеется моно-
морфная желудочковая тахикардия. При попытках ее купирования с помощью частой
стимуляцнги желудочков, наносимой имплантированным устройством, она трансформи¬
руется Б полиморфную желудочковую тахикардию с более высокой частотой
130КардиологияПосле проведения РЧА в этой зоне было выполнено контрольное ЭФИ,
при котором вновь индуцирована желудочковая тахикардия иной морфологии
и частоты (ЧСС 110 уд/мин). «Критическая зона» тахикардии располагалась
в заднебоковой области левого желудочка, более латерально по сравнению с
предыдущим вариантом желудочковой тахикардии. В эту зону вновь нанесена
серия аппликаций радиочастотной энергии с прямым восстановлением сину¬
сового ритма. При контрольном ЭФИ приступов устойчивой желудочковой
тахикардии индуцировано не было.Несмотря на повторную радиочастотную аблацию, приступы желудочко¬
вой тахикардии в постоперационном периоде продолжали рецидивировать,
однако не так часто. Кроме того, изменилась морфология тахикардии и дли¬
тельность ее цикла (ЧСС при приступе стала составлять 96—99/мин), что, с
одной стороны, облегчило ее купирование с помощью режима антитахикар-
дитической стимуляции, а, с друг ой стороны, сделало не всегда возможным
своевременную детекцию кардиовертером-дефибриллятором в связи с часто¬
той менее 100/мин.! IПт 21^ИвЯ-в6Рис. 7,6 (а, б). Смена морфологии желудочковой тахикардии после повторной радио¬
частотной аблации у пациента Е., 75 лет
Глава 7. Комбинированное использование интервенционных методов... 131На исходной ЭКГ, зарегистрированной 13.07.06 г. {рис. 7.6) — желудочковая
тахикардия из левого желудочка с ЧСС 107/мин {рис. 7.6, а). На/?мс. 7.6, б (ЭКГ от
22.07.06 г.) — желудочковая тахикардия, развивигаяся у пациента в раннем посто-
перационном периоде после повторной радиочастотной аблации. Определяется
изменение морфологаи QRS при желудочковой тахикардии (комплексы QRS в
стандартных отведениях до и после радиочастотной аблации имеют противопо¬
ложную направленность), удлинение цикла тахикардии (ЧСС 99/мин).Была предпринята еще одна попытка назначения кордаронав дозе 800 мг/суг
внутрь (в течение первых 3-х дней дополнительно 600 мг/денъ внутривен¬
но капельно), которая оказалась эффективной. После периода накогысния
препарата в течение почти года пароксизмы ЖТ не возникали. Пациент посто¬
янно получает подцерживаюшую терапию кордароном 400 мг/сут, обзиданом
40 мг/сут, ренитеком 10 ліг/сут, тромбо-АССом 100 мг/сут, плавиксом 75 мг/
сут, крестором 10 мг/сут.Каждый из методов лечения, предпринятьгх у нашего пациента, имеет
самостоятельное значение в достигнутом положительном результате.
Реваскуляризация миокарда в данном случае не сопровождалась антиаритмиче-
ским эффектом. Более того, после стентирования правой коронарной артерии
приступы ЖТ стали чаще, что, вероятно, обусловлено эффектом реперфузии
«дремлющих^ аріттмогеннмх зон, изменением физико-химической гетероген¬
ности в ранее ишемизированных участках и, как следствие, изменением реф¬
рактерных периодов с возможным формированием новых петель ре-ентри.Проведение РЧА у больного затруднялось наличием множественных петель
ре-ентри, сочетанием несколысих видов левожелудочковой тахикардии, часть
из которых не сопровождалась тяжелыми гемодинамическиші расстройства¬
ми и могла быть подвергнута радиочастотному воздействию. Другие вариан¬
ты желудочковой тахикардии протекали с нарушениями гемодинамики, что
делало невозможным их картирование и устранение с помощью метода РЧА.
Ретроспективно можно констатировать, что основная роль метода РЧА заклю¬
чалась в изменении свойств желудочковой тахикардии таким образом, что
ранее неэффективный амиодарон стал оказывать антиаритмичсское действие.Имплантация кардиовертера-дефибриллятора сыграла ключевую роль в
спасении данного больного (с нескольких точек зрения).1. Имплантация кардиовертера-дефибриллятора позволила осуществить
вторичную профилактику внезапной сердечной смерти. С помощью РЧА у
больного не была надежно устранена возможность возникновения устойчивых
приступов желудочковой тахикардии, сопрождавшихся тяжелыми расстрой¬
ствами гемодинамики, а также возможность возникновения фибрилляции
желудочков, у больного с ИВС, перенесшего инфаркт миокарда, риск их
рецидивирования в дальнейшем оставался крайне высоким, даже несмотря на
терапию амиодароном. По результатам международных исследований только
имплантируемые кардиовертеры-дефибрилляторы являются наиболее эффек¬
тивным средством вторшшой профилактики внезапной аритмической смерти.2. Имплантированный кардиовертер-дефибриллятор устранял большую часть
пароксизмов желудочковой тахикардии, возникавших в периоде между двумя
/«32 Кардиологиярадиочастотными аблациями. Это с учетом резистентности пристутіов к купиру¬
ющей антиаритмической терапии позволило снизить количество наружных кар-
диовсрсии. В связи с этим следует отметить необходимость учета взаимодействия
назначаемой антиаритмической терапии и алгоритмов работы кардиовертера-
дефибриллятора. У нашего пациента такое взаимодействие выражалось:• в изменении эффективности режимов антитахикардитической стиму¬
ляции при назначении различных лекарственных препаратов; лидокаин
облепіал купирование пароксизмов, а этацизин, наоборот, приводил к
трансформации возникавшей первоначально желудочковой тахикардии в
ее более неблагоприятный вариант под воздействием антитахикардитиче-
ской стимуляции;• при назначении антиаритмических препаратов и под воздействием радио¬
частотного воздействия удлинялся цикл желудочковой тахикардии, что
требовало перепрограммирования имплантированного устройства для
своевременной детекции аритмии;• низкая ЧСС при желудочковой тахикардии (около 100/мин) требует посто¬
янного проведения ритм-урежающей терапии для исключения ложного
срабатьгвания ИКД на фоне синусового ритма с аналогичной частотой.3, Работа ИКД в режиме обычного кардиостим\'лятора позволила избежать
развития брадиаритмий и назначить адекватные дозы амиодарона, не опасаясь
развития критического урежения ЧСС (в настоящее время у пациента доминиру¬
ет ритм ИКД, что, вероятно, связано со скрытой дисф>'нкцией синусового узла).Таким образом, лишь комбинированное использование всего арсенала
интервенционных и лекарственных методов лечения желудочковых тахикардий
позволило добиться положительного результата в лечении данного пациента.Нарушения сердечного ритма и нроводимости — одна из самых актуальных
проблем кардиологии. Наличие аритмии у пациента не только снижает каче¬
ство жизни, но и нередко является определяющим для прогноза заболевания.
В последние десятилетия альтернативой лекарственным методам лечения, а
зачастую и единственным эффективным способом радикального устранения
нарушений сердечного ритма, профилактики внезапной аритмической смерти
являются методы интервенционной (малоинвазивной) кардиологии: РЧА зон
и имплантация антиаритмических устройств. Объединяет эти методики необ¬
ходимость использования в процессе оперативного лечения рентгеновского
контроля, в настоящее время в Первом Московском государственном меди¬
цинском университете им. И.М, Сеченова применяются все самые современ¬
ные методики диагностики и лечения нарушений сердечного ритма.При РЧА воздействие электрического тока высокой частоты (500 кГц) на
ткань миокарда за счет ее разогрева позво.вдет вызвать необратимое повреж¬
дение аритмогенного фокуса или критической зоны петли re-entry арит¬
мии. Эффективность подобного лечения в зависимости от вида нарушения
ритма достигает 85-100%, частота рецидивирования аритмии — около 5%,
а риск осложнений в ходе процедуры не превышает 1%, Высокая эффектив¬
ность, «мини-инвазивность*> и низкий риск катетерных операций позволяют
использовать их в качестве метода выбора у больных с пароксизмальными
Глава 7. Комбинированное использование интервенционных методов... 133наджелудочковыми и желудочковыми тахикардиями, трепетанием предсердий,
частой экстрасистолией. Результаты международных исследований позволяют
рекомендовать методику РЧА при этих нарушениях ритма как терапию выбора,
отдавая ей предпочтение перед постоянным приемом медикаментов.Одной из наиболее трудно поддающихся лечению аритмий является
фибрилляция предсердий. Актуальность проблемы обусловлена в первую оче¬
редь повышением риска развития ишемического инсульта на фоне этого нару¬
шения ритма. Лекарственная терапия далеко не всегда способна эффективно и
длительно устранять фибрилляцию предсердий. В последние годы у пациентов
без грубых структурных изменений в сердце РЧА все активнее используется
для радикального устранения этой аритмии. Целью подобного вмеятательства
является изоляция устьев легочных вен для исключения триггерной активации
фибрилляции предсердий. Технически данная операция является одной из
наиболее сложных в интервенционной аритмологии, сопряжена с большим
риском для пациента. В связи с этим проведение подобного вмешательства
требует специальной подготовки больного, включая доопераиионное проведе¬
ние мультиспиральной компьютерной томографии сердца с контрастировани¬
ем левого предсердия для определения анатомических особенностей впадения
легочных вен. Эффективность РЧА при фибрилляции предсердий составляет
65-90%. В Первом МГМУ им. И.М. Сеченова данный вид оперативного вме¬
шательства освоен и с успехом используется у больных с фибрилляцией пред¬
сердий при неэффективности медикаментозной аіітиаритмической терапии.К ограничениям методики относят необходимость с>’щес'гвования аритмии
в ходе операции либо возможности ее индукции в ходе вщ'трисердечноі'о ЭЛеК'
трофизиологического исследования; опасность воздействия на аритмогенный
фокус при его близком расположении к важным анатомическим структурам
сердца (проводящие пути, коронарные артерии).При проведении катетерных операций на сердце в нашей рентгенонера¬
ционной используется новейшее диагностическое оборудование — система
нефлюороскопического картирования CARTO ХР (производитель — Biosense
Webster). Применение специального навигационного катетера со встроенным
в его кончик сенсором и системы координат, создаваемой располагающимися
в проекции сердца магнитами, позволяет получать трехмерное изображение
камеры сердца. В результате точность топической диагностики аритмии увели¬
чивается до 4-5 мм.Вторым направлением интервенционной аритмологии является имплан¬
тация антиаритмических устройств. Наиболее традиционное направление —
имплантация электрокардиостимуляторов (ЭКС) с целью лечения блокад
сердца, синдрома слабости синусового узла — в последние годы вышло на
новый этап развития. Основой его явилось создание новых, полностью циф¬
ровых электрокардиостимуляторов. Это позволяет расширить как диагно¬
стические (запись эпизодов аритмий в палшть элекфокардиостимуляторов с
последующим анализом при программировании), так и лечебные возможности
подобных устройств (создание наиболее физиологичных алгоритмов стимуля¬
ции сердца, предотвращения или купирования нарушений ритма).
134 КардиологияПри невозможности радикального устранения желудочковых наруше¬
ний сердечного ритма, сохраняющемся высоком риске внезапной сердечной
смерти пациентам показана имплантация специального антиаритмическо-
го устройства — имшіантируемого кардиовертера-дефибриллятора (ИКД).
Многочисленные международные исследования продемонстрирова-іи сниже¬
ние смертности при использовании таких устройств у больных из группы риска
развития жизнеугрожающих аритмий: при сердечной недостаточности и низ¬
кой ФВ левого желудочка, при гипертрофической кардиомиопатии, наслед¬
ственных кана^юпатиях (синдроме Бругада, синдроме удлиненного интервала
QTи др>тих). Современные имгыантируемые кардиовертеры-дефибрилляторы
автоматически определяют момент возникновения желудочковой тахикардии
или фибрилляции желудочков и устраняют ее сверхчастой стимуляцией или
электрическим разрядом. Кроме того, они выполняют функцию обычного
электрокардиостимулятора, позволяя проводить медикаментозную антиарит-
мическую терапию, не опасаясь развития брадикардии или блокад.У больных со сниженной ФВ левого желудочка и блокадой левой ножки
пучка Гиса существенный вклад в усугубление сердечной недостаточности
вносит нарупіение синхронности сокращения правого и левого желудочков.
Устранить эту диссинхронию можно, имплантировав пациенту спепиальное
устройство для ресинхронизируюшей терапии (большинство таких устройств
включают и функции кapдиoвepтepa-дeфибpиJЪ'lятopa). Помимо установки
электродов в правое предсердие и правый желудочек, третий электрод про¬
водится в коронарный синус и далее в одну из латеральных вен сердца, обе¬
спечивая стимуляцию левого желудочка. В результате достигается синхронное
сокращение обоих желудочков, что позволяет улучшить результаты лечения
этой труднокурабельной группы паииентов: уменьшить проявления сердечной
недостаточности, снизить риск сердечно-сосудистой смерти.Еще одно из современных направлений кардиологии, в развитии которого
принимает активное участие интервенционная аритмология, — диагностика
причин синкопальных состояний. Нередко все проведенное обследование не
позволяет уточнить причину обморока. В этой ситуации вьмвить нарушения
ритма или проводимости, которые приводят к внезапной потере сознания,
позволяет имплантация под кожу небольшого, весом менее 20 г, петлевого
регистратора, принцип действия которого напоминает холтеровское монито-
рирование ЭКГ. Однако время мониторирования у подобного устройства пре¬
вышает 1 год. Устройство атстивируется пациентом при возникновении типич¬
ных жалоб либо автоматически при возникновении частого или редкого ритма
и позволяет зарегистрировать даже редко возникающие аритмии.В Первом МГМУ им. И.М. Сеченова все эти высокотехнологичные мето¬
ды медицинской помощи доступны для пациентов и активно применяются в
повседневной практике.Комментарий ВЛ. Сулимова — профессора, зав. кафедрой факультетской терапии№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукДанный клинртческий пример наг^тядно демонстрирует современные дости¬
жения в области кардиологии. Особенно ярко они проявляются при лечении
Глава 7. Комбинированное использование интервенционных методов,.. 135больных как с острыми, так и с хроническими формами ИБС, а также с раз¬
личными наруиіениями ритма сердца. Не вызывает сомнений, "гго, помимо
медикаментозной терапии, краеугольным камнем в лечении кардиологиче¬
ских больных являются возможности современной интервенционной кар¬
диологии, Это касается и методов реваскуляризации миокарда с помошью
новых высокотехнологичных методов лечения, которыми являются баллон¬
ная ангиопластика и стентирование коронарных артерий, и методов катетер-
ной радиочастотной аблации в лечении различных аритмий.Если говорить о чрескожных вмешательствах на коронарных артериях, то в
. настоящее время общепризнаїіо, что первичная баллонная ангиопластика
и стентирование коронарньгх ар^герий являются методом выбора в лечении
больных острым инфарктом миокарда с подъемом сегмента ST на ЭКГ. Это
справсд,чиво и для большинства больных с острым коронарным синдромом
без подъема сегмента ST на ЭКГ, имеющих высокий риск развития сердечно¬
сосудистых осложнений. Все большему числу больных со стабильными фор¬
мами И БС выполняется реваскуляризация миокарда с помошью чрескожных
коронарных вмешательств, и в настоящее время число выполняемых чре¬
скожных коронарных вмешательств в мире значительно превышает количе¬
ство операций коронарного шунтирования.Внедрение в клиническую практику' метода радиочастотной катетерной
аблации позволило полностью устранять аритмии у большого числа молодых
людей, ранее обреченных пожизненно принимать различные антиаритмиче-
ские препараты, В первую очередь это касаегся больных с наджелудочковыми
пароксизма-тьными тахикардиями на фоне синдрома WPW. больных с узло¬
выми пароксизма-тьными тахикардиями, больных с «классическим» трепета¬
нием предсердий. У этой категории больньи( радиочастная аблация является
методом выбора в устранении нарушений ритма.Сложнее обстоит дело у больных с желудочковыми нарушениями ритма
сердца, особеїшо потенциально опасными для жизни, к которым отіюсят-
ся желудочковая тахикардия и фибрилляция желудочков. Несмотря на то,
что в России в связи с зкономи^іескими факторами число имплантаций
кардиовертеров-дефибрилляторов крайне мало и основным способом про-
филакгки внезапной сердечной смерти у больных высокого риска остаются
лекарственные препараты, здесь тоже наметился определенный прогресс,
что и продемонстрировал представленный случай. Даже у больньгх, которым
бьит имп.тантирован кардиовертер-дефибриллятор, возникает необходимость
в постоянной медикаментозной антиаритмической терапии с целью про¬
филактики рецидїівов возникновения фатальных желудочковьис аритмий.
Кардиовертер-дефибриллятор способен устранить возникшие жизнеугрожа-
юшие нарушения ритма, такие как желудочковая тахикардия или фибрил¬
ляция желудочков, однако он не способен предупредить их возникновение.
Это задача меллкаментозной антиаритмической терапии, которую трудно
переоценить, поскольку чем реже будут возникать эпизоды желудочковых
аритмий, требутоших вмешательства кардиовертера-дефибриллятора, тем
дольше он будет служить, поскольку его батарея будет истощаться медленнее.
136 КардиологияВ то же время необходимо понимать, что эффективность современных анти-
аритмических препаратов в отношении профилактики рецидивов желудоч¬
ковой тахикардии и фибрилляиии желудочков крайне низка. Это прекрасно
продемонстрировал данный клинический случай, подтвердивший низк>то
эффективность различных антиаритмических препаратов в плане их возмож¬
ностей вторичной профилактики внезапной сердечной смерти. Это согласу¬
ется со всеми ранее проведенными клиническими исследованиями, которые
показали, что эффективность самых «мощных» современных антиаритмиче-
ских препаратов 111 класса в отношении профилактики рецидивов желудоч¬
ковых тахикардий, к которым относятся амиодарон и соталол, составляет не
более 25-30%.Помимо этого, даі^шьій клинический случай наглялно подтвердил воз¬
можность возникновения тяжелых, нередко фатальных проаритмических
эффектов антиаритм^іеских препаратов I класса при их назначении боль¬
ным с ишемической болезнью сердца, в особенности перенесшим инфаркт
миокарда.В заключение, я думаю, что ссли бы эта ситуация возникта 10 лет назад,
то нашего пациента вряд ли удалось бы спасти, поскольку положительный
результат его лечения был обусловлен только комплексным использованием
всех самых современных возможностей интервентгаошюй и традиционной
кардиологии; реваскуляризации миокарда с помошью чрескожных коронар¬
ных вмешательств, радиочастотной аблации аритмогенньгх зон в левом желу¬
дочке, имплантации кардиовертсра-дефибриллятора и медикаментозной
антиаритмической терапии.
Глава 8АРТЕРИАЛЬНАЯ ГИПЕРТОНИЯ
И ЦЕРЕБРОВАСКУЛЯРНАЯ ПАТОЛОГИЯ —
ПАТОГЕНЕТИЧЕСКАЯ СВЯЗЬ И ПОДХОДЫ
К ЛЕЧЕНИЮН.Д. Саркисова, О.В. Благова, А.В. Недоступ,Л./О. Сгпойда, Л.Ю. Зайцев, В.Е. СмирновНесмотря на то, что дебют эссенциальной артериальной гипертонии
(гипертонической болезни) все чаше приходится на относительно молодые
годы (в том числе на возраст моложе 30 лет), в значительном числе случаев
артериальная гипертония у молодых иосит все же симитоматический харак¬
тер. Об этом позволяют судить ее устойчивый характер, недостаточная эффек¬
тивность современной гипотензивной терапии, высокая степень повышения
АД, нередко — высокий уровень диастолического давления. Вместе с тем
установить конкретную форму вторичной артериа-'іьной гипертонии бывает
очень непросто даже при использовании всего арсенала современных лабо¬
раторных и инструментальных исследований; далеко не единичны случаи,
в которых обследование приносит противоречивые результаты, и выявить
убедительную причину симптоматической гипертонии так и не удается. Мы
представляем результаты длительного (более 20 лет) наблюдения за молодой
пациенткой с высокой артериальной гипертензией, в процессе которого
менялись как представления о механизмах гипертонии, так и подходы к ее
лечению, в частности очень сушественным этапом в ведении больной стало
выявление у нее врожденной цереброваск>’лярной патологии с последующим
хирургическим лечением. После операции наблюдение за больной было про¬
должено еще в течение 10 лет.Больная К., 40 леї , поступила в Факультетскую терапевтическую клинику
им. В.Н. Виноградова 19.02.2001 г. с жалобами на практически постоянное
ощущение «загруженной», «чужой» головы; головные боли различной лока¬
лизации и интенсивности (диффузные, в затьточной области, в лобных
областях, нравосторонние дсргающего характера с ощущением онемения
правой половины лица); головокружения, неустойчивость при ходьбе, эпи¬
зоды кратковременной потери сознания в душных помещениях; ухудшение
зреиия, снижение памяти; выраженные подъемы АД до 260 и 160 мм рт.ст.,
возникающие на фоне постоянно повышенного до 180—220 и 120-110 мм
ртхт. АД, нередко без видимой причины и-'1и в связи с эмоциональными
нагрузками, иногда сопровождающиеся >^ащснным сердцебиением; одышку
138Кардиологияпри умеренных физических нагрузках; выраженное снижение трудоспособно¬
сти; преходяшие отеки голеней, кистей и стоп; периоды онемения, слабости в
левой руке с неловкостью при простых движениях.Из анамнеза известно, что у родителей отмечаются умеренные подъемы АД
с пожилого возраста, у сына 15 лет дважды после физической нагрузки фик¬
сировались подъемы АД до 140-150 и 90 мм рт.ст. Курит с молодого возраста
по 10 сигарет в день. Беременности в 20 и 25 лет зак0№шлись срочными родами,
протекали без осложнений. С 1991 г. — миома матки (с 1999 г. — множествен¬
ная), с 1994 г — диффузная фиброзно-кистозная мастопатия. С 13 лет — реци¬
дивирующая невралгия правого тройничного нерва. Подъем АД до 160 и 130 мм
рхст. впервые зафиксирован в возрасте 27 лет {рис. 8,1), При повторных изме¬
рениях АД оставалось постоянно повышенным (130 и 100 мм рт.ст.), В 1988 г. в
стационаре по месту жительства состояние расценивалось как гипертоническая
болезнь, рекомендовался прием адельфана (без эффекта). Стали беспокоить
диффузные головные боли, периодическое ощущение «чужой» головы, колю¬
щие и ноющие боли в левой половине грудной клетки, не связанные с физи¬
ческой нагрузкой, сердцебиения. С этими жалобами в возрасте 30 лет впервые1974
27 лет1988 1991 19932000 2001
IIММАГоловные боли
Головокружение
Сердцебиение
Нарушение зренияОдышка
АД, мм рт.ст.130Внутривен¬наяурографияАнгиогра¬фия++++ ++++260160130100200130260160180-220110-120ДИАГНОЗ:ДвустороннийнефроптозСимптоматическая АГАГ смешанного генеза
тяжелого теченияРис. 8.1. Анамиез больной К., 40 лет, до 2001 г.
Глава 8. Артериальная гипертония и цереброваскулярная патология... 139поступила в Факультетскую терапевтическую клинику им. В.Н. Виноградова,
где гипертония рассматривалась как симптоматическая.В первую очередь исключался нефрогенный характер гипертензии. При
УЗИ изменений в паренхиме почек не отмечалось. В 1991 п при в/в урофа-
фии был выявлен двусторонний нефроптоз (с перегибом в мочеточниково¬
лоханочном сегменте обеих почек), который расненивался как наиболее
вероятная причина артериальной гипертензии, был поставлен диагноз
«двусторонний нефроптоз с ротацией правой почки. Артериа.тьная гипер¬
тония». В 1993 г. при нефросцинтиграфии полу^іеньт признаки снижения
кровотока в левой почке, умеренного нарушения секреторной функции и
кана-іьцевой экскреции. Через 8 лет, когда можно было ожидать как прогрес¬
сирования исходных нарушений в почках, так и развития гипертонической
нефропатии, нефросцинтиграфия показала нормальную функциональную
способность обеих почек. При ангиографии (1993, 2000 гг) были выявлены
ретроаортальное положение левой почечной вены с компрессионным сдав¬
лением ее ствола и длительной задержкой выведения с ретроградным током
крови (по последним данным, компрессии не было), а также удвоение левой
почечной артерии с 20% стенозом верхней ветви; отвергнут стеноз правой
почечной артерии, подозрение на который возникло при ультразвуковом
допплеровском исследовании, выполнявшемся в 1999 г. Состояние рас¬
ценивалось как «артериальная гипертензия смешанного генеза, кризового
течения. Перегиб правой почечной артерии с признаками стенозирования.
Ретроаортальное положение левой почечной вены с компрессионным сдав¬
лением ее ствола? Двусторонний нефроптоз». Хирургическое вмешательство
не рекомендовалось.Параллельно проводилось исключение эндокринных причин артериальной
гипертензии. Клинических и лабораторно-инструментальных признаков гипо-
ШІИ гипертиреоза у больной никогда не было. Неоднократно определялись как
суточная экскреция с мочой катехоламинов, альдостерона, ренина и кортизо¬
ла, так и содержание их в крови из различных отделов почечных вен, В 1993 г.
фиксировались отклонения по уровню альдостерона {табл. 8.1), которые в
анализе 2000 г. оказались выражены на порядок меньше. При трехкратной
ко.мпьютерной томографии надпочечников не удавалось визуализировать опу¬
холь, не было выявлено изменений турецкого седла при рентгенографических
исследованиях черепа.Таким образом, ни один из известных нам вариантов симптоматической
артериальной гипертензии (включая центральные формы ~ зндефа^іитьі, трав¬
мы и опухоли мозга) за 10 лет наблюдения выяатен не бьш. Отметим, что уже
при первой встрече с 30-летней больной показалось целесообразным оценить
мозговое кровоснабжение ввиду отчетливой неврологической симптоматики,
Были проведены ультразвуковое допплеровское исследование экстракрани-
альньЕС артерий (кровоток по внутренним сонным артериям нарушен не был)
и рентгенография шейного отдела позвоночника, выявившая выраженный
унковертебральный артроз с экзостозами в сторону позвоночного канала, что
вносило свой вклад в развитие энцефалопатии. При электроэнцефа.Юфафии
140КардиологияТаблица 8JИсследования уровня гормонов у больной К.
А. Селективный забор крови из почечных вен1993 г.2000 г.Правая почечная вена
выше места впадения над¬
почечниковойРенин — 0,976 нг/мл/ч,
альдостерон — 105,5 пг/млРенин 0,98 нг/мл/ч, альдо¬
стерон 139,3 пг/млПравая почечная вена
ниже места впадения над¬
почечниковойРенин — 0,853 нг/мл/ч,
альдостерон — 104,6 пг/млРенин 2,07 нг/мл/ч, альдо¬
стерон 290,7 пг/\шЛевая почечная вена выше
места впадения надпочеч¬
никовойРенин — 0,757 нг/лш/ч,
альдостерон — 1267 пг/мл
(норма 15-150 пг/мл)Ренин 2,16 нг/мл/ч, альдо¬
стерон 268,7 пг/мл (норма
8-172)Левая почечная вена ниже
места впадения надпочеч¬
никовойРенин — 1,218 нг/мл/ч,
альдостерон — 149,0 пг/млРенин 2,346 нг/мл/ч, аль¬
достерон 234,5 пг/млБ. Суточная экскреция с мочойГодПоказательЗначениеОпенка показателя1993Альдостерон108 нмольНорма1999Адреналин32,8 нмольНорма1999Норадреналин141,8 нмольНорма1999вмк15,09 мкмольНорма1999гвк24,4 мкмольНормаотмечались признаки дисфункции срединных структур головного мозга и
«заинтересованность» левой височной области.Обращали на себя внимание как быстрое возрастание максимальных
цифр АД и высокая резистентность к терапии, так и выраженное прогресси¬
рование неврологических нарушений (с отчетливыми психовегетативными
реакциями), гипертонической ангиопатии сетчатки при отсутствии суще¬
ственных изменений на ЭК.Г и при ЭхоКГ. Уже к 1994 г. АД стало достигать
200 и 130 мм рт.ст. Проводилась комбинированная гипотензивная (анта¬
гонисты кальция, ингибиторы АПФ, диуретики, р-блокаторы, кар дура) и
психотропная терапия (в/в реланиум, людиамил, клоназепам, сонапакс)
практически без эффекта. Гипертензия приобрела стабильный характер,
однако при суточном мониторировании АД было зафиксировано ночное
снижение АД до 120 и 80 мм рт.ст. , что заставляло лишний раз задуматься об
особенностях его регуляции. За последний год отметила резкое ухудшение
самочувствия, что проявлялось в плохой переносимости обычных физиче¬
ских нагрузок, в появлении и прогрессировании ухудшения зрения и сни¬
жения памяти, эпизодов онемения и слабости в левой руке, в постоянных
головных болях и выраженных головокружениях, нарастании одышки. АД
Глава 8. Артериальная гипертония и цереброваскулярная патология... 141достигало 260 и 160 мм рт.ст., цифры ниже 220 и 120 мм рт.ст, практически
не фиксировались.При осмотре в Факультетской терапевтической клинике им, В.Н. Виногра¬
дова в феврале 2001 г. состояние расценивалось как относительно удовлетвори¬
тельное, Больная гиперстенической конституции с равномерным распределе¬
нием подкожной жировой клетчатки. Кожные покровы нормальной окраски,
стрий растяжения нет. Голени и стопы пастозны. Дыхание везикулярное, хри¬
пов нет, ЧД 18 в минуту. Сердце в размерах не увеличено, верхушечный толчок
не усіїлен, отмечается акцент И тона над аортой, шумов нет. ЧСС 78 ударов в
минуту, ритм правильный, АД на руках симметрично, при поступлении 220 и
120 мм рт.ст. Шумы в проекции почечных артерий не выслушиваются. Живот
мягкий, безболезненный, печень и селезенка не увеличены.В анализах крови и мочи, как и за все время наблюдения в Факультетской
терапевтической клинике им. В.Н, Виноградова, существенных отклоне¬
ний от нормы не выявлено. Оставался нормальным уровень креатинина
(1,2 мг%).На ЭКГ— начальные признаки гипертрофии левого желудочка, упло¬
щенные двухфазные зубцы Т в отведениях V^—V^. По данным ЭхоКГ, сердце
нормальных размеров, толщина стенок левого желедочка 1,0 см, ФВ левого
желудочка 65%. Была продолжена комбинированная гипотензивная терапия
(энап, локрен, кардура, верошпирон, клоназепам с добавлением фуросемида,
диована), которая не давала эффекта. Генез артериальной гипертензии рас¬
сматривался нами как смешанный — сочетание умеренного вазоренального
конфликта с несовершенством центральных и вегетативных механизмов
регуляции сосудистого тонуса у больной с выраженной психоэмоциональной
лабильностью. Для уточнения значимости стеноза левой почечной артерии
больная была проконсультирована врачами межклинического отделения
ангиографии Л. Ю. Стойдой, канд. мед. наук В.Е. Смирновым, канд. мед. наук
А.Ю. Зайцевым — было высказано сомнение в наличии стеноза левой почеч¬
ной артерии и предложено провести МРТ головного мозга с контрастиро¬
ванием сосудов (предполагалась врожденная аномалия, выражающаяся в
нейроваскулярной компрессии позвоночной артерией (ее сегментом V4)
вентролатеральной части продолговатого мозга, клиническим проявлением
которой является триада «невралгия тройничного нерва, артериальная гипер¬
тензия, энцефалопатия»).По результатам МРТ (рис. 8.2, 8.3) изменений в головном мозге и в интра-
краниааьных сосудах обнар>’жено не было, и гипотеза о нейроваскулярной
компрессии была отвергнута. Однако при исследовании экстракраниалъных
сосудов выявлены S-образная извитость и перегиб левой позвоночной арте¬
рии у места ее отхождения от подключичной артерии. Обе внутренние сонные
артерии делают петли в области основания черепа, отмечено также снижение
магнитно-резонансного сигнала от правой подключичной артерии, не исюїю-
чался 40—50% стеноз левой подключичной артерии у места ее отхождения от
дуги аорты.
М2КардиологияРис. 8.2. MPT экстракраниальных
сосудов больной к. {левая сторона)Рис. 8.3. МРТ экстракраниальных сосу¬
дов больной к. (правая сторона)Рис. 8.4. Ангиограмма левой внутренней
сонной артерии больной К.Рис. 8.5. Ангиоірамма правой внутренней
сонной артерии больной К.
Глава 8. Артериальная гипертония и цереброваскулярная патология.., 143Было решено провести повторн>то ангиографию почечных артерий, артерий
головы и шеи, при которой стенозы почечных артерий были отвергнуты, пока¬
зано не удвоение, но раннее деление левой почечной артерии. Ангиотрафия
также подтвердила наличие полных петель обеих внутренних сонных артерий
{рис. 8.4, 8.5), извитость левой позвоночной артерии, перегиб левой подклю¬
чичной артерии до места отхождения позвоночной артерии.Повторное ультразвуковое допплеровское исследование показало признаки
40% стенозов обеих внутренних сонных артерий, снижение кровотока по левой
позвоночной артерии.Каков бы ни бьы вклад выявленных нарушений мозгового кровоснабжения
в генез гипертонии, уже само по себе наличие ишемии мозга с клинически
значимой и быстро прогрессируюшей энцефалопатией явилось показанием к
оперативному вмешательству на измененных сосудах. Бо.іьная была переведе¬
на в медсанчасть №1 ЗИЛа, где в два этапа (12 апреля и 8 сентября) зав. отде¬
лением сосудистой хирургии А. Г. Евдокимовым ей была выполнена операция
реимплантации внутренней сонной артерии в общую сонную артерию справа и
слева. Обратило на себя внимание изменение стенок артерий по типу фиброз¬
номышечной дисплазии, что заставляет предполагать подобные изменения и в
других артериальных бассейнах (включая почечные) с потенциальной возмож¬
ностью их стенозирования. Через 1-2 нед головные боли прекратились прак¬
тически полностью, значительно укіеньшились головокружения, не отмечено
рецидивов невратгии тройничного нерва, заметно повысились работоспособ¬
ность, общий тонус больной, что позволило ей уже через 10 дней после повтор¬
ной операции участвовать в автомобильной поездке в Крым. На фоне посто¬
янной гипотензивной терапии (энап 20 мг, атенолол 100 мг, верошпирон 50 мг,
клоназепам 1,5 мг) АД стойко снизилось с 260 и 160 до 170-180 и 100-110 мм
рт.ст., изредка повышаясь до 200 и 120 мм рт.ст., что на общем благополучном
фоне приводило к появлению головных болей (ранее чувствительность к подъ¬
емам АД была полностью утрачена). Однако эти цифры АД нельзя признать
окончательным итогом операций, так как судить о нем можно было лишь через
полгода. Регулярно принимает также трентал, кавинтон, ноотропил.Таким образом, диагноз на сегодняшний день представляется следую¬
щим: «Артериальная гипертензия смешанного генеза, тяжелого течения.
Фиброзномышечная дисплазия сонных артерий: полные петли обеих вну¬
тренних сонных артерий. Раннее деление левой почечной артерии без при¬
знаков стенозирования. Ретроаортальное положение левой почечной вены.
Начальный стеноз левой подключичной артерии с явлениями ишемии.
Недостаточность кровообращения I стадии. Дисциркуляторная энцефалопатия
смешанного генеза (ишемическая, гипертоническая, вертеброгенная) с цефал-
гическим синдромом. Преходящая невралгия правого тройничного нерва.
Распространенный остеохондроз позвоночника с преимущественным пораже¬
нием шейного отдела. Аденомиоз. Множественная миома матки. Диффузная
фиброзно-кистозная мастопатия».В табл. 8.2 представлен перечень диагнозов, которые ставились больной на
разных этапах обследования и наблюдения за ней.
144КардиологияТаблица 8.2Эволюция диагнозов больной К. в 1988-2001 гг.ГодДиагаоз1988(по
местужительства)Гипертоническая болезнь.1991Двусторонний нефроптоз с ротацией правой почки.
Артериалъттая гипертония.Распространенный остеохондроз позвоночника1993Симптоматическая артериальная гипертония (вазореналышя?).
Двусторонний нефроптоз.Распространенный остеохондроз иозвоно’шика1994Артериа.1ьная гипертония.Двусторонний нефроптоз.Распространенный остеохондроз позвоночника.
Диффузная двусторонняя фиброзно-кистозная мастопатия.
Миома матки1999-2000Артериальная гипертензия смешанного геттеза, кризового течения.
Перегиб правой почечной артерии с признаками стенозирования.
Ретроаортальное положение левой почечной вены с компрессионным
сдавлением ее ствола?Двусторонний нефроптоз.Недостаточность кровообраиіения I стадии.Распространенный остеохондроз позвоночника с преил(>тцественным
поражением шейного отдела.Дисциркуляторная .энцефалопатия с цсфалгическим синдромом.
Преходящая невралгия правого тройничного нерва,Множественная миома матки.Диффузная фиброзно-кистозттая мастопатия2001Артериа.1ьная гипертензия смептаптюго гснсза, тяжелого течения.
Фиброзно-мышечная дисплазия сонных артерий: полные петли обеих
внутренних сонньгх артерий.Раннее деление левой почечной артерии без признаков стенозироватшя.
Ретроаортальное положение левой почечной вены.Начальный стеноз левой подключичной артерии с явлениями ишемии.
Недостаточность кровообратпения Г стадии.Дисииркуляторная энцефалопатия смешанного генеза (ишемі^ческая,
гипертоническая, вертеброгетшая) с цcфaJи•ичecким синдромом.
Преходяшая невралгия правого тройничного нерва.Распространенный остеохондроз позвоночника с преиму'шественным
поражением шейного отдела.Аленомиоз.Множественная миома матки.Диффузная фиброзно-кистозная мастопатия
Глава 8. Артериальная гипертония и цереброваскулярная патология... 145Комі^гентарий Н.Д. Саркисовой — заведующей отделением кардиологии
Факультетской терапевтической клиники им. В.Ы, Винофадова, канд. мед. наукИзложенная выше история болезни представляет интерес по целоліу ряду
причин. На протяжении 10 лет наблюдения за больной обращали на себя
внимание отчетливая тенденция к стабилизации артериального давления
(ках систолического, так и диастолического) на высоких цифрах — 230—250
и 130-140 мм рхст., постепенное развитие устойчивости к проводимой
гипотензивной терапии, включавшей все известные фуппы гипотензивных
препаратов и их сочетания. На этом фоне у больной нарастали явления сосу¬
дистой церебральной недостаточности, в то время как сердце и почки оста¬
ваясь практически интактными. Следует обратить внтшанис на трудности
диагностики, с которыми нам пришлось столкнуться в данном случае. Как
видно из истории болезни, больной .многократно проводились исследования
гормонального статуса, триж,т;ьт — ангиоірафичсское исследование с целью
исключения вазоренальной гипертонии, практически каждую госпитализа¬
цию проводилась оценка функциональной способности почек, исследова¬
лась структура надпочечников и т.д. Однако полу»[енные в резулыате обсле¬
дования данные не только не проясняли причину столь высокой гипертонии
у 40-летней женщины, но и, напротив, затрудняли постановку диагноза, так
как носили противоречивый, а порой — взаимоисюїюч^іющий характер.С другой стороны, в результате многолетнего наблюдения, анализа получен¬
ных данных и их сопоставления становится очевидным, что в основе такой
устойчивой гипертонии лежат, скорее всего, несколько причин: раннее деле¬
ние левой ночсчной артерии, ретроаортальное положение левой почечной
вены, \тиеренный двусторонний нсфроптоз, регистрировавшееся знa^штeль-
ное повышение уровня альдостерона в крови, выявленные при ангиографи-
ческом исследовании магистральных сосудов головы полные петли обеих
внутренних сонных артерий. Каждая из вышеперечисленных причин не
смогла бы сама по себе объяснить своеобразие клини^геской картины у нашей
больной. Вероятнее всего, все они потенциировали действие друг друга, усу¬
губляя течение болезни, что и нашло наиболее полное отражение в последнем
диагнозе. Все же создается впечатление об особом, ведущем месте церебро¬
васкулярной патологии в патогенезе симптоматической аргсрисшьной гипер¬
тензии у данной больной.Комментарий А.В. Недоступа — профессора кафедры факультетской тераіши
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукЯ согласен с Н.Д.Саркисовой в том, что патология сосудов головы имеет в
данном слу^ше особое значение. Об этом говоряі, во-первых, явная недо¬
статочность реноваскулярных (и, возможно, гормональных) изменеїшй для
формирования столь резкой степени выраженности артериальной гипсргеп-
зии, во-вторых, четкий, хоть и неполный эффект оперативного лечения —
коррекции дефектов магисгральных сосудов головы. Своеобразие субъек¬
тивной симптоматики играло роль, скорее, маркера цереброваскулярного
146 Кардиологияконфликта. Я думаю, что по крайней мере на сегодняшний день, эта патоло¬
гия была ведущей в сложном генсзе гипертензии у нашей больной.Данное наблюдение имеет принципиальное значение. Вероятно, мы стол-
кнуішсь с одной из совершенно особых (во всяком случае для терапевюв)
форм силптгоматической аріериальной гипертензии из разряда пентралъных.
Обычно сюда относят гипертонические состояния, обусловленные арахноиди-
талш, энцефалитами, травмами или опухолями головного мозга. Здесь же речь
идет о цереброваскулярной (по аналогии с реноваскулярной) гиперіеизии,
обусловленной — в данном случае — своеобразной патологией (фибромуску-
лярной дисплазией) машстральньг!с сосудов головы. При этом клиническая
картина гипертензии, как мы видим, иная, чем при известной церсброішіеми-
ческой гипертонии пожильпс лиц, для которой типичны кризы, нестабильность,
психи^теская обусловленность (см., например, работы B.C. Смоленского).
При этом необычность именно церебральной симптоматики у данной боль¬
ной была очевидна на протяжение всего времени наблюдения.Вообще роль органной ишемии — и не только почечной — мало изучена и
весьма любопытна. Известно мнение о нормализации АД у больньк после
инфаркта миокарда именно вследствие исчезновения (в результате некро¬
за) постоянного очага ишемии миокарда. Тем более вероятна артериальная
гипертония вследствие ишемии мозга (с его центрами регуляции функций
сердечно-сосудистой системы). Сегодня мы слишком мало знаем о новом
для нас виде симптоматрпеской, а именно цереброваскулярной гипертонии,
чтобы систематизировать ее клинические проявления. Примечательно, что
для врачей Факультетской терапевтической клиники им. В.Н. Винофадова с
самого начала был очевиден симптоматический характер гипертензии у дан¬
ной больной, хотя тщательные исследования не выявляли ее происхождения.
Можно сказать, что нам помог «счастливый случай» — встреча со специали¬
стами в области ангиографии, знаколшми с данной патологией (хотя их пред¬
варительное предположение о врожденной аномалии мозжечковой артерии
не подтвердилось). Напомним здесь же, что поводом для очередной такой
встречи послужила меняющаяся от исследования к исследованию картина
состояния сосудистого русла почек (причиной чему служит, вероятно, как
недостаточное совершенствование технических возможностей, так и разноч¬
тения в интерпретации результатов исследования).Уже было сказано о положительных результатах оперативного лечения — ста¬
билизации артериального flaBJiefiHH на более низком уровне, значиїельном
улучшении субъективной симптоматики. Мы не знаем, какова будет дальней¬
шая динамика состояния больной; не исключено, что многолетняя ишемия
отделов мозга, ведающих сосудистой регуляцией, могла привести к их необ¬
ратимому повреждению, при котором уже невозможно ожидать нормали¬
зации сосудистого тонуса. Возможно, более раннее вмешательство дало бы
лучший непосредственный результат. Не исключена, конечно, поддержива¬
ющая артериальную іипертонию роль изменений почечного кровотока, хоть
и нерезко выраженных. Я воздержусь от дальнейших рассуждений — слиш¬
ком мало мы пока знаем о новой разновидности ишемшіеской гипертонии.
Глава 8, Артериальная гипертония и цереброваскулярная патология... І47Однако можно с уверенностью сказать, что датьнейшие исследования в
этом направлении представляются весьма интересными и целесообразными.
Очень может быть, что спустя некоторое время в студенческих учебниках и
руководствах по кардиологии в разделе о симптоматических гипертониях
появится несколько новых строчек.Комментарий А.Ю. Стойды, А.Ю. Зайцева, В.Е. Смирнова— сотрудников
отделения ангиографии отдела лучевой диагностики Первого МГМУ им.
И. М. Сеченова, канд. мед. наукУдлинение сонных артерий, проявляющееся в их извитости, петлеобразова¬
нии и перегибах, остается до сих пор малоизученной проблемой, которой не
уделяется того внимания, которого она, безусловно, достойна. Значимость
данной патологии определяется прежде всего ее высокой распросгрален-
ностью среди населения (до 15%), зачастую врожденным характером, зна¬
чительным влиянием на качество жизни, возможностью развития тяжелых
осложнений (транзиторных ишемических атак, инсультов). Патогенез раз¬
вития данного заболевания во многом неясен, однако взаимозависимость
удлинения сонных артерий и артериальной гипертензии у нас в настоящее
время не вызывает сомнений. Наш предыдущий опыт работы с такого рода
пациентами позволяет предположить развитие так называемого порочного
круга: наличие петли сонной артерии за счет компрометации мозгового кро¬
вотока ведет к подъему артериального давления, которое, в свою очередь,
усугубляет петлеобразование и сопротивление кровотоку за счет непосред¬
ственного влияния на измененную стенку сосуда. Однако мы полашем, что
данный механизм развития артериальной гипертензии наверняка не един¬
ственный.В механизме подъема АД может участвовать чрезвычайно богатое соб¬
ственное симпатическое нервное сплетение сонных артерий, которое,
по-видимому, вовлекается в патологический процесс в данной ситуации.
Возможно непосредственное механическое раздражение петлей пршіегаю-
щих к ней нервных структур (черепно-мозговых нервов, симпатртческих и
парасимпатических ганглиев и др.). К такого рода взаимосвязям относится
и первоначально высказанное нами предположение о развитии артериаль¬
ной гипертензии вследствие нейроваскулярной компрессии ствола голов¬
ного мозга позвоночной артерией, которое бьыо отвергнуто в результате
дальнейшего обследования. Кроме того, нельзя исключить участие в про¬
цессе других брахиоцефальных артерий и их ветвей, которые у данной кате¬
гории больных, как правило, также изменены. В пользу последнего говорит
стойкое снижение артериального давления, которое мы наблюдали у боль¬
ных после стентирования перегибов подключичных артерий, Зіідоваскуляр-
ной окклюзии затылочных артерий при их гипертрофии различного генеза,
различных щунтирующих процессах и т.д. Данные мировой литературы по
обсуждаемой проблеме немногочисленны и преимущественно касаются
хирургической техники лечения этой патологии. Тем ценнее представлен¬
ное наблюдение, возможно первое, отличающееся полнотой обследования
i4S Кардиологияи значительной дліггельностью наблюдения за больной с симптоматическойартериальной гипертензией и удлинением — петлеобразованием сонныхартерий,P.S, В дальнейшем больная в течение нескольких лет не обращалась в
клинику лдя стационарного лечения, что было связано с целым рядом семей¬
ных обстоятельств. Непродолжительное время принимала диротон 10 мг/сут,
локрен 40 мг/сут, фуросемид. периодически — клофелин; в даньнейшем регу¬
лярный прием препаратов прекратила. АД колебалось от 140 и 80 мм рт.ст до
180-200 и 100—120 мм рт.ст., изредка возникали и более выраженные подъемы
(до 280 и 120 мм рт.ст.), которые больная субъективно не ощущала. Летом
2008 г. перенесла сильнейший стресс (гибель сына в автомобильной катастро¬
фе), контроля за гипотензивной терапией в это время не бьито; отмечалось
динамическое нарушение мозгового кровообращения с преходящей дизартри¬
ей. В ноябре 2008 г на фоне подъема АД до 260 и 100 мм рт.ст. перенесла ише¬
мический инсульт в бассейне левой среднемозговой артерии с постепенным
восстановлением утраченных функций в результате интенсивной сосудистой
терапии и возобнов^тения адекватной гипотензивной терапии.В январе 2009 г находилась на стационарном лечении в Факультетской
терапевтической клинике им. В.Н. Виноградова. Наряду с подъемами АД
отмечалась одышка при умеренной физической нагрузке. На ЭКГ и по дан¬
ным ЭхоКГ по-прежнему отсутствовали выраженные признаки гипертрофии
левого желудочка, однако выявлены признаки диастолической дисф>тікции
левого желудочка. Не отмечено признаков гипертонической нефропатии. При
МРТ головного мозга выявлена картина немногочисленных очагов в белом
веществе, вероятно, сосудистого генеза. В результате терапии диротоном
20 мг/сут, лозаном 50 мг/сут, метопрололом 100 мг/сут, верошпироном 50 мг/сут,
фуросемидом 40 мг 2 раза в неделю, клоназепамом 0,5 мг на ночь, сонапаксом
20 мг/сут, а также в/в вливаний реланиума АД удалось стабилизировать
на уровне 130-140 и 80 мм рт.ст. с нечастыми подъемами до 160-180 и
90 мм рт.ст., уменьшилась одышка, улучшилось общее самочувствие больной.
Рекомендованы также повторные курсы сосудистой терапии. В течение после¬
дующих 1,5 лет самочувствие больной оставалось относительно стабильным, от
госпитализации в клинику отказывалась по семейным обстоятельствам.
Глава 9ПСЕВДОКЛАПАННЫЙ ВАРИАНТ ИНФЕКЦИОННО¬
ИММУННОГО МИОКАРДИТА ИЛИ РЕВМОКАРДИТ?Н.Д- Саркисова, О.В. Благова, А.В. НедоступДанным наблюдением мы открываем серию клинических разборов, посвя¬
щенных некоронарогенной патологии миокарда — обширной группе заболе¬
ваний сердца, которая, в отличие от ИБС, артериальной гипертонии, пороков
сердца, остается недостаточно изученной и не приштекаст к себе внимания
широкого круга терапевтов и кардиологов — по-видимому, ввиду большой
сложности диагностики отдельных нозологических вариантов, тем более их
лечения, отсутствия достаточного количества международньос исследований
у этой категории больных. Вместе с тем таких больных много. В Москве на
сегодняшний день практически отсутствуют крупные иентры, которые целена¬
правленно занимались бы этой патологией: при относительно блаїюприятном
течении заболевания пациенты оказываются под наблюдением терапевтов и
кардиологов, не всегда подготовленных к их ведению, при развитии драматиче¬
ских осложнений (сердечной недостаточности, угрожающих жизни нарушений
ритма и проводимости) они попадают в кардиохирургические стационары, где
в ряде случаев им может быть оказана существенная помощь, однако этиопато-
генетическая терапия (даже там, где она возможна), как правило, остается вне
поля зрения хирургов. Очевидно, что на успех в лечении этих больных можно
рассчитывать лишь при тесном взаимодействии кардиологов, кардиохирургов,
морфологов, генетиков, иммунологов, вирусологов.Представленного больного мы наблюдали в 2004-2005 гг. — сегодня, веро¬
ятно, кое-что мы сделали бы ішаче: накопился некоторый опыт, несколько
изменились наши возможности и представления о лечении (хотя эффекта
по-прежнему удается добиться редко), однако в целом данный случай является
весьма показательным и поднимает вопросы, которые еще до:ио останутся
актуальными. Особый интерес представ,тяют дифференпиальная диагности¬
ка ревматического и неревматического миокардитов у молодых пациентов, а
также возможность клинически значимого вирусного эндокардита с пораже¬
нием клапанов сердца, которая обсуждается на примере данного больного.Больной X., 34 лет, впервые поступил в отделение кардиологии Факультетской
терапевтической клиники им. В.Н.Виноградова 24.05.2004 т. с жалобами
на одышку при ултеренпых физических нагрузках (подъем по лестнице на
2—3 этажа), приступообразный кашель практически без отделения мокроты,
ноюшие боли в левой половине грудной клетки, возникающие во время каїшія,
нечастое ощущение перебоев в работе сердца, потливость.Из анамнеза жизни\ отец 70 лет, хроническими заболеваниями не страдает,
мать умерла в возрасте 51 года, внезапно, причину тотао указать затрудняется
150Кардиология(страдала неврологическим, психическим? заболеванием), брат 39 лет и дочь
2 лет здоровы. Родился в Баку в 1970 г., служил в действующей армии (в
Карабахе) с 1988 по 1990 г., в последующем работал тренером по восточной
борьбе, занимался тяжелой атлетикой. Не курит, алкоголь употребляет в уме¬
ренных количествах. С детства и до настоящего времени страдал ангинами
1—2 раза в год, тонзиллэктомия не проводилась. В течение ряда лет периоди¬
чески отмечались эпизоды сухого кашля, сопровождавшиеся появлением дис¬
танционных сухих хрипов, которые проходили самостоятельно.Анамнез заболевания {рис. 9.1): чувствовал себя удовлетворительно и хорошо
переносил болыггае физические нагрузки до декабря 2003 г., когда просту¬
дился — появились першение в горле, сухой кашель, потливость. Отмечалось
небольшое повышение температуры. Предполагалась правосторонняя брон¬
хопневмония. Лечился бисептолом, затем антибиотиками (названия не пом¬
нит), тера-флю. Через несколько дней самочувствие улучшилось, однако в
первых числах января возобновился кашель, потливость, длившиеся 3—4 дня
и полностью купировавшиеся на фоне короткого курса антибактериальной
терапии. Через 2 нед (конец января) — вновь эпизод кашля и потливости; тем¬
пературу не измерял, лечился виталіинами, инъекциями алоэ, самочувствие
улучшилось. В начале февраля уехал в Баку, где на фоне тренировок появилась
и стала нарастать одышка при небольшой физической нагрузке, а затем и в
покое, noHBHjmcb перебои в работе сердца, возобновился кашель. 10.02.2004 г.
был госпитализирован в стационар г. Баку, где при ЭхоКГ выявлены выражен-
1юс расширение полостей обоих желудочков и предсердий, митральная регур-
гитация 111 степени, снижение ФВ левого желудочка до 28%. Лабораторные
показатели — без существенных отк^юнений от нормы. Состояние былоХП.ОЗ 1.04конец1.0411.04 IV.04
нагрузки ???V.04XI1.04лихорадка,
потливостьявления ОРВИодышкакашельперебои, боли в
области сердцаЭхо-КГлечение бисептол а/6 а/б витамины
тера-флю алоэРис. 9.1. Анамнез больного X., 34 годаЛЖ 9,0 ом
ПЖ 3,2 см
ФВ 27%8,8 см31%преднизолон 30 мг в/в 30 мг
дигоксин, энап,
верошпирон,
фуросемид
Глава 9. Псевдоклапанный вариант инфекционно-иммунного миокардита... І5Ірасценено как дилатационная кардиомиопатия. Выявлялись нарушения сер¬
дечного ритма в виде желудочковой экстрасистолии. Проводилась терапия
преднизолоном 30 мг/сут в/в, нитратами в/в, дигоксином 0,25 мг/сут, фуро-
семидом, альдактоном, энапом, кордароном. Самочувствие быстро улу^іши-
лось, уменьшилась одышка, повыси-чась переносимость физических нагрузок.
После выписки из стационара принимал энап 10 мг/сут, альдактон 50 мг/сут,
фуросемид 40 мг ежедневно, кордарон 100—200 мг/сут, дигоксин 0,25 mf/cjt:,
нигросорбид, продолжал прием преднизолона 2,5—5 мг/сут до апреля 2004 г.
На этом фоне сохранялась одышка при умеренных физических нагрузках,
периодически ощущал перебои в работе сердца. С 22 мая возобновился сухой
приступообразный кашель, усилилась потливость. Поступил в Факультетскую
терапевтическую клинику им. В.Н.Виноградова для обследования и лечения.При осмотре: состояние средней тяжести. Результаты термометрии (с интер¬
валом в 3 ч) представлены в табл. 9. L — даіпше характерны скорее для нару¬
шения тсрморегу^шиии, чем для воспалительного процесса. Кожные покровы
чистьте, отеков нет. Число дыханий 18 в минуту, дыхание жесткое, проводится
во все отделы, на форсированном выдохе выслушиваются свистящие и басовые
хрипы, преимущественно в нижних отделах правого легкого. Границы сердца
значительно расширены влево и вверх, верхушечный толчок в 6-м межре-
берье. Тоны сердпа глухие, ритм галопа, систолический шум с эпицентром
на верхушке, экстрасистолия до 8—10 в минуту. ЧСС78 уд/мин, АД 150 и
80 мм рт.ст. Живот мягкий, безболезне11^1ый при пальпации во всех отделах,
нсчень выступает из-іюд края реберной дуіи на 1,5 см, селезенка не увеличена.При лабораторном обследовании в анализах крови НЬ 15,7 г%, эритроци¬
ты 5,3 млн, цв. показатель 0,89, лейкоциты 8,4 тыс., нейтрофюіьі 68%, лимфо¬
циты 21 %, моноциты 9%, эозинофилы 1 %, базофилы 1 %, СОЭ 7 мм/ч, тромбо¬
циты 270 тыс., обш. белок 8,6 г%, альб>'мины 5,1 г%, глк. 83 мг%, креатинин1,4 мг%, азот мочевины 17 мг%, мочевая кислота 6,8 мг%, общ. билирубин1,0 мг%, ACT 23,7 ед/л, АЛТ 19,0 ед/л, гамма-ГТ 18,2 ед/л, ЩФ 173 ед/л,
натрий 139,6 мэкв/л, калий 4,0 мэкв/л.В крови бьы выявлена положительная реакция на СРВ (+), титры анти-0-
стрентолизина повышены не были. Проводилась серодиагностика миокардита
{табл. 9.2). Были получены диагностические титры антител к миокарду, к
стрептококкам класса IgG, а также к цитомегаловирусу и вирусу простого гер¬
песа. Антитела к ВИЧ обнаружены не были.Результаты термометрии у больного X. каждые 3 ч ( С)Таблица 9. tПод мышкойПол языкомРазница36,537,00,537,037,10,136,737.00,336,837,00,237,236.5-0,737,236.8-0,4
/52КардиологияСеродиагностика миокардита у больного X.Таблица 9.2ДиагностикаБольной
(май 2004 г.)Больной
(декабрь 2004 г.)Диагностический
титр АТ к миокарду TgMОО>1:10АТ к миокарду TgG1:4001:400>1:100АТ к Staph, aureus TgM>1;І0AT к Siaph. aureus IgG1:200>1:100AT к Strepu IgM (антіїгиалуро-
нидаза) >1:10AT к Strept. IgG
(антигиалуро H идаза)1:4001:400>1:100IgG к Clamidia (общ.)3,9<1 стрия.
>5 иолож.IgG к MycoplasmaТоже
<0,9 отрнп.
>1,1 полож.IgG к Cytomegalovirus kominis3,8IgG к Herpes simplex virus I3,8ТожеAT к пир. Коксаки В IgM>1:10AT к вир. Коксаки В IgG1:100>1:100В общем анализе мочи pH 5, уд. вес 1024, мутная, белка, сахара, ацетона*
желчных пигментов нет, уробилин выше нормы, лейк. и эритр. единичные в
препарате, слизи много, бактерий немного.На ЭКГ {рис. 9.2) определялись лсвожелудочковая экстрасистолия, син¬
дром гипертрофии левого желудочка с нарушением реполяризаиии, признаки
гипертрофии левого предсердия.холтеровском мопиторироваиии проведенном в период насыщения
кордароном, ЧСС 56—188 в минугу, днем ср. ЧСС 88/мин, ночью — 74/мин,
зафиксировано около 1600 желудочковых экстрасистол с периодам би- и три-
гсминии и 1100 наджелудочковых экстрасистол.По данным ЭхоКГ, левый желудочек 8,6 см, левое предсердие 4,9x7,1x7,3 см,
оценить правый желудочек не представлялось возможным из-за выраженного рас¬
ширения левых камер. Толщина стенок: МЖІТ 1,0 см, тЗС 1,0 см. Определялось
вьфаженное диффу:їное снижение сократительной способности миокарда и
на этом фоне — гипоакипезия переднего и сешального сегментов, ФВ левого
желудочка 28%. Митральные створки неравномерно утолщеньт, уплотнены,
движение задней сгворки несколько ограни^гено. Аортальный клапан не изме¬
нен. Клапан лешчной артерии и трикуспидальный клапаны также не изменеїш.
Стенки аорты не изменены. Выявлена митральная регургитация III стел єни,
пиковый диастолический градиент на митра.іьном клапане 11 мм рт.ст., средний
6,4 мм рт.ст,, аортальная регургитация II степени, пиковый систолический
градиент 13,6 мм рт.ст., трикуспидальная реіургитация I—П степени.При рентгенографии органов грудной клетки выявлено рас і дирение сосудов в
верхних отделах легких, уплотнение стенок бронхов, значительное увеличение
сердца в размерах, расширение влево и кзади (поперечник 21 см).
Глава 9. Псевдоклапанный вариант инфекционно-иммунного миокардита,., 153" К “ч-:-■мштт-iff pf
I 'ii\: ї- ьщРис. 9.2, Электрокардиограмма болі>ного X. Скорость записи 25 мм/с (пояснения в
тексте)При определении функпии внешнего дыхания выявлены признаки умерен¬
ной бронхиальной обструкции. Проба с атровентом через небулайзер показала
преимущественно необратимый характер бронхиальной обструкции (прирост
OФB^ составил 6%).При УЗИ органов брюшной полости патологии не выявлено. При ЭГДС —
недостаточность кардии, скользящая фьска пищеводного отверстия диафраг¬
мы, острая геморрагическая эрозия терминального отдела пищевода, поверх¬
ностный гастритБольной был осмотрен оториноларингологом — выяатсны искривление
носовой перегородки, хронический тонзил^тит вне обострения, в мазках с мин-
даттин на микрофлору выделены Streptococcus viridans и Neisseria sp.Таким образом, с учетом всего вышеперечисленного, дифференциатьный
диагноз проводился между миокардитом, дилатапионной кардиомиопатией и
ревмокардитом, В пользу неревматического характера миокардита (см. также
табл. 9.3) свидетельствовали следующие данные.1. Довольно отчетливая связь начала заболевания с вирусной инфекцией.2. Субфебрильная температура.3. Повышение титра IgG к миокарду в 4 раза (1:400 при норме ) ;100).4. Повышенные титры антител к цитомегаловирусу5. Отчетливый положительный эффект от терапии преднизолоном (даже
небольшими лозами) во время лечения в Баку. Хорошая переносимость
154КардиологияТаблица 9.3Дифференциальная диагностика ревматических и неревматических миокардитовпо А.Н. ОкороковуПризнакиЧто предшество¬
валоРевматический миокардитОбострение хронргческого тон¬
зиллита, острая носоглоточная
инфекцияJ|egeBMai^^ОРВИ, аллергическая реак¬
цияЛатентный период2-4 нед1—2 нед, иногда сразуВозраст7-15 летВ OCIIOnilOM с^едтп^Суставной син¬
дромХарактерноНе характерноНачалоОстрое или подостроеПостепенноеСистолический
ішти на верхушкеПостепе н н о ус и л и вается, стано¬
вится музыкальнымНефомкий, постепентю
ослабевает и исчезает при
успеиптом леченииКлапаныУтолшение створок и хорд
митра.'1ьного клапана, офаниче-
ние подвижности задней створ-
ки. пролапс, регургитаиияБез измененийПерикардитЧастоРедкоАнтитела в кровиКCTgCптококкуИримечанне. Жирным кошуром обозначены признаки, шюрые имелись у больного X. в мае 20041;больным значительных длительных физических нагрузок в течение многих лет
вплоть до начала заболевания делала диагноз дилагационной кардиомиопагии
маловероятным.О развитии ревмокардита заставляли дз^мать следующие факты.• Частые ангины и наличие хронического тонзиллита.• Выделение зеленяпдего стрептококка при посеве с MHimajiHH.• Повышение TgG к стрсптогиалуронидазе в 4 раза (1:400 при норме 1:100).• Уплотнение и неравномерное утолшение створок митрального клапана
с ограничением движения задней створки по данным ЭхоКГ, вьшвлснис
повышенного фалиента на митральном клапане в анамнезе. В го же время
возраст для развития первичного ревмокардита был поздний.Рассматривались следующие диапюстические концепции:1) подострый миокардит вирусной этиологии с минимальными изменения¬
ми клапанов, которые выявляются только при ЭхоКГ (наиболее вероятно);2) перенесенная ранее атака ревматизма с формированием умеренно
выраженного порока сердца + подострый миокардит вирусной этиологии
(вероятно);3) пapaJЪ^Ieльнoe развитие вирусного (инфекционно-аллергического?) мио¬
кардита и ревмокардита с постепенным формированием ревматического поро¬
ка сердца (возможно);4) острая (повторная?) ревматическая лихорадка с выраженным миокарди¬
том и формированием порока сердца (наименее вероятно).
Глава 9. Псевдоклапанный вариант инфекционно-иммунного миокардита... 155Диагноз на данном этапе был сформулирован следующим образом: постин-
фекционный миокардит подострого течения с развитием выраженной дила-
тации полостей сердца. Нарушения ритма сердца: желудочковая и надже-
лудочковая экстрасистолия. Недостаточность кровообрашения НА стадии.
Хронический обструктивный бронхит в фазе обострения. Недостаточность
кардии. Скользящая фыжа пищеводного отверстия диафрагмы. Острая эрозия
терминального отдела пищевода. Хронический тонзиллит вне обострения.
Искривление носовой перегородки.в клинике проводилась терапия: преднизолон 30 мг/сут, цефотаксим3,0 г/суг в/м в течение 2 нед, энап 20 мг/сут, кордарон 0,2 3 таб./сут, затем
2 таб./сут, верошпирон 100 мг/сут, фуросемид 40 мг через день, омез 20 мг
2 таб./сут, маалокс, Б результате состояние больного улучшилось: повысилась
толерантность к физической нагрузке, уменьшился кашель, нормализовалась
температура тела, укїеньшилось количество экстрасистол. При контрольной
ЭхоКГ отмечено небольшое увеличение ФВ левого желудочка. Больной был
выписан с рекомендациями продолжить прием преднизолона по 15 мг утром
и 15 мг днем в течение 1 мес (затем начать постепенное снижение дозы по2,5 мг в неделю до полной отмены), кордарона 300 мг/сут, метопролола
25 мг/сут, диуретиков, энапа и омеза в прежних дозах.Повторно поступил в юшніску в декабре 2004 г. в состоянии альвеолярно¬
го отека легких. После выписки из клиники дозу преднизолона постепенно
снижал вплоть до полной отмены в середине октября, остальные препараты
(за исключением фуросемида и омеза) к октябрю также постепенно отменил,
выполнял умеренные физические нагрузки, в начале октября перенес корот¬
кую простуду, в течение последнего месяца, несмотря на ежедневный прием
фуросемида, заметно наросла одышка (стала возникать при малейших нагруз¬
ках), появилось чувство тяжести в правом подреберье.Состояние при поступлении расценивалось как тяжелое. Определялись
акроцианоз, пастозность голеней, стоп. Дыхание резко ослаблено, выслу'-
шивалось значительное количество свистящих, ж>окжащих хрипов над всей
поверхностью легких. Число дыханий 26-28 в минут\^ Левая граница сердца
расширена до передней подмышечной линии, I тон ослаблен, акцент II тона во2 межреберье слева, ритм галопа, систолический шум с эпицентром на верхуш¬
ке, слабый диастолический шум на верхушке, диастолический шум в т. Боткина.
ЧСС 110 в минуту, ритм сердечных сокращений правильный, на этом фоне —
экстрасистолия 4—6 в минуту АД 140 и 65 мм рт.ст. Печень на 3—4 см выступала
из-под края реберной дуги, была чувствительна при пальпации.Анализы крови (общий, биохимический) практически не изменились: НЬ
14,1 г%, эритроциты 4,8 лшн, цв. показатель 0,87, лейкоциты 6,8 тыс., ней-
трофилы 72%, лимфоциты 22%, моноыиты 3%, эозинофилы 3%, базофилы
1%, СОЭ 12 мм/ч, тромбоциты 219 тыс., общ. белок 6,5 г%, альбумин 4,3 г%,
глюкоза ПО мг%, креатинин 1,2 мт%, азот мочевины 21 мг%, мочевая кис¬
лота 7,0 мг%, общ. билирубин 1,3 мг%, ACT 21 ед/л, АЛТ 19 ед/л, гамма-ГТ
15 ед/л, ЩФ 54 ед/л, натрий 143 мэкв/л, калий 3,6 мэкв/л. Обращали на себя
внимание лишь умеренное повышение уровня фибриногена и положительный
І56 КардиологияСРБ (+++). При повторном серологическом исследовании крови вновь отме¬
чено повышение титров антител к миокарду (IgG 1:400, см. табл. 9.2) и гиалу-
ронидазе (IgG 1:400). Антитела к вирусам Коксаки В не повышены.ЭКГ практически не отличалась от предыдущей, при холтеровском мони-
торировании ЭКГ, проведенном на 6-й день после возобновления терапии
кордароном, число желудочковых экстрасистол достигало 4000 в сутки (в том
числе по типу би- и тригеминии), выявлена также политопная наджелудочко-
вая экстрасистолия (всего 800 в сутки).При ЭхоКГ отмечено дальнейшее расширение левых камер сердпа — левого
желудочка до 10 см, левого предсердия до 6,0x7,4x6,7 см; ФВ левого желудочка
составляла 30%; определялось диффузное снижение сократимости с акинезией
задней стенки на всем протяжении. Створки митрального клапана неравно¬
мерно утолщены, уплотнены, подвижность их ограничена, выявлен макси¬
мальный гшковый градиент на клапане 17 мм рт.ст., регургитация ПІ степени.
Створки аортального клапана также были уплотнены, регургитация II степени.В клинике проводилась терапия: мовалис 7,5 мг/сут, цефазолин 2 г/сут, кор-
дарон 600 мг/сут, моноприл 10—15 мг/сут, карведилол 6,25 мг/сут, верошпирон
150 мг/сут, лазикс 120-60 мг/сут, тромбо-АСС 100 мг, атровент и лазолван через
небулайзер, омез 40 мг/сут, вентер 1,5 г/сут.С учетом динамики аускультативной картины и выявленных при ЭхоКГ
изменений на митральном и аортальном клапанах предстояло вернуться к диф¬
ференциальной диагностике ревматического и неревматического миокардита.Диагноз миокардита у нас с самого начала не вызывал сомнений. Картина
заболевания достаточно точно укладывалась в представления о так называемом
инфекционно-аллергическом миокардите, однако даже наличие четкой связи
дебюта заболевания с острой инфекцией (как было и в нашем случае) требует
исключения других причин миокардита. Рассмотрим возможную этиологию
миокардита.1. Инфекционный. В нашем случае отмечалась явная временная связь
миокардита с повторными респираторными инфекциями, однако основную
массу причин инфекционного миокардита можно бьыо сразу исключить,
поскольку для представленных в табл. 9.4 инфекций характерно полиор-
ганное поражение, причем миокардит среди них является далеко не самым
ярким и тяжелым (исключая дифтерию, сыпной тиф, лихорадку Q и болезнь
Чагаса). То же самое касается грибов гельминтов. Напротив, вирусная
этиология миокардита с самого начала представлялась нам наиболее вероят¬
ной, причем речь шла о таких вирусах, при поражении которыми миокардит
может быть ведущим или даже единственным клиническим проявлением (эти
вирусы перечислены справа). По клинической картине можно лишь заподо¬
зрить ту или иную вирусную инфекцию. Диагностика вирусного миокардита
основана на выявлении специфических антител. Наиболее точным методом
является обнаружение ДНК- или РНК-вируса в ткани миокарда методом
ПНР или гибридизации in situ (для этого необходимо проведение эндомио¬
кардиальной биопсии). Этим методом доказана энтеровирусная, аденови¬
русная, герпетическая и цитомегаловирусная этиология миокардита в 42%
Глава 9, Псевдоклапанный вариант инфекционно-иммунного миокардита,.. 157случаев (но и при дилатационной кардиомиопатии вирусный геном выявлен
у 12%, у 17% получены признаки воспаления; Maisch В., 2004). В нашем слу¬
чае исключена ВИЧ-инфекция, во время настоящей госпитализации не полу¬
чено высоких титров антител к вирусам Коксаки В, выявлены повышенные
титры антител к цитомегаловирусу и к вирусу простого герпеса, антитела к
другим вирусам (например, к ЕСНО-вирусам) не определялись (в основном
по финансовым пррічинам), о чем приходится сожалеть. Необходимо подчер¬
кнуть, что отсутствие повышенных титров антител к вирусам Коксаки через
год от начала болезни нисколько не исключает их этиологической роли и
может говорить лишь о переходе заболевания в инфекционно-аллергическую
стадию. На сегодня выделяется единый патогенетический вариант — инфек¬
ционно-иммунный миокардит.2. Аллергический (5-7% всех миокардитов, развиваются при «больших»
аллергических болезнях), протекает с эозинофилией крови. Если же аллер¬
гический миокардит не связан с «большой» аллергической болезнью, то
понятие это становится довольно размытым и включает идиопатические,
аутоиммунные, по сути, варианты, в том числе злокачественный гигантоюте-
точный миокардит, не связанный с известными гранулематозными болезня¬
ми и клинически протекающий как миокардит Фидлера. Доказательством
иммунной природы гигантоклеточного миокардита служит его воспроизве¬
дение у крыс путем введения миозина; не исключается роль вирусов Коксаки
В2 в запуске иммунных реакций. Особенно характерен для гигантоклеточ¬
ного миокардита недостаточный эффект кортикостероидов, в связи с чем
именно при этой форме чаще, чем при других, назначаются цитостатики, и
даже в пересаженном сердце возможен рецидив миокардита. В нашем случае
миокардит близок по течению к варианту Фидлера, однако четкая связь с
острыми респираторными инфекциями все же не позволяет считать его иди-
опатическим.3. Аутоиммунный вариант, по сути, является разновидностью аллергическо¬
го и может быть диагностирован при болезнях с доказанной аутоиммунизаци¬
ей; при диффузных болезнях соединительной ткани, системных васкулитах,
инфекционном эндокардите и т.д. Сюда же следует, по-видимому, отнести и
ревматический миокардит.4. Токсический (уремия, тиреотоксикоз, токсикоз беременных, >тарный газ,
соли тяжелых металлов, кокаин и другие наркотики).5. Лекарственно-индуцированный — по природе своей обычно является
аллергическим, реже — токсическим, может развиваться при лечении множе¬
ством препаратов, обычно в рамках «большой» лекарственной болезни. Наш
пациент лишь кратковременно принимал антибнотикі-і и тера-флю, после
отмены которых состояние его продолжало ухудшаться.6. Радиационный (развивается при лучевой терапии опухолей легких и сре¬
достения).7. Ожоговый — тоже токсический по своей сути.8. Трансплантационный — по механизму является аутоиммунным.9. Неизвестной этиологии.
158КардиологияЭтиология инфекционных миокардитовТаблица 9.4БактериальныйРиккетсиозныйбруцеллылихорадка скалистых горклостридиилихорадка Qкоринебактерии дифтериицуцугамушивозбудители туляремии {Fr. Tularensis)сыпной тифгонококкиСпирохетозныйгемофилъная палочкаборрелиоз (болезнь Лайма)легионеллылептоспирозменингококкисифилисмикобактериимикоплазмыПротозойныйстрептококки, в том числе пневмококкиэнтамебиазстафилококкилейшманиозTropherima whippetiiтрипаносомоз (болезнь Чагаса)токсоплазмозГрибковыйГельминтозныйактиномицетыиистицеркозаспергиллыэхинококкозбластомицетышистозомотозкандидытрихинел-іезкокцидиоидыкриптококкигистоплазмыспоротриксВирусныйарбовирусыаденовирусыаренавирусвирусы Коксаки Ввирус энцефаломиокардитаЕСНО-вирусывирус гепатита Вдругие энтеровирусывирус гепатита Сцитомегаловирусвирус эпидемического паротитавирус Эпштейна—Баррвирус полиомиелитавирус простого герпесавирус бешенстваВИЧреспираторно-синцитиальный вирусвирус гриппавирус краснухипарвовирус В19вирус коривирус герпеса 6-го типавирусы оспыТаким образом, в нашем случае могли быть заподозрены лишь вирусный,
инфекыионно-иммунный варианты миокардита, в меньшей степени — идио-
патический (в том числе гигантоклеточный) и ревматический варианты.Однако вполне очевидная картина осложнилась описанием в протоколе
ЭхоКГ признаков вальвулита, о чем уже шла речь. При этом не было выявлено
никаких аускультативных признаков, характерных для митрального стеноза
и аортальной недостаточности; складывалось однозначное впечатление, что
первичного поражения створок с развитием порока сердца у больного нет.
Происхождение же шума митральной регургитации находило объяснение
Глава 9. Псевдоклапанный вариант инфекционно-иммунного миокардита... 159в выраженной дилатации левого желудочка с растяжением кольца митрально¬
го клапана. Представлялось, что в установлении точного диагноза решающее
значение будут иметь результаты проспективного наблюдения за больным.
Сегодня мы имели возможность оценить его состояние по прошествии 5-ти
месяцев. Каковы главные итоги этих 5-ти месяцев для больного?1. Очевидно, что заболевание прогрессирует, и связано это не только с
отменой больным кардиотропной терапии, Ни кордарон, ни ингибиторы АПФ
с р-блокаторами и аспирином не смогли бы оказать решающею влияния на
течение заболеваїшя. Размеры левого желудочка продолжают увеличиваться,
ФВ левого желудочка не нарастает, в клинику больной поступает в состоянии
интерстициального отека легких, причем тяжесть его состояния по-прежнему
определяется поражением миокарда, а не клапанов (по-прежнему выслушива¬
ется ритм галопа).2. Кортикостероиды, с одной стороны, оказывали от^ютливый клинический
эффект, который сохранялся до конца приема преднизолона, но с другой сто¬
роны, его отмена после 4-месячного курса лечения практически сразу привела
к ухудшению состояния, т.е. патологический процесс так и не бььт подавлен.3. Б'швиый итог в диагностическом плане — появление слабого диастоличе¬
ского шума на верхушке (без типичной хмелодии митрального стеноза), а также
диастолического шума аортальной регургитации в точке Боткина. Этому соот¬
ветствуют нарастание градиента на митральном юіапане с 11 до 17 мм рт.ст.,
прогрессирующая дилатация левого предсердия (по данным ЭКГ и ЭхоКГ).На сегодняшний день мы должны констатировать формирование у боль¬
ного двух пороков сердца, которые прогрессируют: митрального стеноза в
сочетании с регургитаиией и аортального порока с преобладанием недоста¬
точности. В этой ситуации единственно возможлым диагнозом представля¬
ется ревматизм. Здесь уместно вспомнить, что после первого обсуждения не
иск.1ючалась возможность параллельно протекающих ревмокардита и вирус¬
ного миокардита. При такой картине стал бы понятен двоякий эффект кор¬
тикостероидов — подавление ревмокардита привело к улучшению, в то время
как вирусный миокардит прогрессировал. Однако такая картина представля¬
ется все же достаточно умозрительной и недоказуемой. И если стремиться к
постановке одного диагноза, то это должен бьпь ревматизм. Однако сомнения
все же остаются.Наиболее серьезные вопросы, которые возникают у нас на данном этапе и
не получают объяснения в концепции «ревматизм», таковы:1) явное несоответствие выраженности миокардита, который прогрессиру¬
ет, продолжает определять тяжесть состояния больного, и степени поражения
клапанов — аортальный порок выражен умеренно, митральный стеноз остается
весьма умеренным (о чем косвенно говорит отсутствие мерцательной аритмии,
хотя левое предсердие и увеличено). Отсутствует типичный протодиастоличе-
ский шум, нет признаков сращения створок по данным ЭхоКГ;2) дебют заболевания четко был связан с повторными острыми респиратор¬
ными заболеваниями, что в диагностике неревматического миокардита являет¬
ся очень важным признаком;
160 Кардиология3) бьша и остается спокойной кровь. В нашей лаборатории ни в первую, ни
в настоящую госпитализацию не было выявлено повышения титра антисфеп-
тококховых антител (к гиалуронидазе), лишь уровень СРБ колеблется от + до
+++, но остаются нормальными уровень лейкоцитов, лейкоцитарная форму¬
ла, СОЭ, белковый спектр крови. При такой выраженности ревмокардита это
трудно объяснить, даже с учетом лекомпенсации. Титр выявленных в другой
лаборатории антител к гиалуронидазе был повышен в 4 раза (можно было ожи¬
дать гораздо большего повышения), и относились они к классу IgG, хотя сле¬
довало бы ожидать высоких титров антител класса IgM. Необходимо подчер¬
кнуть, что специфического лабораторного маркера ревматизма по-прежнему
не существует, антитела к стрептококку могут повышаться и при тонзиллите
(у больного высеян с миндалин Stn viridans)',4) ни в анамнезе, ни в настоящее время не было других проявлений ревма¬
тической лихорадки (хотя бы артралгий), в том числе при достаточно тяжелых
ангинах, что при столь активном ревмокардите тоже представляется несколько
необычным. Отсутствует сколько-нибудь значимая лихорадка;5) наконец, возраст больного тоже представляется не вполне типичным для
развития первичного ревмокардита, которым, как известно, заболевают обыч¬
но на 10—20 лет раньше. Еще в меньшей степени характерно развитие первич¬
ного диффузного миокардита после 30 лет.Для сравнения приведем представленное израильскими авторами описа¬
ние случаев острой ревматической лихорадки у 23 взрослых (средний возраст
55 лет), которые составили всего 5% от общего числа заболевших: кардит
встречался всего в 35% случаев, тогда как артрит — в 83%; все больные имели
не менее 3-х малых критериев диагноза по Джонсу; 39% больных уже имели в
анамнезе ревматическую атаку (в среднем за 20 лет до настоящего эпизода);
даже при наличии сердечной недостаточности СОЭ во всех случаях была не
менее 50 мм/ч, у 70% имелась анемия и гииерглобулинсмия, у 66% — гипер-
калиемия; ответ на терапию был хорошим, и только у 1 больного из 13, пере¬
носивших атаку впервые, развился порок сердца. Авторы обзора отмечают, что
смерть от острой ревматической лихорадки развивается редко и лишь у боль¬
ных с предшествовавшим поражением сердца,Ссылки на неизвестный нам, принципиально «новый» по своим свойствам
ревматогенный стрептококк, на кавказское происхождение нашего больного
не снимают этих вопросов. Таким образом, единственным основанием, на
котором сегодня базируется диагноз ревматизма, является формирование
сочетанного порока сердца, и в первую очередь митрального стеноза. Поэтому
далее мы остановимся на вопросе о том, насколько специфичным маркером
ревматизма является митральный стеноз (в том числе в сочетании с аортальной
недостаточіюстью).Из всех приобретенных пороков сердца именно митральный стеноз счита¬
ется результатом почти исключительно ревматической лихорадки, причем это
мнение является очень устойчивым на протяжении десятилетий.в руководстве А.Л. Мясникова «Основы диагностики и частной пато¬
логии (пропедевтика) внутренних болезней», 1951 г отмечено: «Этот порок
Глава 9. Псевдоклапанный вариант инфекционно-иммунного миокардита... 161(митрішьньїй стеноз) всегда вызывается ревматическим эндокардитом.
Врожденный митральный стеноз у женшин представляет редкость, и его суще¬
ствование даже вызывает сомненртс».У Е.М. Тареева в руководстве по внугренним болезням (тот же 195і г.) чита¬
ем: «Согласно современным взглядам, мшральный стеноз — это следствие
только ревматического вальвулита, следовательно, всегда без исключения рев¬
матической природы, даже при отсутствии всяких иных указаний на ревматизм
в анамнезе».В моноірафии А.И. Нестерова и Я.А. Сигидина «Клиника коллагеновьтх
болезней» (1966 г.) указано следующее: «Картина такого порока сердца (affectio
mitralis) почти с абсолютной точностью свидетельствует о ревматическом про¬
исхождении порока и всей болезни в целом».Наконец, совсем недавно Н.М. Шевченко обозначил митральный стеноз
как «клеймо ревматизма».Вместе с тем в различных руководствах начиная уже с 1960-х гг. (возможно
и ранее — мы не ставили перед собой задачи исчерпывающе изучить историю
вопроса) регулярно упоминаются другие, казуистически редкие причины разви¬
тия митрального стеноза, в том числе и не связанные с воспалением эндокарда.
К ним относят следующие :}аболевания.1. Опухоли сердца, главным образом миксома левого предсердия (при¬
мерно в 40% случаев миксома имеет другую локализацию в сердце). В нашем
случае этот диагноз легко исключается данными повторньгх ЭхоКГ и всей
картиной заболевания. Из других опухолей, которые могут имитировать порок
сердца, следует упомянуть кардиальную папиллярную фиброэластому, излю¬
бленной локализацией которой являются створки митрального и аортального
клапанов. К 2002 г. было описано 725 случаев, поражаются в основном лица
старше 70 лет.2. Инфекционный эндокардит, при котором за счет массивных вегета¬
ций исключительно редко могут определяться признаки нерезкого сужения
митрального отверстия без выраженного нарушения внутрисердечной гемо¬
динамики. У нашего молодого реактивного больного отсутствуют такие кар¬
динальные признаки инфекционного эндокардита, как лихорадка, ознобы,
увеличение СОЭ, анемия, спленомегалия, собственно массивные вегетации;
мы не получили ухудшсіїия состояния на фоне терапии преднизолоіюм, что
моию бы произойти в с.лучае инфекционного эндокардита.3. Антифосфолипидный синдром (АФС). Механизм поражения клапанов
сердца не вполне понятен, описанный у таких больных митральный стеноз
был весьма умеренным. Основную роль играет, видимо, иммунный вальвулит
в сочетании с наложением тромботических масс на клапанах. Более редкой
причиной является тромбоз левого предсердия, который полностью имитирует
картину митрального стеноза и выявляется при ЭхоКГ (при вьывлении внутри-
сердечного тромбоза неясной этиологии определение антител к кардиолипину
является обязательным). Диагноз порока сердца в рамках антифосфолипид-
ного синдрома ставится путем исключения других причин порока; назначе¬
ние преднизолона существенного влияния на течение порока не оказывает.
162 КардиологияО диагнозе антифосфолипидного синдрома должно заставить задуматься соче¬
тание инфаркта миокарда и трудно объяснимого митрального или аортального
порока сердца.В описанных случаях диагноз антифосфолипидного синдрома ставился
обычно после манифестного тромбоза, поражение сердіїа чаще проявлялось
перикардиальным выпотом. В отдельных работах частота поражения клапанов
при первичном антифосфолипидном синдроме превышала 30% и коррели¬
ровала с частотой артериальных тромбозов; частота собственно митрального
стеноза была в 10 раз меньше. Наиболее часто описывают утолщение створок
.митрального клапана с развитием регургитаиии. При развитии митрального
стеноза и мерцательной аритмии риск тромбоэмболий многократно повы¬
шается. Для лечения используются непрямые антикоагулянты, кортикосте¬
роиды, плазмаферез. У нашего больноїх) можно было предполагать развитие
антифосфолипидного синдрома в рамках вирусной инфекции, хотя типичные
проявления синдрома (артериальные, в том числе коронарные, и венозные
тромбозы, тромбоцитопения, аутоиммунная гемолитическая анемия, положи¬
тельная реакция Вассермана) у него отсутствуют. Мы провели анализ и антител
к кардиолипину, их титры повышены не были.4. Системная красная волчанка (СКВ). Эндокардит Либмана—Сакса при
волчанке хорошо известен, но крайне редко приводит к формированию
митрального стеноза (наряду с недостаточностью); по данным отдельных
авторов, развитие АФС в рамках волчанки не повышало частоты поражения
клапанов, хотя это представлялось бы вполне вероятным. Описаны случаи
успешного протезирования митрального клапана у таких больных, прюїем при
гистологическом исследовании клапана выявлялись как признаки эндокарди¬
та Либмана—Сакса, так и отложения антител к кардиолипину, что позволило
расценить митральный стеноз как неревматичсский. Однако диагностические
признаки системной красной волчанки у нашего больного отсутствуют.5. Ревматоидный артрит. Отложение ревматоидішіх узелков в клапанах
сердца в абсо.1ЮТном большинстве случаев ведет к развитию их недостаточ¬
ности, а не стеноза отверсіий; кроме того, заболевание не может проявляться
исключительно поражением клапанов и миокарда (ревматоидный миокардит
не бывает и столь выраженным) — у больного нет каких-либо признаков пора¬
жения суставов, отсутствует гораздо более характерный перикардит, диагноз
исключается.6. Системная склеродермия. Клинические проявления кардиоск-іероза
в рамках склеродермии не являются единственным и ранним проявлением
болезни. По данным Н.Г. Гусевой, поражение сердца развивается на II-ITT ста¬
диях болезни, причем из 65 больных с диагнозом «склеродермическое сердце»
лишь у 1 сформировался митральный стеноз.Кроме того, уверенно могли бьггь исключены следующие из возможных
редких причин митрального стеноза.7. Болезнь Уиппля (в качестве морфологической основы митрального
стеноза описывают всгетацрш на контактирующих друг с другом поверхно¬
стях митральных створок, причем заболевание принципиально отличается
Глава 9. Псевдоклапанный вариант инфекционно-иммунного миокардита... І63от инфекционного эндокардита, поскольку носит хронический, персистирую-
щий характер и не ведет к быстрому разрушению клапана).8. Амилоидоз. Клапанный вариант амилоидоза сердца является одним из
самых редких и проявляется, как правило, митральной недостаточностью.9. Мукополисахаридоз фенотипа Хантера-Херлера, болезнь Фабри (лизо-
сомальные болезни накопления, при которых развивается рестриктивное
поражение миокарда, поражение митрального клапана релдо и обьмно про-
яатяется его недостаточностью).10. Эозинофильный фиброэластоз (фибропластический эндокардит
Леффлера). Случаи митрального стеноза редки, но описаны (в сочетании с
трикуспидальным). В отсутствие эозинофилии диагноз исключается.11. Карциноидный синдром.12. Дегенеративный кальциноз. Крайне редко выраженное уплотнение
створок и подклапанных структур может приводить к сужению митрального
отверстия, причем этиология этого состояния весьма разнообразна.13. Врожденный митральный стеноз. Кроме того, что его наличие вообще
вызывает сомнения и встречается он в основном у девочек, в нашем случае
такой диагноз исключается, поскольку порок развивается «на глазах». Еше
более редким вариантом является трехпредсердное сердце, при котором мем¬
брана в полости левого предсердия может имитировать митральный стеноз.14. Синдром Лютембаше (сочетание митрального стеноза с дефектом меж-
предсердной перегородки) — считается, что в этом случае лишь дефект являет¬
ся врожденным (у нашего больного его нет), а митральный стеноз может иметь
ревматическую природу. Описаны также сочетания (и это типично) врожден¬
ного митрального стеноза с фиброэластозом эндокарда, коарктацией аорты,
незаращением боталлова протока, дефектом межжелудо^іковой перегородки.Для всех представленных в пунктах 1-14 заболеваний характерно одно
очень существенное отличие от нащего случая — они протекают без столь
выраженного, определяющего клиническую картину и прогностически крайне
неблагоприятного миокардита. Наконец, большинство этих заболеваний дает
картину изолированного митрального стеноза без поражения аортального кла¬
пана (сочетанное поражение возможно при инфекционном эндокардите, деге¬
неративном кальцинозе, при системных заболеваниях, антифосфолипидном
синдроме, врожденных пороках, амилоидозе, болезнях накопления).15. Прием метисергида (вазоди^тататор, использующийся при головных
болях), что описано в 1974 г Возможно, что при этом развивается кардиотроп-
ная имму'нная реакция. Наш больной препарат не принимал. В литературе
нам встретился также случай развития митрального порока сердда у больного,
получавшего противопаркинсонический препарат перголид.16. Относительный митрхтьный стеноз при аортальной недостаточно¬
сти — хорошо известен феномен появления диастолического шума на вер¬
хушке (шум Флинта), который обусловлен тем, что мощная струя аортальной
регургитации приподнимает створки митрального к,ттапана в диастолу и
создает относительное препятствие току' крови через митральное отверстие.
В нашем случае об этой возможности не следует забывать, однако степень
164 Кардиологияаортального порока пока явно недостаточна для появления шума Флинта;
имеются также уплотнение, неравномерное утолшение створок митрального
клапана, и градиент растет.Кроме того, потребуется объяснить природу аортального порока,
Нерсвматическая этиология аортальных пороков сердца (в том числе с преоб¬
ладанием аортальной недостаточности) хорошо известна.Причины клапанной и относительной аортальной недостаточности1. Инфекционный эндокардит.2. Сифилитический мезаортит.3. Дегенеративный кальциноз.4. Миксоматозная дегенерация.5. Синдром Марфаііа.6. Длительно существующая артериальная гипертония с развитием аневриз¬
мы аорты.7. Болезнь Такаясу8. Анкилозирующий спонди^тоартрит (болезнь Бехтерева).9. Ревматоидіїьій артрит.10. Системная красная волчанка. Описаны случаи вьывления довольно
массивных тромботических вегетаций, приведших к формированию стеноза
устья аорты.11. Антифосфолипидный синдром. Поражение аортального клапана
проявляется уплотнением его створок, наложением тромботических вегета¬
ций, которое может приводить к клинической значимой регургитации или
стенозу, причем описаны случаи постепенного перехода недостаточности
в стеноз.12. Синдром Бехчета, триггером для которого слу'жит стрептококковая
инфекция {Strept, agalactiae).13. Системная склеродерміія (из имевших поражение сердца 65 пациентов,
по данным Н.Г Гусевой, аортальная регургитапия развилась у одного), причем
эхокардиографические данные позво^тяют до некоторой степени определить
специфику поражения сердца,14. Болезнь Уиппля.15. Болезнь Крона.16. Травма сердца.17. Пролабировнние створки аортального клапана в сторону дефекта меж-
жслудочковой перегородки.18. Врожденный норок (двустворчатый аортальный клапан).19. Несовершенный остеогенез (растяжение корня аорты).20. Лечение фенфлюрамином (в виде монотерапии или в комбинации
с фентермином) — за счет повышения тканевого уровня серотонина, роль
которого обсуждают и в патогенезе безэозинофильного фиброэластоза. Мы
встретили описание трех случаев вальвулопатии на фоне такого лечения с мор¬
фологическими изменениями митрального и аортального клапанов по типу
миксоидной дегенерации с развитием регургитации, В то же время при специ¬
альном исследовании 5437 пациентов, получавших селективные ингибиторы
Глава 9. Псевдоклапанный вариант инфекционно-иммунного миокардита,.. 165обратного захвата серотонина, частота выявления зт^іеренной MHTpavibHoii
и/или аортальной рег>ргитации оказалась не выше, чем в контрольной грулпе.Для нас важна не только очень малая вероятность подобного происхожде¬
ния аортального порока у больного, но и невозможность при данных заболе¬
ваниях одновременного развития тяжелого миокардита. В нашем слу^іае этио¬
логический фактор должен быть способным одновременно вызывать тяжелый
миокардит и сочетанное поражение митрального и аортального клапанов
(причем с формированием стенозов). Из всех упомянутых сегодня заболеваний
лишь инфекционный эндокардит и диффузные болезни соединительной ткани
в какой-то степени отвечают этому критерию, но их отсутствие у нашего боль¬
ного не вызывает сомнений. Однако если выйти за рамки хорошо изученных на
сегодня заболеваний, то возможными неревматическими причинами сочетан¬
ного воспалительного поражения мио- и эндокарда могли бы быть иммунное
воспаление и кардиотропный вирус.Тезис о первичном иммунном миоэндокардите на сегодняшний день
представляется достаточно абстрактным. Закрепились в классификациях
инфекционно-аллергический миокардит, аллергический перикардит, при кото¬
рых не удается выявить первичный инфекционный агент, однако описаний
первичного аллергического эндокардита или инфекционно-аллергического
эндокардита нам найти не удалось.Что касается вирусного эндокардита (в сочетании с миокардитом), то такой
диагноз до сих пор не принимается во внимание, хотя, начиная с середины
1960-х гг., такие работы появляются неоднократно. Еш;е в 1939 г. (параллельно
с работами Ашоффа) Пирс показал развитие панкардита при заражении кро¬
ликов так называемым вирусом III. В середине 1960-х гг группа американских
ученых под руководством G. Burch получила в эксперименте у мышей развитие
эндокардита с вальвулитом при заражении их Коксаки-вирусами, аденовируса¬
ми и вирусом энцефаломиокардита. Наконец, в 1966 г. в многомесячном экспе¬
рименте на обезьянах, которым вводили культуру вируса Коксаки В4, получено
развитие митрально-аортального вальвулита у 5 из 7 обезьян, причем у двух
развился типичный митральный стеноз; в 1967 г. описан Коксаки-вирусный
панкардит, сходный с ревматическим, у обезьян.Еще в 1967 г. G. Burch, который может считаться пионером в этой области,
методом ИФА обнаружил антиген вируса Коксаки В в клапанах сердца при
рутинной аутопсии. Кстати, несколько ранее тем же автораі^і удалось доказать
Коксаки-вирусную природу перикардитов, считавшихся идиопатическими.
В 1974 г. антиген вирусов Коксаки выделен у больных с «ревматическим поро¬
ком сердца» (С. Ward). В 1979 г. была опу^бликована работа индийских авторов,
выявивших антитела к вирусу Коксаки В у больных с поражением клапанов
сердца, которое расценивалось как ревматическое (типичную ревматическую
атаку перенесли .лишь 12 из них). Авторы берут этот диагноз в кавьпки, посколь¬
ку в грутіпе 29 больных с митральным стенозом (у 12 — и с аортальной недоста¬
точностью) антитела к вирусам Коксаки ВЗ выявлялись достоверно чаще, чем в
контрольной группе. Авторы делают вывод о том, что вирусы Коксаки по мень¬
шей мере участвуют в патогенезе вальвулита у больных с ревматизмом.
J66 КардиологияНаконец, у больных с клинически выраженным миокардитом, аортальной
регургитацией и нефритом антиген вирусов Коксаки В выявлен в участках нарі-
большего повреждения, в том числе в аортальном клапане. При биопсии пред¬
сердий и клапанов у больных с Коксаки-миокардитом выявлены антигены не
только вируса Коксаки, но и вирусов гриппа, полиомиелита, ЕСНО-вирусов.
Неоднократно описаны случаи Коксаки-вирусного миокардита с появлением
систолического и диастолического шумов, которые могли на фоне лечения
исчезать, но могли и сохраняться, В России подобный материал накоплен
в МОНИКИ сотрудниками Н.Р. Пал сева (более 300 случаев инфекционно-
аллергического и идиопатического миокардита к 1984 г.), подробно описавши¬
ми клинические проявления поражения эндокарда у таких больных.Например, еще в 1968 г. сотрудник МОНИКИ МЛ. Гуревич описал псевдо-
клапанный вариант миокардита Фидпера, а в 1987 т. он же с соавторами пред¬
ставил описание псевдоклапанного варианта миокардита у больного 38 лет,
длительное время наблюдавшегося по поводу митрально-аортального порока
сердца (митральный стеноз с недостаточностью, аортальная недостаточность)
с выраженным миокардитом, который расценивался, естественно, как рев¬
матический. Терапия преднизолоііом не проводилась, больной погиб, однако
на вскрытии выявлено лишь очень умеренное утолщение створок клапанов,
эндокарда, укорочение хорд и абсолютно неспецифические микроскопические
признаки миокардита (в основном склероз и единичные лимфоидные инфиль¬
траты), что не позволило подтвердить диагноз ревматизма. Авторы говорято том, что ранее им неоднократно приходилось сталкиваться с поражением
митрального клапана при неревматических миокардитах, и причиной ошибоч¬
ной диагностики ревматического порока в данном случае считают имевшуюся
картину аортального порока.Имеется довольно обширная литература по воспалительному поражению
сердца в рамках ВИЧ-инфекции. Кроме того, что вирус, безусловно, может
вызывать тяжелый миокардртт, неоднократно описаны случаи поражения
аортального клапана — диссекция аорты с развитием аортальной недостаточ¬
ности. У подобных нашему больных определение антител к ВИЧ должно стать
обязательным методом обследования. При хламидийной инфекции (Ch. pneu¬
moniae), роль которой в патогенезе атеросклероза широко обсуждается, опи¬
сано lgA-опосредованное воспалительное поражение аорты с развитием ее
ригидности, что также может вести к аортальной недостаточности. Описано
развитие эндокардита с поражением митрального клапана при хронической
лихорадке Q, которое не укладывается в рамки инфекционного эндокардита,
но протекает более доброкачественно. Это единичные случаи, но важно, что
они есть. Одним из самых ярких примеров вирусного поражения эндокарда
служит развитие врожденных пороков сердца (в том числе стеноза легочной
артерии, тетрады Фалло) в результате внутриутробного заражения вирусом
краснухи, хотя этол^у факту не придается значения в клинике внутренних
болезней у взрослых. Роль вирусов Коксаки, парвовируса В19 в формировании
врожденных пороков сердца также доказана. Таким образом, кардиотропные
вирусы рассматриваются как этиологический фактор в развитии хронической
Глава 9. Псевдоклапанный вариант инфекционно-иммунного миокардита... 167«ревматической» болезни сердца с поражением всех трех оболочек (панкар¬
дита). Предложен термин «вирусная болезнь клапанов сердца», который не
следует путать с «классическим» инфекционным эндокардитом (с увеличением
селезенки, анемией и т.д.). Его вирусная этиология, кстати, очень сомнительна:
ведущие специалисты приводят лишь единичные экспериментальные данные,
даже среди редких возбудителей вирусы называются не всегда, т.с. поражение
эндокарда при вирусной инфекции — иное; по-видимому то, о котором мы
сегодня говорим. Каковы же возможные механизмы поражения эндокарда и
клапанов сердца при вирусном миокардите? В морфологических исследова¬
ниях доказано, что в эндокарде развивается тот же процесс воспаления, что и
в миокарде — как за счет непосредственного проникновения вирусов, так и за
счет иммунных механизмов. Выраженная дилатация сердца (в первую очередь
левого желудочка) приводит к растяжению фиброзного кольца митрального
клапана, а также к центробежному движению хорд, в результате чего створки
в диастолу закрываются раньше и создают относительный стеноз. Описано
появление диастолического шума при выраженной митральной регургитации
за счет несоответствия увеличенного объема крови и площади митрального
кольца. Страдает в результате воспаления и клапанный аппарат (папиллярные
нити). Степень этих изменений коррелирует с тяжестью миокардита и может
уменьшаться при эффективном лечении (у нашего больного интенсивность
шумов ослабевает). И все же клинически значимая клапанная дисфункция
(особенно стеноз) развивается очень редко, поэтому большое значение при¬
дают факторам, предрасполагающим к вальвулиту — и в ряду с мргкротравма-
тизапией (в том числе волной регургитации) и ишемией, а также, вероятно,
генетической предрасположенностью, называют стрептококковую инфекцию,
что для нашего слу^тая представляется очень существенным.Хоропю известно, что при хроническом тонзиллите постоянная антигенная
стимуляция приводит к выработке антистрептококковых антител, которые
перекрестно реагируют с тканями сердца, но могут не приводить к развитию
ревматизма, вызывая лишь минимальное поражение сердца (например, экс-
трасистолию). Такое состояние (оно достаточно точно обозначалось термином
«тонзилло-кардиальный синдром»), безусловно, способствует развитию вирус¬
ного вальвулита. Кроме тоїо, доказан сильный иммуносупрессивный эффект
Р-гемолитического стрептококка группы А. Одним из результатов этого явля¬
ется активация латентной вирусной инфекции в тканях сердца, что доказано (в
частности, в эксперименте с заражением мышей стрептококками и вирусами
Коксаки), Именно такое взаимодействие представ.тяется очень вероятным в
нашем случае.Еще Атпофф, один из классиков морфологического изучения ревматизма,
заметил в 1939 г.: «Можно допустить, что этот термин (ревматизм) использу¬
ется слишком широко, и в дальнейше.м под ним могут подразумевать симптом
или группу симптомов, которые возникают при множес'гве условий».Таким
образом, мы находим возможным по-прежнему считать наиболее вероятным
диагноз инфекционно-иммунного (исходно вирусного) миокардита, течение
которого осложнилось не только выраженной дилатацртей полостей с тяжелой
168 Кардиологиясердечной недостаточностью, но и эндокардитом с вальвулитом, до некоторой
степени имитирующим картину ревматической болезни сердца.Больной был проконсультирован акалемиком Н.Р. Палеевьш, многократно
наблюдавшим подобную к.іиническую картину: заболевание было расценено
как несомненный инфекционно-аллергический миокардит тяжелого теченші;
по его рекомендации доза преднизолона была увеличена до 40 мг/сут.Каковывозможные терапевтические подходы у нашего больного? Поскольку
вирусное поражение клапанов по мере успешного лечения может уменьшать¬
ся, проспективное наблюдение ш больным по-прежнему важно для уточне¬
ния диагноза. При сохранении активности процесса нам придется обсуждать
вопрос о добавлении к лечению иммуномодулируюіцих препаратов, что воз¬
можно лишь после развернутого анализа иммунного статуса, а также о назна¬
чении цитосгатиков в комплексе с кардиопротективными метаболическими
препаратами. Попытка проведения противовирусной терапии также может
оказаться оправданной, поскольку наличие активного вирусного процесса мы
исключить не можем. Если согласиться с ревматической концепцией заболева¬
ния, то следует, по-видимому, проводить регулярные инъекции SKCTeHUHvXIHHa.
Трансплантация сердца остается лишь теоретически возможной (не исключен
и рецидив в пересаженном сердце). Обсуждались и иные возможности хирур¬
гического лечения (в частности, операция по созданию мышечного каркаса),
однако на данный момент возможности проведения такой операции нет.Что касается иммуномодулируюшей терапии, механизмы и маркеры злока¬
чественного течения инфекционно-иммунного миокардита в последнее время
хорошо изучены, но возможности целенаправленного воздействия на эти
механизмы пока очень ограничены. Из достаточно широко апробированных
препаратов можно назвать лишь инфликсимаб (римикеіід).Маркеры злокачественного течения инфекционно-иммунного миокардита (по
Ф.Н. Палееву, 2004 п)1. Повышенная экспрессия CD25 лимфоцитами.2. Высокий уровень фактора некроза опухолей типа а.3. Повыпгение уровня интерферопа-а.4. Повышение уровней интерлейкинов 1а, ip, 4, 6 и 12.5. Повышение уровня аутоантител к двуспирааьной ДНК и кардиомиозинуОтвечая на вопрос о правомерности назначения стероидной терапии вотсутствие биопсии миокарда, следует отметить: стероидная терапия у дан¬
ного больного оправдывается отчетливой связью улучшения состояния с
назначением этой терапии и ухудшения — с отменой преднизолона (дважды
в анамнезе). Мы не проводили биопсию миокарда, главным образом в связи
с труднодоступностью этой процедуры; мы также не имеем на сегодняшний
день возможности детально исследовать иммунный статус больного и выявить
MMMyTiHbie маркеры злокачественного течения заболевания, Но прогресси¬
рующий, по-прежне\ту активный характер заболевания (по сути дела, мы и
сегодгш не можем говорить о подавлени и активного воспаления) в отсутствие
признаков текущего инфекционного процесса делают стероидную терапию
патогенетически обоснованной.
Глава 9. Псевдоклапанный вариант инфекционно-иммунного миокардита,., 169P.S. В течение года больной продолжал прием предпизолона в поддер¬
живающей дозе 7,5 мг/сут, получал оста^іьную подобранную в клинике тера¬
пию, состояние его остава^тось относительно стабильным. При контрольном
осмотре определялся ритм галопа, диастолический шум на верхушке сердца
не выслушивался, слабый диастолический в точке Боткина сохранялся.
Новых аускультативных феноменов не выявлено. При ЭхоКГ отмечено неко¬
торое уменьшение диастолического диаметра левого желудочка (до 9,0 см),
ФВ левого желудочка составляла 30%. Градиент на митральном клапане не
определялся, сохранялись митральная регургигаиия II степени и аорта.-іьная
рсгургитация I степени. Таким образом, диагноз инфскциокно-иммунного
миокардита на данном этапе наблюдения за больным не вызывает сомнений.
Сведения о да,тьнейшей судьбе больного отсутствуют.ЛИТЕРАТУРАГуревич М.Л., Янковская М.О., Вишняк А.М., Банина В.Б. О псев до клана шюм
варианте миокардита // Кардиология. — 1987. — № 27 (12). — С. 101-103.Палеев И.Р., Гуревич М.А., Одинакова В,А., Смирнов В.Б. Поражение эндо¬
карда при миокардите и кардиомиопатии // Советская медицина. — 1984. —
№ 5. - С. 39-44.Палеев Ф.Н. Патогенез ауіоиммунноіо миокардита — механизмы поврежде¬
ния и зашиты: Автореф. ... дис. д-ра мед. наук. — М., 2004.Burch G.E., Colcolough H.L. Prograssive Coxackie viral pancarditis and nephritis //
Ann. Int. Ned. 1969, 71; 963-970.Burch G.E., DePasquaie N.P., Sun 5.С et al. Endocarditis in mice infectc with
Coxackie virus B4//Science. 1966, 151:447.Burch G.E., Sun S.C., Colcolough H.L. et al. Coxackie В viral myocarditis and va]-
vulitis identified in routine autopsic .specimens by immunolluorescent techniques //
Am, Heart J. 1967, 74:13.Burch G.E., Walsh J.J., DeMasi C.J. Pericardiris due to infectious mononucleosis //
Am. Heart J. 1964, 67; 421-422.Chandy K.G., John T.J., Mukundan P.et G. Cherian. Coxackie В antibodies in
“rhcumatic” valvular heart disease // Lancet. 1979, 313(17): 381.DePasquaie N.P., Burch G.E., Sun S.C. et al. Experimental Coxackie viais B4
valvulitis in cynomolgus monkeys // Am. Heart J. 1966, 71: 678.Pears J.M. Cardiac lesions in rabbits produced by a filterable virus (virus III) // Arc.
Path. (Chicago). 1939, 28: 827-845.Sun S.C., Sohal R.S., Burch G.E. Coxackie virus B4 pancarditis in cynomolgus
monkeys tesembling rheumatic heart lesions // Brit. J. Exp. Path., 1967, 48; 655.Ward C., Ward A.M. Acquired vaKular heart disease in patients who keep pet
birds j I Lancet. 1974, 2: 734.Ward C., Ward A.M. Viral antigen demonstrated in valvular heart disease // Lancet,
1974, 1:755.
Глава 10МИОКАРДИТ С ВЫРАЖЕННЫМИ ИММУННЫМИ
ПРОЯВЛЕНИЯМИ и НЕФРОПАТИЕЙ — ТРУДНОСТИ
НОЗОЛОГИЧЕСКОЙ ДИАГНОСТИКИOS. Благова, Л,В. Недоступ, ЕМ. ШиловХорошо известно, что, наряду с другими органными проявлюіиями, в рам¬
ках системной красной волчанки (СКВ) может развиваться клинически зна¬
чимый миокардит. В то же время миокардит как самостоятельное заболевание
чаще всего носит инфекционно-иммунный характер, что делает возможным
развитие сходных по механизмам внекардиальных проявлений болезни (хотя
описания подобного рода в литературе встречаю!ся нечасто). Представляем
описание клинического случая, в котором дифференциальный диагаоз пред¬
ставляет значительные сложности при несомненном иммунном патогенезе
заболевания, Выявление у больного антифосфолипидных антител и интрапе-
рикарлиаіьньїх кист дополнительно затрудняло иозологическую диагностику.Больной Д., 30 лет, впервые поступил в отделение кардиологии Факультетской
терапевтической клиники им. В.Н. Виноградова 05,09.2006 г с жшобами на
одышку, возникающую при бысгрой ходьбе, подъеме на 3—4 этажа; тяжесть в
области сердца, усиливающуюся при вдохе; небольшие очски голеней и стоп,
учащенное ритмичное сердцебиение (как в покое, так и при нагрузках); прак¬
тически постоянную ноющую боль в левой эпигастральной области; снижение
массы тела на 10 кг (с июня этого года).Из анамнеза жизни известно, что отец пациента умер в 65 лет (причина
смерти неизвестна), мать 56 лет, хроническими заболеваниями не сірадает;
имеет четырех братьев (32, 27, 24, 18 лет) и двух сестер (34 и 26 лет), которые
здоровы. Родился и живет в Чечне, в настоящее время не работает, до болезни
работал в торговле. В армии не служил, участие в военных действиях также
отрицает. Не курит, алкоголь практически не употребляет Детские инфекции
отрицает, периодически (не каждый год) переносил острые респираторные
заболевания. Аллергологичсский анамнез не отягошен.Анамнез заболевания {рис. 10.1): до мая 2006 г, чувствовал себя удовлетвори¬
тельно, физические нагрузки переносил хорошо. В конце мая перенес острое
респираторное заболевание (с лихорадкой до 38 °С, легкими катаральными
явлениями), проводилась сит^штоматичсская терапия. Через 2 нед (в начале
июня) вновь перенес острое респираторное заболевание, сразу после которого
стал отмечать прогрессирующую общую слабость, повышенную yroMjifleMOCTb,
нарастающую одышку при умеренных физических нагрузках, учащенное
сердцебиение, тяжесть в области сердца, появление боли в области сердца
при вдохе. За медицинской помощью не обращался. С июля появились отеки
Глава 10. Миокардит с выраженными иммунными проявлениями,..тна ногах, которые быстро генерализовались (отмечалась отечность лица, под¬
кожной клетчатки), значительно прибавил в весе (точной цифры не знает),
несмотря на снижение аппетита. Температура тела оставалась нормальной.
В связи с нарастанием одышки (в покое) и отеков в конце htojir был госпита¬
лизирован в Центральную районную больницу г. Грозный.При осмотре были выявлены акроиианоз, анасарка, двусторонний выпот
в плевральных полостях, расширение границ сердца влево, тахикардия до
96-100 уд/мин, систолический шум на верхушке, при ЭхоКГ — умеренное
расширение всех полостей сердца (левый желудочек 6,0 см, левое предсердие
4,1 см, правый желудочек 3,8 см), снижение сократительной функции мио¬
карда (ФВ левого желудочка не указана). По данным УЗИ органов брюшной
полости, имелись свободная жидкость в брюшной полости и умеренная гепа-
тоспленомегалия (размеры селезенки 154x70 мм). В единственном приведен¬
ном в выписке обшем анализе мочи имелась протеинурия 3,3%о (других дан¬
ных нет). СОЭ 25 мм/ч, НЬ 121 г/л. Состояние было расценено как миокардит
подострого течения, тяжелой степени, с развитием вторичной дилатационной
кардиомиопатии (ДКМП) и застойной сердечной недостаточности.лихорадкакатаральные
явленияобщая слабостьсердцебиениетяжесть, боли
в области сердцаодышкаотекигидротораксгепатоспленомегалияЭхо-КГпротеинуриялечениесимптоматическоеРис. 10.1. Анамнез больного Д., 30 лет05.2006 06.2006 07.2006 08.2006 5.9.2006
1\^>пункциядилатация всех камер
однократно 3,3%опреднизолон 25 мг/сут
172 КардиологияБыла сделана пункция плевральной полости справа (данных контрольной
рентгенографии нет), эвак>'ировано 200 мл жидкости соломенного цвета;
микобактерий туберк>'леза не обнаружено (других данных о составе плев¬
рального выпота нет). С 1 августа был назначен преднизолон 25 мг/сут, про¬
водилась также терапия диклофенаком 100 мг/сут, верошпироном 100 мг/сут,
фуросемидом 40 мг/сут 2 раза в неделю, диротоном 2,5 мг/сут, тромбо-
АССом 100 мг/сут, гасталом, квамателом. В результате проводимой тера¬
пии состояние несколько улучшилось: одышка уменьшилась, сохранялись
пастозность ног, тяжесть в области сердца, сердцебиение. После выписки
(14 августа) продолжал принимать преднизолон 25 мг/сут и подобранную
кардиотропную терапию. За время лечения, несмотря на стероидную тера¬
пию, потерял в весе 10 кг (вес снизился несколько ниже привычного до
болезни). Лихорадка не возобновлялась. Поступил в Факультетскую тера¬
певтическую клинику им. В.Н. Виноградова для контрольного обследова¬
ния и коррекции терапии.При поступлении состояние относительно удовлетворительное. Вес 93 кг,
рост 188 см. Температура тела 36,8 “С. Кожные покровы чистые, умеренно
бледные, нормальной влажности. Голени и стопы пастозны. Доступные паль¬
пации лимфоузлы не увеличены. Число дыханий 18 в минуту, дыхание жесткое,
плохо проводится в базальные отделы правого легкого, хрипов нет. Левая гра¬
ница сердца определяется по левой среднеключичной линии. ЧСС 96 уд/мин,
ритм сердца правильный. Выслушивается трехчленный ритм без выраженного
ослабления тонов, шумов нет. АД 120/70 мм рт.ст. Живот мягкий, ч>ъстви-
тельный при пальпации в левом подреберье. Печень выступает на 2 см из-под
края реберной дуги, мягко-эластической консистенции, край безболезненный.
Селезенка несколько увеличена (12x6 см), пальпируется нижний полюс у края
реберной дуги. Дизурии нет. Симгггом поколачивания отрицательный с обеих
сторон. Щитовидная железа пальпаторно не увеличена.В общем анализе крови обратило на себя внимание лишь небольшое сни¬
жение уровня гемоглобина и цветового показателя (НЬ 114,0 г/л, эритроциты
4,3х10'7л, цветовой показатель 0,79, лейкоциты 6,4х10Ул, нейтрофилы 55,4%,
лимфоциты 31,4%, моноциты 9,9%, эозинофилы 2,6%, базофильг 0,7%, тром-
бощггы 267,3x107л, СОЭ 12 мм/ч). Данные изменения сохранялись и в повтор¬
ном анатизе, проведенном через 2 нед; в нем отмечено также некоторое нарас¬
тание количества лейкоцитов и СОЭ (при отсутствии клинических признаков
воспаления): НЬ 116,5 г/л, эритроциты 4,4xlO'V^, цветовой показатель 0,79,
лейкоциты 10,6х10Ул, нейтрофилы 61,9%, лимфоциты 27,0%, моноциты 9,0%,
эозинофилы 1,7%, базофилы 0,4%, іромбоцитьг 194,ЗхЮ7л, СОЭ 20 мм/ч.В биохимическом анализе крови при поступлении еше выявлялись небо.іьшая
гипоальбуминемия и гипопротеинемия, а также повьпиение уровня МВ-КФК
до 24 ед/л (у-ГТ 123 ед/л (0-55), ACT 18 ед/л, АЛТ 32 ед/л, общий белок 5,5 г/дл,
альбумин 3,2 г/дл, креатинин 1,1 мг/дл, неорг. фосфор 4,4 мг/дл, глюкоза 76 мг/дл,
азот мочевины 20 мг/дл, мочевая кислота 4,5 мг/дл, обший билирубин 0,8 мг/дл,
Na"^ 136,7 мэкв/л, K' 4,65мэкв/л, МВ-КФК 24 ед/л (2,3-10,5), триглицериды
76 мг/дл, общий холестерин 174 мг/дл).
Глава to. Миокардит с выраженными иммунными проявлениями... 173В динамике эти показатели нормализовались, оставался несколько повы¬
шенным лишь уровень гамма-ГТ: у-ГТ 118 ед/л (0-55), ACT 14 ед/л, АЛТ
50 ед/л, общий белок 6,33 т/лд, альбумин 3,52 г/дл, креатинин 0,88 мг/дл, неорг.
фосфор 4,28 мг/дл, глюкоза 87 мг/дл, азот мочевины 31 мг/дл, общий билиру¬
бин 1,1 мг/дл, Na"^ 142 мэкв/л, 4,8 мэкв/л (3,5-5,0), МВ-КФК 7 ед/л. В связи
с наличием гипохромной анемии легкой степени был определен уровень сыво¬
роточного железа, который оказался нормальным — 102 мкг/дл (40—160).При электрофорезе беакое существенных отклонений от нормы не выявля¬
лось [альбумин 58,1% (54,7—68,7), а,-глобулины 4,0% (3,7—7,8), аз-глобулины
9,0% (5,2-10,7), р-глобулины 11,3% (8,6-13,7), у-глобулины 17,6% (10,7-19,3)].
Оставался нормальным протромбиновый индекс (104%), не было выявлено
маркеров вирусов гепатита В и С (HBsAg и HCVAb). С учетом того, ^гго инфек¬
ция ВИЧ примерно в 10% случаев сопровождается картиной клинически зна¬
чимого миокардита, исключалось наличие данного вируса — антитела к ВИЧ
не выявлены. Серологические реакции на сифилис и РФ в повторных анализах
отрицательны, уровень иммуноглобулинов крови оставался нормальным (TgA
285 мг/дл, IgM 105 мг/дл, IgG 1300 мг/дл). Исходно было выявлено небольшое
повышение СРВ (1 мг/дл при норме до 0,8) и антистрептолизина-0 (131 МЕ/мл
при норме до 125), которое в дальнейшем не определялось.В лаборатории «МедБиоСпектр» проведена серодиагностика миокардита:
выявлено 4-кратное повышение титра IgG к сулїмарному миокардиальному
антигену и гиалуронидазе — 1:400 при норме не более 1:100. Не выявлено диа¬
гностически значимых титров антител к вирусам фуппы Коксаки, выявлено
двукратное повышение титра антител класса IgG к различным антигенам виру¬
са Эпштейна—Барр и цитомегаловирусу.В общем анализе мочи, выполненном при поступлении, протеинурия была
невысокой, отмечалось повышение количества эритроцитов и единичные
гиалиновые цилиндры (уд, вес 1018, pH 5,0, прозрачность неполная, сахара,
ацетона нет, белок 0,335%с, желч. пигм. — отр., уробилин выше нормы, эпи-
тел. клетки полиморфные — немного, лейкоциты 2-4 в п/зр., эритроциты
1-3 в п/зр., в скоплениях до 40, цилиндры гиалиновые 0001 в п/зр., слизи и
бактерий много, оксалатов и уратов немного. В повторном анализе, вьшолнен-
ном через 9 дней, количество белка уменьшилось (до 0,195%о), а микрогемату¬
рия наросла (до 30-40 эритроцитов в п/зр.), цилиндры не определялись.В аиа.тзах по Нечипоренко данные изменения сохранялись, причем коли:че-
ство эритроцитов колебалось от почти нормального до 250 ООО на 1 nlt мочи.
Суточная потеря белка с мочой составила 770 мг. На фоне отмены диурети¬
ков была проведена проба Реберга, которая показала сохранность функции
почек — клубочковая фильтрация составила 107 мл/мин, реабсорбция 98,9%.На ЭКГ {рис. 20.2) при поступлении определялись умеренная синусовая
тахикардия (ЧСС 87/мин), отчетливые признаки гипертрофии левого пред¬
сердия (двугорбый зубец Р длительностью 0,13 с), снижение амплитуды з^-бцов
Т в отведениях V^—Vg. Электрическая ось сердца расположена нормально,
интервал PQ 0,16 с, длительность комплекса QRS 0,92 с, величина интервала
QT 360 мс, величина корригированного интервала QT — 432 мс. На повторных
174КардиологияЭКГ отмечалось появление преходящих неглубоких отрицательных зубцов Т
в отведениях V3—V^.На третий день пребывания в стационаре было проведено холтеровское
мониторирование ЭКГ в течение 5 ч, при котором подтверждено наличие устой¬
чивой синусовой тахикардии (ЧСС 76-132 уд/мин, ср. ЧСС 86 уд/мин на фоне
терапии метопрололом 25 мг утром), никаких нарушений ритма и проводимо¬
сти не выявлено.По данным ЭхоКГ сохранялась умеренная дилатация всех камер сердца,
кроме левого желудочка (КДР левого желудочка 5,3 см, левое предсердие
4,3x5,8x4,4 см, правый желудочек 2,8 см, правое предсердие 5,2x3,8 см),
тМЖП 1,0 см, тЗС 0,9 см, тПЖ 0,3 см; характер движения стенок не изменен,
ближе к верхушке выявлена дополнительная хорда, общая сократительная
функция не нарушена, ФВ левого желудочка 65%. Имелся пролапс передней
створки митрального клапана с регургитацией 1 степени, другие клапаны, стен¬
ки аорты не изменены, просвет корня аорты 3,3 см, функция диастолического
расслабления миокарда левого желудочка не нарушена (Е/А=2,0).При рентгенографии органов грудной клетки подтверждено наличие свобод¬
ной жидкости в правой плевральной полости (ниже уровня 5 ребра), жидкость
пращевидно поднимается вверх. В нижней доле правого легкого выявлено
уплотнение легочной ткани, полностью нельзя исключить инфильтрацию,
в других отделах -- сгущение сосудистого рисунка, преимущественно в цен¬
тральных отделах легких. Корни легких не структурны. Диафрагма слева обыч¬
но расположена, латеральный синус сглажен, междолевые плевры утолщены
(отечны). Сердце увеличено в размерах, аорта не изменена. Таким образом,
рентгенологом, наряду с выраженным застоем в малом круге кровообращения,
не исключалась правосторонняя нижнедолевая плевропневмония, в том числеРис. 10,2. Электрокардиограмма больного Д. Скорость записи 25 мм/с. Пояснения в
тексте
Глава W. Миокардит с выраженными иммунными проявлениями...175и посшнфарктного характера. С учетом отсутствия соответствующей клиниче¬
ской картины была выполнена КТ органов грудной клетки.По данным КТ органов грудной клетки с в/в контрастированием (рис. 10.3), в
базальных отделах легких в субплевральных отделах — явления плеврогенного
фиброза. В правой плевральной полости имеется свободная и частично осум-
кованная жидкость с затеком в междолевую плевру, а также большая воздуш¬
ная полость с горизонтальііьім уровнем (43 мм) жидкости и несколько мелких
полостей. Учасжов легких, подозрительных на инфарктную пневмонию, не
вьывлено. при компьютерной ангиопульмонографии дефектов натюлнения в
легочных сосудах не выявлено. В верхнем отделе средостения визуализируют¬
ся множественные лимфатические узлы с тенденцией к слиянию; еДРП1ИЧНЫе
лимфатические узлы парааортальной и нижней паратрахеальной групп. Сердце
больших размеров, листок перикарда тонкий с наличием тонких петрифика-
тов. На уровне нижнего полюса левого желудочка визуализируется округлое
полостное образование с наличием мягкотканного содержимого, размером
29x21x21мм. Рядом имеются еще 2 маленьких аналогичных образования (по
8 мм). Обращает на себя внимание большой диаметр нижней полой вены
на уровне правого предсердия (49 мм). Заключение: правосторонний гидро¬
пневмоторакс. Плеврогенный фиброз. Медиастинальная лимфоаденопатия.
Паразитарные кисты перикарда (?).Налшіие воздуха в правой плевральной полости было связано, по-видимому,
с проведенной в г. Грозный плевральной пункцией (результаты контрольной
рентгенографии в выписке не описаны). КТ была выполнена с шагом 7 мм,
что не давало возможности однозначно связать выявленные кисты именно с
перикардом.Рентгенологические данные (наличие так называемого симптома «погре¬
мушки» — полостного образования с мягкотканным содержимым) требовали
исключения в первую очередь эхинококкоза. Отсутствие эозинофилии крови
могло объясняться проводившейся терапией преднизолоном. Больной был
направлен на консультацию к специалисту по паразитарным заболеваниям —
профессору В.Д. Завойкину. Были проведены иммунологические анализы кровиРис. 10.3. Компьютерные томограммы органов грудной клетки (сентябрь 2006 г.).
Выделена наиболее крупная киста перикарда. Пояснения в тексте
176 Кардиология(иммунофермеитнътй анааиз) на эхинококкоз и токсакароз, которые оказались
Офицательными. Тем не менее проф. В.Д. Завойкин не исключал парази¬
тарную природу данных кист (поскольку специфические иммунные реакции
могли быть подавлены преднизолоном) и рекомендовал повторное обследова¬
ние после отмены преднизолона.При УЗИ органов брюшной полости подтверждено наличие небольшой гепато-
сгшеномегалии (правая доля печени 155 мм, левая 84 mw, селезенка 141x56 мм).
Паренхима печени и селезенки гомогенна. Внутрипеченочные желчные про¬
токи не расширены, воротная вена расширена до 15 мм, селезеночная вена до
10 мм, нижняя полая вснадо 30 мм. Имеется жидкость в ложе желчного пузыря.
Паренхима почек нормальной толщины (до 20—22 мм), асцита нет. Была выпол¬
нена ЭГДС, при которой выявлены лишь явления атрофии и очаговой гипере¬
мии в антральном отделе желудка. Таким образом, боли в левой эпигастральной
области отражали, скорее всего, растяжение капсулы селезенки.Для оценки состояния внутрибрюшных лимфоузлов, печени и селезенки
бы.та выполнена КТ органов брюшной полости с пероральньтм контрастировани¬
ем (5/5 мм); выявлено более существенное увеличение печени, чем по данным
УЗИ (270x124 мм), и серенное снижение ее плотности; размеры селезенки
(123x61 мм, по вертикали 154 мм) и крупных вен совпадают с данными УЗИ.
Отмечены уплотнение лоханок почек, отечность жировой клетчатки брюшной
полости (отечности желчного пузыря не выявлено). Увеличение лимфоузлов
не выявлено.Таким образом, состояние расценивалось нами как подострый инфекди-
0Ш10-иммут1ный миокардит с развитием дилатации камер сердца и сердечной
недостаточносги. В то же время оставались неясными характер кист в области
верхушки перикарда, а также характер изменений мочевого осадка. Разрешению
этих вопросов и был посвящен дальнейший диагностический поиск.Наличие у больного миокардита не вызывало сомнений. В пользу этого
диагноза свидетельствовали четкая связь дебюта заболевания с перенесенной
острой респираторной инфекцией; дл.ительные боли, чувство тяжести в области
сердца; устойчивая синусовая тахикардия (в том числе в покое); бысгрое раз¬
витие сердечной недостаточности с застоем по обоим кругам кровообращения;
дилатация всех камер сердца и снижение сократимости миокарда по данным
ЭхоКГ в г. Грозном (частично эти изменения сохранялись и во время гоепи-
тализатщи в Факультетск^то терапевтическую клинику им. В.Н. Виноградова);
отчетливая обратная динамика в результате терапии преднизолоном и кардио-
тропными средствами; преходящие нарушения реполяризации на ЭКГ; четы¬
рехкратное повышение титра антител к миокарду; повышение титров антител
к стрептококку, вирусу Эпштейна-Барр, иитомегаловирусу. Данные ктиниче-
ские и лабораторные признаки позволяли говорить не только о миокардите,
но и об инфекционно-иммунном его варианте. Учитывая сроки появления
симптомов (более 2 мес назад), речь шла о подостром инфекционно-иммунном
миокардите среднетяжелого течения.Если опираться на международные критерии диагностики этого заболева¬
ния, то наиболее употребительным остается алгоритм, предложенный NYHA.
Глава 10. Миокардит с выраженными иммунными проявлениями... 177I. Связь с перенесенной инфекиией, дока:занная клиническими и лабора¬
торными данными: выделение возбудителя и его антигенов, выяатение антител
к инфекционным патогенам, лейкоцитоз, увеличение СОЭ, появление СРБ.II. Признаки поражения миокарда.Большие признаки:- патологические изменения на ЭКГ (нарушения реполяризации, ритма
и проводимости);- повышение концентрации кардиоселективных ферментов и белков
(КФК, МВ-КФК, ЛДГ, трононин Т);- увеличение размеров сердца по данным рентгенографии или эхокар-
диофафии;- кардиогеїшьій шок.Малые критерии: тахикардия (или брадикардия), ослабление I тона, ритм
галопа.И хотя многие авторы указывают на преимущественное значение этого
алгоритма в диагностике острого миокардита (об этом іоворит, например,
включение в критерии кардиогенного шока, который предлагалось заменить на
иммунные нарушения), в нашем случае этот алгоритм позволяет ставить диа¬
гноз миокардита достаточно уверенно. У больного имеется главный признак —
связь с перенесенной инфекцией, доказанная выяБлением антител к инфек¬
ционным патогенам, а также нарулиения реполяризации на ЭКГ (лабильный
зубец 7), повышение концентрации МВ-КФК, увеличение размеров сердца
по данным как рентгенографии, так и ЭхоКГ, тахикардия и трехчленный ритм
(можно думать о том, что при более выраженной дилатации левого желудочка и
снижении его сократимости на высоте болезни выслушивался и классический
ритм галопа).Поскольку инфекция (и, в частности, вирусная инфекция) может быть лишь
неспецифическим факгором, который приводит к реа/шзации генетических
дефектов и развитию одного из вариантов первичной кардиомиопатии, необ¬
ходимо было думать и о такой возможности. Однако диагнозу дилатационной
кардиомиопатии противоречила постепенная нормализация размеров полостей
сердца; в пользу гипертрофической кардиомиопатии не было выявлено при¬
знаков гипертрофии желудочков ни при ЭКГ, ни при ЭхоКГ, отсутствовали
также нарушения ритма. Для исключения амилоидоза бььта проведена биопсия
слизистой оболочки десны на амшіоид, которая дала отрицательный результат (о
возможности амилоидоза заставляло думать и поражение почек, хотя микро¬
гематурия совершенно нетипична д)Ш этого заболевания). Нельзя было сразу
исключить и наличие саркоидоза, при котором возможно достаточно раннее
поражение сердца — однако отсутствовали столь характерные для этого состоя¬
ния нарушения ритма и проводимости (при наличии выраженной дилататщи и
сердечной недостаточности). Таким образом, диагноз подосгрого инфекционно-
иммуіпюго миокардита представлялся наиболее обоснованным.Однако при всей очевидности этого диагноза возникал целый ряд вопро¬
сов. Во-первых, требовалось установить причинно-следственные отноше¬
ния между выраженным отечным синдромом в анамнезе (анасарка, выпот в
Ї78Кардиологияплевральных полостях) и проте- СердечнаяОстрыйгломерулонефитЗастойнаянефропатияОтечный синдроминурией {рис. 10.4). Выраженная недостаточность
протеинурия (3,3%о белка в общем
анализе мочи) могла быть как
следствием остро развившейся
застойной нефропатии, так и про¬
явлением самостоятельного пора-
жения почек. Уровень альбумина ,9.4, возможный патогенез отечного син-НН МОМ6НТ рЭ-ЗВИТИЯ ЗіННСЯрКИ НЯМ ДрОМЙ у GOJLbHOTO Д*неизвестен, однако едва ли он былочень низким; в течение августа аппетит у больного оставался значительно
сниженным, белковые препараты еліу не назначались, тем не менее к момен¬
ту поступления в клинику альбумин почти достиг нормы (3,2 г%). Развитие
отеков в рамках нефротического синдрома представлялось маловероятным.Значительное уменьшение протеинурии на фоне терапии преднизолоном
также можно расценить двояко: либо уменьшение степени сердечной недоста¬
точности привело к соответствующему уменьшению выраженности застойной
нефропатии, либо самостоятельное поражение почек подверглось обратной
динамике в результате терапии преднизолоном. Тот факт, что у больного сохра¬
няется и периодически нарастает микрогематурия (в отсутствие терапии анти¬
коагулянтами и антиагрегантами), заставлял искать самостоятельное, вполне
доброкачественное поражение почек, которое имело бы, тем не менее, патоге¬
нетическую связь с миокардитом.Наличие высокого титра антител к стрептококку требовало включения в
круг дифференциальной диагностики ревматического миокардита. Сочетание
постстрептококкового нефрита и миокардита неоднократно описано как у
детей, так и у взрослых, причем миокардит в таких случаях, как правило, пред¬
шествует нефриту; диагноз нефрита у взрослых пациентов с острой ревматиче¬
ской лихорадкой был подтвержден гистологически. Прогноз у таких больных,
как правило, благоприятный. И все-таки перекрестное поражение сердца и
почек возникает обычно при воздействии разных штаммов стрептококков
фуппы А— у больных ревмокардитом чаше обнаруживается стрептококк
типа М5, у больных нефритом — типа ТІ2.В абсолкугном большинстве случаев один тип иммунной реакции на стреп¬
тококк практически исключает другой: сочетание нефрита и ревмокардита
крайне нетипично. У нашего больного маловероятны как ревмокардит сам по
себе (поздний возраст для развития первой атаки и отсутствие подобных атак
в анамнезе), так и вообще постстрептококковая природа заболевания — бо.іь-
ной достаточно четко описывает связь дебюта болезни с повторными острыми
респираторными инфекциями, ангины в анамнезе отсутствуют. Нехарактерны
для постстрептококковой патологии также гепатоспленомегалия и внутригруд-
ная лимфаденопатия, которые сохранялись к моменту поступления в клиникуПоскольку миокардит был патогенетически связан с воздействием вируса,
наиболее логичным представлялось расценить и данные изменения ретику-
ло-эндотелиальной системы, и возможное самостоятельное поражение почек
Глава 10. Миокардит с выраженными иммунными проявлениями... 179в рамках вирусной инфекции. И вирус Эпштейна—Барр, и цитомегаловирус, титр
антител к которым был повышен у больного, хорошо известны как этиологи¬
ческие факторы системной патологии (сердце является лишь одним из органов
мишеней). Каков же спектр внутренней патологии при инфекции этими виру¬
сами?Наряду с общими симптомами, которые больной описывает лишь в дебюте
болезни (общая слабость, лихорадка), в рамках цитомегаловирусной инфекции
возможны лимфаденопатия с гепатоспленомегалией, мифирующие артрал-
гии или артриты, миокардит, который достаточно часто приводит к развитию
дилатапионной кардиомиопатии, и поражение почек по тину нефрита —
латентного, нефротического, в том числе и с развитием острой почечной
недостаточности. Довольно часто развиваются геморрагический (язвенный)
колит и гемофагоцитарный синдром с панцитопенией. Кроме того, характерны
довольно специфичные иммунные реакции, которые, в свою очередь, прояв¬
ляются особым полисистемным поражением. Так, довольно часто описывают
связь цитомегаловирусной инфекции с антифосфолипидным синдромом и
развитием криоглобулинемии II типа, которая нрояв;іяется кожной сыпью, в
том числе затяжного течения, альвеолитом с диффузными легочными гемор¬
рагиями; возможно также развитие моноклональной гаммапатии, вторичного
дефицита иммуноглобулинов с инфекционным эндокардитом аортального
клапана. Комбинации данных поражений могут быть самыми разными, и диа¬
гноз системной цитомегаловирусной инфекции у нашего больного представ¬
лялся вполне реальным.Кроме того, и вирус Эпштейна—Барр, и целый ряд других вирусов могут
приводить к полиорганной патологии, включающей миокардит, нефрит и
активацию ретикулоэндотелиальной системы. В действии каждого вируса есть
определенные особенности, однако лишь по клинической картине диагноз той
или иной вирусной инфекции поставить достаточно сложно.Больной бьш проконсультирован ифекционистом — на момент осмотра
данных за острую инфекционную патологию не выявлено, однако наличие
системной вирусной инфекции представлялось вполне вероятным, рекомен¬
довалось определение генома цитомегаловируса и вируса Эпштейна-Барр
методом ПЦР, а также проведение серологических реакций на бруцеллез,
поскольку эта бактериальная инфекция может протекать с клинически значи¬
мым миокардитом. Методом ПЦР геном вируса Эпштейна—Барр и цитомега¬
ловируса выявлен не бььт, и это существенно снижало вероятность того, что мы
имеем дело с системной вирусной инфекцией. Если нефрит и миокардит могуг
носить постинфекционный (иммунный) характер, то подобное происхождение
умеренной гепатоспленомегалии и лимфаденопатии представлялось нам мало¬
вероятным. Трудно представить, чтобы на фоне терапии прсднизолоном геном
вируса исчез, а картина болезни сохраня;шсь в полном объеме. Известно также,
что сами антитела к цитомегаловирусу могут быть неспецифическим проявле¬
нием аутоиммунного процесса.Реакции Райта и Хед2ціьсона (на бруцеллез) также дали отрицательный
результат, хотя диагноз бруцеллеза и не рассматривался как достаточно
І80 Кардиологиявероятный. Если говорить о других возбудителях, которые могут приводить
к сочетанному поражению миокарда и почек, то следует упомянуть микоплаз¬
му (однако основным проявлением этой инфекции является пневмония, и
протекает она достаточно остро), а также внутриклеточного паразита Babesia
microti, для которого также не характерно длительное течение.Нельзя было исюиочить инфекцию теми вирусами, которые могут приво¬
дить к системной патологии и диагностику которых мы не проводили (аде¬
новирусы, парвовирус В19, многочисленные энтеровирусы), однако этот путь
бьш очень гипотетическим, обследование — дорогим, и, кроме того, даже
обнаружение генома одною из этих вирусов не давало нам окончательной уве¬
ренности в диагнозе. Поэтому поиск был продолжен в ином направлении.В первую очередь следовало вернуться к изменениям, выявленным при
КТ органов грудной к-іетки. Наиболее часто кисты в грудной клетке яшшются
проявлением эхинококкоза, и поскольку паразитологом этот диагноз не бьи
отвергнет, следовало рассмотреть такую возможность. Эхинококк может пора¬
жать практически любую часть человеческого организма, и поражение пери¬
карда еще не самое редкое, Оію выявляется примерно у 0,4—2,0% всех больных
эхинококкозом. Могут поражаться не только перикард, но и другие структуры
сердца (предсердия, желудочки, перегородки, клапаны), что проявляется сер¬
дечной недостаточностью и опасно в первую очередь разрывом кист с тромбо¬
эмболиями легочных и иных сосудов. Описано развитие эхинококкоза сердца у
больного с митральным пороком сердца. Диагноз эхинококкоза сердца ставится
при сочетании эозинофилии, положительных иммунных тестов на эхинококк и
кист по данным ЭхоКГ, КТ или МРТ В описании многочисленных случаев вігу-
фифудного эхинококкоза (наиболее полный обзор включал анатиз 1619 паци¬
ентов) нам не встретилось случаев спонтанной ремиссии. Лечение бьио глав¬
ным образом оперативным, в качестве химиопрепарата до и после операции
использовался альбендазол или мебендазол. В некоторых случаях эхинококкоза
сердца операция в связи с высоким риском не проводилась.Поскольку КТ у нашего больного проводилась с шагом 7 мм, нельзя было
исключить расположение кист в ткани легкого, а не перикарда, и тогда диагноз
эхинококкоза становился еще более вероятным. Другие паразитарные заболе¬
вания (например, стронгилоидоз) приводят к формированию кист сушествен-
но реже; непаразитарные же кисты легких, как правило, носят врожденный
характер (либо кистозные полости образуются в опухоляк, в бронхоэктазах).
Описания непаразитарных кист перикарда нам не встретилось. Во всяком
случае оставанось признать эхинокковое происхождение выявленных кист
наиболее вероятным за отсутствием других объяснений. Связать эти кисты с
основным заболеванием никак не удавалось — следовало признать их второй
болезнью, по-видимому, более «старой», протекавшей и протекаюш[ей бес¬
симптомно. Учитывая проживание нашего больного в чеченской деревне, это
казалось вполне вероятным.Отдельного внимания заслуживали внутрифудная лимфоаденопатия и
петрификаты в перикарде, которые наводили на \шсль о туберкулезе. Однако
этот диагноз в нашем случае мог быть исключен — больной в течение 1,5 мес
Глава 10. Миокардит с выраженными иммунными проявлениями... 181получал терапию преднизолоном, и это не привело к генерализации процесса;
ни разу за время лечения не было отмечено даже субфебрильной лихорадки.
Столь же ма^ювероятным представлялась и возможность первичного заболе¬
вания крови.Таким образом, все альтернативные диагностические концепции были
отвергнуты, и наиболее вероятным по-прежнему представлялся диагноз
инфекционно-иммунного миокардита в сочетании с кистами перикарда
(или легких) неясной этиологии. Планировалась консультация нефролога
для уточнения характера изменений мочевого осадка; обсуждался также
вопрос о проведении биопсии почки или печени в диагностических целях.
Для исключения гемолитического характера анемии (в рамках вирусной
инфекции) была проведена реакция Кумбса, которая оказалась отрица¬
тельной. Кроме того, с самого нача,па больному была взята кровь лля про¬
ведения ряда иммунологических тестов, д.чя которых не было конкретных
оснований. Криоглобулины выявлены не были, комплемент оставался
нормальным.По аналогии с недавно находившимся в отделении 30-летним больным
с дилатацией всех камер, у которого, помимо картины миокардита, имелись
постинфарктные изменения на ЭКГ, при коронарографии изменений выявлено
не было, но оказался повышенным уровень антител к кардиолипину, у нашего
пациента также был определен уровень антител к кардиолипину Очаговых
изменений миокарда у него не бьто, но бьито выявлено диаіност№іески зна¬
чимое повышение антител к кардиолипину класса TgG (50,91 МЕ/мл при норме
до 23), Наличие волчаночного антикоагулянта при нормальном АЧТВ можно
было исключить, уровень антител к (32-гликопротеиду-1 не определялся.Нельзя сказать, чтобы эти данные облегчили постановку диаіноза. Как
правило, выявлеьше антител к кардиолипину (особенно класса TgG) имеет
клиническое значение, хотя они могут и не быть патогенными (не приводить к
развитию собственно антифосфолипид ного синдрома). В нашем случае клас¬
сического антифосфолипидного синдрома у больного не было — он не отвечал
критериям диагностики этого состояния, предложенным в 1992 г: отсутствова¬
ли тромбозы какой-либо локализации, сетчатое ливедо и язвы голени. Анемия
не носила гемолитического характера, оставался нормальным уровень тромбо¬
цитов.Однако в поражении миокарда и почек эти антитела могли играть впол¬
не опре дел енн\то роль. Главньцц образом, развивается поражение сосудов
(тромбоз). Тромбоз мелких (интрамиокардиальных, в частности, сосудов)
носит название тромботической микроангиопатии (ТМА). Данный синдром
бьш впервые описан при тромботической тромбоцитопенической пурпуре.
Тромботическая микроангиопатия сосудов сердца проявляется ишемией,
вплоть до развития ишемической кардиомиопатии, и именно это состояние
было вполне вероятно у нашего больного. Других, более частых и очевидных
проявлений поражения сердца в рамках антифосфолипидного синдрома у
него не было. К таким проявлениям относятся (табл. 10. /) внутрипредсерд-
ный тромбоз, тромбоэндокардит с развитием клапанньгх пороков сердца (как
182 Кардиологиянедостаточности, так и стеноза), коронарный атеросклероз и тромбоз с раз-
вт-ггием инфаркта миокарда, тромбоз крупных и мелких почечных, легочных
сосудов, брющного отдела аорты с развитием системной и легочной гипер¬
тонии. Тромбоз печеночных вен (синдром Бадда—Киари) может имитировать
застойную гепатомегалию, но в нашем случае данные УЗИ и КТ позволяли
исключить такую возможность. Показаний к назначению варфарина у нашего
пациента также не было, поскольку его рекомендуют назначать только при
наличии внутрисердечного тромбоза, тромбоэндокардита, легочной гипертен¬
зии и сосудистого тромбоза в отсутствие атеросклероза (при наличии атеро¬
склероза рекомендуется аспирин).Варианты поражения сердца в рамках антифосфолипидного синдрома:— тромботшіеская микроангиопатия (ТМА) интрамиокардиальных сосудов
с развитием ишемии и хронической ишемической кардиомиопатии;— внутрипредсердный тромбоз;— тромбоэндокардит с развитием клапанных пороков сердца (как недо¬
статочности, так и стеноза);— коронарный атеросклероз и тромбоз с развитием инфаркта миокарда;— тромбоз крупных и мелких почечных, легочных сосудов, брюшного
отдела аорты с развитием системной и легочной гипертонии;— тромбоз печеночных вен (синдром Бадда-Киари) может имитировать
картину кардио генного застоя в печени.Терапия варфарином рекомендуется при наличии внутрипредсердных тром¬
бов, тромбоэндокардита, легочной гипертензии, сосудистом тромбозе в отсут¬
ствие атеросклероза.Диагноз кардиомиопатии вследствие тромботической микроангиопатии
можно поставить только методом иск-тючения (вплоть до проведения коро-
нарографии) или с помощью биопсии миокарда. Единственным методом,
который хотя бы косвенно позволяет судить о состоянии кровоснабжения
миокарда, является сцинтиграфия, которая и была выполнена нашему боль¬
ному. Были выявлены нарушения перфузии, характерные д,ія некоронароген-
ных поражений миокарда (неравномерное распределение индикатора в левом
желудочке с участками гипоаккумуляции в области передней, задней стенки
левого желудочка и базальных отделов перегородки), что не иcключaJ^OJ но и
не подтверждало поражение сердца в рамках тромботической микроангиопа¬
тии. Нельзя исключить, что в острый период картина оказалась бы иной — во
всяком случае, описана полная обратная динамика тромботической микроан¬
гиопатии миокарда в результате терапии преднизолоном.Нефропатия в рамках антифосфолипидного синдрома достаточно хоро¬
шо известна, и связана она также с поражением почечных сосудов разного
калибра. Тромбоз крупной почечной артерии приводит к инфаркту почек, а
поражение более мелких (внутрилочечных) артерий по типу тромботической
микроангиопатии проявляется в первую очередь системной артериальной
гипертонией и постепенным или острым снижением функции почек, в свою
очередь, системіїая артериальная гипертония, которая развивается при анпі-
фосфолипидном синдроме (не только в результате поражения почечных
Глава 10. Миокардит с выраженными иммунными проявлениями... 183артерий), приводит к вторившому поражению почек по типу артериолоскле-
ротического нефросклероза, и на этом этапе возможно развитие протеинурии.
Однако очень важно подчеркнуть, что развитие классического нефрита для
первичного аитифосфолипидного синдрома нехарактерно (хотя и возможно).Доказать, что поражение почек связано именно с антифосфолипидным
синдромом, весьма непросто, Оптима,чьным методом диагностики остается
биопсия почек, при которой возможно обнаружение микротромбозов вну¬
три почечных сосудов. Однако супіествует и неинвазивный метод косвенной
диагностики этого состояния — ультразвукое допплеровское исследование
сосудов, которое позволяет исследовать почечный кровоток в трех режимах: 1)
в обычном режиме (при этом может быть выявлен тромбоз крупной почечной
артерии); 2) в режиме цветового допплеровского каргирования (выявляется
обеднение дистального — коркового — кровотока); 3) в импульсно-волновом
режиме с определением параметров кровотока в интраренальных сосудах
(сегментарных, межяолевых и луговых артериях). Признаком тромботической
микроангионатии является обеднение внутрипочечного кровотока, причем
эти изменения заметно уменьшаются в результате терапии непрямыми анти¬
коагулянтами.Именно назначение варфарина и его аналогов является главным методом
лечения тромботической микроангиопатии (хорошо известно, что при других
формах аитифосфолипидного синдрома могут использоваться как низкомо-
лекуллрные гепарины, так и аспирин, а также сочетания этих препаратов).
Использование низкомолекулярных гепаринов в виде курсов по 4-6 нед при
антифосфолипидной нефропатии также обсуждается.Что касается этиологии возможного аитифосфолипидного синдрома, то
с учетом выявленных антител к вирусам именно вирусная инфекция пред¬
ставлялась наиболее очевидной причиной вторичного аитифосфолипидного
синдрома у нашего больного (при цитомегаловирусной инфекции антитела к
фосфолипидам выявляются достаточно часто). Тем не менее формально наи¬
более частой причиной вторичноіо аитифосфолипидного синдрома является
системная красная волчанка, в связи с чем были дополнительно проведены
соответствующие иммунные тесты.Их результаї ьт снова оказались неожиданными. У больного были обнару¬
жены LE-клетки (выражен феномен агглютинации). Тигр антител к нативной
ДНК оказался повышен более чем в 2 раза (43,56 МЕ/мл при норме до 20).
Антинуклеарный фактор не выявлен. Появление LE-клеток и антител к ДНК
описано и у больных с антифосфолипидным синдромом без клинической кар¬
тины СКВ, однако их обнаружение заставило нас по-новому рассмотреть всю
картину болезни у нашего пациента.Какие симптомы могли быть расценены как проявления СКВ? Пол паци¬
ента нетипичен, но возраст достаточно типичен для дебюта СІСВ. Начало после
острой респираторной инфекции весьма характерно для всех иммунных забо¬
леваний. В пользу диагноза СКВ говорят также гепатоспленомегалия и внутри-
грудная лимфоаденопатия, безусловно — изменения мочевого осадка с преоб¬
ладанием эритроцитурии (нефрит?), анемия, миокардит, регрессировавший
184 Кардиологияна преднизолоне. Кроме того, выпот в плевральную полость, который рас¬
ценивался при лечении в г. Грозный как гидроторакс в рамках выраженной
сердечной недостаточности, до сих пор сохраняется, частично осумковался и
скорее должен расцениваться как экссудативный плеврит (результаты исследо¬
вания плевральной жидкости в Грозном неизвестны). Петрификаты перикарда
могут быть расценены как результат регрессировавшего перикардита. Таким
образом, можно было говорить о наличии полисерозита, и диагноз СКВ стано¬
вился еще более вероятным. В то же время у больного полностью отсутствуют
изменения на коже, какие-либо признаки поражения суставов.На данном этапе консультация нефролога приобрела дополнительный
смысл. Планировалось обсудить не только возможность расценивать изме¬
нения мочевого осадка как проявления нефрита, но и целесообразность про¬
ведения биопсии почки, которая мог.аа бы подтвердить не только диагноз
неспецифического нефрита, но и собственно люпус-нефрита. По-прежнему
была не вполне ясна роль нефрита в развитии отеков в дебюте болезни, роль
антител к кардиолипину в клинической картине болезни. Требовала обсужде¬
ния лечебная тактика (сохранение признаков нефрита могло препятствовать
снижению дозы преднизолона). Наконец, требовала обсуждения правомер¬
ность постановки диагноза системной красной волчанки.Больной бьш проконсультирован в Клинике терапии, нефрологии и професси¬
ональных заболеваний им. Е.М. Тареева профессором Е.М. Шиловым', у больного
полиорганная lIaтoJЮгия, включающая поражение миокарда (по типу миокар¬
дита), почек (минимальный мочевой синдром с гематурией), полисерозит (плев¬
рит, признаки поражения перикарда), системную лимфоаденопатию, анемию в
сочетании с лабораторными иммунными отклонениями. Диагноз СКВ вполне
вероятен (возможна как системная вирусная инфекция, так и поражение почек
и миокарда в рамках ангифосфолипидного синдрома). Для исключения тромбо¬
тической микроангиопатии в рамках ангифосфолипидного синдрома показано
проведение ультразв^тсового допплеровского исследования сосудов почек с
оценкой микроциркуляпии. Проведение биопсии почки на данный момент не
представляется возможным. С учетом сохраняющихся изменений в анализах
мочи, с одной стороны, и норма,1ьной функции почек — с другой, следует уве¬
личить дозу преднизолона до 40 мг/сут, через неделю повторить анализы крови и
мочи. Необходим контроль состояния кисты в грудной клеже.в клинике им. Е.М. Тареева было выполнено ультразвуковое допплеровское
исследование почечных артерий, по данным которого как магистра^тьпый, так
и внутрипочечный кровоток не изменен. Таким образом, данных за тромбо¬
тическую микроангиопатию не получено, значение антител к кардиолипину
в развитии поражения почек и миокарда поставлено под сомнение (хотя в
острый период аналогичное обследование не проводилось). Во всяком случае
на данном этапе болезни антитела к кардиолипину большого клинического
значения, по-видимому, не имели, лечения антикоагулянтами не требовалось.Доза преднизолона была увеличена до 40 мг/сут, проводи.'шсь также тера¬
пия делаїилом 0,25 по 1 таб. па почь, мовалисом 7,5 мг по 1 таб. 2 раза в день
(через 2 нед отменен), престариумом 8 мг/сут, далее моноприлом 5—10 мг/сут.
Глава 10. Миокардит с выраженными иммунными проявлениями.,, 185карведилолом, далее метопрололом 25—150 мг/с>т, всрошпироном 100 мг/сут,
лазиксом 40 мг через день, далее фуросемидом 40 мг 2—3 раза в неделю, омезом
40 мг/сут, далее 20 мг на ночь. Практически полностью купировались явления
застоя 1Ю большому и малому кругам кровообращения, повысилась переноси¬
мость физических нагрузок, значительно уменьшилось количество жидкости и
воздуха в правой плевральной полости (по данным контрольной рентгеногра¬
фии — до полного исчезновения).в ана,1изе крови через неделю после увелюїения дозы преднизолона — пол¬
ная нормализация уровня гемоглобина (140,8 г/л), нарастание лейкоцитоза
до 16 тыс. В анализе мочи — небольшая протеинурия (0,180%о) и единичные
эритроциты в поле зрения, что расценено как эффект преднизолона. В кон¬
трольных имм>ттологических анализах крови — сохранение титра антител к
кардиолипину класса IgG (51,26 МЕ/мл при норме до 10), некоторое увеличе¬
ние уровня комплемента, отсутствие антител к нативной ДНК и — впервые —
обнаружение антинук/іеарного фактора в титре 1:40 (гомогенное свечение +).Согласно рекомендациям Американской ревматологической ассоциации, тре¬
буется не менее 4 критериев из 11 для постановки диагноза СКВ.1. Высыпания на ск>'лах и щеках («бабочка»),2. Дискоидные высьшания.3. Фотосенсибилизация,4. Изъязвления в полости рта и носоглотке, обычно болезненные.5. Артрит — неэрозивный, двух и более периферических суставов.6. Серозит — плеврит (боли, шум трения плевры, плевральный выпот) или
перикардит.7. Нефрит — стойкая протеинурия более 0,5 г/сут или цилиндрурия (эри-
троцитарные, зернистые, смешанные).8. Неврологические нарушения (судороги, припадки или психозы).9. Гематологические нарушения (гемолитическая анемия с ретикулощгго-
зом, лейкопитопения менее 4000/мК1, лимфопения менее 1500/млк или тром-
боцитопения менее І00 тыс./мкл.10. Иммунологические нарушения: LE-клетки, повышенные титры АТ к
нат ДНК, антигену Смита, ложноположительная РВ.11. Повышенные титры антииуклеарных АТ (иммунофлюоресценция).У данного больного с некоторой натяжкой имеются 5 критериев: серозит,
нефрит (во всяком случае нефропатия с минимальными изменениями моче¬
вого осадка), анемия (которая не являлась гемолитической, но «ушла» при
терапии предішзолоном), а также 2 иммунологических критерия. Ecjui пользо¬
ваться критериями диагноза СКВ, предложеннылш В.А. Насоновой, го диагноз
представлялся еще более обоснованным: имеются 3 больших критерия (нефрит
и LE-клетки), а также целый ряд малых: немотивированная потеря массы тела,
полисерозит, лимфаденопатия, гепатоспленомегалия, миоксірдит, положитель¬
ный АНФ в низком тигре.Таким образом, состояние больного было расценено как системная
красная волчанка подострого течения с поражением сердца (миокардит),
серозных оболочек (экссудативный плеврит, перикардит в анамнезе), почек
186 Кардиология(гломерулонефрит с нефротическим синдромом в анамнезе?), с лимфаде-
нопатией, антифосфолипидным синдромом, анемией TU степени активно¬
сти, леченной глюкокортикостероидами. Недостаточность кровообращения
11А сталии. Кисты легких (перикарда?) неясной этиологии (эхинокковые?).
Мы не исключали, что эхинококкоз был фактором, который запустил раз¬
витие вторившого волчаночноподобного синдрома. Больной был выписан с
рекомендациями np040jT?KHrb терапию в полном объеме в течение месяца,
после чего повторно обследоваться в Факультетской терапевтической клини¬
ке им. В.Н. Виноградова. Планировались решение вопроса о снижении дозы
преднизолона и опенка динамики кист в легких.Насколько же типично подобное течение волчанки с выраженным миокар¬
дитом в дебюте болезни? Прежде всего мы не можем полностью исключить
простого сочетания вирусного миокардита и СКВ, которые дебютировали
одновременно, либо СКВ возникла раньше, В литературе описано и более ред¬
кое сочетание — СКВ и гигантоклеточного миокардита, который вначале был
расценен как волчаночный и диагностирован лишь при биопсии. Клинически
значимый миокардит при волчанке — относительная редкость (он встречается
менее чем у 10% больных), но описаны случаи развития полной АВ-блокады,
внезапной смерти, отека легких, кардиогенного шока. Описан даже фульми-
нантный волчаночный миокардит с геморрагиями. На аутопсии миокардит у
больных с СКВ выявляется значительно чаш,е (до 50%).Развитие выраженного миокардита в дебюте СКВ описано неоднократно:
как правило, у таких больных выявляются полисерозит и иммунные наруше¬
ния, реже — артрит и нефрит. Показано, что при волчанке миокардит чаще
развивается при на^тичии антител к кардиолипину класса IgG, а также антител
к Ro-антигену (растворт-гмый тканевой рибонуклеарный протеин), которые
ифают роль в развитии врожденных блокад (блокады развиваются, в част¬
ности, у детей матерей, страдающих СКВ). Наиболее характерном признаком
волчаночного миокардита при биопсии являются депозиты TgG. Терапия сте¬
роидами и (при необходимости) цитостатиками дает отчетливый эффект; опи¬
сан также положительный эффект гамма-глобулина и плазмафереза.Клинические варианты нефрита при системной красной волчанке
(И.Е. Тарсева, Н.А. М>'хин):— быстро прогрессирующий волчаночный нефрит (10—45%):
нарастание почечной недостаточности,
нефротический синдром,эритроцитурия,
артериальная гипертония;— медленно прогрессирующий волчаночный нефрит с нефротическим
синдромом (30—40%);протеинурия редко бывает высокой, обычно неселективная,
нередки гематурия, артериальная гипертония;— активный волчаночный нефрит с выраженным мочевым синдромом
(30%):протеинурия более 0,5 г/сут,
Глава 10, Миокардит с выраженными иммунными проявлениями... 187эритроцитурия, лейкоцитурия,
нередко — артериальная гипертония;— волчаночный нефрит с минимальным мочевым синдромом — протеи-
нурия <0,5 г/сут.Если рассуждать о том, какой вариант волчаночного нефрита развился у
нашего больного, то речь идет, видимо, об активном волчаночном нефрите
с выраженным мочевым синдромом, хотя в дебюте мы не можем исключить
нефротический синдром, а отсутствие артериальной гипертонии и невысокая
протеинурия ближе к нефриту с минимальным мочевым синдромом. Правда,
при этой форме не бывает эритроцитурии. Во всяком случае вероятность того,
что в биоптатах не будет выявлено специфичного волчаночного нефрита,
достаточно высока — более вероятно выявление мезангиального нефрита или
минимальных изменений. Необходимо подчеркнуть, что в специа^тьном иссле¬
довании не была доказана роль антител к кардиолипину в развитии волчаноч¬
ного нефрита, т.е. нефрит у подобных нашему больных обусловлен именно
системной красной волчанкой.Наконец, следует кратко сказать о том, возможно ли развитие кист в легких
(или перикарде) в рамках СКВ или антифосфолипидного синдрома. Найти
описание подобных случаев не удалось. Для самой СКВ характерно развитие
пневмонита с дисковидными ателектазами, существенно реже — с множествен¬
ными кистами в легких (лшіфоцитарньїй интерстициальный пневмонит); при
одновременном начичии антифосфолипидного синдрома развиваются тромбо¬
зы легочных сосудов, внутриальвеолярные кровотечения с кровохарканьем и
легочная гипертензия.Через месяц с небольшим больной был повторно госпитализирован в
Факультетскую терапевтическую клинику им. В.Я. Виноградова в удовлетвори¬
тельном состоянии. Сохранялись жалобы на практически постоянные боли в
области сердца; стали беспокоить также перебои в работе сердца. В анализах
крови — уровень гемоглобина оставался нормааьным (142,1 г/л), цветовой
показатель несколько снижен (0,83), лейкоциты — 12,5 тыс., эозинофилия
по-прежнему отсутствует, несколько повышены уровни фибриногена (4,78 г/л)
и СРВ (1,74 мг/дл). LE-клетки и антитела к ДНК не найдены, титр антител к
кардиолипину уменьшился (33,96 МЕ/мл при норме до 10), титр АНФ увели¬
чился (1:80, свечение гомогенное +-Ь). В обшем анализе мочи — небольшая
изолированная протеинурия (0,405%о).По данным ЭхоКГ размеры камер сердца полностью норма.іизовались,
исчезли митральная недостаточность, пролапс митрального клапана и допол¬
нительная хорда. При холтеровском мониторировании ЭКГ зафиксированы
небольшое число наджелудочковых экстрасистол (на фоне терапии локреном
20 мг/сут), а также лабильность зубца Т.Особый интерес представляли результаты контрольной КТ органов грудной
клетки, поскольку увеличение размеров кист было весьма вероятным. Была
проведена МСКТ легких, по данным которой определялись участки фиброза
в 9-м и 10-м сегментах правого легкого, а в верхушках обоих легких — участ¬
ки фиброза. Над диафрагмой справа — жидкость с частичным осулткованием
188 Кардиологияв задненижнем отделе плевральной полости (максимальная толшина слоя
3 см). Стенки бронхов утолщены. В верхнем и среднем отделах средостения
определяются множественные лимфатические узлы до 10 мм в поперечнике.
Сердце обычной конфигурации и размеров. Перикард утолщен до 5 мм, с еди¬
ничными мелкими кальцинатами; кистозные образования не выявлены; струк¬
туры, визуализирующиеся на поперечных срезах на уровне левого желудочка,
обусловлены листками перикарда.Бессимптомное исчезновение кист с мягкотканным содержимым трудно
объяснить. Ошибки в первом исследовании, по-видимому, не было: кисты
действительно хорошо визуализировались, самая кр\ттная имела размер 2x3 см.
Предполагать иммунную природу этих кист, которая оказалась бы чувстви¬
тельной к преднизолону, очень сложно — подобных описаний мы не встретили
не только при СКВ, но и при др>тих иммунных болезнях. Можно упомянуть
единственное описание саркоидоза в сочетании с антифосфолипидным син¬
дромом, при котором в легких определялись полости (но без мягкотканного
содержимого), исчезнувшие при терапии преднизолоном. Инфекционные
кисты могли быть следствием иммуносупрессивной терапии, но в этом случае
их исчезновение при наращивании дозы преднизолона также необъяснимо.
Остава^чось предполагать, что кисты (все три) спонтанно лопнули, и поскольку
это не сопровождалось никакими клиническими проявлениями, они вряд ли
содержали эхинококки.По согласованию с профессором Е.М. Шиловым больному бьшо рекомендо¬
вано начать снижение дозы преднизолона по 'Лтаб. в неделю до уровіія 20 мг/сут,
после чего он должен бы.1 обратиться в клинику им. Е.М. Тареева. Однако боль¬
ной самостоятельно продолжил снижение дозы до 10 мг/сут (последние 2 таб,
он отменил в течение недели), после чего был срочно вызван в Факультетскую
терапевтическую клинику им. Б.Н. Виноградова. В анализе мочи отмечено появ¬
ление гематурии (5—7 эритроцитов в п/зр,), белка практически не было. В связи
с возобновлением одышки (при отсутствии динамики ЭКГ и ультразвуковых
параметров сердца) доза верошпирона увеличена до 100 мг/сут. Рекомендован
прием 15 мг преднизолона в сутки с консультапией через месяц.Комментарий В.И. Мако.іікина — профессора кафедры факрьтетской терапии
№ 1 лечебного факультета Первого МГМУ им. И. М. Сеченова, член-корр. РАМНМне кажется более убедительным диагноз, который был поставлен паци¬
енту вначале (в том числе в Факультетской терапевтической клинике им.
В.Н. Винофадова). Почему это не может быть вирусный миокардит и вирус¬
ный нефрит? Тяжелый миокардит в рамках СКВ мы не раз наблюдали в отде¬
лении патологии суставов и соединительной ткани нашей клиники, но это
всегда была тяжелая, высокоактивная волчанка.Комментарий Н.В. Петуховой — заведующей лечебно-диагаостическим отделе¬
нием Центра суставной боли Первого МГМУ им. И. М. СеченоваПо критериям — да, получается волчанка. Но есть противоречия. Плеврит?
У него вроде бы была пневмония. Перикардит? Кальций в перикарде
Глава 10. Миокардит с выраженными иммунными проявлениями... 1S9нетипичен для волчанки. Может быть, необычность течения СКВ объясня¬
ется тем, что это мужчина. Выявлены LE-клетки — это рассматривается как
признак нелеченой волчанки, но при этом должен быть высокий титр АНФ.
Если говорить о 3-й степени активности, то лечение доліжно состоять в назна¬
чении 60 мг преднизолона в сочетании с цитостатиками и проведении пульс-
терапии. Однако миниматъная выраженность нефрита все-таки не позволяет
ставить 3-ю степень активности.Комментарий А.В, Недоступа — профессора кафедры фа^льтетской терапии
№ 1 лечебного факультета Первого МГМУ им. И. М. Сеченова, д-ра мед. наукЕсли посмотреть на больного, отвлекаясь от форксулировки его диагноза, то
проводившаяся ему терапия кажется абсолютно адекватной степени органно¬
го поражения (к примеру, СОЭ за все время болезни не была высокой). Как
правильно назвать это системное заболевание, им^гунную природу^ которого
мы хорошо понимаем? Наверное, волчаночноподобный синдром у больно¬
го с тяжелым, острейшим миокардитом, который, безусловно, лидировал
в клинической картине. А поражение почек могло носить как иммунный,
так и первично вирусный характер (вирусная этиология нефритов хорошо
известна).P.S. В течение последующего года пациент находился в Чечне, перио¬
дически звонил — на фоне постепенного снижения дозы преднизолона и, в
последующем, его полной самостоятельной отмены самочувствие остава-тось
удоатетворительным; контрольные анализы крови и мочи проводились по
месту жительства, однако результаты их нам не известны. В дальнейшем кон¬
такт с больным был утрачен, мы надеемся, что это обусловлено его стабильно
хорошим самочувствием. В том случае, если произошло по.іное восстановле¬
ние функций сердца и почек и пациент не нуждается в стероидной терапии,
можно с большой уверенностью говорить о том, что мы имели дело не с дебю¬
том системной красной волчанки, а с миокардитом с выраженной иммунной
окраской. Однако достоверной информации на этот счет у нас нет.
Глава 11
ФУЛЬМИНАНТНЫЙ МИОКАРДИТ: ДИАГНОЗ,
ЭТИОЛОГИЯ, ЛЕЧЕНИЕ, ПРОГНОЗИЛ. Новикова, М.Ю. Гиляров, А.В. Седов,
ДА, Парфенов, Н.В. Гагарина, Е.С. Белышева,
ВЛ. Седов, А.Л. СыркинФульминантный миокардит — особый, крайне тяжелый вариант течения
острого миокардита различной этиологии, описания которого все чаще появ¬
ляются в медицинской литературе. Критерием тяжести заболевания являет¬
ся необходимость искусственного поддержания функций жизненно важных
органов (в первую очередь сердца и легких), которая возникает у большинства
таюіх больных — их жизнь в острый период практически полностью зависит от
своевременности оказания полномасштабной медицинской помощи. В даль¬
нейшем судьба больных, переживших фульминантный миокардит, различна —
одними из самых спорных вопросов являются целесообразность применения у
них иммуносупрессивной терапии и возможность (условия, механизмы) спон¬
танного восстановления сократимости миокарда.Данное клиническое наблюдение иллюстрирует фактически мгновенное
(менее чем за одни сутки) развитие критической для жизни дисфункции
миокарда у молодого человека, потребовавшее немедленного начала искус¬
ственной вентиляции легких; интенсивная терапия в отделении реанимации
привела к выраженному клиническому улучшению, однако этиология заболе¬
вания (обсуждались концепции бактериального и вирусного миокардита) и его
прогноз послужили поводом для серьезного обсуждения.Больной т., 17 лет, переведен из городской инфекционной больницы в
отделение реанимации и интенсивной терапии (ОРИТ) Клиники кардиологии
ММА им. И.М. Сеченова 20.09.2009 п на продолжавшейся аппаратной искус¬
ственной вентиляции легких (аИВЛ).Из анамнеза, собранного со слов родственников, известно, что в конце июля —
начале августа 2009 г перенес острую респираторную вирусную инфекцию,
сопровождавшуюся катаральными явлениями, лихорадкой до 38 °С, кашлем с
отхождением небольшого количества мокроты; данные симптомы купировались
самостоятельно. В середине августа (за месяц до госпитализации) отметил укус
ктеща (в Северной Осетии), за медицинской помош^.ю не обращался,В сентябре начал обучение в институте, 17-18 сентября вновь отмечался
эпизод субфебрилитета. Днем 20 сентября появились лихорадка до 38,5 Х,
тошнота, рвота, общая слабость, холодный липкий пот Был экстренно госпи¬
тализирован в инфекционною больницу с подозрением на пищевую токсико-
инфекцию. в больнице появились и стали нарастать боли в грудной клетке,
Глава и. Фульминантный миокардит: диагноз, этиология, лечение, прогноз 19Іусиливающиеся при наклоне туловища вперед, одышка. При рентгенографии
органов фудной клетки были выявлены признаки двусторонней нижнедо¬
левой пневмонии, в крови отмечался лейкоцитоз до 32,7х107л. со сдвигом
нейтрофильной формулы влево, к вечеру отмечалось резкое падение уровня
АД до 60/40 мм рт.ст., развитие альвеолярного отека легких, в связи с чем было
принято решение о начале инотропной терапии, произведена интубация тра¬
хеи, начата аппаратная искусственная вентиляция легких. При ЭхоКГ бьыо
выявлено снижение фракции выброса левого желудочка до 27%. В связи с
этим больной был переведен в отделение реанимации и интенсивной терапии
іОшники кардиологии ММА им И.М. Сеченова.При постутепии состояние крайне тяжелое. Температура тела составля¬
ла 38,5 “С, кожные покровы бледные, чистые. В легких на фоне аппаратной
искусственной вентиляции легких выслушивались рассеянные, сухие хрипы,
больше в нижних отделах. Тоны сердца глухие, ритмичные, ЧСС 140 уд/мин,
АД ПО и 70 мм рт.ст. (на фоне инфузии допамина 10 мг/кг в минуту). Живот
мягкий, безболезненный при пальпации, печень и селезенка не увелгтчены.Была произведена катетеризация легочной артерии катетером Swan-Ganz.
При измерении показателей центральной гемодинамики выявлен гипокине¬
тический тип центральной гемодинамики. На фоне продолжающейся ино¬
тропной поддержки минутный объем составлял 2,30 л/мин (норма — 3,5-5,5),
сердечный индекс 1,24 л/мин/м^ (норма 2,7—3,0), ЧСС 128 уд/мин, АД сист.
94 мм рт.ст., АД диаст. 69 мм рт.ст., АД сред. 77 мм рт.ст., СДЛА 21 мм рт.ст.,
ДДЛА 18 мм рт.ст., ДЛА сред. 19 мм рт.ст., ДЗЛА22 мм рт.ст. (в норме 8—12).Таким образом, у больного были все клинические и гемодинамические при¬
знаки кардиогенного шока.На ЭКГщж поступлении регистрировались синусовая тахикардия с ЧСС до
140 уд/мин, отрицательные зубцы Тв отведениях Т, aVL, V —{рис. 11.1).і і:j , ■ j- ■ j-гг *VRme■Рис. ll.L ЭКГ больного Т. при іюстуїиіении. Скорость записи 25 мм/с. Поясненні в
тексте
І92 КардиологияВ клиническом анализе крови, выполненном по cito, отмечались нейтрофиль-
нътй лейкоцитоз до 33,7х10Ул, НЬ 170 г/л, эритроциты 6,35 млн, тромбоциты
268 тыс.В биохимическом анализе крови обращало на себя внимание повышение
уровня КФК до 486 ед/л, МВ-КФК до 62 ед/л и практически шестикратное
повышение уровня тропонина-Т (до 0,5і нг/мл). Уровень креатинина состав¬
лял 1,51 мг/дл (вероятнее всего, на фоне тяжелой левожелудочковой недоста¬
точности).В иммунологических исследованиях: HBsAg, HCVAb, антитела к ВИЧ не
обнаружены. Среди серологических реакций на сифилис обращали на себя
внимание положительный результат иммунофлюоресцентиого анализа и сла¬
боположительный результат реакции прямой гемагглютинации.Отмечалось увеличение уровня фибриногена до 4,66 г/л, СРБ до 8,87 мг/дл;
исследования крови на анти-О-стреитолизин и РФ дати отрицательный
результат.В общем анализе мочи патологии вьшатено не бььао.Учигьгвая положительные результаты серологических реакций на сифилис,
наличие в анамнезе укуса клеша, клиническуто картину заболевания, было
высказано предположение о болезни Лайма, а полученные серологические
реакции, по всей вероятности, могли быть неспецифическими перекрестны¬
ми. Проводилось определение антител к Borrelia burgdorferi в крови, однако
результат данного исследования дважды был сомнительным: IgM 20,0 Ед/мл
и 22,0 Ед/мл (<10 Ед/мл отрицательно, 18-22 Ед/мл сомнительно, >22 Ед/мл
положительно). Таким образом, убедительных данных за боррелиоз получено не
было. Повторные анализы на сифилис Тсікжс дали отрицательный результат.Для установления этиологии миокардита проводились серологические
исследования:1) не обнаружено IgG и TgM к Mycoplasma hominis. Mycoplasma pneumonia,
Clamidia pneumonia;2) не обнаружено специфических антител к Salmonela А, В, С1, С2, D, I,
Yersinia enterocolitica. Yersinia pseudotuberculosis\3) методом ПЦР не обнаружено генома вируса герпеса VI типа, вируса гер¬
песа зостер, энтеро вируса, цитомегаловируса, Toxoplasma gondii;4) методом ПЦР в крови выявлена. ДНК вируса Эпштейна—Барр (качествен¬
ная реакция).Также исследовались биологические среды больного (посев крови, мочи,
мокроты), в которых во всех случаях был выявлен рост Staphylococcus epidermidis
с одинаковой чувствительностью к антибиотикам. Уровень прокальцитонина в
крови составил менее 0,05 нг/мл (норма до 0,250).При Эхо КГ, выполненной при поступлении, регистрировалось выраженное
нарушение систолической функции левого желудочка, ФВ составляла около
25%, отмечались диффузный гипокинез, тенденция к увеличению левого
желудочка — КДР 5,6 см, КДО 97 мл, КСО 69 мл, тМЖП 0,9 см, тЗСЛЖ 0,9 см
{рис. 11.2); правые камеры не увеличены. Аорта: скорость кровотока 83 см/с,
регургитации нет. Митральный клапан: регургитация 0—1 степени, Е 72 см/с.
Глава И. Фульминантный миокардит: диагноз, этиология, лечение, прогноз 193Рис, 11,2, Эхокардиограмма больного Т. при поступлении. Пояснение в текстеРис. 11.3. МСКТ органов грудной клетки больного Т. Пояснения в текстеТрикуспидальный клапан: регургитация 0—1 степени, среднее давление в легоч¬
ной артерии составило 30 мм рт.ст. При выполненной позднее нреспищеводтй
ЭхоКГ патологических эхопозитивных изменений на створках клапанов и в
полостях сердца не выявлено.При МСКТ органов грудной клетки (рис. IL3) в задних отделах нижних долей
обоих легких определялись участки консолидации легочной ткани, на фоне
которых прослеживались воздушные просветы бронхов, в плевральных поло¬
стях определя^юсь незначительное количество жидкости, другой патологии
выявлено не бьшо.По данным МСКТ сердца (рис. 11.4) коронарные артерии не изменены,
миокард не истончен; в артериальную и отсроченную фазы контрастирования
тКардиологияРис. 11.4. МСКТ сердца бсшьного Т. Пояснения в текстеопределяется мозаичный характер накопления контрастного препарата с участ¬
ками повышенного контрастирования субэпикардиально на протяжении боко¬
вой стенки левого желудочка и интрамиокардиально в области средней фсга
межжелудочковой перегородки, нижневерхушечной и высокой боковой лока¬
лизации. Также в отсроченную фазу контрастирования определялось повы¬
шенное накопление контрастного препарата миокардом правого желудочка.При проведении MFT сердца на отсроченной томограмме (полученной
через 10 мин от момента внутривенного введения гадодиамида в дозировке
0,1 ммоль/кг массы тела пациента) определялись участки накопления препа¬
рата в стенках левого желудочка {рис. И.5, показаны стрелками).Рис. 11.5. МРТ сердца больного Т. с гадолинием, отсроченная фаза. Стрелками обозна¬
чены зоны отсроченіюго ттакопления. Пояснения в тексте
Глава //. Фульминантный миокардит: диагноз, этиология, лечение, прогноз 195Таким образом, на основании клинической картины (мояниеносное начало
заболевания, лихорадка, болевой синдром в грудной клетке, развитие кардио-
генного шока), данных ЭКГ (синусовая тахикардия, отрицательные зубцы Гв 1,
aVL, Vj-V^), ЭхоКГ (диффузный гапокинез стенок левого желудочка, снижение
ФВ левого желудочка до 25%), МСКТ (мозаичный характер накопления кон¬
трастного препарата), МРТ сердца, данных лабораторных исследований (ней-
трофилъный лейкоцитоз, повышенное СОЭ, повышение уровня тропонина-Т)
установлен диагноз: фульминантный миокардит тяжелого течения, осложненный
острой левожелудочковой недостаточностью (КіШр IV). Высевание в трех средах
одного и того же возбудителя с одинаковой чувствительностью к антибактериа^іь-
ным препаратам позволило заподозрить бактериальную природу миокардита.В к-1инике в течение 12 дней проводилась антибактериальная терапия лен-
дацином (цефтриаксоном) в дозе 2 г/сут внутривенно, метронидазолом 200,0
внутривенно, клацидом (кларитромицином) 1 г/сут. Также проводилось лече¬
ние сердечной недостаточности лазиксом 40 мг внутривенно, всрошпироном
50 мг/сут, престариумом 2,5 мг/сут, метопрололом 125 мг/еут, аспирином 100
мг/сут, подкожно вводился фраксипарин в профилактической дозе.На фоне терапии состояние больного существенно улучшалось: уже на вто¬
рой день пребывания в отделении реанимации и интенсивной терапии он был
экстубирован (далее в течение суток проводилась неинвазивная респираторная
поддержка ВІРАР), больше не нуждался в инотропной поддержке допамином,
температура тела нормализовалась, значительно уменьшались явления сер¬
дечной недостаточности, воспалительные изменения в анализах крови (через
10 дней уровень лейкоцитов снизился до 10 тыс., СОЭ — до 5 мм/ч, тропони-
на Т — до 0,15 нг/мл). Сохранялись явления астенического синдрома, тахикар¬
дия. Несмотря на достаточно большую дозу р-блокатора, не удавалось достичь
целевых значений ЧСС, в связи с чем к терапии был добавлен кораксан в дозе
15 мг/сут, на фоне приема которого ЧСС составляла 60—64 уд/мин.По данным повторной ЭхоКТ {рис. 11.6) появились признаки выраженного
утолшения миокарда (его толщина достигала 2 см), повышенной эхогенно-
сти стенок левого желудочка с уменьшением его размера, вероятнее всего, за
счет отека, который в дальнейшем бььл подтвержден при МРТ; определялось
небольшое количество избыточной жидкости в полости перикарда, в связи с
чем к терапии был добавлен диклофенак в дозе 150 мг/сут. ФВ левого желудоч¬
ка составля.іа 54%.За время лечения отчетливо прослеживалась положительная динамика
в достаточно короткие сроки. Менее чем через месяц, к моменту выписки
из стационара, стабилизировались ЧСС и АД. Физическая активизация паци¬
ента не сопровождалась клиническими проявлениями сердечной недостаточ¬
ности. Нормализовались общий и биохимический анализы крови. По данным
ЭхоКГ в динамике (рис. 1L 7) отмечались уменьшение толщины миокарда лево¬
го желудочка до 1,3-1,4 см и увеличение ФВ левого желудочка до 66% с норма¬
лизацией размера левого желудочка (КДР 4,1 см, КДО 64 мл, КСО 22 мл).Пациент в относительно удовлетворительном состоянии был выписан из
стационара с рекомендациями продолжить прием фуросемида 40 мг 2 раза
196КардиологияРис. 11.6. Эхокардиограмма болыюго Т. на Ю-й день пребывания в отделении реанима¬
ции и интенсивной терапии. Стрелками указано «утолщением стенок миокардаРис. 11.7, Эхокардиограмма больного Т. к моменту' выписки из стационарав неделю, верошпирона 12,5 мг утром, престариума 2,5 мг вечером, комкора
5 мг утром, мовалиса 15 мг в сутки в течение 1 мес.После прохождения курса реабилитации в кардиологическом санатории
пациент приехал в клинику. При осмотре жалоб не предъявлял. Признаков
сердечной недостаточности не бьшо. Физические нагрузки переносил удовлет¬
ворительно. При контрольной ЭКГ патологии выявлено не было (рис. 11.8).По данным ЭхоКГ {рис. 11,9), выполненной в то же время, нарушений
лока'іьной и глобальной сократимости левого желудочка не бьито. ФВ левого
желудочка составляла 65%. Толщина стенок левого желудочка не превышала0,9 см. Размеры камер сердца оставались в пределах нормы. Избыточной жид¬
кости в полости перикарда не определялось.
Рис. 11.8. ЭКГ больного Т. через месяц после выписки. Скорость аалиси 25 мм/сРис. 11.9. Зхокардиоірамма больного Т. через месяц после выпискиВ заключение нужно сказать, что данный клинический случай редок в меди¬
цинской практике. Мы видим, как «молниеносно» развивались тяжелейшая
острая левожел>'дочковая недостаточность, кардиогенный ток, что требовало
инотропной поддержки и аппаратной искусственной вентиляции легких.Как правило, врачи сталкиваются с последствиями перенесенного мио¬
кардита уже на стадии выраженной дилатации камер сердца и выраженных
признаков тяжелой сердечной недостаточности, что, как правило, обозначают
как дилатапионную кардиомиопатию. Трудность данного случая заключалась
в определении этиологии миокардита в целях выбора патогенетической тера¬
пии. На основании лабораторно-инстру^іентального исследования данное
поражение миокарда было расценено как инфекционный (бактериальный)
миокардит. В результате проведенной антибактериальной терапии отмечалась
достаточно быстрая положительная динамика клинических, инструменталь¬
ных и лабораторных показателей.Особенность данного наблюдения — возможность динамического
наблюдения за морфоф>'нкциональными показателями сердца по данным
198 Кардиологияэхокардиографического исследования. В самом начале обращали на себя вни¬
мание диффузная гипокинезия всех стенок миокарда левого желудочка и его
выраженная систолическая дисфункция. Через 10 дней было зарегистрировано
значительное утолщение стенок левого желудочка, что интерпретировалось
как отек миокарда. В дальнейшем отмечено уменьшение толщины миокарда
(отека) и улучшение систолітческой функции левого желудочка. Антитела к
миокарду, определенные через 3 мсс в одной из лабораторий Федерального
научного центра трансп-тантологии, оказа,іись отрицательными (титр - 0). Это
позволяет говорить о незаинтересованности специфического иммунитета в
развитии молниеносного миокардита, а также о благоприятном долгосрочном
прогнозе у нашего больного.Миокардит — очаговое шти диффузное воспаление миокарда, развивающее¬
ся в результате различных инфекций, воздействия токсинов, лекарственных
препаратов или иммунологических реакций, приводящих к повреждению кар-
диомиоцитов и развитию дисфункции миокарда.Термин «миокардит» был предложен в начале XIX в. Жаном Николя
Корвизаром де Маре (1755-1821) — лейб-медиком Наполеона I и основопо¬
ложником клинической медицины во Франции.Миокардит может наблюдаться в любом возрасте, но чаше развивается у
детей и лиц молодого возраста. Истинная распространенность миокардитов
неизвестна. Легкие формы заболевания могут протекать бессилштомно. По
данным J. Parrillo (1998), у 24-33% больных возможно бессимптомное течение
миокардита. Признаки воспа.іительного поражения миокарда выявляются в
4—9% аутопсий.Современные юшссификации наибольшее внимание уделяют этиологии мио¬
кардита. Миокардит могут вызьшать практически все известные возбудители.
Считается, что вирусные инфекции являются причиной большинства случаев
миокардита в Северной Америке и Европе, хотя вирусный геном идентифи¬
цируется в миокарде лишь у 10-20% пациентов. Также выделяют миокардиты
бактериальные, риккетсиозные, спирохетозные, грибковые, протозойные, ге.іь-
минтные. Кроме того, возможны миокардиты, вызванные укусами (яд змеи, осы
и др.), лечебными сыворотками, вакцинами и лекарствами (антибиотики, суль¬
фаниламиды, антрациклины, спиронолактон, фенитоин и др.), химическими
агентами (углеводороды, угарный газ, мышьяк, ртуть и др.), физи^іескими фак¬
торами (ионизирующее излучение, перегревание, переохлаждение). Миокардит
может развиться при системных воспалительных заболеваниях (системная крас¬
ная волчанка, склеродермия, ревматоидный артрит, болезнь Кавасаки, болезнь
Крона, синдром Черджа—Стросс и др.), острой ревматической лихорадке.Е. Lieberman (1991) предложена также клинико-патологическая классифи¬
кация миокардитов, в основе которой лежит характер течения заболевания.
Выделяют следующие варианты.1. Фульминаитиый (от лат. fulminis — молния) — молниеносный вариант,
характеризующийся внезапным развитием тяжелейшей сердечной недостаточ¬
ности (кардиоге иного шока) и заканчивающийся смертью или полным выздо¬
ровлением.
Глава її. Фульминантный миокардит: диагноз, этиология, лечение, прогноз 1992. Острый вариант.3. Хронический персистирующий вариант.4. Хронический активный вариант.В патогенезе поражения миокарда играют рагтъ прямой цитотокс№іеский
эффект повреждающего агента, вторичный иммунный ответ, воздействие на
миокард различных питокинов (синтетазы оксида азота, фактора некроза опухо-
.чи, интерлейкина-б) и аберрантная индукция апоптоза. Необходимо отметить,
что в большинстве публикаций речь идет только о патогенезе вирусного миокар¬
дита. Гораздо меньше сведений имееі ся об особенностях патогенеза и течения
бактериальных миокардитов. Тем не менее развитие молниеносного миокардита
может наблюдаться при бруцел^тсзе, менингококковой инфекции, сальмонел¬
лезе, стафилококковых инфекциях, дифтерии. В патогенезе бактериальных
миокардитов, помимо прямой инвазии бактерий и действия токсинов, вьфаба-
тываемых микроорганизмами (что наиболее характерно для дифтеритического
миокардита), большую роль играет дисф>тікдия миокарда, вызванная сепсисом.
В подавлении сократительной функции миокарда при сепсисе, вероятнее всего,
участвуют такие циркулируюигие цитокины, как ФНО-а, интерлейкины 1р и 6.
Гораздо труднее представить себе развитие молниеносного миокардита вслед¬
ствие вторичного имм>'нного ответа, который требует времени для реализации.Клинические проявления миокардита неспецифичны. Они могут варьировать
от легких форм без признаков сердечной недостаточности до тяжелейшей
недостаточности кровообращения. Фульминантный миокардит обычно начи¬
нается с развития острой сердечной недостаточности. На протяжении 7 лет
G.M. Felker с коллегами наблюдали пациентов с фульминантным и острым
нефульминантным миокардитом. В отличие от пациентов с острым миокар¬
дитом, сопровождающимся сердечной недостаточностью на уровне II—III ФК,
у Псщиентов с фульминантным миокардитом быстро развиваются симптомы
кардиогенного шока. Также у большинства больных за 2-4 нед до начала забо¬
левания отмечаются гринпоподобные симптомы, такие, как лихорадка, недо¬
могание, артралгии и др.Первичные результаты лабораторных исследований у пациентов с миокарди¬
том выявляют лейкоцитоз, эозинофилию, повышение СОЭ, а также повыше¬
ние уровня Т-тропонина и МВ-КФК. Кроме того, у пациентов с фульминаш-
ным миокардитом могут выявляться повышение уровня азота мочевины крови,
креатинина, трансаминаз, КФК и СРВ, Изменения ЭКГ (нарушения внутри-
желудочковой проводимости, желудочковые аритмии, расширение комплекса
QRS), снижение ФВ левого желудочка чаще встречаются у пациентов с фуль¬
минантным миокардитом.Визуализация играет ключевую роль в диагностике фульминантного миокар¬
дита. Проведение коронароаіниографии рекомендуется больгаинству взросльгх
пациентов для исключения острого инфаркта миокарда как причины кардио¬
генного шока. ЭхоКГ остается одним из основных визуализирующих исследо¬
ваний для оценки функции левого желудочка. У пациентов с фульминантным
миокардитом чаще встречается нормальный размер левого желудочка, утол¬
щение его стенок и межжелудочковой перегородки, снижение сократимости
200 Кардиологиялевого желудочка, что может быть обусловлено выраженным воспа.чительным
процессом и развитием интерстициачьното отека. Однако при высокой ртнфор-
мативности этот метод, к сожалению, не обладает высокой специфичностью.МРТ сердца в настоящее время является наиболее точныл< неинвазивным
визуализирующим исследованием для диагностики миокардита, однако ввиду
тяжести и нестабильности состояния пациентов с фульминантным миокарди¬
том использование МРТ для диагностики миокардита в первые часы невоз¬
можно. В связи с этим отсутствует информация о возможностях МРТ в диффе¬
ренциальной диагностике фульминантного и нефульминантного миокардита.
Третьим методом, который может быть использован для диагностики мио¬
кардита, является сцинтифафия с мечеными антимиозиновьтми антителами,
однако в связи с вариабельной ^іувствительностью и низкой специфичностью
использование этого метода стало более редким в последние несколько лет.Эндомиокардиальная биопсия играет важную po.fib в диагностике мпокардага
у паїщентов с неясной острой сердечной недостаточностью и в настоягщее время
является «золотым» стандартом, Биопсия помогает быстро и точно дифференци¬
ровать гигантоклеточный миокардит и эозинофильный некротический миокардит
от лимфоцрггарного миокардита для определения тактики лечения, так как имму-
носуцрессивная терапия показана только в первых двух слу^гаях. Максимштьную
чувствительность эндомиокардиальная биопсия имеет сразу же после появления
симптомов заболевания. Однако в настоящее время показания к биопсии миокар¬
да точно не определены. При молниеносном течении миокардита возможности
проведения биопсии офаничены из-за тяжести состояния больного.У гемодинамически нестабильных и находящихся в KapflHorenHONf шоке
пациентов с фульминантным миокардитом на первый план выходит медика-
ментозная поддерживающая терапия. Большинство пациентов фебуют ино-
фопной поддержки, в некоторых случаях необходимо прибегать к внутриа-
ортальной баллонной контрпульсации для поддержания кровяного давления
и повышения сердечного выброса. При неэффективности поддерживающей
терапии от нескольких часов до нескольких дней необходимо рассмафивать
вопрос об использовании искусственного желудочка — ventricular assist device
(VAD). У пациентов с преобладающей дисфункцией левого желудочка имплан¬
тация усфойства может яв,іяться шагом перед пересадкой сердца либо перед
подбором оптимальной медикаментозной терапии.После имплантации VAD назна^шется стандартная терапия, используемая при
сердечной недостаточности (ингибиторы АПФ, сарганы, ^-адреноблокаторы,
антагонисты альдостерона). Дигоксин следует ncnojfbsoBarb с осторожностью (в
экспериментальных моделях на животных он способствовал росту смертности).
На фоне медикаментозной шрапии восстановление функции желудочков про¬
исходит в течение примерно нескольких недель от начата фульминантного мио¬
кардита. Роль иммуносупрессивной терапии в лечеіши фульминантного мио¬
кардита остается неясной. Пока благоприятное влияние иммуносупрессивной
шрапии не доказано ни в одном рандомизированном клиническом испытании.При своевременной диагностике фульминантного миокардита и вовремя
начатом медикаментозном лечении кардиоген ного шока или использовании
3 4 5 6 7 8
Лет с момента постановки диагноза9 10 1112Рис. 11.10. Кривая Каплана-Майера: выживаемость среди пациентов с фульминант-
ным и нефульминантным (острым) миокардитом, не подвергшихся пересадке сердца
(Gupta S., 2008)искусственного желудочка долгосрочный прогноз благоприятный, и функция
миокарда полностью восстанавливается {рис. 11. Щ.KoivfMeHTapHif О. В. Благовой — доцента кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И. М. Сеченова, канд. мед. наукНадо сказать, что описания фульминантного миокардита уже не являются
казуистикой — 13 базе данных Medline имеется более 300 работ на эту тем>',
причем 75% этих работ появилось в последнее десятилетие. По-видимому, это
связано не столько с истинным увеличением частоты фульминантного мио¬
кардита, сколько с выделением его в отдельную форму, а также с успехами в
непосредственной терапии этого драматически протекающего заболевания (в
том числе с применением искусственноголевого желудочка). Этиологически
фульминантный миокардит мало чем отличается от обьпшого миокардита —
он представляет собой, по-видимому, лишь особ>то форму течения вирус¬
ного, бактериального, возможно, аллергического и иммунного миокардита.
Почему у части больных «обычные» причины вызывают столь катастрофи¬
ческое течение заболевания неизвестно, но очевидно, что это обусловлено
состоянием макроорганизма (по И.В. Давыдовскому, «патогенез есть свойст¬
во реагирующего субстрата»).Генетика миокардитов также является областью науки, в которой далеко
до получения определенных ответов — по-видимому, способность заболеть
202 Кардиологиямиокардитом в ответ на контакт с достаточно банальной инфекцией или дру-
1’ими неспецифическими факторами наследуется по мулътифакториальному
принципу. И представленный в данном наблюдении пациент, и больные,
описанные в главах 9 и 10, — молодые мужчины кавказской национальности
(осетин, азербайджанец и чеченец), что ед;ва ли случайно, до некоторой сте¬
пени подтверждает генетическую предрасположенность к этОхМу заболеванию
и всегда >'читывается нами при постановке диагаоза. Однако и собственный
опыт, и данные литерат}фы показывают, что миокардитом болеюг не только
молодые люди, не только \тужчины и не только кавказцы. По-видимому, в
значительной степени генетически занроіраммирован и вариант, по которо-
м>' будет развиваться миокардит, в том числе фульминантное его течение.
Концепция лечащих врачей об исключительно бактериальной этиологии
миокардита у представленного пациента вызывает определенные сомнения.
Безусловно, острое начало с лихорадкой вьппе 38 °С, высокий нейтрофиль-
ный лейкоцитоз, признаки двусторонней пневмонии, полу'іенньге при ком¬
пьютерной томографии, и быстрое улучшение состояния на фоне (в резуль¬
тате?) тройной антибактериальной терапии говорят в пользу этой концепции,
но едва ли высеянный из крови, мочи и мокроты Staphylococcus epidermidis
может рассматриваться в качестве этиологического агента. Данный микроб
нередко попадает во взятьте для посева биологические среды с кожи меди¬
цинского персонала — его обнар>’жение во внутренних средах всегда вызыва¬
ет сомнения. Непонятно также, почему микроб оказаіся не только в мокроте
(не будучи типичным возбудителем пневмонии), но и в крови, и Б моче — у
пациента не был диагностирован сепсис, уровень прокальцитоншш крови
ос'іаваїся совершенно нормальным.Лечаишс врачи осторожно высказьтаются об этиологической роли Staphylo¬
coccus epidermidis, однако обнаружению в крови ДНК вируса Эпштейна-Барр
вообще не придается значения, с чем мы не можем согласиться. Речь идет
не об обнаружении антител класса IgG к этому вирусу (они действительно в
том или ином титре встречаются у большинства взрослых), но о вьіяшіении
ДНК кардиотропного вируса в крови. Эта ситуация не является банальной —
регулярно проводя диагностику вирусньгк инфекций с помощью ПЦР у паци¬
ентов с вероятным или верифицированным миокардитом, мы можем пере¬
числить лишь единичные случаи выявления ДНК вируса Эпшгейна-Барр
в крови: слу^іаи острого миокардита (с интенсивным болевым синдромом,
инфарктоподобными изменениями на ЭКГ и повьппенным тропонином) и
перикардита (также с выраженными болями и изменениями на ЭКГ); случай
тяжелого сочетанного поражения печени и миокарда (с картиной дилата-
ционной карлиомиопатии); случай тяжелого хронического миокардита, в
дебюте доказанного с помоиц^ю биопсии миокарда (однако диагностика
вирусной инфекции бьша проведена лишь через 7 лет); случай выявления
вируса в крови у больной с наследственной миопатией и иммунодефицитом,
которая поступила в клинику в связи с драматическим нарастанием сердеч¬
ной недостаточности. В литературе также неоднократно описаны случаи
тяжелого миокардита, вызванного вирусом Эпштейна—Барр, в том числе и
Глава 11. Фульминантный миокардит: диагноз, этиология, лечение, прогноз 203фульм^шантного течения, причем непосредственное участие вируса в пора¬
жении миокарда доказано методом гибридизации ш 5ІШ.Мы не знаем, насколько выраженный лейкоцитоз может сопутствовать
активной вирусной инфекции, — во всяком случае он не исключает вирус¬
ной этиологии заболевания; возможность развития вирусной пневмонии
хорошо известна. Можно обсуждать также развитие у пациента микст-
инфекции (вирусно-бактериальной): первый эпизод острой респираторно-
вирусной инфекции отмечен за месяц до развития кардиогенного шока
(типичный срок для развития вирусно-иммунного миокардита); присоеди¬
нение бактериа.1ьной инфекции через месяц могло сыфать роковую роль
для «подготовленного» вирусом миокарда, однако о конкретных механизмах
такого взаимодействия мы можем сегодня лишь догадываться. Возможно
и обратное влияние — на фоне тяжелой бактериальной инфекции вирус
Эпштейна—Барр перешел из разряда «свидетелей» к активному состоянию
и «ударил» по миокарду. Пациенту проводилась только антибактериальная
(не противовирусная) терапия, однако ее роль в быстром клиническом
улучшении нам также до конца неизвестна (хотя и представляется весьма
вероятной) — возможно, восстановление сократимости миокарда произо¬
шло лишь благодаря своевременной кардиопульмональной поддержке
(значение которой для спасения жизни пациента невозможно переоценить)
и естественным закономерностям течения процесса.Больному не проводилась ни иммуносупрсссивная (стероиды), ни имму-
номодулируюшая (гамма-глобулин) терапия. Однако неизвестно, каким
было бы решение лечаших врачей в случае менее благоприятного течения
заболевания. Действительно, доказательств эффективности кортикосте¬
роидов и гамма-глобулина, полученных в рандомизированных исследо¬
ваниях, нет и долго еше не будет — в масштабах доказательной медицины
больные с фульминантным миокардитом единичны, причем значительная
их часть все-таки умирает в первые дни заболевания (когда речь идет о
благоприятном прогнозе, имеют в виду тех пациентов, которые пережили
острый период и в дальнейшем не подверглись трансплантации сердца).
Без биопсии миокарда никогда нельзя быть уверенным в том, что у данно¬
го пациента миокардит не является гигантоклеточным или эозинофиль¬
ным, но и при наличии «банального» (тем не менее, фульминантного)
лимфоцитарного миокардита попытки назначения иммуносупрессивной
терапии представляются нам оправданными — во всяком случае вред
такого лечения не доказан, а данные об эффективности, в том числе при
вирусном миокардите, встречаются.Наконец, остается неясным прогноз у представленного пациента и у боль¬
ных, переживших острый фульминантный миокардит, в целом. Работы, в
которых обобшались бы результаты отдаленного наблюдения за такими боль¬
ными, единичны (возможно, ввиду кажущегося благополучия этих пациен¬
тов). В частности, в одной из работ под наб.чюдением авторов находились 15
больных фульминантным миокардитом (8% среди всех больных острым мио¬
кардитом), из них лишь у 6 (40%) отмечено полное восстановление функции
204 Кардиологиямиокарда — 4 больных умерло, 2 подверглось экстренной трансплантации,
еще у 3 отмечено развитие стойкой дисфункции миокарда. При этом в каче¬
стве достоверного фактора неблагоприятного прогноза выступал низкий
уровень тропонина (менее 1,0 нг/мл). Под нашим наблюдением находится
пациентка 26 лет, которая также недавно поступила в отделение реанима¬
ции и интенсивной терапии с клинической картиной тяжелого острого мио¬
кардита (ФВ левого желудочка при поступлении 25%, этиологию процесса
выявить не удалось, антибактериальная терапия ограничилась авелоксом, в
отделении реанимации и интенсивной терапии была начата терапия мети-
предом 16 мг/сут) — несмотря на полное восстановление функции левого
желудочка, у больной сохраняются лабильные зубиы на ЭКГ; кроме того,
через 4 и 6 мес от начала заболевания отмечено повышение титра анти-
кардиальных антител, что яв,чяется основанием для продолжения терапии
метипредом в поддерживающей дозе 4 мг/сут.Эти пациенты нуждаются в наблюдении даже при клинически благопри¬
ятном течении заболевания — мы не знаем, какой процесс запущен в серд¬
це и не придет ли к нам этот больной через 20 лет с развернутой картиной
диыатационной кардиомиопатии. Предстааляется оправданным регулярное
(по крайней мере, через 6-12 мес) определение уровня антикардиальных
антител, регистрация ЭКГ, проведение холтеровского мониторирования и
контрольной ЭхоКГ. К сожалению, стандарт в определении антикардиаль¬
ных антител не отработан — по нашему опыту, наиболее точно совпадает с
клинической и морфологической картиной анализ на антитела к эндокарду,
кардиомиоцитам, проводящей системе и специфический антинуклеарньтй
фактор (с антигеном сердца быка), который выполняется в лаборатории
Федерального научного центра трансплантологии. В качестве скрининга
достаточно удобно использовать также определение IgM и IgG к миокарди¬
альному антигену' (лаборатория «МедБиоСпектр»). У представленного боль¬
ного уровень антикардиальных антител определялся в другой лаборатории,
опьгга работы с которой мы не имеем. На наш взгляд, необходимы повторное
определение уровня антикардиальных антител, а также мониторинг вирусной
инфекции (проведение ПЦР и определение уровня противовирусных антител
в динамике).ЛИТЕРАТУРАПьгяревский C.R Миокардиты: современные подходы к диагностике и лече¬
ние. — М.: Медиа Сфера, 2008. — 328 с.Кривопустов С.Л. Миокардит у детей. Современный взгляд на проблему //
Здоровье Украины. — 2008. — № 10/1. — С. 32—33.Amabile N., Fraisse А., Bouvenot J. et al Outcome of acute fulminant myocarditis
in children // Heart. 2006; 92(9): 1269-1273.FelkerG.M., BoehmerJ.P., HrubanR.H. etal Echocardiographic findings in fulmi¬
nant and acute myocarditis j I J. Am. Coll. Cardiol. 2000; 36: 221-232.
Глава IL Фульминантный миокардит: диагноз, этиология, лечение, прогноз 205FreixaX., Sionis А., Castel А. et ai Low troponin-1 levels on admission are associ¬
ated with worse prognosis in patients with fulminant myocarditis // Transplant Proc.
2009; 41(6): 2234-2236.Gupta S., Markham D.W., Drainer MM., Mammen Р.Л. Fulminant myocarditis.
Nature Clinical Practice // Cardiovascular Medicine. 2008; 11, Vol.5: 693—706.Koga М., Fujiwara М., Ariga S. et at. CD8+ T-lymphocytes infiltrate the myo¬
cardium in fulminant Ьефез virus myocarditis 11 Pediatr. Pathol. Мої. Med. 2001;
20(3):189-195.SeeburgerJ., Doll N., Doll S. et al. Mechanical assist and transplantation for treat¬
ment of giant cell myocarditis // Can J Cardiol. 2010; 26(2):96-97,
Глава 12ОТ «ИДИОПАТИЧЕСКОЙ» МЕРЦАТЕЛЬНОЙ
АРИТМИИ К ПОСТАНОВКЕ НОЗОЛОГИЧЕСКОГО
ДИАГНОЗАО.В. Благова, А.В. Иедоступ, ЕЛ. Коган, В.Л. СулимоеМерцательная аритмия (МА) у молодых пациентов, не имеющих очевидных
органических заболеваний сердца, как правило, расценивается как идиопати-
ческая. Пациентам с мерцательной аритмией старше 50—60 лет также нередко
ставится этот диагноз, если в анамнезе отсутствуют ишемическая болезнь серд¬
ца, артериальная гипертония, пороки сердца, а на ЭКГ и при эхокардиографи¬
ческом исследовании не вьывляются какие-либо существенные отклонения
от нормы. Вместе с тем очевидно, что термин «идиопатическая мерцательная
аритмия» означает лишь нашу неспособность на данном этапе установить ее
причину. Представленное наблюдение и,тлюстрирует положение о том, что за
диагнозом «идиопатическая мерцательная аритмия» нередко кроется нерас¬
познанное, достаточно серьезное и потенциально курабельное поражение
миокарда определенной этиологии. Совокупность минимальных клинических
и лабораторно-инструментальных признаков позволило лишь заподозрить
это поражение и определить показания к проведению эндомиокардиальной
биопсии, которая полностью подтвердила предполагаемый диагноз. Отдельно
обсуждаются вопросы микроваскулярной ишемии миокарда, патогенеза и
лечения трикуспидальной недостаточности после имплантации электрокар¬
диостимулятора (ЭКС).Больная Ч,, 45 лет, поступила в отделение кардиологии Факультетской
терапевтической клиники им. В.Н, Виноградова 01.11.2007 г. с жалобами на
ухудшение общего самоч>ъствия при подъемах АД до 150 и 90—100 мм рт.ст.
(при обычном АД 120 и 70—80 мм рт.ст.), возникающее иногда кратковремен¬
ное ощущение перебоев в работе сердца, некоторое снижение переносимости
значительных физических нагрузок.Из анамнеза жизни известно, что мать больной умерла в 67 лет от инсуль¬
та, страдала артериальной гипертонией, отец умер в 83 года, хроническими
заболеваниями не страдал. Имеет здорового сына 12 лет, живет в полноценной
семье. По образованию врач, в настоящее время работает в отделении функ¬
циональной диагностики. Вредных привычек не имеет. В анамнезе: 3 бере¬
менности, 2 аборта, наблюдается гинекологом по поводу опущения матки
(планируется оперативное вмешательство). В детстве перенесла ветряную оспу,
краснуху; в подростковом возрасте — частые ангины, в 19 лет произведена тон-
зиллэктомия. В дальнейшем неоднократно отмечала высыпания herpes labialis.
Год назад после 12-часового перелета развился острый тендовагинит ахиллова
Глава 12. От «идиопатической» мерцательной аритмии к постановке.,.207сухожилия, проведены курсы терапии витаминами группы В и физиотерапии с
эффектом. Аллергологический анамнез не отягощен.Анамнез заболевания {рис. J2.1). В подростковом возрасте страда-ча частыми
ангинами, во время одной из них появились боли в области сердца, которые не
сопровождшшсь изменениями на ЭКГ. В 19 лет произведена тoнзилJlЭктoмия.
В возрасте 26 лет после физической наїрузки впервые развился приступ уча¬
щенного неритмичного сердцебиения, который купировался самостоятельно
через несколько часов. В последующие 6 лет (до 1994 г) приступы сердце¬
биения рецидивировали раз в 1—1,5 года (на ЭКГ фиксировалась мерцатель¬
ная аритмия), купировались самостоятельно. Частота приступов постепенно
нарастала. В 1992 г. при эхокардиографическом исследоваїши вьіяаіен пролапс
митрального клапана без регурітггации. До 1997 г. пароксизмы мерцательной
аритмии полностью прекратились, однако с этого года возобновились, а с
осени 1998 г. значительно участились (до 1 раза в 1—2 мес), купировались в/в
введением новокаинамида, а также приемом 600 ритмонорма или хинидина.
Постоянная антиаритмическая терапия не назначалась.В декабре 1999 г развился затяжной пароксизм мерцательной аритмии;
начала прием кордарона, который бьш отменен в связи с брадикардией. Бьша
впервые госпитализирована в Факультетскую терапевтическую клинику им,
В.Н, Виноградова, где вновь был назначен кордарон в насыщающей дозе
600 мг/сут. На второй день лечения отмечено восстановление синусового
ритма. Продолжала принимать кордарон в дозе 400 мг/сут, однако в связи с
фотосенсибилизацией он был заменен на сотаїекс.198119992004ЭКС2007новокаинамидхинидинпропафенонЗИТ
нибентанодышкаАВ-блокада
депрессия STМАкупирующая
терапияпостоянная
терапиядигоксинкордаронэтацизиналлапининхинидин
флекаинидРис. 12.1. Анамнез больной Ч., 45 лет. МА — мсрцателы1ая аритмия, ЭКС — электро-
кардиостимулятор, ЗИТ — электроимпульсная терапия
20S КардиологияНа этом фоне в январе 2001 г. развился рецидив мерцательной аритмии,
которая спонтанно не купировалась, сопровождалась появлением небольшой
одышки при физических натрузках. Бьша госпитализирована в Факультетскую
терапевтическую клинику им. В.Н. Виноградова, где после плановой подготов¬
ки кордароном и фенилином произведено две попытки электрической кардио¬
версии, а также попытка устранения аритмии с помощью нибентана без эффек¬
та. Были назначены дигоксин 0,25 мг/сут, паиангин, энап, фенилин через 1 мес
заменен на аспирин-кардио 325 мг. На этом фоне через 7 мес произошло спон¬
танное восстановление синусового ритма, в течение 3-х месяцев отмечались
короткие рецидивы мерцательной аритмии, во время которых возобновляла
прием дигоксина, анаприлина. В дальнейшем возобновлен регулярный прием
кордарона 400 мг/сут, который после развития фoтoccнcибиJ^изauии был заме¬
нен на этадизин 150 мг/сут. До мая 2003 г. аритмия не репидивирова.'іа.Была проконсультирована в отделении хирургического лечения тахиарит¬
мий Научного центра сердечно-сосудистой хирургии им. А.Н. Бакулева про¬
фессором А.Ш. Peeuiuewm, в проведении операции радиочастотной аблации с
изоляцией устьев легочных вен было отказано в связи с низкой вероятностью
хорошего эффекта; определялся повышенный (в 6 раз) уровень антимиокарди-
алъных ангител. Терапия по этому поводу не назначалась. В мае 2003 г. после
сильной физической нагрузки развился очередной эпизод мерцательной арит¬
мии, который спонтанно не купировался. Бьт возобновлен прием дигоксина0,125 мг/сут; сохранялись приступы учащенного неритмичного сердцебиения,
несколько раз возникали предобморочные состояния. При амбулаторном
холтеровском мониторировании ЭКГ отмечались ночные гтаузы до ЗД с. К
терапии был добавлен анаприлин в утреннее и дневное время. В декабре 2003 т.
была повторно госпита^тизирована в Факультетскуто терапевтическ>то клинику
им, В.Н. Винофадова, по данным повторного холтеровского мониторирования
ЭКГ сохранялась тахисистолия днем (средняя ЧСС 100/мин) в сочетании с
ночными паузами до 3,34 с, в связи с чем в июне 2004 г в Городской клиниче¬
ской больнице № 4 г. Москвы был имплантирован постоянный ЭКС в режиме
WI, продолжена урежаюшая ритм терапия. При проведении ЭхоКГ отмечалась
умеренная дилатация обоих предсердий. Кроме того, при холтеровском мони¬
торировании ЭКГ бььта впервые выявлена горизонтальная депрессия сегмента
STдо 0,1 мВ, которая не сопровождалась субъективными симптомами.До конца 2004 г сохранялась мерцательная аритмия, с целью урежсния
желудочкового ритма проводилась терапия дигоксином 0,125—0,25 мг/сут,
при возобновлении ощущения учащенного сердцебиения (преимушественно
по утрам) дополнительно принимала атенолол 12,5—25 мг с хорошим субъек-
тивньтм эффектом, кроме того, регулярно принимала аспирин-кардио 325 мг
Однако в конце 2004 г. было вновь отмечено спонтанное восстановление сину¬
сового ритма, в связи с чем возобновили попытки профилактической анти-
аритмической терапии (с отменой дигоксина и заменой аспирина-кардио на
тромбо-АСС 100 мг): этапизин 150 мг/сут (на лом фоне отмечались эпизоды
мерцательной аритмии, которые дли^тись до нескольких дней и самостоятельно
кзшировались), этацизин 25 мг 3 раза в день в сочетании с кордароном 100 мг
Глава 12. От «идиопатической» мерцательной аритмии к постановке... 209З раза в день (весной в связи с развитием фотодерматита комбинация отмене¬
на), хинидин-дурулес 600 мг/сут в сочетании с атенололом (эпизоды мерца¬
тельной аритмии рецидивировали, субъективная переносттмость терапии была
не очень хорошей), аллапинин с атенололом (отменены в связи с плохой пере¬
носимостью). С лета 2005 г. была начата терапия тамбокором (флскаинидом)
200-250 мг/сут, на фоне которой короткий пароксизм мерцательной аритмии
развился однократно; переносимость терапии была хорошей.Через год (летом 2006 г.) в связи с временным отсутствием у больной тамбо-
кора она была переведена на прием этацизина 150 мг/сут. Повторно в лабора¬
тории «МедБиоСпектр» (канд. мед. наук Г.Н, Чувиров) проведены иммуноло-
пгческие анализы крови, которые выявили 4-кратное повьпиение уровня IgG к
\гаокарду, сірсптококкам, вирусам герпетической фуппы. Бьита начата терапия
плаквенилом 0,2 мг/сут, проведен курс противовирусной терапии (ва^ітрекс,
амиксин); через полгода титры антител к миокарду и стрептококкам оставались
повышенными, в связи с чем курс приема плаквенила был продлен до года,
отмечала хороший субъективный эффект аг данной терапии (исчезновение
предвестников развития мерцательной аритмии при нафузке в виде перебоев);
при посеве из зева роста микрофлоры не получено, поэтому санация не прово-
дкіась. В течение всего периода лечения и до настоящего времени мерцатель¬
ная аритмия не рецидивирова,'іа. Последний контроль работы ЭКС в 2007 г. —
желудочковая стимуляция составляла 7% от общего числа сокращений.В последние месяцы стала отмечать некоторое повьшіение утомляемости.
В октябре 2007 г в рамках обследования для подтверждения инвалидности было
рекомендовано проведение федмил-теста. Во время вьшолнения нагрузки и в
восстановительном периоде зафиксирована горизонтальная депрессия cenvfewra
ST от 1 до 2 мм в отведениях с по V^; максимальное АД сосгавило 200 и 100 мм
рт.ст В последующем при однократных измерениях АД достигало 150 и 100 мм
рт.ст (при обычном АД 120 и 70 мм рт.ст). Пекл упила в Факультетскую терапевти¬
ческую клинику им. В.Н. Винофадова для обследования и коррекции терапии.Оценивая анамнез (см. рис. 12.7), в котором отражены особенности течения
мерцательной аритмии, необходимо отметить неудобство принятого с 2001 г.
разделения мерцательной аритмии на пароксизмальную, персистируюшую и
постояішую: у нашей больной сочетаются самые различные варианты, причем
затяжные эпизоды мерцательной аритмии не могут быть, согласно принятой
классификации, расценены ни как постоянная форма (поскольку ритм спон¬
танно восстанавливается), ни как персистируюшая (поскольку спонтанному
восстановлению ритма предшествовали две неэффективные попытки электри¬
ческой кардиоверсии). Мы условно назвсыи мерцательную аритмию у больной
персистируюшей, однако удовлетворения от этого термина не испытываем.При поступлении состояние больной расценивалось как относительно удо¬
влетворительное. Кожные покровы нормальной окраски и влажности, отеков
нет. ЧД 17 в минуту, дыхание везикулярное, хрипов нет. ЧСС 65 уд/мин, ритм
правильный, тоны сохранены, выслушивается систолический шум над мече¬
видным отростком. АД 150 и 100 мм рт.ст, пульс ненапряженный. Живот мяг¬
кий, безболезненный во всех отделах, псчеиь и селезенка не увеличены.
2 JO КардиологияВ общем анализе крови без отклонений от лормы |НЬ 139,1 г/л, эритроциты
4,6 млн, цветовой показатель 0,9, лейкоциты 7,7 тыс., лейкоцитарная формула
в пределах нормы (лимфоциты 22%, нейтрофилы 70, моноциты 4%, эозинофи-
лы 4%), тромбоциты 262 тыс., СОЭ 3 мм/ч].В биохимическом анализе — незначительное повышение МВ-КФК до 22 ед/л
(при норме до 20) и азота мочевины до 22 мг/дл (при норме до 20), в остальном
в пределах нормы [об. белок 73,9 г/л, альб. 4,4 г%, креатинин 1,0 мг%, мочевая
кислота 4,2 мг%, глюкоза 87 мг%, об. билирубин 9,0 мкмоль/л, ACT 19 ед/л,
АЛТ 30 ед/л, гамма-ГТ 29 ед/л, ШФ 56 ед/л, ЛДГ 333 ед/л, КФК 136 ед/л
(норма до 174), натрий 144 ммоль/л, калий 5,1 ммоль/л]. Нормаїьньї показа¬
тели липидного спектра (триглицериды 55 мг/дл, обш. холестерин 185 мг/дл,
ЛВП 44 мг/дл, ЛНП ] 30 мг/д.'і, ЛОНП 11 мг/дл, КА 3,2), хотя в анамнезе одно¬
кратно бьіла выявлена умеренная гиперлип идемия, после чего больная начала
соблюдение диеты.Элек'грофорез белков без существенных отклонений от нормы (альбу¬
мины 65,2%, а-1-глобулины 3,4% при норме от 3,7%, a-2-глобулины 6,2%,
(3-глобулины 9,9%, у-глобулины 15,3%).Коагулограмма; фибриноген 2,49, АЧТВ 1,08 ед.Гормоны щитовидной железы: (сумм.) 1,21 нмоль/л (норма 1,0-3,0),(св.) 13,4 пмояь/л (10,0-25,0). ТТГ 4,06 МЕ/л (0,17-4,05), антитела к тирео-
пероксидазе 19,0 МЕ/мл (норма до 30).HBsAg, HCVAb, реакция Вассермана, антитела к ВИЧ отрицательны.С учетом выявления повышенных титров антител к миокарду (в анамнезе)
был проведен подробный иммунологический анализ крови; антитела к натив¬
ной ДНК, АНФ, СРВ, анти-О-стреитолизии отрицательны. Иммуноглобулины
крови: А — 128 мг/дл, М — 105 мг/дл, G — 1250 мг/лл- Антитела к кардиолипи-
ну класса IgM 2,38 МЕ/мл (норма 0—7), класса IgG 2,98 МЕ/мл (норма 0-10).
Обратило на себя внимание снижение уровня комплемента до 16,1 гем. ед.
(норма 20—40), которое обычно отражает активное образование циркулирую¬
щих иммунных комплексов.В табл. 12.1 представлены peayjfbTaTbi определения антител к миокарду, кар-
диотропным вирусам и стрептококку (лаборатория «МедБиоСпектр»), а также
естественных антител (лаборатория «Иммункулус») к различным антигенам
миокарда в период с июля 2006 г. по ноябрь 2007 т. Повышение титров было
выявлено при первом обследовании, в результате противовирусного лечения и
терапии плаквеншюм отмечено снижение всех титров, в настоящее же время
(почти через полгода после отмены плаквснила) вновь отмечено повышение
титров антител к лшокарду, стрептококкам и кардиотропным вирусам.В общем анализе мочи pH 5, уд. вес 1016, прозрачность неполная, белка, саха¬
ра, ацетона, желчных пигментов нет, уробилин в пределах нормы, лейкоциты001 в п/зр., эритроциты един, в препарате, оксалатов немного, слизь в умерен¬
ном количестве, бактерий немного.На ЭКГ на момент поступления — синусовый ритм, электрическая ось
сердца расположена полувертикально, ЧСС 62/мин. АВ-блокада 1 степени {PQ0,24 с). Признаков ишемии, гипертрофии различных отделов сердца нет. Зубец
Глава 12. От «идиопатической» мерцательной аритмии к постановке...211Таблица 12.1Серодиагностика миокардита у больной Ч. ЦМВ — цитомегаловирус,ВПГ — вирус простого герпеса, АТ — антителаПоказатель6.07.06 г.13.02.07 г.12.09.07 г.29.11.07 г.НормаIgG к миокарду1:4001:2001:2001:300<1:100IgG к Streptococcus (гиа-
луронидаза) 1:4001:3001:2001:400<1:100IgG к ЦМВ3,02Л1,7<1 отр. >5 пол.IgG к ВПГ-10,12,1<1,2IgG к ВЭБобнар.обнар.нетАнтитела к цитоплазма¬
тическому белку CoS-
05-40-40-677-30...+20Антитела к мембранно¬
му белку СоМ-015-1569-66-20-11-30...+20Антитела к
р-адренорецепторам45-58-218-30...+20Антитела к
NO-синтетазе28-28-15-8-30...+20Р уплощен, длительность 0,06 с, продолжительность комплекса QRS =0,1 с,
длительность интервала QT = 404 мс, длительность корригированиого интер¬
вала QT= 410 мс.Во время тредмил-тестау который стал непосредственным поводом к
последней госпитализации, максимальная мощность нагрузки составила 5,6
(75 Вт). ЧСС 83-123/мин, АД 140/100— 200/100 мм рт.ст. Причина прекра¬
щения нагрузки — изменения на ЭКГ (при нагрузке и в восстановительном
периоде — горизонтальная депрессия сегмента ST в отведениях с по до
2 мм, рис. 12.2). На остановке — одышка. Толерантность к нагрузке средняя.
Тип реакции сердечно-сосудистой системы на нагрузку — гипертонический.
Восстановление показателей гемодинамики к 9-й минуте (неполное восста¬
новление АД), Проба положительная.По данньил ЭхоКГ, полость левого желудочка 5,2 см (норма до 5,5 см),
КДО 132 мл, КСО 35 мл, ФВ .тевого желудочка 73%, тМЖП 0,9 см, тЗС 0,8 см.
Нарушений обшей и локальной сократимости нет. Диастолическая функция
не изменена (Е/А 1,22). Правый желудочек 2,5 см (норма до 2,6 см), тПЖ
0,46 см (норма до 0,5). Левое предсердие 42 \li, правое 35 мл (норма, однако
в анамнезе выявлялось увеличение линейных размеров обоих предсердий).
Межжелудочковая перегородка без особенностей. Митральный и аортальный
клапаны не изменены, митральная регургитация 1 степени. Трикуспидальная
регургитапия Н—III степени. Систолическое давление в легочной артерии
30 мм рт.ст. (норма до 25). Клапан легочной артерии не изменен. Стенки аорты
не изменены. Жидкости в полости перикарда нет.Было выявлено значительно нарастание трикуспидальной недостаточности
по сравнению с исследованиями от 2004—2006 г. (регургитация не превышала
212Кардиология7Г4 lQoutt/пУ
40aeyMJ 4<buip<MUSF(a«)-0.T ' - ' ■-».1 -«.2я П H■^2 -0Л-3.4 -LSJit U) «}S3 ^-1.6’jii»—Рис. 12*2. Изменения ЭКГ у больной Ч. во время проведетїия тредмил-теста на высоте
нагрузки (пояснения в тексте)I степени). В качестве наиболее вероятной причины этого рассматривалось
нар>чиение положения электрода ЭКС в правых камерах сердца, в связи с чем
профессором В.П. Седовым было проведено прицельное эхокардиографиче¬
ское исследование: лоцируется электрод стимулятора в правых отделах сердца,
который двигается синхронно с септальной створкой трикуспидального клапа¬
на (спаяние со створкой).Сцинтиграфия миокарда, проведение которой планировшіось для подтверж¬
дения ишемии миокарда, не была выполнена по техническим причинам. Для
уточнения состояния левого предсердия (в анамнезе выявлялось умеренное
увеличение обоих предсердий, в том числе на синусовом ритме, которое не под¬
твердилось в ходе данной госпитализации) была выполнена компьютерная томо¬
графия с контрастированием (в НЦССХ им. А.Н. Бакулева): сердце не увеличено
в размерах (кардиоторакальный индекс 49%), перикард не изменен, жидкость в
его полости не визуализируется. Контрастирование левого предсердия и его ушка
равномерное, без дефектов; левое предсердие умеренно увеличено в размерах: кра-
ниокаудалънътй размер 67 мм, передне-задний 36 кгм, медиолатеральный 67 мм,
объем с учетом ушка 109 мл (норма 68Л±14,8 мл), индекс объема 60,6 мл/м^ (норма
34,4±6,6 мл/м“). Легочные вены имеют типичный ход и несколько увеличенные
диаметры: правая верхняя легочная вена 21 мм (норма 1б,0±0,9 мм); правая ниж¬
няя легочная вена 19 мм (норма 15,7+0,7 мм), левая верхняя легочная вена 21 мм
(норма 16,2+1,1 мм), левая нижняя легочная вена 17 мм (норма 14,7±1,2 ші).При рентгенографии органов грудной клетки и УЗИ щитовидной железы
ОТК.ТОНЄНИЙ от нормы не выявлено. По данным УЗИ органов брюшной полости
в обеих почках — мелкие гиперэхогенные включения до 2,0—2,1 мм (солевые
депозиты), в остальном без отклонений от нормы.
Глава 12. От «идиопатической» мерцательной аритмии к постановке... 2ІЗTajKiiM образом, неинвазивное обследование было завершено, и полшмо вопро¬
са о том, как классифицировать мерцательную аритмию, вставал вопрос о ее
этиологии. У больной отсутствуют какие-либо очевидные причины мерцательной
аритмии, которая впервые развилась в 26 лет и уже тогда расценивалась как идио-
патическая. Тем не менее диагноз «идиопатическая мерцательная аритмия» явля¬
ется диагнозом исключения и, можно сказать, диагнозом «отчаяния», и даже при
исключении более или менее частых причин развития мерцательной аритмии сле¬
дует иметь в виду следующие, гораздо менее очевидные состояния, которые могут
лежать в основе так называемой идиопатической (lone) мерцательной аритмии.1. Миокардит, в том числе очаговый миокардит предсердий, который чрез¬
вычайно трудно диагностировать. Если пользоваться критериями NYHA, кото¬
рые предложены для выявления острого миокардита (см. табл. 10. J), то оче¬
видно, что нашей больной такой диагноз поставлен быть не может. Однако еще
раз подчеркнем, что данньте критерии касаются только острого миокардита,
имеющего яркие клинические проявления. Как же диагностировать миокардит
хронического течения, который проявляется главным образом наруптениями
ритма и/или проводимости? Международных рекомендаций на этот счет не
сушествует, однако отечественными авторами (М.В. Дерюгин, С.А. Бойцов,
М.В. Носкова и др.) предложен целый ряд критериев, совокупное обнаружение
которык существенно помогает в диагностике именно хронического миокар¬
дита. К важным диагностическим признакам относят:— связь дебюта аритмии с перенесенной инфекцией;— выявление диагностически значимого титра специфических антимио-
кардиальных антител (IgG >1:200) и антител к кардиотропным вирусам,
стрептококку, хламидиям (?);— признаки многоуровневого поражения проводящей системы;— гиперсимпатикотонию в ночное время;— умеренную дилатацию предсердий или желудочков;— снижение ФВ левого желудочка;— субклиническую (до II степени) клапанную регургитацию;— уплотнение, утолщение, сепарацию листков перикарда;— наличие зон фиброзной ткани в миокарде желудочков (МРТ,
УЗ-денситометрия);— диффузное или лока.тьное истончение стенки левого или правого желу¬
дочка;— зоны гипоперфузии ьшокарда и зоны накопления аутолейкоцитов,
меченых ^'^Тс-ГМПАО (гсксаметилпропиленаминооксим, препарат
«Ceretec») в покое (сцинтиграфия); данная методика выполняегся на
сегодня только в Санкт-Петербурге, поэтому не могла быть нами при¬
менена, как и МРТ (в связи с наличием у больной постоянного ЭКС).2. Постмиокардитический кардиосклероз — состояние, которое отличается
от хронического миокардита лишь отсутствием повышенных титров антител
к миокарду и очагов накопления аутолейкоцитов и диагностируется с еще
большим трудом (нередко без должны?^ оснований, как диагноз исключения у
относительно молодых больных с нарушениями ритма).
214 Кардиология3. Генетические дефекты, для которых более или менее доказана связь с
развитием «идиопатической» мерцательной аритмии, можно до некоторой
степени условно относить к нозологиям; тем не менее ряд таких дефектов
сопровождается совершенно определенной клинической картиной и позво¬
ляет ставить нозологический диагноз. В первую очередь это хорошо извест¬
ный синдром Бругады, который обусловлен дефектом натриевых каналов
SCN5A. Мерцательная аритмия встречается примерно у 20% больных, связана
с замедлением внутрипредсердного проведения и всегда сочетается с более
типичными проявлениями синдрома Бругады — пароксизмами мономорфной
или полиморфной желудочковой тахикардии типа torsades depointes и/или эпи¬
зодами внезапной смерти, блокадой правой ножки пучка Гиса и преходяшим
подъемом сегмента ST в правых грудных отведениях. В реализации генетиче¬
ского дефекта играет роль вирусная инфекция.Той же группой авторов под руководством Р. Bragada описаны синдром укоро¬
ченного интервала QT (дефект гена быстрых калиевых каналов прі-шодит к уко¬
рочению потенциата действия предсердий и желудочков, что клинически про¬
является пароксизмами мерцательной аритмии, трепетания предсердий и/или
желудочковой тахикардии) и так назьгеаемая семейная мерцательная аритмия,
также связанная с дефектом гена белка калиевых каналов (предполагается также
роль дефекта гена р-адренорецептора). Характер наследования аутосомньгй,
заболевают преимущественно женщины молодого возраста (до 40 лет), первый
приступ мерцательной аритмии возникает в возрасте от 2 до 50 лет. Клинически
мерцательная аритмия носит характер «идиопатической», хотя сходный генный
дефект может быть выявлен у больных гипертрофической кардиомиопатией,
страдающих мерцательной аритмией. Описан целый ряд дефектов генов калие¬
вых каналов (KCNE4, KCNE1, KCNQ1, KCNA5), которые могут быть ответствен¬
ны за развитие мерцательной аритмии у больных без семейного анамнеза.В последнее время в развитии «идиопатической» мерцательной аритмии
большое значение придается также дефектам гена коннексина-40, который
«отвечает» за внутрипредсердное проведение.Описано сочетание дефекта гена коннесина-40 и гена натриевых каналов
SCN5A, которое в номенклатуре генетических заболеваний получило название
предсердной кардиомиопатии с нарушением проводимости. По клинической
картине данное заболевание отличается от изолированной мерцательной
аритмии, поскольку включает постепенное развитие полного механического и
электрического паралича правого предсердия. Однако на ранних этапах, когда
нарушения проводимости еще не столь выражены, заболевание легко спутать с
«обьпшой» дилатацией предсердий, которая неоднократно описана у больных
с мерцательной аритмией.4. В качестве причины «идиопатической» мерцательной аритмии в реко¬
мендациях 2006 г. впервые назван синдром сонного апноэ: патогенетическими
механизмами развития мерцательной аритмии являются легочная и системная
гипертензия, гипоксия, симпатикотония.5. Следует упомянуть и о таких трудно и редко диагностируемых причинах
«идиопатической» мерцательной аритмии, как изолированный предсердный
Глава 12. От «идиопатической» мерцательной аритмии к постановке... 215амилоидоз и липоматозная гипертрофия межпредсердной перегородки. Оба
заболевания поражают преимущественно пожилых людей, липоматозная
гипертрофия диагностируется чаше у женпшн, страдающих ожирением; харак¬
терно сочетание мерцательной аритмии с синдромом слабости синусового узла
и/и,чи АВ-блокадами.Далее речь пойдет о так клинических подтипах больных с «идио¬патической» мерцательной аритмией — это подгруппы больных с определен¬
ными клиническими особенностями аритмии, которые НС могут пока рассма¬
триваться как определенная нозология.Хорошо известно выделение Филиппом Кумелем ваготонического и симпа-
тикотонического клинических вариантов мерцательной аритмии. Их нозоло¬
гическая принадлежность остается неясной, как не вполне ясен и механизм
реализации влияния вегетативной нервной системы на сердечный ритм. Здесь
можно приводить много интересных фактов, которые нередко противоречат
друг другу: например, неоднократно показано возрастание активности как
симпатического, так и парасимпатического звена непосредственно перед
пароксизмом мерцательной аритмии, причем нередко у одного и того же
больного. Среди больных с «идиопатической» мерцательной аритмией преоб¬
ладают ваготоники (63,5%); у больных же с органическим заболеванием сердца
пароксизму мерцательной аритмии чаще предпіествует повышение активности
симпатического звена (67,2%).Необходимо упомянуть и данные С.С. Васюкова, А.В. Недоступа,
В.И. Федоровой и С.А. Гордеева о том, что развитию пароксизма мерцательной
аритмии у больных с пароксизмальной мерцательной аритмией, не имеющих
фубых органических заболеваний сердца или центральной нервной системы, а
также панических атак, предшествует примерно за сутки сочетанное повыше¬
ние активности а-, р- и 0-ритмов, что у-кладывается в представления о «парок¬
сизмальном мозге». И снова встает вопрос о нозологии.В связи с этим необходимо упомянуть данные генетика-аритмолога
Е.В, Заклязьминской о том, что белки натриевых каналов не являются строго
специфичным!^! ДЛЯ ссрдца: по меньшей мере 4 из 9 а-субъединиц экспресси¬
руются как в миокарде, так и в центральной нервной системе, так же как и все
известные р-субъединицы. Авгор подчеркивает, ^гго мутации в соответствующих
генах будут приводить к одновременной патологии сердца и мозга, и интерпрета¬
ция эпизодов «эпилепсии» или «повьшієііпой судорожной готовности» у больных
с первичными аритмиям!! может быть неправильной: эти больные моїуг иметь
и то, и другое. Е.В. Заклязъминская приводит собственные данные о 4 больных
(31%) с мутацией в гене натриевых каналов SCN5A, у которых имелись судороги,
повышенная судорожная готовность на электроэнцефалограмме или повышен¬
ная эмоциональная лабильность, потребовавшая медикаментозного лечения.Новосибирский хирург Е.А, Покушалов разрабатывает предложенную
К.Паппоне методику радиочастотной аблации (РЧА) симпатических гангли¬
ев в левом предсердии, которая приводит к повышению парасимпатических
влияний на сердце и в то же время оказывается достаточно эффективной у
широкого круга больных с пароксизмальной мерцательной аритмией. Только
216 Кардиологияли в устранении симпатикотонии дело? Недавно показано, что существует пря¬
мой холинергический противовоспалительный путь: стимуляция блуждающего
нерва блокирует выделение целого ряда провоспалительных цитокинов (в част¬
ности, ФНО) и защищает клетки от повреждающего действия эндотоксинов и
реперфузии.После внедрения в 1998 г методики интервенционного лечения мерца¬
тельной аритмии с помощью радиочастотной аблации устьев легочных вен
хирургами было вьшвинуто положение о так называемой эктопической форме
мерцательной аритмии, при которой основную роль в ее запуске ифает непре¬
рывная частая импульсаиия из мышечных муфт в устьях легочных вен (при
этом предсердїія, как правило, не изменены и выполняют роль пассивного
субстрата, поддерживающего процесс microreentry). Клинически эта форма
характеризуется частыми непрерывно рецидивирующими, устойчивыми к
терапии пароксизмами, которым предществует частая ранняя («Р на Т») надже-
лудо^іковая экстрасистолия. Делаются попытки установить, ^гго лежит в основе
патологической импульсации — в мышечных муфтах больных с мерцательной
аритмией были выделены псйсмейкерные к,1стки, что является, по-видимому,
аномалией формирования сердца в период эмбриогенеза. Пока это тоже не
нозология, хотя у таких больных отмечаются и макроаномсити в строении легоч¬
ных вен — общий коллектор двух вен, широкий вестибюль. Эти структурные
аномалии предлагается рассматривать в качестве самостоятельной причины
мерцательной аритмии.Еще менее понятна нозологическая принадлежность многочисленных
электрофизиологических изменений в предсердиях, которые выявляются у
больных с «идиопатической» мерцательной аритмией (повышенная дисперсия
рефрактерною периода предсердий, снижение скорости предсердного прове¬
дения, уязвимость предсердий, те. возникновение пароксизма мерцательной
аритмии длительностью более 23 с в ответ на один или несколько предсердных
экстрастимулов, неспособность предсердий адаптировать рефрактерный пери¬
од к изменению частоты ритма, отсутствие супернормального предсердного
проведения). Они говорят лишь о том, что сердце больных с мерцательной
аритмией никогда, по-видимому, нельзя считать здоровым.Значительная часть больных с идиопатической мерцательной аритмией
имеет изолированную дилатацию одного или обоих предсердий, при этом не уда¬
ется выявить других (даже минимальных) признаков хронического миокар¬
дита. В рекомендациях 2006 г. «идиопатическая» атриомегалия сама по себе
была впервые отнесена к этиологическим факторам мерцательной аритмии.
Показано, что даже при отсутствии атриомегалии размеры левого предсердия
(линейный размер и объем в расчете на единицу поверхности тела) у больных
с идиопатической мерцательной аритмией достоверно больше, чем в группе
контроля, независимо от числа приступов мерцательной аритмии в анамнезе,
т.с. и у больных с впервые возникшей мерцательной аритмией тоже. Кроме
того, причиной идиопатической мерцательной аритмии может оказаться пер¬
вичное расширение кольца митрального клапана без зна^гительной митральной
регургитации. Хорошо известно, что и са.ма мерцательная аритмия (в том числе
Глава 12. От «идиопатической» мерцательной аритмии к постановке.,, 217пароксизмштьная) имеет патогенетическое значение в развитии ди^чатации
левого предсердия. Тем не менее в качестве наиболее вероятной прт^чины изо¬
лированной атриомегалии у больных с мерцательной аритмией рассматрива¬
ют локальный миокардит. Ряд генетических синдромов, о которых шла речь,
также может приводить к дилатации предсердий.Наконец, этиопатогенетическая связь «идиопатической» мерцательной
аритмии с такими состояниями, как синдром мезенхимальной дисплазии, вос¬
палительная и дисгормональная миокардиодистрофия, остается неясной, хотя
клинически такие сочетания хорошо известны.Какие из перечисленных заболеваний и патогенетических факторов могли
обсуждаться у данной бо;и>ной? Надо сказать, ^гго с самого начала нам ірудно
было расценить ее мерцательную аритмию как идиопагическую, несмотря на
очень ранний возраст начала аритмии — 26 лет. У больной отсутствовали семей¬
ный анамнез аритмии, проявления ваготонии (и связь эпизодов мерцательной
аритмии с развитием брадикардии), как не было и отчетливой симпатикотоиии
(несмотря на связь большинства эпизодов мерцательной аритмии с физической
нагрузкой). Отсутствовали клинические признаки «эктопической» мерцатель¬
ной аритмии (именно поэтому ей и было отказано в проведении радиочастот¬
ной аблации устьев легочных вен в 2004 г., когда «эктопическая» мерцательная
арит-мия являлась единственным безусловным показанием к этой операции).
В то же время в анамнезе у больной имелись ангины, во время одной из кото¬
рых появились боли в области сердца; в дальнейшем неоднократно отмечштись
герпетические высыпания на губах (последнее во время настоящей госпитали¬
зации); очень важным представл^ьюсь сочетание мерцательной аритмии с про¬
грессирующей АВ-блокадой и умеренным, но достаточно стабильным увеличе¬
нием обоих предсердий (оно сохранялось и в периоды синусового ритма).На первых этапах это позволило рассматривать в качестве при^гины мерца¬
тельной аритмии постмиокардитический кардиосклероз, однако прогресси¬
рование заболевания (нарастание АВ-блокады и утяжеление течения мерца¬
тельной аритмии без видимых оснований), наличие ишемических изменений
сегмента ST при невысокой вероятности коронарного атеросклероза в соче¬
тании с неоднократно подтвержденным в разных лабораториях повышени¬
ем титра аитимиокардиальньгх, противовирусных и протиБОСтрептококко-
вых антител и хороший субъективный и антиаритмический эффект терапии
плаквснилом позволили нам пересмотреть диагноз в пользу хронического
инфекционно-иммунного миокардита и принять решение о проведении коро-
нарографии в сочетании с эндомиокардиальной биопсией. Планироватось
также генетическое исследование.07.11.2007 Е больной бьь'ш вьптолнена коронароангиография в сочетании с эндо-
миокардиа.1ьной биопсией (проф. В.А. Сулимов, д-р мед. наук М.В. Пурецкий)
5 участков правого желудо^пса (при установке биотома вблизи межжелудочковой
перегородки отмечено ПОЯВЛЄІШС частой желудочковой экстрасистолии, в связи с
чем от биопсии данного участка решено было юздержаться).Во время установки проводника д-тя биотома у больной отмечено раз¬
витие мерцательной аритмии, которую не удалось купировать введением
218 Кардиологияновокаинамида и кордарона; от иопытки электрической кардиоверсии больная
отказалась (ввиду ее неэффективности в анамнезе). Была начата урежаюшая
терапия дигоксином 0,25 мг/сут в сочетании с малыми дозами метопролола
(12,5—25 мг/сут), в первые дни терапии проведено холтеровское мониторирование
ЭКГ в течение суток: мерцательная аритмия. Работа ЭКС в режиме WT с мини¬
мальной ЧСС 60/мин — 33% от общего количества QRS. ЧСС днем 60-152/мин
(ср. ЧСС 87/мин), ЧСС ночью 60-82/мин (ср. 60/мин). Желудочковых экстра¬
систол 79, 1 куплет. При физической нагрузке с ЧСС 150/мин горизонтальная
депрессия сегмента і'Т'до 0,1 мВ.При коронароангиографии значимых изменений сосудов не выявлено: сба¬
лансированный тип кровоснабжения сердца, ствол левой коронарной артерии
не изменен. Передняя межжелудочковая артерия в проксимальном сегменте
имеет неровности контуров, далее не изменена. Огибающая и правая коронар¬
ная артерия не изменены.Результаты эндомиокардиальной биопсии будут предстаатены по каждому
участку отдельно.1. Субэндокардиальный участок свободной стенки правого желудочка:
кусочек не ориентирован. Кардиомиоциты неравномерно птертрофиро-
ваны, местами с исчезновением поперечной исчсрченности; ядра сохране¬
ны. Интерстиций неравномерно расширен, содержит лимфогистиодитарную
инфильтрацию (более 14 лимфоцитов в поле зрения при большом увеличении)
и продуктивные капилляриты с пролиферацией эндотелиальных клеток, сте-
нозированием просвета и периваскулярными лимфогистиоиитарными эле¬
ментами {рис. 12.3, см. цветную вклейку). В одном из кархшомиоцитов выявлен
лимфоцит (внутриклеточно). При окраске по Ван Гизону слабо выраженный
склероз интерстиция.2. Субэндокардиальный участок верхушки правого желудочка; кусочек не
ориентирован, Кардиомиоциты неравномерно гипертрофированы, местами с
исчезновением поперечной исчсрченности; ядра сохранены. При окраске по
Ван Гизону^ склероз интерстиция (рис. 12.4, см. цветную вклейку). Интерстиций
неравномерно расширен, содержит очаг липоматоза и единичные лимфо-
гистиоцитарные элементы (рис. 12.5, см. цветную вклейку). Микрососуды
со склерозированными стенками с пролиферацией эндотелиатьных клеток,
стенозированием просвета и периваскулярными лимфогистиоиитарными эле¬
ментами; продуктивные капилляриты, В целом изменения в данном участке
более «старые» по сравнению с предыдуш;им — менее выражена инфильтрация,
более выражен склероз, имеется участок липоматоза.3. Субэндокардиальньте у^іастки свободной стенки правого желудочка: два
кусочка, не ориентированы. Кардиомиопигьт неравномерно гипертрофирова¬
ны, местами с исчезновением поперечной исчерченности вплоть до некроза
отдельных кардиомиоцитов с гомогенизацией цитоплазмы и кариолизисом
{рис. 12,6—12.8, см. цветную вклейку). Интерстиций неравномерно расширен,
содержит лимфогистионитарные элементы (более 14 лимфоцитов в поле зре¬
ния при большом увелртчении). Микрососуды со склерозированными стен¬
ками с пролиферацией эндотелиальных клеток, стенозированием просвета
Глава 12. От «идиопатической» мерцательной аритмии к постановке... 219и периваскулярными лимфогистиоцитарньтми элементами, продуктивные
капилляриты. При окраске по Ван Гизону склероз интерстипия. В данном
фрагменте активность воспаления наиболее выражена (наряду с лимфо-гисти-
оцитарной инфильтраяией выявлены некрозы кардиомиоиитов).4. Субэндокардиальный участок базальнььх отделов правого желудочка.
Эндокард незначительно утолщен, склерозирован {рис. 12.9, см. цветную вклей¬
ку), что отражает его вовлечение в воспалительный процесс и может отчасти
объяснить спаяние электрода стимулятора со створкой трехстворчатого клапа¬
на. Кардиомиоииты неравномерно гипертрофированы, местами с исчезновени¬
ем поперечной исчерченности. Интерстиций неравномерно расширен, содер¬
жит лимфогистиоцитарньте элементы (более 14 лимфоцитов в поле зрения при
большом увеличении). Микрососуды со склерозированными стенками с про¬
лиферацией эндотелиальных клеток, стенозированием просвета и периваску¬
лярными лимфогистиоцитарными элементами — продуктивные капилляриты,
наиболее выраженные именно в субэндокардиальных отделах (рис. 12.10, 12.11,
см. цветную вклейку). При окраске по Ван Гизону — склероз интерстиция.Общее заключение по эндомиокардиальной биопсии (профессор кафедры
патологической анатомии Е.А. Коган): межуточный миокардит с признака¬
ми активности воспаления, продуктивными васкулитами сосудов Тебезия и
продуктивными капил,1яритами, с неравномерной гипертрофией и дистро¬
фическими изменениями кардиомиоцитов вплоть до некроза отдельных кар-
диомиоцитов в области верхушки правого желудочка, очаговый липоматоз и
склероз интерстиция.Таким образом, согласно далласским критериям, у больной выявлен активный
\шокардит. Методом ПЦР геном (ДНК) вирусов простого герпеса 1, 2, 6 типов,
цитомегаловируса, вируса Эпштейна—Барр в ткани биоптата не обнаружено
(лаборатория «Литех»),Морфологическая диагностика мнокарілита (далласские критерии)— Острый (активный) миокардит:♦ инфильтрат (диффузный или локальный);♦ количественный подсчет иммуногистохимическим методом: не
менее 14 инфильтрирующих лимфоцитов на 1 мм- (главным обра¬
зом Т-лимфоциты (CD45) или активированные Т-лимфоциты) и до4 макрофагов;♦ некроз или дегенерация;♦ учитывается фиброз (на-тичие его необязательно).— Хронический миокардит:♦ инфильтрат (не менее 14 лимфоцгггов на 1 мм^ и до 4 макрофагов);♦ некроз и дегенерация обычно не выражены;♦ учитывается фиброз.— Отсутствие миокардита: инфильтрирующих клеток нет или их количе¬
ство менее 14 на 1 мм^Всем критериям может сопутствовать или не сопутствовать фиброз.Окончательный диагноз сформулирован следующим образом: хрониче¬
ский активный инфекционно-иммунный миокардит с нарушениями ритма
220 Кардиологияи проводимости сердца; персистирующая форма мерцательной аритмии,
имплантация постоянного ЭКС в режиме W1 в 2004 г. по поводу атриовен¬
трикулярной блокады (паузы более 3,3 с). Спаяние электрода стимулятора с
септальной створкой трикуспидального клапана. Трикуспидальная недостаточ¬
ность II—ЦТ степени. Гипертоническая болезнь I стадии (2 степень повышения
АД, риск 2). Недостаточность кровообращения Т стадии, I функциональный
класс NYHA.В настоящий момент проводится терапия плаквенилом 0,2 по 2 таб. на ночь,
дигоксином 0,25 мг по Уз таб. утром, метопрололом 50 ш по Уз таб. утром (непо¬
стоянно), тромбо-АССом 100 мг по I таб. вечером, престариумом 4 мг по 1 таб.
утром. Шанируется назначение преднизолона.Каковы результаты эндомиокар^шальной биопсии у больных с нарушениями
ритма и проводимости по данным мировой литературы? Надо сказать, что по
сей день таких работ явно недостаточно — в рекомендациях по проведению
биопсии от октября 2007 г. подробная аннотация всех работ уместилась в одной
небольшой таблице, причем количество больных в каждой из работ колеблется
от 10 до 53 (в среднем 23 больных). Мы остановимся на важнейших из этих
работ.Результаты эндомиокардиальной биопсии у больных с «идиопатической» мер¬
цательной аритмией, устойчивой к медикаментозной терапии, в работах А. Fhistaci
и соавт.- Биопсия левого желудочка (1991, 14 больных, средний возраст 37 лет):♦ 22% — активный миокардит (лимфоцитарный и эозинофильный),♦ 57% — неспецифический некроз/фиброз;♦ 21% — кардиомиопатия;♦ стероиды в дозе 50 мг/м^ в дополнение к антиаритмикам привели
к устранению мерцательной аритмии у больных с миокардитом (у
остальных больных аритмия сохранялась).- Биопсия межпредсердной перегородки и желудочков (1997, 12 больных,средний возраст 32 года):♦ 66% — миокардит в предсердиях (в том числе активный у 25%);♦ 17% — невоспалительная кардиомиопатия;♦ 17% — фиброз;♦ в желудочках — миокардит у тех же 25%.Главным энтузиастом и пионером эндомиокардиальной биопсии у больных
с идиопатическими нарушениями ритма и проводимости является римский
кардиолог Андреа Фрустачи (А. Frustaci), который проводил биопсию пред-
сердий и желудочков у больных с идиопатической мерцательной аритмией,
синдромом слабости синусового узла, синдромом Бругады, аритмогенной
дисплазией правого желудочка, WPW-синдромом, жизнеугрожаюшими желу¬
дочковыми аритмиями. Это единственный, насколько нам удалось установить,
ученый, который прицельно выполнял эндомиокардиальную биопсию у боль¬
ной с «идиопатической» (кавьики — А. Фрустачи) мерцательной аритмией,
резистентной к медикаментозной терапии. Результаты двух его основопола¬
гающих работ представлены выше.
Глава 12. От «идиопатической» мерцательной аритмии к постановке,.. 221Ни у одного больного с «идиопатргческой» мерцательной аритмией не было
получено нормальной гистолоп^ческой картины. Проведя биопсию желудоч¬
ков, автор выявил миокардит у 22%; через 6 лет, проведя одновременно биоп¬
сию желудочков и межлредсердной перегородки (которая вообще выполняется
редко), он получил картину миокардита в предсердиях у 66%, у 25% — актив¬
ного (у тех же больных был выявлен миокардит желудочков). Эти данные стали
основанием для проведения у больных с признаками миокардита терапии
стероидами в дозе 50 мг/м- поверхности тела, в результате которой отмечено
восстановление синусового ритма (у больных с картиной кардиомиопатии,
дистрофии и фиброза лечение не проводилось, мерцательная аритмия сохра¬
нялась).При других аритмиях лишь у больных с WPW-синдромом (они составили
контрольную группу) ни в одном случае не было выявлено патологической
гистологической картины. У больных, перенесших остановку синусового узла
неустановленной этиологии, миокардит выявлен А, Фрустачи в 18% (всего
специфические изменения имелись у 65%, неспецифііческие — у 35%). При
синдроме Бругады, генетическая природа которого установлена, признаки
активного миокардита обнаружены у 78% (у 22% выявлен вирусный геном), у
39% — микроаневризмы, у 22% — признаки кардиомиопатии (здесь уместно
вспомнить данные о большой роли вирусной инфекции в реализации гене¬
тического дефекта у больных с синдромом Бругады). У больных, которым с
помощью неинвазивного обследования (МРТ и др.) бьо поставлен диагноз
аритмогенной дисплазии правого желудочка, гистологическое подтверждение
этого диагноза (на основании обнаружения жировой ткани более 40% и фибро¬
за) получено лишь у 30%, у остальных же 70% выявлен миокардит. Наконец, у
больных с «идиопатическими» желудочковыми аритмиями, имевших признаки
микроаневризм коронарных сосудов по данным коронарографии, миокардит
выявлен в 100% биоптатов левого желудочка и в 20% биоптатов правого желу¬
дочка; у 42% больных в ткани миокарда выявлен вирусный геном.При анализе работ других авторов выявляются знач^ітельньте отличия в
частоте обнаружения той или иной гистологической картины у больных с
«идиопатическими» нарушениями ритма и проводимости (табл. 12.2), что обу¬
словлено, видимо, очень различным контингентом больных. Следует отметить,
что не так редко выявляется липоматоз, значение которого остается д.ія нас не
вполне понятным. Жир в правом желудочке — это прежде всего аритмогенная
дисплазия, но при этом заболевании жировая ткань обязательно сочетается с
выраженным фиброзом. В левом желудочке неоднократно описано появление
жира в зоне постинфарктных рубцов. Жир вообще может сопутствовать рубцо¬
вой ткани и отражать, таким образом, достаточно позднюю стадию процесса.
Рядом авторов липоматоз миокарда рассматривается как нормальное явление.Что касается васкулита, который обратил на себя внимание у нашей боль¬
ной, то частота его обнаружения у пациентов с аритмиями очень невысо¬
ка — максимум 8% (в работах А. Фрустачи у больных с аритмиями васкулит
специально не упомянут ни разу). Какова же нозологическая принадлежность
миокардиального васкулита? Прежде всего он может бьггь одним из проявлений
222КардиологияТаблица 12.2Частота обнаружения различных гистологических признаков в биоптатах желудочков
у больных с «идиопатическими» нарушениями ритма и проводимости
(ло данным разных авторов)Показатель%Авторы, годНорма0-80R Drago, 1999; J. Kazmierczak, 1998; А. Frustaci, 1994;
V Thongtang, 1994 Миокардит0-78А. Uemura, 20Q1; F. Drago, 1999; V. Thongtang, 1994Кардиомиопатия17-42М. Teragakl, 1999; Н.В. Wiles, 1992Дегенерациякардиомиоцитоц23-42А. Uemura, 2004; F. Drago, 1999; I. Segava, 1996; S, Peters,
1996; М. Di Blase, 1992 Фиброз4-70J. Kazmierczak, 1998; М. Teragaki, 1999; I. Segava, 1996;
S. Peters. 1996Липоматоз4-15F. Drago, 1999; S. Peters, 1996; C. Contini, 1992Васкулит0-8M. Di Biase, 1992миокардита — как первичного, так и в рамках других заболеваний. В нашем
случае мы расцениваем обнаруженный васкулит именно в рамках миокардита
(хорошо известен псевдоишемический вариант миокардита, обусловленный
васкулитом). Миокардиальный васк>лит может быть одним из проявлений
системных васкулитов, поражающих мелкие сосуды, — в нашем случае нет
оснований подозревать какое-либо из перечисленных заболеваний.Наконец, описаны случаи изолированного миокардиального васкулита,
причину которого найти не удавалось. В одной из работ такая гистологическая
картина бьша обнаружена у пациента с «идиопатической» желудочковой тахи¬
кардией. А. Фрустачи описал больную с васкулитом (он назвал этот васкулит
идиопатическим), который клинически проявлялся картиной рестриктивной
кардиомиопатии; диагноз был поставлен только после открытой биопсии серд¬
ца (в эндомиокардиальных биоптатах сосуды обнаружены не были), проведена
терапия стероидами 50 мг/м^ поверхности тела в сочетании с цитостатиками,
получен хороший клинический эффект.Понятие «болезнь мелких сосудов сердца» более широкое, нежели миокар¬
диальный васкулит. Большое внимание следует уделять поражению так назьт-
вае\шх сосудов Вьессена—Тебезия (описаны почти одновременно — в конце
XVTII в. — Адамом Христианом Тебезием в его труде ««Disputatio medica inau-
guralis de circulo sanguinis in corde» и Раймоном Вьессеном), которые называют
также vasa cordis minima. Сосуды Тебезия располагаются субэндокардиально, и
поражение их, несомненно, играет роль в развитии симптомов ишемии.Показано, что у пациентов с болями в сердце поражение мелких сосудов
сердца обнаруживают при эндомиокардиальной биопсии в два раза чаще, чем
у пациентов без таких болей; при этом наличие болей в сердце прямо коррели¬
рует с выраженностью поражения мелких сосудов сердца: из всех пациентов с
болями в сердце 18% имели выраженное поражение сосудов; 45% пациентов
с выраженным поражением сосудов имели боли в сердце. Поражение мелких
сосудов сердца у больных с застойной сердечной недостаточностью и/или
аритмиями, клинической картиной стенокардии и нормальными результатами
Глава 12. От «идиопатической» мерцательной аритмии к постановке... 223коронарографии состоит в фибромускулярной гипсршшзии, гипертрофии
медии, пролиферации интимы и дегенерации эндотелия. При нормальных
коронарограммах патология мелких сосудов сердца выявляется у 15% больных
сердечной недостаточностью, стенокардией, аритмиями.Нам нередко приходрпся ставить диагноз «коронарный синдром X» или
«микроваскулярная стенокардия» у больных с доказанной ишемией и неизме¬
ненными коронарными артериями. Но мы никогда не знаем, что реально стоит
за этим диагнозом у каждого конкретного больного — по сути, он тоже является
диагнозом исключения. На сегодня общепризншшых нсинвазивньгх методов,
которые 1ЮЗВ0ЛЯЛИ бы адекватно оценить состояние микроциркуляторного русла
сердца, не существует. Упомянем лишь об одном из методов, который может
найти применение с этой целью. Речь идет о контрастной ЭхоКГ, предложенной
в конце 1980-х гг: интракоронарно или внутривенно вводится эхоконтрастное
вещество (газ, образующий микропузьтрьки и даюшцй УЗ-резонанс), которое
заполняет камеры сердца, а после введения вазодилатирующего агента (адено-
зинтрифосфат) — vasa cordis minima. В зоне с нарушенной микроциркуляцией
контрастное вещество не накапливается или накапливается плохо (рис. 12.12).
В качестве показаний к исследованию рассматриваются синдром X, артериальная
гипертония, сахарный диабет, гиперлшшдемия.В заключение рассмотрим спаяние створки трикуспидалъного клапана с
электродом ЭКС, которое было выявлено у нашей больной. Необходимо ска¬
зать о том, что, помимо истинной, возможна псевдотрикуспидальная недо¬
статочность у больных с синдромом экс — при стимуляции правого жел>^-
дочка может возникнуть вентрикулоагриальное проведение, которое приведет
к сокращению предсердий при закрытых атриовентрику.тяриых к-шпанах,
выбросу крови в полые вены и пульсации печени, шейных сосудов, которая
имитирует картину трикуспидальиой недостаточности. При этом собственно
регургитация на клапане обычно отсутствует,Рис. 12.12. Контрастная зхокардиоірафия.LV — полость левого желудочка, Р — задняя стенка левого желудочка, S — меж-
желудочковая перегородка, apex — верхушка левого желудочка, а — до введения
УЗ-контрастітого вещества; б — после введения УЗ-контрастного вещества (контрасти-
руется полость левого желудочка); в — после введеттия вазодилататора (контрастируют-
ся мелкие сосуды в стенках левого желудочка; стрелками обозначена зона нарушенной
микроииркуляции в задней сі'енке левого желудочка
224 КардиологияТрикуспидальная недостаточность минимальной степени хорошо известна у
больных с электродом в правом сердце — она возникает за счет систолического
сближения створки и электрода, который всегда в некоторой степени препят¬
ствует полному закрытию клапана. Надо сказать, что минимальная (0—1 сте¬
пени) трикуспидальная регургитация наблюдалась у данной больной еще до
иміьіантации ЭКС и не усилилась в первые годы после нее. Прогрессирование
недостаточности произошло в период между летом 2006 г. и ноябрем 2007 г.Случаи серьезной трикуспидальной недостаточности, по данным литера¬
туры, возникают редко — как правило, такие случаи отдельно описываются.
Нам удалось найти описаіше около 50 таких слу^шев, А.В. Ардашев сообщает об
одном собственном наблюдении, і случай известен и сотрудникам нашего отде¬
ления интервенпионной кардиологии. В докторской диссертации ЕВ. Чудинова
(2006 г, Ростов), посвященной методам экстракции электродов ЭКС, сращения
со стенкой подключичной вены наблюдаются в 72%, с безымянной веной — б
48%, с верхней полой веной — в 36%, с правым предсердием — в 41%, правым
желудочком — в 71%, с элементами трсхстворчатого к-іапана — в 16% случаев.
Выделено 3 механизма формирования инкапсулирующей электрод фиброзной
ткани; организация микротромбов в местах травмирования зіщотелия, нару¬
шение ламинарного кровотока вокруг электрода и формирование пролежня
сосудистой (сердечной) стенки. Нри этом осложнения, требующие экстракции
электрода, возникали в 1,5% случаев. Протезирование трикуспида'іьного кла¬
пана (при наїичии регургитации более 11 степени) бьию выполнено у 8% всех
больных, подвергшихся экстракции злекіродов, среднее число которых у каж¬
дою больного приближалось к 3. У пациентов с признаками инфицирования
системы ЭКС Б 57% гюдтверждена воспалительная реакция вокруг электрода.В одной из зарубежііьіх работ проанализирован опыт оперативіюго лече¬
ния больных с трикуспидальной недостаточностью, развившейся вследствие
взаимодействия электрода ЭКС и трехстворчатого клапана: из 41 бо.шного у
7 выявлена перфорация створки электродом, у 16 — соударение электрода со
створками в момент систолы, у 4 электрод «запутатся» в клапане и у 14 боль¬
ных отмечено спаяние электрода со створкой клапана. Всем больным после
удаления электрода потребовалась реконструкция клапана (22 — протез, 19 —
аннулопластика), интраопсрационно умер 1 больной, в период наблюдения (от
1 до 99 мес) еще четверо.Таким образом, операция эта достаточно травматичная (несмотря на созда¬
ние лазерных сисгем для экстракции электродов), и показанием к ней считают
лишь выраженную клиническую симптоматику (застой по большому кругу
кровообращения). Натиа пациентка обратилась в отделение хирургического
лечения тахиаритмий НЦССХ им. А.Н. Бакулева, где была повторно прокон¬
сультирована член-корр. РАМН, профессором А.Ш. Ревишвили: на сегодняш¬
ний день показаний к экстракции электрода нет, вопрос о проведении опера¬
ции радиочастотной аблации по поводу мерцательной аритмии может решаться
.лишь носле проведения этиотропной (противовоспалительной) терапии.Больной планируется назначение преднизолона в дозе 20 мг/сут.
Многоцентровых рандомизированных исследований, в которых оценивалась
Глава 12. От «идиопатической» мерцательной аритмии к постановке... 225бы эффекгавность стероидной терапии у больных с хроническим миокардитом,
практически не существует. Небольшое число таких работ касается преимуще¬
ственно больных с острым или под острым инфекционно-имлгунным миокар¬
дитом: в 20 неконтролируемых и 3 контролируемых (суммарно 370 человек)
исследованиях в целом не получено преимущества терапии преднизолоном,
его комбинациями с циклоспорином и азатиоприном по сравнению с обычной
терапией по шгаянию на смертность и ФВ левого желудочкіі (при отчетливой
редукции гистолошческих признаков воспаления), но имелись больные, (УІВС-
тившие на иммуносупрессивную терапию (ФВ левого желудочка увели^гилась
с 26 до 47%), у которых, в отличие от не ответивших, выявлялись антитела к
миокарду (90%) и была доказана персистенция вируса (85%). Отсюда вывод:
требуется выработка более дифференцированных показаний к проведению
иммуносупрессивной терапии и назначению гамма-глобуііина.В своей практике мы добивались хорошего клинического результата у боль¬
ных с активным миокардитом с помопіью назначения 20—30 мг преднизолона в
сутки. Исходя из этого (и в огсугствие определенных международных рекомен¬
даций на этот счет) у больной с минимальной сердечной недостаточностью, но
с упорными нарушениями ритма, проводимости и ишемическими симптомами
решено остановиться на дозе 20 мг/сут. Об эффективности терапии можно
будет судить по восстановлению синусового ритма, нормализации титров
антител к миокарду и по само^іувствию больной. Наряду с преднизолоном,
іиіанируется продолжить терапию плаквенилом.Комментарий Л.В. Недоступа — профессора кафеіфьі факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукМногие годы мы применяли аминохинолиновый препарат делагил в качестве
антиаритмика и у некоторых больных получали эффект (в то время из анти-
аритміріеских препаратов мы имели только гликозиды и хинидин). Эти пре¬
параты (делагил, аііаквенил) оказывают не противовоспалительное, а именно
иммуиосупрессивное (пусть и слабое) действие, которое могло вносить свой
вклад в их эффект у больных с аритмиями. Мы, безусловно, продолжим тера¬
пию плаквенилом (одновременно с преднизолоном и после его отмены) в
течение не менее чем двух лет.Что касается классификации мерцательной аритмии, которая принята на
сегодня, она плохая и ничего не дает для практики (поэтому и плохая). Мы
пытаемся набросать свои варианты классификации — она должна быть опи¬
сательной, от терминов «персистирующая» и «перманентная» вообще следует
отказаться. Мерцательная аритмия настолько разнообразна в своем течении,
что пытаться уложить ее в жесткие рамки невозможію. Тот эпизод, который
развился у нашей больной, — это, по суги, рецидив хронической формы мер¬
цательной аригмии.Как ставить диагноз миокардита? Это действительно о^гень трудно, когда он
нетяжелый (диагноз тяжелого миокардита поставить несложно). Мы сплошь
и рядом пропускаем нетяжелые миокардиты — сколько обострений аритмии
и атеросюїеротических событий (если тут замешан вирус) мы видим после
226 Кардиологияэпвдемии гриппа в Москве! В течение последних 1,5 лет мы работаем с раз¬
личными лабораториями, которые определяют уровень антител к миокар¬
ду, пытаемся лечить таких больных, имеем определенные результаты. Это
направление требует изучения.Миокардит, диагаоз ко'горого был поставлен у нашей больной чрісто логиче¬
ским путем, полностью подтвердился на биопсии. К обнаруженному васку-
литу я сначала отнесся скептргчески (помня давнюю историю о том, как более
чем у половины больных с аритмиями мы обнаруживали сначала амилоид, а
затем кожный васкулит). Однако обнаружение еще более выраженного васку-
лита при следующей биопсии (у другой больной) заставляет думать, что это не
случайно. Все это (при наличии клинической картины ишемии у обеих боль¬
ных) — основание для изучения микроциркуляции. Как в клинике оценивать
микроциркуляцию? Когда-нибудь появится такой метод, который позволит
контрастировать самые мелкие сосуды.Что касается преднизолона, то в малых дозах он оказывает не иммуносупрес-
сивный, а противовоспалительный эффект. И все-таки противовоспатительньш
эффект преднизолона ~ это не противовоспалительный эффект нестероидных
противовоспалительных препаратов — действие преднизалона шире, надежнее,
и мы отдаем ему предпо'ггение (хотя это чисто эмпирическое убеждение).Комментарий В.И. Маколкина — профессора кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И. М. Сеченова, член-корр. РАМНЯ бы хотел особо отмстить два аспекта этого клинического разбора. Во-первых,
было четко показано, что воспалительный процесс (будь то миокард или почки)
может быть локальным. Мы говорим «миокардит» и подразумеваем процесс
диффузный, но изолированный миокардит предсердий — это реальность, и
диагностировать такой миокардит чрезвычайно сложно. И второй аспект — это
значимость микроциркулящии. Методов ее изучения очень много, существуют
хорошие обзоры на эту тему, хотя изучать сердце в этом плане наиболее сложно.
Кардиологам не повезло: сердце — орган, наиболее трудный для морфологиче¬
ского изучения, любые манипуляции на сердце потенциально намного опас¬
нее, чем на печени или почках. В целом сегоднядший случай, помимо научной,
имеет и четкую практическую направленность.P.S. Через 4 нед после начала терапии преднизолоном в дозе 20 мг/сут у
больной отмечено восстановление синусового ритма, дигоксин отменен, назна¬
чен тамбокор 300 мг/сут. В дальнейшем (к июлю 2008 г.) преднизолон полно¬
стью отменен, при снижении дозы до 10 мг/сут отмечался 10-дневный эпизод
мерцательной аритмии, который купировался самостоятельно; доза плаквенила
увелїгчена до 400 мг, доза тамбокора постепенно снижена до 200 мг/сут. В связи
с появлением сухого кашля престариум заменен на апровель.В сентябре 2008 г. (через 9 мес после начала иммуносупрессивной терапии,
через 2 мес после отмены преднизолона и увеличения дозы плаквенила) про¬
ведены контрольные анализы крови на антикардиальиые антитела {табл. 12.3):
выявлено некоторое нарастание титров, терапия оставлена без изменений.
Глава 12. От «идиопатической» мерцательной аритмии к постановке.,.227В январе 2009 г. (в связи с возобновлением кратковременных перебоев в
работе сердца преимущественно ночью, после зевоты) анализ в лаборатории
Федерального научного центра трансплантологии проведен повторно— с
У’четом сохранявшихся повышенных титров антител к антигенам эндотелия и
проводяш;ей системы дополните.щьно к плаквенилу 400 мг/сут назначен мети-
пред 4 мг. К декабрю титры антител практически нормализовались, в течение
года рецидивов мерцательной аритмии не было (в том числе во время и после
гинекологической операции), продо.іжала постоянную терапию тамбокором
200 мг/сут.В январе 2010 г. на фоне сильного длительного стресса развился очередной
эпизод мерцательной аритмии, который к>тгировался самостоятельно менее
чем через месяц, в качестве антиаритмического препарата назначен этацизин
150 мг/сут. В июне проведен контрольный анализ крови на антикардиальные
антитела — терапия метипредом в поддерживающей дозе 4 мг утром продол¬
жена.Таким образом, можно говорить о некоторой антиаритмической эффектив¬
ности небольших доз кортикостероидов и плаквенила — за 2,5 года, прошедших
после начала специфической терапии, отмечено лишь 2 относительно корот¬
ких эпизода мерцательной аритмии (10 дней и 1 мес), которые купировались
самостоятельно. Самочувствие больной все это время остается удовлетвори¬
тельным, она активно работает. По данным ежегодных эхокардиографических
исследований степень трикуспидальной недостаточности уменьшилась до II,
клинических признаков сердечной недостаточности и стенокардии у больной
не появилось, Возможно, назначение более высоких доз кортикостероидов
могло бы оказать и более стойкий антиаритмический эффект, однако субъек¬
тивная переносимость терапии бьиіа не очень хорошей, и в настояшее время
качество жизни больной удовлетворительное.Таб^гица 12.3Уровень антикардиальных антител у больной Ч. в процессе терапииДата20.09.08 г.12.01.09 г.09.12.09 г.07.06.10 г.НормаАТ к МТ IgG1:2001:100АНФ (срезы быка)положит.нетнетнетнетАТ к эндотелию1:1601:3201:801:801:40АТ к КМЦ1:1601:801:401:201:40АТ к гл. мышцам1:401:401:401:401:40АТ к провод .сист.1:3201:1601:801:1601:40Примечание. АТ — антитела, МТ— NfflOKapAHaflbHaa ткань, АНФ — антинуклеарный фаістор,
КМЦ — кардиомиоциты.ЛИТЕРАТУРААрдашев А.Е,, Джанджгава А.О., Желяков Е.Г., Шаваров А.Л. Постоянная
элекгрокардиостимуляция и дефибрилляция в клинической практике. — М.:
Медпрактика-М, 2007, — 224 с.
228 КардиологияДерюгин М. В., Бойцов С Л. Хронические миокардиты. — Эл би-СПб, 2005. —
287 с.Заклязьминская Е.В. Генетические аспекты нарутпений сердечного ритма:
Дис.... д-ра мед. наук. — М., 2007.Недоступ А,В,, Федорова В.И., Васюков С.С., Гордеев С.Л. Новое в патогенезе
мерцательной аритмии: взаимосвязь изменений биоэлектрической актив¬
ности мозга с рецидивированисм пароксизмов фибрилляции предсердий //
Терапевтический архив. — 2007. — № 9. — С. 38—45.Носкова М. В., Рееишвили Л.Ш., Александрова С Л. Возможные подходы к
диагаостике постмиокардит№іеского кардиосклероза и латентных миокарди¬
тов неревматической этиологии у пациентов с желудочковыми нарушениями
ритма // Вестник аритмологии. — 2004. — № 34. ~ С. 18—23,Покушалов Е.Л., Туров А.И., Шугаев П.Л., Сырцева Я. В. Новый подход в лече¬
нии фибршыяиии предсердий: катетерная аблация ганглионарных сгиіетений в
левом предсердии II Вестник аритмологии. — 2006. — № 45. — С. 17—27.Чудинов Г. В. Показания, методы и клинические результаты удаления эндо-
кардиалъных электродов для постоянной элекгрокардиостимуляции: Авто-
реф. дис.... д-ра мед. наук. — М., 2006. — 32 с.ACC/AHA/ESC 2006 guidelines for the management of patients with atrial fibril¬
lation // Eur. Heart J. 2006. Vbl. 27. P. 1979-2030.АЯА/ACCF/ESC scientific statement. The role of endomyocardial biopsy in the
management of cardiovascular disease // JACC. 2007. Vol. 50. № 19, 1914-1932.Chimenti C., Calabrese F., Thiene G. et al. Inflammatory left ventricular microaneu¬
rysms as a causc of apparently idiopathic ventricular tachyarrhythmias I j Circulation.
2001; 104(2):168-173.Chimenti C., Pieroni М., Maseri A., Frustaci Frustaci. Histologic findings in patients
with clinical and instrumental diagnosis of sporadic arrhythmogenic right ventricular
dysplasia //J. Am. Coll. Cardiol. 2004; 43(12):2305-2313.Coumel P.H., Atluel P., Leclercq LF., Friocourt P. Arythmic auriculaire d’origine
vagale on catccholergique: effets compares due traitement beta-bloquani et phenom-
ene d’echappement //Arch. Mai. Coeur. 1982; 75:373—388.Czura CJ., Friedman S.G., Tracey KJ. Neural inhibition of inflammation: the cho¬
linergic anti-inflammatoiy pathway //J. Endotoxin, Res. 2003; 9(6):409—413.Fioranelli М., Piccoti М., Mileto G. M. etal Analysis of heart rate variability five min¬
utes before the onset of paroxysmal atrial fibrillation // Pacing. Clin. Electrophysiol,
1999;22(5):743-749.Frustaci A., Caldamlo М., Buffon A. et al Cardiac biopsy in patients with “primary”
atrial fibrillation. Histologic evidence of occult myocardial diseases j j Chest. 1991;
100(2):303-306,Frustaci A., Cameli S., ZeppilU P. Biopsy evidence of atrial myocarditis in an athlete
developing transient sinoatrial disease // Chest. 1995; 108(5): 1460-1462.Frustaci A., Chimenti C., Beliocci F. et al. Histological substrate of atrial biopsies in
patients with lone atrial fibrillation // Circulation. 1997; 96(4): 1180—1184.Frustaci A., Chimenti C., Pieroni M. Idiopathic myocardial vasculitis presenting as
restrictive cardiomyopathy//Chest. 1997;! 11;1462-1464.
Глава І2. От «идиопатической» мерцательной аритмии к постановке,.. 229Frustaci А., Priori S.G., Pieroni М. et al Cardiac histological substrate in patients
with clinical phenotype of Brugada syndrome // Circulation. 2005;! 12(24): 3680—
3687.GoUob M.H., Jones D.L., Krahn A.D. et al. Somatic mutations in the connexin 40
gene (GJA5) in atrial fibriUation // N. Engl. J. Med. 2006; 354(25):2677-2688.Hosenpud J.D., McAnulty J.H., and Niles N.R. Unexpected myocardial disease in
patients with life threatening arrhythmias I j Br. Heart J. 1986; 56(1): 55—61.Huang J.L., Wen Z.C., Lee W.L. etai Changes of autonomic tone before the onset
of paroxysmal atrial fibrillation // Int. J. Cardiol. 1998; 66(3): 275—283.Letsas K., Sideris A., Efremidis M. etal. Prevalence of paroxysmal atrial fibrillation
in Brugada syndrome: a case series and a review of the literature // J. Cardiovasc. Med.
(Hagerstown). 2007; 8(10):803-806.Lin G., Nishimura R.A., Connolly H.M. et al Severe symptomatic tricuspid valve
regurgitation due to permanent pacemaker or implantable cardioverter-defibrinator
leads //J. Am. CoU. Cardiol. 2005, 17; 45(10):1672-1675.Malone S., Giunla A., Betocchi S. et al. Two-dimensional echocardiography in
idiopathic enlargement of the right atrium. Reliability and limitations // Cardiology
1983; 70(4):216-222.Makita N., Sasaki K., Groenewegen W.A. etal Congenital atrial standstiH associated
with coinheritance of a novel SCN5A mutation and connexin 40 polymorphisms I j
Heart. Rhythm. 2005; 2(10):1128-1134.Mosseri М., Yarom R., Gotsman M.S., Hasin У. Histologic evidence for small-vessel
coronary’ artery disease in patients with angina pectoris and patent large coronary
arteries II Circulation. 1986; 74(5):964-972.Otsuji Y, Kumanohoso Т., Yoshifuku S. etal. Isolated annular dilation docs not usu¬
ally cause important functional mitral regurgitation: comparison between patients with
lone atria] fibrillation and those vidth idiopathic or ischemic cardiomyopathy // J. Am.
Coll. Cardiol. 2002; 39(10): 1651-1656.PengS.K., French W.J. Morphological changes in small vessels on endomyocardial
biopsy //Ann. Clin. Lab. Sci. 1986; 16(3); 180-188.Pugliatti P., Patanu S., De Gregorio C. et at. Lipomatous hypertrophy of the intcr-
atrial septum // Int. J. Cardiol. 2008 Nov 12;130(2):294-295.Sitges М., Teijeira V.A., Scalise A. et al Is there an anatomical substrate for idio¬
pathic paroxysmal atrial fibrillation? A case-control echocardiographic study //
Europaee. 2007 May; 9(5):294—298.van Hoeven K.H., Factor S.M. Endomyocardial biopsy diagnosis of small vessel
disease: a clinicopathologic study 11 Tnt. J. Cardiol. 1990; 26(1);103-110.
Глава 13МИОКАРДИАЛЬНЫЙ ВАСКУЛИТ: ПУТЬ
К ДИАГНОЗУ, КЛИНИЧЕСКИЕ ВАРИАНТЫ, ПОПЫТКИ
ПАТОГЕНЕТИЧЕСКОЙ ТЕРАПИИА.В. Недоступ, О.В. Благова, ЕА. Коган, ВЛ. Сулимое,
Н.В. Чткова, КС. ЩедринаВ прельщу шей главе была описана больная, у которой в рамках морфологи¬
чески верифицированного хрон№іеского миокардита развился интрамиокар-
диальный васкулит, что проявлялось безболевой ишелгаей миокарда. В данной
главе представлены два пациента, в клинической картине которых не было
ничего общего; в первом случае доминирующим проявлением заболевания
сердпа являлась преходящая блокада левой ножки пу^іка Гиса, ограничиваю¬
щая профессиональные возможности молодого пациента; во втором случае,
у пожилой женщины, заболевание сердца проявлялось тяжелой стенокардией
и сердечной недостаточностью. Тем не менее при биопсии миокарда у обоих
больных был выявлен выраженный продуктивный васкулит (с минимальными
признаками миокардита), который при неизмененньгх крупных коронарных
артериях и в отсутствие признаков поражения других органов был расценен
нами как миокардиальный васку'литТакого диагноза на сегодняшний день не существует, но и описания при¬
жизненной биопсии миокарда у подобных больных единичны; в то же время
клиницистам хорошо известна большая группа пациентов с так называемым
коронарным синдромом X, нозологическая принадлежность которого остает¬
ся неясной. Можно дулшть о том, что представленные пациенты находятся на
начальной и развернутой стадии одного и того же заболевания. Обоим паци¬
ентам проводилась иммунос>ттрессивная терапия, и в обоих случаях получен
удовлетворительный клинический эффект, в заключение приводится описа¬
ние больной с дилатационной кардиомиопатией и стенокардией, у которой
выявлен выраженный склероз мелких коронарных сосудов и, несмотря на
бронхиальную астму в анамнезе, данных за системный васкулит не полу^іено.Больной С., 34 года, поступил в отделение кардиологии Факультетской
терапевтической клиники им. В.Н. Виноградова 29.04.2009 г. Жалоб иди посту¬
плении не предъявлял.Из анамнеза жизни: мать, 55 лет, здорова, отец, 65 лет, страдает глаукомой;
профессия пациента связана со значительными физическими и эмоциональ¬
ными нагрузками, которые он переносит хорошо, регулярно проводит дли¬
тельные тренировки, профессионально занимался каратэ. Во время трени¬
ровок получает специальное питание с повышенной общей калорийностью.
Не курит, алкоголем не злоупотребляет.
Глава 13. Миокардиальный заскулит: путь к диагнозу... 231Анамнез заболевания-, в 2003 г. (в возрасте 29 лет) во время планового
медосмотра при нагрузочной пробе (велоэргометрия лежа) впервые заре¬
гистрирована деформация комплекса QRS, подозрительная на наличие
синдрома WPW. Было проведено чреспищеводное электрофизиологическое
исследование, при котором возникло подозрение на наличие дополни¬
тельного предсердно-желудочкового пути проведения без развития тахи¬
кардии. Тренировки продолжал, приступов внезапного сердцебиения не
отмечал, В июне 2005 г. при плановом тредмил-тесте на высоте нагрузки
(100 Вт, ЧСС 146 уд/мин) зарегисгрировано появление бессимптомной
полной блокады левой ножки пучка Гиса (ЛНПГ), которая исчезла в покое.
В январе 2006 г. для уточнения природы изменений комплекса QRS был
проконсультирован в НЦССХ им. А.Н. Бакулева член-корр. РАМН, про¬
фессором А.Ш. Ревишвили, проведено внутрисердечное электрофизиологиче¬
ское исследование, при котором данных за наливше дополнительных путей
предсердножелудочкового проведения, нарушений ритма сердца и прово¬
димости получено НС было.в апреле 2006 г. перенес лакунарную ангину (с лихорадкой до 39 °С), выска¬
зывалось предположение о развитии миокардита, однако полноценное обсле¬
дование по этому поводу не проводилось, в июне 2006 г. во время проведения
очередного тредАШЛ-теста вновь возникла преходящая полная блокада левой
ножки пучка Гиса. Такая же картина повторилась в ноябре 2006 г. при велоэр-
гометрической пробе. Для исключения вялотекущего миокардита кровь была
исследована методом ПЦР на вирусы простого герпеса, цитомегаловирус и
вирус Эпштейна—Барр: генома вирусов не выявлено. Самочувствие больного
оставалось удовлетворительным, переносил нагрузки хорошо.В ноябре 2006 г. был госпитализирован в Институт клинической кардиоло¬
гии им. А.Л. Мясникова, где проведено развернутое инструментальное обсле¬
дование.При суточном мониторировании ЭКГ по Холтеру — ритм синусовый,
ЧСС 49—136/мин (ср. 77 уд/мин), 14 наджелудочковых экстрасистол. Эпизоды
тахизависимой блокады левой ножки ггу^іка Гиса (минимальная ЧСС при воз¬
никновении блокады 86 уд/мин). ST-Tбез ишемической динамики.При чреспищеводной стиліуляции сердца с частотой 120 уд/мин отмечалось
развитие блокады левой ножки пучка Гиса, по мерс увеличения частоты стиму¬
ляции интервал от стимула до QRS увеличивается. Эффективный рефрактер¬
ный период предсердно-желудочковой системы увеличивается по мерс увели¬
чения частоты базисной стимуляции, что указывает на проведение импульсов
по ЛВ-узлу и исключает наличие аномального пути проведения. Данных за
наличие аномального пути предсердно-желудочкового проведения не полу¬
чено, функция синусового узла и АВ-проводимость не нарушены. ВВФСУ
1063 мс, КВВФСУ 209 мс, г. Венксбаха 160/мин.При проведении стресс-ЭхоКГ с велоэргометрической пробой еще до
начала нагрузки, при ЧСС 88 уд/мин отмечено развитие блокады левой ножки
пучка Гиса. Выполнена нагрузка 150 Вт в течение 3 мин. Исходно и на момент
нагрузки зон нарушения локальной сократимости миокарда левого желудочка
232 Кардиологияне отмечалось. Проба на выявление скрытой коронарной недостаточности
отрицательная.При сцинтиграфии миокарда с ^’Тс-МИБИ в покое регастрировалось умерен¬
ное снижение включения радиофармпрепарата нижнеперегородочной и передней
локализации, зон нарушения локаїьной сократимости не выявлено. В ответ на
нагрузку — небольшое увеличение глубины дефекта перфузрш миокарда нргжнепе-
регородочной и переднебоковой локализации, что расценено как следствие прехо-
дятцей блокады левой ножки пучка Гиса; изменения ФВ и нарушений локальной
сократимости миокарда левого желудочка при нагрузке не отмечалось.При проведении МРТ сердца с контрастированием очагового поражения
миокарда ишемического или воспалительного характера не выявлено. Камеры
сердца в размерах не увеличены. Размеры правого желудочка на верхней гра¬
нице нормы. Толшіина миокарда правого желудочка 3—4 мм. Миокард лево¬
го желудочка равномерно утолш;ается в сїтстолу, нарушений сегментарной
сократимости не выявлено. Аномальных потоков в полостях сердца нет. После
введения контрастного препарата патологического накопления его в миокарде
левого желудочка ишемического или воспалительного характера нет.Наконец, 27.11.2006 г. бьша выполнена коронароангиография, при которой
признаков агсросклсрогическоі'о поражения коронарных артерий и аномалий
строения коронарных артерий не выявлено. Сбалансированный тип крово¬
снабжения сердца.Больной был выписан под дальнейшее наблюдение с диагнозом «нару¬
шение проводимости сердца: преходящая частотно-зависимая блокада левой
ножки пучка Гиса*>.Через полгода после вьптиски, в июле 2007 г., в лаборатории «Иммункулус»
был выполнен анализ на естественные антикардиальные антитела: были
несколько повышены уровни антител к [3-рецепторам и NO-синтетазе (36
и 33 при норме от -30 до +20), дальнейшее обследование по этому поводу
не проводилось до февраля 2009 г., когда пациент был осмоірен профессо¬
ром А.В. Иедоступом, проведены развернутые иммунологические анализы
крови, направленные на диагностику миокардита {табл. 13.1). По данным
лаборатории «МедБиоСпектр» (канд. мед. наук ГН. Чувиров), повышения
уровня антител к миокардиальному антигену не выявлено, однако по данным
иммунологической лаборатории Федерального научного ценгра трансплан¬
тологии и искусственных органов им. акад. Б.И. Шумакова (канд. мед. наук
А.Г. Куприянова, канд. мед. наук В.А. Заиденов, д-р мед. наук Л.В. Белецкая)
были выявлены специфический антинуклеарный фактор (АНФ) с антигеном
сердца быка в титре 1:80, а также умеренно повышенные (при норме 1:40)
титры антител к проводящей системе (1:160), гладкой мускула'гуре (1:160), кар-
диомиоцитам (1:80) и эндотелию (1:80).Было выявлено также повышение IgG к стрептококкам (антигиалуронидаза
1:300 при норме 1:100); уровень антител к вирусу простого герпеса и вирусам
Коксаки труппы В повьппен не был (IgM и IgG 1:50).С у^іетом этих данных в марте 2009 г. в лаборатории Российского научного
центра хирургии им. Б.В. Петровского (зав. — д-р мед. наукЕ.Б. Свиршевский)
Глава 13. Миокардиальный васкулит: путь к диагнозу..233Таблица ШТитры антикардиальных и антистрептококковых антител у больного С.ПоказательПациентНормаАТ к миокарду (igG)1:1001:100АТ к стрептококкам1:3001:100АНФ (сердце быка)1:80нетАТ к эндотелию1:801:40АТ к кардиомиоцитам1:R01:40АТ к і дадкой мускулатуре1:1601:40АТ к проводящей системе1:1601:40была проведена радиоизотопная компьютерная томография левого желудочка
(рис. 13. /): с первого порога нафузки отмечены измелепия комплексов QRS,
характерные для блокады левой ножки пучка Гиса; в условиях покоя отмечена
умеренная гипоперфузия переднеперегородочной и нижнеперегородочной
стенок левого желудочка на среднем уровне и в области выходного отдела, с
да.1ьнейшим увеличением выраженности гипоперфузии (ишемия) при физиче¬
ской нагрузке иереднеперегородочной, перегородки и нижнеперегородочной
стенок с распространением гипоперфузии на участки этих стенок, примыкаю¬
щих к верхутнке.Для уточнения наличия и характера заболевания сердца больной бьт
госпитализирован в отделение кардиологии Факультетской терапевтической
клиники.При поступлении: состояние относительно удовлетворительное. Кожные
покровы обычной окраски. Отеков нет. Периферические лимфоузлы не уве¬
личены. В легких дыхание везикулярное, хрипов нет. Число дыханий 18/мин.
Тоны сердца ритмичные, ясные, ЧСС 70 уд/мин, АД 110/70 мм рт.ст. Живот
мягкий, безболезненный во всех отделах, печень и селезенка не ^твеличены.в оби^ем анализе крови НЬ 153,3 г/л, эритроциты 4,86 MjIh, цветовой показа¬
тель 0,94, лейкоциты 4,42 тыс., нейтрофилы 56,4%, лимфоциты 33,8%, моноци¬
ты 6,7%, эозинофилы 2,5%, базофилы 0,6%, СОЭ 3 мм/ч, тромбоциты 228 тыс.В биохимическом анализе крови также без отклонений от нормы: обший
белок 69,1 г/л, альбумин 44,8 г/л, креатинин 0,82 мг/дл, глюкоза 4,9 мг/дл, азот
мочевины 5,8 ммоль/л, мочевая кислота 217,7 мкмоль/л, общий билирубин
13,2 мкмоль/л, натрий 144 мэкв/л, калий 4,7 мэкв/дл, кальций 2,35 ммоль/л,
железо 84 мк1-/дл, ACT 16 сд/л, АЛТ 33 ед/л, у-ГГ 38 ед/л, ЩФ 106 ед/л.В липидном спектре — гинсрлипидемия 4 типа: триглицериды 238 мг/дл (150—
250), общий холестерин 160 мі/дл (150-250), ЛОНП 47,6 мг/дл (10-30), ЛВП
30 мг/дл (35-75), ЛНП 82,4 мг/дл (100-160), коэффициент атерогенности 4,33.Электрофорез белков в пределах нормы: альбумин 65,9%, альфа-1 2,7%,
альфа-2 6,5%, бета 13,2%, гамма 11,7%.Коагулограмма: АЧТВ 1,02, протромбиновый индекс 95%, фибриноген
2,78 г/л.Гормоны щитовидной железы: Т^(своб.) 14,9 пмоль/л (0-25,0), ТТГ
1,48 МЕ/л (0,3-4,0), антитела к тиреопероксидазе 44,0 МЕ/мл.
234Кардиология>40%25% to 40%
10% to 25%
0%to 10%
-10% to 0%
<-10%% Thickening
AnteriorEnd Systole
Volume =29 ml
Ejection
Fraction = 57%m)Scores; 0=Normal 1=Equivocal 2= Moderately Reduced 3=Severely Reduced 4=AbsentStiess
Total
Severity
Score = 109InferiorSummed Rest Score = 1 Summed Difference Score = 6Рис. 13.1. Ралиоизотопная компьютерная томофафия левого желудочка больного С.
(мар! 2009 г., пояснения в тексте)В иммунологическом анализе IgA 410 мг/дл (50—300), IgM 72 мг/д,пі (40-200),
IgG 1870 мг/дл (600—2000), комплемент 36,6 гем.ед., РФ и СРБ отрицательны,
анти-О-стрептояизин 220 МЕ/мл (норма до 125).Маркеры вирусных гепатитов В и С, антитела к ВИЧ не выявлены; полу¬
чены положителы1ыс реакции на сифилис — иммунофлуоресцентный анализ
(анти-ТР антитела) и реакция прямой гемагглютинации (++++); кардиолипин
отрицательный. В связи с этим больной проконсультирован дерматовенероло¬
гом: выявленные положительные серологические реакции на сифилис явля¬
ются следовыми, после проведенного в 2007 г. курса специфической противо-
сифилитической терапии. В настоящее время в лечении не нуждается, может
находиться в терапевтическом стационаре.В общем анализе мочи — без отклонений от нормы.
Глава ІЗ. Миокардиальный васкулит: путь к диагнозу...235П'-кВtpj,- ....It'■рігг4шш• ,4-щ%Рис. 13.2. ЭКГ больного С. при поступлении в клинику (скорость записи 25 мм/с)На ЭКГ, зарегистрированной при пост>ттлении (рис. 13.2), ритм синусовый,
ЧСС 68 уд/мин, ЭОС расположена нормально. Признаков ишемии, гипертро¬
фии различных отделов сердца нет. Зубец Р 0,08 с, PQ 0,14 с, QRS 0,1 с, QT 380
мс (корригированный 399 мс).По данным ЭхоКГ, размеры левого желудочка не увеличены (КДР 5,4 см,
КДО 154 \Li, КСО 72 мл, тМЖП 0,7 см, тЗС 0,9 см. ФВ 54%, выявлено сниже¬
ние экскурсии заднебазального сегмента. Диастолическая функция не наруше¬
на (Е/А 1,5). Правый желудочек 2,0 см, тПЖ 0,5 см, характер движения стенок
не изменен. Левое предсердие 59 мл (5,7x3,9 см), правое предсердие 55 \иг
(4,5x3,3 см). Клапаны и аорта не изменены. Жидкости в полости перикарда нет.При суточном мониторировании ЭКГ по Холтеру, проведенном в отсут¬
ствие кардиотропной терапии, ритм синусовый. ЧСС 58-148/мин (ср. ~
86 уд/мин). Перемежающаяся блокада левой ножки пучка Гиса (рис. 13.3).
Наджелудочковых экстрасистол 5. Участки ускоренного ритма, завершающи¬
еся удлиненными RR (RRmax 1184 мс). Желудочковых экстрасистол 5. ST-T:
снижение амплитуды Г-зубца при ЧСС >90/мин (на фоне «разблокированных»
QRS комплексов).Повторно выполнен также тредмил-тест по протоколу Bruce (на «чистом»
фоне); максимальная мощность нагрузки 11,2 МЕТ (225 ВТ), G 16%,
V 6,4 км/ч. Исходная ЧСС 89 уд/мин, исходное АД 140/100 мм рт.ст., макси¬
мальная ЧСС 167 уд/мин, максимальное АД 180/70 мм рт.ст. Причина пре¬
кращения нафузки: достижение субмаксима-іьной ЧСС. Жалоб во время про¬
ведения теста не предъявлял, на 2-й минуте нагрузки (при ЧСС 109 уд/мин)
отмечена переходящая блокада левой ножки пучка Гиса, которая исчезла к 5-й
минуте восстановительного периода. Толерантность к физическим нагрузкам
высокая. Заключение: проба отрицательная.
236КардиологияРис. 13.3. Фрагменты записи суточного монїтторирования ЭКГ, проведенного у боль¬
ного С. на «чистом» фоне (на нижнем фрагменте при ЧСС 137 уд/мин — блокада левой
ножки пучка Гиса)При рентгенографии органов грудной клетки: грудная клетка гиперстеника.
Легкие без свежих очаговых и инфильтративньгх изменений. Корни легких
стр>тстурньт. Диафрагма расположена на уровне переднего отрезка 5-го ребра.
Плевральные синусы свободны. Сердце горизонтально расположено, аорта
рентгенологически не изменена.При ЭГДС патологических изменений не вьшвлено.Проконсультирован ЛОР-врачо\г. перегородка искривлена, Миндалины
удалены. Задняя стенка глотки гиперемирована, лимфоидные гранулы гипер¬
трофированы. Хронический фарингит (стрептококковый?). Атрофический
ринит. В мазке из зева получен рост Streptococcus pyogenes в титре 10^.Таким образом, каиническая картина заболевания указывала на высокую
вероятность хронического миокардита с выраженным коронарным микрова-
скулитом; в пользу этого диагноза свидетельствовали;• отягощенный инфекционный анамнез (хронический тонзиллит, ангина
в анамнезе, повышенный титр антистрептококковых антител в сочетании
с высевом стрептококка из зева в значимом титре);• «необъяснимая» преходяшая блокада левой ножки пучка Гиса;• признаки стресс-индуцированной ишемии по данным сцинтиграфии мио¬
карда (при неизмененных коронарных артериях);• повышенные в 2—3 раза титры антикардиальных антител (в том чис¬
ле к эндотелию и гладкой мускулатуре) в сочетании с обнаружением
Глава 13. Миокардиальный васкулит: путь к диагнозу...237специфического АНФ (в отсутствие менее специфических маркеров
иммунного воспаления).Поскольку как преходящая блокада левой ножки пучка Гиса (даже при
отсутствии других симптомов поражения сердца), так и назначение активной
иммуносупрессивной терапии ех juvantibus, без достоверной верификации
диагноза, ставили под вопрос профессиональное будущее пациента, бьыо при¬
нято решение о проведении эндомиокардиальной биопсии правого желудочка:05.05.2009 г доступом через правую бедренную вену осуществлен забор 5 участ¬
ков верхушки, свободной стенки правого желудочка и межжелудочковой пере¬
городки. Сразу после процедуры регистрировалась блокада левой ножки пу^гка
Гиса (рис. 13.4), в дальнейшем проводимость восстановилась.При исследовании биоптата методом real-time PCR (ООО «Многопрофильная
диагностическая лаборатория», канд. мед. наук А.Е. Донников) генома вирусов
простого герпеса 1 -го, 2-го, 6-го типов, вируса герпеса зостер. питомегаловиру-
са, вируса Эпштейна—Барр, парвовируса В19 и аденовирусов не выявлено.При морфологическом исследовании биоптатов (профессор Е.А. Коган)1. Субэндокардиальный участок свободной стенки правого желудочка.
Эндокард утолщен, склерозирован, покрыт пластом эндотелиальных клеток.
Кардиомиоциты с исчезновением поперечной исчерченности. Ядра неравно¬
мерно гипертрофированы, сохранны, Интерстиций неравномерно расши¬
рен, набухший, содержит периваскулярные лимфогистиоцитарные элементы.
Микрососудьт с набухшим эндотелием, отдельные со склсрозированными
стенками.2. Субэндокардиальный участок межжелудочковой перегородки {рис. 13.5,
см. цветную вклейку). Эндокард склерозирован и утолщен. КардиомиоцитыРис. 13.4. ЭКГ больного С. сразу после проведения зтгдо\іиокардиальной биопсии
238 Кардиологияс исчезновением поперечной исчерченности. Ядра неравномерно гипер¬
трофированы, сохранны. Интерстиций неравномерно расширен, набухший,
содержит периваскулярные скопления лимфогистиоцитарных элементов.
Микрососуды с явлениями продуктивного васкулита.3, Субэндокардиальный участок верхушки правого желудочка (рис. 13.6,
см. цветную вюгейку). Эндокард склерозирован и утолщен. Кардиомиоциты
с исчезновением поперечной исчерченности. Ядра сохранны. Интерстиций
неравномерно расширен, набухший, содержит единичные лимфогистиоцитар-
ные элементы (7—10 лимфоцитов при большом увеличении), продуктивные
капилляриты.4. Субэндокардиальный участок свободной стенки правого желудочка
(рис. 13.7, см. цветную вклейку). Кардиомиоциты с исчезновением попереч¬
ной исчерченности. Ядра сохранны. Интерстиций неравномерно расширен,
содержит отдельные периваскулярные лимфогистиоцитарные инфильтраты.
Продуктивные васкулиты с пролиферацией эндотелиальных клеток и лимфо-
гистиоцитарными элементами.Заключение: межуточный миокардит с продуктивными васкулитами и дис¬
трофическими изменениями кардиомиоцитов по ишемическому типу.Таким образом, изменения в интерстиции (его отечность, единичные лим¬
фогистиоцитарные элементы) соответствовали скорее картине пограничного
миокардита, однако преобладала картина выраженного воспалительного пора¬
жения сосудов с частичной или полной облитерацией просвета и развитием
вторичной (ишемической) миокардиодистрофии. Участков некроза кардио¬
миоцитов, интерстициального склероза выявлено не было, что также свиде¬
тельствовало о невысокой активности собственно миокаріїита и преобладании
сосудистых изменений.Генома основных кардиотропньгх вирусов в миокарде выявлено не было,
в связи с чем этиология процесса оставалась не вполне ясной. Можно было
думать о постстрептококковой неревматической природе иммунного воспале¬
ния, однако это недоказуемо.Кроме того, обнаружение в крови маркеров перенесенной сифилитиче¬
ской инфекции требовало исключения специфического поражения мио¬
карда. В современных руководствах по кардиологии и терапии сведения о
сифилитическом поражении сердца довольно скудны — главным образом, в
связи с крайней редкостью этого состояния. Пик морфологического изучения
сифилиса сердца пришелся, по-видимому, на 30-40-е гг. XX в. В руководстве
А.И. Абрикосова (1940 г.) читаем:«Сифилис самого сердца является большой редкостью. <,..> Многие кли¬
ницисты переоценивают сифилис как этиологический фактор заболеваний
сердца и неосновательно часто ставят диагноз: "сифилис сердца”, "сифили¬
тический эндокардит, миокардит, панкардит, коронарит" и т.д, в тех случаях,
когда дело идет о банальном неспецифическом (или ревматическом) миокар¬
дите, эндокардите или об атеросклерозе венечных артерий с кардиосклерозом
у больных с сифилисом в анамнезе или с положительной реакцией Вассермана.
<...> Настоящее сифилитическое поражение сердца имеет в основе развитие
Глава 13. Миокардиальный заскулит: путь к диагнозу... 239сифилитического процесса в миокарде. Изменения могут выражаться или в
образовании ту\ш, или в хроническом межуточном миокардите, обозначаемом
как гуммозный.Гуммозный миокардит представляет собой хронический межуточный про¬
дуктивный миокардит с распространением пролиферата из лимфоидных, плаз¬
матических клеток, единичных эозинофилов <...> снача^іа по ходу сосудов, а в
дальнейшем между мышечными волокнами».В более позднем руководстве по кардиологии Братислава Йонаша (1963 г):«Гуммы в миокарде обыкновенно не вызывают никаких определенных кли¬
нических признаков и, таким образом, они при жизни просматриваются <...>
Если при гуммозном процессе в межжелудочковой перегородке поражается
специфическая проводящая система, то могут появиться признаки расстрой¬
ства проводимости между предсердиями и желудочками или картина
блокады ножки пучка Гиса. Было также отмечено развитие полной предсердно-
желудочковой блокады с синдромом Эдемса-Стокса из неполной предсердно-
желудочковой блокады. Это явление необходимо оценивать в качестве тера¬
певтического парадокса.В настоящее время существование самостоятельного приобретенного
сифи-іитического миокардита без гумм большинством авторов берется под
сомнение, <...> в миокарде сифилитиков могут обнаруживаться свежие и
более старые специфические воспалительные изменения, также как и у лиц, не
страдающих сифилисом».Несмотря на некоторое сходство описываемой морфологической картины
сифилитического миокардита (не всегда г>т^мозного) с обнаруженной у нашего
больного, диагноз активной сифилитической инфекции все же мог быть отвер¬
гнут на основании серологических данных (отрицательная реакция Вассермана
с кардиолипином) и полного отсутствия симптомов поражения других органов
и систем.Кшнический диагноз бьиі сформулирован следующим образом: хронический
инфекционно-иммунный миокардит с явлениями продуктивного миокар¬
диального васкулита. Нарушения проводимости сердца: частотнозависимая
блокада левой ножки пучка Гиса. Гиперлипидемия 4-го типа. Хронический
стрептококковый фарингит. Атрофический ринитв течение мая 2009 г. больной получал мовалис 15 мг/сут, с 01.06.2009 г
(после получения результатов морфологического исследования) были назначе¬
ны метипред в начальной дозе 20 мг/сут и плаквенил 200 мг/сут; проводилась
также терапия ультопом (омепразолом) 20 мг по I капсуле на ночь, оротатом
калия 0,5 по 1 таб. 2 раза в день, конкором 2,5 мг по 1 таб. утром; с учетом
результатов посева из зева в течение 5 дней проведен курс терапии цифраном
500 мг по 1 таб. 2 раза в день.Больной переносил терапию удовлетворительно, соблюдал диету с ограни¬
чением жирной пищи, продолжал умеренные физические тренировки. За все
время лечения прибавил в весе не более 2 кг. Липидный спектр крови норма¬
лизовался. С 22.08 доза метипреда бьиа снижена до 16 мг/сут, с 15.09 начато ее
дальнейшее медленное снижение (на Уг таб. раз в 3 нед).
240КардиологияНа 4-м месяце терапии (09.09.2009 г.) после предварительной отмены кок-
кора по месту работы пациента проведено контрольное суточное мониториро-
вание ЭКГ по Холтеру: ритм синусовый, ЧСС 58—174 уд/мин (ср. 91 уд/мин).
Максимальная ЧСС достигнута на беговой дорожке. В течение суток — сину¬
совая аритмия, в ночной период единичные эпизоды брадиаритмии, СА бло¬
кады 2 степени и миграции источника ритма ио правому предсердию. Днем —
тенденция к умеренном^' учащению синусового ритма. Изменения конечной
части желудочкового комплекса по типу синдрома ранней ре поляризации
желудочков. Заключение: на фоне комплексной противовоспалительной тера¬
пии достигнута выраженная положительная динамика — отсутствие полной
блокады левой ножки пучка Гиса весь период регистрации ЭКГ {рис. 13.Я).Через 2 нед также на «чистом» фоне выполнен контрольный тредмил-тест;
время нагрузки 09:05, максимальная ЧСС 155 уд/мин, АД 163/75 мм рт.ст.,
максимальная рабочая нагрузка 10,3 МЕТ. Причина прекращения нагрузки —
достижение запланированной ЧСС (более 75% от 185 уд/мин). В покое—
синусовая аритмия дыхательного типа. Ответ ЧСС на нагрузку адекватный.
Боли в груди нет. Изменения сегмента ST: косовосходящее смещение (сивдром
ранней реполяризации). Эпизодов преходящей блокады левой ножки пучка
Гиса не зафиксировано (рис. J3.9). Проба нормальная,Планировалось также проведение контрольной сиинтиграфии миокар¬
да. В конце сентября больной перенес кратковременную простуду, в связи с
чем исследование отложено. Самочувствие пациента оставалось стабильным,
однако в ноябре при очередном нафузочном тесте вновь зафиксировано раз¬
витие преходящей блокады левой ножки пучка Гиса при ЧСС 134 уд/мин.16.11.2009 г. выполнен контрольный анализ крови на антикардиальные
антитела в лаборатории Федерального научііого центра трансплантологии
(табл. 13.2): отмечалось небольшое снижение титра антител к гладкой муску-
лат>'ре и проводящей системе по сравнению с исходными, отсутствие спец¬
ифического АНФ. С начала декабря пациент самостоятельно увеличил дозу
метипреда до 16 мг/сут, при контрольном иммунологическом анализе от25.02.2010 г — норма.тизапия титров антител к эндотелию и кардиомиопитам,Рис. 13.8. Фрагмент заииси контрольного холтеровского мониторттрования -ЭКГ у боль¬
ного С. При ЧСС 166 уд/мин блокада левой ножки пучка Гиса не регистрируется
Глава 13. Миокардиальный васкулит: путь к диагнозу...241ИСХОДНЫЙНАГРУЗКА00!yj/мия.0.03 иВ
0.S1 м ite4)910Л2Ш■О.ОЗ-0.S4-0.01 '
-І.Ї4aV-rf^
0.0J
0.52-0.02•0.11IVtAKC. ST
HAn>>3KA
9-.06І53 ул^ииї.
!63у7і m«HsМАКС.НАГРУЗКА остановкаНАГРУЗКА9:06153 удУмші,
тпі «MUgВОСГТАНОВ6.SSМ уд/мин,
BWSiwHg0.001.73■0.200.«i■0.22•l.«0.00173rr ^
-0.20
D.42m-0i22-1.6«?ІГГ.vtV*'0.ИI.S9■O.Zl-0.64Oil■1-34aVL0.111.59aVF«021•0.640.011.00-Л.09o.«sU1-0.11-0.69aVrft/Hv-
004
-1 44aVT^'^
O.lM
0.62■O.IO0.2SИСХОДНЫЙНАГРУЗКА0:0iJ5 удгчин.MAKC.STНАГРУЗКА$•06153 удчшн.
»631/75 HuHg;,?f
0.69 »Г«И-JМАКС.НАГтКАНАГРУЗКА9Й6153 удЛіив.163/75 «k(HgV2"^h V2-^|Л :0,410.410J5 ,4.38' 4,3« *1,4Ї !V4"^0.14;5.34.V5-^lr4>.07
?,00,4Vd-0.33ОСТАНОВКАboccTAHoa6:55!4 уа/я»к
133/85 imHgМ3...і
>.2б ІРис. 13.9. Диігамика комплекса QRS во время контрольного їрсдмил-теста у больною С.
Блокада левой ножки пучка Гиса, в том числе при максимальной ЧСС 153 уд/мин, не
регистрироваласьТаблица 13.2Уровень антикардиальных антител у больного С. в динамике. ЛТ — антителаФевраль 2009 г.16.11.2009 г.25,02.2010 г.АІіФ (сердце быка)1;80нетнетАтггитела к эндотелию1:801:80[:40Антитела к кардиомиоцитам1:801:801:40Антитела к гладкой мускулатуре1:1601:801:160Антитела к проводящей системе1:1601:801:80стойкое отсутствие АНФ, сохранение минимально повышенного титра анти¬
тел к проводящей системе (при некотором возрастании уровня антител к глад¬
кой мускулатуре, что можно рассматривать как первичный или вторичный
механизм повреждения мелких сосудов сердца).Начато снижение дозы метипреда, которая к маю 2010 г. (концу первого года
терапии) достигла 8 мг/сут. На этом фоне были выполнены контрольные холте-
ровское мониторирование ЭКГ (с максимальной ЧСС 130 уд/мин) и тредмил-тсст
(с максимальной ЧСС 160 уд/мин), при котором эпизодов преходящей блокады
левой ножки гг^’чка Гиса не зафиксировано. Дальнейшее снижение дозы метипре¬
да приостановлено. Прием плаквенила 200 мг/сут все это время продолжался.Таким образом, можно говорить о безусловной эффективности проводимой
больному двухкомпонентной иммуносупрессивной терапии и в то же время
242 Кардиологияо нестойкости достигнутого эффекта (временное возобновление эпизодов
блокады левой ножки пучка Гиса после перенесенной простуды). Несмотря
на минимальные (на сегодняшний день) клинические проявления миокар¬
диального васкулита (преходящая блокада левой ножки пучка Гиса, признаки
стрссс-индуцированной ишемии при сцинтиграфии миокарда), очевидна
необходимость длительной поддерживающей терапии и постоянного контроля
за состоянием больного. Его профессиональная судьба остается пока неопре¬
деленной.Комментарий A.B. Недоступа — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукДанное наблюдение представляет интерес с нескольких точек зрения. Прежде
всего оно убедительно демонстрирует наличие длительно текущих маїюма-
нифсстных форм миокардита. Действительно, единственным клиническим
проявитением миокардита было профсссирующее нарушение проводимости
по левой ножке пучка Гиса. Никаких ртных симптомов; признаков хрониче¬
ской сердечной недостаточности, кардиштгий, нарушений сердечного ритма,
увеличения размеров сердца, глухих тонов и т.д. — не было. Предположениео миокардите возникло у нас далеко не сразу. Мы наблюдали больного около
трех лет при регулярных консультативных осмотрах, но мысль о возможности
у него миокардита как причины блокады левой ножки пучка Гиса появилась у
нас лишь после того, как мы приобрели первый опыт выявления морфологи¬
чески яркого (что демонстрируют результагы эндомиокардиальной биопсии)
и клинически маломанифестного миокардита у больных с так называемыми
идиопати^іескими аритмиями. Собственно, мысль о возможности миокар¬
дита всегда должна возникать при неясных по происхождению нарушениях
ритма и проводимости, но отсутствие «классических» признаков .миокардита
до настоящего времени сразу исключало его наличие (или оставляло возмож¬
ность предположения о постмиокардитическом кардиосклерозе). Сегодня
мы можем верифицировать диагноз с помощью тонких методов лаборатор¬
ной (иммунологической) диагностики и биопсии сердца.Диагностические возможности эндомиокардиальной биопсшт, действительно,
уникатьны, и мы неоднократно убеждались в этом. Однако на вопрос о том,
будет ли эют метод когда-нибудь, достаточно безопасен, чгобы его можію было
рекомендовать к широкому использованию, сегодня трудно дать положитель¬
ный ответ. На сегодняшний день следует сосредоточить усшшя в области поиска
высокоинформативных лабораторно-инструментальных методов диагностики
воспалительного поражения сердечной мъшшьь Результаты использования нами
в настоящее время методики выявления антйкардиальных антител (антитела к
антигенам эндотелия, кардиомиоцитов, гладкой мускулатуры, волокон прово¬
дящей системы, лаборатория Федерального научного центра трансплантологии,
канд. мед. наук А Г. Куприянова, канд. мед. наук В. А. Зайденов, проф., д-р мед.
наук Л, В. Белецкая) позволяют надеяться на реальность достижения этой пели.
Еще одна важная деталь данного наблюдения — выявление у пациен¬
та распространенного васкулита сердца. Его наличие было заподозрено
Глава ІЗ. Миокардиальный васкулит: путь к диагнозу... 243по результатам сцинтиграфии миокарда (нараставшая при нагрузке гипо¬
перфузия перегородки, переднеперегородочной и нижнеиерегородочной
стенок при неизмененных коронарных сосудах по данным коронарографии)
и подтверждено эндомиокардиальной биопсией. Удивляет полное отсутствие
болей, столь характерных для синдрома X, а также ишемической депрессии
сегмента ST при тестах с физической нагрузкой. Аналогичную картину мы
видели и у других больных с выявленным в результате биопсии сердца мио-
кардіітом. Объяснить выявленную диссоциацию мы пока не можем.
Правильность диагноза подтверждают результаты терапии — исчезновение
блокады левой ножки пучка Гиса на фоне иммуносупрессивной терапии.
Роль инфекции в запуске иммунного механизма подтверждается рецидивом
возникновения блокады после перенесенного «простудного» заболевания (и
ее исчезновением после увеличения дозы преднизолона).
в целом приведенное наблюдение убеждает в большой вероятности гораздо
более широкого распространения хронических маломанифестных миокарди¬
тов и, вероятно, васкулитов, чем это принято считать в настоящее время.Механизмы развития у пациента преходящей блокады левой ножки пучка Гиса
в рамках миокардиального васкулита могут обсуждаться. В биоптатах отсут¬
ствуют очаги субэндокардиального липоматоза и интерстициального фиброза,
которые, по нашим данным, являются морфологическим маркером аритмий у
больных с миокардитом. Этот факт следует рассматривать как прогностически
благоприятный, поскольку данные изменения — в случае их появления — уже
не подвергаются обратному развитию. По-видимому, блокада левой ножки
пучка Гиса развивается как следствие нарастания ишемии при нагрузке, при
этом само по себе увеличение ЧСС облегчает развитие блокады иожки пучка
Гиса в результате того, что частота ритма превышает рефрактерный период
провоіиших волокон (феномен тахизависимой аберрации проведения хорошо
известен).В связи с представленным ютиническим наблюдением заслуживают обсуж¬
дения и некоторые другие вопросы. Изолированная блокада левой ножки
пучка Гиса редко становится предметом специальных исследований ввиду
относительной доброкачественности этого состояния. Можно ссьшаться лишь
на отдельные клинические наблюдения, в которых удавалось установить при¬
чину «идиопатической» блокады левой ножки пучка Гиса.1. Прежде всего при синдроме WPW на ЭКГ может определяться псевдо¬
блокада левой ножки пучка Гиса, что создает определенные диагностические
трудности и может потребовать дополнительного обследования. Описан слу¬
чай ошибочной диагностики блокады левой ножки пучка Гиса и инфаркта
миокарда у относительно молодой женщины с болями в сердце; позднее при
стресс-тесте воспроизведено появление типичной ЭКГ-картины предвозбуж-
дения. Возможна и обратная диагностическая ошибка: картина блокады левой
ножки пучка Гиса на ЭКГ может быть трудно отличима от признаков предвоз-
буждения, особенно если она выявляется у молодого «здорового» пациента.
Нам известен такой случай; пациентке 45 лет с картиной «синдрома WPW» и
244 Кардиологияприступами учащенного сердцебиения, жительнице Дальнего Востока, дважды
выполня.аась попытка радиочастотного устранения дополнительного пути про¬
ведения, однако оба раза неудачно; диагноз был пересмотрен в пользу блокады
левой ножки пучка Гиса, для выяснения этиологии которой была выполнена
биопсия правого желудочка. Выявлена картина хаотичного расположения
кардиомиоцитов, характерная для генетических кардиомиопатий, однако в
связи с отсутствием на данном этапе других клинических проявлений, которые
помогли бы сузить крут предполагаемых диагнозов, проведение молекулярно¬
генетической диагностики представляет значительные трудности.2. По jmTepaxypHbiM данным, появлением блокады левой ножки пучка Гиса
может манифестировать целый ряд генетически детерминированных заболева¬
ний миокарда:— прогрессирующие семейные блокады серлда; заболевание наследуется
по аутосомно-доминантному типу; избирательное поражение системы Гиса-
Пуркинье описано при мутапиях в генах кальциевых кана.юв (локус хромосо¬
мы 19ql3.3);— синдром некомпактного миокарда, при котором блокада левой ножки
пучка Гиса может бьггь ранним и едршственным проявлением (до развития
клинически значимой сердечной недостаточности).3. Блокада левой ножки пучка Гиса может быть ранним проявлением пора¬
жения сердца в рамках саркоидоза, которому посвящена следующая глава
данного сборника, хотя для этого заболевания гораздо более типично развитие
блокады правой ножки пучка Гиса. По-видимому, и другие редкие кардиоми-
опатии могут манифестировать нарушением проводимости по левой ножке
пучка Гиса.4. В частности, есть данные о том, что при кардиомиопатии такотсубо
частота выявления блокады левой ножки пучка Гиса составляет 9%, хотя кли¬
ническая картина этого состояния является достаточно яркой, острой, и вслед
за выявлением блокады левой ножки пучка Гиса обнаруживаются и другие диа¬
гностические признаки.5. Описано развитие блокады левой ножки пучка Гиса (как правило, обрати¬
мой) под действием различных средств, не относящихся к разряду кардиотроп-
пых: севофлюрана, ремифснтанила; тразтуцумаба. По-видимому, это следует
учитывать при лечении и другими относительно новыми препаратами, в част¬
ности, относятцимися к группе биологических агентов.6. Наконец, блокада левой ножки пучка Гиса может быть единственным
кардиальным проявлением системного васкулита: описано развитие блокады
на фоне синусовой тахикардии у 21-летней пациентки с бронхиальной астмой;
в крови были выявлены гиперэозинофилия и повышение уровня тропонина;
возможные причины вторичной эозинофилии были исключены.Довольно трудны для интерпретации локальные нарушения сократимости
и перфузии левого желудочка, которые определяются у больных с блокадой
левой ножки пучка Гиса, что видно и на примере нашего больного: перво¬
начально нарушения перфузии, выявленные при сцинтиграфии миокарда,
были расценены как следствие блокады левой ножки пучка Гиса, но не как
Глава 13. Миокардиальный васкулит: путь к диагнозу^.. 245ее возможная причина. Данные литературы также весьма разноречивы. Так,
при блокаде левой ножки пучка Гиса у больных с сохранной функцией левого
желудочка нарушения перфузии по данным стресс-теста с дипиридамолом в
38,5% сочетаются с нормальной коронарограммой (особенно часто у женшин),
что, по-видимому, может отражать иные (неатеросклеротические) механизмы
нарушения интракоронарного кровотока. По другим данным, дефект перфу¬
зии в переднесептальном и верхушечном сегментах по данным стцштиірафии
миокарда с ^^Тс-М1В1 у больных с блокадой левой ножки пучка Гиса отражает
значимый (более 50%) стеноз передней межжелудочховой артерии (чувстви¬
тельность теста составила 88%, специфичность — 67%); отсутствие апикаль¬
ного дефекта перфузии по данным сцинтиграфии миокарда с ^^Тс-М1В1 спе¬
цифично для интактности передней межжелудочковой артерии.Было показано также, что нарушения перфузии перегородки (по данным
сцинтиграфии) при блокаде левой ножки пучка Гиса и стимуляции правого
желудочка идентичны, что как будто подтверждает вторичное (по отноше¬
нию к ненормальной последовательности возбуждения желудочков) проис¬
хождение этих нарушений. В то же время установлено, что дефекты перфузии,
возникаюш;ие при спонтанной или индуцированной с помощью стимуляции
блокаде левой ножки пучка Гиса, усиливаются при нагрузке (по данным фотон¬
ной эмиссионной компьютерной томографии) и частично обратимы в покое.
Развитие септальньгх дефектов перфузии вследствие блокады левой ножки
пучка Гиса подтверждено в эксперименте, причем в качестве механизма рас¬
сматривается перераспределение кровотока в результате снижения функцио¬
нальной нагрузки на межжелудочковую перегородку.Тем не менее наш случай показывает, что интерпретация локальных (пре¬
имущественно септальных) нарушений перфузии у больных с блокадой левой
ножки пучка Гиса не должна сводиться к констатации вторичньи функцио¬
нальных изменений, связанных с самой блокадой, — у пациента дефекты пер¬
фузии нарастали со временем, что заставило исключать самостоятельное пора¬
жение интрамиокардиальньЕк сосудов; кроме того, блокада левой ножки пучка
Гиса носила у него преходяшлй характер. Корреляция подобных нарушений
перфузии с поражением передней межжелудочковой артерии также говорит о
том, что блокада левой ножки пучка Гиса может быть не только их причиной,
но и прямым следствием.Наконец, необходимо сказать о тех данных, которые имеются в литературе
относительно поражения мелких коронарных артерий у больных с клиничес¬
кой картиной стенокардии, сердечной недостаточности и нарушениями ритма.
Хорошо известен диагноз «коронарный синдром X», который обычно ставится
при доказанной ишемии в отсутствие поражения крупных коронарных арте¬
рий. По сути дела, это не нозологический диагноз (не случайно — «синдром»), а
констатация нашего незнания механизмов развития ишемии миокарда в отсут¬
ствие атеросклероза крупных коронарных артерий. Несколько точнее офажает
суть происходящего у подобных больных термин «микроваскулярная стено-
кардия», который мы предпочитаем использовать. Однако природа поражештя
мелких коронарных сосудов остается не вполне понятной. Кроме того, далеко
246Кардиологияне всегда их поражение проявляется именно стенокардией, что хорошо и;ыю-
стрирует представленное клиническое наблюдение. Как уже бьшо сказано в
предыдущей главе, биопсия миокарда остается фактически единственным
методом оценки состояния интрамиокардиальньгх сосудов.В работе М. Mosseri и соавт. (1986) проведена эндомиокардиальная биопсия
шестерым больным с типичной стенокардией и неиз.мененными коронарны¬
ми артериями (по данным ангиографии). Клинически у них имелись также
застойная сердечная недостаточность, наджелудочковые нарушения ритма,
различные нарушения проводимости. В биоптатах были выявлены измене¬
ния как мелких сосудов (набухание и дегенерация эндотелиальных клеток,
гиперпластическое фибромьгаїечное утолщение стенок мелких артерий и
капилляров, уменьшение просвета сосудов), так и кардиомиоцитов (сочетание
гипертрофии и дегенерации миофибрилл, включения липофусцина, участки
липоматоза), что обозначено авторами как болезнь мелких сосудов. Приведем
описание двух больных из этой публикации.У первого пациента 44 лет боли по типу стенокардии возобновились через
3 года после успешного стеіітирования коронарной артерии, однако при повтор¬
ной коронарографии стенозов выявлено не бьшо. По данным ЭхоКГ, имелась
умеренная гипертрофия межжелудочковой перегородки (15 мм). В биоптатах
правого желудочка выявлены умеренная гипертрофия миофибрилл и выражен¬
ное утолщение интрамуральных коронарных артерий (рис, 13.10, а). При окра¬
ске на соединительную ткань отмечена преимущественная фибромускулярная
гиперплазия медии при малоизмененной интиме. При электронной микро¬
скопии (рис. 13.10, 6) видно, что NmKpococvflbi спазмированы, зндотелиаіьньїе
клетки имеют патологический вид.У второш пациента 72 лет стенокардия (с типичной динамикой сегмента ST
во время приступа) отмечаїась в течение 14 лет; со временем развились застой¬
ная сердечная недостаточность, мерцательная аритмия, АВ-блокада, которая
потребовала имплантации ЭКС, умеренная артериальная гипертония. За этиа бРис. 13.10. Поражение интрамиокардиальных сосудов по данным биопсии право¬
го желудочка у больного 44 лет (М. Mosseri и соавт, 1986): а — большое увеличение;
б — электронная микроскопия. Пояснения в тексте
Глава 13, Миокардиальный васкулит: путь к диагнозу...247Рис. 13.11. Поражение интрамиокардиаль-
ных сосудов по данным биопсии правого
желудочка у больного 72 лет (М. Mosseri,
1986). Большое увеличение. Пояснетіия
в текстегоды коронарография выполнялась
трижды, изменения в коронарных
артериях отсутствовали. Кроме того,
пациент неоднократно госпитализи-
роваїся в связи с потерей массы тела,
железодефицитной анемией, тром-
боцитопенией (которая усилилась
при назначении хинидина), паро¬
титом, лимфоаденопатией, генато-
спленомегалией. Был заподозрен
системный васку.іиг, но при биопсии
.тимфоузлов, костного мозга, слюн¬
ной железы, кожи, десны не было
выявлено поражения мелких арте¬
рии. При последнем обследовании
выявлены признаки гипертрофии
левого желудочка (тМЖП 14 мм),
небольшой выпот в перикарде; прикоронарографии — чистые коронарные артерии, снижение скорости движения
контрастного вещесгва. Вбиоптатах правого желудочка {рис. 13.il)— выра¬
женный jrnnoMaToa, утолщение стенок артерий (пролиферация гладких мыпгц,
коллаген).Авторы вьщеляют следующие клинические особенности болезни мелких
сосудов сердца:• стенокардия типичная, хорошо купируется нитратами, может носить про¬
грессирующий и нестабильный характер;• нарушения ритма и проводимости разнообразны, но желудочковые встре¬
чаются редко (мерцательная аритмия, предсердная тахикардия, блокады в
системе ножек пучка Гиса);• во время нагрузочного теста типично появление боли без динамики сег¬
мента ST (5 больных), лишь в одном случае зафиксирована типичная
депрессия ST (без боли);• при ЭхоКГ типично выявление гипертрофии межжелудочковой перего¬
родки;• ФВ левого желудочка остается нормальной (57—77%), отсутствует легоч¬
ная гипертензия;• диастолическая дисфункция коррелирует с клиникой застойной сердеч¬
ной недостаточности (у двух больных).Мы остановились на особенностях невоспалительного поражения мелких
сосудов, нозологическая принадлежность которого остается неясной: можно
думать о вторичных изменениях мелких сосудов в рамках атеросклероза (в том
числе без поражения крупных коронарных артерий), гипертонии, гипертро¬
фии миокарда, различных метаболических расстройств (сахарного диабета,
возможно, дисгормона^чьной миокардиодистрофии, ожирения), амилоидоза.
Описано также выраженное утолщение стенок интрамиокардиальных сосудов
248 Кардиология(за счет коллагеновых и эластических волокон и субэндотелиальных депози¬
тов, состоящих из аморфной субстанции) у больных без каких-либо факторов
риска («идиопатическая болезнь мелких сосудов»).Однако не реже (если не чаще) поражение мелких сосудов сердца носит
характер васкулита, который развивается в рамках миокардита, диффузных
заболеваний соединительной ткани, системных васкулитов и, по-видимому, в
отдельных случаях — изолированно.Причины миокардиального васкулита:• миокардит:— первичный,— в рамках других заболеваний (системная красная волчанка, саркоидоз,
ревматоидный артрит, воспалительные заболевания кишечника и др.);• системные васкулиты:— болезнь Кавасаки,— болезнь Такая су,— синдром Черджа—Стросс,— іранулематоз Вегенера,— болезнь Бехчета,— гиттерсснситивный (аллерпріеский) васкулит;• идиопатический миокардиальный васкулит:— рестриктивная кардиомиопатия (эффективна терапия стероидами и
циклофосфамидом),— «идиопатическая» желудочковая тахикардия, фибрилляция желудочков.Для болезни Кавасаки характерно образование аневризм коронарных сосу¬
дов, поражение мелких сосудов развивается в рамках нередкого при этом забо¬
левании миокардита. При болезни Бехчета описывают развитие эндрмиокар-
дита с микротромбозами коронарных артерий, перикардита, острого инфаркта
миокарда, аневризм, внутрижелудочкового тромбоза, застойной кардиомиопа-
тии и клапанной дисфункции. Оба заболевания развиваются преимущественно
у детей.Синдром Черджа—Стросс относится к системным васкулитам с преимуще¬
ственным поражением мелких сосудов: вовлечение в воспалительный процесс
миокардиальных сосудов является при этом вполне закономерным. Поражение
сердца носит характер эндомиокардита с вовлечением клапанов, реже — пери¬
кардита и во многом определяет прогноз заболевания. Ключевым лабора¬
торным маркером синдрома Черджа-Стросс является высокая эозинофилия
крови, однако у больных с поражением сердца она определяется реже, чем без
него; для них типично также отсутствие антител к цитоплазме нсйірофилов, что
осложняет диагностику этого варианта васкулита. Типичная клиническая кар¬
тина включает эозинофильную бронхиальную астму, мононевриты, поражение
кожи, однако описано и практически изолированное поражение сердца с разви¬
тием некротического васкулита {рис. 13.12). Нам приходилось сталкиваться со
своеобразной формой этого заболевания, при которой, несмотря на сочетание
у молодой женшдны преходящей эозинофилии, стенокардии, мерцательной
аритмии, геморрагической сыпи, признаков поражения церебральных сосудов,
Глава 13. Миокардиальный васкулит: путь к диагнозу,..249Рис. 13.12. Некротаческий эозинофильный
васкул ИТ (А) у пациента с синдромом Ч ерджа—
Стросс (Frustaci А., 1998). Пояснения п текстеВ биоптатах миокарда были выяв¬
лены признаки весьма умеренного
миокардита с васкулитом, который
не носил характера некротического.При болезни Такаясу, поража¬
ющей преимущественно аорту и
ее ветви, развитие миокардита с
выраженным поражением мелких
сосудов в результате отложения
иммунных комплексов в эндотелии
также не является исключением.Мы наблюдали пациентку 40 лет, у
которой в течение 10 лет отмечаїшсь
выраженное повышение СОЭ (до
40—70 мм/ч), лабораторные марке¬
ры воспаления, однако клиническая симптоматика оставалась минималь¬
ной, подробное обследование не позволяло выявить причину лабораторных
изменений; развитие картины дилатационной кардиомиопатии и сердечной
недостаточности стало первым серьезным проявлением болезни. В качестве
непосредственного механизма поражения интрамиокардиальных сосудов при
гиперсенситивном (аллергическом) васкулитс также описывают утолщение
базальных мембран артериол и капилляров. Типичным следствием дегрануля¬
ции эозинофилов является развитие микротромбозов; характерно вовлечение
в воспалительный процесс эндокарда.Гранулематоз Вегенера, как правило, не приводит к тяжелому поражению
миокардиальных сосудов, однако в рамках этого АМСА-ассоциированного
васкулита с ііекротическим поражением верхних дыхательных пугей, легких
и почек возможно развитие миокардита, перикардита, артериита; поражение
эндокарда с вальвулитом в ряде случаев требует проведения дифференциаль¬
ного диагноза с инфекционным эндокардитом.В литературе всіречаются отисаиия и других форм системных васкулитов с
ювлечением сердца (например, лейкокластического с развитием лихорадки, пур¬
пуры, множественных инфарктов печени и легочных геморрагий) - по-видимому,
далеко не все формьт еще приобрели нозологи^їескую определенность.у натпсго пациента полностью отсутствовали признаки системного пора¬
жения, не было выявлено в крови повышенного титра антител к цитоплазме
нейтрофилов; ни разу не регистрировался повышенный уровень эозинофилов.
Кроме того, выраженность собственно миокардита (межуточного воепаления)
была у него небольшой по сравнению с поражением микрососудов.В литературе встречаются лишь единичные упоминания изолїфованного
миокардиального васкулита. Так, описана больная 61 года, имевшая клини¬
ческую картину рес'іриктивной кардиомиопатии, устойчивой к лечению. На
ЭКГ выявлялись низкий вольтаж комплексов QRS, АВ-блокада I степени, при
ЭхоКГ — атриомегалия, ФВ 60%, тМЖП 12 мм, тЗС 11 мм, СДЛА 42 мм рт.ст.,
при МРТ сердца данных за констриктивный перикардит получено не было.
250 КардиологияБыла выполнена эндомиокардиальная биопсия правого желудочка: выявлены
расширение и фиброз интерстиция, амилоида нет; в связи с отсутствием в био-
птатах интрамиокардиальных сосудов биопсия сердца была выполнена повтор¬
но открытым доступом, при этом обнаружены периваскулярные инфильтраты
с некрозом сосудистой стенки и формированием микроаневризм (рис. 13.13).
После исключения всех возможных причин васкулита, включая различные
формы системного васкулита, был поставлен диагноз «идиопатичесюїй мио¬
кардиальный васкулит», проведена иммуносупрессивная терапия (прсднизо-
лон 1,5 мг/кг в течение недели, далее 1 мг/кг, циклофосфан 2 мг/кг, затем в
течение 6 мес — преднизолон 0,33 мг/кг и циклофосфан 0,5 мг/кг) , в результате
которой явления сердечной недостаточности регрессировали.Упомянем также случай изолированного лимфоцитарного миокардиально¬
го васкулита у одного из 12 больнььх с необъяснимыми уірожающими жизни
аритмиями {рис. 13.14) — интерстициальное воспаление у больного полностью
отсутствовало.Таким образом, миокардиальный васкулит, в том числе изолированный —
реальное заболевание, имеюшее широкий спектр клинических проявлений, в
чем убедили нас еще два собственных клинических наблюдения, которые мы и
приводим в завершение данной главы.Больная Г., 61 года, посіупила в отделение кардиологии Факультетской
терапевтической клиники им. В.Н. Виноградова 02.12.2008 г с жоіюбами на
приступы сжимающих болей за грудиной и в области сердца, возникающие
при небольших физических нагрузках, иррадиирующие в левую руку, быстро
купирующиеся приемом нитроглицерина, одышку при небольших физиче¬
ских нагрузках (подьем по лестниде на 1-2 пролета), возникающие в раз¬
личное время суток приступы удушья, которые сопровождаются онемением
рук, постепенно купируются после дополнїггельного приема нитроглицерина,
преходящие отеки голеней и стон, приступообразный сухой кашель, возника¬
ющий в различное время суток, перебои в работе сердца, короткие приступы
учащенного неритмичною сердцебиения, нечастые подъемы АД до 150 и80 мм рт.ст. при обычном АД 120—110 и 70—80 мм рт.ст.Анамнез жизни: в детстве часто
болела ангинами, которые явны¬
ми осложнениями не сопрово¬
ждались; тонзиллэктомия не про¬
водилась. В юношеском возрасте
ангины прекратились. На про¬
тяжении всей жизни физические
наїрузки переносила хорошо, в
течение 9 лет работала рентген-Р»с. 13,13. Иднопатический миокарлиаль- лаборантом, в качестве медсестрыный васкулит у больной С рестриктивной кар- контактировала с пенициллиномдиомиопатией (Fnistaci Д., 1997), Пояснєїшя (что привело к развитию дермати-в тексте та предплечий; отмечались также
Глава ІЗ. Миокардиальный васкулит: путь к диагнозу...251Рис. 13.14. Изолированный лимфоцитар¬
ный инфильтрат вокруї' венульт у больно¬
го 28 лет, пережившего внезапную смерть
(HosenpLid J.D., 1986). Пояснения п текстеаллергические реакции на в/в вли¬
вание раствора глюкозы — лихо¬
радочная реакция, отек Квинке).Во время беременности перенесла
пиелонефрит. Акушерский анам¬
нез без особенностей, менопауза
с 40 лет. Страдает хроническим
бронхитом с астматическим ком¬
понентом (обострения до двух раз
в год в виде лихорадки, продуктив¬
ного кашля, антибактериальная
терапия с эффектом, последнее
обострение — в декабре 2006 г.),
язвенной болезнью желудка (выяв¬
лена в мае 2008 г., сопровождаласьболями в эпигастрии, проведен курс лечения), мочекаменной болезнью; в
2002 г. проведена холецистэктомия, около 10 лет — сахарный диабет, с мая
2008 г. проводится терапия глюкофажем 500 мг/д, уровень гликемии обычно
не превышает 7 ммоль/л.Анамнез заболевания {рис. 13.15)\ около 10 лет назад (в 1998 г., в возрасте
51 года) без видимой причины стачи беспокоить сжимающие, жгучие боли
за грудиной при умеренной физической нагрузке, которые conpOBO*4ajiHCb
иррадиацией в левую руку, быстро купировались нрггратами. Постоянная тера¬
пия не проводилась. Иногда фиксировались подъемы АД до 150 и 80 мм рт.ст,
(при обьічном АД 110 и 70 мм рт.ст.). В 2000 г (53 года) развился интенсивный
приступ болей за грудиной, по поводу которого была госпитализирована в
сельскую больницу, на основании клинической картины и изменений на ЭКГ
состояние было расценено как распространенный переднеперегородочный
инфаркт миокарда. В дальнейшем приступы загрудинных болей сохранялись,
появилась небольшая одышка, проводилась терапия нитратами.В апреле 2006 г. была повторно госпитализирована (в ГКБ № 70) в связи
с выраженным приступом загрудинных болей, определение кардиоспеци-
фичных ферментов не проводилось, на основании динамики ЭКГ состояние
было расценено как повторный инфаркт миокарда нижней стенки без Q-зубца
(сформировались отрицательные зубиы Т, выявлены блокада передней ветви
левой ножки пучка Гиса, комготексы QS в отведениях V,-V,). При ЭхоКГ был
выявлен гипокинез верхушки с переходом на нижнюю треть межжелудочковой
перегородки, снижение ФВ левого желудочка до 47-50%, митральная регур-
гитация I степени (размеры камер и толщина стенок в пределах нормы), при
сцинтиграфии миокарда в покое — гипоперфузия передне перегородочной (1—2
сегмента из 17) и нижне-задней (3-4 сегмента из 17) стенок левого желудоч¬
ка, убедительных данных за крупноочаговое рубцовое поражение миокарда
не получено; при холтеровском мониторировании ЭКГ нарушений ритма и
депрессии сегмента STне отмечено. Через 2 нед отметила учащение приступов
стенокардии, в НИИ скорой по.моши им. И.В. Ск^аифосовского проведена
252Кардиология1998 200020062008ангиныбронхитстенокардияодышкаэкстрасистолияблокада ПВЛНПГ
фракция выбросатерапия111 Iі ІМІІ і47%40%35%нитратымономак
конкор
аспирин
престариум
тулипРис. 13.15. Анамнез больной Г., 61 годверошпиронфуросемидкоропароангиография, при которой изменений в коронарных артериях не выяв¬
лено, тип кровоснабжения правый. Была подобрана терапия мономаком
80 мг/с>т, конкором 5 мг/сут, тромбо-АССом 100 мг, престариумом 2 мг/сут,
тулипом 10 мг/сут (уровень холестерина составлял 7—8 ммоль/л), на фоне
которой тфиступы стенокардии сохранялись, реже требовали дополнительного
применения нитратов.В декабре 2006 г, перенесла ангину, обострение хронического бронхита;
примерно с этого времени стали отмечаться нечастые перебои в работе серд¬
ца, кратковременные (не больше нескольких мин>т) эпизоды неритмичного
сердцебиения, которые врачом при физическом исследовании расценивались
как мерцательная аритмия; однако на ЭКГ она не зарегистрирована, терапия
кордароном проводилась кратковременно. Стала заметно нарастать одышка
при небольших физических или эмоциональных нафузках, а также в покое,
появился сухой приступообразный кашель, участились приступы стенокардии.
При контрольной ЭхоКГ (март 2007 г., госпитализация в Городскую клиниче¬
скую больницу № І 5 г. Москвы) отмечено дальнейшее снижение ФВ левого
желудочка до 38-40%, диастолическая дисфункция левого желудочка; при
холтеровском мониторировати зафиксированы пароксизм наджелудочковой
Глава 13. Миокардиальный васкулит: путь к диагнозу... 253тахикардии (ЧСС 133/мин) длительностью 3 мин, который сопровождался
нарастанием одышки, единичные желудочковые экстрасистолы. К терапии
были добавлены верошпирон, фуросемид.С начала 2008 г. наряду с приступами стенокардии и выраженной одыш¬
кой появились приступы удушья, которые провоцировались назначительной
физической (или эмоциональной) нагрузкой; с одним из приступов была
в апреле госпитализирована в Городскую клиническую больницу № 70 г.
Москвы, где проводилась консервативная терапия с некоторым эффектом.
В мае находилась на обследовании в отделении приобретенных пороков
сердца в Научном центре сердечно-сосудистой хирургии им. А.Н. Бакулева.
При холтеровском мониторировании зарегистрировано 1200 желудочковых
экстрасистол двух морфологий, единичные наджелудочковые экстрасисто¬
лы и короткие (до 4-х комплексов) пробежки наджелудочковой тахикардии;
антиаритмики не назначались, при повторном исследовании (конкор 2,5 мг)
число экстрасистол снизилось до 215. Уровень антител к кардиолипину не
определялся, изменений в других иммунологических анализах, дистиреоза
не выявлено. Повторно проведена коронарография, при которой измене¬
ний также не выявлено, и ангиография почечных артерий (стенозов нет).
По данным ЭхоКГ, МРТ сердца и МСКТ сердца размеры камер сердца суш;е-
ственно не увеличены, ФВ левого желудочка колебалась в пределах 35-40%,
бьша выявлена выраженная желудочковая диссинхрония (в отсутствие пол¬
ной блокады левой ножки пучка Гиса); имелись нарушения локачьной
сократимости по данным ЭхоКГ и МРТ: гипокинез верхушечной, передне-
перегородочной областей левого желудочка, акинез верхушки, элементы
дискинеза передней стенки, акинез верхушки правого желудочка и дис-
кинез с истончением его передней стенки; снижение перфузии заднеба¬
зальных отделов левого желудочка по данным сцинтиграфии, гипокинез
заднебазального сегмента по данным вентрикулографии. Давление в легоч¬
ной артерии составляло 20—40 (32) мм рт.ст. по данным вентрикулографии,
45—50 мм рт.ст. по данным ЭхоКГ. Отмечено также нарушение трансмитраль¬
ного кровотока (от диастолической дисфункции до рестрикции), небольшое
количество жидкости в полости перикарда (по данным МРТ — сепарация
листков перикарда до 4 мм), его локальное утолщение до 6 мм и перикарди¬
альные спайки (по данным МСКТ и МРТ).Диагноз оставался неясным, наиболее вероятным представлялось наличие
постмиокардитического кардиосклероза, не исключался амилоидоз. Бьша
направлена на продолжение обследования в Факультетскую терапевтическую
клинику им. В.Н. Виноградова, терапия оставалась прежней (доза верошпиро-
на составляла 25 мг/сут); мономак и фуросемид больная принимала по потреб¬
ности; приступы стенокардии сохранялись.В июне 2008 г. была проконсультирована в Факультетской терапевтиче¬
ской клинике им. В.Н. Виноградова, рекомендовано определение антитезі к
миокарду, стрептококку и кардиотропным вирусам, которые по данным двух
лабораторий оказались умеренно повышены: антитела к миокардиальной
ткани класса TgG 1:300, к стрептококку 1:400 (норма 1:100), к вирусу герпеса
254 Кардиологиязостер 1:800 (норма), к цитомегаловирусу 0,8 (норма), к вирусу простого
герпеса 1 типа 2,0 (>1,2 положит.) и второго типа — 0,3 (норма), антител
к вирусу Эпштейна-Барр не обнаружено (лаборатория «МедБиоСпектр»).
АНФ с антигеном сердца быка выявлен не был, титр антител к антигенам
эндотелия составил 1:40, к кардиомиоцитам и гладкой мускулатуре 1:80,
к волокнам проводящей системы — 1:160 (норма 1:40, Федеральный науч¬
ный центр трансплантологии). Планировалось проведение эндомиокарди¬
альной биопсии, от которого больная на тот момент отказалась. С учетом
трехкратного повышения титра антител была начата терапия плаквенилом
200 мг/сут, продолжался прием кардиотропной терапии (в том числе верош-
пирон 100 мг, фуросемид 1—2 раза в неделю). Самочувствие улучшилось,
повысилась толерантность к физическим нагрузкам. В повторном анализе
крови от 22.09.2008 г. — АНФ и антитела к антигенам эндотелия не обна¬
ружены, титр антител к кардиомиоцитам и волокнам проводящей системы
составил 1:80, к гладкой мускулатуре — 1:40. Доза верошпирона была сни¬
жена до 50 мг/сут, прием фуросемида прекратила.Проведена ЭхоКГ (проф. В.П. Седов), при которой данных за инфильтра-
тивное поражение миокарда не получено, выявлен гипокинез заднебазальных
отделов левого желудочка, ФВ желудочка составила 46%, толш;ина стенок и
размеры камер сердца в пределах нормы, имелось небольшое количество жид¬
кости в полости перикарда, митральная регургитация минимальна.Ухудшение состояния — с конца ноября, когда вновь заметно наросла
одышка при незначительных физических нагрузках, возобновились приступы
удушья, сухого капыя, боли за фудиной. Поступила в Факультетскую тера¬
певтическую клинику им. В.Н. Виноградова для повторного обследования и
коррекции терапии.При поступлении состояние средней тяжести. Кожные покровы сухие, акро-
пианоз. Периферических отеков нет. Периферические лимфоузлы не увеличе¬
ны. В легких дыхание жесткое, хрипы не выслушиваются. Число дыханий 24
в минуту. Тоны сердца звучные, на фоне правильного ритма выслушиваются
экстрасистолы 2-4 в минуту. ЧСС 74 в минуту, АД 110/70 мм рт.ст. Живот
мягкий, безболезненный во всех отделах. Печень, селезенка не увеличены.
Симптом Пастернацкого отрицателен с обеих сторон. Щитовидная железа не
увеличена.В общем анализе крови без отклонений от нор\га: НЬ 126,5 г/л, эритроциты
4,1 млн, цветовой показатель 0,93, лейкоциты 7,2x1 ОУл, нейтрофилы 62,5%,
лимфоциты 23,4%, моноциты 8,4%, эозинофилы 4,7%, базофилы 1%, СОЭ
6 мм/ч, тромбоциты 277,2 тыс.В биохимическом анализе — начальные признаки почечной недостаточ¬
ности, гипергликемия: общий белок 78,0 г/л, альбумин 49,5 г/л, креатининI,47 мг/дл, глюкоза 5,9 мг/дл (в 11 ч— 6,0 ммоль/л), азот мочевиныII,3 ммоль/л (9,8), мочевая кислота 642,7 мкмоль/л (434,5), общий билиру¬
бин 19Д мкмоль/л, пр. билирубин 3,8 мкмоль/л, натрий 146 мэкв/л, калий
4,7 мэкв/дл, железо 89 мкг/дл, кальций 2,47 ммоль/л (2,08-2,65), Ферменты
сыворотки без отклонений от нормы: ACT 19 ед/л, АЛТ 4 ед/л, у-ГТ 21 ед/л.
Глава ІЗ. Миокардиальный васкулит: путь к диагнозу... 255ЩФ 64,3 ед/л, ЛДГ 293 ед/л, холинэстераза 10960 ед/л, КФК 61,1 ед/л,
МВ-КФК 1 ед/л.Электрофорез белков в пределах нормы: альбумин 63,5%, альфа-1 3,1%,
альфа-2 8,8%, бета 11,9%, гамма 12,7%.Липидный спектр-, триглицериды 237 мг/дл (50-150), общий холестерин
267 мг/дш (150-250), ЛВП 39,9 мг/дл (27-89), ЛПОНП-хс 47,4 мг/дл (10-30),
коэффициент атерогенности 5,69. На фоне возобновления терапии статика¬
ми триглицериды 216 мг/дл, обший холестерин 134 мг/лд, ЛВП 29,4 мг/дл,
ЛПОНП-хс 43,2 мг/дл.Коагулограмма: АЧТВ 1,24, протромбиновый индекс 99%. фибриноген
4,22 г/л.Гормоны щитовидной железы: Tj(cyMM.) — 1,99 нмоль/л (1,0—3,0), Т4(своб.) —
19,0 пмолъ/л (норма 10-25), ТТГ 6,0 МЕ/л (0,3-4,0). Антитела к ТПО 11,0 МЕ/мл.HBs Ag, HCV, реакция Вассермана отрицательны. Антитела к ВИЧ не выяв¬
лены.При развернушм иммунологическом исследовании отклонений от нормы
также выявлено не было: комплемент — 36,6 гем.ед. (20—40), антитела к ДНК
1,11 МЕ/мл (0—20), антитела к кардиолипинам IgM 0,67 ME/.\li (0—7), IgG0,29 МЕ/мл (0—10), АНФ отрииат., СРБ — отрицат., антистрептолизин-О — О,
РФ отрипат, cANCA (антитела к протеиназе 3) О ЕД/мл, pANCA (антитела к
миелопероксидазе) 0,71 МЕ/мл (норма 0-5).В общем анализе мочи pH 5, уд. вес 1012, мутная, белка, сахара, ацетона,
желчных пигментов нет, лейкоциты 2—6 в п/зр., эритроциты едан. в поле зре¬
ния, слизь в умеренном колйгчестве, бактерий значительное количество.Обращали на себя внимание своеобразные изменеиия на ЭКГ {рис. 13.J6)'.
ритм синусовый, политопная (лево/правожелудочковая) зкстрасисі олия, элек¬
трическая ось сердца резко отклонена влево. ЧСС 56 уд/мин. Зубец Р упло¬
щенный, 0,18 с, QRS 0,11 с, QT/QTc 464/440 мс. Недостаточное нарастание
зубцов R в грудньгх отведениях, комплексы QS в отведениях Vj-Vj, снижение
амплитуды зубца R (до 1 мм) и уплощенные/отрицательные зубцы Т в отведе¬
ниях II, ІП, aVF. В динамике (на фоне терапии кордароном 600 мг/сут) расши¬
рение комплекса QRS до 0,14 с.При холтеровско.ч мониторировании ЭКГ, проведенном на фоне терапии
конкором 2,5 м1’/сут, ритм синусовый. Миграция водителя ритма по пред¬
сердиям. ЧСС днем 54-108/мин (ср. 70/мин), ночью 48—95/мин (ср. 60/мин).
Наджелудочковые экстрасистолы, всего 45, эпизод наджелудочковой тахикар¬
дии из 8 Q/?5c ЧСС 150/мин. Политопные желудочковые экстрасистолы, в том
числе поздние, сливные, всего 5600, максима^'іьно 490/ч (с 7:00 до 8:00), кушю-
тов 27, частые эпизоды би-, тригеминии. ST-T: без диагностически значимой
динамики.Исследование было выполнено повторно после насыщения кордаро¬
ном (на фоне приема 400 .мг/сут), отмечен полный антиаритмический
эффект препарата: ритм синусовый. ЧСС днем 62-і 11/мин (ср. 67/мин),
ночью 49—79/мин (ср. 57/мин). Наджелудочковые экстрасистолы, всего 9.
Желудочковые экстрасистолы, всего 4. ST-T: без существенной динамиюі.
256'Кардиология‘r-П'ГП^\ГТ~ГЧї#"лг^~JJ»—«JL/^—Рис, 13.16, Злектрокардиоірамма больтіой Г. при поступленирт в Факультетскую тера¬
певтическую клитіику им. В.Н. Виноградова. Скорость записи 25 м/с. Пояснения в
текстеПо данным ^оЛГГлевый желудочек не увеличен (КДР 4,5 см, КДО 90 мл,
КСО 51 лш). Толщина стенок левого желудочка (межжелудочковая перегородка
и задняя стенка) = 0,9 см. Глобальная сократительная функция левого желудоч¬
ка снижена, ФВ 43%. Умеренная гииокинезия задней стснки в верхней трети и
снижение степени систолического уіолшения миокарда в двух верхних третях
септального сегмента. Диастолическая функция снижеиа (Е/А 0,8). Полость
правого желудочка 2,1 см, тПЖ 0,35 см, характер движения стенок не изменен.
Левое предсердие 52 мл, правое предсердие 38 \ы. Нижняя полая вена 1,8 см,
коллабирует после глубокого вдоха более, чем на 50%. Уплотнение фиброзных
колец митрального и аортального клапанов. Признаков легочной гипертензии
и регургитации нет (АТ/ЕТ 0,45). Диаметр ствола легочной артерии: 1,9 см.
Диаметр корня аорты: 2,8 см. Стенкм аорты уплотнены. Жидкости в полости
перикарда нет.Таким образом, выявлено лишь снижение локальной и глобальной сократи¬
мости левого желудочка в сочетании с нарушением диастолической функции.По данным рентгенологического исследования органов фудная клетка дефор¬
мирована за счет S-образного сколиоза. Легкие — без свежих очаговых и
инфильтративных изменений, соответствуют возрасту. Корни легких структур¬
ны. Сердце — аортальной конфигурации, несколько расширено влево, аорта
рентгенологически не изменена.С пелью исключения внутригрудной лимфоаденопатии и оценки состо¬
яния перикарда была выполнена МСКТ органов грудной клетки: легочная
ткань без свежих очаговых и инфильтративных изменений. Писвматизация и
Глава 13, Миокардиальный васкулит: путь к диагнозу... 257васкуляризация легочной ткани не нарушена. Жидкости в плевральных поло¬
стях не определяется. Структуры средостения и корней легких дифференци¬
рованы. Визуализируются единичные медиастинальные лимфоузлы до 5 мм.
В полости перикарда в области верхушки сердца незначительное ограниченное
скопление жидкости, толщина слоя до 5 мм.При УЗИ органов брюшной полости печень, селезенка не изменены, выяв¬
лены изменения поджелудочной железы — контуры неровные, нечеткие,
паренхима повышенной эхогенности, диффузно неоднородная. Почки обыч¬
но расположены, правая 67x45 мм, визуализируется нечетко, паренхима
до 11 мм, плохо дифференцированной эхоструктуры, чашечно-лоханочная
система не расширена, в среднем сегменте конкремент размером до 6 мм,
левая почка 110x36 мм, паренхима до 11 м, определяется паренхиматозная
перемьпіка, ЧЛСне расширена, область надпочечников не изменена. При
ЭГДС — недостаточность кардии, постоянный рефлюкс пенистой желчи из
двенадцатиперстной кишки в желудок.Таким образом, у больной имелись типичные приступы стенокардии, руб¬
цовоподобные изменения переднеперегородочиых сегментов, нижней стенки
левого желудочка при неизмененных коронарных артериях, левожелудочко-
вая сердечная недостаточность с приступами сердечной астмы и снижением
ФВ левого желудочка до 35—45% (без дилатации полостей сердца).Проводился дифференциальный диагноз между антифосфолипидным син¬
дромом (повышения титра антител к кардиолипину и снижения АЧТВ не
выявлено), системным васкулитом с преимущественным поражением сердца
(уровни антител к цитоплазме нейтрофилов в пределах нормы, что не исклю¬
чает на,1ичия васкулита), хроническим миокардитом и постмиокардитическим
кардиосклерозом; не исключались также инфшхьтративные заболевания мио¬
карда. Весьма вероятным представлялось обнаружение выраженных полей
фиброза и дистрофических изменений в отсутствие признаков активного вос¬
паления.Для верификации диагноза 11.12.2008 п выполнена эндомиокардиальная
биопсия правого желудочка. Методом ПЦР генома вирусов простого герпеса1-го, 2-го, 6-го типов, вируса герпеса зостер, вируса Эпштейна-Барр и цито-
мегаловируса не выявлено.При гистологическом исследовании биоптатов (профессор Е.А. Коган)
выявлено следующее.1. Субэндокардиальный участок свободной стенки правого желудочка.
Эндокард тонкий, представлен пластом эндотелиа-'шных клеток и незначи¬
тельно утолщенной базальной мембраной. Кардиомиоциты с исчезновением
поперечной исчерченности и очагами иммунного цитолиза. 51дра сохранны.
Интсрстиций неравномерно расширен, набухший, содержит лимфогистиопи-
тарные элементы (немногим более 14 лимфоцитов при большом увеличении,
рис. 13.17, а, см. цветную вклейку). Микрососуды с пролиферацией эндотели¬
альных клеток и перицитов, отдельные со склерозированными и гиалинизиро-
ванными yroJtrueHHMMH стенками и резким слокением просветов. При окраске
по Ван Гизону слабо выраженный склероз интерстиция.
258 Кардиология2, Субэндокардиальный участок свободной стенки правого желудочка.
Кардиомиоциты с исчезновением поперечной исчерченности. Ядра сохранны.
Интерстиций неравномерно расширен, содержит жировую ткань и лимфо-
гистиоиитарную инфильтрацию (более 14 лимфоцитов в поле зрения при
большом увеличении) и продуктивные васкулиты с пролиферацией эндоте¬
лиальных KjieTOK и лимфогастиоцитарными элементами {рис. 13.17, 6, г, см.
цветную вклейку). При окраске по Ван Гизону слабо выраженный склероз
интерстиция.3. Субэндокардиальный участок верхушки правого желудочка. Эндокард
тонкий, представлен пластом эндотелиальных клеток и незначительно утол¬
щенной базальной мембраной. Кардиомиоциты с исчезновением попереч¬
ной исчерченности. Ядра сохранны. Интерстиций неравномерно растпирен,
набухший, содержит лимфогистиоцитарные элементы (7—10 лимфоцитов
при большом увеличении). Встречаются фигуры иммунного цитолиза кар-
диомиоцитов с эмпериполезисом. Микрососуды с пролиферацией эндо¬
телиальных клеток и перицитов, отдельные со склерозированными и гиа-
линизированными утолщенными стенками и резким сужением просветов
{рис. 13,17, в, С.М. цветную вклейку). При окраске по Ван Гизону склероз
интерстиция НС выявляется.при окраске конго красным амилоида не выявлено.Заключение: идиопатический миокардиальный продуктивный васкулит с
минимальными признаками межуточного миокардита с развитием иммунного
цитолиза и дистрофическими изменениями отдельных кардиомиоцитов, скле¬
роз интерстиция.Несмотря на наличие признаков межуточного миокардита, явления выра¬
женного продуктивного васкулита, безусловно, преобладали, что объясняло и
наиболее раннее появление в клинической картине болезни приступов стено¬
кардии. Наличие признаков активного воспаления при умеренной выражен¬
ности фиброза и отсутствии вирусного генома в миокарде делало воз.можнътм
проведение иммуносупрессивной терапии,Ктнический диагноз бьы сформулирован слсдуютцим образом: инфек¬
ционно-иммунный миокардит с явлениями выраженного миокардиального
васкулита. Стенокардия 11-111 ФК. Нарушения ритма и проводимости серд¬
ца: блокада передней ветви левой ножки пучка Гиса, преходяш,ая полная бло¬
када левой ножки пучка Гиса, частая желудочковая экстрасистолия, пробежки
наджелудочковой тахикардии. Гипертоническая болезнь ЇТ стадии, 1 степени
повышения АД, риск 4. Недостаточность кровообращения ПБ стадии, 111
функциональный класс (NYHA). Гиперлипидемия 4-го типа. Гиперурикемия,
леченная аллопуринолом. Мочекаменная болезнь. Вторично сморщенная
почка. Холецистэктомия в 2002 т. Сахарный диабет 2-го типа, среднетяжелого
течения, в фазе декомпенсации углеводного обмена. Язвенная болезнь желуд¬
ка в фазе ремиссии. Недостаточность кардии. Дуоденогастра;гьный рефлюкс.
Хронический панкреатит в фазе стихающего обострения. Хронический
бронхит с астматическим компонентом вне обострения. Субклинический
гипотиреоз.
Глава ІЗ. Миокардиальный заскулит: путь к диагнозу... 259Проводилась терапия: кордарон 200 мг/сут, верошпирон 50 мг/сут, фуросе-
мид 40 мг, чередуя с диувером 10 мг ежедневно, тромбо-АСС 0,1/сут, плаквенил
200 мг/сут, сиофор 500 мг/сут, тулип 5 мг/сут, аллопуринол 100 мг/сут, клона-
зепам 1,5 мг/сут; попытка назначения мономака сопровождалась гипотонией
и интенсивной головной болью, после его отмены стенокардия возобновилась.
С 10.01.2009 г. была начата терапия метипредом 16 мг/сут. На этом фоне отме¬
чена дестабилизация уровня глюкозы крови, начата терапия маниншюм без
существенного эффекта. 20.01.2010 г была проконсультирована академиком
РАМН Н.Л. Мухиньш и профессором Л.В. Козловской’, рекомендовано допол¬
нительное определение антител к р-2 гликопротеинам и криоглобулинам (не
выявлены) с последующим назначением азатиоприна.Через месяц от начала приема метипреда была повторно госпитализирова¬
на в Факультетскую терапевтическую клинику им. В.Н. Виноградова с целью
коррекции терапии.К этому времени состояние улучшилось, приступы стенокардии (в отсут¬
ствие терапии нитратами) и сердечной астмы прекрати-іись практически пол¬
ностью, уменьшилась одышка, несколько повысилась толерантность к физи¬
ческим нагрузкам, С 10.02.2010 г. была начата терапия азатиоприном 75 мг/сут,
подобрана сахароснижаюшая терапия {новомикс 2 мт по 1 таб. 3 раза в день,
сиофор 500 .мг по 1 таб. 2 раза в день), однако в связи с сохранением вечерних
подъемов уровня глюкозы до 10—11 ммоль/л начато постепенное (на Уз таб.
раз в 2 нед) снижение дозы метипреда вплоть до полной отмены. За время
пребывания в клинике развился эпизод опоясывающих болей в эпигастрии,
несколько позднее — жидкий стул, однократная рвота, ^гго в сочетании с дан¬
ными УЗИ органов брюшной полости расценено как обострение панкреатита.
К лечению были добавлены омез 20 мг по 1 капе. 2 раза в день, мезим-форте
по 1 капе. 3 раза в день, дюспаталин по 1 капе. 3 раза в день, временно отменен
азатиоприн (в дальнейшем вновь назначен в дозе 50 мг/сут); симптомы купи¬
ровались.В последующем еще дважды отмечались обострения панкреатита, связан¬
ные с приемом азатиоприна, с осени 2010 г препарат полностью отменен.
Терапия метипредом не возобновлялась в связи с отсутствием стойкой ком¬
пенсации сахарного диабета. Самочувствие больной оставалось относительно
стаби,1ьным, однако на фоне самостоятельного уменьшения дозы диуретиков
возобновились приступы удушья, в ноябре 2009 г. проведена контрольная
эхокардиография: ФВ левого желудочка в покое составила 29%, после нагруз¬
ки — 44%, в остальном без динамики. Возобновлена терапия метипредом 4 мг
по 1 таб., верошпироном 50 мг/сут, кордароном (который больная временно
отменяла). Данную терапию переносила удовлетворительно, приступы стено¬
кардии и одышки практически отсутствовали.Таким образом, несмотря на существенные трудности при проведении
иммуносупрессивной терапии, связанные с наличием сопутствующих забо¬
леваний, состояние больной остается достаточно стабильным; в перспекти¬
ве может рассматриваться вопрос об имплантации ресинхронизируюшего
устройства.
260 КардиологияВ третьем клиническом наблюдении мы столкнулись с финальной (морфо¬
логически) стадией поражения мелких коронарных артерий, на которой прове¬
дение консервативной (иммуносупрессивной) терапии не имело смысла; через
два года, несмотря на критическое снижение систолической функции левого
желудочка, больной с успехом была выполнена реконструктивная операция на
сердце. Наличие в анамнезе бронхиальной астмы заставляло искать признаки
системного васкулита (по типу синдрома Черджа—Стросс), однако убедитель¬
ных данных в его пользу получено не было.Больная Т., 60 лет, поступила в отделение общей терапии Факультетской
терапевтической клиники им. В.Н. Винофадова 02.11.2007 г с жалобами на
одышку при незначительной физической нагрузке, а также подъемы АД до 200—
180 и 110—90 мм рт.ст., ночные боли в области сердца сжимаюшего характера.Анамнез заболевания: в течение последних 15 лет отмечались периодически
возникающие головные боли при подъемах АД максимально до 200 и 110 мм
рт. СТ.; регулярная гипотензивная терапия не проводилась. В 2003 г. (в возрас¬
те 56 лег) стали беспокоить ощущения сведения, онемения в нижних конеч¬
ностях; обследовалась в клинике нервных болезней им. А.Я. Кожевникова
Московской медицинской академии им. И.М. Сеченова, где данные явления
были расценены как последствие острого нарушения спинального кровообра¬
щения (от июня 2003 г.). Проводилась нейротропная и гипотензивная терапия
(мидокалм 50 мг/суг, инъекции витаминов В^, В^^, вливания растворов трента-
ла, псрсбролизина, атенолол 25 от/с^т, верошпирон 25 мг/сут, энап 5 мг/сут,
омник 400 мк/сут, предуктал MB),С 2005 г. (58 лет) без видимой причины стали беспокоить выраженная
одыщка, кашель, по месту жительства состояние расценивалось как ишеми¬
ческая болезнь сердца, атеросклероз аорты, коронарных артерий, дилатаци-
опная кардиомиопатия, гипертоническая болезнь, хроническая сердечная
недостаточность; проводимую в тот момент кардиотропную терапию больная
не помнит. В декабре 2006 г. находилась на стационарном лечении в пульмоно¬
логическом отделении Московской городской больницы № 50 по поводу впер¬
вые выявленной бронхиальной астмы, была начата терапия ингаляционными
глюкокортикостероидами.С января 2007 г. отмечала нарастание одышки, учащение приступов удушья,
появление болей в области сердца, в связи с чем была вновь госпитализирована
по месту жительства; выявлена правосторонняя нижнедолевая очаговая пнев¬
мония. Согласно выписке, во время госпитализации у больной возник эпизол
остановки сердца с развитием отека легкого, проводились реанимационные
мероприятия. Была подобрана терапия дигоксином 0,25 мг/сут, оликардом
40 мг/сут, верошпироном 50 мт/сут, эналаприлом 20 мг/сут, тромбо-АССом
100 мг на ночь, верапамилом 120 мг/сут. В течение года отмечались нараста¬
ние одышки, которая к декабрю возникала при незначительных физических
нагрузках, учащение болей стенокардитического характера (преимуществен¬
но ночью).При поступлении состояние средней тяжести. Нормостеническое телосло¬
жение. Отеков нет. Лимфоузлы не увеличены. Число дыханий 18/мин, дыхание
Глава 13. Миокардиальный васкулит: путь к диагнозу..261жесткое, выслушиваются незвонкие мелкопузырчатые хрипы в нижних отде¬
лах с обеих сторон, границы сердца расширены, тоны глухие, ритмичные,
выслушивается систолический шум на верхушке, акцент II тона над легочной
артерией. ЧСС 82 уд/мин, ритм правильный. АД 130/80 мм ртхт. Жшзот мяг¬
кий, безболезненный, печень и селезенка не лъеличены.При рутинном лабораторном обследовании сушественных отклонений от
нормы не выяачено. В общем анализе крови: НЬ 147,3 г/л, эритроциты 4,8 млн,
цветовой показатель 0,98, лейкоциты 8,0 тыс, нейтрофилы 65,8%, лимфоци¬
ты 22,0%, моноциты 7,8%, эозинофшш 3,5%, базофилы 0,8%, тромбоциты
215,8 тыс., СОЭ 3 мм/ч, В биохимическом анализе общий белок 61,9 г/л, альбу¬
мин 3,9 г/л, креатинин 1,45 мг/дл, глюкоза 102 мг/дл, азот мочевины 26 мг/дл,
мочевая кислота 408,3 мг/дл, общий билирубин 13,5 мг/д.і, калий 5,5 мэкв/д,
натрий 149 мэкв/л, у-ГТ 28 ед/л, ACT 30 ед/л, АЛТ 36 ед/л, холинэстераза
5011 ед/л. Электрофорез белков в пределах нормы. Липидный спектр: тригли¬
цериды 113 мг/дл, обший холестерин 282 мг/дл, ЛПВП-хс 85 мг/дл, ЛПНП-хс
174,4 мг/д;Т, ЛПОНП-хс 22,6 мг/дл, коэффициент атерогенности 2,32.В анализах мочи — признаки хронической мочевой инфекции.При иммунологическом обследовании выявлено повышение IgE до 283 МЕ/мл,
титр антител к миокардиальной ткани класса TgG резко повышен (1:600 при
норме 1:100), IgM не выявлены; антитела к Streptococcus (гишіуронидаза) IgG
1:400, титр антител к вирусам Коксаки группы В в пределах нормы (лаборато¬
рия «МедБиоСпектр»).На ЭКГ {рис. 13.18) — ритм синусовый, ЧСС 88 уд/мин, электрическая ось
сердца отклонена влево. Признаки нарушения проводимости в системе левой
ножки пучка Гиса. Признаки гипертрофии левого желудочка, обоих предсер¬
дий. PQ 0,17 с, QRS 0,12 с, QT/QTc 400/480 мс.litI fimIРис. 13.18. Электрокардиограмма больной X, скорость записи 25 мм/с‘"NT
262 КардиологияПо данным суточного мониторирования ЭКГ по Холтеру — синусовый
ритм. ЧССднем 66-121/мин (ср. 85/мин), ночью 64-113/мин (ср. 80/мин),
Наджелудочковые экстрасистолы, всего 85, куплетов 5, триплет 1. Политопные
желудочковые экстрасистолы, в том числе поздние, сливные PQRST, всего
100. Куплеты, в том числе разнонаправленные, всего 9. Фоновая депрессия
сегмента ST до 0,05 мВ, негативный зубец Т, при ЧСС > 100/мин усугубление
депрессии сегмента до 1,5 мВ.При ЭхоКГ: левый желудочек (КДР) 7Д см, тМЖП и тЗС 0,8 см, ФВ 34%.
Нарушений локальной сократимости нет Определяется выраженное наруше¬
ние диастолической функции по рестриктивному типу: Е/А 0,8/0,2. Полость
правого желудочка 3,5 см, тПЖ 0,53 см, характер движения стенок не изме¬
нен. Левое предсердие 81 мл, правое предсердие 46 мл. Уплотнение фиброз¬
ных колец митрального и аортального клапанов. Митральная регургитацияII-ПІ степени, непостоянная аортальная регургитация в раннюю диастолу,
трикуспидальная регургитация Т степени. Систолическое давление в правом
желудочке 72 мм рт.ст. Признаки легочной гипертензии (АТ/ЕТ 0,30). Стенки
аорты угшотнены.При рентгенологическом исследовании без свежих очаговых и инфиль-тративных изменений. Легочный рисунок несколько усилен за счет сосу¬
дистого рисунка, сосуды уплотнены. Корни легких структ>фны. Диафрагма
расположена обычно. Плевральные синусы свободны. Сердце расширено в
обе стороны и кзади, в поперечнике 17,5 см, аорта и сосудистый пучок справа
уплотнены.По данным исследования ФВД, имелись умеренные вентиляционные нару¬
шения смешанного типа: ЖЕЛ >т«еренно снижена (2270 мл, 75%), ОФВ, 76%
(после ингаляции атровента 76%), MOC,^ 110% (146%), МОС5^70% (107%),
М0С,5 37% (47%), ОФВуФЖЕЛ 78% (81%). Бронхиальная обструкция умерен¬
но выражена. Реакция на атровент положительная.С учетом болей по типу стенокардии, ишемической динамики сегмента
ST по данным холтеровского мониторирования (нагрузочные пробы не про¬
водились в связи с выраженной одышкой), наличия факторов риска ишеми¬
ческой болезни сердца (возраст, артериальная гипертензия, гиперлипидемия)
бьыа выполнена коронароангиография: сбалансированный тип кровоснабжения
сердца. Ствол левой коронарной артерии не изменен. Передняя межжелудоч-
ковая артерия не изменена. Огибающая артерия не изменена. Правая коронар¬
ная артерия не изменена.В связи с отсутствием изменений коронарных артерий, наличием дилатации
левых камер сердца с выраженным нарушением систолической и диастоличе¬
ской функции левого желудочка неясного генеза, блокады левой ножки пучка
Гиса, стенокардии, повышения титра антикардиачьных антител в завершение
обследования выполнена эндомиокардиа>гьиая биопсия правого желудочка.Методом ПЦР генома вирусов простого герпеса 1-го, 2-го, 6-го типов, виру¬
са герпеса зостер, вируса Эпштейна—Барр и цитомегаловируса не выявлено.При гистологическом исследовании биоптатов (профессор Е.А. Коган) выяв¬
лено следующее.
Глава 13, Миокардиальный заскулит: путь к диагнозу,.. 2631. Субэндокардиальный участок свободной стенки правого желудочка.
Эндокард утолщен, склерозирован. В субэндокардиал ьных отделах адипозо-
циты и фиброзные септы. Сосуды Тебезия не обнаруживаются. При окраске по
Ван Гизону слабо выраженный склероз интсрстиция.2. Субэндокардиальный участок верхушки правого желудочка. Кусочек
не ориентирован. В субэндокардиал ьных отделах адинозоциты и фиброзные
септы.3. Субэндокардиальный участок выводного отдела правого желудочка.
Кусочек не ориентирован. В субэндокардиа-чьных отделах адипозоциты и
фиброзные септы. Кардиомиоциты неравномерно гипертрофированы, места¬
ми с исчезновением поперечной исчсрченности и очаговой гомогенизацией
цитоплазмы. Интерстиций нежный, содержит отдельные .іимфоплазмоклеточ-
ные элементы (менее 14 лимфоцитов в поле зрения при большом увеличении).
Микрососуды капиллярного типа, полнокровны.4. Субэндокардиа.1ьньтй участок межжелудочковой перегородки. Эвдокард
утолщен, ск.іерозирован. В субэндокардиал ьных отделах адинозоциты и
фиброзные септы. Сосуды Тебезия со склерозированными стенками, с про¬
лиферацией эндотелиальных: клеток, стенозированием просвета, периваску-
лярными лимфогистиоцитарньтми элементами и тромботическими массами в
просвете отдельных сосудов; продуктивные капилляриты.Заключение: обнаружено сочетание продуктивного васкулита с пораже¬
нием сосудов Тебезия, неравномерной гипертрофией и дистрофически¬
ми изменениями кардиомиоцитов правого желудочка, распространенным
субэндокардиальным липоматозом. Необходимо проведение дифференци-
ачьного диагноза между постмиокардитическими изменениями и синдромом
Черджа-Стросс.А^'г««ичесл:1/й^«ог«азбылсформулированследующимобразом:инфекционно-
иммунный миокардит с явлениями выраженного продуктивного васкулита,
тяжелого течения, с развитием дилатации всех камер сердца. Нарушение
проводимости в системе левой ножки пучка Гиса. Гипертоническая болезнь111 стадии, 3 степени повышения АД, риск 4. Недостаточность кровообра¬
щения ПА стадии, III функциональный к.іасс (NYHA). Бронхиальная астма,
инфекционно-аллергическая, средней степени тяжести, в фазе стихаюдіего
обострения. Атеросклероз аорты. THnepjmnHfleMHH 2а типа.Несмотря на наличие у пациентки бронхиальной астмы, клинических
данных было недостаточно, чтобы говорить о наїичии системного васкули¬
та: отсутствовали эозинофилия, кожная сыпь, поражение легких и почек,
антитела к цитоплазме нейтрофилов; нейропатия в анамнезе расценивалась
как следствие нарушения мозгового кровообращения. Кроме того, обнару¬
женный в биоптатах васкулит не носил характера некротического. В связи
с преобладанием фиброзных изменений иммуносупрессивная терапия не
назначалась.Проводилась терапия всрошпироном 50 мг/суг, фуросемидом 40 мг через
день, престариумом 2 мг/сут, небилетом 2,5 мг/сут, кордароном 400 мг/суі,
вазилипом 20 мг/сут, фликсотидом 750 мкг/сут. Одыщка и боли в области
264 Кардиологиясердца несколько уменьшились. В дальііейшем вновь отмечено значительное
нарастание одътшки, которая к концу 2009 г. стала возникать при малейших
физических нагрузках и в покое, развитие признаков застоя по большому кругу
кровообращения (отеки, гепатомегалия).Была госпитализирована в отделение хирургического лечения дисфункций
миокарда и сердечной недостаточности Российского научного центра хирургии
им. акад. Б.В. Петровского РАМН. При обследовании выявлены увеличение
продолжительности комплекса QRS до 0,15 с, снижение ФВ левого желудочка
до 14%, нарастание митральной (111—IV степень) и трикуспидальной (111 сте¬
пень) регургитации, а также умеренная межжелудочковая диссинхрония
(лево-правая задержка 52 мс при норме менее 40 мс). Решением консилиума
определены показания к реконструктивной операции, 27.10.2009 г выпол¬
нены протезирование митрального клапана протезом МИКС-27, пластика
левого прсдсердия и ремоделирование полости левого желудочка, аннулогыа-
стика трикуспидального клапана по Де-Вега (профессор С.Л, Дземешкевич).
Послеоперационный период протекал с явлениями сердечно-сосудистой недо¬
статочности, потребовавшей продленной искусственной вентиляции легких в
течение 3-х суток, инфузии малых доз катехоламинов, сердечных гликозидов,
повторной инфузии левосимендана, В дальнейшем гемодинамика стабили¬
зировалась, при контрольной ЭхоКГ отмечено уменьшение полости левого
желудочка с 7,3 до 6,5 см, увеличение его ФВ с 14 до 28%, отсутствие мсжже-
луд очковой диссинхронии (задержка 22 мс). Через пол год а после операции
состояние больной оставалось стабильным, толерантность к физическим
нагрузкам заметно возросла.Таким образом, представлено описание различных стадий миокардита
с резким преобладанием воспалительного поражения мелких коронарных
артерий — от минимальных клинических проявлений (преходящая блока¬
да левой ножки пучка Гиса) и активного васкулита в отсутствие фиброза у
молодого пациента до тяжелой стенокардии и сердечной недостаточности
с преобладанием склеротических изменений сосудов Тебезия у пациенток
60 лет. У всех больных отсутствие поражения кругшых коронарных артерий
бьшо доказано с помощью коронароаш-иофафии, диагноз миокардиального
васкулита был поставлен только с помощью эндомиокардиальной биопсии
(специфических иммунных маркеров его на сегодняшний день не найдено,
антитела к цитоплазме нейтрофилов ни у одного из пациентов выявлены не
были). Нозологическая принадлежность данного васкулита не вполне ясна —
можно говорить как об особом варианте течения инфекционно-иммунного
(иммунного?) миокардита с преимущественным и выраженным поражением
сосудов по типу продуктивного васкулита, так и об изо.тированном (без при¬
знаков системного поражения) миокардиальном васкулите с минимальными
явлениями миокардита.
Глава 13. Миокардиальный васкулит: путь к диагнозу... 265ЛИТЕРАТУРААбрикосов А.И. Часгаая патологическая анатомия. — 1940. — С. 167.Йонаш В. Частная кардиология. — 1963. — Т. 2. — С. 575.Adams Е.Е., Aluquin V.P., Bingham С.А. et ai Cardiae tumor in juvenile onset
Behget’s disease: case report and review of the literature // Pediatr Cardiol. 2010;
31(2):277~279.Alexdnderson E., Mannting F., Gomez-Martin D. et al. Technetium-99m-Sestamibi
SPECT myocardial perfusion imaging in patients with complete left bundle branch
block//Arch. Med. Res. 2004; 35(2):150-156.Breinholt J.P. Tnstani-Firouzi М., Bohnsack J.F., Shaddy R.E. Evidence for
early vessel involvement in the dysfunctional myocardium of Takayasu’s arteritis I j
Pediatr. Cardiol. 2001; 22(1):74-76.Fallahi B., Beiki D., Eftekhari M. et al High accuracy of myocardial perfusion
imaging in patients with left bundle branch block: comparison of four interpretation
approaches // Hell. J. Nucl. Med. 2009; 12 (2):132—137.Frustaci A., Chimenti C., Pieroni M. Idiopathic myocardial vasculitis presenting as
restrictive cardiomyopathy // Chest. 1997; 111 (5): 1462-1464.Frustaci A., Gentiloni N., Chimenti C. et al. Necrotizing myocardial vasculitis in
Churg-Strauss syndrome: cUnicohistologic evaluation of steroids and immunosup¬
pressive therapy // Chest. 1998; 114(5): 1484-1489.Goodfietd N.E., Bhandari S., Plant W,D. et al Cardiac involvement in Wegener’s
granulomatosis // Br. Heart. J. 1995; 73(2): 110-115.Hoefflinghaus Т., Husmann L, Valenta /. et al Role of attenuation correction to
discriminate defects caused by left bundle branch block versus coronary stenosis in
single photon emission computed tomography myocardial perfusion imaging // Chn.
Nud. Med. 2008 Nov;33(ll);748-751.Hosenpud J.D., McAnulty J.If., Niles N.R. Unexpected myocardial disease in
patients with life threatening arrhythmias // Br. Heart. J. 1986; 56(1): 55-61.Hung J.T., Yang Ї.Н., Hsiao C.H. et al Leukocytoclastic vasculitis with
severe cardiac involvement in an infant: a case report I j Clin. Rlieumatol. 2008;
27(7):945-947.Jin S.J., Mm H.S., Chung S.J. et al Acute myocardial infarction due to sinus of
Valsalva aneurysm in a patient with Behget's disease // Clin. Exp. Rheumatol. 2008;
26(4 Suppl 50):S117-120.Khouzam R.N. Wolf-Parkinson-White alternans diagnosis unveiled by adenosine
stress test // J. Electrocardiol. 2010; 43(2): 144-145.KoepJIi P., Wyss C.A., Gaemperli O. et al Left bundle branch block causes rela¬
tive but not absolute septal undcrperfusion during exercise // Eur. Heart. J. 2009;
30(24):2993-2299.Konno Т., Shimizu М., Ino H. et al. A rare type of alternating bundle branch block in
a patient with cardiac sarcoidosis - a case report //Angiology 2005; 56(1): 115-117.Kruse М., Schulze-Bahr E., Софе Id V. etal Impaired endocytosis of the ion chan¬
nel TRPM4 is associated with human progressive familial heart block type I // J. Clin.
Invest. 2009; 119(9):2737-2744.
266 КардиологияMizuno J., Kato S., Ino K. et al. [Intermittent bradycardia-dependent bundle
branch block during sevoflurane and remifentanil anesthesia] LArticle in Japanese] //
Masui. 2009; 58(8):976-979.MoUerJ., Warwick]., Bouma H. [Myocardial perfusion scintigraphy with Tc-99m
MIBI in patients with left bundle branch block: Visual quantification of the anterosep-
tal perfusion imaging for the diagnosis of left anterior descending artery stenosis]
[Article in Afrikaans] // Cardiovasc. J. S. Afr. 2005; 16(2):95-101.Mosseri М., Yarom Я, Gotsman M.S., Basin Ї. Histologic evidence for small-vessel
coronary artery disease in patients witii angina pectoris and patent large coronary
arteries // Circulation. 1986; 74(5):964-972.Neumann Т., Manger B., Schmid M. et al. Cardiac involvement in Churg-Strauss
syndrome: impact of endomyocarditis // Medicine (Baltimore). 2009; 88(4):236-
243.Padi A, SilvermanB., Schneider A. Twenty-one year old woman witli severe eosino-
phiiia and left bundle branch blocic. // Allergy Asthma Proc. 2009; 30(5):558—562.Parodi G., Salvadori C., Del Pace S. et al. Left bundle branch block as an electro¬
cardiographic pattern al presentation of patients with Tako-tsubo cardiomyopathy //
J. Cardiovasc. Med. (Hagerstown). 2009; 10(1): 100-103.Peng S.K., French WJ. Moфhological changes in small vessels on endomyocardial
biopsy//Ann. Clin. Lab. Sci. 1986; 16(3): 180-188.Rossi М., Marin-Neto J., Uchida £., Ramos S. Basement membrane thickening
in small intramyocardial vessels in eosinophilic myocarditis j I Acta Cardiol. 1996;
51(3):271-277.Steffel J., Kobza R., Oechslin E. et al Electrocardiographic characteristics al initial
diagnosis in patienls wilh isolated left ventricular noncompaction // Am. J. Cardiol.
2009; 104(7): 984-989.Ти C.M., Chu K.M., Yang S.P. et al Trastuzumab (Herceptin)-associalcd cardio¬
myopathy prcsenlcd as new onsei of complete left bundle-branch block mimicking
acute coronary syndrome: a case report and literature review // Am. J. Emerg. Med.
2009;27(7):903.el-3.Vernooy K., Verbeek X.A., Feschar M. et al. Left bundle branch block induces
ventricular remodelling and functional septal hypoperfusion // Eur. Heart. J. 2005;
26(l):91-98.
Глава 14ГЕНЕРАЛИЗОВАННЫЙ САРКОИДОЗ
С ПРЕИМУЩЕСТВЕННЫМ ПОРАЖЕНИЕМ СЕРДЦА:
ВЕРИФИКАЦИЯ ДИАГНОЗА И ТЕРАПИЯДА. Иванова, А.В. Недоступ, ДА. Царегородцев,
С.Е. Борисов, СЛ. ПашаПри наблюдении пациента с уже развившейся кардиомегалией и ее ослож¬
нениями в виде недостаточности кровообращения или аритмий часто бывает
трудно определить, финальной стадией какого заболевания она является.
При этом следует помнить не только о наиболее частых причинах подобного
состояния, которыми являются ИБС, перенесенный миокардит, пороки или
идиопатическая (в большинстве случаев — генетически детерминированная)
кардиомиопатия, но и о большой группе «редких*^ и потенциально курабель-
ных заболеваний сердца. В представляемом наблюдении пациенту с пораже¬
нием сердца по типу дилатационной кардиомиопатии был поставлен диагноз
одного из таких заболеваний, что потребовало проведения морфологического
исследования и повлекло за собой не только назначение специфической меди¬
каментозной терапии, но и интервенционное лечение.Больной Т., 52 года, поступил в Факультетскую терапевтическую клинику
им. В.Н, Виноградова 16.03.2004 г. с жалобами на одьпику при небольшой
физической нагрузке (подъем на один лестничный пролет, ходьба на расстоя¬
ние 20—50 м), иногда в покое; редкие ночные эпизоды нехватки воздуха; частые
перебои в работе сердца; длительные ноюшие боли в прекардиальной области
без четкой связи с физической нагрузкой.Из анамнеза жизни известно, что пациент в течение многих лет работал инже¬
нером на монтажном предприятии без особых профессиональньпс вредностей.
Курил с 20 лет максимально до 2 пачек в день, 2 года назад бросил курение. Среди
перенесенных заболеванш! — детские инфекции, ангины; в 1998 г — дебют моче¬
каменной болезни в виде почечной колики с отхождением камня; в дальнейшем
повторное образование камня в лоханке левой почки. Отец больного умер в воз¬
расте 60 лет, причина смерти неизвестна; мать и тетка (сестра матери) умерли в
возрасте 45—50 лет от неизвестного заболевания сердца. Пациент имеет двух сыно¬
вей 34 и 20 лет, у младшего недавно выявлена желудо^жовая экстрасистолия.Анамнез заболевания {рис. 14.1). Впервые перебои в работе сердца отметил
в юношеском возрасте; на ЭКГ были зафиксированы какие-то изменения,
которые послужили причиной освобождения от воинской службы, в после¬
дующем перебои в работе сердца исчезли, при повторных профилактических
осмотрах никакой патологии сердца не выяштялось. Возобновление перебо¬
ев отметил 10 лет назад. Они возникали преимущественно в вечернее время
268КардиологияИ не сопровождались значимыми изменениями самочувствия. Последний
профосмотр в 1998 г. включал флюорографию органов грудной клетки, патоло¬
гии выявлено не было.В декабре 2001 г. впервые отметил появление одышки при умеренной
физической нагрузке, а в конце февраля - начале марта 2002 г. — учащение
перебоев. 8 марта — внезапное нарастание частоты перебоев с переходом в
учащенное аритмичное сердцебиение, сопровождающееся резкой слабостью,
затуманенностью сознания. Бригадой СМП на ЭКГ зарегистрирована желу¬
дочковая тахикардия с частотой 120 уд/мин ірис. 14.2); синусовый ритм восста¬
новлен с помощью электрической кардиоверсии. Больной госпитализирован
в больницу г. Курска. При повторной регистрации ЭКГ выявлены неполная
блокада правой и передней ветви левой ножки пучка Гиса. При ЭхоКГ на
фоне нерезкой дилатации полости левого желудочка и диффузного снижения«Перебои»'
в работе сердца
Пароксизмы
тахиаритмииОдышка смешанного
характераКашель
Боли в прекар-
диальной области
Масса телаТолерантность
к физической
нагрузкеНарушенияпроводимостиРазмеры и функция
левых отделов
сердцаИзменения в легких
ТерапияНачало2001 г.2002 г.2003 г.2004 г.90-х гг.ДекабрьМарт АпрельАпрель Июнь Июль ОктябрьНебольшая БПНПГ
Блокада ПВ ЛНПГ+ АВ-блокада I ст.
+ полная БПНПГ+ нарушение
внутрижелудоч-
ковой проводи¬
мостиЛП, ЛЖ на верхней
границе нормы, ФВ?ЛП, ЛЖ т,
ФВ=41%ЛП, ЛЖ Т,
ФВ=35%ФВ=35%Расшир.корней+ гиповентиляция Sg слева, Sg
справа. Стеноз в/долевыхбронхов?Кордарон
200-100 мг/с,
нитросорбид,
верапамилРис. 14.1. Анамнез больного Т., 52 годаКордарон
100-200 мг/с,
нитраты, энап
5-10 мг/с,
триампур,
верошпирон+ Индометацин,
витамин Е
Глава 14. Генерализованный саркоидоз с преимущественным поражением.., 269его сократительной функции — гипокинез с переходом в акинез верхушки,
участков заднебазальной и нижней стенок. Состояние расценено как мел¬
коочаговый инфаркт миокарда задней стенки неустановленной давности с
нарушениями сердечного ритма и проводимости. Назначались нитросорбид,
верапамил, аспирин, кордарон в максимальной дозе 400 мг/сут. Состояние
оставалось стабильным, пароксизмы желудочковой тахикардии не рецидиви¬
ровали; сохранялись желудочковая экстрасистолия, нарушения проводимости,
одышка. Появился кашель со скудной слизистой мокротой. На рентгенограм¬
ме впервые выявлено расширение корней легких, при повторной рентгеногра¬
фии, выполненной после выписки, — снижение прозрачности в проекции S6
справа и S2 слева; «справа неоднородная инфильтрация с буллезными вздутия¬
ми» и гракцией кверху междолевой плевры; расширение, уплотнение корней
легких. Попытки антибактериальной терапии цефалоспоринами «двусторон¬
ней полисегментарной пневмонии» (как были расценены данные изменения)
оказались безуспешны, включая отсутствие рентгенологической динамики. На
срединных томограммах — выраженное расширение средостения, корней лег¬
ких за счет лимфоузлов, сужение верхнедолевых бронхов; впервые заподозрен
саркоидоз легких и внутригрудных лимфатических узлов. При бронхоскопии
бьит выявлен диффузный необструктивный деформирующий эндобронхит, при
гистологическом исследовании трансбронхиа^тьных биоптатов данных за зло¬
качественное поражение не получено, целенаттравленный поиск саркоидных
фанулем не проводился. Трансторакальная биопсия не проводилась. Больной
продолжал полу^іать нитраты, эналаприл, мочегонные, кордарон, аспирин.Постепенно нарастали одышка, нарушения внутрижелудочковой проводи¬
мости, дилатация левых камер сердца со снижением фракции выброса до 35%.
Появились ноюшие боли в прекардиальной области. Кроме того, за период с
конца 2002 т. до начала 2004 г. отмети.! снижение массы тела на 15 кг. В апреле,
июне, июле 2003 г. — повторные пароксизмы устойчивой желудочковой тахи¬
кардии, первые два из которых купированы электрической кардиоверсией, а
последний — внутривенным введением больших доз кордарона. В дальней¬
шем кордарон получал постоянно в дозе 400-200 мг/сут, на этом фоне сохра¬
нялась частая желудочковая экстрасистолия. На ЭКГ, помимо усугубления
внутрижелудочковой блокады (расширение комплекса QRS до 0,24 с), отме¬
чено появление АВ блокады I степени. Неоднократно проходил стационарноеРис. 14.2. Электрокардиофамма больного Т. (март 2002 г.). Пояснения в тексте
270 Кардиологияобследование; в июле 2003 г, на основании клинических данных и рентгено¬
логической динамики диагностирован саркоидоз внутригрудных лимфатт^е-
ских узлов и легких, назначены индометацин и витамин Е, которые пациент
принимал до февраля 2004 г без значимого эффекта. Направлен в Московский
НИИ фтизиопульмонологии для верификации диагноза. При проведении
КТ органов грудной клетки увеличения внутригрудных лимфатических узлов
выявлено не было, отмечено налігчие выраженного перибронхиального фибро¬
за, изменения в легких расценены как «застойные)>. Фибробронхоскопия не
проводилась в связи с высоким риском фатальной аритмии; посев мокроты
на микобактерии туберкулеза отрицателен. Диагноз саркоидоза с учетом пере¬
численных данных сочтен сомнительным. Изменения в легких и сердце расце¬
нены как проявления постинфарктного кардиосклероза, в связи с чем больной
направлен в Факультетскую терапевтическую клинику им. В.И. Виноградова.При осмотре в клинике обращали на себя внимание бочкообразная форма
грудной клетки, при перкуссии расширение границ средостения, звук с коро¬
бочным оттенком; при аускультации легких единичные незвонкие мелкопу¬
зырчатые хрипы в базальных отделах на фоне жесткого дыхания. Сердце перку-
торно расширено влево до передней подмышечной линии, тоны приглушены,
акцент второго тона над легочным стволом. На верхушке, легочном стволе
выслушивается систолический шум, над аортой — короткий диастолический
шум. Частота сердечных сокрашений 64Дган, тоны сердца аритмичные, экс-
трасистолия до 3-4 в минуту. АД 110/60 мм рт.ст. Печень и селезенка не уве.іи-
чены, отеков нет. Периферические лимфоузлы не увеличены.в анализах крови отмечено увеличение СОЭ до 20 мм/ч при отсутствии
лейкоцитоза (6,4 тыс., формула не изменена. НЬ 155 г/л, эритроциты 5,2 млн,
цветовой показатель 0,89, тромбоциты 199 тыс.),В биохимическом анализе крови — умеренная гиперпротеинемия (8,8 г%,
альбумин 3,9 г%), гипергаммаглобулинемия (29,6%), в остальном без отклоне¬
ний от нормы: креатинин 1,1 мг%, общий би.тирубин 0,9 мг%, глюкоза 87 мг%,
калий 4,9 мэкв/л, натрий 139 мэкв/л, ЩФ 207 ед/л, ACT 19 ед/л, АЛТ 13 ед/л,
у-ГТ 22 ед/л, холестерин 244 мг%, триглицериды 151 мг%.Выявлено увеличение уровня IgG до 2080 мг%, ТТГ — до 6 МЕ/л при нор¬
мальных значениях гормонов шитовидной железы, что, по-видимому, объ¬
ясняется субклиническим кордарон-индуцированным гипотиреозом. Sat О2
снижена до 94,2%.В анализах мочи — удельный вес 1025, белок 0,055%о, лейкоциты 2—4
в п/зр., эритроциты 3—5 в п/зр., в скоплениях до 20, много уратов. Определялась
незначительная протеинурия (63 мг/сут).На ЭКГ {рис. 14.3) — АВ-блокада I степени {PQ 0,25 с), выраженные нару¬
шения внутрижелудочковой проводимости; QRS 0,24 с, полная блокада правой
и передней ветви левой ножки пучка Гиса, единичные желудочковые экстра¬
систолы.При суточном мониторировании ЭКГ по Холтеру — синусовый ритм, PQ
до 0,25 с. ЧССднем 60-107/мин (сред. 75/мин), ночью 60-91/мин (сред.
70/мин). Зарегистрировано 10 наджелудочковых экстрасистол, полигонные
Рис. 14.3. ЭКГ больного Т. (2004 г., ФТК). Скорость записи 25 м/с. Пояснения в текстежелудочковые экстрасистолы, всего около 2000, часто поздние, сливные, мак¬
симально 207/Ч, 1 эпизод бигеминии, 41 эпизод тригеминии, 110 парных, чаще
по типу выскальзывающих в постэкстрасистол и ческой паузе, 5 триплетов из
полиморфных экстрасистол.При ЭхоКГ — выраженная дилатация левого желудочка (диастолическіїй
диаметр 7,3 см), акинезия верхушки на фоне диффузного снижения сократи¬
тельной функции (фракция выброса 30%); стенки не утолщены (тМЖП 0,8 см,
тЗС 0,9 см), умеренная дилатация левого предсердия (4,2x6,2x3,8 см), правый
желудочек не изменен. Уплотнение створок митрального и аорта.1ьного кла¬
пана, стенок аорты; аортальная, митральная и трикуспидальная регургитацияI степени, признаки легочной гипертензии.При сциитиграфии миокарда стехнетрилом, выполненной в покое {рис. 14.4,
см. цветную вклейку), выявлены увеличение полости левого желудочка, выра¬
женная гипоперфузия примыкающих к верхушке участков задне-нижней,
заднебоковой, боковой, передней и переднеперегородочной стенок на всем
протяжении, включая область выходного тракта.При проведении МСКТ органов грудной клетки (рис. 14.5, см. цветную вклей-
к^У) — уплотнение перибронхиального интерстиция по типу «муфт*>, мно¬
жественные мелкие очаги размером 1,5-3 мм. Тракнионные бронхоэктазы
некоторых сегмснтарньк бронхов. «Зазубренность» контуров коста.іьной и
мeдиacтинaJ^ьнoй плевры. В средостении — множественные лимфатические
узлы паратрахеальной, парааортальной, субаортальной и бронхопульмональной
272 Кардиологиягрупп с обеих сторон размером 5-24 мм; конгломерат лимфоузлов в области
бифуркации и по ходу верхнедолсвых бронхов.При исследовании ФДД определяются умеренные изменения как по рестрик¬
тивному (ЖЕЛ 71 %), так и по обструктивному (OOBj 75%, МОС^^ 65%, МОС.^
56%, МО48%, индекс Тиффно 77%) типам.По данным УЗИ органов брюшной полости печень не увеличена, диффуз¬
но неоднородна, селезенка умеренно увеличена (123x58 мм), неоднородной
сгруктуры. Вены портальной системы не изменены. Почки не увеличены,
справа в нижней чашечке камень 13 мм с УЗ-тенью.Таким образом, в клинической картине выявлялся синдром дилатационной
кардиомиопатии неясной этиологии с тяжелыми нарушениями ритма и прово¬
димости в сочетании с поражением легких и виутригрудных лимфоузлов.Возникал вопрос: существуют ли одновременно две нозологии, или изме¬
нения сердца и легких имеют один и тот же гснез? Диагноз генерализованного
саркоидоза с поражением легких, внутригрудных лимфоузлов, сердца, селезен¬
ки представлялся вероятным, особенно с учетом иммуновоспалительных изме¬
нений в анализе крови, однако не бесспорным. Смущали небольшой размер
внутригрудных лимфатических узлов и, главное, отсутствие морфологической
верификации диагноза. Проведение трансторакальной биопсии лимфоузлов и
легкого у данного пациента бьыо сопряжепо с высоким риском развития угро¬
жающей жизни аритмии.Считается, что при невозможности или неинформативности биопсии для
диагностики саркоидоза возможно проведение пробы Квейма, однако сложно¬
сти приготовления Квейм-антигена, длительный период ожидания результатов
(до 6 нед), возможность ложноположительной реакции, небольшая диагности¬
ческая информативность (30—70% по данным разных авторов) и высокий риск
инфицирования в последнее время значительно охладили интерес к данной
методике. Она не входит в стандарты диагностики саркоидоза и в нашей стра¬
не почти не испо.тьзустся. Все это ограничивает применение теста Квейма—
Зильтцбаха и в конкретной клинической ситуации. Уровень ангиотензинпрев-
ращаюшего фермента (АЛФ) крови не определялся у пациента в связи с тем,
что он длительно находился на постоянной терапии ингибиторами АПФ,В качестве самостоятельного заболевания, которое могло бы являться при¬
чиной дилатационной кардиомиопатии, рассматривалась ИБС. У пациента
отсутствовали стенокардия, гиперлипидемия, гипертонический анамнез, одна¬
ко имелись другие факторы риска; пол, возраст и курение. Аргументом в пользу
ИБС бьши также очаговость поражения, быстрое развитие кардиомегалии
(бессимптомный инфаркт миокарда?). Единственным методом, который мог
бы подтвердить или опровергнуть диагноз ИБС, оставалась коронароангио-
графия.Обсуждалась также возможность постмиокардити^геского кардиосклероза,
идиопати^іеского или наследственного варианта дилатационной кардиомио¬
патии. Последнее предположение основывалось на семейном анамнезе (ран¬
ние смерти от неизвестной патологии сердца, желудочковая экстрасистолия
у сына больного); обращало на себя внимание также возникновение аритмии
Глава 14. Генерализованный саркоидоз с преимущественным поражением,,. 273в молодом возрасте у нашего пациента. В то же время не вполне типичны для
первичной дилатационной кардиомиопатии манифестация заболевания с
желудочковых аритмий с присоединением тяжелых нарушений проводимо¬
сти, выявленные при сдинтиграфии миокарда крупные очаги гипоперфузии.
Кровь больного бьыа отправлена на генетическое исследование для вьывления
возможнъгк мутапий генов л амина А и С, с возникновением которых может
быть связана одна из форм наследственных кардиомиопатий, — ламинопатии
не выявлено.Кроме того, при отсутствии классических симптомов гсмохроматоза:
пигментадии кожи, «бронзового» диабета, выраженной гепатомегалии —
были выявлены значимое повышение в крови уровня сывороточного желе¬
за (243 мкг% при нормальных значениях до 170 мкі%) и снижение уровня
трансферрина до 174 мг%. Для диаіностики первичного гемохроматоза более
показательным является повышение уровня ферритина сыворотки более 900
мкг/л в сочетании с повышением процента насыщения трансферрина желе¬
зом более 60%. У нашего больного эти цифры cocTaoHjm 1033 мкг/л и 99%
соответственно. Однако определялось и повышение ферритина гемолизата до
134 мкг/г НЬ (норма 5—10 мкг/г НЬ), а также тенденция к повышению уровня
трансферриновых рецепторов сыворотки (3 мкі/мл при норме до 2,5 мкг/мл).
Эти noKa3aTejm более характерны для вторичной перегрузки железом. С учетом
противоречивости полученных данных в Медико-генетическом научном цен¬
тре РАМН бьшо проведено молекулярно-генетическое обследование для обнару¬
жения мажорных мутаций (C282Y и H63D) гена наследственного гемохрома¬
тоза HFE. У 95% больных с наследственным гемохроматозом обнаруживается
гомозиготное состояние по мутации C282Y, чего у нашего больного выявлено
не бьыо. Обнаружена лишь мутация H63D в гетерозиготном состоянии (носи-
тельство), что встречается у 20% населения. Значение этого феномена для син¬
дрома перегрузки железом на данный момент изучается.На данном этапе больному проводилась терапия престариумом 4 мі/сут,
верошпироном 50 мг/сут, фуросемидом 40 мг через день, тромбо-АССом
100 мг/сут, прсдукталом-МВ 70 мг/сут, кордароном 300 мг/сут. После повторно¬
го обсуждения больного со специалистами НИИ фтизиопульмонологии решено
начать терапию метипредом в стартовой дозе 24 мг/сут. Ограничением в отноше¬
нии назначения р-адреноблокаторов являлось нарушение АВ-проводимости,
однако попытка добавления низких доз р-адреноблокаторов представля^тась
вполне оправданной.Комментарий М.Г. Полтавской — ассистента кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед. наукДиаіноз генерализованного саркоидоза с поражением сердца, легких, ВГЛУ,
возможно, селезенки и печени в данном случае представляется весьма веро-
ятньп^і. Если рассматривать поражение сердца отдельно, то наиболее частой
причиной развития кардиомегалии является постинфаркгный кардиоскле¬
роз. Инфаркт миокарда пациент мог перенести бессил-штомно, причем для
относительно молодого возраста нашего больного с отсутствием развитых
274 Кардиологияколлатералей коронарного кровотока массивность поражения миокарда и
быстрое развитие кардиомегалии достаточно характерны. Не противоречат
этом>' диагнозу данные ЭхоКГ и сцинтиграфии миокарда, указывающие на
очаговость поражения. Конечно, отсутствие стенокардии и гиперлипидемии
не очень укладывается в концепцию ИБС, но их наличие совершенно необя¬
зательно. В связи с этим проведение коронароангиографии в данном случае
явится одним из наиболее важных методов дифференциальной диагностики.
Не слишком типично течение заболевания и для идиопатической дилатанион-
ной кардиомиопатии. Обычно жизнеугрожаюище желудочковые аритмии при
этой болезни возникают у пациентов с тяжелой застойной недостаточностью
кровообращения и мерцательной аритмией. Здесь же заболевание манифести¬
ровало сразу с желудочковых нарутпений ритма в сочетании с нарушениями
проводимости. При ЭхоКГ у бальньтх с дилатационной кардиомиопатией
нарушениям сократимости диффузного характера могут сопутствовать локаль¬
ные гипокинезии отдельных участков миокарда, но вот данные сцинтиграфии
нетипичны. При дилатационной кардиомиопатии мы ожидати бы увидеть
более диффузные и «мелкоочаговые» нарушения перфузии.Сочетание изменений в миокарде с поражением легких и внутригрудными
лимфатическими узлами делает диагноз саркоидоза сердца наиболее вероят¬
ным. Он позволяет объяснить и очаговость поражения миокарда (гранулема-
тоз), и превалирование в клинической картине жизнеуфожающих желудоч¬
ковых аритмий, в том числе в дебюте заболевания, и najm4He выраженных
нарушений проводимости.Комментарий О.В. Благовой — доцента кафедры факультетской терапиіі № і
лечебного факультета Первого МГМУ нм. И. М. Сеченова, кацд. мед. наукВ кардиальной патологии данного пациента ведущим синдромом, наряду
с кардиомегалией, являются тяжелые нарушения ритма и проводимости,
которые на данный момент в значительной степени определяют прогноз
заболевания. Комбинация злокачественных желудочковых аритмий с глубо¬
ким нарушением проводимости в АВ-соединении и системе Гиса—Пуркинье
весьма тип№1на для поражения сердца в рамках генерализованного саркоидо¬
за. Однако сам по себе длительный аритмический анамнез (экстрасистолия
в юности, ставшая достаточным основанием для освобождения от службы
в армии, возобновление нарутпений ритма около 10 лет назад) застав-іяет
усомниться в четкой связи аритмий и саркоидоза — отсутствует корреляция
между стадией поражения легких в рамках саркоидоза и тяжестью поражения
сердца. Насколько можно судить по литературным данным, поражение серд¬
ца в рамках саркоидоза развшзается на более поздних стадиях лсшчіюго про¬
цесса. В нашем случае поражение сердца (аритмии) долгое время находилось
на первом плане. Это заставляет исключать первичные аритмогенныс забо¬
левания, для большинства из которых характерен наследственный харакгср.
В анамнезе жизни обращают на себя внимание внезапные смерти родствен¬
ников в относительно молодом возрасте (отец, мать, тетка но матери), а также
желудочковая экстрасистолия у сына. Поскольку саркоидоз не наследуется.
Глава 14. Генерализованный саркоидоз с преимущественным поражением... 2 75в качестве возможных причин наследуемых желудочковых: аритмий следует
рассматривать аритмогенную дисплазию правого желудочка, другие канало-
патии; нельзя исключать также наследственные варианты кардиомиопатий
(дилатационной, гипертрофической с исходом в дилатацию), которые могут
сочетаться с нарушениями ритма и проводимости сердца, Для угочнения
причины аритмий целесообразно проведение внутрисердечного элекгро-
физиологического исследования, которое одновременно может уточнить
показания к хирургическому лечению нарушений ритма и проводимости
(в первую очередь к имплантации кардиовсртера-дефибриллятора), а также
МРТ для исключения аритмогенной дисплазии правого желудочка.Комментарион M.B, Шеянова— ассистента кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед. наукНекоторое время назад нам пришлось наблюдать весьма сходный клиниче¬
ский случай. У пятидесятилетнего мужчины, предъявлявшего жалобы на уме¬
ренную одышку при физической нафузке, перебои в работе сердца и неболь¬
шие отеки голеней и стоп, имели место совершенно аналогичное поражеііис
миокарда с аритмиями и диффузным снижением сократимости, увеличение
внутригрудных лимфатических узлов, а также массивное диффузно-очаговое
поражение легочной ткани с вовлечением плевры и небольшим выпотом в
плевральную полость. При исследовании ФВД выявлялись преиліупїественно
рестриктивные изменения. Коронароангиография не проводилась, однако
клинических данных за ишемическую природу поражения сердца получено
не было. Дифференциатьный диагноз проводился между іранулсматозньгми
процессами (туберкулез, саркоидоз), лимфопролиферативньтми заболева¬
ниями (наиболее актуальным представ-тялось предположение о лимфоме
внутригрудных лимфатических узлов), прочими опухолями, васк>'литами
и т.п. С учетом серьезности дифференцируемых процессов и очевидной
потребности в этиопатогенетической терапии представляліось совершенно
необходимым установление максимально точного, морфологически под¬
твержденного диагноза. После тшательноіо ана'шза аргументов как в пользу,
так и против проведения инвазивных диагностических вмешательств было
принято решение о видеоторакоскопической биопсии легкого. При исследо¬
вании полученного материала были обнаружены характерные гранулемы без
казеозного некроза, что позволило диагностировать у больного саркоидоз с
поражением сердца, легких и внутрифудных лимфатических узлов. Начата
системная кортикостероидная терапия, состояние пациента улучшилось.
Возвращаясь к обсуждаемому клиническому случаю, прежде всего хотел бы
отметить явное сходство этих двух пациентов и согласиться с предположе¬
нием о саркоидной природе процесса. Однако признаем: без морфологиче¬
ской верификации диагноз саркоидоза так и останется вероятным, причем
его необходимо будет дифференцировать с серьезными и в клиническом, и
в прогностическом смысле процессами, лечение которьтх совершенно раз¬
лично. Нуждается ли обсуждаемый пациент в торакоскопической биопсии
легкого и внутрифудных лимфагическтгх узлов? Что возобладает в данном
276 Кардиологияслучае: соображения безопасности (наркоз и торакоскопия у пациента с пора¬
жением сердца и желудочковыми аритмиями высоких градаций, конечно,
связаны с определенным риском) или необходимость максимально точного
диагаоза? Безусловно, сделать подобный выбор — это неотъемлемое право и
прерогатива лечашего врача. Выскажу лиіиь собственное мнение: мы нередко
преувеличиваем риск инвазивных лечсбно-диагносгических процедур у паци¬
ентов с сердечно-сосудистой патологией. Решившись же на их проведение
(разумеется, после тщательного рассмотрения всех аргументов за и против),
мы нередко можем избежать многах сомнений и ктинических проблем и чув¬
ствовать себя значительно увереннее в подобных клинических ситуациях.
Хотел бы поддержать решение лечашдгх врачей о назначении пациенту
системных стероидов. Наливше у больного туберкулеза или злокачественной
опухоли маловероягно, а польза от подавления вероятного фанулематозного
воспаления, в том числе замедления необратимых фиброзньг>[ изменений в
сердце и легких, представляется очевидной. Очевидно также, что от стеро¬
идной терапии у данного пациента нельзя ожидать быстрого и разительного
эффекта — в сердце и легких уже развились малообратимые изменения, и
выздоровление в подобной ситуации определенно будет выздоровлением с
заметным функциональным дефектом.Комментарий А.В. Недоступа — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукТаким образом, проведенное обсуждение не позволило однозначно оста¬
новиться на каком-либо из предполагаемых диагнозов, однако более четко
очертило круг дальнейших диагностртческих мероприятий. Для исключения
ИБО у нашего больного необходимо проведение коронароангиофафии,
для уточнения характера поражения селезенки и печени — КТ органов
брюшной іюлости, для диагностики саркоидоза — сцинтиграфия с галлием.
Безусловно, говорить всерьез о саркоидозе можно будет лишь после морфо¬
логической верификации диагноза. Из какого органа мы сможем получить
необходимый гистологический материал? В связи с тяжелыми нарушениями
ритма и проводимости однозначно отпадает мысль об эндомиокардиальной
биопсии. Значителен риск развития жизнеугрожающих аритмий и при транс-
торака,'ШНой биопсии легких, но все же возможность видеоторакоскопии мы
планируем обсудить с хирургами. Третьим «источником*> гистологического
материала для поиска гранулемы может явиться печень, но лишь в случае
обнаружения при КТ убедительных признаков ее поражения. При любом
результате наптего диагностического поиска, с >четом тяжелых нарушений
проводимости, офаничивающих медикаментозную антиаритмическую тера¬
пию, патщенту показана имплантация кардиовертера-дефибриллятора.P.S. Обследование больного было продолжено. Для верификации диагноза
ИБО бььта выполнена коронароангиография: выявлен 10% стеноз передней
межжелудочковой артерии, значимых атеросклеротических изменений
коронарных артерий нет
Глава 14, Генерализованный саркоидоз с преимуи^ественным поражением... 277При КТ органов брюшной полости, выполненной с целью оценки распро¬
страненности лимфоаденопатки, визуальной оценки печени и селезенки,
выявлено: печень умеренно увеличена (235x145 мм), контуры мелкобугристые,
плотность повышена (71—85 едН), диффузно неоднородна, сосудистый рису¬
нок усилен. Селезенка умеренно увеличена (120x40 мм), плотность паренхимы
60 едН. Почки; справа в нижней чашечке несколько мелких или один кора^і-
ловидный конкремент до 14 мм длиной. Позади желудка — округлая структура
15x10 мм плотностью 50 едН, которая может соотаетствовать лимфоузлу. По
ходу аорты, больше слева, не исключается наличие отдельных увеличенных
лимфоузлов размерами до 9 мм.Данные изменения весьма напоминали цирроз. Кроме того, не исключа¬
лось увеличение параортальных лимфатических узлов. С учетом полученных
данных была проведена пункционная биопсия печени. При гистологическом
исследовании выявлены участки гидропической дистрофии, отдельщ.іе дис-
пластичные гепатоциты с гиперхромными ядрами, умеренная лимфоидная
инфильтрация портальных трактов, широкое поле фиброза со склерозиро-
ванными фанулемами, содержащилто немного эпителиоидных и отдельные
гигантские многоядерные клетки. Гистологическая картина соответствова-іа
фанулематозному саркоидному поражению печени с развитием выраженного
фиброза и некоторым нарушением долькового строения печени. Признаков
гемохроматоза обнаружено не бы-то.После повторной консультации в НИИ фтизиопульмонологии диагноз был
сформулирован след>'ющим образом: генерализованный саркоидоз с пораже¬
нием внутригрудных и внутрибрюшных лимфатических узлов, легких, сердца
(синдром дилатационной кардиомиопатии с нарушениями ритма и прово¬
димости: устойчивые пароксизмы желудочковой тахикардии, частая поли-
топная желудочковая эксфасистолия, АБ-блокада I степени, полная блокада
правой ножки пучка Гиса, блокада передней ветви левой ножки п>"чка Гиса),
печени (фанулематозный гепатит, фиброз). Недостаточность кровообращения
НА стадии, HI функционального класса (NYHA).В результате терапии метипредом 24 мг/сут при повторной КТ легких отме¬
чена положительная динамика в виде повышения пневматизации легких за
счет уменьшения инфильфативных изменений, уменьшение размеров лимфа-
тичесюїх узлов средостения (до 6,5 мм). Картина ЭКГ существенных измене¬
ний не претерпела. Наиболее вероятно, что изменения в миокарде в настоящее
время уже носят характер ск;іеротических и вряд ли поддадутся гормональной
терапии, однако окончательно судить об этом можно будет .чипіь при более
длительном наблюдении за пациентом. В связи с высоким риском рециди¬
ва жизнеуфожающей желудочковой тахикардии, у^штывая сохраняющуюся
эктопическую желудочковую активность, выраженное снижение насосной
функции левого желудочка, в Научном центре сердечно-сосудистой хирургии
им, А.Н. Бакулева РАМН 10.06.2004 г. выполнена имплантация кардиовертера-
дефибриллятора. Больной вернулся в г. Курск, дальнейшая информация о его
состоянии отсутствует.
27S КардиологияХотя саркоидоз как нозологшіеская форма известен более ста лет, вариант
с поражением сердца был впервые описан в 1929 г, М. Bernstein и соавторами
(саркоидный миокардит был выявлен при аутопсии 52-летней русской эми-
трантки с мультисистемным процессом). В последнее время проблема пора¬
жения сердца при саркоидозе привлекает все большее внимание. По данным
разных авторов, частота этой патологии колеблется в пределах от 5 до 60%.
Такой широкий интервал во многом обусловлен трудностями своевременной
диагностики. Если у 5% больных диагноз устанавливается прижизненно, то
у 50% его подтверждают при аутопсии, причем у половины из них именно
поражение сердца является непосредственной причиной смерти в результате
желудочковьгх аритмий и нарушений проводимости.Доказано отсутствие четкой корреляции между течением легочно-
медиастинального и кардиального процессов. У одних пациентов с I стадией
внугрифудного саркоидоза может быть тяжелое поражение сердца, тогда как
у других даже в IV стадии не наблюдается значимых нарушений сердечной
деятельности. Более того, изолированное поражение сердца может предше¬
ствовать легочным изменениям. Сообщения о таких случаях периодически
появляюі'ся в литературе, и зарубежные исследователи даже рекомендуют
подозревать саркоидоз в каждом неясном случае тяжелой кардиомиопатии
или фатальной аритмии. У I/3 больных кардиосаркоидоз дебютирует на фоне
ремиссии легочно-медиастинального процесса; он часто сочетается со II рент¬
генологической стадией, поражением кожи, глаз, печени. Обсуждается гене¬
тическая обусловленность поражения сердца при саркоидозе (ассоциация с
аллелью HLA-DQB1*0601 и атипичной аллелью гена ФНО-а - TNFA^?).Из всех структур сердца чаше всего поражается лгаокард. Из-за постоян¬
ных ритмических сокращений гранулемы не успевают оформиться. Иногда
при ярком гранулематозе других органов в сердце находят лишь глыбки гиа-
лина. Так же, как и в других органах, процесс в сердце имеет стадийность:
нифильтрация, отек — формирование гранулем — их созревание — фиброз,
Инфильтративные изменения могут охватывать коронарные артерии, прони¬
кать в их адвентицию и мышечную стенку, не В.1ИЯЯ на кровоток (при коро-
нарографии просвет артерий не изменен), но повышая риск коронароспазма.
Описано как очаговое, так и диффузное поражение сердца, с соответствующи¬
ми клиническими прояатсниями. Излюбленной локализацией очаговых изме¬
нений в миокарде являются проксимальные отделы межжелудочковой пере¬
городки (реже межпредсердная перегородка), клетки АВ-соединения и ствола
пучка Тиса, проксимальные отделы свободных стенок обоих желудочков {рис.
14.6). Очаговое поражение «рабочего» миокарда напоминает инфаркт, возмож¬
но формирование аневризмы. Локализация гранулем в сосочковых мьшшах и
области митрального клапана нередко приводит к недостаточности последнего.
Интерстициальное воспаление приводит снача^та к диастолической дисфунк¬
ции — именно она обнаруживается у большинства больнык. Последующийфиброз ведет к нарушению систолической функции, развитию диффузной ШІИлокальной гипокинезии чаще в области перегородки с переходом на верхушку.
Возможен исход в кардиомиопатию по дилатационному либо рестриктивном^'
Глава М, Генерализованный саркоидоз с преимущественным поражением.., 279Рис. 14.6. Локализация поражения сердца
при кардиосаркоидозс. Пояснения в текстетипу. Выраженная легочная гипертен¬
зия и формирование легочного сердца
возникают в основном у больных с
тяжелыми рестриктивны ми изменени¬
ями, грубым фиброзом легких в рамках
ni-IV стадии саркоидоза. Иногда (в
20% случаев) появляется выпот в пери¬
карде, чаще не значимый клинически.Течение кардиосаркоидоза доволь¬
но вариабельно — от субклинических
слуїаев до кардиотенного шока в дебю¬
те. Обычно юшническая картина доста¬
точно неспедифична — именно это
затрудняет диагностику. Основными
синдромами ЯБЛ51ЮТСЯ; болевой, нару¬
шения ритма и проводимости, недоста¬
точность кровообращения. Кардиалгии
обычно однотипны, длительны (до
получаса и более), возникают после
окончания физической наїрузки и в
покое, плохо снимаются нитратами и«уходят» на фоне стероидной терапии. Могут быть достаточно интенсивными,
симулируя инфаркт миокарда. По мнению многих исследователей, кардиалги-
ческий си^щром является следствием нарущений микроциркуляции.Нарушения ритма и проводимости, возникающие у пациентов, многооб¬
разны. Именно они чаще определяют прогноз. Наиболее часто встречаются
компоненты триады:• атриовентрикулярная блокада;• блокада правой ножки пучка Гиса;• желудочковые аритмии.Желудочковая экстрасистолия встречается у большинства больных. Она
может быть мономорфной, с источником чаще в правом желудочке и поли¬
морфной — при тяжелом диффузном поражении миокарда с дилатацией камер.
Злокачественный характер эксфасистолии нарастает обычно параллельно
активности заболевания. При этом возможен переход в желудочковую тахи¬
кардию (по механизму re-entry), рефрактерную к антиаритмикам. Возможно
развитие мерцания и трепетания предсердий, синоатриальной дисфункции.
Остановка синусового узла описана даже в качестве дебюта заболевания.
Частота полной поперечной блокады достигает 33%; приступы Морганьи-
Эдамса-Стокса могут доминировать в клинической картине. Регулярная реги¬
страция ЭКГ у определенного больного может выявить постепенное нараста¬
ние степени блокады соответственно росту активности процесса и, наоборот,
улучшение АВ-проведения в результате стероидной терапии. Описаны случаи
рецидива АВ-блокады после плановой отмены кортикостероидов. Кроме
нарушений ритма и проводимости, на ЭКГ у пациентов с саркоидозом сердца
280Кардиологияможно выявить инверсию зубца Т (как правило, в грудных отведениях), рас¬
ширение /^-зубца, появление патолопіческого зубца Q.При ЭхоКГ можно выявить;• гаперзхогеїшьіе включения в миокарде (нечасто), рис. М. 7;• утолшение или истончение перегородки и задней стенки левого же.тудочка;• локальный и диффузный гипокинез;• дилагацию левого, реже — правого желудочков и предсердий;• признаки аневризмы;• пролапс митрального клапана с регургитацией, трикуспидальную регур-
гитадию;• легочную гипертензию;• диастолическую и систолическую дисфункцию миокарда;• перикардиальный выпот, утолщение листков перикарда.Для подтверждения саркоидной природы всех этих нарушений исполь¬
зуются: сцинтиграфия миокарда с различными изотопами, МРТ или пози-
тронно-эмиссионная томография (которая выявляет снижение накопления
[13К]-аммония — псевдоишсмический тип метаболизма, маркер активного
воспаления). При МРТ признаками кардиосаркоидозаявляются очаговое нако¬
пление контраста в отсроченную фазу на Т1 -изображениях (характерна субэпи-
кардиальная. локализация очагов замедленного накопления) и фокальное повы¬
шение интенсивности сигнала на Т2-изображениях. Преиліуществом метода
являются высокая разрешаюш;ая способность, способность дифференцировать
ишемию и воспаление; в то же время МРТ сердца остается в России малодо¬
ступным методом, она не может использоваться у больных с имплантируемыми
устройствами, обладает низкой чувствительностью и специфичностью при пер¬
вичном обследовании больного со стероидной терапией в анамнезе.С помощью радионуклидных
методик можно визуализировать
гранулемы двумя способами: или
как дефект накопления изотопа,
или, наоборот, его локальную кон¬
центрацию. К первой группе изото¬
пов относятся таллий-201 и Тс-99т-
сестамиби; сцинтиграмма при этом
очень может напоминать таковую
при ИБС, однако, в отличие от ише¬
мических изменений, при нагруз¬
ке дефекты накопления изотопа
уменьшаются в размерах вплоть до
полного исчезновения (так назы¬
ваемый феномен обратного рас¬
пределения, рис. 14.8, см. цветную
вклейку). К другой группе изотопов
относится галлий-67, отличающий¬
ся более высокой специфичностью.Рис. 14.7. Выявление саркошных гранулем
(обозначены стрелками) в миокарде методом
ЭхоКГ
Глава 14. Генерализованный саркоидоз с преимущественным поражением... 281но низкой чувствительностью. Магаитно-резонансная томоірафия с примене¬
нием соли гадолиния иногда позволяет визуализировать гранулематозные очаги
в миокарде. В целом, учитывая сложность окончательной, морфологической
верификации диагноза, именно эти методы становятся «коне^гной точкой» в
диагностическом поиске. При их недоступности диагноз ставится на основании
эхо-признаков при исключении других причин подобных изменений.Несомненно, что достоверный диагноз возможен только после морфологи¬
ческой верификации — исследования эндомиокардиального биоптата, однако
технические трудности и низкий процент «точного попадания» обусловливают
чувствительность метода при саркоидозе не выше 20%. В связи с этим, как
правило, пациента избавляют от необходимости инвазивного вмешательства,
однако при подозрении на изолированный саркоидоз сердца биопсия миокар¬
да остается методом выбора,В 1993 г. предложены критерии для диагностики саркоидоза сердца
{табл. J4.J). Они подразумевают, что диагноз внекардиального саркоидо¬
за должен быть верифицирован морфологически. В этом случае выявление
определенного набора характерных признаков поражения сердца позволяет
расценивать его в рамках саркоидоза — именно таким образом и был поставлен
диагноз кардиосаркоидоза у нашего больного. При диагностике поражения
сердца у пациента с доказанным диагнозом внесердечного саркоидоза возни¬
кает целый ряд вопросов.• Следует ли подозревать (и активно выявлять) поражение сердца у каждого
больного саркоидозом?• Стоит ли при диагностике кардиосаркоидоза учитывать все кардиаль¬
ные жалобы (или некоторые из них должны заведомо расцениваться как
неспецифические)?Таблица 14.2Диагностические критерии саркоидоза сердца
(Japanese Ministry of Health & Welfare, 1993)КритерииПризнаки поражения сердцаГистологическиеЭпителиоидноклеточные гранулемы без казеозаКлиническиеМорфологическая верификация эксгракар диально го саркоидоза
+ критерий (а) и >1 критерия (б-д) (по одному компоненту каж¬
дого критерия:а) полная блокада правой тюжки пучка Гиса, атриовентрикуляр¬
ная блокада, отклонение электрической оси сердца влево, желу¬
дочковые аритмии (класс II и выше по Lown), патологический
зубец С?, изменения ST-Tна ЭКГ;б) дискинезия, локальное истончение, дилатация левого желудоч¬
ка при ЭхоКГ;в) дефекты накопления при сцинтиграфии миокарда с 201TI-
х^юридом, повышенный захват б70а-цитрата, 99Тс-пирофосфага;г) наруитения внутрисердечного давления и сократительной функ¬
ции при катетеризации сердца;д) интерстициальный фиброз, клеточная инфильтрация в биопта-
тах миокарда
2Н2 Кардиология• Оправдано ли назначение стероидов при отсутствии кардиальных жалоб
и показаний со стороны легочного процесса, но при наличии инструмен¬
тальных доказательств кардиосаркоидоза?Наше исследование (Иванова Д.А., Борисов С.Е., Недоступ А.В., Па¬
ша С.П., 2008), выполненное на группах пациентов саркоидозом с кардиаль¬
ными жалобами и их полным отсутствием, позволило выработать алгоритм
диагностики высоковероятного кардиосаркоидоза без использования МРТ
сердца и эндомиокардиальной биопсии {рис. 14.9).Принципиальными отличиями нашего алгоритма от ранее предлагаемой
модели (Schulte W. et al., 2005) являются: а) неинвазивный харакгер; б) рас¬
пределение роли первого этапа диагностики между ЭКГ, ЭхоКГ, субъектив¬
ными симптомами и фактором генерализации; в) ключевое значение ОФЭКТ;
г) доступность большинства исследований, включенных в алгоритм.При подозрении на саркоидоз сердца проводится оценка объема генера¬
лизации саркоидоза, характера жалоб, данных ЭКГ и ЭхоКГ (первый этап);
при получении любых данных, указанных в алгоритме, проводится суточное
мониторирование ЭКГ по Холтеру (второй этап). При неполучении — дела¬
ется заключение о низкой вероятности поражения сердца у данного больного,
диагностический поиск прекращается. Основная роль суточного монитори-
рования — выявление и уточнение характера транзиторной ЭКГ-патологии.
Третьим обязательным этапом является ОФЭКТ миокарда с '^^"^Tc-MIBL При
выявлении на данном этапе нарушений перфузии и/или наличия характер¬
ной патологии ЭКГ и ЭхоКГ проводятся дифференциально-диагностические
исследования четвертого этапа. Перечень их определяется спецификой выяв¬
ленных ранее нарушений. Подтверждение другого заболевания сердца, полно¬
стью объясняющего эти нарушения, или же сочетание нормальной перфузии
миокарда с отсутствием ЭКГ- и/или ЭхоКГ-критериев позволяют исключить
кардиосаркоидоз,Диагноз саркоидоза сердца, таким образом, ставится при наличии: а) ЭКГ-
и ЭхоКГ-критериев, в том числе при нормальных данных ОФЭКТ, после
исключения других заболеваний сердца, и^ш б) ЭКГ-критериев и перфузион-
ных нарушеїіий, или в) только перфузионных нарушений, после исключения
других причин соответствутошей ОФЭКТ-картины.Основой лечения саркоидоза сердца, как и вообще саркоидоза, являются
глюкокортикостероиды. Поражение сердца требует назначения более высо¬
ких доз гормонов (до 1,5 мг/кг/сут), в среднем от 30 до 60 мг/сут. Конечно,
они неэффективны, когда процесс переходит в склеротическую стадию,
однако в отсутствие стероидной терапии поражение сердца неизбежно про¬
грессирует. Однако в делом стероиды улучшают прогноз при саркоидозе
сердца, замедляют его прогрессирование, предупреждают развичис сокра¬
тительной дисфункции и ремоделирования камер у больных с исходной
ФВ >30%, улу^ішают проводимость, но обычно не уменьшают частоту желу¬
дочковых аритмий,По нашим данным, кардиальная симптоматика прогрессировала без назна¬
чения стероидов, в то же время проведение кортикостероидной терапии
САРКОИДОЗ ОРГАНОВ ДЫХАНИЯОценка гене¬
рализации>2 экстратора-
капьных
локализацийАнализ жалобI «Перебои» в работе!
сердца, приступы
сердцебиения,
одышка >2 баллов
по MRCDSЭКГ в 12 отведенияхПолная блокада правой ножки пучка
Гиса, желудочковые экстрасистолы,
патологический зубец О, отрица¬
тельные зубцы Т в >2 отведениях,
отклонение ЭОС влево, АВ-блокадаЭхоКГСнижение ФВ, локальные
гипокинезии, дилатация.
гипертрофия или истончение
стенок ЛЖ, диастолическая
дисфункция Отсутствие всех перечисленных симптомовIСАРКОИДОЗ СЕРДЦА МАЛОВЕРОЯТЕНДинамическое наблюдениеНарушения пер¬
фузии + любые
данные ЭКГ
и ЭхоКГНормальная перфузия+ сочетание любого из перечисленных
изменений ЭКГ (ХМ-ЭКГ) с патологией
ЭхоКГНормальная перфузия+ отсутствие перечисленных
изменений ЭКГ (ХМ-ЭКГ)
и/или ЭхоКГЕсть другие заболевания, объясняющие симптоматикуСАРКОИДОЗ СЕРДЦА ВЫСОКОВЕРОЯТЕНРис- 14.9. Алгоригм диагностических мероприятий при подозрении на поражение сердца у больных саркоидозо.м
284 Кардиологияоказываяо стабилизирующее влияние на течение процесса в сердце, который
на фоне терапии протекал волнообразно (по-видимому, это отражает наличие
рецидивов). Максимальный эффект стероидной терапии проявлялся к концу
первого и на втором год>^ наблюдения. Среди получавших стероиды лучшая
динамика отмечена у больных с феноменом обратного перераспределения при
исходной ОФЭКТ, что позволяет предполагать роль этого феномена как воз¬
можного критерия активности саркоидоза сердца. При отсутствии стероидной
терапии динамика носила одинаково прогрессирующий характер независимо
от исходного наличия кардиальных жалоб.В качестве основного средства профилактики внезапной смерти больных
кардиосаркоидозом рекомендуется имплантация кардиостим>^лятора уже при
АВ-блокаде I степени; имплантация кардиовертера-дефибриллятора при нали¬
чии желудочковой экстрасистолии высоких градаций, эпизодов желудочковой
тахикардии. Возможно применение антиаритмиков, однако всеми авторами
подчеркивается их крайне низкая эффективность. Лечение недостаточности
кровообращения проводится по общим правилам. В случаях с обширным
жизнеутрожающим поражением миокарда, рефрактерным к терапии, показана
трансплантация сердца.Прогноз при кардиосаркоидозе точно не определен. Ранее считалось,
что продолжительность жизни при наличии симптомов поражения сердца
составляет не более 2 лет. Последние исследования показали, что пятилетняя
выживаемость достигает у этих больных 40—60%; к примеру, в исследованиях
на японской популяции она составляет всего 10% без стероидной терапии, но
повышается до 75% при ее проведении. Независимыми предикторами леталь¬
ности являются высокий функциональный класс недостаточности кровообра¬
щения (по NYHA), большой конечно-диастолический размер левого желудоч¬
ка, наличие устойчивой желудочковой тахикардии.
Глава 15ТЯЖЕЛЫЙ ИНФЕКЦИОННЫЙ ЭНДОКАРДИТ КРАЙНЕ
РЕДКОЙ ЭТИОЛОГИИ У БОЛЬНОЙ С ВРОЖДЕННЫМ
ИММУНОДЕФИЦИТОМ: ОСОБЕННОСТИ
ДИАГНОСТИКИ И ЛЕЧЕНИЕА.В. Вахляев, А.И. Катков, АЛ. Нестеров,
ИЛ. Новикова, Я.С. Овчинников, В.П. Седов, А.Л. СыркинНесмотря на прогресс медицинской науки и техники, диагаостика и лече¬
ние подострого инфекционного эндокардита лишь усложняются, что связано
с вариабельностью его клинической картины, широким спектром этиологи¬
ческих факторов, распространением резистентности к старым и вновь соз¬
даваемым антибиотикам, отсутствием полноценной фундаментальной базы.
В представленном клиническом наблюдении возбудителем заболевания явил¬
ся представитель класса водорослей, что объясня.ю тяжесть и необычность
клинической симптоматики и заставило заподозрить и диагностировать у
больной врожденный иммунодефицит. Успех в долгом и драматическом лече¬
нии молодой пациентки был достигнут только благодаря коллегиальному
взаимодействию между кардиологами терапевтического и хирургического
профиля, специалистами лучевой диагностики, аритмологами, клиническими
микологами и иммунологами, что лишний раз подтверждает; проблема инфек¬
ционного эндокардита есть проблема обшемедипинская, требуюшая постоян¬
ного обмена практическими и теоретическими знаниями.Больная В., 31 год, поступила в клинику кардиологии Московской меди¬
цинской академии имени И.М. Сеченова 14.09.2009 г. с жалобами на перебои в
работе сердца, одышку, возникающую при физической нагрузке и проходящую
в покое, подъемы температуры тела до 38 °С, общую слабость.Анамнез {рис. 15.1). Заболела остро 08.08.2009 г., когда впервые поднялась
температура до 39—40“С; 09.08.2009 г. в связи с продо.іжающейся лихорадкой
вызвала бригаду С МП, проведена в/в инъекция (название препарата неизвест¬
но), температура снизилась. 12.08.2009 г. вновь отмечался подъем температуры
до 40°С, по поводу чего была вновь вызвана бригада СМП. Участковый тера¬
певт поставил диагноз «ангина?», проводилось лечение сумамедом. 17.08,2009 г.
появились головная боль, тошнота, рвота. Больная бьша госпитализирована в
инфекционное отделение п. Монино с диагнозом «лихорадка неясной этиоло¬
гии». Была проконсультирована неврологом, рекомендовано проведение МРТ
головного мозга с контрастированием.При выполненной 21.08.2009 г МРТ головного мозга выявлены образова¬
ния, расцененные как множественные метастатические поражения головного
Глава 15, Тяжелый инфекционный эндокардит крайне редкой этиологии... 287Таблица 15.1Схема антибиотикотерапии, проводившейся больной 6.Сроки проведения терапииАнтибиотикотераоияС 21.08.2009 по 13.09.2009Цефотаксим + Рифампидин + Ванкомииїш +
ФлуконазолЦефотаксим + Гснтамицин
Моксифлоксацин С 14.09.2009 по 28.09.2009Амикацин 500 мг/сут + Амоксиклав 14,4 г/сут +
Флуконазол 50 мг/сутС 29.09.2009 по 16.10.2009Меронем 2 г/сут + Ваикомицин 2 г/сут + Диоксидин
900 мг/с>т С 16.10.2009 по 21.10.2009Цефуроксим 2,25 г/суг + Амикацин 100 мг/суг +
Диоксидин 300 мг/сут С 21.10.2009 по 03.11.2009Линсзолид 1200 ш'/суг + Амфотерицин В (фунгизон)
50 мг/сутЛинєіолид 1200 мг/сут + Амфотерицин В (амфолип)
50 мг/сут€04.11.2009 по 04.12.2009Линезолид 1200 мг/сут + Вориконазол 200 мг/с>тС 12.12.2009 по 12.01.2010Флуконазол 200 мг/с>тпоявление вегетаций на аортальном клапане, левом предсердии. Больная кон¬
сультирована иифскнионртстом: изменения головного мозга расценены как
вторичный менингоэнцефалит, множественные абсцессы головного мозга.В отделении проводилась терапия; рифампицин, ванкомипин, цефотаксим,
флуконазол, по.гяризующая смесь, хлоропирамин, ацетазоламид, ферогшскс,
мсксидол, фолиевая кислота, моксифлоксацин (см, табл. 15.1). Несмотря
на проводимое лечение, сохранялось повышение температуры (13.09.2009 г.
вечером 38 °С, 14.09-2009 г. утром 37,2 °С), Последнее введение моксифлокса-
цина 13.09.2009 г вечером, 14.09.2009 г. выписана из Московского областного
научно-исследовательского клинического института им. М.Ф, Владимирского
и госпитализирована в отделение реанимации и интенсивной терапии клиники
кардиологии Московской медициііской академии имени И.М. Сеченова.Эпидемиологический анамнез: в течение жизни считала себя практически здо¬
ровой, нрост>^дньтми заболеваниями страдала не чаше 1 раза в 2 года, к врачам не
обращалась, медицинского обследования не проходила. В зпилемиолог№іеском
анамнезе имеются указания на купание 25.07.2009 г, в Большом Медвежьем озере
в Щелковском районе Московской области, на кру гом берегу которого распола¬
гается кяадбише {рис. 15,3). Компакте инфекционными больными отрицает.При поступлении: состояние средней тяжести. Кожные покровы блед¬
ные, теплые, сухие. Температура тела 37,2 *С. Дыхание жесткое, хрипов нет.
Систолодиастолический шум на верхутнке, проводящийся на спину, диасто¬
лический шум в точке Боткина. ЧСС 100 в минуту, АД 100/60 мм рт.ст. Печень
по краю реберной дуги, селезенка не пальпируется. Неврологический дефицит
минимален.На ЭКГ при поступлении синусовая тахикардия, на ЭКГ от 18.09.2009 i:
частая предсердная экстрасистолия {рис. 15.4).
2В8КардиологияРис. 15.3. Большое Мсдвежт>е озеро Щелковского района, в KOTopoKf купалась больная В.Г^ІГ:w4^VA-•.: <<—Рис. 15.4. Злекірокардиограмма больной С. от 18.09,2009 г., скорость записи 25 мм/сВ анализах кроеи отмечались гипохромная анемия, низкое содержание
сывороточного железа, относительный моноцитоз и повышенная СОЭ: НЬ
87,7 г/л, эритроциты 3,47 млн, лейкоциты 6,18 тыс., моноциты 12,85%, эози-
нофилы 6,67%, СОЭ — 30 мм/ч, железо — 22 мкг/д;і, трансферрин 180 мг/дл.
процент насыщения железом — 8,7%.
Глава 15. Тяжелый инфекционный эндокардит крайне редкой этиологии... 289При ЭхоКГ, проведенной из трансторакального доступа, получены дан¬
ные, не отличавшиеся от результатов исследования в Московском областном
научно-исследовательском клиническом институте им, М.Ф. Владимирского.
При повторной МРТ головного мозга от 16.09.2009 г. отмечалось некоторое
уменьшение инфильтрации вещества мозга и образование четких полостей,
данные за новые очаговые изменения при сравнении с данными М РТ головно¬
го мозга от 21.08.09 г. не получены.При рентгенографии органов грудной клетки, УЗИ органов брюшной поло¬
сти и щитовидной железы патологических изменений не выявлено, при КТ
органов брюшной полости с контрастированием септические очаги также не
обнаружены. При колоноскопии получена нормальная эндоскопическая кар¬
тина, при ЭГДС — острый очаговый геморрагшіеский гастрит.Согласно данным исследований и клинической картине, диагноз инфек¬
ционного эндокардита с поражением аортального и митрального кланапов и
абсцессами в головном мозге не вызывал сомнений. Он был сформулирован
следующим образом. Сепсис. Перврічньїй подострый бактериальный эндокар¬
дит с поражением аортального клапана, митрального клапана. Недостатотаость
аортального клапана П степени, митрального клапана ІП степени. Абсцесс
фиброзного тела сердца. Недостаточность кровообращения ПА стадии.
Множественные абсцессы головного мозга. Хроііический тонзиллит вне обо¬
стрения. Острый геморрагический гастрит.Была продолжена комбинированная антибиотикотерапия амикацином
500 мг/сут, амоксиклавом 14,4 г/суг, флуконазолом 50 мг/сут (см. табл. 15.1).
На фоне проводимой терапии сохраня^іась лихорадка. Были взяты анализы
крови на посев, однако рост микрофлоры выявлен не был. С целью уточнения
степени поражения сердца выполнена чреспищеводная ЭхоКГ.Выявлены признаки эндокардита митрального, аортального клапанов и
патологическая полость в области фиброзного тела с образованием фистулы
между корнем аорты и левым предсердием {рис. 15.5). Характер гсмодинамиче-
ских нарушений делал медикаментозное лечение малоэффективным и беспер¬
спективным; восстановление центральной гемодинамики и удаление инфи-
цированіїьіх тканей сердца являлось одним из ключевых пунктов лечебной
стратегии. Стабильное состояние пациентки позволяло предпринять попытку
хирургического вметиательства, и после консультации кардиохирурга больная
была переведена в отделение кардиохирургии Клиники сердечно-сосудистой и
общей хирургии Московской медицинской академии им. И.М. Сеченова.Несмотря на развитие современных хирургических технологий, эндокардит
с вовлечением в деструктивный процесс корня аорты и фиброзного тела до
сих пор является реконструктивной проблемой. Объем планируемого вмеша¬
тельства состоял из удаления пораженных клапанов, аорто-митральной зана¬
вески и пораженных тканей фиброзного тела с последующей реконструкцией
приточно-отгочного отдела левого желудочка, а также корня аорты.С учетом молодого возраста пациентки с ней обсуждался вопрос о возмож¬
ности последующей беременности, было принято ее пожелание об импланта¬
ции биологических протезов аортального и митрального клапанов. По этой
290КардиологияРис. 15.5. Чреспищеводная ЭхоКГ больной С. от 16.09.2009 г. Дефект фиброзного тела
сердца с формированием патологической полости и свиша межцу корнем аорты и
левьом предсердиемже причине встал вопрос о сохранении аннуло-папиллярной непрерывности
левого желудочка для сохранения его систолической и диастолической функ¬
ции. Операция была выполнена 29.09.2009 г. (хирург А.И. Катков).Доступ к сердцу был осуществлен через серединную стернотомию.
Операция выполнена на фоне системной гепаринизации, искусственного
кровообращения с бикавальной каиюляцией и охлаждением иадиентки до
32 °С. После пережатия аорты и поперечной аортотомии сердце остановлено
селективным введением раствора «Кустодиол»^ по общепринятым методикам.
Дальнейшая экспозиция зоны поражения достигнута путем расширения
аортотомии на аорто-митральную занавеску и крышу левого предсердия с
использованием техники, предложенной Т. David. После иссечения ство¬
рок аортального клапана и пораженных тканей крыши левого предсердия
дальнейшая ревизия показала «санированный» абспесс в левом фиброзном
треугольнике и перфорацию передней створки мигра.||ьною клапана 3x5 мм
в сегменте А2 {рис. І5.6, см. цветную вклейку), а также значительную удален¬
ность от операционного поля головок папиллярных мышц, что затрудняет
воссоздание аннуло-папиллярной непрерывности. Доступ расширен двупред¬
сердной атриотомисй по Guiradon {рис. /5.7). После получения адекватной
экспозиции была иссечена передняя створка митрального клапана с сохране¬
нием интактной задней с ее подклапанным аппаратом, резецирована инфици¬
рованная часть левого фиброзного треугольника. Для воссоздания передних
подклапанных структур головки папи.ишрных мышц проіиитьт PTFE-нитями
GoreTex CV5 {рис. 15.8, см. цветную вклейку), свободные концы которых после
восстановления целостности митрального кольца фиксированы на 10-м и
2-м часах. Реконструкция митрального отверстия, выходного тракта левого
желудочка и крыши левого предсердия выполнена двумя ксеноперикардиаль-
ными лоскутами (рис. /5.9) по методике, описанной Т. David. В воссозданные
митральное и аортальное отверстия имплантированы биологические протезы
Глава 15. Тяжелый инфекционный эндокардит крайне редкой этиологии... 291Рис. 15.7. Конверсия трансаортального досту¬
па к аортомитральной занавеске в биатриаль-
ный доступSorin Pericarbon MORE № 27 и
Sorin Pericarbon MORE № 21 соот¬
ветственно. Дальнейшее закрытие
камер сердца и восходящей аорты
было выполнено в последователь¬
ности, обратной экспонированию
зоны интереса.Время пережатия составило 260
мин. После восстановления крово¬
тока сердечная деятельность восста¬
новилась самостоятельно с узловым
ритмом 40-50 в минуту. После под¬
ключения электрокардиостимуля¬
тора в режиме DDT пациентка была
без проблем отключена от аппарата
искусственного кровообращения.Интраоперационная чреспищевод-
ная ЭхоКГ не выявила нарушений
функции протезов и патологиче¬
ских потоков.Вегетации с клапанов, створки
аортального и митрального клапа¬
нов и содержимое абсцесса были
отправлены на микробиологическое
и гистологическое исследования.Дано следующее заключение: скле¬
роз и гиалиноз аортального клапана,Строма отечна, с лимфомакрофа-
гальной инфильтрацией. В створках
.митрального клапана выраженная
лимфомакрофагальная инфильтра¬
ция с примесью полиморфно-ядер¬
ных лейкоцитов, очаги некроза. На
поверхности тромботические нало¬
жения. Морфологические измене¬
ния соответствуют гранулематозно¬
му воспалению с некрозом в центре
фанулемы іфис. 15.10, см. цветную
вклейку).В послеоперационном периоде
проводилась антимикробная тера¬
пия меропенемом 2 г/сут, ванко-
мицином 2 г/сут, гидроксиметилхиноксилиндиоксидом 900 мг/сут (см. табл.
J5.1). 01.10.2009 г. назначена терапия варфарином, целевые значения МНО
2,0—3,0 были достигнуты 26.10.2009 г.Рис. 15.9. Реконструкция митрального отвер¬
стия, выходного тракта левого желудочка и
крыши левого предсердия выполнена двумя
ксеноперикардиальными лоскутами
Рис. 15.12. ЭКГ больной В. от 01.10.2009 г. Скорость записи 25 мм/с. Пояснения в текстеММА к-ка
кардиологии27.10.09 04.11.09 04.12.09 11.12.09Рис. 15.13. Анамнез больной В., 31 гол, с 27.10.2009 г. до выписки из клиники кардиологииНазначено: линезолид 1200 мг/сут, фунгизон (амфотерииин В) 50 мг/сут
(см. /nad'i. ISJ). В связи с плохой переносимостью фунгизона, проявлявшей¬
ся тошнотой, рвотой, нарастанием креатинина крови, режим дозирования
изменен на 50 мг/сут через день. 27.10.2009 г. больная переведена в клинику
кардиологии (р«с. ISJJ).Продолжена терапия фунгизоном и линезолидом по прежней схеме.
Несмотря на комбинированную терапию, сохранялась субфебрильная
292КардиологияРанний послеоперационный период сопровождался выраженной потливо¬
стью, тошнотой, лихорадкой до 38 “С (бьыи взяты анализы крови на посев),
АВ-блокадой 111 степени {рис. I5.IL 15.12). Больной проводилась временная
эндокардиальная стимуляция. В связи с сохранявшейся АВ-блокадой III степе¬
ни 16.10.2009 г. больной имплантирован ЭКС C60DR. Ритм навязан в режиме
DD1 с частотой 60 импульсов в минуту.При ЭхоКГ в позициях митрального и аортального клапанов визуали¬
зировались нормально функционирующие протезы без патологических
потоков. Индекс площади эффективного отверстия аортального протеза
составил 0,85 cmVm^, что соответствует удовлетворительным критериям
соотноятения «эффективная площадь протеза/площадь поверхности тела
больного».В связи с сохраняющейся лихорадкой изменена схема антибиагикотерапии.
Назначено: цефуроксим 750 мг 3 раза в сутки, амикацин 100 мг/сут, гидрокси-
метилхиноксшшндиоксид 300 мг/сут (см. табл. 15. /). Несмотря на комбини¬
рованную антимикробн\то терапию, с 21.10.2009 г. вновь возобновилась суб¬
фебрильная лихорадка. В посева крови от 05.10.2009 г. и 08.10.2009 г.
выявлен рост Prototheca wickerhamii. Изменена антимикробная терапия.14.09.0928.09.0916.10.09 21.10.0927.10.09Рис. 15.11. Анамнез больной В., 31 год, с момента поступления в клиник>^ кардиологии
до 27.10.2009 г.
-Д<м;^Рис. 15.12. ЭКГ больной В. от 01.10,2009 г. Скорость записи 25 мм/с. Пояснения в текстеММ А к-ка
кардиологииТ27.10.09 04.11.09 04.12.09 11.12.09Рис. 15.13. Аналшез больной В., 31 год, с 27.10.2009 г. до выписки из клиники кардиологииНазначено: линезолид 1200 мг/сут, фунгизон (амфотсрицин В) 50 мг/сут
(см. табл. 15. /). В связи с плохой переносимостью фунгизона, проявлявшей¬
ся тошнотой, рвотой, нарастанием креатинина крови, режим дозирования
изменен на 50 мг/сут через день. 27,10.2009 г больная переведена в клинику
кардиологии (;?мс, 15J3).Продолжена терапия фунгизоном и линезолидом по прежней схеме.
Несмотря на комбинированную терапию, сохранялась субфебрильная
294 Кардиологиялихорадцка. Продолжена терапия фунгизоном в суточной дозе 25 мг на 5% глю¬
козе в/в капельно в течение 3-4 ч ежедневно, линезолидом в дозе 1200 мг/сут.
По причине нарастания креатинина крови фунгизон заменен на липосомаль-
ную форму амфотерицина В — амфолип (см. табл. 15.1). Креатинин крови от26.10.2009 г. — 2,17 мг/дл, 02.11.2009 г. — 1,62 мг/дл. Состояние расценено как
ятрогенная острая почечная недостаточность П степени (клиренс креатинина
по Кокрофт—Голт 27 мл/мин).Тактика лечения больной была обсуждена с заведующим кафедрой кли¬
нической микологии Санкт-Петербургской медицинской академии постди¬
пломного образования, профессором Н.Н. Кіимко. В связи с неэффективно¬
стью химиотерапии и развитием острой почечной недостаточности принято
решение отменить амфотерицин В, продолжить терапию линезолидом в дозе
1200 мг/суг, назначить вориконазол в суточной дозе 400 мг/сут. С 04.11.2009 г.
назначеііа данная схема.Установленный возбудитель Prototheca wickerhamii является крайне ред¬
кой причиной развития инфекционных заболеваний млекопитающих. По
данным литературы, все случаи данной инфекции возникали у лиц с имму¬
нодефицитом. Так как в анамнезе не было указаний на наличие иммунодефи-
иитного состояния, было выдвинуто предположение о возможном дефиците
миелопероксидазы — первичном скрытом иммунодефиците, проявляющемся
преимущественно снижением фунгицидной активности фагоцитов. Данный
иммунодефицит подтвержден количественным (табл. 15.2) и качественным —
цитохимическим {рис. 15.14, aw. цветную вк.^ейку) — методами. Вьывлен дефи¬
цит миелопероксидазы. Специфической имм>'Н0К0ррекции данного иммуно¬
дефицита не существусг.Полное заключение по результатам исследования иммунного статуса боль¬
ной, проведенного в лаборатории иммунодиагностики и иммунокоррекции
Федерального научного центра трансплантологии и искусственных органов
им. академика В.И. Шумакова РАМН (см. табл. 15.2), звучало следующим
образом; дисб'олаис иммунорегуляции за счет снижения CD4+ клеток; актива¬
ция естественной цитотоксичности; снижение сывороточного IgA; снижение
поглотительной способности нейтрофилов; снижение уровня миелоперокси¬
дазы; повышение оксидазной активности и адгезии нейтрофилов.В результате терапии состояние улучшилось, симптомы интоксикации
исчезли, креатинин крови от 13.11.2009 г. составил 0,87 мг/дл. Температура
нормализовалась к 14-м суткам приема вориконазола (вифенда). Было принято
решение продлить курс антимикробной терапии до 04.12.2009 г С 05.12.2009 г
антимикробная терапия отменена. Состояние оставалось стабильно удовлет¬
ворительным, лихорадка не рецидивировала. В анализах крови сохранялась
гипохромная анемия, однако на фоне проводимой терапии препаратами железа
и эпоэтином альфа показатели сывороточного железа пришли к нормальным
значениям, увеличилось число ретикулоцитов в периферической крови с 11%С
до 32%о. По данным эхокардиографии, центральная гемодинамика оставалась
стабильной и соответствовала нормальным значениям. На ЭКГ регистриро¬
вался синусовый рит.м {рис. 15.15).
<*V3*cТЪблглца JS.2Исследование иммунологического статуса больной В. от 03.11 и 10.11.2009 г.Показатель03.11.2009 г.,%10.11.2009 г.,%%вмклЛейкоциты55004000-9000Лимфоциты3425-401800-2500Т-лимфопиты (CD3)706460-751100-1700Т-хелперы (CD4)304039-50600-700CD8+ ІС1ЄТКИ242819-35270-350Иммунорегуляторный индекс
(CD4/CD8)1,31,41,8-2,0NK (CD16+KJI.)3114,810-17200-400С016+0К+кл.7,17,42-6HLADR+кл.16,017,08-15CD3+CD8+KJI.24,04,019-35270-350С025+кл. с рецептором к fL27,313,81-5С095+кл. (апоптоз)18,018,00-10В-лимфоциты (CD 19)108-12150-300IgG г/л15,511,012-14IgAr/л0,81,92,1-2,9IgM і/л1,81Д1,3-L7ЦИК 3% ПЭГ (крупные)455314-35ЦИК 4% (средние)435152-96Соотношение ЦИК 4/3% ПЭГ0,960,962,5-3,5ЦИК 6% (мелкие)7783До 500Нейтрофюш: сегментоядерные3847-723000-4000аалочкоядерт F ые141-6Моноциты111-7Эозинофи^1Ы31-5Фагоцитарный индекс (96)4070-80Фагоцитартгос число (микр, тел)2,34-7Абсолютный фагоцитарный показа¬
тель (микр. тел)24006000-9000нет спонт.15124680-99нет ИНД.124105130-253Индекс стимулятщи0,820,431,7-3,0МПО спонт. (уе.)451666597-699МПО ИНД. (у.е.)267145630-830МПО и.с.0,221,0-1,05Катионные белки споит (уе.)10447477,8-92,8Катионные белки иид. (уе.)67459Адгезия спонт. (у.е.)16623155Адгезия ШІД. (у.е.)92223
296КардиологияРис. 15.15. ЭКГ больной В. при выписке из клиники кардиологии. Скорость записи
25 мм/сБольная была выписана домой 11,12.2009 г. с клиническим диагнозом', сеттсис,
генерализованный прототекоз. Подострый бактериальный эндокардит с пораже¬
нием аортального клапана, митрального клапана и формированием гранулемы с
распадом левого фиброзного треугольника. Аортальная недостаточность ТТ сте¬
пени, митральная недостаточность IИ степени. Состояние после протезирования
(БИО) аортального клапана, протезирования митрального клапана, резекіщи
левого фиброзного треуіюльника, аорто-митральной занавески, крыши левого
предсердия с реконструкцией ксеноперикардом 29.09.2009 г АВ-блокада 111 сте¬
пени. Имплаїітаїщя постоянного ЭКС 16.10.2009 г. Абсцессы головного мозга в
стадии формирования кист Первичный иммунодефицит: дефицит миелоперок-
сидазы. Анемия тяжелых состояний. Хронический тонзиллит вне обострения.Даны рекомендации по приему варфарина 5 мг/сут под контролем МНО,
омепразола 40 мг/сут, сорбифер-дурулеса 320/60 мг 4 таб. в сутки и флуконазо-
ла 200 мг/сут в течение 30 дней.После выписки из стационара пациентка продолжила наблюдаться в кли¬
нике кардиологии амбулаторно. По данным обследования от 15.01.2010 г
у нее отмечена нормализация показателей крови (НЬ 129,5 г/л, эритроциты
3,96 млн), восстановление АВ-проводимости (точка Венкебаха 180 импульсов
в минуту), данные ЭхоКГ не отличались от таковых при выписке.Инфекционный эндокардит (ИЭ) — инфекционно-воспалительное заболе¬
вание клапанов сердца и эндокарда различной этиологии. В качестве инфек¬
ционных агентов чаще других выступакл бактерии, из числа последних —
представители рода Staphylococcus, В последние годы во всем мире отмечается
рост заболеваемости сепсисом и инфекционным эндокардитом, причин тому
несколько. Среди социальных факторов следует шметить продолжающийся
Глава 15. Тяжелый инфекционный эндокардит крайне редкой этиологии... 297рост инъекционной наркомании. Широкое применение методов интервенци¬
онной кардиологии, увеличение числа больных с протезированными клапа¬
нами сердца также внесли свой вк.іал в рост заболеваемости инфекционным
эндокардитом. Таким образом, несмотря на достижения фармакологов в сфере
разработки новых лекарственных средств и рационализации схем применения
старых антимикробных препаратов, эпидемиологические перспективы инфек¬
ционного эндокардита остаются мало обнадеживаюшими. Кроме того, следует
отметить, что, по мнению экологов и микробиологов, в свете глобального
потепления ожидается значительный рост инфекционной патологии, обуслов¬
ленной ірибковьіми возбудителями.По характеру течения выделяют острый инфекционный эндокардит (раз¬
вивающийся в сроки до 2 мес), подосгрый (более 2 мес) и затяжной (более
6 мес). Подострый инфекционный эндокардит— особая форма сепсиса,
обусловленная наличием внутрисердечного инфекционною очага, который
вызывает рецидивирующую септицемию, эмболии, нарастающие изменения
в иммунной системе, приводящие к развитию нефрита, васкулита, синовита,
полисерозита. Этот вариант заболевания возникает при маловирулентном воз¬
будителе (например, грибы) или при недостаточно эффективной антибактери¬
альной терапии.Первое клиническое описание инфекционного эндокардита принадлежит
У. Ослсру и относится к 1885 г. Из отечественных ученых, занимавшихся пробле¬
мой под острого и затяжного инфекционного эндокардита, следует особо отме¬
тить Б.А. Черногубова, который первым доказал, что «затяжной септический
эндокардит — не проблема ревматизма, а проблема сепсиса». Огромный вклад
в изучение морфологии подострого и затяжного инфекционного эндокардита
внес И.В, Давыдовский, который своими работами доказал, что sepsis lenta есть
ничто иное, как септический вариант течения инфекционного эндокардита с
очагом инфекции в сердце. С началом эры антибиотиков появшшсъ надежды
на снижение смертности от этого тяжелейшего инфекционного заболевания.
Однако довольно быстро перед врачами и микробиологами всего мира возникла
проблема антибиотикорезистентности инфекционных агентов. Стало очевидно,
что для успешного лечения инфекционного эндокардита необходим комплекс¬
ный подход с применением как терапевтических, так и хирурі'ических методов.
Совершенствование медицинских технологий создало базу для формирования
такой дисциплины, как гнойно-септическая кардиохирургия, большой вклад в
развитие которой внес наш соотечественник Ю.Л. Шевченко.Однако совместных усилий хирургов и терапевтов оказалось недостаточно,
и смертность от инфекционного эндокардита по-прежнему остается на высо¬
ком уровне, особенно при наличии сердечной недостаточности, По данным
зарубежной литературы, смертность в таких случаях при консервативном
лечении составляет 55-85%, при сочетании терапевтическою и хирургиче¬
ского лечения колеблется в пределах 10-35%. Хуже протекает инфекциогшый
эндокардит, вызванный грибами. Отмечается значительное увеличение эмбо¬
лических осложнений, склонность к абсцедированию, а низкая эффективность
фунгицидных препаратов по отношению к грибам, находящимся в вегетациях.
295 Кардиологияпривела к тому, что грибковая этиология инфекционного эндокардита счита¬
ется одним из показаний к хирургическому вмешательству. Смертность при
грибковом инфекционном эндокардите превышает таковую при инфекцион¬
ном эндокардите другой этиологии и составляет от 40 до 82%. Высокий уровень
смертности при грибковом поражении сердца обусловлен не только частыми
и ранними осложнениями, но и трудностью своевременной диагностики.
Согласно рекомендациям европейских кардиохирургов, в случае грибкового
инфекционного э1Щ0кардита желательно как можно более раннее хирургиче¬
ское лечение с санацией внутрисердечных очагов инфекции.Лабораторная и инструментальная диагностика инфекционного эндо¬
кардита во многом ограничена возможностями используемых методов.
Изменения крови при инфекционном эндокардите не являются специфич¬
ными и позволяют заподозрить септическое состояние у больного: харак¬
терно появление сдвига лейкоцитарной формулы влево при нормальном
или пониженном числе лейкоцитов, анемии, тромбоцитопении, повышение
уровня СРБ. Выявление положительной гемокультуры значительно упрощает
диагностику и выбор медикаментозной терапии инфекционного эадокарди-
та. По данным разных авторов, полу^шть положіггельньїе результаты посева
крови при соблюдении правил забора материала удается в 85-98% случаев до
назначения антибиотиков и лишь в 30—40% случаев с предшествующей анти-
биотикотсрапией. Вместе с тем необходимо помнить, что, по разным оценкам,
около 50% случаев положительной гемокультуры являются ложноположитсль-
ными. принимая во внимание тот факт, что бактериальный инфекционный
эндокардит представляет собой особый вариант течения бактериального сеп¬
сиса, представляется закономерным изменение уровня маркеров системного
воспа^іешія, например прокальцитонина. В своих работах Mueller и соавт.
показаній, что уровень прокальцитонина крови действительно повышается
при бактериальном инфекционном эндокардите и анализ на прокальцитонин
может использоваться в качестве дополнительного теста при подозрении на
наличие инфекционного эндокардита у пациента. Однако отрицательный
тест на прокальцитонин не исключает диагноза инфекционного эндокардита
и позволяет предположить грибковую этиологию. По данным литературы, отО до 50% посевов крови позволяют получить рост возбудителя при грибковом
инфекционном эндокардите.Лейкоцитарный индекс интоксикации (ЛИИ) =(5 X промиелоцит + 4 X миелоцит + 3 х метамиелоцит + 2 х палочкоядерные
нейтрофилы + сегментоядерныс) + (плазматические клетки + 1) (лимфоциты + моноциты) X (эозинофилы + 1)По нашему мнению, в такой ситуации полезным может оказаться лейко¬
цитарный индекс интоксикации, рассчитываемый по модифицированной
формуле, предложенной Я.Я. Кальф—Калифом в 1941 п Нормальным считается
ЛИИ, равный 1,6+0,5. Значительное повышение этого индекса свидетельствуето наличии возбудителя в крови (как бактериальной, так и грибковой природы).
Глава 15. Тяжелый инфекционный эндокардит крайне редкой этиологии... 299Проблема диагностики инфекционного эндокардита в целом значительно
упростилась с широким распространением эхокардиографического исследо¬
вания в практической медицине. По нашему мнению, чреспищеводная ЭхоКГ
должна быть в числе первых исследований (в идеале в течение первых суток от
момента поступления в стационар) у пациентов с лихорадкой неясного генеза.
Данные, полученные при трансторакальной ЭхоКГ, не дают возможности досто¬
верно исключить инфекционное поражение сердца. При ультразвуковой диа¬
гностике инфекционного эндокардита следует учитывать следующие данные:• при использовании трансторакальной ЭхоКГ вегетации на клапанах
сердца обнаруживаются в 60% случаев при инфекционном эндокардите
неизмененных клапанов и в 20% — при инфекционном эндокардите изме¬
ненных клапанов;• при использовании чреспишеводной ЭхоКГ обнаружить вегетации на
неизмененных клапанах удается в 90—100% случаев, на измененных —
более 90%;• внутрисердечные абсцессы, характерные в большей степени для грибково¬
го инфекционного эндокардита, выявляются при чреспишеводной ЭхоКГ в
95% случаев в сравнении с 28% при применентт трансторакальной ЭхоКГ;• при использовании чреспишеводной ЭхоКГ более чем в 90% случаев
удается визуализировать вегетации на электродах или трикуспвдальном
клапане в случае кардиостимулятор-ассоциированного инфекционного
эндокардита, при использовании трансторакальной ЭхоКГ визуализиру¬
ется около 50% вегетаций.Следует учесть, что данные ЭхоКГ не являются достаточными для поста¬
новки диагноза инфекционного эндокардита, они дополняют клиническую
картину и позволяют судить о риске системных эмболий. Выделяют 6 эхокар¬
диографических критериев риска системной эмболии: клапанные вегетации
более 10 мм в диаметре, множественный характер вегетаций, подвижные
фиксированные на ножке вегетации, отсутствие кальцинирования вегетаций,
увеличение размеров вегетаций при исследовании в динамике и пролабирова-
ние вегетаций. Отсутствие характерных эхокардиографических признаков не
исключает диагноз инфекционного эндокардита.Для своевременной и четко структурированной диагностики инфекционно¬
го эндокардита удобно пользоваться критериями Duke. В 1994 г. Durack и соавт.
разделили диагностические критерии инфекционного эндокардита на морфоло¬
гические и клинические, среди последних в свою очередь выделены основные и
дополнительные {та&ь 15.3). Наличие инфекционного эндокардита подтверж¬
дается выявлением 2 основных критериев, или 1 основного и 3 дополнительных,
И.ТИ 5 дополнительных критериев. Отсутствие инфекционного эндокардита можно
констатировать при наличии другого объяснения клинической симптоматики, ее
разрешении на фоне короткой (4 дня) антабиотикотерапші, отсутствии морфоло¬
гических доказательств инфекшюнного эндокардита во время операции ілш. аутоп¬
сии, после кратковременной (менее 4 дней) терапии антибиотиками. Вероятным
диагноз инфекционного эндокардита следует считать при выявлении признаков,
не соответствующих ни наличию, ни отсутствию инфекционного эндокардита.
300КардиологияТаблица 15.3Критерии инфекционного эндокардита DukeОсновные критерииДополнительные критерииПоложительная гемокультура, характерная для
инфекционного эндокардитаА. Типичный для инфекционного эндокардита
микроорганизм, выделенный из дв^-х флаконов:— Streptococcus viridans, Streptococcus
bovis, ffaemophillus spp., Actinobacillus
actinomycetemcomitans, Cardiobacterium hominis,
Eikenella spp., KingeUa kingae;— внеболъничный штамм Staphylococcus aureus
или энтерококка в отсутствие определенного
гнойного очага.Б. Повторный высев культуры, способной вызы¬
вать иттфекционный эндокардит:— п образце крови, взятой с интервалом более
) 2 ч после предыдуще1'о;— во всех трех или в большинстве из четырех
или болсс образцов крови, взятой на посев после
болсс чем часового промежутка.Доказательства вовлечения эндокардаА. Наличие харакгерных эхокардиографичсских
признаков:— вегетации на клапанах или других структурах,
или по ходу потоков регургитации крови, или на
имплантированных материалах в отсутствие дру¬
гих анатомических отклонений;— абсцессы;— измененные искусстпенные клапаны.Б. Появление новых признаков регургитации
крови через клапаны (увеличение или изменение
прелшествутощих шумов не учитывается)Пред шествую ш,ие заболевания
сердца или внутривенное введе¬
ние наркотиков.Лихорадка выше 38 “С.
Сосудистые проявления — круп-
ттые артериальные эмболы,
септические инфаркты легких,
микотическая аневризма, внутри¬
черепные кровоизлияния, гемор¬
рагии в конъюнктиву.Иммунные нарушения — гломе¬
рулонефрит, узелки Ослера, пятна
Рота, положительная проба на
ревматоидный фактор.
Микробиологическое под¬
тверждение — положительный
результат посева крови с вьще-
лением флоры, не соответствую¬
щей основным критериям, или
серологическое подтверждение
активной инфекции в отсутствие
микроорганизма, обычно вызы-
ваюшего инфекционный эндо¬
кардит.Эхокардиографические при¬
знаки, сходные с таковыми при
инфекционном эндокардите, но
не соответствующие основным
критериямВедущее место в лечении инфекционного эндокардита занимает этио-
тропная терапия. В отличие от острого инфекционного эндокардита, изме¬
нения клапанного аппарата при подостром инфекционном эндокардите уже
существенны, и ожидать стремительного ухудшения их функции не следует.
Это позволяет уделить несколько больше времени выявлению возбудителя,
что в свою очередь дает возможность начать этиотропную антибиотикотера-
иию с учетом результатов антибиотикограммы. Однако в случае неудачи при
использовании микробиологических методов, высоком риске септических
осложнений следует начать лечение с антибиотиков широкого спектра. Выбор
конкретного препарата во многом определяется анамнестическими данными в
сопоставлении с результатами крупных эпидемиологических исследований по
инфекционному эндокардиту. Так, в случае нозокомиального или катетерного
инфекционного эндокардита логично предполагать наличие полирезистент-
ного возбудителя, характерного для данного лечебного учреждения. Следует
Глава 15. Тяжелый инфекционный эндокардит крайне редкой этиологии.., 301также учесть, что в литературе уже давно описана способность S, aureus свя¬
зываться с доменами фибронектина и фибрина — основных компонентов
фибринового тромба, неизбежно образующегося на катетере в просвете сосуда.
Это во многом определяет приоритет S. aureus среди этиологических факторов
нозокомиального сепсиса и инфекционного эндокардита. Проблема лечения
стафилококкового инфекционного эндокардита осложняется выраженной
гетерогенностью гр\ттпы золотистого стафилококка. Уже давно клиницистам
всего мира известны штаммы, резистентные к метициллину, — данную пробле¬
му многие годы с переменным успехом решал ванкомицин. Однако в послед¬
нее время все чаще упоминаются такие подгруппы золотистого стафилококка,
как VRSA и VTSA — стафилококки резистентные или с «промежуточной» чув¬
ствительностью к ванкомицину (МПК более 16 мкг/мл и 4—8 мкг/мл соответ¬
ственно). Большие надежды связываются с применением линезолида и нового
препарата даптомипина.Эффективное лечение грибкового инфекционного эндокардита исклю¬
чительно .медикаментозно едва ли возможью. Как уже упоминалось выше,
грибковое поражение сердца является одним из показаний к как можно
более раннему хирургическому вмешательству. Генерализованные грибковые
инфекции всегда возникают на фоне иммуносупрессивного состояния, поэто-
\fy необходимо тщательно исследовать иммунологический статус больного
и использовать все возможности по укреплению иммунитета. Следует также
стремиться к как можно более раннему^ удалению внутривенных катетеров,
при необходимости продления внутривенных введений лекарственных средств
избегать развития флебитов посредством частой смены места постановки
катетера. Противомикробная терапия всегда носит пролонгированный харак¬
тер. Рекомендации по дозированию противогрибковых средств при лечении
инфекционного эндокардита приведены в табл. 15.4. Следует помнить, что
многие противогрибковые препараты плохо переносятся больными, а про¬
лонгированное назначение этих препаратов в достаточно высоких дозах часто
сопровождается развитием побочных эффектов, что требует постоянного вра¬
чебного и лабораторного контроля.В случае, описанном нами, клиническая картина начала разворачиваться с
лихорадки гектического типа и дово.тьно ранних эмболических осложнений,
принятых вначале за опухолевый процесс в головном мозге, что в совокуп¬
ности с низкой эффективностью проводимой антибиотикотерапии позволило
заподозрить, а позднее и выделить атипичного возбудителя.Prototheca wickerhamii {рис. 15.16) является ахлорофильной водорослью
и по своей биологии более всего близка к грибам. Она относится к домену
Eukaryota, царству Viridiplantae, отряду Chlorophyta, классу Trebouxiophyceae,
порядку Chlorellales, семейству Chlorellaceae, роду Prototheca, который включа¬
ет 5 видов. Р. wickerhamii представляет собой шаровидную клетку размерами
8-16 мкм; по типу питания является гетеротрофом; размножается путем фор¬
мирования эндоспор (в количестве от 2 до 20); клеточный цикл длится 5—6 ч.Прототекоз является антропозоонозной инфекцией; кроме человека, боле¬
ют собаки, кошки и скот Первый случай прототекоза человека описал Davies
300КардиологияТаблица 15.3Критерии инфекционного эндокардита Duke(ЗсновшёПоложительная гемокультура, характерная для
инфекционного эндокардитаА. Типичный для инфекционного эндокардита
микроорганизм, выделенный из двух флаконов:— Streptococcus viridans. Streptococcus
bovis, Haemophillus spp., Aciinohacillus
actinomycetemcomitans, Cardiobacterium hominis,
EikeneUa spp., Kingella kingae;— внебольничный пггамм Staphylococcus aureus
или энтерококха в отсутстпис определенного
гнойного очага.Б. Повторный высеп культуры, способной вызы¬
вать инфекционный эндокардит;— в образце крови, взятой с интервалом более
12 ч после предьідуїцего;— во всех трех или в большинстве из четырех
или более образцов крови, взятой на посев после
более чем часового промежутка.Доказательства вовлечения эндокардаА. Натичие характерных эхокардиографических
признаков:— вегетации на клапанах или других сіруктурах,
или по ходу потоков регу'ргитации крови, или на
имплантированных материа.іах в отсутствие дру¬
гих анатомических отклонений;— абсцессы;— измененные искусственные клапаны.Б. Появление новых признаков регургитации
крови через клапаны (увеличение или изменение
предшествующих шумов не учитывается) предшествующие заболевания
сердца или внутривенное введе¬
ние наркотиков-
Лихорадка выше 38 ’С.Сосудис тые проявления - - кр-^ті-ные артериальные эмболы,
сеіггические инфаркты легких,
микотическая аневризма, внутри¬
черепные кровоизлияния, гемор¬
рагии в конъюнктиву
Иммунные нарушения — гломе¬
рулонефрит, узелки Ослера, пятна
Рота, положительная проба на
ревматоидный фактор,
Микробиологическое под¬
тверждение — положительный
результат посева крови с вьще-
лением флоры, не соответствую¬
щей основным критериям, или
серологическое подтверждение
активной инфекции в отсутствие
микроорганизма, обычно вызы¬
вающего инфекционный этшо-
кардитЭхокардиографические при¬
знаки, сходные с таковыми при
инфекционном эндокардите, но
не cooraeTCTByromiHc основным
критериямВедущее место в лечении инфекционного эндокардита занимает этио-
тропная терапия. В отличие от острого инфекционного эндокардита, изме-
1ІЄНИЯ клапанного аппарата при подостром инфекционном эндокардите уже
существенны, и ожидать стремительного ухудшения их функции не следует
Это позволяет уделить несколько больше времени выявлению возбудителя,
что в свою очередь дает возможность начать этиотропную антибиотикотера-пию с уч^етол* г^с^улътатов атибу1отнкогря\тл1ы. (J^najca в случае неудачи приШШІІІЙ8ШШІІ методов, высоком риске септическихосложнений следует начать лечение с антибиотиков широкого спектра. Выбор
конкретного препарата во многом определяется анамнесгическями данными в
сопоставлении с результатами крупных эпидемиологических исследований по
инфекционному эндокардиту. Так, в случае нозокомиального или катетерного
инфекционного эндокардита логично предполагать наличие полирезистент-
ного возбудителя, характерного для данного лечебного учреждения. Следует
302КардиологияТаблица 15.4Противогрибковые средства, применяемые для лечения грибкового инфекционногоэндокардитаПрепаратДозировкаПобочные эффектыАмфотерицин ВРастворимый; 0,5-1 мг/кг/сут,
липосомальный: 3-5 мг/кг/сутОстрая почечная недостаточность,
острая печеночная недостаточ¬
ность, гипотензия, флебит, тошно¬
та, рвота, лихорадга Флуконазол600-800 мг/сут вн>трь или в/в
(при КК 21—50 мл/мин >ти;ень-
шение дозы на 50%, при КК
<20-на 75%)Лекарственный гепатит, холестаз,
острая печеночная недостаточ¬
ностьКаспофунгин70 мг/сут в/в однократно,
далее 50 мг/с\тМожет способствовать прогрес¬
сированию почечной недостаточ¬
ности; гепатит, угнетение кровет¬
воренияВориконазолНагрузочная доза: 6 мг/кг
в 2 приема в/в за 2 ч, поддер¬
живающая доза 4 мг/кг/сутГепатит, зрительные нарушения,
лихорадка, сыпь, рвота, диарея,
периферические отеки, боль в
животе, синдром Стивенса-
ДжонсонаПозаконазол200 мг/сутТошнота, рвота, тромбоцитопения,
диарея, сыпь, удлинение интервала
QT, повышение трансаминаз в 1964 г. Различают кожную и генерализованную формы, а также бурсит лок¬
тевого сустава. В литературе описано 117 случаев прототекоза человека, из
них всего 22 представлены генерализованной формой, которая развивается у
лиц с иммунодефицитным состоянием (дефектами клеточного иммунитета,
дефектами фагоцитоза). При этом лишь у 2 из 13 пациентов с онкологически¬
ми заболеваниями и прототекозом
отмечена лейкопения (по Torres и
соавт.). Характерно развитие забо¬
левания в возрасте старше 30 лет,
хотя описаны случаи заболевания у
новорожденных. Среди животных
заболевают преимущественно особи
женского пола. Предположительный
патогенез прототекоза представлен
на рис. 15.17.При генера-вдзованном прототе-
козе описано поражение глаз, почек,
печени, сердца (и, в частности, мио¬
карда), толстого ю-гшечника, щито¬
видной железы, поджелудочнойРис. 15.16. Pmtotheca wickerhamii при микро- железы, головного мозга, брюши-
скопическом исследовании ^ диафрагмы. В пораженных
Глава 15. Тяжелый инфекционный эндокардит крайне редкой этиологии... 303Вода, содержащая
Prototheca spp.ЖКТ (М-клетки?)НезавершенныйфагоцитозАлагемияПоражение органов
и тканейіФормирование
гранулем (ГЗТ)Рис. 15.17. Предполо¬
жительный патогенез
прототекозатканях выявляется гранулематозное воспаление с преоб¬
ладанием лимфомакрофагальной инфильтрации с приме¬
сью полиморфно-ялерных лейкоцитов. Специфической
KjiHHM4ecK0»T картины не существует, она складывается
из признаков поражения вовлеченных в процесс органов.В диагностике имеют решающее значение данные эпиде¬
миологического анамнеза (водоросли содержатся в водо¬
емах с большим содержанием оргашіческих веществ),
микробиологическое исследование и морфологическое
исследование пораженных тканей.Наличие в структуре клеточной стенки представите¬
лей рода Prototheca эргостерола позволяет применять с
различной степенью эффективности фунгицидные пре¬
параты класса азолов и амфотерицин В. Из критериев
Duke у нашей пациентки имелся 1 основной критерий
(доказательства вовлечения эндокарда) и 2 дополни¬
тельных (лихорадка выше 38 “С, крупные артериальные
эмбольт с формированием отдаленных септических оча¬
гов), позднее была получена положительная гемокулыу-
ра Prototheca wickerhamii, что является 3-м дополнительным критерием. Вместе
с тем диагноз подострого эндокардита был поставлен, несмотря на неполное
соответствие критериям Duke; была выбрана агрессивная тактика ведения
больной.Главными показаниями к раннему хирургическому лечению (от момента
поступления пациентки в клинику до выполнения вмешательства прошло
15 дней — время, необходимое на подготовку к операции) явились сердечная
недостаточность и риск повторных эмболических осложнений. Вероятно,
выделить возбудителя из крови в послеоперационном периоде стало возмож¬
ным благодаря иск>^сствеиному кровообрашению. Дело в том, что одним из
возможных механизмов внедрения в организм человека Р. wickerhamii является
эндоцитобиоз, т.е. способность сохраняться живым внутри фагоцитов. При
искусственном кровообращении повреждение мембран клеток неизбежно, а
объемная и травматичная операция приводит к вторичному иммупосупрес-
сивному состоянию, что создает предпосылки к повторной алгасмии и полу¬
чению положительного посева крови. Полученные позднее данные гисто¬
логического исследования к.'іапанного аппарата и фиброзного тела сердца
также свидетельствовали в пользу первичного поражения сердца указанным
возбудителем.Общей чертой прототекозов (инфекциошіьіх заболеваний млекопитаю¬
щих, вызванных водорослями рода Prototheca) и грибковых эндокардитов
является морфологическая картина гранулематозного воспаления, условием
развития которого яатяется незавершенный фагоцитоз. В то же время, по
да^шым литературы, в условиях функциональной полноценности фагоцитов
(полиморфно-ядерных лейкоцитов) аннигиляция р. wickerhamii осуществля¬
ется в течение 60 мин, Указания на то, что данный микроорганизм способен
304 Кардиологияк паразитированию у млекопитающих только на фоне иміуіунодефицитного
или иммуносупрессивного состояния, привели к необходимости детализации
анамнеза с целью выявления признаков недостаточіюсти иммунитета. В связи
с отсутствием клинических признаков иммунодефицита и обязательного
наличия данного состояния для развития прототекоза бьыо выдвинуто пред¬
положение о наличии первичного скрытого иммунодефицита — дефицита
миелопероксидазы.Миелопероксидаза — один из внутриклеточных ферментов лейкоцитов,
ответственный за синтез гипохлорита, обладающего выраженной бактери¬
цидной и фунгицидной активностью. Частота дефицита миелопероксидазы
в популяции составляет 1:2000. Лица с дефицитом миелопероксидазы более
подвержены грибковым инфекциям; в то же время вирусные и бактериальные
заболевания развиваются у них не чаще, чем у лиц с полноценным иммуни¬
тетом. Диагноз дефицита миелопероксидазы ставится на основании каче¬
ственного и количественного анаїиза. В лаборатории їтммунодиагностики
и иммунокоррекции Федерального научного центра трансплантологии под
руководством профессора B.C. Сусковой было выполнено исследование имму-
HOjmrH4ecKoro статуса пациентки (см. табл. 15.2), по результатам которого
был установлен количественный дефицит миелопероксидазы и значительное
повышение лейкоцитарного индекса интоксикации, свидетельствовавшее о
наличии септического состояния. Позднее был выполнен качественный ана¬
лиз на миелопероксидазу, выявивший полное отс>тствие гранул, содержащих
миелоисроксидазу, в полиморфно-ядерных лейкоцитах. Дефицит миелоперок¬
сидазы, по сути, является молекулярной основой феномена незавершенного
фагоцитоза.С учетом данных микробиологического исследования, а также выявленного
фонового имліунодефицита бьшо принято решение о проведении пролонгиро-
вашшго курса противогрибковых препаратов. Длительность курса должна была
перекрывать время жизни фагоцитов и тем самым обеспечить полную санацию
организма, включая внутриклеточное пространство фагов. Амфотерицин В
является препаратом первой линии лечения прототекоза, и с него следует
начинать лечение данного заболевания, невзирая на результаты антибио-
тикофаммы, так как на сегодняшний день не существует рекомендаций по
проведению тестов на чувствительность к противомикробным препаратам
водорослей рода Proiotheca. К сожалению, на фоне терапии амфотерицином В у
пациентки развилась острая почечная недостаточность, что вынудило сменить
препарат. Из числа азолов наиболее выраженной супрессивной активностью
по отношению к Р. wickerhamii обладает вориконазол. Кро.ме того, д.ія ворико-
назола характерна высокая эффективность при лечении грибковой инфекиш!
це^ітральной нервной системы, что бьио значимо в нашем случае, учитывая
наличие осложнения — абсцедирующего менингоэнцефалита, вероятно, той
же этиологии.На сегодняшний день можно говорить об эффективности проведенного
больной комбинированного лечения и надеяться на отсутствие рецидивов
заболевания в будущем.
Глава 15. Тяжелый инфекционный эндокардит крайне редкой этиологии... 305Комментарий Н.А. Новиковой — профессора кафедры профилактической и
неотложной кардиологии Первого МГМУ им. И.М. Сеченова, д-ра мед. наукПредставленный сл^^ай, безусловно, является уникальным. Очевидно, что
с пояа^енисм нового типа возбудителя эндокардита (водоросли) тершін
«инфекшюнный эндокархшт» наиболее точно отражает суть заболевания.
Прежде всего необходимо отметить, что успех лечения был достигнет во
многом благодаря коллегиальному подходу к лечению. Нет никаких сомне¬
ний, что инфекционный эндокардит в равной степени является проблемой
как хир\ргов, так и терапевтов. Но данный клинический случай показал, что
решение неординарных задач требует более широкого подхода и привлече¬
ния спепиалистов из других областей медицины. Хочется особо отметить
вклад врача-иммунолога Федерального научного центра трансплантологии и
искусственных органов имени академика В. И. Шумакова Л.П. Ермаковой и
заведующего кафедрой клинической микологии Санкт-Петербургской меди¬
цинской академии постдипломного образования профессора Н.Н. Клиліко.
Вторым немаловажным фактором успешного лечения яшіяется этиопато-
генетический подход. Изучение и понимание этиологии и патогенеза не
только инфекционіюго эндокардита в целом, но и в случае конкретного
больного позволяет определить оптимальную медикаментозную тактик>' и
прогноз. На сегодняшний день нег четких рекомендаций по лечению про-
тотекоза. Однако всеми авторами работ по данной патологии отмечено, что
наличие іш\іунодефииита в сл>'чае генерализованного процесса говорит о
плохом прогнозе и требует длительного лечения фунгицидными препара¬
тами.Представляется, что не последнюю роль в обострении процесса и получе¬
нии положительных гемокультур в послеоперационном периоде сыграло
искусственное кровообраш,сние. При всех положительных моментах искус¬
ственного кровообращения данная процедура всегда сопряжена с механиче¬
ским повреждением мембран клеток крови. Вероятным патогенетическим
механизмом «ускользания» от иммунитета и терапии в данном случае бьиі
феномен незавершенного фагоцитоза. На основании этого можно пред¬
положить, что после искусственного кровообращения возбудитель вновь
іюпал в кровь из поврежденных клеток и вызвал обосгрение заболевания.
Подобный «вклад» искусственного кровообращения в развитие инфекци¬
онного процесса на сегодняшний день недооценен и, вероятно, требует от
терапевтов и хирургов более агрессивной антимикробной терапии в самом
раннем послеоперационном периоде с применением не только антибиоти¬
ков, но и противогрибковых препаратов в лечебных дозах.Комментарий А.В. Вахляева — врача отделения интенсивной терапии и реанима¬
ции Клиники кардиологии Первого МГМУ им. И.М. СеченоваВозвращаясь к вопросу о прогнозе для данной пациентки, следует заметить,
что он скорее неопределенный. Выявленный иммунодефицит (дефицит мие-
лопероксидазы) является основой феномена незавершенного фагоцитоза.
306 КардиологияПродолжительность антимикробной терапии также опредсля.'шсь наличием
дефицита миелопероксидазы. Нами было предположено, что имеет местоЭНДОЦИТОбИОЗ — сохранение возбудителя внутри фагоцитирующих KjICTOKв активном состоянии, что обусловило необходимость достижения как вне¬
клеточной, так и внутриклеточной санации организма. Как известно, к
фагоцитам относятся лейкоциты и моноцитарное звено. Если пул первых
полностью обновлясгся в течение месяца, то моноциты, трансформируясь в
тканевые макрофаги, молуг существовать многие месяцы. Этот факт, а также
отсугстБие методов коррекции данного нарушения имліунитета позволяют
говорить о высоком риске рецидива заболевания у пациентки В. Безусловно,
данная больная требует дальнейшего пристального наблюдения со стороны
кардиологов с повторными инструментальными исследованиями (ЭхоКГ,
ЭКГ), а также инфекционного контроля, включаюш;сго рсгу.іярную термо¬
метрию и аншгизы крови на воспалительные маркеры.ЛИТЕРАТУРАBrusch J.L. FACR Infective Endocarditis // Medscape. Updated; Aug 23, 2009.Chalta S., Prayaga A.K., Vemu L. et al. Fungal Endocarditis: An Autopsy Study //
Asian Cardiovasc. Thorac. Aim. 2004;12:95-98.Delahaye F., Celard М., Roth O., G. de Gevigney. Indications and optimal timing for
surgery in infective endocarditis // Heart. 2004; 90(6): 618—620.Durack D.T., Lukes A.S,, Bright D.K. New criteria for diagnosis of infcclive
endocarditis; utilization of specific echocardiographic findings: Duke Endocarditis
Service //Am. J. Med. 1994; 96: 200-209.Falagas M.E., Mania K.G., Vardakas F.N. , Vardakas K.Z. Linezolid for the treat¬
ment of patients with endocarditis: a systematic review of the pubhshed evidence //
Journal of Antimicrobial Chemotherapy. 2006; 58(2): 273-280.Fowler V.G.Jr, Boucher H. W., Corey G.R. etal Daptomycin versus standard therapy
for bacteremia and endocarditis caused by Staphylococcus aureus // N. Engl. J. Med.,
2006; 355:653-665.Herrmann М., Lai Q.J., Albrecht R.M. et al. Adhesion of Staphylococcus aureus
to surface-bound platelets; role of fibrinogen/fibrin and platelet integrins // J. Infect.
Dis. 1993; 167(2):312-322.Lass-FlorlC., MayrA, Human Protothecosis// Clinical microbiology reviews, Apr.
2007; X 20(2);230-242.Linares М., Solis F. and Casal Л/. In vitro activity of voriconazole against Prototheca
wickerhamii: comparative evaluation of Sensititre and NCCLS M27-A2 methods of
detection // J. Clin. Microbiol. 2005; 43: 2520-2522.Mueller C., Huber P., Laifer G. et al. Procalcitonin and the Early Diagnosis of
Inlective Endocarditis // Circulation. 2004;109:1707-1710.Olaison L., Pettersson G. Current best practices and guidehnes indications for
surgical intervention in infective endocarditis // infect. Dis. Clin. North Am. 2002:
16(2):453-475.
Глава 15, Тяжелый инфекционный эндокардит крайне редкой этиологии... 307Ретап J.E., Canton Е., Caiabuig М. et ai In vitro activity of voriconazolc against
yeast and algae isolates according to new resistance pattern break points // Rev. Esp.
Quimioter. 2006; 19:21-33.FhairJ., ШИатз J., Bassaris H. et ai Phagocytosis and algicidal activity of human
роІутофЬописІеаг neutrophils against Prototheca wiclcerhamii // J. Infect. Dis.
1981; 144:72-77.Pierrotti L.C., Baddour L.M. Fungal Endocarditis, 1995—2000 I j CHEST. July.
2002; 122, 1:302-310.Schwartz S., Ruhnke М., Ribaud P. et ai Improved outcome in central nervous
system aspergillosis, using voriconazole treatment j I Blood. 2005; 106,8:2641—2645.Tolan R.W, Endocarditis, Fungal: Treatment & Medication// Medscape. Updated:
Feb 2, 2009.Toy P.T., Lai L.W., Drake T.A., Sande М.Л. Effect of fibronectin on adherence
of Staphylococcus aureus to fibrin thrombi in vitro // Infect Imraun. 1985; 48(1):
83-86.Vaudawc P., Pittet D., Haeherli A. et al. Fibronectin is more active than fibrin or
fibrinogen in promoting Staphylococcus aureus adherence to inserted intravascular
catheters//J. Infect. Dis. 1993; 167(3):633-641.
Глава 16БОЛЕЗНЬ ЛАЙМА: УСПЕШНОЕ ЛЕЧЕНИЕ
ТЯЖЕЛОГО ОСТРОГО ПЕРИКАРДИТА НА ОСНОВЕ
ТОЧНОГО ЭТИОЛОГИЧЕСКОГО ДИАГНОЗАД.В. герок, СЛ. Сучкова, АЛ. Нестеров,
М.Ю. Гиляров, НА. Новикова, А.Л СыркинПерикардит (тем более острый) — заболевание, с которым не так часто
сталкиваются даже кардиологи. Как яркая клиническая картина, так и измене¬
ния на ЭКГ при остром перикардите — многократно описанные, но далеко не
всегда узнаваемые на практике — нередко становятся основанием для ошибоч¬
ной диагностики острого коронарного синдрома; еще более непростой задачей
является постановка этиологического диагноза. В представленном клини¬
ческом наблюдении своевременное выявление необычной этиологии пери¬
кардита позволило провести эффективную этиотропную терапию и добиться
разрешения процесса.Эта глава завершает серию клинических наблюдений, в которых рассматрива¬
ются острые неревматические воспалительные заболевания сердца (эндо-, мио- и
перикардит): об их тяжести свидетельствует тот факт, что все три наблюдения
предстаїілеїш отделением интенсивной терапии и реанимации. Поиск этиологии
процесса проводился нарящ^' с ургентными мероприятиями и во всех случаях
оказался эффективным. Именно при остром гсченрш заболевания (недавнем
его нача.ис) мы имеем дело преимущественно с инфекционной фазой процесса,
в которой этиотропное лечение наиболее оправданно и эффективно. В случае
хронизации воспаления, как правило, основное патогенетическое значение при¬
обретают иммунные реакции, выявить зтиологическиіі агент становится суще¬
ственно сложнее, и эффективность этиотропной терапии уже не столь высока.Больной С., 49 лет, госпитализирован в отделение реанимации и интен¬
сивной терапии Клиники кардиологии Московской медицинской академии
им. И.М. Сеченова в июле 2009 г с жалобами на общую слабость, одышку при
привычных физических нагрузках, боли в грудной клетке, усиливающиеся
при движениях и наклонах туловища вперед, учащенное сердцебиение, боли в
горле, головные боли (преимущественно в височных областях).Анамнез {рис. 16.1). В течение длительного времени считал себя здоровым
человеком, не обследовался, не лечился, в последние 2 нед до госпитализации
стал отмечать общее недомогание, слабость, «іюзнабливание», был консульти¬
рован кардиологом, на ЭКГ патологии не выявлено, АД в пределах нормы.01,06.2009 г. развились интенсивные давящие боли в грудной клетке (в покое,
стоя), усиливающиеся при изменении положения тела, наклонах вперед, боли
в горле; также стало беспокоить учащенное сердцебиение. 03.07.09 г. обрати,тся
Глава 16. Болезнь Лайма: успешное лечение тяжелого острого...309укус клещаобщая слабость, «познабливание>Ітелаинтенсивные давящие боли в грудной клеткеЧСС до 100-120 уд/миниюнь 2009 г. ~ 15-17.06.2009 г.Рис. 16.1, Анамнез больного С., 49 лет01.07.2009 г.03.07.2009 г,Г\Гrvr■л/U/M№я?MМї:Рис. 16.2. Злектрокардиоірамма больного С. при постуїшении, скорость записи 25 M\f/cв клинику кардиологии, на ЭКГ зарегистрирован подъем сегмента STло 3 мм в
I, II, III, аУД Vj-Vg отведениях, с подозрением на развитие инфаркта миокарда
госпитализирован в отделение реанимации и интенсивной терапии Клиники
кардиологии Московской медицинской академии им. И.М. Сеченова. Также
из анамнеза известно, что за месяц до госпитализации пациента укусил
клещ (в районе г. Талдом Московской области; вакцинацию не проходил).
Сопутствующие заболевания: сахарный диабет типа LADA (Latent Autoimmune
Diabetes of Adulthood), дебют 8 лет назад, сахароснижающие препараты не при¬
нимает, гликемия натощак до 16 ммоль/л.
310 КардиологияПри постутении состояние средней тяжести. Температура тела 37,2 X.
Кожные покровы обычной окраски и влажности, высыпаний, отеков нет.
Пальпировались увел№1енныс передние шейные лимфоузлы, подмьиыечные
лимфоузлы слева. При аускультации выслушивалось везикулярное дыхание,
хрипов не бьио. Число дыханий 16 в минуту. Тоны сердца ясные, ритмичные,
шумов нет. ЧСС 94 в минуту, АД 125/80 мм ртст Живот мягкий, безболезнен¬
ный, печень не увеличена. В неврологическом статусе; парезов нет, сухожиль¬
ные рефлексы на руках и ногах D=S.На ^А'Гпри поступлении — синусовый ритм с ЧСС 100 уд/мин, элевация
сегмента ST в Т, П, 111, aVP, V^—отведениях максимально до 3 мм, депрессия
PQ во И, Vj-V^ отведениях (рис. 16.2).В общем анализе крови значимой патологии выявлено не было: НЬ 151,1 г/л,
эритроциты 5,0 млн, цветовой показатель 0,91, лейкоциты 6,8 тыс., нейтрофи-
лы 59,41%, лимфоциты 29,09%, моноциты 7,22%, базофилы 0,59%, тромбоци¬
ты 185,3 тыс., СОЭ 6 мм/ч.В биохимическом анализе крови отмечалось небольшое увеличение уровня азота
мочевиііьі до 10,4 ммоль/л, гипергликемия до 11,9 ммать/л. Также регистрирова¬
лось повьшіение уровней КФК до 766 ед/л (МВ-фракция КФК = 32 ед/л), Г-ГТ до
77 ед/л, ACT до 44 ед/л. При этом уровень сердечного тропонина Т был отрицатель¬
ным. Кроме того, при электрофорезе белков было выявлено небольшое снижение
аішбумина до 55% при увеличении al- и а2-фракций глобулина до 4,3 и 14% соот¬
ветственно. В иммунологических исследованпиях HBsAg, НСЛАЬ, антитела к ВИЧ
не обнаружены, комплекс серологических реакций на сифилис отрицательный.
Отмечатось увел№іение уровня фибриногена до 4,66 г/л, СРБ до 1,2 мг/дд, пофа-
>1ичные значения антистрсптолизина-0 (108 МЕ/мл) и РФ (20 МЕ/мл).В общем анализе мочи определялись следы белка, глюкоза, при этом суточ¬
ная глюкозурия составила 0,7 г%.При рентгенологическом исследовании органов грудной клетки патологиче¬
ских изменений выявлено не было.При суточном мониторировании ЭКГ по Холтеру значимых нарушений ритма
и проводимости не зарегистрировано.При ЭхоКГ диагностировано нарушение диастолы 1 -го типа, также опреде¬
лялась сепарация листков перикарда до 0,5-0,7 см за стенкой правого желу¬
дочка {рис. 16.3).Поскольку в анамнезе больного было указание на укус клепіа, мы провели
исследование антител кburgdorferi, уровень TgM составил 63,1 ед/л (более
22 ед/л — положительньш результат), TgG — менее 5 ед/мл (отрицательный).Таким образом, на основании клинической картины, данных ЭКГ (конкор-
дантный подъем сегмента ST, депрессия сегмента FQ), ЭхоКГ (выпот в полости
перикарда) установлен диагноз острого экссудативного перикардита. Учитывая
связь ухудшения состояния с укусом клеша, наличие лихорадки и лимфоадено-
патии, а также повышение титров антител кВоггеІіа burgdorferi, диагностирован
Лайм-боррелиоз с поражением сердечно-сосудистой системы.В качестве этиотропной терапии назначен цефтриаксон 2 г/сут с пере¬
ходом на доксициклин 100 мг по 1 таб. 2 раза в день; проведено лечение
Глава 16. Болезнь Лайма: успешное лечение тяжелого острого... 311Рис, 16.3. ЭхоКГ больного С. при исступлении (стрелкой указан пыпот в полости пери¬
карда)нестероидными противовоспалительными препаратами (диклофенак 150 мг/сут
в/м, затем внутрь), также начат подбор сахароснижающей терапии.В результате проводимой терапии отмечено значительное улучшение состо¬
яния больного: боли в грудной клетке, горле прошли на второй день анти-
биогикотерапии, с этого же времени норма^'іизовалась температура тела,
значительно уменьшилась обишя слабость, перестало беспокоить учащенное
сердцебиение. На ЭКГ при выписке зарегистрировано возвращение сегментов
5Ги PQk изолинии {рис. 16.4). При контрольной ЭхоКГ (07.07.2009 г.) выпо¬
та в полости перикарда нет. Пациент выписан с рекомендациями продолжить
антибактериальную терапию доксициклином в течение 28 дней.Впервые сообщение о болезни Лайма (клещевом боррелиозе, Лайм-
боррелиозе) появилось в 1976 г. в США, штате Коннектикут, где в г. Лайм
были зафиксированы случаи ювенильного артрита, развившегося после укуса
клещей. Болезнь Лайма — инфекционное трансмиссивное заболевание, обла¬
дающее большим полиморфизмом клинических проявлений и вызываемое по
крайней мере тремя видами бактерий рода Borrelia, семейства Spirochaetaceae.
BorreUa burgdofferi доминирует как возбудитель боррелиоза в США, в то время
как Borrelia afzelii и BorreUa garinii — в Европе.В Российской Федераїтии ежегодно регистрируют около 8 тыс. больных бор-
релиозом (рис. 16.5), хотя по предварительным расчетам их количество может
быть существенно больше, в настоящее время заболевание диагностируется
на территориях более чем 70 административных образований. Заболеваемость
Лайм-боррелиозом состав,іяет 6 случаев на 100 тыс. населения в год в США,
в РФ в 2008 г — 5,5 диагностированных случаев на 100 тыс. населения.Боррелии (рис. 16.6, см. цветную вклейку) — грамотрицательные, под¬
вижные бактерии, их относят к облигатным внутриклеточным паразитам.
Они передаются человеку через укус инфицированных иксодовых клещей,
принадлежащих к нескольким видам рода Ixodes {рис. 16.7, см. цветную вклей¬
ку). Инфицирование людей может происходить только при укусе нимфы или
имаго (половозрелой формы клеща). На территории России распространены
/, ricinus, L persulcatus.
312КардиологияX*-rv
її—\r—Л-4ЛaVRI I i ‘-r- AИ-Л/МЛРис. 16.4. ЭКГ бального С. при выписке (скорость записи 25 мм/с)Всего заболевших — 7706 человекДальневосточный _ ^ Южный ФО - 48
ФО - 247Уральский
ФО - 1077Северо-ЗападныйФО-1197Центральный
ФО - 1961Сибирский
ФО - 1549ПриволжскийФО-1627Рис. 16.5. Распределение случаев клешевого боррелиоза (болезнь Лайма) в РФ в 2008 г.Инкубационный период при боррелиозе варьирует от 5 дней до 1 мес (в
среднем 2—3 нед). Заболевание обычно начинается с появления характерного
кожного поражения — мигрирующей эритемы (рис. 16.8, см. цветную вклейку).
В дальнейшем, через дни или недели, боррслии распространяются гематоген¬
но, при этом в процесс могут вовлекаться любые органы и системы, возникают
артриты, кардиты, неврологические проявления (диссеминированная стадия).
Через месяцы или годы развивается персистирующая стадия, включающая
хронические или интермиттирующие артриты, энцефалопатию или полиней¬
ропатию, акродерматит. Клиническая классификация боррелиозов приведена
в табл. 16.1.
Глава 16, Болезнь Лайма: успешное лечение тяжелого острого.313Возможно клинически манифестное и латентное течение заболевания.
Кроме того, выделяют острое, подострое и хроническое течение болезни, а по
признакам инфипированности — серопозитивный и серонегативный вариан¬
ты. При остром и подостром течении развиваются эритематозная и безэрите-
матозная формы боррелиоза. Хроническое течение может быть непрерывным
и рецидивирующим.Обычно симптомы проявляются с мая по сентябрь, так как в это время раз¬
виваются нимфы клещей. Из-за небольшого размера клеща пациенты часто не
могут указать место укуса. Стадия локализованной инфекции обычно начи¬
нается с появления в месте укуса клеща распространяющегося кольцевидного
кожного покраснения — мигрирующей эритемы. Первоначально на коже
возникает небольшое пятно (в большинстве случаев его возникновение не
сопровождается чувством зуда и жжения), которое в течение нескольких дней
увеличивается в размерах за счет центробежного роста, достигая 15—20 см и
более в диаметре. По мере периферїгчгеского роста центральная часть эритемы
может бледнеть, формируя характерную классическую кольцевидную форму,
хотя весьма часто бывает гомогенно окрашенной. Края мигрирующей эритемы
несколько возвышаются над непораженной кожей. Изредка в центре пятна
формируются папулы или везикулы, которые могут трансформироваться в
язвочки. У 20% больных мигрирующая эритема не развивается.В 10—30% случаев у больных может выявляться регионарный лимфаденит.
На фоне развития мигрирующей эритемы общее состояние изменяется незна¬
чительно, могут возникать такие неспецифические проявления, как озноб,
повышение температуры тела, головная боль, артралгии, миалгии, лимфоаде-
нопатия, выраженная слабость и утомляемость. Менее чем в 7% случаев стадия
локализованной инфекции протекает бессимптомно, У 5—8% больных уже
в острый период П0ЯВ.1ЯЮТСЯ признаки поражения мягких оболочек мозга,Таблищ 16.1Клиническая классификация боррелиозовПериодыРашгай период (до 6 мес)Поздний период (свыше 6 мес)СтадииболезниЛокализованная
(от нескольких
дней до 4 нед)Диссеминиропатт-
ная* (1—6 мес)П ерсистирующая
(6 мес—годы)Резидуальная
(«постлайм-
ский синд¬
ром»)ВариантытеченияКожный (мигри¬
рующая эритема)КОЖШ.ІЙ, сустап-
ной, невро¬
логический,
кардиальный,
офтальмологиче¬
ский, смешанныйКожный, сустав¬
ной, неврологи¬
ческий,
кардиааьный,
oфтaльмoJЮги-
ческий, смешан¬
ный-ТяжестьтеченияЛегкое,среднетяжелоеЛегкое,Среднетяжелое,тяжелоеЛегкое,среднетяжелое,тяжелое-* Возможно формирование первично-диссеминированной стадии боррелиоза.
314 Кардиологияпроявляющиеся общемозговой симптоматикой. Как правило, I стадия длится
от 3 до 30 дней.Исходом I стадии может быть выздоровление, вероятность которого значи¬
тельно возрастает при проведении адекватного антибактериального лечения. В
противном слу^те даже при нормализации температуры тела и исчезновении
эритемы болезнь постепенно переходит в диссеминированную, а затем перси-
стируюшуго стадии.При диссеминированной стадии, помимо вторичного поражения кожи,
развивается головная боль, характерны напряжение мышц шеи, лихорадка,
миі'рирующие артриты и миалгии, нарастает слабость. Реже развиваются гене¬
рализованная лимфоаденопатия, сп.існомегсі-'іия, гепатит, ангина, бронхит,
конъюнктивит, ирит, хориоретинит, панофтальмит, микрогематурия и проте-
инурия, орхит.Неврологические симптомы могут проявляться в виде менингита, менин-
гоэнцсфалита с лимфоцитарным плейоцитозом цереброспинальной жидко¬
сти, пареза черепных нервов и периферической радикулопатии. Из черепных
нервов чаще поражается лицевой, причем изолированный паралич какого-либо
краниального нерва может быть единственным проявлением болезни Лайма,Прояштения кардита чаще всего развиваются через 3 нед-5 мес после инфи¬
цирования. Зачастую указания на укус клеща отсутствуют', однако пациенты
могут вспомнить, что были в лесу или в парке. Наиболее часто возникают
нарущения проводимости (87% всех случаев Лайм-кардита) в виде АВ-блокады
различной степени, также описаны случаи блокады правой ножки пучка Гиса.
Зафиксировать преходящую блокаду довольно трудно, но регистрация ЭКГ
желательна у всех пациентов с мигрирующей кольцевидной эритемой, посколь¬
ку полной поперечной блокаде обычно предшествуют менее выраженные
нар\тпения ритма. В некоторых случаях развивающиеся нарушения проводи¬
мости требуют временной электрокардиостимуляции. Сердцебиение — самый
частый симптом поражения сердца, в большинстве случаев оно обусловлено
неустойчивой желудочковой тахикардией. Перикардиты, миокардиты и дила-
тационная кардиомиопатия встречаются реже. Зарегистрированы редкие слу¬
чаи фатального панкардита.Персистирующая стадия развивается у 10% больных через 6 мес-2 года
после острого периода. Наиболее изученными в этом периоде яатяются пора¬
жения суставов (хронический Лайм-артрит), поражение кожи (атрофический
акродерматит), а также хронические неврологические синдромы, напоминаю¬
щие по срокам развития нейросифилис.Часто возникает интермиттирующий олигоартрит с преимущественным
поражением крупных суставов (например, коленных), он может рецидивиро¬
вать в течение нескольких лет и приводить к деструкции костей и хрящей.Поражение нервной системы проявляется хроническим подострым энце¬
фалитом, периферическими нейропатиями, когнитивньп^ш и поведенческими
расстройствами, нарушениями сна, атаксией. В редких случаях первым прояв¬
лением боррелиоза могут быть энцефа^томиелит или лейкоэнцефалит, при этом
остро развиваются спастический паранарез и нарушение тазовых функций.
Глава 16, Болезнь Лайма: успешное лечение тяжелого острого... 315К поздним кожным проявлениям относят хронический атрофический
акродерматит; чаше всего он ассоциирован с В. afzelii и встречается у пожилых
ЖЄНЩРІН. По мере прогрессирования процесса нарастает атрофия кожи и под¬
кожной клетчатки, в результате чего эпидермис истончается и приобретает
вид «папиросной бумаги». На участках пораженной кожи происходит разрас¬
тание соединительной ткани с формированием узелков цвета слоновой кости.
Также встречается доброкачественная лимфоцитома, имеющая вид плотного,
отечного, малинового цвета узелка (инфильтрат) и вызывающая болезненные
ощущения при пальпации.Проявлениями резидуальной стадии боррелиоза или «постлаймского синдро¬
ма» считают артралгии, миажии, когнитивные нарушения, устшюсть, которые
возникают после эффективной антибактериальной терапии и элиминации бак¬
терий из организма. Учитывая неспецифичность симптомов, в рекомендациях
Американского общества инфекционных болезней особое внимание уделено
критериям «постлаймского синдрома». В частности, другая активная нелеченная
инфекция, другае причины указанных симптомов (синдром хронической устало¬
сти, фибромиалгия, предшествующие боррелиозу), положительные иммунологи¬
ческие тесты на боррелиоз и ПЦР, документированные нейроборрелиоз или реф¬
рактерный к лечению артрит позволяют отвергнуть «постлаймский синдром».Во многих случаях диагноз Лайм-боррелиоза устанавливают на основании
клинической картины и эпидемиологического анамнеза {табл. 16.2). В част¬
ности, наличия мигрирующей эритемы и указаний на укус клеша может быть
достаточно для постановки диагноза, тем более что в первые 2 нед болезни
антитела к боррелиям могут отсутствовать.Наиболее специфичными считаются методы, прямо выявляющие воз¬
будитель: культивирование на питательных средах, обнаружение боррелий
с помощью световой или электронной микроскопии, полимеразная цепная
реакция для обнаружения специфической ДНК. Косвенно факт инфициро¬
вания устанавливается по формированию специфического иммунного ответа:Таблица 16.2Диагностика боррелиозаМигрирующая эритема в виде кожного поражения, медленно распространяющегося
в течение дней или недель и представляюшего собой округлый участок гиперемии,
часто с просветлением в центре, диаметром не менее 5 см.По крайней мере, одно из следующих клин№іеских и лабораторных проявлений;• поражение нервной системы; лимфоцитарный менингит, неврит черепных нервов,
радикулонейропатия, реже — энцефаломиелит (с выяштением антител к боррели¬
ям в цереброспина.1ьной жидкости);• поражение сердетао-сосудистой системы: остро возникшая АВ-блокада II или
ITT степени, проходящая в течение недель или месяцев (в некоторых случаях она
может быть ассоциирована с миокардитом);• поражение опорно-двигательного аппарата: короткие повторяющиеся артратгии
(длительностью от нескольких недель до нескольких месяцев), отек одного или
нескольких суставов, иногда приводящие к развитию хронического артрита;• выделение в. Ьиі^йофгі из ткани или культуры клеток или выявление антител
к 5. burgdorferi
316 Кардиологиягуморального (антиборрелиозные антитела) и клеточного (тест специфической
стимуляции лимфоцитов).Согласно рекомендациям Международного общества тто болезни Лайма
и ассоциированным заболеваниям, а также американского Центра контроля
болезней, серологическая диагностика включает 2 этапа: тест ELTSA (enzyme-
linked immunosorbent assay) либо реакцию непрямой иммунофлуоресценции и
вестерн-блоттинг. Серологическое тестирование на болезнь Лайма считается
положительным, если в одной сьгеоротке оба метода дали положительные
результаты.В России ocHOBHbLM лабораторным тестом для массовых серологических иссле¬
дований является реакция непрямой иммунофлуоресценции. Следует помнить,
что этот метод, как и другие серологические тесты, не всегда способен верифици¬
ровать диагноз из-за сложного иммунопатогенеза при боррелііозах. Только лишь
выявление диагностического титра антител не может быть достаточным для поста¬
новки диагноза. Ложноположительные серологические реакции на боррелиоз
могут выявляться при пелом ряде инфекционных и иммунных заболеваний:— сифилисе;— пинта;— лейшманиозе;— беджеле (арабском сифилисе);— лептоспирозе;— ювенильном ревматоидном артрите;— системной красной волчанке;— мононуклеозе;— подостром бактериальном эндокардите.Сходные с мигрирующей эритемой кожные проявления могут наблюдать¬
ся при стрептококковом целлюлите, аллергических реакциях (в том числе на
слюну клеща). Следует учитывать, что с укусом клеша возможно также зараже¬
ние бабезиозом или анагиазмозом. Паралич лицевой мускулатуры, встречаю¬
щийся при диссеминированной стадии боррелиоза, следует дифференцировать
с таковым при герпесе. Дифференциальный диагноз олигоартрита следует
проводить с реактивным артритом (у взрослых) и ювенильным ревматоидным
артритом. Наибольшими трудностями сопровождается дифференциальная
диагностика резидуального боррелиоза и синдрома хронической усталости, а
также фибромиалгии.Этиотропная терапия больным боррелиозом показана независимо от ста¬
дии, варианта и тяжести течения заболевания. Проведение этиотропного
лечения персистирующей стадии болезни целесообразно только в период обо¬
стрения. Курс и длительность антибактериальной терапии зависят от стадии и
варианта заболевания.Основные схемы лечения, согласно рекомендациям Американского обще¬
ства инфекционных болезней, приведены в табл. 16.3.Патогенетическое лечение проводится по показаниям и предусматриваетприме-
нение дезинтоксикационной терапии (5% р-р глюкозы, кристаллоидные и колло¬
идные растворы), нестероидных противовоспалителъньпс препаратов (оиклофенак,
Глава 16. Болезнь Лайма: успешное лечение тяжелого острого..317Таблица 16.3 ПериодРанний периодЛечение Лайм-боррелиозаЛечениеРанний период при
наличии невроло¬
гических прояв¬
лений (менингит,
радикулопатия) или
АВ-блокалы ТТТ сте¬
пениПоздний период:
артрит без неврологи-
ческой симптоматики[Взрослые:доксициклин 100 МҐ X 2 р./сут, |амоксициллин 500 мг х 3 р./сут, 'щефуроксим 500 мг X 2 р./сут в течение 14—21 сут. ^;Дети:^амоксициллин 50 мг/кг/сут (дозу следует разделить на 3 прие-
ма/сут, максимальная доза 500 мг),і доксициклин (для детей старше 8 лет) 1—2 мг/кг/сут (2 прие-
'ма/сут, максимальная доза 100 мг).'цефуроксим 30 мг/кі/сут допустим в качестве альтернативного
^ препарата,в/в введение цефтриаксона ііе рекомендуется (его эффсктив- ;
jHOCTb не превышает эффективности вышеуказанной псро-ральной терапии) JВзрослые:■ цефтриаксон 2 г/сут в/в в течение 14—28 дней;Iпрепаратами выбора могут быть пенициллин или цефотаксим; ^
' при устойчивости к указанным препаратам возможно назна- і
ічение доксицик^іина 200—400 мг/сут внутрь или внутривенно ■
на 14-28 дней.Дети: і’ цефтриаксон или цефотаксим в/в,і препарат выбора — пенициллин : Пероральный прием антибиотиков (см. схему лечения при
раннем периоде) IПоздний период;
сохраняющийся после
перораяьной терапии
рецидивирующий
артритВзрослые;'цефтриаксон 2 г/сут в/в 14-28 дней,
пенициллин или цефотаксим;: при устойчивости к указанным препаратам возможно назначе¬
ние доксицик.11ина 200—400 мг/сут внутрь или в/в 14-28 дней,
і Дети:цефтриаксон или цефотаксим в/в,препарат выбора — пеницшшин Поздний период: со- і Симптоматическая терапия
храняюшийся реци¬
дивирующий артрит
после 2 курсов анти¬
бактериальной тератши ,Поздний период с
поражением цен-
тратьной и.'1и пери¬
ферической нервной
системыРезидуальный борре-
лиозI Взрослые:, цефтриаксон 2 г/сут в/в 14-28 дней,
пеницилтин или цефотаксим;1при устойчивости к указанным препаратам возможтіо назна¬
чение доксипиклина 200-400 мг/с\т втгутрь или в/п в течениеі 14-28 дней.Дети:цефтриаксон или цефотаксим в/в,'препарат выбора — пенициллин і Симптоматическая терапия
318 Кардиологияиндометашш), десенсибилизирующей терапии, витаминных препаратов (фуппы В
и С) и др. Такие ранее обсуждавшиеся методы лечения, как озонотерапия, гиперба-
рическая оксигенация, холестира\шн, в настоящее время не показаны.Специфическая профилактика болезни Лайма в настоящее время не раз¬
работана. Меры неспецифической профилактики аналогичны таковым при
клещевом энцефалите (использование защитной одежды и репеллентов). Если
обнаружен клеш, севший на любой участок кожи, его надо аккуратно удалить.
Нельзя раздавливать клеща, так как возможно заражение через неповрежден¬
ную кожу. Клещи часто прикрепляются к домашним животным, поэтому во
время клещевого сезона надо их осматривать после прогулки.После укуса клеща npoфиJlaктичecкyю антибиотикотерапию (доксициоин
200 мг однократно) следует назначать, если время с момента прикрепления
клеща составляет от 24 до 72 ч. Если клеш находился на коже менее 24 ч, то
назначение доксициклина нецелесообразно, а если более 72 ч, то его эффектив¬
ность не доказана. Согласно рекомендациям Американского общества инфек¬
ционных болезней, профилактическое назначение доксипиклина показано,
если можно идентифицировать присосавшийся клещ как нимфу или имаго
(оценку проводят не менее чем через 36 ч от момента прикрепления клеща на
основании степени наполнения клеща кровью), если нет противопоказаний к
приему доксициклина и время после удаления клеша составляет не более 72 ч.В заключение необходимо отметить, что Б представленном сл>^ае клини¬
ческая картина была нетипична: в стадии локализованной инфекции у боль¬
ного отсутствовала мигрирующая эритема, имелись лишь неспецифические
проявления в виде общего недомогания, слабости, «шознабливания», что не
позволіио диаі’ностировать боррелиоз. Кроме того, при данном кардиальном
варианте течения боррелиоза не было нарушений проводимости, которые наи¬
более типичны для Лайм-кардита, заболевание протекало как экссудативный
перикардит.Коїуїментарий НЛ. Новиковой — профессора кафедры профилактической и
неотложной кардиологии Первого МГМУ им. И.М. Сеченова, д-ра мед. наукВ представленном клиническом случае у больного отмечались боли в груд¬
ной клетке достаточно высокой интенсивности и элевация сегмента ST
на ЭКГ. В связи с этим определенные трудности представлял собой диффе¬
ренциальный диагноз острого перикардита и острого коронарного синдрома
с подъемом сегмента ST. В неотложной кардиологии подъем сегмента ST на
ЭКГ чаще всего наблюдается в острую фазу трансмурального инфаркта мио¬
карда. Однако у данного пациента подъем сегмента ST во всех отведениях,
отсутствие реципрокных изменений и депрессия сегмента FQ говорят против
этого диагноза. Диагноз инфаркта миокарда был окончательно отвергнут на
основании отрицательного анаїиза крови на сердечный тропонин Т. Таким
образоАї, всегда необходим быстрый, но внимательный анализ ЭКГ, посколь¬
ку тромболизис, необходимый при инфаркте миокарда, при перикардите не
показан и может привести к тяжелым, подчас смертельным осложнениям в
виде тампонады сердца.
Глава 16. Болезнь Лайма: успешное лечение тяжелого острого... 319Коіиментарий В.И. Маколкина — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, члея-корр.
РАМННе стоит умалять роль расспроса больного в постановке диагноза. Большое
зиачепие имеет эпидемиологический анамнез, поскольку в ряде случаев
поражение сердца может иметь инфекционный характер. У описанного
больного полноценный сбор анамнеза, в котором было указание на укус
клеща, помог заподозрить этиологию заболевания. Это да.'Ю возможность
быстро начать этисугропную терапию и добиться значимого клинического
улучшения в короткие сроки (что в свою очередь подтвердило диагноз).
Правильно поставленный диагноз позволил сократить продолжительность
госиига.'гизат1ии и избежать объемного диагностического поиска для уточ¬
нения инфекционного агента, что в свою очередь уменьшило экономиче¬
ские затраты.Комментарий А-Л. Сыркина — заведующего кафедрой профилактической и неот¬
ложной кар^диологии ФППО Первого МГМУ нм. И.М. Сеченова, д-ра мед. наук
Как мы видим из описанного случая, опасность заражения боррелиозом
существует не только у лиц, побывавших в Сибири или на Дальнем Востоке.
В настоящее время вероятность укуса клеша существует и при нахождений в
центральном регионе в России, в том числе в Москве и Московской области.
Как было указано, перикардит не является типигчньше поражением сердца
при боррслиозе — для этой инфекции более характерны миокардиты с раз¬
витием нарушений проводимости в виде атриовентрикулярных или внутри-
желудочковьгх блокад. В описанном случае клшіическая картина в целом
также была не совсем типичной. В частности, у больного в месте укуса клеща
не было характерной д.ія заболевания эритемы, что говорит о необходимости
помнить о ншшчии безэритематозных форм боррелиоза.Комментарий О.В. Благовой — доцента кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, кавд. мед. наукОсобый интерес представляют сведения о возможносги длительного хро¬
нического течения боррс.'Ш10за с поражением не только нервной системы и
опорно-двигательного аппарата, но и сердца (в том тасле изолированно).
Принадлежность боррелий к порядку спирохет объясняет некоторое сходство
стадийного течения боррелиоза с хорошо известными периодами сифилиса,
при котором поражение сердечно-сосудистой системы (в том числе сифи¬
литический миокардит) является закономерным. При обсуждении данного
клинического наблюдения профессором М.Г. Полтавской была упомянута
пациентка, у которой длительное время не удавалось установить характер
поражения сердца; наряду с другими возможными этиологическими факто¬
рами, не исключался и боррелиоз; бьыи выяачены высокие титры антител к
боррелиям, однако большая длительность болезни не давала осііовапий рас¬
считывать на выраженный эффект аіітибактериальной терапии (пациентка
320 Кардиологияушла из-под наблюдения, сведений об эффективности лечения нет).
Недавно опубликованы результаты изучения эндомиокардиальных био-
птатов у 39 больных с сердечной недостаточностью неясной этиологии и
давностью заболевания до года: у 21% больных боррелии были выявлены
в миокарде при электронной микроскопии или с помощью ПЦР, причем
ни у кого из них НС было АВ-блокады и внекардиальных признаков бор¬
релиоза, а антитела к боррелиям класса IgG были выявлены только у двух
больных (IgM — ни в одном случае). В течение трех недель проводилась
в/в терапия цефтриаксоном, в результате которой состояние больных,
функция и морфология левого желудочка существенно улучшились. По
другим данным, аналогичная антибактериальная терапия у пациентов с
дилатационной кардиомиопатией (средняя ФВ левого желудочка около
30%), ассоциированной с антителами к В. burgdorferi (большая часть
больных имела также соответствующий анамнез), привела к полной
нормализации ФВ левого желудочка через полгода у 55% больных и к
ее повышению еще у 27%. Во всяком случае, возможность существенно
улучшить функциональное состояние миокарда, установив этиологию
дилатационной кардиомиопатии, хотя бы у части больных представляется
очень заманчивой.По-видимому, определение уровня антител к боррелиям, а также ПЦР на
выявление генома боррелий в эндомиокардиальных биоптатах имеет смысл
включать в круг исследований у всех пациентов с неясным характером вос¬
палительного поражения сердца (миокарда и перикарда), особенно при нали¬
чии укусов к,іеша в анамнезе (в том числе в достаточно отдаленные сроки),
сопутствуюппгх артралгий, нейропатии неясного происхождения, при отсут¬
ствии других этиологических факторов миокардита.ЛИТЕРАТУРАМалое В,А., Горобченко Л.Н. Иксодовьте клещевые боррелиозы (Лайм-
боррелиоз) // Лечащий врач. — 2004. — № 6.Лайм-боррслиоз или иксодовые клещевые боррелиозы. Часть 1. Этиология,
клиника, диагностика. — В кн.: Ананьева Л.П. Инфекции и антимикробная
терапия. — 2002. — Т. 4, 2. — С. 42-45.CDC. Recommendations for test performance and ітефгеїаііоп from the sec¬
ond national conference on serologic diagnosis of Lyme disease // MMWR. 1995:
44:590-591.CTGNA Healthcare 8/15/2008 0400 Lyme Disease Treatment.Evidence-based guidelines for the management of Lyme disease. The International
Lyme and Associated Diseases Society // Expert Rev, Anti-infect. Then 2004; 2(1).Gasser R., Fruhwald F., Schumacher M. et al. Reversal of Borrelia burgdorferi
associated dilated cardiomyopathy by antibiotic treatment? // Cardiovasc Drugs Ther.
1996; 10 (3):351-360.Harrison's principles of Internal Medicine, 16^*’ Edition. Editors: D.L. Kasper,
Глава I в. Болезнь Лайма: успешное лечение тяжелого острого... 32 ІЕ. Brawnwald, A.S. Fauci, D.L. Longo, S.L. Hauser, J.L. Jameson. McGrow-Hill
Medical Publishing Division. 2007.Lyme carditis: a United Kingdom perspective // Br. Heart. J. 1993; 70; 15—16.
Lyme carditis: an important cause of reversible heart block. McAlister М.,
Klemcntowicz R, Andrews C. //Ann. Intern. Med. 1989; 110:339—345.Palecek Т., Kuchynka P., HuUnska D. et al Presence of Borrelia burgdorferi in
endomyocardial biopsies in patients with new-onset unexplained dilated cardiomy¬
opathy// Med Microbiol Immunol. 2010; 199(2):139—143.SieereA.C. Lyme disease//N. Eng. J. Med, 2001, 12; 345 (2):П5-125.Wormser G.P., Datiwyler RJ., Shapiro E.D., Halperin JJ., Steere Л.С., Klempner
M.S. et al The chnical assessment, treatment, and prevention of lyme disease, human
granulocytic anaplasmosis, and babesiosis: clinical practice guidelines by the Infectious
Diseases Society of America // Clin. Infect. Dis. 2006; 43(9): 1089—1134.
Глава 17ДЛИТЕЛЬНОЕ ТЕЧЕНИЕ НЕРАСПОЗНАННОГО
КОНСТРИКТИВНОГО ПЕРИКАРДИТА И
ПСЕВДОАНЕВРИЗМЫ ЛЕВОГО ЖЕЛУДОЧКА
У БОЛЬНОГО С ИСТИННОЙ ПОСТИНФАРКТНОЙАНЕВРИЗМОЙА.В. Недоступ, КС, Морозова, МЛ. Троицкая,
О.В, Благова, Н.В. Гагарина, В.П. СедовЕсли истинная аневризма левого желудочка является типичным осложне¬
нием трансмурального (особенно переднего) инфаркта миокарда, то случаи
развития констриктивного перикардита и, тем более, псевдоаневризмы у
больных, перенесших инфаркт миокарда, гораздо менее типичны, а сочетание
длительно существующих истинной и ложной аневризмы можно, безусловно,
отнести к казуистике.Представляем историю болезни пациента С., 61 год, поступивше¬
го в отделение кардиологии Факультетской терапевтической клиники
им. В.Н. Виноградова 24.02.2009 г. с жалобами на одышку и давящие боли
за грудиной при умеренной физической нафузке, купирующиеся приемом
нитроглицерина, увеличение в объеме живота, эпизодические боли в области
правого подреберья, не связанные с приемом пищи.Из семейного анамнеза известно, что отец пациента 83 лет страдает ишеми¬
ческой болезнью сердца; мать 85 лет и сестра 55 лет страдают гипертоннгческой
болезнью, дети (сын 33 лет и дочь 24 лет) практически здоровы. По профессии
пациент — инженер-конструктор. Ограничивает потребление поваренной
соли. Не курит; алкоголем не злоупотребляет. Перенес детские инфекции
(эпидемический паротит, коклюш), перелом левой голени (в молодости).
Аллергологический анамнез не отягощен.Анамнез заболевания {рис. 17.1). В июле 1995 т. (в возрасте 47 лет) после
эмоционального стресса, без предшествующей стенокардии, перенес острый
трансмуральный инфаркт миокарда передней стенки левого желудочка, ослож¬
ненный формированием аневризмы верхушки левого жел>’дочка, по поводу
чего находился на лечении в Городской клинической больнице № 1 г. Москвы.
Проводилось лечение нитратами, антиагрегантами, антикоагулянтами.
Р-адреноблокаторами. Через 2 нед от начала заболевания отмечалось повы¬
шение температуры тела до 39 X, сохранявшееся на фоне антибактериальной
терапии; несмотря на это, был вьшисан. В августе, сентябре 1995 г. лихорадка
сохранялась; отметил появление одышки, отеков голеней, в связи с чем в сен¬
тябре 1995 г. был госпитализирован в Городскую клиническую больницу № 15
Глава 17. Длительное течение нераспознанного констриктивного..323г. Москвы, где состояние было расценено как ишемическая болезнь сердца:
постинфаркгный кардиосклероз; хроническая аневризма левого желудочка с при¬
стеночным тромбозом; рецидивирующий синдром Дресслера, недостаточность
кровообращения 11А стадии. Был выявлен экссудативный перикардит, неодно¬
кратно производились пункции перикарда, при которых была получена светлая
жидкость. Стероидная терапия не назначалась. При одной из повторных пунюіий
было получено 800 мл гаойного отделяемого, при посеве которого вьщелен золо¬
тистый стафилококк. В дальнейшем в связи с недостаточной эффективностью
антибактериальной терапии проводилось дренирование перикарда, в течение 7
дней — перикардиальный диализ, температура тела постепенно нормализовалась.
Проводилось лечение диуретиками, сердечными гликозидами, нестероидными
противовоспатительными препаратами, анаболическими препаратами.После выписки сохранялись отеки ног, небольшое количество жидкости
в левом плевральном синусе; принимал дигоксин, аспирин, верошпирон,
фуросемид. Сохранялась небольшая одышка, болей в грудной клетке не было,
чувствовал себя относительно удовлетворительно, с 1995 по 1998 г несколько
раз проводились курсы стационарного лечения по поводу усиления одышки,
увеличения в объеме живота, появления отеков на ногах с некоторым эффек¬
том (медицинская документация не представлена).07.1995 г.
ГКБ No 109.1995 г.
ГКБ № 151995-
1998 гг.11.1998 г
санаторий1998-
2008 гг.Лихорадка4ОдышкаОтекиголеней+ 4-Асциті іі іккБоли
в области
сердца#4»ДиагнозОИМ,аневризмаверхушкиЛЖСиндромДрессле¬раСиндромДрессле¬раЛечениеНитратыантиагре-гантыантикоагу¬лянты|3-АБ,АБПункции,дрениро¬ваниеперикар¬да,перикард.диализДигоксин,фуросе-мид,верошпи¬рон,аспиринПЗ,нитраты,диуретикиФуросе-мид,бисопро-лол,плевраль¬ныепункцииФуросе-мид,бисопро-лолРис. 17.1. Анамнез больного С., 61 год
324 КардиологияВ ноябре 1998 г. во время пребывания в санатории пациент отметил нарас¬
тание одышки, отеков, появление давяших болей в области сердпа, возоб¬
новление лихорадки. Состояние бьито расценено как синдром Дресслера,
проводилось лечение нитратами, диуретиками. Со слов пациента, назначалась
кратковременная терапия преднизолоном (дозу и длительность лечения не
помнит), в результате проведенного лечения температура тела нормализова¬
лась, уменьшились одышка и отеки. После окончания санаторного лечения
сохранялась одышка, продолжали беспокоить боли в левой половине грудной
клетки. В дальнейшем неоднократно госпитализировался в связи с явлениями
недостаточности кровообрашения (усилением отеков ног, одышки, увеличе¬
нием объема живота). В 1999 г. был выявлен (впервые?) двусторонний гидро¬
торакс, отмечено также учащение приступов болей за грудиной до нескольких
раз в месяц. Проводилась терапия диуретиками, нитраты не назначались.
Наблюдался у кардиолога по месту жите.іьства. Принимал фуросемид при
появлении отеков, бисопролол 5 мг/сут.В последующие 10 лет неоднократно госпитализировался, многократно
проводилась лечебная плевральная пункция, медикаментозная терапия суще¬
ственно не меня-'шсь, состояние оставалось относительно стабильным. В тече¬
ние последнего года отметил усиление одышки, эпизодически — появление
отеков, заметное увеличение объема живота, появление эпизодов болей в
области правого подреберья без связи с приемом пищи. Приступы стенокардии
беспокоя'г несколько раз в месяц при умеренной физической нагрузке, купиру¬
ются приемом нитроглицерина. Поступил в Факультетскую терапевтическую
клинику им. В.Н. Виноградова в связи с нарастанием яатений сердечной недо¬
статочности для обследования, коррекции терапии.При осмотре состояние средней тяжести. Температура тела нормальная.
Кожные покровы бледные, акроцианоз. Отеков нет; лимфоузлы не увеличены.
Костно-мышечная система без видимых: патолопгческих изменений. Число
дыханий 18 в минуту, при перкуссии над легкими — притупление ниже углов
лопаток, при аускультации — везикулярное дыхание, ослабленное с обеих сто¬
рон ниже углов лопаток, хрипов нет. Тоны сердца приглушены, ритм правиль¬
ный. ЧСС 80 ударов в минуту, АД 110/70 мм рт.ст. Живот мягкий, безболезнен¬
ный при пальпации. Печень увеличена, отстоит от края реберной дуги на 10 см,
плотно-эластической консистенции, безболезненна; селезенка не увеличена.В общем анализе крови: ПЬ 154,7 г/л, эритроциты 4,8 млн, ЦП 0,96; лейкоци¬
ты 4,9 тыс., формула не изменена, тромбоциты 159,9 тыс., СОЭ 4 мм/ч.В биохимическом анализе крови', общий белок 80,5 г/л, альбумин 44,1 г/л, кре-
атинин 1,05 мг/дл, глюкоза 4,2 .ммоль/л, азот мочевины 9,1 ммоль/л (3,2-8,2),
общий билирубин 36,0 мкмоль/л (5,0—21,0), прямой билирубин 16,4 мклтоль/л
(0-5,0), АЛТ 9 ед/л, лет 14 ед/л, Г-ГТ 53 ед/л., ЩФ 3 сд/л. При электрофорезе
белков — диспротеинемия.Липидный спектр: триглицериды 70 мг/дл, общий холестерин 112 мг/дл,
ЛПОНП-хс 14,0 мг/дл, ЛПВП-хс 19 мг/дл, ЛПНП-хс 79,0мг/дл, КА 4,89.В коагулограмме снижение уровня фибриногена (1,66 г/л) и протромбино-
вого индекса (81%).
Глава 17. Длительное течение нераспознанного констриктивного.., 325При иммунологическом исследовании крови отмечалось повышение уровня
иммуноглобулинов А (380 мг/дл) и G (2150 мг/дд), а также уровня общего PSA
(6,82 нг/мл). Маркеры гепатитов В и С, сифилиса, ВИЧ отрицательные.Гормоны шитовидной железы в пределах нормы.в общем анализе мочи эритроциты 5—7 в п/зр., при исследовании мочи по
Нечипоренко — эритроциты в пределах нормы, белок 0,030%о. Реакция кала
на скрытую кровь слабо положительная.За время госпитализации перенес острую респираторную вирусную
инфекцию, отмечено появление кашля с мокротой (в анализе — лейкоциты
густо в п/зр.; эритроциты 3-8-20 в п/зр.; атипичных клеток и бактерий тубер¬
кулеза не найдено).При рентгенографии органов грудной клетки при поступлении — ждцкостъ
в плевральных полостях (справа — до переднего отрезка 3 ребра, слева — до
5 ребра).При плевральной пункции справа удалено 1600 мл серозной жидкости (уд. вес
1021, белок 87,0%о, проба Ривальта положительная, pH 8,0, лейкоциты 6-12 в
п/зр., лимфоциты 88%, нейтрофилы 18%, бактерии туберкулеза, в том числе
методом ПЦР, не найдены). При бактериологическом исследовании плев¬
ральной жидкости рост микрофлоры не выявлен. При цитологическом иссле¬
довании выявлены клетки пролиферирующего мезотелия, лейкоциты до 12 в
п/зр. при исследовании плевральной жидкости в Нау'чно-исследовательском
инстиуте фтизиопульмонологии микобактерии туберкулеза методами ПЦР и
иммунофлуореспенции выявлены не были.При повторном рентгенологическом исследовании органов фудной клетки
после проведенной плевральной пункции: в правой плевральной полости коли¬
чество жидкости уменьшилось до переднего отрезка 5 ребра. Максимальная
толщина слоя 11 см. Жидкость в главной междолевой щели. В левой плевраль¬
ной полости также определяется небольшое количество жидкости, в видимых
отделах легкие без свежих очаговых и инфильтративных изменений. Корни
легких структурны. Сердце горизонтально расположено, в проекции левого
желудочка определяется обызвествление, в остальном данные ирежние.На ЭКГ (рис. 17.2) — снижение вольтажа комплексов QKS в стандартных отве¬
дениях, комплекс QS и небольшой подъем сегмента STв отведением с V, по V^.При суточном мониторировании ЭКГ по Холтеру — пробежки наджелудочко-
вой тахикардии, мерцательной аритмии, 2 пробежки желудочковой тахикардии
из 4 QRS.В межклиническом отделении функциональной диагностики бьиш проведе¬
на ЭхоКГ, выявлены нарушение локальной и общей сократительной функции
левого желудочка с формированием хронической аневризмы левого желудоч¬
ка, умеренное расширение обоих предсердий, большое количество жидкости в
обеих плевральных полостях.При УЗИ органов брюшной полости отмечены аспит, расширение сосудов
печени, дилатация нижней полой вены.Несмотря на наличие очевидной причины сердечной недостаточности
(постинфарктный кардиосклероз с формированием аневризмы), настораживала
Рис, 17.2. Электрокардиограмма больнотчэ С. Скорость записи 25 мм/с. Пояснения в
текстенеобычность ее проявлений: массивный двусторонний гидроторакс при уме¬
ренной одышке и отсутствии положения ортопноэ, а также наличие асцита при
отсутствии периферических отеков. Это в сочетании с указаниями на перене¬
сенный после инфаркта перикардит (сначала в рамках синдрома Дресслера, а
.затем гнойный) заставило предположить наличие перикардита с весьма веро¬
ятной тяжелой констрикцией, возможно, с сохранением выпота.Для верификации диагноза ЭхоКГ была выполнена повторно (проф.В.П. Седов, рис. П.Зу. КДР левого желудочка 5,2 см, КДО 70 мл, КСО 44 мл,
ФВ 37%, левое предсердие 4,9 см (объем 95 мл), правое предсердие 63 мл,
правый желудочек 2,3 см. Аортальный клапан уплотнен, амп^титуда раскрытия
не уменьшена (1,7 см). Митральный клапан уплотнен, кальцинирован, под¬
вижность створок не ограничена, регургитация I степени, трансмитральный
поток: Е 100 см/с, А 51 см/с, Е/А=2. Перикард уплотнен, утолщен до 6 мм,
расхождение листков в систолу отсутствует. Нижняя полая вена спадается на
вдохе менее чем на 50%. Сделано заключение о наличии постинфарктной анев¬
ризмы верхушки левого желудочка и акинезии базальной части перегородки,
констриктивного перикардита, систолической и диастолической дисфункции
по констриктивпому типуДля уточнения возможных показаний к операции, выявления кальцинатов
в листках перикарда, уточнения этиологии перикардита выполнена КТ органов
грудной клетки: определялись двусторонний гидроторакс, массивные кальци-
наты в перикарде, аневризма верхушки левого желудочка, нельзя было исклю¬
чить аневризму перегородки.На этом этапе больной был обсужден с кардиохирургом клиники неот¬
ложной, сердечно-сосудистой и обшей хирургии Московской медицинской
Глава 17. Длительное течение нераспознанного констриктивного...327Рис, 17.3. Эхо кардиография. М-режим: утолщение листков перикарда до 0,6 см.
Пояснение R текстеакадемии им. И.М. Сеченова, оперативное лечение в клинике не рекомендо¬
вано.Для уточнения характера поражения мио- и перикарда спетшалистом по
лучевой диагностике (канд. мед. наук Н.В. Гагариной) рекомендовано про¬
ведение мультиспиральной компьютерной томографии сердца с в/в контрасти¬
рованием, при которой выявлены множественные массивные кальцинаты в
коронарных артериях, уплотнение и утолщение листков перикарда, массивные
кальцинаты в перикарде по правой и левой предсердно-желудочковым бороз¬
дам, тесно прилежащие к правой коронарной артерии, до дистальных отделов;
признаки констрикции при 40-исследовании. Миокард левого желудочка в
области нижней трети передней стенки, перегородки и верхушки истончены
до 2 мм, кальцинирован, визуализируется аневризма верхутпки, в области ниж¬
ней трети перегородки оиределяется дефект с затеком контрастного препарата
в полость перикарда под правый желудочек — ложная аневризма. Размеры ее
около 35x46 мм, полость Офаничсна перикардом и тромбами неравномерной
толщины {рис. 17.4, см. цветную вклейку).Клинический диагноз был сформулирован следующим образом. ИБС: стено¬
кардия 11 ФК, атеросклеротический и постинфарктный кардиосклероз, ослож¬
ненный развитием аневризмы передне перегородочной области левого желу¬
дочка и синдромом Дресслера, леченным повторными пункциями перикарда,
с развитием гнойного (стафилококкового) перикардита. Констриктивный
перикардит. Ложная аневризма левого желудочка. Нарушения ритма сердца;
328 Кардиологияпароксизмальная форма мерцательной аритмии, неустойчивые пароксизмы
желудочковой тахикардии. Недостаточность кровообращения ПБ стадии: дву¬
сторонний гидроторакс, асяит. Плевральная пункция справа от 10.03.2009 г.
Атеросклероз аорты, коронарных артерий. Желчно-каменная болезнь.В клинике проводилось лечение: кордарон 600—400 мг/сут, конкор 5 мг
*/2 таб. 2 раза в сутки, энап 5 мг іДтаб. утром, верошпирон 25 мг 1 таб. 2 раза в сутки,
лазикс 60 мг в/в через день в течение 2 нед, далее фуросемид 40 мг 1 таб. утром
(2 раза в неделю), панангин 10,0 + р-р глюкозы 5% 100,0 в/в капельно № 10.В результате проводимой терапии значительно уменьшилась выраженность
одышки, признаков асцита не отмечалось, приступы болей в области сердца
не рецидивировали. Однако данное улучшение носило временный характер,
у больного имелись безусловные показания к операции, в связи с чем он
был повторно проконсультирован кардиохирургом, директором Российского
научного центра хирургии РАМН им, акад. Б.В. Петровского, профессоромС.Л. Дземешкевичем. Несмотря на риск, оперативное вмешательство признано
целесообразным, в первую очередь в связи с неизбежностью прогрессирования
сердечной недостаточности. Предполагаемый объем оперативного вмеша¬
тельства включал перикардэктомию, резекцітю псевдоаневризмы с пластикой
левого желудочка, а также аорто-коронарное шунтирование (вопрос о его
проведении должен решаться после выполнения коронарографии, хотя уже
данные КТ говорят о выраженном поражении коронарных артерий с кальци-
натами). Однако от предложенного оперативного лечения больной отказался.
В дальнейшем существенно снизил уровень физических нагрузок (в частности,
полностью отказался от огородных работ на садовом участке). Через год был
повторно госпитализирован в клинику в связи с нарастанием одышки; выявле¬
на жидкость в плевральных полостях до ТТ ребра, проведена лечебная гыевраль-
ная пункция. Объем медикаментозной терапии остается прежним.Синдром Дресслера назван по имени американского врача (W. Dressier,
1890-1969), описавшего его в 1956 г. как идиопатический возвратный доброка¬
чественный перикардит у пациентов, перенесших инфаркт миокарда. Сегодня
термином «синдром Дресслера» иногда называют не только постинфарктный
перикардит, но и перикардит после радиочастотной аблации, стентирования
коронарных артерий и даже постперикардиотолшый синдром, поскольку все
они имеют обший патогенез. Основным проявлением синдрома Дресслера
является перикардит (обычно не склонный к констрикции), несколько реже
развиваются плеврит, пневмонит, артрит; известны единичные описания
геморрагического васкулита и острого ^юмерулонефрита в рамках синдрома
Дресслера. Обычно синдром Дресслера развивается на 2-4-й неделе инфаркта
миокарда (хотя возможно его появление и на 1-й неделе заболевания, и через
несколько месяцев), что обусловлено иммуніилм патогенезом синдрома: в его
основе лежит выработка антител к антигенам миокарда и перикарда, а также
к компонентам крови, попавшей в полость перикарда. Бэру тромболизиса
частота развития синдрома Дресслера заметно снизилась (до 0,5% по сравне¬
нию с 4% во времена Дресслера), что связано с успсіпной репсрфузией миокар¬
да и ограничением зоны некроза. С другой стороны, применение гепарина и
Глава 17. Длительное течение нераспознанного констриктивного... 329тромболитических препаратов способствует попаданию небольших количеств
крови в полость перикарда в зоне некроза. И частота синдрома Дресслера после
тромболизиса, по некоторым данным, остается достаточно высокой (5—6%).
Высокоэффективным способом лечения синдрома Дресслера являются кор¬
тикостероиды в сочетании с нестероидными противовоспа.чительными препа¬
ратами (которые позволяют быстро купировать боль); показанием к пункции
перикарда может быть только развитие тампонады сердца.Случаи развития тампонады сердца, в том числе гемоперикарда, при син¬
дроме Дресслера описаны, хотя это осложнение не является частым. Что
касается развития констриктивного перикардита в исходе постиифарктііого
синдрома Дресслера, то в базе данных Medline удалось обнаружить лишь
5 подобных описаний, последнее — в 1991 г; констрикция развилась в сроки
от 1 до 10 мсс, во всех случаях проведена успешная псрикардэктомия. С y^^eтoм
крайней редкости такого осложнения синдрома Дресслера мы не склонны
считать, что констриктивный перикардит у нашего пациента был первичным
осложнением самого синдрома Дресслера. В литературе приводятся два слу¬
чая развития псевдоаневризмы левого желудочка у пациентов с синдромом
Дресслера, на которых мы остановимся подробнее. Наконеті[, случаев развития
стафилококкового перикардита у пациентов с синдромом Дресслера в доступ¬
ной литературе не описано, что связано в первую очередь с тем, что повторные
пункции перикарда не используются для лечения этого заболевания,В связи с тем, что предстоит рассказать о механизмах развития псевдоа¬
невризмы сердца, несколько слов необходимо сказать о разрывах миокарда
при инфаркте. Частота случаев отрыва папиллярных мышц при инфаркте
колеблется от 0,5 до 5,0%, случаев разрыва межжелудочковой перегородки —
в пределах 1—2%. Разрывы свободной стенки левого желудочка составляют
15—25% среди фатальных случаев инфаркта миокарда и 2,6—3,7% среди всех
случаев инфаркта миокарда. Однако по результатам недавнею многоцентро¬
вого исследования, проведенного с помош,ью чрсснищеводной ЭхоКГ, частота
разрывов была несколько меньше: свободной стенки левого желудочка — 0,8%,
межжелудочковой перегородки — 0,6% (частота отрыва сосочковых мышц не
оценивалась отдельно от их дисфункции). Описано также развитие двойного
разрыва миокарда левого желудочка, частота которого составляет около 0,3%.
Фатальные разрывы миокарда развиваются в первые 2 нед инфаркта: 60% — в
первые 3 дня, сше 24% — на 4—7-й день и лишь 16% — на 8-14-й день.Псевдоаневризма левого желудочка возникает при сочетании разрыва мио¬
карда с перикардитом {рис. 17.5): кровь из желудочка поступает в полость
перикарда, огран№іенную перикардиальными спайками, что препятствует раз¬
витию тампонады сердца. Пседдоансвризма увеличивается из-за поступления
крови из левого желудочка и может превышать сам левый желудочек. В поло¬
сти псевдоапевризмьт, как правило, образуется тромб.Клинические проявления псевдоаневризмы включают (они могут полно¬
стью отсутствовать) нарастание сердечной недостаточности, пульсацию у
левой границы относительной тупости сердца, систолический шум, сохране¬
ние подъема сегмента ST на ЭКГ (при инфаркте), аритмии, эмболии. Риск
3Z0Кардиологияистинная аневризмаложная аневризматромбРис. 17,5. Схема развития истинной и ложлой аневризмы левого желудочка. Пояснения
п текстеразрыва псевдоаневризмы очень велик, поскольку в этой зоне стсика левого
желудочка состоит только из тромба и перикарда. Лечение псевдоаневризмы
состоит в безотлагательном хирургическом вмешательстве.Первые описания псевдоаневризмы левого желудочка относятся ко вто¬
рой половине 1960-х гг., среди них есть и отечественная работа, в которой
описано развитие псевдоаневризмы после резекции истинной аневризмы
левого желудочка. По-видимому, это одно из первых или первое описание
постоперационной ложной аневризмы — в первые 10 лет описания касались
почти исключительно постинфарктной или посттравматичсской ложной
аневризмы, причем публикации за год бьши единичны. Дальнейший рост
числа публикаций (они и сегодня, как правило, представляют собой описание
отдельных случаев) связан не только с улучшением способов диагностики, но
и с нарастанием случаев развития ложной аневризмы в результате операций
и процедур на сердце. К последним Ш годам относится болсс половины опи¬
саний случаев псевдоаневризмы, причем за 2008—2009 гг. описано уже около
100 случаев.Основные причины образования псевдоаневризмы левого желудочка:• инфакт миокарда;— псевдоаневризму следует заподозрить при трудно объяснимой сердеч¬
ной недостаточности,— чаще образуется в заднебазальном, апикальном сегментах,— наибольшая давность ложной аневризмы — 7 лет;• операції на сердце;• травма;• инфекция;• редкие причины:— синдром Бехчета.
Глава 17. Длительное течение нераспознанного констриктивного... 331К основным причинам развития псевдоаневризмы левого желудочка отно¬
сятся инфаркт миокарда. Несколько реже к развитию псевдоаневризмы при¬
водят операции на сердце и его сосудах, травмы и инфекции с вовлечением
сердца и его оболочек. Описаны и гораздо более редкие причины (синдром
Бехчета).Как уже было сказано, описано 2 случая сочетания псевдоаневризмы с
синдромом Дресслера — мы остановимся на них подробнее. Первый случай
развития псевдоаневризмы в сочетании с постинфарктным перикардитом опи¬
сан авторами из Мюнстера (Германия). Мужчина 51 года перенес обпгарный
передний инфаркт миокарда, проводился троболизис без достаточного эффек¬
та. Через 2 нед была выполнена чрескожная ангиопластика передней межжелу-
дочковой артерии, еще через 2 нед развилась тампонада сердца, что расценено
как синдром Дресслера, проведена пункция перикарда (удалено более 700 мл
стерильной серозной жидкости). Еще через 2 нед уда^тено еще 100 мл жидкости
из перикарда, развились лихорадка, двусторонний плевральный выпот. Для
полноценного лаважа перикардиальной полости произведена стернотомия,
удален стерильный фибринозный экссудат, антибиотики не назначались. Еще
через месяц, на фоне клинического улучшения, при ЭхоКГ впервые выявлен
разрыв стенки левого жел>'дочка с форлгарованием ложной аневризмы, разме¬
ры которой быстро нарастали в течение 1,5 месяцев (рис. 17.6); больной взят на
повторную операцию.Псевдоаневризма была вьщелена из окружающих спаек, частично резе¬
цирована, на края дефекта наложена заплата, послеоперационный период
протекал без осложнений, больной выписан через 2 нед. Сведений о назна¬
чении нестероидных противовоспалительных препаратов или кортикосте¬
роидов своему больному авторы из Мюнстера не приводят. Данный клини¬
ческий случай во многом схож с нашим, за исключением гораздо меньшего
срока, прошедшего до постановки диагноза и операции, отсутствия явныха 6Рнс. 17.6. Эхокардиофаммы больного, 51 год, из работы Н. Reinecke и соавт. (1998).
Появление (а) и нарастание объема (б) псевдоаневризмы (указана стрелками).
Пояснения в тексте
332 Кардиологиябактериальных осложнений и выраженного кальциноза перикарда, что позво¬
лило авторам расценить перфорацию миокарда как осложнение синдроіма
Дресслера. У нашего больного именно давность процесса (обилие спаек) и
выраженная картина панцирного сердца представляют наибольшую слож¬
ность для хирургов.Во втором из описанных случаев гигантская псевдоаневризма левого
желудочка была выявлена через год после развития острого инфаркта мио¬
карда, осложненного синдромом Дресслера (рис. 17.7, см. цветную вклейку).
Клинически отмечалось появление и нарастание одышки. Псевдоаневризма
оперативно устранена (дополнительно выполнено кардиопульмональное шун¬
тирование). Авторы также придают синдрому Дресслера основное значение в
развитии разрьгеа миокарда, поскольку обычный (более ранний, в отсутствие
спаяния перикарда) разрыв миокарда привел бы к смерти.Ятрогенные причины псевдоаневризмы левого желудочка:• операции на сердце;— протезирование митрального клапана (0,56%, смертность 57,4%),— закрытая митральная комиссуротомия,— трансаортальная септальная миотомия при ИГСС,— аортокоронарное шунтирование,— аневризмэктомия, пластика септального дефекта после инфаркта,— операции Росса и Бентадла (на аорте и аортальном клапане),— оперативное лечение WPW-синдрома (операция по Кули),— процедура Норвуда (при гипоплазии левого сердца),— операция по Дору (передняя гастропексия);• интервенционные вмешательства на сердце:— перикардиоцентез,— ангиография, коронарное стентирование,— РЧЛ (при WPW-синдроме с заднебоковым расположением пучка),— чрескожная баллонная аортальная вальвулопластика,— механическая поддержка деятельности сердца (канюляция).Оперативные вмешательства стоят на втором по частоте месте после инфар¬
кта как причина развития псевдоаневризмьт и, возможно, со временем выйдут
на первое. Псевдоаневризма описана как осложнение самых различных опе¬
раций и интервенционных вмешательств на сердце. На одном из первых мест
стоит протезирование митрального клапана, в том числе с использованием
протеза большего, чем необходимо, диаметра. Поданным австрийских авторов,
проанализировавших почти 11 тыс. случаев протезирования, частота развития
псевдоаневризмы составляет 0,56%, причем летальность достигает 57,4%.Описано также развитие псевдоанеризмьт левого желудочка в результате
закрытой митра^чьной комиссуротомии, трансаортальной септальной миото-
мии при гипертрофической кардиомиопатии, аортокоронарного шунтирова¬
ния, аневризмэктомии, пластики септального дефекта после инфаркта, опе¬
раций Росса и Бенталла, оперативного лечения WPW-синдрома (операция по
Кули), процедуры Норвуда (при гипоплазии левого сердца), операции по Дору
(передняя гастропексия), а также различных интервенционных вмешательств
Глава 17. Длительное течение нераспознанного констриктивного... 333на сердце — от перикардиоцентеза до ангаографии, коронарного стентиро-
вания, радиочастотной аблации (при WPW-синдроме с заднебоковым рас¬
положением пучка), чрескожной баллонной аортальной вальвулопластики,
канюляции сердца с целью временной механической поддержки.Для травматической псевдоаневризмы типично расположение по перед¬
ней стенке левого желудочка. Китайскими авторами описан случай; женщина
35 лет в 4-летнем возрасте перенесла тупую травму грудной клетки в результате
падения, в 22 года без осложнений родила ребенка, за 10 лет до выявления
аневризмы стала отмечать одышку. При аускультации выслушивался систоли¬
ческий шум по левому краю грудины с иррадиацией в подмышечную область.
На ЭКГ — глубокие отрицательные зубцы Т\ псевдоаневризма размерами
5x7 см была отчетливо видна уже при ЭхоКГ и подтверждалась остальными
методами. Больной успешно выполнена резекция аневризмы.Инфекционное поражение любой из трех оболочек сердиа также может
привести к развитию псевдоаневризмы, причем речь идет в первую очередь
о бакгериальньк инфекці^іях, склонных к развитию гнойного расплавления.
Так, описаны случаи формирования псевдоаневризмы при стафилококковом
сепсисе {Staphylococcus aureus) с развитием перикардита, первичном бакте¬
риальном перикардите {Streptococcus viridans), инфекционном эндокардите,
а также в результате нагноения истинной аневризмы {Salmonella virchow),
бактериального миокардита {Salmonella enteritidis) и в качестве осложнения
туберкулемы миокарда [Halim], бруцеллезного панкардита. Возможно также
инфицирование тромба в полости ложной аневризмы с развитием вторичного
гнойного перикардита.Дифференциальной диагноз при подозрении на ложную аневризму левого
желудочка необходимо проводить с истинной аневризмой левого желудочка,
причем крайне редко встречается сочетание истинной и ложной аневризмы
(описано всего около десяти случаев, и мы столкнулись именно с этим крайне
редким сочетанием), с интрамиокардиальной гематомой (нетрансмураль-
ный надрыв миокарда), псевдо-ложной аневризмой, при которой образуется
сообщение между левым и правым желудочками с образованием тонкостенной
полости в правом желудочке, и опухолями сердца.Наиболее частыми осложнениями аневризмы левого желудочка являют¬
ся разрыв (он составляет 32% среди причин смерти при ложной аневризме),
острая тампонада сердца, системные эмболии, нагноение, прорыв в легочную
паренхиму с появлением гнойной мокроты и кровохарканья.Существует несколько способов лечения псевдоаневризмы левого желу¬
дочка ~ реже удается выполнить чрескожное закрытие аневризмы (окклюдср
Amplatzer) или эмболизацию, существенно чаще выполняется открытая опера¬
ция на сердце: 1) ушивание аневризмы; 2) пластика левого желудка заплатой
из перикарда. Необходимо также у^гитывать, что при острой псевдоаневризме
показания к операции более жесткие, чем при хронической, в связи с большим
риском ее разрыва.Статистических данных о результатах хирургического лечения псевдоа¬
невризмы левого желудочка практически нет, поскольку описания подобных
334 Кардиологияслучаев единичны; лишь в отдельных работах авторы анализируют одновре¬
менно 3—5 случаев. Мы приведем результаты американских авторов, в 2007 г.
проаналіізировавших результаты хирургаческого лечения псевдоаневризмы у
30 больных. Их средний возраст составил 68 лет, 70% из них были мужчины.
Изолированное ушивание аневризмы проведено у 5,17% больных, пластика
аневризмы — 25,83%, у 70% вмешательство на псевдоаневризме сочеталось
с другими операциями (в том числе в 17,57% случаев — с аортокоронарным
шунтированием, в 9,3% — с операцией на митральном клапане). В 29% случаев
операция носила экстренный характер.Летальность составила 20%, выживаемость в течение 1 года — 73%, в
течение 5 лет ~ 59%, в течение 8 лет — 45%. Оценивая достаточно высокую
летальность, необходимо иметь в виду, что без операции риск разрыва псев¬
доаневризмы существенно больше, кроме того, высокий операционный риск у
данных пациентов связан с инфарктом миокарда или иными серьезными забо¬
леваниями сердца в анамнезе. Надо сказать, что описания длительного суще¬
ствования постинфарктной псевдоаневризмы сердца без развития фатальных
осложнений единичны; наибольшая давность ее существования в доступной
нам литературе составила 6 лет. Исключение составляют случаи постгравма-
тической псевдоаневризмы: описано появление первых симптомов лишь через
25 лет после получения травмы.Комментарий Н.С. Морозовой — доцента кафедры факулы^тской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед. наукВ нашем случае наиболее вероятный механизм развития псевдоаневризмы
левого желудочка представляется следующим образом. Течение обширного
переднего инфаркта миокарда осложнилось развитием не только аневризмы,
но и синдрома Дресслера, который не был своевременно распознан (противо¬
воспалительная терапия не назначалась); неоднократные и недостаточно обо¬
снованные перикардиальные пункции привели к инфицированию экссудата и
развитию тяжелого гнойного перикардита, который также требовал пункций
и установки дренажа. В результате прямого повреждения миокарда пункцион-
ной иглой либо расплавления миокарда в зоне нагноения (но не в зоне истин¬
ной аневризмы) возник разрыв миокарда, который не закончился тампонадой
сердца и смертью благодаря тому, что к этому времени в результате длительно¬
го воспалительного процесса успели образоваться перикардиальные спайки,
ограничившие зону разрьгеа и сформировавшие стенки ложной аневризмы.
В дальнейшем перикард кальцифицировался, что наряду с нарастанием раз¬
мера ложной аневризмы привело к прогрессированию сердечной недостаточ¬
ности преимущественно по большому кругу кровообращения, однако в целом
заболевание протекало относительно стабильно, что является уникальной
особенностью данного случая (наряду с необычностью самого сочетания
синдромов), хотя, к сожалению, не гарантирует благоприятного прогноза в
отсутствие оперативного лечения, от которого пациент отказывается.Больной наблюдается в клинике в течение полутора лет, его повторные
госпитализации (две за это время) связаны с нарастанием явлений сердечной
Глава 17. Длительное течение нераспознанного констриктивного... 335недостаточности и необходимостью проведения лечебных плевральных пунк¬
ций в сочетании с парентеральным введением диуретиков. Однако в целом
можно говорить об относительной стабильности состояния пациента.ЛИТЕРАТУРАСыркинА.Л. Инфаркт миокарда. — М., 2003. — 465 с.Горнак К.А., Козлов И.З., Кох В.К. Псевдоаневризма сердца вследствие
резекідии хронической аневризмы левого желудочка // Вестник хирургии им.
И.И. Грекова. - 1966. - № 97(11). - С. 125-127.Akyildiz E.U., CeVtk S., Ersoy G. [Cardiac ruptures following myocardial infarc¬
tion in medicolegal cases] [Article in Turkish] // Anadolu Kardiyol Derg. 2007;
7(3):253-256.Лтік F. A. , Navia J. L., Vega P. Vega P. etal Surgical treatment of postinfarction left
ventricular pseudoaneurysm //Ann. Thorac. Surg. 2007; 83(2):526—531.Beaufils P., BardetJ., TemkineJ. etal [Dressler’s syndrome: constrictive pericardi¬
tis following myocardial infarction operated on with success] [Article in French] I j
Arch. Mai. Coeur. Vaiss. 1975; 68(6):651-656.Benouaich V., Marcheix B., Grunenwald E. et al. [Late complications of a pseudo
aneurysm of the left ventricle; thrombus infection and purulent pericarditis] [Article in
French) //Ann. Cardiol. Angeiol (Paris). 2007; 56(6):316—318.Betigeri V.M., Kareem R.A., Nair R.S. et al. Left ventricular posterior wall
pseudoaneurysm: a rare sequela of mitral valve infective endocarditis in a chronic
patient of HLA-B27 positive spondyloarthritis // Ann. Thorac. Surg. 2006;
82(6):2294-2296.Biyik L, Oto O., Ergene O. Brucella pancarditis with dissectmg aortic root abscess,
left ventricular pseudoaneurysm and ventricular septal defect //S. Int. Med. Res. 2007;
35(3):422-426.Blinc A., Noc М., Pohar B. et al. Subacute rupture of the left ventricular free wall
after acute myocardial infarction. Three cases of long-term survival without emer¬
gency surgical repair//Chest. 1996; 109(2):565-567.Carcagni CarcagniA., Nusca A., Covino E. et al. Dissecting intramyocardial hema¬
toma masquerading as a pseudoaneurysm of left ventricular free wall: an unusual case
of myocardial rupture // Catheter Cardiovasc Interv. 2006; 67(5):724—727.Cheung P.K., Myers M.L., Arnold J.M. Early constrictive pericarditis and anemia
after Dressler’s syndrome and inferior wall myocardial infarction // Br. Heart. J. 1991;
65{6);360-362.Choi J.B., Choi S.H., Oh S.K., Kim N.H. Left ventricular pseudoaneurysm after
coronary artery bypass and valve replacement for post-infarction mitral regurgitation //
Tex. Heart. Inst. J. 2006; 33(4):505-507.Cua C.L., Sanghavi D., Voss S. et al. Right ventricular pseudoaneurysm after modi¬
fied Norwood procedure //Ann. Thorac. Surg. 2004; 78(4);e72-73.Das A.K., Wilson G.M., Fumary A.P. Coincidence of true and false left ventricular
aneurysm//Arm. Thorac. Surg. 1997; 64(3):831—834.
336 КардиологияDavidson К.Н., Parisi A.F. , Harrington JJ. et al. Pseudoaneurysm of the left ven¬
tricle: an unusual echocardiographic presentation. Review of the literature // Ann.
Intern. Med. 1977; 86(4):430-433.Davis N., Sistino JJ. Review of ventricular rupture; key concepts and diagnostic
tools for success // Perfusion. 2002; 17(l):63-67.Dobrilovic N., Passik C.S., ShawR. Pseudoaneurysrn of the left ventricle in the pres¬
ence of Dresslefs syndrome // Tex. Heart. Inst. J. 2007; 34(2):252-253.Dressier W. A post-myocardial infarction syndrome; preliminary report of a com¬
plication resembling idiopathic, recurrent, benign pericarditis I j J. Am. Med. Assoc.
1956; 160(16): 1379-1383.Echevarria S., Atjona R., Alonso J. False aneurysm formation after Salmonella
virchow infection of a pre-existent ventricular aneurysm — survival after surgical resec¬
tion // Postgrad. Med. J. 1989; 65(761):168-170.Elshershari H., Gossett J.G., Hijazi Z.M. Percutaneous closure of left ventricular
pseudoaneurysms after Ross procedure //Ann. Thorac. Surg. 2008; 85(2):634-636.FaludiR., TothJL., KomocsiA. etal. Chronic postinfarction pseudo-pseudoaneurysm
diagnosed by cardiac MRl j I J. Magn. Reson. Imaging. 2007; 26(6): 1656—1658.Filsoufi F., Salzhef^ S.P., Rahmanian P.B., Adams D.H. Left ventricular false aneu¬
rysm following percutaneus balloon aortic valvuloplasty: magnetic resonance imaging
as diagnostic tool // Eur. J. Cardiothorac Surg. 2006; 30(1): 193.Fukuda L, Kohno М., Shigeta O. et al IPseudo-false aneurysm of the left ventricle
perforated into the right ventricle - a case reportl 1 Article in Japanese] // Nippon
Kyobu Geka Gakkai Zasshi. 1993; 41(2):332-336.Goldhaber S.Z., Lorell B.H., Green L.H. Constrictive pericarditis: a case requiring
pericardiectomy following Dressler’s postmyocardial infarction syndrome // J.
Thorac, Cardiovasc. Surg. 1981; 81(5):793-796.Gueret P., Khalife K., Jobic Y et al Echocardiographic assessment of the incidence
of mechanical complications during the early phase of myocardial infarction in the
reperfusion era: a French multiccntrc prospective registry // Arch. Cardiovasc. Dis.
2008; 101(l):41-47.Haiat R., Desoutter P., Stoltz J.P. et al. [Constrictive pericarditis secondary to
myocardial infarction. Surgical carel [Article in Frenchl 11 Arch. Mai, Coeur. Vaiss.
1981; 74(11):1349-1352.Halim M.A., Mercer E.N., Guinn G.A. Myocardial tuberculoma with rupture and
pseudoaneurysm formation — successftil surgical treatment // Br. Heart. J. 1985;
54(6):603-604.Hertzeanu H., Almog C., Algom M. Cardiac tamponade in Dressler’s syndrome.
Case report II Cardiology. 1983; 70(1):31-36.Indik J.H., Alpert J.S. Post-Myocardial Infarction Pericarditis // Curr Treat
Options. Cardiovasc. Med. 2000; 2(4):351-356.Jiang C., Zhao R., Yang X. Six-year follow-up of a left ventricular pseudoaneurysm
without surgical repair. 2007; 23(9):739-741.Kalkan M.E., Arslan S., Sevimli S., Gurlertop H.Y. Ventricular double rupture
ease of long-term survival without surgical repair // Eur, J. Echocardiogr. 2009;
10(2):329-331.
Глава 17. Длительное течение нераспознанного констриктивного... 337Kamada М., Ohsaka К., Nagamine S., Kakihata Н. Left ventricular rupture
following mitral valve replacement due to oversize prosthesis // Jpn. J. Thorac.
Cardiovasc. Surg. 2004; 52(12):589-591.Kanawaty D.S., Burggraf GW., AbdoUah N. Constrictive pericarditis and anemia
post myocardial infarction//Can. J. Cardiol. 1989; 5(3):147—148.Kang L.M., Zhang J., Fan C.M. eiai Traumatic left ventricular pseudoaneurysm //
Chin. Med. J. (Engl). 2009; 122(6):758-760.Kasahara H., Beran G., Mohl W. Left ventricular pseudoaneurysm following mitral
valve repair // Gen. Thorac. Cardiovasc. Surg. 2009; 57{4);221—223.Kotschet £., Aggarwal A., Esmore D,, Kaye D. Left ventricular apical infection
and rupture complicating left ventricular assist device explantation in 2 women with
postpartum cardiomyopathy // J. Heart. Lung. Transplant. 2005; 24(3);350-354.Leff R.A,, Hoffman I. Ventricular free wall rupture: ten year survival after surgical
repair // Open. Cardiovasc. Med. J. 2008; 2:1—2.Lopez-Sendon J., Gonzalez A., Lopez de Sa E. et al. Diagnosis of subacute
ventricular wall rupture after acute myocardial infarction: sensitivity and specificity of
clinical, hemodynamic and echocardiographic criteria // J, Am. Coll. Cardiol. 1992;
19(6): 1145-1153.Makaryus A.N,, Manetta F., Goidner B. Large left ventricular pseudoaneurysm
presenting 25 years after penetrating chest trauma I I J. intcrv. Cardiol. 2005;
18(3);193-200.Marashi S.M., Eghiesadi-Araghi P., Mandegar M.H. A large left ventricular
pseudoaneurj'sm in Behget’s disease; a case report // BMC Surg. 2005; 5:13.Miura Т., YamazakiK., KiharaS. etal. Transatrial repair of submitral left ventricular
pseudoaneur>'sm // Ann. Thorac. Surg. 2008; 85(2);643-645,Otahbachi М., Cevik C., Meyerrose G., Malki Q. Left ventricular free wall rupture
and large pseudoaneurysm after percutaneous coronarv’ intervention // Cardiovasc.
Revasc. Med. 2009; 10(2): 140-141.Paelinck B., Dendale Р.Л. Images in otinical mcdicine. Cardiac tamponade in
Dresslcr’s syndrome //N. Engl. J. Med. 2003; 348(23)ie8.Patane F, Sansone F, Centofanti P. , Rinaldi M. Left ventricular pseudoaneurysm
after pericardiocenlesis // Interact. Cardiovasc. Thorac. Surg. 2008; 7(6):1112-1123.Perek B., Jemielity М., Misterski М., Dyszkiewicz IV. 1 Chronic left ventricular
pseudoaneurysrn caused by Staphylococcus aureus septicemia accompanicd by
endocarditis] [Article in Polish] // Pol. Merkur Lekarski. 2005; 19(109):69-70.Reinecke H., Mchter Т., Weyand M. Left ventricular pseudoaneurysm in a patient
with Dressler’s syndrome after myocardial infarction // Heart. 1998; 80(1):98-100.Rentoukas EJ., Lazaros G.A., Kaoukis A.F., Matsakas E.P. Double rupture of inter¬
ventricular septum and free wall of the left ventricle, as a mechanical complication of
acute myoccu-dial infarction: a case report //J. Med. Case. Reports. 2008; 2:85.Salazer T.F, Bacharach J.M., Bresnahan J.F. et al. Fistulous pseudoaneurysm
complicating surgiccil accessory pathway interruption for Wolff-Parkinson-White syn¬
drome // Mayo Clin. Proc. 1992; 67(7):663—666.ShaharA., Hod H., Barabash G.M. etal Disappearance of a syndrome: Dresslcr’s
syndrome in the era of thrombolysis j j Cardiology. 1994; 85(3-4):255—258.
338 КардиологияShao J.H., Aronow W.S., Kupersmith A. et al Pseudoaneurysm with thrombus
and left ventricular inflow obstruction after left circumflex stenting // Am. J. Then
2008;15(2):180-183.Tew F.T,, Mantle J.A., Russell R.O. Jr, Rackley C.E. Cardiac tamponade with
nonhemorrhagic pericardial fluid complicating Dresskr’s syndrome j j Chest, І977;
72(l):93-95.Utley J.R., Story J.R., Dandilides P.C. Resection of infected ventricular aneurysm
(Salmonella) following septic saddle embolus//J. Card. Surg. 1993; 8 (2): 143-147.Vehi C., Mestres С.Л., Igual A., Murtra M, Ixft ventricular pseudoaneurysm
after closed transapical mitral commissurotomy // Thorac. Cardiovasc. Surg. 1985
Oct;33(5):322-323.Verkkala K., Maamies Т., Kupari M. et al. Pseudoaneurysm of the left ventricle
following mitral valve replacement. Report of two cases and review of the literature //
J. Cardiovasc. Surg. (Torino). 1990; 31(2):242-246.Vijayvergiya R., Chongiham D.S., Thingnam S.K. et al. Left ventricular pseudoan¬
eurysm with infective pericarditis; a rare cause of intractable hemoptysis 11 Angiology.
2008; 59(4):507-509.Yamahi H., imanaka K., Tanabe H. et al f Pseudoaneurysm of the left ventricle fol¬
lowing suppurative pericarditis and sepsis due to Staphylococcus aureus: a case report]
[Article in Japanese] // J. Cardiol. 2004; 44.
Глава 18ПОДКЛАПАННЫЙ СТЕНОЗ ЛЕГОЧНОЙ АРТЕРИИ -
ВРОЖДЕННЫЙ ПОРОК ИЛИ КАРДИОМИОПАТИЯ?AS. Недоступ, О.В. Благова, ГМ. Папашн, В.А. КапустинаТерапевты-кардиологи, работающие со взрослыми пациентами, не так
часто сталкиваются с некорригированными врожденными пороками сердца;
тем более это касается врожденного стеноза легочной артерии — диагноз
обычно устанавливается в детском возрасте, пациенты наблюдаются и лечат¬
ся в кардиохирургических стационарах. В то же время отсугствие «детского»
анамнеза, хорошая переносимость физических нагрузок в течение многих лет
жизни, предшествующих болезни, всегда обусловливают сомнения в наличии
тяжелого врожденного порока сердца. Мы представляем описание немоло¬
дой больной, которая до поступления в клинику обследовалась во многих
кардиологических центрах Москвы, включая НЦССХ им. А.Н. Бакулева,
но у которой диагноз особого варианта гипертрофической кардиомиопатии
был заподозрен на основании некоторых особенностей болезни как у самой
больной, так и у ее сестры и поставлен лишь после целенаправленного поис¬
ка подтверждающих его инструментальных данных. Дополнительную слож¬
ность представляло наличие у бо.іьной и ее сестры выпотного перикардита.
Обсуждается соотношение понятий врожденного порока сердца и генетиче¬
ской кардиомиопатии.Больная К., 59 лет, поступила в Факультетскую терапевтическую клинику
им. В.Н. Виноградова 09.02.2006 г. с жалобами на одышку при минимальной
физической нагрузке, учащенное сердцебиение в покос (до 100 уд/мин и
выше), ошушение «распирания» в эпигастрии, отечность голеней, малосим-
птомные подъемы АД до 160-170/90 мм рт.ст. (при обычном АД 130/80 мм
рт.ст.), повышенную утомляемость,в семейном анамнезе прослеживается линия сердечно-сосудистых заболе¬
ваний {рис. 18.1): отец страдал гипертонической болезнью, умер в 49 лет от
инсульта; мать страдала пароксизмальной тахикардией, умерла в 75 лет от рака
легких; тетя умерла в 41 год, страдала заболеванием сердца (более точных све¬
дений нет), ее сьш умер в 49 лет от инфаркта миокарда, дочь 53 лет страдает
тахикардией (двоюродные брат и сестра больной К.); другая двоюродная сестра
по матери, 65 лет, в течение последних 10 лет страдает перикардитом, по пово¬
ду синдрома слабости синусового узла ей имплантирован постоянный ЭКС, ее
сын 40 лет перенес инфекционный эндокардит, протезирование митрального
клапана. Больная К. имеет сына 38 лет, который клинически здоров.По образованию инженер, в настоящее время инвалид II группы. Вредные
привычки отрицает. В 29 лет перенесла операцию экстирпации матки
по поводу миомы. В 35 дет — аппендэктомия. Отмечает аллергическую
340КардиологияГБ,
инсул ьт
49 лет59 лет,
ВПС?■Ф0,6Рак
легких,
тахикардия?
79 летСердце?
41 годИМ,49 лет53 года,
тахикардия38 лет,
здоров— мужчина45 лет,
здоровЕЗПогиб
в войну65 лет,Q перикардитQ) —женщинаРис. 18,1. Родословная больной К.20 лет,
здорова40 лет,
ИЭ15 лет,
здоровреакцию на сульфаниламиды в виде кожного зуда, на неселективные
Р-адреноблокагоры — бронхоспазм.Анамнез заболевания {рис. 18.2). В детстве часто болела острыми респиратор¬
ными вирусными инфекциями, ангинами (тонзиллэктомия не проводилась).
В возрасте 15 лет впервые был выявлен шум в сердце, состояние расценивалось
как ревматический порок сердца; до 30 лет проводилась бициллинопрофилак-
тика. Самочувствие оставалось удовлетворительным. В возрасте 35 лет (1981 г.)
перенесла острое респираторное вирусное заболевание, после которого дли¬
тельное время сохранялись субфебрильная лихорадка, увеличение СОЭ, стало
бсспокоіггь учащенное сердцебиение. Состояние было расценено как миокар¬
дит, по месту жительства проводштась терапия антибиотиками, коргликоном.
С этого времени постоянно принима,іа целанид. Самочувствие несколько
улучшилось, однако вскоре появилась и постепенно нарастала одышка при
физических нагрузках, стали беспокоить периодические сердцебиения, сни¬
зилась толерантность к нагрузке. В 1995 г. (в возрасте 48 лет) отметила появ¬
ление небольших отеков голеней. Было впервые проведено эхо кардиографи¬
ческое исследование: выявлена жидкость в полости перикарда, расцененная,
по всей видимости, как проявление перикардита. Стационарно проводилось
лечение антибиотиками, мочегонными, короткий курс терапии преднизоло-
ном 15 мг/сут, в результате чего было отмечено снижение количества жидко¬
сти в перикарде. Одышка, сердцебиения, слабость сохранялись.С 2000 г. наросли отеки голеней, состояние расценивалось как недо¬
статочность кровообращения, усилена диуретическая терапия с некоторым
эффектом. В 2002 г. (в возрасте 55 дет) впервые зафиксирована мерцательная
Глава 18. Подклапанный стеноз легочной артерии — врожденный порок... 3412000 20022005 2006одышкасердце¬
биения -слабостьотеки ног_шум
в сердцеУЗИ сердца-130 мл 350 млдиагнозлечениеревм,пороксердцамио¬кардитгидро¬перикардВПС, ВПС, 2-
НК МА гидро- камер.перикард ПЖбициллин АБв/м аб, кордарон коргликон,в/м коргликон, мочегонные генные (ДОІ0.05) НПВП,^ целанид пз 15 мг ПЗ 15 мг,(до 1995 г.) мочегонныеРис. 18.2. Анамнез больной К., 59 летаритмия, был назначен кордарон в дозе 600 мг с последующим уменьшением
до 200 мг/суг. В апреле 2005 г. на ЭКГ зафиксирован синусовый ритм, в осталь¬
ное время сохранялось трепетание предсердий с меняющимся коэффициен¬
том проведения (от 2:1 до 4:1). в октябре 2005 г. находилась на стационарном
лечении в Городской клинической больнице № 15 г Москвы. По данным
ЗхоїСГ, в полости перикарда определялась жидкость в коли^іестве 130 мл,
были впервые выявлены умеренный стеноз ствола легочной артерии, легоч¬
ная гипертензия. Состояние расценивалось как врожденный порок сердца:
стеноз легочной артерии, гидроперикард, недостаточность кровообращения
І1А стадии. Проводились внутривенные инъекции коргликона, поляризующей
смеси, внутримышечные инъекции ортофена, в течение 2 нед проведен ку'рс
терапии преднизолоном 15 мг/сут; была продолжена терапия фуросемидом,
верошпироном, назначен тромбо-АСС 100 мг/сут. С учетом сохраняющегося
трепетания предсердий была попытка замены кордарона на соталекс, а затем
на атенолол, однако в связи с развившимся бронхоспазмом возобновлен прием
кордарона в поддерживающей дозе 200 мг/сут в сочетании с дигоксином0,25 мг/сут. Состояние несколько улучшилось.Амбулаторно продолжала подобранную терапию (за исключением дигокси-
на). В январе 2006 г. проведена эхокардиография в Научно-исследовательском
институте профилактической медицины им. А.Л. Мясникова. Подтверждено
наличие врожденного порока сердца (выявлены двухкамерный правый желу¬
дочек, признаки рестрикции левого желудочка, расширение предсердий,
342 Кардиологиянедостаточность митрального и трикуспидального клапанов, легочная гипер¬
тензия). В полости перикарда определялась жидкость в количестве 800 мл,
признаки тампонады сердца. В тот же день эхокардиографическое иссле¬
дование было повторно проведено в НЦССХ им. А.Н. Бакулева, отмечено
лишь 300 мл жидкости в полости перикарда. В конпе января 2006 г. в связи
с подозрением на туберкулезный характер перикардита была обследова¬
на в Научно-Рїсслсдовательском институте фтизиопульмонологии: кггинико-
инструментальньте исследования в динамике позволили исключить туберкулез
как причину хронического экссудативного перикардита. В связи с неясньтм
характером перикардита, сохраняющимися одышкой, слабостью, перифери¬
ческими отеками для обследования и подбора терапии госпитализирована в
Факультетскую тсрапевтшіескую клинику им. В.Н. Винофадова.При поступлении состояние средней тяжести. Конституция гиперстениче¬
ская, индекс массы тела — 30 кг/м1 Кожные покровы чистые, на лице румянец.
Отеки голеней и стоп. Над легкими жесткое дыхание, хрипов нет. Число дыха¬
ний 17/мин. Границы сердца не расширены, 1 тон ослаблен, выслушиваются
трехчленный ритм и слабый систолический шум с эпицентром над мечевид¬
ным отростком. ЧСС 105 уд/мин, ритм неправильный. АД 150 и 100 мм рт.ст.
Печень, селезенка не увеличены. Вены нижних конечностей варикозно рас¬
ширены. Щитовидная железа увеличена (1-11 степень).В общем анализе крови эритроциты 5 млн, НЬ 161 г/л, гематокрит 45%, цве¬
товой показатель 0,95, лейкоциты 7,9 тыс., нейтрофилы 63%, лимфоциты 26%,
моноциты 7,2%, эозинофилы 2,1%, базофилы 0,5%, тромбоциты 217 тыс., СОЭ
5 мм/ч. В биохимическом анализе крови общий белок 6,9 г%, альбумргн 4,5 г%,
креатииин 1,1 мг%, азот мочевины 30 мг%, глюкоза 99 мг%, обшїій билирубин1,0 мг%, у-ГГ 152 ед/л (норма 0-61), ACT 29 Ел/л, АЛТ 30 Ед/л, холинэстераза
12 753 Ед/л (4400-15 500), мочевая кислота 7,5 мг/дл (2,5-7,0), триглицериды
146 мг/дл, обший холестерин 211 мг/дл, натрий 145 мэкв/л, калий 4,7 мэкв/л,
кальций 10,4 мг/дл. В динамике уровень мочевой кислоты повысился до 9 мг%.
Проведена проба Реберга: креатинин мочи 90,6 мг/дл, креатинин крови 1,3 мг/дд,
клубочковая фильтрация 29 мл/мин, реабсорбция 98,6%. Экскреция мочевой
кислоты 333 мг/сут, клиренс мочевой кислоты 2,6 мл/мин. Электрофорез бел¬
ков: альбумин 62,5%, а^-глобулины 6,6%, а^-глобулины 11,3%, р-глобулины
10,4%, у-глобулины 9,2 отн.%. Выявлен С-реактивный белок — 1,93 мг/мл
(норма 0-0,8).В общем анализе мочи pH 5, удельный вес 1016, прозрачность полная, белок0,085%о, сахара, ацетона, желчных пигментов нет, уробилин в пределах нормы,
лейкоциты 6—8 в поле зрения, эритроциты единичны в препарате, слизи уме¬
ренное количество, бактерий немного. В анаиизе по Нечипоренко белок 0,04%о,
лейкоциты 2250 в 1 лит, эритроциты 250 в 1 мл. Суточная протеипурия 146 мг, в
динамике 35 мг. Реакция коїш на скрытую кровь отрицательная.При рентгенографии органов грудной клетки легкие без свежих очаговых и
инфильтративньгх изменений, в язычковом сегменте (Sj) верхней доли лево¬
го легкого определяется линейный участок уплотнения легочной ткани —
фиброз? Корни легких структурны. Плевральные синусы свободны. Сердце
Глава І8. Подклапанный стеноз легочной артерии — врожденный порок... 343Рис. 18,3. Электрокардиограмма больной К. при поступлении в клинику. Скорость
записи 25 мм/с. Пояснения в текстеувелртчено в размерах, расширено в обе стороны и кзади, в поперечнике 18 см.
Аорта уплотнена. При спирографии выявлены умеренные вентиляционные
нарушения рестриктивного типа: ЖЕЛ 2100 мл (71%), ОФВ^ 1830 мл (79%),
ОФВ,/ФЖЕЛ 79%, MOq, 88%, МОС.^^ 91%, МОС„ 68%.На электрокардиограмме при поступлении {рис. і8.3) трепетание предсер¬
дий с коэффициентом проведения 2;1 и ЧСС 99 уд/мин, резкое отклонение
электрической оси сердца влево (блокада передней ветви левой ножки пучка
Гиса), признаки гипертрофии правого желудочка.При суточном мониторировании ЭКГ по Холтеру, проведенном на фоне
терапии дигоксином0,25 мг/сут и небилетом 5 мг/сут, регистрировалось тре¬
петание предсердий с меняющимся коэффициентом проведения (от 2:1 до
9:1): 448 мс, 2672 мс. ЧСС: днем 62-113/мин (ср. 103/мин), ночью
41—103/мин (ср, 74/мин). Пауз более 2 с всего 11, преимущественно в ночное
время (макс. 2672 мс в 04:55). Желудочковые экстрасистолы, всего 17. ST-T:
без значимой динамики. С учетом наличия пауз, периодического увеличения
коэффициента проведения до 9:1 дигоксин был отменен, доза небилета сни¬
жена вдвое, на этом фоне сохранялось трепетание предсердий с коэффициен¬
том проведения от 2:1 до 9:1, составил 1424 мс, пауз более 2 с не было,
однако усилилась тахиаритмия — ЧСС днем 80—91/мин (ср. 85/мин), ночью
60-90/мин (ср. 84/мин).При эхокардиографическом исследовании — диастолический размер лево¬
го желудочка 3,6 см, левое предсердие 5,1x5,8x4,2 см, правый желудочек2,3 см, правое предсердие 6,2x5,1 см. Толщина стенок: МЖП — 9 мм, ЗС —
10 мм, ПЖ — 5 мм. Характер двргжения стенок не изменен. Общая сокра¬
тительная функция не нарушена, фракция выброса левого желудочка —
55%. Митральный, трикуспидальный и аортальный клапаны не изменены.
Выявлены признаки легочной гипертензии (Р ПЖ 44 мм рт.ст.). Стенки
344 Кардиологияаорты уплотнены. При допплеровском ультразвуковом исследовании — карти¬
на трикуспидальной регургитации I степени. В полости перикарда лоцируется
небольшое количество жидкости (сепарация листков по задней стенке левого
желудочка и передней стенке правого желудочка 0,9 см), количество жидкости
меняется при перемене положения тела, на висцеральном листке перикарда
отме^іеньт наложения фибрина.При сравнении данного протокола с результатами обследования в НЦССХ
им. А.Н. Бакулева, проведенного 10 днями раньше, выявлены некоторые
расхождения: правый желудочек в последнем случае описывался как двух¬
камерный (за счет наличия аномальной циркулярной мышцы и гипертрофии
стенок), легочная гипертензия была более выражена ПЖ 75 мм рт.ст.),
толщина МЖП достигала 11 мм, имелись митральная регургитация I—II степе¬
ни и трикуспидальная регургитация ITT степени; количество жидкости в поло¬
сти перикарда составило около 350 мл.Для уточнения состояния правых отделов сердца, подтверждения диагноза
врожденного порока сердца и определения возможных показаний к оперативно¬
му вмешательству была проведена чреспищеводная ЭхоКГ в отделении врожден¬
ных пороков сердца НЦССХ им. А.Н. Бакулева: лоцируется жидкость в полости
перикарда в количестве 350 мл (за задней стенкой левого желудочка — 15 мм,
перед передней стенкой правого желудочка — 10 мм, в области верхушхи — 8 мм).
Листки перрпсарда утолщены до 3—4 мм. ФВ левого желудочка 60%, ФВ правого
желудочка — 53%. Аномальная мышца в правом желудочке на іранице при¬
тока и оттока, создающая даатенис в правом желудочке, 60 мм рт.ст., ірадиент
давления — 38 мм ртст. Приточный отдел правого желудочка гипертрофиро¬
ван. Трикуспидальный клапан: створки тонкие, подвижішіе, фиброзное кольцо43 мм, хорды несколько укорочены, недостаточность клапана 3+. Митральный
кланан: створки не изменены, регургитация 1,5+. Пик А отсутствует, рестрик¬
тивный тип. Аортальный клапан: створки уплотнены, регургитация до 1+,
Клапан легочной артерии не изменен, фиброзное кольцо 26 мм, регурги гация до
1+. Давление в легочной артерии 14 мм рт.ст. Даїшьіх за легочную гипертенз^по
нет (вероятно, ранее повышенное давление в полости правого желудочка за счет
аномаїьной мыщцы ошибочно расценивалось как аналог легочной гипертен¬
зии). Межпредсердная и межжелудочковая перегородки не изменены. Таким
образом, подтверждено наличие врожденного порока сердца (изолированный
подклапанный стеноз легочной артерии, ипфундибулярный стеноз, с форми¬
рованием двухкамерного правого желудочка). Показаний к операции нет.Несмотря на проведенное обследование, характер поражения правого
желудочка оставался не вполне ясным: одновременно с концепцией о врож¬
денном пороке сердца — стенозе легочной артерии — в связи с выраженными
мышечными изменениями правого желудочка высказано предположение о
наличии у больной гипертрофической кардиомиопотыи с изолированным пора¬
жением правого желудочка и формированием подклапанного стеноза легочной
артерии, аналогично так называемому идиопатическому гипертрофическому
субаортальному стенозу (т.е. гипертроф№іеской обструктивной кардиомиопа-
тии левого желудочка).
Глава 18, Подклапанный стеноз легочной артерии — врожденный порок... 345Требовал уточнения и характер перикардита, в первую очередь были про¬
ведены развернутая серо диагностика инфекции кардиотропными вирусами
{табл. 18.1) и определение антител к миокарду (е учетом высокой частоты
сочетанного поражения мио- и перикарда в рамках вирусной инфекции).
Обнаружены трехкратное повышение титра антител к миокардиальной ткани
класса IgG, а также повышенные титры антител класса IgG к вирусу простого
герпеса, цитомегаловирусу. Однако генома вирусов с помощью ПЦР выявлено
не было, что свидетельствовало об элиминации вируса. Таким образом, данные
серодиагностики в сочетании с длительным анамнезом доброкачественного
перикардита, данными о наличии фибрина на висцеральном листке перикарда
(по данным ЭхоКГ) и указаниями на хороший клинический эффект от тера¬
пии преднизолоном и нестероидными протиБОвоспалительными препаратами
позволили поставить диагноз инфекционно-иммуиного миоперикардита хрониче¬
ского течения.С учетом семейного характера перикардита (на протяжении многих лет
выявляется у двоюродной сестры больной к.), а также выявленных у больной
рестриктивного поражения сердца, нарушений ритма, отеков голеней, протеи-
нурии необходимо было исключить амилоидоз. Проведена биопсия огизистой
оболочки прямой кишки, амилоида в биоптатах не выявлено. Больная была про¬
консультирована генетиком, диапюз семейного амилоидоза признан сомни¬
тельным, его молекулярно-генетическая диагностика — нецелесообразной.Наконец, учитывая длительно существующий перикардиа.1ьный выпот,
терапию кордароном, а также выявленное при осмотре увеличение щитовид¬
ной железы, проведены УЗИ щитовидной железы (подтверждено ее увеличениеI степени, в правой доле на фоне гомогенной структуры визуализируется узел4,5 мм в диаметре с гипоэхогенным венчиком) и определение уровня гормоновСеродиагностика миоперикардита у больной К.Таблица 18.1ПоказательЗначение у больнойДиагаостический титрАнтитела к миокарду IgM0>1:10Антитела к миокарду IgG1:300>1:100Антитела к ЦМВ IgM1,15>1,1Антитела к ЦМВ IgG146,9>22Антитела к ВПГ 1 типа IgM0,28>1ЛАнтитела к ВПГ 1 типа fgG73,3>22Антитела к ВПГ 2 типа IgM0,41>1,1Антитела к ВПГ 2 типа IgG2,1>22Антитела к вирусу ЭБ IgM0>1Антитела к вирусу ЭБ IgG0>1Антитела к S. aureus IgM0>1:10Антитела к S. aureus IgG1:2001:100Антитела к Streptococcus IgM01:10Антитела к Streptococcus IgG1:4001:100
346 Кардиологиящитовидной железы: своб. 20,3 пмоль/л (норма 9,0-23,32), ТТГ 2,64 МЕ/л
(0,36—4,84), антитела к тиреопероксидазе 108 МЕ/мл (0-30). Состояние рас¬
ценено эндокринологом как узловой эутиреоидный зоб.При УЗИ органов брюшной полости печень, селезенка fie изменены, выяв¬
лены парапелъвикальные кисты левой почки. Учитывая наличие показаний к
антикоагулянтной терапии (трепетание предсердий в сочетании с артериаль¬
ной гипертензией, ожирением), проведена ЭГДС, обнаружены явления очаго¬
вого гастрита.В клинике проводилась терапия: небилет 5 мг по 1 таб. утром, затем 1/2 таб.
утром, дигоксин 0,25 мг по 1 таб. с последующим уменьшением дозы и отме¬
ной, моноприл 1 о мг, затем престариум 4 мг I по 1/2 таб./сут, верошпирон 25 мг
по 2 таб. утром, фуросемид 40 мг по 1 таб. 2 раза в неделю, аспирин-кардио
300 мг, затем варфарин 2,5 мг по 1 таб. вечером, плаквенил 200 мг по 1 таб.2 раза в день, мовалис 15 мг по 1 таб. вечером, аллопуринол 100 мг по 1 таб.
днем. В результате лечения состояние больной несколько улучшилось: умень¬
шилась одышка, повысилась толерантность к физической нагрузке. В то же
время сохранялось сердцебиение при нагрузках, работоспособность оставалась
значительно сниженной.Инфундибулярный стеноз — один из трех вариантов так называемого стено¬
за легочной артерии. Основные анатомические варианты легочного стеноза
представлены на рис. 18.4. Помимо истинного стеноза легочной артерии, к этой
же фуппе пороков относят стеноз клапана лего’шой артерии {рис. 18.4, б) и подкла-
панный стеноз на уровне так называемой инфундибулярной части правого желу¬
дочка (те. выводного тракта). Последний и вьіяішен у больной. Сужение выводного
тракта образовано в типичных случаях мъгшечной пластинкой или фиброзным
тяжем. В большинстве случаев инфундибулярный отдел сохраняет коническую
форму и постепеїшо сужается по направлению к клапану {рис. 18.4, в). Реже отме¬
чается стеноз на всем протяжении инфундибулярного отдела (рис. 18.4, г). Иногда
через гипертрофированную мышечную ткань проходит несколько канальцев
неправильной формы, которые соединяют полость правого желудочка с устьем
легочной артерии {рис. 18А, д). Наконец, участи больных имеется локальное суже¬
ние, которое фактически образует добавочный третий желудочек (над местом суже¬
ния), достигающий наибольших размеров при низком инфундибулярном стенозе
(рис. 18.4, е). Стенка третьего желудочка может быть как і ипертрофирована, так и
фиброзно истончена. Такой вариант и выявлен у больной. Возможны (и нередки)
сочетания клапанного и подклапанного стеноза (рис. 18.4, ж). Ствол легочной
артерии бывает обычно сужен и лишь при клапанном стенозе расширяется, что
является определешіьім дифференциально-диагностическим признаком.Частота легочного стеноза составляет 0,08—0,36 на 1000 человек, причем
90% случаев приходятся на клапанный стеноз. Частота оперативных вмеша¬
тельств по поводу данного порока составляет, по некоторым данным, 0,19% от
всех операций на сердце и 0,46% от операций по поводу врожденных пороков
сердца. Изолированный инфундибулярный стеноз правого желудочка — ред¬
кая врожденная патология. Медиовентрикулярный стеноз с интактной межже-
лудочковой перегородкой — еще более редкое состояние: имеется обструкция
Глава 18. Подклапанный стеноз легочной артерии — врожденный порок... 347Рис. 18-4. Различные анатомические варианты легочного стеноза (по Б. Йонашу).
Обозначения: а — норма; 6 — клапанный (диафрагмальный) стеноз; в — типичный
инфундибулярный стеноз; г — длинный инфундибулярный стеноз; д — кіультиканали-
кулярный инфундибулярный стеноз; е — «двухкамерный» правый желудочек; ж — соче¬
тание «двухкамерного» правого желудочка и клапанного стенозатрабекулярной зоны правого желудочка за счет гипертрофированной средней
части с аномальными мышечными ножками или без них.В пользу врожденного характера инфундибулярного стеноза говорит его
нередкое сочетание с другими врожденными аномалиями; синдромом Нунана,
дефектом межжелудочковой перегородки, в том числе в рамках тетрады Фалло,
с атрезией трехстворчатого (трикуспидального) клапана, транспозицией круп¬
ных сосудов, единым желудочком. Генетические исследования проводились,
насколько удалось установить, только у мышей, Двойной правый желудочек
оказался характерен для мышей с трисомией 13 и развивался за счет ненор¬
мального расположения гребней в правом желудочке.Помимо врожденного инфундибулярного стеноза, описано его возникнове¬
ние у 28-летнего пациента (в сочетании со стенозом коронарной артерии) через
24 года после лучевой терапии (суммарная доза составила 40 Грэй) по поводу
неходжкинской лимфомы, а также в аналогичной ситуации годы спустя после
лучевой терапии лимфомы Ходжкина (облучается средостение). Кроме того, опи¬
сано развитие инфундибулярного стеноза в ралпсах гипертрофической кардиоми-
опатии, гликогеноза или лимфомы с инфильтрацией миокарда. Иными словами,
диагноз инфундибулярного стеноза может быть синдромальным и требует в этом
случае установления этиологии. Например, пршодится описание ^тгикального
случая этого заболевания, причиной которого стала перетяжка перикарда без
предшествующего анамнеза перикардита, операций на сердце и в отсутствие
кальция в перикарде. Диагноз бьш поставлен с помощью вентрикулофафии.Клинические проявления зависят от выраженности градиента давления
на клапане легочной артерии (ниже 50 мм рт.ст. — легкий стеноз, 50-80 мм
ртхт. — умеренный, более 80 мм рт.ст. — тяжелый). Пиковый систолический
348 Кардиологияградиент в правом желудочке может быть весьма значительным (до 230 мм
рт.ст.), при этом давление в правом желудочке иногда превышает системное.
Основными клиническими проявлениями инфундибулярного стеноза явля¬
ются одышка, обмороки, наджелудочковые аритмии, а также боли по тип>'
стенокардитических, тромбоэмболии в систему легочной артерии; возможно
бессимптомное течение и при серьезном стенозе. Чаще первые признаки забо¬
левания появляются во взрослом возрасте. Цианоз, как прави.10, отсутствует
или является незначительным и поздним. Систолический шум и кошачье
мурлыкание определяются ниже, чем при клапанном стенозе: в TV межреберье
или в области верхушки. Шулі довольно грубый, проводится к левой ключице
и в левую половину шеи, а также хорошо выслушивается у нижнего угла левой
лопатки, слабо зависит от дыхания и положения тела. П тон бывает сохранен
не только при инфундибулярном, но и при клапанном стенозе (за счет прове¬
дения звука с аортального клапана).Для диагностики инфундибулярного стеноза в большинстве сл>'чаев доста¬
точно использования обычных методов исследования. ЭКГ и рентгенография
органов грудной клетки позволяют выявить признаки гипертрофии правых
отделов, при этом на рентгенограммах в прямой проекции может отмечаться
расширение тени сердца не только вправо, но и влево (за счет смещения лево¬
го желудочка увеличенным правым); иногда это сопровождается погружением
тени верхушки сердца в диафрагщ. В косых ттроекциях определяются сужение
ретрокардиального пространства и приближение передней поверхности сердца
к грудной стенке. При рентгеноскопии можно выявить увеличение амплитуды
сокращений правого желудочка. Поскольку степень задержки легочного ком¬
понента И тона (Р2) на фонокардиограмме прямо зависит от степени обструк¬
ции, этот метод может использоваться для определения выраженности стеноза,
а также для верификации позднего шума изгнания.Но основную роль в диагностике инфундибулярного стеноза играет эхокар-
диография. Помимо собственно градиента и различных изменений просвета
правого желудочка, описаны (причем у абсолютного большинства наблюдав¬
шихся больных, независимо от этиологии инфундибулярного стеноза) ано¬
мальное СИСТОЛІГЇЄСКОЄ движение клапана легочной артерии, дрожание ство¬
рок клапана, связанное с турбулентным движением крови дистальнее места
обструкции (этого никогда не бывает при клапанном стенозе) и раннее или
среднесистолическое закрытие клапана. Градиент даатения на к^тапане легоч¬
ной артерии при этом отсутствует (если инфундибулярный стеноз не сочета¬
ется с клапанным). В ряде случаев трансторакального эхокардиографического
исследования оказывается недостаточно и для уточнения расположения ано¬
мальных структур в правом желудочке проводится чреспищеводная Эхо КГУ некоторых больных для постановки диагноза инфундибулярного стеноза
необходимо выполнение МРТ сердца, поскольку возможности ЭхоКГ оказы-
' ваются недостаточными; метод позволяет детально оценить особенности ана¬
томии правого желудочка у каждого больного (расширение и/или смешение
септомаргинальных и септопариетальных трабекул или средней части жел>'-
дочка; дополнительная папиллярная мышца, гипертрофированный мышечный
Глава 18. Подклапанный стеноз легочной артерии — врожденный порок... 349гребень на париетальной стенке). Наконец, окончательно подтверждает диа¬
гноз ангиовентрикулография, которая выявляет не только увеличение правого
предсердия, но и затруднение оттока крови из него (обратный ток контраст¬
ного вещества), уменьшение полости правого желудочка и его плохое опо¬
рожнение, замедленное наполнение легочной артерии. Зондирование правых
камер выявляет градиент давления на уровне сужения и позволяет исключить
дефекты перегородок.Нашей больной были выполнены оба варианта ЭхоКГ (трансторакальная —
неоднократно), по данным которых диагноз инфундибулярного стеноза пред¬
ставлялся несомненным (лишь в отношении количества жидкости в перикарде
и самого характера перикардита имелись существенные разногласия). Но сму-
шали два обстоятельства. Во-первых, сам характер поражения правого желу¬
дочка (гипертрофированная циркулярная мышца), который сильно напоминал
поражение миокарда в рамках первичной гипертрофической кардиомиопатии
(но только слева). Во-вторых, у больной К. доказан инфекционно-иммунный
характер миоперикардита; и в то же время перикардит имелся у ее двоюродной
сестры 62 лет. Единственный семейный вариант перикардита (амшюидоз) в
результате обследования с большой долей вероятности отвергнут. Так имеем ли
мы все-таки дело с семейной патологией сердца?Ответ на этот вопрос могло дать обследование сестры. Но живет она в
Санкт-Петербурге, поэтому удалось получить лишь протокол ее эхокардио¬
графического исследования. Результат оказался довольно неожиданным: под¬
тверждено наличие выпота в полости перикарда (5 мм в области задней стенки
и за правым предсердием, по-видимому, без утолщения листков перикарда),
но основное внимание обратили на себя выраженные изменения левого желу¬
дочка: сужение его полости до 3,5 см в диастолу и асимметричная гипертро¬
фия стенок (толщина межжелудочковой перегородки от 16 до 20 мм, задней
стенки — от 12 до 16 мм). При этом зон гипокинезии нет, ФВ левого желудоч¬
ка 69%, диастолическая функция и глобальная сократимость не нарушены;
левое предсердие >’величено (5,1 см), правые камеры не расширены, створки
митрального клапана обычные, кальциноз кольца +++ и папиллярных мышц,
ограничивающий подвижность задней створки, регургитация I степени, аорта
не расширена, склерозирована, кальциноз +, легочный и трикуспидальный
клапаны не изменены, давление в легочной артерии 36 мм рт.ст., трикуспи-
дальная недостаточность I степени, в правом предсердии и правом желудочке
лоцируется электрод, фиксированный в области верхушки.Сестра нашей больной страдает умеренной артериальной гипертензией,
что не мешает расценить выявленную у нее выраженную асимметричную
гипертрофию левого желудочка вполне однозначно: речь идет о гипертро¬
фической кардиомиопатии. Мы не имеем достаточных сведений о времени
появления гипертонии и гипертрофии, но необходимо подчеркнуть, что
для вторичной гипертрофии в рамках артериальной гипертонии крайне
нехарактерно сужение полости левого желудочка, которое имеется у сестры
нашей больной; в то же время для гипертрофической кардиомиопатии
у пожилых больных весьма характерно кальцинирование митрального
350Кардиологияклапана. Для подтверждения диагноза гипертрофической кардиомиопа-
тии у сестры больной К. мы воспользовались критериями W.J. McKenna и
соавт. {табл. 18.2), которые были разработаны специально для пациентов
с семейной формой гипертрофической кардиомиопатии без ярких клини¬
ческих проявлений. Диагноз является достоверным при сочетании одного
большого критерия и одного малого (ЭхоКГ) или одного малого критерия
(ЭхоКГ) и двух малых (ЭКГ), Мы не имели ЭКГ, но даже по сочетанию
одного большого (толщина МЖП >16 мм) и одного малого (толщина ЗС
>12 мм) УЗ-критериев диагноз гипертрофической кардиомиопатии являет¬
ся у сестры больной К. достоверным.Согласно современной анатомической классификации (см. ниже), данный
вариант гипертрофической кардиомиопатии следует расценивать как асимме¬
тричную гипертрофию перегородки, по-видимому, с обструкцией. Этот вари¬
ант особенно часто (более чем у половины больных) носит семейный характер
и наследуется преимушественно по аутосомно-доминантному типу И здесь
уместно было вернуться к предположению, которое теперь казалось нам еще
более вероятным: не является ли инфундибулярный стеноз у нашей больной
лишь вариантом гипертрофической кардиомиопатии с преи\г>тцественным
(или даже изолированным) поражением правого желудочка? Дальше мы попы¬
тались ответить на этот вопрос, который имеет и практическое (в частности,
прогностическое) значение для бо.іьной.Анатомическая классификация гипертрофической кардиомиопатии1. Гипертрофическая кардиомиопатии с вовлечением левого желудочка.1.1. Асимметричная шпертрофия:• межжелудочковой перегородки с обструкцией (или без нее) вьшосяшего
тракта левого желудочка;Таблица 18.2Инструментальные критерии диагноза гипертрофической кардиомиопатии
(W.J. McKenna и соавт., 1997)ИсследованиеБольшие критерииМалые критерииЭКГ• признаки гипертрофии лево¬
го желудочка с нарушением его
реполяризации;• инверсия Гв I, aVL, V^-Vg (>3 мм)
или II, 1И, aVF (>5 мм);• аномальные Q (>25 мс или 1/4 R)
по крайней мере в двух отв. от II,
III, aVE V,-V, или 1, aVL, V-V,• блокада одной из ножек пучка
Гиса или умеренно выражен¬
ные нарушения проводимости
(V.-V,);• умеренные нарушения ре по¬
ляризации в V^—V^;• глубокий S в ответвлении Vj
(>25 мм)Эхокардио-графия• тМЖП (передней части) >13 мм,
тМЖП (задней части) >15 мм,
тЗС >13 мм, тЛЖ (своб.) >15 мм;♦ систолич. сметдение створок
митрального клапана (контакт
створки с межжелудочковой пере¬
городкой)• тМЖП (передней части)
>12 мм, тМЖП (задней части)
>14 мм, тЗС >12 мм, тЛЖ
(своб.) >14 мм — умеренное
систолическое смещение
створок митрального кла¬
пана — увеличение створок
митрального клапана
Глава 18. Подклапанный стеноз легочной артерии — врожденный порок... 351• верхушки сердца (апикальная);• мезовентрикулярная обструктивная (по типу «песотаых часов»);• заднеперегородочного отдела и/или боковой стенки;• переднебоковой области левого желудочка (без вовлечения перегородки).1.2. Симметричная (концентрическая) гипертрофия.2. Гипертрофическая кардиомиопатия с вовлечением правого желудочка.Изменения правого желудочка в рамках гипертрофической кардиомиопатии
уже достаточно хорошо известны, но чаще всего носят вторичный характер:
прежде всего нарушается диастолическая функция правого желудочка за счет
асимметричной гипертрофии межжелудочковой перегородки. Частота выяв¬
ления гипертрофии правого желудочка (более 5 мм) составляет 67%, асимме¬
тричной гипертрофии — 45%, частота развития правосторонней обструкции
(необязательно в виде инфундибулярного стеноза) — 15%. Поражение право¬
го желудочка может быть столь же неоднородным, как и левого: от средней
концентрической гипертрофии до более необычных вариантов обструкции.
Правосторонняя обструкция может сочетаться со всеми известными при
гипертрофической кардиомиопатии типами гипертрофии левого желудочка.
Правый желудочек может раньше дилатироваться (дилатация, как известно,
возможна при гипертрофической кардиомиопатии, но лишь на поздних ста¬
диях заболевания). Генетика больных с сушественным вовлечением правого
желудочка фактически не изучена. В то же время гистология весьма сходна с
изменсниядш в левом желудочке.Далее нас интересовали случаи преимущественного или даже изолирован¬
ного поражения правого желудочка в рамках гипертрофической кардиомио-
патии. Во всех подобных слу'іаях процесс установления диагноза бьш весьма
сложным. Так, описано выраженное поражение обоих желудочков в рамках
этого заболевания, причем преимущественное поражение правого желудочка
по типу инфундибулярного стеноза стало причиной ошибочной диагностики
врожденного порока в возрасте 5 лет. И лищь повторная катетеризация сердца
в 14 лет, которая выявила не только значительное нарастание ірадиента в пра¬
вом желудочке, но и поражение левого желудочка без обструкции, позволила
поставить диагноз гипертрофической кардиомиопатии. К 18 годам появился
и левосторонний градиент, по-прежнему уступавший правостороннему (88 и
65 мм рт.ст. соответственно).Интересно сообщение о больном, имевшем систолический шум изгнания
и ЭКГ-признаки гипертрофии левого желудочка. Вопреки ожиданию, при
ЭхоКГ у него был выявлен лишь один признак гипертрофической кардио¬
миопатии (асимметричная гипертрофия межжелудочковой перегородки) без
аномального движения передней створки митрального клапана и в то же время
обнаружены систолическое дрожание и частичное раннесистолическое при¬
крытие клапана легочной артерии, что позволило поставить диагноз і ипертро-
фической кардиомиопатирт с обструкцией правого желудочка (был подтверж¬
ден при вентрикулографии).В тех случаях, когда поражение правого желудочка было изолирован¬
ным, решающим моментом диагностики гипертрофической кардиомиопатии
352 Кардиологиястановилось выявление гипертрофии межжелудочковой перегородки. В част¬
ности, описана апикальная гипертрофическая кардиомиопатия со значитель¬
ным вовлечением правого желудочка, перегородки и градиентом на уровне
выводного тракта правого желудочка с выраженным сужением его полости (без
градиента в полости левого желудочка). Сообщается о развитии правосторон¬
ней гипертрофической каряиомиопатии у ребенка, чья мать страдала сахарным
диабетом (диабет вообще относят к факторам риска развития гипертрофиче¬
ской кардиомиопатии).Выявление одновременного обструктивного поражения правого и левого
желудочков интерпретируют по-разному. Одни авторы расценивают это как
сочетание двух разлшных заболеваний — гипертрофической кардиомиопатии
и инфундибулярного стеноза — у одного больного (по данным Браунвальда.
такое сочетание диагностируется у 5% больных с инфундибулярньш стенозом),
другие говорят о бивентрикулярном поражении в рамках гипертрофической
кардиомиопатии, К примеру, корейскими авторами инфундибулярньш сте¬
ноз сразу был диагностирован в рамках гипертрофической кардиомиопатии,
поскольку к моменту постановки диагноза имелась уже обструкция обоих
желудочков (диагноз поставлен с помощью эхокардиографии и вентрикуло-
графии).Наконец, необходимо упомянуть наблюдения отечественных авторов.
Е.А. Коровина, которая много лет занимается этой проблемой, также описала
в 1995 г больную с правосторонней гипертрофической кардиомиопатией, а
М.М. Миррахимов и соавт. — изолированную правостороннюю гипертрофи¬
ческую кардиомиопатию у фуппы горцев; причем у них имелась гипергрофия
разных отделов правого желудочка,Таким образом, теоретически возможность развития правосторонней гипер¬
трофической кардиомиопатии по типу инфундибулярного стеноза не вызывала
сомнений. Какие же данные в пользу возможного диагноза гипертрофической
кардиомиопатии и против него имелись у нашей больной? Аргутчентов «за» ока¬
залось неожиданно много. Это и отягошснный семейный анамнез, и сужение
полости левого желудочка (КДР = 3,5 см), на которое мы вначале не обратили
внимание, и нарушение АВ-проводимости (трепетание предсердий с периоди¬
чески возникающим проведением 9:1), и блокада передней ветви левой ножки
пучка Гиса (косвенный признак поражения перегородки), и отсутствие других
врожденных аномалий сердца, столь типичных для больных с инфундибу-
лярным стенозом, и, что очень важно, отсутствие признаков стеноза клапана
легочной артерии, который мог бы стать причиной вторичной гипертрофии
правого желудочка. Аргумент «против» был только один — отсутствие гипер¬
трофии межжелудочковой перегородки и стенок левого желудочка по данным
повторных эхокардиографических исследований. Но это возражение настолько
серьезно, что постановка диагноза гипертрофической кардиомиопатии стала
бы возможна лишь при получении новых убедительных данных в его пользуВсе критерии диагноза гипертрофической кардиомиопатии касаются толь¬
ко типичного поражения левого желудочка и очень плохо применимы к диа¬
гностике преимуіцественно правосторонних форм. У нас в запасе оставались
Глава 18. Подклапанный стеноз легочной артерии — врожденный порок... 353три метода диагностики: МРТ сердца, которая могла выявить поражение
левого желудочка и перегородки, генетическая диагностика и биопсия мио¬
карда. Наиболее привлекательной представлялась генетическая диагностика,
но, к сожалению, па сегодня таких возможностей в России нет (гены длинные,
их типирование стоит очень дорого). От возможности проведения биопсии
(особенно интраопсрационной) мы полностью не отказывались, но сначала
как наиболее доступный метод в НЦССХ им. А.Н. Бакулева была выполнена
MFT сердца {рис. 18.5): отмечались дилатация обоих предсердий, гипертрофия
миокарда обоих желудочков (задняя стенка левого желудочка от 8 до 15 мм
в области верхушки, межжелудочковая перегородка от 8 до 16 мм, передняя
стенка правого желудочка 5—9 мм); миокард левого желудочка умеренно утол-
шается в систолу; нарушений локальной сократимости пе выявлено. Сужение
выпосятпего тракта правого желудочка; визуализировался низкоинтенсивный
поток трикуспидальной регургитации. Грудная аорта имела ровные контуры,
отмечался однородный сигнал от кровотока в се просвете. Легочная аорта и
ветви не расширены. В полости перикарда определялось скопление жидко¬
сти толшиной 6—14 мм, обший объем жидкости около 200 мл. Заключение:
гипертрофия миокарда обоих желудочков, умеренная дилатация предсердий.
Жидкость в полости перикарда.Результаты этого исследования дали однознатаый ответ на поставленные
вопросы. У больной не просто выявлена достоверная гипертрофия межже-
лудочковой перегородки, которая не описана ни в одном протоколе ультра¬
звукового исследования сердца, но и имеется настоящая бивентрикулярная
гипертрофия, которая делает диагноз гипертрофической кардиомиопатии
несомненным. Интересно, что утолщение межжелудочковой перегородки
очень неравномерно, что отчасти и может объяснять трудности эхокардиогра¬
фической диагностики, но все же не полностью. Подтверждением тому, что
гипертрофия межжелудочковой перегородки могла быть выявлена при ультра¬
звуковом исследовании сердца, служат результаты повторной Эхо КГ, выпол¬
ненной после получения результатов МРТ: было выявлено неравномерноеКДРлж3,7 смКСРлж2,0 смлп4,2 смКДРпж2,4 смКСРпж1,5 смпп6,1 смгМЖП16 ммтЗС15 ммтПЖ19 ммЛЛА1,9 смПЛА1,6 смРис. 18.5. МРТ сердца у больной К. Пояснения п тексте
354 Кардиологияутолщение межжелудочковой перегородки с максимальной ее толщиной
23 мм. В то же время данное исследование не лавхю однозначного заключения
о поражении правого желудочка; была выявлена высокая легочная гипертензия
(систолическое давление до 70 мм рт.ст,), но правый желудочек не выглядел как
двухкамерный.По-видимому, имеются объективные трудности в выявлении гипертрофии
левого желудочка у нашей больной, которые создавали трудности в диагности¬
ке; возможно, поставленный в юности диагноз врожденного порока оказывал
невольное давление на врачей, производивших исследование, тем более что
получаемые данные ему не противоречили.Таким образом, окончательный клинический диагноз был сформулирован
следующим образом: гипертрофическая бивентрикулярная кардиомиопатия:
необструктивная кардиомиопатия левого желудочка, обструктивная кардио¬
миопатия правого желудочка с формированием инфунаибулярного стеноза.
Инфекционно-иммунный миоперикардит хронического течения. Нарушения
ритма и проводимости сердца: блокада передней ветви левой ножки пучка Гиса,
постоянная форма трепетания предсердий с меняющимся коэффициентом про¬
ведения (от 2; I до 9:1), редкая желудочковая экстрасистолия. Гипертоническая
болезнь ТТ стадии, 1-й степени повышения АД, риск 2, Недостаточность кро¬
вообращения ІІА стадии, II класса (NYHA). Гипер>риксмия. Узловой эутирео-
идный зоб. Варикозное расширение вен нижних конечностей.Была обследована вторая двоюродная сестра больной К., при эхокардио-
храфическом исследовании и холтеровском мониторировании ЭКГ патологии
не выявлено. Планируется обследование сына больной К. Необходимо напом¬
нить, что сын петербургской сестры, т.е. двоюродный племянник больной к.,
перенес, по всей видимости, инфекционный эндокардит, который порой (при¬
мерно в 10% случаев) осложняет течение гипертрофической кардиомиопатии.Теперь необходимо вернуться к вопросу о перикардите, семейный характер
которого с самого начала обращал на себя внимание. Не только результаты
серодиагностики у нашей больной, но и 10-летнее доброкачественное течение
перикардита позволяют остановиться на его инфекционно-иммунной природе
(во всяком случае, отвергнуть подозрение о констриктивном перикардите). Ни
одного упоминания о сочетании инфундибулярного стеноза с перикардитом
нам найти не удалось. Что касается гипертрофической кардиомиопатии, то ее
сочетание с вирусным миоперикардитом достаточно хорошо известно. В обзоре
Ю.И. Новикова и соавт. гипертрофическая кардиомиопатия была выявлена у 10
из 64 больных, перенесших вирусный миоперикардит, т.е. почти в 16% случаев.
Есть довольно много исследований подобного типа, вплоть до обнаружения
более чем в 10% случаев антител к вирусу гепатита С у больных с гипсріро-
фической кардиомиопатией (в сравнении с 6,3% у больных с дилататщонной
кардиомиопатией). Речь идет о том, что вирусная инфекция нередко приводит
к дебюту кардиомиопатии; в нашем случае анамнез инфундибулярного стеноза
гораздо более ранний, но важен сам факт частого сочетания двух заболеваний.Другое исследование было построено по обратному принципу — с помо¬
щью биопсии определяли частоту миокардита у больных с дилатационной
Глава Ї8. Подклапанный стеноз легочной артерии — врожденный порок... 355кардиомиопатией (145 человек), гипертрофической кардиомиопатией
(174 человека) и так называемыми идиопатическими аритмиями (241 чело¬
век) — процент выявления постмиокардитических изменений составил соот¬
ветственно 15, 1,7 и 8,7, т.е. при гипертрофической кардиомиопатии он был
наименьшим, но все же не нулевым. Примерно в том же соотношении удава¬
лось Выявить в анамнезе связь с острыми респираторными вирусными забо¬
леваниями. Интересно, что ни у кого из больных с миокардитом по данным
биопсии не отмечено семейного характера кардиомиопатии или аритмии, те.
миокардит мог явиться основным пусковым фактором у больных с недоста¬
точно «злокачественными» мутациями, которые сами по себе еще не приводят
к развитию заболевания, но способствуют именно такому (развитие гипертро¬
фической кардиомиопатии) ответу на вирусную инфекцию.Как расценивать перикардит у сестры? Течение его доброкачественное, что
позволяет исключить констриктивный вариант. Наиболее вероятно, что и в
этом случае на фоне гипертрофической кардиомиопатии развился вирусный
перикардит (или миоперикардит), т.е. это можно считать просто ;побопытным
совпадением. Но нельзя исключить, что гипертрофическая кардиомиопагия
каким-то специфическим образом способствует развитию и хронизации добро¬
качественного перикардита. Полностью нельзя исключить и того, что у обеих
сестер есть генетические дефекты, предрасполагающие к хрон№іескому пери¬
кардиальному выпоту. Известны семейные варианты перикардита, которые раз¬
виваются в рамках других врожденньпс аномалий (например, сочетание «кампто-
дакгилия — соха vam — перикардит^> или семейный констрикгивньтй перикардит
у больных с порфирией). Еще более интересно сообщение из клиники Мэйо об
идиопатическом (правда, констриктивном) перикардите у 5 членов одной семьи
(по-видимому, амилоидов был исключен). Во всяком случае, сочетание гипер¬
трофической кардиомиопатии с миоперикардитом интересно и в таком варианте
(у двух членов семьи) ни разу не встретилось нам в литературе.Наконец, еще несколько слов о том, что заставило исключить амилоидоз
у нашей больной. Дело не только в том, что у нее имелся семейный анамнез
перикардита. Известно, что мутация в гене транстиретина (TTR) ведет к раз¬
витию семейного амилоидоза не только с полинейропатией, но и с «гипертро¬
фией» миокарда. Сложность диагностики таких случаев амилоидоза состоит
в том, что он редко обнаруживается в слизистой оболочке прямой кишки и
жировой ткани. Шведские авторы выбрали 46 больных с несомненным диа¬
гнозом гипертрофической кардиомиопатии и провели диагностику муіаїтий
не только в саркомерных белках, но и в гене транстиретина. И 3 больным
(т.е. в 6,5% случаев) был посташтен диагноз семейного амилоидоза (мутация
Val30Met). Много говорится о схожести эхокардиографических данньос при
амилоидозе сердца и гипертрофической кардиомиопатии (правда, имеется в
виду типичная гипертрофическая кардиомиопатия с поражением левого желу¬
дочка). Упоминаний о том, что инфундибулярный стеноз может быть проявле¬
нием амилоидоза сердца, нами не найдено.Какое практическое значение имеет постановка нашей больной диагноза
гипертрофической кардиомиопатии? Это в первую очередь выбор наиболее
356 Кардиологияадекватного лечения, а также определение прогноза для больной и ее родствен¬
ников. Надо сказать, что методы лечения инфундибулярного стеноза и гипертро¬
фической кардиомиопатии во многом схожи. Медикаментозная терапия при
обоих заболеваниях напрашіена на расслабление гипертрофированной мышцы
желудочка и снижение градиента давления, подавление аритмий (в том числе
желудочковых, угрожающих жизни) и терапию развивающейся сердечной
недостаточности; всем трем целям служит назначение р-блокаторов. Терапия
при гипертрофшіеской кардиомиопатии лучше разработана — широко реко¬
мендуется использование верапамила или дилтиазема. В ряде исследований
с успехом применялись антиаритмики 1А класса с выраженным отрицатель¬
ным инотропным эффектом — дизопирамид и цибензолин. В частности, при
би вентрикулярном поражении после неэффективной терапии пропранолом
бьы использован цибензолин в дозе 200—300 мг/с>т, который позволит сни¬
зить градиенты давления в обоих желудочках примерно в 2 раза и поддержи¬
вать их на этом уровне в течение 8 мес; отдаленные последствия не изуча¬
лись. Оптимальное лечение гипертрофической кардиомиопатии с поражением
правого желудочка неизвестно. Терапия сердечной недостаточности при обоих
заболеваниях проводится по общим принципам, исключая нежелательность
назначения дигоксина.Методы хирургического лечения также во многом схожи: оно показано при
наличии клинической симптоматики (но без выраженной сердечной недоста¬
точности) в сочетании с градиентом более 50-70 мм рт.ст.:• трансаортальная или трансвенозная миотомия (резекция миокарда) в
области межжелудочковой перегородки (при инфундибулярком стенозе
она может проводиться транспульмоналъным доступом); при гипертрофи¬
ческой кардиомиопатии операция может дополняться протезированием
митрального клапана и является наиболее радикальной; роль этой опе¬
рации при инфундибулярном стенозе широко обсуждается — в качестве
показания рассматривают высокое давление в правом желудочке, превы¬
шающее системное;• при интактной межжелудочковой перегородке выполняют операцию по
Doty (или се правосторонний вариант), которая бьша предложена для под-
юіапанного аортального стеноза; результаты при инфундибулярном сте¬
нозе также хорошие (снижение градиента дашісния на клапане легочной
артерии в 3 и более раз); после операции может сохраняться функциональ¬
ный инфундибулярный стеноз;• чрескоронарная алкогольная аблация перегородки (ее искусственный
инфаркт) при наличии градиентов давления в любом из же.лудочков (с
целью снизить динамическую обструкцию выводных отделов);• наконец, при инфундибулярном стенозе разрабатывается баллонная дила-
тация инфундибулярной части с последующей имплантацией стального
стента; в результате падает градиент давления между правым и левым желу¬
дочками, возрастает сатурация кислородом, снижается частота аритмий,
но возможны рестенозы; процедура является альтернативой традиционной
паллиативной операции;
fAOsa 18. Подклапанный стеноз легочной артерии — врожденный порок.357• предложено использование двухкамерной кардиостимуляции (DDD) для
снижения градиента и синхронизации работы сердца при обоих заболева¬
ниях; интересно расположение электродов у больных с инфундибулярным
стенозом: один электрод (сенсорный в данном случае) традиционно уста¬
навливается в правое предсердие, а второй, стимулирующий, — в левый, а
не правый желудочек. В результате верхушка правого желудочка возбужда¬
ется раньше (из левого желудочка), чем его средняя гипертрофированная
часть, и градиент в правом желудочке снижается, т.е. стимулятор оказывает
определенное синхронизирующее действие.Необходимо подчеркнуть, что влияние всех перетасленных операций на
отдаленный прогноз заболеваний не установлено; они выполняются неболь¬
шому количеству больных и по-прежнему носят характер экспериментальных.Различия в терапии двух заболеваний начинаются на уровне профилактики
внезапной смерти. Если для гапертрофической кардиомиопатии этот вопрос
довольно хорошо разработан, то в отношении инфундибулярного стеноза
таких данных практически нет, но умирают больные чаше от прогрессирования
сердечной недостаточности; нередки случаи доживання до очень преклонных
лет. У нашей больной на сегодня практически нет маркеров высокого риска
внезапной смерти {табл. 18.3): из представленного списка она имеет лишь
наименее значимый признак (боль в фуди/одьтшка), остаются неустановлен¬
ными тип мутации и возможность индуцировать желудочковую тахикардию
при внутрисердечном электрофизиологаческом исслсдовашкш. Но необходимо
подчеркнуть, что значение выраженной гипертрофии правого желудочка и
правостороннего фадиента остается абсолютно неизученным.Наиболее эффективным методом профшшктики внезапной смерти при
гипертрофической кардиомиопатии является имплантация кардиоверте-
ра-дефибри^члятора, из препаратов рекомендуется использование главнымТаблица 18.3Определение риска внезапной смерти при гипертрофической кардиомиопатииПризнакКлассрекомендацийУровень доказа¬
тельностиОстановка сердца (или устойчивая ЖТ)IВСемейный анамнез ВСНаВОбморокиТТаВВыраженная ГЛЖ (>3 см)11авСнижение АД при нагрузкеПавГрадиент давления в ЛЖІПвНеустой^швая ЖТПавПароксизмальная МА111вМутации высокого рискатвИндуцируемая ЖТ/ФЖIIIсМитральная недостаточность (умеренная —
тяжелая)111сБоль в грули/одышкаUIс
358 Кардиологияобразом амиодарона(класс рекомендаций ПЬ, уровень доказательности В), и то
.1ишь для вторившей профилактики внезапной смерти. У нашей больной пока
стоит вопрос лишь об имплантации двухкамерного стимулятора (невозмож¬
ность проведения адекватной урежающей ритм терапии в связи с нарушениями
атриовентрикулярной проводимости).В заключение хочется подчеркнуть, что гипертрофическая кардиомиопатия
и инфундибулярный стеноз, которые чаше всего рассматриваются как раз¬
ные заболевания, во многом очень схожи {табл, 18.4): в обоих случаях имеет
место генетическая предрасположенность, нередки сочетания с другими гене¬
тически обусловленными аномалиями [гипертрофическая кардиомиопатия
может развиваться в рамках синдрома LEOPARD, синдрома Нунана (Noonan),
гликогенозов Ї, III типов, болезни Фабри, сочетаться с нейрофиброматозом,
микросфероцитозом, атаксией Фридрейха]; оба заболевания особенно часто
встречаются в Азии, особенно в Японии, имеют сходные клиническую карти¬
ну, эхокардиографические проявления, методы лечения. Едва ли такое сход¬
ство является случайным.Встает вопрос: не являются ли классическая гипертрофическая кардио¬
миопатия и инфундибулярный стеноз различными вариантами одного и того
же заболевания, при котором в результате наследственных или спорадических
мутаций развивается гипертрофия миокарда с пороком сердца или без тако¬
вого? На сегодня установлено, что оба заболевания имеют общий патогенез,
клинические проявления и могут одновременно встречаться у одного и того
же больною. Д.ЛЯ того чтобы говорить о единой нозологии, необходимо в
первую очередь выяснить гснстические механизмы инфундибулярного сте¬
ноза, на новом уровне из>^ить его морфологию, а также вьшвить факторы,
определяющие прогноз при данном заболевании. Практический вывод из
нашего сообшения звучит следующим образом: каждый случай изолирован¬
ного инфуадибулярного стеноза (возможно, и при его сочетаниях с другими
врожденными анома^іиями сердца) может оказаться проявлением гипертрофи¬
ческой кардиомиопатии.Не исключено, что в дальнейшем инфундибулярный стеноз займет место
в классификации гипертрофической кардиомиопатии. Интересно вспомнить,
что на рубеже Х1Х-ХХ вв., когда появились первые описания субаортального
мышечного стеїюза, это заболевание трактовали как врожденный порок серд¬
ца. Позднее его стали называть «идиопатическим гипертрофическим субаор-
тальным стенозом», и лишь в 1957 г W. Brigden рассмотрел это заболевание
как один из вариантов первичного поражения миокарда, который мы сегодня
называем гипертрофической кардиомиопатией.Комментарий А.В. Недоступа — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукДействительно, мы имеем дело с достаточно редким вариантом течения
гипертрофической кардиомиопатии. Постоянно приходится говорить о том,
что наши методы диагностики несовершенны: неоднократное ультразвуко¬
вое исследование сердца, выполнявшееся больной, не позволяло поставить
Глаьа 18. Подклапанный стеноз легочной артерии — врожденный порок... 359Таблица 18.4Сходства и разлияия гипертрофической кардиомиопатии и инфундибулярного стенозаПризнакгкмпИнфуцдибулярный стенозНаследственныйхарактерОколо 50%, в остальных слу¬
чаях — споради^іеские муга-
гщиЧастота неизвестнаВрожценный характерИзвестна врождепіїая формаВ большинстве случаевРаспространенность0,02-0,2 на 10000,01-0,04ГеографияАзия, Тихий океан (в
Японии — 23% ССЗ)ЯпонияПол, расаЧаще мужчины, не негрыДанных нетГенетикаГены саркомерных белков,
тяжелых р-цепей, легких
цепей миозитш, тропонина
(хромосомы 1, 14, 15)У мышей — три сом ИЯ 13Сочетанные врожден¬
ные состоянияСиндром LEOPARD, нейро-
фиброматоз, микросферони-
тоз, атаксия Фридрейха, стш-
лром Noonan, болезнь Фабри,
гликогснозы I и 111 типовВ большинстве случаев —
дефект МЖП, реже — тетрада
Фалло, открытый Боталоп
проток, транспозиция кр\тт-
ных сосудов, синдром NoonanБиопсияГипертрофия, дезоргатіиза-
ЦШ1, фиброзДанных нетКлинические сим¬
птомыОдышка, обмороки, юлово-
кружения, стенокардия, ЖНР,
МА, АВ-блокады, эмболииОдышка, обмороки, стено¬
кардия, наджелудочковые
аритмии, ТЭЛАПараметры проводи¬
мостиДостаточно типичныеЧастота неизвестнаПpи^шны смертиФЖ, эмболии, ХСН, ИЭБ основном — ХСНДанные ЭхоКГ
(помимо гипертро¬
фии)Аномальное систолическое
движотие передней створки
МК, флоттирование створок
АКАномальное сисюлическое
движение, фло-ггирование
створки, раннее закрытие ЛКМеликамснто'знаятерапия[}-Блокаторы, антагонисты Са,
антиаритмики 1А, III классовр-БлокаторыХирурі ическое лече¬
ниеМиотомия, алкогольная абла¬
ция МЖПМиотомия, алкогольная абла¬
ция, стентиропаниеОсобГіїе показания к
имплантации DDDСнижение градиента в левом
желудочкеСнижение фадиента в правом
желудочкеПрогнозОпределяется риском ВСОтносительно благоприятныйдиагноз гипертрофической кардиомиопатии, это лишний раз говорит о боль¬
шой субъективности метода и зависимости результатов от того, в чьих руках
он находится. Каковы псрспектгивы лечения у нашей больной? Имеет смысл
пытаться восстановить синусовый ритм (тромбов в предсердиях не выявле¬
но), в том числе с помош,ью аблации перешейка правого предсердия (хотя
трепетание предсердий у больной не вполне тииичное, процедура может не
360 Кардиологияиметь успеха), поскольку подобрать оптимальную урежшошую терапию будет
трудно. При неудачах в восстановлении и удержании ритма понадобится
продолжение урежающей терапии, что потребует, скорее всего, имплантации
ЭКС. Хирургические мс'годики лечения гипертрофической кардиомиопатии,
по-видимому, на сегодняшний день недостаточно эффективны. Кроме того,
у больной, несомненно, есть миоперикардит, который тоже требует лечения
(противовосналі-ггельного).Комментарий BA Сулимова — заведующего кафедрой факультетской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наук, проф.Да, речь идет о зеркштьном варианте гипертрофической кардиомиопатии
справа. Такая постановка вопроса, конечно, не нова, но в данном случае мы
впервые, пожалуй, столкнулись с подобным больным, увидели такой вари¬
ант гипертрофической кардиомиопатии на реальном клиническом примере,
причем диагноз был поставлен в клинике во многом вопреки разноречи¬
вым данным ультразвукового исследования сердца. Что касается лечения,
то попытки устранения ірепетания предсердий тем или иным способом не
имеют большого смысла, поскольку удерживать синусовый ритм практи¬
чески нечем: кордарон оказался недостаточно эффективным, а назначение
антиаритмичсских препаратов 1 класса в данном случае противопоказано
в связи с наличием выраженной гипертрофии миокарда. Действительно,
интересен вопрос о расположении электродов в случае имплантации больной
постоянного ЭКС. По-видимому, желудочковый электрод должен распола¬
гаться в области межжелудочковой перегородки, последовательность распро¬
странения возбуждения при этом сильно не изменится.P.S. После вьтиски из клиники больная обратилась в Парный центр сер¬
дечно-сосудистой хирургии им. А.Н. Бакулева, где ей 6buja выполнена имплан¬
тация ЭКС в сочетании с радиочастотной аблацией АВ-соединения.ЛИТЕРАТУРАКоровина ЕА,, Медвежиикова Т.Н., Васильев В.В. Случай правосторонней
гипертрофической кардиомиопатии // Тср. архив. — 1996, 68 (4): 82-83.Миррахимов М. М., Руденко Р.И., Мейманалиев Т.С. Правосторонние гипер¬
трофические кардиомиопатии // Тер. архив. — 1988. — № 7. — 20-24.Новиков Ю.И., Миан С.Л., Стулова МЛ. Гипертрофртческая кардиомиопатии и
вирусный, идиопатический миоперикардит // Клин. мед. — 2000. — № 78 (9). —
С. 15-21.Adachi S., Amano J., lio R. et ai РофЬугіа cutanea tarda with constrictive peri¬
carditis in a family // Jpn. Heart J, 1997 Sep; 38 (5): 749—753.Akcoral A., Oran B., Tavli V. et al. Transient right sided hypertrophic cardiomyo¬
pathy in an infant bom to a diabetic mother I I Indian J. Pediatr., 1996 Sep-Oct; 63
(5): 700-703.
Глава 18. Подклапанный стеноз легочной артерии — врожденный порок... 36ІAngelkov L., Trajic S., Popovich L. et al. Acute effects of DDD pacing in patients
with pulmonary infundibular stenosis // Am. J. Cardiol. 1999, Jul 1; 84 (1): 1 IT¬
US, A9.Brigden W. Uncommon myocardial disease 11 Lancet, 1957 Feb; 2; 1179-1183.CheslerE., MllhaA.S., Matisson R.E., Rogers M.N, Subpulmonic stenosis as a result
of noncalcific constrictive pericarditis // Chest. 1976 Mar; 69 (3): 425-427.Choi B.R., Lim Y.H., Joo K.B. et al. Camptodactyly, arthropathy, coxa vara, peri¬
carditis (CACP) syndrome: a case report 11 J. Korean Med. Sci. 2004 Dec; 19 (6):
907-910.DeLlne J. М., Cable D.G. Clustering of recurrent pericarditis with effusion and con¬
striction in a family // Mayo Clin. Proc. 2002 Jan; 77 (1): 39-43.Gibbs J.L., Uzun O., Blackburn M.E. et al. Right ventricular outflow stent implan¬
tation: an alternative to palliative surgical relief of infundibular pulmonary stenosis j j
Heart, 1997 Sep; 78 (3): 320.Иіат G., Hamada М., Shigematsu Y. et al. Attenuation of biventricular pressure
gradients by cibenzoline in an 18-year-old patient with hypertrophic obstructive car-
diomyoparhy // Circ. J., 2002 Dec; 66 (12): 1173-1175.khinose Т., Nakazato Y., Mivano H. et al. Severe infundibular pulmonary stenosis
and coronary artery stenosis with ventricular tachycardia 24 years after mediastinal
irradiation // intern, Med., 2005, Sep; 44 (9): 963—966.Kronik G., Fitscha P., Slany J,, Mosslacher H. Echocardiographic diagnosis of sub¬
pulmonic obstruction in hypertrophic cardiomyopathy (a case report) // Z. Kardiol.
1979 Jun; 68 (6): 415-418.Mills P. , Wolfe C., Redwood D. et al. Non-invasive diagnosis of subpulmonary out¬
flow tract obstruction// Br. Heart J. 1980 Mar; 43 (3): 276-283.MomerS., Heliman U., SuhrO.B. etal Amyloid heart disease mimicking hypertro¬
phic cardiomyopathy //J. Tntem. Med. 2005 Sep; 258 (3): 225—230.Mozaffarian D,, Caldwell J.H. Right ventricular involvement in hypertrophic car¬
diomyopathy; a case report and literature review // Clin, Cardiol. 2001 Jan; 24 (1):
2-8.Park S.H., Park K.S., Park H.G. et al Hypertrophic obstructive cardiomyopathy
with infundibular stenosis treated by alcohol ablation therapy // J. Korean Med. Sci.
2003 Aug; 18 (4): 585-588.Take М., Sekiguchi М., Hiroe М., Hirosawo K. A clinicopathologic study on a cause
of idiopathic cardiomyopathy and arrythmia and conduction disturbance employing
endomyocardial biopsy // Heart Vessels Suppl. 1985; 1: 159-164.Vuillemin М., Pexieder Т., Winking H. Pathogenesis of various forms of double
outlet right ventricle in mouse fetal trisomy 13 // int. J, Cardiol. 1991 Nov; 33 (2):
291-304.
Глава 19«ИДИОПАТИЧЕСКАЯ» ТРИКУСПИДАЛЬНАЯ
НЕДОСТАТОЧНОСТЬ И «НЕМОЕ» ПРЕДСЕРДИЕ —
НОВЫЙ ГЕНЕТИЧЕСКИЙ СИНДРОМ (ПРЕДСЕРДНАЯ
КАРДИОМИОПАТИЯ С НАРУШЕНИЯМИ
ПРОВОДИМОСТИ)О.В. Благова, Е.В. Заклязьминская, AS. НедоступКолргчсство генетически детерминированных заболеваний (в том числе
моногенных) огромно — клиницистам терапевтического профиля известна
(к основном теоретически) лишь малая их часть. Тем не менее возможность
обнаружения одного из таких, в том числе очень редких, заболеваний всегда
существует — и шансы растут по мере повышения специализации врача и
медицинского учреждения в целом. Мы Представляем наблюдение, в котором
клиническая симптоматика (тяжелая недостаточность трехстворчатого клапа¬
на, потребовавшая его протезирования, в сочетании с серьезными нарушения¬
ми ритма и проводимости и «немым предсердием») не находила объяснения в
рамках известных нам заболеваний, что с учетом относительно молодого воз¬
раста пациентки послужило поводом для обращения к клиническому генетику.
В результате был поставлен диагноз заболевания (подтвержденный генетиче¬
ски и морфологически), описаний которого в России еще не было; обследова¬
ны дочери больной, у которых выявлена сходная мутация, что требует дальней¬
шего наблюдения. Обсуждаются вопросы этиологии изолированных пороков
трехстворчатого клапана, синдрома «немого предсердия», роль отдельных
генов в происхождении различных клинических вариантов поражения сердца.Больная С., 45 лет, впервые поступила в Факульчстскую тератіевтическую
клинику им. В.Н. Виноградова на дежурную койку в отделение патологии суста¬
вов в апреле 2005 г, с жалобами на одашку при умеренных физшіескпх нагрузках
(подъем но лестнипс на один этаж, ходьба по ровной местности на расстояние
до 500 м), отеки стоп, голеней и бедер, перебои в работе сердца, обшую слабость,
быструю утомляемость, головокружение при ходьбе, чувство вздутия живота.Из семейного анамнеза известно, что мать больной умерла в 65 лет от инфар¬
кта миокарда, осложнившегося отрывом хорды митрального клапана; паци¬
ентка по профессии — врач-офтальмолог, имеет двух дочерей 14 лет (разнояй¬
цевые близнецы); с 20 до 40 лет курила по 10 сигарет в день; в 1965 г (в возрасте
5 лет) перенесла тонзиллэктомию, в 2002 г. — правостороннюю флебэктомию,
в 2000 г. (в возрасте 40 лет) диагностирован узловой эутиреоидный зоб.Анамнез заболевания (рис. 19. /). До 5 лет страдала частыми ангинами, состоя¬
ла на учете у ревматолога; в 5 лет произведена тонзиллэктомия, с у^іета снята.
Глава 19. «Идиопатическая» трикуспидальная недостаточность...363В возрасте 18 лет развился артрит мелких суставов кистей (проксимальных
межфаланговых и пястно-фаланговых). Не обследовалась, артрит купировался
самостоятельно. В дальнейшем чувствовала себя удовлетворительно. С 28 лет
стала ощущать эпизодические сердцебиения. В 2000 г. (в возрасте 40 лет) без
видимой причины развился приступ учащенного сердцебиения, во время кото¬
рого на ЭКГ зафиксирована АВ-узловая тахикардия с ЧСС около 210 уд/мин
{рис. 19.2).Приступ был к>Т1ирован, обследовалась в диагностическом центре по месту
жительства: при суточном мониторировании ЭКГ по Холтеру выявлено около
10 тыс. желудочковых экстрасистол, которые больная omymajia слабо (судить
о нарушениях ритма в более ранний период не представляется возможным).
При ЭхоКГ отклонений от нормы выявлено не было; диагностирован узло¬
вой эутиреоидный зоб. Антиаритмическая терапия не назначалась. Приступы
АВ-узловой тахикардии повторно возникали в 2001 г. и в январе 2002 г., сопро¬
вождались появлением холодного пота, цианозом лица, выраженной общейiitангины
полиартрит —АВ-узловаятахикардияжелудочковаяэкстрасистолиябрадикардия
отеки ног 1965 1978 2000 2001 2002 2.2005 4.2005
йодышкаЭхо-КГлечениек к і???ЧСС 40/минмедленный АВ-ритмNТН IIHV ст.тонзиллэктомияРис. 19.1. Анамнез больной С., 45 летатенолол флебэктомия диуретики
25 мг/сут нолипрел3*Ц||' '•f і И ' *• . ч ,Рис. 19.2. Электрокардиограмма больной С., зафиксированная во время приступа серд¬
цебиения. Скорость записи 25 мм/с. Пояснения в тексте
364 Кардиологияслабостью; в межприступный период беспокоили перебои в работе сердца.
Была сделана попытка назначения атенолола в небольшой дозе (25 мг/сут), что
привело к развитию синусовой брадикардии до 40 уд/мин. Атенолол был отме¬
нен, от дальнейших попыток антиаритмії^іеской терапии отказались.С 2002 г. стали отмечаться отеки ног, которые больная расценила как про¬
явление хронической венозной недостаточности в рамках варикозного расши¬
рения вен нижних конечностей; в том же году проведена флебэктомия справа,
однако отеки сохранялись и постепенно нарастали. Медикаментозная терапі-ія
не проводилась. В 2003 т. повторно проведено холтеровское мониторирование
ЭКГ, во время которого фиксировались частая жeJ^yдoчкoвaя и наджелудочко-
вая (около 5 тыс.) экстрасистолия, а также эпизоды АВ-диссоциации. На ЭКГ
периодически определялся ускоренный узловой ритм. Обш;ее самочувствие
оставалось удовлетворительным.Значительное ухудшение состояния — с 04.02.2005 г, когда появилась
выраженная одышка, на снятой амбулаторно ЭКГ зафиксирован узловой
ритм с ЧСС 46 уд/мин. На следующий день отметила ^іувство вздутия живо¬
та. Самостоятельно принимала верошпирон 100 мг/сут с незначительным
положительным эффектом. На 10-й день после появления одышки была
госпита/шзирована в Городскую клиническую больницу № 23 г. Москвы, где в
качестве наиболее вероятной причины ухудшения состояния рассматривалась
тромбоэмболия легочной артерии (ХЭЛА), однако верифицировать этот диа¬
гноз не удалось. При ЭхоКГ впервые была выявлена трикуспидальная недо¬
статочность ПТ—TV степени, на ЭКГ сохранялся медленный узловой ритм.
Состояние расценивалось как посттромбоэмболический синдром (?), право¬
желудочковая недостаточность. Была начата терапия дигоксином, однако в
связи с урежением ритма до 40 уд/мин препарат отменен. Проводилась терапия
нолипрелом по 1 таб./сут, фуросемидом 40 мг ежедневно, в результате которой
состояние несколько улучшилось; амбулаторно продолжала прием фуросе-
мида 40 мг ежедневно, однако сохранялись одышка при небольших физиче¬
ских нагрузках, отеки ног, перебои в работе сердца, обшая слабость. С этими
жа^юбами госпитализирована в Факультетскую терапевтическую клинику им.
В.Н. Виноградова в апреле 2005 г.При осмотре состояние больной расценивалось как среднетяжелое, консти¬
туция астеническая. Обращали на себя внимание бледность кожных покровов,
выраженная сосудистая сеть на лице, отеки до нижней трети бедер. Число
дыханий составляло 18/мин, аускультативно дыхание имело жесткий оттенок,
хрипы не выслушивались. ЧСС составляла 46/мин, на фоне правильного ритма
выслушивались единичные экстрасистольт; тоны сердца были приглушены,
определялся систолический шум с эпицентром у основания мечевидного
отростка, АД 150/90 мм рт.ст. Перкуторных признаков асиита не было, гепато-
спленомегалии не выявлено.В общем анализе крови обратила на себя внимание лишь умеренная гипох-
ромная анемия (НЬ 9,8 г%, эритроциты 4,2 млн, цветовой показатель 0,7),
лейкоциты 3,6 тыс. (нейтрофилы — 49%, лимфоциты — 34%, эозинофилы —
2%, моноциты — 14%, базофилы — \%), тромбоциты 167 тыс., СОЭ 10 мм/ч;
Глава 19. «Идиопатическая» трикуспидальная недостаточность...365оставались нормальными уровень фибриногена и другие показатели коагуло-
граммы. Биохимический анализ крови подтвердил железодефицитный характер
анемии (железо — 24 мкг/дл, общая железосвязывающая способность сыво¬
ротки крови — 307 мг/дл, процент насыщения трансферрина железом 5,5),
других отклонений от нормы не выявлено, в крови отсутствовали СРБ и РФ,
IgA — 289 мг/дл, IgM — 65 мг/дл, IgG — 920 мг/дл.В общем анализе.мочи — удельный вес 10І2, белок — 0,70%о, осадок в преде¬
лах нормы, суточная потеря белка состави^та 500 мг.На ЭКГ (рис. 19.3) — уатовой ритм с ЧСС 40/мин, изменения сегмента ST
напоминали дигиталисные, но, поскольку длительность приема дигоксина
в Городской клинической больнице № 23 г. Москвы не превышала I сут, эти
изменения расценены как неспецифические. При суточном мониторироеа-
нии ЭКГ по Холтеру, проведенном на фоне терапии коринфаром 30 мг/сут,
определялись: узловой ритм; короткие участки наджеяудочкового (синусово¬
го?) ритма с АВ-блокадой 1 степени {PQ 0,28 с) с ЧСС около 80/мин; эпизод
ускоренного суправентрикулярного ритма с ЧСС около 95/мин (11 комплек¬
сов QRS): ЧСС днем 40-89/мин (ср. 49/мин), ночью — 39-72/мин (ср. 43/
мин), максимальный RR 1,52 с; единичные наджелудочковые экстрасистолыі?ГГШ'ПAiii iJvL,L ^ -Is li ' L ''T'T'«.;„L■44...i.•да-і’"П„iL/'ж: iize; «i:]^ i ! l:'f І5"Г г rl;" : i m ‘Vr t l'n : ii Mr i hT, ; i.. L,. I. lJ.J.iXi.. i ...i..;. -j--;... ..............i..,.'-r-vi- ; ГТРис. 19.3. Электрокардиограмма больной С. (апрель 2005 г.). Скорость записи 25 м/с.
Пояснения я тексте
366 Кардиологияи политопные желудочковые экстрасистолы, всего 1100, иногда по типу би-,
тригеминии; 3 парные, I триплет; фоновая депрессия сегмента STдо 0,1 мВ.При ЭхоКГ в первую очередь обращало на себя внимание выраженное
расширение правых отделов сердца — объем правого предсердия составил
150 \Li (левое предсердие 4,5 см, объем 75 мл), размер правого желудочка —4,1 см. Подтверждено наличие трик>^сггидалъной регургитации ПТ—TV степени
при отсутствии изменения створок клапана, легочной гипертензии (СДЛА
49 мм рт.ст., ДДЛА 18 мм рт.ст.), нижняя полая вена была значительно рас¬
ширена (не спадалась). КДР левого желудочка (4,6 см) и толщина его стенок
(8-9 мм) оставались нормальными, ФВ левого желудочка была лишь незна¬
чительно снижена (53%), имелись признают его диастолической дисфункции
П типа TV степени (Е/А = 4,02). Митральный и аортальный клапаны не были
изменены. Несколько позже исследование повторно проведено в НЦССХ
им. А.Н. Бакулева — дополнительно был выяштен краевой фиброз створок
трикуспидального клапана и небольшой пролапс митрального клапана с регур-
гитацией I степени.Для уточнения характера поражения трикуспидального клапана была про¬
ведена чреспищеводная ЭхоКГ, по данным которой створки трикуспидального
клапана были уплотнены, передняя пролабировала в правое предсердие. Было
сделано заключение о наличии выраженной дилатации правых камер сердца,
обусловленной тяжелой недостаточностью трикуспидального клапана, наибо¬
лее вероятной причиной которой являлся частичный отрыв хордальных нитей.Д.чя дальнейшего уточнения характера поражения К;іапана в НЦССХ
им. А.Н. Бакулева бьыа выполнена МРТ сердца (рис. 19.4), по данным кото¬
рой сердце увеличено в размерах (кардиоторакальный индекс 57%), в первую
очередь за счет выраженного увеличения правого предсердия (его размеры
6,9x6,3 см), имелись признаки трикуспидальной недостаточности III степе¬
ни и митральной недостаточности (между I и ТТ степенью); левое предсердие
4,6x7,2 см, левый желудочек: КДР 4,4 см, КС? 3,6 см; правый желудочек:
КДР 4,8 мм, КС? 4Д см, выводной тракт расширен до 3,4 см, без признаковРис. 19,4. МРТ сердца болыгой С. Пояснения в тексте
Глава 19. «Идиопатическая» трикуспидальная недостаточность... 367истончения миокарда и локального гипокинеза передней стенки, толщина
стенки 4 мм в диастолу, 6—7 мм в систолу; ствол легочной артерии незначи¬
тельно расширен (2,7 см), расширены полые вены (верхняя — 2,5x2,6 см,
нижняя — 2,6x4,1 см); определялся дискинез межжелудочковой перегородки,
более выраженный в нижней трети. Впервые бьши вы>1влены также уголтцение
и уплотнение перикарда преимущественно в области верхушки сердца (4 мм),
а также по свободной стенке правого желудочка и боковой стеикс левого желу¬
дочка, плевро-перикардиальные спайки в обоих легких. На основании этих
данных было сделано заключение о возможном наличии у больной консірик-
тивного фибринозно-спаечного перикардита.При УЗИ органов брюшной полости свободной жидкости не обнаружено, раз¬
меры печени и селезенки оставались в пределах нормы, выявлена дисформия
желчного пузыря. С учетом того, что в анамнезе имелся эпизод, подозритель¬
ный на ТЭЛА, было проведено ультразвуковое допплеровское исследование вен
нижних конечностей, признаков тромбоза не выявлено; справа определялось
состояние после флебэктомии, слева — несостоятельность клапана соустья и
расширение ствола большой подкожной вены. Эти изменения не могли стать
причиной выраженных симметричных отеков.Таким образом, при несомненной трикуспидальной недостаточности в
сочетании с весьма специфичными нарушениями ритма и проводимости у
относительно молодой женщины трудность состояла в установлении нозологи¬
ческого диагноза- В первую очередь необходимо было исключать заболевания,
которые моїут приводить к развитию органической трикуспидальной недоста¬
точности, т.е. к поражению створок клапана и клапанного аппарата.1. При ревматизме трехстворчатый клапан поражается значительно реже
митрального и аортального, но все же не исключительно редко (примерно у
20% умерших больных). Однако изолированное поражение трехстворчато¬
го клапана встречается действительно редко. У больной до 5 лет отмечались
частые ангины, но в последующие почти 40 лет никаких признаков деком¬
пенсации по большому кругу не отмечалось (не было выявлено порока и при
ЭхоКГ в 2000 г.). Совершенно нетипично для ревматического порока отсет-
ствие мерцательной аритмии (при большом правом предсердии) и появление
вместо этого стойкого узлового ритма. Отсутствуют даже минимальные при¬
знаки стеноза правого атриовентрикулярного отверстия, которые делали бы
диагноз ревматизма гораздо более вероятным.2. Врожденная трикуспидальная недостаточность в чистом виде не встре¬
чается, она описана при низком расположении клапана (в полости правого
желудочка), в том числе у больных с аномалией Эбштейна, при сочетании
расщепления передней створки трикуспидального клапана с дефектом меж-
предсердной перегородки. Недавно описаны уникальные слу^іаи врожденной
трикуспидальной недостаточности в сочетании с частичным отсутствием
перикарда справа и вторичного разрыва передней створки трикуспидального
клапана у больного с врожденным отсутствием перикарда слева, оба успеш¬
но прооперированы. Трикуспидальную недостаточность выявляют примерно
у трети больных с тетрадой Фалло, она вторична по отношению к легочной
368 Кардиологиярегургитации. Диагноз врожденного порока исключается достаточно благопо¬
лучным анамнезом и данными ЭхоКГ (в 2000 п все показатели были в норме).3. Инфекционный эндокардит с поражением трихуспидального клапана
встречается не только у наркоманов, но и после длительной катетеризации,
других манипуляний на венах; в подобных случала из крови нередко высева¬
ется золотистый стафилококк. Отсутствие лихорадки, сплеііомегалии, увели¬
чения СОЭ, каких-либо острофазовых, иммунных нарушений и вегетаций на
клапане (по данным чреспищеводной ЭхоКГ) при том, что антибактериальная
терапия не проводилась, позволило исключить этот диагноз у нашей больной.4. Пролапс трикуспидааьного клапана. При чреспищеводной ЭхоКГ как
будто был выявлен пролапс передней створки, но он крайне редко приводит
к столь выраженной регургитации; экстрасистолия и предсердные аритмии
довольно характерны для больных с пролапсом, но совершенно нетипичны
фубые нарутиения проводимости.5. Инфаркт сосочковых мышц правого желудочка. У больной в анамнезе
действительно отмечена резкая декомпенсация по большо\іу кругу кровоо¬
бращения с появлением трикуспидальной недостаточности, однако на тот
момент состояние было расценено как ТЭЛА, данных за инфаркт не было.
Чреспишсводная ЭхоКГ не позволяет исключить отрыв сосочковой мышиы
передней створки, но однозначного заключения не даст. Ретроспективно под¬
твердить инфаркт сосочковой мьппцы вообше довольно сложно. У пациентки
отсутствуют не только типичные симптомы ишемии, но и факторы риска коро¬
нарного атеросклероза. Если рассматривать более редкие причины возможного
инфаркта, то в первую очередь необходимо исключить антифосфолипидный
синдром, о котором всегда следует дултать при неясной патологии клапанов
ссрдтта.6. Антифосфолипидный синдром. При данном состоянии развитие трикуспи¬
дальной недостаточности может быть вторичным — как ответ на повторные
тромбозы мелких ветвей легочных артерий, всдутцие к развитию выраженной
легочной гипертензии- Описаны комбинированное поражение трикуспидаль-
ного клапана — относительная недостаточность с наложением тромботических
вегетаций на створках, а также случаи изолированного поражения трикуспи-
дального клапана у больных с первичным антифосфолипидным синдромом и
тромбозами мелких легочных артерий. У больной имелся эпизод, подозритель¬
ный на ТЭЛА (при этом источник эмболии не выявлен, и можііо предполагать
тромбоз in situ), но для диагноза антифосфолипидного синдрома этого недо¬
статочно: отсутствовали тромбозы иных локализацией, патология беремен¬
ности, снижение уровня тромбоцитов. Не укладываются в картину первичного
антифосфолипидного синдрома и нарушения проводимости. Им можно было
бы найти объяснение в рамках вторичного антифосфолипидного синдрома, но
предполагать системггую красную волчанку или ревматоидный арірит со столь
необычным эндокардитом у нас тоже нет оснований.7. Гораздо труднее исключить миокардит (хронический или перенесен¬
ный в прошлом) с преимущественным поражением правых отделов сердца.
Трикуспидальная недостаточность в этом случае носит уже относительный
Глава 19, «Идиопатическая» трикуспидальная недостаточность... 369характер (является следствием растяжения фиброзного кольца клапана).
В пользу вялотекущего или перенесенного миокардита могут свидете.'іьство-
вать нарушения ритма и проводимости, утолщение и уплотнение листков пери¬
карда, плевроперикардиальные спайки поданным МРТ. В литературе описаны
подобные случаи, в частности развитие так называемой правожелудочковой
кардиомиопатии у молодой женщины во время беременности, закончившейся
спонтанным абортом на 2-м месяце: в биоптате были выявлены несомненные
признаки воспаления. Сообщается о морфологически подтвержденном изоли¬
рованном «предсердном» миокардите у спортсмена с предсердной тахикардией
и синдромом слабости синусового узла. В другом сообщении воспаление мио¬
карда предсердий у двух больных с предсердной тахикардией также было под¬
тверждено биопсией, причем в желудочках воспалительные изменения отсут¬
ствовали, а у одного из больных бьши выявлены антитела к ЕСНО-вирусам,
Однако такой миокардит обычно не приводит к развитию сердечной недо¬
статочности (если не возникает постоянная форма мерцательной аритмии) и
в целом протекает достаточно благоприятно. В нашем случае отсутствовала
связь дебюта заболевания с инфекцией; тем не менее окончательно исключить
атипичный миокардит не представлялось возможным до проведения биопсии
миокарда.8. В то же время необходимо было исключать и более редкие причины кар¬
диомиопатии. В частішсти, амилоидоз правого сердца с поражением трехствор¬
чатого клапана. Амилоидоз может протекать не только с клинической карти¬
ной рестриктивной кардиомиопатии, но и в форме изолированного поражения
предсердий, которое проявляет себя только нарушениями ритма (наджелудоч-
ковой экстрасистолией и мерцательной аритмией), иногда в сочетании с нару¬
шениями проводимости. Порсіженис сердца наиболее характерно д.тя первич¬
ного (AL) и семейного амшюидоза, клиническая картина которого чаще всего
формируется уже после 40 лет. Известна мутация гена транстирентина (пре-
альбумина), при которой встречается семейный амилоидоз с изолированным
поражением сердца, РСлапанный вариант амилоидоза сердца является одним из
самых редких и проявляется, как правило, митральной недостаточностью.Биопсия слизистых оболочек прямой кишки и десны на амилоид, проведепная
у больной, дала отрицательный результат; при ЭхоКГ отсутствовали призна¬
ки утолщения клапанов, межжелудочковой и межпредесрдной перегородок,
стенок желудочков, однако до проведения биопсии миокарда нельзя было
окончательно исключить изолированный амилоидоз правого предсердия (с
поражением клапана?). Для саркоидоза изолированное поражение сердца
нехарактерно (патологии внутригрудных лимфоузлов у больной выявлено не
было). Типичные для гемохроматоза стойкие нарушения обмена железа также
не обнаружены.9. Амилоидоз трехстворчатого клапана описан и как осложнение карци-
ноидпого синдрома с локализацией первичной опухоли в двенадцатиперстной
кишке. Поражение эндокарда при карциноиде развивается и без амилоидоза
и обусловлено прямым воздействием 5-гидрокситриптамина, который, про¬
ходя из печеночных метастазов в кровоток, взаимодействует только с правыми
370 Кардиологияотделами сердца. Поражение сердца диагаостируют примерно у 3% больных
карциноидом, причем более типично развитие стеноза. Основные симптомы
данного заболевания (сыпь, диарея, бронхоспазм) у больной отсутствовали.10. Необходимо исключать также опухоли сердца с вовлечением правых
отделов и трикуспидального клапана, которые развиваются как раз в среднем
возрасте: аншосаркома сердца, лейомиоматоз (первичная опухоль в мочевой
системе) с метастазом в трехстворчатый клапан. Данные МРТ позволили
исключить диагноз опухоли сердца.11. Примерно у 0,1% госпитализированных по поводу травмы описывают
травматическую трикуспидальную недостаточность, связанную с отрывом
папиллярных мышц передней створки или разрывом хорд. Соответствующий
анамнез у больной отсутствовал; кроме того, трудно объяснить травмой нару¬
шения проводимости и аритмии.12. Выявление при МРТ сердца (и только при МРТ) утолщенных до 4 мм
и уплотненных листков перикарда требовало исключения констриктивного
перикардита, при котором закономерно развитие декомпенсации по боль¬
шому кругу. Однако отсутствовали характерные для данного заболевания
симптомы.13. В клинической практике наиболее часто встречаются случаи относи¬
тельной недостаточности трикуспидального клапана, связанной с легочной
гипертензией любого происхождения. В нашем случае легочная гипертензия
носила явно вторичный характер; она развилась через много лет после мани¬
фестации нарушений ритма и проводимости, и какие-либо внсссрдечиые при¬
чины для нее отсутствовали.14. Наконец, описаію развитие недостаточности атриовентрикулярных
клапанов на фоне длительного приема противопаркинсонического препарата
перголида, который больная никогда не принимала.Таким образом, нельзя было уверенно исключить лишь два заболевания —
миокардит и амилоидоз сердца. Если допустить отрыв хорды, то нроисхожаїение
его оставалось непонятным, как и нарушения ритма и проводимости, которые
не могли бъггь объяснены лишь дилатацией предсердия. Сама выраженная
дилатация правого предсердия, наиболее ярко описанная при МРТ, несколько
выходила за рамки банальной трикуспидальной недостаточности. Выраженные
нарушения проводимости заставляли предполагать и наследственный характер
патологии, однако оставалось непонятным поражение правьгх отделов сердца
(врожденные АВ-блокады могут сочетаться с миодистрофиями и картиной
дилатационной кардиомиопатии с дилатацией в первую очередь левых отде¬
лов сердца). Идиопатические АВ-блокады (болезни Лева и Ленегра) носят
дегенеративный характер и протекают изолированно (без поражения миокар¬
да). Кардиохирург из Российского научного центра хирургии РАМН им. акад.
Б.В. Петровского расценивал поражение сердца как аритмогенную кардиомиопа-
тию, что могло обсуждаться с учетом выраженной правожелудочковой недоста¬
точности и нарушений ритма (максимальное число экстрасистол 10 тыс./сут), но
не объясняло первичного (по-видимому) характера поражения клапана и грубых
нарушений проводимости (к этому предположению мы еше вернемся).
Глава 19. «Идиопатическая» трикуспидальная недостаточность... 371Диагноз, который бьш поставлен больной, был построен по синдромалыю-
му принципу: хроническая сердечная недостаточность (правожелудочковая),
IV функциональный класс по NYHA, класс С но АН А. Недостаточность грику-
спидального клапана (регургитаиия IV степени). Частичный отрыв хорд перед¬
ней створки трикуспидального клапана? Диастолическая дисфункция левого
желудочка. Нарушения сердечного ритма и проводимости: АВ-узловой ритм,
суправентрикулярная и желудочковая экстрасистолия. Хроническая железоде¬
фицитная анемия.Проводилась терапия фуросемидом 40 мг по 1 таб. ежедневно, веротппи-
роном 25 мг по 2 таб. 2 раза в день, престариумом 4 мг по 1 таб. и сорбифе-
ром-дурулес по 1 таб. 2 раза в день. Однако у больной имелись абсолютные
показания к оперативному в.мешательству, в связи с чем она была направлена в
НИССХ им. А.Н. Бакулева.В отделении хирургического лечения тахиаритмий (руководитель — член-
корр. РАМН, проф. А.Ш. Ревишівили) НЦССХ им. А.Н. Бакулева доїтолни-
тельно было выполнено внутрисердечное электрофизиологическое исследование
сердца. При стиму^тяции предсердий тахикардия не индуцировалась, выявлено
полное отсутствие электрической и механической активности правого пред¬
сердия, паузы после стимуляции достигали 5 с. При стимуляции желудочков
тахикардия также не бьыа индуцирована, установлен временный эндокарди-
альный электрод. 9 июня больной было выполнено протезирование трику¬
спидального клапана с тромбэктомией из ушек левого и правого предсердий.
Таким образом, был установлен источник возможной ТЭЛА (ранее ни одно
из исследований тромбоза предсердий не выявля^ю). Через неделю, 16 июня,
имплантирован электрокардиостимулятор SS1-3200 в режиме WIR (поскольку
стимулировать предсердия не имело смысла) с базовой частотой 80/мин.Интраоперационно была проведена биопсия, при этом в биоптатах правого
предсердия выявлены рыхлая неоформленная соединительнотканная клетчат¬
ка; участки жировой ткани (процент содержания жира не указан); единичный
мелкий лимфогистиоцитарный инфильтрат и единичное субэпикардиальное
кровоизлияние. Обратило на себя внимание практически полное отсутствие
мышечной ткани. Макроскопически предсердие было сильно истончено, что
позволило сразу исключить его амилоидоз. Изменения в биоптатах желудоч¬
ков были менее специфичны: мелкоочаговьтй интерстициальный фиброз и
гипертрофия отдельных кардиомиоцитов. Створки трикуспидального клапана
были несколько уплотнены, отрыв хорды не подтвердился; НС было морфоло¬
гических данных и за констриктивный перикардит. Заключения по морфологи¬
ческим данным не было. Диагноз, поставленный в НЦССХ им. А.Н. Бакулева,
также носил синдромный характер; к терапии были добавлены варфарин,
предуктали верапамил (в связи с сохранявшейся экстрасистолией).В результате оперативного лечения состояние больной заметно улучшилось:
уменьшились одышка (она возникала лишь при значительных нагрузках),
общая слабость, купировались отеки; перебои в работе сердца coxpaHHjmcb.
В июле 2005 г. больная бьша повторно госпита^шзирована в Факультетскую
терапевтическую клинику им. В.Н. Виноградова (в отделение кардиологии), где
372 Кардиологияее состояние расценивалось как относите.іьно удовлетворительное. Отеков не
было, число дыханий 17/мин, хрипы в легких не выслушивались; шумы над
сердцем не выслушивались, на фоне ритма стимулятора определялись единич¬
ные экстрасистольт; АД составило 120/80 мм рт.ст. Печень и селезенка увели¬
чены не были. В анализе крови отмечена нормализация уровня НЬ (12,0 г%), в
анализе мочи — отсутствис белка.На ЭКГ — стимуляция желудочков с ЧСС 80/мин. При 5-часовом монито-
рировании ЭКГ по Хо.шеру — ритм стимулятора, политопные желудочковые
экстрасистолы, всего более 1200, часто с образованием сливных комплексов
с импульсами стимулятора, максимально 500/ч, При контрольной Эхо КГ
отмечена нормализация размеров левого предсердия (3,8 см) и правого
желудочка (2,2 см), уменьшение размеров правого предсердия (4,8x4,5 см),
отсутствие трикуспидальной регургитации; сохранялась умеренная легочная
гипертензия. Больной проводилась терапия соталексом 160 мг/сут (число
экстрасистол снизилось до 800/сут), верошпироном 100 мг/сут (необходи¬
мости в приеме фуросемиданс было), престариумом 2 мг/схт, варфарином
6,25 мг/сут, предукталом MB 70 мг/сут и сорбифером-дурулес по 1 таб. пер¬
вые 10 дней каждого месяца.При повторной госпитализации хорошо обследованной больной в клинику
(и первой — в отделение кардиологии) предстояло решить вопрос о том, в каком
направлении вести Дсьтьнейший диагностический поиск, поскольку нозологи¬
ческий диагноз по-црежнему отсутствовал. Каковы бьши возможные опорные
точки диагноза^. Попытки отталкиваться от трикуспидальной недостаточности
завели нас в тупик: инпраоперационная биопсия и макроскопическое иссле¬
дование предсердия позволили окончательно исключить диагнозы миокар¬
дита, амилоидоза сердца, констриктивного перикардита, отрыва сосочковой
мышцы. Нарушения ритма и проводимости бьши не настолько специфичны,
чтобы можно было думать о каком-то конкретном нозологическом вариан¬
те. Единственное, что обращало на себя наше внимание, — особый характер
поражения правого предсердия. Помимо описанной на дооперационном этапе
выраженной его дилатации, были выявлены еще три факта, которые требовали
объяснения. Во-первых, выраженное истончение стенки правого предсердия
(оно напоминало пергаментное сердце при болезни Уля), на кскгорое обратили
внимание хирурги. Создавалось впечатление, что вся болезнь вьишіа из право¬
го предсердия, достигла трикуспидшіьного клапана и на этом рубеже остано¬
вилась (размеры других камер после операции нормализовались). Во-вторых,
практически полное отсутствие в биоптате предсердия мышечных, а также вос¬
палительных клеток; процесс явно носил дегенеративный характер. И, нако¬
нец, при внутрисердечном злекірофизиологическом исследовании выявлена
полная невозбудимоегь правого предсердия. Ситуация эта крайне необычна
для банальной трикуспидсільной недостаточности, существовавшей не более
5 лет. От этих фактов мы и отталкивались.Английским термином «atrial standstill (немое предсердие) описываются
три ситуации: 1) отсутствие механической систолы предсердий при сохра¬
ненном синусовом ритме (чаще всего — в первые дни после восстановления
Глава 19. «Идиопатическая» трикуспидальная недостаточность.,. 373синусового ритма у больных с мерцательной аритмией, иногда — при выра¬
женной кардиомегалии, амилоидозе); 2) проведение синусового импульса
к АВ-узлу без полноценного возбуждения предсердий (так называемый
синовентрикулярньтй ритм); 3) полный электрический паралич предсердия с
отсутствием синусовых импульсов и ответа на эндокардиальную стимуляцию,
что и выявлено в нашем случае. Последняя ситуация соответствует терми¬
ну «atrial standstill» в наиболее строгом его понимании. Синдром истинного
немого предсердия неоднократно описан в литературе, его диагностические
критерии хорошо известны.1. Отсутствие /*-зубцов на ЭКГ (узловой или желудочковый ритм).2. Отсутствие югулярной а-волны на флебограммах (отражает сокращение
предсердий).3. Отсутствие механического сокращения предсердий (поданным рентгено¬
скопии или ЭхоКГ — неподвижность передних створок атриовентрикулярных
клапанов, которая и была выявлена у нашей больной, но расценивалась как
самостоятельная патология).4. Отсутствие электрического ответа предсердий на внуїрисердечную сти¬
муляцию — основной признак немого предсердия.5. В качестве дополнительного диагностического признака японскими
авторами описано «эндокринное молчание» — резкое снижение секреции
предсердного натрийуретического гормона.Для возникновения немого предсердия необходимо, как правило, соче¬
тание выраженной патологии миокарда предсердий и проводящей системы.
Понятно, что подобная ситуация встречается в первую очередь при тяжелых
органических заболеваниях сердца. Имеются описания немого предсердия при
следующих заболеваниях сердца (группа органических пр№шн):• тяжелый миокардит, при котором восстановления функции нрсдсердия
удалось добиться терапией глюкокортикоидами (нс.мое предсердие опи¬
сано при таких редких в России формах миокардита, как болезнь Чагаса,
лихорадка Цуцугамуши у собаки);• ревматический порок сердца — в терминальной стадии мерцательная арит¬
мия может трансформироваться в предсердный и далее — узловой ритм,
что всегда говорит о выраженной дегенерации предсердия; нам встрети¬
лось описание 45-летнего больного, у которого отсутствовали зубцы Р и
определялись два желудочковых ритма — регулярный и нерегулярный;
при внутрисердечном электрофизиологическом исследовании оказалось,
что во время регулярного pHTNfa предсердия полностью невозбудимы, ритм
возникает в атриовентрику.лярном соединении, а при нерегулярном ритме
возбудима лишь нижняя часть правого предсердия (вблизи трикуспидаль-
ного клапана), где возникает ритм наподобие фибрилляции с частотой
около 300/мин;• аномалия Эбштейна (семейная, с низким расположением трехстворчатого
ютапана, или изолированная), врожденный стеноз легочной артерии в
сочетании с много>'ровневым нарушением проводимости и немым пред¬
сердием;
374 Кардиология• инфаркт миокарда (с окклюзией правой коронарной артерии; восстанов¬
ление кровотока может привести и к восстановлению синусового ритма);• кардиомиопатия различного характера (с парциальной электрической
невозбудимостью обоих предсердий и клинической картиной синдрома
слабости синусового узла), в том числе дилатационная;• ЯПОНСКІІМ11 авторами описан семейный случай немого предсердия (у 3
из 9 членов семьи), в основе которого лежа.4 изолированный амилоидоз
правого предсердия (биоптаты желудочка и кожи не дали результата,
отсутствовало поражение почек, желудочно-кишечного тракта, нервной
системы);• немое предсердие в сочетании с полной АВ-блокадой описано при систем¬
ной красной волчанке, а также у пациента с тяжелой гипертонией и уре¬
мией (что следует расценивать как очень редкое состояние при данных
заболеваниях);• к развитию синдрома немого предсердия может вести и лекарственная
интоксикация: описан подобный случай после внутривенного введения
флекаинида во время электрофизиологического исследования у 79-летнего
пациента с сердечной недостаточностью, исходными нарушениями ритма
и проводимости; синусовый ритм полностью восстановился лишь через
5 ч; аналогичная ситуация возникла у пожилого пациента на фоне терапии
верапамилом.Интересно, что при многих из этих заболеваний, несмотря на их тяжесть,
синдром немого предсердия является обратимым состоянием.Этот круг заболеваний уже был исключен у нашей больной, требовал¬
ся поиск более редких причин немого предсердия. Складывалось все более
усто№ШВое убеждение, что мы имеем дело с генетргчески обусловленным
заболеванием. Проблема состояла в том, что симптомы полностью не укла¬
дывались в картину ни одного из известных нам наследственных заболеваний
сердца. Поэтому клинический диагноз бьш сформулирован следующим обра¬
зом: первичная дегенерация миокарда правого предсердия, трехстворчатого
клапана (?) с развитием трикуспидальной недостаточности. Состояние после
протезирования трикуспидального клапана, тромбэктомии из правого и лево¬
го предсердий от 09.06.2005 г. Нарушения ритма и проводимости; имплан¬
тация ЭКС от 16.06.2005 г. по поводу АВ-узлового ритма, пароксизмальная
АВ-узловая тахикардия (в анамнезе), политопная желудочковая экстраси-
столия. Недостаточность кровообращения ПА стадии, И функционального
класса NYHA. Хроническая железодефицитная анемия легкой степени, меди¬
каментозно компенсированная. Узловой эутиреоидный зоб. Правосторонняя
флебэктомия по поводу варикозного расширения вен в 2002 г. Нельзя бьио
иск.1ючить роль стрептококковой или вирусной инфекции в проявлении и
пр01 рсссировании заболевания.Далее мы попытадись определить круг наиболее вероятных генетически
обусловленных заболеваний. Их оказалось немного.I. Аритмогенная дисплазия правого желудочка (табл. 19.1). Изолированное
поражение правого сердца в сочетании с правожелудочковыми аритмиями
Глава 19. «Идиопатическая» трикуспидальная недостаточность...375всегда требует исключения этого заболевания, особенно у женщин средних
лет. Диагаоз аритмогенной дисплазии правого желудочка ставится по сово¬
купности больших и малых критериев Европейской ассоциации кардиологов,
из которых у нашей больной имелись лишь дилатация правого желудочка со
снижением сократительной функции (причем после операции размеры желу¬
дочка нормализовались, что говорит скорее о его перегрузке, а не о первичном
поражении), частая желудочковая экстрасистолия и единичные лимфоцитар¬
ные инфильтраты. При этом дилатация правого желудочка скорее является
вторичной по отношению к дилатации предсердия с растяжением фиброзного
кольца клапана, а типичные морфологические изменения (истончение стенки,
лимфоцитарные инфильтратьт) были выявлены в предсердии, а не в желудочке.
Тем не менее, нельзя было исключить НС вполне типичный вариант аритмоген¬
ной дисплазии правого желудочка.Таблица 19. іКритерии диагностики аритмогенной дисплазии правого желудочка (1998 г.)ФакторБольшие критерииМалые критерииСемейныйанамнезДоказанные аутопсией/биоп¬
сией с^іучаи аритмогенной
дисплазии правого желудочка1. Случаи внезапной смерти в моло¬
дом возрасте.2. Доказанные клинически случаи
аритмогенной дисплазии правого
желудочкаЭКГV1-V3: эпсилон-полна (є) в
конце QRSV1-V3: 0Д5’>О,11 с (призна¬
ки замедленной деполяриза¬
ции желудочков)1. Более 1 ООО ЖЭ в сутки.2. Мономорфная желудочковая тахи¬
кардия с морфологаей блокады левой
ножки п>'чка Гиса.3. Нарушение реполяризации в
V1-V3 (отрицательный зубец Г, подъ¬
ем ST) у лиц старше 12 лет без блока¬
ды правой ножки.4. Поздние потенциалы желудочковГистологияЖировая ткань >40%1. Жировая ткань >3%.2. Лимфоцитарные инфильтратыДисфункция
правого желу¬
дочка1. Значимая дилатация со
снижением фракции выброса.2. Ссгментартюс поражение
с вовлечением левого желу¬
дочка,3. АневризмыУмерепнші дилатация без снижения
фракции выбросаВовлечение в патологический процесс правого предсердия описывают
крайне редко. Но итальянскими авторами, которые чаще других диагности¬
руют эту патологию, описана скрыто протекавшая аритмогенная дисплазия
правого желудочка, которая проявилась в первую очередь расширением право¬
го предсердия и развитием синдрома «тахи-бради» без желудочковых аритмий.
В другом случае аритмогенной дисплазии правого желудочка желудочковые
аритмии сочетались с электрическим параличом предсердия. Японскими
з 76 Кардиологияавторами также описан случай аритмогенной дисплазии правого желудочка с
поражением правого предсердия, сииусового и атриовентрикулярного узлов,
причелт в биоптатах правых отделов сердца преобладал фиброз. Столь же ред¬
ким симптомом при аритмогенной дисплазии правого желудочка является
тромбоз правого, а тем более обоих предсердий. В нашем случае тромбоз пред¬
сердий легко объясним с учетом отсутствия их электрической и механической
активности.Несмотря на наличие подобных случаев, диагноз аритмогенной дисплазии
правого желудочка представлялся все же весьма маловероятным (главным
образом в связи со слабым поражением правого желудочка).2. При подозрении lia наследственную кардиомионатию всегда следует
исключать большую группу миодистрофий. Большинство из них достаточно
рано проявляются поражением тех или иных скелетных мышц. Нашей боль¬
ной 45 лет, поэтому необходимо бьью исключать те миодистрофии, которые,
во-первых, поздно приводят к поражению скелетной мускулатуры; во-вторых,
протекают с поражением сердца (вплоть до развития немого предсердия).
К таким заболеваниям относятся синдром Кугулъберга—Веландера, дистрофия
Эмери-Дрейфуса, миодистрофия мышц тазового пояса, возможно — неко¬
торые другие варианты миодисгрофий. Больная была прицельно осмотрена
невропатологом, никаких микросимигомов миопатии у нее не выяв.ттено.Таким образом, и эта группа заболеваний не могла быть диагностирована
у больной. Однако убеждение в генетическом характере заболевания сохраня¬
лось, и оставалось предположить, что мы столкнулись с каким-то неизвестным
нам генетически детерминированным заболеванием сердтта, что давало осно¬
вания для дальнейшего изучения публикаций и обращения за консультацией в
Медико-гснетический парный центр РАМН.Описания больных, очень сходньгх с нашей, встречаются в литературе
уже более 25 лет, но причина заболевания до последнего времени оставалась
неясной. Так, в 1979 г. швейцарскими авторами описан случай идиопатиче-
ской семейной дилатации правого предсердия (IERA), которая сочеталась с
пролапсом митрального клапана и наджелудочковыми нар\тпениями ритма.
Природа этого наследственного, по-вилимому, синдрома не была ясна. Уже
через 5 лет наблюдения у больных было отмечено появление трикуспидальной
недостаточности различной степени; в двух случаях развился выпот в полость
перикарда. Наконец, к 2004 г. из 9 здоровых к началу наблюдения членов семьи
умеренная дилатация предсердия развилась у четверых.Еще раньше в литературе бьыи описаны случаи «немого предсердия» у3 пациентов (два из которых — братья) без какого-либо известного заболева¬
ния сердца. Надо сказать, что подобные случаи всегда воспринимались как
достаточно уникальные, описания нередко касались 1-2 пациентов. В 1975 г
пациент с идиопатическим расширением правого предсердия и его полным
параличом был описан Р. Coumel и соавт. При гистологическом исследова¬
нии у подобных пациентов находили фиброз правых отделов сердца либо их
выраженную дегенерацию. Сообщения наиболее часто приходили из Италии,
Японии, реже — из других европейских стран (Испании, Голландии, Англии);
Глава 19. «Идиопатическая» трикуспидальная недостаточность... 377типичным было сочетание расширения правого предсердия, его электрическо¬
го паралича, которому порой предшествовали наджелудочковые аритмии, и
нарушений проводимости, нередко — семейный характер заболевания (напри¬
мер, 8 случаев — у жителей компактною поселка в горах Италии).Уже к ссрединс 1980-х гг появились обобтцаюище работы. Предполагаюсь,
что полный и неполный электрический паралич предсердия, который выявлял¬
ся у разных ^шеноБ больных семей, является стадией одного заболевания, свя¬
занного с нарушением развития мышечного слоя предсердий, причем неполно¬
му параличу соответствует так называемый аневризматический тип дилатации
предсердия. Уже к 1987 г. было описано 43 случая дегенерации правого прел-
серлия (40 из них — тотальная) и 30 случаев аневризматической дегенерации
левого предсердия, а также 7 случаев частичной дегенерации обоих предсердий.
Идиопатическое расширение правого предсердия (IERA) с его частичной невоз-
будимостью и трикуспидальной недостаточностью описано и у очень пожилых
пациентов (отсутствие другой патологии сердца подтверждено при аутопсии),
и у детей, в целом органические случаи немого предсердия, безусловно, преоб¬
ладают (в одной из японских работ соотношение составило 9 к 2).Наконец, в 2003 г группой авторов из Голландии была описана генетическая
основа семейной формы немого предсердия. Из 44 членов одной семьи с этим
заболеванием у 8 человек была выявлена новая мутация гена натриевых кана¬
лов SCM5A (D1275N), причем облигатный носитель данной мутации умер. Еще
у 8 членов семьи был выявлен полиморфизм генов, кодир>тощих специфичный
для предсердий соединительнотканный белок коннексин-40 (замены глутами¬
на аргинином в положении 44 и обратная замена — в положении 71). И лишь
у 3 человек, имевших мутации обоих генов, развилась клиническая картина
идиопатической дилатации правого предсердия с нарушениями ритма и про¬
водимости. Авторы предположили, что именно комбинация двух мутаций,
каждая из которых сама по себе не имеет большого клинического значения,
приводит к развитию немого предсердия. В другом исследовании те же авто¬
ры показали связь выявленного ими полиморфизма гена коннексина-40 с так
называемой уязвимостью предсердий (дисперсией рефрактерности) и частотой
развития пароксизмальной мерцательной аритмии.Японские коллеги (при участии авторов первой публикации) занялись
поиском сходных мутаций в семье с немым предссрдисм. у пробанда и его
здорового отца была выявлена новая мутация гена SCN5A (L212P), а от асим-
птомной матери пробанд получил полиморфизм гена коннексина-40, который,
по-видимом>^ и модифицирует клинические проявления первой мутации.
Через год описан случай синдрома Бругада в сочетании с немым предсердием и
спонтанной фибрилляцией желудочков, генетический анализ выявил миссенс-
мутацию гена SCISSA {R367H), которая привела к дефекту натриевых каналов.
О патологии гена коннексина в данной публикации не сообщается.Если попытаться определить место того заболевания, о котором идет речь, в
ряду других, известных заболеваний, то оно представляет собой один из видов
так называемых кана,іопатий — генетически детерминированных аритмоген-
ных заболеваний, при которых выявляются дефекты генов ионных каналов.
378 КардиологияНа сегодня известны следующие каналопатии; 1) синдром удлиненного интер¬
вала QT, 2) синдром укороченного интервала QT, 3) синдром Бругада; 4) кате-
холаминзависимая желудочковая тахикардия; к этой же группе можно условно
отнести аритмоіенную дисплазию правого желудочка, хотя спектр генной
патологии, лежащей в основе этого заболевания, не исчерпывается каналопа-
тиялга. Интересно, что почти при всех перечисленных заболеваниях (за исклю¬
чением 3 и 4) описаны дефекты гена SCN5A, Как и при диффузных болезнях
соединительной ткани, в основе которых нередко лежат мутации в группе
генов НLA-системы, уже описаны перекрестные формы каналопатий.Клиническая картина «идиопатической дилатации правого предсердия»
весьма характерна:• «идиопатические» наджедудочковые нарушения ритма (АБ-узловая, пред¬
сердная тахикардия, мерцание, трепетание предсердий);• нарушения поперечной проводимости — от различных проявлений син¬
дрома слабости синусового узла до полной АВ-блокады с появлением
АВ-узлового или желудочкового ритма; при этом наджелудочковые арит¬
мии постепенно исчезают; если для немого предсердия при тяжелых
органических заболеваниях сердца характерна эволюция от постоянной
формы мерцательной аритмии к эктопическому предсердному и далее —
идиовснтрикулярному ритму, то для больных с идиопатическим «немым
предсердием» развитие постоянной формы мерцательной аритмии абсо¬
лютно не характерно (видимо, в силу отсутствия необходимой для этого
критической массы миокарда, который у них изначально дефектен);
синдром «тахи-бради!» у больных с 1ERA заканчивается не мерцательной
аритмией, а полным дарал№юм предсердия, который (в отличие от многих
ситуаций с немым предсердием при органических заболеваниях) абсолют¬
но необратим;• выраженная дилатация правого предсердия с развитием его полного
механического и электрического паралича, который подтверждается при
рентгеноскопии, ЭхоКГ (в том числе по неподвижности передней створки
атриовентрикулярных клапанов), внутрисердечном электрофизиологиче-
ском исследовании; макроскопически определяется истончение стенки
предсердия, микроскопически — преобладание фиброза, уменьшение
числа мышечных волокон;• относительная трик>'спидальная недостаточность и дилатация правого
желудочка с декомпенсацией по большому кругу кровообращения, появ¬
лением желудочковой экстрасистолии;• тромбообразование в предсердиях с развитием повторных тромбоэмбо¬
лий в систему легочной артерии, которые приводят к прогрессированию
правожелудочковой недостаточности;• возможно появление выпота в полости перикарда;• нередко — наїїичие аналогичных симптомов у родственников;• единственным эффективным методом лечения является постоянная кар¬
диостимуляция в режиме VVIR, при необходимости — протезирование или
пластика трикуспидального к,іапана.
Глава 19. «Идиопатическая» трикуспидальная недостаточность... 379Однако данные литературы оставались д,чя нас абстрактными: мы не могли
быть уверены ни в наличии, ни в отсутствии у больной какого-либо генетиче¬
ского заболевания (речь идет не только о лабораторном подтверждении, но и о
клиническом взгляде на больного) до тех пор, пока она не бьыа проконсульти¬
рована специалистом — клиническим генетиком.Комментарий E.B. Заклязьминской — заведующей лабораторией медицинской
генетики РНЦХ им. акад. Б.В. Петровского РАМН, д-ра мед. наукМне хотелось бы рассказать о наследственных кардиомиопатиях, которые
встречаются достаточно часто. На сегодняшний день мы знаем о них доволь¬
но много, и можно вьщелить некоторые их общие признаки.1. Прежде всего это независимость клинического течения генетически обу¬
словленного заболевания, которое развивается по своей программе.2. При этом первичная кардиомиопатия довольно часто диагностируется
случайно — дебютирует в связи либо с острой инфекцией, либо с эпизодом
острой сердечной недостаточности. Очень многим подобным больным, к
сожалению, ставится диагноз «постмиокардитический кардиосклероз».
Нам достаточно часто приходится сталкиваться с семейным накопле¬
нием заболевания, которое расценивается врачами подобным образом.
Проблема состоит в том, что разные члены семьи наблюдаются у разных
докторов.3. Как правило, эти заболевания манифестируют в так называемом «преише-
мическом» возрасте (до 40—45 лет). Хотя возможна манифестация и сразу
после рождения — в этих случаях в качестве причины нередко рассматри¬
вается внутриутробная инфекция, даже при отсутствии достоверного под¬
тверждения.4. К сожалению, наследственные кардиомиопатии характеризуются неуклон¬
но прогрессируюпшм течением.5. Причиной смерти, как правило, является развитие жизнеугрожающих
нарушений ритма и проводимости.По анатомическому принципу первичные кардиомиопатии можно разделить
на две группы:1) заболевания с первичным и доминирующим поражением предсердий — к
ним относится заболевание, о котором мы сегодня говорим, и которое, как
мы предполагаем, есть у больной. Оно не имеет названия по автору, в базе
данных в сети Интернет (она включает все известные на сегодня генети¬
ческие заболевания — около 4 тыс. синдромов, из них около 2 тыс. сопро¬
вождаются тем или иным поражением сердечно-сосудистой системы)
получило нагтменование «предсердная кардиомиопатия с нарушениями
проводимости» и имеет свой номер в этом регистре (М1М* 108770);2) к первичным кардиомиопатиям с поражениям миокарда желудочков отно¬
сят дилатационную кардиомиопатию, гипертрофическую кардиомиопа-
тию, рестриктивную кардиомиопатию, не так давно описанный синдром
некомпактного (или несостоятельного) левого желудочка и аритмогснную
дисплазию правого желудочка.
380 КардиологияПредсердная кардиомиопатия с нарушениями проводимости характеризуется
следующими признаками;1) манифестация заболевания приходится, как правило, на 2—3-є десятилетие
жизни;2) характерная морфологическая картина — прогрессир>тощий фиброз право¬
го предсердия вплоть до полного отсутствия электрического и механического
ответа, что и имело место в нашем случае;3) прогрессирующие нар\тиения проводимости — достаточно часто забо¬
левание может манифестировать нарушениями проводимости, а признаки
фиброзной дисплазші правого предсердия могут появ-чяться позже; более
того, нарушения проводимости могут возникать внезапно, у больных без
установленного ранее диагноза, и изменения предсердия выявляются только
при аутопсии;4) на сегодняшний день описаны как полные, так и частичные формы забо¬
левания (тотштьная и частичная невозбудимость предсердия) при разной
степени вовлеченности клапана в процесс;5) тип наследования: долгое время считалось, что оно аутосомно-доминантное
(за развитие заболевания отвечает ген коннексина-40), в настоящее время
рассматривается гипотеза дигеїшого наследования (т,е. заболевание встреча¬
ется, если одновременно имеются изменения двух генов — SCN5A, который
кодирует а-субъедашицу натриевых каналов, и гена коннексина-40). На
сегодняшний день выявлен один и тот же полиморфизм гена коннексина-40,
который достаточно редко встречается в популяции (не чаще 7%) — замена
а^танина на гуанин и гуанина на аланин в разных позициях (44 (G/A) и +71
(A/G), нетранслируемая часть гена). Различные мутации гена SCN5A лежат в
основе целого ряда аллельных заболеваний, и в рамках одной семьи мутации
могут проявляться по-разному.При доминантном наследовании заболевание передается из поколения в
поколение (т.е. не наблюдаются пропуски поколений), до,ія пораженных
среди потомства составляет 50%, передача генов может ос>’ществляться от
отца к сын>’ и нет преимущественного поражения одного пола. В данной
семье мы имеем ограниченные сведения о семейном анамнезе (рис. 19.S): мать
пробанда (нашей больной) умерла в 65 лет от инфаркта миокарда. Но име¬
лись ли поражение клапанного аппарата, частичный отрыв хорд — мы точно
не знаем, и мы не готовы утверждать, что мать пробанда страдала тем же забо¬
леванием. Тем не менее, с учетом выраженного ютинического полиморфизма
заболевания, вполне возможно, что в возрасте 65 лет мама больной могла
иметь более мягкое течение данного заболевания (предсердной кардиомио-
патии с нарушениями проводимости), в результате чего оно осталось нерас¬
познанным. В отношении двух дочерей больной можно говорить; сейчас кли¬
нически здоровы. Для нас актуален вопрос: больна только мама или больны
две девочки, которые являются разнояйцевыми близнецами. Для того чтобы
найти ответ на этот вопрос, необходимо провести генетическое исследование:
прямую ДНК-диагностику мутащтй и значимых полиморфизмов в генах GJA5
и SCN5A с целью верификации диагноза и уточнения прогноза заболевания, а
Глава 19. «Идиопатическая» трикуспидальная недостаточность... 3SiРис. 19.5. Родословная семьи больной С, (отмечена стрелкой). Пояснения в текстев случае выявления первичного генетического дефекта ~ ДНК-диагностику
дочерей пробанда.Генетика относится к профилактической области медицины. Одна из
основных наших задач — пресимптоматическая диагностика. Очень важен
как \гожно более ранний диагноз, поскольку при первичных кардиоми-
опатиях примерно 30% больных погибают внезапно. После постановки
диагноза мы рассматриваем вопрос о превентивной установке кардиости¬
мулятора. Иногда бывает, что наши пациенты по различным критериям
не имеют достаточных оснований для установки кардиостимулятора, но
беда в том, что до того как полный набор критериев проявится, они могут
умереть внезапно.Что такое коннексины и почему дефекты коннексиновых генов мог>т вести к
поражению сердца? На сегодняшний день известно 8 коннексинов человека,
но кардиоспепифичны только іри — 40, 43 и 45-й. Коннексин-40 экспрес¬
сируется преимущественно в миокарде (экспрессируется — значит, он там
необходим и синтезируется с очень большой скоростью). Он выявляется как
в предсердиях, так и в проводящей системе сердца. В АБ-узле в основном
представлен коннексин-43, а коннексины-40 и -43 — в пучке Гиса и волок¬
нах Пуркинье. Коннексины представляют собой довольно короткие белки,
которые формируют межмьипечные каналы, известные нам как «шелевые
контакты» {рис. 19.6, см. цветную вюгейку). Эти контакты моїуг пропускать
либо ионы, либо молекулы малого размера. Кроме того, наличие коннекси¬
нов в сердце обеспечивает быструю переда^іу электрического импульса по
миокарду. Поэтому, как только представлена генетически детерминирован¬
ная паталогия коннексинов, у больных выявляются либо нарушения про¬
водимости, либо структурные изменения миокарда. На сегодняшний день в
группе больных с пороками сердца в ряде случаев выявляются изолирован¬
ные мутации гена коннексина-40, и среди этих врожденных пороков сердца
наблюдаются поражения трикуспидального и митрального клапанов. Но в
отсутствие мутации в гене натриевых каналов это то.іько морфологические
подтвержденные пороки сердца разной степени выраженности без наруше¬
ний проводимости.Мутации, которые происходят в гене натриевого канала, могут проявлять себя
по-разному Когда мы говорим об изолированной мутации этого гена, мы,
382 Кардиологиякак правило, имеем дело с первичными нарушениями ритма и проводимости,
которые составляют ф>т[пу аллельных заболеваний (т.е. связаны с мутациями
в одном гене).1. Это синдром удлиненного интервала QT 3-го типа, когда мутация происхо¬
дит по типу усиления ф>таадии. Как только вьіяйііяется эта мутация, мы сразу
рекомендуем больным менять терапию, поскольку в отсутствие генетическо¬
го подтверждения базовой терапией синдрома удшненного интервала QT
являются р-блокаторы, а у больных с 3-м типом синдрома совершенно иной
молекулярный механизм повреждения, и поэто\£у данные вещества не только
не улучшают состояние, но зачастую вредны. Больным с третьим вариантом
показано назначение блокаторов натриевых каналов — дифенина, мексиле-
тина, аллапинина, которые не удлиняют интервала QT.2. При синдроме Бругада другие мутации в том же гене приводят к абсолютно
ино\іу электрофизиологическому состоянию.3. в ряде слу^шев — синдром внезапной детской смерти, нередко ночью, при
этом возникает вопрос об удушении ребенка, если он спит вместе с матерью,
и генетическая диагностика помогает выяснить истинную причину смерти.4. При аритмогенной дисплазии правого желудочка 5-го типа также выявле¬
ны мутации этого гена.5. При ряде форм дилатационной кардиомиопатии также бывают нарушения
проводимости.6. Синдром, который больше известен как болезнь Леви-Ленегра, также
вызывается мутациями в гене натриевого канала.Почему так много болезней? Разные изменения в гене приводят к разным
изменениям белка. Функцию можно как усилить, так и притормозить.
В зависимости от того, как меняется функция натриевого канала, мы видим
совершенно разные заболевания. И именно поэтому изолированно встре¬
тившаяся мутация в гене может не привести к развитию заболевания, а соче¬
тания двух мутаций (в гене коннексина и в гене натриевого канала) может
быть достаточно, чтобы обусловить клиническую картину того заболевания,о котором мы сегодня говорим.Несколько слов о других первичных кардиомиопатиях, в частности о гипер¬
трофической кардиомиопатии. Частота ее в популяции очень высока — 0,2%.
При этом, по современным оценкам, на долю генетически детерминирован¬
ных форм приходится не менее 50% случаев. И причиной заболевания явля¬
ются мутации в генах саркомерных белков миокарда. На сегодняшний день
известно более 10 генов, мутации в которых приводят к первичной гипертро¬
фической кардиомиопатии; при этом часть мутаций являются злокачествен¬
ными, и у больных даже с минимальной выраженностью гипертрофического
процесса, обструкции вьгеодного тракта наблюдаются нарушения ритма.
Частота дилатационной кардиомиопатии несколько меньше — около
1:10 ООО населения, на долю наследственных форм приходится не менее 40%,
А причиной заболевания являются мутации в генах, кодирующих структур¬
ные и саркомерные белки миокарда. В таблице 19.2 вьщелены мутации тех
генов, которые ответственны за развитие дилатационной кардиомиопатии
Глава 19. «Идиопатическая» трикуспидальная недостаточность... 383Таблица 19.2Гены, ответственные за развитие дидатационной кардиомиопатии
с нарушениями ритма и проводимостиГенЛокусБелокLMNAlqll-23Ламин А и Сdesmin2q35ДесминSCN5AЗр22-24Натриевый каналетеппXq28Эмерин6q23с нарушениями ритма и проводимости. Присієм нередко миокард бывал
достагочно сохранен, и на первый план выходили аритмические симптомы
(включая внезапную смерть). В частности, таковы мутации в гене ламина.
Этот ген отвечает и за часть случаев болезни Эмери—Дрейфуса — прогрес¬
сирующей мышечной дистрофии, о которой мы также думали в отношении
больной С., потому что при ней также отмечается немое предсердие. Она
может манифестировать в возрасте позже 3—4-го десятилетия жизни — в этом
случае обязательно наблюдаются контрактуры. Поскольку пациентка бьша у
невролога и контрактур не вьіяв,іено, как и признаков атрофии и гипотрофии
мышц, мы считали возможным агказаться от данного диагноза.Ген ламина достаточно коварен и может приводить к развитию изолирован¬
ной дилатационной кардиомиопатии; в ряде случаев выявление его мутации
требует превентивной установки кардиоверісра-дефибриллятора. Иногда
заболевание манифестирует на 1 -м году, когда фракция выброса снижена еще
не настолько, чтобы говорить с кардиохирургом о трансплантации сердца, а
в лист ожидания на трансплантацию можно попасть лишь с 14 лет. На сегод¬
няшний день удалось договориться с хирургами о том, что если мы ставим
диалгоз и знаем прогноз, злаем, что это неуклонно профессирующее заболе-
ванрте, то ребенок должен іюпасть в лист ожидания.При рестриктивной кардиомиопатии генетические формы также доминиру¬
ют; имеется ряд генов, которые отвечают за это заболевание.Аритмогенная дисплазия правого желудочка встречается с частотой от 6 до44 (на юге Италии) на Ш ООО населения (ддя наследственных заболеваний
частота 1 на 10 ООО уже считается высокой). Известны случаи, когда в процесс
вовлекаюіхі^я и межжелудочковая перегородка, и левый желудочек, но, ках
правило, если поражается правое предсердие, то правый желудочек бывает
уже поражен. Это одна из причин того, почему мы не рассматриваем арит-
моїснную дисплазию правого желудочка применительно к нашей больной.
Градиент изменений все-таки направлен снизу вверх, от желудочка к пред¬
сердию, а не наоборот. Известен целый ряд генов, ответственных за развитие
аритмогенной дисплазии правого желудочка; к сожалению, очень многие
гены неизвестны. В основном страдают молекулы клеточной адгезии, кото¬
рые обеспечивают адекватность межклеточных контактов.ДНК-диагностика — это прежде всего стратификация риска. В случае мно¬
гих заболеваний мы имеем достаточно информации для того, чтобы строить
384 Кардиологияпрогаоз. Разные генеттеские варианты одного и того же заболевания под¬
разумевают разные уровни риска внезапной сердечной смерти. Кроме того,
для многих заболеваний мы сейчас имеем возможность предлагать не гено-
терапию, конечно, но геноспенифическую терапию. Например, большая
часть больных синдромом удлиненного интервала QT — это пациенты с
лїутациями в гене калиевого канала, и для них действительно подходят
(3-блокаторы. Но если это 2-й тип синдрома, го оптимальной является тера¬
пия препаратами, которые увеличивают содержание калия в крови. Для нас
принципиальны пресимптоматическая диагностика и выявление группы
риска. И, что очень важно, \ш имеем возможность поставить диагноз в1 фиместрс беременности, на сроке до 14 над, и сообщить о нем родителям.
Если семья считает возможным сохранить беременность, то уже в родах
ребенка принимает кардиолог.Комментарий А. В. Недоступа — арофессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукПриведенное наблюдение действительно является уникальным. Мы всту-
]таем в ту область кардиологии, которая совершенно незнакома клини¬
цистам. Представляется неизбежным расширение списка генетически
обусловленных заболеваний сердца, которые ранее трактовались как
идиопатическис, а также включались в группы наиболее распространен¬
ных заболеваний (ишемическая болезнь сердца, постмиокардитический
кардиосклероз и т.д.), причем скорее автоматически, по одному возраст¬
ному признаку (иигемическая болезнь сердца) или нал№шю ангин либо
гриппа в анамнезе. Можно догадываться, что, например, генные дефекты
играют важную роль в происхождении дилатационной кардиомиопатии.
Действительно, как может быть, что достаточно стереотипная патология
(резкое расширение полостей сердца) возникает у эндокринологических
больных («диабетическая кардиомиопатия»), при ишемической болезни
сердца («ишемическая кардиомиопатия»), у некоторых больных, пере¬
несших вирусную инфекцию (собственно дилатационная кардиомиопа¬
тия) и т.д.? Не логичнее ли предположить, что в действительности эта
патология обусловлена генным повреждением, а диабет, ишемическая
болезнь сердца, миокардит служат своего рода «ложем» (или триггером),
на котором манифестирует основное заболевание? Между прочим, это
лишний раз свидетельствует о крайнем несовершенстве наших знаний об
этиологии в клинике внутренних болезней вообще, о чем неоднократно
говорил еще Е.М. Тареев.Возвращаясь к данному случаю, можно сказать, что описанная патология,
конечно, чрезвьпгайно редка. Но вместе с тем совсем не так редко мы встре¬
чаем изолированну'ю атриомегалию (чаще левого или обоих предсердий), при
этом как будто без всяких гемодинамических (в виде недостаточности атри¬
овентрикулярного отверстия) оснований. Кто знает, не лежит ли в основе и
этой патологии генный дефект?
Глава 19. «Идиопатическая» трикуспидальная недостаточность... 385Комментарий В.А. Сулимова — заведующего Еафедрой фаі^льтетской терапии № 1
лечебного факультета Первого МГМУ им. И.М.С^ченова, д-ра мед. наук, проф.
Сообщение Е.В. Заклязьминской исключительно интересно, но хоте¬
лось бы расставить акценты: генетически детерминированные заболевания
составляют лишь 5% причин внезапной смерти, а 85% — это внезапная
смерть у больных с различными формами ишемической болезни сердца.
По-видимому, сомневаться в диагнозе нашей больной нет оснований (уже
сейчас его можно ставить с вероятностью 95%), однако очень желательно
все-таки провести генетическое исследование (ген коннексина в даішой
лаборатории до сих пор не исследовался, поскольку не бьшо больных с
подобной патологией — эта больная будет первой).P.S. В Медико-генетическом научном центре РАМН было проведено
молекулярно-генетическое исследование, в гене GJ5A, кодируюш,ем
коннексин-40, в гетерозиготном состоянии были идентифицированы
редкие полиморфизмы; с.—44g>a и c.+71a>g, наличие которых приводит
к снижению уровня экспрессии коннексина-40. Поскольку были описаны
случаи дигенного наследования заболевания, был проведен анализ генов
SCN5A и LMNA. Мутаций выявлено не было. ДНК-диагностика была также
проведена двум клинически бессимптомным (?) в настоящее время доче¬
рям больной. У обеих также бьыи выявлены замены с.—44g>a и c.+71a>g
в гене GJ5A. Эта находка свидетельствует о высоком генетическом риске
развития кардиомиопатии у девочек и необходимости динамического
наблюдения за ними.Позже получены развернутые результаты исследования биоптатов миокарда
правого предсердия в НЦССХ им. А.Н. Бакулева (фотофафии любезно пре¬
доставлены лечащим врачом больной С. в отделении хирургического лече¬
ния тахиаритмий НЦССХ М.В. Носковой, рис. 19.1, см. цветную вклейку).
Стенка правого предсердия представлена рыхлой соединительнотканной
клетчаткой с прослойками жировой клетчатки {рис. 19.7, а). В соедини¬
тельной ткани содержатся гладкомышечные клетки (окрашивание на глад-
комышечный а-акпш, рис. J9.7, б), фибробласты с миогенной дифферсн-
цировкой (окрашивание на маркер фибробластов виментин, рис. 19.7, г) и
единичные кардиомиоциты, находящиеся в состоянии утраты миофибрилл
(окрашивание на десмин — маркер зрелых кардиомиоцитов, рис. 19.7, в).
На ультраструкт>тэном уровне в обнаруженных в стенке правого предсердия
единичных кардиомиоцитах выявлены нарушения сократительного аппа¬
рата: нарушение структуры Z-полос саркомсров и хаотичное расположение
миофибрилл (электронные микрофотографии, 19.7, д, е). Данные изме¬
нения полностью соответствуют поставленному диагнозу.В последующие 3,5 года больная продолжала постоянную антиаритмическую
терапию (соталекс был заменен кордароном в связи с сохраняющейся желу¬
дочковой экстрасистолией, а также периодами частого АВ-узлового ритма),
прием варфарина (под контролем МНО), всрошпирона, престариума; пери¬
одически к ЛЄЧЄІШЮ добавляли фуросемидв связи с возобновлением отеков,
386 Кардиологиянекоторым нарастанием одышки. Состояние оставалось относительно ста¬
бильным. В декабре 2008 г. в связи с выраженным усилением одышки была
госпитализирована в Научно-исследовательский инсттуг скорой помощи
им. Н.В. Склифосовского, где у больной развилась клиншеская смерть;
несмотря на успешную реанимацию, она погибла в ближайшие сутки, в каче¬
стве нричины смерти диагностирована ТЭЛА.ЛИТЕРАТУРАAccorsi F., Caruso G., FiorUli R. et al. Idiopathic dilatation of the atria: a syn¬
drome? Description of a case of idiopathic biatrial dilatation, review of the literature
and a proposal for a pathogenetic interpretation // G. Ital. Cardiol. 1987; 17 (10):
874-882,Antonio J.H., Diniz M.C., Miranda D. Persistent atria! standstill with limb girdle
muscular dystrophy // Cardiology. 1978; 63 (1): 39-46.Baseman D.G., O’Suilleabhain P.E., Reimold S.C. et al, Pergolidc use in Parkinson
disease is associated with cardiac valve regurgitation // Neurology. 2004; 63 (2): 301—
304.Belhassen B., Shapira L, Hammerman C. Unusual manifestations of arrhythmoge-
nic right ventricular dysplasia as ventricular fibrillation, atrial paralysis, and hypoexci-
table right ventricle // Br. Heart J. 1988; 59 (2): 263—265.Benchimol C.B., Schlesinger P., Ginefra P. Persistent atrial standstill j j koXdi Cardiol.
1975; 30 (4): 3J3-322.Brechenmacher C. , Coumel P., Slama R, Apparent auricular paralysis and disorders
of auriculo-ventricular conduction: anatomo-clinical study j j Arch. Mai. Coeur Vaiss.
1975; 68 (6): 575-580.Brucato A., Baudo F., Barberis M. et al. Pulmonary hypertension secondary to
thrombosis of the pulmonary vessels in a patient with the primary antiphospholipid
syndrome //J. Rheumatol. 1994; 21 (5): 942—944.Chatzis A,C., Giannopoulos N.M,, Sarris G.E. Isolated congenital tricuspid insuf¬
ficiency associated with right-sided congenital partial absence of the pericardium j j J.
Heart Valve Dis. 2004; 13 (5); 790-791.Disertori М., Guamerio М., Vergara G. et al Familial endemic persistent atrial
standstill in a small mountain community: review of eight cases // Eur. Heart J. 1983;4 (5): 354-361.Effendy F.N., Bolognesi R., Bianchi G., Visioli O. Alternation of partial and total
atrial standstill//J. Electrocardiol. 1979; 12(1): 121-127.Firouzi М., Ramanna B., Kok B. et al. Association of human connexin-40 gene
polymorphisms with atrial vuhicrability as a risk factor for idiopathic atrial fibrilla¬
tion // Circ. Res. 2004; 95 (4): е29-еЗЗ.Fromer М., Genton C., SchlaepferJ. etal. Is there an isolated arrhythmogenic right
atrial myocarditis? //Eur. Heart J. 1990; 11 (6): 566—571.FrustaciA., Cameli S., Zeppilli P. Biopsy evidence of atrial myocarditis in an athlete
developing transient sinoatrial disease // Chest. 1995; 108 (5): 1460—1462.
Глава 19. «Идиопатическая» трикуспидальная недостаточность... 387Goetz W.A., LieboldA., Vogt F, Birnbaum D.E. Tricuspid valve repair in a case with
congenital absence of left thoracic pericardium // Em. J. Cardiothorac. Surg. 2004;
26 (4): 848-849.Groenewegen W.A., Firouzi М. , Bezzina C R. etal. A cardiac sodium channel muta¬
tion cosegregates with a rare connexin-40 genotype in familial atrial standstill j j Circ.
Res. 2003; 92(1): 14-22.Risaki R., Yutani C., Imakita M. et al Histopathological study of valvular deposits
of amyloid protein in cardiac amyloidosis [Article in Japanese] I j J. Cardiol. 1996: 27
Suppl 2: 31-37.Hover A.R., Koppes G.M. Atrial standstill and complete heart block in systemic
lupus erythematosus // Chest. 1979; 76 (2): 230-231.Ismailov R.M., JVeiss H.B., Ness R.B. et al Blunt cardiac injury associated with cardiac
valve insufficiency: trauma Unks to chronic disease? I I Injury, 2005; 36 (9): 1022—1028.Jacobovitz !>., Dustin P. Jr. Right heart valvular amyloidosis in a patient with duo¬
denal carcinoid tumours //J. Pathol. 1974; 112 (3): 195-197.Jenni R., Gobel N., Schmeider L. et al. Idiopathic familial right atrial dilatation j I
Schweiz, Med. Wochenschr. 1981; ill (42): 1565-1572.Jeong М.Я. , Ahn YK., Gill G.C. et al. Tsutsugamushi myocarditis with congestive
heart failure and persistent atrial standstill // Jpn Circ, J. 1996; 60 (6): 382-388.Kambara H., Phillips J.H. Prolonged atrial standstill // Angiology. 1976; 27 (7):
455-462.Kodama-Takahashi K., Ohshima K. et al. An elderly case of idiopathic dilatation
of the right atrium in which right-sided heart failure was exacerbated by drug-induced
bradyarrhythmia // Nippon Ronen Igakkai Zasshi. 2001; 38 (4): 544-547.KoshimizM T.A., Komori S., Ishihara T. Restored atrial excitability after late reca¬
nalization in a patient with atrial standstill and acute myocardial infarction // Pacing
Clin. Electrophysiol. 2002; 25 (2): 217-219.Kurokawa A., Kurita A., Kasai G., Kimura E. Persistent atrial standstill, report of
three cases//J. Electrocardiol. 1975; 8 (4): 357-362.Kurz D.J., Oechslin E.N., Kobza R., Jenni R. Idiopathic enlargement of the right
atrium: 23 year follow up of a familial cluster and their unaffected relatives // Heart,
2004; 90(11): 1310-1314.Liu Y.B., Chen W.J., Lee Y.T. Atrial standstill in a case of Kugelberg-Welander
syndrome with cardiac involvement: an electrophysiologic study // Int. J. Cardiol.
1999; 70 (2): 207-210.Maeda S., Tanaka Т., Hayashi T. Familial atrial standstiH caused by amyloidosis //
Br. Heart. J. 1988; 59 (4): 498-500.Makita N., Sasaki K., Groenewegen W.A. et al. Congenital atrial standstill
associated with coinheritance of a novel SCN5A mutation and connexin-40 poly-
тофЫ&т8 // Heart Rhythm. 2005; 2 (10): 1128-1134.Nogami A., Adachi Nitta J. etal. Arrhythmogenic right ventricular dysplasia with
sick sinus syndrome and atrioventricular conduction disturbance // Jpn Heart J. 1990;
31 (3): 417-423.Ohshita Т., Chida K., Ueda S. et al. An autopsy case of elderiy idiopathic enlarge¬
ment of the right atrium // Nippon Ronen Igakkai Zasshi. 1999; 36 (1): 59-64.
388 КардиологияOkutan К, Yavuz Т., Bilgin S. et ai Congenital cleft of anterior tricuspid leaflet in
adolescent // Asian Cardiovasc. Thorac. Ann. 2002; 10 (3): 262-263.Pierard L.A., Henrard L., Demoulm J.C. Persistent atrial standstill in familial
Ebstein’s anomaly // Br. Heart J. 1985; 53 (6): 594-597.Proclemer A., Ciani R., Feruglio G.A. Atrial involvement in arrhythmogenic right
ventricular dysplasia: primary or secondary? Description of a case of occult ventricular
dysplasia with right atrial enlargement and exclusively sinoatrial arrhythmia [Article in
Italianl //G. Ital. Cardiol. 1988; 18 (8): 671-675.Ross A.M., Proper M.C., Aronson A,L. Sinoventricular conduction in atrial stand¬
still//J. Electrocardiol 1976; 9 (2): 161-164.Sakuragawa K., Kae A., Hano O. et al Case of Emer>'—Dreifuss syndrome associ¬
ated with atrial standstill // Nippon Naika Gakkai Zasshi. 1997; 86 (2): 310-311.Seine Y., Shimai S., Ibuki C. et ai Disturbed secretion of atrial natriuretic pep¬
tide in patients with persistent atrial standstill: endocrinoiogic silence j I J. Am. Coll.
Cardiol. 1991; 18 (2): 459-463.Straumanis J. P. , IHies KB., Case C.L. Resolution of atrial standstill in a child with
myocarditis// Pacing Clin. Electrophysiol. 1993; 16 (11): 2196-2201.Takehara N., Makita N., Kawabe J. etaL A cardiac sodium channel mutation iden¬
tified in Brugada syndrome associated with atrial standstill I I J. Intern. Med. 2004; 255
(1): 137-142.Thukkani N., Ravichandran P.S., Das A., Slater M.S. Leiomyomatosis metastatic
to the tricuspid valve complicated by pelvic hemorrhage // Ann. Thorac. Surg. 2005;
79 (2): 707-709.Tognarini S., Pardini E. A case of atrial paralysis during the use of intravenous
flecainide acetate // Cardiologia. 1989; 34 (8): 725-729.Turjanski A.A., Finkielman J.D., Vazquez-Blanco M. et al. Isolated tricuspid valve
disease in antiphospholipid syndrome I j Lupus. 1999; 8 (6): 474-476.Ward D.E., Ho S. Y., Shinehourne E.A. Familial atrial standstill and inexcitability in
childhood // Am. J. Cardiol. 1984; 53 (7): 965-967.Yoong J.K., Jau/eerally F.R, Isolated tricuspid valve vegetations and steno-insuf-
ficiency in primary antiphospholipid syndrome // Singapore Med. J. 2004; 45 (3):
127-129.Zolezzi F., Filippi E., Rosso R. etal. Chronic myocarditis leading to a right ventricu¬
lar cardiomyopathy Case report IIG. Ital. Cardiol. 1986; 16 (3): 273-275.
Глава 20
СЛУЧАЙ БОЛЕЗНИ ФАБРИ У ВЗРОСЛОГО ГЛАЗАМИ
КАРДИОЛОГА, МОРФОЛОГА И ГЕНЕТИКА
(ТРИ СТУПЕНИ КДИАГНОЗУ)О.В. Благова, Е.В. Заклязьминская, А.В. Недоступ, ЕЛ. Коган,ГМ. ПапакинДиагноз редкого заболевания у пациента с довольно стандартной картиной
поражения сердца поставить сложно, особенно если врач-кардиолог раньше с
такой болезнью не сталкивался. Мы приводим описание клинического случая,
в котором поэтапная расшифровка характера поражения сердца, вплоть до
проведения эндомиокардиальной биопсии, привела кардиологов к предвари¬
тельному диагнозу болезни накопления и к необходимости привлечения врача-
генетика, оценившего клиническую картину иными глазами и поставившего
окон'їательньїй диагноз, подтвержденный генетически и биохимически.Данное наблюдение продолжает серию случаев, в которых сотрудничество с
морфологом и клиническим генетиком оказалось исключительно полезным и
незаменимым для интернистов.Обсуждаются вопросы клинических проявлений, диагностики болезни
Фабри и возможности проведения специфической ферментзаместительной
терапии.Больной П., 32 года, поступил в отделение кардиологии Факультетской тера¬
певтической клиники им. В.Н. Виноградова 21.11.2008 г с жа/юбами на перио¬
дически возникающее (без связи с физической нагрузкой) ощущение неритмртч-
ного сердцебиения, преходящие отеки голеней и стоп, бессимптомные подъемы
АД до 140/90 мм рт.ст. (при обычном АД 120—130/80 мм рт.ст.), оііємєниє и пока¬
лывание в кончиках пальцев, плохую переносимость жары и холода.Из семейного анамнеза; отец 54 лет страдает гипертонической болезнью;
пациент служил в армии, 7 лет занимался греблей (кандидат в мастера спорта),
в настоящее время работает плотником; не курит, алкоголем не злоупотребляет.
В возрасте 3 лет и 21 года перенес пневмонию, в 2 года — ожог бедра, в 18 лет —
ожог предплечья, в 27 лет — ампугацию концевой фаланги II пальца справа в
связи с обморожением; 2 года назад самостоятельно выявил правостороннюю
паховую грьпку; аллергологический анамнез не отягощен.Анамнез заболевания {рис. 20.1): с 15 лет фиксировались хюдьсмы АД до
140/90 мм рт.ст. без клинических симптомов, лечение не проводилось. На ЭКГ
от 2003 г ритм синусовый, в дальнейшем ЭКГ не регистрировалась. В течение
последних 2—3 лет отмечает эпизоды неритмичного сердцебиения, не связан¬
ные с нагрузкой, не обследовался. С мая 2008 г. стали периодически возникать
отеки голеней и стоп, которые пациент связьшал с избыточным приемом
390Кардиология15лет(1991}2003 2005 лето 2008подъемы АД до
140/90 мм рт.ст.неритмичноесердцебиениеотеки голеней
и стоппокалывание и
онемение
в конечностяхампутацияфалангиРис. 20.1. Анамнез больного П., 32 годажидкости. Нагрузки по-прежнему переноси.1 хорошо. В ноябре 2008 г. пла¬
нировалась госпитализация с целью оперативного лечения паховой грыжи; в
рамках предоперационного обследования зарегистрирована ЭКГ, на которой
впервые выявлена мерцательная аритмия. Поступил в Факультетскую терапев-
T№iecK>TO ьслинику для обследования и лечения.При поступлении: состояние относительно удовлетворительное. Конституция
гиперстеническая. Отеков нет. Число дыханий 17/мин, дыхание везикулярное,
удовлетворительно проводится во все отделы, хрипов нет. границы сердца не
расширены, верхушетаый толчок не изменен, тоны ясные, шумы не выслушива¬
ются. ЧСС 65/мин, ритм неправильный (мерцательная аритмия), АД 130/80 мм
рт.ст. Живот мягкий, безболезненный, печень и селезенка не увел№іеньі.В общем анализе крови НЬ 150,5 г/л, эритроциты 5,5 \lth, цветовой показа¬
тель 0,81, лейкоциты 5,7 тыс., лейкоцитарная формула не изменена, тромбо¬
циты 276,4 тыс., СОЭ 5 мм/ч. В биохимическом анализе крови: общий белок
7,7 г/л, альбумин 43,7 г/л, глюкоза 5,3 ммоль/л, креатинин 1,34 мг/дл, азот
мочевины 5,2 ммоль/л, общий билирубин 23,4 мкмоль/л (5-21), прямой били¬
рубин 4,4 мкмоль/л, лет 16 Ед/л, АЛТ 24 Ед/л, у-ГТ 21 Ед/л, ЩФ 40 Ед/л, ЛДГ
287 Ед/л, КФК 82 Ед/л, калий 5,0 мэкв/л, натрий 142 мэкв/л.Липидный спектр: триглицериды 126 мг/дл (50-150), общий холестерин
327 мг/дл (150-250), ЛПОНП 25,2 мг/дл, ЛПВП 77,5 мг/дл, ЛПНП 224,3 мг/дл.При электрофорезе белков отклонений от нормы не выявлено.В коагулограмме: А4ТВ 0,91, протромбиновый индекс 99%, фибриноген
3,09 г/л.В иммунологических анализах: HB^Ag, HCV Ab, комплекс серологических
реакдий на сифилис, антитела к ВИЧ, С-реактивный белок, ревматоидный
фактор, антинуклеарный фактор, антистретгголизин-О отрицательны.
Глава 20. Случай болезни Фабри у взрослого глазами кардиолога... 39ЇГормоны щитовидной железы: (своб.) 14,8 пмолъ/л, ТТГ 6,6 МЕ/л (норма
0,3-4,0 МЕ/л), антитела к ТПО 23,0 МЕ/мл.Проведена серологическая диагностика миокардита: в лаборатории
«МедБиоСпектр» антитела к миокарду класса IgG 1:400, к гиалуронидазе 1:400
(норма до 1:100); в лаборатории Федерального научного центра трансшіанто-
логии и иск>'сственных органов им. акад. В.И. Шумакова АНФ (с антигеном
сердца быка) был отрицателен, антитела к антигенам эндотелия, кардио-
миоцитов и проводящей системы 1:80, к антигенам гладкой мускулатуры 1:160
(норма до 1:40).В общем анализе мочи pH 5, прозрачность неполная, сахар — следы, белка,
ацетона, желчных пигментов нет, уробилин в пределах нормы, лейкоциты и
эритроциты единичны в препарате, слизь в умеренном количестве, бактерий
немного. Реакция кала с бензидином отрицательна.При рентгенографии органов грудной клетки: легкие без свежих очаговых и
инфильтративных изменений. Корни легких структурны. Диафрагма располо¬
жена обычно. Плевральные синусы свободны. Сердце и аорта рентгенологиче¬
ски не изменены.При УЗИ органов брюшной полости отклонений от нормы не выявлено. При
ЭГДС пищевод свободно проходим, не изменен, кардия смыкается. В желудке
умеренное количество светлой жидкости со слизью, рельеф не изменен, скіадки
эластичные, воздухом расправляются, слизистая оболочка неравномерно окра¬
шена, в антральном отдєігє с очаговой гиперемией. По малой кривизне антраль¬
ного отдела плоская эрозия с фибринозным налетом и перифокальной гипере¬
мией. Малая кривизна и угол ровные, привратникокруглый, свободно проходим.
Луковица двенадцатиперстной кишки и постбульбарный отдел не изменены.
Заключение: антральный очаговый поверхностный гастрит с единичной эрозией.На ЭКГ в отсутствие кардиотропной терапии (рис. 20.2) — брадисистоли-
ческая форма мерцательной аритмии (синусовый ритм не регистрировался),
неполная блокада правой ножки пучка Гиса, признаки птертрофии левого
желудочка.По данным суточного мониторирования ЭКГ по Холтеру, проведенного
на «чистом» фоне, регистрируется мерцательная аритмия (RR^i„ 464 мс,
днем 43-112/мин (ср. 70/мин), ЧСС ночью 36-67/мин
(ср. 57/мин); желудочковых экстрасистол 4; пауз больше 2 с 1950, преимуще¬
ственно в ночные часы, из них 35 пауз больше 3 с и одна пауза 4,5 с (рис. 20.3);
ST-T без динамики. При повторном исследовании — мерцательная арит.мия
448 мс, 4472 мс), ЧСС днем 39—115/мин (ср. 56/мин), ЧСС ночью
27-68/мин (ср. 4б/мин.); желудочковых политопных экстрасистол и выскаль¬
зывающих сокращений 54, один куплет; пауз бо.тьше 2 с 3796, преимуществен¬
но в ночные часы (максимально 551/ч с 4 до 5 ч), 110 пауз от 3 до 4 с, 18 пауз
больше 4 с; без динамики.Была выполнена ЭхоКГ, по данным которой стенки аорты не изменены,
диаметр корня 3,3 с.м. Левое предсердие 4,4х6,2х5,4 см, объем 101 мл, левый
желудочек: КДР 4,8 см, КДО 121 мл, КСО 36 мл, МЖП 1,22 с.м, ЗСЛЖ 1,3 см,
ФВ 70%; локальная сократительная функция не нарушена. Правый желудочек
392КардиологияІІІІІіЩіІІШ ІІІІІ ііііІІІІЕгдйШУЇІІііІ^^ІІІ..1У-• ; ,Рис. 20.2. Электрокардиограмма больного П. Скорость записи 25 мм/с. Пояснен mi в
текстеРис. 20.3, Фрагметгт записи ЭКГ, полученной при холтеровском мониторировании в
отсутствие терапии
Глава 20. Случай болезни Фабри у взрослого глазами кардиолога..^ 3932,4 см, толщина стенки 3 мм, тфавое предсердие 6,0x4,5 см, объем 80 мл.
Митральный клапан; неравномерное уплотнение створок, систолический про¬
гиб створок до фиброзного кольца, незначительная регургитация в раннюю
систолу. Аортальный клалан не изменен. Трикуспидальный клапан: систоли¬
ческий прогиб створок до фиброзного кольца, незначительная регургитация
в раннюю систолу. Признаков легочной гипертензии нет. Нижняя полая вена2 см, на вдохе спадается более чем на 50%. Жидкости в полости перикарда нетПоскольку при ЭхоКГ были вьшаїеньї изменения (дилатация обоих пред¬
сердий, гипертрофия стенок левого желудочка), которые требовали уточнения,
исследование было проведено повторно профессором в,п. Седовым.При повторной ЭхоКГ (проф. В. П. Седов,20.4): аорта — синус Вальсальвы3,6 см, синотубулярное сужение 3 см, восходящий отдел 2,9 см; левое гфедсердие
203 мл (105 мл/м' при норме до 30). Левый желудочек: КДР4.8 см, КДО 113 мл,
КСО 35 мл, ФВ левого желудочка 68%, нарушений локальной сократимости нет;
ПЖ 3 см, МЖП 14 мм, ЗСЛЖ 15 мм. Митральный клапан: створки не уплот¬
нены, диаметр фиброзного кольца 4,1 см, регургитация 11—ИІ, dP/dt (скорость
нарастания давления, определяемая по струе митральной регургитации) более
1500 мм рт.ст. Аортальный юіапан: регургитапии нет. Трикуспидальный клапан:
регургитация I. СДЛА 27 мм рт.ст., легочная регургитаїцтя 1. Жидкость в полости
перикарда менее 150 мл. Заключение: гипертрофия левого желудочка средней
степени выраженности. Выраженная дилатация левого предсердия. Пролапс
задней створки митрального и септадьной створки трикуспидальиого клапана.
Митральная регургитация II—П1 степеїіи. Умеренное количество жидкости в
полости перикарда. Систоли^іеская функция левого желудочка сохранена при
уменьшении ударного объема за счет митральной регургитации.По данным нреспищеводной признаков внутрипредсерднош тромбоза,включая ушко левого предсердия, нет.Выявлены значительное увеличение левого предсердия и гипертрофия меж-
желудочковой перегородки.Рис. 20.4. Эхокардиография, изображение в 4-камерной позиции
394КардиологияТаким образом, у молодого человека, хорошо переносящего физіиеские
нагрузки, в течение нескольких лет имелась мерцательная аритмия, в зна¬
чительной степени обусловленная митральной регургитацией с выраженной
дилатацией левого предсердия, в сочетании с АВ-блокадой и неполной блока¬
дой правой ножхи пучка Гиса. При этом желудочковые аритмии практически
отсутствовали, несмотря на отчетливые признаки гипертрофии левого желу¬
дочка (без обструкции) по данным ЭКГ и Эхо КГ, не было признаков сердечной
недостаточности.Нааичие регургитации и пролабирования створок клапанов в сочетании с
паховой фьтжей заставляли думать о синдроме мезенхимальной дисплазии;
гипертрофия миокарда могла объясняться длительными тренировками («спор¬
тивное сердце»), а также быть проявлением истинной гиперірофической кардио-
миопатии, либо, что также не исключалось, болезни накопления. В то же время
4-кратное повышение титра антител к суммарному миокардиальному антигену
в сочетании с нарушениями ритма, проводимости и небольшим количеством
жидкости в перикарде могло отражать воспалительное поражение сердца (в том
числе в сочетании с одним из перечисленных состояний). Можно было подозре-
вать и различные сочетания перечисленных состояний (рис. 20.5). На этом этапе
случай обсуждался с генетиком, рекомендовано нpoлoлж^пъ обследоваїше.С учетом неясного характера первичного поражения сердца (диагноз оста¬
вался синдромны.м) было принято решение о проведении эндомиокардиальной
биопсии. Доступом через бедренную вену произведен забор 5 участков миокарда
правого желудочка и межжелудочковой перегородки (проф. В.А. Сулимов).
При исследовании биоптатов методом ПЦР (лаборатория <»ЛИТБХ») генома
вирусов Эпштейна—Барр, простого герпеса 1, 2, 6 типов, герпеса зостер и
цитомегаловируса не выявлено. Гистологическое исследование проводилось
на кафедре патологической анато.мии с курсом общей патологии ММА им.
И.М. Сеченова (проф. ЕЛ, Коган).При окраске гематоксилином-эозином {рис. 20.6, слева, см. цветную
вклейку) эндокард тонкмй, сосуды Тебезия со ск.піерозированньши стенками.инфекционно¬иммунныймиокардит«спортивноесердца»генетическаяпатология(синдроммезенхи¬мальнойдисплазии,нарушенияпроводимости)инфильтративноезаболеваниеРис, 20.5. Возможные диаптозы, которые обсуждались у больного П.
Глава 20. Случай болезни Фабри у взрослого глазами кардиолога.,, 395Кардиомиоциты с очаговым накоплением некой субстанции, вытесняющей в
виде округлой вакуоли все компоненты цитоплазмы по типу очагов миолиза с
формированием пустот в цитоплазме. При окраске по Ван Гизону слабо выра¬
женный склероз интерстиция. При ШИК-реаюдии обнаруживается накопле¬
ние мембраносвязанного ШИК-положительного вещества {рис. 20.6, справа).Наиболее вероятно, что данным веществом являлся гликоген, однако поло¬
жительную реакцию с реактивом Шиффа (фуксинсернистой кислотой) дают
также гликопротеины, полисахариды, ряд мукополисахаридов, гликолипиды и
ряд жирных кислот, При постановке ШИК-реакции реактив Шиффа (фуксин-
сернистая кислота) обрабатывается йодной кислотой; в случае положительной
реакции исследуемая ткань окрашивается в лИv^oвo-красный цвет.Клиническая картина в сочетании с данными биопсии позволяла думать
в первую очередь о взрослой форме гликогеноза 2-го типа (болезни Помпе),
при которой гликоген накапливается в лизосомах вследствие отсутствия лизо-
сомальной альфа-D-глюкозидазы и кислой мальтазът; характерно сочетание
миопатии с медленно прогрессирующей слабостью проксимальных отделов
преимущественно нижних конечностей, сколиоза грудного отдела, лордоза,
крыловидных лопаток, «гипертрофической» кардиомиопатии, медленно про¬
грессирующей сердечной недостаточности, АВ-блокады, гиперлипидемии.Описан, например, случай развития трепетания предсердий, эмболии
почечной артерии, АВ-блокады, гипертрофии левого желудочка и тяжелой
сердечной недостаточности (со снижением ФВ левого желудочка до 9%) в
отсугствие миопатии и поражения печени у пациента 45 лет с болезнью Помпе,
которому также была выполнена эндомиокардиальная биопсия.Кроме того, в литературе имеются описания сходной клинической картины
у пациентов с болезнью Фабри — представлен, в частности, больной 50 лет с
признаками гипертрофии сердца, снижением ФВ левого желудочка до 32%,
постоянной формой мерцательной аритмии и отсутствием ангиокератом,
парестезий в конечностях, гипогидроза и почечной недостаточности, которому
диагноз поставлен по результатам биопсии сердца; эффект проведенной фер-
ментзаместительной терапии подтвержден при повторной биопсии.Таким образом, требовалась окончательная верификация диагноза с
проведением биохимического и генетического исследований, в связи с
чем пациент был направлен к врачу-генетику. Больному проводилась тера¬
пия арифоном-ретард 1,5 мг/сут, омезом 40 мг/сут, де-нолом. По заверше¬
нии противоязвенного курса повторно проведена ЭГДС, эрозий не выяв¬
лено, назначена терапия тромбо-АССом 100 мг/сут. После выписки из
Факультетской терапевтической клиники им, В.Н. Виноградова отметил
постепенное снижение переносимости физических нагрузок, во время кото¬
рых стали беспокоить слабость, головокружение. В Российском научном цен¬
тре хирургии им. акад. Б.В. Петровского пациенту имплантирован постоян¬
ный ЭКС в режиме WIR, после чего его самочувствие заметно улучшилось.
Проконсультирован кардиохирургом — показаний к хирургическому лече¬
нию митральной недостаточности и проведению пластики левого предсердия
на данный момент нет.
396 КардиологияКомментарии Е.В. Заклязьминской — заведующей лабораторией медицинской
геветики РНЦХ им. акад. Б.В. Петровского РАМН, д-ра мед. наукНа первичном приеме врача-генетика были проведены общий осмотр паци¬
ента, анализ данных клинических и инструментальных исследований, осу¬
ществленных в Московской медицинской академии им. И.М. Сеченова, сбор
семейного анамнеза.При осмотре было обращено внимание на грубые черты лица (признак, харак¬
терный для большинства лизосомаїьньїх болезней накопления и связанный
с отложением патологического вещества в мягких тканях), множественные
ангиокератомы в нижней трети жітота, поясничной и ягодичной областях,
правостороннюю паховую грыжу (рис. 20.7, см. цветную вклейку).Из семейного анамнеза {рис. 20.8, а): дедушка по материнской линии умер в
возрасте 38 лет от хронической почечной недостаточности, у него имелись
жалобы на боли в сердце, однако точный диагноз остался неизвестным; у
матери пациента также имеются множественные ангиокератомы аналогич¬
ной локализации.Сочетание кардиальных («гипертрофическая» кардиомиопатия, мерцатель¬
ная аритмия, ШИК-позитивная инфильтрация в миокарде, немотивирован¬
ные подъемы АД) и экстракардиальных (молодой возраст, грубые черты лица,
ангиокератомы типичной локализации, нарушенная толерантность к теплу и
холоду, ампутация дистальной фаланги пальца, гипогидроз, паховая ірьгжа,
хроническая почечная недостаточность у близкого родственника) симптомов
no3B0jTMjiH предположить заболевание из группы наследственных болезней
обмена веществ. В качестве возможных вариантов рассматривались болезнь
Фабри, болезнь Данона, взрослая форма гликогеноза 2 (болезнь Помпе) или
митохондриальная кардиомиопатия {табл. 20. /).Как видно из табл. 20.1, наиболее вероятным представлялся диагноз болезни
Фабри.С целью подтверждающей диагностики было проведено биохимическое иссле¬
дование — определение акгивности фермента а-галактозидазы. Остаточная
активность а-галактозидазы составила 5,1 нМ/мг в час (норма 48,1-
150,3 нМ/мг в час). Таким образом, диагноз болезни Фабри был подтвержден.
Был также проведен поиск мутаций в гене X-Gal. У больного П. была выяв¬
лена новая мутация р. Q283K [замена аминокислоты глутамина (Gin, Q) на
лизин (Lys, К) в положении 283] в гемизиготном состоянии (рис. 20.8, б).
Выявление мутации, ответственной за заболевание, позволило провести
ДНК-диагностику другим членам семьи с целью вьывления носительства у
сестры больного. Выявление носительства мутаций у родственников больных
с болезнью Фабри имеет практическое значение, В настоящее время извест¬
но, что гетерозиготные носительницы мутаций в гене X-Ga/ могут иметь кли¬
нические признаки заболевания (от минимально выраженных до значитель¬
ных) и также нуждаются в динамическом наблюдении и лечении. В данной
семье три женшины ИЛ, 111.3, IV. 1 (см. рис. 20.8, а) являются носительницами
мутации, носительство мутации для ребенка (IV3) не определя-вдсь.
Схема представленности клинических особенностей пациента П. вкоторые рассматривались в качествеТаблица 20.1симитомокомплексе наследственных заболеваний,
вероятного диагнозаСимптомы, выявленные у
пациеитаБолезнь ФабриБолезнь ДанонаБолезнь Помпе,
взрослая формаМитохондриальнаякардиомиопатияГрубые черты лицаТипичноНе противоречитНехарактерноНехарактерноГиперфофия миокардаНе прогаворечитНе противоречитНе противоречитНе противоречитМерцательная аритмияНе противоречитНе противоречитНе противоречитНе противоречитПодъемы АДНе противоречитНе противоречитНехарактерноНе противоречитАктивные занятия спортом
(ка>шидат в мастера спорта,
спортиБная гребля)Не противоречитНе противоречитПротиворечит диа-
птозуПротиворечит диагнозуНакопление ШИК-
П03ИТИВН01Х) субстрата в
миокардеТипичноТипичноТипичноПрагиворечитАнгиокератомыТипичноНехарактерноНехарактерноНехарактерноГипогидрозТипичноНехарактерноНехарактерноНехарактерноАкропарестсзии, ампута¬
ции дистальных фалангТипичноНехарактерноНехарактерноНехарактерноБолезни сердца и/или
почек у рОДСТПеПЕІИКОВТипичноТипичноВозможноТипично«Вертикальное» наследо¬
вание, мужчины болеют
заметно тяжелееТипичноТипичноПротиворечит диа¬
гнозуНехарактеріго
398 КардиологияБолезнь Фабри — наследственное мультисистемное заболевание, обу¬
словленное мутациями в гене X-Gal, кодирующем лизосо\гаый фермент
а-галактозидазу. Снижение активности фермента ведет к прогрессируюшеліу
накоплению глоботриаозилкерамида (GB-3) и родственных гликосфинго-
лшшдов в лизосомах клеток эндотелия сосудов, нервных, миокардиальных,
всех типах ренальных клеток. Заболевание наследуется по Х-сцепленному
рецессивному типу, при этом женщины — носительницы мутаций — также
могут иметь клинические признаки заболевания.По данным на 1998 г., заболеваемость болезнью Фабри среди мальчиков
составляла 1:1 ООО ООО. По данным европейских скрининговых исследовании,
распространенность заболевания на сегодняшний день составляет около
1:40 ООО населения, однако в некоторых клинических группах его частота
значт-ггельно выше. Представление о том, что болезнью Фабри болеют только
мужчины, на сегодняшний день не соответствует истине; у женшин — носи¬
тельниц генетической мутации заболевание также развивается, но в более
поздние сроки и в менее яркой форме, в связи с чем точный учет заболе¬
ваемости среди женщин труден. Последние данные отражают более честный
подход к учету заболевишх, который основан на изменившихся представле¬
ниях о диагностике латентных форм болезни.По данным разных авторов, 3—12% пациентов с необъяснимой гипер¬
трофией левого желудочка (чаще всего концентрической), около 2%
больных с ишемическими инсультами и 0,5% больных с хронической
почечной недостаточностью страдают этим заболеванием. В настоящее
время выявляемость болезни Фабри остается низкой. Хотя клинические
признаки заболевания проявляются еще в детском возрасте, оно долгое
время остается нераспознанным. Средний возраст постановки правиль¬
ного диагноза составляет около 30 лет. Приведенный случай выявления
болезни Фабри у пациента П, в возрасте 32 лет является примером такой
диагностики.Болезнь Фабри необходимо исключать, если у пациента наблюдается сочета¬
ние трех или более вышеперечисленных признаков:1) гипертрофическая необструктивная кардиомиопатия;2) микроальбуминурия, протеинурия или хроническая почечная недостаточ¬
ность неясной этиологии;3) ранние инсульты (до 55 лет);4) ангиокератомы, особенно в нижней трети живота, паховой и ягодичной
областях;5) артериальная гипертензия;6) акропарестезии (ощущение жжения или покалывания в кончиках пальцев
кистей и стоп, особенно на холоде или в тепле), плохая переносимость жары
и холода, частые ожоги или обморожения;7) гипогидроз (сниженное потоотделение);8) нар>тпения зрения и/или слуха;9) наличие вышеперечисленных заболеваний у родственников, особенно
мужского пола.
Глава 20. Случай болезни Фабри у взрослого глазами кардиолога..399IV1 год4 года5 летG Т А А С ТС А G А Т G G С С С НОРМА
G Т А А С ТА А G А Т G G С С С М\ОАЦИЯ Q283KРис. 20-8. Родословная семьи П. и фрагмент прямого секвениропания последова¬
тельности экзона 6 гена X-Gal: а — римскими цифрами отмечены номера поко¬
лений, арабскими — помер человека в поколении. Стрелкой отмечен пробанд
(пациент П.). Темными символами отмечены больные члены семьи, шірихован-
ными — женщины — носительницы мутации p.Glu23}jLys; б — стрелкой отмечено
место мутации. Вверху приведена расшифровка выявленной нуклеотидной после¬
довательности, для сравнения выше приведен нормальный фрагмент последова¬
тельности гена X-GalНа рисунке 20.9 представлены примерные сроки манифестации различных
юшнических проявлений болезни Фабри. Поражение сердца относится к
одним из наиболее поздних проявлений заболевания; клиническая диагно¬
стика существенно затрудняется в отсутствие наиболее типичной патологии
400Кардиология(почечной), которая, как правило, машіфестирует уже в детском возрасте и
служит основой для диагностики болезни Фабри у детей.Динамическое наблюдение за пациентами с болезнью Фабри должно
включать:• каждые 6 мес — лабораторные исследования мочи и крови (общий белок,
альбумин, креатинин, мочевина, 25-OHvitD, гемоглобин, тромбоциты,
липидный профиль, электролиты);• каждый год — ЭКГ, холтеровское мониторирование ЭКГ, ультразвуковое
исследование сердца, почек, консультацию окулиста;• 1 раз в 2 года — аудиофамму;• МРТ головного мозга, догшлерографию при постановке диагноза, далее —
по показаниям.Патогенетигческой терапией болезни Фабри является пожизненная фермент¬
ная заместительная терапия. В этом году в России бьыи зарегистрированы
два препарата, представляющие собой рекомбинантные белки: альфа-галак-
тозидаза и бета-галактозидаза. В настоящее время решается вопрос о предо¬
ставлении пациенту П. ферментной заместительной терапии.С целью коррекции кардиологических проявлений болезни используются:• исключение курения и других факторов риска;• антиангинальные средства (р-адреноблокаторьт, блокаторы кальциевых
каналов, нитраты);• медикаментозное лечение сердечной недостаточности (диуретики, инги¬
биторы АПФ, дигоксин);Заболевания сердцаЗаболевания ЦНСЗаболевания почек
АкропарестезииУтомляемость, депрес¬
сии, трудности
в обученииг10Возрастманифестации“Т20Возраст, годы30 а 40Возраст
постановки диагнозаРис. 20.9. Сроки манифестации клинических проявлений болезни Фабри
Глава 20. Случай болезни Фабри у взрослого глазами кардиолога... 401• антиаритмические препараты, имплантация ЭКС или кардиовертера-
дефибриллятора;• антиатрегантные или антикоагу;іянтньіе препараты;• статины;• хирургическая коррекция клапанной патологии сердца, трансплантация
сердца.Кроме того, ингибиторы АПФ и/или блокаторы рецепторов к ангиотензи-
ну применяются у больных с почечными проявлениями болезни Фабри; с
осторожностью назначаются препараты, обладающие нефротоксичностью;
на поздних стадиях болезни применяются гемодиализ (выживаемость невы¬
сокая) и трансплантация почек (неродственная либо родственная с исклю¬
ченным носительством мутаций в гене X-Gal).При наличии желудочно-кишечных расстройств используются низкожиро¬
вая диета, частое дробное питание, средства, улучшающие перистальтику,
панкреатические ферменты. Ангиоксратомы, которые доставляют бес¬
покойство больному, могут уда,тяться с помощью лазера. При [іеобходимо-
сти проводятся также коррекция зрения/слуха, терапия болевых кризов,
назначаются антидепрессанты, осуществляется психологическое сопрово¬
ждение больных и их родственников. Важным аспектом помощи пациен¬
там с болезнью Фабри яв;іяется медико-генетическое консультирование и
помощь в планировании семьи.Таким образом, диагноз, который оказался трудным для интернистов, мог
быть с самого начала заподозрен на основании не только поражения сердца,
но и друтих клинических признаков, на которые сразу обратила внимание
ї'енетик. Одіїако, по-видимому, в данном случае подтвердилась правиль¬
ность известного принципа «диагностируешь то, что знаешь» (еще точ¬
нее — что видел). До получения данных эндомиокардиальной биопсии мы
рассмагривали болезни накопления лишь как одну из нескольких причин
выявленного у пациента поражения сердца.Необходимо отметить, что в России на сегодняпший день выявлено 11 паци¬
ентов с болезнью Фабри, включая данный клинический случай.ЛИТЕРАТУРАBen-Ami R., Pugfisi J., Haider Т., Mehta D. The Momit Sinai Hospital clinical
pathological conference: a 45-year-old man with Pompe’s disease and dilated cardio¬
myopathy // Mt. Sinai J. Med. 2001; 68 (3): 205-212,Brenner B., Gruunfeld J.-P. Renoprotection by enzyme replacement therapy I j
Curr. Opin. Nephrol. Hypertens. 2004, 13: 231—241.Eng C.M., Germain D.P., Banikazemi M. et al. Fabr>' disease: Guidelines for the
evaluation and management of multi-organ system involvement // Genet. Med. 2006;
Vol. 8. N 9: 539-548.Eng C.M., Guffon -N., Wilcox W. et al. Safety and efficacy of recombinant human
A-galactosidase; A replacement therapy in Fabry’s disease // NEJM; V. 345, № 1; 9—16.
402 КардиологияFrustaci А., Chimenti С., Ricci /?. et al. Improvement in cardiac function in the
cardiac variant of Fabr>’’s disease with galactose-inlusion therapy // N. Engl. J. Med.
2001 Jul 5; 345 (1); 25-32.Sims K., PoUtei J., Banikazemi M. et al. Stroke in Fabry disease frequently occur
before diagnosis and in the absence of other clinical events // Stroke, 2009, 40; 2-7.Wang R. Y., Letts A., Mirocha J. et al. Heterozygous Fabry women arc not just car¬
riers, but have a significant burden of disease and impaired quality of life // Genet.
Med. 2007.9(1): 34-45.
Глава 21АРИТМОГЕННАЯ ДИСПЛАЗИЯ ПРАВОГО
ЖЕЛУДОЧКА (ПРАВОЖЕЛУДОЧКОВАЯ
КАРДИОМИОПАТИЯ): ПОЛИМОРФИЗМ
КЛИНИЧЕСКИХ ПРОЯВЛЕНИЙО.В. Благова, Л.В. Недоступ, И£, Морозова,ЕЛ. Коган, Н.В. Гагарина, В.П. Седов, Е.В. Заклязьминская,
Ю.В. Фролова, С.Л. ДземешкевичЕше 10—15 лет назад диагноз «аритмогенная дисплазия правого желудочка»
(АДПЖ) практически не ставился в Факультетской терапевтической клинике
им. В.Н. Виноградова, хотя такие больные, безусловно, попадали в поле наше¬
го зрения.Представление об этом генетическом заболевании, которое традиционно
рассматривается в одном ряду с каналопатиями, пришло к нам от интервенци¬
онных аритмологов (что в значрггельной степени было обусловлено внедрением
метода радиочастотной аблации и имплантации кардиовертеров-дефибрилля-
торов в лечение жизнеугрожаюших желудочковых нарушений ритма) и долгое
время было достаточно ограниченным: диагноз аритмогенной дисплазии пред¬
полагался в перв>то очередь у молодых женщин с «идиопатической» частой
правожелудочковой экстрасистолией. Возможность проведения МРТ сердца с
целью выявления жировых включений в миокарде сделала постановку диагноза
впо.ше реатьной. Однако лишь использование морфологической диагностики
(как прижизненной, так, к сожалению, и посмертной) позволило нам ради¬
кально изменить представление об этом заболевании и рассматривать его не
просто как одну из причин «идиопатических» аритмий, но как одну из нередких
первичных кардиомиопатий, которая приводит к выраженному поражению
миокарда обоих жел>'дочков и, кроме того, в половине случаев сочетается с
миокардитом, вносящим существенный вклад в клиническую картину болезни.Мы приводим анализ собственного опыта наблюдения за 15 пациентами с
достоверным и вероятным диагнозом аритмогенной дисплазии правого желу¬
дочка (диагноз ставился согласно оригинальным, а затем модифицированным
европейским критериям болезни), на основании которого можно выделить
отдельные клинические варианты болезни и пред^тожить дифференцирован¬
ную терапию.Первое описание заболевания было представлено в 1977 г. G. Fontaine.
Термин «аритмогенная дисплазия правого желудочка» был предложен для
обозначения болезни, ведущей к внезапной смерти у молодых людей с пра¬
вожелудочковой тахикардией, не имеющих структурных аномалий сердца.
404 КардиологияДля лечения тахикардии бьыо предложено выполнение вентрикулотомии;
при этом определялось выраженное истощение мышцы правого желудочка
и ее жировое замещение, что позволило проводить аналогии с болезнью Уля
(«пергаментное сердце») и говорить о генетической природе заболевания. На
сегодняшний день аритмогенная дисплазия правого желудо^іка определяется
как генетически детерминированное фиброзно-жировое замещение миокарда
преимущественно правого желудочка, которое проявляется в перв>то очередь
правожслудочковыми нарушениями ритма (экстраеистолией, желудочковой
тахикардией) с высоким риском внезапной сердечной смерти. В классифи¬
кации АСС 2006 г. аритмогенная дисплазия правого желудочка отнесена к
первичным генетртческмм кардиомиопатртям и носит название «правожелудоч¬
ковая кардиомиопатия».К 1982 г бьито описано 56 случаев заболевания, 24 из которых диагно¬
стировали G. Fontaine и соавт, На сегодняшний лень частота встречаемости
аритмотснпой дисплазии правого желудочка в общей популяции составляет
1 на 2—5 тыс. населения, что почти сопоставимо с частотой выявления гипер¬
трофической кардиомиопатии или системной красной волчанки. Однако
аритмогенная дисплазия правого желудочка гораздо менее известна не только
широкому кругу врачей, но и специалистам — кардиологам, кардиохирургам,
а также морфологам. Заболевание традиционно рассматривается в разряде
каналопахий, диагностируется главным образом клиническими и интервенци¬
онными аригмологами, при постановке диагноза рассматривается как показа¬
ние к консультаиии генетика. Хотя основной тип наследования аритмогенной
дисплазии правого желудочка — аутосомно-доминантный, женщины болеют в
3 раза чаще муж^шн.Генетический дефект, ведущий к развитию аритмогенной дисплазии правого
желудочка, залюжен на уровне белков десмосом — плакоглобина, десмоплаки-
на, плакофилшш , десмоглеи на. Нормальные десмосомы обеспечивают проч¬
ный механический контакт между клетками в тканях, которые подвергаются
серьезным механическим нагрузкам (кожа, мышцы). Интересно отметить, что
с синтезом аутоантител к десмосомам кожного эпителия связывают развитие
пузырчатки: это приводит к разрыву слоев эпидермиса. Описана и врожденная
(буллезная) пузырчатка. Видимо, аналогичным образом можно представить
себе процессы, происходящие в сердце.В 1994 г были предложены критерии постановки диагноза аритмогенной
дисплазии правого желудочка, которыми мы пользовались до последнего вре¬
мен и {табл. 21.1). Наряду с отягощенным семейным анамнезом (в том числе
случаями внезапной смерти в молодом возрасте) и гистологией (основное
значение придавалось обнаружению жировой ткани), решающее значение
имели две группы признаков: правожелудочковые аритмии в сочетании со
специфическими изменениями в правых грудных отведениях и дисфункция
правого желудочка с наличием аневризм и участков дискинеза. Методы опенки
правош желудочка могли быть разными, но в последнее 10-летие «золотым*
стандартом неинвазивной диаіностики аритмогенной дисплазии правого
желудочка стала МРТ сердца, которая позво^тяет выявлять жировые включения
Глава 21. Аритмогенная дисплазия правого желудочка,..405Европейские критерии диагностики АДПЖ (1994 г.)Таблица 21.1ФакторБольшие критерииМалые критерииСемейныйанамнезДоказанные аутопсией/биоп¬
сией случаи аритмогенной дис¬
плазии правого желудочка1, Случаи внезапной смерти п моло¬
дом возрасте.2. Клинически доказанные случаи
аритктогснной дисплазии правого
желудочка ЭКГVI—V3; эпсилон-волна (є) в
конце QRSV1-V3: QRS >0,11 с (признаки
замедленной деполяризации
желудочков)1. Более 1000 ЖЭ в сутки.2. Мономорфная желудочковая тахи¬
кардия с ЭКГ-картиной блокады
левой ножки пучка Гиса.3. Нарушение рсполяризации в VI—V3
(отрицательный зубец 7', подъем ST) у
лиц старше 12 лет без блокады правой
ножки пучка Гиса.4. Поздние потенциалыжелудочковГистологияЖировая ткань >40%]. Жировая ткань >3%.2. Лимфоцитарные инфильтратыДисфтекиияправогожелудочка1. Значимая дилатация со
снижением фракции выброса
правого желудочка.2. Сегментарное поражение с
вовлечением левого жел>'Дочка.3. Аневризмы Умеренная дилатация без снижения
фракции выбросав миокарде правого желудочка. Этот признак не нашел отражения в критериях,
но именно на него в первую очередь ориентирова-тись клиницисты.Наш опыт постановки диагноза аритмогенной дисплазии правого желудоч¬
ка включает около полутора десятков пациентов, свидетельствует о большом
клиническом полиморфизме этого заболевания и позволяеі' говорить как
минимум о трех вариантах течения заболевания, которые мы и рассмотрим.
В 9 случаях диагноз аритмогенной дисплазии правого желлдачка не вызывает
сомнений, еще у 6 пациентов он рассматривается как вероятный.Вариант I назван типичным, поскольку именно таково было наше пред¬
ставление о больных аритмогенной дисплазией правого желудочка, и именно
этот вариант пока преобладает среди наших больных. Итак, в типичном случае
пациент с аритмогенной дисплазией правого желудочка — это молодая жен¬
щина (обычно 30—40 лет, но диагноз ставится и в более позднем возрасте), у
которой выявлена частая (обычно более 10 тыс. в сутки) правожелудочковая
экстрасистолия, нередко упорная, устойчивая к антиаритмическим препаратам
(могут развиваться и эпизоды желудочковой тахикардии, чаше неустойчивой).
При этом отсутств\тот признаки так называемого органического поражения
сердца (в первую очередь структурно-функциональные изменения, выявляе¬
мые при ЭхоКГ) и не связанные с аритмией кардиальные симптомы; экстра¬
систолия у них чаще всего рассматривается как идиопатическая. Ключом к
постановке диагноза аритмогенной дисплазии правого желудочка становится
обнаружение жира в правом желудочке при МРТ.
406 КардиологияПервая больная (М., 45 лет) с диагнозом аритмогенной дисплазии право¬
го желудочка, поставленным в НЦССХ им. А.Н. Бакулева, была именно
такой. С 35 лет она отмечала появление перебоев в работе сердца, сердце¬
биения; R 2001 г. при обследовшши в Факультетской терапевтической клинике
им. В.Н. Виноградова было зарегистрировано около 2500 желудочковых экстра¬
систол в сутки, состояние было расценено как нейроциркуляторная дистония,
назначен атенолол. Однако вскоре отмечено нарастание числа желудочковых
экстрасистол до 5,5-10 тыс./сут, назначался кордарон. В 2003 г. в НЦССХ
им. А.Н, Бакулева была проведена МРТ сердца: при небольших размерах
правою желудочка (КДР 25 мм) отмечены расширение его выводного отдела
до 33 мм, а также волнистость контура свободной стенки правого желудочка с
участками локального истончения до 2—3 мм. Поставлен диагноз аритмогенной
дисплазии правого желудочка и предложено проведение радиочастотной абла¬
ции, от которой больная отказалась; в качестве антиаритмического препарата
назначен соталол, для подбора медикаментозной терапии бьша направлена в
Факультетскую терапевтическую клинику им. В.П. Виноградова. На ЭКГ реги¬
стрировалась частая правожелудочковая экстрасистолия, специф№іеских изме¬
нений комплекса QRS в ответвлении V, и отрицательных зубцов Тне 6ы,ю.В процессе подбора антиаритмической терапии выяснилось, что соталол
оказался эффективнее этацизина, и больная продолжала принимать его в
максимально переносимой дозе (80 мг/сут). При этом к 2007 г. число правоже¬
лудочковых экстрасистол снизилось до 107/сут, особенно после проведенного
по поводу невралгии курса терапии нестероидными противовоспалительными
препаратами. Столь необычное течение «аритмогенной дисплазии правого
желудочка» заставило провести обследование больной на миокардит: были
выявлены высокие титры антикардиальных антител: IgG к миокардиальной
ткани 1:400 при норме до 1:100, АНФ (с антигеном сердца быка) 1:160, анти¬
тела к антигенам эндотелия 1:320 (при норме до 1:40). Эти данные в сочетании
с благоприятным течением заболевания позволили пересмотреть исходный
диагноз аритмогенной дисплазии правого желудочка в пользу миокардита.
После к>тзса специфической терапии (ацикловир, плаквенил) желудочковая
экстрасистолия на фоне терапии соталолом отсутствовала. По сути дела, у
больной никогда не было достоверных признаков аритмогенной дисплазии
правого желудочка и даже включений жировой ткани в миокард правого желу¬
дочка по данным МРТ сердца — диагноз был поставлен лишь на основании
наличия частой правожелудочковой экстрасистолии в сочетании с минималь¬
ными изменениями правого желу'дочка по МРТ сердца.Уже первое наше столкновение с диагнозом аритмогенной дисплазии
правого желудочка показало необходимость дифференциальной диагностики с
миокардитом. В Итатии (г. Падуя), где число больных с аритмогенной диспла¬
зией правого желудочка существенно выше, чем в европейской популяции, и
і де у\теют ставить этот диагноз, была выполнена эндомиокардиальная биопсия
у 30 больных с достоверной (согласно критериям 1994 г) аритмогенной дис¬
плазией правого желудочка: диагноз был подтвер>ідіен только в 50% случаев,
у второй половины больных выявлены морфологические признаки активного
Глава 21. Аритмогенпая дисплазия правого желудочка... 407миокардита. Верификация диагноза определила верную тактик}^ лечения:
среди 13 больных с аритмогснной дисплазией правого желудочка, которым
имилантирован кардиовсргер-дефибриллятор, его срабатывание отмечено у
47%; среди больных миокардитом кардиовертср-дефибриллятор бььт имплан¬
тирован только одному пациенту, рецидивов аритмии у него не было.У следующей нашей больной (И., 34 года) дифференциальная диагностика
шла именно по такому пути. С 25 лет у нее без видимой причины возникла
частсш желудочковая экстрасистолия (до 24 тыс./сут), однократно (на 5-й день
приема этацизина) развился эпизод желудочковой тахикардии с потерей
сознания; при внутриссрдечном электрофизиологическом исследовании бьыа
индуцирована желудочковая тахикардия из выводного отдела правого желу¬
дочка. Была проведена радиочастотная аблация аритмогенной зоны выводного
отдела правого желудочка, после которой развилась субфебри.'іьная лихорадка.
В связи с подозрением на миокардит проводилась терапия нестероидными
противовоспалительными препаратами. Через 2 года, в 27 лет, у больной при
проведении чреспищеводного электрофизиологического исследования была
индуцирована АВ-узловая реципрокная тахикардия. Повторно была выполне¬
на радиочастотная аблация, в этот раз направленная на устранение медленного
атриовентрикулярного пути проведения в АВ-соединении. Одновременно в
связи с выявленным гипертирсозом был проведен курс терапии мерказолилом
В дальнейшем эпизодов АВ-узловой реципрокной тахикардии не было, число
желудочковых экорасистол на фойе терапии конкором, соталолом, ритмо-
нормом было невелико. Однако в течение последнего года отмечено возобнов¬
ление частой желудочковой эксграсистолии (до 24 тыс./сут), которая хорошо
поддавалась терапии пропафсноном (450 мг/сут).Волнообразность течения болезни, периодические боли в области сердца,
снижение толерантности к физическим нагрузкам, наливше неглубоких отри¬
цательных зубцов Т на ЭКГ {рис. 21.1) требовали исключения миокардита,
наряду с аритмогенной дисплазией правого желудочка. При МРТ сердца по
передней стенке правого желудочка выявлен участок истончения миокарда
(около 11 мм) с наличием жировых включений и признаками локального дис-
кинеза; выводной тракт правого желудочка бьы расширен (37 мм), с признака¬
ми гипокинезии передней стенки правого желудочка, что свидетельствовало в
пользу аритмогеїшой дисплазии правого желудочка. Однако выявлены также
утолшение и уплотнение перикарда лракт№іески по всему периметру с сепа¬
рацией листков перикарда до 6 мм и утолщением слоя эпикардиального жира,
что было расценено специаіистами по лучевой диагностике как поствоспа^чи-
тельные изменения. Среди антикардиальных антител были повышены (1:300)
только TgG к суммарно\гу миокардиальному антигену. Специфического АИФ
обнаружено не было, повышения титра антитела к антигенам эндотелия, кар-
диомиоцитов и проводящей системы сердца (1:80) также не отмечено.Таким образом, имелись лишь 3 малых ЭКГ-критерия аритмогенной диспла¬
зии правого желудочка (более 1 ООО желудочковых экстрасистол в с>тки, моно-
морфная желудочковая тахикардия с ЭКГ-морфологией блокады левой ножтси
пучка Гиса, отрицательный Г в V — V^), два из которых могли трактоваться в
40SКардиология- .Ш :: L1'■ / J'( ■' ■.. ■■1■йотгJr-Цчщ ■VРис. 21.1. ЭКГ больной И., 34 года (диагноз аритмогенной дисплазии правого желудоч¬
ка подтвержден морфологичсскії)рамках миокардита. Точный диагноз, определяющий дальнейшую тактику
лечения, не мог быть постааіен без морфологического исследования. Больной
была выполнена эндомиокардиальная биопсия из правого желудочка, при
которой полностью подтвержден диагноз ариї могенной дисплазии: выявлены
уто.чшение и склероз эндотелия, в субэндокардиальньтх отделах адипозониты
занимают до 50% площади, отмечаются фиброз и перестройка архитектоники
с образованием фиброзных септ, сосуды единичны; признаков миокардита не
выявлено (проф. Е.А. Коган). С учетом этих данных больной имплантирован
кардиовертер-дефибриллятор, продолжена терапия пропафсноном.В третьем случае (больная И-ва, 43 года) наличие миокардита с самого нача¬
ла не вызывало у нас сомнений (рис. 22,2): желудочковая экстрасистолия впер¬
вые была выявлена у больной в возрасте 17 лет, однако случаи ее появления
значительно участились в 2007 г. после перенесенного острого респираторного
вирусного заболевания; тохда же появились слабость, тяжесть в области серд¬
ца, выявлены повышенные титры антител к миокарду (1:400) и герпетическим
вирусам, отмечались умеренная дилатация камер сердца, блокада левой ножки
пучка Гиса. Бьгл проведен курс лечения ацикловиром. Толерантность к нагруз¬
кам оставалась сниженной. К концу 2009 г. число желудочковых экстрасистол
возросло до 37 тыс./сут, соталол эффекта не давал. В начале 2010 г обследова¬
лась в Факультетской терапевтической клинике им. В.Н. Винофадова, было
начато насыщение кордароном, на фоне которого число желудочковых экс¬
трасистол снизилось до 6 тыс./сут.Сохранялась умеренная дилатация камер сердца (КДР левого желудочка6,2 см) со снижением ФВ левого желудочка до 49% и лока,1ьными гипо-
кинезами переднего, переднеперегородочного и всех сегментов верхушки.
Титры антикардиальньтх антител оказались сутцественно повышены (антитела
Глава 21. Аритмогенная дисплазия правого желудочка.40917 лет 2007 04.2008 11.2009 02.2010 03.2011ОРВИЖЭдилатация камер КДР 6,2 см, ФВ 49%гипокинез,терапия ацикловир плаквенил 400 мг.валтрексРис. 21.2. Анамнез заболевания пациентки И-пой, 43 года (сочетание миокардита и
аритмогенной дисплазии правого желудочка)к эндотелию 1:160, к проводящей системе 1 ;320, к кардиомиоцитам и гладкой
мускулатуре 1:80, специфического АНФ выявлено не было). Были выяв^тены
IgG к герпетическим вирусам, парвовирусу В19. Бьыа начата терапия вал-
трексом мовалисом и плаквенил ом 400 мг/сут, в результате которой лабора¬
торные признаки активности иммунного воспа-'іения значительно снизились,
число желудочковых экстрасистол на фоне терапии кордароном не превы¬
шало 1500/с>т. Однако с марта 2011 г., после очередной острой респираторной
вирусной инфекции, вновь отмечено нарастание числа желудочковых экстра¬
систол до 10 тыс./сут и утвеличение титра антикардиальных антител.На ЭКГ от 2010 г. (c.w. рис. 21.3), наряду с признаками полной блокады левой
ножки пучка Гиса, отмечались двухфазные (отрииательные) зубцы Т в правых
грудных отведениях, которые рассматривались в рамках миокардита. Через
год этих изменений не было. При оценке динамики эхокардиографичсских
параметров в течение того же срока отмечена полная нормализация размеров
левого желудочка (КДР 4,7 см) и ФВ левого желудочка (64%), однако правый
желудочек оставался увеличенным (в 2010 г. — 4,2 см, в 2011 г. — 3,3 см при
норме до 3 см). Эти данные, а также правожелудочковый характер экстраси¬
стол ии заставили, несмотря на не вызывающий сомнений миокардит, провести■ ' 'ІіИіРис. 21.3. ЭКГ (отведения VI—V3) больной И-вой, 43 года (2010 г. слева, 2011 г. справа)
410 КардиологияMPT сердиа дяя исключения аритмогенной дисплазии правого желудочка; при
этом выявлены выраженное расширение правого желудочка (до 57 мм в диа¬
столу) в сочетании с волнообразностью контуров его стенки и ее локальным
выбуханием. Если обратиться к критериям аритмогенной дисплазии правого
желудочка 1998 г., то у болыюй имеются 1 большой (значимая дилатация пра¬
вого желудочка) и 2 малых критерия (более 1000 желудочковых экстрасистол
в сутки, па ЭКГ — отрицательные Т в V,—V,), что позволяет говорить лишь о
вероятном диагнозе.Однако в конце 2010 г. на основании многолетнего анализа opHrnnajTbHbix
критериев 1994 1. были предложены модифицированные критерии аритмо¬
генной дисшшзии правого желудочка {табл. 21.2), в которых существенно
уточнена диагностически значимая степень поражения правого желудочка (для
каждого из методов исследования отдельно, включая МРТ сердца). При этом
обнаружение жировой ткани в миокарде правого желудочка при магнитно-
резонансной томографии сердца по-прежнему не рассматривается в качестве
критерия диагностики аритмогенной дисгьтазии правого желудочка. Авторы
модифицированных критериев пишут о том, что само по себе обнаружение
жировой ткани в миокарде правого желудочка при МРТ сердца (без признаков
фиброза) возможно и у здоровых людей и не может считаться специфичным.
Важно отметить, что и в гистологических критериях аритмогенной дисіитазии
правого желудочка подчеркивается необязательность обнаружения жировой
ткани в миокарде правого желудочка: главным для постановки диагноза арит¬
могенной дисплазии является наличие массивного фиброза правого желудочка
с замеш,ением как минимум 25—40% кардиомиоцитов. С др>той стороны, и
оценка фиброза с помощью отсроченного накопления гадолиния в правом
желудочке затруднена в связи с тонкостью ею стенки и наличием жировых
включений, которые осложняют диагностикуЭКГ-критерии разделены на три группы, каждой из которых придается
самостоятельное значение: инверсия зубцов Т в правых отведениях, эпсилон-
волна и возникновение желудочковой тахикардии с морфологией блокады
левой ножки пучка Гиса; меньшее значение имеет наличие поздних потен¬
циалов желудочков (которые мы практически никогда не проверяем). Очень
существенно снижено пороговое количество желудочковых экстрасистол —
достаточно всего 500 желудочковых экстрасистол в сутки, частая желудочковая
экстрасистолия не делает диагноз более достоверным. В графу «семейный
анамнез» добавлено указание на идентификацию патогенных мутаций у самого
пациента (в прежних критериях указаний на генетику не было).Применив модифицированные критерии к пациенгке И-вой, 43 лет, мы
обнаруживаем у нее 2 больших критерия (расширение правого желудочка с
нарушением его локальной сократимости, отрицательные зубцы Т на ЭКГ в
правых грудных отведениях) и 1 малый (более 500 жел>'дочковьгх экстраси¬
стол в сутки), что делает диагноз аритмогенной дисплазии правого желудочка
достоверным. Однако с у^іетом преходящего характера H3.vfeHeHHft зубцов Т в
правых грудных отведениях ЭКГ планируется верификация диагноза с помо¬
щью ДНК-диагностики. О сочетании миокардита и аритмогенной дисплазии
Глава 21. Аритмогенная дисплазия правого желудочка.4UТаблица 21.2Модифицированные критерии диагностики АДПЖ, 2010 г.ПараметрБольшие критерииМалые критерииI. Еюбальная/
региональная
дисфункция и
структ>фные
измененияПри ЭхоКГ:1) региональная акинезия, дис-
кршезия или аневризма правого
желудочка;2) и один или более признаков
(конец диастолы):• ПЖ (длинная ось) >32 мм
(индекс >19 мм/м-);• ПЖ (короткая ось) >36 мм
(индекс >21 мм/м^);• или региональные наруше¬
ния <33%.При МРТІ1) региональная акинезия, или
дискинезия, или диссинхрония
сокращения правого желудочка;2) и один или более признаков:• отношение КДО ПЖ к
поверхности тела >110 мл/м^
(у мужчин) и >100 мл/м^ (у
женщин);• или ФВ правого желудочкаПри ЭхоКГ:1) региональная акинезия или
дискттнезия правого желудочка;2) и один признак или более
(конец диастолы):• ПЖ (длинная ось) 29-31 мм
(индекс 16—18 ммДг);• ПЖ (короткая ось) 32-35 мм
(индекс 18—20 мм/м^);• или регион ап ыгьте нарчтпе-
ния 34-40%.При МРТ:1) региона.г1ьная акинезия, или
дискинезия, или диссинхрония
сокращения правого желудочка;2) и один признак или более:• отношение КДО ПЖ к
поверхности тела 100-
109 мл/М' (у мужчин) и
90-99 мл/м^ (у женшин);• или ФВ правого желудочка
41-При вентрикулографии правого
желудочка:региональная акинезия, дис¬
кинезия или аневризма правого
желудочкаТТ. ГистологияСохранные миоциты <60% при
морфо метрическом анализе
(или <50% при точной оценке)
с фиброзным замещением мио¬
карда свободной стенки правого
желудочка в >1 участке, с жиро¬
вым замещением ткани (при
эндомиокардиальной биопсии)
или без негоСохранные миоциты 60-75%
при морфомстрическом анализе
(50—65% при точной оценке) с
фиброзным замещением мио¬
карда свободной стеттки правого
желудочка в >1 участке, с жиро¬
вым замещением ткани (при
эндомиокардиальной биопсии)
или без него11І.Нарушенияреполяриза¬цииИнверсия зубцов Т в правых
грудных отведениях (V1-V3) или
дальше у лип старше 14 лет (в
отсутствие полной блокады пра¬
вой ножки пучка Гиса с шириной
ОУг^-^ПОмс)Инверсия зубцов г в отведени¬
ях V1-V2 у лиц старше 14 лет
(в отсугствие полной блокады
правой ножки пучка Гйса) или в
V4-V5, и.'Ш в V6.Инверсия зубцов Т в отведениях
V1-V4 у лиц старше 14 лет при
наличии полной блокады правой
ножки пучка Гиса
412КардиологияОкончание таблицы 21.2IV. Нарушения
леполяриза-
ции/проведе-
нияЭпсилон-волна (воспроизводи¬
мый низкоамшіитудньїй сигнал
между окончанием комплекса
QRS и началом зубиа 7) в правых
грудных отведениях (V1-V3)L Поздние потенциалы желу¬
дочков (по 1—3 параметрам) на
сигнал-усредненной ЭКГ
в отсутствие расширения10 мс на стандартной ЭКГ;• фильтрованная длительность
0/?5’>114mc;• продолжительность конеч¬
ной части QRS (аіитєльность
низкоамплитудного сигнала)
>38 мс;• JRMS вольтаж конечной части
QRS <20 мВ,2. Продолжительность конечной
активации QRS >55 мс (от верши¬
ны зубда S до конца QRS, вклю¬
чая R'Б отведениях VI, V2 или
V3 в отсутствие блокады правой
ножки пучка Гиса) V. АритмииНеустойчивая или устойчивая
желудочковая тахикардия с мор¬
фологией блокады левой ножки
пу'чка Іиса и верхней осью (отри¬
цательные или неопределенные
комплексы QRS в отведениях И,
ПІ, aVF и положительные в отве¬
дении aVL)Неустойчивая или устойчивая
желудочковая тахикардия из
выводного тракта правого желу¬
дочка или с морфологией бло¬
кады левой ножки пучка Гиса и
нижней осью (положительные
комплексы QRS в отведениях
П, пт, aVF и отрицательные в
отведении aVL) или неизвестной
осью.Более 500 желудочковых экс¬
трасистол в сутки (холтеровское
мониторирование)VT. Семейный
анамнезАДПЖ у родственников первой
степени (согласно критериям диа¬
гноза),АДПЖ, подтвержденная морфо¬
логически, у родственников пер¬
вой степени.Идентификация у самого паци¬
ента патогенных мутаций с дока¬
занной или вероятной связью с
АДПЖАДПЖ у родственников первой
степени (когда невозможно опре¬
делить, удовлетворяют ли члены
семьи критериям диагноза).
Внезапная сердечная смерть (в
возрасте до 35 лет) вследствие
предполагаемой АДПЖ у род¬
ственников первой степени.
АДПЖ, подтвержденная морфо¬
логически или согласно крите¬
риям диагноза у родственников
второй степени Дос'1'oверный диагноз: 2 болыпих кри терия и.та 1 большой и 2 малых (различных категорий).
Вероятный диагноз; 1 большой критерий +1 малый или 4 мачых критерия.Возможный диагноз: 1 большой критерий или 2 малых (различных категорий).
Глава 21. Аритмогенная дисплазия правого желудочка... 413правого желудочка, которое наблюдается у данной больной, мы еще будем
говорить подробнее.У целой группы пациентов (на сегодня их не менее 6) диагноз типичного
варианта аритмогенной дисплазии правого желудочка рассматрттеается как
вероятный. По-видимому, это самый распространенный вариант, который с
трудом может быть дифференцирован от других причин желудочковой экстра-
систолии, в первую очередь миокардита. У этих больных пока отсутствугот такие
кардинальные признаки заболевания, как устойчивая желудочковая тахикардия
с ЭКГ-морфологией блокады левой ножки пучка Гиса, е-волна (лишь у 1 боль¬
ного есть нечто похожее, но во II отведении, рис. 21.4), выраженная дилатация
правого желудочка по данным ЭхоКГ. Этих пациентов разного пола и возраста
(2 мужчины и 4 женщины от 27 до 69 лет) объединяют частая правожелудочко¬
вая экстрасистолия (максимальное количество от 3 до 69 тыс./сут), нередко в
сочетании с пробежками неустойчивой желудочковой тахикардии (у 4 из 6 боль¬
ных), которая существует длительно (давность аритмического анамнеза от 5 до
15 лет) и, как правило, имеет прогрессирующее течение, а также обнаружение
при МРТ сердца утолщения перикардиального жира по передней стенке право¬
го желудочка с «наползанием» этих участков на миокард правого желудочка в
области верхушки, увеличения КДР правого желудочка (35-47 мм), расшире-
ні^ія выводного отдела правого желудочка (28—33 мм) и участков истончения
и дискинеза передней стенки правого желудочка. Специфичным считается
обнаружение структурных изменений во входном, выводном отделах правого
желудочка и в области верхушки («треуго.іьник дисплазии»).Поскольку обнаружение участков жировой ткани в миокарде правого жел}’-
дочка при подсчете критериев не учитывается, следует говорить о сочетании
I большого и 1 малого либо 2 маїьіх критериев у пациентов этой груттпы
(диагноз возможный или вероятный). У половины из них не выявлено зна¬
чимого повышения титра антикардиалъных антител (специфический АИФ
отсутствует, остальные миокардиальные антитела в титре 1:40—1:80), что сле¬
дует, по-видимому, считать характерным для изолированной аритмогенной
дисплазии правого желудочка и расценивать в качестве аргу’мента в пользу
этого диагноза у больных с «идиопатической» желудочковой экстрасистолией.
Однако у трех больных титры миокардиальных антител были повышены зна¬
чительно (1:160—1:320, в том числе АНФ 1:160 у одной пациентки), что в соче¬
тании с данными анамнеза (связь обострения экстрасистолии с инфекциями)
позволяет думать о сочетании аритмогенной дисплазии правого желудочка и
миокардита, как и в представленном ранее более ярком случае (больная И-ва,
43 лет). У самой пожилой пациентки этой гр>ттпы выявлен также геном вирусаРис. 21.4. фрагмент ЭКГ больного Б. Пояснения в тексте
414 КардиологияЭтитейна—Барр в крови (методом ПЦР), что заставляет думать о миокардите
как ведущей причине реализации аномальной генетической программы в столь
позднем возрасте. На данном этапе (до появления новых признаков) лишь гене¬
тическая и морфологическая диагностика мог>пг сделать диагноз достоверным.Второй (И) вариант течения аритмогенной дисплазии правого желудочка
(с правожелудочковой недостаточностью) гораздо в меньшей степени отвечает
традиционному представлению об этой болезни и представляет для нас сегодня
наибольший интерес, Нам пришлось столкнуться с 5 подобными больными —
у всех диагноз аритмогенной дисплазии правого желудочка может рассма¬
тривается как достоверный, однако во всех случаях возникли значительные
трудности с постановкой нозологического диагноза; у двух больных он был
верифицирован лишь при аутопсии. Прежде чем рассмотреть отдельных паци¬
ентов, сформулируем особенности данного варианта течения аритмогенной
дисплазии правого желудочка.Возраст больных молодой и средний, мужчины и женщины болеют одина¬
ково часто. Правожелудочковая экстрасистолия (с желудочковой тахикардией
или без нее) всегда тфисутствует, но может уходить на второй план. Ведущим
клиническим проявлением, которое (наряду с аритмией или независимо от
нее) приводит пациента к врачу, является «необъяснимое» увеличение правого
желудочка с развитием выраженного застоя по большому кругу' кровообра¬
щения. Как правило, выявляется также дисфункция и левого желудочка без
значительного его увеличения, что становится основанием для постановки
диагнозов «миокардит» или «дилатационная кардиомиопатия». К дисфункции
левого желудочка могут приводить различные причины (чаще — их сочета¬
ние): 1) миокардит (вирусный?); 2) первичное фиброзно-жировое замещение
миокарда; 3) сдавление резко увеличенным правым желудочком. Чаще, чем
при «типичном» варианте, выявляются большие ЭКГ-критерии аритмоген¬
ной дисплазии правого желудочка (тем не менее распознаются они редко).
Жировая ткань в миокарде правого или обоих желудочков может выявлять¬
ся при компьютерной или магнитно-резонансной томофафии сердца, но
может и отсутствовать (особенно если ее не искать) — по-видимому, процессы
фиброзирования у бо.іьньїх с клиническими проявлениями сердечной недо¬
статочности резко преобладают. Типичным, по нашим наблюдениям, является
снижение вольтажа комплексов QRS в стандартных отведениях ЭКГ, причина
которого понятна (массивное замещение жизнеспособного миокарда), однако
в литературе имеются лишь единичные указания на значение этого признака в
диагностике аритмогенной дисплазии правого желудочка.Первая из этой группы больная (Е., 22 года) наблюдалась в Российском
научном центре хирургии РАМН им. акад. Б.В. Петровского. Известно, что
с 20 лет без видимых причин появилась и нарастала одышка; бьш поставлен
диагноз дилатационной кардиомиопатии. Уже в мае 2009 г. встал вопрос о пере¬
садке сердца, больная была направлена в Российский научный центр хирургии
РАМН им, Б.В. Петровского, однако от госпитализации отказывалась до дека¬
бря, когда состояние резко ухудшилось: значительно наросла одышка, появи¬
лись отеки и асцит. Была госпитализирована в январе 2010 т. в крайне тяжелом
Глава 21. Аритмогенная дисплазия правого желудочка..415состоянии и через 2 дня уліерла от кардиогснного шока. Известно также, что в
Кардиологическом научном центре была выполнена МРТ сердца (результатов
мы не имеем), при холтсровском мониторировании регистрировалась желу-
дочковая экстрасистолия (количество не известно). На ЭКГ {рис. 21.S) — рез¬
кое снижение вольтажа комплексов QRS, блокада правой ножки пустка Гиса,
отрицательные зубцы Т в отведениях V^—V^.При ЭхоКГ, выполненной в Российском научном центре хирургии РАМН
им. акад. Б.В. Петровского, не было выявлено діигатации левого желудочка
(КДР 5 см); тем не менее ФВ левого желудочка была резко снижена (17%);
отмечено расширение правых камер сердца с трикуспидальной регургитацией
3-4 степени в отсутствие значимой легочной гипертензии. При исследовании
миокарда методом ПЦР был выявлен геном вируса герпеса 6-го тина. При
морфологическом исследовании сердца — картина выраженного фиброзно-
жирового замещения миокарда правого желудочка с образованием соеди¬
нительнотканных сснт, прослойки жировой ткани в клапанах в сочетании с
лимфогистиоцитарной инфилырацией и единичными «вирусными» клетка¬
ми в левом желудочке {рис. 2L6, см. цветную вклейку). В отдельных участках
кардиомиоциты занимают менее 25% площади. Данная картина совершенно
типична для аритмогенной дисплазии правого желудочка; причиной бурной
декомпенсации в последние месяцы жизни стшт, по-видимому, присоеди¬
нившийся вирусный миокардит. Согласно критериям, диаіноз аритмогенной
дисплазии правого желудочка был достоверным еще до получения данных
аутопсии (выраженная дилатация правого желудочка со снижением его ФВ,
отрицательные Т и ЖЭ), однако в отсутствие данных биопсии диагностика
аритмогенной дисплазии правого желудочка, коюрая сочетается с активным
миокардитом, крайне сложна, что подтверждает и следующее наблюдение.Больной Ч., 40 лет, имел длительный кардиологический анамнез {рис. 21.7).
Его мать во время беременности перенесла острую респираторную вирус¬
ную инфекцию; при рождении диагностирован врожденный порок сердца, в
возрасте 5 лет в связи с одышкой при незначительных нагрузках проведена
пластика межжелудочковой перегородки синтетической заплатой, инфунди-
булотомия, инструментальная легочная чрезжелудочковая вальвулодилатация
(проф. Е.Н. Мешалкин). С этого времени на ЭКГ регастрируется полнаяIt- ■ Г. ^' VШ -і-■■aVLi''V6Рис. 21.5. ЭК1'больной Е., 22 лет (диагноз аритмогенной дисплазии правого желудочка
верифищірован морфологически)
416Кардиология1975 198819932006 2007 2008 2009 2010 29.09.10одышка.;
отеки
ОРВИлихорадка
потливостьЭКГ, ХМКДР ЛЖФВ, %лечениеоперацияпредниаолонHZVл..І6.0 5,8 5,3 ;45 25 42 35 34 2I Iритмилен верапамил ПНВП DDDR тирозол
индометацин аллапининРис. 21.7. Анамнез заболевания палиента Ч., 40 летблокада правой ножки пучка Гиса. В 1988 г. (18 лет) выявлены наджелудочко-
вые экстрасистолы, назначались ритмилен, индо\гетацин. До 1993 г. нагрузки
переносил нормально. В 1993 г. (23 года) через 2 нед после острой респиратор¬
ной вирусной инфекции возник пароксизм мерцания-трепетания предсердий
(купирован всраиамилом), появились потливость, субфебрилитет. Повторный
эпизод трепетания предсердий отмечется через месяц во время ветряной оспы,
при ЭхоКГ — умеренное расширение полостей желудочков. В дальнейшем
периодттчески госпитализировался по поводу желудочковой и наджслудочко-
вой экстрасистолии, получал верапамил.В начале 2006 г. отметил чувство вн>'тренней дрожт^, жар, субфебрилитет,
зафиксирована частая желудочковіїя экстрасистолия, проведен курс терапии
нестероидными противовоспалительными препаратами (в связи с подозрени¬
ем на миокардит) без улу^ппения. В октябре 2006 г. после острой респиратор¬
ной вирусной инфекции появились слабость, отеки, субфебрилитет, предоб¬
морочные состояния, было выявлено 6 тыс. желудочковььх эксграсистол в
сутки, кораїкис пароксизмы неустойчивой желудочковой тахикардии (ЧСС
203/мин), АВ-блокада ТТ степени 2 типа, паузы до 2,4 с, брадикардия (средняя
ЧСС ночью 38/мин, минимальная 25—20/мин), снижение ФВ левого желу¬
дочка до 45%. В марте 2007 г. в Российском научном центре хирургии РАМН
им. акад. Б.В. Петровского после короткого курса терапии преднизолоном
25 мг/сут (с субъективным эффектом) имплантирован ЭКС в режиме DDDR.
Интраоперационно диагностированы инпизионная предсердная тахикардия,
желудочковая экстрасистолия четырех морфологий, Назначены аллапишш.
затем кордарон200 мг/сут, Сохранялись ночные ознобы, Через 1,5 года возникли
Глава 2L Аритмогеиная дисплазия правого желудочка... 417стойкая желудочковая экстрасистолия, одышка при минимальной нагрузке,
снижение массы тела на 8 кг, отеки степени анасарки, снижение ФВ левого
желудочка до 25%. Был диагностирован тиреотоксикоз, терапия преднизолоном
25 мг/суг и тирозоломбО мг/сут дала быстрый эффект, ФВ левого желудочка воз¬
росла до 42%; к сентябрю 2009 г. прием преднизолона был прекрашсн.В ноябре 2009 г. вновь возникли зксірасистолия, субфебрилитет, возобнов¬
лена терапия преднизолоном 20 мг/сут, соталексом 80 мг/сут. С января 2010 г
ііаблюдался в Факультетской терапевтической клинике им. В.Н. Виноградова.
Зарегистрированы постоянная мерцательная аритмия, а также более 7 тыс.
желудочковых экстрасистол. Кроме того, при ЭхоКГ (проф. В.П. Седов) выяв¬
лены некомпактный слой миокарда, высокий дефект межжелудочковой пере¬
городки с минимальным сбросом. Отмечено повышение титров антител к
эндотелию и проводящей системе сердца до 1:160, методом ПЦР геном вирусов
не выявлен. Планировалось проведение эндомиокардиальной биопсии правого
желудочка (по техническим причинам была отложена, в дальнейшем нациснт
от исследования отказался). Консультирован генетиком — определение кари-
отипа на фоне терапии ілюкокортикоидами выполнить не удалось. В связи с
отсутствием эффекта соталекса, неоптимальным режимом стимуляции реко¬
мендована замена ЭКС на кардиовертер-дефибриллятор. В марте перенес
острый обструктивный бронхит с лихорадкой, отметил значительное нарас¬
тание одышки и отеков. В апреле—мае в Факультетской терапевтической кли¬
нике им. В.Н. Виноградова при ЭхоКГ отчетливой отрицательной динамики не
выявлено, в анализах крови — отсутствие признаков активности миокардита, в
то же время регистрировались более 11 тыс. желудочковых экстрасистол в сутки
и 400 эпизодов желудочковой тахикардии продолжительностью до 3 мин.Начато насыщение кордароном, доза преднизолона увеличена до 30 мг/сут.
Одыипса, число желудочковых экстрасистол и пробежек желудочковой тахи¬
кардии уменьшились; сохранялись низкая субфебрильная лріхорадка и пот¬
ливость 110 ночам (при нормальных гормонах щитовидной железы). Вновь
рекомендована замена ЭКС на кардиовертер-дефибри^гіятор. Чувствова^т себя
относительно удовлетворительно до августа, проводююсь ачановос снижение
дозы преднизолона вплоть до полной отмены к 14 сентября. Был консультиро¬
ван кардиологом из клиники Шарите (Берлин): в связи с наличием выраженной
трикуспидальной регургитации, желудочково-предсердной фистулы и невоз¬
можностью исключить текущий миокардит высказаны сомнения в целесоо¬
бразности имплантации кардиовертера-дефибриллятора, пред-южеио обследо¬
вание и лечение в Германии, которое было запланировано на конец сентября.
Поступил в Факультетскую терапевтическую клинику им. В.Н. Виноградова
в связи с нарастанием отеков и одышки; при ЭхоКГ отмечено снижение
ФВ левого желудочка до 24% при нормальных его размерах. Число экстраси¬
стол было умеренным. 29.09.2010 г. пациент был обнаружен мертвым в палате,
реанимационные мероприятия не проводились.Необходимо обратить внимание на четкую связь начала «второго» заболева¬
ния и многих обострений с острой респираторной вирусной инфекцией, четкий
эффект преднизолона, в результате назначения которого уходила одышка, но
418Кардиологиявозобновлялись периоды потливости и субфебрилитета. В то же время выя¬
вить признаки активной вирусной инфекции не удавалось (геном вирусов
Эпштейна-Барр, цитомегаловируса, герпеса 6-го типа, парвовируса В19, TgG к
парвовирусу и герпесу 6-го типа не обнаружены), титры аитикардиальных анти¬
тел были повышены умеренно, и лишь в последнюю госпитализацию (результат
анализа был полу^іен после смерти) отмечен их резкий скачок (специфический
АНФ, антитела к проводящей системе сердца 1:160, к эндотелию — 1:320).На ЭКГ, зарегистрированных до имплантации ЭКС (1992 г — рис, 21.8;
2003 г.), — полная блокада правой ножки пучка Гиса в сочетании с отрицатель¬
ными зубцами Г в отведениях V^-V^, что могло трактоваться как последствия
оперативного лечения врожденного порока. При внутрисердечном элекгро-
физиологическом исследовании, выполненном в Российском научном центре
хирургии РАМН им. акад. Б.В. Петровского, желудочковая тахикардия не бььта
индуцирована, в связи с чем пациенту бьы имплантирован ЭКС без функции
дефибриллятора. На ЭКГ от 2010 г регистрировались постоянная желудоч¬
ковая стимуляция, экстрасистолы из правого желудочка, при холтеровском
мониторировании в мае 2010 г. — эпизоды устойчивой желудочковой тахикар¬
дии, топику которой определить сложно. На последних ЭКГ {рис, 21.9) обра-
шали на себя внимание низкий вольтаж, полное отсутствие зубцов R в фудных
отведениях, выраженное расширение и деформация комплексов после
экстрастимула.При оценке динамики зхокардиографшіеских параметров за последние
3 года видно отчетливое снижение ФВ левого желудочка в периоды обострения
миокардита (одышка, субфебрилитет, потливость после острой респираторной
вирусной инфекции, бронхита), а также при развитии тиреотоксикоза; при
этом КДР левого жел>дачка никогда сутцествснно не увеличивался, легочная
гипертензия оставалась умеренной; начиная с 2009 г отмечалось расширение
правого желудочка с тpикycnидaJ^ыioй регургитацией П-ПТ степени.При последней ЭхоКГ, выполненной проф. В.П. Седовым в сентябре 2010 г.
(pifc. 21.10), КДР левого желудочка 5,3 см, ФВ левого желудочка составила
24%, митральная регургитация Т—IT степени, dP/dt 355 мм рт.сх, VTI 8,5 см,
.левое предсердие 120 мл, правое предсердие 222 мл, передне-задний раз¬
мер правого желудочка 3,5 см (норма до 3,8 см), ФВ правого желудочка 65%,Рис. 21.8. ЭКГ больного Ч., 40 лет, от 1992 г. (зарегистрирована в возрасте 22 лет)
Глава 21. Аритмогенная дисплазия правого желудочка..419.ji.itiiijv:.Л:;;;.:;:к::. 1}. ^Т W“~~ V''" ' \Г~- ’V^Рис. 21.9. ЭКГ больного Ч., 40 лет, от сентября 2010 г.Рис. 21.10. Данные ЭхоКГ больного Ч., 40 лет, от 2010 г. Слева — некомпактный слой
миокарда левого желудочка. Справа — выраженная дилатация правых камер сердца,
трикуспидальная регургитация; расширение фиброзного кольца трикуспидального
ютапанатрикуспидальная регургитация III степени, фиброзное колыю 60 мм, СДЛА
41 мм рт.ст. По-прежнему определяются признаки иодаортального дефекта
межжелудочковой перегородки. Выраженная трабекулярность левого желудоч¬
ка (некомпактный миокард?).По данным МСКТ сердца, в области межжелудочковой перегородки и
вокруг устья легочной артерии визуализируются стрі-ктурн повышенной плот¬
ности (послеоперационные изменения). Определяется подклапанное сужение
легочной артерии до 17 мм, диаметр на уровне юіапана 28 мм. На расстоянии
] 4 мм ниже створки аорта.1ьного клапана, в зоне послеоперационных измене¬
ний визуализируется дефект межжелудочковой перегородки размером 8 мм, под
трикуспидальньгм клапаном визуализируется зона контрастирования размером
15 мм — сброс? Миокард левого желудочка с повышенной трабекулярностью в
области верхушки и боковой стенки. Коронарные артерии интактны.
420 КардиологияС wexoM всех данных в посмертный диагноз было вынесено три конкури¬
рующих заболевания;1) хронический инфекционно-иммунный миокардит тяжелого течения,
леченный глюкокортикоидами;2) врожденный порок сердца: дефект межжелудочковой перегородки, сте¬
ноз выходного отдела правого жел>дочка, оперативное лечение в 1975 г.;3) первичная (генетически детерминированная) кардиомиопатия? Синдром
некомпактного миокарда.Высокий дефект межжелудочковой перегородки носил, скорее всего, вто¬
ричный (послеоперационный?) характер и, наряду с тиреотоксикозом в анам¬
незе и межжелудочковой диссинхронией, мог вносить вклад в дисфункцию
желудочков. Наибольшие сомнения вызвал у патологоанатомов третий пункт;
однако наличие врожденного порока сердца, эхокардиографических призна¬
ков некомпактного миокарда, прогрессирующее поражение не то^тько левых,
но и правых отделов сердца (с развитием тяжелой трикуспидальной недоста¬
точности) заставляли думать о первичной (генетически детерминированной)
кардиомиопатии, в том числе об аритмогенной дисплазии правого желудочка;
МРТ ссрдтта не проводилась в связи с наличием ЭКС.При аутопсии (проф. Б.Б. Салтыков): вес сердца 400 т. Левое предсердие
увеличено незначительно, правое — значительно. Трикуспидальный кла¬
пан интактен, периметр 9,5 см; над клапаном — участок кальциноза (рубец
после инфундибулотомии?). Правый желудочек гипертрофирован (6 мм на
уровне клапана), мышца с очагами фиброза и жировой дистрофии (белесая,
плотная при разрезе); эндокард не гладкий, плотный (поствоспалительный?
пристеночный эндокардит? карциноид?); повышенная трабекулярность.
Левый желудочек гипертрофирован (15 мм), гипертрофированы трабекулы,
мышца тусклая, без крупных очагов некроза; кардиосклероз (в отсутствие
поражения коронарных артерий), эндокард гладкий. Дефект межжелудочко¬
вой перегородки не выявлен (определяются ее выпячивания справа налево).
По заключению патологоанатома после макроскопического исследования, в
качестве основного заболевания следует рассматривать врожденный порок
сердца.Однако при исследовании миокарда методом ПЦР выявлен геном вирусов
герпеса 6-го типа (в обоих желудочках) и 1-го типа (в левом желудочке), при
морфологическом исследовании (проф, Е.А. Коган, рис. 2І.П, см. цветную
вклейку): в левом желудочке — слой эпикардиального жира, выраженные поля
фиброза, местами с образованием соединительнотканных септ, дистрофия
и гипертрофия кардиомиоцитов, в некоторых из них — с утратой попереч¬
ной исчерченности, межуточные и периваскулярные лимфогистиоцитарные
инфильтраты (более 14 клеток при большом увеличении); в правом желудоч¬
ке — обширный участок субэндокардиального фиброза с участками сохранен¬
ных кардиомиоцитов (в месте расположения электрода? в зоне оперативного
вмешательства в области выводного тракта?), обширнъте поля жировой ткани,
занимающие до 60—70% площади, в сочетании с выраженным фиброзом и
образованием соединительнотканных септ; сохраненные кардиомиоциты в
Глава 21. Аритмогенная дисплазия правого желудочка... 421состоянии дистрофии; опреде^іяются клетки с крупными, деформированными
ядрами и перинуклеарным лизисом цитоплазмы (вирусные клетки).Данная картина убедительно свидетельствовала о сочетании активного
вирусного миокардита с выраженным интерстициальным фиброзом и при¬
знаками аритмогенной дисплазии правого желудочка. Однако морфолог,
проводивший вскрытие, после микроскопшіеского исследования поставил в
качестве основного диагноза миокардит, отнеся порок сердца к сопутствую¬
щим заболеваниям и указав на гипердиагностику первичной кардиомиопатии.
Этот факт говорит о том, что морфологам аритмогенная дисішазия правого
желудочка знакома так же мало, как и клиницистам. Тем не менее у больно¬
го имеются как минимум 1 большой (гистология) и 2 малых (отрицательные
зубцы Т на ЭКГ в правьж груд^шх отведениях, желудочковая экстрасистолия
и желудочковая тахикардия неуточненной морфологии) критерия заболевания
(мы не имеем возможности точно оценить состояние правого желудочка), что
делает диагноз аритмогенной дисплазии правого желудочка достоверным.Существует мнение, которого придерживаются многие патологоанатомы:
наличие жировой ткани в миокарде правого желудочка при дилатационной
кардиомиопатии — обычное явление. Однако критерием аритмогенной дис¬
плазии правого желудочка является обнаружение не только жировой гкани,
но и фиброза с формированием соединительнотканных септ и перестройкой
архитектоники; при этом вовлечение левого желудочка развивается поздно
(фиброз, жир, инфильтраты). По данным Падуанскою университета, про¬
цент жировой ткани в миокарде при дилатационной кардиомиопатии (0,07%)
сопоставим с контролем (0,33%) и никогда не бывает столь высок, как при
аритмогенной дисплазии правого желудочка (13,3%): содержание жира в био-
птатах более 3,21% с чувствительностью 67% и специфичностью 92% позволяет
ставить диагноз аритмогенной дисплазии правого желудочка. Аритмогенная
дисплазия правого желудочка отличается от банальной дилатационной карди¬
омиопатии также большей выраженностью фиброза (24,6 и 21,8%) и меньшим
количеством сохранных кардиомиоцитов (47,3 и 63,4%). Картина, которую мы
видели у наших пациентов, безусловно, выходит за рамки ди.іатационной кар¬
диомиопатии и не требует дальнейшей верификации.Однако в сложных случаях может быть использован иммуногистохимиче-
ский анализ, который выявляет при аритмогенной дисплазии правого желудоч¬
ка отсутствие катгерина, плакоглобина, десмоплакина, плакофиллина; причем
исчезновение этих белков специфично для аритмогенной дисплазии правого
желудочка и, в отличие от коннексина, не выявляется при гипертрофической,
дилатационной или так называемой ишемїтческой кардиомиопатии.В третьем случае у пациентки с поражением обоих желудочков речь тоже
пойдет о сочетании аритмогенной дисплазии правого желудочка и активного
миокардита. Необьшность данного случая в том, что ключом к постановке
диагноза стали данные МСКТ сердца. У больной К., 55 лет, с гипертонией и
развернутым метаболическим синдромом, давность аритмического анамнеза
составляет более 20 лет (в 34 года после ангины — тахикардия, в 40 лет после
холецистэкгомии — экстрасистолия, учашение которой отмечено с 2003 г.;
422 Кардиологияіюлучача эгшток). В 2010 г. отметила появление давящих болей в области сердца,
снижение толерантности к нагрузкам; при обследовании выявлены снижение
ФВ левого желудочка до 30%, частая желудочковая и наджелудочковая экс-
трасистолия. Поданным ультразвукового исследования сердца, выполненного
в Факультетской терапевтрггеской клинике им. В.Н. Виноградова, левый желу¬
дочек не расширен (КДР 5,3 см), ФВ левого желудочка 42%, отмечено преиму¬
щественное снижение экскурсии переднего сегмента в ср/3, правый желудочек
1,6 см. При суточном мониторировании ЭКГ по Холтеру — 482 наджелудочко-
вые экстрасистолы, 6397 желудочковых экстрасистол, в том числе 74 куплета,
3 триплета, 51 эпизод бигеминии, 4 эпизода тригеминии; лабильность ST-T.
При сцинтиірафии миокарда выявлен дефект перфузии распространенной
передней локализации (апикальные и средние отделы передней стенки левого
же^тудочка). В свете ншшчия болей и факторов риска ишемической болезни
сердца необходима была оценка коронарных артерий. С другой стороны, выяв¬
лено выраженное увеличение титров антикардиальных антител (к эндотелию
1:320, к кардиомиодитам и проводящей системе 1:160, к гладкой мускулатуре
1:80), IgG к вирусу герпеса 6-го типа, парвовирусу В19 (в отсутствие генома), что
позволяло рассматривать в качестве основной причины аритмий и систоличе¬
ской дисфункции миокардит.Для верификации диагнозов была выполнена МСКТ сердца и коронарных
артерий с контрастированием (Н.В. Гагарина); кальцинат в проекции прок¬
симального сегмента передней межжелудочковой артерии объемом 2 см^ КИ
3 Ед, коронарные артерии интактны. Миокард правого желудочка выраженно
неоднороден, с множественными включениями жировой плотности в свобод¬
ной стенке, верхущке и хордах правого желудочка. Участок жировой плотности
определяется субэпикардиа^іьно в верхушечно-боковом сегменте левого желу¬
дочка, Б отсроченную фазу — у^іастки неактивного накопления контрастного
препарата в центральном и субэпикардиальном слое перегородки и боковой
стенки левого желудочка. Впервые мы столкнулись с тем, что участки жиро¬
вой инфильтрации миокарда могут быть выявлены при КТ; для верификации
диагноза аритмогенной дисплазии правого желудочка (миокардит не вызывал
сомнений) бьша выполнена МРТ сердца (НЦССХ им. А.Н. Бакулева): верхуш¬
ка правого желудочка расширена, повышено содержание эпикардаального
жира по передней стенке (7 мм), в области верхушки (4 мм), по боковой стенке
левого желудочка (5 мм) с «наползаниєм» на миокард правого желудочка; стен¬
ка правого желудочка неровная (истончение до 1,5-2 мм и микроаневризмы), в
области верхушки — участки дискинеза, жировой инфильтрации (повышение
сигнала наТ1-ВИ, изоинтенсивность на T1-FS); выводной отдел правого желу¬
дочка резко расширен (39 мм), КДР правого желудочка 43 мм, трабекулярность
правого желудочка несколько повышена, левого — неравномерная (с образо¬
ванием «карманов»), КДР левого желудочка 58 мм, ФВ левого желудочка 40%;
диастолическая дисф>тїкция обоих желудочков.При целенаправленном анализе ЭКГ {рис. 21.12) в отведении V, выявлено
расширение комплекса QRS до 0,11 с за счет е-волны на восходящем коле¬
не зубца 5; вольтаж комплекса QRS снижен. При повторной ЭхоКГ (проф.
Глава 21. Аритмогенная дисплазия правого желудочка,,.423 Л.——Д -JUРис. 21.12. ЭКГ больной К., 55 летВ.П. Седов) отмечено расширение левого желудочка (ЬСДР 6,5 см); отчетливых
признаков расширения и нар>аиений локальной сократимости правого желу¬
дочка не выявлено. Таким образом, на основании 2 больших (расширение
и нарушения локальной сократимости правого желудочка по данным МРТ,
с-волна) и 1 малого (желудочковая экстрасистолия, пробежки желудочковой
тахикардии неуточнеиной морфологии) больной был поставлен достоверный
диагноз аритмогенной дисплазии правого желудочка в сочетании с активным
вирусно-иммунным миокардитом, который, видимо, играет основную роль в
дисфункции левого жел>дочка (хотя отложения жировой ткани в нем также
отмечены, что позволяет говорить о возможности бивентрикулярной формы
аритмогенной дисплазии правого желудочка).Четвертый пациент из этой подгруппы (Б., 42 года) поступил в клинику для
уточнения природы синдрома дилатапиоиной кардиомиопатии. В течение
жизни он страдал частыми ангинами, последняя (тяжелая) возникла в 2007 г,
С декабря 2009 г. отметил появление одышки, диагностирована постоянная
форма мерцательной аритмии; в апреле 2010 г. при ЭхоКГ (выполнено впер¬
вые) выявлена картина дилатационной кардиомиопатии. Б сентябре 2010 г.
после острою респираторного вирусного заболевания отметил нарастание
одышки, появление отеков, гепатомегалии, асцита, при повторном ультра¬
звуковом исследовании сердца — картина дилатационной кардиомиопатии
со снижением ФВ левого и правого желудочков. Анамнез требовал в первую
очередь исключения миокардита: при обследовании в клинике не выявлено
генома кардиотропных вирусов в крови, однако обнаружены IgG к парвовиру-
су В19 и вирусу герпеса 6-го типа; спектр антикардиальных антител не вполне
типичен для активного миокардита с систолической дисфункцией (нет анти¬
тел к кардиомиоцитам, АНФ), однако антитела к эндотелию выявлены в титре
424 Кардиологияболее 1:320. Одновременно при КТ легких выявлена практически бессимптом¬
ная инфильтраци>1 нижних долей обоих легких с двусторонним выпотом и
полостью распада: установить этиологию процесса не удавалось, длительная
антибактериальная терапия не давала эффекта; иммуносупрессивная терапия
во всяком случае не была возможна. Нельзя исключить и единую этиологию
поражения легких и миокарда.При ЭхоКГ, выполненной в клинике, обратило на себя внимание расши¬
рение не только левых камер сердца (КДР левого желудочка 7,3 см, индекс
2,9 см/м^, ФВ левого желудочка 36%, левое предсердие 136 мл, митральная
реіургитация И степени, dP/dt 659 мм рт.ст., VTT 8,5 см), но и правых (передне¬
задний размер правого желудочка 4,5 см, ФВ правого желудочка 48%, правое
предсердие 177 мл, трикуспидальная рсгургитация Ш степени) с диффузным
снижением сократимости обоих желудочков; при этом выраженной легочной
гипертензии нет (СДЛА 30 мм рт.ст.). В клинике также преобладали при¬
знаки застоя по большому кругу кровообращения (отеки, застойная печень,
выраженный аснит), на ЭКГ — отклонение электрической оси сердца вправо,
правожелудочковая экстрасистол ия, низкий вольтаж комплексов QRS, практи¬
чески полное отсутствие зубцов R в отведениях а также е-волна на вос¬
ходящем колене зубца S в отведении V^. При холтеровском мониторировании
зарегистрировано более 800 политопньгх желудочковых экстрасистол в сутки,
пробежки правожелудочковой тахикардии до 5 комплексов QRS {рис. 21.13).При МСКТ органов грудной клетки: данных за ТЭЛА и поражение коро¬
нарных артерий не получено; отмечается равномерное истончение миокарда
левого желудочка, миокард правого желудочка не утолщен (2-2,7 мм), опреде¬
ляется обширная зона жировой плотности в области свободной стенки и вер¬
хушки правого желудочка, подобная зона небольших размеров — в прилежапі;их
отделах верхушки левого желудочка. Как и у предыдущей больной, параллель¬
но была выполнена МРТ сердца с гадолинием (Лечебно-реабилитационный
центр Росздрава, проф. В.Е. Синицын): КДР левого желудочка 8 см, ФВ <20%,JІН-■ f.h " А\j'lЇЩ.—кг-Ч >і V г— У ^ \- :Г-. ’ «.1 «2. іI Рис. 21.13. ЭКГ (слева) и фрагмент холтеровского мониториропания ЭКГ (справа)
больного Б., 42 года
Глава 2Ї. Аритмогенная дисплазия правого желудочка...425Рис. 21Л4. Данные МСКТ (слева) и MPT сердца (в центре и справа) больнош Б., 42 годаТУ ТТТ\ г п /Г КДР правого желудочка 5,7 см; участков локального выбухания, зон дискинегза
стенки правого желудочка не выявлено; при просмотре результатов МСКТ —
тонкий слой висцерального жира (норма), признаки жировой инфильтрации
правого желудочка не выявлены; в отсроченную фазу участков накопления
гадолиния не выявлено (отсутствие фиброза и воспаления). Тем не менее диа¬
гноз аритмогенной дисплазии правого желудотеа у данного больного представ¬
ляется достоверным на основании наличия 2 больших критериев (выраженное
расширение правого желл^дочка со снижением его сократимости, с-волна) и
1 малого (правожелудочковая экстрасистолия и неустойчивая желудочковая
тахикардия). Вопрос о миокардите как причине быстрой декомпенсации в
данном случае остается открытым {рис. 21.(4).Упомяіієм также пациента С., 26 лет, который был госпитализирован в
Российский научный центр хирургии РАМН им. акад. Б.В. Петровского в
связи с выраженной правожелудочковой недостаточностью с трикуспидальной
регургитацией ТТІ степени. В 20 лет ем>' бьшо проведено ушивание дефекта
межпредсердной перегородки; примерно через 2 года появились и стали нарас¬
тать экстрасистолия, одышка, признаки декомпенсации по большому кругу.
При обследовании в Российском научном центре хирургии РАМН им. акад.
Б,В. Петровского: 2573 желудочковых экстрасистол (в том числе парные) по
данным холтеровского мониторировапия; снижение фракции выброса левого
желудочка до 46% при нормальных сш размерах (КДР 4,3 см) и дшштация
полости правого желудочка (4 см) с участками акинеза его стенки и снижением
фрактщи уменьшения площади правого желудочка до 19% (при норме 39—45) в
сочетании с трикуспида^тьной недостаточностью ПТ степени по данным ЭхоКГ.
Легочной гипертензии и реканализации дефекта межпредсердной перегородки
как причин персірузки правых отделов не выявлено. По данным МРТ серд¬
ца — отсроченное контрастирование в стенке правого желудочка, КДР правого
желудочка 6,6 см, некоторое повышение трабекулярности в полости правого
желудочка, четких данных за наличие жира в миокарде правого желудочка не
получено. ЭКГ пациента {рис. 21.15), на которой выявляются с-волпа, расши¬
рение QRS в отведении Vj до 0,11 си отрицательные зубцы Т во всех фудных
отведениях (преимущественно в правых), позволяют говорить о достоверной
426КардиологияРис. 21Л5. ЭКГ больного С., 26 лет (Российскітй научный цетр хирургии РАМН им.
акад. Б.В. Петровского)аритмогенной дисплазии правого желудочка (3 больших критерия и 1 малый)
как о причине правоже.тудочковой недостаточности.Таких больных — с выраженной дилатацией правого желудочка и преоб¬
ладанием застоя по большо\су кругу — среди пациентов с синдромом дилата-
ционной кардиомиопатии не так много, и обьганое объяснение «это бывает»
здесь не подходит; каждый из них требует исключения аритмогенной дисплазии
правого желудочка. Показано, что при идиопатической дилатациониой кардио¬
миопатии существует строгая корреляция, размеров левого желудочка и степени
«отставания» размеров правого желудочка: по мере роста КДО левого желудочка
растет соотношение КДО левого желудочка/КДО правого желудочка (1,0-1,5—
2,0 и т.д.), т.е. объем левого желудочка все в большей степени преобладает над
объемом правого. Не выявлено также различий по соотношению КДО левого и
правого желудочков у папиентов с идиопатической и ишемической кардиомио-
патией (1,26 и 1,24), хотя фракция выброса правого желудочка оказалась ниже у
больных с идиопатической дилатаиионной кардиомиопатией.Описаний миокардита/дилатационной кардиомиопатии с преимушествен-
ным поражением правого желудочка практически нет. Приніпіпиальиьім, каче¬
ственным отличием поражения правого желудочка при аритмогенной дисплазии
от его вовлечения в патологический процесс при дилатационной кардиомиопа¬
тии является наличие локальных дискинезов, аневризм и истончения стенки
правого желудочка, а также его повышенная трабекулярность, которые надо
активно искать. Кроме того, в протокол обследования больных с подозрением
на аритмогенную дисплазию правого желудочка (особенно при наличии синдро¬
ма дилатационной кардиомиопагии) должно входить определение КДО, КСО
правого желудочка, их индексов, ФВ правого желудочка и соотношения КДО
левого и правого желудочков. При отсутствии дилатации левого желудочка диа¬
гноз аритмогенной дисплазии правого желудочка становится более вероятным.В то же время частота поражения левого желудочка при аритмогенной
дисплазии правого желудочка достигает, по данным морфологического
исследования погибших, особенно пожилых больных, 100%, однако по.чное
Глава 21, Аритмогенная дисплазия правого желудочка... 427фиброзно-жировое замещение нехарактерно: гораздо типичнее обнаружение
гипертрофии с локатьными участками истончения, воспалительных инфиль¬
тратов, атрофии МИОЩІТОВ, реже — некроза. Описаны генетические варианты
аритмогенной дисплазии правого желудочка (мутация гена десмоплакина) с
преобладанием поражения левого желудочка; сочетание аритмогенной дис¬
плазии левого желудочка (фиброзно-жировое замещение) с некомпактным
миокардом; дебют заболевания в виде миокардита с дисфункцией левого желу¬
дочка с последующей трансформацией в типичную аритмогенную дисплазию
правого желудочка с дилатацией правого желудочка и развитием фибрилляции
желудочков; фульминантное течение миокардита у больных с аритмогенной
дисплазией правого желудочка.Вообще, по представлениям ряда авторов, частота трансформации острого
миокардита в аритмогенную дисплазию правого желудочка может достигать
60%. Достаточно утвердившимся является представление о том, что миокардит
способствует реализации аномальной генетической программы. С другой сто¬
роны, генетически неполноценный миокард становится благодатной почвой
для развития активного миокардита. Мишенью для выработки аутоантител
могут становиться дефектные белки десмосом; нельзя исключить и вторичное
происхождение аритмогенной дисплазии правого желудочка в результате выра¬
ботки при миокардите антидесмосомных антител (работ по их определению
при аритмогенной дисплазии правого желудочка найти не удалось). Известно
также, что протеаза 2А вирусов Коксаки группы В вызывает повреждение
дистрофина, а частота обнаружения генома энтеро- и аденовирусов при арит¬
могенной дисплазии правого желудочка достигает 75%. По-видимому, случаи
трансформации миокардита в аритмогенную дисплазию правого желудочка
или их сочетание наиболее трудны для диагностики.Наконец, ПІ вариант течения аритмогенной дисплазии правого желудочка
может быть назван развернутым; на первый план в клинической картине выхо¬
дят жизнеугрожающие желудочковые нарушения ритма — рецидивирующие
пароксизмы устойчивой желудочковой тахикардии и фибрилляции желудоч¬
ков; после того как доказано отсутствие тяжелой ишемической болезни сердца,
в качестве причин жизнеугрожаюших аритмий рассматриваются различные
некоронарогенньте факторы, при этом их значение нередко переоценивается
(особенно если пациент — мужчина пожилого или среднего возраста). В то же
время другие (наряду с аритмиями) типичные признаки аритмогенной диспла¬
зии правого желудочка (данные ЭКГ, ЭхоКГ) не распознаются, КТ или МРТ
сердца не проводятся, поскольку диагноз аритмогенной дисплазии правого
желудочка не предполагается.Приводим описание такого пациента. Больной К., 71 год, отмечает перебои
в работе сердца в течение последних 20 лет; в 1981 г на ЭКГ регистрировались
отрицательные зубцы Т в грудных отведениях ij)uc, 21.16). В 1982 г. на фоне
стресса и учашения перебоев впервые развился приступ сердцебиения, слабо¬
сти, головокружения, который купировался самостоятельно; выявлена частая
желудочковая экстрасистолия, состояние расценено как ишемическая болезнь
сердца (постинфарктный кардиосклероз). В дальнейшем антиаритмическая
428Кардиология1980(51 год) 1982 1995 1998ЖЭ2004 2008 2011ЖТ/ФЖЭКГ
АД0г фф ФФФ0Ф«—»Хнеполная БПНПГтМЖПантиаритмики1,4 смкордарон + ритмилен, ритмонорм этацизин
ИКДКАГ; мостик цкд
ПМЖАвмешательства
Рис. 21.16. Анамнез заболевание пациента К., 71 годИКД ИКДтерапия не проводилась, периодически ощущал перебои в работе сердца.
В 1995 г. во время игры в футбол — повторный эпизод сердцебиения, была заре¬
гистрирована желудочковая тахикардия (купирована новокаинамидом), подъ¬
ем АД до 220 и 140 мм рт.ст На ЭКГ — неполная блокада правой ножки пучка
Гиса. Подобрана гипотензивная терапия, назначен кордарон. На этом фоне в
1998 г. при умеренной физической нафузке дважды развились эпизоды желу¬
дочковой тахикардии, купированные методом электроимпульсной терапии;
тенденция к брадикардии ограничивала возможность терапии кордароном.
Были выявлены поздние потенциалы желудочков.В НЦССХ им. А.Н. Бакулева проведена коронарография, выявлен мышеч¬
ный мостик в средней трети передней межжелудочковой артерии; с этого
времени в качестве причины желудочковой тахикардии рассматривалось
гипертоническое сердце (тМЖП 1,4 см). Имплантирован кардиовертер-
дефибриллятор, после чего проводилась терапия кордароном 300 мт/сут
с периодическим добавлением ритмилена, ритмонорма, комбинированная
гипотензивная терапия. Отмечались нечастые срабатывания кардиовертера-
дефибриллятора, в 2004 и 2008 гг проводилась его замена. В 2004 г. в связи
с развитием силыюго кашля на фоне бронхиальной астмы среднетяжелого
течения (не исключалось развитие «кордаронового легкого?») кордарон бььт
заменен этацизином (на этом фоне — до 3880 желудочковых экстрасистол в
сутки). Кроме того, в 2003 г. перенес нарушение мозгового кровообращения
по ишемическому типу, несколько позже зарегистрированы эпизоды мер¬
цательной аритмии, назначен варфарин. АД в последние годы оставалось
относительно стабильным. С начала декабря 2010 г на фоне стресса — повтор¬
ные сердцебиения, 17 декабря — потеря сознания на улице, срабатывание
кардиовертера-дефибриллятора. Госпитализирован в отделение реанимации
клиники кардиологии Первого МГМУ им. И.М. Сеченова с пароксизмом
устойчивой желудочковой тахикардии, которая развилась после купирования
Глава 21. Аритмогенная дисплазия правого желудочка.429фибрилляции желудочков разрядом кардиовертера. Желудочковая тахикардия
с ЧСС 150/мин имела ЭКГ-морфологию блокады левой ножки пучка Гиса
с нижней осью (положительные комплексы QRS в отведениях II, III, aVF и
отрицательные в отведении aVL, рис, 21.27), была купирована электрической
кардиоверсией после введения лидокаина и кордароиа, начато насыщение
кордароном.Течение аритмии было необычно тяжелым для пациента с гипертоническим
сердцем; кроме того, появление желудочковой экстрасистолии и желудочковой
тахикардии отмечено задолго до развития высокой артериальной гиперто¬
нии и гипертрофии левого желудочка. Это заставляло искать другие причи¬
ны аритмии. При ЭхоКГ, выполненной в отделении реанимации, отмечены
диффузная гипертрофия стенок левого желудочка высокой степени (тМЖП
20 мм, тЗС 14 мм); КДР левого желудочка 5 см, КДО/КСО 74/27 мл, ФВ левого
желудочка 64%, митральной регургитации нет, Е 73 см/с, А 89 см/с, Е/А 0,83,
левое предсердие 71 мл, правое расширено, передне-задний размер правого
желудочка 4,6 см (норма до 3,8 см), тПЖ 8 мм, трикуспидальная регургитация
1 степени. На основании этих данных состояние было расценено в отделении
реанимации как гипертрофическая кардиомиопатия, и больной был переведен
в Факультетскую терапевтическую клиник>' им. В.Н. Виноградова для продол¬
жения лечения.Наличие гипертрофртческой кардиомиопатии объяснило бы агрессивный
аритмический анамнез. Однако совершенно необычной для гипертрофической
кардиомиопатии бьыа ЭКГ больного {рис. 21.18): на ней отсутствуют призна¬
ки гипертрофии левого желудочка; вольтаж QRS снижен, экстрасистолия —
правожелудочковая (как и желудочковая тахикардия), определяются неполная
блокада правой ножки пучка Гиса и отрицательные зубцы Тв отведениях V^—V^.
Кроме того, обращает на себя внимание увеличение правого желудочка до■ііівіІІШШЇішШЯІИРис. 21.17. ЭКГ больного К., 71 год, после перевода из отделения реанимации (2010 г.)
430Кардиология-NіІв4ЯІНі8Іі:вїйіІЯЇ^^'i '^Іг; J’id’'’^ІїНІ’ІГ:^
.'■■ ' ^ і ■■ і- І- ,р;^Рис. 21.18. ЭКГ больного К., 71 год, от 2001 г (слева) и сразу после к>т[ирования желу¬
дочковой тахикардии в 2010 г. (справа). Пояснения в тексте4,8 см, которое не могло объясняться длительным нахождением электродов в
правых камерах сердца. Для оценки степени гипертрофии левого желудочка,
а также выявления возможных признаков аритмогенной дисплазии правого
желудочка (дискинезы, аневризмы правого желудочка) и амилоидоза (неодно¬
родность миокарда, рестрикция) больной был направлен на повторную ЭхоКГ
к проф. В.П. Седову: степень гипертрофии левого желудочка оказалась уме¬
ренной (не более 1,4—1,6 см), подтверждено расширение правого желудочка,
локальных дискинезов и легочной гипертензии не выявлено.Далее были проанализированы все доступные ЭКГ, и на самой старой из
них (от 2001 г., см, рис. 21.18, cjieea) вьывлены (еше в отсутствие неполной
блокады правой ножки пучка Гиса) расширение комплекса QRS до 0,12-0,13 с
за счет наличия отчетливой s-волны (хорошо видна в отведениях V,—Vj, И, III,
aVF), отрицательные значения зубца Т в отведениях V—V^. «Остатки» є-волньї
можно видеть и на зубце г нынешней ЭКГ; однако еще необычнее выглядели
комплексы QRS в правых отведениях сразу после к>тіирования желудочковой
тахикардии с введением лидокаинаи кордарона {ш. рис. 21.18, справа): отчет¬
ливо определялись Бругада-подобные изменения сводчатого типа, наиболее
характерного для симптомных больных с синдромом Бругада, в отведениях Vj-
Vj, которые исчезли в течение суток. Это факт говорит о том, что генетическая
основа аритмогенной дисплазии правого желудочка у данного пациента может
быть не вполне обычна — речь может идти о патологии белков натриевых кана¬
лов (ген SCN5A). В литературе описаны единичные случаи одновременного
наличия признаков аритмогенной дисплазии правого желудочка и синдрома
Брутада — например, молодой пациент с желудочковой тахикардией и положи¬
тельным аймалиновым тестом, у брата и сестры которого выявлена дилатаиия
правого желудочка с включениями в его миокард жировой ткани по данным
МРТ, что позволило авторам говорить о латентной форме аритмогенной дис¬
плазии правого желудочка у самого пациента.
Глава 21. Аритмогенная дисплазия правого желудочка...431В нашем случае речь, безусловно, идет об аритмогенной дисплазии правого
желудочка. При МСКТ сердца подтверждена умеренная степень гипертрофии
левого желудочка; при специальном анализе выявлены небольшие включения
жировой ткани в отдельных структурах правого желудочка; в коронарных арте¬
риях — начальные проявления атеросклероза; данных за ТЭЛА нет. У больного
имеются 3 больших критерия заболевания {выраженная дилатация правого
желудочка, отрицательные Т в отсутствие блокады правой ножки пучка Гиса,
е-волна) и 3 малых (отрицательные Т при наличии блокады правой ножки
пучка Гиса, поздние потенциалы желудочков при неизвестной ширине QRS и
расширение QRS до развития блокады правой ножки пучка Гиса, устойчивая
желудочковая тахикардия с ЭКГ-морфологией блокады левой ножки пучка
Гиса в сочетании с желудочковой экстрасистолией до 3880/сут на фоне тера¬
пии в анамнезе). В настоящее время больной ждет очередной реимплантации
кардиовсртера-дефибриллятора.Наконец, упомянем больную У., 71 год, которая в 2006 г. обследова¬
лась в отделении кардиологии Факультетской терапевтической к,тиники
им. В.Н. Виноградова по поводу обмороков, наджелудочковой экстрасисто-
лии и пароксизмальной наджелудочковой тахикардии; методом чреспише-
водной стимуляции тахикардия не была индуцирована, обмороки расценены
как вазовагальные, в качестве причины нарушений ритма рассматривалась
ишемическая болезнь сердца. В 2011 г. проведена МСКТ органов грудной
клетки, при которой признаков атеросклероза коронарных артерий не выяв¬
лено; обратила на себя внимание ЭКГ {рис. 21.19), на которой (в отсутствие
преходящей неполной блокады правой ножки пучка Гиса) наблюдаются дваЛ-7ХWt-rv.'TV'І'r'Рис. 21.19. ЭКГ больной У., 71 год
432 Кардиологиябольтіїих критерия аритмогеиной дисплазии правого жел>^дочка: с-волна и
отрицательные зубцы Т в правых грудных отведениях. По данным МСКТ,
имелись включения жировой ткани в миокарде правого желудочка. Больной
планируется проведение внутрисердечного электрофизиологического иссле¬
дования для решения вопроса об имплантации кардиовертера-дефибрилля¬
тора. При подтверждении аритмогенного характера обмороков можно гово¬
рить о развернутом клиническом варианте аритмогенной дисплазии правого
желудочка у данной больной. Интересно, что возраст постановки диагноза
аритмогенной дисплазии правого желудочка у обоих пациентов с развернутой
формой одршаков.Таким образом, на сегодняшний день мы наблюдаем более десятка пациен¬
тов с достоверным и вероятным диагнозом аритмогенной дисплазии правого
желудочка, у половины из которых диагностирован также миокардит. Диагноз
представляется наиболее убедительным при наличии морфологической вери¬
фикации, а также при выявлении больших ЭКГ-критериев (у-волна, отри¬
цательные Т в правых отведениях в отсутствие блокады правой ножки пу^іка
Гиса). Отдельную подгруппу составляют пациенты с частой правожелудоч¬
ковой экстрасистолией, пробежками желудочковой тахикардии и данными
МРТ сердца, характерными для аритмогенной дисплазии правого желудочка,
однако в отсугствие больших ЭКГ-критериев диагноз остается вероятным,
необходимо продолжать наблюдение. Более чем по.їїовинє больных уже прово¬
дится ДНК-диагностика.Основным вопросом в лечении аритмогенной дисплазии правого желу¬
дочка является определение показаний к имплантации кардиовертера-
дсфибриллятора. На сегодняшний день к ним относятся (класс рекомендаций
И А, уровень С): перенесенная остановка кровообращения, устойчивая моно-
морфная желудочковая тахикардия с потерей сознания, полиморфная жeJгyдoч-
ковая тахикардия, доказанное выраженное поражение миокарда правого желу¬
дочка, аневризма правого желудочка, вовлечение в процесс левого желудочка
(бивентрикулярная форма). Среди наших больных двое умерли (у обоих стоял
вопрос о пересадке сердца, у одного из них — о замене ЭКС на кардиовертер-
дефибриллятор), двоим имплантирован кардиовертер-дефибриллятор, еше
у 7 этот вопрос решается. Половина больных получает в качестве медикамен¬
тозной антиаритмической терапии кордарон, всем больным с миокардитом (за
исключением одной ут^гершей) проводилась или проводится иммуносупрессив-
ная терапия.Аритмогенная дисплазия правого желудочка — заболевание с достаточно
серьезным прогнозом. В 5% случаев она является причиной внезапной смер¬
ти взрослого населения Америки и в 25% — причиной внезапной смерти при
нагрузках населения региона Венето (Италия); обшая смертность при этом
заболевании (данные G. Fontaine) составляет 2,3% в год; при этом смерть
от прогрессирования сердечной недостаточности наступает в 2 раза чаше,
чем внезапная аритмическая смерть; 10-летняя смертность достигает 21%.
Прогностически неблагоприятны необходимость назначения кордарона.
появление дисфункции правого желудочка и выраженной трикуспилальной
Глава 21. Аритмогенная дисплазия правого желудочка... 433недостаточности; при этом правожелудочковая или бивентрикулярная сер¬
дечная недостаточность развивается обычно в сроки от 4 до 8 лет после появ¬
ления полной блокады правой ножки пучка Гиса, хотя, как сказано выше,
описаны и случаи фульминантіюго течения при присоединении миокардита.Подводя итог клинической части, отметим, что еще Б 1995 г. пионер изуче¬
ния аритмогенной дисплазии правого желудочка G, Fontaine выделш! три кли-
ншіеские формы заболевания.1. «Аритмическая» форма (с нормальной фракцией выброса левого желу¬
дочка) — наиболее частый вариант; клинические проявления различны в зави¬
симости от степени дилатапии правого желудочка.2. Стабильная форма с вовлечением левого желудочка различной степени
тяжести (ФВ левого желудочка от 30 до 50%); при этом в обоих желудочках раз¬
виваются сходные патологические процессы.3. Прогрессирующая деградация миокарда с развитием бивентрикулярной
сердечной недостаточности в первые 10 лет после появления симптомов; при
этом клинические проявления сходны с дилатапионной кардиомиопатисй,
морфологически характерны фиброз, лимфоцитарная инфильтрация желудоч¬
ков (вторичный иммунный феномен?).G. Fontaine создал эту классификацию, анализируя 4 ра;знородньгх случая
аритмогенной дисплазии правого желудочка; в своей недавней работе «The
multiple faves of right ventricular cardiomyopathies» (2011) он развивает прежнюю
концепцию, уделяя особое внимание тем изменениям, которые вносит в кли-
нртческую картину аритмогенной дисплазии правого желудочка миокардит.
Недостатком данной классификации нам представ.тяется шсугствие разделения
аритъ^гической формы на развернутую и латентіїую (что имеет большое значение
в клинической диагностике), а также недооценка роли мттокардита в появлении
и прогрессировании сердечной недостаточности, в частности левожелудочко¬
вой, следствием чего является огсутствие рекомендаций по противовосііа,іи-
тельному лечению. На основании анализа течения болезни у наших пациентов
можно предложить выделение следующих форм арігтмогенной дисплазии правого
желудочка.1. Типичная (латентная аритмическая) форма.A. Изолированная правожелудочковая эксграсистолия без миокардита.Б. Неустойчивая желудочковая тахикардия без миокардита.B. Изолированная правожслудочковая экстрасистолия/неустойчивая желу¬
дочковая тахикардия с миокардатом.2. Развернутая (аритмическая) форма.A. Устойчивая желудочковая тахикардия без дилатапии правого желудочка
без миокардита.Б. Устойчивая желудачковая тахикардия с дилатацией правого желудочка
без миокардита.B. Устойчивая желудочковая тахикардия с миокардитом.3. АДПЖ с проірессирующей сердечной недостаточностью.А. Изолированная правожелудочковая недостаточность без миокардита.Б, Бивентрикулярная недостаточность без миокардита.
434 КардиологияВ. Бивентрикулярная недостаточность с миокардитом.Возможен переход к более тяжелым вариантам внутри одной формы, а
также от одной формы к другой, хотя, по-видимому, та или иная тяжесть
течения во многом предопределена у каждого пациента в зависимо¬
сти от особенностей его генотипа. На наш взгляд, данная классифика¬
ция достаточно четко определяет показания к специфическому лечению
(антиаритмики, радиочастотная аблация, имплантация кардиовертера-
дефибриллятора, иммуносупрессивная терапия, трансплантация) и круг
заболеваний, с которыми необходимо проводить дифференциальный диа¬
гноз: идиопатические желудочковые нарушения ритма (в частности, тахи¬
кардия из выводного отдела правого желудочка), синдром Бругада и другие
каналопатии, миокардит и дилатационная кардиомиопатия как самостоя¬
тельные заболевания, синдром некомпактного миокарда, в отдельных слу¬
чаях — инфаркт миокарда.В заключение отметим тс особенности, которые необходимо учитывать при
диагностике аритмогенной дисплазии правого желудочка:• заболевание наследуется по аутосомно-доминантному типу и одинаково
часто встречается у мужчин и женщин;• обнаружение в миокарде правого желудочка жировой ткани при МРТ
сердца не является обязательным для постановки диагноза аритмогеїіной
дисплазии правого желудочка; решающее значение имеют опенка состоя¬
ния правого желудочка и ана^шз ЭКГ (в том числе топики аритмии);• жировая ткань в миокарде правого желудочка может быть также успешно
выявлена при МСКТ сердца;• желудочковые аритмии присутствуют всегда, но могут уходить на второй
план в клинической картине болезни;• ведущим клиничесютм проявлением может быть «необъяснимая» нраво¬
желудочковая недостаточность;• аритмогеїшая дисплазия правого желудочка нередко сочетается как с
другими теистически детерминированными кардиомиопатиями, так и с
активным вирусным (инфекционно-иммунным) миокардитом;• дисфункция левого желудочка связана как собственно с аритмогенной
дисплазией правого желудочка, так и с миокардитом и может определять
клиническую картину;• биопсия является высокоинформативным методом верификации как
аритмогенной дисплазии правого желудочка, так и сопутствующего мио¬
кардита; обязательна вирусологическая диагностика, жслагельно проведе¬
ние высокоспецифичных иммуногистохимических исследований.Комментарий С.И. Овчаренко — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И. М. Сеченова, д-ра мед. наукНесмотря на то, что и в оригинальных, и в модифицированных критериях
диагноза аритмогенной дисплазии правого желудочка отсутствует указание
на жировую ткань в правом желудочке, вы постоянно упомина-'ш о выявле¬
нии жировой ткани как важном методе диагностики. Каково его значение?
Глава 21. Аритмогенная дисплазия правого желудочка,.. 435Комментарий О.В. Благовой — доцента кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед. наукОтсутствие указаний на выявление жировой ткани в правом желудочке
методом магнитно-резонансной томографии в критериях диагноза арит-
могенной дисплазии правого желудочка объясняется, видимо, недоста¬
точной специфичностью и чувствительностью этого признака, связанного
с трудностью дифференцировки с нормальной жировой тканью, располо¬
женной эпикардиально (трудности разграничения очагов жировой ткани
и фиброза в истонченном миокарде правого желудочка). Одиако метод
МРТ по-прежнему остается одним из главных в неинвазивной диагно¬
стике аритмогенной дисплазии правого желудочка. По нашему впечат¬
лению, обнаружение жирового замещения миокарда правого желудочка,
безусловно, помогает в диагностике аритмогенной дисплазии; именно
этот признак нередко становится поводом для активного вьывления дру¬
гих критериев болезни. Отмстим, что у пациентки И-ко, у которой диагноз
был подтвержден с помощью эндомиокардиальной биопсии, жировые
включения были сначала выявлены при МРТ, те. данные биопсии и МРТ
полностью совпали. Убедительным выглядит одновременное выявление
жирового замещения по данным МСКТ и МРТ сердца у части наших
больных. В то же время отс>'тствие выявления жировой ткани, особенно у
больных с выраженной сердечной недостаточностью (когда можно пред¬
полагать преобладание процессов фиброзирования) ни в коей мере не
исключает аритмогенную дисплазию правого желудочка. Остается наде¬
яться, что в последующих модификациях критериев аритмогенной дис¬
плазии правого желудочка выявление жировой ткани в миокарде получит
какое-то отражение.Комментарий С.И. Овчаренко — профессора кафедры факультетской терапии
X® 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукИзменилась бы ваша тактика ведения пациента Ч. в гом случае, если бы уда¬
лось выполнить ему биопсию миокарда?Комментарий О.В. Благовой — доцента кафедры факультетской терапии X® 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед. наукБезусловно. Мы имели бы очень веские основания не просто рекомендовать
(учитывая большие сомнения пациента), но настаивать на замене стимулято¬
ра на кардиовертер-дефибриллятор; мы использовали бы более высокие дозы
преднизодона в сочетании с противовируснымм препаратами (в крови ника¬
ких маркеров вирусной инфекции не бьшо); кроме того, пересадка ссрдтщ (от
которой пациент отказьцзался) стала бы неизбежной, вопрос о иатлиативной
операции (протезировании трикуспидштьного клапана) уже вряд ли обсуж¬
дался бы, хотя такие операции описаны у больных с аритмогенной дисплази¬
ей правого желудочка.
436 КардиологияКомментарий С.И. Овчаренко — профессора кафедры факультетской терапии
№ 1 лечебного факу.іьтета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукКаковы, по ваше\fv представлению, взаимоотношения миокардита и аритмо¬
генной дисп-'шзии правого желудочка у больных с поздним дебютом аритмо¬
генной диспла'іии?Комментарий О.В. Благовой — доцента кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, кацд. мед. наукИменно у этих больных, которые до 50—60 лет жили без явных проявлений
аритмогенной дисплазии правого желудочка, можно с большой вероятно¬
стью предполагать, что присоединение активного (вирусного у одной из
паниенток) миокардита могло не просто реализовать «дремавш>то» до того
аномальную генетическую программу, но стать первшшым фактором аутоим¬
мунного повреждения белков десмосом.Комментарий С. Р. Белоусова — заведующего терапевтическим отделением
Факультетской терапевтической клиники им. В.Н. Виноградова, канд. мед. наукМожно ли говорить о единой болезни при столь различной частоте встре¬
чаемости заболевания (нанример, в России и в регионе Венето в Италии),
столь рахіичньтх клинических проявлениях, при постоянной модификации
критериев диагноза и описании признаков болезни не только у человека, но
и у животных?Комментарий О.В, Благовой — доцента кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, канд. мед. наукМожно гоюрить о разных вариантах одной болезни, что вообще достаточно
типи^шо для моногснных заболеваний, к которым относится аритмогенная дис¬
плазия правого желудочка. В качестве примера можно привести различные кли-
ніічсские варианты врожденного синдрома удяинеьшого интервала QTу носите¬
лей разных генетических \тугаций. Модификация критериев диагноза является в
данном случае нормадьньш процессом — заболевание известно нe^шoгим более
30 лет, точнсШ диагностика стала возможна совсем недавно на основании выде¬
ления специфических мутаций, и именно благодаря изучению клинических
признаков у больных с генетшіески верифиіщрованньш диагнозом и >точнены
критерии аритмогенной дисплазии правого желудочка. Доказателъстюм того,
что дашшя болезнь является единой и самостоятельной нозологической формой,
является единство се этиолопти (генетические мутации в белках одной группы),
морфологии (фиброзно-жировое замещение миокарда) и патогенеза.Комментарии £.В. Заклязьминской — заведующей лабораторией медицинской
генетики РНЦХ им. акад. Б. В. Петровского РАМН, д-ра мед. наукАритмогенная дисплазия правого желудочка относится к моногенным
заболеваниям, т.е. для развития этого заболевания достаточно мутации в
одішм гене. Однако се экспрессивность и пенетрантность очень варьируют,
Глава 21. Аритмогенная дисплазия правого желудочка...437Таблица 21.3Гены, ответственные за развитие аритмогенной дисплазии правого желудочкаТкпГенБелокХромосомаАДПЖ1TGF3Трансформирующий фактор
роста бета 314q23-q24АДПЖ2SYJt2Рианодиновый рецептор, тип 2Iq42-q43АДПЖЗ14ql2-q22АДПЖ414д32.1-32.3АДПЖ5ТМЕМ43TpaHCMeNfбранный белок 433р23АДПЖ610р14-р12АДПЖ710q22.3АДПЖ8DSPДесмоплакинбр24АДПЖ9РКР2Плакофилин 212р11АДПЖ10DSG2Десмоглеин 218ql2.1-ql2АДЛЖ11DSC2Десмосомный гликонротеин II/
11118ql2АДПЖ12JVPПлакоглобин17q21отсутствие типичных клинических признаков в достаточно позднем возрасте
еще не позволяет говорить об отсутствии болезни. Различная распространен¬
ность в разных регионах говорит не о различном хараю ере болезни, но лишь
об эффекте основателя,Болъшинсгво генетических вариантов аритмогенной дисплазии правого желу¬
дочка (с ! по И) наследуются по аутосомно-доминантному гипу, однако для
12-го тшта (болезнь Наксоса, по названию греческого ос грова, на котором живет
большое количество носителей мутации) характерен аутосомно-рецессивньгй
тип наследования, т.е, больной ребенок может родиться у двух ютиничсски
здоровых родителей. Вместе с тем и при аутосомно-доминантном птпе насле¬
дования отсутствие больных родственников ни в коей мере не исключает гене¬
тического характера заболевания, поскольку вероятность появления мугаций
de novo достаточно высока. Этот факт особенно важен для юіинииистов.На сегодняшний день описано 12 генетических вариантов аритмогенной дис¬
плазии правого желудочка {табл. 2J.3), для четырех из которьЕх точная лока¬
лизация генетического дефекта неизвестна. Это означает, что невыявление
известных генетических мутаций не исключает этого диагноза, абсолютное
значение имеет лишь положительная диагностика.Описаны геноспецифические особенности заболевания: так, аритмогенная
дисаіазия правого желудочка 1-го типа иногда проявляется так называемой
аномалией Уля («папиросное» или «пергаментное» сердце, для которого
характерно тота^тьное замещение правого желудочка; болезнь несовместима
с жизнью).Аритлюгенная дисплазия правого желудочка 2-го типа часто сопровождается
стресс-индуцированной правожелудочковой тахикардией.Аритмогенная дисгыазия правого желудочка 8-го типа (мутация в гене
438КардиологияТаблица 21.4Возможности диагностики аритмогенвой дисллазин правого желудочка в лабо¬
ратории медицинской генетики Российского научного центра хирургии РАМНим. Б.В. ПетровскогоФормаГенЧисло экзоновБелокСостояние вопросаАДПЖ9РКР214Плакофилин 2ВыполняетсяАДПЖ10DSG215Десмоглеин 2ВыполняетсяАДПЖІDSC224ДесмоплакинВ разработкедесмоплакина) характеризуется более частым вовлечением в процесс левого
желудочка и межжелудочковой перегородки, высоким риском внезапной
сердечной смерти.Артмогенная дисплазия правого желудочка 12-го типа (болезнь Наксоса)
характеризуется, помимо кардиомиопатии, наличием мягкой кожи, тонких
шелковистых волос, дистрофией ногтей и ладонно-подошвенным гиперке¬
ратозом.Изучаются также перекрестные формы. Например, сочетание клиниче¬
ских признаков аритмогенной дисплазии правого желудочка и синдрома
Бругада, которое было отмечено у пациента К., требует поиска мутаций в
гене натриевых каналов SCN5A. Важно отметить, что при синдроме Бругады
выявляются изменения не только на ЭКГ, но и при морфологическом иссле¬
довании миокарда — в том числе и такие, которые сильно напоминают кар¬
тину ариткто1€нной дисплазии правого желудочка; жировая инфильтрация,
интерстициальный фиброз, лимфопитарная инфильтрация, дезорганизация
миофибрилл. Появление 8-волны в правых фудньгх 0ТВЄДЄНИ5ІХ отражает, по
всей видимости, нарушение процессов реполяризации; есть предпатожения
о нарушении функции ионных канатов при арит\іогенной дисплазии право¬
го желудочка, которое может приводить к клини^іеской картине, сходной с
клиникой гснетическнх каналопатий.Скрининг всех известных генов позволяет выявить мутации у 40—50% бать-
ных с направляющим диагнозом аритмогенной дисплазии правого желудоч¬
ка. В Европе существует всего два пентра, в которых возможно проведение
полного спектра генетической диагностики этого заболевания. В России до
последнего времени такая диагностика не проводилась, на сегодняшний день
в лаборатории медицинской генетики Российского научного пентра хирур¬
гии РАМН им. Б.В. Петровского выполняется диагностика двух наиболее
часіых генетических вариантов аритмогенной дисплазии правого желудочка
(табд. 21.4); еще один ген находится в разработке.После того как генетическая диагностика будет вьшолнена представленным
сегодня пациентам, крайне интересными будут анализ клинического течения
болезни, а также решение вопроса о первичности или вторичности миокар¬
дита у больных с картиной аретмогенной дисплазии правого желудочка.
По завершении диагностики мы пла^іируем вернуться к обсуждению многих
из поставлені 1ых сегодня клиницистами вопросов.
Глава 2І. Аритмогенная дисплазия правого желудочка... 439Комментарий А. В, Недоступа — профессора кафедры фаі^льтетской терапии
№ I лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукЛет 30 назад Евгений Михайлович Тареев говорил, что в наше время любая
новая нозология рождается в муках. Все простые нозологии давно описаны
и хорошо известны. Остались сложные. Сегодняшний клинический разбор
показывает, что аритмогенная дисплазия правого желудочка — одна из таких
нозологий — представляет собой айсберг, и мы пока наблюдаем лишь его вер¬
шину. Материал, представленный выше, уникален и наводит на очень многие
размьштления. Уже понятно, что термин «аритмогенная дисплазия правого
желудочка» не совсем точно отражает особеїшости этой болезни: она не всег¬
да аритмогенная (аритмии не всегда являются ведущим симптомом и далеко
не всегда — единственным), не всегда поражает только правый желудочек,
может очень напоминать дилатационную кардиомиопатию и т.д. Сегодня мы
лишь в начале пути.Таким образом, представлен анализ клинических проявлений аритмогенной
дисплазии правого желудочка, которая может протекать в типичной или
латентной аритмической форме («идиопатическая» правожелудочковая экс-
трасистолия, неустойчивая желудочковая тахикардия в отсутствие признаков
сердечной недостаточности и клинически значимой дилатании правого желу¬
дочка), в развернутой аритмической форме (с пароксизмсши устойчивой желу¬
дочковой тахикардии, появлением «больших» ЭКГ-критериев заболевания и
на поздних этапах — выраженной дилатации правого желудочка), а также в
форме правожелудочковой (чаще — бивентрикулярной) сердечной недоста¬
точности, для которой также типично выяв,чение «больших» ЭКГ-критериев;
при этом желудочковые аритмии могут уходить на второй план в клинической
картине болезни. Именно последний клинический вариант аритмогеьшой
дисплазии правого желудочка имеет наиболее неблагоприятный прогноз
и представляет наибольшие трудности в диагностике. Морфологическая
верификащ!я диагноза у 3 больных, в том числе у 2 пациентов с тяжелой
бивентртсулярной недостаточностью, заставила нас сущесгвенно расширить
круг больных, у которых необходимо подозревать аритмогенную дисплазию
правого желудочка, активно проводить поиск критериев болезни и определять
показания к интервенционному и хирургическому лечению (имплантация
кардиовертсра-дефибриллятора, пересадка сердца).Отдельно обсуждаются вопросы диагностики и лечения активного миокарди¬
та у больных с аритмогенной дисплазией правоїх) желудочка, их патогенети¬
ческие взаимоотношения и особенности клинической картины аритмогенной
дисплазии правого желудочка (как аритмических ее форм, гак и аритмогенной
дисплазии правого желудочка с сердечной недостаточностью) в сочетании с
миокардитом, который диагностирован (на основант клинико-лаборатор¬
ных и морфологигіеских данных) у 50% больных. Начата ДНК-диагностика
у больных с аритмогегшой дисплазией правого желудочка, после получения
результатов которой мы планируем вернуться к обсуждению данной темы.
440 КардиологияЛИТЕРАТУРАМоисеев B.C., Киякбаев Г.К. Проблема классификации кардиомиопатий //
Кардиология. — 2009; 49 (1): 65-70.AndreoleUi L., Leveque N., Boulagnon С. etal Viral causes of human myocarditis //
Arch. Cardiovasc. Dis. 2009 Jun-Jul; 102 (6-7): 559-568.AngeliniA., ТЫепе (7., Boffa C.M. et al. Endomyocardia] biopsy in right ventricular
cardiomyopathy// int. J. Cardiol. 1993; 40 (3): 273-282.Azaouagh A., Churzidse S., Konorza Т., Erhel R. Arrhythmogenic right ventricular
cardiomyopathy/dysplasia: a review and update 11 Clin. Res. Cardiol. 2011; 100 (5):
383-394.Badoiff C., Lee G.H., Lamphear B.J. et al Enteroviral protease 2A cleaves dystro¬
phin: evidence of cytoskeletal disruption in an acquired cardiomyopathy// Nat. Med.
1999; 5: 320-326.Bowles N.E., Ni J., Marcus F., Towbin J.A. The detection of cardiotropic viruses in
the myocardium of patients with arrhythmogenic right ventricular dysplasia/cardio¬
myopathy//J. Am. Coll. Cardiol. 2002; 39 (5): 892-895.Fontaine G. , Brestescher C., Fontaliran F. et al. Outcomc of arrhythmogenic right
ventricular dysplasia. Apropos of 4 cases. 1 Article in French] j j Arch. Mai. Coeur
Vaiss. 1995; 88 (7): 973-979.Fontaine G., Cuiraudon G,, Frank R. et al. Stimulation studies and epicardial map¬
ping in ventricular tachycardia: study of mechanisms and selection for surgery //
Kulbertus H.E., ed. Reentrant arrhythmias: mechanisms and treatment. — Lancaster:
MTP Press Limited, 1977. - P. 334-350.Fontaine G.H. The multiple facets of right ventricular cardiomyopathies j I Eur.
Heart J. 2011; 32 (9): 1049-1051.Kih P., Bootsma М., Bax J. et al. Arrhythmogenic right ventricular dysplasia/cardio¬
myopathy: screening, diagnosis, and treatment I j Heart Rhythm. 2006; 3 (2): 225—234.La Vecchia L., ZanoUa L., Varotto L. et al. Reduced right ventricular ejection frac¬
tion as a marker for idiopathic dilated cardiomyopathy compared with ischemic left
ventricular dysfunction // Am. Heart J. 2001; 142 (1): 181-189.Lobo F. V., Silver M.D., Butany J., Heggtveit H.A. Left ventricular involvement in
right ventricular dysplasia/cardiomyopathy // Can. J. Cardiol. 1999 Nov; 15 (11):
1239-1247.Marcus F.L, Fontaine G., Guiraudon G. Right ventricular dysplasia: a report of 24
adult cases // Circulation 1982; 65: 384-399.Marcus F.L., McKenna W.J., Sherrill D. et al. Diagnosis of arrhythmogenic right
ventricular cardiomyopathy/dysplasia: proposed modification of the task force crite¬
ria//Circulation. 2010 Apr6; 121 (13): 1533—1541.Matsukuma S., Eishi K., Hashizume K. et ai Arrhythmogenic left ventricular car¬
diomyopathy associated with noncompaction I j Ann. Thorac. Surg. 2010; 90 (6):
2044-2046.McKenna W.J., Thiene G,, Nava A. et al. Diagnosis of arrhythmogenic right ven¬
tricular dysplasia/cardiomyopathy / Task Force of the Working Group Myocardial and
Pericardial Disease of the European Society of Cardiology and of the Scientific Council
Глава 21. Аритмогенная дисплазия правого желудочка... 441on Cardiomyopathies of the International Society and Federation of Cardiology // Br.
Heart J. 1994; 71(3): 215-218.Navarro-Manchon J., Fernandez E., Igual B. et al. Left dominant arrhythmogenic
cardiomyopathy caused by a novel nonsense mutation in desmoplakin // Rev. Esp.
Cardiol. 2011 Mar 30.Ohkubo K., Watanabe L, Okumura Y. et al Right ventricular histological substrate and
conduction delay in patients with Brugada syndrome // Int. Heart J. 2010; 51 (1); 17—23.Pieroni M,, Delia Russo A., Marzo F. et al. High prevalence of myocarditis mimick¬
ing arrhythmogcnic right ventricular cardiomyopathy differential diagnosis by elcctro-
anatomic mapping-guided endomyocardial biopsy // J, Аш. Coll. Cardiol. 2009; 53
(8): 681-689.Pinamonti B., Dragos AM., Pyxaras S.A. et al. Prognostic predictors in arrhyth¬
mogenic right ventricular cardiomyopathy: results from a 10-year registry I j Eun Heart
J. 2011 Feb 28, [Epub ahead of printj.Plehn G., Vormbrock J., Lefringhausen L. et al Prevalence of ventricular discor¬
dance and its relation to functional capacity in idiopathic dilated cardiomyopathy //
Clin. Res. Cardiol. 2009; 98 (6): 371-378.Schmidt Т., Gerckens V., Ortmeyer D. et at. Brugada syndrome or ARVD (arrhyth¬
mogenic right ventricular dysplasia) or both? Significance and value of right precordial
ECG changes [Article in German] //Z. Kardiol. 2002; 91 (5): 416-422.Suzuki H., Sumiyoshi М., Kawai S. et al. Arrhvthmogenic right ventricular car¬
diomyopathy with an initial manifestation of severe left ventricular impairment and
normal contraction of the right ventricle // Jpn Circ. J. 2000; 64 (3): 209—213.Yoda М., Tanabe H., Kishi М., Suma H. Alternative technique for implanting an
epicardial cardioverter defibrillation patch during a tricuspid valve replacement for
arrhythmogenic right ventricular cardiomyopathy // Interact. Cardiovasc. Thorac.
SuiB. 2011; 12 (4): 628-630.
Глава 22АМИЛОИДОЗ СЕРДЦА — РУТИННЫЙ ДИАГНОЗ?С.И. Овчаре нко, Л.В. Ледоступ, В Л Седов, Е.А. Сон,F.A. Окиилева, ОЯ. Благова, ВА. Варшавский, Е.А. Коган,В.И. МаколкинАмилоид03 (первичный идиопатический, вторичный, при периодической
болезни, генетический) — заболевание, в отношении которого всегда насто¬
рожены врачи самых разных специальностей. Среди кардиологов существует
исписанное правило: «В случае любого неясного заболевания сердца подозре¬
вай амилоидоз». Но когда выявляется сочетание «инфарктной» ЭКГ с низким
вольтажом комплексов QRS (в отсутствие анамнестических и ультразвуковых
признаков инфаркта) и выраженной «гипертрофии» миокарда при Эхо КГ (в
сочетании с признаками рестрикции, снижением нередко не только диастоли¬
ческой, но и систолической ф>"нк11ии, «светящимся» миокардом и без призна-
ков гипертрофии на ЭКГ), особенно у больных среднего и пожилого возраста,
диагноз амилоидоза до^тжен рассматриваться как высоковероятный даже в
отсутствие признаков системности.Мы приводим два клинических наблюдения, в одном из которых диагноз
системного AL амилоидоза с поражением сердца был поставлен с помощью
биопсии подкожной жировой клетчатки, в другом — отсутствие внекардиаль-
ных проявлений потребовсшо проведения эндомиокардиальной биопсии, диа¬
гноз семейного TTR-амилоидоза подтвержден генетически.Обсуждаются вопросы классификации, лечения и прогноза.Больная Т., 50 лет, поступила в отделение общей терапии Факультетской
терапевтической к-іиники им. В.Н. Виноградова 5 февраля 2007 г. с жалобами
на одышку при незначительной физической нагрузке и в положении лежа,
чувство «кома в горле», периодическое ощущение тяжести за грудиной, не
связанное с физической нагрузкой, преходящие отеки голеней, повышенную
кровоточивость десен и легкое образование гематом, «онемение» пальцев рук,
преимущественно в холодную погоду, похудание на 6 кг в течение последнего
года.Из анамнеза заболевания известно, что в июле 2004 г. стала отмечать одышку
и онемение нижней челюсти вне связи с физической нагрузкой, а также «оне¬
мение» пальцев рук, преимущественно в холодную погоду в поликлинике по
месту жительства в общем анализе крови патологии не выявлено, а на ЭКГ
зарегистрированы комплекс QS в отведениях V — V^, желудочковая экстрасисто-
лия. Бьш назначен эгилок50-100 мг/сут с положительным эффектом (одышка
и боли в грудной клетке прекратились); данных по трактовке комп-текса QS на
тот момент не представлено. Больная ^гувствовала себя удовлетворительно, за
исключением сохраняющегося «онемения» пальцев рук, до июля 2005 г, когда
Глава 22. Амилоидоз сердца — рутинный диагноз? 443стала отмечать появление «свистов» и «хрипов» в трудной клетке при дыхании,
снова появилась и начаіга нарастать одышка. При флюорографии патологии не
выявлено. На протяжении осени 2006 г. состояние постепенно ухудшалось:
одышка старта прогрессировать, появилась в положении лежа, стали беспокоить
чувство «кома в горле», тяжесть за грудиной, отеки голеней, повышенная крово¬
точивость десен. Пациентка отметила похудание на 6 кг, в связи с чем в январе
2007 г. обратилась в амбулаторно-полик.іиническое отделение Факультетской
терапевтической клиники им. В.Н. Виноградова. В анализах крови отклонений
от нормы выявлено не было. В общем анализе мочи отмечалась протеинурия.
При КТ органов грудной клетки выявлен двусторонний плевральный выпот. ПриАТ признаков гипертрофии и дилатапии отделов сердца, нарушений локаль¬
ной и обшей сократимости, легочной гипертензии выяштено не было; отмечено
наличие жидкости в полости перикарда и плевральных полостях.Больная была проконсультирована в Научно-исследовательском инсти¬
туте фтизиопульмонологии — данных за туберкулез не получено. В связи с
сохраняющимися жалобами 05.02,2007 г. пациентка была госпитализирована в
Факультетскую терапевтическую клинику им. В.Н. Виноградова для обследо¬
вания и верификации диагноза.При поступлении состояние средней тяжести. Пациентка лежит с высоко
поднятым головным концом. Температура тела 36,8 °С. Кожные покровы блед¬
ные, обычной влажности, параорбита^іьньїе геморрагии на веках. В положении
лежа отмечались синюшность липа, набухание шейных вен. Число дыханий
в положении сидя 18/мин. При перкуссии легких отмечается притупление
перкуторного звука в базальных отделах с обеих сторон, там же при аускуль¬
тации — резкое ослабление дыхания. Тоны сердца приглушены, аритмичные
(экстрасистолы?), шумов нет. ЧСС 94/мин. АД 130/85 мм рт.ст. Живот при
пальпации мягкий, безболезненный, печень не увеличена, выступает из-под
реберной дуги на 1 см, селезенка перкуторно не увеличена, не пальпируется.
Симптом поколачивания отрицательный с обеих сторон. Щитовидная железа
при пальпации не увеличена. В неврологическом статусе без очаговой и менин-
геальной симптоматики.В общем, биохимическом анализах крови существенных отклонений от нормы
выявлено не бьто. В коагулограмме: фибриноген 4,7 г/л, растворимые ком¬
плексы фибринмономеров 0,540 (норма 0,350-0,470), снижение коллаген-
индуцированной агрегации тромбоцитов.В иммунологическом анализе крови: уровень иммуноглобулинов в пределах
нормы, анти-О-стрептолизин отрицательный, СРВ 0,88 ш/дл (норма 0—0,8),
в динамике отрицательный, cANCA (антитела к протеиназе 3) 2,98 Ед/мл
(0—5), pANCA (антитела к миелопероксидазе) 1,41 МЕ/льт (0-7), антитела к
кардиолипину IgG 1,46 МЕ/мл (0—10), комплемент 28,6 гем. ед., LE-клетки не
обнаружены.В общем анализе мочи при поступлении отмечена протеинурия 0,700%о.
Суточная протеинурия, измеренная в первые дни госпитализации, состави¬
ла 735 мг/сут. В анализе мочи по Нечипоренко также выявлена протеинурия
0,170%с, эритроцитурия до 10 250/мл.
-* —* W-J-Рис. 22.1. Электрокарлиотрамма больной Т. Скорость записи 25 мм/с. Пояснения
в текстеНа ЭКГ {рис. 22.1) обраща^іи на себя внимание резкое снижение вольтажа
комплекса QRS в отведениях от конечностей, отклонение электрической оси
сердца влево, АВ-блокада I степени, блокада передней ветви левой ножки
пучка Гиса, комплекс типа QS в отведениях V^-V^, патологический зубец Q в
отведении V^.При признаков гипертрофии и дилатации отделов сердца, нарушенийлокальной и обшей сократимости, легочной гипертензии выявлено не было.
Однако обращали на себя внимание нарушение диастолической функции
левого желудочка по рестриктивному тиггу {Е/А = 3) и низкий ударный объем
(39 мл) при нормальной фракции выброса (72%). После проведения плевраль¬
ной пункции и эвакуации из левой плевральной полости 750 мл жидкости,
соответствующей по характеристикам транссудату, существенного изменения
эхокардиографической картины отмечено не было.Непосредственно после эвакуации жидкости из плевральной полости
состояние больной значительно улучшилось; одышка практически не беспо¬
коила, «свисты» и «хрипы» в грудной клетке не отмечались, синюшность лица
и набухание шейных вен в положении лежа не регистрировались. Состояние
оставалось стабильным на протяжении дальнейшего пребывания в стационаре
на фоне проводимой симптоматической терапии: верошпирон 50 мг/сут, фуро-
семид 40 мг/сут, эгилок 100 мг/сут; курса лечебной дыхательной гимнастики.По результатам проведенного обследования на первый план выступало
поражение сердца с развитием хронической сердечной недостаточности.
В связи с этим в крут дальнейшего дифференциально-диагностического поис¬
ка были включены ишемическая болезнь сердца (возможный перенесенный
безболевой инфаркт миокарда), поражение сердца при системных заболевани¬
ях соединительной ткани, паранеопластическое поражение сердца, поражение
сердца при системных болезнях накоатения (в первую очередь системном
Глава 22. Амилоидоз сердца — рутинный диагноз? 445амилоидозе). Параліельно необходимо было исключить гипотиреоз; наиме¬
нее вероятным, но также требующим исключения представлялось поражение
почек.Перфузионная томосцинтиграфия миокарда позволила отвергнуть предпо¬
ложение о перенесенном безболевом инфаркте миокарда, так как признаков
очагового поражения миокарда выявлено не бьыо. Гипотиреоз также был
исключен (гормоны щитовидной железы в пределах нормы). По результатам
иммунологических исследований крови данных за патологию соединительной
ткани не пол>'чено. Входе проведенного онкопоиска (исследование уровня
онкомаркеров, УЗИ и КТ брюшной полости, сигмоскопші) признаков злока¬
чественных новообразований не выявлено,В ходе проведенного обследования обращала на себя особое внимание поли-
органность поражения с вовлечением сердца (выраженные ЭКГ-изменения в
сочетании с диастолической дисфункцией), почек (протеинурия, изменения
осадка мочи), гидроторакс (транссудат) и гидроперикард, что с большой
долей вероятности заставляло предположить на.іичие у больной системной
болезни накопления (в первую очередь системного амилоидоза). Учитывая,
что в ходе проведенного обследования не бььто обнаружно достоверных при¬
знаков онкопатологии, хронических воспалительных и ревматических забо¬
леваний, наиболее вероятным представлялось натичие у больной первичного
ами^юидоза. Случай бьш обсужпен с членом-корреспондентом РАМН, проф.В.И. Маколкиным, который с уверенностью поддержал данную концепцию и
рекомендовал повторно провести Эхо КГПри Эхо КГ, выполненной проф. В. П. Седовым {рис. 22.2), выявлены зна¬
чительная гипертрофия межжелудочковой перегородки до 1,5 см и задней
стенки левого желудочка до 1,3 см, диастолическая дисфутнкция левого желу¬
дочка по рестріпстивному типу, незначительное количество жидкости в поло¬
сти перикарда. Особое внимание обращало на себя наличие гиперэхогенных
включений в толще миокарда, придающих ему «блестящий» или «сальный»
вид. С учетом данных ЭКГ (низкий вольтаж зубцов в стандартных отведениях,
узкий патологический зубец Q в отведениях V^—V.), эхокардиографическая
картина была расценена как типичная для рестриктивной кардиомиопатии
(инфильтративной), вероятнее всего — амилоидоза сердца.Рис. 22.2. Эхокардиограммы больной Т. Пояснения в тексте
446 КардиологияДля морфолопіческой верификации амилоидоза была взята биопсия слизистой
оболочки десны и прямой кишки на амилоид, одаако амилоида в биоптатах обна¬
ружено не было. Несмотря на это, мы все же скдоняиись к диагнозу первичного
амилоидоза с поражением сердца и цочек. Эту же точку зрения после консульта¬
ции больной высказал канд. мед. наук В.В. Рамеев (сотрудник Клиники терапии
и профзаболеваний им. Е.М. Тареева), занимающийся проблемами амилоидоза:
«Сочетание рестриктивной кардиомиопатии с поражением почек (протеинурия,
сохранная функция почек), кожным геморрагическим синдромом (периорбиталь-
ная пурпура) и М-градиентом в крови с высокой вероятностью позволяет обсуж¬
дать диагноз системного AL-амилоидоза. Тенденция к снижению веса, вероятнее
всего, обусловлена периферической амилоидной нейропатией. Незначительное
повышение СРБ позволяет сомневаться в наличии миеломной болезни и с боль¬
шей долей вероятности предполагать первичный характер амилоидоза».Было рекомендовано проведение стернальной пункции (с подсчетом плаз¬
матических клеток), иммуноэлектрофореза с применением иммунофиксации,
рентгенографии плоских костей и для дополнительной морфологической
верификации амилоидоза — биопсии кожи и подкожной клетчатки передней
брюшной стенки.Нри рентгенографии костей свода черепа и костей таза патологических
изменений не выявлено. Больная была проконсультирована неврологом: дан¬
ных за полинейропатический синдром не получено.При исследовании пунктата костного мозга, полученного при стернальной
пункции, было выявлено незначительное повышение количества плазматиче¬
ских клеток до 3,9%, что не являлось диагностическим критерием миеломной
болезни, однако весьма характерно для первичного AL-амилоидоза.При исследовании белковых фракций крови в процессе динамического
наблюдения был выявлен М-градиент 7,1-7,4%. При иммунохимическом
исследовании белков сыворотки и мочи выявлена моноклональная секреция
G/v (4,8 г/л) и белка Бене-Джонса X (следы); воспалительная диспротеинемия
по данным денситограммы и уровню СРБ (6,8 мг/л при норме до 6 мг/л);
небольшое повышение содержания р2"Микроглобулина в сыворотке (2,6 мг/л
при норме до 2,4 мг/л); неселективная клубочковая протеинурия. Полученные
данные характерны для первичного AL-амилоидоза.В биоптате подкожной жировой клетчатки (проф. В.А. Варшавский) в
сосочковом слое дермы по ходу коллагеновых волокон отмечено отложение
амилоида, окрашиваемого и дающего поляризацию. После обработки допол¬
нительных срезов щелочным гуанидином с последующей окраской конго
красным в обычном и поляризованном свете обнаружено: конгофилия амило¬
идных масс и их свойство двойного лучепреломления исчезает через 1 мин от
начала инкубации. Вместе с тем следует отметить, что данный метод типирова-
ния амилоида является приблизительным и не позволяет дать точного ответа.
Наиболее точен иммуногистохимический метод с использованием монокло¬
нальных антител к белкам — предшественникам амилоида. В настоящее время
в нашей стране он практически недоступен; планируется его выполнение в
специализированной клинике в Германии.
Глава 22. Амилоидоз сердца — рутинный диагноз? 447Таким образом, учитывая клиническую картину, наиболее вероятно, что у
больной имеет место первичный AL-амилоидоз. Семейный амилоидоз мало¬
вероятен в связи с отсутствием сенс орно-моторной невропатии и нарушения
вегетативных функций. Данных за миеломную болезнь не получено, Другие
формы амилоилоза еще менее вероятны,С учетом данных анамнеза, клинической картины, данных лабораторных и
инструментальных исследований окончательный диагноз был сформулирован
следующим образом: первичный AL-амилоидоз с поражением сердца и почек:
диастолическая хроническая сердечная недостаточность И—ТТІ (NYHA), ами¬
лоидная нефропатия, двусторонний гидроторакс, гидроперикард.На фоне проводимой в клинике терапии состояние больной оставалось ста¬
бильным: одышка практически не беспокоила, «свисты» и «хрипы» в грудной
клетке не отмечались, синюшность лица и набухание шейных вен в положении
лежа не регистрировались, температура тела оставалась в пределах нормы, ЧСС
64—84/мин, при аускультации легких дыхание везикулярное, проводится во
все отделы, хрипы не выслушивались. Однако по данным КТ органов грудной
клетки сохранялось небольшое количество жидкости в плевральных синусах,
изменения ЭКГ оставались без динамики, сохранялись протеинурия и эритро-
цитурия.В удовлетворительном состоянии больная была выписана с рекоменда¬
циями продолжить проводимую симптоматическую терапию и направлена
на госпита.'[изаиию в Клинику терапии и профзаболеваний им. Е.М. Тареева
Московской медицинской академии им. И.М, Сеченова для проведения спец-
иф№іеского лечения, где ей был проведен первый курс специфической терапии
амилоидоза мелфаланом в дозе 0,15 мг/кг в сутки в сочетании с преднизолоном
0,8 мг/кг в сутки. Отмечена хорошая переносимость препаратов, стойкое удо¬
влетворительное состояние больной, отсутствие ухудшения функции почек.
Планируется проведение повторных курсов химиотерапии.Амилоидоз — 1'руппа заболеваний, отличт^тельным признаком которых
является отложение в тканях нерастворимого фибриллярного белка амилоида.В XVII в. Боне описал «саговую селезенку» у больного с абсцессом печени.Рудольф Вирхов дал название внеклеточному материалу, выявленному в
печени на аутопсии, — «амилоид» (от феч. amylon — крахмал).В 1842 г. Карл Рокитанский установил связь «сальной болезни» с туберкуле¬
зом, сифилисом, риккетсиозами.В 1856 г. Уилкс описал «жирные органы» у «здорового» человека, в 1876 г
Сойка — у стариков.Уже в 20-е гг. XX в. Бенхольд установил такие свойства амилоида, как кон-
гофилия и двойное лучепреломление.в 1937 г. Аткинсон описал амилоидоз при миеломной болезни, в 1952 г
Андраде выделил наследственные его формы.в 1959 г. Коген и Калкинс установили фибриллярную структуру амилоида.Проблеме амилоидоза посвящены основополагающие работы отечествен¬
ных патологов и клиницистов; В.В. Серова, О.М. Виноградовой, Н.А. Мухина,В.А. Варшавского, В.В. Суры, B.C. Рукосуева, И.А. Шамова (в 1983 г.
448КардиологияТаблица 22.!Классификация амилоидоза в зависимости от белка-нредшествеиника (ВОЗ, 1993 г.)Белок амилоидаБелок-оредшествениикКлиническая форма
амилоидоза (А)ААSAAВторичный А, периодическая
болезнь, синдром Макла-
УэльсаALЛегкие цепи IGПервичный А, ММ, болез!гь
Вальденстрема ATTRТранстиретинСемейные формы Л, систем-
ный старческий ААр2МР2М-микрогло6улинДиализный ЛАрЭ-протеинБолезнь Альцгеймера, син¬
дром Дауна, наследственные
кровоиз.<1Иянш1 в мозг с А
(Голландия)AIAPPАмилинИзолированный А остропкоп
Лангерганса (сахарный диабет
ТТ типа, инсулинома)AANFПНУПИзолированный амилоидоз
предсердий AGelГелсолинФинская семейная амилоид¬
ная полинейропатияAFibФибриногенАмилоидная нефропатияACalПрокалі.цитонинПри медуллярном раке щито¬
видной железыACysИистатинНаследственные кровоизлия-
пия Ті мозг с А (Исландия)ААроА!Аполиноиротеин АІАмилоидная полинейропатия
(111 тип. van Allen, 1956 і:)APrPSerПрионовый белокБолезнь Крейтцфельда-
Якоба, болезнь Герсгманна—
Штраус слера—Шейн кераза исследование проблемы амилоидоза им присуждена Государственная пре¬
мия СССР).Амилоидоз — традиционная тема Девичьего поля, у интернистов всех спе-
циа^тьностей существует постоянная насторожешюсть в отношении этого не
столь уж редкого заболевания.Согласно классификации ВОЗ 1993 г., в зависимости от структуры бслка-
ирсдшественника выделено около 25 форм амилоадоза (табл. 22.1), которые
клинически разделяются на системные формы (встречаются редко) и локаль¬
ные — старческие (выделенные В.В. Серовым эндокринные и неэндокринные
формы) и нестарческие.Системные формы амилоидоза представлены на рис. 22.3.В основе различных форм AL-амилоидоза лежит плазмоклсточная.
В-лимфоцитарная дискразия: в костном мозге возникает аномальный клон
Глава 22. Амилоидоз сердца —рутинный диагноз?449Рис. 22.3. Системные формы амилоидозаплазматических клеток или В-лимфоцитов, которые продуцируют моно¬
клональные иммуноглобулины, обладающие амилоидогсниостью. Если в
нормальном пунктате костного мозга плазмоциты составляют <1%, то при
первичном (идиопатическом) амилоидозе их количество уве^іичено до 5—10%,
а при миеломной болезни, которая также может осложняться развитием ами¬
лоидоза, — >12—30%.К основным органам-мишеням относятся сердце (поражение до 100%),
почки (более 80%), желудочно-кишечный тракт, адвентиций мелких/средних/
крупных сосудов, язык, нервная система, мышцы, кожа.Лечение во многом сходно с лечением парапротеинемических лейкозов и
состоит в назначении различных схем полихимиотерапии (винкристин, мел-
фалан, адриамицин + дексаметазон, прсднизолон). Возможно последующее
введение аутологичных стволовых клеток, которые получают методом лейка-
фереза крови больного после предварительной их мобилизации из костного
мозга под влиянием внутривенного введения гранулоцитарного колониести¬
мулирующего фактора.При АА-амилоидозе белком-предшественником является подобный СРВ
SAA-а-глобулин (на сегодня известно 5 его фракций). Этот тип амилоида
синтезируется нри хронических воспалительных, в том числе нагноительных
процессах, скорость амилоидогенеза зависит от уровня SAA-белка.Среди органов-мишеней чаще всего поражаются почки (91-100%), а также
желудочно-кишечный тракт, печень, селезенка, надпочечники, редко — сердце.
450 КардиологияЛечение состоит в терапии осноізлого заболевания. Кроме того, показано,
что синтез и секрецию SAA блокирует колхицин. Возможна попытка резорб¬
ции (растворения) амилоида димексидом, фибриллексом.Критериями эффективности лечения является снижение уровней С-реак-
тивного белка и SAA. Риск прогрессирования амилоидоза существенно снижа¬
ется при SAA < 10 мг/л. Прогноз АА-амилоидоза в большинстве случаев зависит
от прогноза и течени:я основного заболевания.Своеобразным патогенезом, к.'шнической картиной и прогнозом отличается
TTR-амилоидоз, при котором белком-предшественником является транстире-
тин — белок, в норме синтезируемый печенью и имеющий тетрамерную струк¬
туру. при мутации в гене транстиретина субъединицы аномального белка стано¬
вятся основой для синтеза амилоида; описаны как семейные (нейропатические и
кардиопатические), так и спорадические формы. Для поражения нервной систе¬
мы характерно развитие сенсорно-моторной периферической полиііейропатии,
нарушение автономных вегетативных функций, синдро.м карпального канала.
Помимо нервной системы и сердца, могут поражаться желудочно-кишечный
тракт, стекловидное тело, редко — почки, но системные проявления могут пол¬
ностью отсутствовать. При данной форме амилоидоза медикаментозная терапия
неэффективна — лечение состоит в трансплантации печени (при тяжелом пора¬
жении сердца — в сочетании с трансплантацией сердца). Коррекции не подлежат
необрати.мые дегенеративные изменения нервных стволов.Клинические проявления системного амилоидоза зависят от типа амилоида
и стадии болезни. Для системного ами^тоидоза, особенно для первичного идио-
патического AL-амилоидоза, характерно последовательное присоединение
новых симптомов, создающих полиморфную клиническую картину с многоор¬
ганными проявлениями, не характерную для какой-либо иной нозологии. Для
морфологической верификации диагноза проводится биопсия пораженных
органов: почки, печени, селезенки (информативность 90—100%), слизистой
оболочкіі прямой кишки (50—70%), десны, при AL-амилоидозе — биопсия
подкожной жировой клетчатки из передней брюшной стенки.При выявлении ами.’юида при окраске конго красным и при исследовании
в поляризующем свете проводится его типирование — мегодом обработки пре¬
паратов амилоида растворами трипсина, щелочного гуанвдина, перманганата
ка.1ия (АА-амилоид теряет розовую окраску и утрачивает свойство двойного
лучепреломления в течение 1 ч вследствие меньшей устойчивости к протеоли-
зу, для AL-амилоида характерна задержка более 1 —2 ч) или (более точно) имму-
ногистохимическмм методом (типирование с моноклональными антителами к
фибриллярному белку амилоиду, кроме диализного амилоидоза).Поражение сердца при амилоидозе является фактором, непосредственно
влияющим на качество жизни пациента , а в большинстве случаев — и жизнен¬
ный прогноз, поэтому раннее выявление амилоидной кардиопатии — крайне
важный момент в диагностике амилоидоза. Поражение сердца встречается как
при локальном амшгоидозе, так и при системных его формах:• AANF-амилоидоз предсердий (локальный старческий);• первичный (идиопатический) AL-амилоидоз;
Глава 22. Амилоидоз сердца — рутинный диагноз? 451• вторичньтй АА-амилоидоз (редко);• ApjM-амилоидоз (гемодиализный);• ATTR-амилоидоз (семейный и системный старческий амилоидоз).Степень выраженности амилоидного поражения сердца зависит от типаамилоидоза. При изолированном амилоидозе предсердий она минимальна,
и клиническое значение этого процесса не вполне ясно. Поражение сердца
при Ар^М-амилоидозе также носит второстепенный характер и не определя¬
ет прогноз. По-другому обстоит дело с первичным AL-амилоидозом, кото¬
рый по праву называют сердечно-сосудистым. По данным В.В. Рамеева,
Л.В. Козловской и соавт., поражение сердца встречается в 82,4% случаев боль¬
ных AL-амилоидозом.При инфильтрации миокарда амилоидными массами (особое значение имеет
поражение миокарда желудочков) развивается диастолическая дисфунісция,
которая быстро трансформируется в классическую рестриктивную кардиомио-
патию и клинически проявляется симптоматикой хронической сердечной недо¬
статочности по диастолическому типу В 1983 г. R.E Kyle и соавт. на 229 пациентах
с AL-амилоидозом показали, что в 23% наблюдений имела место клин№іеская
картина застойной сердечной недостаточности. Нарушение диастолической
функции сердца коррелирует не только с тяжестью состояния, толерантностью
к физическим нагрузкам, и, следовательно, со снижением качества жизни, но
и с эффективностью лечения и прогнозом. Диагноз диастолической сердечной
недостаточности устанавливается по общим принципам, включающим наличие
си\штомов и признаков хронической сердечной недостаточности, сохранную
или незначительно сниженную систолическую функцию левого желудочка
(ФБ 45—50%) и выявление нарушения расслабления и/или заполнения левого
желудочка, признаки повышенной «жесткости» левого желудочка.В случае выявления диастолической сердечной недостаточности требуется
исключить другие, более частые ее причины, такие как артериальїіая гипер¬
тензия, гипертрофия миокарда, ишемия миокарда, констриктивный пери¬
кардит, а также констриктивные поражения миокарда другой этиологии. При
их исключении речь может идти о болезнях накопления, в первую очередь об
амилоидозе сердца.На ЭКГ больных с амилоидозом сердца в 70% случаев можно выявить
снижение вольтажа (амплитуда QRS <5 мВ в отведениях от конечностей и/или
<10 мВ в грудных отведениях) и в 75% «инфарктоподобные)> изменения (пато¬
логический зубец Q в двух и более смежных отведениях) при отсутствии рубцо¬
вых изменений по данным ЭхоКГ и сцинтиграфии миокарда в покое, а также
различные нарушения проводимости. Объяснить это можно тем, что амилоид,
отложившийся в толще миокарда, не обладает таки\ш «электрическими» свой¬
ствами кардиомиоцитов, как возбудимость и проводимость, гюэтому симули¬
рует наличие рубцовой (электрически неактивной) ткани.Амилоид может откладываться по ходу проводящей системы сердца.
Клинические проявления этого патологического процесса весьма неспецифич¬
ны и зависят от локализации амилоида в проводящей системе: при его о'гложе-
ияи в синусовом или АВ-узлах развиваются синдром слабости синусового узла,
452 КардиологияАВ-блокада 1—Ш степени; при поражении амшіоидом синоатриальных или вну-
трижелудочковых ітроводїпцих путей — синоатриальная блокада и блокады ножек
пучка Гиса. Отложение амилоида в миокарде может проявляться и различными
нарушениями pwrma сердца, в том числе фибрилляцией и трепетанттем предсер¬
дий, желудочковой тахикардией, узловым ритмом, удлинением интервала QT.При ультразвуковом исследовании сердца характерны псевдогипертрофия
(симметричное утолщение стенок желудо^іков не за счет увеличенной массы
миокарда, а за счет пропитывания ее амилоидом, при этом на ЭКГ отсутствуют
признаки гапсртрофии миокарда); изменение трансмитрального диастоли¬
ческого потока (соотношение пиков Е/Л)\ феномен «блестящего» миокарда
(амилоид, будучи фибpИJЪ^яpным белком, по своей ультразвуковой плотности
напомиїіает коллаген, входящий в состав фиброзного кольца и клапанов серд¬
ца, поэтому плотность миокарда, инфильтрированного амилоидом, сравнима
с ультразвуковой плотностью этих структур).Таким образом, амилоидоз сердца можно заподозрить ттри сочетании выше¬
перечисленных клинических, электрокардиографических и ультразвуковых
признаков. Однако эти признаки не являются специфическими, наличие и
степень их выраженности могут сильно варьировать в зависимости от объема
амилоидных масс в миокарде. Поэтому единственным достоверным критери¬
ем диагноза амилоидоза является морфологическая верификация. Учитывая
сложности проведения биопсии миокарда, в первую очередь используют менее
инвазивные способы, к которым относятся биопсия слизистой оболочки десны
и прямой кишки, а также все чаще применяемая методика аспирационной
биопсии подкожной жировой клетчатки (при AL-амилоидозе).При наличии клинически выраженной амилоидной кардиомиопатии лече¬
ние ее, по сути, сводится к лечению диастолической сердечной недостаточно¬
сти. При этом повышенная «жесткость» миокарда обусловлена накоплением
в интерстициальном матриксе амилоида и не зависит от активности ренин-
ангиотензин-альдостсроновой системы, поэтому терапия ингибиторами АПФ,
блокаторами рецепторов ангиотензина Пи антагонистами альдостерона не
столь эффективна, как при других вариантах диастолической сердечной недо¬
статочности.Степень нарушения диастолы посредством измерения трансмитрального
диастолического потока, как известно, может быть подразделена на 3 ста¬
дии: замедленная релаксация {Е/А <1), псевдонормализация {Е/А = 1—2),
рестрикция {Е/Л>1). У пациентов с клинически выраженным амилоидным
поражением сердца соотношение пиков Е/А обычно бывает более 2,5, что
свидетельствует о крайней степени выраженности рестрикции. При пора¬
жении сердца по рестриктивному типу нарушается расслабление миокарда
левого желудочка, что ведет к уменьшению конечного диастолического
объема. В этой ситуации даже при сохранной ФВ левого желудочка умень¬
шается ударный объем и, следовательно, сердечный выброс, который, в свою
очередь, определяет поддержание периферического артериа^тьного давле¬
ния. Все это приводит к артериальной гипотензии. Назначение ингибиторов
АПФ, особенно в целевых дозах для лечения сердечной недостаточности.
Глава 22. Амилоидоз сердца — рутинный диагноз? 453ведет к еще большему усугублению гипотензий и вследствие этого часто ста¬
новится практически невозможным. Кроме того, при первичном амилоидозе
часто поражается вегетативная нервная система с развитием ортостатиче¬
ской гипотензии.р-Адреноблокаторы при лечении диастолической сердечной недостаточно¬
сти не влияют на податливость миокарда левого желудочка и только ухудшают
пропессы активной релаксации. Назначение их оправдано только в фазу замед¬
ленной релаксации (Е/А < 1) у больных с тахикардией. Однако на этой стадии
больные амилоидозом сердца обьгшо не попадают в поле зрения врачей.
Терапия мочегонными также ограничивается низким уровнем артериального
давления. Показания для применения дигоксина достаточно противоречивы и
требуют предельной осторожности, поскольку он связывается с ЭКС1рацСЛЛЮ-
лярно расположенными фибриллами амилоида и может быть причиной повы¬
шенной чувствительности и токсичности.Таким образом, медикаментозное лечение сердечной недостаточности,
развившейся вследствие амилоидной кардиопатии, представляется сложной и
практичесю! не решенной задачей. Амилоид, отложившийся в тканях, будучи
по своей структуре фибрил..1ярным белком, достаточно устойчив к резорбции
(растворению) димексидом или фибриллексом; следовательно, лечение ами-
лоидоза в основном направлено на торможение процесса амилоидогенеза.
Именно поэтому в сложившейся ситуации особое значение придается ранней
диагностике амилоидной кардиопатии, поскольку только при своевременно
начатом воздействии на процесс амилоидогенеза в целом можно ожидать улуч¬
шения прогноза таких пациентов.Воздействие на амилоидогенез при AL-амилоидозе, так же как и при других
плазмоклеточных дискразиях, осуществляется путем подавления в костном
мозге клона плазматических клеток, синтезирующих белок-предшественник,
которым являются легкие цепи иммуноглобулинов, с этой целью применя¬
ются различные схемы полихимиотерапии. На сегодняшний день накоплены
данные об эффективности перорального приема мелфалана в сочетании с
преднизолоном или высоких доз химиотерапевтических препаратов с последу¬
ющей трансплантацией аутологичных стволовых клеток, однако у пациентов,
страдающих AL-амилоидозом с поражением сердца, выживаемость значитель¬
но хуже.Представляем второе клиническое наблюдение.Больной Ш., 63 года, поступил в отделение кардиологии Факультетской
терапевтической клиники им. В.И. Виноградова 23.10.2008 г с жалобами
на одышку при у\їеренньіх физических нагрузках (подъем по лестнице на
1-2 этажа), эпизоды неритмичного сердцебиения, перебои в работе сердца,
ощущение дискомфорта в области сердца, эпизоды сжимающих болей в обла¬
сти сердца с иррадиацией в левую лопатку, общую слабость.Из семейного анамнеза известно, что отец страдал инсулинозависимым
сахарным диабетом, ишемической болезнью сердца, перенес инфаркт миокар¬
да, умер в 60 лет; мать умерла от инсульта в 74 года; трое детей здоровы. Больной
работает на ускорителе (имеет профессиональный контакт с радиацией).
454 КардиологияНе курит, алкоголем не злоупотребляет. Перенес аппендэктомию в 1997 г.,
страдает хроііическим отитом (после травмы левого ушного прохода в 1988 г.),
гайморитом, язвенной болезнью двенадцатиперстной кишки (единственное
обострение было диагностировано в 1995 г). Лиергологический анамнез не отя¬
гощен.Анамнез заболевания: считает себя больным в течение последних 2 нед перед
госпитализацией, хотя до этого времени иногда беспокоили ощущение дис¬
комфорта в области сердца, небольшая одышка. С начала октября отметил
появление одышки при небольшой физической нагрузке, с 20 октября беспо¬
коили сжимающие боли в области сердца с иррадиацией в левую лопатку. При
амбулаторном обследовании на ЭКГ выявлены комплексы 05 в 111 и левых
грудных отведениях, при ЭхоКГ данных за очаговые изменения миокарда, а
также иных изменений не выявлено. Для дальнейшего обследования поступил
в Факультетскую терапевтическую клинику им. В.Н. Виноградова.При осмотре: состояние относительно удовлетворительное. Конституция
гиперстеническая. Рост 174 см, вес 98 кг. Кожные покровы чистые, нормальной
окраски и влажности. Голени пастозны. Число дыханий 17/мин, дыхание вези¬
кулярное, хрипов нет. Тоны сердца аритмичные, приглушены. ЧСС 70/мин, АД
150/100 мм рт.ст. Живот мягкий, безболезненный при пальпации во всех отде¬
лах, печень и селезенка не увеличены. Симптом Пастернацкого отрицательный
с обеих сторон. Щитовидная железа пальпаторно не увеличена.В общем анализе крови НЬ 154 г/л, эритроциты 4,7 млн, цветовой показатель0,92, лейкоциты 9,3 тыс., нейтрофилы 52,2%, лимфоциты 38,1%, моноциты
6,6%, эозинофилы 2,1%, базофилы 1%, тромбоциты 181,4 тыс., СОЭ 8 мм/ч.
Тропонин при поступлении отрицательный. В биохимическом анализе крови
выявлено повышение уровня креатинина до 1,60 мг/дл, обшего билирубина до
64,8 мкмоль/л, у-ГТ до 153 Ед/л, в остальном без существенных отклонений от
нормы (кальций 2,16 ммоль/л, общий белок 64,8 г/л, альбумин 40,7 г/л, глюко¬
за 4,8 ммоль/л, азот мочевины 5,2 ммоль/л, мочевая кислота 377,1 мкмоль/л,
АЛТ 41 £д/л, лет 28 Ед/л, холинэстераза 5797 Ед/л, натрий 138 мэкв/л, калий4,9 мэкв/л, КФК72 Ед/л, МВ-КФК 11 Ед/л). Выявлена гиперлипидемия
4~го типа: триглицериды 301 мг/дл, обищй холестерин 199 мг/дл, ЛПОНП-хс60,2 мг/дл, ЛПНП-хс 100,8 мг/дл, ЛПВП-хс 38 мг/дл, КА 4,24.Электрофорез белков, гормоны щитовидной железы, иммуноглобулины
крови без отклонений от нормы. РФ, СРБ отрицательны, анти-О-стрептолизин
125 МЕ/мл. АЧТВ 1,13 Ед, протромбиновый индекс 100%, фибриноген 2,8 г/л.В общем анализе мочи: удельный вес 1006, pH 5, белка, сахара, ацетона нет,
уробилин в пределах нормы, лейкоциты и эритроциты единичны в поле зре¬
ния, слизи много, бактерий немного.По данным рентгенографии органов грудной клетки, легкие без свежих оча-
говььч и инфилыративных изменений. Корни легких структурны. Диафрагма
расположена обычно. Плевральные синусы свободны. Сердце расположено
горизонтально, несколько расширено влево, аорта уплотнена.Обращала на себя внимание ЭКГ {рис, 22.4): на фоне синусового ритма опре¬
деляются частые наджелудочковые экстрасистолы. Электрическая ось сердца
Глава 22. Амилоидоз сердца — рутинный диагноз?455—ґ-Y^—'Ґ I,л-1Л, .1fX^CРис. 22.4. Электрокардиограмма болытого Ш, Скорость записи 25 мм/с. Пояснения в
текстерезко отклонена влеьо (блокада передней ветви левой ножки пучка Гиса) —
выраженный зубец R в отведении aVR говорит о том, что ось отклонена более
чем на -60“. ЧСС 66/мин. АБ-блокада I степени (интерсші PQ 0,22 с). Зубец Р
двугорбый, расширен (0,14 с), уплощен. Определяются комплексы 05 в отве¬
дениях И, ТТГ, aVF, а также с V, по V^, в отведениях V<^-Vg амплитуда зубца R
резко снижена. QRS 0,1 с, 0Г41О мс. Уплошенный зубец Т в отведениях 1, aVL.При суточном мониторировании ЭКГ по Холтеру, выполненном за 2 нед
до госпитализации: смена источника автоматизма по предсердиям. Картина
взаимодействия двух уровней ритма, постояттно сменяющих друг друга: с
ЧСС 50—60 и 70—80/мин. АВ-блокада I степени {PQ 0,25—0,27 с). Политопные
суправентрикулярные экстрасистолы, в том числе поздние, всего >13 ООО;
куплеты >80, триплеты >70, частыс эпизоды би-, тригемипии. Частые эпизо¬
ды политопной наджелудочковой тахикардии с ЧСС 100/мин, максимум 28 с,
всего >100; выскальзывающие паджелудочковьте сокращения. Политопные
желудочковые экстрасистолы, всего 20, в том числе выскальзывающие желу¬
дочковые комплексы. В 02:14 — выскальзывающий желудочковый куплет.
Частые эпизоды удлинения RR интервалов, в том числе связанные с удлине¬
нием постэкстрасисто-тической паузы и посггахикардитической депрессией
ритма, при смене двух уровней ритма. Признаки снижения функциональной
способности синоатриальной и атриовентрикулярной систем.Таким образом, несмотря на досгаточно острый характер появления жалоб, в
том числе эпизодических сжимающ>гк болей в области сердца с иррадиацией в
левую лопатку, и «рубцовые» изменения ЭКГ у пожилого мужчины с отягощенной
по сердечно-сосудистым заболеваниям наследствснностью, диаі ноз ишемической
456Кардиологияболезни сердца представлялся крайне маловероятным. Обращало на себя внима-
1ше несоответствие выраженных изменений на ЭКГ (если интерпретировать ее
формально, имелись признаки рубцовой фазы 0-инфаркта двух локализаций —
нижней и переднепереіюродочно-верхушечной) и довольно невыразительных
болей в области сердца, установить наличие которых удалось лишь при тищтель-
ном опросе. Это само по себе весьма необычно для двух трансмуратьных инфар¬
ктов миокарда, по меньшей мере один из которых развился в последние 2 нед.
Нетипично явное преобладание наджелудочковых нарушений ритма. Кроме того,
не бьшо выявлено повышения уровня тропонина в крови и полностью ОТС>ТС1БО-
вали (при такой ЭКГ) нарушеїшя локальной сократимости по данным проведен¬
ной амбулаторно ЭхоКГ. Все это заставило д>’ыать о том, что изменения на ЭКГ
носят псевдоинфарктный характер и обусловлены диффузным поражснттем мио¬
карда неишемического характера. В качестве наиболее вероятного диагноза рас¬
сматривался амилоидоз сердца, в связи с чем больной был направлен на повторное
эхокардиографичсское исследование к проф. В.П. Седову.По данным повторной ЭхоКГ {рис. 22.5), полость левого желудочка не рас¬
ширена: КДР 5,2 см, КДО 116 мл, КСО 78 мл. Толш,ина стенок левого же.іу-
дочка: МЖП 1,7—1,8 см, задняя стенка 1,8 см. Общая сократительная функция
снижена, ФВ левого желудочка 34%. Нарушений локатъной сократимостиРис. 22.5. Эхокардиограммы больного Ш. В верхнем ряду — расчет показателей систо¬
лической (слева, ФВ) и диастолической (справа, Е/А) ф>'нкций левого жел>'ДОчка.
В нижнем ряду — \толщение стенок левого жел>'дочка и его выраженная неоднород¬
ность (белыми стрелками >’казат1ы «светящиеся» участки повышенной плотности мио¬
карда)
Глава 22. Амилоидоз сердца — рутинный диагноз? 457не вьшвлено. Полость правого желудочка 2,9 см. Левое предсердие 4,2 см,
объем 57 мл. Правое предсердие 52 мл. Митральная регургитация II степени.
Трансмитральный поток: Е — 103 см/с; А — 37 см/с; Е/А 2,8; DecT — 138 мс.
Аортальный клапан: аматятуда раскрытия не уліеньшена — 2,1 см (норма
>1,5 см), градиент средний 2,3, максимальный 4,7 мм ртхт., скорость крово¬
тока 109 см/с, VTT 21 см/с, dP/dt 650 мм рт.ст. Трикуспидальная регургитация
0—1 степени. Клапан легочной артерии: скорость кровотока 66 см/с, признаков
легочной гипертензии нет; СДЛА 20 мм рт.ст. Нижняя полая вена не расши¬
рена, на входе спадается >50%. Заключение: выраженная гипертрофия левого
желудочка, в том числе и верхних отделов, со снижением глобальной сокра¬
тимости. Митра.чьная регургитация И степени. Диастолическая дисфункция
левого желудочка по рестриктивному типу. Эхокардиографичсские признаки
могут указывать на гипертрофическую кардиомиопатию. Выраженная гиперэ-
хогенность миокарда не исключает амилоидоз сердца.Выявленное при ЭхоКГ утолщение сгенок левого желудочка формально могло
бьпъ расценено как гипертрофия, однако ЭКГ и систолическая дисфункция не
соответствовали зтоліу процессу. Кроме утолщения миокарда, В.П. Седовым было
отмечено также его характерное свечение, местами фанулярносгь, а также выра¬
женные нарушения диастолической функции левого желудочка по рестриктивно¬
му типу, *гго делало диагноз амилоидоза сердца еще более вероятным. По сравне¬
нию с проведенной амбулаторно ЭхоКГ отмечена также зііачительно более низкая
ФВ левого желудочка, что соответствовало имевшейся у больного одьппке; зон
гипокинезии левого желудочка, как и при первом исследовании, не выявлено.Тем не менсс, несмотря на высокую вероятность амилоидоза, нельзя было
полностью исключить другие инфильтративные заболевания сердца, требовалась
морфологическая верифіжаиия диагноза. Выполнены биопсия слизистой обо¬
лочки десны и прямой кишки (при окраске кото красным отложения амилоида
не выявлены), одновременно (с учетом недостаточной диагностической значимо¬
сти данных исследований, особенно в случае отрицательного результата) принято
решение о проведении эндомиокардиальной биопсии правого желудочка.Для определения возможных признаков системности заболевания про¬
ведено УЗИ органов брюшной полости: печень не увеличена, контуры ров¬
ные, паренхима однородной структуры, обычной эхогснности, сосудистый
рисунок не изменен, внуїрипечеіючньїе желчные протоки не расширены.
Желчный пузырь не увеличен, в теле и в шейке перегиб, стенки не изменены.
В просвете эхоструктур не выявлено, общртй желчный проток не расширен.
Поджелудочная железа не увеличена, контуры ровные, четкие, паренхима
гиперэхогенная с явлениями липоматоза. Селезенка не увеличена, паренхима
однородной структуры. Заключение: эхопризнаки дисформии желчного пузы¬
ря, липоматоз поджелудочной железы.Как предшес'івующий биопсии этап, с учетом формальных признаков
«рубцов» на ЭКГ, была выполнена короиароангыография: сбалансированный
тип кровоснабжения сердца. Ствол левой коронарной ащерии не изменен.
Передняя межжелудочковая артерия не изменена. Огибающая артерия не
изменена. Правая коронарная артерия не изменена.
458 КардиологияДалее выполнена эндомиокардиальная биопсия правого желудочка (проф.В.А. Сулимов): полу^іено 5 у^гастков межжелудочковой перегородки и свобод¬
ной стснки правого желудочка. Морфологическое исследование биоптатов
проведено проф. ЕЛ. Коган ірис. 22.6, см. цветную вклейку).• Межжелудочковая перегородка — эндокард тонкий с очагом утолще¬
ния предсташтен пластом эндотелиальных клеток и утолщенной базаль¬
ной мембраной. Кардиомиоциты с очаговым исчезновением поперечной
исчерченности и фанулами липофусцина. Интсрстиций неравномерно
расширен, содержит сосуды Тебезия с утолщенными стенками, не окра-
щенными фуксином ггри окраске по Ван Гизону.• Межжелудочковая перегородка вблизи верхушки — эндокард тонкий с o^[a-
гом утолщения, представлен пластом эндотелиальных клеток и утолщенной
базальной мембраной. Крупный очаг гиалиноподобной ткани с тенями
кардиомиоцитов, не содержапщх ядер, оплетенных экстрацеллюлярным
матриксом, и сосудом с утолщенными стенками за счет гиалипоподобных
масс, негативных по Ван Гизону. В других участках кардиомиоциты с очаго¬
вым исчезновением поперечной исчерченнос'ги и гранулами липофусщіна.
Интерстипий неравномерно расширен, содержит сосуды Тебезия с утолщен¬
ными стенкііми. Кроме того, иод эндокардом обнаружен очаг липоматоза.• Субэндокардиштьный участок миокарда свободной стенки правого желу¬
дочка. В субэ1щокардиальных участках сохраняются отдельные гипертро¬
фированные кардиомиоциты, большинство «мумифицированного» вида,
не содержат ядер, оплетены гиалиноподобной тканью, при окраске по Ван
Гизону — негативной.• Субэндокардиальный участок стенки основания правого желудочка.
В субэндокардиальных участках сохраняются отдельные гипертрофиро¬
ванные кардиомиоциты, многие «мумифицированного» вида, не содержат
ядер, оплетены гиалиноподобной тканью, при окраске по Ван Гизону —
негативной. Кроме того, на месте отдельных кардиомиоцитов кистозные
пустоты, ограниченные перимизием.• При окраске конго красным с исследованием в поляризационном микро¬
скопе обнаружены массы амилоида в интерстиции и стенках сосудов.Заключение, амшюидоз сердца.Бьшо проведено титрование амилоида', выявлено слабое свечение по ходу
сарколеммы мышечных волокон и в стснках мелких сосудов при добавлении
антител к легким цепям (каппа и лямбда), а также интенсивное свечение при
добавлении антител к преальбумину (транстиретину).Таким образом, диагноз первичного амшюидоза сердца был полностью
подтвержден. Наиболее вероятно, что предшественником амилоида является
транстиретин (TTR-тип амилоида).Окончательный диагноз был сфор\іулирован следующим образом: первич¬
ный амилоидоз сердца (TTR-амилоидоз?). Нарушения ритма и проводимости
сердца: синдром слабости синусового узла (синусовая брадикардия, периоды
миграции водителя ритма по предсердиям), АБ-блокада I степени, блокада
передней ветви левой ножки пучка Гиса, частая политопная наджелудочковая
Глава 22, Амилоидоз сердца — рутинный диагноз?459экстрасистол ИЯ, пробежки наджелудочковой тахикардии, редкая желудочко¬
вая экстрасистол ИЯ. Недостаточность кровообращения ІІА стадии, II функ¬
циональный класс (NYHA). Гиперлипидемия 4 типа. Хроническая почечная
недостаточность, I стадия. Язвенная болезнь двенадцатиперстной кишки вне
обострения. Дисформия желчного пузыря. Холестатический синдром.Ключом к постановке данного диагноза стала в первую очередь крайне
необычная ЭКГ, которая, с учетом клинических данных, не соответствовала
диагнозам ишемической болезни сердца, гипертрофической кардиомиопатии
(весьма типичны для ами.іоидоза именно псевдоинфарктные изменения, кото¬
рые описывают чаше, чем снижение вольтажа комплекса QBS). Для сравнения
приводим ЭКГ больного с TTR-амилоидозом сердца, описанного немецкими
авторами (рис. 22.7).Не совсем обычен для выраженного амилоидоза сердца столь короткий
анамнез заболевания, который заставлял думать об острых причинах ухудше¬
ния состояния больного. В то же время симптоматика и на момент обращения
больного в Факультетскую терапевтическую клинику им. В.Н. Виноградова
оставалась умеренно выраженной (несмотря на объективно тяжелое пораже¬
ние сердца, в том числе интрамуральных сосудов, и развитие частой экстра-
систолии). Это говорит о том, что пациент мог не ощущать и гораздо раньше
появившихся симптомов.в клинике проводилась терапия: престариум 2 мг (отменен в связи с разви¬
тием гипотонии), кордарон0,2 по 1 таб. утром, конкор2,5 мг по 1/2 таб. утром
(отменен в связи с развитием синусовой брадикардии до 40-44/мин), тромбо-
АССОД по 1 таб, вечером, торвакард20 мг по 1 таб. вечером, клоназепам2 мг
по 1/4 таб. на ночь, урсосан 250 мг по 1 таб. на ночь. В результате терапии
состояние несколько улучшилось: перестали беспокоить перебои в работеРис. 22.7. Электрокардиограм.ма пациента, страдающего TTR-амилоидозом сердца (из
статьи А. Hesse и соавт., 1993 г.)
460Кардиологиясердца, практически не беспокоили боли в области сердца; одышка сохраня¬
лась на прежнем уровне. Больной был выписан с рекомендациями продолжить
подобранную ему симптоматическую терапию, направлен в Клинику терапии,
нефрологии и профессиональных заболеваний им. Е.М. Тареева для консуль¬
тации по поводу основного заболевания.Проведена генетическая диагностика (лаборатория молекулярной генетики
человека при Научно-исследовательском институте физико-химической меди-
1ЩНЫ Росздрава, зав. канд. биол. наук Э.В. Генерозов): в резу^чьтате сканирова¬
ния гена ТТЯ в представленном образце геномной ДНК выявлена нуклеотид¬
ная замена С >А, приводящая к аминокислотной замене Thr >Asn в 40-м кодоне
кодируемого геном белке транстиретина (рис. 22.8). Обнаруженный генетиче¬
ский вариант выявлен в гетерозиготном состоянии и не бьш описан ранее.
Аналогичная мутация выявлена у сестры пациента, клинически здоровой.
Исходя из того, что аминокислотная замена Thr40Asn является негомологич¬
ной, возможно предположить, что данная мутация может быть ассоциирована
с нарушениями, приводящими к гиперагрегации транстиретина и, как след¬
ствие, — развитию амилоидной болезни.Учитывая вьшвленный тип амилоида (транстиретиновый), проведение
медикаментозной терапии представляется малоперспективным. Обсуждаются
возможности хирургического лечения заболевания (трансплантация печени?),
поскольку именно это вмешательство на сегодняшний день признается един¬
ственным эффективным методом лечения TTR-амилоидоза. В связи с тем что
имеются сведения о продолжении прогрессирования амилоидоза сердца после
трансплантации печени, в литературе, как уже сказано выше, предлагается
одновременное проведение трансплантации сердца и печени.P.S. В течение 1,5 лет состояние больного оставалось стабильным, он про¬
должал работать. В январе 2010 г после перенесенной энтеровирусной (?)
инфекции отметил заметное усиление одышки (появляется при подъеме на
несколько ступеней), появление перебоев в работе сердца. В Факультетскую
терапевтическую клинику им. В.Н, Виноградова обратился через 2 мес, на ЭКГТ G С Т
220G А Т G
225АС N230С Т G G G
235А G С С А Т
240Т ТРис. 22.8. Спектрограмма секвенирования фрагментов нуклеотидной последователь¬
ности гена TTR. Стрелкой указана позиция нуклеотидной замены, цриводящей к ами¬
нокислотной замене Thr >Asn в 40-м кодоне гена
Глава 22. Амилоидоз сердца — рутинный диагноз?461зарегистрирована мерцательная аритмия {рис. 22.9). При ЭхоКГ, выполненной
проф. В.П. Седовым, отмечено некоторое уменьшение объемов левого желу¬
дочка (КДО 83 мл, КСО 55 м.т, УО 28 мл), увеличение размеров левого (4,7 см,
79 мл) и правого предсердий (65 мл); толщина стенок сердца и ФВ левого
желудочка (34%) остались на прежнем уровне. При чреспищеводной ЭхоКГ
выполненной дважды, внутрипредсердного тромбоза не выявлено, определя.1-
ся эффект спонтанного эхоконтрастирования.После плановой подготовки (кордарон400 мг/сут, варфарин) проведена
электрическая кардиоверсия бифазным разрядом 180 Дж, после которой
регистрировался АВ-узловой ритм с ЧСС 36/мин. Реакции на повторные
инъекции атропина не было, в результате инфузии добутамина частота
узлового ритма увеличилась до 50/мин. Начата временная эндокардиальная
стимуляция предсердий с частотой 60/мин. Через сутки отмечено восста¬
новление синусового ритма с ЧСС 54/мин {рис. 22.10), на этом фоне сохра¬
нялись одышка при ходьбе и умеренная гипотония (100/60—70 мм рт.ст.).
Амиодарон полностью отменен, варфарин заменен инъекциями фраксипари-
на по 0,6 мл 2 раза в день подкожно. В связи с невозможностью назначения
адекватной антиаритмической терапии, плохой переносимостью синусовой
брадикардии, опасностью рецидива узлового ритма больной был переведен
в Городскую клиническую больницу № 4 г. Москвы с целью имплантации
постоянного экс в режиме DDDR, где в имплантации ЭКС было отказано в
связи с отсутствием показаний к его установке. В настоящее время решается
вопрос об имплантации ЭКС (ИКД?) в другом учреждении и возобновлении
антиаритмической терапии.Рис, 22.9. Электрокардиогра\ша больного Ш. (апрель 2010 г.). Скорость записи 25 мм/с.Пояснения в тексте
462КардиологияЯв11■ЬіГтSil4^--авіЕкШти .. ''sP_ :H ;Щ'ЇГ £vf’N Tv'l-щшЯтшГІН-- г,r1Ч-т: fr
ifjfи-І!rinq-:!:j'іД'jjiііШЩ“л/IЯ♦FH-ШШііШїї#tiг:г£ill‘ ^ ТГ іійit::4,-~rРис. 22.10. Электрокардиограмма больного Ш. после кардиоверсии. Скорость записи
25 мм/с. Пояснения в текстеКомментарий О.В. Благовой — доцента кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И. М. Сеченова, канд. мед. наукТаким образом, признаки, заставившие подозревать амилоидоз сердца, у
каждого из пациентов были достаточно очевидны (и схожи), однако у обоих
в анамнезе — «нормальные*> эхокардиографические протоколы и отсут¬
ствие адекватной интерпретации ЭКГ. Если ЭКГ является обшедоступным
и достаточно объективным методом, то результаты ЭхоКГ в значительной
степени зависят от настороженности врача ультразвуковой диагностики в
отношении амилоидоза сердца и опыта его диагностики. Большое значе¬
ние имеет также и возраст — хотя единичные случаи амилоидоза сердца у
детей описаны, у молодых пациентов он гораздо менее вероятен; картина
рестриктивной кардиомипатии с «гипертрофией» стенок сердца требует
включения в кр>т дифференциальной диагностики других инфильтратив-
ньтх заболеваний — различных болезней накопления (см. описание паци¬
ента с болезнью Фабри в главе 20) в первую очередь. Дифференциальным
признаком при этом может служить наличие признаков гипертрофии
левого желудочка в грудных отведениях на ЭКГ (в сочетании со сниже¬
нием вольтажа в стандартных), характерное для этих больных. Второе
клиническое наблюдение демонстрирует, что отрицательные результаты
«периферической» биопсии должны быть .1ишь дополнительным доводом
в пользу проведения эндомиокардиальной биопсии, затягивать с проведе¬
нием которой в отсутствие явных признаков системности не имеет смысла.
Глава 22. Амилоидоз сердца — рутинный диагноз? 463ЛИТЕРАТУРАРамеев В.В., Козловская Л.В., Саркисова ИЛ. Амилоидоз: вопросы диагно¬
стики и лечения // Клиницист — 2006. — № 4. — С. 35—41.Chew С., Ziady G.M., Raphael M.J., Oakley С.М. The functional defect in amyloid
heart disease: the stiff heart syndrome // Am. J. Cardiol. 1975; 36: 438—444.Dubrey S.W., Cha K., Anderson J. et al The cHnical features of immunoglobulin
light-chain (AL) amyloidosis with heart involvement // QJM. 1998; 91: 141-157.Grazi G.L., Cescon М., Salvi F. et al. Combined heart and liver transplantation for
familial amyloidotic neuropathy: considerations from the hepatic point of view //
Liver Transpl. 2003 Sep; 9 (9): 986—992.Hesse A., Altland K., Linke R.F. et al. Cardiac amyloidosis: a review and report of a
new transthyretin (prealbumin) variant // Br. Heart L 1993 Aug; 70 (2): 111—115.Keyur B. Shah, Yoshio fnoue, Mandeep R. Mehra. Amyloidosis and the Heart //
Arch. Intern. Med. 2006; 166; 1805-1813.Kyle R.A., Gertz M.A., Greipp P.R. et al. A trial of three regimens for primary amy¬
loidosis: colchicines alone, melphalan and prednisone, and melphalan, prednisone,
and colchicines //N. Engl. J. Med. 1997; 336: 1202-1207.Kyle R.A., Greipp PR. Amyloidosis (AL). Clinical and laboratory features in 229
cases // Mayo Clin. Proc. 1983; 58: 665—683.Liepnieks J.J., Benson M.D. Progression of cardiac amyloid deposition in heredi¬
tary transthyretin amyloidosis patients after liver transplantation I j Amyloid. 2007
Dec; 14 (4): 277-282.Rubinow A., Skinner М., Cohen A.S. Didoxin sensitivity in amyloid cardiomy¬
opathy 11 Circulation. 1981; 63: 1285-1288.Skinner М., Anderson J., Simms R. et al Treatment of 100 pacients with primary
amyloidosis: a randomized trial of melphalan, prednisone, and colchicines versus
colchicines only//Am. J. Med. 1996; 100: 290-298.Swanton R.H., Brooksby LA., Davies MJ. et al. Systolic and diastolic ventricular
function in cardiac amyloidosis: studies in six cases diagnosed with endomyocardial
biopsy j I Am. J. Cardiol. 1977; 39: 658-664.Walid Hassan, Hani Al-Sef'gani, Walid Mourad, Rashed Tabbaa. Amyloid heart
disease // Tex. Heart Inst. J. 2005; 32 (2): 178—184.Westermark P., Benson M.D., Buxbaum J.N. etal. Amyloid fibril protein nomencla¬
ture: 2002//Amyloid. 2002; 9: 197-200.Westermark P., Johansson B., NatvigJ.B. Senile cardiac amyloidosis: evidence of
two different amyloid substances in the ageing heart // Scand. J. Immunol. 1979; 10:
303-308.
Глава 23ПЕРВИЧНЫЕ ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ
СЕРДЦА (ОПЫТ ТЕРАПЕВТОВ)0.R Благова, ИД. Саркисова, А.В. Ледоступ, С.Л. Дзсмешкевич,
В.Е. Синицын, И.В. Гагарина, В.П. СедовМы ттредсттіяем описание двух клинических случаев, между которыми
прошло 10 лет. За эти годы нам больше не встретилось подобных больных, и
мы не можем говорить о накоплении опыта работы с ними; стал иным уровень
доступной нам диагностики, но постановка точного прижизненного диагноза
первшшой злокачественной опухоли сердца и выбор тактики лечения остаются
крайне сложной задачей, решать которую приходится не только узким специ¬
алистам (онкологам, кардиохирургам, лучевым диагностам), но и терапевтам и
кардиологам широкого профиля.Приводим первое наблюдение.Больная К., 41 год, поступила в отделение кардиологии Факультетской
терапевтической клиники им. В.Н. Виноградова Московской медицинской
академии им. И.М. Сеченова 02.06.1999 г. с жалобами на постоянную одышку
в покое, которая усиливается в положении лежа и при малейших нагрузках,
разлитую ноющую боль и чувство стеснения за грудиной, в левой половине
грудной клетки с иррадиацией в левые лопатку и плечо (боль несколько умень¬
шается в положении сидя с наклоном вперед), постоянное учащенное нерит¬
мичное сердцебиение, сухой приступообразный кашель, преходящие отеки
голеней и стоп, периодические подъемы температуры до 37,5—37,3 'С, иногда с
кратковременным ознобом, тошноту, снижение аппетита, выраженную общую
слабость, отсутствие сна.Из анамнеза: проживала в Белгородской области, в 130 км от асбестового
производства, в 50 км от цементного и кирпи^шого заводов. По профессии —
фармацевт; наблюдалась аллергическая сыпь на вдыхание паров пенициллина.
С 1989 г — ежегодные аллергические артриты мелких суставов кистей и стоп
на тополиный иух, которые иногда сопровождались явлениями бронхоспазма;
несколько раз парентерапьно применялся преднизолон с быстрым положи¬
тельным эффектом. Последний подобный эпизод — весной 1998 г В детстве
ставился диагноз мочекаменной болезни (выявляJ^ocь два камня слева), про¬
водилось лечение.В январе 1999 г. перенесла острую респираторнуто вирусную инфекцию
(грипп?) без явных осложнений, самочувствие полностью нормализовалось,
активно работала {рис. 23.1)', 3 апреля внезапно появилось сердцебиение,
сопровождавшееся одышкой при нагрузке, слабостью, несколько позже — суб¬
фебрилитет, сухой приступообразный кашель. При обследовании в стационаре
Глава 23, Первичные злокачественные опухоли сердца (опыт терапевтов) 465г. Воронежа зафиксировано трепетание предсердий с ЧСС 130/мин, по данным
ЭхоКГ левое предсердие несколько расширено (до 4 см), имелась жидкость в
полости перикарда. Попытки восстановления синусового ритма пугем вну¬
тривенного введения новокаинамида, кордарона, дигоксина успеха не имели.
Переведена в больницу г. Белгорода, где состояние расценивалось как инфек-
ционно-аллсргический миокардит подострого течения; отмечались норма^чь-
ные уровни бшіирубина, ACT, АЛТ, при осмотре гинекологом патологии не
выявлено. Проведено лечение ампициллиііом внутримыхиечно, бицшитином
(2 инъекции), нестероидными противовоспалительными препаратами, корда-
роном 600-800 мг/сут, на фоне которого нормализовалась температура тела,
одьшіка и тахикардия сохранялись, 20 мая больная отмстила резкое усиление
одышки, кашля, появление бесцветной мокроты, цианоза губ, субфебрилитета.
С этого времени сохранялась постоянная одышка в покое, которая периоди¬
чески приступообразно усиливалась, больная не могла лежать, потеряла в весе
7 кг. От приема ортофена отказалась в связи с выраженной тошнотой, прини¬
мала кордарон400 мг/сут. Поступила в клинику по экстренным показаниям,
При поступлении состояние тяжелое. Температура тела 36,8 “С. Кожные
покровы и склеры субиктеричны. Отеков нет Лимфоузлы не >ъеличены,
безболезненны. Число дыханий 36—40/мин, перкуторный звук притуплен
справа ниже уровня IV ребра, дыхание жесткое, практически не проводится в1989Янв.1999 3.IV1999 5.IV 20.V 20.VI.99 7.V1
РВРГ?подъем тела
36,5-37,5°суставной с-мІампициллин, бициллинТТбронхоспазмТПодышкавыпот в перикар,це??? 1выпот в плевре???тошнота, рвотагепатомегалиялейкоциты крови11,6 тыс. 19,8об/пр. билирубин9,4 мкмоль/л2,6 мг/% -
11,9 мкмоль/лАЛТ/АСТ0,3/25 ед/л325/725 319/323ГГТ/ЩФ2.6 2,5 3,5креатининлейкоциты мочи2-3-3 в п/зрд.преднизолонв/вкордарон мг/сут600-800-600-400 мг 600 мг/сутнпвс ^Рис. 23Л. Анамнез болі.ной К., 41 год
466 Кардиологиябазальные отделы правого легкого, умеренно ослаблено в базальных отделах
слева, хрипов нет. Визуально определяется яремная вена слева на 1/2 длины.
Верхушечный толчок не усилен, умеренно смещен влево, тоны сердца при¬
глушены, в положении стоя выслушивается непостоянный III тон, шумов
нет. ЧСС 120—130/мин, ритм неправильный, дефицит пульса до 20/мин,
наполнение пульса на лучевых артериях снижено. АД 120/80 мм рт.ст. Живот
мягкий, безболезненный во всех отделах. Печень увеличена преимущественно
за счет левой доли, выступает из-под края реберной дуги на 2 см, плотно-эла-
стической консистенции, безболезненна, селезенка не увеличена. Симптом
Пастернацкого отрицательный с обеих сторон.На ЭКГ— трепетание предсердий с коэффициентом проведения 2:1 и ЧСС
130/мин, ЭОС расположена нормально. Неглубокие отрицательные зубцы Т в
отведениях V^—Vfj. Признаков гипертрофии желудочков нет. Поздние потен¬
циалы желудочков не выявлены. С учетом безуспешных в прошлом попыток
медикамеїітозного купирования трепетания синусовый ритм с ЧСС 76/мин
восстановлен в день поступления методом чреспищеводной электрической
стимуляции предсердий ірис. 23.2); одышка несколько уменьшилась, однако
существенного улучшения самочувствия не отмечалось. Было начато обследо¬
вание.Лабораторные показатели {табл. 23.1): в общем анализе крови отмечался
лейкоцитоз (12 тыс.) без сдвига формулы влево, НЬ 12,4 г%, СОЭ 7 мм/ч.
Значительная гиперфермснтсмия (ACT 723 ME, АЛТ 265 ME, у-ГТ 952 Ед/л при
норме до 32, ЩФ 1071 Ед/л при норме до 280, уровень КФКв норме), общий
билирубин 2,6 мг%, креатинин 2,3 мг%, азот мочевины 98 мг%, при электрофо¬
резе белков отмечалось повышение аз-глобулинов (до 16,1 отн.%) и снижение
у-глобу.пинов (до 15,8 отн.%), СРВ +++, RW ++++, остальные иммуноло¬
гические показатели не изменены (латекс-тест, АНФ, анти-О-стретолизин,
АНФ отрицательны, LE-оетки, антитела к ВИЧ не обнаружены, антитела ку—у—^^ ^Рис. 23,2. Элекфокардиофамма больной К. после кардітоперсии. Скорость записи25 мм/с. Пояснения в тексте
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 467Таблица 23.1Результаты анализов крови больной К. в динамикеПоказатель3 июня8 нюня12-14июняНЬ12,4 г9,2 г%Цветовой показатель0,78Эритроциты4,3 млнЛейкоциты11,6 тыс.19,8 тыс.Нейтрофилы палочкоядерньте1%10%Нейтрофилы сегментоядерные70%79%Лимфоциты28%9%МоноцитыЭозинофилыСОЭ7 мм/ч7 мм/чОбший белок6,2 г%Альбумин, або. кол-во30 г/л49,5 отн.%Альбумин (фракция)а] -глобулины6,1 отн.а2-глобулины16,1 отн,%Р-глобулины12,4 отн.$у-глобулины15,8 0ТН.ЇACT725 ME (Nao40)319 MEАЛТ265 ME (N до 40)323 MEКФК29 ME78 MEУ-ГТ192 ME(Nj(o60)952 Е/л (N до 32)ЩФ1071 Е/л (N до 280)Обший билирубин2,6 мг%11,9 мкмоль/л (N до 17,1)Креатииин170 мкмоль/л (N до 8,0)Мочевина18,2 мкмоль/л (N до 8,3)201 мг%Калий4,2 ммоль/л2,9-3,2
ммоль/лІлюкоза170 мг%нативной ДНК 1,3, к денатурированной ДНК 1,4), маркеры вирусов гепатита
В и С отрицательные. Общий анализ мочи в пределах нормы.При рентгенографии органов грудной клетки подтверждено наличие жид¬
кости ниже уровня IV ребра справа и небольшого количества слева, сердце
увеличено в размерах, на повторных снимках после плевральной пункции
дополнительных изменений не выявлено. Плевральная пункция проводилась
дважды, так как за 4 дня после первой пункдии выпот накопился в прежнем
объеме 1,5 л. Пунктат оба раза носил характер геморрагического экссудата
с высоким содержанием лимфоцитов (до 83%), содержанием белка до 10%о,
сахара — 150 мг%, большим количеством пролиферирующих мезотелиаль-
ных клеток, в отдельных группах которых — признаки клеточного и ядерного
468 Кардиологияполиморфизма; проба Ривальта отрицательная, удельный вес 1005, pH 8, при
посеве роста микрофлоры не пол>'чено, атипичных клеток, микобактерий
туберкулеза не выявлено, ПЦР на микобактерии туберкулеза отрицательная.ЭхоКГ: клапаны не изменены, левое предсердие 4,6 см, количественно опре¬
делить другие камеры сложно из-за жидкости в полости перикарда (по задней
стенке левого желудочка 1,11 см, по передней — 0,52 см), по этой же причине
не представляется возможным оценить сократітге.іьную функцию левого желу¬
дочка. Полость левого желудочка 2,8 см (КДР), значительно уменьшена ампли¬
туда движения боковой и передней стенок левого желудочка, висцеральные
листки перикарда утолщены. Кровоток в легочной артерии 138 см/с, фадиент
на клапане легочной артерии 15 мм рт.ст.При УЗИ органов брюшной полости отмечалось лишь небольшое увеличение
печени за счет левой доли. Щитовидная железа, по данным УЗИ, не изменена.В течение всего пребывания больной в клинике диагноз оставался неясным.
Несомненно, ведушим в клинической картине было тяжелое поражение миокар¬
да и развитие в связи с этим прогрессирующей недостаточности кровообращения
по обоим кругам. С первьц( дней наиболее вероятным, с учетом перенесенного
в январе острою респираторного вирусного заболевания, развития трепетания
предсердий, появления и нарастания одышки, прогрессирующего увеличения
левого предссрдїїя, наличия экссудативного перикардита, стойких изменений на
ЭКГ в виде отрицательных зубцов 7в левых грудных отведениях, представлялось
наличие у больной постинфекпионного миокардита подострого течения. Была
начата терапия кордароном 600 мг/сут, альдактоном 100 мг/сут, преднизолоном
30 мг/сут (вну'ірь), аспирином 0,125 на ночь. В связи с выявленной гиперфер-
ментемией (в то же время отмечалось появ.ттение болезненности при пальпации
края печени, некоторое увеличение ее размеров и напряженности, кратковре¬
менное потемнение мота) доза преднизолона до получения маркеров вирусов
гепатита В и С была снижена до 20 мг, а на третий день лечения в связи с появ¬
лением лихорадки до 38 °С с ознобом препарат был временно отменен, хотя
складывалось впечатление о некотором улу’чщении самочувствия на его фоне.
Через 2 дня лихорадка прекратилась.Высокие уровни трансаминаз не позволяли расценить гепатит как исключи¬
тельно застойный. Анамнестически никаких указаний на заболевание печени
не было, вероятнее было ее вторичное поражение (лекарственный гепатит?
диклофенак?). Биопсия печени >трожала развитием кровотечения в связи с
наличием выраженного застойного компонента. Диагнозы хронического актив¬
ного гепатита с системными проявлениями, диффузных болезней соединитель¬
ной ткани, протекающих с кардитом, гепатитом, полисерозитом (системная
красная волчанка, ревматоидный артрит), предстаилялись маловероятными
в связи с норма-гьными иммунологичесісими показателями и нетипичностью
клинической картины для какого бы то ни было из них. В повторщзіх анализах
отмечались нормализация уровня билирубина, снижение ACT до 325 ME.В крови были выявлены антитела к вирусу Коксаки А9 в диагностическом
титре, что свидетельствовало о перенесенной инфекции указанным вирусом,
но не могло служить объяснением всего спектра клинической и лабораторной
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 469симптоматики. Кроме того, тяжелые миокардиты гораздо более характерны
для инфекции вирусами Коксаки группы В.Наибольшую диагностическую проблему представляло собой наличие
быстро рецидивирующего геморрагического экссудата в плевральной полости
при отсутствии каких-либо рентгенологических изменений в легких. Пункция
перикарда не проводилась в связи с небольшим количеством жидкости в его
полости, к сожалению, отсутствовала возможность провести КТ органов груд¬
ной К.1ЄТКИ. Планировалось проведение плевроскопии, сцинтиграфии легких.
Наиболее вероятными представлялись диагнозы опухоли (мезотелиомы плев¬
ры, возможно перикарда; данных за первичную опухоль с метастазами в плевру
не бьшо, хотя полностью она не исключа.іась) и туберкулеза (для которого
менее характерен геморрагический характер экссудата). Предположение о раз¬
витии у больной одновременно двух тяжелых болезней вызывало сомнения, но
было принято как рабочая гипотеза.Выявленная резко положительная реакция Вассермана рассматривалась как
неспецифическая, однако позже получены результаты специфических реак¬
ций: РИФ-200 +-Ь, РИФ-абс. +++-І-, РИБТ 52% (диагностический титр). Это,
несмотря на отсутствие очевидных клинических проявлений сифшштической
инфекции, не П03В0ЛИ.10 исключить наличие у больной скрытого сифилиса с
висцеральными проявлениями (миокардит, перикардит, гепатит).Состояние больной прогрессивно ухудшалось — развилась стоіікая гипото¬
ния, быстро нарастал (BnjioTb до асцита и анасарки) отечный синдром, рези¬
стентный к введению высоких доз лазикса (до 700 мг/сут) на фоне постоянной
инфузии доб>тамина с дофамином, появились клинические и лабораторные
признаки начальной фазы острого ДВС-синдрома (терапия гепарішом не про¬
водилась в связи с геморрагическим характером выпота в полость гитевры и,
весьма вероятно, перикарда), уровень креатинина возрос до 3,5 мг%, однако
уровень калия был значительно снижен, что способствовало возникновению
рецидивов мерцательной аритмии — 14 июня, на 12-й день пребывания в
клинике, при явлениях острой почечной недостаточности (анурия в течение
последних 1,5 сут), констатирована смерть больной К., 41 год, через асистолию.Клинический диагноз был сфорліулирован следующим образом.Конкурируюище заболеванияПодострый миокардит (постинфекдионный) тяжелого течения.
Экссудативный перикардит.2, Правосторонний экссудативный геморрагический плеврит неуточненной
этиологии (мезотелиома плевры? туберкулез?).3. Скрытый сифилис, неуточненный как ранний или поздний (сифилитиче¬
ский миокардит, перикардит, сифилитический гепатит?).Осложнения конкурируюших заболеваний: трепетание предсердий, устра¬
ненное чреспишеводной электрической стимуляцией сердца, рецидивирующая
мерцательная аритмия, идиовентрикулярныйррттм, асртстолия. Недостаточность
кровообращения ТП стадии: кардиальная астма, застойная печень, асцит, ана-
сарка. Острая почечная недостаточность. Тромбоэмболия мелких ветвей легоч¬
ной артерии. ДВС-синдром. Тромбофлебит правых подключичной и яремной
470 Кардиологиявен после пункции правой подключичной вены. Лимфостаз. Пункпия левой
подключичной вены. Катетеризация мочевого пузыря.Сопутствующее заболевание: лекарственный гепатит.Этот диапіоз, содержащий многочисленные вопросы, оставался синдром¬
ным — заболевания, обозначенные нами как конкурирующие, были по сути
дела взаимоисключающими (тяжелый миокардит, мезотелиома плевры с рас¬
пространением в средостение, сифїшис), мы лишь перечислили те варианты,
которые казались нам вероятными или хотя бы возможными, однако единая
картина заболевания не складывалась.При аутопсии — сердце размерами 14x16x6 см, вес 800—1000 г, миокард
практически полностью замещен плотной неоднородной пестрой тканью,
включает значительное количество полостных образований с геморрагическим
содержимым размерами около 1 см, одно — 3 см. Толщина стенок правого
желудочка 2 см, левого — 1,5—2 см, полость левого желудочка уменьшена.
В полости правого желудочка имеются гроздьевидньте образования на ножках,
синюшного цвета, размерами до 1 см, аналогичными образованиями замещен
трикуспидальный клапан, остальные клапаны не изменены. Аорта не изме¬
нена, коронарные артерии сдавлены замещающей миокард тканью. Листки
перикарда утолщены максимально до 5 мм, разделить их не удалось, жидкости
в полости перикарда нет.В правой плевральной гюлости — 1,5 л геморрагической жидкости (послед¬
няя пункция была проведена за 3 дня до смерти). Легкие: несколько очагов
инфаркта и свежие тромбы в мелких ветвях легочной артерии. На поверхности
пріівого легкого, покрытой висцеральной плеврой, — небольшой участок изме¬
ненной ткани бурого цвета с изъязвленной поверхностью. Печень большая,
NtyCKaTHan, на поверхности — два бурых округлых образования с цианотичным
оттенком размерами 1,5-2 см, аналогичных образованиям в полости правого
желудочка. Почки нормальных размеров, шоковые. Множественные миома-
тозные у 3-1Ы в матке. Предварительный диагноз, подтвержденный при срочном
гистологическом исследовании, — ангиосаркома сердца с метастазами в легкое
(и плевру), печень.Опухолевые поражения сердца вообще редки, среди них гораздо чаше, в
20—40 раз, встречаются метастатические опухоли (по Барденгейеру, злокаче¬
ственные опухоли различных органов в 2,3% случаев дают метастазы в сердце;
по современным данным, этот процент колеблется от 0,3 до 27), чем первичные
(не чаше, чем в 0,5-6,4% от числа всех вскрытий, в среднем процент еще ниже —
от 0,0017 до 0,28). Врастание в сердце по венам «опухолевого тромба» (опухоли
почки, придатков, костей, шитовидной железы) возникает на этапе, когда доста¬
точно выражена симптоматика, обусловленная первичной опухолью.Среди первичных опухолей явно преобладают доброкачественные, глав¬
ным образом миксомы (около 50%, а по данным кардиохирургов — и до 90%);
встречаются также рабдомиомы (около 20%, впервые описана Реклингаузеном
в 1862 г.), фибромы, лейомиомы и др. (в том числе мезотелиома АБ-узла).
Из 135 больных опухолями сердца, наблюдавшихся в Российском научном
центре хирургии РАМН им. акад. Б.В. Петровского, злокачественная опухоль
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 471была найдена лишь у 7 человек. По данным вскрытий, 25% опухолей сердца
оказываются злокачественными, более 2/3 из них — саркомы. В «Частной
патологической анатомии» А.И. Абрикосова (1940 г.) среди злокачественных
опухолей сердца упоминаюіх;я первичные раки сердца (из мезотелия перикар¬
да) и саркомы, которые могут исходить из любого к^іеточного элемента сердца
(веретено-, шганто- и круглоклеточпыс). К тому времени было описано около
45 случаев сарком. На сегодняшний день среди злокачественных опухолей чаще
встречаются ангиосаркома (2,1—7,3% всех новообразований сердца, 5 случаев
в группе больных из Российского научного центра хирургии РАМН им. акад.
Б.В. Петровского), рабдомиосаркома (более свойственна детям) и мезотслиома.
К ангиосаркомам относят и саркому Капоши (выявлялась у больных СПИДом
и пациентов, получаюш;их иммуносупрессивную терапию после іранспланта-
пии). Особо должны обсуждаться карпиноидныс опухоли сердца.Ангиосаркома сердца является разновидностью злокачественной геман-
гиоэндотелиомы и гемангиоперицитомы, имеющих схожие течение и про¬
гноз. Гистологически ткань чрезвычайно полиморфна даже в пределах одной
опухоли, характерна высокая степень анаплазии. Макроскопически опухоль
представляет собой плотное образование с очагами некроза и кровоизлияний,
инфшіьтрируюшее окруокающие ткани, описаны полиповидные разрастания в
полостях сердца. Характерно возникновение сосудистых полостей и каналов
ра:зличного размера, связанных между собой и заполненных кровью. Чаще
поражаются правые отделы сердца (80%), внутриполостной рост отмечается
примерно в четверти случаев.В 1968 г. D. Glancy опубликовал анализ 41 случая (всех описанных к тому вре¬
мени в доступной ему литературе) ангиосаркомы сердца, упоминавшейся под
различными названиями. К 1978 г бьиіо описано 71 наблюдение, а в большом
обзоре 1986 г. сопоставлено 139 случаев этой опухоли. Не отмечено заметного
роста заболеваемости — счет в мире по-прежнему идет на отдельные случаи,
растет лиигь процент прижизненной диагностики. Нами получено (из базы дан¬
ных Medline, включающей в информацию с 1966 г.) упоминание о 140 случаях
ангиосаркомы сердца (большая часть из них датирована 80—90-ми гг. XX в.).Ангиосаркома описана у больных от 8 до 80 лет, но в 70% случаев она воз¬
никает в возрасте 20—50 лет. Соотношение заболевпгих мужчин и женщин
остается постоянным ~ 2—3:1. В подавляющем большинстве рассмотренных
нами случаев опухоль исходила из правого предсердия, об изолированном
поражении правого желудочка имеются единичные упоминания, не намного
чаще опухоль прорастала в него из предсердия. Еще реже (в 4 случаях) источ¬
ником ощ'холи было левое предсердие, в 2 из них — одновременно с правым, в
одном — опухоль имела форму полипа, симулировала миксому и была успешно
прооперирована.Наиболее специфичным и постоянным симптоліом опухоли, который часто
служит поводом для обращения к врачу, является геморрагический выпот в
полость перикарда, чаще — в большом количестве, приводящий к тампонаде
сердца (рис. 23,3). Первая же пункция перикарда обычно заставляет усомниться
в исходном диагнозе вирусного перикардита, для которого геморрагический
472КардиологияОтносительно специфические симптомы1. Геморрагический выпот в полость перикарда
(цитологическое исследование пунктата позволило установить диагноз лишьв 1 случае).2. Синдром ВПВ, не коррелирующий с объемом перикардиального выпота.ДИАГНОЗ НЕ МЕНЕЕ ЧЕМ В 80 СЛУЧАЯХ БЫЛ ПОСТАВЛЕН ПРИЖИЗНЕННОобзор 1968 года - в 4 случаях из 41доминируют малоспецифичные симптомы,
обусловленные поражением сердца: застой по
обоим кругам кровообращения, аритмии (нечасто),
различные боли в грудной клеткеIвыражена симптоматика
метастазов (наряду
с сердечными симптомами
или при полном их отсут¬
ствии)1Б. Транспи- ■*-- 1А. Транстора-—>
щеводная. кальная Эхо-КГ
показания: (>1/2 сл. - диагноз
уточнение опухоли),данных 1А трудности:• малая эхогенная
насыщенность
сигналов от
ангиосарком;• их схожесть
с артефактами;• неопределен¬
ность признаков
самого образова¬
ниянедостаточнь! возможности УЗИ
в определении структуры ткани
(некроз и пр.)т3. Пневмопе¬
рикард4. КТ/МРТ
сомнения
в данных
Эхо-КГ,
уточнение
анатомии
опухоли;
определение
структуры
ткани2. Ангиокаолио-наибольшее число неграфия.поставленных при жизнипоказания:диагнозов• дифференци¬Метастазы;альный1) контактные (плевра,диагнозсредостение);с атеросклеро¬2) лимфо-/гематогенные:зом коронар¬(по частоте):ных артерий;• в легкие - чаще• визуализациявсего выявляютсяопухолитолько рентгенологи¬в полостяхчески (отдельныесердца;очаги, диссемина-• определениеция), возможныпатологичес¬симптомы от одышкиких соустий;до двустороннегобиопсияпневмоторакса,опухоли:кровохарканья,не всегдафатального кровоте¬позволялаченияпоставитьи терминальной ДН;точный диагноз• в печень ґнередко(давала картинуобнаруживалисьот мезенхи¬только при аутоп¬мальнойсии);опухоли до• в головной и спиннойотсутствиямозг:атипизма)1•в мягкие ткани.Срок жизни после постановки диагноза; 2 месяца-2 года (у 70-80% - метастазы)ЛЕЧЕНИЕ;1. Операция:• паллиативная;• трансплантация2. Полихимиотерапия
(ифосфамид, эпируби-
цин, дакарбазин
и др.)3. Лучевая терапия
на фоне приема
разоксанаРис. 23.3. Диагностика и лечение ангиосаркомы серлпа
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 473характер экссудата гораздо менее характерен, чем для туберкулеза, радиацион¬
ного и неопластического поражения перикарда, перикардита в рамках систем¬
ной красной волчанки и ревматоидного артрита. Клиническим указанием на
злокачественный перикардит нередко становится развитие синдрома верхней
полой вены, не коррелирующее с объемом выпота, что и отмечалось у нашей
больной в последние дни.в типичных случаях доминируют симптомы сердечной недостаточности
(обычно с преобладанием правожелудочковой). Сердечные шумы обуслов¬
лены разрушением трехстворчатого клапана или препятствием току крови в
результате сдавления раз^тичных отделов сердца. Боли в грудной клетке могут
носить типичный ангинозный характер, но чаще они длительные и упорные.
Возможны обмороки. Около 0,0025% внезапных смертей приходится на опу¬
холи сердца. Описано 120 случаев внезапной смерти при первичных опухо.іях
сердца (наиболее часто — при поражении АВ-узла), 17 из них бьши злокаче¬
ственными. Богатство клинической симптоматики при ангиосаркоме связано
с ее ранним мстастазированием.Опухоль дает как контактные (в ішевру и средостение), так и отдаленные
метастазы в различные органы (примерно в 2 раза реже к моменту установ¬
ления диагноза), в первую очередь в легкие (в том числе диссеминированное
инфильтративное поражение легких), по поводу которых проводится биопсия,
но определить источник опухолевых клеток в изученных слу^іаях не удавалось,
за исключением одного, когда был поставлен диаіноз саркомы; существенно
реже — в печень, в головной и спинной мозг, кости и \{ягкие ткани (метаста¬
зы в кожу могут имитировать меланому, саркому Капоши), надпочечники.
Генерализованные метастазы являются одной из основных причин смерти этих
больных. Они же создают наибольшие диаі ностические трудности — описаны
больные с фатальными легочными кровотечениями, кровохарканьем, двусто¬
ронним спонтанным пневмотораксом, у которых кардиальные симптомы ухо-
тяж на второй план вообще не выявлялись.Неясно, следует ли считать случайным обнаружение у нашей больной мно¬
жественных миоматозных узлов в матке (с учетом того, что эта опухоль исходит
из гладкомышечного органа). В литературе нам встретились аналогичные
сочетания. Показано, что у больньгх с миксомами сердца в 26,7% случаев име¬
ются и другие заболевалия опухолевой природы, в том числе множественные
папилломы кожи, невусы, гемангиомы печени, миомы и другие опухоли матки
и придатков; у них также оказывался повышен уровень ракового эмбриона.'1Ь-
ного антигена крови даже после оперативного удаления миксомы.Из рассмотренных нами случаев не менее чем в 80 диагноз первичной
опухоли сердца был поставлен при жизни и позволил начать радикальное или
паллиативное лечение. В обзоре 1968 г. прижизненный диагноз бьы установлен
у 4 больных из 41, ни одному из них не проводилось хирургическое лечение.
Такой очевидный прогресс связан с широким внедрением преимуществен¬
но трех методов: эхокардиографии, компьютерной и магнитно-резонансной
томографии, а также ангиографии с биопсией миокарда, В такой последова¬
тельности они обычно и применяются.
474 КардиологияПримерно в половине случаев опухоль правого предсердия выявлялась
уже при трансторакальной Эхо КГ и описывалась обьпшо как избыточная
сердечная ткань. Для миксом, как известно, характерны поражение левого
предсердия и полипообразный рост — обнаружение опухоли правых отделов
застав.1яло думать о более редких вариантах. Саркомы, по данным Российского
научного центра хирургии РАМН им, акад. Б. В. Пеіровского, наиболее трудны
для УЗ-диагностики среди опухолей сердца в связи с малой эхогенной насы¬
щенностью сигналов от оггухоли, их схожестью с различными артефактными
проявлениями, неопределенностью эхографических признаков самого обра¬
зования.Чреспищеводная ЭхоКГ чаще помогала подтвердить диагноз опухоли,
чем давала о ней первую информацию; метод достаточно точен — получен¬
ные с его помощью данные коррелировали с картиной, открывавшейся во
время операции. В менее типичных случаях, когда обычная трансторакяльная
ЭхоКГ не позволяла определиться с диагнозом, введение датчика в пищевод
редко позволяло получить решающую информацию (описана опухоль, кото¬
рая в обоих случаях выглядела как псевдоаневризма аорты). Многие авторы
отметили недостаточные возможности ультразвука в определении структуры
ткани (зон некроза и т.д.). В нашем случае, видимо, ткань опухоли, включав¬
шая заполненные кровью полости, воспринималась как жидкость в полости
перикарда.Применение КТ и, чаще, МРТ сердца (спин-эхо, эхо с постоянным гради¬
ентом — steady-state gradient) оправдано во всех случаях, особенно в тех, когда
данные улыразвукового исследования вызывают сомнение (упомянутая выше
«псевдоаневризма» была распознана как опухоль при МРТ; в другом случае
выявленное при ЭхоКГ утолщение листков перикарда выглядело при МРТ как
разрастания перикарда по типу «цветной капусты» и было верно расценено как
опухоль; «тромбы^ в полости правого предсердия оказались неоднородными
разрастаниями с полями высокой и низкой плотности, подозрительными на
очаги некроза и кровоизлияний). И при банальной, не вызывающей сомнений
ультразвуковой картине применение компьютерной и магнитно-резонансной
томографии оправдано при отсутствии уверенности в качестве ЭхоКГ и нали¬
чии необъяснимых в рамках рабочего диагноза клинических симптомов (в
нашем случае КТ рассматривалась как диагностическая процедура первой
необходимости). В одном случае КТ позволила правильно дифференцировать
множественные метастазы в легкие от туберкулеза.У больных с подозрением на наличие опухоли сердца по данным ультразву¬
кового исследования КТ и МРТ широко применяются для решении вопросао возможности и объеме оперативного вмешательства. Методики (в большей
степени МРТ) позволяют уточнить патологоанатомическис характеристики
(размеры, фаницы) внутриполостных, клапанных, мио-, пери-, юкстакарди-
альных опухолевых масс, в ряде случаев судить о злокачественности процесса,
при динамическом исследовании — оценить сократительную способность
миокарда. В то же время отмечено, что разнообразные опухоли выглядели при
МРТ довольно однородію.
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 475Отечественными авторами описан случай прижизненной диагаостики опу¬
холи сердца у больной с выпотным геморрагическим перикардитом методом
пневмоперикарда с последующей рентгенографией (подозрение на опухоль
правых отделов возникло при ЭхоКГ) — выявлено дополнительное образова¬
ние с ровным округлым контуром, тип опухоли установлен после операции.Ангиокардиография (с визуализацией полостей сердца, коронарных арте¬
рий, сосудистого рисунка опухоли, определением гемодинамических пока¬
зателей) также является значимым методом в диагностике опухолей сердца.
Поводом для ее проведения далеко не всегда было подозрение на опухоль, что
и определяет ее самостоятельное значение. В одном случае коронарография
была предпринята в связи с типичной картиной грудной жабы и выявила про¬
растание опухоли в коронарную артерию, в другом аналогичная картина была
выявлена в пораженной атеросклерозом артерии (ранее была диагностирована
ишемическая болезнь сердца, исследование проводилось повторно), в тре¬
тьем — и ультразвуковое исследование, и коронарография. выявляли аневриз\ту
правой коронарной артерии, опухолевый характер которой был установлен
только после операции. Если опухоль была заподозрена при ЭхоКГ, то анги¬
ография проводилась с целью биопсии патологического материала (наряду с
интраоперационной биопсией это дает возможность установить точный диа¬
гноз), выявления патологических соустий между полостями и сосудами (тесна
связь правых предсердия и коронарной артерии). Впрочем, биопсия также не
всегда давала точный диагноз, показывая картину от мезенхимальной опухоли
до полного отсутствия признаков атипизма. Описаны случаи постановки диа¬
гноза при повторных биопсиях (при первой получена картина организовавше¬
гося тромба).В некоторых случаях операция проводилась с неясным или неправи-іьньїм
предварительным диагнозом и позволяла его установить (с помощью имму-
ногистохимических исследований материа^іа) — при подозрении на опухоль
средостения, с целью удаления «тромба» из правого желудочка, для устранения
патологического шунта из правого предсердия в полость перикарда (цитологи¬
ческое исследование перикардиального выпота лишь в одном из рассмотрен¬
ных случаев позволило установить точный диагноз). 25-летнему пациенту с
тампонадой сердца в течение 4 нед не удавалось поставить диагноз (несмотря
на использование всех современных методик), и была предпринята диагности¬
ческая срединная стернотомия, полностью себя оправдавшая. В другом случае
ангиосаркома была диагностирована во время экстренной операции по поводу
разрыва сердца у больного с «констриктивным перикардитом».Приведем краткое описание нескольких случаев, в которых диагноз до
аутопсии поставлен не был. 47-летний пациент с двусторонними диффузными
инфильтраталш в легких (без кардиомегалии и каких-либо сердечных сим¬
птомов) страдал кровохарканьем и умер от легочного кровотечения. Другому
пациенту с аналогичной клинической картиной была проведена биопсия лег¬
кого, показавшая мелкоузловые депозиты опухолевой ткани; больной умер от
дыхательной недостаточности. 66-летней женщине с двусторонними псевдоно-
дулярными инфильтратами в легких в связи с тампонадой сердца был проведен
476 Кардиологияперикардиоиентез, получена геморрагическая жидкость без атипичных клеток;
посмертно выявлен также одиночный метастаз в печень, 30-летний шжчина
с тампонадой сердца (жидкость геморрагическая), двусторонними метаста¬
зами в легкие (КТ) и двусторонним геморрагическим плевральным выпотом,
позднее — клинически значимыми метастазами в головной мозг (КТ), умер на
20-й день госпитализации с неясным диагнозом, на вскрытии выявлена ангио¬
саркома сердца, инфильтрирующая стенки правого предсердия. У 62-летнего
мужчины с метастазами неизвестной опухоли в легкие и спинной мозг (экстра-
дурально) развились гипоксемия, желудочно-кишечное кровотечение, громбо-
цитопения, микроангиопатическая анемия. Противораковое лечение не про¬
водилось в связи с тяжелым общим состоянием. На вскрытии — ангиосаркома
правого предсердия, метастазы в легких, печени, надпочечниках, деснах и
позвонках. Различные гематологические нарушения были, возможно, резуль¬
татом широкой опухолевой инфильтрации сосудов.Во всех приведенных случаях богатство клинической симптоматики служи¬
ло скорее препятствием, чем опорой в постановке диагноза. Даже очевидные
признаки злокачественного опухолевого процесса не помогали в установлении
его источника — опухоли сердца не включаются большинством клиницистов в
круг дифференциальной диагностики, проводится выбор между более привыч¬
ными заболеваниями, в этой ситуации минимальные указания на правильный
диагноз остаются незамеченными, а отрицательные результаты воспринима¬
ются как достоверные. Так, нами не было обращено внимания на несоответ¬
ствие увеличения левого желудочка по данным рентгенографии и уменьшения
его полости по данным ЭхоКГ В то же время мезотелиома плевры, о которой
д>'малось постоянно в связи с характером экссудата, бьша вынесена в диагноз,
несмотря на отрицательные данные двух цитологических анализов и отсутствие
данных КТ Более лока.тьная симптоматика заставляет врачей точнее выбирать
методы диагностики и учитывать возможность более редких заболеваний.Попытки лечения предпринимались в большинстве случаев прижизнен¬
но диагностированных ангиосарком. Операции чаще всего носили характер
паллиативных или экстренных (при разрывах сердца, критической сердечной
недостаточности) — опухоль резецировалась частично, проводились пластика
различных отделов и шунтирование. Одно из первых сообщений об ортото-
пической трансплантации сердца у двух больных с ангиосаркомой правого
предсердия появилось в 1993 г, пациенты прожили 8 и 9 мес и >'мерли от
множественных метастазов в мозг Обычно операция служила первым этапом
комбинированной терапии. В дальнейшем большинству пациентов проводи¬
лась полихимиотерапия, некоторым — лучевая терапия. Реже химиотерапия
начиналась еще до операции. Оптимальных схем лечения нет.Большинство больных умирает в сроки от 2 мес до 2 лет после появления
симптомов, у 70-80% к моменту смерти имеются метастазы. Наихудшие
результаты комбинированной терапии у больных с саркомами сердца наблю¬
дались именно при ангиосаркомах. Упомянем о нескольких случаях, в кото¬
рых лечение было относительно успешным. В течение года после частичной
резекции первичной опухоли пациенту с метастазами было проведено 6 курсов
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 477химиотерапии (ифосфамид, эпирубицин, дакарбазин) с перерывом на луче¬
вую терапию, потенциированную назначением разоксана. Первичная опухоль
оставалась в фазе субтотальной ремиссии, однако рост метастазов остановлен
не был. До и после трансплантации сердца проведены курсы лучевой и хими¬
отерапии, через 33 мес после операции отсутствовали признаки рецидива опл^-
холи или метастазов. Через год после частичной резекции и химиотерапии у
больного при ЭхоКГ определялась резидуальная опухоль правого предсердия и
отсутствовали какие-либо симптомы болезни.Уникален случай выявления опухоли у 27-легней беременной женщины
(срок 23 нед) с тампонадой сердца: после проведения ЭхоКГ, МРТ и ангиогра¬
фии с биопсией установлен точный диагноз, назначение глюкокортикоидов
привело к исчезновению перикардиального выпота, проведена экстренная
операция в связи с критической обструкцией опухолью трикуспидального
клапана, после чего наступшіа внутриматочная смерть плода, проводилась
химиотерапия. Через 8 мес возник рецидив опухоли, проведена транспланта¬
ция сердца, через 2 мес после которой выявлены метастазы в легкие. Смерть
наступила через 20 мес после появления симптомов.Таким образом, в описанном нами сл>'чае отмечались как типичные, так и
крайне редкие для ангиосаркомы сердца черты, затруднившие и без того слож¬
ную диагностику. К сожалению, даже успешная прижизненная диагностика в
нашей клинике, очевидно, не могла бы не только спасти, но и простить жизнь
больной.Приводим второе наблюдение.Больной Е., 43 года, поступил в отделение кардиологии Факультетской
терапевтической клиники им. В.Н. Виноградова 14 октября 2008 г. с жадобами
на одышку при небольших физических нагрузках (ходьба с незначительным
подъемом, по лестнице на один этаж, быстрая ходьба, наклон вперед), при¬
ступообразный непродуктивный кашель, который заметно усиливается в
положении на спине, возникает на протяжении всех суток; подъемы темпера¬
туры тела максимально до 38,2 °С, возникающие в различное время суток, не
каждый день (периодичность различна), сопровождающиеся чувством жара,
легким ознобом; выраженную потливость, которая усиливается при подъемах
температуры тела и ночью; непостоянную осиплость голоса, серенную общую
слабость.Семейный анамнез: отец пациента умер в 62 года от рака легких (?); матери
69 лет, она перенесла саркоидоз (лечилась глюкокортикоидами, снята с учета),
У больного два сына — 19 и 10 лет, они здоровы. Преподавал биологию и
химию, работал в администрации Костромской области (заместителем началь¬
ника департамента); с 2007 г. — монах, с этого времени не ест мяса. Постоянно
живет в скиту (местность сырая, отопление печное, в остальном условия удо¬
влетворительные). Никогда не курил. Перенесенных детских инфекций не
помнит. Аллергологический анамнез не отягощен.Анамнез заболевания (рис. 23.4). В юности профессионально занимался
лыжным спортом, регулярно проходил медосмотры, в 1986 г. во время служ¬
бы на полигоне Новая Земля подвергся облучению (в результате выброса
478Кардиологиярадиоактивных веществ); доза неизвестна. Тогда же на ногах перенес «просту¬
ду», обследования не проходил. В 1987 г. бьита выявлена округлая тень в вер¬
хушке правого легкого, проведена резекция доли, диагноз неизвестен (со слов
больного, данных за туберкулез и опухоль не было, речь шла о хронической
пневмонии). После операции постепенно вернулся к значительным физиче¬
ским нагрузкам.С июня 2003 г (в возрасте 38 лет) наблюдается незначительное снижение
переносимости нагрузок; дважды отмечены кратковременные эпизоды серд¬
цебиения до 200 уд./мин (в бане и при плавании). В сентябре на фоне стресса
возникла интенсивная боль в левой половине челюсти, которая купирова^іась
после денервации зуба, а через 5 дней бригадой скорой медицинской помо¬
щи зафиксирована желудочковая тахикардия, купированная внутривенным
введением изоптина. Состояние расценено как инфаркт миокарда; тогда же
выявлены признаки гипертрофической кардиомиопатии, умеренного стеноза
легочной артерии. В ноябре был госпитализирован с повторным пароксизмом
тахикардии в больницу г Кострома, на фоне введения кордарона отмечалось
чередование желудочковой тахикардии и синусового ритма с АВ-блокадой 11—
III степени. От имплантации ЭКС отказался и самостоятельно приехал в кли¬
нику кардиологии Московской медицинской академии им. И.М. Сеченова.
При ЭхоКГ (проф. В.П. Седов) подтверждено наличие гипертрофической
кардиомиопатии без признаков обструкции (толщина МЖП 25 мм, ЗСЛЖ
17 мм, ПЖ 6—7 мм, гиперкинез стенок левого же.іудочка), умеренного стеноза
устья легочной артерии (градиент на клапане составлял 16 мм рт.ст.), выявлена1986 г.
21 год1987 г.«простуда» і
одышкаЖТАВ-блокада
перикардитдиагноз хроническая
пневмонияоперациярезекцияправоголегкого2003: VI IX XI 2006 2007: VI! X 2008: VII IXкашель,‘ttttпотливостьAiГКМП. Врожденный стеноз ЛА,
Выпотной перикардит неясногоИКД реИКДВПС: стеноз
легочной артериибалонная
дилатация
легочного клапанаРис. 23.4. Анамнез бо.тьного Е., 43 года
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 479митральная и трикуспидальная регургитация, С этого времени имеются досто¬
верные сведения о наличии выиота в полости перикарда.При попытке записи внутрисердсчной ЭКГ индуцирована желудочковая
тахикардия с ЧСС 200—220/мин и с паузой 2,8 с в момент спонтанного вос¬
становления синусового ритма. На фоне проводимой временной эндокарди-а,1Ьной электрической стимуляции сердца больной бьи экстренно переведен в
НЦССХ им. А.Н. Бакулева, в отделение хирургического лечения тахиаритмий
(заведующий — член-корр. РАМН, проф. А.Ш. Ревишвили), где ему имплан¬
тирован двухкамерный кардиовертер-дефибриллятор. Бы.чо подтверждено
наличие гипертрофической кардиомиопатии, перикардита (сепарация листков
перикарда 6—7 мм) и стеноза устья легочной артерии, назначена терапия сога-
лексом, верогапироном. До лета 2004 г. отмечено 5 случаев срабатывания кар-
диовертера-дефибриллятора по поводу эпизодов желудочковой тахикардии.
После изменения медикаментозной антиаритмической терапии: замены сота-
лола на кордарон 200 мг/сут — приступы желудочковой тахикардии прекрати¬
лись (при попытке его временной отмены — возобновлялись). Неоднократно
отмечалось изменение количества жидкости в полости перикарда (от мини¬
мального до значительного). В сентябре 2006 г. проведена плановая смена кар-
диовертера-дефибриллятора (истощение батареи) , тогда же в связи с развитием
тампонады дваждьі проводилась пункция перикарда (суммарно удалено более1 л серозной жидкости), данные о составе пунктата скудные, обследования не
проводилось.Летом 2007 г отметил появление тяжести в области сердца, значительное
снижение переносимости нагрузок. Обследовался в Костроме. Выявлены уве¬
личение СОЭ до 30 мм/ч, тампонада (сепарация листков перикарда 14-25 мм,
спайки), проведена пункция перикарда (удалено 500 мл) с субъективным
у.'їучшением. Серозный пунктат на 81% состоял из лимфоцитов, выявлялись
полибласты (?) в количестве 3%, мезотелий 5%. При КТ без контрастирова¬
ния в легких и средостении изменений не найдено (рис. 23,5). Реакция Мату
нормоэргическая, наличие туберкулеза признано маловероятным. К лечению
добавлены петлевые диуретики, диклофенак. Больной отмечал пик своей
физической активности, ездил на велосипеде, играл в баскетбол.Рис. 23.5. Компьютерные томограммы органов грудной клетки (Кострома, 2007 г)
480 КардиологияС октября 2007 г. впервые отметил появление и нарастание одышки при
нагрузках. Тогда же переехал в скит и принял постриг. Планировалась госпита¬
лизация в Факультетскую терапевтическую клинику им. В.Н. Виноградова, от
которой пациент отказался. В январе 2008 г. в Костроме выявлено нарастание
фадиента на клапане легочной артерии до 66 мм ртхт., выраженная гипертро¬
фия обоих желудочков. Весной появились выраженная потливость (темпера¬
туру не измерял), сухой кашель без мокроты; инфильтративных изменений
в легких не было, в НЦССХ им. А.Н. Бакулева подтверждено нарастание
градиента на к-тапане легочной артерии до 65—70 мм рт.ст., сам кіапан плохо
визуа.1изировался (что расценено как его агенезия), отчетливо преобладала
гипер^грофия правого желудочка, выпота в полости перикарда больше не было.
С этого времени в качестве основного рассматривался диагноз врожденного
порока сердца.В июле бьи госпитализирован в HUCCX им. А.Н. Бакулева для оператив¬
ного лечения порока. При вентрикулоангиографии выявлено поражение не
только на уровне клапана и подклапанных структур (с повышением давления
в правом желудочке в систолу до 100 мм рт.ст.), но и выраженное сужение
обеих легочных артерий, что расценено как их врожденная гипоплазия.
Был консультирован акад. РАМН, проф. В.П, Подзолковым: характер поро¬
ка был не вполне ясен. Обсуждались разные варианты операции (стенти-
рование, протезирование клапана). В результате 09 июля 2008 г. выполнена
баллонная вальвулопластика (остаточный градиент на клапане 33 мм рт.ст.) с
выраженным эффектом: одышка купировалась практически полностью, воз¬
обновил активные физические нагрузки. Однако уже с конца августа вновь
отметил появление сухого каш.тя, потливости, слабости, нарастание одыш¬
ки. К началу сентября с трудом мог сделать несколько шагов. В октябре про¬
консультирован в НЦССХ им. А.Н, Бакулева: по данным ЭхоКГ давление в
правом желудочке составило 65—70 мм рт.ст., наросла легочная гипертензия
(диастолическое давление 25 м.м рт.ст., 50% от системного). Состояние
расценено как бронхит с декомпенсацией правых отделов, назначены аве-
локс и микосистс некоторым эффектом, и 14 октября больной поступил в
Факультетскую терапевтическую клинику им. В.Н. Виноградова для долечи¬
вания бронхита.Таким образом, на протяжении 5 лет характер заболевания оценивал¬
ся по-разному {табл. 23.2). Данных за инфаркт миокарда не было, в то же
время утрожаюш:ие жизни нарушения ритма и проводимости, возраст боль¬
ного и данные ЭхоКГ были типичны для гипертрофической кардиомиопатии.
Правда, уже тогда были выявлены небольшой перепад давления на клапане
легочной артерии и выпот в перикарде, После имшіантации кардиовертера-
дефибриллятора как минимум дважды развива.тась тампонада сердца, однако
в НЦССХ им. А,Н. Бакулева обследования по этому поводу не проводилось, а
в Костроме оно не дало результата. За год до госпитализации в Факуітьтетскую
терапевтическую клинику им. В.Н. Виноградова отмечено появление одьшіки
и нарастание градиента на клапане легочной артерии, в результате на первый
план вышел диагноз врожденного порока сердца, хотя всю жизнь больной
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 481Таблица 23.2Диагнозы, которые ставились больному £. на разных этапах болеши09.2003
г. КостромаИ Б С: передний крупноочаговый высоко¬
боковой инфаркт миокарда от 12 сентября 2003 г.
Гипертрофическая кардисмиопатия 11.2003
г. КостромаГипертрофическая кардисмиопатия. Врожденный порок
сердца: стеноз легочной артерии. ИБС: постинфарктный
кардиосклероз12,2003Клиника кардиологии
ММАим. И.М. СеченоваГипертрофическая кардиомиопатия. Врожденный порок
сердца: стеноз устья легочной артерии. (Экссудативный
перикардит)Гипертрофическая кардиомттопатия без обструкции пьто-
дного тракта левого желудочка. Выпотной (осумкован¬
ный?) перикардит неясной этиологии12.2003, 08.2006
Научный денгр сердечно¬
сосудистой хирургии
им. А.Н. Бакулева 07.2007
г. КостромаРетщдивирующий экссудативный перикардит
Гипертрофическая необструктивная кардиомиопатия04.2008
г. КостромаГипертрофическая кардиомиопатия, необструктивная
форма. Рецидивирующий экссудативнь[й перикардит.
Врожденный порок сердца; комбитшрованный стеноз
легочной артерии 07.2008Научный центр сердечно¬
сосудистой хирургии
им. А.Н. Бакулева Врождетптый порок сердца: комбинированный стеноз
легочной артерии, Рецидивирующий перикардит неясной
этиологии (в аналшезе)прекрасно переносил нагрузки. Операция на клапане дала эффект, но очень
кратковременный.При анализе результатов ЭхоКГ видно {табл. 23.3), что при исходной кар¬
тине гипертрофической кардиомиопатии без обструкции выводного тракта
левого желудочка на первый план лишь со временем вышли изменения правых
отделов сердца, т.е. «врожденный порок сердца» мог быть проявлением самой
гипертрофической кардиомиопатии с развитием инфундибулярнош стеноза,
как мы недавно видели это у нашей больной. При этом толщина задней стенки
левого желудочка заметно снижалась.При поступлении состояние больного было среднетяжелым. Температура
тела за время госпитализации поднима-іась до 37,6 °С и выше. Конституция
астеническая, рост 176 см, вес 58 кі: Кожные покровы бледные, чистые, влаж¬
ность повышена, на коже передней грудной стенки видны мелкие подкожные
вены. Отеков нет; лимфатические узлы не увелигчены. Голос осипший (непо¬
стоянно). Число дыханий 17/мин, дыхание везикуішрное, хрипов нет. Слабый
сердечный толчок, верхушечный тол^юк не изменен; тоны сердца ритмичны,
ЧСС 64/мин, грубый пансистолический шум с эпицентром во П-ИІ меж-
реберье слева от грудины (выслутиивается также на верхушке и над аортой);
АД 100/60 мм рт.ст., наполнение пульса достатотеое. Живот мягкий, умерен¬
но болезненный в левой подвздошной области; печень +1,5-2 см, плотно¬
эластической консистенции; селезенка не увеличена.
482КардиологияТаблица 23.3Динамика эхокардиографнческих параметров больного Е.Параметр12.0312.037,074.087.0810.08ЛЖ, см4,74,64.04,34,44,8тМЖП, мм25Гипертрофия21212118тЗСЛЖ, мм1718-22201311ФВЛЖ706560606460пж2,7тПЖ, мм6-7ГипертрофиявопжГипертрофияВОПЖГипертрофияМР, ст.II1 С1.1-11 ст.1-11 ст.ТР0-Т стTTI-TVct.11 ст.11-111Давление в ЛАНорма25 (д.)Градиен г на
клапане ЛА,
мм рт.ст.161465-706020Давление в
ПЖ, мм рт.ст.2575-8010065-70СепарацияперикардаЕсть6—7 мм14-24мм9 ммВ общем анализе крови — тенденция к лейкоцитозу при нормальной фор¬
муле, умеренное увеличение СОЭ (эритроциты 4,7 nlih, НЬ 153,1 г/л, цвето¬
вой показатель 0,97, лейкоциты 9 тыс., нейтрофилы 68%, лимфоциты 22%,
моноциты 8%, эозинофилы 1%, базофилы 0,4%, тромбоциты 235 тыс., СОЭ
35 мм/ч). В биохимическом анализе — минимальные признаки холестаза,
пограничное значение креатинина (обший белок 77,2 г/л, альбумин 40,4 г/л,
креатинин 1,47 мг/д.а, глюкоза 5 ммоль/л, азот мочевины 6,9 ммоль/л, общий
билирубин 22,9 мкмоль/л, прямой билирубин 8 мкмоль/л, ACT 21 Ед/л, АЛТ
17 Ед/л, у-ГТ 124 Ед/л (норма до 55), КФК 46 Ед/л, натрий 136 мэкв/л, калий
5,7 мэкв/л, железо 91 мкг/дл).Выявлена небольшая диспротеинемия: альбумин 55,7% (58,8-69,6),
аJ-глобулины 3,7% (1,8“3,3), а^-глобулины 9,8% (3,7-13,1), |3-глобулины
12,2% (8,9-13,6), у-глобулины 18,4% (8,4-18,3). СРВ +-Н-Н+. На фоне длитель¬
ной терапии кордароном уровень ТТГ повышен до 14 МЕ/л. HB^Ag, HCV Ab,
КСР на сифилис отрицательны.Общий анализ мочи — без отклонений от нормы, реакция кала на скрытую
кровь оірицательна.На ЭКГ ірис. 23.6} — непрерывная двухкамерная стимуляция. При рент¬
генографии органов грудной клетки очаговых и инфильтративных изменений в
легких не выявлено, имеются участки плеврогенного фиброза, спайки, рас-
гпирснис корней легких; легочный рисунок усилен преимушественно за счет
уттлотненного интсрстиция в прикорневых отделах. При сравнении с рснтгс-
нофаммами от лета 2007 г., когда разви^чась тампонада, заметно уменьшение
размеров тени сердца, в то же время ширина срединной тени увеличилась
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 483Г~НгжРис. 23.6. Электрокардиограмма больного E. (октябрь 2008 г.). Скорость записи 25 мм/с.
Пояснения в текстеШІшшРис. 23,7. Ретигенограммы органов грудной клетки, прямая проекпия. Слева — данные
лета 2007 г., справа — октября 2008 г. Пояснения в тексте(рис. 23.7). По данным спирометрии: ЖЕЛ снижена умеренно (3440 мл, 74% от
нормы), существенных обструктивных нарушений нет (ОФВ^ 78%, МОС^. 84%,
МОС,, 63%, МОС„ 69%, ОФВ/ФЖЕЛ 82%).При ЭхоКГ (проф. В.П. Седов, рис. 23.8) толщина правого желудочка
(2,4 см) практически равна толщине иерегородют (2,5 см), задняя стенка левого
желудочка всего 13 мм, ФВ левого желудочка незначительно снижена (53%).
Полость левого желудочка: КДР 4,2 см, КДО 76 мл, КСО 35 мл. Нар>тііений
локальной сократимости не выявлено. Полость правого желудочка: 3,7 см,
484КардиологияРис. 23.8. Эхокардиограммы больного Е. Слепа — данные ЭхоКГ из парастернального
дост>тта (длинная ось) в В-режиме: 1 — КДР правого желудочка, 2, 3 — КДР левого
жел>’дочка, 4 — толщина межжелудочковой перегородки. В центре — данные ЭхоКГ
из парастернального дост\тта (короткая ось) в В-режиме: в верхней части эхограммы —
правый желудочек с резко утолщенными стенками. Справа — 3D-эхокардиограмма из
парастерітального доступа (короткая ось). В верхней части эхофам.мы — правый желу¬
дочек с резко утолщенными стенкамисократимость снижена. Левое предсердие 47 мл (3,5 см), правое предсердие
58 мл. Аортальный клапан не изменен. Митральная и аортальная регургитация
Т степени. Легочный клапан; регургитация 111 степени, СДЛА 64 мм рт.ст., время
ускорения кровотока 244 мс, градиент давления 19,4 лш рт.ст. Обструкции
выводного тракта левого желудочка, парадоксального движения передней
створки митрального клапана не выявлено. Регургитацию на легочном кла¬
пане можно было связать с баллонной дилатацией, остаточный градиент — с
инфундибуляриым стенозом, но этиология .дегочной гипертензии оставалась
непоіштной. Жидкости в полости перикарда не было. В заключении диагноза
гипертрофической кардиомиопатии не было, оно звучало следующим обра¬
зом: у папиента с врожденным стенозом клапана легочной артерии имеются
признаки стенозирования надклапанных отделов, выраженная гипертрофия
правых отделов сердца.Таким образом, эхокардиографическое исследование не добавило ясно¬
сти: мы констатировали факты, которые не могли объяснить. У больного
имелись безусловные показания к проведению КТ органов грудной клетки:
рецидивируюгций перикардит сам по себе, а также его сочетание с лихорад¬
кой, ночной потливостью, упорным кашлем, слабостью, резекцией верхушки
правого легкого и жизнью в скиту (что делало вероятным наличие туберку¬
леза). На третий день пребывания в клинике больному была выполнена КТ
органов грудной клетки. Данных за туберкулез получено не было, но в средо¬
стении были выявлены конгломераты лимфоузлов. Сравнение со снимками2007 г. оказалось невозможным в связи с мягким режимом той съемки. Стало
очевидно, что легочная артерия (и ес клапан) сдавлены лимфоузлами извне.
Причиной столь выраженного увеличения лимфоузлов могли быть лимфо¬
гранулематоз, саркоидоз, что оставляло надежду на успешную медикаментоз-
н)Щ) терапию.Однако проведенная дополнительно КТ органов грудной клетки с внутри¬
венным контрастированием позволила расценить «конгломерат лимфоузлов»
как единую опухолевую массу {рис. 23.9). Объемные образования в паренхиме
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 485Рис. 23.9. Компьютерные томограммы органов грудной клетки бального Е. (октябрь
2008 г.). В нижнем ряд>^ контрастируется резко суженный просвет легочных артерийлегких не выявлены. Справа во 2-м сегменте имеются зона фиброза и мел¬
кие кальцинаты, В средней доле справа и язычковых сегментах справа также
определяются участки фиброза. Стенки бронхов уплотнены. Сосудистый и
интерстициальный рисунок не изменен. Жидкости в плевральной полости нет.
Трахея и крупные бронхи свободно проходимы, не деформированы.После введения контрастного препарата: в средостении определятся обра¬
зование без четких фанип, заполняющее собой практически всс средостение,
распространяющееся по ходу сосудов и в область сердца, преимутцественио
его правых отделов. Легочный ствол — максимально до 27 мм, минимальный
размер 20 мм. ПЛА 4-10 мм, ЛЛА 6-9,5 мм. Просвет артерий резко сужен,
деформирован. Отмечается распространение опухоли по ходу легочных арте¬
рий и легочных вен, больше справа. Дефекты контрастирования в легочных
артериях и их ветвях до субсегментарного уровня не выяштены. В области
ствола легочной артерии по передней и левой поверхности определяются
дефект контрастирования, деформация и изъеденность контура. Выводной
тракт правого желудочка резко сужен, стенка в этой области и в области ушка
правого предсердия резко утолщены, Восходящая аорта — 23 мм, аорта в
области дуги — 16 мм, нисходящая аорта — 18,5 мм. Толщина стенок аорты
в области дуги до 18 мм, сонных артерий — до 7 мм. Коронарные артерии
сужены, несколько смещены, раздвинуты опухолью. При контрастировании
4S6Кардиологияобразование умеренно, достаточно равномерно накапливает контрастный пре¬
парат (с 38-42 сдН до 65-72 едН).Заключение было сформулировано следующим образом: инфильтративно расту¬
щая опухоль средостения (вероятнее всего, исходящая из сердца или сосудистых
оболочек, менее вероятно лимфопролиферативное заболевание). Таким образом,
речь шла уже не о конгломерате лимфоузлов, а о диффузно растущей опухоли
сердца, и это существенно меняло и тактику, и прогноз. Проведение МРТ у нашего
пациента в связи с налившем имплантированного кардиовертера-дефибриллятора
было крайне нежелательным, но была вьтолнена высококачественная рекон¬
струкция изображения, пол>^енного при КТ органов грудной клетки {рис. 23.10).Получив эти данные, мы вернулись к результатам ЭхоКГ. Выделить саму'
опухоль не удавалось, но утолщенная стенка сердца выглядела очень неодно¬
родной, как будто с по-лостями распада {рис. 23. П), т.е. можно бьыо думать
об оп>^олевой инфильтрации миокарда с развитием псевдогипертрофии.
В какой-то степени становилась понятной изменчивость толщины стенок.
И можно было рассчитывать на то, что при эндомиокардиальной биопсии мы
получим ткань опухоли.Вопрос о проведении биопсии встал сразу, нам это казалось безуслов¬
но необходимым. Эндомиокардиальная биопсия рассматривалась в первую
очередь, пациент обсуждался с проф. С.А. Абуговым — основные сомнения
касаіись обеспечения кардиохирургической поддержки на случай неконтроли¬
руемого кровотечения, а также информативности такой биопсии и ее целесоо¬
бразности с точки зрения онкологов.Рис. 23.10. Компьютерные томограммы органов ірудной ктетки больного Е. (октябрь
2008 г.), трехмсрітая реконструкция, Опухолевая масса серого цвета сдавливает просвет
всех крупных сосудов, исходящих из сердца и входящих в сердце.
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 487Рис. 23,11. Эхо кард иоірамма из парастернального доступа (длинная ось) в В-режиме
(слева) и М'режимс (справа): 1 — толшина стеттки правого желудочка; 2 — толщина
мсжжел>'д очковой перегородки; 3 — толщина задней стен кіт левого желудочка. В меж-
желудочкопой перегородке на уровне среза — неоднородность эхоструктурыПервыми специалистами, к которым мы обратились, были гематологи:
первоначальное впечатление о конгломерате лимфоузлов требовало про¬
яснения. Кроме того, в Гематологическом научном центре РАМН имеется
больтпой опыт проведения медцастинальных биопсий, поэтому снимки
консультировали одновременно гематолог, хирург и заведующий отделением
лучевой диагностики. Заключение консилиума было таково: диагноз лимфо-
пролиферативного заболевания очень маловероятен. Было вь[сказано пред¬
положение о фиброзной природе средостенных масс. Несмотря на эго, после
очной консультации могла обсуждаться госпитситизация больного с входным
диагнозом «лимфогранулематоз» с целью проведения биопсии опухоли в
заднем средостении.Эиа возможность была оставлена на крайний случай: госпитализация боль¬
ного с подозрением на опухоль сердца в Гематологический научный центр
РАМН не позволяла рассчитывать на кардиохирургическую поддержку; риск
открытой процедуры также предстоя,'Ю оценить. Поскольку лимфопролифе-
ративнос заболевание было фактически отвергнуто специалистами, требова¬
лась консультация онколога более широкого профиля — не кардиохирурі а,
поскольку речь могла пойти о химио- и лучевой терапии. Мы обратились за
консультацией к директору Российского онкологическою научного центра им.Н.Н. Блохина, акад. М.И. ДавыдовуВ Центре компакт-диск с записью результатов КТ органов грудной клетки
был проконсультирован специалистами по лучевой диагностике. Дано сле¬
дующее консультативное заютчение: в правых камерах сердца установлены
488 Кардиологияэлектроды искусственного водителя ритма, проведенные через вены левой
руки и верхнюю полую вену. Грудная клетка обычных размеров и формы,
изменений в структуре ребер, позвонков, лопаток и ключиц не выявлено,
в полости перикарда определяется патологическое образование мягкоткан-
ной а-ютности, повторяющее форму камер сердца и окутывающее все сосуды
в полости перикарда и в верхнем средостении. Наибольшая толщина опухоле¬
вых масс определяется в области душ аорты, общего ствола и обеих легочных
артерий, вдоль передней поверхности сердечной мышцы, особенно передней
стенки правого желудочка. Перикард не дифференцируется. Опухолевые
массы циркулярно охватывают дугу аорты (их толщина в парааортальном про¬
странстве достигает 3 см) и продолжаются наверх, паравазально, вдоль ветвей
аорты. Ниже опухолевые массы охватывают общий ствол легочной артерии,
однако просвет его представляется расширеіїньтм до 3 см. В области бифур¬
кации ствола формируется с>'жение обеих легочных артерий, которые на всем
протяжении сужены до 2-5 мм за счет давления извне, имеют неровные,
бугристые контуры. Это сужение продолжается на долевые ветви, особенно
выражено в корне правого легкого. Выводной отдел правого желудочка и под-
клапанное пространство сужены и удлинены на протяжении 4 см, просвет его
не иревыщает 2 см, толшина стенок достигает 3 см. Все пространство между
легочными артериями сверху и верхней стенкой левого предсердия снизу
заполнено мягкотканными массами. Левое предсердие оттеснено вниз, опухо¬
левые массы распространяются вдоль верхней и боковой стенок предсердия.
Верхние легочные вены резко сужены.Верхняя полая вена имеет нитевидный просвет, кровоток сохраняется за
счет установленных в ней электродов. Основная масса крови проникает в
правые камеры сердца через анастомозы непарной вены. В переднем средосте¬
нии — отдельные лимфатические узлы, увеличенные до 2 см. В легочной гкани
отмечается резкое обеднение легочного рисунка, обусловленное сдавлением
легочных артерий. В верхних долях легких определяется утолщение междоль-
коБЫх перегородок, а также диффузное утолщение стенок всех крупных брон¬
хов, что обусловлено веноокклюзионным синдромом — сдавлением устьев
легочных вен. Просветы бронхов не изменены, стенки их диффузно утолщены.
Междолевые щели и синусы свободны, жидкости в плевральных полостях нет.
Заключение: изменения в фудной полости могут быть обусловлены интрапе-
рикардиальным образованием, в том числе новообразованием миокарда (пер¬
вичным?) по типу саркомы со сдавлением крупных легочных сосудов, право¬
го желудочка, левого предсердия, легочных вен и верхней полой вены, при
наливши клинических показаний уточнение характера процесса возможно при
трансторакальной пункционной биопсии под контролем КТ.Проведение закрытой игольной биопсии опухоли в переднем средостении
(с учетом ее близкого расположения к поверхности грудной клетки) представ¬
лялось нам оптимальным, причем именно в стенах Онкоцентра можно бьую
рассчитывать на быструю морфологическую верификацию характера опухоли
и начало терапии. Однако М.И. Давьщов исходил в первую очередь из возмож¬
ности оперативного лечения и, ознакомившись с заключением по результатам
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 489КТ о массивной опухоли сердца, рекомендовал консультацию в Российском
кардиологическом научно-производственном комплексе кардиохирурга, проф.
С.Л. Дземешкевича идя решения вопроса о возможности оперативного лече¬
ния (трансплантация?).Больной бьиі проконсультирован в Российском кардиологическом научно-
производственном комплексе проф, С.Л. Дзвмешкевичем (23.10.2008 г.): почти
однозначный вывод о саркоме вызвал сомнения, не было выявлено и клини¬
ческих признаков полного сдавления верхней полой вены. Хорошая переноси¬
мость значительных физических нагрузок в течение всей жизни полностью про¬
тиворечила ставивше\гуся ранее диагнозу врожденного порока сердца. Картина
опухоли, которая снаружи давит на крьпиу левого предсердия и расположена в
основном ретроаортатьно, могла соответствовать параганглиоме (вненадпочеч-
никовой феохромоцитоме), имеющей богатое кровоснабжение из коронарных
артерий (для верификации нужна коронарофафия). Предварительная биопсия
в этой ситуации опасна (опухоль богато васкуляризирована) — но главное, пока¬
зания к операции не зависят от типа опухоли и определяются наличием «меха¬
нических» факторов (сдавление сердца и сосудов). Обш;ий вывод бьы таков:
лечение должно быть радикальным, т.е. оперативным. С этой целью показана
госпитализация в Российский кардиологический научію-производственный
Ko\ffl.icKc д.'1я обследования, которое нужно еще раз провести с начала.Больной бьиі направлен на получение квоты для оказа[шя высокотехно¬
логичной медицинской помощи и выписан с диагнозом: первичная ону'холь
сердца с распространением в средостение. Гипертрофическая кардиомиопа-
тия? Обструкция выводного тракта правого желудочка. Состояние после кате-
терной баллонной пластики клапана легочной артерии от 09 ию.ія 2008 г
Недостаточность клапана леї очной артерии. Обструкция легочных артерий с раз¬
витием легочной гипертензии. Нарушения ритма и проводимости сердца; парок¬
сизмальная желудочковая тахикардия (из выводного отдела и верхушки левого
желудочка), желудочковая экстрасистолия, АВ-блокала П-ПТ степени, имплан¬
тация кардиовертера-дефибриллятора в режиме DDD в 2003 г., реимшгантания
кардиовертера-дефибриллятора в режиме DDDR в 2006 г Недостаточіюсть кро¬
вообращения НА стадии, Н1 функциональный класс MYHA. Рецидивируюпшй
выпотной перикардит в анамнезе. Резекция верхупжи правого легкого в 1987 г.
Субклинический гипотиреоз. Подобрана терапия кордароном 300 мг/сут, конко-
ром 2,5 мг, верошпироном 100 мг/сут и диувером по 10 мг через день.Вопрос о проведении биопсии отпал, однако до операции можно было
пытаться сіроить предположения о характере опухоли. Опухоли сердца выяв¬
ляются менее чем в 1% вскрытий, причем метастатические встречаются в
25—40 раз чаще первичных (рис. 23J2). До 10% больных, умерших от рака и
гемобластозов, имеют на вскрытии метастазы в сердце, хотя клинически они
редко успевают проявиться. В нашем случае оітухоль явно носила первичный
характер.Из первичных опухолей 3/4 составляют доброкачественные, а среди них
абсолютное большинство — миксомы; растут оіш, как правило, локально, в
форме узла, хотя могут расти иіітрамиокардиально. Наряду с параганглиомой,
490КардиологияКЛАССИФИКАЦИЯ ОПУХОЛЕЙ СЕРДЦА0,1-0,5% вскрытий0,00017-0,1%первичные75-80%доброкачест¬венныезлокачест¬венныемиксом а
липома
фиброэластома
рабдомиома
фиброма
гемангиома
тератома
мезотелиомаангиосаркома
рабдомиосаркома
фибросаркома
липосаркома
синовиальная саркома
злокачественная
мезотелиома
лимфомапараган глиома
невриномаРис. 23Л2. Классификаиия опу’холей ссрдиа1В 25-40 раз чащевторичные (метастазы)меланома
рак молочной железы
рак легких
рак желудка
рак щитовидной железы
гипернефрома
злокачественная
лейкемия
лимфомау нашего больного могли рассматриваться злокачественные опухоли — сар¬
комы, которые отличаются бурным ростом, мезотелиома. Крайне редким
вариантом злокачественной опухоли является лимфома, которая не только
метастазируст в сердце, но и может исходить из него первично.Недавно в Российском онкологическом научном центре им. Н.Н. Блохина
было впервые в России успешно проведено хирургическое лечение параганглио-
мы сердца {рис. 23.13, а). Всего описаний этой опухоли насчитывается немної им
более 70, Опухоль была выявлена при ЭхоКГ. имела мягкотканіїую плотность,
прорастала левое предсердие, прилегала к восходящей аорте, верхней полой вене
и пищеводу. Она была полностью уда.іена с пластикой предсердия и митрального
клапана (хирурги акад. М.И. Давыдов, проф. С.Л. Дземешкевич и др.), пациент
32 лет жив и полностью реабилитирован. Васкуляризация параганглиомы непо¬
средственно из коронарной артерии является одним из характерных признаков
этой опухоли (рис. 23.13, б), хотя это возможно и при ангиосаркоме.Лечение абсолютного большинства опухолей сердца хирургическое; опера¬
ция, как правило, не зкстрешіая, но достаточно срочная. Из последних 50 слу¬
чаев первичных опухолей сердца у взросішіх, исключая миксомъг, у 88% лечение
бьыо начато с операции без предварительной верификации диагноза и лишь у
12% — с морфологической верификацией опухоли. Показаниями к биопсии стали
подозрение на метастатическое поражение сердца, на ішмфому, а также неопе-
рабельность опухоли (т.е. оценка возможности хи\гаотерапии). Трансплантация
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 491Рис- 23.13. Инструментальная диагностика разлрічньїл опухолей сердца; а — параган-
глиома сердца (КТ, Давглдов М.И. и соавт., 2008); б — параганглиома сердца (корона-
роангиография, Kennelly R. cl, al., 2008); в — саркома легочной артерии (МРТ; ощ-холь
указана стрелками, Mader М.Т. et. al., 1997); г,д — злокачественные мезотелиомы пери¬
карда (КХ Сидоренко Б.А. и соавт., 2009; Kainuma S., et. al. 2008); e — саркома легочной
артерии (КХ Omura А. et. al., 2008)сердца не противопоказана при злокачественных опухолях сердца (они редко
метастазирутот), однако сам трансплангант является хорошей почвой для развития
опухолей. Исходы пересадки сердца больше зависят от типа опухоли, чем исходы
обычной резекции, поэтому предварительный диагноз обязателен. Описана также
серия аутотрансплантаций у 20 больных. Поскольку химио- и лучевая терапия
обычно не имеет самостоятельного значения, при неоперабельных опухолях воз¬
можен отказ от лечения без диагноза. У нашего больного 6bL4 выбран первый пут ь,
хотя перед операцией планировалось по возможности уточнить характер опухоли.
Дачьше события развивались следующим образом.Квоту по месту жительства в Костроме больной получил, однако до 25 ноя¬
бря госпитааизация в Российский кардиологический на\^но-производствен-
ный комгиіекс по квотам для оказания высокотехнологичной медицинской
помощи была прекращена. Состояние больного прогрессивно ухудшалось; к
декабрю он уже практически не мог ходить, кашель не прекращался, отмеча¬
лось появление темной крови в мокроте. Госпитализация по-прсжнем>' бьша
закрыта. Больной пришел к выводу о неизбежной смерти и принял решение об
отказе от операции, но от повторного обследования не отказывался. В конце
декабря он отмети-1 резкое нарастание одышки; бьы пострижен в схиму. Затем
состояние его несколько стабилизировалось (возможно, он перенес ТЭЛА,
492 Кардиологияно это только предположение). После новогодних каникул данные КТ были
повторно консультированы проф. С.Л, Дземешкевичем, обсуждалась воз¬
можность госпитализации в Российский научный центр хирургии РАМН им.
акад. Б.В. Петровского или в Российский онкологический научный центр им.Н.Н. Блохина. Для уточнения характера опухоли компакт-диск с данными КТ
был направлен на консультацию проф. В.Е. Синицыну, от которого было полу¬
чено устное заключение о саркоме (первоначально рассматривался диагноз
лимфомы; данных за параганглиому выявлено не было). Это резко снижаю
шансы на успех операции, но смысл в госпитализации в Российский онколо¬
гический научный центр им. Н.Н, Блохина все-таки сохранялся.В начале февраля больной бы.-! осмотрен по месту жительства: отмечена
выраженная отрицательная динамика по сравнению с октябрем. Больной не
мог не только ходить, но и лежать (после нескольких вынужденных шагов в
течение 10 мин сохранялись мучительный кашель и одышка). Стали также
беспокоить длительные ночные приступы учащенного сердцебиения (мерца¬
тельная аритмия?). При осмотре отмечено появление выраженных отеков до
бедра, Была увеличена доза кордарона (до 400 мг/сут) и диуретиков (диувер
ежедневно) с небольшим положительным эффектом.24 февраля больной бьш повторно проконсультирован академиком РАМН и
РАН М.И. Давыдовым (заочно). С weTOM мнения рентгенологов и кардиохи¬
рурга состояние расценено как неоперабельная саркома сердца, в связи с чем в
госпитализации в Российский онкологический научный центр им. Н.Н. Блохина
отказано. Больной повторно обсужден с проф. С.Л. Дземешкевичем, который
согласился с выводом о неоперабельности опухоли; химиотерапия и транс¬
плантация сердца в случае саркомы также признаны бесперспективными.Таким образом, можно бьито думать лишь о возможности паллиативной
помощи умирающему больному. Пациент бьш обсужден с доц. кафедры пал¬
лиативной онкологии Московской медицинской академии им. И.М. СеченоваВ.В, Самойленко, Госпитализация в отделение паллиативной онкологии
Городской клинической больницы № 11 была невозможна в связи с костром¬
ской пропиской пациента. Регулярное наблюдение и подбор паллиативной
терапии в онкологическом диспансере по месту прописки также бьши затруд¬
нительны в связи с тем, что больной проживал вдали от Костромы, По мест>^
его жительства онкологическая помошь оказана быть не могла. Учитывая
эти обстоятельства, в качестве паллиативного средства (с целью уменьшения
одышки и проявлений компрессионного синдрома) с 10 марта бьш назначен
дексаметазон в небольшой дозе (по 1 таб. 0,5 мг 4 раза в день) в сочетании с
омезом 20 мг на ночь (предварительно провести ЭГДС не удалось в связи с раз¬
витием удушья).На следующий день пациент был осмотрен повторно: отмечено практически
полное исчезновение кашля в покое, субъективное улучшение самочувствия.
При осмотре впервые обращено внимание на практически полное исчезнове-
ІШЄ грубого систолического шума вдоль левого края грудины, что нельзя бьшо
считать результатом однодневной терапии дексаметазоном. Возможно, интен¬
сивность шума резко ослабла в связи с падением сердечного выброса, однако
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 493реальных объяснений данному факту мы не находили. Из-за пояштения воз¬
буждения доза дексаметазона была вскоре снижена до 3 таб. в сутки, одышка
стала несколько уменьшаться.С решением хирургов о неоперабельности больного мы согласились, дове¬
ряя им, но возникал целый ряд серьезных вопросов, на которые версия о нали¬
чии у больного саркомы не давала ответа.1. Почему больной до сих пор жив? Известны слу^іаи саркомы непосред¬
ственно легочной артерии (см, рис. 23.13, в, е) с 5-летним выживанием после
первичной операции, но наш больной фактически не лечился и типичной
для этой болезни рецидивирующей ТЭЛА у него тоже не бьшо, в массе своей
больные саркомами сердца и крупных сосудов — даже те, которых активно
лечат, — умирают в пределах 1,5-2 лет {рис. 23.14). Здесь, конечно, возникал
следующий вопрос.2. Как давно пациент страдает опухолью? Как минимум с момента бурного
нарастания обструкции правых отделов (те. не меньше года). Но уже перикар¬
дит с тампонадой сердца следует считать достоверным проявлением опухоли,
а с этого момента прошло уже как минимум 3 года. А сама гипертрофия с
желудочковыми аритмиями и АВ-блокадой не могла бьггь началом опухоли?
Следующий вопрос.3. Была ли у пациента гипертрофическая кардиомиопатия? Развилась ли
опухоль на фоне гипертрофической кардиомиопатии или это одна болезнь?
Конечно, аритмии и диффузное утолщение стенок типичны для указанного100-Г--75Нлоя 50
шсо25-1218Месяцы■“Г"243036Рис. 23.14. Выживаемость больных с саркомами сердца и крупных сосудов (Мауег F. et.
al., 2007)
494 Кардиологиязаболевания, но в то же время пациент с юности активно занимался спортом,
и обмороков никогда не было. Можно считать это благоприятным течением
заболевания, но уменьшение гипертрофии левых отделов не находит объяс¬
нения в рамках диагноза гипертрофической кардиомиопатии. Ее сочетания с
опухолями сердца описаны, но это всегда шаровидно растущие опухоли; гораз¬
до чаще инфи^аьтративныс опухоли сердпа ошибочно принимают за гипертро-
фическ^то кардиомиопатию. А если так, то пациент болеет 5 лет.4. Почему перикардиальный выпот не был геморрагическим, если это сар¬
кома?5. Какие полибласты находили в перикардиальном пунктате в 2007 г.?6. Почему у пациента не бьшо и нет боли, которая так типична д^ія сарком и
мезотелиом с прорастанием перикарда?7. Поче^їу исчез шум?8. Почему пациент\^ медленно, но верно становится лучше на абсолютно
паллиативной терапии, эффект которой при саркомах никогда не держится
долго?9. Что это может быть, если не саркома? Структура и характер роста опухоли
заставляли проводить дифференциальный диагноз с мезотелиомой. Недавно
в журнале «Кардиология* был описан случай злокачественной мезотелиомы
перикарда, которую ошибочно принимали за ангиосаркому {см. рис. 23.13, г).
Заболевание дебютировало клиникой острого перикардита с болями, через
год с небольшим больной погиб от метастазов. В других случаях преобладает
констрикиия (см. рис. 23.13, д), но при неоперабельных мезотелиомах химио- и
лучевая терапия столь же малоэффективны, как и при саркомах. Единственная
злокачественная опухоль сердца, которая могла бы с успехом быть вьыечена
без операции, — это лимфома.Нам встретился ряд описаний успешной химиотерапии при лимфомах серд¬
ца. В первом из них (рис. 23.15, а, в) на магнитно-резонансных томограммах
видна обиіирная инфильтрация всех камер образованием, которое отлично
снабжается кровью («зажигается» почти одновременно с миокардом), хотя
раннее контрастирование может встречаться и при ангиосаркоме. Диагноз
лимфомы бьи заподозрен в связи с одновременным наличием спленомегалии
и внутригрудной лимфаденопатии и поставлен с помощью трансторакаль¬
ной биопсии. Через 2 нед после начала стандартной химиотерапии (по схеме
R-CHOP) толщина миокарда уменьшилась почти вдвое {рис. 23.15, б—г), шансы
на полное ИЗ.ПЄЧЄНИЄ оценивались как хорошие. Описаны и другие случаи пол¬
ной рефессии опухоли в результате химиотерапии {рис. 23.16). Лимфома редко
требует операции — эта единственная опухоль сердца, при которой эффектив¬
на химиотерапия.С учетом некоторого ответа на дексаметазон можно было думать и о
возможности воспалительного поражения средостения — фиброзир>тощем
медиа стините. Это диффузная воспалительная инфильтрация средостения
с быстрым исходом в фиброз, которая сдавливает перикард, плевру и сосуды (в
том числе легочную артерию, см. рис. 23.13, е), может возникать после тубер¬
кулеза и обычно хорошо поддается терапии глюкокортикоидами. Возможно
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 495Рис. 23.15. Магнитяо-резоттансные томограммы (левый столбец, сверх\' — по длинной
оси, снизу — но корочкой) и эхокардиофаммы (правый столбец, парастертта.1ьный
доступ, В-режіїм, цілинная ось; сверху — до лечения, стти:*у — после лечения) больного
с первичной лимфомой сердца (http;//www.valsalva.ru/viewtopic.php)стентирование легочной артерии. Диашоз ставится с помощью биопсии или
при операции. Вспомнилось и предположение рентгенолога из гематологиче¬
ского центра о фиброзе, которое тогда не бьшо нам понятно.Таким образом, не зная диагноза, мы могли пройти мимо эффективного
лечения. На 3-й нед приема дсксаметазонабольной стал периодически лежать,
он мог сделать несколько шагов, улучшился аппетит; 26 марта пациент был
вызван на контрольное обследование. Объективно уменьшилась выраженность
отеков, шума в сердце по-прежнему не было. На ЭКГ впервые бьыо зафик¬
сировано трепетание предсердий, что потребовало перепрограммирования
имшіантированного кардиовертера-дефибриллятора. Кроме того, бьта выпол¬
нена МСКТ сердца с внутривенным контрастированием (в первую очередь для
ИСК.1ЮЧЄНИЯ метастазов в легкие и оценки динамики процесса).Результат оказался неожиданным: просвет легочной артерии увеличился
больше чем в 2 раза (рис. 23.17), что по.іностью соответствовало исчезновению
шума по левому краю фудины. С другой стороны, опухоль достигла крупных
бронхов, чего раньше не отмечалось. Метастазы не выявлены. Объем оптаоли
496КардиологияРис. 23Л6. Динамика данных КТ при первичной лимфоме сердца в результате стандарт¬
ной химиотерапии. Слева — томограммы до лечения, справа — после лечения (опухоль
практически не определяется)Рис. 23.17. Динамика оиухоли по данным КТ у больного Е. Слева — томограммы
при поступлении в Факультетскую терапевтическую ісіинику им. В.Н. Виноградова
(16 октября 2008 г.), справа — томограммы от 26 марта 2009 г. При сравнении верхних
томограмм отмечается расширение просвета легочттых артерий, при сравнении нижних
томофамм — прорастание опухоли до крупных бронхов (указаны стрелками)
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 497увеличился незначительно, она приобрела местами почти узловатую структуру
и стала активно накапливать контрастное вещество, в том числе в передней
стенке левого желудочка (раньше артериальная фаза не изучалась). Такой
активный характер накопления контраста практически исключал фибрози-
рующий медиастинит. В ушке правого предсердия был выявлен іромб — вместе
с появлением трепетания это ставило вопрос о назначении варфарииа, но при
неясном характере процесса, склонности опухоли к дес фуктивному (в направ¬
лении бронхов) росту и очень ненадежном контроле за антикоагулянтной тера¬
пией этот вопрос oTnaji. Диагноз саркомы стал еще более сомнительным: если
это распад опухоли, то слишком удачный.С учетом того, что окончательное заключение о саркоме было получено из
отделения В.Е. Синицына, данные первичной и повторной КТ бьши привезе¬
ны ему на консультацию. Личное заключение проф. В.Е. Синицына было таково:
при просмотре изображений от 16.10.2008 г. и 26.03.2009 г. не видна опухоль,
исходящая непосредственно из сердца. Мягкотканные массы преимуществен¬
но локализованы в средостении, они окружают аорту, легочный ствол, устья
легочньо( вен, инфильтрируют перикард, миокард левого и правого желудочка
(особенно в верхних отделах), коронарные артерии. Обращает на себя внима¬
ние симметричная гипертрофия левого желудочка с участками инфильтрации
(это видно на отсроченных изображениях). Тромб в ушке правого предсердия
(за электродом). Узлы в переднем средостении контрастируются негомо¬
генно (см. отсроченные изображения). Отл^ечается незначительное умень¬
шение объема мягкотканных масс в средостении по сравнению с октябрем2008 г. (так, увеличился ігросвет левой легочной артерии с 4—5 до 10—14 мм).
«Мозаичное» кон'фастирование печени (застойная печень? не исключалось
также специфическое поражение), расширение нижней полой вены, непарной
вены. Зак>ш)чение: можно высказать предположение о лимфоме сердиа и средо¬
стения, с признаками инфильтрации перикарда и миокарда желудочков, нару¬
шением функции сердца по рестриктивному типу. Рекомендуется рассмотреть
вопрос о биопсии масс в переднем средостении.предположение о лимфоме, подтвержденное столь авторитетным специ¬
алистом по лучевой диагностике, было очень убедительным — только оно
снимало все поставленные вопросы. Почему пациент жив? — потому что это
лимфома. Болеет лимфомой он, видимо, с самого начала. Болезнь, скорее
всего, одна (сочетания лимфомы сердца и гипертрофической кардиомиопатии
не описано — но описано несколько случаев мимикрии). При лимфоме выпот
и не должен быть геморрагическим, а полибласты — те же опухолевые лим¬
фоциты, недооцененные морфологом. Боли нет, потому что это не саркома.
Больному становится лу^іше потому, что лимфопролиферативные заболевания
сами по себе текут вариабельно; кроме тою, в данном случае дексаметазон
оказался не только паллиативным, но и лечебным препаратом. Самые частые
проявления лимфомы сердца по данным литературы — констриктивная сер¬
дечная недостаточность, выпот в перикарде, синдром верхней полой вены и
аритмии. Именно из этих симптомов и складывалась клиническая картина у
нашего больною.
498 КардиологияС у*іетом возможности эффективной химиотерапии стала очевид¬
ной необходимость морфологического подтверждения диагноза лимфомы.
Госпитализация в Гематологический научный центр (где после биопсии сразу
могла быть начата специфическая терапия) не была возможна по техническим
причинам. С целью проведения медиастииальной биопсии (предположи¬
тельно — видеоторакоскопической) больной после предварительной очной
консультации был госпитализирован в институг грудной хирургии в составе
Медико-хирургического научного центра и\т. Н.И. Пирогова. Однако при
обследовании в центре (эхокардиография) данных за опухоль средостения не
выявлено, поражение сердца рассматривалось в рамках врожленного порока
сердца в сочетании с последствиями оперативного вмешательства на сердце,
Больной был выписан без проведения биопсии.На данном этапе пациент был вновь обсужден с директором Российского
научного центра хирургии РАМН им. акад. Б.В. Петровского, проф.С.Л. Дземешкевичем. Принято решение о его госпитализации в отделение
хирургии легких и средостения данного центра. Консультирован заведующим
этого отделения, проф. В.Д. Паршиным: диагноз фиброзирующего медиасти-
нита представлялся маловероятным (данный процесс чаше распространяется
вдоль венозных сосудов), рассматривались в первую очередь саркома легочной
артерии и мезотелиома перикарда. Оптимальным пpeдcтaвляJ^ocb проведение
открытой биопсии (путем торакотомии), которая не требовала отключения
легкого и позволяла получить достаточное количество материала.К моменту госпитализации в Российский научный центр хирургии
(19-05.2009 г.) больной мог медленно пройти около 1,5 км. Отеки сохраня¬
лись только на стопах. В крови — нейтрофильный лейкоцитоз 22,3 тыс., СОЭ
61 мм/ч, повышение шелочной фосфатазы и у-ГТ, некоторое снижение про¬
тромбина. В связи с нарастанием уровня тиреотропного гормона и снижением
уровня ТЗ в плазме крови доза кордарона бьта снижена до 200 мг, с середины
июня начата осторожная терапия эутироксом 12,5 мкг/сут. При УЗИ доступ¬
ных для биопсии лимфоузлов обнаружить не удалось, однако был выявлен
очаг в печени, которого не было в октябре. Больной был проконсультирован
акад. М.И. Перельманом, предположение о саркоидном поражении кожи не
подтвердилось, но сам по себе спектр предполагаемых диагнозов (от саркомы
до саркоидоза) лишний раз говорил о необходимости биопсии. Новые ком¬
пьютерные томограммы бьши проконсультированы проф. В.Е. Синицыным:
его диагноз остался прежним, отмечено дальнейшее оформление структуры
опухоли, некоторое уменьшение ее объема спереди и увеличение вдоль аорты.
В печени опреде.чшюсь до 10 образований, по плотности очень напоминающих
кисты. Вопрос о целесообразности биопсии печени откладывался до проведе¬
ния бронхоскопии, которая предполагалась как этап в подготовке к торакото¬
мии.Однако при бронхоскопии с обеих сторон была выявлена подслизистая
инфильтрация бронхов опухолью: просветы промежуточного бронха и В9 спра¬
ва сужены наполовину за счет выбухания задней стенки (сдавление извне); про¬
свет дистальной части левого главного бронха и устье нижнедолевого бронха
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 499слева сужены наполовину за счет под слизистой инфильтрации слизистой; про¬
светы бронха язычковых сешентов и ВЗ обт>рированы за счет подслизистой
оболочки инфильтрации стенок. Это позволило прицельно взять биопсию в
одном из участков (ВЗ), где бронх бьы практически полностью обтурирован.В биоптате обнаружено множество опутолсвых клеток с мелкими и сред¬
ними полиморфными ядрами с признаками атипии, которые располагаются
в рыхлой соединительнотканной строме с тонкостенными сосудами и лимфо¬
идноклеточной инфильтрацией. При цитологическом исследовании мазков-
отпечатков обнаружены пол\^разру1пенные «голые» ядра крупного размера с
гиперпролиферированными нукіеолами, выраженным полиморфизмом. Было
сделано заключение о наличии низкодифференцированной злокачественной
опухоли, возможно неэпителиального характера, и соответствующим образом
сформулирован основной диагноз: недифференцированное неэпителиальное
новообразование переднего средостения с инвазией сердца, магистральных
сосудов (верхняя полая вена, легочная артерия), бронхиального дерева, вто¬
ричными изменениями в печени. Гипертрофическая кардиомионатия.Далее микропрепараты были проанализированы в Отделе патологической
анатомии опухолей человека Российского онкологического нау^шого центра
им. Н.Н. Блохина специалистом по лимфомам, в.н.с. А.М. Ковригиной; в гото¬
вых препаратах ку'сочек опухолевой ткани, на некотором протяжении покры¬
тый респираторным эпителием, с инфильтратом из мелких и крупньк клеток
с округло-овальными ядрами, с артифициальными изменениями цитоплазмы,
принад,іежащими субстрату крупноклеточной лимфомы (рис. 23.18, а, б, см.
цветную вклейку). Опухолевый инфильтрат с явлениями деформации. В цито¬
логическом препарате среди мерцательного эпителия крупные и средние клет¬
ки с бластной структурой хроматина, высоким ядерно-цитоплазматическим
соотношением, принадлежащие крупноклеточной лимфоме {рис. 23.18, в).
Заключение', морфологическая картина диффузной В-крупнокле гочной лимфо¬
мы. Для проведения дифференциальной диагностики между первичной медиа-
стинальной (тимической) В-крупноклеточной лимфомой с инфильтрацией
ткани легкого, средостения и экстранодальной диффузной В-крупноклеточной
лимфомой (сердца?) необходимо иммуногистохимическое исследование на
парафиновом блоке с учетом клинико-рентгенологических данных.На данном этапе типирование бьию невозможно в связи с отсутствием
материала в парафиновом блоке, однако это не мешало начинать химиотера¬
пию по стандартной для лимфом схеме. Заключение бьио представлено проф.С.Л. Дземешкевичу; состоялся консилиум с участием акад. М.И. Давьщова и
гематологов Российского онкологігческого научного центра им. Н.Н. Блохина,
по результатам которого 18 июня 2009 г. больной был госпитализирован в отде¬
ление химиотерапии гемобластозов Российского онкологического научного
центра.Согласно современной классификации В-клеточных лимфом, оба предпо¬
лагаемых варианта — диффузная крупноклеточная и медиастинальная — оі но-
сятся к так называемым агрессивным, низкодифференцированным лимфомам,
требующим высокодозной химиотерапии. Общая 5-летняя выживаемость даже
500 Кардиологияпри активном лечении этих лимфом не превышает 50%, но все же эти цифры
отличаются от летальности при саркомах.Опухоли из предшественников В-лимфопитовВ-лимфобластный лейкоз/лимфома из предшественников В-клеток (острый
лимфобластный лейкоз из предшественников В-клеток).В-клеточные опухоли с фенотипом зрелых лимфоцитовХронический лимфоцитарный лейкоз/лимфоцитарная лимфома.В-клеточный пролимфоцитарный лейкоз.Лимфоплазмоцитарная лимфома.Селезеночная лимфома маргинальной зоны.Волосатоклеточный лейкоз.Плазмоклеточная мислома.Моноклонатьная гаммапатия неопределенного значения,Солитарная плазмоцитома.Внекостная плазмоцитома.Первичный амилоид03.Болезни тяжелых цепей.Экстранодальная В-юіеточная лимфома маргинальной зоны лимфоидной
ткани, ассоциированной со слизистыми оболочками (MALT-лимфома).Нодальная В-клеточная лимфома маргинальной зоны.Фолликулярная лимфома.Лимфома из клеток зоны мантии.Диффузная крупнок^іеточная В-клеточная лимфома,Медиастинальная крупноклеточная В-клеточная лимфома.Внутрисосудистая крупноклеточная В-юіеточная лимфома.Первичная лимфома серозных полостей.Лимфома Бёркитта/лейкоз Бсркитта.В-клеточные лимфопролиферативные процессы с неопределенным опухолевым
потенциаломЛимфоматоидный гранулематоз.Посттрансшшнтационное лимфопролиферативное заболевание, полиморф-НОК.ІЄТОЧНОЄ.Как соотносятся эти лимфомы с понятием «первичная лимфома сердца»,
которого нет в классификации? Первичная лимфома сердца — клинический диа¬
гноз, который ставится при поражении исключительно миокарда и/или пери¬
карда. Менее строгое определение допускает позднее метастазирование в лим¬
фоузлы и другие органы при исходном поражении сердца. Морфологически это
чаще всего экстранодальная диффузная В-крупноклеточная лимфома, гораздо
реже — лимфома Бёркитта или Т-клеточная лимфома. «Медиастина'іьная лим¬
фома» тоже долгое время оставаїась клиническим диагнозом — она первитао
поражает средостение (не лимфоузлы) и при массивном росте распространя¬
ется на соседние органы, в том числе перикард. Морфологически, помимо
Т-клеточных лимфом, выделена и особая форма В-крупноклеточной лимфо¬
мы. Более чем в половине сл>^аев ее путают с тимомой или злокачественной
параганглиомой.
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 50ІМетастазы других лимфом в сердце возникают поздно, первичная лимфома
серозных полостей не поражает миокард и лимфоузлы. Остаются варианты
В-крупноклеточной лимфомы, обозначенные морфологом. Клинически их
сложно различить (уже первое описание можно трактовать в обе стороны), но
мы все-таки склонны считать это первичной лимфомой сердца; поражение
сердца имелось давно, а расширения средостения долгое время не бьиіо.Первичная лимфома сердца — крайне редкое заболевание. В отличие от
лимфогранулематоза, доля всех неходжкинских лимфом среди опухолей сре¬
достения составляет всего 5%; частота первичной лимфомы сердца среди всех
экстранодальных лимфом — 0,5%, а среди всех первичных опухолей сердца —1,3-2%. В отечественных монографиях по опухолям сердца, написанных на
материале трех крупнейших кардиохирургических центров — Российского
научного центра хир>'ргии РАМН им. акад. Б.В. Петровского, Научного цен¬
тра сердечно-сосудистой хирургии им. А.Н. Бакулева и киевского Института
сердечно-сосудистой хирургии им, И.М. Амосова — и охватывающих суммар¬
но 788 случаев, можно встретить упоминание лишь о 3 случаях метастатическо¬
го поражения сердца при лимфомах, первичные лимфомы не описаны.Предрасполагают к лимфоме сердца любые им\тунодефицитные состояния,
в том числе герпетическая и ВИЧ-инфекция, синдром Шегрена, химио- и луче¬
вая терапия (например, при лимфоме Ходжкина). Описаны случаи лимфомы
трансплантированного сердца, в частности случай поражения передней створки
митрального клапана донорского сердца {рис. 23.19, а, см. цветную вісгейку). Наш
пациент тоже пережил эпизод облучения неизвестной мощности.В доступной литературе нам встретилось около 210 случаев первичной лим-
фомы сердца у больных без ВИЧ-инфекции (в том числе 142 с описанием) —
несколько чаще болеют мужчины, возраст обычно пожилой, смертность невысо¬
кая, но описывают в основном удачные случаи. Лимфома Бёркитта и Т-клеточная
лимфома встречались у единичньгх больных. Поражение правых камер (особенно
предсердия), безусловно, преобладало — рост обычно инфильтративный, в том
числе с обструкцией трехстБорчатого клапана и выводного тракта правого желу¬
дочка {рис. 23.19, б, в, г, см. цветную вклейку). Из клинических симптомов чаше
всего встречались сердечная недостаточность, выпот в перикарде, АВ-блокада и
аритмии (при этом упоминание об имплантации кардиовертсра-дефибриллятора
больному с первичной лимфомой сердца встретилось нам лишь однажды); син¬
дром верхней полой вены и боль не столь характерны.Патогномоничных признаков лимфом нет, но характерно редкое (в сравне¬
нии с саркомалш) вовлечение клапанов, поражение нескольких камер, плохое
накопление контраста при КТ, относительно гомогенный (за счет отсутствия
некроза и кровоизлияний) сигнал при МРТ, изо/гипоинтенсивность в режиме
Т1 {рис. 23.19, д), различная интенсивность в режиме Т2 и различный характер
накопления гадолиния (на рис. 23.19, е — участок ненакопления). В нашем
сл\^ае решающим признаком ста.ю отсутствие опухоли, исходящей непосред¬
ственно из сердца.Количество вариантов биопсии при лимфоме сердца лишь подтверждает
объективную сложность постановки этого диагноза. Чаще всего он ставится
502 Кардиологияпри операции, диагностической торакотомии, эндомиокардиальной биопсии и
цитологическом исследовании перикардиального пунктата, но описано также
успешное применение игольной биопсии, плевральной пункции, биопсии
периферических лимфоузлов, печени, кожи {табл, 23.4). Ни в одном случае
диагноз не был поставлен с помощью эндобронхиальной биопсии (частота
поражения бронхов при всех лимфомах составляет лишь 1,8%, что существенно
ниже, чем при саркомах). Сіщнтиграфия с галлием и позитронно-эмиссионная
томография имеют лишь вспомогательное значение.Оперативное лечение при .оимфомах проводится значительно реже, чем
при других опухолях сердца, и основным показанием является критиче¬
ская обструкция, т.н. debulking surgery {bulky означает массивную опухоль).
Лимфома может имитировать миксому, другие («обычные») опухоли сердца,
тромбы, вегетации, пороки сердца и не всегда распознается как опухоль даже
визуально; она может приводить к дисфункции протезированного клапана,
особенно биологического. Поводом к операции могут стать рецидивирующая
тампонада сердца, образование патологических шунтов. При таких опера¬
циях лимфома в большинстве случаев становится полной неожиданностью.
Операция на клапане у нашего больного была закрытой и диагнозу не помогла.С 18 июня по 10 июля больной находился в omdejWHuu химиотерапии гемо-
бластозов Российского онкологического научного центра им. Н.Н. Блохина.
При лабораторном обследовании отмечено уменьшение выраженности лей¬
коцитоза (13,8 тыс.), выявлены гипергликемия (8,2 ммоль/л), повышение
уровня ЛДГ (565 Ед/л), фибриногена (1094 мг/дл), растворимых комплексов
фибрин-мономера (тест резко положительный), снижение протромбинового
индекса до 74%. В пунктате костного мозга и в трепанобиоптате признаков
специфического поражения костного мозга не выявлено. С целью имму-
ногистохимического исследования повторно выполнена эндобронхиальная
биопсия, ткань опухоли получена, однако типирование провести не удалось вТаблица 23.4Способы постановки морфологического диагноза при первичной лимфоме сердца(обзор 142 случаев у больных без ВИЧ-ин(>екцни)Способ морфологической диагностикиЧастота успешного
использования,%Операция21,8Стернотомия или торакотомия20,4Эндомиокардиальная биопсия19,7Цитологическое исследование перикардиальной жидкости14,1Парастернальная иголыгая биоисия9,2Цитологи^іеское исследование плевральной жидкости2,8Биопсия тиейного/подмышсчпого лимфоузла1,4Биопсия печени0,7Биопсия кожи0,7Аутопсия6,3Эндобронхиальная биопсия0
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 503связи с патоморфозом на фоне терапии глюкокортикоидами. От типирования
зависело лишь дополнительное назначение ритуксимаба (моноклональные
антитела к рецепторам CD20), показанием для назначения которого является
наличие рецепторов CD20; попытку планирова-юсь повторить.При ;шрингоскопии поражения глоточного кольца не выявлено. При гастро¬
скопии обнаружены сдавление пищевода извне, формирующиеся полипы, био-
птат без существенных изменений. По дaнньл^^ ЭхоКГ, толщина стенок сердца
была несколько лїєньшє, чем в октябре (МЖП 17 мм, ПЖ 15 мм), давление в
легочной артерии оставалось повышенным (СДЛА 29 мм рт.ст.) при нор.мальном
ее диамеїре (19,9 мм). Вьіяшіеїшт нарушешгя локальной сократимости и диасто¬
лической функции левого желудочка. Выполнено ультразвуковое сканирование
с трехмерной реконструкцией, при котором выявлены два увеличенных перифе-
ри^іеских лимфоузла (справа уходящий за ключицу размером до 3x1,8 см, слева1,2 см; в правой подмьшіечной области лимфоузел 1,7x0,8 см) и очаговые образо¬
вания в печени; кровоток в системе верхней полой вены замедлен, но тромбозов
нег. На повторных компьютерных томограммах, помимо основной опухолевой
массы, выявлены конгломераты увелртченных лимфоузов в корнях легких.Согласно принятой системе стадирования лимфом в зависимости от коли¬
чества пораженных органов и лимфоузлов {табл. 23.S), болезнь у нашего
пациента соответствовала TV стадии (поражение сердца, печени, легких и лим¬
фоузлов), до начала терапии глюкокортикоидами имелись все три В-симптома;
лихорадка свыше 38 "С, выраженная ночная потливость и потеря массы тела.Если пользоваться развернутыми прогностическими критериями Россий¬
ского онкологического научного центра им. Н.Н. Блохина (см. список ниже),
то у нашего больного выявлена прилхерно половина факторов неблагоприят¬
ного прогноза: поздняя стадия, большое количество зон поражения, повьшіен-
ный уровень ЛДГ, наличие симпто.мов интоксикации, поражение легких.Развернутые прогностические критерии Российского 0НК0Л0ГИЧЄСК0ІХ> научного
центра им. Н.Н. Блохина• Высокая группа риска по международному прогностическо\су индексу
(возраст, стадия, активность, ЛДГ).• Поздняя стадия.• Большое количество зон поражения.• Повышенный уровень сывороточной ЛДГ.• Уровень НЬ менее 100 г/л.• Уровень альбу\іина .менее 35 г/л,• Уровень общего белка менее 65 г/л.• На.1ичие симптомов интоксикации.• Поражение внутрибрюшных и забрюшинных лимфоузлов.• Поражение легких.Международный прогностический индекс рассчитывается несколько проще
(табл. 23.6). Оценивается общее состояние — наш больной половину и больше
дневного времени проводит в постели, 3 балла. Далее рассчитывается соб¬
ственно международный индекс: у нашего пациогга 4 неблагоприятных фак¬
тора, он попадает в группу высокого риска. Это значит, что при его диффузной
504КардиологияСтадии злокачественных лимфом (Анн-Арбор, 1971 г.).Таблица 23.5СтадияПризнакиПоражентге одной груттпьс лимфоузлов.
Поражеттие одного нелимфоидного органаПоражение двух и более ірупп лимфоузлов.Поражение двух и более нелимфоидных оргаттов по одну сторону диа-
фрагмы ПІПоражение нескольких областей лимфоузлов.Поражение нелимфоидных органов по обе стороны диафрагмыJVДиффузное или диссеминированное поражение более чем одного неяимфоид-
ного органа с сопутствующим поражением лимфоуінов или без пего.
Поражение костного мозга КатегорияВНеобъяснимая потеря более 10% веса за 6 мес.
Необъяснимая лихорадка >38 X.Ионные поты <»0 мокрой подушкой» В-симитомы отсутствуютВ-крупноклеточной лимфоме 5-летняя выживаемость прогнозируется не на
среднем уровне 40-50%, а существеино ниже — 22%.Тем не менее прогноз во многом опреде^тяется ответом на первую линию
тералии. В течение 8 дней больно\іу проведен первый курс полихимиотера-
1ПТИ по стандартной схеме CHOP (табл. 23.7) — циклофосфан, доксорубипин,
винкристин и медрол, причем последний назначается только на время курса.
С учетом кардиотоксичности доксорубицина его доза бьыа существенно сни¬
жена по сравнению со стандартной, но в последний день вливание проведено
повторно. У больного появилась тошнота, но он оставался активен. Во время
курса назначались также аллоттуринол, фраксипарин и париет, в течение 7 дней
в связи с J^иxopaдкoй внутривенно вводились авелокс и противогрибковый
антибиотик, температура нормализовалась. 10 июля нациент был выписан с
рекомендацией провести в Костроме еще три курса с интервалом в 21 день,
после чего приехать на контроль в Онкоцентр. На это время доксорубицин
было рекомендовано заменить менее токсичным митоксантроном.При выписке отмечаюсь уменьшение одышки, отечности лица, снизилась
потребность в диуреіиках; сохранялись тошнота, рвота и жидкий сіул. В ана¬
лизах крови цитопении не было, нормализовался уровень ЛДГ (лейкоциты
8,0 тыс., НЬ 114 г/л, тромбоциты 275 тыс., глюкоза 6,6 ммоль/л, обш.ий белок66,3 г/л, альбумин 32,6 г/л, ЛДГ 415 Ед/л, ПИ 90%, АЧТВ 34 с, фибриноген
828 мг/дп, РКФМ-тест по.южительный). При выполненной в конце курса
контрольной рентгенографии отмечено (по сравнению с исследованием двух¬
недельной давности) уменьшение размеров опухолевого конгломерата в средо¬
стении: ширина срединной тени на уровне передних отрезков 1-Н ребер сокра¬
тилась с 9,1 —9,5 до 7,8-8,2 см (на 1,5 см), поперечный размер сердечной тени на
уровне передних отрезков 1V—Vребер сократился с 13,7-15,4 см до 12,7—14,9 см
(на 1—0,5 см), что позволяло говорить об эффективности терапии. Бы.'Ш все
основания рассчитывать на то, что и дальнейшее лечение будет эффективным.
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 505Таблица 23.6Определение международного прогностического индекса при лимфомахОценка общего состояния ао шкале ECOGНет симптомовЕсть симптомы, повседневная активность сохраненаМснсе половины лневтюго времени проводит в постелиПоловину и более дневного времени проводит в постелиНе встает, трсбуеі' уходаМеждународный прогностический индекс (МТТИ)ПараметрНеблагоприятныйвариантВозрастБольиге 60 летБалл1>уппа рискаECOG2-40-1НизкаяУровень ЛДГПовышенПромежуточная/низкаяЭкстранодальныеочагиБольше /Промежуточная/ высокаяСтадияЯ/-/У4-5Высокая5-летняя выживаемость с учетом МТТИДиффузттая
В-круттттокл сточная
лимфомаОбніая45%Низкийрнск72%Высокийриск22%Таблица 23.7Схема первого курса полихимиотерапии, проведенного больному Е.ПрепаратДозаСхемаОбычные дозыCyclophosphamide (цикчофосфаіО1000 мг в/в1 -й день750 мт/м^Hydroxyldaunorubicin (доксорубипин)40 \гг в/в1 и 8-й дни50 мг/м^Oncovin (винкристин)2 мг в/в1-й день1,4мг/м2Prednizon (медрол)48 мг внутрь1—5-й дни40 мг/м‘Однако на 3-й день после выписки состояние больного резко ухудшилось:
впервые за три года сработал кардиовертер-дефибриллятор. Причинами тому
могли быть электролитные расстройства в результате рвоты/диареи, снижение
дозы кордарона до 200 мг/сут, назначение эутирокса, прямое кардиотоксиче-
ское действие доксорубицина, ремоделирование миокарда на фоне химиотера¬
пии (некроз? фиброз? вослаленис?). Еще накануне вечером больной, находясь
в скиту, отметил появление интенсивной боли в нижней части живота, которой
ш^когда раньше не было (трамал оказал слабый временный эффект). Одышки,
кашля, цианоза не было, отмечалась резкая слабость, АД составило 60/40 мм
рт.ст. Пациент был экстренно госпитализирован в Кардиологический диспансер
г. Костромы: при поступлении состояние крайне тяжелое, диффузный цианоз,
число дыханий 26/мин, АД 60/40 MNf рт.ст., ЧСС 140/мин (трепетание предсер¬
дий? ритм кардиовертера-дефибриллятора? экстрасистолия?). Язык обложен
коричневым налетом, живот мягкий, болезненный в околопуиочной области,
печень выступает из-под края реберной дуги на 2 см, симптомы раздражения
506 Кардиологиябрюшины отрицательны, перистальтика не выслушивается. Состояние расце¬
нено как мезентериальный тромбоз, от экс фснной операции решено воздер¬
жаться в связи с состоянием шока у больного. Проводилась симптоматическая
терапия (промедол, іспарин, преднизолон, кордарон, верошпирон, реополи-
глюкин, адреналин), которая эффекта не имела: в тот же день констатирована
смерть больного. Вскрытия не проводилось; наряду с основной версией, в
качестве непосредственной причины смеруги могли обсуждаться также ТЭЛА,
кардиогенный шок (в том числе в результаге токсического действия доксору-
бииина), внутреннее кровотечение.Однако наиболее вероятной причиной смерти бьыа тромбоэмболия (тром¬
боз in 5/Yw?). Опухоли сами по себе повышают риск тромбоза и не являются абсо¬
лютным противопоказанием к назначению антикоагулянтов. Об оперативном
удалении тромба в предсердии речь не шла, но о назначении антикоагулянтов
можно было думать. В недавнем исследовании больным с лимфомами, пере¬
жившим эпизод венозной эмболии, назначали варфарин либо низкомолску-
лярный гепарин — суммарная частота повторных эмболий и больших крово¬
течений в группе варфарина превысила 40%, смертность составила 6,5%, но и
при лечении гепарином малые кровотечения развились у 27%. Однозначных
рекомендаций в такой ситуации нет и, видимо, быть не может.В нашем слу'чае показания к антикоагулянтной терапии, безусловно, бьши
(трепетание предсердий в сочетании с тромбозом правого предсердия). Однако
и доводов против было достаточно: мы не знали, с какой опухолью мы имеем
дело; се объем и склонность к инфильтративно-деструктивному росту созда¬
вали риск кровотечения; достоверных эпизодов эмболрги не бьшо; регулярный
контроль МНО, а тем более экстренная помотць в случае кровотечения были
сильно затруднены; после нача;іа химиотерапии появился дополнительный
риск тромбоцитопении, анемии, кровотечения в результате лизиса ткани опу¬
холи. Мы анализируем все за и против задним числом, но даже сейчас трудно
ответить на постаатенный вопрос.Мы слишком долго ставили диагноз. Прежде всего необходимо подчер¬
кнуть, что смысл в морфологической верификации диагноза был, независимо
от решения об операции. Это была необычная опухоль сердца — не шаровид¬
ная, не растущая в полость сердца (недаром она не распознавалась при Эхо КГ
и при венгрикулографии), с выраженным распространением в средостение, и
эта необычность требовала биопсии. На том этапе (когда не было поражения
лимфоузлов, печени, бронхов) — все-таки эндомиокардиальной. Когда сам
вопрос об операции встал в зависимость от диагноза, отсутствие морфологии
стало очень мешать. За неясным диагнозом стояли потенциально курабельные
заболевания. Без уверенности в саркоме не мог однозначно рептаться вопрос
о нехмрургичсском лечении, а также о пересадке сердца. Во многом нас оста¬
навливало состояние больного — в это время он НС мог даже лежать. Но и в
такой ситуации могут быть обнаружены новые очаги поражения, доступные
для биопсии. К активным действиям нас подтолкнуло заключеіше проф.
Б.Е. Синицына, которое совпало с улучшением в состоянии больного, но пока¬
зания к биопсии были независимо от него.
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 507Комментарий С.Л. Дземешкевича — директора Российского научного центра
хїфурпіи РАМН им. акад, Б.В. Петровского, д-ра мед. наук, проф.Этот больной — из тех, что запомршаются. Здесь было представ.іено все
поэтапно, однако диагаостический процесс шел сложнее. Вначале мы сразу
пришли к выводу, что это не врожденный порок сердца: все течение заболева¬
ния было совершенно не похоже. Кардиомиопатия? Думаешь обьпно о том,
что знаешь. У нас бьшо неско.чько удачных операций при параганглиомах
сердца. Эта опухоль растет чаще всего из предсердно-желудочковой борозды.
В дальнейшем вмешивались субъективные обстоятельства. Когда мы верну¬
лись к диагностике, речь пошла о саркоме. Информация о саркоме пришла от
В.Е. Синицына. Какая хирургия была возможна в такой ситуации? Пластика?
Полностью убирать легочную артерию? А третий этап — когда терапевты
снова звонили по поводу того больного — оказалось, что он жив, и стаю
понятно, что надо его брать и разбираться. При активной терапии опухоль
уменьшалась, больной попадал в эти 22%. Он и в Российском научном центре
хирургии уже активно ходил, ни о какой хирургии речи не шло.Судя по тому, что тут было рассказано о последних днях (все начиналось с
абдоминальных симптомов), погиб он все-таки от мезентериальной эмболии,
Внутрисердечный тромбоз развился на фоне мощной химиотерапии — как
было показано, толщина стенок >'меньшается в 2 раза, развивается настоя¬
щий эндокардит, пристеночное воспаление, и тут нужна была антикоагулянт-
ная терапия. Хотя риск громадный. Биопсия обсуждалась с самого начала, но
тогда думали, что на операции будет и морфология. Потом, когда отказались
от операции, совершенно было понятно, зачем он уезжает в свой скит. Вот
тогда можно было думать о биопсии, наверное, торакальной. Думая об уро¬
ках, необходимо сказать о выпотном перикардите — вот на этом этапе надо
было начинать ставить диагноз, там было бы больше шансов, чем 22%. И,
наверное, хирурги должны были более активно идти на биопсию.Комментарий А.В. Недоступа — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукМногое сказано. Какие выводы можно делать? Первое — не слишком хорошо
вьпглядит блуждание пациента по главным институтам страны. Только здесь, в
Российском научном центре хирургии РАМН им. акад. Б.В. Петровского, было
то, что и должно было бьггъ. Второе — этот больной вопрос об антикоагулянтах.
Тут еще был эффект отвлечения внимания: мы все время занимались не тем,
не до этого было. Если спросить студента 6 курса — трепетание, тромб в пред¬
сердии, все ясно. Хотя, конечно, мы знаем, как на обычном аспирине возникает
почти смертельное кровотечение. Третье — морфология. Мы все время говорїтм
о важности морфологической диагностики. С тех пор как мы стати делать биоп¬
сию, мы постоянно это видим: что ни случай, то открьгше. Здесь-то биопсия, по
сути, случайно получилась. Как можно еще диагностировать эту опухоль? У нас
опьгг очень маленький (я видел 5—6 случаев), у хирургов он значительно боль¬
ше. При ЭхоКГ можно увидеть толст>то стенку сердца и заподозрить болезнь
508 Кардиологиянакопления, но как можно было в этом случае заподозрить опухоль? Наверное,
единственное, что могло бы навести на мысль об опухоли, — неоднородность
стенки сердца, которая местами напомината полости распада.Таким образом, оба представленных клинических случая закончились, к
сожалению, фатально — и если в первом случае больная попала в поле зре¬
ния врачей слишком поздно, то во втором — пациент наблюдался в крупных
медицинских центрах в течение последних 5 лет своей жизни, но оконча¬
тельный диагноз, несмотря на значительный прогресс инструментальной
диагностики, был поставлен лишь за месяц до смерти. Возможно, активная
химиотерапия стала одним из факторов, ускоривших гибель пациента, одна¬
ко в отсутствие терапии его скорая гибель была неизбежна.ЛИТЕРАТУРААбрикосов Л. И. Частная патологическая анатомия. Ч. II. — М., 1940.Давыдов М.И., Дземешкевич С.Л., Герасимов С.С, и др. Случай успешного
хирургического лечения больного первичной опухолью сердца // Вестник
московского онкологического общества. — 2008. — № 11. — С. 2-3.Кнышов Г.В., Витовский Р. М., Захарова В.П. Опухоли сердца. Проблемы диа¬
гностики и хирургического лечения. — Киев: Пресса Украины, 2005. — 256 с.Ковригина А.М., Лробатова Н.А. Лимфома Ходжкина и крупноклеточные
лимфомы. — М., 2007. — 214 с.Мазуров В.И., Криволапое Ю. А. Классификация лимфом. Морфология, имму¬
нофенотип, молеку'лярная генетика неходжкинских .іимфом // Практическая
онкология, — 2004, — Т. 5, № 3. — С, 169—175.Петровский Б.В,, Константинов Б.А., Нечаенко МЛ. Первичные опухоли
сердца. — М.: Медицина, 1997. — 148 с.Поддубная И.В., Бабичева Л.Г. Факторы прогноза при диффузной крупнокле¬
точной В-клеточной лимфоме // Материалы VIII Российского онкологического
конгресса. Москва, 22—24 ноября 2004 г //www.rosoncoweb.ru/congress/ru/.Поддубная И.В., Демина Е.Л. Диагностика и определение распространен¬
ности (стадирование) неходжинских лимфом // Практическая онкология. —
2004. - Т 5, № 3. - С. 176-184.Сергеев О.И., Буторина Л.И., Коршунов А.И, и др. Ангиосаркома сердца //
Кардиология. — 1993, — № 3, — С. 90—92.Сидоренко Б А., Домницкая Т.М., Гришин А.М. и др. Диагностика злокаче¬
ственной мезотелиомы перикарда // Кардиология. — 2009. — № 1. — С. 84-89.Федосеев Г.Б., Ильин М.П., Крякунов К.Н. и др. Синдромная диагностика
внутренних болезней. — СПб., 1996. — X 1, ~ С. 429—430.Цукерман Г. И., Малашенков А.И., Кавсадзе В.Э. Опухоли сердца, — М.;
Изд-во НЦССХ им. А.Н. Бакулева РАМН, 1999. — 268 с.Ananthasubramaniam К., Farha А. Primary right atrial angiosarcoma mimicking acute
pericarditis, pulmonary embolism, and tricuspid stenosis // Heart. 1999; 81 (5): 556-558.
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 509Bagwan I.N., Desai S., Wotherspoon A., Sheppard M.N. Unusual presentation
of primary cardiac lymphoma // Interact. Cardiovasc, Thorac. Surg, 2009; 9 (1);
127-129.Bennett K.R., Brandon L.H., Bennett F.T. Angina pectoris from an unexpected
cause 11J. Miss, State Med. Assoc. 1997; 38 (12): 441—445.Bergler-Klein J., Knoebl P., Kos T. et al. Myocardial involvement in a patient
with Burkitt’s lymphoma mimicking hypertrophic cardiomyopathy // J. Am. Soc.
Echocardiogr. 2003; 16 (12): 1326-1330.Bertali F., Remon Valera JA., Arrocha R. Angiosarcoma of the heart and its spon¬
taneous rupture. A rare cause of effusive-constrictive pericarditis. A case report and
review of the literature [Article in Spanish] // Rev. Med. Panama. 1995 Sep; 20 (3):
84-91.Blackmon S.H., Patel A.R., Bruckner B.A. et al. Cardiac autotransplantation for
malignant or complex primary left-heart tumors // Tex, Heart Inst. J., 2008; 35 (3):
296-^300.Cina SJ., Smialek J.E., Burke Л.Р. et al. Primary cardiac tumors causing sud¬
den death: a review of the literature // Am. J. Forensic Med, Pathol. 1996; 17 (4):
271-281.Colucci Ж 5. , Schoen FJ., Braunwatd E. Primar>' tumors of the heart // Braunwald
E, A Textbook of cardiovascular medicine. — 5th ed., 1996. — P, 1464-1476.Crespo M.G., Pulpon LA., Pradas G. et al Heart transplantation for cardiac angio¬
sarcoma; should its indication be questioned? I j J. Heart Lung Transplant. 1993;
12 (3): 527-530.ЕЫ N., Yamamoto H. , Sakai J. et al. Angiosarcoma of the heart presenting as fatal
pulmonary hemorrhage // Intern. Med. 1997; 36 (3): 191-193.Edwards R.L., ChalkS.M., McEvoyJ.D. etal Pulmonary haemorrhage in dissemi¬
nated cardiac haemangiosarcoma 11 Br. J. Dis, Chest 1977, 71 (2): 127-131.Fujita Y., Ikebuchi М., Tarui S., Irie H. Successful combined treatment of primary'
cardiac malignant lymphoma with urgent cardiac operation and chemotherapy j j
Circ. J. 2009; 73 (5)! 967-969.Glancy D.L., Morales J.B. Jr., Roberts W.C. Angiosarcoma of the heart // Am. J.
Cardiol. 1968; 21 (3): 413-419.Guhl L., Grawunder H.J., Arlart I.P. Magnetic resonance tomographic findings in
cardiac tumors [Article in German] // Radiologe. 1993; 33 (3): 153-158,HoffmeierA., Semik М. , Schmid Ch. et al. Primary Burkitt lymphoma of the heart —
diagnosis and therapy [Article in German] // Z. Kardiol. 2002 Apr; 91 (4); 347—351.http ://doctor. lymphadenopathy.ru/.http ://w'vm valsalva.ru/viewtopic.php.Janigan D.T., Husain A, Robinson NA. Cardiac angiosarcomas. A review and a
case report II Cancer, 1986; 57 (4): 852—859.Kainuma S., Masai Т., Yamauchi T. et al. Primary malignant pericardial mesothe¬
lioma presenting as pericardial constriction // Ann. Thorac. Cardiovasc. Surg. 2008;
14 (6): 396-398.Kawahito K., Ino Т., Adachi H. et al. A case of primary angiosarcoma of the heart
[Article in Japanese! // Nippon Kyobu Geka Gakkai Zasshi. 1994; 42 (7): 1069—1072.
5!0 КардиологияKennetly К, Aziz R., Toner М., Young V. Right atrial paraganglioma: an unusual
primary cardiac tumour // Eur. J. Cardiottiorac. Surg. 2008; 33 (6): 1150-1152.Klima U, Wlmmer-Greinecker G., Harringer W. et a!. Cardiac angiosarcoma — a
diagnostic dilemma // Cardiovasc. Surg. 1993; 1 (6): 674-676.KohJ O., Hblschermann H., Pmile H. et al Therapy-resistant ventricular tachycar¬
dia in a woman with primary cardiac non-Hodgkin lymphoma [Article in German] //
Med. Klin. (Munich). 2000 Sep 15; 95 (9): 517-522.Lee P. W., Woo K.S., Chow L. T. et al. Images in cardiovascular medicine. Diffuse
infiltration of lymphoma of the myocardium mimicking clinical hypertrophic cardio¬
myopathy // Circulation. 2006; 113(12): е662-е664.Lin Т.К., Stech J.M., Eckert W.G. et al. Pericardial angiosarcoma simulating peri¬
cardial effusion by echocardiography// Chest. 1978; 73 (6): 881-883.Llombart-Cussac A., PivotX., Contesso G. etai. Adjuvant chemotherapy for primary
cardiac sarcomas: the IGR experience // Br. J. Cancer. 1998; 78 (12): 1624-1628.Mader M. T, Poulton T.B., White R.D. Malignant tumors of the heart and great ves¬
sels: MR imaging appearance// Radiographics. 1997 Jan-Feb; 17 (1): 145-153.Mayer F., Aebert H., Rudert M. et al Primary malignant sarcomas of the heart and
great vessels in adult patients — a single-center experience // Oncologist. 2007 Sep;
12(9): 1134-1142.Muslimani A.A., Spiro T.P., Chaudhry A.A. et al. Venous thromboembolism in
lymphoma: how effectively are we treating patients? // Am. J. Clin. Oncol. 2009
Jun 19.Nitta R., Sakomura Y., Tanimoto K. etai Primary cardiac angiosarcoma of the right
atrium undiagnosed by transvenous endocardial tumor biopsy // Intern. Med. 1998;
37 (12): 1023-1026.Omura A., Tobe S., Yoshida K., Yamaguchi M. Surgical treatment for recurrent pul¬
monary arter>' sarcoma // Gen. Thorac. Cardiovasc. Surg. 2008; 56 (1): 28-31.Ortiz de Mura J.A., Avila M.C. et al. Primary pericardial angiosarcoma with mul¬
tiple lung and a solitary liver metastases: the clinical and anatomicopathological find¬
ings [Article Ш Spanish] // Rev. Esp. Cardiol. 1994; 47 (10): 710-712,Rodman Т., Pastor BM. Mediastinal lymphoma simulating primary heart disease I j
Am. J. Cardiol. 1958; 1 (5): 652-657.Rhomberg W , Grass M. Angiosarcoma of the right atrium: local control via low
radiation doses and razoxane. A case report [Article in German] // Strahlenther
Onkol. 1999 Mar; 175 (3): 102-104.Ryu S.J., Choi B. Ж, Choe K.O. CT and MR findings of primary cardiac lymphoma:
report upon 2 cases and review // Yonsei Med. J. 2001; 42 (4): 451—456.Sawamura Т., Takiya H., Yamada T. et al. A case of cardiac angiosarcoma with a
pseudoaneurysm formed in the right coronary artery [Article in Japanese] // Kyobu
Geka. 1994; 47 (7): 565-568.Simon B.C., Funck R., Drude L. et al. Malignant angiosarcoma of the right atrium
in pregnancy. Diagnostic and therapeutic problems lArticle in German] // Herz. 1994;
19 (3): 166-170.Skalidis E.L, Parthenakis F.L, Zacharis E.A. et al. Pulmonary tumor embolism
from primary cardiac B-cell lymphoma// Chest. 1999 Nov; 116 (5): 1489-1490.
Глава 23. Первичные злокачественные опухоли сердца (опыт терапевтов) 511Soiomonov Л., Zuckerman Т., Goralnik L. et al Non-Hodgkin’s lymphoma present¬
ing as an endobronchial tumor: report of eight cases and literature review // Am. J.
Hematol. 2008 May; 83 (5): 416-419.Stein M.j Deitling F., Cantor A. et al. Primary cardiac angiosarcoma: a case report
and review of therapeutic options // Med. Pediatr. Oncol, 1994; 23 (2): 149-152.Tada H., Asazuma K., Ohya E. et al Images in cardiovascular medicine. Priman^
cardiac B-cell lymphoma // Circulation. 1998 Jan 20; 97 (2); 220-221.Thiessen Я, Matzinger F.R., Seely J. etal. Fibrosing mediastinitis; successful stent-
ing of the pulmonary artery j I Can. Respir. J. 2008; 15(1): 41-44,Tsuda Я-, fmazeki N., Fuse У. et al. Cardiac angiosarcoma with gastrointestinal
bleeding, hypoxemia, thrombocytopenia and microangiopathic hemolytic anemia
[Article in Japanese] // Gan No Rinsho. 1986; 32 (9): 1035-1040.Watanabe Y., Fukuda Т., Araki М., Hiraki S. A case of angiosarcoma of the heart
with cardiac tamponade and repeated hemoptysis fArticle in Japanese] // Nihon
Kyobu Shikkan Gakkai Zasshi. 1993; 31 (1 1): 1485-3488.Werner D., SchmeisserA., Daniel IV.G. Images in cardiology: Primary'cardiac lym¬
phoblastic T ccll lymphoma // Heart. 2001; 86 (6): 618.Ying A.J., Myerowitz PD., Marsh W.L. Jr. Posttransplantation lymphoprolif-
erative disorder in cardiac transplant allografts // Ami, Thorac. Surg. 1997; 64 (6):
1822-1824.Zyssman /., Cantor A., Steyn М., Meyer T. Multiple intracavitary' cardiac masses;
an uncommon presentation of African Burkitt’s lymphoma j j Int. J, Cardiol. 1992; 37
(3): 421-423.
Глава 24УСПЕШНОЕ ЛЕЧЕНИЕ МАССИВНОГО ТРОМБОЗА
НИЖНЕЙ ПОЛОЙ ВЕНЫ С НЕФРОТИЧЕСКИМ
СИНДРОМОМ И ХРОНИЧЕСКОЙ ДВУСТОРОННЕЙ
ТРОМБОЭМБОЛИЕЙ ВЕТВЕЙ ЛЕГОЧНОЙ АРТЕРИИ
У ПАЦИЕНТА С ГЕНЕТИЧЕСКИ ОБУСЛОВЛЕННОЙ
ТРОМБОФИЛИЕЙО.В. Благова, С.Л. Дземешкевт, И.Л. Козловская, А.В. Недоступ,
И.Д. Саркисова, ВЛ. Седов, Ю.В. Фролова, В.В. Раскин,
Л.С. Дземешлевич, Е.А. Меришна, В.Е. Синицын, Е.М, Шилов,
Е.Ю. ГорностаеваС «необъяснимыми» тромбозами ра;ути^гных локализаций, нередко у моло¬
дых пациентов, все чатпе приходится сталкиваться юшнинистам ра;зкых спеыи-
а/;ьностей; кардиологам, неврологам, хиргргам, нефрологам, гепатологам и др.
По-видимому, в значительной степени это связано с ростом распространенности
аутоиммунной патологии (первичного и вторичного антифосфояипидного синдро¬
ма), а гакжс с накоплением в популяции профомбогенных мутаций. Представляем
пациента, у которого массивный тромбоз нижней полой вснът на всем ее протяже¬
нии, почечных и подвздоишых вен разви.'1ся после тупой іравмьі, в течение полуто¬
ра лет привел к формированию стойкого нефротического синдрома и хронической
двусторонней тромбоэмболии ветвей легочной артерии (ТЭЛА) с высокой легоч¬
ной гипертензией и тяжелой переір>'зкой правых отделов сердца. Судьба молодого
пациента зависела от возможности радикальной тромбэктомии (уникальная опе¬
рация была успешно вьіпошісна в РНЦХ им. акад. Б.В. Петровского). Участие в его
дальнейшей судьбе широкого круга специалистов (в первую очередь нефро.'Югов из
клиники терапии и профзаболеваний им. ЕМ. Тареева), постоянное наблюдение
за больнъгм, а также его сознательное отношение к лечению позволяют рассчрггы-
вать на максимаїьную реабилитацию пациента.Больной Г., 23 года, поступил в Факультетскую терапевтическую клини¬
ку им. В.Н, Виноградова 22.04.2010 г с жалобами на одышку при небольших
физических нагрузках (ходьба на 100 м, подъем на один лестничный пролет),
постепенно проходящую в покое, периодический сухой кашель, отеки голеней,
стоп, бедер, наружных половых органов, увеличение в объеме живота, перио¬
дические ноющие боли в области сердца, в левой поясничной области.Ил семейного анамнеза: родителям по 43 года, отец здоров, мать страдает
гипертонической болезнью (уже после проведения разбора, в апреле 2011 г.,
она і'мерла от тромбоза мозжечковой артерии); брат 16 лет (по матери) перенес
Глава 24. Успешное лечение массивного тромбоза нижней полой вены... 5134 кардиохирургичсских вмстиательства по поводу тетрады Фалло, По другим
заболеваниям семейный анамнез не отягощен. В течение всей жизни физиче¬
ские нагрузки переносил хорошо, занимался спортом (хоккеем, футболом, в
течение 9 лет — лыжным спортом, имел 2-й взрослый разряд; после окончания
школы регулярные занятия прекратил). Образование среднее специальное,
работал поваром. Курил по 10 сигарет в день до августа 2010 г., употребление
наркотиков категоірически отрицает. Аллергологический анамнез не отягощен.В марте 2009 г. попал с серьезную драку, получил множество травм, втом числе
сильный удар ногой в область поясницы {рис. 24.1). Больше месяца сохранялись
выраженные боли в поясничной области с обеих сторон, обширные синяки на
коже; изменения цвета мочи не отмечал. Периодически внутримышечио вводи¬
лись анальгетики, обследования не проводились. Через 1,5—2 мес после драки
появились отеки обеих ног, которые затем спонтанно уменьшились. Несколько
позже (в конце апреля 2009 г.) во время физической нагрузки возникло чувство
резкой нехвагеті воздуха, дурноты, боль в области сердца; одьияка сохраішіась,
стали отмечаться подье?ш>і температуры тела до 38 °С, Вызванной бригадой
скорой медицинской помощи бьит госпитализирован в городскую больнищ' по
месту жительства с диагнозом «левосторонняя пневмония», проведено лечение
ципринолом, мегрожилом, амикадином, цефтриаксоном, сумамедом ; темпе¬
ратура тела нормализовалась. Одышка и оі€ки продолжали периоди^іески бес¬
покоить, выраженность их несколько уменьшилась.После выписки из больницы ОТДЫХШ1 на юге; за несколько дііей до воз¬
вращения отметил появление резких болей в правой поясничной области,
усиление отечности правой ноги; госпитатизирован по месту жительства, в
связи с изменениями мочи состояние расценено как гломерулонефрит; кроме
того, заподозрен инфекционный эндокардит с поражением трикуспидально-
го клапана, направлен в Московский областной научно-иccлeдoвaтeJJЬcкий
клинический институт им. М.Ф. Владимирского. При обследовании были
выявлены признаки тромбоэмболии ветвей легочной артерии, тромбоз нижней
полой вены; больной был направлен в Городскую клиническую больницу № 1
г Москвы для решения вопроса об имплантации кава-фильтра. Одышка, шски
ног и (периодически) лица сохранялись.В декабре 2009 г. в Городской клинической больнице № 11. Москвы при уль¬
тразвуковом исследовании были диагностированы неокклюзируюишй тром¬
боз нижней полой вены (от правой почечной вены до правого предсердия) с
флотирующим участком тромба около 5 см, выраженная гипертрофия и дила-
тация правого желудочка, трикуспидальная недостаточность II—ТТЇ степени,
легочная гипертензия. При КТ — картина хронической двусторонней ТЭЛА,
участки посгинфарктной пневмонии с обеих сторон, тромбоз инфра- и супра-
репального отделов нижней полой вены и обеих почечных вен, небольшое
количество жидкости в брюшной полости; данных за о]г>’холь почки получе¬
но не бьио. в анализе мочи — белок 0,66 г/л, лейкоциты 7-8 в ноле зрения, в
крови — снижение уровня общего белка (34 г/л), выраженная иптерхолестсри-
иемия (15,6 ммоль/л), что расценено как нефротический синдром. В течение
недели отмечалась лихорадка до 38 °С, проводилась терапия антибиотиками.
Март2009АпрельЛето2009ДекабрьЯнварь 2010Февраль 2010Март 2010 Апрель-июль 2010Боль в 'I
поясницеОтеки
Одышка
Боль в об
сердцаласти1справаострая боль в
правой пахо-Ітела38 "С38 “СГ оспиталі.ізацияДубнаМОНИКИ1 ГКБДубнанцссхДубна ФТКАнализкровиібелок 34 г/лtxc15,6 ммоль/лІ6ЄЛОК41 г/л
ТСБР
19,2 мг/л^альбумин 12 г/лТАЛТ, act до 200 ед/л, ЛДГ 642 ед/л
КФК 964 ед/л4^НЬ 81-100 г/л, HCV-Ab, Hbs отр„
MHO 2.5-3,0Анализмочи+0,66% белка,
7-8 л. в п/зр500 мг/дл белкабелок ++-I-+, умеренный мочевой
синдром, цилиндры зернистые (2-3)
и гиалиновые (1-3)Диагнозлевосто¬ронняяпневмо¬ниянефрит?иэ?ТЭЛАтромбозНПВтромбоз
НПВ, обеих
почечных
вен, ТЭЛАилеофемора-льныйтромбозЧПЭхоКГ: данных
за ИЭ нет1дМ к фосфолипидам 2,9 Ед/мл {менее
10)IgG - 1,6 Ед/мл, других данных нетЛечениеанальге¬
тики в/мципринолметрожиламикацинцефтриа-ксонсумамедантибиотикиварфариндетралексомезгепаринреополиглю-кинтренталдетралекстромбо-АССфенилин,детралекс,лиотонтромбо-АССкомпрес.терапия ПИ 31%фенилин, нейромультивит, сорбифер,
дигоксин, конкор, диувер, диакарб
2 раза в неделю: преднизолон 60 мг/сут
(в течение 10 дн,), 30 мг/сут (10 дней),
до 20 мг (10 дней) с дальнейшей
отменойРис. 24.1. Анамнез заболеваниуг больного Г., 23 года
Глава 24, Успешное лечение массивного тромбоза нижней полой вены... 515варфарином (МНО ниже терапевтических значений), детралексом, омезом;
направлен в НЦССХ им. А.Н. Бакулева на консультацию ангиохирурга.В январе 2010 г. был повторно госпитализирован в городскую больницу по
месту жительства в связи с появлением острой боли в правой паховой области,
отека ноги до паховой складки; выявлен илеофеморальный тромбоз. В анали¬
зах крови сохранялись гипопротеинемия (41 г/л), повышение СРБ (19,2 мг/л),
фибриногена, МНО составляло 1,5. Проводилась терапия гепарином, реополи-
глюкином, тренталом, актовегином, детралексом, тромбо-АССом. Состояние
расценивалось как возможный инфекционный эндокардит, повторно реко¬
мендована консультация в НЦССХ им. А.Н. Бакулева.В феврале был госпитализирован в отделение приобретенных пороков
сердца Научного центра сердечно-сосудистой хирургии им. А.Н. Бакулева.
При обследовании по данным чреспищеводной Эхо КГ вегетаций не выявлено;
отмечены пролапс митрального клапана с минимальной регургитацией, неко¬
торое уплотнение септальной створки трикуспидального клапана, некоторое
втяжение его створок в полость правого желудочка, реіургитация ПІ степени,
систолическое давление в правом желудочке 65 мм рт.ст., тромб в устье и просве¬
те нижней полой вены. Кроме того, выявлены тромбоз правой общей бедрен¬
ной вены до сафено-феморального соустья, тромбоз глубокой и поверхностной
вен, подколенной вены, при КТ — тромбоз правой и левой легочных артерий,
полисегментарные изменения с обеих сторон, в анализах крови — альбумин
12 г/л, в моче — белок 5 г/л, функция почек сохранена. Проконсультирован
сосудистым хирургом (рекомендовано консервативное лечение — фенилин,
детралекс, лиотон, компрессионная терапия), а также кардиохирургом: дан¬
ных за инфекционный эндокардит нет, хирургическое лечение не показано.
К моменту выписки на фоне терапии фенилином 90 мг/сут протромбиновый
индекс составлял 31%; принимал также тромбо-АСС, детралекс. Все это время
одышка и отеки ног, а также лица и наружных половых органов сохранялись,
постепенно усиливались.В марте 2010 г вновь был госпитализирован по месту жительства, отме¬
чалось нарастание уровней АЛТ и ACT (до 2000 Ед/л), ЛДГ (642 Ед/л) и
КФК(964 Ед/л), снижение гемоглобина до 81—100 г/л, появление юных
форм лейкоцитов (в отсутствие лейкоцитоза); маркеры вирусных гепатитов
оставались отрицательными, МНО находилось в терапевтическом диапазоне
(2,5-3,0). Предполагался диагноз антифосфолипидного синдрома (IgM к фос¬
фолипидам 2,9 Ед/мл при норме менее 10, IgG — 1,6 Ед/мл, других данных
нет). При выписке рекомендована терапия фенитином 2,5 таб. в сутки, ней-
ромультивитом и сорбифером в течение 20 дней, дигоксином 0,25 мг в день,
конкором 2,5 ш утром, диувером 10 мг ежедневно, диакарбом 2 раза в неде¬
лю; кроме того, начата терапия преднизолоном 60 мг/сут (в течение 10 дней)
с последующим снижением дозы до 30 мг/сут (10 дней), до 20 мг (10 дней) и
дальнейщим снижением до 2,5 таб. Субъективного улучшения само^гувствия
не отмечал. После выписки диувер был заменен фуросемидом 40 мг еже¬
дневно (диурез на этом фоне недостаточный). Бинтование ног прекратил в
связи с нарастанием отеков. Отеки и одышка сохранялись, отметил некоторое
5І6 Кардиологияувеличение живота в объеме. Поступил в Факультетскую терапевтическую
клинику им. В.Н. Виноградова для дообследования и определения дальнейшей
тактики лечения.При поступлении в Факультетскую терапевтическую клинику
им. В.Н. Виноградова: состояние средней тяжести. Конституция нормостени¬
ческая, рост 176 см, вес 73 кг. Кожные покровы чистые, нормальной окраски и
влажности. Напряженные отеки обеих ног (больше — правой), подкожной клет¬
чатки туловища, нар>окных половых органов, отечность лица. Периферические
лимфоузлы не увеличены, В легких дыхание жесткое, удовлетворительно про¬
водится во все отделы, хрипы не выслушиваются. Число дыханий 20/мин. Тоны
сердца приглушены, ритм правильный, акцент II тона над легочной артерией,
грубый систолический шум над мечевидным отростком и по левому краю
грудины. ЧСС 100—110/мин, АД 120/80 мм рт.ст. Живот мягкий, несколько
увеличен в объсхме за счет асцита, безболезненный. Печень +2 см, селезенка не
увеличена. Симптом Пастернацкого слабо положительный слева.^анализах крови\ НЬ 132,1 г/л, эритроциты 4,8 млн, цветовой показатель0,82, лейкоциты 7,6 тыс., палочкоядерные 1%, сегментоядерные 39%, лим¬
фоциты 53%, моноциты 5%, эозинофилы 2%, СОЭ 45 мм/ч, тромбоциты
310 тыс.; общий белок 35,2 г/л, альбумин 18,9 г/л, креатинин 0,65 мг/д,і, глю¬
коза 3,5 мг/дл, мочевая кислота 328 мкмоль/л, общий билирубин 5 мкмоль/л,
натрий 148 мэкв/л, калий 4,8 мэкв/дл. При электрофорезе белков шіьбумин
38,6% (55,8-66,1), а, 7,2% (2,9-4,9), а, 30,3% (7,1-11,8), р 11,3% (7,9-13,7), у
12,6% (11,1-18,8). Липидный спектр: триглицериды 2,92 ммоль/л (0,57—2,28),
обший холестерин 11,8 ммоль/л (3,88-6,47), ЛВП не осаждаются, ЛПОНП-хс0,6 ммоль/л (0,114-0,342).В повторных анализах крови, выполнявшихся в мае, июне и июле, суще¬
ственной динамики не было: сохранялись выраженное увеличение СОЭ (до
50—60 мм/ч), относительный лимфоцитоз, признаки нефротического синдро¬
ма (гипоальбуминемия на уровне 20—21 г/л, диспротеинемия, гиперлипиде-
мия, степень которой уменьшилась в результате терапии статинами — уровень
обшего холестерина снизючся до 6,9-7,3 ммоль/л, уровень триглицеридов
нормализовался),СРВ при пост>ч1лении составил 1,21 мг/дл (0-0,8), антистрептолизин-0 —30,1 МЕ/м.1 (норма до 125), комплемент, антитела к ДНК, РФ, иммуноглобу¬
лины крови, гормоны шитовидной железы в пределах норлш. ACT 25 Ед/л,
АЛТ 17 Ед/л, у-ГТ 152 Ед/л, щелочная фосфатаза — 169 Ед/л, ЛДГ 200 Ед/л,
КФК 82,3 Ед/л, МБ фракция креатинфосфокиназы 33 Ед/л, Коагулограмма
(на фоне терапии фенилином 60 мг/сут): АЧТВ 1,41, протромбиновый индекс
53%, уровень фибриногена значительно повышен (9,03 г/л), МНО 2,19.
Маркеры вирусных гепатитов, RW, антитела к ВИЧ не вьшвлены. Повышения
титра антител к кардиолипину при двукратном исследовании не обнаружено.В общем анализемони: pH 6, удельный вес 1028, мутная, белок 8,1 г/л, сахара
и ацетона нет, желчные пигменты — следы, уробилин выше нормы, лейкоци¬
ты 3—5 в поле зрения, эритроциты 6—9 в поле зрения, цилиндры гиалиновые1—2 в поле зрения, зернистые 0,1—3 в поле зрения, слизи и бактерий много.
Глава 24. Успешное лечение массивного тромбоза нижней полой вены...517оксалатов немного, клеток почечного эпителия немного (с явлениями жиро¬
вого перерождения), в динамике (июнь, июль) — без существенных измене¬
ний (белок до 12,6%о). Суточная протеинурия составляла 12,15 г. В анализе по
Нечипоренко лейкоциты 750/мл, эритроциты 7000/мл. В суточной моче 2,75 г
белка. Проба Реберга: скорость клубочковой фильтрации 96 мл/мин, реабсорб¬
ция 98,8%.Для подтверждения возможной генетической природы массивного тром¬
боза проведен анализ полиморфизмов генов свертывания крови: мутаций гена
протромбина и Лейденского фактора не выявлено, однако o6Hap\r»ceHbi 1
гомозиготная и 5 потенциально протромбогенных гетерозиготных мутаций
{табл. 24.1). Уровень гомоцистеина крови оказался нормальным (6,67 мкмоль/л
при норме 6,26-15,01).На ЭКГ {рис. 24,2): синусовая тахикардия, ЧСС 108/мин. Отклонение элек¬
трической оси сердца вправо. Неполная блокада правой ножки пучка Гиса,
отрицательные зубцы Т в отведениях V^-V^. Зубец Р не изменен, PQ 0,14 с,
QRS 0,09 с, QT/QTc 356/414 мс. Признаков ишемии, гипертрофии различных
отделов сердца нет. При холтеровском мониторировании ЭКГ, выполненном
на фоне приема 12,5 мг метопролола, — синусовая тахикардия (ЧСС днем91-128/мин, средняя 106/мин, ночью 67-101/мин, средняя 95/мин), значи¬
мых нарушений ритма и динамики ST-Tнет.При ЭхоКГ (проф. В.П. Седов, рис. 24.3, верхний ряд, см. цветную вклей¬
ку): КДР левого желу^дочка 3,2 см, тМЖП 0,9 см, ФВ левого желудочка
более 60%, нарушений локальной сократимости нет. Правый желудочек: ПЗР
4,8 см (N до 3,8 см), толщина свободной стенки 0,8 см. Правое предсерлие
136 мл, левое не увеличено. Аортальный и митральный клапаны не изменены.Таблица 24,1Исследование полиморфизмов генов свертывания крови больного Г.ГенОбозна¬ВозможнаяГенотипчениемутаїщяпациентаПротромбин (коагуляционный фактор 11)F2G20210AG>AGGФактор Ляйдена (коаіуляциоііньсй фактор V)F5R506Q G >AGGИнгибитор активатора плазминогенаPAJ-I-675 5D >4G4G/5GФибриногенFGBb-455 G>AGAТромбоцитарный рецептор фибриногенаGPIIlaL33P T >CTTМетилентетрагидрофолатредуктазаMTllFRA223VC677TC >TCTМетионинсинтаза редуктазаMTRR122MA66GA X?AGМетионинсинтазаMTRD919G2756A >GGGКоагу.гшиионный фактор VTTFVllR353Q G >AGAИнтегрин альфа-2GPUF224F, C807TC >TCTТромбоцитарный гликопрогеин 1ВGP IBA(-5)T>CTTТромбоцитарный гликопротеии 1ВOP IBAT145M482 0TCCР-селектип лиганд гликопротеина (CD 162)SELPLGM621 G >AGGС-реактивный белокGRPC3872T С >TCCЯнус-киназаJAK2V617F G >TGG
518 КардиологияТрикуспидальный клапан: диаметр фиброзного кольца 4 см, регургитаиия ПТ сте¬
пени. Систолическое дашіение в легочной артерии 120 мм рт.сх, время ускорения
потока в легочной артерии 50 мс. Парадоксальное движение межжелудочковой
перегородки. В нижней полой вене определяется тромб на всем протяжении с
флотирующей верхушкой в правом предсердии. На уровне бифуркации легоч¬
ной артерии и в правой ветви также определяется подвижное эхопозитивное
образование (тромб?). В полости перикарда — среднее количество жидкости без
признаков сдавления сердца (около 400 лш), с толщиной слоя 0,7-1,1 см.При рентгенографии органов грудной клетки выявлено снижение воздуш¬
ности легочной ткани сливного характера в нижнем отделе левого легкого,
диффузное усиление легочного рисунка за счет смешанного компонента, сгла¬
женность правого плеврального синуса. Поданным ФВДЖЕЛ 45%, OФBJ 46%,
ОФВ/ФЖЕЛ 85%, Sato, 93%.При МСКТ органов грудной клетки и брюшной полости (канд. мед. наукН.В. Гагарина, рис. 24А на цветной вклейке) — скопление жидкости в обеих
плевральных полостях (до 33 мм слева и до 20 мм справа), перикарде (до
20 мм), брюшной полости, выраженная отечность подкожной жировой клет¬
чатки; субплевральные участки консолидации легочной ткани в сегментах S3,
S6 правого легкого, в S8 левого легкого на фоне участков консолидации — воз¬
душная полость с неровными контурами (28x22x49 мм). Лимфоузлы средосте¬
ния не увеличены. Легочный ствол 37 мм, правая главная ветвь легочной арте¬
рии — 21 мм, левая главная ветвь легочной артерии — 27 мм. В правой главной
ветви легочной артерии определяются тромботические массы, более чем на
60% закрывающие ее просвет, распространяющиеся на верхнедолевую ветвь,
окклюзируя ее от устья, и на промежуточщто, S6, S9 ветви (суживая их на 50%).
Определяется значимое сужение левой главной ветви легочной артерии (более
60-70%), тромботические массы распространяются на нижнедолевую ветвь
(со значимым ее сужением, вероятнее с окклюзией язычковых сегментарных
ветвей), нельзя исключить значимый стеноз сегментарной S8 ветви).- Illг- aVR-V'—'■'-'Г' - Г'--
^ aVL'"Г : aVF..л—1-..-— л__—-А.'-—'V4V5 к ^ —'I-— ^—^-I'¬
veРис. 24,2. Электрокардиограмма больного Г. Скорость записи 25 мм/с. Поясненияв тексте
Глава 24, Успешное лечение массивного тромбоза нижней полой вены,,. 519Рис. 24,3. Эхокардио1раммы больного Г., 23 лет. Верхний ряд — исследоваттие от апреля
2010 i:: слева — выраженное расширение полости правого желудочка со сдавлением
левого, жидкость в полости перикарда (с толщиной слоя 0,7—1,1 см); в центре — выра¬
женное расширение иолости правого предсердия (заштриховано, объем 136 мл) и желу¬
дочка; справа — массивный тромб в просвете расширенной нижней полой вены с фло¬
тирующим >^астком в полости правого предсердия. Нижний ряд — исследование через
3 нед после операции: слева — нормализация размера правою желудочка и 0'і'с>тствие
сдавления левою; в центре — норл<ализаци>і размеров правых камер, выравнивание
объемов левого и правого предсердий (заштріїховани); справа — остаточный плотный
пристеночный тромб в просвете нижней полой вены без признаков флотацииВ правой почке в среднем и верхнем сегментах — участки со сниженной
интенсивностью контрастирования. В нижней полой вене практически на
всем протяжении опреде.тяется тромб (верхняя граница на расстоянии 25 мм от
правого предсердия, нижняя — конфлюэнс подвздошных вен), в супрареналь-
ном отделе тромба имеются участки обызвествления. Участки пристеночноіо
тромбоза также определяются в общих, правой наружной подвздошных венах.
Признаков тромбоза печеночных вен не отмечено,Через месяц в центре лучевой диагностики Лечебно-реабилитационного
центра Росздрава (проф. В.Е. Синицын, канд. мед. наук Е.А. Мершина,
рис. 24.4, см. цветную вклейку) бьша выполнена компьютерная томография
сосудов легких с оценкой легочной перфузии: динамики по сравнению с
данными предыдущей КТ не отмечено, псрфузируемый объем левого легкого
снижен на 32%, правого легкого на 68%; определяются множественные очаги
отсутствия перфузии в верхних и средних долях обоих легких.По данным УЗИ — картина окклюзивного тромбоза нижней полой вены,
пристеночного тромбоза общей и наружной подвздошных вен справа; тром¬
боз глубоких вен правой нижней конечности в стадии реканализации (общая
бедренная, бедренная, глубокая вена бедра, подколенная). Проходимость под¬
кожных вен обеих нижних конечностей, а также глубоких и поверхностных вен
обеих верхних конечностей не нарушена.
520 КардиологияПри ЭГДС — недостаточность кардии, скользящая грыжа пищеводного
отверстия диафрагмы.Таким образом, проведенное в клинике обследование подтвердило наличие
у больного массивного хронического тромбоза — глубоких вен правой нижней
конечности, начиная с подколенной, почечных вен, нижней полой вены на
всем протяжении и обеих легочных артерий от главных до субсегментарных
ветвей с давлением около 120 мм рт.ст. и выраженной дилатацией правых отде¬
лов сердца. Антикоагулянтная терапия не оказывала практически никакого
эффекта, в тромбе нижней полой вены появились признаки кальцинирования.
Естественно, возникал вопрос о причине столь тяжелого поражеііия у молодо¬
го пациента.Для объяснения тромбозов любой локализации предложена теория «двойного
удара». Факторов, которые способствуют формированию тромбов, достаточно
много: беременность, хирургические операции, интеркуррентные инфекции,
стресс, курение, пожилой возраст, малоподвижный образ жизни, артериаль¬
ная гипертония, пероральные контрацептивы, гормональная заместительная
тераиия и др. Травмы стоят среди разрешающих факторов на одном из первых
мест; однако особенно часто они «срабатывают» при наличии генетической
предрасположенности к тромбообразованию либо антифосфолипидных анти¬
тел. У нашего пациента, как уже сказано, выявлены 1 гомозиготная и 5 гетеро¬
зиготных мутаций, потенциально предрасполаїающих к тромбозу, в том числе
полиморфизм СТ в гене метилентетрагидрофолатрсдуктазы: подобный гено¬
тип встречается примерно у 40% жрггелей Европы и обусловливает умеренное
снижение активности ключевого фермента ферментного цикла. Результаюм
обьшно становится повышение уровня гомоцистеина (чего не отмечено у
нашего больного). В то же время уровень фибриногена в повторных анализах
остается у него значительно повышенным (7—9 г/л), что частично связано с
мутацией в гене фибриногена. Одна из мутаций (в гене ингибитора активатора
плазминогена) снижает активность противосвертывающей системы. С другой
стороны, мутаїїия в гене VII фактора снижает активность тромбообразования.
Несмотря на отсутствие гомозиготных мутаций, большое количество полимор¬
физмов в генах свертывания позволяет говорить о генетической тромбофилии у
нашего пациента.Данных за антифосфолипидный синдром не получено: отсутствуют анти¬
тела к фосфолипидам, кардиолипину (мы не имели возможности провести
анализ на антитела к р,-гликопротеидам), отмечен нормальный уровень
АЧТВ при неадекватной антикоагуляитной терапии (что косвенно исключает
нішичие волчаночного антикоагулянта), уровень тромбоцитов никогда не сни¬
жался, отсутствует сетчатое ливедо; кроме того, массивнь[й тромбоз нижней
полой вены при антифосфолипидлом синдроме крайне редок, травму не отно¬
сят к основным факторам риска при данном заболевании; поражение почек
также нетипично (развернутый нефротический синдром, полностью сохранная
функция почек, отсутствие артериальной гипертензии).Среди причин массивного тромбоза нижней полой вены описаны, в перв>то
очередь, опухоли (рак почки, гепатоцеллюляркая карцинома и др.), а также
Глава 24. Успешное лечение массивного тромбоза нижней полой вены... 521различные тромбофилии (генетически обусловленный дефицит протеинов С
или S, лейденская мутация, первичный или вторичный антифосфолипшіньїй
синдром и др.), травма, обострение хронического панкреатита, расслоение
аневризмы брюшной аорты с формированием фистулы и компрессией нижней
полой вены. В ряде случаев причин>^ выявить не удается. Крайне редко встре¬
чаются описания кальцифицированного тромбоза нижней полой вены.Развитие тромбоза нижней полой вены (нередко у молодых людей) вскоре
после тупой травмы весьма характерно и во многих случаях быстро заканчива¬
ется летально в результате массивной ТЭЛА. Наш пациент не только пережил
повторные эпизоды ТЭЛА и постинфарктной пневмонии, но и многие месяцы
жил с резким снижением легочной перфузии и давлением в легочной артерии,
фактически превышающим системное. Нередко описывают повреждение
паренхиматозных органов (печени, поджелудочной железы и др.), которое
предшествовало венозному тромбозу; наш пациент своевременно не обследо-
ва-'їся, в дальнейшем следов такого повреждения выявлено не было.Сочетание тромбоза нижней полой вены с тромбозом почечных вен и
нефротическим синдромом требовало исключения первичного характера
нефропатии, поскольку развитие локального венозного тромбоза является
довольно частым осложнением нефротического синдрома (в том числе идио-
патичсской мембранозной нефропатии) вследствие нескольких факторов;
тромбоцитоза, гиперфибриногенемии, снижения уровня антитромбина III,
повышения уровня протеинов с и S. Изолированный тромбоз печеночных вен
всегда требует исключения нефротического синдрома, хотя может развиваться
и по другим причинам (травма, прием оральных контрацептивов, сдавление
вены извне и др.). У больных с нефротическим синдромом, особенно иолу-
чаюших терапию глюкокортикоидами, описано также развитие массивного
двустороннего тромбоза почечных вен с распространением тромба в нижнюю
полую вену, однако последовательность событий у нашего пациента (травма,
длительные боли в пояснице, отеки ног, симптомы ТЭЛА, стационарное лече¬
ние по поводу «пневмонии» и лишь затем — появление и нарастание лабо¬
раторных признаков нефротического синдрома) делают первичный характер
нефропатии крайне маловероятным; тем не менее развившийся вторично
нефротический синдром мог способствовать профессированию фомбоза.
Если думать о развитии нефропатии в рамках антифосфолипидного синдрома,
то нефротический синдром для нее совершенно не характерен. (Отметим, что
при гипернефромах опухолевый тромбоз нижней полой вены и нефротический
синдром как проявление паранеопластического синдрома могут развиваться
независимо друг от друга.)В то же вре.мя тромбоз почечных вен является одной из хорошо известнь[х
црїічин нефротического синдрома — в таких случаях чаше всего развивается
мембранозная нефропатия, хотя при биопсии может быть выявлена также
картина фокального сегментарного гломерулосклероза и гломерулонефрита с
минимальными изменениями; факторами неблагоприятного тромбоза являют¬
ся мужской пол, возраст старше 50 лет, выраженный нефротический синдром
е цротеинурией более 10 г/сут, артериальная гипертония, раннее повышение
522 Кардиол огияуровня креатинина крови (в первые 3—5 лет), выраженные тубулоинтерсти-
циальные изменения, отсутствие ремиссий (спонтанных или после лечения).
Даже в отсутствие массивной ТЭЛА смертность при этой патологии высока
(11 из 27 пациентов) и связана с геморрагическими осложнениями, сепсисом,
эмболиями; острый тромбоз может сопровождаться развитием фульминантной
почечной недостаточности; в то же время при хроническом тромбозе функция
почек нередко остается совершенно сохранной. При мембранозной нефро¬
патии прогноз в отношении нефропатии существенно лучтпе, чем при др^тих
морфологических вариантах поражения почек, ассоциированных с тромбозом
почечных вен, однако риск тромбоэмболий и в этом случае остается высоким,
что требует оперативного удаления тромбов.У нашего пациента имелись безусловные показания к тромбэктомии как из
нижней полой вены, так и из легочных артерий. Операция тромбэндартерэкто-
мии из легочных артерий при хроншіеской ТЭЛА выполняется в мире с 1962 п
(С. Hufnagel), отработка методики этой операции связана с именем Стюарта
Джемисона (S.W. Jamieson, Сан-Диего, Калифорния), который вместе с кол¬
легами провел около половины из более чем 5000 подобных операций, выпол¬
ненных в мире к настоящему времени. Условием успешной операции является
полноценная эндартерэктомия в пределах меди и.Показаниями к проведению тромбэндартерэктомии при хронической ТЭЛА
(обычно более 6 мес или более 3 мес на фоне активной антикоагулянтной
терапии) являются одышка III-IV ФК или ее значительное нарастание при
нафузках, .легочное сосудистое сопротивление >300 дин. - с > см~\ хирургиче¬
ски доступные тромбы в главной, долевой, сегментарной, субсегментарной
артериях, отсутствие серьезных сопутствующих заболеваний. Единственное
абсолютное противопоказание — серьезная рестриктивная или обструктивная
болезнь легких. С. Джемисон сформулировал принципы успешной хирургии.1. Операция выполняется на обоих легких.2. Основной хир>ргический этап проводится в условиях циркуляторного
ареста.3. Необходимо выполнить тромбоэндаргерэктомию в пределах медии.В Российском нау'шом центре хирургии РАМН им. акад. Б.В. Петровского,
где с 2009 г. успешно начато проведение этих операций, дополнительно сфор¬
мулированы ешс два принципа.4. Имплантация кава-фильтра после удаления тромбов в системе нижней
полой вены.5. Дооперационный скрининг на генетические тромбофилии, антифосфо-
липидный синдром.Удаляется не просто тромб, но фактически слепок легочных артерий
(рис. 24.5, см. цветную вклейку). Подробную информацию о локализации
тромбов дает КТ сосудов легких с реконструкцией, которая является обяза¬
тельным дооперационным исследованием. Хронїпіеская ТЭЛА развивается
не так часто — примерно у 4% больных, перенесших острую ТЭЛА, — но по
степени ре моделирования легочных сосудов она напоминает первичную легоч¬
ную гипертензию; без эндартерэктомии снизить легочное давление у таких
Глава 24. Успешное лечение массивного тромбоза нижней полой вены... 523пациентов невозможно, В центре С. Джемисона операция является достаточно
безопасной; летальность среди 1100 пациентов составила всего 4,7%, причем
были больные старше 80 лет; более чем 100 пациентам одномоментно выпол¬
нено коронарное шунтарование или протезирование клапана (летальность
при этом закономерно росла). Легочное давление более 100 мм рт.ст. также
существенно повышало риск операции (летальность 10,9%), но именно у этих
больных прогноз без операции особенно плохой. К этой категории относится
и наш пациентОписания успешного оперативного лечения массивного тромбоза нижней
полой вены, не связанного с опухолями, немногочисленны. Тромболизис может
оказаться эффективным только при достаточно остром венозном тромбозе.
Чаще применяется открытая операция, но в ряде случаев возможно эндова-
скулярное лечение (стентирование нижней полой вены), при идиопатическом
тромбозе нижней полой вены описан спонтанный регресс в течение 2 мес. Что
касается одномоментной или двухэтапной тромбэктомии из нижней полой
вены, подвздошной, почечной вен и двусторонней тромбэндартерэктомии
из легочных артерий, то аналогичных случаев в доступной литературе найти
не удалось. Встретились лишь описания одномоментного удаления эмбола
из легочной артерии во время операций по поводу лейомиосаркомы нижней
полой вены, забрюшинной саркомы.Больной проконсультирован нефрологами (проф. Е.М. Шиловым иН.Л. Козловской) в клинике терапии и профзаболеваний им. Е.М. Тареева
Первого МГМУ им, И.М. Сеченова: принимая во внимание картину чистого
нефротического синдрома без артериальной гипертонии и нарушения функции
почек у молодого пациента с тромбозом почечных вен, наиболее вероятным
представлялся диагноз мембранозного гломерулонефрита, который требовал
морфологического подтверждения. Наличие множественных полиморфизмов
в генах гемостаза свидетельствовало о наследственной тромбофилии, являю¬
щейся фактором риска рецидивирования тромбозов при тяжелом нефротиче¬
ском синдроме, в связи с этим рекомендовано вернуться к длительной терапии
клексаном 80 мг/сут. Обсуждалась возможность проведения биопсии почки
для уточнения морфологического варианта нефрита и решения вопроса о так¬
тике иммуносупрессивной терапии.Однако в связи с первоочередным значением радикального (хирурги¬
ческого) лечения больной был также проконсультирован директором
Российского научного центра хирургии РАМН им. акад. Б.В. Петровского,
проф, С,Л. Дземешкевичем, который счел возможным проведение двухэтапно¬
го оперативного лечения (тромбэктомия из нижней полой вены с имплантаци¬
ей кава-фильтра и последующая тромбэндартерэктомия из легочных артерий).
В случае успеха можно бьшо рассчитывать и на рефесс нефропатии; во всяком
случае, назначение иммуносупрессивной терапии было отложено на послеопе¬
рационный период.Клинический диагноз был сформулирован следующим образом: пост-
травматический хронический окклюзивный тромбоз нижней полой вены,
подвздошных, почечных (в анамнезе) вен. Тромбоз глубоких вен правой
524 Кардиологиянижней конечности в стадии реканализации. Хроническая массивная дву¬
сторонняя тромбоэмболия легочных артерий. Мультигенная тромбофилия.
Постпневмонический фиброз. Высокая легочная гипертензия. Дыхательная
недостаточность 1—11 степени. Хроническое легочное сердце. Относительная
недостаточность трехстворчатого клапана III степени. Неполная блокада
правой ножки пучка Гиса. Недостаточность кровообращения ІТБ стадии.
Хронический гломерулонефрит нефротического типа с сохранной функцией
почек. Отечный синдром смешанного генеза (застойный, гипоалъбумине-
мический, веноокклюзионный); двусторонний гидроторакс, гидроперикард,
асцит, анасарка. Недостаточность кардии. Скользящая грыжа пищеводного
отверстия диафрагмы-В клинике проводилась терапия клексаном 0,4—0,6 два раза в день в
течение 1 мес с последующим переходом на фенилин 90 мг/с\т (значения
МНО на уровне 2,5-3,5), альбу\тином 10% — 100 ли внутривенно капельно,
верошпироном 50 мг по 1 капе, утром, фуросемидом 40 мг по 1 таб. утром
натощак ежедневно, диувером 10 мг по 1/2 таб. утром, метопрололом 50 мг
по 1/2 таб. \т:ром и вечером, престариумом 5 мг по 1 таб. днем, торвакардом
40 мг по 1 таб. на ночь. В ожидании квоты на операцию в Российском научном
центре хирургии РАМН им. акад. Б.В. Петровского лечение до конца мая про¬
водилось в Факультетской терапевтической клинике им. В.И. Виноградова,
затем — в больнице по месту жительства, затем — до конца июля — снова в
Факультетской терапевтической клинике им. В.Н. Винофадова. Состояние
постепенно ул^^шилось; несколько улсеньшилась одышка, ушла анасарка,
небольшие отеки сохранялись только на ногах (больше справа). Однократно
(в июне) отмечался зпизод усиления одышки, что потребовало увеличенрія
дозы клексана.На госпитализацию в отделение хирургического лечения дисфункций
миокарда и сердечной недостаточности Российского научного центра хирур¬
гии РАМН им. акад. Б.В. Петровского 17.08.2010 г. пациент приехал один,
на электричке. Он достаточно свободно передвигался, продолжал курить и
вьтпіядел относительно здоровым. Тем не менее результаты обследования
оставались прежними, показания к операции — абсолютными, Все это время
пациент ждал операцию с радостью и нетерпением, хорошо понимая, что это
его единственный шанс, и не сомневаясь в успехе. В Российском научном
центре хирургии РАМН им. акад. Б.В. Петровского было принято решение
отказаться от первоначального плана двухэтапной операции и провести ее
одномоментно. 26.08.2010 г. в условиях искусственного кровообращения
и фармакохолодовой кардиоплегии выполнены тромбэктомия из нижней
полой вены, правой подвздошной и левой почечной вен, тромбэндарте-
рэктомия из легочных артерий, ушивание выявленного интраоперационно
дефекта межпредсердной перегородки, установка кава-фильтра ниже места
отхождения правой почечной вены. Время нача.іа операции 09:45, время
окончания 20:15 (продолжительность 10,5 ч), время искусственного крово¬
обращения 296 мин, время ишемии миокарда ПО мин; 1-й циркуляторный
арест (правая легочная артерия) — 21 мин, 2-й циркуляторный арест (левая
Глава 24. Успешное лечение массивного тромбоза нижней полой вены.525легочная артерия) — 22 мин, 3-й циркуляторный арест (тромбэктомия из
нижней полой вены) — 15 мин. Общее время полной остановки кровоо¬
бращения составило 58 мин. Операционная бригада: С.Л. Дземешкевич,В.В. Раскин, А.С. Дземешкевич, Н.А. Трекова, А.А. Еременко, СА. Абугов,А.Б. Степаненко, О.Г. Скипенко,Больной пережил эту операцию, чему в немалой степени способствовал его
возраст. На 2—3-й сутки стало понятно, что полиорганной недостаточности и
неврологических дефектов он избежал. В течение 2 сут он находился на искус¬
ственной аппаратной вентиляции легких, несколько дней проводилась ультра-
фильтрация, позднее потребовалось проведение небулайзерной терапии; был
эпизод болей в животе, но подозрение на рецидив тромбоза не подтвердилось.
Огромный шов заживал без осложнений, признаков кровотечения, несмотря
на постоянную антикоаг>'лянтную терапию (гепарин, затем фенилин), не
было. Сразу после операции больной бросил курить и через 3 нед вернулся в
Факультетскую терапевтическую клинику им. В.Н. Виноградова, где посте¬
пенно расширял физические нагрузки. На рисунке 24.6 представлена схема
операции, нарисованная пациентом со слов хирургов. Эффект радикально
выполненной операции сказался очень быстро.Менее чем через месяц (ЭхоКГ от 20.09.2010 г., проф. В.П. Седов, см.
рис. 24.3, нижний ряд) размеры правых
камер сердца сократились до нормы (пра¬
вый желудочек — с 4,8 до 2,8 см, правое
предсердие — со 136 до 45 мл), исчез шум
трикуспидальной недостаточности, рас¬
правились левые камеры сердца. В ниж¬
ней полой вене определяется лишь оста¬
ток плотного тромба, тесно сросшегося
со стенкой вены. Легочное давление сни¬
зилось со 120 до 40-45 лш рт.ст,, что явля¬
ется главным объективным показателем
эффективности операции. На ЭКГ при¬
знаки перегрузки правых отделов сохра¬
нялись, нарушений ритма по-прежнему
не было.Через 2,5 мес после операции выпол¬
нена контрольная КТ сосудов легких
(Лечебно-реабилитационный центр
Росздрава): тромбы в обеих легочных
артериях практически не определяются
(отмечаются лишь единичные присте¬
ночные тромбы в сегментарных ветвях
справа), значительно у.ттучшилась пер¬
фузия обоих легких. При исследовании
с помощью КТ системы нижней полой
вены дефект контрастирования отмеченЛегкиеСердцеНижняя полая венаПочкиФильтрРис. 24.6. Схема операт^ии (рисунок
пациента)
526Кардиологиятолько на уровне нормально функционирующего кава-фильтра, венозных
тромбозов нетДальше необходимо было оценить динамику нефропатии (после удаления
тромба из нижней полой и левой почечной вен). В раннем послеоперацион¬
ном периоде уровень белка крови (46,6 г/л) и альбумина (27,1 т/л) поднялся
за счет вливаний больших доз альбумина, однако через 3 мес вновь упшт до
исходной величины — обший белок 40,5 г/л, атгьбумин 22,5 г/л. Сохранялись
выраженная диспротеинемия (альбумин 40,6%, а^-глобулин 8,2%, а^-глобулин
32,1%, р-глобулин 12,4%, у-глобулин 6,6%), протеинурия (до 19 г/сут), изме¬
нения мочевого осадка (белок до 8,7%о, лейкоциты 5-7 в поле зрения, эри¬
троциты 8-10 в поле зрения, гиалиновые цилиндры 4 в препарате). Отмечено
значительное (в 3 раза) увеличение скорости клубочковой фильтрации, кото¬
рая достигала 301 мл/мин. Больной был повторно проконсультирован проф.
Е.М. Шихтовым; снова обсуждался вопрос о проведении биопсии почки, но эта
процедура потребовала бы временной отмены антикоагулянтов, поэтому от нее
пришлось отказаться. Рекомендовано дообследование.При динамической сцинтиграфии почек нарушения их накопительно-
выделительной функции не выявлено (рис. 24.7), почки функционируют абсо¬
лютно синхронно. При дутексном сканировании почек с оценкой внутрипочечной
гемодинамики (канд. мед. наук ТВ. Кирсанова) отмечено увеличение размера
правой почки (13,4x4,8 см), выраженный капсулярный кровоток в обеих
почках, а также колебания индекса резистентности на уровне междолевых и
дуговых артерий обеих почек, что может отражать как первичную патологию
(тромботическую микроангиопатию в рамках антифосфолипидного синдро¬
ма), так и вторичные нарушения почечной гемодинамики. Тромбоза почечных
сосудов, как и при КТ, не вьшвлено.С этими данными больной повторно проконсультирован в клинике
им. Е.М. Тареева Первого МГМУ им, И.М. Сеченова (проф. Е.М. Шилов
и проф. Н.Л. Козловская): определены показания к иммуносупрессивной
терапии, которая могла проводиться в двух вариантах — пульс-тераггия пред-
низолоном (по 500 мг 3 дня подряд) и циютофосфаном (800 мг в первый день
введения преднизолона) ежемесячно № 4-6 в сочетании с приемом преднизо-—Левая почка
—Мочевой пузырь-Правая почкаFunctionРис. 24.7, Динамическая нефросцинтиграфия пациента Г. через 3 мес после операции.
Пояснения в тексте
Глава 24. Успешное лечение массивного тромбоза нижней полой вены... 527лона per os в дозе 60 мг/суг либо (что было предпочтительнее) — преднизолон30 мг/сут per os с циклоспорином А в дозе 3 мг/кг, т.е. 200 мг/сут. С 25 ноя¬
бря 2010 г. начата терапия преднизолоном 30 мг/сут. Через месяц пациент
был госпитализирован в отделение нефрологии клиники им. Е.М. Тареева
Первого МГМУ им. И.М. Сеченова, к лечению добавлен циклоспорин А в дозе
200 мг/суг под контролем концентрации сандиммуна в крови (временно потре¬
бовалось увеличение дозы до 300 мг/сут). Фенилин был заменен клексаном0,6x2 раза в день подкожно, проводилась также терапия фомбо-АССом 0,1 по1 таб. вечером, кальцием-ВЗ-никомсд 500 мг 2 раза в день, конкором 5 мг по1 таб. утром и вечером, моноприлом 10 мг по 1 таб. утром и вечером (после
начала терапии глюкокортикоидами отмечены подъемы ДД выше 140/80 мм
рт.ст), торвакардом 20 мг по 1 таб. на ночь, омезом 20 мг по І капе. 2 раза в
день. Переносимость лечения бьша хорошей, пациент отмстил практически
полное отсутствие отеков на ногах. За весь послеоперационный период при¬
бавил в весе около 5 кг (в настоящее время весит 72 кг). С февраля начато сни¬
жение дозы преднизолона на 1/4 таб. в 3 дня до 10 мг/сут.Коммеіггарий С.Л. Дземешкевича — директора Российского научного центра
хирургии РАМН им. акад. Б.В. Петровского, д-ра мед. наук, проф.К кому приходят такие больные? Они приходят к кардиологам — с одышкой,
перефузкой правых отделов, декомпенсацией. Мы эти операции в отделении
кардиомиопатий и сердечной недостаточности рассматриваем как операции
по устранению тяжелой правожелудочковой недостаточности. Традиционное
название этой операции — легочная тромбэндартерэктомия. В Сан-Диего у
С. Джемисона я несколько раз был, видел эти операции. Возник вопрос по
поводу кава-фшштра: это статистика Джемисона. Без фильтра они умирают
чаще. Фильтр закрывает нижнюю полую вену, но бывают еще тромбозы в
системе верхней полой. Я спрашивал у Джемисона, что он делает в таких
случаях. Сделать ничего нельзя. Должна каким-то образом отрабатьшаться
послеоперационная антикоагуляптная терапия, в том числе с применением
новых препаратов. Этот больной — не такой, как другие больные, которьг5с
мы уже оперировали. У него, кроме ТЭЛА, была затромбирована вся систе¬
ма нижней полой вены. Сначала я не представлял, что тут можно сделать.
В решении его оперировать сыграл роль возраст. И еше то, что он был избит.
Наверняка вначале были и гематомы. Таким образом у него проявилась гене¬
тика.Провели стернолапаротомию, огромный разрез. Сразу прішілось убирать
верхнюю часть тромба, который пролабировал не только в правое пред¬
сердие, а чуть ли не через трикуспидальный клапан. Верхнюю часть убрали.
Дшіьше — стандартная операция на легочных артериях. Если упустить часть
тромбов, смысла в операции не будет — можно очистить все центратъные
ветви, а периферия будет забита. Нужна полная остановка кровообращения.
Провели кардиоплегию (остановили сердце), ох-таждали его до 19 °С. Да.'шше
было 20 мин на то, "гтобы разобраться с правым легким. Затем снова запу^-
стили кровообращение, чтобы устранить те повреждения, которые возникли
528 Кардиологияза время остановки. Второй раз остановили сердце (левая легочная артерия).
Обычно сразу появляется ощущение, если все прошло успещно,Но оставалась еще нижняя полая вена. Остановами кровообращение в третий
раз. Мобилизовали печень, вывели вену на всем протяжении, практически от
диафрагмы, вскрыли ее, убрали кальцинированный участок. Очень тщатель¬
но убирали все из почечных вен. Безусловно, необходтіьтм компонентом
операпии стала установка кава-фи.тьтра в нижнюю полуго вену.Комментарии Н.Л. Козловской — профессора кафедры нефрологии и гемодиали¬
за ФППО Первого МГМУ им, И.М. Сеченова, д-ра мед. наукПринимая во внимание тяжесть нефротического синдрома, выражениооъ
гаперкоагуляционных нарушений и обусловленный эти\ш факторами высо¬
кий риск повторных тромбозов у больного с мультигенной громбофилией,
необходимо бьиіо добиться как можно более быстрою к>ттирования нефроти¬
ческого синдрома, в данной ситуации препаратом выбора считается цикло¬
спорин А, который позволяет быстро уменьшить выраженность протеинурии
у пациентов с некоторыми морфологическими вариантами хронического
гломерулонефрита, в том числе и с мембранозным нефритом. В связи с этим
практически сразу был назначен сандиммутї неораї в начальной дозе 2,5 мг/кг
в сутки (200 мг/сут). Через 3 нед лечения протеинурия снизилась до 8,5 г/сут,
уровни общего белка и альбумина крови возросли до 47,6 и 28,5 г/л соответ¬
ственно. Паратле.'Ц>но отмечено снижение скорости клубочковой фильтрации
до 220 мл/мин. Эффективность препарата не вызывала сомнений, однако в
связи с ei’O низкой концетрацией в крови доза бьша повышена до 225 мг/сут.
Одновременно начато снижение поддерживающей дозы преднизолона. Еще
через 3 нед лечения, перед выпиской из клиники в феврале 2011 г, отмече¬
но снижение протеинурии до 4 г/сут, уровень обпіего белка составил 49 г/л,
альбумина — 30 г/л. Отеки по.іностью исчезли, одышка зііачительно умень¬
шилась. Пациент был выписан на амбулаторное лечение с рекомендациями
продолжить прием сандиммзпта в дозе 225 мг/сут, постепенно снижать пред-
низолон до 10 мг/сут, продолжить лечение клексаном в дозе 80 мг/суч.
Наличие у пациента хронического гломерулонефрита дает основания обсуж¬
дать взаимосвязи между нефротическим синдромом и тромбозом почечнььк
вен, которые мог>т быть весьма многообразны. Венозные тромбозы, в перв>то
очередь глубоких вен ГОЛЄ1ІЄЙ, реже — необычных локализаций, в том чітсле
почечных вен, являются наиболее частыми осложнениями нефротическо¬
го синдрома. Частота венозных тромбозов при нефротическом синдроме
составляет 25—35%, а у больных мембранозной нефропатией достигает 60%.
Тромбоз почечных вен развивается примерно у 10% больнъгк с нефроти¬
ческим сиіщромом в целом и более чем у 30% пациентов с мембранозным
нефритом, с другой стороіш, среди причин тромбоза почечных вен на долю
последнего приходится около 60%, хотя его развитие возможно и при других
видах патолопш почек. Билатеральный тромбоз почечных вен, как полага¬
ют, чаще развивается у пациентов с тромбозом нижней полой вены, как это
имело место у нашего больного.
Глава 24. Успешное лечение массивного тромбоза нижней полой вены...529Нарушения в системе
гемокоагуляции•Повышенная концентра¬
ция в плазме крови ф-ра
фон Виллебранда, V, X
и VII факторов свертыва¬
ния• Повышенная вязкость
крови• Г иперфункция тромбоци¬
тов вследствие гипоаль-
буминемии, гиперфибри-
ногенемии, гиперлипиде-
мии• Гиперфибриногенемия• Ускоренная трансформа¬
ция фибриногенав фибрин• Снижение концентрации
антитромбина• Нарушение процессовфибринолизаНСМеханизмы нарушения функцио¬
нальной активности тромбоцитов• Высокая концентрация ф-ра фон
Виллебранда в плазме — усиление
адгезии• Г ипоальбуминемия — ускоренный
метаболизм тромбоцитарных
простагландинов, усиление
агрегации• Г иперфибриногенемия — усиление
агрегации• Г иперлипидемия — усиление
спонтанной агрегации за счет
уменьшения продукции эндотели¬
ем N0 в результате индуцирован¬
ной LDL эндотелиотоксичностиРоль лекарственных препаратов' Глюкокортикостероиды:- повышают концентрацию
некоторых плазменных факторов
свертывания;- укорачивают протромбиновое
время и АЧТВ;- в высоких дозах способствуют
повышению уровня антитромби¬
на и подавлению агрегации
тромбоцитов;■ Диуретики- повышают вязкость крови;- повышают концентрацию
фибриногенаРкс. 24.8, Механизмы развития тромбозов при нефротическом синдромеВ патогенезе іромбозоіз ітри нефротическом синдроме центральные роли игра¬
ют активация прокоагуляптных и депрессия антикоаг>'лянтиых механизмов
(рис, 24.8), Первая характеризуется значительным повытиением >ровня фибри¬
ногена и Х1ІТ фактора свертывания, фактора фон Виллебранда, а также гипер¬
функцией тромбоцитов, зависяш,ей от выраженности гипоальбуминсмии,
гиперфибриногенемии и гиперлипидсмии, вторая — дефицитом антитром¬
бина 111 и других естественных антикоагулянтов (протеины С и S) вследствие
массивной прогеин>'рии и снижением фибринолитической активности крови.
Однако, несмотря на выраженность шперкоагуляционных изменений, не
все они ассоциированы с тромбозами. Факторами риска тромбообразования
ЯШ1ЯЮТСЯ нротеинурия более 10 г/с, гипоа.1ьбуминемия ниже 25 г/л, длитель¬
ность нефрогического синдрома, гиперфибриногенемия, гиповолемия и
уровень антитромбина 111 менее 75%, а также стартиий возраст пациентов.
Однако даже ншшчис большинства из них вряд ли приведет к развитию столь
530 Кардиологиямассивных рецидивирующих венозных тромбозов и эпизодов ТЭЛА, как в
нашем наблюдении, тем более что, по современным представлениям, при¬
обретенные факторы риска рассматриваются скорее не как непосредствен¬
ные причины, а как локальные триггерные механизмы тромбообразования
у пациентов, имеюпиїх предрасположенность к их развитию. Основными
причинами такой предрасположенности являются антифосфолипидный
синдром и генетическая форма тромбофилии.Отсутствие серологических маркеров антифосфолипидного синдрома позво¬
лило нам отвергнугь этот диагноз, однако у нашего больного были выявлены
множественные мугации генов гемостаза, представленные 1 гомозиготным и6 гетерозиготными полиморфизмами. Сегодня установлено, что у пациентов
с наследственной тромбофилисй тромбозы часто обусловлены сочетанием
нескольких генных полиморфизмов системы гемостаза. При этом гомози¬
готные мутации или сочетание двух и более гетерозиготных полиморфизмов
(мультигенная тромбофилия), как правило, приводят к развитию тромбозов в
молодом возрасте (менее 50 лет) и ассоциированы со сютонностью к рециди¬
вам, что мы и наблюдали у нашего больного. Можно преднолагагь, что разви¬
тие у него столь распространенных тромбозов было обусловлено сочетанием
т енетической тромбофилии и приобретенных нарушений в механизмах свер-
тьшания крови, свойственных нефротическому синдрому Представленное
наблюдение подтверждает данные R.M. Bertina, свидетельствующие о том,
что 50% тромбозов любых локализаций у пациентов с наследственной іром-
бофилией ассоциировано с наличием не менее одного приобрегенного фак¬
тора риска, к которым у нашего пациента относятся тяжелая травма и нефро-
1ИЧЄСКИЙ синдром с протеинурией, достигавшей 19 г/сут, уровнем альбумина
менее 20 г/л, выраженной гиперфибриногенемией.Характер течения болезни у нашего пациента ставит вопрос о причинно-
следственных связях между тромбозом почечных вен и нефротическим син¬
дромом. До настоящего времени этот вопрос не решен. Хотя в большигнстве
слу^іаев тромбоз почечных вен осложняет нефротический синдром, однако
существует точка зрения, что он является не причиной, а следствием тромбо¬
за, поскольку, как было продемонсфировано в эксперименте iia животных,
длительная окклюзия почечных вен может привести к развитию протеину-
рии. Сегодня считается, что единственным видом патологии почек, который,
по-видимому, может развиться у больных с двусторонним тромбозом почеч¬
ных вен, является мембранозная нефропатия, однако механизм их взаимос¬
вязи требует уточнения.в нашем наблюдении морфологическая верификация диагноза оказалась
невозможной, в связи с чем утверждать, что пациент страдает мембранозным
гломерулонефритом, голько на основании распространенных тромботиче¬
ских ос;южнений и тяжести нефротиггеского синдрома было бы опрометчи¬
во, поскольку сходный вариант течения, в том числе и развитие тромбозов,
отмечается при болезни минимальных изменений и фокально-сегментарном
гломерулосклерозе, включая быстрый ответ на циклоспорин. Нам представ¬
ляется, что у молодого пацисііта с мультигенной тромбофилией, возможно.
Глава 24. Успешное лечение массивного тромбоза нижней полой вены... 53 Ідостаточно долго имелся латентный гломерулонефрит, ничем себя не про¬
являвший до момента тяжелой тупой травмы поясницы, которая могла стать
не только пусковым механизмом первого тромботического эпизода, но и
причиной обострения болезни, проявившегося формированием нефротиче¬
ского синдрома. Последний, в свою очередь, усугубил гиперкоахуляционныс
изменения гемостаза, послужившие причиной рецидивирования тромбооб-
разования в системе нижней полой вены.До купирования нефротического синдрома, несмотря на лечение антикоагу¬
лянтами, сохраняется высокий риск рецидива тромбозов, причем не только
венозных, но и артериальных. Разорвать этот порочный круг может лишь
ремиссия нефротического синдрома в результате адекватной иммуносупрес-
сивной терапии. По крайней мере до ее достижения пациент нуждается в
продолжении антикоагулянтной терапии низкомолекулярными гепаринами,
тем более что e\fy имплантирован кава-фильтр, поскольку у больных с нефро¬
тическим синдромом применение варфарина увеличивает риск геморрагиче¬
ских осложнений.Комментарий В.А. Сулимова — заведующего кафедрой факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наук,
проф.Таким образом, в представленном наблюдении развитие массивного хро¬
нического сосудистого тромбоза у пациента 23 лет обусловлено сочетанием
генетических дефектов, предрасполагаюшцх к тромбообразованию, и много-
^шсленных приобретенных факторов риска, которые реализовались после
тяжелой тупой травмы поясницы.Рецидивированию тромбоза с практически полной окклюзией системы
нижней полой вены и хронической массивной двусторонней ТЭЛА способ¬
ствовали поздняя диагностика, длительное отсутствие адекватной антикоагу¬
лянтной терапии и тяжелый нефротический синдром как проявление хрони¬
ческого гломерулонефрита с характерными для него гиперкоахуляционными
нарушениями.Развитие лего^гной гипертензии и хронического легочного сердца, угро¬
жающих жизни больного, стало поводом для обращения к кардиологам.
Изменить крайне неблагоприятный прогноз позволила уникальная одно¬
моментная операция радикальной іромбзктомии, успешно выполненная
кардиохирургами в Российском научном центре хирургии РАМН им. акад.
Б,В. Петровского.Сочетание иммуносупрессивной и антикоагулянтной терапии, начатой после
операции нефрологами, направлено на достижение ремиссии хронической
почечной недостаточности. Купирование нефротического синдрома должно
привести к нормализации гемокоагуляїдионного потенциала крови и, таким
образом, устранить имеющиеся факторы риска рецидивирования тромбозов.
Мы обсудили уникальную клиническую ситуацию. Это наблюдение уни¬
кально не только тем, что подобные одномоментные операции нигде в мире
не выполнялись (во всяком слу^гае, публикаций об этом в литературе нет),
532 Кардиологияно и тем, что оно продемонстррфовало, насколько важен в современной
медицине мультидисииплинарный подход. Только ИНТефНЦИЯ УСИ-ТШЙ врачей
различных специальностей, участие специалистов самого разного профиля
(клшіические кардиологи, специалисты в области лучевой диагностики,
кардиохирурги, нефрологи) делает возможным успепшое лечение подобных
крайне тяжелых пациентов.ЛИТЕРАТУРАНефрология. Руководство для врачей / Под ред. И.Е. Тареевой. — 2-е изд.,
персраб. и доп. — М., 2000. — 688 с.Anand N.K., Chand С., Talib V.H. et al. Hemostatic profile in nephrotic syndro¬
me 11 Indian Pediatr. 1996; 33 (12): 1005-1012.Beilomo K, Afkim R.C Membranous nephropathy and thromboembolism: Is pro¬
phylactic anticoagulation warranted? // Nephron. 1993; 6 (3): 249—254.Benina R.M. Genetic approach to thrombophilia // Thromb, Haemost. 2001; 86;92-99.Cagnoli L., Viglietta G., Madia G. et al. Acute bilateral renal vein thrombosis super¬
imposed on calcified thrombus of the inferior vena cava in a patient with membranous
lupus nephritis // Nephrol. Dial. Transplant. 1990; 5 Suppl 1; 71-74.Chikaraishi Т., Kobayashi S., Harada H. et al. Idiopathic and spontaneously
regressing thrombus in right renal vein and inferior vena cava // Int. J. Urol. 1997; 4
(1): 83-85.Crew R.J., Radhakrishnan S., Appel G. Complications of nephrotic syndrome
and their treatment // Clin. Nephrol. 2004; 62: 245—251$; Oxlord Textbook of
Clinical Nephrology 3rd ed. / Ed. by A,M. Davison, S.J. Cameron, J.P Grunfeld,C. Ponticelli, E. Ritz, C. Wmearls, C. Ypersele. — Oxford University Press, 2005.Funami М., Takaba Т., Tanaka H. etal. Treatment of renal vein thrombosis associ¬
ated with nephrotic syndrome [Article in Japanese] j j Nippon Geka Gakkai Zasshi.
1988; 89 (6): 952-956.Ikeda D., Kohashi K. Bilateral renal vein thrombosis extending into the inferior
vena cava associated with nephrotic syndrome: a case report [Article in Japanese] //
Hinyokika Kiyo. 1998; 44 (4): 277-279.Janda , Zdbrodsky V., Spatenka J., Тйта S. Thrombosis of the inferior vena
cava with successive lung embolization in a 15-year-old boy with nephrotic syndrome
[Article in German] j j Padiatr. Padol. 1986; 21 (1): 69—74.Kau E., Patel R., Fiske J., Shah 0. Isolated renal vein thrombosis after blunt trau¬
ma 11 Urology 2004; 64 (4): 807-808.Kimoto Т., Kohno H., Uchida M. et al. Inferior vena caval thrombosis after trau¬
matic liver injury // HPB Surg. 1998; 11 (2): 111—116.Kriiger Т., Mustafi M., Nadalin S.,AebertH, Vena cava sarcoma with tumor embolus in
the puknonary artery: sui^ical treatment //Ann. Thorac. Surg. 2010; 90 (2): 642-644.Lane D.A., Mannucci P.M., Bauer K.A. et al. Inherited thrombophilia. Part 1 //
Thromb Haemost. 1996; 76: 651-662,
Глава 24. Успешное лечение массивного тромбоза нижней полой вены... 533Laville М,, Aguilera D., Maillet PJ. et al. The prognosis of renal vein thrombosis: a
re-evaluation of 27 cases //Nephrol. Dial. Transplant, 1988; 3 (3): 247—256.Lin H. H., Hsieh C.B., Chu H.C. et al. Acute pulmonary embolism as the first mani¬
festation of hepatocellular carcinoma complicated with tumor thrombi in the inferior
vena cava: surgery or not? // Dig. Dis. Sci. 2007; 52 (6): 1554-1557.Llach F. Hypercoagulability, renal vein thrombosis and other thrombotic complica¬
tions of nephrotic syndrome // Kidney Tnt. 1985; 28: 429-436.Louis C.U., Mof'genstern B.Z., Bufani L. Thrombotic complications in childhood-
onset idiopathic membranous nephropathy // Pediatr. Nephrol. 2003; 18 (12):
1298-1300.Mahmoodi B.K., Ten Kate M.K., Waanders F. et al. High absolute risks and pre¬
dictors of venous and arterial thromboembolic events in patients with nephrotic
syndrome. Results from a large retrospective cohort study // Circulation. 2008; 117:
224-230.Mayzlik J., ProchdzJca V,, Michahky R., Docekal B. Surgical treatment of post-
traumatic thrombosis of the inferior vena cava [Article in Czech] // Rozhl. Chir. 1992;
71 (1): 43-46.Ohno A., Hayashida K., Matsuo H., Nishimura T. Inferior vena cava occlusion with
pulmonary embolism because of complications due to ruptured abdominal aneu¬
rysm demonstrated by radionuchde venography // Clin. Nucl. Med. 1995; 20 (5):
436-439.Ohta H., Hachiya T. A case of mferior vena cava thrombosis and pulmonary embo¬
lism secondary to acute exacerbation of chronic pancreatitis; a rare finding in radio¬
nuclide venography //Ann. Nucl. Med. 2002; 16 (2): 147-149.Ohwada S., Ishikawa iS”., Kawashima Y, et al. Intraoperative massive pulmonar>'
tumor embolism from clear cell sarcoma in the retropcritoneum: successful treat¬
ment using cardiopulmonary bypass // Hepatogastroenterology. 2004; 51 (58):
987-989.Orth S,R., Ritz E. The nephrotic syndrome // N. Eng, J. Med. 1998; 338: 1202-
1211.Poliak V.E., Weiss M.A. Renal vein thrombosis // Renal pathology with clinical and
functional correlations / Ed. by C.C. Tisher and B.M.Brenner, — Philadelphia; J,B.
Lippincott Comp., 1994. - Vol. Tl. - Ch. 37. - R 1185-1200,Rabelink T.J., Zwaginga J.J., Koomans H.F. et al. Thrombosis and hemostasis in
renal disease // Kidney Int. 1994; 46: 287-296.Robert A., OlmerM., SampolJ. etal. Clinical correlation between hypercoagulabil¬
ity and thrombo-embolic phenomena 11 Kidney Tnt. 1994; 45: 578-585.Roubey R.A.S. Mechanisms of autoantibody-mediated thrombosis // Lupus. 1998;
7: S114-S119.Takeuchi М., Maniyama K., Nakamura M. et al. Posttraumatic inferior vena
caval thrombosis: case report and review of the literature // J. Trauma. 1995; 39 (3):
605-608.Thistlethwaite P.A., Kaneko K., Modoni M.M., Jamieson S.W. Technique and out¬
comes of pulmonary^ endarterectomy surgery // Ann. Thorac. Cardiovasc. Surg. 2008;
14 (5): 274-282.
534 КардиологияThompson С.S., Cohen M.J., Wesley J.M. Endovascular treatment of obliterative
hepatocavopathy with inferior vena cava occlusion and renal vein thrombosis // J.
Vase. Surg. 2006; 44 (1): 206-209.Tsuji K, Goto A., Hara L et al. Renal cell carcinoma with extension of tumor
thrombus into the vena cava: surgical strategy and prognosis // J. Vase. Surg. 2001; 33(4): 789-796.Ushijima Т., Yachi Т., Nishida Y. Successful surgical treatment of chronic inferior
vena caval thrombosis following blunt trauma // Gen. Thorac. Cardiovasc. Surg. 2007;
55 (6): 255-258.Wack C, Wolfle K.D., Loeprecht H. Early and late results of transperitoneal
thrombectomy in thrombosis of the inferior vena cava [Article in German] //
Zentralbl. Chir. 2001; 126 (6): 456-460.
СИСТЕМНЫЕ ЗАБОЛЕВАНИЯГЛАВА 25ТЯЖЕЛАЯ ЛЕГОЧНАЯ ГИПЕРТЕНЗИЯ
КАК РЕЗУЛЬТАТ СОЧЕТАНИЯ ДВУХ РЕДКИХ
ЗАБОЛЕВАНИЙ: СИСТЕМНОЙ СКЛЕРОДЕРМИИ
И САРКОИДОЗАН.Д. Саркисова, О.В. Благова, А.В, НедоступЛегочная гипертензия осложняет многие заболевания сердца и легких —
причины ее, как правило, достаточно очевидны, а степень чаше умеренная.
В данном случае мы столкнулись с исключительно высокой легочной гипер¬
тонией, которая определяла тяжесть состояния больной и причины которой
оставались неясньши, несмотря на установленный характер основного забо¬
левания. Постановка точного диагноза второй болезни имела принципиальное
значение ДЛЯ выбора лечебной тактики — это стало основанием для проведе¬
ния инвазивного обследования, которое, к сожалению, больная не перенесла.
Обсуждается крайне непростой вопрос соотношєііия возможного риска и
пользы проведенного диагностического вмеїиательства в данной клинической
ситуации.Больная Ю., 54 года, поступила в отделение кардиологии Факультетской
терапевтической клиники им. В.Н. Виноградова 06.02.2008 г с жалобами на
выраженную одышку, возникающую при незначительной физической нагруз¬
ке (при ходьбе менее 100 м, подъеме на один этаж) и постепенно стихающую
в покое, периодический сухой кашель, боли в области сердца, возникаюшие
как в покое, так и при незначительной физической нагрузке, иррадиирующис
Б левое плечо, лопатку, длящиеся менее 15 мин, купирующиеся приемом кор¬
валола; головные боли, головокружения, мушки перед глазами, в основном
при повышении АД до 160/100 мм рт.ст. (при обычном АД 120-130/80-90 мм
рт.ст.), практически постоянное онемение пальцев рук и ног, периодически
возникаюшие болезненные язвы на коже конпевых фаланг пальцев рук,
сухость во рту, невозможность употребления сухой пищи, отсутствие аппетита,
снижение массы тела на И кг за последние 6-7 мес.Из семейного анамнеза известно; отец умер в 78 лет от сердечной недостаточ¬
ности, мать — в 75 лет от инсульта, старший брат — в 43 года от инфаркта мио¬
карда, младший лечшіся по поводу туберкулемы верхней доли правого легкого.
Вдова. Старший сын 34 лет страдает атопическим дерматитом, младший 29 лет
536Системные заболеванияпрактически здоров. Родилась и живет в Московской области. Работала фель¬
дшером в психиатрическом стационаре, имела контакт с больными туберкуле¬
зом, с 2007 г. инвалид II і^зупиьі. Вредных привычек не имеет. 4 беременности,2 родов (оба ребенка родились с гипотрофией), 1 аборт, 1 внематочная бсрсмсн-
ность, в возрасте 31 года — киста левого яичника; при осмотре гинекологом в
2007 г. патологии не выявлено. В 42 года — холецистэктомия по поводу желчно¬
каменной болезни. В 1985 г. однократный эпизод гипергликемии (до 200 мг%)
на фоне психоэмоциональной перегрузки (смерть мужа) с последующей стой¬
кой нормализацией уровня глюкозы. В 2007 г гликозилированный НЬ 5,7%,
выявлена умеренная гипергликемия. Состояние расценено как сахарный диабет
2-го типа. Лечение не проводилось. В 2005 г выявлен умеренный первичный
гипотиреоз (субклинический), принимает L-тироксин 50 мкг/сут. В анамнезе
отмечалась аллергическая реакция на антибиотик (какой — неизвестно).Анамнез заболевания (рис. 25.]): в возрасте 29 лет (после вторых родов) впер¬
вые появилась резкая боль в концевых фалангах второго и третьего пальцев
левой кисти, которая сопровождалась побледнением кожи, сменившимся
цианозом, интенсивной бол ью. При обращении к врачу бьшо высказано пред¬
положение о синдроме Рейно. Проводились курсы лечения препаратами нико¬
тиновой кислоты с некоторым эффектом. В дальнейшем указанные симптомы
распространились на обе кисти, отмечались атрофические изменения конце¬
вых фаланг кистей рук с деформацией ногтей, уплотнением кожи, развитием
цианоза и онемения концевых пальцев рук. Периодически на коже тьыьной
поверхности концевых фаланг кистей рук появлялись небольшие язвы, про¬
ходящие самостоятельно. К врачам не обращалась, продолжала работать.1982 г.
(29 лет)конец
1980-х гг.весна
2006 г.май
2007 г.февраль
2008 г.Синдром РейноАртериальнаягипертензияОдышкаСухой кашель
Похудение
Анализы крови
ТерапияНикотиноваякислотаЭналаприлАНФ,цикТ
креатинин NЭналаприл,кораксан,рибоксин,милдронатРве. 25.1. Анамнез больной Ю., 54 года
Глава 25. Тяжелая легочная гипертензия как результат сочетания... 537Около 20 лет отмечаются подъемы АД до 160/ J 00 мм рт.ст. при обычном АД
120-130/80-90 мм рт.ст. Эпизодически при подъемах АД принимала гипотен¬
зивные препараты. Систематического котроля и гипотензивной терапии не
проводилось. В дальнейшем стали отмечаться нечастые боли в левой половине
грудной клетки разнообразного характера, длительные, ноюшие, колюш,ие,
давящие, возникавшие без четкой связи с физической нагрузкой, проходившие
самостоятельно или после приема корвалола. Иногда беспокоили перебои в
работе сердца.В 2006 г. без видимой причины появилась и стала нарастать одышка,
несколько позже появился сухой кашель. В мае 2007 г. в связи с появлени¬
ем сухого кашля, нарастанием одышки, ухудшением общего самочувствия,
похуданием была госпитализирована в кардиопульмонологическое отделение
МОНИКИ, где проведено тщательное обследование. Среди лабораторных
показателей обращали на себя внимание повышение уровня ЦИК (0,137 при
норме 0,035-0,04) и положительная реакция на АНФ. На серии ЭКГ (от апре.тя,
июня и июля 2007 г., рис. 25.2, 25.3) отмечались признаки постепенно нарас¬
тающей перегрузки правых камер сердца и поворот электрической оси сердца
вправо.При ЭхоКГ были выявлены выраженная легочная гипертензия (70—80 мм
рт.ст.), расширение правых камер сердца (предсердие 4,6 см, желудочек 3,6 см)
и гипертрофия правого желудочка (тПЖ 7мм), трикуспидальная регургитация.
В первую очередь проводилось исключение тромбоэмболии ветвей легочной
артерии (ТЭЛА) ~ при выполнении КТ легких с внутривенны.м контрасти¬
рованием существенных изменений легочной ткани не выявлено. Отмечалосьї/«ЯКо : ..ti) J(3/ ^ ^тт‘V >' ‘Рис. 25.2. ЭКГ больной Ю. от апреля 2007 г Пояснения в тексте
538Системные заболеванияJxl'fliiilili ^....ШіШшшШшШш&тїіІІііІЇІ*; Д:;.:.:.;;Г«7я нм/Ли...:.:«р^»г'ИЩїі№Мі
їйіРис. 25.3. чЭКГ больной Ю. от июля 2007 г. Пояснения в текстеумеренное увеличение внутригрудных лимфоузлов от 5—9 до 10—12 мм, данных
за ТЭЛА получено не было. Кроме того, отмечалось резкое снижение диффу¬
зионной способности легких. Был поставлен следующий диагноз: гипертони¬
ческая болезнь II стадии. Хроническая сердечная недостаточность II функ¬
ционального класса (NYHA). Варикозная болезнь вен нижних конечностей.
Сахарный диабет 2-го типа, впервые выявленный. Первичный гипотиреоз
средней тяжести в фазе медикаментозной компенсации. Рубромикоз гладкой
кожи и ногтей. Астсноневротическое состояние с вегсгативно-сосудисгыми
пароксизмами. Болезнь Рейно.Проводилась терапия аспирином, энапом, рибоксином, кораксаном, детра-
лексом, L-тироксином 50 мкг/сут с незначительным субъективным эффектом.В.месте с тем обсуждалось наличие у больной системного заболевания соеди¬
нительной ткани, в частности склеродермии, системной красной волчанки.
В связи с этим проводилась биопсия слизистой оболочки десны, однако пунк-
тат бьы неинформативен, специфических изменений вьывлено не было. После
выписки из МОНИКИ в июне 2007 г. у больной продолжала нарастать одышка,
усилились кашель, сухость во рту, сухость кожи, по-прежнему отсутствовал
аппетит, отмечалось похудание в общей сложности на 14 кг, резко снизилась
переносимость физических нагрузок. Для обследования с целью уточнения
диагноза и лечения поступила в Факультетскую терапевтическую клинику
им. В.Н. Виноградова.
Глава 25. Тяжелая легочная гипертензия как результат сочетания,., 539При осмотре', общее состояние средней тяжести, температура тела 36,7 "С.
Конституция астеническая. Кожные покровы бледные, сухие, тургор резко
снижен, кожа пальцев шчогная, холодная, со следами небольших язв, выражен¬
ный акроцианоз, выраженный сосудистый рисунок на руках. Пальцы рук пол¬
ностью не разгибаются {рис. 25.4, см. цветную вклейку). На коже лица — теле-
ангиэктазии. Начаїьньїе признаки симптома кисета. Отеков нет. Лимфоузлы
не увеличены. Скелетные мышды гипотрофичны, безболезненны. Уменьшена
длина концевых фаланг пальцев рук. Сколиоз грудного отдела позвоночника.
Частота дыханий 20/мин. Перкуторный звук легочный, аускультативно дыха¬
ние симметрично ослаблено, хрипов нет. Определяется сердечный толчок.
Тоны сердца звучные, акцент П тона над легочной артерией, шумов нет. ЧСС
76/мин, АД 140/90 мм рт.ст. Живот мягкий, безболезненный при пальпации.
Печень, селезенка не увеличены. Щитовидная железа не увеличена,В общем анализе крови эритроциты 5,7 млн, НЬ 161,6 г/л, цветовой показатель0,84, лейкоциты 9,9 тыс., нейтрофилы 66,6%, лимфоциты 25,3%, моноциты
6,3%, эозинофилы 1,4%, базофилы 0,4%, тромбоциты 239 тыс., СОЭ 6 мм/ч.^биохимическом анализе от 07.02.2008 г: общий белок 65,6 г/л, альбу¬
мин 38,6 г/л, креатинин 1,7 мг/дл, глюкоза 7,2 ммоль/л, азот мочевины9,1 ммоль/л, мочевая кислота 246,1 мкмоль/л, общий билирубин 18,6 ммоль/л,
у-ГТ 170 Ед/л, ACT 38 Ед/л, АЛТ 62 Ед/л, холинэстераза 5679 Ед/л, щелоч¬
ная фосфатаза 537 Ед/л, натрий 141 мэкв/л, калий 5,2 мэкв/л, кальций
10,3 мг/дл, ЛДГ 602 Ед/л, КФК43 Ед/л, МВ-КФК 29 Ед/л, триглицериды159 мг/дл, общий холестерин 178 мг/дл, ЛПВП-хс 37 мг/дл, ЛПНП-хс
109,2 мг/дл, ЛПОНП-хс 31,8 мг/дл, КА 3,81.В анализе от 11.03.2008 г.; креатинин 1,9 мг/дл, глюкоза 6,7 ммоль/л, азот
мочевины 14,8 ммоль/л, у-ГТ 259 Ед/л, ACT 61 Ед/л, АЛТ 94 Ед/л, щелочная
фосфатаза 549 Ед/л,Электрофорез белков: альбумин 51,6%, 4,5%, 12,2%, р 14,3%, у 17,4%.
Гтиколизированный НЬ 6,6%.Коагулограмма: АЧТВ 0,92, протромбиновый индекс 91%, фибриноген
3,76 г/л.HBjAg отрицательный, HCVAb положительны. Комплекс серологических
реакций на сифилис отрицательный, Гормоны щитовидной железы в пределах
нормы.СРВ 0,45 мг/дл, РФ (качественная реакция) и анти-О-стрептолизин отри¬
цательны, комплемент 36 гем. ед. (20-40), антитела к натуральной ДНК (каче¬
ственная реакция) отрицательны, cANCA (антитела к протеиназе 3) 1,3 Ед/мл
(0-5), pANCA 3,95 Ед/мл (0—5), антитела к кардиолипину не выявлены. IgA160 мг/дл, IgM 140 мг/лд, IgG 1220 мг/дл.Было выполнено дополнительное иммунологическое исследование в Институте
ревматологии: криоглобулины 1+, реакция на АНФ положительная, ЦИК 275 Ед,
АНФ-Нер 1:320 SP, Анти-РНП +, антитела к Scl-70 — слабо положительны.В общем анализе мочи: pH 5, удельный вес 1006, прозрачность полная, белка,
сахара, ацетона, желчных пигментов нет, уробилин в норме, эпителиальные
клетки плоские в умеренном количестве, лейкоциты единичны в поле зрения,
540Системные заболеванияэритроциты единичны в поле зрения, оксалатов немного, слизи немного, бак¬
терий немного. Проба Реберга: креатинин крови 1,7 мг/дл, креатинин мочи44,5 мг/дл, концентрационный индекс 26,3, суточный диурез 1400 мл, мини¬
мальный диурез 0,97 мл/мин, фильтрация 26 мл/мин (на фоне терапии верош-
пироном), реабсорбция 96,2%. Исследование мочи по Нечипоренко: количество
мочи 110 мл, pH 5, следы белка, лейкоцитов 7750, эритроцитов 500.На ЭКГ (рис. 25.5) — сиртусовый ритм, неполная блокада правой ножки
пучка Гиса. ЭОС резко отклонена вправо, ЧСС 90/мин. P-pulmonale, выра¬
женные признаки гипертрофии перегрузки правого желудочка (зубец S в отве¬
дении V5 20 мм). PQ 0,14 с, QRS 0,09 с. Зубец Т отрицателен в Признаков
ишемии, гипертрофии левых отделов сердца нет.При суточном мониторировании ЭКГ по Холтеру — синусовый ритм.
ЧСС днем 61-105/мин (ср. ~80/мин), ночью 57-91/мин (ср. ~65/мин).
Суправентрикулярные экстрасистолы (~30). К>ттлет (1), желудочковые экстра¬
систолы (5), триплет (1). ST-T: без диагностически значимой динамики.При ЭхоКГ, выполненной профессором В.П. Седовым, аорта уплотнена,
не расширена, 3,2 см. Левое предсердие 2,9 см (норма до 4 см). Левый желу¬
дочек не расширен, КДР 3 см (норма до 5,6 см), МЖП 1 см, ЗСЛЖ 1 см (до1,1 см). Локальная сократимость не нарушена. Правый желудочек расширен,
ПЗР 4,5 см, тПЖ 1,2 см (рис. 25.6). Правое предсердие расширено. Аортальный
клапан уплотнен, амплитуда раскрытия не уменьшена, 1,9 см (норма >1,5 см),
регургитации нет, стеноза нет. Митральный клапан; створки не уплотнены,
регургитация 0—1 степени. Трикуспидальный клапан: створки уплотнены, под¬
вижность створок не ограничена, регургитация ПТ степени. Легочный клапан:
скорость кровотока 47 см/с, регургитация 0—1 степени. Признаки легочнойbVLРис. 25.5. ЭКГ больной Ю. or февраля 2007 г. Пояснения в тексте
Глава 25. Тяжелая легочная гипертензия как результат сочетания.., 541Рис. 25.6. Эхокардиограмма больной Ю,: 1, 2 — ветви легочной артерии; 3 — легочный
ствол. Пояснения в текстегипертензии: систолическое давление в легочной артерии 110 мм рт.ст. Нижняя
полая вена расширена, на вдохе спадается <50%.Сделано заключение о наличии выраженной дилатащш правых камер сердца,
гипертрофии правого желудочка с парадоксальным движением межжелудочковой
перегородки, тяжелой трикуспидатьной регургитации, признаков тяжелой легоч¬
ной гипертензии, в полости перикарда определяется небольшое количество жид¬
кости (до 200 мл). При отсутствии убедительных признаков врожденного порока
сердца легочная гипертензия может быть обусловлена первичным поражением
легочных сосудов, с це.їїью исключения дефекта межпредсердной перегородки
как причины перегрузки правых отделов сердца была выполнена чресшщеводная
Эхо КГ: определяется непрерывность межпредсердной перегородки. При допил е-
рографическом исследовании признаков межпредсердного шунтирования не
выявлено. При внутривенном введении 0,9% раствора NaCl произведено контра¬
стирование правого предсердия без признаков межпредсердного шунтирования.По данным исследования ФВД\ ЖЕЛ 2520 мл (77%). ОФВ^ 1898 (73%, после
ингаляции агровента 81%, МОС^з 113% (144%), МОС^, 58% (78%), МОС,^ 23%
(33%), ОФВ,/ФЖЕЛ 73% (76%), сатурация кислородом 88%. Бронхиальная
обструкция умеренно выражена. Реакция на атровент положительная.
Вентиляционные нарушения смешанного типа. Диффузионная способность лег¬
ких: 1,9 ммоль/кПа-мин. (21% от нop^шI), 1,9 ммоль/кПа-мин (21% от
нормы), D,^q/VA 0,80 (20% от нормы). Показатели оксигенации крови, изме¬
ренные методом пульсоксиметрии в покое, снижены, SpO, 86-88%.По данным рентгенографии органов грудной клетки (рис. 25.7): легкие без
свежих очаговых и инфильтративных изменений. Корни легких расширены за
счет ветвей легочных артерий, уплотнены, в прикорневых отделах несколько
усилен сосудистый рисунок. Диафрагма расположена обычно. Плевральные
синусы свободны. Сердце увеличено в размерах, расширено в основном влево,
аорта угиотнена, дуга аорты фрагментарно обызвествлена.
542 Системные заболеванияТаким образом, клиническая картина заболевания (в первую очередь пора¬
жение кожи по тапу склеродактилии в сочетании с синдромом Рейно) позволя¬
ла думать о наличии у больной системной склеродермии. В то же время выра¬
женность легочной гипертензии, которая сама по себе достаточно типична для
указанного заболевания, представлялась необычной. Больная была прокон¬
сультирована заведующей отделением патологии суставов и соединительной
ткани Факультетской терапевтической клиники Н.В. Петуховой: с наибольшей
вероятностью можно думать о наличии у больной склеродермии хронического
течения с поражением сосудов (синдром Рейно), кожи, почек с формирова¬
нием начальных признаков почечной недостаточности, возможно легких. Для
уточнения диагноза целесообразно проведение анализа крови на специфиче¬
ские антитела, рентгенографии кистей, КТ органов грудной клетки.При проведении МСКТ органов грудной клетки (рис. 25.8) в нижней доле
правого легкого в S6 и на костальной плевре на уровне средней доли визуа¬
лизируются два очага по 5 мм. В нижней доле левого легкого в S10 имеется
аналогичный очаг размером 6 мм. Прослеживаются просветы бронхов до
сегментарных разветвлений, стенки их уплотнены. Листки плевры тонкие,
жидкости в плевральных полостях не определяется. Структуры средостения и
корней легких дифференцированы. Визуализируются множественные лимфа¬
тические узлы верхней и нижней паратрахеальных групп размером до 5—6 мм,
конгломераты лимфоузлов на уровне аорто-пульмонального окна (до 27 мм).
Диаметр ствола легочной артерии 37 мм, правая ЛА — 24 мм, левая ЛА — 25 мм.
В перикарде жидкость с толщиной слоя до 17 мм. Заключение: очаговые обра¬
зования правого легкого. Медиастинальная лимфаденопатия. Гидроперикард.
Признаки легочной гипертензии. КТ-картина может быть обусловлена систем¬
ным процессом (системная склеродермия?).По данным УЗИ органов брюшной полости, печень и се лезенка не увеличены,
почки обычно расположены, нормальных размеров, с достаточно ровными
контурами, дилатапии чашечно-лоханочной системы и теней конкрементов не
выявлено, паренхима до 10-11 мм.Рис. 25.7, Рентгенография органов грудной клетки больной Ю. Пояснения в тексте
Глава 25. Тяжелая легочная гипертензия как результат сочетания...543Для оценки моторики пищевода бьта вьшолнена рентгенография верхних
отделов желудочно-кишечного тракта: пищевод свободно проходим, в средней
трети определяется непостоянный овальный дефект наполнения размером
15x8 мм. Складки слизистой оболочки при этом прослеживаются на всем про¬
тяжении, эластичность степок пишсвода не изменена. Функцртя кардии сохра¬
нена. Заключение: рентгенологическая картина не позволяет исключить неболь¬
шую лейомиому средней трети пищевода. По данным ЭГДС, пищевод свободно
проходим, с эластичными стенками, ровными контурами, обычной слизистой
оболочкой. Кардия смыкается не полностью. Имеется выраженный гастрит:
геморрагический в теле желудка, поверхностный в антральном отделе.При рентгенографии кистей определяется диффузный остеопороз с кистовидной
перестройкой преимущественно в фалангах, небольшое сужение рентгеновских
суставных щелей в проксимальных межфалашовых суставах 4-5-го пальцев обеих
кистей и проксимального межфалангового сустава 2-го пальца правой кисти.При УЗИ щитовидной железы патологических изменений не выявлено.
Эндокринологом состояние расценено как нарушение толерантности к глюко¬
зе, первичный гипотиреоз, медикаментозно компенсированный, гиперлипи-
демия 4-го типа. Рекомендована попытка отмены L-тироксина.С целью проведения биопсии кожи больная была проконсул ьтирована дерма¬
тологом: кожные покровы сухие (пергаментовидные), при натяжении — блеск.Рис. 25.8. Компьютерные томограммы органов грудной клетки. Пояснения в тексте
544 Системные заболеванияМест очаговой атрофии, выраженного ушютнения ис отмечается. Опреде;іяется
атрофия эпидермиса, подкожно-жировой клетчатки. Возможна системная скле¬
родермия без выраженных кожных проявлений. Диагноз: атрофия эпидермиса.
Ксероз кожи. Рекомендовано: крем Vit «А*^, Проведение биопсии не реко¬
мендовано в связи с отсутствием выраженных склеродсрмических изменений.С учетом отягощенного эпидемиологического анамнеза, наличия внутри-
грудной лимфаденопатии и выпота в полости перикарда больная проконсуль¬
тирована фтизиатром: убедительных данных за специфический процесс нет.
Показано дообследование (фиброброкхоскопия с исследованием бронхиаль¬
ного смыва на атршичпые клетки, на микобактерии туберк>^леза методом ПЦР,
цитологическое исследование бронхиального смыва, иммуноферментный
анализ крови, при возможносги — реакция Манту, пункция перикарда с про¬
ведением ПЦР). Учитывая возможность назначения терапии глюкокортикои-
дами, показана противотуберкулезная терапия (изониазид 0,6 г/сут ежедневно,
рифампицин 0,45 г/сут ежедневно, витамин В^).При фибробронхоскопии бронхиа-чьное дерево осмотрено до субссгментарно-
го уровня. Слизистая оболочка ис изменена, сосудистый рисунок прослежива¬
ется на всем протяжении. Секрет в небольшом количестве, слизистый, в верх¬
них отделах. Шпоры и устья сегментарных бронхов не расширены, проходимы.
Органической патологии не выявлено. Взят смыв. Закііюнеиие\ эндобронхит.Анализ бронхиального смыва: лейкоциты 1—3, до 10 в поле зрения, эритро¬
циты 0,01 в поле зрения, эпителий цилиндрический — умеренное количество,
макрофаги — много, клетки сердечных пороков, спирали Куршмана, кристал¬
лы Шар ко-Лейдена, эластичные волокна, атипичные клетки, микобактерии
туберкулеза не найдены, Мелкие кокки в незначительном количестве, клетки
бронхиального эпителия 44%, макрофаги — 31,8%, нейтрофилы 21%, лимфо¬
циты 2,8%, тучные клетки, эозинофилы 0%. Сдан смыв на ПЦР (по техниче¬
ским причинам анализ не выполнен), люминесцентную микроскопию (резуль¬
тат отрицательный) и кровь на иммуноферментный анализ для исключения
туберкулеза; результат бьш отрицательным.Таким образом, у^штывая типичное начало заболевания с синдрома Рейно,
наличие элементов CREST-синдрома (склеродактилии, синдрома Рсйно, теле-
ангиэктазий), изъязвлений концевыч фаланг пальцев в анамнезе, хронической
почечной недостаточности (в отсутствие иных причин), типичных иммуно¬
логических маркеров в крови диагноз системной склеродерлши не вызывал
сомнений. Вместе с тем оставались не вполне ясными следующие факты.1. Причина выраженной внутригрудной лимфаденопатии, что требовало
исключения в первую очередь туберкулеза, саркоидоза, неопластического про¬
цесса.2. Несоответствие столь выраженной легочной гипертензии довольно уме¬
ренным изменениям в легких.3. Гиперфермеитемия, одной из причин которой мог быть активный вирус¬
ный гепатит с.с у^іетом вышеперечисленного диагноз был сформулирован следующим
образом: системная склеродермия хронического течения с поражением
Глава 25. Тяжелая легочная гипертензия как результат сочетания.,. 545сосудов (синдром Рейнс), кожи (склеродактилия), почек (хроническая почеч¬
ная недостаточность, начальная степень), легких? Внуфигрудная лимфадено-
патия. Выраженная легочная гипертензия. Бронхообструктивньтй синдром.
Дыхательная недостаточность ТІ степени. Хроническое легочное сердце в фазе
субкомпенсации. Неполная блокада правой ножки пучка Гиса. Гипертоническая
болезнь II стадии, 2 степени повышения АД, риск 3. Наруїиение толерантно¬
сти к глюкозе. Первичный гипотиреоз, медикаментозно компенсированный.
Хронический вирусный гепатит С? Геморрагический гастрит. Холецистэктомия
в 1996 г.В клинике проводилось лечение', оксигенотерапия, кораксан 5 мг по 1 таб.
утром и вечером, моноприл 10 мг/сут (отменен в связи с гипотонией, попыт¬
ка назначения нормодипина с целью снижения давления в легочной артерии
также безуспешны), верошпирон 25 мг по 2 таб. утром, диувер 10 мг по 1 таб,2 раза в неделю, тромбо-АСС 100 мг вечером, де-нол 0,112 мг I таб. 3 раза в
день, омез, далее нексиум 20 мг по 1 таб. 2 раза в день, атровент по 2 вдоха3 раза в день, L-тироксин 50 мкг/сут (далее отменен).С учетом планировавшейся иммуносупрессивной терапии по поводу основ¬
ного заболевания (и необходимости предварительного исключения тубер¬
кулеза) встала необходимость в проведении пункционной биопсии легкого
и внутригрудных лимфоузлов (трансброїтхиальной или трансторакальной,
оба исследования проводятся под наркозом), В связи с этим больная была
проконсультирована зав. торакальным отделением Национального медико-
хирургического центра им. Н,И. Пирогова профессором Ю.А. Аблицовым.
Результаты ірансбронхиальной биопсии, по его мнению и по мнению других
специалистов, в данном случае могли быть малоинформативными. Решено
было предпринять попытку проведения трансторакальной биопсии лимфоуз¬
лов и легочной ткани, хотя это было сопряжено с высоким риском. 12 марта
больная была переведена в Национальный медико-хирургический центр
им. Н.И. Пирогова. 13 марта ей была проведена трансторакальная биопсия
медиастинальных лимфоузлов и ткани легкого. Процедура прошла без каких-
либо очевидных осложнений, больная была переведена в реанимационное
отделение. Однако, к сожалению, данное диагностическое вмешательство
окончилось для больной трагически — в ночь с 13 на 14 марта она погибла от
острой легочно-сердечной недостаточности.Прежде чем обратиться к результатам морфологического исследования,
необходимо еще раз остановиться на некоторых этапах диагностического
поиска и показаниях к проведению трансторакальной биопсии у данной боль¬
ной. Надо сказать, что при предварительном знакомстве с выписками больной
на первый план выходила выраженная легочная гипертензия в сочетании с
иммунологическими нарушениями в крови, но при осмотре, наряду с одышкой
и цианозом, сразу обратили на себя внимание изменения кистей и лица, что в
сочетании с синдромом Рейно в анамнезе заставило думать не прос гх) о систем¬
ном заболевании, но именно о склеродермии.Диагноз системной склеродермии ставится на основании критери¬
ев Американской ревматологической ассоциации, предложенных в 1980 г.
546 Системные заболеванияБольшим критерием является склеродермическое поражение кожи туловища
(проксимальная склеродермия), К малым относят склеродактилию; рубцы на
подушечках пальцев; симметричный базальный пневмофиброз. Диагноз счи¬
тается достоверным при сочетании 1 большого и 2 малых критериев. В нашем
случае трудно было говорить о налігчии проксимальной склеродермии, поэто¬
му мы воспользовались более детальными и хорошо разработанными критери¬
ями, которые предложены ведущим специалистом по склеродермии в нашей
стране Н.Г. Гусевой (в редакции 1993 и 1997 гг.).К основным признакам системной склеродермии Н.Г. Гусева относит сле¬
дующие.1. Склеродермическое поражение кожи: «плотный» отек, индураиия и атро¬
фия с преимущественным поражением лица (маскообразность), кистей (скле-
родактилия) или тотальным вовлечением кожи.2. Синдром Рейно.3. Суставно-мышечный синдром: ревматоидноподобный артрит, периарти-
кулярные изменения, фиброзируюіций миозит с развитием стойких контрак¬
тур.4. Остеолиз ногтевых, реже — средних и основных фаланг пальцев рук
(реже — ног).5. Синдром Тибьержа-Вейссенбаха: отложение солей кальция преимуіце-
ственно в области пальцев рук и периартикулярно, в подкожной клетчатке,
иногда — по ходу фасций и сухожилий.6. Поражение желудочно-кишечного тракта: эзофагит с дисфагией, дила-
тация пищевода, гастрит, дуоденит, нарушение моторики кишечника, мальаб-
сорбция.7. Поражение сердца: первичный крупноочаговый кардиосклероз.8. Поражение легких; базальный пневмосклероз, «сотовое» легкое.9. Истинная склеродермическая почка: внезапное повьпиение АД и разви¬
тие острой почечной недостаточности.10. Специфические антинуклеарные антитела: анти-8с1-70 и антицентро-
мерные антитела.11. Капилляроскопические признаки: увеличение числа, дилатация капил¬
ляров.Вьщелены также дополнительные признаки.1. Периферические: гиперпигментация, телеангиэктазии, трофические
нарушения, синдром Шегрена, полиартралгии, полимиалгии, полимиозит.2. Висцеральные; полисерозит (чаше адгезивньтй), хроническая нефропа¬
тия, полиневрит, тригеминит.3. Обшие: потеря массы тела (более 10 кг).4. Лабораторные: СОЭ >20 мм/ч, гиперпротеинемия (>85 г/л), гипер-
гаммаглобулинемия (>23%), антитела к ДНК, положительные реакции на
АНФ, РФ.У нашей больной имелись типичная ск-іеродактилия, некоторые элементы
маскообразности липа, синдром Рейно, сгибательные контрактуры пальцев
рук и дополнительный признак — телеангиэктазии, т.е. 3 из 5 элементов так
Глава 25. Тяжелая легочная гипертензия как результат сочетания... 547называемого CREST-синдрома (кальциноз, синдром Рейно, эзофагит, скле-
родактилия, телеангиэктазии). Остеолиз не был подтвержден при рентгено¬
графии кистей, выявленный при ЭГДС гастрит трудно расценивать как спе¬
цифический.Отсутствовали типичные признаки поражения легких (базальный пневмо¬
фиброз шт «сотовое» легкое), сердца (ЭКГ-проявления крупноочагового кар¬
диосклероза, нарушеніія ритма и проводимости). Поражение почек (прогрес¬
сирующая почечная недостаточность) могло расцениваться как хроническая
нефропатия, но не как истинная склеродермическая почка (так называемый
почечный криз с развитием острой почечной недостаточности и артериальной
гипертензии). В крови были выявлены специфические антитела к топоизоме-
разе I, АНФ, из дополнительных признаков имелись также трофические нару¬
шения, потеря массы тела, перикардитТаким образом, на основании сочетания 3 основных и 4 дополнительных
признаков диагноз системной склеродермии мог считаться достоверным и не
вызывал у нас сомнений. И в то же время не все клинические проявления мы
могли уверенно объяснить в рамках системной склеродермии. Проанализируем
их еще раз.Главным оставалось поражение пальцев рук (склеродактилия, рубцы от
язв, синдром Рейно, сгибательные контрактуры) в сочетании с телсангиэк-
тазиями, хотя дерматолог и не счел эти изменения достаточно типичными.
Поражение кожи лица и туловища действительно было менее ярким, кожа
легко смещалась, а ее сухость и атрофия могли быть связаны с гипотиреозом и
быстрым похуданием. Типичного симптома кисета не было — открытие рта не
затруднено. Парестезии в конечностях могли быть проявлением как синдрома
Рейно, так и симметричной периферической нейропатии. Больная описывала
не просто сухость во рту (что можно связывать с гипергликемией), но именно
невозможность есть всухомятку. Мы расценили это как синдром Шегрена,
наличие которого свидетельствовало в пользу системного заболевания вообще,
но именно для склеродермии он не является особенно характерным (как для
ревматоидного артрита, например).Потеря в весе 14 кг за 7 мес являлась признаком активности заболевания и
для обострения склеродермии весьма характерна. Одновременное нарастание
уровня креатинина (в мае он был еще совершенно нормален) в отсутствие
других причин расценивалось нами как проявление хронической нефропатии
в рамках склеродермии (гипертония носила умеренный характер). Поскольку
механизмом такой нефропатии является поражение мелких почечных сосудов
с развитием ишемии без воспаления, отсутствие мочевого синдрома весьма
характерно. Артериальная гипертензия имела длительный анамнез и задолго
предшествовала развитию хронической почечной недостаточности; тем не
менее преимущественное повышение диастолического АД говорило о наличии
почечного компонента,Анти-8с1-70 и АНФ, безусловно, укладьшались в картину склеродермии,
но перикардит не является частым ее проявлением и мог иметь иное про¬
исхождение (во всяком случае, не застойное, поскольку другие признаки
548 Системные заболеваниядекомпенсации легочного сердца отсутствовали). Развитие гипотиреоза
настолько характерно для сісіеродермрш, что существовала даже эндокринная
теория происхождения этой болезни. Выявленный недавно диабет (нарушение
толерантности к глюкозе?) также можно было расценивать в рамках склеродер¬
мии (синдрома Шеірсна).Признаки прогрессирующего поражения печени для склеродермии совер¬
шенно не характерны (хотя и описаны), но при наличии антител к HCV повы¬
шение ферментов могло расцениваться как вирусный гепатит.ТакихМ образом, единственным, что не укладывалось в картину болезни,
было поражение легких — тяжелая легочная гипертензия, очаги в легких и
внутри груд ная лимфаденопатия,На первый взгляд, легочная гипертензия является одним из самых частых
висцеральных проявлений склеродермии. Но степень ее у нашей больной
оказалась чрезвычайно высока. При этом отсутствуют признаки типичного
для склеродерлгии интерстициального поражения легких — базальный пнев¬
мофиброз, тем более «сотовое» легкое, не выявлено рестриктивных изменений
по данным спирографии, хотя диффузионная способность легких значительно
снижена. Смущало также то, что при клинически быстром прогрессировании
заболевания (появление и нарастание легочной гипертензии, почечной недо¬
статочности, перикардита, формирование очагов в легких и внутригрудной
лимфаденопатии, потеря в весе 14 кг) прогрессирование поражения кожи, а
также лабораторные признаки высокой активности заболевания отсутствова¬
ли. Не укладывались в картину болезни выраженный бронхообструктивный
синдром с преимущественным поражением мелких бронхов (хотя облитериру-
ющий бронхиолит с организующейся пневмонией при склеродермии описан)
и лимфаденопатия.По данным Н.Г. Гусевой, при общей частоте поражения легких 79%
(у 63% — пневмофиброз, у остальных — начальные функциональные
изменения) рентгенологические признаки легочной гипертензии имеют¬
ся у 18%, а классическое легочное сердце формируется лишь у 3% (у 6 из
200 наблюдавшихся больных). Легочная гипертензия развивается, как пра¬
вило, параллельно с пневмофиброзом, в изолированном виде возможна
нетяжелая легочная гипертензия (возможно, по типу синдрома Рейно
легочных сосудов). Характерно медленное прогрессирование легочного
поражения; быстрое формирование пневмофиброза и легочного сердца чаще
отмечается при остром и подостром течении. Для обострений легочного
поражения характерно прежде всего развитие интерстициальной пневмонии
(вплоть до формирования легочных кист вследствие некроза), фиброзирую-
щего альвеолита. Лимфаденопатия вообще редка при системной склеродер¬
мии, выявляется при остром или подостром течении болезни и носит обычно
генерализованный характер.Вьщеляют две формы системной склеродермии, которые различаются объ¬
емом поражения кожи, внутренних органов и прогнозом. Для диффузной
формы характерно проксимальное поражение кожи (выше локтевых и колен¬
ных суставов) в сочетаїши с синдромом Рейно, поражением сердца, почек и
Глава 25. Тяжелая легочная гипертензия как результат сочетания,,. 549легких по типу базаіьного пневмофиброза, который развивается у 30—60%
больных, прогрессирует и является одной из основных причин смерти, в то же
время легочная гипертензия развивается чрезвычайно редко.Для лимитированной (ограниченной) формы, которая встречается
несколько чаше и захватывает лишь дистальные отделы конечностей, пора¬
жение внутренних органов не характерно, многие годы кожным измене¬
ниям сопутствуют лишь элементы CREST-синдрома, но позднее у 8—28%
присоединяется легочная гипертензия, которая определяет неблагопри¬
ятный прогноз. Клиническая картина определяется различными типами
антител — к топоизомеразе при диффузной форме и к центромерам при
лимитированной.В нашем случае речь скорее идет о лимитированной форме, хотя определить
уровень антител к центромерам нам не удалось. И все же возможно ли практи¬
чески изолированное развитие легочной гипертензии столь высокой степени?В одной из работ специально проводилось сравнение больных склеродер¬
мией с признаками интерстициального поражения легких и без него — частота
легочной гипертензии оказалась примерно одинаковой, хотя степень ее не
сравнивалась. В целом она встречается при склеродермии довольно часто
(10—15%), растет ее доля среди причин смерти от склеродермии, прогноз у
таких больных даже хуже, чем у больных с первичной легочной гипертензией.
Иными словами, в принципе высокую легочную гипертензию можно было бы
рассматривать в рамках склеродермии.Тем не менее с самого начала в круг диагностического поиска были вклю¬
чены другие возможные причины высокой легочной гипертензии. Наиболее
вероятным нам представлялось наличие системного васкулита и антифосфо-
липидного синдрома.В рамках системного васкулита возможны не только легочная гипертен¬
зия, но и внутригрудная лимфаденопатия, поражение почечных артерий с
формированием хронической почечной недостаточности, синдром Рейно,
ливедо, невриты; типично повышение уровня циркулирующих иммунных
комплексов, которое было выявлено еще в Московском областном научно-
исследовательском клини^іеском институте им. М.Ф. Владимирского. Однако
поражение кожи было характерно все-таки для склеродермии (хотя выражен¬
ные трофические нарушения вплоть до некрозов и возможны при васкулитах),
и это заставляло думать о возможности сочетания склеродермии (CREST-
синдрома) и системного васкулита. Подобные сочетания описаны (например,
с микроскопическим полиартериитом), но такие васкулиты обычно ANCA-
позитивны, а у нашей больной ANCA оставались в нормальных пределах.
Описано также развитие некротизируюш.его (саркоидного) ангиита в рамках
склеродермии с поражением почек, лимфаденопатией, а также при синдроме
диссеминированного внутрисосудистого свертывания — подобного варианта
мы иск^тючить полностью не могли, хотя ангиит протекает бурно и без лечения
довольно быстро приводит к смерти, о наличии антител к цитоплазме ней-
трофилов у подобных больных не сообщается. Ставится такой диагноз только
морфологически.
550 Системные заболеванияЕще более катастрофичным является развитие легочно-почечного синдро¬
ма при склеродермии (нормотензивная острая почечная недостаточность и
легочные геморрагии, связанные с васкулитом и тромботической михроангио-
патией) — в нашем случае этот вариант можно было исключить.Антифосфолипыдный синдром приводит не только к острой легочной гипер¬
тензии (при ТЭЛА или тромбозе крупной ветви легочной артерии), но и к
хронической (в 1,8—3,5% случаев) в результате множественных тромбозов мел¬
ких артерий in situ. Такой же тромботической микроангиопатией можно было
объяснить и поражение почек без признаков нефрита, и поражение печени,
В анамнезе у больной — плацентарная недостаточность (оба ребенка родились
с гипотрофией). Описано развитие антифосфолипидного синдрома у женщин
42—68 лет как до появления симптомов склеродермии, так и на ее фоне. Однако
отсутствие антител к кардиолипину и нормальное АЧТВ позволили с высокой
долей вероятности исключить антифосфолипидный синдром как причину
высокой легочной гипертензии.Обнаружение при проведении КТ конгломератов лимфоузлов до 27 мм в
сочетании с узлами в легких сразу заставило искать другие причины поражения
легких. Лишь у 8% больных склеродермией выявляется изолированная лимфа-
денопатия, причем очень умеренная (узлы более 1 см). Считают, что в основе
ее лежат скрытая инфекция или начальные стадии поражения интерстиция
легких. Но у большинства больных (независимо от формы склеродермии) лим-
фаденопатия четко коррелирует со степенью интерстициального поражения:
она закономерно выявляется только при наличии «сотового» легкого или изме¬
нений по типу матового стекла. Тем не менее обнар>'жение лимфаденопатии у
больных со склеродермией всегда требует исключения второй болезни — сар-
коидоза, туберкулеза, опухоли.Сочетание саркоидоза со склеродермией (как с диффузной, так и с огра¬
ниченной формой) описано неоднократно (Н,Г. Гусевой и до нее) и объ¬
ясняется общностью патогенеза этих заболеваний. При этом саркоидоз
может предшествовать склеродермии, развиваться на ее фоне (что бывает
чаще) или одновременно; описаны тройные ассоциации; склеродермия,
саркоидоз и рак легкого, а также первичный билиарный цирроз и аденокар¬
цинома пищевода; поражение печени в рамках саркоидоза также развивается
нередко. Заподозрить саркоидоз на фоне склеродермии помогают необычно
выраженные легочные симптомы с профессирующим нарушением функции,
лихорадка (не всегда), потеря массы тела, внутригрудная лимфаденопатия,
появление узлов в легких, перикардита, синдромов Лефгрена, Шегрена.
Примерно в 1 -4% случаев саркоидоз дебютирует легочной гипертензией. Из
иммунологических сдвигов у больных со склеродермией и саркоидозом наи¬
более характерно выявление АНФ (94% в сравнении с анти-8с1-70 в 38% и
АСА в 25% случаев). Диагноз саркоидоза в подобных случаях ставится только
по данным биопсии легких и лимфоузлов.В качестве примера можно представить ана.-іиз 5 случаев сочетания скле¬
родермии (в основном диффузной формы) и саркоидоза {рис. 25.9). Легочную
гипертензию авторы рассматривают как проявление ск-іеродермии, и даже
Глава 25. Тяжелая легочная гипертензия как результат сочетания...55/Саркоидозлихорадкалимф-
аденопатиясиндром
Лефгренаузловатая
эритемасиндром
Шегренаповышение
АПФповышение
Сагранулема
в легкомРис. 25.9. Частота петречасмости различных симптомов у больных с сочетанием саркои-
доза и системной склеродермии (по данным Dc Bandt М. и соавт.)при сочетании с саркоидозом она была выявлена всего у 1 из 5 больных.
Лимфаденоїтатия также была выявлена не у всех б0лы1ых, чаще других встреча¬
лись лихорадка и синдром Шегрена, абсолютно патогномоничным было лишь
обнаружение саркоидных гранулем в лeгкo^f.Как только были выявлены увеличенные лимфоузлы, встал вопрос об
исключении туберкулеза. Сочетание туберкулеза и склеродермии описано
многократно (как на фоне терапии глюкокортикоидами, так и без нее).
В анамнезе жизни нашей больной — контакт с братом, страдавшим тубер-
кулемой, и профессиональный контакт с больными туберкулезом. И нас,
и фтизиатра насторожил перикардит, который появился одновременно с
нарастанием легочной симптоматики. В этой ситуации отсутствие лихо¬
радки, ночных потов, лимфоцитоза в бронхиальном смыве, отрицательные
реакции на туберкулез, тем не менее, не позволяли исключить этот диагноз.
Прогрессирующее поражение печени (не исключено, что также туберку¬
лезное) не позволяло назначать не только лечебные, но и профилактиче¬
ские дозы Ty6epKyjf0CTaTWK0B. Назначение иммуносупрессивной терапии до
исключения туберкулеза не представлялось нам возможным, и это требовало
проведения биопсии не только легкого, но и в первую очередь внутригруд-
ных лимфоузлов.
552 Системные заболеванияСтоль же вероятным было и развитие опухолщ которая не ограничивала нас
в назначении глюкокортикоидов и цитостатиков, но могла потребовать и более
жесткой, чем при склеродермии, терапии. Частота злокачественных опухолей
ири обеих формах (диффузной и ограниченной) системной склеродермии
составляет 3,6—10,7%. Наиболее часто встречается рак легкого, частота кото¬
рого, по некоторым данным, может достигать 21%. Факторами риска являются
возраст, женский пол, диффузная форма склеродермии, но не какой-либо
определенный тип аутоантител. Относительный риск развития неходжкинских
лимфом при системной склеродермии составляет 9,6 (1,1—34,5), характерно
одновременное поражение печени. Некоторые лимфомьт могут сопровождать¬
ся склеродермоподобным поражением кожи, которое регрессирует на химио¬
терапии.Наконец, прогрессирующее на глазах поражение печени, которому мы
вначале не придавали значения, могло иметь прямое отношение к разви¬
тию легочной гипертензии. Среди внепеченочных проявлений инфекции
вирусом гепатита С поражение легких стоит далеко не на последнем месте,
отражая выраженные и.ммунные сдвиги ири этом заболевании. У HCV-
инфицированных больных описано развитие синдрома Рейно, первичной
легочной гипертензии, интерстициального пневмонита, легочного фибро¬
за, доказано более тяжелое течение хронической обструктивной болезни
легких (и peipecc при лечении интерфероном), а также синдрома Шегрена,
злокачественных лимфом. Учитывая активность печеночного процесса,
мы не могли исключить связь поражения легких с вирусом гепатита С, что
стало дополнительным основанием для развернутого вирусологическоіо
анализа. При наличии цирроза, явных признаков которого у нашей больной
не было, развитие легочной гипертензии становится характерным осложне¬
нием и объясняется попаданием избытка серотонина в легочный кровоток
вследствие открытия порто-кавальных анастомозов. Описана и вторичная
легочная гипертензия в ответ на патологическую дилатацию легочных
капилляров и аіьвеолярную гипоксию (так называемый гепатопульмональ-
ный синдром), о котором можно думать при более низком, чем у наїлей
больной, pOj.Таким образом, из всех рассмотренных нами причин поражения легких
вьтсоковероятными оставались, наряду со склеродермией, саркоидоз, туберку¬
лез, опухоли и лимфомы легкого. Повторный анализ в лаборатории «ЛИТЕХ»
показал отсутствие у больной ршфекции вирусом гепатита С, что делало непо¬
нятным поражение печени и повышало вероятность туберкулеза, саркоидоза,
опухолей.Непосредственными показаниями к проведению трансторакальной биопсии
легкого и лимфоуз.аов явились невысокая вероятность развития столь выражен¬
ной легочной гипертензии в рамках исключительно системной склеродермии;
очень низкая вероятность развития лимфаденопатии в рамках системной
склеродермии у данной больной (без интерстиниального поражения легких);
фактическая невозможность проведения длительной традиционной (антаго¬
нисты Са, ингибиторы АЛФ) и современной (за исключением вазопростана)
Глава 25. Тяжелая легочная гипертензия как результат сочетания... 553симптоматической терапии по поводу легочной гипертензии в связи с отсут¬
ствием препаратов в России или их высокой стоимостью (сиалис, виафа);
невозможность назначения любой иммуиосупрессивной терапии по пово¬
ду склеродермии до исключения туберкулезного процесса; невозможность
назначения профилактической тубсркулостатической терапии в связи с про-
фессирующим поражением печени; возможность проведения специфической
шрапии в случае верификации диагноза саркоидоза, лимфомы; высокий риск
смерти без лечения (средняя продолжительность жизни у больных с легочной
гипертензией IV функционального класса 6 мес).Патологоанатомический диагноз, поставленный в Национальном медико¬
хирургическом ценфе им. Н.И. Пирогова, звучал следующим образом.
Основное заболевание1. Системная склеродермия хронического течения с лимитированным
поражением кожи: склеродактилия (по клиническим данным), синдром
Рейно (по клиническим данным), склероз мелких артерий и организованные
инфаркты коркового вещества почек, базальный пневмофиброз, диффузный
кардиосклероз.2. Саркоидоз с поражением внутригрудных лимфоузлов и печени. Операция:
видеоторакоскопия справа, атипичная резекция правого легкого, иссечение
лимфоузла корня легкого, грудная симпатэктомия.Осложнения основного заболеванияХроническое легочное сердце (толщина стенки правого желудочка 0,8 см,
масса сердца 470 г, желудочковый индекс 2,0). Венозное полнокровие и дис¬
трофия внутренних органов. Набухание головного мозга.Непосредственная причина смерти: легочно-сердечная недостаточность.Комментарий С.И. Овчаренко — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сечевова, д-ра мед. наук
Представлено действительно редкое сочетание двух заболеваний, поражаю-
тцих легкие, — системной склеродермии и саркоидоза. Данные ультразвуко¬
вого исследования относительно максимального давления в легочной артерии
(более 100 мм рт.ст.) представляются маловероятными — мы практически не
всфечаемся с такими цифрами в юшнической практике. До проведения биоп-
скш действительно можно было думать о саркоидном ангиите, осложнившем
течение склеродермии. Это состояние описано, этиология его не ясна.Комментарий В.П. Седова — профессора кафедры лучевой диагностики и луче¬
вой терапии Первого МГМУ им. И.М. Сеченова, д-ра мед. наукТакую степень легочной гипертензии мы видим при ультразвуковом иссле¬
довании фактически только в двух ситуациях — при врожденном пороке
сердца (синдром Эйзенменгера), в связи с чем мы прицельно искали дефект
перегородки, и при первичной легочной гипертензии. Исследование у дан¬
ной больной показало, что выраженное препятствие кровотоку находится на
уровне мелких легочных артерий.
554 Системные заболеванияКомментарий В,И. Маколкина — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, члена-корр.
РАМН, д-ра мед. наукНадо сказать, что такую тяжелую легочную гипертензию мы видим не при
врожденных пороках сердца, а скорее при митральном стенозе. В данном
случае клиницистам следовало поставить перед собой вопрос: ^ггo важнее —
увеличенные лимфоуз,1ы или легочная гипертензия; и, выбрав, безусловно,
второе, проводить только симптоматическую терапию. Рассчитывать на то,
что патогенетїгческая терапия сможет повлиять на столь выраженную легоч¬
ную гипертензию, было сложно.Комментарий В.А. Сулимова — заведующего кафедрой факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наук,
проф.Известно, что давление в легочной артерии выше 60 мм рт.ст. представляет
значительный риск для различных диагностических и операгивных вмеша¬
тельств; в интервенционной кардиологии такой уровень легочной гипер¬
тензии считается противопоказанием к проведению пульмонангиографии.
В этом случае я бы не стал оценивать решение лечащих врачей с позиции
человека, которому известен исход биопсии. Мне іюнятна активная тактика
врачей, понятна и степень риска.Комментарий A.B. Недоетупа — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукНам и сегодня не вполне ясно, следовало ли так рисковать и проводить
морфологическое исследование. В отношении симптоматической тера¬
пии возможности наши были очень скудными: мы не могли назначать не
только современные препараты, предназначенные для борьбы с легочной
гипертензией (в связи с их отсутствием в России или крайне высокой
стоимостью), но и давно использующиеся антагонисты Са, ингибиторы
АПФ, поскольку назначение даже минима.тьных доз этих препаратов
вызывало у больной выраженную системную гипотензию. В нашем реше¬
нии сыграло роль и доверие хирургу, хорошо нам известному профессору
Ю.А. Аблииову, который также считал возможным выполнение процедуры
у нашей больной. Я не соглашусь с тем, что установление прилганы лимфа-
денонатии ис имело пля. больной значения: назначение глюкокортикоидов
могло оказать существенный эффект, но без иск.іючеііия туберкулезного
процесса не было возможным. Для себя я еще раз убедился в том, что при
подозрении на саркоидоз очень эффективным и относительно безопасным
диагностическим приемом является биопсия печени, которая обсуждалась
и в нашем случае.Нам, несмотря на проведенное морфологическое исследование, так и оста¬
лась не вполне ясной причина столь выраженной легочной гипертензии:
морфолог не описал классических признаков васкулита; в ю же время
Глава 25. Тяжелая легочная гипертензия как результат сочетания... 555очевидно, что обнаруженный фиброз легочных сосудов должен являться
следствием воспалительного процесса. Остался не вполне понятным и непо¬
средственный механизм танатогенеза.ЛИТЕРАТУРАВест С.Дж. Секреты ревматологии. — М.: Бином, 2001. — С. 188—198.Гусева HJ. Системная склеродермия. — М.: Медицина, 1975. — 271 с.Насонов Е.Л. Антифосфолипидный синдром. — М.: Литтерра, 2004. — 434 с.Bandt M.D., Meyer О., Masson С. et аІ. Systemic sclcrodcrma and sarcoidosis: 3
new cases [Article in French] 11 Ann. Med. Interne (Paris). 1996; 147 (8): 590-594.Bar Ehrenfeld М., Rozenman J. et al. Pulmonary-renal syndrome in systemic
sclerosis // Semin. Arthritis Rheum. 2001; 30 (6): 403-410.Brown D.A., Breit S.N. Scleroderma lung disease: appropriate management j I
BioDrugs. 1997; 8 (3): 185-192.Cepeda E.J.f Reveille J.D. Autoantibodies in systemic sclerosis and fibrosing syn¬
dromes: clinical indications and relevance // Curr. Opin. Rheumatol. 2004; 16 (6):
723-732.Cox D., Conant E., Earle L. Sarcoidosis in systemic sclerosis: report of 7 cases // J.
Rheumatol. 1995; 22 (5): 881-885.De Bandt М., Perrot S., Masson C., Meyer 0. Systemic sclerosis and sarcoidosis, a
report of five cases// Br. J. Rheumatol. 1997; 36 (1): 117-119.Grassegger A.y Pohla-Gubo G., Frauscher М., Hintner ff. Autoantibodies in systemic
sclerosis (scleroderma): clues for clinical evaluation, prognosis and pathogenesis //
Wien. Med. 'W)chenschr. 2008; 158 (1-2): 19-28.Kamouchi M,, Yoshinari М., Goto H. et al Disseminated intravascular coagulation
in a patient with progressive systemic sclerosis associated with necrotizing angiitis and
generalized lymphadenopathy //ActaHaematol. 1991; 86 (4): 203-205.Launay D., Mouthon L., Hachulla E. etal. Prevalence and characteristics of moder¬
ate to severe pulmonary hypertension in systemic sclerosis with and without interstitial
lung disease //J. Rheumatol. 2007; 34 (5): 1005—1011.Lens X.M., Fernandez E., Panades MJ. et al. Progressive systemic sclerosis and
palmar hyperkeratosis as a paraneoplastic syndrome in non-Hodgkin’s lymphoma //
Nephrol. Dial. Transplant. 1992; 7 (11): 1166-1167.Maekawa Y., Nogami R. A case of progressive systemic sclerosis associated with
sarcoidosis and esophageal adenocarcinoma // J. Dermatol. 1993 Jan; 20 (1): 45—48.Meyer 0. Prognostic markers for systemic sclerosis // Joint Bone Spine. 2006; 73(5): 490-494.Miyamura Т., Yamamoto М., Shimada H., Suematsu E. Systemic sclerosis associ¬
ated with microscopic polyangitis presenting with high myeloperoxidase (MPO) titer
and necrotizing angitis: a case report lArticle in Japanese] // Ryumachi. 2002; 42 (6):
910-914.Moorman J., Saad М., Kosseifi S., Krishnaswamy G. Hepatitis С virus and the lung:
implications for therapy // Chest. 2005; 128 (4): 2882-2892.
556 Системные заболеванияRosenthal Л.К., McLaughlin J.K., Liner M.S., Persson I. Scleroderma and malig¬
nancy: an epidemiological study//Ann. Rheum. Dis. 1993; 52 (7): 531—533.Shimizu Y., Tsukagoshi H., Nemoto T. etai Recurrent bronchiolitis obliterans orga¬
nizing pneumonia in a patient with limited cutaneous systemic sclerosis // Rheumatol.
Tnt. 2002; 22 (5): 216-218.Steen V.D., Lucas М., Fertig N. , Medsger T.A. Jn Pulmonary arterial hyperten¬
sion and severe pulmonary fibrosis in systemic sclerosis patients with a nucleolar
antibody//J. Rheumatol. 2007; 34 (11): 2230-2235.Steen V.D., Powell D.L., Medsger T.A. Jr. Clinical correlations and prognosis based
on serum autoantibodies in patients with systemic sclerosis // Arthritis Rheum, 1988;31 (2); 196-203,Wechsler R.J., Steiner R.M., Spirn P. W. et at. The relationship of thoracic lymph-
adenopathy to pulmonary interstitial disease in diffuse and limited systemic sclerosis:
CT fmdii^s//Am. J. Roentgenol. 1996; 167 (1): 101-104.Wooten M. Systemic sclerosis and malignancy: a review of the literature // South.
Med. J. 2008; 101 (1): 59-62.Zandman-Goddard G. , Tweezer-Zaks N., Shalev T. etal A novel overlap syndrome:
systemic sclerosis associated with antiphospholipid syndrome — a case series // Ann.
N. Y. Acad. Sci. 2007; 1108: 497-504.
Глава 26ГРАНУЛЕМАТОЗ ВЕГЕНЕРА У БОЛЬНОЙ
С ДЛИТЕЛЬНЫМ АНАМНЕЗОМ ХРОНИЧЕСКОЙ
ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ: ПУТЬ
К ДИАГНОЗУ И СПЕЦИФИЧЕСКАЯ ТЕРАПИЯИ.В, Чичкова, И.С, ЩедринаЗаболевания из группы системных васкулитов не так редко встречаются в
практике врача-интерниста; чаще других специалистов сталкиваются с ними
ревматологи, нефрологи и пульмонологи. В представленном клиническом
наблюдении больная длительно страдала обструктивной болезнью легких с
периодическими обострениями, и лишь в последнюю госпита-аизацию высо¬
кая лихорадка не уступала антибиотикам, что в сочетании с рядом других сим¬
птомов, и поражением почек прежде всего, заставило проводить дифферен¬
циальный диагноз между инфекционными, онкологическими и системными
заболеваниями. Обнаружение в крови антинейтрофильных антител и клини¬
ческая картина быстропрогрессирующего нефрита сделали диагноз ANCA-
ассоциированного васкулита высоковероятньтм — эффективность активной
иммуносупрессивной терапии его подтвердила. Обсуждаются вопросы диффе¬
ренциальной диагностики в группе микроскопических васкулитов.Больная А., 60 лет, поступила в отделение общей терапии Факультетской
терапевтической клиники им. В.Н. Виноградова 27.12.2006 г. с жалобами на
повышение температуры тела до 38,5 X, сопровождающееся ознобами; при¬
ступообразный кашель с трудноотделяемой мокротой; одышку при умеренной
физической нагрузке; дизурические прояшгения в виде болей при мочеиспу¬
скании; выраженную слабость; снижение массы тела за 3 мес на 7 кг; отс\т-
ствие аппетита. Анамнез жизни без особенностей.Анамнез заболевания {рис. 26.1): в 1998 т. после респираторной инфекции
появились кашель с трудноотделяемой мокротой, субфебрильная температура.
При стационарном обследовании состояние было расценено как хронический
обструктивний бронхит в фазе обострения, проводилась антибактериатьная тера¬
пия, в дшіьнейшем рекомендовано применение беродуала или атровента. На фоне
лечения состояние улучшилось, однако рекомендаций после выписки не соблю-
дшіа. В ноябре 1999 г. после респираторной инфекции — очередное обострение
заболевания, которое сопровождалось появлением одышки, эпизодов нехватки
воздуха, субфебрильной лихорадкой, что послужило причиной госпитатіизации в
2000 г. в Факультетскую терапевтическую клинику им. В.Н. Виноградова.В процессе обследования были выявлены следующие изменения; лей¬
коцитарный и эозинофильный характер мокроты; не полностью обратимая
бронхіїальная обструкция по данным спирометрии; при проведении КТ
558Системные заболевания1998
(ГКБ 14)февраль 2000
(ФТК)2001—2005октябрь2006ноябрь2006ЛихорадкаА/\ААААААКашель
с трудно-
отделяемоР
мокротой'*Ч0ФВ1 = 42%Слабость^ — 'Снижение
массы тела—8 кг Гемоглобинг/лСОЭ мм/ч143 г/л
10 мм/ч106,3 Г/л
20 мм/ч
Г ематурияДиагнозХроничес¬
кий обстру¬
ктивный
бронхитБА инфекционно¬
аллергическая.
Хронический
обструктивный
бронхит. Диф.
пневмоскле¬
роз ДН IIПневмонияЛечениеРентам ицинТеотард, сальбу-
тамол, бекотид,
беродуал или
атровент, дыха¬
тельная
гимнастикаАнтибактери¬альнаябронхолити-ческаяи муколитиче-
ская терапия
в период
обостренияАмокси-клав10ОО г/сут
7 дней,
гентами-
цин160 мг/сут
7 днейНолицин
200 мг/сут
5 дней,
клацид
500 мг/сут
5 днейРис. 26.1. Анамнез больной А., 60 летлегких обращала на себя внимание картина диффузного хронического брон¬
хита, цилиндрических бронхоэктазов. Проводилось также аллергологическое
обследование, выявившее сенсибилизацию к бытовым аллергенам. На этом
основании состояние было расценено как инфекционно-аллергическая брон¬
хиальная астма, хронический обструктивный бронхит. Проводимое лечение
бронхолитиками, ингаляционными Рз-агонистами и глюкокортикоидами было
зффектішно. Рекомендованная терапия проводилась недлительно. В течение
последующих лет также отмечались обострения заболевания, как правило, в
результате перенесенной респираторной инфекции, протекавшие аналогично
описанным выше.Значительное ухудшение состояния с октября 2006 г., когда без явной при¬
чины отметила стойкое повышение температуры, появление приступообразного
кашля с трудноотделяемой мокротой, одышки, при обращении к врачу по месту
жительства на основании измененной ауск\'льтативной картины состояние было
расценено как пневмония. В связи с этим бьта начата антибактериальная тера¬
пия амоксиклавом 1000 мг/сут, затем геїтгамицином 160 мг/суг в течение 5 дней
Глава 26. Гранулематоз Вегенера у больной с длительным анамнезом.., 559без существенного эффекта. Сохранялась лихорадка (от субфебрильной до
фебрильной), появилась проірессирующая слабость, отметила потерю массы
тела. В ноябре появились дизурические явления, в анализах мочи впервые были
выявлены протеинурия (0,3%о), лейкоцитурия (10-15 в поле зрения), эритро-
цитурия (25—30 в поле зрения). В связи с измененным мочевым осадком был
назначен нолииин 200 мг/сут в течение 5 дней, а затем, в связи с сохраняющей¬
ся лихорадкой, клацид 500 мг/сут. Кроме того, в связи с изменениями при УЗИ
почек, подозрительными на новообразование правой почки, была вьптолнена
МСКТ почек с внутривенпым контрастированием раствором омнипака, не
выявившая каких-либо изменений в почках и мочевыводящих путях. За это
время пациентка продолжала прогрессивно худеть (в общей сложности на7 кг), значительно снизился аппетит, наросла слабость, сохранялась лихорадка,
что послужило причиной госпитализации в отделение.При поступлении рост 156 см, вес 35 кг Температура тела 37,6 °С. Кожные
покровы и видимые слизистые оболочки чистые. Отеков нет. Лимфоузлы уве¬
личены. Число дыханий 20—22/мин. В легких дыхание ослаблено в базальных
отде.іах, выслушивались басовые, влажные разнокалиберные и свистящие
хрипы. Тоны сердца не изменены, шумов нет. Печень, селезенка iie увеличены.В общем анализе крови: гемоглобин 104,5 г/л, эритроциты 3,5 млн, цветовой
показатель 0,9, лейкоциты 10,1 тыс., нейтрофилы 70,8%, лимфоциты 20,3%,
моноциты 5,7%, эозинофилы 2,9%, базофилы 0,3%, тромбоциты 543,9 тыс.,
СОЭ 37 мм/ч.В биохимическом анализе крови: общий белок 7,4 г/л, альбумин 3,5 г/л,
глюкоза 83 мг/дл, креатинин 2,1 мг/дл, азот мочевины 43 мг/дл, мочевая кис¬
лота 5,6 мг/дл, общий билирубин 1 мг/дл, ACT 14 Ед/л, АЛТ 11 Ед/л, у-ГГ
29 Ед/л, натрий 140 мэкв/л, калий 4,4 мэкв/л. При электрофорезе белков: аль¬
бумин 54,4%, а,-глобулины 3,6%, а^-глобулины 17,9%, р-глобулины 11,1%,
у'глобулины 13%. СРВ 8,3 мг/дл (норма 0—0,8).Обратили на себя внимание небольшой лейкоцитоз, тромбоцитоз, увеличе¬
ние СОЭ, СРВ, умеренная нормохромная анемия, повышение уровня креати-
нина и азота мочевины.В общем анализе мочи: удельный вес 1012, белок 0,195%о, сахара, ацето¬
на, желчных пигментов нет, уробилин в пределах нормы, лейкоциты 1—3 в
поле зрения, эритроциты 100-130 в поле зрения, слизи и бактерий немного.
В суточной моче белок 0,140%о (210 мг/сут). В анализе по Нечипоренко: pH 8,5,
белок 0,210% в 1 мл мочи, лейкоциты 9,750, эритроциты 418,750.При КТ органов грудной к./іетки (рис. 26.2) выявлена картина диффузного
интерстициального фиброза, эмфиземы, хронического бронхита с на.іичием
бронхоэктазов и явления бронхообструкции.По данным исследования ФВД (табл. 26.1), жизненная емкость легких была
значительно снижена. Генерализованная обструкция резко выражена. Кривая
объем-поток — эмфизематозный вариант. Выявлены резкие вентилляционные
нарушения обструктивно-рестриктивного типа.Таким образом, было решено, что пациентка страдает хронической
обстр>тстивной болезнью легких тяжелого течения в фазе обострения, что
560Системные заболеванияРис. 26,2, Компьютерная томограмма органов
ірудной клеткиnofliBep^ajiM острофазовые пока¬
затели (лейкоцитоз, СОЭ), данные
ФВД и КТ органов фудиой клетки.
В то же время неясными представ¬
лялись изменения в анализах мочи,
а также повышение уровня креати-
нина, что, несомненно, требовало
дальнейшего обследования. С уче¬
том клинической картины обостре¬
ния хронической обструктивной
болезни легких при поступлении
в отделение была начата терапия
ципрофлоксапином, который, в
связи с сохраняющейся лихорад¬
кой, бьш заменен на клафоран и
мегрожил. Полученные биохимические данные (креатинин, азот мочевины), а
также низкий вес больной потребовали корректировки доз антибактериальных
препаратов. Кроме того, проводилась терапия бронхолитиками через небулай-
зер.За время нахождения в стационаре состояние больной претерпело следующие
изменения: отмечено существенное улучшение в течении хронической обсрук-
тивной болезни легких, что подтверждалось значительным уменьшением
кашля, отсутствием дыхательной недостаточности, улучшением аускульта¬
тивной кар'гины и параметров ФВД. В то же время сохранялись фебрильная
лихорадка с максимальными подъемами температуры до 39,5 “С, выраженные
астенические жалобы, нарастание СОЭ и усугубление анемии. А главное, было
отмечено суш:ественное ухудшение почечной функции: за 2 недели выявлено
нарастание уровня креатинина до 3,8 мг/дл {рис. 26.3).Полученные лабораторные данные и динамика развития болезни потребо¬
вали изменения диагностической концепции. Необходимо бьшо рассмотреть
комплекс клинико-лабораторных синдромов: фебрильную лихорадку, соче¬
тающуюся с лейкоцитозом и увеличением СОЭ, измененный мочевой осадок в
виде гематурии и протеинурии, снижение функции почек (креатинин 3,8 мг/дл,
скорость КФ 22 мл/мин).Таблица 26. /Параметры функции внешнего дыхания до и после ингаляции беродуалаПоказательРезультатПосле ингаляции беродуалаЖЕЛ1490 (52%)-0ФВ1780 (35%)920 (41%)МОС2520%28%МОС5015%22%МОС7513%20%0ФВ1/ФЖЕЛ46%49%
Глава 26. Гранулематоз Вегенера у больной с длительным анамнезом...56128.12.0608.01.0719.0122.0124.0131.01Температура тела37,238,838,036,636,636,6соэГемоглобин, г/л37 мм/ч104,545 мм/ч100,165 мм/ч92,148 мм/ч87,640 мм/ч95,520 мм/чтз..Изменения
мочевого осадкаЛейкоциты9750Эритроциты
1418750Креатинин2,1 мг/дл3,8 мг/дл4,0.bar/flfK4,4 мг/дл3,4мг/дл2,9 мг/длПреднизо-
лон 20 мгТерапия Ципрофлок- Отменасацин02-08.02,
клафоран1,0 мг/сут,
метрогил
500 мг/сут1Ъ|с. 26.3, Динамика ли.хорадки и лабораторных данных за время госпитализацииСреди наиболее вероятных причин рассматривались следующие.Ї. Инфекционно-воспалительные (бактериальная инфекция, туберкулез, в
том числе с поражением почек?).2. Онкологическая патология, в том числе почек и мочевыводящих путей.3. Аутоиммунные заболевания: диффузные болезни соединительной ткани
и системные васкулиты.4. Лекарственные нефропатии.Для исключения 6aKmepuajibH0u инфекции проводились посевы крови и
мочи, исследование прокальцитонина сыворотки крови (результат отрица¬
тельный). Больная 6hL'ia проконсу.іьтирована в Научно-исследовательском
институте фтизиопульмонологии: данных за т>'беркулез почек не получено.
Длительный период фебрильной лихорадки с неэффективностью антибакте¬
риальной терапии ставил под сомнение инфекционный генез лихорадочного
состояния.Был проведен тщательный оикопоиск, а также \рологическое обследование.
Больная была проконсультирована в клинике урологии проф. Ю.Г. Аляевым,
проводились повторные ультразвуковые исследования почек и мочевого пузы¬
ря, что позволило исключить из списка возможных причин гематурии патоло¬
гию мочевыводящих путей и мочевого пузыря.
562 Системные заболеванияУчитывая клинико-лабораторные данные, можно было говорить о фор¬
мировании у больной быстропрогрсссирующего гломерулонефрита, в связи с
чем она была проконсультирована нефрологом, проф. Н.Л. Козловской. Было
высказано предположение о развитии у больной острого интерстициального
лекарственного нефрита. Данное предположение было основано на анамне¬
стических данных, подтверждавших массивное использование нефротоксич-
ных антибиотиков (аминогликозидов, полусинтетических пенициллинов), а
также проведение внутривенного контрастирования омнипаком, усугубившего
нарушение почечной функции. В связи с этим была прекраш;ена антибактери¬
альная терапия.В качестве одной из наиболее вероятных причин выявленных синдромов
рассматривались диффузные болезни соединительной ткани и системные васку-
литы. Проведено развернутое иммунологическое обследование: антитела к
ДНК и АНФ не выявлены, комшіемент 38,5 гем. ед., РФ 299 МЕ/мл. Дебют рев¬
матоидного артрита казался нам маловероятным ввиду отсутствия суставного
синдрома. Также не могла обсуждаться и системная красная волчанка, так как
не было комплекса диагностических критериев этого заболевания. Имевшееся
в течение многих лет поражение легких в виде хронической обструктивной
болезни легких, эффективность ранее проводимой антибактериальной тера¬
пии при обострении хронической обструктивной болезни легких, отсутствие
кровохарканья и инфильтративньгх изменений в легких делали маловероятным
развитие у больной легочно-почечного синдрома, ютассическим вариантом
которого является синдром Гудпасчера.Наконец, было выявлено значительное повышение уровня антинейтро-
фиігьньїх антител: cANCA (антитела к протеиназе 3) 5,07 Ед/мл (норма 0—5),
pANCA (антитела к миелопероксидазе) >100 Ед/мл (норма 0-5). В сочетании
с поражением почек в виде быстропрогрессируюшего гломерулонефрита с
хронической почечной недостаточностью, фебрильной лихорадкой, изменен¬
ными острофазовыми показателями крови это делало высоковероятным дебют
системного ANCA-ассоциированного васкулита. ANCA могут выявляться
не только при васкулитах — их обнаруживают у больных с неспецифическим
язвенным колитом, болезнью Крона, инфекционным эндокардитом, ревма¬
тоидным артритом, системной красной волчанкой, гипернефромой, нсход-
жкинскими лимфомами, однако эти заболевания обсуждались нами ранее и не
нашли своего подтверждения.К ANCA-ассоциированным васкулитам отііосятся следуюіцие:• фанулематоз Вегенера;• микроскропический полиангиит;• синдром Черджа—Стросс.Наиболее сходными по клиническим проявлениям заболеваниями являют¬
ся гранулематоз Вегенера и микроскропический полиангиит. Это васкулиты
мелких сосудов, их характеризует тяжелое течение и высокая вероятность
летального исхода. При диагностике необходимо иметь в виду, что AN С А при
этих заболеваниях выявляются не постоянно, при любом из них могут присут¬
ствовать как cANCA, так и pANCA. Сходство в том, что только внепочечные
Глава 26. Гранулематоз Вегенера у больной с длительным анамнезом.563изменения являются единственным признаком, позволяющим их различить.
Этим отличительным признаком может быть более частое поражение верхних
дыхательных путей при гранулематозе Вегенера, У нашей больной были выяв¬
лены серозно-кровянистые корки в области левой верхней носовой раковины
и на задней стенке глотки.Полученные нами данные согласуются с критериями диагноза гранулемато-
за Вегенера (табл. 26.2).Таким образом, окончательный клинический диагноз был сформули¬
рован следующим образом: гранулематоз Вегенера с поражением верхних
дыхательных путей и почек. Быстропрогрессирующий гломерулонефрит.
Хроническая почечная недостаточность II стадии. Хроническая обструктив¬
ная болезнь легких тяжелого течения с формированием бронхоэктазов в фазе
обострения. Эмфизема легких. Пневмосклероз. Дыхательная недостаточ¬
ность II степени.Согласно общепринятой схеме лечения гранулематоза Вегенера, нами
была проведена (с учетом веса) пульс-терапия циклофосфаном 200 мг и пред-
низолоном 300 мг N9 3, преднизолон назначен также внутрь в дозе 25 мг/сут.
В результате нормализовалась температура тела, снизился уровень креатинина
(с 4,4 до 2,9 мг/дд), возрос уровень гемоглобина. Больная выписана в удовлет¬
ворительном состоянии с рекомендацией продолжить лечение в клинике тера¬
пии и профзаболеваний им. Е.М. Тареева Московской медицинской академии
им. И.М. Сеченова.Системные васкулиты — группа острых или хронических заболеваний,
морфологическим признаком которых является поражение стенки сосудов
любого калибра по типу очагового или сегментарного воспаления и некроза, а
клинические проявления зависят от типа, размера и локализации пораженных
сосудов, а также от активности воспаления. Помимо собственно системных
васкулитов (первичных), вьщеляют и вторичные, которые развиваются в рам¬
ках других заболеваний: острых и хронических инфекций, диффузных заболе¬
ваний соединительной ткани, злокачественных новообразований, лекарствен¬
ной болезни, хронических вирусных заболеваний печени. Васкулиты также
делят по калибру пораженных сосудов и наличию транулем {табл. 26,3).Таблица 26.2Критерии диагноза гранулематоза ВегенераКритерийОпределениеВоспаление носа и полости ртаЯзвы в полости рта, пюйтіьте или кровяни¬
стые выде.тения из носаИзменения в легких при рентгеновском
исследованииУзелки, инфильтраты или полости в легкихИзменения в анализе мочиМикрогематурия (>5 эритроцитов в поле
зрения) или скопления эритроцитов в осад¬
ке мочиБиопсияГранулематозное воспаление в стенке арте¬
рии или в периваскулярном и экстраваску-
лярном пространстве
564Системные заболеванияТаблица 26.3Классификация системных васкулитовКалибр пораженных сосудовНаличие гранулемОтсутствие гранулемКрупные сосудыВисочный артериит
(гигантоклеточный)
Артериит ТакаясуСредние сосудыКлассический узелковый
полиартериит
Болезнь КавасакиМелкие сосудыГранулематоз Вегенера
Эозинофильный ангиит
Черджа—СтроссМикроскопический полиангиит
Пурпура Шейнлейна-Гсноха
Криоглобулинемический
васкулитКурсивом выделены ANCA-accouHHpoBaHHbie васкулитыСистемные васкулиты, в отличие от многих других имАїунньїх заболеваний,
чаще встречаются у мужчин, чем у жешдин; они могут развиваться в любом
возрасте, но чаще — у лиц среднего и пожилого возраста; пик заболеваемости
приходится на зи\гу и весну. В последние годы отмечена тенденция к увеличе¬
нию их распространенности.Микроскопическіїе васк>"литы описаны как самостоятельные нозологиче¬
ские формы относительно недавно: в 1939 г. F. Wegener представил подробное
описание гранулематозно-некротического васк>^лита с поражением верхних и
нижних дыхательных путей и почек (гранулематоз Вегенера); в 1951 г. J. Churg
и L. Strauss опубликовали клиническое наблюдение 13 больных бронхиальной
астмой, эозинофилией, гранулематозным воспалением, некротизирующим
васкулитом и некротизирующим гломерулонефритом (синдром Черджа—
Стросс); в 1980-1990 гг. из понятия узелкового полиартериита выделена
отдельная нозологическая форма, характеризующаяся поражением мельчай¬
ших артерий и венул, — микроскопический полиангиит. Позже в патогенезе
всех ipcx видов васкулита установлена роль антинейтрофильных антител.ANCA {рис. 26.4, см. цветную в/сгейку) — органоспещіфические антитела,
направленные к антигенам цитоплазматических гранул нейтрофилов (впер¬
вые описаны D. Davies в 1982 г). Цитоплазматические ANCA — антитела к
протеиназе-3, в большинстве случаев выявляются у больных гранулематозом
Вегенера, псринуклеарные ANCA — антитела к миелопероксидазе, в бо.тьшин-
стве слу'чаев выявляются у больных микроскопическим полиангиитом и синдро¬
мом Черджа-Стросс; однако 10% больных ANCA-ассоциированными васкулита-
ми не имеют указанных антител в крови, что не исключает данных заболеваний.Гранулематоз Вегенера — системный гранулематозный некротизирующий
васкулит артерий мелкого калибра с преимущественным поражением верхних
дыхательных путей, легких и почек. Возможны также поражения:• кожи (подкожные узелки, папулы и др.);• глаз (развитие пссвдоопухоли глазного яблока);• суставов (мигрирующий олигоартрит);• центральной и периферической нервной системы (дистальная симметрич-
НІІЯ полинейропатия);
Глава 26. Гранулематоз Вегенера у больной с длительным анамнезом,., 565• органов слуха (средний отит).Поражение респираторного тракта встречается у 85% больных:• боль в области придаточных пазух носа;• изъязвления слизистой оболочки носа, гортани и кровотечения из них;• перфорация носовой перегородки;• седловидная деформация носа;• язвенно-некротический трахеобронхит;• прогрессирующий стеноз трахеи;• пневмонии с распадом и образованием полостей в легких.Поражение почек выявляется у 75--85% больных:• клинический синдром «бътстропрогрессирующего гломерулонефрита»:
гломерулонефрит с быстро нарастающей почечной недостаточностью и
необратимым поражением клубочков;• морфологически: фокально-сегкіентарнмй некротизирующий гломеруло¬
нефрит с формированием «полулуний»; деструкция клубочков проявляет¬
ся фибриноидным некрозом капилляров.Микроскопический полиангиит представляет собой некротизир>тощий васку-
лит микроциркуляторного русла с развитием фокально-сегментарного нскро-
тизирующего гломерулонефрита и геморрагического альвеолита при отсут¬
ствии имм>тн[ных комплексов и гранулематозного воспаления.Его клиническая картина складывается:1) из неспецифических симптомов (лихорадка, слабость, похудание);2) изменений верхних дыхательных путей у 30% больных (атрофия слизи¬
стой оболочки носа, некротический ринит), которые обратимы и не приводят
к деструктивным изменениям и деформации носа;3) поражения легких у 30% больных (боли в грудной клетке, кашель, крово¬
харканье; морфологически — некротизирующий альвеолит; рентгенологиче¬
ски — инфильтраты без распада, часто с реакцией плевры);4) основного признака — поражения почек у 100% больных (выраженная
гематурия, умеренная протеинурия, редко — нефротический синдром, клини¬
чески — быстропрогрессирующий гломерулонефрит с формированием хрони¬
ческой почечной недостаточности, морфологически фокально-сегментарный
некротизирующий экстракапиллярный гломерулонефрит с «полулуниями»
при отсутствии гранулематозного воспаления).Дифференциальный диагноз гранулематоза Вегенера и микроскопического
полиангиита строится на клинических, морфологических отличиях (наличие
гранулем при гранулематозе Вегенера и их отсутствие при микроскопическом
полиангиите) и разном профиле ANCA: у большинства больных іранулемато-
зом Вегенера обнаруживаются cANCA (к протеиназе-3), у большинства боль¬
ных микроскопическим ангиитом — pANCA (к миелопероксидазе).Предложены следующие критерии оценки клинической активности ANCA-
ассоциированных васкулитов (Birmingham Vasculitis Activity Score — 1994) с
расчетом суммы баллов (клинических проявлений васк>^лита):• полная ремиссия — отсутствие признаков активности и необходимости в
терапии при нормальном уровне СРБ;
566 Системные заболевания• частичная ремиссия — уменьшение на фоне лечения общей суммы балловна 50% от первоначальной;• «большое обострение» ~ вовлечение в воспалительный процесс жизненноважных органов, требуется назначение глюкокортикоидов, цитостатиков;• «малое обострение?» — возврат заболевания с увеличением суммы баллов до 5.Проводится определение степени повреждения органов и систем — расчетиндекса повреждения (повреждение органов и систем не подвергается обратному
развитию). Оценка повреждения имеет значение для прогнозирования заболева¬
ния, а также для подбора адекватных доз глюкокортикоидов и цитостатиков.Стандартная схема лечения ANCA-ассоциированного васкулита включает
следуюш;ее:• комбинированную терапию глюкокортрткоїщами и циклофосфамидом:- иреднизолон — 1—2 мг/кг в сутки, с постепенным снижением дозы;
длительность не менее 12 мес;- циклофосфамид — 1—2 мг/кг в сутки длительно в течение 12 мес под
контролем уровня лейкоцитов крови;- возможно проведение пульс-терапии преднизолоном и циклофосфами¬
дом с последующим пероральным их назначением;• вспомогательные лекарственные средства:- антиагреганты (низкие дозы аспирина);- вазодилататоры;- ингибиторы АПФ;- антимикробные средства (триметоприм), антивирусные препараты
(интерферон альфа).Среди препаратов, возможности применения которых активно изучаются
при ANCA-ассоциированньгх васкулитах, следует назвать внутривенное при¬
менение иммуноглобулина.Таким образом, в представленном случае ьслючевым в постановке диагно¬
за васкулита стало появление бьтстропрогрессирующего гломерулонефрита в
сочетании с обнаружением антинейтрофильных антител — при этом выявле¬
ние поражения верхних дыхательных путей позволило остановиться на диа¬
гнозе гранулематоза Вегенера и начать специфическую терапию.
Глава 27ТРУДНОСТИ ПОСТАНОВКИ НОЗОЛОГИЧЕСКОГО
ДИАГНОЗА ПРИ КОНСТРИКТИВНОМ ПОЛИСЕРОЗИТЕOS, Благова, Д.А. Царегородцев, А.В. Недоступ, М.П. Троицкая,
ВЛ Седов, И.В, ПетуховаКонстриктиБный полисерозит (перикардит, реже плеврит шш их сочетание)
является обычно лишь синдромом, но диагностика основного заболевания
нередко представляет значительные сложности. Мы приводим клини^іеское
наблюдение, в котором констриктивное поражение плевры, а затем перикарда
(вначале принятое гепатологами за цирроз печени), безусловно, доминировало
в клинической картине, дважды проведено оперативное лечение и, казалось бы,
выявление причины этого процесса уже не имело решающего значения. Однако
долгий и сложный путь к нозологическоАлу диагнозу полностью себя оправда.1,
поскольку TOjfbKo назначенная больному специфическая терапия позволила
подавить активность процесса и, надеемся, повлиять на его прогноз.Больной П., 53 года, поступил в клинику 02.09.2008 г с жалобами на появление
сыпи преи\{ушественно на руках и ногах, отеки голеней и стоп, незначительную
одышку при физической нагрузке, периодическое головокружение, общую сла¬
бость, периодически возникающие ноющие боли в коленных, плечевых суста¬
вах, мелких суставах кистей, обьпшо не требующие прртменения анальгетиков.Из семейного анамнеза: отец умер в 68 лет (причина смерти неизвестна),
мать — ъ1А года (страдала заболеванием сердца), сестра 68 лет страдает гипер¬
тонической болезнью, ишемической болезнью сердца; дочь 31 года практи¬
чески здорова. По профессии — сантехник (работа связана с пребыванием в
холодном влажном помещении). Ограничивает потребление жирной пищи.
Курит с ] 8 лет по 10 сигарет в день; в настоящее время алкоголь практически не
употребляет (ранее, со слов больного, употреблял в умеренных количествах).Перенесенные заболевания: в молодости — перелом левой голени; в 1997 г.
(в 43 года) на фоне болей в эпигастральной области — кровотечение из язвы
двенадцатиперстной кииіки, произведено ушивание дефекта, с тех пор явных
обострений заболевания не было. Аллергологтеский анамнез не отягощен.Анамнез заболевания (рис. 27. /): в январе 2007 г. на фоне частого переох¬
лаждения отметил появление сухого приступообразного кашля, нарастаю¬
щую выраженную слабость, повышение температуры тела до 37,7 "С, боль и
утреннюю скованность в плечевьгк, лучезапястных, коленных, голеностоп¬
ных суставах. При амбулаторном рентіенологическом исследовании органов
фудной клетки выявлены признаки правостороннего выпотного плеврита,
в связи с чем был госпитализирован в Российский научный центр хирургии
РАМН им. акад. Б.В. Петровского, где бьыа двукратно проведена плевральная
568Системные заболевания01.200704.2008май —18.07.200808.2008Ш.лихорадка
кашель
одышкаплевр, выпот
артралгии Шотекиасцитвыпот в перикарде
сыпьСРБ/РФЩФ/у-ГТдиагнозлечениепанцирное
легкое
пункции, а/б
декортикация++++/++++
132/52 ед/л
цирроз ДКМПомез, обзидан
верошпирон++++/++++
407/63 ед/л I
к. перикардит, плеврит
(tbc?). Цирроз, ТЭЛА
диуретики, метипред,
изониазид, варфаринРис. 27Л. Анамнез больного П., 53 годапункция (выпот сохранялся). В плевральном пунктате микобактерий туберку¬
леза и атипичных клеток не обнаружено, 87% клеток составляли лимфоциты.
При КТ легких отмечалось утолшение висцеральной плевры в нижних отделах
правого легкого до 1,5 см. Диагностировано панцирное легкое, проведена
декортикация нижней доли правого легкого с париетальной плеврэктомией
(проф. В.Д. Паршин). По данным гистологического исследования плевры —
картина хронического неспецифического воспаления. После выписки чув¬
ствовал себя удовлетворительно, медикаментозной терапии не получал.С апреля 2008 г. стал отмечать нарастание общей слабости, появление и
нарастание отеков нижних конечностей до верхней трети бедра, также беспо¬
коили одышка при умеренной физической активности, боли в суставах кистей,
лучевых, плечевых, коленHbLX суставах, в связи с чем был госпитализирован в
Клинику пропедевтики внутренних болезней им. В.Х. Василенко Московской
медицинской академии им. И.М. Сеченова. При лабораторном обследовании в
общем анализе крови значимых отклонений от нормы не выявлено, обраш;ало
на себя внимание повышение уровня С-реактивного белка и ревматошшого
фактора до -I-+++, умеренное повышение щелочной фосфатазы (152 Ед/л).
При выявлена диастолическая дисфункция I типа; других отклонений отнормы, в том числе дилатации полостей, не было. По данным КТ органов груд¬
ной клетки имелись левосторонний гидроторакс, утолщение листка перикарда
максимально до 1,2 см, ^гто бьщо расценено как начинаюшийся гидроперикард.
При ЭГДС выявлено варикозное расширение вен пищевода Т степени. При КТ
органов брюшной полости: печень 23x19 см, плотность паренхимы снижена,
Глава 27. Трудности постановка нозологического диагноза... 569структура неоднородная; селезенка 10x4 см, воротная вена 13 мм, селезеночная
вена 11 мм; просвет нижней полой вены неравномерно контрастируется (нару¬
шения гемодинамики?).Диагноз был сформулирован следующим образом; криптогенный цир¬
роз ИЄ4ЄНИ, класс А по Чайлду—Пью, без признаков биохимической актив¬
ности. Портальная гипертензия: варикозное расширение вен пищевода
I степени. Язвенная болезнь двенадцатиперстной кишки в стадии ремиссии.
Дилатационная кардиомиопатия токсической этиологии. Недостаточность
кровообращения ПБ стадии. В клинике проводилось лечение омезом, анапри-
лином 20 мг/сут, верошпироном 100 мг/сут без существенного эффекта. 13 мая
для дальнейшего наблюдения и обследования впервые поступил в отделение
кардиологии Факультетской терапевтической клиники им. В.Н. Виноградова.При пос'іушіении предъявлял жалобы на выраженную общую слабость,
незначительную одышку при физической нагрузке, периодические боли в
коленных суставах, мелких суставах кистей.При осмотре: состояние средней степени тяжести. Температура тела нор¬
мальная. Кожные покровы неско.іько бледные; отмечались набухание шей¬
ных вен, отеки голеней, периферические лимфоузлы не уве.іиченьї, костно-
мыщечная система без видимых изменений, число дыханий 17/мин, в легких
справа — крепитация, слева — ослабленное везикулярное дыхание, хрипы не
выслушивались. Тоны сердца приглушены, ритм правильный. ЧСС 90/мин,
АД 100/70 мм рт.ст, Живот мягкий, безболезненный при пальпации. Печень
увеличена, отстоит от края реберной дуги на 5-6 см, плотно-эластической
консистеніши, безболезненная; селезенка не увеличена.В общем анализе крови отмечалось снижение цветового показателя при
нормальном уровне гемоглобина: эритроциты 5,2 млн, НЬ 132 г/л, цвето¬
вой показатель 0,75, лейкоциты 7,1 тыс., нейтрофилы 68,84%, лимфоциты
21,14%, моноциты 8,86%, эозинофилы 0,58%, базофильт 0,58%, тромбоциты227,5 тыс., СОЭ 5 мм/ч. В динамике отмечалось повышение уровня СОЭ
до 19 мм/ч. В биохимическом анализе крови: общий белок 73,3 г/я, альбумин
33,7 г/л, креатинин 1,25 мг/дл, глюкоза 3,8 ммоль/л, азот мочевины 6 ммоль/л,
общий билирубин 27,2 мкмоль/л, прямой билирубин 11,6 мкмоль/л, мочевая
кислота 333,4 мкмоль/л, АЛТ 23 Ед/л, ACT 25 Ед/л, у-ГГ 58 Ед/л, холинэ-
стераза 3572 Ед/л, ЩФ 518 Ед/л, амилаза 34 Ед/л, КФК 38 Ед/л, натрий
133 мэкв/л, калий 4,4 мэкв/л, кальций 9,7 мг/дл, железо 35 мкг/дл, трансфер-
рин 261 мг/дл, процент насыщения железом 9,5%, При электрофорезе белков
плазмы крови — диснротеинемия: снижение уровня альбумина, повышение
уровня а^-глобулинов, р-глобулинов, у-глобулинов. СРВ +-Ы-+, РФ ++++.
Маркеры вирусного гепатита В и С, сифилиса, ВИЧ отрицательные. Уровень
гормонов щитовидной железы в пределах нормы.В общем анализе мочи патологии не выявлено, при исследовании мочи по
Нечипоренко эритроциты составили 1500/мл. Реакция кала на скрытую кровь
отрицательная. При рентгенологическом исследовании органов грудной клетки:
уплотнение легочного интерстиция, облитерация плеврального синуса спра¬
ва, также отмечена митральная конфигурация сердца, уплотнение аорты.
570 Системные заболеванияНа ЭКГ обращало на себя внимание снижение вольтажа зубцов QRS во всех
стандартных отведениях. При суточном мониторировании ЭКГ — практически
постоянная синусовая тахикардия, небольшое количество наджелудочковых и
желудочковых экстрасистол, лабильность зубца Т.При ЭхоКГ, выполненной профессором В.П. Седовым; аорта расширена
(4,2 см), ЛИ 4,2 см; объем 53 мл. Левый желудочек не расширен. КДР 4 см.
МЖП I см, ЗСЛЖ 0,9 см. ФВ левого желудочка 50%. Локальная сократитель¬
ная функция не нарушена. Правый желудочек: передне-задний размер 2,5 см.
Правое предсердие 63 мл. Аортальный клапан уплотнен, амплитуда открытия
не уменьшена — 2,3 см. Аортальная регургитаиия Т степени. Митральный юіа-
пан уплотнен, подвижность створок не ограничена, регургитаиия I—П степени.
Трансмитральный поток: £"= 56 см/с, /4 = 25 см/с, Е/А = 2,3. Трикуспидальный
клапан не уплотнен, подвижность створок не Офаничена, регургитаиия I сте¬
пени. Легочный клапан: скорость кровотока 47 см/с. Нижняя полая вена 2,6 см,
на вдохе спадается менее 50%. Заключение: размеры камер сердца не увеличе¬
ны. Аорта расширена на уровне синуса Вальсальвы. Митральная, аортальная и
трикуспидальная регургитация. Отмечаются утолщение и сепарация листков
перикарда без CHCTOJmqecKoro расхождения. Расширена нижняя полая вена, со
значительным снижением скорости кровотока, о чем свидетельствует эффект
спонтанного контрастирования. Признаки диастолической дисфункции лево¬
го желудочка по рестриктивному типу. С учетом выявленных изменений можно
думать о констриктивном перикардите.В пользу констриктивного перикардита говорил и также следующие клинико-
инструментальные симптомы: периферические отеки в отсутствие выраженной
систолической дисфункции миокарда, набухание шейных вен, вероятіїо, асиит
и штевра-'1ьпый выпот слева как возможные проявления констрикиии; арте¬
риальная гипотония, синусовая тахикардия, низкий вольтаж комплекса QRS,
минимальный подъем сегмента ST и P-pulmonale на ЭКГ, утолщение перикарда
по данным КТ (12 мм/3,5 мм), расширение нижней полой вены и ее недоста¬
точное (менее 50%) спадение на вдохе.Таким образом, проявления констриктивного перикардита выходили на
первый план в клини^геской картине и определяли тяжесть состояния больного.
Бььт начат поиск возможной этиологии перикардита. При исследовании анти¬
тел к миокарду и кардиотропньтм вирусам было выявлено в основном умерен¬
ное повышение титров: к Cytomegalovirus hominis (IgG) 1,6; к Herpes simplex virus /
(IgG) 4,3; к Herpes simplex virus //(IgG) 0,5, к вирусу Эпштейна-Барр (IgG) поло¬
жит., титр специфических антител к миокардиальной ткани IgG 1:200, к вирусу
Коксаіси IgG I; 100, гиалуронидаза IgG 1:300 (норма 1:100). АНФ (с антигеном
сердца быка) 1:40 (в норме нет), антитела к антигенам эндотелия 1:160, к анти-
іенам кардиомиоцитов 1:20, гладкой мускулатуры 1:40, волокон проводящей
системы 1:320 (норма до 1:40). Вирусная инфекция как единственная причина
конс'гриктивного перикардита представлялась маловероятной.Гораздо более вероятной с самого начала представлялась туберкулезная
этиология перикардита и плеврита (несмотря на отрицательные результаты
исследования удхіенной в 2007 г. плевры). Была проведена бронхоскопия.
Глава 27. Трудности постановки нозологического диагноза... 571При исследовании бронхиального смыва методом ПЦР ДНК микобактерий тубер¬
кулеза не обнаружено. При бактериологическом исследовании выявлены
Streptococcus pneumoniae и Haemophilus sp. в значимых титрах. Для дальнейшей
верификации диагноза туберкулеза была проведена проба Манту, которая оказа¬
лась сомнительной. Также бьиі осушествлен специфический хемилюминссцент-
ный тест, который не дал однозначного ответа: лейкоциты ответили увеличением
хемилюминесценции на все стимуляторы. При сравнении с нормой более высо¬
кий ответ отмечен на туберкулин. Учитывая результаты теста (есть тенденция
в ответе на стимуляторы, характерная д,чя туберкулеза), можно было предпо¬
ложить специфическое воспаление. При повторном гистологическом исследо¬
вании удаленной плевры подтвержден неспециф№1еский характер воспаления.При УЗИ органов брюшной полости обращали на себя внимание наличие
асцита, умеренное увеличение размеров печени, дилатация нижней полой
вены, утолщение и уплотнение стенок желчного пузыря, изменения поджелу¬
дочной железы. Размеры селезенки и селезеночной вены оставались HopMajib-
ными. При ЭГДС: расширение вен терминального отдела пищевода I степени.
Смешанный гастрит. Деформация луковицы двенадцатиперстной кишки.Таким образом, этиологический диагноз оставался неясным. Несмотря на
отрицательные результаты лабораторньгс тестов, диагноз туберкулеза, в том
числе с поражением печени, по-прежнему не мог быть отвергнут как одна
из наиболее частых причин констриктивного серозита. Оставался не вполне
ясным и характер поражения печени. В связи с этим было принято решениео проведении пункционной биопсии печени. Однако утром того дня, на который
было запланировано проведение биопсии, больной отметил резко возникшую
одышку, продуктивный кашель с прожилками крови, боль в нижнем отделе
грудной клетки, что было расценено как ТЭЛА. Биопсия печени была отмене¬
на. При экстренной МСКТ органов грудной клетки с контрастированием диа¬
гноз был подтвержден: в левой плевральной полости значительное количество
жидкости, толщина слоя 77 мм, базальные отделы левого легкого коллабиро-
ваны. Диаметр легочного ствола 33,7 мм, правой легочной артерии 23,3 мм,
левой легочной артерии 19,3 мм. Визуализируются дефекты контрастирования
верхней ветви легочной артерии, сегментарных и терминальных разветвлений,
нижней ветви правой легочной артерии, сегментарных и терминальных ветвей,
единичные дефекты контрастирования терминальных ветвей средней легочной
артерии. Единичные дефекты контрастирования терминальньгх ветвей верхней
левой легочной артерии. Заключение: признаки распространенной тромбоэм¬
болии легочных артерий. Левосторонний гидроторакс.При рентгенологическом исследовании органов грудной клетки отмечались
увеличение количества жидкости в левой гыевральной полости по сравнению
с данными при поступлении, а также участок уплотнения легочной ткани
справа. После проведения плевраіьной пункции рентгенологическая картина
соответствовала левостороннему гидротораксу, инфаркту базальных отделов
правого легкого. В связи с развитием постинфарктной пневмонии у больного
отмечено появление мокроты, которая исследовалась на туберкулез: микобак¬
терий туберкулеза не выявлено. При исследовании плевральной жидкости их
572 Системные заболеваниятакже не выявлено, жидкость имеет характер транссудата, отмечаются клетки
мезотелия с выраженной пролиферацией, лимфоциты составили 80%.Проводился поиск источника ТЭЛА. По данным ультразвукового доппле¬
ровского исследования глубокие и подкожные вены нижних конечностей не
изменены. Антитела к кардиолипину находились в пределах нормы. К тера¬
пии был добавлен варфарин, от проведения биопсии печени пришлось отка¬
заться. Несмотря на невозможность полностью исключить туберкулез, более
вероятной представлялась иммунная природа полисерозита, в связи с чем
рассматриваїся вопрос о назначении терапии глюкокортикоидами под при¬
крытием туберкулостатиков ех juvantibus. Больной бьы проконсультирован
профессором В.М. Маховым: можно рассматривать поражение печени как
реакцию на системный воспалительный процесс, наиболее вероятно — тубер¬
кулез. Функциональное состояние печени позволяет, несмотря на снижение
уровня холинэстеразы, провести пробную стадию противотуберкулезной тера¬
пии под контролем АЛТ, ACT, холинэстеразы, альбуминов сыворотки, холесте¬
рина. К терапии целесообразно добавить гептрал.Больной был также проконсультирован профессором НИИ фтизиопуль-
монологии С.Е. Борисовым: на основании имеющихся данных туберкулезная
этиология плеврита и перикардита ни достоверно подтверждена, ни с уверен¬
ностью отвергнута быть не может. Однако отсутствие характерных данных для
активного или спонтанно излеченного туберкулеза, изменений в средостении
и легких, отсутствие интоксикационного синдрома при полуторагодичном
течении заболевания снижают вероятность туберкулеза. Из исследований
целесообразно лишь проведение ПЦР в плевратьной или перикардиальной
жидкости, проведение пробы Манту. Противопоказаний к проведению глюко-
кортикоидной терапии нет. Однако при необходимости продолжения терапии
более 4 нед назначить противотуберкулезную терапию по интермиттирующей
схеме (изонртазид или изониазид + этамбутол),С середины июля была начата терапия ех juvantibus метипредом 20 мг/сут под
прикрытием туберкулостатической терапии. При контрольной рентгеногра¬
фии грудной клетки признаков нарастания выпота не было. Заключительный
клинический диагноз был сформулирован следующим образом: констриктив-
ный перикардит неясной этиологии (туберкулезной?) с развитием застой¬
ной недостаточности кровообращения в большом круге кровообращения.
Недостаточность кровообращения ПБ стадии. Плеврит неясной этиологии
(туберкулезной?). Состояние после декортикации нижней доли правого лег¬
кого с париетальной гыеврэктомией в 2007 г. Криптогенный цирроз пече¬
ни, класс А по Чайлду—Пью, без признаков биохимической активности.
Портальная гипертензия: варикозное расширение вен пищевода Т степе¬
ни, асцит. Рецидивирующая (?) тромбоэмболия ветвей легочной артерии с
неустановленным источником. Инфаркт базальных отделов правого легкого.
Язвенная болезнь двенадцатиперстной кишки вне обострения.В клинике проводилась терапия: кораксан 15 мг/сут, верошпирон 100 мг/сут,
фуросемид 40 мг/сут через день, далее 2 раза в неделю, аминокапроновая
кислота 5% 100 мл внутривенно капельно № 5, дицинон 2,0 внутримышечно
Глава 27. Трудности постановки нозологического диагноза... 573№ 10, глюкоза 5% — 200 мл внутривенно капельно № 10, амоксиклав 375 мг по
1 таб. 3 раза в день в течение 10 дней, фраксипарин 0,3 подкожно 2 раза в день,
заменен варфарином 2,5 мг с чередованием 1 и 1 1/2 таб., сорбифер дурулес по1 таб./день, омез 20 мг по 1 таб. вечером, клоназепам 2 мг по 1/4 таб. на ночь,
гептрал 400 внутримышечно № 10, изониазид 30 мг по 1 таб. (утром) и 1/2 таб.
(вечером), пиридоксин 40 мг/день, метипред 4 мг по 4 таб. утром.На фоне лечения отмечена положительная динамика в самочувствии:
уменьшилась слабость, одышка не беспокоила, боли в суставах практически не
беспокоили. После выписки чувствовал себя относительно удовлетворительно,
рекомендации соблюдал. В конце августа отметил появление сыпи на коже ног,
а также возобновление отеков голеней и стоп. 01 сентября 2008 г самостоятель¬
но отменил прием варфарина. 02 сентября 2008 г повторно госпитаїизирован в
Факультетскую терапевтическую к-іиник>^ им. В.Н. Виноградова.При осмотре', состояние средней тяжести. Геморрагическая сыпь на коже
всего туловища {рис, 27.2, см. и^ветную вшейку), позже — и на слизистой поло¬
сти рта; пастозность голеней. При аускультации с обеих сторон дыхание осла¬
бленное везикулярное, хрипов нет. Тоны сердца приглушены, ритм правиль¬
ный. ЧСС 76/мин. АД 100/70 мм рт.ст. Живот мягкий безболезненный, печень
выступает из-под реберной дуги на 2 см, мягко-эластической консистенции,
безболезненная при пальпации, селезенка не увеличена.На 12-й день госпитализации пациент отметил увеличение в объеме, боль
при движении в левом коленном суставе. В связи с подозрением на гемартроз
срочно было проведено УЗИ. коленных суставов, однако признаков жидкости в
верхних заворотах коленных суставов не выявлено. Проконсультирован ревма¬
тологом: клинически и по данным УЗИ признаков гемартроза нет. Через пять
дней отметил смещение боли в левую икроножную мышцу, отек левой голени,
пояшіение сильной хромоты, в связи с чем был проконсультирован ангиохи¬
рургом, которым состояние расценено как тромбофлебит глубоких вен левой
голени, связанный с отменой варфарина; рекомендована терапия фраксипа-
рином. Однако создавалось впечатление о первичном поражении (гематоме?)
икроножных мышц.Повторно проведено УЗИ коленных суставов (жидкости в полости сустава
на выявлено), ультразвуковое допплеровское исследование бедренных, под¬
коленных, большеберцовых вен слева (данньос за нарушение проходимости
нет), В то же время при УЗИ икроножной мышцы определялись множественные
лакунарные структуры, что подтвердило предполагаемый диагноз внутрилш-
шечной гематомы вследствие васкулита. Также пациент был проконсульти¬
рован дерматологом. Заключение', геморрагический васкулит. Рекомендована
консультация гематолога.В обш,ем анализе крови', эритроциты 5,1 лшн, НЬ 149,1 г/л, цветовой показа¬
тель 0,88, лейкоциты 9,3 тыс., нейтрофилы 77%, лимфоциты 18%, моноциты
5%, тромбоциты 177,5 тыс., СОЭ 4 мм/ч. Лейкоцитоз расценивался как резуль¬
тат терапии глюкокортикоидами. В биохимическом анализе крови сохранялись
признаки холестаза, выявлено небольшое повышение уровня трансаминаз:
общий белок 59,4 г/л, альбухіин 32,3 г/л, крсатинин 0,98 мг/дл, глюкоза
574 Системные заболевания3,4 ммоль/л, азот мочевины 7,9 ммоль/л, общий билирубин 25,2 мкмоль/л,
прямой билирубин 7,8 мкмоль/л, мочевая кислота 289,7 мкмоль/л, АЛТ
81 Ед/л, ACT 47 Ед/л, у-ГТ 212 Ед/л, ЩФ 277 Ед/л, кальций 8,1 мг/дл, натрий
137 мэкв/л, калий 4,0 мэкв/л, железо 99 мкг/дл.Триглицериды 54 мг/дл, общий холестерин 255 мг/дл, ЛПОНП 10,8 мг/дл,
ЛПВП-хс 34 мг/дл, ЛПНП-хс 210,2 мг/дл, КА 6,50. Тип гиперлршидемии 2а.Сохранялась диспротеинемия; альбумин 56,8%, а^-глобулины 4,0%,
а^-глобулины 7,4%, р-глобулины 21,1%, у-глобулины 10,7%. При иммуноло¬
гическом исследовании крови’. RW отрицательный HCV, HB^Ag отрицательный,
СРБ ++-ь+ (в повторном исследовании 2,48 мг/дл при норме 0-0,8), РФ ++++,
РФ (кол-во) 467 МЕ/мл, повторно — 337 МЕ/мл (0—20), антитела к ВИЧ не
выявлены, анти-О-стрептолизин отрицательный, комплемент 24 гем. ед. PSA
обший 0,49 нг/мл, антитела к нативной ДНК (кол-во) 8,28 МЕ/мл (0-20), АНФ
отрицательный, антитела к кардиолипину IgM 4,4, IgG 7,96 МЕ/л (в пределах
нормы), сАМСА (антитела к протеиназе 3) 0,93 Ед/мл, cANCA (антитела к мие-
лопероксидазе) 0,86 Ед/мл (в пределах нормы), IgA 530 мг/дл (50-300 мг/дл),
IgM 172 мг/дл, TgG 1500 мг/дл.Коагулограмма: АЧТВ 0,83, протромбиновый индекс 93%, фибриноген
3,32 г/л, агрегация тромбоцитов, индуцированная АДФ в концентрации
3,3 ммоль, — 47%, в концентрации 10 ммоль — 58% (в пределах нормы).Обилий анализ мочи: pH 6,0, удельный вес 1026, прозрачность полная, белка
нет, сахара нет, эпителиальные клетки единичны в поле зрения, лейкощггьт
единичны в поле зрения, эритроциты 1—3 в поле зрения.ЭКГ (рис. 27.3): ритм синусовый. Нормальное положение электрической
оси сердца. Признаки гипертрофии правого предсердия. Подъем сегмента ST
с V,—до 1 мм. Снижение вольтажа зубцов QRS во всех стандартньк отведе¬
ниях.По данным повторной ЭхоКГ, выполненной проф. В.П. Седовым, сохра¬
няются признаки констриктивного перикардита. ЛП 4 см; объем 54 мл. Левый
желудочек не расширен. КДР 4,4 см, МЖП 1 см, ЗСЛЖ 0,9 см. Правый желу¬
дочек не расширен, передне-задний размер 2,9 см. Правое предсердие 44 мл.
Регургитации на клапанах нет. Трансмитральный поток: £ = 48 см/с, А =
30 см/с, Е/Л = 1,6. Нижняя полая вена расширена до 3,2 см, на вдохе спадает¬
ся менее чем на 50%. В левой плевральной полости определяется избыточное
количество жидкости.При рентгенологическом исследовании органов грудной клетки: в средней доле
справа определяются у^іастки фиброза, стенки бронхов утолщены. Корни лег¬
ких структурны. Плевральные синусы свободны. Сердце небольших размеров,
аорта уплотнена.При МСКТорганов грудной клетки от 08.09.2008 г (рис, 27.4, верхний ряд): во
2-м сегменте правого легкого определяется участок консолидации легочной
паренхимы неправильной формы с четкими контурами размером 23x16 мм.
На фоне консолидации видны B03fl;>TnHHe просветы бронхов. Чуть выше опре¬
деляются 2 очага неправильной формы размером 9 мм и 6,5 мм. В окружаю¬
щей легочной паренхиме определяется зона повышения плотности легочной
Глава 27. Трудности постановки нозологического диагноза...575 . пЛ. >\J »n^L--V-■■■-ГХ.А.. rrju———гчА.-чгу-^ v"f———ч'>-~■г—VJп.* ;лХ-.- ,/\-L ' I .aXiL_aA,■ЇЛР:; ::Рис. 27.3. Электрокардиограмма больного П. Скорость записи 25 мм/с. Пояснения в
текстеРис. 27.4. МСКТ органов грудной клетки. Верхний ряд — при иоступлении в клинику,нижний ряд — на фоне лечения. Пояснения в тексте
576 Системные заболеванияпаренхимы по типу «матового стекла», В средней доле справа также имеются
участки повышения плотности легочной паренхимы но типу «матового стек¬
ла» и участки фиброза. Субплеврально в 8-м сегменте справа имеется у^іасток
фиброза. В плевральной полости слева определяется жидкость с толщиной
слоя до 10,5 мм. Трахея и круїшьте бронхи свободно проходимы, не деформи¬
рованы. Справа определяются единичные трахеобронхиальные лимфоузлы
размером до ]2 мм. Заключение'. КТ-картина может соответствовать правосто¬
ронней верхнедолевой пневмонии (кровоизлияние?).Поскольку нельзя было исключить развитие «свежей» пневмонии на фоне
терапии глюкокортикоидами, был проведен курс терапии сумамедом, однако
при повторной МСКТ органов грудной кпетки четкой положительной дина¬
мики не отмечено: выявлена «фрагментациях» участка уплотнения легочной
ткани, определяемого при предыдущем исследовании. Жидкость в плевраль¬
ных полостях не определяется. Неравномерное утолщение перикарда до 3,5 мм,
В остальном картина без существенной динамики. Нельзя было исключить
постинфарктный характер изменений в верхушке правого легкого, но с учетом
плотности выявленных изменений наиболее вероятным представлялось разви¬
тие геморраі ического пропитывания ткани легкого в рамках васкулита.При УЗИ органов брюшной nwwcmw. в брюшной полости в малом тазу опреде¬
ляется значительное количество свободной жидкости. Печень у’вели^іена за
счет обеих долей (толщина левой доли до 90 мм, правой — до 165 мм), конту¬
ры ровные, паренхима средней степени эхогениости, однородной структуры,
сосудистый рисунок не изменен, внутрипечсночные желчные протоки не
расширены, воротная вена до 12 мм, Селезенка 90x36 мм, контуры четкие,
ровные, наренхима однородной структуры. При эзофагогастродуоденоскопии
признаков обострения язвенной болезни, варикозного расширения вен пище¬
вода не выявлено.Для исключения системного васкулита пациент был проконсультирован
профессором Е.Н. Семенковой — наличие системного васкулита (в том числе
геморрагического) как самостоятельного заболевания признано маювероят-
ным. Диагноз представляет значительные трудности. Учитывая наличие поли¬
серозита, в том числе констриктивного перикардита, новых очагов в легочной
ткани, а также параграхеальных лимфоузлов, нельзя исключить туберкулез с
параспецифическими реакциями, возможно, с поражением печени алкоголь¬
ной этиологии. Распространенные геморрагические высыпания могуг быть
связаны с применением лекарств или проявлением неспспифической реакции
на основное заболевание. Дополнительно рекомендуется исследование крио-
глобулинов и криофибриногена, консультация в Нау^шо-исслсдовательском
институте туберкулеза.Для решения вопроса о характере поражения кожи и целесообразности про¬
ведения ее биопсии пациент был проконсультирован проф. О.Л. Ивановым:
генерализованные петехиально-пурпурозные высыпания без субъективных
ошушений, вероятнее всего, представляют собой медикаментозную реак¬
цию (на варфарин?). В настоящее время процесс склонен к отцветанию.
Рекомендуется продолжить лечение метипредом. Местно крем целестодерм
Глава 27. Трудности постановки нозологического диагноза... 5772 раза в суткл. Необходимо клиническое наблюдение. Повторная консультация
дерматолога через 2-3 нед. Проведение биопсии кожи признано нецелесоо¬
бразным, так как изменения в коже, наиболее вероятно, носят неспецифиче¬
ский характер.Для оценки признаков поражения печени, которые, на наш взгляд, не
соответствовали диагнозу цирроза, пациент был проконсультирован проф.
В,М. Маховым: результаты биохимического исследования крови свидетель¬
ствуют о синдролїе вну трипе ченочното холе стаза умеренной активности и
минимальном печеночном цитолизе. Весьма вероятно, что эти изменения
отражают реакцию на лекарственную терапию либо являются проявлением
основного заболевания (туберкулез? диффузное заболевание соединитель¬
ной ткани?). Независимо от этиологии целесообразно назначить или урсо-
фадіьк 500 мг, или внутривенно капельно гептрал 400—800 мг. В настоящее
время проведение пуикционной биопсии печени на фоне изменений кожи
нежелательно.В связи с тем, что диагноз туберкулеза не был полностью исключен, пациеігі
был проконсультирован нроф, З.Х. Корниловой (Центральный научно-иссле¬
довательский институт туберкулеза), специалистом по внелегочным формам
туберкулеза: в настоящее время основной патологией является геморрагиче¬
ский васкулит (] енера-шзованного характера, не исключаются подобные изме¬
нения в паренхиматозных органах) лекарственной этиологии. Выявленные
изменения легких больше укладываются в тромбоэмболию, после ликвидации
проявлений васкулита необходимо проведение повторной КТ и консультации
фтизиатра при сохранении изменений для решения вопроса о проведении
бронхоскопии.Таким образом, был проделан большой диагностический путь (включавший
и оценку терапии ех juvantibus), который позволил нам сделать сле^туюшие
выводы.1. У пациента нет туберкулеза: об этом говорят отсутствие генерализации
процесса на фоне терапии глюкокортикоидами (в том числе после отмены
единственного туберкулостатика в связи с появлением генерализованной
сыпи), отсутствие лихорадки, потов, лимфаденопатии практически на всем
протяжении болезни, плотность очагов в легких характерна для кровоизлияния
или фиброза, данные очаги не дают интоксикации,2. У пациента нет цирроза печени, поскольку на проводимой диуретической
терапии печень заметно сократилась, уменьши.тась ее плотность, нет сплено-
мегалии, портальной гипертензии (в том числе варикозных вен в пищеводе),
печеночной недостаточности; целый ряд факторов мог привести к развитию
холестаза и гепатомегалии (алкоголь, застой, изониази^п:, основная болезнь?).3. У пациента нет аутоиммунного гепатита с системными проявления.ми (о
котором можно было бы думать), поскольку поражение печени не «лидирует» в
клинической картине, иммунная «окраска» заболевания довольно бедна, кон-
стриктивный перикардит при аутоиммунном гепатите крайне маловероятен,4. У пациента нет системного васкулита, поскольку картина не соответству¬
ет 1Ш одному известному васкулиту.
578 Системные заболевания5. Наконец, все проявления заболевания нельзя объяснить исключительно
лекарственным поражением, гак как большая часть симптомов возникла eп^e
до начала лечения.Что же составляло клиническую картину заболевания и требовало интер¬
претации?• Относительная стабилизация состояния в результате терапии малыми
дозами глюкокортикоидов делала наиболее вероятным первично иммун¬
ный характер поражения; в его пользу говорили также полисистемность
поражения, полисерозит, плеврит (на первых этапах болезни выпот, безу¬
словно, не был связан с застоем и носил первично воспалительный харак¬
тер), перикардит; в этом же ряду следует рассматривать асцит и артрит.• Особенностью серозита была склонность к развитию констрикции в его
исходе (необходимость в декортикации легкого в анамнезе, сохраняющие¬
ся признаки констриктивного перикардита).• Геморрагический васкулит может носить характер как первично иммунно¬
го (недостаточная доза глюкокортикоидов?), так и лекарственного (варфа-
рин, изониазид, др.?).• Холестатический синдром наблюдается практически с самого начала забо¬
левания и может быть обусловлен целым рядом причин, не связаїшьгх с
развитием цирроза (алкоголь, застой по большому круг)' кровообращения,
изониазид, основная болезнь?).• На последнем месте по значимости и выраженности рассматривались
постоянные артралгии разли^шой интенсивности с минимальными изме¬
нениями суставов кистей, которые вполне укладывались в картину иммун¬
ного полисерозита; однако симптом этот никогда полностью не исчезал
на протяжении более чем 1,5 лет болезни, в том числе на фоне терапии
глюкокортикоидами.• И, наконец, наиболее характерным изменением в иммунологических
анализах крови было изолированное, выраженное и упорное повышение
>ровня СРБ и РФ (до 15-20 норм), также не исчезавшее на всем протяже¬
нии болезни (в том числе и после назначения небольшой дозы глюкокор¬
тикоидов).Все это, с учетом отвергнутььх ранее диагнозов, позволило в качестве един¬
ственного реального диагноза, который мог бы объяснить все имеющиеся у
больного клинические и лабораторные синдромы, рассматривать ревматоид¬
ный артрит с преимущественно системными проявлениями.Впервые за время болезни было выполнено рентгенологическое исследование
кистей {рис, 27.5): выявлен диффузный остеопороз с кистовидной перестрой¬
кой, неравномерное сужение 1-го пястно-фалангового сустава левой кисти,
краевые косгньте разрастания в области дистальных межфаланговых суставов
обеих кистей. При рентгенографии коленных суставов: суставные щели не суже¬
ны; краевые костные разрастания в области межмыщелковых возвышений.
При рентгенографии стоп: диффузный остеопороз, сужение рентгеновской
суставной щели первых плюсне-фаланговых суставов обеих стоп. Изменения в
мелких суставах не носили специфичного характера, но были вполне типичны
Глава 27, Трудности постановки нозологического диагноза..579Рис. 27.5. Рентгенофафия кистей. Поясне¬
ния в текстедля ранней стадии ревматоидно¬
го поражения суставов. Исходя из
этого бъшо выполнено определение
высокоспеиифичного для ревмато¬
идного артрита иммунологического
маркера — антител к циклиниче-
скому цитруллинированному пептиду
(АЦЦП). Их отсутствие не исклю¬
чает диагноза ревматоидного артри¬
та (чувствительность 41-80%), но
их обнаружение делает этот диагноз
вьтсокодостоверным (специфич¬
ность 93—99%).При норме до 5 Ед/мл уровень
АДЦП у нашего пациента составил
>100 Ед/мл, что окончательно убе¬
дило нас в наличии у него именно ревматоидного артрита. Если пользоваться
стандартными критериями АРА, то большинство из них у нашего пациента
имеются; утренняя скованность (в дебюте; более часа?), симметричность пора¬
жения суставов, поражение трех и более групп суставов, поражение мелких
суставов кистей (пястно-фаланговых), начальные, но типичные изменения на
рентгенограммах, на,іичие ревматоидного фактора в крови.Был проведен консипиум в составе проф. В.А. Сулимова, В.И. Маколкина,
В.М. Махова, А.В. Недоступа и зав, артрологическим отделением Н.В. Пету¬
ховой: наиболее вероятным представляется наличие у больного ревматоид¬
ного полиартрита с системными проявлениями: плевритом, перикардитом,
асцитом. Отсутствие специфических изменений на рентгенограммах кистей и
коленных суставов может быть связано с относительно небольшой давностью
болезни. Поражение кожи, наиболее вероятно, является проявлением лекар¬
ственной аллергии (варфарин, изониазид?). Диагноз цирроза печени может
быть отвергнут, поражение печени имеет смешанный генез (токсический,
медикаментозный), может быть проявлением основного заболевания. Дозу
метипреда целесообразно увеличить до 24 мг/сут, провести пульс-терапию
метипредом (суммарно 1000 мг) в сочетании с плазмаферезом.Окончательный /ошиический диагноз бьы сформулирован следующим обра¬
зом: ревматоидный полиартрит, серопозитивный, I—П рентгенологической
стадии, ФН I, с системными проявлениями: констриктивный плеврит, асцит,
перикардит с элементами констрикции. Недостаточность кровообращения
ПБ стадии. Геморрагический васкулит (лекарственный? ревматоидный?) с пре¬
имущественным поражением кожи, мышц, легкого. Тромбоэмболия легочной
артерии от июня 2008 г. Состояние после декортикации нижней доли правого
легкого с париетальной плеврэктомией в 2007 г. Хронический гепатит смешан¬
ной этиологии (токсіїческий, лекарственный) с холестатическим синдромом.
Язвенная болезнь двенадцатиперстной кишки, осложненная кровотечением в
1997 г., вне обострения.
580 Системные заболеванияВ клинике проводилась следующая терапия: плазмаферез № 6, метипред
4 мг по 4 таб. утром, далее — по 3 таб. 2 раза в день, метипред 250 мг на 200 мл
физ. раствора внутривенно капельно № 4, кораксан 15 мг/сут (временно отме-
Н5ІЛСЯ), верошиирон 100 мг/сут, фуросемид 40 мг/сут через день (отменялся
на неделю), сумамсд 500 мг/день № 5, фамотидин 40 мг, да.іее омез 20 мг
по 1 таб. вечером. Назначение базисной терапии было отложено до полного
купирования явлений геморрагического васкулита. После 3-го сеанса ачаз-
мафереза в сочетании с пульс-терапией метипредом отмечено полное исчез¬
новение хромоты, болезненности в левой голени и нормализация ее объема.
Несколько позже началось отцветание сыпи по всему телу с практически
полным исчезновением мелких элементов на коже ту'ловиша, груди и живота;
новых элементов не было.Отмечена также положительная динамика картины компьютерной томо¬
графии легких (см. рис. 27.4, нижний ряд): во 2-м сегменте правого легкого
сохраняется небольшой участок фиброза, структуры типа «дерево с почками»
и единичные мелкие очаги с нечеткими контурами (размеры их существенно
уменьшились по сравнению с исходными). В язычковых сегментах левого лег¬
кого определяется зона повышения плотности легочной паренхимы по типу
«матового стекла» и утолщение интерстиция. Жидкости в плевральной полости
нет. Тем самым подтверждена связь выявленных в верхушке легкого очагов с
развитием и обратной динамикой геморрагического васкулита.ГТослс выписки из стационара пациент регулярно принимал метипред 4 мг
по 3 таб. утром и 3 таб. днем, верошпирон 25 мг 2 таб. 2 раза в день, фуросемид
40 мг 1 таб. раз в неделю, кораксан 7,5 мг по 1 таб. 2 раза в день, омез 20 мг
1 капе, на ночь. Сыпь регрессировала, одышка и отеки не рецидивировали,
однако сохранялась боль при движении в мелких суставах кистей, лучезапяст¬
ных суставах; также отметил снижение массы тела на 5 кг за 1,5 мес, нарастание
общей слабости.Повторная госпитализация в Факультетскую терапевтическую клинику
им. В.Н. Виноградова для подбора базисной терапии ревматоидного артрита
04.12.2008 г. В тот же день не принял обеденную дозу метипреда (12 мг).
К вечеру отметил усиление боли в суставах. Утром 05,12.2008 г. предъявлял
жалобы на резкую болезненность во всех мелких суставах кистей, лучезапяст¬
ных суставах, левом голеностопном суставе, позвоночнике. При осмотре и
пальпации отмечена выраженная приггухлость, гипертермия кожи над суста¬
вами, болезненность при пальпации мелких суставов кистей, лучезапястных
суставов, левого голеностопного сустава, что было расценено как реакция
отмены и окончательно подтвердило диагноз ревматоидного артрита. Была
начата базисная терапия метотрексатом 10 мг/нед. Переносимость терапии
хорошая, боли в суставах купировались полностью.Констриктивный перикардит — состояние, по-видимому, гораздо более
частое, чем констриктивный плеврит, если судить по количеству статей.
Наиболее частой причиной констриктивного плеврита и/или перикарди¬
та является, очевидно, туберкулез. Далее следует назвать такие причи¬
ны, как облучение грудной клетки и средостения (при лечении опухолей
Глава 27. Трудности постановки нозологического диагноза.., 58Іи др.) и операции, которые сопровождаются перикардио- и шіевротомией.
Ревматоидный артрит как причина констрикции стоит иа первом месте
среди всех системных заболеваний. Существенно реже, чем при ревматоид¬
ном артрите, констриктивный перикардит может развиваться при систем¬
ной красной волчанке, дерматомиозитс. Периодическая болезнь относится
к достаточно редким, но хорошо известным причинам констриктивного
серозита. При уремии утолщение плевры с констрикцией может развиться
в исходе некротизирующего фиброзного экссудата и в ряде слу^іаев требует
декортикации.Причины констриктивного плеврита и/или перикардита:• туберкулез;• обл>'чение органов средостения/операции;• ревматоидный артрит (реже — СКВ, дерматомиозит);• асбестоз, силикоз;• периодическая болезнь;• уремия;• серозит, индуцированный приемом практолола;• семейный фиброзирующий плеврит/серозит;• идиопатический фиброзирующий плеврит;• идиопатический (?) фиброзирующий медиастинит;• ретроперитонеальньга фиброз с распространением в средостение.Констриктивное билатеральное поражение верхушечной плевры описано убольных с асбестозом, силикозом (при наличии соответствующих изменений
лимфоузлов средостения и фиброза альвеолярной стенки). Описаны также
сл>'чай констриктивного плевроперикардита в результате длительного приема
практолола (несмотря на отмену препарата и терапию глюкокортикоидами,
наступил летальный исход); случай констриктивного плевроперикардита в
сочетании с деформирующей артропатией нижних конечностей у двух сес гер
(гистологически в серозных оболочках выявлен фиброз), что расценено как
семейный фиброзирующий серозит, и случай двустороннего фиброзирующего
плеврита у братьев в сочетании с синдромом Фанкони. Известны и спорадиче¬
ские случаи двустороннего фиброзирующего плеврита, д^ія которого характер¬
но преимущественное поражение верхушек.Особый интерес представляет так называемый фиброзирующий медиасти¬
нит — воспаление с быстрым исходом в фиброз. Описан случай с развитием
двустороннего плеврита и картины легочной констрикции (диагноз поставлен
при биопсии патологических масс в средостении, проведена терапия глюко¬
кортикоидами с эффектом). Существует описание и целой серии (12) подобных
случаев: средний возраст пациентов составил 40 лет, преобладали женщины,
в 7 случаях заболевание расценено как идиопатическое, в 5 удалось выявить
его этиологию (преимущественно ту'беркулез). Сообщается іакже о роли
аспергилл, аномального иммунного ответа на инфекцию гисгоплазмамн в раз¬
витии данного состояния. У нашего пациента отсутствовал основной признак
данного заболевания — локальные и-ш диффузные патологические массы в
переднем средостении по данным КТ легких. Еще реже на средостение может
582 Системные заболеванияраспространяться ретроперитонеальный фиброз, тоже, как правило, идиопати-
ческий и поддающийся терапии глюкокоргикоидами.Необходимо сказать о том, что констриктивный перикардит может про¬
текать в нетипичной форме, что существенно затрудняет его выявление и
могло сыграть роль на начальных этапах диагаостики у нашего больного. Так,
неоднократно описаны экссудативно-констриктивный, локализованный, пре¬
ходящий, скрьггьгй (оккультный) варианты констриктивного перикардита, а
также констриктивный перикардит с нормальной толщиной перикарда — до
18% больных.При ревматоидном артрите описаны практически все известные формы
плеврита и перикардита, включая и такой редкий вариант, как холестериновый
перикардит. К 1975 г. было описано 46 случаев констриктивного перикардита
при ревматоидном артрите, к 1992 г. — 78. Частота констриктивного перикар¬
дита составляет, по некоторым данным, 0,64% среди мужчин и 0,06% среди
женщин, страдающих ревматоидным артритом. Возможно сочетание ревмато¬
идного артрита и серозита туберкулезной этиологии.Ревматоидный артрит стал причиной 5 из 47 (П%) случаев констрикции
перикарда по данным перикардиотомии; все 5 больных имели ревматоидный
артрит и ревматоидные узелки, 3 — ревматоидный плеврит, 2 — легочный
фиброз, 1 — кожный васкулит; 4 из 5 имели констриктивную форму перикар¬
дита, \ — экссудативно-констриктивную. Наиболее частым ошибоннъш диагно¬
зом было первичное поражение печени. Причиной такого диагноза становятся
не только наличие асцита, но и лабораторные признаки поражения печени (в
том числе синдром холестаза).Констриктивный перикардит и тампонада сердца могут развиваться при
умеренной выраженности симптомов ревматоидного артрита, а также предше¬
ствовать атаке артрита; однако более типично присоединение констриктивного
перикардита на 4-9-м году болезни. Гистологически в перикарде наиболее часто
обиар>'живается неспецифическое воспаление с инфильтрацией літмфоцитами
и плазмацитами. Основными методами лечения являются терапия глюкокор-
тикоидами, перикардиоцентез и перикардиотомия; есть данные об эффектив¬
ности колхицина 1 мг/день при рецидивирующей тампонаде сердца.Поражение легких при ревматоидном артрите чаще возникает у мужчин,
имеющих ревматоидный фактор в крови и ревматоидные узелки, и может
включать легочный васкулит, фиброзируюший альвеолит, интерстициальный
фиброз, узелки в ткаии легких, синдром Каплана, облитерирующий брон-
хиолит с организующейся пневмонией, D-пеницилламин-индуцированный
констриктивный бронхиолит, метотрексат-индуцированный пневмонит.
Имеются и единичные описания изолированного легочного капиллярита,
который приводил к развитию легочного кровотечения, хотя вообще для
ревматоидного артрита эта форма поражения легких менее характерна, чем
для других системных заболеваний. Не менее интересны и описания слу¬
чаев «идиопатического» легочного гемосидероза у больных ревматоидным
артритом, которые тоже следует рассматривать как следствие легочного
васкулита.
Глава 27. Трудности постановки нозологического диагноза.., 583Ревматоидный артрит рассматривается как самостоятельный фактор риска
развития тромбоэмболии легочной артерии. В литературе часто встречаются
описания случаев тромбоэмболии легочной артерии у больных ревматоидным
артритом, при которых очевидного источника эмболии найдено не было. Так,
на аутопсии у пациентки, страдавшей ревматоидным артритом и не полу¬
чавшей адекватной терапии, наряду с массивной ТЭЛА из неустановленного
источника, были найдены и тромбозы мелких легочных артериол с реканализа¬
цией, что рассматривается авторами как следствие обнаруженного ими васку-
лита. Можно думать, что именно такой механизм лежал в основе изменений,
выявлен1Ц>тх при КТ легких в последнюю госпитализацию у нашего 6oJO>Horo
(вскоре после отмены варфарина). Дополнительными факторами риска ТЭЛА
при ревматоидном артрите являются снижение подвижности, протезирование
суставов, внутрисуставные инъекции глюкокортикоидов, поражение легких с
гипертензией и бронхиолитом, подвздошно-поясничный бурсит; возможно,
терапия инфликсимабом.Острый гепатит с развитием печеночной недостаточности описан лишь в
рамках синдрома Стилла. В то же время из 27 больных хроническим аутоим¬
мунным гепатитом диаіноз ревматоидною артрита был поставлен 11%. Гепатит
в данном случае рассматривался как самостоятельное заболевание, поскольку
у больных имелись соответствующие иммунологические маркеры: АНФ, аши-
тела к митохондриям (АМА). В то же время описаны случаи развития при рев¬
матоидном артрите гепашта, который не отвечает критериям аутоиммунного
(антигела к митохондриям отрицательны, к микросомам — положительны
в одном случае из двух). Гепатит проявлялся умеренным цитолитическим и
холестатическим сиіщромами. Существует также описание первичного бшш-
арного цирроза без антител к митохондриям у больной с ревматоидным ар'гри-
том. У большинства упомянутых больных определялся АНФ. Выраженным
гепатотоксическям действием обладает большинство препаратов, которые
используются для длительной терапии ревматоидного артрита (метотрексат,
азатиоприн, D-пеницилламин, сульфасалазин, препарагы золота, лефлюно-
мид, мелоксикам, другие нестероидные противовоспалительные препараты).Частота развития кожного васкулита (по данным турецких авторов, проана¬
лизировавших кожные проявления у 214 больных с ревматоидным артритом)
состав-тяет около 1%. Описаны следующие формы кожного васкулита при
ревматоидном артрите:1) лейкоцитокласгический (в основе — воспаление венул, проявляется
геморрагической сыпью, выступающей над поверхностью кожи, — «пальпи¬
руемая пурпура»);2) васкулит мєлкрїх артерий (мелкие инфаркты кончиков па^шцев, сочетает¬
ся с васкулитом vasa vasorum — периферическая сенсорная нейропатия);3) васкулит средних артерий (проявления сходны с узелковым псриарте-
риитом);4) ганфенозная пиодермия.В нашем случае клиническая картина не позволяла исключить лишь лсйко-
кластический характер васкулита.
584 Системные заболеванияОднако тот же вариант васкулига может развиться при лечеиии варфари-
ном. Из кожных осложнений терапии этим препаратом чаше всего возникают
экхимозы и пурпура, которые напряліую связаны с его антикоагулянтным
действием. Возможность развития различных а-'иісргических реакций на вар-
фарин, в том числе тяжелого васкулита, также хорошо известна. Наиболее
специфичен некротизирующий васкулит, которьгй может развиться в первые
дни лечения и связан с наличием скрытого дефицита протеинов S или С —
витамин-К-зависимых противосвертывающих белков,Поскольку период полувыведения протеина С значишльно короче, чем у
витамин-К-зависимьЕХ факторов свертьгвания, варфарин вызывает прежде всего
резкое снижение концентрации протеина С, что приводит к временному повы-
тпению свертываемости крови и тромбозу сосудов кожи с последующим ее инфар¬
ктом на 3—10-й день от начала терапии. Сначала пояатяется красная плотная
бляшка с четкими границами, которая быстро превращается в четко очерченный
у^іасток некроза фиолетового или черного цвета. На пораженной коже возникают
пузыри с геморрагическим содержимым, глубокая язва и струп. Заживление идет
медлешіо. Осложнение чаще развивается у женщин, поражает кожу молочных
желез, бедер и ягодиц. Лечение состоит в назначении витамина К, шпарина и
концентрата протеина С, Частота данного осложнения не превышает 0,01—0,1 %.Однако неоднократно описано развитие васкулита и в более поздние сроки.
Так, у одного из пациентов на 2-м месяце терапии развилась сыпь на животе
и нижних конечііостях (в сочетании с поражением почек), которая бьта пред¬
ставлена красными выступающими пятнами; гистологически выявлен эози¬
нофильный васкулит. Описаны и друі ие случаи развития лейкоклас гического
васкулита, в том числе через несколько лет от начала терапии, причем возоб¬
новление терапии варфарином после некоторого периода его отмены привело
к рецидиву васкулита.Нельзя исключить, что развитие васкулита у нашего больного было спровоци¬
ровано приемом изониазида, который был назначен немногим позже варфарина
(хотя этот препарат чаше вызывает аіигергический дерматит). Нестсроидные
противовоспалительные препараты также относятся к одним из самых аллерго¬
генных; наряду с развитием крапивницы, экземы, синдрома Стивена-Джонсона
неоднократно описан и кожный васкулит, однако нати пациент принимал несгс-
роидные противовоспалительные препараты лишь зпизодшіески, что не позво¬
ляет считать их этиологическим фактором BacK>7inTa.Наконец, необходимо остановиться на значении определения антител к
циклиническому цитруллипированному пептиду в диагностике ревматоидного
артрита. Ревматоидный фактор является недостаточно специфичным в диагно¬
стике ревматоидного артрита: вьшвляясь у 50—80% больных, он в значительном
проценте случаев обнаруживается и при других иммунных заболеваниях, а
также у 15% здоровых людей, В связи с этим ведется поиск других иммуноло¬
гических маркеров ревматоидіюго артрита. К ним относятся:1) антиперинуклеарный фактор (АПФ), который является компонен¬
том кератогиалиновых транул, окружающих ядро (реакция непрямой имму¬
нофлюоресценции с использованием клеток слизистой оболочки шеки);
Глава 27. Трудности постановки нозологического диагноза... 585чувствительность АГТФ составляет 49—91%, специфичность 73—99%; однако
его определение ТЄХН№ІЄСКИ сложно, поскольку АПФ-позитивные клетки
слизистой оболочки шеки имеются в достаточном для проведения реакции
количестве лишь у 5% доноров;2) антикератиновые антитела (АКА), которые определяются в реакции
непрямой иммунофлюоресиенции с клетками пищевода мышей, что также
трудновыполнимо в рутинной клинической практике; их чувствительность
составляет 36-59%, специфичность — 88-99%.Оба типа антител появляются на ранней стадии ревматоидного артрита,
общим антигеном для них является филлагрин (фшіамент-аірегирующий белок
эпителиальных клеток), в рсзульташ дефосфорилирования которого образуется
питруллин. Это стало основанием для определения антител к цитруллипнгу. Улалось
доказать, что у предрасположенных лиц (имеющих HLA DR1 и DR4) цитруллин-
содержащие эпитопы запускают специфичную для ревматоидного артрита акти¬
вацию Т-лимфопитов с последующей выработкой специфичных антител, что
существенно облегчило лабораторную диагаостику, поскольку питруллин может
быть искусствешш синтезирован. Высказьгеается также предположение о том,
что определенную роль в «запл'ске» иммунных реакций при ревматоидном артри¬
те может иірать вирус папилломы человека, гомологиршый профиллагрину.Теми же голландскими авторами в 2000 г была установлена высокая диа¬
гностическая значимость АЦЦП: чувствительность метода составила 68%
(45—80%, по данным других лабораторий Европы), специфичность — 98% (96-
100%); АЦЦП удавалось обнаружить у 35% серонегативных по РФ больных.
В работах последних лет эти данные многократно подтверждены {табл. 27. [у.
чувствительность АЦЦП в диагностике ревматодного артрита (в том числе его
ранних форм) составляет 63,5-82,9%, специфичность — 92,4-100%.Несмотря на столь высокую специфичность АЦЦП для ревматоидного
артрита, они могут выявляться и при других заболеваниях. Для этих слі'чаев
характерны невысокие титры АЦЦП и наличие артрита в рамках основного
заболевания, который может носить характер эрозивного и не всегда легко
дифференцируется от ревматоидного артрита. Так, АЦЦП были выявлены у
33% больных хроническим вирусным гепатитом С с внепеченочными прояв¬
лениями (с артритом), достоверно более часто — эрозивным (ревматоидный
артрит?); корреляция АЦЦП с АНФ и РФ не выявлена, как и с наличием
криоглобулинов, причем титры АЦЦП у этих больных умеренные и низкие. По
другим данным, АЦЦП (в отличие от РФ) выявляются только при сочетании
ревматоидного артрита и хронического вирусного гепатита С, но не при изоли¬
рованном вирусном гепатите С (независимо от наличия полиартрита в рамках
этого заболевания). При волчаночном артрите повышенные титры АЦЦП не
бьши выявлены ни у одного больного. По другим данным, наличие эрозивного
артрита у больных е системной красной волчанкой (который составил 11 % всех
больных с волчаночным артритом) ассоциировалось (у 8% больных) с наличи¬
ем АЦЦП (титры неизвестны, ОР 28,5; 95% ДИ 4,7-173,8, р = 0,001).В низких титрах (менее 7,5 Ед/мл) АЦЦП выяв,тяются также у 9,7% боль¬
ных псориатическим артритом (но не с изолированным кожным псориазом) и
586Системные заболеванияТаблица 27.!Диагностическая значимость определения антител к циклическому
цитруллинированному пептиду при ревматоидном артритеРаботаЧувствительность, %Специфичность,Беллсва И.Б. и соавт., 200763,597,8ОігеШ F, etal., 200471,495.2Enriconi Dos Anlos L.M., 200878,6 (2-е поколение)
82,9 (3-є поколение)94,3 (2-е поколение)
93,2 (3-є поколение)Hayashi N. et al.. 200876,192,4Sghiri R. ct al., 200872,496.1Cho S.Y. et al„ 200872,2100Коса S.S. et al., 200797,8у 14,6% больных остеоаргритом; также в низких титрах — при системной сюїе-
родермии (2,6%), синдроме Шегрена (4,2%), болезни Бехчета (2,2%). Авторы
рассмафивают определение АЦЦП как способ дифференцировать ревмато¬
идный артрит у больных с вирусным гепатитом С от полиартрита в рамках
гепатита и перекрестного синдрома (ревматоидньтй артрит — склеродермия)
от изолированной склеродермии. Предполагается также, что положительные
АЦЦП при «псориатическом» и других формах артрита могут свидетельство¬
вать о дебюте или особом варианте течения ревматоидного артрита, который
не может быть диагностирован согласно общепринятым критериям этого
заболевания.Существует единственная работа, в которой показан достаточно высокий про¬
цент вьтяачения АЦЦП у больных с активным легочньш туберкулезом (37%),
однако эти антитела не ингибируются добавлением к сыворотке самого питрул-
линироваїшого пептида, как это бывает у больных с ревматоидным артритом. Не
ясна причина высокой частоты обнаружения АЦЦП у пациентов с синдромом
Дауна — 57,1 % среди положительных по РФ больных и 47,7% — среди отрицатель¬
ных: ассоциации с развитием артрита у больных, имеющих АЦЦП, не отмечено.Доказано, что у куршдих больных с ревматоидішім артритом титрь[ АЦЦП
достоверно превыщают таковые у некуряпщх. Нали^іие АЦЦП при раннем (менее
1 года) ревматоидном артрите яштяется предиктором достоверно более выражен¬
ных рентгенологических изменений через 6 лет болезни в сравнении с бо^івньтми,
у которых АЦЦП не выявляются. Неоднократно показана корреляция АЦЦП и
эрозивньос изменений суставов. Доказаііа ассоциация АЦЦП с более частым разви¬
тием внесуставных проявлений при ревматоидном артрите, с наличием РФ. В то же
время четких корреляций между ревматоидным васкулитом и АЦЦП не выявлено.
Наконец, покіїзано отсутствие корреляции между выявлением АЦЦП и развитием
бронхио,чита при ревматоидном артрите; не найдено описаний перикардита, плев¬
рита, случаев ТЭЛА и легочного кровотечения у бо^шных, имеютцих АЦЦП.Комментарий О.В. Благовой — доцента кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И. М. Сеченова, канд. мед. наукОсобенностью нашего случая является значительно отсроченное появление
главного признака заболевания — типичного ревматоидного артрита — с дли¬
тельным преобладанием в клинической картине выраженных и своеобразных
Глава 27. Трудности постановки нозологического диагноза,.. 5S7системных проявлений, которые на разных этапах требовали проведения
дифференциального диагноза с циррозом печени, туберкулезом, системным
васкулитом. Ключом к постановке диагноза стало постепенное исключение
данных заболеваний, а также стойкое выявление РФ и обнаружение высоко
специфичных АЦЦП в высоком титре.В течение последующих 9 мес непрерывно проводилась базисная терапия; мето¬
трексат 10 мг/нед внутримьппечно и мегапред 4 мг, доза которого постепенно
была снижена до 1 таб. утром. Кроме того, больной получат кораксан 15 мг/сут,
верошпирон 100 мг/сут. фуроселовд 40 мг по 1 таб. 2 раза в неделю, далее через
день, омез 20 мг по 1 таб. на ночь. На этом фоне боли в суставах купировались
полностью, при контрольной рентгенографии кистей и коленных суставов про¬
грессирования поражения не от\їечено; уровни СРБ и РФ снизились по срав¬
нению с исходными, но оставались повьппенньтми; сохранялись лабораторные
признаки умеренного холестаза. Осложнений базисной терагши не отмечено.
Несмотря на увеличение кратности приема фуросемида (вплоть до ежедневно¬
го), с июля 2009 г больной от.метил возобновление и нарастание отеков нижних
конечностей, увеличение в объеме жиюта. В сентябре был повторно госпита¬
лизирован в Факультетскую терапевтическую клинику им. В.Н. Виноградова,
отмечено нарастание признаков констриктивного перикардита.Больной бьш направлен в Российский нау^іньїй центр хирургии РАМН
им. акад. Б.В. Петровского, где ему на фоне временной отмены метотрексата
выполнена субтотальная перикардэктомия (проф. С.Я. Дземешкевші); при
гистологическом исследовании пер]йкарда — признаки неспецифического вос¬
паления. После операции состояние больного существенно улучшилось; посте¬
пенно купировался асцит, отеки не рецидивировали, повысилась толерантность
к физическим нагрузкам. В течение года больной продолжает получать базис¬
ную терапию; доза метотрексата периодически снижается до 5—7,5 мг/нед в
связи с юзрастанием до 2-3 норм уровня печеночных ферментов; однократно
проведен курс терапии гептралом с хорошим эффектом. Боли в суставах не
рецидивировали, появления новых признаков болезни не отмечено.ЛИТЕРАТУРАБеляева И.Б., Лапин С.В., Созина А.В. и др. Антитела к цитруллин-содержа-
щим антигенам в диагностике и прогнозировании течения раннего ревматоид¬
ного артрита // Медицинская иммунология. — 2007. — Т. 9, № 1. — С. 77—84.Вест С.Дж. Секреты ревматологии: Пер, с англ. / Под ред. В.Н. Хирманова. —
М.; СПб.; Бином: Невский диалект, 2001. — 767 с.Гиляревский С.Р. Диагностика и лечение заболеваний перикарда, — М.;
Медиа Сфера, 2004. — 132 с.Ahmad М., Weinstein A.J., Hughes J.A., Cosgrove D.E. Granulomatous mediastini-
tls due to Aspergillus flavus in a nonimmunosuppressed patient // Am. J. Med. 1981
Apr; 70 (4): 887-890.
588 Системные заболеванияЛтагаригкаг D.N., Amarapurkar A.D. Role of autoimmunity in nonviral chronic
liver disease // J. Assoc. Physicians India. 2000 Nov; 48 (11): 1064-1069,Anaya J.M., Diethelm L., Ortiz L.A. et al. Pulmonaiy involvement in rheumatoid
arthritis I I Semin. Arthritis Rheum. 1995 Feb; 24 (4): 242-254.Bologna C., Poirier J.L., Herisson C., Simon L. Constrictive pericardhis in severe
seronegative rheumatoid polyarthritis [Article in French] // Rev. Med. Interne. 1992
Jan-Feb; 13(1): 64-68.Bombardieri М., Alessandri C., Labbadia G. et al Role of anti-cyclic citruUinated
peptide antibodies in discriminating patients with rheumatoid arthritis from patients
with chronic hepatitis С infection-associated polyarticular involvement // Arthritis
Res. Ther. 2004; 6 (2): R137-R141.Buchanan D.R., Johnston I.D., Kerr I.H, etai Cryptogenic bilateral fibrosing pleu¬
ritis // Br. J. Dis. Chest. 1988 Apr; 82 (2): 186-193.Candia L., Marquez J., Gonzalez C. et ai Low frequency of anticyclic citruUi-
natcd peptide antibodies in psoriatic arthritis but not in cutaneous psoriasis // J. Clin.
Rheumatol. 2006 Oct; 12 (5); 226-229.Chan M. Т., Owen P., Dunphy J. et al. Associations of erosive arthritis with anti-
cyclic citruUinatcd peptide antibodies and MHC Class П alleles in systemic lupus
erythematosus // J. Rheumatol, 2008 Jan; 35 (1): 77—83.Chan Y.C., Valenti D., Mansfield A.O., Stansby G. Warfarin induced skin necrosis //
Br. J. Surg. 2000 Mar; 87 (3): 266-272.Cho S. Y., Kang 5. Lee H.J., Lee WJ. \ comparative evaluation of the diagnostic
value of anti-cyclic citruUinated peptide and rheumatoid factor in rheumatoid arthritis
[Article in Korean] // Korean J. Lab. Med. 2008 Feb; 28 (1): 39-45.Damidn-Abrego G.N., CabiedesJ., CabralA.R. Anti-citruUinated peptide antibodies in
lupus patients with or without deforming arthropathy j I Lupus, 2008; 17 (4): 300-304.Devaraj A., Griffin N., Nicholson A.G., Padley S.P. Computed tomography findings
in fibrosing mediastinitis // Clin. Radiol. 2007 Aug; 62 (8): 781-786.Dyer N.H., Varley C.C. Letter: practolol-induced pleurisy and constrictive peri¬
carditis // Br Med. J. 1975 May 24; 2 (5968): 443.Enriconi Dos Anjos L.M., Pereira LA. et al. A comparative study of IgG second- and
third-generation anti-cyclic citruUinated peptide (CCP) ELlSAs and their combination
with IgA third-generation CCP ELTSA for the diagnosis of rheumatoid arthritis // Clin.
Rheumatol. 2009 Feb; 28 (2): 153-158.Eigun Т., Inane N., Tuney D. et al. Skin manifestations of rheumatoid arthritis: a
study of 215 Turkish patients // Int. J. Dermatol. 2008 Sep; 47 (9): 894-902.Girelli F., Foschi F.G., Bedeschi E. et al. Is Anti Cyclic citruUinated peptide a use¬
ful laborator>^ test for the diagnosis of rheumatoid arthritis? // Eur. Ann. Allergy Clin.
Immunol. 2004 Apr; 36 (4): 127-130.Hakala М., Pettersson Т., Tarkka M. et al. Rheumatoid arthritis as a cause of
cardiac compression. Favourable long-term outcome of pericardiectomy // Clin.
Rheumatol. 1993 Jun; 12 (2): 199-203.Hashimoto K., Nakanishi H., Yamasaki A, et al. Pulmonary findings without the
influence of therapy in a patient with rheumatoid arthritis: an autopsy case // J. Med,
Invest. 2007 Aug; 54 (3-4): 340-344.
Глава 27, Трудности постановки нозологического диагноза.,. 589Hayashi N., Nishimura К., Kumagai S. New biomarkers for rheumatoid arthritis
[Article in Japanese] // Rinsho Byori. 2008 Apr; 56 (4): 297-308.Hayes J.R, H^iggins J., Ward K. et al. Fanulial cr>’ptogenic fibrosing pleuritis with
Fanconi’s syndrome (renal tubular acidosis). A new syndrome // Chest. 1995 Feb; 107(2): 576-578.Kakumanu P., Yamagata H., Sobel E.S. et al. Patients with pulmonary tuberculosis
are frequently positive for anti-cyclic citrullinated peptide antibodies, but their sera
also react with unmodified arginine-containing peptide //Arthritis Rheum. 2008 Jun;
58 (6): 1576-1581.Kapoor K,G., Bekaii-Saab T ’Wkrfarin-induced allergic interstitial nephritis and
leucocytoclastic vasculitis j j Intern. Med. J. 2008 Apr; 38 (4): 281-283.Kim S.K., Park S.K, Shin I.H., Choe J.Y, Anti-cyclic citrullinated peptide anti¬
body, smoking, alcohol consumption, and disease duration as risk factors for extraar-
ticular manifestations in Korean patients with rheumatoid arthritis // J. Rheumatol.
2008 Jun; 35 (6): 995-1001.Коса S.S., Akbuiut H., Dag S. et al Anti-cyclic citrullinated peptide antibodies in
rheumatoid arthritis and Behget’s disease // Tohoku J. Exp. Med. 2007 Dec; 213 (4):
297-304.Kroot E.J., de JongB.A., van Leeuwen M.A. et al. The prognostic value of anti-cyclic
citrullinated peptide antibody in patients with recent-onset rheumatoid arthritis //
Arthritis Rheum. 2000 Aug; 43 (8): 1831-1835.Lee D.M., Phillips R., Hagan E.M. etal. Quantifying Anti-CCP titer: chnical utility
and association with tobacco exposure in patients with rheumatoid arthritis // Ann.
Rheum. Dis. 2008 Apr 7.L’HuiUier J.P., Desrues B., Chales G. et al. Idiopathic pulmonary hemosiderosis
and rheumatoid arthritis. Apropos of a case [Article in French] // Rev. Pneumol. Clin.
1988; 44 (3): 136-139.Linde B., Oelzner P., Katenkamp K. et al. Fulminate liver failure in a 39-year-old
female patient with leukocytosis, unclear fever, and arthralgic pain [Article in Ger¬
man] // Med. Klin. (Munich). 2007 Oct 15; 102 (10): 846-851.Liu F.C., Chao Y.C., Hou T. Y. et al. Usefulness of anti-CCP antibodies in patients
with hepatitis С virus infection with or without arthritis, rheumatoid factor, or crj-'o-
globulinemia // Chn. Rheumatol. 2008 Apr; 27 (4): 463-467.Manji H., Raven P. Calcific constrictive pericarditis due to rheumatoid arthritis //
Postgrad. Med. J. 1990 Jan; 66 (771): 57-58.Miyachi K., Takano S., Sekiyama N. et al. Two cases of rheumatoid arthritis pre¬
senting autoimmune hepatic diseases [Article in Japanese] // Ryumachi. 1994 Jun; 34(3): 639-645.Marita Y., Muro Y., Sugiura K., Tomita Y. Anti-cyclic citrullinated peptide antibody
in systemic sclerosis j j Clin. Exp. Rheumatol. 2008 Jul—Aug; 26 (4): 542—545.Nakano Т., Ishlbashi H., Matsui M. et al. A case of primary biliary cirrhosis with
negative anti-mitochondrial antibody anteceded by rheumatoid arthritis [Article in
Japanese] // Fukuoka Igaku Zasshi. 1992 Mar; 83 (3): 144-148.Nisihara R.M., Skare T L., Siha M.B. et al High positivity of anti-CCP antibodies
inpatients with Down syndrome I j Clin. Rheumatol. 2007 Dec; 26 (12): 2031-2035.
590 Системные заболеванияOhnishi Y., Katada Н., Kasuga Н. et al An operative case of chronic constrictive
pericarditis with silicosis and lumbar caries [Article in Japanese] // Kekkaku. 1990
Mar; 65 (3): 237-242.Oliver R.M., Neville E. Progressive apical pleural fibrosis: a ‘constrictive’ ventllatoiy
defect // Br. J. Dis. Chest. 1988 Oct; 82 (4): 439-443.Oz B.S., Asgun F., Oz K., Kuraiay E. , Tatar H. Warfarin-induced skin necrose after
open heart sui^ery due to protein S and С deficiency // Heart Vessels. 2007 Jan; 22
(1): 64-66.Raposo L, Andrade M.J., Ferreira /. et al. Cholesterol pericarditis — relapsing
pericardial effusion in a patient with rheumatoid arthritis I I Rev. Port. Cardiol. 2005
May; 24 (5): 737-745.Riccio A., PostigUone L,, La Dogana P. et al. Anti-cyclic citruUinated peptide
antibodies in patients affected by HCV-related arthritis // J, Biol, Regul. Homeost.
Agents. 2008 Jan-Mar; 22 (1): 57-61.Rossi S.E., McAdams H.P., Rosado-de-Christenson M.L. etal. Fibrosing mediastini-
tis 11 Radiographics. 2001 May-Jun; 21 (3): 131-151.Sanchez-Borges M,, Capriles-Hulett A., Caballero-Fonseca F. Risk of skin reactions
when using ibuprofen-based medicines // Expert Opin. Drug Saf. 2005 Sep; 4 (5);
837-848.Schellekens G.A., de Jong B.A, van den Hoogen F,H. et al. CitruUine is an essential
constituent of antigenic determinants recognized by rheumatoid arthritis-specific
autoantibodies //J. Clm. Invest. 1998 Jan 1; 101 (1): 273-281.Schellekens G,A., VisserM., de Jong B.A. et al. The diagnostic properties of rheuma¬
toid arthritis antibodies recognizing a cyclic citruUinated peptide // Arthritis Rheum.
2000 Jan; 43 (1): 155-163.Schwafz M.L, Zamora М.Я, Hodges T.N. etal. Isolated pulmonary capillaritis and
difHise alveolar hemorrhage in rheumatoid arthritis and mixed connective tissue dis¬
ease 11 Chest. 1998 Jun; 113 (6): 1609-1615.Seve P., Stankovic K., Broussolle C. Effectiveness of colchicine in a case of
recurrent compressive rheumatoid pericarditis // Rheumatol. Int. 2005 Sep; 25 (7):
558-561.Sghiri R., Bouajina E., Bargaoui D. Value of anti-mutated citruUinated vimentin
antibodies in diagnosing rheumatoid arthritis // Rheumatol. Int. 2008 Nov; 29 (1):
59-62.Shi J., Sun X., Zhao Y. et al. Prevalence and significance of antibodies to citrulli-
nated human papillomavirus-47 E2345-362 in rheumatoid arthritis //J. Autoimmun.
2008 Sep; 31 (2): 131-135.Shimizu Т., Furuichi S., Takahashi N. et al. A case of intrathoracic extension of
retroperitoneal fibrosis [Article in Japanese] //Nihon Kokyuki Gakkai Zasshi, 2001
Oct; 39(10): 748-752.Tada Y., Onoue H., Koarada S. et al. A case of idiopathic fibrosing mediastinitis
presented with bilateral pleural effusion [Article in Japanese] // Nihon Rinsho Meneki
Gakkai Kaishi. 2002 Apr; 25 (2): 177-180.Tamir R., Pick AJ., Theodor E. Constrictive pericarditis complicating dermato-
myositis//Ann. Rheum. Dis. 1988 Nov; 47 (11): 961-963.
Глава 27. Трудности постановки нозологического диагноза... 591Thadani U., fveson J.M., Wright V, Cardiae tamponade, constrictive pericarditis
and pericardial resection in rheumatoid arthritis // Medicine (Baltimore). 1975 May;
54 (3): 261-270.ThouldA.K. Constrictive pericarditis in rheumatoid arthritis // Ann. Rheum. Dis.
1986 Feb; 45 (2); 89-94.UnlUer E.E., Denizba^i A. A pulmonary embolism case presenting with upper
abdominal and flank pain // Eur. J. Emerg. Med. 2003 Jun; 10 (2): 135-138.Verma U.N., Misra R., Radhakrisnan S. et ai A syndrome of fibrosing pleuritis,
pericarditis, and synovitis with infantile contractures of fingers and toes in 2 sisters:
“familial fibrosing serositis” //J. Rheumatol. 1995 Dec; 22 (12): 2349—2355.Wolf R. E., KingJ. ]V., Brown T.A. Antimyosin antibodies and constrictive pericardi¬
tis in lupus erythematosus//J. Rheumatol. 1988 Aug; 15 (8): 1284-1287.Yaghoubian B., Ngo S., Mak M. et al. Warfarin-induced leukocytoclastic vasculi¬
tis // Cutis. 2005 Jun; 75 (6): 329-338.Zemer D., Cobili S., Revach М., Shahin N. Constrictive pericarditis in familial
Mediterranean fever// Tsr. J. Med. Sci. 1977 Jan; 13 (1): 55—58.
Глава 28СЛУЧАЙ ДЛИТЕЛЬНОГО ТЕЧЕНИЯ СИНДРОМА
ФЕЛТИ: ОСОБЕННОСТИ ДИАГНОСТИКИ
и ТЕРАПЕВТИЧЕСКОЙ ТАКТИКИН.В. Петухова, НМ. Михлина, Е.В. СоколПредставлен случай особого варианта серопозитивного ревматоидного
артрита, так называемого сиидрома Фелти, который отличается от классиче¬
ского ревматоидного артрита наличием нейтропении (в данном сл^'чае имелась
практически панцитоисния), спленомегалии и высокой частотой инфекцион¬
ных осложнений, в большинстве случаев ответственных за неблагоприятный
исход заболевания. Обсуждаются вопросы диагностики синдрома Фелти и
сложности проведения базисной терапии (назначение цигостатиков при нали¬
чии исходной нейтропении). Особенностью данной больной яатяется длитель¬
ное течение заболевания, которое удается медикаментозно контролировать,
несмотря на неоднократное развитие инфекционных осложнений.Больная Л., 68 лет, поступила в отделение патологии суставов Факультетской
терапевтической клиники им. В,Н. Виноградова 17.11.2008 г с жалобами на
боли и офаничение подвижности в мелких суставах кистей и стоп, л>'чезапяст-
ных, плечевых, коленных суставах, утреннюю скованность в суставах длитель¬
ностью 30—40 мин, эпизоды повышения АД до 160/90 мм рт.ст, сопровождаю¬
щиеся головной болью, прси\гущественно в затылочной области, ощущение
неритмичного сердцебиения, головокружение, общую слабость.Из семейного анамнеза известно следующее: отец умер в возрасте 69 лет, стра-
да.,1 раком легких; мать умерла в возрасте 59 лет (заболевание сердиа?), сестра
умерла в возрасте 67 лет, перенесла острый инфаркт миокарда, брат умер в воз¬
расте 55 лет (онкологическое заболевание?); сын 32 лет практически здоров.Из анамнеза жизни: родилась в 1940 г. в Калужской области, по профессии
инженер, с 1989 г. не работает, инвалид 1 группы по основному заболеванию.
Вредных привычек нет Менопауза с 49 лет. В 1972 г. ставшіся диагноз эрозии
шейки матки, проводилась терапия, В детстве часто болела ангинами, в 1990 г.
(в возрасте 50 лет) перенесла криодеструкцию миндалин. В возрасте 24 лет
была оперирована по поводу адгезивного правостороннего отита. В 1994 г.
выявлена желчекаменная болезнь. Аллергологический анамнез не отягощен.Анамнез заболевания (рис. 2S.I): считает себя больной с лета 1983 г., когда
впервые после отдыха на юге, пребывания на солнце стали беспокоить сильные
боли в колеіиіьіх и лучезапястных суставах, появился субфебрилитет. В ана¬
лизах крови выявлен положительный РФ, была консультирована в Научно-
исследовательском институте ревматологии РАМН, Лечилась ибупрофеном,
делагилом, препараты принимала нерегулярно. До 1987 г. чувствовала себя
Глава 28. Случай длительного течения синдрома Фелти...593удовлетворительно. В апреле 1987 г. после санаторно-курортного лечения
появились боли в плечевых суставах и изменения в анализах крови (впервые
выявлены нейтропения, лимфоцитоз), далее стали беспокоить боли и скован¬
ность в голеностопных суставах, затем скованность в коленных и локтевых
суставах, боли в шейном отделе позвоночника. Дважды (осенью 1987 и 1988 гг)
обследовалась в Научно-исследовательском институте ревматологии РАМН,
где с целью исключения лимфопролиферативного заболевания (по поводу
изменений Б анализах крови) проводились стернальная пункция и трепано-
биопсия. При осмотре пациентки в области локтевого сустава выявлен рев¬
матоидный узелок. В это же врелш было высказано предположение о Haj’lH4HH
синдрома Фелти. С 1988 г. ста-ш получать преднизолон в дозе 5—10 мг/сут,
плаквенил 200 мі/сут, внутрисуставно вводился кснатог с положительным1983 г.
НИИР1987-
1988 гг.
НИИР РАМН▲ А ▲ АРевм. узелок1990 г.
ФТК1990-
1991 гг.
ФТК▲ ▲▲Спленомегалия1991-1999гг.200420062008Утренняяскован¬ностьСубфеб¬рилитет/3Уровеньлейкоци¬тов3,5 тыс./мл,
п/я о, с/я 21,
зернистость2,0 тыс./мл,
п/я о, с/я 583,0тыс./мл,
п/я 13%;
с/я 352 тыс.
мл,
Тр. 98
тыс./
мл,7тыс./мл3,17тыс./млитыс./млСтерналь¬
ная пункция
трепано
биопсияПанариции,Боли вНеод-паронихии,поясни¬но-удаление пр.це:крат-фаланги 1компрес¬ныепальца лев.сионныегоспи¬стопыіерело-тали¬мызацииTh12L2-3АДТерапияНПВП.
делагил
2 р/недПреднизо¬
гон1 о мг/сут,
кеналог в/с,
НПВППТ ПЗ 750
мг №3
плаквенил
200 мг/сут,
в/с метипредПТ ПЗ
1 г № 3,
ЛФК,
плакве¬
нил
200
мг/сутСуль-фаса-лазинПТМе¬ти¬пред(4мг),плак-ВЄ'НИЛПлакве-нил,мо-ва-лисМети¬
пред
8 мг,
плакве¬
нилРис. 28л. Анамнез больной Л., 68 лет
594 Системные заболеванияэффектом, в 1990 г. появилась повышенная сютонность к нагноительным про¬
цессам (панариций, паронихии, постоянные боли в горле). В феврале 1990 г. по
поводу нагноения было произведено удаление дистальной фаланги 1-го пальца
левой стопы.С мая—июня 1990 г. наблюдается в Факультетской терапевтической клинике
им. В.Н. Виноградова с диагаозом: ревматоидный артрит с системными про¬
явлениями (синдром Фелти, амиотрофии, сетчатое ливедо, полинейропатия).
При обследовании впервые бьша выявлена спленомсгалия, а в анализах —
помимо лейкопении до 2 тыс., протеинурия (0,225%о), гематурия, лейкодиту-
рия. В связи с высокой активностью заболевания (ПТ степень) и противопока¬
заниями к назначению базисных препаратов (гнойные процессы, лейкопения,
патология мочевого осадка) в 1990 г проводились пульс-терапия преднизоло-
ном (750 мг внутривенно капельно), внутрисуставные инъекции метипреда (в
лучезапястные суставы) с умеренным положительным эффектом. В этом же
году по поводу хронического тонзиллита и казеозньгх пробок в лакунах про¬
ведена криодеструкция миндалин. Также проводилась биопсия на выяатение
амилоида (результат отрицательный).В авіусте 1990 г. после травмы (падение на спину) появились и стали
нарастать боли в поясничном и нижнем грудном отделах позвоночника.
В Факультетской терапевтической клинике им. В.Н. Виноградова был диагно¬
стирован генерализованный остеопороз с компрессионными переломами тел
Th,j и Ц_з позвонков. В мае 1991 г. по поводу выраженной активности заболе¬
вания (анемия, нейтропения, СОЭ 51 мм/ч) в Факультетской терапевтической
клинике им. В.Н. Винофадова был проведен повторный курс пульс-терапии
преднизолоном по 1 г (внутривенно капельно № 3), продолжала получать плак-
венил 200 мг/сут, внутрисуставно вводился кеналог (в коленные, голеностоп¬
ные, лучезапястные суставы). Также проходила курсы физиолечения, массажа,
лечебной физкультуры.с 1991 по 1999 гг пациентка неоднократно госпитализировалась в отделение
для динамического наблюдения. Уровень лейкоцитов в анализах около 3 тыс.,
продолжала получать плановую терапию. В связи с обострением суставного
синдрома в марте 1999 г находилась на лечении в Факультетской терапевтиче¬
ской клинике им. В.Н. Виноградова, где проводилась терапия диклофенаком,
сульфассшазином 500 мг/сут (был отменен в связи с усугублением лейкопении
до 2 тыс.), пульс-терапия преднизолоном 500 мг/сут в связи с лейкопенией
и тромбоцитопенией (98 тыс.), а после отмены сульфасалазина повторная
пульс-терапия преднизолоном в дозе 250 мг/сут, через 1 нед — 500 мг/сут,
курс плазмафереза (№ 8), физиотерапия. После выписки принимала метипред
6 мг/сут, начала прием кальция ДЗ по 1 таб. 2 раза в день. В начале лета 1999 г,
отмечалось нагноение ревматоидного узла на правой стопе. Было проведено
вскрытие абсцесса, однако длительно сохранялась незаживающая рана, обо¬
стрился суставной синдром, в связи с чем поступила в Факультетскую терапев¬
тическую клинику им. В.Н. Виноградова, где проводилось лечение метипредом4 мг/сут, диклофенаком, обзиданом (в связи с тенденцией к тахикардии), вве¬
дение ксналога в плечевые и дипроспана в коленные суставы, перевязки раны
Глава 28. Случай длительного течения синдрома Фелти.,, 595с левомеколевой мазью. С этого же времени отмечает периодические подъ¬
емы АД до 170—І80/100 мм рт.ст. Очередная госпитализация в Факультетскую
терапевтическую клинику им. В.Н. Виноградова в марте 2004 г; проводилось
лечение плаквенилом, мовалисом, изоптином SR 240 мг/сут, омезом 20 мг/сут.,
тренталом, курсы физиотерапии.До осени 2005 г. чувствовала себя удовлетворительно, потом стала отмечать
боли по ходу 5-6-ГО ребер, в коленных суставах. Поступила в Факультетскую
терапевтическую клинику им. В.Н. Виноградова в 2006 г для коррекции тера-
ПШІ и обследования. В анализах лейкоциты 3,17 тыс., СОЭ 16 мм/ч, СРВ 0,49,
РФ 147 МЕ/мл; проводилась терапия плаквенилом 200 мг/сут, мовалисом7,5 мг/сут, подобрана антигипертензивная терапия моноприлом 20 мг/суп
Продолжала прием рекомендованных препаратов. Самочувствие оставалось
удовлетворительным. Значительное ухудшение состояния — с лета 2008 г,
когда без видимого провоцирующего фактора появились сильные боли в
мелких суставах кистей и стоп, лучезапястных, коленных:, плечевых суста¬
вах, выраженная утренняя скованность длительностью около 30—40 мин.
Увеличила дозу принимаемого мелоксикама до 15 мг/сут. Болевой синдром
незначительно уменьшился. В октябре 2008 г. был выполнен общий анализ
крови, выявлены значительная лейкопения (до 1,9 тыс.), лимфоцитоз, СОЭ12 мм/ч. Продолжала прием нестероидных противовоспалительных препа¬
ратов с незначительным положительным эффектом. Затем самостоятельно
начала прием метипреда 2 таб./сут (с середины ноября) с некоторым улу^іше-
нием состояния — несколько уменьшилась интенсивность болевого синдрома;
продолжает прием плаквенила. Также сохраняются эпизоды повышения АД до
160/90 мм рт.ст. — пациентка прекратила прием моноприла. Госпитализирована
для обследования, коррекции терапии.При осмотре обращали на себя внимание; генерализованные амиотрофии,
ульнарная девиация кистей рук, выраженная деформация мелких суставов
кистей и стоп по типу «бутоньерки», деформация коленных:, голеностопных,
лучезапястных суставов, ограничение активных и пассивных движений в них.В анализах при поступлении: в общем анализе крови выявлено снижение
уровня гемоглобина до 118 г/л (эритроциты 4,2 \lth, цветовой показатель0,84); кроме того, отмечается выраженная лейкопения (1,71 тыс.), нейтро-
пения (34%), тромбоцитопения (129,1 тыс.); СОЭ 8 мм/ч. Ъ биохимическом
анализе крови отмечается повышение уровня азота мочевины (9,8 ммоль/л)
при нормальном значении креатинина (0,9.1 мг/дл); общий белок 81 г/л, аль¬
бумин 40,4 г/л, общий билирубин 13,9 мкмоль/л, ACT 40 Ед/л, АЛТ 20 Ед/л,
у-ГГ 27 Ед/л, глюкоза 4,6 ммоль/л. При исследовании липидного спектра
вьывлена гиперлипидемия IV типа: триглицериды 184 мг/дл (50-150), общий
холестерин 182 мг/дл, ЛПВП 45,2 мг/дл, ЛПНП 100 мг/дл, Л ПОПП 36,8 мг/дл
(10—30). При электрофорезе белков альбумин 53,4% (54,7—68,7), а,-глобулины
3,2% (1,8-3,3), а^-глобулины 4,9% (3,7—13,1), р-глобулины 13,8% (8,9-13,6),
у-глобулины 24,7% (8,4-18,3). В иммунологических анализах крови отмечает¬
ся небольшое повышение уровня РФ (33 Ед/мл) при нормальном значении
СРВ (0,46 мг/дл), некоторое повышение уровня IgA (460 мг/дл). В общем
596Системные заболеванияанализе мочи — белок (0,055%о), большое количество бактерий, в анализе мочи
по Нечипоренко — эритроцитурия 1250/мл, что незначительно превышает
норму; в суточном анализе мочи — следы белка, роста микрофлоры при посеве
мочи не въывлено.При постушіении у пациентки на ЭКГ регастрировался синусовый ритм,
отмечены также признаки гипертрофии левого желудочка. Однако на следую¬
щий день пациентка предъявила жалобы на ощущение неритмичного учащен¬
ного сердцебиения, что сопровождалось выраженной общей слабостью. На
ЭКГ — мерцательная аритмия с ЧСС около 110/мин (рис. 28.2). Синусовый
ритм восстановлен внутривенным введением кордарона.Впоследствии выполнена Эхо КГ: КДР левого желудочка 4,6 мм, КДО 65 мл,
КСО 19 М.І, тМЖП 1,2 см, ЗС 1,2 см; ФВ левого желудочка 71 %. Диастолическая
функция снижена, Е/А 0,54, Левое предсердие 42 мл (4,6x3,5 см), правое пред¬
сердие 39 мл (4,3x3,4 см). Аортальный клапан — уплотнение створок и фиброз¬
ного кольца, другие клапаны не изменены. Стенки аорты уплотнены.При суточном мониторировании ЭКГ по Хо.шеру: базовый ритм синусовый.
В течение всего дня непрерывно — рецидивирующие пароксизмы фибрилля¬
ции предсердий максимально около 4 ч с ЧСС 50-140/мин, паузой до 2 с в
ночное время.При УЗИ органов брюшной по.тсти выяатено увеличение печени за счет
правой доли (до 169 мм), паренхима однородной структуры, изменена по типу
жировой дистрофии. Признаки калькулезного холецистита. Селезенка увели¬
чена в размерах до 170x78 мм, сниженной эхогенности. Селезеночная вена на
уровне тела поджелудочной железы до 13 мм.Выполнена также рентгенография органов грудной клетки (рис. 28.3): в лег¬
ких диффузный пневмосклероз, на боковой рентгенограмме в грудном отделе
позвоночника определяется резко выраженный кифоз, распространенный
остеохондроз с максимальным снижением высоты межпозвонковых дисков на
высоте кифоза, деформирующий спондилез, спондилоартроз.При рентгенографии кистей и стоп (рис. 28.4) выявлены типичные для рев¬
матоидного артрита изменения.Рис- 28.2. Электрокардиограмма больной Л. во время пароксизма мерцательной арит¬
мии. Скорость записи 25 мм/с. Стандартные отведения
Глава 28. Случай длительного течения синдрома Фелти..,597На основании жа.юб, данных
анамнеза, объективного осмотра,
с учетом данных лабораторно-
инструментальных исследований
основной диагноз сформулирован
следующим образом. Ревматоидный
артрит: серопозитивный полиартрит
с системными проявлениями (син¬
дром Фелти, ревматоидные узелки,
амиотрофии, лихорадка в анамнезе,
сетчатое ливедо, геморрагический
васкулит в анамнезе), II степени Рис. 28.3. Рентгенография органов грудной
активности, IV рентгенологической клетки, прямая проекция. Пояснения в тексте
стадии, функциональная недостаточность III степени. Генерализованный осте-
опороз смешанного генеза с компрессионными переломами Th^В клинике проводилась терапия: метипред 4 мг 2 таб. утром, мовалис 15 мг,
затем 7,5 мг/сут, плаквенил 200 мг 1 таб. вечером, моноприл 10 мг/суг, тромбо-
АСС 100 мг/сут, кордарон (отменен в связи с сохранением пароксизмов мерца¬
тельной аритмии). С учетом выраженной лейкопении, нейтропении проведена
пульс-терапия метипредом 500 мг № 3. После этого в анализах отмечена отчет¬
ливая положительная динамика — повышение уровіія гемоглобина (139,2 г/л),
лейкоцитов (5,6 тыс.), нейтрофилов (72%), тромбоцитов (202 тыс.). Однако в
течение 2 нед при контрольных анализах вновь отмечалось снижение уровня
лейкоцитов до 3,2 тыс. (нейтрофилы 54%), в связи с чем доза мстипреда была
увеличена до 4 таб./с>'т.Синдром Фелти (СФ) — особый вариант течения серопозитивного ревма¬
тоидного артрита, отличительными проявлениями которого, помимо харак¬
терных эрозивно-деструктивных поражений суставов, являются лейкопения
(нейтропения) и спленомегалия.Ревматоидный артрит является, по-видимому, весьма древним заболе¬
ванием. При раскопках древних индейских поселений обнаружены остатки
скелетов (4500 лет до н.э.) со следами эрозивного поражения суставов. ПервоеРис. 28.4. Ретттгенография кистей (слева) и стоп (справа)
598 Системные заболеванияописание клинической картины генерализованного деформирующего артри¬
та, вызывающего инвапидизацию больного, принадлежит Галену (129 или
131 — около 200). В 1677 г. Sydenham описал заболевание суставов, характери¬
зующееся хроническим течением и формированием деформаций по типу «шеи
лебедя». Первое достоверное описание клинической картины ревматоидного
артрита относится к 1800 г и принадлежит Landre-Beauvais, который относил
это заболевание к группе подагрических артритов и назвал «простая астениче¬
ская подагра». Термин «ревматоидньгй артрит» был предложен в 1858 г. Garrod
в труде «Природа и лечение подагры и ревматоидной подагры». В 20-х гг XX в.
из группы ревматоидного артрита был выделен остеоартроз, в конце 50-х гг.
XX в. — серонегативные артриты. В 1924 г. американский врач Augustus Felty
описал особую форму первично-хронического полиартрита «с опухолью селе¬
зенки, лейкопенией, анемией и коричневатой пигментацией открытых участ¬
ков тела».Ассоциация ревматологов России предлагает следующее определение син¬
дрома Фелти: синдром Фелти — симптомокомплекс, включающий, помимо
характерного для ревматоидного артрита тяжелого эрозивно-деструктивного
поражения суставов, нейтропению, спленомегалию, гепатомегалию, вне-
суставные проявления (васкулит, нейропатия, легочный фиброз, синдром
Шегрена), гиперпигментацию кожи и высокий риск инфекционных ослож¬
нений.Главным признаком синдрома Фелти является нейтропения. Возможность
использования спленомегалии в качестве диагностштеского критерия огра-
ни^гена тем, что при синдроме Фелти ее степень может сильно варьировать от
значительного увеличения селезенки (до 3-4 норм) до минимальной степени
выраженности у 5—10% больных. Кроме того, умеренное увеличение селезенки
встречается у достаточно большого числа больных неосложненными формами
ревматоидного артрита, с чем связано предложение некоторых авторов вообще
исключить этот признак из критериев диагноза синдрома Фелти.У некоторых больных с синдромом Фелти встречается гепатомегалия
вследствие узловой регенеративной гиперплазии печени с формированием
синдрома портальной гипертензии и возможными осложнениями в виде кро¬
вотечений из варикозно расширенных вен пищевода, желудка и геморроидаль¬
ных вен. Причиньг формирования узловой гиперплазии печени при синдроме
Фелти точно не известны; возможно, важную роль в ее возникновении играет
ревматоидный васк>:литНа момент установления диагноза синдрома Фелти у большинства больных
уже имеется тяжелое эрозивно-деструктивное поражение суставов. Однако
описаны случаи клинически мало выраженного суставного синдрома (чаще
всего при значительной лабораторной активности) и даже дебюта так называе¬
мой беспричинной нейтропении до появления суставного синдрома. В таких
случаях возникает необходимость в проведении дифференциальной диа¬
гностики с онкогематологическими заболеваниями. Тяжесть инфекционных
осложнений (при уровне гранулоцитов выше 1500/мм^) также напрямую со
степенью нейтропении не коррелирует.
Глава 2S. Случай длительного течения синдрома Фелти... 599Синдром Фелти чаще всего развивается на фоне длительно текущего (более
10 лет) серопозитивного ревматоидного артрита в среднем у 1—3% больных.
Пик заболеваемости приход^ггся на возраст 50-70 лет, большинство боль¬
ных — женщины. Существует' наследственная предрасттоложенность к Тїгжелому
деструктивному поражению суставов при ревматоидном артрите и развитию
синдрома Фелти. Это подтверждается обнаружением у 95% больных с синдромом
Фе.тги аллеля DR4 антигена главного комплекса гистосовместимости класса П.
Характерной особенностью этого аллеля считают специфическую аминокис¬
лотную последовательность в одной из цепей HLA, которая получила название
«обший эпитоп» {sharedepitop — SE). Существует несколько гипотез о связи носи-
тельства SE с развитием поражения суставов. Предполагае'гся, что носительство
SE приводит к экспрессии на поверхности антигеїшрезентируюших клеток HLA-
DR, эффективно презентируюших CD4+ Т-лимфоцитам артритогенный пептид.
Согласно другой модели, при возникновении молекулярной мимикрии между SE
и артритогенным антигеном сам SE может индуцировать активацию Т-клеток.Выявление аллеля DR4 не только имеет важное диагностическое и проїтто-
стического значение, но и влияет на тактику ведения таких больных. Показано,
что у носителей данного гена в случае действия огфеделенных факторов
внешней среды (курение, прием оральных контрацептивов, употребление
кофеинсодержащих продуктов) резко увеличивается риск развития тяжелых
форм серопозитивного ревматоидного артрита. Модификация этих факторов
риска позволяет отдалить развитие инвалидизирующих стадий ревматоидного
артрита.Синдром Фелти характеризуется плохим прогнозом: около трети больных
(36%) погибает в течение 5 лет с момента установления диагноза, чаще всего
от фатальных инфекционных осложнений. Кроме того, увеличивается риск
развития неходжкинских яимфом. Довольно редким осложнением является
профузное кровотечение из варикозно расширенных вен пищевода. В целом
частота внесуставных проявлений при синдроме Фелти выше, чем при неос¬
ложненных формах ревматоидного артрита {табл. 28.1).Центральным патогенетическим звеном синдрома Фелти является грануло-
цитопения, однако механизмы ее развития сложны и изучены недостаточно.
Существует несколько гипотез возникновения гранулопитопении при синдро¬
ме Фелти;• циркуляция антигранулоцитарных антител (связываясь с мембраной гра-
нулоцитов, способствуют их разрушению клетками ретикулоэндотелиаль-
ной системы) и избыточное образование иммуткных комплексов;• подавление гранулоцитопоэза (пролиферации клеток-предшественников)
гуморальными медиаторами или супрессорными Т-;шмфоцитами;• синтез антител против гранулоцитарного колониести\іулируюшего факто¬
ра и/или снижение чувствительности миелоидных клеток к нему;• образование факторов, индуцирующих апоптоз нейтрофилов (FasL);• разрушение фанулоцитов в селезенке.Лечение синдрома Фелти разработано недостаточно. Стандартных прото¬
колов ведения таких больных не существует, что связано с полным отсутствием
600Системные заболеванияТаблица 28.1Внесуставные проявления и иммунологические нарушения при синдроме ФелтиПроявлешіяЧастота возникновения, %Ревматотиные узлы76Похудание68Синдром Шеірена56Лимфаценопатия34Язвы голеней25Плеврит19ПигментацЕся кожи17Невропатия17Эписклсрит8Ревматоидный фактор100 (высокие титры)Антинуклеарный фактор62-80Иммунные комплексы100 (высокий уровень)крупных рандомизїфованньїх многоцентровых исследований, которые могли
бы позволить оценить эффективность того или иного способа лечения. Это,
в свою очередь, обусловлено крайне малым числом пациентов с данной пато¬
логией. П0ЭТ0\ТУ лечение пациентов с синдромом Фелти ЯВ.1ЯСТСЯ процессом
«творческим»: выбор препарата для лечения остается полностью на усмотрение
лечащего врача.Основной целью лечения является борьба с іранулопитопенией для предот¬
вращения развития серьезных инфекционных осложнений или их лечения.
Кроме того, в пели лечения входят коррекция анемии, тромбоцитопении;
подавление симптомов артрита и системных проявлений, что необходимо для
улучщения качества жизни пациентов и увеличения ее продолжительности.Критериями эффективности лечения синдрома Фелти являются следующие.Критерии высокой эффективности лечения:• увеличение количества гранулоцитов до 2000/мм^и более;• улучшение как мини\тум 2 из следующих параметров;- снижение частоты возникновения инфекционных осложнений на 50%;- снижение частоты развития кожных язв на 50%;- снижение частоты развития приступов лихорадки на 50%.Критерии умеренной эффективности лечения:• увеличение количества гранулоцитов до 1000-2000/мм^;• улу’ішение как минимум 2 из следующих параметров:- снижение частоты возникновения инфскционньгх осложнений на 25%;- снижение частоты развития кожных язв на 25%;- снижение частоты развития приступов лихорадки на 25%.В лечении больных с синдромом Фелти используется весь спектр лекар¬
ственных препаратов, применяемых в качестве базисной терапии ревматоид¬
ного артрита, а также глюкокортикоиды и биологические препараты (моно¬
клональные антитела, колониестимулирующие факторы — гранулоцитарный
Глава 28. Случай длительного течения синдрома Фелти... 601и гранулоцитарно-макрофагальный). Хирургическое лечение (спленэкто-
мия) является «методом отчаяния» при неэффективности медикаментозной
терапии.Мелика ментозное лечение:• метофексат;• парентеральные соли золота;• антагонисты пиримидинов (лефлуномид);• гидроксихлорохин;• иеницилламин;• циклоспорин;• глюкокортикоиды;• высокие дозы у-глобулиноіз;• ритуксимаб;• колониестимулирующие факторы (G-CSF, GM-CSF);• ттсрсливание компонентов крови?Хирургическое лечение: снленэктомия.Парентеральные соли золота, являясь достаточно старыми препаратами,
обладают большим количеством побочных действий и эффективны лишь при
умеренной нейтропении и отсутствии тяжелых инфекционных осложнений.
Их эффективность в таком случае не превышает 60%.Переливание компонентов крови практически не применяется, за исключе¬
нием случаев тяжелой анемии и тромбоцитопении при выраженном синдроме
гиперспленизма. Это связано с высоким риском осложнений трансфузий, что
особенно характерно для препаратов донорских лейкоцитов (СОПЛ и др.)-
Кроме того, имеются данные о высоком риске сердечно-сосудистых осложне¬
ний у больных с синдромом Фелти, получавших гемотрансфузии.Наибольшее количество исследований посвящено применению метотрек¬
сата, глюкокортикоидов и колониестимулирующих факторов.Метотрексат является одним из основных препаратов для базисной тера¬
пии ревматоидного артрита. В большинстве слу^іаев поводом для его назна¬
чения является выраженность суставного синдрома, а не гематологические
наруїпения. В литературе описаны примеры назначения метотрексата именно
в качестве препарата для лечения гранулоиитопении при синдроме Фелти.
В большинстве случаев при назначении метотрексата в среднетерапевтических
дозах (7,5—10 мг в неделю) в среднем через 4-5 нед приема удавалось достичь
улучшеі£ия гематологической картины. Максимум эффекта наблюдался на
6-12-й нед приема.Однако не следует забывать, что метотрексат сам обладает миелосупрессив-
ной активностью и может вызывать тяжелую лейкопению віьтоть до афану'
лоцитоза. Поэтому принять решение о назначении этого препарата пациенту
с исходно имеющейся нейтропенией психологически бывает очень непросто.
При развитии лейкопении у пациента, лтительно получающего метотрек¬
сат, возникает необходимость в проведении дифференциальной диагности¬
ки между мислосупрессией и синдромом Фелти. в этом случае решающее
значение имеет биопсия костного мозга; при лейкопении вследствие приема
602 Системные заболеванияметотрексата выяшшется картина угаетения кроветворения, что не характерно
для синдрома Фелти.Широко в лечении ревматоидного артрита, в том числе синдрома Фелти,
применяются глюкокортикоиды. Они обладают двойственным действием на
иммунную систему человека, активируя одни механизмы и подавляя другие.
Из-за этого глюкокортикоиды имеют ряд как потенциально полезных эффек¬
тов при синдроме Фелти, так и отрицательных.«Полезные» эффекты глюкокортикоидов при синдроме Фелти:• увеличивают нейтрофилопоэз;• повышают чувствительность клеток костного мозга к G-CSF, GM-CSF и
интерлейкинам;• снижают чувствительность клеток костного мозга к действию химио- и
лучевой терапии;• снижают эозинофилопоэз;• тормозят созревание и дифференцировку Т- и В-лимфоцитов;• снижают продукцию lgB-лимфоцитами и плазматическими клетками.Отрицательные эффекты глюкокортикоидов при синдроме Фелти:• угнетают фагоцитарную активность;• замедляют хемотаксис в очаге воспаления;• снижают экссудацию в очаге воспаления.Учитывая, что больные с синдромом Фелти страдают преимушественно
бактериальными инфекциями, угнетение фагоцитоза и замедлеіше хемотак¬
сиса иммунокомпетентных клеток в очаге воспапсния приводит к увеличению
риска более тяжелого течения и генерализации инфекций. Этот факт был про¬
демонстрирован в проведенных исследованиях: риск развития инфекционных
осложнений на фоне терапии глюкокортикоидами у больных с синдромом
Фелти повышался.Когда же применяют глюкокортикоиды? Для быстрого улучшения гемато¬
логической картины больным назначают достаточно высокие дозы гормонов
(более 30 мг/сут), при афанулоцитозе проводятся курсы пульс-терапии по стан¬
дартной схеме. Однако, несмотря на быстрое увеличение числа гранулоцитов в
периферической крови, эффект от такого лечения временный и при попытке
снижения дозы глюкокортикоидов нейфопения чаще всего рецидивирует.Весьма перспективным направлением в лечении больных с синдромом
Фе.тги является исполыювание колониестимулирующих факторов (CSF) —
гранулоцитарного (G-CSF) и гранулоцитарно-макрофагального (GM-CSF).
CSF — гликопротеины, у^іаствуюшие в регуляции гранулоцитопоэза в орга*
пизме человека. Они стимулируют пролиферацию и созрсванис прекурсоров
фанулоцитов, а также активируюі’ зрелые нейтрофильт. После их назначения
достоверно увеличивается общее число лейкоцитов и число нейтрофилов в
периферической крови, кроме того, некоторые авторы указывают на умень¬
шение числа больших фанулярных (зернистых) лейкоцитов в периферической
крови больных, получающих препараты CSF.Пул больших фанулярных лейкоцитов представлен N К-клетками и цито-
токсическими Т-лимфоцитами. Было отмечено, что у больных с синдромом
Глава 28. Случай длительного течения синдрома Фелти... 603Фелти в периферической крови циркулирует увеличенное число больших
гранулярных лимфоцитов, что, как считается, может иметь определенное пато¬
генетическое значение в развитии нейтропении; однако в настоящий момент
роль больших гранулярных лимфоцитов точно не известна.CSF используются преимущественно в онкологии для коррекции миелосу-
прессивного синдрома при проведении химиотерапии, а также в трансплан¬
тологии (для вьщеления стволовых полипотентных клеток из периферической
крови), в этих случаях курс приема препаратов CSF чаще всего короткий и
число возникающих побочных эффектов сравнительно невелико. При лече¬
нии гранулоцитопении у больных с синдромом Фелти возникает необходи¬
мость в неопределенно долгом применении этих препаратов (есть описание
более чем 3-летней непрерывной терапии), с чем связано больщое количество
побочных эффектов;• тошнота;• гриппоподобный синдром {обшее недомогание, профузные поты);• генерализованные боли в костях;• усиление суставного синдрома (обострение ревматоидного артрита);• кожная сыпь;• тромбоцитопения.Для снижения числа нежелательных эффектов терапии предложены сле¬
дующие меры;• снижение стартовой дозы с постепенным ее увеличением до минимально
эффективной;• уменьшение кратности введения препаратов (чаще до 2 раз в неделю);• использование препаратов негликозилированных G-CSF (филграстин —
нейпоген);• применение совместно с глюкокортикоидами.У большинства больных возникает необходимость в уменьшении дозы или
смене препарата в связи с плохой переносимостью терапии. CSF, синтезируе¬
мые в организме, представлены негликозилированными молекулами. С этим
связана лучшая переносимость препаратов негликозилированных CSF.К хирургическому лечению — спленэктомии — прибегают лишь в случае
тяжелых инфекционных осложнений и неэффективности медикаментозной
терапии, у 80% больных спленэктомия вызывает быстрый (в течение несколь¬
ких часов после операции!) рост числа нейтрофилов в периферической крови,
однако эффективность оперативного вмешательства представляется сомни¬
тельной: у 25% больных гранулоцитопения рецидивирует, у 26—60% рециди¬
вируют тяжелые инфекционные осложнения, а у 12% операция оказывается
неэффективной — гранулоцитопения персистирует.Комментарий Н.В. Петуховой — заведующей лечебно-диагностическим отделе¬
нием Центра суставной боли Первого МГМУ им. И. М. СеченоваРевматоидный артрит — хроническое системное иммуноопосредован-ное воспалительное заболевание с преимущественным поражени¬
ем периферических (синовиальных) суставов по типу симметричного
604 Системные заболеванияэрозивно-деструктивного полиартрита, сопровождающееся пролифераци¬
ей синовиоцитов и неоангиогенезом. что сближает его с онкологическими
заболеваниями. Типичный суставной синдром может сопровождаться
разнообразными системными проявлениями (лихорадкой, похуданием,
лимфаденопатией, мышечной атрофией, анемией, гепатоспленомегалией,
серозитами, поражением легких, гломерулонефритом, поражением глаз,
изменениями психологического статуса), которые в первую очередь харак¬
терны для серопозитивного варианта болезни. Особым вариантом серо¬
позитивного ревматоидного артрита является синдром Фелти, развива¬
ющийся у очень небольшого числа больных (0,5-3%). Характерная его
особенность — нейтропения с высокой склонностью к инфекционным
осложнениям, при этом цитопения при ревматоидном артрите всегда
требует проведения дифференциального диагноза между лекарственными
поражениями кроветворения (все базисные препараты могут вызывать
тяжелую лейкопению вплоть до агранулоцитоза) и собственно развитием
синдрома Фелти.Демонстрация пациентки Л. с синдромом Фелти преследовала несколько
задач. Во-первых, мы хотели бы привлечь внимание к гетерогенности кли¬
нических вариантов ревматоидного артрита, которые обусловлены генети¬
ческими, половыми, возрастными и другими особенностями. Во-вторых,
учитьгеая отсутствие сведений доказательной медицины по поводу преиму¬
щества того или иного лекарственного средства в терапии синдрома Фелти,
хотелось бы остановиться на обсуждении наиболее распространенных под¬
ходов к лечению этого состояния.Среди базисных препаратов большинство авторов отдает предпочте¬
ние метотрексату и парентеральным солям золота, глюкокортикоиды
относятся к препаратам второй линии. При это.м, как говорилось ранее,
у всех базисных препаратов основным побочным эффектом является
лейкопения. В связи с этим назначение нашей пациентке при наливши
всего лишь 1700 лейкоцитов любого из базисных препаратов нам пред¬
ставлялось весьма рискованным, тем более что печальный опыт развития
агранулоцитоза у больной, принимавщей метотрексат в сочетании с
нестероидными противовоспалительными препаратами (диклофена-
ком), у нас был.Соли золота в настоящее время малодоступны: отечественный препа¬
рат кризанол отсутствует, а немецкий препарат тауредон в Российской
Федерации не зарегистрирован. Пероральные препараты золота (аурано-
фин) не оправда.1И возлагавшихся на них надежд из-за длительного латент¬
ного периода действия и наличия частых гастроэнтерологических побочных
эффектов.Применение гранулоцитостимулируюшего фактора у нашей пациентки
могло быть весьма полезным, однако, к сожалению, возможность лечения
этим препаратом ограничена из-за его высокой стоимости и малой доступ¬
ности.
Глава 28. Случай длительного течения синдрома Фелти... 605В связи с этим нами выбрана следующая тактика: падиентке назначены
гормоны (метипред) в дозе 8 мг/сут и проведена пульс-терапия этим сред¬
ством по 500 мг внутривенно в течение 3 последующих дней, в результате
состояние больной улучшилось, значительно улїеньшились боли в суставах,
количество лейкоцитов достигло 5590. Пациентка в удовлетворительном
состоянии бьша выписана из клиники.Таким образом, синдром Фелти представляет собой особый редкий вари¬
ант течения серопозитивного ревматоидного артрита, главным признаком
которого является нейтропения различной степени выраженности; возни¬
кает у наследственно предрасположенных лиц и характеризуется тяжелым
течением и плохим прогнозом Б основном из-за высокого риска развития
фатальных инфекционных (бактериальных) осложнений. Лечение больных
с синдромом Фелти разработано недостаточно. Пи одна из применяющихся
в настоящее вре\ія схем лечения не обеспечивает стабильного положитель¬
ного результата.
Глава 29НЕОБЫЧНЫЙ ВАРИАНТ ТЕЧЕНИЯ ВИСЦЕРАЛЬНОГО
ТУБЕРКУЛЕЗА С РЕФРАКТЕРНОЙ АНЕМИЕЙН.Д. Саркисова, О.В. Благова, А.В. Недоступ,
Е.Л. Лукина, Д.Л. СапожниковТуберкулез — древнейшее инфекционное заболевание, сложный, логичный
и загадочный в своем развитии патологический процесс, в изучении которого
большую роль сыграли отечественные патологи, и одновременно — постоян¬
ный спутник клиницистов любой специальности. Постоянная насторожен¬
ность в отношении туберкулеза, тесное взаимодействие хирургов, терапевтов
и морфологов позволили достаточно быстро диагностировать его внелегочную
форму в представленном клиническом наблюдении (туберкулез лимфатиче¬
ских узлов, плеврит, перикардит), однако особенностью заболевания пожилой
больной бььча тяжелая рефрактерная к лечению гиперхромная анемия, воз¬
можные механизмы которой и подходы к лечению подробно обсуждаются
специалистом-гематологом. Кроме того, на фоне в целом эффективной тубер¬
кулостатической терапии у больной отмечено появление множественных кост¬
ных переломов и субплевральной округлой тени в верхушке правого легкого,
что потребовало проведения дифференциальной диагностики с раком и поста¬
вило вопрос об оправданности дальнейшей инвазивной диагностики.Больная П,, 80 лет, переведена из Факультетской хирургической к.чиники
им. Н.Н. Бурденко в отделение кардиологии Факультетской терапевтической
клиники им. В.Н. Виноградова 15 мая 2006 г. с жалобами на выраженную
общую слабость, одышку при незначительных физических нагрузках, голово¬
кружения, неустойчивость при ходьбе, ежевечерние подъемы температуры до
37,2—38,7 °С, обильные ночные поты, снижение аппетита, резкое похудание за
последние 3 мес (точнее оценить затрудняется), периодически возникаюш,ее
ощущение дискомфорта в левой половине грудной клетки, эпизоды учащенно¬
го ритмичного сердцебиения, которые купируются самостоятельно.Из семейного анамнеза: отец больной погиб на фронте, мать умерла в
90 лет (по-видимому, от инсульта); старший сын (56 лет) курит, долго рабо¬
тал на Севере, на этом фоне у него длительное время отмечается кашель,
при рентгенофафии, выполненной по нашей рекомендации в июне 2006 г.,
очаговых и инфильтративных изменений выявлено не было. Средний сын
(52 лет) страдает артериальной гипертонией, младшие дети (дочь 50 лет и сын
48 лет) и внуки относительно здоровы. Больная родилась и живет в Брянской
области (со старшим сыном); во время войны 3 мес находилась в концлагере.
Работала продавцом. Никогда не курила, питается относительно полноценно.
Гинекологические заболевания отрицает. В 3 года в результате травмы потеряла
Глава 29. Необычный вариант течения висцерального туберкулеза...607левый глаз; детских инфекций не помнит, в дальнейшем никакими заболе¬
ваниями не страдала; никогда не обследовалась и не лечилась стационарно.
Аллергологический анамнез не отягощен.Анамнез заболевания (рис. 29. })'. в последних числах декабря 2005 г после
переохлаждения появилась лихорадка до 38 “С в вечернее время (с умерен¬
ными ознобами и проливным потом ночью). Появились и постепенно нарас¬
тали одышка с выраженным затруднением вдоха, общая слабость, снижение
аппетита, стал беспокоить запор. Занималась самолечением до февраля 2006 г.,
когда в тяжелом состояние бьша госпитализирована в Центральную районную
больницу. Проводилась инфузионная и антибактериальная терапия, в резуль¬
тате которой самочувствие несколько улучшшюсь, снизилась температура тела.
Однако после выписки вновь отмечены нарастание одышки, возобновление
лихорадки до прежних показателей, в связи с чем повторно госпитализирована
в Центральную районную больницу в марте. Был диагностирован правосто¬
ронний экссудативный плеврит, дважды проводилась плевральная пуикция с
удалением в целом около 3 л серозной жидкости. При исследовании пунктата
микобактерий туберкулеза, атипичньгс клеток найдено не было, продолжена
антибактериальная терапия (препараты не известны). Состояние улучшилось:
исчезла одышка, температура снизилась до субфебрильных цифр, улучшился
аппетит, исчез запор.С учетом выраженной анемии, увеличения СОЭ бьши проведены ЭГДС,
бронхоскопия, ирригоскоиия, больная была осмотрена гинекологом, патологииХИ/2005февральмартапрельлихорадканочные поты37 °Сслабость, головокр.одышкаплевральныйвыпотНЬ 4,7 г%анемия ШИМИШИИЯИЕИИантибиотикицелестондиклофенакРис. 29.1. Анамнез больной П., 80 лет
608 Системные заболеваниявыявлено не было. После выписки сохранялись выраженная астения, субфе¬
брилитет. В апреле была направлена в Факультетскую терапевтическую кли¬
нику им. В.Н. Виноградова, где при КТ органов грудной клетки подтверждено
на.1ичие правостороннего экссудативного плеврита. Была госпитализирована
в Факультетскую хирургическую клинику им. Н.Н. Бурденко. В течение 5 дней
проводилась терапия амоксиктавом 3,6 г/сут и метрогилом 100 м^і внутривен¬
но капельно в сочетании с нистатином, трижды — инъекции целестона по 4 мг,
инфузионная терапия (аминостерил, 10% раствор глюкозы), инъекиии гепари¬
на, внуфь получала всрошпирон 50 мг, панангин, рибоксин, однократно пере¬
лита эритродитарная масса; проведена лечебно-диагностическая плевральная
пункция. Самочувствие улучшилось: уменьшились одышка, обшая слабость,
однако лихорадка сохранялась. Переведена в Факу.гьтетскую терапевтическую
клинику им. В.Н. Виноградова для дальнейшего обследования и лечения.При постутении в Факультетскую терапевтическую клинику им. В.Н. Ви¬
ноградова состояние средней тяжести. Конституция астеническая. Температура
тела вечером 37,8 "С (максимальное повышение за время пребывания в клини¬
ке — 38,2 °С). При предшествующем осмотре в Факу.тьтетской хирургической
к*тинике им. Н.Н. Бурденко была выявлена группа уплотненных и увеличенных
(от 6 до 14 мм) бобовидных надключичных лимфатических узлов справа, три
узла были резецированы, над местом их расположения определялся свежий
рубец. Отеков нет. Число дыханий 17/мин, дыхание везикулярное, умеренно
ослаблено в базальных отделах правого легкого, хрипов нет. Сердце не увели¬
чено, тоны звучные, выслушивается слабый систолический итум на аорте. ЧСС
84—90 уд./мин, ритм сердца правильный. АД 100/60 мм. рг.ст, nyjTbc достаточ¬
ного наполнения. Живот мягкий, безболезненный при пальпации во всех отде¬
лах, печень и селезенка не увеличены. Щитовидная железа не увеличена.Далее мы будем излагать результаты обследования, проведенного с 16 апре¬
ля в обеих клиниках. Сразу обратили на себя внимание выраженные измене¬
ния общего анализа крови (фактически ни один показатель не был норма.'іен).
Определялась выраженная анемия (исходно НЬ 47 г/л, повышение его до
58,9 г/л отмечено лишь после переливания крови), цветовой показатель был
устойчиво повышен до 1,1, профессировала лейкопения (с 4,6 до 3 тыс.), в пер¬
вую очередь за счет снижения числа нейтрофилов (с 69 до 23%) с нарастанием
не только относительного количества лимфоцитов (с 26 до 67%), но и абсолют¬
ного (с 1,1 до 2 тыс.). Были значительно увеличены количество фомбонитов
(от 741 до 803 тыс.) и СОЭ (от 81 до 50 мм/ч); уровень ретикулоцитов до начала
терапии не определяется.В биохимическом анализе крови обратили на себя внимание лишь уме¬
ренная гипоальбуминемия (3,3 г/л) и гипергликемия (163 мг/дл), которые
в повторных анализах не определялись. Оставался несколько повышенным
уровень калия (5,2—5,1 ммоль/л). Был нормальным уровень сывороточного
железа (80 мкі/дл). Общий белок 6,7 г%, креатинин 0,7 мг%, азот мочевины13 мг%, мочевая кислота 2,5 мг%, общий билирубин 0,4 мг%, АЛТ 17 Ед/л,
лет 12 Ед/л, у-ГТ 21,1 Ед/л, ЩФ 82 Ед/л), ЛДГ 195 Ед/л, КФК 12 Ед/л, натрий
136 ммоль/л.
Глава 29. Необычный вариант течения висцерального туберкулеза,,.609Были ярко выражены общевоспалительные изменения: диспротеинемия
(альбумин 49,2%, а^-глобулины 5%, аз-глобулины 11%, р-глобулины 12,4%,
у-глобулины 22,4%), десятикратное повышение уровня СРБ (8,42 мг/дл), повы¬
шение уровня иммуноглобулинов А (500 мг/дл) и G (2860 мг/дл). Оставались
нормальными уровень фибриногеиа (3,54 г/л) и анти-О-стрептолизина
(109 МЕ/мл). Австралийский антиген, реакция Вассермана, антитела к вирусу
гепатита С, к ВИЧ отрицательны. ТТГ 1,42 МЕ/л. При двукратном посеве крови
роста микрофлоры не получено.Обилий анализ мочи'. pH 7, удельный вес 1006, прозрачность полная, белка, саха¬
ра, ацетона, желчных пигментов нет, уробилин в пределах нормы, клетки плоско¬
го эпителия в небольшом количестве, лейкотщты и эритроциты единичны в пре¬
парате, слизь в умсренно.м количестве, бактерий немного, в анализе от 25 апреля
отмечалось появление белка, сахара, ацетона, лейкоцитов 5—7 в поле зрения и
эри'фоцитов 2—3 в поле зрения, а также солей мочевой кислоты, однако в дшгь-
нейшем показатели нормализовались. Реакция мочи оставалась щелочной.На ЭКГ {рис. 29.2) отклонений от нормы нет (синусовый ритм, ЧСС 75/мин,
электрическая ось сердца расположена нормально, признаков ише.мии, гипер¬
трофии различных отделов сердца нет, зубец Р 0,1 с, PQ — 0,16 с, QT 356 мс,
корригированный — 398 мс, QRS — 0,09 с). При суточном мониторировании
ЭКГ по Холтеру зафиксирована короткая (5 комплексов QRS) пробежка надже-
лудочковой тахикардии с ЧСС 117/мин, которая субъективно не ощущалась, а
также редкая экстрасистолия (154 желудочковые экстрасистолы и 142 наджелу-
дочковые). ЧСС днем 73-122/мин (ср. 88/мин), ЧСС ночью 63—97/мин (ср. 70/
мин). Ишемической динамики STне выявлено.По данным спирометрии снижена ЖЕЛ (1680 мл, 67%), обструктивных
изменений нетSOaiMva.Ot (АТ-'.С4РС lc4 5 712,CtjРис. 29,2. Электрокардиофамма больной П. Скорость записи 25 мм/с
610 Системные заболеванияПри Эхо КГ расширения камер сердца, гипертрофии стенок и снижения
ФВ левого желудочка ііе выявлено, в перикарде обнаружено небольшое коли¬
чество жидкости (по задней и боковой стенкам — 0,8 см, по передней стенке —0,4 см, по правому контуру — 0,9 см); клапаны уплотнены, свежих вегетаций на
них не выявлено, имеются небольшой градиент на аортальном клапане (15,3—
16,0 мм. рт.ст.), незначительная митральная и ірикуспидальная регургитация;
функция диастолического расслабления миокарда снижена {Е/А = 0,7/0,9).При постутшении в Факультетскую хирургическую клинику им. Н.Н. Бур¬
денко была выполнена рентгенография органов грудной клетки, по данным
которой имелась осумкованная жидкость справа (в нередненижнем отделе и
в правой междолевой щели). По данным УЗИ коли^гество этой жидкости (с
множественными перегородками) составляло 300—350 мл. При КТ органов
грудной клетки в правой плевральной полости визуализировалось большое
количество свободной жидкости с затеком в междолевую плевру в верхних и
нижних ее отделах, а также зона уплотнения легочной ткани в базальных отде¬
лах правого легкого на фоне диффузного интерстициального фиброза (гипер¬
вентиляция? инфильтрация?), В средостении признаков лимфаденопатии не
выявлено. Имелись мелкие обызвествленные лимфатические узлы правой
бронхо-пульмональной группы. Подтверждено наличие небольшого количе¬
ства жидкости в перикарде.17 апреля проведена плевральная пункция справа, аспирировано 340 мл
прозрачной жидкости соломенного цвета. При КТ органов грудной клетки
после пункции {рис. 29.3) свежих очаговых и инфильтративных изменений
в легких не выявлено; во всех отделах правого легкого определялись множе¬
ственные очаги фиброза, в 10-м сегменте правого легкого — эмфизематозная
булла 20 мм в поперечнике. Главная междолевая плевра справа неравномерно
утолщена. В передненижнем отделе правой плевральной полости определялась
только осумкованная, в основном организовавшаяся жидкость; в передней
хмедиастинальной области выявлены множественные лимфатические узлы до
8 мм, в левой нижней паратрахеальной области — до 9 мм, в бифуркационнойРис. 29.3. Компьютерные томофаммы органов грудной клетки от 17 апреля 2006 г.
Глава 29. Необычный вариант течения висцерального туберкулеза... 611области — до 10 мм в поперечнике, а в трахеобронхиальной области и в корне
правого легкого — обътзвестшгенные лимфатические узлы. Отмечено неравно¬
мерное утолщение перикарда (до 10 мм).При иитологическом исследовании пунктата выявлены единичные клетки
мезотелия, лимфоцитарная инфильтраиия (до 30). При посеве роста микро¬
флоры не пол>'чено. Относительная плотность жидкости 1014, цвет соломенно-
желтый, белок 61,500%о, мутная, проба Ривалъта положительная, pH 7,5,
глюкоза 100 мг%, билирубин отрицательный, лейкоциты 20-30 в поле зрения,
эритроциты 5—10 в поле зрения, клеток мезотелия немного, атипичные клетки
не найдены. Микроскопия: лимфоциты 98%, нейтрофильт 2%, микобакте¬
рий туберкулеза и флоры не найдено. Люминесцентная микроскопия осадка
по Цилю-Нельсену: кислотоустойчивые микобактерии не выявлены. ПЦР:
ДНК микобактерий т^^беркулезного комплекса не обнаружено.Таким образом, мы имели дело не просто с лихорадкой неясного генеза.
Она сочеталась с лимфоцитарным плевральным выпотом (причем имелся
также выпот в перикарде с утолщением его листков), гиперхромной анемией,
лейкопенией, тромбоцитозом и лимфаденопатией (не только внуїригрудной,
но и надключичной). Особенностью самой лихорадки был ее правилышй
характер (подъемы температуры тела по вечерам и ночное падение с обильным
потоотделением). В каких направлениях прежде всего следовало вести диагно¬
стический поиск?Наиболее вероятным представлялся диагноз туберкулеза; однако неясными
оставались локализация первичного очага (по-видимому, в легких активного
воспаления не было, следовало думать прежде всего о поражении лимфо¬
узлов), а также причины столь выраженно10 гематологического синдрома.
Выраженная лимфаденопатия требовала исключения лимфопролиферагивно-
го заболевания (лимфомы, лимфоцитарного и парапротеинемических лейко¬
зов, а также первичного тромбоцитарного лейкоза). Высокую СОЭ нельзя было
считать специфичной, поскольку во многом она была обусловлена выражен¬
ной анемией. Наконец, возраст больной, наличие выраженной гиперхромной
анемии заставляло искать солитарную опухоль, пояатение которой привело к
развитию паранеошшстического синдрома. Нельзя было иск^почить и сочета¬
ние онколог№іеского заболевания с туберкулезом, развившимся на фоне изме¬
ненной иммунной реактивности организма.Менее вероятным, но все же возможным прслставля^тось развитие у боль¬
ной инфекционного эндокардита: несколько необычна столь выраженная
реактивность в пожилом возрасте, однако у больной имеется формируюпцш-
ся атеросклеротический стеноз устья аорты, который мог стать основой для
развития вторичного эндокардита; при попытках кратковременной терапии
антибиотиками в обычных дозах отмечался слабый положительный эффект.
Противоречили этому диагнозу не столько отсутствие вегетаций по данным
трансторакальной ЭхоКГ и отрицательный посев крови, сколько отсутствие
клапанной регургитации через полгода от начала болезни. Существовала веро¬
ятность и септического процесса с неустановленной локализацией первич¬
ного очага инфекции, однако в этом случае было труднообъяснимо развитие
6/2 Системные заболеванияполисерозита. Возможным было развитие у больной одного из диффузных
заболеваний соединительной ткани (однако отсутствие в крови РФ, АНФ
при столь выраженной системности практически исключало этот диагноз).
Наконец, внутригрудная лимфаденопатия требовала вк.іючения в круг диффе¬
ренцируемых заболеваний саркоидоза.Отдельного внимания требовал тромбоцитоз, с которым мы сталкиваемся
очень редко и хуже знаем причины его развития. Помимо тромбоцитарного и
других лейкозов, к тромбоцитозу могут вести те заболевания, которые уже вклю¬
чены в круг дифференциальной диагностики: инфекции, злокачественные опу¬
холи, диффузные заболевания соединительной ткани, саркоидоз. Остальные
причины тромбоцитоза у нашей больной отсутствовали (аспленический статус,
операции, нефротический синдром или болезнь Иценко—Кушинга), а для пер¬
вичного тромбоцитарного лейкоза число тромбоцитов недостаточно высоко.
Таким образом, круг диагностического поиска бьт очерчен.В первую очередь был проведен расширенный онкопоиск, который позво¬
лил исключить не только рак легкого, но и опухоль брюшной полости, гастро¬
дуоденальной зоны, толстого кишечника, органов малого таза и шитовидной
железы. При КТ брюшной полости не было получено данных и за локальный
абсцесс. При ЭГДС выявлен атрофический гастрит, который мог играть роль в
развитии анемии.Для уточнения характера анемии и исключения первичного поражения
костного мозга дважды проведена стернальная пункция и однократно — тре-
панобиопсия. Несмотря на гиперхромный характер анемии и отсутствие тера¬
пии витамином в костном мозге не было выявлено мегалобластного типа
кроветворения, что не позволило подтвердить диагноз Bjj- или фолиеводефи¬
цитной анемии. Число плазмоцитов (3,5%, в повторном пунктате до 6,5%) и
лимфоцитов (16,9%) не достигало диагностически значимого уровня, т.е. нель¬
зя бьь'ю говорить ни о лейкозе, ни о парапротеинемиях; не бьию данных и за
тромбоцитарный лейкоз (мегакариоциты найдены в достатотаом количестве,
всех степеней зрелости). Опухолевое поражение костного мозга исключали и
дашіьіе остеосцинтифафии.В трепанобиоптате мегалоидные формы встречались относительно часто,
данных за лейкоз также не полу’іено; гранулопоэз не сужен, представлен
преимущественно зрелыми формами; число мегакариоцитов немного сни¬
жено, обнаруживаются в основном мелкие и голоядерные формы, они лежат
поодиночке возле расигиренньгх синусов; в небольшом количестве рассеяны
плазмоци'гы, выявлено несколько мелких скоплений лимфоцитов. Учитывая
высокую специфичность повышения цветового показателя, мы все же считали
одним из механизмов анемии у больной с атрофическим гастритом дефицит
витамина и/или фолиевой кислоты.Прямые данные для постановки диагноза (в первую очередь разфаничения
туберкулеза и лимфопролиферации) могло дать морфологическое исследование
лимфоузлов. 27 апре,тя была произведена резекция увеличенных надключичных
лимфатических узлов справа. В результате изучения биоптата в Российском
онкологическом научном центре им. Н.Н. Блохина дано заключение:
Глава 29. Необычный вариант течения висцерального туберкулеза... 613в лимфоузлах хроническое гранулематозное воспаление — туберкулезное? Во
всяком случае, признаков лимфопролиферативного заболевания выявлено
не было, что подтвердило иммунное исслєдоваїше биоптата с типированием
лимфоцитов. Учитывая специализацию онкоцентра, мы считали необходимым
повторное исследование биоптатов в Научно-исследовательском институте
фтизиопульмонологии, но по техническим причинам процесс этот несколько
затянулся.Однако имевшихся данных, по нашему мнению, было достаточно для юго,
чтобы остановиться на диагнозе туберкулеза и начать специфическую терапию.
В пользу туберкулеза с первичным поражением лимфатических узлов говорили;• лимфоцитарный плевральный выпот (с содержанием лимфоцитов 98%,
что следует, по-видимому, считать наиболее специфичным признаком при
отрицательных иммунных реакциях на туберкулез);• осумкованная жидкость в правой плевральной полости (что заставляло
думать об истинном, а не реактивном туберкулезном плеврите);• перикардит с утолшением листков перикарда до 10 мм;• медиастинальная лимфаденопатия;• гранулематозный процесс в удаленном лимфатическом узле;• характерная лихорадка с ночными потами.Очень важными аргументами были отсутствие солитарной опухоли и четких
данных признаков лимфопролиферации по данным всестороннего обследова¬
ния. В этой ситуации анемию можно было расценить как смешанную (наряду
с дефицитом витамина Вр и фолиевой кислоты, играло роль токсическое
воздействие), а тромбоцитоз счетать реактивным, хотя сама выраженность
гематологического синдрома оставляла определенные сомнения в отношении
его вторичности, с лечебной и диагностической целью была начата терапия
витамином В|2 по 400 г ежедневно.Для определения режима туберкулостатической терапии больная бьша про¬
консультирована фтизиатром, который не нашел четких данных за туберку¬
лез, однако согласился с необходимостью начать лечение двумя препаратами
(изониазид 0,6 г/сут, рифампицин 0,3 г/сут в сочетании с витамином 10 мг
в день). В то же время больная была заочно проконсультирована гематоло¬
гом Гематологического научного центра, проф. Е.А. Лукиной. Вторичный
характер анемии и тромбоцитоза признан вполне вероятным, рекомендовано
продолжить терапию витамином начать также терапию фолиевой кис¬
лотой, витаминами группы В, в целях уменьшения концентрации тромбоци¬
тов — инфузионную терапию, инъекции фраксипарина с переходом на прием
антиагрегантов внутрь; от переливания крови воздержаться для оценки эффек¬
тивности терапии. Было сказано и о том, что быстрое развитие токсического
гепатита в ответ на туберкулостатики весьма специфично для лимфопролифе-
ративных заболеваний и потребует пересмотра диагноза.Таким образом, была начата терапия рифампицином 300 мг/сут, изопиа-
зидом 300 мг/сут, пиридоксина гидрохлоридом 10 мг/сут, фолиевой кислотой
20 мг/сут, «Ундевитом» по 1 драже и «Пентавитом» по 2 таб., фраксипарином0,3 мл 2 раза в день подкожно в течение 10 дней, далее — тромбо-АССом
614 Системные заболевания0,05 г по 1 таб. вечером, проводились ежедневные внутривенные капельные
вливания 400 мл 5% р-ра глюкозы в течение 3 нед, продолжены вргутримышеч-
ные инъекции р-ра витамина по 400 г.Параллельно проведено исследование биоптата лимфоузлов в Научно-
исследовательском институте фтизиощ^їїьмонологии — выявлена субтотальная
казификация с фиброзио-грануляционным отграничительным валом, диа¬
гноз активного туберкулеза не вызывал сомнений. В соответствии с этим доза
рифамгшцина была увеличена фтизиатром до 450 мг/сут, назначен третий
туберкулостатический препарат — пиразинамид но 1 г/сут.Через месяц терапии можно бьшо говорить об отчетливом положительном
ответе: стойко нормализовалась температура тела, исчезли ночные поты (в
конце июня развился рецидив лихорадки до 39,2 "С, что было расценено нами
как суперинфекция — вероятно, вирусная; на фоне дополнительного назна¬
чения клафорана 2 г/сут температура полностью нормализовалась в течение5 дней). У больной полностью исчезла одышка, заметно улучшилось общее
самочувствие, она прибавила в весе около 5 кг; уменьшилась выраженность
головокружений; жидкость в плевральной полости не накапливатась (по дан¬
ным КТ сохраііялась лишь ос^кованная жидкость справа). Лечение субъек¬
тивно хорошо переносилось. На второй неделе бьш отмечен подъем уровней
ACT и АЛТ (максимально до 2,5 норм) с полной нормализацией в течение
недели.При ЭТОЛ1 показатели обтцего анализа крови совершенно не улучшились
(кроме снижения СОЭ до 43—53 мм/ч — по-видимому, за счет воспалительного
ее компонента при сохранении анемии). Гемоглобин не достиг даже уровня
60 г/л, сохранялись гиперхромия, лейкопения, тромбоцитоз, повышение уров¬
ня ретикулоцитов было очень незначительным (до 15%о при исходном уровне
10%о). в связи с этим мы повторно обратились к Е.А. Лукиной, было рекомен¬
довано проведение специального биохимического анализа крови, направлен¬
ного на >’точнение механизмов анемии.Выявленное (рис. 29.4) повышение уровней сывороточного железа, ферри-
тина (депо железа), процента насыщения при нормальной общей железосвя¬
зывающей способности сыворотки крови характерно для так называемой желе-
зоперераспределителыюй анемии, или анемии хронических состояний, при
которой общий пул железа в организме не снижен, но большая его часть нахо¬
дится в депо, что связано с активизацией ретикулоэндотелиальной системы.Гематологом в связи с этим рекомендовано по возможности воздержаться
от переливания крови во избежание «перегрузки» организма железом. И в то
же время уровни витамина В^, и фолатов как в сыворотке, так и в эритроцитах
оставались на нижней фанице нормы и определяли гиперхромный характер
анемии (что несвойственно «чистой» анемии хронических состояний). С уче¬
том длительной заместительной терапии это следует расценивать как признак
резистентности к витамину В,., и фолиевой кислоте (возможно, на фоне тубер¬
кулостатической терапии). По-видимому, кобаламин и фолаты интенсивно
расходуются в каких-то процессах и «не доходят» до костного мозга. Отсутствие
признаков поражения нервной системы также, по-видимому, говорит о том,
Глава 29. Необычный вариант течения висцерального туберкулеза..615ферритин сывороткиферритин эритроцитовжелезо сывороткиожсспроцент насыщения железомтрансферринрецепторы к трансферринувитамин сывороткивитамин В^2 эритроцитовфолаты сывороткифолаты эритроцитовэритропоэтинЦИКмедьцинкгомоцистеинэндотелии16.06норма408 мкг/л40-8035,7мкг/гНЬ| 5-1028 мкг/л10-21,558 мкм/л48%2,1 г/л40-7025-^5ДО 2,62,8 мг/мл1,5-2,5300 пг/гНЬ300-900103 пг/гНЬ60-3004,8 нг/мл4-142,7 пг/гНЬ200 mU/мл26511 мкг/л16 мкм/л20 мкм/л10 нг/л5^55-10до 14011-2512-19до 12ДОЗРис. 29.4. Биохимический анализ крови больной П., июнь 2006 г.что общее количество витамина В,2 и фолатов близко к нормальному.Лечение этими препаратами необходимо продолжить, 20-кратное повы¬
шение уровня эритропоэтина говорит о сохранности системы регуляции эри-
тропоэза (адекватный ответ на выраженную анемию). Повышенный уровень
гомотщстеина отражает дефицит кобаламина, фолиевой кислоты и витамина
которые необходимы для его нормального метаболизма; с другой стороны,
он является дополнительным фактором, предрасполагаюшим к тромбозам по
целому ряду механизмов (усиливает образование фомбина, ингибирует ткане¬
вой ингибитор плазминогена и пр.).Гематолог сочла возможным продолжение этой терапии в амбулаторном
режиме. Пребывание больной в стационаре несколько затянулось в связи с
падением, привсдтпим к компрессионному перелому Ц-позвонка. К лечению
были добавлены миокальиик интраназально, препараты Са, ношение корсета,
и 5 июля больная была выписана с рекомендациями продолжить терапию в
полном объеме (инъекции витамина В,^ — раз в неделю) под контролем пока¬
зателей крови.Диагноз при выписке был сформулирован следующим образом: туберку¬
лез лимфатических узлов. Паратуберкулезньтй правосторонний экссудатив¬
ный шгеврит, экссудативный перикардит'. Гиперхромная анемия смешанно¬
го характера (анемия хронических состояний, В,^-, фолиеводефицитная?),
тяжелой степени. Реактивный тромбоцитоз. Атеросклероз аорты, коронар¬
ных, мозговых артерий. Атеросклеротический стеноз устья аорты начальной
степени. Кисты печени. Кисты правой ночки. Диффузный пневмосклероз.
616 Системные заболеванияЭмфизематозная булла 10-го сегмента правого легкого. Узлы щитовидной
железы. Компрессионный перелом Ь^-позвонка от 26 июня. Диффузный
остеопороз.В течение июля, августа и сентября больная продолжала терапию в полном
объеме, за исключением инъекций витамина В,2 и рекомендованного курса
терапии миокальциком, который был проведен не в полном объеме. В послед¬
ние 2 нед сентября прекратила прием фолиевой кислоты. Самочувствие оста¬
валось относительно удовлетворительным, температура тела регулярно кон¬
тролировалась и НС превышала 37,0 °С. Однако сохранялись боли в пояснице,
которые несколько раз (в том числе при подъеме 2—5 кг) заметно ус^шивштись.
В августе амбулаторно был проведен анализ крови, результаты которого будут
представлены ниже.С начала сентября состояние ухудшилось — после заметного переохлажде¬
ния возобновилась лихорадка без ознобов и потов (в основном субфебриль-
ная, но трижды отмечались подъемы температуры до 37,8-38 ”С), появилась
.іегкая одышка, беспокоили боли в области нижних ребер и подреберья, кото¬
рые усиливались при вдохе. В связи с этим 5 октября повторно обратилась в
Факультетскую терапевтическую клинику им. В.Н. Виноградова. При осмо¬
тре — бледность кожных покровов, боли при пальпации остистых отростков
верхних поясничных позвонков; увеличения лимфоузлов не выявлено, при¬
знаки выпота в плевральных полостях не определялись, в базальных отделах
правого легкого выслушивалась локальная крепитапия.Проведена КТ органов грудной клетки {рис. 29.5) у при которой субплев-
рально справа на фоне понижения воздушности легочной ткани выявлены
два участка уплотнения неправильно округлой формы, слева также отмечено
появление участка пониженной воздушной легочной ткани с участками консо¬
лидации, что с учетом клинической картины расценивалось как двусторонняя
полиссгментарная пневмония. Выпот в плевральных полостях не определялся,
что подтверждало эффективность противотуберкулезной терапии, сохранялось
уплотнение межполевой плевры справа, размеры лимфоузлов не изменились.Рнс. 29,5, Компьютерные томограммы органов фудной клетки от 5 октября 2006 г
(слева) и от 18 октября 2005 г. (после курса терапии амоксиклавом)
гаава 29. Необычный вариант течения висцерального туберкулеза... 617Несколько нетипичным для пневмонии представлялось полное отсутствие
аускультативных симтомов и дтительное течение (около 1 мес), однако с уче¬
том лихорадки и заключения рентгенолога дополнительно к прежней терапии
были начаты внутривенные вливания амоксиклава по 1,2 г 2 раза в день на
5% растворе глюкозы, возобновлены инъекции витамина по 400 г 1 раз в
неделю и прием фолиевой кислоты. При усилении болей в спине вводился
кетонал с хороыптм эффектом (в среднем 1 раз в 2-3 дня). К 4-му дню тем¬
пература тела нормализовалась, и в дальнейшем лишь однократно отмечен
се подъем вечером до 37,2 °С. Аускультативная картина в легких не меня.аась.
Больная была проконсультирована фтизиатром, противотуберкулезную тера¬
пию рекомендовано продолжить в течение 2 мес.В общем анализе крови при постушіении картина прежняя: НЬ 56,3 г/л, эри¬
троциты 1,5 млн, цветовой показатель 1Л, ретикулоциты 12%о, нейтрофилы
46%, тромбоциты 726 тыс., СОЭ 46 мм/ч. В амбулаторном анализе крови от
08 августа было отмечено повышение НЬ до 75 г/л, снижение тромбоцитов
до 192 тыс., поэтому можно говорить о кратковременной положительной
динамике в тот период. По завершении курса терапии амоксиклавом (на
13-й день) в клинике повторно проведен анализ крови, в котором отмечено
снижение СОЭ до 30 мм/ч и изменение лейкоцитарной формулы — КОЛ№ІЄ-
ство нейтрофилов снизилось до 19%, количество лимфоцитов повысилось до
77%. Тромбоциты — 848 тыс. Таким образом, выраженность гематологического
синдрома не уменьшилась ни на фоне длительной и эффективной противо¬
туберкулезной терапии, ни после курса неспецифи^іеской антибактериальной
терапии. В биохимическом анализе крови изменений по сравнению с анализами
от июня также не выявлено (сохранны печеночная и почечная функции, сохра¬
няются признаки перегрузки железом).В связи с интенсивными болями в пояснице и в области нижних ребер
повторно выполнена рентгенография позвоночника-, если 28 июня после падения
был с некоторой натяжкой диагносгирован лишь перелом L, позвонка, то на
этот раз на фоне вырсшенного диффузного остеопороза выявлен отчетливый
компрессионный перелом Th,2 позвонка, а также снижение высоты тела Th^
позвонка, снижение высоты и уплощение тел Lp Ц, позвонков. По данным
денситометрии, имелся выраженный диффузный остеопороз (обший пока¬
затель МП КТ 4,4) с максимальным снижением плотности костной ткани на
уровне (МПКТ 5,3)- Тем не менее мы не считали возможным полностью
исключить специфическое поражение позвонков.Наконец, на 13-й день терапии амоксиклавом выполнена контрольная
КТ органов грудной клетки. При этом положительная динамика была очень
незначительной — уменьшился участок пониженной воздушности слева, но
справа сохраняются участки уплотнения легочной ткани с неровными конту¬
рами, а также небольшое количество жидкости в полости перикарда, которое
определялось и ранее (см. рис. 29.5). Поскольку клинический эффект терапия
амоксиклавом все же оказала (отсутствие лихорадки и снижение СОЭ), данные
изменения уже нельзя было расценивать как неспецифическую пневмонию;
они требуют проведения дифференциального диагноза между туберкулезным
6Ї8 Системные заболеваниявоспалением (что гтрсдставлястся нам маловероятным) и раком легкого в пер¬
вую очередь.Прежде чем вернуться к обсуждению больной, приведем литературную
справку.Диагностику висцерального туберкулеза облегчает то, что почти у половины
больных с этим заболеванием (42,6%) при рентгенографии органов грудной
клетки выявляются признаки поражения паренхимы легких; но при этом лишь
у 11,2% диагноз внелегочного туберкулеза удавалось подтвердить. Интернист
сталкивается со следующими формами висцерального туберкулеза.1. Туберкулезный плеврит — наиболее частая внелегочыая локализация
туберкулеза, которая как раз и развилась у нашей больной; диагностирован у
35,6% из 319 больных внелегочным туберкулезом. В большинстве случаев явля¬
ется осложнением туберкулеза легких или лимфоузлов средостения. Возможны
три варианта: паратуберкулезный (реак'гивный) плеврит, контактное пораже¬
ние (прорыв каверны) или б\торчатка плевры в результате лимфогенной или
гематогенной диссеминации. Микобактерии туберкулеза редко выявляются
даже при бугорчатке, методом верификации диагноза (при отсутствии других
возможностей) является торакоскопия с биопсией плевры.Преобладания какой-либо из сторон в локализации выпота не отмечено
(в 11 % выпот развивается на стороне, противоположной стороне активных
изменений в легком). Двусторонний выпот возникает редко (1,5%). Местные
симптомы встречаются чаще (72,4%), чем обшие (52,2%). Характерны боль на
стороне поражения (48,1 %), лейкоцитоз — 12,8%, анемия — 50,3%, увеличение
СОЭ-79,3%, СРВ-63,1%.Характеристики плеврального выпота при туберкулезе; преобладает сероз¬
ный выпот, в 18% выяв.1яется его эозинофилия (более 10%), но значительно
чаше доминир>тот лимфоциты; в 4,4% развивается геморрагшіеский выпот,
в 1,5% — эмпиема плевры. Возможны низкая ішотность выпота (менее
1012 — у 10%) и низкое содержание белка (ниже 30 г/л — у 35%). Достоверно
выше, чем при злокачественных опухолях, уровни CD4+, интерлейкина-16,
интерферона-а и аденозиндеаминазы; повышен уровень СРВ в сравнении с
лимфоцитарными плевритами иной этиологии; уровень интсрферона-у выше
240 пг/мл является маркером туберкулеза с чувствительностью 94,9% и специ¬
фичностью 96,3%.Описан больной с двусторонним экссудативным плевритом, у которого в
экссудате с обеих сторон выявлены микобактерии туберкулеза, но слева более
90% составили лимфоциты, а справа — нейтрофилы. Описаны случаи туберку¬
лезного іьіеврита без преобладания лимфоцитов — так, в случае двустороннего
выпота процент содержания лимфоцитов в штевральном пунктате составил
лишь 47%, и диагноз был поставлен в результате обнаружения микобактерий
туберкулеза в биоптате плевры (гранулем при этом также не было).2. Туберкулезный перикардит — среди больных туберкулезом легких встре¬
чается в 1-8% случаев. Возможны острый перикардит с выпотом или без
него, тампонада, кальцификация перикарда, абсцесс, но наиболее характе¬
рен хронический экссудативно-констриктивный перикардит, нередко без
Глава 29. Необычный вариант течения висцерального туберкулеза.., 619симптомов интоксикации. Констрихиия перикарда без лечения наблюдается
в 30—50% случаев. Механизмы развития перикардита те же, что и при плев¬
рите. Интересны уже довольно старые данные о том, что результаты биопсии
неувеличенных лимфоузлов правых лестничных мышц во всех случаях гово¬
рили о наличии туберкулезного процесса. При гистологическом исследова¬
нии перикарда изменения могут быть неспепифичны даже при обнаружении
микобактерий туберкулеза в экссудате. При исследовании экссудата сохраняет
значение обнаружение аденозиндеаминазы и интерферона-у.3. Туберкулез миокарда — очень редкое поражение, осложняющее тубер¬
кулезный перикардит; чаще поражается левый желудочек, что может сопро¬
вождаться развитием его аневризмы. Японскими авторами описана 35-летняя
женщина с выраженными общими симптомами, плевритом, кровохарканьем и
туберкулезным воспалением стенки аорты, которое привело к ее разрыву; бьыа
выполнена экстренная операция с хорошим исходом. Важно, что поражение
аорты не бьшо изолированным.4. Туберкулезный мезаденит (поражение брыжеечных лимфоузлов) —
основная форма абдоминального туберкулеза. Наряду с болями в правой око-
лопупочной области, нарушениями моторики и признаками интоксикации,
развивается синдром мальабсорбции с нарушением главным образом жирового
обмена (поскольку жиры всасываются через лимфу); характерна кальцифи¬
кация пораженных лимфоузлов. Туберкулезный перитонит может осложнять
мезаденит или развиваться гематогенно; характерен лимфоцитарный состав
экссудата, однако он может носить гнойный ріли геморрагический характер.
Типично развитие спаечного процесса и осумкование экссудата. Диагноз под¬
тверждается при лапароскопии.5. Гастроинтестинальный туберкулез — проявления его неспецифичны: асцит,
«опухоль» желудка или кишечника, обструкция кишечника, язвенный колит,
перианальные фистулы, аппендицит либо только рецидивирующая анемия. Во
многих случаях терапия назначается ех juvantibus, поскольку даже гистологиче¬
ское исследование не всегда дает однозначный ответ. Помощь в диагностике
оказывает наличие обших симптомов. Описаны случаи, когда для выявления
источника кровотечения использовалась ангиофафия. Частота гастроиіггести-
navibHoro туберкулеза и/или туберкулеза брющины составляет 4,5% среди всех
случаев туберкулеза (48,5% — кишечная локализация, 33% — поражение брю¬
щины, 18,5% — сочетанное поражение). Чаще эта локализация встречается у
молодых пациентов, у 55% — в сочетании с иными локализациями туберкулеза.
Дифференциальный диагноз наиболее часто проводится с опухолью.6. Туберкулез печени — общие симптомы (лихорадка с потами, воспалитель¬
ный синдром, нормохромная анемия) сочетаются с болями в правом подребе¬
рье и гепатомегалией. Ключ к диагнозу — данные УЗИ (могут обнаруживаться
узелки размерами от 11 до 50 мм в обеих долях печени) + данные биопсии
печени и брюшины (типичные грануле.мы с казеозом и гигантскими клетками);
терапия эффективна (в том числе с применением рифампицина).7. Туберкулез селезенки — та форма висцера-іьного туберкулеза, о которой
можно бьшо думать в нашем случае, однако у нашей больной по данным УЗИ
620 Системные заболеванияи КТ не было ни спленомегалии, ни структурных изменений селезенки; диа¬
гноз туберкулеза чаще всего ставится при лапароскопии или диагностической
спленэктомии.8. Туберкулез надпочечников — обшие симптомы в сочетании с картиной
надпочечниковой недостаточности; при КТ — гепатоспленометалия и пора¬
жение надпочечников, при биопсии их — туберкулезные гранулемы. Терапия
глюкокортикоидами в сочетании с туберкулостатиками не всегда эффективна.9. Туберкулез поджелудочной железы — помимо общих симптомов, про¬
является болями в животе, спине, обструктивной желтухой (75, 38 и 31%),
абсцессами поджелудочной железы, массивными желудочно-кишечными кро¬
вотечениями, картиной острого или хронического панкреатита, вторичным
сахарным диабетом, тромбозом селезеночной вены, псевдоопухолью поджелу¬
дочной железы, у 69% больных повышены уровни ACT, АЛТ, у-ГТ и щелочной
фосфатазы. При УЗИ выявляется отечность поджелудочной железы различной
степени у 75% больных. При КТ плотность железы понижена, у 56% пациентов
выявляется кальцификация, в 38% случаев видны увеличенные околопанкреа-
тические лимфоузлы. Данные ретроградной холангиопанкреатографии могут
быть нормальными. Диагноз ставится с помощью лапаротомии с аспираци-
онной биопсией — в 75% случаев выявляются гранулемы, в 38% — казеозный
некроз. Химиотерапия достаточно эффективна.10. Костно-суставной туберкулез, безусловно, должен обсуждаться в нашем
случае. Может поражаться любой участок скелета, но чаще всего — позво¬
ночник. Туберкулезный очаг формируется непосредственно в костной ткани,
далее процесс распространяется на сустав с развитием абсцессов и свищей.
Клиническими вариантами туберкулеза костей являются дакгилит, остеоне¬
кроз, остеомиелит. Для туберкулезного спондилита характерны остеопороз
тел позвонков, сужение межпозвонковых щелей, разрушение и уплощение
тел позвонков, полости распада, тени натечных абсцессов. У нашей больной
полностью нельзя исключить туберкулезное поражение позвоночника, однако
острое развитие симптомов в результате падения, выраженный остеопороз,
полное отсутствие изменений позвонков до переломов и отсутствие признаков
нагноения делают этот диагноз маловероятным.11. Туберкулез почек — как правило, представляет собой урологическую
проблему, поскольку основной процесс развивается на уровне лоханок и ниже
(хотя начинается он с коры); возможно формирование каверн; характерна
триада: кислая реакция мочи, микрогематурия, асептическая пиурия. Обші^е
симптомы отсутствуют или выражены слабо (если туберкулез мочевой системы
протекает изолированно), но нередко туберкулез почек является лищь одним
из проявлений генерализованного процесса. В большинстве случаев наблю¬
даются асимметричные изменения пиелограммы (в одной из почек процесс
протекает латентно).12. Изолированный туберкзшез лимфоузлов — чаще всего заболевают дети
(так называемая золотуха), реже — пожилые люди. Чаще поражаются шейные
и подчелюстные лимфоузлы, реже — паховые и подмышечные, механизм
инфицирования — лимфогематогенный (у взрослых — в результате эндогенной
Глава 29. Необычный вариант течения висцерального туберкулеза... 621реактивации в заживших очагах первичного туберкулеза). У нашей больной
очагом реактивации, скорее всего, явились обызвествленные лимфоузлы в
корне правого легкого. Помимо казеозной формы поражения лимфоузлов,
выявленной у нашей больной, возможны их гиперплазі^ія с небольшим количе¬
ством гранулем и рубцовые изменения, при которых диагностическая ценность
биопсии не столь высока. Сами узлы бывают увеличены максимально до 5 см,
уплотнены, спаены между собой и с окружающей тканью, возможно формиро¬
вание свищей.13. Туберкулез костного мозга — о нем речь пойдет ниже.14. Паратуберкулезные реакции — развиваются в результате сенсиби¬
лизации организма к токсинам микобактерий туберкулеза при отсутствии
самих микобактерий в пораженных иммунным воспалением тканях (при
биопсии обнаруживаются лимфоцитарная и макрофагальная инфи^тьтрация,
неспецифические васкулиты с фибриноидным некрозом) и представляют
большую дифференциально-диагностическую проблему: полисерозит (плев¬
рит, перикардит, доброкачественный асцит молодых девушек); ревматоид
(туберкулезный полиартрит) Понсе (сходны с ревматоидным артритом не
только клинические проявления, но и рентгенологические изменения суста¬
вов); волчаночноподобные реакции («бабочка», артралгии, трофические и
иммунологические расстройства); панцитопения; лимфаденопатия, гепато-
спленомегалия; узловатая эритема, панникулит, геморрагическт^й васкулит;
гломерулонефрит с нефротическим синдромом, амилоидоз почек; кардит;
гепатит; кератоконъюнктивит, увеит, эписклерит. Сложность состоит в том,
что при поражении того или иного органа (даже при установленном диагно¬
зе туберкулеза) приходится дифференцировать специфический процесс от
параспецифического иммунного воспаления (хотя принципиального значе¬
ния для лечения это не имеет).Диагностика туберкулеза проводится с помощью трех групп методов.1, Обнаружение микобактерий туберкулеза в ткани пораженного органа:• люмігнесцентная микроскопия по Ци^тю—Нельсену; микобактерии тубер¬
кулеза обнаруживаются при наличии не менее 100 тыс. микробных тел в1 мл материала; для большей концентрации микобактерий туберкулеза
используют метод флогтации (встряхивание жидкого материала, смешан¬
ного с углеводородом); метод бактериоскопии выяштяет групт^ микобак¬
терий; у больных с милиарным туберкулезом микобактерии обнаружшза-
ются в 37% случаев;• бактериологическое (культуральное) исследование — посев материала на
яичную среду Левенштейна-Йенсена; рост микобактерий туберкулеза
происходит через 14-90 дней, достаточно 20-100 микробных тел в 1 мл
материала;• биологическая проба с заражением морских свинок: положительный
результат у 90% больных с милиарным туберкулезом, в основном при
исследовании мокроты и бронхоальвеолярного лаважа (достаточно попа¬
дания 5 микробных тел в 1 мл), но возможна потеря микобактериями
туберкулеза вирулентности;
622 Системные заболевания• обнаружение ДНК микобактерий методом ПЦР. При исследовании плев¬
рального пунктата чувствительность реакции составляет 50%, специфич¬
ность 61%. При наличии подозрения на туберкулезное поражение мочевой
системы может быть предпринято исследование мочи;• испо.іьзование бактериофага для амплификации микобактерий туберку¬
леза;• использование колометрической гибридизации (СоМ РНА) с целью ампли¬
фикации микобактерий туберкулеза, которое дает положительный резуль¬
тат и при отрицательной ПЦР; методы амплификации ДНК пока не полу¬
чили широкого распространения, но являются наиболее перспективными.
Необходимо отметить, что микробактериологическое подтверждение диа¬
гноза было получено лишь у 23,7% больных с внелегочным туберкулезом;
средний период от появления симптомов до постановки диагноза составил
у них 96 дней.2. Методы выявления иммунного ответа на инфицирование микобактерия¬
ми туберкулеза:• туберкулиновая проба: положительна лишь у 32% больных с милиарным
туберкулезом; отрицательный результат пробы совершенно не исключает
активного туберкулеза;• обнаружение антител к микобактериям туберкулеза методом имм>нофлю-
оресцентного анализа (материал — кровь, которая может быть исследована
и прямыми методами);• реакция бласттрансформации лимфоцитов (наиболее выражена у больных
с благоприятным течением туберкулеза) и реакция торможения миграции
лимфоцитов в присутствии туберкулина (выражена при прогрессирующем
течении т\'беркулеза).3. Выявление специфичных, гранулем (с казеозным некрозом и гигантски¬
ми клетками Пирогова-Лангханса) в ткани пораженного органа. У больных
с милиарным туберкулезом удалось обнаружить фанулСхМы в легких в 85%,
в печени — в 100%, в костном мозге — в 56% случаев. Вообще роль биопсии
печени, по-видимому, недооценивается в постановке диагноза туберкулеза, и
четкие показания к ней в подобных ситуациях не выработаны. При микроско¬
пии гранулем у больных с ми^іиарньїм туберкулезом микобактерий туберку^леза
не удалось o6Hap>^HTb ни разу, подтверждением характера гранулемы служила
положительная ПЦР — 47% случаев.Изменения общего анализа крови далеко не всегда становятся подспорьем
в постановке диагноза туберкулеза, поскольку у разных больных они бывают
совершенно разнонаправлешшми, Важно то, что при туберкулезе кровь редко
бывает нормальной.1. Чаше всего выявляется анемия — по данным разных авторов, в 32—93,6%,
присієм обычно она бывает нормохромной нормопитарной — 66—86%.2. Нейтропения — 45,2%.3. Лейкопения — достоверно чаще встречалась у больных с милиарным
туберкулезом по сравнению с легочным (25 и 0%) и была связана главным
образом с нейтропенией.
Глава 29. Необычный вариант течения висцерального туберкулеза... 6234. Лейкотщтоз (нсйтрофильньтй), напротив, характерен для больных с
аісгивньїм легочным туберкулезом, вьывляется в 18-40%.5. Лимфопения — 4,8—46%.6. Лимфощггоз ~ 6-8,4%.7. Моноцитопения 50% уьш моноцитоз 28%.8. Тромбоцитоз — 8-52%.9. Тромбоцитопения — 8—18%; достоверно чаще встречалась у больных с
диссеминированным милиарным туберкулезом по сравнению с легочным.10. Панщиопения — у больных с милиарным туберкулезом; описана также
при некрозе костного мозга.И. Увеличение СОЭ — 80-93,6%; у больных с туберкулезом костного мозга
достигала 168 мм/ч.Таким образом, картина крови у нашей больной вполне укладывалась в диа¬
гноз туберкулеза. У больных с туберкулезом легких выраженность гематологи¬
ческого синдрома тесно коррелирует с тяжестью основного процесса. Нередко
встречается панцитопения; рекомендуют во всех случаях неясной панцитопе¬
нии в сочетании с лихорадкой исключать туберкулез (в частности, с помощью
биопсии печени).Необходимо кратко остановиться на значении тромбоцитоза при туберку¬
лезе. Максимальное число тромбоцитов при туберкулезе, которое встрети¬
лось нам в литературе, 1,372 тыс. (3200 у больного, который погиб на фоне
химиотерапии по поводу тромбоцитарного лейкоза — на вскрытии туберкулез).
Тромбоцитоз характерен для больных с активным легочным туберкулезом,
прїгчем степень его тесно коррелирует с величиной СОЭ, СРБ и уровнем
интерлейкина-6. Агрегационная функция тромбоцитов повышена, что, наряд>^
с повышением уровней фибриногена, фактора VIH, ингибитора активатора
плазминогена-1 и снижением уровней антитромбина 3 и протеина С предрас¬
полагает к тромбообразованию (в частности, оиисаны тромбозы глубоких вен).
Таким образом, назначение фраксипарина и аспирина представляется совер¬
шенно оправданным — без лечения частота тромбоза глубоких вен у больных с
туберкулезом и тромбоцитозом достигала 50%.Анемия является обьгшым осложнением туберкулеза и может развиваться
по целому ряду механизмов.1. Анемия хронических состояний; ее называют также железоперераспре¬
делительной, поскольку имеет место не столько истинный дефицит железа в
организме, сколько изменения количества и свойств трансферрина, связы¬
вание железа посредством свободаорадикальных процессов и мобилизации
системы антиоксидантной защиты; в отличие от истинной железодефицитной
анемии, общая железосвязывающая способность сыворотки крови чаще оста¬
ется нормальной, может не быть сильно Сішжен цветовой показатель. Нельзя
не учитывать и алиментарный фактор (интоксикация приводит к выраженному
снижению аппетита).2. Кровопотеря в результате деструктивных процессов (описан деструктив¬
ный язвенный колит с геморрагической диареей у пациента с почечным транс-
шіантатом).
624 Системные заболевания3. Сидероахрестическая анемия — при туберкулезе она является вариантом
анемии хронических состояний и может усугубляться в результате назначения
некоторых туберкулостатикос (изониазид, протиснамид и др.), которые свя¬
зывают пиридоксаль-5-фосфат и тем самым нар>тиают биофансформацию
витамина В^; доказательством данного механизма анемии являются не только
гипохромия и повышение сывороточного железа, но и сидеробластоз костно¬
го мозга; описано и развитие сидероахрестической анемии исключительно в
результате длительной терапии изониазидом.4. Анемия как проявление синдрома мальабсорбции (при туберку;гезе
кишечника).5. Аутоиммунная гемолитическая анемия, которая является результатом
действия антиэритроцитарных антител либо активизации ретикулоэндотс-
лиальной системы; кроме того, гемолитическая анемия может быть индуци¬
рована рифампицином или ПАСК; признаком внутрисосудистого гемолиза
является резкое снижение уровня гаптоглобина. Развернутая кіиничсская кар¬
тина с желтухой описана у 8-летнего ребенка с абдоминальным туберкулезом;
параллельно с туберкулостатической терапией были назначены глюкокорти-
коиды с хорошим эффектом. Аналогичный механизм анемии описан у больных
с диссеминированным милиарным туберкулезом; у больных с деструктивным
туберкулезом легких антитела к эритроцитам определялись в 66,7% при нали¬
чии анемии и у 36,9% без анемии.6. Туберкулез селезенки также может приводить к развитию гемолиза и
анемии.7. Непосредственно туберкулезные гранулемы в костном мозге с развити¬
ем гемофагоцитарного синдрома (макрофаги фагоцитируют клетки крови в
костном мозге), при котором важную роль играют определенные цитокины;
интерлейкин-18, slCAM-1, sVCAM-1; к лечению также подключаются глю-
кокортикоиды; частота поражения костного мозга у больных с туберкулезом
составляет, по некоторым данным, всего 0,46%, непосредственным механизмом
является гематогенная диссеминация; особенностью периферической крови у
таких больных являются обязательная лимфоцитопения и моноиитопеяия,
в гранулемах могут отсутствовать гигантские клетки Пирогова—Лангханса;
характерно снижение запасов железа.8. Описаны случаи некроза костного мозга в результате его туберкулезно¬
го ііоражсния; клинически это проявляется болями, лихорадкой, желтухой в
сочетании с панцитопенией, повышением уровней ЛД Г, щелочной фосфатазы;
окончательный диагноз ставится при трепанобиопсии.9. Аплазия костного мозга (нормохромная нормоцитарная анемия со
снижением числа ретикулоцитов и предшественников эритроцитов в кост¬
ном мозге); данная реакция в качестве казуистики описана и при других
инфекциях (гепатит С); показано, что у больных с активным туберкулезом и
уровнем НЬ ниже 110 г/л уровень эритропоэтина в крови достоверно ниже,
чем у больных с НЬ выше 110 г/л и боііьньїх с железодефицитной анемией,
что объясняют воздействием фактора некроза опухоли а, активирующего
макрофаги.
Глава 29. Необычный вариант течения висцерального туберкулеза... 62510. Наконец, возможно сочетание туберкулеза с анемиями иного проис¬
хождения, усугубление имевшихся іематологических нарушений в результате
развития туберкулеза; помимо простых сочетаний (например, туберкулез и
банатьная железодефицитная анемия), возможны и более сложііьіє; описано
сочетсшие миелодиспластического синдрома и туберкулеза; через три года у
больною развернулась клиника острого лейкоза с рецидивом туберкулеза,
что потребовало одновременного проведения цитостатического и туберку-
лосгатического лечения; гематологической ремиссии достигнуть не удалось.
Последний вариант нам особенно интересен, так как для него характерна
как раз гиперхромная рефрактерная анемия; но при грепанобиопсии не было
выяаюно бластов и повышенного цитоза с дисплазией трех ростков, характер¬
ной для данного состояния.Что касается дефицита витамина и связанной с ним анемии при тубер¬
кулезе, то показано, что сывороточный уровень витамина В^2 не отличается у
больных туберкулезом и контрольной фуппьт, у больных туберкулезом с раз¬
ной степенью анемии, у больньгх с локальной и диссеминированной формами
болезни. Поданным других авторов, уровень витамина повышен в сыворот¬
ке у 57% больных с туберкулезом леї'ких, а фолаты сыворо'гки и эритроцитов
находятся в нормальных пределах у 83% больных. Описания гиперхроміїой ане¬
мии, связанной исключите.тп>но с губеркушезом, нам обнаружить не удалось.Лечение анемии при т>беркулсзе имеет некоторые особенности;• препараты xejjeaa: nocKOjrbKy трудно разграничить анемию хронического
воспаления и железодефицитную анемию, в одной из работ болы1ым с
туберкулезом легких и анемией HasHanavin плацебо, чистое железо и желе¬
зо в сочетании с другими препаратами, влияюшими на уровень гемоглоби¬
на, независимо от механизма анемии; через месяц у больных, получавших
железо, достоверно улучшилось насыщение трансферрина, однако уже
через 2 мес и через полгода показатели крови одинаково улучшились во
всех трех группах, что говорит об основной роли этиотропного лечения;• витамин В^ обязательно используют в комбинации с туберкулостатиками,
при этом он может предотврапіать или оказывать лечебный эффект при
сидероахрестической анемии; важен правильный выбор дозы — если для
коррекции побочного действия туберкулостатиков достаточно назначения
5-10 мг/сут, то лечебная доза при сидероахрестической анемии в 10 раз
больше — от 50 до 200 мг/сут; в паптем случае признаков сидеробластной
анемии еще нет (нормобластичсское кроветворение, высокий цветовой
показатель), однако нарастание уровня железа заставляет думать об увели¬
чении дозы пиридоксина;• по данным наших авторов, использование токоферола и рибоксина у
больных с активным леючным туберку.ітезом и анемией давало лу^іший
результат, чем применение феррошіекса;• применение, наряду с туберкулостатической терапией, глюкокортикои-
дов — описан благоприятный эффект при аутоиммунной гемолитической
анемии, гранулематозном поражении костного мозга с развитием гемофа-
гоцитарного синдрома; однако в друїих работах даже при аутоиммунной
626 Системные заболеваниягемояитической анемии с положительной реакцией Кумбса или грануле¬
матозном поражении костного мозга для нормализации показателей крови
было достаточно туберкулостатической терапии, которая является основ¬
ным и наиболее эффективным способом лечения анемии при туберкулезе,
но в нашем случае практически не дала эффекта.Этот факт в сочетании с данными последней КТ легких заставляет в пер¬
вую очередь думать о раке легких. Известно, что туберкулез легких в пред¬
шествующие 20 лет повышает риск развития рака легкого в 2,5 раза, может
прещиествовать раку или выявляться одновременно с ним; данное сочетание
встречается преимущественно у пациентов пожилого возраста (старше 70 лет).
Вид противотуберкулезной терапии на частоту рака не влияет. Микобактерии
туберкулеза удавалось обнаружить в ткани рака легкого методом ПДР (этиоло¬
гическая роль микобактерий туберкулеза?). Частота рака легкого у больных с
активным туберкулезом 0,7%, лечение в большинстве таких случаев успешно.
Напротив, частота активного туберкулеза среди нелеченных больных с раком
легкого 1,9%, причем наличие туберкулеза не позволяет проводить полный
курс лечения рака. В большинстве случаев локализация рака и туберкулеза в
легком не зависят друг от друга. Есть данные о том, что из 325 пациентов с
туберкулезом 10 умерло в течение года от рака (в основном легкого).К сожалению, клинических данных в пользу рака легкого и факторов риска
достаточно много:• возраст (80 лет);• наличие предрасполагаюш,его заболевания (туберкулез легких);• возможно, повышенный уровень радиации (больная всю жизнь живет в
Брянской области);• терапия витамином В,^;• появление округлого образования в легком на фоне эффективной (по дру¬
гим признакам) туберкулостатической терапии;• быстрый рост образования в легком (отсутствие его 3,5 мес назад);• внешний вид этого образования (неровность контуров);• сохранение признаков внутригрудной лимфаденопатии и изменений в ана¬
лизе крови на фоне эффективной (по другим признакам) туберкулостати¬
ческой терапии — уменьшились лишь признаки системного воспаления;• развитие повторного «перелома» грудного позвонка Thj^, не связанного с
травмой и приведшего к резкому нарушению структуры позвонка и упор¬
ным болям, пока уступающим анальгетикам, также застав.іяет думать о
метастатическом поражении позвоночника, типичном для рака легкого.Если ду.мать о том, что еще могло привести к подобной картине на томо¬
граммах, то следует, по-видимому, исключать грибковое воспаление. В пользу
этого диагноза говорят и длительная антибактериальная терапия в сочетании
с нейтропенией, и быстрый рост непонятного «образования», и отсутствие его
реакции на амоксиклав. Но при этом все-таки наступило клиническое улуч¬
шение, которого нельзя было бы ждать при фибковой пневмонии; с самого
начала отсутствовала сколько-нибудь яркая клиника, в том числе эозинофилия
крови; с трудом можно объяснить и возобновление рефрактерной анемии.
Глава 29. Необычный вариант течения висцерального туберкулеза... 627Естественно, вновь встает вопрос о морфологргческой верификации диа¬
гноза, В присутствии хирурга была проведена торакоскопия — образование
находится субплевралъно и недалеко от подключичной артерии. Со слов хирур¬
га, достаточно реальна опасность развития пневмоторакса в случае транстора¬
кальной биопсии. Кроме того, из-за болей пациентке трудно поднимать руки.
Рассчитывать на бронхоскопию при таком расположении узла сложно.В заключение мы бы хотели предложить ряд вопросов, которые остаются
для нас не вполне ясными и заслуживают обсуждения.L Можно ли расценивать образование в верхушке лравого легкого как
«недолеченный» туберкулез? С учетом обшей положительной динамики и
отсутствия плеврита — едва ли, как нам кажется.2. Следует ли провести курс противогрибковой терапии? По-видимому, да
(в том числе ехjuvantibus).3. Какова природа выраженного гематологического синдрома (рефрактер¬
ная гиперхромная анемия, лейкопения, нейтропения, тромбоцитоз) — тубер¬
кулез? рак? сочетание? самостоятельное заболевание крови, проявившееся
на фоне основного? Ответить на этот вопрос мы предлагаем ЕА. Лукиной.
Наиболее вероятным нам представляется сочетание рака и туберкулеза.4. Какова природа поражения позвонков? К сожалению, метастаз весьма
вероятен.5. Возможно ли проведение оперативного лечения рака легкого в случае
подтверждения этого диагноза? У больной — тяжелая анемия, которую можно
скорректировать то,іько массивными переливаниями крови.6. Целесообразно ли проведение операции при невозможности химиотера¬
пии по поводу рака легкого? На наш взгляд, скорее нет, особенно если учесть
возможные метастазы в позвоночник. Как известно, исключительно хирурги¬
ческое лечение рака легких не дает длительного эффекта.7. Возможно ли применение фотодинамической терапии рака легкого в слу¬
чае подтверждения данного диагноза? Этот метод, видимо, можно обсуждать со
специалистами.8. Следует ли проводить попытку трансторакальной биопсии образования
в верхушке правого легкого? Ответ на этот вопрос во многом зависит от того,
пойдут ли хирурги на операцию.9. И, наконец: что в наибольшей степени угрожает жизни больной (каков
прогноз)? По-видимому, если это рак, то он наиболее опасен, поскольку к
анемии она адаптирована. Достаточно высок риск и суперинфекции, которая
может оказаться фатальной.Комментарии E.A. Лукиной — профессора Гематологического научного центра
РАМН, д-ра мед. наукВо-первых, я считаю, что нельзя говорить о неэффективности противотубер¬
кулезной терапии в целом. Ушел плеврит, ушли лихорадка и поты, пациент¬
ка и сама отмечает, что ей летом стало заметно лучше. Теперь что касается
крови. К сожалению, я не разрешу этого вопроса окончательно. Мы исходим
из нормы гемоглобина 120 г/л. На самом деле для пациентки 80 лет, когорая
6*28 Системные заболеванияпоследний раз сдавала анализ крови, по-видимому, во время последней бере¬
менности, вполне возможно, что она последние лет 30 живет с гемоглобином
80 г/л. С этим постоянно приходится сталкиваться в клинической практике:
женщина, которая прекрасно себя ^fyвcтвycт, сдает анализ крови, узнает, что у
нес гемоглобин 60 г/л, и категорически не хочет брать больничный по этому
поводу, утверждая, что у нес нет никаких проблем. К сожалению, сейчас это
встречается нередко, посколък>' диспансеризация у нас прекратилась.Если исходить из нормы гемоглобина 120 г/л, то у больной действительно
имеется глубокая анемия. Еще хорошо, что у нее есть признаки перегрузки
железом, noTo\ty что в противном случае ей постоянно назначали бы препа¬
раты железа. За протпедшие 2—3 мес вы просто могли не увидеть положитель¬
ный гематологический эффект от противотуберкулезной терапии, поскольку
вновь развилось острое воспаление. Оно могло привести к тому, что просто
нивелировался тот эффект, который вы должны были увидеть, но позже.
Система крови инертна, она не восстанааіивается за 2-3 нед, и процесс
повышения гемоглобина может занять несколько месяцев (если уходит очаг
воспатения). Опять же — до какой нормы?Какова причина? Я бы хотела несколько слов сказать об обмене железа. На
сегодняшний день произошел существенный прогресс в этой области наших
знаний. Нам хорошо известна метаболическая регуляция обмена железа.
Меньше всего имеет значение то железо, которое всасьтается: это всего
1—2 мг/сут. На самом деле основной вклад в процесс гемопоэза вносят те
20-30 мг железа, которые постоянно хранятся в клетках ретикулоэндотели-
алъной системы. И если этот процесс рециркуляции железа выключается, то,
сколько бы мы ни давали железа перорально, мы не получим хороший гемо¬
глобин, пока не уйдет тот депрессирующий агент, который нарушает процесс
рециркуляции. Таким агентом является воспатение. Вьпслючается иммунный
механизм регуляции обмена железа, и мы, как правило, имеем его перерас¬
пределительный дефицит. Здесь же в силу неизвестных обстоятельств имеют¬
ся лабораторные признаки персфузки железом. По крайней мере не возника¬
ет вопроса — понятно, что пациентке не показаны препараты железа.Почему анемия гиперхромная, почему пациентке давали витамин В,^?
Лабораторным обоснованием был низкий уровень сывороточного витамина
В,,, но это не соответствует тому представлению о В,2-дефипитной анемии, к
коч'орому мы все привыкли, которое подразумевает наличие расширенного
красною ростка, мегалобластов и т.д. В последние годы хорошо изучены \гута-
ции гена фермента, который участвует в обмене метионина. Гетерозиготное
носительство приводит к снижению активности фермента примерно на 30%,
и это, как правило, не проявляется клинически. А вот 8—10% людей (дис¬
сертация на эту тему появилась и в нашей стране) являются гомозиготами, у
которых активность этого фермента снижена уже существенно, на 50—60%;
это предрасполагает к раннему атеросклерозу и т.д.Этот дефект гспа, особенно при наличии внешних обстоятельств, приводит к
дефициту ферменч а и накоплению в крови промежуточного продукта обмена
метионина — гомоцистеина, обладающего выраженными прокоагулянтными
Глава 29. Необычный вариант течения висцерального туберкулеза... 629свойствами. Генетику изменить нельзя, но можно скорректировать дефект
метаболизма, и с этой целью используется комплекс витаминов. В,^, фолие¬
вая кислота, Bp^j, В^ работают как катализаторы нарушенной реакции.
В последние 2 года мы широко используем эти знания: когда видим генети¬
ческую аномалию (наша больная сдала кровь на определение полиморфизма
соответствующих генов, анализ находится в работе) либо гомоцистеинемию,
не связанную с генетическим дефектом (при поражении печени, почек и т.д.),
то проводим курсы терапии перечисленными витаминами, но не для устра¬
нения В J2"дефицитного состояния, а для ликвидации того прокоагулянтного
субстрата в крови, который может быть одним из механизмов мaJЮкpoвия.
Это та микроангиопатическая анемия, которую мы почти не умеем диагности¬
ровать в клинике и которая связана с нарушениями в микроциркуляторном
русле. Эритроциты не проходят в систему микроциркуляции, и за счет этого
нарушаются метаболические процессы в печени и нормальная регуляция
гемопоэза. В данной ситуации курс витаминотерапии проводился ис по пово¬
ду Bj^-дефицитной анемии (хотя гиперхромная анемия присутствовала), а для
ликвидации гипергомоцистеиие\гаи, одного из механизмов тех микроцирку-
ляторных нарушений, который связан с прокоагулянтными свойствами іомо-
цистеина. Не увидели эффекта. Правда, где-то в анализе мелькнула цифра
75 г/л, но я крайне сдержанно отношу^сь к анализам по месту жительства.
Думаю, мы просто не успели увидеть эффекта в силу обстоятельств — возник¬
ло новое воспаление. Мне показалось нецслесообразньтм отходить от концеп¬
ции туберкулеза. Надо учесть возраст больной, все остальные обстоятельства
и решать: надо ли идти на морфологическую верификацию опухоли, которую
мы подозреваем, или продолжить на определенный промежуток времени
лечение противотуберкулезными и симптомагическими препаратами.Кроме того, мне бы хотелось остановиться на картине тяжелого остеопороза.
К 80 годам человек «имеет право» на развитие остеопороза, особенно жен¬
щина. Остеопороз был выявлен еще при первой КТ органов грудной клетки.
И в том, что он peшшзoвavlCя в повторные переломы позвонков, играет роль
интерлейкин-6, з'ровень которого особенно повышается при туберкулезе,
с другой стороны, с каждым годом жизни прогрессивно увеличивается риск
развития миеломы. В трепанобиоптате были не только рассеянные плазмати¬
ческие клетки, но и их скопления по 2—3 штуки, и есть основания повторно
провести стерншіьную пункцию или трепанобиопсию и посмотреть, не раз¬
вивается ли миелома, хотя в июне месяце и уровни иммуноі'.'юбулинов, и тре-
панобиоптат не давали оснований для такого диагноза; 80 лет, хроническое
воспаление и интерлейкин-6, который играет ключевую роль при миеломе,
должны учитываться при объяснении переломов позвонков.Краткое резюме. Я не объясню до конца механизмы анемии — э^го и иммун¬
ные механизмы нарушения обмена железа, это и микроциркуляторные нару¬
шения, связанные с гипервязкостъю, в том числе и в результате тромбонито-
за. Уровень тромбоцитоза — он колеблется от 600 до 800 тътс. — у пациентки
на ірани реактивного (тромбоцитоз до 600 тыс. считается реактивным), и нет
никаких другїпі проявлений первичного заболевания. Пациентке не угрожает
630 Системные заболеванияее анемия — как вы видели, она абссоготао к ней адаптарована. У нее нет
ни одышки, никаких симптомов того грозного состояния, которое требует
немедленной гемотрансфузии. Напротив, если мы будем планово переливать
ей кровь, мы усугубим микроцирку;шторные нарушения и дополнительно
перегрузим ее железом. Срок жизни перелрггьгх эритроцрггов у нее окажется
сниженным — не 4, а 2-3 нед; на 2-3 дня мы улучшим ее состояние, после
чего железо осядет в печени и селезенке.Тромбоцитоз требует коррекции. Конечно, эффект терапии хорошо проверять
лаборагорнмми тестами, но можно удовлетвориться и аспирином. Может быть,
ттеет смыст проводить инфузионную терапию, добавить инъекции трентала;
во всяком случаев обеспечить хорошую гидраташто. Больте я бы ничего не
прєдприниі^іала. Плюс — повторное исследование костного мозга для исключе¬
ния развития миеломы. В принципе, мы имеем право здесь говорить о миелоди-
сплазии вторичного характера. И я бы продолжила противот>'беркулезную тера-
ІШЮ до получения эффекта, воздержавшись от хирургических манипуляций.Комментарий С.И. Овчаренко — профессора кафедры факультетской тера¬
пии № 1 лечебного факультета Первого МГМУ им. И.М. Сеченова,
д-ра мед. наукКогда я слушала доклад, я представляла совсем другую пациентку — совер¬
шенно больного старого человека, задыхаюш,егося, анемичного. И когда я
увидела женщину здесь — да, это старая женщина, но в своем уме, не имею¬
щая одышки, адекватно на все реагирующая и имеющая бо:ш в позвоночни¬
ке. Это первое. Второе: у меня, как и у всех присутствующих здесь, диагноз
туберкулеза не вызывает сомнения, и он был адекватно поставлен в самом
начале, до получения морфологического подтверждения. Эффект кратко¬
срочной терапии также не вызывает сомнений. Дальше, отвечая на вопросы,
которые вы поставили, я хочу начать с того, чего можно ожидать при сочета¬
нии туберкулеза и рака у женщины в этом возрасте. 80 лет, она чувствует себя
относительно удовлетворительно, и идти на морфологическую верификацию
диагноза я бы не стала, хотя желание такое есть. Потому ^гго если у больной
развился рак, то операция не поможет (больная погибнет), эффекта от фото-
динамической терапии рака также ждать не приходится.Грибковое поражение мы сбрасьшать со счетов не можем (иммуносупрессия,
массивная антибактериальная терапия). Не очень похоже по характеру на
аспергиллому, но, с другой стороны, мы не так часто их видим. Думаю, что
проведение антигрибковой терапии целесообразно. Я бы также продолжила
противотуберкулезную терапию. Поддерживаю и точку зрения о проведении
повторной ірспанобиопсии (и в исходііьіх анализах уровень плазмоцитов
достигал 6%). А в отношении позвоночника — не хочется думать, что это
метастазы. Настолько сильно вьфажен остеопороз, и потом она активная
женщина, она не лежит только и не сидит, она вьгеодит на лавочку, она стира¬
ет, и, может быть, это послужило причиной повторного перелома. И, отвечая
на последний вопрос (что в наибольшей степени угрожает жизни больной),
я бы сказата — очередной перелом с травмой спинного мозга.
Глава 29. Необычный вариант течения висцерального туберкулеза... 631Комментарий Л.В. Недоступа — профессора кафедры факультетской терапик
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед.
наукФактологически добавлять что-то невозможно, все очень хорошо обсудили
с участием пограничных специа^тистов. Могу высказать только свои впечат¬
ления. Во-первых, не надо забывать (среди нас много молодежи), что мы
имели дело с лихорадкой неясного гснеза. В хирургию она попала агучайно,
но к очень хорошему хирургу (доктор д.л. Сапожников), который, к сожа¬
лению, не смог принять участия в сеюдняшнем разборе. Он замечательно
провел диагностический поиск — так, как надо было его проводить. Мы
всегда говорим, что по^гги не бывает чистой лихорадки неясного генеза без
какой-нибудь небольшой зацепки. Бывает, конечно, что человек лихорадит,
и больше — ничего. У нее бьта зацепка в виде стойкого плеврального выпо¬
та, и, ухватившись за это звено, мы вытащили постепенно всю цепь, как это
и бывает чаше всего.И окончательно решила вопрос все-таки морфология (что шже характерно
Д.ТЯ лихорадки неясного генеза) — морфологи с улицы Достоевского нам очень
помогли. Хотя там изначально многое было за туберкулез, и когда больная при-
ULia к нам, мы счигали, *гго она иришла с туберкулезом, и очень быстро Ha4ajiH
его лечить. Еще раз скажу, что ту-беркулез Пироговки — это не туберкулез улицы
Достоевского! Никакие фтизиатры не моїуг помочь нам с этим диагнозом. Так
было и здесь: они пришли и сказали, что может бьггь да, а может быть — и нет.
Часто ли мы видим внелегочный туберкулез? Надо сказать, ^гго при той эпиде¬
мии туберкулеза, которая бушует в стране, еще не так часто.Хотя полгода на;зад в этих стенах проходила демонстрация больного с цир¬
розом печени и плевральным выпотом туберкулезной этиологии. Довольно
давно мы демонстрировали с Н.Д. Саркисовой туберкулез селезенки у боль¬
ной с ревматическим пороком сердца, которая поступила к нам с лихораткой
и спленомегалией. В этой ситуации ей, конечно, был поставлен диагноз
инфекционного эндокардита, в течение полугода с переменным успехом про¬
водилось лечение антибиотиками, больная успела перенести тромбоэмбо¬
лию, что еще больше укрепило нас в мыслях об инфекционном эндокардите.
Но обратили внимание на то, что она болеет уже полгода, выздоровления не
наступает, но при этом не развились ни свежий порок сердца, ни нефрит, ни
миокардит, а селезенка выросла до очень больших размеров. Тогда пошли на
лапаротомию и обнаружили печень, пораженную узлами, и такую же селе¬
зенку. Селезенку потеряли по дороге в патанатомию (она исчезла), но сохра¬
нились биоптаты узлов печени. Характер фанулем в печени не был ясным:
В.В. Серов утверждал, что это лимфограііулематоз, а Д.С. Саркисов уверенно
ставил диагноз туберкулеза. Мы рассудили, что если лечить т>беркулез, то
при нали'пш лимфогранулематоза вреда это не принесет, а если лечить лим¬
фогранулематоз, то больная может погибн>ть от диссеминации. Больная
выздоровела от туберкулеза и погибла, к сожалению, от прогрессирования
порока сердца.
632 Системные заболеванияВ нашем случае диагноз ставился не очень трудно, но трудность создают поя¬
вившаяся тень в легком и анемия, которую мы без Е.А. Лукиной не смогли
бы осмыслить и как следует лечить. Подводя итоги, мне бы хотелось сказать о
том, что Факультетская терапевтическая клиника остается многопрофильной
университетской клиникой, а не узкоспециализированной (все-таки доклад
идет из отделения кардиологии), хотя углубление медицины по каждой
отдельной специальности все усиливается, и без помощи специалистов мы
уже не справляемся.Теперь что касается конкретики. Здесь действительно трудные вопросы.
Я думаю, что противогрибковую терапию проводить сгоиг, мы ничего не
теряем, а эффект получить можем. Я бы не сбрасывал со счета, несмотря
на не очень типичный вид тени в лепсом, и туберкулез. Мы не так хорошо
знаем туберкулез, чтобы отказываться от этой мысли так просто. Палотоа
сейчас, как известно, мутировала, туберкулез современный — это не тубер¬
кулез позавчерашнего дня. Это может быть устойчивая палочка, которая
дает совершенно иную клинріческую картину. Поэтому я согласен с тем,
что противотуберкулезную терапию надо продолжать. А вот в отношении
верификации агрессивной — тут я бы пошел на риск и попытался все-таки
получить какое-то морфологическое заключение. Без этого мы н№іего не
решим. А если получим рак ~ там видно будет. Но это мое субъективное, не
обоснованное ничем лшение.Комментарий B.M. Махова — профессора кафедры факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед.
наукМое мнение такое, что, учитывая возраст больной (даже если бы мы и
получили какие-то данные по поводу рака легких), ничего е ней делать не
надо, потому что операцию она не выдержит. Вспомним М.И. Непорента,
который нам показывал больных, по 7 и 12 лет живших с раком легкого (он
не прогрессировал). Если верификация принесет вред больной, то не стоит
ее проводить. Точно так же я бы воздержался от противогрибковой тера¬
пии — явной клиники нет, а активная противогрибковая терапия является
далеко не безразлрршой, нередко — драматической. Особенно в сочетании с
противотуберкулезной. Мы демонстрировали больного с циррозом и тубер¬
кулезным выпотом — туберкулез там ушел, но цирроз печени декомпенси-
ровался, и бо;ц>ной находился в состоянии хронической энцефачопатии.Комментарий BA. Сулимова — заведующего кафеіфой факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наук,
проф.Я думаю, что сегодняшняя демонстрация чрезвьггайно интересна. Втом
числе это демонстрация того, что не всегда мы можем все выяснить до конца.
Можно, конечно, щюдолжать диагностический поиск и дифференциальную
диагностику опухоли, туберкулеза, грибкового поражения, т.е. идти по пути
морфологической верификации. Вопрос — надо ли? Если бы это как-то
Глава 29. Необычный вариант течения висцерального туберкулеза.,, 633повлияло на тактику лечения и на прогноз жизни больной, наверное, стоило
бы. Вопрос — повлияет ли? Если мы увидим, что это опухоль, пойдем ли мы
дальше? Скорее всего, ответ будет отрицательный. Все равно мы оперативное
лечение предлаїатьне будем. Химиотерапия? — результатьт понятны. Поэтому
я ду\іаю, что, НС имея возможности радикально изменить лечение и прогноз
больной (даже если мы верифицируем рак легкого), не стоит идти этим путем,
хотя мы и не удовлетворим свою медицинскую любознательность, врачу всег¬
да важно поставить окончательный диагноз, но здесь надо вовремя остано¬
виться. Всегда есть какая-то граница, дальше которой фанатизм не оправдан,
в отношении переломов — хочется все это привязать к одной проблеме (опу¬
холевое поражение или туберкулезное). Явных признаков какого-то органи¬
ческого поражения позвоночника не получили. Не получим мы без морфо¬
логии ответа и на этот вопрос — в чем причина поражения позвоночника.
Осталась до конца не ясной и гематологическая ситуация — комплекс, как
нам наша уважаемая коллега сказала. Наверное, мы должны как-то смирить¬
ся с этой ситуацией. Важно продолжать туберкулостатическую терапию (это
ключевой момент) и максимально длительно наблюдать за больной.ЛИТЕРАТУРАВолошина В.В., Фомичева Н.И. Эффективность лечения новых случаев
деструктивного туберкулеза легких при одновременном наличии железодефи¬
цитной анемии // Проблемы туберкулеза. — 2002. — № 2. — С. 10-12.Каминская Г.О., Абдумаев Р.Ю. Метаболизм железа у больных с различными
формами туберкулеза легких // Проблемы туберкулеза. — 2002. — № 12. — С. 49—51.Минина М.И., Артамонова В.Ю. Антитела к эритроцитам и анемия при
туберкулезе легких// Проблемы туберкулеза. — 2002. — № 4. — С. 41-44.Akintunde Е.О., Shokunbi W.A., Adekunle С.О. Leucocyte count, platelet count and
erythrocyte sedimentation rate in pulmonary tuberculosis // Air. J. Med. Sci. 1995; 24
(2): 131-134.Bakhshi 5., Rao LS. , Jain V., Arya L.S, Autoimmune hemolytic anemia complicat¬
ing disseminated childhood tuberculosis 11 Indian J. Pediatr. 2004; 71 (6): 549-551.Bernard J.F., MercierJ.C,, Richard B., BoivinP. Pancytopenic form of acute tuber¬
culosis [Article in French] // Sem. Hop. 1975; 51 (37—38); 2239—2245.Bozoky G., Ruby £., Goher I. et at. Hematologic abnormalities in pulmonary tuber¬
culosis [Article in Hungarian] // Orv. Hetil. 1997; 138 (17): 1053—1056.Cameron SJ. Tuberculosis and the blood; a special relationship? // Tubercle. 1974;
55: 55-72.Chitnis A.S., Jochi V.R., Cherian A. et al. Utility of scalene node biopsy in the
diagnosis of pleuro-pericardial tuberculosis // J. Assoc. Physicians India 1974; 22:
805-808.Cho S.N., van der VlietG.M., Park S. etal Colorimetric microwell plate hybridiza¬
tion assay for detection of amplified Mycobactcrium tuberculosis DNA from sputum
samples //J. Clin. Microbiol. 1995; 33 (3): 752-754.
634 Системные заболеванияCulafic D., Вогісіс L, Vojinovic-Culafic V., Zdrnja М. Hepatic tuberculomas. А case
report// Rom. J. Gastroenterol. 2005; 14 (1): 71—74.Das B.S., Devi U., Mohan Rao C. et al. Effect of iron supplementation on
mild to moderate anaemia in pulmonary tuberculosis j j Br. J, Nutr. 2003; 90 (3):
541-550.D’Cruz S., Sachdev A., Kaur L. et al Fine needle aspiration diagnosis of isolated
pancreatic tuberculosis. A case report and review of literature j j JOP. 2003; 4 (4):
158-162.Demiroglu H., Dundar S. Vitamin B6 responsive sideroblastic anaemia in a patient
with tuberculosis I I Br. J, Clin. Pract. 1997; 51(1): 51-52.Ebrahim O., Folb P.I., Robson S.C., Jacobs P. Blunted erythropoietin response to
anaemia in tuberculosis // Eur. J. Haematol. 1995; 55 (4): 251-254.Fujiki R., Shiraishi K., Noda K. etal. A case of hemophagocytic syndrome associat¬
ed with miliary tuberculosis [Article in Japanese] j I Kekkaku. 2003; 78 (6): 443-448.Gupta V., Bhatia B.D. Abdominal tuberculosis with autoimmune hemolytic ane¬
mia I I Indian J. Pediatr. 2005; 72 (2): 175-176.Ismail Y., Muhamad A. Protean manifestations of gastrointestinal tuberculosis //
Med. J. Malaysia. 2003; 58 (3); 345-349.Twaki Chavez R, Bussalleu Rivera A. Gastrointestinal and peritoneal tuberculosis
[Article in Spanish] // Rev. Gastroenterol. Peru. 1994; 14 (2): 99—113.Kandutsch S., FeixA., Haas M. et at. A rare cause of anemia due to intestinal tuber¬
culosis in a renal transplant recipient // Clin. Nephrol. 2004; 62 (2): 158-161.Knox-Macaulay H.H. Serum cobalamin concentration in tuberculosis. A study in
the Guinea savanna of Nigeria //Trop. Geogr. Med. 1990; 42 (2): 146-150.Lefkovits М., Reusser P. An unusual presentation of tuberculosis [Article in
German] // Schwciz. Med. VVbchenschr. 1996; 126 (51—52): 2241-2243.Liu S., Chen W. , Liu W. Diagnosis and treatment of tuberculosis of bone marrow
[Article in Chinese] // Zhonghua Jie He He HuXi Za Zhi. 1998; 21 (9): 559-561.Lombard E.H., Mansvelt E.P. Haematological changes associated with miliary
tuberculosis of the bone marrow// Tuber. Lung. Dis. 1993; 74 (2): 131-135.Luman W,, Ng K,L. Audit of investigations in patients with iron deficicncy anae¬
mia // Singapore Med. J. 2003; 44 (10): 504-510.MertA., Bilir М., Tabak F. etal Miliary tuberculosis: chnical manifestations, diag¬
nosis and outcome in 38 adults j I Respiroiogy. 2001; 6 (3): 217-224.Morris C.D., Bird A.R., Nell H. The haematological and biochemical changes in
severe pulmonar>4uberculosis//Q. J. Med. 1989; 73 (272): 1151-1159,Morris C.D. The radiography, haematology and biochemistry of pulmonary tuber¬
culosis in the aged // Q. J. Med. 1989 Jun; 71 (266): 529-536,Murin S., Moritz E. Bilateral tuberculous pleural effusions with markedly difTerent
characteristics // Chest. 1996; 110 (3): 849-850.Oianiyi J.A., Aken'Ova Y.A. Haematological profile of patients with pulmonary
tuberculosis in Ibadan, Nigeria //Afr. J. Med. Sci. 2003; 32 (3): 239-242.Pay das S., Ergin М., BaslamisH F. et al Bone marrow necrosis: clinicopatho-
logic analysis of 20 cases and review of the literature j j Am. J. Hematol. 2002; 70 (4):
300-305.
Глава 29. Необычный вариант течения висцерального туберкулеза... 635Peng L., Luo Y.A., Wang G.Z. A study of standardization to the rapid detection of
Mycobacteriurn tuberculosis based on ptiage amplified biologically assay [Article in
Chinese] // Zhonghua Jie He He Hu Xi Za Zhi. 2004; 27 (12): 806-810.Ping-Hung K., Pan-Chyr Y., Shoo-Shown K., Kwen-Tay L. Severe immune hemo¬
lytic anemia in disseminated tuberculosis with response to antituberculosis therapy //
Chest. 2001; 119: 1961-1963.Reechaipichitkul W., Lulitanond V., Sungkeeree S., Patjanasoontorn B. Rapid diag¬
nosis of tuberculous pleural effusion using polymerase chain reaction // Southeast
Asian J. Trop. Med. F4iblic Health. 2000; 31 (3): 509-514.RhazalF., Lahlou M.K., Benamer S. etat. Splenomegaly and splenic pseudotumor
due to tuberculosis: six new cases [Article in French] // Ann. Chir. 2004; 129 (8):
410-414.Shin B.C., Kim 5.Ж, Ha S. W. et al Hemophagocytic syndrome associated with
bilateral adrenal gland tuberculosis // Korean J. Intern. Med. 2004; 19 (1): 70-73.Singh KJ., Ahluwalia G., Sharma S.K. et al. Significance of haematoiogical mani¬
festations in patients with tuberculosis // J. Assoc. Physicians India. 2001; 49: 788,
790-794.Sinha A.K., Agarwal A., Lakhey M. et a(. Pure red cell aplasia — report of 11 cases
from eastern Nepal // Indian. J. Pathol. Microbiol. 2003; 46 (3); 405—408.Sugane Т., Takahashi N., Koura T. et al. A case of tuberculous aneurysm of the
aorta [Article in Japanese] I I Kekkaku, 2000; 75 (10): 589-593.Tabbera LA. Hemolytic anemia: diagnosis and management j I Med. Clin. North.
Am. 1992; 765:649-668.Turken 0., Kunter E., Sezer M. et al. Hemostatic changes in active pulmonary
tuberculosis // Int. J. Tuberc. Lung Dis. 2002; 6 (10): 927—932.Ugo V., Ramon S., Delmer A. et al. Myelodysplasia and tuberculosis [Article in
French] I I Bull. Cancer. 1996; 83 (7): 548-552.Vnsal E., Aksaray S., Koksal D., Sipit T. Potential role of interleukin 6 in reactive
thrombocytosis and acute phase response in pulmonary tuberculosis // Postgrad. Med.
J. 2005; 81 (959): 604-607.Wagner J.B., Numberger H.R., Frede K.E. Complicated intestinal tuberculosis of
the mesenteric root [Article in Germanl // Dtsch Med. Wochenschr. 1997; 122 (20):
643-647.Wongtim S., Silachamroon U, Ruxrungtham K, etal. Interferon gamma for diagnos¬
ing tuberculous pleural effusions // Thorax. 1999; 54 (10): 921-924.Xia R, Poon R.T., Wang S.G. et al. Tuberculosis of pancreas and peripancre-
atic lymph nodes in inununocompetent patients; experience from China // World J.
Gastroenterol. 2003; 9 (6): 1361-1364.Yoon H.J,, Song Y.G., Park W.L et ai Clinical manifestations and diagnosis of
extrapulmonary tuberculosis // Yonsei Med. J. 2004; 45 (3): 453—461.Yoshimoto S., Takeuchi М., Tada A. Secondaiy sideroblastic anemia caused by
long term administration of anti-tuberculous agents including isoniazid [Article in
Japanese] // Rinsho Ketsueki. 1992; 33 (7): 986—990.
ГЕМАТОЛОГИЯГлава 30АНЕМИИ ХРОНИЧЕСКИХ ЗАБОЛЕВАНИЙ:
СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О ПАТОГЕНЕЗЕ
И ПОДХОДЫ К ЛЕЧЕНИЮЕЛ, Лукина, А.В, Недоступ, О.В. БлаговаДанная глава является непосредственным продолжением предыдущей, в
которой обсуждался необычный вариант течения висцерального туберкулеза
с рефрактерной анемией и были затронуты вопросы патогенеза и лечения так
называемой анемии хронических состояний.Здесь мы предстаатяем развернутое сообщение гематолога, профессора
Гематологмгческого научного пентра РАМН Е.А. Лукиной на эту тему, за кото¬
рым следует клиническое наблюдение. В нем обсуждается достаточно типич¬
ная для отделения кардиологии больная с ревматическим пороком сердца и
многочисленной сопутствующей патологией, у которой в анализах крови опре¬
деляется нетяжелая, но стойкая анемия с нормальным цветовым показателем.
После использования дополнительных лабораторных возможностей (в част¬
ности, помогающих дифференцировать анемию хронических заболеваний от
других) предлагаются наиболее вероятные гипотезы о происхождении анемии
у больной с протезированным клапаном, хронической сердечной и почечной
недостаточностью, которые анализируются гематологом. В качестве ведущего
механизма анемии у больной рассматривается микроангиопатический, обсуж¬
даются вопросы лечения.Профессор Гематологического научного центра РАМН Е.А. ЛукинаЯ представлю взгляд гематолога на проблему, которая, безусловно, вам
знакома. Думаю, что многие вещи, о которых я буду говорить, известны в
Факультетской терапевтической клинике им. В.Н. Виноградова Московской
медицинской академии им. И.М. Сеченова. Но мое желание выступить перед
вами продиктовано тем, что я много лет консультирую больных в терапев¬
тическом отделении поликлиники и часто встречаюсь с проблемами диффе¬
ренциальной диагностики железодефицитной анемии и анемии, связанной
с воспалением. В последние годы сложность диагностики связана не только
с медицинскими проблемами, но и с чисто социальными факторами. После
того как исчезло понятие диспансеризации, у многих пациентов, приходящих
в поликлинику с катаральными явлениями, острым воспалительным процес¬
сом, острыми респираторными вирусными заболеваниями, проводится анализ
Глава ЗО. Анемии хронических заболеваний: современные представления... 637іфови, и доктора, отмечая сниженный уровень гемоглобина, эритроцитов и,
как правило, сывороточного железа, ставят диагноз железодефинитной ане¬
мии, назначают препараты железа, причем зачастую вместе с антибиотиками.
Ниже представлены современные знания, которые существенно изменились за
последние годы.Железо — один из 15 эссенпиальных (необходимых) микроэлементов, физи¬
ологическая ро-ть которого определяется ролью тех белков, в состав которых
оно входит:1) широко известные гемоглобин и миоглобин;2) ферменты, участвующие в биологическом окислении, а следовательно, в
детоксикации ксенобиотиков и продуктов эндогенного распада;3) ферменты, нейтрализующие активные формы кислорода;4) ферменты, участвующие в синтезе белка и делении клеток.Отсюда вытекает роль железа в обновлении клеток крови, реализации не
только специфического иммунного ответа, но и неспецифической иммунной
резистентности.Кроме того, хорошо известно на сегодняшний день, что железо является
потенциально весьма токсичным микроэлементом. Это переходный металл,
легко отдающий один радикал и активно участвующий в свободнорадикаль¬
ных реакциях, которые могут приводить к перекиснот^іу окислению липидов
(и повреждению мембраны). Повреждения белка и рибонуклеиновых кислот
очень трудно клинически доказать, но на сегодняшний день они хорошо
известны; известны также мутагенные эффекты перегрузки железом и инакти¬
вация ферментов. Если раньше мы больше внимания уделяли вредным послед¬
ствиям дефицита железа, то в последние годы в клинике и в эксперименте
гораздо большее значение придается его патологической роли.Она очень хорошо известна гематологам (меньше — терапевтам) на моде¬
ли наследственного гемохроматоза, при котором избыток железа приводит к
поражению печени с развитием цирроза, сердца, легких. В последние годы
существенное внимание привлекает кардиотоксичностъ свободного железа.
В качестве двух основных механизмов кардиотоксичности рассматриваются
нарушение проводимости и свободнорадикальное повреждение кардиомио-
цитов. Наконец, значительный интерес прикован к патогенезу нейродегенера-
тивных заболеваний. Неправи.тьный обмен железа и его отложение в нервной
ткани связывают со многими патологическими симптомами при нейродегене-
ративных заболеваниях. Имеется первый опыт применения хилаторов железа
(препаратов, выводящих этот элемент) в лечении таких заболеваний.Основанием для такого внимания послужили некоторые наследственные
дефекты в метаболизме железа, например ацерулоплазминемия, и экспери¬
ментальные модели, где сознательно были «выбиты» гены, отвечающие за
некоторые белки, которые участвуют в обмене железа. Было обнаружено, что
эти наследственные дефекты генов ассоциируются с клинической картиной
нейродегенерации со сложной симптоматикой, зачастую психической, невро¬
логической. Разрабатываются новые хилаторы железа. На сегодняшний день
в клинике доступен лишь внутривенно вводящийся дефероксамин (десферал),
638 Гематологияно в Европе за последние годы зарегистрировано несколько пероральных
хилаторов железа. Один из них почти зарегистрирован в России, и скоро мы
получим возможность его применения, в том числе в терапевтической и кар¬
диологической практике.Дефицит железа, как и переірузка железом, имеет катастрофические послед¬
ствия для организма человека. Общее количество этого элемента в организме
поддерживается в достаточно узких рамках, что позволяет говорить о его гоме¬
остазе. Практически все железо в организме человека связано с белками — в
свободной форме оно практически не встречается, а если встречается, то его
токсические эффекты крайне опасны. Следующая часть моего сообщения
будет посвящена краткой характеристике тех белков, которые участвуют в
метаболизме железа и используются нами в лабораторной диагностике железо¬
дефицитной анемии и анемии хронических заболеваний.Хорошо известен трансферрин — белок, который отвечает за внек^аеточный
транспорт железа. Он циркулирует в сыворотке крови в довольно большом
количестве (2-3 г/л). Основным продуцентом этого белка являются клетки
печени, поэтому снижение уровня трансферрина в сыворотке крови наблю¬
дается при нарушении функции печени или свидетельствует о перегрузке
железом. Но, к сожалению, в жизни эти закономерности несколько сложнее, и
ориентироваться на уровень трансферрина в дифференциальной диагностике
сложно. Именно с трансферрином, переносчиком железа, связаны хорошо
известные показатели — железо сыворотки (по сути, это количество железа,
которое транспортируется главным образом трансферрином), ОЖСС (общая
железосвязываюшая способность сыворотки, отражает резервную, незапол¬
ненную железом емкость трансферрина) и показатель, который высчитывается
на основании уровня сывороточного железа и ОЖСС — НТЖ (насыщение
трансферрина железом). Если в одном из основных показателей ошибка, то
неправильным будет и третий.Как работает трансферрин? Практически! все клетки нуждаются в железе,
поэтому любая из них имеет поверхностный рецептор для трансферрина. Это
трансмембранный гликопротеин, функция которого — фагоцитоз трансфер¬
рина, насыщенного железом. Наиболее значительное количество таких рецеп¬
торов имеют клетки, которые сильно нуждаются в железе: быстро размножаю¬
щиеся (в том числе и опухолевые), но особенно эритроидные. Соответственно
этот показатель (количество трансферриновых рецепторов) характеризует
состояние эритропоэза. В сыворотке крови циркулируют растворимые фраг¬
менты рецепторов трансферрина {растворимые трансферриновые рецепторы),
которые слущиваются с поверхности кочетки. Их количество отражает физио¬
логическое состояние гемопоэза (наличие/отсутствие дефицита железа), но
при гематологических заболеваниях этот показатель работает плохо. Его сни¬
жение отражает угнетение эритропоэза, а при гемолитических анемиях пока¬
затель значительно увеличивается за счет эритроидной гиперплазии. Иными
словами, в этих случаях уровень трансферриновых рецепторов не отражает
состояния метаболизма железа. Но этот показатель оказался очень полезен,
потому что он не реагирует на воспаление.
Глава ЗО. Анемии хронических заболеваний: современные представления... 639После того как трансферрин, насыщенный железом, соединился с транс-
ферриновым рецептором на поверхности клетки, этот комплекс поступает
внутрь клетки, расщепляется, трансферриновые рецепторы возвращаются
на поверхность мембраны и функционируют как прежде; лишенный железа
трансферрин поступает в плазму крови, а железо остается в клетке и исполь¬
зуется для синтетических процессов. Избытки железа соединяются с белком,
который носит название ферритам и призван депонировать железо преиму¬
щественно внутриклсточно. Это очень крупный белок (его молекулярный вес
практически идентичен молекулярному весу фибриногена), он может вмещать
колоссальное количество атомов железа (по сути дела это ядро, вокруг которо¬
го располагается до 4500 атомов железа). Но, помимо внутриклеточного фер-
ритина, в сыворотке крови непрерывно циркулирует определенное количество
так называемого сывороточного ферритина. Предполагается, что этот белок
секретирустся клетками печени, макрофагами. В фгтзиологических условиях
он отражает запасы железа в организме, но при наличии воспаления (инфек¬
ция, опухоль) он работает как белок острой фазы, отмечается его значительное
повышение (более 1000 мкг/л).В последние годы описан целый ряд других белков, которые участвуют в
обмене железа. В полости двенадцатиперстной кишки имеется так называемый
пищевой переносчик двухвалентных металлов (DMT-I ~ Nramp-1, т.е. natural
resistance-associated macrophage protein — pH-зависимая помпа Fe-^, изфагосом), и пищевое железо транспортируется с помощью этого белка внутрь
энтероцита. Очень важен белок ферропортин, функция которого — экспорт, т.е.
выведение железа из клетки. Поступление железа в клетку обеспечивается и
грансферрином, и пишевым переносчиком двухвалентных металлов, и макрофа¬
гами, которые могут поглощать железо и эритроциты, но выход железа из клет¬
ки обеспечивается только ферропортином. Описаны наследственные дефекты
генов, кодирующих ферропортин, в результате которых железо блокируется в
энгероцитах, макрофагах, гепатоцитах. Фенотип этого заболевания характеризу¬
ется глубокой гипохромной, зачастую микроцитарной анемией, которая по всем
признакам соответствует железодефииитной, но сочетается с тканевой переіруз-
кой железа. Выделены соотвстствуюшис формы гсмохроматоза.Очень важны ферменты феррооксидазы (Си^), которые в составе внутри¬
клеточного ферритина переводят двухвалентіюе железо в трехвалентное (такое
железо может соединиться с трансферрином). И, наконец, самое важное откры¬
тие последних 5 лет, которое явилось маленькой революцией в представлениях
об обмене железа, — это белок гепсидин (Hepaticus + Caeder), который проду¬
цируется клетками печени и регулирует внеклеточный пул железа. Он связьта-
ется с ферропортином, который представляет собой трансмембранный белок,
интернализируется (поступает внутрь клетки) и блокирует внутриклеточное
железо — оно не выходит из энтероцитов, гепатоцитов, макрофагов, при этом
развивается малокровие, которое симулирует железодефицитную анемию.Коротко о метаболизме железа в организме. Оно не синтезируется в орга¬
низме, стартовый запас плод получает через плаценту (примерно 300 мг),
далее в раннем детском возрасте за счет пищевого железа быстро достигается
640 Гематологияфизиологический уровень, который варьирует в зависимости от конституции
от 3 до 5 г, и этот уровень поддерживается в течение жизни. Ежедневные физио¬
логические потери очень невелики — это 1 —2 мг (слушивание эндотелия желу¬
дочно-кишечного тракта, потоотделение), У женщин серьезные физиологиче¬
ские потери связаны с известными процессами (менструальные потери около
15 мг, беременность и роды — около 800 мг). Это количество компенсируется
постуїшением пищевого железа (1—2 мг/сут).В полости двенадцатиперстной кишки, где в основном происходит всасы¬
вание железа, с помощью белка-переносчика железо доставляется в полость
энтероцита, окисляется, и далее его судьба решается гормоном гепсидином:
при избытке оно блокируется в энтероците, который в дальнейшем слуши¬
вается (таким образом железо из организма удаляется); при недостаточных
запасах (решает гепсидин) быстро поступает в кровоток и соединяется с
трансфсррином. Для того чтобы это соединение осуществилось, ионы железа
должны быть ферропортином выведены из клетки и переведены из двух- в
трехвалентнос состояние (на уровне кишечника эту функцию несет белок
гефестин).Из энтероцита с портальным кровотоком железо в первую очередь попада¬
ет в печень, где часть его хранится в виде запаса (печень располагает самыми
больптими запасами — примерно 1 г — и при необходимости может быстро
этот ион высвобождать). Основная масса железа поступает с трансферрином в
костный мозг, где происходит продукция эритроцитов, значительно \геньшая
его часть — к быстро делящимся клеткам, которые имеют большое количество
трансферриновьтх рецепторов. Далее оно в составе эритроцитов циркулирует в
крови (в норме 120 дней), затем разрушается макрофагами печени и селезенки.
Освобождается железо, которое да-тее должно опять поступить в обпшй крово¬
ток. Но для этого снова должны быть выполнены определенные условия: вывод
железа из макрофага (а это единственный белок ферропортин) и окисление
до той формы, которая может поступить в трансферрин, с помощью церуло-
плазмина. Ацерулоплазминемия — модель именно такой анемии, при которой
малокровие сочетается с тканевой перегрузкой железа.Если железо нормально поступает в трансферрин, оно возвращается в цир¬
куляцию — этот процесс носит название рециркуляїщи железа. Пищевое желе¬
зо (1-2 мг) в отсутствие массивных кровотечений компенсирует естественные
потери, а процесс кроветворения требует ежедневно от 20 до 30 мг железа, т.е.
на порядок выше. Именно это количество железа ежедневно рециркулирует,
т.е. возвращается в циркуляцию макрофагами печени и селезенки. Этот про¬
цесс рециркуляции играет гораздо большую роль, чем недостаточное поступле¬
ние пищевого железа.Как регулируется хметаболизм железа низкомолекулярным белком гепси-
дином, который называют гормоном? В норме продукция гепсидина гепато-
цитами зависит от уровня всосавшегося железа (рис. 30. /); если он достаточно
велик, то синтез гепсидина клетками печени усиливается, гепсидин блокирует
функцию ферропортина, и железо блокируется в клетках. Прекращаются вса¬
сывание (железо блокируется в энтероцитах), рециркуляция макрофаіами,
Глава ЗО. Анемии хронических заболеваний: современные представления... 64/fFe плазмы—атоцит)—Всасывание—► РециркуляцияДепо FeРис. зол. Регуляция обмена железа гепсилиномне высвобождаются запасы из печени. Далее уровень железа в сыворотке крови
падает, снижается синтез гепсидина и восстанавливается выход железа из
эитероыитов, гепагоцитов и макрофагов. Эта продуманная регуляция зависит,
таким образом, от уровня железа и кислорода.Но оказалось, что есть второй путь регуляции обмена железа через гепси-
дин, который зависит от провоспалительных цитокинов, в первую очередь
от интерлейкина-6. При наличии воспалительного или опухолевого протіесса
повышается уровень провоспалительных цитокинов, что приводит к повы¬
шению синтеза гепсидина, и развиваются те же процессы, что и при физио¬
логическом повышении уровня гспсидина, которые приводят к перераспреде¬
лительному дефициту железа.Я напомню о том, что анемии хронических заболеваний, или анемии вос¬
паления (не очень удобный термин, но он прижился), — это многофакторный
процесс, в котором ключевую роль играет активация клеток им\і>'нной систе¬
мы (это в основном макрофаги и В-лимфоциты), которые под воздействием
разли^шых стимулов (инфекции, опухоли, продукты деструкции ткани) про¬
дуцируют провосналительные иитокины. В результате развивается нарушение
баланса между продукцией эритроцитов в костном мозге и их разрушением —
развивается та самая анемия хронических заболеваний. В этом нарушении
баланса важную роль играют дефекты метаболизма железа.Клк это происходит? Давно было известно, что перераспределительный
дефицит железа развивается в результате снижения его всасывания, наруше¬
ния процессов рециркуляции {рис. 30.2). После того как был открыт гепсидин
и доказана его роль, выяснился механизм этих процессов: очаг воспаления —
повышение продукции провоспалительных цитокинов — повышение про¬
дукции гепсидина, который выключает функцию ферропортина, и железо
блокируется внутри клетки таким образом, что прекраш,аются все нормальные
процессы.Предполагается, что железо удаляется из доступной циркуляции в связи
с тем, что опухолевые клетки, микробные клетки нуждакугся в поступлении
этого элемента, и механизм носит характер приспособительного иммунного
механизма. Менее известно, что свободные ионы железа подавляют активность
ключевого цитокина — интерферона-у, который запускает все звенья иммун¬
ного ответа (и клеточную цитотоксичность, и ответ макрофагов). Среди всех
приспособительных механизмов, которые придумала природа, есть один —
снижение всасывания железа, — который мы можем преодолеть. Известно,
что довольно значительный процент людей (17% белого населения Амерріки)
является гетерозиготами по гену гемохроматоза — это приводит к толсу, что
642ГематологияПовьішение продукции гепсидинаНарушениеБлокада депорециркуляции FeFeПерераспределительный дефицит железаСнижение синтеза гемоглобинаРис. 30.2. Изменения метаболизма железа при анемии хронических заболеванийесли во время воспалительного процесса давать пациенту большое количество
железа, оно всасывается. Мы можем преодолеть механизм защитного пере¬
распределительного дефицита железа. К чему это приводит, я хотела бы про¬
демонстрировать на нашем очень давнем клиническом примере. Я не берусь
отстаивать положение о том, что к такому результату привели именно таблетки
железа, но тем не менее ірис. 30.3).Пациенту было примерно 40 лет, когда он перенес острый вирусный
гепатит в достаточно тяжелой форме. После реконвалесценции у него
оставался сниженным гемоглобин (гипохромная анемия). Терапевтом
были назначены препараты железа, которые он принимал сначала эпизо¬
дическими курсами, а затем практически постоянно на протяжении 10 лет.
Уровень гемоглобина постепенно снизился до 70 г/л, и пациент поступил
в нашу клинику. Выяснилось, что у него тяжелая перегрузка железом. В то
время невозможно было оценить маркеры наследственного гемохромато-
за, и трудно было сказать, что сыграло роль в развитии этого состояния.
У пациента имелся хронический вирусный гепатит С, биопсия печени
выявила признаки цирроза (3 балла). Мы проводили периодические курсы
хилаторной терапии, плазмафереза, интерферона. Его гемоглобин стаби¬
лизировался на уровне 80-90 г/л, к которому он был абсолютно адаптиро¬
ван. Но еще через 2-3 года при тех же гематологических показателях было
обнаружено очаговое поражение печени, которое очень быстро преврати¬
лось в многоочаговое поражение, через полгода больной погиб от гепато-
целлюлярной карциномы.К сожалению, таких случаев много, просто не все они до конца нами про¬
слежены. Мне бы хотелось, чтобы этот пример вспомнился, когда после пере¬
несенной инфекции или воспаления приходит пациент с малокровием.
Глава ЗО, Анемии хронических заболеваний: современные представления... 643ЛечениеБиопсияпечениСелезенкаПеченьНЬдесферал
фиброз 3 б. циррозі і іHCV-RNA+Fe = 47Ферритин = 68001999 г.10.2002 г.
morsРис. 30.3. Схема истории болезни пациента Н., 1947 г.р.Анемия хронических ЖелезодефицитнаяФерритинЖелезоНТЖТрансферринРастворимые
рецепторы
к трансферринузаболеванийtП♦tИ*анемия♦♦tРис. 30.4. Дифференциальная диагностика анемии хронических заболеваний и железо¬
дефицитной анемииЧто нужно использовать в дифференциальной диагностике анемии хро¬
нических заболеваний и железодефицитной анемии? На рис. 30.4 выделены
те параметры, на которые, к сожалению, полагаться нельзя (это большой
опыт — и наш, и зарубежный). Ни железо сыворотки крови, ни уровень
трансферрина, ни тем более расчетный показатель (процент насыщения
железом) не могут служить надежным критерием в дифференциальной диа¬
гностике. Надежным показателем яшіяется повышение уровня сывороточного
644 Гематологияферритина; растворимые рецепторы к трансферрину тоже имеют значение.
При жслезодефииитной анемии отмечается низкий уровень сывороточного
ферритина.На сегодняшний день понятно, что, к сожалению, и уровень ферритина не
является абсолютным показателем — при патологических процессах в печени
он может быть низким, но это все равно не будет истинная железодефицитная
анемия.Остальные показатели находятся в состоянии изучения. Здесь приводится
минимальная панель, которая достаточна для изучения состояния метаболизма
железа в общей практике. Растворимые рецепторы к трансферрину — это для
специализированных лабораторий, они имеют большое значение в трудных
случаях. ВОЗ в 2004 г. провозгласила, что железодефицитная анемия и анемия
хронических заболеваний не имеют морфологических различий (нельзя ори¬
ентироваться на микропитоз), и только два показателя — ферритин и раство¬
римые рецепторы к трансферрину — вместе с уровнем гемоглобина являются
дифференциально-диагностртческими критериями.Итак, на сегодняшний день установлено, что регуляция обмена железа в
организме определяется двумя механизмами — метаболическим (т.е. уровнем
запаса элемента в организме) и иммунным (через провоспалительные цито-
кины). Печень является центральным органом, который включен в регуляцию
метаболизма железа. Она поддерживает основной физиологический механизм
возвращения железа в циркуляцию (нишевой механизм играет не главную
роль); осуществляет продукцию провоспалительных цитоишов, которые в
основном попадают в цирк>'ляцию из макрофагов и клеток Купфера, а также
гепсидина, который регулирует BHeKJieT04H>T0 концентрацию железа, других
железосвязывающих белков; наконец, является основным депо железа в орга¬
низме. Наши исследования совместно с гепатологами показали, что заболе¬
вания печени сопровождаются нарушениями в метаболизме железа, характер
которых зачастую достоверно связан с клинико-морфологическими прояв¬
лениями заболевания печени, и что показатели обмена железа несут ценную
информацию для характеристики сталии и активности заболевания. Патология
печени зачаст>'Ю латентна и проявляется лишь на поздних стадиях, поэтому
выявление анемии неясного генеза может сл>окить ключом к постановке более
раннего диагноза заболевания печени.Если пациент имеет заболевание печени, то в большинстве случаев у него
отмечается анемия хронических заболеваний, те. диагноз железодефицита
должен быть очень серьезно доказан, и только в этом сл>'чае могут быть назна¬
чены препараты железа.Приводим клиническое наблюдение из отделения кардиологии
Факультетской терапевтической к.іиники им. В.Н. Виноградова.Больная К., 72 года, поступи.іа в Факультетскую терапевтическую клинику
им. В.Н. Виноградова 27.09.2007 г. с жалобами на умеренную общую слабость,
одышку при умеренных физических нагрузках, отеки голеней и стоп, неча¬
стые ноюшие боли в области сердца, которые четко не связаны с физически¬
ми нагрузками и купируются самостоятельно, ощущение онемения в ногах
Глава ЗО. Анемии хронических заболеваний: современные представления,.. 645(вк-щючая стопы), чувство «ватных ног», неустойчивость при ходьбе, прибавку
в весе около 10 кг за 4 мес.Из семейного анамнеза известно, что отец умер в 80 лет от острого нарушения
мозгового кровообращения, мать — в 72 года (причина неизвестна), брат умер
в 51 год от прободной язвы; два сына (46 и 52 лет) здоровы. Родилась в 1934 г
в Тверской области, в возрасте 8—9 лет находи.іась в немецком концентраци¬
онном лагере. По профессии — крановщица, в настоящее время на пенсии,
инвалид 11 группы. Вредных привычек нет, В 1997 г. — резекдия шитовидной
железы по поводу узлового зоба II1-IV степени. В июне 2007 г — правосто¬
ронняя гемитиреоидэктомия по поводу цистаденомы, с этого времени полу¬
чает L-THpoKCPfH 25-50 мкг/сут. В 2006 г. при ЭГДС была выявлена рубцовая
деформация пилоробульбарной зоны (явных обострений не было); в январе2007 г. — эрозивный бульбит, проведен курс противоязвенной терапии. Более
2 лет страдает псориазом (лечение дермосалом с некоторым эффектом).Анамнез заболевания (рис. 30.5): сведений о ревматических атаках в детском и
подростковом возрасте нет. В 1976 г (в возрасте 42 лег) перенесла гнойную ашттну.
С 1978 г. стала отмечать кратковременные приступы сердцебиения, которые про¬
ходили самостоятельно. С1980 г. приступы сердцебиения участились, на ЭКГ фик¬
сировалась мерцательная аритмия, приступы куттировались бригадами «Скорой
помощи» внутривенным введением изоптина. Ухудшилось общее состояние, поя¬
вилась одышка. В том же году бьи диагностирован ревматический митральный
порок с преобладанием стеноза. С 1990 г наблюдается в Факультетской терапевти¬
ческой клинике им. В.Н. Винофадова, регулярно госпитализируется. С 1992 г —
постоянная форма мерцательной аритмии, с этого времени регулярно принимала
дигоксин (до 0,25 мг/сут). Прогрессировала недостаточность кровообращения по
обоим кругам, в связи с чем в 1995 г. в Институте сердечно-сосудистой хирургии
им. А.Н. Бакулева вьшолнены протезирование мифального клапана, пластика
TpHKycr^avTbHoro клапана, с этого времени постоянно принимаїа фенил ин,
В течение нескольких лет П0С.1Є этого одьшжа была выражена умеренно, затем
вновь начала нарастать, возобновились периферические отеки.Во время очередной госпитализации в 2001 г. при холтеровском монито-
рировании ЭКГ бььти зафиксированы периоды урежения ритма до 45/мин,
а также же.іудочковая экстрасистолия и пробежки желудочковой тахикар¬
дии; гликозиды были временно отменены, проводилась терапия дифенином,
затем соталексом и эгилоком в сочетании с дигоксином. В 2005 г. в связи с
возобновлением желудочковых нарушений ритма дигоксин окончательно
отменен, однако в начале 2006 т. на фоне приема эгилока у больной развшіся
обструктивный бронхит, и она самостоятельно вернулась к приему дигоксина.
В декабре 2006 т. была госпитализирована в Факультетскую терапевтическую
клинику им. В.Н. Виноградова в связи с выраженной декомпенсацией по боль¬
шому и малому кругам кровообращения, развитием кардиальной астмы; при
холтеровском мониторировании выявлено 3800 желудочковых экстрасистол (в
том числе по типу би- и тригеминии, 4 пробежки желудочковой тахикардии).
Подтверждено наличие генерализованной бронхиальной обструкции (ЖЕЛ
51%, ОФВ, после ингаляции атровента 51%, МОС^, — 30%, — 19%,
646Гематология1976 г, 1978 г. 1992 г. 1995 г. 11.05 12.06 5.07ангинамерцательнаяаритмияодышкакардиальнаяастмаотеки голеней
и стопжелудочковыеаритмиидигоксинкордаронлечениеРис. 30.5. Анамнез больной К.. 72 годапротез МКрезекция ЩЖМОС^^ — 19%). Попытка терапии дифенином без эффекта. Гормоны щито¬
видной железы оставались в пределах нормы, в ткани железы имелись узловые
образования. С учетом жизнеугрожаюшего характера аритмии была начата
терапия кордароном в поддерживающей дозе 400 мг/с>т, число экстрасистол
снизилось примерно до 1000/сут, пробежки желудочковой тахикардии не
фиксировались. Однако через полгода от начала терапии отмечено нарастание
одышки, ттоявление ошушения перебоев в работе сердца; зафиксировано более
12 тыс. экстрасистол в сутки. Диагностирована цистаденома перешейка щито¬
видной железы размерами 3x2 см, в мае 2007 г произведена гемитиреоидэк-
томия с последующим назначением L-тироксина в дозе 25, далее 50 мкг/с>'т.
Был продолжен прием кордарона 400 мг/сут в сочетании с верапамилом. Сразу
после операции было выявлено устойчивое повышение уровня креатинина (до
2 мг%). Продолжала получать верошпирон, петлевые диуретики, фени^іин.В течение последних 4 мес самочувствие стабилизировалось; перебои в
работе сердца и кардиальная астма не беспокоили; отметила прибавку в весе10 кг, а также нарастание ощутцения онемения в ногах, которое появилось неза¬
долго до операции.Необходимо остановиться на сведениях об анемии, которые удалось полу¬
чить из выписных эпикризов, о наличии легкой нормохромной анемии досто¬
верно известно с 2003 г. Уровень гемоглобина колебался в пределах 113—123 г%
(цветовой показатель на уровне 0,96), его последнее заметное снижение (до
108 г%) возникло вскоре после резекции щитовидной железы, уровень ретику-
лоцитов не определїшся.
Глава ЗО. Анемии хронических заболеваний: современные представления... 647При поступлении в клинику в конце сентября 2007 г. состояние средней
тяжести. Вес 96 кг, рост 164 см. Акроцианоз, псориатические бляшки на коже
предплечий, голени, груди. Отеки голеней и стоп (до коленных суставов).
Число дыханий 18/мин, дыхание жесткое, в базальных отделах справа — еди¬
ничные незвонкие мелкопузырчатые хрипы. ЧСС 55/мин, на фоне правильно-
го ритма — не более 1 экстрасистольт в минуту, мелодия протеза, акпент П тона
над легочной артерией, систолический шум на верхушке, диастолический шум
в точке Боткина. Живот мягкий, болезненности нет, печень + 4 см, селезенка
12x5 см, нижний полюс селезенки не пальпируется.В общих анализах крови от 28 сентября, 4 октября и 9 октября НЬ 106,8; 114,5
и 108,2 г/л, эритроциты 3,3; 3,4 и 3,2 млн, цветовой показатель 0,98; 0,99 и
1,02, лейкоциты 5,8; 7,2 и 6,8 тыс., нейтрофилы 67, 65 и 64%, лимфоциты 22,
25 и 24%, моноциты 7, 7 и 9%, эозинофилы К О и 0%, базофилы 3%, СОЭ І0,
27 и 15 мм/ч, тромбоциты 244, 226 и 215 тыс. Ретикулопиты в последних двух
анализах 33%с.В биохимическом анализе крови обш:ий белок 6,8 г%, альбумин 4,3 г%, креа-
тинин 1,7 мг%, глюкоза 98 мг%, азот мочевины 36 мг%, мочевая кислота5.5 мг%, общий билирубин 1,1 мг%, натрий 137 шкв/л, калий 4,8 мэкв/дл.
Триглицериды 76 мг/дл, обший холестерин 182 мг/дл, ACT 26 Ед/л, АЛТ
21 Ед/л. Железо 121 мкг/дл, трансферрин 253 мг/дл, % насыщения железом
33,9- В повторном анализе креатинин 1,9 мг%, азот мочевины 45 Nfr/дл, общий
билирубин 0,8 мг/дл. Электрофорез белков: альбумин 75,2%, а,-глобулины
3%, а,-глобулины 9,8%, р-глобулины 10,8%, у-глобулины 19,2%. Фибриноген3.05 г/л, ПИ 76%, АЧТВ (нормализованное отношение) 1,31, МНО 1,38. СРВ,
анти-О-стрептолизин отрицателен, РФ+. Реакция Кумбса не проведена по
техническим причинам.Гормоны щитовидной железы: ТЗ (сумм.) 1,91 нмоль/л; Т4 (своб.) 11,7 пмоль/л;
ТТГ 53,7 МЕ/л; антите.та к ТПО 16 МЕ/мл. В повторном анализе через 2 нед Т4
(своб.) 9,8 пмоль/л, ТТГ 67,4 МЕ/л.В общем анализе мочи: удельный вес 1016, pH 8, прозрачность неполная;
бедка, сахара, ацетона, желчных пигментов нет, уробилин в пределах нормы,
лейкоциты и эритроциты единичные в поле зрения, слизи немного, бактерий
много.Реакция кала на скрытую кровь (с бензидином) отрицательная.На ЭКГ при поступлении наджелудочковый ритм (ритм из АВ-соединения)
с ЧСС 46/мин, электрическая ось сердца расположена нормально. Полная бло¬
када левой ножкіг пуїка Гиса. QRS 0,16 с, QT’0,48 с, QTc 0,44 с.При суточном мониторировании ЭКГ по Холтеру (на фоне постоянного при¬
ема кордарона 200 мг/сут) суправенгрикулярный ритм, ЧСС днем 48—89/мин
(ср. 55/мин), ЧСС ночью 47-В5/мин (ср. 50/мин); отмечались резкие изме¬
нения ЧСС (напр. 50-80—50/мин в 06:40-07:20); желудочковых экстрасистол
около 2000, максимально 267/час (с 10 до 11 часов). Анализ ІТ—7 .затруднен в
связи с нарушениями проводимости.При ЭхоКГжелудочек 6 см, левое предсердие 5,7x7,3x6,1 см, правый
желудочек 2,4 см, правое предсердие 6,7x5,1 см, ФВ левого желудочка 40—58%,
64S ГематологиятМЖП 1,2 см, тЗС 1,2 см, тПЖ 0,7 см. Неравномерность степени систоличе¬
ского утолщения миокарда левого желудочка. Митральный клапан: эхосигна-
лы протеза 15 мм рт.ст., 5,9 мм рт.ст.). Аортальный клапан: уплотнение
створок (Руакс рт.ст., Ррр 8,5 мм рт.ст.). Систолическое давление в правом
желудочке 38 мм рт.ст. Трикуспидальный клапан не изменен, стснки аорты
уіь'іотненьї. При допплеровской эхокардиохрафии — митральная и аортальная
регургитация ТТ степени, трикуспилалъная регургитация I степени.При рентгенографии органов грудной клетки: свежих очаговых и инфиль-
тративных изменений в легких не выявлено. Сосудистый рисунок обогащен,
калибр сосудов расширен преимущественно в верхних отделах; корни легких
частично скрыты за тенью сердпа, уплотнены. Диафрагма расположена на
уровне переднего отрезка 7-го ребра. Плевральные синусы свободны. Сердце
значительно увеличено в размерах, расширено в обе стороны и кзади, в попе¬
речнике 20,5 см, в проекции митрального клапана определяется протез. Аорта
уплотнена, возможно расширена в восходящем отделе; сосудистый пучок спра¬
ва уплотнен.При ЭГДС. пишевод свободно проходим, не изменен; кардия смыкается.
В желудке немного прозрачной жидкости, рельеф не изменен, складки рас¬
правляются воздухом; слизистая оболочка в теле и угле розовая, в антраль¬
ном отделе с участками атрофии, гиперемии; малая кривизна и угол ровные.
Привратник округлый, свободно проходим. Луковица двенадцатиперстной
кищки грубо рубцово деформирована, проходима; слизистая оболочка луко¬
вицы без выраженных воспалительных изменений. Постбульбарный отдел не
изменен. Заключение: рубцовая деформация луковицы двенадцатиперстной
кишки. Антральный гастрит с атрофией слизистой оболочки.В связи с подозрением на фуникулярный миелоз больная бьиа проконсуль¬
тирована выявлены недоведение глазных яблок вверх, недостаточ¬
ность VH и ХП пар черепных нервов по центральному типу слева. Парезов нет.
Сухожильные рефлексы на руках и ногах симметричны. Гипэстезия на ногах
по типу коротких носков. Заключение: клинически имеет место хроническая
цереброваскулярная недостаточность ТТ степени в рамках основного заболева¬
ния. Нарушения памяти. Полинейропатический синдром (смешанная форма).
Нарушение сна.Таким образом, у больной имеется целый ряд факторов, которые можно
рассматривать в качестве причин анемии.1. Хроническая недостаточность кровообращения ТТБ стадии, которая
сегодня njHpOKo обсуждается как причина недостаточной выработки эритропо-
этина. Речь идет не только об абсолютном ее снижении, но и о недостаточном
ее повышении в ответ на гипорегенераторные анемии, связанные с другими
факторами. Мы не будем касаться вопроса о прогностической значимости
анемии у больных с застойной сердечной недостаточностью, на сегодняшний
день она совершенно четко показана; анемия является одним из независимых
факторов, повышающих смсргносгь таких больных.2. Наличие у больной устойчивого ретикулоцитоза в отсутствие признаков
кровотечения и заместительной терапии заставляет рассматривать в качестве
Глава ЗО. Анемии хронических заболеваний: современные представления.,. 649весьма вероятной причины анемии механический протез митрального iciana-
на. Гемолитическіш анемия у бо.тьных с протезированными клапанами и сосу¬
дами носит механический характер и описывается почти у 10% больных с про¬
тезами аортального клапана. При наличии протеза митрального клапана такая
анемия встречается реже вследствие меньшего градиента давления (особенно
при наличии околопротезной регургиташи, которая как раз имеется у нашей
больной). Гемолиз может развиваться даже в отсутствие протеза у больных с
выраженным кальцинозом аортального клапана (механическое препятствие
кровотоку), а также на искусственном материале заплаты на дефекте межпред-
сердной перегородки и даже у больных с аоргобедренным шунтированием.Выделяют три механизма такого гемолиза: сила сдвига, действующая иа
мембрану эритроцитов в турбулентном потоке (например, околопротезная
регургитация); прямое механическое повреждение эритроцитов в момент
закрытия запирательного элемента (особенно стеллитового, в меньшей степе¬
ни — силиконового; биопротезы практически не приводят к развитию меха¬
нического гемолиза) и отложение фибрина в >'частках неплогного прилегания
кольца клапана к тканям сердца с разрушением проходящих через нити фибри¬
на эритроцитов.Уровень гемоглобина у больных с аортальными протезами может снижаться
до 50—70 г/л; имеют значение не только общие лабораторные признаки гемо¬
литической анемии (ретикулоцитоз, повышение уровней ЛДГ и непрямого
билирубина, чего, кстати, не было у нашей больной), но и обнаружение в мазке
периферической крови шизоцитов — осколков эритроцитов, которые возника¬
ют при их механическом повреждении и характерны не для всех видов гемоли¬
тической анемии (рис. 30.6, см, цветную вклейку). В нашем случае мы просили
визуально опенить состояние эритроцитов, однако никаких патологических
феноменов найдено не было. При массивном гемолизе с гемоглобинурией воз¬
можно развитие дефицита железа, изредка — положительная реакция Кумбса.Лечение анемии у больных с протезами клапанов предполагает в первую
очередь ограничение физических нагрузок и другие способы снижения сер¬
дечного выброса (в том числе усіранение самой анемии), а также устранение
околопротезной регургитации (вплоть до смены протеза) и при необходимо¬
сти — восполнение дефицита железа.3. Хроническая почечная недостаточность, которая сохраняется у нащей
больной в течение 4 мес после тиреоидэктомии, приводит к развитию анемии в
результате снижения выработки эритропоэтина, а также значительного укоро¬
чения срока жизни эритроцитов на фоне уремии. По-видимому, основной при¬
чиной хронической почечной недостаточности явршся длительно существую¬
щий застой но большому круїу кровообращения, нельзя исключить и развитие
атеросклероза почечных артерий. Наркоз сыфал роль разрешаюпі;его фактора.4. Несомненно, усугубил анемию нараставший после тиреоидэктомии гипо¬
тиреоз, который за счет снижения основного обмена приводит к снижению
чувствительности клеток, продуцирующих эршропоэтин, измене!шю достав¬
ки кислорода, кроме того, при гипотиреозе снижается всасывание железа и
фолиевой кислоты.
650Гематология5. Наконец, весьма вероятным представлялось наїичие у больной дефицита
витамина — возникла тенденция к гиперхромии, которой не бьыо раньше,
наросли явления онемения в ногах; отчасти В^2-дефицитным компонентом мог
объясняться и гемолиз, хотя макроцитоза периферической крови обнаружено
не было. Больная потребляла мясо в недостаточном количестве; кроме того, у
нее имеется атрофический гастрит.Для уточнения роли всех описанных механизмов был выполнен специальный
биохимический анализ крови в Гематологи^іеском научном центре РАМН {рис.
30.7). Уровень ферритина оказался выше 300 мкг/л, но не превысил 1000 мкг/л.
Фолаты сыворотки находятся на нижней фанидс нормы, недостаточно высок
и уровень цианкобаламина в сыворотке крови. Закономерным представляется
снижение уровня эритропоэтина и повышение уровня гомоцистеина у нашей
больной. Повышен и уровень гепсидина, о котором шла речь выше.Таким образом, анемия у нашей больной, по всей видимости, носит сме¬
шанный характер. Диагноз сформулирован следующим образом. Ревматизм,
неактивная фаза. Митральный порок сердца: протезирование митра.тьного
юшпана в 1995 г. Аортальный порок сердца с преобладанием недостаточности.
Пластика трикуспидального юіапана в 1995 г. Относительная недостаточность
трикуспидального клапана. Нарушения ритма и проводимости сердца: полная
блокада левой ножки пучка Гиса, постоянная форма мерцательной аритмии
с трансформацией в предсердный ритм, частая желудочковая экстрасисто-
JJИя, пробежки желудочковой тахикардии. Дисцирку.тяторная энцефалопатия.
Недостаточность кровообращения НБ стадии, 111 функциональный класс
NYHA, Резекция щитовидной железы в 1997 г по поводу узлового зоба HI—IV
стадии. Правосторонняя гемитиреоид:жтомия от 22.05.2007 г. по поводу циста-
деномы перешейка. Первичный гипотиреоз, медикаментозно субкомпенси-
рованный. Хроническая нормохромная анемия смешанного генеза, легкойпоказатель9.10.2007[ нормаферритин сыворотки322,7 мкг/л \Г 40-80 1трансферрин2,6 г/лГ до 2,6рецепторы к трансферрину5,4 мг/мл Аt 1,5-2.5витамин В,2 сыворотки480 пг/гНЬ300-900фолаты сыворотки6 и г/м лI4-141эритропоэтин4 ми/мл уУ 5-10ЦИК165Лдо 140Lгомоцистеин32 мкм/л \f Д012эндотелии2,2 нг/л J1 дозтромбомодулин
(рецептор тромбина)7г6-10Рис. 30.7. Специальный биохимический анализ крови больной К., сделатшый в
Гематологическом тіаучном центре РАМН
Глава ЗО. Анемии хронических заболеваний: современные представления... 651степени. Хронический обструктивный бронхит средней степени тяжести в
фазе ремиссии. Язвенная болезнь желудка и двенадцатиперстной кишки вне
обострения.На сегодняшний день больной проводится следующая терапия: кордарон0,2 по 1/2 таб. 2 раза в день, синкумар 2 мг по 2 таб. вечером, верошпирон 25 мг
по 2 таб. 2 раза в день, фуросемид 40 мг по 1 таб. по нечетным, диувер 10 мг
по 1 таб. по четным, L-тироксин 50/75 мкг (через день), клоназепам 2 мг по
1/4 таб. на ночь.Каковы могут быть подходы к лечению анемии^ Назначение препаратов желе¬
за больной безусловно не показано. Инъекции витамина прием фолиевой
кислоты наверняка будут ей полезны. В ближайшее время мы надеемся добить¬
ся компенсации гипотиреоза, что должно снизить уровень анемии. В то же
время нам вряд ли удастся устранить почечную недостаточность, существенно
уменьшить застой по большому кругу и устранить околопротезную регургита-
цию. Для нас остается открытым вопрос о целесообразности назначения эри-
тропоэтина. По-видимому, мы воздержимся от этого до получения эффекта от
перечисленньк мероприятий, что, возможно, и неправильно. Поэтому нам бы
хотелось выслушать мнение гематолога о представленной больной, о механиз¬
мах анемии и возможностях ее устранения.Комментарий ЕЛ. Лукиной — профессора Гематологического научного центра
РАМН, д-ра мед. наукЛегкая анемия, которая имеется у больной (клинически незначимая, я
бы сказала) имеет классические признаки микроангиопатической анемии,
связанной с протезированием клапанов сердца: эритроциты, многократно
проходя через искусственный клапан сердца, «бьются» о протез, что приво¬
дит к их механическому повреждению (оно усугубляется при прохождении
дефектных клеток через мелкие сосуды) и выбраковке клетками печени и
селезенки (макрофагами). В отличие от многих других гемолитических ане¬
мий, гемолиз осуществляют макрофаги. Эта анемия недостаточно широко
известна, но в данной ситуации ее подтверждают сочетание ретикулоцитоза
и протезированного клапана. Это по сути дела ее индивидуальная норма
(даже если принять во внимание, что она находится в менопаузе), и эритро-
поэтин здесь не обсуждается. Доказательства значимости терапии эритро-
поэтином у таких больных не представляются мне убедительными.Второе, что важно у этой больной, — умеренная (по современным критери¬
ям) гипергомоцистеинемия, которая, вероятно, имеет прямое отношение
ко многим проблемам этой пациентки. Накопление гомоцистеина (наслед¬
ственное или приобретенное, что вполне вероятно у этой больной 72 лет
со множеством метаболических нарушений) может в какой-то степени
поддерживать анемию; кроме того, это гиперкоагуляпионный синдром,
который ухудшает микроциркуляцию. Токсических эффектов много, а кор¬
рекция легка и дешева. В такой ситуации это стандартный путы витамин В,2
(у нее все-таки явно гиперхромная анемия, парестезии я бы тоже отнесла
за счет дефицита витамина B^j), В^ и В^. Существует препарат ангиовит,
652 Гематологияразработанный в Барнауле, который стоило бы назначить в первую очередь
для коррекции гипергомоцистеинемии.При анемии очень важно нарушение реологии крови. Гипоксия определя¬
ется в основном способностью гемоглобина отдать кислород. Иногда при
гемоглобине 140 г/л кислород отдается хуже, чем при гемоглобине 110 г/л.
я думаю, что со временем нынешние нормы гемоглобина будут пересма¬
триваться. Во всяком случае, норма гемоглобина может быть индивидуаль¬
на. Многие нормы носят формальный характер. Например, клиническое
значение имеет подъем уровня ферритина выше 300, а не 80 (как указано в
таблице) мкг/л. При уровне выше 1000 мкг/л необходим серьезный поиск.
В отношении витамина В,2 — вы определяли его уровень в сыворотке, но не
менее важно оценить уровень в эритроцитах (хотя в рутинной клинической
практике это не делается).Ангиовит шртроко используется при разных наследственных дефектах генов
системы свертывания крови в том числе, и число мутаций, которые можно
проверить, постоянно растет. Пациентам с тромбофилией и повышенным
уровнем гомоцистеина этот препарат мы назначаем часто. Для повышения
достоверности anajiHsa на гомоцистеин необходимо проводить его через
30 мин после забора крови. Гипергомоцистеинемию делят на легкую, уме¬
ренную и высокую (при высокой пациенты нежизнеспособны и умирают
от острой сердечно-сосудистой недостаточности, связанной с тромбозами).
Уровень гомоцистеина ниже 20 мкм/л не имеет большого клинического
значения, но у данной больной имеется умеренная гипергомоцистеинемия,
которая, безусловно, требует коррекции. Гемоглобин у нее уже не вырастет,
но улучшится реология крови.Комментарий ВЛ. Сулимова — заведующего кафедрой факультетской терапии
№ 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наук,
проф.Я бы хотел четко расставить акценты. В кардиологии оценка эффектив¬
ности терапии проводится в первую очередь по влиянию на конечные
точки, т.е. на смертность. Коррекция гипергомоцистеинемии и связанных
с ней нарушений реологии крови, безусловно, важна, но в исследовании
на пациентах с имплантированными кардиовертерами-дефибрилляторами
(это больные с желудочковыми нарушениями ритма и высоким риском вне¬
запной сердечной смерти) было показано, что нормализация уровня гомо¬
цистеина не приводила к снижению смертности. Исследования на более
широком контингенте кардиологических больных, которые показывали бы
значимость коррекции гипергомоцистеинемии, практически отсутствуют.
На сегодняшний день вопрос остается открытым, хотя улучшение реоло¬
гии крови — это то, к чему следует стремиться. Остаются и другие неясные
вопросы, затронутые Е.А. Лукиной, например какова клиническая значи¬
мость лабораторных исследований различных показателей обмена железа.
Таким образом, данная клиническая демонстрация показала, что патогенез
анемии у больных (в том числе кардиологических), имеющих одновременно
Глава ЗО. Анемии хронических заболеваний: современные представления... 653целый ряд хронических заболеваний, достаточно сложен: необходимо выде¬
ление его ведущих механизмов и назначение корректирующей терапии; в то
же время препараты железа должны назначаться с осторожностью и лишь
при безусловно доказанном истинном дефиците железа, который сопрово¬
ждается снижением уровня ферритина крови.
Глава 31ВПЕРВЫЕ ВЫЯВЛЕННАЯ МНОЖЕСТВЕННАЯ
МИЕЛОМА В СОЧЕТАНИИ С ТЯЖЕЛОЙ
ТРИКУСПИДАЛЬНОЙ РЕГУРГИТАЦИЕЙ£,С Родионова, В.Л. Осадная,
ДА, Царегородцев, В.В. СамойленкоМножественная миелома (миеломная болезнь) является одним из парапро-
теинемических лейкозов, клиническая картина ее достаточно хорошо извест¬
на: поражение сердца не относится к ранним и частым ее проявлениям.Мы представляем клиническое наблюдение, в котором практически одно¬
временно были диагностированы заболевание сердца (нарушения проводи¬
мости с обмороками, потребовавшие имплантации ЭКС, несколько позже —
тяжелая недостаточность трехстворчатого клапана и застойная сердечная
недостаточность) и типичные симптомы миеломы.Обсуждаются вопросы диагностики, лечения и прогноза множественной
миеломы, возможные механизмы развития кардиальной патологии — от
осложнений, связанных с имплантацией стимулятора, до специфической мие-
ломной кардиомиопатии (не только амилоидоза).Больная Ц., 61 год, поступила в отделение обшей терапии Факультетской
терапевтической клиники им. В.Н. Винофадова с жалобами на выраженную
общую слабость, повышенную утомляемость, одышку В покое, значительно
усиливающуюся при минимальной физической нагрузке, отеки голеней и
стоп, увеличение живота в объеме, боли в грудном отделе позвоночника, чув¬
ство тяжести в правом подреберье и чувство горечи во рту.Из семейного анамнеза известно, что отец больной страдал ишемической
болезнью сердца и умер в возрасте 65 лет от инфаркта миокарда, мать умерла
в 72 года от рака слепой кишки. Больная имеет среднее техническое образова¬
ние, работала технологом по обработке металтов, в настоящее время на пен¬
сии, проживает в Подмосковье. Аллергологический анамнез не отягощен. Из
сопутствующих заболеванртй: в течение 10—12 лет страдает сахарным диабетом
2-го типа и артериальной гипертонией (И стадии, 2 степени, риск 4), контроль
гликемии и уровня артериа.1ьного давления удовлетворительный.Из анамнеза заболевания {рис. 31.1) известно, что в июле—августе 2008 г
почувствовала эпизоды немотивированной слабости, повышенной утомля¬
емости. В сентябре 2008 г. впервые возникло предобморочное состояние, За
медицинской помощью не обращалась. В октябре 2008 г. у больной неодно¬
кратные эпизоды потери сознания, по поводу чего она бьита госпитализирова¬
на в Факультетскую терапевтическую клинику им. В.Н. Виноградова, где при
обследовании (холтеровское мониторирование ЭКГ и тест чреспищеводной
Глава 31. Впервые выявленная множественная миелома в сочетании..655Июль Сентябрь Октябрь- Декабрь Январь
2008 г. 2008 г. ноябрь 2008 г. 2009 г.2008 г. ФТКФевраль 2009 г.
ФТКСлабость,
утомляемость
Эпизоды потери
сознания
Одышка
ОтекиУвеличение
живота
Тяжесть
в правом
подреберьеБолив позвоночникеэксГоспитализация в ФТКРис* 31.1, Анамнез больной Ц., 61 годэлектрической стимуляции сердца) выявлен синдром слабости синусового
узла, проведена имплантация двухкамерного ЭКС в режиме DDD. Процедура
прошла без технических проблем и осложнений.Также в ходе обследования у пациентки при КТ органов грудной клетки
выявлены мелкие очаговые образования в легких, диффузный остеопороз с
неравномерной структурой тел позвонков с наличием участков разрежения
округлой формы, при остеосцинтиграфии достоверных изменений выявлено
не было. Пациентка была выписана под наблюдение по месту жительства с
рекомендациями продолжить прием метопролола (беталок Зок), аспирина
(тромбо-АСС), манинила и инсулина Лантус.С января 2009 г. отметила появление нарастающей обшей слабости, сни¬
жение переносимости привычных; физических нафузок, повышенную утом¬
ляемость, одышку, сухой кашель, а также боли в спине. Госпитализирована
по месту жительства, состояние расценено как пневмония, начата антибакте¬
риальная терапия без отчетливого положительного эффекта. Также отметила
появление отеков нижних конечностей, увеличение живота в объеме, тяжесть
в правом подреберье и чувство горечи во рту. 04.02.2009 г. амбулаторно прове¬
дена КТ органов грудной клетки, при которой выявлены признаки диффузного
хронического бронхита, бронхиолита, правосторонней нижнедолевой пнев¬
монии, правостороннего гидроторакса, асцита, очагового поражения костей
позвоночника. Для обследования была госпитализирована в Факультетскую
терапевтическую клинику им. В.Н. Виноградова 09.02.2009 г.При поступлении: состояние средней степени тяжести, кожные покровы
бледные, чистые, умеренной влажности. Склеры субиктеричны. Отеки голеней
и стоп, в легких жесткое дыхание, в заднебазальных отделах справа ослаблен¬
ное. Число дыханий 22/мин. Тоны сердца ритмичные, определяется ослабле¬
ние I тона на верхушке и в проекции трик^^спидального клапана, в этих же
656 Гематологияточках аускультации выслушивается интенсивный систолический шум. ЧСС
66/міш. АД 110/70 мм рт.ст. Живот увеличен в объеме, отмечается притупле¬
ние перкуторного звука в отлогих местах. При пальпации живот мягкий, чув¬
ствительный в эпигастральной области и правом подреберье. Печень на 3 см
выступает из-под реберной дуги, край се округлый, поверхность гладкая, кон¬
систенция мягкоэластическая, безболезненная. Селезенка не пальпируется,
перкуторно размеры 9x6 см. Щитовидная железа при пальнатщи не увеличена.
Неврологический статус без особенностей.В общем анализе крови — гемоглобин на нижней границе нормы
(119,9 г/л), эритроциты 4 Mjm, цветовой показатель 0,95, небольшой лейко¬
цитоз (9,6 тыс ./мм") при нормальной лейкоцитарной формуле (нейтрофюіьі
37,1%; лимфоциты 53,1%, моноииты 6%, эозинофилы 3,6%, базофилы 0,3%),
тромбоциты 252,9 тыс., СОЭ 13 мм/ч.В биохимическом анааизе крови выявлены умеренно выраженные признаки
холестат№іеского синдрома (у-ГТ 354 Ед/л, ЩФ 117 Ед/л, общий билиру-бин
24,2 мкмоль/л, прямой билирубин 5,4 мкмоль/л). Обший белок 80,6 г/л, аль-
6>TviHH 38,8 г/л, глюкоза 5,8 \™оль/л, ACT 30 Ед/л, АЛТ 37 Ед/л, холинэстераза
7553 Ед/л, креатинин 1,09 мг/дл.В иммунологическом анализе крови: IgA 48 мг/дл (норма 50—300), IgM
58 мг/дл (40-200), TgG 2880 мг/дл (600-2000).В общем анализе мочи\ pH 5, белок 0,040%о, сахар положителен, уробилин
выше нормы, лейкоциты 0—1 в поле зрения, эритроциты 0-1 в иоле зрения,
оксалаты — >^еренно, слизи много, бактерий нет.При повторной КТ органов грудной клетки по сравнению с КТ от 04.02.2009 г.
без существенной динамики. В плевральной полости справа определяется жид¬
кость с толщиной слоя до 35 мм. Данных за ТЭЛА не получено.По данным КТ органов брюшной полости — очаговые изменения костей
таза, позвонков и ребер (миеломная болезнь?). Асцит. Грьгжа брюшной стенки.
Жировой гспатоз.Таким образом, в клинической картине можно было выделить три основные
линии. Во-первых, развернутая картина недостаточности кровообращения по
большому кругу в сочетании с признаками клапанной дисфункции (трикуспи-
дальной недостаточности). Во-вторых, отрицательная динамика изменений
костей по данным компьютерной томографии в течение короткого времени
(около 3 мес): от диффузного остеогтороза с неравномерной структурой тел
позвонков и наличием у^гастков разрежения округлой формы до отчетливых
очаговых изменений. В-третьих, не вызывающая сомнений правосторонняя
нижнедолевая пневмония, течение которой затянулось, по-видимому, вслед¬
ствие изначально неадеквагной антимикробной терапии (пациентке для лече¬
ния пневмонии по месту жительства был назначен линкомицин).Что касается первой диагностической проблемы, то пациентке была про¬
ведена ЭхоКГ, при которой выяв.лены с.ледующие изменения: гипертрофия
стенок левого желудочка (МЖП 1,5 см, ЗС 1,3 см), умеренное расширение
обоих предсердий, атеросклсрот№іеские изменения аорты, аорта-іьного кла¬
пана, фиброзных колец, умеренная недостаточность митрального клапана
Глава 31. Впервые выявленная множественная миелома в сочетании... 657(регургитадия 1 степени), недостаточность трикуспидального клапана (регур-
гитация 1Т—III степени), легочная гипертензия. КДР левого желудочка соста¬
вил 4,2 см, ФВ — 61%. Отмечено незначительное снижение функции диасто¬
лического расслаблсния миокарда: Е/Л = 0,66 / 0,76 = 0,87.Исходя из того, что до има'іантации ЭКС подобной регургитации у паци¬
ентки не выявлялось, логично предположить пряліую сиязь возникших нару¬
шений работы клапана с имплантированным желудочковым электродом.Насколько редка подобная ситуация? В одном из исследований среди
пациентов с трикусішдальной рсгургитацией на фоне имплантироваішого
ЭКС тяжелая степень реіургитшщи (1IT-1V) выявлялась у 8% больнь[\. При
этом на основании большей встречаемости регургитации у больных с низкой
фракцией выброса и сопутсгвующсй митральной недостаточностью авто¬
ры делают вывод о Зсшисимости возникновения регургитации от основного
заболевания пациента и сократительной способности миокарда. В другом
исследовании, по данным анализа оперативных вмешательств у пациентов с
трикуспидальной регургитацией, ее причина была связана с имплантирован¬
ным ЭКС в 2,8% случаев.Что может лежать в основе дисфункции клапана при имплантации желудоч-
кового электрода? Интраоперационно установлено, что к непосредственному
нарушению функции клапана приводили «прилипание» электрода к створке,
се «запутывание» и,іи перфорация, а также травматизация при «соударении
створки и электрода». В 36,5% слуїаев это сочеталось со вторичной дилатацией
фиброзного кольца. Хотя у нашей пациенгки при транстора калькой, чреспи-
щеводной ЭхоКГ каких-либо дефектов створок, «запутывания» электрода,
перфорации, спаивания выявлено не бьию, полностью исключить одну из этих
причин не представляется возможным. Ктиническая картина трикуспидаль¬
ной реіургитации у нашей больной развилась через достаточно короткий срок
после оперативного вмешательства, что не очень характерно дая подобных
ситуаций. Согласно литературным данным, минимальный срок развития юш-
нических проявлений трикуспидсі-іїьной недостаточности после имнлантации
ЭКС составляет 4 мес, тогда как средний — 6-7 лет.Возникает вопрос: насколько оправдана имплантация двухкамерных ЭКС
у больных с синдромом cjra6ocTH синусового узла без сопугствуюищх наруше¬
ний атриовентрикулярной проводимости? В ряде зарубежных и отечествен¬
ных работ показано, что частота возникновения АВ-блокады II—III степени в
течение года у подобной гр>тіпьі пациентов составляет 0,6-2%, при наличии
сопутствующей блокады ножки ітучка Гиса — до 7%, Значимой разницы по
выживаемости у больных с предсердной и дв)т(камерной стимуляцией выяв¬
лено не было, в то время как дисфункция электродов выявля-iacb в 2 раза
чаще у пациентов, которым был имплантирован двухкамерный ЭКС. Таким
образом, имплантация однокамерного ЭКС д;гя проведения предсердной
стимуляции у больных с синдромом слабости синусового узла без нарушений
АВ-проводимости может явиться действенным способом предотвращения
развития недостаточности трехстворчатого к-іапана без суш;ественного ущер¬
ба для выживаемости пациентов. На другой чаше весов лежит воз.можная
658ГематологияТаблица 31.1Наиболее частые первичные локализации при метастазироваиии в костиОстеосклеротичесіоіе метастазыОстеолитические метастазыРак молочтюй железыМедуллобластомаПереходноклеточный ракОпухоли желудочно-кишечного трактаЛимфамыМеланомаРак почкиРак щитовидной железы
Рак легкогонеобходимость более ранней замены ЭКС на двухкамерную систему сти\іуля-
ции при появлении нарушений АВ-проводимости.В ходе обследования очаговые остеолити^геские изменения костной ткани
были выявлены не только в позвоночнике, 1І0 и в костях таза и ребрах. Таким
образом, дальнейшая диагностическая стратегия бьыа направлена на под¬
тверждение или исключение множественной миеломы, а также выявление
первичных источников, характеризуюш,ихся остеолитическим характером
метастазирования в кости (наиболее частые из них представлены в табл, 31J).В рамках онкопоиска были проведены КТ органов брюшной полости, ЭГДС,
ирригоскопия, УЗИ шитовидной железы и органов малого таза, маммофафия,
при которых данных за первичный неопластический процесс получено не
бьыо.В то же время при проведении электрофореза белков сыворотки в зоне
у-глобулинов был выявлен М-градиент (PPIgGX) 27,1% (альбумин 48,3%,
а,-глобулины 3,3%, а2-глобулины 8,7%, р-глобулины 9,6%, у-глобулины
30,1%).При исследовании суточной мочи протеинурия составила 2 г/сут, белок
Бене-Джонса не обнаружен, скорость к-тубочковой фильтрации (по пробе
Реберт) составила 41 мл/мин на 1,73 м^.Пациентке проведена стернальная пункция: пунктат костного мозга доста-
ТОЧ1ІО клеточный, количество плазматических клеток (11%) и лимфоцитов
(16,8%) несколько увеличено, созревание нейтрофилов ускорено, эритропоэз
нормобластический, мегакариоциты найдены.Таким образом, с учетом клинической картины и на основании малых кри¬
териев миеломы Де Вита (плазмоцитоз в костном мозге 10-30%, пик при элек¬
трофорезе белков сыворотки, литическое поражение костей — 2-я рентгено¬
логическая стадия) состояние может быть расценено как впервые вьывленная
миеломная болезнь (множественная миелома) с клиническими признаками
поражения органов-мишеней (CRAB) (табл. 31.2—31.3). Диагноз ставится при
наличии 1 большого и 1 малого критерия или 3 малых критериев.Для оценки активности опухолевого процесса были определены
С-реактивный белок (0,86 мг/дл) и ЛДГ (386 Ед/л), для определения объема
опухолевой массы — р2-микроглобулин (2,76 мг/л при нормальных значениях
от 0,67 до 2,33), Повышенный уровень р2-микроглобулина, но при этом не
превышающий пороговое классификационное значение 5,5 мг/л, при сниже¬
нии уровня альбумина менее 3,5 г/дл свидетельствует о наличии у пациентки
Глава ЗІ. Впервые выявленная множественная миелома в сочетании...659Таблица 31.2Классификация моноклональных гаммапатийМоноклональная гаммапатия неясного генезаСывороточный М-протеин <3 г/длСодержание плазмоцитов в пункгате костного мозга <10%Отсутствие анемии, поражения почек, гиперкальциемии и остеолити^іеских измене¬
нийБессимптомная множественная миелома (ММ)Тлеющая ММВялотекушая ММСывороточный М-протеин >3 г/дл и/или
содержание плазмоцитов в пункгате кост¬
ного мозга >10%Плазмоцитоз в костном мозге (>10%)Отсутствие анемии, поражения почек,
гиперкальциемии и остеолитических изме¬
ненийЛегкая анемия или одиночные неболь
шис остеолитическис измененияСтабильный уровень М-протеина в сьгео-
ротке крови или в мочеОтсутствие клинических проявленийНаличие М-протеина п сыворотке крови
или в мочеКлинически выраженная множественная миелома (ММ)Содержание плазмоцитов в птактате костного мозга >10%Клинические проявления (CRAB): гиперкальциемия, почечная недостаточность,
анемия или остеолитическое поражение костейТаблица 31.3Диагностические критерии множественной миеломыБольшие критерииМалые критерииПодтвержденная при биопсии плазмоцитома10—30% плазмоцитов в пунктате кост¬
ного мозга30% и более плазмоцитов в пунктате костного
мозгаНебольшое увеличение моноклональ¬
ного иммучіогл обули на в кропи или
моче (<3 г/дл)Высокий уровень моноклонального иммуно¬
глобулина в крови или моче (более 3 г/дл)Остеопения/остеолитические пора¬
женияСнижение уровня других иммуногло¬
булинов в кропиТаблица 31.4Определение стадии множественной миеломыInternationa] Staging System (ISS)СтадияКритерийМедиана выживаемости (мес)IР^-Микроглобулин <3,5 мг/л
альбумин >3,5 г/дл62И*Не соответствует I или ТП44III(5,-Микроглобулин >5,5 мг/л29Greipp et ai. // J. Clin. OncoJ. - 2005; - N 23. - P. 3412-3420.
вьоГематологияII стадии по Inlemational Staging System, что совпадает с определением стадии
по системе Durie-Salmon (табл. 31.4).Множественная миелома представляет собой злокачественное лимфопро-
лиферативное заболевание, морфологическим субстратом которого яштяются
плазматические клетки, продуцирующие моноклональный иммуноглобулин
(парапротсші). Она относится к периферическим В-клеточным лимфоидным
опухолям.Заболеваемость в России составляет 1,24 на 100 тыс. населения, средний
возраст на момент диагностики 69 лет. Медиана выживаемости 3 года. Факторы
высокого риска неблагоприятного исхода подразде.іяют на две группы:1) генетические (рис. 312):— t(4;14) и t( 14; 16) транслокация;— del(13q) и dcl(17p) хромосомные аномалии;— гиподиплоидный каришип;2) другие:— возраст старше 75 лет;— высокий уровень р^-микроглобулина;— высокий пролиферативный индекс плазматических клеток;— почечная недостаточность.В течение периода обследования пациентка, помимо своей постоянной
терапии, получала ди>'ретики (фуросемид 120—360 мг/сут, диувер 5—10 мг/сут,
верошпирон 100 мг/сут, ацетазоламид 250 мг/с>т) и антибактериальные пре¬
параты (амоксиклав).При определении лечебной тактики в первую очередь стоял вопрос об
этиологии сердечной недостаточности. На первый взгляд, травматиче¬
ская природа трикуспидальной недостаточности с развитием последующихВремя (дни)Рис. 31.2. Вьгжипаемость при множественной миеломе в зависимости от генотипа
(Avet-Loiseau Н. et al., IMW 2007, Abstract SI.5)
Глава 31. Впервые выявленная множественная миелома в сочетании.., ввігемодинамических нарушений бьыа наиболее подходящей диагностической
концепцией. В таком случае возникает вопрос; чем можно помочь пациентке
в настоящее время, помимо консервативной терапии сердечной недостаточ¬
ности? Согласно литературным данным, оперативное лечение тяжелой ірику-
спидальной регургитации, причиной которой являлся желудочковый электрод
ЭКС, в 59% случаев состоя.то в протезировании клапана, у 41% пациентов была
проведена аннулопластика. У нашей пациентки с учетом тяжелого коморбид-
ного фона (прежде всего миеломной болезни) риск подобных вмешательств
представлялся крайне высоким.Поэтому в качестве первого шага могла рассматриваться попытка экс¬
тракции желудочкового электрода с последующей оценкой клинического
результата. К сожалению, не было твердой уверенности в том, что подобное
паллиативное вмешательство у нашей пациентки окажется :іффективньгм для
устранения выраженной недостаточности трехстворчатого клапана. С другой
стороны, полиорганность поражения (сердце, печень, почки) при достаточно
низкой активности опухолевого процесса может свидетельствовать в пользу
наличия у пациентки амилоидоза.Не вызывает сомнений, что активная миелома требует специфическо¬
го лечения. Выживаемость постоянно возрастала по мере появления новых
классов лекарственных препаратов и комбинированных схем лечения множе¬
ственной миеломы {рис. 31. ЗУ, тем не менее эффективность терапии остается
недостаточно высокой.Комбинация мелфалана (препарат цитостатического действия) и предни-
золона до сих пор является основой лечения пациентов пожилого возраста,
у которых не планируется забор стволовых к.іеток для аутотрансплантации.
Эффективность комбинации повышается при добавлении к схеме талидоми-
да — ингибитора ангиогенеза.35% Мелфалан (1962)Преднизолон (1968)
Циклофосфамид (1972)Высокие дозыдексаметазона (1984)
Бифосфонаты (1996)Эритропоэтин {1996}Высокие дозы мелфаланав сочетании с введением
стволовых клеток (1996)
Талидомид (1999)Бортезомиб (2003)Тандемная трансплантация (2003)
Леналидомид (2005)1950 1960 1970 1980 1990 2000 Малые дозы дексаметазона (2007)_ Пегилированный липосомальныйг оды постановки диагноза доксорубицин (2007)Рис. 31.3. Улучшение 5-летней выживаемости при множестпенной ми ел оме в связи с
появлением новых лекарственных препаратов
662ГематологияТаблица 31.5Эффективкость терапии и критерии ответа на лечение при множественной миеломеКритерийПризнакиПолный ответ (CR)Стандартное определеігае*; 75% редукции
урсвття миеломного протеина в сыворотке
(более 90% в моче)Дейстпительный полный ответБолее точное определение: элиминация
М-компонента из сыворотки и мочи плюс
отсутствие признаков миеломы в костном
\f03reПарциальный (частичный) ответ (PR)Более 50%, но менее 70% регрессииОбъективный ответ (OR)Стабильная болезнь — более 25%, по менее
50% регрессииОтсутствис ответа (NR)Прогрессирование заболевания. Менее 25%
регрессии* Давнее определение, использовавшееся SWOG (Северо-западной онкологической группой).В случаях, когда пациенту планируется забор стволовых клеток для ауто¬
трансплантации, применяются курсы высокоактивной кратковременной тера¬
пии препаратами, не оказывающими повреждаюшего действия на стромальные
клетки костного мозга. В частности, достаточную эффективность продемон-
сфировали комбинация ингибитора ангиогенеза леналидомида (Reviimid) и
дексаметазона и монотерапия бортезомибом (Велкейд) — ингибитором про-
тсазосом. Бортезомиб относится к препаратам таргетной терапии, действует
на субъединицу 26S протеосом — протеиновых комплексов, присутствующих в
цитоплазме эукариотических клеток и играющих важную роль в метаболизме
и регуляции. Данные препараты применяются в комбинации с другими аген¬
тами при резистентной, рецидивирующей мисломе, а также миеломе высокого
риска. Критерии эффективности лечения представлены в табл. ЗІ.5.В данном случае наличие выраженной сердечной недостаточности и при¬
знаков дисфункции печени (снижение альбумина и активности холинэстера-
зы) в кон'фолъных анализах, низкий функциональный класс (ECOG 3) пред¬
ставляли существенное препятствие для назначения специфической терапии.
Пациентка была выписана под наблюдение по месту жительства для паллиа¬
тивного лечения и скончачась через 3 нед при нарастающих явлениях сердеч¬
ной недостаточности, резистентной к терапии большими дозами диуретиков.Комментарий О. В. Благовой — доцента кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И. М. Сеченова, канд. мед. наукХотелось бы еще раз вернуться к вопросу о происхождении у больной быстро¬
прогрессирующей преимущественно правожелудочковой сердечной недоста-
тотоости. Проведенная ЭхоКГ не выявила причин выраженной одышки (не
отмечено ни снижения ФВ левого желудочка, ни существенного нарушения
диастолической функции левого желудочка, ни его расщирения). Одьпика в
значтельной степени может объясняться поражением легочной паренхимы
и наличием правостороннего гидроторакса.
Глава 31. Впервые выявленная множественная лшелома в сочетании... 663Что касается связи трикусттадальной недостаточности с установкой электрода
стимулятора в правый желудочек, нам приходилось сталкиваться с подобной
ситуацией (она описана в главе 12); у нашей пациентки недостаточность
трехстворчатого клапана наросла через несколько лет после имплантации
ЭКС (максимально — до II—III степени), при ЭхоКГ возникло подозрение
на спалние створки клапана с электродом (что было вполне объяснимо с
учетом активного эндомиокардита). И, тем не менее, никаких клини^іеских
проявлений застоя по большому кругу кровообращения у больной не было,
через 2 года степень регургитации на к^іапане уменьшилась до IT, вопрос об
оперативном вмешательстве не стоял.В сегодняшнем случае быстрота развития симптомов тяжелой сердечной
недостатотаости (не более 3 мес — в ноябре отеков и одашки еше не было;
при ЭхоКГ и сегодня, несмотря на тяжелую трикусиидальную недостаточ¬
ность, не выявлено дилатации правого желудочка, что подтверждает остроту
процесса) кажется очень маловероятной для обсуждавшейся механической
причины. Но если посмотреть на анамнез (рис. 31.1, 31.4 на цветной вюіейке)
и сравнить лабораторные (отсутсгвие М-градиента) и инструментальные
данные (степень костных изменений) в ноябре и в ходе нынешней госпитали¬
зации — это тесно коррелирует с появлением и нарастанием признаков самой
миеломной болезни. В ноябре ни сердечной недостаточности, ни диашоза
множественной миеломы еш;е не было — в феврале и то, и другое налицо.
Нам представляется, что не имнлантация стимулятора, но миелоидное
поражение миокарда стало причиной сердечной недостаточности, хотя
наличие электрода и могло сыграть роль в преимущественном поражении
правых отделов. Между прочим, возникает вопрос, который здесь совсем
не обсуждался — а какова этиология нарушений проводимости, потребо¬
вавших имплантации ЭКС? Конечно, можно расценить синдром слабо¬
сти синусового узла с обмороками как банштьную ситуацию у женщины
61 года, но не говорит ли появление этих симптомов всего за 1—2 мес до
манифестации миеломы об их прямой патогенетической связи? Наконец,
при ультразвуковом исследовании сердца была выявлена значимая гипер¬
трофия стенок левого желудочка, которой также, по-видимому, не было в
ноябре и которая не найдет объяснения в имевшейся у больной нетяжелой
артериальной гипертонии. Не есть ли эта «гипертрофиям^ прямой признак
инфильтрации миокарда?Говоря о миелоидном поражении сердца, можно в первую очередь подразуме¬
вать две ситуации:1) развитие AL-амилоидоза (о котором шла речь в главе 22) с поражением
сердца, в том числе клапанов и проводящей системы;2) собственно миелоидную инфильтрацию легкими цепями иммуноглобули¬
нов без формирования амилоида: подобные наблюдения с выраженной сер¬
дечной недостаточностью, нарушениями ритма и «гипертрофией» миокарда
описаны; при этом в биоптатах миокарда выяв^тяют конго-негативные отло¬
жения иммуноглобулинов, отмечается отчетливый положительный эффект
химиотерапии.
664 ГематологияНаверное, для развития амилоидоза нужны несколько большие сроки; диа¬
гноз у больной мог бы бьггь верифицирован с помошью биопсии подкожной
жировой клетчатки, однако, по-видимому, это уже не имело решающего
значения.Наконец, при множественной миеломе с поражением костей описана особая
(не амилоидная и не лекарственная) сердечная недостаточность с высоким
сердечным выбросом (10-15 л/мин), для которой характерна низкая эффек¬
тивность диуретиков, но описана регрессия симптомов в результате специфи¬
ческой химиотерапии. Механизмом считают образование многочисленных
интрамедуллярньтх артериовенозных фистул в поражешіьіх костях, методом
лечения — «фармакологическое закрытие*» этих фистул с помощью подавле¬
ния ангиогенсза (талидомид и др.). К сожалению, мы не имеем сведений о
сердечном индексе у представленной больной (кроме того, в условиях кар¬
диостимуляции этот показатель может не отражать истинную ситуацию).ЛИТЕРАТУРАFabbian F., Stabellini К , Sartori S. et ai Light chain deposition disease presenting
as paroxysmal atrial fibrillation: a case report // J. Med. Case Reports. 2007; 1: 187.Inanir S., Haznedar R., Atavci S., Uni M. Arteriovenous shunting in patients with
multiple myeloma and high-output failure j I J. Nucl. Med. 1998; 39 (1): 1—3.Nakamura М., Satoh М., Kowada S. et al Reversible restrictive cardiomyopathy
due to light-chain deposition disease I j Mayo Clin. Proc. 2002; 77 (2): 193-196.Robin J., Fintel B., Pikovskaya O. et al. Multiple myeloma presenting with high-
output heart failure and improving with anti-angiogenesis therapy: two case reports
and a review of the literature // J. Med. Case Reports. 2008; 2; 229.
ГАСТРОЭНТЕРОЛОГИЯГЛАВА 32
ВТОРИЧНЫЙ ПОЛИМИОЗИТ КАК ПЕРВОЕ
КЛИНИЧЕСКОЕ ПРОЯВЛЕНИЕ ОПУХОЛИ
КИШЕЧНИКАН,В, Чткова, И.С. ЩедринаНастороженность в отношении ларанеопластшеского происхождения многих
иммунных и иных по патогенезу синдромов всегда оправдана; особенно это каса¬
ется пожилых больных с впервые диагностированным дермато-/полимиозитом.
Предстаатяем клиническое наблюдение, в котором именно симптомы тяжелого
полимиозита заставили пациента обратиться к врачу; при обследовании не только
бьш подтвержден диаі’ноз собственно ііолимиозита (воспалительной миопатии),
но и диагностированы сначата метастаз в иечени, а затем и первичная опу’холь
в поперечной ободочной кишке. Признаки стенозирования кишки и наличие
метастаза говорили не о ранней стадии опухоли; тем не менее ярюге клинических
симптомов не было вплоть до развития мьппечной слабости. Первичный очаг
оперирован, однако удаление метастаза признано невозможным; одновременно
начата терапия глюкокортикоидами. Обсуждаются вопросы этиологии воспали¬
тельных миопатий, патогенеза паранеопластического синдрома.Больной О., 70 лет, поступил в отделение общей терапии Факультетской
терапевтической клиники им. В.Н. Виноградова 01.10.2008 г с жалобами на
слабость и боль в мышнах бедер, верхнего плечевого пояса, шеи; отеки голе¬
ней, кистей рук, лина; затруднения при глотании; изменение голоса; одышку
нри умеренной физической нагрузке; общую слабость; снижение массы тела.Анамнез жизни: семейный ана\шез без особенностей. По профессии про¬
граммист, профессиональные вредности отсутствуют. Отрицает к\фсние и
злоупо'фебление алкоголем. Аиергологтеский анамнез не отягощен.Из анамнеза заболевания (рис. 32.7): до мая 2008 г. чувствовал себя удовлегво-
рительно, В мае 2008 г. появились жалобы на тошноту, рвоту без определенной
причины, которые в дальнейшем прошли самостоятельно. Было предпринятоа.мбулаторнос обследование, включавшее ЭГДС, колоноскопию. Проведенные
обследования не выявили какой-либо значимой патологии. В дальнейшем
самочувствие оставалось удовлетворительным. Пациент продолжал работать.
Ухудшение состояния с августа 2008 г., когда стал отмечать появление обшей
и мышечной слабости, болей в мышцах бедер и верхнего плечевого пояса,
шеи, отеков голеней, кистей рук, лица. В течение месяца мышечная слабость
666Гастроэнтерология05.2008 08.2008 09.200810.200811.2008ДисфагияМышечная слабостьэгдсколоноскопияОтекиДисфонияОдышкаЛечениеРис, 32.1. Анамнез больного О., 70 летМети пред
80 мг/сОперация23.10.08Метипред
70 мг/спроірессировала и к концу сентября стала значимой. Появились трудности
при подъеме по лестнице, вхождении в транспорт, одевании. В дальней¬
шем отметил затруднение при вставании с постели, появилась одышка при
физической нагрузке, постепенно масса тела снизилась на 5 кг. Незадолго
до госпитализации появились затруднения при глотании, а также дисфония.
Госпитализирован в клинику для обследования и лечения,При осмотре состояние средней тяжести. Кожные покровы бледные. Отеки
голеней, кистей рук, параорбитаяъный отек. Суставы не изменены. Обращали на
себя внимание тихий голос, измененная походка, затруднение при подъеме с кро¬
вати, одевании рубашки, что >'казывало на слабость проксимаїьньїх групп мышц,
Ли.мфатические узлы не увеличены. Число дьгканий 18/мин. На фоне жесткого
дыхания креіпггирующие хрштьт в базальных отделах легких. Границы сердца не
расширены, тоны не изменены, шу.мов нет. Печень, селезенка не увеличены.При первом знакомстве с больным доминирующими предсташіялись миал-
гии, астенические жалобы, отечный синдром. Кроме того, обращали на себя
внимание жалобы на одьшіку и измененная аускультативная картина.В общем анализе крови выявлены умеренная гипохромная анемия и нейтро-
фильньтй лейкоцитоз: гемоглобин і 13 г/л, эритроциты 4,1 лшн, цветовой пока¬
затель 0,81, лейкоциты 12,3 тыс., нейтрофилы 70%, лимфоциты 13%, моноци¬
ты 12%, эозшюфилы 4,3%, тромбоциты 343 тыс., СОЭ 10 мм/ч.В биохимическом анализе крови: общий белок 54 г/л, альбумин 24 г/л,
креатинин 1,1 мг/дл, глюкоза 4,8 ммоль/л, общий билирубин 10,4 мкмоль/л,
ACT 586 Ед/л, АЛТ 330 Ед/л, у-ГТ 18 Цд/л, ЩФ 183 Ед/л, КФК 10114 Ед/л,
Глава 32. Вторичный полимиозит как первое клиническое проявление... 667МБ-КФК484 Ед/л. Иммунологическое исследование крови: уровень гормонов
щитовидной железы и ТТГ в пределах нормы.В общем анализе мочи: удельный вес 1008, белка, сахара, ацетона нет, лейко¬
циты 4-6 в поле зрения, эритроциты 0—1 в поле зрения. Ана-1из кала на скры¬
тую кровь отрицательный.Данные ЭКГ без существенных отклонений от возрастной нормы. При
ЭхоКТ: КДР 4,6 см, КДО 69 мл, КСО 24 мл, тМЖП 1 см, тЗС 1 см, ФВ левого
желудочка 64%. Нарушений локальной сократимости нет. Диастолическая
функция снижена. Полость правого желудочка 2 см, толщина свободной стен¬
ки 0,4 см. Левое предсердие 39 мл, правое 35 мл. Уплотнение створок и фиброз¬
ных колец митрального и аортального клапанов. Стенки аорты уплотнены.
Жидкости в полости перикарда нет.Можно было выделить несколько лабораторных синдромов.• Умеренная гипохромная анемия, нейтрофильный лейкоцрггоз.• Повышение уровня креатининфосфокиназы и ее MB фракции, транса-
миназ.• Гипоальбуминемия, гипопротеинемия.• Сочетание характерного поражения мышц (симметричной проксимшіь-
ной мышечной слабости, поражения мышц глотки, гортани, пищевода —
дисфония, дисфагия; отека мышц) со значительным повышением уровня
креатинфосфокиназы заставляло думать прежде всего о полимиозите как
причине данных проявлений. Дальнейшее обследование было направлено
на подтверждение этого диагноза. «Золотым стандартом» диагностики
являются ЭМГ и биопсия мышцы.При электромиографии выявлены признаки патологической спонтанной
активности миофибрилл, что подтверждало миогенный характер поражения.Произведена биопсия четырехглавой мышцы левого плеча. Морфологическое
заключение звучало следующим образом; мышечные волокна местами гомо¬
генизированы, с потерей фибриллярности, небольшие очаги фрагментации и
некроза мышечных волокон. Очаги склероза местами расположены поперек
пучков мышечных волокон. Винтерстиции очаги воспалительной инфиль-
тарции (лимфоциты, нейтрофилы, плазмоциты). Перестройка стромы. Эти
данные подтвердили диагноз полимиозита.Таким образом, из диагностических критериев полимиозита (Tanimoto К. et
al., 1995) у больного выявлены четыре.1. Поражение кожи.2. Проксимоііьная мышечная слабость.3. Повышение уровня креатинфосфокиназы или альдолазы в сыворотке.4. Боли в мышцах при пальпации и миалгии.5. Миогенные изменения при электромиографии.6. Обнаружение антител Jo-1 (антитела к гистидил тРНК-синтетазе).7. Недеструктивный артрит или артралгии.8. Признаки системного воспаления.9. Морфологические изменения, соответствующие воспалительному миозиту.Это достаточно для постановки диагноза полимиозита.
668 ГастроэнтерологияСреди многообразия форм идиопатических воспалительных миопатий, пред¬
ставленных в классификации {приведена ниже), можно было обсуждать как
первичный идиопатический полимиозит, так и миозит, ассоциированный со злокаче¬
ственными опухолями. Последний представлялся наиболее вероятным, учитывая
возраст пациента и выраженные астенические жалобы. Дальнейшее обследова¬
ние было направлено на выявление злокачественного новообразования.Классификация идиопатических воспалительных миопатий• Первичный идиопатический полимиозит.• Первичный идиопатический дерматомиозит.• Ювенильный ДМ/ПМ.• Миозит, сочетающийся с ДЗСТ.• Миозит, сочетающийся со злокачественными опухолями.• Миозит с внутриклеточными включениями.• Другие формы воспалительных миопатий:- фанулематозный миозит;~ эозинофильный миозит;- миозит при васкулитах;- op6HTajTbHbm миозит;- фокальный миозит;- оссифицируюший миозит.при исследовании крови на онкомаркеры (PSA, а-фетопротеин, SEA,
SA-19) патологии не выявлено. При рентгенографии органов грудной кііетки
были выявлены изменения, не позволявшие полностью исключить ТЭЛА: в
базальных отделах нижней доли правого легкого участки уплотнения легочной
ткани, расположенные субплеврально; слева небольшие участки уплотнения
легочной ткани по типу фиброза.В связи с этим проведена КТ органов грудной клетки с внутривенным кон¬
трастированием: в субплевральных отделах правого легкого множественные
участки фиброза, утолщения интерстицш. В нижней доле субплеврально —
линейные зоны консолидации неправильной формы (рис. 32.2). В базальных
отделах слева также участки фиброза и зоны повышения плотности легочной
паренхимы. В 6-м сегменте слева определяется очаг неправильной формы
размером 9 мм ~ фиброз. В плевральной полости справа — небольшое коли¬
чество жидкости, толшина слоя до 9 мм. Трахея и крупные бронхи свободно
проходимы, не деформированы. Лимфатические узлы средостенья не увели¬
чены. После внутривенного контрастирования: ствол легочной артерии 29 мм,
правая главная ветвь легочной артерии 29 мм, левая главная ветвь легочной
артерии 22 мм. Дефектов контрастирования в легочных артериях и их ветвях
не выявлено- Восходящая аорта 34 мм, аорта в области дзти 28 мм, нисходя¬
щая аорта 26 мм. Заключение: убедительных данных за тромбоэмболию ветвей
легочной артерии не получено. Учитывая изменения в легких и расширение
правой главной ветви легочной артерии, нельзя полностью исключить тромбо¬
эмболию (тромбоз?) мелких ее ветвей.Проведено ультразвуковое допплеровское исследование глубоких вен
нижних конечностей', выявлен тромбоз глубоких вен обеих нижних
Глава 32. Вторичный полимиозит как первое клиническое проявление...669конечностей — пристеночныи
тромбоз вен голени и окклюзивный
тромбоз подколенной вены справа,
пристеночный тромбоз подколен¬
ной вены слева.При исследовании ФВД выяв¬
лены умеренные рестриктивно-
обструктивные изменения.при УЗИ органов брюшной поло¬
сти обнаружено гипоэхогенное
образование 42x30 мм в 8-м сег¬
менте печени, в связи с чем боль-
HO\iy была проведена МСКТорганов
брюшной полости {рис. 32.3): обна¬
ружено поддиафрагмальное обра-Рис. 32,2. Компьютерная томограмма органов
грудной клетки. Пояснения в текстезование печени в 8-м сегменте неправильной формы около 4 см в диаметре,
слабо неравномерно накапливаюшее контрастный препарат. По своим харак¬
теристикам образование печени соответствовало метастатическому. Обращено
внимание на отечность подкожно-жировой клетчатки передней брюшной
стенки. Продолжено обследование, направленное на выявление первичной
локализации опухоли.При ЭГДС выявлены эрозивный гастрит, постьязвенный рубец в луковице
двенадцатиперстной кишки.Наконец, при колоноскопии в средней трети восходящего отдела толстой
кишки выявлено экзофитное образование, резко суживающее просвет кишки.
Ткани в этой зоне резко кровоточивы, плотные, с участками некроза, покры¬
тыми фибрином. Эндоскоп провести ниже не удается. В остальных отделах
толстой кишки слизистая оболочка розовая, гладкая, просвет кишки не изме¬
нен. Заключение: опухоль средней трети восходящего отдела толстой кишки
с признаками стенозирования. Патогистологическое исследование: элементы
аденокарциномы.Учитывая полученные данные, целесообразно отметить изменения при
МСКТ легких, которые сочетали в себе различные варианты поражения:• изменения, характерные для полимиозита (интерстициальный легочный
фиброз);• тромбоэмболию мелких ветвей правой легочной артерии и последствия
инфарктов легкого (множественные участки фиброза субплевральной
локализации);• карциноматоз правого легкого — участки консолидации в нижней доле,
выпот в плевральной полости.Таким образом, больной страдал злокачественным новообразованием —
аденокарциномой толстой кишки с метастатическим поражением печени,
возможно, карциноматозом легких. Полимиозит расценивался как ассоци¬
ированный со злокачественным образованием. Вьшаденный тромбоз глубо¬
ких вен голеней, осложненный тромбоэмболией ветвей легочной артерии,
670ГастроэнтерологияРис. 32.3. Компьютерная томограмма органов
брюшной иолости. Пояснения в текстерассматривался в рамках паранео-
пластического синдрома. Диагноз
был сформулирован следующим
образом; вторичный полимиозит,
подострое течение: поражение
мышц верхних и нижних конеч¬
ностей, глотки, гортани, пищево¬
да. Аденокарцинома восходящего
отделатолстойкишки. Образование
печени. Тромбоз глубоких вен ниж¬
них конечностей. Тромбоэмболия
мелких ветвей правой легочной
артерии. Хронический эрозивный
антральный гастрит, обострение.
Язвенная болезнь двенадцатипер¬
стной кишки в стадии ремиссии.Тяжесть состояния больного, поражение практически всех групп мышц
(скелетных мышц, мьшіц гортани, глотки, пищевода), а также вовлечение в
процесс легких требовали незамедлительного начала лечения (сразу после
электромиографического подтверждения полимиозита). Была начата терапия
глгококортикоидами: преднизолоном в дозе 1 мг на 1 кг в сутки. Для нашего
пациента доза составила 80 мг/сут. Был отмечен некоторый положитель¬
ный эффект терапии в виде уменьшения мышечной слабости и дисфагии.
Проводилась также противоязвенная терапия, терапия непрямыми антико¬
агулянтами. В связи с гипоальбуминемией парентерально вводился раствор
альбумина.Больной нуждался в хирургическом лечении в связи с выявленной адено¬
карциномой восходящего отдела толстой кишки. Обсуждалась также воз¬
можность удаления единичного метастаза печени. Предполагаемым резуль¬
татом хирургического лечения был обратный регресс явлений полимиозита.
После проведенной предоперационной подготовки больной был переведен
в Факультетскую хирургическую к,іинику им. Н.Н. Бурденко Московской
медицинской академии им. И.М. Сеченова, где 23.10.2008 г, была выполнена
операция: резекция поперечной ободочной кишки. В средней трети опреде¬
лялась опухоль, циркулярно суживающая просвет кишки, не прорастающая
серозную оболочку, размерами 3x2x2 см. Регионарные лимфатические узлы
мягкоэластической консистенции, макроскопически не изменены. На диа¬
фрагмальной поверхности печени в 8-м сегменте определяется хрящевидной
плотности образование размерами 4x3 см (метастаз). Интраоперационный
диагноз: рак поперечноободочной кишки, инфильтративно-язвенная форма,
T2N0M1.При интраоперационном УЗИ в 8-м сегменте печени определяется изо-
эхогенное образование неоднородной структуры с неровными четкими кон¬
турами 4-5 см в диаметре. С медиальной стороны к образованию прилежит
нижняя полая вена. С учетом интимного прилежания нижней полой вены к
Глава 32. Вторичный полимиозит как первое клиническое проявление... 67Іобразованию резекция печени признана невыполнимой. Проведенное морфо¬
логам еское исследование удаленной опухоли подтвердило диагноз умеренно
дифференцированной аденокарциномы. Временный переход на парентераль¬
ное введение глюкокортикоидов в адекватных дозах в послеоперационный
период вызвал ухудшение состояния больного, нарастание мышечной слабости,
дисфагии; заживление послсопераиионной раны прошло в стандартные сроки.БыУ1 возобновлен прием метипреда из расчета 1 мг на 1 кг массы тела с неко¬
торым положительным эффектом в виде уменьшения дисфагии и мышечной
слабости. Больной был выписан на 14-й день после операции с рекомендация¬
ми проведения курса химиотерапіто кселодом.Воспалительные миолатии — приобретенные заболевания, характеризую¬
щиеся воспалением мыши. Среди них выделяют инфекционные миопатии
(бактериальные, вирусные, грибковые и др.), токсические, лекарственные, а
также идиопатические воспалительные миопатии, не связанные с конкретным
этиологическим фактором.К идиопатическим воспалительным миопатиям (хроническим диффуз¬
ным заболеваниям поперечнополосатой мускулатуры, основным проявлением
которых является мышечная слабость) относят;• 1ІОЛИМИОЗИТ и дерматомиозит;• ювенильный дерматомиозит;• миозит с «включениями»;• миозит, ассоциируюшийся с системными заболеваниями соединительной
ткани;• паранеотастический полимиозит.Паранеопластическнй полимиозит является проявлением параиеопла-
стических синдромов — опосредованных клинических признаков опухо¬
левых заболеваний, проявляющихся со стороны определенных органов и
тканей и возникающих в результате каких-либо биохимических, гормональ¬
ных, иммунологических или наследственных нарушений. Вполне понятно,
что такое определение симптомов является условным. Тем не менее они
дают важные в практическом отношении «маркеры» или информацию,
позволяющие выйти на более своевременную и даже раннюю диагностик>'.
В ряде случаев они могут проявляться задолго до клинически выявляемой
опухоли.Опухоли различных локализаций на определенных этапах до появления
местной симгггоматики могут проявляться неспецифическими признаками,
ошибочно трактующимися как самостоятельные заболевания.Паранеоплазии нельзя объяснить прямым проявлением злокачественной
опухоли или ее метастазов, Они чрезвычайно разнообразны и в одних случа¬
ях обусловлены глубокими биохимическими нарушениями, свойственными
развернутым стадиям рака, в других — являются результатом аутоиммунных
реакций, гормональных сдвигов, возникающих уже на ранних этапах раз¬
вития опухоли. Параисопластические синдромы встречаются с частотой
10—15% у больных с онкопатологией, часто являются первыми признаками
заболевания.
6Г2 ГастроттерологияВ 70-х гг. прошлого века были сформулированы критерии паранеопластиче-
ских синдромов.1. Онкопатология и паранеопластический синдром должны появляться в
одно время, выраженность их не должна существенно различаться.2. Паранеогыастические синдромы редко связаны с распространенностью
опухолевого проиесса.3. Паранеопластические синдромы и онкопатология должны быть патофи¬
зиологически связаны.Эти критерии остаются достоверными и в настоящее время, но следует угги-
тывать, что онкологический процесс не всегда поддастся диагностике рутин¬
ными методами, и функционирование опухолевой ткани может прояв-іяться
задолго до ее детекции. Существует несколько гипотез относительно патогене¬
за паранеопластичсских синдромов.1. Биохимическая. Опухолевая ткань представляет собой «ловушку» для
метаболитов (азота, глюкозы, липидов, витаминов и т.д.). Длительное ее функ-
иионирование изменяет биохимический обмен в организме, истощая ресурсы
здоровых тканей и их функциональную активность.2. Иммунная. Сходство антигенов опухоли и здоровых тканей вызывает
реакцию гуморального и клеточного иммунитета, способствуя развитию ауто¬
иммунных сдвигов.3. Гормональная. Опухолевые к-тетки вырабатывают биологически актив¬
ные вещества и гормоны, что ослабляет чувствительность тканей-мишеней
к гормональному воздействию и приводит к расстройству эндокринной
регуляции.Многие ревматологические заболевания связаны с повышенным риском
развития онкопатолот ИИ. В то же время неопластические процессы часто мани¬
фестируют как проявления ревматологических болезней. Паранеопластические
синдромы являются результатом наличия опухоли, но не находятся в прямой
зависимости от ее объема и количества метастазов.Опухоли могут нарушать функции других органов и систем путем экто¬
пической продукции биологически активных веществ. Например, гиперкаль¬
цием ия при злокачественных процессах может быть результатом эктопиче¬
ской продукции протеина, подобного паратиреоидному гормону (чаше при
опухолях почек, карциноме легких). Клинические проявления эффектов
паратиреоидподобного протеина неотличимы от действия паратиреоидного
гормона, уровень костной резорбции коррелирует с уровнем гиперкаль-
циемии. с уменьшением массы опухоли концентрация кальция снижается.
Паратирсоидподобный протеин может индуцировать опухолевую прогрес¬
сию и метастазирование.Кроме того, иммунная система вырабатывает аутоантитела под действием
антигенов опухоли, например к р53 (anti-p53), онкопротеинам (anti-HER2/
neu), ассоциированным с пролиферацией антигенам (anti-cyclin), онконев-
ральным белкам.Хронология возникновения паранеопластического синдрома по отношению
к появлению локальных симптомов первичной опухоли может быть различной.
Глава 32. Вторичный полимиозит как первое клиническое проявление.,, 673В одних случаях клинические проявления предшествуют местным симптомам
опухоли, в других — появляются одновременно с ними; наконец, мотуг воз¬
никать уже после верификации опухолевого процесса. Наибольшие трудности
возникают в тех ситуациях, когда различные паранеопластические синдромы
(лихорадка, кожные поражения, тромбофлебиты) предшествуют местным про¬
явлениям опухолевого роста и трактуются как самостоятельные заболевания
или синдромы, служащие поводом для назначения соответствующего лечения.
Следует подчеркнуть, что в большинстве случаев паранеопластические сии-
дромы резистентны к лечению (глюкокортикоиды, нестероидные противовос¬
палительные препараты, антикоагулянты и др.) и склонны к рсцидивированию
(рецидивирующая узловатая эритема, мигрирующие тромбофлебиты). В то же
время паранеопластические сивдромы могут ослабляться или вовсе исчезать
на фоне лечения опухоли (хирургическое удаїение, химиотерапия) и появ¬
ляться вновь при рецидиве оігухоли или ее метастазировании. Возможно соче¬
тание нескольких паранеопластических синдромов с различными клинико¬
лабораторными проявлениями, что усложняет диагностику и своевременное
распознавание опухоли.Все паранеопластические реакции делят на две группы:1) «изолированные» (моносимптомы и мопосиндромы):— лихорадка;— гипертрофическая остеоартропатия;— нефротический синдром;— синдром Рейно;— сухой синдром (синдром Шефсна);— узловатая эритема;— крапивница;~ эозинофилия;— тромбоцитопеническая пурпура;— миалгии;— тромботические осложнения;— гемолитическая анемия;2) «системные»:— полимиозит/дерматомиозит',— ревматоидный артрит;— геморрагический васкулит;— склеродермия;— системная красная вол^шнка;— эндокринопатии;— полисерозиты;— амилоидоз;— миопатии;— нейропатии.Дерматомиозит (полимиозит) — системное заболевание с преимущественным
поражением скелетной и гладкой мускулагуры с нарушением ее двигательной
функции и кожными проявлениями.
674 ГастроэнтерологияМиозит, ассоциированный с опухолями, составляет около 20% случаев
идиопатичсских воспалительных миопагий. Онколи могут развиваться как до
появления признаков полимиозита, так и одновременно с ними или после их
появления. Наиболее часто вторичньп^і (опухолевым) полимиозитом сопрово¬
ждаются:• аденокарцинома (70% случаев паранеопластичсского полимиозита);• рак легких;• рак яичников;• рак молочных желез;• рак желудка и толстого кишечника, поджелудочной железы;• лимфопролифсративные заболевания.У 30% пациентов с дерматомиозитом и полимиозитом в дальнейшем диагно¬
стируют рак. Вероятность развития рака наиболее высока в первые 3 года после
постановки диагноза. Грутша риска — мужчины старше 50 лет (более 70%),Опухолевые клетки способны напрямую и опосредованно активировать
свертывающую систему крови. Большое количество прокоагулянтных субстан¬
ций выделено из опухолевых клеток. Тромботичсскме осложнения могут быть
проявлениями паранеопластичсского синдрома. В 1865 г. Арман Труссо впер¬
вые описал «болезненное белое воспалепие» вследствие венозного тромбоза
множественных локализаций на фоне опухолевого заболевания и туберкулеза.
Впоследствии бьы выделен синдром труссо, характеризующийся возникно¬
вением тромбоза крупных вен, нередко атипичной локализации, носятцсго
мигрирующий характер и резистентного к терапии антикоагулянтами. Данный
синдром описан при опухолях различных локализаций, чаше на фоне гастро¬
интестинальных и гепатобилиарных опухолей.Следует отметить также, что современная химиотерапия повышает риск
тромбозов. Точные механизмы этого явления неизвестны, хотя предположи¬
тельно основной из них — прямое повреждающее действие тщтотоксических
препаратов на эндотелий. Интересным является тот факт, что применение
антикоагулянтов, в частности варфарина, уменьшает риск развития опухолей у
больных тромбозами, не связанными с опухолями, благодаря антинеопласти-
ческому действию данного препарата.Лечение парансопластических синдромов включает удаление первичной
опухоли и ее метастазов, оперативное вмешательство и химиотерапию, воз¬
можен полный регресс клинической симптоматики парансопластических
синдромов. В плане симптоматической терапии для лечения вторичного поли¬
миозита используются глюкокортикоидьт — 1 мг/кг в сутки до хирургического
вмешательства, далее возможна их полная постепенная отмена при исчезнове¬
нии клинических и лабораторных признаков полимиозита. Лечение тромбо¬
тических осложнений проводится по общепринятым схемам лечения анти-
коагуляшами.Что касается поражения легких при дермато-/полимиозите, то оно встреча¬
ется у 30% больных. Манифестация легочного поражения может идти по трем
различным путям; соответственно разнообразны и изменения, выявляемые
при КТ. Это могут быть очаги субплевральной консолидации, тракционные
Глава 32. Вторичный полимиозит как первое клиническое проявление,., 675бронхоэктазы и бронхиолоэктазьт, изменения по типу «матовых стекол»,
интерстициальный фиброз. Наиболее часто встречаются интерстициальные
поражения легких.1. Острая интерстициальная пневмония (остро развивающаяся одышка,
гипоксемия, лихорадка, инфильтраты в базальных отделах легких, неэффек¬
тивность антибиотиков; преобладающий гистологический вариант — диффуз¬
ное повреждение альвеол).2. Прогрессирующий интерстициа.аьный легочный фиброз (кашель, про¬
грессирующая одышка, рестриктивные изменения показателей ФВД; преоб¬
ладающие гистологические варианты — неспецифическая интерстициальная
пневмония, обычная интерстициальная пневмония).3. Бессимптомные нарушения легочной вентиляции, бессимптомные изме¬
нения при КТ легких (преобладающий гистологический вариант — организую¬
щаяся пневмония).ЛИТЕРАТУРАTanimoto К., Nakano К., Капо К. et ai Classification criteria for polymyositis and
dermatomyositis //J. Rlieumatol. 1995; 22(4):668-6774.
Глава 33ОСОБЕННОСТИ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО
ВИРУСНОГО ГЕПАТИТА В У ПАЦИЕНТОВ
С ЦИРРОЗОМ ПЕЧЕНИЯМ Махов, Л.И. УгрюмоваЗатсіючительная глава не вполне типична для данного издания. Она демон¬
стрирует, в чем, собственно, состоит специализация, в том числе в рамках
единой терапевтической клиники: в центр рассмотрения вынесен вопрос лече¬
ния заболевания с хорошо известной этиологией — хронического вирусного
гепатита В. Сегодня это лечение не просто возможно — оно высоко диффе¬
ренцировано и требует от специалиста глубокого знания патогенеза, иммуно¬
логических аспектов заболевания, особенностей назначения противовирусных
препаратов с разными механизмами действия, различий в действии препаратов
внутри одной 1руппы, а главное — постоянной практики в назначении этих
препаратов. Представляем пациента с циррозом печени, развившимся на фоне
хронического гепатита В (HB^Ag-положительного), леченного ламивудином с
последующей заменой препарата на энтекавир.Больной М., 65 лет, поступил в отделение гастроэнтерологии Факультетской
терапевтической клиники им. В.Н. Виноградова 07.11.2008 г. с жсигобами на
выраженную слабость, утомляемость, носовые кровотечения, кровоточивость
десен при чистке зубов, снижение массы тела на 10 кг (при сохраненном кал-
лоражс и объеме принимаемой пищи).Семейный анамнез не отягощен. Имеет среднее техническое образование,
работает наладчиком станков; профессионаїьньїх вредностей нет. До 2005 г.
считал себя здоровым человеком, вел активный образ жизни. В анамнезе опе-
ративньох вмешательств и переливаїшй крови не было.Аішмнез заболевания {рис. 33.1): в мае 2005 г. пациент стал отмечать повы¬
шенную утомляемость при выполнении обычной работы. На этом фоне воз¬
никло повышение температуры тела до 38 "С, появилась иктеріїчность скяер,
в связи с чем был госпитализирован в городскую иііфекпионную больницу
№ 1. При проведении рутинных лабораторных исследований было выявлено
повышение активности ACT до 500 Ед/л, АЛТ до 700 Ед/л, обнаружен НВ^.
На основании полученных данных состояние было расценено как острый
вирусный гепатит В. В течение двух недель проводилась терапия фосфогливом
(внутривенно капельно), ферментными препаратами, после чего самочувствие
пациента улучшилось: уменьшилась слабость. При контрольном исследовании
было отмечено снижение активности трансаминаз сыворотки крови (ACT до
50 Ед/л, АЛТ до 120 Ед/л). После выписки было рекомендовано соблюдение
диеты в рамках стола № 5, а также прием фосфоглива по 1 капсуле 3 раза
в день. На протяжении последующего года пациент по-прежнему ощущал
Глава 33. Особенности лечения хронического вирусного гепатита В...677Слабость
Температура
Иктеричность склерНосовыекровотечениякровоточивостьдесенACT (ед./л) N до 40АЛТ(ед./л) N до 40ДНК HBV-виремия2005 г.
май2005 г.
июнь36,7 °С2006 г.
сентябрь2006 г.
октябрь36,6 "С 36,6 °С505698491207094MBsАд ^АФП (МЕ/мл) N до 10Лечение ФосфогливФосфоглив150Ламивудин(зефикс)100 мг/сутЛамивудин(зефикс)100 мг/сутРис. 33.1. Анамнез больного М., 65 лет (до 2007 г.)слабость, однако продолжал работать. Контроль биохимических показателей
крови не осуществлялся.В сентябре 2006 г. усилилась слабость, возникли носовые кровотече¬
ния и кровоточивость десен, что послужило поводом для госпитализации в
Центральный научно-исследовательский институт гастроэнтерологии, где
было выявлено пятикратное повышение активности транса мин аз, повы¬
шение альфа-фетопротеина (АФП) до 150 МЕ/мл (в норме до 10 МЕ/мл), а
также впервые обнаружена ДНК вируса гепатита В. При УЗИ органов брюшной
полости отмечались гепато- и спленомегалия. При ЭГДС обнаружены уси¬
ление печеночного процесса и ухудшение состояния больного, была начата
противовирусная терапия ламивудином (группа аналогов нуклеозидов) в дозе
100 мг/сут. Данный препарат пациент переносил хорошо, После 14 мес приема
он отметил улучшение самочувствия, показатели ACT и АЛТ нормализовались,
уровень АФП снизи,1ся до 6,4 МЕ/мл, виремия не опреде;шлась, в связи с чем
ламивудин был отменен.Однако через 2 нед после отмены препарата самочувствие пациента ухуд¬
шилось, вновь появилась кровоточивость десен, возобновились носовые кро¬
вотечения. в анализе крови отмечалось трехкратное повышение активности
ACT, четырехкратное повышение активности АЛТ. При постановке ПЦР была
обнаружена HBV-ДНК с мутацией YMDD в количестве 5,2x10"^ МЕ/мл.Учитывая ухудшение состояния и неблагоприятные лабораторные показа¬
тели, в декабре 2007 г, пациент был повторно госпитализирован в Центральный
678Гастроэнтерология2007 г. 2007 г. 2008 Г. 2008 г. 2008 Г. 2008 г.
ноябрь декабрь январь март октябрь ноябрьСлабостьНосовые кровотечения
Кровоточивость десен
Лейкоциты (10х9/л)
Тромбоциты (10х9/л)
ACT (ед./л) N до 40
АЛТ(ед./л) N до 40
ДНК HBV-виремияHBsAg
АФП (МЕ/мл) N до 10
ЛечениеНормаНорма6,4Отменаламиву-дина5,2x10x4МЕ/мл>3,664,325,346663,971,1306704233853431,2x10x71260МЕ/млМЕ/мл♦♦♦1163223,76■лив Энтаковир Энтаковир Энтаковир
(бараклюд) (бараклюд) (бараклюд)
500 мг/с 500 мг/с 500 мг/сРис. 33,2. Анамнез больного М., 65 лет (после 2007 г.)научію-исследовательский инстит>'т гастроэнтерологии {рис. 33.2). Повышение
уровня АФП составаїїо 400 МЕ/мл (в 40 раз выше нормы). В связи с высокими
показателями онхомаркера бьита проведена МРТ органов брюшной полости,
при которой ншіичие опухолевого образования не подтвердилось, а также были
получены данные, иозволяюпше поставить диагноз дирроза печени. Входе
лечения был проведен курс внутривенных инфузий фосфоглива.С марта 2008 г. пациент наблюдается в отделении гастроэнтерологии
Факультетской терапевтической клиники им. В.Н. Виноградова. В анализах
крови пациента были выявлены признаки активности печеночного про¬
цесса (восьмикратное повышение активности трансаминаз, виремия до
1,2x10’ МЕ/мл, АФП 116 МЕ/мл), а также признаки гиперспленизма: сниже¬
ние тромбоцитов до 60 тыс., лейкоцитов до 3,6 тыс. Для уточнения диагноза
цирроза печени больному бьиш проведены компьютерная томография органов
брюшной полости и пункционная биопсия печени.С учетом картины цитолиза и наличия HBV-ДИК с мутацией YMDD паци¬
енту бьию рекомендовано начать противовирусн>то терапию энтекавиром
(бараклюд) в дозе 500 мг/сут (который, как и ламивудин, относится к аналогам
нуклеозидов). Спустя полгода после начала лечения отмечалась положитель¬
ная динамика в виде снижения уровня АФП, активности фансаминаз. Однако
сохранялись жалобы на носовые кровотечения, кровоточивость десен. В ноя¬
бре этого года пациент был вновь госпитализирован в Фак>'льтетскую терапев¬
тическую клинику им. В.Н. Виноградова.При осмотре состояние удовлетворительное. Кожные покровы чистые —
внепеченочных знаков ііет. Больной достаточного питания (индекс массы
Глава 33. Особенности лечения хронического вирусного гепатита В... 679тела 23 кг/м^). Отеков ист. Со стороны легких и сердечно-сосудистой системы
паїологии не выявлено. Перкуторно свободной жидкости в брюшной полости
не определяется. Живот мягкий, безболезненный. Печень выступает на 2 см
из-под края реберной дуги, край ее унлотнен, поверхность гладкая, безболез¬
ненная. Размер печени по среднеключичной линии 16 см. Край селезенки не
пальпируется, перкуторно размеры 14x9 см,В общем аиашзе крови выявлены следующие отклонения от нормы: лим¬
фоциты 38,9% (19-37%), эозинофилы 8,9% (0-5%), тромбоциты 71Д тыс.
(180-320). НЬ 140,2 г/л, эритроциты 4 млн, цветовой показатель 0,99, лейко-
тшты 5,3 гьтс., СОЭ 5 мм/ч.В биохимическом анализе крови выявлено умеренное повышение обще¬
го билирубина до 28,4 мкмоль/л (5-21), а также повышение активности
щелочной фосфатазы до 121,8 Ед/л (0-92) при нормальных показателях у-ГГ
(49 Ед/л; 0—55), значительное повышение уровня железа сыворотки крови
до 255 мгк/дл (40-160) и умеренное снижение активности холинэстсразьт до
3554 Ед/л (3930-11 500). При этом уровень ітрямого билирубина составляет8,5 мкмоль/л (0-5), ACT 42 Ед/л (0-40), АЛТ 43 Ед/л (0-40), IgA 460 мг/дл
(50-300), IgG 2370 мг/дл (600-2000), АФП 23,76 нг/мл (0-14,4). Патолопти
со стороны свертывающей системы крови не выяв.лено. Показатели общего
анализа мочи в пределах нормы. При вирусологическом исследовании крови были
обнаружены HB^Ag, антитела к фрагментам вируса гепатита В (НВ^^ АЬ (сумм),
HB^Ag).УЗИ органов брюшной полости позволило выявить увеличение печени (пра¬
вая доля 171 мм, левая 77 мм), повышение ее эхогенности, увеличение диаме¬
тра портальной вены до 13,3 мм. Также было отмечено увеличение селезенки
до 139x64 мм.При ЭГДС в нижней трети пищевода в толще слизистой оболочки были
обнаружены расширенные венозные стволы без варикозных изменений.Поскольку по-прежнему сохранялись высокие значения АФП, бьто решено
провести КТ органов брюшной полости, в результате которой бьши выявлены сле¬
дующие патологические признаки: неоднородность структуры печеїш за счет
множественных изоденситньтх узлов, увеличение диаметра воротной вены до
15 мм, селезеночной вены — до 9,5 мм, верхней брыжеечной вены — до 13 мм.При морфологическом исследовании биоптата печени была выявлена гиперх-
ромность части гепатоцитов, их деформация, диснластические изменения,
участки фиброза, а также выраженная эозинофильная инфильграция.На основе полученных данных был поставлен диагноз: цирроз печени вирус¬
ной этиологии юшсс А (по Чайлду-Пью), активность 1 степени. Портальная
гипер'1'ензия: распгарение воротной вены, селезеночной вены, спленомегалия,
гипсрспленизм (тромбоиитопения). в клинике пациент продолжал прием энте-
кавира в дозе 500 мг/сут, а также іюлуїал крсон 10 ООО Ед по 1 таб. 3 раза в деш>.Таким образом, замена ламивудина энтекавиром и прием его в течение
9 мес привели к нормализации биохимических показателей, снижению вире-
мии и уровня АФП. Представленный клинический случай свидетельствует о
правильно выбранной тактике лечения, которая максимально эффективно
680 Гастроэнтерологиявоздействовала на этиологический фактор заболевания, что привело к улучше¬
нию самочувствия пациента и прогноза его жизни без каких-либо побочных
эффектов для здоровья.Комментарий В.М. Махова — профессора кафедры факультетской терапии № 1
лечебного факультета Первого МГМУ им. И.М. Сеченова, д-ра мед. наукРаспространенность хронического гепатита В среди всего населения зем¬
ного шара составляет 5%. Приб^тизителъно у 2 млрд человек (1/3 мировой
популяции) обнаруживают маркеры инфекции вирусом гепатита В (в том
числе перенесенной), из них маркеры хронической инфекции — у 350 млн.
В обш;ем ряду причин смертности хронический гепатит В занимает 9-е место,
следуя непосредственно за хроническими заболеваниями легких и заметно
опережая СПИД. Заболеваемость хроническим гепатитом В по Российской
Федерации, по данным на 2002 г,, составляла 47,8 слу'чаев на 100 тыс. насе¬
ления. Также известна более высокая частота хронизации гепатита В у муж¬
чин по сравнению с женщинами. Заболевание охватывает весь земной
шар, с большей распространенностью в Африке и странах Центральной и
Юго-Восточной Азии (на Тайване до 20%). Северная Америка, Западная
Европа, Австралия, Новая Зеландия и Япония в этом отношении более
эпидемшшски благополучны (распространенность составляет менее 1%).
Россия относится к странам со средней распространенностью хрони^іеских
вирусных гепатитов. Приблизительно у 1/3—1/4 лиц с хронртчсской инфек¬
цией вирусом гепатита В возможно развитие цирроза печени и гепатоцел-
люлярной карциномы.Вирус гепатита В — ДНК-содержаший вирус (рис. 33. J). Лшюпротеидная обо¬
лочка содержит поверхностный HB^Ag (австралийский антшен). Kpre-Sl- и
рге-52-регионам HB^Ag вырабатьшаются вируснейтрализуюшие антитела, нару¬
шение синтеза которых способствует хронизации инфекции. HB^Ag — важный
диагностический маркер. В структуру ііуклеокапсида (ядерного антигена —
HB^^^^Ag) входят субъединица HB^Ag, ДНК-полимераза, нротеинкиназа и ДНК.
HB^^^Ag, HB^Ag и ДНК также имеют важную диагностическую ценность.
Особое значение для течения заболевания, лечения и прогноза имеют мутации
вируса. Наиболее широко изучена и наиболее значима мутация в виде замены
гуанина на аденик в геноме вируса, что приводит к нарушению продукции
HBgAg. Таким образом, выделяют НВ^-положительную и НВ^-негативную
формы хронического гепатита В (табы. 33.1). На основании наличия или
отсутствия вьппеописанной мутации выделяют два клинико-серологических
варианта хронического гепатита В: классический («дикий») и мутантный
тип. Вирус-мутант вызывает более тяжелое течение гепатита, чем «дикий»
вирус, поскольку обладает способностью избегать иммунного распознавания
хозяином. Кроме того, мутанты способны вызьгеать не только хронический
гепатит В, но и фульминантные формы. Лечение НВ^-негативных пациентов
имеет свои особенности. Помимо этого, необходимо помнить о возможности
возникновения мутаций в процессе терапии. Это серьезная клиническая про¬
блема, которая заслуживает особого внимания.
Глава 33. Особенности лечения хронического вирусного гепатита В...68ЇДНК ВГВооpreS2HBcAg, HBeAgHBsAg, основной белок ВГВСредний
белок ВГВ^ Филаменты
с вариабельной длиной,017—25 нмРис. 33,3, Строение вируса гепатита В. Пояснения в текстеТаблица 33.1Клинико-серологические варианты хронического гепатита ВВарианты ХГВСывороточныемаркерыУровень виремииКлинико¬
морфологические характе¬
ристикиКлассический
«дикий» типHBsAg+HBeAg+Высокий или умерен-
тгыйДНК ВГВ >10=Хронический гепатит
(от мягкой до высокой
активности)«Мутантный» типHBsAgH-HBeAg-Лити-НВеТаблица 33.2Фазы развития хроническоі о гепатита ВФазаМаркерыИм\гуио-толерантнаяHBsAg+++, ДНК ВГВ+++, HBeAg+, анти-НВс—, анти-
НВсоге lgG+, анти-НВсоге lgM+/-, анти-HBs-, АЛТ — NИммуно-элиминационнаяHBsAg+, ДНК ВГВ+, HBeAg+/-, анти-НВе+/-, анти-
НВсоге IgG+, анти-НВсоге IgM+/-, анти-HBs, АЛТ
100-150 ЕдП острепл икатипнаяHBsAg+, ДНК ВГВ- HBeAg-, анти-НВе+, анти-НВсоге
IgG-H, анти-НВсоге IgM—, АЛТ — менее 75 Ед
682 ГастроэнтерологияВ течении хронического гепатита В вьщеляют три фазы {табл. 33:2): иммуно-
толерангную, имм^ио-элиминационную, пострепликативную. В первую
фазу характерны толерантность к вирусу и малые иммунные реакции; высо¬
кая концентрация вируса сочетается с малыми повреждениями нсчени.
В иммуно-элиминационную фазу Т-клстки распознают инфицированные
гепатоциты и элиминируют их, В этой фазе обычно нaбJuoдaeтcя серокон-
версия; падает концентрация и.'Ш исчезает HB^Ag, образуются анти-НВ^,
В случае пролонгирования этой фазы длительное повреждение печени может
относительно быстро приводить к развитию цирроза печени. В пострепли-
кативн^то фазу поверхностный антиген вируса гепатита В участвует в инте¬
грации вирусной частицы с гепатоцитом. Прогрессирование хронического
гепатита замедляется.После подтверждения диагноза определяют тактику лечения. Хотелось в
первую очередь сказать об общітх мероприятиях: постельный режим и дру¬
гое ограничение двигате^іьной активности, которые предписывались таким
пациентам ранее, не оказывают никакого влияния на течение заболевания.
То же можно сказать и о диетических рекомендациях, которые при отсут¬
ствии эпцефалопатии и асиита оказываются бесполезными. Дополнительно
назначаслтьте витамины не изменяют активности заболевания. Однако для
пациента важно исключить употребление алкоголя.Что касается лекарственной терапии хронического гепатита Д то в настоя¬
щее время применяют две группы препаратов: интерферон-альфа и аналоги
нутаеозидов. Препараты интерферона, в свою очередь, делятся на пегили-
рованныс (пегасис, пегИнтрон) и нспегалированные (альфарона, диаферон,
ишрон А, лайфферон, реатьдирон, роферон). Аналоги н}татеозидов послед¬
него поколения представлены такими препаратами, как адефовир (гепсера)
и тенофовир (вирид). Адефовир в России не зарегистрирован, а тенофовир
бьш одобрен FDA только в 2008 г. В России зарегистрированы такіїе препа¬
раты, как ламивудин (эпивир, зеффикс), фамцикдовир (фамвир), энтекавир
(бараклюд), телбивудин (себиво).В отношении использоваііия этих препаратов сущссгвуют две точки зрения.
Некоторые авторы предпочитают монотерапию интерфероном или аналога¬
ми нуклеозидов. Некоторые предлагают комбинировать препараты из обеих
групп. По данным последних публикаций, предпо^ггительнее комбинировать
различные аналоги нуклеозидов. И поскольку единого мнения на этот счет
нет, терапевтическая тактика подбирается эмпирически.Терапия интерфероном показана:• при обнаружении HB^Ag и HB^Ag в сыворсггке;• повышении уровня трансаминаз;• хроническом гепатите по данным биопсии печени;• отсутствии сопутствующих заболеваний (в особенности сохраняющейся
алкогольной зависимости);• наличии желания больноі о;• отсутствии противопоказаний к назначению интерфероне в, которых
гораздо больше, чем показаний.
Глава 33. Особенности лечения хронического вирусного гепатита В.683Терапия интерфероном мохет иметь грозные осложнения при иммуносу¬
прессии, выраженной тромбоцитопении (<100 тыс.) и лейкопении (<3 тыс.),
эндогенной депрессии, психозе, беременности, гепатоцеллюлярной карци¬
номе, состоянии после трансплантации почки, аутоиммунных заболеваниях
(включая гиперфункцию щитовидной железы).К благоприятным прогностическим факторам высокого терапевтического
ответа при лечении интерфероном относят высокий уровень трансаминаз
(более 200 Ед/л), высок>то активность воспаления по результатам гистоло¬
гического исследования, краткий анамнез (менее 5 лет), низкую вирусщто
нагрузку (ДНК вируса менее 200 пг/мл), отсутствие сопутствующей инфек¬
ции и женский пол. Из неблагоприятных прогностических факторов можно
выделить следующие: возраст пациента на момент заражения старше 40 лет,
многолетнее течение заболевания, виремию >10^ ожирение, шткогольную
интоксикацию, наркоманию, избыточное накопление железа.Схема назначения препарата и результаты лечения существенно различают¬
ся в зависимости от наличия/отсутствия HB^Ag (табл. 33. J). При на.іичии
«дикого» вируса интерферон назначают в меньшей дозе (4—6 млн Ед 3 раза
в неделю) и с меньшей продолжите.льностью — 6 мес. При обнаружении
мутантного вируса доза препарата составляет 9-10 млн Ед 3 раза в неделю, а
длительность терапии — минимум 1 год. При НВ^-негативном хроническом
гепатите В нормализация уровня АЛТ и сероконверсия не достигаются, а
виремия перестает определяться только в 8% случаев.Терапия интерфероном имеет множество побочных эффектов. Гриппопо-
добньгй синдром развивается практически у всех пациентов. Весьма непри¬
ятны для пациентов и такие последствия, как повышенное выпадение волос,
слабость, психическая депрессия, транзиторный гипотиреоз. А такие побоч¬
ные эффекты, как нейтропения и тромбоцитопения, могут иметь серьезныеТа&гица 33.3Сравнительная характеристика лечения хронического гепатита В
с HBeAg в крови и без негоТерапияHBeAg+НВєі^—Проведение леченияЛекарственный препаратИФН-аИФН-аДоза4-6 млн Ед ИФН 3 раза
в неделю подкожно5-6 млн Ед (9-10) 3 раза
в неделю подкожноПродолжительность6 месМинимум 1 годПоказатели эффективности леченияНормализация уровня АЛТ33%-Сероконверсия HBeAg в
анти-НЬе или8%Сероконверсия HBsAg в анти-
HBs илиСмена положителытых
результатов определения
ДНК ВГВ на отрицательные37%8%
684Гастроэнтерологияпоследствия, поскольку у пациентов с циррозом эти симптомы уже присут¬
ствуют Таким образом, лечение интерфероном пациентов с хроническим
гепатитом В, у которых уже диагностирована стадия цирроза, может быть
даже опасно. Опасность заключается в развитии печеночной недостаточно¬
сти или сепсиса, часто не распознаваемого на нача-чьной стадии.Данные осложнения могут быть спровоцированы даже очень малыми дозами
интерферона (например, 1 -3 млн Ед 1 -3 раза в неделю). Перед началом тера¬
пии необходимо определить стадию цирроза по Чайлду—Пью. Интерферон
можно назначать только на стадии А. На стадии В это рискованно, а на ста¬
дии С уже невозможно. Таким образом, необдуманное назначение интерфе¬
рона пациентам с циррозом может закончиться весьма печатьно. Поэтому у
нашего пациента выбор был сделан в пользу аналогов нук^теозидов, которые
более безопасны в такой ситуации.В настоящее время аналоги нуклеозидов представляют собой единственную
альтернативу препаратам интерферона. Механизм их действия заключается
в том, что они встраиваются в растушую нуклеотидную последовательность,
вызьшая ее прерывание (рис. 33.4), Это происходит во время как обратной
транскрипции первой, так и синтеза второй цепочки ДНК,Из аналогов нуклеозидов в клинической практике наиболее распространен
ламивудин. Это нук.іеозидньій аналог цитозина. Ламивудин блокирует РНК-
зависимую ДНК-полимеразу. Препарат обычно назначают в дозе 100 мгБлокирование
РНК-зависимой
ДНК-полимеразыEntryRemovsi of
RNmHStrandSynttw«i«:P»}|enc«psWetion Sigiwi (d: 8SSlP»t-trMnsc(^f)tional Rodutaiory tPftE)Рис. 33.4. Механизм действия нуклеозидных аналогов. Пояснения в тексте
Глава 33. Особенности лечения хронического вирусного гепатита В...685ежедневно в течение минимум 1 года. Эффективность его по сравнению с
плацебо очевидна. Наблюдается улучшение гистологических показателей
более чем в половине случаев. Сероконверсия по HB^Ag происходит в трети
случаев, виремия перестает определяться в 44% случаев. Биохимические
показатели нормализуются в 41% случаев. Однако к препарату часто развива¬
ется резистентность. По разным данным, через год применения устойчивость
выявляют у 14-80% пациентов.Ламивудин показан в следующих случаях: пациенты с индуцированным виру¬
сом гепатита В циррозом печени, HBV-положительные пациенты с гломе¬
рулонефритом или после трансплантации почки, анти-НВ^-положительные
пациенты с активной репликацией вируса, HB^Ag- и HBgAg-пoлoжитe;u.ныe
пациенты, не ответившие на монотерапию интерфероном, пациенты после
трансплантации печени при хронической инфекции вирусом гепатита В,
пациенты, у которых есть противопоказания к назначению интерферона.
Несмотря на положительные стороны терапии аналогами ргуклеозидов, суше-
ствует достаточно высокая вероятность мутаций в геноме вируса гепатита В,
приводяшдх к резистентности в отношении этих препаратов. Большая часть
мутаций, вызванных лекарственной тератгией, происходит в гене обратной
транскриптазы (рис. 33.5). Разные аналоги нуклеозидов вызывают мутации в
типичных локусах (А, В, С, D, Е). Мутация YMDD, обнаруженная у нашего
пациента, расположена в локусе С. Она связана с развитием резистентіюсти к
ламивудин>' Наименьшее количество м>таций вызывает новый перспектив¬
ный препарат тенофовир.По данным К.ЛЇШИЧЄСКИХ исследований, эффективность (оценивалась по
наступлению сероконверсии) наиболее распространенных аналогов нуклео¬
зидов распределяется следующим образом: адефовир — 12%, ламивудин —
18%, энтекавир — 21%.Недавно завершилось клиническое исследование по сравнению эффектив¬
ности ламивудина и телбивудина {табл. 33.4). В нем принимали участие
921 НВ^-положительных пациентов и 446 НВ^-негативных. Пациенты
получали препараты ежедневно в соответствующей терапевтической дозеTerminProtei(TP)rtL80V/lrtV84MrtV173LІІА181ТЛ/rtl169Trtl164TrtL180MHS184GrtA181T/VrtM204V/l/SrtQ215SrtS202l/GrtV214ALMVrADVrETVrTDFrРис. 33.5, Мутации вируса гепатита В, вызванные противовирусными препаратами.
Пояснения в тексте
686ГастроэнтерологияСравнительная характеристика телбивудина и ла.мивудинаТаблица 33.4ПараметрТелбивудин,%Ламивудин, %ЭффективностьHBeAg+6348HBcAg-7866CepOKQHверсия29,624,7Развитие резистентности10,825.9Побочные эффекты (повышение актив-
ности креатининфосфокиназы) 12,94,1на протяжении 2 лет. Эффективность оценивалась по снижению вирусной
нагрузки и сероконверсии и^іи нормализации биохимических показателей
(у НВ^-негативных пациентов). Очевидна большая эффективность телби¬
вудина по сравнению с ламивудином как у НВ^-положительных пациен¬
тов, так и у НВ^-негативных. Сероконверсия также наблюдалась чаще при
назначении телбивудина, а устойчивость к нему развивалась реже больше
чем в 2 раза. Однако у этого препарата отмечена большая частота побочных
эффектов.В настоящее время клинические испытания проходит большое количество
препаратов. На 3-й стадии испытаний находятся два препарата; эмтрииита-
бин и клевудин (в Южной Корее одобрен с 2006 г., коммерческое название —
левовир). На клевудин возлагают большие надежды, потому что он обла¬
дает уникальным свойством: противовирусный эффект сохраняется после
окончания терапии. В США и Европе в этом году бьит допушен к широкому
применению тенофовир (вирид). Поскольку препарат совсем новый, данных
о его применении не представлено.Таким образом, терапевтические возможности и перспективы в отношении
хронического гепатита В весьма обширны. Это позволяет осуществлять
индивидуальный подбор препаратов с учетом картины заболевания и доби¬
ваться высоких результатов, что и было продемонстрировано на конкретном
клиническом примере.
КЛИНИЧЕСКИЕ
РАЗБОРЫВ ФАКУЛЬТЕТСКОЙ
ТЕРАПЕВТИЧЕСКОЙ
КЛИНИКЕ
им. В.Н. ВИНОГРАДОВАРЕДКИЕ И ДИАГНОСТИЧЕСКИ ТРУДНЫЕ
ЗАБОЛЕВАНИЯ В КЛИНИКЕ ВНУТРЕННИХ БОЛЕЗНЕЙПод РЕДАКЦИЕЙ В.А. Сулимова, О.В. БлаговойКнига представляет собой сборник клинических разборов, проходивших в
Факультетской терапевтической клинике им. В.Н. Виноградова на протяжении
последних лет. Каждая из 33 глав состоит из подробного описания клиниче¬
ского случая, изложения современного теоретического материала, который
привлекался врачами в процессе постановки диагноза, определения тактики и
оценки результатов лечения, а также из комментариев (нередко полемичных)
сотрудников клиники и приглашенных специалистов (нефрологов, гематоло¬
гов, кардиохирургов, генетиков и др.).Клинические разборы отражают все традиционные направления работы
клиники (пульмонология, кардиология, гастроэнтерология, ревматология, от¬
части гематология). Вместе с тем они объединены единством подхода к боль¬
ному, который, по ГА. Захарьину, подразумевает «достижение связи всех яв¬
лений данного болезненного строя». Представлялось важным сохранить все
нюансы диагностического поиска. Многие из представленных в книге случаев
уникальны: но и при относительно нередких заболеваниях индивидуализация
особенностей пациента делает разборы интересными и поучительными. Осо¬
бенностями разборов в целом стали заметное преобладание инфекционной,
иммунной и генетической патологии и широкое использование прижизненной
морфологической диагностики.Издание адресовано студентам старших курсов, начинающим врачам, ин¬
тернам и клиницистам различных специальностей.