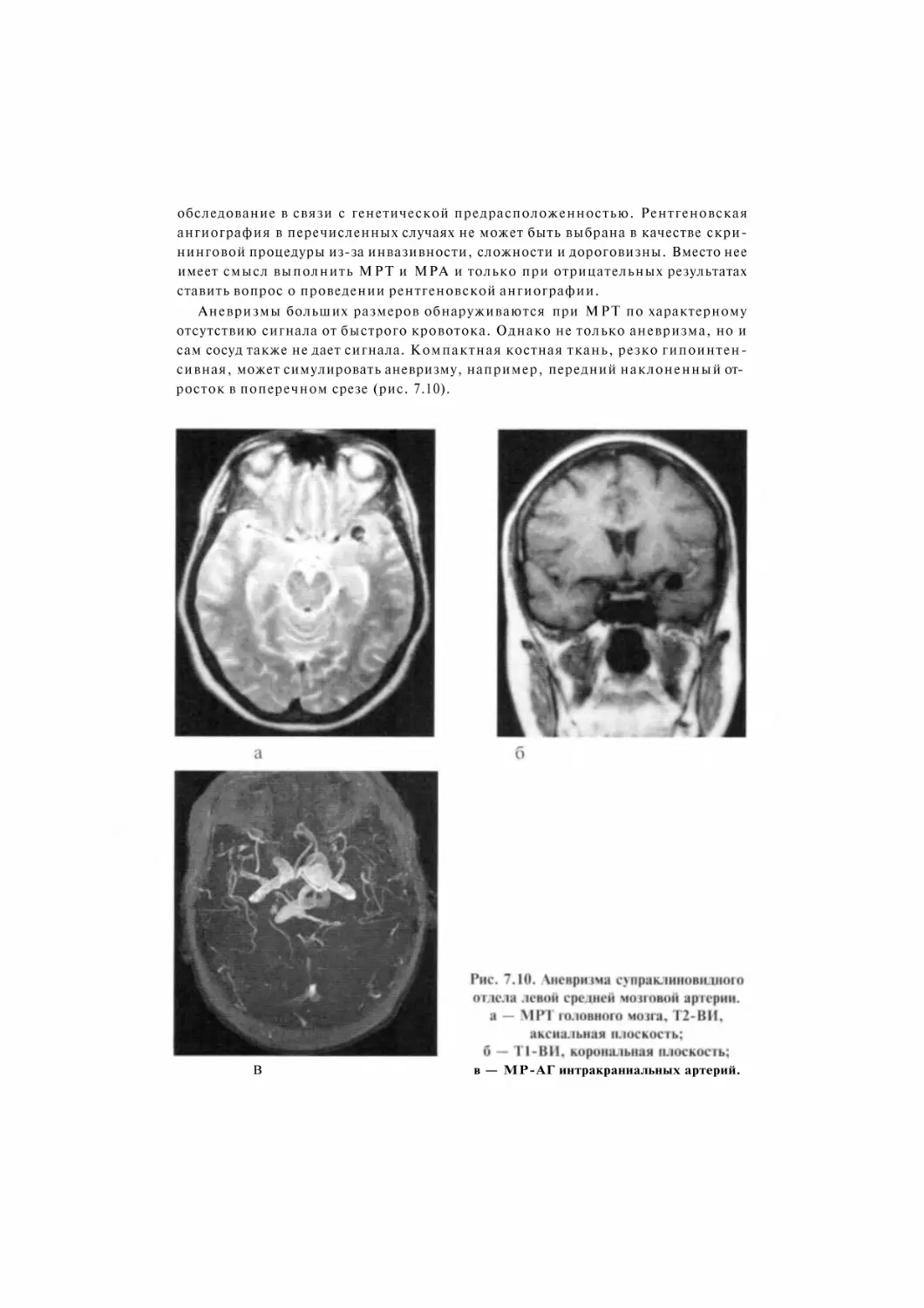
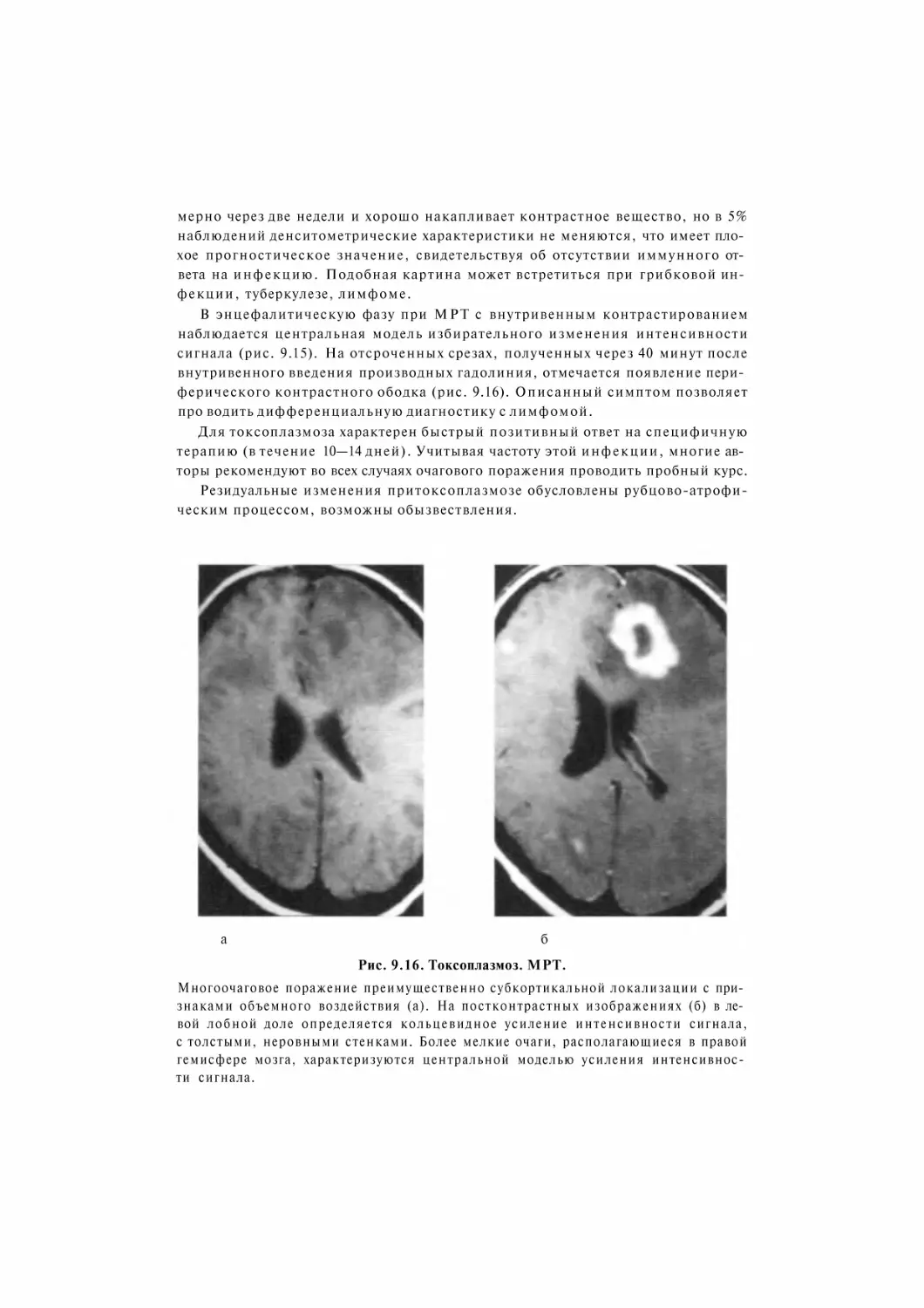
Author: Трофимовой Т.Н. Ананьева Н.И. Назинкина Ю.В. Карпченко А.К. Халиков А.Д.
Tags: нервная система невропатология неврология патология сердечно-сосудистой системы сердечно-сосудистые заболевания алкоголизм как болезнь нейрохирургия психиатрия внутренние болезни радиология нейрорадиология издательский дом спбмапо
Year: 2005
НЕЙРОРАДИОЛОГИЯ
Под редакцией Т.Н.Трофимовой
Санкт П етербург
Издательский дом СПбМАПО
2005
ББК 56.12:54.10
Н46
УДК 616.8:616.12
Нейрорадиология / Под ред. Т.Н.Трофимовой.--- СПб.: Издательский дом
СПбМАПО, 2005. 288 с, ил.
Авторы:
Трофимова Татьяна Николаевна, д р мед. наук, профессор, заведующая кафед-
рой рентгенологии, проректор по научной и издательской работе Санкт
Петербургской медицинской академии последипломного образования, главный
специалист по лучевой диагностике МЦ ФГУП «Адмиралтейские верфи»;
Ананьева Наталия Исаевна, д р мед. наук, профессор кафедры рентгенологии
Санкт Петербургской медицинской академии последипломного образования,
заведующая отделением лучевой диагностики Санкт Петербургского научно
исследовательского психоневрологического института им. В.М.Бехтерева;
Карпенко Алла Красовна, канд. мед. наук, доцент кафедры рентгенологии Санкт
Петербургской медицинской академии последипломного образования, заведу-
ющая отделением лучевой диагностики Ленинградской детской областной кли-
нической больницы;
На шика на Юлия Викторовна, канд. мед. наук, доцент кафедры рентгенологии
Санкт Петербургской медицинской академии последипломного образования;
Халиков Азиз Джауланович, канд. мед. наук, ассистент кафедры рентгенологии
Санкт Петербургской медицинской академии последипломного образования.
Рецензент --- начальник Главного госпиталя МВД, лауреат Государственной
премии, заслуженный деятель науки РФ, член корреспондент РАМН, профес-
сор А.Ю.Васильев.
Авторы выражают признательность за финансовую поддержку издания фирме
«Nycomed Amersham».
В монографии обобщен опыт лучевой диагностики аномалий развития голов-
ного мозга, черепно мозговой травмы, гидроцефалии различной этиологии, демие
линизирующих поражений, цереброваскулярных заболеваний, нейроинфекции.
Детально представлена нормальная анатомия головного мозга в лучевом изображе-
нии, а также нейрорадиология комы. Освещены вопросы дифференциальной ди-
агностики очаговых поражений головного мозга.
Книга предназначена для рентгенологов, врачей лучевой диагностики, невро-
патологов, нейрохирургов, педиатров, представителей смежных специальностей,
студентов медицинских вузов. Монография может быть рекомендована для подго-
товки в рамках системы последипломного профессионального образования.
На первой странице обложки --- Жак Линар (1600 1645) «Vanitas» (Суета сует), холст, масло.
ISBN 5 98037 044 7
© Коллектив авторов, 2005 г.
© Издательский дом СПбМАПО, 2005 г.
ОГЛАВЛЕНИЕ
Предисловие
7
Список сокращений
8
Глава 1
.ТУЧЕВАЯ АНАТОМИЯ ГОЛОВНОГО МОЗГА И ЧЕРЕПА
9
Анатомо физиологические особенности мозга новорожденного
10
Лучевое исследование головного мозга новорожденного
11
Изображение головного мозга новорожденного при нейросонографии
(совместно с А.Б.Овчаренко)
11
Изображение мозга новорожденного при компьютерной томографии
13
Изображение головного мозга новорожденного
при магнитно резонанасной томографии
13
Лучевая анатомия задней черепной ямки
15
Лучевая анатомия супратенториальных отделов головного мозга
23
Лучевая анатомия турецкого седла
31
Анатомия сосудов головного мозга и их изображение
при лучевых ангиографических исследованиях
33
Артерии головного мозга
33
Вены головного мозга
40
Глава 2
ИСПОЛЬЗОВАНИЕ МАГНИТНО РЕЗОНАНСНОЙ ТОМОГРАФИИ
В ОЦЕНКЕ СОСТОЯНИЯ ГОЛОВНОГО МОЗГА ПЛОДА
В АНТЕНАТАЛЬНОМ ПЕРИОДЕ
43
Показания к проведению магнитно резонансной томографии
в антенатальном периоде
43
Противопоказания кпроведению магнитно резонансной томографии
в антенатальном периоде
44
Формирование коры головного мозга плода
45
Методики проведения магнитно резонансной томографии плода
46
МРТ диагностика аномалий развития головного мозга
в антенатальном периоде
47
Глава 3
АНОМАЛИИ РАЗВИТИЯ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ
52
Развитие центральной нервной системы
52
Аномалии развития центральной нервной системы
54
Классификация врожденных пороков развития головного мозга
54
I. Нарушения органогенеза
55
Нарушение закрытия нейрональной трубки
55
Аном&чии Арнольда --- Киари
56
Кисты задней черепной ямки
60
Ретроцеребеллярная киста
62
Кистозная трансформация IV желудочка
62
Mega cisterna magna
62
Аномалии мозолистого тела
62
Кисты средней линии
65
Нарушение дивертикуляции
68
Нарушения формирования извилин и клеточной миграции
(мальформации кортикального развития)
70
Аномалии размеров
84
Деструктивные изменения
85
Обструктивные изменения
86
II. Нарушения гистогенеза
86
Нейрофиброматозы
86
Туберозный склероз
88
Ангиоматоз центральной нервной системы
(болезнь Гиппеля --- Линдау)
89
Опухолевидные образования
90
Кистозные образования
90
Глава 4
ГИДРОЦЕФАЛИЯ
94
Окклюзионные гидроцефалии
102
Открытые (сообщающиеся) гидроцефалии
105
Глава 5
НЕЙРОРАДИОЛОГИЯ КОМЫ
109
Кома и ограничения резервных пространств
115
Кома и нейрональное повреждение
123
Кома и аксональное повреждение
126
Кома и синаптическая недостаточность
129
Глава 6
ЧЕРЕПНО МОЗГОВАЯ ТРАВМА
132
Переломы костей черепа
132
Линейные переломы
133
Вдавленные переломы
134
Фронтобазальные переломы
135
Внутричерепные кровоизлияния
135
Эпидуральная гематома
135
Субдуральная гематома
138
Ушибы головного мозга
144
Глава 7
СОСУДИСТЫЕ ЗАБОЛЕВАНИЯ ГОЛОВНОГО МОЗГА
152
Пороки сосудов головного мозга
153
Терминология
153
Классификация
154
Кавернозные и промежуточные ангиомы
154
Телеангиоэктазии
157
Венозные мальформации
158
Артериовенозные мальформации
159
Факоматозы
162
Персистируюшие сосуды
165
Аневризматическая болезнь
166
Алгоритм обследования пациентов
169
Нарушения мозгового кровообращения
172
Применение методов нейровизуализации в диагностике ишемических
инсультов
174
КТ и МРТ диагностика ишемических инсультов
180
Расслоение артерий (артериальные диссекции)
197
Венозные инфаркты
197
Этиология и патогенез геморрагических инсультов
199
Применение методов нейровизуализации в диагностике
геморрагического инсульта
199
Инсульты у наркоманов
204
Этиология, патогенез и диагностика субарахноидальных
кровоизлияний
205
Этиология и патогенез хронической недостаточности мозгового
кровообращения. Роль методов лучевой диагностики в выявлении
и изучении хронической недостаточности мозгового кровообращения ... 206
Глава 8
ДЕМИЕЛИНИЗИРУЮЩИЕ ЗАБОЛЕВАНИЯ ЦЕНТРАЛЬНОЙ
НЕРВНОЙ СИСТЕМЫ (совместно с Н.А. Тотолян и Е.А. Трофимовым) 212
Лучевые проявления демиелинизирующих заболеваний ЦНС
218
Рассеянный склероз
218
МРТ проявления других демиелинизирующих заболеваний ЦНС
229
МРТ проявления системных аутоиммунных заболеваний
и других васкулопатий
245
Глава 9
ИНФЕКЦИОННЫЕ ЗАБОЛЕВАНИЯ ГОЛОВНОГО МОЗГА
249
Лучевая семиотика менингитов
251
Лучевая семиотика осложнений менингита
253
Лучевая семиотика энцефалитов (совместно с Е.Ю.Гореликом)
254
Лучевая семиотика абсцесса
258
Лучевая семиотика вентрикулита
260
Лучевая семиотика васкулитов
261
Лучевая семиотика нейротуберкулеза
261
Диагностика и дифференциальная диагностика поражений центральной
нервной системы у ВИЧ инфицированных и больных СПИДом
264
Глава 10
ЛУЧЕВАЯ ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ОЧАГОВЫХ
ПОРАЖЕНИЙ ГОЛОВНОГО МОЗГА
274
Заюиочение
284
ПРЕДИСЛОВИЕ
Современная клиническая медицина не мыслима без адекватной диагности-
ки, в которой достойное место занимают методы визуализации. Бурное разви-
тие информационных технологий обеспечило стремительный прогресс лучевой
диагностики --- процесс, продолжающийся и ныне. Это в полной мере относит-
ся к нейрорадиологии. В настоящее время сложились устойчивые представле-
ния о лидерах диагностических технологий в контексте конкретных нозологии,
корректном использовании новой техники, лучевой семиотике разнообразных
неврологических и нейрохирургических состояний.
За прошедшие годы появились замечательные книги по лучевой диагности-
ке, но и сегодня ситуацию с профессиональной литературой по нейровизуали-
зации можно оценить как достаточно сложную.
В основу предлагаемой монографии положен многолетний опыт работы в ней
рорентгенологии, рожденный втесном содружестве с нейрохирургами, невроло-
гами, нейрореаниматологами, педиатрами, представителями других смежных
специальностей. Авторы старались отразить насущные потребности клиничес-
кой практики. Этим обусловлено появление актуальных и, в определенной сте-
пени, спорных глав, посвященных лучевой диагностике аномалий развития,
в том числе МРТ плода, демиелинизирующих процессов, нейроинфекций, це
реброваскулярных заболеваний. С другой стороны, очевидна важность посто-
янного повторения, казалось бы, азбучных истин лучевой анатомии, семиотики
гидроцефалии, паттернов дислокаций и т. д. Авторы сознательно не касались
вопросов нейроонкологии. Нам кажется, что целая серия прекрасных книг, вы-
шедших из под пера, прежде всего, сотрудников отдела лучевой диагностики ин-
ститута им. Н.Н.Бурденко, сегодня весьма удачно заполняет эту нишу.
Мы внимательно отнеслись к использованию литературного материала, по-
стоянно сопоставляя его с личным опытом.
В заключение считаем своим долгом выразить благодарность коллегам из
Санкт Петербургской медицинской академии последипломного образования за
бесценную помощь, оказанную в подготовке рукописи и иллюстративного ма-
териала.
Авторы надеются, что это руководство будет полезно лучевым диагностам,
невропатологам, нейрохирургам, представителям смежных специальностей,
а также окажет помощь студентам медицинских вузов. Мы с благодарностью
примем критические замечания и постараемся их использовать в дальнейшей
работе.
Профессор Т.Н.Трофимова
СПИСОК СОКРАЩЕНИЙ
ABM
--- артериовенозные мальформации
АГ
--- артериальная гипертензия
БГА
--- бифуркационно гемодинамические аневризмы
ВЖК
--- внутрижелудочковое кровоизлияние
ВИ
--- взвешенное изображение
ВИЧ
--- вирус иммунодефицита человека
ВСА
--- внутренняя сонная артерия
ГЭБ
--- гематоэнцефалический барьер
ДСА
--- дигитальная субтракционная ангиография
ДЭ
--- дисциркуляторная энцефалопатия
ед.Х
--- единицы Хаунсфилда
ЗСА
--- задняя соединительная артерия
ИЛ
--- интерлейкины
ИП
--- импульсная последовательность
ИС
--- интенсивность сигнала
KB
--- контрастирующее вещество
КТ
--- рентгеновская компьютерная томография
MРА
--- магнитно резонансная ангиография
МРТ
--- магнитно резонансная томография
МЦР
--- микроциркуляторное русло
HMК
--- нарушение мозгового кровообращения
НСА
--- наружная сонная артерия
ОДЭ
--- острый диссеминированный энцефалит
ОДЭМ
--- острый диссеминированный энцефаломиелит
ОНМК --- острое нарушение мозгового кровообращения
ОСА
--- общая сонная артерия
ОФЭКТ --- однофотонная эмиссионная компьютерная томография
ОФЭТ
--- однофотонная эмиссионная томография
ПА
--- позвоночная артерия
ПМА
--- передняя мозговая артерия
ПМГ
--- полимикрогирия
ПСА
--- передняя соединительная артерия
ПЭТ
--- позитронно эмиссионная томография
PC
--- рассеянный склероз
САК
--- субарахноидальное кровоизлияние
СМ
--- сосудистые мальформации
СМА
--- средняя мозговая артерия
СПИД --- синдром приобретенного иммунодефицита
Т1 , Т2 ВИ --- TI , Т2 взвешенные изображения
ТИА
--- транзиторная ишемическая атака
ТИКБ
--- тотальный инсульт в каротидном бассейне
ТКДГ
--- транскраниальная допплерография
УЗИ
--- ультразвуковое исследование
ФКД
--- фокальная кортикальная дисплазия
ЦМВ
--- цитомегаловирусная инфекция
ЦНС
--- центральная нервная система
ЦСЖ
--- цереброспинальная жидкость
ЧМТ
--- черепно мозговая травма
FLAIR, 1R, SPGR^n, GRE--- варианты импульсных последовательностей
Ig
--- иммуноглобулины
Т
--- тесла, единица напряженности магнитного поля
Глава 1
ЛУЧЕВАЯ АНАТОМИЯ ГОЛОВНОГО МОЗГА
И ЧЕРЕПА
До открытия Рентгена анатомия была наукой о строе-
нии мертвых элементов. В свете рентгеновских лучей она
стала анатомией на живом для живого.
В. В. Тонкое
В те времена, когда медицина базировалась преимущественно на результа-
тах физикального обследования человека, наименее доступным оставался го-
ловной мозг, скрытый черепной коробкой. Применение компьютерной (КТ) и
магнитно резонансной томографии (МРТ) совершило переворот в медицине,
позволив объективно оценивать состояние вещества головного мозга. Эти мето-
ды объединены понятием нейровизуализации. Их использование позволяет от-
ветить на вопрос: есть ли изменения и где они локализуются, оценить состояние
ликворсодержащей системы и прилегающих к патологическому очагу тканей
и, наконец, определить природу патологического процесса. Ответить на постав-
ленные вопросы невозможно без знания нормальной лучевой анатомии голов-
ного мозга. С учетом особенностей морфологии и физиологии головного мозга
отдельно описана лучевая анатомия задней черепной ямки и структур, лежащих
выше намета мозжечка.
Из лучевых методов диагностики в настоящее время достаточно широко при-
меняются ультразвуковое исследование головного мозга (нейросонография), КТ,
М РТ. Эти методы, имея свои достоинства и недостатки, взаимно дополняют друг
друга. В арсенале отделения лучевой диагностики многопрофильной больницы
наиболее целесообразно применение всех вышеперечисленных методик. Реше-
ние о выборе метода в каждом конкретном случае принимается коллегиально
врачом клиницистом и врачом лучевой диагностики.
Достоинствами нейросонографии являются доступность, простота приме-
нения, возможность использования у постели больного, отсутствие необходи-
мости в специальной предварительной подготовке. Однако результаты
нейросонографии существенно зависят от профессионализма исследователя,
качества применяемой аппаратуры. Высока степень субъективности оценки
получаемых данных. Несмотря на это, УЗИ головного мозга до сих пор явля-
ется основным методом диагностики у новорожденных и детей раннего воз-
раста.
КТ позволяет выявить патологию, более точно оценить динамику поврежде-
ния головного мозга. Из недостатков КТ следует отметить действие ионизирую-
щего излучения на пациента во время исследования, а у детей раннего возрас-
та --- необходимость применения анестезиологического пособия.
MPT становится все более доступным методом лучевой диагностики, позво-
ляя наиболее полно оценить процессы развития мозга новорожденного, выявить
изменения и уточнить динамику течения заболевания. Это единственный метод,
позволяющий наблюдать за процессами миелинизации головного мозга. Одна-
ко проведение МРТ предъявляет особые требования к материлам, помещаемым
в рабочую зону магнита, требует специального оборудования для обследования
больных, находящихся в реанимации, занимает много времени, у детей раннего
возраста требует анестезиологического пособия.
АНАТОМО ФИЗИОЛОГИЧЕСКИЕ ОСОБЕННОСТИ МОЗГА
НОВОРОЖДЕННОГО
Головной мозг новорожденного относительно велик, его масса составляет 10%
от массы тела, в то время как у взрослого человека она не превышает 2---2,5%.
Крупные борозды и извилины выражены очень хорошо, но имеют малую глуби-
ну. Мелких борозд мало, они появляются только в первые годы жизни. Размеры
лобной доли меньше, чем у взрослых, а затылочной, наоборот, больше. Мозже-
чок развит слабо, характеризуется малой толщиной, небольшими размерами по-
лушарий и поверхностными бороздами. Боковые желудочки крупные, представ-
ляются растянутыми. Твердая мозговая оболочка у новорожденных тонкая, ее
наружный листок на большой площади сращен с костями черепа. Венозные
пазухи тонкостенные и уже, чем у взрослых. Мягкая и паутинная оболочки моз-
га тонкие, субдуральное и субарахноидальное пространства узкие. Цистерны,
расположенные на основании мозга, напротив, относительно крупные. Водопро-
вод мозга шире, чем у взрослых. К моменту рождения мозг содержит около 88%
воды, к 2 годам этот показатель снижается до 82%. Одновременно растет кон-
центрация липидов. Процесс миелинизации (формирования миелиновой мемб-
раны вокруг аксона) к моменту рождения не завершен. Наиболее миелинизиро
ваны проводящие пути спинного и продолговатого мозга.
Развитие нервных путей и окончаний идет центростремительно, в цефалока
удальном направлении и поэтапно, в строгом соответствии с биологическим
возрастом ребенка. Базальные ганглии составляют гораздо большую часть моз-
га у недоношенного ребенка, чем у доношенного, и развиваются раньше коры
головного мозга и белого вещества.
Ткань субэпендимального терминального матрикса, расположенного пер-
воначально над головкой и телом хвостатого ядра, в основном снабжается
кровью артерией Гюбнера с дополнительным кровоснабжением из конечных
ветвей латеральных стриарных и хориоидных артерий. Артерия Гюбнера и
хориоидные артерии имеют особенно большой диаметр у недоношенных. В 80%
случаев интравентрикулярные геморрагии связаны с терминальным матрик
сом. Субэпендимальный матрикс содержит незрелую сосудистую сеть, кото-
рая, начиная с 32 й недели гестации, преобразуется во вполне развитое капил-
лярное ложе. В это время роль артерии Гюбнера снижается до кровоснабжения
маленькой области головки хвостатого ядра.
ЛУЧЕВОЕ ИССЛЕДОВАНИЕ ГОЛОВНОГО МОЗГА НОВОРОЖДЕННОГО
Изображение головного мозга новорожденного
при нейросонографии
Нейросонография, благодаря своей простоте, доступности и качеству полу-
чаемого изображения, является оптимальной методикой для выявления структур-
ных изменений головного мозга детей на раннем этапе обследования.
Как при всяком ультразвуковом исследовании, все видимые структуры го-
ловного мозга по эхогенности можно подразделить на гипер , гипо , изо и ан
эхогенные. Наиболее яркими --- гиперэхогенными --- выглядят кости черепа. Со-
судистые сплетения желудочков также гиперэхогенны. Особенно хорошо лоци
руются сплетения боковых желудочков, которые, распространяясь в теле,
височном роге и области треугольника бокового желудочка, при сканировании
в сагиттальной плоскости формируют «фигуру перстня». При исследовании во
фронтальной и аксиальной плоскостях сплетения отчетливо визуализируются
в виде ярких линейных структур на фоне анэхогенной --- темной --- спинномоз-
говой жидкости в желудочках. Форма и симметричность сосудистых сплетений
имеют большое диагностическое значение. Утолщение одного из них по отно-
шению к другому позволяет заподозрить внутрижелудочковое кровоизлияние
(ВЖК). Кисты сосудистых сплетений также являются нередкими находками
у новорожденных --- 3% по данным Т.ШеЬе1 (1992).
Червь мозжечка, стенки мозговых артерий также определяются как гиперэхо
генные образования. Ярким выглядит и рисунок борозд, обусловленный мягкой
мозговой оболочкой. Само серое вещество выглядит гипоэхогенным, и яркие бо-
розды контурируют извилины большого мозга, формируя рисунок коры. В виде
гипоэхогенных образований представлены полушария мозжечка и стволовые
структуры. Подкорковые ядра имеют несколько большую акустическую плотность
по сравнению с окружающим белым веществом. При получении срединного изоб-
ражения в сагиттальной плоскости отчетливо визуализируется гипоэхогенное мо-
золистое тело, четко отграниченное от серого вещества коры гиперэхогенной пе
рикаллезной цистерной. Здесьже определяются структуры, расположенные строго
по средней линии: III желудочек, водопровод мозга, IV желудочек. Пространства,
заполненные спинномозговой жидкостью, а именно желудочки мозга, большая
цистерна, субарахноидальные пространства по конвекситальной поверхности
мозга, видны как анэхогенные образования. Исключением являются цистерны
основания мозга, которые при сканировании в аксиальной плоскости формируют
типичный гиперэхогенный рисунок. Эти ликворосодержащие пространства на-
ряду со спинномозговой жидкостью содержат пульсирующие артерии артериаль-
ного круга мозга, которые обусловливают высокую гиперэхогенность и значитель-
но улучшают визуализацию гипоэхогенных структур среднего мозга --- пласти-
ны четверохолмия, ножекмозга, водопровода, который представлен двумя тонкими
короткими полосками, параллельными друг другу.
Рисунок базальных цистерн дополняет расположенная над одноименной пла-
стиной четверохолмная цистерна, которая сзади ограничена верхними отдела
ми червя мозжечка, а по бокам --- краями вырезки намета мозжечка. Огибая
с обеих сторон средний мозг, она переходит в охватывающую цистерну, которая
располагается между латеральными краями среднего мозга и парагиппокам
пальными извилинами, сливаясь затем между ножками мозга в межножковую
цистерну. Передняя часть межножковой цистерны окружает изоэхогенную моз-
гу воронку гипофиза с рисунком инфундибулярного кармана III желудочка в виде
двух тонких гиперэхогенных полосок с анэхогенным промежутком между ними,
который соответствует изображению спинномозговой жидкости III желудочка.
Кпереди от межножковой цистерны располагается перекрест зрительных нервов,
также окруженный ликворсодержашим пространством, которое носит название
супраселлярной цистерны. Цистерна латеральной щели отделяет задние опер
кулярные отделы лобной доли от передних отделов височной доли.
Ультразвуковое исследование проводится в режиме реального времени и по-
зволяет визуализировать пульсирующие сосуды головного мозга. При скани-
ровании в аксиальной плоскости в области охватывающей цистерны можно уви-
деть заднюю мозговую артерию, латеральнее воронки гипофиза отмечаются
поперечные сечения сонных артерий, между ножками мозга --- поперечник ба
зилярной артерии. При сканировании во фронтальной плоскости в проекции
латеральных щелей мозга четко визуализируются пульсирующие средние моз-
говые артерии, а в передних отделах межполушарной щели --- передние мозго-
вые артерии.
Следует отметить, что при чрезродничковом сканировании у детей первого
месяца жизни перивентрикулярное белое вещество в проекции треугольников
боковых желудочков может выглядеть гиперэхогенным. Это изображение в ли-
тературе носит название перивентрикулярного «halo» (Grant Е., 1983), илиоко
лотреугольникового «blush» (Di Pietro М.А., 1986). Эти феномены пытаются
объяснить большим содержанием макромолекул воды в мозге новорожденного из
за незавершенного процесса миелинизации, а также возможными артефактами
отражения ультразвукового луча от сосудистых сплетений, расположенных в тре-
угольниках боковых желудочков. Данное изображение следует дифференциро-
вать от гипоксически ишемического поражения белого вещества --- перивентри
кулярной лейкомаляции, которое на раннем этапе характеризуется гиперэхоген
ными зонами, чаще всего в районе передних рогов и треугольников боковых
желудочков. Ведущую роль при этом играет неврологическая симптоматика.
При нейросонографии обязательно измеряют ширину внутренних ликворсо
держащих пространств. Чаще всего в практической деятельности пользуются схе-
мой измерения, которая была предложена M.S.Leven (1985). Измерение осуществ-
ляется при сканировании во фронтальной плоскости на уровне отверстий Мон-
ро. Здесь измеряют ширину боковых желудочков --- как расстояние от средней
линии до самой латеральной точки желудочка (13 мм), косой размер --- как дис-
танцию между самой выпуклой и самой вогнутой точками передних рогов (2 3 мм),
и ширину 111 желудочка (до 4 мм). Допускается незначительная (в пределах 2 мм)
асимметрия боковых желудочков. Между передними рогами может лоцировать
ся полость прозрачной перегородки, ширина которой у доношенного ребенка не
должна превышать 2 мм. У недоношенных детей она, как правило, шире и требу
ет мониторирования, так как в случае ее роста, из за сдавливания отверстий Монро,
может развиться бивентрикулярная гидроцефалия.
Изображение мозга новорожденного
при компьютерной томографии
Картина мозга новорожденного при КТ и МРТ значительно отличается от
картины мозга детей других возрастных периодов и взрослых.
Поскольку мозг новорожденного содержит относительно много воды и мало
липидов, то плотность мозговой ткани новорожденного при КТ меньше и повы-
шается с возрастом (табл. 1.1).
Таблица 1.1
Плотность мозговой ткани при компьютерной томографии
в различные возрастные периоды (ед.)
Возрастной
период
Белое
веществ
0
Белое вещество
после
внутривенного
контрастирования
Серое
вещество
Серое вещество
после
внутривенного
контрастирования
Недоношен-
ные
16
---
28.3
---
0 2 года
26,3
28,5
32,7
36 37
2 15 лет
29,2
31
35,6
38 39
Разница в плотности между белым и серым веществом в любом возрасте бо-
лее 10 ед. должна рассматриваться как патология. Бол ьшая цистерна мозга у но-
ворожденных имеет значительные размеры и составляет от 2 мм до 9--- 10 мм, в за-
висимости от индивидуальных особенностей. На обычных компьютерных то-
мограммах, а особенно на постконтрастных изображениях задней черепной ямки,
в некоторых случаях хорошо видны лентовидные уплотнения поперечного и сиг-
мовидного синусов. Величина их индивидуальна у разных детей, встречается
асимметрия правой и левой сторон. При значительном расширении венозных
коллекторов можно заподозрить сосудистую патологию и рекомендовать про-
ведение ангиографического исследования.
Ширина 111 желудочка составляет 2---4 мм, боковых желудочков --- 6 мм. Су
барахноидальные щели конвекситальной поверхности мозга шире (около 2 мм),
но менее глубоки. Латеральные и межполушарная щели также более широкие и
короткие.
Изображение головного мозга новорожденного
при магнитно резонанасной томографии
Различие изображений серого и белого вещества на Т1 ВИ определяется раз-
личными временами их релаксации. Серое вещество гиперинтенсивно по срав
нению с белым. По мере развития мозга уменьшается количество воды и соот-
ветственно --- время релаксации серого вещества, оно становится гипоинтенсив
ным по отношению к белому. Изображение спинномозговой жидкости гипоин
тенсивное. На Т2 ВИ изображение мозга противоположно изображению на Т1
ВИ (серое вещество и спинномозговая жидкость гиперинтенсивны).
Миелинизация --- это динамический процесс, который начинается с наибо-
лее древних структур. Такие старые в филогенетическом отношении отделы, как
ствол мозга, обычно полностью миелинизированы кмоменту рождения. Кора,
напротив, демонстрирует наибольшие изменения в течение первых двух лет жиз-
ни, в связи с тем, что часть волокон осталась немиелинизированной в период
нормального внутриутробного развития.
R.B.Dietrich описал три стадии процесса миелинизации.
1 я стадия --- младенческая --- от момента рождения до 6 го месяца жизни,
характеризуется более интенсивным сигналом от белого вещества головного
мозга по сравнению с серым веществом коры. Это взаимоотношение является
обратным изображению мозга у взрослых.
2 я стадия --- от 8 го до 12 го месяца --- является переходной, интенсивность
сигнала от белого и серого вещества практически одинакова.
В 3 й --- взрослой стадии --- выделяют раннюю взрослую. Она длится от 10 го
до 31 го месяца жизни, и в этот период миелинизация представляется в основ-
ном завершенной, за исключением области семиовальных центров.
К. Flechsig в 1920 г. предположил, что процесс миелинизации осуществля-
ется в определенной последовательности, в зависимости от функции соответ-
ствующих отделов белого вещества. Начинается он с чувствительных или аф-
ферентных путей, затем переходит на эфферентные пути, распространяясь от
коры к подкорковым зонам. Заканчивается процесс миелинизацией ассоци-
ативного пути.
Процесс распространяется с каудального в краниальном и с дорсального
в вентральном направлении таким образом, что затылочные зоны миелинизи
руются раньше, чем лобные, а ствол мозга --- раньше, чем полушария.
В первую очередь созревают основные чувствительные пути. Если к моменту
рождения в продолговатом мозге, дорсальных отделах среднего мозга и мозжеч-
ке наблюдаются незначительные признаки миелинизации, то к 3 месяцам моз-
жечок уже имеет характерное для взрослого изображение, хотя процесс созрева-
ния в его полушариях еще продолжается. Появление признаков миелинизации
в задней части внутренней капсулы и уменьшение интенсивности сигнала вок-
руг нее может быть расценено как завершение процесса в этой зоне. Вслед за этим
в течение 2---3 месяцев появляются признаки зрелости передних отделов внут-
ренней капсулы. Большинство описанных изменений встречаются на Т1 ВИ.
НаТ2 ВИ интенсивность сигнала от большинства глубоко идущих проводящих
путей снижается в возрасте 6--- 12 месяцев, при этом процесс созревания продол-
жается в направлении от задних отделов мозга к передним.
Оценивая структуры внутренней капсулы, можно сказать, что задний лимб
созревает к 10 му, а передний --- к 11 му месяцам жизни. Мозолистое тело также
созревает в направлении от задних отделов мозга к передним. Очевидные при
знаки миелинизации задних отделов видны к 6 му месяцу, а колена --- к 8 му
месяцу жизни.
В семиовальных центрах отмечаются наиболее отсроченные изменения ин-
тенсивности сигнала, что может быть обнаружено в течение первого и второ-
го десятилетий жизни. Эта зона характеризуется большим количеством ней-
ронов, вовлеченных в ассоциативный путь. Она может сохранять высокую ин-
тенсивность сигнала и в 20 лет, что должно быть расценено как норма, а не
демиелинизирующий процесс. В оценке развития белого вещества головного
мозга наиболее значимыми являются изменения, которые происходят в тече-
ние первых двух лет жизни, позже --- с 3 до 20 лет --- отслеживается лишь не-
значительная динамика.
С точки зрения химического процесса созревание белого вещества заключа-
ется в том, что аксоны накапливают холестерол и гликолипиды в своей нейт-
ральной оболочке. Эта оболочка, защищенная олигодендроцитами, крайне гид-
рофильна и связывает свободную воду. Количество молекул свободной воды
уменьшается, изменяется время релаксации и уменьшается интенсивность сиг-
нала наТ1 иТ2 ВИ.
Подводя итог вышесказанному, следует еще раз уточнить, что от момента
рождения до 4---6 го месяцев жизни интенсивность сигнала от белого вещества
является обратной той, которая типична для головного мозга взрослых. После
переходной изоинтенсивной стадии определяется сначала ранняя взрослая ста-
дия изображения головного мозга, и лишь за ней --- взрослая модель.
У доношенных младенцев задний край внутренней капсулы, центральная
часть лучистого венца и ножки мозга миелинизированы уже к рождению. Со-
зревание семиовальных центров продолжается в направлении от задних отделов
мозга к передни м. Такие хорошо определяемые структуры, как мозол истое тело
и передний лимб внутренней капсулы, не миелинизированы при рождении нор-
мального младенца. В этих отделах можно проследить процесс созревания.
Ствол мозга и центральные ядра миелинизируются раньше, чем кора (т. е.
лобные, височные, теменные и затылочные доли). Субкортикальные отделы бе-
лого вещества созревают позже. Очевидные признаки миелинизации затылоч-
ной области отмечаются между 9 м и 12 м месяцами жизни, а лобной --- между
11 ми 12 м. В основном этот процесс завершается к 2 годам.
ЛУЧЕВАЯ АНАТОМИЯ ЗАДНЕЙ ЧЕРЕПНОЙ ЯМКИ
Задняя черепная ямка представляет собой часть основания черепа, ограни-
ченную центрально спереди спинкой турецкого седла и скатом, в переднебоко
вых отделах --- пирамидами височных костей, снизу --- базальной частью заты-
лочной кости, по заднелатеральным поверхностям --- ее чешуей. Она сообщает-
ся через большое затылочное отверстие с просветом позвоночного канала.
Следует отметить, что в настоящее время оптимальным методом исследова-
ния структур задней черепной ямки является МРТ, которая, в отличие от КТ,
лишена артефактов от костных структур.
Для удобства анализа на КТ и МР изображениях принято выделять не-
сколько уровней получения изображений.
На КТ срезе, выполненном по верхнему краю большого затылочного отвер-
стия, дифференцируются продолговатый мозг, оболочки мозга, ликворсодержащие
пространства, сосудистые структуры (рис. 1.1). Иногда можно видеть располо-
женные латерально нижние полюса миндалин мозжечка (рис. 1.2).
Мозжечок заполняет практически весь объем задней черепной ямки. Его по-
перечный размер (9---10 см) значительно превышает переднезадний (до 5 см).
Спереди мозжечок прилежит к продолговатому мозгу, мосту и четверохолмию и
соединен с ними посредством трех пар ножек. Верхняя пара ножек идет к четве-
рохолмию, средняя --- к мосту, нижняя --- к продолговатому мозгу. Выявление зон
патологической плотности (сигнала) в этих отделах позволяет говорить о воз-
можном поражении той или иной ножки. Поскольку ножки мозжечка представ-
лены белым веществом, они легко дифференцируются на фоне более плотной
коры мозжечка. Мозжечок состоит из двух гемисфер, между ними располагает-
ся червь, который хорошо визуализируется на КТ и МРТ срезах благодаря ха-
рактерным коротким, идущим во фронтальной плоскости параллельно друг дру-
гу извилинам. Более того, червь мозжечка имеет относительно большую плот-
ность, чем гемисферы. Червь идет косо снизу сзади вверх и вперед, что позволяет
Рис. 1.1. Уровень большого
затылочного отверстия:
а --- аксиальный срез КТ;
б --- аксиальный срез МРТ (Т1 ВИ);
в --- аксиальный срез МРТ (Т2 ВИ).
--- сошник; 2 --- затылочная кость;
3 --- продолговатый мозг; 4 --- мозже-
чок; 5 --- верхнечелюстная пазуха; 6 ---
большая цистерна; 7 --- головка ниж-
ней челюсти; 8 --- сосцевидный отрос-
ток; 9 --- позвоночная артерия; 10 ---
носоглотка.
Рис. 1.2. Уровень над большим
затылочным отверстием:
а --- аксиальный срез КТ;
б --- аксиальный срез МРТ (Т1 ВИ);
в --- аксиальный срез МРТ (Т2 ВИ).
1 --- височная доля; 2 --- скат; 3 --- про-
долговатый мозг; 4 --- полушарие моз-
жечка; 5 --- базилярная артерия; 6 ---
миндалина мозжечка; 7 --- основная
пазуха; 8 --- височная кость; 9 --- вал
лекула; 10 --- большая цистерна.
анализировать состояние его нижних и верхних отделов. Нижние отделы моз-
жечка вентрально прилежат к продолговатому мозгу, расположенному на ниж-
них отделах ската. Его размеры в продольном направлении составляют до 3 см,
в поперечном --- до 2 см. Он имеет округлую форму и срединную щель по пере-
дней и задней поверхности. На 2 см выше начинает визуализироваться мост, впе-
реди которого проходит отчетливо различаемая на фоне передней цистерны мо-
ста базилярная артерия. По бокам от моста визуализируются вершины и задние
поверхности пирамид височных костей, отделенные от последнего мостомозжеч
ковыми цистернами. На срезах изображение моста напоминает квадрат с зак-
ругленными углами. Между стволом мозга спереди и мозжечком сзади располо-
жен непарный IV желудочек. На аксиальных КТ и МРТ срезах он локализует-
ся строго центрально, имеет полулунную форму. Его боковые карманы в норме
должны быть строго симметричны (рис. 1.3). Отсутствие изображения IVжелу-
дочка, его смешение, деформация, шаровидная форма являются косвенными
признаками патологического процесса и требуют дообследования. Размеры
IV желудочка достаточно вариабельны и не играют существенной роли в отне-
сении наблюдений по этому признаку к норме или патологии. IVжелудочек со-
общается посредством водопровода мозга с III желудочком. В норме водопровод
на поперечных срезахне визуализируется. Существуют три отверстия, соединя-
ющие IV желудочек с подпаутинным пространством --- срединное и два латераль-
ных, расположенных в боковых карманах. Эти отверстия в норме не удается
дифференцировать (рис. 1.4, 1.5).
Следует остановиться на анатомии подпаутинных пространств задней черепной
ямки (рис. 1.6,1.7). Выделяют большую цистерну мозга (церебелломедуллярную
цистерну). Она представляет собой пространство между продолговатым мозгом,
дном IV желудочка и нижней поверхностью мозжечка. Ее ширина приближает-
ся к 3 см, а переднезадний размер составляет 2 см. Между основанием черепа и
нижней поверхностью мозга от большого затылочного отверстия вдоль ската и
спинки турецкого седла простирается задняя базальная цистерна. В зависимо-
сти от расположенных рядом анатомических структур выделяют переднюю (ме-
диальную) цистерну моста, которая проходит между скатом и мостом (ширина до
1 см), и две боковые цистерны моста. Медиальная цистерна моста содержит ба
зилярную артерию, а боковая --- тройничный нерв и верхнюю мозжечковую ар-
терию. В мостомозжечковых углах лежат церебеллопонтийные цистерны. С ними
Рис. 1.3. Уровень четвертого желу-
дочка, а --- аксиальный срез КТ;
б --- аксиальный срез МРТ (Т1 ВИ);
в --- аксиальный срез МРТ (Т2 ВИ).
1---серпмозга;2---лобнаядоля;3---
латеральная щель; 4 --- височный рог
бокового желудочка; 5 --- мост; 6 ---
четвертый желудочек; 7 --- червь моз-
жечка; 8 --- верхняя полулунная доль-
ка; 9 --- орбита; 10 --- клиновидная па-
зуха; 11 --- мостомозжечковая цистер-
на; 12 --- средние ножки мозжечка;
13 --- межполушарная щель; 14 --- ба
зилярная артерия; 15 --- глазное ябло-
ко; 16 --- височная доля; 17 ---полуша-
рие мозжечка.
Рис. 1.4. Уровень задних отделов тел боковых желудочков. МРТ. Коронарные срезы,
а --- Т1 взвешенное изображение; б --- Т2 взвешенное изображение.
1 --- верхняя теменная долька; 2 --- поясная борозда; 3 --- цистерна большой вены
мозга (вены Галена); 4 --- четвертый желудочек; 5 --- предцентральная извилина; 6 ---
центральная борозда; 7 --- постцентральная извилина; 8 --- надкраевая извилина;
9 --- поясная извилина; 10 --- латеральная щель; 11 --- верхняя височная извилина;
12 --- нижняя височная извилина; 13 --- намет мозжечка; 14 --- зубчатое ядро; 15 ---
спинной мозг; 16 --- треугольник бокового желудочка; 17 --- миндалина мозжечка.
Рис. 1.5. Уровень позади боковых желудочков. МРТ. Коронарные срезы,
а --- T1 взвешенное изображение; б --- Т2 взвешенное изображение.
1 --- серп; 2 --- предклинье; 3 --- перикаллезная цистерна; 4 --- намет мозжечка; 5 ---
верхняя теменная долька; 6 --- угловая извилина; 7 --- межтеменная борозда; 8 --- за-
тылочный рог; 9 --- теменно затылочная щель; 10 --- язычная извилина; 11 --- верх-
няя полулунная долька; 12 --- горизонтальная щель; 13 --- передняя доля мозжечка.
Рис. 1.6. Срединный сагиттальный срез МРТ.
а --- Т1 взвешенное изображение; б --- Т2 взвешенное изображение.
1 --- колено мозолистого тела; 2 --- свод; 3 --- воронка; 4 --- мост; 5 --- водопровод
мозга; 6 --- четверохолмие; 7 --- продолговатый мозг; 8 --- спинной мозг; 9 --- пояс-
ная извилина; 10 --- мозолистое тело; 11 --- валик мозолистого тела; 12 --- межнож
ковая цистерна; 13 --- четвертый желудочек; 14 --- большая цистерна; 15 --- поясная
борозда; 16 --- перикаллезная цистерна; 17 --- боковой желудочек; 18 --- передняя
мозговая артерия; 19 --- базилярная артерия; 20 --- парацентральная долька; 21 ---
предклинье; 22 --- клин; 23 --- цистерна большой вены мозга; 24 --- прямой синус;
25 --- миндалина мозжечка.
Рис. 1.7. Уровень тела бокового желудочка. Сагиттальные срезы МРТ.
а --- ТІ взвешенное изображение; б --- Т2 взвешенное изображение.
1 --- верхняя лобная извилина; 2 --- хвостатое ядро; 3 --- латеральная щель; 4 --- глаз-
ное яблоко; 5 --- предцентральная борозда; 6 --- центральная борозда; 7 --- постцен-
тральная извилина; 8 --- верхняя теменная долька; 9 --- боковой желудочек; 10 ---
язычная извилина; 11 --- парагиппокампальная извилина; 12 --- средняя лобная из-
вилина; 13 --- боковая цистерна моста; 14 --- затылочная доля; 15 --- мозжечок.
связаны боковые карманы IVжелудочка посредством боковых отверстий (отвер-
стий Люшка). Верхняя порция задней базальной цистерны формирует межнож
ковую цистерну, которая обязательно должна прослеживаться на соответствующем
срезе и располагаться строго срединно. Кнаружи от ножек мозга лежит охваты-
вающая цистерна, формирующая ликворсодержащее пространство в пределах
тенториальной вырезки. Она сообщается с межножковой цистерной, охватыва-
ет боковые поверхности ножек мозга и продолжается кзади в четверохолмную ци-
стерну, а выше связана с перикаллезной и парной межгемисферной цистернами.
Между наметом и передней поверхностью мозжечка находится верхняя моз-
жечковая цистерна. От затылочных долей большого мозга мозжечок отделен
отростком твердой мозговой оболочки, которая дает на КТ срезах характерную
гиперденсивную тень, простирающуюся от верхних граней пирамид височных
костей кверху и кнутри, повторяя форму палатки, и завершается тенториальной
Рис. 1.8. Уровень над четвертым
желудочком, а --- аксиальный срез КТ;
б --- аксиальный срез МРТ (Т1 ВИ);
в --- аксиальный срез МРТ (Т2 ВИ).
1 --- лобная доля; 2 --- лобный рог бо-
кового желудочка; 3 --- латеральная
щель мозга; 4 --- третий желудочек; 5 ---
ножка мозга; 6 --- цистерна четверохол-
мия; 7 --- височная доля; 8 --- верхний
сагиттальный синус; 9 --- серп мозга; 10
31
22
головка хвостатого ядра; 11 --- кора остро-
вка; 12 --- скорлупа; 13 --- внутренняя вена мозга; 14 --- четверохолмие; 15 --- полуша-
рие мозжечка; 16 --- зрительный нерв; 17 --- височный рог бокового желудочка; 18 ---
гиппокамп; 19 --- передняя долька мозжечка; 20 --- хиазма; 21 --- внутренняя сонная
артерия; 22 --- охватывающая цистерна; 23 --- четвертый желудочек; 24 --- прямая
извилина; 25 --- ольфакторная борозда; 26 --- средняя мозговая артерия; 27 --- червь;
28 --- затылочная доля; 29 --- клетчатка орбиты; 30 --- передняя мозговая артерия;
31 --- межножковая цистерна.
вырезкой, через которую проходит ствол мозга. Наличие в этой области ликво
ропроводящих путей позволяет уверенно оценивать ее состояние, что играет важ-
ную роль в диагностике дислокаций (рис. 1.8). На КТ срезах сверху мост гра-
ничит со средним мозгом, а именно с четверохолмием (рис. 1.9). Задний контур
нижних холмиков в виде изломанной линии, подчеркнутой четверохолмной ци-
стерной, позволяет уверенно дифференцировать эту зону Чуть выше и кпереди
от четверохолмия располагаются ножки мозга в виде двух расходящихся корот-
ких, достаточно толстых продолговатых образований, между которыми прохо-
дит межножковая цистерна, имеющая треугольную форму с вершиной, обращен-
ной кзади.
Рис. 1.9. Уровень отверстия
мозжечкового намета,
а --- аксиальный срез КТ после
контрастирования;
б --- аксиальный срез МРТ
(Т1 ВИ); в --- аксиальный срез
МРТ (Т2 ВИ).
1 --- серп; 2 --- мозолистое тело; 3 ---
лобный рог; 4 --- колонки свода;
5 --- третий желудочек; 6 --- шиш-
ковидная железа; 7 --- цистерна
четверохолмия; 8 --- контрастиро
ванный намет мозжечка; 9 --- верхняя лобная извилина; 10 --- головка хвостатого
ядра; 11 --- прозрачная перегородка; 12 --- поводок; 13 --- червь; 14 --- колено мозоли-
стого тела; 15 --- скорлупа; 16 --- верхняя височная извилина; 17 --- свод; 18 --- край
намета; 19 --- средняя лобная извилина; 20 --- нижняя лобная извилина; 21 --- кора
островка; 22 --- полость прозрачной перегородки; 23 --- наружная затылочная изви-
лина; 24 --- средняя мозговая артерия; 25 --- четверохолмие; 26 --- поясная борозда;
27 --- бледный шар; 28 --- височный рог бокового желудочка.
ЛУЧЕВАЯ АНАТОМИЯ СУПРАТЕНТОРИАЛЬНЫХ ОТДЕЛОВ
ГОЛОВНОГО МОЗГА
В латеральных отделах дно передней черепной ямки образовано крышами
глазниц, а в центральных --- продырявленной пластинкой. Базальные отделы
лобных долей представлены короткими, идущими продольно глазничными изви-
линами. На более высоких срезах удается дифференцировать, особенно у людей
пожилого возраста, верхнюю, среднюю и нижнюю лобные извилины. Структу-
ры средней черепной ямки ограничены спереди малым крылом основной кости,
снизу --- большим крылом, сзади --- передней поверхностью пирамиды височной
кости. На тонких срезах (толщина среза 1---2 мм, «edge» или «Ьопе» --- алгоритм
реконструкции изображения) отчетливо дифференцируются округлое, овальное
и рваное отверстия. В верхнемедиальной части передней поверхности пирамиды
височной кости прослеживается площадка узла тройничного нерва.
Содержимое средней черепной ямки представлено базальными отделами ви-
сочной доли. Самые нижние срезы в латеральных отделах позволяют оценить
нижнюю височную извилину, а в медиальных --- парагиппокампальную, рас-
положенную между височным (нижним) рогом бокового желудочка и каверноз-
ным синусом. Височный рог бокового желудочка визуализируется в виде тон-
кого полумесяца. Кавернозный синус располагается параселлярно в виде гипер
ленсивной структуры с плоским, вогнутым или умеренно выбухающим
контуром, которая после внутривенного контрастирования демонстрирует ин
Рис. 1.10. Уровень хиазмальной (супраселлярной цистерны),
а --- аксиальный срез KT; б --- аксиальный срез MPT (Т2 ВИ).
1 --- внутренняя сонная артерия; 2 --- миндалевидное тело; 3 --- мост; 4 --- хиазма;
5 --- спинка турецкого седла; 6 --- базилярная артерия; 7 --- боковая цистерна моста;
8 --- передняя мозговая артерия; 9 --- средняя мозговая артерия; 10 --- задняя соеди-
нительная артерия; 11 --- ножка мозга; 12 --- четверохолмие; 13 --- бугорок турецкого
седла; 14 --- воронка; 15 --- хиазмальная цистерна; 16 --- задние мозговые артерии;
17 --- межножковая цистерна; 18 --- охватывающая цистерна.
тенсивное и достаточно равномерное накопление контрастирующего вещества.
Отдельные структуры параселлярной области (пещеристый синус с внутренней
сонной артерией, черепные нервы) дифференцировать на КТ изображениях не
удается, для их оценки используют МРТ. Центральные отделы основания чере-
па занимает турецкое седло. В полости турецкого седла визуализируется оваль-
ной или округлой формы гипофиз (4---6 мм).
Сразу над турецким седлом расположена супраселлярная цистерна в виде
правильной формы четырехугольника, а чаще пятиугольника (рис. 1.10). Весь-
ма важной при анализе супраселлярной цистерны является оценка симметрич-
ности изображения ее крыльев. Малейшая асимметрия должна быть тщательно
зафиксирована в протоколе, так как подобные изменения могут быть мани
10 ю
Рис. 1.11. Уровень третьего желудочка,
а --- аксиальный срез КТ;
б --- аксиальный срез МРТ (Т1 ВИ);
в --- аксиальный срез МРТ (Т2 ВИ).
--- серп мозга; 2 --- верхняя лобная из-
вилина; 3 --- средняя лобная извилина;
4 --- нижняя лобная извилина; 5 --- голов-
ка хвостатого ядра; 6 --- внутренняя кап-
сула; 7 --- наружная капсула; 8 --- третий
желудочек; 9 --- четверохолмие; 10 ---
межполушарная щель; 11 --- лобный рог
бокового желудочка; 12 --- кора островка;
13 --- латеральная щель; 14 --- цистерна терминальной пластинки; 15 --- полушарие
мозжечка; 16 --- верхняя полулунная долька; 17 --- лобная доля; 18 --- поясная изви-
лина; 19 --- межжелудочковое отверстие; 20 --- таламус; 21 --- шишковидная железа;
22 --- зрительная лучистость; 23 --- затылочная доля; 24 --- треугольник бокового же-
лудочка; 25 --- передняя мозговая артерия; 26 --- валик мозолистого тела; 27 --- про-
зрачная перегородка; 28 --- верхняя височная извилина; 29 --- теменно затылочная
борозда; 30 --- шпорная борозда.
фестацией развивающегося поперечного смещения. На тонких срезах в пере-
дних отделах супраселлярной цистерны удается проследить перекрест зритель-
ных нервов. Еще вентральнее расположена линейной формы терминальная ци-
стерна, ориентированная в переднезаднем направлении по срединной сагит
татьной линии.
В верхнецентральных отделах супраселлярного региона часто удается просле-
дить изображение гипоталамуса, имеющего вид двух треугольников, основани-
ями ориентированных кпереди. На этом уровне начинают прослеживаться нижние
отделы 111 желудочка. Описанные выше ликворсодержащие структуры называ-
ют срединными. К ним также относят серповидный отросток твердой мозговой
Рис. 1.12. Уровень нижних отделов
боковых желудочков,
а --- аксиальный срез КТ после
контрастирования;
б --- аксиальный срез МРТ (Т1 ВИ);
в --- аксиальный срез МРТ (Т2 ВИ).
1 --- серп; 2 --- верхняя лобная извили-
на; 3 --- средняя лобная извилина; 4 ---
передняя мозговая артерия; 5 --- лате-
ральная щель; 6 --- таламус; 7 --- тре-
угольник бокового желудочка; 8 ---
червь; 9 --- поясная борозда; 10 --- ниж-
няя лобная извилина; 11 --- верхняя височная извилина; 12 --- шишковидная желе-
за; 13 --- цистерна четверохолмия; 14 --- прямой синус; 15 --- лобный рог; 16 --- голов-
ка хвостатого ядра; 17 --- передний отдел латеральной щели; 18 --- внутренняя кап-
сула; 19 --- боковой отдел латеральной щели; 20 --- валик мозолистого тела; 21 ---
теменно затылочная борозда; 22 --- шпорная борозда; 23 --- предцентральная из-
вилина; 24 --- центральная борозда; 25 --- постцентральная извилина; 26--- средняя
височная извилина; 27 --- затылочная доля; 28 --- внутренняя вена мозга; 29 --- за-
тылочный рог; 30 --- поперечная височная извилина (извилина Гешле); 31 --- на-
ружная затылочная извилина; 32 --- шпорная извилина; 33 --- мозолистое тело.
оболочки, прозрачную перегородку, эпифиз. III желудочек наиболее удачно пред-
ставлен на следующем срезе (см. рис. 1.9). Его стенки должны быть расположе-
ны параллельно относительно друг друга, допускается их легкое выбухание или
вогнутость, но ширина в норме не превышает 4 мм для обследуемых любого воз-
раста. Впереди III желудочка в виде симметричных дугообразно изогнутых лик
ворсодержащих структур прослеживаются передние рога боковых желудочков,
разделенные прозрачной перегородкой. В норме дисталъные отделы передних рогов
остроконечные. Это весьма важно в практическом отношении, так как развитие
гидроцефалии ведет в первую очередь к баллонообразной деформации передних
рогов боковых желудочков.
По латеральному контуру каждого рога отчетливо дифференцируется более
плотное анатомическое образование --- головка хвостатого ядра, латеральнее и
чуть дорсальнее которой проходит линейной формы переднее бедро внутренней
Рис. 1.13. Уровень тел боковых
желудочков,
а --- аксиальный срез КТ;
б --- аксиальный срез МРТ (Т1 ВИ);
в --- аксиальный срез МРТ (Т2 ВИ).
1 --- серп; 2 --- мозолистое тело; 3 ---
тело бокового желудочка; 4 --- верх-
ний сагиттальный синус; 5 --- верх-
няя лобная извилина; 6 --- средняя
лобная извилина; 7 --- предцент
ральная извилина; 8 --- постцент-
ральная извилина; 9 --- надкраевая извилина; 10 --- угловая извилина; 11 --- поясная
извилина; 12 --- хвостатое тело; 13 --- валик мозолистого тела; 14 --- теменно заты
лочная борозда; 15 --- центральная борозда; 16 --- латеральная щель; 17 --- полуоваль-
ный центр; 18 --- затылочная доля.
капсулы, идущее косо. Приближаясь к III желудочку, внутренняя капсула ме-
няет направление хода, образуя при этом колено, и идет латерально кзади. Эта
часть внутренней капсулы называется задним бедром. Оно разделяет зритель-
ный бугор и лентикулярные ядра, которые имеют треугольную форму. Позади
зрительного бугра идет ретроталамическая цистерна, ориентированная во фрон-
тальной плоскости.
Центральное место в этом регионе занимает ретропинеальная цистерна
с шишковидной железой, также относящаяся к срединным структурам голов-
ного мозга и располагающаяся позади III желудочка. Она имеет округлую фор-
му, размеры не превышают 1 см в диаметре. В передних отделах прослеживаются
поводки, идущие в сагиттальной плоскости. Именно с них начинается обызве-
ствление шишковидной железы. Латеральные отделы головного мозга на этом
уровне представлены островком височной доли, который легко распознается бла-
годаря обилию субарахноидальных пространств, отражающих короткие изви-
тые борозды, присущие этой анатомической структуре (рис. 1.11). Над наметом
мозжечка расположены затылочные доли, разделенные задней частью серповид
6
9
"10
В---11
12
13
Рис. 1.14. Уровень верхних отделов
боковых желудочков,
а --- аксиальный срез КТ;
б --- аксиальный срез МРТ (Т1 ВИ);
в --- аксиальный срез МРТ (Т2 ВИ).
1 --- серп; 2 --- мозолистое тело; 3 --- боко-
вой желудочек; 4 --- полуовальный центр;
5 --- клин; 6 --- верхняя лобная извилина;
7 --- средняя лобная извилина; 8 --- пред
центральная извилина; 9 --- центральная 16
борозда; 10 --- постцентральная извили-
на; 11 --- латеральная щель; 12 --- надкрае в
вая извилина; 13 --- угловая извилина;
14--- поясная борозда; 15 --- теменно за
тылочная борозда; 16 --- межтеменные борозды
З
Рис. 1.15. Уровень над боковыми
желудочками.
^
а --- аксиальный срез КТ;
б --- аксиальный срез МРТ (Т1 ВИ);
6
в --- аксиальный срез МРТ (Т2 ВИ).
1 --- краевая борозда; 2 --- верхняя лоб-
ная извилина; 3 --- средняя лобная
извилина; 4 --- предцентральная изви-
лина; 5 --- центральная борозда; 6 ---
постцентральная извилина; 7 --- лате-
ральная щель; 8 --- надкраевая извили-
на; 9 --- угловая извилина; 10 --- темен
но затылочная борозда.
ного отростка твердой мозговой оболочки. Отдельные извилины затылочных
долей не принято выделять, но по медиальной поверхности они короткие и ха-
рактеризуются поперечным ходом.
Впереди затылочных долей располагается утолщение мозолистого тела с боль-
шими и малыми щипцами, латеральнее --- задние рога тел боковых желудочков,
на фоне которых обычно хорошо прослеживаются сосудистые сплетения (рис. 1.12).
На следующем срезе представлены тела боковых желудочков, разделенные мо-
золистым телом, которое в переднем отделе образует колено. Абсолютные и отно-
сительные размеры боковых желудочков в практической работе рассчитывают-
ся достаточно редко, как правило, вполне достаточна приблизительная оценка их
размеров, конфигурации и симметричности (рис. 1.13). Для оценки желудочко-
вой системы разработаны специальные планиметрические критерии.
Параллельно латеральному контуру каждого бокового желудочка прослежи-
вается более плотная, по сравнению с белым веществом перивентрикулярной
области, линейная структура, обусловленная телом хвостатого ядра. На этом и
на следующем уровне удается отчетливо дифференцировать белое и серое веще-
ство, благодаря существенным различиям в их денситометрических характери
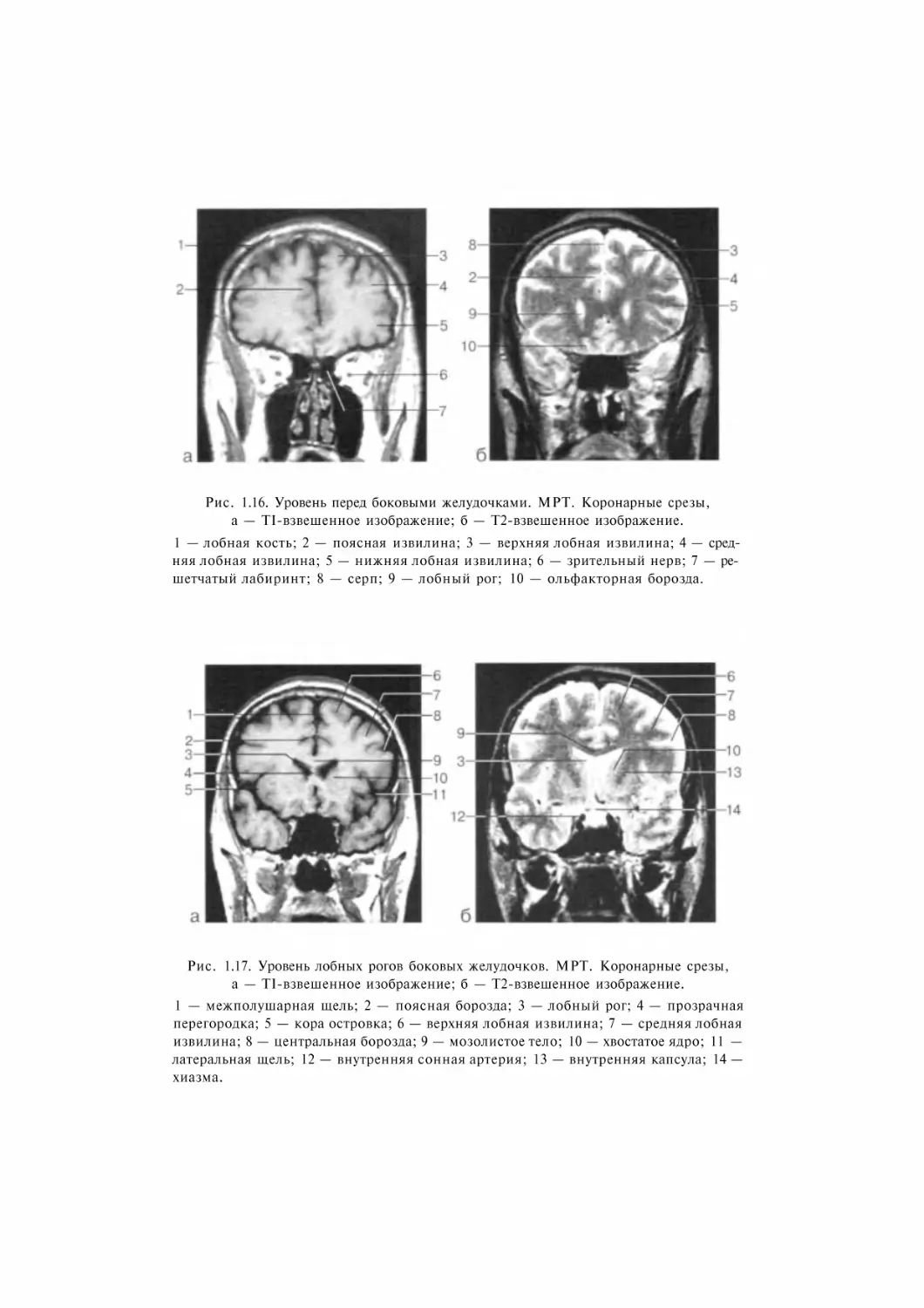
Рис. 1.16. Уровень перед боковыми желудочками. МРТ. Коронарные срезы,
а --- ТІ взвешенное изображение; б --- Т2 взвешенное изображение.
1 --- лобная кость; 2 --- поясная извилина; 3 --- верхняя лобная извилина; 4 --- сред-
няя лобная извилина; 5 --- нижняя лобная извилина; 6 --- зрительный нерв; 7 --- ре-
шетчатый лабиринт; 8 --- серп; 9 --- лобный рог; 10 --- ольфакторная борозда.
Рис. 1.17. Уровень лобных рогов боковых желудочков. МРТ. Коронарные срезы,
а --- ТІ взвешенное изображение; б --- T2 взвешенное изображение.
1 --- межполушарная щель; 2 --- поясная борозда; 3 --- лобный рог; 4 --- прозрачная
перегородка; 5 --- кора островка; 6 --- верхняя лобная извилина; 7 --- средняя лобная
извилина; 8 --- центральная борозда; 9 --- мозолистое тело; 10 --- хвостатое ядро; 11 ---
латеральная щель; 12 --- внутренняя сонная артерия; 13 --- внутренняя капсула; 14 ---
хиазма.
Рис. 1.18. Уровень бокового отдела орбиты. МРТ. Сагиттальные срезы,
а --- Т1 взвешенное изображение; б --- Т2 взвешенное изображение.
1 --- средняя лобная извилина; 2 --- нижняя лобная извилина; 3 --- кора островка;
4 --- средняя мозговая артерия; 5 --- верхняя височная извилина; 6 --- средняя ви-
сочная извилина; 7 --- нижняя височная извилина; 8 --- предцентральная извили-
на; 9 --- центральная борозда; 10 --- постцентральная извилина; 11 --- надкраевая из-
вилина; 12 --- угловая извилина; 13 --- височный рог; 14 --- наружная затылочная из-
вилина; 15 --- верхняя полулунная долька; 16 --- нижняя полулунная долька; 17 ---
латеральная щель; 18 --- горизонтальная щель; 19 --- поперечная височная извили-
на (Гешле).
стиках (белое вещество --- 30---35 ед. X; серое --- 35---45 ед. X). Существует доста-
точное количество схем, на которых представлена топика отдельных извилин
применительно к КТ и МРТ срезам (рис. 1.14---1.18).
Лобную и височную доли разделяет условная линия, проведенная между наи-
более дисталъной точкой переднего рога бокового желудочка и костями свода на
томже срезе, атакже по ходу латеральной цистерны (сильвиевой щели). Височ-
ная и затылочная доли могут быть разделены линией, проведенной от наиболее
дистальной точки затылочного рога к костям свода черепа. Считается, что гра-
ница между затылочной и теменной доля ми проходит на уровне тел боковых же-
лудочков, и структуры, расположенные выше, относятся к теменной доле,
ниже --- к затылочной.
Граница между лобной и теменной долями проходит по центральной борозде,
которая обычно достаточно хорошо прослеживается у людей любого возраста.
Выше тел боковых желудочков расположен уровень семиовальных центров.
Обсуждая вопросы нормальной анатомии головного мозга, необходимо об-
ратить внимание на структуры, в которых может наблюдаться физиологичес-
кая кал ьцификация. К ним относятся дериваты твердой мозговой оболочки ---
серповидный отросток, намет мозжечка, параселлярные и петроклиноидные
связки, сосудистые сплетения в проекции задних рогов тел боковых желудоч-
ков и боковых выворотов IV желудочка. Очень рано начинает обызвествляться
шишковидная железа. При гистологическом исследовании уже у трехлетних
детей отмечается отложение солей кальция в толше эпифиза. С возрастом час-
тота обызвествлений шишковидной железы возрастает, достигая 83---90% у об-
следуемых старше 30---40 лет. Очень нежное точечное обызвествление может на-
блюдаться в проекции бледного шара у людей пожилого возраста.
ЛУЧЕВАЯ АНАТОМИЯ ТУРЕЦКОГО СЕДЛА
Турецкое седло сверху ограничено диафрагмой, а по бокам --- пещеристыми
пазухами. Над седлом расположена цистерна перекреста зрительных нервов,
которая содержит верхнюю часть воронки, зрительные нервы, надклиновидные
части сифонов внутренней сонной артерии и артериальный круг мозга (вилли
зиев круг).
Форма турецкого седла у новорожденных чашеобразная, с широким входом.
Эта форма --- кажущаяся, ибо верхняя половина спинки седла еще хрящевая и
не видна на обзорном снимке. К 1 му году спинка седла окостеневает, но сагит-
тальный диаметр его остается больше, чем глубина. На 2---3 м году жизни турец-
кое седло становится круглым и остается таким до предпубертатного возраста.
С начала полового развития и до климактерического периода турецкое седло
приобретает постоянную форму с отчетливыми индивидуальными чертами, что
может служить основой для идентификации личности по ранее выполненным
краниограммам при судебно медицинском исследовании. У большинства взрос-
лых людей турецкое седло имеет слегка удлиненную форму, поскольку передне
задний его размер преобладает над глубиной. Сохранение у взрослого человека
круглого седла является одним из признаков инфантилизма.
У людей пожилого возраста несколько нарастает переднезадний размер сед-
ла за счет истончения (очень легкого) центрального и нижнего отделов спинки
вследствие умеренной гиперплазии аденогипофиза.
На форму турецкого седла оказывает влияние и размер клиновидной пазухи:
при выраженной ее пневматизации оно становится плоским.
Размеры седла измерялись различными методами, однако внедрение в прак-
тику КТ и МРТ остановило совершенствование систем измерения седла по рен-
тгенограммам. Для практических целей площадь и объем турецкого седла не
оценивают, а пользуются определением его сагиттального размера и глубины по
боковой краниограмме или по прицельному снимку седла. Для измерения сагит-
тального размера находят максимальное расстояние между наиболее удаленны-
ми точками переднего ската и передней поверхности спинки седла. При совре-
менных условиях съемки (фокусное расстояние не менее 1 метра) средний размер
составляет 10,5---11 мм, максимальный --- 14,5---15 мм. При обычной форме сед-
ла максимальный сагиттальный размер располагается посередине его высоты.
Для измерения глубины турецкого седла требуется проведение вспомогатель-
ных линий: реконструируют вход в седло, т. е. соединяют бугорок с вершиной
спинки, затем проводят линию, касательную кдну турецкого седла и параллель-
ную клиновидному возвышению (planum), из точки касания этой линии вверх
восстанавливают перпендикуляр до пересечения с линией входа. Отрезок этого
перпендикуляра между дном седла и его входом соответствует глубине. Средний
показатель составляет 8 мм, максимальный --- 11 мм.
КТ и МРТ обеспечивают хорошую визуализацию и анализ патологических
процессов в области турецкого седла. Относительное взаиморасположение ана-
томических структур в этой области делает фронтальную проекцию оптималь-
ной для визуализации.
Потребность в КТ цистернографии снизилась с техническим развитием КТ
и МРТ. Обычная рентгенография и линейная томография области турецкого
седла постепенно уходят в прошлое.
Денситометрические характеристики гипофиза достаточно вариабельны (при
нативном исследовании они составляют 24---40 ед. X, после внутривенного кон-
трастирования не превышают 50 ед. X). При денситометрии гипофиза необходимо
выбирать возможно более центрально расположенные изображения. Это позво-
ляет избежать попадания в зону и нтереса сосудистых структур (внутренняя сонная
артерия, кавернозные синусы) и избежать гипердиагностики микроаденом гитго
Рис. 1.19. Уровень третьего желудочка
и турецкого седла. МРТ.
Коронарные срезы,
а --- Т1 взвешенное изображение;
б --- Т2 взвешенное изображение;
в --- Т1 взвешенное изображение.
1 --- мозолистое тело; 2 --- боковой желу-
дочек; 3 --- третий желудочек; 4 --- хиаз
мальная цистерна; 5 --- свод; 6 --- хвоста-
тое ядро; 7 --- внутренняя капсула; 8 ---
латеральная щель; 9 --- серп; 10 --- пара
гиппокампальная извилина; 11 --- пояс-
ная извилина; 12 --- перикаллезная цис-
терна; 13 --- воронка; 14 --- основная па-
зуха; 15 --- скорлупа; 16 --- наружная
капсула; 17 --- кора островка.
физа. Строение гипофиза можно детально изучить на сагиттальных МРТ: задняя
доля гипофиза имеет яркую, высокую интенсивность MP сигнала, промежуточ-
ная доля --- низкую интенсивность. Над задней и интермедиарной частями гипо-
физа расположена его воронка, идущая параллельно спинке турецкого седла вверх
к гипоталамусу (см. рис. 1.6; рис. 1.19). Диафрагма турецкого седла достаточно от-
четливо прослеживается в сагиттальной плоскости. В норме она может быть плоская,
выпуклая и вогнутая, но допустимая девиация не превышает 1 ---2 мм.
Размеры гипофиза несколько отличаются от размеров турецкого седла. Нор-
мальная высота гипофиза составляет 3---8 мм, а ширина --- 10---17 мм. Верхняя
поверхность его обычно плоская или несколько вогнутая, реже выпуклая. Вы-
пуклая поверхность гипофиза чаше встречается у молодых женщин репродук-
тивного возраста.
АНАТОМИЯ СОСУДОВ ГОЛОВНОГО МОЗГА И ИХ ИЗОБРАЖЕНИЕ
ПРИ ЛУЧЕВЫХ АНГИОГРАФИЧЕСКИХ ИССЛЕДОВАНИЯХ
Артерии головного мозга
Кровоснабжение головного мозга осуществляется через две сонные и две по
звоночные артерии. Располагаясь в толще шеи, эти сосуды достигают основа-
ния черепа и проникают в полость твердой мозговой оболочки, образуя на осно-
вании мозга систему основных мозговых артерий.
С анатомической и клинико рентгенологической точки зрения целесообраз-
но выделять экстра и интракраниальные отделы артерий.
Мы разберем «классический» вариант строения, а затем остановимся наряде
основных анатомических вариантов, учитывая, что морфологическая органи-
зация сосудов головного мозга более чем в 50% случаев отличается от того типа,
который принято считать нормальным: отдельные артерии иногда отсутствуют
или бывают резко гипоплазированы, отмечаются особенности их отхождения,
ветвления и анастомозирования, присутствие дополнительных и персистирую
ших сосудов. Это играет важную роль, поскольку от особенностей строения ар-
териальной системы головного мозга во многом зависит, разовьется ли в создав-
шихся патологических условиях поражение мозга, какова будет его степень,
локализация и клиническая симптоматика.
I. Экстракраниальные артерии
К экстракраниальным артериям относятся все сосуды и сосудистые сегмен-
ты, несущие кровь в направлении к голове между сердцем и основанием черепа.
Хотя надо отметить, что при ряде патологических состояний эти артерии могут
менять направление потока и включаться в кровоснабжение верхней конечнос-
ти. Экстракраниальные артерии включают в себя: дугу аорты до отхождения
левой подключичной артерии, общую сонную артерию, плечеголовной ствол,
проксимальные отделы подключичных артерий до отхождения позвоночных
артерий, общую сонную артерию, внутреннюю сонную артерию и позвоночную
артерию до вхождения их в полость черепа.
1. Каротидная система.
Плечеголовной ствол (truncus brachiocephalic's) --- непарная артерия, отходя-
щая отдута аорты и направляющаяся косо вправо и вверх. Кпереди от него распо-
лагается левая безымянная вена, вилочковая железа, сзади---трахея. Плечеголовной
ствол не дает ветвей и на уровне правого фудино ключичного сочленения делится
на правую общую сонную и подключичную артерии. В некоторых случаях от него
отходит еще третья ветвь --- срединная артерия щитовидной железы, которая идет
кверху по передней поверхности трахеи к нижнему полюсу щитовидной железы.
Общая сонная артерия (а. carotis communis) (ОСА) справа отходит от плече
головного ствола. Левая общая сонная артерия отходит от дуги аорты в самой
высокой ее точке --- у места отхождения брахиоцефального ствола. Обе артерии
переходят на область шеи позади грудино ключичного сочленения между нож-
ками фудино ключично сосцевидноймышиы. ОСА проходят латеральнее трахеи
и гортани, кзади и медиальнее от яремных вен. Внутренняя яремная вена, ОСА и
блуждающий нерв находятся в одном влагалище и образуют сосудистый пучок
шеи, кзади от которого лежит шейный отдел симпатического ствола. Грудино
ключично сосцевидная мышца прикрывает общую сонную артерию спереди.
Задняя поверхность правой ОСА прилежит к лестничным мышцам, алевой, кроме
того, еще и к выступающему краю пищевода. На уровне верхнего края щитовид-
ного хряща ОСА расширяется, образуя бифуркацию, и делится на внутреннюю
(ВСА) и наружную (НСА) сонные артерии. В некоторых случаях от бифуркации
отходит восходящая артерия глотки. Деление ОСА может происходить на различ-
ных уровнях шеи --- у ее основания, на середине или выше щитовидного хряща.
Уровень бифуркации крайне вариабелен: 1% --- на уровне Сп, 16% --- Сш, 66% ---
Clv, 16% --- Cv, 1 % --- CV|. ОСАдо своего деления не отдает ни одной ветви. Обыч-
но артерия расширяется в области бифуркации в так назы ваемую каротидную лу
ковицу, которая распространяется на ВСА. В наружном слое луковицы распола-
гаются чувствительные нервные окончания, раздражение которых вызывает
замедление работы сердца, снижение артериального давления, расширение пе-
риферических сосудов. Эта область называется синокаротидной рефлексоген-
ной зоной. Раздражение ее может наблюдаться при грубой пальпации сосуда на
этом уровне, а также вовремя ангиографии (пункции артерии, параартериаль
ном введении контрастирующего вещества).
Первый отрезок ВСА обычно проходит снаружи или снаружи и кзади от НСА,
угол расхождения во многом определяется возрастом и длиной сосудов. Иногда
эти сосуды расходятся в виде канделябра. Вскоре после бифуркации ВСА вновь
приближается к НСА, идет рядом и перед вхождением в каротидный канал дела-
ет поворот медиально. В том случае, когда ВСА отходит кзадимедиально по от-
ношению к НСА, она затем делает петлю вокруг НСА. ВСА не дает ветвей до
вхождения в полость черепа.
НСА после отхождения от общей сонной артерии направляется вверх и почти
сразу начинает отдавать ветви. Затем она идет вдоль заднего края нижней челю-
сти и на уровне суставного отростка этой кости делится на две конечные ветви:
поверхностную височную и внутреннюю челюстную артерии. Все ветви НСА
делятся на следующие:
1) передние --- a. thyreoidea superior, a. lingualis, a. maxillaris externa;
2) задние --- a. sternoclaidomastoidea, a. occipitalis, a. auricularis posterior;
3) медиальные --- a. pharingea ascendens;
4) конечные --- a. temporalis superficialis, а. maxillaris interna.
Основное значение этих ветвей, с нейрохирургической точки зрения, состо-
ит в том, что при окклюзии обшей или внутренней сонной артерии на шее они могут
принимать участие в коллатеральном кровоснабжении головного мозга.
2. Вертебрально базилярная система.
Подключичная артерия отходит слева непосредственно от дуги аорты, спра-
ва---от плечеголовного ствола. Выходя из грудной полости через верхнее отвер-
стие грудной клетки, подключичная артерия огибает купол плевры, располага-
ясь в межлестничном треугольнике позади передней лестничной мышцы. Затем
артерия идет под ключицей, подходит к 1 ребру и перегибается через него. В под-
ключичной артерии различают три отдела: 1 --- до входа ее в промежуток между
лестничными мышцами, 2 --- на протяжении межлестничного промежутка и 3 ---
от места выхода артерии из межлестничного промежутка до нижнего края I реб-
ра. В 1 м отделе отходят позвоночная артерия, внутренняя артерия молочной
железы и щитовидно шейный ствол, во 2 м --- реберно шейный ствол и в 3 м ---
поперечная артерия шеи.
Позвоночная артерия (ПА) является первой ветвью подключичной, хотя
иногда отходит непосредственно от дуги аорты (4% случаев слева и очень редко
справа). После отхождения от наивысшей точки подключичной дуги или зад
немедиальной части ее, ПА поднимается кпереди от лестничной мышцы, слегка
извиваясь или делая S образный изгиб (VI сегмент) при вхождении в отвер-
стие поперечного отростка (90% случаев), реже Cv (5% случаев), и затем идет
почти вертикально вверх через отверстия в поперечных отростках позвонков
(V2 сегмент). Выйдя из отверстия Сп, она поворачивает латерально и опять идет
почти вертикально между аксисом и атлантом или поворачивает кнаружи перед
вхождением в поперечный отросток атланта под углом 45°. Выйдя из отверстия
в поперечном отростке атланта, сосуд идет назад примерно на 1 см кзади от
атланта, затем поворачивает медиально (петля атланта --- V3 сегмент). Затем
артерия отдает свои мышечные ветви, которые анастомозируют с веточками
затылочной артерии, отходящей от НСА (затылочно позвоночный анастомоз).
Кзади и медиально от атлантоокципитального сочленения (V4) ПА проходит
через атлантоокципитальную мембрану, пронзает твердую мозговую и арахно
идальную оболочки.
Кроме затылочно позвоночного анастомоза ПА формирует анастомозы с вет-
вями тиреоцервикального и костоцервикального стволов. В среднем диаметр их
составляет 3,5 мм (1,5---5 мм). Правая и левая ПА имеют одинаковый диаметр
примерно в 25% случаев, обычно левая ПА шире правой. В 10% наблюдений
отмечается маленький диаметр сосуда --- его гипоплазия.
II. Интракраниальные сосуды
В области основания к мозгу подходят и сообщаются между собой все 4 снаб-
жающие его кровью артериальные магистрали: передние --- внутренние сонные
и задние --- позвоночные артерии.
ВСА входит в полость черепа через каротидное отверстие (foramen caroticum),
которое находится кзадимедиально от яремного отверстия (foramenjugularis). Она
проходит через канал в височной кости (височная часть) и дважды в нем изгиба-
ется под углом 90° соответственно изгибам канала. Выйдя через рваное отвер-
стие (foramen lacerum), идет на небольшом протяжении почти вертикально в ка-
вернозном синусе, расположенном кнаружи от основной кости (кавернозная
часть --- сегмент С5), затем поворачивает кпереди и кверху --- сегмент С4, и за-
тем опять кзади под передним клиновидным отростком --- сегмент СЗ. После этого
ВСА покидает кавернозный синус и проходит ниже зрительного нерва в суба
рахноидальном цистернальном пространстве (цистернальная часть С2). Ее ко-
нечная часть --- сегмент С1 --- идет кзади и латерально до делен ия на среднюю и
переднюю мозговые артерии. На ангиограммах в боковой проекции каверноз-
ный и супраклиноидный отрезки ВСА имеют форму S образного изгиба, кото-
рый называется сифоном ВСА. Различают двойной, ординарный и выпрямлен-
ный типы сифона. Наиболее часто встречается двойной сифон, при котором,
кроме заднего (соответствует повороту артерии в кавернозный синус) и переднего
(место перехода субклиноидной части ВСА в супраклиноидную) дугообразных
изгибов, имеется еще третий дугообразный изгиб кзади дистальной части суп
раклиноидного отрезка. При ординарном сифоне третий изгиб отсутствует. Вып-
рямленный сифон представляет собой разновидность ординарного и характери-
зуется крутым подъемом кпереди супраклиноидного отрезка ВСА. Знание фор-
мы сифона необходимо для топической диагностики объемных образований
параселлярной области.
Глазничная артерия начинается от сегмента С2---СЗ, задняя соединительная
артерия (ЗСА) --- от сегмента СІ, за исключением 10% случаев, когда задние
мозговые артерии (ЗМА) начинаются непосредственно от ВСА. Диаметр ВСА
в среднем составляет 2,8 3,3 мм. Первые свои ветви ВСАдает на основании че-
репа. Это объясняет тот факт, что окклюзия ВСА у бифуркации обязательно
прослеживается до основания черепа. Очень большое значение в диагностике
придается глазничной артерии. Она обычно отходит от заднемедиальной части
передней петли каротидного сифона (сегменты С2, СЗ), поворачивает медиаль-
но от ВСА и входит в зрительный канал ниже и кнутри от зрительного нерва. За-
тем она направляется к верхнемедиальному отделу глазницы и, подойдя к бло-
ку, делится на конечные ветви --- надблоковую и надглазничную, которые име-
ют анастомозы с конечными ветвями НСА. Надо отметить, что имеется также
анастомоз между средней оболочечной артерией, точнее, ее ветвью --- верхнече-
люстной артерией --- и ветвями глазничной артерии.
ЗСА начинается от задней стенки ВСАу места ее максимального изгиба кза-
ди. Артерия идет кзади вдоль внутренней поверхности глазодвигательного не-
рва, затем медиально и впадает в заднюю мозговую артерию (ЗМА). Таким об-
разом, ЗСАявляется как бы анастомозом между ВСА и ЗМА. На своем пути ЗСА
кровоснабжает лежащие рядом образования (перекрест зрительных нервов, зри-
тельный тракт, серый бугор).
От задней поверхности ВСА несколько дистальнее ЗСА отходит передняя
артерия сосудистого сплетения. Она идет кзади и вверх вдоль зрительного трак
та, входит в боковой желудочек и разветвляется в сосудистом сплетении его ниж-
него рога, кровоснабжает заднюю треть скорлупы, зрительный бугор и внутрен-
нюю часть внутренней капсулы.
Средняя мозговая артерия (a. cerebri media) (СМА) отходит от сегмента С1
ВСА. Ее основной ствол равен в среднем 16,2 мм (5---24 мм), а диаметр --- 2,7 мм
(1,5---3,5 мм). Главный ствол (сегмент М1) делится на 2 и более ветвей (до 5), что
соответствует сегменту С2. Деление ВСА может быть рассыпным и магистраль-
ным. При магистральном типе деления ВСА продолжается в СМА, а ЗСА и пе-
редняя мозговая артерия (ПМА) являются ветвями, при рассыпном ветвление
происходит в одной точке.
Веточки СМА сначала идут в том же направлении, что и основной ствол, осо-
бенно если он короткий, а затем в области островка отходят под острым углом
вверх, некоторые веточки поворачивают медиально. Эта точка (сильвиева точ-
ка) обычно располагается на расстоянии 30 мм от внутренней поверхности че-
шуи височной кости.
В зависимости от направления ветвей и области их кровоснабжения разли-
чают группы передних ветвей, идущих к лобной области, верхних --- поднимаю-
щихся к моторной и сенсорной областям, задних --- продолжающих ход основ-
ного ствола и направляющихся к теменной и затылочной долям и нижних ---
опоясывающих сверху вниз височную долю. Артерия кровоснабжает большую
часть боковой поверхности полушария мозга и островок.
ПМА отходит от ВСА и идет вперед и медиально, проходя над хиазмой или
зрительным трактом под передним продырявленным пространством, либо стро-
го по прямой, либо делая изгиб (сегмент А1). В этом сегменте от нее отходит
несколько перфорирующих ветвей, из которых наиболее крупной ветвью яв-
ляется гюбнеровская артерия. Передние перфорирующие артерии входят в мозг
через переднее продырявленное пространство и питают головку хвостатого ядра,
переднюю часть чечевицеобразного ядра, а также внутренней и наружной
капсул. Изредка с одной стороны наблюдается гипоплазия (4% случаев) или
аплазия (1 % случаев), однако небольшая разница в диаметре между сторона-
ми являются правилом. В среднем две ПМА соединяются над зрительным пе-
рекрестом короткой передней соединительной артерией (ПСА), длина которой
в среднем составляет 2,6 мм. В 74% случаев ПСА одна, в 10% их две, реже на-
блюдается плексиформная или другие атипичные конфигурации. Очень ред-
ко имеется ее аплазия (0,3% случаев) либо гипоплазия (9% случаев). После от
хождения передней соединительной артерии ПМА идет кпереди и вверх (А2)
по медиальной поверхности полушарий над мозолистым телом. Часть артерии,
расположенная дистальнее изгиба мозолистого тела, носит название перикал
лозной артерии. Она кровоснабжает медиальные отделы полушарий мозга, ядра
большого мозга, мозолистое тело, частично наружную поверхность лобной и
теменной долей.
Вертебрально базилярная система
После вхождения в субарахноидальное пространство ПА проходит между
стволом мозга и скатом прямо или слегка извиваясь либо делая небольшую
петлю кзади, и соединяется с противоположной ПА обычно у заднего края мое
та. Диаметр левой ПА составляет 2,2---2,3 мм, правой --- 2,1 мм. Первая круп-
ная ветвь ПА --- задняя нижняя мозжечковая артерия. Она вариабельна по
своему ходу и отхождению: в 10% наблюдений отходит от БА, в 10% случа-
ев одна из артерий отсутствует. Задняя нижняя мозжечковая артерия идет про-
ксимально к началу БА, отдавая веточки к стволу и мозжечку. Артерия от-
ходит над большим затылочным отверстием в 57% случаев, ниже --- в 18% на-
блюдений, на уровне отверстия --- в 4% случаев. Часто артерия делает
«каудальную петлю», которая может достигать дуги атланта. В среднем ее ди-
аметр 1,2 мм.
Передняя спинальная артерия --- небольшая ветвь, которая начинается в сред-
нем на расстоянии 5,8 мм от соединения позвоночных артерий и достигает пере-
дней поверхности ствола. Ее диаметр составляет 0,4---0,75 мм.
БА образуется при соединении позвоночных артерий и затем делится на две
задние мозговые артерии. Она имеет длину в среднем 30 мм (24---41 мм) и диа-
метр в среднем 3 мм (2,5---3,5 мм). Обычно она прямая, но может и слегка повора-
чивать в сторону (10---20%). Иногда она образует S образный изгиб между ска-
том и стволом мозга.
Передняя нижняя мозжечковая артерия начинается от нижней трети БА при-
мерно в половине наблюдений и от средней трети --- в остальных случаях. Ухо-
дит к передненижним отделам мозжечка, кровоснабжая их. Обычно она намно-
го тоньше, чем задняя нижняя мозжечковая артерия.
Верхняя мозжечковая артерия обычно отходит от конечной части БА. Пер-
вые несколько сантиметров она идет вперед и латерально, почти параллельно
ЗМА. В среднем ее диаметр составляет 1,9 мм. Перегибается через ножки мозга
и идет к верхней поверхности мозжечка, кровоснабжая ее.
ЗМА является анатомически и функционально пограничным сосудом меж-
ду каротидной и вертебрально базилярной системами. Фило и онтогенетичес-
ки она происходит из ВСА и только позже развивается ее связь с БА. Примерно
у 10% взрослых ЗМА отходит от ВСА (так называемая задняя трифуркация
ВСА). Ее первый сегмент (PI) идет кпереди и кнаружи до ЗСА и затем поворачи-
вает кзади вокруг ножки мозга (Р2), прилегая к краю тенториального отверстия,
идет вверх и латерально по нижней поверхности затылочной доли, отдавая кор-
ковые периферические ветви, которые кровоснабжают затылочную и частично
височную доли. Диаметр PI составляет 2,1 мм, Р2 --- 2 3,3 мм. В начальном сег-
менте отдает перфорирующие ветви, которые, проходя через заднее продыряв-
ленное отверстие, кровоснабжают подкорковые узлы, ножки мозга, сосудистое
сплетение III и боковых желудочков.
ЗСА имеет множество вариантов развития. В 22% наблюдений она гипопла
стична. В среднем ее длина 14 мм, диаметр --- 1,2 мм. Примерное 15% случаев
отмечается аплазия с одной или обеих сторон. Она идет кзади и слегка латераль-
ноотЗМАкВСА.
III. Коллатеральное кровоснабжение
Коллатеральные пути могут компенсировать уменьшенный поток, когда
высокая степень стеноза или окклюзия развиваются в экстра и интракрани
альных артериях. Артерии, которые в норме не принимают участия в крово
снабжении мозга, могут включаться в кровоток и, реже, сосуды мозга могут
включаться в кровоснабжение верхней конечности (обкрадывание из позво-
ночной, базилярной или сонной артерий при окклюзии проксимального уча-
стка подключичной артерии или плечеголовного ствола). Включение колла-
теральных путей и направление кровотока зависит от градиента давления.
/. Глазничные коллатерали.
Глазничная артерия в норме кровоснабжается из ВСА, и ее конечные вет-
ви анастомозируют с ипси и контралатеральными НСА. Водораздел суще-
ствует в области фронтоорбитального анастомоза. При стенозе высокой сте-
пени ВСА проксимальнее места отхождения глазничной артерии водораздел
смещается из экстра в интраорбитальную область. Выраженное уменьшение
потока в ВСА и НСА с одной стороны вызывает ретроградный кровоток че-
рез соответствующие орбитальные артерии из ветвей контралатеральной НСА
(ветви артерии спинки носа и дистальные анастомозы в области надблоковых
артерий).
2. Затылочно позвоночные анастомозы.
Анастомозы между ветвями затылочной артерии и мышечными ветвями УЗ
сегмента ПА формируют главную экстракраниальную связь между каротидной
и вертебрально базилярной системами. При проксимальной окклюзии ПА пер-
фузию дистального участка могут обеспечить затылочно позвоночные анасто-
мозы, также как при окклюзии ОСА и проксимальной НСА направление кро-
вотока может реверсировать.
3. Позвоночная артерия как коллатеральный путь.
Дефицит, вызываемый унилатеральной окклюзией ПА, компенсируется со-
ответствующим увеличением потока через противоположную ПА. Реверсирова-
ние коллатерального потока через ПА может иметь место при окклюзии прокси-
мального участка подключичной артерии или брахиоцефального ствола. Поток
из ПА или, реже, из БА носит название подключичного обкрадывания.
4. Артериальный круг большого мозга (виллизиев круг).
Этот анастомоз на основании мозга соединяет каротидные системы друг
с другом и с вертебрально базилярной системой через передние и задние соеди-
нительные артерии.
Артериальный круг --- наиболее важная система уравнивания и распределе-
ния давления в артериях, снабжающих мозг. Она может быть чрезвычайно ва-
риабельна и в 3---4% случаев незамкнута. Классическая ее конфигурация име-
ется лишь у 20% людей, в других случаях те или иные участки крута гипоплас
тичны. При гипо или аплазии одной из передних мозговых артерий
кровоснабжение на стороне недоразвития осуществляется за счет противополож-
ной сонной артерии. Такой вариант развития, при котором одна ВСА питает кро-
вью СМАи обе ПМА, называется передней трифуркацией ВСА.
Задние соединительные артерии наиболее вариабельны. Часто одна из арте-
рий по диаметру меньше другой.
Наибольшего внимания заслуживают варианты развития, при которых от-
сутствует одна из соединительных артерий. В таких случаях артериальный круг
большого мозга оказывается разомкнутым.
Вены головного мозга
Венозная система головного мозга представлена венами мозга и мозговыми
синусами. Различают поверхностные и глубокие вены мозга.
Поверхностные вены расположены в извилинах коры мозга и впадают в ве-
нозные синусы. По распределению и количеству поверхностные вены мозга
очень варьируют. Между ними имеется большое количество анастомозов. По-
верхностные вены широко анастомозируют также с глубокими венами мозга
посредством системы венозных каналов, проходящих через толщу белого и се-
рого вещества полушарий мозга.
Глубокие вены собирают кровь из глубоких структур мозга (подкорковые
узлы, сосудистые сплетения и стенки желудочков). Они представлены веной
прозрачной перегородки, конечной веной, расположенной между хвостатым
ядром и зрительным бугром, и веной сосудистого сплетения. Эти три вены, сли-
ваясь, образуют внутреннюю вену мозга, в которую затем впадает базальная вена,
собирающая кровь из извилин основания мозга и дна III желудочка. При слия-
нии правой и левой внутренних вен образуется большая вена мозга (вена Гале
на), которая идет по внутренней поверхности утолщения мозолистого тела и впа-
дает в прямой синус.
Оттекающая по поверхностным и глубоким венам кровь собирается в веноз-
ных синусах мозга.
Венозные синусы представляют собой полости, расположенные в расщепле-
ниях твердой мозговой оболочки. Перед впадением в синус вены на протяжении
1 ---2 см могут свободно лежать в субарахноидал ьном пространстве.
Синусы бывают непарными (расположенными по средней линии) и парными.
Среди непарных синусов различают следующие:
1. Верхний продольный синус, расположенный в месте прикрепления серпо-
видного отростка к своду черепа. Он собирает кровь из поверхностных вен лоб-
ной, теменной и затылочной долей мозга и частично из костей свода черепа.
2. Нижний продольный синус, идущий по нижнему краю серповидного от-
ростка над мозолистым телом и впадающий в прямой синус, собирает кровь из
мозолистого тела и внутренней поверхности полушарий мозга.
3. Прямой синус, идущий по линии соединения серповидного отростка с на-
метом мозжечка. В него впадают большая мозговая вена и нижний продольный
синус. Прямой синус, соединяясь с верхним продольным, образует в области
затылочного бугра слияние (сток) синусов.
4. Затылочный синус, который начинается от внутреннего бугра затылочной
кости и идет по линии прикрепления серповидного отростка мозжечка к заты-
лочной кости. Этот синус направляется к большому затылочному отверстию,
обходя его справа и слева и впадая в сигмовидный синус.
Основными из парных синусов являются следующие:
1. Пещеристый синус, располагающийся на основании черепа по обеим сто-
ронам от турецкого седла. Внутри синуса расположены внутренняя сонная ар-
терия с симпатическим нервным сплетением и отводящий нерв. В верхней стен-
ке синуса проходят глазодвигательный и блоковидный нервы, в латеральной ---
I ветвь тройничного нерва. В пещеристый синус впадают верхняя и нижняя глаз-
ничные вены, которые через многочисленные анастомозы сообщаются с вена-
ми лица. Поэтому воспалительные заболевания лица могут распространяться
в полость черепа.
2. Клиновидно теменной синус, который начинается в теменной области и
идет вниз вдоль заднего края малых крыльев основной кости. Он соединяет ка-
вернозный синус с верхним продольным.
3. Верхний каменистый и нижний каменистый синусы, начинающиеся от
кавернозного синуса. Идут соответственно по верхнему и нижнему краям пира-
миды височной кости, затем впадают в сигмовидный синус.
4. Поперечный синус, идущий от места слияния синусов латерально по линии
прикрепления намета мозжечка к черепу в борозде поперечного синуса.
5. Сигмовидный синус, являющийся непосредственным продолжением по-
перечного. S образно изгибаясь, этот синус располагается в борозде сигмовид-
ного синуса височной кости и впадает в луковицу внутренней яремной вены,
которая через яремное отверстие выходит из полости черепа.
Таким образом, основная масса венозной крови оттекает от головного мозга
по внутренней яремной вене. Однако эта вена является не единственным путем
оттока крови. Множество эмиссариев в костях черепа и связь синусов твердой
мозговой оболочки с диплоическими венами черепа обеспечивают отток крови
в вены мягких тканей головы, т. е. в экстракраниальную венозную систему.
Список литературы
1. Авдеев Г.А. Томография черепа.--- Л.: Медицина, 1965.--- 196 с.
2. Алыпгаузен H.H. Нейрорентгенология детского возраста.--- М.: Медгиз,
1956. 180 с.
3. Верещагин Н.В., Брагина Л.К., Вавилов СБ., Левина Г.Я. Компьютерная то-
мография мозга.--- М.: Медицина, 1986.--- 251 с.
4. Дьяченко В.А. Рентгеноостеология.--- М.: Медгиз, 1954.--- 298 с.
5. Есиновская Г.Н. Краткое пособие по нейрорентгенологии.--- М.: Медици-
на, 1965. 270 с.
6. Злотник Э., Антонов И., Кастрицкая 3., Олешкевич Ф. Ангиографическая
диагностика сосудистых поражений и опухолей головного мозга.--- Минск: Бе-
ларусь, 1973. 296 с.
7. Коваль Г.Ю. Клиническая рентгеноанатомия.--- Киев: Здоров'я, 1975.---
600 с.
8. Коновалов А.Н., Корниенко В.Н. Компьютерная томография в нейрохирур-
гической клинике.--- М.: Медицина, 1985.--- 290 с.
9. Коновалов А. Н., Корниенко ВН., Пронин H.H. Магнитно резонансная то-
мография в нейрохирургии.--- М.: Видар, 1997.--- 315 с.
10. Копылов М.Б. Основы рентгенодиагностики заболеваний головного моз-
га.--- М.: Медицина, 1968.--- 115 с.
11. Корниенко В.Н., Озерова В.И. Детская нейрорентгенология.--- М.: Меди-
цина, 1993. 445 с.
12. Майкова Строганова В. С., Рохлин Д. Г. Кости и суставы в рентгеновском
изображении.--- Т. 1.--- М.: Медгиз, 1957.--- 475 с.
13. Общее руководство по радиологии / Под ред. П.Петтерссона.--- Nicer,
1995. 558 с.
14. Трофимова Т.Н., Назинкина Ю.В., Ананьева H.H. и др. Нормальная луче-
вая анатомия головного мозга (KT, MPT, УЗИ).--- СПб.: СПбМАПО, 2004.---
51 с.
15. Файзуллин М.Х. Рентгенодиагностика заболеваний и повреждений при-
даточных полостей носа.--- М.: Медгиз, 1961.--- 224 с.
16. Шлифер И. Г. Рентгенодиагностика.---Т. 1.--- Киев, 1941.---544 с.
17. Higgins СВ., Hricak Н., Helms CA. Magnetic resonance imaging of the body.
2nd ed.---New York: Raven Press, 1992.--- P. 355 381.
18. Pancoast H., Pendergrass E., Schaeffer J. The Head and Neck in Roentgen
Diagnosis.--- Philadelphia, 1940.---974 c.
19. Robett R., John R. Clinical Magnetic Resonance Imagine.--- Philadelphia,
1990. P. 528 622.
20. Stark D.D., Bradley W.G. Magnetic resonance imaging. 2nd ed.--- St. Louis:
Mosby Year Book, 1992. P. 988 1165.
21. Taverns J., Wood E. Diagnostic Neuroradiology--- Baltimore, 1964.--- 1960 p.
Глава 2
ИСПОЛЬЗОВАНИЕ МАГНИТНО
РЕЗОНАНСНОЙ ТОМОГРАФИИ В ОЦЕНКЕ
СОСТОЯНИЯ ГОЛОВНОГО МОЗГА ПЛОДА
В АНТЕНАТАЛЬНОМ ПЕРИОДЕ
Все, что нам нужно, уже есть в наших головах.
Теодор Рузвельт
Первые сведения о проведении МРТ плода in utero относятся к началу 1980 х
годов, но эти исследования не получили широкого распространения. Это связа-
но, в первую очередь, с движениями плода, которые являются причиной возник-
новения значительных артефактов. Для того чтобы уменьшить его двигательную
активность, ранее приходилось применять различные седативные средства, ку
рарезацию, что, несомненно, было потенциально опасно для здоровья как мате-
ри, так и ребенка. Использование быстрых импульсных последовательностей
(fast MR imaging sequences), которые проводятся на задержке дыхания беремен-
ной, позволяет избежать применения фармакологических препаратов, препят-
ствует появлению артефактов, создаваемых движениями матери и плода.
Показания к проведению магнитно резонансной
томографии в антенатальном периоде
УЗИ является методом выбора при оценке состояния плода. Сонография по-
зволяет визуализировать различные аномалии развития, получить изображения
в условиях реального времени, характеризуется низкой стоимостью, является
безопасным методом. При ее проведении в большинстве случаев не возникает
каких либо трудностей. Однако ожирение матери, ягодичное предлежание пло-
да и олигогидрамнион значительно ухудшают визуализацию плода. В III триме-
стре беременности может происходить оссификация свода черепа плода, что
делает невозможной детальную оценку многих структур головного мозга вслед-
ствие реверберации и плохого проникновения сигнала.
Итак, в Ш триместре беременности возникают трудности в диагностике ано-
малий головного мозга только по данным сонографии и появляется необходи-
мость использовать альтернативные методы визуализации. Компьютерная то-
мография дает возможность выявить некоторые аномалии развития головного
мозга плода. Однако применение этого метода в гинекологической практике ог-
раничено из за ионизирующего излучения. МРТ обладает более высокой разре-
шающей способностью в визуализации структур головного мозга, позволяет по
лучать мультипланарные изображения с большим полем обзора, не связана
с ионизирующим излучением. Таким образом, МРТ является дополнительным
методом оценки состояния плода во 11 и 111 триместрах беременности в тех слу-
чаях, когда возможности УЗИ ограничены.
МРТ не претендует на место скринингового метода при исследовании плода,
оставляя приоритет за УЗИ. Однако она позволяет не только уточнить характер
аномалии, выявленной или заподозренной при УЗИ, но и идентифицировать те
изменения, визуализация которых находится за пределами возможностей соног
рафии, например, при нарушениях нейрональной миграции.
Противопоказания к проведению магнитно резонансной
томографии в антенатальном периоде
МРТ считается безвредной для плода, рискухудшения его состояния крайне
мал и несущественен. Неопределенность и сомнения относительно проведения
М РТ в течение беременности обусловлены отсутствием исследований, сфоку-
сированных на возможных эффектах воздействия на человеческий эмбрион или
плод. Хотя большинство исследований не выявило тератогенного эффекта маг-
нитного поля, параметры которого соответствуют используемым в клинической
практике (1,5 Т), существует необоснованный скептицизм, обусловленный не-
сколькими ранними публикациями. Проведение исследований с использова-
нием MP томографов напряженностью 1,5 Т не влияет на рост и массу тела пло-
да. Контрольные обследования детей, у которых в антенатальном периоде была
проведена МРТ, проводимые втечение 3 лет, также не выявили существенных
отклонений в их развитии. Обследование женщин --- сотрудников кабинетов
М РТ не зарегистрировало существенного увеличения частоты развития ослож-
нений беременности и неблагоприятных ее исходов.
Согласно инструкции Комитета защиты при Обществе М РТ, проведение ис-
следования показано беременным в том случае, если использование других ме-
тодов неинформативно, а также есть надежда получить важную информацию,
которая может быть получена только с применением ионизирующих методов.
Вследствие этого проведение МРТ в период беременности требует получения
информированного согласия женщины, несмотря на отсутствие данных о том,
что данная процедура может сопровождаться отрицательными эффектами.
Известно, что процесс клеточной пролиферации при развитии плода втечение
I триместра беременности, чувствителен к воздействию внешних физических
факторов. Поэтому в этот период рекомендуется ограничить проведение М РТ.
Не рекомендуется использование контрастирующих веществ в антенаталь-
ном периоде. После внутривенного введения препараты гадолиния проникают
через плаценту и скапливаются в мочевом пузыре плода. Из мочевого пузыря
они экскретируется в амниотическую жидкость, откуда может происходить ре
абсорбция в желудочно кишечный тракт, что потенциально может нанести вред
плоду. Тем не менее риск возникновения осложнений после введения одной дозы
препарата гадолиния невелик.
Остальные противопоказания для проведения М РТ являются стандартны-
ми (наличие кардиостимуляторов, ферромагнитных имплантантов, клаустрофо-
бия и т. д.).
Формирование коры головного мозга плода
Усовершенствование технологий проведения МРТ позволяет диагностиро-
вать различные аномалии и повреждения головного мозга плода, поэтому зна-
ния о процессах нормального формирования и созревания головного мозга важ-
ны для адекватной интерпретации результатов исследований. Для оценки раз-
вития головного мозга проводились корреляционные исследования, в которых
результаты МРТ (как in vitro, так и in vivo) сравнивались с данными гистологи-
ческих исследований.
Эмбриологические данные свидетельствуют о том, что на 10 й неделе гес
тации кора имеет индивидуальное строение. В глубоких отделах мозга, над
эпендимой, определяется большая плотная полоса незрелых клеток, окружа-
ющих желудочек, которая называется терминальной зоной (или матриксом).
После 10 недель матрикс располагается над ганглиевым возвышением (в бо-
розде между хвостатым ядром и таламусом), простираясь от лобного до височ-
ного рогов боковых желудочков. В дальнейшем матрикс истончается. С 7 й до
16 й недели гестации концентрические волны или параллельные ряды мигри-
рующих клеток видны в промежуточной зоне. Эти популяции клеток форми-
руют кору изнутри кнаружи. Митозы нейронов в юкста вентрикулярной об-
ласти прекращаются к 15--- 16 й неделе гестации. В матриксе определяются ред-
кие митозы. Процессы миграции уменьшаются, но миграция дочерних и
глиальных клеток продолжается, пока матрикс не истощится. К 26---28 й неделе
гестации небольшое количество незрелых клеток остается в перивентрикуляр
ной зоне. Исключениями являются ганглиевое возвышение, наружная стен-
ка затылочного рога желудочка, часть височного рога. Во всех случаях шес
тислойный паттерн моторной коры заканчивает формирование к 28 й неделе
внутриутробного развития.
С 19 й недели гестации размеры головного мозга становятся достаточными
для дифференциации отдельных структур на МРТ изображениях. При этом
определяется корреляция между МРТ изображениями слоев и гистологически-
ми группами клеток. На 16 й неделе гестации пространственное разрешение не
позволяет отделить матрикс от мигрирующих клеток, поэтому дифференциру-
ется трехслойный паттерн головного мозга.
С 19 й по 22 ю неделю гестации дифференцируются 4 слоя. Первый слой
соответствует терминальному матриксу второй слой, имеющий промежуточную
интенсивность сигнала,--- нейроглиальным мигрирующим клеткам, третий
слой --- наружной области промежуточной зоны, наружный --- коре (рис. 2.1).
На 27 й неделе беременности дифференцируются 3 слоя. Первый слой соот-
ветствует матриксу, содержащему небольшое количество мигрирующих клеток,
промежуточная зона --- белому веществу, наружная зона --- зрелой коре, которая
имеет определенную ламинацию слоев.
а
б
Рис. 2.1. Беременность 21---22 недели. МРТ.
а --- аксиальная плоскость, SS FSE ИП, Т2 ВИ;
б --- корональная плоскость, SS FSE ИП, Т2 ВИ.
Дифференцируется четырехслойная картина головного мозга: внутренний слой ---
терминальный матрикс, располагающийся в виде тонкой полосы вокруг желудоч-
ков, характеризующийся гипоинтенсивным сигналом: 2 й слой имеет среднюю ин-
тенсивность сигнала и соответствует полосе мигрирующих клеток; 3 й слой --- про-
межуточная зона (формирующееся белое вещество); наружный слой --- кора. Кар-
тина соответствует сроку гестации.
На 34 й неделе гестации визуализируются только два слоя: внутренний, со-
ответствующий белому веществу, и наружный --- кора.
Имеется зависимость между интенсивностью сигнала на МРТ изображени
ях и клеточной плотностью при гистологическом исследовании. Терминальный
матрикс и кортикальная пластинка имеют высокую клеточную плотность, что
проявляется сигналом высокой интенсивности на Т1 ВИ и низкой интенсив-
ности наТ2 ВИ.
Методики проведения магнитно резонансной
томографии плода
Основная проблема при проведении МРТ в антенатальном периоде связана
с движениями плода. В 80---90 х годах прошлого столетия для ее решения ис-
пользовались седативные средства. Перед исследованием женщина принимала
1 г бензодиазепина или флунитрозепама, что обеспечивало уменьшение дви-
гательной активности плода и получение качественных изображений. Имеются
публикации о катетеризации пупочной вены с введением курареподобных пре
паратов (панкурония бромида). Общее время исследования составляло более
2 часов, что, конечно же, тяжело переносилось женщиной.
Позднее стали использоваться эхо планарные изображения. Они отличают-
ся коротким временем получения, что позволяет проводить исследование на за-
держке дыхания и тем самым избегать использования фармакологических пре-
паратов. Однако эхо планарные изображения характеризуются значительной
магнитной чувствительностью, что проявляется искажениями и нечеткостью
изображений.
На современном этапе наиболее широкое распространение получили быст-
рые импульсные последовательности на основе полупреобразования Фурье,
когда К пространство заполняется не полностью, а наполовину, что в два раза
уменьшает время получения данных. В программный пакет большинства совре-
менных диагностических MP томографов входят быстрые импульсные после-
довательности (single shot fast spin echo и half Fourier acquisition turbo spin echo),
позволяющие получать Т2 ВИ высокого качества за очень короткое время, 1---
2 секунды. Таким образом, использование быстрых импульсных последователь-
ностей ИП позволяет эффективно «заморозить» движения плода и получить се-
рию изображений за время однократной задержки дыхания.
Исследование проводится в положении беременной лежа на спине или на
боку. Первым этапом является получение пристрелочных (локализационных)
изображений, далее в трех ортогональных плоскостях. Особенностью методики
внутриутробного обследования плода является неоднократное планирование
расположения срезов, что связано с изменением положения плода во время ис-
следования.
МРТ диагностика аномалий развития головного мозга
в антенатальном периоде
МРТ является эффективным методом выявления опухолей, нарушений моз-
гового кровообращения, аномалий развития головного мозга плода: мозолисто-
го тела, структур задней черепной ямки, мальформаций кортикального разви-
тия (рис. 2.2---2.4).
Диагностика мальформаций мозолистого тела поданным УЗИ часто пред-
ставляет сложности. Результаты МРТ обследования плода на сроке более 20 не-
дель гестации по своей информативности сравнимы с данными МРТ в пост
натальном периоде (рис. 2.5,2.6).
УЗИ характеризуется низкой чувствительностью в выявлении мальформа-
ций кортикального развития. МРТ позволяет диагностировать такие наруше-
ния нейрональной миграции, как лиссэнцефалия, гетеротопия, шизэнцефа
лия.
Поданным D.Levine и соавт, МРТ в 55% случаев предоставляет дополни-
тельные данные, что в 39% наблюдений позволяет изменить первоначальный
диагноз. Результаты исследований отечественных авторов показывают, что МРТ
позволяет уточнить данные клинического и УЗ исследования в 74% случаев.
а
б
Рис. 2.2. Беременность 37 недель.
Опухоль головного мозга плода (хориоидпапилома). МРТ.
а --- аксиальная плоскость, SS FSE ИП, Т2 ВИ. В левой гемисфере головного мозга
плода выявляется больших размеров патологическое образование неоднородной
структуры с наличием кистозного компонента. Правый боковой желудочек значи-
тельно расширен. Атрофия белого вещества правой гемисферы большого мозга,
б --- сагиттальная плоскость, SS FSE ИП, Т2 ВИ. Вариант аномалии Денди --- Уол
кера. Гипоплазия червя мозжечка, увеличение размеров большой цистерны мозга.
Рис. 2.3. Беременность 21---22
недели. Расщелина верхней губы.
МРТ, аксиальная плоскость,
SS FSE ИП, Т2 ВИ.
Расщелина верхней губы (стрелка) и,
вероятно, верхней челюсти, распола-
гается парамедианно справа. Дефор-
мация лицевого черепа плода в обла-
сти верхней челюсти.
Рис. 2.4. Беременность 28 29 недель. Вариант аномалии Денди --- Уолкера. МРТ.
а --- сагиттальная плоскость, SS FSE ИП, Т2 ВИ; б --- корональная плоскость, SS FSE
ИП, Т2 ВИ.
Гипоплазия нижнего червя мозжечка. Расширение ретроцебеллярного субарахно
идального пространства. Умеренно выраженная вентрикуломегалия.
а
б
Рис. 2.5. Беременность 28---29 недель. Вентрикуломегалия, сочетающаяся
с агенезией мозолистого тела. MPT, SS FSE ИП, Т2 ВИ.
а --- корональная плоскость. Мозолистое тело отсутствует. Определяется высокое
расположение третьего желудочка. Боковые желудочки широко расставлены,
б --- аксиальная плоскость. Задние отделы боковых желудочков колбообразно рас-
ширены. Отмечается расширение межполушарной щели.
Рис. 2.6. Беременность 36
недель. Гидроцефалия. МРТ.
Сагиттальная плоскость,
SS FSE, Т2 ВИ.
Значительное расширение боко-
вого желудочка.
МРТ является дополнитель-
ным способом визуализации
структур головного мозга плода.
Он дополняет УЗ И в тех случа-
ях, когда применение соногра
фии технически ограничено
либо ее результаты сомнительны
и противоречивы.
Список литературы
1. Smith F.M., Adam А.Н., Phillips W.D. NMR imaging in pregnancy // Lancet---
1983. Vol. !.--- P. 61 62.
2. Sonigo PC, Rypens F.F., Carteret M. et al. MR imaging of fetal cerebral anoma-
lies // Pediatr. Radiol. 1998. Vol. 28. P. 212 222.
3. Garel C, Brisse H., Sebag G. et al. MR imaging of the fetus // Pediatr. Radiol.---
1998. Vol. 28. P. 201 210.
4. Amin R.S., Nikolaidis P., Kawashima A. et al. Normal anatomy of the fetus at MR
imaging// Radiographics.--- 1999.--- Vol. 19. P. 201 214.
5. Kubik Huch R.A., Wisser Т., Ladd M.E. et al. Prenatal diagnosis of fetal
malformations by ultrafast magnetic resonance imaging // Prenat. Diagn.--- 1998.---
Vol. 18. P. 1205 1208.
6. Levine D., Barnes P.D., Madsen J.R. et al. Fetal central nervous system anomalies:
MR imaging augments sonographic diagnosis // Radiology--- 1997.--- Vol. 204.---
P. 635 642.
7. Levine D., Edelman R.R. Fast MRI and its application in obstetrics // Abdom
Imaging. 1997. Vol. 22. P. 589 596.
8. Levine D., Barnes P.D., Edelman R.R. Obstetric MR imaging // Radiology.---
1999. Vol. 211. P. 609 617.
9. Girard N.J., Raybaud C.A. Ventriculomegaly and pericerebral CSF collection in
the fetus: early stage of benign external hydrocephalus? // Child's Nerv. Syst.--- 2001 .---
Vol. 17. P. 239 245.
10. Glastonbury СМ., Kennedy A.M. Ultrafast MRI of the fetus // Australian
Radiology 2002. Vol. 46. P. 22 32.
11. Chong B. W., Babcook С J., Salamat M.S. et al. A magnetic resonance template for
neuronal migration in the fetus // Neurosurgery.--- 1996.--- Vol. 39, No 1.--- P. 110 116.
12. Kanal E. Pregnancy and the safety of magnetic resonance imaging // Magn.
Reson. Imaging Clin. North Amer.- 1994.- Vol. 2.- P. 309-317.
13. Brisse H., Faller C, Sebag G. etal. Supratentorial parenchyma in the developing
fetal brain: in vitro MR study with histologic comparison // A. J. N. R.--- 1997.---
Vol. 18.- P. 1491-1497.
14. Girard N., Raybaud C.A., Poncet M. In vivo MR study of brain maturation in
normal fetuses // A. J. N. R.--- 1995.- Vol. 16.- P. 407-413.
15. Coakley F. V., Hrisak H., Filly R.A. et al. Complex fetal disorders: effect of MR
imaging on management-preliminary clinical experience // Radiology.--- 1999.---
Vol. 213.- P. 691-696.
16. Lan L.M., Yamashita Y., Tang Y. et al. Normal fetal brain development: MR
imaging with a Half-Fourier rapid acquisition with relaxation enhancement
sequence.- Radiology- 2000.- Vol. 215.- P. 205-210.
17. Mitchell L.A., Simon E.M., Filly R.A., Barkovich A.J. Antenatal diagnosis of
subependymal heterotopia // A. J. N. R.- 2000.- Vol. 21.- P. 296-300.
Глава 3
АНОМАЛИИ РАЗВИТИЯ ЦЕНТРАЛЬНОЙ
НЕРВНОЙ СИСТЕМЫ
С каждым шагом методики вперед мы как бы поднима-
емся ступенью выше, с которой открывается нам более
широкий горизонт, с невидимыми раньше предметами.
И. П. Павлов
Выявление и клиническая интерпретация симптоматики при патологических
процессах головного мозга у новорожденных и детей раннего возраста традици-
онно вызывает большие трудности. Нейрорадиологические исследования зача-
стую существенно дополняют и помогают в постановке диагноза, оценке дина-
мики и исхода заболевания.
Абсолютные показания к использованию нейрорадиологических методов
следующие:
недоношенность (особенно до 32 й недели гестации удетей с массой тела
менее 1500 г);
неврологическая симптоматика поражения головного мозга (судорожный
синдром, задержка психомоторного развития, гидроцефальный синдром, при-
знаки органического или инфекционного поражения ЦНС);
родовая травма;
множественные стигмы дизэмбриогенеза;
проявления асфиксии и гипоксии в родах.
При прочих осложнениях антенатального и интранатального периодов вопрос
о применении дополнительных методов исследования решается индивидуально.
РАЗВИТИЕ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ
Нервная система развивается из наружного зародышевого листка --- экто-
дермы. Ее утолщение, расположенное вдоль дорсальной поверхности туловища,
формирует нервную пластинку (2 я неделя гестации).
В дальнейшем края нервной пластинки утолщаются и сближаются, в то вре-
мя как сама пластинка углубляется и образует нервную бороздку. Края плас-
тинки, принявшие форму нервных валиков, соединяются и образуют нервную
трубку, которая, погружаясь в глубину, отшнуровывается от эктодермы (3 я не-
деля гестации).
Одновременно из клеток, входящих в состав нервных валиков, образуются
узловые (ганглиозные) пластинки. В дальнейшем они расщепляются: часть их,
располагаясь в виде валиков по бокам нервной трубки, ближе к ее дорсальной
поверхности, образуют спинномозговые узлы; другие нервные клетки мигриру-
ют на периферию, образуя узлы вегетативной нервной системы.
Различная дифференцировка и неравномерность роста нервной трубки зна-
чительно изменяют ее внутреннюю структуру, внешний вид и форму полости.
Расширенный краниальный отдел нервной трубки развивается в головной мозг,
а остальная ее часть --- в спинной мозг.
На 4 й неделе гестации после закрытия переднего отверстия нервной трубки
образуются три первичных мозговых пузыря: прозэнцефалон (передний мозг),
мезэнцефалон (средний мозг) и ромбэнцефалон (задний мозг). Затем происхо-
дит быстрый рост трубки с формированием изгибов в области среднего мозга и
между задним мозгом и спинным мозгом.
На 5 й неделе гестации передний мозг делится на два пузыря: телэнцефалон
(конечный мозг) идиэнцефалон (промежуточный мозг). Средний мозг не делит-
ся и становится третьим мозговым пузырем. Ромбовидный мозг делится на ме
тэнцефалон (задний) и миелэнцефалон (промежуточный) мозг. Одновременно
образуется ряд изгибов: теменной на уровне среднего мозгового пузыря, мосто-
вой --- в области заднего мозгового пузыря и затылочный --- в месте перехода
спинного мозга в продолговатый.
Со временем стенки мозговых пузырей утолщаются, рельеф поверхности ус-
ложняется, в центральных отделах формируются различные по величине и по-
ложению полости, из которых в дальнейшем развиваются желудочки мозга. Они
заполнены спинномозговой жидкостью и сообщаются между собой и с централь-
ным каналом спинного мозга. Стенка каждого мозгового пузыря развивается
в определенную часть головного мозга, а полость превращается в соответству-
ющий желудочек. Вентральная часть ромбовидного мозга преобразуется в про-
долговатый мозг, его задняя стенка остается тонкой пластинкой и образует ниж-
ний мозговой парус. Задний мозг составляют мозжечок и мост. Полость ромбо-
видного мозга превращается в IV желудочек, который посредством отверстий
сообщается с подпаутинным пространством. Ворсинчатая подстилка формиру-
ется из тонкой эпендимальной крыши IV желудочка и имеющей мезенхималь
ное происхождение мягкой мозговой оболочки (pia mater). Путем пролиферации
васкуляризированной мягкой мозговой оболочки ворсинчатая подстилка вне-
дряется в IV желудочек и дифференцируется в ворсинчатое сплетение. Так фор-
мируются все 4 ворсинчатые сплетения (в III, боковых и IVжелудочках). На 9 й
неделе беременности клетки сосудистого сплетения становятся секретирующи
ми и начинают продуцировать спинномозговую жидкость.
Дорсальная стенка III мозгового пузыря образует крышу среднего мозга, или
четверохолмие, а вентральная --- ножки мозга. Полость среднего мозга превра-
щается в узкий канал --- водопровод мозга, соединяющий III и IV желудочки.
Конечный мозг представлен правым и левым полушариями большого мозга,
расположенными над всеми остальными мозговыми пузырями. Полушария состоят
из наружно расположенной коры большого мозга (плащ), белого вещества состав-
ляющего почти всю массу полушарий, базальных ядер, локализующихся в обла-
сти нижних отделов полушарий, и обонятельного мозга, занимающего наиболее
вентральное положение. Полость конечного мозга образует два боковых желудочка.
АНОМАЛИИ РАЗВИТИЯ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ
Аномалии развития ЦНС наблюдаются достаточно часто. Описано более
2000 врожденных мальформаций головного мозга. Встречаются они примерно у
1 % живорожденных. 75% мертворожденных имеют пороки головного мозга,
и'/ всех значительных аномалий развития включают в себя патологию ЦНС.
Выявлено, что 10% интракраниальных аномалий обусловлены хромосомны-
ми аберрациями; 20% --- наследственными факторами; 10% --- повреждающими
внутриутробными факторами (инфекцией); в 60% случаев причина не иденти-
фицирована. Их характер обусловлен стадией развития ЦНС, во время которой
действует повреждающий фактор, его особенностями, интенсивностью и про-
должительностью воздействия. Нарушения органогенеза и гистогенеза могут
привести к возникновению разнообразных пороков развития.
КЛАССИФИКАЦИЯ ВРОЖДЕННЫХ ПОРОКОВ РАЗВИТИЯ
ГОЛОВНОГО МОЗГА
Большинство врожденных пороков ЦНС может быть распознано с помощью
нейрорадиологических методов, таких как КТ, МРТ, УЗИ. В общей совокупно-
сти клинических, лабораторных, лучевых исследований УЗИ является первич-
ным этапом скрининга головного мозга новорожденных. Нередко в процессе
исследования удается определить характер порока. В других случаях результа-
ты УЗИ нуждаются в подкреплении данными КТ, МРТ, генетических исследо-
ваний и т. д.
Все мальформаций разделяются на пороки, обусловленные нарушением ор-
ганогенеза и нарушением гистогенеза (Harwood Nash D., 1992).
1. Нарушения органогенеза (нарушения развития мозга с нормальным гисто-
генезом).
/. Нарушения закрытия нейрональной трубки:
аномалия Арнольда ---Киари;
цефалоцеле;
агенезия мозолистого тела и другие его аномалии;
комплекс Денди --- Уолкера;
краниошизис (менингоцеле, энцефалоцеле и т. д.).
2. Нарушения дшертикуляции или деления мозга:
голопрозэнцефалия (алобарная, семилобарная, лобарная);
септооптическаядисплазия (синдром de Morsier).
3. Нарушения образования извилин и клеточной миграции (мальформаций кор-
тикального развития):
мальформаций, обусловленные измененной нейронной и глиальной про-
лиферацией;
мальформаций, обусловленные изменением нейронной миграции;
мальформаций, обусловленные нарушениями кортикальной организации;
мальформаций кортикального развития, еще не классифицированные.
4. Нарушения размеров:
микроцефалия;
макроцефалия.
5. Деструктивные поражения:
гидранэнцефалия;
порэнцефалия;
воспалительные заболевания, обусловленные краснухой, токсоплазмозом,
герпесом;
гипоксически аноксические поражения.
6. Обструктивные изменения:
стеноз водопровода.
II. Нарушения гистогенеза (общая структура мозга нормальная, но появля-
ются аномальные клетки, которые продолжаются дифференцироваться):
Л Нейрокожные синдромы:
нейрофиброматозы;
энцефалотригеминальный ангиоматоз (синдром Стерджа --- Вебера);
туберозный склероз (болезнь Бурневилля --- Прингла);
цереброретинальный ангиоматоз (болезнь Гиппеля --- Линдау).
2. Сосудистые поражения.
3. Врожденные опухоли:
опухоли и опухолевидные образования.
III. Нарушения цитогенеза
1. Врожденные нарушения метаболизма:
аминоацидурия;
мукополисахаридоз;
липидоз.
2. Лейкодистрофии.
3. Нейрональная дегенерация.
I. НАРУШЕНИЯ ОРГАНОГЕНЕЗА
Нарушение закрытия нейрональной трубки
Цефалоцеле (менингоцеле, энцефалоцеле, энцефаломенингоцеле) представ-
ляет собой дефект черепа, обычно по средней линии, через который пролабиру
ют менингеальные оболочки и вещество мозга. Менингоцеле содержит менин
геальные оболочки и спинномозговую жидкость. Энцефалоцеле включает и моз-
говую ткань, а в энцефаломенингоцеле присутствуют также желудочковые
структуры. Для таких детей типична микроцефалия. Клиническая симптома-
тика широко варьируется --- от минимальной до тяжелой.
Наиболее типичны грыжи лобно решетчатые, в области намета мозжечка,
краниовертебрального перехода. Вариантом затылочного энцефалоцеле являет-
ся аномалия Арнольда --- Киари III, при которой грыжа пролабирует в большое
затылочное отверстие.
Цефалоцеле часто сочетается с дисгенезией мозолистого тела, аномалиями
миграции, кистой Денди --- Уолкера.
Черепно мозговые грыжи часто диагностируются внутриутробно ввиду ти-
пичной ультразвуковой картины --- экстрацеребрального образования, распо-
ложенного чаще в затылочной области с признаками гидроцефалии.
Аномалии Арнольда --- Киари
Аномалия Арнольда --- Киари (I---IV) --- группа не связанных между собой ано-
малий, первоначально описанная Н.СТпап (1981 г.). Вначале были выделены три
типа порока ромбовидного мозга с гидроцефалией. Позднее включена еще и чет-
вертая группа, сочетающаяся с гипоплазией мозжечка.
Аномалия Арнольда --- Киари 1---11 встречается достаточно часто.
Аномалия Арнольда --- Киари I представляет собой тонзиллярную эктопию,
при которой деформированная миндалина мозжечка смещается ниже уровня
большого затылочного отверстия в верхнюю часть цервикального канала
(рис. 3.1). Тонзиллярная эктопия на 3---4 мм является бессимптомной. При сме-
щении миндалин мозжечка на 5 мм и более появляются начальные клинические
признаки. Эта аномалия развития в 20---25% наблюдений связана с сирингогид
ромиелией и умеренной гидроцефалией. Часто она сочетается с аномалией кра
Рис. 3.1. Аномалия Арнольда --- Киари I. МРТ.
а --- корональная плоскость, Т1 ВИ. Миндалины мозжечка удлинены, располага-
ются ниже плоскости большого затылочного отверстия.
б --- сагиттальная плоскость, Т1 ВИ. Большая затылочная цистерна отсутствует.
Ствол мозга смещен кпереди, отмечается сглаженность моста.
Рис 3.2. Аномалия Арнольда --- Киари, сочетающаяся с сирингогидромиелией.
а --- схема срединного сагиттального изображения. Низкое расположение миндали-
ны мозжечка (большая стрелка), сирингомиелия (стрелки).
б --- МРТ, Т1 ВИ, сагиттальная плоскость. Миндалины мозжечка пролабируют ниже
уровня большого затылочного отверстия. Большая цистерна мозга не прослежива-
ется. Продолговатый мозг смешен кпереди, понто медуллярная цистерна сужена.
Сирингомиелия на уровне C, Thr На уровне Th2 прослеживается расширение цен-
трального спинномозгового канала.
в --- МРТ, Т2 ВИ, аксиальный срез на уровне большого затылочного отверстия. Мин-
далины мозжечка плотно выполняют затылочное отверстие, субарахноидальное
пространство не прослеживается.
ниовертебральной области: базилярной импрессией (25% случаев), сращением
С, с затылочной костью (10%), синдромом Клиппеля --- Фейля (10%), незавер-
шенной оссификацией С,(5%) (рис. 3.2).
Применение МРТ предпочтительнее, чем КТ. При МРТ на срединном сагит-
тальном срезе, лучше на Т1 ВИ, определяются удлиненные миндалины мозжеч-
ка, располагающиеся ниже плоскости большого затылочного отверстия. Пролапс
должен быть не менее 3 мм. Большая затылочная цистерна мала или отсутствует.
Часто определяются также смещение ствола мозга кпереди и сглаженность мо-
ста. Смещение ствола мозга приводит к появлению симптома «ступеньки» в месте
перехода продолговатого мозга в спинной.
Аномалия Арнольда --- Киари II --- комплекс пороков, поражающих позвоноч-
ник, череп, твердую мозговую оболочку, ромбовидный мозг. В отличие от анома-
лии Арнольда --- Киари I, она всегда связана с некоторыми формами спиналь
ногодизморфизма, а также менингоцеле или миеломенингоцеле и гидроцефа-
лией (рис. 3.3). Достаточно часто сочетается с супратенториальными пороками.
Рис. 3.3. Беременность 32---33
недели. Аномалия Арнольда ---
Киари II. Вентрикуломегалия.
МРТ. ssFSE ИП, Т2 ВИ.
а, б, в --- изображения головного
мозга в аксиальной, сагиттальной и
корональной плоскостях. Выра-
женное расширение задних отделов
боковых желудочков. Низкое рас-
положение миндалин мозжечка.
Ангуляция шейного отдела позво-
ночника. Спинномозговая грыжа
крестцового отдела позвоночника
(указана стрелкой).
Пороки при аномалии Арнольда --- Киари II многочисленные и сложные. Луче-
вые исследования помогают различать их степени и комбинации.
Аномалии Арнольда --- Киари II может сочетаться с другими пороками развития
(черепа, позвоночника, твердой мозговой оболочки, желудочков мозга, аномалиями
ствола мозга, спинного мозга, мальформациями кортикального развития).
Дисплазия губчатых костей, ведущая к фестончатому истончению свода че-
репа, является не мальформацией, а только сопутствующим симптомом и редко
встречается у детей старше 6 месяцев. Она проявляется низким расположением
синусного стока и поперечных синусов, следствием чего является маленькая и
мелкая задняя черепная ямка; расширенным большим затылочным отверстием,
тенториальной гипоплазией с широкой вырезкой; червь и мозжечок могут про
лабировать вверх через тенториальную вырезку (псевдоопухолъ мозжечка). Также
могут наблюдаться различной степени гипоплазия серпа большого мозга или
срашение его с примыкающей извилиной, что придает межполушарной щели
фестончатый или губчатый вид, уплотнение костей. Скат может казаться вог-
нутым в задних отделах.
Дизгенезия ствола мозга ведет к смещению вниз продолговатого мозга и моз-
жечка. Происходит изгиб продолговатого мозга, выпячивание покрышки и пе
реднемедиальный рост мозжечка по бокам ствола мозга.
Размеры боковых желудочков варьируют от нормальныхдо значительно ди
латированных, часто асимметричных, с выступающими височными рогами, пе-
редние и задние рога могут быть отшнурованы. Таким образом, желудочки час-
то имеют фестончатый вид.
Прозрачная перегородка либо отсутствует, либо сообщается с желудочковой
системой.
III желудочек часто увеличен, с деформированным передним карманом.
IV желудочек нередко удлинен, имеет небольшие размеры, смещен каудально.
Может определяться стеноз или окклюзия водопровода мозга.
Аномалия Арнольда --- Киари 11 может сочетаться с мальформациями корти-
кального развития. Наиболее частыми ассоциированными кортикальными дис
плазиями являются гетеротопия серого вещества, полимикрогирия. Также к со
четанным аномалиям относят аномалии полосатого тела (обычно частичное от-
сутствие либо гипоплазия).
Спинальный дисрафизм, миеломенингоцеле присутствуют почти всегда.
Наиболее часто встречающейся патологией является миеломенингоцеле. В 75%
случаев поражается поясничио крестцовый отдел позвоночника. В спинном мозге
может определяться сирингогидромиелия. Поражение спинного мозга в ряде
случаев обусловлено сдавлением липомой, диастематомиелией.
Аномалия Арнольда --- Киари III встречается редко и представляет собой ано-
малию Арнольда --- Киари II с низким затылочным и высоким шейным энцефа
лоцеле.
Аномалия Арнольда --- Киари IV характеризуется выраженной гипоплазией
мозжечка. Это очень редкая аномалия, не существующая как отдельная нозо-
логическая единица. Определяются отсутствие или гипоплазия мозжечка, ма-
ленький ствол мозга, большая задняя черепная ямка.
При М РТ хорошо видны аномалии краниовертебрального стыка, низкое
расположение удлиненного желудочка (ниже линии, соединяющей бугорок ту-
рецкого седла и внутреннего возвышения затылочной кости), гидромиелия, а
также перечисленные выше сопутствующие дисрафии.
Кисты задней черепной ямки
Эта группа аномалий включает в себя мальформацию Денди --- Уолкера, ва-
рианты аномалии Денди --- Уолкера, ретроцеребеллярные кисты, кистозное рас-
ширение IV желудочка.
Мальформация Денди --- Уолкера представляет собой дисгенезию или агене
зию червя мозжечка, выраженное кистозное расширение IVжелудочка и гипо-
плазию гемисфер мозжечка. Формирование этого порока развития может быть
обусловлено генетически: трисомией 13,18,21 пар хромосом, недостатком в диете
беременной рибофлавина или избытком галактофлавина, а также воздействием
химических агентов и радиации. Точная причина возникновения мальформа
ции Денди --- Уокера неизвестна, но наиболее вероятно происходит нарушение
развития передней медуллярной оболочки (эмбриональной крыши IVжелудоч-
ка), атрезия выводящих отверстий, задержка открытия срединной апертуры
IV желудочка (отверстия Мажанди), кровоизлияния (различной степени) в обе-
их развивающихся мозжечковых гемисферах и в I Ужелудочке. Отверстия Люш
ка и Мажанди отсутствуют. Баллонообразный, кистозно расширенный ^же
лудочек соединяется с большой примитивной кистой, которая оттесняет кпере-
ди гипоплазированный мозжечок. Намет мозжечка смещен кверху (рис. 3.4).
При УЗИ в корональной и сагиттальной плоскостях выявляется следую-
щая характерная картина: в задней черепной ямке выявляется крупная кис-
та, включающая в себя IV желудо-
чек, червь мозжечка не определя-
ется, полушария мозжечка резко
Рис. 3.4. Схема аномалии
Денди --- Уолкера.
Дисгенезия червя мозжечка, выра-
женное кистозное расширение
IV желудочка, который соединяется
с большой примитивной кистой,
смещающей кпереди гипоплазиро-
ванный мозжечок. Намет мозжечка
приподнят кверху.
Рис. 3.5. Вариант аномалии
Денди Уолкера. МРТ. Т1 ВИ,
сагиттальная плоскость.
Червь мозжечка гипоплазирован,
четвертый желудочек и большая ци-
стерна мозга расширены. Намет
мозжечка располагается обычно.
уменьшены в размерах, мозжеч-
ковый намет смешен кверху, III и
боковые желудочки расширены
в различной степени.
Хотя данная патология хорошо
диагностируется и при КТ, и при
МРТ, последняя предпочтитель-
нее: на сагиттальных срезах хорошо видны аномалия червя, киста задней че-
репной ямки, высокое стояние намета мозжечка, аномалия мозолистого тела,
гетеротопии.
а
б
Рис. 3.6. Вариант аномалии Денди --- Уолкера. Частичная агенезия мозолистого тела.
МРТ.
а --- Т1 ВИ, сагиттальная плокость. Нижние отделы червя мозжечка гипоплазиро
ваны. Отверстие Мажанди расширено, полость TV желудочка и большая цистерна
мозга широко соединяются. Большая цистерна мозга и понтомедуллярная цистер-
на расширены.
б --- Т1 ВИ, корональная плоскость. Колено мозолистого тела отсутствует. Межпо
лушарная щель расширена. Атрофия белого вещества мозга.
Варианты аномалии Денди --- Уолкера встречаются более часто. В таких слу-
чаях нижний червь и гемисферы мозжечка менее диспластичны, кистозная транс-
формация IV желудочка имеет менее выраженный характер. Серповидный от-
росток червя часто присутствует (рис. 3.5).
Дифференцировать мальформации Денди --- Уолкера приходится с ретроцере
беллярной арахноидальной кистой. В отличие от мальформации Денди --- Уолкера,
при ретроцеребеллярныхарахноидалъных кистах присутствуют червь, смешенный,
но нормально сформированный, IVжелудочек, отверстия Мажанди, Люшка.
Мальформации Денди --- Уокера более чем в 60% случаев сочетаются с дру-
гими пороками развития головного мозга --- гидроцефалией, дисгенезией мозо-
листого тела, мальформациями кортикального развития (полимикрогирия, ге
теротопии серого вещества), затылочным цефалоцеле, с аномалиями других ор-
ганов и систем организма --- пороками сердца, полидактилией и др. (рис. 3.6).
Ретроцеребеллярная киста
Формируется путем инвагинации ворсинчатого тела IV желудочка кверху и
кзади от интактного червя. Обычно сообщается с IVжелудочком и субарахнои
дальным пространством. Намет мозжечка может быть раздвоен, приподнят,
IV желудочек смещен кпереди и кверху. Желудочковая система умеренно или зна-
чительно расширена (рис. 3.7).
Кистозная трансформация IV желудочка
Кистозное расширение IV желудочка развивается вторично при атрезии отвер-
стий желудочка или эпендимальной кисте. Изолированное кистозное расшире-
ние IV желудочка вызывает верхнее транстенториальное вклинение (рис. 3.8).
Mega cisterna magna
Mega cisterna magna, вероятно, является только вариацией аномалии Денди ---
Уолкера. В этом случае определяются обычно расположенный синус герофили,
нормальный червь мозжечка.
Шунтирование желудочков и кист может привести к ошибкам при проведе-
нии KT и МРТ в послеоперационном периоде, поэтому предоперационное ис-
следование необходимо для постановки правильного диагноза.
Нужно отметить, что так называемый вариант Денди --- Уолкера и mega cisterna
magna являются видами кистозной мальформации задней ямки и в настоящее
время не рассматриваются как самостоятельные нозологические единицы.
Аномалии мозолистого тела
Мозолистое тело развивается на 3---4 м месяце внутриутробной жизни. Его
формирование в основном происходит спереди назад, за исключением клюва.
15
Агенезия может быть полной или частичной. Ее степень зависит от периода раз-
вития головного мозга плода, во время которого произошло повреждение. При ча-
стичной агенезии всегда есть колено, тогда как валик и (или) клюв отсутствуют.
Пороки развития мозолистого тела часто (до 50% случаев) связаны с другими по-
роками ЦНС, такими как мальформации кортикального развития (гетеротопия,
полимикрогирия), с аномалиями Арнольда --- Киари или Денди --- Уолкера, ли-
помами, цефалоцеле, межполушарными арахноидал ьными кистами и т. д.
Под воздействием внешних повреждающих факторов (травматического, ток-
сического, ишемического генеза) может происходить вторичная деструкция мо-
золистого тела.
а
б
Рис. 3.8. Кистозная трансформация IV желудочка. МРТ.
а --- Т1 ВИ, сагиттальная плоскость. IV желудочек имеет округлую форму, резко рас-
ширен. Червь мозжечка гипоплазирован, миндалины располагаются ниже уровня
большого затылочного отверстия. Имеется восходящее мозжечково транстентори
альное вклинение с компрессией четыреххолмной цистерны. Мост и продолгова-
тый мозг смещены кпереди.
б --- Т1 ВИ, коронарная плоскость. Расширение полости IV желудочка выражено не
павномерно, левая гемисфера мозжечка атрофирована в большей степени.
Классические нейрорадиологические признаки агенезии мозолистого тела
:ледующие:
1. Передние рога и тела боковых желудочков широко расставлены и парал-
лельны (не изогнуты). Передние рога узкие, остроугольные. Задние рога ча-
сто диспропорционально увеличены (кольпоцефалия). Вогнутые медиальные
границы боковых желудочков обусловлены протрузией продольных пучков
Пробста.
2. III желудочек обычно дилатирован и приподнят с различной степенью дор-
сального расширения и смешения между боковыми желудочками. Межжелудоч-
ковые отверстия часто удлинены. (
3. Межполушарная борозда кажется продолжением переднего отдела
III желудочка, так как отсутствует колено. Вкорональной проекции межполу-
шарная борозда расширяется книзу между боковыми желудочками по направ-
лению к крыше 111 желудочка. В сагиттальной плоскости обычная поясная из-
вилина отсутствует, и средние борозды имеют радиальную или спицеобразную
конфигурацию. Вокруг III желудочка часто видны межполушарные кисты. При
увеличении размеров эти кисты могут приобретать аномальную конфигурацию
и скрывать нижележащие пороки (рис. 3.9).
Рис. 3.9. Агенезия мозолистого тела,
а --- Т2 ВИ, сагиттальная плоскость;
б --- FLAIR ИП, аксиальная плоскость;
в --- Т1 ВИ, корональная плоскость.
Мозолистое тело отсутствует. На его ме-
сте визуализируются внутренние и боль-
шая вены. Боковые желудочки широко
расставлены, задние рога боковых желу-
дочков диспропорционально расшире-
ны, передние рога узкие, щелевидные.
Контуры задних рогов боковых желудоч-
ков волнистые. Выявляется ретроцебел
лярная киста.
Кисты средней линии
Среди кист средней линии выделяют следующие:
1) кисту прозрачной перегородки (са\тдт вертл реЦийод);
2) кисту Верги (саушп Уег§ае);
3) кисту промежуточного паруса (сауит уеП пиегровШ).
ЭТИ ПОЛОСТИ ЯВЛЯЮТСЯ нормальными структурами головного мозга плода и
часто выявляются при обследовании недоношенных детей. Они запустевают
после рождения, у детей старшего возраста и взрослых являются случайной на-
ходкой. Обычно не сопровождаются клинической симптоматикой, однако при
а
б
Рис. ЗЛО. Киста прозрачной перегодки. МРТ.
а --- Т2 ВИ, аксиальная плоскость. Киста располагается между передними рогами
боковых желудочков, спереди ограничена коленом мозолистого тела,
б --- Т1 ВИ, корональная плоскость. Киста имеет овальную форму, контуры ее вы-
пуклые, оказывает объемное воздействие на передние рога боковых желудочков.
больших размерах могут оказывать давление на прилежащие структуры, а так-
же вызывать нарушения ликвородинамики. Описано нередкое сочетание кист
с эпилепсией, психическими заболеваниями и т. д.
Прозрачная перегородка является медиальной стенкой боковых желудочков,
состоит из двух листков, между которыми находится полость шириной 1---2 мм.
Спереди она ограничена коленом мозолистого тела, сверху --- мозолистым телом,
сзади --- столбами свода. Если полость имеет большие размеры, то она называ-
ется кистой прозрачной перегородки или Vжелудочком (рис. 3.10).
Киста Верги образуется при распространении полости прозрачной перего-
родки кзади и расположена между медиальными стенками боковых желудоч-
ков, мозолистым телом и столбами свода. Эта полость впервые была описа-
на итальянским анатомом Andrea Verga в 1851 г. и в дальнейшем названа его
именем (иногда ее также называют VI желудочком). Она обычно сообщается
с полостью прозрачной перегородки, но может также присутствовать как
изолированная полость. Прозрачная перегородка обычно развивается совместно
с мозолистым телом на 12---19 й неделе внутриутробного развития. Полость про-
зрачной перегородки запустевает постепенно, начиная с задней части. Кис-
та Верги исчезает, начиная с 6 месяцев гестации, полость прозрачной перего-
родки --- вскоре после рождения. После 6 месяцев она встречается у 10% де-
тей и редко у взрослых. Обычно полость не имеет связи с желудочками. Иногда
а
б
Рис. 3.11. Киста промежуточного паруса. МРТ
а --- Т2 ВИ, сагиттальная плоскость. Между III желудочком и задними отделами ство-
ла, валика мозолистого тела располагается полость в форме запятой,
б --- Т2 ВИ, на аксиальном срезе киста имеет треугольную форму, вершина тре-
угольника располагается на уровне межжелудочковых отверстий.
при изменении давления внутри или извне возможна спонтанная перфорация
ее стенки.
Киста прозрачной перегородки выявляется как линзообразная полость меж-
ду медиальными стенками лобных рогов, на фронтальных томограммах распо-
лагается кверху от III желудочка, полость Верги --- как полость между телами
желудочков. Часто обе полости выявляются совместно.
Киста промежуточного паруса --- полость треугольной формы кпереди от чет
верохолмной цистерны, кверху от III желудочка (рис. 3.11). Она формируется
иным образом, нежели вышеописанные кисты: при росте мозолистого тела кза-
ди оно несет на своей нижней поверхности сосудистую мембрану, образующую
крышу III желудочка. Нижняя порция сопровождает крышу III желудочка до
эпифиза, верхняя порция прилежит к мозолистому телу, и, проходя вокруг вали-
ка мозолистого тела, соединяется с сосудистой оболочкой, покрывающей меди-
альную поверхность полушарий. Так образуется щель, содержащая сосудистую
подстилку III желудочка. В большинстве случаев эта щель в дальнейшем запу
стевает. Если она остается открытой, то образует цистерну промежуточного па-
руса, а при больших размерах --- кисту промежуточного паруса.
Киста промежуточного паруса выявляется как треугольная структура между
треугольни ками боковых желудочков. Вершина треугольника лежит на уровне
отверстий Монро, основание образуют передние отделы четверохолмной цистер-
ны. На томограммах в сагиттальной плоскости полость по форме напоминает
запятую.
Нарушение дивертикуляции
К этой группе аномалий развития относится голопрозэнцефалия.
Голопрозэнцефалия --- это порок развития, связанный с нарушением форми-
рования переднего мозга (prosencephalon) на ранних стадиях развития плода, на
3 й неделе гестации, когда существуют 3---5 мозговых пузырей. С ней часто со-
четаются разнообразные пороки развития лицевого скелета: циклопия (единствен-
ная глазница, расположенная по средней линии), этмоцефалия (отсутствие но-
совых костей, раковин, этмоидальной перегородки), цебоцефалия (единственный
зрительный канал, отсутствие носовой перегородки и резцовой кости) и т. д.
Этиологическими факторами считают трисомию 13 й, 15 й, 21 й пар хромосом,
синдром Дауна, другие хромосомные абберации, воздействие ионизирующего
излучения. Голопрозэнцефалия часто встречается у детей, матери которых име-
ли тяжелую форму сахарного диабета.
В зависимости от степени тяжести различают 3 вида голопрозэнцефалий:
алобарную, семилобарную и лобарную. Это деление основано на степени выра-
женности нарушения дивертикуляции.
Алобарная голопрозэнцефалия является наиболее тяжелой формой, характе-
ризуется наличием моновентрикулярного мозга без разделения его на доли и
полушария (рис. 3.12).
Семилобарная голопрозэнцефалия --- частичное разделение мозга при непол-
ном образовании долей. Частично имеется межполушарная щель.
Лобарная голопрозэнцефалия характеризуется отсутствием прозрачной пере-
городки при наличии сформированных долей и межполушарной щели. Не сфор-
мирована кора лобных долей, имеется непарная передняя мозговая артерия. Эта
форма часто сочетается с пороками развития глаз (от циклопии до колобомы).
Типичные проявления различных видов нарушения дивертикуляции голов-
ного мозга представлены в табл. 3.1.
Септооптическая дисплазия (синдром de Morsier) является одной из формло
барной голопрозэнцефалий. Характеризуется отсутствием прозрачной перего-
родки, гипоплазией зрительных
нервов, хиазмы и воронки. Чаще
встречается у женщин. У больных
отмечаются слепота, судорожные
припадки, задержка психомотор-
ного развития.
Рис. 3.12. Голопрозэнцефалия.
МРТ.
Т2 ВИ, корональная плоскость.
Срашение гемисфер мозга, боковых
желудочков. Прозрачная перего-
родка отсутствует.
Таблица 3.1
Проявления нарушений дивертикуляции головного мозга
Виды голопрозэнцефалии
Анатомические
структуры
алобарная
семилобарная
лобарная
Септооптическая
дисплазия
Боковые желудочки Моновентрикулия
Не разделены
примитивные
височные рога
Почти нормальные
прямоугольные
передние рога, отсут-
ствие прозрачной
перегородки
Расширение перед-
них рогов, отсут ствие
прозрачной
перегородки
III желудочек
Отсутствует
Рудиментарный
Почти норма
Увеличены передние
завороты
Базальные ядра
Отсутствует разделение
Разные степени
слияния
Почти норма
Норма
Сосудистые
аномалии
Отсутствие или гипопла-
зия вены и синуса сред ней
линии, передних мозговых
артерий
Выражены менее,
чем при алобар
ной
Аномалии передних
мозговых артерий
Аномалии передних
мозговых артерий
Серповидный
отросток твердой
мозговой оболочки
Отсутствует
Частично
отсутствует
Отсутствует в
передних отделах
Норма
Межполушарная
щель
Отсутствует
Отсутствует в
переднем отделе
Норма
Норма
Лицевые изменения Различная степень
выраженности
Менее тяжелые,
чем при алобарной
Норма, иногда
расщелина твердого
неба
Норма
Другие аномалии
Агенезия сосудистой
системы
Дисгенезия сосу-
дистой системы
(обычно в перед-
них отделах)
Норма
Дисплазия зритель-
ного нерва и хиазмы,
шизэнцефалия в 50%
случаев
Рис. 3.13. Септооптическая дисплазия. МРТ.
а --- Т1 ВИ, аксиальная плоскость; б --- Т1 ВИ, сагиттальная плоскость.
Гипоплазия зрительных нервов и хиазмы. Хиазма и зрительные нервы не опреде-
ляются. Зрительные тракты не изменены.
Передние рога боковых желудочков вздуты и закруглены, напоминая карти-
ну лобарной голопрозэнцефалии. В отличие от нее, обычно хорошо сформированы
межполушарная щель и серповидный отросток твердой мозговой оболочки.
При КТ и МРТ выявляются гипоплазия хиазмы и зрительных нервов, отсут-
ствие прозрачной перегородки, расширенные лобные рога боковых желудочков,
увеличение передних заворотов III желудочка (рис. 3.13). При МРТ нередко вы-
является и непарная передняя мозговая артерия.
Септооптическая дисплазия часто сочетается с мальформациями кортикаль-
ного развития, в первую очередь с шизэнцефалией.
Дифференцировать голопрозэнцефалию необходимо с гидранэнцефалией,
кистами Денди --- Уолкера, гидроцефалией тяжелой степени.
Отсутствие или частичное формирование фалькса и межполушарной щели
свидетельствуют в пользу голопрозэнцефалии.
Нарушения формирования извилин и клеточной миграции
(мальформации кортикального развития)
С развитием методов нейровизуализации мальформации кортикального раз-
вития, являющиеся причиной эпилепсии, отставания в развитии и других пси
хо неврологических нарушений, стали диагностироваться все чаще.
Причиной формирования кортикальных дисплазий является нарушение кле-
точной пролиферации, нейронной миграции и организации коры. На 5 й неделе
гестации головной мозг состоит из терминального матрикса и радиальных гли
альных волокон. Пролиферация нейробластов наблюдается между 7 й и 16 й
неделями гестации, а миграция нейробластов происходит между 12 й и 24 й не-
делями в виде шести последовательных волн. На ранних стадиях нейробласты миг
Рис. 3.14. Схема нейрональной миграции
(по А.Л.Вагкоукп).
1 --- терминальная зона; 2 --- радиальное волокно;
3 --- нейробласт.
рируют от 1 до 3 дней. В поздние фазы необходи-
мо более чем 2 недели для того, чтобы они заняли
свое окончательное место в коре. Нейробласты
мигрируют из терминального матрикса вдоль
глиальных волокон (рис. 3.14). После окончания
процесса нейробласты, которые мигрировали
раньше, располагаются в более глубоких слоях,
тогда как мигрировавшие позже располагаются
поверхностно.
Г
Таким образом, нейробласты, формирующие
поверхностные слои, для достижения своей цели (<
должны пройти уже сформировавшиеся слои.
Кортикальные дисплазии являются следстви-
ем нарушения любой фазы миграции. Патологи-
ческие изменения коры головного мозга зависят
от срока возникновения дефекта развития.
Существует большое количество классифи-
каций матьформаций кортикального развития.
Это приводит к тому, что идентичные изменения трактуются неодинаково и по-
лучают различные названия. Мы считаем, что наиболее подробной и удобной
в практической работе является классификация, предложенная АЛ.ВагкоуюЬ,
основанная на эмбриологических, генетических, гистологических принципах
и данных методов нейровизуализации.
Классификация мальформаций кортикального развития
(поА.Л.Вагкоу1сп, 1996)
I. Мальформаций, обусловленные измененной нейронной и глиальной проли-
ферацией
А. Генерализованные.
1. 4Пролиферация --- микролиссэнцефалия.
2. ТПролиферация --- неизвестно.
3. Измененная (патологическая) пролиферация (измененный тип кле-
ток) --- неизвестно --- возможно, несовместима с жизнью.
Б. Фокальные и мультифокальные.
1. ^Пролиферация --- некоторые шизэнцефалии.
2. ТПролиферация --- не известно.
3. Измененная (патологическая) пролиферация (измененный тип клеток):
а) неопухолевая,
--- туберозный склероз, 1 йи2 йтип,
--- фокальная,
--- гемимегалэнцефалия:
а) изолированная;
б) с кожно невральным синдромом:
1) эпидермальный невус,
2) гипомеланоз,
3) нейрофиброматоз 1 го тина;
б) Опухолевые (сопровождающиеся дисорганизацией коры):
--- дизэмбриопластические нейроэпителиальные опухоли,
--- ганглиоглиома,
--- ганглиоцитома.
II. Мальформации, обусловленные изменением нейронной миграции.
А. Генерализованные.
1. Классическая (1 й тип) лиссэнцефалия (агирия пахигирия):
а) связанная с 17 й хромосомой:
--- синдром Miller --- Dieker,
--- изолированная лиссэнцефалия;
б) Х связанная:
--- Х связанная лиссэнцефалия,
--- субкортикальная лентовидная гетеротопия;
в) другой локализации.
2. Лиссэнцефалия по типу «булыжной мостовой»:
а) врожденная мышечная дистрофия Fucuyama;
б) синдром Walker --- Warburg;
в) болезнь «мышцы глаза мозга».
3. Неклассифицированные лиссэнцефалии.
4. Гетеротопия:
а) субэпендимальная:
--- Х связанная (билатеральная перивентрикулярная узловая гете-
ротопия),
--- спорадическая;
б)субкортикальная;
в) складчатость коры (симметричная);
г) краевая глионейрональная гетеротопия.
Б. Фокальные или мультифокальные мальформации при нейронной мигра-
ции.
1. Фокальная агирия/пахигирия (частичная лиссэнцефалия):
а) двухсторонняя задняя пахигирия;
б) двухсторонняя теменная пахигирия.
2. Фокальная и мультифокальная гетеротопия:
а) фокальная узловая субэпендимальная;
б) фокальная узловая субкортикальная;
в) фокальная смешанная субкортикальная/субэпендимальная;
г) складчатость коры (унилатеральная);
д) краевая глионейрональная гетеротопия:
--- фетальный алкогольный синдром,
--- другие.
3. Фокальная или мультифокальная гетеротопия с изменением организа-
ции коры:
а) фокальная узловая субэпендимальная;
б) фокальная узловая субкортикальная;
в) фокальная смешанная субкортикальная/субэпендимальная:
--- синдром Аісагаі,
--- пероксисомальные нарушения,
--- дефи цит ацил КоА дегидрогеназы;
г) складчатость коры (унилатеральная);
д) краевая глионейрональная гетеротопия.
4. Одиночная эктопия белого вещества.
III. Мальформации, обусловленные кортикальной организацией.
А. Генерализованные.
1. Полимикрогирия (ПМГ).
Б. Фокальная или мультифокальная.
1. Полимикрогирия/шизэнцефалия:
а) двухсторонняя симметричная полимикрогирия:
--- двухсторонняя передняя ПМГ,
--- двухсторонняя перисильварная ПМГ,
--- двухсторонняя задняя ПМГ;
б) асимметричная ПМГ;
в) шизэнцефалия и смешанная шизэнцефалия/ПМ Г.
2. Фокальная или мультифокальная кортикальная дисплазия без наличия
баллонных клеток.
3. Микродисгенезия.
IV. Мальформации кортикального развития, еще не классифицированные.
Аллельные и возможно аллельные.
Туберозный склероз (болезнь Бурневилля --- Прингла) --- см. раздел «Нару-
шения гистогенеза».
Нейрональные и смешанные нейронально глиальные опухоли---достаточно редко
встречающиеся новообразования, образованные полностью или частично из кле-
ток нейронального происхождения, высокой степени дифференцировки.
Дизэмбриопластическая нейроэпителиальная опухоль (ДНЕО) --- это полимор-
фная нейронально глиальная опухоль, которая располагается в кортикальных
отделах, чаще в височной доле и встречается у людей молодого возраста (до
30 лет). Клинически ДНЕО характеризуется парциальными судорогами, рези-
стентными к медикаментозному лечению, без неврологического дефицита. При
этом на МРТ изображениях определяется многоузловое образование, располо-
женное кортикально и характеризующееся гипоинтенсивным сигналом наТ1
ВИ и гиперинтенсивным --- на Т2 ВИ (рис. 3.15). Нередко структура опухоли
неоднородная, с кистозным компонентом и кальцификатами. Перифокальный
Рис. 3.15. Дизэмбриопластическая нейроэпителиальная опухоль (ДНЕО). МРТ.
На Т2 ВИ в левой лобно теменной области в кортикальных и субкортикальных от-
делах выявляется опухоль, характеризующаяся гиперинтенсивным сигналом, с чет-
кими контурами, без признаков перифокального отека.
отек нехарактерен. На постконтрастных изображениях в 50% случаев отмечает-
ся усиление интенсивности сигнала, может наблюдаться кольцевидный харак-
тер накопления контрастирующего препарата. Наблюдение за больными в ди-
намике обычно выявляет медленные темпы роста этих новообразований.
Ганглиоцитома располагается по ходу извилины, характеризуется изоинтен
сивным сигналом наТ1 ВИ и умеренно гиперинтенсивным --- наТ2 ВИ. В строме
опухоли могут выявляться петрификаты. Смещение соседних структур не на-
блюдается. Усиление на постконтрастных изображениях нехарактерно. Наблю-
дение за больными в динамике не выявляет признаков роста опухоли.
Ганглиоглиома характеризуется гипоинтенсивным сигналом на Т1 ВИ и ги-
перинтенсивным сигналом на Т2 ВИ. Структура опухоли неоднородная: с кис
тозным компонентом, кальцификатами (рис. 3.16). Вокруг опухоли определяет-
ся перифокальный отек. Характерным признаком является усиление на пост-
контрастных изображениях.
Гемимегалэнцефалия, или односторонняя мегалэнцефалия,--- это гамартама
тозное увеличение полушария мозга или ее части, сочетающееся с нарушением
нейронной миграции. В измененной гемисфере могут определяться зоны пахи
гирии, гетеротопии, полимикрогирии, а также глиоза в белом веществе. На МРТ
изображениях гемисфера увеличена в размере, кора пахигирична, утолщена,
извилины широкие, плоские, граница между серым и белым веществом смазан-
ная, нечеткая. В белом веществе обычно выявляются изоинтенсивные серому
а
б
Рис. 3.16. Ганглиоглиома. МРТ.
а --- FLAIR ИП, аксиальная плоскость. В левой гемисфере мозга определяется боль-
ших размеров опухоль, поражающая лобную и теменную долю. Структура опухоли
неоднородная за счет кистозного компонента. Выраженные перифокальные изме-
нения.
б --- постконтрастное Т1 ВИ, аксиальная плоскость. Контрастное усиление наблю-
дается в солидном компоненте образования, располагающемся в центре опухоли, а
также по периферии опухолевой кисты.
веществу участки гетеротопии, которые могут достигать больших размеров, ги-
перинтенсивные на Т2 ВИ участки глиоза. Боковой желудочек увеличенной
гемисферы расширен, передний рог его выпрямлен и удлинен.
Фокальная кортикальная дисплазия (ФКД) --- характеризуется изменением
коркового серого вещества, с нарушением архитектоники и организации коры.
Изменения белого вещества обусловлены нейроналъной гетеротопией. Гистоло-
гические проявления кортикальной дисплазии варьируют в широком спектре
от небольших изменений цитоархитектуры коры до полного нарушения форми-
рования ее слоев с эктопией в прилежащее белое вещество, нарушением ориен-
тации нейронов с наличием баллонных (N) клеток в субкортикальных отделах.
Данная мальформация кортикального развития была описана в 1971 г. D.C. Taylor
и соавт. Вследствие того, что термин «фокальная кортикальная дисплазия» час-
то используется для обозначения различных локальных изменений развития
коры головного мозга, возникают неточности и путаница, обусловленная отсут-
ствием универсальной терминологии. Поэтому для обозначения данной маль
формации многие авторы применяют термин «фокальная кортикальная дисп
лазия Тейлора».
ФКД можно классифицировать на два типа. Первый тип гистологически
характеризуется умеренно выраженными изменениями архитектуры коры, бал-
лонные клетки не определяются. При втором типе ФКД наблюдаются выражен-
ная кортикальная дисорганизация, наличие баллонных клеток, астроцитоз, эк-
топия белого вещества. ФКД локализуется в височной и, чаще, в лобной доле.
В височной доле более часто встречается первый тип, в лобной --- второй.
На МРТ изображениях выявляемые изменения зависят от степени гистоло-
гических нарушений. Первый тип ФКД зачастую не определяется. В некоторых
случаях архитектоника серого и белого вещества представляется измененной
в виде нечеткости границы серого и белого вещества, нарушения строения бе-
лого вещества. На Т2 ВИ может выявляться минимальное усиление сигнала.
Толщина коры не изменена (рис. 3.17).
Чувствительность М РТ для выявления второго типа ФКД составляет 80---90%.
Изменения локализуются в лобной доле. МРТ семиотика заключается в утол-
щении коры, деформации извилин, появлении мелких борозд. В белом веществе
мозга определяется конической формы зона гиперинтенсивного сигнала на Т2
ВИ с вершиной, направленной к боковому желудочку.
а
б
Рис. 3.17. Фокальная кортикальная дисплазия. МРТ.
а --- FLAIR ИП, аксиальная плоскость. В субкортикальных отделах белого вещества
правой лобной доли выявляется зона измененного сигнала треугольной формы,
направленная вершиной к переднему рогу бокового желудочка,
б --- IR ИП, аксиальная плоскость. Кора правой лобной доли утолщена.
Для диагностики ФКД рекомендуется использовать IR, SPGRHIl, которые
подчеркивают дифференциацию между серым и белым веществом. Для выявле-
ния гиперинтенсивной зоны в субкортикальных отделах белого вещества опти
матьной является FLAIR ИП.
ФКД второго типа необходимо дифференцировать с неопластическими про-
цессами. В обоих случаях определяется повышение интенсивности сигнала на
Т2 ВИ, деформация борозд. Характерными особенностями ФКД являются уве-
личение толщины коры, однородность измененного сигнала наТ2 ВИ, кони-
ческая форма гиперинтенсивной зоны в субкортикальных отделах, распростра-
няющаяся до бокового желудочка. Введение контрастного вещества не дает до-
полнительной информации.
Лиссэнцефалия, или генерализованная агирия пахигирия, представляет собой
«гладкий мозг», борозды отсутствуют, либо определяется несколько мелких борозд.
Задержка радиальной нейронной миграции приводит к формированию по-
лосы серого вещества, которая располагается субкортикально и отделена слоем
белого вещества от измененной тонкой коры. Ширина сепаратного слоя белого
вещества вариабельна. У больных с тяжелой формой лиссэнцефалии она опре-
деляется как широкий слой, отделяющий кору от полосы гетеротопированных
нейронов. В менее выраженных случаях лиссэнцефалии выявляется более тон-
кая полоса гетеротопированных нейронов и слоя белого вещества, отделяющего
их от коры. Толщина и направленность извилин резко изменены.
На МРТ изображениях при агирии извилины на поверхности мозга полнос-
тью отсутствуют, кора резко утолщена, желудочки мозга расширены. Латераль-
ные борозды (сильвиевы щели) поверхностные, вертикально ориентированные,
вследствие чего на аксиальном срезе головной мозг имеет форму восьмерки. При
пахигирии определяются широкие, плоские извилины, разделенные небольшим
количеством мелких борозд. Кора утолщена, но ее ширина меньше сочетанной
толщины полосы гетеротопированных нейронов и отделяющего их от коры слоя
белого вещества. Изменения могут затрагивать как весь головной мозг, так и его
отдельные доли. Диффузная агирия без признаков пахигирии встречается ред-
ко. Наиболее распространенным вариантом является сочетание теменно заты
лочной агирии и лобно височной пахигирии (рис. 3.18). Агирия может сочетаться
с гипогенезией мозолистого тела, агенезией червя мозжечка и гипоплазией ствола
мозга вследствие несформированности кортикоспинального и кортикобульбар
ного трактов. Средняя мозговая артерия не имеет своей борозды и располагается
близко к основанию черепа.
Гетеротопия --- это аномальное скопление и необычное расположение серого
вещества в различных участках головного мозга. Она обусловлена нарушением
миграции нейронов из терминального матрикса вдоль глиальных волокон в кору
мозга. Клинические проявления определяются выраженностью изменений: от
бессимптомного течения до судорог, которые могут сопровождаться значитель-
ной умственной отсталостью. В настоящее время МРТ является оптимальным
методом исследования, особенно IR И П.
Различают следующие формы гетеротопии: перивентрикулярную узловую,
перивентрикулярную и субкортикальную как с изменением, так и без измене
а
б
Рис. 3.18. Лиссэнцефалия. МРТ.
а --- Т1 ВИ, сагиттальная плоскость. Агирия затылочной доли. Извилины темен-
ной доли утолщены, широкие.
б --- IR ИП, аксиальная плоскость. Толщина коры увеличена, желудочки мозга рас-
ширены.
а
б
Рис. 3.19. Перивентрикулярная гетеротопия. МРТ.
а --- IR ИП, аксиальная плоскость; б --- IR ИП, корональная плоскость.
Множественные узлы гетеротопии располагаются вдоль стенок боковых желудочков.
ния строения коры, гигантскую, сочетающуюся с кортикальной дисплазией, и
лентовидную.
Перивентрикулярная узловая гетеротопия характеризуется четко очерченны-
ми узлами, расположенными вдоль стенки желудочка мозга. Узлы могут быть
как одиночными, так и множественными и обычно вдаются в полость желудоч-
ка (рис. 3.19).
Перивентрикулярная и субкортикальная гетеротопия как с изменением, так
и без изменения строения коры проявляется узловой перивентрикулярной гете
ротопией и скоплением серого вещества в субкортикальных отделах. Пораже-
ние в большинстве случаев одностороннее. Субкортикальное скопление серого
вещества может приводить к локальной деформации борозд и утолщению коры
(рис. 3.20).
Гигантская форма гетеротопии с изменением строения коры --- большое по
протяженности скопление серого вещества, занимающее большую часть гемис
феры, от стенки желудочка до поверхности коры, приводящее к деформации
кортикальной поверхности мозга. Приданной форме гетеротопии скопления
серого вещества в виде отдельных узлов не наблюдается. Гигантскую форму ге-
теротопии, вследствие большого размера зоны поражения, необходимо диффе-
ренцировать с патологическими образованиями. При гетеротопии, в отличие от
а
б
Рис. 3.20. Перивентрикулярно субкортикальная гетеротопия. МРТ.
а --- IR ИП, аксиальная плоскость. Узлы гетеротопии располагаются вдоль стенки
левого бокового желудочка и в субкортикальных отделах белого вещества. Между
субкортикальными узлами сохраняются прослойки белого вещества. Поверхность
коры деформирована.
б --- Т2 ВИ, корональная плоскость. Субэпендимальные узлы вдаются в полость ле-
вого бокового желудочка, что делает его контуры волнистыми.
а
б
Рис. 3.22. Двусторонняя открытая шизэнцефалия. МРТ.
а --- Т2 ВИ, аксиальная плоскость; б --- Т1 ВИ, корональная плоскость.
В обеих гемисферах мозга определяются расщелины, распространяющиеся от су
барахноидального пространства до бокового желудочка. В правой гемисфере име-
ется широкое сообщение между субарахноидальным пространством и боковым же-
лудочком. В левой гемисфере мозга расщелина узкая. Желудочки мозга расшире-
ны, деформированы.
а
б
Рис. 3.23. Открытая шизэнцефалия правой лобной доли. МРТ.
а --- IR ИП, аксиальная плоскость. Края расщелины, располагающейся в правой
лобной доле, представлены диспластичным серым веществом. Полость расщели-
ны заполнена ликвором. В левой гемисфере определяется изменение хода борозд
и утолщение коры.
б --- Т1 ВИ, корональная плоскость. В лобной доле выявлена расщелина сложной
формы с образованием нескольких небольших слепо заканчивающихся ответвле-
ний. Прилежащее субарахноидальное пространство и передний рог бокового же-
лудочка расширены.
опухолей, не определяются перифокальный отек, смещение срединных струк-
тур, нет усиления сигнала после введения контрастирующего вещества.
Лентовидная гетеротопия, или синдром двойной коры, проявляется четко
очерченным лентовидньгм слоем нейронов, отделенным от коры полосой белого
вещества. Диагностировать данную патологию можно только по данным МРТ.
При этом на изображениях выявляется ровная, четко очерченная полоса се-
рого вещества, расположенная параллельно боковому желудочку и отделенная
от коры и стенки желудочка слоем серого вещества. Кора мозга может быть
неизмененной либо может быть изменена от умеренно выраженной пахигирии
до полной агирии (рис. 3.21). В белом веществе на Т2 ВИ могут определять-
ся очаги гиперинтенсивного сигнала. Лентовидную гетеротопию достаточно
сложно дифференцировать с лиссэнцефалией: они, вероятно, представляют
собой различные степени одного общего процесса нарушения миграции ней-
ронов. В отличие от лиссэнцефалии, при лентовидной гетеротопии изменения
коры выражены меньше.
Шизэнцефалия представляет собой вариант кортикальной дисплазии, когда
определяется расщелина, проходящая через все полушарие головного мозга ---
от бокового желудочка до кортикальной поверхности. Клинические симптомы
зависят от степени выраженности изменений и проявляются судорогами, геми
парезом, отставанием вразвитии. Наиболее часто расщелина локализуется в пре
и постцентральной извилине и может быть как односторонней, так и двухсто-
ронней (рис. 3.22). В большинстве случаев при унилатеральной шизэнцефалии
в контралатеральной гемисфере выявляются другие виды кортикальных дисп-
лазии (пахигирия, полимикрогирия) (рис. 3.23). В области расщелины просле-
живаются крупные сосуды. Серое вещество, покрывающее расщелину, диспла
стичное, утолщенное, имеет неровную внутреннюю и наружную поверхность.
При открытой шизэнцефалии края расщелины разделены, и цереброспиналь-
ная жидкость заполняет ее от бокового желудочка до субарахноидального про-
странства. При закрытой шизэнцефалии стенки расщелины соприкасаются,
сращены, в месте сообщения с боковым желудочком может выявляться углуб-
ление, «ямка». Для идентификации и локализации расщелины при открытом
типе шизэнцефалии достаточно получить изображения в двух ортогональных
а
б
Рис. 3.24. Полимикрогирия лобных долей. МРТ.
а --- SRGR ИП, аксиальная плоскость, толщина среза 1,2 мм;
б --- FLAIR ИП, аксиальная плоскость.
В лобных долях определяются множественные мелкие извилины. Толщина корти-
кальной пластинки не изменена. Субарахноидальное пространство лобной облас-
ти расширено.
проекциях --- Т1 и Т2 ВИ. При закрытой шизэнцефалии в некоторых случаях
возникает необходимость получения ЗО изображений.
Полимикрогирия --- аномалия развития, при которой нейроны достигают коры,
но вследствие неправильного распределения формируют множество мелких из-
вилин. Клинически полимикрогирия (ПМГ) проявляется судорогами и отстава-
нием в развитии. Наиболее часто ПМГ локализуется в области латеральной бо-
розды (силъвиевой щели). Гистологические изменения коры могут быть выражены
в различной степени, что обусловливает разнообразие картины на МРТ изобра
жениях. На поверхности коры могут быть видны множественные, мелкие изви-
лины (рис. 3.24) или она может быть парадоксально гладкой, так как извилины
очень малы, либо сливаются между собой. Если мелкие извилины сливаются между
собой, то на МРТ изображениях кора будет выглядеть утолщенной, как при
пахигирии (рис. 3.25). На обьгчнъгх МРТ изображениях дифференцировать ПМГ
и пахигирию затруднительно (рис. 3.26). Для выявления неровности, буклирован
ности соединения серого и белого вещества при ПМГ необходимо получать ЗО
изображения. Изменения коры характеризуются изоинтенсивным сигналом. В бе-
лом веществе субкортикально на Т2 В И могут определяться очаги гиперинтен-
сивного сигнала, в отдельных случаях наблюдаются участки обызвествления.
В области дисплазии субарахноидальные пространства локально расширены, там
же обычно располагаются аномально расширенные венозные сосуды. «Крайним»
вариантом развития ПМГявляется шизэнцефалия.
а
б
Рис. 3.25. Полимикрогирия. МРТ.
а --- IR ИП, аксиальная плоскость. Утолщение коры верхней и средней лобных из-
вилин левой гемисферы мозга.
б --- Т2 ВИ, корональная плоскость. В белом веществе левой лобной доли определя-
ется зона гиперинтенсивного сигнала, обусловленная глиозными изменениями. Тело
левого бокового желудочка расширено и подтянуто к этой зоне.
а
б
Рис. 3.26. Пахигирия / полимикрогирия. МРТ.
а --- IR ИП, аксиальная плоскость. В левой гемисфере в лобно теменной области
выявляется утолщение коры, изменение формы белого вещества. Извилины в этой
области широкие, прилежащее субарахноидальное пространство расширено,
б --- Т2 ВИ, аксиальная плоскость. В левой гемисфере мозга определяется аномаль-
ная глубокая широкая борозда. Кора по краям борозды утолщена. Латеральный кон-
тур левого бокового желудочка деформирован.
Аномалии размеров
Микроцефалия, или микроэнцефалия,--- аномально маленький головной мозг.
Обычно это является результатом внутриутробного сосудистого инсульта или
внутриутробной ТХЖСН инфекции, также причиной могут быть метаболичес-
кие нарушения, в частности фенилкетонурия. Отмечаются редкие формы истин-
ной микроцефалии, когда полушария симметричны и анатомически интактны.
Чаще встречаются энцефалокластические формы, при которых выявляются
атрофия, энцефаломаляция, порэнцефалия, утолщение костей свода черепа и
кальцификация.
Макроцефалия, или генерализованная мегалэнцефалия, часто бывает семей-
ной, с правильно сформированным мозгом, размеры которого находятся в гра-
ницах возрастной нормы. Мегалэнцефалия может быть также вызвана питуи
тарным гигантизмом, иногда встречается при нейрофиброматозе. Ее причиной
бывают и метаболические нарушения --- болезнь Канавана, болезнь Ал ександе
ра, метахроматическаялейкодистрофия, мукополисахаридоз.
Деструктивные изменения
Порэнцефалия --- это ликворосодержащая полость, связанная с субарахнои
дальным пространством или желудочками мозга.
Порэнцефалия может быть истинной и ложной, которые отличаются нали-
чием или отсутствием серого вещества по краю расщелины. Истинная порэн-
цефалия (шизэнцефалия) всегда носит врожденный характер и предполагает
существование расщелин в веществе мозга, которые соединяют желудочек и су
барахноидальное пространство. Шизэнцефалия обычно сочетается с гетерото
пией серого вещества, агенезией мозолистого тела и т. д. Причиной является на-
рушение нейронной миграции и организации коры вследствие ишемических,
токсических поражений головного мозга плода.
Вторичная порэнцефалия является последствием травмы, воспалительных
процессов (менингита, энцефалита, вентрикулита), цереброваскулярных пора-
жений (внутримозгового кровоизлияния), оперативного вмешательства (в том
числе после пункции желудочка, а также возникает вследствие плохого функ-
ционирования шунта).
Клинические проявления зависят от локализации и размеров повреждения
головного мозга. У детей обычно определяется задержка психомоторного разви-
тия различной степени выраженности, гемипарез, фокальные моторные припад-
ки и т. д. Симптомы обычно односторонние.
На краниограммах может выявляться как истончение, так и утолщение кос-
тей свода черепа. На KT и МРТ изображениях --- зона ликворной плотности
(интенсивности сигнала), связанная с желудочком и (или) субарахноидальным
пространством. Асимметричное расширение желудочков со смешением за сред-
нюю линию или без него, что обусловлено наличием градиента давлений между
полушариями. После введения контрастного вещества усиление сигнала от сте-
нок полости отсутствует. Применение цистернографии или вентрикулографии
позволяет выявить сообщение полости с желудочком или субарахноидальным
пространством.
МРТ позволяет достаточно легко дифференцировать шизэнцефалию и вто-
ричную порэннефалию. Если при шизэнцефалии края полости представляют
собой диспластичное, утолщенное серое вещество, то при вторичной порэнце
фалии --- белое вещество. Возможность выполнения М Р цистернографии дела-
ет МРТ методом выбора при обследовании больных с порэнцефалией.
Признаком, отличающим порэнцефалию от абсцессов и кистозных опухо-
лей, является отсутствие усиления интенсивности сигнала от стенок полости пос-
ле внутривенного контрастирования.
Гидранэнцефалия является следствием полной или неполной деструкции и
реабсорбции полушарий при сохранении таламусов и мозжечка. Менингеаль
ные оболочки и свод черепа также обычно интактны. Фальке сохранен. Счита-
ется, что гидранэнцефалия возникает в результате билатерального мозгового ин-
сульта в ранние сроки беременности из за окклюзии сонных артерий, обуслов-
ленной инфекцией (врожденным токсоплазмозом или цитомегаловирусным
энцефалитом). При МРТ и КТ определяется отсутствие полушарий мозга при
сохранении промежуточного мозга и мозжечка. Ствол мозга атрофичен. При
МРТ нередко видна тонкая глиальная мембрана в качестве мозгового плаща.
Наличие фалькса позволяет отвергнуть диагноз голопрозэнцефалии.
Обструктивные изменения
Стеноз водопровода мозга. Хотя обструктивные изменения водопровода час-
то разделяют на стеноз, расщепление и атрезию, различить их с использованием
методов лучевой диагностики не представляется возможным. Стеноз водопро-
вода часто сочетается с аномалией Арнольда --- Киари II. Конгениальный ток
соплазмоз может также вызывать сужение или окклюзию водопровода мозга из
за поствоспалительного глиоза.
При МРТ и КТ выявляется выраженное расширение боковых и III желудоч-
ков с признаками внутрижелудочковой гипертензии при наличии небольшого
IV желудочка.
II. НАРУШЕНИЯ ГИСТОГЕНЕЗА
Нейрофиброматозы
В последнее время описаны 8 отдельных форм нейрофиброматоза, из кото-
рых наиболее часто встречаются два типа --- болезнь Реклингхаузена (нейрофи
боматоз 1) и нейрофиброматоз с двусторонней невриномой (шванномой) слу-
хового нерва (нейрофиброматоз 2). Термины «центральный» и «периферический
нейрофиброматоз» можно изъять из употребления, поскольку они неточны. Как
нейрофиброматоз 1, так и нейрофиброматоз 2 представляют собой поражение
ЦНС. Эти изменения отражают дисгистогенез нейроэктодермальной и мезодер
мальной тканей. Совсем недавно был выявлен хромосомный локус для нейро-
фиброматоза 1 и нейрофиброматоза 2.
Болезнь Реклингхаузена (нейрофиброматоз 1) встречается приблизительно у 1
из 4000 новорожденных. Составляет более чем 90% всех нейрофиброматозов.
Наследуется по аутосомно доминантному типу, без половых различий, генети
ческийлокус--- 17 я хромосома.
Клинические проявления нейрофиброматоза могут различными: наличие на
коже пятен цвета «кофе с молоком», нейрофибромы различных типов, гамарто
мы радужки (так называемые узелки Лише), подмышечные или паховые роди-
мые пятна, глиома зрительного нерва, поражения костей (например, дисплазия
крыла клиновидной кости, кифосколиозит.д.).
Поражения ЦНС определяются в 15---20% случаев. Самым частым проявле-
нием нейрофиброматоза 1 является глиома зрительного нерва. Могут быть из-
менены как один, так и оба зрительных нерва, хиазма, зрительные тракты, бо-
ковые коленчатые тела, сетчатая формация. На рентгеновских снимках опреде-
ляется одно или двустороннее расширение канала зрительного нерва. При КТ
и МРТ рекомендуется получать прицельные изображения зрительных нервов,
толщина среза 1 ---3 мм. Наиболее информативными являются изображения с по-
давлением сигнала от параорбитальной жировой клетчатки, полученные после
внутривенного контрастирования.
На МРТ глиома зрительного нерва характеризуется изо или гипоинтенсив
ным сигналом наТ1 ВИ, гиперинтенсивным --- на Т2 ВИ.
Неоптическая глиома обычно локализуется в области дна III желудочка в пок-
рышке и вокруг водопровода, в стволе мозга и т. д. Редко встречаются анаплас
тическая астроцитома или мультиформная глиобластома. Нейрофиброматоз
сплетений имеет экстракраниальное происхождение, но часто распространяет-
ся интракраниально вдоль естественных отверстий, шелей (из глазницы, верх-
нечелюстной ямки в кавернозный синус). Развитие неглиальных опухолей не
характерно для нейрофиброматоза 1.
Часто на Т2 ВИ видны гиперинтенсивные участки без масс эффекта в об-
ласти базальных ганглиев, внутренней капсулы моста, ножек мозга, мозжечка
и т. д. Эти же участки не видны на Т1 ВИ и, вероятно, представляют собой га
мартомы или очаги дисмиелинизании.
К сосудистым аномалиям отностяся диспластический стеноз сосудов арте-
риального круга большого мозга (виллизиева круга), интра и экстракраниаль-
ные аневризмы.
Часто поражение ЦНС обусловлено деформацией черепа: макрокранией,
аномальной кальцификацией, гипоплазией большого крыла клиновидной кос-
ти. Так, при гипоплазии крыла клиновидной кости происходит выпячивание
височной доли в глазницу и развивается экзофтальм.
Поражение позвоночника может проявляться кифосколиозом, эрозией ос-
тистых отростков, менингоцеле. Самым частым проявлением поражения позво-
ночника является кифосколиоз, наблюдающийся у'/, пациентов и обусловлен-
ный первичной мезодермальной дисплазией. Изменения обычно располагают-
ся на уровне Thm V|1. Обычно характерно легкое течение, но возможно быстрое
прогрессирование заболевания с развитием параплегии. Латеральное менинго-
целе, вероятно, вызывается ослабленной диспластичной менингеальной оболоч-
кой, которая пролабирует через расширенное межпозвоночное отверстие (пуль-
сирующий дивертикул). Чаще поражается грудной отдел позвоночника, обыч-
но справа. Пояснично крестновая и шейная локализация встречается реже. На
КТ изображениях определяются расширение межпозвоночного отверстия с про
трузией мозговой оболочки, а также истончение отростков и искривление по-
звоночника. На МРТ --- менингоцеле имеет характерный для спинномозговой
жидкости сигнал на всех типах взвешенности.
Нейрофиброматоз 2 встречается с частотой приблизительно 1 на 50 ООО но-
ворожденных и характеризуется двухсторонними шванномами VIII черепного
нерва. Наследуется по аутосомно доминантному типу, не связан с полом. Ген-
ным локусом является 22 я хромосома. Клиническая симптоматика связана
с поражением VIII нерва. Кожные проявления встречаются реже, чем при ней
рофиброматозе 1. Опухоль VIII черепного нерва может быть односторонней и со-
четаться с нейрофибромами, менингиомами (как интракраниальными, так и
спинальными), шванномами других черепных нервов, астроцитомами и эпен
димомами спинного мозга. Внутриполушарные шванномы встречаются редко
и в настоящее время расцениваются как десмопластические ганглиоглиомы.
Энцефалотригеминальный ангиоматоз (болезнь Штурге --- Вебера) --- см. гла-
ву: «Сосудистые заболевания головного мозга».
Туберозный склероз
Туберозный склероз, или болезнь Бурневилля --- Прингла, относится к факома
тозам и клинически проявляется судорогами, психическими нарушениями.
Частота составляет 1 на 10000---50000. Наследуется по аутосомно доминантно
му типу.
Туберозный склероз --- мультиорганное заболевание с поражением ЦНС, лег-
ких, сердца (рабдомиома), почек (ангиолипоматоз), печени (лейомиома, адено-
ма), черепа (множественные костные островки в диплоэ), сетчатки глаз.
Причиной туберозного склероза является изменение роста и дифференциа-
ции нейронов, а также глиальных клеток, сопровождающееся нарушением миг-
рации нейронов и организации коры, в некоторых случаях с неопластическими
процессами. Туберозный склероз характеризуется наличием субэпендимальных
узлов, вдающихся в полость боковых желудочков, и кортикальных узлов.
На краниограммах определяются кальцификаты, расположенные перивен
трикулярно и в веществе мозга. На КТ изображениях в стенках желудочков вид-
ны кальцификаты, представляющие собой петрифицированную часть субэпен
димал ьного узла. В 15% случаев обнаруживается субэпендимал ьная гиганток
леточная астроцитома. Вентрикуломегалия либо диспластическая, либо
вторичная из за обструкции отверстия Монро гигантоклеточной астроцитомой.
На МРТ изображениях определяются субэпендимальные узлы, характери-
зующиеся изоинтенсивным сигналом относительно белого вещества на Т1 ВИ
и умеренно гиперинтенсивным --- на Т2 ВИ. Интенсивность сигнала узла зави-
сит от степени кальцификации. Если кальцифицирована большая часть узла,
то он характеризуется гипоинтенсивным сигналом во всех импульсных после-
довательностях (рис. 3.27).
Кортикальные узлы при туберозном склерозе располагаются в коре и в при-
лежащих отделах белого вещества и симулируют картину пахигирии. Интенсив-
ность сигнала коры не изменена, но в смежных субкортикальных отделах опре-
деляются зоны гиперинтенсивного сигнала на Т2 ВИ, обусловленные глиозом
и дефектной миелинизацией нервных волокон. В 15% случаев при туберозном
склерозе в полости бокового желудочка выявляется субэпендимарная гиганто
клеточная астроцитома. Наиболее часто образование располагается в области
межжелудочкового отверстия, имеет неоднородную структуру за счет участков
некроза, кальцификатов, характеризуется гипо и изоинтенсивным сигналом
на Т1 ВИ и гиперинтенсивным --- на Т2 В И. На контрастных изображениях от-
мечается усиление интенсивности сигнала от субэпендимальных узлов (исклю-
чая обызвествленную часть), субэпендимальной гигантоклеточной астроцито
мы. Кортикальные узлы и прилежащие субкортикальные зоны в большинстве
случаев контрастного вещества не накапливают.
Рис. 3.27. Туберозный склероз. МРТ.
а --- FLAIR ИП, аксиальная плоскость. Суб
эпендимально расположенные узлы вдаются
в полость тела боковых желудочков. В заты-
лочных долях определяются субкортикаль-
ные узлы.
б --- аксиальная плоскость, Т1 ВИ после вве-
дения контрастного препарата. Усиление сиг-
нала от субэпендимального очага, располо-
женного у переднего рога левого бокового же-
лудочка.
в --- КТ. Выявляются обызвествленные суб
эпендимальные узлы, расположенные вдоль
латеральных стенок боковых желудочков. Из-
менения в субкортикальных отделах голов-
ного мозга не визуализируются.
Ангиоматоз центральной нервной системы
(болезнь Гиппеля --- Линдау)
Болезнь Гиппеля --- Линдау наследуется по аутосомно доминантному типу.
Заболевание характеризуется унилатеральной или билатеральной гемангиобла
стомой (ангиоретикулемой) и отслойкой сетчатки глаз. В 30---60% случаев опре-
деляется гемангиобластома мозжечка. Гемангиобластомы могут наблюдаться
также в спинном мозге. Почти 60---80% гемангиобластом имеют кистозную
структуру. Наиболее часто определяется опухолевая киста, располагающаяся
в полушарии мозжечка. На постконтрастных изображениях в ее стенках визуа-
лизируются один или несколько небольших опухолевых узлов. Висцеральные
повреждения включают в себя аденокарциному почки, феохромоцитому, кисты
почек и других органов.
Опухолевидные образования
Липома составляет 0,5% внутри мозговых образований. Происходит из остат-
ков примитивного эмбрионального жира. Чаще всего локализуется в мозолис-
том теле и в 50% случаев сочетается с его агенезией. Липома может располагать-
ся как в самом мозолистом теле, так и перикаллезно. Реже встречаются липомы
пинеальной области (которые могут распространяться в охватывающую цис-
терну), воронки гипофиза, гипоталамуса, мостомозжечкового угла. Клиничес-
ки липомы протекают бессимптомно, иногда наблюдаются судорожные припад-
ки и умственная отсталость. Обычно определяется как патологическое образо-
вание, гиперинтенсивное на Т1 ВИ и менее интенсивное на Т2 ВИ, без
масс эффекта и перифокального отека. На КТ изображениях и краниограммах
определяется характерное округлое обызвествление по контуру липомы. На КТ
изображениях --- узел с четкими контурами резко пониженной плотностью (---80
и более ед. X), отчетливо прослеживается обызвествление, достаточно типичное
для этого опухолевидного процесса.
Кистозные образования
Арахноидальные кисты --- часто встречающийся порок развития. Как прави-
ло, протекает бессимптомно. Может быть случайной находкой при КТ и МРТ
исследовании. Локализация арахноидальных кист различная --- везде, где есть
арахноидальные оболочки, но наиболее часто они располагаются в области ла-
теральной борозды (сильвиевой щели), межполушарной щели, супраселлярно,
ретроцеребеллярно, в области мостомозжечкового утла.
Существует две теории образования арахноидальных кист. Первая заключа-
ется в том, что происходит расщепление и образование дупликатуры арахнои
дальной оболочки, т. е. кисты интраарахноидальные. Обычно они не связаны
с субарахноидальным пространством, т.е. несообщаюшиеся. Согласно другой
теории, кисты образуются вторично, в результате слипчивых процессов в обо-
лочках и являются субарахноидальными или сообщающимися.
Увеличение размера кисты может быть следствием осмотического пассажа
жидкости в кисту из субарахноидального пространства, секреции спинномоз-
говой жидкости эпендимой, выстилающей стенки кисты, посредством клапан-
ного механизма.
Обычно арахноидальные кисты выявляются в детском возрасте, но иногда
симптомы появляются у взрослых. Частым симптомом является повышение
внутричерепного давления. Кисты средней черепной ямки могут вызывать рас
ширение верхней глазничной щели, экзофтальм. Супраселлярные кисты иног-
да сопровождаются атрофией зрительных нервов, выпадением полей зрения,
вызывают гипопитуитарные нарушения, кисты задней черепной ямкп --- моз-
жечковую атаксию.
При больших кистах на обзорных краниограммах, КТ и МРТ изображе
ниях в зависимости от локализации выявляются истончение и выбухание
костей свода, расширение верхней глазничной щели, смещение крыльев кли-
новидной кости.
При ангиографии наблюдается смещение соответствующих сегментов сосудов.
При КТ определяется образование пониженной (соответствующей парамет-
рам ликвора) плотности, с тонкими стенками, не накапливающее контрастное
вещество. Необходимо оценить размеры, локализацию, наличие масс эффекта
и гидроцефалии. Для выявления возможной связи с субарахноидальным про
Таблица 3.2
Развитие центральной нервной системы и ее аномалии
Сроки
геста
ции, нед
Формирование анатомических
структур в норме
Вид аномалии
2 я
Нервная пластинка
Анэнцефалия
3 я
Нервная трубка
Дистрофия: энцефалоцеле,
миеломенингоцеле,
аномалия Арнольда --- Киари
4 я
Три мозговых пузыря: прозэнцефа
лон, метэнцефалон, ромбэцефалон
5 я
5 мозговых пузырей: прозэнцефа
лон, телэнцефалон, диэнцефалон
Голопрозэнцефалия и
лицевые аномалии
6 я
Комиссуральная пластинка
Агенезия мозолистого тела
Развитие желудочков
и цистерн мозга
7 8 я
Сосудистое сплетение, перфо-
рация IV желудочка, субарахнои
дальное пространство
Арахноидальные кисты,
гидроцефалия, аномалия
Арнольда --- Киари
Клеточная
пролиферация
3 6 я
Пролиферация
недифференцированных клеток
(нейробласта)
Гипоплазия мозжечка или
мальформация Денди ---
Уолкера, факоматозы
Нейрональная
миграция
6 7 я
Миграция нейробласта,
формирование примитивной
формы серого вещества
Гидранэнцефалия, шизэнце
фалия, порэнцефалия,
гетеротопия серого вещества
20 я
Первичные борозды
Гетеротопия серого
вещества
Лиссэнцефалия, микрогирия
24 40 я Вторичные борозды
Макрогирия
36 40 я Третичные борозды
странством иногда приходится прибегать к компьютерной цистернографии, на
основании которой выделяют 4 типа арахноидальных кист:
отсутствует заполнение;
раннее заполнение и раннее опорожнение;
раннее заполнение и отсроченное освобождение;
отсроченное заполнение и отсроченное освобождение.
При больших кистах средней черепной ямки достаточно часто прибегают
к оперативному вмешательству из за опасности развития вторичной геморра-
гии, связанной с разрывом поверхностных вен.
При МРТ иногда можно заметить, что содержимое кисты отличается по ин-
тенсивности сигнала от спинномозговой жидкости из за отсутствия пульсации
и примеси белка.
Список основной литературы
1. Алиханов A.A., Синицын В.Е., Перепелова Е.М. и др. Использование режима
3D FSPGR магнитно---резонансной диагностике кортикальный дисплазий у де-
тей // Вестн. рентгенол.--- 2001.--- No 2.--- С. 9 16.
2. Ватолин К. В. Ультразвуковая диагностика заболеваний головного мозга
у детей.--- М.: Видар, 1995.--- 120 с.
3. Володин H.H., Медведев М.И., Горбунов A.B. Компьютерная томография
головного мозга у новорожденных и детей раннего возраста.--- М.: Издательский
дом ГЭОТАР МЕД, 2002. 120 с.
4. Иова A.C., Гармашов Ю.Н., Анрущенко Н.В., Паутницкая Т.С. Ультрасоно
графия в нейропедиатрии. Новые возможности и перспективы. Ультрасоногра
фический атлас--- СПб.: Петроградский и Ко, 1997.--- 160 с.
5. Коновалов А.Н., Блинков СМ., Пуцилло М.В. Атлас нейрохирургической
анатомии.--- М.: Медицина, 1990.--- 336 с.
6. Коновалов А.Н., Корниенко В.Н., Озерова В.И, Пронин H.H. Нейрорентге
нология детского возраста.--- М.: Антидор, 2001.--- С. 60---113.
7. Медведев Ю.А., МацкоД.Е. Аневризмы и пороки развития сосудов мозга.---
СПб.: РНХИ им. проф. А.Л.Поленова, 1993. 190 с.
8. Barkovich J.A. Pediatric neuroimaging.--- 3rd ed.--- Philadelphia: Lippincott Wil
liams&Wilkins, 2000. 850 p.
9. Barkovich A.J., Kuzniecky R.l. Gray matter heterotopia // Neurology.--- 2000.---
Vol. 55. P. 1603 1608.
10. Barkovich A.J., Kuzniecky R.I., Dobbyns W.B. et al. A classification scheme
for malformations of cortical development // Neuropediatrics.--- 1996.--- Vol. 27.---
P. 59 63.
11. Bísese J.H., Wang A.-M. Pediatric cranial MRI. An atlas of normal develop-
ment.--- N.-Y.: Springer-Verlag, 1994.--- 183 p.
12. Bronen R.A., Vives K.P., Kim J.H. etal. Focal cortical dysplasia of Taylor balloon
cell subtype.--- MR differentation from low-grade tumors // A. J. N. R.--- 1997.---
Vol. 18.- P. 1141-1151.
13. Dobbyns W.B., Truwit CL. Lissencephaly and other malformations of cortical
development: 1995 update // Neuropediatrics.--- 1995.--- Vol. 26.--- P. 132-147.
14. Guerrini R., Barkovich A.J., Sztriha L., Dobyns W.B. Bilateral frontal polymicro-
gyria // Neurology- 2000.- Vol. 54.- P. 909-913.
15. Guerrini R., Dubeau F., Dulac 0. et at. Bilateral parasagittal parietooccipital
polymicrogyria and epilepsy // Ann. Neurol. 1997.--- Vol. 41.--- P. 65-73.
16. Hannan A.J.. Servotte S., Katsnelson A. et at. Characterization of nodular
neuronal heterotopia in children // Brain.--- 1999.--- Vol. 122.--- P. 219-238.
17. Hanvood-Nash D.C., Peterson H. Pediatric Radiology, 1992.--- 324 p.
18. Huk W.I., Gadermann G. MRI of Central Nervous System Deseases.--- N.-Y.:
Springer-Verlag, 1995.
19. Leventer R.J., Phelan E.M., Coleman L. T. et at. Clinical and imaging features of
cortical malformations in childhood // Neurology--- 1999.--- Vol. 53.--- P. 715-722.
20. Norman M.G., McGillivray B.C., Kalousek D.K. et at. Congenital Malformations
of the brain // Pathologic, Embryologic, Clinical, Radiologic and Genetic Aspects.---
Oxford: University Press, 1995.- P. 223-307.
21. Raymond A.A., Fish D.R., Sisodiya S.M. et at. Abnormalities of gyration, hetero-
topias, tuberous sclerosis, focal cortical dysplasia, microdysgenesis, dysembryoplastic
neuroepithelial tumor and dysgenesis of the archicortex in epilepsy: clinical, EEG and
neuroimaging features in 100 adult patients // Brain.--- 1995.--- Vol. 118.--- P. 629-
660.22. Shorvon S. MRI of cortical dysgenesis // Epilepsya.--- 1997.--- Vol. 38,
Suppl. 10.- P. 13-18.
Глава 4
ГИДРОЦЕФАЛИЯ
«Уребенка вода в голове»,--- говорит обыватель. «Уре-
бенка гидроцефалия»,--- серьезно произносит врач, в сущ-
ности, лишь повторяя по гречески то, что обыватель на-
звал по простому. Но что такое эта жидкость? Отку-
да она берется?Вот что должен выяснить врач».
Франсуа Мажанди, 1842
Гидроцефалией (водянкой) называется расширение ликворосодержащих по-
лостей головного мозга. Желудочки и субарахноидальное пространство запол-
нены спинномозговой жидкостью, которую постоянно образуют сосудистые (хо
риоидальные) сплетения, находящиеся в обоих боковых, III и IVжелудочках. Она
всасывается в венозную кровь через пахионовы грануляции, расположенные
в одноименных ямочках на внутренней кортикальной пластинке костей черепа.
Рис. 4.1. Схема ликворных
пространств
(по Netter F.H., 1958).
А --- паутинная оболочка; AG ---
арахноидальные грануляции;
AS --- сильвиев водопровод;
ССМ --- церебелломедуллярная
цистерна; CI --- межножковая
цистерна; CPLV --- сосудистое
сплетение бокового желудочка;
CPV3 --- сосудистое сплетение
3 го желудочка; CPV4 --- сосуди-
стое сплетение 4 го желудочка;
CS --- верхняя цистерна; D ---
твердая мозговая оболочка;
FM --- отверстие Мажанди;
GCV --- большая цистерна мозга;
IF --- межжелудочковое отвер-
стие; SAS --- субарахноидальное
пространство; SSS --- верхний са-
гиттальный синус.
Спинномозговая жидкость вытекает из боковых желудочков через межжелудоч-
ковые отверстия (отверстия Монро) и попадает в III желудочек, откуда по водо-
проводу мозга поступает в I Ужелудочек, из которого вытекает через срединную
апертуру IV желудочка (отверстие Мажанди) --- в большую цистерну, а через бо-
ковые отверстия (Люшка) --- в мостомозжечковые цистерны, т. е. оказывается
в субарахноидальном пространстве. Из цистерн задней черепной ямки спин-
номозговая жидкость заполняет субарахноидальные пространства спинного и
головного мозга, достигая мест своего всасывания (рис. 4.1). Общий объем спин-
номозговой жидкости не превышает 150 мл и трижды в течение суток полностью
обновляется, при этом скорость ее образования составляет 0,35---0,4 мл/мин.
Гидроцефалия формируется, главным образом, в двух ситуациях: если нару-
шается равновесие между секрецией и резорбцией спинномозговой жидкости
либо если возникает препятствие на путях ее транспорта.
Существует несколько принципов классификации гидроцефалии (по этио-
логии, по локализации расширенных ликворсодержащих пространств, по тече-
нию и т. д.). В зависимости от причины все гидроцефалии делятся на гиперсек-
реторные, гипорезорбтивные иокклюзионные. Гиперсекреторные и гипорезор
бтивные водянки объединены в группу открытых, сообщающихся,
неокклюзионных гидроцефалии. Еще одной нередкой причиной гидроцефалии
являются атрофические изменения головного мозга, в этом случае водянка фор-
мируется ex vacuo, т. е. является заместительной.
Изолированное или преимущественное расширение желудочков мозга назы-
вается внутренней гидроцефалией (в которой выделяют MOHO , би и тривентри
кулярные водянки), расширение субарахноидального пространства называет-
ся наружной гидроцефалией, комбинация расширенных желудочков и субарах
ноидальных щелей соответствует смешанной гидроцефалии.
По течению гидроцефал и и делятся на прогрессирующие, компенсированные
и регрессирующие, т. е. находящиеся в стадии обратного развития.
По уровню внутричерепного давления различают гипертензивные, нормотен
зивные и гипотензивные гидроцефалии.
По срокам возникновения гидроцефалии делят на врожденные и приобретенные.
При диагностике гидроцефалии важно не только оценить анатомические
размеры ликворсодержащих полостей, но и по возможности приблизиться к по-
ниманию причин их расширения, темпов нарастания водянки, ближайшего
прогноза, без чего немыслимо этиопатогенетическое лечение, которое может быть
как хирургическим, так и консервативным. Кроме того, выявленная ситуация
может не нуждаться в коррекции.
Оптимальными методами лучевой диагностики гидроцефалии стали КТ и
МРТ. Чрезродничковая и транскраниальная нейросонография может служить
для скрининга и наблюдения в динамике, особенно в детском возрасте, а крани-
ография и, тем более, пневмоэнцефалография утратили свою актуальность.
Современные методы лучевой диагностики позволяют выявить водянку еще
на доклиническом этапе, установить причину развития патологического про-
цесса, высказаться о возможном патогенезе, осуществить динамический конт-
роль, оценить эффективность проводимых лечебных мероприятий.
Для выявления окклюзионной гидроцефалии необходимо анализировать
разные отделы ликворсодержащей системы, последовательно переходя от оцен-
ки наиболее податливых зон к более устойчивым участкам.
1. Самые ранние изменения возникают в височных рогах боковых желудоч-
ков, которые расширяются и становятся хорошо различимыми даже на акси-
альных КТ срезах в виде выпуклого кпереди серпа. Задние отделы расширен
Рис. 4.2. Развитие внутренней открытой гиперсекреторной гидроцефалии у ребенка
2 лет на фоне менингита. КТ.
а --- первое исследование: начальное расширение височных и лобных рогов боко-
вых желудочков.
ного височного рога приобретают округлый просвет. Такая форма височного рога
отличается от его «заместительного» расширения, при котором происходит ло-
кальное выбухание стенки, подтянутой к рубцовой зоне, либо (при атрофии гип
покампа) возникает уплощение его медиобазальной стенки, которая при окк
люзионной гидроцефалии остается втянутой довольно долго.
2. Следующий этап развития гидроцефалии --- расширение лобных рогов
боковых желудочков. Все его стенки становятся выпуклыми, за исключением
участка, к которому прилежит головка хвостатого ядра (рис. 4.2, а). На акси-
альных срезах угол, образованный медиальными стенками лобных рогов обоих
Рис. 4.2. Продолжение.
б --- второе исследование через 3 недели: расширение боковых и третьего желудоч-
ков.
боковых желудочков, уменьшается и становится острым, в то время как при за-
местительной гидроцефалии между медиальными стенками расширенныхлоб
ных рогов сохраняется тупой угол.
3. Увеличение и баллонообразная деформация 111 желудочка приводит к тому,
что все его стенки, в первую очередь боковые, становятся выпуклыми, и только
крыша может оставаться плоской под влиянием расположенных выше и рас-
ширенных боковых желудочков. Такой «вздутый» 111 желудочек можно выявить
Рис. 4.2. Окончание.
в --- третье исследование спустя две недели: нарастание гидроцефалии всей желу-
дочковой системы.
У
лись.
на аксиальных и корональных срезах (рис. 4.3). При анализе сагиттальных изоб-
ражений следует особенно внимательно оценить заднюю стенку III желудочка:
появление вмятин от соседних мозговых структур (ножек мозга, сосочковых тел
и серого бутра) служит одним из признаков мозжечково тенториального вкли-
нения. В отличие от окклюзионной гидроцефалии, заместительная водянка
III желудочка сохраняет плоскую форму его боковых стенок, поэтому они оста-
ются параллельными.
4. Значительное расширение тел боковых желудочков приводит к подъему и
выбуханию их верхних стенок, что ведет к истончению и дугообразной дефор-
мации мозолистого тела, особенно отчетливо видимой на сагиттальном срезе. При
этом на томограммах в корональной плоскости треугольный просвет тел боко-
вых желудочков превращается почти в шаровидный, плоскими остаются толь-
ко примыкающие друг к другу медиальные стенки, образующие прозрачную
перегородку. Наружные стенки боковых желудочков могут иметь фестончатый
контур, что указывает на быстрое нарастание гидроцефалии.
5. Расширение ГУ желудочка может возникнуть при низкой окклюзии, одна-
ко иногда оно наблюдается и при супратенториальных процессах, если расши-
ряющиеся боковые и III желудочки вызываютвисочно тенториальное вклине-
ние, которое препятствует транспорту спинномозговой жидкости из цистерн
задней черепной ямки в субарахноидальное пространство больших полушарий.
Вместе с тем нередко IV желудочек остается неизмененным при окклюзии водо-
провода мозга, III желудочка или межжелудочкового отверстия Монро.
6. Перивентрикулярный отек обусловлен пропотеванием ликвора при повы-
шении давления внутри желудочка. При этом происходит снижение плотности
белого вещества головного мозга вокруг расширенных лобных рогов боковых
желудочков на КТ срезах и выявляются признаки отека той же зоны на магнит-
но резонансных томограммах.
7. Сужение субарахноидальных щелей является важным признаком гидро-
цефалии у пациентов старшей возрастной группы, поскольку та или иная сте
Рис. 4.4. Наружная гидроцефалия. КТ.
а --- расширение субарахноидального пространства надлобными долями.
Рис. 4.4. Окончание.
б --- после шунтирующей операции.
пень атрофии коры является признаком нормального старения. Поэтому отсут-
ствие ожидаемого расширения субарахноидального пространства у человека
пожилого возраста должно привлечь к себе внимание врача.
8. Расширение субарахноидального пространства возникает при наружной
гидроцефалии и, как правило, служит показателем нормального внутричереп-
ного давления (рис. 4.4).
КТ и М РТ семиотика гидроцефалии достаточно хорошо изучена. Вместе с тем
практика использования КТ в нейрохирургической клинике показывает, что воз-
можны ошибки и существенные затруднения в оценке причины развития гид-
роцефалии, выраженности внутрижелудочковой гипертензии, выявлении ослож-
нении. Большие ограничения связаны с возможностью получения изображений
только в аксиальной плоскости. Так, диагностика стеноза водопровода мозга
базируется только на косвенных признаках. Весьма сложным является выявле
ние изменений в оболочках головного мозга. Одной из причин может быть недо-
статочно полное следование методическим принципам, например, отказ от внут-
ривенного контрастирования. Особые трудности возникают в тех случаях, ког-
да прямые признаки патологического процесса отсутствуют.
ОККЛЮЗИОННЫЕ ГИДРОЦЕФАЛИИ
Препятствие току спинномозговой жидкости легче всего возникает в узких
местах ликворсодержащей системы, к которым относятся отверстия Монро,
задний отдел III желудочка и водопровод мозга (сильвиев водопровод).
Рис. 4.5. Окклюзионная гидроцефалия обоих боковых желудочков. КТ.
1 --- опухоль III желудочка, обтурируюшая оба межжелудочковых отверстия; 2 --- пе
ривентрикулярный отек вокруг боковых желудочков.
Рис. 4.6. Стеноз водопровода мозга. КТ.
а --- баллонообразное расширение III желудочка.
Сдавление межжелудочкового отверстия Монро вызывают:
--- коллоидная киста III желудочка;
--- эпендимома (рис. 4.5);
--- тератома;
--- врожденная атрезия отверстия;
--- врастание глиомы смежных отделов мозга (см. рис. 4.3);
--- внутричерепные гематомы и ушибы головного мозга, вызывающие зна-
чительную латеральную дислокацию срединных структур, при этом, вследствие
сдавления отверстия Монро, возникает острая дислокационная гидроцефалия
бокового желудочка на стороне, противоположной поврежденному полушарию.
Рис. 4.6. Окончание.
б --- быстрое нарастание гидроцефалии формирует фестончатый контур тел боко-
вых желудочков.
Сдавление заднего отдела III желудочка происходит в двух ситуациях:
--- опухоли шишковидной железы (герминома, тератома и тератокарцинома,
пинеобластома и пинеоцитома);
--- аневризмы большой мозговой вены (вены Галена).
Проходимость водопровода мозга нарушают:
--- стеноз водопровода мозга (рис. 4.6);
--- глиомы, растущие вокруг водопровода мозга и сдавливающие его;
--- артериовенозные мальформации;
--- кисты, расположенные над пластинкой четверохолмия.
Проходимость IV желудочка нарушается как при внутрижелудочковых опу-
холях, так и при иных объемных образованиях задней черепной ямки, сдавлива-
ющих IVжелудочек извне (рис. 4.7).
Рис. 4.7. Окклюзионная тривентрикулярная гидроцефалия. KT.
1 --- опухоль мозжечка, сдавливающая IV желудочек.
ОТКРЫТЫЕ (СООБЩАЮЩИЕСЯ) ГИДРОЦЕФАЛИИ
Открытые гидроцефалии могут быть вызваны перенесенной инфекцией или
кровоизлиянием любого происхождения (травма, хирургическое вмешательство,
спонтанный разрыв аневризмы). Открытая гидроцефалия возникает также при
субарахноидальных отсевах опухоли (менингокарциноматоз), при повышении
содержания белка в спинномозговой жидкости на фоне спинальных опухолей,
чаще всего при эпендимомах. Врожденные гидроцефалии также в большинстве
своем являются открытыми.
В 1965 г. R.D.Adams, C.M.Fisher и S.Hakim впервые описали идиопатичес
кую открытую гидроцефалию у пациентов пожилого возраста, протекающую
при нормальном внутричерепном давлении (гидроцефалия нормального дав
ления). Клиническая картина включала в себя триаду симптомов: нарушение
походки, когнитивные расстройства и недержание мочи,--- которые отчетли-
во регрессировали после выполнения шунтирующих операций. Самым пока-
зательным было восстановление возможности самостоятельной ходьбы у боль-
ных, которые до операции передвигались на кресле либо вообще были прико-
ваны к постели. Эти сообщения послужили основанием для выполнения серии
подобных операций пациентам с гидроцефалией, страдающих двигательны-
ми и мнестическими нарушениями. Вместе с тем оказалось, что у большой
группы пациентов шунтирование не привело к изменению состояния либо после
короткого периода улучшения клинические симптомы вновь нарастали. Оче-
видно, что требуется более строгий отбор больных для выполнения шунтиро-
вания, чтобы в эту группу не попали пациенты с заместительными водянка-
ми, например, обусловленными болезнью Альцгеймера и иными атрофичес
кими процессами в головном мозге, которые имеют не только сходную
с триадой R.D.Adams --- S.Hakim клиническую картину, но и почти аналогич-
ные изменения на КТ и МРТ изображениях. Для отбора кандидатов на шун-
тирующие операции применяют:
1) мониторирование внутричерепного давления;
2) оценку его изменений в ответ на выведение части спинномозговой жидко-
сти или надополнительное введение в ликворсодержащую систему изотоничес-
кого раствора натрия хлорида;
3) радионуклидную цистернографию, позволяющую оценить динамику пе-
ремещения радиоактивного маркера с током спинномозговой жидкости;
4) изучение мозгового кровотока.
Вместе с тем до сих пор нет единого принципа, применяя который можно с уве-
ренностью предсказать успех шунтирующей операции при открытой гидроце-
фалии или отказаться от неоправданного вмешательства.
В последние годы появление позитронно эмиссионной томографии, с помо-
щью которой можно изучать метаболические процессы головного мозга, и фун-
кциональной магнитно резонансной томографии вновь обострило интерес
к проблеме хирургического лечения открытой гидроцефалии.
Современные методы визуализации позволяют не только выявить водянку
мозга, но дифференцировать внутрижелудочковую ги пертензию от нормотензии
или даже гипотензии, что наблюдается при гидроцефалии ex vacuo (заместитель-
ной гидроцефалии). Экспансия нижнего рецессуса Ш желудочка, расширение
височных рогов и баллонообразная дилатация передних рогов, уменьшение мам
милопонтийного расстояния (в норме и при атрофии соответствует 11,5--- 12,0 мм,
при окклюзионной гидроцефалии --- менее 10 мм), депрессия заднего форникса
и смещение вниз гипоталамуса, истончение (менее 6 мм) мозолистого тела в са-
гиттальной плоскости и его элевация --- типичны для внутрижелудочковой ги
пертензии. Начальные этапы развития окклюзионной гидроцефалии весьма
сложно бывает дифференцировать от нормотензивной или даже гипотензивной
гидроцефалии, наблюдаемой при атрофии вещества мозга.
Для внутрижелудочковой гипертензии характерен перивентрикулярный отек
(см. рис. 4.5). Необходимо иметь в виду, что умеренная выраженность пери
вентрикулярного свечения в области передних рогов, так называемые «пери
вентрикулярные шапочки», на МРТ изображениях не является признаком по-
вышения внутрижелудочкового давления. Гистологические исследования этой
субэпендимарной зоны выявили сеть аксонов с низким содержанием миели-
на, а также лоскутное уменьшение эпендимы в передних рогах. Ситуация усу-
губляется особенностями движения интерстициальной жидкости в перивен
трикулярном регионе.
С практической точки зрения целесообразно выделение нескольких вари-
антов лучевой картины, отражающей различную степень повышения внутри
желудочкового давления. Описывают следующие стадии перивентрикулярного
отека:
I стадия --- размытость контуров верхненаружных углов передних рогов или
четко отграниченная кайма пониженной плотности той же локализации;
II стадия --- понижение плотности у передних и задних рогов;
III стадия --- отек по периметру боковых желудочков;
IV стадия --- фестончатость контуров боковых желудочков, истончение веще-
ства мозга.
Ошибки, связанные с применением МРТ, можно разбить на несколько групп.
Прежде всего, они обусловлены использованием магнитно резонансных томог-
рафов разной индукции, что приводит к существенным различиям выявляемых
изменений и требует коррекции дифференциально диагностических критери-
ев. Большие трудности связаны с визуализацией интравентрикулярного конца
шунта при МРТ. Отдельно стоят ошибки, обусловленные погрешностями мето-
дики. Это следствие недостаточно полного использования возможностей совре-
менных MP томографов, квалификации персонала, особенно на начальной ста-
дии освоения метода.
Отдельную группу составляют ошибки в установлении наличия декомпен
сированной внутрижелудочковой гипертензии, когда стенки желудочков при-
обретают волнистые или зазубренные контуры, мантия мозга истончена, а пе
ривентрикулярное свечение отсутствует.
Достаточно часто при МРТ в «узких» местах ликворных путей возникают
артефакты, обусловленные движением ликвора. В норме отсутствие сигнала от
ликвора лучше видно наТ2 взвешенном изображении в проекции водопровода
мозга, каудальных отделах IV желудочка, реже III желудочка. При исследова-
нии больныхс вентрикуломегалией и гидроцефалией наличие сигнала более по-
лезно, чем отсутствие его, так как указывает на возможную обструкцию, хотя не
точно определяет ее уровень. Симптом «отсутствия потока» чаще встречается при
хронической нормотензивной гидроцефалии, реже при острой сообщающейся
гидроцефалии.
Говоря об осложнении течения гидроцефалии, необходимо упомянуть о нару-
шении кровообращения по передним мозговым артериям, обусловленном зна-
чительным расширением Ш желудочка, с развитием ишемии базальных отде-
лов и медиальных поверхностей больших полушарий. Эти изменения находят
отражение на КГ и МРТ в виде типичных проявлений острого нарушения моз-
гового кровообращения по ишемическому типу в бассейне передней мозговой
или перикаллезной артерии. Осложнения течения гидроцефалии как в доопера
ционном периоде, так и после шунтирующей операции требуют дополнительно-
го углубленного изучения.
Список основной литературы
1. Вавилов СБ., Брагина Л.К., Верещагин Н.В., Левина Г.Я. Компьютерная то-
мография головного мозга в норме // Верещагин Н.В., Брагина Л.К., Вави-
лов СБ., Левина Г.Я. Компьютерная томография мозга.--- М.: Медицина,
1986. 256 с.
2. Володин H.H., Медведев М.И., Горбунов A.B. Компьютерная томография го-
ловного мозга у новорожденных и детей раннего возраста.--- М.: ГЭОТАР МЕД,
2002. 120 с.
3. Сорокина М.Н., Иванов В.В., Скрипченко Н.В. Бактериальные менингиты
у детей,--- М.: Медицина, 2003.--- 320 с.
4. Хачатрян В.А., Берснев В.П., Сафин Ш.М., Орлов Ю.А., Трофимова Т.Н. Гид-
роцефалия (патогенез,диагностика, хирургическое вмешательство).--- СПб.:
Изд. РНХИ им. проф. А.Л.Поленова, 1998. 234 с.
5. Barkovich A. J. Hydrocephalus // Barkovich A.J. Pediatric Neuroimaging.---
3rd ed. Philodelphia: Lippincott; Williams and Wilkins, 2000. P. 581 621.
6. Bradley W.G., Quencer R.M. Hydrocephalus, Atrophy, and CSF Flow //
Stark D.D., Bradley W.G., Magnetic resonance imaging.--- 2"d ed.--- St. Louis: Mosby
YearBook, 1992. P. 891 963.
7. Netter F.H. The ciba collection of medical illustration // Nervous system.---
Vol. 1. New York: Color Press, 1958. P. 44.
Глава 5
НЕЙРОРАДИОЛОГИЯ КОМЫ
Тот, кто владеет ключом к управлению процессом отека
и набуханий, тот владеет ключом жизни и смерти боль-
ного.
Н.Н.Бурденко
Кома --- понятие сугубо клиническое, отражающее сомноленцию и ступор,
развивающиеся при различных ургентных патологических состояниях, и опре-
деляющее клинические признаки и критерии, относящиеся к утрате сознания. Это
ставит кому над привычными неврологическими категориями, такими как травма,
опухоль, воспаление, дегенеративные процессы, метаболические расстройства и
цереброваскулярные заболевания.
Самые ранние описания комы встречаются в древнеегипетских папиру-
сах. Уже тогда утрата сознания справедливо связывалась с тяжестью череп-
но мозговой травмы и рассматривалась как неблагоприятный прогностичес-
кий фактор. В дальнейшем на протяжении всей истории человечества коме
отдавали дань уважения и поэты, например Гомер, и ученые. Время все рас-
ставляет по местам. То, что вчера казалось незыблемым, сегодня рассеива-
ется как туман и представляет лишь пресловутый исторический интерес. Это
ни в коей мере не касается представлений о коме. Как и много веков назад,
ее развитие прежде всего связывают с тяжелой ЧМТ, а в случаях пролонги-
рованного бессознательного состояния наиболее типичной находкой являются
нисходящая транстенториальная дислокация головного мозга и вторичное
повреждение его ствола.
Знание лучевых проявлений комы крайне необходимо для нейрорадиолога,
поскольку эффективность лечения зависит, втом числе, от адекватности и сво-
евременности интерпретации KT и МРТ проявлений.
Патологические изменения, ведущие к развитию комы, могут локализоваться
супратенториально, инфратенториально, а также иметь диффузный или муль
тифокальный характер.
К обширным супратенториальным экстралимбическим поражениям, со-
провождающимся развитием комы, относятся травма, острые и подострые
васкулопатии, инфекции (рис. 5.1). Травма, несомненно, является наиболее
частой причиной комы. При этом особое значение имеют диффузное аксо
нальное повреждение, гематомы, эмболии и отек мозга (рис. 5.2). Тромбоэм-
болия ведет к коме в тех случаях, когда в процесс вовлекается несколько
сосудистых территорий с поражением больших областей мозга. Кома, обус-
ловленная васкулитом, обычно развивается при геморрагических инфарктах,
нередко двухсторонних. Тромбоз верхнего и нижнего сагиттальных, попереч
Рис. 5.2. Жировая эмболия
мелких сосудов головного
мозга. МРТ. Т2 ВИ,
сагиттальная плоскость.
Множественные очаги рас-
полагаются в белом веществе
мозга суправентрикулярного
уровня по ходу перфорирую-
щих сосудов.
Рис. 5.3. Тромбоз правого
поперечного синуса. МРТ.
FLAIR ИП, аксиальная
плоскость.
Гиперинтенсивный сигнал от
правого поперечного синуса.
Рис. 5.4. Тромбоз верхнего сагиттального
синуса. Венозный инфаркт левой
теменной доли,
а --- PC GRE ИП (венография),
сагиттальная плоскость;
б --- Т2 ВИ, аксиальная плоскость;
в --- постконтрастное Т1 ВИ,
корональная плоскость.
Изображение верхнего сагиттального си-
нуса на всем протяжении отсутствует (а).
В субкортикальных отделах левой темен-
ной доли выявляется зона патологичес-
кого сигнала (отек и кровоизлияние), ин-
тенсивно накапливающая контрастное
вещество (б, в).
ных, сигмовидных, прямых и пещеристых синусов, а также вен с развитием
тромбофлебита влечет за собой кому (рис. 5.3, 5.4). К этому грозному состо-
янию также может привести широкий спектр энцефалитов и менингитов
(рис. 5.5).
Наиболее частыми причинами развития комы при инфратенториальной ло-
кализации изменений являются ишемия, обычно обусловленная диссекцией ба
зилярной артерии, и центральный понтинный миелинолиз.
Центральный понтинный миелинолиз (осмотическая демиелинизация) ---
это острый демиелинизирующий процесс, связанный с передозировкой ле
Рис. 5.6. Центральный понтинный
миелинолиз. МРТ.
В центральной части увеличенно-
го в размерах моста мозга опреде-
ляется зона патологического сиг-
нала --- гиперинтенсивного на Т2
ВИ (а, б) и гипоинтенсивного на
Tl ВИ (в). Периферические отде-
лы моста интактны.
ГЖРг
карственных средств или алкоголя, а также с электролитными расстройства-
ми. Он часто наблюдается при резкой коррекции гипонатриемии (рис. 5.6).
Главными клиническими чертами такого состояния являются кома, тетра
парез и псевдобульбарный паралич. В противоположность понтийной ише-
мии сосуды, обеспечивающие кровоснабжение моста мозга, остаются интак
тными.
Последняя большая группа заболеваний, ведущих к коме, связана с диффуз-
ными, мультифокальными и метаболическими энцефалопатиями.
Перечень заболеваний, ведущих к развитию коматозных состояний, состав-
ленный с учетом клинической картины и эффективности КТ и МРТ исследо
ваний, представлен в табл. 5.1.
Таблица 5.1
Заболевания, ведущие к развитию комы
Ведущий
симптомокомплекс
Нозологические формы
I Стволовые рефлек-
сы не нарушены,
латерализованная
очаговая симптома-
тика отсутствует,
лучевые исследова-
ния эффективны
Отравление, метаболическая энцефалопатия, гипер-
тоническая энцефалопатия, менингит, негерпетиче-
ский вирусный энцефалит, жировая эмболия, суба
рахноидальное кровоизлияние, болезнь Крейтц
фельдта---Якоба, гидроцефалия, субдуральная
гематома, ушиб головного мозга, отек, диффузное
аксональное повреждение, острый диссеминирован
ный энцефаломиелит
II Стволовые рефлек-
сы не нарушены,
латерализованная
очаговая симптома-
тика отсутствует,
лучевые исследова-
ния неэффективны
Эпилепсия, истерическая кома или кататонический
ступор, субарахноидальное кровоизлияние, болезнь
Крейтцфельдта---Якоба, менингит
III Стволовые рефлек-
сы не нарушены,
имеется латерали-
зованная очаговая
симптоматика, луче-
вые исследования
эффективны
Кровоизлияние в мозг (базальные ядра, таламус),
субдуральная или эпидуральная гематома,
ишемический инсульт, герпетический энцефалит,
абсцесс мозга, васкулит, опухоль головного мозга,
парциальный эпилептический припадок
IV Множественные
нарушения стволо-
вых рефлексов,
лучевые исследова-
ния эффективны
Кровоизлияние в варолиев мост, средний мозг,
мозжечок;
Опухоль или абсцесс мозжечка, ишемический
инсульт мозжечка;
Объемное образование в полушарии головного
мозга со сдавлением верхних отделов ствола
мозга;
Опухоль, демиелинизация, энцефалит, абсцесс,
ушиб, кровоизлияние, инсульт ствола мозга;
Центральный понтинный миелинолиз
У коматозных больных, независимо от генеза этого грозного осложнения,
обычно выделяют три модели:
--- обширные двухсторонние неокортикальные поражения;
--- диффузное поражение белого вещества;
--- двухстороннее поражение ядер серого вещества.
При этом основными паттернами комы являются:
--- ограничение резервных пространств;
--- диффузное аксиальное поражение;
--- нейроналъные некрозы;
--- синаптическая недостаточность.
КОМА И ОГРАНИЧЕНИЯ РЕЗЕРВНЫХ ПРОСТРАНСТВ
Головной мозг хорошо защищен от неблагоприятных воздействий внешней
среды. Кости и твердая мозговая оболочка формируют замкнутое простран-
ство, сообщающееся лишь посредством жестко фиксированных отверстий:
большое затылочное отверстие и вырезка намета мозжечка. Интракраниаль
ное пространство также ограничено плотной дупликатурой твердой мозговой
оболочки --- большим серповидным отростком. При этом содержимое полос-
ти черепа оказывается разделенным на три связанные друг с другом полости ---
две в супратенториальных отделах и одну, расположенную инфратенториально.
Указанные факторы резко ограничивают возможности головного мозга к уве-
личению в объеме.
Рис. 5.7. Схема дислокаций
головного мозга.
I --- корональная плоскость; II --- ак
сиальная плоскость; III
тальная плоскость.
1 --- смещение поясной извилины
под фалькс; 2 --- нисходящее височ
но тенториальное смещение; 3 ---
восходящее транстенториальное
смещение; 4 --- смещение миндали-
ны мозжечка в большое затылочное
отверстие; 5 --- трансаллярное сме-
щение.
Повышение внутричерепного давления часто встречается при травме, ин-
фекционных, сосудистых и опухолевых процессах. При этом наблюдается
сужение резервных пространств, усугубляющее повышение внутричерепного
давления. В таких случаях развиваются дислокации головного мозга. В зави-
симости от объема поражения, его локализации, скорости нарастания изме-
нений выделяют несколько вариантов смешений, наиболее частыми из кото-
рых являются (рис. 5.7):
--- смещение поясной извилины под свободный край серповидного отростка
твердой мозговой оболочки (субфальксиальное, илицингулярное, смещение);
Рис. 5.8. Субфальксиальное
смешение. МРТ.
а --- постконтрастное Т1 ВИ,
корональная плоскость;
б--- постконтрастное Т1 ВИ,
аксиальная плоскость;
в --- Т2 ВИ, сагиттальная плоскость.
В правой лобной области определя-
ется парасагиттальная менингиома,
прилежащая к верхнему сагитталь-
ному синусу и серпу мозга, окружен-
ная зоной перифокального отека.
Определяется смещение правой по-
ясной извилины под свободный
край серповидного отростка твердой
мозговой оболочки. Тело правого
бокового желудочка сдавлено и сме-
щено.
--- одно иди двухстороннее смещение гиппокампов в вырезку намета моз-
жечка --- височно тенториальное вклинение;
--- смещение обоих гиппокампов, подушек зрительных бугров, сосочковых
телец, валика мозолистого тела в вырезку намета мозжечка --- центральная дис-
локация, являющаяся крайней формой двухстороннего височно тенториального
вклинения;
--- смещение мозжечка в вырезку намета --- восходящее транстенториальное
вклинение;
--- смещение структур задней черепной ямки, и прежде всего миндалин моз-
жечка, в большое затылочное отверстие --- нисходящее аксиальное вклинение.
Локальное или диффузное увеличение объема головного мозга обязательно
сопровождается сдавлением субарахноидального пространства и уплощением
извилин, отражая ограничение резервных пространств.
При одностороннем патологическом процессе, расположенном латерально и
достаточно высоко, развивается боковое смещение, проявляющееся уплощением
извилин, сдавлением бокового желудочка на стороне поражения, дислокацией
церебральных извилин через срединную линию под серповидный отросток твер-
дой мозговой оболочки и водянкой контралатерального бокового желудочка из
за сдавления межжелудочкового отверстия (рис. 5.8). Описанные изменения
обусловлены действием горизонтального вектора силы. Подавление направле-
но в разные стороны, поэтому целесообразно выделить его вертикальную состав-
ляющую.
Воздействие вертикального вектора силы ведет к сдавлению бокового крыла
супраселлярной цистерны, смещению и деформации межножковой цистерны.
При этом развивается нисходящее транстенториальное вклинение гиппокампа
Рис. 5.9. Схема нисходящего височно тенториального смещения.
I --- корональная плоскость; II --- аксиальная плоскость.
Смещение крючка гиппокампа в вырезку намета мозжечка (толстая стрелка).
Интактный гиппокамп (тонкая стрелка).
а
б
Рис. 5.10. Нисходящее транстенториальное вклинение. МРТ.
а --- Т1 ВИ, корональная плоскость; б --- Т2 ВИ, аксиальная плоскость.
Патологическое образование левой височной доли с выраженным перифокальным
отеком. Вклинение гиппокампа левой височной доли в вырезку намета мозжечка.
Медиобазальные структуры левой височной доли смещены в вырезку намета моз-
жечка и деформируют левую ножку мозга.
(крючок, парагиппокампальный регион) на стороне поражения в фиксирован-
ное кольцо вырезки намета мозжечка (рис. 5.9). В таких случаях наблюдаются
укорочение ножки мозга на стороне поражения, укорочение и расширение ип
силатерального крыла охватывающей цистерны, удлинение ее контралатераль
ного крыла (рис. 5.10). Вклинение крючка височной доли вызывает механичес-
кую компрессию глазодвигательного нерва в углу кливуса, что проявляется про-
стым, но важным диагностическим признаком мидриаза на той же стороне.
В зависимости от локализации и объема очага выделяют несколько вариан-
тов височно тенториального смещения и деформации ствола мозга: переднее,
боковое, заднее. Далеко за-
шедшим случаем является
полулунное смещение, соче
Рис. 5.11. Схема
передне заднебокового
(«полулунного») смещения.
тающее все три перечисленных выше варианта (рис. 5.11). При поражении ви
сочно теменно затылочной области наблюдается уплощение и деформация хол-
миков четверохолмия с сужением четверохолмной цистерны и медиальным сме-
щением ее крыла на стороне поражения.
При двухсторонней задней локализации процесса развивается деформация
по типу «стремени» с симметричным медиальным смещением боковых крыльев
четверохолмной цистерны.
Нисходящее транстенториальное вклинение обычно развивается вследствие
острого или подострого супратенториального поражения, которое, если немед-
ленно не купировано, ведет к необратимым повреждениям ствола мозга с кро-
воизлиянием и ишемией в бассейне задней мозговой артерии с фатальным ис-
ходом.
При срединно расположенных процессах развивается центральное смеще-
ние, сопровождающееся компрессией III желудочка и водопровода мозга.
Развитие внутричерепной гипертензии с давлением, превосходящим таковое
во внутренних сонных артериях, ведет к остановке кровотока на уровне их си-
фонов, тогда как циркуляция по наружным сонным артериям сохранена. Эти
изменения носят билатеральный характер. Параллельно при МР венографии
регистрируется отсутствие потока крови в верхнем сагиттальном синусе. Кли
нико инструментально фиксируется смерть мозга.
Восходящее транстенториальное смещение развивается реже. Оно может быть
спонтанной или ятрогенной природы, вызванной, например, внезапным умень-
шением интракраниального давления при вентрикулярном шунтировании у боль-
ного с объемным процессом, расположенным инфратенториально. При этом
кульмен мозжечка смещается вверх, вызывая компрессию водопровода мозга и
тривентрикулярную окклюзионную гидроцефалию (рис. 5.12).
Значительное повышение интракраниального давления ведет к развитию
аксиального смещения, сопровождающегося развитием бульбарной симптома-
тики. При этом структуры, расположенные в задней черепной ямке, буквально
выдавливаются в большое затылочное отверстие. Их компрессия о костный край
отверстия бывает столь выражена, что формируется странгуляционная борозда
и развивается некроз.
Примером острых состояний с односторонней локализацией изменений, со-
провождающихся развитием комы, могут быть О НМ К, гематомалюбой этио-
логии, воспалительные изменения, например, абсцессы. Опухоли, даже быстро
растущие, не эволюционируют столь стремительно.
Говоря о коме, невозможно не упомянуть об отеке головного мозга --- состоя-
нии, развивающемся при самых разнообразных патологических процессах. В за-
висимости от патогенетического механизма принято выделять несколько видов
отека: вазогенный, цитотоксический, гидростатический, гипоосмотический,
интерстициальный (перивентрикулярный). Вазогенный тип отека обусловлен
увеличением проницаемости ГЭБ для плазмы, что влечет за собой повышение
содержания внеклеточной жидкости, преимущественно в белом веществе. Этот
вид отека типичен для черепно мозговой травмы. Максимальная выраженность
изменений приходится на первые сутки после травмы. Аноксически ишемические
В
Рис. 5.12. Восходящее
транстенториальное вклинение,
нисходящее вклинение мозжечка в большое
затылочное отверстие. МРТ.
а --- Т2 ВИ, сагиттальная плоскость;
б --- Т1 ВИ, корональная плоскость;
в --- Т1 ВИ, аксиальная плоскость.
Вклинение левой миндалины мозжеч-
ка в шейно затылочную воронку. Ком-
прессия большой цистерны мозга,
V! желудочка. Ствол мозга смещен кпе-
реди, понтомедуллярная цистерна сдав-
лена. Отмечается восходящее тран-
стенториальное вклинение мозжечка.
Четверохолмная цистерна сдавлена.
Левые холмики четверохолмия дефор-
мированы, смещены вправо и кверху.
повреждения головного мозга обычно приводят к цитотоксическому отеку, дос-
тигающему наибольшей выраженности на 5---10 е сутки от инициации процес-
са. Патогенез данных изменений связан со скоплением внутриклеточной жидко-
сти. Гидростатический отек мозга развивается у больных со значительной внут-
ричерепной ги! юртензией в случае резкого изменения давления, например, при
декомпрессионной трепанации черепа. При этом ГЭБ остается интактным. Сни
жение осмолярности плазмы, обусловленное чрезмерными ннфузиями или нару-
шением гипофизарно гипоталамической системы ведет к гипоосмотическому
отеку с выходом жидкости из внутрисосудистого пространства во внесосудистое.
Внутрижелудочковая гипертензия манифестирует, в частности, интерстициальным
отеком вследствие пропотивания жидкости непосредственно в белое вещество. По
данным КТ отек характеризуется снижением плотности мозга, больше выражен-
ном в белом веществе. При этом кортикомедуллярная граница становится менее
Рис. 5.13. ЧМТ. Вазогенный тип отека правой гемисферы большого мозга.
КТ, аксиальные срезы.
Состояние после костно пластической трепанации. Плотность белого вещества
правой гемисферы головного мозга понижена. Граница между серым и белым ве-
ществом четко не прослеживается. Борозды правого полушария мозга компреми
рованы. Вещество правой лобной и теменной долей мозга пролабирует в трепана
ционный костный дефект.
Рис. 5.14. Порфирия. Цитотоксический отек левого полушария большого мозга.
Аноксически ишемическое повреждение головного мозга,
обусловленное ангиоспазмом. МРТ.
а --- Т2 ВИ, сагиттальная плоскость; б --- FLAIR ИП, аксиальная плоскость;
в --- Т1 ВИ, корональная плоскость; г --- 3D TOF ИП, ангиография,
корональная плоскость.
В левой гемисфере определяется отек белого вещества мозга, характеризующийся
гиперинтенсивным сигналом на Т2 ВИ, FLAIR ИП, гипоинтенсивным на Т1 ВИ.
Извилины левой теменной области сглажены, прилежащее субарахноидальное
пространство компремировано. Отмечается сужение ветвей средних мозговых ар-
терий, позвоночных артерий, основной артерии.
отчетливой, что создает ощущение «монотонноеTM» изображения (рис. 5.13). При
МРТ наблюдается стандартное изменение интенсивности сигнала: гипоинтен
сивныйнаТ1 ВИ и гиперинтенсивный наТ2 ВИ (рис. 5.14).
Диффузное увеличение объема головного мозга приводит к тотальному огра-
ничению резервных пространств --- сужению субарахноидального пространства,
в том числе базальных цистерн, и сдавлению желудочковой системы.
КОМА И НЕЙРОНАЛЬНОЕ ПОВРЕЖДЕНИЕ
Нейроны крайне чувствительны к дефициту кислорода и глюкозы, недо-
статок которых приводит к коме либо аноксически ишемической, либо гипог
ликемической природы. На начальных этапах наблюдается нарушение фун-
кции нейрональных клеток. Эта стадия является обратимой. При пролонги-
рованном воздействии развивается структурное повреждение в виде отека и
некроза с последующей кистозно глиозной перестройкой на фоне атрофичес
ких изменений (рис. 5.15). Потеря нейронов коры головного мозга ведет к нео-
братимым изменениям. КТ и МРТ не позволяют оценить сохранность мета-
болизма и потенции коры головного мозга в подобных случаях. Ответ на этот
вопрос на сегодняшний день может дать только ПЭТ.
Наиболее информативным методом при обследовании таких больных следу-
ет признать МРТ, хотя КТ также позволяет выявить очаговые изменения и отек
мозга. Для тяжелой гипоксии характерным является поражение белого вещества
с формированием зон перивентрикуляр
нойлейкомаляции. В динамике наблю-
дается постепенное уменьшение объема
белого вещества с компенсаторным рас-
ширением боковых желудочков. Наибо-
лее уязвимыми оказываются теменно
затылочные регионы, в которых в острый
период определяются участки патологи-
ческой интенсивности, соответствую-
щие параметрам отека, а на более по
Рис. 5.15. Последствия
гипогликемической комы. МРТ.
FLAIR ИП, аксиальная плоскость.
Рис. 5.16. Больная Б., 28 лет. Эклампсия.
МРТ. Т2 ВИ, аксиальная плоскость.
В теменно затылочной области обеих ге
мисфер выявлены зоны патологической
интенсивности сигнала.
зднем этапе отмечается формирование
симметричных зон рубпово атрофичес
ких изменений. Аналогичная картина
наблюдается у женщин с эклампсией
(рис. 5.16). Клинически она проявляет-
ся двухсторонней слепотой. Изменения
обычно обратимы при своевременной
адекватной терапии.
Подобная лучевая картина формиру-
ется и в случаях гипогликемической
комы. Иногда такие изменения выявля-
ются у детей, матери которых во время беременности имели субклинический са-
харный диабет, компенсация которого обеспечивалась плодом. После родов они
попадают в реанимацию в связи с гипергликемией, тогда как у новорожденного
вследствие гипогликемии возникает повреждение теменно затылочных регио-
нов. Как правило, эти дети являются инвалидами детства по зрению, а пораже-
ние головного мозга ошибочно связывают не с перенесенной гипогликемией, а
с возможной родовой травмой.
Крайне сложно на ранних этапах предсказать исход аноксическо ишемичес
кой комы. Известно, что новорожденные, перенесшие тяжелую перинатальную
гипоксию, могут жить некоторое время, несмотря на значительное повреждение
мозга. Иногда у детей даже с острой децеребрацией после гипоксии отмечается
достаточно долгий латентный период, свободный от очевидного неврологического
дефицита. Как результат некротизации при аноксии ишемии формируется редкое
педиатрическое состояние --- статус морморатус, проявляющееся рассеянными
микрокальцинатами на уровне базальных ядер на фоне диффузной атрофии
вещества мозга.
При некоторых патологических состояниях, например при отеке головного
мозга любого генеза, процесс носит диффузный характер, отражая поврежде-
ние не только серого, но и белого вещества. Примерами таких заболеваний яв-
ляются воспалительные процессы (церебральная малярия, энцефалит, прионо
вая болезнь и т. д.), метаболические повреждения (интоксикации, почечная и пе-
ченочная недостаточность, энзимопатии, гепатоцеребральная дегенерация и
Рис. 5.17. Отравление угарным газом. МРТ.
а, б --- Т2 ВИ, аксиальная плоскость;
в --- FLAIR ИП, аксиальная плоскость;
г --- Т2 ВИ, аксиальная плоскость.
Симметричное поражение хвостатого ядра, скорлупы, бледного шара (а), белого
вещества (б), коры головного мозга, с преимущественным поражением лобных до-
лей (в). Отек головного мозга ведет к ограничению резервных пространств со сдав-
лен ием желудочков мозга и субарахноидального пространства конвекса. Послед-
ствие отравлением угарным газом с формированием симметричных кистозных из-
менений в базальных ядрах (г).
т. д.). Крайне показательно как в остром, так и в отдаленном периоде тяжелое
отравление угарным газом, проявляющееся билатеральным некрозом лентику
лярныхядер, особенно бледных шаров (рис. 5.17). Аноксическо ишемическая
энцефалопатия может быть вызвана кардиогенным шоком.
КОМА И АКСОНАЛЬНОЕ ПОВРЕЖДЕНИЕ
Тяжелая ЧМТ почти в 50% случаев сопровождается диффузным аксональ
ным повреждением. Именно это состояние в остром периоде обусловливает 35%
случаев летального исхода, а в отдаленном периоде является наиболее частой
Рис. 5.18. ЧМТ. Диффузное аксональное
повреждение. МРТ.
а --- FLAIR ИП, аксиальная
плоскость;
б --- Т1 ВИ, корональная плоскость;
в --- Т2 ВИ, сагиттальная плоскость.
Мозолистое тело характеризуется из-
мененной интенсивностью сигнала,
неоднородной структурой, неровны-
ми краями, увеличено в объеме.
а
б
Рис. 5.19. Последствия повреждения мозолистого тела. МРТ.
а --- Т1 ВИ, сагиттальная плоскость; б --- FLAIR ИП, аксиальная плоскость.
Атрофия мозолистого тела, обусловленная посттравматическими кистозно глиоз
ными изменениями. Выраженная посттравматическая энцефалопатия. Двухсторон-
ние хронические субдуральные гематомы.
причиной формирования вегетативного статуса и тяжелой инвалидности. При
морфологическом исследовании в случае диффузного аксонального поврежде-
ния выявляют отечные и утолщенные аксоны с разрывами между телами и отро-
стками нейронов ствола мозга, мозолистого тела, базальных ганглиев, в облас-
ти стыка между серым и белым веществом (рис. 5.18,5.19).
Изменение субкортикальных отделов белого вещества и мозолистого тела
является крайне показательным и объясняется механизмом травмы. Изолиро-
ванное поражение ствола мозга встречается достаточно редко и, скорее все-
го, обусловлено последствиями транстенториального вклинения. При КТ и МРТ
определяются участки патологической плотности или интенсивности сигна-
ла, обусловленные отеком и геморрагиями. В тех случаях, когда преобладает
отек аксонов, КТ картина может быть обычной. МРТ позволяет оценить ха-
рактер травмы в большем объеме, но гораздо меньшем, чем истинная распро-
страненность процесса. При геморрагиях изменения отчетливо дифференци-
руются и при КТ , и при МРТ исследованиях. Иногда первоначально неге-
моррагическое диффузное аксональное повреждение через несколько суток
трансформируется в геморрагическое, что сопровождается появлением типе
Рис. 5.20. ЧМТ. Диффузное аксональное
повреждение. МРТ.
FLAIR ИП, аксиальная плоскость.
В субкортикальных отделах обеих геми
сфер большого мозга выявляются мелкие
очаги аксонального поражения.
ринтенсивных сигналов на Т1 ВИ. Нередко развивающаяся травматизация
субэпендимальных капилляров и венул влечет за собой формирование внут
рижелудочковых кровоизлияний. Диффузное аксональное повреждение час-
то сочетается с ушибами головного мозга, субарахноидальными, субдураль
ными и эпидуральными гематомами (рис. 5.20). Его исходом может быть вто-
ричная валлерианова дегенерация, развивающаяся спустя месяцы и годы
(рис. 5.21).
а
б
Рис. 5.21. Последствие ЧМТ. Вторичная Валлерианова дегенерация МРТ.
а --- Т1 ВИ, корональная плоскость; б --- Т2 ВИ, аксиальная плоскость.
Нейродегенеративные изменения по ходу кортико спинальных трактов.
КОМА И СИНАПТИЧЕСКАЯ НЕДОСТАТОЧНОСТЬ
Короткий период бессознательного состояния с ретроградной амнезией дос-
таточно типичен для церебральной коммоции и обусловлен синаптической не-
достаточностью, как правило, исчезающей со временем. Вместе с тем повтор-
ные ушибы мозга могут привести к утрате этой способности, что реализуется
в особой форме деменции, наиболее часто встречающейся у боксеров. М РТ и
КТ проявления при этом неспецифичны, отражая фокальные и диффузные трав-
матические изменения.
Вегетативный статус
Неблагоприятным исходом комы любого генеза может быть формирование
вегетативного статуса --- тяжелого нарушения сознания, развивающегося в ре-
зультате повреждения ЦНС и ведущего к тотальной потере способности боль
Рис. 5.22. Вегетативный статус. МРТ.
Т2 ВИ, аксиальная плоскость.
Диффузное поражение коры головного
мозга, субкортикальных отделов белого
вещества. Симметричные изменения
влентикулярных ядрах.
ного к интерактивным действиям. Если
кома продолжается более 4 недель, то си-
туацию оценивают как персистирую
щий вегетативный статус. Наиболее ча-
стыми причинами развития такого ос-
ложнения являются травма, инсульт,
постаноксическая энцефалопатия, опу-
холь, энцефалит. При МРТ визуализи-
руется моногоочаговое поражение го-
ловного мозга на фоне выраженной
диффузной атрофии, особенно ствола
(рис. 5.22). При этом мост мозга резко
уплощается, теряя свою обычную кон-
фигурацию. Обязательным атрибутом является смешанная гидроцефалия за-
местительного характера. Несомненный след оставляет и патологический
процесс, сыгравший фатальную роль в жизни больного.
Список основной литературы
1. Блинков СМ., Смирнов H.A. Смещения и деформации головного мозга.---
Л.: Медицина, 1967. 201 с.
2. Кузъменко В.А., Лихтерман Л.Б., Корниенко В.Н., Потапов A.A. Компьютер-
ная томография в диагностике дислокационных синдромов при черепно моз-
говой травме // Вопросы нейрохирургии.--- 1988, No 3. --- С. 11 15.
3. Потапов A.A., Лихтерман Л.Б., Зельман В.Л., Корниенко В.Н., Кравчук А.Д.
Доказательная нейротравматология.--- М.:, 2003.--- С. 408---464.
4. Уолнер А.Э. Смерть мозга.--- М.: Медицина, 1998.--- 157 с.
5. Bauer R. et al. Ontogenetic aspects of traumatic brain edema --- facts and
suggestions // Exp. Toxicol. Pathol. 1999, 51.--- P. 143 50.
6. Beltramello A., Piovan E., Pizzini F. Neuroradiological evaluation of coma //
Rivista di neuroradiologia.--- 2000, Vol. 13, Suppl. 2.--- P. 45 76.
7. Conti F. The problems of coma: a neurophysiological perspective // Rivista di
neuroradiologia. 2000, Vol. 13, Suppl. 2. P. 31 35.
8. Di Summa A., Beltramello A., Fratucello G.B., Bongiovanni L.G., Zanette G.,
Polo A. Cerebral fat embolism: debated acute posttraumatic encephalopathy // Eur.
Neurol. 1998, 40. P. 55 56.
9. Edelman R.R., Hesselink J.R. Clinical magnetic resonance imaging.---
Philadelphia: W.B. Saunders company, 1990.--- P. 483-598.
10. Firsching R., Woischneck D., Klein S. et al. Classification of severe head injury
based on magnetic resonsnce imaging // Acta Neurochir.--- Wien, 2001, 143.--- P. 263---
271.11. Gentleman S. et al. Axonal injury: a universal consequence of fatal closed head
injury // Acta Neurophatal.- 1995, 89.- P. 537-543.
12. Gentry L. Imaging of closed head injury // Radiol.--- 1994, 191.--- P. 1 --- 17.
13. Gentiy L.R., Godersky J.C., Thompson B. MR imaging of head trauma: review
of the distribution and radiopathologic features of traumattic lesions // Am. J. Roent-
genol.- 1988, 150/3.- P. 663-672.
14. Goodwin L. Use of MRI in prediction of recovery from persistent vegetative state //
J. Insur. Med.- 1998, 30/2.- P. 113-114.
15. Gotoh M., Kuyama H., Asari S., Ohmoto T, Akoka T, Lai M.Y. Sequential
changes in MR images of the brain in acute carbon monoxide poisoning //
Computerized Medical Imaging and Graphics.--- 1993, 17, 1.--- P. 55---59.
16. Jones KM., Barnes P.D. MR diagnosis of brain death // A.J.N.R.- 1992, 13.-
P. 65-66.
17. Kampfl A., Schmutzhard E., Franz G, Pfausler B., Flaring H.P., Ulmer H., Fel-
ber S., Golaszewski S., Aichner F. Prediction of recovery from post-traumatic vegetative
state with cerebral magnetic-resonance imaging // Lancet.--- 1998. 351.--- P. 1763---
1767.
18. Manfredi M., Beltramello A., Bongiovanni L.G., Polo A., Pistoia L., Rizzuto N.
Eclamptic encephalopathy: imaging and pathogenetic considerations // Acta Neurol.
Scand.- 1997, 96.- P. 277-282.
19. Orrison W.W. Neuroimaging.--- Philadelphia: WB Sounders Company, 2000,
Ch. 26.- P. 884-915.
20. Salvolini U. Considerations on neuroradiological evaluation of coma // Rivista
di ncuroradiologia.--- 2000, Vol. 13, Suppl. 2.--- P. 77-80.
21. Stark D.D., Bradley W.G Magnetic resonance imaging.--- St. Louis: Mosby-
Year Book, 1992, Vol. I, Ch. II.- P. 557-963.
22. Vallasciani M., Gironelli L., Tulli D., Chiaramoni L., Salvolini U. Neuro-
radiological investigations in patients with persistent vegetative state // Rivista di neuro-
radiologia.- 2000, Vol. 13, Suppl. 2.- P. 81-85.
23. Walter GF. Neuropathology of impaired consciousness // Rivista di neuro-
radiologia.- 2000, Vol. 13, Suppl. 2.- P. 37-43.
Глава 6
ЧЕРЕПНО МОЗГОВАЯ ТРАВМА
Нет такой отрасли медицинских знаний, которая не сде-
лала бы полезного для себя применения из новооткрытых
лучей...
Е. С.Лондон
Возможности лучевой диагностики черепно мозговой травмы (ЧМТ) реши-
тельно изменились после внедрения в клиническую практику рентгеновской
компьютерной, а затем и магнитно резонансной томографии. Появление КГ
повлияло на клиническую диагностику и ведение пациентов с ЧМТ. Самое тща-
тельное неврологическое обследование уступало компьютерной томографии
в точности оценки типа и локализации внутричерепных повреждений. Неин
вазивное получение КТ изображений значительно превосходило по диагнос-
тическим возможностям церебральную ангиографию. Одновременное выяв-
ление на аксиальных КТ срезах переломов костей черепа, оболочечных и внут
римозговых гематом, возможность отличить кровоизлияния от отека мозга
сделали компьютерную томографию методом выбора в диагностике острой
ЧМТ.
При равных диагностических возможностях КТ и МРТ в распознавании
кровоизлияний магнитно резонансная томография более чувствительна в вы-
явлении диффузных аксональных поражений, негеморрагических ушибов моз-
га и части субдуральных гематом. МРТ предъявляет более жесткие требования
к применению седативных средств, занимает больше времени, чем КТ, не выяв-
ляет переломы черепа и сверхострые кровоизлияния, но превосходит компью-
терную томографию в распознавании вторичных посттравматических ишемий
мозга. Поэтому МРТ стала методом выбора при изучении подострого периода и
отдаленных последствий ЧМТ.
ПЕРЕЛОМЫ КОСТЕЙ ЧЕРЕПА
Выявление переломов на обзорных краниограммах указывает на то, что к го-
лове пострадавшего была приложена значительная травмирующая сила, одна-
ко отсутствие перелома (или его изображения) не исключает повреждения го-
ловного мозга. Применение КТ с одновременной оценкой костных и внутриче-
репных изменений превосходит диагностические возможности краниографии,
позволяя быстрее и точнее оценить возникшие повреждения и определить так-
тику лечения пациента. Для оценки переломов костей черепа при КТ необходи-
мо использовать широкое (так называемое костное) окно. Переломы основания
черепа лучше выявляются на тонких срезах: 1---3 мм для переломов пирамид ви-
сочных костей, до 5 мм --- для переломов задней черепной ямки.
Линейные переломы
Линейные переломы могут быть выявлены при КТ только тогда, когда их
направление перпендикулярно плоскости сканирования (рис. 6.1); если пере-
лом идет параллельно плоскости среза, то он становится невидимым. Эти осо-
бенности справедливы для переломов свода черепа, в том числе и для выявления
травматического расхождения швов (рис. 6.2).
Переломы основания черепа, как правило, совпадают с плоскостью среза,
но их плоскость расположена перпендикулярно поверхности кости, что создает
оптимальные условия для выявления этих повреждений. Косвенными призна-
ками перелома могут быть:
1) уровень жидкости (крови) в околоносовых пазухах, в том числе в воздухо-
носных сосцевидных клетках височных костей;
2) эпидуральные гематомы, включая самые малые;
3) утолщение экстракраниальных мягких тканей за счет подапоневротичес
кого кровоизлияния.
а
б
Рис. 6.1. Линейный перелом левой половины чешуи затылочной кости.
а --- задняя полуаксиальная краниограмма: направление линии перелома перпен-
дикулярно направлению плоскости сканирования при компьютерной томографии;
б --- аксиальные компьютерные томограммы: линейный перелом отчетливо диф-
ференцируется.
Рис. 6.2. Прямая задняя кранио
грамма.
Представленный перелом правой
теменной кости не выявляется при
КТ, поскольку направление линии
перелома образует с плоскостью
аксиальной компьютерной томо-
граммы угол 45°.
Вдавленные переломы
В отличие от линейных, вдавленные переломы одинаково успешно распоз-
наются как на обзорных краниограммах, так и на компьютерных томограммах
(рис. 6.3). При выявлении вдавленного перелома необходимо оценить размеры
отломка и глубину его интракраниального внедрения, повреждение твердой моз-
говой оболочки, ушибы подлежащего мозга и внемозговые гематомы. На выбор
хирургического или консервативного способа лечения влияет и локализация
вдавленного перелома, особенно его соседство с венозными синусами, которые
могут стать источником серьезного кровотечения при неосторожном удалении
костного фрагмента.
Фронтобазальные переломы
Эти повреждения диагностируются при выявлении перелома чешуи лобной
кости (линейного или вдавленного), продолженного на дно передней черепной
ямки. Поскольку при таких переломах, как правило, повреждаются околоносо-
вые пазухи (лобная или решетчатая) и верхняя стенка полости носа (ситовидная
пластинка), фронтобазальные переломы относятся к открытым повреждениям,
сообщающимся с внешней средой, с высоким риском инфицирования. Одно-
временное повреждение оболочек мозга приводит к назальной ликворее, что уве-
личивает опасность проникновения инфекции в полость черепа.
Если пострадавший после травмы утратил зрение на один глаз (травматичес-
кая слепота), то следует обратить самое пристальное внимание на состояние
стенок зрительного канала для проведения экстренной хирургической декомп
ресии зрительного нерва.
ВНУТРИЧЕРЕПНЫЕ КРОВОИЗЛИЯНИЯ
Эпидуральная гематома
Эпидуральная гематома всегда прилежит к кости и, как правило, имеет фор-
му двояковыпуклой линзы. Значительно реже наблюдается локальное втяжение
внутреннего контура или неправильная форма эпидуральной гематомы, что за-
висит от характера отслоенной твердой мозговой оболочки.
Источником кровотечения в эпидуральную гематому становятся поврежден-
ные ветви оболочечныхартерий, диплоические вены или венозные синусы. Эти
нарушения возникают преимущественно при переломах костей черепа, что по-
буждает к активному поиску перелома при обнаружении эпидуральной гемато-
мы. Поскольку источником крови в эпидуральной гематоме наиболее часто яв-
ляется средняя оболочечная артерия, неудивительно, что эпидуральная гемато-
ма в большинстве случаев располагается вдоль чешуи височной кости (рис. 6.4),
т. е. совпадает с местом ветвления артерии, значительно реже встречаются те-
менные, лобные и затылочные гематомы. Задняя черепная ямка относится к ред-
ким локализациям эпидуральной гематомы, однако из за возникающего при
этом повреждения ствола мозга клиническое значение ее чрезвычайно велико,
поэтому оценивать содержимое задней черепной ямки и состояние ее костных
стенок нужно особенно внимательно (рис. 6.5). Из за обилия костных артефак-
тов при КТ никогда не следует пренебрегать выполнением тонких срезов этой
зоны, а при неуверенности в трактовке выявленных нарушений полезно изме-
нить направление сканирования либо выполнить М РТ.
Рис. 6.4. Эпидуральные гематомы. КТ.
а --- правосторонняя конвекситальная
височная эпидуральная гематома: на ме-
диальной поверхности гематомы --- фраг-
мент внутренней кортикальной плас-
тинки, смещенный вместе с отслоенной
твердой мозговой оболочкой (стрелка);
б --- левосторонняя конвекситальная за
тылочно теменная эпидуральная гема-
тома;
в --- правосторонняя базальная височная
эпидуральная гематома.
Рис. 6.5. Эпидуральная гематома суб
и супратенториальной локализации.
а --- КТ через верхний отдел задней че-
репной ямки, субтенториальная часть
эпидуральной гематомы;
б, в --- КТ на уровне боковых желудоч-
ков, супратенториальная часть эпиду-
ральной гематомы, отслаивающей левую
половину поперечного и смежный уча-
сток верхнего сагиттального синуса.
Двояковыпуклая линза эпидуральной гематомы обусловлена тем, что наруж-
ный ее контур совпадает с всегда выпуклой внутренней костной пластинкой, а
внутренним контуром гематомы служит отслоенная от кости и погруженная
интракраниально твердая мозговая оболочка. Следовательно, оба контура эпи-
дуральной гематомы будут четкими. Угол между внутренним и наружным кон-
турами приближается к прямому, хотя и остается чуть меньше 90°. Диаметр ге-
матомы превышает ее толщину в 3---5 раз. Структура гематомы на КТ срезах
зависит от ее давности. Острые эпидуральные гематомы имеют однородную ги
перденсивную структуру с показателями плотности 60---70 ел. X. Через 7---10 дней
в гематоме образуется сгусток крови, вокруг которого остается гиподенсивная
сыворотка крови, лишенная железосодержащих эритроцитов.
Хронические эпидуральные гематомы, в отличие отсубдуральных, встреча-
ются очень редко. Это связано с тем, что эпидуральные гематомы накапливают-
ся быстро (артериальное кровотечение), из за трудного отслоения твердой моз-
говой оболочки имеют значительную толщину, т. е. грубо и внезапно деформи-
руют подлежащую мозговую кору, что не может не сопровождаться яркими
очаговыми клиническими симптомами, которые побуждают клинициста к ак-
тивным поискам причины тяжелого состояния пациента. Тем не менее, если ис-
точником кровотечения становится поврежденная вена или венозный синус,
гематома из за низкого венозного давления накапливается медленно, не дости-
гает большого объема и потому не вызывает значительных изменений подлежа-
щего участка мозга. Такие «венозные» эпидуральные гематомы могут быть вы-
явлены в более поздние сроки, когда их гиперденсивная структура меняется на
изо или гиподенсивную за счет разрушения эритроцитов и частичного всасы
вания продуктов их распада.
Маленькие эпидуральные гематомы диаметром меньше 2 см рассасываются
самостоятельно. У детей, вследствие зияния плоскости перелома, эпидуральная
гематома даже больших размеров может дренироваться через зону перелома
в экстракраниальные мягкие ткани, откуда ее при необходимости удаляют по-
средством пункции.
Субдуральная гематома
Субдуральная гематома возникает при разрыве переходных вен, впадающих
в венозные синусы. Более редкими источниками субдуральной гематомы явля-
ются поврежденные корковые артерии или поверхностные контузионные очаги.
В отличие отэпидуральной гематомы, которая всегда локальна, субдураль-
ная гематома простирается весьма далеко, иногда окружая все полушарие го-
ловного мозга. Это связано с тем, что кровь может свободно растекаться в по-
тенциальном субдуральном пространстве, не испытывая сопротивления. Поэто-
му субдуральная гематома может располагаться не только вдоль костей черепа,
но и вдоль серпа мозга или намета мозжечка.
В большинстве наблюдений острая субдуральная гематома имеет выпуклую
наружную и втянутую внутреннюю границы, т. е. ее форма напоминает серп с ост-
рыми углами по краям (рис. 6.6). Наружный контур гематомы ровный и четкий,
а внутренний почти всегда неровный, так как повторяет форму коры головного
мозга, и может быть нечетким. Вследствие гиперденсивной однородной структуры
субдуральная гематома может сливаться с изображением костей при изучении
обычного для головного мозга окна. В этом случае необъяснимый масс эффект
должен заставить врача изменить окно (расширить его или увеличить значение
его центра), чтобы различить кость и примыкающую к ней гематому.
К концу первой недели после травмы гематома становится неоднородной из
за появления в ней сгустков крови на фоне лишенной эритроцитов сыворотки
а
б
Рис. 6.6. Субдуральные гематомы. КТ.
а --- правосторонняя субдуральная гематома типичной локализации;
б --- правосторонняя базальная субдуральная гематома, распространившаяся вдоль
правой половины мозжечкового намета.
крови или спинномозговой жидкости. Если гематома остается в полости черепа
2---4 недели, то форменные элементы крови разрушаются и удаляются, что сни-
жает ее рентгеновскую плотность, однако объем гематомы при этом не только не
уменьшается, но часто увеличивается. Это происходит из за того, что белки кро-
ви, скопившейся в субдуральном пространстве, образуют капсулу гематомы, ко-
торая имеет свойства полупроницаемой мембраны. Поскольку онкотическое и
осмотическое давление крови выше этих показателей в тканевой жидкости, пос-
ледняя медленно просачивается в полость гематомы, увеличивая ее объем до
момента выравнивания осмотических давлений содержимого гематомы и тка-
невой жидкости.
Вследствие описанных процессов в течение первых недель после травмы суб-
дуральная гематома становится изоденсивной по отношению к мозговой ткани,
а ее внутренний контур может из втянутого превратиться в плоский. Выявить
изоденсивную подострую субдуральную гематому можно втом случае, если уда-
стся увидеть отодвинутую от внутренней костной пластинки кору головного моз-
га (рис. 6.7). Выполнение этой задачи облегчается применением тонких срезов
А
а
Рис. 6.7. Подострая левосторонняя субдуральная гематома, изоденсивная коре
головного мозга. КТ.
а --- латеральная дислокация прозрачной перегородки;
б --- кора левой лобной доли отодвинута от костей черепа субдуральной гематомой.
или внутривенного контрастирования, при котором ставшие более яркими кор-
ковые сосуды подчеркнут поверхность головного мозга. Следует иметь в виду,
что даже острая субдуральная гематома может быть изоденсивной головному
мозгу, если у пострадавшего имелась выраженная анемия.
Хроническая субдуральная гематома может существовать бессимптомно
в течение многих месяцев, а иногда и лет. В этих случаях поводом для обра-
щения к врачу может стать повторная даже незначительная травма или иная
причина декомпенсации. При КТ выявляется гиподенсивное линзовидное
скопление жидкости, формой напоминающее эпидуральную гематому (рис. 6.8).
На постконтрастных, а иногда и на нативных срезах видна капсула, отделя-
ющая жидкость от поверхности мозга. Если хроническая субдуральная гема-
тома существует с детства, то кость над ней истончена и выбухает. Степень сдав
ления подлежащих субарахноидальных щелей и бокового желудочка, смещения
срединных структур и транстенториального вклинения невелики, либо они вовсе
отсутствуют из за адекватного увеличения размеров соответствующего отдела
черепа и атрофии мозга.
Дифференциальная диагностика эпи и субдуральных гематом представ-
лен в табл. 6.1.
Рис. 6.8. Хроническая левосторонняя
субдуральная гематома, возникшая
в детстве. КТ.
Истончение левой половины чешуи лоб-
ной кости. Капсула хронической гематомы
(стрелка). Вследствие атрофии левой лоб-
ной доли срединные структуры смещены
влево.
Сочетание на одной стороне эпи и суб
дуральной гематомы приводит к комбина-
ции их признаков. При этом очаговые
признаки соответствуют эпидуральной ге-
матоме, а степень дислокации срединных
структур и транстенториального вклине-
ния --- субдуральной.
Нередко субдуральная гематома при-
обретает в остром периоде линзовидную
форму, что создает ложное впечатление
эпидурального объема. Это может быть обусловлено атрофическими изменени-
ями головного мозга, особенно на уровне латеральной борозды (сильвиевой щели),
когда субдуральная кровь занимает место атрофированных отделов.
Некоторые диагностические трудности возникают при двусторонних подострых,
т. е. изоденсивных субдуральных гематомах. В этом случае отсутствует и очаго-
вая семиотика, и главный «общемозговой» признак --- смещение срединных струк-
тур. У таких пациентов побудительной причиной для активного поиска оттеснен-
ной от кости коры головного мозга должны стать узкие желудочки со сближен-
ными лобными рогами, резко сдавленные субарахноидальные пространства и
транстенториальное вклинение. Внутривенное контрастирование и применение
тонких срезов делают диагностическое заключение более достоверным.
Растекание субдуральной крови вдоль намета мозжечка заставляет диффе-
ренцировать суб и супратенториальные субдуральные гематомы. При проведе-
нии дифференциальной диагностики следует оценить на аксиальных срезах
наружный и внутренний контуры гематомы и деформацию бокового желудоч-
ка: при супратенториальной гематоме четким будет ее медиальный контур, за-
тылочный рог и треугольник бокового желудочка на стороне гематомы будут
сдавлены и смещены вперед и вверх по сравнению с симметричной стороной;
субтенториальная субдуральная гематома, напротив, будет иметь четкий наруж-
ный контур, деформация бокового желудочка отсутствует, но появляется моз
жечково тенториальное вклинение (рис. 6.9). При необходимости следует изме-
нить направление сканирования либо выполнить М РТ.
Субдуральная гематома межполушарной щели располагается преимуще-
ственно вдоль задней половины серпа, что отличает ее от субарахноидального
Таблица 6.1
Дифференциально диагностические критерии эпидуральных
и субдуральных гематом
Признак
Эпидуральная гематома
Субдуральная гематома
Форма
Двояковыпуклая линза
Серповидная
Угол между
Большой, близок к 90°
Малый, очень острый
внутренним и
наружным контуром
Соотношение
5:1
10:1
диаметра и толщины
Внутренний контур
Четкий, ровный
Неровный, иногда
нечеткий
Структура в остром
Может содержать на
Ничего плотнее крови не
периоде
фоне жидкой крови
более плотный сгусток,
содержит, сгустки
формируются во всей
тромбирующий
толще гематомы
поврежденную артерию
Локализация
Только вдоль кости
Часто распространяется
на межполушарную щель
или намет мозжечка
Смещение срединных Меньше толщины
Больше толщины
структур
гематомы
гематомы
Вклинения
Возникают редко, только
при больших гематомах
Постоянны
Отслаивание попереч- Имеется при
Не бывает
ного или верхнего
соответствующей
сагиттального синуса
локализации
Ушибы головного
Отсутствуют или
Возникают часто,
мозга
формируются в
противоположном
полушарии
в том же полушарии
Переломы костей
Очень часты над
Могут быть выявлены
черепа
гематомой
над противоположным
полушарием
кровоизлияния по медиальной поверхности полушария, которое преобладает
в передних отделах межполушарной щели.
Помимо крови, в субдуральном пространстве может скапливаться спинно-
мозговая жидкость, которая попадает туда при надрыве паутинной оболочки.
Истечение спинномозговой жидкости в субдуральное пространство прекраща-
ется, как только давление в субдуральной гигроме уравняется с давлением спин-
номозговой жидкости. Обычно гигромы формируются на фоне спадения, кол-
лапса мозга и внутричерепной гипотензии. Субдуральные гигромы не вызыва-
ют сдавления мозга и не сопровождаются иными признаками масс эффекта.
Рис. 6.9. Острая субтенториальная
субдуральная гематома. Правостороннее
мозжечково тенториальное вклинение.
КТ.
а, б --- субдуральная кровь прилежит к че-
шуе затылочной кости и задней поверхно-
сти пирамиды височной кости;
в --- субдуральная кровь под наметом моз-
жечка.
б
Как правило, субдуральные гигромы не подлежат хирургическому удалению и
исчезают при расправлении головного мозга и повышении внутричерепного
давления до нормального уровня. Для дифференцирования субдуральной гиг-
ромы и атрофии мозга следует найти на фоне изображения спинномозговой
жидкости кортикальные вены: при гигроме они прижаты к коре головного моз-
га, а при атрофии пересекают толщу спинномозговой жидкости.
Хорошо изучена МРТ семиотикасубдуральных гематом. Морфологические
признаки совпадают с данными рентгеновской компьютерной томографии, а
интенсивность сигнала зависит от «возраста» гематомы. В остром периоде (до
2---3 дней после травмы) субдуральная гематома изоинтенсивна или слегка ги
поинтенсивна по сравнению с корой мозга наТ1 ВИ иоченьгипоинтенсивна
наТ2 ВИ. В раннем подостром периоде (4---14дней) появляется гиперинтенсив-
ная кайма, окружающая гипоинтенсивный центр как на Т1 , так и на Т2 ВИ.
Поздние подострые гематомы (от 15 дня до месяца) становятся гиперинтенсив-
ными на ТТ и Т2 ВИ. Хронические субдуральные гематомы (существующие
дольше 1 месяца) остаются гиперинтенсивными наТ2 ВИ, но вновь становятся
гипоинтенсивными наТ1 ВИ.
УШИБЫ ГОЛОВНОГО МОЗГА
Несмотря на высокий удельный вес переломов костей черепа и оболочеч
ных гематом, чаще всего при черепно мозговой травме формируются ушибы
или контузионные очаги в веществе мозга. В зоне ушиба наблюдаются раз
а
б
Рис. 6.10. Зависимость локализации ушибов мозга по механизму противоудара
от места перелома. КТ.
а --- ушиб полюса правой лобной доли при срединно левостороннем переломе че-
шуи затылочной кости;
б --- ушибы конвекситальных отделов правых лобной и височной долей при лате-
ральном левостороннем переломе чешуи затылочной кости.
Стрелками показаны места переломов.
Рис. 6.11. Ушиб левой височной доли. Левостороннее височно тенториальное
вклинение.
мозжение (некроз) мозговой ткани, кровоизлияние и отек. Эти повреждения
могут развиваться как в месте приложения травмирующей силы, так и на от-
далении от него. В зависимости от локализации различают ушибы мозга,
сформированные по механизму «удара» и по механизму «противоудара».
Патогенез ушиба в месте удара очевиден: кость, внедряющаяся интракрани
ально под действием внешней силы, деформирует подлежащий мозг и вызы-
вает его повреждение.
Формирование ушиба по механизму «противоудара» возникает в том слу-
чае, когда мозг с его ликворсодержащими полостями как единая гидродина-
мическая система продолжает движение внутри черепа в направлении прило-
женной травмирующей силы и сталкивается с неподвижными костями или
мембранами твердой мозговой оболочки в противоположной по отношению
к месту удара стороне. Такое столкновение мозга и кости вызывает повреж-
дение мозговой ткани, т. е. ушиб (рис. 6.10). При ударе по затылочной, темен-
ной, височной или заднелобной областям ушибы формируются либо только по
противоудару, либо в месте удара размеры контузионного очага и степень раз
мозжения головного мозга уступают величине ушибу в месте противоудара.
Если же удар был нанесен по центральной лобной области, ушибы, как пра-
вило, формируются только в месте удара. Эти закономерности легко объясняют
тот факт, что более половины всех контузионных очагов расположено в лоб-
ных долях мозга.
Рис. 6.12. Внутримозговая гематома заднего отдела правой лобной доли,
прослеженная в течение месяца. КТ.
а --- первые сутки после травмы, гематома имеет четкие контуры и окружена узкой
зоной отека;
б --- четвертые сутки после травмы, появилась перифокальная ишемия мозга и его
пролапс в трепанационный дефект;
в --- три недели спустя: гематома рассасывается, но пролапс сохраняется вследствие
сохранения ишемического отека;
г --- через месяц после ЧМТ: обратное развитие ишемических нарушений.
КТ семиотика ушиба головного мозга включает в себя зону гетерогенной
плотности, состоящую из гиподенсивного фона (размозжение) с яркими гипер
денсивными участками (кровоизлияниями) (рис. 6.11). В зависимости от вели-
чины кровоизлияний различают ушибы четырех типов:
1 --- субпиальное кровоизлияние;
2 --- мелкие (диаметром до 1 см) очажки кровоизлияний;
3 --- более крупные скопления крови (диаметром 1,5---2,5 см);
4 --- весь контузионный очаг представлен внутримозговой гематомой.
Контуры контузионных очагов нечеткие, локализация --- обязательно на по-
верхности мозга, примыкающей к внутренней костной пластинке либо к мемб-
ранам твердой мозговой оболочки (серпу или намету мозжечка). Ушиб мозга
вызывает объемное воздействие (масс эффект) в виде сдавления смежных су
барахноидальных щелей, деформации и сдавления ближайшего желудочка моз-
га, смещение срединных структур, транстенториальные вклинения и внедрение
миндалин мозжечка в шейно затылочную дуральную воронку. Крупные ушибы
передних отделов лобных долей могут вызвать аксиальное вклинение.
Эволюция ушибов мозга включает в себя рассасывание кровоизлияний и
размозженных тканей. На их месте формируется мозговой рубец, в котором мо-
гут находиться кисты. На компьютерных томограммах рубцово атрофические
Рис. 6.13. Вторичная посттравматическая ишемия головного мозга. КТ.
1 --- перифокальная ишемия вокруг очага ушиба левой лобной доли; 2 --- ишемия
смежных отделов височной доли в пределах бассейна левой средней мозговой арте-
рии; 3 --- дистантная ишемия в бассейне правой задней мозговой артерии.
изменения мозга соответствуют участкам значительного снижения плотности
(вследствие липидной дегенерации). Объем этих участков всегда меньше объе-
ма нормального мозга, поэтому соседние ликворсодержащие структуры расши-
ряются и подтягиваются к рубцу.
Вместе с тем при выполнении повторных КГ головного мозга в остром пери-
оде ЧМТ было выявлено, что рассасывание кровоизлияний и формирование
рубца --- не единственный вариант эволюции ушибов мозга. Нередко механи-
ческое повреждение мозговой ткани и ее сосудов сочетается с нарушением то-
нуса сосудистой стенки, что приводит либо к повторным кровоизлияниям, либо
Рис. 6.14. Развитие ишемических
нарушений при черепно мозговой
травме. КТ.
а --- острая левосторонняя субдураль
ная гематома;
б --- после удаления гематомы разви-
лись ишемические нарушения в зад-
нем отделе бассейна левой средней
мозговой артерии;
в --- рубцово атрофические изменения
на месте вторичной посттравматичес-
кой ишемии и у переднего края трепа
национного дефекта.
к вазоспазму. КТ семиотика повторных кровоизлияний очевидна: либо появ-
ление новых гиперденсивных зон в веществе мозга, либо увеличение размеров
ранее выявленных. Вазоспазм приводит к ишемии мозга, что проявляется гипо
денсивной зоной конической формы с четкими контурами. Отек, возникающий
в зоне ишемии, усиливает масс эффект (рис. 6.12).
Зоны вторичной посттравматической ишемии чаще всего расположены вок-
руг первичного контузионного очага и являются перифокальными, но могут
располагаться эксцентрично в смежных отделах мозга, или на значительном
отдалении от первичного очага ушиба (рис. 6.13). Зоны вторичной ишемии моз-
га сопровождают не только контузионные повреждения, но и оболочечные ге-
матомы (рис. 6.14). В дальнейшем небольшие ишемические повреждения ис-
чезают бесследно, а более крупные закономерно сменяются рубцово атрофи
ческим процессом. Преморбидные аномалии сосудов головного мозга
оказываются главным фактором риска развития вторичных посттравматичес-
ких ишемических нарушений, что и объясняет их высокую частоту у пациентов
молодого возраста.
Вторичная посттравматическая ишемия мозга становится серьезным ослож-
нением черепно мозговой травмы, приводит к быстрому появлению и нараста-
нию вклинений и существенно увеличивает летальность. Распознавание вторич-
ной ишемии с помощью бесконтрастной компьютерной томографии возможно
лишь на вторые сутки после ее возникновения, когда появляется отчетливая
конической формы зона цитотоксического отека. Возможности медикаментоз-
ной коррекции вазоспазма в это время уже ограничены. Надежды на раннее его
выявление путем транскраниальной допплерографии не оправдались, посколь
а
б
Рис. 6.15. ПЭТ.
а --- аксиальная; б --- корональная томограммы.
Зона гипоперфузии в полюсно базальном отделе левой лобной доли.
Рис. 6.16. Перфузионная КТ в остром периоде черепно мозговой травмы.
а --- стандартная КТ, выполненная в первые, третьи и пятнадцатые сутки травмы;
б --- перфузионная КТ, выполненная в первые сутки травмы.
Зона уменьшения объемного кровотока (гСВУ), замедления времени прохождения
контрастного болюса (гМТТ) и гипоперфузии (гСВР) в правой лобной доле не вы-
зывает сомнений при перфузионной КТ. При стандартной КТ отек выявляется
значительно позже, только на 15 й день после травмы.
ку измерения линейной скорости кровотока и других гемодинамических пока-
зателей проводятся на уровне магистральных артерий, а вазоспазм чаше разви-
вается в более мелких разветвлениях. Кроме того, в участках мозга, смежных
с ишемизированной зоной, нередко появляется компенсаторное усиление кро-
вотока в виде гиперперфузии с соответствующим ускорением региональной ско-
рости кровотока, поэтому допплерографическое исследование магистральных
артерий при развитии вторичной посттравматической ишемии может выявить
либо признаки вазоспазма, либо признаки гиперемии, либо продемонстрировать
нормальные показатели.
Новыми направлениями в изучении регионального мозгового кровотока
у пациента с черепно мозговой травмой стали однофотонная эмиссионная ком-
пьютерная томография (ОФЭКТ), позитронно эмиссионная томография
(ПЭТ), но особенно перспективной является перфузионная компьютерная то-
мография (ПКТ). Методами ОФЭКТ и ПЭТ (рис. 6.15) можно получить до-
стоверные показатели мозгового кровотока, однако их выполнение требует до
рогостоящего оборудования, большого штата обслуживающего персонала и
поэтому может использоваться лишь в небольшом числе крупных медицин-
ских центров. Перфузионная KT выполняется на мультиспиральном компь-
ютерном томографе с внутривенным введением небольшого объема (40 мл)
контрастного вещества и последующей обработкой изображений с помощью
специальной программы, позволяющей количественно оценить в каждом
единичном объеме региональный объемный кровоток, среднее время прохож-
дения контрастного болюса и региональный мозговой кровоток. Помимо
параметрической оценки возможно получение цветовых карт мозгового кро-
вотока, что делает изображения особенно демонстративными. Перфузионная
KT обеспечивает более раннее по сравнению со стандартным исследованием
выявление вторичной посттравматической ишемии, что улучшает результаты
лечения этой категории больных (рис. 6.16).
Список литературы
1. Корниенко В.Н., Потапов A.A., Пронин H.H., Захарова Н.Е. Диагностиче-
ские возможности компьютерной и магнитно резонансной томографии при че-
репно мозговой травме. Доказательная нейротравматология / Под ред. А.А.По-
тапова, Л.Б.Лихтермана.--- Москва, НИИ нейрохирургии им. Н.Н.Бурденко,
2003. С. 408 463.
2. Касумова СЮ. Патологическая анатомия черепно мозговой травмы. Кли-
ническое руководство по черепно мозговой травме / Под ред. А.Н.Коновалова,
Л.Б.Лихтермана, А.А.Потапова.--- Москва: Антидор, 1998.--- Т. 1, С. 169---230.
3. Корниенко В.Н., Васин В.А., Кузьменко В.А. Компьютерная томография в ди-
агностике черепно мозговой травмы. --- Москва: Медицина, 1987.--- 288 с.
4. Черемисин В.М. и соавт. Лучевая диагностика травмы черепа и головного
мозга.--- СПб., 2002. 20 с.
5. Abe М., Udono Н., Tabuchi К. et al. Analyses of ischemic brain damage in cases
of acute subdural hematomas / Surg. Neurol., 2003; 59.--- P. 464---472.
6. Orrison W.W. Neuroimaging. Chapter 26: Neuroimaging and head trauma.---
WB Sounders Company, 2000. P. 884 915.
Глава 7
СОСУДИСТЫ Е ЗАБО Л ЕВАН ИЯ
ГОЛОВНОГО МОЗГА
Страшны не только смерть, старость и безумие.
Существует, например, апоплексия ---это громовой удар,
он поражает вас, но не уничтожает, однако после него
все кончено. Это все еще вы и уже не вы; вы, который были
почти ангелом, становитесь неподвижной массой, кото-
рая уже почти животное; на человеческом языке это
называется попросту апоплексией...
Александр Дюма отец, «Граф Монте Кристо»
Изучение сосудистых заболеваний головного мозга является одним из при-
оритетных направлений неврологии. Большая распространенность, высокая
смертность, частая инвалидизация больных, причем нередко молодого, трудо-
способного возраста, ставят эту проблему в ряд социально значимых.
В последние десятилетия достигнут несомненный прогресс в раскрытии и
понимании механизмов мозговой гемодинамики благодаря использованию ме-
тодов нейро и ангиовизуализации.
В России наибольшее распространение получила классификация сосуди-
стых поражений головного и спинного мозга, предложенная Е.В.Шмидтом и
Г.А.Максудовым (1971), уточненная и видоизмененная Е.В.Шмидтом.
Классификация сосудистых поражений головного мозга (Шмидт Е.В., 1985)
I. Заболевания и патологические состояния, приводящие к нарушениям кро-
вообращения в головном мозге (атеросклероз, гипертоническая болезнь и
т. д.).
II. Нарушения мозгового кровообращения.
A. Начальные проявления недостаточности мозгового кровообращения.
Б. Преходящие нарушения мозгового кровообращения.
B. Инсульт:
1. Субарахноидальное нетравматическое кровоизлияние.
2. Геморрагический инсульт.
3. Ишемический инсульт.
Г. Прогрессирующие нарушения мозгового кровообращения.
1. Дисциркуляторная энцефалопатия:
1.1. Атеросклеротическая.
1.2. Гипертоническая.
1.3. Венозные и другие или неуточненные.
ПОРОКИ СОСУДОВ ГОЛОВНОГО МОЗГА
В настоящее время к порокам развития сосудов головного и спинного мозга
(сосудистым мальформациям) относят гетерогенную группу дисэмбриогенети
ческих образований преимущественно ангиоматозного строения. Сюда же от-
носят персистирующие эмбриональные сосуды, а также всякого рода шунты и
фистулы. В периоде на русский язык термин «мальформация» означает «порок
развития». Что же касается многочисленных отклонений в строении артериаль-
ного круга мозга (виллизиева круга), то они являются скорее вариантами нор-
мы, а не аномалиями.
Терминология
Большое число терминологических неточностей и отсутствие единой клас-
сификации приводят к досадной путанице. В связи с этим хочется остано-
виться на определении наиболее часто встречающихся сосудистых мальфор
маций.
1. Артериовенозная мальформация нередко обозначается как артериове
нозная аневризма, однако эти образования не имеют ничего общего с истин-
ными аневризмами, т. е. ограниченным расширением артерий. По той же при-
чине следует избегать термина «аневризма вены Галена», так как расширение
вен обозначается не как аневризма, а как флебэктазия, варикоз или варико
целе.
2. Ангиомы --- кавернозные пороки развития, от слова «кавернозус» --- пеще-
ристый. Это скопление сосудистых полостей, разделенных между собой общи-
ми для нескольких полостей соединительнотканными септами, выстланными
изнутри эндотелием. Мозговое вещество или элементы мягкой мозговой оболочки
между отдельными сосудистыми полостями отсутствуют.
3. Рацемозные пороки развития --- прежнее название «ветвистые ангио-
мы» --- сборная группа, представленная несколькими вариантами сосудис-
тых мальформаций, для которых характерно наличие мозгового вещества или
иной ткани между сосудистыми стволами. Эта группа включает в себя теле
ангиоэктазии --- очаговые скопления капилляроподобных расширенных со-
судов, стенки которых практически лишены соединительной, мышечной и
эластической ткани и представлены лишь базальной мембраной, выстланной
эндотелием. Между отдельными сосудистыми компонентами располагается
ткань мозга.
4. Сочетанные ангиодисплазии (факоматозы) --- группа синдромов, которые
характеризуются сосудистыми мальформациями, локализующимися в ЦНС и
иных органах и тканях.
5. Варикоз --- резкое и стойкое расширение одной вены.
Термины «сосудистая мальформация» и «ангиодисплазия» являются сино-
нимами (в первом случае речь идет о латинских корнях определения, во втором ---
о греческих).
Классификация
Существует большое количество классификаций сосудистых мальформаций.
Наиболее полной и точной, на наш взгляд, является классификация, пред-
ложенная Д.Е.Мацко. Она включает в себя следующие группы:
I. Ангиоматозные пороки развития:
1. Кавернозные.
2. Промежуточные.
3. Рацемозные:
а) телеангиоэктазии;
б) венозные;
в) артериовенозные (в том числе с варикозом большой вены мозга).
4. Смешанные.
5. Сочетанные:
а) в пределах ЦНС;
б) факоматозы:
нервно кожный (болезнь Стерджа --- Вебера),
с поражением конечностей и спинного мозга (синдром Клиппеля ---
Треноне),
редкие и недостаточно доказанные факоматозы.
П. Неангиматозные пороки развития:
1. Варикоз (в том числе изолированный варикоз большой вены мозга).
2. Артериовенозные (синусные) фистулы и соустья (в том числе с варикозом
большой вены мозга).
3. Персистирующие эмбриональные сосуды.
4. Другие неангиоматозные пороки развития.
III. Неклассифицируемые пороки развития.
КАВЕРНОЗНЫЕ И ПРОМЕЖУТОЧНЫЕ АНГИОМЫ
Составляют 5---13% всех пороков развития головного мозга. Кавернозные
ангиомы могут встречаться практически во всех отделах головного мозга, но чаще
всего наблюдается их супратенториальная локализация --- в белом веществе. Они
описаны в подкорковых ганглиях, мозжечке, синусах твердой мозговой оболоч-
ки, гипофизе, сосудистых сплетениях, стенках и полостях желудочков мозга,
эпифизе, внутреннем слуховом проходе и т. д. Располагаясь по средней линии,
кавернозные ангиомы способны приводить к эндокринным нарушениям, могут
давать симптоматику поражения тройничного нерва и сочетаться с патологией
других сосудов и внутренних органов. Размеры могут колебаться от микромаль
формаций до гигантских, занимающих целую долю. Форма обычно приближа-
ется к округло овальной. Иногда можно различить капсулу, но чаще она отсут-
ствует. На вскрытии очаг имеет темно красный цвет и напоминает небольшую
гематому, однако уже с помощью лупы можно разглядеть губчатую структуру
образования. Нередко этот вид пороков сопровождается обызвествлением --- от
в
г
Рис. 7.1. МРТ головного мозга. Кавернозная гемангиома в белом веществе правой
лобной доли.
а --- Т2 ВИ, аксиальная плоскость;
б --- Т1 ВИ после введения контрастного вещества;
в --- Flair ИП, аксиальная плоскость;
г --- томограмма, взвешенная по протонной плотности, корональная плоскость.
небольших вкраплений до тотального.
Есть сообщения о сопутствующих
внутримозговым кавернозным ангио-
мам кистах, генез которых видимо свя
Рис. 7.2. МРТ головного мозга, Т2 ВИ,
сагиттальная проекция. Гигантская
кавернозная гемангиома в мосту мозга.
зан с кровоизлиянием из сосудистой мальформации. Нередко до операции эти
случаи трактуются как кистозные глиомы. Кавернозные пороки развития нередко
бывают множественными (поданным МРТ, до 50% случаев).
Клинически манифестируют в молодом возрасте (средний возраст 23,5 года)
судорожным синдромом (35---50% случаев), картиной прогрессирующих невро
логическихвыпадений, симулирующих опухоль (35,5---50% случаев), или сим-
птоматикой внутричерепного кровоизлияния (20---30% случаев). Возможны со-
четания этих вариантов либо развитие более редких, например, с нарушением
психики, с выраженной тромбоцитопенией и склонностью к кровотечениям (син-
дром Карабаха --- Меритта). Описано появление первых клинических симпто-
мов у женщин на фоне беременности, родов или приема эстрогенов, что, по ви-
димому, можно объяснить увеличением объема порока из за нарушения веноз-
ного оттока при повышении внутрибрюшного давления либо специфической
чувствительностью к определенным гормонам.
Вопрос о росте кавернозных ангиом является предметом дискуссий. Распро-
странена точка зрения, согласно которой они увеличиваются за счет растяже-
ния сосудистых полостей под постоянным влиянием давления крови.
Ангиографическая картина неспецифична: в 20% случаев не выявляется
никакой патологии, в 45,5% наблюдений регистрируется бессосудистая зона, и
лишь у 35,5% пациентов отмечаются элементы артериовенозного шунтирования
и дренирующие сосуды.
КТ картина неспецифична: масс эффект обычно отсутствует, в 35% случаев
определяются зоны повышенной плотности, связанные с кальцификацией.
Можно наблюдать контрастное усиление и признаки острого кровоизлияния.
Лишь внедрение в клиническую практику МРТ улучшило прижизненную
диагностику этого вида СМ. Выявляется кольцо гемосидерина, окружающее
небольшое многоузловое ядро смешанной интенсивности сигнала. Гемосидерин
и (или) обызвествления выявляются в виде зон гипоинтенсивности на Т2 ВИ.
При наличии геморрагии картина зависит от давности ее. Иногда наблюдается
слабое контрастное усиление (рис. 7.1,7.2).
По ряду клинико анатомических особенностей (отсутствие крупных пита-
ющих и дренирующих сосудов, весьма медленный ток крови, выраженная склон-
ность к тромбообразованию, хорошая отграниченность вплоть до наличия ис-
тинной капсулы) этот вариант является едва ли не самым благоприятным объек
том среди всех сосудистых мальформаций для радикального хирургического
вмешательства.
Телеангиоэктазии
Телеангиоэктазии --- это один из видов ангиоматозных рацемозных (развет-
вленных) пороков. Они характеризуются скоплением расширенных капилля
роподобных структур, между которыми расположена ткань мозга. Типичная ло-
кализация --- мост мозга. Часто они обнаруживаются в белом веществе больших
полушарий. Их размер в среднем составляет 5---6 мм.
Клинически телеангиоэктазии являются самым доброкачественным типом
сосудистых мальформаций. Не имея склонности к разрывам, они редко прояв-
ляются клинически. Лишь в отдельных случаях протекают по геморрагическо-
му (казуистика) и псевдоопухолевому типу. Описаны телеангиоэктазии в адено
гипофизе. Они могут быть также оболочечным компонентом болезни Стерджа ---
Вебера. Нередким является сочетание телеангиоэктазии с кавернозными СМ.
Микроскопически телеангиоэктазии представляют собой расширенные со-
суды, выстланные эндотелием, лежащим на базальной мембране, эластический
и мышечный слои отсутствуют. Глиоз, обызвествление или скопление гемоси
дерина не характерны.
Возможность обнаружения телеангиоэктазии при ангиографии или КТ ис
следовании категорически опровергается большинством авторов. Лишь изред-
ка описано их обнаружение при проведении М РТ в виде небольшой зоны кон-
трастного усиления или отсутствия потока (рис. 7.3). В присутствии геморрагии
телеангиоэктазии схожи с кавернозными аневризмами.
а
б
Рис. 7.3. МРТ головного мозга. Телеангиоэктазии в белом веществе правой
теменной доли и левом зрительном бугре у больного с болезнью Рендю --- Ослера.
а --- Т2 ВИ, аксиальная плоскость; б --- Т1 ВИ, сагиттальная плоскость.
Венозные мальформации
Венозные мальформации могут быть рацемозными, либо иметь сходство с ва
рикозом и другими фистульными вариантами. Их особенностью является час-
тая локализация в мягкой мозговой оболочке, склонность к поражению спин-
ного мозга.
в
г
Рис. 7.4. Венозная ангиома правой лобной доли.
а --- томограмма, взвешенная по протонной плотности, аксиальная плоскость;
б --- Т1 ВИ, после внутривенного контрастирования, аксиальная плоскость;
в, г --- Т1 ВИ, Ш, корональная плоскость.
Венозные мальформации могут быть проявлением синдрома Стерджа ---
Вебера. Клинически для них характерны судорожный синдром и атаксия, иног-
да они могут протекать по геморрагическому типу (1 % случаев).
При МРТ венозные мальформации состоят из небольших вен, которые про-
ходят через мозговую паренхиму и впадают в дренирующую коллекторную вену,
нередко напоминая медузу (рис. 7.4).
При КТ с контрастным усилением можно увидеть коллекторную вену, но
синдром «медузы» видение так четко, как при МРТ.
Артериовенозные мальформации
Артериовенозные мальформации (АВМ) наиболее значимы с клинической
точки зрения. Они являются причиной 5--- 10% всех случаев субарахноидальных
кровоизлияний, причиной смерти 1 % больных, перенесших инсульт, и встреча-
ются с частотой 1 ---3% на 100 ООО жителей. АВМ чаше локализуются в системе
ВСА, чаще средней мозговой артерии (СМА). Достаточно часто АВМ кровоснаб
жаются из нескольких артерий, которые могут принадлежать даже к разным
сосудистым бассейнам.
Микроскопически АВМ представляют собой конгломерат извитых и пере-
плетающихся сосудов различного диаметра. Размеры АВМ колеблются от мик-
роскопических до гигантских, поражающих целиком все полушарие.
С хирургической точки зрения выделяют следующие анатомические вари-
анты АВМ:
1. Ангиоматозный, или пиальный, вариант, при котором связь артерий с ве-
нами осуществляется через клубок диспластических сосудов («классический
вариант»).
2. Фистулезный, или дуралънътй, вариант, при котором имеется непосредствен-
ный переход артерии в вену с возможной эктазией переходного участка.
3. Сочетание редкого фистулезного с гораздо более часто встречающимся
ангиоматозным вариантом.
Кроме того, все АВМ разделяют по количеству питающих и дренирующих
сосудов --- один питающий и один дренирующий, несколько питающих и один
дренирующий, несколько питающих и несколько дренирующих сосудов.
Клинические симптомы АВМ обусловлены кровоизлиянием, масс эффек
том и ишемией. Вследствие ишемии, глиоза и предшествовавших кровоизлия-
ний развивается судорожный синдром. АВМ склонны к разрывам. Вероятность
их составляет 3---4% в год.
В 60---80% случаев АВМ расположены субтенториально, причем большие
АВМ имеют и пиальный, и дуральный компоненты. Пиальные АВМ обычно
поверхностные, дуральные, напротив, чаше расположены инфратенториально,
в том числе в позвоночном канале.
При МРТ АВМ выглядят как аморфные образования, гипоинтенсивные на
Т1 и Т2 ВИ. Реже встречаются АВМ клиновидной формы, с верхушкой, обра-
щенной в сторону желудочков. Отека нет. Вокруг узла извитых сосудов на МРТ
могут обнаруживаться участки кровоизлияния, иногда кальцификации и часто
зона ишемии. Дальнейшая тактика исследования АВМ, как правило, сводится
к проведению традиционной рентгеновской ангиографии. Вместе с тем может
использоваться и МРА (рис. 7.5).
Перед МРА ставится задача выявления артериального сосуда, питающего
узел, и вены, дренирующей его. Сосуд, питающий АВМ, достаточно хорошо
демонстрируется стандартной 3D TOF методикой. С методической точки зре-
ния важно внимательно просматривать исходные тонкие срезы, а также делать
МIP реконструкцию в узком поле и с неполным набором срезов. Важно опреде-
лить, питается ли АВМ из одной или нескольких терминальных артерий, либо
из артерий, одновременно кровоснабжающих АВМ и нормальные ткани мозга.
В последнем случае невозможно выполнить клипирование или эмболизацию.
При М РА трудно различить границы истинного клубка сосудов в АВ М от окру-
жающих его ангиоматозно измененных коллатеральных сосудов. В принципе
ангиоматозно измененные коллатеральные сосуды имеют более медленный кро
воток, чем в узле. Поэтому они могут быть выделены на фазово контрастных
ангиограммах с низким значением Vene. В самом узле кровоток сложный, там
имеются шунты и иногда аневризмы с быстрым кровотоком, а также и участки
с замедленным кровотоком. На обычных 3D TOF ангиограммах участки с за-
медленным кровотоком не видны. Для их визуализации следует прибегнуть к со-
четанию 3 D TOF методики с внутривенным контрастированием. Венозный дре-
наж через поверхностную кортикальную вену виден на томограммах. Глубокий
дренаж, если он имеется, можно увидеть на 2D TOF или фазово контрастных
ангиограммах с низким значением Vene. Его выявление важно для нейрохирур-
гов, так как он существенно усложняет оперативное вмешательство.
Дуральные АВМ принципиально отличаются от пиальных по клиническому
течению и прогнозу. Эти повреждения обычно связаны с тромбозом вены или
синуса и последующей реканализацией с развитием коллатеральных путей кро-
вотока. Периодически при увеличении кровотока и снижении венозного дрена-
жа в синус наблюдается перераспределение потока через кортикальные вены,
что может привести к внутримозговому или субарахноидальному кровоизлия-
нию либо венозному инфаркту. Симптоматика связана со сдавлением окружа-
ющих структур --- головные боли, парез лицевого нерва, судорожные припадки.
Дуральные АВМ трудно диагностировать при КГ и МРТ. Необходимо обращать
внимание на наличие тромбоза синуса и расширенных кортикальных вен. При
отсутствии этих симптомов диагностика затрудняется. Иногда выявляется рас-
ширение среднеоболочечной артерии или вены либо расширенное остистое от-
верстие. Наиболее точна диагностика дуральных АВМ при традиционной анги-
ографии.
У детей с АВМ, сочетающейся с варикозом большой вены мозга, симптома-
тика связана с гидроцефалией, возникающей вследствие компрессии водопро-
вода мозга, и сердечной недостаточностью, обусловленной прямым сообщени-
ем артерий и вен. Течение, как правило, медленное (рис. 7.6).
Факоматозы
Энцефалотригеминальный ангиоматоз (болезнь Стерджа --- Вебера) характе-
ризуется односторонним ангиоматозом (невусом) на лице, часто в области ин-
нервации тройничного нерва. В 90% случаев имеется судорожный синдром,
обычно возникающий уже в первый год жизни. Часто встречаются умственная
отсталость, гемиплегия, гомонимная гемианопсия, односторонняя глаукома.
Интракраниал ьно имеется лептоменингеальный венозный ангиоматоз, чаще
локализующийся в задневисочной и затылочной областях на той же стороне,
что и кожные проявления. Сосудистое сплетение ипсилатерального бокового
желудочка увеличено. Под ангиоматозной пиальной оболочкой имеются ги
ральное обызвествление коры и ипсилатеральная атрофия. Обызвествления и
атрофия прогрессируют с возрастом и могут распространяться кпереди на ви-
сочную и лобную доли. Редко встречается поражение обоих полушарий. Часто
наблюдается сочетание с аномалией или отсутствием поверхностных корти-
кальных вен.
Рис. 7.7. Окончание.
г, д, е, ж --- МРТ головного мозга, Т2 ВИ, аксиальная плоскость. Гемиатрофия левого
полушария. Пахигирия левого полушария. Глиоз в субкортикальном белом веще-
стве левых лобной и теменной долей.
Диагноз болезни Стерджа --- Вебера нередко становится очевидным уже при
рассмотрении обзорных краниограмм --- определяются двухконтурные обызве-
ствления, повторяющие ход извилин.
При МРТ выявляется снижение сигнала на Т2 ВИ в участках кальцифика
тов коры. Определяется атрофия мозга в виде расширения щелей. Иногда наблю-
даются очаги повышенного сигнала на Т2 ВИ из за реактивного глиоза ниже-
лежащего белого вещества. Может выявляться коллатеральный венозный дренаж
в виде расширенных медуллярных субэпендимальных вен (рис. 7.7).
Персистирующие сосуды
Персистирующие сосуды --- это атипичные каротидно базилярные анасто-
мозы, возникающие из за персистенции функционирующих в эмбриональном
периоде сосудов --- примитивной тройничной, подъязычной, ушной и проатлан
тной артерий.
В норме эти сосуды в антенатальном периоде, по мере развития задней соеди-
нительной артерии, подвергаются обратному развитию. Однако в 0,1 ---0,6% слу-
чаев они выявляются при ангиографии. Наиболее часто встречается примитив
Рис. 7.8. Персистирующие артерии.
а --- схема: 1 --- задняя соединительная ар-
терия; 2 --- тройничный нерв; 3 --- подъя-
зычная артерия; 4 --- проатлантная арте-
рия; 5 --- позвоночная артерия; 6 --- внут-
ренняя сонная артерия; 7 --- ушная
артерия.
б --- МР ангиография интракраниальных
артерий. Примитивная тройничная арте-
рия (показана стрелкой).
ная тройничная артерия, соединяющая интракавернозную часть ВСАи бази
лярную артерию. Она может быть причиной невралгии тройничного нерва, су
барахноидального кровоизлияния (рис. 7.8).
Аневризматическая болезнь
Происхождение термина «аневризма» своеобразно. Слово это греческое, в ос-
нове лежит глагол «расширяю». На латинском языке этот термин перестал обо-
значать расширение вообще, а стал обозначать расширение только артерий.
Аневризма --- это местное расширение просвета артерии вследствие измене-
ний или повреждений ее стенок. По форме расширение может быть мешотчатым
или веретенообразным.
Ошибочным является использование этого термина для обозначения расши-
рения вен и капилляров. Неверно говорить об артериальных аневризмах, так как
аневризмы всегда артериальные.
Уместно напомнить, что расширение вен при его диффузном характере при-
нято обозначать термином «флебэктазия», а при ограниченном --- называть ва
рикозом или узлами.
В классификации, разработанной в Нейрохирургическом институте им. проф.
А.Л. Поленова, насчитывается около 30 разновидностей аневризм, различаю-
щихся по происхождению и механизмам развития.
Классификация аневризм головного мозга
1. Бифуркапионно гемодинамические --- БГА (бывшие «такназываемые врож-
денные»).
1.1. БГА при системных артериальных гипертензиях:
1.1.1. Гипертоническая болезнь (эссенциальная гипертензия).
1.1.2. Поликистозная дисплазия почек.
1.1.3.Коарктация аорты.
1.1.4. Другие системные артериальные гипертензии.
1.2. БГА при региональных гемодинамических нарушениях:
1.2.1. Артериовенозный порок развития.
1.2.2. Фиброзно мышечная дисплазия.
1.2.3. Болезнь Нисимото --- Такеути --- Кудо (моя моя).
1.2.4. Черепно мозговая травма.
1.2.5. Пороки развития артериального круга большого мозга.
1.3. БГА, происхождение которых остается невыясненным.
2. Аневризмы при некоторых наследственных мезенхимопатиях.
2.1. Синдром Марфана.
2.2. Синдром Элерса --- Данлоса.
2.3. Синдром Гренблад --- Страндберга.
3. Дегенеративно дистрофические аневризмы.
3.1. Атеросклеротические.
3.2. Гипертонические (внутримозговые милиарные).
3.3. Лучевые.
4. Травматические аневризмы (при Ч МТ).
4.1. Аневризмы в зоне прямого (первичного) воздействия.
4.2. Аневризмы вне зоны прямого повреждения:
4.2.1. Гемодинамический стресс.
4.2.2. Вторичные повреждения артерий.
5. Воспалительные.
6. Эмболические.
6.1. Бактериальные (микробные).
6.2. Микотические (грибковые).
6.3. Онкогенные:
6.3.1. «Доброкачественные» (при миксомах сердца).
6.3.2. «Злокачественные» (при злокачественных опухолях).
7. Дизэмбриогенетические аневризмы и аневризмоподобные образования.
7.1. «Детские».
7.2. Из так называемых остаточных сосудов.
7.3. Воронкообразное расширение устья задней соединительной артерии.
7.4. Долихоэктазия.
8. Ятрогенные аневризмы.
8.1. После хирургических вмешательств.
8.2. После лучевого лечения.
9. Прочие аневризмы.
9.1. Синдром Фридрейха.
9.2. Синдром Блюма.
9.3. Болезнь Помпе (системный гликогеноз II типа).
Этиология аневризм головного мозга различна, а патогенез подавляющего
большинства из них един. Он укладывается в диалектический принцип проти-
воборствующих начал, взаимоуравновешенность которых обеспечивает подвиж-
ную стабильность.
Так, атеросклеротические или фузиформные аневризмы связаны с атероск
леротическим расширением чаще всего позвоночных и (или) базилярной арте-
рий. Расслаивающие аневризмы чаще встречаются после травм. Онкогенные
аневризмы встречаются при эмболии из опухоли или прорастании опухолью
стенки сосуда. Они чаще встречаются при миксомах предсердий и хориокарци
номах. Микотические аневризмы --- это результат эндокардита с септической
эмболизацией в сосуды с вторичным разрушением сосудистой стенки, так что
от сосуда остается только интима.
Но практически вся проблема аневризм головного мозга, если взять ее ней-
рохирургический аспект, сводится именно к 1 й группе --- БГА, которые долгое
время фигурировали в специальной литературе, как врожденные, затем как так
называемые врожденные. Не менее 90% аневризм артериального круга большо-
го мозга --- это бифуркационно гемодинамические аневризмы, остальные со-
ставляют доли процента. Бифуркационно гемодинамические аневризмы назы-
ваются так потому, что они располагаются исключительно в местах развилок
артерий, т. е. это болезнь тройников артериального крута большого мозга.
Важно то, что в области тройников, развилок сосудов, в силу законов гидро-
динамики имеет место сложная функциональная коллизия, устойчивость кото-
рой намного меньше, чем на прямых отрезках сосудов. Функциональная неус-
тойчивость (с недавних пор совокупное влияние гемодинамических факторов
на сосудистую стенку обозначают как гемодинамический стресс --- турбулент-
ность и вихревые потоки крови в местах ветвлений сосудов, пульсовая волна)
сочетается с рядом структурных аномалий в области тройников (своеобразные
желобки, скрепляющие расходящиеся артерии, дефекты медии, асимметрия
углов отхождения дочерних стволов и неодинаковость диаметров, а с возрас-
том --- гиперэластоз, коллагеноз, стенозы). Тройник артериального круга боль-
шого мозга, на территории которого происходит столкновение двух противопо-
ложно направленных потоков крови, представляет собой своего рода напряжен-
ный транспортный перекресток, где в тугой узел завязаны внутренние
противоречия функционального и органического характера. Термин «бифурка
ционно гемодинамические аневризмы» имеет в своей основе желание увязать
воедино уязвимые места стыковки сосудов с заложенными в них природой «стро-
ительными недоделками», с особо сложными гемодинамическими ситуациями,
возникающими здесь.
Примерно у 80% обследованных в местах развилок артерий обнаруживаются
дефекты мышечной оболочки сосуда --- медии. В этих участках, испытывающих
наибольшие гидравлические нагрузки, интима располагается непосредственно
на адвентиции, следовательно, эластические свойства стенки снижены.
Частота выявления аневризм составляет 1---4% случаев внутричерепной па-
тологии. Множественные аневризмы наблюдаются в 15---20% общего числа слу-
чаев заболевания. Большинство таких аневризм располагаются в передних от-
делах артериального круга большого мозга, только пятая часть их --- в задних
отделах. Они чаще встречаются на развилках внутричерепной части ВСА --- 34---
51%наблюдений, ПМА ПСА--- '/,наблюдений, втройникахСМА --- 12---27%
наблюдений, артериях вертебрально базилярного бассейна --- 10% случаев
(рис. 7.9).
Размеры БГА, как правило, небольшие --- менее 5 мм, однако примерно в 8---
10% случаев встречаются размеры более 10 мм. Аневризмы диаметром от 10 до
20 мм принято называть крупными, более 20 мм --- гигантскими.
Крупные и гигантские аневризмы протекают, как правило, по псевдотумо
розномутипу с очаговой неврологической симптоматикой, обусловленной сдав
лением мозговых структур и инсультами.
В настоящее время аневризмы большого размера не считаются «выросши-
ми», так как резервы роста БГА не очень значительны, они рвутся раньше, чем
достигают больших размеров.
В аневризмах принято различать дно, шейку, входное отверстие. Типичные
мелкие БГА не склонны к тромбообразованию в полости. В аневризмах, разме-
ры которых составляют более 10 мм, тромботические массы присутствуют по-
чти постоянно, внутренние контуры аневризматической полости при этом име-
ют неправильные очертания, что позволяет диагностировать частичное ее тром
бирование.
Рис. 7.9. Частота выявления
аневризм сосудов головного
мозга (по К. Sartor).
I---хиазма;2---28%;3---пере-
дняя мозговая артерия; 4 --- внут-
ренняя сонная артерия; 5 --- пе-
редняя соединительная артерия;
6 --- передняя хориоидальная ар-
терия; 7 --- задняя соединитель-
наяартерия;8---3%;9---5%:
10 --- глазничная артерия; 11 ---
средняя менингеальная артерия;
12 4%;13 20,9%;14 сред-
няя мозговая артерия; 15 --- 25%;
16 --- задняя мозговая артерия;
17 --- зрительный тракт; 18 --- пе-
редняя нижняя мозжечковая ар-
терия; 19 --- основная артерия;
20 --- задняя нижняя мозжечко-
вая артерия; 21 --- позвоночная
артерия.
Часть бифуркационно гемодинамических аневризм протекает без клинических
проявлений --- это так называемое аневризмоносительство. Клинически не ма-
нифестирующие при жизни аневризмы распознаются пока редко и большей ча-
стью случайно. Другая часть БГА проявляет себя клинической симптоматикой ---
по апоплектическому типу, либо клинической картиной объемного процесса. На
долю апоплектического (геморрагического) варианта приходится 90,4% наблю-
дений. Около половины больных с апоплексиями умирают на догоспитальном
этапе. Геморрагии при разрыве аневризмы бывают разными --- от незначительных
субарахноидальныхдо обширных субархноидально паренхиматозных. По лока-
лизации кровоизлияния нередко можно заподозрить локализацию разорвавшейся
аневризмы. Так, при наличии крови в межполушарной щели и боковых желудочках,
вероятнее всего, разорвалась аневризма ПСА. Кровоизлияние в латеральной
борозде указывает на разрыв аневризмы СМА, наличие крови в ГУ желудочке
связано с разрывом аневризмы задней нижней мозжечковой артерии.
АЛГОРИТМ ОБСЛЕДОВАНИЯ ПАЦИЕНТОВ
Настораживающими клиническими симптомами являются эпизод субарах
ноидального кровоизлияния, тяжелые головные боли неясной этиологии, нару-
шение функции черепного нерва, что может быть проявлением масс эффекта,
транзиторной ишемии без очевидной связи с атеросклерозом, эндокардит или
васкулит в анамнезе в сочетании с неврологической симптоматикой. При нали-
чии аневризм у близких родственников и поликистоза почек также показано
обследование в связи с генетической предрасположенностью. Рентгеновская
ангиография в перечисленных случаях не может быть выбрана в качестве скри
нинговой процедуры из за инвазивности, сложности и дороговизны. Вместо нее
имеет смысл выполнить МРТ и МРА и только при отрицательных результатах
ставить вопрос о проведении рентгеновской ангиографии.
Аневризмы больших размеров обнаруживаются при МРТ по характерному
отсутствию сигнала от быстрого кровотока. Однако не только аневризма, но и
сам сосуд также не дает сигнала. Компактная костная ткань, резко гипоинтен
сивная, может симулировать аневризму, например, передний наклоненный от-
росток в поперечном срезе (рис. 7.10).
В
в --- МР АГ интракраниальных артерий.
МР ангиографический скрининг неразорвавшихся аневризм начинается
с исследования артериального круга большого мозга по методике 3D TOF. Стан-
дартный протокол включает в себя градиентную или турбо градиентную после-
довательность с минимально возможным значением ТЕ, матрицей 256x256 или
256x512 и полем видения около 200 мм. Выше блока срезов устанавливается
полоса насыщения, чтобы не проявлялся венозный кровоток.
Анализ МРА изображений всегда начинается с просмотра первичных попе-
речных изображений. Затем осуществляются М1Р преобразование и повороты
в разных плоскостях.
Мешотчатые аневризмы обычно локализуются в области каротидного сифо-
на. Они отходят от ВСА перпендикулярно вбок, как «ягода». Для них типичен
вихревой кровоток в центре, что приводит к дефекту внутри аневризмы на МРА
изображениях.
Веретенообразные аневризмы хуже выявляются при МРА, так как имеют
медленный пристеночный кровоток. С другой стороны, пристеночный тромб
на обычных Т1 ВИ всегда яркий, что помогает находить этот тип аневризм
(рис. 7.11).
Гигантские аневризмы приводят к масс эффекту и вторичной ишемии. На
обычных томограммах внутри них всегда смешанный сигнал. Несмотря на боль-
шие размеры, на стандартных 3D TOF ангиограммах гигантская аневризма мо-
жет быть и не видна. Это объясняется тромбозом или медленным кровотоком
в аневризме. В таком случае помогает контрастирование или фазово контраст
ная ангиография.
Рис. 7.11. МРТ головного мозга. Фузиформная аневризма основной артерии,
а--- Т2 ВИ, аксиальная плоскость; б --- Т1 ВИ, корональная плоскость.
Рис. 7.12. Аневризматическое
субарахноидальное кровоизлияние.
Аневризма была выявлена при дигиталь
ной субтракционной ангиографии в об-
ласти развилки правой средней мозговой
артерии (сегменты М1 М2).
Считается, что чувствительность
МРТ в комбинации с МРА по отноше-
нию к аневризмам составляет не менее
95%. Однако до настоящего времени рентгеновская ангиография остается точ-
нее, так как не зависит от характеристик кровотока и имеет более высокую про-
странственную разрешающую способность.
Главная опасность разрыва аневризм, как уже упоминалось, связана с кро-
воизлиянием. В год наблюдается примерно 1 на 10 ООО населения субарахнои-
дальное кровоизлияние. Половина из них приходится на разорвавшиеся анев-
ризмы. Локализация кровоизлияния зависит от местонахождения аневризмы:
медиальная поверхность лобных долей наблюдается при разрыве аневризмы
ПМА ПСА, базальные субарахноидальные цистерны --- при разрыве аневриз-
мы супраклиноидного отдела ВСА (рис. 7.12).
НАРУШЕНИЯ МОЗГОВОГО КРОВООБРАЩЕНИЯ
Инсульт --- это быстро развивающееся фокальное или глобальное наруше-
ние функций мозга, длящееся более 24 часов или приводящее к смерти, при ис-
ключении иного генезазаболевания (определение ВОЗ).
Выделяют три основные нозологические формы --- ишемический (тромботи
ческий, нетромботический, эмболический) инсульт, кровоизлияние в мозг (ге-
моррагический инсульт), субарахноидальное кровоизлияние.
Ишемический инсульт --- самая частая форма острых нарушений мозгового
кровообращения. Ишемические инсульты составляют около 80% общего числа
инсультов. Понятие «ишемический инсульт» отражает только факт развития
заболевания, обусловленного уменьшением кровотока в определенной зоне мозга
и характеризующегося формированием ограниченного инфаркта. Инфаркт
мозга --- это зона некроза, образовавшаяся вследствие грубых, стойких нару-
шений метаболизма нейрональных и глиальных структур, возникших в резуль-
тате недостаточного кровообеспечения из за стеноза (окклюзии) магистральных
артерий головы или артерий мозга, приводящих к дефициту перфузионного дав-
ления, либо из за тромбоза или эмболии артерий мозга.
В настоящее время клинические данные в сочетании с результатами приме-
нения современных методов инструментальных исследований позволяют клас-
сифицировать острые церебральные ишемии с учетом четырех принципов:
1) в зависимости от продолжительности существования неврологического
дефицита;
2) по степени тяжести состояния больного;
3) соответственно локализации инфаркта;
4) применительно к патогенезу ишемического инсульта.
Классификация, основанная на локализации инфаркта мозга, базируется на
соответствии топической характеристики очаговой неврологической симптома-
тики определенным артериальным бассейнам.
Рис. 7.13. Зоны кровоснабжения головного мозга (по К.Sartor).
а --- передняя мозговая артерия; б --- средняя мозговая артерия; в --- задняя мозговая
артерия; г --- мозжечковая артерия; д --- передняя хороидальная артерия; е --- ленти
кулостриальные артерии; ж --- задняя хороидальная артерия; з --- основная артерия.
Традиционные классификации, основанные на клиническихданных, выде-
ляют переднециркуляторные (в каротидном бассейне) и заднециркуляторные
(в вертебрально базилярном бассейне) инсульты. Представляется разумным ис-
пользовать это деление, потому что такие инсульты имеют характерные клини-
ческие проявления. Что касается интракраниального кровообращения, то су-
ществуют значительные различия между строением, анастомотическим потен-
циалом, функциональными зонами мелких, глубинных перфорирующих
артерий, корковых артерий и крупных артерий. Соответственно каждый случай
инсульта в переднем или заднем бассейне нужно ограничить поражением под-
корковых областей, поверхностных корковых областей и вовлечением всей зоны
кровоснабжения (рис. 7.13).
Патогенетическая классификация
Территориальный инфаркт, развивающийся обычно вследствие тромботичес
кой или тромбоэмболической окклюзии крупного артериального ствола.
Инфаркт в конечных ветвях крупных артерий мозга или в пограничных
зонах вследствие резкого снижения перфузионного давления на периферии круп-
ных артерий мозга.
Лакунарные инфаркты в области таламуса, внутренней капсулы или ство-
ла мозга, а также множественные мелкие инфаркты в белом веществе, обуслов-
ленные повторными микроэмболиями или локальными нарушениями кровото-
ка в области ангиопатий в артериях малого калибра.
С.ШаНоуу (1998) предлагает выделять следующие клинические синдромы:
Синдром тотального поражения в каротидном бассейне (ТИКБ), клини-
ческими признаками которого являются гемиплегия, нарушение полей зрения
на той же стороне и нарушение высших корковых функций, относящихся к это-
му же полушарию.
Синдром частичного поражения в каротидном бассейне, куда включены
менее обширные нарушения, чем при синдроме ТИКБ, однако у пациентов име-
ются нарушения высших корковых функций и анатомически ограниченные
нарушения движений и чувствительности.
Синдромы лакунарного поражения, к которым относят чисто двигательный
или чисто сенсорный инсульты, одностороннюю атаксию и парез стопы, синд-
ром дизартрии и неловкой руки, атаксический гемипарез, сенсомоторный инсульт.
Синдромы поражения в вертебрально базилярном бассейне, которые пред-
ставлены гетерогенной группой в отношении как паренхиматозного, так и со-
судистого поражения.
ПРИМЕНЕНИЕ МЕТОДОВ НЕЙРОВИЗУАЛИЗАЦИИ В ДИАГНОСТИКЕ
ИШЕМИЧЕСКИХ ИНСУЛЬТОВ
Этиопатогенез инфаркта мозга принято рассматривать с учетом концепции
гетерогенности ишемического инсульта, разработанной Н.В.Верещагиным
(1996). Он обосновал роль патологии магистральных артерий головы, пораже
ний сердца различной этиологии, нарушений центральной и церебральной ге-
модинамики в этиологии и патогенезе ишемического инсульта. Е.В.Гусев (1991 ---
1996) детально охарактеризовал патобиохимические изменения в мозговых
структурах, приводящие к формированию инфаркта мозга. Среди условий, пред-
располагающих к развитию инфаркта мозга, правомерно выделять локальные
и системные факторы. Наиболее частыми локальными факторами являются
атеросклеротические поражения магистральных артерий головы и артерий моз-
га, а также сопряженное с ними локальное тромбообразование, различные по-
ражения сердца как источник кардиоэмболий. Одно из центральных мест в со-
временной медицине занимает проблема атеросклероза. Обусловленная атерос-
клерозом патология сосудов головного мозга является наиболее частой причиной
развития НМК, особенно ишемических инсультов, занимающих основное ме-
сто в структуре сосудистой патологии мозга.
Существенную роль в механизмах атерогенеза играет гемодинамический
фактор. Он проявляется в виде повреждающего воздействия потока крови на
стенку сосуда, прежде всего на эндотелий в местах физиологических изгибов
сосудов и деления их на ветви. Особенно резко гемодинамический фактор про-
является при повышенном артериальном давлении. Повреждение эндотелия
приводит к нарушению его проницаемости, проникновению во внутреннюю
оболочку артерий различных компонентов плазмы крови. Это стимулирует про-
лиферацию миоцитов, клеток соединительной ткани и приводит к локальному
утолщению внутренней оболочки.
Многолетнее изучение структурных изменений артериальной системы мозга
при атеросклерозе позволило обозначить весь комплекс обнаруженных взаимо-
связанных и многообразных процессов в сосудах на разных уровнях сосудис-
той системы мозга и в мозговой паренхиме термином «атеросклеротическая ан
гиоэнцефалопатия». К взаимосвязанным процессам при атеросклеротической
ангиоэнцефалопатии относятся: формирование атеросклеротических бляшек
с деструктивными и репаративными изменениями в них, характерный для ате-
росклероза стеноз (атеростеноз), закрытие просвета артерии бляшкой (атерооб
литерация), эмболия материалом распавшейся бляшки (атероэмболия), тромбоз
в области бляшки и за ее пределами, вторичные структурные изменения сосу-
дов, связанные с гемодинамическими нарушениями (перекалибровка и др.).
Проявления атеросклеротической ангиопатии имеют свои особенности на
каждом из трех основных структурно функциональных уровнях сосудистой
системы мозга. Магистральные артерии головы (сонные и позвоночные арте-
рии) , основной функцией которых является доставка крови к мозгу и в опреде-
ленной степени регуляция объема притекающей крови, образуют первый уро-
вень. Второй уровень --- артерии основания мозга, распределяющие кровь по
основным сосудистым бассейнам. Третий уровень (метаболический) --- сосуды
микроциркуляторного русла, обеспечивающие обменные процессы в головном
мозге. Атеросклеротические бляшки локализуются в сосудах первого и второго
уровней. На этих же уровнях при атеростенозе, сопровождающемся редукцией
кровотока, наблюдается динамическая структурно функциональная перестрой-
ка артерий на участках дистальнее стеноза. На третьем «метаболическом» уров
не атеросклеротическая ангиопатия проявляется в виде структурной перестрой-
ки микрососудов, характерной для гипоксии.
Еще в 60---80 е годы в многочисленных работах (Шмидт Е.В., 1963---1976;
Верещагин Н.В., 1980) было продемонстрировано, что по механизму сосудис-
той недостаточности возникает примерно 40% инфарктов мозга при стенозе и
тромбозе экстракраниальных артерий. В экстракраниальных артериях наибо-
лее ярко прослеживается преимущественная локализация атеросклеротических
бляшек в участках бифуркаций артерий.
Атеросклеротическая ангиопатия интрацеребральных артерий проявляется
в виде пере калибровки артерий в результате редуцированного кровотока по ним,
обусловленного атеростенозом экстрацеребральных и интракраниальных арте-
рий, особенно при эшелонированном стенозе.
На определенном этапе эволюции и прогрессирования атеросклеротичес
кой ангиопатии головного мозга возникает существенное снижение или пре-
кращение локального мозгового кровотока, что приводит к очаговой или рас-
пространенной гипоксии и ишемии мозга с его структурными изменениями,
различными по локализации, тяжести и протяженности. Возникает картина
атеросклеротической ангиоэнцефалопатии, которая клинически проявляется
в виде определенных симптомов и синдромов. Изменения мозга имеют диф-
фузный или очаговый характер и варьируют от ишемических изменений от-
дельных нервных клеток до инфарктов мозга различной величины, локализации
и степени давности.
Наиболее распространенным и тяжелым по своим последствиям среди сосу-
дистых поражений головного мозга является инсульт, летальность при котором
нередко выше, чем при инфаркте миокарда, а перспективы восстановления тру-
доспособности весьма ограничены.
Ишемические инсульты при атеросклерозе характеризуются большим раз-
нообразием форм и механизмов развития. При анализе патогенеза необходи-
мо учитывать результаты исследований всей многоуровневой артериальной си-
стемы мозга: магистральные артерии головы, сосуды основания мозга, арте-
рии конвекситальной и медиальной поверхностей полушарий мозга, его ствола
и мозжечка, интрацеребральные артерии, а также сосуды микроциркулятор
ного русла.
Инсульт является исходом многих различных по характеру патологических
состояний системы кровообращения. При этом общими для них в итоге стано-
вятся лишь территория и структуры мозга, в которых развертывались финаль-
ные деструктивные процессы, тогда как патогенез их был различен и до настоя-
щего времени не всегда ясен. Помимо атеротромботического и артериоартери
ального эмболического генеза возможно гемодинамическое происхождение
инфарктов, развивающихся по механизму сосудистой мозговой недостаточно-
сти при патологии экстракраниальных отделов магистральных артерий головы.
В рамках концепции гетерогенности ишемического инсульта были установле-
ны и другие столь же часто встречающиеся причины инфарктов мозга. К ним
были отнесены изменения мелких внутримозговьтх артерий, характерные преж-
де всего для артериальной гипертензии (АГ). Типичные клиническая картина,
морфология, КТ и МРТ изменения (преимущественно в белом веществе моз-
га) определили клиническую обособленность --- лакунарный инсульт. Однако
вскоре было показано, что наряду с гипертоническими малыми глубинными (ла
кунарными) инфарктами, обусловленными характерными для артериальной
гипертензии изменениями стенок мелких внутримозговых перфорирующих ар-
терий, причинами возникновения этих инфарктов могут быть также (хотя и реже)
стенозирующий эшелонированный атеросклероз экстра и интракраниальных
артерий, артериоартериальная и кардиогенная эмболия этих артерий, васкули
ты, нарушения общей и церебральной гемодинамики, изменения реологических
свойств крови.
В настоящее время установлено многофакторное повреждающее действие
артериальной гипертензии на сосуды и головной мозг, что приводит не только
к развитию острых (плазморрагии, фибриноидный некроз, милиарные аневриз-
мы) и хронических (гиалиноз, склероз) изменений мелких интрацеребральных
артерий, но и к разрушению эластического каркаса магистральных артерий
головы и образованию деформаций с септальными стенозами. Она также уско-
ряет темпы прогрессирования атеросклеротических изменений экстра и инт-
ракраниальных артерий. Давно известно, что артериальная гипертензия явля-
ется ведущей причиной кровоизлияний в мозг и острой гипертонической энце-
фалопатии. В последние годы убедительно показано, что она столь же часто
приводит к возникновению различных форм острых и хронических ишемичес
ких НМК, в первую очередь малых глубинных (лакунарных) инфарктов мозга
и субкортикальной атеросклеротической энцефалопатии, лежащей в основе со-
судистой деменции бинсвангеровского типа.
В настоящее время установлено, что полиморфизм инсульта как клиничес-
кого синдрома зависит не только от разнообразия непосредственных причин,
приводящих к развитию инфаркта мозга, но и от патофизиологических особен-
ностей этого процесса. Кпоследним относятся: темпы формирования инфаркта
мозга (медленно нарастающий тромбоз или внезапная закупорка крупного со-
суда эмболом), состояние коллатерального кровообращения, калибр окклюзи
рованного сосуда и протяженность закупорки, состояние общей гемодинами-
ки, артериального и перфузионного давления, цереброваскулярная реактивность
и механизмы ауторегуляции, изменения реологических свойств крови. Различ-
ные патофизиологические механизмы, в свою очередь, определяют локализацию
и величину очага ишемии, характер морфологических изменений мозга в зоне
ишемии (полный и неполный некроз), а также наличие и размеры зоны ишеми
ческой полутени. Кроме того, величина обратимого и необратимого поврежде-
ния мозга в значительной степени зависит от состояния гемодинамического,
коллатерального, перфузионного и метаболического резервов мозга. Все эти фак-
торы в совокупности обусловливают клинический полиморфизм ишемическо
го инсульта --- различия как в особенностях начала и течения (внезапное, посте-
пенное, ступенеобразное, флюктуирующее, прогрессирующее), так и в исходе
инсульта.
Надо отметить, что выявление всех этих факторов до настоящего времени
является трудной задачей как для клиницистов, так и для специалистов лучевой
диагностики. Данные литературы разноречивы, до сих пор четко не определено
место каждого из методов в диагностике как структурно морфологических из-
менений, так и функциональных нарушений гемодинамики, влияющих на те-
чение и исход заболевания.
Таким образом, гетерогенность ишемического инсульта не только на уровне
вызывающих его развитие причин и факторов, но и на всей протяженности его
патофизиологических последствий, вплоть до структурного и функционально-
го исхода, вызывает необходимость тщательного выявления и изучения особен-
ностей течения заболевания в каждом конкретном случае.
Вопрос обратимости ишемических очагов при различных видах церебровас
кулярной патологии, разработка эффективных методов консервативного и хи-
рургического лечения имеет исключительное значение. Последние 10---15 лет
характеризуются существенным углублением наших представлений о патоге-
незе ишемических нарушений и расширением возможностей лучевой диагно-
стики. В результате многочисленных патофизиологических исследований
возникла концепция о существовании «нейрофизиологически молчащих кле-
ток», которые могут сохраняться относительно длительный период времени
в условиях снижения перфузии. Продолжительность времени переживания
нейронов при критическом уровне кровотока остается до конца невыяснен-
ной. Однако считается, что возвращение кровотока к нормальным значени-
ям может приводить к восстановлению функции нейронов. Эта зона «ленивых
нейронов», окружающих очаг инфаркта, получила специальное название ---
полутень, или пенумбра (penumbra). Концепция ее существования послужи-
ла активным стимулом к разработке методов изучения ишемизированной тка-
ни. Успехи в области изучения церебральной ишемии привели к углублению
представлений о сложных взаимосвязанных каскадных патобиохимических
реакциях, приводящих в короткий промежуток времени сначала к обратимо-
му функциональному, а при увеличении продолжительности ишемии --- к не-
обратимому повреждению мозга.
В связи с этим получила дальнейшее развитие концепция «окна терапевти-
ческих возможностей» --- отрезка времени, непосредственно следующего за раз-
витием инсульта, в течение которого проведение адекватной терапии может
уменьшить необратимые изменения мозга и улучшить исход инсульта. В преде-
лах этого периода выделяют «реперфузионное окно» --- период, во время которо-
го церебральная рециркуляция может обеспечить полное восстановление функ-
ции, а также «цитопротекторное окно», в течение которого назначение цитопро
текторов может обеспечить уменьшение выраженности необратимых изменений
ткани мозга. Показано, что назначение цитопротекторов в первые 4---6 часов
после развития ишемического инсульта может предотвратить необратимые из-
менения вещества мозга в области «ишемической полутени», несмотря на сохра-
няющуюся недостаточность мозгового кровотока. «Реперфузионное окно» оп-
ределяется тем же периодом времени, что и «цитопротекторное окно». Оно ис-
пользуется для восстановления проходимости закупоренной церебральной
артерии и обеспечения кровотока в очаге ишемии, в первую очередь и с наиболь-
шим эффектом --- в зоне ишемической полутени.
Вышеизложенное свидетельствует о решающем влиянии фактора времени на
развитие последствий ишемии мозга. Это требует специальных подходов к ди-
агностике в острейшем периоде инсульта, в период критического состояния боль-
ного. Однако многообразие и сложность методов, применяемых для обследова-
ния таких пациентов, затрудняют их активное внедрение в практическую меди-
цину. В большинстве своем эти методы трудоемки, сложновыполнимы, доступны
для применения лишь в специализированных, хорошо оснащенных лаборато-
риях, что не всегда достижимо, учитывая тяжесть состояния больного и неболь-
шой временной интервал, в течение которого исследование должно быть прове-
дено. Все это требует поиска более простых, доступных методик, которые могут
быть выполнены в большинстве неврологических клиник, располагающих стан-
дартными методами лучевой диагностики.
Несмотря на то, что клиническая диагностика инсульта хорошо разработа-
на, она не решает таких важных задач как определение протяженности пораже-
ния и прогноза. В связи с этим современная диагностика инсульта обязательно
включает в себя методы нейровизуализации.
Таблица 7.1
Причины развития инсультов у пациентов молодого возраста
Причина
о//о
инсультов
Факторы риска
Характерные данные KT,
MPT
Атеросклероз
5 20
Курение,
гиперлипидемия
Стеноз ВСА
Кардиогенная
эмболия
20 35
Множественные
периферические инфаркты
Расслоение
артерии
5 25
Фибромаскулярная
дисплазия,
коллагенозы
Повышение интенсивности
периартериального сигна-
ла на МР изображениях,
стенозы, окклюзии,
псевдоаневризмы
Синус
тромбоз
5
Беременность,
дегидратация,
гиперкоагулопатия
Дефект наполнения на КТ
и МРТ изображениях,
отсутствие сигнала при МР
венографии, субкортикаль-
ные инфаркты
Наркомания
5
Амфетамин, кокаин Кровоизлияния,
лакунарные инфаркты
Серповидно
клеточная
анемия
LO
Сужение и окклюзии
супраклиноидного отдела
ВСА
Васкулит
5
Наркомания,
воспалительные
изменения в
сосудистой стенке
Перемежающееся сужение
и расширение артерий на
ангиограммах, многоочаго-
вые изменения,кровоизли-
яния, инсульты
В последние годы большое значение приобретает диагностика ишемических
инсультов у пациентов молодого возраста (до 45 лет). По данным J.Bogousslavsky
(1987), примерно 12% первых ишемических инсультов происходит у больных
45 лет и моложе. Однако факторы риска, этиология и прогноз существенно от-
личаются от таковых у пациентов пожилого возраста. Атеросклероз (обычно в со-
четании с гиперлипидемией, курением и артериальной гипертензией) выявля-
ются у 5---20% пациентов молодого возраста. Однако другие факторы риска,
такие, как наркомания и синус тромбоз, нередко возникающий при беремен-
ности, гораздо чаще встречаются в этой возрастной группе (табл. 7.1).
КГ И МРТ ДИАГНОСТИКА ИШЕМИЧЕСКИХ ИНСУЛЬТОВ
Из всех методов нейровизуализации компьютерная рентгеновская томогра-
фия как метод диагностики инфаркта получила наибольшее распространение.
КТ обладает принципиальными преимуществами перед результатами невроло-
гического обследования. Так, поданным В.А.Карлова (1996), количество оши-
бочных клинических диагнозов в острой стадии геморрагического инсульта раз-
личалось от ошибочных диагнозов по результатам КТ в 8,5 раз --- соответствен-
но 17% и 2%. При ишемическом инсульте аналогичные показатели различались
в 2 раза --- соответственно 15% и 8%.
В большинстве неврологических клиник мира, даже имеющих магнитно ре-
зонансные томографы, КТ остается основным скрининговым методом иссле-
дования у больных с ОНМК. По данным литературы, возможности КТ диагно
стики выросли за последние годы с 56% до 95% у больных с полушарными ин-
сультами. В работах последних лет говорится даже о почти стопроцентной
диагностике острых инсультов, что сравнимо с данными МРТ. Однако анализ
литературы показал, что эти данные были получены лишь при исследовании
возможностей обнаружения обширных корково подкорковых инсультов (Уор
лоуЧ., 1999).
Первостепенное значение имеют сроки выявления ишемического поражения
мозга. В течение первого десятилетия существования КТ визуализация инфар-
кта была ограничена техническими возможностями. Считалось необычным при
церебральном инфаркте видеть патологические изменения на компьютерных
томограммах головного мозга ранее, чем через 24---48 часов после начала. Поз-
же, с развитием новых технологий КТ, стали выявляться едва уловимые, ранние
признаки церебрального инфаркта (рис. 7.14).
Симптом повышения плотности артерий --- ранний косвенный признак ише-
мического инсульта. При этом острая окклюзия крупной мозговой артерии про-
является в виде увеличения плотности ее изображения (рис. 7.15). Многие авто-
ры настаивают на важности выявления этого симптома, являющегося, по их мне-
нию, индикатором тромбоза ВСА, но надежность его сомнительна. Он часто
сопутствует обширным инфарктам, однако, по данным ряда авторов, не связан
с прогнозом плохого исхода: 20% пациентов с этим симптомом поправлялись
в течение двух недель.
Рис. 7.14. Изменения
на компьютерных
томограммах
в разные сроки
ишемического
инсульта (по Р.Ьавде).
100
80
60
40
20
ни
Mass effect
in 25%
--- Postcontrast
--- Precontrast
Hyperdense
Г"
Fluid density
Hypodense
14 21 days
2 months
Phase 1
Phase 2
Phase 3
К ранним симпто-
мам полушарного ише-
мического инсульта
многие авторы также
относят утрату возмож-
ности визуализации
островка и исчезновение нормальных очертаний лентикулярного ядра, утрату диф
ференцировки серого и белого вещества и сглаженность корковых извилин
(рис. 7.16).
Небольшие инфаркты выяатяются позже, чем большие, т. е. вероятность вы-
явления лакунарных инфарктов в течение первых 24 часов мата. В литерату-
ре также указывается на трудность обнаружения при КТ небольших инфар-
ктов ствола и мозжечка из за артефактов, возникающих от пирамид височ-
ных костей.
Для второй стадии эволюции инфаркта мозга характерны нарастающий отек,
начало распада некротизированной ткани. Ее продолжительность составляет до
8 суток. При КТ исследовании в этот период определяются снижение плотнос-
ти в пределах инфаркта. Причем в белом веществе определяется наиболее низ-
кая плотность мозговой ткани.
Третья стадия эволюции инфаркта начинается с 9 х и продолжается до 21 х
суток. Для нее характерно сначала изоденсивное, а затем гиподенсивное состо-
яние ткани мозга. Изоденсивное состояние, продолжающееся 8--- 12 или 9--- 14 су-
ток, объясняется так называемым эффектом затуманивания, который отражает,
по видимому, уменьшение отека в области инфаркта. Развивающееся с 15 х суток
гиподенсивное состояние обусловлено массивным скоплением зернистых шаров.
В инфарктах с геморрагическим компонентом в эти сроки могут определять-
ся зоны повышенной или гетерогенной плотности ткани, что отражает наличие
множествен н ых кровои злия НИИ.
Четвертая стадия эволюции инфаркта характеризуется завершением репа
ративных процессов и формированием глиомезодермального рубца с полос
а
б
Рис. 7.15. КТ головного мозга.
а --- тромбоз правой средней мозговой артерии; б --- территориальный инсульт в бас-
сейне правой СМА.
тью --- псевдокисты. Эта псевдокиста при КТ соответствует области мозга со
стабильно низкими показателями плотности, близкими к коэффициентам по-
глощения цереброспинальной жидкости (позднее гиподенсивное состояние).
Однако надо заметить, что возможности КТ в диагностике острых ишеми
ческих инсультов ограничены. Именно поэтому МРТ в последнее время особен-
но привлекает внимание исследователей, учитывая ее физические основы, от-
сутствие лучевой нагрузки, получение томограмм в любых заданных плоскостях,
отсутствие артефактов от костей в области задней черепной ямки. Преимуще-
ства М РТ перед КТ хорошо известны. Вопрос о целесообразности применения
МРТ или КТ на первом этапе диагности
^_
_
,
ки определяется, помимо доступности,
В
4
точкой зрения исследователей на эффек
¥
5^ ^1
тивность этих методов. Некоторые авто
Рис. 7.16. КТ головного мозга.
Ранние косвенные признаки ишемичес
кого инсульта в правой лобно теменной
области (1 сутки).
ры свидетельствуют о практически одинаковой чувствительности КТ и МРТ
в выявлении ишемических инсультов. В других исследованиях утверждается, что
в остром периоде клинически явного ишемического инсульта КТ выявляет из-
менения только в 50% случаев. КТ хуже, чем МРТ, позволяет визуализировать
очаг при небольших глубинных инсультах и инфарктах в области задней череп-
ной ямки.
Данные литературы убедительно свидетельствуют о гораздо большей чувстви-
тельности и точности диагностики ишемических инсультов в ранние сроки с ис-
пользованием МРТ, которая существенно расширяети дополняет диагностические
возможности КТ. Так, признаки острой очаговой ишемии мозга при МРТ опре-
деляются уже в первые 6 часов от момента развития ишемии, т. е. задолго до ви-
зуализации изменений с помощью КТ. Это объясняется тем, что уже самые ран-
ние стадии церебральной ишемии сопровождаются увеличением содержания воды
в ткани мозга.
Самыми ранними ишемическими изменениями, воспринимаемыми с помо-
щью обычной МРТ, являются: исчезновение нормальной «пустоты потока» в ар-
терии, соответствующей симптоматике (в пределах нескольких минут после
начала), что равнозначно симптому повышения плотности артерии при КТ. Так,
в литературе описы ваются случаи его выявления в момент остановки сердца во
время проведения МРТ.
На обычных Т1 и Т2 ВИ большие инфаркты часто видны уже в пределах
6 часов (рис. 7.17). Диффузионно взвешенное изображение может выявить от-
клонения в пределах нескольких минут от начала, но эта методика широко не
применяется в клинической практике. В пределах первых суток изменения на
MP томограммах выявляются у 90% больных с инсультами. Методика МРТ спо-
собна хорошо выявлять небольшие инфаркты, особенно лакунарные. МРТ бо-
лее чувствительна, чем КТ, к небольшим очагам поражения в стволе и задней
черепной ямке из за отсутствия артефактов от костей. Однако КТ в равной сте-
пени с МРТ может успешно выявлять ранние ишемические изменения при по
лушарных инсультах.
В связи с тем, что ишемические инсульты составляют 80% в структуре всех
НМК, приоритетным направлением исследований в области ангионеврологии
стало изучение патофизиологических и нейрохимических механизмов развития
очаговой ишемии мозга, включая изучение ее эволюции во времени --- от момента
возникновения до развития необратимых изменений. В связи с высокой чувстви-
тельностью нервных клеток к гипоксии все эти исследования проводятся с уче-
том важной проблемы ургентной ангионеврологии --- проблемы предупреждения
необратимого поражения мозга в первые часы развития ишемии, в пределах так
называемого терапевтического окна. Поэтому целесообразно было бы начинать
диагностический процесс на уровне выявления патологических факторов, т. е.
когда еще страдает только микроциркуляция и происходят первые метаболичес-
кие изменения. Этой цели служат несколько методов: определение перфузии с по-
мощью МРТ и однофотонной эмиссионной томографии (ОФЭТ), оценкадиф
фузии, исследование распределения и концентрации метаболитов с помощью
ПЭТ и МР спектроскопии.
Кровоток мозга контролируется комплексом ауторегуляторньгх механизмов,
способных поддерживать снабжение кислородом и глюкозой при широком спек-
тре физиологических состояний. Принципиально механизм основан на мест-
ных изменениях сосудистого сопротивления посредством расширения так на-
зываемых резистивных сосудов (артериол, прекапилляров). Расширение сосу-
дов вызывает вторичное расширение капиллярного ложа и дренирующих вен.
Это дает возможность поддерживать кровоток мозга (СВР) вплоть до давления
70 мм рт. ст., но при давлении ниже этого уровня кровоток мозга снижается. При
уменьшении кровотока кровь проходит через мозг медленнее, приводя к увели-
чению среднего времени прохождения (МТТ) и фракции экстрагируемого кис-
лорода. Вторичное расширение сосудов позволяет мозгу поддерживать метабо-
лизм кислорода до тех пор, пока артериальное давление не достигнет порядка
40 мм рт.с т. Сложность механизма ауторегуляции означает, что клинические ис-
следования кровотока в идеале должны включать индикаторы объема крови
в мозге (СВУ) и МТТ. На практике такие измерения сложны.
Позитронно эмиссионная томография, используя воду с меченым кислоро-
дом 13, позволяет получать изображения кровотока и делать абсолютные изме-
рения СВУи МТТ. Однако оборудование и радионуклиды крайне дороги, время
сканирования продолжительное, поэтому ПЭТ является методом ограниченно-
го применения.
Наиболее широко используемый индикатор перфузии мозга гексаметилпро
ниленамин оксим, меченный технецием 99т (99тТс --- НМРАО). Он вводится
внутривенно и захватывается нейронами, причем прямо пропорционально ме-
таболизму глюкозы. Метод отражает как региональную перфузию, так и регио-
нальную активность мозга. Радионуклид относительно долго живет и позволяет
использовать для получения изображения распределения препарата ОФЭТ. Этот
метод способен выявлять очаги поражения в пределах нескольких часов от на-
чала инсульта и демонстрирует зоны относительной гипоперфузии у большин-
ства обследованных пациентов. Однако нарушение ГЭБ при остром ишемичес
ком инсульте меняет поведение радионуклидов и предопределяет появление
ошибок в точности и интерпретации изображения. ОФЭТ дает только информа-
цию об относительных показателях распределения радионуклида и не позволя-
ет точно измерить CBF, СВУили МТТ.
Применение KT с ксеноном 133 дает возможность рассчитывать CBV и кар-
ты кровотока в мозге на стандартных спиральных аппаратах. Несмотря на от-
носительную простоту и возможности количественных расчетов, метод исполь-
зуется только в специализированных научных центрах.
Получение отображения перфузии путем МРТ с контрастирующим препа-
ратом в динамике было впервые предложено F. Villinger и J.Rosen (1988,1989). Ос-
новой для визуализации перфузии служат изменения сигнала, происходящие при
прохождении молекул гадолиния по капиллярам, расположенным внутри вок
села. По кривой концентрация --- время определяются относительный объем
крови вучастке мозга (CBV) и относительное среднее время прохождения (МТТ*).
Эти показатели отличаются в ишемизированных тканях по сравнению с нор-
мальными, что дает надежду на диагностику ишемий в сверхострую стадию,
когда может помочь тромболитическая терапия. Вместе с тем, помимо чисто тех-
нических сложностей, имеются проблемы в расчете и трактовке показателей пер-
фузии. Самые последние методические и технические достижения позволили
в значительной мере преодолеть упомянутые проблемы. С другой стороны, по-
добные усложнения исключают массовое применение методики.
В последние годы особенно велик интерес к методу получения изображений,
отражающих диффузию (DWT). Диффузия --- это проникновение молекул одного
вещества между молекулами другого вследствие хаотичного микроскопическо-
го их движения, известного как броуновское движение. Изображение оценива-
ется как визуально, так и количественно, путем расчета коэффициента диффу-
зии (ADC). Изображения, основанные на диффузии, позволяют диагностировать
ишемический инсульт уже в первые минуты. В ишемическом участке нарушается
переход ионов через клеточную мембрану, что приводит к перераспределению воды.
Она накапливается внутри клетки (цитотоксический отек), что приводит к сни-
жению ADC и увеличению сигнала в зоне ишемии. Несмотря на широкие возмож-
ности метода диффузии в раннем выявлении инсульта, применение его в практи-
ческой медицине сдерживается экономическими факторами: требуется дорого-
стоящая модернизация MP томографа и наличие в программном обеспечении ИП
эхо планарного типа.
Безусловно научный интерес имеет и изучение метаболизма в зонах ишемии
с помощью MP спектроскопии. В немногочисленных пока исследованиях
в острую стадию инсульта отмечено снижение содержания N ацетиласпартата.
Перечисленные новейшие методы нейровизуализации могут расширить
наши представления о патогенезе инсультов. Однако инсульты представляют
собой острое состояние, требующее срочного диагностического исследования.
Доставка в специализированные центры, обладающие такими техническими
возможностями, в ургентной ситуации весьма проблематична. К тому же пере-
численные методы мало подходят для проведения диагностики в предельно сжа-
тые сроки.
В связи с этим основными задачами, встающими перед КТ и МРТ, становят-
ся дифференциальная диагностика между сосудистой и несосудистой патоло-
гией мозга, ишемическим и геморрагическим инсультом. Не менее важной за-
дачей, стоящей перед методами лучевой диагностики в остром периоде НМК,
является как можно более раннее выявление объема повреждения ткани мозга,
уточнение бассейна нарушенного кровоснабжения.
МРТ контрастирование при острых инсультах пока не нашло широкого при-
менения. С 1 х по 6 е сутки выявляется внутрисосудистое и оболочечное кон-
трастирование при обширных корково подкорковых инсультах, вероятнее все-
го, связанное со снижением кровотока в сосудах, вызванным дистальным вазо
стазом, в ответ на гиперкапнию и тканевой ацидоз, и, возможно, отражающее
активацию коллатерального кровотока в зоне инсульта (рис. 7.18). Однако мне-
ния о возможных причинах этих видов накопления контрастного препарата и
их корреляция с клинической картиной и прогнозом течения инсульта крайне
противоречивы. С 3 х суток начинается паренхиматозное накопление, макси-
мально выраженное на 2---3 й неделе, механизм этого явления, вероятно, объяс-
няется повышением проницаемости ГЭБ, реваскуляризацией и нарушением
ауторегуляции кровотока.
Вопрос о необходимости применения МР
ангиографии при остром инсульте остается до
конца не решенным. С одной стороны, сроки
исследования удлиняются, что нежелательно
для пациента в тяжелом состоянии, с другой ---
в ряде случаев можно получить дополнитель-
ную информацию. До конца не ясны возмож-
ности оценки степени стенозирования сосудов,
особенно при крайних степенях стеноза, слож-
на диагностика стенозирования сосудов в ме-
стах возникновения естественной турбулентно
Рис. 7.18. Ишемический инсульт, давностью
2 суток. МРТ головного мозга, постконтрастное
Т1 ВИ. Сосудистое (тонкая стрелка) и оболочеч-
ное (толстая стрелка) контрастирование.
сти (луковица ВСА, перегибы сосудов). Противоречивы данные различных ав-
торов, сопоставлявших диагностические возможности MP ангиографии, дуп-
лексного сканирования, транскраниальной допплерографии (ТКДГ) и рентге
ноконтрастной ангиографии в выявлении стеноза. До настоящего времени ос-
тается открытым вопрос, может ли комплексное использование МРА,
дуплексного сканирования и ТКДГ применяться в качестве неинвазивных ме-
тодик выявления каротидных стенозов, приближающихся по точности к стан-
дартной рентгеноконтрастной ангиографии (рис. 7.19).
Важными представляются проблемы организации инсульта и, следователь-
но, диагностики инфарктов в поздние сроки. В эти сроки большое значение при-
обретают вопросы дифференциальной диагностики инфарктов и, кроме этого,
вопросы корректной опенки постинсультных изменений. Как известно, форми-
рование псевдокисты начинается с 21 х суток. Организация мелких инфарктов
завершается к 1 --- 1,5 месяцам, крупных --- значительно позднее. Например, яв-
ляется спорным вопрос об увеличении сроков организации инфарктов и возмож-
ных причинах этого явления. До настоящего времени не решена проблема диаг-
ностики инфарктов одной и той же локализации, когда в пределах крупных све-
жих и организующихся инфарктов находятся инфаркты меньшего объема, но
большей давности. В литературе недостаточно полно освещен вопрос о диагно-
стике вторичной дегенерации волокон белого вещества, прерванных инфарк-
том --- дегенерации Тюрка --- Валлера, которая прослеживается на разных уров-
нях полушарий, ствола мозга и спинного мозга, но часто недостаточно правиль-
но интерпретируется исследователями.
Таким образом, для первых трех стадий эволюции полушарного инфаркта
характерны сначала косвенные КТ симптомы инфаркта в виде симптома по-
вышения плотности артерии (симптом гиперденсивной артерии), ухудшения
визуализации островка и лентикулярного ядра, утраты возможности дифферен
цировки белого и серого вещества, сглаженности извилин с появлением в более
поздние сроки (6---24 часа в зависимости от объема инфаркта) различного по
степени выраженности снижения плотности мозгового вещества в зоне инфар-
кта. В инфарктах с геморрагическим компонентом в эти сроки могут определять-
ся зоны повышенной или гетерогенной плотности ткани, что отражает наличие
множественных кровоизлияний.
Выявление ишемических изменений на КТ и МРТ изображениях в ранние
сроки зависит от многих патофизиологических факторов, которые часто соче-
таются (табл. 7.2).
Острое нарушение церебральной гемодинамики (так называемый феномен
нарушение кинематики потока) может быть обнаружено при МРТ немедленно
при его возникновении. Оно выявляется в виде исчезновения нормальной пус-
тоты потока от крупного артериального ствола и сосудистого усиления после
введения контрастного вещества, связанного с замедлением кровотока в неболь-
ших артериях, артериолах. В нашем исследовании феномен исчезновения нор-
мальной пустоты потока выявлялся в ранние сроки (первые 6 часов) во всех слу-
чаях тромбоза ВСА, подтвержденного затем при дигитальной субтракционной
ангиографии (ДСА). Этот феномен лучше выявлялся на Т2 ВИ из за высокой
В
Г
Рис. 7.19. Болезнь моя моя. Больная 3., 2 года. МРТ.
а --- FLAIR ИП, аксиальная плоскость;
б --- постконтрастное Т1 ВИ, корональная плоскость;
в, г --- МР ангиография, 3D TOF, аксиальная, корональная плоскость.
Нарушение мозгового кровообращения по ишемическому типу в кортикальных и
субкортикальных отделах обеих гемисфер мозга. Изменения характеризуются ги-
перинтенсивным сигналом на FLAIR ИП (а), интенсивно накапливают контраст-
ное вещество (б). Отмечается сглаженность извилин теменных долей.
В левом каротидном бассейне отсутствует изображение всех отделов средней моз-
говой артерии, начиная от развилки внутренней сонной артерии, а в правом сохра-
няется узкий просвет Ml, что обеспечивает избирательное заполнение кровью не-
которых ветвей средней мозговой артерии. На фоне резкого обеднения сосудисто-
го рисунка сосуды, отходящие от сифона внутренней сонной артери (хороидальные
артерии) и от начальных участков передних мозговых артерий (лентикулостриар
ные и перфорантные артерии), имеют избыточный калибр и извитой ход (в, г).
Динамика лучевых проявлений ишемических инсультов
Таблица 7.2
МРТ
Масс
Контрастирование
Наличие геморрагии
Сроки
КТ плотность
интенсивность
эффект
Границы
КТ
МРТ
КТ
МРТ
1 сутки Снижается посте-
ТТ2
В зависи- Нечеткие
---
Артериальное,
Макси-
Т2/Т1
пенно в зависимости (через 8 ч)
мости от
позже менинге
мальное
Ш
от объема, нечет-
4, Т1
объема
альное, паренхи-
повыше-
кость границы серое (через 16 ч) (уже через
матозное
ние плот-
/ белое вещество ---
50 70%. Повышена Из за цитоток
сического оте-
2 4 ч, луч-
ше виден
ности
плотность крупного
ка
на Т1 ВИ)
артериального ство-
ла (при тромбозе) ---
35 50%
1 не- Снижена гомогенно ТТ2
Макси-
Более
Корти-
Артериальное,
Постепен- ТТ1
деля
1л
мальный четкие
кальное
менингеальное,
паренхиматозное
но снижа-
ется
1 ме- Дальнейшее сниже- Варьирует в
Постепен- Становятся Корти-
Выраженное
Переста- ТТ1
сяц
ние при инсультах в
белом веществе,
при инсультах в ко-
ре --- изоплотные
зависимости
от объема,
наличия ге-
моррагии
но умень-
шается
неровными
кальное
паренхиматозное
ет визуа-
лизиро-
ваться
Более Снижена
ТТ2
Атрофия, Четкие
---
Паренхиматозное Снижение I Т2
1 ме-
4. Т1
кисты, ак
усиление посте-
плотности (гемоси
сяца
сональ
ная деге-
нерация
пенно исчезает
в сроки, завися-
щие в основном от
объема ишемии ---
обычно более 1 2
месяцев)
дерин,
персисти
рующий
метгемо
глобин)
Примечание: Т --- гиперинтенсивный сигнал; гипоинтенсивныи сигнал.
чувствительности к движению при больших ТЕ и из за хорошего разрешения
между низкой интенсивностью сигнала от сосуда и высокой --- от окружающих
сосуд ликворсодержащих пространств. Этот феномен выявлялся и при КТ в виде
повышения плотности артерии, однако, с нашей точки зрения, специфичность
его при КТ гораздо меньше, и он может быть ложноположительным.
Наличие сосудистого контрастирования в ранние сроки инсульта также по-
вышает точность и специфичность диагностики нарушения мозгового крово-
обращения, особенно в острейшем периоде. Оно выявляется в виде усиления сиг-
нала от сосудов --- как крупных, так и более мелких кортикальных артерий. Ве-
роятнее всего, этот феномен связан с замедлением кровотока вокруг зоны
инфаркта. Сопоставление с данными других методов --- ДСА, ТКДГ --- показа-
ло, что, наличие сосудистого усиления свидетельствует о максимальном раскры-
тии сосудов пиал ьно капиллярной сети в ответ на гипоксию головного мозга,
приводящего к снижению цереброваскулярного резерва. Этот феномен удалось
выявить у больных с окклюзией крупного магистрального ствола и с наличием
ретроградного коллатерального кровотока либо при гемодинамически значимом
стенозе с замедлением антеградного кровотока. В случае адекватного кровото-
ка дистальнее стеноза, выявленного при ТКДГ, выявить сосудистое усиление
в остром периоде ишемического инсульта не удается.
Надо отметить, что во всех случаях появления этого феномена инсульт обя-
зательно захватывал кору. Ни в одном случае изолированного глубокого инфар-
кта выявить усиление сигнала от терминальных ветвей, кровоснабжающих эти
зоны, нам не удалось. По видимому, это связано с их меньшими размерами, а,
возможно, и с различиями в ангиоархитектонике серого и белого вещества. Из-
вестно, что белое вещество обеспечивается наиболее дистальными ветвями це-
ребральных артерий, у которых коллатерали развиты слабо или отсутствуют,
и поэтому, с одной стороны, эти зоны наиболее чувствительны к редукции моз-
гового кровотока, а с другой, ввиду малых размеров и отсутствия коллатералей,
хуже визуализируются при введении контрастирующего вещества. Наилучшим
образом наличие сосудистого контрастирования выявляется на Т1 ВИ в акси-
альной проекции, что обусловлено ходом сосудов.
Сосудистое усиление выявляется в сроки от 2 часов до 21 суток от начала
заболевания. Исчезновение сосудистого усиления обычно сопровождается по-
явлением выраженного паренхиматозного контрастирования, что, вероятно, оп-
ределяется несколькими механизмами --- пролиферацией коллатеральных сосу-
дов в очаге, а возможно, и реканализацией тромбированной артерии.
С учетом вышеизложенного выявление сосудистого усиления свидетельствует
о наличии плохого коллатерального кровообращения у больных с окклюзиями
и гемодинамически значимыми стенозами и, следовательно, может служить
индикатором тяжести инфаркта и худшего прогноза заболевания. С нашей точ-
ки зрения, этот симптом можно использовать в качестве одного из критериев от-
бора больных на проведение тромболизиса.
В эти же сроки нередко выявляется так называемое менингеальное усиление,
или контрастирование по оболочкам. Возможно, этот тип контрастного усиле-
ния по механизму развития сходен с сосудистым усилением и свидетельствует
о замедлении кровотока в оболочечных сосудах, так как этот симптом выявлял-
ся только при инсультах в коре.
Для развития и, соответственно, выявления при МРТ морфологических (био-
физиологических) изменений должно пройти время. К биофизиологическим
изменениям при остром ишемическом инсульте, выявляемым при МРТ, следует
отнести:
--- проявления масс эффекта наТ1 ВИ, связанные с развитием цитотокси
ческого отека (2---4 часа);
--- изменения сигнала на Т2 ВИ, связанные с нарушением ГЭБ, вазогенным
отеком, макромолекулярным связыванием (8 часов);
--- изменения сигнала наТ1 ВИ, обусловленные нарушением ГЭБ, вазоген-
ным отеком, макромолекулярным связыванием (16---24 часа).
Изменения сигнала на Т1 ВИ, связанные с цитотоксическим отеком, явля-
ются одним из наиболее ранних MP симптомов острого ишемического инсуль-
та. Вопрос о причинах набухания ткани мозга при отсутствии изменений сигна-
ла до конца не ясен. Мы разделяем точку зрения M.Brant Zavadzki, что эти из-
менения определяются развитием цитотоксического отека с увеличением
количества внутриклеточной жидкости, свободной от макромолекул и белков,
причем перемещение жидкости из сосудистого русла внутрь клетки увеличива-
ет количество жидкости в среднем не более чем на 3%, что, возможно, и опреде-
ляет отсутствие изменения сигнала на Т1 ВИ.
Выявление масс эффекта в эти сроки в основном определяется объемом зоны
ишемии. При кортикальных инсультах можно видеть сдавление борозд, причем
эти изменения наилучшим образом выявляются на Т1 ВИ, что связано с луч-
шим разрешением между ликворсодержащими пространствами и корой. При
обширных кортикально субкортикальных инсультах эти изменения нередко
сочетаются и со сдавлением срединных структур.
Изменения сигнала на Т2 ВИ обычно выявляются не ранее 8 часов от начала
заболевания. До конца не ясно, почему повышение сигнала на Т2 ВИ возника-
ет не сразу. По видимому, это определяется развитием внеклеточного набухания
или вазогенного отека, причиной которых является нарушение ГЭБ, что сопро-
вождается перемещением воды, макромолекул и белков во вне и внутриклеточ-
ные пространства, и требует определенного времени (см. табл. 7.2).
Изменения сигнала на Т1 ВИ являются наиболее отсроченными. Однако,
с нашей точки зрения, ценность этих изменений неоспорима. НаТ1 ВИ выяв-
ляется не только снижение сигнала, связанное с наличием отека, но и повыше-
ние его, которое определяется как ранней диапедезной геморрагией в зону ише-
мии, так и наличием большого количества белка в зоне некроза паренхимы, что
опять таки указывает на возможность развития вторичной геморрагии в эту зону
впоследствии.
Раннее паренхиматозное усиление указывает на раннее нарушение ГЭБ и
(или) наличие локальной гиперемии.
По данным литературы, паренхиматозное усиление обычно не выявляется
ранее 6 х суток, часто имеет место на протяжении подострой стадии (7---30 е сут-
ки) и постепенно исчезает во время хронической стадии (более 30 суток). Ра
ционально выделять две группы пациентов с наличием паренхиматозного уси-
ления:
--- с типичным вариантом, описанным выше;
--- с вариантом раннего паренхиматозного усиления.
Два этих варианта отражают патофиологические изменения, возникающие
в очаге ишемии, описанные C.Virapongse и соавт. (1986). Эти авторы предложи-
ли гипотетическую модель ишемического инсульта. Они разделили инсульт на
две категории: полная ишемия (с отсутствием перфузии) и неполная ишемия
(с частично сохраненной перфузией).
При полной ишемии раннего паренхиматозного усиления в зоне ишемии не
возникает из за отсутствия перфузии. При этом изменения сигнала на Т2 ВИ
возникают раньше и более интенсивны.
В отличие от этого раннее паренхиматозное усиление свидетельствует о со-
хранении перфузии в очаге и, следовательно, о неполной ишемии. У этой кате-
гории больных повышение сигнала на Т2 ВИ менее интенсивно и возникает
в более поздние сроки. Вместе с тем им чаще присуща вторичная диапедезная
геморрагия в зону ишемии из за выраженной реперфузии в этой зоне.
Наличие раннего паренхиматозного усиления при введении контрастного
вещества и позднее, слабоинтенсивное повышение сигнала на Т2 ВИ можно
рассматривать как один из критериев отказа от применения тромболизиса в ран-
ние сроки.
Изменения, которые могут быть выявлены при МРТ в ранние сроки разви-
тия острого ишемического инсульта, с объяснением возможных причин появле-
ния того или иного феномена представлены в табл. 7.3.
Данные о сопоставлении выявленных при МРТ изменений при полной и не-
полной ишемии представлены в табл. 7.4.
Таким образом, вид контрастного усиления и сроки его появления не только
помогают раскрыть патогенетические механизмы развития ишемии в каждом
конкретном случае, но и в определенной степени предопределяют исход инсуль-
та и, возможно, могут являться одним из критериев отбора больных для активной
терапии с применением эндоваскулярного тромболизиса в ранние сроки инсульта.
Информативность МРТ по сравнению с КТ в диагностике малых глубинных
(лакунарньгх) инфарктов, особенно локализующихся перивентрикулярно, в ос-
новании моста, а также в задней черепной ямке, чрезвычайно велика.
По данным литературы, в начальной стадии лакунарного инсульта соответ-
ствующие клинической симптоматике очаговые изменения мозга с помощью
МРТ могут быть выявлены в 92% случаев, тогда как КТ не выявляет каких либо
изменений у большинства больных. Лакунарные инсульты выявляются у 1/3
больных с острыми ишемическими инсультами, однако, при наличии множе-
ственных поражений только сопоставление с клинической симптоматикой и
введение контрастного вещества помогает отличить старые очаги от «свежих».
Малые глубинные (лакунарные) инфаркты представляют собой самую час-
тую форму ишемических нарушений мозгового кровообращения, обусловленных
атеросклерозом и артериальной гипертензией. Клинически эти инфаркты чаще
всего протекают в виде транзиторных ишемических атак или малого ишемичес
Таблица 7.3
Данные магнитно резонансной томографии при острых ишемических
инсультах и возможные причины развития этих изменений
Механизм
Данные МРТ
Возможные причины
Время
выявления
Изменения
кинетики
потока
Отсутствие потока
Артериальное усиление
Медленный кровоток
Первые
минуты
Биофизио-
логические
механизмы
Изменения на Т1 ВИ
в виде масс эффекта
Изменения сигнала на
Т2 ВИ
Изменения сигнала на
Т1 ВИ
Цитотоксический отек
(свободная вода)
Нарушение ГЭБ, вазо
генный отек, связыва-
ние макромолекул
Нарушение ГЭБ, вазо
генный отек, связыва-
ние макромолекул
2 4 ч
8ч
16 24 ч
Сочетание Отсроченное паренхима-
тозное усиление (типич-
но при кортикальных ин-
фарктах)
Чрезмерное и(или) ран-
нее паренхиматозное
усиление (при ТИА,
частичных окклюзиях,
инфарктах водораздела)
Ухудшение поступле-
ния контрастирующего
вещества
Поступление контраста
не изменено, наруше-
ние ГЭБ, очаговая
гиперемия
Более 24 ч
(обычно не
ранее 5 7 х
суток)
2 4 ч
кого инсульта. Такие инфаркты, как правило, находятся в стадии полной орга-
низации, т. е. в виде мелких кист --- лакун.
Характер очаговых неврологических симптомов у больных отражает ограни-
ченную локализацию инфарктов. В случаях преимущественно двигательных
нарушений при КТ и МРТ выявляются инфаркты во внутренней капсуле, бе-
лом веществе полушарий мозга, мосту и чечевицеобразном ядре. При наличии
преимущественно нарушений чувствительности очаги располагаются в задних
отделах внутренней капсулы и смежных отделах таламуса.
Однако очаговая неврологическая симптоматика, течение и исход этого вида
нарушений мозгового кровообращения зависят не только от величины и лока-
лизации инфаркта, но и в значительной степени от предшествующих и сопут-
ствующих диффузных и очаговых изменений ткани мозга. Поэтому обычно для
большинства лакунарных инфарктов, развившихся впервые, характерно бла-
гоприятное течение, при повторных же инфарктах, развивающихся у больных
с ангиоэнцефалопатией, симптоматика более выраженная.
Для дифференцирования лакунарных изменений от расширенных про-
странств Вирхова --- Робена можно выделить следующие симптомы:
1. Лакунарные инфаркты обычно выглядят как небольшие зоны понижен-
ной плотности, на МРТ изображениях --- повышенного сигнала на Т2 ВИ, чаще
Таблица 7.4
МРТ проявления полной и неполной ишемии
Полная ишемия
Данные МРТ
кортикальная
некортикальная
Неполная
ишемия (раннее /
интенсивное
усиление)
Паренхиматозное
усиление:
острая стадия
(меньше 7 сут)
подострая
стадия
(больше 7 сут)
Характер
усиления
Обычно
отсутствует
Обычно по извили-
нам (гирального
типа)
Обычно по интен-
сивности не превы-
шает сигнал на Т2
ВИ
Обычно
отсутствует
Обычно по извили-
нам (гирального
типа)
Обычно по интен-
сивности не превы-
шает сигнал на Т2
ВИ
Обычно имеется
Выражено
По интенсивно-
сти часто пре-
вышает сигнал
на Т2 ВИ
Артериальное
усиление
Часто
Нечасто
Нечасто
Клинический
исход
Инфаркт
Инфаркт
Обратимые
изменения (во
многих случаях
инфаркт в зоне
водораздела)
всего округлой и овальной формы. Они расположены в белом веществе полуша-
рий мозга, внутренней капсуле, лентикулярных ядрах, зрительном бугре и мос-
ту. Размер инфарктов обычно 10---15 мм. Инфаркты обнаруживаются к концу
1 ---2 х суток с момента развития инсульта. При этом изменение плотности и сиг-
нала не бывает интенсивным, границы нечеткие. В конце 2 й --- начале 3 й неде-
ли инфаркты могут вообще не визуализироваться на КТ изображениях, что свя-
зано с регрессом отека. Однако у всех этих больных визуализация инфаркта при
МРТ остается хорошей. Через 1---2 месяца инфаркты хорошо визуализируются,
имеют четкие границы, что обусловлено формированием небольшой псевдоки-
сты --- лакуны.
2. Расширенные периваскулярные пространства (криблюры) обычно имеют
меньшие размеры, чем лакунарные инфаркты, располагаются в типичных
местах (белом веществе полушарий, лентикулярных ядрах), имеют двусторон-
ний, множественный характер. В большинстве случаев они сочетаются с ат
рофическими изменениями мозгового вещества в виде диффузного расширения
борозд субарахноидального пространства и желудочковой системы. При на-
блюдении в динамике не выявляется изменения четкости их границ, измене-
ния плотности сигнала от них, их размеры со временем не меняются.
Возможность диагностики как ишемических, так и геморрагических изме-
нений при КТ во многом определяется сроками обследования и точность КТ ди-
агностики инсультов снижается по мере увеличения длительности заболевания.
Так, поданным D.Wardlow (1998), точную диагностику геморрагии и инфаркта
мозга при использовании КТ можно провести в течение 5 дней после инсульта.
Позже соответствующие геморрагии очаги повышенной плотности на КТ могут
исчезать, более крупные различимы в пределах примерно 2 недель. Лишь со вре-
менем плотность их вновь снижается, и они выявляются в виде кист. Однако оп-
ределить в эти сроки, какой инсульт был перенесен больным (ишемический или
геморрагический), поданным КТ затруднительно. Лишьлокализация инсульта
и характер полости (более щелевидная после перенесенных геморрагии и округ-
лая как последствие ишемии) являются недостоверными косвенными призна-
ками различия типов инсульта со временем.
К концу 1 ---2 й недели (в зависимости от объема очага) отек в области инсульта
снижается, и визуализация очага пониженной плотности может исчезнуть, что
делает зону инфаркта едва различимой (эффект «затуманивания»)
Опухоли мозга часто представляют большие трудности в плане дифференци-
ации с медленно развивающимся ишемическим инсультом --- хронической «опу
холеподобной» формой, обусловленной постепенным стенозированием крупных
мозговых артерий. При этом неврологический дефицит формируется на протя-
жении месяцев или даже нескольких лет. Основные особенности, отличающие
«опухолеподобный» вариант ишемического инсульта от опухолей, базируются на
клинической симптоматике. К ним относят постепенное прогрессирование не-
врологического дефицита, соответствующее определенному сосудистому бассей-
ну и не сопровождающееся головными болями, эпилептическими припадками.
Застойные зрительные диски не выявляются. Однако достоверная дифференци-
ация опухолей и прогрессирующих форм ишемического инсульта, основанная
только на клинических данных, невозможна. Исчерпывающую информацию,
позволяющую подтвердить или исключить наличие инфаркта или определить
локализацию и величину опухоли, дают результаты КТ, МРТ и, часто, ПЭТ.
Данные литературы и собственные наблюдения позволили нам прийти к вы-
воду, что при анализе КТ и М РТ изображений необходимо обращать внимание:
1) на соответствие зоны патологических изменений определенному сосудис-
тому бассейну;
2) на характер накопления контрастного вещества.
Нередко только исследование в динамике (с повторным проведением КТ либо
М РТ) помогает поставить правильный диагноз.
Вместе с тем оказалось, что возможности МРТ не безграничны. Метод имеет
свои преимущества и недостатки. В целом ряде случаев лишь введение контра-
стирующих препаратов помогало выявить наличие поражения и его характер.
Плохо, по сравнению с КТ, МРТ выявляет участки обызвествления и распрос-
траненность зоны костной деструкции, с наличием которой связан рост некото-
рых опухолей. На сегодняшний день эти методы дополняют друг друга, позво-
ляя более точно и с большей специфичностью характеризовать патологический
процесс.
Расслоение артерий (артериальные диссекции)
Расслоение артерий шеи обычно возникает вследствие трех причин:
1) явная травма;
2) спонтанно, без травмы;
3) при так называемой обычной травме (движения и определенные позиции
головы и шеи при активных физических упражнениях, вызывающих натяже-
ние сосудов).
Артериальные диссекции являются причиной развития 10---25% ишемичес
ких инсультов у пациентов молодого возраста. Поступление крови расслаи-
вает артериальную стенку и формирует интрамуральные гематомы. Ишеми
ческий инсульт возникает из за окклюзии истинного просвета сосуда, про-
лонгирующего тромба внутри истинного просвета, эмболии с поверхности
тромба.
Наиболее часто встречаются диссекции ВСАна шейном уровне. Приблизи-
тельно 65% диссекции позвоночных артерий встречаются на уровне тел С, "
шейных позвонков и только 15% --- в интракраниальном сегменте артерии.
КТ может быть негативной. Иногда наблюдается гиперденсивный участок
в области ВСА (расслаивающаяся аневризма).
При контрастном усилении наблюдаются истинный и ложный поток, разде-
ленные линейной полоской.
На М РТ изображениях интрамуральная гематома в острую стадию изоин
тенсивна, вподострую стадию --- гиперинтенсивнанаТ1 иТ2 ВИ (рис. 7.20).
Венозные инфаркты
Венозные инфаркты встречаются намного реже, чем артериальные. Венозные
инфаркты полезно рассматривать с двух точек зрения: наличия паренхиматоз-
ного поражения и симптомы синус тромбоза. Ключевыми дифференциальны-
ми признаками венозных инфарктов являются следующие:
Рис. 7.21. МР венография.
Локальный тромбоз в заднем отделе
верхнего сагиттального синуса.
--- локализация инсульта не
вполне соответствует бассейну оп-
ределенной артерии;
--- присутствует выраженный
перифокальный отек;
--- уже в первые часы отмечает-
ся отчетливое снижение плотности
на КГ;
--- часто в центре инфаркта на-
блюдается пальцевидное или пятнистое кровоизлияние;
--- могут выявляться симптомы синус тромбоза.
Венозный тромбоз является причиной развития 1 % ОН М К. Причина тром-
боза может быть разнообразна --- травма, инфекция, воспаление, беременность,
прием оральных контрацептивов, метаболические нарушения при дегидратации,
тиреотоксикозе, циррозе и т. д., коагулопатия, васкулиты (синдром Бехчета и
т. д.) (рис. 7.21).
а
б
Рис. 7.22. Венозный инфаркт в правой затылочной доле (большая стрелка). Тромбоз
правого поперечного синуса (маленькая стрелка). Поперечный синус справа не
визуализируется. Слева --- кровоток в поперечном синусе нормальный (стрелка).
а --- МРТ головного мозга, Т1 ВИ, корональная плоскость; б --- МР венография.
При КТ отмечаются следующие изменения:
--- повышение плотности от дурального синуса;
--- кортикальные и (или) субкортикальные геморрагии, отек;
--- при окклюзии внутренней мозговой вены наблюдается снижение плотно-
сти зрительных бугров и базальных ганглиев
При КТ с контрастированием выявляется знак «пустой дельты» --- контрас
тируется твердая мозговая оболочка, окружающая тромбированный синус (25---
30% случаев).
М РТ проявления варьируют в зависимости от стадии процесса:
В острую стадию нет феномена пустоты потока. Тромб гипоинтенсивен на 12
ВИ, изоинтенсивен наТ1 ВИ. В подострую стадию он становится гиперинтен
сивен на Т2 и Т1 ВИ.
Венозные инфаркты возникают в 50% случаев и характеризуются:
--- сдавлением борозд и извилин;
--- гиперинтенсивным сигналом на Т1 ВИ, FLAIR;
--- петехиальными геморрагиями (кортикальными, субкортикальными);
--- точечным усилением (рис. 7.22).
Алгоритм обследования больных с подозрением на венозный инфаркт.
1. КТ и КТ с контрастным усилением. При необходимости КТ венография.
2. Если данные КТ негативны, то необходимо применять МРТ с МР вено
графией.
3. Если данные все таки недостоверны, то прибегнуть кДСА.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ГЕМОРРАГИЧЕСКИХ ИНСУЛЬТОВ
Применение методов нейровизуализации в диагностике
геморрагического инсульта
Важность выявления патогенетического типа инсульта определяется тем, что
лечение, прогноз, да и последующая профилактика диаметрально различны при
ишемических и геморрагических инсультах. Кровоизлияние в мозг (внутримоз
говая гематома) --- клиническая форма ОНМК, обусловленная разрывом внут
римозгового сосуда и проникновением крови в паренхиму. Причинами крово-
излияния в мозг могут быть травмы, резкие повышения артериального давле-
ния, вторичные геморрагии в стволе и продолговатом мозге, артерииты,
коагулопатии и опухоли мозга. Перечисленные патологические процессы при-
водят к возникновению кровоизлияний при наличии предшествующих измене-
ний артерий. В подавляющем большинстве случаев это гиалиноз артерий мало-
го калибра и артериол, при котором формируются множественные микроанев-
ризмы, а иногда локальные некрозы интимы. Кровоизлияния возникают также
в зонах, где локализуются различные сосудистые мальформации.
Причины первичных внутримозговых кровоизлияний
Аневризматическая болезнь
Геморрагический инфаркт (артериальный, венозный)
Гипертензивное, атеросклеротическое кровоизлияние
Опухоли (первичные, метастатические)
Черепно мозговая травма
Васкулит
Сосудистые мальформации
Амилоидная ангиопатия
Лекарственные средства (кокаин, амфетамин, фенилпропраноламин)
Гематологические заболевания:
Дефицит антитромбина III
Дефицит протеина С + S
Антифосфолипидные антитела
Дефицит фактора 7
Дефицит фактора 8
Дефицит фактора 9
Дефицит фактора Виллебранда
Коагулопатии
Тромбоцитопения
Уремия
Миеломная болезнь
Лейкемия
Ишемические инсульты и первичные мозговые кровоизлияния --- инсульты
с различными причинами, прогнозом в отношении выживания и повторения и
различными подходами к терапевтическому и хирургическому лечению, поэто-
му самой важной и первоочередной задачей, стоящей перед методами лучевой
диагностики, является разграничение этих двух состояний. И хотя клиничес-
кие данные могут оказать определенную помощь, большинством авторов в на-
стоящее время признается, что «золотым стандартом» для их разграничения яв-
ляются КТ и МРТ.
Сразу же после кровоизлияния при КТ исследовании отмечается возраста-
ние плотности до примерно 80 ед. X, что, по видимому, является следствием как
повышения содержания гемоглобина, так и структуры неподвижной крови (или
сгустка). Эта область обычно окружена различной по размерам зоной понижен-
ной плотности, появляющейся вследствие сочетания отека и ишемии сдавлен-
ной ткани мозга. Кроме этого, внутримозговые гематомы дают масс эффект,
зависящий от их размера и локализации. Вследствие распада гемоглобина плот-
ность гематомы уменьшается со временем, становясь идентичной плотности
мозгового вещества в сроки от нескольких дней до нескольких недель, и в это
время КТ диагностика геморрагии становится крайне затруднительной.
Изображение геморрагии при М РТ зависит от парамагнитных свойств про-
дуктов распада гемоглобина. К настоящему времени имеются многочисленные
публикации, описывающие картину кровоизлияния при МРТ в разные сроки
от начала заболевания (табл. 7.5; рис. 7.23,7.24). Более того, МРТ, очевидно, луч-
ше, чем КТ, позволяет выяснить причину внутримозгового кровоизлияния. МРТ
прекрасно выявляетартериовенозные мальформации, аневризмы, тромбоз ве
Таблица 7.5
Динамика КТ и МРТ изменений при геморрагических инсультах
МРТ
Сроки
КТ
Т2 ВИ
Т1 ВИ
Масс
эффект
1 сутки
Плотность резко
повышена
Гипер , в центре
гипоинтенсивный
сигнал
Чаще
изоинтенсивно
++
1 неделя Плотность
умеренно
повышена
То же
Кольцо гиперин-
тенсивного
сигнала
+
1 месяц Плотностные
характеристики
зависят от объема
То же
То же
+
Более
1 месяца
Плотность снижена Гемосидерин ---
гипоинтенсивен
---
Примечание: ++ --- выраженные изменения;
+ --- умеренно выраженные изменения;
изменения отсутствуют.
а
б
Рис. 7.23. Внутримозговая гематома в лентикулярных ядрах справа.
Давность заболевания --- 2 суток.
а --- Т2 ВИ, аксиальная плоскость; б --- Т1 ВИ, корональная плоскость.
В
в --- Т1 ВИ, корональная плоскость.
нозных синусов. М РТ помогает ответить на вопрос, был ли патологический очаг
инфарктом или кровоизлиянием в сроки, когда надежное разграничение этих
состояний при помощи КГ уже невозможно.
В сверхострую стадию (менее 6 часов):
В центре гематомы --- изо/гиперинтенсивый сигнал на Т2 ВИ, Т2* ВИ;
По периферии --- гипоинтенсивный сигнал на Т2 ВИ,Т2* ВИ;
Вокруг гематомы --- кольцо, обусловленное вазогенным отеком --- гипоин
тенсивное наТ1 ВИ, гиперинтенсивное наТ2 ВИ;
Снижение сигнала на Т2* ВИ примерно в случаев.
Таблица 7.6
МРТ характеристики внутримозговой гематомы
в зависимости от стадии распада гемоглобина
Время
Состав
Т1
Т2
Острейший
(< 24 часов)
Оксигемоглобин
Изотенсивная
Гиперинтенсивная
Острая (1 3 дня) Деоксигемоглобин Гипоинтенсивная Гипоинтенсивная
Ранняя подострая
(3 7 дней)
Внутриклеточный
гемоглобин
Гиперинтенсивная Гипоинтенсивная
Поздняя подост-
рая (1 2 недели) Внеклеточный
гемоглобин
Гиперинтенсивная Гиперинтенсивная
Хроническая
(более 2 х недель)
Гипоинтенсивная
гемосидерин
Гипоинтенсивная
гемосидерин
Детально изучены изменения MP сигнала в зависимости от стадии распада
гемоглобина (табл. 7.6).
Однако до настоящего времени крайне разноречивы данные о возможности
диагностики и дифференциальной диагностики первичного внутримозгового
кровоизлияния от ишемического инсульта в первые часы после инсульта. Дол-
гое время считался несомненным приоритет КТ перед МРТ при подозрении на
внутримозговое и субарахноидальное кровоизлияние. Например, J.Toole (1992)
пишет, что КТ дает возможность дифференцировать ишемический инсульт от
геморрагического в 95% случаев, а МРТ --- в 91---92% случаев. Однако в после-
днее время в литературе стали появляться упоминания об одинаковой чувстви-
тельности обоих методов как для диагностики ишемий, так и геморрагии в ост-
рейшем периоде, особенно при использовании Т2* ВИ.
До настоящего времени вызывает затруднения дифференциальная диагнос-
тика геморрагической трансформации инфаркта (так называемого геморраги-
ческого инфаркта) и первичного внутримозгового кровоизлияния. Исследова-
ния с использованием КТ и МРТ позволяют предположить, что геморрагичес-
кая трансформация той или иной степени по типу петехиалъных кровоизлияний
происходит у 15---45% пациентов, а с образованием внутриинфарктной парен-
химатозной гематомы --- у 5% больных. Результаты опубликованных исследо-
ваний (Уорлоу Ч., 1999) свидетельствуют, что геморрагическая трансформация
чаще встречается при обширных инфарктах и что ее возникновение сочетается
с менее благоприятным клиническим исходом.
Считается, что признаки перенесенной геморрагии сохраняются на МРТ
изображениях неопределенно долго, поэтому МРТ можно использовать для оп-
ределения характера перенесенного ранее инсульта. Однако эта общеприня-
тая точка зрения кажется сомнительной. В последние годы появляются пуб-
ликации об отсутствии МРТ признаков, указывающих на геморрагический
характер перенесенного инсульта, несмотря на то, что у больных в остром
периоде выявлялись внутримозговые гематомы. По видимому, это вопрос еще
окончательно не решен, и истинный процент пациентов, у которых не выяв
ляются следы гемосидерина после перенесенного геморрагического инсульта,
еще предстоит определить.
Алгоритм обследования больных с подозрением на геморрагический инсульт
1. Если при КТ выявлены признаки кровоизлияния, а анамнез типичен для
артериальной гипертензии, то на этом обследование можно закончить.
2. Если признаки геморрагии нетипичны или неясна этиология, то необходи-
мо проведение МРТ с введением контрастного вещества (желательно GRE, если
имеется микрогеморрагия).
3. ДСА --- если предполагается сосудистая мальформация.
Дифференциальный диагноз
Артериальная гипертензия или амилоидная ангиопатия:
--- и то и другое в старшей возрастной группе;
--- и в том и в другом случае в анамнезе могут быть предшествующие кровоиз-
лияния;
--- при артериальной гипертензии кровоизлияние локализуется в базальных
ганглиях, а при амилоидной ангиопатии кровоизлияние полушарное.
Артериальная гипертензия, или сосудистая мальформация, или опухоль:
--- артериальная гипертензия редко у пациентов молодого возраста, за исклю-
чением наркоманов (особенно употребляющих кокаин);
--- при кровоизлиянии в опухоль часто необычная трансформация гематомы
и наличие зоны контрастного усиления.
ИНСУЛЬТЫ У НАРКОМАНОВ
В настоящее время наркомания является наиболее частой причиной разви-
тия инсультов у пациентов молодого возраста. Так, по данным M.Sloan ( 1991 ),
инсульты у наркоманов выявлялись в 10% случаев. Механизм развития ин-
сульта не всегда ясен и зависит от вида употребляемого наркотика. К потен-
циальным причинам возникновения инсульта относят кровоизлияние из не-
распознанной сосудистой мальформации, эмболия чужеродным материалом,
васкулит, вазоспазм и ассоциированная инфекция, такая как инфекционный
эндокардит.
50% инсультов у наркоманов связаны с употреблением кокаина, амфетами-
на и героина.
Кокаин употребляется в двух формах: кокаина гидрохлорид, который нюха-
ют или вводят внутривенно, и алколоидная форма «крэк», которая вдыхается при
курении. Кокаина гидрохлорид может вызывать внутримозговое кровоизлияние,
тогда как алколоид кокаина является причиной развития как геморрагических,
так и ишемических инсультов в равных долях. Во всех случаях инсульт возни-
кает уже через несколько часов после употребления.
Механизмы возникновения инсульта при употреблении амфетамина сводят-
ся к выраженной гипертензии и вазоспазму из за симпатомиметических свойств
препарата.
ЭТИОЛОГИЯ, ПАТОГЕНЕЗ И ДИАГНОСТИКА СУБАРАХНОИДАЛЬНЫХ
КРОВОИЗЛИЯНИЙ
Субарахноидальное кровоизлияние является синдромом, обусловленным
проникновением крови в субарахноидальное пространство. Особенности кли-
нической симптоматики связаны с многообразием этиологии и патогенетичес-
ких факторов, вызывающих заболевание. Наиболее частыми причинами раз-
вития нетравматических субарахноидальных кровоизлияний являются разры-
вы аневризм или артериовенозных мальформаций. Приблизительно 85% всех
спонтанных кровоизлияний в субарахноидальное пространство возникает в ре-
зультате разрыва мешотчатых аневризм сосудов основания мозга.
Частота развития инфекпионно токсических, паранеопластических пораже-
ний сосудов, артериитов различной этиологии, заболеваний системы крови,
тромбозов мозговых вен и синусов составляет в общей сложности 5---10%. По
данным Ч.Ворлоу (1998), около 10% из всех случаев субарахноидальных крово-
излияний составляют больные с неаневризматическими перимезэнцефаличес
кими кровоизлияниями.
Причины субарахноидальных кровоизлияний
Аневризматическая болезнь
Сосудистая мальформация
Кровоизлияние в опухоль
Черепно мозговая травма
При субарахноидальном кровоизлиянии (САК) КТ и МРТ позволяют обна-
руживать кровь в субарахноидальном пространстве в 90---95% в течение первых
суток. Относительно КТ и МРТ в литературе имеются прямо противоположные
точки зрения. Поданным K.Siegel (1988), КТ выявляет САКвтечение суток у 95%
больных, а на 3 й сутки --- у 74%. Возможность раннего обнаружения САК в 85---
90% случаев подтверждают эксперты ВОЗ (1989). Вместе с тем, по мнению ряда
специалистов, оба метода эффективны не более чем в 75% случаев, начиная со
2---3 х суток с момента заболевания, да и то только при массивных скоплениях
крови в субарахноидальных пространствах. САК малого объема, поданным боль-
шинства авторов, трудно поддаются диагностике.
Данные о распространении излившейся крови, полученные с помощью КТ
либо МРТ, очень важны для выявления и локализации источника геморрагии, а
также при планировании показаний к проведению ангиографии и ее объема,
особенно у пациентов пожилого возраста, которым хирургическое лечение не
всегда показано. Внутримозговые гематомы указывают достаточно точно место
разорвавшейся аневризмы, независимо оттого, является ли кровоизлияние су
барахноидальным, либо захватывает и вещество головного мозга.
А.П.Негрецким (1992) показана зависимость характера кровоизлияния от
локализации разорвавшейся аневризмы:
1) субарахноидальные и субарахноидально вентрикулярные кровоизлияния
с тампонадой желудочков чаще возникают при разрыве аневризм ВСА (28% и
39% случаев соответственно);
2) субарахноидально паренхиматозные кровоизлияния чаше развиваются
при разрыве аневризм СМА (25% случаев);
3) субарахноидалъно паренхиматозно вентрикулярные кровоизлияния с там-
понадой желудочков мозга --- при разрыве аневризм ПМА ПСА (32% случаев).
Наиболее достоверным методом выявления источника САК является катете
ризационная ангиография, однако надо отметить, что риск инсульта у пациен-
тов с недавним САК составляет, поданным ряда авторов, до 1%, не говоря уже
о том, что аневризма может разорваться во время процедуры. Поэтому до насто-
ящего времени критерии отбора таких больных на ангиографическое исследо-
вание чрезвычайно разнятся в тех или иных клиниках, хотя, вероятнее, предпо-
лагаемые преимущества должны перевешивать риск у каждого конкретного па-
циента и ангиография должна, по видимому, проводиться только в при
применении хирургического лечения или, в исключительных случаях, для уста-
новления более точного прогноза.
М РА имеет чувствительность около 85 % и специфичность около 90% по срав
нению с обычной ангиографией. Минимальный размер аневризмы, выявляемой
при МРА, составляет 3 мм, аневризмы меньшего размера обычно пропускают-
ся. При спиральной КТ результаты несколько выше, однако методика поиска
аневризм до конца не отработана, и результаты разнятся у разных авторов.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ХРОНИЧЕСКОЙ НЕДОСТАТОЧНОСТИ
МОЗГОВОГО КРОВООБРАЩЕНИЯ. РОЛЬ МЕТОДОВ ЛУЧЕВОЙ
ДИАГНОСТИКИ В ВЫЯВЛЕНИИ И ИЗУЧЕНИИ ХРОНИЧЕСКОЙ
НЕДОСТАТОЧНОСТИ МОЗГОВОГО КРОВООБРАЩЕНИЯ
Естественное течение сосудистых заболеваний мозга происходит в двухос-
новных направлениях --- острое развитие инсультов, обычно с двигательными и
речевыми дефектами, и хроническое прогрессирующее течение с частым исхо-
дом в сосудистую деменцию. Надо отметить, что в структуре цереброваскуляр
ных заболеваний в последнее время все больший удельный вес занимают хро-
нические формы. Прогредиентное течение дисциркуляторной энцефалопатии
приводит к выраженным нервно психическим нарушениям и инвалидизации
больных, что определяет медико социальную значимость ее ранней диагности-
ки, адекватной терапии и профилактики. Хронические прогрессирующие со-
судистые заболевания мозга часто развиваются при таких наиболее распрост-
раненных болезнях системы кровообращения, как атеросклероз и артериальная
гипертензия, и приводят к нарастанию интеллектуально мнестических наруше-
ний вплоть до деменции.
Основной причиной развития деменции являются множественные инфарк-
ты (мультиинфарктнаядеменция), локализующиеся чаще в коре мозга (корко-
вая деменция), реже --- в подкорковых структурах (подкорковая деменция), а так-
же в коре и подкорковых структурах (смешанная деменция). Инфаркты, приво-
дящие к деменции, могут быть малыми поверхностными множественными
(гранулярная атрофия коры), малыми глубинными (лакунарными) с формиро
ванием лакунарного состояния мозга, а также средними и большими. Деменция
может развиться также при единичных мелких инфарктах, локализующихся
в угловой извилине, в коре медиобазальных отделов височных долей, белом ве-
ществе лобных долей, колене внутренней капсулы и в таламусе. Все эти образо-
вания относятся к важнейшим для осуществления когнитивных функций обла-
стям мозга.
Некоторые инфаркты при дисциркуляторной энцефалопатии протекают бес-
симптомно. Это «немые» инфаркты, т. е. протекающие без клинических прояв-
лений, которые локализуются, как правило, в глубоких отделах мозга и диагно-
стируются только при КТ и МРТ. «Немые» инфаркты встречаются у '/3 пациен-
тов с выраженным атеростенозом ВСА, формируются медленно, по видимому,
во время сна или в период бодрствования при минимальной активности больно-
го. «Немые» инфаркты играют определенную роль в развитии сосудистой муль
тиинфарктной деменции. Они также способствуют развитию тяжелых Н М К.
При развитии большого количества атеросклеротических малых глубинных
(лакунарных) инфарктов наблюдается формирование лакунарного состояния
мозга. Эта особо тяжелая форма патологии развивается при резко выраженной
атеросклеротической ангиопатии мозга и характеризуется наличием не только
множественных инфарктов, находящихся в разных стадиях организации, но и
рядом других патологических изменений мозга. К последним относятся вторич-
ная дегенерация волокон белого вещества --- дегенерация Тюрка --- Валлера ---
изменения нервных клеток, аксоны которых прерваны инфарктами (рис. 7.25),
а также изменения, обусловленные гипоксией: неполный некроз нервных кле-
ток и белого вещества не только вокруг инфарктов, но и на значительном отда-
лении от них, образование криблюр (т. е. расширенных периваскулярных про-
странств в результате персистируюшего отека мозга, локализованного преиму-
щественно вокруг инфарктов), уменьшение объема и массы мозга за счет
множественных инфарктов и описанных выше сопутствующих им изменений
мозга диффузного и очагового характера. Вокруг зон ишемии нередко наблю-
дается персистирование, т. е. длительное существование отека ткани мозга, ко-
торый поддерживается за счет возникновения все новых лакунарных инфарк-
тов и очагов неполного некроза. Сливаясь, эти зоны отека могут распространять-
ся на значительные территории мозга.
Однако не только атеросклероз может приводить к развитию хронической
недостаточности мозгового кровообращения, столь же велика роль артериаль-
ной гипертензии. Малоизвестна такая форма патологии мозга ишемического
характера, возникающая при артериальной гипертензии, как гипертоническая
лейкоэнцефалопатия, т. е. прогрессирующая диффузная деструкция волокон бе-
лого вещества полушарий большого мозга. Гипертоническая лейкоэнцефалопа-
тия приводит к развитию сосудистой деменции подкоркового типа --- субкорти-
кальной артериолосклеротической энцефалопатии, или болезни Бинсвангера.
Широкое внедрение в клиническую практику КТ и МРТ позволило диагности-
ровать не только различные виды инсультов, но и мелкоочаговые и диффузные
формы патологии мозга, обусловленные артериальной гипертензией, включая
их ранние и доклинические проявления.
Рис. 7.25. Последствия перенесенного
инсульта в теле хвостатого ядра левого
полушария с аксональной дегенерацией
по ходу кортико спинального тракта.
а, б, в --- FLAIR ИП, аксиальная плоскость;
г --- Т1 ВИ, корональная плоскость.
Кистозно глиозные изменения в теле хвос-
татого ядра слева, левой ножке мозга, левой
половине моста с викарным расширением
тела левого бокового желудочка,
д --- схема аксональной дегенерации (указаны
стрелками) (по B.Rabin).
В результате морфологических исследований мозга при инсульте, обуслов-
ленном артериальной гипертензией, клинического изучения ее цереброваскуляр
ных осложнений с применением методов визуализации, развития представле-
ния о механизмах морфологических изменений сосудов и ткани мозга при этой
патологии значительно расширились и углубились. Это относится как к остро-
му повышению артериального давления, при котором гипоксия мозга развива-
ется в результате срыва реакции ауторегуляции с нарастающим отеком мозга и
последующим сдавлением сосудов микроциркуляторного русла, так и к хрони-
ческому течению артериальной гипертензии, при котором изменяется архитек-
тоника кровеносного русла: уменьшается просвет сосудов сопротивления вслед-
ствие утолщения их стенок, затем облитерируется часть артериол и разрежается
сеть сосудов, что ведет к локальной гипоксии и ишемии мозга.
Для экстрацеребральных артерий более характерны адаптивные процессы,
которые призваны обеспечивать поддержание адекватного кровоснабжения го-
ловного мозга в условиях длительно текущей артериальной гипертензии. Трав
матизирующее воздействие на сосудистую стенку высокого артериального дав-
ления приводит к патологическим изменениям эластического каркаса и после-
дующим извитости и перегибам в наиболее уязвимых участках внутренних
сонных и позвоночных артерий перед входом их в череп. Развивающиеся при
АГ патологические процессы в сосудистой системе обусловливают патологичес-
кие изменения мозга и находятся под влиянием этой церебральной патологии.
К характерным для гипертонической ангиоэнцефалопатии мелкоочаговым и
диффузным изменениям относятся изменения, обусловленные повышением про-
ницаемости стенок сосудов. Выход плазмы крови за пределы сосудистой стен-
ки приводит к некрозу ткани мозга в периваскулярной зоне. Этот феномен ха-
рактеризуется формированием крупных полостей вокруг сосудов.
Частота выявления лейкоареоза при МРТ головного мозга колеблется от 8%
до 92% в зависимости от используемых критериев диагностики и характерис-
тик обследуемого контингента (возраст, основное и сопутствующее заболева-
ния). Распространенность лейроареоза среди пациентов с различными церебро
васкулярными заболеваниями возрастает с 5% в возрасте 30---39 лет до 100% в воз-
расте 90 лет и старше. Во многих работах показано, что лейкоареоз весьма часто
определяется у людей пожилого возраста, у которых нарушения когнитивных
функций отсутствуют либо выявляются только при специальном нейропсихо
логическом исследовании.
Установлено, что лейкоареоз обнаруживается не только при цереброваскулярных
заболеваниях, но и при ряде других заболеваний и патологических состояний,
сопровождающихся очаговыми и диффузными изменениями белого вещества
полушарий мозга, например при болезни Алыггеймера, амилоидной ангиопатии,
прогрессирующей мультифокальной лейкоэнцефалопатии, лейкоэнцефалитах,
болезни Крейтцфельдта --- Якоба, травматическом поражении, радиационной и
метаболической энцефалопатиях, нормотензивной гидроцефалии и т. д.
Все это свидетельствует о необходимости оценки диагностической и прогно-
стической значимости феномена лейкоареоза, изучения ведущих патогенетичес-
ких факторов его развития.
Однако вопрос об определенных дифференциально диагностических крите-
риях хронических цереброваскулярных заболеваний остается до настоящего
времени открытым. Несмотря на внедрение в клиническую практику методов
нейровизуал изации, диагностика и дифференциальная диагностика церебровас-
кулярных заболеваний все еще чрезвычайно сложна.
Список литературы
1. Верещагин Н.В., Борисенко В.В., Власенко А.Г. Мозговое кровообращение.
Современные методы исследования в клинической неврологии,--- М.: Медици-
на, 1993. 208 с.
2. Верещагин Н.В., Брагина Л.К., Вавилов СБ., Левина Г.Я. Компьютерная
томография головного мозга.--- М.: Медицина, 1986.--- 256 с.
3. Виленскии Б.С. Инсульт.--- СПб., 1995.--- 288 с.
4. Вордлоу Д. Нейровизуализация при инсульте: достижения и преимуще-
ства// Ж. неврол. и психиатр.--- 2000.--- No 8.--- С. 35---37.
5. Ворлоу Ч.П., Деннис М.С, ван Гейн Ж., Ханкий Г.Ж., Сандеркок П.А.Г., Бам
форд Ж.М., Вордлоу Ж. Инсульт. Практическое руководство для ведения боль-
ных.--- СПб.: Политехника, 1998.--- 629 с.
6. Гусев Е.И. Ишемическая болезнь мозга.--- М., 1992.--- 328 с.
7. Жулев Н.М., Яковлев Н.А., Кандыба Д.В., Сокуренко Г.Ю. Инсульты экс-
тракраниального генеза.--- СПб.: Издательский дом СПбМАПО, 2004.--- 588 с.
8. Людковская И.Г., Моргунов В.А. Атеросклеротическая ангиопатия // Очер-
ки по патологии нервной системы / Под ред. Ю.А.Медведева, Д.Е.Мацко.---
СПб., 1996. С. 145 159.
9. Медведев Ю.А., Мацко Д.Е. Аневризмы и пороки развития сосудов мозга.---
СПб., 1993. Т. 1. 136 с.
10. Одинак М.М., Михайленко А.А., Иванов Ю.С и др. Сосудистое заболева-
ние головного мозга.--- СПб., 1997.--- 160 с.
11. Уорлоу Ч. Влияние результатов рандомизированных исследований на так-
тику ведения больных острым инсультом // Ж. невропат, и психиатр,--- 1999.---
Т. 99, No 2. С. 47 50.
12. Шмидт Е.В. Классификация сосудистых поражений головного и спин-
ного мозга // Ж. невропат, и психиатр,--- 1985.--- No 9.--- С. 1281 1288.
13. Albers G.W. Diffusion weighted MR1 for evaluation of acute stroke // Neuro-
logy 1998. Vol. 51, Suppl. 3. P. 47 49.
14. Brandt Zawadski M., Atkinson D., Detrick M., Bradley IV.G., Scidmore G.
Fluid attenuated inversion recovery (FLAIR) for assessment of cerebral infarction.
Initial clinical experience in 50 patient // Stroke.
--- 1996.--- Vol. 27, N 7.--- P. 1187---
1191.
15. Grain M., Yuh W., Greene G, Loes D., Ryals Т., Sato Y., Hart M. Cerebral ishe
mia: Evaluation with Contrast Enhanced MR Imaging//A. J. N. R.--- 1991.---Vol. 12,
N 4. P. 631 639.
16. Edelman R.R., Mattle H.P., Atkinson D.J. etal. Cerebral Blood Flow: Assessment
with Dynamic Contrast enhanced T2 weighted MR Imaging at 1.5 T // Radiology---
1990. Vol. 176. P. 211 220.
Глава 8
ДЕМИЕЛИНИЗИРУЮЩИЕ ЗАБОЛЕВАНИЯ
ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ
Никто не может научиться тому, о чем не задумыва-
ется.
К.Хибран
Идиопатические воспалительные демиелинизирующие заболевания централь-
ной нервной системы представляют собой чрезвычайно гетерогенную по клини-
ческим проявлениям и по прогнозу группу заболеваний и состояний, объединя-
емых по одному из основных патоморфологических признаков --- первичной
демиелинизации, которая развивается на фоне (или вследствие) воспаления.
Эти заболевания занимают особое место в неврологии. Это обусловлено их
широким распространением, преимущественно среди людей молодого возрас-
та, полиморфизмом клинической симптоматики, вызывающей затруднения
даже у опытных специалистов. Патогенез демиелинизации затрагивает фунда-
ментальные основы неврологии, иммунологии, генетики и вирусологии. Пато-
логический процесс может протекать остро (острый диссеминированный энце-
фаломиелит, острый геморрагический лейкоэнцефатит) или хронически с пе-
риодическими обострениями (рассеянный склероз).
Причины возникновения демиелинизирующих заболеваний точно не извес-
тны. Однако в многочисленных работах, посвященных проблемам этиопатоге
неза, подчеркивается, что развитие демиелинизации связано со случайным со-
четанием ряда эндогенных и экзогенных факторов. К неблагоприятным внешним
факторам относятся частые бактериальные и вирусные инфекции, влияние ток-
сичных веществ, действие ионизирующего излучения, особенности питания, ЧМТ,
место проживания (особенно при развитии РС), а также частые стрессовые си-
туации. К внутренним индукторам относится генетическая предрасположенность,
связанная с аллелем НЬА ОЯ2 НЬА класса II и соответствующим гаплотипом
ОЯ2 фШ) ОЯВ1*1501 ООА1*0102 ЭОВ1*0602, что ведет к нарушениям
иммунорегуляции. Существуют данные о наличии протективных локусов, выяв-
ляемых у здоровых людей и отсутствующих у больных с такого рода патологичес-
ким процессом. Ни один из указанных факторов при отдельном рассмотрении не
имеет значения в возникновении заболевания, только их определенное сочетание
влечет за собой развитие демиелинизирующего процесса.
Не исключено, что для некоторых случаев может быть выявлен один этиоло-
гический агент --- инфекционный, как это произошло с такими демиелинизи
рующими заболеваниями, как спастический тропический парапарез (вирус
НТьУ1) и прогрессирующая мультифокальная лейкокоэнцефалопатия (папо
ва вирусы, .ГСУ). Перечисленные вероятные патогенетические варианты соот
ношения демиелинизации, воспаления и инфекции подчеркивают гетероген-
ность и недостаточную изученность идиопатических воспалительных демиели
низирующих заболеваний.
Патогенез демиелинизации связан с реактивацией, в том числе под действи-
ем антгигенов микроглии, сенсибилизированных Т клеток памяти. Следую-
щее за этим увеличение продукции интерлейкина 1 (ИЛ 1), ИЧР и и ТИБ а
ведет к образованию адгезионных молекул на мембране эндотелиоцитов и лей-
коцитов. Действие ИЛ 1 также связано с активацией как иммунных, так и не-
иммунных клеток, продуцирующих хемотаксические хемокины (ИЛ 8, ИЛ
6, моноцитарньгй хемоаттрактантнъгй протеин), интерфероны, ростовые и транс-
формирующие факторы. Известно, что ИЛ 8 обладает наиболее активными
хемотаксическими свойствами по отношению к нейтрофилам и вызывает их
быстрое движение к эндотелию с последующим взаимодействием посредством
эндотелиально лейкоцитарных адгезивных молекул. В результате повышения
функциональной активности гранулоцитов и агранулоцитов увеличивается
продукция активных кислородных метаболитов. Итогом их массивного выб-
роса является окислительный стресс с повреждением эндотелиоцитов и, как
следствие, повышение проницаемости ГЭБ.
Нарушение проницаемости ГЭБ, трансэндотелиальная миграция активиро-
ванных лейкоцитов, а также увеличение продукции провоспалительных цито
кинов и хемокинов параллельно с уменьшением экспрессии противовоспали-
тельных цитокинов ведет к повреждению миелина и клеток глии с образованием
фокуса воспаления в нервной ткани.
Таким образом, ведущими паттернами демиелинизации являются наруше-
ние ГЭБ, воспаление, очаговое разрушение миелина, глиоз и потеря аксонов. Все
перечисленные изменения находят отражение на МР томограммах.
Интактный ГЭБ не пропускает гадолиний, поэтому нарушение его прони-
цаемости проявляется избирательным изменением интенсивности сигнала на
постконтрастных изображениях. На ранних этапах развития патологическо-
го процесса возможны две модели накопления гадолиния: центральная (изби-
рательное изменение сигнала в массиве очага воспаления) и ранняя перифе-
рическая (рис. 8.1). Последний вариант наблюдается в случаях выраженно-
го повреждения миелина и выглядит как равномерный по толщине ободок
гиперинтенсивного сигнала на Т1 ВИ. В дальнейшем наиболее типичной
оказывается поздняя периферическая модель, характеризующаяся фрагмен-
тарным неравномерным по толщине и интенсивности накоплением контраст-
ного вещества по периферии очага. Контрастное усиление на введение гадо-
линия исчезает спустя 4---6 недель после инициации патологического процесса,
что отражает восстановление ГЭБ.
Воспалительная реакция развивается вслед за поражением ГЭБ и проявляет-
ся очаговыми изменениями, визуализирующимися на изображениях любого типа
взвешенности в виде стандартного изменения интенсивности сигнала: гиперин-
тенсивный сигнал на Т2 ВИ и гипоинтенсивный --- на Т1 ВИ. Так как в основе
воспаления лежит отек тканей, то на Т1 ВИ отмечаются умеренно выраженные
изменения.
Рис. 8.1. Рассеянный склероз. МРТ. Постконтрастные Т1 ВИ.
Периферическая (а) и центральная (б) модели накопления контрастного препа-
рата.
Уже на этом этапе в формировании картины начинает принимать участие
повреждение миелина, и в тех случаях, когда процесс протекает крайне тяжело,
на Т1 ВИ визуализируются участки резко гипоинтенсивного сигнала, так на-
зываемые черные ямы, имеющие вид кистоподобных зон (рис. 8.2).
Острая демиелинизация сопровождается высвобождением липидов и повы-
шением концентрации воды, поэтому она отчетливо видна в острую фазу, а при
MP спектроскопии регистрируется пик липидов. Острый очаг существует от
нескольких недель до нескольких месяцев. Его размеры первоначально увели-
чиваются, а позже --- уменьшаются.
Хроническая демиелинизация на Т1 ВИ не визуализируется, тогда как на Т2
ВИ проявляется неспецифическими очагами. На этом этапе внутривенное кон-
трастирование неэффективно, поскольку целостность ГЭБ не нарушена.
Немаловажную роль в достаточно пестрой и изменчивой картине хроничес-
кой демиелинизации играет возможность ремиелинизации, обусловленная фун-
кциональной сохранностью олигодендроцитов, гибель которых влечет утрату
этой способности. В таких случаях все более активную роль начинает играть
глиоз, вызванный пролиферацией астороцитов и пронизывающий весь массив
зоны демиелинизации. Именно эти очаги характеризуются гипоинтенсивным
сигналом на Т1 ВИ. Остаточная гиперинтенсивная зона, видимая на Т2 ВИ,
обусловлена как резидуальной демиелинизацией, такиглиозом (рис. 8.3).
Параллельно с демиелинизацией и развитием глиоза идет процесс утраты
аксонов --- итог разыгрывающейся в веществе мозга драмы. Изменения иногда
а
Рис. 8.2. Больная 3., 23 лет.
Рассеянный склероз, дебют. МРТ.
а --- Т2 ВИ, очаг в белом веществе пра-
вой гемисферы;
б --- Т1 ВИ, до внутривенного контрас-
тирования;
в --- Т1 ВИ, после внутривенного кон-
трастирования. МРТ признаки наруше-
ния целостности гематоэнцефаличес
кого барьера.
В
отчетливо выражены, как, например, при дегенерации Тюрка --- Валлера, но обыч-
но рано или поздно приводят к диффузному атрофическому процессу, проявля-
ющемуся смешанной гидроцефалией заместительного характера с преимуще-
ственным расширением тел желудочков. Признаки внутрижелудочковой гипер
тензии не выявляются. Потеря аксонов может быть зарегистрирована при
МР спектроскопии появлением пика (1Ч ацетил аспартата).
а
б
Рис. 8.3. МРТ. Больная Д., 32 года. Рассеянный склероз, ремиттирующее течение.
а Т2 ВИ;б Т1 ВИ.
Многоочаговое поражение головного мозга.
По мнению некоторых авторов, церебральная атрофия может играть прогно-
стическую роль. Если она появляется уже в первый год болезни, то прогноз не-
благоприятный и наиболее вероятно злокачественное течение процесса. Появ-
ление атрофии через 5 лет после начала заболевания свидетельствует об относи-
тельной доброкачественности его течения. Имеются данные о корреляционной
зависимости между атрофией мозолистого тела и деменцией при PC (рис. 8.4).
Разнообразие лучевых проявлений демиелинизирующих заболеваний, в ос-
нове которых лежит очаговое поражение, объясняет попытки специалистов си-
стематизировать видимые при МРТ изменения. Такие взгляды, положенные в ос-
нову синдромального подхода, позволили выделить следующие лучевые синд-
ромы, встречающиеся при демиелинизирующих поражениях ЦНС:
--- синдром острой воспалительной демиелинизации;
--- синдром хронической воспалительной демиелинизации;
--- синдром мультифокально дегенеративнойлейкоэнцефалопатии;
--- синдром сочетанной мультифокально диффузной лейкоэнцефалопатии.
/. Синдром острой воспалительной демиелинизации. Для острой воспалитель-
ной демиелинизации характерно поражение и белого, и серого вещества, с воз-
можным умеренным масс эффектом, не соответствующим объему поражения,
Рис. 8.4. Нейродегенеративные
изменения при рассеянном склерозе.
МРТ.
а --- постконтрастное Т1 ВИ, сагит-
тальная плоскость. Атрофия мозоли-
стого тела.
б, в --- Т1 ВИ, аксиальная плоскость.
Расширение тел боковых желудоч-
ков. Очаги хронической демиелини
зации.
избирательным изменением сигнала на постконтрастных изображениях, обра-
тимостью изменений. В ряде случаев очаги визуализируются при КТ. Интенсив-
ность сигнала при МРТ отражает все ведущие паттерны этого патологического
процесса: нарушение ГЭБ, воспаление, демиелинизацию.
2. Синдром хронической воспалительной демиелинизации проявляется много-
очаговым поражением белого вещества без признаков перифокалъного отека, масс
эффекта, нарушения ГЭБ. Размеры очагов варьируются от 0,5 до 1,0 см. Типичной
является субэпендималъная локализация с частым поражением мозолистого тела,
белого вещества вокруг рогов боковых желудочков, а также его субкортикаль
ных отделов (рис. 8.5). Очаги,
обычно овальной или округлой
формы, ориентированы преимуще
том теле.
Рис. 8.5. Больной Ю, 35 лет.
Рассеянный склероз.
МРТ, Т2 ВИ.
Очаговые изменения в мозолис
ственно перпендикулярно сагиттальной плоскости. При сравнении количества
очагов обращает на себя внимание большая разница между объемом изменений,
видимых на Т2 ВИ, и значительно меньшим поражением, визуализируемым на
ТI В И. Это обусловлено тем, что на Т1 В И дифференцируются только очаги с вы-
раженным глиозом. При хронической демиелинизации существенный вклад
в формирование лучевой картины вносит утрата аксонов, проявляющаяся сме-
шанной, преимущественно внутренней, гидроцефалией. Картина меняется при
обострении процесса, когда начинают визуализироваться перифокальный отек,
избирательное изменение интенсивности сигнала на постконтрастных изобра-
жениях, увеличение размеров старых очагов и появление новых. Изменения видны
только при МРТ.
3. Синдром мультифокально дегенератшной лейкоэнцефалопатии отличается
крайне скудным количеством мелких очагов на фоне диспропорционально вы-
раженной атрофии. Внутривенное контрастирование, как правило, неэффективно.
4. Синдром сочетанной мулыпифокально диффузной лейкоэнцефалопатии,
кроме типичного многоочагового поражения, характеризуется диффузными из-
менениями белого вещества.
ЛУЧЕВЫЕ ПРОЯВЛЕНИЯ
ДЕМИЕЛИНИЗИРУЮЩИХ ЗАБОЛЕВАНИЙ ЦНС
Рассеянный склероз
В группе идиопатических воспалительных демиелинизирующих заболеваний
наиболее актуальной проблемой является рассеянный склероз (РС), на долю
которого приходится более 90% всех случаев у взрослых.
Распространенность РС в регионах со средним и высоким риском заболева-
ния, в том числе и в изученных регионах России составляет более 30---50 человек
на 100 000 населения, а в странах Западной и Восточной Европы --- 50---150 слу-
чаев на 100 000 населения. У 85---90% пациентов заболевание прогрессирует, при-
водя к тяжелой необратимой инвалидизации часто в молодом возрасте, в сред-
нем через 8--- 15 лет от начала болезни. Вместе с тем, РС чрезвычайно разнообра
зен и включает какдоброкачественные, так и злокачественные формы, прогно-
зировать которые на ранних стадиях болезни затруднительно.
Особенно выделяют клинико лучевые и даже генетические отличия первич-
но прогрессирующего РС.
Специфических методов диагностики этого заболевания нет, поэтому при по-
становке диагноза ориентируются на данные клинико лабораторного (сероло-
гического) обследования и результаты МРТ, которые в ряде случаев позволяют
подтвердить диагноз уже во время первого клинического эпизода болезни, выя-
вить группы риска развития достоверного РС, обеспечить объективное монито
рирование течения процесса. Трудно переоценить значимость этого диагности-
ческого исследования, поскольку РС, если исключить эпилепсию и головную
боль, является самым частым нетравматическим неврологическим заболевани-
ем у людей молодого возраста в Европе и Северной Америке. Вместе с тем широ-
кое использование МРТ в диагностике РС выявило как ограничения возмож-
ностей этого метода, так и множество новых вопросов, которые сегодня являют-
ся предметом многочисленных исследований.
Типичная М РТ картина развернутого РС настолько характерна, что не вы-
зывает затруднений у нейрорадиологов. Однако встречаются варианты, кото-
рые первоначально заставляют усомниться в диагнозе, а иногда приводят к се-
рьезным диагностическим ошибкам. К ним, в частности, можно отнести круп-
ные, «псевдотуморозные» очаги, сопровождающиеся масс эффектом.
Полученные в последние годы данные о патоморфологической гетерогенно-
сти РС объясняют многообразие лучевых проявлений, а также коррелирующие
с ними клинические и морфологические признаки.
В настоящее время выделяют несколько клинических вариантов течения РС:
--- латентное (субклиническое) течение;
--- ремиттирующее течение;
--- первично прогрессирующее течение;
--- вторично прогрессирующее течение;
--- прогрессирующе ремиттирующее течение.
Данные о корреляции между количеством, локализацией очагов и течением
заболевания противоречивы. Как правило, имеется связь между количеством
очагов и длительностью течения заболевания у пациентов с ремиттирующим РС.
Наиболее тесные связи прослеживаются между очагами, расположенными ин
фратенториально, и их клиническими проявлениями. Известно, что в случае
нелеченного РС отмечается ежегодное увеличение количества очагов в среднем
на 10% по сравнению с аналогичным вариантом течения заболевания у пациен-
тов, получающих адекватное лечение.
Ремиттируюший РС обычно наблюдается на ранней стадии заболевания. Он
характеризуется внезапными и непредсказуемыми обострениями, перемежаю-
щимися ремиссиями, и со временем переходит во вторично прогрессирующий
вариант. При лучевом исследовании отмечается многоочаговое поражение, со-
ответствующее синдрому хронической демиелинизации (79% наблюдений).
Вторично прогрессирующее течение характеризуется таким же многоочаго-
вым поражением, но его отличительной особенностью является выраженный
атрофический процесс. У больных с вторично прогрессируюшим вариантом
течения РС связь между количеством очагов и длительностью заболевания от-
сутствует, также как и корреляция между количеством перенесенных обостре-
ний и общим объемом очагов демиелинизации. В 4% случаев такой вариант
течения проявляется синдромом сочетанной мультифокально диффузной лей
коэнцефалопатии, ассоциируется с тяжелым течением РС и может свидетель-
ствовать о врожденных дефектах миелиногенеза или диффузном поражении оли
годендроцитов (рис. 8.6).
Первично прогрессирующий РС характеризуется неуклонно прогрессиру-
ющим течением с самого начала заболевания без явных обострений, так же как
и явных ремиссий. Болеют, как правило, люди старше 40 лет. Для первично про-
грессирующего РС характерен синдром мультифокально дегенеративной лей
коэнцефалопатии, наблюдающийся у 60% пациентов с таким вариантом тече-
ния заболевания. В остальных 40% случаев МРТ картина соответствует синд-
рому хронической воспалительнойдемиелинизации, и особенности клинической
картины указывают на высокую вероятность «классического» РС в фазе вто-
ричного прогрессирования (рис. 8.7).
Синдром острой воспалительнойдемиелинизации встречается нечасто (око-
ло 9% случаев) и, как правило, соответствует дебюту заболевания. При этом
синдроме наблюдается более массивное поражение, с крупными очагами и вы-
раженным перифокальным отеком. Его вариантами являются псевдотумороз
ный и ОДЭМ подобный, имеющий сходство с проявлениями острого диссеми
нированного энцефаломиелита.
Неспецифичность лучевых прояв-
лений и многообразие патологических
состояний, которые характеризуются
очаговым поражением, заставляют за-
думаться над критериями достоверно-
сти РС. Современные диагностические
критерии разрабатываются с учетом
двух категорий требований: 1) они дол-
жны служить достоверным источни
Рис. 8.6. Больная Т., 44 года.
Рассеянный склероз,
вторично прогрессирующее течение.
Активная фаза. МРТ, Т2 ВИ.
Многоочаговое поражение с выражен-
ным перифокальным отеком.
Рис. 8.7. Рассеянный склероз,
первично прогрессирующее течение.
МРТ.
Изображения, взвешенные по протон-
ной плотности.
ком информации для научных исследований и 2) удовлетворять потребностям
качественной клинической практики. Если в научно исследовательской рабо-
те точный диагноз важен для достоверной оценки всех изучаемых характерис-
тик болезни, то в клинической практике точная и ранняя диагностика означает
Таблица 8.1
Диагностические МРТ критерии рассеянного склероза
Авторы, год
Критерии
ОЖРату и соавт., 1988 Для людей моложе 50 лет, не имеющих факторов
риска инсульта:
4 очага или
3 очага, один из которых перивентрикулярный
Диаметр очагов более 3 мм
Р.Рагекаэ и соавт., 1988 Включая людей старше 50 лет, имеющих факторы
риска инсульта:
Очаги, прилежащие к телам боковых желудочков
Очаг инфратенториальной локализации
Очаг размером не менее 6 мм
Необходимо наличие не менее двух перечисленных
критериев
РВагкгют и соавт., 1997
М.Ттгаге и соавт., 2000*
Очаг, накапливающий контрастирующее вещество,
или 9 гиперинтенсивных очагов на Т2 ВИ
Не менее 1 инфратенториального очага
Не менее 1 субкортикального очага
Не менее 3 перивентрикулярных очагов
Необходимо наличие не менее трех перечисленных
критериев
* Критерии приняты на Международном совещании по диагностике рассеянного
склероза (2001).
своевременное лечение и возможность контролировать течение болезни. В отно-
шении РС последнее приобрело особую актуальность в связи с регистрацией пре-
паратов, модифицирующих течение болезни (препараты Ь интерферонов, гла
тирамера ацетат и митоксантрон).
Исходя из этих требований, диагностический метод должен обеспечить точ-
ность диагностики при минимальной сложности выполнения, с возможностью
широкого применения в практической медицине. Использование первых диаг-
ностических МРТ критериев ОЖРагу и РРагеказ (табл. 8.1) выявило их высо-
кую чувствительность, которая составляет до 95% при клинически достоверном
диагнозе РС. Это означает, что при наличии двух обострений болезни и клини-
ческих признаков двух отдельных очагов типичные изменения на МРТ выявля-
ются у 95% больных.
Однако последующее широкое использование критериев привело к осозна-
нию того, что они имеют недостаточную специфичность для диагностики РС,
поскольку подобные изменения на МРТ изображениях нередко регистрируют-
ся при других неврологических заболеваниях. Новые МРТ критерии рассеян-
ного склероза ЕВагкйоГи М.Ттхоге (см. табл. 8.1) разрабатывались для повы-
шения диагностической специфичности исследования. Последняя увеличива-
ется в основном за счет количественных параметров, а именно необходимости
регистрации большего количества очагов (не менее 9). Вместе с тем известно, что
у 1 % пациентов с достоверным диагнозом РС МРТ картина головного мозга не
изменена, а у 5,5% больных имеется не более 2 очагов.
Диагностическая чувствительность МРТ критериев при клинически досто-
верном РС высокая и составляет 92---94%. Однако во время первого клиничес-
кого эпизода болезни, когда клинический диагноз не является достоверным и
требует подтверждения, чувствительность этих критериев существенно ниже. По
нашим данным, в период до 5 месяцев от начала первых симптомов РС, число
пациентов, не удовлетворяющих критериям О.ХУ.Рагу и РРагекав, составляет
20%. В этой же группе доля больных, не удовлетворяющих критериям ЕВагкгюГ,
достигает 34%. Особенно сложным является подтверждение диагноза именно
в тех случаях, когда и клинические проявления не являются специфичными для
РС, в частности, при одноочаговых симптомах, включая спинальные.
Недостаточно высокая чувствительность МРТ исследования в «дебюте» РС
подчеркивает значимость дополнительных дифференциально диагностических
признаков. Возможны случаи нормальной МРТ картины головного мозга при
наличии очагов РС в спинном мозге. Более того, встречаются варианты, когда
клинические проявления демиелинизирующего поражения опережают измене-
ния, выявляемые при МРТ, на несколько лет.
Вместе с тем, говоря о соответствии М РТ находок и клинической картины,
нельзя не отметить, что при лучевом исследовании, как правило, мы видим боль-
ше, чем предполагаем по клиническим данным. Этот феномен может быть объяс-
нен функциональной сохранностью ЦНС, когда в результате транслокации
происходит перераспределение функций головного мозга. Немаловажную роль
играют субъективность и относительная грубость методов регистрации невро-
логического дефицита, в частности методов количественной оценки когнитив-
ных функций и поведенческих особенностей пациента, отсутствие базовых пре
морбидных исследований. Более того, у ряда пациентов при наличии клиничес-
кой картины, позволяющей заподозрить РС, какие либо очаговые изменения
при МРТ не выявляются. В таких случаях вероятность развития РС не превы-
шает 10%, хотя полностью нельзя опровергнуть наличие этого заболевания.
Во многих художественных произведениях звучит медицинская тематика. Не
обойден вниманием и РС. Наиболее яркое описание заболевания принадлежит
Н.Островскому: «... получаю удар за ударом. Едва успеваю подняться на ноги
после одного, как новый, немилосерднее первого, обрушивается на меня. Самое
страшное в том, что я бессилен сопротивляться. Отказалась подчиняться левая
рука. Это было тяжело, но вслед изменили ноги, и я, без того еле двигавшийся
(в пределах комнаты), сейчас с трудом добираюсь от кровати к столу. Но ведь
это, наверное, еще не все. Что принесет мне завтра --- неизвестно...» (из писем
брату).
Трагедия, эмоционально переданная Н.Островским, отражает еще одну ха-
рактерную особенность РС --- диссеминацию во времени. Группа исследовате-
лей во главе с \У.I.МасОопаШ в 2001 г. предложила М РТ критерии диссемина
ции во времени, которые были приняты международным сообществом. Эти кри-
терии базируются на возможности визуализиции нарушения ГЭБ на
МРТ изображениях с внутривенным контрастированием.
Так, о диссеминации во времени можно говорить, если при исследовании,
выполненном через 3 месяца после манифестации заболевания, появляются оча-
ги контрастного усиления, имеющие иную локализацию, чем поражение, кото-
рым объясняется клиническая симптоматика. При отсутствии таких изменений
исследование повторяют еще через 3 месяца и считают, что речь идет о РС, если
выявлено накопление контрастного вещества или очаг гиперинтенсивного сиг-
нала на Т2 ВИ. В тех случаях, когда первое исследование проводится менее чем
через 3 месяца после начала клинического обострения, выявление признаков
нарушения ГЭБ при втором исследовании, проведенном не ранее чем через 3 ме-
сяца после первого, доказывает диссеменацию во времени. Факт диссеминации
во времени также считается установленным, если и при втором исследовании
не выявлен очаг контрастного усиления, но при последующем МРТ контроле
в динамике, проведенном не ранее, чем через 3 месяца, выявлен новый очаг на
Т2 ВИ или на постконтрастном изображении. Примечательно, что даже отри-
цательные результаты при повторном исследовании не исключают диагноз РС.
С практической точки зрения крайне важным является вопрос установления
активности РС, что невозможно без внутривенного контрастирования с приме-
нением препаратов на основе гадолиния (Сё БТРА), позволяющих оценить
состояние ГЭБ. Этот методических прием позволяет выявлять «свежие» очаги,
реактивацию старых и, следовательно, делает возможным проведение монито-
ринга активности патологического процесса. Каждое появление нового очага
или увеличение размеров старого сопровождается накоплением контрастирую-
щего препарата. Возможны различные варианты усиления сигнала от «старых»
бляшек РС. Как правило, через 4 минуты после введения контрастного веще-
ства определяется кольцевидное усиление сигнала, через 15---20 минут очаг на-
копления становится гомогенным. В некоторых случаях отмечается избиратель-
ное изменение сигнала только в центре или только по периферии очага. Повы-
шение дозы контрастного вещества до 0,3 ммоль/кг массы тела увеличивает
достоверность выявления очаговых изменений дополнительно у 65% больных.
Использование Т1 ВИ с контрастным усилением с применением переноса
намагниченности удваивает соотношение контраст/шум между усиленными
очагами и белым веществом, что позволяется уменьшить дозу контрастного пре-
парата (рис. 8.8). Применение этой методики с одинарной дозой соответствует
постконтрастному Т1 ВИ с тройной дозой контрастирующего препарата.
Реактивация бляшки РС проявляется появлением перифокального отека,
нарушением однородности очагов, увеличением размеров старых поражений и
появлением новых, а также изменением интенсивности сигнала на постконтра-
стных изображениях (рис. 8.9).
Общеизвестно, что далеко не всегда данные МРТ коррелируют с клиничес-
кими представлениями об активности процесса. Новые очаги, видимые на МРТ,
могут появиться при отсутствии клинических признаков обострения.
В ряде случаев МРТ подтверждает стабилизацию воспалительного процесса
в виде отсутствия активных очагов, а инвалидизация продолжает нарастать.
В соответствии с современными представлениями о демиелинизации и пос-
ледующей нейродегенерации при РС, только раннее лечение может предотвра
Рис. 8.8. Рассеянный склероз, активная фаза. МРТ, аксиальная плоскость.
Изображения, выполненные на уровне тел боковых желудочков Т2 ВИ (a), Pd (б),
Т1 ВИ после введения контрастного вещества (в) и с переносом намагниченности
(г).
На Т2 ВИ и на изображении, взвешенном по протонной плотности, в белом веще-
стве мозга, преимущественно в субэпендимальных отделах, определяется множе-
ство очагов демиелинизации. После введения контрастного вещества усиление
интенсивности сигнала от очага в левой лобной доле выявляется только на изобра-
жении с использованием переноса намагниченности.
Рис. 8.9. Больная Б. 18 лет. Рассеянный склероз. МРТ.
а --- Т2 ВИ; б --- Т1 ВИ с контрастным усилением. Изменения в веществе мозга не
выявляются.
в --- Т2 ВИ через I месяц; г --- Т1 ВИ с контрастным усилением через 1 месяц. При
динамическом контроле через 1 месяц на Т2 ВИ в заднем бедре левой внутренней
капсулы определяется очаг с нечеткими контурами, изменяющий интенсивность
сигнала на постконтрастном изображении.
тить необратимую инвалидизацию. Поэтому особое внимание в разработке ди-
агностических тестов уделяется обеспечению ранней диагностики. В основе со-
временной диагностики РС лежит принцип приоритета клинических проявле-
ний с подтверждением (при необходимости) дополнительными методами, а имен-
но: МРТ головного мозга, исследованием цереброспинальной жидкости на
наличие гиперпродукции олигоклональных иммуноглобулинов (изв) и, реже,
исследованием вызванных потенциалов. Тем не менее, экспертами в области РС
подчеркивается, что ряд заболеваний может проявлять ссходство с РС, включая
клинические, МРТ и иммунологические критерии. К таким заболеваниям от-
носятся острый диссеминированный энцефаломиелит, нейроинфекции (вирус-
ные инфекции, боррелиоз, сифилис) (рис. 8.10), заболевания с церебральными
васкулопатиями и васкулитами (системная красная волчанка, другие коллаге
нозы, болезнь Бехчета, изолированный ангиит ЦНС, САОАБИ., первичный ан
тифосфолипидныйсиндром) (рис. 8.11), воспалительные (саркоидоз) ирегеди
тарные заболевания (адренолейкодистрофия, зрительная атрофия Лебера). Если
же ограничиваться только клиническими или лучевыми проявлениями, то пере-
чень дифференцируемых состояний оказывается значительно больше. Это от-
ражает недостатки современной диагностики РС и необходимость разработки
новых диагностических тестов.
Наибольшие трудности в диагностике РС возникают у детей и у лиц старше
45---50 лет. Они обусловлены редкостью заболевания в этих возрастных катего-
риях, связанной с этим недостаточной осведомленностью врачей, возможными
различиями клинических проявлений РС и иным спектром дифференциально
диагностических состояний.
Рис. 8.11. Первичный антифосфолипилный синдром. МРТ.
а --- FLAIR ИП. Поражение белого вещества на фоне выраженного атрофического
процесса.
Рис. 8.11. Окончание.
б Т2 ВИ.
МРТ ПРОЯВЛЕНИЯ ДРУГИХ ДЕМИЕЛИНИЗИРУЮЩИХ
ЗАБОЛЕВАНИЙ ЦНС
Другие идиопатические воспалительные демиелинизирующие заболевания
изучены гораздо меньше рассеянного склероза. Отсутствует их единая класси-
фикация. Те нозологические единицы, которые представлены раздельно в Меж-
дународной Классификации Болезней (МКБ 10), внаучной литературе тракту-
ются как варианты РС: оптиконевромиелит, концентрический склероз Бало,
диффузный склероз Шильдера. Наиболее патогенетически близкое к РС забо-
левание --- острый диссеминированный энцефаломиелит (ОДЭМ), особенно его
рецидивирующие и мультифазные формы, в МКБ 10 рассматриваются в дру-
гой рубрике: РС --- в группе демиелинизирующих заболеваний (С35), а ОДЭМ ---
в группе воспалительных (С04). Такие состояния, как неврит зрительного не-
рва или поперечный миелит, могут встречаться как изолированные синдромы
или в рамках других идиопатических воспалительных демиелинизирующих за
болеваний. Дифференциально диагностические различия между этими состо-
яниями и заболеваниями недостаточно разработаны, а вместе с тем их система-
тизация представляет чрезвычайно важную клиническую задачу, поскольку речь
идет о прогнозировании (монофазный, саморазрешающийся характер процес-
са или мультифазный, прогрессирующий) и о разработке показаний для проти
ворецидивной терапии.
Острый диссеминированный энцефаломиелит, очевидно, представляет собой
спектр близких состояний, возникающих после вакцинации (поствакциналь-
ный ОДЭМ), а также после или на фоне инфекционного процесса (пост или
параинфекционный ОДЭМ). Этиология и распространенность клинических
форм ОДЭМ поданным исследования, проведенного в 1996---2002 гг. в Санкт
Петербургском Научно исследовательском институте детских инфекций МЗ,
представлена на рис. 8.12.
Классический ОДЭМ является монофазным заболеванием с различной тя-
жестью проявлений и разными исходами. Возвратный и мультифазный ОДЭМ
по течению сходен с PC, однако при мультифазном варианте атаки болезни сле-
дуют друг за другом почти непрерывно и прогноз заболевания в целом неблагоп-
риятный. Иногда возвратный и мультифазный ОДЭМ впоследствии трансфор-
мируются в типичный PC. МРТ картина монофазного ОДЭМ представляет
собой синдром острой воспалительной демиелинизации с крупными очагами,
однако, в отличие от PC, исследование через 3 и 6 месяцев подтверждает завер-
шение процесса возвратного и мультифазного ОДЭМа, как и PC, характерна
диссеминация во времени (рис. 8.13).
Сравнение МРТ семиотики при PC и ОДЭМ выявило следующие особен-
ности последнего.
Сходство с PC:
1) наличие перивентрикулярныхочагов (обычно множественных);
2) очаги в мозолистом теле;
3) инфратенториальные очаги;
ВПГ2
ВЭБ
Грипп А
Парво В19
Стрептококк
В ЦМВ
ввз
Вирус КЭ
Боррелии
Неуточненная
Рис. 8.12. Этиологическая структура диссеминированных энцефаломиелитов
у детей.
их гемисфер большого мозга. Отчетливо про-
слеживается тенденция очагов к слиянию,
б --- Т1 ВИ, аксиальная плоскость. Умерен-
но гипоинтенсивный сигнал в семиовальный центрах слева.
в --- Т1 ВИ после внутривенного контрастирования, аксиальная плоскость. Цент-
ральная модель изменения интенсивности сигнала.
г --- Т1 ВИ, корональная плоскость. Признаки легкого объемного воздействия.
Рис. 8.13. Окончание.
д --- Т2 ВИ, аксиальная плоскость. Поло-
жительная динамика через 4 месяца.
4) наличие очагов 5---10 мм диаметром;
5) наличие очагов с перифокальным
отеком.
Отличия от РС:
1) много крупных очагов, часто с пе-
рифокальным отеком, с признаками
умеренного объемного воздействия;
2) склонность очагов к слиянию
(рис. 8.14);
3) вовлечение в процесс белого и (или)
серого вещества;
а
б
Рис. 8.14. МРТ. Больная В., 25 лет. Острый диссеминированный энцефаломиелит.
МРТ, Т1 ВИ до (а) и после (б) внутривенного контрастирования. Синдром острой
воспалительной демиелинизации. Периферическая модель усиления.
4) более массивный объем поражения;
5) возможность монофокальных вариантов.
Установить этиологию ОДЭМ поданным лучевого обследования не представ-
ляется возможным. В зависимости от объема и локализации изменений выделя-
ют несколько клинических форм заболевания:
--- диссеминированный энцефалит/энцефаломиелит характеризуется мно-
гоочаговым поражением белого вещества, а в последнем случае и спинного
мозга;
--- полиоэнцефалит --- более 50% очагов локализуется в сером веществе;
--- лейкоэнцефалит --- формирование сливных полей демиелинизации
(рис. 8.15);
--- оптикоэнцефаломиелит --- поражение зрительных нервов и головного
мозга;
--- диссеминированный миелит --- изолированное поражение спинного мозга.
В настоящее время нет единой классификации ОДЭМ. Выделяют монофаз-
ный, рецидивирующий и мультифазный ОДЭМ, что согласуется с острым,
подострым и хроническим вариантами течения ОДЭМ. Хронический вариант,
как правило, соответствует представлениям о лейкоэнцефалите. Его продол-
жительность превышает 6 и даже 12 месяцев.
Исходы ОДЭМ до конца не изучены. Очевидно, что в ряде случаев, особенно
при остром монофазном течении, происходит структурно функциональное вос
Рис. 8.15. Больная 8 лет. Лейкоэнцефалит. MPT. FLAIR ИП.
Выявляются сливные поля демиелинизации (а). Структурное восстановление че-
рез 6 месяцев (б).
становление. При тяжелом деструктивном процессе возможно формирование ре
зидуальных кистозно глиозных изменений. При подостром и хроническом те-
чении велик риск трансформации заболевания в РС.
Оптикомиелит, или синдром Девика, в европеоидной популяции по совокуп-
ности клинико инструментальных и лабораторных признаков в большинстве
случаев может быть отнесен к категории ОДЭМ. В некоторых наблюдениях бо-
лезнь со временем приобретает сходство с РС и формально соответствует его
диагностическим критериям. Очевидно, в рамках оптикомиелита также есть
гетерогенность, характерная для других форм демиелинизирующих заболеваний.
Основные МРТ проявления во всех случаях характеризуются тяжелым пора-
жением спинного мозга с наличием очагов, занимающих по протяженности не-
сколько сегментов, а по поперечнику часто наблюдается тотальное или субто-
тальное поражение (рис. 8.16). Для острого периода миелита характерно верете-
нообразное утолщение спинного мозга в зоне воспаления, а в отдаленном
периоде --- выраженная его атрофия.
При РС очаги в спинном мозге по длиннику редко захватывают зону более
одного сегмента, а на поперечных срезах характерно асимметричное парциаль-
ное поражение. МР семиотика поражения спинного мозга при РС представле-
на в табл. 8.2.
а
б
Рис. 8.16. Миелит, острый период. МРТ.
Очаги поражения в продолговатом мозге
и в шейном отделе позвоночника.
а --- STIR ИП, сагиттальная плоскость,
б --- Т2 ВИ, аксиальная плоскость.
Объем продолговатого мозга и спинно-
го мозга (уровень сегмента С6) увеличе-
ны. Субтотальное поражение попереч-
ника спинного мозга.
Таблица 8.2
Магнитно резонансная семиотика поражений спинного мозга
МР признак
Частота, %
Локализация очага:
весь поперечник
30
передние отделы
23
задние отделы
41
центральные отделы
6
Отек спинного мозга
11
Атрофия спинного мозга
см
Нарушение гематоэнцефалического барьера
7
Гиперинтенсивные очаги на Т2 ВИ
100
Гипоинтенсивные очаги на Т1 ВИ
00
Изоинтенсивные очаги на Т1 ВИ
92
Идиопатические воспалительные демиелинизирующие заболевания ЦНС с учетом
и иммунопатологических проявлений
Таблица 8.3
клинических, лучевых
со
О)
Категория
Основные клинические
проявления
Данные МРТ
Интратекальный
гуморальный
иммунный ответ
Комментарии
Рассеянный склероз (РС)
Латентный РС
Клинические симптомы
отсутствуют или соответ-
ствуют сопутствующему
заболеванию
Головной мозг: синдром
хронической воспали-
тельной демиелинизации
Присутствует
Типичные изменения на
МРТ и в ЦСЖ удовлетво-
ряют диагностическим
критериям РС**
Рецидивирующе
ремиттирующий
РС---
доброкачествен-
ный вариант ---
классический
вариант (Шарко)
Симптомокомплексы
типичные, указывают на
многоочаговое пораже-
ние белого вещества
головного и спинного
мозга. Обострения
сменяются ремиссиями,
интервал между обостре-
ниями более 1 месяца
Головной мозг: синдром
хронической воспали-
тельной демиелиниза-
ции, редко --- острой
воспалительной демие-
линизации, мультифо
кально диффузной
лейкоэнцефалопатии;
МРТ в пределах нормы
у 5% больных. Спинной
мозг,
шейный отдел:
типичные изменения
у 60 70% больных
Присутствует
у 90 95% боль-
ных. Выражен-
ный, преоблада-
ние синтеза
к цепей по
частоте и выра-
женности
При доброкачественном
РС менее выражены
МРТ активность и
иммунопатологические
проявления
Вторично
прогрессирую-
щий РС
Симптомокомплексы
типичные. Неуклонно
нарастает неврологиче-
ский дефицит, возможны
флюктуации симптомов и
периоды стабилизации
Головной мозг: синдром
хронической воспали-
тельной демиелиниза-
ции, редко --- мульти
фокально диффузной
лейкоэнцефалопатии.
Спинной мозг,
шейный
отдел: типичные изме-
нения у 85% больных
Присутствует
у 90 95% боль-
ных. Выражен-
ный, преоблада-
ние синтеза
к цепей по
частоте и выра-
женности
Первично
прогрессирую-
щийРС
истинный
Синдром хронической
прогрессирующей миело
патии у 80% больных.
Прогрессирование
неврологического
дефицита с первых
проявлений
Головной мозг: синдром
мультифокально
дегенеративной
лейкоэнцефалопатии.
Спинной мозг,
шейный
отдел: типичные изме-
нения у 85% больных
Присутствует
у 90 95% больных.
Выраженный,
преобладание
синтеза к цепей по
частоте и
выраженности
Первично
прогрессирую-
щийРС
симптоматиче-
ский
Симптомокомплексы
типичные. Прогресси-
рование неврологиче-
ского дефицита с первых
проявлений
Головной мозг: синдром
хронической воспали-
тельной демиелини
зации. Спинной мозг,
шейный
отдел:
типичные изменения
у 85% больных
Присутствует
у 90 95% больных.
Выраженный,
преобладание
синтеза к цепей по
частоте и
выраженности
Транзиторный
прогрессирую-
щий РС
Симптомокомплексы
типичные. После одного
обострения и ремиссии
неуклонное прогрессиро-
вание неврологического
дефицита
Головной мозг: синдром
хронической воспали-
тельной демиелиниза
ции. Спинной мозг,
шейный
отдел:
типичные изменения
Выраженный,
преобладает
синтез к цепей
Прогрессирую
ще рецидиви
рующий РС
Симптомокомплексы
типичные. Прогрессиро-
вание неврологического
дефицита с первых про-
явлений, наслаиваю-
щиеся обострения
Головной мозг: синдром
хронической воспали-
тельной демиелини
зации. Спинной мозг,
шейный
отдел:
типичные изменения
Выраженный,
преобладает
синтез к цепей
го
со
го
со
со
Категория
Основные клинические
проявления
Данные МРТ
Интратекальный
гуморальный
иммунный ответ
Комментарии
Фульминантный
PC (Марбурга) Симптомокомплексы
типичные,сочетание
быстро прогрессирующих
полушарных, стволовых
и спинальных симптомов,
обычно со смертельным
исходом в первые
несколько месяцев
Головной мозг: синдром
острой воспалительной
демиелинизации с немно-
гочисленными, крупными,
сливающимися, иногда
опухолеподобными очага-
ми в полушариях большого
мозга. Большинство очагов
накапливают контраст (нет
диссеминации во времени,
в том числе в связи с быс-
тротечностью и постоян-
ной активностью процесса)
Отсутствует
Редкая форма
демиелинизирующего
заболевания
PC,
ассоциирован-
ный с нейро
инфекцией
Симптомокомплексы
типичные для рециди
вирующе ремиттирую
щего РС, более частые и
тяжелые обострения,
возможны проявления со
стороны других систем и
органов, характерные
для соответствующего
инфекционного процесса
Головной мозг: синдром
острой воспалительной
демиелинизации (часто)
или синдром хронической
воспалительной демиели-
низации, иногда в сочета-
нии с нехарактерными для
PC изменениями (гипокси
чески ишемическими,
геморрагическими, вовле-
чением серого вещества).
Спинной мозг,
шейный
отдел: типичные
изменения
Выраженный,
нередко «парал-
лельный»
интратекальный
синтез как к ,
так и Х цепей
Подтверждение нали-
чия инфекции при
комплексном исследо-
вании ЦСЖ и сыворот-
ки. Целесообразно
зтиотропное лечение,
которое может благо-
приятно повлиять на
последующее течение
болезни
Острый
диссеминированный
энцефаломиелит
одэм,
Монофазный
Острое или подострое
развитие общемозговой
и очаговой / многоочаго-
вой симптоматики, указы-
вающей на вовлечение
белого и серого вещест-
ва головного мозга.
У взрослых нередко под-
острое прогрессирование
симптомов. Возможны
системные проявления.
Последующая стабилиза-
ция процесса и разная
степень восстановления
функций
Головной мозг: синдром
острой воспалительной
демиелинизации с мно-
гочисленными очагами
в белом и нередко ---
сером веществе (кора,
базальные ганглии),
массивность пораже-
ния, нетдиссеминации
во времени. Спинной
мозг вовлекается реже,
чем при РС
Отсутствует
у большинства
больных
Идиопатический вариант
ОДЭМ по клиническим и
другим проявлениям
часто не отличается от
поствакцинального и
постинфекционного
ОДЭМ,
рецидиви-
рующий
Симптомы не отличаются
от монофазного ОДЭМ.
Рецидивы чаще единич-
ные, развиваются либо
в первый год болезни,
либо спустя много лет
Головной мозг: синдром
острой воспалительной
демиелинизации
с очагами в белом и
нередко --- в сером ве-
ществе (кора, базаль-
ные ганглии), массив-
ность поражения. Реци-
див часто сопровожда-
ется появлением новых
очагов
Чаще
отсутствует
Прогностические
факторы
рецидивирующего
течения не
идентифицированы
го
со
со
Категория
Основные клинические
проявления
Данные МРТ
Интратекальный
гуморальный
иммунный ответ
Комментарии
ОДЭМ,
мультифазный Острое развитие обще-
мозговой и очаговой /
многоочаговой симпто-
матики, указывающей на
вовлечение белого и се-
рого вещества головного
мозга. Короткие периоды
стабилизации (2 3 неде-
ли) сменяются усилени-
ем прежних и (или) появ-
лением новых симпто-
мов. В течение года воз-
можна стабилизация про-
цесса и разная степень
восстановления функций
Головной мозг: синдром
острой воспалительной
демиелинизации
с очагами в белом и
нередко --- в сером ве-
ществе (кора, базаль
ные ганглии), массив-
ность поражения.
Характерна диссемина
ция во времени.
Спинной мозг,
шейный
отдел: изменения,
типичные для РС
Чаще
отсутствует
Вероятна ассоциация
с нейроинфекцией
(вирусы герпетической
группы)
ОДЭМ,
ассоциирован-
ный с нейро
инфекцией
Проявления, характер-
ные для ОДЭМ, чаще
рецидивирующее или
мультифазное течение.
Длительность активности
болезни может быть
связана с активностью
сопутствующей
инфекции
Головной мозг: синдром
острой воспалительной
демиелинизации
с очагами в белом и
нередко --- в сером
веществе (кора, базаль
ные ганглии), часто мас-
сивность поражения.
Возможна диссемина
ция во времени.
В одних случаях
отсутствует, в
других--- при-
сутствует на фо-
не системного
ответа, нередко
с «параллель-
ной» гиперпро-
дукцией как к ,
так и ^ цепей
Переходная
форма
демиелинизи
рующего
заболевания
Начальный период болез-
ни (до 1 2 лет) соответ-
ствует рецидивирующему
или мультифазному
ОДЭМ, в дальнейшем
клинические проявления
не противоречат рециди
вирующе ремиттирующе
му РС
В начальный период бо-
лезни МРТ проявления
соответствуют мульти-
фазному ОДЭМ, в даль-
нейшем могут быть
неотличимы от РС
В одних случаях
отсутствует, в
других --- выра-
женный. Тип
ответа не меня-
ется в ходе
заболевания
Редкая форма
демиелинизирующего
заболевания
Другие
демиелинизирующие
заболевания
Неврит
зрительного
нерва, односто-
ронний
Типичные: локальная
боль за глазным
яблоком, снижение
остроты зрения, скотома
Головной мозг: без из-
менений или единичные
мелкие очаги*. Специ-
альные МРТ режимы
иногда выявляют пора-
жение зрительного
нерва
Отсутствует
Если выявлены типичные
изменения на МРТ и в
ЦСЖ, устанавливают
диагноз РС**
Неврит
зрительного
нерва, двусто-
ронний***
Типичные: локальная
боль, снижение остроты
зрения, скотома. Интер-
вал между поражением
одного и другого нервов
1 2 месяца
Головной мозг: без
изменений или единич-
ные мелкие очаги. Стан-
дартные МРТ режимы
могут выявлять
поражение зрительных
нервов
Отсутствует
Как изолированный синд-
ром чаще встречается в
детском возрасте.
У взрослых в большин-
стве случаев как началь-
ное проявление оптико
миелита. Если выявлены
типичные изменения на
МРТ и в ЦСЖ, устанавли-
вают диагноз РС**
Категория
Основные клинические
проявления
Данные МРТ
Интратекальный
гуморальный
иммунный ответ
Комментарии
Острый
поперечный
миелит ---
монофазный ---
рецидиви-
рующий
Симптомы указывают на
симметричное субтоталь-
ное поперечное поражение
спинного мозга, чаще на
шейно грудном уровне.
При рецидивирующем те-
чении рецидивы чаще еди-
ничные, иногда с интерва-
лом несколько лет
Головной мозг: без изме-
нений или единичные мел-
кие очаги. Спинной мозг:
очаги по протяженности
более 2 позвоночных
сегментов, на аксиальных
срезах --- субтотальное
поперечное поражение,
в остром периоде отек
с веретенообразным утол-
щением спинного мозга
Чаще
отсутствует
Может быть начальным
проявлением оптикомие
лита. Клинические приз-
наки асимметричного
парциального поражения
спинного мозга, МРТ
очаги по протяженности
менее 2 позвоночных сег-
ментов, типичные изме-
нения на МРТ головного
мозга и в ЦСЖ указывают
на РС**
Оптикомиелит
Девика ---
монофазный ---
рецидивирую-
щий
Развитие 2 стороннего
неврита зрительных нер-
вов с последующим попе-
речным миелитом (или в
обратной последователь-
ности). При рецидивирую-
щем варианте интервал
между поражением разных
отделов --- от нескольких
месяцев до нескольких
лет. Восстановление функ-
ций незначительное, тяже-
лый остаточный невроло-
гический дефицит. Редко
хороший регресс
Головной мозг: без изме-
нений или единичные мел-
кие очаги. Может визуали-
зироваться поражение
зрительных нервов с выра-
женными признаками оте-
ка. Спинной мозг: очаги по
протяженности более
2 позвоночных сегментов,
на аксиальных срезах ---
субтотальное поперечное
поражение, в остром пери-
оде отек с веретенообраз-
ным утолщением спинного
мозга
Чаще
отсутствует
Заболевание редкое
у лиц европеоидной ра-
сы, чаще встречается
в этнических группах юго
восточной Азии. В слу-
чаях рецидивирующего
оптикомиелита с МРТ и
ЦСЖ признаками, типич-
ными для РС, устанавли-
вают диагноз РС**
Концентриче-
ский склероз
(Бало)
Острое, быстро прогрессиру-
ющее развитие общемозго-
вой и очаговой / многоочаго-
вой симптоматики, указыва-
ющей на вовлечение белого
и серого вещества головного
мозга, обычно со смертель-
ным исходом в первые неде-
ли --- месяцы болезни
Диффузный
склероз
(Шильдера)
Первые проявления острые
(эпилептиформные припад-
ки) или подостро прогресси-
рующие (когнитивные, пове-
денческие расстройства),
свидетельствующие о вовле-
чении серого вещества; впо-
следствии присоединяются
симптомокомплексы, харак-
терные для поражения бело-
го вещества головного моз-
га. Течение прогрессирую-
щее, возможны периоды ста-
билизации. Смертельный
исход через 1 2 года
Головной мозг: единичные,
увеличивающиеся в диамет-
ре опухолеподобные очаги
в полушариях большого моз-
га с характерной концентри-
ческой полосатой исчерчен
ностью (на Т2 , а также на
Т1 постконтрастных изобра-
жениях). Зрительные нервы,
ствол и мозжечок интактны.
Спинной мозг не изменен
Описан в час-
ти случаев
Редкая форма демие
линизирующего забо-
левания, встречается
преимущественно
в этнических группах
юго восточной Азии
Головной мозг: 2 увеличива-
ющихся в размерах очага
в полушариях большого моз-
га (по одному в каждом)
с распространенным пери
фокальным отеком; или уве-
личивающиеся пери и пара
вентрикулярные поля изме-
ненного сигнала, впослед-
ствии с субтотальным вовле-
чением супратенториального
белого вещества, «пятнис-
тым» контрастированием.
Спинной мозг не изменен
Отсутствует.
Может наблю-
даться крайне
низкое содер-
жание 1д и
легких цепей
1двЦСЖ
Редкая форма демие
линизирующего забо-
левания. Вероятна
ассоциация с актива
циией нейроинфекции
(вирусы герпетической
группы)
со
Категория
Основные клинические
проявления
Данные МРТ
Интратекальный
гуморальный
иммунный ответ
Комментарии
Неуточненное
демиелинизи
рующее
заболевание
ЦНС
Клинические проявления
(симптомы, топика пора-
жения, особенности тече-
ния) не позволяют отнес-
ти заболевание к другим
категориям
Гэловной мозг: очаги,
как правило, немного-
численные, не позво-
ляющие судить об их
специфичности
Присутствует
синтез к цепей,
чаще выражен
слабо
Целесообразно динами-
ческое наблюдение и
повторное обследование
для уточнения диагноза
* МРТ очаги, гиперинтенсивные на Т2 изображениях и изо или гипоинтенсивные на Т1 изображениях.
** В соответствии с критериями W.I.McDonald.
*** Двухсторонний неврит зрительного нерва условно относится к одноочаговым синдромам при развитии
двухстороннего поражения с интервалом менее 1 мес.
Чаще всего поражается шейный отдел спинного мозга, как правило, верхне-
шейные сегменты, что объясняется большим количеством миелинизированных
волокон по сравнению с другими отделами.
Оптикомиелит также характеризуется последовательным или одновремен-
ным двусторонним тяжелым поражением зрительных нервов, с отеком в остром
периоде и последующей атрофией (рис. 8.17). Изменения в зрительных нервах
видны как при исследовании глазного дна, так и на МРТ изображениях. Пос-
ледние, в отличие от PC, захватывают зрительные нервы на большом протяже-
нии. В головном мозге регистрируются единичные мелкие очажки, не имеющие
специфических признаков. В некоторых случаях имеет место более массивное
поражение головного мозга, соответствующее PC.
МРТ различия, выявляемые при разных клинических вариантах ОДЭМ,
а также при оптикомиелите, вряд ли отражают только степень тяжести заболе-
вания. Иммунологические характеристики вариантов демиелинизирующихза-
болеваний также различаются, что позволяет интерпретировать часть случаев как
атипичный PC. Стратифицированный подход к лечению в будущем может по-
зволить систематизировать эти редкие формы демиелинизирующих заболева-
ний (табл. 8.3).
МРТ ПРОЯВЛЕНИЯ СИСТЕМНЫХ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ
И ДРУГИХ ВАСКУЛОПАТИЙ
Проявления системных аутоиммунных заболеваний включают в себя васкули
ты, васкулопатии и коагулопатии. Реже эти синдромы сопровождают органоспе
цифические аутоиммунные заболевания, например, аутоиммунные тиреоидиты.
В тех и других случаях возможно поражение нервной системы, как обусловленное
самим иммунопатологическим процессом, в частности аутоантителами, так и опос-
редованное поражением сосудов. Последнее формирует состояния с разным мор-
фологическим субстратом, но обозначаемые единым термином «small vessel
disease* --- ангиопатия с поражением мелких сосудов. Диагностические трудности
особенно велики, когда неврологические проявления преобладают или даже явля-
ются изолированными на фоне субклинического течения основного заболевания.
При лучевом исследовании в таких случаях может быть выявлена картина
многоочагового поражения, напоминающая PC и описываемая в литературе как
«МРТ синдром РС». Кроме того, сходство с PC могут иметь МРТ проявления
ангиопатии и микроангиопатии при цереброваскулярных заболеваниях, кото-
рые встречаются у 5% лиц старших возрастных групп, а также при артериаль-
ных гипертензиях и сахарном диабете в молодом возрасте.
У большинства пациентов с системными аутоиммунными заболеваниями и
другими васкулопатиями МРТ картина имеет отличия от таковой при PC
(табл. 8.4).
Иногда интерпретация МРТ данных представляет значительные затруднения.
В таких случаях имеют место как признаки, характерные для ангиопатий/мик
роангиопатий, так и типичные черты PC. Всегда следует помнить, что МРТ яв
ляется лишь дополнительным методом диагностики, и тем не менее данные ней
ровизуализации не следует игнорировать. Учитывая значительную распростра-
ненность как РС, так и многих аутоиммунных заболеваний, в каждом подобном
случае необходимо предположить возможность одного из следующих вариантов:
а) случайное сочетание двух заболеваний;
Таблица 8.4
Характеристика многоочаговых МРТ изменений при церебральных
ангиопатиях/микроангиопатиях и рассеянном склерозе
МРТ
семиотика
Изменения при ангиопатиях
Изменения при рассеянном
склерозе
Очаговые
изменения
в белом
веществе
Мелкие очаги, округлой или
неправильной формы («звезд-
ное небо», «клочья ваты»);
субэпендимальные очаги еди-
ничные; в паравентрикулярных
зонах смежного кровообраще-
ния --- очаги в виде «нитки
бус», вытянутой в переднезад
нем направлении; более круп-
ные ишемические очаги могут
быть типичной клиновидной
формы
Округлые и овоидные очаги,
с преимущественной локализа-
цией в субэпендимальных и
субкортикальных отделах бе-
лого вещества, ориентирован-
ных длинной осью перпендику-
лярно стенке желудочка; часто
очаги в средних ножках моз-
жечка, мозолистом теле
Возможность
выявления
изменений на
Т2 и Т1 ВИ
Визуализируются с одинаковой
частотой
На Т1 ВИ отмечается меньшее
количество очагов, чем на Т2
ВИ
Очаги в сером
веществе
Типичны
Встречаются крайне редко
Реакция на
внутривен-
ное контра-
стирование
Наблюдается редко, только в
острых случаях
Наблюдается нередко, типична
при обострении процесса,
характерны одномоментное
наличие активных очагов и
изменений, не реагирующих на
внутривенное контрастирова-
ние, а также диссеминация во
времени
Лейкоарайоз Зональные изменения сигнала
от белого вещества преиму-
щественно у задних и в мень-
шей степени у передних рогов
боковых желудочков, могут
сочетаться с очагами (чаще
неправильной или треугольной
формы, могут быть
симметричными)
Зональные или более диф-
фузные изменения сигнала от
белого вещества у задних и
передних рогов боковых
желудочков; в этих же зонах
могут быть типичные для РС
овоидные и/или округлые
Окончание табл. 8.4
МРТ
семиотика
Изменения при ангиопатиях
Изменения при рассеянном
склерозе
Расширение
периваску
лярных
пространств
Резко выражено как в супра
тенториальных отделах белого
вещества, так и на уровне ба
зальных ганглиев. Часто сим-
метричное, иногда --- резко
асимметричное. FLAIR ИП
нередко выявляет кистозно
глиозные изменения. Множест-
венные вытянутые, щелевид
ной формы участки в белом
веществе у задних рогов боко-
вых желудочков, расположен-
ных радиально от желудочков
к коре; реже подобные измене-
ния видны на сагиттальных
срезах в семиовальных цент-
рах
Выраженность слабая;
нарастает с возрастом
больного; умеренная --- при
длительном РС.Щелевидной
формы участки измененного
сигнала, чаще у задних рогов,
расположенные радиально,
вытянутые от желудочков
к коре. Практически всегда
сочетаются с типичными РС
очагами
Расширение
ликворсодер
жащих прост-
ранств
Смешанная заместительная
гидроцефалия, возможно ви-
карное расширение желудочка,
если очаг прилежит к нему
Преимущественно внутренняя
заместительная гидроцефа-
лия, связанная с утратой
аксонов
б) общность эндогенных факторов, которые способствуют развитию одного
заболевания при наличии другого (в этом случае эпидемиологические данные
указывают на более высокую, чем случайная, частоту сочетаний);
в) наличие фенокопии, т. е. «синдрома» PC при системном аутоиммунном
заболевании.
В практической деятельности в подобных случаях целесообразно устанавли-
вать диагноз PC не только в соответствии с международными критериями, но и
с использованием всего спектра диагностических инструментов: данных клини-
ческого, инструментального (МРТ и исследование вызванных потенциалов), а
также лабораторного обследования (исследование цереброспинальной жидкости
для выявления характерного интратекального синтеза иммуноглобулинов).
Список литературы
1. Бринар В.В., Позер Ч.М. Лабораторные методы в диагностике рассеянного
склероза //Журн. неврол. и психиатр.--- 2002.--- No 1 (специальный выпуск).---
С. 7 14.
2. Poser СМ. et al. New diagnostic criteria for multiple sclerosis: guidelines for
research protocols//Ann. Neurol.--- 1983.---Vol. 13.--- P. 227 231.
Глава 9
ИНФЕКЦИОННЫЕ3АБОЛЕВАНИЯ
ГОЛОВНОГО МОЗГА
Если твой сосед по парте
стал источником заразы,
Обними его --- ив школу
две недели не пойдешь
Г. Остер
Методы нейровизуализации играют важную роль в диагностике изменений
и мониторинге состояния мозга при инфекционных заболеваниях. Перед ней
рорадиологом ставится ряд стандартных вопросов, на которые должен быть дан
ответ:
--- наличие патологического процесса и объяснение причины неврологичес-
кой дисфункции;
--- локализация изменений;
--- пути инфицирования;
--- характер патологического процесса;
--- осложнения;
--- прогноз;
--- динамический контроль, оценка эффективности проводимых лечебных
мероприятий.
Головной мозг хорошо защищен от патогенных факторов. Череп, твердая
мозговая оболочка, гематоэнцефалический и гематоликворный барьеры, об-
разуют несколько уровней достаточно эффективной защиты. Так, даже ин
траартериальное введение патогенной флоры далеко не всегда вызывает фор-
мирование очага воспаления, столь надежен ГЭБ. Вместе с тем, некоторые
структуры лишены этой защиты, например сосудистые сплетения, гипофиз,
эпифиз, гипоталамус, становясь, при неблагоприятном развитии событий,
входными воротами для инфекции. Проникновение инфекции возможно не-
сколькими путями: гематогенным, лимфогенным, контактным (путем прямой
пенетрации (рис. 9.1)) и ретроградным --- по периферическим нервам с аксо
нальной струей. Последний путь играет особую роль при вирусных инфек-
циях.
Принято выделять внутримозговую, внутрижелудочковую и оболочечную
локализацию изменений, но изолированные варианты встречаются нечасто. Как
правило, наблюдается сочетание --- менингоэнцефалит, эмпиема и абсцедиро
вание, энцефалит и вентрикулит и т. д.
в
б
Рис. 9.1. Аспергиллез головного мозга.
МРТ.
а --- Т2 ВИ, аксиальная плоскость;
б --- Т1 ВИ, корональная плоскость;
в --- Т1 ВИ, корональная плоскость после
контрастирования.
Массивное поражение левой гемисферы.
Изменения неоднородной структуры, ха-
рактеризуются изоинтенсивным сигна-
лом на Т2 ВИ (а), слабогиперинтенсив
ным на преконтрастном TI ВИ (б). Боко-
вой желудочек и субарахноидальное
пространство левой гемисферы мозга
компремированы. После контрастирова-
ния (в) наблюдается выраженное усиле-
ние интенсивности сигнала, выявляются
множественные полости, различного раз-
мера и формы.
ЛУЧЕВАЯ СЕМИОТИКА МЕНИНГИТОВ
Возможности лучевой диагностики при менингитахдостаточно ограничены.
Так, не удается определить этиологию менингита, часто патологические изме-
нения не определяются. Все это определяет место лучевых исследований в ком-
плексе диагностических мероприятий и показания к их проведению: диагнос-
тические трудности, стойкий неврологический дефицит, развитие осложнений,
медленное выздоровление.
Рис. 9.2. Менингит. МРТ.
В конвекситальных отделах левой те-
менной доли выявляется локальное
расширение субарахноидального про-
странства, интенсивность сигнала от
которого отличается от ликвора и ха-
рактеризуется гиперинтенсивным сиг-
налом на FLAIR ИП (а) и изображе-
нии, взвешенном по протонной плот-
ности (б). После ведения контрастного
вещества отмечается усиление интен-
сивности сигнала от твердой мозговой
оболочки (в).
При подозрении на менингит оптимальным методом исследования является
МРТ обязательно с внутривенным контрастированием.
В случаях не осложненного гнойного менингита КТ и МРТ изображения,
как правило, не изменены. На изображениях, полученных с помощью FLAIR
ИП, может отмечаться умеренно гиперинтенсивный сигнал от ликвора в су
барахноидальном пространстве, по сравнению с его неизмененными участками,
а также ликвором в желудочках мозга (рис. 9.2). Скопление экссудата обыч-
но локализуется прежде всего в проекции лобных долей и по ходу межполушар
ной щели. При этом иногда отмечается легкая сглаженность извилин. Наи-
более достоверным признаком воспалительного процесса является избиратель-
ное повышение интенсивности сигнала от оболочек мозга на постконтрастных
изображениях (рис. 9.3).
ЛУЧЕВАЯ СЕМИОТИКА ОСЛОЖНЕНИЙ МЕНИНГИТА
Лучевая диагностика оказывается наиболее эффективной и целесообразной
при развитии осложнений, к которым относятся гидроцефалия, венозный тром-
боз и васкулиты, субдуральный выпот, энцефалит, вентрикулит. Лучевая семи-
отика гидроцефалии, венозного тромбоза и васкулитов, осложненных венозным
инфарктом или OHM К соответственно, стандартна и описана в соответствую-
щих главах.
Выпот. У детей с менингитом, вызванном гемофильной палочкой, часто раз-
вивается стерильный субдуральный выпот. В таких случаях на КТ или МРТ
изображениях в лобно теменных отделах визуализируются серповидной формы
зоны патологического сигнала, характеристики которого соответствуют пара-
метрам неизмененного ликвора. Поражение всегда двухстороннее, регрессиру-
ющее в течение нескольких дней. Внутривенное контрастирование, какправи
Рис. 9.4. Менингит, осложненный
интракраниальной эмпиемой. МРТ.
Т1 ВИ после введения контрастного
вещества, корональная плоскость.
В конвекситальных отделах правой лоб-
ной доли выявляется линейной формы
эмпиема (указана стрелкой). Отмеча-
ется избирательное повышение интен-
сивности сигнала от измененной твер-
дой мозговой оболочки и капсулы эм-
пиемы.
Рис. 9.5. Эмпиема. КТ.
Накопление контрастного вещества по
капсуле.
ло, не эффективно. Иногда на пост-
контрастных изображениях отмечает-
ся локальное усиление прилежащей
поверхности вещества мозга, свиде-
тельствующее о наличии там острого
патологического процесса по типу вос-
паления или ишемии.
Интракраниальная эмпиема являет-
ся осложнением гнойного менингита,
особенно пневмококкового. Локали-
зация изменений зависит от расположения первичного фокуса воспаления. Так,
в случае конвекситалъного менингита эмпиема локализуется по конвексу, после
отита или синусита --- вдоль межполушарной щели, намета мозжечка, дна пе-
редней или средней черепной ямок. Эмпиема редко бывает двухсторонней. Кон-
фигурация патологической зоны может быть различная: линейная, серповид-
ная, линзовидная. По данным КТ денситометрии бывает сложно отличить гной
от иного морфологического субстрата. МРТ в этом отношении более эффек-
тивна: экссудат характеризуется гиперинтенсивным сигналом по сравнению
с ликвором. В прилежащих отделах вещества мозга возможно формирование
участка воспаления или ишемии, что прослеживается при лучевом исследо-
вании. На начальных стадиях формирования эмпиемы внутривенное контра-
стирование не эффективно. Через 1---3 недели на постконтрастных изображе-
ниях отчетливо прослеживается кольцевидное усиление, обусловленое либо на-
коплением препарата по капсуле, либо изменением прилежащего вещества
мозга (рис. 9.4, 9.5).
ЛУЧЕВАЯ СЕМИОТИКА ЭНЦЕФАЛИТОВ
При внутримозговой локализации процесса изменения могут носить очаго-
вый или диффузный характер. В качестве возбудителя могут выступать вирусы,
простейшие, патогенные грибы, бактерии. Фокальные поражения представле-
ны энцефалитами и абсцессами.
Энцефалит может развиваться как осложнение менингита при распрост-
ранении инфекционного процесса через тромбированные вены в паренхиму
мозга. При иных путях инфицирования фокус воспаления носит первичный
характер.
Энцефалит проявляется при МРТ участками патологической интенсивнос-
ти сигнала, параметры которого соответствуют отеку мозга. На постконтраст-
ном изображении отчетливо визуализируется нарушение ГЭБ. В процесс вовле-
кается^ белое, и серое вещество. На КТ изображениях энцефалит характери-
зуется зоной пониженной плотности, накапливающей контрастное вещество.
Чувствительность МРТ выше, чем КТ. В связи с тем, что не все случаи менинго
энцефалита видны на нативных М Р изображениях, внутривенное контрасти-
рование является обязательным методическим приемом при подозрение на вос-
паление вещества головного мозга.
Все большее значение в развитии патологического процесса в веществе моз-
га придается вирусу простого герпеса. По мнению A.C.Jackson вирус простого
герпеса является причиной острого вирусного энцефалита в 5---10% случаев.
Поражение обычно локализуется в медиальных отделах височных долей и ниж-
них лобных извилинах, теменно затылочных регионах. МРТ более чувстви-
тельный метод, чем КТ. Лучевая семиотика герпетического энцефалита не от-
личается от изменений, наблюдаемых в случаях иной этиологии. После вве-
дения контрастного препарата интенсивность сигнала изменяется во всем
объеме или только в сером веществе пораженной зоны. При этом в 80% слу-
чаев изменения носят двухсторонний характер и симметричны. У 75% боль-
ных наблюдается выраженный масс эффект, в 15% случаев прослеживается
геморрагический компонент, обусловленный выраженным некрозом вещества
мозга.
Лучевая семиотика герпетических энцефалитов у детей отличается от кар-
тины, наблюдаемой у взрослых. Ранние проявления поражения обусловлены
отеком мозга и визуализируются при КТ уже на вторые сутки после начала
заболевания в виде снижения плотности вещества до 12---15 и даже 5---8 ед. X
с признаками масс эффекта. При МРТ отек головного мозга отчетливо диф-
ференцируется уже на 1---2 й день после манифестации заболевания. У детей
первых 2 лет жизни изменения чаще носят диффузный характер, захватывая
до 60---85% площади. В большей степени плотность снижается у детей ранне-
го возраста, особенно недоношенных новорожденных, что связано с более вы-
сокой гидрофилъностью ткани мозга. Кроме снижения плотности в зоне оте-
ка наблюдается грубое нарушение структурности изображения мозга с отсут-
ствием дифференциации коры и белого вещества. В тяжелых случаях боковые
желудочки и другие ликворосодержащие пространства не дифференцируют-
ся, что отражает как сдавление данных структур вследствие значительного
масс эффекта, так и грубое снижение плотности перивентрикулярных отде-
лов белого вещества. При неонатальном герпетическом энцефалите указанные
изменения могут сохраняться в течение 2---3 недель. У детей более старшего
возраста и взрослых в остром периоде заболевания отек мозга обычно носит
менее выраженный характер. Это проявляется снижением плотности вещества
до 13,2---32,1 ед. X при объеме поражения, не превышающем 45---65% площа-
ди. В этой возрастной группе чаще выявляются локальные изменения. Наи-
более отчетливо признаки очагового поражения мозга при КТ визуализируются
на 4---7 й день заболевания, а у детей старше 3---4 лет и в более ранние сроки
(со 2---3 го дня болезни). Изменения обычно локализуются в височных и
в базальных отделах лобных долей в виде участков пониженной плотности
(6,7---16,2 ед. X), отражая известную тропность вируса простого герпеса к струк-
турам обонятельного мозга и лимбической системы. Изменения могут быть как
двух , так и односторонними, всегда сопровождаются объемным воздействием
на прилежащие структуры. Внутривенное контрастирование позволяет более
отчетливо визуализировать патологический участок, благодаря диффузному
накоплению контрастного препарата. Этот феномен отмечается уже с первых
дней заболевания, а его длительность коррелирует с продолжительностью вос-
палительного процесса в ЦНС, выявляемого при исследовании цереброспи-
нальной жидкости, и является его косвенным подтверждением.
Характерными признаками герпетического энцефалита являются деструк-
тивные изменения, обусловленные колликвационным некрозом. При морфоло-
гических исследованиях они наблюдаются более чем в 90% наблюдений уже на
3---5 й день болезни. При КТ признаки энцефаломаляции с формированием оча-
гов некроза удается проследить с 6---9 го дня болезни у 70---85% больных виде
гиподенсивных зон с нечеткими контурами (рис. 9.6). У новорожденных и детей
раннего возраста распознавай ие признаков формирующегося некроза отчетли-
во определяется лишь с 11 --- 19 го дня болезни.
В 17---55% случаев в остром периоде герпетического энцефалита развивают-
ся внутри мозговые кровоизлияния, выявляющиеся на 6---9 й день болезни
(рис. 9.7). Наиболее характерны мелкоточечные геморрагии до 0,5---0,8 см. Они
обычно локализуются в коре и субкортикальных отделах белого вещества боль-
ших полушарий, причем наибольшее их количество наблюдается в зонах мак-
симального поражения мозга на границе с очагами деструкции. Часто геморра
Рис. 9.6. Энцефалит. КТ.
Рис. 9.7. Больная К., 9 мес. Герпетический энцефалит. МРТ.
Массивная зона деструктивных изменений в левой височной доле (а, Т2 ВИ) с фор-
мированием внутримозговой гематомы в субкортикальных отделах белого вещества
(б, Т1 ВИ).
гни выявляются в подкорковых образованиях, преимущественно в области зри-
тельных бугров. У детей раннего возраста нередко определяется линейной фор-
мы имбибиция кровью границы коры и субкортикальных отделов белого веще-
ства. Реже выявляются более крупные кровоизлияния с формированием внут-
римозговой гематомы. Они имеют вид неправильной формы зон повышенной
плотности, размеры которых варьируют от 1,0 до 2,0 см. Возможны внутриже
лудочковые кровоизлияния.
Характер изменения М Р сигнала при герпетическом энцефалите зависит от
выраженности отека и кровоизлияния. Его параметры не отличаются от обыч-
ных характеристик этих морфологических субстратов. Манипулируя импульс-
ными последовательностями при МРТ, удается выявить участки деструкции и
формирующиеся кисты, а также дифференцировать их от отека на более ранних
сроках (на 5---7 й день болезни). Известны описания подкорковых и стволовых
форм герпетического энцефалита у детей старшего возраста и взрослых, подтвер-
ждаемые обнаружением очагов колликвационного некроза при патоморфологи
ческих исследованиях.
Лучевые методы исследования, в первую очередь КТ и МРТ, позволяют не
только диагностировать герпетический энцефалит, но и мониторировать про-
цесс, в том числе эффективность проводимой терапии. При этом оценивают
размеры старых очагов поражения и появление новых. Важным критерием яв
ляется сохраняющееся накопление контрастного вещества, указывающее на
продолжающийся воспалительный процесс.
Резидуальные изменения после герпетического энцефалита выявляются у де-
тей более чем в 85---90% случаев. Как правило, в преобладающем большинстве
наблюдений они сводятся к грубым кистозно глиозным изменениям на фоне
атрофического процесса различной степени выраженности с викарным расши-
рением ликворных пространств, выявляемым уже со 2---3 го месяца после забо-
левания. Очаговые изменения преобладают у детей, начиная с 3 лет жизни, и фор-
мируются к 3---4 му месяцу. Удетей первыхлетжизни изменения более чем впо
ловине случаев носят диффузный характер. Последствия поражения
подкорковых структур и мозжечка выявляются соответственно у 12% и 8% боль-
ных в виде кистозно атрофической перестройки вещества мозга.
Для оценки резидуальных изменений целесообразно проведение повторного
МРТ не ранее 4---6 месяцев от начала заболевания. Как правило, к этому сроку
формируется окончательная картина нейроструктурных изменений после пере-
несенного энцефалита. В дальнейшем возможно лишь незначительное нараста-
ние атрофическихявлений, не сказывающееся на состоянии пациента и не име-
ющее существенной диагностической значимости. Однако в ряде случаев при
динамическом наблюдении наблюдается уменьшение размеров локальных ки
стозно атрофических изменений на протяжении 1 ---3 лет, отражающее течение
репаративных процессов в ЦНС.
ЛУЧЕВАЯ СЕМИОТИКА АБСЦЕССА
При неблагоприятном течении энцефалита развивается абсцедирование.
Абсцесс вызывают практически все возбудители --- аэробы, анаэробы, грибы,
простейшие. Лучевая семиотика не зависит от вида возбудителя и будет одина-
кова и при криптококкозной, и при туберкулезной, и при бактериальной этио-
логии. Среди механизмов формирования абсцесса особую роль играет эмболия
и прямое распространение воспаления из соседнего очага, в том числе при трав-
мах. Сроки формирования капсулы варьируют в зависимости от иммунного
статуса больного, патогенных свойств возбудителя и др. Известно, что, чем ме-
нее выражено формирование капсулы, тем хуже прогноз заболевания. Выделя-
ют две стадии формирования абсцесса --- энцефалитическую и, непосредствен-
но, абсцедирование.
На КТ изображениях абсцесс представлен участком пониженной плотнос-
ти с перифокальным отеком и выраженным масс эффектом. Излюбленная ло-
кализация --- базальные ядра и субкортикальные отделы белого вещества. Как
правило, наблюдается выраженное кольцевидное накопление контрастирующе-
го препарата по капсуле, формирующейся примерно через две недели, что под-
черкивает зону некроза. Накопление контрастного вещества носит минималь-
ный характер у больных с иммунодефицитом, отражая низкую способность к от-
граничению процесса. Сказанное делает описанный выше симптом достаточно
важным прогностическим критерием.
контрастирования.
В субкортикальных отделах правой гемисферы мозга располагается патологичес-
кое образование с четкими контурами и отчетливо дифференцирующейся капсу-
лой. После введения контрастного вещества отмечается избирательное усиление
интенсивности сигнала по капсуле абсцесса. Выраженный масс эффект.
МРТ семиотика абсцессов существенно не отличается от описанной выше:
одиночное или множественные округлой формы поражения различных разме-
ров, с выраженным перифокальным отеком и объемным воздействием. Внутри-
венное введение производных гадолиния ведет к периферическому изменению
интенсивности сигнала, соответствуя капсуле абсцесса (рис. 9.8). Внутривен-
ное контрастирование при МРТ также позволяет прогнозировать формирова-
ние абсцесса в зоне энцефалита. В таких случаях на фоне фокуса воспаления
в месте формирования абсцесса начинают визуализироваться мелкие точечные
очаги избирательного повышения интенсивности сигнала.
Абсцедирование у детей отличается от формирования изменений у взрослых
большими размерами, быстрым ростом, перивентрикулярной локализацией,
плохим формированием капсулы.
ЛУЧЕВАЯ СЕМИОТИКА ВЕНТРИКУЛИТА
Вентрикулит --- достаточно частое осложнение. Наиболее типичный при-
знак --- появление патологических зон в гравитационнозависимых отделах же-
лудочковой системы: затылочные рога при положении пациента на спине и пе-
редние рога --- при положении на животе. На КТ и МРТ изображениях, указан-
ные отделы желудочковой системы кажутся «обрубленными». Желудочки всегда
дилатированы, а их стенки утолщены. На постконтрастных изображениях от-
мечается накопление контрастирующего препарата в эпендиме (рис. 9.9). Наи-
более тяжелое осложнение вентрикулита --- некроз перивентрикулярных отделов
белого вещества, обусловленный окклюзией субэпендимальных и перивентри-
кулярных вен. Исходом некроза является формирование множественных поло-
стей различных размеров, отделенных тонкими глиозными перегородками, что
отчетливо дифференцируется при использовании FLAIR ИП. В ряде случаев
формируются напряженные кисты «под давлением».
а
б
Рис. 9.9. Вентрикулит. МРТ.
На преконтрастном Т1 ВИ (а, корональная плоскость) правый боковой желудочек
компремирован, его стенки утолщены, интенсивность сигнала от ликвора в нем из-
менена, субэпендимальные отделы белого вещества отечны (стрелка). После введе-
ния контрастного вещества (б, аксиальная плоскость) отмечается усиление интен-
сивности сигнала от эпендимы переднего рога правого бокового желудочка. В бе-
лом веществе лобно височной области видны мелкие очаги накопления
контрастного вещества. Эффект «обрубленного» затылочного рога правого боково-
го желудочка.
ЛУЧЕВАЯ СЕМИОТИКА ВАСКУЛИТОВ
Многие инфекционные агенты вызывают церебральные васкулиты. Особенно
часто поражаются мелкие сосуды, расположенные в основании мозга. Инфици-
рование происходит путем гематогенной диссеминации или прямого контакта из
первоначального менингеального или паренхиматозного фокуса. Если патоло-
гический процесс исходит из стенки сосуда, то говорят о первичном васкулите.
Распространение воспаления из расположенной рядом паренхимы или оболочек
может вызывать вторичный васкулит. При гистологическом исследовании вы-
являют инфильтрацию стенки сосуда лейкоцитами, отек и пролиферативные
изменения в интиме. Это ведет к сужению сосуда и его тромбозу, чему способствуют
септические эмболы, с последующим инфарктом или разрывом сосуда с крово-
излиянием. При лучевом исследовании такие случаи манифестируют многооча-
говым поражением, представленным мелкими фокусами с признаками геморрагии.
У 35% больных с васкулитом развиваются ишемические изменения.
К редким васкулитам относятся гранулематозные ангииты, часто связанные
с инфекцией и лимфомой. При этом заболевании отмечается гигантоклеточная
инфильтрация мелкихлептоменингеальных артериол и венул, сопровождающа-
яся диффузной, часто двухсторонней моделью отека и петехиальными геморра
гиями, главным образом в белое вещество. Возможен тромбоз крупных артери-
альных стволов, что часто ведет к фатальному массивному инфаркту.
ЛУЧЕВАЯ СЕМИОТИКА НЕЙРОТУБЕРКУЛЕЗА
Туберкулезный менингит развивается вследствие гематогенной и лимфоген
ной диссеминации. Отчетливые неврологические проявления отмечаются при-
мерно через 6 месяцев после инфицирования. Менингит возникает при разры-
вах маленьких туберкулем коры головного и спинного мозга, их оболочек, сосу-
дистых сплетений. Патологический экссудат распространяется вдоль мягкой
оболочки по базальным цистернам, особенно по передней цистерне моста, вы-
зывая воспаление стенок менингиальных сосудов с последующими микро и
макроинфарктами. В результате блокады ликворных путей у больных развива-
ется гидроцефалия. Течение специфического васкулита может осложниться при-
соединением ОНМК.
МРТ позволяет идентифицировать экссудат, параметры которого отличны от
ликвора. Кроме этого, на изображениях, полученных в сагиттальной плоскости,
обращает внимание своеобразная конфигурация базальных цистерн, обуслов-
ленная толстым слоем желеобразного экссудата. На постконтрастных изобра-
жениях наблюдается значительное избирательное изменение интенсивности
сигнала от оболочек мозга. При развитии ишемических осложнений более чем
в 50% случаев поражаются базальные ядра и таламусы, связанные с вовлечени-
ем в процесс лентикулостриальных и таламо перфорирутощих артерий. Могут
быть кортикальные инфаркты. Их КТ и МРТ характеристики не отличаются от
обычной семиотики ишемии.
Рис. 9.10. Туберкулез головного мозга. КТ.
а --- преконтрастное изображение; б --- после введения контрастного вещества.
Многоочаговое поражение головного мозга. Очаги располагаются в субкортикаль-
ных отделах белого вещества, в левом зрительном бугре, накапливают контрастное
вещество.
б --- МРТ, корональная плоскость.
В зрительном бугре левой гемисферы определяется одиночный очаг, интенсивно,
гомогенно накапливающий контрастное вещество. Гранулема оказывает объемное
воздействие на третий желудочек.
Туберкулемы проявляются одиночными и множественными патологически-
ми очагами, расположенными в области базальных ядер, атакже на стыке бело-
го и серого вещества. Мелкие туберкуломы визуализируются при КТ как зоны
пониженной плотности, активно накапливающие контрастное вещество, с при-
знаками объемного воздействия (рис. 9.10). Крупные туберкулемы имеют вид
патологического образования повышенной плотности, окруженного умеренно
выраженным отеком. Достаточно часто они обызвестлены. При МРТ отсутствие
сигнала в случае обызвестления наблюдается только при достаточно большом
отложении извести. В целом, туберкулема гипоинтенсивна на Т2 ВИ. На пост-
контрастном изображении и при КТ, и при МРТ отмечается выраженное узло-
вое или кольцевидное накопление контрастного вещества (рис. 9.11). Как пра-
вило, внутривенное контрастирование позволяет проследить связь с изменен-
ными оболочками мозга.
Прионовая болезнь (болезнь Крейнцфельда --- Якоба или спонгиозная эн-
цефалопатия), как правило, при КТ не дифференцируется или отмечаются при-
знаки кортикальной атрофии. МРТ позволяет выявить на фоне атрофии сим-
метричные билатеральные изменения базальных ядер, зрительных бугров, ги-
поталамусов, периакведуктального региона (рис. 9.12). Возможно вовлечение
а
б
Рис. 9.12. Прионовая болезнь (болезнь Крейнцфельда --- Якоба).
МРТ, аксиальная плоскость, FLAIR ИП.
Симметричное поражение зрительных бугров (а), периакведуктального региона и
гипоталамуса (б).
в процесс серого и белого вещества церебральных гемисфер. Внутривенное кон-
трастирование не эффективно. Масс эффект не определяется.
Независимо от характера инфекции, обызвествления головного мозга яв-
ляются универсальными резидуальными изменениями. Они носят неспецифич-
ный характер и даже при морфологическом исследовании определить их эти-
ологию не представляется возможным. В зависимости от выраженности дес-
труктивного процесса развиваются рубцово атрофические изменения,
сопровождающиеся смешанной гидроцефалией. Отсроченным осложнением
герпетической инфекции является вторичная демиелинизация, с которой при-
ходиться сталкиваться в последние годы.
ДИАГНОСТИКА И ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ПОРАЖЕНИЙ
ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ У ВИЧ ИНФИЦИРОВАННЫХ
И БОЛЬНЫХ СПИДОМ
Широкое распространение синдрома приобретенного иммунодефицита
(СПИДа), принявшее время характер пандемии, полиорганность поражения и
неотвратимость исхода этого заболевания объясняют пристальное внимание
специалистов самого различного профиля. Поражение центральной нервной си-
стемы встречается в 30 90% случаев. Считается, что у 40---90% инфицирован-
ных заболевание манифестирует неврологическими проявлениями. Диагности-
ка на ранних этапах развития патологического процесса, когда лечебно профи-
лактические мероприятия наиболее эффективны, затруднена. Очаговая
неврологическая симптоматика становится очевидной, как правило, в терми-
нальном периоде развития заболевания.
Изменения головного мозга у ВИЧ инфицированных и больных СПИДом
могут быть обусловлены оппортунистической инфекцией, опухолью, церебровас
кулярным заболеванием, демиелинизирующим процессом, а также непосредствен-
ным действием вируса иммунодефицита. Поражения ЦНС могут развиваться од-
новременно или метахронно. Оппортунистические инфекции встречаются у 30%
больных. К ним относятся токсоплазмоз, герпетическая, цитомегаловирусная,
криптококковая, туберкулезная, паповавирусная и другие инфекции. Опухоли,
наблюдающиеся при иммунодефиците, обычно встречаются редко или протекают
атипично, как правило, речь идет о лимфоме. Примечательно, что клинические
проявления поражения головного мозга больше зависит от локализации измене-
ний, чем от этиологии. В 15---20% случаев встречаются одно и многоочаговые
поражения, сопровождающиеся масс эффектом или без него. Как и при воспа-
лительных заболеваниях у лиц с неизмененным иммунитетом, диагностика ба-
зируется на оценке прямых признаков патологического процесса и модели уси-
ления, которое менее отчетливо выражено, чем обычно.
Наиболее часто поражение головного мозга при иммунодефиците, без при-
знаков другой нейроинфекции, проявляется диффузной атрофией, которая на-
блюдается у 31 % обследуемых с бессимптомной формой ВИЧ инфекции, у 29%
пациентов с лимфаденопатическим синдромом, у 59% --- при наличии СПИД
связанных комплексов и у 70% больных СПИДом. Подобные изменения в кон-
трольной ВИЧ негативной группе составляют 9%. Ее клинико неврологичес
кий эквивалент --- СПИД ассоциированная деменция. Широко обсуждается
вопрос о роли цитомегаловирусной инфекции (ЦМВ) и высказывается пред-
положение, что именно сочетание ВИЧ и ЦМВ инфекций ведет к развитию
СПИД ассоциированной деменции. Особенно ярко картина ВИЧ энцефало-
патии проявляется у детей и, возможно, это связано с незрелостью вещества
мозга и, следовательно, его крайней ранимостью, как на этапе инфицирова-
ния, так и в дальнейшем. В таких случаях на фоне неблагоприятного премор
бидного фона и парентерального инфицирования, серьезные проявления не-
достаточности клеточного иммунитета, а также ВИЧ энцефалопатия разви-
ваются за относительно короткий период времени (5---8 лет). Так как ранним
симптомом ВИЧ энцефалопатии являются поведенческие изменения, то по-
явление данных симптомов требует включения в комплекс обследования КТ
или МРТ для своевременной диагностики поражения ЦНС и назначения спе-
цифической терапии.
Подострый ВИЧ энцефалит характеризуется выраженным атрофическим
процессом, прежде всего коры головного мозга, что при лучевом исследова-
нии проявляется расширением субарахноидального пространства и желудочков
мозга. Помимо атрофии возможны очаговые поражения. В таких случаях при
микроскопическом исследовании выявляется паренхиматозная и периваску
лярная инфильтрация лимфоцитами и макрофагами вокруг вен и капилляров
на уровне семиовальных центров, базальных ганглиев, моста. При этом в суб-
кортикальных отделах белого вещества лобных и теменных долей визуализи-
руются очаги, обусловленные демиелинизацией интракортикальных волокон
(рис. 9.13). При прогрессировании заболевания энцефалитические фокусы на-
чинают дифференцироваться и при КТ в ви-
де зон пониженной плотности с четкими кон-
турами. Внутривенное контрастирование не
эффективно. Изменения часто носят двусто-
ронний характер.
Описанная картина неспецифична и
встречается также при ЦМВ инфекции, кото-
рая также может проявляться диффузным по-
ражением глубоких отделов белого вещества
Рис. 9.13. Подострый ВИЧ энцефалит.
Т2 ВИ, аксиальная плоскость.
В субкортикальных отделах лобных и теменных
долей выявляются множественные очаги гипер-
интенсивного сигнала.
с четкими контурами, без перифокального отека. Такого рода изменения хоро-
шо видны при КГ. Характерно накопление контрастирующего препарата. Воз-
можно развитие вентрикулита с вовлечением в процесс перивентрикулярного
белого вещества.
Наиболее частой оппортунистической инфекцией у ВИЧ инфицированных
является токсоплазмоз, наблюдаемый у 33---70% больных. С морфологической
точки зрения он проявляется менингоэнцефалитом, абсцессами и гранулемами.
Поражение носит одно или многоочаговый характер с признаками масс
эффекта. Возможны кровоизлияния. При КГ определяется зона пониженной
плотности, активно накапливающая контрастное вещество, окруженная пе
рифокальным отеком. На постконтрастных изображениях выявляется цент-
ральная модель накопления контрастного препарата. Изменения локализуются
в субкортикальных отделах белого вещества, базальных ганглиях (рис. 9.14).
Одним из осложнений является формирование абсцесса. Абсцедирование
в своем развитии проходит несколько стадий и не отличается от обычных ха-
рактеристик абсцессов головного мозга другой этиологии. Подобно наблюде-
ниям за больными с неизмененным иммунитетом, капсула формируется при
а
б
Рис. 9.14. Токсоплазмоз. КТ.
На преконтрастном изображении (а) в зрительном бугре правой гемисферы распо-
лагается зона пониженной плотности, округлой формы, неоднородной структуры,
окруженная перифокальным отеком. Срединные структуры смещены. На посткон-
трастном изображении отмечается выраженное, гомогенное накопление контрас-
тного вещества (б).
Рис. 9.15. Токсоплазмоз. МРТ.
а --- Т2 ВИ, аксиальная плоскость;
б --- Т1 ВИ, аксиальная плоскость;
в --- постконтрастное Т1 ВИ,
аксиальная плоскость.
Многоочаговое поражение обеих
гемисфер мозга. Очаги окружены
зоной перифокального отека. Тела
боковых желудочков компремиро
ваны, борозды лобных долей сдав-
лены. На постконтрастном изобра-
жении отмечается усиление ин-
тенсивности сигнала от очагов.
мерно через две недели и хорошо накапливает контрастное вещество, но в 5%
наблюдений денситометрические характеристики не меняются, что имеет пло-
хое прогностическое значение, свидетельствуя об отсутствии иммунного от-
вета на инфекцию. Подобная картина может встретиться при грибковой ин-
фекции, туберкулезе, лимфоме.
В энцефалитическую фазу при МРТ с внутривенным контрастированием
наблюдается центральная модель избирательного изменения интенсивности
сигнала (рис. 9.15). На отсроченных срезах, полученных через 40 минут после
внутривенного введения производных гадолиния, отмечается появление пери-
ферического контрастного ободка (рис. 9.16). Описанный симптом позволяет
про водить дифференциальную диагностику с лимфомой.
Для токсоплазмоза характерен быстрый позитивный ответ на специфичную
терапию (в течение 10---14 дней). Учитывая частоту этой инфекции, многие ав-
торы рекомендуют во всех случаях очагового поражения проводить пробный курс.
Резидуальные изменения притоксоплазмозе обусловлены рубцово атрофи
ческим процессом, возможны обызвествления.
а
б
Рис. 9.16. Токсоплазмоз. МРТ.
Многоочаговое поражение преимущественно субкортикальной локализации с при-
знаками объемного воздействия (а). На постконтрастных изображениях (б) в ле-
вой лобной доле определяется кольцевидное усиление интенсивности сигнала,
с толстыми, неровными стенками. Более мелкие очаги, располагающиеся в правой
гемисфере мозга, характеризуются центральной моделью усиления интенсивнос-
ти сигнала.
Частым осложением ВИЧ инфекции является туберкулез, втом числе тубер-
кулезный менингит. Установлено, что ВИЧ инфекция усиливает риск развития
туберкулезного менингита, но не измененяет его клинического течения. В 37%
случаев встречаются паренхиматозные изменения. Гидроцефалия развивается
более чем у половины больных. Возможны вентрикулиты, эпендимиты, прояв-
ляющиеся утолщением стенки желудочка, изменением характеристик зоны ин-
тереса, активно реагирующей на введение контрастирующих препаратов. КТ и
МРТ проявления менингита неспецифичны. При возникновении некротичес-
ких изменений формируется одна или несколько гранулем (туберкулем)
(рис. 9.17). Масс эффект обычно отсутствует, перифокальный отек минимален.
Диагноз туберкулемы более вероятен при наличии обызвестлений в очаге. Тубер
кулема может осложнится присоединением васкулита. Обычно вовлекаются со-
суды основания мозга, особенно ВСА и базилярная артерия, а также их прокси-
мальные ветви. Конвекситальные сосуды поражаются менее часто. Течение це-
ребрального туберкулеза может осложниться развитием артериального инфаркта
как в бассейне крупного, так и мелкого сосуда или венозного инфаркта в ре-
зультате синус тромбоза. Абсцесс формируется редко. КТ и МРТ характерис-
тики идентичны с проявлениями пиогенного абсцесса: фокальное поражение
сначала солидного, позже кистоподобного типа с тонкой стенкой, перифокаль
ным отеком и явлениями масс эффекта.
Криптококкоз --- еще одна характерная для СПИДа нейроинфекция, встре-
чающаяся у 5---10% больных. Манифестирует заболевание менингитом, энце
Рис. 9.17. Туберкулезная гранулема. КТ.
а --- преконтрастное изображение; б --- постконтрастное изображение.
фалитом и, крайне редко, абсцессом. Два последних варианта представляют
собой фазы одного процесса. КТ и МРТ картина неспецифична --- отмечается
очаговое поражение с масс эффектом. Стенки у абсцесса обычно тонкие. Чаше
встречается криптококковый менингит. При этом наблюдается расширение пе
риваскулярных пространств, обусловленное скоплением мукоидного экссуда-
та в результате пролиферации криптококков. Методы интраскопии не могут эф-
фективно идентифицировать криптококкозный менингит, но МРТ отличается
более высокой чувствительностью, чем КТ. На уровне базальных ганглиев, ство-
ла мозга, конвекса визуализируются мелкие зоны патологической пониженной
плотности или измененного сигнала (подобно ликвору), следующие по ходу пер-
форирующих артерий. Их характеристики не отличаются от параметров неиз-
мененного ликвора. Перифокальный отек отсутствует. Примечательна неэффек-
тивность контрастного усиления при криптококкозном поражении, что объяс-
няется уникальными характеристиками этой инфекции и особенностями
иммунного статуса.
Нейросифилис встречается у 1,5--- 1,8% ВИЧ инфицированных, что состав-
ляет примерно 30% не леченных больных сифилисом. При этой инфекции раз-
вивается менинговаскулярное поражение или грануломатозный менингит, про-
являющийся в виде инсультов, васкулитов или гумм. Некоторые авторы счи-
тают, что при наличии острого нарушения мозгового кровообращения у больных
со СПИДом необходимо исключать нейросифилис. Фокальное поражение
(гумма) встречается достаточно редко --- менее 6% от всех больных с нейро
сифилисом. КТ и МРТ данные неспецифичны, наблюдается масс эффект,
умеренный перифокальный отек, реакция на внутривенное контрастирование.
Поражение, как правило, одиночное, локализующееся в области коры и обо-
лочек головного мозга.
Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) пред-
ставляет собой демиелинизирующее заболевание, являющееся результатом ре-
активации паповавируса у пациентов с иммунодефицитом любого генеза. По-
ражение ЦНС встречается, как правило, на поздних стадиях и только у 10%
больных ВИЧ инфекция манифестирует подобным образом. Поражаются
гемисферы, ствол мозга, мозжечок и спинной мозг. При гистологическом
исследовании выявляют изменения близкие к бляшкам рассеянного склеро-
за. Эффективной терапии нет. Летальный исход наступает в течение несколь-
ких месяцев. На MP томограммах выявляют округлые или овальные очаги
с тенденцией к слиянию. Изменения часто носят асимметричный характер. Пер-
воначально процесс локализуется в субкортикальных отделах белого вещества,
что при достаточно больших размерах очага придает фестончатость внешне-
му контуру. По мере прогрессирования заболевания поражаются перивентри
кулярные отделы белого вещества. Масс эффект и реакция на внутривенное
контрастирование отсутствуют.
Наиболее частой опухолью у ВИЧ инфицированных является первичная
лимфома, которая у пациентов с обычным иммунитетом встречается достаточно
редко --- менее 2%. При СПИДе частота этой опухоли увеличивается до 6% и,
как правило, связана с инфицированием вирусом Эпштейна --- Барр. Процесс
возникает вокруг сосудов и представлен иммунобластными клетками. Обычно
опухоль имеет вид солидного узла, но в половине случаев встречается многооча-
говое поражение. Поданным аутопсии эта цифра составляет 80---100%. Возмож-
но распространение на оболочки мозга. Геморрагии и обызвествления редки. Из-
менения локализуются в перивентрикулярном регионе, часто в процесс вовле-
каются базальные ганглии, таламус, прозрачная перегородка, мозолистое тело.
Наблюдается выраженный перифокальный отек. Опухолевые массы характе-
ризуются умеренно гипоинтенсивным на Т1 ВИ и умеренно гипер или изоин
тенсивным наТ2 ВИ сигналом при МРТ. После внутривенного введения кон-
трастного препарата отмечается изменение интенсивности сигнала по кольце-
видному или солидному типу. На КТ изображениях определяется гипо , изо
иногда умеренно гиперденсивное патологическое образование с гомогенным и
интенсивным накоплением контраста веером веществе или в периферических
отделах опухоли. Дифференцировать эту картину от изменений, присущих ток
соплазмозу, не представляется возможным, особенно при монофокальном вари-
анте поражения. В таких случаях целесообразно выполнение отсроченного по-
стконтрастного лучевого исследования. При токсоплазмозе на изображениях,
полученных через 40 минут после внутривенного контрастирования, отмечает-
ся появление или сохранение кольцевидной модели усиления, что не встречает-
ся прилимфоме.
Анализируя возможности лучевой диагностики следует отметить, что МРТ
отличается более высокой информативностью, чем КТ, уступая ей только в слу-
чаях обызвествлений (последствиях перенесенных ранее воспалительных про-
цессов). Уточнение этиологии воспалительного процесса или гистоструктуры
опухоли лишь по данным КТи М РТ представляется проблематичным. Только
комплексное клинико инструментальное обследование пациента позволяет от-
ветить на этот вопрос и то не всегда. Выявляемость и выраженность МРТ нахо-
док обычно не коррелирует с тяжестью иммунодефицита.
Таким образом, современные методы лучевой диагностики позволяют дать
адекватную оценку состоянию как вещества головного мозга, так и ликворных
пространств, что делает их незаменимыми при обследовании больных с подо-
зрением на нейроинфекцию. Обобщение опыта использования различных ме-
тодов нейровизуализации при инфекционных заболеваниях показывает, что ни
один из них не может гарантировать получение исчерпывающей диагностичес-
кой информации, что диктует в ряде случаев необходимость комплексного под-
хода и проведения динамического контроля.
Список основной литературы
1. Лобзин Ю.В. Руководство по инфекционным болезням.--- СПб.: Фолиант,
2000. С. 74 82.
2. Михайленко A.A., Осетров Б.А. Дифференциальная диагностика нервных
болезней: Руководство для врачей / Под ред. ГА. Акимова, М.М. Одинака.---
СПб.: Гиппократ, 2001. С. 635 647.
Глава 10
ЛУЧЕВАЯ ДИФФЕРЕНЦИАЛЬНАЯ
ДИАГНОСТИКА ОЧАГОВЫХ ПОРАЖЕНИЙ
ГОЛОВНОГО МОЗГА
Размышляя, мы создаем мир
Будда
К очаговым поражениям головного мозга принято относить разнообразные
патологические состояния сосудистого, опухолевого, демиелинизируюшего,
инфекционного и нейродегенеративного характера: ОДЭМ, дисциркуляторная
энцефалопатия (ДЭ), ВИЧ энцефалит, метастатическое поражение и др. Они
представляют собой весьма распространенные заболевания ЦНС и являются
частой причиной потери трудоспособности, инвалидности, а также смерти боль-
ных. Выбор оптимального метода лечения зависит от своевременного распозна-
вания характера патологического процесса, фазы развития, выявления точной
локализации и оценки распространенности зоны поражения. Очевидно, что раз-
нообразие патологических процессов, лежащих в основе очаговых поражений
ЦНС, создает серьезные диагностические проблемы, в разрешении которых
важную роль играют методы лучевого исследования.
М РТ представляет собой наиболее чувствительный метод выявления заболе-
ваний белого вещества. Изменения могут быть визуализированы раньше и
в большем объеме, чем при компьютерной томографии. Оптимальный алгоритм
МРТ обследования больных с подозрением на очаговое поражение головного
мозга включает:
1. Стандартное исследование головного мозга, представляющее собой пос-
ледовательное получение:
пристрелочные изображения в 3 плоскостях (определение анатомо топо
графических особенностей, планирование расположения диагностических изоб-
ражений в различных импульсных последовательностях);
Т2 ВИ и Pd (VE, FVE или FSE, SE ИП) в аксиальной плоскости (высокая
чувствительность позволяет выявить большинство возможных патологических
процессов при оптимальной толщине среза 5 мм, что позволяет избежать час-
тичного объемного эффекта);
Т1 ВИ (SEHn) в коронарной плоскости (выявление и уточнение характера
объемного воздействия).
2. При подозрении надемиелинизирующий процесс:
FLAIR ИП в аксиальной плоскости (подтверждение и уточнение характера
очагового поражения головного мозга);
Т2 ВИ (SE ИП) в сагиттальной плоскости (выявление изменений мозоли-
стого тела).
3. При подозрении на неопластический процесс:
постконтрастное Т1 ВИ (SE И П) в аксиальной плоскости, которое может
быть дополнено изображениями, выполненными в других плоскостях (подтвер-
ждение наличия неопластического процесса, возможное уточнение степени анап
лазии и гистологической структуры);
контрастная MP ангиография (выявление собственной сети опухоли).
4. При подозрении на сосудистое заболевание:
Т1 ВИ (SE ИП) и FLA1R ИП в оптимальное плоскости (выявление крово-
излияний);
МРАинтра или экстракраниальных сосудов (установление причины раз-
вития интрацеребрального процесса).
КГ является методом второго этапа, позволяет повысить специфичность ис-
следования и оказывает существенную помощь в проведении дифференциаль-
ной диагностики. Его применение обязательно при подозрении на обызвествле-
ние, острую гематому, повреждение костных структур.
Многообразие патологических процессов в головном мозге проявляется дос-
таточно ограниченным количеством лучевых синдромов, адекватно отражающих
патоморфологические изменения и встречающихся как изолированно, так и
в сочетании. Поэтому интерпретация МРТ и КТ изображений должна предус-
матривать не только констатацию наличия изменений, но и сопоставление их
с ведущими лучевыми синдромами. Это позволяет сузить круг заболеваний для
последующей внутрисиндромной дифференциальной диагностики.
Выделяют следующие лучевые синдромы.
Синдром острой воспалительной демиелинизации («дебют» или обострение PC,
ОДЭМ) представлен одно или многоочаговым поражением с признаками пери
фокального отека и тенденцией к слиянию. Отдельные очаги имеют крупные раз-
меры. В ряде случаев возникают значительные трудности при дифференциаль-
ной диагностике с опухолевым поражением, в разрешении которых помогает М РТ
контроль в динамике. При значительных размерах очага возможен умеренный
масс эффект, не соответствующий объему поражения. Изменения локализуются
в основном в белом веществе пери и суправентрикулярного регионов, преиму-
щественно субэпендимально и субкортикально, во внутренних капсулах, ство-
ле мозга. Вместе с тем при ОДЭМ изменения нередко наблюдаются в зрительных
буграх, лентикулярных ядрах. Наиболее чувствительным является Т2 ВИ, но
специфичность FLAIR ИП выше. НаТ1 ВИ прослеживаются умеренно гипоин
тенсивные очаги. Некоторые из них характеризуются резко пониженным сигналом
с формированием феномена «черных ям», отражающего участки наиболее глубо-
кого повреждения миелина. Внутривенное введение контрастного вещества обычно
приводит к изменению интенсивности сигнала на Т1 ВИ, отражая повышение
проницаемости ГЭБ. Как правило, такие изменения начинают визуализироваться
в первую неделю с момента инициации процесса. Реакция усиления постепен-
но исчезает спустя месяц с момента развития заболевания. Первоначально пост-
контрастные изображения демонстрируют центральную гомогенную модель
избирательного изменения сигнала, которая постепенно становится менее выра-
женной, неоднородной, со смещением зон усиления в периферические области.
При изначально грубом повреждении миелина на изображениях визуализируются
кистоподобные участки с однородным сигналом от центральных отделов, пара-
метры которого соответствуют характеристикам спинномозговой жидкости, с пе-
риферической моделью накопления производных гадолиния. МРТ и КТ при
знаки геморрагии в патологических зонах не выявляются. Очаги острой воспа-
лительной демиелинизации дифференцируются при КТ.
Характерным отличием острого очага является обратимость изменений, что
отчетливо проявляется при МРТ контроле в динамике.
Синдром хронической демиелинизации (РС, прогрессирующая мультифокальная
лейкоэнцефалопатия). Хронические бляшки РС в фазе ремиссии характеризу-
ются многоочаговыми изменениями типичной локализации, округлой или оваль-
ной формы, без признаков объемного воздействия, перифокального отека, нару-
шения ГЭБ. На Т1 ВИ и при КТ очаги не дифференцируются. Очаги имеют пра-
вильную округлую или овальную форму и ориентированы по ходу перфорирующих
сосудов, как правило, перивенулярно (перпендикулярно сагиттальной плоско-
сти). Для хронической демиелинизации типично поражение только белого веще-
ства. По мере прогрессирования заболевания нарастает атрофия вещества моз-
га, проявляющаяся сначала внутренней, а затем смешанной гидроцефалией. Фор-
мирование астроглиоза в бляшке приводит к появлению очагов на Т1 ВИ и носит
необратимый характер. Неоднородная структура хронической бляшки встреча-
ется при обострении заболевания. В этой фазе возможно появление патологических
изменений, присущих острой демиелинизации (отек, изменение интенсивности
сигнала на постконтрастных Т1 ВИ, тенденция отдельных очагов к слиянию), но
обычно менее выраженных, чем при манифестации заболевания. Для бляшек РС
характерна рассеянность во времени и пространстве, когда одни очаги появля-
ются, а другие исчезают. На одном срезе видны и очаги, находящиеся в стадии
обострения, и изменения, типичные для фазы ремиссии.
Синдром острой ишемии (ОНМ К) характеризуется зоной гиперинтенсивно-
го сигнала наТ2 ВИ и умеренно или слабогипоинтенсивного сигнала на Т1
ВИ с признаками объемного воздействия. Внутривенное введение контрастиру-
ющего препарата приводит к незначительному периферическому повышению
сигнала наТ1 ВИ по гиральному типу. Изменения визуализируются и при КТ
в виде гиподенсивных зон. Как правило, локализация поражения соответству-
ет бассейну кровоснабжения одного из магистральных сосудов. Типично рас-
пространение изменений на серое и белое вещество, вовлечение в процесс ба
зальных ядер, зрительных бугров. МРА обычно позволяет выявить причину ин
трацеребральных изменений.
Синдром хронической ишемии (энцефалопатия сосудистого генеза) проявля-
ется многоочаговым поражением. Все очаги отчетливо выявляются на Т2 и Т1
ВИ, а также при КТ. Характерной особенностью является паравентрикулярная
локализация изменений, что обусловлено особенностями кровоснабжения го-
ловного мозга. Субэпендимальная зона остается сравнительно интактной. Бо-
лее того, при расположении очага в непосредственной близости от стенки боко-
вого желудочка наблюдается ее подтягивание к сформировавшемуся глиомезо
дермальному рубцу, а при расположении поблизости от субарахноидального
пространства --- локальное расширение последнего. Типично вовлечение в про-
цесс базальных ядер и зрительных бугров. Очаги чаше всего ориентированы
параллельно сагиттальной плоскости, имеют крупные размеры и неправильную
форму. Их структура обычно неоднородная, возможна постишемическая кис
топодобная перестройка. Нередко выявляются последствия небольших крово-
излияний. Введение контрастирующего препарата не сопровождается измене-
нием МРТ или КТ картины. Планиметрические показатели свидетельствуют
о выраженных атрофических изменениях вещества, проявляющихся как внут-
ренней, так и наружной гидроцефалией.
Синдром геморрагии характеризуется разнообразными проявлениями, зави-
сящими от объема геморрагии и сроков, прошедших с момента кровоизлияния.
В острую фазу наиболее чувствительна КТ, демонстрирующая патогномонич
ное повышение плотности до 75 ед. X. Со временем специфичность КТ снижает-
ся, и через 2---3 месяца метод не позволяет дифференцировать постгеморрагичес-
кую кисту от постишемической. При МРТ свежая кровь проявляется в острей-
шую фазу резко гипоинтенсивным сигналом на Т2 ВИ. В дальнейшем
патогномоничные изменения начинают определяться в виде повышения интен-
сивности сигнала на Т1 ВИ лишь спустя несколько дней (3 суток) от момента
кровоизлияния. Исключение составляет FLAIR И П, позволяющая визуализи-
ровать свежую кровь в более ранние сроки. В дальнейшем М РТ картина обус-
ловлена степенью деградации эритроцитов. Но даже через несколько лет на ос-
новании данных МРТ (неоднородная структура патологического очага на Т1
ВИ, где участки повышенного сигнала чередуются с зонами пониженной
интенсивности, а также наличие характерного гемосидеринового ободка на Т2
ВИ) удается уверенно оценить природу изменений. Наряду с прямыми призна-
ками патологического процесса в зависимости от фазы эволюции очага гемор-
рагии выявляется локальное объемное воздействие.
Синдром рубцово атрофических изменений отражает резидуальное локальное
уменьшение объема вещества головного мозга и имеет неспецифический харак-
тер. Рубцово атрофические изменения обычно представлены кистозной пере-
стройкой с явлениями перифокального глиоза различной степени выраженнос-
ти, викарным расширением прилежащих отделов желудочковой системы и су
барахноидальных пространств. Оптимальные условия для дифференциации
кистозного компонента от астроглиоза создаются при использовании FLAIR И Р,
благодаря подавлению сигнала от спинномозговой жидкости. Изменения хоро-
шо визуализируются при КТ. Внутривенное введение контрастирующего пре-
парата свидетельствуют о сохранности ГЭБ.
Синдром бластоматозного роста проявляется одно или многоузловым пора-
жением, как правило, неоднородной структуры, с перифокальным отеком, при-
знаками нарушения ГЭБ и явлениями объемного воздействия. Этот синдром,
несомненно, является наиболее спорным, что обусловлено разнородностью и
неспецифичностью лучевых проявлений опухолевых поражений. Вместе с тем
любая опухоль характеризуется перифокальным отеком той или иной степени
выраженности. Патогномоничным, но сравнительно редко встречающимся при-
знаком следует считать лептоменингеальное метастазирование, выявляемое на
постконтрастных MP изображениях. Метастазы часто локализуются на стыке
белого и серого вещества.
Выявлена закономерность поражения различных отделов головного мозга.
Ограничения интракраниальныхрезервных пространств обусловлены, прежде
всего, локализацией, размерами опухоли и выраженностью перитуморозных
измененеий. Характер этих изменений зависит от гистоструктуры опухоли, типа
роста, ее размеров, близости кликворосодержащим пространствам. Бесконтра-
стная М РА позволяет оценить дислокацию сосудов в области интереса. Важная
диагностическая информация может быть получена при контрастной М РА, если
удается визуализировать собственную сосудистую сеть опухоли и артериовеноз
ные шунты, присущие злокачественным новообразованиям.
Синдром хронической нейроинфекции проявляется одно или многоочаговым
поражением без признаком масс эффекта. Изменения локализуются преимуще-
ственно в субкортикальных отделах белого вещества, а также в проекции базапьных
ядер. Субэпендимальные отделы остаются сравнительно интактными. Типична
атрофия головного мозга, проявляющаяся наружной или смешанной гидроцефа-
лией. Наиболее чувствительным оказывается Т2 ВИ. КТ и Т1 ВИ не позволяют
выявить очаги. При МРТ контроле в динамике увеличение или уменьшение
размеров очагов, признаки активизации процесса не определяются.
Синдром острой нейроинфекции характеризуется одно или многоочаговым
поражением головного мозга с признаками нарушения ГЭБ. Изменения могут
локализоваться в сером и белом веществе, а также оболочках головного мозга.
В наиболее тяжелых случаях поражение носит диффузный характер. Типично
выраженное объемное воздействие. При динамическом контроле прослежива-
ется прогрессирование или, наоборот, стихание признаков острого воспаления.
Хотя МРТ позволяет получить больший объем информации, КТ является мето-
дом выбора, благодаря удачному сочетанию скорости, информативности и дос-
тупности этого исследования.
Симметричное поражение подкорковых образований встречается при самых
разнообразных патологических состояниях: различных токсических воздействи-
ях, нейродегенеративных процессах, метаболических расстройствах, инфекци-
онных поражениях и т.д. Особое место среди симметричных поражений занима-
ют отложения тяжелых металлов (железа, марганца, меди).
Отложения железа в глубоких отделах серого вещества (бледные шары, пута
мены, хвостатые ядра, таламусы), также как в зубчатых ядрах, черной субстан-
ции, красных ядрах проявляются наТ2 ВИ гипоинтенсивными зонами и явля-
ются непрямым маркером церебрального нейродегенеративного процесса. Из-
вестно, что у молодых здоровых людей в норме может быть незначительное
отложение железа в черной субстанции, красных ядрах, зубчатых ядрах. В нор-
ме участки пониженной интенсивности, обусловленные отложением железа в ггу
тамене, начинают визуализироваться не ранее 60 лет. Гипоинтенсивный сигнал
отталамусов и хвостатых ядер во всех случаях, независимо от возраста, являет-
ся признаком патологического процесса. Отложение железа или его патологи-
ческое распределение может наблюдаться при различных заболеваниях ЦНС:
лейкодистрофии, аноксии мозга, цереброваскулярной болезни, болезни Галлер
вордена --- Шпатца, метаболических расстройствах, последствиях тяжелой че-
репно мозговой травмы.
Болезнь Галлервордена --- Шпатца является редким наследственным нейро
дегенеративным расстройством, связанным с патологическим накоплением в ве-
ществе мозга (бледные шары, ретикулярная часть черной субстации, красные ядра)
железосодержащего пигмента. Согласно современным представлениям эта болезнь
может быть отнесена к конформационным болезням ЦНС с дефектом простран-
ственной укладки нейрональных белков. Клиническая картина характеризует-
ся прогрессирующими экстрапирамидными и пирамидными нарушениями,
дистонией, хореоатетозом, тремором, поведенческими нарушениями, деменци
ей, дегенерацией сетчатки. Наиболее показательны симметричные изменения,
выявляемые при МРТ. Базальные ядра, прежде всего бледные шары, характери-
зуются гипоинтенсивным сигналом, независимо от типа взвешенности (рис. 10.1).
В ряде случаев на Т2 ВИ в центральных отделах зоны пониженной интенсивно-
сти определяется небольших размеров правильной формы участок гиперинтен-
сивного сигнала. Такая картина носит название «глаза тифа» и обусловлена умень-
шением объема ткани в связи с вакуолизацией и глиозом. В белом веществе воз-
можно появление признаков демиелинизации. Фоном описанных изменений
является диффузный атрофический процесса различной степени выраженнос-
ти. Верификация базируется на увеличении захвата59Fe базальными ганглиями.
Сравнительно малое количество патологических процессов манифестирует
гиперинтенсивным сигналом на Т1 ВИ. К ним относятся острая гематома, от-
равления марганцем, встречающиеся у электросварщиков, наркоманов, а так-
же у больных с печеночной недостаточностью, длительно находящихся на то-
тальном парентеральном питании. Клинико анамнестические данные, а также
профессиональный анамнез позволяют без особого труда решить дифференци-
ально диагностические проблемы.
Отравление марганцем проявляется на Т1 ВИ зонами повышенной интенсив-
ности сигнала, локализующимися вбазальныхядрах, с нечеткими очертаниями,
постепенно сливающимися с неизмененным веществом мозга (рис. 10.2). Т2 ВИ
неинформативно. Внутривенное контрастирование не эффективно. Масс эффект
не определяется. Фоном описанных изменений является диффузная атрофия,
возможны постишемические изменения. Описанная картина, выявленная у под-
ростка или молодого человека, позволяет с большой степенью достоверности
говорить о хроническом отравлении марганцем, обусловленном парентеральным
введением марганецсодержащих веществ (наркомания, токсикомания).
Энцефалопатия, обусловленная печеночной недостаточностью, характери-
зуется гиперинтенсивным сигналом, видимым наТ1 ВИ, в проекции лентику
лярных ядер, зрительных бугров, ствола мозга на фоне диффузного атрофичес
кого процесса, что связано с портосистемными шунтами и парентеральным пи-
танием с высоким содержанием марганца.
Особое место среди нейродегенеративных процессов занимает болезнь Ко-
новалова --- Вильсона (гепатолентикулярная дегенерация), обусловленная дефи-
цитом церрулоплазмина --- белка, переносчика меди. При этом развивается на-
рушение ее метаболизма и патологическое отложение в различных органах, преж
де всего в печени и головном мозге. Неврологическая симптоматика может как
быть обусловлена непосредственным отложением меди, так и быть результатом
энцефалопатии, обусловленной печеночной недостаточностью. У больных на-
блюдается псевдопаркинсонизм, двигательные нарушения, дисграфия, сниже
а
б
Рис. 10.1. Болезнь
Галлервордена --- Шпаца. МРТ.
а --- FLAIR ИП, аксиальная
плоскость;
б --- FLAIR ИП, корональная
плоскость;
в --- Т2 ВИ, аксиальная плоскость.
Бледные шары и черная субстация
имеют характерное понижение ин-
тенсивности сигнала.
Рис. 10.2. Отравление марганцем. МРТ.
Т1 ВИ.
В латеральном членике бледных шаров
видны четко очерченные зоны гиперин-
тенсивного сигнала.
мне понимания, психические расстрой
1
ства. Определенную помощь в диагно
3
стике оказывает офтальмологический
признак ---кольцо Кайзера ---Флейше BBt
рана радужке, связанное с отложением
меди. При МРТ чаще всего визуализи-
руется диффузная атрофия. Кпатогно
моничным признакам болезни Конова IL
•¥
Ш
лова --- Вильсона следует отнести выра-
женные гиперинтенсивные изменения на Т2 ВИ в базальныхядрах и таламусах,
также как и в белом веществе (рис. 10.3). Особенно часто поражаются путамены
и хвостатые ядра. Изменения могут быть выявлены в стволе мозга и в белом ве-
ществе мозжечка. Иногда на фоне умеренно повышенного сигн&та от лентику
лярных ядер определяются мелкие кистоподобные зоны. На Т1 ВИ они имеют
вид умеренно гипоинтенсивных изменений. Описанная картина обусловлена
отложением меди, а особенности сигнала объясняются ее парамагнитными свой-
ствами. При КТ отмечается снижение рентгеновской плотности от базальных
ядер. Верификация диагноза базируется на выявлении высокого содержания меди
в моче и церулоплазмина в сыворотке крови.
Таким образом, комбинация возможностей КТ (денситометрия, реакция на
внутривенное контрастирование) и МРТ (манипуляции различными типами
взвешенностей, модель усиления) позволяет высказать предположение о возмож-
ном морфологическом субстрате. Косвенные признаки, отражающие характер
деформации головного мозга и тип гидроцефально гипертензионнъгх изменений,
а также данные анамнеза и клинического обследования необходимы для под-
тверждения дифференциально диагностических сопоставлений. При интерпре-
тации изображений целесообразно выделение одноочаговых (большинство пер-
вичных новообразований, аномалии развития сосудов, нетравматические гема-
томы, ОНМК) и многоочаговых (PC, энцефалопатия сосудистого генеза,
метастазы и т.д.). Размеры, форма, локализация изменений, связь с анатоми-
ческими структурами позволяют определить модель патологического процесса.
Поэтому дифференциальная диагностика очаговых поражений базируется на
сопоставлении выявленных изменений с типичной моделью, учитывающей ко-
личество, локализацию, размеры, форму и структуру очагов, их реакцию на внут
Рис. 10.3. Болезнь Вильсона --- Коновалова. МРТ.
FLAIR ИП, аксиальная плоскость.
Поражение скорлупы, таламусов, белого вещества. Диффузная атрофия вещества
мозга.
ривенное контрастирование, состояние ликворосодержащих пространств и со-
судистых структур.
Основные принципы лучевой дифференциальной диагностики очаговых пора-
жений головного мозга
1. Патогенетический (локализация, ориентация, форма изменений). Так, в си-
лу особенностей морфогенеза бластоматозного процесса, можно говорить о пре-
имущественной локализации того или иного новообразования. Это верно и для
других типов патологических процессов.
2. Морфологический (интенсивность сигнала, а также изменение характерис-
тик очагов в зависимости от типа взвешенности, рентгеновской плотности в зоне
интереса, реакции на введение контрастирующего препарата). Морфологичес-
кий субстрат патологического очага определяет его лучевую семиотику.
3. Плани волюметрический (характер деформации и атрофии вещества мозга).
В тех случаях, когда выявленные изменения не соответствуют клиническим
проявлениям и не укладываются в типичную модель, наиболее информативны-
ми следует признать иммунологические исследования цереброспинальной жид-
кости с определением олигоклональных полос \% С, их индекса, свободных це-
пей 1я С различных типов. Кроме этого, дополнительная информация может быть
получена при нейрофизиологических исследованиях, позволяющих выявить
тонкие изменения функционального характера, связанные с нарушениями био-
химического обмена или микроциркуляции. В сложных случаях ответ может
быть получен только при динамическом контроле и пункционной биопсии с при-
менением МРТ/КТ для стереотаксического наведения, что представляет собой
третий этап диагностического процесса.
Большие надежды связаны с развитием таких современных технологий, как
перфузионная KT, исследование диффузии и перфузии при MPT, M Р спектро
скопия, ПЭТ и т.д. Но они требуют дорогостоящего оборудования, специально-
го программного обеспечения, высокой квалификации персонала и, что крайне
важно, детально разработанных и утвержденных стандартов. В настоящее вре-
мя в преобладающем большинстве случаев перечисленные технологии --- удел
единичных, в масштабе страны, лечебно профилактических и научно исследо-
вательских учреждений. Только поэтому мы позволили себе лишь вскользь кос-
нуться их возможностей и подробно остановиться на реально используемых
в практической работе методах и методиках.
Использование синдромного подхода для систематизации многообразных
M РТ и КТ проявлений очаговых поражений является одним из перспективных
путей повышения эффективности нозологической диагностики заболеваний
головного мозга.
Список основной литературы
1. Коновалов А.Н., Корниенко В.Н., Озерова В.И, Пронин И.Н. Нейрорентге
нология детского возраста.--- М.: Антидор, 2001.--- С. 60---113.
2. Коновалов А.П., Корниенко В.Н., Пронин И.Н. Магнитно резонансная то-
мография в нейрохирургии.--- М.: Видар, 1997.--- 315 с.
3. Шток В.Н., Иванова Смоленская H.A., Левин В.Н. Экстрапирамидные рас-
стройства: Руководство по диагностике и лечению.--- М.: МЕДпресс информ,
2002.
4. Юдина Г.К., Шоломов И.И. Семейный случай болезни Галлевордина ---
Шпатца // Журн. неврол. и психиатр.--- 2003.--- No 1.--- С. 49---50.
5. Barkovich J.A. Pediatric neuroimaging. 2 ed.--- N.Y.: Raven Press, 2000.
6. Edelman R.R., Hesselink J.R. Clinical magnetic resonance imaging.---
Philadelphia: W.B. Saunders company, 1990.--- P. 483 598.
7. Miller D.H., Kesselring J., McDonald W.I. etal. Magnetic Resonance in Multiple
Sclerosis.--- Cambridge: Cambridge University Press, 1997.--- 200 p.
8. Sartor K. Diagnostic and interventional neuroradiology. Thieme.--- Stuttgart New
York. 2002.
9. Stark D.D., Bradley W.G. Magnetic resonance imaging. 2nd ed.--- St. Louis:
Mosby Year Book, 1992. P. 988 1165.
10. ValkJ., van der Knaap M.S. Magnetic resonance of myelin, myeliniation and
disorders.--- Berlin: Springer Verlag, 1989.--- 325 p.
11. Warlow CR, Dennis M.S., van Gign J. etal. Stroke: a practical guide to mana-
gement.--- 2nd ed.--- Blackwell Science, 2002.--- 630 p.
ЗАКЛЮЧЕНИЕ
«Чем больше мы понимаем, как устроен головной мозг, тем лучше мы мо-
жем лечить его заболевания...» --- известная и всеми принимаемая мысль. Еще
в 1534 году Андрей Везалий произвел революцию в анатомии, опубликовав труд
«De Humani Corporis Fabrica» («О строении человеческого тела»), иллюстра-
ции для которого были написаны учениками Тициана, использовавшими в ка-
честве моделей головы казненных преступников. За прошедшие столетия че-
ловечество существенно продвинулось по пути знания и понимания святая
святых человека --- головного мозга. Достигнутый на сегодняшний день уро-
вень развития диагностических технологий позволяет успешно оценивать не
только структурные изменения, но и нарушения функционального характе-
ра. Поэтому методы нейровизуализации --- КТ, МРТ, ПЭТ --- должны рассмат-
риваться как взаимодополняющие, а не конкурирующие, что накладывает
дополнительную ответственность и предъявляет особые требования к специ-
алистам, участвующим в обследовании и лечении больных. Очевидно, что при
разработке диагностических тестов особое внимание должно уделяться ран-
ней диагностике. Наряду с этим требуется высокая специфичность. Поэтому
только комплексный мультидисциплинарный подход, включающий методы
лучевой диагностики, исследования цереброспинальной жидкости, нейрофи-
зиологические исследования и др., позволяет своевременно решить диагнос-
тические проблемы. Сегодня, несмотря на значительные успехи, мы как ни-
когда отчетливо понимаем ограниченность наших знаний и возможностей и
с тем большими надеждами вглядываемся в будущее, пытаясь ответить на
вечный вопрос: «Что день грядущий нам готовит?».