Author: Лидин Р.А. Молочко В.А. Андреева Л.Л.
Tags: неорганическая химия общая и неорганическая химия серия высшее образование химическая термодинамика издательство дрофа константы веществ химические формулы химическая терминология
ISBN: 5-7107-8085-5
Year: 2006
г—s—v^n^ v—I
I Высшее образование!
Константы
неорганических
веществ
СПРАВОЧНИК
Р. А. Лидин
Л. Л. Андреева
В. А. Молочко
Под редакцией
Р. А. Лидина
2-е издание,
переработанное
и дополненное
Москва-2006
УДК 546@35)
ББК 24.1я2
Л55
Лидии, Р. А.
Л 5 5 Константы неорганических веществ: справочник / Р. А. Лидин,
Л. Л. Андреева, В. А. Молочко ; под ред. Р. А. Лидина. — 2-е изд.,
перераб. и доп. — М.: Дрофа, 2006. —685, [3] с.
ISBN 5-7107-8085-5
Справочник включает сведения о более чем 3600 неорганических веществ
и 2400 минералах, выбор которых проводился с учетом их научно-лабораторной
и промышленной важности.
Константы веществ представлены в общепринятой табличной форме. Таблицы
всех разделов составлены по единому принципу, «входом» всегда служит химическая
формула.
Приведены физические свойства, необходимые химику, а также атомно-
молекулярные и термодинамические свойства, данные по окислительно-восста-
окислительно-восстановительной и кислотно-основной способности, растворимости веществ, сформу-
сформулированы основные положения номенклатуры и терминологии в химии.
Для студентов вузов, обучающихся по химическим и химико-технологическим
специальностям. Может быть использован преподавателями вузов, аспирантами,
научными сотрудниками, инженерно-техническими работниками.
УДК 546@35)
ББК 24.1я2
ISBN 5-7107-8085-5 © ООО «Дрофа», 2006
Неорганические
вещества
1. Классификация
Классификация неорганических веществ прошла долгий путь раз-
развития и складывалась постепенно, начиная с первых опытов алхими-
алхимиков, вплоть до наших дней, когда ученые-химики получили в свое
распоряжение совершенные физические приборы для исследования
состава, строения и взаимодействия веществ.
Классификация неорганических веществ базируется на их химиче-
химическом составе — наиболее простой и постоянной во времени характе-
характеристике. Химический состав вещества показывает, какие элементы
присутствуют в нем и в каком числовом отношении для их атомов.
Символы и названия химических элементов приведены в Пери-
Периодической системе элементов Д. И. Менделеева.
Элементы условно делятся на элементы с металлическими и неме-
неметаллическими свойствами. Первые из них чаще входят в состав
катионов многоэлементных веществ {металлические свойства),
вторые — в состав анионов (неметаллические свойства). В соот-
соответствии с Периодическим законом в периодах и группах между эти-
этими элементами находятся амфотерные элементы, проявляющие одно-
одновременно в той или иной мере металлические и неметаллические (ам-
(амфотерные, двойственные) свойства. Элементы VIIIA-группы продол-
продолжают рассматривать отдельно (благородные газы), хотя для Аг, Кг, Хе и
Rn обнаружены явно неметаллические свойства (элементы Не и Ne
химически инертны).
Классификация неорганических веществ приведена в сводной схеме.
Соответственно делению элементов классифицируют простые ве-
вещества, одноэлементные по составу и представляющие собой формы
нахождения элементов в свободном виде.
Все двух- и многоэлементные вещества называют сложными веще-
веществами, а многоатомные простые вещества и все сложные вещества
вместе — химическими соединениями (в них атомы одного или разных
элементов соединены между собой химическими связями).
Классификация сложных веществ первых трех классов по
составу основана на обязательном наличии в них самого распро-
распространенного в природе элемента —кислорода и на самом рас-
распространенном соединении кислорода — воде.
I. Неорганические вещества
Сводная схема классов веществ
1. Неорганические вещества
2.1. Металлы
Na, К, Мд, Са, Ва
2.2. Неметаллы
F2,O2,N2,CI2J
S,C
2.3. Амфотерные
(амфигены)
Al, Pb, Fe, Cr, Zn
2.4. Благородные
газы (аэрогены)
Не, Ne, Ar, Kr,
Хе, Rn
4.1. Основные
Na2O, K2O, МдО, СаО
4.2. Кислотные
СО2, Р2О5
4.3. Амфотерные
ZnO, AI2O3
4.4. Двойные
(Fe"FegH4
4. Оксиды
4.5. Несолеобразующие
СО, NO, SiO
5.1. Основные (основания)
NaOH, КОН, Мд(ОНJ, Са(ОНJ
5.2. Кислотные
(кислоты)
Н2СО3, H2SO4, HNO3
5. Гидроксиды
5.3. Амфотерные
Zn(OHJ, Pb(OHJ, AI(OHK, АЮ(ОН)
6.1. Средние
Na2CO3, K2SO4, Mg(NO3J, Ca3(PO4J
6.2. Кислые
NaHCO3, KHSO4, Са(Н2РО4J
6.3. Основные
Cu2CO3(OHJ, Fe(NO3)OH
6.4. Двойные
CaMg(CO3J, KAI(SO4J, K2Mg(SO4J
7.1. Бескислородные кислоты
HF, HCI, HBr, HI, H2S, HCN
7.2. Бескислородные соли
KBr, Na2S, Ba(HSJ, NH4CI, KMgCI3
7.3. Прочие
0F2, H2O2, NH3, CaH2, CaC2, Mg3N2, SCI2O2
CO
о
о
*
z
г
(D
00
CD
?
CD
О
H
n
6. Соли
7. Бинарные
соединения
I. Неорганические вещества
Первый класс сложных веществ — это оксиды, соединения ка-
катионов элементов (реальных или формальных) с кислородом(—II); их
общая формула 3x0y. К оксидам не относятся соединения кислорода
с фтором (простейшее из них O^F^1), а также пероксиды и надпе-
роксиды (Na2O2, КОО, включающие анионы из химически связанных
атомов кислорода О2~ и О^.
Второй класс сложных веществ — гидроксиды, получающиеся
при соединении оксидов с водой (чаще формально, реже реально).
По химическим свойствам различают кислотные (Н^ЭО^), основные
иамфотерные [M(OH)J гидроксиды, соответствующие кислотным,
основным и амфотерным оксидам.
Третий класс сложных веществ — соли, продукты взаимодейст-
взаимодействия (реального и формального) гидроксидов. Разные типы гидрокси-
дов реагируют между собой и образуют кислородсодержащие соли,
имеющие общую формулу МХ(ЭО^)Я и состоящие из катионов Мп+ и
анионов (кислотных остатков) ЭО*~. Такие соли называют средними
солями, а если они содержат два химически разных катиона — двой-
двойными. При наличии водорода в составе кислотного остатка соли назы-
называются кислыми, а при наличии гидроксогрупп ОН~ (иногда и ионов
О2~) — основными солями.
Четвертый класс сложных веществ — бинарные соединения, их
существование и образование логически не вытекает из цепочки пер-
первых трех классов (оксиды —> гидроксиды —> соли).
Классификация бинарных соединений не связана с наличием в них
кислорода(-И) и не основана на соединении такого кислорода — воде.
Фактически это обширный класс неорганических сложных ве-
веществ, не относящихся к оксидам, гидроксидам и солям и имеющих
разнообразные химические свойства.
Ниже даны определения (дефиниции) классов неорганических ве-
веществ с сохранением нумерации рубрик сводной таблицы.
1. Неорганические вещества — соединения, образуемые всеми хи-
химическими элементами (кроме большинства органических соедине-
соединений углерода). По химическому составу делятся на простые и слож-
сложные вещества.
2. Простые вещества образованы атомами одного элемента. По хи-
химическим свойствам делятся на металлы, неметаллы, амфотерные
простые вещества и благородные газы.
2.1. Металлы — простые вещества элементов с металлическими
свойствами (низкая электроотрицательность), например Li, Na, К,
Mg, Ca, Ba. Обладают высокой восстановительной способностью по
сравнению с типичными неметаллами. В электрохимическом ряду на-
напряжений стоят значительно левее водорода.
I. Неорганические вещества
2.2. Неметаллы — простые вещества элементов с неметаллически-
неметаллическими свойствами (высокая электроотрицательность), например F2, О2,
N2, Cl2, S, С. Обладают высокой окислительной способностью по
сравнению с типичными металлами.
2.3. Амфотерные простые вещества (амфигены) образованы элемен-
элементами с амфотерными (двойственными) свойствами (электроотрица-
(электроотрицательность промежуточная между металлами и неметаллами), напри-
например Be, Zn, Al, Cr, Pb, Fe. Обладают более низкой восстановительной
способностью по сравнению с типичными металлами. В электрохи-
электрохимическом ряду напряжений примыкают слева к водороду или стоят за
ним справа.
2.4. Благородные газы (аэрогены) — элементы VHIA-группы в сво-
свободном виде; Не и Ne химически пассивны, а Аг, Кг, Хе и Rn прояв-
проявляют некоторые свойства неметаллов с высокой электроотрицатель-
электроотрицательностью.
3. Сложные вещества образованы атомами разных элементов. По
составу и химическим свойствам делятся на оксиды, гидроксиды, со-
соли и бинарные соединения.
4. Оксиды — соединения элементов с кислородом (кроме соедине-
соединений фтора); не образуют соединений с кислородом только Не, Ne
и Аг. Степень окисления кислорода в оксидах равна -П. По составу
и химическим свойствам делятся на основные, кислотные, амфотер-
амфотерные, двойные и несолеобразующие оксиды.
4.1. Основные оксиды — продукты полной дегидратации (реальной
или условной) основных гидроксидов, например Li2O, Na2O, K2O,
MgO, CaO, BaO. Сохраняют химические свойства основных гидро-
гидроксидов.
4.2. Кислотные оксиды — продукты полной дегидратации (реаль-
(реальной или условной) кислотных гидроксидов, например СО2, SiO2, SO2,
SO3, P2O5. Сохраняют химические свойства кислотных гидроксидов.
Исключение: у оксида NO2 нет соответствующего кислотного гидро-
ксида, но при взаимодействии со щелочами он образует две соли, на-
например NaNO2 и NaNO3.
4.3. Амфотерные оксиды — продукты полной дегидратации (реаль-
(реальной или условной) амфотерных гидроксидов, например BeO, ZnO,
А12О3, Сг2О3, PbO, Fe2O3. Сохраняют химические свойства амфотер-
амфотерных гидроксидов.
4.4. Двойные оксиды образованы либо атомами одного амфотерно-
го элемента в разных степенях окисления, либо атомами двух разных
(металлических, амфотерных) элементов, что и определяет их хими-
химические свойства, например (FeIIFe2II)O4, (Pb2IPbIV)O4, (MgAl2)O4,
(CaTi)O3.
I. Неорганические вещества
4.5. Несолеобразующие оксиды — оксиды неметаллов, не имеющие
кислотных гидроксидов и не вступающие в реакции солеобразования
(отличие от основных, кислотных и амфотерных оксидов), например
СО, NO, N20, SiO, S20.
5. Гидроксиды — соединения элементов с гидроксогруппами ОН"
и (не всегда) кислородом 0~п. В гидроксидах степень окисления эле-
элемента всегда положительная — от +1 до +VII. Число гидроксогрупп от
1 до 6. По химическим свойствам делятся на основные, кислотные и
амфотерные гидроксиды.
5.1. Основные гидроксиды (основания) образованы металлическими
элементами, например LiOH, NaOH, КОН, Mg(OHJ, Ca(OHJ,
Ва(ОНJ. Замещают свои гидроксогруппы на кислотные остатки по
правилам валентности с образованием солей, металлические элемен-
элементы сохраняют свою степень окисления в катионах солей. При полной
дегидратации переходят в основные оксиды: 21Л0Н = Н2О + Li2O,
Са(ОНJ = Н20 + СаО.
5.2. Кислотные гидроксиды (кислоты) образованы неметаллически-
неметаллическими элементами. Примеры:
Состав СО(ОНJ NO2(OH) PO(OHK PO2(OH) SO2(OHJ
Формула Н2СО3 HNO3 H3PO4 HPO3 H2SO4
Состоят из водорода H+I и кислотных остатков С03~~, N0^, Р04~,
Р01, S04~. Исключение: оксиду S02 в качестве кислотного гидрокси-
да соответствует полигидрат S02 • яН2О. Замещают (полностью или
частично) водород на металлы по правилам валентности с образова-
образованием солей, кислотные остатки — средние (С03~) и кислые (НСО 3) —
сохраняют свой состав и заряд в анионах солей. При полной дегидра-
дегидратации переходят в кислотные оксиды: Н2СО3 = Н20 + С02, H2SO4 =
= Н2О + S03. В отличие от бескислородных кислот кислотные гидро-
гидроксиды называют кислородсодержащими кислотами или оксокислотами.
5.3. Амфотерные гидроксиды образованы амфотерными элемента-
элементами, например Ве(ОНJ, Zn(OHJ, A1(OHK и АЮ(ОН), Сг(ОНK и
СгО(ОН), Pb(OHJ, FeO(OH). Проявляют свойства основных и кис-
кислотных гидроксидов; образуют два вида солей, в которых амфотерный
элемент входит в состав либо катионов солей, либо их анионов. При
полной дегидратации переходят в амфотерные оксиды: Zn(OHJ =
= Н20 + ZnO; А1@НK = Н2О + АЮ(ОН), 2АЮ(ОН) = Н20 + А12О3.
6. Соли — соединения катионов металлических или амфотерных
элементов с анионами (остатками) кислотных или амфотерных гид-
гидроксидов. Образуются при взаимодействии, с одной стороны, основ-
основных и амфотерных (в роли основных) гидроксидов и оксидов и, с
другой — кислотных и амфотерных (в роли кислотных) гидроксидов и
оксидов (реакции солеобразования). В отличие от бескислородных
I. Неорганические вещества
солей называются кислородсодержащими солями или оксосолями.
Комплексные соединения, содержащие воду или гидроксид-ионы
(аквагидроксокомплексы), также относятся к солям, например
[Cu(H2OL]SO4, K2[Zn(OHL]. По составу катионов и анионов делятся
на средние, кислые, основные и двойные соли.
6.1. Средние соли содержат средние кислотные остатки (без водо-
водорода), например К2СО3, Mg(NO3J, Na2SO4, Ca3(PO4J. Образуются
при взаимодействии эквивалентных количеств гидроксидов или их
оксидов:
а) Основание + Кислота —> Соль + Н2О
2NaOH + H2SO4 = Na2SO4 + 2Н2О
Zn(OHJ + 2HNO3 = Zn(NO3J + 2H2O
KOH + A1(OHK расплав> КА1О2 + 2Н2О
б) Основный оксид + Кислота —> Соль + Н2О
СаО + H2SO4 = CaSO4 + Н2О
ZnO + 2HNO3 = Zn(NO3J + H2O
Na2O + 2A1(OHK расплав> 2NaA102 + 3H2O
в) Основание + Кислотный оксид —> Соль + Н2О
2L1OH + SO3 = Li2SO4 + Н2О
Zn(OHJ + N2O5 = Zn(NO3J + H2O
2NaOH + ZnO расплав> Na2Zn02 + H2O
г) Основный оксид + Кислотный оксид —> Соль
ВаО + СО2 = ВаСО3
A12O3 + 3SO3 = A12(SO4K
Na2O + A12O3 = 2NaA102
6.2. Кислые соли содержат кислые кислотные остатки (с водоро-
водородом), например КНСО3, NaHSO4, MgHPO4, Ca(H2PO4J. Образуются
при действии на основный гидроксид избытка кислотного гидроксида
не менее чем с двумя атомами водорода в формульной единице, на-
например Са(ОНJ + 2H2SO4 = Ca(HSO4J + 2Н2О.
6.3. Основные соли содержат гидроксогруппы, например (FeOH)NO3,
(CuOHJCO3. Точнее формулы основных солей записывают
Fe(NO3)OH, Cu2CO3(OHJ (гидроксогруппы рассматривают как от-
отдельные анионы). Образуются при действии на кислотный гидроксид
8
I. Неорганические вещества
избытка основного гидроксида не менее чем с двумя гидроксогруп-
пами в формульной единице, например 2Са(ОНJ + H2SO4 =
= Ca2SO4(OHJ + 2Н2О.
6.4. Двойные соли содержат два химически разных катиона, напри-
например CaMg(CO3J, KA1(SO4J, Fe(NH4J(SO4J, LiAl(SiO3J. Иногда вы-
выделяют еще редкую группу смешанных солей с двумя разными аниона-
анионами, например Na3(HCO3)CO3, Na2(IO3)NO3.
7. Бинарные соединения — вещества, не относящиеся ко всем пре-
предыдущим классам сложных веществ, например OF2, HF, KBr, H2S,
A12S3, NH3, CaC2, SiH4, CaH2, Mg3N2, NH4C1, SC12O2, H2O2, Na2O2,
KO2. Химические свойства разнообразны; часто разделяются по груп-
группам с одинаковым анионом (реальным или условным) — галогениды
(OF2, HF, KBr, NH4C1), халькогениды (H2S, Na2S, As2S3), нитриды
(NH3, Mg3N2), карбиды (СаС2), гидриды (CaH2, SiH4), пероксиды (Н2О2,
Na2O2), надпероксиды (КО2) и др., по группам ковалентных (OF2, HF,
H2S, NH3, SiH4, SC12O2, H2O2) и ионных соединений (KBr, CaC2, CaH2,
Mg3N2, NH4C1, Na2O2, KO2). Встречаются двойные бинарные со-
соединения, например KMgCl3 и (FeIIICuI)S2, и смешанные бинар-
бинарные соединения, например Pb(Cl)F, SC12O2, AsOF3, Bi(Cl)O. Все так
называемые комплексные соединения (кроме аква- и гидроксокомп-
лексов) также относятся к этому классу сложных веществ, например
[Cu(NH3L]Cl2, K[Ag(CNJ], K4(Fe(CNN], Na3[AlF6], K2[SiF6], [Fe(COM].
Отдельно рассматриваются бескислородные кислоты и соли.
7.1. Бескислородные кислоты содержат подвижный водород H+I и
поэтому проявляют некоторые химические свойства кислотных гид-
роксидов, например HF, HC1, HBr, HI, HCN, H2S. При замещении
водорода на металл образуются бескислородные соли.
7.2. Бескислородные соли образованы катионами металлических
элементов или сложными катионами (NH 4) и анионами бескисло-
бескислородных кислот, например AgF, KBr, Na2S, Ba(HSJ, NaCN, NH4C1.
Проявляют некоторые химические свойства солей кислородсодержа-
кислородсодержащих кислот (кислотных гидроксидов).
7.3. Прочие бинарные соединения — все другие соединения этого
класса, не относящиеся к бескислородным кислотам и их солям.
2. Номенклатура ИЮПАК
2.1. Современные номенклатурные правила
Составление химических формул и названий неорганических
веществ проводится в соответствии с номенклатурными правила-
правилами Международного союза теоретической и прикладной химии
I. Неорганические вещества
(ИЮПАК), адаптированными к русскому химическому языку в
1983 г.
Химическая формула полностью отражает состав вещества. По фор-
формуле строится систематическое название вещества, оно так-
также полностью отражает его состав. Для распространенных веществ
применяются и другие названия — традиционные (отражаю-
(отражающие состав не полностью) и специальные (совсем не отражаю-
отражающие состав). Эти названия обычно более короткие и поэтому более
удобны в использовании. Однако расширять список подобных назва-
названий (путем составления новых терминов и терминов по аналогии)
ИЮПАК не рекомендует.
В формуле сложного вещества на первом месте слева записывают
обозначение электроположительной составляющей (ре-
(реальный или условный катион), за ним — обозначение электро-
электроотрицательной составляющей (реальный или условный анион).
Примеры:
Формула Катион(ы) Анион(ы)
Na2O Na+ О2-
SF6 S+VI F
Са3(РО4J Са2+ РО^
(MgAl2)O4 Mg2+,A13+ O2-
KCr(SO4J K+, Cr3+ SO2-
N(O)F3 N+v О1, F
FeO(OH) Fe3+ О2", ОН"
Cu2CO3(OHJ Cu2+ CO^, OH-
Систематические названия сложных веществ строятся по формуле
справа налево и состоят из двух слов: первое слово (в имени-
именительном падеже) — название аниона, второе слово (в родительном
падеже) — название катиона; названия одноименных составляю-
составляющих (двух анионов, двух катионов) пишутся через дефис.
Для построения названий катионов (всегда) и названий анионов
(как правило) используются корни (иногда усеченные) русских
названий элементов. Названия простых (одноэлементных) анионов
оканчиваются на -ид, названия сложных анионов — на -ат, например:
алюминий — алюминат, бериллий — бериллат; фосфор — фосфид,
фосфат; хлор — хлорид, хлорат.
По традиции и для благозвучия в названиях анионов применяются
корни латинских названий некоторых элементов:
10
I. Неорганические вещества
Элемент
символ
Ag
As
Аи
С
Си
Fe
Н
Hg
Мп
N
Ni
О
РЬ
S
Sb
Si
Sn
название
Серебро
Мышьяк
Золото
Углерод
Медь
Железо
Водород
Ртуть
Марганец
Азот
Никель
Кислород
Свинец
Сера
Сурьма
Кремний
Олово
Латинский
корень
Аргент-
Арсен-
Аур-
Карб-
Карбон-
Купр-
Ферр-
Гидр-
Меркур-
Манган-
Нитр-
Никкол-
Окс-
Плюмб-
Сульф-
Стиб-
Силиц-
Силик-
Станн-
Название аниона
(анионов)
Аргенгат
Арсенид, арсенат
Аурат
Карбид
Карбонат
Купрат
Феррат
Гидрид
Меркурат
Манганат
Нитрид, нитрат
Никколат
Оксид
Плюмбат
Сульфид, сульфат
Стибат
Силицид
Силикат
Станнат
Число анионов и катионов рекомендуется обозначать пристав-
приставками (универсальный способ указания состава предпочтителен для
соединений неметаллов) или степенями окисления
(предпочтителен для катионов металлов, особенно если их не-
несколько у данного элемента, при точно известном заряде аниона,
в редких случаях этот заряд также указывается). Примеры:
Формула
СО
со2
so3
N2O5
SC12O2
CuO
Предпочтительное название
Монооксид углерода
Диоксид углерода
Триоксид серы
Пентаоксид диазота
Диоксид-дихлорид серы
Оксид меди(П)
Допустимое название
Оксид углерода(П)
Оксид углеродаAУ)
Оксид cepbi(VI)
Оксид азота(У)
—
Монооксид меди
11
I. Неорганические вещества
Окончание табл.
Формула
Сг2О3
FeCl2
FeCl3
Pb(Cl)F
(FeI11CuI)S2
Fe(S2)
Предпочтительное название
Оксид хрома(Ш)
Хлорид железа(Н)
Хлорид железа(Ш)
Фторид-хлорид свинца
Сульфид медиA)-железа(Ш)
ДисульфидB-) железа(Н)
Допустимое название
Триоксид дихрома
Дихлорид железа
Трихлорид железа
—
—
—
При мечания:
1. Названия числовых приставок:
1 — моно- 5 — пента- 9 — нона-
2 — ди- 6 — гекса- 10 — дека-
3 — три- 7 — гепта- 11 — ундека-
4 — тетра- 8 — окта- 12 — додека-
Большие чем 12, значения приставок записываются цифрами A3, 14,15,...).
Неопределенное число обозначается приставкой «поли-».
2. Указание на степень окисления пишется всегда вместе со словом и чи-
читается как количественное числительное мужского рода в именительном
падеже:
... углерода(П) — углерода-два
... азота(У) — азота-пять
... хрома(Ш) — хрома-три
... железа(И) — железа-два
... медиA)-железа(Ш) — меди-один-железа-три
3. Для соединений металлов с единственной степенью окисления послед-
последняя не указывается, но подразумевается:
Na2S — сульфид натрия
А12О3 — оксид алюминия
LiH — гидрид лития
СаВг2 — бромид кальция
Для широко известных простых и сложных веществ, а также для
ряда катионов и анионов ИЮПАК рекомендует использовать специ-
специальные названия:
Простые вещества
а-С — графит
Р-С — алмаз
О3 — озон
Р4 — белый фосфор
Сложные вещества
AsH3 — арсин
В^Ну— боран
C(NH2JO — карбамид
CS(NH2J — тиокарбамид
12
I. Неорганические вещества
NH3OH+ — гидроксиламиний
NO+ — нитрозил
NO 2 — нитроил
GeH4 — герман
НВг — бромоводород
HCN — циановодород
НС1 — хлороводород
HF — фтороводород
HI — иодоводород
HN3 — азидоводород
Н2О — вода
H2S — сероводород
H2SW — сульфан
H2Se — селеноводород
Н2Те — теллуроводород
ND3 — дейтериоаммиак
NH3 — аммиак
N2H4 — гидразин
NH2C1 — хлорамин
NHF2 — дифторамин
NH2OH — гидроксиламин
РН3 — фосфин
Р2Н4 — дифосфан
Si^Hy — силан
SbH3 — стибин
SnH4 — станнан
Катионы
Н3О+ — оксоний
NH4 — аммоний
N2H з — гидразинийA+)
N2H l+ — гидразинийB+)
Гидроксиды металлов в степени окисления +III, содержащие од-
одновременно ионы 02~ и ОН", называют с использованием специаль-
специальной приставки мета-:
АЮ(ОН) — метагидроксид алюминия
FeO(OH) — метагидроксид железа
Катионы металлов с присоединенными к ним анионами ОН"
(обычно в растворе) называют с приставкой гидроксо-:
СиОН+ — катион гидроксомеди(И)
Ti(OHJ+ — катион дигидроксотитана(ГУ)
PHJ
uof
vo2+
диоксигенил
— фосфоний
— уранил
— ванадил
Анионы
с\--
CN--
- ацетиленид
— цианид
— цианамид
CNO~ — фульминат
HF2
но2
HS"-
HSe"
НТе"
Щ-
NCS"
NH2"
NH2
N0"
02-
0J —
OCN
ОН"
S2~ -
— гидродифторид
— гидропероксид
- гидросульфид
— гидроселенид
— гидротеллурид
азид
— тиоцианат
— имид
— амид
— нитрозид
надпероксид
- пероксид
озонид
" — цианат
— гидроксид
- полисульфидB-)
13
I. Неорганические вещества
Для ограниченного числа распространенных оксокислот и кислот-
кислотных остатков в оксосолях используются традиционные названия (про-
(прочерк означает, что кислота не существует):
Кислота
Кислотный остаток
HAsO2 — метамышьяковистая
H3AsO3 — ортомышьяковистая
H3AsO4 — мышьяковая
НВО2 — метаборная
НВгО — бромноватистая
НВгО3 -
НВЮ4-
Н2СО3-
НСЮ-
НС1О2-
НС1О3-
НСЮ4-
Н2Сг04-
Н2Сг207
бромноватая
бромная
¦ угольная
хлорноватистая
хлористая
хлорноватая
хлорная
- хромовая
— дихромовая
H2Ge03 — германиевая
НЮ — иодноватистая
НЮ3 — йодноватая
НЮ4 — метаиодная
Н5Ю6 — ортоиодная
НМпО4 — марганцовая
HNO2 — азотистая
HNO3 — азотная
H2N2O2 — азотноватистая
Н(РН2О2) — фосфиновая
AsO2 — метаарсенит
AsO3~ — ортоарсенит
AsO4~ — арсенат
ВО 2 — метаборат
ВО3~ — ортоборат
В4Оу~ — тетраборат
BiO3 — висмутат
ВгО~ — гипобромит
ВгО2 — бромит
ВгО^ — бромат
ВгО4 — пербромат
СО3~ — карбонат
СЮ" — гипохлорит
СЮ 2 —хлорит
СЮ2 —хлорат
СЮ 4 — перхлорат
СгО4~ — хромат
Сг2О7~ — дихромат
FeO4~ — феррат
GeO3~ — германат
Ю~ — гипоиодит
Ю3 — иодат
Ю4 — метапериодат
IOg" — ортопериодат
МпО4 — перманганат
МпО4~ — манганат
МоО4~ — молибдат
NO2 —нитрит
N0^" — нитрат
N2O2~ — гипонитрит
РН2О2 — фосфинат
14
I. Неорганические вещества
Окончание табл.
Кислота
Н2(РНО3) — фосфоновая
НРО3 — метафосфорная
Н3РО4 — ортофосфорная
Н4Р2О7 — дифосфорная
—
—
SO2 • иН2О — полигидрат SO2
H2SO4 — серная
H2S2G7 — дисерная
H2SWO6 — политионовая
H2S2O6(O2) — пероксодисерная
H2(SO3S) — тиосерная
H2Se03 — селенистая
H2Se04 — селеновая
H2Se207 — диселеновая
H2SiO3 — метакремниевая
H4Si04 — ортокремниевая
—
НТсО4 — технециевая
Н2Те03 — теллуристая
Н2Те04 — метателлуровая
Н6Те06 — ортотеллуровая
—
—
—
Кислотный остаток
РНО3~ — фосфонат
РО^ — метафосфат
РО4~ — ортофосфат
Р2О7~ — дифосфат
ReO4 — перренат
ReO4~ — ренат
SO3~ — сульфит
SO4~ — сульфат
S2O7~ — дисульфат
SwOg~ — политионат
S2O6(O2J~ — пероксодисульфат
SO3S2~ — тиосульфат
SeO3~ — селенит
SeO4~ — селенат
Se2O7~ — диселенат
SiO3~ — метасиликат
SiO4~ — ортосиликат
Si2O7~ — дисиликат
ТсО4 — пертехнетат
ТеО3~ — теллурит
ТеО4~ — метателлурат
TeOg" — ортотеллурат
VO^ — метаванадат
VO4~ — ортованадат
WO4~ — вольфрамат
Кислые анионы многоосновных кислот, перечисленных в таблице
(см. выше), называют с приставкой гидро-:
Н2РО 4 — дигидроортофосфат
НРО4~ — гидроортофосфат
Традиционные названия анионов входят в названия соответствую-
соответствующих солей:
NaBO2 — метаборат натрия
Na2B4O7 — тетраборат натрия
15
I. Неорганические вещества
Cu2CO3(OHJ — дигидроксид-карбонат меди(И)
Са(С1ОJ — гипохлорит кальция
КСЮ3 — хлорат калия
NH4NO3 — нитрат аммония
Na3PO4 — ортофосфат натрия
Na2HPO4 — гидроортофосфат натрия
NaH2PO4 — дигидроортофосфат натрия
BaSO4 — сульфат бария
Pb(HSO4J — гидросульфат свинца(П)
KCr(SO4J — сульфат хрома(Ш)-калия
Ba(HSJ — гидросульфид бария
Остальные соли (обычно встречающиеся реже) получают система-
систематические названия (как комплексные соединения, см. далее):
NaA102 — диоксоалюминат(Ш) натрия
KRuO4 — тетраоксорутенат(УН) калия
Ва2ХеО6 — гексаоксоксенонат(УШ) бария
В комплексных соединениях формула собственно комплекса — нейт-
нейтрального (без внешней сферы) и заряженного положительно или от-
отрицательно (катиона или аниона) — всегда заключается в квадратные
скобки, в отличие от формул обычных веществ, катионов и анионов.
В состав формулы комплекса входят центральный атомМ
в некоторой степени окисления и определенное число п лигандов
L (нейтральных, отрицательно или положительно заряженных):
Формула
[Fe(COM]
[Co(NH3KCl3]
[А1(Н2ОN]3+
[Co(NH3N]2+
[Co(NH3N]3+
М
Fe°
Com
А1Ш
Co"
Сош
L
CO
NH3, Cl-
H2O
NH3
NH3
Формула
[A1(OHL]"
[PtCl6]2"
[Fe(CNN]4-
[SiF6]2-
[Pt(N2H5JCl2]2+
M
Al1»
ptiv
Fe»
Silv
Pt"
L
OH-
ci-
CN-
F-
N2H + , Cl-
Названия анионных лигандов получают соединительную
гласную -о-, например:
F~ — фторо ОН" — гидроксо
С1~ — хлоро CN~ — циано
О2~ — оксо Н~ — гидридо
16
NCS" — тиоцианато
NOJ — нитро
SO3~ — сульфито
I. Неорганические вещества
Названия нейтральных лигандовследующие:
Н2О — аква N0 — нитрозил С2Н4 — этилен
NH3 — аммин N2 — диазот С6Н6 — бензол
СО — карбонил N2H4 — гидразин C5H5N — пиридин
Для катионных лигандов (они встречаются весьма редко) на-
названия будут такими:
Н+ — гидро N0+ — нитрозилий
N2H5 — гидразиний NO J — нитроилий
Систематические названия комплексов строятся по схеме
«п + L + М» (т. е. справа налево по формуле).
Названия нейтральных комплексных соединений:
[Сг(С6Н6J] — дибензолхром
[Ni(COL] — тетракарбонилникель
[Co(NH3KCl3] — трихлоротриамминкобальт
Названия соединений с катионными комплексами, вклю-
включающие указание на степень окисления центрального атома М:
[Cu(H2OL]SO4 — сульфат тетрааквамеди(И)
[Ag(NH3J]ClO4 — перхлорат диамминсеребраA)
[Rh(C5H5NN]Br2— бромид гексапиридинродия(Н)
Названия соединений с анионными комплексами, включаю-
включающие суффикс -ат и указание на степень окисления М:
H2[PtCl6] — гексахлороплатинатAУ) водорода
Na[Al(OHL] — тетрагидроксоалюминат(Ш) натрия
K2[Fe(NO+)(CNM] — пентацианонитрозилийферрат(П) калия
Названия гидратированных веществ складываются из группового
слова «гидрат» с указанием числа молекул воды и названия безводно-
безводного вещества:
NH3 • Н20 — гидрат аммиака
KCr(SO4J • 12Н2О — додекагидрат сульфата хрома(Ш)-калия
Sn(NO3J • 20Н2О — 20-гидрат нитрата олова(Н)
Для более сложных гидратов вместо приставок указывают число-
числовое отношение частей (первая цифра — число молекул воды в фор-
формульной единице гидрата):
8С12 • 46Н2О — гидрат молекулярно^о^етора^б/^
3CdSO4 • 8Н2О — гидрат сульфата к*дМ№*{Щ («Ш
17
I. Неорганические вещества
2.2. Тривиальные названия веществ и смесей
Использование тривиальных (неноменклатурных, исторически
сложившихся) названий неорганических веществ, их смесей, раство-
растворов и сплавов допускается (но необязательно рекомендуется) в научно-
технической и учебной литературе, лабораторной практике и в быту.
Индивидуальные вещества
Азот йодистый I3N • «NH3
Аланат лития Li[AlH4]
Алебастр CaSO4 • 0,5Н2О
Алюмогель А12О3 • 0,25Н2О
Алюмогидрид лития Li[AlH4]
Ангидрон Mg(C104J
Антихлор Na2(SO3S) • 5Н2О
Барит едкий Ва(ОНJ
Белила
баритовые BaSO4
жемчужные Bi(NO3)O
испанские Bi(NO3)O
китайские ZnO
титановые TiO2
цинковые ZnO
Бензол неорганический B3H6N3
Бикарбонат NaHCO3
Бланфикс BaSO4
Боразон p-BN
Бура Na2B4O7 • 10Н2О
ювелирная Na2B4O7 • 5Н2О
Ванадоцен [V(C5H5J]
Вода
полутяжелая [Н2НО (HDO)
сверхтяжелая 3Н2О (Т2О)
тяжелая 2Н2О (D2O)
Газ
болотный СН4
веселящий N2O
инертный Не, Ne, Аг, Кг, Хе
или Rn
природный СН4
рудничный СН4
сернистый SO2
угарный СО
углекислый СО2
Гипосульфит Na2(SO3S) • 5Н2О
Гипс жжёный CaSO4 • 0,5Н2О
Глинозём А12О3
Графит белый a-BN
Зелень
Веронезе Cu3(As04J • 4Н2О
Гинье Сг2О3 • лН2О
касселева ВаМпО4
марганцевая ВаМпО4
Земля
известковая СаО
инфузорная SiO2
Золото
муссивное SnS2
сусальное Аи (фольга)
Известь
гашёная Са(ОНJ
едкая Са(ОНJ
жжёная СаО
негашёная СаО
Кали едкое КОН
Камень
квасцовый KA13(SO4J(OHN
оловянный SnO2
синий CuSO4 • 5Н2О
Карбид
железа Fe3C
кальция СаС2
Карборунд SiC
Каустик NaOH
Квасцы
алюмокалиевые KA1(SO4J •
• 12Н2О
жжёные KA1(SO4J
хромокалиевые KCr(SO4J •
•2Н2О
18
I. Неорганические вещества
Кизельгур SiO2
Кислота Каро H2SO3(O2)
Кобальтоцен [Со(С5Н5J]
Кремнезём SiO2
Крокус Fe2O3
Крон
зеленый Сг2О3
свинцовый РЬСгО4
Купорос
белый ZnSO4 • 7Н2О
железный FeSO4 • 7Н2О
зеленый FeSO4 • 7Н2О
изумрудно-зеленый NiSO4-
•7Н2О
кобальтовый CoSO4 • 7Н2О
медный CuSO4 • 5Н2О
никелевый NiSO4 • 7Н2О
свинцовый PbSO4
синий CuSO4 • 5Н2О
хромовый CrSO4 • 7Н2О
цинковый ZnSO4 • 7Н2О
Лазурь берлинская
KFeIIl[FeH(CNN]
Лед сухой СО2 (твердый)
Магнезия жжёная MgO
Масло
оловянное SnCl4 (жидкий)
сурьмяное SbCl3 (жидкий)
Метабисульфит K2S2O5
Моногидрат H2SO4
Мочевина C(NH2JO
Мышьяк белый As2O3
Натр Na2O
едкий NaOH
Никелоцен [Ni(C5H5J]
Нитропруссид натрия
Na2[Fe(NO+)(CNM] • 2Н2О
Осмоцен [Os(C5H5J]
Песок SiO2
Печень серная Na2Sw
Порошок алгаротов Sb4Cl2O5
Поташ К2СО3
Преципинат СаНРО4 • 2Н2О
Ртуть гремучая
Hg(CNOJ • 0,5Н2О
Рутеноцен [Ru(C5H5J]
Сажа С (графит, дисперсный)
Сахар свинцовый
РЬ(СН3СООJ • ЗН2О
Селитра
индийская KNO3
норвежская Ca(NO3J • 4Н2О
чилийская NaNO3
Серебро гремучее Ag3N
Силикагель SiO2 • яН2О
Синь
тенарова (СопА12)О4
турнбуллева KFein[Fen(CNN]
Сода
двууглекислая NaHCO3
кальцинированная Na2CO3
каустическая NaOH
кристаллическая Na2CO3 * 10Н2О
питьевая NaHCO3
стиральная Na2CO3
Соль
английская MgSO4 • 7Н2О
бертоллетова КС1О3
Бульриха NaHCO3
глауберова Na2SO4 • 10Н2О
Гмелина K3[Fe(CNN]
горькая MgSO4 • 7Н2О
Джонсона К[1AJ] • Н2О
желтая кровяная
K4[Fe(CNN] • ЗН2О
Жерара транс-[Рг(ЫН3JС\4]
золотая Na[AuCl4] • 2Н2О
каменная NaCl
Клёве *<wc-[Pt(NH3JCl4]
красная кровяная
K3[Fe(CNN]
Магнуса [Pt(NH3L][PtHCl4]
Мора Fe(NH4J(SO4J • 6Н2О
морская NaCl
оловянная [Sn(H2O)Cl2] • Н2О
Пейронё ^wc-[Pt(NH3JCl2]
пищевая NaCl
19
I. Неорганические вещества
Феррицианид K3[Fe(CNN]
Ферроцен [Fe(C5H5J]
Ферроцианид K4[Fe(CNN] • ЗН2О
Фиксаж Na2(SO3S) • 5Н2О
Фосген СС12О
Хлорид
II основания Рейзе
mpaHC-[Pt(NH3JCl2]
золота Н[АиС14] • 4Н2О
Хромоцен [Сг(С5Н5J]
Хромпик К2Сг207
Цвет серный S (порошок)
Цементит Fe3C
Чернь платиновая Pt (дисперсная)
Элементы редкоземельные
Y, La—Lu (иногда Sc)
поваренная NaCl
препаратная Na2[Sn(OHN]
Фишера K3[Co(NO2N]
Цёйзе K[Pt(C2H4)Cl3] • Н2О
Шлйппе Na3[SbS4] • 9Н2О
Спирт С2Н5ОН
древесный СН3ОН
Станиоль Sn (фольга)
Сулема HgCl2
Сульфат Na2SO4
Сульфит Na2SO3
Суперфосфат двойной
Са(Н2РО4J • Н2О
Тиомочевина CS(NH2J
Тиофосген C(S)C12
Титаноцен [Ti(C5H5J]
Смеси, растворы
Алунд — огнеупорный химически стойкий материал на основе А12О3
Аммофос — смесь NH4H2PO4 и (NH4JHPO4 (минеральное удобрение)
Белила свинцовые — смесь РЬСО3 и РЬ(ОНJ
Вода
аммиачная —25%-й водный раствор NH3
баритовая — насыщенный водный раствор Ва(ОНJ
бромная — насыщенный водный раствор Вг2 (содержит НВг, НВгО)
гипсовая — насыщенный водный раствор CaSO4
жавелевая —водный раствор КОН, насыщенный хлором С12 (содержит
КС1, КС1О)
известковая —насыщенный водный раствор Са(ОНJ
йодная —раствор 12 в водном растворе KI (содержит К[1A2)])
лабарракова — водный раствор NaOH, насыщенный хлором С12 (со-
(содержит NaCl, NaCIO)
сероводородная — насыщенный водный раствор H2S
хлорная — насыщенный водный раствор С12 (содержит НС1, НС1О)
Водка царская — смесь концентрированных HNO3 и НС1 A : 3 по объему)
Газ
водяной —смесь СО и Н2
генераторный — смесь СО, N2, CO2
гремучий — смесь Н2 и О2 B : 1 по объему)
Глина белая — см. Каолин
Жидкость
бордосская — раствор CuSO4 в известковом молоке
Ваккенродера — водный раствор H2SWO6 (п = 3—6)
Извёстка — смесь Са(ОНJ, SiO2, H2O
20
I. Неорганические вещества
Известь
белильная -смесь Са(СЮJ, СаС12, Са(ОНJ, Н2О
натронная — смесь CaO, Ca(OHJ, NaOH
хлорная — смесь Са(СЮJ, СаС12, Са(ОНJ, Н2О
Камень адский — см. Ляпис
Каолин — смесь каолинита Al4(Si4O10)(OH)8 и SiO2
Кислота
дымящая серная — см. Олеум
плавиковая — концентрированный D0%-й) водный раствор HF
сероводородная — водный раствор H2S
синильная — водный раствор HCN
соляная — концентрированный C5—36%-й) водный раствор НС1
фтороводородная — разбавленный водный раствор HF
хлороводородная — разбавленный водный раствор НС1
Литопон — осажденная смесь BaSO4 и ZnS
Ляпис — плавленая смесь AgNO3 и KNO3
Масло купоросное — техническая концентрированная серная кислота H2SO4
Мел — спёк осажденного СаСО3 (с примесями)
Молоко известковое — суспензия Са(ОНJ в известковой воде
Наждак — смесь А12О3 и (FeIIFe2II)O4
Олеум — раствор SO3 в безводной H2SO4 (содержит H2S2O7)
Охра — смесь Fe2O3, A12O3, SiO2
Пергидроль — 30%-й водный раствор Н2О2
Реактив Несслера — щелочной раствор K2[HgI4]
Смесь
магнезиальная — раствор MgCl2 и NH4C1 в аммиачной воде
хромовая — раствор К2Сг207 и СгО3 в 60%-й H2SO4
Эшка — смесь порошков MgO и Na2CO3
Спирт нашатырный — 3—10%-й водный раствор NH3
Стекло
жидкое —щелочной водный раствор Na2Si03 и K2SiO3
растворимое — смесь Na2Si03, K2Si03, SiO2
Суперфосфат простой — смесь Са(Н2РО4J • Н2О и CaSO4
Термит — смесь порошков А1 и (FenFe2n)O4
Углекислота — насыщенный водный раствор СО2
Щёлок
калийный —водный раствор КОН
натровый — водный раствор NaOH
Сплавы
(элементный состав выражен массовой долей, %)
Алюмель - на основе Ni, содержит А11,8-2,5, Мп 1,8—2,2, Si 0,85-2,0,
иногда Fe 0,5
Амальгама — на основе Hg, содержит один из металлов IA-, НА-, 1Б- или
ИБ-групп
21
I. Неорганические вещества
Баббит
оловянный —Sn 82—84, Sb 10—12, Си 6
свинцовый -РЬ 80—82, Sb 16—18, Си 2
Бронза — на основе Си и Sn, содержит Al, Be, Pb, Cr, Si
Дюраль (дуралюмин) — на основе А1, содержит Си, Mg, Mn
Инвар - Fe 63, Ni 36, Mn 0,5, С 0,5
Константан — Си 60, Ni 40
Латунь — на основе Си и Zn (до 50), содержит Al, Fe, Mn, Ni, Pb
Манганин — Си 83, Mn 13, Ni 4
Мельхиор — на основе Си и Ni B7—29), содержит Fe, Mn
Монель-металл — на основе Ni и Си B7—29), содержит Fe, Mn
Нержавеющая сталь
хромоникелевая — сталь, содержит Сг 18, Ni 9
хромистая — сталь, содержит Сг 13—27
Никелин — на основе Си и Ni B5—35), содержит Mn, Fe, Zn
Нихром — Ni 65—80, Сг 15, содержит Si, Al
Нойзильбер — Си 82-20, Ni 5—35, Zn 13-45
Победит - WC - 90, Со « 10
Платинородий — Pt 90, Rh 10
Припой - Sn 30-70, Pb 70-30
Сплав Вуда - Bi 50, Pb 25, Sn 12,5, Cd 12,5
Сталь (обычная) — на основе Fe, содержит С 0,02—2,06
Ферросплавы (для легирования сталей)
феррованадий - V 35—80, Si 3,5, Al > 2, С 1, Р 0,1-0,2, S 0,1-0,2,
остальное Fe
ферровольфрам - W 65-80, Si 0,4-1, Mn 0,2—0,7, С 0,5, Си 0,3,
остальное Fe
ферромарганец — Мп > 70, С 6—7, Si < 2, Р > 0,35, S 0,03, остальное Fe
ферромолибден — Мо > 55, Si 1—2, Р 0,2, С 0,1, S 0,1, остальное Fe
феррониобий - Nb + Та 23-75, Si 10-11, Ti 7, Al 7, S < 0,5, P 0,15,
остальное Fe
ферросилиций — Si 12—90, остальное Fe
ферротитан - Ti 18-25 или 40-45, Al 5—8, Si 3-6, Cu 3, C, S и Р -
0,1, остальное Fe
феррохром — Сг 60—85, остальное Fe
ферроцирконий — Zr 40, Si 10, Al 8—10, остальное Fe
Хромель — на основе Ni, содержит Сг 9—10, Co 1
Чугун — на основе Fe, содержит С более 2,06 (обычно 3,0—4,5), а также
Mn, Si, S, Ридр.
2.3. Несуществующие вещества
Перечислены всё еще встречающиеся в химической литературе
формулы и названия неорганических веществ, которые не известны
науке. Они не получены в лаборатории и не обнаружены в природе,
22
I. Неорганические вещества
т. е. такие вещества не выделены в безводном или гидратированном
виде, а также в виде раствора, содержащего их молекулы или ионы.
Если известно реальное вещество, отвечающее составу неполучен-
неполученного вещества, то приводятся его современная (номенклатурная)
формула и соответствующее название.
Применение всех формул и названий несуществующих веществ за-
запрещено правилами ИЮПАК.
Реально полученное вещество
Несуществующее вещество
AgOH гидроксид серебраA)
А12(СО3K карбонат алюминия
А1О \~ ортоалюминат
HAsO3 метамышьяковая кислота
М3ВО3 (М = Na, К) ортобораты
НВгО2 бромистая кислота
Сг2(СО3K карбонат хрома(Ш)
СгС16 хлорид хрома(У1)
Cul2 иодид меди(П)
Fe2(CO3K карбонат железа(Ш)
FeCl6 хлорид железа(У1)
FeCl8 хлорид железа(УШ)
Fel3 иодид железа(Ш)
Fe3O4 тетраоксид трижелеза 1
FeO • Fe2O3 оксид железа(И, III)
Fe(FeO2J феррат(Ш) железа(И) J
Fe(OHK гидроксид железа(Ш)
Fe2S3 сульфид железа(Ш)
HgCO3 карбонат ртути(П)
Hg2O оксид ртутиA)
Hg2S сульфид ртутиA)
МпС17 хлорид марганца(УИ)
NH4OH гидроксид аммония
(NH4KPO4 ортофосфат аммония
(NH4JS сульфид аммония
Не получен, из водного раство-
раствора выпадает оксид Ag2O
Не получен
Не получен
Не получена
Не получены
Не получена
Не получен
Не получен
Не получен
Не получен
Не получен
Не получен
Не получен
(FenFe2n)O4
Оксид дижелеза(Ш)-железа(П)
Не получен, известны Fe2O3 •
• лН2О и FeO(OH)
Не получен
Не получен
Не получен
Не получен
Не получен
NH3 • Н2О гидрат аммиака
Не получен
Не существует в водном раство-
растворе, переходит в NH4(HS)
23
I. Неорганические вещества
Окончание табл.
Несуществующее вещество
РЬ3О4 тетраоксид трисвинца 1
2РЬО • РЬО2 оксид свинца(И, IV) >
РЬ2(РЬО4) оргоплюмбатAУ) свинца(И) J
SC16 хлорид серы(У1)
S2O \~ персульфат
H2SO3 сернистая кислота
H2S2O8 надсерная кислота
SeCl6 хлорид селена(У1)
K4Si04 ортосиликат калия
SnCO3 карбонат олова(Н)
VC15 хлорид ванадия(У)
Реально полученное вещество
/туи II r>i*.IV\/"\
(rb2 PbIV)O4
Оксид свинцаAУ)-дисвинца(И)
Не получен
S2O6(O2J~ пероксодисульфат
Не получена, существует толь-
только полигидрат SO2 • яН2О
H2S2O6(O2) пероксодисерная
кислота
Не получен
Не получен
Не получен
Не получен
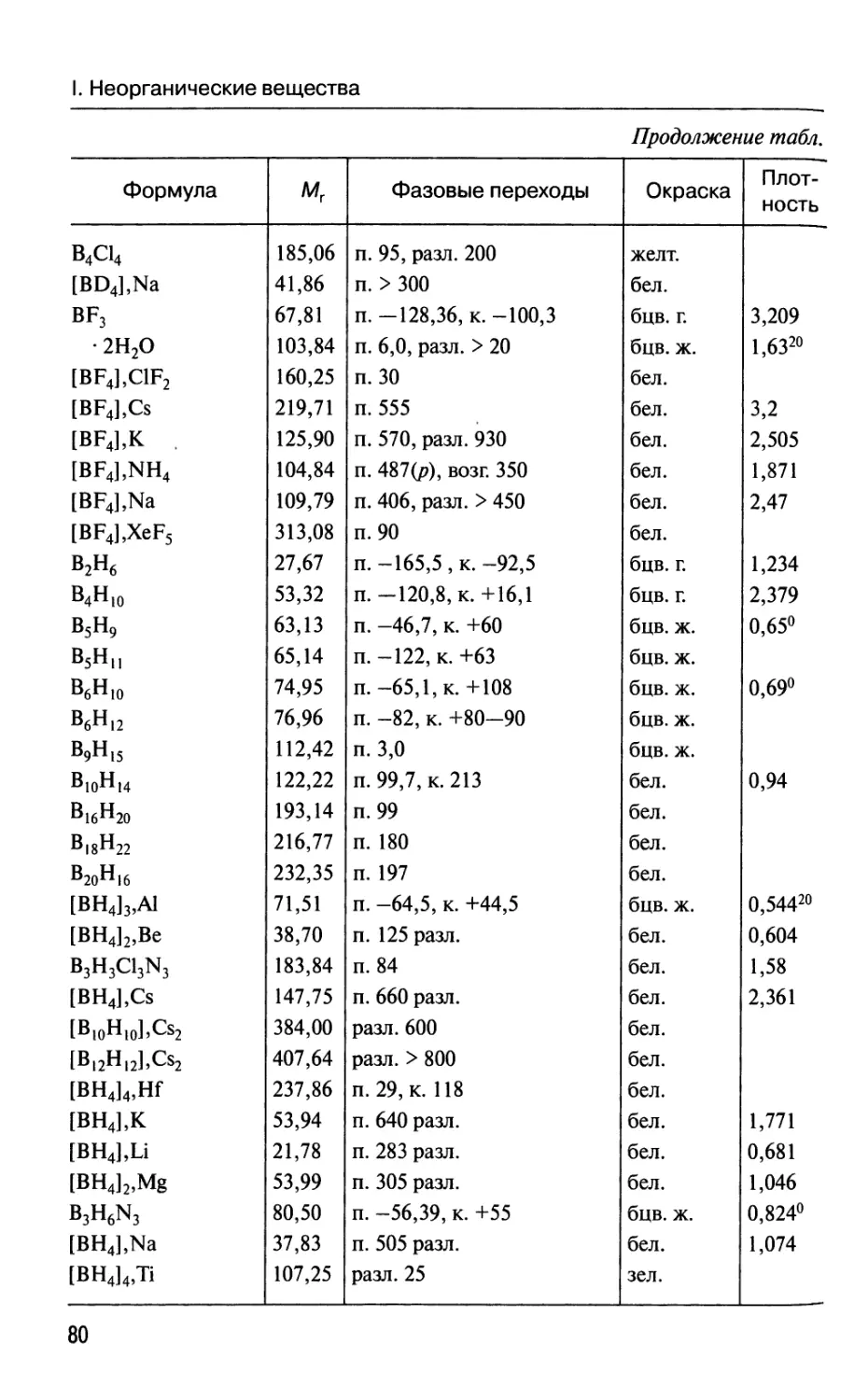
2.4. Рекомендуемые формулы и названия
В таблице приведены рекомендуемые ИЮПАК химические фор-
формулы и названия всех неорганических веществ, которые присутствуют
в разделе 3 («Физические свойства»). Все пояснения, необходимые
для данной таблицы, находятся во введении к тому же разделу.
Ас актиний
АсВг3 бромид актиния(Ш)
АсС13 хлорид актиния(Ш)
Ас(С1)О оксид-хлорид актиния
AcF3 фторид актиния(Ш)
Ac(NO3K нитрат актиния(Ш)
Ас2О3 оксид актиния(Ш)
Ac(O)F фторид-оксид актиния
Ас(ОНK гидроксид актиния(Ш)
АсРО4 ортофосфат актиния(Ш)
Ac2S3 сульфид актиния(Ш)
Ag серебро
(AgIAgIII)O2 оксид серебра(Ш)-се-
ребраA)
AgAs моноарсенид серебра
Ag3As03 ортоарсенит серебраA)
Ag3As04 арсенат серебраA)
AgAsS2 дитиометаарсенит сереб-
раA)
Ag3AsS3 тритиоортоарсенит сереб-
раA)
AgBr бромид серебраA)
AgBrO3 бромат серебраA)
Ag2C2 ацетиленид серебраA)
Ag(CH3COO) ацетат серебраA)
AgCN цианид серебраA)
Ag2CN2 цианамид серебраA)
[Ag(CNJ],K дицианоаргентатA)
калия
AgCNO фульминат серебраA)
Ag2CO3 карбонат серебраA)
Ag2C2O4 оксалат серебраA)
AgCl хлорид серебраA)
24
I. Неорганические вещества
AgC102 хлорит серебраA)
AgC103 хлорат серебраA)
AgC104 перхлорат серебраA)
Ag2Cr04 хромат серебраA)
Ag2Cr207 дихромат серебраA)
AgF фторид серебраA)
AgF2 фторид серебра(И)
Ag2F фторид дисеребра
Ag(HCOO) формиат серебраA)
Ag2H3IO6 тригидроортопериодат
серебраA)
Ag2H4Te06 тетрагидроортотеллу-
рат серебраA)
Agl иодид серебраA)
AgIO3 иодат серебраA)
AgIO4 метапериодат серебраA)
Ag3IO5 пентаоксоиодат(УИ) сереб-
раA)
AgMnO4 перманганат серебраA)
AgN3 азид серебраA)
Ag3N нитрид серебраA)
AgNCS тиоцианат серебраA)
AgNO2 нитрит серебраA)
AgNO3 нитрат серебраA)
Ag2N2O2 гипонитрит серебраA)
Ag2O оксид серебраA)
Ag2O3 оксид серебра(Ш)
AgOCN цианат серебраA)
AgPO3 метафосфат серебраA)
Ag3PO4 ортофосфат серебраA)
Ag4P2O7 дифосфат серебраA)
(Ag^Pb)O2 оксид свинца(П)-дисе-
ребраA)
AgReO4 перренат серебраA)
Ag2S сульфид серебраA)
Ag2SO3 сульфит серебраA)
Ag2SO4 сульфат серебраA)
Ag2(SO3S) тиосульфат серебраA)
[Ag(SO3SJ],Na3 ди(тиосульфа-
то)аргентатA) натрия
(AgSbUI)S2 сульфид сурь-
мы(Ш)-серебраA)
(Ag3SbUI)S3 сульфид сурь-
мы(Ш)-ТрисеребраA)
(Ag5SbIH)S4 сульфид сурь-
мы(Ш)-пентасеребраA)
Ag2Se селенид серебраA)
Ag2Se04 селенат серебраA)
Ag2Te теллурид серебраA)
Ag2Te03 теллурит серебраA)
А1 алюминий
AlAs моноарсенид алюминия
AlAsO4 арсенат алюминия
А1В2 диборид алюминия
А1В]2 додекаборид алюминия
А1Вг3 бромид алюминия
А1(ВгО3K бромат алюминия
А14С3 трикарбид тетраалюминия
А1(СН3СООK ацетат алюминия
A1(CNK цианид алюминия
А12(С2О4K оксалат алюминия
[А1(С2О4K],К3 триоксалатоалюми-
нат(Ш) калия
А1С13 хлорид алюминия
[А1С14],1п тетрахлороалюми-
нат(Ш) индияA)
[A1C14],NH4 тетрахлороалюми-
нат(Ш) аммония
[AlCl4],Na тетрахлороалюми-
нат(Ш) натрия
А1(С1)О оксид-хлорид алюминия
А1(С1О3K хлорат алюминия
А1(С1О4K перхлорат алюминия
А1С1(ОНJ дигидроксид-хлорид
алюминия
[AlD4],Li тетрадейтеридоалюми-
нат(Ш) лития
A1F3 фторид алюминия
[A1F6],K3 гексафтороалюми-
нат(Ш) калия
[AlF6],Li3 гексафтороалюми-
нат(Ш) лития
[A1F6],(NH4K гексафтороалюми-
нат(Ш) аммония
[AlF6],Na3 гексафтороалюми-
нат(Ш) натрия
А1Н3 гидрид алюминия
25
I. Неорганические вещества
А1(Н)Вг2 дибромид-гидрид алюми-
алюминия
А1Н2Вг бромид-дигидрид алюми-
алюминия
А1(Н)С12 дихлорид-гидрид алюми-
алюминия
А1Н2С1 хлорид-дигидрид алюми-
алюминия
А1(НI2 дииодид-гидрид алюминия
А1Н21 иодид-дигидрид алюминия
[AlH4],Li тетрагидридоалюми-
нат(Ш) лития
[AlH4],Na тетрагидридоалюми-
нат(Ш) натрия
А113 иодид алюминия
A1(IO3JNO3 нитрат-дииодат алю-
алюминия
A1N нитрид алюминия
A1(N3K азид алюминия
A1NH4(SO4J сульфат аммо-
аммония-алюминия
A1(NO3K нитрат алюминия
А12О3 оксид алюминия
А12 67О4 тетраоксид 2,67-алюминия
А1(ОНK гидроксид алюминия
[Al(OHL],Na тетрагидроксоалю-
минат(Ш) натрия
АЮ(ОН) метагидроксид алюми-
алюминия
А1Р фосфид алюминия
А1РО4 ортофосфат алюминия
А1(РО3K метафосфат алюминия
А13(РО4J(ОНK тригидрок-
сид-ди(ортофосфат) алюминия
A12S3 сульфид алюминия
A12(SO4K сульфат алюминия
A1(SO4)OH гидроксид-сульфат
алюминия
A12SO4(OHL тетрагидроксид-суль-
фат алюминия
AlSb стибид алюминия
Al2Se3 селенид алюминия
Al2Si207 дисиликат алюминия
Al2(SiO4)O оксид-ортосиликат
алюминия
А12Те3 теллурид алюминия
Am америций
Ат2(С2О4K оксалат америция(Ш)
АтС13 хлорид америция(Ш)
AmF3 фторид америция(Ш)
AmF4 фторид америцияAУ)
Am(NO3K нитрат америция(Ш)
АтО2 оксид америция(ГУ)
Ат2О3 оксид америция(Ш)
Ат(ОНK гидроксид америция(Ш)
Ат(ОНL гидроксид америцияAУ)
Аг аргон
As мышьяк
As4 тетрамышьяк
AsBr3 трибромид мышьяка
AsCl3 трихлорид мышьяка
AsCl5 пентахлорид мышьяка
As(Cl)O оксид-хлорид мышьяка
AsF3 трифторид мышьяка
AsF5 пентафторид мышьяка
[AsF6],H гексафтороарсенат(У) во-
водорода
[AsF6],Li гексафтороарсенат(У)
лития
AsH3 арсин
Asl3 трииодид мышьяка
As2I4 тетраиодид димышьяка
AsN мононитрид мышьяка
As2O3 триоксид димышьяка
As2O5 пентаоксид димышьяка
As(O)F3 трифторид-оксид мышья-
мышьяка
AsP монофосфид мышьяка
As2S3 трисульфид димышьяка
As2S5 пентасульфид димышьяка
As4S4 тетрасульфид тетрамышьяка
As2Se3 триселенид димышьяка
26
I. Неорганические вещества
As2Te3 трителлурид димышьяка
H3As04 мышьяковая кислота
At2 диастат
Аи золото
AuIAgI(Te4) тетрателлуридB-) се-
ребраA)-золотаA)
(Аи^3)Те2 теллурид трисереб-
раA)-золотаA)
AuBr бромид золотаA)
AuBr3 бромид золота(Ш)
[АиВг4],Ктетрабромоаурат(Ш) ка-
калия
Аи2С2 ацетиленид золотаA)
AuCN цианид золотаA)
Au(CNK цианид золота(Ш)
) ка-
калия
[Au(CNL],K тетрацианоаурат(Ш)
калия
AuCl хлорид золотаA)
АиС13 хлорид золота(Ш)
[AuCl4],Cs тетрахлороаурат(Ш) це-
цезия
[АиС14],Н тетрахлороаурат(Ш) во-
водорода
[АиС14],Ктетрахлороаурат(Ш) ка-
калия
[AuCl4],NH4 тетрахлороаурат(Ш)
аммония
[AuCl4],Na тетрахлороаурат(Ш)
натрия
Аи(С1)О оксид-хлорид золота
AuF3 фторид золота(Ш)
AuF5 фторид золота(У)
Aul иодид золотаA)
Aul3 иодид золота(Ш)
AuNCS тиоцианат золотаA)
[Au(NO3L],H тетранитратоау-
рат(Ш) водорода
Аи2О3 оксид золота(Ш)
[Аи(ОНL] ,К тетрагидроксоау-
Рат(Ш) калия
АиО(ОН) метагидроксид золота
Au2S сульфид золотаA)
Au2(S2) дисульфидB-) золотаA)
Au2S3 сульфид золота(Ш)
[Au(SO3SJ],Na3 ди(тиосульфа-
то)ауратA) натрия
Au2(Se04K селенат золота(Ш)
АиТе2 дителлурид золота
В бор
BAs моноарсенид бора
(BAs)O4 тетраоксид мышьяка-бора
ВВг3 трибромид бора
В4С карбид тетрабора
В13С2дикарбид 13-бора
В(СН3СООK триацетат бора
В(СН3ОK триметоксиборан
В(С2Н5ОK триэтоксиборан
ВС13 трихлорид бора
В2С14 тетрахлорид дибора
[BD4],Na тетрадейтеридобо-
рат(Ш) натрия
BF3 трифторид бора
[BF4],C1F2 тетрафтороборат(Ш)
дифторохлора(Ш)
[ВР4],С8тетрафтороборат(Ш) це-
цезия
[ВР4],Ктетрафтороборат(Ш) ка-
калия
[BF4],NH4 тетрафтороборат(Ш)
аммония
[BF4],Na тетрафтороборат(Ш)
натрия
[BF4],XeF5 тетрафтороборат(Ш)
пентафтороксенона(У1)
В2Н6 диборан(б)
В4Н10 тетраборан(Ю)
В5Н9 пентаборан(9)
В5Н! { пентаборан( 11)
В6Н10 гексаборан(Ю)
В6Н12 гексаборанA2)
В9Н15 нонаборанA5)
В10Н,4декаборанA4)
В16Н2016-боранB0) \
В18Н2218-боранB2)
27
I. Неорганические вещества
В20Н1620-боранA6)
[ВН4]3,А1 тетрагидридоборат(Ш)
алюминия
[ВН4]2,Ве тетрагидридоборат(Ш)
бериллия
B3H3CI3N3 трихлороборазин
[BH4],Cs тетрагидридоборат(Ш)
цезия
[B10H10],Cs2 декаборанат(Ю) дице-
зия
[B12H12]Cs2 додекаборанатA2) ди-
цезия
[ВН4]4,Н1*тетрагидридоборат(Ш)
гафния(ГУ)
[ВН4],К тетрагидридоборат(Ш)
калия
[BH4],Li тетрагидридоборат(Ш)
лития
[BH4]2,Mg тетрагидридоборат(Ш)
магния
B3H6N3 боразин
[BH4],Na тетрагидридоборат(Ш)
натрия
[BH4]4,Ti тетрагидридоборат(Ш)
титанаAУ)
[BH4]4,U тетрагидридоборат(Ш)
уранаAУ)
[BH4]2,Zn тетрагидридоборат(Ш)
цинка(П)
[BH4]4,Zr тетрагидридоборат(Ш)
цирконияAУ)
В13 трииодид бора
ВA)Вг2 дибромид-иодид бора
BN нитрид бора
[B(NH3)F3] трифтороамминбор
[BN2],U3 динитридоборат(Ш)
лития
В2О3 триоксид дибора
В(ОНK тригидроксид бора
[B2(O2J(OHL],Na2 тетрагидроксо-
дипероксодиборат(Ш) натрия
ВР фосфид бора
(ВР)О4 тетраоксид фосфора-бора
B2S3 трисульфид дибора
[B(SO3FL],K тетра(фторосульфо-
нато)борат(Ш) калия
B3Si силицид трибора
B4Si силицид тетрабора
B6Si силицид гексабора
[BW12O40],H5 40-оксододекавольф-
рамоборат(Ш) водорода
НВО2 метаборная кислота
Ва барий
Ba3As2 арсенид бария
(BaAs2)O6 оксид димышья-
ка(У)-бария
Ba2As207 диарсенат бария
Ba3(As04J арсенат бария
ВаВ6 гексаборид бария
ВаВг2 бромид бария
Ва(ВгО3J бромат бария
ВаС2 ацетиленид бария
Ва(СН3СООJ ацетат бария
ВаСО3 карбонат бария
ВаС2О4 оксалат бария
ВаСа(СО3J карбонат каль-
кальция-бария
ВаС12 хлорид бария
Ba2(Cl)N нитрид-хлорид бария
Ва(С1ОJ гипохлорит бария
Ва(СЮ2J хлорит бария
Ва(С1О3J хлорат бария
Ва(С1О4J перхлорат бария
ВаСгО4 хромат бария
ВаСг2О7 дихромат бария
BaF2 фторид бария
ВаН2 гидрид бария
BaHAsO4 гидроарсенат бария
ВаНРО4 гидроортофосфат бария
Ва(Н2РО4J дигидроортофосфат
бария
Ba(HSJ гидросульфид бария
Ва12 иодид бария
Ва(Ю3J иодат бария
ВаМпО4 манганат бария
Ва(МпО4J перманганат бария
ВаМоО4 молибдат бария
28
I. Неорганические вещества
Ba(N3J азид бария
Ba3N2 нитрид бария
Ba(NCSJ тиоцианат бария
Ba(NH2J амид бария
[Ba(NH3N]I2 иодид гексаамминба-
рия(Н)
BaN2O2 гипонитрит бария
Ba(NO2J нитрит бария
Ba(NO3J нитрат бария
ВаО оксид бария
ВаО2 пероксид бария
Ва(О2J надпероксид бария
Ва(ОНJ гидроксид бария
Ва(РН2О2J фосфинат бария
Ва2Р2О7 дифосфат бария
Ва3(РО4J ортофосфат бария
Ba(ReO4J перренат бария
BaS сульфид бария
Ba(S2) дисульфидB-) бария
Ba(S3) трисульфидB-) бария
Ba(S4) тетрасульфидB-) бария
BaSO3 сульфит бария
BaSO4 сульфат бария
BaS2O6 дитионат бария
BaS2O6(O2) пероксодисульфат бария
Ba(SO3S) тиосульфат бария
BaSe селенид бария
BaSeO4 селенат бария
BaSiO3 метасиликат бария
(ВаТа2)О6 оксид дитанта-
ла(У)-бария
ВаТе теллурид бария
ВаТеО4 метателлурат бария
(BaTi)O3 оксид титанаAУ)-бария
Ba2V2O7 гептаоксодиванадат(У) ба-
бария
BaWO4 вольфрамат бария
Ва3Хе06 гексаоксоксенонат(У1)
бария
(BaZr)O3 оксид циркония(ГУ)-бария
Be бериллий
(ВеА12)О4 оксид диалюминия-бе-
риллия
(BeAs2)O6 оксид димышья-
ка(У)-бериллия
ВеВг2 бромид бериллия
Ве2С карбид дибериллия
[Ве(С5Н5J] бис(циклопентади-
енил)бериллий
Ве(СН3СООJ ацетат бериллия
Ве4(СН3СООNО оксид-гексааце-
тат бериллия
ВеСО3 карбонат бериллия
[Ве(С2О4J],Ве диоксалатоберил-
лат(И) бериллия
ВеС12 хлорид бериллия
Ве(С1О4J перхлорат бериллия
Ве4(С1О4NО оксид-гексаперхло-
рат бериллия
BeF2 фторид бериллия
[BeF4],K2 тетрафторобериллат(П)
калия
[BeF4],Li2 тетрафторобериллат(И)
лития
[BeF4],(NH4J тетрафтороберил-
лат(И) аммония
[BeF4],Na2 тетрафтороберил-
лат(П) натрия
ВеН2 гидрид бериллия
Ве4(НСООNО оксид-гексаформи-
ат бериллия
Ве12 иодид бериллия
Be3N2 нитрид бериллия
BeNH4As04 арсенат аммония-бе-
аммония-бериллия
[Be(NH3L]Cl2 хлорид тетрааммин-
бериллия(П)
BeNH4PO4 ортофосфат аммо-
аммония-бериллия
Be(NO3J нитрат бериллия
Be4(NO3NO оксид-гексанитрат бе-
бериллия
ВеО оксид бериллия
Ве(ОНJ гидроксид бериллия
BeS сульфид бериллия
BeSO4 сульфат бериллия
BeSe селенид бериллия
BeSeO4 селенат бериллия
29
I. Неорганические вещества
Be2Si04 ортосиликат бериллия
ВеТе теллурид бериллия
Bi висмут
BiAsO4 арсенат висмута(Ш)
(BiinBiv)O4 оксид висмута(У)-вис-
мута(Ш)
BiBr3 бромид висмута(Ш)
Bi(Br)O оксид-бромид висмута
Bi2(C2O4K оксалат висмута(Ш)
Bi2CO3(OHL тетрагидроксид-кар-
бонат дивисмута
BiCl3 хлорид висмута(Ш)
Bi24Cl28 28-хлорид 24-висмута
Bi(Cl)O оксид-хлорид висмута
BiC104@HJ дигидроксид-перхло-
рат висмута
BiF3 фторид висмута(Ш)
BiF5 фторид висмута(V)
Bil3 иодид висмута(Ш)
Bi(I)O оксид-иодид висмута
Bi2(MoO4K молибдат висмута(Ш)
Bi(NO3K нитрат висмута(Ш)
BiNO3(OHJ дигидроксид-нитрат
висмута
BiO оксид висмута(Н)
Bi2O3 оксид висмута(Ш)
Bi2O5 оксид висмута(У)
Bi(O)F фторид-оксид висмута
Bi(OHK гидроксид висмута(Ш)
BiO(OH) метагидроксид висмута
BiPO4 ортофосфат висмута(Ш)
Bi2S3 сульфид висмута(Ш)
Bi2(SO4K сульфат висмута(Ш)
Bi2Se3 селенид висмута(Ш)
Bi4(Si04K ортосиликат висмута(Ш)
Bi2Te3 теллурид висмута(Ш)
Вк берклий
ВЮ2 оксид берклияA\0
Вг2 дибром
[BrAg2]NO3 нитрат дисереб-
роA)брома(—I)
[Br(Br)Cl],Cs хлоробромобро-
матA) цезия
[Br(BrJ],Cs дибромоброматA) цезия
ВгС1 монохлорид брома
[Br(ClJ],Cs дихлороброматA) цезия
BrF монофторид брома
BrF3 трифторид брома
BrF5 пентафторид брома
[BrF4],K тетрафторобромат(Ш)
калия
BrNO3 мононитрат брома
Br(NO3K тринитрат брома
Вг2О оксид диброма
Вг2О4 тетраоксид диброма
Br(O)F3 трифторид-оксид брома
BrO2F фторид-диоксид брома
BrO3F фторид-триоксид брома
[Br(OJ(FJJ,K дифтородиоксобро-
мат(У) калия
НВг бромоводород
а-С графит
Р-С алмаз
СВг4 тетрабромид углерода
СС14 тетрахлорид углерода
(СС13 )С1О4 перхлорат трихлороуг-
лерода(ГУ)
CC12F2 дифторид-дихлорид угле-
углерода
СС12О оксид-дихлорид углерода
CF4 тетрафторид углерода
(CF3 )С1О гипохлорит трифторо-
углеродаAУ)
(CF3 )С1О4 перхлорат трифтороуг-
лерода(ГУ)
СН4 метан
С2Н2 ацетилен
С2Н4 этилен
С6Н6 бензол
СН3С(Н)О ацетальдегид
CH3CN ацетонитрил
СН3СООН уксусная кислота
СНС13 хлороформ
C2H8N2 этилендиамин
30
I. Неорганические вещества
C5H5N пиридин
СН3ОН метанол
С2Н5ОН этанол
С14 тетраиодид углерода
C2N2 дициан
C6N6 гексациан
(CN)Br бромциан
(CN)C1 хлорциан
(CN)F фторциан
C(NH2JO карбамид
(CN)I иодциан
СО монооксид углерода
СО2 диоксид углерода
C(O)F2 дифторид-оксид углерода
CS2 сероуглерод
C3S2 дисульфид триуглерода
C(S)C12 дихлорид-сульфид углерода
CS(NH2J тиокарбамид
C(S)O оксид-сульфид углерода
CSe2 селеноуглерод
CSe(NH2J селенокарбамид
C(Se)O оксид-селенид углерода
C(Se)S сульфид-селенид углерода
C(Te)S сульфид-теллурид углерода
HCN циановодород
H2CN2 цианамид водорода
Н2С2О4 щавелевая кислота
НСООН муравьиная кислота
H2CS3 тритиоугольная кислота
Са кальций
(СаА12)О4 оксид диалюми-
ния-кальция
Ca3As2 арсенид кальция
Ca(AsO2J метаарсенит кальция
(CaAs2)O6 оксид димышья-
ка(У)-кальция
Ca3(As04J арсенат кальция
СаВ6 гексаборид кальция
Са(ВО2J метаборат кальция
Са2В2О5 пентаоксодиборат(Ш)
кальция
Са3(ВО3J ортоборат кальция
СаВг2 бромид кальция
Са(ВгО3J бромат кальция
СаС2 ацетиленид кальция
Са(СН3СООJ ацетат кальция
CaCN2 цианамид кальция
Ca(CNJ цианид кальция
СаСО3 карбонат кальция
СаС2О4 оксалат кальция
СаС12 хлорид кальция
Са(С1ОJ гипохлорит кальция
Са(С1О2J хлорит кальция
Са(С1О3J хлорат кальция
Са(С1О4J перхлорат кальция
СаСЮ4 хромат кальция
(СаСг2)О4 оксид дихро-
ма(Ш)-кальция
CaF2 фторид кальция
(CaFe2)O4 оксид дижеле-
за(Ш)-кальция
СаН2 гидрид кальция
Са(НСООJ формиат кальция
СаНРО4 гидроортофосфат кальция
Са(Н2РО4J дигидроортофосфат
кальция
Ca(HSJ гидросульфид кальция
Са12 иодид кальция
Са(Ю3J иодат кальция
CaMg(CO3J карбонат магния-
кальция
CaMgSiO4 ортосиликат магния-
кальция
CaMg(SiO3J метасиликат магния-
кальция
Са(МпО4J перманганат кальция
СаМоО4 молибдат кальция
Ca(N3J азид кальция
Ca3N2 нитрид кальция
CaNH4As04 арсенат аммо-
аммония-кальция
[Ca(NH3N]I2 иодид гексааммин-
кальция(И)
Ca(NO2J нитрит кальция
Ca(NO3J нитрат кальция
СаО оксид кальция
СаО2 пероксид кальция
31
I. Неорганические вещества.
Са(ОНJ гидроксид кальция
Са3Р2 фосфид кальция
Са(РН2О2J фосфинат кальция
Са(РО3J метафосфат кальция
Са2Р2О7 дифосфат кальция
Са3(РО4J ортофосфат кальция
Ca(PO3F) фтороортофосфат каль-
кальция
Ca5(PO4KF фторид-три(ортофос-
фат) кальция
CaS сульфид кальция
CaSO3 сульфит кальция
CaSO4 сульфат кальция
Ca(SO3S) тиосульфат кальция
CaSe селенид кальция
CaSeO4 селенат кальция
CaSi моносилицид кальция
CaSi2 дисилицид кальция
CaSiO3 метасиликат кальция
Ca2SiO4 ортосиликат кальция
Ca3Si05 пентаоксосиликатAУ)
кальция
Ca3Si207 дисиликат кальция
(СаТа2)О6 оксид дитанта-
ла(У)-кальция
СаТе теллурид кальция
СаТеО3 теллурит кальция
СаТеО4 метателлурат кальция
(CaTi)O3 оксид титанаAУ)-кальция
Ca(VO3J метаванадат кальция
Ca2V2O7 гептаоксодиванадат(У)
кальция
Ca3(VO4J ортованадат кальция
CaWO4 вольфрамат кальция
(CaZr)O3 оксид цирко-
ния(ГУ)-кальция
Cd кадмий
CdAs2 диарсенид кадмия
Cd3As2 арсенид кадмия(П)
CdBr2 бромид кадмия(Н)
Cd(CH3COOJ ацетат кадмия(И)
Cd(CNJ цианид кадмия(Н)
[Cd(CNL],K2 тетрацианокад-
мат(И) калия
CdCO3 карбонат кадмия(Н)
CdC2O4 оксалат кадмия(Н)
CdCl2 хлорид кадмия(И)
Cd(C103J хлорат кадмия(П)
CdF2 фторид кадмия(Н)
Cd(H2PO4J дигидроортофосфат
кадмия(И)
Cdl2 иодид кадмия(П)
Cd(IO3J иодат кадмия(П)
Cd(MnO4J перманганат кад-
мия(П)
CdMoO4 молибдат кадмия(П)
Cd(NH2J амид кадмия(П)
Cd(NH4J(SO4J сульфат диаммо-
ния-кадмия(П)
Cd(NO3J нитрат кадмия(Н)
CdO оксид кадмия(П)
Cd(OHJ гидроксид кадмия(П)
Cd3P2 фосфид кадмия(Н)
Cd2P2O7 дифосфат кадмия(П)
CdS сульфид кадмия(Н)
CdSO4 сульфат кадмия(П)
CdSb моностибид кадмия
CdSe селенид кадмия(Н)
CdSeO4 селенат кадмия(П)
CdSiO3 метасиликат кадмия(Н)
Cd2Si04 ортосиликат кадмия(И)
CdTe теллурид кадмия(П)
Се церий
СеВ6 гексаборид церия
СеВг3 бромид церия(Ш)
СеС2 дикарбид церия
Се2(С2О4K оксалат церия(Ш)
СеС13 хлорид церия(Ш)
(Се1ИСг)О3 оксид хрома(Ш)-це-
рия(Ш)
CeF3 фторид церия(Ш)
CeF4 фторид церия (IV)
СеН3 гидрид церия(Ш)
Се13 иодид церия(Ш)
Се2(МоО4K молибдат церия(Ш)
CeNH4(SO4J сульфат аммония-
церия(Ш)
32
I. Неорганические вещества
Ce(NO3K нитрат церия(Ш)
[Ce(NO3N[,(NH4J гексанитрато-
церат(ГУ) аммония
Ce(NO3KOH гидроксид-тринит-
рат церия
СеО2 оксид церияAУ)
Се2О3 оксид церия(Ш)
Се(ОНK гидроксид церия(Ш)
СеРО4 ортофосфат церия(Ш)
Ce2S3 сульфид церия(Ш)
Ce(SO4J сульфат церия(ГУ)
Ce2(S)O2 диоксид-сульфид церия
Ce2(SO4K сульфат церия(Ш)
Ce2(Se04K селенат церия(Ш)
Ce2(WO4K вольфрамат церия(Ш)
Cf калифорний
CfBr3 бромид калифорния(Ш)
CfCl3 хлорид калифорния(Ш)
СЮ2 оксид калифорнияAУ)
Cf2O3 оксид калифорния(Ш)
С12 дихлор
[ClAg2]NO3 нитрат дисереб-
роA)хлора(-1)
C1F монофторид хлора
C1F5 пентафторид хлора
C12F6 гексафторид дихлора
[C1F4],(NO+) тетрафторохло-
рат(Ш) нитрозилия
C1N3 азид хлораA)
C13N нитрид трихлора
СЮ2 диоксид хлора
С12О оксид дихлора
С12О6 гексаоксид дихлора
С12О7 гептаоксид дихлора
(СЮ J )С1О гипохлорит триоксох-
лора(УН)
C1(O)F3 трифторид-оксид хлора
C1O2F фторид-диоксид хлора
C1O2F3 трифторид-диоксид хлора
C1O3F фторид-триоксид хлора
C1(SO3F) фторосульфонат хлораA)
НС1 хлороводород
НС1О4 хлорная кислота
Cm кюрий
Ст2(С2О4K оксалат кюрия(Ш)
CmF3 фторид кюрияAУ)
СтО2 оксид кюрияAУ)
Ст2О3 оксид кюрия(Ш)
Со кобальт
(СоА12)О4 оксид диалюминия-ко-
бальта(П)
CoAs моноарсенид кобальта
CoAs2 диарсенид кобальта
CoAs3 триарсенид кобальта
Co2As арсенид дикобальта
Co3(AsO4J арсенат кобальта(Н)
Co(As)S сульфид-арсенид кобальта
СоВ моноборид кобальта
Со2В борид дикобальта
Со3В борид трикобальта
СоВг2 бромид кобальта(И)
Со2С карбид дикобальта
[Со(С5Н5J] бис(циклопентади-
енил)кобальт
Со(СН3СООJ ацетат кобальта(И)
Со(СН3СООK ацетат кобальта(Ш)
[Co(C2H8N2K]Br3 бромид трис(эти-
лендиамин)кобальта(Ш)
[Со(С5Н5J]ОН гидроксид
бис(циклопентадиенил) ко-
бальта(Ш)
[CoH(CNN],Co2 гексацианоко-
бальтат(П) кобальта(Н)
[Co(CNN],K3 гексацианокобаль-
тат(Ш) калия
[Co(CNN],K4 гексацианокобаль-
тат(И) калия
СоСО3 карбонат кобальта(П)
СоС2О4 оксалат кобальта(Н)
[Со2(СО)8] октакарбонилдикобальт
[Со4(СОI2] додекакарбонилтетра-
кобальт
[Со(СОJС5Н5] (циклопентади-
енил)дикарбонилкобальт
33
I. Неорганические вещества
СоС12 хлорид кобальта(Н)
Со(С1О3J хлорат кобальта(Н)
Со(С1О4J перхлорат кобальта(И)
(СопСо 2П)О4 оксид дикобаль-
та(Ш)-кобальтаA1)
(СопСо 2H)S4 сульфид дикобаль-
та(Ш)-кобальта(П)
(СоиСо 2П)Те4 теллурид дикобаль-
та(Ш)-кобальта(Н)
CoF2 фторид кобальта(П)
CoF3 фторид кобальта(Ш)
[СоН(СОL] тетракарбонилгидро-
кобальт
Со(НСООJ формиат кобальта(Н)
Со12 иодид кобальта(Н)
Со(Ю3J иодат кобальта(И)
Co2N нитрид дикобальта
Co(NCSJ тиоцианат кобальта(Н)
Co(NH2K амид кобальта(Ш)
[Co(NH3N]Br2 бромид гексаам-
минкобальта(И)
[Co(NH3N]Cl2 хлорид гексааммин-
кобальта(Н)
[Co(NH3N]Cl3 хлорид гексааммин-
кобальта(Ш)
[Co(NH3LCl2]Gl хлорид дихлоро-
тетраамминкобальта(Ш)
[Co(NH3MCl]Cl2 хлорид хлоропен-
таамминкобальта(Ш)
[Co(NH3N]I2 иодид гексаамминко-
бальта(П)
[Co(NH3N]I3 иодид гексаамминко-
бальта(Ш)
[Co(NH3K(NO2K] тринитротриам-
минкобальт
[Co(NH3N](NO3K нитрат гексаам-
минкобальта(Ш)
[Co(NH3MNO2]Cl2 хлорид нитро-
пентаамминкобальта(Ш)
Co(NH4J(SO4J сульфат диаммо-
ния - кобал ьта( II)
[Co(NH3N]2(SO4K сульфат гекса-
амминкобальта(Ш)
Co(NO3J нитрат кобальта(Н)
[Co(NOK] тринитрозилкобальт
Co(NO3K нитрат кобальта(Ш)
[Co(NO+)(COK] трикарбонилнит-
розилийкобальт
[Co(NO2N],K3 гексанитрокобаль-
тат(Ш) калия
[Co(NO2N],K2Na гексанитроко-
бальтат(Н1) натрия-дикалия
[Co(NO2N],Na3 гексанитрокобаль-
тат(Ш) натрия
СоО оксид кобальта(И)
Со2О3 оксид кобальта(Ш)
Со(ОНJ гидроксид кобальта(И)
СоО(ОН) метагидроксид кобальта
СоР монофосфид кобальта
Со2Р фосфид дикобальта
Со3(РО4J ортофосфат кобальта(Н)
CoS сульфид кобальта(П)
Co(S2) дисульфидB-) кобальта(И)
Co9S8 октасульфид нонакобальта
CoSO4 сульфат кобальта(Н)
Co2(SO4K сульфат кобальта(Ш)
CoSb моностибид кобальта
CoSb2 дистибид кобальта
CoSb3 тристибид кобальта
CoSe селенид кобальта(Н)
Co(Se2) диселенидB-) кобальта(П)
CoSeO4 селенат кобальта(Н)
CoSi моносилицид кобальта
CoSi2 дисилицид кобальта
Co2Si силицид дикобальта
CoSiO3 метасиликат кобальта(П)
Co2SiO4 ортосиликат кобальта(П)
Со(Те2) дителлуридB-) кобальта(И)
Сг хром
СгВ моноборид хрома
СгВ2 диборид хрома
Сг2В борид дихрома
СгВг2 бромид хрома(Н)
СгВг3 бромид хрома(Ш)
Сг3С2 дикарбид трихрома
[Сг(С5Н5J] бис(циклопентади-
енил)хром
[Сг(С6Н6J] дибензолхром
34
I. Неорганические вещества
[Cr(CNN],K3 гексацианохро-
мат(Ш) калия
[Сг(СОN] гексакарбонилхром
СгС12 хлорид хрома(И)
СгС13 хлорид хрома(Ш)
Сг(С1)О оксид-хлорид хрома
СгС12О2 диоксид-дихлорид хрома
СгС13О оксид-трихлорид хрома
CrF2 фторид хрома(П)
CrF3 фторид хрома(Ш)
CrF4 фторид хромаA\0
CrF5 фторид хрома(У)
CrF6 фторид хрома(У1)
(Cr?nFe)O4 оксид железа(И)-дих-
рома(Ш)
[Сг(Н2ОLС12]С1 хлорид дихлоро-
тетрааквахромаA II)
[Сг(Н2ОMС1]С12 хлорид хлоропен-
тааквахрома(Ш)
Сг12 иодид хрома(П)
Сг13 иодид хрома(Ш)
CrN мононитрид хрома
Cr2N нитрид дихрома
[Cr(NCSN],K3 гекса(тиоциана-
то)хромат(Ш) калия
[Cr(NH3N]Cl3 хлорид гексаам-
минхрома(Ш)
[Cr(NH3MCl]Cl2 хлорид хлоропен-
таамминхрома(Ш)
CrNH4(SO4J сульфат аммо-
ния-хрома(Ш)
Cr(NO3K нитрат хрома(Ш)
[Cr(NOL] тетранитрозилхром
СЮ оксид хрома(П)
СгО2 оксид хромаAУ)
СгО3 оксид хрома(У1)
Сг2О3 оксид хрома(Ш)
Cr(O)F4 тетрафторид-оксид хрома
CrO2F2 дифторид-диоксид хрома
Сг(ОНJ гидроксид хрома(Н)
Сг(ОНK гидроксид хрома(Ш)
[Cr(OHN],Na3 гексагидроксохро-
мат(Ш) натрия
[Сг(О2L],к3 тетрапероксохро-
мат(У) калия
[Cr(O2L],Na3 тетрапероксохро-
мат(\^ натрия
СгО(ОН) метагидроксид хрома
СгР монофосфид хрома
Сг3Р фосфид трихрома
[Cr(PF3N] гексакис(трифторофос-
фор)хром
СгРО4 ортофосфат хрома(Ш)
CrS сульфид хрома(И)
Cr2S3 сульфид хрома(Ш)
CrSO4 сульфат хрома(И)
Cr2(SO4K сульфат хрома(Ш)
CrSi моносилицид хрома
CrSi2 дисилицид хрома
Cr3Si силицид трихрома
Cr5Si3 трисилицид пентахрома
CrTlI(SO4J сульфат таллияA)-хро-
ма(Ш)
CrVO4 ортованадат хрома(Ш)
(Cr^nZn)O4 оксид цинка(И)-дих-
рома(Ш)
Cs цезий
CsAl(SO4J сульфат алюминия-цезия
CsBr бромид цезия
CsBrO3 бромат цезия
Cs(CH3COO) ацетат цезия
Cs2CO3 карбонат цезия
CsCl хлорид цезия
CsC102 хлорит цезия
CsC103 хлорат цезия
CsC104 перхлорат цезия
Cs2Cr04 хромат цезия
Cs2Cr207 дихромат цезия
CsCr(SO4J сульфат хрома(Ш)-цезия
CsF фторид цезия
CsFe(SO4J сульфат железа(Ш)-це-
зия
Cs2Fe(SO4J сульфат железа(И)-ди-
цезия
CsGa(SO4J сульфат галлия(Ш)-
цезия
CsH гидрид цезия
CsHCO3 гидрокарбонат цезия
Cs(HCOO) формиат цезия
35
I. Неорганические вещества
CsHSO4 гидросульфат цезия
Csl иодид цезия
CsIO3 иодат цезия
CsIO4 метапериодат цезия
CsMnO4 перманганат цезия
CsN3 азид цезия
CsNH2 амид цезия
CsNO2 нитрит цезия
CsNO3 нитрат цезия
CsO2 надпероксид цезия
CsO3 озонид цезия
Cs2O оксид цезия
Cs2O2 пероксид цезия
CsOH гидроксид цезия
Cs2S сульфид цезия
Cs2(S2) дисульфидB-) цезия
Cs2(S3) трисульфидB-) цезия
Cs2(S5) пентасульфидB-) цезия
Cs2(S6) гексасульфидB-) цезия
Cs2SO4 сульфат цезия
Cs2S2O7 дисульфат цезия
Cs3Sb стибид трицезия
Cs2Se04 селенат цезия
CsV(SO4J сульфат вана-
дия(Ш)-цезия
Си медь
Cu3As арсенид медиA)
Cu3(As04J арсенат меди(П)
Cu2(AsO4)OH гидроксид-арсенат
меди(Н)
Cu3AsS4 тетратиоарсенат медиA)
CuBr бромид медиA)
CuBr2 бромид меди(Н)
Cu(BrO3J бромат меди(П)
Си2С2 ацетиленид медиA)
Си(СН3СООJ ацетат меди(П)
CuCN цианид медиA)
Cu(CNJ цианид меди(И)
СиС2О4 оксалат меди(Н)
Си2СО3 карбонат медиA)
Си2СО3(ОНJ дигидроксид-карбо-
нат меди(П)
Си3(СО3J(ОНJ дигидроксид-ди-
карбонат меди(П)
CuCl хлорид медиA)
СиС12 хлорид меди(И)
Си(С1О3J хлорат меди(П)
Си(С1О4J перхлорат меди(П)
СиСЮ2 диоксохромат(Ш) медиA)
CuF2 фторид меди(И)
СиН гидрид медиA)
Си(НСООJ формиат меди(И)
Cul иодид медиA)
Си(Ю3J иодат меди(П)
Cu(N3J азид меди(И)
Cu3N нитрид медиA)
CuNCS тиоцианат медиA)
[Cu(NH2CH2COOJ] диглицинато-
медь
[Cu(NH3N]Cl2 хлорид гексааммин-
меди(И)
[Cu(NH3L](NO3J нитрат тетраам-
минмеди(И)
[Cu(NH3L]SO4 сульфат тетраам-
минмеди(И)
Cu(NO3J нитрат меди(П)
СиО оксид меди(П)
Си2О оксид медиA)
Си2О3 оксид меди(Ш)
Си(ОНJ гидроксид меди(П)
[Си(ОНL],К тетрагидроксокуп-
рат(Ш) калия
[Cu(OHL],Na2 тетрагидроксокуп-
рат(Н) натрия
СиР2 дифосфид меди
Си3Р фосфид медиA)
CuS сульфид меди(И)
Cu(S2) дисульфидB-) меди(П)
Cu2S сульфид медиA)
CuSO4 сульфат меди(И)
Cu2SO4 сульфат медиA)
Cu4SO4(OHN гексагидрок-
сид-сульфат меди(П)
Cu3Sb стибид тримеди
CuSe селенид меди(П)
Cu2Se селенид медиA)
36
I. Неорганические вещества
CuSeO4 селенат меди(Н)
Cu2Te теллурид медиA)
D2 дидейтерий
DBr бромид дейтерия
DC1 хлорид дейтерия
DF фторид дейтерия
DI иодид дейтерия
D2O оксид дейтерия
D3PO4 ортофосфат дейтерия
D2S сульфид дейтерия
D2SO4 сульфат дейтерия
DT дейтериотритий
Dy диспрозий
DyBr3 бромид диспрозия(Ш)
Dy(BrO3K бромат диспрозия(Ш)
Dy2(C2O4K оксалат диспрозия(Ш)
DyCl3 хлорид диспрозия(Ш)
DyF3 фторид диспрозия(Ш)
Dyl3 иодид диспрозия(Ш)
Dy(NO3K нитрат диспрозия(Ш)
Dy2O3 оксид диспрозия(Ш)
Dy(OHK гидроксид диспрозия(Ш)
Dy2S3 сульфид диспрозия(Ш)
Dy2(SO4K сульфат диспрозия(Ш)
Ег эрбий
ЕгВг3 бромид эрбия(Ш)
Ег(СН3СООK ацетат эрбия(Ш)
Ег2(С2О4K оксалат эрбия(Ш)
ЕгС13 хлорид эрбия(Ш)
ErF3 фторид эрбия(Ш)
Erl3 иодид эрбия(Ш)
Er(NO3K нитрат эрбия(Ш)
Ег2О3 оксид эрбия(Ш)
Ег(ОНK гидроксид эрбия(Ш)
Er2S3 сульфид эрбия(Ш)
Er2(SO4K сульфат эрбия(Ш)
Es эйнштейний
Ей европий
EuBr2 бромид европия(И)
EuBr3 бромид европия(Ш)
Еи2(С2О4K оксалат европия(Ш)
ЕиС12 хлорид европия(П)
ЕиС13 хлорид европия(Ш)
EuF2 фторид европия(И)
EuF3 фторид европия(Ш)
Eul2 иодид европия(Н)
Eul3 иодид европия(Ш)
Eu(NO3K нитрат европия(Ш)
ЕиО оксид европия(И)
Еи2О3 оксид европия(Ш)
Еи(ОНJ гидроксид европия(И)
Еи(ОНK гидроксид европия(Ш)
EuS сульфид европия(П)
Eu2S3 сульфид европия(Ш)
EuSO4 сульфат европия(П)
Eu2(SO4K сульфат европия(Ш)
F2 дифтор
HF фтороводород
Fe железо
(FeAl2)O4 оксид диалюминия-же-
леза(И)
FeAs моноарсенид железа
FeAs2 диарсенид железа
FeAsO4 арсенат железа(Ш)
Fe(As)S сульфид-арсенид железа
FeB моноборид железа
FeBr2 бромид железа(И)
FeBr3 бромид железа(Ш)
Fe3C карбид трижелеза
[Fe5C(COI5] 15-карбонилуглерод-
пентажелезо
[Fe(C5H5J] бис(циклопентади-
енил)железо
[Fe(C5H5J]NO3 нитрат бис(цикло-
пентадиенил)железа(Ш)
[Feni(CNN],Fe гексацианофер-
рат(Ш) железа(Ш)
[Fen(CNN],Fe2 гексацианофер-
рат(И) железа(И)
[Fe(CNN],H3 гексацианофер-
рат(Ш) водорода
37
I. Неорганические вещества
[Fe(CNN],H4 гексацианофер-
рат(Н) водорода
[Fe(CNN],K3 гексацианофер-
рат(Ш) калия
[Fe(CNN],K4 гексацианофер-
рат(Н) калия
[Fen(CNN],KFe гексацианофер-
рат(П) железа(Ш)-калия
FeCO3 карбонат железа(Н)
FeC2O4 оксалат железа(И)
[Fe(COM] пентакарбонилжелезо
Fe2(C2O4K оксалат железа(Ш)
[Fe2(CO)9] нонакарбонилдижелезо
[Fe3(COI2] додекакарбонилтриже-
лезо
[Fe(C2O4K],K3 триоксалатофер-
рат(Ш) калия
[Fe(C2O4K],(NH4K триоксалато-
феррат(Ш) аммония
[Fe(C2O4K],Na3 триоксалатофер-
рат(Ш) натрия
FeCl2 хлорид железа(П)
FeCl3 хлорид железа(Ш)
Fe(Cl)O оксид-хлорид железа
Fe(C104J перхлорат железа(П)
Fe(C104K перхлорат железа(Ш)
FeCu(S2) дисульфидB-) меди-же-
меди-железа
FeF2 фторид железа(Н)
FeF3 фторид железа(Ш)
(FenFeI11[)F5 фторид желе-
за(Ш)-железа(Н)
(FenFe 2И)О4 оксид дижелеза(Ш)-
железа(Н)
[Fe(H2O)Cl5],K2 пентахлороаква-
феррат(Ш) калия
Fel2 иод ид железа(П)
Fe2N нитрид дижелеза
Fe3N нитрид трижелеза
Fe4N нитрид тетражелеза
FeNH4(SO4J сульфат аммо-
ния-железа(Ш)
Fe(NH4J(SO4J сульфат диаммо-
ния-железа(Н)
Fe(NO3J нитрат железа(П)
Fe(NO3K нитрат железа(Ш)
[Fe(NOL] тетранитрозилжелезо
[Fe(NO+)(CNM],Na2 пентациано-
нитрозилийферрат(П) натрия
(Fe2nNi)O4 оксид никеля(П)-ди-
железа(Ш)
FeO оксид железа(И)
Fe2O3 оксид железа(Ш)
Fe2 67О4 тетраоксид 2,67-железа
Fe(OHJ гидроксид железа(П)
FeO(OH) метагидроксид железа
FeP монофосфид железа
FeP2 дифосфид железа
Fe2P фосфид дижелеза
Fe3P фосфид трижелеза
[Fe(PF3M] пентакис(трифторофос-
фор)железо
FePO4 ортофосфат железа(Ш)
Fe3(PO4J ортофосфат железа(П)
FeS сульфид железа(Н)
Fe(S2) дисульфидB-) железа(И)
[Ре82],Кдитиоферрат(Ш) калия
FeSO4 сульфат железа(И)
Fe2(SO4K сульфат железа(Ш)
FeSi моносилицид железа
FeSi2 дисилицид железа
Fe3Si силицид трижелеза
FeSiO3 метасиликат железа(Н)
Fe2Si04 ортосиликат железа(П)
FeVO4 ортованадат железа(Ш)
FeWO4 вольфрамат железа(П)
(Fe^nZn)O4 оксид цинка(П)-диже-
леза(Ш)
Fm фермий
Fir франций
Ga2 дигаллий
GaAs моноарсенид галлия
GaBr бромид галлияA)
GaBr3 бромид галлия(Ш)
[GamBr4],Ga тетрабромогал-
лат(Ш) галлияA)
38
I. Неорганические вещества
[Ga 2П Br7] ,Ga гептабромодигал-
лат(Ш) галлияA)
GaCl3 хлорид галлия(Ш)
[GaHICl4],Ga тетрахлорогал-
лат(Ш) галлияA)
[Ga2nCl7],Ga гептахлородигал-
лат(Ш) галлияA)
[GaCl2],H дихлорогаллатA) водо-
водорода
Ga(C104K перхлорат галлия(Ш)
GaF3 фторид галлия(Ш)
Gal иодид галлияA)
Gal3 иодид галлия(Ш)
[GaIHI4],Ga тетраиодогаллат(Ш)
галлияA)
GaN мононитрид галлия
GaNH4(SO4J сульфат аммо-
ния-галлия(Ш)
[GaN2],Li3 динитридогаллат(Ш)
лития
Ga(NO3K нитрат галлия(Ш)
Ga2O оксид галлияA)
Ga2O3 оксид галлия(Ш)
Ga(OHK гидроксид галлия(Ш)
GaO(OH) метагидроксид галлия
GaP монофосфид галлия
GaPO4 ортофосфат галлия(Ш)
Ga2(S2) дисульфидB-) галлияA)
Ga2S3 сульфид галлия(Ш)
Ga2(SO4K сульфат галлия(Ш)
GaSb моностибид галлия
Ga2Se3 селенид галлия(Ш)
Ga2Te3 теллурид галлия(Ш)
Gd гадолиний
GdBr3 бромид гадолиния(Ш)
Gd2(C2O4K оксалат гадолиния(Ш)
GdCl3 хлорид гадолиния(Ш)
GdF3 фторид гадолиния(Ш)
Gdl3 иодид гадолиния(Ш)
Gd(NO3K нитрат гадолиния(Ш)
Gd2O3 оксид гадолиния(Ш)
Gd(OHK гидроксид гадолиния(Ш)
Gd2S3 сульфид гадолиния(Ш)
Gd2(SO4K сульфат гадолиния(Ш)
Gd2(SeO4K селенат гадолиния(Ш)
Ge германий
GeBr2 бромид германия(Н)
GeBr4 бромид германияAУ)
Ge(CH3COOL ацетат герма-
нияAУ)
Ge(CNL цианид германия(ГУ)
GeCl хлорид германияA)
GeCl2 хлорид германия(П)
GeCl4 хлорид германияAУ)
GeF2 фторид германия(И)
GeF4 фторид германия(ГУ)
[GeF6],K2 гексафторогерманат(ГУ)
калия
[GeF6],Mg гексафторогерма-
нат(ГУ) магнрш
[GeF6],Na2 гексафторогерма-
натAУ) натрия
GeH4 моногерман
Ge2H6 дигерман
Ge3H8 тригерман
Ge4H10 тетрагерман
Ge5H12 пентагерман
Gel2 иодид германия(П)
Gel4 иодид германияAУ)
Ge3N4 нитрид германияAУ)
GeO оксид германия(И)
GeO2 оксид германияAУ)
GeP монофосфид германия
GeS сульфид германия(Н)
GeS2 сульфид германияAУ)
GeSe селенид германия(П)
GeSe2 селенид германияAУ)
GeTe теллурид германия(П)
Н2 диводород
Н2О вода
НТ протиотритий
Не гелий
Hf гафний
HfB2 диборид гафния
39
I. Неорганические вещества
HfBr4 бромид гафнияAУ)
HfC0 94 0,94-карбид гафния
[Hf(C5H5JCl2] дихлоробис(циклог
пентадиенил)гафний
HfCl4 хлорид гафнияAУ)
HfCl2O оксид-дихлорид гафния
HfF4 фторид гафния(ГУ)
[HfF6],K2 гексафторогафнатAУ)
калия
[HfF7],(NH4K гептафторогаф-
нат(ГУ) аммония
Hfl4 иодид гафния(ГУ)
HfN мононитрид гафния
Hf(NO3JO оксид-динитрат гаф-
ния(П)
НЮ2 оксид гафнияAУ)
НЮ(ОНJ дигидроксид-оксид
гафния(ГУ)
Hf(SO4J сульфат гафния(ГУ)
HfSi2 дисилицид гафния
Hg ртуть
Hg3(As04J арсенат ртути(И)
HgBr2 бромид ртути(Н)
Hg2Br2 дибромид диртути
Hg(BrO3J бромат ртути(П)
Hg2(Br03J дибромат диртути
Hg2C2 ацетиленид диртути
Hg(CH3COOJ ацетат ртути(И)
Hg(CNJ цианид ртути(Н)
Hg(CNOJ фульминат ртути(И)
Hg2CO3 карбонат диртути
HgCl2 хлорид ртути(И)
Hg2Cl2 дихлорид диртути
HgCl(NH2) амид-хлорид ртути(И)
Hg(C103J хлорат ртути(П)
Hg(C104J перхлорат ртути(П)
Hg2(C103J дихлорат диртути
Hg2(C104J диперхлорат диртути
HgF2 фторид ртути(И)
Hg2F2 дифторид диртути
Hgl2 иодид ртути(Н)
Hg2I2 дииодид диртути
[HgI4],Ag2 тетраиодомеркурат(И)
серебраA)
[HgI3],Kтpииoдoмepкypaт(II) калия
[HgI4],K2 тетраиодомеркурат(П)
калия
Hg(NCSJ тиоцианат ртути(П)
Hg(NO3J нитрат ртути(И)
Hg2(NO2J динитрит диртути
Hg2(NO3J динитрат диртути
HgO оксид ртути(И)
HgS сульфид ртути(П)
Hg(S2) дисульфид B-) ртути(П)
HgSO4 сульфат ртути(И)
Hg2SO4 сульфат диртути
HgSe селенид ртути(Н)
HgTe теллурид ртути(П)
Но гольмий
НоВг3 бромид гольмия(Ш)
Но2(С2О4K оксалат гольмия(Ш)
НоС13 хлорид гольмия(Ш)
HoF3 фторид гольмия(Ш)
Но13 иодид гольмия(Ш)
Ho(NO3K нитрат гольмия(Ш)
Но2О3 оксид гольмия(Ш)
Но(ОНK гидроксид гольмия(Ш)
Ho2(SO4K сульфат гольмия(Ш)
12 дииод
[IAg2]NO3 нитрат дисереб-
раA)иода(-1)
1Вг монобромид иода
[I(Br)Cl],Cs хлоробромоиодатA)
цезия
[I(BrJ],Cs дибромоиодатA) цезия
[1(ВгJ],К дибромоиодатA) калия
IC1 монохлорид иода
12С16 гексахлорид дииода
[I(ClJ],Cs дихлороиодатA) цезия
[I(ClL],Cs тетрахлороиодат(Ш)
цезия
[1(С1L],Н тетрахлороиодат(Ш) во-
водорода
[1(С1J],К дихлороиодатA) калия
40
I. Неорганические вещества
[1(С1L],Ктетрахлороиодат(Ш) ка-
калия
IF монофторид иода
IF3 трифторид иода
IF5 пентафторид иода
IF7 гептафторид иода
[I(IJ],Cs дииодоиодатA) цезия
[1AJ],КдииодоиодатA) калия
[I(IJ],NH4 дииодоиодатA) аммония
[I(IJ],Rb дииодоиодатA) рубидия
I3N нитрид трииода
I(NO3K тринитрат иода
12О5 пентаоксид дииода
I(O)F3 трифторид-оксид иода
I(O)F5 пентафторид-оксид иода
IO2F фторид-диоксид иода
IO2F3 трифторид-диоксид иода
IO3F фторид-триоксид иода
[I(OJF4],H тетрафтородиоксоио-
дат(УП) водорода
(Ю+)Ю3 иодат оксоиода(Ш)
A0 2 )Ю4 метапериодат диоксоио-
да(У)
HI иодоводород
НЮ3 йодноватая кислота
НЮ4 метаиодная кислота
Н412О9 нонаоксодииодат(УИ) во-
водорода
Н5Ю6 ортоиодная кислота
In индий
InAs моноарсенид индия
InBr бромид индияA)
InBr3 бромид индия(Ш)
[1пП1Вг4],1п тетрабромоиндат(Ш)
индияA)
1пС1 хлорид индияA)
1пС13 хлорид индия(Ш)
[1пшС14],1п тетрахлороиндат(Ш)
индияA)
[InlnCl6] ,In3 гексахлороиндат(Ш)
индияA)
jn(C104K перхлорат индия(Ш)
1прз Фторид индия(Ш)
Inl иодид индияA)
Inl3 иодид индия(Ш)
[InHII4],In тетраиодоиндат(Ш) ин-
индия^)
InN нитрид индия(Ш)
In(NO3K нитрат индия(Ш)
1п2О оксид индияA)
1п2О3 оксид индия(Ш)
1п@НK гидроксид индия(Ш)
InP фосфид индия(Ш)
1пРО4 ортофосфат индия(Ш)
In2S сульфид индияA)
In2S3 сульфид индия(Ш)
[IninS2],Cu дитиоиндат(Ш) медиA)
[1пш82],1пдитиоиндат(Ш) индияA)
In2(SO4K сульфат индия(Ш)
InSb моностибид индия
In2Se3 селенид индия(Ш)
[InniSe2],In диселенидоиндат(Ш)
индияA)
1п2Те3 теллурид индия(Ш)
[1пшТе2],1п дителлуридоиндат(Ш)
индияA)
1г иридий
[IrBr6],Na3 гексабромоиридат(Ш)
натрия
[1г(С2О4K],К3 триоксалатоири-
дат(Ш) калия
[Ir2(CO)8] октакарбонилдииридий
[1г4(СОI2] додекакарбонилтетра-
иридий
1гС13 хлорид иридия(Ш)
1гС14 хлорид иридия(ГУ)
[1гС16],Н2 гексахлороиридатAУ)
водорода
[1гС16],К2 гексахлороиридат(ГУ)
калия
[1гС16],К3 гексахлороиридат(Ш)
калия
[1гС16],К4 гексахлороиридат(П) ка-
калия
[IrCl6],(NH4J гексахлороири-
датAУ) аммония
41
I. Неорганические вещества
[IrCl6],Na2 гексахлороиридатAУ)
натрия
[IrCl6],Na3 гексахлороиридат(Ш)
натрия
IrF3 фторид иридия(Ш)
IrF4 фторид иридияAУ)
IrF5 фторид иридия(У)
IrF6 фторид иридия(У1)
[Ir2(NH3I0] декаамминдииридий
[Ir(NH3N]Cl3 хлорид гексаамми-
ниридия(Ш)
[Ir(NH3MCl]Cl2 хлорид хлоропен-
таамминиридия(Ш)
[Ir(NH3N](NO3K нитрат гексаам-
миниридия(Ш)
IrNH4(SO4J сульфат аммо-
ния-иридия(Ш)
1гО2 оксид иридияAУ)
1гО3 оксид иридия(У1)
1г2О3 оксид иридия(Ш)
IrS2 сульфид иридияAУ)
Ir2S3 сульфид иридия(Ш)
Ir2(SO4K сульфат иридия(Ш)
К калий
KAg(NO3J нитрат серебраA)-калия
KA1(SO4J сульфат алюминия-ка-
алюминия-калия
KA13(SO4J(OHN гексагидрок-
сид-бис(сульфат) триалюми-
ния-калия
КВО2 метаборат калия
КВ5О8 октаоксопентаборат(Ш) ка-
калия
К2В4О7 тетраборат калия
KBi2 дивисмутид калия
K3Bi висмутид трикалия
K3Bi2 дивисмутид трикалия
КВг бромид калия
КВгО3 бромат калия-
КВгО4 пербромат калия
К(СН3СОО) ацетат калия
К2(С4Н4О6) тартрат калия
KCN цианид калия
К2СО3 карбонат калия
К2С2О4 оксалат калия
К2С2О4(О2) пероксотетраоксоди-
карбонатAУ) калия
K2Ca(SO4J сульфат кальция-дика-
лия
K2Cd(SO4J сульфат кадмия(П)-
дикалия
КС1 хлорид калия
КС1О2 хлорит калия
КС1О3 хлорат калия
КС1О4 перхлорат калия
K2Co(SO4J сульфат кобаль-
та(П)-дикалия
К2Сг04 хромат калия
К2Сг207 дихромат калия
К2Сг3О10 декаоксотрихромат(У1)
калия
К2Сг401313-оксотетрахромат(У1)
калия
К(СгО3С1) хлорохромат калия
KCr(SO4J сульфат хрома(Ш)-калия
KD2PO4 дидейтериоортофосфат
калия
KF фторид калия
K2Fe04 феррат калия
KFe(SO4J сульфат железа(Ш)-ка-
лия
K2Fe(SO4J сульфат железа(П)-ди-
калия
K2Ge03 германат калия
КН гидрид калия
KH2As04 дигидроарсенат калия
K2HAs04 гидроарсенат калия
КНС4Н4О6 гидротартрат калия
КНСО3 гидрокарбонат калия
КНС2О4 гидрооксалат калия
К(НСОО) формиат калия
КНСО2(О2) гидропероксокарбо-
нат калия
K(HF2) гидродифторид калия
КН(РНО3) гидрофосфонат калия
КН2РО4 дигидроортофосфат калия
К2НРО4 гидроортофосфат калия
42
I. Неорганические вещества
KHS гидросульфид калия
KHSO3 гидросульфит калия
KHSO4 гидросульфат калия
KHSO3(O2) гидропероксосульфат
калия
К2Н4Те06 тетрагидроортотеллурат
калия
KHg ртутькалий
KHg2 диртутькалий
KI иодид калия
КЮ3 иодат калия
КЮ4 метапериодат калия
KMgCl3 хлорид магния-калия
K2Mg(SO4J сульфат магния-дика-
лия
KMg(SO4)Cl хлорид-сульфат маг-
магния-калия
K2Mg(Se04J селенат магния-ди-
калия
КМпО4 перманганат калия
К2Мп04 манганат калия
К2МоО4 молибдат калия
KN3 азид калия
KNCS тиоцианат калия
KNCSe селеноцианат калия
KNH2 амид калия
KNO2 нитрит калия
KNO3 нитрат калия
KNa2 динатрийкалий
KNa(C4H4O6) тартрат натрия-калия
KNaCO3 карбонат натрия-калия
K2Ni(SO4J сульфат никеля(П)-ди-
калия
КО2 надпероксид калия
КО3 озонид калия
К2О оксид калия
К2О2 пероксид калия
KOCN цианат калия
КОН гидроксид калия
К3Р фосфид калия
К(РН2О2) фосфинат калия
К2(РНО3) фосфонат калия
КРО3 метафосфат калия
кзРО4 ортофосфат калия
К4Р2О7 дифосфат калия
К5Р3О10 декаоксотрифосфат(У) ка-
калия
K2(PO3F) фтороортофосфат калия
КРЬ свинецкалий
KReO4 перренат калия
KRh(SO4J сульфат родия(Ш)-калия
KRuO4 тетраоксорутенат(У11) калия
K2Ru04 тетраоксорутенат(У1) калия
K2S сульфид калия
K2(S2) дисульфидB-) калия
K2(S3) трисульфидB-) калия
K2(S4) тетрасульфидB-) калия
K2(S5) пентасульфидB-) калия
K2(S6) гексасульфидB-) калия
K2SO3 сульфит калия
K2SO4 сульфат калия
K2S2O5 пентаоксодисульфат(ГУ)
калия
K2S2O6 дитионат калия
K2S2O7 дисульфат калия
K2S3O6 тритионат калия
K2S4O6 тетратионат калия
K2S5O6 пентатионат калия
K2S6O6 гексатионат калия
K(SO2F) фторосульфит калия
K(SO3F) фторосульфонат калия
K2S2O6(O2) пероксодисульфат ка-
калия
K2(SO3S) тиосульфат калия
KSb моностибид калия
K3Sb стибид трикалия
K2Se селенид калия
K2Se04 селенат калия
K2Si03 метасиликат калия
K2Si205 пентаоксодисиликатAУ)
калия
K2Si409 нонаоксотетрасили-
катAУ) калия
К2Те теллурид калия
К2Те03 теллурит калия
(K2Ti)O3 оксид титанаAУ)-дикалия
K2UO2(SO4J сульфат уранила-ди-
калия
43
I. Неорганические вещества
KVO3 метаванадат калия
K3VO4 ортованадат калия
K4V2O7 гептаоксодиванадат(У) ка-
калия
KV(SO4J сульфат ванадияA II)-ка-
II)-калия
K2WO4 вольфрамат калия
Кг криптон
KrF2 дифторид криптона
La лантан
(LaAl)O3 оксид алюминия-ланта-
на(Ш)
LaB6 гексаборид лантана
LaBr3 бромид лантана(Ш)
LaC2 дикарбид лантана
La2(C2O4K оксалат лантана(Ш)
LaCl3 хлорид лантана(Ш)
(LaCrm)O3 оксид хрома(Ш)-лан-
тана(Ш)
LaF3 фторид лантана(Ш)
LaH3 гидрид лантана(Ш)
Lal3 иодид лантана(Ш)
La2(MoO4K молибдат лантана(Ш)
La(NO3K нитрат лантанаA II)
La2O3 оксид лантана(Ш)
La(OHK гидроксид лантана(Ш)
LaS моносульфид лантана
La2S3 сульфид лантана(Ш)
La2(SO4K сульфат лантана(III)
La2(Se04K селенат лантана(Ш)
LaSi2 дисилицид лантана
Li литий
LiA102 диоксоалюминат(Ш) лития
Li3As04 арсенат лития
LiBO2 метаборат лития
Li2B4O7 тетраборат лития
LiBr бромид лития
Li2C2 ацетиленид лития
Li(CH3COO) ацетат лития
Li2CO3 карбонат лития
Li2C2O4 оксалат лития
LiCl хлорид лития
LiCIO гипохлорит лития
LiC102 хлорит лития
LiC103 хлорат лития
ЫС104 перхлорат лития
Li2Cr04 хромат лития
Ы2Сг207 дихромат лития
LiD дейтерид лития
LiF фторид лития
Li2Ge03 германат лития
LiH гидрид лития
Li(HCOO) формиат лития
Li(HF2) гидродифторид лития
LiH2PO4 дигидроортофосфат лития
LiHSO4 гидросульфат лития
LiHg ртутьлитий
Lil иодид лития
LiMnO4 перманганат лития
Li2MoO4 молибдат лития
LiN3 азид лития
Li3N нитрид лития
LiNH2 амид лития
Li2NH имид лития
LiNO2 нитрит лития
LiNO3 нитрат лития
(LiNb)O3 оксид ниобия(У)-лития
Li2O оксид лития
Li2O2 пероксид лития
LiOH гидроксид лития
Li3PO4 ортофосфат лития
Li2S сульфид лития
Li2SO3 сульфит лития
Li2SO4 сульфат лития
Li(SO3F) фторосульфонат лития
Li3Sb стибид лития
Li2Si03 метасиликат лития
Li2Si205 пентаоксодисиликатAУ)
лития
Li4Si04 ортосиликат лития
(LiTa)O3 оксид тантала(У) -лития
Li2WO4 вольфрамат лития
Lr лоуренсий
Lu лютеций
LuBr3 бромид лютеция(Ш)
44
I. Неорганические вещества
Lu2(C2O4K оксалат лютеция(Ш)
LuCl3 хлорид лютеция(Ш)
LuF3 фторид лютеция(Ш)
Lul3 иодид лютеция(Ш)
Lu2O3 оксид лютеция(Ш)
Lu(OHK гидроксид лютеция(Ш)
Lu2(SO4K сульфат лютеция(Ш)
Md менделевий
Mg магний
(MgAl2)O4 оксид диалюми-
ния-магния
Mg3As2 арсенид магния
(MgAs2)O6 оксид димышья-
ка(У)-магния
Mg3(As04J арсенат магния
MgB2 диборид магния
Mg(BO2J метаборат магния
Mg3(BO3J ортоборат магния
Mg3Bi2 висмутид магния
MgBr2 бромид магния
Mg(BrO3J бромат магния
MgC2 ацетиленид магния
Mg2C3 трикарбид димагния
[Mg(C5H5J] бис(циклопентади-
енил)магний
Mg(CH3COOJ ацетат магния
MgCN2 цианамид магния
MgCO3 карбонат магния
MgC2O4 оксалат магния
MgCl2 хлорид магния
Mg(C103J хлорат магния
Mg(C104J перхлорат магния
MgCrO4 хромат магния
(MgCr2)O4 оксид дихро-
ма(Ш)-магния
MgF2 фторид магния
(MgFe2)O4 оксид дижеле-
за(Ш)-магния
MgH2 гидрид магния
MgHAsO4 гидроарсенат магния
MgHPO4 гидроортофосфат магния
Mgl2 иодид магния
Mg(IO3J иодат магния
MgMoO4 молибдат магния
Mg3N2 нитрид магния
MgNH4As04 арсенат аммо-
аммония-магния
MgNH4PO4 ортофосфат аммо-
аммония-магния
Mg(NH4J(SO4J сульфат диаммо-
ния-магния
Mg(NO3J нитрат магния
MgO оксид магния
MgO2 пероксид магния
Mg(OHJ гидроксид магния
Mg3P2 фосфид магния
Mg(PH2O2J фосфинат магния
Mg2P2O7 дифосфат магния
Mg3(PO4J ортофосфат магния
MgS сульфид магния
MgSO3 сульфит магния
MgSO4 сульфат магния
Mg(SO3S) тиосульфат магния
Mg3Sb2 стибид магния
Mg2Si силицид димагния
Mg2Si04 ортосиликат магния
(MgTi)O3 оксид титана(ГУ)-магния
(Mg2Ti)O4 оксид титанаAУ)-ДИ-
магния
Mg(VO3J метаванадат магния
MgWO4 вольфрамат магния
Мп марганец
(МпА12)О4 оксид диалюми-
ния-марганца(И)
MnAs моноарсенид марганца
МпВ2 диборид марганца
МпВг2 бромид марганца(Н)
Мп3С карбид тримарганца
[Мп(С5Н5J] бис(циклопентади-
енил)марганец
МпСО3 карбонат марганца(И)
[Мп2(СОI0] декакарбонилдимар-
ганец
[Мп(СОMВг] бромопентакарбо-
нилмарганец
45
I. Неорганические вещества
[Мп(СОKС5Н5] (циклопентади-
енил)трикарбонилмарганец
[Мп(СОMС1] хлоропентакарбо-
нилмарганец
[Мп(СОM1] иодопентакарбонил-
марганец
[Mn(COLNO] нитрозилтетракар-
бонилмарганец
МпС12 хлорид марганца(П)
(Мп2пСи)О4 оксид меди(П)-ди-
марганца(Ш)
MnF2 фторид марганца(П)
MnF3 фторид марганца(Ш)
MnF4 фторид марганца(ГУ)
(MnnFe2)O4 оксид дижеле-
за(Ш)-марганца(П)
[МпН(СОM] пентакарбонилгидро-
марганец
Mnl2 иодид марганца(Н)
(МппМп 2И)О4 оксид димарган-
ца(Ш)-марганца(Н)
Mn(NH4J(SO4J сульфат диаммо-
ния-марганца(Н)
Mn(NO3J нитрат марганца(И)
МпО оксид марганца(Н)
МпО2 оксид марганцаAУ)
Мп2О3 оксид марганца(Ш)
Мп2О7 оксид марганца(УИ)
MnO3F фторид-триоксид марган-
марганца
Мп(ОНJ гидроксид марганца(П)
МпО(ОН) метагидроксид марган-
марганца
МпР монофосфид марганца
Мп2Р фосфид димарганца
Мп3Р фосфид тримарганца
Мп3Р2 дифосфид тримарганца
Мп4Р фосфид тетрамарганца
Мп2Р2О7 дифосфат марганца(И)
Мп3(РО4J ортофосфат марган-
ца(И)
MnS сульфид марганца(Н)
Mn(S2) дисульфидB-) марган-
ца(Н)
MnSO4 сульфат марганца(П)
Mn2(SO4K сульфат марганца(Ш)
MnSe селенид марганца(П)
MnSi моносилицид марганца
Mn2Si силицид димарганца
Mn3Si силицид тримарганца
Mn5Si3 трисилицид пентамарганца
MnSiO3 метасиликат марганца(И)
Mn2Si04 ортосиликат марганца(П)
MnWO4 вольфрамат марганца(И)
(Mn2nZn)O4 оксид цинка(Н)-ди-
марганца(Ш)
НМпО4 марганцовая кислота
Мо молибден
МоВ моноборид молибдена
Мо2В борид димолибдена
Мо2В5 пентаборид димолибдена
МоВг2 бромид молибдена(П)
МоВг3 бромид молибдена(Ш)
МоВг4 бромид молибдена(ГУ)
МоВг2О2 диоксид-дибромид мо-
молибдена
МоВг3О оксид-трибромид молиб-
молибдена
МоС монокарбид молибдена
Мо2С карбид димолибдена
[Mo(CN)8],K4 октацианомолиб-
дат(ГУ) калия
[Мо(СОN] гексакарбонилмолиб-
ден
[Мо2(СОL(С5Н5J] бис(циклопен-
тадиенил)тетракарбонилдимо-
либден
МоС12 хлорид молибдена(П)
МоС13 хлорид молибдена(Ш)
МоС14 хлорид молибдена(ГУ)
МоС15 хлорид молибдена(У)
MoCl3N нитрид-трихлорид молиб-
молибдена
МоС12О2 диоксид-дихлорид мо-
молибдена
МоС13О оксид-трихлорид молиб-
молибдена
46
I. Неорганические вещества
МоС14О оксид-тетрахлорид мо-
молибдена
MoF3 фторид молибдена(Ш)
MoF5 фторид молибдена(У)
MoF6 фторид молибдена(У1)
[MoF6],K3 гексафторомолиб-
дат(Ш) калия
Мо12 иодид молибдена(Н)
Мо13 иодид молибдена(Ш)
Мо14 иодид молибденаAУ)
Mo2N нитрид димолибдена
МоО2 оксид молибденаAУ)
МоО3 оксид молибдена(У1)
Мо4О! (ундекаоксид тетрамолиб-.
дена
Mo(O)F4 тетрафторид-оксид мо-
молибдена
MoO2F2 дифторид-диоксид мо-
молибдена
МоО(ОНJ дигидроксид-оксид
молибдена
МоО(ОНK тригидроксид-оксид
молибдена
[Mo(PF3N] гексакис(трифторо-
фосфор)молибден
MoS2 сульфид молибденаAУ)
MoS3 сульфид молибдена(УГ)
Mo2S3 сульфид молибдена(Ш)
MoSe2 селенид молибденаAУ)
MoSi2 дисилицид молибдена
N2 диазот
N(C1)F2 дифторид-хлорид азота
ND3 тридейтериоаммиак
ND4C1 хлорид тетрадейтериоам-
мония
NF3 трифторид азота
N2F2 дифторид диазота
N2F4 тетрафторид диазота
N3F фторид триазота
NH3 аммиак
NH гидразин
JB4°7 тетраборат аммония
4Вг бромид аммония
NH4(CH3COO) ацетат аммония
N2H5(CH3COO) ацетат гидрази-
нияA+)
NH4CN цианид аммония
(NH4JCO3 карбонат аммония
(NH4JC2O4 оксалат аммония
NH2C1 хлорамин
NH4C1 хлорид аммония
N2H5C1 хлорид гидразинияA+)
N2H6C12 хдорид гидразинияB+)
NH4C1O3 хлорат аммония
NH4C1O4 перхлорат аммония
N2H5C1O4 перхлорат гидрази-
нияA+)
(NH4JCr04 хромат аммония
(NH4JCr207 дихромат аммония
(NH)F2 дифторамин
NH4F фторид аммония
NH4(H2As04) дигидроарсенат ам-
аммония
NH4HCO3 гидрокарбонат аммония
1ч[Н4НС2О4тидрооксалат аммония
NH4(HCOO) формиат аммония
NH4(HF2) гидродифторид аммо-
аммония
NH4H(PHO3) гидрофосфонат ам-
аммония
NH4(H2PO4) дигидроортофосфат
аммония
(NH4JHPO4 гидроортофосфат ам-
аммония
NH4HS гидросульфид аммония
NH4HSO3 гидросульфит аммония
NH4HSO4 гидросульфат аммония
(NH4I0H2W12O42 42-оксододека-
вольфрамат(У1) диводоро-
да-декааммония
NH4I иодид аммония
NH4IO3 иодат аммония
NH4IO4 метапериодат аммония
NH4Mn04 перманганат аммония
(NH4NMo7O24 24-оксогептамолиб-
дат(У1) аммония
NH4N3 азид аммония
47
I. Неорганические вещества
N2H5N3 азид гидразинияA+)
NH4NCS тиоцианат аммония
NH4(NH2COO) карбамат аммония
NH4NO2 нитрит аммония
NH4NO3 нитрат аммония
N2H5NO3 нитрат гидразинияA+)
N2H6(NO3J нитрат гидразинияB+)
NH4OCN цианат аммония
NH2OH гидроксиламин
(NH3OH)C1 хлорид гидроксилами-
ния
(NH3OH)C1O4 перхлорат гидро-
ксиламиния
(NH3OH)HSO4 гидросульфат гид-
роксиламиния
(NH3OH)NO3 нитрат гидроксила-
миния
(NH3OHJSO4 сульфат гидрокси-
ламиния
NH4(PH2O2) фосфинат аммония
NH4Re04 перренат аммония
N2H6SO4 сульфат гидразинияB+)
(NH4JSO3 сульфит аммония
(NH4JSO4 сульфат аммония
(N2H5JSO4 сульфат гидразинияA+)
NH4(SO3F) фторосульфонат аммо-
аммония
(NH4JS2O6(O2) пероксодисульфат
аммония
(NH4J(SO3S) тиосульфат аммония
(NH4JSe04 селенат аммония
NH4Tc04 пертехнетат аммония
(NH4JTeO4 метателлурат аммония
(NH4JU2O7 гептаоксодиура-
нат(У1) аммония
NH4VO3 метаванадат аммония
(NH4KVS4 тетратиоортованадат
аммония
N0 монооксид азота
N02 диоксид азота
N20 оксид диазота
N2O3 триоксид диазота
N2O5 пентаоксид диазота
(NO)Br бромид нитрозила
(NO)C1 хлорид нитрозила
(NO2)C1 хлорид нитроила
(N0)C104 перхлорат нитрозила
(N02)C10 гипохлорит нитроила
(NO2)C1O4 перхлорат нитроила
(NO)F фторид нитрозила
N(O)F3 трифторид-оксид азота
(NO2)F фторид нитроила
(NO)HSO4 гидросульфат нитрозила
(NO2)NH2 амид нитроила
(NO2)OF фторооксигенат(О) нит-
нитроила
(NOJS2O7 дисульфат нитрозила
(NO2JS2O7 дисульфат нитроила
NO2(SO3F) фторосульфонат нит-
нитроила
HN3 азидоводород
HNCO цианат-N водорода
HNCS тиоцианат водорода
HNO3 азотная кислота
H2N2O2 азотноватистая кислота
Na натрий
NaA102 диоксоалюминат(Ш) натрия
NaAl(SO4J сульфат алюми-
алюминия-натрия
NaAsO2 метаарсенит натрия
NaAsO3 триоксоарсенат(У) натрия
Na3As04 арсенат натрия
Na4As207 гептаоксодиарсенат(У)
натрия
Na3AsS4 тетратиоарсенат натрия
NaBO2 метаборат натрия
NaB3O5 пентаоксотриборат(Ш)
натрия
NaB5O8 октаоксопентаборат(Ш)
натрия
Na2B4O7 тетраборат натрия
Na2B8Oi3 13-оксооктаборат(Ш)
натрия
NaBr бромид натрия
NaBrO2 бромит натрия
NaBrO3 бромат натрия
Na2C2 ацетиленид натрия
48
I. Неорганические вещества
Na(CH3COO) ацетат натрия
NaCN цианид натрия
Na2CO3 карбонат натрия
Na2C2O4 оксалат натрия
Na2Ca(CO3J карбонат каль-
ция-динатрия
Na2Ca(SO4J сульфат кальция-ди-
натрия
NaCl хлорид натрия
NaCIO гипохлорит натрия
NaC102 хлорит натрия
NaC103 хлорат натрия
NaC104 перхлорат натрия
NaCrO2 диоксохромат(Ш) натрия
Na2Cr04 хромат натрия
Na2Cr207 дихромат натрия
NaCrS2 дитиохромат(Ш) натрия
NaF фторид натрия
NaFeO2 диоксоферрат(Ш) натрия
Na2Ge03 германат натрия
NaH гидрид натрия
NaH2As04 дигидроарсенат натрия
Na2HAs04 гидроарсенат натрия
Na2H2As207 гептаоксодиарсе-
нат(У) диводорода-динатрия
NaHCO3 гидрокарбонат натрия
Na3(HCO3)CO3 карбонат-гидро-
карбонат-гидрокарбонат натрия
Na(HCOO) формиат натрия
Na(HF2) гидродифторид натрия
Na2H2Ge04 тетраоксогерма-
нат(ГУ) диводорода-динатрия
NaH4IO6 тетрагидроортопериодат
натрия
Na3H2IO6 дигидроортопериодат
натрия
NaH(PHO3) гидрофосфонат натрия
NaH2PO4 дигидроортофосфат нат-
натрия
Na2HPO4 гидроортофосфат натрия
Na2H2P^vo6 гексаоксодифос-
фатAУ) диводорода-динатрия
Na2H2P2O7 дигидродифосфат нат-
натрия
NaHS гидросульфид натрия
NaHSO3 гидросульфит натрия
NaHSO4 гидросульфат натрия
NaHSeO3 гидроселенит натрия
Na2H4Te06 тетрагидроортотеллу-
рат натрия
NaHg ртутьнатрий
NaHg2 диртутьнатрий
NaHg4 тетрартутьнатрий
Na3Hg ртутьтринатрий
Na3Hg2 диртутьтринатрий
Na5Hg2 диртутьпентанатрий
Na7Hg8 октартутьгептанатрий
Nal иодид натрия
NaIO3 иодат натрия
NaIO4 метапериодат натрия
Na5IO6 ортопериодат натрия
Na2Mg(CO3J карбонат магния-ди-
натрия
Na2Mg(SO4J сульфат магния-ди-
натрия
NaMnO4 перманганат натрия
Na2Mn04 манганат натрия
Na3Mn04 тетраоксоманганат(У)
натрия
Na2MoO4 молибдат натрия
NaN3 азид натрия
Na3N нитрид натрия
NaNCS тиоцианат натрия
NaNH2 амид натрия
[Na(NH3L]I иодид тетрааммин-
натрияA)
NaNH4HPO4 гидроортофосфат ам-
аммония-натрия
NaNO2 нитрит натрия
NaNO3 нитрат натрия
Na2N2O2 гипонитрит натрия
Na4N2O4 тетраоксодинитрат(П)
натрия
(NaNb)O3 триоксид ниобия-нат-
ниобия-натрия
NaO2 надпероксид натрия
Na2O оксид натрия
Na2O2 пероксид натрия
49
I. Неорганические вещества
NaOCN цианат натрия
NaOH гидроксид натрия
Na(PH2O2) фосфинат натрия
Na2(PHO3) фосфонат натрия
NaPO3 метафосфат натрия
Na3PO4 ортофосфат натрия
Na4P2vO6 гексаоксодифосфатAУ)
натрия
Na4P2O7 дифосфат натрия
Na5P3O10 декаоксотрифосфат(У)
натрия
Na2(PO3F) фтороортофосфат нат-
натрия
NaReO4 перренат натрия
Na2S сульфид натрия
Na2(S2) дисульфидB-) натрия
Na2(S4) тетрасульфидB-) натрия
Na2(S5) пентасульфидB-) натрия
Na2SO3 сульфит натрия
Na2SO4 сульфат натрия
Na2S2O4 тетраоксодисульфат(Ш)
натрия
Na2S2O5 пентаоксодисульфатAУ)
натрия
Na2S2O6 дитионат натрия
Na2S2O7 дисульфат натрия
Na2S2O6(O2) пероксодисульфат
натрия
Na2(SO3S) тиосульфат натрия
Na3Sb стибид натрия
NaSbO2 диоксостибат(Ш) натрия
Na2Se селенид натрия
Na2Se03 селенит натрия
Na2Se04 селенат натрия
Na2Si03 метасиликат натрия
Na2Si205 пентаоксодисиликатAУ)
натрия
Na2Si307 гептаоксотрисиликатAУ)
натрия
Na4Si04 ортосиликат натрия
Na6Si207 дисиликат натрия
(NaTa)O3 триоксид тантала-натрия
Na2Te теллурид натрия
(Na2Ti)O3 триоксид титана-динат-
рия
NaVO3 метаванадат натрия
Na3VO4 ортованадат натрия
Na4V2O7 гептаоксодиванадат(У)
натрия
Na2WO4 вольфрамат натрия
Na6W7O24 24-оксогептавольфра-
мат(У1) натрия
Na4Xe06 гексаоксоксенонат(УШ)
натрия
(Na2Zr)O3 триоксид циркония-ди-
натрия
Nb ниобий
Nb3Al алюминийтриниобий
NbB2 диборид ниобия
NbBr4 бромид ниобия(ГУ)
NbBr5 бромид ниобия(У)
Nb3Br8 октабромид триниобия
NbBr3O оксид-трибромид ниобия
NbC монокарбид ниобия
Nb2C карбид диниобия
[Nb(C5H5)Cl3] трихлоро(цикло-
пентадиенил)ниобий
[Nb(C5H5JCl2] дихлоробис(цикло-
пентадиенил)ниобий
[Nb(COLC5H5] (циклопентади-
енил)тетракарбонилниобий
NbCl4 хлорид ниобияAУ)
NbCl5 хлорид ниобия(У)
Nb3Cl8 октахлорид триниобия
[Nb6Cl12]Cl2 дихлорид додекахло-
рогексаниобия
NbCl3O оксид-трихлорид ниобия
NbF5 фторид ниобия(V)
[NbF7],K2 гептафторониобат(У)
калия
Nb3Ga галлийтриниобий
Nb3Ge германийтриниобий
NbH моногидрид ниобия
NbH2 дигидрид ниобия
Nbl4 иодид ниобияAУ)
Nbl5 иодид ниобия(У)
Nb3I8 октаиодид триниобия
Nb6Iu ундекаиодид гексаниобия
NbI2O оксид-дииодид ниобия
50
I. Неорганические вещества
NbI3O оксид-трииодид ниобия
jsjbN мононитрид ниобия
Nb2N нитрид диниобия
NbO оксид ниобия(П)
NbO2 оксид ниобияAУ)
Nb2O5 оксид ниобия(У)
[Nb(O)F6],(NH4K гексафторооксо-
ниобат(У) аммония
NbS2 сульфид ниобияAУ)
Nb2(SO4)O4 тетраоксид-сульфат
диниобия
Nb2(SO4JO3 триоксид-бис(суль-
фат) диниобия
NbSi2 дисилицид ниобия
NbSi4 тетрасилицид ниобия
Nb3Si силицид триниобия
Nb5Si3 трисилицид пентаниобия
Nb3Sn оловотриниобий
Nd неодим
NdB6 гексаборид неодима
NdBr3 бромид неодима(Ш)
Nd(BrO3K бромат неодима(Ш)
NdC2 дикарбид неодима
Nd2(C2O4K оксалат неодима(Ш)
NdCl3 хлорид неодима(Ш)
Nd(C104K перхлорат неодима(Ш)
NdF3 фторид неодима(Ш)
Ndl3 иодид неодима(Ш)
Nd2(MoO4K молибдат неодима(Ш)
Nd2O3 оксид неодима(Ш)
Nd(OHK гидроксид неодима(Ш)
Nd2S3 сульфид неодима(Ш)
Nd2(S)O2 диоксид-сульфид неодима
Nd2(SO4K сульфат неодима(Ш)
Ne неон
Ni никель
(NiAl2)O4 оксид диалюминия-ни-
келя(Н)
NiAs моноарсенид никеля
NiAs2 диарсенид никеля
Nl3(As04J арсенат никеля(И)
Ni(As)S сульфид-арсенид никеля
Ni2B борид диникеля
NiBr2 бромид никеля(П)
Ni3C карбид триникеля
[Ni(C5H5J] бис(циклопентади-
енил)никель
Ni(CH3COOJ ацетат никеля(И)
[Ni(C4H7O2N2J] бис(диметилгли-
оксимато)никель
Ni(CNJ цианид никеля(П)
[Ni(CNL],K2 тетрацианоникко-
лат(П) калия
NiCO3 карбонат никеля(П)
[Ni(COL] тетракарбонилникель
[Ni2(COJ(C5H5J] бис(циклопен-
тадиенил)дикарбонилдиникель
NiCl2 хлорид никеля(П)
Ni(C104J перхлорат никеля(И)
NiF2 фторид никеля(П)
[NiF6],K2 гексафтороникколатAУ)
калия
[NiF6],K3 гексафтороникко-
лат(Ш) калия
Ni(HCO3J гидрокарбонат нике-
ля(П)
Ni(HCOOJ формиат никеля(П)
Nil2 иодид никеля(И)
Ni(IO3J иодат никеля(П)
Ni3N нитрид триникеля
Ni3N2 динитрид триникеля
Ni(NH2J амид никеля(Н)
[Ni(NH3N]Br2 бромид гексаам-
минникеля(Н)
[Ni(NH3N]Cl2 хлорид гексааммин-
никеля(Н)
[Ni(NH3N]I2 иодид гексаамминни-
келя(П)
Ni(NH4J(SO4J сульфат диаммо-
ния-никеля(П)
Ni(NO3J нитрат никеля(Н)
NiO оксид никеля(П)
Ni2O3 оксид никеля(Ш)
Ni(OHJ гидроксид никеля(Н)
NiO(OH) метагидроксид никеля
51
I. Неорганические вещества
Ni2P фосфид диникеля
Ni3P фосфид триникеля
Ni5P2 дифосфид пентаникеля
[Ni(PF3L] тетракис(трифторофос-
фор)никель
Ni2P2O7 дифосфат никеля(П)
Ni3(PO4J ортофосфат никеля(Н)
NiS сульфид никеля(П)
Ni(S2) дисульфидB-) никеля(Н)
Ni3S2 дисульфид триникеля
Ni3S4 тетрасульфид триникеля
NiSO4 сульфат никеля(Н)
NiS2O6 дитионат никеля(И)
NiSb моностибид никеля
Ni(Sb)S сульфид-стибид никеля
NiSe селенид никеля(И)
Ni(Se2) диселенид B—) никеля(Н)
NiSeO4 селенат никеля(И)
NiSi моносилицид никеля
NiSi2 дисилицид никеля
Ni2Si силицид диникеля
Ni2Si04 ортосиликат никеля(Н)
Ni(Te2) дителлуридB-) никеля(И)
No нобелий
Np нептуний
NpBr3 бромид нептуния(Ш)
NpBr4 бромид нептуния(ГУ)
Np(C2O4J оксалат нептунияAУ)
NpCl3 хлорид нептуния(Ш)
NpCl4 хлорид нептунияAУ)
NpF3 фторид нептуния(Ш)
NpF4 фторид нептуния(ГУ)
NpF5 фторид нептуния(V)
NpF6 фторид нептуния(У1)
Npl3 иодид нептуния(Ш)
(Np^ Npvl)O8 оксид непту-
нептуния (У1)-динептуния(У)
NpO2 оксид нептуния(ГУ)
Np2O5 оксид нептуния(V)
Np(O)F4 тетрафторид-оксид неп-
нептуния
Np(OHK гидроксид нептуния(Ш)
Np(OHL гидроксид нептунияAУ)
NpO2(OH) гидроксид-диоксид
нептуния
NpO2(OHJ дигидроксид-диоксид
нептуния
NpO3(OH) гидроксид-триоксид
нептуния
02 дикислород
03 озон
OF2 дифторид кислорода
O2F2 дифторид дикислорода
O3F2 дифторид трикислорода
O4F2 дифторид тетракислорода
O5F2 дифторид пентакислорода
Н2О2 пероксид водорода
HOF фторооксигенат(О) водорода
Os осмий
[Os(C5H5J] бис(циклопентади-
енил) осмий
[Os(COM] пентакарбонилосмий
[Os2(CO)9] нонакарбонилдиосмий
[Os3(COI2] додекакарбонилтриос-
мий
[Os(COKCl2] дихлоротрикарбони-
лосмий
[Os(COLCl2] дихлоротетракарбо-
нилосмий
OsCl3 хлорид осмия(Ш)
OsCl4 хлорид осмия(ГУ)
[OsCl6],K2 гексахлороосматAУ) ка-
калия
[OsCl6],K3 гексахлороосмат(Ш)
калия
[OsCl6],(NH4J гексахлороос-
мат(ГУ) аммония
[OsCl4O2],K2 диоксотетрахлороос-
мат(У1) калия
OsF4 фторид осмияAУ)
OsF5 фторид осмия(У)
OsF6 фторид осмия(VI)
[OsH2(COL] тетракарбонилдигид-
роосмий
52
I. Неорганические вещества
[Os(N)O3],K триоксонитридоос-
мат(УШ) калия
OsO2 оксид осмияAУ)
OsO4 ОКСИД ОСМИЯ(УШ)
Os(O)F5 пентафторид-оксид осмия
OsO3F2 дифторид-триоксид осмия
Os(OHL гидроксид осмияAУ)
[OsO2(OHL],K2 тетрагидроксоди-
оксоосмат(У1) калия
Os(S2) дисульфидB-) осмия(Н)
Р фосфор
Р4 тетрафосфор
РВг3 трибромид фосфора
РВг5 пентабромид фосфора
Р(Вг)С12О оксид-дихлорид-бро-
мид фосфора
РВг2(С1)О оксид-хлорид-дибро-
мид фосфора
P(Br)Cl(O)F фторид-оксид-хло-
фторид-оксид-хлорид-бромид фосфора
P(Br)F2 дифторид-бромид фосфора
PBr2F фторид-дибромид фосфора
PBr2F3 трифторид-дибромид фос-
фосфора
(PBr4)F фторид тетрабромофосфо-
pa(V)
(PBr2)N нитрид дибромофосфо-
pa(V)
РВг3О оксид-трибромид фосфора
PBr(O)F2 дифторид-оксид-бро-
мид фосфора
PBr2(O)F фторид-оксид-дибро-
мид фосфора
P(CNK трицианид фосфора
РС13 трихлорид фосфора
РС15 пентафторид фосфора
°2С14 тетрахлорид дифосфора
P(C1)F2 дифторид-хлорид фосфора
P(C1)F4 тетрафторид-хлорид фос-
фосфора
PC12F фторид-дихлорид фосфора
pCl2F3 трифторид-дихлорид фос-
фосфора
PC14F фторид-тетрахлорид фосфо-
фосфора
(PC14)F фторид тетрахлорофосфо-
pa(V)
(PC12K(NK тринитрид трис(дихло-
рофосфора)
(PC12L(NL тетранитрид тетра-
кис(дихлорофосфора)
РС13О оксид-трихлорид фосфора
Р2С14О3 триоксид-тетрахлорид ди-
дифосфора
PC1(O)F2 дифторид-оксид-хлорид
фосфора
PC12(O)F фторид-оксид-дихлорид
фосфора
[РС12О2],Н диоксодихлорофос-
фат(У) водорода
PF3 трифторид фосфора
PF5 пентафторид фосфора
[PF6],H гексафторофосфат(У) во-
водорода
[PF6],K гексафторофосфат(У) ка-
калия
[PF6],NH4 гексафторофосфат(У)
аммония
[PF6],Na гексафторофосфат(У)
натрия
[PF6],PC14 гексафторофосфат(У)
тетрахлорофосфора(У)
РН3 фосфин
Р2Н4 дифосфан
РН4Вг бромид фосфония
РН4С1 хлорид фосфония
(PH)F2 дифторофосфин
РН41 иодид фосфония
Р13 трииодид фосфора
Р214 тетраиодид дифосфора
Р12С13 трихлорид-дииодид фосфора
Р13О оксид-трииодид фосфора
[РМо12О40],Н3 40-оксододекамо-
либдофосфат(У) водорода
PN мононитрид фосфора
P3N5 пентанитрид трифосфора
P(NH2KO оксид-триамид фосфора
53
I. Неорганические вещества
[P(NH2JO2],H диоксодиамидо-
фосфат(У) водорода
[P(NH2)O3],H2 триоксоамидофос-
фат(У) водорода
PN(NH) имид-нитрид фосфора
PN(NH2J диамид-нитрид фосфора
Р4О оксид тетрафосфора
Р4О6 гексаоксид тетрафосфора
Р4О8 октаоксид тетрафосфора
Р4О10 декаоксид тетрафосфора
P(O)F3 трифторид-оксид фосфора
P2(O)F6 гексафторид-оксид ди-
фосфора
[PO2F2],H дифтородиоксофос-
фат(У) водорода
[PO3F],H2 фторотриоксофос-
фат(У) водорода
[PO3F],K2 фторотриоксофос-
фат(У) калия
[PO3F],Na2 фторотриоксофос-
фат(У) натрия
[Р(ОНL]СЮ4 перхлорат тетрагид-
роксофосфора(У)
P4S2 дисульфид тетрафосфора
P4S3 трисульфид тетрафосфора
P4S5 пентасульфид тетрафосфора
P4S6 гексасульфид тетрафосфора
P4S7 гептасульфид тетрафосфора
P4S9 нонасульфид тетрафосфора
P4S10 декасульфид тетрафосфора
P(S)Br3 трибромид-сульфид фос-
фосфора
PS(Br)Cl2 дихлорид-бромид-суль-
фид фосфора
P(S)Br(Cl)F фторид-хлорид-бро-
фторид-хлорид-бромид-сульфид фосфора
PS(Br)F2 дифторид-бромид-суль-
фид фосфора
P(S)Br2F фторид-дибромид-суль-
фид фосфора
P(S)C13 трихлорид-сульфид фос-
фосфора
PS(C1)F2 дифторид-хлорид-суль-
фид фосфора
P(S)C12F фторид-дихлорид-суль-
фид фосфора
P(S)F3 трифторид-сульфид фос-
фосфора
P(S)I3 трииодид-сульфид фосфора
PS(NH2K триамид-сульфид фос-
фосфора
P4Se3 триселенид тетрафосфора
[PV12O36],(NH4O 36-оксододекава-
надофосфат(У) аммония
[Р\?12О40],Нз 40-оксододекавольф-
рамофосфат(У) водорода
Н(РН2О2) фосфиновая кислота
Н2(РНО3) фосфоновая кислота
Н2(Р2Н2О5) пентаоксодигидроди-
фосфат(Ш) водорода
H(PHO2F) фторофосфоновая кис-
кислота
НРО3 метафосфорная кислота
Н3РО4 ортофосфорная кислота
H4P2VO6 гексаоксодифосфатAУ)
водорода
Н4Р2О7 дифосфорная кислота
Ра протактиний
РаВг5 бромид протактиния(У)
РаС14 хлорид протактинияAУ)
РаС15 хлорид протактиния(У)
PaF4 фторид протактиния(ГУ)
PaF5 фторид протактиния(У)
Ра15 иодид протактиния(У)
Ра2О5 оксид протактиния(V)
Ра(ОНM гидроксид протактиния(У)
РЬ свинец
Pb2As207 гептаоксодиарсенат(У)
свинца(П)
Pb3(As04J арсенат свинца(И)
РЬ(ВО2J метаборат свинца(П)
РЬВг2 бромид свинца(И)
РЬ(ВгО3J бромат свинца(П)
РЬ(СН3СООJ ацетат свинца(И)
РЬ(СН3СООL ацетат свинцаAУ)
РЬСО3 карбонат свинца(П)
54
I. Неорганические вещества
PbC2O4 оксалат свинца(П)
РЬ2(СО3)С12 дихлорид-карбонат
дисвинца
РЬ3(СО3J(ОНJ дигидроксид-ди-
карбонат трисвинца
РЬС12 хлорид свинца(П)
РЬС14 хлорид свинцаAУ)
Pb(Cl)F фторид-хлорид свинца
[РЬС16],К2 гексахлороплюмбатAУ)
калия
[PbCl6],(NH4J гексахлороплюм-
батAУ) аммония
РЬ(С1О2J хлорит свинца(П)
РЬ(СЮ3J хлорат свинца(И)
РЬ(С1О4J перхлорат свинца(И)
РЬС1(ОН) гидроксид-хлорид свинца
РЬСгО4 хромат свинца(И)
PbF2 фторид свинца(И)
PbF4 фторид свинцаAУ)
PbHAsO4 гидроарсенат свинца(П)
РЬ(НСООJ формиат свинца(П)
РЬ12 иодид свинца(П)
[РЬ13],Ктрииодоплюмбат(П) калия
РЬ(Ю3J иодат свинца(Н)
РЬМоО4 молибдат свинца(П)
Pb(N3J азид свинца(И)
Pb(NCSJ тиоцианат свинца(И)
Pb(NO3J нитрат свинца(П)
Pb(NO3)OH гидроксид-нитрат
свинца
РЬО оксид свинца(П)
РЬО2 оксид свинца(ГУ)
РЬ(ОНJ гидроксид свинца(П)
[Pb(OHN],Na2 гексагидроксоп-
люмбатAУ) натрия
РЬ2Р2О7 дифосфат свинца(П)
рЬ3(РО4J ортофосфат свинца(И)
РЬ5(РО4KС1 хлорид-трис(ортофос-
фат) пентасвинца
(РЬ»РЬ^)о4 оксид евин-
ЦаAУ)-Дисвинца(Н)
pbS сульфид свинца(И)
PbSO4 сульфат свинца(П)
Pb2(SO4)O оксид-сульфат дисвинца
Pb(SO3S) тиосульфат свинца(Н)
PbSe селенид свинца(П)
PbSeO4 селенат свинца(И)
PbSiO3 метасиликат свинца(П)
РЬТе теллурид свинца(П)
Pb5(VO4KCl хлорид-трис(ортова-
надат) пентасвинца
PbWO4 вольфрамат свинца(И)
Pd палладий
PdBr2 бромид палладия(И)
Pd(CNJ цианид палладия(П)
Pd(CNL цианид палладияAУ)
[Pd(CNL],K2 тетрацианопалла-
дат(П) калия
PdCl2 хлорид палладия(П)
[PdCl4],K2 тетрахлоропалладат(П)
калия
[PdCl6],K2 гексахлоропалладатAУ)
калия
[PdCl4],(NH4J тетрахлоропалла-
дат(И) аммония
[PdCl6],(NH4J гексахлоропалла-
дат(ГУ) аммония
PdF2 фторид палладия(П)
PdF3 фторид палладия(Ш)
PdH моногидрид палладия
Pdl2 иодид палладия(П)
[Pd(NH3JCl2] дихлородиаммин-
палладий
[Pd(NH3JCl4] тетрахлородиам-
минпалладий
[Pd(NH3L]Cl2 хлорид тетрааммин-
палладия(Н)
[Pd(NH3L][PdHCl4] тетрахлоро-
палладат(П) тетраамминпалла-
дия(И)
Pd(NO3J нитрат палладия(Н)
[Pd(NO2L],K2 тетранитропалла-
дат(П) калия
PdO оксид палладия(Н)
PdO2 оксид палладияAУ)
Pd(OHJ гидроксид палладия(П)
55
I. Неорганические вещества
[Pd(OHL],Na2 тетрагидроксопал-
ладат(И) натрия
PdS сульфид палладия(Н)
Pd(S2) дисульфидB-) палладия(П)
PdSO4 сульфат палладия(П)
PdSe селенид палладия(П)
Pd(Se2) диселенидB-) палладия(Н)
PdSeO4 селенат палладия(Н)
Рт прометий
РтВг3 бромид прометия(Ш)
РтС13 хлорид прометия(Ш)
PmF3 фторид прометия(Ш)
Pml3 иодид прометия(Ш)
Рт2О3 оксид прометия(Ш)
Рш(ОНK гидроксид прометия(Ш)
Ро полоний
РоВг2 бромид полония(П)
РоВг4 бромид полония (IV)
РоС12 хлорид полония(И)
РоС14 хлорид полония(ГУ)
РоО2 оксид полония(ГУ)
РоО(ОНJ дигидроксид-оксид по-
полония
PoS сульфид полония(П)
Po(SO4J сульфат полония(ГУ)
Рг празеодим
РгВг3 бромид празеодима(Ш)
Рг(ВгО3K бромат празеодима(Ш)
РгС2 дикарбид празеодима
Рг2(С2О4K оксалат празеодима(Ш)
РгС13 хлорид празеодима(Ш)
PrF3 фторид празеодима(Ш)
PrF4 фторид празеодимаAУ)
Рг13 иодид празеодима(Ш)
Рг2(МоО4K молибдат празеоди-
ма(Ш)
Pr(NO3K нитрат празеодима(Ш)
РгО2 оксид празеодима(ГУ)
Рг2О3 оксид празеодима(Ш)
Рг(ОНK гидроксид празеодима(Ш)
PrS2 сульфид празеодимаAУ)
Pr2S3 сульфид празеодима(Ш)
Pr2(SO4K сульфат празеодима(Ш)
Pt платина
PtAs2 диарсенид платины
PtBr2 бромид платины(П)
PtBr4 бромид платины(ГУ)
[PtBr4],K2 тетрабромоплатинат(Н)
калия
[PtBr6],K2 гексабромоплати-
натAУ) калия
[PtBr6],(NH4J гексабромоплати-
натAУ) аммония
[PtBr6],Na2 гексабромоплати-
натAУ) натрия
[PtBr6],Ptn гексабромоплати-
натAУ) платины(П)
[Pt2(C2H4JCl4] тетрахлородиэти-
лендиплатина
[Pt(C2H4)Cl3],K трихлоро(этилен)
платинат(П) калия
[Pt(CNL],Ba тетрацианоплати-
нат(И) бария
[Pt(CNL],H2 тетрацианоплати-
нат(И) водорода
[Pt(CNL],K2 тетрацианоплати-
нат(И) калия
[Pt(CNN],K2 гексацианоплати-
натAУ) калия
[Pt(CNL],Mg тетрацианоплати-
нат(П) магния
[Pt(CNL],(NH4J тетрацианопла-
тинат(Н) аммония
[Pt(CNL],Na2 тетрацианоплати-
нат(И) натрия
[Pt2(COJBr4] тетрабромодикарбо-
нилдиплатина
[Pt(COJCl2] дихлородикарбо-
нил платина
[Pt2(COJCl4] тетрахлородикарбо-
нилдиплатина
[Pt2(COKCl4] тетрахлоротрикарбо-
нилдиплатина
56
I. Неорганические вещества
fPt (СОJ14] тетраиододикарбо-
нилдиплатина
PtCl2 хлорид платины(Н)
PtCl4 хлорид платиныAУ)
[PtCl4],Ba тетрахлороплатинат(И)
бария
[PtCl6],Ba гексахлороплатинат(ГУ)
бария
[PtCl6] ,Cs2 гексахлороплатинат(ГУ)
цезия
[PtCl6],H2 гексахлороплатинатAУ)
водорода
[PtCl4],K2 тетрахлороплатинат(И)
калия
[PtCl6],K2 гексахлороплатинатAУ)
калия
[PtCl6] ,Mg гексахлороплатинатAУ)
магния
[PtCl4],(NH4J тетрахлороплати-
нат(П) аммония
[PtCl6],(NH4J гексахлороплати-
натAУ) аммония
[PtCl4],Na2 тетрахлороплати-
нат(П) натрия
[PtCl6],Na2 гексахлороплати-
натAУ) натрия
[PtCl6],Ptn гексахлороплатинатAУ)
платины(П)
[PtCl6],Rb2 гексахлороплати-
натAУ) рубидия
PtF4 фторид ллатиныAУ)
PtF5 фторид платины(У)
PtF6 фторид платины(У1)
[PtF6],K гексафтороплатинат(У)
калия
>Кг гексафтороплатинатA\0
калия
О^) гексафтороплати-
нат(У) диоксигенила
e1 гексафтороплатинат(У)
ксенонаA)
Pt^2 иодид платины(И)
Ptl4 иодид платиныAУ)
[PtI6],Ptn гексаиодоплатинатAУ)
платины(И)
[Pt(NH3JCl2] дихлородиамминп-
латина
[Pt(NH3JCl4] тетрахлородиам-
минплатина
[Pt(NH3L]Cl2 хлорид тетраам-
минплатины(П)
[Pt(NH3J(NO2J] динитродиам-
минплатина
[Pt(NH3L][PtnCl4] тетрахлоропла-
тинат(И) тетраамминплати-
ны(И)
[Pt(NO2L],K2 тетранитроплати-
нат(П) калия
[Pt(NO2L],Na2 тетранитроплати-
нат(Н) натрия
PtO оксид платины(И)
PtO2 оксид платины(ГУ)
Pt(OHJ гидроксид платины(П)
[Pt(OHN],K2 гексагидроксоплати-
натAУ) калия
[Pt(OHN],Na2 гексагидроксопла-
тинатAУ) натрия
РЮ(О2) пероксид-оксид платины
PtP2 дифосфид платины
[Pt(PF3L] тетракис(трифторофос-
фор)платина
PtP2O7 дифосфат платиныAУ)
PtS сульфид платины(П)
PtS2 сульфид платины(ГУ)
Pt(Se2) диселенидB-) платины(П)
Pt(Te2) дителлуридB-) плати-
ны(П)
Ри плутоний
PuBr3 бромид плутония(Ш)
РиС0 85 0,85-карбид плутония
Ри2С3 трикарбид диплутония
Ри(С2О4J оксалат плутонияAУ)
РиС13 хлорид плутония(Ш)
PuF3 фторид плутония(Ш)
PuF4 фторид плутонияAУ)
PuF6 фторид плутония(У1)
57
I. Неорганические вещества
PuH2 дигидрид плутония
Pul3 иодид плутонияAП)
PuN мононитрид плутония
Pu(NO3L нитрат плутонияAУ)
РиО оксид плутония(П)
РиО2 оксид шгутонияAУ)
Ри2О3 оксид плутония(Ш)
Pu(O)F фторид-оксид плутония
Ри(ОНK гидроксид шгутония(Ш)
Ри(ОНL гидроксид плутонияAУ)
PuO2(NO3J динитрат плутония
PuP монофосфид плутония
PuS сульфид плутония(И)
PuSi моносилицид плутония
PuSi2 дисилицид плутония
Pu2Si3 трисилицид диплутония
Ra радий
RaBr2 бромид радия
RaCO3 карбонат радия
RaCl2 хлорид радия
Ra(NO3J нитрат радия
RaS сульфид радия
RaSO4 сульфат радия
Rb рубидий
RbAl(SO4J сульфат алюминия-ру-
алюминия-рубидия
RbBr бромид рубидия
RbBrO3 бромат рубидия
Rb(CH3COO) ацетат рубидия
Rb2CO3 карбонат рубидия
RbCl хлорид рубидия
RbClO2 хлорит рубидия
RbC103 хлорат рубидия
RbC104 перхлорат рубидия
Rb2Cr04 хромат рубидия
Rb2Cr207 дихромат рубидия
RbCr(SO4J сульфат хрома(Ш)-ру-
хрома(Ш)-рубидия
RbF фторид рубидия
RbFe(SO4J сульфат железа(Ш)-
рубидия
RbFe(SeO4J селенат желе-
за(Ш)-рубидия
RbH гидрид рубидия
RbHCO3 гидрокарбонат рубидия
Rb(HF2) гидродифторид рубидия
RbHSO4 гидросульфат рубидия
Rbl иодид рубидия
RbIO3 иодат рубидия
RbIO4 метапериодат рубидия
RbMnO4 перманганат рубидия
RbMn(SO4J сульфат марган-
ца(Ш)-рубидия
RbN3 азид рубидия
RbNH2 амид рубидия
RbNO2 нитрит рубидия
RbNO3 нитрат рубидия
RbO2 надпероксид рубидия
RbO3 озонид рубидия
Rb2O оксид рубидия
Rb2O2 пероксид рубидия
RbOH гидроксид рубидия
Rb2S сульфид рубидия
Rb2(S2) дисульфидB-) рубидия
Rb2(S3) трисульфидB-) рубидия
Rb2(S5) пентасульфидB-) рубидия
Rb2SO4 сульфат рубидия
Rb2S2O7 дисульфат рубидия
Rb(SO3F) фторосульфонат руби-
рубидия
Rb2Se04 селенат рубидия
RbV(SO4J сульфат вана-
дияA II)-рубидия
Re рений
ReBr3 бромид рения(Ш)
ReBr4 бромид ренияAУ)
Re(Br)O3 триоксид-бромид рения
[Re(CNLO2],K3 диоксотетраци-
аноренат(У) калия
[Re2(COI0] декакарбонилдирений
[Re(COMBr] бромопентакарбонил-
рений
[Re(COKC5H5] (циклопентади-
енил)трикарбонилрений
58
I. Неорганические вещества
[Re(COMCl] хлоропентакарбонил-
рений
[Re(COMI] иодопентакарбонилре-
ний
ReCl3 хлорид рения(Ш)
ReCl4 хлорид ренияA\0
ReCl5 хлорид рения(У)
[ReCl6],K2 гексахлороренатAУ) ка-
калия
[Re2Cl8],K2 октахлородиренат(Ш)
калия
Re(Cl)O3 триоксид-хлорид рения
ReCl4O оксид-тетрахлорид рения
[ReCl5O],Cs2 оксопентахлороре-
нат(У) цезия
ReF4 фторид ренияAУ)
ReF5 фторид рения(У)
ReF6 фторид рения(У1)
ReF7 фторид рения(УП)
[ReH(COM] пентакарбонилгидро-
рений
[ReH9],K2 нонагидридоренат(УИ)
калия
[ReH9],Na2 нонагидридоре-
нат(УИ) натрия
Rel3 иодид рения(Ш)
[ReI6],K2 гексаиодоренатA\0 ка-
калия
Re2N0,86 0,86-нитрид дирения
ReO2 оксид ренияAУ)
ReO3 оксид рения(У1)
Re2O5 оксид рения(У)
Re2O7 оксид рения(УИ)
Re(O)F4 тетрафторид-оксид рения
Re(O)F5 пентафторид-оксид рения
ReO2F2 дифторид-диоксид рения
ReO2F3 трифторид-диоксид рения
ReO3F фторид-триоксид рения
Re(OHL гидроксид ренияAУ)
[Ke2(PF3)]0] декакис( трифторо-
фосфор)ДИрений
ReS2 сульфид ренияAУ)
Re2S7 сульфид рения(УН)
KeSi2 дисилицид рения
H4Re209 нонаоксодиренат(УП) во-
водорода
Rh родий
RhBr3 бромид родия(Ш)
[Rh2(CO)8] октакарбонилдиродий
[Rh4(COI2] додекакарбонилтетра-
родий
[Rh6(COI6] 16-карбонилгексаро-
дий
[Rh(COJC5H5] (циклопентади-
енил)дикарбонилродий
[Rh2(COK(C5H5J] бис(циклопен-
тадиенил)трикарбонилдиродий
[Rh2(COLCl2] дихлоротетракарбо-
нилдиродий
[Rh(C2O4K],K3 триоксалаторо-
дат(Ш) калия
RhCl3 хлорид родия(Ш)
[RhCl6],Cs2 гексахлорородатAУ)
цезия
[RhCl6],K3 гексахлорородат(Ш)
калия
[RhCl6],Na3 гексахлорородат(Ш)
натрия
RhF3 фторид родия(Ш)
RhF5 фторид родия(У)
RhF6 фторид родия(У1)
Rh(HSK гидросульфид родия(Ш)
Rhl3 иодид родия(Ш)
[Rh(NH3N]Cl3 хлорид гексааммин-
родия(Ш)
Rh(NO3K нитрат родия(Ш)
[Rh(NO2N],K3 гексанитроро-
дат(Ш) калия
[Rh(NO2N],Na3 гексанитроро-
дат(Ш) натрия
Rh2O3 оксид родия(Ш)
Rh(OHK гидроксид родия(Ш)
Rh2S3 сульфид родия(Ш)
Rn радон
Ru рутений
RuBr3 бромид рутения(Ш)
59
I. Неорганические вещества
[Ru(C5H5J] бис(циклопентади-
енил)рутений
[Ru(C5H7O2K] трис(ацетилацето-
нато)рутений
[Ru(COM] пентакарбонилрутений
[Ru3(COI2] додекакарбонилтриру-
тений
[Ru2(COL(C5H5J] бис(циклопен-
тадиенил)тетракарбонилдиру-
тений
[Ru2(CONCl4] тетрахлорогексакар-
бонилдирутений
[Ru(COLI2] дииодотетракарбо-
нилрутений
RuCl3 хлорид рутения(Ш)
[RuCl6],K2 гексахлорорутенатAУ)
калия
[RuCl6],(NH4J гексахлороруте-
нат(ГУ) аммония
[ Ru2Cl 10О], К4 оксодекахл ородиру-
тенатAУ) калия
RuF5 фторид рутения(У)
RuF6 фторид рутения(У1)
[Ru(H2O)Cl5],K2 пентахлороаква-
рутенат(Ш) калия
Rul3 иодид рутения(Ш)
[Ru3(NH3I4O2]Cl6 хлорид дикис-
лород( 14-аммин)трируте-
ния(П)
[Ru(NO+)Cl5],K2 пентахлоронит-
розилийрутенат(П) калия
[Ru(NO+)Cl5],(NH4J пентахлоро-
нитрозилийрутенат(Н) аммо-
аммония
[Ru(NO+)(NO2LOH],Na2 гидро-
ксотетранитронитрозилийруте-
нат(П) натрия
RuO2 оксид рутенияAУ)
RuO4 оксид рутения(VIII)
Ru(O)F4 тетрафторид-оксид руте-
рутения
Ru(S2) дисульфидB-) рутения(П)
S8 октасера
S2Br2 дибромид дисеры
SBr2O оке ид-дибромид серы
S(Br)O2F фторид-диоксид-бромид
серы
(SCNJ дитиоциан
SC12 дихлорид серы
SC14 тетрахлорид серы
S2C12 дихлорид дисеры
S(C1)F5 пентафторид-хлорид серы
SC12O оксид-дихлорид серы
SC12O2 диоксид-дихлорид серы
S2C14O оксид-тетрахлорид дисеры
SC1(O)F фторид-оксид-хлорид серы
S(C1)O2F фторид-диоксид-хлорид
серы
SF4 тетрафторид серы
SF6 гексафторид серы
S2F2 дифторид дисеры
S2F10 декафторид дисеры
(SFK(NK тринитрид трис(фторо-
серы)
(SFL(NL тетранитрид тетра-
кис(фторосеры)
S2I2 дииодид дисеры
S4N2 динитрид тетрасеры
S4N4 тетранитрид тетрасеры
S(N)F3 трифторид-нитрид серы
S(NH)O оксид-имид серы
S(NH2JO2 диоксид-диамид серы
502 диоксид серы
503 триоксид серы
S2O оксид дисеры
S(O)F2 дифторид-оксид серы
S(O)F4 тетрафторид-оксид серы
SO2F2 дифторид-диоксид серы
SO2(O2) пероксид-диоксид серы
S(S)F2 дифторид-сульфид серы
H2S сероводород
H2(S2) дисульфан
H2(S3) трисульфан
H2(S4) тетрасульфан
H2(S5) пентасульфан
H2(S6) гексасульфан
H2(S7) гептасульфан
H2(S8) октасульфан
60
I. Неорганические вещества
H,SO4 серная кислота
H~S2O7 дисерная кислота
HSO3C1 хлоросульфоновая кислота
HSO3F фторосульфоновая кислота
HSO3(NH2) аминосульфоновая
кислота
H2SO3(O2) пероксосерная кислота
H2S2O6(O2) пероксодисерная кис-
кислота
H2SO3S тиосерная кислота
Sb сурьма
SbBr3 бромид сурьмы(Ш)
SbCl3 хлорид сурьмы(Ш)
SbCl5 хлорид сурьмы(У)
SbCl3F2 дифторид-трихлорид сурь-
сурьмы
[SbCl6],H гексахлоростибат(У) во-
водорода
[SbvCl6],[I(I)Cl] гексахлорости-
бат(У) хлороиодоиода(Ш)
Sb(Cl)O оксид-хлорид сурьмы
SbF3 фторид сурьмы(Ш)
SbF5 фторид сурьмы (V)
[SbF6],(C102) гексафторости-
бат(У) диоксохлора(У)
[SbF6],H гексафторостибат(У) во-
водорода
[SbF6],Na гексафторостибат(У)
натрия
SbH3 стибин
Sbl3 иодид сурьмы(Ш)
Sbl5 иодид сурьмы(У)
Sb2O3 оксид сурьмы(Ш)
Sb2O5 оксид сурьмы(У)
[Sb(OHN],K гексагидроксости-
бат(У) калия
[Sb(OHN],Na гексагидроксости-
бат(У) натрия
Sb2S3 сульфид сурьмы(Ш)
Sb2S5 сульфид сурьмы(У)
Sb(S)I иодид-сульфид сурьмы
bbS3],Na3 тритиостибат(Ш) натрия
LbbS4],Na3 тетратиосгибат(У) натрия
Sb7(SO4K сульфат сурьмы(Ш)
(SbmSbv)O4 оксид сурь-
мы(У)-сурьмы(Н1)
Sb2Se3 селенид сурьмы(Ш)
Sb2Te3 теллурид сурьмы(Ш)
Sc скандий
ScB2 диборид скандия
ScBrx бромид скандия(Ш)
ScC монокарбид скандия
Sc2(C2O4K оксалат скандия(Ш)
ScCl3 хлорид скандия(Ш)
ScF3 фторид скандия(Ш)
Scl3 иодид скандия(Ш)
ScN нитрид скандия(Ш)
Sc(NO3K нитрат скандия(Ш)
Sc2O3 оксид скандия(Ш)
Sc(OHK гидроксид скандия(Ш)
[Sc(OHL],Na тетрагидроксоскан-
датAП) натрия
[Sc(OHN],Na3 гексагидроксоскан-
дат(Ш) натрия
ScO(OH) метагидроксид скандия
ScPO4 ортофосфат скандия(Ш)
Sc2S3 сульфид скандия(Ш)
Sc2(SO4K сульфат скандия(Ш)
Se селен
Se8 октаселен
SeBr4 тетрабромид селена
Se2Br2 дибромид диселена
Se(Br)Cl3 трихлорид-бромид селена
SeBr2O оксид-дибромид селена
SeCl4 тетрахлорид селена
Se2Cl2 дихлорид диселена
SeCl2O оксид-дихлорид селена
SeF4 тетрафторид селена
SeF6 гексафторид селена
SeO2 диоксид селена
SeO3 триоксид селена
Se(O)F2 дифторид-оксид селена
(SeO2+)SeO4 селенат оксоселенаB+)
Se4S4 тетрасульфид тетраселена
H2Se селеноводород
61
I. Неорганические вещества
H2Se03 селенистая кислота
H2Se04 селеновая кислота
Si кремний
SiBr4 тетрабромид кремния
SiC монокарбид кремния
SiCl4 тетрахлорид кремния
Si2Cl6 гексахлорид дикремния
Si3Cl8 октахлорид трикремния
Si(Cl)F3 трифторид-хлорид крем-
кремния
SiCl2F2 дифторид-дихлорид крем-
кремния
SiCl3F фторид-трихлорид кремния
Si2Cl60 оксид-гексахлорид дик-
дикремния
Si3Cl802 диоксид-октахлорид три-
трикремния
Si4Cl804 тетраоксид-октахлорид
тетракремния
SiF4 тетрафторид кремния
Si2F6 гексафторид дикремния
Si3F8 октафторид трикремния
Si4FI0 декафторид тетракремния
[SiF6],Ba гексафторосиликат(ГУ)
бария
[SiF6],Ca гексафторосиликатAУ)
кальция
[SiF6],Co гексафторосиликат(ГУ)
кобальта(П)
[SiF6],Cs2 гексафторосиликат(ГУ)
цезия
[SiF6],Cu гексафторосиликатAУ)
меди(П)
[SiF6],Fe гексафторосиликат(ГУ)
железа(Н)
[SiF6],K2 гексафторосиликатAУ)
калия
[SiF6],Li2 гексафторосиликатAУ)
лития
[SiF6],Mg гексафторосиликатAУ)
магния
[SiF6],Mn гексафторосиликатAУ)
марганца(И)
[SiF6],(NH4J гексафторосили-
кат(ГУ) аммония
[SiF6],Na2 гексафторосиликат(ГУ)
натрия
[SiF6],Ni гексафторосиликатAУ)
никеля(П)
(SiFj JО оксид бис(трифторок-
ремния)
[SiF6],Rb2 гексафторосиликатAУ)
рубидия
[SiF6],Sr гексафторосиликатAУ)
стронция
[SiF6],Tl2 гексафторосиликатAУ)
таллияA)
SiH4 (моно)силан
Si2H6 дисилан
Si3H8 трисилан
Si4H10 тетрасилан
Si(H)Cl3 трихлоросилан
SiH2Cl2 дихлоросилан
SiH3Cl хлоросилан
Si(H)Cl2F фтородихлоросилан
Si(H)F3 трифторосилан
SiH2F2 дифторосилан
Si(H)I3 трииодосилан
SiH2I2 дииодосилан
SiH3I иодосилан
Sil4 тетраиодид кремния
[SiMoI2O40],H4 40-оксододекамо-
либдосиликатAУ) водорода
Si3N4 тетранитрид трикремния
Si(NCOL тетрацианат-N кремния
SiO монооксид кремния
SiO2 диоксид кремния
Si(OCNL тетрацианат кремния
SiP монофосфид кремния
SiS2 дисульфид кремния
[SiW12O40],H4 40-оксододекавольф-
рамосиликатAУ) водорода
Sm самарий
SmB6 гексаборид самария
SmBr2 бромид самария(П)
SmBr3 бромид самария(Ш)
62
I. Неорганические вещества
Sm(BrO3K бромат самария(Ш)
SmC2 дикарбвд самария
$т2(С2О4K оксалат самария(Ш)
SmCl2 хлорид самария(И)
SmCl3 хлорвд самария(Ш)
(SmnlCr)O3 оксид хрома(Ш)-сама-
рия(Ш)
SmF3 фторид самария(Ш)
Sml2 иодвд самария(П)
Sml3 иодвд самария(Ш)
Sm2(MoO4K молибдат самария(Ш)
Sm(NO3K нитрат самария(Ш)
Sm2O3 оксид самария(Ш)
Sm(OHK гидроксвд самария(Ш)
SmS сульфид самария(П)
Sm2S3 сульфид самария(Ш)
Sm2(S)O2 диоксид-сульфвд диса-
мария
Sm2(SO4K сульфат самария(Ш)
Sn олово
SnBr2 бромвд олова(П)
SnBr4 бромвд олова(ГУ)
Sn(Br)Cl3 трихлорид-бромид олова
SnBr3Cl хлорид-трибромид олова
Sn(CH3COOJ ацетат олова(Н)
Sn(CH3COOL ацетат оловаAУ)
SnC2O4 оксалат олова(П)
SnCl2 хлорид олова(П)
SnCl4 хлорвд олова(ГУ)
[SnCl6],Cs2 гексахлоростаннатAУ)
цезия
Sn(Cl)F фторид-хлорвд олова
[SnCl6],H2 гексахлоростаннатAУ)
водорода
[SnCl6],K2 гексахлоростаннатAУ)
калия
[SnCl6],(NH4J гексахлоростан-
натAУ) аммония
SnF2 фторвд олова(П)
SnF4 фторвд оловаAУ)
[^п^б]Д2 гексафторостаннат(ГУ)
калия
S"H4 станнан
Sn(HCOOJ формиат олова(П)
Snl2 иодид олова(П)
Snl4 иодид оловаAУ)
SnI2Br2 дибромид-дииодид олова
SnI2Cl2 дихлорид-дииодид олова
Sn(NO3J нитрат олова(П)
Sn(NO3L нитрат оловаAУ)
SnO оксид олова(И)
SnO2 оксид олова(ГУ)
Sn(OHJ гидроксвд олова(П)
[Sn(OHN],K2 гексагидроксостан-
нат(ГУ) калия
[Sn(OHK],Na тригидроксостан-
нат(И) натрия
[Sn(OHN],Na2 гексагидроксостан-
натAУ) натрия
Sn2P2O7 дифосфат олова(П)
SnS сульфид олова(И)
SnS2 сульфид оловаAУ)
[SnS3],K2 тритиостаннатAУ) калия
SnSO4 сульфат олова(П)
Sn(SO4J сульфат олова(ГУ)
SnSe селенвд олова(П)
SnSe2 селенид оловаAУ)
(SnnSnIV)S3 сульфвд оло-
ваAУ)-олова(П)
(Sn^1 SnIV)S4 сульфвд оло-
ваAУ)-Диолова(Н)
SnTe теллурид олова(П)
Sr стронций
(SrAs2)O6 оксвд димышья-
ка(У)-стронция
SrBr2 бромид стронция
SrB6 гексаборид стронция
Sr(BrO3J бромат стронция
SrC2 ацетиленид стронция
Sr(CH3COOJ ацетат стронция
SrCO3 карбонат стронция
SrC2O4 оксалат стронция
SrCl2 хлорид стронция
Sr(Cl)F фторвд-хлорвд стронция
Sr(ClO3J хлорат стронция
Sr(C104J перхлорат стронция
63
I. Неорганические вещества
SrCrO4 хромат стронция
SrCr2O7 дихромат стронция
SrF2 фторид стронция
SrH2 гидрид стронция
SrHPO4 гидроортофосфат стронция
Sr(HSJ гидросульфид стронция
(SrHf)O3 оксид гафнияAУ)-строн-
ция
Srl2 иодид стронция
Sr(IO3J иодат стронция
Sr(MnO4J перманганат стронция
SrMoO4 молибдат стронция
Sr3N2 нитрид стронция
Sr(NCSJ тиоцианат стронция
SrN2O2 гипонитрит стронция
Sr(NO2J нитрит стронция
Sr(NO3J нитрат стронция
SrO оксид стронция
SrO2 пероксид стронция
Sr(OHJ гидроксид стронция
Sr3(PO4J ортофосфат стронция
SrS сульфид стронция
SrSO4 сульфат стронция
SrS2O6 дитионат стронция
SrS4O6 тетратионат стронция
Sr(SO3S) тиосульфат стронция
SrSe селенид стронция
SrSeO4 селенат стронция
SrSiO3 метасиликат стронция
Sr2Si04 ортосиликат стронция
SrTe теллурид стронция
(SrTi)O3 оксид титана(ГУ)-стронция
SrWO4 вольфрамат стронция
(SrZr)O3 оксид цирко-
нияAУ)-стронция
Т2 дитритий
Т2О оксид трития
Та тантал
ТаВ2 диборид тантала
ТаВг4 бромид танталаAУ)
ТаВг5 бромид тантала(У)
Та6Вг1515-бромидгексатантала
ТаС монокарбид тантала
Та2С карбид дитантала
[Та(С5Н5)С14] тетрахлоро(цикло-
пентадиенил)тантал
ТаС13 хлорид тантала(Ш)
ТаС14 хлорид тантала( IV)
ТаС15 хлорид тантала(У)
Та6С115 15-хлорид гексатантала
ТаС13О оксид-трихлорид тантала
TaF5 фторид тантала(У)
[TaF7],K2 гептафторотанталат(У)
калия
[TaF8],K3 октафторотанталат(У)
калия
(Ta2FeIl)O6 оксид железа(И)-ди-
тантала(У)
Та2Н гидрид дитантала
Та14 иодид тантала(ГУ)
Та15 иодид тантала(У)
Та6114 14-иодид гексатантала
(Та2Мпп)О6 оксид марган-
ца(И)-дитантала(У)
TaN мононитрид тантала
Ta3N5 пентанитрид тритантала
Та2О5 оксид тантала(У)
Ta(O)F3 трифторид-оксид тантала
TaO2F фторид-диоксид тантала
Ta3O7F фторид-гептаоксид тритан-
тритантала
Ta2(SO4M сульфат тантала(У)
TaSi2 дисилицид тантала
ТЬ тербий
ТЬ2(С2О4K оксалаттербия(Ш)
ТЬС13 хлорид тербия(Ш)
TbF3 фторид тербия(Ш)
TbF4 фторид тербияAУ)
Tb(NO3K нитрат тербия(Ш)
ТЬ2О3 оксид тербия(Ш)
ТЬ(ОНK гидроксид тербия(Ш)
Tb2(SO4K сульфат тербия(Ш)
Тс технеций
ТсВг3О оксид-трибромид технеция
64
I. Неорганические вещества
[Тс(С5Н5J] бис(циклопентади- ,
енил)техне4ий ?
[Тс2(СОI0] декакарбонилдитехне-
ций
[Тс(СОKС5Н5] (циклопентади-
енил)трикарбонилтехнеций
ТсС14 хлорид технеция(ГУ)
ТсС16 хлорид технеция(У1)
[ТсС16],К2 гексахлоротехнетатAУ)
калия
Тс(С1)О3 триоксид-хлорид техне-
технеция
ТсС13О оксид-трихлорид технеция
TcF5 фторид технеция(У)
TcF6 фторид технеция(У1)
[TcF6],K гексафторотехнетат(У)
калия
[TcF6],K2 гексафторотехнетат(ГУ)
калия
ТсО2 оксид технеция(ГУ)
Тс2О7 оксид технеция(УИ)
Tc(O)F4 тетрафторид-оксид техне-
технеция
TcO3F фторид-триоксид технеция
Тс(ОНL гидроксид технеция(ГУ)
Tc2S7 сульфид технеция(УН)
НТсО4 технециевая кислота
Те теллур
ТеВг2 дибромид теллура
ТеВг4 тетрабромид теллура
ТеС12 дихлорид теллура
ТеС14 тетрахлорид теллура
TeF4 тетрафторид теллура
TeF6 гексафторид теллура
Те14 тетраиодид теллура
[TeMo6O24],(NH4N 24-оксогекса-
молибдотеллурат(У1) аммония
ТеО2 диоксид теллура
ТеО3 диоксид теллура
(ГеО +)ТеО4 метателлурат оксотел-
лураB+)
Н2Те теллуроводород
Н2Те03 теллуристая кислота
Н6Те06 ортотеллуровая кислота
Th торий
ThB6 гексаборид тория
ThBr4 бромид тория(ГУ)
ThC монокарбид тория
ThC2 дикарбид тория
ThCl4 хлорид тория(ГУ)
ThF4 фторид тория(ГУ)
ThH2 дигидрид тория
Thl4 иодид торияAУ)
ThN мононитрид тория
Th(NO3L нитрат тория(ГУ)
ThO2 оксид торияAУ)
Th(OHL гидроксид торияAУ)
Th(PO3L метафосфат тория(ГУ)
ThS2 сульфид торияAУ)
Th(SO4J сульфат торияAУ)
Th(SeO4J селенат торияAУ)
ThSi2 дисилицид тория
ThSiO4 ортосиликат торияAУ)
Ti титан
TiB2 диборид титана
TiBr2 бромид титана(П)
TiBr3 бромид титана(Ш)
TiBr4 бромид титана(ГУ)
TiC монокарбид титана
[Ti(C5H5J] бис(циклопентади-
енил)титан
[Ti(C5H5)Cl3] трихлоро(циклопен-
тадиенил)титан
[Ti(C5H5JCl] хлоробис(циклопен-
тадиенил)титан
[Ti(C5H5JCl2] дихлоробис(цикло-
пентадиенил)титан
[Ti(COJ(C5H5J] бис(циклопента-
диенил)дикарбонилтитан
TiCl2 хлорид титана(П)
TiCl3 хлорид титана(Ш)
TiCl4 хлорид титана(ГУ)
Ti(Cl)F3 трифторид-хлорид титана
TiCl2O оксид-дихлорид титана
3 - 2004
65
I. Неорганические вещества
Ti(C104L перхлорат титанаAУ)
(TiCoH)O3 оксид кобальта(Н)-ти-
танаAУ)
(TiCo " )О4 оксид дикобаль-
та(П)-титана(ГУ)
TiF2 фторид титана(И)
TiF3 фторид титана(Ш)
TiF4 фторид титанаAУ)
[TiF6],K2 гексафторотитанатAУ)
калия
(TiFeH)O3 оксид железа(И)-тита-
наAУ)
(TiFe2I)O4 оксид дижелеза(И)-ти-
тана(ГУ)
TiH2 дигидрид титана
Til2 иодид титана(Н)
Til3 иодид титана(Ш)
Til4 иодид титанаAУ)
TiI2O оксид-дииодид титана
(TiMnn)O3 оксид марганца(Н)-ти-
тана(ГУ)
(TiMn 2I)O4 оксид димарган-
цаA1)-титанаAУ)
TiN мононитрид титана
Ti(NO3L нитрат титана(ГУ)
TiO оксид титана(И)
TiO2 оксид титана(ГУ)
Ti2O3 оксид титана(Ш)
Ti(O)F2 дифторид-оксид титана
Ti(OHK гидроксид титана(Ш)
ТЮ(ОНJ дигидроксид-оксид ти-
титана
TiP монофосфид титана
(TiPbn)O3 оксид свинца(И)-тита-
наAУ)
TiS сульфид титана(И)
TiS2 сульфид титанаAУ)
Ti2S3 сульфид титана(Ш)
Ti2(SO4K сульфат титана(Ш)
Ti(SO4)O оксид-сульфат титана
TiSO4(OHJ дигидроксид-сульфат
титана
TiSi моносилицид титана
66
TiSi2 дисилицид титана
Ti5Si3 трисилицид пентатитана
П таллий
T1A1(SO4J сульфат алюминия-тал-
лияA)
Tl3AsS4 тетратиоарсенат таллияA)
Т1Вг бромид таллияA)
Т1С5Н5 циклопентадиенид тал-
лияA)
Т1(СН3СОО) ацетат таллияA)
Т1(СН3СООK ацетат таллия(Ш)
Т12СО3 карбонат таллияA)
Т12С2О4 оксалат таллияA)
Т1С1 хлорид таллияA)
Т1С13 хлорид таллия(Ш)
Т1С1О3 хлорат таллияA)
Т1С1О4 перхлорат таллияA)
Т12Сг04 хромат таллияA)
Т12Сг207 дихромат таллияA)
T1F фторид таллияA)
T1F3 фторид таллия(Ш)
Т1(НСОО) формиат таллияA)
Т1Н2РО4 дигидроортофосфат тал-
лияA)
Т12НРО4 гидроортофосфат тал-
таллия^)
T1HSO4 гидросульфат таллияA)
ТП иодид таллияA)
T1N3 азид таллияA)
T1NCS тиоцианат таллияA)
T1NO2 нитрит таллияA)
T1NO3 нитрат таллияA)
T1(NO3K нитрат таллия(Ш)
Т12О оксид таллияA)
Т12О3 оксид таллия(Ш)
Т1ОН гидроксид таллияA)
Т13РО4 ортофосфат таллияA)
Т14Р2О7 дифосфат таллияA)
T12S сульфид таллияA)
T12S3 сульфид таллия(Ш)
T12SO4 сульфат таллияA)
T12S2O6 дитионат таллияA)
T12(SO3S) тиосульфат таллияA)
I. Неорганические вещества
Xl2Se селенид таллияA)
Tl2Se04 селенат таллияA)
TlVO3 метаванадат таллияA)
Ita тулий
TmBr3 бромид тулия(Ш)
Тт2(С2О4Kоксалат тулия(Ш)
ТтС13 хлорид тулия(Ш)
TmF3 фторид тулия(Ш)
Tml3 иодид тулия(Ш)
Тт2О3 оксид тулия(Ш)
Tm2(SO4K сульфат тулия(Ш)
U уран
UB2 диборид урана
UB4 тетраборид урана
UB12 додекаборид урана
UBr3 бромид урана(Ш)
UBr4 бромид урана(ГУ)
UBr5 бромид урана(У)
UC монокарбид урана
UC2 дикарбид урана
U2C3 трикарбид диурана
UC13 хлорид урана(Ш)
UC14 хлорид урана(ГУ)
UC15 хлорид урана(У)
UC16 хлорид урана(У1)
UF3 фторид урана(Ш)
UF4 фторид уранаAУ)
UF5 фторид урана(У)
UF6 фторид урана(У1)
fUF5],NH4 пентафтороуранатAУ)
аммония
UH3 тригидрид урана
UI3 иодид урана(Ш)
UI4 иодид уранаAУ)
UN мононитрид урана
U3N2 динитрид триурана
UO2 оксид уранаAУ)
UO3 оксид урана(У1)
иО2(СН3СООJ ацетат уранила
(UO2)CO3 карбонат уранила
ШО2)С2О4 оксалат уранила
(UO2)Q2 хлорид уранила
UO2(C1O4J перхлорат уранила
U(O)F4 тетрафторид-оксид урана
(UO2)F2 фторид уранила
[UO2F5],(NH4K пентафтородиок-
соуранат(У1) аммония
U(OHL гидроксид уранаAУ)
UO2(NO3J нитрат уранила
UO2(O2) пероксид уранила
UO2(OHJ гидроксид уранила
(UO2)S сульфид уранила
(UO2)SO4 сульфат уранила
UP монофосфид урана
US сульфид урана(П)
US2 сульфид уранаAУ)
U(SO4J сульфат уранаAУ)
USi2 дисилицид урана
U3Si2 дисилицид триурана
USiO4 ортосиликат уранаAУ)
(U У UVI)O8 оксид урана(У1)-диура-
на(У)
V ванадий
VB2 диборид ванадия
VBr2 бромид ванадия(Н)
VBr3 бромид ванадия(Ш)
V(Br)O оксид-бромид ванадия
VBr2O оксид-дибромид ванадия
VBr3O оксид-трибромид ванадия
VC монокарбид ванадия
V2C карбид диванадия
[V(C5H5J] бис(циклопентади-
енил)ванадий
[V(CON] гексакарбонилванадий
[V(COLC5H5] (циклопентади-
енил)тетракарбонилванадий
[V(CON],Na гексакарбонилвана-
дат(—I) натрия
VC12 хлорид ванадия(П)
VC13 хлорид ванадия(Ш)
VC14 хлорид ванадия(ГУ)
V(C1)O оксид-хлорид ванадия
V(C1)O2 диоксид-хлорид ванадия
VC13O оксид-трихлорид ванадия
VF3 фторид ванадия(Ш)
67
I. Неорганические вещества
VF4 фторид ванадия(ГУ)
VF5 фторид ванадия(У)
[VF6],K гексафторованадат(У) калия
[VF6],(NH4K гексафторована-
дат(Ш) аммония
VI2 иодид ванадия(П)
VI3 иодид ванадия(Ш)
VN мононитрид ванадия
V2N нитрид диванадия
VNH4(SO4J сульфат аммония-ва-
надия(Ш)
VO оксид ванадия(И)
VO2 оксид ванадияAУ)
V2O3 оксид ванадия(Ш)
V2O5 оксид ванадия(У)
(VO)Br2 бромид ванадила
(VO)C12 хлорид ванадила
(VO2)C1 хлорид диоксованадия(У)
V(O)F3 трифторид-оксид ванадия
V(OHK гидроксид ванадия(Ш)
VO(OH) метагидроксид ванадия
VO(OHJ дигидроксид-оксид вана-
ванадия
(VO)SO4 сульфат ванадила
VS сульфид ванадия(П)
VS2 сульфид ванадияAУ)
V2S3 сульфид ванадия(Ш)
V2S5 сульфид ванадия(У)
VSO4 сульфат ванадия(П)
V2(SO4K сульфат ванадия(Ш)
VSi2 дисилицид ванадия
V3Si силицид триванадия
V5Si3 трисилицид пентаванадия
W вольфрам
WB2 диборид вольфрама
W2B5 пентаборид дивольфрама
WBr2 бромид вольфрама(П)
WBr3 бромид вольфрама(Ш)
WBr4 бромид вольфрамаAУ)
WBr5 бромид вольфрама(У)
WBr6 бромид вольфрама(У1)
WBr2O оксид-дибромид вольфрама
WBr2O2 диоксид-дибромид вольф-
вольфрама
WBr3O оксид-трибромид вольфрама
WBr4O оксид-тетрабромид вольф-
вольфрама
WC монокарбид вольфрама
W2C карбид дивольфрама
[W(CON] гексакарбонилвольфрам
WC12 хлорид вольфрама(П)
WC13 хлорид вольфрама(Ш)
WC14 хлорид вольфрамаAУ)
WC15 хлорид вольфрама(У)
WC16 хлорид вольфрама(У1)
WC12O оксид-дихлорид вольфрама
WC12O2 диоксид-дихлорид вольф-
вольфрама
WC13O оксид-трихлорид вольфрама
WC14O оксид-тетрахлорид вольф-
вольфрама
WF6 гексафторид вольфрама
WFe2 дижелезовольфрам
[WH2(C5H5J] бис(циклопентади-
енил)дигидровольфрам
WI2 иодид вольфрама(Н)
WI3 иодид вольфрама(Ш)
W(I)O2 диоксид-иодид вольфрама
WI2O2 диоксид-дииодид вольфрама
WO2 оксид вольфрамаAУ)
WO3 оксид вольфрама(У1)
W(O)F4 тетрафторид-оксид вольф-
вольфрама
WS2 сульфид вольфрамаAУ)
WSe2 селенид вольфрамаAУ)
WSi2 дисилицид вольфрама
Хе ксенон
Xe(CF3COOJ бис(трифтороаце-
тат) ксенона
ХеС12 дихлорид ксенона
XeF2 дифторид ксенона
XeF4 тетрафторид ксенона
XeF6 гексафторид ксенона
[XeF8],(NO+J октафтороксено-
нат(УТ) нитрозилия
68
I. Неорганические вещества
ХеО3 триоксид ксенона
ХеО4 тетраоксид ксенона
Xe(O)F2 дифторид-оксид ксенона
Xe(O)F4 тетрафторид-оксид ксе-
ксенона
XeO2F2 дифторид-диоксид ксенона
Хе(ОНL тетрагидроксид ксенона
Y иттрий
(YA1)O3 оксид алюминия-ит-
трия(Ш)
YB6 гексаборид иттрия
YBr3 бромид иттрия(Ш)
Y(BrO3K бромат иттрия(Ш)
Y2(C2O4K оксалат иттрия(Ш)
YC13 хлорид иттрия(Ш)
(YCrin)O3 оксид хрома(Ш)-ит-
трия(Ш)
YF3 фторид иттрия(Ш)
YH3 гидрид иттрия(Ш)
YI3 иодид иттрия(Ш)
Y(NO3K нитрат иттрия(Ш)
Y2O3 оксид иттрия(Ш)
Y(OHK гидроксид иттрия(Ш)
YPO4 ортофосфат иттрия(Ш)
Y2S3 сульфид иттрия(Ш)
Y2(S)O2 диоксид-сульфид иттрия
Y2(SO4K сульфат иттрия(Ш)
YSb стибид иттрия(Ш)
YSi моносилицид иттрия
Yb иттербий
YbBr2 бромид иттербия(И)
YbBr3 бромид иттербия(Ш)
Yb(CH3COOK ацетат иттербия(Ш)
Yb2(C2O4K оксалат иттербия(Ш)
YbCl2 хлорид иттербия(И)
YbCl3 хлорид иттербия(Ш)
YbF2 фторид иттербия(И)
^ЬР3 Фторид иттербия(Ш)
Yblj иодид иттербия(И)
Yb(NO3K нитрат иттербия(Ш)
^Оз оксид иттербия(Ш)
Yb(OHK гидроксид иттербия(Ш)
Yb2(SO4K сульфат иттербия(Ш)
Zn цинк
(ZnAl2)O4 оксид диалюми-
ния-цинка(И)
Zn3As2 арсенид цинка(П)
Zn3(As04J арсенат цинка(П)
ZnBr2 бромид цинка(И)
Zn(BrO3J бромат цинка(П)
Zn(CH3COOJ ацетат цинка(П)
Zn(CNJ цианид цинка(П)
ZnCO3 карбонат цинка(П)
ZnCl2 хлорид цинка(И)
[ZnCl4],(NH4J тетрахлороцин-
кат(И) аммония
Zn(C103J хлорат цинка(П)
Zn(C104J перхлорат цинка(И)
ZnF2 фторид цинка(П)
Zn(HCOOJ формиат цинка(П)
Znl2 иодид цинка(П)
Zn3N2 нитрид цинка(И)
[Zn(NH3JCl2] дихлородиаммин-
цинк
Zn(NO3J нитрат цинка(П)
ZnO оксид цинка(И)
Zn(OHJ гидроксид цинка(П)
[Zn(OHL],Na2 тетрагидроксоцин-
кат(П) натрия
Zn3P2 фосфид цинка(П)
Zn2P2O7 дифосфат цинка(П)
Zn3(PO4J ортофосфат цинка(П)
ZnS сульфид цинка(П)
ZnSO4 сульфат цинка(П)
ZnSb моностибид цинка
Zn3Sb2 стибид цинка(П)
ZnSe селенид цинка(Н)
ZnSiO3 метасиликат цинка(П)
Zn2SiO4 ортосиликат цинка(П)
ZnTe теллурид цинка(П)
ZnWO4 вольфрамат цинка(И)
Zr цирконий
ZrB2 диборид циркония
ZrB12 додекаборид циркония
I. Неорганические вещества
ZrBr4 бромид цирконияAУ)
ZrC монокарбид циркония
[Zr(C5H5JCl2] дихлоробис(цикло-
пентадиенил)цирконий
ZrCl2 хлорид циркония(Н)
ZrCl3 хлорид циркония(Ш)
ZrCl4 хлорид цирконияAУ)
[ZrCl6],K2 гексахлороцирко-
натAУ) калия
ZrCl2O оксид-дихлорид циркония
ZrF2 фторид циркония(П)
ZrF3 фторид циркония(Ш)
ZrF4 фторид цирконияAУ)
[ZrF6],K2 гексафтороцирконатAУ)
калия
[ZrF7],K3 гептафтороцирконат(ГУ)
калия
[ZrF7],(NH4K гептафтороцирко-
натAУ) аммония
ZrH2 дигидрид циркония
Zr(HAsO4J гидроарсенат цирко-
циркония^ V)
Zrl4 иодид цирконияAУ)
ZrN мононитрид циркония
Zr3N4 нитрид цирконияAУ)
Zr(NCSL тиоцианат циркония(ГУ)
ZrO2 оксид цирконияAУ)
ZrO(OHJ дигидроксид-оксид
циркония
ZrP2O7 дифосфат цирконияAУ)
(ZrPbH)O3 оксид свинца(П)-цир-
конияAУ)
ZrS2 сульфид циркония(ГУ)
Zr(SO4J сульфат циркония(ГУ)
ZrSi моносилицид циркония
ZrSi2 дисилицид циркония
Zr2Si силицид дициркония
ZrSiO4 ортосиликат цирконияAУ)
3. Физические свойства
Таблица физических свойств неорганических веществ разбита на
рубрики, каждая из которых относится к одному элементу (первому
слева в формулах). Рубрики следуют по алфавиту символов элемен-
элементов, т. е. Ac, Ag, Al, Am, Аг, As, At, Аи, В и т. д.
В рубрике после формулы простого вещества (элемента в свобод-
свободном виде) перечислены формулы соединений данного элемента. Так,
в рубрике «Ас» после самого Ас следуют, по алфавиту, формулы его
соединений — АсВг3, АсС13, Ас(С1)О, AcF3 и т. д.
Вслед за формулами безводных веществ даны формулы их гидра-
гидратов, например, в рубрике «А1»:
AlAsO4 — свойства безводного вещества
• 8Н2О — свойства гидрата с полной формулой AlAsO4 • 8Н2О
Число молекул воды, приходящихся на одну формульную единицу
безводного вещества, обычно отвечает кристаллизации из водного
раствора при комнатной температуре. Если безводное вещество не
получено, это указано словами «Не получен» (см., например, в рубри-
рубрике «Ас» вещество АсРО4, для которого известен только гидрат
AsPO4 • 0,5Н2О).
70
I. Неорганические вещества
формулы соединений с комплексным анионом, образованным
элементом данной рубрики, представлены в инвертированной форме
(анион, катион):
Дано Следует читать
[Ag(CNJ],K K[Ag(CNJ]
[AlF6],Na3 Na3[AlF6]
Кислоты (бескислородные, кислородсодержащие) указаны в руб-
рубриках соответствующих элементов в конце списка соединений, на-
например, в конце рубрики «С» приведены данные для кислот HCN,
H2CN2, Н2С2О4, НСООН, H2CS3.
При образовании бертоллидов — веществ с некоторой областью го-
гомогенности и, как следствие, с переменным составом (недостаток или
избыток одного из элементов) это указано в формуле через «±л» и ниже
обычно приведен интервал значений х (например, -0,1 < х < 0,2).
Физические свойства, рассмотренные в таблице:
1) относительная молекулярная масса (Мг), рассчитанная по форму-
формуле вещества, приведенной в первой (слева) колонке. Для бертоллидов
указанные значения Мх соответствуют идеальному составу, например,
для вещества СеН3_х— составу СеН3;
2) температуры плавления (п.) и кипения (к.), выраженные в граду-
градусах Цельсия (°С). Если эти температуры не существуют или неизвест-
неизвестны, то даются температуры разложения (например, разл. 360), возгонки
(возг. 170) или размягчения (разм. 240). Другие обозначения в этих ко-
колонках:
~ 3200 — при температуре около 3200 °С
> 360 — при температуре выше 360 °С
< 120 — при температуре ниже 120 °С
192,6(/?) — вещество плавится (кипит) при указанной тем-
температуре под избыточным давлением
410 (вак.) — соответствующий процесс протекает при указан-
указанной температуре в вакууме (под пониженным
давлением)
346 разл. — вещество плавится (кипит) при указанной тем-
температуре, а выше этой температуры разлагается
160—> А12О3 — вещество при указанной температуре разлагает-
разлагается без плавления (кипения) и образует продукт,
основной для данной рубрики
-Н2О 337 — гидрат теряет всю воду при указанной темпера-
температуре и переходит в безводное вещество
—2Н2О 480 — гидрат частично теряет воду и переходит в гидрат
с меньшим содержанием воды;
71
I. Неорганические вещества
3) окраска и плотность для указанного агрегатного состояния
(г. — газ, ж. — жидкость, остальные вещества — твердые).
Использованные сокращения цвета:
бел. — белый оранж. — оранжевый
бур. — бурый роз. — розовый
бцв. — бесцветный св. — светло-
гол. — голубой сер. — серый
желт. — желтый син. — синий
зел. — зеленый т. — темно-
кор. — коричневый фиол. — фиолетовый
краен. — красный черн. — черный
Записи типа «красн.-кор.» следует читать «красно-коричневый»
(первый цвет — оттенок, второй цвет — основной).
Единицы плотности веществ:
газы — в г/л при н. у.
жидкости — в г/мл (верхний индекс — температура)
твердые вещества — в г/см3
Формула
Ас
АсВг3
АсС13
Ас(С1)О
AcF3
Ac(NO3K
Ас2О3
Ac(O)F
Ас(ОНK
АсРО4
• 0,5Н2О
Ac2S3
Ag
(AgIAgIII)O2
AgAs
Ag3As03
Ag3AsO4
AgAsS2
4
227,028
466,74
333,39
278,48
284,02
413,04
502,05
262,03
278,05
322,00
331,01
550,25
107,868
247,73
182,79
446,52
462,52
246,92
Фазовые переходы
п. 1051, к. 3198
возг. 800
возг. 960
п. > 1000
возг. > 1050
600 -> Ас2О3
п.« 2500
п.> 1100
1100^Ас2О3
Не получен
разл. > 1500
п. - 1900
п. 961,78, к. 2162
> 100 — Ag
п. 1740
150 разл.
« 830 разл.
п. 417, разл. > 500
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
черн.
бел.
т.-сер.
сер.
св.-желт.
т.-кор.
сер.-черн.
Плот-
Плотность
10,07
5,85
7,81
7,23
7,88
9,19
8,28
5,48
6,75
10,494
7,483
3,598
6,657
72
I. Неорганические вещества
Продолжение табл.
формула
Ag3AsS3
AgBr
AgBrO3
Ag2C2
Ag(CH3COO)
AgCN
Ag2CN2
[Ag(CNJ],K
AgCNO
Ag2CO3
Ag2C2O4
AgCl
AgC102
AgC103
AgC104
Ag2Cr04
Ag2Cr207
AgF
AgF2
Ag2F
Ag(HCOO)
Ag2H3IO6
Ag2H4Te06
Agl
AgIO3
AgIO4
Ag3IO5
AgMnO4
AgN3
Ag3N
AgNCS
AgNO2
AgNO3
4
494,72
187,77
235,77
239,76
166,91
133,89
255,76
199,00
149,89
275,74
303,75
143,32
175,32
191,32
207,32
331,73
431,72
126,87
145,86
234,73
152,89
441,66
443,36
234,77
282,77
298,77
530,50
226,80
149,89
337,61
165,95
153,87
169,87
Фазовые переходы
п. 496, разл. 600
п. 432, 700 - Ag
разл. ~ 360
>20 —Ag
> 300 — Ag
п. 350(р), > 250 — Ag
300 - Ag
> 250 — Ag-
разл. > 120
140 —Ag2O, >210 —Ag
110-Ag,Ag2CO3,
> 230 - Ag
п. 455, к. 1550
> 250 — AgCl
п. 230, > 270 — AgCl
486 — AgCl
> 300 — Ag
> 200 - Ag
n. 435, к. 663
n. 690, > 700 - AgF
>115-Ag,AgF
> 300 — Ag
n. 60 разл.
разл. > 200
п. 554, > 560 — Ag
п. - 200, > 250 — Agl
180-Agl
разл. > 320
> 160 —Ag
п. 252, 300 - Ag
> 165 — Ag
170 —Ag
120 разл., 160 —Ag
n. 209,7, > 300 — Ag
Окраска
т.-краен.
св.-желт.
бел.
бел.
бел.
бел.
желт.
бел.
сер.
св.-желт.
бел.
бел.
желт.
бел.
бел.
св.-краен.
т.-краен.
бел.
св.-син.
желт.-зел.
бел.
желт.
желт.
желт.
бел.
желт.
черн.
черн.
бел.
т.-кор.
бел.
св.-желт.
бел.
Плот-
Плотность
5,629
6,473
5,21
3,259
3,95
2,36
6,077
5,029
5,56
4,439
2,806
5,625
4,77
5,852
4,57
8,64
5,68
5,67
5,525
5,57
4,4
9,0
4,453
4,352
73
I. Неорганические вещества
Продолжение табл.
Формула
Ag2N2O2
Ag2O
Ag2O3
AgOCN
AgPO3
Ag3PO4
Ag4P2O7
(Ag2Pb)O2
AgReO4
Ag2S
Ag2SO3
Ag2SO4
Ag2(SO3S)
[Ag(SO3SJ],Na3
(AgSb"')S2
(Ag3Sbm)S3
(Ag5Sbm)S4
Ag2Se
Ag2Se04
Ag2Te
Ag2Te03
Al
AlAs
AlAsO4
•8H2O
A1B2
A1B12
AlBr3
•6H2O
Al(BrO3K
•9H2O
A14C3
A1(CH3COOK
4
275,75
231,74
263,73
149,89
186,84
418,57
605,41
454,93
358,07
247,80
295,80
311,80
327,87
401,10
293,76
541,56
789,36
294,70
358,69
343,34
391,33
26,982
101,90
165,90
310,02
48,60
156,71
266,69
374,78
410,69
572,82
143,96
204,11
Фазовые переходы
110 —Ag
п. 815(/?), 160 —Ag
20 - (AgIAgII1)O2
147 —AgCN, >250 —Ag
n. 482 разл.
п. 849
п. 585
492 -Ag
п. 455
п. 832
разл. > 100
п.-660, 1100 —Ag
разл. > 250
разл. > 350
п. 509, разл. > 1000
п. 486
разл. 600
п. 897
700 —Ag
п. 960
п. 450
п. 660,32, к. 2519
п. 1740
разл. > 1000
-Н2О 335
1400 — А1
п. - 2200
п. 97,5, к. 265
п. 93, разл.> 120
Не получен
п. 62,3, разл. 100
п. 2100, > 2200 —А1
разл. > 370
Окраска
желт.
т.-кор.
сер.
бел.
бел.
желт.
бел.
черн.
бел.
сер.-черн.
бел.
бел.
бел.
бел.
сер.-черн.
краен.
кор.-черн.
черн.
бел.
сер.-син.
св.-желт.
бел.
оранж.
бел.
бел.
т.-краен.
черн.
бел.
бел.
бел.
желт.
бел.
Плот-
Плотность
5,75
7,143
7,029
4,0
6,37
6,375
5,306
6,96
7,317
5,45
5,2
5,85
6,25
8,187
5,72
8,35
2,702
3,81
3,25
3,01
3,19
2,55
3,205
2,54
2,95
74
I. Неорганические вещества
Продолжение табл.
Формула
A1(CNK
А12(С2О4K
•4Н2О
[А1(С2О4K],К3
•ЗН2О
А1С13
•6Н2О
[А1С14],1п
[A1C14],NH4
[AlCl4],Na
А1(С1)О
А1(С1О3)з
•6Н2О
А1(СЮ4K
•6Н2О
А1С1(ОНJ
[AlD4],Li
A1F3
Н2О
[A1F6],K3
[AlF6],Li3
[A1F6],(NH4K
[AlF6],Na3
A1H3
Al(H)Br2
AlH2Br
A1(H)C12
A1H2C1
A1(H)I,
A1H2I
tAlH4],Li
[AlH4],Na
¦—— .
Mr
105,04
318,02
390,08
408,33
462,38
133,34
241,43
283,61
186,83
191,78
78,43
277,33
385,42
325,33
433,42
96,45
41,98
83,98
101,99
258,26
161,79
195,09
209,94
30,01
187,80
108,90
98,90
64,45
281,80
155,90
37,96
54,00
Фазовые переходы
разл. 100
He получен
290 — A12O3
400 - A12O3
-H2O 120
n. 192,80?), возг. 179,7
150-*A1C1(OHJ,
450 — A12O3
n.268
n.303
n. 156, >800 — AlCl3
разл. > 500
разл. 350
-H2O > 140
возг. > 100 (вак.),
427 - А12О3
п. 121, -Н2О 178
350 — А1(С1)О
п. 175 разл.
возг. 1279
-Н2О 150
возг. - 1300
п.-900, разл. 1100
разл. 305
п. 1027, разл. > 1200
> 105 — А1
разл. > 55
разл. > 35
разл. > 60
разл. > 40
п. 80, разл. 250
п. 35, разл. 200
150-170 —А1
п. 183, 220-230 — А1
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
св.-желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бцв. ж.
бцв. ж.
бцв. ж.
бцв. ж.
бел.
бел.
бел.
бел.
Плот-
Плотность
2,465
2,398
2,02
2,882
2,17
1,837
2,975
1,45
0,917
1,28
75
I. Неорганические вещества
Продолжение табл.
Формула
А113
•6Н2О
A1(IO3JNO3
•6Н2О
A1N
A1(N3K
A1NH4(SO4J
• 12Н2О
A1(NO3K
•9Н2О
А12О3
Al2i67O4
А1@НK
[Al(OHL],Na
а-АЮ(ОН)
у-АЮ(ОН)
А1Р
A1PO4
•2H2O
A1(PO3K
A13(PO4J(OHK
•5H2O
A12S3
A12(SO4K
• 13,5H2O
• 16H2O
• 18H2O
A1(SO4)OH
A12SO4(OHL
AlSb
Al2Se3
Al2Si207
•4H2O
Al2(SiO4)O
4
407,69
515,78
438,79
546,88
40,99
153,05
237,15
453,33
212,99
375,13
101,96
136,04
78,00
118,00
59,99
59,99
57,96
121,95
157,98
263,90
321,91
411,98
150,16
342,15
585,35
630,39
666,42
140,05
218,05.
148,74
290,84
222,13
330,22
162,05
Фазовые переходы
п. 188,3, к. 382,5
разл.185
Не получен
разл. > 100
п.2430, 1800(вак.)-А1
> 200 - A1N
500 — А12О3
п. 93,5, -Н2О > 250
п. 66 разл., > 150 -+ А12О3
п. 73,5 разл., 350 - АЮ(ОН)
п. 2053, к. 3530
1000 — А12О3
200-у-А1О(ОН)
800 — NaAlO2
575 — А12О3
300-А12N7О4
п. 1700, > 2000 — А1
п. ~ 1650 разл.
-Н2О - 350
п. 1240
Не получен
разл. > 1000
п. 1120(р),возг. 1550
п. 770 разл., 860 -* А12О3
разл. > 290
п. 86 разл.
п. 86,5 разл.,-Н2О 420
разл. 450, > 500 -* А12О3
разл. 600, > 600 — А12О3
п. 1060
разл. 1000, > 1000 — А1
п.« 1700 разл.
-Н2О 400
п. 1545 разл.
Окраска
бел.
св.-желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
сер.-желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
син.-сер.
желт.
бел.
бел.
бел.
Плот-
Плотность
3,98
2,63
3,12
2,039
1,64
1,89
3,97
2,424
3,35
3,01
2,41
2,56
2,54
2,78
2,3
2,32
2,71
1,69
1,65
4,218
2,61
2,1
3,61
76
I. Неорганические вещества
Продолжение табл.
формула
А12Те3
Am
Am2(C2O4K
• 10Н2О
АтС13
AmF3
A1T1F4
Am(NO3K
АтО2
Ат2О3
Ат(ОНK
Ат(ОНL
Аг
a-As
p-As
As4
AsBr3
AsCl3
AsCl5
As(Cl)O
AsF3
AsF5
[AsF6],H
•H2O
[AsF6],Li
AsH3
Asl3
As2I4
AsN
As2°3 (аморфн.)
oc-As203
.
4
436,76
243,061
750,18
930,33
349,42
300,06
319,05
429,07
275,06
534,12
294,08
311,09
39,948
74,922
74,922
299,69
314,63
181,28
252,19
126,37
131,92
169,91
189,92
207,93
195,85
77,95
455,63
657,46
88,93
197,84
197,84
Фазовые переходы
разл. 900
п. 1176, к. 2607
Не получен
> 300 -> Ат2О3
п. 850, к. 1750
п. 1393, к. 2070
возг. 850 (вак.)
> 250 — Ат2О3
> 1000 — Ат2О3
п. 2200
> 350 -* Ат2О3
400 — АтО2
п. -189,35, к. -185,85
п. 8170?), возг. 614
270 - a-As
358 — a-As
п. 31,2, к. 221
п.-16,2, к.+131,4
п. -40, разл. -28
разл. 60
п. -5,94, к. +57,8
п. -79,8, к. -52,8
Не получен
разл. 193
разл.350
п.-116,92, к.-62,47
п. 141, к. 371
п. 136—1370?), разл. > 230
« 300 — As
разм. > 140, возг. 195
п. 278, 223 — p-As2O3
Окраска
т.-кор.
бел.
роз.
роз.
роз.
св.-кор.
роз.
т.-кор.
оранж.
роз.
кор.-черн.
бел.
бцв. ж.
бцв. г.
сер.
черн.
желт.
бел.
бцв. ж.
бцв. ж.
кор. ж.
бцв. ж.
бцв. г.
бел.
бел.
бцв. г.
краен.
т.-краен.
св.-краен.
бел.
бел.
Плот-
Плотность
13,67
1,6290
! 40-186
1,7837
5,727
4,9
2,03
3,54
2,1620
2,7315
7,71
3,5023
4,39
3,74
3,87
77
I. Неорганические вещества
Продолжение табл.
Формула
p-As2O3
As2O5
As(O)F3
AsP
As2S3
As2S5
a-As4S4
P-AS4S4
As2Se3
As2Te3
H3As04
• 0,5H2O
At2
Au
AuIAgI(Te4)
(Au'Ag^Te,
AuBr
AuBr3
[AuBr4],K
•2H2O
Au2C2
AuCN
Au(CNK
•3H2O
[Au(CNJ],K
[Au(CNL],K
• 1,5H2O
AuCl
AuCl3
[AuCl4],Cs
[AuCl4],H
•4H2O
[AuCl4],K
• 0,5H2O
4
197,84
229,84
147,92
105,90
246,04
310,17
427,95
427,95
386,72
532,64
141,94
150,95
419,974
196,967
815,24
775,77
276,87
436,68
555,68
591,71
417,96
222,99
275,02
329,07
288,10
340,14
367,16
232,42
303,33
471,68
339,79
411,85
377,88
386,88
Фазовые переходы
п. 314, к. 461
730 — As2O3
п. -68, к. -26
750 —As
п. 310, к. 708
190 разд., 500 — As2S3
п. 321, к. 534
250 — <x-As4S4
п. 360, к. 861
п. 385, к. 1027
Не получена
п. 35,5, 280 -> As2O5
п. 302, к. 337
п. 1064,18, к. 2856
разл. > 800
разл. > 500
250 — Аи
200 — АиВг
Не получен
разл. 120
разл. > 25
> 200 — Аи
Не получен
50 — Аи
> 250 — Аи
> 250 — Аи
-Н2О 200
289 — Аи
возг. 180, > 200-* AuCl
разл. ~ 460
205 -> AuCl
п. 196(р), -Н2О 100
разл. ~ 350
-Н2О 100
Окраска
бел.
бел.
бцв. г.
краен.
т.-желт.
желт.
краен.-кор.
краен.-кор.
кор.
т.-сер.
бел.
желт.
т.-сер.
т.-сер.
желт.
кор.
краен.
желт.
желт.
бел.
бел.
бел.
бел.
св.-желт.
т.-краен.
желт.
св.-желт.
св.-желт.
желт.
св.-желт.
Плот-
Плотность
4Д5
4,1
6,6
3,43
3,506
3,254
4,75
6,23
2,25
19,31
8,1
8,85
7,9
4,08
7,12
3,45
7,8
4,3
3,9
2,44
3,75
78
I. Неорганические вещества
Продолжение табл.
формула
[AuCl4],NH4
[AuCl4],Na
•2Н2О
Au(Cl)O
AuF3
AuF5
Aul
Aul3
AuNCS
[Au(NO3L],H
•3H2O
Au2O3
n\\2O
[Au(OHL],K
•H2O
AuO(OH)
Au2S
Au2(S2)
Au2S3
[Au(SO3SJ],Na3
•2H2O
Au2(Se04K
AuTe2
В
BAs
(BAs)O4
BBr3
B4C
b,3c2
B(CH3COOK
B(CH3OK
B(C2H5OK
BC13
b2ci4
———
4
356,82
361,77
397,80
248,42
253,96
291,96
323,87
577,68
255,06
445,99
500,04
441,93
—
304,09
322,11
229,97
426,00
458,07
490,13
490,20
526,23
822,80
452,17
10,811
85,73
149,73
250,52
55,26
164,57
187,94
103,91
145,99
117,17
163,43
Фазовые переходы
п. 520
разл.« 250
-Н2О 80 (вак.)
> 290 — Аи
возг. 300, 400—500 -> Аи
п. 75(р), возг. > 80
> 100 ^ Аи
> 20 — Aul
140 — Аи
Не получен
72,5 разл., > 150->Аи
> 160 — Аи
100 — АиО(ОН)
Не получен
> 300 — Аи
~130-*Аи2О3
240 -> Аи
> 140 — Au2S
200 -* Au2S
разл. 300
-Н2О 150
> 700 — Аи
п. 464, > 500 — Аи
п. 2075, к. 4000
п.> 2000
возг. - 700
п. -45,84, к. +89,8
разл. > 2450
п. 2460
п. 149
п. -29, к. +68,7
к. 118,6
п.-107,3, к.+12,6
п. -92,6, разл. +20
Окраска
желт.
желт.
св.-желт.
краен.
оранж.
краен.-кор.
т.-желт.
т.-зел.
бел.
желт.
кор.-черн.
св.-кор.
св.-желт.
св.-кор.
кор.-черн.
т.-кор.
черн.
бел.
бел.
желт.
желт.
сер.-черн.
св.-кор.
бел.
бцв. ж.
черн.
черн.
бел.
бцв. ж.
бцв. ж.
бцв. ж.
бцв. ж.
Плот-
Плотность
6,7
8,25
10,61
9,0
8,75
3,09
9,35
2,34
3,64
2,65°
2,52
2,46
1,343И
79
I. Неорганические вещества
Продолжение табл.
Формула
В4С14
[BD4],Na
BF3
•2Н2О
[BF4],C1F2
[BF4],Cs
[BF4],K
[BF4],NH4
[BF4],Na
[BF4],XeF5
в2н6
B4H10
B5H9
B5H11
B6H10
B6H12
B9H15
B10H14
B16H20
BlgH22
B20H16
[BH4]3,A1
[BH4]2,Be
B3H3CI3N3
[BH4],Cs
[B10H10],Cs2
[B12H12],Cs2
[BH4]4,Hf
[BH4],K
[BH4],Li
[BH4]2,Mg
B3H6N3
[BH4],Na
[BH4]4,Ti
и
185,06
41,86
67,81
103,84
160,25
219,71
125,90
104,84
109,79
313,08
27,67
53,32
63,13
65,14
74,95
76,96
112,42
122,22
193,14
216,77
232,35
71,51
38,70
183,84
147,75
384,00
407,64
237,86
53,94
21,78
53,99
80,50
37,83
107,25
Фазовые переходы
п. 95, разл. 200
п. > 300
п.-128,36, к.-100,3
п. 6,0, разл. > 20
п. 30
п. 555
п. 570, разл. 930
п. 4870?), возг. 350
п. 406, разл. > 450
п. 90
п. -165,5 , к. -92,5
п.-120,8, к.+16,1
п. -46,7, к. +60
п. -122, к. +63
п.-65,1, к.+108
п. -82, к. +80—90
п. 3,0
п. 99,7, к. 213
п. 99
п. 180
п. 197
п. -64,5, к. +44,5
п. 125 разл.
п. 84
п. 660 разл.
разл. 600
разл. > 800
п. 29, к. 118
п. 640 разл.
п. 283 разл.
п. 305 разл.
п. -56,39, к. +55
п. 505 разл.
разл. 25
Окраска
желт.
бел.
бцв. г.
бцв. ж.
бел.
бел.
бел.
бел.
бел.
бел.
бцв. г.
бцв. г.
бцв. ж.
бцв. ж.
бцв. ж.
бцв. ж.
бцв. ж.
бел.
бел.
бел.
бел.
бцв. ж.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бцв. ж.
бел.
зел.
Плот-
Плотность
3,209
1,6320
3,2
2,505
1,871
2,47
1,234
2,379
0,65°
0,69°
0,94
0,54420
0,604
1,58
2,361
1,771
0,681
1,046
0,824°
1,074
80
I. Неорганические вещества
Продолжение табл.
формула
[BH4]4,U
[BH4]2,Zn
[BH4]4,Zr
BI3
B(I)Br2
a-BN
p-BN
[B(NH3)F3]
[BN2],Li3
в2о3
B2O3 (аморфн.)
B(OHK
[B2(O2J(OHL],Na2
•6H2O
BP
(BP)O4
B2S3
[B(SO3FL],K
B3Si
B4Si
B6Si
[BW12O40],H5
• 30H2O
HBO2
Ba
Ba3As2
(BaAs2)O6
Ba2As207
Ba3(As04J
BaB6
BaBr2
•2H2O
Ba(BrO3J
H2O
Mr
297,40
95,08
150,60
391,52
297,52
24,82
24,82
84,84
59,65
69,62
69,62
61,83
199,63
307,72
41,79
105,78
117,82
446,15
60,52
71,33
92,95
2861,89
3402,34
43,82
137,327
561,83
383,17
536,49
689,82
202,19
297,14
333,17
393,13
411,14
Фазовые переходы
разл. 70
разл. 85
п. 28,7, к. 128
п. 49,7, к. 209,5 разл.
к. 125
п. ~ 3000
п. > 3200
п. 162(/?), к. > 125 разл.
п. 870
п. 450, к. 2250
п. 325-450
п. 170,9(р), разл. 107,5
разл. 160
п. 63,5, -Н2О 70
п. 2250, 2400 — В
п. 1600
п.-310
п. 65 разл.
п. - 2500
разл. 1345, > 1350 - B3Si
разл. 1864, > 1870 -^ B3Si
Не получен
п. 48,5, разл. 60
п. 236 разл.
п. 727, к. 1897
п. > 1000,
п. 958 -> Ba2As207
разл. > 1000
п. 1605
п. 2270
п. 847 к. 1980
-Н2О 120
270 — ВаВг2
-Н2О 180
Окраска
зел.
бел.
бел.
бел.
бцв. ж.
бел.
черн.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
св.-кор.
бел.
бел.
бел.
черн.
черн.
черн.
бел.
бел.
бел.
кор.
бел.
бел.
бел.
т.-сер.
бел.
бел.
бел.
бел.
Плот-
Плотность
ЫЗ
3,35
2,29
3,45
1,854
2,46
1,812
1,46
1,731
2,52
1,55
2,52
3,0
2,486
3,51
4,1
5,095
4,36
4,79
3,58
3,99
81
Неорганические вещества
Продолжение табл.
Формула
ВаС2
Ва(СН3СООJ
•ЗН2О
ВаСО3
ВаС2О4
•Н2О
ВаСа(СО3J
ВаС12
•2Н2О
Ba2(Cl)N
Ва(С1ОJ
•2Н2О
Ва(С1О2J
Ва(С1О3J
•Н2О
Ва(СЮ4J
• ЗН2О
ВаСЮ4
ВаСг2О7
•2Н2О
BaF2
ВаН2
BaHAsO4
•Н2О
ВаНРО4
Ва(Н2РО4J
Ba(HSJ
•4Н2О
Ва12
•6Н2О
Ва(Ю3J
•Н2О
ВаМпО4
Ва(МпО4J
Мг
161,35
255,42
309,46
197,34
225,35
243,36
297,42
208,23
244,26
324,11
240,23
276,26
272,23
304,23
322,24
336,23
390,27
253,32
353,31
389,34
175,32
139,34
277,25
295,27
233,31
331,30
203,48
275,54
391,14
499,23
487,13
505,14
256,26
375,20
Фазовые переходы
п. > 1780, разл. 2000
п. 490 разл.
-Н2О 144
п. 15550), > 1000 — ВаО
Не получен
разл. 400
разл. « 1000, > 1000 -» ВаО
п. 961, к. 2047
-Н2О113
п. 965
Не получен
> 185 -> ВаС12
разл. 235
п. 414 разл., > 450 -* ВаС12
-Н2О 120 (вак.), разл. > 250
477 — ВаС12
-Н2О 260
п. 1380, > 1550-ВаО
> 550 -* ВаСгО4
-Н2О 120
п. 1368, к ~ 2250
п. 675 разл., >750 —Ва
900 — Ba2As207
-Н2О 150
> 700 -> Ва2Р2О7
разл. > 340
> 500 — BaS
-Н2О 50 (вак.)
п. 740 разл., >740-* Ва
-Н2О 175
> 400 - Ва12
-Н2О 130
разл. 1000
220 — ВаМпО4
Окраска
сер.-черн.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.-сер.
бел.
бел.
бел.
бел.
бел.
бел.
желт.
краен.
оранж.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
черн.-зел.
черн.-фиол.
Плот-
Плотность
3,895
2,468
2,02
4,25
2,658
3,65
3,856
3,097
3,347
3,18
3,574
2,74
4,498
4,893
4,22
3,93
1,93
4Д7
2,9
5,15
2,6
5,0
4,66
4,85
3,77
82
I. Неорганические вещества
Продолжение табл.
формула
ВаМоО4
Ba(N3J
•6Н2О
Ba3N2
Ba(NCSJ
•ЗН2О
Ba(NH2J
[Ba(NH3N]I2
BaN2O2
•4H2O
Ba(NO2J
•H2O
Ba(NO3J
BaO
BaO2
•8H2O
Ba(O2J
Ba(OHJ
•8H2O
Ba(PH2O2J
H2O
Ba2P2O7
Ba3(PO4J
Ba(ReO4J
BaS
Ba(S2)
Ba(S3)
Ba(S4)
BaSO3
BaSO4
BaS2O6
•2H2O
BaS2O6(O2)
•4H2O
Mr
297,26
221,37
329,46
440,00
253,50
307,54
169,37
493,32
197,34
269,40
229,34
247,35
261,34
153,33
169,33
313,45
201,32
171,34
315,46
267,30
285,32
448,60
601,92
637,73
169,39
201,46
233,53
265,59
217,39
233,39
297,45
333,48
329,45
401,51
Фазовые переходы
п. 1458
> 220 - Ba
120 — Ba
п. - 1000(р), > 500 -* Ba
разл. 400
-Н2О 130
п. 290, разл. 500
разл. > 20
500 — ВаО
-Н2О 100
п. 277, 670 — ВаО
-Н2О115
п. 595 разл., > 620 — ВаО
п. 2017, возг. > 1377
п. 450(/>), > 700 — ВаО
-Н2О 100
разл. 50
п. 408, 800 -> ВаО
п. 78, -Н2О 130
Не получен
разл.« 100
п. 1430, 1500 — Ва3(РО4J
п. 1605
п. 799
п. - 2000 разл., > 2100 -> Ва
п. 925 разл.
п. 554 разл.
разл. 300
разл. 600
п. 1580, 1700 ^ ВаО
> 140 — BaSO4
-Н2О 120
Не получен
разл. 100
Окраска
бел.
бел.
бел..
сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.-зел.
бел.
бел.
бел.
бел.
бел.
•
бел.
бел.
желт.
т.-желт.
св.-краен.
бел.
бел.
бел.
бел.
бел.
Плот-
Плотность
4,95
2,94
4,78
2,268
3,89
2,74
3,23
3,173
3,23
5,72
5,64
2,292
4,5
2,18
2,9
3,9
4,1
5,91
4,25
2,99
4,5
4,536
83
I. Неорганические вещества
Продолжение табл.
Формула
Ba(SO3S)
•Н2О
BaSe
BaSeO4
BaSiO3
(ВаТа2)О6
ВаТе
ВаТеО4
•4Н2О
(BaTi)O3
Ba2V2O7
BaWO4
Ba3Xe06
(BaZr)O3
Be
(ВеА12)О4
(BeAs2)O6
BeBr2
Be2C
[Be(C5H5J]
Be(CH3COOJ
Be4(CH3COONO
BeCO3
•4H2O
[Be(C2O4J],Be
•3H2O
BeCl2
•4H2O
Be(C104J
•4H2O
Be4(C104N0
BeF2
[BeF4],K2
4
249,46
267,47
216,29
280,28
213,41
595,22
264,93
328,92
400,98
233,20
488,53
385,16
639,27
276,55
9,012
126,97
254,85
168,82
30,04
139,20
127,10
406,31
69,02
357,26
194,06
248,11
79,92
151,98
207,91
279,97
648,74
47,01
163,20
Фазовые переходы
He получен
разл.100
п.1780
разл.« 1500
п.> 1600
п. 1410
п. 1510
разл.-1700
-Н2О 400
п. 1616
п. 863
п. 1475, к. 1730
разл. 250
п. - 2690
п. 1287, к. 2471
п. 1870
разл. 574
п. 488, к. 540
п. 2400, > 2500 -> Be
возг. > 45
п. 295 разл.
п. 284, к. 331
> 180 - ВеО
-Н2О 100 (вак.)
350 — ВеО
-Н2О 220
п. 416, к. 550
п. 96, разл. > 176
Не получен
разл. 250
п. 165
п. 803, к. 1175
п. 791
Окраска
бел.
бел.
бел.
бел.
бел.
св.-желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
сер.
желт.-зел.
бел.
бел.
св.-красн.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
Плот-
Плотность
3,45
5,02
4,61
4,4
5,13
4,48
6,08
5,04
1,848
3,76
3,47
2,44
1,9
1,986
84
I. Неорганические вещества
Продолжение табл.
Формула
[BeF4],Li2
[BeF4],(NH4J
[BeF4],Na2
ВеН2
Ве4(НСООNО
Bel2
Be3N2
BeNH4As04
[Be(NH3L]Cl2
BeNH4PO4
Be(NO3J
•4H2O
Be4(NO3NO
BeO
Be(OHJ
BeS
BeSO4
•4H2O
BeSe
BeSeO4
•4H2O
Be2Si04
BeTe
Bi
BiAsO4
(В1«1В^О4
•2H2O
BiBr3
Bi(Br)O
Bi2(C2O4K
•7H2O
Bi2CO3(OHL
BiCl3
H2O
MT
98,89
121,08
130,98
11,03
322,15
262,82
55,05
165,97
148,04
122,02
133,02
205,08
424,07
25,01
43,03
41,08
105,07
177,13
87,97
151,97
224,03
110,11
136,31
208,980
347,90
481,96
517,99
448,69
304,88
682,01
808,12
546,00
315,34
333,35
Фазовые переходы
п. 459,1
п. 230 разл., 800 ^BeF2
п.~ 590
> 100 — Be
возг. 247 (вак.)
п. 510, к. 530
п.« 2200 разл.
разл. 400 *
разл. > 200
разл. 700
разл. 125 (вак.), > 300 — ВеО
п. 60, разл. 100
возг. 125
п. 2578, к. 4260
> 200 — ВеО
разл. 1800
п. 540, 600^ ВеО
-Н2О > 220
п.« 1000
730 — ВеО
-Н2О213
п. 1560
п.« 1200
п. 271,44, к. 1564
п. 1150 разл.
п. 305, 550 -> Bi2O3
-Н2О180
п. 219, к. 461
разл. 560
800 — Bi2O3
-Н2О 150
380 — Bi2O3
п. 234, к. 440
280 — Bi(Cl)O
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
св.-сер.
бел.
бел.
св.-сер.
бел.
бел.
бел.
св.-сер.
св.-сер.
бел.
бур.
т.-краен.
желт.
бел.
бел.
бел.
бел.
бел.
бел.
Плот-
Плотность
0,8
4,325
2,72
3,03
1,92
2,36
2,433
1,713
4,32
2,03
2,98
5,09
9,79
7,142
5,6
5,72
8,106
6,86
4,75
85
I. Неорганические вещества
Продолжение табл.
Формула
^24^28
Bi(Cl)O
BiC104@HJ
BiF3
BiF5
Bil3
Bi(I)O
Bi2(MoO4K
Bi(NO3K
•5H2O
BiNO3(OHJ
BiO
Bi2O3
Bi2O5
Bi(O)F
Bi(OHK
BiO(OH)
BiPO4
Bi2S3
Bi2(SO4K
Bi2Se3
Bi4(Si04K
Bi2Te3
Bk
BkO2
Br2
[BrAg2]NO3
[Br(Br)Cl],Cs
[Br(BrJ],Cs
BrCl
[Br(ClJ],Cs
BrF
BrF3
Mr
6008,20
260,43
342,44
265,97
303,97
589,69
351,88
897,77
394,99
485,07
305,00
224,98
465,96
497,96
243,98
260,00
241,99
303,95
514,16
706,15
654,84
1112,17
800,76
247,070
279,07
159,808
357,64
328,17
372,62
115,36
283,72
98,90
136,90
Фазовые переходы
п. 163, разл. 320
п. 232,5, разл. 575
разл. > 100
п. 757, к. 900
п. 151, к. 230
п. 407,7, к. 542 разл.
разл. 300
п. 643
700 — Bi2O3
п. 75,5, 110^BiNO3(OHJ
260 - Bi2O3
п. 902, к. 1647
п. 825, к. 1890
> 350 -> (BimBiv)O4
разл. > 1000
100 -> ВЮ(ОН)
п.415,600-В12О3
разл. > 1300
п. 775(р), разл. >685
п. 7100?), разл. > 400
п. 706, к. 1007
п. 1020
п. 585, к. 1172
п. - 1050, к. - 2630
разл. 500
п. -7,25, к. +58,78
п. 182, разл. > 250
п. 1910)
п. 180, разл. >220
п. —66, к. —5 разл.
п. 2050?), разл. 150
п.-33, к. +20 разл.
п. 8,77, к. 125,75
Окраска
черн.-бур.
бел.
бел.
бел.
бел.
т.-краен.
т.-оранж.
желт.
бел.
бел.
бел.
черн.
желт.
т.-краен.
бел.
бел.
бел.
бел.
сер.
бел.
т.-сер.
бел.
черн.
бел.
желт.
т.-краен, ж.
бел.
св.-красн.
т.-желт.
желт. г.
желт.
краен, ж.
св.-желт. ж.
Плот-
Плотность
7,76
7,927
5,4
5,64
8,013
6,07
2,83
4,93
7,175
8,9
5,1
7,5
4,36
6,32
7,39
5,08
7,4
7,859
14,78
3,11920
2,8439
86
I. Неорганические вещества
Продолжение табл.
формула
BrF5
[BrF4],K
BrNO3
Br(NO3K
Вг2О
Br2O4
Br(O)F3
BrO2F
BrO3F
[Br(OJ(FJ],K
HBr
a-C
p-c
CBr4
CC14
(CC1+)C1O4
CC12F2
CC12O
CF4
(CF^CIO
(CF3f)C104
CH4
с2н2
C2H4
с6н6
CH3C(H)O
CH3CN
CH3COOH
CHC13
C2H8N2
C5H5N
CH3OH
Mr
174,89
194,99
141,91
265,92
175,81
223,80
152,90
130,90
146,90
189,00
80,91
12,011
12,011
331,63
153,82
217,82
120,91
98,92
88,00
120,46
168,45
16,04
26,04
28,05
78,11
44,05
41,05
60,05
119,38
60,10
79,10
32,04
Фазовые переходы
п. -60,5, к. +40,76
п. 330, разл. >350
п. —42, разл. > 0
п. 48 разл.
п. -17@
разл. -40 (вак.),
-39 - Вг2О
п. « 0, > 19,5 — BrF3
п. -9, > 52 — BrF3, Br2
п.-110,35, к.+2,35
разл. 87
п.-86,91, к.-66,77
возг. 3652
1800 — а-С
п. 92,5, к. 189,5 разл.
п. -22,96, к. +76,75
п.-55
п. -158,2, к. -29,8
п.-118,8, к.+7,56
п.-183,6, к.-128
п.-142, к.-46
п.+10, разл. > 100
п.-182,5, к.-161,6
возг. —83,6
п.-169,15, к.-103,7
п. 5,51, к. 80,1
п.-123,5, к.+20,2
п.-45,72, к.+81,6
п. 16,75, к. 118,1
п.-63,5, к.+61,1
п. 8,5, к. 117
п.-41,7, к.+115,2
п. -93,9, к. +64,96
Окраска
бцв. ж.
бел.
желт. ж.
бел.
бур. ж.
св.-желт.
бцв. ж.
бцв. ж.
бцв. г.
бел.
бцв. г.
черн.
бел.
св.-желт.
бцв. ж.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бцв. ж.
бцв. ж.
бцв. ж.
бцв. ж.
бцв. ж.
бцв. ж.
бцв. ж.
бцв. ж.
Плот-
Плотность
2,57°
6,554
3,6445
2,25
3,515
3,42
1,59420
5,394
4,413
3,94
0,7168
1,1716
1,245
0,87920
0,78820
0,78420
1,04920
1,48320
0,90120
0,98420
0,79120
87
I. Неорганические вещества
Продолжение табл.
Формула
С2Н5ОН
С14
C2N2
C6N6
(CN)Br
(CN)C1
(CN)F
C(NH2JO
(CN)I
CO
CO2
C(O)F2
CS2
C3S2
C(S)C12
CS(NH2J
C(S)O
CSe2
CSe(NH2J
C(Se)O
C(Se)S
C(Te)S
HCN
H2CN2
H2C2O4
• 2H2O
HCOOH
H2CS3
Ca
(CaAl2)O4
Ca3As2
Ca(AsO2J
(CaAs2)O6
Mr
46,07
519,63
52,04
156,11
105,92
61,47
45,02
60,06
152,92
28,01
44,01
66,01
76,14
100,17
114,98
76,12
60,08
169,93
123,02
106,97
123,04
171,68
27,03
42,04
90,03
126,06
46,03
110,23
40,078
158,04
270,08
253,92
285,92
Фазовые переходы
п.-114,15, к.+78,39
п. 171 разл., > 172 — сс-С
п.-27,83, к.-21,15
п. 119, к. 262
п. 51,3, к. 61,3
п.-6,9, к.+12,66
п. -82, к. -46
п. 132,7, разл. > 240
п. 146(/?), возг. > 45
п.-205,02, к.-191,5
возг. -78,476
п.-114, к.-83,1
п.-111,9, к.+46,24
п. —1, разл. 90
к. 73,5
п. 182, разл. « 210
п. -138,82, к. -50,24
п.-43,7, к.+125
п. 202 разл.
п.-124,4, к.-21,7
п. -85, к. +84,5
п. -54, разл. >20
п. -13,3, к. +25,65
п. 46 разл., к. 140 (вак.)
п. 189,5, возг. 125
п. 101,5,-Н2О 120 (вак.)
п. 8,3, к. 100,8
п. -26,9, > 0 — CS2
п. 842, к. 1484
п. 1602 разл.
разл. > 1300
разл. 500
разл. 821
Окраска
бцв. ж.
краен.
бцв. г.
бел.
бел.
бцв. г.
бцв. г.
бел.
бел.
бцв. г.
бцв. г.
бцв. г.
бцв. ж.
краен, ж.
краен, ж.
бел.
бцв. г.
желт. ж.
бел.
бцв. г.
желт. ж.
краен, ж.
бцв. ж.
бел.
бел.
бел.
бцв. ж.
краен, ж.
бел.
бел.
краен.
бел.
бел.
Плот-
Плотность
0,78920
4,34
2,335
2,015
1,222
2,01
1,335
2,84
1,25
1,9768
2,95
1,26122
1,2720
1,50915
1,405
2,68
2,68220
1,9920
0,69922
1,0729
1,653
1,2220
1,48°
1,54
2,981
3,03
I. Неорганические вещества
Продолжение табл.
формула
Ca3(As04J
5Н2О
СаВ6
Са(ВО2J
•2Н2О
•6Н2О
Са2В2О5
Са3(ВО3J
СаВг2
•6Н2О
Са(ВгО3J
•Н2О
СаС2
Са(СН3СООJ
•Н2О
CaCN2
Ca(CNJ
СаСО3
СаС2О4
Н2О
СаС12
Н2О
•2Н2О
•4Н2О
•6Н2О
Са(С1ОJ
•зн2о
Са(С1О2J
Са(С1О3J
•2Н2О
Са(СЮ4J
•4Н2О
СаСгО4
•2Н2О
Ч
398,07
488,15
104,94
125,70
161,73
233,79
181,77
237,85
199,89
307,98
295,88
313,90
64,10
158,17
176,16
80,10
92,11
100,09
128,10
146,11
110,98
129,00
147,01
183,04
219,07
142,98
197,03
174,98
206,98
243,01
238,98
311,04
156,07
192,10
Фазовые переходы
п. 1500
-Н2О310
п.2230
п.1154
-Н2О 400
-4Н2О 500
п. 1298
п. 1479
п. 742, к. 1827
п. 38,2, -Н2О 180
> 200 — СаВг2
-Н2О 180
п. 2300, разл. 2400
разл. > 350
-Н2О 100
п. 1300(/>), разл. > 1150
п. 640
п. 1327(р), 1150 ^СаО
> 400 - СаСО3
-Н2О 200
п. 775, к. 1957
-Н2О 250
-1Н2О 175,9
-2Н2О45,1
п. 29,92, -2Н2О 30,9
180 -> СаС12
п. 86(р), -Н2О < 50
разл. 450
разл. 340
п. 76, -Н2О110
477 — СаС12
п. 75,4, -Н2О 120 (вак.)
п. 1150(р), 1022 — (СаСг2)О4
-Н2О > 200
Окраска
бел.
бел.
черн.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.
желт.
Плот-
Плотность
2,7
2,33
2,696
1,88
1,87
2,58
3,46
3,353
2,30
3,329
2,204
2,2
2,72
2,2
2,512
2,15
1,68
2,35
2,1
2,71
2,711
2,651
3,12
I. Неорганические вещества
Продолжение табл.
Формула
(СаСг2)О4
CaF2
(CaFe2)O4
СаН2
Са(НСООJ
СаНРО4
•2Н2О
Са(Н2РО4J
•Н2О
Ca(HSJ
•6Н2О
Са12
•6Н2О
Са(Ю3J
CaMg(CO3J
CaMgSiO4
CaMg(SiO3J
Ca(MnO4J
CaMoO4
Ca(N3J
Ca3N2
CaNH4As04
•6H2O
[Ca(NH3N]I2
Ca(NO2J
• 4H2O
Ca(NO3J
•4H2O
CaO
CaO2
•8H2O
Ca(OHJ
Ca3P2
4
208,07
78,07
215,77
42,09
130,11
136,06
172,09
234,05
252,07
106,23
214,32
293,89
401,98
389,88
184,40
156,47
216,55
277,95
200,01
124,12
148,25
197,04
305,13
396,07
132,09
204,15
164,09
236,15
56,08
72,08
216,20
74,09
182,18
Фазовые переходы
п. 2170
п. 1418, к. «2530
п. 1220
п. 815, >1000-Са
разл. 400—495
> 900 — Са2Р2О7
-Н2О 109 (вак.), > 360 —
Са2Р2О7
п. 150—200 разл.
-Н2О 109
Не получен
п. > 20 разл., -Н2О400
п. 783, к. 1757
-Н2О 40 (вак.)
разл. 540, > 540 — Са12
750 — СаО
п.« 1500
п. 1392
разл.« 200
п. 1449
разл. 160
п. 1195
Не получен
разл. 140
разл. 96
п. 220 разл., 600^ СаО
-Н2О 100
п. 561(/>),450 — Ca(NO2J
п. 42,7, -Н2О 100
п. 2627, к. 2850
430 — СаО
-Н2О130(вак.)
580 — СаО
п. - 1600(р), > 1250 — Са
Окраска
т.-зел.
бел.
т.-краен.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
св.-желт.
бел.
бел.
бел.
бел.
т.-красн.
бел.
бел.
т.-бур.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
краен.-кор.
Плот-
Плотность
4,98
3,181
5,08
1,9
2,02
2,89
2,306
2,22
3,956
2,55
4,519
2,86
3,2
3,28
2,4
4,25
2,63
1,91
2,23
1,674
2,36
1,86
3,37
3,18
1,7
2,34
2,51
90
I. Неорганические вещества
Продолжение табл.
формула
Са(РН2О2J
Са(РО3J
Са2Р2О7
•5Н2О
Са3(РО4J
Ca(PO3F)
•2Н2О
Ca5(PO4KF
CaS
CaSO3
•2Н2О
CaSO4
• 0,5Н2О
• 2Н2О
Ca(SO3S)
•6Н2О
CaSe
CaSeO4
•2Н2О
CaSi
CaSi2
CaSiO3
Ca2Si04
Ca3Si05
Ca3Si207
(CaTa2)O6
CaTe
CaTeO3
CaTeO4
(CaTi)O3
Ca(VO3J
Ca2V2o7
Ca3(VO4J
CaWO4
Mr
170,05
198,02
254,10
344,17
310,17
138,05
174,08
504,30
72,14
120,14
156,17
136,14
145,15
172,17
152,21
260,30
119,04
183,03
219,06
68,16
96,25
116,16
172,24
228,32
288,40
497,97
167,68
215,68
231,67
135,96
237,96
294,03
350,11
287,91
Фазовые переходы
разл. > 200
п. 984
п. 1355, разл. 1500
-Н2О = 300
п.1777
разл. 400
-Н2О 170
разл.« 1800
п. 2525, > 2600 — Са
> 550 -* СаО
-Н2О 100
п. 1460(/>), > 960 -> СаО
-Н2О 163-200
-1,5Н2О 128
Не получен
п. « 40, разл. « 250
п. « 1400 разл., > 1400 -> Са
разл. - 1350
-Н2О~150
п. 1245
п. * 1000 — CaSi
п.1544
п. 2130
п. 2070 разл.
п.« 1450
п. 1958
разл.« 1600
разл. > 960
п.« 1000
п. 1980
п. 775 разл.
п. 1015 разл.
п. 1400 разл.
п.1580
Окраска
св.-сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
сер.
т.-сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
св.-желт.
желт.
желт.
бел.
Плот-
Плотность
2,82
3,09
2,25
3,067
3,2
2,18
2,98
2,7
2,3
1,872
3,82
2,93
2,68
2,5
2,915
3,13
3,25
2,96
7,59
4,02
3,59
3,36
3,17
6,12
91
I. Неорганические вещества
Продолжение табл. ;
Формула
(CaZr)O3
Cd
CdAs2
Cd3As2
CdBr2
•4H2O
Cd(CH3COOJ
•2H2O
Cd(CNJ
[Cd(CNL],K2
CdCO3
CdC2O4
CdCl2
• 2,5H2O
Cd(C103J
•2H2O
CdF2
•2H2O
Cd(H2PO4J
•2H2O
Cdl2
Cd(IO3J
Cd(MnO4J
•6H2O
CdMoO4
Cd(NH2J
Cd(NH4J(SO4J
• 6H2O
Cd(NO3J
•4H2O
CdO
Cd(OHJ
Cd3P2
4
179,30
112,411
262,26
487,08
272,22
344,28
230,50
266,53
164,45
294,68
172,42
200,43
183,32
228,35
279,31
315,34
150,41
186,44
306,38
342,41
366,22
462,21
350,28
458,37
272,35
144,46
340,61
448,70
236,42
308,48
128,41
146,43
399,18
Фазовые переходы
п. - 2350
п. 320,9, к. 765
п. 621
п. 721
п. 568, к. 865
-Н2О 125
п. 256 разл.
-Н2О 130
разл. > 200
п. « 450
> 300 — CdO
разл. 340
п. 568,5, к. 964
-Н2О 170
Не получен
п. 80
п. 1072, к.1753
-Н2О 40 (вак.)
Не получен
разл. > 100
п. 388, к. 744
разл. 800
Не получен
разл. > 95
п. - 1600
разл. 120
разл. > 650
-Н2О 100
п. 353 разл., > 400 — CdO
п. 59,4, -Н2О 132 (вак.)
возг. 1570
> 170 — CdO
п. 739, разл. > 750
Окраска
бел.
бел.
сер.
т.-сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
фиол.
бел.
бел.
бел.
бел.
бел.
бел.
кор.
бел.
сер.-зел.
Плот-
Плотность
4,78
8,642
5,64
6,21
5,196
2,341
2,01
2,23
1,85
5,02
3,32
4,047
3,327
2,28
6,33
2,74
5,67
6,43
2,81
5,35
3,05
2,06
2,455
8,15
4,81
5,6
92
I. Неорганические вещества
Продолжение табл.
.— —¦
формула
Cd2P2O7
•2Н2О
CdS
CdSO4
• 2,67H2O
CdSb
CdSe
CdSeO4
•2H2O
CdSiO3
Cd2Si04
CdTe
Ce
CeB6
CeBr3
CeC2
Ce2(C2O4K
• 10H2O
CeCl3
•7H2O
(СешСг)О3
CeF3
CeF4
•7H2O
CeH3_x
@<jc<0,2)
Cel3
ce2(MoO4K
ceNH4(SO4J
•4H2O
Ce(NO3K
•6H2O
1Се^°зN], (NH4J
——
Mr
398,76
434,79
144,48
208,47
256,57
234,17
191,37
255,37
291,40
188,49
316,90
240,01
140,115
204,98
379,83
164,14
544,28
724,43
246,47
372,58
240,11
197,11
216,11
342,21
143,14
520,83
760,04
350,28
422,34
326,13
434,22
548,22
Фазовые переходы
п. 900
-H2O - 200
п. 1475
п. 1135(^), 1300 — CdO
-Н2О 200
п. 456
п. 1263
« 1200 - CdO
-Н2О 170
п. 1242
п.1252
п. 1092
п. 799, к. 3424
п. 2190 разл., > 2200 -* Се
п. 732, к. 1560
п. 2290
Не получен
разл. > 500
п. 848, к. 1650
-Н2О 400
п. 2300
п. 1430, к. 2180
возг. > 700
390 - CeF3
разл. 600—800
п. 755, к. 1400
п. 973
600 — СеО2
-Н2О 150
700 - СеО2
п. 39, -Н2О 40 (вак.)
разл. 180—280
Окраска
бел.
бел.
желт.
бел.
бел.
сер.
т.-краен.
бел.
бел.
бел.
бел.
т.-бур.
сер.
св.-син.
бел.
краен.
бел.
бел.
бел.
т.-зел.
бел.
бел.
бел.
т.-сер.
желт.
желт.
бел.
бел.
бел.
бел.
св.-краен.
Плот-
Плотность
4,97
4,824
4,691
3,084
6,66
5,81
3,63
4,93
5,86
6,77
5,6
3,97
3,92
6,84
6,16
4,77
4,76
5,5
4,83
2,52
93
I. Неорганические вещества
Продолжение табл.
Формула
Ce(NO3KOH
•ЗН2О
СеО2
Се2О3
Се(ОНK
СеРО4
Ce2S3
Ce(SO4J
•8Н2О
Ce2(S)O2
Ce2(SO4K
•8Н2О
Ce2(SeO4K
Ce2(WO4K
Cf
CfBr3
CfCl3
CfO2
Cf2O3
Cl2
• 5,75H2O
[ClAg2]NO3
C1F
C1F5
C12F6
[C1F4],(NO)+
C1N3
C13N
C1O2
C12O
C12O6
Mr
343,13
397,18
172,11
328,23
191,14
235,09
376,43
332,24
476,36
344,29
568,42
712,54
709,10
1023,74
251,080
490,79
357,44
283,08
550,16
70,906
174,49
313,19
54,45
130,44
184,89
141,45
77,47
120,37
67,45
86,91
166,90
Фазовые переходы
He получен
200-550 -> CeO2
п. 2400
п. 2180
> 400 — Ce2O3
п. - 2000
п. 1890
> 300 — Ce2(SO4K
-Н2О 195
п.« 1950
850 — СеО2
-Н2О > 300
разл. > 650
п.1079
п. 900, к. 1227
п. 700
п. 545
разл. > 400
п. 1750
п. -101,5, к. -34,04
п. 9,6 разл., -Н2О> 10
п. 160
п.-155,65, к.-100,15
п.-103, к.-13,1
п.-76,31, к.+11,76
п. -25 разл., -24 -¦ C12F6
п.-100, к.-15
п. -27, к. +71
п. -59, к. +9,7
п.-120,6, к.+2
п. +3, разл. > 20
Окраска
краен.
св.-желт.
желт.
бел.
т.-желт.
т.-фиол.
т.-желт.
желт.
кор.-черн.
бел.
бел.
бел.
желт.
бел.
зел.
желт.
черн.
бел.
желт.-зел. г.
бцв. ж.
бел.
желт.
бел.
бцв. г.
бцв. г.
зел. ж.
бел.
бцв. г.
желт. ж.
желт. г.
оранж. г.
краен, ж.
Плот-
Плотность
7,132
6,86
5,22
5,18
3,01
5,99
3,912
2,886
4,46
6,77
3,214
1,565
1,9
1,29
1,86610
1,6520
3,214
3,89
2,0234
94
I. Неорганические вещества
Продолжение табл.
формула
С12О7
(CIOJ)CIO
C1(O)F3
C1O2F
C1O2F3
CIO3F
CKSO3F)
HC1
НСЮ4
•H2O
Cm
Cm2(C2O4K
• 10H2O
CmF3
CmO2
Cm2O3
Co
(CoAl2)O4
CoAs
CoAs2
CoAs3-*
Co2As
Co3(AsO4J
•8H2O
Co(As)S
CoB
Co2B
Co3B
CoBr2
•6H2O
Co2C
[Co(C5H5J]
C°(CH3COOJ
•4H2O
4
182,90
134,90
108,45
86,45
124,45
102,45
134,51
36,46
100,46
118,47
247,070
758,19
938,34
304,06
279,07
542,14
58,933
176,89
133,86
208,78
283,70
192,79
454,64
598,76
165,92
69,74
128,68
187,61
218,74
326,83
129,88
189,12
177,02
249,08
Фазовые переходы
п. -93,4, к. +87
п.-117, к.+44,5
п. -42, к. +29
п.-115, к.-6
п.-81, к.-22
п. -146, к. -46,7
п. —84,3, к. +43,4 разл.
п.-114,0, к.-85,08
п.-101, к. +106 разл.
п. 49,9, -Н2О 50
п. 1345, к. * 3200
Не получен
разл. ~ 360
п. 1410
> 380 — Ст2О3
п.« 2270
п. 1495, к. 2927
п. 1960
п. 1180
850 — Co2As
800 — CoAs2
958 -* CoAs, Co
разл. 1000
-Н2О 400
разл. 1000
п. 1460
п. 1280
п. 1180
п. 678, к. 927
п. 43,6, -Н2О 130-140
разл. 3000
п. 174
разл. 250
-Н2О 140
Окраска
бцв. ж.
св.-желт. ж.
бцв. ж.
бцв. г.
бцв. г.
бцв. г.
св.-желт. ж.
бцв. г.
бцв. ж.
бел.
бел.
бел.
бел.
черн.
т.-зел.
сер.
син.
бел.
бел.
бел.
сер.
роз.
св.-роз.
св.-краен.
сер.
сер.
сер.
зел.
фиол.
сер.
фиол.
св.-роз.
краен.
Плот-
Плотность
1,80525
1,82°
1,7120
1,6391
ljei20
13,51
9,7
8,9
4,37
7,4
6,5
8,28
3,178
2,948
6,33
4,909
2,46
1,72
95
I. Неорганические вещества
Продолжение табл.
Формула
Со(СН3СООK
[Co(C2H8N2K]Br3
•ЗН2О
[Со(С5Н5J]ОН
[Con(CNN),Co2
•7Н2О
[Co(CNN],K3
[Co(CNN],K4
СоСО3
•6Н2О
СоС2О4
•2Н2О
[Со2(СО)8]
[Со4(СОI2]
[Со(СОJС5Н5]
СоС12
Н2О
•2Н2О
•6Н2О
Со(С1О3J
•6Н2О
Со(С1О4J
•6Н2О
(СопСо2п)О4
(CoIICo2II)S4
(СоиСо2п)Те4
CoF2
•4Н2О
CoF3
• 3,5Н2О
[СоН(СОL]
Со(НСООJ
•2Н2О
Ч
236,07
478,95
532,99
206,13
332,91
459,01
332,34
371,43
118,94
227,03
146,95
182,98
341,95
571,85
180,05
129,84
147,85
165,87
237,93
225,83
333,92
257,83
365,92
240,80
305,06
687,20
96,93
168,99
115,93
178,98
171,98
148,97
185,00
Фазовые переходы
разл. 100
разл. > 400
п. 271
разл. 350
разл. 450
-Н2О > 280
разл. > 250
разл. 300
350 -> СоО
-Н2О 140
Не получен
разл. 175
п. 51 разл.
п. 60, разл. 300
п.-22, к.+139,5
п. 740, к. 1049
п. 335(/?),-Н2О110
п. 206(/?),-1Н2О90
п. 51,2(/?),-4Н2О60
Не получен
п. 50, разл. 100
450 — СоС12
п. 170, -Н2О 220
> 900 -> СоО
п. 625, > 680 — CoS
п. 1010
п. 1127, к. 1740
-Н2О 300
> 350 — CoF2
-Н2О 225 (вак.)
п. -20, к. +10 разл.
разл. 175
-Н2О 140
Окраска
св.-зел.
желт.
св.-желт.
желт.
фиол.
т.-роз.
св.-желт.
св.-кор.
краен.
роз.
роз.-краен.
оранж.
черн.
т.-красн. ж.
гол.
син.-фиол.
фиол.
роз.
краен.
краен.
св.-красн.
черн.-сер.
т.-сер.
черн.-сер.
роз.
роз.
св.-кор.
зел.
желт. ж.
краен.
краен.
Плот-
Плотность
1,85
1,87
1,88
2,04
4,13
3,021
1,73
3,356
1,92
1,92
3,33
6,073
4,86
4,46
2,19
3,89
2,31
2,13
96
I. Неорганические вещества
Продолжение табл.
формула
Col2
•6Н2О
Со(Ю3J
•6Н2О
Co2N
Co(NCSJ
•ЗН2О
Co(NH2K
[Co(NH3N]Br2
[Co(NH3N]Cl2
[Co(NH3N]Cl3
[Co(NH3LCl2]Cl
•H2O
[Co(NH3MCl]Cl2
[Co(NH3N]I2
[Co(NH3N]I3
[Co(NH3K(NO2K]
[Co(NH3N](NO3K
[Co(NH3MNO2]Cl2
Co(NH4J(SO4J
•6H2O
Ico(NH3N]2(SO4K
•5H2O
Co(NO3J
•6H2O
[Co(NOK]
Co(NO3K
[Co(NO+)(COK]
[C°(NO2N],K3
[C°(NO2N],K2Na
H2O
-—-
4
312,74
420,83
408,74
516,83
131,87
175,10
229,15
107,00
320,93
232,03
267,48
233,42
251,43
250,45
414,93
541,83
248,04
347,13
261,00
228,20
395,23
610,42
700,50
182,94
291,03
148,95
244,95
172,97
452,26
436,15
454,16
403,93
Фазовые переходы
п. 516, к. 760
п. 27, -Н2О 130
разл. 200
п.61,-Н2О75(вак.)
> 250 - Со
разл. > 275
-Н2О 105
169 (вак.) — Co2N
разл. 250
> 150 — СоС12
> 420 — СоС12
> 360 -> СоС12
-Н2О 100
> 450 — СоС12
разл. > 120
разл. < 100
150-^Со2О3
разл. > 100
разл. > 210
разл.« 200
-Н2О 80
разл. > 375
-Н2О 150
1000 — СоО
п. 55, >180-(СоиСо2п)О4
разл. 100
возг. 40 (вак.), разл. > 60
п. -1,к. +78,5 разл.
> 200 — СоО
Не получен
п. 135
250 — СоО
Окраска
кор.-красн.
т.-краен.
фиол.-гол.
краен.
сер.-черн.
краен.-
фиол.
краен.
кор.
т.-роз.
св.-краен.
т.-бур.
зел.
зел.
т.-краен.
роз.
т.-краен.
желт.
желт.
желт.-кор.
гол.-фиол.
краен.
т.-желт.
желт.
роз.
роз.
черн.
желт.
т.-краен, ж.
желт.
желт.
желт.
Плот-
Плотность
5,68 .
2,9
5,01
3,69
6,4
1,87
1,479
1,7016
1,86
1,847
1,783
2,1
2,75
1,99
1,8
1,8
1,9
1,8
1,89
2,64
1,63
97
4 - 2004
I. Неорганические вещества
Продолжение табл.
Формула
Со,_хО
Со2О3
•лН2О
Со(ОНJ
СоО(ОН)
•Н2О
СоР
Со2Р
Со3(РО4J
•8Н2О
Co1+xS
(х = 0,04-0,12)
Co(S2)
Co9S8
COSO4
•Н2О
•6Н2О
•7Н2О
Co2(SO4K
• 18Н2О
CoSb
CoSb2
CoSb3
CoSe
Co(Se2)
CoSeO4
•7H2O
CoSi
CoSi2
Co2Si
CoSiO3
Co2SiO4
Co(Te2)
4
74,93
165,86
—
92,95
91,94
109,95
89,91
148,84
366,74
510,86
91,00
123,07
786,93
155,00
173,01
263,09
281,10
406,05
730,32
180,69
302,45
424,20
137,89
216,85
201,89
327,99
87,02
115,11
145,95
135,02
209,95
314,13
Фазовые переходы
п. 18100?),
>390-(Со11Со2и)О4
>400-(СопСо2и)О4
250 — СоО(ОН)
> 170 — СоО
600-(СоиСо^)О4
-Н2О 100
п.1520
п.1386
п.1160
-Н2О 200
п. 1180, > 1220 — Со
п. 953 разд., > 953 — CoS
п. 835, > 835 — CoS
>6W->(CoIICo?1I)O4
-Н2О 250-420
-5Н2О71
-1Н2О 41-43
Не получен
разл. > 30
п. 1202
п. 919 разд., >920 — CoSb
п. 859 разд., > 860 ¦— CoSb2
п. 1055
п. 960 разл., > 960 — CoSe
Не получен
разл. > 500
п. 1395
п.1327
п.1332
разл. > 1000
п. 1415
п. 749 разл.
Окраска
т.-зел.
черн.
т.-кор.
фиол.
сер.-черн.
сер.-черн.
фиол.
роз.
бел.
сер.-черн.
черн.
роз.
роз.
краен.
краен.
гол.-зел.
сер.
т.-сер.
черн.-сер.
св.-фиол.
черн.
краен.
краен.
т.-син.
сер.
св.-фиол.
фиол.
сер.-черн.
Плот-
Плотность
6,47
5,18
3,597
4,72
4,29
7,4
6,4
2,584
2,77
5,45
4,73
5,24
3,71
3,075
2,029
1,948
8,82
8,24
7,62
7,65
2,14
6,6
5,3
7,28
4,63
I. Неорганические вещества
Продолжение табл.
формула
Сг
СгВ
СгВ2
Сг2В
СгВг2
СгВг3
•6Н2О
Сг3С2
[Сг(С5Н5J]
[Сг(С6Н6J]
[Cr(CNN],K3
[Сг(СОN]
СгС12
•2Н2О
•4Н2О
СгС13
•ЗН2О
•6Н2О
Сг(С1)О
СгС12О2
СгС13О
CrF2
CrF3
CrF4
CrF5
CrF6
(Cr2"Fe)O4
[Cr(H2OLCl2)Cl
•2H2O
[Cr(H2OMCl]Cl2
H2O
Crl2
Crl3
•9H2O
Mr
51,996
62,81
73,62
114,80
211,80
291,71
399,80
180,01
182,19
208,22
325,40
220,06
122,90
158,93
194,96
158,36
212,40
266,45
103,45
154,90
174,35
89,99
108,99
127,99
146,99
165,98
223,84
230,42
266,45
248,43
266,45
305,81
432,71
594,84
Фазовые переходы
п. 1906, к. 2671
п. 2090
п. 2200
п.1870
п. 842
возг. 800
разл. > 500
п. 1895
п. 173,5
п. 284, > 300 — Сг
разл. > 150
п. 153(/>),230-Сг
п. 824, к. 1330
-Н2О113
-2Н2О 70 (вак.)
п. 1152, разл. 1330
разл. > 200
п. 95, 650 -» Сг2О3
800 — СгС13, Сг2О3
п.-96, к.+116
разл. > 60
п. 894, к. 1820
п. 1100, к. 1400
п. 277(р), возг. 295
п. 102, к. 117
разл. 100 (вак.)
п. 2153
650 — Сг2О3
п. 83,-Н2О110
Не получен
разл. > 50
п. 856, к. 1248
п. 857, > 670 — Crl2
разл. 350
Окраска
сер.
сер.
сер.
черк.
бел.
зел.-черн.
фиол.
сер.-черн.
краен.
кор.-черн.
св.-желт.
бел.
бел.
св.-зел.
т.-гол.
св.-фиол.
кор.
сер.-гол.
фиол.-зел.
т.-краен, ж.
т.-краен.
син.-зел.
зел.
кор.
краен.
т.-желт.
т.-кор.
т.-зел.
т.-зел.
св.-зел.
св.-кор.
черн.
фиол.
Плот-
Плотность
7,2
6,17
5,6
6,07
4,356
4,25
5,4
6,68
1,71
1,77
2,88
3,03
1,76
3,5
1,91120
4,11
3,78
2,89
5,1
1,585
1,76
5,2
4,92
99
I. Неорганические вещества
Продолжение табл.
Формула
CrN
Cr2N
[Cr(NCSN],K3
•4Н2О
[Cr(NH3N]Cl3
[Cr(NH3MCl]Cl2
CrNH4(SO4J
• 12H2O
Cr(NO3K
•9H2O
[Cr(NOL]
CrO
CrO2 + JC
(-0,99 <x< +0,013)
CrO3
Cr2O3
Cr(O)F4
CrO2F2
Cr(OHJ
•4H2O
Cr(OHK
[Cr(OHN],Na3
[Cr(O2L],K3
[Cr(O2L],Na3
CrO(OH)
CrP
Cr3P
[Cr(PF3N]
CrPO4
•6H2O
CrS
Cr2S3
CrSO4
•5H2O
4
66,00
118,00
517,79
589,85
260,54
243,51
262,16
478,34
238,01
400,14
172,02
68,00
83,99
99,99
151,99
143,99
121,99
86,01
158,07
103,02
223,01
297,28
248,96
85,00
82,97
186,96
579,80
146,97
255,06
84,06
200,19
148,06
238,13
Фазовые переходы
> 1500 - Cr2N
п. 1650
разл. > 500
-H2O110
> 600 — CrCl3
550 — СгС13
700 -* Cr2O3
п. 94, разл. > 100
Не получен
п. 66, > 125 - СгО(ОН)
п. 38,5(/>), разл. > 20
п. 15500?), > 700 —Сг2О3
510 — Сг2О3
180-202, > 370 - СЮ2
п. 2334, к. 3000
п. 55
п. 31,6(р), возг. 29,6
Не получен
> 150 - СгО(ОН)
100 — СгО(ОН)
400 — NaCrO2
разл. > 170
разл. 115
550 — Сг2О3
п. 1600
п.1510
п. 1930), возг. 20
разл. > 1000
п. 100, -Н2О 300
п.1550
п. ~ 1000(/>),
1350 (вак.) — CrS
500 — Сг2О3
-Н2О 265 (вак.)
Окраска
черн.
черн.
т.-краен.
фиол.
т.-желт.
т.-краен.
краен.
фиол.
т.-фиол,
черн.-кор.
черн.
черн.
т.-краен.
т.-зел.
краен.
св.-фиол.
желт.
сер.-гол.
зел.
кор.-краен.
красн.-кор.
зел.
т.-сер.
т.-сер.
бел.
сер.-бур.
зел.-фиол.
черн.
черн.
бел.
гол.
Плот-
Плотность
6,14
6,51
1,711
1,59
1,69
1,72
4,95
2,82
5,21
3,21
2,9
4,57
5,7
3,05
2,12
4,85
3,77
100
I. Неорганические вещества
Продолжение табл.
формула
Cr2(SO4K
• 18Н2О
CrSi
CrSi2
Cr3Si
Cr5Si3
CrT^SO^
• 12H2O
CrVO4
(Cr2"Zn)O4
Cs
CsAl(SO4J
• 12H2O
CsBr
CsBrO3
Cs(CH3COO)
Cs2CO3
CsCl
CsC102
CsC103
CsC104
Cs2Cr04
Cs2Cr207
CsCr(SO4J
• 12H2O
CsF
csFe(SO4J
• 12H2O
Cs2Fe(SO4J
•6H2O
CsGa(SO4J
• 12H2O
CsH
4
392,18
716,45
80,08
108,17
184,07
344,24
448,50
664,68
166,93
233,38
132,905
352,01
568,19
212,81
260,81
191,95
325,82
168,36
200,36
216,36
232,35
381,80
481,80
377,03
593,21
151,90
380,88
597,06
513,78
621,87
394,75
610,93
133,91
Фазовые переходы
640 - Cr2O3
п. 80,-Н2О>115(вак.)
п. 1475 разл.
п. 1490-1550
п. 1770
п. 1600
> 750 - Сг2О3
п. 92, -Н2О 220
п. 917 разл.
п. - 2050
п. 28,44, к. 671
разл. 800
п. 117,-Н2О120
п. 637,1297
п. 420 разл.
п. 194
п. 7930i), > 620 — Cs2O
п. 646, к. 1295
> 100 — CsCl
п. 388, разл. > 483
п. 577 разл., > 580 —CsCl
п. 982
п. 384, разл. - 600
разл. > 700
п. 116,-Н2О400
п. 703, к. 1253
Не получен
разл. > 175
Не получен
разл.« 200
Не получен
разл. 250
п. 5280?), > 200 — Cs
Окраска
краен.-кор.
син.-фиол.
сер.
т.-сер.
сер.-черн.
черн.
краен.
фиол.
т.-кор.
св.-зел.
желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.
оранж.
краен.
фиол.
бел.
св.-фиол.
св.-зел.
бел.
бел.
Плот-
Плотность
3,012
1,7
5,37
5,0
5,5
2,39
3,89
5,92
1,873
1,97
4,43
4,11
3,983
3,57
3,319
4,237
2,06
3,59
2,06
2,79
2,11
3,42
101
I. Неорганические вещества
Продолжение табл.
Формула
CsHCO3
Cs(HCOO)
CsHSO4
Csl
CsIO3
CsIO4
CsMnO4
CsN3
CsNH2
CsNO2
CsNO3
•HNO3
• 2HNO3
CsO2
CsO3
Cs2O
Cs2O2
CsOH
•H2O
Cs2S
•4H2O
Cs2(S2)
Cs2(S3)
Cs2(S5) .
Cs2(S6)
Cs2SO4
Cs2S2O7
Cs3Sb
Cs2Se04
CsV(SO4J
• 12H2O
Cu
Cu3As
4
193,92
177,92
229,98
259,81
307,81
323,81
251,84
174,93
148,93
178,91
194,91
257,92
320,93
164,90
180,90
281,81
297,81
149,91
167,93
297,88
369,94
329,94
362,01
426,14
458,21
361,84
441,94
520,47
408,77
375,97
592,15
63,546
265,56
Фазовые переходы
175 — Cs2CO3
п. 265
- 220 — Cs2S2O7
п. 632, к. 1280
п. 565
> 900 - Csl
разл. 320
п. 326, разл. 390
п. 262, разл. « 500
п. 398
п. 409, 585 — CsNO2
п. 104, 650 - CsNO2
п. 39, 670 — CsNO2
п. 450(/?), > 400 — Cs2O2
80 — CsO2
п. 595(/?), > 300 — Cs2O2, Cs
п. 594, 640 — Cs
п. 343
п. 180,-Н2О300
п.« 500
-Н2О 150 (вак.)
п. 460, 600 -* Cs2S
n.217,600-Cs2S
п. 210,600 —Cs2S
п. 185, 600 - Cs2S
п. 1015(р), возг. 900
п. 280
п. 725
п. 985
разл. > 350
п. 82, -Н2О 230
п. 1084,62, к. 2562
п. 830
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
фиол.
бел.
бел.
желт.
бел.
бел.
бел.
желт.-кор.
краен.
т.-краен.
св.-желт.
бел.
бел.
бел.
бел.
желт.
оранж.
краен.
краен.-кор.
бел.
бел.
черн.
бел.
краен.
св.-краен.
краен.
т.-сер.
Плот-
Плотность
3,35
4,509
4,85
4,26
3,597
2,93
3,43
3,643
3,76
3,65
4,36
4,47
3,675
2,81
4,246
4,46
4,45
2,03
8,92
102
I. Неорганические вещества
Продолжение табл.
формула
Cu3(As04J
•4Н2О
Cu2(AsO4)OH
Cu3AsS4
CuBr
CuBr2
•4H2O
Cu(BrO3J
•6H2O
Cu2C2
Cu(CH3COOJ
•H2O
CuCN
Cu(CNJ
CuC2O4
Cu2CO3
Cu2CO3(OHJ
Cu3(CO3J(OHJ
CuCl
CuCl2
•2H2O
Cu(C103J
•6H2O
Cu(C104J
•6H2O
CuCrO2
CuF2
•2H2O
CuH
Cu(HCOOJ
•4H2O
Cul
Cu(IO3J
* 0,67H2O
4
468,47
540,33
283,02
393,82
143,45
223,35
295,41
319,35
427,44
151,11
181,63
199,65
89,56
115,58
151,56
187,10
221,11
344,67
99,00
134,45
170,48
230,45
338,54
262,44
370,53
147,54
101,54
137,57
64,55
153,58
225,64
190,45
413,35
425,42
Фазовые переходы
разл. > 750
-H2O 440
разл. 490
разл. 700
п. 504, к. 1350
п. 498 разл., > 498 -> CuBr
140 — CuBr
разл. 550
-Н2О 200
> 20 -* Си
- 250 -> Си
п. 115 разл., -Н2О 95 (вак.)
п. 473, разл. 550
разл. > 20
420 — СиО
> 100 - Си2О
200 — СиО
> 220 - СиО
п. 430, к. 1490
п. 596, к. 993 разл.
-Н2О 150
Не получен
п. 65, разл. 100
230 - СиС12
п. 82, -Н2О 100 (вак.)
разл.« 1700
п. 950 разл., > 950 -* Си
-Н2О 280
НО —Си
разл.» 200
-Н2О 80 (вак.)
п. 605, к. 1320
290 - Cul
-Н2О 240
Окраска
бел.
син.-зел.
сер.-бел.
сер.-черн.
бел.
зел.-черн.
син.
бел.
зел.-гол.
краен.-кор.
син.-зел.
т.-зел.
бел.
бур.-желт.
син.-зел.
желт.
т.-зел.
син.
бел.
т.-кор.
гол.-зел.
зел.
желт.-зел.
св.-гол.
сер.-зел.
бел.
св.-син.
св.-кор.
син.-зел.
гол.
бел.
зел.
гол.
Плот-
Плотность
3,86
4,54
4,44
4,72
4,77
2,58
1,93
1,882
2,92
4,4
4,03
3,78
4,14
3,386
2,54
2,225
5,49
4,23
2,93
5,72
1,83
5,62
5,24
103
I. Неорганические вещества
Продолжение табл.
Формула
Cu(N3J
Cu3N
CuNCS
[Cu(NH2CH2COOJ]
[Cu(NH3N]Cl2
[Cu(NH3L](NO3J
[Cu(NH3L]SO4
•H2O
Cu(NO3J
•3H2O
•6H2O
CuO
Cu2_xO
Cu2O3
Cu(OHJ
[Cu(OHL],K
[Cu(OHL],Na2
CuP2
Cu3P
CuS
Cu(S2)
Cu^S
CuSO4
•H2O
•3H2O
•5H2O
Cu2SO4
Cu4SO4(OHN
Cu3Sb
CuSe
Cu2Se
CuSeO4
•5H2O
Mr
147,59
204,65
121,63
211,66
236,64
255,68
227,73
245,75
187,55
241,60
295,64
79,55
143,09
175,09
97,56
170,67
177,55
125,49
221,61
95,61
127,68
159,16
159,61
177,62
213,65
249,68
223,15
452,29
312,40
142,51
206,05
206,50
296,58
Фазовые переходы
300 - Cu3N
470 - Cu
n. 1084
n. 130, разл. 400
> 350 - CuCl2
> 200 - CuO
He получен
250 — CuSO4
n. 255(p), > 170 — CuO
n. 114,5, разл. 120
п. 24,4, -H2O < 100 (вак.)
п. 1447(р), 1026 — Си2О
п. 1242, 1800 -* Си
разл. 400
200 — СиО
разл. > 200
разл. > 175
п. 891
п. 1022
п. 502(р), 220 — Cu2S
100 — CuS
п. 1129, > 700 (вак.) — Си
п. 200, 650 — СиО
п. 313(р),-Н2О250
п. 116,6,-2Н2О 190
п. 95,88,-2Н2О 111
> 100 — Си2О
п. 300 разл.
п. 687
п. 382 разл., > 400 — Cu2Se
п.1113
550 — СиО
-Н2О 150
Окраска
черн.-кор.
т.-зел.
бел.
гол.
СИН.
Т.-СИН.
СИН.
бел.
гол.
гол.
черн.
краен.-кор.
т.-красн.
гол.
краен.
СИН.
сер.
сер.
сйн.-черн.
черн.
черн.-сер.
бел.
бел.
гол.
гол.
св.-сер.
зел.
сер.
черн.-зел.
черн.
бел.
гол.
Плот-
Плотность
2,604
5,84
2,85
1,48
1,91
1,81
2,32
2,074
6,51
6Д
3,368
4,68
4,24
5,81
3,603
3,15
2,7
2,284
3,605
3,78
8,51
5,99
6,75
2,56
104
I. Неорганические вещества
Продолжение табл.
формула
Cu2Te
2
DBr
DC1
DF
DI
D2O
D3PO4
D2S
D2SO4
DT
Dy
DyBr3
Dy(BrO3K
•9H2O
Dy2(C2O4K
• 10H2O
DyCl3
DyF3
Dyl3
Dy(NO3K
•5H2O
Dy2O3
Dy(OHK
Dy2S3
Dy2(SO4K
•8H2O
Er
ErBr3
Er(CH3COOK
*4H2O
Er2(C2O4K
•6H2O
MT
254,69
4,028
81,92
37,47
21,01
128,92
20,03
101,01
36,09
100,09
5,030
162,500
402,21
546,20
708,34
589,05
769,20
268,86
219,49
543,22
348,51
438,59
373,00
213,52
421,20
613,19
757,31
167,260
406,97
344,39
416,45
598,57
706,66
Фазовые переходы
п. 855
п. -254,42, к. -249,48
п. -87,6, к. -66,85
п.-114,7, к.-84,75
п.-83,6, к.+18,36
п. -51,82, к. -36,2
п. 3,823, к. 101,44
п. 49,45
п. -86,01, к. «-60
п. 14,35
п. -248,77
п. 1411, к. 2561
п. 881, к. 1485
> 600 — Dy2O3
п. 75, -Н2О 140
Не получен
> 550 -> Dy2O3
п. 654, к. 1627
п. 1157,> 2200
п. 983, к. 1320
400 — Dy2O3
п. 88,6, -Н2О 150 (вак.)
п. 2400, к. - 1320
800 — Dy2O3
п.1490
900 - Dy2O3
-Н2О 360
п. 1529, к. 2862
п. 950, к. 1460
Не получен
разл. 400
Не получен
575 — Ег2О3
Окраска
син.
бцв. г.
бцв. ж.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бцв. ж.
бел.
бцв. г.
бцв. ж.
бцв. г.
бел.
бел.
желт.
желт.
желт.
бел.
бел.
бел.
бел.
желт.
бел.
желт.
т.-желт.
бел.
желт.
бел.
фиол.
краен.
краен.
Плот-
Плотность
7,27
0,1797
0,1751
3,654
1,672
0,937
5,752
1,106й
1,91
1,61
1,85725
0,2244
8,551
3,617
7,466
8,16
9,066
2,11
2,64
105
I. Неорганические вещества
Продолжение табл.
Формула
ЕгС13
•6Н2О
ErF3
Erl3
Er(NO3K
•5Н2О
Er2O3
Er(OHK
Er2S3
Er2(SO4K
¦8Н2О
Es
Eu
EuBr2
EuBr3
Eu2(C2O4K
• 10H2O
EuCl2
EuCl3
•6H2O
EuF2
EuF3
Eul2
Eul3
Eu(NO3K
•6H2O
EuO
Eu2O3
Eu(OHJ
•H2O
Eu(OHK
EuS
Eu2S3
4
273,62
381,71
224,25
547,98
353,27
443,35
382,52
218,28
430,72
622,71
766,83
252,083
151,965
311,77
391,68
567,98
748,13
222,87
258,32
366,41
189,96
208,96
405,77
532,68
337,98
446,07
167,96
351,93
185,98
203,99
202,99
184,03
400,13
Фазовые переходы
п. 776, к. 1500
п. 153, -Н2О 320
п. 1146, к. 2230
п. 1015, к.1280
430 — Ег2О3
-Н2О 130
п. 2380, к. < 3500
850 — Ег2О3
п. 1730
900 - Ег2О3
-Н2О 400
п. 860
п. 822, к. 1596
п. 683, к. 1880
п. 705, 800 — ЕиВг2
Не получен
> 550 — Еи2О3
п. 854, к. 2060
626 разд., 700-^ ЕиС12
-Н2О - 350
п. 1416, к. 2400
п. 1276, к. 2280
п. 580, к. 1775
п. 880, 900 - Eul2
Не получен
п. 85, > 550 -> Еи2О3
п. 1980
>2200
570 — EuO
-Н2О 270
820 — Еи2О3
п. « 2400
- 1200 — EuS
Окраска
роз.-фиол.
роз.
св.-роз.
фиол.
роз.
краен.
св.-роз.
роз.
желт.-кор.
роз.
краен.
св.-сер.
бел.
бел.
бел.
бел.
бел.
желт.
св.-желт.
бел.
бел.
бел.
бел.
краен.-кор.
бел.
бел.
бел.
бел.
кор.-фиол.
бел.
Плот-
Плотность
4Д
8,64
6,05
3,678
3,217
5,244
4,89
4,88
4,89
4,47
6,5
5,5
8,2
6,55
4,467
106
I. Неорганические вещества
Продолжение табл.
формула
EuSO4
Eu2(SO4K
•8Н2О
F2
HF
Fe
(FeAl2)O4
FeAs
FeAs2
FeAsO4
•2H2O
Fe(As)S
FeB
FeBr2
•6H2O
FeBr3
•6H2O
Fe3C
[Fe5C(COI5]
[Fe(C5H5J]
[Fe(C5H5J]NO3
[Feni(CNN],Fe
[Fen(CNN],Fe2
[Fe(CNN],H3
[pe(CNN]5H4
fpe(CNN],K3
[Fe(CNN],K4
•зн2о
tFen(CNN],KFe
FeCO3
Mr
248,03
592,12
736,24
37,996
20,01
55,847
173,81
130,77
205,69
194,77
230,80
162,84
66,66
215,66
323,75
295,56
403,65
179,55
711,40
186,04
248,04
267,80
323,65
214,98
215,99
329,25
368,35
422,39
306,90
115,86
Фазовые переходы
разл. 750
1600 — Eu2O3
-H2O 375
п.-219,622, к.-188,12
п.-83,36, к.+19,52
п. 1538, к. 2861
п. 1440
п. 1030
п. 990
разл.» 1000
-Н2О 200
разл. 770
п. 1650
п. 684(/>), к. 927
-Н2О 100 (вак.)
п. 227(р), > 139 — FeBr2
п. 27, разл. > 100
п. 1650 разл., > 1650^ Fe, С
разл. ПО
п. 173, к. 249
разл. 400
разл. > 250
разл. 500
разл. 100
разл. 190
350 — Fe3C
650 - Fe3C
п. 70, -Н2О 87,3
> 560 — Fe3C
490^(РеиРе2п)О4
Окраска
бел.
бел.
св.-роз.
св.-зел. г.
св.-желт. ж.
бел.
бцв. г.
бцв. ж.
бел.
т.-зел.
св.-сер.
св.-сер.
желт.
зел.
бел.
сер.
желт.-кор.
св.-зел.
краен.-бур.
краен.
сер.
черн.
оранж.
т.-гол.
бур.
бел.
св.-кор.
бел.
т.-краен.
желт.
св.-желт.
син.
бел.
Плот-
Плотность
4,98
4,95
1,69
1,5189
1,7
1,693
0,9813
7,86
4,392
7,83
7,45
3,18
6,07
7,15
4,636
7,69
1,49
1,54
1,845
1,935
1,853
3,8
107
I. Неорганические вещества
Продолжение табл.
Формула
FeC2O4
•2Н2О
[Fe(COM]
Fe2(C2O4K
[Fe2(CO)9]
[Fe3(COI2]
[Fe(C2O4K],K3
•3H2O
[Fe(C2O4K],(NH4K
•3H2O
[Fe(C2O4K],Na3
• 5,5H2O
FeCl2
•4H2O
FeCl3
•6H2O
Fe(Cl)O
Fe(C104J
•6H2O
Fe(C104K
• 10H2O
FeCu(S2)
FeF2
•8H2O
FeF3
• 4,5H2O
(FeIIFeIII)F5
(FenFe2n)O4
•2H2O
[Fe(H2O)Cl5],K2
Fel2
•4H2O
Fe2 + XN
@<jc<0,5)
4
143,87
179,90
195,90
375,75
363,78
503,66
437,20
491,24
374,02
428,06
388,87
487,95
126,75
198,81
162,21
270,30
107,30
254,75
362,84
354,19
534,34
183,53
93,84
237,96
112,84
193,91
206,68
231,54
267,57
329,32
309,66
381,72
125,70
Фазовые переходы
He получен
разл. > 160
п.-20, к.+103
разл. > 100
п. 100, разл. 110
возг. 70 (вак.), 140 -* Fe
разл. 230
-Н2О 100
Не получен
разл. 165
Не получен
разл. 300
п. 677, к. 1026
п. 90, -Н2О 220
п. 309, к. 320
п. 37, к. 219
разл. > 300
Не.получен
разл. > 100
Не получен
разл. > 120
п. 1000, разл. > 1300
п. 1102, к. 1837
-Н2О 200
п. 1027, к. 1327
разл. > 350
разл. 1200
п. 1594, > 1600 - FeO
-Н2О > 300
разл. > 170
п. 587, к. 827
п. 90, разл. > 100
п. 500(р), 200 — Fe3N
Окраска
св.-желт.
св.-желт. ж.
св.-желт.
желт.
черн.-зел.
желт.
зел.
зел.
зел.
бел.
зел.-гол.
зел.-краен.
желт.-кор.
св.-краен.
св.-зел.
роз.
желт.
бел.
бел.
св.-зел.
св.-роз.
гол.-сер.
черн.
т.-бур.
краен.
краен.-кор.
зел.
сер.-черн.
Плот-
Плотность
2,28
1,45720
2,08
2,085
2,0
2,13
1,78
1,97
3,162
1,937
2,898
3,1
4,2
4,09
2,09
3,52
3,34
5,12
2,32
5,315
2,87
6,35
108
I. Неорганические вещества
Продолжение табл.
формула
Fe3N
Fe4N
FeNH4(SO4J
• 12H2O
Fe(NH4J(SO4J
•6H2O
Fe(NO3J
•6H2O
Fe(NO3K
•6H2O
•9H2O
[Fe(NOL]
[Fe(NO+)(CNM],Na2
•2H2O
(Fe2MNi)O4
Fe,_xO
@,05 <x< 0,11)
Fe2O3
/iH2O
Fe267O4
Fe(OHJ
FeO(OH)
FeP
FeP2
Fe2P
Fe3P
[Fe(PF3M]
FePO4
•2H2O
Рез(РО4J
•8H2O
4
181,55
237,40
266,01
482,19
284,05
392,14
179,86
287,95
241,86
349,95
403,99
175,87
261,92
297,95
234,38
71,85
159,69
—
213,11
89,86
88,85
86,82
117,80
142,67
198,52
495,69
150,82
186,85
357,48
501,60
87,91
Фазовые переходы
420 — Fe4N
680 - Fe
480 — Fe2(SO4K
п.40,-Н2О150(вак.)
разл. 300
-H2O 100-110
He получен
п. 60,5, > 600 — Fe2O3
Не получен
п. 47,2, к. 125,1
п. 50,1,-ЗН2О 150 (вак.)
разл. > 100
п. 68700,400 — Fe3C
-Н2О 50-100
п. 1660 разл.
п. 1369(р),
560-(FenFe2n)O4
п. 15650?),
1390 — (FenFe2n)O4
250 — FeO(OH)
1200 — Fe2O3
150-200 -FeO
500 - Fe2O3
разл. > 1150
разл. > 500
п.1290
п. 1100 разл.
п. 45(/0, возг. > 20
п. - 1600
-Н2О > 250
п. - 1700
-Н2О 180
п. 1193
Окраска
сер.-черн.
сер.-черн.
бел.
фиол.
бел.
св.-зел.
бел.
св.-фиол.
черн.
т.-краен.
краен.
кор.-черн.
черн.
краен.-кор.
бур.
т.-кор.
бел.
св.-кор.
сер.-черн.
черн.
сер.-черн.
сер.-черн.
св.-желт.
св.-желт.
роз.
бел.
св.-гол.
кор.-черн.
Плот-
Плотность
7,21
2,49
1,71
1,864
1,684
1,81
1,72
5,2
5,75
5,24
3,0-
3,12
4,88
3,4
4,28
6,07
5,07
6,56
6,74
2,74
2,58
4,79
109
I. Неорганические вещества
Продолжение табл.
Формула
cc-Fe(S2)
P-Fe(S2)
[FeS2],K
FeSO4
•7H2O
Fe2(SO4K
•9H2O
FeSi
FeSi2
Fe3Si
FeSiO3
Fe2Si04
FeVO4
FeWO4
(Fe2nZn)O4
Fm
EV
Ga2
GaAs
GaBr
GaBr3
[GainBr4],Ga
[Ga2HBr7],Ga
GaCl3
[GainCl4],Ga
[Ga2"Cl7],Ga
[GaCl2],H
Ga(C104K
GaF3
•3H2O
Gal
4
119,98
119,98
159,08
151,91
278,01
399,88
562,02
83,93
112,02
195,63
131,93
203,78
170,79
303,68
241,08
257,095
223,020
139,446
144,65
149,63
309,44
459,06
768,50
176,08
281,26
457,34
141,64
368,07
126,72
180,76
196,62
Фазовые переходы
450 - p-Fe(S2),
1170(вак.)-> FeS
п. 743(р), 1170 (вак.) — FeS
п. « 950
700 -> Fe2O3
п. 64, -H2O < 250
500-900 - Fe2O3
-H2O 175
п. 1410
п. 1210 разд., > 1250 -^ FeSi
п.1300
п. 1146
п. 1217
п. 840 разл.
п.-1700
п.1590
п.1527
п. 27, к. 677
п. 29,78, к. 2403 (— Ga^
п.1238
п. 158 разд.,
> 158-*GaBr3, Ga
п. 122,5, к. 278
п. 166, к. 462
разл. 81
п. 77,8, к. 200,5
п. 175, к. 595
п. 87
п. 29
разл.175
п. 1000(/>,), возг. 950
разл. > 140
п. 270 разд., > 270 — Gal3, Ga
Окраска
св.-желт.
т.-желт.
т.-краен.
бел.
гол.-зел.
бел.
св.-фиол.
желт.-сер.
т.-сер.
сер.-желт.
сер.-зел.
зел.-желт.
красн.-кор.
черн.
черн.
бел.
св.-сер.
т.-сер.
т.-желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
кор.
Плот-
Плотность
4,86
5,03
2,56
3,14
1,898
3,097
2,1
6,01
5,06
3,5
4,34
7,5
5,34
2,3-2,5
5,904
5,317
3,74
3,47
2,47
2,4173
4,47
110
I. Неорганические вещества
Продолжение табл.
формула
Gal3
[GanII4],Ga
GaN
GaNH4(SO4J
• 12H2O
[GaN2],Li3
Ga(NO3K
•9H2O
Ga2O
Ga2O3
Ga(OHK
GaO(OH)
GaP
GaPO4
Ga2(S2)
Ga2S3
Ga2(SO4K
• 20H2O
GaSb
Ga2Se3
Ga2Te3
Gd
GdBr3
•6H2O
Gd2(C2O4K
• юн2о
GdCl3
•6H2O
GdF3
Gdl3
Gd(NO3K
•5H2O
Gd2O3
4
450,44
647,06
83,73
279,89
496,07
118,56
255,74
417,87
155,45
187,44
120,74
102,73
100,70
164,69
203,58
235,64
427,63
787,93
191,48
376,33
522,25
157,250
396,96
505,05
578,55
758,70
263,61
371,70
214,24
537,96
343,26
433,34
362,50
Фазовые переходы
п. 213, к. 345
п. 211, к. 469
п. 1700(/?), разл. 1200
Не получен
разл. > 250
разл. 800
200 — Ga2O3
-Н2О 60 (вак.)
п. 650, к. 725
п. 1725(р), >1200 —Ga2O
400 — GaO(OH)
600 — Ga2O3
п. 1790
п. 1670
п.1015
п. 1125(/>),950^Ga2(S2)
> 520 -> Ga2O3
-Н2О 350
п. 712
п. 960
п. 810
п. 1314, к. 3264
п. 778, к. 1490
-Н2О 250-300
Не получен
> 500 — Gd2O3
п. 605, к. 1595
-Н2О 225
п. 1232, к.2280
п. 929, к. 1340
Не получен
п. 92, > 530 - Gd2O3
п. 2350
Окраска
желт.
желт.
желт.-бур.
бел.
св.-желт.
бел.
бел.
т.-кор.
бел.
бел.
бел.
зел.-желт.
бел.
желт.
желт.
бел.
бел.
св.-желт.
т.-краен.
черн.
черн.-сер.
бел.
бел.
бел.
бел.
бел.
бел.
св.-желт.
бел.
бел.
Плот-
Плотность
4,15
6,1
1,78
4,77
5,88
4,1297
3,26
3,75
3,74
5,6137
5,03
5,57
5,582
2,844
4,52
2,424
7,058
2,406
7,618
111
I. Неорганические вещества
Продолжение табл.
Формула
Gd(OHK
Gd2S3
Gd2(SO4K
•8H2O
Gd2(Se04K
•8H2O
Ge
GeBr2
GeBr4
Ge(CH3COOL
Ge(CNL
GeCl2
GeCl4
GeF2
GeF4
•3H2O
[GeF6],K2
[GeF6],Mg
[GeF6],Na2
GeH4
Ge2H6
Ge3H8
Ge4H10
Ge5H12
Gel2
Gel4
Ge3N4
GeO
cc-GeO2
p-GeO2
«H2O
4
208,27
410,70
602,69
746,81
743,37
887,49
72,610
232,42
392,23
308,79
176,68
108,06
143,52
214,42
110,61
148,60
202,65
264,79
210,90
232,58
76,64
151,27
225,89
300,52
375,15
326,42
580,23
273,86
88,61
104,61
104,61
—
Фазовые Переходы
920 — Gd2O3
п.1885
> 650 — Gd2O3
-H2O 400
разл. 700
-H2O 130 (вак.)
п. 938,25, к. 2833
п. 144, возг. 130 (вак.)
п. 26,1, к. 186,5
п. 156
разл. 80
разл. 300—520
> 75 -* GeCl4, Ge
п.-49,5, к.+83,1
п. ПО, 160 — GeF4, Ge
п. -15(/?), +1000 — Ge
> 100 — GeO2
п. 730, к. 835
разл. 465
п. 623
п. -165,8, к. -88,5
п. -109, к. +30
п.-105,6, к.+110,7
к. 177
к. 235
п. 460(/?), возг. 240 (вак.)
п. 146, к. 348
разл. 450-1400
> 600 — GeO2, Ge,
возг. 710 (вак.)
1035 — p-GeO2
п. 1115
-Н2О 380
Окраска
бел.
желт.
бел.
бел.
бел.
бел.
св.-сер.
бел.
бцв. ж.
бел.
бел.
краен.-кор.
бел.
бцв. ж.
бел.
бцв. г.
бел.
бел.
бел.
бел.
бцв. г.
бцв. г.
бцв. ж.
бцв. ж.
бцв. ж.
т.-желт.
т.-оранж.
желт.
т.-желт.
бел.
бел.
бел.
Плот-
Плотность
3,8
4,139
3,01
3,31
5,35
3,12227
1,8720
6,65
3,32
3,43
6,749
5,37
4,53
5,25
4,4
6,277
4,28
112
I. Неорганические вещества
Продолжение табл.
формула
GeP
GeS
GeS2
GeSe
GeSe2
GeTe
H2
H2O
HT
He
Hf
HfB2
HfBr4
HfC0,94
[Hf(C5H5JCl2]
HfCi4
HfCl2O
•8H2O
HfF4
WfF6],K2
[HfF7],(NH4K
нп4
HfN
Hf(NO3JO
HfO2
«H2O
-—
4
103,58
104,68
136,74
151,57
230,53
200,21
2,016
18,02
4,024
4,003
178,490
200,11
498,11
189,78
379,59
320,30
265,40
409,52
254,48
370,67
365,59
686,11
192,50
318,50
210,49
—
228,50
Фазовые переходы
п. 725
п. 840
п. 675
п. 707 разл.
п. 725
п. -259,34, к. -252,87
п. 0,00, к. 100,00
к. -250,23
п. -272,2, к. -268,9
п. 2233, к. 4603
п. 3380
п. 4200?), возг. 332
п. 3890 разл.
п. 231,5
п. 4320?), возг. 315
300 — HfCl4, НЮ2
-Н2О 65 (вак.), > 400 - НГО2
п. 10200?), возг. 970
п. 608 разл.
240-600 — HfF4
п. 4490?), возг. 397
п. 3300
400-640 — НЮ2
п. 2780, к. - 5400
140 — НЮ(ОНJ
1000 — НГО2
Окраска
св.-кор.
сер.-черн.
бел.
т.-кор.
оранж.
сер.
бцв. г.
бцв. ж.
бел.
бцв. ж.
бцв. г.
бел. (лёд)
бцв. г.
бцв. г.
бцв. ж.
бел.-сер.
сер.
бел.
сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
св.-оранж.
т.-кор.
бел.
бел.
желт.
бел.
Плот-
Плотность
4,012
3,01
5,52
4,56
0,0899
0,066~249
0,087
1,004
0,598101
0,917
0,1827
0,1785
0,15-272
13,31
4,9
12,68
7,13
2,8
5,6
13,38
9,68
113
I. Неорганические вещества
Продолжение табл.
Формула
Hf(SO4J
•4Н2О
HfSi2
Hg
Hg3(As04J
HgBr2
Hg2Br2
Hg(BrO3J
•2H2O
Hg2(Br03J
Hg2C2
Hg(CH3COOJ
Hg(CNJ
Hg(CNOJ
Hg2CO3
HgCl2
Hg2Cl2
HgCl(NH2)
Hg(C103J
Hg(C104J
Hg2(C103J
Hg2(C104J
HgF2
Hg2F2
a-HgI2
P-Hgl2
Hg2I2
[HgI4],Ag2
[HgI3],K
•H2O
[HgI4],K2
•2H2O
4
370,61
442,67
234,66
200,590
879,61
360,40
560,99
456,39
492,42
656,98
425,20
318,68
252,63
284,62
461,19
271,50
472,09
252,07
367,49
399,49
568,08
600,08
238,59
439,18
454,40
454,40
654,99
923,94
620,40
638,42
786,40
822,43
Фазовые переходы
800 - НЮ2
-H2O < 300
n. 1750
n. -38,83, к. +356,73
разл. > 300
п. 238,1, к. 319
возг. 345
Не получен
разл. > 130
разл. > 200
разл. 100
п. 180 разл.
> 320 — Hg
разл. 180
130 - HgO, Hg
п. 280, к. 301,8
п. 525(/?), 383,7 - HgCl2, Hg
разл. 400
300 - HgCl2
п. 170, 327 - HgCl2
250 - Hg2Cl2
247 - Hg2Cl2
п. 645, к. 647
п. 570, свет — HgF2, Hg
127 - p-HgI2
п. 256, к. 354
возг. 140, < 290 — Hgl2, Hg
разл. > 158
п. 105, 320 — Hgl2
-Н2О 60
400 -* Hgl2
-1Н2О90
Окраска
бел.
бел.
сер.
св.-сер. ж.
бел.
желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
сер.-бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
св.-желт.
краен.
желт.
желт.
желт.
св.-желт.
желт.
желт.
св.-желт.
Плот-
Плотность
8,03
13,5520
14,193
6,11
7,307
3,27
3,4
4,42
5,44
7,15
5,7
5,0
6,409
8,95
8,73
6,48
6,094
7,683
6,02
114
I. Неорганические вещества
Продолжение табл.
формула
Hg(NCSJ
Hg(NO3J
• 0,5Н2О
•н2о
Hg2(NO2J
Hg2(NO3J
•2Н2О
HgO
a-HgS
P-HgS
Hg(S2)
HgSO4
•H2O
Hg2SO4
Hg,_,Se
@<x<0,01)
Hg,_Je
@,05 <jc< 0,6)
Ho
HoBr3
Ho2(C2O4K
• 10H2O
H0CI3
H0F3
H0I3
Ho(NO3K
•5H2O
Ho2O3
Ho(OHK
Ho2(SO4K
•8H2O
I2
lIAg2]NO3
Mr
316,76
324,60
333,61
342,61
493,19
525,19
561,22
216,59
232,66
232,66
264,72
296,65
314,67
497,24
279,55
328,19
164,930
404,64
593,91
774,06
271,29
221,92
545,64
350,94
441,02
377,86
215,95
618,05
762,17
253,808
404,64
Фазовые переходы
165 - HgS
> 360 — HgO
n. 79 разл., -0,5Н2О 79 (вак.)
-0,5Н2О40(вак.)
разл. > 100
150 - HgO
-H2O 40 (вак.)
450 -> Hg
345 -> P-HgS
п. 825(/?), возг. 580
разл. 390
> 550 -> Hg
-Н2О 350
600 — Hg
п. 799
п. 670
п. 1472, к. 2694
п. 919, к. 1336
Не получен
600 - Но2О3
п. 720, к. 1507
п. 1143, к. > 2200
п. 989, к. 1300
Не получен
разл. 560
п. 2360
850 — Но2О3
850 — Но2О3
-Н2О < 400
п. 113,7, к. 184,4
п. 94
Окраска
бел.
бел.
бел.
бел.
желт.
бел.
бел.
краен.
краен.
черн.
бел.
бел.
бел.
бел.
фиол.-черн.
сер.-черн.
св.-сер.
желт.
св.-желт.
желт.
бел.
желт.
желт.
св.-желт.
желт.
желт.
св.-желт.
фиол.-черн.
черн. ж.
бел.
Плот-
Плотность
3,71
7,33
7,79
4,79
11,14
8,19
7,73
6,47
7,56
8,26
8,42
8,795
3,715
7,642
8,24
4,93
3,96120
115
I. Неорганические вещества
Продолжение табл.
Формула
1Вг
[I(Br)Cl],Cs
[I(BrJ],Cs
[I(BrJ],K
IC1
I2C16
[I(ClJ],Cs
[I(ClL],Cs
[I(C1L],H
•4H2O
[I(C1J],K
[I(C1L],K
IF
IF3
IF5
IF7
[I(IJ],Cs
[кадд
•H2O
[I(IJ],NH4
[I(IJ],Rb
I3N
«NH3
I(NO3K
I2O5
I(O)F3
I(O)F5
IO2F
IO2F3
IO3F
[I(OJF4],H
(IO+)IO3
A0^I0,
HI
Mr
206,81
375,17
419,62
325,81
162,36
466,53
330,72
401,62
269,72
341,78
236,91
307,81
145,90
183,90
221,89
259,89
513,62
419,81
437,83
398,75
466,18
394,72
—
312,92
333,80
199,90
237,89
177,90
215,90
193,90
235,90
317,80
349,80
127,91
Фазовые переходы
п. 40,5, к. 116 разл.
п. 235, разл. 290
п. 248, разл. 320
п. 58, разл. 180
п. 27,19, к. 97,4 разл.
п. 101(/>),64^1С1
п. 238, разл. 290
п. 228 разл.
Не получен
п. 19, разл. 124
разл. 215
п. 116 разл.
п. -14, разл. > -10
п. -28, разл. > -20
п. 9,421, к. 104,48
п. 6,45(/?), разл. > 200
п. 215 разл.
Не получен
п. 38, разл. 225
разл. 175
п. 194 разл.
Не получен
> 20 — 12
разл. > 0
п. 300(/>), > 275 — 12
разл. > 100
п. —15, разл. > 40
300 — 12
п. 42,5, к. 147
110^IO2F
п. 36, разл. 130
разл. 130
разл. > 150
п. -50,8, к. -35,36
Окраска
черн.-бур.
св.-краен.
краен.
краен.
т.-краен.
св.-оранж.
оранж.
св.-оранж.
оранж.
оранж.
т.-желт.
краен.
желт.
бцв. ж.
бцв. ж.
черн.
т.-бур.
т.-бур.
черн.
красн.-кор.
желт.
бел.
бел.
бцв. ж.
бел.
желт.
бел.
бел.
желт.
св.-желт.
бцв. г.
Плот-
Плотность
4,4157
4,25
3,85
3,1105
3,86
3,37
176
3,23115
2,87
4,47
3,75
4,03
4,799
3,95
4,97
5,7891
116
I. Неорганические вещества
Продолжение табл.
формула
НЮ3
ню4
h4i2o9
н5ю6
In
InAs
InBr
InBr3
[IninBr4],In
InCl
InCl3
•4H2O
[InnlCl4],In
[InniCl6],In3
In(C104K
•8H2O
InF3
Inl
Inl3
[InmI4],In
InN
In(NO3K
• 4,5H2O
In2O
In2O3
In(OHK
InP
InPO4
•2H2O
In2S
i t>
In2S3
Г I Uln
lInlI1S2],Cu
lInIIIS2],In
~-————
Mr
175,91
191,91
401,83
227,94
114,818
189,74
194,72
354,53
549,25
150,27
221,18
293,24
371,45
671,99
413,17
557,29
171,81
241,72
495,53
737,25
128,83
300,83
381,90
245,64
277,63
165,84
145,79
209,79
245,82
261,70
325,83
242,50
293,77
Фазовые переходы
п. ПО разд., 220-М2О5
возг. ПО
> 100 — НЮ4
80 (вак.) — Н412О9,
> 122 — 12О5
п. 156,634, к. 2072
п. 943
п. 285, к. 662
п.419,7(/>),возг.409
п. 198, к. 638
п. 224, к. 591
п. 586(р), возг. 546
п. 56, разл. 200
п. 240, к. 655
п. 325, к. 640
Не получен
п. 80, разл. 200
п.-1300, к. 1377
п. 365, к. 743
п. 207, к. 447
п. 225
п. 1200
230-250 — 1п2О3
п. 74, -Н2О60(вак.)
п. 325, к. > 700
п. 1910,к.~3300(р)
> 340 — 1п2О3
п. 1070
п. 1600, > 1800 — 1п2О3
-Н2О 300
п. 653 разл.
п. 1098
п. 1080
п. 692
Окраска
бел.
бел.
бел.
бел.
бел.
сер.
краен.
св.-желт.
бел.
желт.
бел.
бел.
бел.
св.-желт.
бел.
бел.
т.-краен.
желт.
краен.-кор.
сер.
бел.
бел.
черн.
св.-желт.
бел.
сер.
бел.
бел.
черн.
краен.-кор.
краен.
краен.
Плот-
Плотность
4,629
7,3
5,666
4,96
4,74
4,22
4,18
3,46
3,65
3,86
4,51
5,39
4,72
4,71
6,99
7,179
4,33
4,787
3,91
5,87
4,9
4,919
5,18
117
I. Неорганические вещества
Продолжение табл.
Формула
In2(SO4K
• 10Н2О
InSb
In2Se3
[InIHSe2],In
In2Te3
[InH1Te2],In
1г
[IrBr6],Na3
• 12Н2О
[1г(С2О4K],К3
•4Н2О
[1г2(СО)8]
[1г4(СОI2]
1гС13
1гС14
[1гС16],Н2
•6Н2О
[1гС16],К2
[1гС16],К3
[1гС16],К4
[IrQ6],(NH4J
[IrCl6],Na2
•6Н2О
[IrCl6],Na3
• 12Н2О
IrF3
IrF4
IrF5
IrF6
[Ir2(NH3I0]
[Ir(NH3N]Cl3
4
517,82
697,97
236,58
466,52
387,56
612,44
484,84
192,220
740,61
956,79
573,57
645,63
608,52
1105,00
298,58
334,03
406,95
515,04
483,13
522,23
561,33
441,02
450,92
559,01
473,91
690,09
249,21
268,21
287,21
306,21
554,75
400,77
Фазовые переходы
> 600 -* In2O3
-H2O 200 (вак.)
п. 525,2
п. 890
п. 660
п. 667
п. 696
п. 2446, к. 4428
750 — 1г
п. 100, -Н2О 150
разл. > 670
-Н2О > 240
возг. 160
возг. 210
> 798 ->Ir
> 700 - Ir
Не получен
> 200 — 1гС14
- 600 — 1гС14
« 500 — 1гС13
> 700 - Ir
440 - Ir
Не получен
600 — Ir
800 ->Ir
-Н2О 50 (вак.)
разл. 250
п. 106, к. « 300
п. 104,5
п. 44,1, к. 53,6
> 90 — Ir
500 — IrCl3
Окраска
бел.
бел.
сер.
т.-фиол.
т.-кор.
черн.
син.-сер.
бел.
зел.-черн.
т.-зел.
зел.
оранж.
желт.-зел.
желт.
т.-зел.
т.-зел.
черн.-
красн.
краен.-
черн.
т.-зел.
черн.
черн.
т.-краен.
т.-зел.
зел.
черн.
красн.-кор.
желт.-зел.
желт.
желт.
бел.
Плот-
ность
3,438
5,7551
5,67
5,7
5,78
6,29
22,421
2,51
5,3
3,549
3,55
2,86
6,0
2,43
118
I. Неорганические вещества
Продолжение табл.
формула
[Ir(NH3MCl]Cl2
[Ir(NH3N](NO3K
IrNH4(SO4J
• 12Н2О
1гО2
•2Н2О
1гО3
1г2О3
•лН2О
IrS2
Ir2S3
Ir2(SO4K
•wH2O
К
KAg(NO3J
KA1(SO4J
• 12H2O
KA13(SO4J(OHN
KBO2
1,33H2O
KB5O8
•4H2O
к2в4о7
•8H2O
KBi2
K3Bi
K3Bi2
KBr
KBrO3
квю4
K(CH3COO)
K2(C4H4O6)
• 0,5H2O
~-
Mr
383,73
480,42
402,38
618,56
224,22
260,25
240,22
432,44
—
256,35
480,64
672,63
—
39,098
270,97
258,20
474,38
414,21
81,91
105,87
221,15
293,21
233,43
377,55
457,06
326,27
535,25
119,00
167,00
183,00
98,14
226,27
235,27
Фазовые переходы
550 — IrCl3
разл. > 500
He получен
п. 106, > 350 — Ir2O3
1100 —Ir
-Н2О 350
к. 1200
> 450 - IrO2, Ir
-Н2О 300
разл. > 300
разл. > 400
Не получен
> 300 — 1г2О3
п. 63,28, к. 759
п. 135, 300 — KNO2
> 800 — K2SO4
п.92,-Н2О120
п. 800 - K2SO4
п. 950
-Н2О 250
п. 780
-Н2О 350
п. 815
-Н2О 420
п. 553
п. 671
п. 420
п. 734, к. 1435
п. 434 разл., >450 —КВг
< 275 - КВгО3, > 390 - КВг
п. 310
Не получен
разл. > 150
Окраска
св.-желт.
бел.
желт.-
красн.
черн.
син.
бцв. г.
син.-черн.
желт.-зел.
кор.-черн.
кор.-черн.
желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
сер.
сер.
сер.
бел.
бел.
бел.
бел.
бел.
Плот-
Плотность
2,68
2,39
11,655
3,15
8,43
9,64
0,862
3,22
2,75
1,757
2,7
2,23
1,74
1,74
2,75
3,25
1,57
119
I. Неорганические вещества
Продолжение табд.
Формула
KCN
К2СО3
• 1,5Н2О
К2С2О4
•Н2О
К2С2О4(О2)
K2Ca(SO4J
•Н2О
K2Cd(SO4J
•2Н2О
КС1
КСЮ2
КС1О3
КС1О4
K2Co(SO4J
•6Н2О
К2Сг04
К2Сг207
К2Сг3О10
К2Сг4013
К(СгО3С1)
KCr(SO4J
• 12Н2О
KD2PO4
KF
•2Н2О
K2FeO4
KFe(SO4J
• 12Н2О
K2Fe(SO4J
•6Н2О
K2Ge03
КН
KH2As04
Ч
65,12
138,20
165,23
166,21
184,23
198,21
310,40
328,41
382,73
418,76
74,55
106,55
122,55
138,55
329,25
437,34
194,19
294,18
394,17
494,17
174,54
283,22
499,40
138,10
58,10
94,13
198,04
287,07
503,25
326,17
434,26
198,80
40,11
180,03
Фазовые переходы
п. 634,5, к. 1625
п. 891, > 1200 —К
-Н2О 160
Не получен
разл. 100—160
> 150 - К2СО3
п. 1004
-Н2О 220
Не получен
разл. > 200
п. 771, к.-1500
разл. 160
п. 357, разл. > 472
п. 580 разл., 620 —КС1
Не получен
разл. > 210
п. 973
п. 396, > 500 - К2Сг04
разл. 243
разл. 210
разл. > 100
> 700 -> K2SO4
п. 89, -Н2О 400
разл. 300
п. 858, к.1510
п. 42, к. 156
разл. 700
> 650 — K2SO4
п. 33, -Н2О 220
Не получен
разл.« 200
п. 830
п. 6190), 400 — К
разл. 211
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
краен.
желт.
т.-оранж.
т.-краен.
кор.-красн.
оранж.
син.-зел.
т.-фиол.
бел.
бел.
бел.
св.-фиол.
бел.
фиол.
св.-зел.
бел.
бел.
бел.
Плот-
Плотность
1,56
2,44
2,127
2,02
2,57
2,92
1,989
2,338
2,536
2,22
2,732
2,684
2,5
1,842
2,344"
2,505
2,454
1,83
2,169
3,4
1,52
Z,oo
>¦
120
I. Неорганические вещества
Продолжение табл.
формула
.—¦—
K2HAs04
КНС4НА
КНСО3
КНС2О4
К(НСОО)
КНСО2(О2)
K(HF2)
КН(РНОз)
КН2РО4
К2НРО4
ЗН2О
KHS
KHSO3
KHSO4
KHSO3(O2)
K2H4Te06
KHg
KHg2
KI
KIO3
KIO4
KMgCl3
•6H2O
K2Mg(SO4J
•6H2O
KMg(SO4)Cl
•зн2о
K2Mg(Se04J
•6H2O
KMnO4
KN,
218,12
188,18
100,11
128,12
84,12
116,11
78,10
120,09
136,08
174,17
228,22
72,17
120,17
136,17
152,17
305,82
239,69
440,28
166,00
214,00
230,00
169,76
277,85
294,63
402,72
194,92
248,96
388,41
496,50
158,03
197,13
238,13
274,16
81,12
Фазовые переходы
K2CO3
разл. 300
разл. > 460
120
разл. 350
п. 168,7, разл. > 250
> 80 - К2СО3
п. 238,7, > 310 —KF
разл. > 275
п. 252,6 разл., > 260 — КРО3
282 - К4Р2О7
-Н2О 48,3
п. 455, > 550 — K2S
разл. - 190
п. 222, 340 - K2S2O7
п. 104, 150 — KHSO4
> 500 — К2Те03
п. 180
п. 270
п. 681, к. 1324
п. 560 разл., 650 —KI
п. 582(р), 290 — КЮ3
п. 487
п. 116,-Н2О265
Не получен
п. 72
Не получен
[. > 200
[. > 625
l2O 180
..л. > 200
600(р), разл. > 190
926, 1400 — К
,0 150-200
355 (вак.) — К
разл.
разл.
-Н2
разл.
п.
п.
-н.
п. 354,
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
т.-фиол.
т.-зел.
бел.
бел.
бел.
2,17
2,04
1,91
2,37
2,338
2,33
1,69
2,4
3,1115
3,93
3,618
1,6
2,03
2,15
2,36
2,703
2,8
3,11
2.056
Плот-
Плотность
121
Неорганические вещества
Продолжение табдг
Формула
KNCS
KNCSe
KNH2
KNO2
KNO3
KNa2
KNa(C4H4O6)
•4H2O
KNaCO3
•6H2O
K2Ni(SO4J
•6H2O
KO2
KO3
K2O
K2O2
KOCN
KOH
•H2O
K3P
K(PH2O2)
K2(PHO3)
KPO3
K3PO4
• 0,5H2O
•3H2O
•7H2O
K4P2O7
•3H2O
K5P3O10
K2(PO3F)
KPb
KReO4
KRh(SO4J
• 12H2O
Mr
97,18
144,08
55,12
85,10
101,10
85,08
210,16
282,22
122,10
230,19
329,01
437,10
71,10
87,10
94,20
110,19
81,12
56,11
74,12
148,27
104,09
158,18
118,07
212,26
221,27
266,31
338,37
330,33
384,38
448,40
176,17
246,30
289,30
334,13
550,31
Фазовые переходы
п. 172,3, 500 разл.
разл. 100—158
п. 338, > 600 — К
п. 440, 900 - К
п. 334,5, 400 — KNO2
п. 7 разл.
разл. 475
п. 75,-Н2О215
разл. > 1000
-Н2О 100 (вак.)
Не получен
разл. > 100
п. 5350?), 290 (вак.) — К2О2
60 - КО2, 02
п. 740(р), 350 - К2О2, К
п. 545(р), > 500 — К
разл. 700—900
п. 405, к. 1325
п. 150,-Н2О 500 (вак.)
разл. > 1200
разл. 605
разл. 745
п. 813, к. 1320
п. 1640
п. 203, -0,5Н2О 250
п. 156,5, -2,5Н2О 170
п. 47,5, -4Н2О 105-110
п. 1104 разл.
-Н2О 300
п. 641,5 разл.
п. 825
п. 568
п. 553, к.1367
Не получен
разл. > 200
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
гол.-зел.
т.-желт.
краен.
бел.
бел.
бел.
бел.
бел.
сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
т.-сер.
бел.
желт.
Плот-
Плотность
1,886
2,347
1,64
1,915
2,109
1,79
1,63
2,12
2,17
2,16
2,32 .
2,39
2,056
2,044
1J5
2,47
2,564 ;
2,83
4,887
2,23
122
I. Неорганические вещества
Продолжение табл.
формула
KRiA
K?RuO4
1
•н2о
•5Н2О
K2(S2)
K2(S3)
K2(S4)
K2(S5)
K2(S6)
K2SO3
•2H2O
K2SO4
K2S2O5
K2S2O6
K2S2O7
K2S3O6
k2s4o6
k2s5o6
• 1,5H2O
k2s6o6
K(SO2F)
K(SO3F)
K2S2O6(O2)
K2(SO3S)
H20
KSb
K3Sb
K2Se
K2Se04
K2Si03
K2Si205
K2Si409
К t*
4
204,16
243,26
261,28
110,26
200,34
142,33
174,39
206,46
238,53
270,59
158,26
194,29
174,26
222,32
238,32
254,32
270,39
302,45
334,52
361,54
366,59
122,16
138,16
270,32
190,33
208,34
160,86
239,05
157,16
221,15
154,28
214,36
334,53
205,80
Фазовые переходы
разл. 200—440
разл. > 1350
-Н2О 200
п. 948
п.60,-Н2О150
п. 477, 600 - K2S
п. 295 разл.
п. 159 разл.
п. 207 разл.
п. 197 разл.
разл. > 600
-Н2О 150
п. 1074, к. « 2000
> 190 — K2SO4
> 258 — K2SO4
п. - 300, > 440 — K2SO4
> 300 -> K2SO4
500 - K2SO4
- 300 — K2SO4
-Н2О 50 (вак.)
« 300 — K2SO4
170 - KF
п. 311
> 70 - K2S2O7
разл. > 430
п. 78,3, -Н2О 200
п. 605
п. 812
п. 820
п. 1020(р), разл. «600
п. 976
п. 1045
разл.« 400
п. - 1000
Окраска
черн.
т.-зел.
св.-зел.
бел.
бел.
желт.
св.-оранж.
оранж.
желт.-кор.
краен.-кор.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
зел.
зел.
бел.
бел.
бел.
бел.
бел.
св.-желт.
Плот-
Плотность
1,805
1,973
2,102
2,128
2,02
2,662
2,34
2,277
2,27
2,336
2,296
2,11
2,477
2,59
2,23
2,35
2,29
3,066
2,46
2,42
2,52
123
I. Неорганические вещества
Продолжение табд.
Формула
К2Те03
(K2Ti)O3
K2UO2(SO4J
•2Н2О
KVO3
K3VO4
K4V2O7
KV(SO4J
• 12H2O
K2WO4
•2H2O
Kr
• 5,75H2O
KrF2
La
(LaAl)O3
LaB6
LaBr3
LaC2
La2(C2O4K
• 10H2O
LaCl3
•7H2O
(LaCrHI)O3
LaF3
LaH3_x
@<jc< 0,1)
Lal3
La2(MoO4K
La(NO3K
•6H2O
Mr
253,79
174,07
540,35
576,38
138,04
232,23
370,27
282,16
498,34
326,03
362,06
83,800
187,39
121,80
138,906
213,89
203,77
378,62
162,93
541,87
722,02
245,27
371,37
238,90
195,90
141,93
519,62
757,62
324,92
433,01
Фазовые переходы
п. 460-470
п. 816
разл.« 700
-Н2О 120
п. 528
п. - 1300
п. 910
Не получен
п. 20, разл. 300
п. 923
-Н2О 320
п.-157,36, к.-153,22
разл. -27,7
возг. > -30
п. 920, к. 3454
п.2383
п. 2740
п. 783, к. - 1700
п. 2360
Не получен
> 600 — La2O3
п. 862, к. 1710
п. 91 разл., разл. 400
п. 2510
п. 1493, к. - 2300
разл. 600—800
п. 779, к. 1580
п.1015
780 — La2O3
п. 43, разл. > 600
Окраска
бел.
бел.
св.-желт.
желт.
бел.
бел.
бел.
фиол.
бел.
бел.
бцв. г.
бцв. ж.
бел.
бел.
бел.
бел.
бел.
св.-фиол.
бел.
желт.
бел.
бел.
бел.
т.-зел.
бел.
т.-сер.
зел.-сер.
св.-сер.
бел.
бел.
Плот-
Плотность
3,58
3,36
2,84
1,78
3,113 '
3,736
2,4153
зд
3,3
6,146 '
5,84
2,61
5,057
5K5 :
3,842 5
6,75 ;
5,936
5,26 4J
5,63
4,77
124
I. Неорганические вещества
Продолжение табл.
формула
La(OHK
LaS
La2S3
La2(SO4K
•9H2O
La2(Se04K
•5H2O
LaSi2
Li
LiA102
Li3As04
LiBO2
•6H2O
Li2B4O7
•5H2O
LiBr
Li2C2
Li(CH3COO)
•2H2O
Li2CO3
U2C2O4
LiCl
H2O
UC1O
LiC102
UCIO3
' 0,25H2O
LiC104
H2O
•зн2о
1 • •->
ЦСгО4
LbCr207
LiD
4
325,81
189,93
170,97
374,01
566,00
728,13
706,68
796,76
195,08
6,941
65,92
159,74
49,75
157,84
169,12
259,19
86,85
37,90
65,99
102,02
73,89
101,90
42,39
60,41
58,39
74,39
90,39
94,89
106,39
124,41
160,44
129,87
229,87
8,96
Фазовые переходы
п. 2313, к. = 4200
> 300 — La2O3
п. 2190
п.2150
1150 —La2O3
-Н2О 600
разл. - 1000
-Н2О 180-200
п. 1520
п. 180,54, к. 1342
п. 1610-1700
п.1150
п. 849, > 1300 — Li2O
п.47,-Н2О110
п. 918
-Н2О 200
п. 552, к. 1310
> 600 — Li
разл. > 275
п.54,5,-Н2О110
п. 618 разл., >732 —Li2O
разл. > 400
п. 610, к. 1382
п. 93,5, -Н2О > 98
> 200 — LiCl
разл. 180
п. 129, разл. 367
п. 42,5, -Н2О 90
п. 247,6, > 438 — LiCl
п. 149, -Н2О210
п.95,1,-2Н2О170
п. - 630
разл. 500
п. 680
Окраска
бел.
бел.
желт.
т.-желт.
бел.
бел.
бел.
бел.
сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.
т.-оранж.
бел.
Плот-
Плотность
6,57
5,75
4,98
3,6
2,801
5,05
0,534
2,56
3,07
1,397
1,38
3,464
1,3
2,111
2,12
2,068
1,78
2,631
2,432
1,841
2,34
0,82
125
I. Неорганические вещества
Продолжение ma(fo
Формула
LiF
Li2Ge03
LiH
Li(HCOO)
Li(HF2)
LiH2PO4
LiHSO4
LiHg
Lil
•3H2O
LiMnO4
•3H2O
Li2MoO4
LiN3
Li3N
LiNH2
Li2NH
LiNO2
• 0,5H2O
LiNO3
•3H2O
(LiNb)O3
Li2O
Li2O2
LiOH
H2O
Li3PO4
Li2S
Li2SO3
•H2O
Li2SO4
•H2O
Li(SO3F)
Li3Sb
Mr
25,94
134,49
7,95
51,96
45,95
103,93
104,01
207,53
133,85
187,89
125,88
179,92
173,82
48,96
34,83
22,96
28,90
52,95
61,95
68,95
122,99
147,84
29,88
45,88
23,95
41,96
115,79
45,95
93,95
111,96
109,94
127,96
106,00
142,58
Фазовые переходы
п. 849, к. - 1700
п. 1239
п. 692, 850 - Li
п. 273, разл. 290-420
разл. 150
п. > 100
п. №(р), > 340 — Li2SO4
п. 596
п. 469, к. 1170 разл.
п. 73, -Н2О 300
Не получен
п. 105, разл. > 190
п. 705
250 — Li3N
п. 8450?), 500 (вак.) — Li
п. 430, > 500 -> Li2NH
> 600 — Li3N
п. 220, 180 (вак.) — Li2O
-Н2О 100-160
п. 253, 475 - Ы2О
п. 30, -Н2О - 70
п. 1260
п. 1453 разл., > 1500 -* Li
400 — Li2O
п. 473, 800 — 1л2О
-Н2О 109
п. 837
п.1370
п. 455 разл.
-Н2О 190
п. 858, 1300-> Li2O
-Н2О < 500
п. 360
п. > 950
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
фиол.
бел.
бел.
зел.-желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
зел.-желт.
бел.
бел.
бел.
бел.
бел.
т.-сер.
Плот-
Плотность
2,6
3,53
0,78
1,46
2,05
2,46
2,123
4,061
3,48
2,06
2,66
1,61
1,38
1,178
1,48
1,615
2,37
1,57
4,628
2,013
2,363
1,44 !¦
1,51
2,537
1,63
2,221
2,06
3,2
¦
126
I. Неорганические вещества
Продолжение табл.
формула
Li2Si03
Li2Si205
Li4Si04
(LiTa)O3
LbWO4
Lr
Lu
LuBr3
Lu2(C2O4K
•6H2O
LuCl3
LuF3
Lul3
Lu2O3
Lu(OHK
Lu2(SO4K
•8H2O
Md
Mg
(MgAl2)O4
Mg3As2
(MgAs2)O6
Mg3(AsO4J
MgB2
Mg(BO2J
• 8H2O~
Mg3(BO3J
Mg3Bi2
MgBr2
•6H2O
%(BrO3J
•6H2O
MgC2
4
89,97
150,05
119,85
235,89
261,72
262,105
174,967
414,68
613,99
722,08
281,33
231,96
555,68
397,93
225,99
638,12
782,24
258,099
24,305
142,27
222,76
270,14
350,75
45,93
109,92
254,04
190,53
490,88
184,11
292,20
280,11
388,20
48,33
Фазовые переходы
п. 1202
п. 1033
п. 1225 разл.
п.1650
п. 740
п.1627
п. 1663, к. 3393
п. 960, к. 1410
Не получен
> 600 — Lu2O3
п. 925, к. 1420
п. 1184, к. 2230
п. 1045, к. 1210
п. 2450
1050 — Lu2O3
> 850 — Lu2O3
-Н2О 650
п. 827
п. 650, к. 1090
п.2135
п. 800
разл. 585
п. 1450(р), разл. > 1100
разл. 1050
п. 988
-Н2О 350
п. 1410
п. 821
п. 711, к. 1250
п. 172,4, -Н2О - 200
разл. > 300
-Н2О 200
500 — Mg2C3
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бур.
бел.
бел.
бел.
бел.
бел.
бел.
краен.-кор.
бел.
бел.
черн.
бел.
бел.
бел.
сер.
бел.
бел.
бел.
бел.
сер.
Плот-
Плотность
2,52
2,28
7,3
3,71
9,841
3,98
8,29
9,424
3,333
1,74
3,55
3,148
3,9
2,29
2,99
5,95
3,72
2,0
2,29
2,073
127
I. Неорганические вещества
Продолжение табл.
Формула
Mg2C3
[Mg(C5H5J]
Mg(CH3COOJ
•4Н2О
MgCN2
MgCO3
•5H2O
MgC2O4
•2H2O
MgCl2
•6H2O
Mg(C103J
•6H2O
Mg(C104J
•6H2O
MgCrO4
•5H2O
(MgCr2)O4
MgF2
(MgFe2)O4
MgH2
MgHAsO4
•7H2O
MgHPO4
•3H2O
Mgl2
Mg(IO3J
•4H2O
MgMoO4
Mg3N2
MgNH4As04
•6H2O
MgNH4PO4
•6H2O
Mr
84,64
154,50
142,39
214,45
64,33
84,31
174,39
112,32
148,35
95,21
203,30
191,21
299,30
223,20
331,29
140,30
230,37
192,29
62,30
200,00
26,32
164,23
290,34
120,28
174,33
278,11
374,11
446,17
184,24
100,93
181,26
289,35
137,31
245,40
Фазовые переходы
> 750 — Mg
п. 177, к. 221
п. 323 разл.
п. 80, -Н2О 134
разл. 1370
п. 990(/?), 650 -> MgO
> 200 — MgO
Не получен
> 150 — MgO
п. 714, к. 1367
п. 117, -Н2О 100-200
Не получен
п. 34,2, разл. > 120
п. 246, разл. > 440
п. 136, 190 — Mg(OHJ
600 -> MgO
-Н2О 200 (вак.)
п. 2350
п. 1263, к. 2272
п. 1750
> 280 — Mg
разл. 650
-Н2О 190
750 -* Mg2P2O7
-Н2О 200
п. 633, к. 1014
> 600 — Mgl2
-Н2О210
п. 1230
п. 2230(/?), > 700 — Mg
Не получен
разл. 800
Не получен
900 - Mg2P2O7
Окраска
св.-сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.
желт.
т.-зел.
бел.
черн.-бур.
сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
св.-желт.
бел.
бел.
Плот-
Плотность
1,42
1,454
3,037
1,72
2,45
2,325
1,56
1,8
2,614
1,97
1,695
4,429
3,127
4,52
1,45
1,94
2,1
4,256
3,3 .
3,87
2,74
1,93
1,71
128
I. Неорганические вещества
Продолжение табл.
формула
•6Н2О
Mg(NO3J
•6Н2О
MgO
MgO2
Mg(OHJ
Mg3P2
Mg(PH2O2J
•6H2O
Mg2P2O7
Mg3(PO4J
•8H2O
MgS
MgSO3
•6H2O
MgSO4
•7H2O
Mg(SO3S)
•6H2O
Mg3Sb2
Mg2Si
Mg2Si04
(MgTi)O3
(Mg2Ti)O4
Mg(VO3J
MgWO4
Mn
(MnAl2)O4
MnAs
MnB2
MnBr2
tMn(C5H5J]
4
252,51
360,60
148,31
256,40
40,30
56,30
58,32
134,86
154,28
262,37
222,55
262,86
406,98
56,37
104,37
212,46
120,37
246,47
136,43
244,52
316,43
76,70
140,69
120,18
160,49
222,18
272,14
54,938
172,90
129,86
76,56
214,75
176,83
185,13
Фазовые переходы
He получен
п. 120, разл. > 250
п. 426(/?,), > 300 - MgO
п. 89,9, 240 — MgO
п. 2827, к. 3600
> 330 - MgO
> 350 — MgO
разл. > 1000
разл. 250—300
-Н2О 180
п.1382
п. 1375
-Н2О 400
п.« 2500 разл.
п. « 500 — MgO
п. 40, -Н2О 200
п. 1137, > 1200-MgO
п. 54, -Н2О 330
разл. 450
п. 82, -Н2О > 240
п. 1250
п. 1102
п. 1890
п. 1630
п. 1732
п. 760 разл.
п. 1360
п. 1246, к. 2061
п. 1560
п. 936
п. 1990
п. 698
п. 1520(/>), разл. 950
п. 173
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
желт.-зел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
сер.
т.-гол.
бел.
бел.
бел.
желт.
бел.
св.-сер.
черн.
черн.
сер.-фиол.
роз.
сер.-черн.
бур.-краен.
Плот-
Плотность
1,72
1,46
3,58
3,29
2,36
2,05
1,59
2,559
2,41
1,64
2,78
1,725
2,66
1,68
1,818
4,09
1,94
3,22
3,91
3,52
5,66
7,2
4,04
6,18
6,9
4,385
6,89
129
5-
2004
I. Неорганические вещества
Продолжение табл.
Формула
МпСО3
[Мп2(СОI0]
[Мп(СОMВг]
[Мп(СОKС5Н5]
[Мп(С0MС1]
[Мп(С0M1]
[Mn(COLNO]
МпС12
•4Н2О
(Мп2пСи)О4
MnF2
MnF3
MnF4
(MnHFe2)O4
[MnH(COM]
Mnl2
(МпиМп2п)О4
Mn(NH4J(SO4J
•6H2O
Mn(NO3J
•6H2O
MnO1+x
@<x<0,13)
MnO2_x
«H2O
Mn2O3
•яН2О
Mn2O7
MnO3F
Mn(OHJ
MnO(OH)
MnP
Mn2P
Mn3P
4
114,95
389,90
274,89
204,06
230,44
321,89
196,98
125,84
197,90
237,42
92,93
111,93
130,93
230,63
196,00
308,75
228,81
283,14
391,23
178,95
287,04
70,94
86,94
—
157,87
—
221,87
121,93
88,95
87,94
85,91
140,85
195,79
Фазовые переходы
разл. > 330
п. 154(р), > 110 — Мп
разл. > 65
п. 77
разл. 120
разл. > 118
п. 1,0, возг. >25
п. 650, к. 1240
п. 58, -Н2О < 198 (вак.)
п. > 1500
п. 900, к. 1640
> 600 -> MnF2
разл. > 70
п. 1570* разл. 1800
п.-25, разл.+150
п. 638
п.1564
Не получен
разл. 180
> 180 — МпО2
п. 25,3, > 160 - МпО2
п.1569
> 530 — Мп2О3
-Н2О 250
940^(МпиМп2п)О4
100 - МпО(ОН)
п. 5,9, > 55 — Мп2О3
п. -38, к. +60(р)
> 220 — МпО
250 — Мп2О3
п. 1147 разл.
п.1327
п. 1105
Окраска
св.-роз.
желт.
оранж.
желт.
св.-желт.
краен.
краен, ж.
роз.
св.-роз.
кор.-черн.
св.-роз.
красн.-бур.
гол.
т.-бур.
бцв. ж.
роз.
кор.-черн.
св.-роз.
св.-роз.
св.-роз.
сер.-зел.
черн.-кор.
черн.
бур.
св.-кор.
т.-зел. ж.
т.-зел. ж.
бел.
черн.
т.-сер.
т.-сер.
сер.-черн.
Плот-
Плотность
3,62
1,75
2,977
2,01
5,01
3,92
3,54
4,87
5,01
4,856
1,83
1,82
5,18
5,026
4,5
2,39620
3,258
4,2
5,39
130
I. Неорганические вещества
Продолжение табл.
формула
Mn3P2
Мп4Р
Мп2Р2О7
Мп3(РО4J
•ЗН2О
MnS
•лН2О
Mn(S2)
MnSO4
•Н2О
•5Н2О
•7Н2О
Mn2(SO4K
• H2SO4 • 4Н2О
MnSe
MnSi
Mn2Si
Mn3Si
Mn5Si3
MnSiO3
Mn2Si04
MnWO4
(Mn2nZn)O4
HMnO4
•2H2O
Mo
MoB
Mo2B
Mo2B5
MoBr2
MoBr3
MoBr4
MoBr2O2
MT
226,76
250,73
283,82
354,75
408,80
87,00
—
119,07
151,00
169,02
241,08
277,11
398,06
568,20
133,90
83,02
137,96
192,90
358,95
131,02
201,96
302,77
239,26
119,94
155,97
95,940
106,75
202,69
245,94
255,75
335,65
415,56
287,75
Фазовйе переходы
разл. 1090
п. 1085 разл.
п. 1195
п.1152
-Н2О 320
п.1530
-Н2О 175
800 - MnS
п. 700,
>850 —(МппМп?!1)О4
-Н2О 280
п. 55 разл.
п. 8,6 разл.
> 300 — MnSO4
> 160 — MnSO4
п.1510
п. 1270
п. 1316
п. 1075 разл.
п.-1300
п.1323
п. 1327
п. > 1400
п. > 2000
Не получена
> 20 — МпО2
п. 2623, к. 4639
п. 2550
п. 2270 разл.
п. 2200 разл.
разл. > 700
500 — МоВг2
> 110-* МоВг3
п. 265(р,), возг. 235
Окраска
т.-сер.
черн.
бур.-роз.
роз.-бел.
св.-роз.
сер.-зел.
св.-роз.
черн.
бел.
св.-роз.
роз.
роз.
зел.
т.-краен.
сер.
сер.
сер.
т.-сер.
т.-сер.
роз.
краен.
желт.
т.-бур.
фиол.
св.-сер.
сер.
сер.
сер.
желт.-кор.
черн.
черн.
т.-зел.
Плот-
Плотность
5,12
3,71
3,1
3,99
3,95
3,46
3,25
2,95
2,103
2,09
3,24
5,55
5,9
6,2
3,72
4,1
7,12
5,2
10,2
8,65
9,26
7,12
4,88
131
I. Неорганические вещества
Продолжение табл.
Формула
МоВг3О
МоС
Мо2С
[Mo(CN)8],K4
•2Н2О
[Мо(СОN]
[Мо2(СОL(С5Н5J]
МоС12
МоС13
МоС14
МоС15
MoCl3N
МоС12О2
МоС13О
МоС14О
MoF3
MoF5
MoF6
[MoF6],K3
Mol2
Mol3
Mol4
Mo2N
MoO2
MoO3
•H2O
•2H2O
Мо4Ои
Mo(O)F4
MoO2F2
MoO(OHJ
MoO(OHK
[Mo(PF3N]
MoS2
4
351,65 "
107,95
203,89
460,48
496,51
264,00
434,11
166,85
202,30
237,75
273,21
216,31
198,84
218,30
253,75
152,93
190,93
209,93
327,22
349,75
476,65
603,56
205,89
127,94
143,94
161,95
179,97
559,75
187,93
165,93
145,95
162,96
623,75
160,07
Фазовые переходы
возг. 391
п. 2570
п. 2400 разл.
разл. > 220
-Н2О 105
п. 148, к. 155 разл.
п. 215-217, > 225 —Мо
разл. 700
разл. 410
возг. ~ 180, разл. > 200
п. 194,4, к. 269
возг. 130
п. 175, к. 357
п. 308
п. 105, к. 253
разл. > 500
п. 67, к. 214
п. 17,58, к. 33,88
п. 734
п.« 700
п. ~ 900
п. ~ 400
п.« 2000
возг. 1030, к. > 1100 разл.
п. 801, к. 1155
-Н2О 150-450
-1Н2О 70-115
п. 818 разл.
п. 97,2, к. 186
возг. 270
900 - МоО2
разл. > 800
п. 196
возг. 450, > 1100 —Mo2S3
Окраска
черн.
сер.
т.-сер.
желт.
желт.
бел.
красн.-бур.
желт.
т.-краен.
кор.
черн.-бур.
красн.-бур.
св.-желт.
кор.-черн.
зел.
св.-зел.
желт.
бцв. ж.
бур.
черн.
черн.
черн.
черн.
кор.
зел.-бел.
бел.
желт.
фиол.
бел.
бел.
т.-зел.
бур.
бел.
сер.
Плот-
Плотность
8,78
9,18
2,34
1,96
3,714
3,578
2,928
3,31
3,15
4,64
3,44
2,54319
6,43
9,44
6,53
4,72
3,112
3,124
4,18
3,41
3,494
5,06
132
I. Неорганические вещества
Продолжение табл.
формула
MoS3
Mo2S3
MoSe2
MoSi2
N2
N(C1)F2
ND3
ND4CI
NF3
транс-N 2^2
j<wc-N2F2
N2F4
N3F
NH3
• 0,5H2O
H2O
•2H2O
N2H4
H2O
(NH4JB4O7
NH4Br
NH4(CH3COO)
N2H5(CH3COO)
NH4CN
(NH4JCO3
(nh4Jc2o4
H2O
NH2C1
NH4C1
N2H5C1
N2H6C12
NH4C1O3
4
192,14
288,08
253,86
152,11
28,014
87,46
20,05
57,52
71,00
66,01
66,01
104,01
61,02
17,03
26,04
35,05
53,06
32,05
50,06
191,32
97,94
77,08
92,10
44,06
96,09
124,10
142,11
51,48
53,49
68,51
104,97
101,49
Фазовые переходы
> 250 — MoS2
п. ~ 1600 разл.
разл. 900 (вак.)
п. 2030
п. -210, к. -195,79
п. -190,5, к. -65,9
п. -74,36, к. -31,04
п. - 300
п. -206,78, к. -129
п.-172, к.-111,4
п. -195, к. -105,7
п.-161,5, к.-74,2
п.-154, к.-82
п. -77,75, к. -33,4
п. -78,2, разл. +80
п. -77 разл.
п. -97, разл. > -85
п. 1,5, к. 113,5
п.-51,6, к.+120,1
разл. 190
> 394 — NH3
п. 114 разл.
п. 101
разл. 36
58 -> NH3
Не получен
разл. > 120
п. —66, разл. > —40
п. 400(/?), возг. > 337,6
п. 92, 350 - N2H4
п. 198 разл.
разл. -100
Окраска
т.-кор.
сер.
т.-сер.
т.-сер.
бцв. г.
бцв. ж.
бел.
бцв. г.
бцв. г.
бел.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
т.-желт. г.
бцв. г.
бел.
бел.
бел.
бцв. ж.
бцв. ж.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бцв. ж.
бел.
бел.
бел.
бел.
Плот-
Плотность
5,8
6,31
1,2506
0,8196
0,8792
3,168
0,771
1,01215
1,03220
2,429
1,073
1,5
1,526
1,42
1,8
133
I. Неорганические вещества
Продолжение табл.
Формула
NH4C1O4
N2H5C1O4
(NH4JCr04
(NH4JCr207
(NH)F2
NH4F
NH4(H2As04)
NH4HCO3
NH4HC2O4
NH4(HCOO)
NH4(HF2)
NH4H(PHO3)
NH4(H2PO4)
(NH4JHPO4
NH4HS
NH4HSO3
NH4HSO4
(NH4I0H2W12O42
NH4I
NH4IO3
NH4IO4
NH4Mn04
(NH4NMo7O24
•4H2O
NH4N3
N2H5N3
NH4NCS
NH4(NH2COO)
NH4NO2
NH4NO3
N2H5NO3
N2H6(NO3J
NH4OCN
NH2OH
Mr
117,49
132,50
152,07
252,06
53,01
37,04
158,97
79,06
107,07
63,06
57,04
99,03
115,03
132,06
51,11
99,11
115,11
3060,56
144,94
192,94
208,94
136,97
1163,79
1235,85
60,06
75,08
76,12
78,07
64,04
80,03
95,06
158,07
60,06
33,03
Фазовые переходы
разл. 210-270
п. 142,4, разл. 150-200
разл. 120—185
> 170 — N2
п.-116,8, к.-23,3
разл. > 167
разл. 284
п. 106(р), разл. 36—70
п. 220 разл.
п. 119, разл. 180
п. 126,45, к. 238 разл.
п. 123, разл. 145
п. 1920), разл. 140
разл. 70
п. 120О), разл. > 20
разл.150
п. 251, к. 490
> 400 - NH3
возг. 404,7, > 450 — NH3
разл. 150
разл. 220
> 60 - N2
> 350 - NH3
-Н2О 90 (вак.)
п. 160
п. 75, разл. 130-170
п. 149,6, к. 170 разл.
п. 133,5, возг. 60
60-70 - N2
п. 169,6, к. 235
п. 70,7, разл. < 300
п. 104 разл.
60 — C(NH2JO
п. 32, к. 58 (вак.)
Окраска
бел.
бел.
желт.
оранж.
бцв. г.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
фиол.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
Плот-
Плотность
1,952
1,91
1,89
2,15
1,002
2,34
1,586
1,27
1,505
1,803
1,619
1,17
2,03
1,78
2,514
3,309
3,06
2,22
2,498
1,436
1,4
1,3057
1,69
1,72
1,68
1,355
134
I. Неорганические вещества
Продолжение табл.
формула
(NH3OH)C1
(NH3OH)C1O4
(NH3OH)HSO4
(NH3OH)NO3
(NH3OHJSO4
NH4(PH2O2)
NH4Re04
N2H6SO4
(NH4JSO3
•H2O
(NH4JSO4
(N2H5JSO4
NH4(SO3F)
(NH4JS2O6(O2)
(NH4J(SO3S)
(NH4JSeO4
NH4Tc04
(NH4JTe04
(NH4JU2O7
NH4VO3
(NH4KVS4
NO
NO2
N2O
N2O3
N2O5
(NO)Br
(NO)C1
(NO2)C1
(NO)C1O4
(NO2)QO
(NO2)QO4
(NO)F
N(O)F3
Mr
69,49
133,49
131,11
96,04
164,14
83,03
268,24
130,12
116,14
134,16
132,14
162,17
117,10
228,20
148,21
179,03
179,94
227,67
624,13
116,98
233,32
30,01
46,01
44,01
76,01
108,01
109,91
65,46
81,46
129,46
94,76
145,45
49,00
87,00
Фазовые переходы
п. 152разл.
п. 89, разл. > 150
п. 57
п. 48, разл. > 100
п. 172 разл.
п. 200, разл. 240
365 (вак.) — N2
п. 254, разл. > 270
п. 80,8, разл. 120—170
-Н2О 20 (вак.)
разл. 235-357
п. ПО, разл. 180
п. 245
разл. 120
разл. 150
разл. > 500
800 - N2
разл. > 575
350 — NH3
п. 138 разл., > 150 — NH3
60-150 — NH3
п.-163,7, к.-151,6
п.-11,2, к.+20,6
п.-91, к.-88,65
п. -101, к. -40 разл.
п. 41(р), возг. 33
п. -55,5, разл. > +25
п. -59,6, к. -5,7
п.-141, к.-14,3
разл. > 140
п. -107, к. +22,3
разл. 150
п. -132,5, к. -59,9
п. -160, к. -85
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.
бел.
т.-фиол.
бцв. г.
бур. г.
бцв. г.
гол. ж.
бел.
краен, г.
т.-оранж. г.
бцв. г.
бел.
св.-желт. ж.
бел.
бцв. г.
бцв. г.
Плот-
Плотность
1,67
2,065
2,515
3,97
1,373
1,41
1,766
1,75
1,982
1,68
2,19
3,01
2,326
1,62
1,3402
2,0527
1,9778
1,4472
2,05
2,992
2,57
2,169
2,22
2,335
3,88
135
I. Неорганические вещества
Продолжение табл.
Формула
(NO2)F
(NO)HSO4
(NO2)NH2
(NO2)OF
(NOJS2O7
(NO2JS2O7
NO2(SO3F)
HN3
HNCO
HNCS
HNO3
H2N2O2
Na
NaAlO2
NaAl(SO4J
• 12H2O
NaAsO2
NaAsO3
Na3As04
• 12H2O
Na4As207
Na3AsS4
NaBO2
•4H2O
NaB3O5
NaB5O8
•5H2O
Na2B4O7
•4H2O
•5H2O
• 10H2O
Na2B8O13
NaBr
•2H2O
4
65,00
127,08
62,03
81
236,14
268,14
145,07
43,03
43,03
59,09
63,01
62,03
22,990
81,97
242,10
458,28
129,91
145,91
207,89
424,07
353,80
272,16
65,80
137,86
135,42
205,04
295,11
201,22
273,28
291,29
381,37
340,46
102,89
138,92
Фазовые переходы
п.-165,9, к.-72,31
п. 73,5 разл.
п. 75 разл.
п. -175, к. -45
п. 233, к. 360
п. 151
п. 218
п. -80, к. +35,7
п. -80, к. +23,5
п. -ПО, разл. +5
п.-41,59, к.+82,6 разл.
25 -> N2O
п. 97,72, к. 883
п.> 1650
800 — Na2SO4
п. 61,-Н2О> 170
разл. 300—550
п. 615
п.« 1050
п. 86,3, -Н2О 150
п. 835, разл.1000
разл. 450—500
п. 966, к. 1434
п. 57, -Н2О 306
п. 765
п. 785 разл., 850 — NaBO2
п. 117,-Н2О350
п. 742, к. 1575 разл.
-4Н2О 380
-1Н2О 136
п. 60,8, -5Н2О > 61
п. 816
п. 747, к. 1390
п. 58, -Н2О 50,6
Окраска
бцв. г.
бел.
бел.
бцв. г.
бел.
бел.
бел.
бцв. ж.
бцв. ж.
бцв. ж.
бцв. ж.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
св.-желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел. '
бел.
бел.
бел.
бел.
бел.
Плот-
Плотность
2,9
1,12620
1Д420
1,50325
0,97
2,693
1,675
1,87
2,301
2,835
1,76
2,21
2,462
1,743
2,2
1,713
2,279
1,903
1,88
1,705
2,32
3,211
2,18
136
I. Неорганические вещества
Продолжение табл.
формула
NaBrO2
NaBrO3
Na2C2
Na(CH3COO)
•3H2O
NaCN
Na2CO3
• 10H2O
• 1,5H2O2
Na2C2O4
Na2Ca(CO3J
•5H2O
Na2Ca(SO4J
•4H2O
NaCl
•2H2O
NaCIO
•5H2O
NaC102
•3H2O
NaC103
NaC104
•H2O
NaCrO2
Na2Cr04
• юн2о
Na2Cr207
•2H2O
NaCrS2
NaF
NaFeO2
Na2Ge03
•7H2O
Xl T 1
NaH
Mr
134,89
150,89
70,00
82,03
136,08
49,01
105,99
286,14
157,01
134,00
206,7
296,15
278,18
350,24
58,44
94,47 .
74,44
164,52
90,44
144,49
106,44
122,44
140,45
106,98
161,97
342,12
261,97
298,00
139,12
41,99
110,84
166,59
292,69
24,00
Фазовые переходы
разл. > 200
п. 380 разл.
п. 800 разл.
п. 324
п. 58, -Н2О 120
п. 563,7, к. 1497
п. 857,5, > 1000 - Na2O
п. 32,5,-Н2О 112,5
-Н2О2140
п. 260, разл. > 400
разл. > 1000
-Н2О 110-130
разл. > 950
-Н2О > 160
п. 800,8, к. 1413
п.0,15,-Н2О~20
Не получен
п. 24,4, разл. 30—50
разл. 180—200
-Н2О 37,4
п. 263, разл. > 465
п. 469 разл., > 525-* NaCl
п. 50,8, -Н2О 130
п. - 1700
п. 794
п. 19,52, -Н2О 100 (вак.)
п. 320, > 400 — Na2Cr04
п. ПО,-Н2О> 120 (вак.)
разл. > 850
п. 996, к. 1700
п. 1350
п. 1060
п. 83, -Н2О 300
п. 638(/>), 430 (вак.) — Na
Окраска
желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
зел.-сер.
желт.
св.-желт.
оранж.
оранж.
сер.-зел.
бел.
кор.-зел.
бел.
бел.
бел.
Плот-
Плотность
3,339
1,6
1,528
1,45
1,5955
2,509
1,446
2,144
2,34
2,04
2,8
2,161
1,574
2,468
2,493
2,495
2,02
4,39
2,723
1,48
2,52
3,2
2,766
4,05
3,31
1,38
137
I. Неорганические вещества
Продолжение табл.
Формула
NaH2As04
•Н2О
Na2HAs04
•7Н2О
Na2H2As207
NaHCO3
Na3(HCO3)CO3
•2Н2О
Na(HCOO)
Na(HF2)
Na2H2Ge04
•6H2O
NaH4IO6
•H2O
Na3H2IO6
NaH(PHO3)
• 2,5H2O
NaH2PO4
•H2O
•2H2O
Na2HPO4
•2H2O
•7H2O
• 12H2O
Na2H2P2vO6
•6H2O
Na2H2P2O7
•6H2O
NaHS
NaHSO3
NaHSO4
•H2O
NaHSeO3
• H2SeO3
Mr
163,92
181,94
185,91
312,01
309,83
84,01
189,99
226,02
68,01
61,99
184,60
292,69
249,92
267,94
293,88
103,98
149,01
119,98
137,99
156,01
141,96
177,99
268,06
358,14
205,94
314,03
221,94
330,03
56,06
104,06
120,06
138,08
150,96
279,93
Фазовые переходы
разл. > 230
-H2O 90
разл. 220
п. 57, -Н2О 100
230 — NaAsO3
> 250 - Na2CO3
Не получен
разл. 135
п. 258, > 300 - Na2C2O4
п. 390(р), 270 - NaF
Не получен
п. 85, разл. > 650
Не получен
разл. 175
п. 200 разл.
разл. - 200
п. 42, -Н2О 100
160 - Na2H2P2O7
п. 57,4, -1Н2О 100
п. 40,8, -1Н2О 55
300 — Na4P2O7
-Н2О 95
п.48,1,-5Н2О50
п. 35,1,-5Н2О40
п. 250, разл. 600
-Н2О 100
> 220 — NaPO3
-Н2О 80 (вак.)
п. 350, 500 — Na2S
> 25 — Na2SO3
п. 186, 320 — Na2S2O7
п. 58,5, -Н2О 125 (вак.)
Не получен
п. 110,2, разл. 320
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
Плот-
Плотность
2,53
1,864
2,159
2,15
1,919
2,16
2,05
2,04
1,91
2,066
1,679
1,52
1,85
1,862
1,85
1,79
1,48
2,476 .
2,103
138
I. Неорганические вещества
Продолжение табл.
формула
Na2H4Te06
NaHg
NaHg2
NaHg4
Na3Hg
Na3Hg2
Na5Hg2
Na7Hg8
Nal
•2H2O
NaIO3
•H2O
NaIO4
•3H2O
Na5IO6
Na2Mg(CO3J
H2O
Na2Mg(SO4J
•4H2O
NaMnO4
•3H2O
Na2Mn04
• юн2о
Na3Mn04
Na2MoO4
•2H2O
NaN3
Na3N
NaNCS
NaNH2
tNa(NH3L]l
NaNH4HPO4
•4H2O
NaNO2 '
4
273,61
223,58
424,17
825,35
269,56
470,15
516,13
1765,65
149,90
185,92
197,89
215,91
213,89
267,94
337,85
190,30
208,32
262,41
334,47
141,92
195,97
164,91
345,06
187,90
205,92
241,95
65,01
82,98
81,07
39,01
218,02
137,01
209,07
69,00
Фазовые переходы
разл. > 250
п. 212
п. 354
п. 136 разл.
п. 35 разл.
п. 119 разл.
п. 66 разл.
п. 222 разл.
п. 661, к. 1307
п. 68,9, -Н2О 80 (вак.)
п. 422, 500 — Nal
-Н2О 100 (вак.)
п. 300 разл., 325 — NaIO3
-Н2О110(вак.)
разл. 800
Не получен
разл. > 250
Не получен
разл. > 240
Не получен
разл. 170
Не получен
п. 17, разл. 470
п. 1250
п. 687
-Н2О 150
п. » 200, разл. 250—300
200 — Na
п. 287, 300 разл.
п. 208, к. 400
п. 3,0, разл. > 25
Не получен
п. 79 разл.
п. 271,700 —Na2O
Окраска
бел.
сер.
сер.
сер.
сер.
сер.
сер.
сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
фиол.
зел.
т.-зел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
Плот-
Плотность
3,6714
2,448
4,277
3,865
3,22
2,41
2,25
2,46
2,68
2,61
3,62
3,28
1,846
1,84
1,735
1,39
1,554
2,168
139
I. Неорганические вещества
Продолжение табл.
Формула
NaNO3
Na2N2O2
Na4N2O4
(NaNb)O3
NaO2
Na2O
Na2O2
NaOCN
NaOH
•H2O
Na(PH2O2)
•H2O
Na2(PHO3)
•5H2O
NaPO3
Na3PO4
• 12H2O
Na4P2vO6
• 10H2O
Na4P2O7
• 10H2O
Na5P3O10
•6H2O
Na2(PO3F)
NaReO4
Na2S
•6H2O
•9H2O
Na2(S2)
Na2(S4)
Na2(S5)
Na2SO3
•7H2O
Na2SO4
• 10H2O
MT
84,99
105,99
183,97
163,89
54,99
61,98
77,98
65,01
40,00
58,01
87,98
105,99
125,96
216,03
101,96
163,94
380,12
249,90
430,05
265,90
446,05
367,86
475,95
143,95
273,19
78,05
186,14
240,18
110,11
174,24
206,31
126,04
252,15
142,04
322,19
Фазовые переходы
п. 306,6, > 380 - NaNO2
разл. 335
разл. 50—100
п. 1422
270 — Na2O2
п. 11320), разл. > 700 (вак.)
п. 596(/?), 540 — Na2O
п. 550, разл. 700 (вак.)
п. 323, к. 1403
п. 65,1, -Н2О 100 (вак.)
разл. 240
-Н2О 170
Не получен
п. 53, разл. 120-250
к. > 630
п. 1340
п. 73,3-76,7, -Н2О > 100
Не получен
разл. > 250
п. 895
п. 79,5, -Н2О 220
п. 692 разл., 700 — Na4P2O7
-Н2О 120
п. 625
п. 300, разл. 410
п. 1168
п. 80,-Н2О110
п. 49, -ЗН2О 60
п. 475, 600 - Na2S
п. 285 разл.
п. 260 разл.
п. 9110?), разл. >600
п.28,-Н2О150
п. 884, к. 1429
п. 32,384, -Н2О 100
Окраска
бел.
бел.
желт.
бел.
т.-желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
св.-желт.
т.-желт.
желт.-кор.
бел.
бел.
бел.
бел.
Плот-
Плотность
2,266
2,466
5,325
2,21
2,37
2,61
1,893
2,02
1,829
2,58
2,536
1,62
1,82
2,534
1,815
2,555
2,12
5,24
1,856
1,426
2,08
2,08
2,633
1,539
2,663
1,465
140
I. Неорганические вещества
Продолжение табл.
формула
Na2S2O4
•2Н2О
Na2S2O5
•7Н2О
Na2S2O6
•2Н2О
Na2S2O7
Na2S2O6(O2)
Na2(SO3S)
•5H2O
Na3Sb
NaSbO2
•3H2O
Na2Se
Na2Se03
•5H2O
Na2Se04
• 10H2O
Na2Si03
•9H2O
Na2Si205
Na2Si307
Na4Si04
Na6Si207
(NaTa)O3
Na2Te
•9H2O
(Na2Ti)O3
NaVO3
•2H2O
Na3VO4
Na4V2O7
Na2\VO4
•2H2O
Mr
174,11
210,14
190,11
316,21
206,11
242,14
222,11
238,10
158,11
248,18
190,73
176,75
230,79
124,94
172,94
263,01
188,94
369,09
122,06
284,20
182,15
242,23
184,04
306,11
251,94
173,58
335,72
141,86
121,93
157,96
183,91
305,84
293,82
329,85
Фазовые переходы
разл. > 52
-H2O 40
150 —Na2SO3
п. 5,5, -Н2О 60
267 — Na2SO4
-Н2О 60-100
п. 405, > 460 - Na2SO4
250 — Na2S2O7
> 220 — Na2SO3
п. 48,5, ~Н2О 100-110
п. 1010
п. > 800
-Н2О 150
п. 875
п. 711 разл., 800 — Na2Se
п. 35,9, -Н2О > 40 (вак.)
п. 730(/>), 500 — Na2Se03
-Н2О 125
п.1088
п. 47, -Н2О 100-300
п. 874
разл. 700
п. 1120 разл.
п. 1115(р), разл. 620
п. 1030
п. 1035
-Н2О 90
п. 1030
п. 632
-Н2О 300-400
п. 1285
п. 654
п. 698
-Н2О 120-150
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
син.-черн.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
сер.
бел.
бел.
сер.
желт.-бел.
бел.
св.-кор.
бел.
бел.
бел.
Плот-
Плотность
1,48
2,175
2,189
2,658
2,345
1,715
2,67
2,86
2,5
3,07
2,7
3,21
1,61
2,61
2,6
2,467
2,58
2,96
2,9
3,195
2,85
2,79
4,179
3,5
141
I. Неорганические вещества
Продолжение табл.
Формула
Na6W7O24
• 16Н2О
Na4Xe06
(Na2Zr)O3
Nb
Nb3Al
NbB2
NbBr4
NbBr5
Nb3Br8 + Jf
@,01 <x< 1,12)
NbBr3O
@<jc<0,3)
Nb2C
[Nb(C5H5)Cl3]
[Nb(C5H5JCl2]
[Nb(COLC5H5]
NbCl4
NbCl5
Nb3Cl8 + JC
@,01<x< 1,39)
[Nb6Cl12]Cl2
NbCl3O
NbF5
[NbF7],K2
•H2O
Nb3Ga
Nb3Ge
NbH,.,
(-0,05 < x < 0,3)
NbH2
Nbl4
Nbl5
4
1808,80
2097,04
319,24
185,20
92,906
305,70
114,53
412,52
492,43
917,95
348,62
104,92
197,82
299,81
294,00
270,04
234,72
270,17
562,34
1053,78
215,26
187,90
304,09
322,10
348,44
351,33
93,91
94,92
600,52
727,43
Фазовые переходы
разл. - 1000
-H2O 300
360 — Na2O
разл.1500
п. 2477, к. 4744
п. 2040 разл.
п.3035
возг. 300
п. 267,5, к. 361,6
возг. 400
разл. > 320
п. 3613
п. 2990 разл.
возг. 210
разл. > 400
п. 146,5
возг. 275, разл. > 320
п. 204,7, к. 247,5
800 — [Nb6Cl12]Cl2
разл. > 900 (вак.)
п. 429 разл.
п. 79,5, к. 234,5
п. 736
разл. 100
п. * 1900 разл.
п. 1970 разл.
600-800 -> Nb
> 400 — Nb
возг. > 420
п. 310, >330-»NbI4
Окраска
бел.
бел.
бел.
бел.
св.-сер.
св.-сер.
бел.
кор.-черн.
т.-краен.
черн.-кор.
желт.
сер.
т.-сер.
т.-краен.
бур.
краен.
кор.-черн.
бел.
черн.-кор.
черн.-кор.
бел.
бел.
бел.
бел.
сер.
сер.
т.-сер.
сер.
сер.
оранж.
Плот-
Плотность
3,99
8,57
6,97
4,72
4,36
5,4
7,82
7,7
3,14
2,75
3,75
3,78
3,19
3,293
3,2
5,64
5,29
142
I. Неорганические вещества
Продолжение табл.
формула
Nb3I8
Nb6In
NbI2O
NbI3O
NbN
Nb2_xN^
NbO,.,
(-0,01 <*< 0,018)
NbO2
Nb2O5
[Nb(O)F6],(NH4K
NbS2
Nb2(SO4)O4
Nb2(SO4JO3
NbSi2
NbSi4
Nb3Si
Nb5Si3
Nb3Sn
Nd
NdB6
NdBr3
Nd(BrO3K
•9H2O
NdC2
Nd2(C2O4K
• юн2о
NdCl3
•6H2O
Nd(C104K
•6H2O
NdF3
XT jt
Ndl3
ч
1293,95
1953,38
362,71
489,62
106,91
199,82
108,91
124,90
265,81
277,01
157,04
345,87
425,93
149,08
205,25
306,80
548,79
397,43
144,240
209,11
383,95
527,94
690,08
168,26
552,53
732,68
250,60
358,69
442,59
550,68
201,23
524,96
Фазовые переходы
800-Nb6In
разл. > 950
разл. > 500
> 150 -> Nb
разл. 2320
п. 2630
п. 1945
п. 1917
п. 1510
разл. 225—420
разл. 1050
> 600 — Nb2O5
разл. 525
п.1950
п.2580
п. 1945 разл.
п. 2480
п. 2130 разл.
п. 1016, к. 3066
п. » 2600
п. 683, к. 1540
разл. 450
п. 66,7, -Н2О 150
п. 2300 разл.
Не получен
> 600 - Nd2O3
п. 758, к. 1690
п. 124, -Н2О > 160
Не получен
разл. > 170
п. 1377, к. 2300
п. 787, к. 1350
Окраска
черн.
черн.-кор.
черн.-кор.
черн.
желт.-сер.
сер.
т.-сер.
черн.
бел.
бел.
черн.
бел.
бел.
сер.
сер.
т.-сер.
т.-сер.
сер.
св.-сер.
син.
фиол.
краен.
св.-краен.
желт.
роз.
роз.-фиол.
краен.
роз.-фиол.
св.-роз.
зел.
Плот-
Плотность
5,89
5,4
8,3
8,23
7,28
5,91
4,55
2,28
3,6
3,42
5,66
8,01
7,53
7,13
7,008
5,15
4,134
2,28
143
I. Неорганические вещества
Продолжение табд.
Формула
Nd2(MoO4K
Nd2O3
Nd(OHK
Nd2S3
Nd2(S)O2
Nd2(SO4K
•8H2O
Ne
Ni
(NiAl2)O4
NiAs
NiAs2
Ni3(As04J
•8H2O
Ni(As)S
Ni2B
NiBr2
•6H2O
Ni3C
[Ni(C5H5J]
Ni(CH3COOJ
•4H2O
[Ni(C4H7O2N2J]
Ni(CNJ
•2H2O
[Ni(CNL],K2
•H2O
NiCO3
•6H2O
[Ni(COL]
[Ni2(COJ(C5H5J]
4
665,62
336,48
195,26
384,68
352,54
576,67
720,79
20,180
58,693
176,65
133,62
208,54
453,92
598,04
165,68
128,20
218,50
326,59
188,09
188,88
176,78
248,84
288,92
110,73
146,76
240,96
258,98
118,70
226,79
170,73
303,60
Фазовые переходы
п.1176
п. 2320, к. ~ 4300
> 350 - Nd2O3
п. 2010 разл.
п. 1990
> 800 — Nd2O3
-Н2О 350
п. -248,59, к. -245,93
п. 1455, к. 2913
п. 2110
п. 964
830 — NiAs
разл. 1000
-Н2О 200
разл. 700
п. 1240
п. 963(р), возг. 919
п. 28,5, -Н2О 150-200
разл. 380—450
разл. 173—200
разл. 250
-Н2О 90
возг. 250
разл. 400
-Н2О 180
разл. 500
-Н2О 100
> 300 -> NiO
разл. 140
п. 17,2, к. 42,2 разл.
п. 139 разл., 180 -* Ni
Окраска
св.-фиол.
гол.-фиол.
роз.
т.-зел.
гол.-бел.
фиол.
краен.
бцв. г.
бцв. ж.
бел.
бел.
гол.
св.-краен.
св.-краен.
желт.
зел.
сер.
желт.-сер.
желт.-кор.
зел.
сер.-черн.
т.-зел.
желт.
зел.
краен.
св.-фиол.
св.-фиол.
св.-краен.
т.-оранж.
желт.-зел.
гол.-зел.
бцв. ж.
т.-зел.
Плот-
Плотность
5,14
7,327
5,49
2,85
0,9002
1,244*
1,444
8,902
4,45
7,78
7,1
3,07
5,9
4,64
5,45
7,97
1,8
1,82
1,875
4,375
1,97
1,3120
144
I. Неорганические вещества
Продолжение табл.
формула
NiCl2
6Н2О
Ni(C104J
•6Н2О
NiF2
•4Н2О
[NiF6],K2
[NiF6],K3
Ni(HCO3J
Ni(HCOOJ
•2H2O
Nil2
•6H2O
Ni(IO3J
• 4H2O
Ni3N
Ni3N2
Ni(NH2J
[Ni(NH3N]Br2
[Ni(NH3N]Cl2
[Ni(NH3N]I2
Ni(NH4J(SO4J
•6H2O
Ni(NO3J
•6H2O
Nb03 • лН2О
Ni(OHJ
NiO(OH)
Ni2p
NI3P
NisP2
lNi(PF3L]
NbP2O7
""
4
129,60
237,69
257,59
365,68
96,69
168,75
250,88
289,98
180,73
148,73
184,76
312,50
420,59
408,50
480,56
190,09
204,09
90,74
320,69
231,79
414,69
286,90
394,99
182,70
290,79
74,69
—
92,71
91,70
148,36
207,05
355,41
410,57
291,33
Фазовые переходы
п. 1009(/>)
-H2O 250
400 - NiCl2
-H2O 140
п. 1452, к. 1474
-Н2О 400
разл. 400
разл. ~ 500
разл. 120
Не получен
разл. > 260
п. 797(/?), > 300 - Ni
п. 43, -Н2О 140
разл. 250
-Н2О-100
разл. > 650
585 - Ni
80 — Ni3N2
160 — NiBr2
> 176,5 — NiCl2
135^NiI2
разл. > 250
-H2O 130
> 500 - NiO
п. 54, 300 — NiO
п. 1682(/>), 1230 -> Ni
200 — NiO(OH)
230-250 -> NiO
> 250 -> NiO
n. 1106
n. 1025
n.1175
n. -55, к. +70,5
n. 1400
Окраска
желт.
зел.
св.-желт.
зел.
зел.-желт.
св.-зел.
т.-краен.
фиол.
св.-зел.
св.-зел.
черн.-зел.
гол.-зел.
желт.
зел.
черн.-сер.
черн.
краен.
гол.-фиол.
гол.-фиол.
св.-гол.
зел.-гол.
зел.
зел.
св.-зел.
желт.
сер.-черн.
св.-зел.
черн.
син.-черн.
черн.-сер.
т.-сер.
бцв. ж.
желт.
Плот-
Плотность
3,54
1,91
4,72
2,219
2,9
5,834
5,07
7,66
7,52
1,84
1,468
2,1
1,92
2,04
7,45
4,83
4,1
4,35
6,31
4,09
145
I. Неорганические вещества
Продолжение табл.
Формула
Ni3(PO4J
•8Н2О
@ < jc < 0,2)
Ni(S2)
Ni3S2
Ni3S4
NiSO4
•7H2O
NiS2O6
•6H2O
NiSb
Ni(Sb)S
Nii_*Se
Ni(Se2)
NiSeO4
•6H2O
NiSi
NiSi2
Ni2Si
Ni2Si04
Ni(Te2)
No
Np
NpBr3
NpBr4
Np(C2O4J
•6H2O
NpCl3
NpCl4
NpF3
NpF4
NpF5
Mr
366,02
510,14
90,76
122,83
240,21
304,34
154,76
280,86
218,82
326,91
180,45
212,52
137,65
216,61
201,65
309,74
86,78
114,87
145,47
209,47
313,89
259,101
237,048
476,76
556,66
413,08
521,17
343,41
378,86
294,04
313,04
332,04
Фазовые переходы
п. 1345
-H2O 260
п. 997
п. 1007
п. 808 разл.
разл. 356
> 700 - NiO
п. 31,5,-Н2О280
110-*NiSO4
-Н2О 70 (вак.)
п. 1160
разл. > 1000
п. 980
разл. 850
Не получен
разл. ~ 300
п. 992
п.1280
п. 1318
разл. 1545
разл. 950
п. 827
п. 644, к. 3902
п. 750
п. 464
Не получен
> 400 — NpO2
п. 802, к. - 1500
п. 518, к. 850
п. 1425, к. 2223
п. 830, к. 1480
разл. > 500
Окраска
желт.
зел.
желт.
т.-сер.
желт.
сер.
св.-желт.
зел.
желт.
зел.
т.-краен.
св.-сер.
сер.
т.-сер.
зел.
сер.-бел.
сер.-бел.
сер.-бел.
св.-зел.
т.-сер.
бел.
зел.
т.-краен.
зел.
сер.-зел.
краен.-кор.
т.-краен.
св.-зел.
роз.-гол.
Плот-
Плотность
4,38
5,4
4,45
5,82
4,78
3,68
1,949
1,91
8,69
6,65
8,46
6,0
2,31
4,84
7,2
4,85
7,3
20,25
6,62
V
5,58 *
4,92
9,12
6,8
146
I. Неорганические вещества
Продолжение табл.
формула
NpO2
npA
Np(O)F4
Np(OHK
Np(OHL
NpO2(OH)
NpO2(OHJ
•H2O
NpO3(OH)
351,04
617,76
839,14
269,05
554,09
329,04
288,07
305,08
286,05
303,06
321,08
302,05
Фазовые переходы
п. 55,0, к. 55,18
п. 767
300 — Np2O5
п. 2560
770 — NpO2
разл. 100
разл. 300
270 — NpO2
250 - Np2O5
разл. > 240
-Н2О 90
разл. * 200
Окраска
оранж.
бур.
бур.
зел.-кор.
т.-кор.
бур.
краен.
сер.-зел.
зел.-фиол.
бур.
бур.
зел.-черн.
Плот-
Плотность
5,0
6,82
11,1
О2
OF2
O2F2
O3F2
O4F2
O5F2
H2O2
HOF
[Os(C5H5J]
[Os(COM]
t°s2(CO)9]
IOs3(COI2]
[Os(COKQ2]
lOs(COLQ2]
OsCl3
31,998
47,997
54,00
69,99
85,99
101,99
117,99
34,01
36,01
n. -218,79, к. -182,95
n.-192,55, к.-111,95
n. -223,8, к. -145,05
n. -154, к. -57 разл.
п.-189, к.-60 разл.
п. —191 разл.
п. <-196, разл.-183
п.-0,43, к. +150 разл.
п.-117, разл. >20
190,230
320,42
330,28
632,55
906,81
345,17
373,18
296,59
бцв. г.
гол. ж.
син.
гол. г.
т.-син. ж.
син.-фиол.
св.-желт. г.
т.-краен, ж.
т.-краен, ж.
краен.-кор.
кор. ж.
бцв. ж.
бцв. ж.
1,42897
u4-i83
1,288
2,141
1,3820
1,728
2,421
1,45~58
1,44820
п. 3033, к. 5012
п. 229,5
п.-15, разл. >+100
п. 64(/?), разл. > 20
п. 224, возг. 130
п. 271, > 300 — Os
возг. 220, > 250 -+ Os
возг. 350, разл. > 500 (вак.)
св.-гол.
св.-желт,
бцв. ж.
оранж.
желт,
бел.
бел.
бур.
22,48
147
I. Неорганические вещества
Продолжение табд
Формула
OsCl4
[OsCy,K2
[OsCl6],K3
•ЗН2О
[OsCl6],(NH4J
[OsCl4O2],K2
OsF4
OsF5
OsF6
[OsH2(COL]
[Os(N)O3],K
OsO2
OsO4
Os(O)F5
OsO3F2
Os(OHL
[OsO2(OHL],K2
Os(S2)
P (краен.)
P (черн.)
P4 (бел.)
PBr3
PBr5
P(Br)Cl2O
PBr2(Cl)O
P(Br)Cl(O)F
P(Br)F2
PBr2F
PBr2F3
(PBr4)F
(PBr2)N
PBr3O
PBr(O)F2
4
332,04
481,14
520,24
574,29
439,03
442,24
266,22
285,22
304,22
304,29
291,33
222,23
254,23
301,22
276,22
258,26
368,45
254,36
30,974
20,974
123,896
270,69
430,49
197,78
242,23
181,33
148,87
209,78
247,78
369,59
204,79
286,69
164,87
Фазовые переходы
п. 450, возг. 650
разл. 600
разл. 450
-Н2О 150
возг. 170, разл. > 500
разл. 200
п. 230
п. 70, к. 233(р)
п. 33,4, к. 47,5
п. 149
разл. > 180
разл. > 500
п. 40,6, к. 131,2
п. 60, к. 100
п. 172
175 — OsO2
разл. > 140
разл. > 1000
п. 593(/?), возг. 429
п. « 1000(/>), возг. 453
п. 44,15, к. 277
п.-40,5, к.+175,3
п. 106 разл., к. 106 разл.
п. 1,1, к. 136,5
п. 31, к. 165
к. 79
п.-133,8, к.-16,1
п.-115, к.+78,5
п. -20, разл. +15
п. 87 разл.
п. 190
п. 55, к. 192
п. -84,8, к. +30,5
Окраска
красн.-кор.
краен.
бур.
т.-краен.
красн.-кор.
краен.
желт.
гол.-зел.
желт.
бел.
св.-оранж.
кор.-черн.
св.-желт.
зел.
оранж.
черн.
св.-фиол.
черн.
краен.
черн.
бел.
бцв. ж.
оранж.
бцв. ж.
желт.
бцв. ж.
бцв. г.
бцв. г.
св.-
красн. ж.
св.-желт.
бел.
бел.
бцв. ж.
Плот-
Плотность
3,42
2,93
3,42
4,2
7,91
4,906
9,47
2,31
2,702
1,828
2,8715
3,57
2,10414
2,82
148
I. Неорганические вещества
Продолжение табл.
формула
pBr,(O)F
P(CNK
РС13
PCIj
Р2С14
P(C1)F2
P(C1)F4
PC12F
PC12F3
PCI4F
(PC14)F
(PC12K(NK
(PC12L(NL
PC13O
P2C14O3
PC1(O)F2
PC12(O)F
[PC12O2],H
PF3
PF5
[PF6],H
•6H2O
tPF6],K
IPF6],NH4
[PF6],Na
H2O
[PF6],PC14
pH3
P2H4
PH4Br
PH4CI
(PH)F2
PH41
pi
4
225,78
109,03
137,33
208,24
203,76
104,42
142,42
120,88
158,87
191,78
191,78
347,66
463,55
153,33
251,76
120,42
136,88
134,89
87,97
125,96
145,97
254,06
184,06
163,00
167,95
185,97
317,75
34,00
65,98
114,91
70,46
69,98
161,91
411,69
Фазовые переходы
п.-117,2, к.+110,1
возг. 130
п. -90,34, к. +75,3
п. 160(/>), 159-300 ^РС13
п.-28,разл.+180
п. -164,8, к. -47,3
п. -132, к. -43,4
п. -144, к. +13,85
п.-125, к.+10
п. -60, > +30 — (PC14)F
п. 1770), возг. 175
п. 114, к. 256
п. 123,5, к. 328,5
п. 1,18, к. 107,2
п.-16,5, к. +47(вак.)
п.-96,4, к.+3,1
п. -84,5, к. +54
п.-28
п.-151,5, к.-101,5
п. -93,75, возг. -84,55
Не получен
п. 32, 150-200-POF3
п. 575, > 600 - PF3
200-250 — PF5
разл. 500—600
-Н2О 80 (вак.), 200 — POF3
возг. 135 разл.
п. -133,8, к. -87,42
п. -99, к. +63,2
возг. 38
п. +28,5(/?), разл. > 0
п. -124, к. -65
п. 18,5, 80 разл.
п. 61, >200-* Р(красн.)
Окраска
бцв. ж.
бел.
бцв. ж.
зел.-бел.
бцв. ж.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бцв. ж.
бел.
бел.
бел.
бцв. ж.
бцв. ж.
бцв. г.
бцв. ж.
бцв. ж.
бцв. г.
бцв. г.
бел.
бел.
бел.
бел.
бел.
бел.
бцв. г.
бцв. ж.
бел.
бел.
бцв. г.
бел.
краен.
Плот-
Плотность
1,55720
2,11
1,59
5,4
1,98
2,18
1,64520
1,8215
1,68625
3,907
5,805
2,18
2,51
2,37
1,5294
1,01220
2,86
3,89
149
I. Неорганические вещества
Продолжение табп
Формула
Р214
Р12С13
Р13О
[PMol2O«J,H3
• 28Н2О
PN1+X
(-0,3 <х< 0,19)
P3N5
P(NH2KO
[P(NH2JO2],H
[P(NH2)O3],H2
PN(NH)
PN(NH2J
P4O
Р4О6
P4O8
Р4ОШ
P(O)F3
P2(O)F6
[PO2F2],H
[PO3F],H2
[PO3F],K2
[PO3F],Na2
[P(OHL]C1O4
P4S2
P4S3
P4S5
p4s6
P4S7
P4S9
P(S)Br3
PS(Br)Cl2
P(S)Br(Cl)F
Mr ,
569,56
391,14
427,69
1825,24
2329,66
44,98
162,96
95,04
96,03
97,01
60,00
77,03
139,90
219,89
251,89
283,89
103,97
191,94
101,98
99,99
176,17
143,95
198,45
188,03
220,09
284,23
316,29
348,36
412,49
444,56
302,75
213,85
197,40
Фазовые переходы
п. 126,1
разл. 259
п. 50
Не получен
п. 78
разл. «1100
800 — PN
п. 160
п. 100 разл.
разл. ПО
разл. 400
п. 162
разл. > 350
п. 23,9, к. 174
возг. 180
п. 580,50i), к. 605,5
п. -39,4, возг. -39,8
п.-18, разл. >+20
п.-96,5, разл.+100
п.-30, к. +185 разл.
п. 825
п.« 800
п. 47
п. 46
п. 172,5, к. 407,5
разм. > 170, разл. 220
п. 232 разл.
п. 312, к. 523
разм. 240, разл. 270
п. 288, к. 514 разл.
п. 38,2, к. 215 разл.
п.-30, к.+156
к. 98
Окраска
оранж.
краен.
фиол.
желт.
желт.-кор.
т.-оранж.
бел.
бел.
бел.
бел.
бел.
краен.-бур.
бел.
бел.
бел.
бцв. г.
бцв. г.
бцв. ж.
бцв. ж.
бел.
бел.
бел.
желт.
т.-желт.
желт.
т.-желт.
св.-желт.
желт.
сер.-желт.
желт.
желт. ж.
желт. ж.
Плот-
Плотность
4,18
2,53
2,6
i
1,891 *
2,135
2,537
2,84
4,8
1,583*
1,818м
2,03
2,17
2,19 [
2,08
2,03.
2,85
2,12°
^
150
I. Неорганические вещества
Продолжение табл.
формула
pS(Br)F2
p(S)Br2F
P(S)C13
PS(C1)F2
P(S)C12F
P(S)F3
P(S)I3
PS(NH2K
P4Se3
[PVI2O36],(NH4O
[PWl2O40],H3
• 24H2O
H(PH2O2)
H2(PHO3)
H2(P2H2O5)
H(PHO2F)
HPO3
H3PO4
H4P2VO6
H4P2O7
Pa
PaBr5
PaCl4
PaCl5
PaF4
PaF5
•2H2O
Г» т
Pal5
Pa2O5
pa(OHM
Pb
Pb2As2O7
Pb3(As04J
^ -
И
180,94
241,85
169,40
136,49
152,94
120,03
443,75
111,11
360,78
1344,52
2880,04
3312,40
66,00
82,00
145,98
83,99
79,98
97,99
161,97
177,97
231,036
630,56
372,85
408,30
307,03
326,03
362,06
865,56
542,07
316,07
207,200
676,24
899,44
Фазовые переходы
п. -136,9, к. +35,5
п.-75,2, к.+125,3
п.-36,2, к.+125
п. -155,2, к. +6,3
п. -96, к. +64,7
п.-149, к.-52
п. 46
п. 118-119
п. 242, к. 360-400
разл. > 450
Не получен
п. 80
п. 26,5, разл. 50—140
п. 73,6, разл. > 170
п. 38, разл. 130
п.-94, к. +112,4
п. «40
п. 42,5, 150 —Н4Р2О7
п. 70 разл.
п.61,300(вак.) — НРО3
п. 1572, к. 4027
п. 283, к. 428
п. 680, к. 850
п. 306, к. 420
п. 1030, к.1630
возг. 500
разл. 160
п. 300 разл.
разл. 1550
< 475 — Ра2О5
п. 327,46, к. 1749
п. 802
п. 1030 разл.
Окраска
желт. ж.
желт. ж.
бцв. ж.
бцв. г.
бцв. ж.
бцв. г.
желт.
бел.
оранж.
т.-краен.
бел.
бел.
бел.
бел.
бцв. ж.
бел.
бел.
бел.
бел.
св.-сер.
оранж.
св.-желт.
св.-желт.
т.-кор.
черн.
черн.-кор.
черн.
бел.
бел.
сер.-гол.
бел.
бел.
Плот-
Плотность
1,63520
1,31
1,493
1,651
1,5825
>2,2
1,88
15,37
4,68
9,0
13,43
11,35
151
I. Неорганические вещества
Продолжение табл.
Формула
РЬ(ВО2J
•Н2О
РЬВг2
РЬ(ВЮ3J
Н2О
РЬ(СН3СООJ
•ЗН2О
РЬ(СН3СООL
РЬСО3
РЬС2О4
РЬ2(СО3)С12
РЬ3(СО3J(ОНJ
РЬС12
РЬС14
Pb(Cl)F
[РЬС16],К2
[PbCl6],(NH4J
Pb(C102J
Pb(C103J
•H2O
Pb(C104J
•3H2O
PbCl(OH)
PbCrO4
PbF2
PbF4
PbHAsO4
Pb(HCOOJ
Pbl2
[PbI3],K
•2H2O
Pb(IO3J
PbMoO4
Pb(N3J
Mr
292,82
310,83
367,01
463,00
481,02
325,29
379,33
443,38
267,21
295,22
509,86
775,63
278,11
349,01
261,65
498,11
456,00
342,10
374,10
392,12
406,10
460,14
259,66
323,19
245,20
283,19
347,13
297,23
461,01
627,01
663,04
557,00
367,14
291,24
Фазовые переходы
п. 600 разл.
-Н2О 160
п. 373, к. 893
Не получен
разл. 180
п. 280
п. 75, -Н2О 100
п. 175—180 разл.
>315 — РЬО
разл. 300
разл. ~ 350
разл. 400
п. 501, к. 953
п.-7,0,+30-100 ^РЬС12
п. 603
разл. > 190
разл. > 130
разл. 126
разл. 230
-Н2О110
разл.« 350
-Н2О > 100
разл. > 140
п. 844, > 850 — РЬО
п. 822, к. 1292
п. - 600
400 — Pb2As207
разл. 190
п. 412, к. 872
п. 349 разл., > 400-* РЬ
-Н2О 97 (вак.)
разл. 300
п. 1060
разл. 300—350
Окраска
бел.
бел.
бел.
бел.
бел.
бел. <
бел.
бел.
бел.
бел.
бел.
бел.
желт. ж.
бел.
св.-желт.
св.-желт.
желт.
бел.
бел.
бел.
бел.
бел.
т.-желт.
бел.
бел.
бел.
бел.
желт.
желт.
св.-желт.
бел.
св.-желт.
бел.
Плот-
Плотность
4,9
6,67
5,53
3,25
2,55
2,22
6,55
5,28
6,1
5,85
3,18°
4,04
3,89
2,6
6,12
8,37
6,7
4,63
6,16
4,21
6,83
4,71
152
I. Неорганические вещества
Продолжение табл.
формула
Pb(NCSJ
Pb(NO3J
Pb(NO3)OH
а-РЬО
B-PbO
г
PbO2
Pb(OHJ
[Pb(OHN],Na2
Pb2P2O7
Pb3(PO4J
Pb5(PO4KCl
(Pb^PbIV)O4
PbS1+jC
@<x< 0,005)
PbSO4
Pb2(SO4)O
•H2O
Pb(SO3S)
PbSeI+JC
@<x< 0,001)
PbSeO4
PbSiO3
PbTe1+JC
@<x< 0,001)
pb5(VO4KCl
PbWO4
Pd ¦—
PdBr2
d(CNJ
pd(CNL
d(CNLl'K2
PdCi
¦^——
4
323,37
331,21
286,21
223,20
223,20
239,20
241,21
355,22
588,34
811,54
1356,36
685,60
239,27
303,26
526,46
544,48
319,33
286,16
350,16
283,28
334,80
1416,27
455,04
106,420
266,23
158,46
210,49
288,69
342,73
177,33
Фазовые переходы
разл. 195
550 - РЬО
разл. 180
590 - р-РЬО
п. 887, к. 1535
>290 —(Pb^PbIV)O4
145 — РЬО
« 700 - РЬО
п. 830
п. 1014
разл.» 1100
п. 830(/>), 570 — РЬО
п. 1113, к.1281
п. 1170, > 1200 ^ РЬО
п. 977
-Н2О 200
разл. > 250
п.1081
разл. > 1200
п. 766
п. 924
разл. > 1300
п. 1123
п. 1554,9, к. 2963
п. 717,
разл. 210
разл. > 20
разл. > 350
-Н2О 200
п. 680(/?), 590-740 -> Pd
Окраска
бел.
бел.
бел.
краен.
желт.
кор.
бел.
бел.
бел.
бел.
оранж.
краен.
т.-сер.
бел.
бел.
бел.
бел.
т.-сер.
бел.
бел.
т.-сер.
краен.
бел.
бел.
бур.
бел.
роз.
бел.
бел.
фиол.-кор.
Плот-
Плотность
3,82
4,538
5,93
9,4
9,63
9,35
3,975
5,8
6,9
6,5
8,92
7,61
6,35
6,92
5,18
8,25
6,37
6,49
8,24
6,9
8,1
12,02
5,173
4,08
153
I. Неорганические вещества
Продолжение пгабА
Формула
[PdCl4],K2
[PdCl6],K2
[PdCl4],(NH4J
[PdCl6],(NH4J
PdF2
PdF3
PdH,.,
@<x<0,4)
Pdl2
[Pd(NH3JCl2]
[Pd(NH3JCl4]
[Pd(NH3L]Cl2
H2O
[Pd(NH3L][PdnCl4]
Pd(NO3J
[Pd(NO2L],K2
PdO
PdO2
A2H2O
Pd(OHJ
[PdOHL],Na2
PdS
Pd(S2)
PdSO4
•2H2O
PdSe
Pd(Se2)
PdSeO4
Pm
PmBr3
PmCl3
PmF3
Pml3
4
326,43
397,33
284,31
355,22
144,42
163,41
107,43
360,23
211,39
282,29
245,45
263,47
422,78
230,43
368,64
122,42
138,42
—
140,43
220,43
138,49
170,55
202,48
238,51
185,38
264,34
249,38
144,913
384,63
251,27
201,91
525,63
Фазовые переходы
п. 525
380 - K2[PdCl4]
разл. > 430
разл. > 300
возг. 500, > 500 — Pd
разл. > 800
разл. 50-100
разл. 350
> 210 — Pd
> 260 — Pd
Не получен
разл. 120—180
разл. > 180
> 350 - PdO
разл. 305
780-850 -> Pd
Не получен
> 200 — PdO
> 500 — PdO
разл. > 300
разл. 970
600 — PdS
разл. > 550
-Н2О 250
п. 960
п. - 1000
разл. 600
п. 1042, к. - 3000
п. 680, к. 1530
п. 740, к. 1670
п. 1140, к.2330
п. 800, к. 1370
Окраска
желт.-кор.
краен.-кор.
т.-зел.
краен.-кор.
св.-фиол.
черн.
сер.
черн.
оранж.
т.-оранж.
бел.
роз.-краен.
кор.-желт.
св.-желт.
черн.
т.-краен.
черн.
желт.
кор.-черн.
черн.-кор.
т.-краен.
краен.-кор.
т.-сер.
сер.-зел.
краен.-кор.
св.-сер.
зел.
желт.
т.-роз.
т.-желт.
Плот,
ность
2,67
2,74
2,17
2,42
5,8
5,06
11,79
6,003
2,5
1,91 .
8,7
6,6
•
i
6,5
7,264 '
154
I. Неорганические вещества
Продолжение табл.
формула
Рт2О3
рт(ОНK
?о
РоВг2
РоВг4
РоС12
РоС14
РоО2±х
РоО(ОНJ
PoS
Po(SO4J
Рг
РгВг3
Рг(ВЮ3)з
•9Н2О
РгС2
Рг2(С2О4K
• 10Н2О
РгС13
•7Н2О
PrF3
PrF4
Prl3
pr2(MoO4K
Pr(NO3K
•6H2O
PrO2
Pr2O3
Pr(OHK
PrS2
Pr2S3
Pr2(SO4K
•8H2O
Mr
337,82
195,93
208,982
368,79
528,60
279,89
350,79
240,98
259,00
241,05
401,11
140,908
380,62
524,61
686,75
164,93
545,87
726,02
247,27
373,37
197,90
216,90
521,62
761,62
326,92
435,01
172,91
329,81
191,93
205,04
378,01
570,00
714,12
Фазовые переходы
п.« 2000
> 350 — Pm2O3
п. 254, к. 962
п. 275
п. 330, к. 360 (вак.)
возг. 196
п. 300, к. 390
разл. 500 (вак.)
разл.« 220
разл.« 700 (вак.)
разл. > 550
п. 931, к. 3510
п. 693, к.1550
разл. 475
п. 58, -Н2О 130
п. 2500 разл.
Не получен
разл. > 600
п. 786, к.1710
п. 115
п. 1395, к. 2300
разл. 90
п. 733, к. 1380
п. 1030
разл. 400
-Н2О 165
разл. 400
п. > 2000, к. - 4300
разл. > 350
п. 1780 разл.
п. 1975
разл. > 850
-Н2О 600
Окраска
св.-фиол.
роз.
бел.
т.-кор.
ярко-краен.
т.-красн.
ярко-желт.
краен.
св.-желт.
черн.
бел.
св.-сер.
зел.
т.-зел.
зел.
желт.
св.-желт.
зел.
зел.
св.-зел.
бел.
зел.
зел.
т.-зел.
зел.
черн.-кор.
желт.-зел.
зел.
т.-зел.
бур.
св.-зел.
зел.
Плот-
Плотность
9,4
6,5
8,96
6,773
5Д
4,02
2,25
4,84
6,82
6,97
5,27
3,73
2,83
155
I. Неорганические вещества
Продолжение табд.
Формула
Pt
PtAs2
PtBr2
PtBr4
[PtBr4],K2
•2H2O
[PtBr6],K2
[PtBr6],(NH4J
[PtBr6],Na2
•6H2O
[PtBr6],Ptn
[Pt2(C2H4JCl4]
[Pt(C2H4)Cl3],K
•H2O
[Pt(CNL],Ba
•4H2O
[Pt(CNL],H2
•5H2O
[Pt(CNL],K2
•3H2O
[Pt(CNN],K2
[Pt(CNL],Mg
•7H2O
[Pt(CNL],(NH4J
[Pt(CNL],Na2
•3H2O
[Pt2(COJBr4]
[Pt(COJCl2]
[Pt2(COJCl4]
[Pt2(COKCl4]
[Pt2(COJI4]
PtCl2
PtCl4
•7H2O
4
195,080
344,92
354,89
514,70
592,89
628,92
752,70
704,53
720,48
828,57
869,58
588,08
368,59
386,61
436,48
508,54
301,17
391,24
377,35
431,39
429,38
323,46
449,56
335,23
345,13
399,18
765,80
322,01
587,99
616,00
953,80
265,99
336,89
463,00
Фазовые переходы
п. 1768,4, к. 3825
разл. > 800
п. 250 разл., 280-^ Pt
разл. > 180
450 - Pt
п. - 100, -Н2О 120 (вак.)
> 400 — Pt
разл. 145
> 350 - Pt
-Н2О 150
280 — PtBr2
200 — PtCl2
> 220 - PtCl2
-Н2О 75-100
разл. > 420
-Н2О 150
Не получен
п. 100 разл., > 110 ^ Pt
400-600 — Pt
-Н2О 100
разл. 395
разл.« 350
-Н2О 270
разл. 200
> 400 — Pt
-Н2О 125
п. 177,7 разл.
п. 103, разл. 210
п. 194, > 300 - Pt
п. 130, разл. 250
п. 140—150 разл.
п. 581 разл., > 583 -^ Pt
разл. 380
п. 100 разл.
Окраска
сер.-бел.
бел.-сер.
бур.
кор.-черн.
кор.
черн.
красн.-кор.
красн.-кор.
краен.
краен.
черн.
оранж.
желт.
желт.
гол.-зел.
желт.-зел.
краен.
св.-желт.
желт.
св.-желт.
св.-красн.
краен.
бел.
желт.
бел.
св.-красн.
бел.
оранж.
т.-желт.
краен.
т.-зел.
красн.-кор.
бур.
Плот-
Плотность
21,45
10,6
6,65
5,69
3,75
4,66
4,27
3,32
2,88
2,076
2,455
2,18
2,65
3,49
4,235
6,05
4,303
2,43
156
I. Неорганические вещества
Продолжение табл.
формула
~~^СПВа
• зн2о
[PtCl6],Ba
•6Н2О
[PtCl6],Cs2
[PtCl6],H2
•6Н2О
[PtCl4],K2
[PtCl6],K2
[PtCl6],Mg
•6H2O
[PtCl4],(NH4J
[PtCl6],(NH4J
[PtCl4],Na2
•4H2O
[PtCl6],Na2
•6H2O
[PtCl6],PtH
[PtCy.Rbj
PtF4
PtF5
PtF6
[PtF6],K
[PtF6],K2
tPtF6],(Oj)
tPtF6],Xe'
Ptl2
Ptl4
(PtU.Pt11
'»peHc-[Pt(NH3JCl2]
*<"с-[Р1(КНзJС12]
wPo«c-[Pt(NH3JCy
4
474,22
528,26
545,13
653,22
673,61
409,81
517,90
415,09
485,99
432,10
540,19
372,97
443,88
382,87
454,93
453,78
561,87
602,88
578,73
271,07
290,07
309,07
348,17
387,26
341,07
440,36
448,89
702,70
1151,58
300,05
300,05
370,95
370,95
Фазовые переходы
> 500 - PtCl2
-H2O 150
320 — PtCl4
-H2O-100
разл. 570—600
He получен
п. 60, 700-750 — Pt
475 — PtCl2
« 250 — PtCl4
разл. > 400
-H2O 90
140 — PtCl2
215-350 - Pt
> 400 — PtCl2
n. 100 разл., -Н2О 120
< 270 — PtCl4
-H2O110
возг. 350, 435 — PtCl2
495-550 - Pt
разл. > 300
п. 80, разл. > 130
п. 69,4, 90-200 - PtF4
750 - Pt
800 — Pt
п. 2190), « ЮО -* PtF5
разл. 165
п. 360 разл., > 400^ Pt
разл. < 1300?)
360 — Pt
> 340 - Pt
270—275 —> транс-язомер
340 — PtCl4
240 —> транс-нзомер
Окраска
т.-красн.
т.-красн.
т.-желт.
желт.
желт.
т.-желт.
т.-красн.
св.-желт.
желт.
желт.
краен.
желт.
краен.
краен.
оранж.
т.-желт.
т.-зел.
желт.
св.-кор.
т.-красн.
т.-красн.
желт.-кор.
св.-желт.
оранж.
краен.
черн.
кор.-черн.
черн.
желт.
т.-желт.
желт.-зел.
св.-желт.
Плот-
Плотность
2,87
2,86
4,2
2,43
3,38
3,499
2,69
2,936
3,065
2,5
5,256
3,94
7,07
3,826
6,403
6,625
3,508
3,42
157
I. Неорганические вещества
Продолжение maffo
Формула
[Pt(NH3L]Cl2
•Н2О
[Pt(NH3J(NO2J]
[Pt(NH3L][PtIICl4]
[Pt(NO2L],K2
•2H2O
[Pt(NO2L],Na2
•2H2O
PtO
PtO2
H2O
•2H2O
•3H2O
•4H2O
Pt(OHJ
[Pt(OHN],K2
[Pt(OHN],Na2
PtO(O2)
Ptp2
[Pt(PF3L]
PtP2O7
PtS
PtS2
Pt(Se2)
Pt(Te2)
Pu
PuBr3
РчС0,85
Pu2C3
Pu(C2O4J
•6H2O
PuCl3
PuF3
4
334,11
352,13
321,15
600,10
457,30
493,33
425,08
461,11
211,08
227,08
245,09
263,11
281,12
299,14
229,09
375,32
343,10
243,08
257,03
546,95
369,02
227,15
259,21
353,00
450,28
244,064
483,78
254,27
524,16
420,10
528,19
350,42
301,06
Фазовые переходы
разл. 250
-H2O110
200 - Pt
< 290 - m/w«c-[Pt(NH3JCl2]
He получен
> 150 — Pt
He получен
> 100 — Pt
> 560 — Pt
n. 45000, 380-400 - Pt
-H2O 160
-1H2O 100
-1H2O 30-40
-1Н2О20,420 —Pt
разл. > 150
160-450 — Pt
150-370-Pt
разл. > 20
п. > 1500
п. -15, +90--Pt
разл. 600
800 — Pt
225-250 - Pt
> 400 — Pt
n. - 1250
n. 640, к. 3228
n. 681, к. 1531
разл. 1654
п. 2050
He получен
380 — PuO2
п. 765, к. 1767
п. 1426, к. 2300
Окраска
бел.
бел.
св.-желт.
т.-зел.
бел.
св.-желт.
черн.
бур.
т.-кор.
кор.
желт.
бел.
черн.
желт.-зел.
желт.
краен.-кор.
сер.
бцв. ж.
желт.-зел.
сер.-черн.
сер.-черн.
черн.
черн.
бел.
зел.
черн.
черн.
желт.-зел.
ярко-зел.
фиол.
Плот*
ность
2,74
14,9
10,2
5,18
9,01
8,847
7,66
12,84
6,69
13,6
12,7
5,7
9,32
158
I. Неорганические вещества
Продолжение табл.
. ¦
формула
PuF4
PuF6
PuH2+x
@<x<0,7)
Pul3
PuN
Pu(NO3L
•5H2O
PuO
PuO2+x
Pu2O3
Pu(O)F
Pu(OHK
Pu(OHL
PuO2(NO3J
•6H2O
PuP
PuS
PuSi
PuSi2
Pu2Si3
Ra
RaBr2
RaCO3
RaCl2
Ra(NO3J
RaS
RaSO4
Rb
RbAl(SO4J
' 12H2O
RbBr
RbBrO^^
4
320,06
358,05
246,08
624,78
258,07
492,08
582,16
260,06
276,06
536,13
279,06
295,09
312,09
400,07
508,16
275,04
276,13
272,15
300,24
572,39
226,025
385,83
286,03
296,93
350,03
258,09
322,09
85,468
304,57
520,75
165,37
213,37
Фазовые переходы
п. 1037, к. 1277
п. 51,59, к. 62,16
> 400 (вак.) — Ри
п. 770
п. 2589 разл.
Не получен
разл. 150-180
п.« 1900
п. 2390
п. 2085
п. > 1635
разл. > 350
800 - РиО2
разл. > 220
п. 140, -Н2О > 150
п. 2600
п. 2350
п.1578
п. 1640
п. 1770
п. 700, к. 1140
п. 728
разл. > 1500
п. 900
разл.« 900
п.« 2000 разл.
разл. > 1600
п. 39,31, к. 688
разл.« 800
п.99,-Н2О115
п. 692, к. 1347
п. 430
Окраска
роз.
желт.-кор.
черн.
св.-зел.
черн.
желт.-зел.
черн.
т.-зел.
зел.
св.-зел.
сер.-гол.
т.-зел.
кор.
роз.-кор.
т.-сер.
т.-желт.
сер.
сер.
сер.
бел.
св.-желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
Плот-
Плотность
7,0
4,86
9,61
6,93
14,35
13,89
11,44
9,76
9,87
10,6
10,15
9,08
8,77
5,0
5,79
4,91
1,532
1,87
1,5528
3,68
159
I. Неорганические вещества
Продолжение табд
Формула
Rb(CH3COO)
Rb2CO3
• 1,5Н2О
RbCl
RbC102
RbC103
RbC104
Rb2Cr04
Rb2Cr207
RbCr(SO4J
• 12H2O
RbF
RbFe(SO4J
• 12H2O
RbFe(SeO4J
• 12H2O
RbH
RbHCO3
Rb(HF2)
RbHSO4
Rbl
RbIO3
RbIO4
RbMnO4
RbMn(SO4J
• 12H2O
RbN3
RbNH2
RbNO2
RbNO3
RbO2
RbO3
Rb2O
Rb2O2
4
144,51
230,94
257,97
120,92
152,92
168,92
184,92
286,93
386,92
329,59
545,77
104,47
333,44
549,62
427,23
643,41
86,48
146,48
124,47
182,54
212,37
260,37
276,37
204,40
332,53
548,71
127,49
101,49
131,47
147,47
117,47
133,47
186,94
202,93
Фазовые переходы
п. 246
п. 873, > 900 (вак.) — Rb2O
-Н2О > 190
п. 723, к. 1387
разл. 120
п. 342, разл. > 480
п. 597 разл., > 600 — RbCl
п. 994
п. 396
> 750 — Rb2SO4
п. 107, -Н2О - 400
п. 795, к. 1427
Не получен
п. 50, разл. « 500
разл. ~ 600
п. 4,5, -Н2О 100
п. 585(/>), > 200 — Rb
разл. > 175
п. 180,05, > 500^ RbF
разл. 250—300
п. 656, к. 1327
разл. > 700
разл. 800—805
разл.« 300
Не получен
п. 22, разл. > 50
п. 321, разл. 395
п. 309
п. 422
п. 310, >540-*RbNO2
п. 540(/0, > 400 — Rb2O2
60-90 — RbO2
п. 505(р), 400 — Rb2O2
п. 570, к. 1010 разл.
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.
оранж.
син.-зел.
фиол.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
св.-фиол.
т.-красн.
бел.
св.-зел.
бел.
бел.
т.-желт.
краен.
бел.
желт.
Плот-
ность
1,4937
3,203
3,035
3,518
3,02
1,95
1,396
1,93
2,31
2,6
зд
2,892
1,6474
4,33
3,918
3,24
2,48
2,58
з,п
3,12
3,08
3,72
3,79
160
I. Неорганические вещества
Продолжение табл.
формула
RbOH
•н2о
¦2Н2О
Rb2S
•4Н2О
Rb2(S2)
Rb2(S3)
Rb2(S5)
Rb2SO4
Rb2S2O7
Rb(SO3F)
Rb2Se04
RbV(SO4J
• 12H2O
Re
ReBr3
ReBr4
Re(Br)O3
[Re(CNLO2],K3
[Re2(COI0]
[Re(COMBr]
[Re(COKC5H5]
[Re(COMCl]
[Re(COMI]
ReCl3
ReCl4
ReCl5
[ЯеСУ,К2
L^e2Cl8]5K2
•2H2O
Re(Cl)O3
eCl4o
4
102,48
120,49
138,51
203,00
275,06
235,07
267,13
331,27
267,00
347,06
184,53
313,89
328,53
544,71
186,207
425,92
505,82
314,11
439,57
652,51
406,16
335,33
361,71
453,16
292,57
328,02
363,47
477,12
734,23
770,26
269,66
344,02
645,28
Фазовые переходы
п. 47, -H2O 250
п. 15, -1Н2О54(вак.)
п.« 600
-Н2О 200 (вак.)
п. 420
п. 213
п. 231
п. 1070, к. - 1700
> 400 — Rb2SO4
п. 304
п.1050
разл. 475
п. 64, -Н2О 220
п. 3186, к. 5596
возг. > 400
> 250 — Re
п. 39,5, к. 163
разл. > 300
п. 177, 250-420 — Re
возг. > 60
п. 111
возг. > 50
возг. < 60
возг. 450, к. 800-850
п. 220, разл. 300
п. 260, к. 360 разл.
разл. > 300
разл. > 290
-Н2О 130
п. 4,5, к. 131
п. 29,3, к. 228
п. > 300
Окраска
бел.
бел.
бел.
бел.
бел.
т.-краен.
св.-краен.
краен.
бел.
бел.
бел.
бел.
желт.
желт.
св.-сер.
черн.
черн.
бел.
св.-кор.
бел.
бел.
бел.
бел.
бел.
т.-красн.
зел.-черн.
кор.-черн.
желт.-зел.
т.-зел.
зел.
бцв. ж.
кор.-краен.
желт.
Плот-
Плотность
3,203
2,79
2,62
3,613
3,9
1,92
21,53
5,47
2,7
4,5
4,9
3,34
3,5
3,8720
3,76
5-2004
161
I. Неорганические вещества
Продолжение табль
Формула
ReF4
ReF5
ReF6
ReF7
[ReH(COM]
[ReH9],K2
[ReH9],Na2
Rel3
[ReI6],K2
Re2N0>86
ReO2
•лН2О
ReO3
Re2O5
Re2O7
Re(O)F4
Re(O)F5
ReO2F2
ReO2F3
ReO3F
Re(OHL
[Re2(PF3I0]
Re,_xS2
Re2S7
ReSi2
H4Re209
Rh
RhBr3
[Rh2(CO)8]
[Rh4(COI2]
[Rh6(COI6]
[Rh(COJC5H5]
[Rh2(COK(C5H5J]
4
262,20
281,20
300,20
319,19
327,27
273,48
241,26
566,92
1025,83
384,46
218,21
—
234,20
452,41
484,41
278,20
297,20
256,20
275,20
253,20
254,24
1252,09
250,34
596,88
242,38
520,44
102,906
342,62
429,89
747,74
1065,60
224,02
420,03
Фазовые переходы
п. 125, к. 735(р)
п. 48, к. 221,3
п. 18,8, к. 33,7
п. 48,3, к. 73,7
п. 13
> 300 — Re
245 — Re
разл. 800
разл. > 400
разл. 280 (вак.)
разл. 850(вак.)
120 (вак.) - Re(OHL
п. 160, к. 620
разл. > 250
п. 301,5, к. 358,5
п. 108, к. 171,2
п. 41, к. 73
п. 156
п. 90, к. 185
п. 147, к. 164
> 400 - ReO2
п. 182
> 700 - Re
350 — ReS2
п. 1980
160 — Re2O7
п. 1964, к. 3695
> 800 — Rh
п. 76, разл. > 100
п. 76, 150-[Rh6(COI6]
220 —Rh
п. -11, к. » +240
п. 139
Окраска
т.-зел.
желт.-зел.
желт. ж.
желт.
бцв. ж.
бел.
черн.
черн.
черн.
сер.-черн.
кор.
т.-краен.
т.-син.
св.-желт.
гол.
бел.
бел.
желт.
желт.
кор.-черн.
бел.
черн.
черн.-кор.
сер.
св.-желт.
бел.
красн.-кор.
оранж.
краен.
черн.
желт. ж.
краен.
Плот-
Плотность
5,38
3,5822
4,32
3,07
6,37
4,4
11,6
7,3
6,14
4,032
7,506
4,866
10,71
4,87
12,4
5,56
162
I. Неорганические вещества
Продолжение табл.
формула
[Rh2(COLCl2]
[Ю1(С2О4K],Кз
• 4,5Н2О
RhCl3
•лН2О
[RhCl6],Cs2
[RhQ6],K3
[RhCl6],Na3
RhF3
RhF5
RhF6
Rh(HSK
Rhl3
[Rh(NH3N]Cl3
Rh(NO3K
[Rh(NO2N],K3
[Rh(NO2N],Na3
Rh2O3
Rh(OHK
Rh2S3
Rn
Ru
RuBr3
[Ru(C5H5J]
[Ru(c5h7o2K]
[Ru(coM]
[Ru3(COI2]
[Ru2(COL(C5H5J]
[Ru2(CONQ4]
lRu(COLI2]
RuCl3
4
388,76
484,25
565,32
209,27
—
581,43
432,92
384,59
159,90
197,90
216,89
202,13
483,62
311,45
288,92
496,23
447,91
253,81
153,93
302,01
222,018
101,070
340,78
231,26
398,40
241,12
639,33
444,37
512,01
466,92
207,43
Фазовые переходы
п. 121
разл. > 600
-Н2О 190
возг. 800, > 964 — Rh
> 180 — Rh2O3
разл. > 200
разл.« 600
> 550 - Rh
возг. > 600
п. 95,5
п. 70, к. 73,5
> 350 -* Rh2S3
> 650 - Rh
разл. > 200
> 600 — Rh2O3
разл. 360—440
разл. 440—460
> 1000 - Rh
200 - Rh2O3
разл. > 900
п.-71, к.-61,7
п. 2334, к. 4150
возг. > 550
п. 199-200
п. 76,4
n.-22,+50-[Ru3(COI2]
п. 155(/?), разл. 150
п. 185
разл. 315
разл. > 140
500-850 - Ru, возг. 777
(вак.)
Окраска
св.-краен.
т.-красн.
краен.
краен.
св.-краен.
зел.
краен.
т.-красн.
краен.
т.-красн.
т.-сер.
бур.
черн.
бел.
желт.-кор.
бел.
бел.
сер.
т.-желт.
черн.
бцв. г.
бцв. ж.
бел.
черн.
желт.
т.-красн.
бцв. ж.
оранж.
оранж.
бел.
желт.
черн.-кор.
Плот-
Плотность
2,17
ЗД1
3,29
5,38
6,4
2,01
2,74
8,2
6,4
9,73
4,42
12,3
5,42
3,11
163
I. Неорганические вещества
Продолжение табд.
Формула
[RuCl6],K2
[RuCl6],(NH4J
[Ru2Cl10O],K4
•Н2О
RuF5
RuF6
[Ru(H2O)Cl5],K2
Rul3
[Ru3(NH3I4O2]Cl6
•4H2O
[Ru(NO+)Cl5],K2
[Ru(NO+)Cl5],
(NH4J
[Ru(NO+)(NO2LOH],
Na2
RuO2
RuO4
Ru(O)F4
Ru(S2)
cc-S8
P-s8
S2Br2
SBr2O
S(Br)O2F
(SCNJ
SC12
SC14
S2C12
S(C1)F5
SC12O
SC12O2
S2C14O
SC1(O)F
ч
391,98
349,87
729,06
747,08
196,06
215,06
374,55
481,78
786,36
858,42
386,54
344,42
378,08
133,07
165,07
193,06
165,20
256,528
256,528
223,94
207,87
162,97
116,17
102,97
173,88
135,04
162,51
118,97
134,97
221,94
102,52
Фазовые переходы
разл. 520
разл. 360
Не получен
разл. > 200
п. 85,4, к. 227
п. 54, > 200 — RuF5
разл. 180
> 300 — Ru
разл. 200—250
-Н2О150
разл. > 570
разл. 320
разл. 200
п. 955(р), 730-750 — Ru
п. 25,5, к. 27
п. 115
разл. > 1000,
п. 110,2(/>),95,5->p-S8
п. 115,21, к. 444,6
п. -40, 90-210 - S
п. -52, к. +138(р)
п. -86, к. +40
п. -2,0, > +20 - (SCN)W
п. -78, к. +59,6
п.-31,>-15^SC12
п.-80, к. 137,1 разл.
п.-64, к.-19,1
п. -99,5, к. +75,6
п.-54,1, к.+69,5
к. 60,5
п.-139,5, к.+12,2
Окраска
т.-краен.
черн.
бур.
т.-зел.
т.-кор.
т.-краен.
черн.
т.-красн.
краен.
т.-красн.
т.-красн.
оранж.
т.-син.
желт.
бел.
т.-зел.
желт.
желт.
т.-красн. ж.
оранж. ж.
бцв. ж.
желт.-бел.
т.-краен, ж.
желт.-
кор. ж.
св.-желт. ж.
бцв. г.
бцв. ж.
бцв. ж.
т.-красн. ж.
бцв. ж.
Плот*
ность
2,963
6,97
3,29
6,99
2,07
1,96
2,62920
2,63520
2,17°
1,62115
1,67825
1,63820
1,677го
1,66°
1,576°
164
I. Неорганические вещества
Продолжение табл.
формула
S(C1)O2F
SF4
SF6
S2F2
/ *
S2Fio
(SFK(NK
(SFL(NL
S2I2
S4N2
S4N4
S(N)F3
S(NH)O
S(NH2JO2
so2
• 7,67H2O
S03
S2O
S(O)F2
S(O)F4
SO2F2
SO2(O2)
S(S)F2
H2S
H2(S2)
H2(S3)
H2(S4)
H2(S5)
H2(S6)
H2(S7)
H2(S8)
It r>
H2so4
H2O
¦2H2O
It e _
H2S2O7
Mr
118,52
108,06
146,05
102,13
254,11
195,21
260,28
317,94
156,28
184,29
103,07
63,08
96,11
64,06
202,24
80,06
80,13
86,06
124,06
102,06
96,06
102,13
34,08
66,15
98,21
130,28
162,35
194,41
226,48
258,54
98,08
116,09
134,11
178,14
Фазовые переходы
п. -124,7, к. +7,1
п.-121, к.-38
п. -50,8, > 700 — S
n.-133,K.+15[—S(S)F2]
п. -52,7, к. +29 разл.
п. 74, к. 93
п. 153 разл.
разл. 30
п. 23 разл., 25—100 -^ S
п. 178, к. 185
п.-72,6, к.-27,1
п. -85, разл. > 20
п. 92,5, разл. 140
п. -75,46, к. -10,6
п. 12, разл. 60—80
п. 16,79, к. 44,7
п. < -196
п. -129,5, к. -43,85
п. -99,6, к. -48,5
п.-135,81, к.-55,37
п. 3,0 разл.
п. -164,6, к. -10,6
п. -85,7, к. -60,35
п. -89,8, к. +70,7
п. -52, к. +69 разл.
п. -86, разл. > 100
п. -50, разл. > 100
разл. > 100
разл. > 130
разл. > 130
п. 10,31, к. 279,6
п. 8,48, к. 223
п.-39,47, к.+174,8
п. 35,22, > 80 — H2SO4
Окраска
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бцв. ж.
бел.
бел.
бур.
краен.
оранж.
бцв. г.
бцв. ж.
бел.
бцв. г.
бцв. ж.
бцв. ж.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бел.
бцв. г.
бцв. г.
св.-желт. ж.
св.-желт. ж.
желт. ж.
св.-зел. ж.
св.-зел. ж.
зел. ж.
зел. ж.
бцв. ж.
бцв. ж.
бцв. ж.
бел.
Плот-
Плотность
5,29
6,976
4,3
2,08°
1,901
2,22
2,9266
1,9718
3,84
3,992
4,3
1,538
1,33420
1,49920
1,58220
1,64420
1,68620
1,72120
1,74720
1,83120
1,77420
1,64720
1,9
165
I. Неорганические вещества
Продолжение табл.
Формула
HSO3C1
HSO3F
HSO3(NH2)
H2SO3(O2)
H2S2O6(O2)
H2SO3S
Sb
SbBr3
SbCl3
SbCl5
SbCl3F2
[SbCl6],H
• 4,5H2O
[SbvCl6],[I(I)Cl]
Sb(Cl)O
SbF3
SbF5
[SbF6],(C10j)
[SbF6],H
•H2O
[SbF6],Na
SbH3
Sbl3
Sbl5
a-Sb2O3
«H2O
C-Sb2O3
Sb2O5
•4H2O
[Sb(OHN],K
[Sb(OHN],Na
Sb2S3
Sb2S5
Mr
116,52
100,07
97,09
114,08
194,14
114,15
121,757
361,47
228,12
299,02
266,11
335,48
416,55
623,74
173,21
178,75
216,75
303,20
236,75
254,77
258,74
124,78
502,47
756,28
291,51
—
291,51
323,51
395,57
262,90
246,79
339,71
403,83
Фазовые переходы
п.-80,5, к. +152разл.
п.-87, к.+163
п. 207 разд., 230 — SO3
п. 47 разд., > 50 -* H2SO4
п. 65 разл., 70 -* H2SO4, SO3
разл. > -78
п. 630,63, к. 1587
п. 96, к. 287
п. 73,4, к. 222,6
п. 3,2, к. 68 (вак.)
п. 55
Не получен
п. 44, 70-80 - SbCl5
п. 70, возг 20
разл. > 170
п. 280, к. 346
п. 6,0, к. 149,5
п. 235
Не получен
разл.357
п. > 350
п. -92,4, к. -18,3
п. 170,5, к. 401,6
п. 79, к. 401
572 — C-Sb2O3
-Н2О 300-350
п. 656, к. 1456
797 - (SbIHSbv)O4
разл. 500
разл. 680
разл. 600
п. 559,5, к. 1160
170 — Sb2S3
Окраска
бцв. ж.
бцв. ж.
бел.
бел.
бел.
бцв. ж.
гол.-бел.
бел.
бел.
бцв. ж.
бел.
св.-зел.
т.-краен.
бел.
бел.
бцв. ж.
бел.
бел.
бел.
бцв. г.
краен.
краен.
бел.
бел.
бел.
желт.
бел.
бел.
бел.
т.-сер.
т.-оранж.
Плот-
Плотность
1,7920
1,7418
2,126
6,684
4,148
ЗД4
2,3320
4,385
2,99322
3,38
4,599
4,92
5,67
5,25
3,8
4,27
4,635
4,12
i —-
166
I. Неорганические вещества
Продолжение табл.
формула
Sb(S)I
[SbS3],Na3
•9H2O
[SbS4],Na3
•9H2O
Sb2(SO4K
(SbIMSbv)O4
Sb2Se3
Sb2Te3
Sc
ScB2
ScBr3
ScC
Sc2(C2O4K
•5H2O
ScCl3
•6H2O
ScF3
Scl3
ScN
Sc(NO3K
•4H2O
Sc2O3
Sc(OHK
tSc(OHL],Na
[Sc(OHN],Na3
ScO(OH)
ScPO4
•2H2O
Sc2S3
Sc2(SO4K
•5H2O
^аморфн^
Mr
280,73
286,93
449,06
318,99
481,13
531,70
307,51
480,39
626,31
44,956
66,58
284,67
56,97
353,97
444,04
151,32
259,41
101,95
425,67
58,96
230,97
303,03
137,91
95,98
135,97
215,97
77,96
139,93
175,96
186,11
378,10
468,17
78,960
Фазовые переходы
п. 400
п.« 600
-Н2О 150
разл. > 420
-Н2О 180
разл. 500
> 930 - Sb2O3
п. 617, к. 1031
п. 621,6, к. 1173
п. 1541, к. 2830
п. 2250
возг. 929
п.1800
Не получен
500 -+ Sc2O3
п. 967(р)9 к. 975
разл. 250
п. 1552, к. 1607
возг. 912
п. 2650
> 300 — Sc2O3
> 220 — Sc2O3
п. 2450,
280 — ScO(OH)
разл. > 300
разл. > 120
460 -> Sc2O3
п.1780
-Н2О 200
п. 1700
> 600 — Sc2O3
-Н2О 250-400
> 72 — Se8
Окраска
краен.
желт.
св.-желт.
зел.
желт.-зел.
бел.
желт.
сер.
сер.
бел.-желт.
сер.
бел.
черн.
бел.
бел.
бел.
бел.
бел.
т.-гол.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.
бел.
бел.
сер.-краен.
Плот-
Плотность
5,19
1,839
3,62
6,52
5,81
6,513
2,989
3,91
2,39
4,2
3,864
2,65
2,8
2,579
2,52
4,28
167
I. Неорганические вещества
Продолжение табл.
Формула
Se (сер.)
Se8
SeBr4
Se2Br2
Se(Br)Cl3
SeBr2O
SeCl4
Se2Cl2
SeCl2O
SeF4
SeF6
SeO2
SeO3
Se(O)F2
(SeO2+)SeO4
Se4S4
H2Se
H2Se03
H2Se04
•H2O
Si
SiBr4
SiC
SiCl4
Si2Cl6
Si3Cl8
Si(Cl)F3
SiCl2F2
SiCl3F
Si2Cl60
Si3Cl8O2
Si4Cl804
SiF4
4
78,96
631,68
398,58
317,73
265,22
254,77
220,77
228,83
165,87
154,95
192,95
110,96
126,96
132,96
237,92
444,10
80,98
128,97
144,97
162,99
28,086
347,70
40,10
169,90
268,89
367,88
120,53
136,99
153,44
284,89
399,88
459,96
104,08
Фазовые переходы
п. 221, к. 685
п. 170
разл. 75
разл. > 100
п. 190
п. 41,6, к. 217 разл.
п. 305(р), возг. 196
п.-85, к.+127 разл.
п. 10,9, к. 179,6 разл.
п. -9,5, к. +101
п. -34,6, возг. -46,6
п. 389(/>), возг. 337
п. 121,>240-*SeO2
п. 15,5, к. 125
п. 224(р), 185 — SeO2
п. 113 разл.
п.-65,72, к.-41,35
п. 66,5, > 72 - SeO2
п. 62,4 , > 260 — SeO2
п. 25,4, к. 205
п. 1414, к. 3265
п. 5,4 , к. 152,6
п. 2540 разл.
п. -68,8, к. +57,5
п.-1,0, к.+144,5
п.-67, к.+215
п. -142, к. -70
п.-139,7, к.-32,2
п.-120,8, к.+12,2
п.-35, к.+137
п. -47, к. +184
п. 77, к. 202
п. -86,8(/>), возг. -95,7
Окраска
сер.
краен.
св.-оранж.
т.-краен, ж.
желт.-кор.
оранж.
св.-желт.
т.-красн. ж.
св.-желт. ж.
бцв. ж.
бцв. г.
бел.
бел.
бцв. ж.
бел.
т.-желт.
бцв. г.
бел.
бел.
бел.
т.-сер.
бцв. ж.
бел.
бцв. ж.
бцв. ж.
бцв. ж.
бцв. г.
бцв. г.
бцв. г.
бцв. ж.
бцв. ж.
бел.
бцв. г.
Плот-
Плотность
4,81
4,46
3,60415
2,7
2,7725
2,44520
2,7525
2,917
3,954
3,6
2,б72°.;
3,58
3,06
3,6643
3,004
2,95
2,63
2,33
2,78920
3,208
1,48120
1,56215
1,6115
4,684
168
I. Неорганические вещества
Продолжение табл.
формула
Si2F6
Si3F8
Si4Fm
[SiF«],Ba
[SiF6],Ca
•2H2O
[SiF6],Co
•6H2O
[SiF6],Cs2
[SiFJ.Cu
•6H2O
[SiF6],Fe
•6H2O
[SiF6],K2
[SiF6],Li2
•2H2O
[SiF6],Mg
•6H2O
[SiFd.Mii
•6H2O
[SiF6],(NH4J
[SiF6],Na2
[SiFJ.Ni
•6H2O
(SiF^JO
[SiFJ.Rbj
tSiF6],Sr
•2H2O
ISiFd.Tlj
SiH4
S'2H6
Si3H8
C'
Sl4H1Q
170,16
236,24
302,32
279,40
182,15
218,18
201,01
309,10
407,88
205,62
313,71
197,92
306,01
220,27
155,96
191,99
166,38
274,47
197,01
305,10
178,15
188,05
200,77
308,86
186,16
313,01
229,69
265,72
550,84
32,12
62,22
92,32
122,42
Фазовые переходы
п.-18,7, к.+19,1
п.-1,2, к.+42
п. 67, к. 85
> 650 - SiF4
> 370 - SiF4
-Н2О < 200
Не получен
разл. 180
245-800 — SiF4
Не получен
разл. > 150
Не получен
разл. > 175
п. 873(р), 700 -> SiF4
> 400 - SiF4
-Н2О 100 (вак.)
350 - SiF4
-Н2О < 120 (вак.)
Не получен
разл. > 160
319 — SiF4
п. 846(р), > 570 — SiF4
Не получен
разл. > 185
п. -47,7, к. -23,2
750 — SiF4
> 420 — SiF4
-Н2О110(вак.)
165 - SiF4
п.-184,67, к.-111,9
п.-131, к.-14,5
п.-117,4, к.+52,9
п.-84,3, к.+108
Окраска
бцв. г.
бцв. ж.
бел.
бел.
бел.
бел.
св.-краен.
бел.
гол.
зел.-бел.
бел.
бел.
бел.
бел.
бел.
роз.
бел.
бел.
зел.
бцв. г.
бел.
бел.
бел.
бел.
бцв. г.
бцв. г.
бцв. ж.
бцв. ж.
Плот-
Плотность
4,279
2,66
2,11
3,37
2,21
1,96
2,67
2,33
1,79
1,9
2,0
2,68
2,13
3,33
2,99
5,72
1,44
2,85
0,73920
0,825°
169
I. Неорганические вещества
Продолжение табл.
Формула
Si(H)Cl3
SiH2CI2
SiH3Cl
Si(H)Cl2F
Si(H)F3
SiH2F2
Si(H)I3
SiH2I2
SiH3I
Sil4
[SiMo12O40],H4
•лН2О
Si3N4
Si(NCOL
SiO
SiO2 (аморфн.)
«H2O
SiO2 (ос-кварц)
(р-кварц)
(а-кристобалит)
(р-кристобалит)
(ос-тридимит)
(р-тридимит)
Si(OCNL
SiP
SiS2
[SiW12O40],H4
•7H2O
Sm
SmB6
SmBr2
SmBr3
•6H2O
4
135,45
101,01
66,56
119,00
86,09
68,10
409,81
283,91
158,01
535,70
1823,36
—
140,29
196,15
44,09
60,08
—
60,08
60,08
60,08
60,08
60,08
60,08
196,15
59,06
92,22
2878,16
3004,26
150,360
215,23
310,17
390,07
498,16
Фазовые переходы
п.-128,2, к.+31,5
п. -122, к. +8,3
п.-118,1, к.-30,4
п. -149,5, к. -54,3
п.-131,2, к.-97,5
п.-122, к.-77,8
п. 8,0, к. 111 (вак.)
п.-1,0, к.+149,5
п. -57, к. +45,4
п. 122,5, к. 290
Не получен
разл. 120—700
возг. 1600, к. > 1650 разл.
п. 26, к. 186
разл. 400—700
разм. 1300
-Н2О 900
575 -> Р-кварц
п. 1610, к. 2950
270 —> р-кристобалит
п. 1723, к. 2950
115 —^ Р-тридимит
п. 1680, к. 2950
п. 35, к. 245
п.1170
п. 1090, к. ИЗО
Не получен
разл. 100—650
п. 1072, к. 1790
п. 2540
п. 669, к. 1880
п. 640, > 1100 —SmBr2
-Н2О 100
Окраска
бцв. ж.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бцв. г.
бцв. ж.
бцв. ж.
бцв. ж.
бел.
желт.
желт.-бел.
бел.
св.-кор.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.-кор.
бел.
бел.
желт.
черн.
т.-кор.
т.-желт.
желт.
Плот-
Плотность
1,34220
3,31420
2,72420
2,07°
4,4
3,192
1,413
2,15
2,21
-2,1
2,655
2,533
2,334
2,23
2,3
2,26
1,41
2,02
7,52
5,1
2,97
170
I. Неорганические вещества
Продолжение табл.
формула
Sm(BrO3K
9Н2О
SmC2
Sm2(C2O4K
• 10Н2О
SmCl2
SmCl3
•6Н2О
(SmnlCr)O3
SmF3
Sml2
Sml3
Sm2(MoO4K
Sm(NO3K
•6H2O
Sm2O3
Sm(OHK
SmS
Sm2S3
Sm2(S)O2
Sm2(SO4K
•8H2O
Sn (сер.)
Sn (бел.)
SnBr2
SnBr4
sn(Br)Cl3
SnBr3Cl
sn(CH3COOJ
Sn(CH3COOL
SnC2O4
SnCl2
•2H2O
Mr
534,06
696,20
174,38
564,77
744,92
221,27
256,72
364,81
250,35
207,35
404,17
531,07
780,53
336,37
444,46
348,72
201,38
182,43
396,92
214,42
588,91
733,03
118,710
118,710
278,52
438,33
304,97
393,88
236,80
354,89
206,73
189,62
225,65
Фазовые переходы
разл. > 500
п.74,5,-Н2О150
п. > 2300
Не получен
> 600 -* Sm2O3
п. 859, к. 1950
п. 678
-Н2О>110
п. 2400
п. 1305, к. 2330
п. 520, к. 1660
п. 816-824, > 830 ->SmI2
п. ИЗО
разл. 525
п. 79, -Н2О 172
п. 2270
> 500 -> Sm2O3
п. 1940
п.1780
п. 1980
> 900 -* Sm2O3
-Н2О 450
> 13,2 ^Sn (бел.)
п. 231,93, к. 2602
п. 215,5, к. 620
п. 31, к. 202
п.-1,0, к.+50
п. 1,0, к. 73
п. 182, к. 240
п. 253
п. 280 разл.
п. 246, к. 652
п. 37,7, -Н2О 130-135
Окраска
т.-желт.
желт.
желт.
желт.
краен.-кор.
желт.
св.-желт.
сер.-зел.
св.-желт.
черн.-зел.
т.-желт.
фиол.
зел.-желт.
св.-желт.
св.-желт.
св.-желт.
кор.
желт.-роз.
т.-желт.
желт.
св.-желт.
сер.
бел.
желт.
бцв. ж.
бцв. ж.
бцв. ж.
св.-желт.
бел.
бел.
бел.
бел.
Плот-
Плотность
5,86
4,56
4,46
2,38
7,28
6,9
5,36
2,38
8,347
5,73
2,93
5,75
7,28
5,12
3,3435
2,5120
3,1220
2,П
3,56
3,95
2,71
171
I. Неорганические вещества
Продолжение табл.
Формула
SnCl4
[SnCl6],Cs2
Sn(Cl)F
[SnCl6],H2
•6H2O
[SnCl6],K2
[SnCl6],(NH4J
SnF2
SnF4
[SnF6],K2
H2O
SnH4
Sn(HCOOJ
Snl2
Snl4
SnI2Br2
SnI2Cl2
Sn(NO3J
• 20H2O
Sn(NO3L
SnO
SnO2
•лН2О
Sn(OHJ
[Sn(OHN],K2
[Sn(OHK],Na
[Sn(OHN],Na2
Sn2P2O7
@<x< 0,00027)
SnS2
[SnS3],K2
•3H2O
4
260,52
597,24
173,16
333,44
441,53
409,62
367,51
156,71
194,70
310,89
328,91
122,74
208,74
372,52
626,33
532,33
443,42
242,72
603,02
366,73
134,71
150,71
—
152,72
298,95
192,72
266,73
411,36
150,78
182,84
293,10
347,15
Фазовъю переходы
п.-33, к.+114,1
разл.« 350
п. 185-190
Не получен
п. 19,2, разл. 30
разл. > 400
разл. > 200
п. 215,05, к. 853
возг. 705
Не получен
разл. > 115
п. -146, к. -52
п. 198 разл.
п. 320, к. 717
п. 144,5, к. 344,5
п. 50, к. 225
к. 297
Не получен
п. 20, разл. > 150
n.91,600-SnO2
разл. > 180
п. 1630, к. 2500
-Н2О 600
120 — SnO
разл. 185
разл. > 30
разл. > 140, 900 -> SnO2
п. 400
п. 881, к. 1230
п. 870(/?), 600 — SnS
разл. > 400
-Н2О 90-100
Окраска
бцв. ж.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бцв. г.
бел.
св.-краен.
желт.
св.-краен.
краен, ж.
бел.
бел.
черн.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
сер.
желт.
т.-кор.
кор. ж.
Плот-
Плотность
2,22620
3,33
1,925
2,71
2,4
5,33
4,78
3,05
2,96
5,19
4,5 •
3,63
1,2
2,65
6,446
7,0096
3,197
4,01
5,08
4,5
1,1820
172
I. Неорганические вещества
Продолжение табл.
формула
SnSO4
•ЗН2О
Sn(SO4J
•2Н2О
SnSe
SnSe2
(SnnSnIV)S3
(Sn^SnIV)S4
SnTe
Sr
(SrAs2)O6
SrB6
SrBr2
•6H2O
Sr(BrO3J
H2O
SrC2
Sr(CH3COOJ
SrCO3
SrC2O4
H2O
SrCl2
•6H2O
Sr(Cl)F
Sr(C103J
•8H2O
Sr(C104J
SrCrO4
SrCr2O7
•зн2о
SrF2
SrH2
Mr
214,77
268,82
310,83
346,86
197,67
276,63
333,62
484,39
246,31
87,620
333,46
152,49
247,43
355,52
343,42
361,44
111,64
205,71
147,63
175,64
193,65
158,53
266,62
142,07
254,52
398,64
286,52
203,61
303,61
357,65
125,62
89,64
183,60
Фззовые переходы
п. 360 разл.
-Н2О 40 (вак.)
200 - SnO2
разл. > 50
п. 880
п. 675
п. 675 разл.
п. 710 разл.
п. 807
п. 777, к. 1382
разл. 979
п. 2235
п. 657, к. 1972
п. 88,62, -Н2О 345
разл. 240 ,
-Н2О 120
п. - 1700
п. 321, разл. 350-400
п. 1494(/?), > 1100-> SrO
450 — SrCO3
-Н2О 150
п. 874, к. 1300
п. 115, -Н2О250
п. 962
> 500 — SrCl2
-Н2О > 120
> 472 — SrCl2
п. 1283 разл.
> 500 -> SrCrO4
-Н2О110
п. 1477, к. 2460
п. 1050 разл.
разл.« 900
Окраска
бел.
бел.
бел.
бел.
т.-сер.
бур.
син.-черн.
черн.
сер.
бел.
бел.
т.-сер.
бел.
бел.
бел.
бел.
черн.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.
краен.
оранж.
бел.
бел.
бел.
Плот-
Плотность
4,18
4,5
6,18
5,13
4,87
6,45
2,54
3,39
4,216
2,358
3,77
3,2
2,1
3,785
3,085
1,954
4,18
3,15
2,947
3,895
4,18
3,27
3,54
173
I. Неорганические вещества
Продолжение табл.
Формула
Sr(HSJ
(SrHf)O3
Srl2
•6Н2О
Sr(IO3J
Sr(MnO4J
•3H2O
SrMoO4
Sr3N2
Sr(NCSJ
•3H2O
SrN2O2
•5H2O
Sr(NO2J
•H2O
Sr(NO3J
•4H2O
SrO
SrO2
•8H2O
Sr(OHJ
•8H2O
Sr3(PO4J
SrS
SrSO4
SrS2O6
•4H2O
SrS4O6
•6H2O
Sr(SO3S)
•5H2O
SrSe
SrSeO4
Mr
153,77
314,11
341,43
449,52
437,42
325,49
379,53
247,56
290,87
203,79
257,83
147,63
237,71
179,63
197,65
211,63
283,69
103,62
119,62
263,74
121,63
265,75
452,80
119,69
183,68
247,75
319,81
311,88
419,97
199,75
289,82
166,58
230,58
Фазовуе переходы
разл. 150—200
п. 2830
п. 538, к. « 1900
разл. 120—350
разл. > 500
Не получен
разл. > 175
п. 1457
разл. > 1000
разл. > 160
-Н2О 100
550 — SrO
-Н2О 100
разл. 240
-Н2О 90-105
п. 570 разл., 600 -> SrO
-Н2О 100
п. 2660, к. - 3000
п. 215, 365-900 —SrO
-Н2О 100 (вак.)
п. 535(р), 400 — SrO
-Н2О110(вак.)
п.1600
п. 2227 разл., > 2250 — Sr
п. 1607(/>), > 1300 — SrO
разл. 150
-Н2О 78
разл. 180
-Н2О > 50
разл. > 200
-Н2О 189
п.1600
разл. > 1650
Окраска
бел.
бел.
бел.
бел.
бел.
фиол.
св.-сер.
сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
Плот-
Плотность
4,549
4,415
5,05
2,75
4,7
2,17
2,87
2,41
2,99
2,25
4,7
4,71
1,95
3,625
1,9
3,64
3,973
2,37
2,15
2,92
2,17
5,54
4,23
174
I. Неорганические вещества
Продолжение табл.
формула
SrSiO3
•2Н2О
Sr2Si04
SrTe
(SrTi)O3
SrWO4
(SrZr)O3
т2
T2O
Та
TaB2
ТаВг4
TaBr5
Ta6Brl5
ТаС
Та2С
[Та(С5Н5)С14]
ТаС13
ТаС14
ТаС15
Та6С115
ТаС13О
TaF5
[TaF7],K2
fTaF8],K3
(Ta2Fe")O6
Ta2H
Tal4
Т т
Tal5
Ta6Il4
Oa2Mn»)O6
TaN
4
163,70
199,73
267,32
215,22
183,50
335,46
226,84
6,032
22,03
180,948
202,57
500,56
580,47
2284,25
192,96
373,91
387,86
287,31
322,76
358,21
1617,48
303,31
275,94
392,13
450,23
513,74
362,90
688,56
815,47
2862,34
512,83
194,96
Фазовые переходы
п. 1580
-H2O 850
п. 2325
п. 1490
п. 2040
п. 1535 разл.
п. 2750
п.-252,52, к.-248,12
п. 4,5, к. 101,55
п. 3017, к. 5458
п. 3035
п. 392
п. 265,8, к. 346
возг. > 450
п. 3985
п. 3500
возг. 230
разл. > 440
возг. 280, разл. > 300
п. 216,5, к. 236
возг. > 470
разм. 327, разл. > 340
п. 96,8, к. 229,2
п. 775
п. 780
разл. > 1900
> 800 - Та
п. 398
п. 496, к. 543
возг. > 535
разл. > 2000
п. 3360 разл.
Окраска
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бцв. г.
бцв. ж.
бцв. ж.
сер.
бел.
т.-кор.
оранж.
черн.-кор.
желт.-сер.
т.-желт.
желт.
зел.
кор.-зел.
бел.
черн.-зел.
бел.
бел.
бел.
бел.
св.-кор.
сер.
черн.
черн.-кор.
зел.
черн.
сер.-гол.
Плот-
Плотность
3,65
3,84
4,83
5,11
6,19
5,0
0,2691
0,25748
1,21520
16,6
12,38
5,77
4,99
6,29
14,4
15,22
5,02
4,35
3,68
5Д
4,98
4,06
7,33
5,798
6,85
7,03
14,34
175
I. Неорганические вещества
Продолжение табл.
Формула
Ta3N5
Та2О5
пН2О
Ta(O)F3
TaO2F
Ta3O7F
Ta2(SO4M
TaSi2
Tb
Tb2(C2O4K
• 10H2O
TbCl3
•6H2O
TbF3
TbF4
Tb(NO3K
•6H2O
Tb2O3
Tb(OHK
Tb2(SO4K
•8H2O
Tc
TcBr3O
[Tc(C5H5J]
[Tc2(COI0]
[Tc(COKC5H5]
TcCl4
TcCl6
[TcCl6],K2
Tc(Cl)O3
TcCl3O
TcF5
TcF6
4
612,88
441,89
—
253,94
231,94
673,84
842,21
237,12
158,925
581,90
762,05
265,28
373,37
215,92
234,92
344,94
453,03
365,85
209,95
606,04
750,16
97,907
353,62
228,10
475,91
247,03
239,72
310,63
388,82
181,36
220,27
192,90
211,90
Фазовые переходы
> 1000 — TaN
п. 1787
-H2O > 600
разл. 400
разл. 500
разл. 900
разл. > 100
п.« 2200
п. 1359, к. 3221
Не получен
> 600 -> ТЬ2О3
п. 582, к. 1552
п. 153, -Н2О 250
п. 1177, к. 2880
> 600 — TbF3
450 — ТЬ2О3
п. 89,3, -Н2О « 200
п. 2390, к. « 4300
750 - ТЬ2О3
разл. > 850
-Н2О 360
п. 2157, к. 4265
возг. 400
п. 155
п. 159-160
п. 87,5
возг. > 300
разл. > 20
разл. 420
к. 25
возг. 900
п. 50
п. 33,4, к. 55,3
Окраска
краен.
бел.
бел.
бел.
бел.
бел.
бел.
сер.
бел.
бел.
бел.
бел.
бел.
желт.
бел.
бел.
бел.
бел.
бел.
бел.
св.-сер.
бур.
ярко-желт.
бел.
бел.
т.-краен.
т.-зел.
желт.
бцв. ж.
бур.
желт.
желт.
Плот-
Плотность
9,85
8,18
9,14
8,23
4,35
7,23
7,5
11,49
3,3
3,6
3,02
—-
176
I. Неорганические вещества
Продолжение табл.
формула
[TcF«],K
[TcF«],K2
L u
TcO2
Tc2O7
Tc(O)F4
TcO3F
Tc(OHL
Tc2S7
HTcO4
Те
ТеВг2
ТеВг4
ТеС12
ТеС14
TeF4
TeF6
Tel4
[TeMo6O24],(NH4N
•7H2O
TeO2
ТеО3
(ТеО2+)ТеО4
Н2Те
Н2Те03
Н6Те06
Th
ThB6
ThBr4
ThC
ThC2
ThCl4
•8H2O
4
250,99
290,09
129,91
307,81
189,90
164,90
165,94
420,28
162,91
127,600
287,41
447,22
198,51
269,41
203,59
241,59
635,22
1195,45
1321,56
159,60
175,60
335,20
129,62
177,61
229,64
232,038
296,90
551,65
244,05
256,06
373,85
517,97
Фазовые переходы
разл. > 150
разл. > 225
> 1100 —Тс
п. 119,5, к. 310,5
п. 134
п. 18, к. 100
400 — ТсО2
разл. > 230
>160 —Тс2О7
п. 449,51, к. 988
п. 280, к. 339
п. 380, к. 421
п. 208, к. 328
п. 224, к. 381,8
п. 129,6, к. 194 разл.
п. -37,8, возг. -38,6
п. 280(/?), разл. 100
Не получен
разл. 550
п. 732, к. 1257
360 — ТеО2
п. 600 разл., > 650 — ТеО2
п.-51, к.-1,8
> 40 — ТеО2
п. 136,220-ТеОз
п. 1750, к. 4788
п. 2195
п. 679, к. 857
п. 2625
п. 2655, к. « 5000
п. 770, к. 921
разл. 200—750
Окраска
св.-желт.
св.-роз.
зел.-черн.
св.-желт.
гол.
желт. ж.
кор.-черн.
краен.
сер.-бел.
бур.
св.-оранж.
бур.
бел.
бел.
бцв. г.
т.-сер.
бел.
бел.
ярко-желт.
сер.
бцв. г.
бел.
бел.
бел.
черн.-фиол.
бел.
желт.
черн.
бел.
бел.
Плот-
Плотность
6,9
3,5
6,25
4,31
7,05
3,01
4,22
10,7
5,05
2,78
5,42
4,18
6,12
5,81
3,05
3,07
11,72
7,31
5,69
9,736
4,6
177
I. Неорганические вещества
Продолжение табл.
Формула
ThF4
•4Н2О
ThH2
Thl4
ThN
Th(NO3L
•5H2O
ThO2
Th(OHL
Th(PO3L
ThS2
Th(SO4J
•9H2O
Th(SeO4J
•9H2O
ThSi2
ThSi4
Ti
TiB2
TiBr2
TiBr3
•6H2O
TiBr4
@<x<0,51)
[Ti(C5H5J]
[Ti(C5H5)Cl3]
[Ti(C5H5JCl]
[Ti(C5H5JCl2]
[Ti(COJ(C5H5J]
TiCl2
TiCl3
TiCl4
Mr
308,03
380,09
234,05
739,65
246,05
480,05
570,13
264,04
300,07
547,92
296,17
424,16
586,30
517,95
680,09
288,21
324,12
47,880
69,50
207,69
287,59
395,68
367,50
59,89
178,07
219,33
213,52
248,98
234,09
118,79
154,24
189,69
Фазовые переходы
п. 1110, к. 1650
разл. 250—700
900 (вак.) — Th
п. 566, к. 837
п. 2630
> 400 — ThO2
разл. 150—270
п. 3350, к. « 4400
> 470 — ThO2
разл. > 1500
п. 1930 разл.
> 950 -> ThO2
-Н2О 350-400
разл. > 600
~Н2О 220
п. 1640 разл.
п. 1975 разл.
п. 1668, к.3287
п. 3225
разл. > 600
разл. > 400
п. 115, -Н2О 180
п. 38,25, к. 231
п. 3257, к. 4300
п. 173
п. 216,75
п. 283
п. 289-291
разл. > 90
п. 1035, к.1515
п. 9200?), разл. 440-700
п.-24,1, к.+136,3
Окраска.
бел.
бел.
т.-сер.
желт.
желт.
бел.
бел.
бел.
бел.
бел.
т.-красн.
бел.
бел.
бел.
бел.
черн.
бел.
бел.
черн.
черн.
т.-син.
фиол.
желт.
сер.
т.-зел.
желт.
бур.
краен.
краен.-кор.
черн.
т.-фиол.
бцв. ж.
Плот-
ность
5,71
3,36
9,2
6,0
П,2
2,8
10,0
4,08
7,36
4,23
2,77
3,03
7,96
6,82
4,5
4,45
4,41
4,24
3,25
4,92
1,6
3,13
2,656
1,726*
178
I. Неорганические вещества
Продолжение табл.
формула
Ti(Cl)F3
Т«С12О
Ti(C104L
СПСо")О3
(TiCo2')O4
TiF2
TiF3
TiF4
[TiF6],K2
•H2O
(TiFe")O3
(TiFe2')O4
TiH2
Til2
Til3
Til4
TiI2O
(TiMn")O3
(TiMn^)O4
TlNi-*
@<x<0,42)
Ti(NO3L
TiOl+;c
(-0,4 <x< 0,26)
P-TiO2
Y-TiO2
(-0,16 <*< 0,14)
Ti(O)F2
*i(OHK
T;n
HP
("ПРЬ«)о3
Mr
140,33
118,79
445,68
154,81
229,74
85,88
104,87
123,87
240,06
258,08
151,72
223,57
49,90
301,69
428,59
555,50
317,69
150,82
221,75
61,89
295,90
63,88
79,88
79,88
79,88
143,76
101,88
98,90
97,89
78,85
303,08
Фазовые переходы
разл. 125
разл. 180—300
п. 85, разл. ПО
п. 1470
п. 1575
разл. > 420
к. 1037 разл.
п. 426(р), возг. 285,5
п. 822
-Н2О 32
п. 1365, разл. > 1900
п.1375
разл. 600—700
п. 600, к. 1170
разл. 350
п. 155, к. 379,5
разл. 105
п. 1360
п. 1455
п. 2947
п. 58
п. 1780, к. 3227
> 400 - Y-TiO2
750 - у-ТЮ2
п. 1870, к.-3000
п. 1842, к.-3000
разл. > 550
> 700 — Ti2O3
600-700 — TiO2
п. 1990 разл.
п. 818
Окраска
желт.
желт.
бел.
желт.-зел.
зел.-черн.
черн.
гол.-фиол.
бел.
бел.
бел.
черн.
т.-кор.
сер.
черн.
фиол.
краен.-кор.
бур.
краен.
краен.
желт.-кор.
бел.
желт.
бел.
бел.
бел.
т.-фиол.
бел.
фиол.
бел.
сер.
желт.
Плот-
Плотность
2,45
5,4
5,07
2,98
2,798
4,75
4,37
3,78
4,99
4,4
4,537
4,49
5,44
2,16
4,93
4,12
4,05
4,235
4,53
2,92
2,6
3,95
7,3
179
I. Неорганические вещества
Продолжение тавд
Формула
TiS
TiS2
Ti2S3 + ,
(-0,74 <jc< 0,18)
Ti2(SO4K
Ti(SO4)O
TiSO4(OHJ
TiSi
TiSi2
Ti5Si3
Tl
T1A1(SO4J
• 12H2O
Tl3AsS4
TlBr
T1(C5H5)
T1(CH3COO)
T1(CH3COOK
T12CO3
T12C2O4
T1C1
T1C13
•4H2O
T1C1O3
T1C1O4
Tl2Cr04
Tl2Cr2O7
T1F
T1F3
Tl(HCOO)
T1H2PO4
T12HPO4
•2H2O
4
79,95
112,01
191,96
383,95
159,94
177,96
75,97
104,05
323,66
204,383
423,49
639,67
816,34
284,29
269,48
263,43
381,52
468,77
496,78
239,84
310,74
382,80
287,83
303,83
524,76
624,75
223,38
261,38
249,40
301,37
504,74
540,77
Фазовые переходы
п. 1930
п.« 800
500 — TiS2
500-600 — TiO2
> 580 -> TiO2
330 - Ti(SO4)O
n.1920
n. 1540
n. 2120
n. 304, к. 1473
разл.« 800
n.91,-H2O110
п. 425
п. 460, к. 824
п. > 230
п. 131, разл. «200
п. 182 разл.
п. 267, 300-360 - Т12О
разл. > 350
п. 431, к. 820
п. 155(р), > 150 — Т1С1
-Н2О 25 (вак.)
разл. 500
п.501,>590-Т1С1
п. 633
п. 360 разл.
п. 326, к. 840 разл.
п. 550 разл.
п. 104, разл. - 200
п. 190
Не получен
200 — Т14Р2О7
Окраска
бур.
желт.
черн.
зел.
бел.
бел.
сер.
св.-сер.
сер.
гол.-бел.
бел.
бел.
краен.
зел.-желт.
св.-желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт.
св.-краен.
бел.
св.-зел.
бел.
бел.
бел.
Плот-
Плотность
3,22
3,58
2,78
4,21
4,13
4,32
11,85
2,32
7,56
3,68
7,24
6,31
7,0
3,03
5,05
4,89
6,91
8,36
8,3
4,73
180
I. Неорганические вещества
Продолжение табл.
формула
T1HSO4
ТИ
T1N3
T1NCS
T1NO2
TINO3
T1(NO3K
•ЗН2О
Т12О
ПА
•лН2О
тюн
•2Н2О
Т13РО4
Т14Р2О7
T12S
T12S3
T12SO4
T12S2O6
T12(SO3S)
Tl2Se
Tl2Se04
T1VO3
Tm
TmBr3
Tm2(C2O4K
•6H2O
TmCl3
•6H2O
T»v.?
iml3
4
301,45
331,29
246,40
262,47
250,39
266,39
390,40
444,44
424,77
456,76
—
221,39
257,42
708,12
991,47
440,83
504,96
504,83
568,89
520,90
487,73
551,72
303,32
168,934
408,65
601,92
710,01
275,29
383,38
225,93
549,65
Фазовые переходы
п. 120разл.
п. 441, к. 833 разл.
п. 334, разл. > 400
п. 234
п. 186
п. 208, разл. 250—500
Не получен
п. 102, 250 - Т12О3
п. 579, к,- 1100
п. 864(/>), 300 - Т12О
-Н2О < 300 (вак.)
п. 130 разл.
-Н2О 45-60
разл. 250
разл. > 120
п. 452, к. 1177
разл. 260
п. 646
250 — T12SO4
разл. 130
п. 390
п. > 400
п. 424
п. 1545, к. 1946
п. 954, к. 1440
Не получен
> 600 — Тт2О3
п. 828, к. 1487
п. 154, -Н2О 330
п. 1158, к. 2230
п. 1020, к. 1260
Окраска
бел.
яр-
ко-красн.
желт.
бел.
желт.
бел.
бел.
черн.
т.-кор.
бур.
желт.
св.-желт.
бел.
бел.
гол.-черн.
черн.
бел.
бел.
бел.
сер.
бел.
сер.
бел.
бел.
св.-зел.
св.-желт.
зел.
св.-зел.
желт.-зел.
Плот-
Плотность
7,07
4,96
5,556
10,4
10,0
7,44
6,89
6,79
8,46
6,67
5,57
9,05
6,88
6,09
9,321
7,95
181
I. Неорганические вещества
Продолжение табД
Формула
Тт2О3
Tm2(SO4K
•8Н2О
и
ив2
ив4
ив12
UBr3
UBr4
UBr5
UC
ис2_,
и2с3
UC13
UC14
UC15
UC16
UF3
UF4
• 2,5Н2О
a-UF5
p-UF5
UF6
[UF5],NH4
UH3_X
UI3
UI4
UN
U3N2
uo2+JC
(-0,03 <x< 0,2)
uo3
Mr
385,87
626,05
770,17
238,029
259,65
281,27
367,76
477,74
557,65
637,55
250,04
262,05
512,09
344,39
379,84
415,29
450,75
295,02
314,02
359,06
333,02
333,02
352,02
351,06
241,05
618,74
745,65
252,04
742,10
270,03
286,03
Фазовые переходы
п. 2370, к. - 4300
> 850 -* Тт2О3
-Н2О 550
п. 1135, к. 4131
п.2385
п. 2495
п. 2145
п. 730
п. 519, к. 765
разл. 80
п. 2400
п. 2500, к. 4370
разл. > 1800
п. 835, к. 1780
п. 590, к. 792
п. 3270?), разл. 50-175
п. 177,5 разл.
п. 1495, к. 2300
п. 1036, к. 1730
-Н2О 300-450
п. 2870?), разл. > 150
п. 348, к. 530
п. 640?), возг. 56,4
разл. 270
разл. 400—500
п. 788, к. - 1750
п. 520 разл.
п. 28550?), разл. > 1700
разл. > 800
п. 2850, возг. 1400
разл. 400—677
Окраска
зел.-бел.
зел.
желт.-зел.
бел.
сер.
сер.
сер.
т.-краен.
т.-кор.
черн.-кор.
черн.
св.-сер.
черн.
зел.
зел.
краен. -
кор.
т.-зел.
св.-фиол.
зел.
зел.-гол.
гол.-бел.
гол.-бел.
желт.-бел.
зел.
сер.-черн.
черн.
черн.
сер.
черн.
кор.-черн.
оранж.
Плот-
ность
9,0
18,95
12,82
9,32
5,65
6,55
5,35
13,63
11,79 .
12,88
5,51
4,87
3,81
3,59
8,54
6,72
4,71 •
6,45
5,81
5,06
10,95
6,76
5,6
14,4
11,24
10,964
7,29
182
I. Неорганические вещества
Продолжение табл.
формула
UO2(CH3COOJ
¦2Н2О
(UO2)CO3
• A,5-2,0)Н2О
(UO2)C2O4
•зн2о
(UO2)C12
•ЗН2О
UO2(C1O4J
•6Н2О
U(O)F4
(UO2)F2
[UO2F5],(NH4K
U(OHL
UO2(NO3J
•6H2O
UO2(O2)
•2H2O
UO2(OHJ
H2O
(UO2)S
(UO2)SO4
•зн2о
UP
us
us2
U(SO4J
•4H2O
USi2
Г to.
USiO4
4
388,12
424,15
330,04
—
358,05
412,09
340,93
394,98
468,93
577,02
330,02
308,02
419,13
306,06
394,04
502,13
302,03
338,06
304,04
322,06
302,09
366,09
420,13
269,00
270,10
302,16
430,15
502,21
294,20
770,26
330,11
842,08
Фазовые переходы
275 - UO3
-H2O110
разл. 500
-H2O 100
разл. 550
-H2O 105
n.578
-H2O 400
разл. > 800
п. 185, -H2O 270
разл. 150
п. 10300?), Разл. > 800
разл. > 185
> 350 - UO2
разл. 350—750
п. 59,5, -Н2О 170-180
Не получен
разл. 260
350 - UO3
-Н2О 100
разл. 40—50
850-^^^H8
-Н2О 175-500
п. 2850
п. 2462
п. 1680 разл.
> 750 — UO2
-Н2О 300
п.1700
п.1600
п.« 1900
1500 (вак.) -> UO2
Окраска
желт.-бел.
желт.-зел.
св.-желт.
желт.-зел.
св.-желт.
желт.
желт.
желт.-зел.
желт.
желт.-зел.
т.-желт.
желт.
желт.-зел.
св.-зел.
желт.
желт.-зел.
св.-желт.
т.-краен.
желт.
черн.-кор.
желт.
желт.-зел.
сер.-черн.
сер.-черн.
сер.-черн.
бел.
св.-зел.
св.-желт.
сер.-кор.
зел.
зел.-черн.
Плот-
Плотность
2,89
5,24
3,07
5,426
2,57
6,4
6,44
2,807
5,926
5,24
10,23
10,87
8,09
3,6
9,0
12,2
>5,1
8,395
183
I. Неорганические вещества
Продолжение табд
Формула
V
VB2
VBr2
VBr3
V(Br)O
VBr2O
VBr3O
@,l<x<0,3)
v2c,_x
@<x<0,2)
[V(C5H5J]
[V(CON]
[V(COLC5H5]
[V(CON],Na
VC12
VC13
VC14
V(C1)O
V(C1)O2
VC13O
VF3
VF4
VF5
[VF6],K
[VF6],(NH4K
cc-VI2
P-vi2
VI3
@<x<0,29)
4
50,942
72,56
210,75
290,65
146,85
226,75
306,65
62,95
113,90
181,13
219,00
228,08
241,99
121,85
157,30
192,75
102,39
118,39
173,30
107,94
126,93
145,93
204,03
219,05
304,75
304,75
431,65
64,95
Фазовые переходы
п. 1910, к. 3407
п. 2745
возг. > 1000
возг. > 280, = 500 — V
разл. 480
возг.« 600
разл. 180
п. 2648, к. = 3900
п. 2165
п. 167,5
60-70 -> V
п. 138, > 150 —V
разл. > 370
п. 1350, возг. 1000
возг. 425 (вак.),
разл. 400—500
п.-20,5, к.+152 разл.
разл. 600
разл. 150
п.-79, к.+126,7
п. 1410, возг. 800
разл. 100—325
п. 19,5, к. 48,3
разл. 330
п. 1400
возг. 800
1400 — V
280 - VI2
п. 2360
Окраска
сер.
сер.
св.-кор.
черн.
фиол.
т.-желт.
краен, ж.
черн.
т.-сер.
фиол.-
черн.
черн.
св.-краен.
желт.
св.-зел.
фиол.
бур. ж.
желт.-кор.
св.-краен.
желт. ж.
зел.
зел.
бел.
бел.
желт.-зел.
т.-фиол.
роз.-
красн.
т.-кор.
желт.
Плот-
Плотность
5,96
5,1
4,58
4,44
4,0
2,93315
5,48
3,09 -
2,87
1,8320
3,44
2,29
1,82920
3,63
2,975
2,177
5,44
5,25
5,2
6,04
—••
184
I. Неорганические вещества
Продолжение табл.
формула
~~~ """"""
2@<*<0,26)
VNH4(SO4J
• 12Н2О
vo1+x
(-0,15 <х< 0,24)
VO2
V2O3
v2o5
(VO)Br2
•5H2O
(VO)C12
(VO2)C1
V(O)F3
V(OHK
VO(OH)
VO(OHJ
(VO)SO4
•3H2O
^11^(^ = 0,17) »
VS2+*
@,17 <jc< 0,53)
V2S3-x
(-0,06 < x < 0,66)
v2s5
vso4
•7H2O
V2(SO4K
•9H2O
Л/о*
VSi2
\/ o»
V3Sl
!f!i
и
115,89
261,11
477,29
66,94
82,94
149,88
181,88
226,75
316,82
137,85
118,39
123,94
101,96
83,95
100,96
163,00
217,05
83,01
115,07
198,08
262,21
147,00
273,11
390,07
552,21
107,11
180,91
338,97
Фазовые переходы
п. - 2000
разл. 250
п. 45, -Н2О 175
п. 1830, к.-3100
п. 1545, к. «2000 разл.
п. 1970, к. = 3000
п. 680, к. 2030 разл.
возг.« 600
разл. 140
450 — V(C1)O
разл. 150
возг. 109,5
80 — VO(OH)
> 300 - V2O3
> 700 — VO2
530 — V2O5
-H2O 260
разл.1400
разл. 520
> 1000 — VS
500 - V2S3
Не получен
400 -> VO2
400 — (VO)SO4
-Н2О 150 (вак.)
п. 1660
п. 1730 разл.
п. 2450
Окраска
черн.
фиол.
св.-фиол.
св.-желт.
син.-черн.
черн.
краен.
т.-кор.
син.
зел.
св.-красн.
св.-желт.
зел.-желт.
черн.
роз.
син.
гол.
т.-кор.
черн.-сер.
черн.
черн.
св.-фиол.
св.-оранж.
т.-желт.
сер.
сер.
сер.
Плот-
Плотность
1,69
5,76
4,34
4,87
3,357
2,88
2,29
2,46
2,21
4,51
2,5
3,7
3,0
4,66
5,74
5,13
185
I. Неорганические вещества
Продолжение табд
Формула
W
WB2
W2B5
WBr2
WBr3
WBr4
WBr5
WBr6
WBr2O
WBr2O2
WBr3O
WBr4O
we
w2c1+x
[W(CON]
WC12
WC13
WC14
WC15
wci6
WC12O
WC12O2
WC13O
WC14O
WF6
WFe2
[WH2(C5H5J]
WI2
WI3
W(I)O2
WI2O2
wo2
Mr
183,840
205,46
421,74
343,65
423,55
503,46
583,34
663,26
359,65
375,65
439,55
519,46
195,85
379,69
351,90
254,75
290,20
325,65
361,11
396,56
270,75
286,74
306,20
341,65
297,83
295,53
316,05
437,65
564,55
342,74
469,65
215,84
Фазовые переходы
п. 3422, к. 5555
п. 2900
п. 2300 разл.
разл. 400
> 180 — WBr2
возг. 240
п. 295, к. 392
п. 309, к. 400 разл.
возг. 450
возг. > 440
возг. > 420
п. 277, к. 327
п. 2720 разл.
п. 2755, к. « 6000
п. 169, к. 175 разл.
разл. > 100
разл. > 200
разл. > 450
п. 244, к. 286
п. 281,5, к. 348
возг. 500
п. 497 разл.
разл. 290
п. 204, к. 224
п. 2,0, к. 17,3
п. 1046
п. 163
> 800 — W
> 600 — WI2
возг. > 410
разл. > 400
п. 1530, к.1730
Окраска
св.-сер.
сер.
сер.
желт.-зел.
т.-зел.
черн.
т.-кор.
т.-син.
т.-сер.
краен.
син.-черн.
т.-кор.
сер.
т.-сер.
бел.
св.-сер.
черн.
черн.
т.-зел.
черн.-фи-
ол.
желт.-кор.
желт.
т.-зел.
т.-краен.
бцв. г.
сер.
желт.
св.-кор.
черн.
син.-черн.
т.-зел.
т.-кор.
Плот-
ность
19,35
12,75
13,0
6,9
6,13
5,87
15,6
17,2
2,65
5,44
4,62
3,87
3,52
5,92
3,95
12,9
6,9
6,39
11,0
-
186
I. Неорганические вещества
Продолжение табл.
формула
wo3
• н2о
2Н2О
W(O)F4
ws2
WSe2
WSi2 + x
Хе
• 5,75H2O
Xe(CF3COOJ
ХеС12
XeF2
XeF4
XeF6
[XeF8],(NO+J
XeO3
XeO4
Xe(O)F2
Xe(O)F4
XeO2F2
Xe(OHL
Y
(VA1)O3
VBr3
V(BrO3K
4
231,84
249,85
267,87
275,83
247,97
341,76
240,01
131,290
234,88
357,32
202,20
169,29
207,28
245,28
343,29
179,29
195,29
185,29
223,28
201,28
199,32
88,906
163,89
153,77
328,62
472,61
634,74
Фазовые переходы
п. 1470, к. 1850
-Н2О 180-350
-1Н2О 70-100
п. 106, к. 185,9
разл.1250
900 (вак.) -> W
п. 2165
п.-111,75, к.-108,04
-Н2О > -3,35
разл. > 20
разл. 80
п. 129,03, 600 - Хе
п. 117,1
п. 49,48, к. 75,65 разл.
разл. 400
возг. 70, > 70 — Хе
п. -35,8, > +20 — ХеО3
> 0 — XeF2
п. -46, > +30 — XeF4
п. 31 разл., >31— XeF2
п. 90, к. 115 разл.
п. 1526, к.3337
п.2150
п. 2300
п. 905, к. 1324
Не получен
п. 74, разл. > 350
Окраска
желт,
желт,
желт,
бел.
сер.-гол.
т.-сер.
гол.-сер.
бцв. г.
бцв. ж.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
желт,
бел.
св.-желт,
св.-желт,
бцв. ж.
бел.
бел.
св.-сер.
бел.
син.-фи-
ол.
бел.
бел.
Плот-
Плотность
7,3
5,5
4,0
5,07
7,5
9,25
5,887
2,9909
2,7
4,32
4,0
3,41
ЗД125
4,469
5,35
187
I. Неорганические вещества
Продолжение табд
Формула
Y2(C2O4K
• 10Н2О
YC13
•6Н2О
(YCrIH)O3
YF3
YH3
Y(NO3K
•5H2O
Y2O3
Y(OHK
YPO4
Y2S3
Y2(S)O2
Y2(SO4K
•8H2O
YSb
YSi
Yb
YbBr2
YbBr3
Yb(CH3COOK
•4H2O
Yb2(C2O4K
•6H2O
YbCl2
YbCl3
•6H2O
YbF2 + ,
YbF3
Ybl2
4
441,87
622,02
195,27
303,36
188,90
145,90
91,93
469,62
274,92
364,99
225,81
139,93
183,88
274,01
241,88
466,00
610,12
210,66
116,99
173,040
332,85
412,75
350,17
422,23
610,13
718,22
243,95
279,40
387,49
211,04
230,03
426,85
Фазовые переходы
He получен
> 700 - Y2O3
п. 721, к. 1482
разл. 150—270
п. 2430
п. 1155, к.2230
разл. 900
п. 997, к. 1310
> 420 — Y2O3
разл. < 280
п. 2430, к. - 4300
> 200 - Y2O3
п. 1950
п. 1925
п. 2120
> 900 - Y2O3
-Н2О 120-400
п. 2310
п. 1840
п. 824, к. 1194
п. 613, к. 1800
п. 943, разл. > 1150
разл. > 220
-Н2О 100
Не получен
> 600 — Yb2O3
п. 702, к. 2033
п. 875, > 1300 — YbCl2
п. 155, -Н2О 180
п. 1407
п. 1162, к. 2200
п. 772
Окраска
бел.
бел.
бел.
т.-зел.
бел.
син.
бел.
бел.
бел.
бел.
желт.-бел.
бел.
желт.
св.-сер.
бел.
бел.
сер.
сер.
бел.
св.-желт.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
сер.
бел.
св.-желт.
Плот,
ность
2,8
2,18
5,76
5,069
2,682
4,85
4,25
3,87
2,52
4,33
6,965
5,91
2,09
2,64
5,08
5,75
2,58
8,168
5,4
188
I. Неорганические вещества
Продолжение табл.
формула
Yb(NO3K
5Н2О
Yb2O3
Yb(OHK
Yb2(SO4K
•8H2O
Zn
(ZnAl2)O4
Zn3As2
Zn3(As04J
•4H2O
ZnBr2
•2H2O
Zn(BrO3J
•6H2O
Zn(CH3COOJ
•2H2O
Zn(CNJ
ZnCO3
ZnCl2
[ZnCl4],(NH4J
Zn(C103J
'4H2O
Zn(C104J
'6H2O
ZnF2
•4H2O
Zn(HCOOJ
•2H2O
Znl2
n3N2
Mr
359,05
449,13
394,08
224,06
634,27
778,39
65,390
183,35
346,01
474,01
546,07
225,20
261,23
321,19
429,28
183,48
219,51
117,43
125,40
136,30
243,28
232,29
304,35
264,29
372,38
103,39
175,45
155,42
191,45
319,20
224,18
170,36
Фазовые переходы
He получен
> 600 — Yb2O3
п. 2430, к. « 4300
800-900 — Yb2O3
900 — Yb2O3
-H2O 600
n. 419,53, к. 907
разл. 1950
п. 1015
разл. > 800
-H2O 350
п. 402, к. 670
п. 37,-Н2О150
разл.« 700
п. 100, -Н2О 200
п. 242, разл. > 270
разл. > 100
разл. 800
297 — ZnO
п. 283, к. 732
п. 150
Не получен
п. 53,9, разл. 60—240
п. 262, разл. 337
п. 100, -Н2О > 100
п. 890, к. 1505
-Н2О > 100 (вак.)
разл. > 213
-Н2О 120
п. 446, к. 727 разл.
разл. 700
п. 210,8, разл. 270
Окраска
бел.
бел.
бел.
бел.
бел.
гол.-бел.
зел.
сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
сер.
бел.
Плот-
Плотность
2,68
10,0
3,793
3,29
7,14
4,58
5,578
3,79
4,2
2,57
1,84
1,73
1,85
4,4
2,907
1,88
2,15
2,25
4,94
2,54
4,736
6,22
2,1
189
I. Неорганические вещества
Продолжение табД
Формула
Zn(NO3J
•6Н2О
ZnO
Zn(OHJ
[Zn(OHL],Na2
Zn3P2
Zn2P2O7
Zn3(PO4J
•4H2O
a-ZnS
P-ZnS
ZnSO4
•7H2O
ZnSb
Zn3Sb2
ZnSe
ZnSiO3
Zn2Si04
H2O
ZnTe
ZnWO4
Zr
ZrB2
ZrB12
ZrBr4
ZrC
[Zr(C5H5JCl2]
ZrCl2
ZrCl3
ZrCl4
[ZrCl6],K2
4
189,40
297,49
81,39
99,40
179,40
258,12
304,72
386,11
458,17
97,46
97,46
161,45
287,56
187,15
439,68
144,35
141,47
222,86
240,88
192,99
313,23
91,224
112,85
220,96
410,84
103,24
292,32
162,13
197,58
233,04
382,14
Фазовые переходы
500 — ZnO
п. 36,4, -Н2О110(вак.)
п. 1975(/>), возг. 1800
100-250 — ZnO
> 100 — ZnO
п.1883
п. 1020
п. 1060
-Н2О210
возг. 1178
п. 1820(/>), возг. 1185
> 930 — ZnO
п. 100, -Н2О 238
п. 546
п. 566
п. 1520
п. 1437
п.1512
-Н2О - 350
п. 1238,5
п. 1200
п. 1855, к. 4409
п. 3225
п. 4500?), возг. 355
п. 3530, к. «5100
п. 243,5
п. 722 разл.
возг. 770
п. 4370?), возг. 333,6
п. 798
Окраска
бел.
бел.
бел.
бел.
бел.
т.-сер.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
сер.
т.-сер.
желт.
бел.
бел.
бел.
краен.
бел.
сер.
сер.
бел.
сер.
бел.
черн.
гол.-сер.
бел.
бел.
Плот,
ность
2,065
5,7
3,03
4,54
4,0
3,104
4,09
4,08
3,74
1,96
6,36
6,33
5,42
3,42
4,103
5,64
7,79
6,49
6,09
3,98
6,66
3,16
3,05
2,8
.
190
I. Неорганические вещества
Окончание табл.
формула
ZrCl2O
8Н2О
ZrF2
ZrF3
ZrF4
[ZrF6],K2
[ZrF7],K3
[ZrF7],(NH4K
ZrH2
Zr(HAsO4J
•H2O
Zrl4
ZrN
Zr3N4
Zr(NCSL
ZrO2
«H2O
гю(онJ
ZrP2O7
(ZrPbn)O3
ZrS2
Zr(SO4J
•4H2O
ZrSi
ZrSi2
Zr2Si
ZrSiO4
Mr
178,13
322,25
129,22
148,22
167,22
283,41
341,50
278,33
93,24
279,85
297,87
598,84
105,23
329,70
323,56
123,22
141,24
265,17
346,42
155,36
283,35
355,41
119,31
147,40
210,53
183,31
Фазовые переходы
разл. > 250
-H2O 115-150,
> 300 - ZrO2
п. 902
разл. > 300
п. 910(/0, возг. 600
п. 600 разл.
п. 920
разл. 365
разл. 850 (вак.)
разл. 280
-Н2О110
п. 500(/>), возг. 418
п. 2955
1000 — ZrN
разм. 40—50, разл. > 60
п. 2710, к. -4500
-Н2О 140
> 300 — ZrO2
п.1550
п. 1570
п.1550
700 — ZrO2
-Н2О 190-340
п. 2150
п. 1700 разл.
п. 1630
п. 1540, разл. 1680
Окраска
бел.
бел.
т.-сер.
гол.-сер.
бел.
бел.
бел.
бел.
сер.-черн.
бел.
бел.
св.-оранж.
желт.
кор.
бел.
бел.
желт.
бел.
бел.
бел.
бур.
бел.
бел.
сер.
сер.
сер.
бел.
Плот-
Плотность
1,91
4,26
4,61
3,48
3,58
2,21
5,62
3,36
4,85
7,3
5,9
5,85
3,25
3,87
3,22
2,8
5,94
4,88
5,99
4,69
191
I. Неорганические вещества
4. Минералы
Приведены формулы около 2400 минералов, их названия — рус
ские и английские, физические свойства — кристаллографическая сие*
тема, твердость, плотность, окраска и содержание других элементов
(не входящих в формулы), применение, названия минералов, имею-
имеющих тот же состав, но отличающихся содержанием других элементов.
Минералы одного состава, но с разными свойствами, а также
кристаллогидраты приведены в рубрике последовательно после фор.
мулы, отделенные друг от друга буквами (а, б, в, ...)• Внутри рубрики
(или ее частей, отделенных буквами) основное название минерала со-
сокращается до первой прописной буквы (с точкой).
Названия минералов, следующие сразу после их формул и набран-
набранные с прописной буквы, являются основными и рекомендуемыми.
Кроме того, в скобках даны традиционные названия (трад.), затем
приводятся устаревшие названия (уст.) и, иногда, неправильные тер-
термины (неправ.).
Полные названия кристаллографических систем (сингоний):
гекс. — гексагональная тетр. — тетрагональная
куб. — кубическая триг. — тригональная
монокл. — моноклинная трикл. — триклинная
ромб. — ромбическая
Твердость (обозначение «НМ») выражена по шкале Мооса:
1 — Тальк (Mg826) 6 — Ортоклаз (К10а)
2— Гипс(Са193в) Магнетит (Fe75)
Галит (NalO7a) 7 — ос-Кварц (Si5e)
3 — Кальцит (Са61г) 8 — Топаз (А148)
Галенит (РЬ51а) 9 — Корунд (А123а)
4— Флюорит (Са83) 10 — Алмаз (С1б)
5 - Апатит (Са185, 1866, 1886)
Шеелит(Са260)
Плотность (обозначение d) выражена в г/см3.
Окраска передается следующими терминами:
бел. — белый, бело- роз. — розовый
бур. — бурый, буро- св. — светло-
гол. — голубой, голубовато- сер. — серый, серовато-
желт. — желтый, желтовато- син. — синий, сине-
зел. — зеленый, зеленовато- т. — темно-
кор. — коричневый, коричнево- фиол. — фиолетовый,
краен. — красный, красно- фиолетово-
оранж. — оранжевый, оранжево- черн. — черный, черно-
192
I. Неорганические вещества
Содержание других элементов, не входящих в формулы, обозначе-
«сод. Аи, Hg, Sb». Сокращение «Ln» используется для указания на
лантаноиды (элементы 57-71).
Применение минералов обозначено так:
ГЦ — драгоценные, полудрагоценные или поделочные камни
г 91 — строительные материалы
|з] — минеральные удобрения
4] — абразивные, огнеупорные и химически стойкие материалы
[51 — минеральные пигменты (краски)
[6] — химическая технология и металлургия
В конце раздела даны указатели русских и латинских названий,
рудных минералов, а также драгоценных, полудрагоценных и поде-
поделочных камней.
1
2
3
Proustite, уст. красная серебряная руда/red silver ore, триг., НМ
2,0—2,5, d5,57, ярко-краен. [6]
(AgI16As2II)S11 — а) Арсенополибазит/Arsenopolybasite, монокл.,
сод. Си, Sb. б) Пирсит/Pearceite, монокл.
5 (AgIBiIII)S2 — Матильдит/Matildite, гекс.
6
10
И
12
13
7-2004
Ag — Серебро/Silver, куб., НМ 2,0—2,7, d 10,5, сер.-бел., сод. Аи,
Hg, Sb, Bi, Си
(AgIAsIII)S2— a) Смитит/Smithite, монокл. б) Трехманит/Trech-
mannite, триг, сер.-черн.
(Ag JAsm)S3 — a) Ксантоконит/Xanthoconite, монокл. б) Прустит/
(AgIBi"I)S5— Павонит/Pavonite, монокл., сод. Си, РЬ
7 (AgIBiIII)Se2 — Бохдановичит/Bohdanowiczite, гекс.
(Ag1BiIII)Te2 — Волынскит/Volynskite, ромб.
AgrBr — Бромаргирит/Bromargyrite, уст. бром(ир)ит/Ь**от(уг)ие,
куб., НМ 1,5—2,5, ^ 6,4, св.-желт. [6]. Иодобромит/Iodobromite —
Б., сод. I
Ag*(Br)Cl - Эмболит/Embolite, куб., НМ 2,0-2,5, rf 5,7, зел.-
желт., сод. I [6]
Ag!Cl -— Хлораргирит/Chlorargyrite, уст. кераргирит/cerargyrite,
роговое серебро/Иргп silver, куб., НМ 2—3, d5,5—5,6, сер.-бел. [6]
(Ag!Cu *)As — Кутинаит/Kutinaite, куб.
(Ag * Си * Hgn)S8 — Балканит/Balkanite, ромб.
193
I. Неорганические вещества
Продолжение табд
)^— Мирсит (mpad. MaEepcMT)/Miersite, куб.
^Pt^Bi^SjQ— Купропавонит/Cupropavonite, монокл.
(Ag^Cu^4Pb^6)Cl62(OHL7 • Н2О — Болеит/Boleite, куб.
(Ag^u^S — Штромейерит/Stromeyerite, уст. серебряно-медный
блеск/silver copper glance, ромб.
(Ag^CuI)S2 — Ялпаит/Jalpaite, тетр.
(Ag'Cu^Se — Эвкайрит/Eucairite, ромб., </7,5, т.-сер.
(AggGeIV)S6 — Аргиродит/Argyrodite, ромб., J6,24, т.-сер.
Ag2Hg3 — Мошелландсбергит/Moschellandsbergite, уст. амальга-
амальгама/amalgam, куб., сер.
Ag3 _ JCHg2 _у (х < 0,8, у < 0,2) — Шахнерит/Schachnerite, гекс.
или ромб, (пара-), сер.
(AgIHgIIAsIII)S3 — Лаффиттит/Laffittite, монокл.
AgJI — Иодаргирит/Iodargyrite, уст. иодирит/iodyrite, гекс, НМ
1,0-1,5, d 5,51-5,7, зел.-желт. [6]
(AgIPbIIAsIII)S3 — Маррит/Marrite, монокл.
(Ag2Pb"As4n)S13 — Ленгенбахит/Lengenbachite, монокл.
(AgIPbIIBi^II)S6- Густавит/Gustavite, ромб.
(Ag^b^Bi^^Sjg — Гейровскиит/Heyrovskyite, ромб.
(AgJPb3I_6BiJ>I^7)S18 — Ширмерит/Schirmerite, ромб.
(Ag^Pb^Bil^S^— Викингит/Vikingite, монокл.
(Ag7Pb"BiI1I5I)S32 — Трежерит/Treasurite, монокл.
(Ag^5Pb^Bi^1,1 )S104- Урейит/Ourayite, ромб. :
(AgIPb2I)Q3F2 — Бидоит (трад. 6TOOKCHT)/Bideauxite, куб., сод. ОН'
Ag^Pb^l(CrO4LSiO4(AsO4)Cl2— Беллит/Bellite, гекс, св.-красн.
(AgIPbIISb1II)S3 — Фрайеслебенит/Freieslebenite, монокл.
(Ag1PbIISb3II)S6— а) Андорит/Andorite, уст. сундтит/sundtite, веб-
нерит/webnerite, ромб, б) Рамдорит/Ramdohrite, ромб.
(Ag2Pb^Sb^H)S15— Овайхиит/Owyheeite, ромб.
(Ag2Pb^Sb^n)S18— Физелиит/Fizelyite, ромб.
194
I. Неорганические вещества
Продолжение табл.
(gJSg — Диафорит/Diaphorite, уст. ультрабазит/ultraba-
site, ромб.
Ag\S — а) Акантит/Acanthite, монокл., НМ 2, d7,2—7,3,
сер.-черн. [6]. б) Аргентит/Argentite, уст. серебряный блеск/silver
glance, ромб., НМ 2,0—2,5, d7,3, т.-сер., сод. Си, Pb, Fe [6].
в) Маккинстриит/McKinstryite, ромб., черн., сод. Си
Agj _ JSb^ — Аллосеребро (трад. алларгентум)/А11ащепШт, гекс,
св.-сер.
Ag Sb C < х < 6) — Дискразит/Dyscrasite, ромб. (Ag3Sb) или куб.
(Ag6Sb), НМ 3,5-4,0, d 9,63-9,82 (Ag3Sb), 10,05 (Ag6Sb), сереб-
ристо-бел. [6]
(AgISbIII)S2— а) Миаргирит/Miargyrite, монокл., НМ 2,5, ^5,2,
сер.-черн. [6]. б) Арамайоит/Aramayoite, трикл., черн., сод. Bi [6]
(Ag3Sbm)S3 — a) Пиростильпнит/Pyrostilpnite, монокл. б) Пирар-
гирит/Pyrargyrite, уст. рубиновое серебро/ruby silver, темно-крас-
темно-красная серебряная руда/dark red silver ore, серебряная обманка/silver
blende, трип, НМ 2,0—2,5, d5,85, т.-красн. [6]
(Ag!jSbm)S4— Штефанит {трад. стефанит)/81ерг1апке, уст. хруп-
хрупкая серебряная руда/brittle silver ore, ромб., НМ 2,0—2,5, d 6,2—
6,3, кор.-черн. [6]
(Ag^Sbv)S6— Биллингслиит/Billingsleyite, ромб., черн., сод. As
(Ag1,6Sb2II)S11 — а) Антимонпирсит/Antimonpearceite, монокл.,
сод. Си, As. б) Полибазит/Polybasite, монокл., т.-сер., сод. Си [6]
Ag*Se — Науманит/Naumannite, ромб., НМ 2,5, d8,2, черн.
Ag^(Se)S — Агиларит (трад. aгвилapит)/Aguilarite, ромб.
(Ag^SnIV)S6— Канфилдит/Canfieldite, ромб.
AgTe — Эмприссит/Empressite, ромб., НМ 3,0—3,5, </7,51,
сер.-черн.
Ag^Te — Гессит/Hessite, уст. теллуристое серебро/tellurium silver,
монокл., НМ 2-3, </8,24—8,45, т.-сер., сод. Аи [6]
(AgITlIPbIIAs*II)S5 — Хатчит (трад. raT4HT)/Hatchite, трикл.
Al8(AlSi3O16)O3(OH) — Маллит (трад. муллит)/Ми1Ше, ромб., НМ
6-7, d 3,15-3,26, бел., сод. Fe, Ti [4]
AlAsO4 • 2Н2О — Мансфилдит/Mansfieldite, ромб., сер.
195
. Неорганические вещества
Продолжение табл
Al3AsO4(OHN • 5Н20 — Лискирдит/Liskeardite, ромб., сод. Fe
А16(ВО3M(ОНK — Еремеевит/Eremeyevite, гекс.
Al7BO3(SiO4KO3 — Дюмортьеит/Dumortierite, ромб., НМ 7,
d 3,26—3,36, зел.-син., сод. Fe, Ti [4]
Al3BiUI(PO4J(OHN- Уэйлендит/Waylandite, трип, сод. Са, ^
А15СО3(ОНI3 • 5Н2О — Скарброит/Scarbroite, трикл., бел.
А114(СО3K(ОНK6 • яН2О — Гидроскарброит/Hydroscarbroite,
трикл., бел.
А1С13 • 6Н2О — Хлоралюминит/Chloraluminite, триг., г/2,4, бел.
А1С1@НJ • 4Н2О — Кадваладерит/Cadwaladerite, аморфн., бел.
[AlF6]2,Ba2Mg — Усовит/Usovite, монокл.
[AlF4]2,Ca — Прозопит/Prosopite, монокл., сод. ОН~
[AlF6]F,Ca2— Карлхинцеит/Carlhintzeite, трикл.
[AlF4]F3,Na2Mg — Веберит/Weberite, ромб.
[AlF6],K2Na — Эльпасолит/Elpasolite, куб., бел.
[AlF6],Na3 — Криолит/Cryolite, уст. ледяной камень/ice stone,
гренландский шпат/Greenland spar, монокл., НМ 2,5, d 2,
95-3,0, бел. [4, 6]
[Al3F14],Na5 — Хиолит/Chiolite, тетр., бел.
[AlF6],NaCa • Н2О — а) Пахнолит/Pachnolite, монокл. б) Томсено-
лит/Thomsenolite, монокл.
[AlF6]2,Na3Li3— Криолитионит/Cryolithionite, куб., НМ 2,5—3,0,
d 2,77, бел.
[Al3F16],NaSr3 — Ярлит/Jarlite, монокл., сод. ОН~
[AlF4]OH,Sr • Н2О — Тихоненковит/Tikhonenkovite, монокл.
A1NH4(SO4J • 12Н2О — Чермигит/Tschermigite, куб., d 1,64, бел.
А12О3— а) Корунд/Corundum, триг., НМ 9, d3,98—4,01, сер.-кор.
Восточный аметист/Oriental amethyst — фиол. К. [1]. Восточный
гиацинт/Oriental hyacinth — краен.-кор. К. [1]. Восточный изумруд/
Oriental emerald — зел. К. [1]. Восточный топаз/Oriental topaz —
желт.-оранж. К. [1]. Наждак/Emery — смесь К. F0—70%) с магне-
магнетитом, гематитом и шпинелью, d 3,75—4,31, бур.-черн. [4].
Рубин/Ruby, уст. красный яхонт/red gem — краен. К., сод. Сг [!]•
196
. Неорганические вещества
Продолжение табл.
Сапфир/Sapphire, уст. синий яхонт/Ыпеgem — Син. К., еод. Fe,
Ti [1]. б) • 0,25Н2О, Акдалаит/Akdalaite, гекс. в) • 2Н2О, Боксит/
Bauxite (горная порода) — смесь байерита, гиббсита, диаспора
и бёмита, аморфн., НМ 1—3, г/2,0—2,5, сер.-бел. [4, 6].
г) • @,7—2,0)SiO2 • иН2О, Аллофан/Allophan, аморфн., НМ 1—3,
d\,9, бел.-гол.
А1(ОНK — а) Байерит/Bayerite, монокл. (а), </2,53, бел. [6]. б)
Гиббсит/Gibbsite, уст. гидраргиллит/hydrargillite, монокл. (у),
НМ 2,5-3,5, d2,35-2,42, бел. [3, 4, 6]. в) Нордстрандит/Nord-
strandite, трикл. ф), НМ 3, d2,44, бел.
[Al(OH)F5]2,Ca3 • Н2О — Ярославит/Yaroslavite, ромб.
А1О(ОН) — а) Диаспор/Diaspore, уст. танатарит/tanatarite, ромб,
(а), НМ 6,5-7,3, d 3,2-3,5, бел., сод. Fe, Mn, Сг [4, 6]. б) Бёмит/
Bohmite (boehmite), ромб, (у), НМ 3,5-4,0, d3,01— 3,06, бел. [6]
А1РО4— а) Берлинит/Berlinite, триг., d 2,56, бел. б) • 2Н2О, Мета-
варисцит/Metavariscite, монокл., гол.-бел. в) • 2Н2О, Варисцит/
Variscite, уст. льюсинит/lucinite, пеганит/peganite, юталит/utahl-
ite, ромб., НМ 4,5, J2,6, гол.-зел., сод. Сг [1]
А12РО4(ОНK — а) Аугелит/Augelite, монокл. б) • Н2О, Сенегалит/
Senegalite, ромб, в) • D—5)Н2О, Боливарит/Bolivarite, аморфн.
А13(РО4J(ОНK — а) • 5Н2О, Уэйвеллит (трад. вавеллит)/\Уауе1Ше,
ромб., НМ 3,5—4,0, d2,3, бел. б) • 9Н2О, Кингит/Kingite, трикл.,
сод. F"
А14(РО4K(ОНK — Троллеит/Trolleite, монокл.
A12PO4(OH)F2 • 7Н2О — Флюэллит/Fluellite, уст. кройцбергит/
kreuzbergite, ромб., НМ 3, d2,16, бел.
A12PO4(SO4)OH • 9Н2О — Санхуанит/Sanjuanite, монокл. (?)
Al3Pb"(AsO4)SO4(OHN— Идальгоит/Hidalgoite, триг., сер.-черн.
А14РЬ^(СО3L(ОН)8 • ЗН2О — Дундасит/Dundasite, ромб.
А13РЬИ(НРО4)РО4(ОНN— Плюмбогуммит/Plumbogummite, триг.
Al3Pbn(PO4)SO4(OHN — Хинсдалит {трад. гинсдалит)/Нп^аШе,
триг., т.-сер., сод. Sr
Al3Pb2ISiO4(Si2O7)O(OH) — Ханкокит/Hancockite, монокл.
A12(SO4K — а) • 13,5Н2О, Метаалуноген/Meta-alunogen, монокл. б)
' 18Н2О, Алуноген/Alunogen, трикл., НМ 1,5—2,0, d 1,65, бел.
197
I. Неорганические вещества
Продолжение та$Л
A1(SO4)OH • 5Н2О — а) Джёрбанит (трад. джурбанит)ДигЬапке,
монокл. б) Ростит/Rostite, уст. хадемит/khademite, ромб.
A12SO4(OHL — а) • 5Н2О, Метаалюминит/Meta-aluminite, мо-
монокл. б) • 7Н2О, Алюминит/Aluminite, монокл., бел.
Al4SO4(OHI0 • 5Н2О — а) Базалюминит/Basaluminite, гекс. (?),
бел. б) Фельшёбаньит/Felsobanyite, ромб. (?)
(Al5Sb*n)O14(OHJ — Бахианит/Bahianite, монокл., св.-кор.
Al13(SiO4MCl(OHI8— Суниит {трад. зуниит)/2ипуйе, куб.,
НМ 7, d 2,88, зел.-бел., сод. F"
Al2(SiO4)O — а) Андалусит/Andalusite, ромб. Су), HM 6,5—7,5,
d 3,16—3,2, бел. [4]. Виридин/Viridine — зел. А., сод. Мп [1].
Хиастолит/Chiastolite — А. с темным крестообразным узором
[1]. б) Силлиманит/Sillimanite, ромб, (р), НМ 6,5—7,5,
d 3,23—3,27, бел. [4]. Фибролит/Fibrolite — волокнистый С. в)
Кианит/Kyanite (cyanite), уст. дистен/disthene, трикл. (а), НМ 5
(вдоль кристалла) или 7 (поперёк), d 3,55—3,66, гол.-бел. [1,4]
Al(Si2O5)OH — Пирофиллит/Pyrophyllite, монокл., НМ 1—2,
d2,65—2,9, зел.-бел., сод. Mg, Fe [4]
Al2(Si205)@HL- a) Дикит/Dickite, монокл., НМ 2,5-3,5,
d2,6, бел. б) Накрит/Nacrite, монокл., бел. в) Каолинит/Ка-
olinite, уст. китайская {или фарфоровая) глина/China (porce-
(porcelain) clay, трикл., НМ 1,5—2,5, d2,6—2,63, бел. [4, 5]. Глина/
Clay (горная порода) — смесь К. с монтморийонитом, гидро-
гидрослюдой, аллофаном, аллуаитом и кварцем [2]. Каолин/Kaolin —
смесь каолинита с кварцем [4]. г) • 2Н2О, Аллуаит {трад. галлу-
a3HT)/Halloysite, монокл., НМ 1—2, d2,0—2,6, сер.-бел., сод.
Fe, Cr. д) • 2Н2О, Энделлит/Endellite, монокл., бел.
Al3(SiO4JOH — Суринамит/Surinamite, монокл., сод. Mg, Fe
Al2(SiO4)(OH)F - Топаз/Topaz, трикл., НМ 8, d3,4-3,6,
желт, или роз., сод. Fe, Ti, Cr, V [1]
A1VO4 • 3H2O — Штайгерит/Steigerite, монокл.
A13VO4(OHN • 2,5Н2О — Альванит/Alvanite, монокл.
A12(VO4)PO4— а) • Н2О, Шодерит/Schoderite, монокл. б) •
6Н2О, Меташодерит/Metaschoderite, монокл.
A12W2O9 — а) • ЗН2О, AHTyaHHT/Ant(h)oinite, трикл. б) • 6Н2О,
Мпоророит/Mpororoite, монокл., сод. Fe
198
I. Неорганические вещества
Продолжение табл.
As — Мышьяк/Arsenic, триг. (а), НМ 3,5, d 5,6—5,8, т.-сер., сод.
Sb,Fe,Ni,Ag,Au,Bi[6]
As4 — Арсеноламприт/Arsenolamprite, ромб., d 1,97, желт.
As2nO3 — а) Арсенолит/Arsenolite, уст. белый мышьяк/white ar-
arsenic, куб. (C), НМ 1,5, ^3,8, бел. б) Клодеит (трад. клаудетит)/
Claudetite, монокл. (а), НМ 2,5, </4,2, бел.
[As6IIO14(OHL],Mn^I6CO3(As^IIO18J- Армангит/Armangite, триг.
As2nS3 — Аурипигмент/Orpiment, уст. желтый мышьяк/yellow ar-
arsenic, монокл., НМ 1,5—2,0, d 3,4—3,5, св.-желт. [6]
As4S — Дюранусит/Duranusite, ромб.
As4S3 — Диморфит/Dimorphite, ромб.
As4S4 — Реальгар/Realgar, уст. рубиновая сера/ruby sulphur, мо-
монокл. (а), (Р), НМ 1,5—2,0, d 3,56, оранж.-красн. [6]
Аи — Золото/Gold, куб., НМ 2,5, d 19,3, желт., сод. Pd, Rh, Си, Bi [6]
AuAgx (x = 0,43—0,82) — Электрум/Electrum, уст. серебристое зо-
золото/silvery gold, куб., НМ 2—3, d 12,5—15,6, св.-желт.
(Аи^^)82 — Эйтенбогардтит {трад. ютенбогордит)/11у1еп-
bogaardtite, тетр.
(AuTAg^)Se2 — Фишессерит/Fischesserite, куб.
Au'Ag^Te^ — Сильванит/Sylvanite, монокл., НМ 1,5, я?8,1, т.-сер.
[6]
(Аи^)Те2— Пецит {трад. neTUHT)/Petzite, куб., НМ 2,5—3,0,
d 8,7—9,0, кор.-черн. [6]
Au2Bi — Малдонит/Maldonite, уст. висмутовое золото/bismuth
gold, куб.
AuICuI(Te4) — Костовит/Kostovite, монокл.
Au4CuTe — Бессмертновит/Bessmertnovite, ромб., сод. РЬ
AuPb5SbTe3S5_8 — Надьягит {трад. HaraaraT)/Nagyagite, уст. чер-
черный теллур/black tellurium, ромб. (?), НМ 1,0—1,5, </6,85-7,46,
т.-сер., сод. Ag, Fe, Se [6]
AuSb2 — Ауростибит/Aurostibite, куб.
AuTe2— a) Калаверит/Calaverite, монокл., НМ 2,5, d 9,35, желт.,
сод. Ag [6]. б) Креннерит/Krennerite, ромб., НМ 2—3, d8,6, бел.-
желт., сод. Ag [6]
199
I. Неорганические вещества
Продолжение табЛ
Аи'пТе3 — Монтбрейит/Montbrayite, трикл.
[BF4],K — Авогадрит/Avogadrite, ромб., d2,5, бел., сод. Cs
[BF4],Na — Ферруччит/Ferruccite, ромб., d2,4, бел.
В(ОНK — Сассолин/Sassolite (sassoline), трикл., НМ 1, d 1,48, бел.
[B(OHL]AsO4,Ca2 — Канит/Cahnite, тетр.
[В(ОНL]2,Са — Фроловит/Frolovite, трикл.
[В4(ОНI8],Са3— Ольшанскиит/Olshanskyite, монокл. (?)
[В(ОНL]С1,Сип- Бандилит/Bandylite, тетр., НМ 2,5, d2,81, син.
[В(ОНL]РО4(ОНJ,Мп^ — Симанит/Seamanite, ромб.
[B6O7(OHN]2(AsO4J,Ca4Mg • 12Н2О - TeppyiTmyTerruggite, монокл.
[B2O3(OHL]CO3,Ca2Mg • 8Н2О - Карбоборит/Carboborite, монокл.
[B2O3(OHK]2(CO3J,Ca4Mg — Боркарит/Borcarite, монокл.
[BO2(OH)]CO3,Mg2 • 5Н2О — Канавесит/Canavesite, монокл.
[В2О(ОНN],Са • 2Н2О — Пентагидроборит/Pentahydroborite, трикл.
[В2О2(ОНL],Са • 2Н2О — Нифонтовит/Nifontovite, монокл.
[В3О5(ОН)],Са — Фабианит/Fabianite, монокл.
[В5О8(ОНK],Са2 — Тыретскит/Tyretskite, трикл.
[В6О8(ОНL],Са • ЗН2О — Гауэрит (трад. royepHT)/Gowerite, монокл.
[B3O3(OHM]2,CaMg • 6Н2О — Индерборит/Inderborite, монокл.
[В4О7(ОНN],Са2Мп'! — Роуит (трад. poBenT)/Roweite, ромб.
[В6О8(ОНL]С1(ОНM,Са4— Солонгоит/Solongoite, монокл.
[B3O3(OHM],Mg • 5Н2О — Индерит/Inderite, уст. лессерит/les-
serite, монокл.
[B4O5(OHL],Mg — а) • 0,5Н2О, Галургит/Halurgite, монокл., бел.
б) • 7Н2О, Хунчжаоит/Hungchaoite, трикл.
[BnO15(OH)9],Mg3— Преображенскит/Preobrazhenskite, ромб.
[B5O6(OHL],NH4 — Лардереллит/Larderellite, монокл.
[B4O5(OHL],Na2- а) • ЗН2О см. Na2B4O7 • 5Н2О. б) • 8Н2О см.
Na2B4O7 • 10Н2О
[B4O6(OHJ],Na2 • ЗН2О см. Na2B4O7 • 4Н2О
200
I. Неорганические вещества
Продолжение табл.
[B5O6(OHL],Na • ЗН2О — Сборгит/Sborgite, монокл.
[B5O8(OH)],Na2 • 2Н2О — Назинит/Nasinite, ромб.
[B4O7(OHJ](OHL,Ca2Mg2— Федоровскит/Fedorovskite, ромб.
[B6O8(OHL]2OH,KMg2 • 5Н2О — Калиборит/Kaliborite, уст. па-
терноит/paternoite, хайнцит/heintzite, хинцеит/hintzeite, монокл.,
НМ 4-5, d 2,12, бел.
[B2O4(OH)]OH,Mg2— Сайбейит (трад. ссайбелиит)/82а^е1уПе,
уст. ашарит/ascharite, ромб., НМ 3, t/2,65, бел.
[В2О4(ОН)]ОН,Мп21 — Суссексит/Sussexite, монокл.
[B5O6(OHL](OHJ,NaCa • 5Н2О - Улексит/Ulexite, уст. боронат-
рокальцит/boronatrocalcite, трикл., НМ 2,5, d 1,96, бел.
[B2O3(OHL]SO4,Mg3 • ЗН2О — Сульфоборит/Sulfoborite, ромб.
[B6O8(OHL],Sr — Стронциоборит/Strontioborite, монокл.
[B6O9(OHJ],Sr • ЗН2О — Таннелит/Tunnelite, монокл.
[BnO16(OHM],Sr2 • Н2О — Витчит/Veatchite, трикл. или монокл.
ВаА12(СО3J(ОНL— а) • 1,5Н2О, Дрессерит/Dresserite, ромб,
б) • ЗН2О, Гидродрессерит/Hydrodresserite, трикл., бел.
ВаА12(РО4J(ОНJ — Яговерит/Jagowerite, трикл.
ВаА13(РО4J(ОНM • Н2О — Горсейксит/Gorceixite, триг.
Ba(AlSiO4J— Цельсиан/Celsian, монокл., НМ 6,0—6,5, d 3,1—3,4,
желт.-бел.
Ba(Al2Si3O10) — а) • ЗН2О, Уэллсит/Wellsite, монокл., сод. Са, К.
б) • 4Н2О, Эдингтонит/Edingtonite, ромб., НМ 4,0—4,5,
d 2,7-2,8, бел.
Ba(AlSi3O8J • 6Н2О — Гармотом/Harmotome, монокл., НМ 4,5,
</2,41-2,47, бел.
Ba2Al5(Si5019HH • ЗН2О — Кимрит/Cymrite, ромб.
Ba5(AsO4KCl — Морлендит/Morelandite, гекс, НМ 3,5—4,0,
^ 5,33, желт.
ВаВе(РО4)ОН — Бабеффит/Babefphite, тетр., сод. F"
BaBe2(Si207) - Барилит/Barylite, ромб., НМ 7, </4,03, бел.
ВаСО3— Витерит/Witherite, ромб., НМ 3,0-3,5, </4,3, желт.-бел.,
сод. Sr, Са [6]
201
I. Неорганические вещества
Продолжение табл.
12
13
14
15
16
17
18
19
20
21
22
23
24
25
26
•27
28
29
30
31
32
33
34
BaCa2Al2(Al4Si9O30) • 2Н2О — Арменит/Armenite, ромб.
ВаСа(СО3J — а) Эвальдит/Ewaldite, гекс, сод. Се, Y, Na.
б) Баритокальцит/Barytocalcite, монокл., НМ 4, d3,64—3,66, сер.
в) Олстонит {трад. anbCTOHHT)/Alstonite, устя. бромлит/bromlite,
трикл. гш/триг., бел.
^ — Бенстонит/Benstonite, триг, НМ 3—4, d3,6—3,65,
желт.-красн., сод. Mg, Mn, Sr
Ba2CaFe2I(Si6017) — Пеллиит/Pellyite, ромб.
BaCa2(Si309) — Вальстрёмит/ХУаМгцтйе, трикл.
BaCa4(Si307M • 11Н2О — Макдоналдит/MacDonaldite, ромб.
Ba10Ca2TiIVMnII(SiO3I0(OHI0- Мюрит/Muirite, тетр., сод. С1~, F~
BaCeIH(CO3JF — Хуанхэит/Hwanghoite, гекс.
BaCe*H(CO3KF2 — Кордилит/Cordylite, гекс, </4,31, св.-желт.
BaCu^(VO4J(OHJ — Везиньиит/Vesignieite, монокл.
BaF2 — Фрэнкдиксонит/Frankdicksonite, куб., ^/4,89, бел.
BaFe2nAl2(PO4K(OHK- Куланит/Kulanite, трикл., сод. Mn, Mg, Ca
BaFen(Si205J — Джиллеспит/Gillespite, тетр.
— Андремейерит/Andremeyerite, монокл.
BaFe3I(Si205J@HL — Анандит/Anandite, монокл., сод. К, Mg, Al, Fe
Ba4Fe2I(V4O15)(OHJ— Гамагарит/Gamagarite, монокл., сод. Mn
BaMg2Al2(PO4J(OHN — Пеникисит/Penikisite, трикл.
BaMg3(AlSiO5J(OHJ — Киношиталит/Kinoshitalite, монокл.,
сод. К, Мп
BaMg(CO3J — Норсетит/Norsethite, триг.
ВаМп21А12(РО4K(ОНK— Бьяребюит/Bjarebyite, монокл., сод. Sr,
Fe,Mg
BaMn^Fe2n(PO4K(OHK— Перлоффит/Perloffite, монокл.
BaMn2IFeIII(Si2O7)O(OH) — Эрикссонит/Ericssonite, монокл. или
ромб.
(BaMnHMn4v)O10 • 2Н2О — Псиломелан/Psilomelane, уст. вад/
wad, болотная {или твердая) марганцевая руда/bog (hard) manga-
manganese ore, черная охра/black ocher, землистый марганец/earthy
manganese, НМ 5—6, d 3J-4J, сер.-черн. [6]. Черный землистый
кобальт/black earthy cobalt — П., сод. Со (до 40%)
202
I. Неорганические вещества
Продолжение табл.
(BaMnnMn?v)O14— Холлендит (трад. голландит)/Но11апсШ;е, мо-
нокл., НМ 4—6, d4,7—4,95, сер.-черн., сод. К, Fe
Ba(MnnMrigV)O16(OHL— Романешит/Romanechite, монокл.
(BaNO3J — Нитробарит/Nitrobarite, уст. баритовая селитра/bary-
селитра/baryta saltpeter, куб., d3,24, бел.
(BaNbv)O3(OH) — Бариопирохлор/Bariopyrochlore, уст. пандаит/
pandaite, куб., т.-желт., сод. Sr, Ti, F~
BaSO4— Барит/Barytes (barite), уст. баритовый {или тяжелый,
персидский) шпат/baryta (heavy, Persian) spar, болонский камень/
Bolognian stone, ромб., НМ 3,0—3,5, d4,3—4,5, гол.-бел., сод. РЬ
[6]. Баритоцелестин/Barytocelestine — барит, сод. Sr, Ca [6]
BaSi2O5 — а) Санборнит/Sanbornite, ромб, б) • ЗН2О, Краускоп-
фит/Krauskopfite, монокл.
BaSnIV(Si309) — Пабстит/Pabstite, гекс, сод. Ti
(Ва2Та^)О6(ОНJ — Бариомикролит/Bariomicrolite, уст. рейкебу-
рит/rijkeboerite, куб., т.-желт., сод. Nb, F"
Ba4TiIVAl3(PO4LO6 — Кьюртонит/Curetonite, монокл., сод. ОН~
Оз— Бафертисит/Bafertisite, монокл., сод. Мп, ОН"
Ba9Ti^vFe2I(Si6O18J(OHN • 6Н2О — Траскит/Traskite, гекс, сод.
С1-, F"
BaTiIV(Si309) — Бенитоит/Benitoite, гекс, НМ 6,0—6,5, </3,6, бел.
илит.-син. [1]
Ba2TiIV(Si04J — Фресноит/Fresnoite, тетр.
Ba(U6O19) • 11Н2О — Бийеит (трад. бильетит)/ВПИеШе, ромб.
Ba(UO2+J(AsO4J— а) • 8Н2О, Метагенрихит/Metaheinrichite,
тетр. б) • A0—12)Н2О, Генрихит/Heinrichite, тетр.
Ba(UO^+J(PO4J— а) • 8Н2О, Метаураноцирцит/Meta-uranocir-
cite, ромб, б) • 12Н2О, Ураноцирцит/Uranocircite, тетр.
Ba(UOfL(PO4J(OHL • 8Н2О - Бергенит/Bergenite, ромб.
Ba(UOfK(SeO3J(OHL • ЗН2О - Гийменит/Guilleminite, ромб.
Ba(UO2+J(VO4J • 5Н2О — Франсвиллит/Francevillite, ромб.
BaV4n(AlSi3O10J(OHL— Черныхит/Chernykhite, монокл., сод. Na
203
I. Неорганические вещества
Продолжение
^SljO^^- Каппленит/Cappelenite, гекс, сод. Са, Се,
Na, La
BaZrIV(Si309) — Бацирит/Bazirite, гекс.
(ВеА12)О4— Хризоберилл/Chrysoberyl, ромб., НМ 8,5, ^/3,65—3,8,
ярко-желт. [1]. Александрит/Alexandrite — ярко-зел. (при днев-
дневном свете) и фиол.-красн. (при искусственном свете) X., сод. Сг
[1]. Цимофан/Cymophane, уст. кошачий глаз/cat's eye — перелив-
переливчатый X. [1]
Be3Al2(Si6018) - Берилл/Beryl, гекс, НМ 7,5—8,0, d2,65-2,8,
желт.-бел. [6]. Аквамарин/Aquamarine — гол.-зел. Б. [1].
Гелиодор/Heliodor — желт.-зел. Б. [1]. Гошенит/Goshenite — бцв.
прозрачный Б. [1]. Изумруд, или смарагд/Emerald — зел. Б.,
сод. Сг [1]. Морганит/Morganite, уст. воробьёвит/vorobyevite —
роз.-фиол. Б. [1]
BeAl(SiO4)OH — Эвклаз/Euclase, монокл., НМ 7,5, ?/3,1, гол.-зел. [1]
Be2(AsO4)OH • 4Н2О — Беарсит/Bearsite, монокл.
Ве2(ВО3)ОН — а) Хамбергит/Hambergite, ромб., НМ 7,5, ?/2,36,
желт.-бел., сод. F~. б) • Н2О, Берборит/Berborite, триг, сод. F~
Be2MnnFe*H(PO4L • 6Н2О — Фейхиит/Faheyite, гекс, сод. Mg
ВеМпп(РО4)ОН — Вяйрюненит/Vayrynenite, монокл., сод. F~
ВеО — Бромеллит/Bromellite, гекс, НМ 9, ?/3,02, бел. [4]
Ве(ОНJ— Бехоит/Behoite, ромб., d 1,92, бел.
[Be2O(OH)]2Mnn(Si3O10J,Ca6— Харстигит/Harstigite, ромб.
Ве2(РО4)ОН • 4Н2О — Морайншит/Moraesite, монокл.
Be3Sc2(Si03N— Баццит/Bazzite, гекс
Be2Si04— Фенакит/Phenakite (phenacite), триг., НМ 7,5—8,0,
d2,91—2>fi, роз.-бел. или бцв. прозрачный [1]
Be3SiO4(OHJ • Н2О - Бериллит/Beryllite, ромб. (?)
Be4Si207@HJ — Бертранит (трад. 6epTpa^wr)/Bertrandite, ромб.,
НМ 6-7, ?/2,59-2,6, желт.-бел. [6]
Be2Y2nFen(SiO4JO2— Гадолинит/Gadolinite, уст. иттербит/ytter-
bite, монокл., НМ 6,5—7,0, ?/4,0—4,5, черн., сод. Ln, Sc, Th [6]
Bi — Висмут/Bismuth, триг, НМ 2,0—2,5, ?/9,8, красн.-бел. [6]
BiIHAsO4— Рузвельтит/Rooseveltite, монокл., ?/7,1, бел.
204
I. Неорганические вещества
Продолжение табл.
Bi2HAsO4(OHK — Арсенобисмит/Arsenobismite, куб.
Bign(AsO4KO5(OHM — Ателестит/Atelestite, уст. рагит/rhagite, мо-
нокл.
Bi^nCO3(OHL— Бисмугит/Bismutite, тетр., НМ 4, </6,86, желт.-бел.
BiUI(Cl)O — Бисмоклит/Bismoclite, тетр., dlj, бел.
Bi2n(MoO4)O2 — Кёхлинит/Koechlinite, ромб.
Bi2HO3 — а) Силленит/Sillenite, куб. б) Бисмит/Bismite, уст. вис-
висмутовая охра/bismuth ocher, монокл., d8,6, зел.-желт.
BiIU(O)F — Заварицкит/Zavaritskite, тетр., d 7,5, бел.
BiniO(OH) - Добреит/Daubreeite, тетр., бел., сод. С1"
Bi2nS3 — Висмутин/Bismuthinite, уст. висмутовый блеск/bismuth
glance, ромб., НМ 2—3, d 6,78, т.-сер., сод. Sb, Se [6]
Bi4HS(S2) — Икунолит/Ikunolite, триг., сер., сод. Se
Bi^HSe3— Гванахуатит/Guanajuatite, уст. френцелит/frenzelite, се-
леновисмутин/selenobismuthinite, селеновисмутовый блеск/sele-
nobismuth glance, ромб, или триг., </6,7, т.-сер., сод. S
Bi4nSe(Se2) — Лайтакариит/Laitakariite, уст. селенжозеит/selenjo-
seite, триг, сер., сод. S
Bi4n(Si04K — Эвлитин/Eulytite (eulytin), уст. висмутовая обман-
обманка/bismuth blende, куб.
BiTe — Цумоит/Tsumoite, триг.
Bi^HTe3 — ТеллуровисмутинДеИигоЫзтиШтке, триг, d 7,6, черн.
Bi3Te4— Раклиджит/Rucklidgeite, триг., сод. РЬ
Bi7Te3 — Хедлиит/Hedleyite, триг.
Bi^nTeO6 • 2Н2О - Монтанит/Montanite, монокл. (?)
BiI1I4ITe13S8 — Тетрадимит/Tetradymite, триг.
BiTe2Se — Кавацулит/Kawazulite, триг.
Bi3(Te)Se — Жозеит/Joseite, триг, сод. S
Bi4nTe(Te2) - Верлит/Wehrlite, триг.
Bi2nU2O9 • ЗН2О — Ураносферит/Uranosphaerite, монокл.
BilnVO4 — а) Клинобисванит/Clinobisvanite, монокл. б) Пукерит/
Pucherite, ромб., d6,25, краен.-кор.
205
I. Неорганические вещества
Продолжение табл.
С — а) Графит/Graphite, уст. плюмбаго/plumbago, черный сви-
свинец/black lead, гекс. (а), НМ 1—2, d2,2, черн. [4—6]. б) Алмаз/Di-
Алмаз/Diamond, куб. (р), НМ 10, ?/3,5—3,53, гол.-бел. [1]. Баллас/Bailas -
мелкие округлые лучистые агрегаты А. [1]. Борт/Bort — зернис-
зернистый А., природный и синтетический (НМ 10), сер. [4]. Карбона-
Карбонадо/Carbonado — мелкозернистый А., природный и синтетический
(НМ 9,87), черн. [4]
(С2)п — Чаоит/Chaoite (природный карбин), гекс, d 3,23—3,3, бел.
C(NH2JO — Мочевина/Urea (природный карбамид), тетр., d 1,3,
бел.
CaAl(AlSi2O8) или NaCa(Al3Si5016) — Лaбpaдop/Labrador(ite),
трикл., НМ 6,0—6,5, d2,7—2,86, сер.-черн., сод. Na, К [1]
Ca2Al(AlSi07) — Геленит/Gehlenite, тетр., бел.
CaAl2(Al2Si2O10)(OHJ— Маргарит/Margarite, уст. жемчужная
слюда/pearl mica, монокл., НМ 3,5—4,5, d 3, роз.-зел., сод. Na, Li,
Fe, Be
Ca2Al(AlSi3O10)(OHJ— Пренит/Prehnite, ромб., НМ 6,0—6,5,
d2,9—2,95, зел.-желт., сод. Fe [1]
Са(А1В3О7) — Йохачидолит/Johachidolite, ромб.
Ca3Al2(BSi4015HH — Тинценит/Tinzenite, трикл., НМ 6,5—7,0,
d 3,27—3,35, син.-кор., сод. Mn, Fe
СаА12(СО3J(ОНL • ЗН2О — Алюмогидрокальцит/Alumohydrocal-
cite, трикл., бел. Книповичит/Knipovichite — син.-зел. А., сод. Сх
(Са12А114)О33 — Майенит/Mayenite, куб.
Са2А1(ОНO • ЗН2О — Гидрокалюмит/Hydrocalumite, монокл., бел.
CaAl(OH)F4 • Н2О — Гирксутит/Gearksutite, монокл., зел.-сер.
СаА1РО4(ОНJ • Н2О — Фоггит/Foggite, ромб.
СаА12(РО4J(ОНJ • Н2О — Гатумбаит/Gatumbaite, монокл.
СаА16(РО4L(ОН)8 • D—5)Н2О — Церулеолактит/Ceruleolactite,
трикл., сод. Си
Са3А1(РО4J(ОНK • Н2О — Дейвисонит/Davisonite, гекс.
СаА13(РО3)О2(ОНN — Крандаллит/Crandallite, триг.
206
I. Неорганические вещества
Продолжение табл.
CaAl3(PO4)SO4(OHN— Вудхаусит/Woodhouseite, трип, сер.-гол.
CaAl2Pb^(Si5012J@HN— Виккенбургит/Wickenburgite, гекс.
Ca3Al2(SO4)F10 • 2Н2О — Кридит/Creedite, монокл., бел., сод. ОН"
Ca6Al2(SO4K(OHI2 • B4—26)Н2О — Эттрингит/Ettringite, гекс.
Ca(AlSiO4J — а) Анортит/Anorthite, уст. индианит/indianite,
кристианит/christianite, сундвикит/sundvikite, трикл., НМ 6,0—
6,5, d2,8, сер.-роз., сод. Na, К. б) Байтаунит (трад. битовнит)/Ву-
townite, трикл., НМ 6, d2,7, бел., сод. Na, К. в) • 2Н2О, Партеит/
Partheite, монокл. г) • 4Н2О, Джисмондин (трад. жисмондин)/
Gismondite, монокл., НМ 4,5, d2,2, бел., сод. К, Na
Ca(Al2Si3O10) — а) • ЗН2О, Сколецит/Scolecite, уст. пуналит/
poonahlite, монокл., НМ 5, d2,25—2,29, бел., сод. Na, К.
б) • E—6)Н2О, Каулсит/Cowlesite, ромб., бел.
Ca(AlSi2O6J — а) • 2Н2О, Вайракит/Wairakite, монокл., НМ 5,0—
5,5, d2,26, бел. б) • 3,5Н2О, Леонхардит/Leonhardite, монокл., св.-
желт. в) • 4Н2О, Ломонит (трад. ломонтит)/Ьаитоп1Йе, монокл.,
НМ 3—4, d 2,25—2,35, красн.-бел. г) • 6Н2О, Левин/Ьеууп(к)е,
триг., НМ 4,5, d 2,1, сер.-бел., сод. Na, К. д) • 6,5Н2О, Хабазит
(трад. шабазит)/СпаЬагке, триг., НМ 4,5, */2,05—2,1, желт.-бел.,
сод. Na, К, Sr
Ca(AlSi3O8J — а) • 4Н2О, Югаваралит/Yugawaralite, монокл.,
НМ 4,5, d 2,2, бел. б) • 5Н2О, Гускрикит/Goosecreekite, мо-
монокл., бел. в) • 5Н2О, Эпистильбит/Epistilbite, уст. орицит/
oryzite, монокл., НМ 4, d2,2, желт.-бел., сод. Na
Ca(Al2Si70]8) — а) • 6Н2О, Хьюлендит (трад. гейландит)/Неи-
landite, трикл., НМ 3,5—4,0, d2,1—2,2, сер.-бел., сод. Na, К.
б) • 7Н2О, Стеллерит/Stellerite, ромб., бел.
CaAl2(Si307L • 6Н2О — Светлозарит/Svetlozarite, ромб., сод. К, Na
Ca3Al2(Si04K — rpoccyjrap/Grossular(ite), уст. грандит/grandite,
куб., НМ 6,5—7,0, d3,59, желт.-зел. [1, 4]. Хессонит/Hessonite,
уст. коричный камень/cinnamon stone — бур.-оранж. Г., сод. FeIH
Ca4(AlSiO4NCO3 — Мейонит/Meionite, тетр.
CaAl(SiO4)OH — Вюаньяит/Vuagnatite, ромб., бел.
CaAl2(SiO4)(OHL— Шанталит/Chantalite, тетр.
CaAl2(Si207)@HJ • Н2О — Лосонит (трад. лавсонит)/Ьа\?8Опке,
ромб., НМ 8, d 3,09, св.-гол.
207
I. Неорганические вещества
Продолжение табл.
Ca2(Al2SiO6)(OHJ— Биккулит (трад. бичулит)/ВюсЬиШе, куб.
Ca3Al2(SiO4J(OHL — Гидрогроссуляр/Hydrogrossular, уст. хиб-
шит/hibschite, монокл., d 3,13, ев. -желт.
Ca12Al2Si18O33(OHK6 — Тахаранит/Tacharanite, монокл.
Ca2Al3(SiO4)(Si2O7)O(OH) — а) Алланит/Allanite, уст. ортит/ог-
thite, таутолит/tautolite, монокл., НМ 5,0—6,5, d 3,3—4,2, кор.,
сод. Fe, Се, La, Y, Na, Mn, Be, Mg. 6) Эпидот/Epidote, уст. писта-
цит/pistacite, монокл., НМ 6—7, d 3,35—3,45, зел., сод. Fe, Ln, Mn
[1]. Тавмавит/Tawmawite — Э., сод. Сг. в) Цоизит/Zoisite, ромб.
(НМ 6, d 3,2—3,4, зел.-кор.) или монокл. (НМ 6,0—6,5, </3,25—
3,33, сер.-зел.), сод. Fe. Танзанит/Tanzanite — прозрачный гол. Ц.
[1]. Тулит/Thulite — ярко-роз. Ц., сод. Мп
Ca2Al2Snlv(Si6018)@HJ • 2Н2О — Икерит {трад. экерит)/ЕакегИе,
монокл.
Ca3(As04J — а) • 9Н2О, Махачкиит/Machatschkiite, триг. б) • 10Н2О,
Рауэнталит/Rauenthalite, монокл. или трикл.
Ca5(As04KCl — Хедифан (трад. гедифануНеёурЬапе, уст. пле-
онектит/pleonectite, гекс, т.-сер., сод. РЬ
Ca5(As04KF — Свабит/Svabite, гекс, af 3,71, сер.-желт.
Ca5(AsO4KOH — Йонбаумит/Johnbaumite, гекс, d3,73, сер.
Ca4B4(BO4)(SiO4K(OHK • Н2О - Бейкерит/Bakerite, монокл., НМ
4,5, </2,73-2,93, зел.-бел.
Са(ВО2J— а) Кальциборит/Calciborite, ромб., d2,7, бел.
б) • 2Н2О, Вимсит/Vimsite, монокл., бел. в) • 2Н2О, Уралборит/
Uralborite, монокл., бел. г) • 6Н2О, Гексагидроборит/Hexahy-
droborite, гекс, d 1,8, бел.
Са(В3О5J— а) • ЗН2О, Волковскит/Volkovskite, монокл., бел., сод.
Sr. б) • 4Н2О, Ноблит/Nobleite, монокл.
Са2В6Оп — а) • 5Н2О, Колманит/Colemanite, монокл., НМ 4,0—4,5,
d 2,42, бел. [6]. б) • 7Н2О, Мейерхофферит/Meyerhofferite, трикл.
в) • 13Н2О, Иньонит/Inyonite, монокл., НМ 2, d 1,875, бел. [6]
Са2В14О23 • 8Н2О — Джинорит/Ginorite, монокл.
Са4В10О19— а) • 7Н2О, Прайсит/Priceite, уст. пандермит/pander-
mite, трикл., НМ 3,0—3,5, t/2,42, бел. б) • 20Н2О, Терчит/Terts-
chite, монокл. (?)
208
I. Неорганические вещества
Продолжение табл.
Са2(В4О7)С12 • 2Н2О — Екатеринит/Ekaterinite, гекс, сод. ОН~
Са2(В5О9)С1 • Н20 — Хильгардит/Hilgardite, монокл. или трикл.
Ca(BSiO4J- Данбурит/Danburite, ромб., НМ 7,0-7,5, йЪ, бел. [1, 6]
Ca(BSiO4)OH — Датолит/Datolite, уст. гумбольдтит/humboldtite,
монокл., НМ 5,0-5,5, d 2,8—3,0, зел.-бел. [1, 6]
Ca2(B5SiO9)(OHM — Хаулит (трад. говлит)/Но\у1йе, монокл.,
НМ 3,5, d 2,58, бел.
Ca4Be2Al2(Si9O26)(OHJ— Бавенит/Bavenite, ромб., НМ 5,5—6,0,
d 2,7, бел. [6]
CaBeMnI1FeIII(PO4K • 2Н2О — Рошерит/Roscherite, монокл. или
трикл., НМ 4,5, d 2,93—2,94, т.-кор. и/шт.-зел.
(CaBeMn2I)Si04— Тримерит/Trimerite, монокл.
СаВе2(РО4J — Хёрлбутит/Hurlbutite, ромб.
CaBe(PO4)F — Гердерит/Herderite, монокл., НМ 5,5, d3, желт.-
бел., сод. ОН~
СаВе(РО4)ОН — Гидроксилгердерит/Hydroxylherderite, монокл.,
НМ 5,5, d2,95—3,01, желт.-бел., сод. F"
СаВе3(РО4J(ОНJ • 4Н2О — Уралолит/Uralolite, монокл.
Ca2Be(Si207) — Мелинофан/Melinophane, уст. мелифанит/те-
liphanite, тетр., сод. Na, Al, OH~, F"
Ca3Be2TiIV(SiAs3nO10J — Асбекасит/Asbecasite, триг.
CaBi2n(CO3JO2— Бейерит/Beyerite, тетр.
CaBiIUCO3(O)F — Кеттнерит/Kettnerite, тетр.
СаСО3— а) Фатерит (трад. BaTepirr)/Vaterite, гекс, d2,66.
б) Арагонит/Aragonite, уст. пизолит/pisolite, гороховый камень/
peastone, ромб., НМ 3,5—4,0, d2,95, бел. [1]. Тарновицит (илитар-
HOBCKHT)/Tamowitzite (tarnowskite) — А., сод. РЬ E%). в) Карбо-
цернаит/Carbocemaite, ромб., сод. Се, Na, Sr. г) Кальцит/Calcite,
уст. известковый шпат/calc spar, триг., НМ 2,7—3,2, d2Jl, бел.,
сод. Mg, Fe, Mn [1, 2, 6]. Исландский шпат/Iceland spar — прозрач-
прозрачный К. с высоким двулучепреломлением. Мексиканский (алжир-
(алжирский) оникс/Mexican (Algerian) onyx — полосчато-окрашенный К.,
НМ 3 [1]. Травертин/Travertine, уст. известковая накипь/calcare-
накипь/calcareous sinter (горная порода) — натёчные скопления К. [1]. Извест-
209
I. Неорганические вещества
Продолжение табд.
няк/Limestone, Мрамор/Marble и Мел/Chalk — горные породы,
состоящие, главным образом, из К. д) • Н2О, Моногидрокальцит/
Monohydrocalcite, гекс, d 2,42. е) • Те1^, Мрозит/Mroseite, ромб.
СаС2О4 — а) • Н2О, Хьюэллит (трад. уэвеллит, вевелит)/\УЬе\уе1-
lite, монокл., НМ 2,5—3,0, d2,2, бел. б) • 2Н2О, Уэдделлит/Wedd-
ellite, тетр., бел.
Са10СО3(РО4N • Н2О — Коллофан/Collophanite, аморф., НМ 4,5,
d2,69—2,77, желт.-бел. Монит/Monite — землистый К., d2,l, бур.
Фтороколлофан/Fluorocollophanite — желт. К., сод. F~
Ca3CeniAl2(SO4)F13 • 10Н2О — Церочухровит/Cerochukhrovite,
куб., сод. Y
CaCeIH(CO3JF — Синхисит/Synchisite, гекс, сод. Ln
CaCe2n(CO3KF2— Парисит/Parisite, трип, НМ 4,5, J4,13—4,36,
желт.-кор., сод. Ln [6]
Ca2Ce3n(CO3MF3— Рёнтгенит/Rontgenite, трип, сод. Ln
CaCe*"(SiO4KO2(OH) - Беккелит/Beckelite, гекс, НМ 5, </4,15,
желт.
Ca3Ce^IITiIV(B2Si2011J— Таджикит/Tadzhikite, монокл.
СаС12 • 6Н2О — Антарктикит/Antarcticite, трип, d 1,68, бел.
Ca2CoH(AsO4J • 2Н2О — а) Розелит/Roselite, монокл., сод. Mg. б)
Бета-розелит/Beta-roselite, трикл.
СаСгО4— Хроматит/Chromatite, тетр., d3,1, желт.
Са2Сг04(Ю3J-Дитцеит/Dietzeite, монокл., НМ 3,5-4,0, </4,59,
т.-желт.
Ca3Cr2n(Si04K _ Уваровит/Uvarovite, куб., НМ 6,5-7,5,
d 3,4—3,5, ярко-зел.
CaCunAl(SiO3J(OHK — Папагоит/Papagoite, монокл.
CaCun(AsO4)OH — Конихальцит/Conichalcite, ромб.
CaCu^CO3(AsO4J(OHL • 6Н2О — Тиролит/Tyrolite, уст. медная
пенка/copper froth, ромб.
Ca6Cu2IPb*I(CO3)8(OHN • 6Н2О — Схёлингит/Schuilingite, мо-
монокл.
CaCu4I(SO4J(OHN • ЗН2О — а) Девиллин/Devillite (devilline), мо-
монокл. б) Серпиерит/Serpierite, монокл., сод. Zn
210
I. Неорганические вещества
Продолжение табл.
CaCun(SiO4) • 2Н2О — Стрингемит/Stringhamite, монокл.
CaCun(Si205J — Купрориваит/Cuprorivaite, тетр.
Ca2Cu2I(SiO3)Si2O7 • 2Н2О — Киноит/Kinoite, монокл.
Ca2Cu3I(TeO3LSO4 • Н6Те06— Тлапаллит/Tlapallite, монокл., сод.
Pb,Zn
CaCun(VO4)OH — Калыдиофольбортит/Calcioolborthite, уст. тан-
геит/tangeite, ромб., зел.-желт.
CaF2 — Флюорит/Fluorite, уст. плавиковый шпат/fluorspar, куб.,
НМ 4, ^3,18, бцв. прозрачный или св.-зел. [6]. Иттроцерит {или
иттрофлюорит)/Уигосегке (yttrofluorite) — фиол., зел. или желт.
Ф., сод. Y, Ln, Th, U, НМ 4,0-4,5, d3,45-4,31 [6]
Ca2FenAl2(BSi4015HH — Ферроаксинит/Ferroaxinite, трикл., НМ
6,5—7,0, ^3,3, зел.-син.
(Ca2FeIHAl)O5 — Браунмиллерит/Brownmillerite, ромб.
Ca4FenAl4(PO4N(OHL • 12Н2О — Кингсмаунтит/Kingsmountite,
монокл.
Ca2FenAl2(SiO4)Si2O7(OHJ • Н2О — Ферропумпеллиит/Ferro-
pumpellyite, монокл.
Ca2Fen(AsO4JOH • 5Н2О — Смольяниновит/Smolianinovite,
ромб., сод. Ni, Mg, Al
Ca2Fen(BSi05J — Гомилит/Homilite, монокл., сод. Mg
CaFeH(CO3J — Анкерит/Ankerite, уст. бурый шпат/brown spar,
трип, НМ 3,5—4,0, d2,95,—3,1, красн.-кор., сод. Mg [6]
CaFeIIFeIII(PO4JOH — Мелонжозефит/Melonjosephite, ромб.
CaFe^Fe^PO^gCOH)^ • 4Н2О - Дюфренит/Dufrenite, монокл.
Ca2FenFeI]I(Si5014HH — Бабингтонит/Babingtonite, трикл., сод. Мп
CaFe2IFeIII(Si2O7)O(OH) — Ильваит/Ilvaite, уст. иенит/yenite,
льеврит/lievrite, ромб., НМ 5,5—6,0, d 3,9—4,1, черн., сод. Мп
Ca2FeHFe2n(SiO4)Si2O7(OHJ • Н2О — Джулголдит/Julgoldite, мо-
монокл., сод. А1
Ca2Fe2IFe2II(WO4O • 9Н2О — Ферритунгстит/Ferritungstite, куб.
— Графтонит/Graftonite, монокл., сод. Мп
211
Неорганические вещества
Продолжение табд
Ca2Fen(PO4J • 2Н2О — а) Анапаит/Anapaite, уст. таманит/tamaiv.
ite, трикл. б) Месселит/Messelite, трикл., сод. Мп
Ca2Fein(PO4JOH • 1,5Н2О — Ксантоксенит/Xanthoxenite, монокл,
или трикл.
Ca3Fe4n(PO4L(OHN • ЗН2О — Митридатит/Mitridatite, монокл.
Ca3FeI1I0I(PO4)8(OHI2— Ришеллит/Richellite, аморфн., сод. F~
CaFe4n(SO4N(OHJ • 19Н2О - Кальциокопьяпит/Calciocopiapite,
трикл.
CaFein(SbniAs2I1[07) — Стенхуггарит/Stenhuggarite, тетр.
CaFen(SiO4) — Кирштайнит/Kirschsteinite, ромб., св.-желт.
CaFen(Si03J — а) Хеденбергит/Hedenbergite, монокл., НМ 6,
d 3,50—3,56, кор.-зел., сод. Mn, Fe111. б) Ферробустамит/Ferrobus-
tamite, трикл., сод. Мп
Ca3Fe*n(Si04K — Андрадит/Andradite, куб., НМ 6,0—7,5, d 3,86,
желт.-кор., сод. А1, Мп [4]. Демантоид/Demantoid — ярко-зел. А.
[1]. Меланит/Melanite — кор.-черн. А., сод. Ti. Топазолит/Тора-
zolite — желт. А. [1]. Шорломит/Schorlomite — черн. А., сод. Ti
Ca2Fe^(Si4OnJ(OHJ— Ферроактинолит/Ferroactinolite, мо-
монокл., т.-зел., сод. Mg, F~
Ca3GeIV(SO4J(OHJ • ЗН2О - Шауртеит/Schaurteite, гекс.
CaHAsO4— а) Вайлит/Weilite, трикл., бел. б) • Н2О, Хайдингервд/
Haidingerite, ромб., бел. в) • 2Н2О, Фармоколит/Pharmacolite,
монокл.
Ca5(HAs04J(As04J — а) • 4Н2О, Сенфелдит/Sainfeldite, монокл.
б) • 5Н2О, Владимирит/Vladimirite, монокл., сер.-бел. в) • 9Н2О,
Геренит/Guerinite, монокл., сер.
СаНВО3 — Сибирскит/Siberskite, монокл. (?)
СаНРО4— а) Монетит/Monetite, трикл., af 2,9, бел. б) • 2Н2О, Бра-
шит (трад. 6pyiimT)/Brushite, монокл., d2,31, бел.
Ca2(HPO4)SO4 • 4Н2О — Ардеалит/Ardealite, монокл.
Са(Ю3J— а) Лаутарит/Lautarite, монокл., НМ 3,5—4,0, af4,59,
бел. б) • Н2О, Брюггенит/Bruggenite, монокл.
CaMg2Al(Al3SiO10)(OHJ— Клинтонит/Clintonite, уст. зейбертит/
seybertite, брандисит/brandisite, ксантофиллит/xanthophyllite,
монокл.
212
I. Неорганические вещества
Продолжение табл.
2323n22 — Чермакит/Tschermakite, монокл.,'
НМ 5-6, </3,02-3,44, зел., сод. Fe, F~
CaMg4Al5(BO3KSi6O18(OHL- Увит/Uvite, триг., НМ 7,0-7,5,
d 2,55, бел.
Ca2MgAl2(BSi4015HH — Магнезиоаксинит/Magnesioaxinite,
трикл., НМ 6,5—7,0, d 3,3, сер.-желт.
Ca2Mg14Al4CO3(OHL2 • 29Н2О — Вермландит/Wermlandite, гекс,
сод. Fe
CaMgAl(PO4JOH • 4Н2О — Оверит/Overite, монокл.
Ca4MgAl4(PO4N(OHL • 12Н2О — Монтгомериит/Montgomeryite,
монокл.
Ca2MgAl2(SiO4)Si2O7(OHJ • Н2О — Пумпеллиит/Pumpellyite, мо-
монокл.
Ca10Mg2Al4(SiO4M(Si2O7J(OHL— Везувиан/Vesuvianite, уст.
идокраз/idocrase, тетр., НМ 6,5—7,0, d 3,33—3,43, зел.-кор., сод.
Fe, F~ [1]. Калифорнит/Californite — бел. крапчатый В. [1]. Ксан-
тит/Xanthite — желт. В. [1]. Циприн/Cyprine — син. В. [1]
Ca2Mg(As04J • 2Н2О — Арсенат-беловит/Arsenate-belovite, уст.
талмессит/talmessite, трикл.
CaMg(AsO4)F — Тиласит/Tilasite, монокл.
CaMg4(AsUI03JF4 — Наньлинит/Nanlingite, триг.
CaMg(AsO4)OH — Аделит/Adelite, ромб.
CaMg(B2O5) — Курчатовит/Kurchatovite, ромб., сод. Мп
CaMg(B6On) • 6Н2О — Гидроборацит/Hydroboracite, монокл., НМ
2-3, ?/2,17, сер.-бел.
Ca5Mg(B4O7N • 30Н2О — Уордсмитит/Wardsmithite, гекс.
Ca3Mg(BO3JCO3 • 0,25Н2О — Сахаит/Sakhaite, куб.
CaMg(CO3J — Доломит/Dolomite, уст. горький (или жемчужный)
шпат/bitter (pearl) spar, триг., НМ 3,5—4,0, d2,9—3,2, бел., сод. Fe
[1, 4, 6]. Доломит/Dolomite rock, уст. магнезиальный известняк/
magnesian limestone (горная порода) — разноокрашенная смесь
минерала Д. с кальцитом, сидеритом, родохрозитом, глиной, квар-
кварцем и др. [4]
CaMg3(CO3L— Хантит (трад. гунтит)/НштШ;е, триг, ?/2,7, бел.
213
I. Неорганические вещества
Продолжение табЛ
Ca2Mgn(CO3I3' 10Н2О - Сергеевит/Sergeevite, триг. (?)
Ca3MgCO3(SO4)Cl2(OHJ • 3,5Н2О - TaTapcKmyTatarskite, ромб. (?)
CaMgCegH(Si04O • лН2О — Церит/Cerite, уст. охроит/ochroite,
трип, НМ 5,5, d4,9, св.-красн., сод. Ln, Fe, F~
CaMg2Cl6 • 12H2O — Тахигидрит/Tachyhydrite, трип, НМ 2, d 1,67,
бел.
CaMg2FenAl2(PO4L(OHJ • 8Н2О - Уайтит/Whiteite, монокл., сод
Мп
CaMgFeIH(PO4JOH • 4Н2О - Зегелерит/Segelerite, ромб.
Ca4MgFe4n(PO4N(OHL • 12Н2О — Кальциоферрит/Calcioferrite,
монокл.
Ca2Mg4FeinSbv(Be2Si4O18)O2- Уэлшит/Welshite, трикл.
Ca4Mg(HAs04J(As04J • 11Н2О — Пикрофармаколит/Picrophar-
macolite, триг.
Ca2Mg(PO4J • 2Н2О — Коллинсит/Collinsite, трикл., сод. Fe
CaMg(PO4)F — Изокит/Isokite, монокл.
CaMg3(PO4J(OHJ — Тадёит/Thadeuite, ромб., сод. Fe, Mn, F~
CaMgSiO4 — Монтичеллит/Monticellite, ромб., НМ 5,5, d 3,1—3,3,
сер.-бел.
CaMg(SiO3J — а) Диопсид/Diopside, монокл., НМ 5,5—6,5,
d 3,22—3,38, бел. Виолан/Violan — син.-фиол. Д. [1]. Джефферсо-
нит/Jeffersonite — т.-зел> Д., сод. Mn, Zn [1]. Салит/Salite —
св.-зел. Д. Хромдиопсид/Chromdiopside, уст. лавровит/lavro-
vite — зел. Д., сод. Сг [1]. б) Омфацит/Omphacite, монокл.,
НМ 5—6, d3,16—3,43, зел., сод. Na, Fe, А1. в) Фассаит/Fassaite,
монокл., НМ 6, d2,96—3,6, св.-зел., сод. Fe, A1
Ca2MgSi207 — а) Окерманит (трад. акерманит)/Акегтапйе
(ekjxrmanite), тетр., бел. б) Мелилит/Melilite, тетр., НМ 5—6,
tf 2,95—3,05, т.-желт., сод. Na, К, Fe, A1
Ca3Mg(Si04J — Мервинит/Merwinite, монокл.
Ca7Mg(Si04L — Бредигит/Bredigite, ромб.
Ca2Mg5(Si4OnJ(OHJ— a) Актинолит/Actinolite,уст. штралит/
strahlite, лучистый камень/radiated stone, монокл., НМ 5—6,
d3,02—3,44, св.-зел., сод. Fe, F~. Биссолит/Byssolite — асбесто-
214
I. Неорганические вещества
Продолжение табл.
видный А. [4]. Нефрит/Nephrite, уст. жад/jade — скрытокристал-
лический А. (иногда — тремолит), НМ 6,0—6,5, d 2,9—3,1, бел.-зел.
[1]. б) Тремолит/Tremolite, уст. грамматит/grammatite, монокл.,
НМ 5,5—6,0, d 2,9-3,2, зел.-бел., сод. Al, F"
CaMg2TiIV(Al2SiO10) — Рёнит/ЯЬцпке, трикл., сод. Fe
CaMg(UOS-+)(CO3K * 12Н2О — Сварцит/Swartzite, монокл.
Ca3Mg3(UOf J(СО3N(ОНL • 18Н2О - Раббиттит/Rabbittite,
монокл.
Ca2MnnAl2(BSi4015HH — Манганаксинит/Manganaxinite, трикл.,
НМ 6,5-7,0, d3,3, красн.-фиол. [1]
Ca2Mnn(As04J • 2Н2О — Брандтит/Brandtite, монокл., сод. Mg
СаМпп(СО3J — Кутнагорит/Kutnahorite, трип, ^ 3,0—3,1, св.-
роз., сод. Mg, Fe
Ca3MnIV(CO3)SO4(OHN • 12Н2О - Журавскит/Jouravskite, гекс.
CaMn2IFe^"(PO4L(OHK • ЗН2О - Кеккит/Keckite, монокл.
Ca2MnnFeni(Si50]4HH — Манганбабингтонит/Manganbabingto-
nite, трикл., сод. Fe11
(СаМп2п)О4 — Марокит/Marokite, ромб.
(CaMnJv)O9 • ЗН2О — Рансиит (трад. paHCbeHT)/Rancieite, гекс.
Са2Мпп(РО4J • 2Н2О — Фэрфилдит/Fairfieldite, трикл., сод. Fe
Ca3Mn4II(PO4L(OHN • ЗН2О — Робертсит/Robertsite, монокл.
Ca3MnJV(SO4J(OHN • ЗН2О — Депюжолит/Despujolsite, гекс.
CaMnnSiO4— Глаукохроит/Glaucochroite, ромб., св.-роз.
CaMnn(Si03J — а) Йоханнсенит/Johannsenite, монокл., НМ 6,
d 3,27—3,54, красн.-кор., сод. Fe. б) см. MnnSiO3
CaMn4I(Si03M см. MnnSiO3
CaMnin(SiO3JOH • 2Н2О — Руисит/Ruizite, монокл.
CaMn4l(Si5014)@HJ • Н2О — Сантаклараит/Santaclaraite, трикл.
Ca2Mn2I(Si3O10)(OHJ • 2Н2О — Ориентит/Orientite, ромб.
Ca2Mn^(Si5014J@HJ • 5Н2О — Инесит/Inesite, трикл.
Ca3Mnyi(SiO4J(OHL — Анритермьеит/Henritermierite, тетр.
Ca2Mn^n(Si04)Si207@HK — Макфаллит/МасГаШ1е, монокл., сод. А1
215
I. Неорганические вещества
Продолжение
174
175
176
177
178
179
180
181
182
183
184
185
186
187
188
189
190
191
Ga2Mn*u(SiO4)(Si2O7)O(OH) — Пьемонтит/Piedmontite, mohokji.,
НМ 6,5, d3,45, фиол.-красн., сод. А1, Fe
СаМоО4— Пауэллит (трад. повеллит)/Ро\уе1Ше, тетр., НМ 3,5,
d492—4,5, зел.-бел., сод. W [6]
Ca(NH4J(SO4J • Н2О — Коктаит/Koktaite, монокл.
Ca(NO3J • 4Н2О — Нитрокальцит/Nitrocalcite, уст. известковая
(или норвежская) селитра/lime (Norwegian) saltpeter, монокл.,
<Л,8,бел. [3]
(CaNb2/)O6— Ферсмит/Fersmite, ромб., сод. Се, Na, Та, Ti, OH~, F~
Ca(Nb^Si2O10) • 3,5Н2О — Комаровит/Komarovite, ромб.,
сод. Mn, F"
Ca4Nbv(SiO4JO2(F) — Ниокалит/Niocalite, трикл.
Ca2Nin(PO4J • 2Н2О — Кассидиит/Cassidyite, трикл., сод. Mg
СаО — а) Известь/Lime, уст. негашёная (или жжёная) известь/
quicklime, куб., d3,3, бел. б) • 0,5А12О3 • 0,5SiO2 • 4Н2О, Штретлюь
гит/Stratlingite, триг. в) • 1,17А12О3 • SiO2 • 6Н2О, Пергамит/Рег-
hamite, гекс. г) • l,2SiO2 • Н2О, Тоберморит/Tobermorite, ромб.
Са(ОНJ— Портлендит/Portlandite, триг., d2, бел.
Са3(РО4J — Уитлокит (трад. витлокит)/\\ЪШоскйе, триг, </3,1,
бел., сод. Mg, Fe, HPO^"
Са5(РО4KС1 — Хлорапатит/Chlorapatite, монокл., НМ 4,5, t/3,18,
бел. [3,4, 6]
Ca5(PO4KF — а) Франколит/Francolite, уст. карбонат-фторапа-
тит/carbonate fluorapatite, дернит/dehrnite, гекс, сод. СО3~. б)
Фторапатит/Fluorapatite, уст. льюистонит/lewistonite, апатит/ap-
апатит/apatite, гекс, НМ 4,5-5,0, </3,2, бел. [3, 4, 6]
Са2(РО4)ОН • 2Н2О — Изоклазит/Isoclasite, монокл. (?)
Са5(РО4KОН — а) Даллит/Dahllite, гекс, сод. СО^-. б) Гидрокси*
лапатит/Hydroxylapatite, уст. фёлькерит/уц1скеп1е (voelckerite),
монокл., НМ 5, d39l5, бел. [3, 4, 6]
Ca2Pbn(Si309) — Маргаросанит/Margarosanite, трикл., сод. Мп
Ca4Pb"(Si207KCl2— Насонит/Nasonite, гекс, сер.
Ca4Pb^(Si207K@HJ- Ганомалит/Ganomalite, гекс, НМ 3, d5,l
сер., сод. Мп
216
I. Неорганические вещества
Продолжение табл.
Ca7Pb^(Si3O7J(SO4J(OHI0— Роблингит/Roeblingite, монокл.
CaSO4— a) Ангидрит/Anhydrite, уст. карстенит/karstenite, кубо-
кубовой шпат/cube spar, ромб., НМ 3,0—3,8, d 2,89—2,98, бел., сод. Sr
[2, 3, 6]. б) • 0,5Н2О, Бассанит/Bassanite, триг., d2,7, бел. в) •
2Н2О, Гипс/Gypsum, монокл., НМ 1,5—2,0, </2,32, бел. [2, 6].
Алебастр/Alabaster — зернистый Г. Атласный шпат/Satin spar —
блестящий волокнистый Г. Гипсовый шпат/Gypsum spar — полу-
полупрозрачный Г. Селенит/Selenite — пластинчатый Г.
Ca2Sb207 — а) Льюисит/Lewisite, куб., сод. Fe, Na, Ti. б) Ромеит/
Roirmite, уст. шнебергит/schneebergite, атопит/atopite, куб., сод.
Fe, Mn, Na, Ti, ОН", F"
(CaSbI1I0I)S6(OI0— Сарабауит/Sarabauite, монокл.
CaSb4n(SO4JO4(OHJ • 2Н2О - Перетаит/Peretaite, монокл.
CaSiO3 — Вулластонит (трад. волластонит)/>Уо11а81опйе, уст. до-
дощатый шпат/tabular spar, трикл. или монокл., НМ 4,5—5,5, с/2,8—
3,0, желт.-бел., сод. Fe, Mn [4]
CaSi2O5 — а) • 2Н2О, Некоит/Nekoite, трикл. б) • 2Н2О, Окенит/
Okenite, трикл. в) • ЗН2О, Маунтинит/Mountainite, монокл.
Ca2Si04 — Ларнит/Larnite, монокл. (р), НМ 5,5, </3,20—3,28, сер.
Ca3Si207— а) Ранкинит/Rankinite, монокл., г/2,96, бел. б) Киль-
хоанит/Kilchoanite, ромб., бел. в) • 0,5Н2О, Киллалаит/Killalaite,
монокл., бел. г) • ЗН2О, Афвиллит/Afwillite, монокл. д) • 3,67Н2О,
Дженнит/Jennite, трикл., бел.
Ca3Si309 • Н2О — Розенханит/Rosenhahnite, трикл.
Ca6Si6018 • Н2О — Ксонотлит/Xonotlite, монокл., НМ 6,5, </2,7,
сер.-бел.
Ca5Si2O7(CO3J — Тиллиит/Tilleyite, монокл.
Ca5(SiO4JCO3 — Спёррит (трад. cnyppHT)/Spurrite, монокл.
Ca7(Si6O18)CO3 • 2Н2О — Скотит/Scawtite, монокл.
Ca4(SiO3JCO3(OHJ — Фукалит/Fukalite, ромб., сод. F"
Ca4(Si207)F2 — Куспидин/Cuspidine, уст. кюстерит/custerite, мо-
монокл., сод. ОН"
Ca3(SiO4)O — Хатрурит/Hatrurite, трикл. (?)
Ca2SiO3(OHJ — Хиллебрандит/Hillebrandite, монокл., бел.
217
I. Неорганические вещества
Продолжение тойд
210
211
212
213
214
215
216
216А
217
218
219
220
221
222
223
224
225
226
227
228
229
230
231
232
Ca2Si205@HJ — Суолунит/Suolunite, ромб.
Ca2Si307@HJ • Н2О — Гиролит/Gyrolite, гекс, бел.
Ca2Si409@HJ — Траскоттит (трад. TpycKOTraT)/Truscottite, триг.
Ca4Si207@HJ — Рустумит/Rustumite, ромб.
Ca4Si307@HN — Цеофиллит/Zeophyllite, трикл., сод. F"
Ca4Si309@HJ — Фошагит/Foshagite, монокл.
Ca5Si6016@HJ • 2Н2О — Риверсайдит/Riversideite, ромб.
Ca5SiO4(PO4)SO4(OH) - Вилькеит/Wilkeite, гекс, d 3,234, роз.
Ca10(SiO4K(SO4KF2- Эллестадит/Ellestadite, гекс, НМ 5, </3,1,
бел.-сер., сод. С1~, ОН"
Ca10(SiO4K(SO4K(OHJ — Гидроксилэллестадит/Hydroxylellesta-
dite, монокл., сод. Cl", F~
CaSnIV(BO3J — Норденшёльдин/Nordenskjoldine, триг.
CaSnIV(Si309) • 2H2O — Стоксит/Stokesite, ромб.
CaSnIV(SiO4)O — Малайяит/Malayaite, монокл.
(CaTav)O6— Рюнерсонит/Rynersonite, ромб., сод. Nb
Ca(Te^vTeVIO8) — Карлфрисит/Carlfriesite, монокл.
CaThIV(CO3JF2 • ЗН2О - Торбастнесит/Thorbastnasite, гекс, сод. Ln
CaThIV(PO4J — Брабантит/Brabantite, монокл.
Ca2ThIV(Si205L— Эканит/Ekanite, тетр., сод. U, Fe, Pb
(CaTi4vFe'")O12 • 4Н2О - Кафетит/Cafetite, ромб.
(CaTiIV)O3 — Перовскит/Perovskite, ромб., НМ 5,5, d 3,98—4,26,
св.-кор., сод. Zn, Fe [6]. Дизаналит/Dysanalyte — П., сод. Na, Nb
[6]. Кнопит/Knopite — П., сод. Ln [6]
(СаТЦу)О4(ОНJ — Кассит/Kassite, ромб.
(CaTi*vSbni)O6(OH) - Стибиобетафит/Stibiobetafite, куб.
CaTiIV(SiO4)O — Титанит/Titanite, уст. сфен/sphene, монокл.,
НМ 5,0—5,5, d 3,45—3,55, зел.-бур. (или бел. прозрачный [1]),соД-
Na, Ln, Sr, В, Al, Fe, Mg, Mn, Nb, Та, V, Cr, Sn, OH~, F" [6]
Ca4Ti2v(SiO4JO3F2— Ферсманит/Fersmanite, трикл., сод. Na,
Nb, OH-
218
I. Неорганические вещества
Продолжение табл.
CaU2O7 • 5Н2О — Кальциоураноит/Calciouranoite, аморфн.
Ca(UO2+J(AsO4J — а) • 8Н2О, Метаураноспинит/Meta-uranospin-
ite, тетр. б) • 10Н2О, Ураноспинит/Uranospinite, тетр.
Ca(UO2+L(AsO4J(OHL • 6Н2О — Арсенуранилит/Arsenuranylite,
ромб.
Ca(UO2+)(CO3J — а) • ЗН2О, Метацеллерит/Metazellerite, ромб, б)
• 5Н2О, Целлерит/Zellerite, ромб.
Ca2(UO^+)(CO3K • 10Н2О — Либихит/Liebigite, уст. ураноталлит/
uranothallite, ромб., зел.
Ca2(UO2+)Cun(CO3L- Фоглит/Voglite, трикл.
Ca(UO^+NO4(OHN • 8Н2О — Беккерелит/Becquerelite, ромб., НМ
2—3, </5,2, т.-желт.
Ca(UOf J(РО4J- а) • B—6)Н2О, Метаотёнит/Meta-autunite,
тетр., сер.-желт. б) • A0— 12)Н2О, Отёнит/Autunite, тетр., НМ
2,0—2,5, d 3,1—3,2, зел.-желт. [6]
Са(иО^+L(РО4J(ОНL • 7Н2О — Фосфуранилит/Phosphuranylite,
ромб.
Ca2(UO^+K(PO4J(OHL • 4Н2О — Фуркалит/Phurcalite, ромб.
Ca(UO2+JSi2O7 • 6Н2О — Бета-уранофан/Beta-uranophane,
монокл. [6]
Ca(U0fJ(Si205K— а) • лН2О (п < 5), Метахейвиит/Metahaiwee-
ite, монокл. (?). б) • 5Н2О, Хейвиит/Haiweeite, уст. ранкилит/гап-
quilite, монокл.
Ca(UOfJ(SiO3J(OHJ • 5Н2О - Уранофан/Uranophane, уст.
уранотил/uranotile, монокл., НМ 2,5, d3,7—3,9, роз.-желт., сод.
Mg,Ba,Pb,Th,Y[6]
Са(иО^+J(УО4J— а) • C—5)Н2О, Метатюямунит/Metatyuyamu-
nite, ромб., зел.-желт. б) • E—8)Н2О, Тюямунит/Tyuyamunite,
ромб., НМ 2, ^/3,7—4,3, ярко-желт.
CaUIV(PO4J • A-2)Н2О - Нингиоит/Ningyoite, ромб.
Ca3UIV(UOfN(CO3J(OHI8 • C-5)Н2О - Уайаргит/Wyartite, ромб.
Ca2ylnAl2(SiO4)(Si2O7)O(OH) — Мухинит/Mukhinite, монокл.
Ca(VO3J — а) • 2Н2О, Метароссит/Metarossite, трикл. б) • 4Н2О,
Россит/Rossite, трикл.
219
I. Неорганические вещества
Продолжение щщ
251
252
253
254
255
256
257
258
259
260
261
261А
262
263
264
265
266
267
268
269
270
271
272
220
CaV4vO9 • 5Н2О -- Симплотит/Simplotite, монокл.
Ca(V3O8J • 9Н2О — Хьюэттит/Hewettite, ромб., d2,55, кор.-красц
Са3(У10О28) • 17Н2О — Паскоит/Pascoite, монокл., d 2,46, оранж.*
краен.
Ca(V02+)(Si205J • 4Н2О - Пентагонит/Pentagonite, ромб.
Ca2VivO9(V^O8J • лН2О — Меланованадит/Melanovanadite,
трикл., черн.
(CaV2v)PO4(OHL • ЗН2О — Синкозит/Sincosite, тетр.
Ca3V2n(Si04K— Голдманит/Goldmanite, куб., НМ 6,0—7,5, лГ3,74,
зел. [4]
Ca9(V4vVyAl2O80) • 56Н2О - Шервудит/Sherwoodite, тетр.
Ca2(VIVV^O24) • 8Н2О — Хендерсонит/Hendersonite, ромб.
CaWO4— Шеелит/Scheelite, тетр., НМ 4,5—5,0, d 5,9—6,1, сер.-
бел., сод. Nb, Та, Ln [6]. Зейригит/Seyrigite — HI., сод. Mo [6]
Ca3YmAl2(SO4)F13 • 10Н2О — Чухровит/Chukhrovite, куб., сод. Се
Са55У^пРеИ1А1(В2812О10L(ОН)8 — Хеллендит (трад. гелландит)/
Hellandite, монокл., НМ 5,5, d 3,7, бур., сод. Ег, Се
(CaYinTi2vN(OH) — Иттробетафит/Yttrobetafite, куб., кор., сод.
Nb, Та, Ln, F"
^^ • Н2О — Просперит/Prosperite, монокл.
CaZnH(AsO4)OH — Остинит (трад. aycTHHMT)/Austinite, ромб.
Ca2Znn(HAsO4J(OHJ — Гейтит/Gaitite, трикл., сер.-бел.
CaZn2r(PO4J • 2Н2О - Шольцит/Scholzite, ромб.
CaZnHSiO4— а) Эсперит/Esperite, монокл., сод. РЬ. б) • Н2О, Клй
ноэдрит/Clinohedrite, монокл.
CaZn2ISi207 • Н2О — Хунитоит/Junitoite, ромб.
Ca2ZnHSi207 — Хардистонит/Hardystonite, тетр., бел.
CaZrIVAl9(BO3)O15— Пейнит/Painite, гекс.
Ca3Zr!,v(Al2SiOI2) - ЬСимцейит/ICimzeyite, куб., НМ 6,0—7,5, d*>
кор.-зел., сод. Ti [4]
CaZrIVSi207— Гиттинсит/Gittinsite, монокл.
I. Неорганические вещества
Продолжение табл.
CaZrIVSi309 • 2Н2О — Кальций-ката1ше(й)ит/Са1сшт-са1ар1еA)йе,
гекс.
CaZr^S^O^' 2,5Н2О — Армстронгит/Armstrongite, монокл., кор.
(CaZrIVTi2v)O7 — Циркелит/Zirkelite, уст. цирконолит/zircono-
lite, монокл., НМ 5,5, d4,7—5,22, черн., сод. Th, Ln, Nb, Fe
(CaZr3vTiIV)O9 — Кальциртит/Calzirtite, тетр.
.—_
Cd — Кадмий/Cadmium, гекс, НМ 2, d8,64, бел.
CdHCO3 — Отавит/Otavite, уст. кадмиевый шпат/cadmium spar,
трип, d4,96, бел.
CdnO — Монтепонит/Monteponite, куб., d 8,15, бур.
CdnS — а) Гринокит/Greenockite, уст. кадмиевая обманка/cadmi-
обманка/cadmium blende, гекс, НМ 3,0—3,5, d 4,8—4,9, желт.-оранж. [4, 5]. б)
Холиит/Hawleyite, куб.
CdnSe — Кадмоселит/Cadmoselite — гекс, J5,81, красн.-кор.
СеП1А13(РО4J(ОНN — Флоренсит/Florencite, триг., d 3,59, желт.-бел.
Се^п(СОзK * 4Н2О — Калкинсит/Calkinsite, ромб., сод. La
CeHI(CO3)F — Бастнесит/Bastnasite (Bastnaesite), уст. хамартит/
hamartite, гекс, НМ 4—5, я?4,6—5,2, желт., сод. La, ОН" [6]
Сеш(СО3)ОН — Гидроксилбастнесит/Hydroxylbastnasite, гекс,
желт., сод. La, F~
CeHIF3— Флюоцерит/Fluocerite, уст. тисонит/tysonite, гекс,
d 5,7—6,13, красн.-желт., сод. Ln
(CeHINbv)O4 — Бета-церийфергюссонит/Beta-ceriumfergussonite,
монокл.
(CemNb^f)O6F — Цериопирохлор/Ceriopyrochlore, уст. маринья-
кит/marignacite, куб., т.-желт., сод. Са, Na, Ln, Та, Ti, OH~ [6]
CeIV02— Церианит/Cerianite, куб., */7,1, св.-желт., сод. Th
СешРО4 — а) Paбдoфaн/Rhabdophan(it)e, уст. сковиллит/scovil-
Hte, гекс, НМ 3,5, d4, бур., сод. Ln. б) Монацит/Monazite, уст.
Урдит/urdite, монокл., НМ 5,0—5,5, d4,6—5,4, желт.-кор., сод.
Ln, Th, Y, Si, U, Са [6]
Ce2H(SiO4JOH — Тёрнебумит/Tornebohmite, гекс, сод. Ln
(CeInTiIVNbv)O6- Эшинит/Eschynite (aeschynite), ромб.,
НМ 5—6, rf 5,0—5,8, кор.-черн., сод. Th, Ln, Fe, Ca
221
I. Неорганические вещества
Продолжение пц^Л
12
13
Ce*nTi^v(Si207H4— Чевкинит/Chevkinite (tscheffkinite), mohokjj.
d 4,2—4,5, черн., сод. La
CemVO4— Кусуит/Kusuite, тетр., сод. РЬ
4
5
9
10
И
12
13
14
CoAs — Лангисит/Langisite, гекс, сод. Ni
CoAs2 — Саффлорит/Safflorite, уст. белый кобальт/white cobalt,
ромб, или монокл., НМ 4—5, d7,4, сер.-бел., сод. Fe, Ni, Bi, Cu, S [6]
CoAs3 — Скуттерудит/Skutterudite, уст. шпейсовый кобальт/spciss
cobalt, куб., НМ 5,5—6,0, fif 6,5, бел., сод. Ni, Fe [4, 6]. Смальтин/
Smaltite, уст. оловянно-белый кобальт/tin white cobalt — С. с не-
недостатком As (СоАБз^, х « 1), НМ 5,0—5,5, сер.-бел. [4]
Con(AsO4J • 8Н2О — Эритрин/Erythrite, уст. кобальтовые цветы/
cobalt bloom, монокл., НМ 1,5—2,5, of 2,95—3,06, т.-роз., сод. Ni
Co(As)S — a) Кобальтин/Cobaltite, уст. кобальтовый блеск/cobalt
glance, куб., НМ 5,5, d6,2—6,33, роз.-бел., сод. Fe, Ni [6]. б) Ал-
локлазит/Alloclasite, ромб, или монокл., сод. Fe. в) Глаукодот/
Glaucodot, уст. данаит/danaite, кобальто-мышьяковый колчедан/
cobalt miBpickel, ромб., сод. Fe [6]
СопСО3 — Сферокобальтит/Spherocobaltite, уст. кобальтокаль-
цит/cobaltocalcite, кобальтовый шпат/cobalt spar, триг., d4,13, роз.
СопС12 • 6Н2О — Олбриттонит/Albrittonite, монокл., dl,92, роз.
(CoIICo^II)S4 — 'Линнеит/Linneite (linnaeite), уст. кобальтовый
колчедан/cobalt pyrites, куб., НМ 5,5, d4,8—5,0, т.-сер., сод. Ni,
Fe, Cu [6]
(Co2nCun)S4— а) Дайингит/Dayingite, куб., сод. Pt. б) Карроллит/
Carrollite, куб., сод. Ni
СошО(ОН) — Гетерогенит/Heterogenite, уст. стеньеит/stainierite,
гекс. илитрит., d4,6, т.-кор.
Co"S, +x(x = 0,04—0,13) — Джайпурит/Jaipurite, гекс, d5,4, сер.-беЛ'
Con(S2) — Каттьеит (трад. KaTTbepHT)/Cattierite, куб., d4,2, сер.-бел.
ConSO4— а) • 4Н2О, Аплоуит/Aplowite, монокл., сод. Mn, U.
б) • 6Н2О, Мурхаусит/Moorhouseite, монокл., сод. Ni, Mn. в)'
7Н2О, Биберит/Bieberite, уст. кобальтовый {или красный) купо-
купорос/cobalt (red) vitriol, монокл., d 1,95, красн.-роз.
Co(Sb)S — а) Виллиамит/Willyamite, псевдокуб., сод. Ni. б)
тибит/Costibite, ромб.
222
I. Неорганические вещества
Продолжение табл.
— Фребольдит/Freboldite, гекс, */7,6, красн.-фиол.
CoH(Se2) — а) Трогталит/Trogtalite, куб. б) Хастит/Hastite, ромб.
Con(Se4) — Борнхардтит/Bornhardtite, куб.
ConSeO3 * 2Н2О — Кобальтоменит/Cobaltomenite, монокл., сод. Ni
Соп(Те2) — Маттагамит/Mattagamite, ромб., сод. Fe
Co^UOf N(SO4K(OHI0 • 16Н2О - Кобальт-циппеит/Cobalt-
zippeite, ромб.
(Сг2пСоп)О4— Кохромит/Cochromite, куб., сод. Ni, Fe, Al
(CrnCr2n)S4— Бржезинаит (трад. 6peimHaHT)/Brezinaite,
монокл.
(CrmCul)O2— Макконнеллит/McConnellite, трип, d5,2, зел.
(Cr*nFeIl)O4— а) Хромит/Chromite, уст. хромистая шпинель/
chrome spinel, хромистый железняк/chrome iron ore, берёзовит/
beresovite, куб., НМ 5,5—7,5, d 3,9—4,8, черн., сод. Mg, Ti, Mn, Ni,
V, Zn [4—6]. 6) Донатит/Donatite, тетр., d4,9, кор.-черн., сод. Mg
Cr2nFen(SO4L • 22H2O — Редингтонит/Redingtonite, монокл., сод.
Mg, Ni, Al
(Cr2nMnn)O4— Манганохромит/Manganochromite, куб., сод. Fe, V
(Cr2IINiII)O4— Нихромит/Nichromite, куб., сод. Co, Fe, Al
Cr*HO3 — Эсколаит/Eskolaite, триг., d5,2, т.-зел.
CrHIO(OH) — a) Брейсуэллит/Bracewellite, ромб, (у), краен.-кор.
б) Гвианаит/Guyanaite, ромб. (|3), г/4,5, зел. в) Гримальдиит/
Grimaldiite, триг. (а), </4,1, гол.-зел.
(CrVIPb^IPb2v)O16- Сантанаит/Santanaite, гекс.
CsAl4[Be4BnO26(OHJ] • Н2О - Родицит/Rhodizite, куб., НМ 8,
<* 3,31-3,34, желт.-зел. [1]
Cs(AlSi2O6) • 0,5Н2О — Поллуцит/Pollucite, уст. поллукс/pollux,
fr, НМ 6,5, ^/2,87-2,98, бел., сод. Na [6]
Си — Медь/Copper, куб., НМ 2,5—3,0, d 8,4—8,9, т.-красн., сод.
Ag, As, Fe, Bi, Hg, Аи [6]
Cu»AlAsO4(OHJ- a) • 0,5H2O, Лютеит/Luetheite, монокл.
^) * 2H2O, Лироконит/Liroconite, монокл.
Cu"Al7(AsO4L(OH)I3 • 11,5H2O - Церулеит/Ceruleite, трикл.
223
I. Неорганические вещества
Продолжение табд
Cu^Al(AsO4K(OHN • ЗН2О — Гаудейит/Goudeyite, гекс.
Cu^Al2(AsO4K(SO4K(OHJ7 • ЗЗН2О - Халькофиллит/Chalcophyl.
lite, уст. эринит/erinite, триг.
Си" А12СО3(ОНI2 • 2Н2О — Карбонат-цианотрихит/Carbonate-cy.
anotrichite, ромб., сод. SO4~
СипА16(РО4L(ОН)8 • 4Н2О — Бирюза/Turquoise, уст. кал(л)аит/
calaite (kallaite), трикл., НМ 5—6, d2,6—2,9, гол.-зел., сод. Fe, Zn [1J
Си*1 A14(PO4K(OH)9 • 4H2O — Сапаталит/Zapatalite, тетр.
CuI1Al2PbII(SO4J(OHN — Осаризаваит/Osarizawaite, триг.
CunAl(SO4JCl • 14H2O — Оберит (трад. аубертит)/АиЬеПке, трвд
Cu^Al(SO4)Cl(OHI2 • ЗН2О - Спанголит/Spangolite, триг.
CuHAl4SO4(OHI2 • ЗН2О — Халькоалюмит/Chalcoalumite, монокл
Cu4 A12SO4(OHI2 • 2Н2О — Цианотрихит/Cyanotrichite, уст. лет-
тсомит/lettsomite, бархатная pyaa/velvet(y) ore, ромб. [6]
Си'As — Домейкит/Domeykite, куб. или триг, т.-сер.
Cu2As3— Паксит/Paxite, ромб.
Cu4As3 — Новакит/Novakite, тетр., сод. Ag
Cu5As2 — Коутекит/Koutekite, гекс.
Cu6As — Алгодонит/Algodonite, ромб., т.-сер.
(CuIIAs2II)O4— Триппкеит/Trippkeite, тетр.
C\xlJ(As04J— Кейит/Keyite, монокл.
Cu^(AsO4)OH — а) Оливенит/Olivenite, монокл., НМ 3, </3,9—4,4,
т.-зел. [6]. б) • 1,25Н2О, Страшимирит/Strashimirite, монокл.
в) • ЗН2О, Эвхроит/Euchroite, ромб.
Си3^04@^1K— IOiHHOiGia3/Clinoclas(it)e, уст. абихит/abichite,
монокл., НМ 2,5—3,0, d4,4, зел. [6]
Cu^(AsO4J(OHL— а) Корнубит/Cornubite, трикл. б) • Н2О, Кор-
Корну оллит/Cornwallite, уст. эринит/erinite, монокл.
Cu^(AsO4K(OHM • ЗН2О — Хлоротил/Chlorotile, гекс, сод. Fe
Cu^(AsO4JSO4(OH)l0 • 7Н2О — Парнауит/Parnauite, ромб.
Cu(As)S — Лаутит/Lautite, ромб.
Cu2(As)S2 — Даоманит/Daomanite, ромб., сод. Pt
224
I. Неорганические вещества
Продолжение табл.
Cu*(AsS4) — а) Арсеносульванит/Arsenosulvanite, уст. лазареви-
чит/lazarevicite, куб. б) Энаргит/Enargite, ромб., НМ 3,0—3,5,
^4,43—4,45, желт.-черн. [6]. в) Лусонит/Luzonite, тетр.
(CujAs^ — Зиннерит/Sinnerite, трикл.
Cu3Au — Аурикуприд/Auricupiide, уст. купроаурид/cuproauride, куб.
Cu^Biin(AsO4K(OHN • ЗН2О - Миксит/Mixite, гекс.
(CuIBiIII)S2 — Эмплектит/Emplectite, ромб.
(Cu^Bi111^ — Виттихенит/Wittichenite, уст. клапротит/klapro-
thite, ромб. [6]
(CuIloBiI1I2I)S23— Купровисмутин/Cuprobismuthinite, монокл.
Си "ССУДОЙ^ — а) Глаукосферит/Glaucospherite, монокл., сод.
Ni. б) Малахит/Malachite, уст. медный шпат/copper spar, горная
(или медная) зелень/mountain (copper) green, монокл., НМ 3,5—
4,0, */3,9—4,0, ярко-зел. [1, 5, 6]. в) Кольвецит/Kolwezite, трикл.,
сод. Со. г) • ЗН2О, Купроартинит/Cuproartinite, монокл., сод. Mg
Сиз1(СО3J(ОНJ — Азурит/Azurite, уст. шессилит/chessylite, мед-
медная лазурь/copper azure, монокл., НМ 3,5—4,0, flf 3,77, ярко-син.
[1,6]
Сиз1(СО3K(ОНL • 6Н2О — Джорджит/Georgeite, аморфн.
Си^(СО3L(ОНJ • 4Н2О — Купрогидромагнезит/Cuprohydromag-
nesite, монокл., сод. Mg
(Cu2CdnSnIV)S4- Черниит/Cernyite, тетр.
CuJCl — Нантокит/Nantokite, куб., rf4,l, бел.
СипС12 • 2Н2О — Эриохальцит/Eriochalcite, ромб., d2,5, гол.
[СипС14], К2 • 2Н2О — Мичерлихит/Mitscherlichite, тетр., зел.
CuI1I9Cl4(NO3J(OHK2 • 2Н2О — Буттгенбахит/Buttgenbachite, гекс.
Сии(С1)ОН • ЗН2О — Антониит/Anthonyite, монокл.
Си2гС1(ОНK— а) Боталлакит/Botallackite, монокл. [6].
б) Атакамит/Atacamite, ромб, или триг., НМ 3,0—3,5, d3,75—3,77,
ярко-зел. [6]
Си^С1(ОНO • яН2О — Кларингбуллит/Claringbullite, гекс.
(Cu^Cun)GeS4— Германит/Germanite, куб., кор.-черн., сод. Fe, As
(Си^Си^Оз— Парамелаконит/Paramelaconite, тетр.
(Cu^Cu!IPbIIBiIII)S11 — Ходрашит/Hodrushite, монокл.
225
8-2004
I. Неорганические вещества
Продолжение тайц
50
51
52
53
54
55
56
57
58
59
60
61
62
63
64
65
66
67
68
69
70
71
72
j^Sg — Ярроуит/Yarxowite, гекс.
(Cu?Cun)S4 — Анилит/Anilite, ромб.
(Cu^Cun)S5 — Дигенит/Digenite, куб., НМ 2,5—3,0, d5,5-5,7,
син.-черн. [6]
— Шпионкопит/Spionkopite, гекс.
(Cu2Cun)Se2 — Умангит/Umangite, тетр.
Cu2Cun(Se2J — Тирреллит/Tyrrellite, куб., сод. Со, Ni
4 — Атабаскаит/Athabascaite, ромб.
(Cu2CunSnIV)S4 — Курамит/Kuramite, тетр.
(Cu4Cun)Te3 — Вайссит/Weissite, псевдокуб.
(CuJCu^)Te5 — Риккардит/Rickardite, ромб., НМ 3,5, dl,54,
т.-краен.
(CuIGaIII)S2— Галлит/Gallite, тетр.
Cu^(GeS4) — Бриарит/Briartite, тетр., сод. Fe, Zn
Cu^(RAsO4J(AsO4J • (8—9)Н2О — Линдаккбрит/Lindackerite, мо-
нокл.
Cu7Hg6 — Колымит/Kolymite, куб.
(CujHgnPbnBiin)Se5- Петровичит/Petrovicite, ромб.
Си!1 — Маршит/Marshite, куб., */5,6, бел.
Cun(IO3J * 0,67Н2О — Беллинджерит/Bellingerite, трикл., d5,2, зел.
з — Сайлсит/Salesite, ромб.
(CuIInIII)S2— Рокесит/Roquesite, тетр.
Си^(МоО4J(ОНJ — Линдгренит/Lindgrenite, монокл.
Cu^NO3(OHK— Герхардтит/Gerhardtite, ромб., гол.
СипО — ТеноритДепогИе, уст. мелаконит/melaconite, черная мед-
медная руда/black copper ore, монокл., НМ 3—4, */6,2—6,4, черн. [6]
Си^О — Куприт/Cuprite, уст. красная (или стекловатая) медная
руда/red (vitreous) copper ore, рубиновая медь/ruby copper, куб.,
НМ 3,5—4,0, d6,l, т.-красн. [6]. Халькотрихит/Chalcotrichite,
уст. плюшевая медная руда/plush copper ore — К. с удлиненным**
и нитевидными кристаллами. Черепичная руда/tile ore — кирпй4'
но-красн. землистая смесь К. с лимонитом [6]
226
I. Неорганические вещества
Продолжение табл.
Сип(ОНJ • 2Н2О — Кальюметит/Calumetite, ромб., гбл., сод. С1
Си'ЧРО4)ОН - Либетенит/Libethenite, ромб., НМ 4, </3,9, зел.
Си^РО4(ОНK — а) Корнетит/Cornetite, ромб, б) Весейит/Veszely-
ite, монокл., сод. Zn
Cu5I(PO4J(OHL • Н2О — Псевдомалахит/Pseudomalachite, уст.
элит/ehlite, фосфохальцит/phosphochalcite, монокл., зел.
CunPbn(AsO4)OH — Дуфтит/Duftite, ромб.
(CuIPbIIAsIII)S3 — Зелигманит/Seligmannite, ромб., т.-сер, [6]
(CuIPbIIBiIII)S3 — а) Айкинит/Aikinite, уст. патринит/patrinite,
ацикулит/aciculite, игольчатая руда/needle ore, ромб. [6].
б) Соучекит/Soucekite, ромб., сод. Se
(CuW^i™1^ — Крупкаит/Krupkaite, ромб.
(CuIPbIIBi^)S9- Гладит/Gladite, ромб.
(CuIPbIIBiI1I1I)S18 — Пекоит/Pekoite, ромб.
(CuIPb'IBi'II)S7- Наффилдит/Nuffieldite, ромб.
(Cu^ Pb'IBi4")S9 — Хаммарит/Hammarite, ромб.
^— Юнонаит/Junoite, монокл., сод. Se
^— Резбаньяит/Rezbbanyaite, ромб. (?)
(Cu^Pb'1Bi'II)S17- Нейит/Neyite, монокл., сод. Ag
(Cu^Pb^Bi^Sjj — Берриит/Berryite, монокл., сод. Ag
(Cu^Pb^Bi7n)S15 — Линдстрёмит/Lindstromite, ромб.
(Cu'Pb^Bi7")S18— Фридрихит/Friedrichite, ромб.
(Cu^Pb4I5Bi5I6I)S132— Праудит/Proudite, монокл., черн.
(Cu^1PbIIBiIII)Sl3 — Ларошит/Larosite, ромб.
(CuIPb'IBi7II)Se4S10— Нордстрёмит/Nordstromite, монокл.
Си^РЬпВг(С1)О6— Мёрдокит/Murdochite, куб.
CuIIPbJICO3(SO4JCl2O — Уэрриит/Whenyite, монокл.,
^6,45, св.-зел., сод. ОН"
Cu^Pb^CO3(SO4K(OHN— Каледонит/Caledonite, ромб.
СипРЬпС12(ОНJ- Персилит/Percylite, куб.
CuIIPb^ICl2(OHL~ Диаболит/Diaboleite, тетр.
227
I. Неорганические вещества
Продолжение табц
• 2Н2О — Псевдоболеит/Pseudoboleite, тетр.,
гол.-сер.
Cu^Pb^Cl^OH)^ — Куменгеит/Cumengeite, тетр.
Си11РЬз1С12О2(ОНJ — Хлороксифит/Chloroxiphite, монокл.
CunPb^(CrO4)PO4(OH) — Вокленит/Vauquelinite, уст. лаксма-
нит/laxmannite, монокл., сер.-зел.
CunPb^PO4(SO4)OH - Цумебит/Tsumebite, монокл.
CuuPbnSO4(OHJ — Линарит/Linarite, монокл., ярко-гол.
CunPbyS04@H)g— Элиит/Elyite, монокл.
(CuIPbIISbIII)S3 — Бурнонит/Bournonite, уст. бертонит/berthonite,
колёсная руда/wheel ore, ромб., НМ 2,5—3,5, dr 5,7—5,9, гол.-сер.,
сод. As, Fe [6]
(CuIPbI1I3Sb"I)S24— Менегинит/Meneghinite, ромб. [6]
CunPbn(TeIV03J • Н2О - Холоалит/Choloalite, куб.
Cu3IPbIITeO4(OHN— Хинит/Khinite, ромб, или гекс.
(CuIPbnTlIAs*II)S5 — Уоллисит/Wallisite, трикл., сод. Ag
CuHPbn(VO4)OH — Моттрамит/Mottramite, уст. купродеклуазит/
cuprodescloizite, ромб., НМ 3,0—3,5, d5,9—6,2, зел., сод. Zn
CunS — Ковеллин/Covellite (covelline), уст. медное индиго/соррег
indigo, гекс, НМ 1,5—2,5, d 4,6—4,76, т.-син. [6]
CuH(S2) — а) Вильяманинит/Villamaninite, куб., сод. Ni, Co, Fe. б)
Маланит/Malanite, куб., сод. Pt, Ir
Си, 94S — Джюрлеит/Djurleite, монокл., НМ 2,2—2,4, </5,5—5,7,
черн.
Cu2S — Халькозин/Chalcosine, уст. халькоцит/chalcocite, редру-
тит/redruthite, медный блеск/copper glance, ромб., НМ 2,5—3,0,
с/5,5-5,8, т.-сер. [6]
CunSO4— а) Халькокианит/Chalcokyanite (chalcocyanite), ромб.,
d3,6, бел. б) • Н2О, Пуатвенит/Poitevinite, монокл., сод. Fe, Zn.
в) • ЗН2О, Бонаттит/Bonattite, монокл. г) • 5Н2О, Халькантит/
Chalcanthite, уст. медный (или синий) купорос/copper (blue) vitri-
vitriol, трикл., НМ 2,5, d2,12-2,3, св.-син. [6] д) • 7Н2О, Бутит/
Boothite, монокл., гол.
228
I. Неорганические вещества
Продолжение табл.
CujI9SO4Cl4(OHK2 • ЗН2О - Коннеллит/Connellite, уст. футит
(трад. футеит)Доо1еИе, церулеофибрит/ceruleofibrite, гекс.
Cu"(SO4)O — Долерофанит/Dolerophanite, монокл., бел.
Cu^SO4(OHL- а) Антлерит/Antlerite, ромб., НМ 3,5-4,0, </3,9,
т.-зел. [6]. б) • 2Н2О, Ктенасит/Ktenasite, монокл., сод. Zn
Cu4ISO4(OHN— a) Брошанит/Brochantite, уст. бланшардит/blan-
chardite, монокл., ярко-зел. б) • Н2О, Познякит/Posnjakite, мо-
монокл., гол. в) • 2Н2О, Раувольфит/Rauwolfite, монокл, г) • 2Н2О,
Лангит/Langite, ромб.
Cu2Sb — Купростибит/Cuprostibite, тетр., сод. Т1
(CuISbIII)S2 — Халькостибит/Chalcostibite, уст. вольфсбергит/
wolfsbergite, ромб.
(Cu^Sb111^— Скиннерит/Skinnerite, монокл.
(Cu^Sbv)S4— Фаматинит/Famatinite, тетр.
(Cu3Sbv)Se4 — Перменжаит/Permingeatite, тетр.
CuHSe — Клокманит/Klockmannite, гекс, af5,9, черн.-зел.
Cun(Se2) — а) Крутаит/Krutaite, куб. б) Бамболлаит/Bambollaite,
тетр., сод. Те
Se — а) Берцелианит/Berzelianite, уст. селенистая медь/sele-
медь/selenium copper, куб., */7,4, черн. б) Беллидоит/Bellidoite, тетр., черн.
в) Круксит/Crookesite, тетр., НМ 2,5—3,0, </6,9, т.-сер., сод. Tl, Ag
CunSeO3 • 2Н2О — Халькоменит/Chalcomenite, ромб, или монокл.
Cu*rSi6017 • 7Н2О — Гилалит/Gilalite, монокл.
Cu^Si6O18 • 6Н2О — Диоптаз/Dioptase, уст. аширит/achirite, мед-
медный изумруд/copper emerald, трип, НМ 5, d 3,28—3,35, зел. [6]
Cu^Si10O29 • 11Н2О — Апачит/Apachite, монокл.
Cu^Si2O5(OHJ • яН2О — Хризоколла/Chrysocolla, уст. корнью-
ит/cornuite, медная смоляная руда/copper pitchy ore, аморфн.,
НМ 2—4, d 1,9-2,4, гол.-зел., сод. А1 [1, 6]
Cu4ISi4011@HJ • 0,5Н2О — Планшит/Plancheite, ромб., св.-гол.
Cu^(SiO3L(OHJ— Шаттакит/Shattuckite, ромб.
СипТе — Вулканит/Vulcanite, ромб.
СипТеО3 — а) Балякинит/Balyakinite, ромб, б) • Н2О, Гремит/
Graemite, ромб., гол.-кор. в) • 2Н2О, Тейнит/Teineite, куб.
229
I. Неорганические вещества
Продолжение mafa
^О5— Райит/Rajite, мрнокл.
Сиз1ТеО4(ОНL— Ксокомекатлит/Xocomecatlite, ромб.
Си^(ТеО3J(ОНN • 2Н2О — Сесбронит/Cesbronite, ромб.
Си^Х^Оу — Цисит/Ziesite, монокл. (Р)
Си^(УО4J • ЗН2О — Фольбортит/Volborthite, уст. узбекит/uzbe-
kite, монокл., зел.-желт., сод. Са, Ва, Mg
(Си^^ — Сульванит/Sulvanite, куб.
CuIIZn'I(As04J— Страньскийит/Strariskiite, трикл.
(CuJZn^AsJ11^^ — Новацкийит/Nowackiite, триг.
CunZnnCO3(OHJ— Розасит/Rosasite, монокл., НМ 4,5, </4,0—
4,2, зел.-гол.
Си2^п^8(СОзJ(ОНN — Аурихальцит/Aurichalcite, ромб., НМ
1—2, </3,6, зел.-гол. [6]
(Cu^ZnnSnIV)S4— Кестерит/Kesterite, уст. изостаннин/isostan-
nite, тетр., сод. Fe
Си4^п"(ТеО3K(ОНI8— Кетсалкотлит/Quetzalcoatlite, гекс, зел.
CuI110Zn^ITeO3(TeO4JCl(OHJ5 • 27Н2О — Тлалокит/Tlalocite, мо-
монокл. (?)
Fe - Железо/Iron, куб. (а), НМ 4,5, d1",3-7,9, сер., сод. Ni B%) [6]
FeAg5_JC— Штютцит/Stutzite, гекс.
(Fe^Ag^Cu^Sb4n)S13— Фрайбергит/Freibergite, уст. блёклая се-
серебряная руда/faded silver ore, куб., НМ 3,0—4,5, d 5,1—5,4, сер.-
черн., сод. Zn, Hg, As [6]
Fe2AgS3 — a) Аргентопирит/Argentopyrite, уст. серебристый кол-
колчедан/silvery pyrites, ромб, б) Штернбергит/Sternbergite, уст. се-
серебряный колчедан/silver pyrites, ромб.
Fe8AgS8 — Аргентопентлендит/Argentopentlandite, куб., сод. Ni
Fe3IIAgI(SO4J(OHN — Аргентохаросит/Argentojarosite, триг.
(FenAg^ SnIV)S4 — Окартит/Hocartite, тетр.
Fe^Al3(AlSi5018) — Секанинаит/Sekaninaite, уст. железный
кордьеит/iron cordierite, ромб., сод. Mg
Fe^Al(AlSi3O10)(OH)8— Шамозит/Chamosite, монокл. ц/
НМ 2,5-3,0, d 3,0-3,4, зел., сод. Mg, Fe111 [6]
230
I. Неорганические вещества
Продолжение табл.
Fe5IAl2(AlSi3011J@HJ— Феррожедрит/Ferrogedrite, монокл.,
НМ 5,5-6,0, 42,85-3,57, зел.
(FenAl2)O4 — Герцинит/Hercynite, уст. железистая шпинель/iron
spinel, куб., НМ 7,5—8,0, 44,4, т.-зел., сод. Mg, Fem
FenAl2(PO4JO • 8Н2О - Сиглоит/Sigloite, трикл., сод. Fe111, ОН"
FenAlPO4(OHJ • Н2О — Чилдренит/Childrenite, ромб., НМ 5,
43.2, желт.-кор., сод. Мп
FenAl2(PO4J(OHJ — а) Скорцалит/Scorzalite, монокл., сод. Mg.
б) • 4Н2О, Метавоксит/Metavauxite, монокл. в) • 6Н2О, Воксит/
Vauxite, трикл., НМ 3,5, 42,38, гол., сод. Мп. г) • 6Н2О, Паравок-
сит/Paravauxite, трикл., НМ 3, 42,29, бел.
FenAl2(SO4L • 22Н2О — Галотрихит/Halotrichite, уст. железные
(или римские) квасцы/iron (Roman) alum, монокл., НМ 1,5, 41,9,
зел.-бел., сод. Mg, Mn
Fe4"Al(SO4NO(OH) • 20Н2О — Алюмокопьяпит/Aluminocopi-
apite, трикл.
Fe*1 Al(SiO4K — Альмандин/Almandite (almandine), куб., НМ 7,0—
7,5, 43,8-4,32, т.-красн. [1, 4]
FenAl2(SiO3J(OHL — Феррокарфолит/Ferrocarpholite, ромб.
Fe^Al9(SiO4LO7(OH) — Ставролит/Staurolite, уст. крестовый ка-
камень/cross stone, монокл., НМ 7,0—7,5, 43,74—3,83, красн.-бур.,
сод. Mg, Zn, Fe111 [1]. Лусакит/Lusakite — С, сод. Со
FeAs — Вестервелдит/Westerveldite, ромб., 47,8, св.-сер.
FeAs2 — Лёллингит/Lollingite, уст. лейкопирит/leucopyrite, ромб.,
НМ 5,0-5,5, 47,1-7,4, сер. [6]
FeinAsO4— а) • 2Н2О, Скородит/Scorodite, ромб., НМ 3,5—4,0,
43.3, зел.-сер., сод. А1, РО^~. б) • 3,5Н2О, Канкит/Kankite, мо-
монокл.
(FenAsy)O6 — Лудлокит/Ludlockite, трикл.
Fe^(AsO4J • 8Н2О — Симплезит/Symplesite, трикл. или монокл.
(Fe^As^O^ — Шнайдерхёнит/Schneiderhohnite, трикл.
Fe4n(AsO4JO3 — Анджелеллит/Angelellite, трикл.
(FemAs'n)O4(OH) - Карибибит/Karibibite, ромб.
231
I. Неорганические вещества
Продолжение табд
Fe*nAsO4(SO4)OH — а) • 5Н2О, Сармьентит/Sarmientite, монокл.
б) • 7Н2О, Буковскиит/Bukovskyite, монокл.
Fe4n(AsO4KSO4(OH) • 15Н2О - Зикаит/Zykaite, ромб.
Fe(As)S — Арсенопирит/Arsenopyrite, уст. мышьяковый колче-
дан/miBpickel (misspickel), ядовитый шпат/poison spar, монокл.,
НМ 5,5—6,0, d5,9—6,3, серебристо-бел., сод. Со, Ni, Аи [6]
з13)С1 — а) Эрикаит/Ericaite, ромб., сод. Мп. б) Конголит/
Congolite, триг., сод. Mg, Mn
Fey(BeSiO4KS - Даналит/Danalite, куб., НМ 5,5-6,0, d 3,35-
3,43, красн.-кор., сод. Мп, Zn
Fe3nBin4PO4J(OHN— Заирит/Zairite, триг, сод. А1
Fe2nBilII(SiO4JOH — Бисмутоферрит/Bismutoferrite, монокл.
Fe3C — Коэнит (трад. когенит)/СоЬепИе, ромб., НМ 6, dl,6, сер.,
сод. Ni, Co. Цементит/Cementite — искусственный К., входит в
состав чугуна и стали
FenCO3 — Сидерит/Siderite, уст. железный шпат/iron spar,
шпатовый железняк/spathic iron ore, халибит/chalybite, триг,
НМ 3,5—4,0, d 3,96, св.-кор. [6]. Олигонит/Oligonite, уст. томеит/
thomaite, олигоновый шпат/oligon spar — С, сод. Мп. Сидеродот/
Siderodote — С, сод. Са [6]. Сидероштезит/Sideroplesite — С, сод.
Mg
FeHC2O4 • 2Н2О — Гумбольдтин/Humboldtine, монокл. (?), </2,2,
св.-желт.
[FeIH(C2O4K],K3 • ЗН2О — Мингуццит/Minguzzite, монокл., t/2,1,
зел.
FeHCl2 • 2Н2О — Рокюнит/Rokiihnite, монокл., d 1,9, зел.-гол.
FeniCl3— Молизит/Molysite, триг, г/2,9, черн.-кор.
[FenCl4]Cl2, K3Na - Риннеит/Rinneite, триг, НМ 3, rf2,35, бел.
[FenCl4],K2 • 2Н2О — Дугласит/Douglasite, монокл., бел.
[FemCl5],K2 • Н2О — Эритросидерит/Erythrosiderite, ромб., бел.
[FeII!Cl5], (NH4J • Н2О — Кремерсит/Kremersite, ромб., бел., сод.к
FeCo — Вайрауит/Wairauite, куб., сер.
Fe9Co9S16— Кобальтпентлендит/Cobaltpentlandite, куб. [6]
232
I. Неорганические вещества
Продолжение табл.
FeIICu4I(AsO4J(OHJ— Шенвиит (трад. шеневиксит)/Спёпе-
vixite, монокл.
(Jo^ — Теннантит/Tennantite, уст. биннит/binnite,
блёклая мышьяковистая руда/grey arsenic ore, куб., НМ 3,0—4,5,
д? 4,6—4,9, сер.-черн., сод. Ag, Zn, Hg, Sb [6]
^^^8 — Хейкокит/Haycockite, ромб.
(Fe'ICu^Cu2ISn2A')S12— Станноидит/Stannoidite, ромб.
(FenCu!I)O2 — Делафоссит/Delafossite, трип, НМ 5,5, черн.
(Fe2nCun)O4 — Купрошпинель/Cuprospinel, куб.
Fe^IICuII(PO4K(OHJ— Эндрьюсит/Andrewsite, ромб.
Fe^IICuII(PO4L(OH)8 • 4Н2О — Халькосидерит/Chalcosiderite,
трикл., зел.
(FeIIICu4PbIIBiIII)S6— Михараит/Miharaite, ромб.
(Fe^Cu^^— Нукундамит/Nukundamite, трип, сер.-черн.
FeCu(S2) — Халькопирит/Chalcopyrite, уст. медный колчедан/
copper pyrites, тетр. (а) или куб. (р), НМ 3,5—4,0, J 4,1—4,3,
т.-желт., сод. Se, Zn, Tl, Ag, Au [6]
(FenCu^)S4- a) Идаит/Idaite, гекс. (?), НМ 2,5, d 4,2, красн.-кор.
[6]. б) Реньеит/Renierite, тетр., сод. Ge, Zn, As
FenCu^(S2L— Фукучилит/Fukuchilite, куб.
(FeHICu5)S4— Борнит/Bornite, уст. эрубесцит/erubescite, павли-
ний медный колчедан/peacock copper pyrites, павлинья (или пур-
пурпуровая) медная руда/peacock (purple) copper ore, куб., НМ 3—4,
d4,9—5,3, т.-красн. [6]
(FenCu]0)S6— Бетехтинит/Betekhtinite, ромб., сод. РЬ
(Fe^Cun)S3 — Кубанит/Cubanite, уст. чалмерсит/chalmersite,
ромб., НМ 3,5, rf4,68, св.-желт.
(Fe^Cun)S4— Валлериит/Valleriite, трип, сод. А1
Fe9Cu9Sl6— Мойхукит/Mooihoekite, тетр.
Fe2IICuII(SO4L • 6Н2О — Рансомит/Ransomite, монокл.
Fe"ICuII(SO4JOH • 4Н2О - Гилдит/Guildite, монокл., бур.
Fe4nCun(SO4N(OHJ • 20Н2О - Купрокопьяпит/Cuprocopiapite,
три
трикл.
233
I. Неорганические вещества
Продолжение тщ
68
69
70
71
72
72А
73
74
75
76
77
78
79
80
81
82
83
84
85
234
13 — Тетраэдрит/Tetrahedrite, уст. панабаз/рапа-
base, блёклая сурьмянистая руда/grey antimony ore, куб., НМ 3,0^
4,5, */4,6—5,1, сер.-черн., сод. Ag, Zn, As [6]. Швацит/Schwazite^
Т., сод. Hg
FeCu(Se2) — Эскеборнит/Eskebornite, куб.
(FenCu^SnIV)S4— Станнин/Stannite, уст. оловянный колчедан/
tin pyrites, тетр., НМ 3—4, d4,3—4,5, сер.-черн., сод. Zn [6]
(FenCu2Sn^v)S8— Родостаннин/Rhodostannite, гекс.
(Fe2nCuJSnIV)S8— Мосонит/Mawsonite, тетр., сер.-черн.
Fe5IFeIII(AlSi3O10)(OH)8 — Тюрингит/Thuringite, монокл., НМ
2-3, </3,15-3,19, т.-зел., сод. Mg [6]
Fe^Fenl(BO4)O — а) Халсит (трад. iyiicHT)/Hulsite, монокл., сод.
Mg, Sn. б) Вонсенит/Vonsenite, уст. пайгеит/paigeite, ромб.
Fe^IFeIII(FeIIISiO5)(OHL— Кронстедтит/Cronstedtite, монокл.,
НМ 2-3, </2,6-3,1, зел.
(FeHFe2n)O4 — Магнетит/Magnetite, уст- магнитный железняк/
magnetic iron ore (или loadstone), куб., НМ 5,5—6,0, d5,2, черн. [6]
FeIIFe^II(PO4J(OHJ— a) Барбосалит/Barbosalite, монокл. б)
Липскомбит/Lipscombite, тетр., сод. Мп. в) • 4Н2О, Уитморит/
Whitmoreite, монокл.
FenFe4n(PO4K(OHM- Рокбриджит/Rockbridgeite, ромб., НМ4,5,
d3,3—3,5, зел.-черн., сод. Мп
FenFe4n(PO4L(OHJ • Н2О — Джиниит/Giniite, ромб., бур.
FenFe*n(PO4L(OHM • 4Н2О — Бераунит/Beraunite, монокл., НМ
3,5—4,0, d 2,8—3,0, красн.-кор.
Fe'IFe^II(PO4L(OHI2 — Лаубманит/Laubmannite, ромб.
(FeIIFe^II)S4— а) Грейгит/Greigite,уст. мельниковит/melnikovite,
куб. б) Смайтит/Smythite, триг.
FenFeJn(SO4L- а) • 14Н2О, Рёмерит/Romerite, трикл., НМ 3,0-
3,5, d 2,2, желт.-оранж. б) • 22Н2О, Билинит/Bilinite, монокл.
FenFe4n(SO4N(OHJ • 2Н2О — Копьяпит/Copiapite, уст. желтый
железный купорос/yellow copperas, трикл., НМ 2,5—3,0, d2,l-~
2,2, желт., сод. Mg, Cu, A1
FeIIFe4IISb4II(S)O12 — Апуанит/Apuanite, тетр.
Fe^IFe4IISbJiII(S)O16— Версильяит/Versiliaite, ромб.
I. Неорганические вещества
Продолжение табл.
FenFe *п (SiO4J — Лайхунит/Laihunite, ромб. '-
Fe^FeJn(Si6O17)O3(OHM — Дирит/Deerite, монокл.
(FeIIFeIIITlI)S3 — Пикополит/Picotpaulite, ромб.
Fe^GeC^) — Бруногайерит/Brunogeierite, куб.
Fe"(GeS4) — Полковичит/Polkovicite, куб., сод. РЬ
Fem(H3O+)(SO4J • ЗН2О — Ромбоклаз/Rhomboclase, ромб.
Fe3n(H3O+)(SO4J(OHN — Оксониохаросит (трад. гидрониояро-
3HT)/Oxoniumjarosite (hydroniumjarosite), триг, т.-желт.
Fe'II(HTeIV03K(TeIV03)Cl — Родалькиларит/Rodalquilarite, трикл.
(FeIIIn*II)S4— Индит/Indite, куб.
Fe5N2 — Cwepa3OT/Siderazot(e), уст. сидеразотит/siderazotite,
триг., d6,5, сер.-черн.
Fen(NH4J(SO4J • 6Н2О — Морит/Mohrite, монокл., d 1,8, св.-зел.
Fe3nNH4(SO4J(OHN — АммонйОхаросит/Ammoniojarosite, триг.
(FeIINi2I)As2— Орегонит/Oregonite, гекс.
FeniNi^(BO4)O — Бонаккорит/Bonaccordite, ромб.
FeJnNi^(CO3K(OHI6 • 4Н2О — Ривсит/Reevesite, триг.
(Fe2nNi)O4— Треворит/Trevorite, куб., t/5,2, бур.-черн.
(FeIINi'II)O4— Виоларит/Violarite, куб.
Fe9Ni9S16— Пентлендит/Pentlandite, уст. никелевый колчедан/
nickel pyrites, инверэрит/inverarite, куб, НМ 3,5—4,0, d4,6—5,0,
желт.-роз., сод. Со [6]
FenO — Вюстит/Wustite, куб., d5,7, черн.
Fe^nO3— а) Маггемит/Maghemite, куб. (у), НМ 5, t/4,88, бур.
б) Гематит/Hematite, уст. красный железняк/red iron ore, триг.
(ос), НМ 5,5-6,5, </4,2-5,2, бур.-красн., сод. Mn, Al, Ti [4, 6].
Красная охра/Red ocher, уст. железный сурик/iron mihium, —
землистый Г. [5]. Почковидная руда/Nodular ore — массивный
гроздевидный Г. Спекулярит/Specularite, уст. железный блеск/
iron glance — зеркальный Г. с ярким металлическим блеском,
т.-сер. Турьит/Turite, уст. тургит/turgite, гидрогематит/hydro-
hematite — Г. с адсорбированной водой, НМ 6,5, d4,29—4,49,
т.-краен.-черн. в) • 1,8Н2О, Ферригидрит/Ferrihydrite, гекс.
235
I. Неорганические вещества
Продолжение пгабд
Fen(OHJ — Амакинит/Amakinite, трип, d3,3, сер.-бел., сод. Mg
FeHIO(OH) — а) Фероксигит/Feroxyhyte, гекс. (8). б) Гётит/Goet-
hite, уст. болотная руда/bod ore, аллхарит/allcharite, ксантоси-
дерит/xanthosiderite, игольчатый железняк/needle iron ore,
ромб, (а), НМ 5,0—5,5, г/4,0—4,37, желт.-бур. [6]. в) Лепидок-
рокит/Lepidocrocite, уст. бурая (или железная) охра/brown (iron)
ocher, рубиновая слюдка/ruby mica, ромб, (у), НМ 4—5, г/4,
красн.-бур., сод. Мп [5, 6]. г) Акаганеит/Akaganeite, тетр., сод. С1.
д) • яН2О, Лимонит/Limonite, уст. гидрогётит/hydrogoethite,
бурый железняк/brown iron ore — гидратированный аморфн.
гётит и/или лепидокрокит с примесями, d 3,6—4,0 [6]. Охра/
Ocher (ochre) — землистая смесь Л. с гематитом, желт. [5]
Fe2P — Баррингерит/Barringerite, гекс, J6,5, сер.-черн., сод. Ni
FemPO4— a) Гетеросит/Heterosite, ромб., бур. б) • 2Н2О, Фосфо-
сидерит/Phosphosiderite, уст. клиноштренгит/clinostrengite, мо- .
нокл., НМ 3,5—4,0, ^2,76, краен. [6]. в) • 2Н2О, Штренгит/Streng-
ite, ромб, г) • ЗН2О, Конинкит/Koninckite, ромб. (?)
Fq^(PO4J — a) Саркопсид/Sarcopside, монокл., сод. Мп.
б) • ЗН2О, Юосфоферрит/РгюБргюГеггке, ромб., сод. Мп.
в) • 4Н2О, Лудламит/Ludlamite, монокл., сод. Mg, Мп. г) • 8Н2О,
Вивианит/Vivianite, уст. железная лазурь/blue iron-earth, монокл.
ытштрикл., НМ 1,5—2,0, d 2,58—2,68, бел.-син., сод. Мп, Mg, Ca,
Fem [5, 6]
Fe"(PO4)F — Цвизелит/Zwieselite, монокл., сод. Мп
Fe"(PO4)OH — Вольфеит/Wolfeite, монокл., сод. Мп
Fe^H(PO4J(OHK— Крыжановскит/Kryzhanovskite, ромб.
FeJ,n(PO4L(OHI5 • 18Н2О — Какоксен/Cacoxenite, гекс.
Fe^nPO4(SO4)OH • 5Н2О — Диадохит/Diadochite, трикл.
FeIIPb4I(As04JCl4— Нилит/Nealite, трикл.
FenPbH(AsO4)OH — Габриельссонит/Gabrielssonite, ромб.
FeinPb^(AsO4JOH — Арсенбраккебушит/Arsenbrackebuschite,
монокл., сод. Zn, H2O
Fe^IIPbII(AsO4J(OHJ— Карминит/Carminite, уст. карминовый
шпат/carmine spar, ромб., ярко-краен.
Fe*IIPbII(AsO4)SO4(OHN- Бёданит/Beudantite, трип, НМ 3,5-
4,5, ^/4,0—4,3, черн., сод. А1
236
I. Неорганические вещества
Продолжение табл.
— Гематофанит/Hematophanite, тетр.
7— Плюмбоферрит/Plumboferrite, трип, кор.-черн.
FenlPb " (РО4JОН • Н2О — Другманит/Drugmanite, монокл., сод. А1
Fe*nPbn(PO4)SO4(OHN- Коркит/Corkite, триг., НМ 3,5-4,5,
^4,3, т.-зел., сод. Си [6]
Fe8PbS8— Шадланит/Shadlunite, куб., сод. Си, Cd
Fe"IPbII(SO4L(OHI2— Плюмбохаросит/Plumbojarosite, триг.,
НМ 2,5—3,5, </3,66, кор.-черн.
(FeIIPb4ISbJII)S14 — Джеймсонит/Jamesonite, монокл. или ромб.,
НМ 2-3, </5,5-6,0, сер.-черн. [6]
Fe2nPb^(SiO4JO — Меланотекит/Melanotekite, ромб.
(FeIIPb^ISn'ISb2/)S14- Цилиндрит/Cylindrite, трикл.,
НМ 2,0-2,5, d 5,42-5,49, черн.-сер.
(FeIIPb^Sn^ISb2^)S14— Франкеит/Franckeite, трикл.,
НМ 2,0-2,5, d 5,55-5,92, сер.-черн.
Fe з1 Pb *< (VO4JO4 - Хейит/Heyite, монокл.
Fe*nPbH(VO4J(OHJ— Мунанаит/Mounanaite, трикл.
Fej^S (x< 0,11) — Пирротин/Pyrrhotite (pyrrhotine),
уст. магнитный колчедан/magnetic pyrites, монокл. или гекс,
НМ 3,5-4,5, </4,58-4,65, т.-желт., сод. Ni, Co, Мп, Си [6]
FeIIS1 _х— Макиноит/Mackinawite, тетр., сод. Ni
FenS — Троилит/Troilite, гекс, НМ 4, d4,6—4,9, т.-желт.
Fen(S2) — а) Пирит/Pyrite, уст. железный (или серный) колчедан/
iron pyrites, куб., НМ 6,0—6,5, af 4,9—5,1, св.-желт., сод. Си, Аи,
Ni, Co [6]. б) Марказит/Marcasite, уст. белый железный
{или гребенчатый, копьевидный, лучистый) колчедан/white iron
(cockscomb, spear, radiated) pyrites, ромб., НМ 6,0—6,5, d4,8—4,9,
желт.-бел., сод. Ni, As [6]. Печёнковый колчедан/Liver pyrites —
плотные массы М. в ассоциации с пиритом [6]
FenSO4— а) • Н2О, Сомольнокит/Szomolnokite, монокл. б) • 4Н2О,
Роценит/Rozenite, монокл., св.-зел. в) • 4Н2О, Хоманит (трад.
гогманнит)/Ногппаппке, трикл., св.-зел. г) • 5Н2О, Сидеротил/Si-
derotil, трикл. д) • 6Н2О, Феррогексагидрит/Ferrohexahydrite, мо-
монокл. е) • 7Н2О, Мелантерит/Melanterite, уст. железный купорос/
copperas, зеленый купорос/green vitriol, монокл., d 1,9, св.-зел.
Пизанит/Pisanite — М., сод. Си
237
I. Неорганические вещества
Продолжение табд
Fe'" (SO4K — а) • 6Н2О, Лаузенит/Lausenite, монокл. б) • 7Н2О,
Корнелит/Kornelite, монокл. в) • 9Н2О, Кокимбит/Coquimbite,
трип, d2,l. г) • 10Н2О, Квенстедтит/Quenstedtite, трикл., желт.
Fe^n(SO4JO • 7Н2О — Амарантит/Amarantite, трикл.
Feln(SO4)OH — а) • 2Н2О, Бутлерит/Butlerite, монокл. или ромб,
б) • 5Н2О, Фиброферрит/Fibroferrite, гекс. (?)
Fe*n(SO4NO(OH) • 20Н2О — Феррикопьяпит/Fenicopiapite, триг.
FeSb2 — Сейняйокит/Seinajokite, ромб.
(FenSb^n)O4— Шафарцикит/Schafarzikite, тетр.
(FenSb^)O6 — Трипугиит/Tripuhyite, тетр.
Fe(Sb)S — Гудмундит/Gudmundite, монокл.
(FenSb*n)S4 — Бертьеит/Berthierite, ромб.
Fe*nSbin(SiO4JOH — Чапманит/Chapmanite, монокл.
FenSe — Ашавалит/Achavalite, гекс.
Fen(Se2) — Ферроселит/Ferroselite, ромб.
Fe2n(Se03K * 4Н2О — Мандариноит/Mandarinoite, монокл., кор.
FenSiO3 — а) Ортоферросилит/Orthoferrosilite, ромб, или монокл,,
НМ 5—6, d 3,96, зел., сод. Mg. б) Пироксферроит/Pyroxferroite,
трикл., сод. Са
Fe^SiO4— Фаялит/Faialite (fayalite), уст. гортонолит/hortonolite,
ромб., НМ 6,5, d4,2—4,4, зел.-желт.
Fem(Si205HH — Феррипирофиллит/FerripyrophyUite, монокл.
Fe'nSi205@HL • 2Н2О — Хизингерит/Hisingeiite, монокл. (?), кор.
Fe^Si2O5(OHL— а) Бертьеин/Berthierine, монокл., сод. Mg, A1
[6]. б) Гриналит/Greenalite, монокл., сод. Fem
Fe 3[ (Si2O5J(OHJ — Миннесотаит/Minnesotaite, монокл., сод. Mg
Fe^S^Oj^^ОЩз— Грюнерит/Grunerite, монокл., НМ 6, rf3,6,
сер.-зел., сод. Mg, Mn, A1. Амосит/Amosite — асбестовидный Г. [4]
Ре^E12О5K(ОНI0— Пиросмалит/Pyrosmalite, триг., сод. Мп, С\
Fen(Te2) — Фробергит/Frohbergite, ромб.
Fe^n(Te03K— Эммонсит/Emmonsite, трикл.
Feni(TeO3)OH • Н2О — Сонораит/Sonoraite, монокл.
238
I. Неорганические вещества
Продолжение табл.
Fein(Te^O5)OH — Маккейит/MacKuyite, тетр.
Fe^n(TeO3JSO4 • ЗН2О — Поит/Poughite, ромб.
(FeIIITlI)S2 — Рагенит/Raguinite, ромб.
FenlVO4- а) • Н2О, Шубнелит/Schubnelite, триг. б.) • 1,25Н2О,
Ферванит/Fervanite, монокл.
FenWO4— а) Вольфрамит/Wolframite, монокл., НМ 4,0—5,5,
d7,2—7,6, сер.-черн., сод. Zn, Mg, Та, Nb [6]. б) Ферберит/Ferber-
ite, монокл., НМ 4,0—5,5, d 7,5—7,6, черн., сод. Mn, Zn, Mg, Та,
Nb[6]
Fe*nZnn(AsO4J(OHJ • 4Н2О - Окуэлаит/Ojuelaite, монокл.
Fe JnZn^(As04K(OHL • 10Н2О — Мапимит/Mapimite, монокл.
(Fe|nZnn)O4 — Франклинит/Franklinite, куб., НМ 6, t/5,3, черн.,
сод. Мп [6]
FenZn^(PO4J • 4Н2О — Фосфофиллит/Phosphophyllite, монокл.,
сод. Мп
FeIIZnIIPbII(As04J • Н2О — Цумкорит/Tsumcorite, монокл.
FeinZnn(SO4JOH • 7Н2О — Цинкоботриоген/Zincobotryogen, мо-
монокл., сод. Mg, Мп
Fe4nZnn(SO4N(OHJ • 18Н2О - Цинкокопьяпит/Zincocopiapite,
трикл.
Ga(OHK — Зёнгеит/Sohngeite, куб., бел.
[Ge(OHN],Fen— Штоттит/Stottite, тетр.
[Ge(OHN](SO4J,Pb^ • ЗН2О — Флайшерит/Fleischerite, гекс.
НВО2 — Метаборит/Metaborite, куб., d 1,7, бел.
Н2О — Лёд/Ice, гекс, НМ 1,5, d0,917, бел. (в толстом слое —
зел.-гол.)
HVO3 см. V2O5 • ЗН2О
4 - а) см. WO3 -Н2О. б) - Н2О, см. WO3 • 2Н2О
4 — Гафнон/Hafnon, тетр., сод. Zr
Hg - Ртуть/Mercury, ниже -38,9 °С: триг, НМ 1, d 14,19, сер.-
бел., выше -38,9 °С: жидк., d 13,6 @ °С), 13,5 B0 °С), серебрис-
серебристо-бел. [6]
239
I. Неорганические вещества
Продолжение табД
9
10
11
12
13
14
15
16
17
(Hg2+)C12 — Каломель/Calomel, уст. роговая ртуть/horn quicksil-
quicksilver, тетр., d 6,56—7,41, бел.
Hg^Cl2O4— Пинчит/Pinchite, ромб.
(Hg2+KC13O(OH) - Эглстонит/Eglestonite, куб.
2 — Терлингваит/Terlinguaite, монокл.
• яН2О — Клайнит/Kleinite, уст. меркураммонит/тег-
curammonite, гекс, сод. SO^~
(Hg2INJSO4— a) Джанеллаит/Gianellaite, куб. б) Мозесит/Moses-
ite, куб., сод. СГ~, МоО^~
HgH0 — Монтройдит/Montroydite, ромб., rf 11, желт.
Hgj1 xS — Гиперциннабарит/Hypercinnabar, гекс, d7,2, кор.-черн.
HgHS — а) Метациннабарит/Metacinnabar, куб., НМ 3, d 7,6—7,8,
черн. Онофрит/Onofrite — М., сод. Se (до 8,4%). б) Киноварь/
Cinnabar, неправ, циннабарит/cinnabarite, триг, НМ 2,0—2,5,
d 8,0—8,2, ярко-краен. [6]. Коралловая руда/Coral ore —
К., сод. глину и/или органические примеси [6]. Печёнковая руда/
Hepatic ore — красн.-кор. плотные массы К., сод. битуминозные
примеси [6]
Hg^S2Cl2— Кордероит/Corderoite, куб.
Hg3I(SO4)O2— Шюттеит/Schuetteite, гекс.
(HgnSb3IISbv)S8 — Ливингстонит/Livingstonite, монокл.
HgnSe — Тиманит/Tiemannite, куб., НМ 2,5, d 8,2, фиол.-черн.,
сод. Cd, S
HgHTe — Колорадоит/Coloradoite, куб., d 8,4, сер.-черн.
(HgIITlIAsIII)S3 — а) Кристит/Christite, монокл. б) Рутьеит/Routh-
ierite, тетр.
(HgjTlJSbJnAs'n)S20- Врбаит/Vrbaite, ромб., </5,3, сер.-черн.
In — Индий/Indium, тетр., НМ 1, d7,3, бел.
1п(ОНK — Джалиндит/Dzhalindite, куб., </4,3, бел.
Ir — Иридий/Iridium, куб., d22,69 бел. Осмирид/Osmiridium, уем
невьянскит/nevyanskite — сплав И. (до 77%) с осмием, куб., НМ
6,5—7,0, d 18,6—21,6, св.-сер., сод. Pt, Rh, Fe, Cu [6]. Рутеносмй
рид/Ruthenosmiridium — сплав И. с осмием к рутением, куб. Г№
тинистый иридий/Platiniridium — сплав И. с платиной, куб. [6]
240
I. Неорганические вещества
Продолжение табл.
IrAs2 — Иридарсенйт/Iridarsenite, монокл.
Ir(As)S — Ирарсит/Irarsite, куб., сод. Ru, Rh, Pt
KAl2(AlSi3O10)(OHJ — a) Мусковит/Muscovite, уст. калиевая (или
обыкновенная) слюда/potash (common) mica, московское окон-
оконное стекло/moscovian window pane, астролит/astrolite, монокл.,
НМ 2,5-3,0, d2,77-2,88, св.-желт., сод. Na, Ba, Li, V, Mn, Mg,
Fe, F~ [2]. Серицит/Sericite — М. с мелкими чешуйчатыми крис-
кристаллами, сод. парагонит, иллит Фуксит/Fuchsite — М., сод. Сг.
б) • Н2О, Гидрослюда/Hydromica, монокл., сод. Na, H3O+.
в) • Н2О, Иллит/Illite, уст. гидромусковит/hydromuscovite, мо-
монокл., d 2,64-2,69, бел., сод. Н3О+, Mg, Fe
KAl2(CrniSi3O10)(OHJ— Марипозит/Mariposite, монокл.
К3А15(НРО4N(РО4J • 13Н2О — Франкоанеллит/Francoanellite, триг.
KA12(PO4JF • 4Н2О — Миньюлит/Minyulite, ромб.
КА13(РО4KОН • 9Н2О — Таранакит/Taranakite, триг., сод. Na,
NHj,Ca,Fe
KA1(SO4J- a) • 11Н2О, Калинит/Kalinite, монокл. (?). б) • 12Н2О,
Калиевые квасцы/Potassium (potash) alum, куб., d 1,7, бел.
KA13(SO4J(OHN — Алунит/Alunite, уст. калафатит/calafatite,
квасцовый камень/alumstone, горные квасцы/rock alum, квасцо-
квасцовый шпат/alum spar, триг, НМ 3,5—4,5, d2,6—2,8, бел., сод. V,
Ga[6]
K(AlSiO4) — а) Калиофилит/Kaliophilite, гекс. б) Калсилит/Kalsil-
ite, гекс, НМ 6, d2,6—2,63, бел., сод. Na. в) Тетракалсилит/Tet-
rakalsilite, гекс, сод. Na. г) Трикалсилит/Trikalsilite, гекс, сод. Na
K(AlSi2O6) — Лейцит/Leucite, уст. амфиген/amphigene, тетр.,
НМ 5,5-6,0, d 2,45-2,50, сер. [6]
K(AlSi3O8), калиевые полевые шпаты/potash feldspars — а) Орток-
лаз/Orthoclase, уст. фельсит/felsite, монокл., НМ 5, d2,56, бел.,
сод. Na, Ba, Rb, Fe. Aдyляp/Adular(ia) — бцв. прозрачный О. [1].
б) Санидин/Sanidine, монокл., НМ 6, d2,57—2,58, бел., сод. Na,
Ba, Са. Ледяной шпат/Ice spar — бцв. прозрачный С. в) Микрок-
лин/Microcline, уст. барбьеит/barbierite, трикл., НМ 6, d2,56,
бел., сод. Na, Са, Ba, Rb, Cs, Fe. Амазонит/Amazonite, уст. ама-
амазонский камень/Amazon stone — гол.-зел. М., сод. Си, РЬ [1]
K2(Al2Si7019) • 9Н2О — Полингит/Paulingite, куб., НМ 5, бел.
241
I. Неорганические вещества
Продолжение mafy
K28)(Al9Si2306J • 23Н2О — Мерлиноит/Merlinoite, ромб., сод. Са,
Ва, Na
КВ5О8 • 4Н2О — Сантит/Santite, ромб.
KBa(AlSi3O8K — Гиалофан/Hyalophane, монокл. или трикл., НМ
6,0-6,5, d 2,6-2,8, бел.
KBa2Ti^v(AlSi5018) • ЗН2О — Джонсит/Jonesite, ромб., сод. Na
KCa2Be2Al(Si12O30) • 0,5Н2О — Миларит/Milarite, гекс, бел.
К2Са(СО3J — а) Фэрчайлдит/Fairchildite, гекс. б) Бючлиит/
Buetschliite, триг.
K2Ca2Cun(SO4L • 4Н2О — Лейтонит/Leightonite, трикл.
KCa2Fe "Реш(А1813ОиJС12 — Дашкесанит/Dashkesanite, монокл.,
черн.
К2 5Caj 5Mg2(Al5Si13O36J' 28Н2О — Маццит/Mazzite, гекс, сер.-бел.
K2Ca2Mg(SO4L • 2Н2О — Полигалит/Polyhalite, трикл., НМ 3,5,
?/2,78, сер.-бел. [3]
K2Ca(SO4J • Н2О — Сингенит/Syngenite, уст. калусит/kaluszite,
монокл., НМ 2,5, ?/2,57, бел.
K2Ca5(SO4N • Н2О — Гёргеиит (трад. roprenT)/Goergeyite, мо-
монокл., НМ 3,5, ?/2,77, бел.
KCa4(Si2O5LF • 8Н2О — Фторапофиллит/Fluorapophyllite, тетр.,
НМ 5, ?/2,37, св.-желт., сод. Na
KCa2(Si205J0H • Н2О — Чароит/Charoite, монокл. (?), НМ 5,5,
t/2,5—2,6, фиол., сод. Ва, Sr, Na, F~ [1]
KCa4(Si205L0H • 8H2O — Гидроксилапофиллит/Hydroxylapophyl-
lite, тетр., НМ 4,5, ?/2,33, бел., сод. Na
K2Ga(U3vlO10J • 9Н2О — Рамоит/Rameauite, монокл.
КС1 — Сильвин/Sylvite, куб., НМ 2, d 1,99, бел., краен., гол. или
желт. [6]. Сильвинит/Sylvinite — смесь С. с галитом
К2Сг04 — Тарапакаит/Tarapacaite, ромб., ?/2,7, желт.
?^2Сх2О1 — Лопесит {трад. лопецш^/Ьбрегке, трикл., d 2,6,
оранж.-краен.
KCu^Al(SiO3)9 • 6Н2О — Ахоит/Ajoite, трикл., сод. Na
K2Cun(SO4J • 6Н2О — Цианохроит/Cyanochroite, монокл.
242
I. Неорганические вещества
Продолжение табл.
K2Cu1-(SO4)Cl2 — Хйоротионит/Chlorothionite, ромб.
KF — Кароббиит/Carobbiite, куб., d2,4, бел.
KFe2IAl(Si05JF2— Сцдерофшшит/81деюр11уШ1е, монокл., сод. ОН"
KFe'IAl3(Al2Si10O30) • Н2О — Осумилит/Osumilite, гекс, </2,64,
син., сод. Na, Mg
KFe^n(AlSi3O10)(OHJ • Н2О — Глауконит/Glauconite, монокл.,
НМ 2-3, rf2,2-3,0, зел., сод. Na, Ca, Mg, Fe11 [3, 5, 6]
KFe"(AlSi3O10)(OHJ — Аннит/Annite, монокл., сод. F~
KFe53(AlSi17O42)(OHI4— Зуссманит/Zussmanite, триг.
KFe4n(AsO4K(OHL • F—7)Н2О — Фармакосидерит/Pharmacosid-
erite, уст кубовая руда/cube ore, куб., НМ 2,5, d 2,8—2,9, т.-зел.,
сод. Р
(KFenFeni)S3 — Расвумит/Rasvumite, ромб.
(K3Fe^Fe*n)S14— Бартонит/Bartonite, тетр.
K2Fe^Fe4H(SO4I2 • 18Н2О — Вольтаит/Voltaite, куб.
KFe^Nbv(PO4JO2 • 2Н2О — Олмстедит/Oimsteadite, ромб., сод.
Та
KFe^n(PO4JOH • 2Н2О — Лейкофосфит/Leucophosphite, монокл.,
бел.
KFeIH(SO4J — а) Явапайит/Yavapaiite, монокл. б) • Н2О, Краусит/
Krausite, монокл. в) • 4Н2О, Голдичит/Goldichite, монокл., т.-желт.
K5Fe*n(SO4NO • 10Н2О — Метавольтин/Metavoltine, гекс.
KFe^n(SO4J(OHN— Харосит (трад. npo3HT)/Jarosite, уст. ютаит/
utahite, триг, НМ 2,5—3,5, d 3,1—3,2, т.-желт., сод. Al, Na
КНСО3 — Калицинит/Kalicinite, монокл., ^2,1, бел.
КН2РО4 — Арчерит/Archerite, тетр., J2,3, бел., сод. NH4
KHSO4— Меркаллит/Mercallite, ромб., d2,3, бел.
KLi3Al(AlSi3O10)F2 — Лепидолит/Lepidolite, монокл., триг. или
Ромб., НМ 2,5-3,5, ^2,8-2,9, роз.-бел., сод. ОН" [6]
KLi2Al(Si205JF2 — Полилитионит/Polylithionite, монокл., сод. F~
KLiFenAl(AlSi3O10)F2 — Циннвальдит/Zinnwaldite, монокл., НМ
2,5-4,0, rf2,9-3,02, св.-фиол., сод. Rb, Fe111, Mn, ОН" [6]
KLiMg2(Si205JF2 — Тейниолит/Taeniolite, монокл.
243
Неорганические вещества
Продолжение табл
KLiMnnAl(AlSi301())F2— Масутомилит/Masutomilite, монокл.,
сод. ОН"
KLi3Sn2v(Si12O30) — Браннокит/Brannockite, гекс, бел.
K2Li2ZrIVFe"(Si^O^) ~~ Согдианит/Sogdianite, гекс, черн., сод.
Na,Al
KMg2Al3(Al2Si1003o) • Н2О — Магний-осумилит/Magnesium osumi-
lite, гекс, зел.-син., сод. Na, Ре
KMg3(AlSi3O10)F2 — Флогопит/Phlogopite, уст. магнезиальная
слюда/magnesian mica, монокл., НМ 2—3, d2,86, зел.-бур., сод.
Na, Rb, Cs, Ba, Fe, Mn, OH"
KMg3(AlSi3O10)(OHJ— Бьоит (трад. 6noTHT)/Biotite, монокл.,
НМ 2,5—3,5, d2,7—3,3, кор.-черн., сод. F" [2]. Лепидомелан/Lep-
idomelane, уст. хотонит (трад. xorroHHT)/haughtonite — Б., бога-
богатый Fe [6]. Манганофиллит/Manganophyllite — Б., сод. Мп
K2Mg(CO3J • 4Н2О — Бейлиссит/Baylissite, монокл.
KMgCl3 • 6Н2О — Карналлит/Camallite, ромб., НМ 2,5, d 1,6, бел.,
сод. Rb, Cs, Br [3, 6]
KMgFeI]I(Si205J@HJ — Селадонит/Celadonite, уст. кмаит/
kmaite, монокл., сод. А1
K2Mg(SO4J — а) • 4Н2О, Леонит/Leonite, уст. калиблёдит/kali-
blodite, монокл., НМ 2,5—3,0, dl,2, бел. б) • 6Н2О, Пикромерит/
Picromerite, уст. шёнит/schonite (schoenite), монокл., НМ 2,5,
?/2,03, бел.
K2Mg2(SO4K — Лангбайнит/Langbeinite, куб., НМ 3,5—4,0, </2,83,
бел.
KMg(SO4)Cl • B,75-3,0)Н2О - Каинит/Kainite, монокл., НМ
2,5-3,0, d2,0-2,2, бел. [3,6]
KMg(V^O14) • 8Н2О — Хаммерит/Hummerite, трикл.
(К2МпиМп^у)О14— Криптомелан/Cryptomelane, монокл., сер. [61
K2Mn^(SO4K— Манганолангбайнит/Manganolangbeinite, куб.
K2Mn^(Si205K@HN— Парсеттенсит/Parsettensite, гекс.
KNH4SO4 — Тейлорит/Taylorite, ромб.
KNO3 — Селитра/Niter, уст. калийная (или индийская) селитра/
potash (Indian) saltpeter, ромб., НМ 2,0—2,5, af 2,1, бел. [3, 6]
244
I. Неорганические вещества
Продолжение табл.
KNa2Al4(B6O15)Cl3 • 13Н2О — Сатимолит/Satimolite, ромб.
Kq 22Na0 78(AlSi04) ~~ Нефелин/Nephelite (nepheline), гекс, НМ
5,5—6,0,' ^2,55—2,66, бел., сод. Са [6]
K4Na4(Al8Si8O32) * ЮН2О — Амицит/Amicite, монокл.
KNa22(CO3J(SO4)9Cl - Ханксит/Hanksite, гекс.
K4Na2Ca9Al18(HPO4I2(PO4N(OHK6 • 8Н2О - Инглишит/EngUshite,
монокл.
K2Na2Ca(Al3Si5O16J • 12Н2О — Филлипсит/Phillipsite, монокл.,
НМ 4,0—4,5, rf2,2, сер.-бел., сод. Ва, Sr
K2Na2Ca] 5Mg(Al3Si9024K • 27Н2О — Эрионит/Erionite, уст. оф-
фретит/offretite, гекс, d2,02, бел.
K2NaCa2(TiIVSi70I9HH — Тинаксит/Tinaksite, трикл.
KNaCun(Si205J — Литидионит/Lithidionite, трикл.
KNa5FeI14Al(PO4I2OH ~ Аррохадит/Arrojadite, монокл., сод. Ва,
Са, Mn, Mg, F"
K3Na8FeI!1(SO4N(OHJ • 10Н2О - Унгемахит/Ungemachite, гекс.
KNaFe]I(Si205J— Фенаксит/Fenaksite, трикл.
KNa3Li2Fe2H(Si12O30) • Н2О — Сугилит/Sugilite, гекс, т.-кор.
KNa2LiTi2vFe2I(SiO3)8— Нептунит/Neptunite, монокл.
KNa2LiTi ™ Mn ^ (SiO3)8 — Манган-нептунит/Mangan-neptunite,
монокл.
KNa2LiZrlvMn^(Si12O30) — Дарапиосит/Darapiosite, гекс, черн.,
сод. Zn
K3Na7Mg2(SO4N(NO3J • 6Н2О — Хамберстонит/Humberstonite,
уст. чилийский лёвеит/Chile loeweite, триг.
K2Na4Mg9(Si12O30J — Айфелит/Eifelite, гекс.
KNa5MnIII4Al(PO4I2OH • Н2О — Дикинсонит/Dickinsonite, мо-
монокл., сод. Ва, Са, Fe, Mg, F~
(K2NaNb2/)O6F — Калипирохлор/Kalipyrochlore, куб., желт., сод.
Та, П, ОН-
K3Na(SO4J — Афтиталит/Aphthitalite, уст. глазерит/glaserite,
гекс,НМЗ, J2,66, бел.
K2Pbn(SO4J — Пальмьеит/Palmierite, триг, сод. Na
245
I. Неорганические вещества
Продолжение табд
96
97
98
99
100
101
102
103
ЮЗА
104
105
106
107
108
109
ПО
111
112
K2Sr(SO4J — Калистронцит/Kalistrontite, трип
K3Na(UO2+)(CO3K * Н2О — Гримселит/Grimselite, геке.
K2SO4 — Арканит/Arcanite, ромб., d2,6, бел.
(KTi*vFeni)O16 — Прайдерит/Priderite, тетр., сод. Ва
KT1HI(HSO4L • 5,5Н2О — Монсмедит/Monsmedite, куб.
K2U3O10 • 4Н2О — Агриньеит/Agrinierite, ромб., сод. Са, Sr
K2U6O19 • 11Н2О — Компреньякит/Compreignacite, ромб.
K(UO|+)AsO4 • 4Н2О — Абернатиит/Abernathyite, тетр.
K(UOf )(H3O+)SiO4 • 2,5Н2О - Болтвудит/Boltwoodite, ромб.
K(UO^+)PO4 • ЗН2О — Метаанколеит/Meta-ankoleite, тетр.
K4(UOf N(SO4K(OHI0 • 16Н2О - Циппеит/Zippeite, уст. урано-
урановые цветы/uranium bloom, ромб.
K2(UOf J(Si205K • 4H2O - Уиксит/Weeksite, ромб.
K(UO2+)VO4 • 1,5Н2О — Карноит {трад. карнотит)/СатоШе, мо-
нокл., НМ 2, dS, ярко-желт. [6]
KVUIAl(AlSi3O10)(OHJ— Росколит (трад. pocKoanHT)/Roscoelite,
монокл., сер.-зел. [6]
i3O10)(OHJ — Хендриксит/Hendricksite, монокл., сод. Мп
K2ZrIV(Si207) — Хибинскит/Khibinskite, монокл.
K2ZrIV(Si309) — Вадеит/Wadeite, гекс.
K2ZrIV(Si205K — Дейлиит/Dalyite, трикл.
1
La^n(CO3K • 8Н2О — Лантанит/Lanthanite, ромб., НМ 2,5—3,0,
d2,6—2,74, св.-роз., сод. Ln
Lain(CO3)F — Лантанобастнесит/Lanthanobastnasite, гекс, желт.,
сод. Се [6]
LiAl(BSi3O10)(OH)8— Манандонит/Manandonite, монокл., НМ
2,5, d 2,6-3,3, зел.
LiAl(PO4)F — Амблигонит/Amblygonite, трикл., НМ 6,0—6,5,
d3,0—3,1, бел., сод. V, ОН" [1, 6]. Фремонтит/Fremontite,уст.
трамблигонит/natrambligonite — А, богатый Na [6]
LiAl(PO4)OH — Монтебраит (трад. MOHTe6pa3HT)/Montebrasite,
трикл., НМ 5,5—6,0, d3, желт.-бел., сод. Na, F~ [6]
246
I. Неорганические вещества
Продолжение табл.
LiAl(SiO4) — Эвкрйптит/Eucryptite, триг.
LiAl(SiO3J — а) Верджилит/Virgilite, гекс. б) Сподумен/Spo-
dumene, уст. трифан/triphane, монокл., НМ 6,5—7,0, d3,03—3,33,
св.-сер., сод. Fe [6]. Гидценит/Hiddenite — ярко-зел. прозрачный
С. [1]. Кунцит/Kunzite — прозрачный С. [1]. в) • Н2О, Бикитаит/
Bikitaite, монокл., бел.
Li(AlSi4O10) — Петалит/Petalite, монокл., НМ 6,0—6,5, </2,4, сер.-
бел., сод. Na, К, Са [6]
Li2Be(Si04) —Либерит/Liberite, ромб.
Li2CaAl8(BO3K(Si6O18)O3(OH) — Лидцикотит/Liddicoatite, триг.,
НМ 7,5, d 3,0-3,4, бур., сод. F"
LiCaAl2(BeAlSi2O10)(OHJ — Битиит/Bityite, монокл.
Li2CaAl4(PO4L(OHL— Бертоссаит/Bertossaite, ромб., сод. Na, F~
Li2Ca3Be3(SiO4KF2 — Сянхуалит/Hsianghualite, куб.
LiFenPO4— Трифилин/Triphylite, ромб., НМ 4—5, d3,3—3,5,
кор., сод. Мп
Li3Fe^n(PO4L— Феррисиклерит/Ferrisicklerite, ромб., сод. Мп
LiFem(PO4)OH — Таворит/Tavorite, трикл.
Li2Mg3Al2(Si4OnJ(OHJ — Хольмквистит/Holmquistite, ромб, или
монокл., сер.-бел., сод. Fe
(LiMnIVAl)O2(OHL — Литиофорит/Lithiophorite, монокл.
LiMnnPO4— а) Литиофилит/Lithiophilite, ромб., роз., сод. Fe11 [6].
б) Сиклерит/Sicklerite, ромб., сод. Fem
Li3PO4 — Литиофосфатит/Lithiophosphatite, ромб., </2,5, бел.
Li2SrAl4(PO4L(OHL — Палермоит/Palermoite, ромб., сод. Na, Са
Mg2Al3(AlSi5018) — Кордьеит (трад. кордиеритУСо^егйе, уст.
иолит/iolite, дихроит/dichroite, ромб., НМ 7,0—7,5, d 2,6—2,66,
гол.-желт., сод. Fe [4]. Водный сапфир/Watersapphire — син. К. [1]
Mg5Al(AlSi3O10)(OH)8 — Клинохлор/Clinochlore, монокл., НМ
1,5—2,5, d2,6—3,3, зел., сод. Fe"
Mg5Al2(AlSi3OnJ(OHJ — а) Магнезиожедрит/Magnesiogedrite,
монокл., НМ 5,5—6,0, d2,85—3,57, сер.-бел. б) Антофиллит/Ап-
thophyllite, ромб., НМ 5,5—6,0, d2,85-3,2, бур., сод. Na, Fe, Mg,
Мп, F~, Cl-
247
I. Неорганические вещества
Продолжение mafai
Mg8Al(AlSi7O20)(OHI0— Кулькеит/Kulkeite, монокл.
Mg3Al6(AlSi2O10)(Si2O7)O4(OH) — Корнерупин/Kornerupine,
ромб., НМ 6,5, d 3,27, бел. Призматин/Prismatine — зел. К., сод
Fe[l]
MgAl(BO4) — Синхалит/Sinhalite, ромб.
MgAl3(BO3)(SiO4)O2 — Грандидьеит/Grandidierite, ромб., сод. Fe
Mg6Al2CO3(OHI6 • 4Н2О — а) Манассеит/Manasseite, гекс, син.-
бел. б) Гидроталькит/Hydrotalcite, триг., НМ 2, d2,05, бел.
Mg5Al3Cl3(OHI6 — Хлорманассеит/Chlormanasseite, гекс, сод. Fe,
он-, со 2-
(MgAl2)O4 — а) Шпинель (благородная)/8рте1 (precious), куб.,
НМ 7,5—8,0, я? 3,55, св.-зел. (гол. прозрачный [1]). Пикотит/
Picotite, уст. хромовая шпинель/chrome spinel — краен, прозрач-
прозрачная Ш., сод. Сг [1]. б) Таффеит/Taaffeite, триг. или гекс, сод. Be
(MgAl4)O7 — Хёгбумит/Hogbomite (hoegbomite), гекс, черн., сод.
Fe,Ti
Mg3Al(OH)9 • 2Н2О — Майкснерит/Meixnerite, триг.
MgAl2(PO4J(OHJ — Лазулит/Lazulite, уст. голубой {или лазоре-
лазоревый, лазурный) шпат/blue (azure) spar, монокл., НМ 5,5—6,0,
d 3,0—3,1, св.-гол., сод. Fe11 [1]
Mg3Al4(PO4L(OHN • 2Н2О — Созалит/Souzalite, монокл.
Mg5Al12(PO4)8(OHJ2 • 32Н2О — Олдерманит (трад. альдерманит)/
Aldermanite, ромб.
MgAl2(SO4L • 22Н2О — Пикерингит/Pickeringite, уст. магнезиаль-
магнезиальные квасцы/magnesia alum, монокл., НМ 1,5, d 1,8, бел., сод. Fe, Mn
Mg3Al2(Si04K— Пироп/Pyrope, куб., НМ 6,5—7,5, rf3,58, т.-красн.
[1,4]
MgAl2(SiO3J(OHL — Магнезиокарфолит/Magnesiocarpholite, ромб.
Mg3(As04J • 8Н2О — Хёрнесит/Hornesite (hoernesite), монокл., бел.
Mg5AsO4(OHO — Магний-хлорофиникит/Magnesium chloroph®-
nicite, монокл., сод. Mn
Mg(BO2J • ЗН2О — Пинноит/Pinnoite, тетр.
Mg(B3O5J- а) • 5Н2О, Аксаит/Aksaite, ромб, б) • 7,5Н2О, Макал-
листерит/McAllisterite, триг.
248
I. Неорганические вещества
Продолжение табл.
Mg2B2O5 — а) Суанит/Suanite, уст. магниоборит/magnioborite,
монокл. б) • 15Н2О, Адмонтит/Admontite, монокл.
Mg2B6On • 15Н2О — Курнаковит/Kurnakovite, трикл. [6]
Mg3(BO3J — Котоит/Kotoite, ромб.
Mg3(B7O12)Cl(O) — Борацит/Boracite, ромб., НМ 7,0—7,5, d2,9—
3,0, гол.-бел., сод. Fe, Mn [6]
Mg5(BO3)O(OHM • 2Н2О — Уайтманит/Wightmanite, монокл.
Mg3B2(PO4J(OHN • 5Н2О — Люнебургит/Luneburgite, монокл.
MgCO3 — a) Магнезит/Magnesite, уст. тальковый шпат/talc spar,
трип, НМ 3,7—4,3, d3, сод. Ni [4, 6]. Бройн(н)ерит/Вгеип(п)егИе,
уст. мезитит/mesitite — смесь М. с сидеритом C0—50%), d 3,3—
3,45, желт.-кор. б) • 2Н2О, Баррингтонит/Barringtonite, трикл.,
бел. в) • 5Н2О, Лансфордит/Lansfordite, монокл.
MgC2O4 • 2Н2О — Глушинскит/Glushinskite, монокл. ф), d 2,4, бел.
Mg2CO3(OHJ — а) Артинит/Artinite, монокл., НМ 2,5, J2, бел.
б) Макгиннессит/McGuinnessite, монокл., сод. Си
Mg5(CO3L(OHJ — а) • 4Н2О, Гидромагнезит/Hydromagnesite,
монокл., НМ 3,5, d2,1— 2,3, бел. б) • 5Н2О, Дипингит/Dypingite,
монокл. (?)
MgCe2n(CO3L — Сахамалит/Sahamalite, монокл.
MgCl2— а) Хлоромагнезит/Chloromagnesite, трип, d2,3, бел.
б) • 6Н2О, Бишофит/Bischofite, монокл., НМ 1—2, Л ,6, бел., сод.
Вг[6]
Mg6Cr2nCO3(OHI6 • 4Н2О — а) Барбертонит/Barbertonite, гекс,
НМ 1,5—2,0, г/2,1, красн.-роз. б) Штихтит/Stichtite, триг.,
краен.-роз.
(MgCr*n)O4 — Магнезиохромит/Magnesiochromite, уст. пикрох-
ромит/picrochromite, куб., г/4,43, краен. [6]
Mg3Cr2n(Si04K— Кноррингит/Knorringite, куб., НМ 6,0—7,5,
</3,76,зел. [4]
Mg2Cu ^ СО3(ОНN • 2Н2О — Каллаганит/Callaghanite, монокл.
Mg2Cu2I(PO4J(OHJ • 5Н2О — Ниссонит/Nissonite, монокл.
MgF2— Селлаит/Sellaite, тетр., d3,\, бел.
(Mg075FeJI25Al2)O4— Плеонаст/Pleonaste, уст. цейлонит/ceylonite
или ceylanite (франц.), куб., кор.-зел.
249
Неорганические вещества
Продолжение табА
42
43
44
45
46
47
48
49
50
51
52
53
54
55
56
57
57А
58
59
60
61
62
250
Mg2Fem(BO5) — а) Азопроит/Azoproite, ромб., сод. Fe11, Ть
б) Людвигит/Ludwigite, ромб.
Mg6FemCO3(OHI3 * 4Н2О — Бруньятеллит/Brugnatellite, трип,
НМ 2, d2,14, ярко-краен., сод. Мп
Mg6Fe2nCO3(OHI6 • 4Н2О — а) Шёгренит/Sjogrenite, гекс, кор.
б) Пироаурит/Pyroaurite, ромб., кор.
Mg4Fem(Cl)O(OH)8 • B-4)Н2О - Айоваит/Iowaite, гекс.
(MgFe2H)O4— Магнезиоферрит/Magnesioferrite, куб., d4,5, т.-кор.
(Mg7Fe4n)O13 • 10Н2О — Мускоксит/Muscoxite, триг.
MgFeHI(PO4)OH — Саттерлиит/Satterlyite, триг.
(Mg3FeJI)S4(OHN — Хаапалаит/Haapalaite, гекс, сод. Ni
(Mg5Fe^)S6(OHI0 — Точилинит/Tochilinite, монокл.
MgFein(SO4JOH • 7Н2О — Ботриоген/Botryogen, монокл.,
НМ 2,0—2,5, d2,\4, оранж.-красн.
MgFe4n(SO4N(OHJ • 20Н2О — Магнезиокопьяпит/Magnesiocopi-
apite, трикл.
MgFen(Si03J — Гиперстен/Hypersthene, ромб, или монокл.,
НМ 5-6, </3,3-3,5, зел.-бур., сод. Fe, Al, Ca, Mn, Ti, Cr, Ni [1]
Mg3Fe2n(Si04K— Мейджорит/Majorite, куб., НМ 6,0—7,5,
d 3,2—4,3, зел.-бур., сод. А1 [4]
MgHAsO4— а) • 4Н2О, Брассит/Brassite, ромб., бел. б) • 7Н2О,
Рёсслерит/Roesslerite (roBlerite), монокл., t/1,94, бел.
Mg(HCO3)OH • 2Н2О — Несквегонит/Nesquehonite, монокл.
MgHPO4— а) • ЗН2О, Ньюбериит/Newberyite, ромб., d2,1, бел.
б) • 7Н2О, Фосфоррёсслерит/Phosphorroesslerite, монокл., бел.
MgMnJ1 Al5(VO4)(SiO4JSi3O10(OHN - Арденнит/Ardennite,
ромб., НМ 6—7, d 3,58—3,66, желт.-кор., сод. As
MgMn xl (AsO4J(OHL • 4H2O - Акрохордит/Akrochordite, монокл»
Mg2Mnin(BO3)O2 — Пинакиолит/Pinakiolite, монокл. или ромб.
Mg6Mn2nCO3(OHI6 • Н2О — Дезотелит/Desautelsite, триг.
Mg5Mn2I(Si4011J@HJ— Тиродит/Tirodite, монокл., НМ 5-6,
d 3,1—3,6, красн.-кор.
(MgMnnZnn)SiO4(OHJ — Герстманит/Gerstmannite, ромб.
I. Неорганические вещества
Продолжение табл.
Mg(NH4J(HPO4J • 4Н2О — Шертелит/Schertelite, ромб.
Mg3(NH4J(HPO4L • 8Н2О - Ханнейит/Hannayite, трикл.
MgNH4PO4— а) • Н2О, Диттмарит/Dittmarite, ромб., бел.
б) • 6Н2О, Струвит/Struvite, ромб., d 1,7, бел.
Mg(NH4J(SO4J • 6Н2О — Буссенгоит/Boussingaultite, монокл.,
Л,7, бел.
Mg(NO3J * 6Н2О — Нитромагнезит/Nitromagnesite, уст. магнези-
магнезиальная селитра/magnesia saltpeter, монокл., d 1,6, бел.
(MgNbpOg— Магноколумбит/Magnocolumbite, ромб., сод. Fe,
Мп, Та [6]
MgO — Периклаз/Periclase, куб., НМ 2,5, d3,56—3,68, бел., сод.
Fe, Zn, Mn, Ni
Mg(OHJ — Брюсит (трад. 6pycHT)/Brucite, триг., НМ 2,5, d2,39,
бел., сод. Zn [4]. Манганбрюсит/Manganbrucite — кор.-сер. Б.,
сод. Мп [4]. Немалит/Nemalite, уст. ферробрюсит/ferrobrucite —
волокнистый Б., сод. Fe, зел.-бел. [4]
Mg3(PO4J • 8Н2О — а) Бобьеррит/Bobierrite, монокл., d 1,6, бел.
б) Барицит/Baricite, монокл., сод. Fe
Mg2(PO4)F — а) Вагнерит/Wagnerite, монокл., сод. Fe, желт,
б) Магниотриплит/Magniotriplite, монокл., сод. Fe, Mn
Mg2(PO4)OH — а) Альтхаусит/Althausite, ромб., сод. F~.
б) Хольтедалит/Holtedahlite, ромб.
Mg2Pb 2! Si2O7(OHJ — Молибдофиллит/Molybdophyllite, гекс,
черн.
MgS — Нинингерит/Niningerite, куб., */2,8, бел., сод. Fe, Mn
MgSO4 — а) • Н2О, Кизерит/Kieserite, монокл., НМ 3,0—3,5,
d2,57, бел. [6]. б) • 4Н2О, Старкиит/Starkeyite, монокл. в) • 5Н2О,
Пентагидрит/Pentahydrite, трикл. г) • 6Н2О, Гексагидрит/Hexahy-
drite, уст. сакиит/sakiite, монокл., d 1,75, бел. д) • 7Н2О, Эпсомит/
Epsomite, уст. эпсомская (или горькая, английская) соль/Epsom
(bitter, English) salt, райхардтит/reichardtite, ромб., НМ 2,0—2,5,
rf 1,68, бел., сод. Ni, Mn, Fe, Zn [6]
(MgSb^Og— Бюстрёмит/Bystromite, тетр.
MgSiO3— а) Пиджинит (трад. mcKOHHT)/Pigeonite, монокл., НМ
6, d 3,17—3,46, зел.-кор., сод. Fe, Ca. б) Энстатит/Enstatite, ромб.
или монокл., НМ 5,5, d3,2l, сер.-желт. Бронзит/Bronzite — зел.-
бел. Э., сод. Fe
251
I. Неорганические вещества
Продолжение табд
79
80
81
82
83
84
85
86
87
88
89
90
91
92
Mg2Si04— Форстерит/Forsterite, ромб., НМ 7, of 3,22, желт. [4].
Перидот/Peridot — зел. Ф. [1]. Хризолит/Chrysolite — золотис-
то-зел. Ф., сод. Fe [1]
Mg3(Si04)F2 — Норбергит/Norbergite, ромб., НМ 6,5, d 3,1—3,2,
оранж.-кор., сод. Fe, OH~
Mg3Si205@HL — а) Антигорит/Antigorite, монокл. или ромб., НМ
2,5—3,5, </2,5—2,6, бел.-желт., сод. Fe. Пикролит/Picrolite — ас-
бестовидный А. б) Лизардит/Lizardite, уст. офит/ophite, монокл.,
НМ 3, г/2,6, бел. [1]. в) Хризотил/Chrysotile, уст. хризотил-асбест/
chrysotile-asbestos, монокл. или ромб., НМ 2,5, J2,55, желт. [2]
Mg3(Si205J@HJ — а) Стивенсит/Stevensite, монокл. б) Тальк/
Talc, монокл. шштрикл., НМ 1, г/2,58—2,83, бел. [4, 6]. Стеатит
(уст. жировик)^еа^е, уст. мыльный камень/soapstone, фран-
французский мел/French chalk — плотный Т. [1]. в) • 4Н2О, Вермику-
лит/Vermiculite, монокл., НМ 1,0—1,5, г/2,3—2,7, зел.-кор., сод.
Fe, Ca, Al, Ni [2, 5]
Mg4(Si205K@HJ • 6Н2О — Сепиолит/Sepiolite, уст. морская пен-
пенка/sea foam (sea froth, meerschaum), монокл., НМ 2,0—2,5, d2,
бел. [1]
Mg5(Si308J@HJ — Джимтомпсонит/Jimthompsonite, ромб, или
монокл., сод. Fp
Mg5(Si205L@HJ • 8Н2О — Палыгорскит/Palygorskite, уст. атта-
пульгит/attapulgite, горная кожа/mountain leather, монокл., НМ
2,0-2,5, </2,2-2,36, бел., сод. А1 [2]
Mg7(Si4OnJ(OHJ— Каммингтонит/Cummingtonite, монокл.,
НМ 5,6, d3,1—3,6, сер., сод. Fe, Mn, A1. Монтазит/Montasite —
торговое название асбестовидного К. [4]
Mg17(Si]0O27J(OHN— Честерит/Chesterite, ромб., сод. Fe
Mg5(SiO4J(OH)F — Хондродит/Chondrodite, монокл., НМ 6,
d 3,1—3,2, желт.-красн., сод. Fe
Mg9(SiO4L(OH)F — Гумит/Humite, ромб, или монокл., сод. Ti, Fe
^^OjQ— Кеннедиит/Kennedyite, ромб.
(MgTilv)O3 — Гейкилит/Geikielite, уст. пикроильменит/picroil-
menite, трип, кор.-черн., сод. Fe
(MgTi2v)O5 — Армолколит/Armalcolite, ромб., сод. Fe
252
I. Неорганические вещества
Продолжение табл.
Mg(UO^+J(AsO4J — а) • D—8)Н2О, Метановачекит/Metanovace-
kite, тетр. б) • 12Н2О, Hobarekum/Novacekite, тетр. б) • 12Н2О,
Hobarekum/Novacekite, тетр
Mg2(UO2+)(CO3K * 18Н2О - Бейлиит/Bayleyite, монокл.
Mg(UO^+J(PO4J • 8Н2О — Салеит/Saleite, тетр.
Mg2(UO^+N(SO4K(OHI0 • 16Н2О — Магний-циппеит/Magnesium
zippeite, ромб.
Mg(UO2+JSi2O7 • 6Н2О — Склодовскит/Sk^odowskite, монокл.
Mg5Zn2ISO4(OHI2 • 4Н2О — Торриит/Torreyite, монокл.
(MnHAg4Sb2n)S6— Самсонит/Samsonite, монокл.
Mn51Al(AlSi3O10)(OH)8— а) Пеннантит/Pennantite, монокл., НМ
1,5—2,5, d2,6—3,3, зел. б) Гровсит/Grovesite, трикл., НМ 2,5,
d 2,6—3,3, зел., сод. Mg
(МппА12)О4— Галаксит/Galaxite, куб., НМ 7,5—8, </4,04, красн.-
черн., сод. Fe [6]
(Mri51Al3)O9(OH) — Магнуссонит/Magnussonite, куб., сод. С1~
МппА1РО4(ОНJ • Н2О — Эосфорит/Eosphorite, ромб., НМ 5,
d 3,1—3,2, роз.-кор., сод. Fe
MnnAl2(SO4L • 22Н2О — Апджонит/Apjohnite, монокл.
Mn*!Al2(Si04K — Шпессартин/Spessartite (spessartine), куб., НМ
6,5-7,5, rf3,8-4,3, красн.-бур. [1]
MnIH(AlSiO4)O — Канонаит/Kanonaite, ромб.
MnIIAl2(SiO3J(OHL— Карфолит/Carpholite, ромб.
Mn^(Al3Si7023)@H)9 — Акатореит/Akatoreite, трикл.
Mn^(AsO4J • 8Н2О — Манганхорнсит/Manganese-hoernesite, мо-
монокл., сод. Mg
Mn^AsmO3(AsO4J(OH)9 • 2Н2О — Синадельфит/Synadelphite, ромб.
MnI1I5AsO3(AsO4J(OHJ3 — Гематолит/Hematolite, триг., сод. Mg, A1
Mn2I(AsO4)OH — а) Саркинит/Sarkinite, уст. хондроарсенит/
chondroarsenite, монокл. б) Эваит/Eveite, ромб.
Mn^AsO4(OHK • Н2О — Гемафибрит/Hemafibrite, ромб., красн.-кор.
Mn^(AsO4J(OHL — Арсеноклазит/Arsenoclasite, ромб.
Mn7I(AsO4J(OH)8 — Аллактит/Allactite, уст. хлорарсениан/chlo-
rarsenian(ite), монокл., св.-зел.
253
I. Неорганические вещества
Продолжение табд
Ми " (ВО3J — Джимбоит/Jimboite, ромб.
Мп^(В7О13)С1 — Чеймберсит/Chambersite, ромб.
МпуВ2О5(ОНL— Визерит/Wiserite, тетр., сод. С1"
MnJ4BeSiO4KS - Гельвин/Helvite, куб., НМ 5,5-6,5, </3,2-3,5,
желт.-кор., сод. Fe, Zn [6]
МппСО3 — Родохрозит/Rhodochrosite, уст. диалогит/dialogite,
малиновый {или марганцевый) шпат/crimson (manganese) spar,
манганокальцит/manganocalcite, триг., НМ 3,5—4,0, d3,l, роз.-
красн. [6]
Мп^(СО3J(ОНI0 — Лосиит/Loseyite, монокл., сод. Zn
Mn ^CO3(SO4L(OHN • 48Н2О — Накауриит/Nakauriite, ромб., сод.
Ni,Cu
МппС12 — Скаккит/Scacchite, триг., d2,9, роз.
[МппС16],К4 — Хлорманганокалит/Chlormanganokalite, триг.
Мп^С1(ОНK— Кемпит/Kempite, ромб.
(Mn2IICuII)O4— Креднерит/Crednerite, монокл., НМ 4, d 4,9—5,1,
кор.-черн. [6]
Mn^Feni(FeinSi3O10)(OH)8- Гоньерит/Gonyerite, ромб., НМ 2,5,
d 2,6—3,3, зел., сод. Mg
MnIIFe2IFeIIIZnII(PO4K(OHJ • 9Н2О - Скунерит/Schoonerite,
ромб.
(MnnFe2n)O4 — а) Якобсит/Jacobsite, куб., d4,S, т.-кор. б) Иваки-
ит/Iwakiite, тетр., сод. Мпш
MnnFen(PO4)F — а) ТриплитДпрШе, монокл., НМ 5,0—5,5,
d 3,5—3,9, кор., сод. Mg, Са, ОН", б) Триплоидит/Triploidite, мо-
монокл.
MnnFe2n(PO4J(OHJ— а) • Н2О, Ландит/Landesite, ромб,
б) • 6Н2О, Штрунцит/Strunzite, трикл., НМ 2,5, желт, в) • 8Н2О,
Псевдолауэит/Pseudolaueite, монокл. г) • 8Н2О, Лауэит/Laueite,
трикл. д) • 8Н2О, Стьюартит/Stewartite, трикл.
MnnFe4n(PO4K(OHM- Фронделит/Frondelite, ромб., НМ 4,5,
d 3,3—3,5, зел., сод. Fe11
MnFe8S8— Манганшадлунит/Manganese-shadlunite, куб., сод. РЬ»
Cd, Си
254
I. Неорганические вещества
Продолжение табл.
MnnFenSiO4 — Кнебелит/Knebelite, уст, манганфаялит/mangan-
faialite, ромб., т.-кор.
Mn^Fe^SiO^ — Колдерит (трад. кальдеритуСаИегке, куб.,
НМ 6,0-7,5, </3,2-4,3, кор.-черн. [4]
Mn" Fe" (SiO4JO2(OHJ — Даннеморит/Dannemorite, монокл.,
НМ 5-6, d 3,1-3,6, зел.-бур.
MnnHAsO4 • Н2О — Краутит/Krautite, монокл.
Мп*1 (НРО4J(РО4J • 4Н2О — Юролит (трад. гюролит)/НигеаиШе,
уст. бастинит/bastinite, монокл.
Mn'IMnIIIAsO4(OHL- Флинкит/Flinkite, ромб.
(Mi^Mn™^ — Браунит/Braunite, тетр., НМ 6,0—6,5, rf4,75—
4,82, кор.-черн., сод. Fe, Ca, Ba, Si [6]
(МппМп*п)О4 см. (Мп1*Мп™H4
(МппМп™H7 • ЗН2О — Аврорит/Aurorite, трикл. (?), сод. Ag, Ca
(MnIIMn4Y)O9 • Н2О — Таканелит/Takanelite, гекс, сод. Са
(Mn^1 MnIV)O4 или (МппМп^п)О4 — Хаусманит (трад. гаусман-
HHT)/Hausmannite, тетр., НМ 5,0—5,5, d4,7—4,8, кор.-черн., сод.
Fe, Zn, Ba, Mg, Ca [6]
MnnMn^n(PO4J(OHJ • 4H2O — Берманит/Bermanite, монокл.
(МппМп™РЬп)О12 • 2Н2О см. (Мп^РЬп)О7 • Н2О
(Mn"Mn7vPbII)O16— Коронадит/Coronadite, тетр. (?)
(Mn 4J Mn ^п Si2Sbv)O24—Лонгбанит (трад. лангбанит)/Ьаг^ЬапИе,
трйг., сод. Ca, Fe
Mn*1 (MnIVSiO7) — Велинит/Welinite, гекс, т.-красн.
MnI1I1Mn4II(SiO4J(AsIIIO3N(OH)8 — Диксенит/Dixenite, триг.
МппО — Манганосит/Manganosite, куб., НМ 6—7, d 5,0—5,4,
т.-зел., сод. Mg, Ca, Fe11 [6] , , г ,
MnIV02 — а) Рамсделлит/RamsdeUite, ромб, б) Пиролюзит/Руго-
lusite, уст. полианит/polianite, тетр., НМ 6,0—6,5, d4,9—5,0,
т.-сер., сод. Ba, Na, К, Н2О [6]
Мп'пО3 — Биксбиит/Bixbyite, уст. курнакит/kumakite, ситапа-
рит/sitaparite, куб. (у), НМ 6,0—6,5, */4,9, красн.-черн. [1,6]
Мпп(ОНJ — Пирохроит/Pyrochroite, уст. манганобрюсит/manga-
nobrucite, триг., df 3,2, бел.-желт.
255
I. Неорганические вещества
Продолжение
57
58
59
60
61
62
63
64
65
66
67
68
69
70
71
72
73
74
75
MnHO(OH) — а) Файткнехтит/Feitknechtite, гекс. (р), ^4,1, бур.
б) Манганит/Manganite, уст. серая марганцевая руда/grey manga*
nese ore, монокл. (у), НМ 3,5—4,0, d4,3—4,4, бур.-черн. [6].
в) Граутит (трад. rpoyraT)/Groutite, ромб, (а), НМ 3,5—4,0,
^4,14, черн.
МпП1РО4— Пурпурит/Purpurite, ромб., кор.-сер.
Мп" (РО4J — а) Бойсит (трад. беусит)/Вешке, уст. магниофи-
лит/magniophilite, монокл., сод. Fe, Ca, Mg. б) • ЗН2О, Реддингит/
Reddingite, ромб., d3,l, св.-роз. в) Свитцерит/Switzerite, монокл.,
сод. Fe
MnIIPb3I(HAs03)(As03J— Тригонит/Trigonite, монокл.
(Мп ™РЬ")О7 • Н2О или (MnnMn JvPbn)O12 • 2Н2О - Сезаролит/
Cesarolite, монокл., НМ 5, т.-сер.
(Mn^IIPbII)O10— Магнетоплюмбит/Magnetoplumbite, гекс, черн.,
сод. Fe
(MnIIPbII)O2(OH) — Кенселит/Quenselite, монокл., черн.
MnIIPbgI(Si207K— Бирисилит/Barysilite, триг.
Mn'"Pb ^(SiO4JO - Кентролит/Kentrolite, ромб.
MnIVPbHTeO6 — Куранахит/Kuranakhite, ромб.
MnIIPb21(VO4J • Н2О — Браккебушит/Brackebuschite, монокл.
MnIIPbII(VO4)OH — Пиробелонит/Pyrobelonite, ромб.
MnHS — Алабандин/Alabandite, уст. марганцевая обманка/man-
ganblende, куб., НМ 3,5-4,0, d 3,95-4,04, сер.-черн. [6]
Mnn(S2) — Хауэрит (трад. гауерит)/НаиегИе, уст. марганцевый
колчедан/manganese pyrites, куб., d3,4, черн. [6]
MnnSO4— а) Н2О, Шмикит (трад. CMHKHT)/Szmikite, монокл.
б) • 4Н2О, Илезит/Ilesite, монокл., сод. Zn, Fe. в) • 5Н2О, Джоко-
куит/Jokokuite, трикл., rf 2,3, роз. г) • 7Н2О, Малларит (трад. мал-
лapдит)/Mallardite, уст. фаузерит/fauserite, марганцевый купо-
купорос/manganese vitriol, монокл., d2,\, роз.
Mn^SO4(OH)]4 • 4Н2О — Мурит/Mooreite, монокл., сод. Zn, Mg
(Mn^SbvAsv)O12— Манганостибиит/Manganostibiite, ромб., соД-**
Mn5ISb2^(Mn4IAl2SiO14J— Катоптрит/Katoptrite, монокл.
(MnHSbI!ISbv)O5— Меланостибит/Melanostibite, триг., черн., сод. &
256
I. Неорганические вещества
Продолжение табл.
Mn4I(Si3AsO12)OH — Тирагаллоит/Tiragalloite, монокл.
MnHSiO3 — а) Каноит/Kanoite, монокл., краен., сод. Mg. б) или
CaMnn(Si03J, Бустамит/Bustamite, трикл., красн.-сер., сод. Са,
Fe. в) Пироксмангит/Pyroxmangite, трикл. г) или CaMn4* (SiO3M,
Родонит/Rhodonite, трикл., НМ 5,5—6,5, d 3,6—3,8, роз., сод. Са,
Fe, Mg [1,6]. Фаулерит/Fowlerite — Р., сод. Zn
Mn^SiC^ — Тефроит/Tephroite, ромб., НМ 6, */4,1, сер.-зел. [6].
Рупперит (трад. ponnepHT)/Roepperite — Т., сод. Zn
Мп"E12О5KС12(ОН)8— Макгиллит/McGillite, триг., зел.-роз.
Mn ^(SiO4J(OHJ — Аллегейниит/Alleghanyite, монокл.
Mn^(Si2O5L(OHJ • (8—9)Н2О — Йофортьеит/Yofortierite, монокл.
Mn"(SiO4K(OHJ— a) Лейкофиникит/Leucophaenicite, монокл.,
роз.-бел. б) Мангангумит/Manganhumite, ромб.
Мп"813О10(ОН)8— Гейджит (трад. rarenT)/Gageite, ромб., сод.
Mg, Zn
Mn8I(Si2O5K(OHI0— a) Бементит/Bementite, монокл., роз.-
красн. б) Кариопилит/Caryopilite, монокл., роз-.красн., сод. Mg.
в) Манганпиросмалит/Manganpyrosmalite, триг., сод. Fe, Cl~. г)
Фриделит/Friedelite, триг, НМ 5, d 3,07—3,17, роз.-кор., сод. Fe,
Са, Zn, As, Cl- [6]
Mn"(SiO4L(OHJ— Сонолит/Sonolite, монокл., сод. F~
Mn^(SiSbAsO12) — Паруэлит/Parwelite, монокл., сод. Mg
Mn^Te^Og) — Шпироффит/Spiroffite, монокл.
MnnWO4 — Хюбнерит (трад. гюбнерит)/НиеЬпегНе, монокл., НМ
4,0—5,5, d7,12—7,2, желт.-красн., сод. Fe, Zn, Mg, Та, Nb [6]
Mn3IZn2IAsO4(OHO — Хлорофиникит/СЫогорЬэешске, монокл.
(Mn2nZnn)O4— Гетеролит/Hetaerolite, тетр., НМ 6, </5,2, кор. [6]
(Mn^Znn)O6 • 2Н2О — Халькофанит/Chalcophanite, трикл., син.-
черн., сод. Fe
(Mn^vZnn)O7 • A—2)Н2О — Вудраффит/Woodruffite, монокл., черн.
Mn^Zn^SO4(OHJ • 4Н2О — Лосонбауэрит/Lawsonbauerite, мо-
монокл., сод. Mg
Mn^IZn1I(SiO4JAsO4(OHK— Крайсслит/Kraisslite, гекс.
Mn » Zn 31 SiO4(AsO4J(OH)8 - Холденит/Holdenite, ромб.
9-2004
257
I. Неорганические вещества
Продолжение табд
MnnZn^SiO4(OHJ— Ходжкинсонит/Hodgkinsonite, монокл.,
красн.-сер.
'SnIV)S8 - Хемусит/Hemusite, куб.
— Тугариновит/Tugarinovite, монокл., d6,4, кор.-фиол.
з — Молибдит/Molybdite, уст. молибденовая oxpa/molibdic
ocher, ромб., */4,6, зел.-бел., сод. Fe
MoIVS2— а) Хордисит (трад. HopflH3HT)/Jordisite, аморфн., d4,7,
сер.-гол. б) Молибденит/Molybdenite, уст. молибденовый блеск/
molybdenum glance, молибденовая обманка/molybdenum blende,
гекс. гш/триг., НМ 1,0—1,5, </4,62—4,73, т.-сер. [6]
MoIVSe2 — Дрисдаллит/Drysdallite, гекс, гол.-сер., сод. S2~
NH4(AlSi308) • 0,5Н2О — Баддингтонит/Buddingtonite, монокл.,
НМ 6,0-6,5, </2,55-2,63, бел.
(NH4JC2O4 • Н2О — Оксаммит/Oxammite, ромб., d 1,5, бел.
NH4C1 — Нашатырь/Salammoniac, куб., d 1,5, бел.
NH4HCO3 — Тешемакерит/Teschemacherite, ромб., d 1,5, бел.
NH4H2PO4— Бифосфаммит/Biphosphammite, тетр., d 1,8, бел.,
сод. К
(NH4JHPO4— Фосфаммит/Phosphammite, монокл. (?), d 1,6, бел.
(NH4K(HSO4)SO4 — Летовицит/Letovicite, монокл., бел.
(NH4JSO4— Масканьит/Mascagnite, ромб., d 1,7, бел.
NaAl2(AlSi3O10)(OHJ— а) Парагонит/Paragonite, монокл., НМ
2,5, d 2,85, бел. б) • Н2О, Браммаллит/Brammallite, монокл.
NaAl(AsO4)F — Дурангит/Durangite, монокл.
NaAl(PO4)F — Лакруаит/Lacroixite, монокл.
NaAl(PO4)OH — Натромонтебраит/Natromontebrasite, трикл.,
сод. Li, F~
NaAl3(PO4)9(OHL — а) Бразилианит/Brazilianite, монокл.
б) • 2Н2О, Уордит (трад. вapдит)/Waгdite, тетр., бел.
NaAl(SO4J— a) • 6Н2О, Тамаругит/Tamarugite, монокл.
б) • 11Н2О, Мендосит/Mendozite, монокл. в) • 12Н2О, Натриевые
квасцы/Sodium (уст. soda) alum, куб., d 1,6, бел.
NaAl3(SO4J(OHN— Натроалунит/Natroalunite, триг.
258
I. Неорганические вещества
Продолжение табл.
Na(AlSi2O6) — а) Жадеит/Jadeite, монокл., НМ 6,5—7,0, */3,24—
3,43, зел., сод. Fe [1]. Жад/Jade — микрокристаллический Ж. [1].
б) • Н2О, Анальцим/Analcite (analcime), куб., НМ 5,5—6,0, */2,24—
2,29, бел., сод. К [4]
Na(AlSi3O8) — a) Альбит/Albite, уст. натриевый полевой шпат/so-
шпат/soda feldspar, трикл., НМ 6,0—6,5, d2,62, бел. [4]. Авантюрин/Aven-
turine, уст. солнечный камень/sunstone — краен. А. [1]. Кливлен-
дит/Cleavelandite — пластинчатый А. б) или NaCa(Al3Si5016), Ан-
дезин/Andesine, трикл., НМ 6,0—6,5, d 2,28—2,68, бел., сод. Са, К
[4]. в) Анортоклаз/Anorthoclase, трикл., НМ 6, d 2,6, бел., сод. К,
Ва, Са. г) Олигоклаз/Oligoclase, трикл., НМ 6, af 2,65, сер., сод. Са
Na(AlSi5O12) — а) • ЗН2О, Морденит/Mordenite, уст. птилолит/
ptilolite, ромб., НМ 3—4, а? 2,12—2,15, бел., сод. К, Са. Аштонит/
Ashtonite — М., сод. Sr. б) • 4Н2О, Клиноптилолит/Clinoptilolite,
монокл., НМ 3,5, J2,15, бел., сод. К, Са [4]
Na2(Al2Si3O10) • 2Н2О — а) Натролит/Natrolite, уст. эшеллит/ech-
ellite, ромб., НМ 5, d2,2—2,26, бел., сод. К, Са [4]. б) Тетранатро-
лит/Tetranatrolite, тетр.
Na5(Al5Si19048) • 12Н2О — Дакьярдит/D'Achiardite, монокл., НМ
4,0-4,5, </2,16, бел., сод. К, Са
Na4(AlSi04KCl - Содалит/Sodalite, куб., НМ 5,5-6,0, d2,27-
2,33, гол.-бел., сод. К, Са. Хакманит/Hackmanite — С, обогащен-
обогащенный серой
Na4(AlSi308KCl — Мариялит/Marialite, тетр.
Na2(AlSi308HH — Уссингит/Ussingite, трикл.
Na8(AlSiO4NSO4 — а) Аюин (трад. гаюин)/Найупке (hauyne),
куб., НМ 5,5—6,0, </2,4—2,5, гол.-бел., сод. Са, S2~. б) Нозеан/
Noselite (nosean), куб., гол.-бел.
NaB3O5 • 2Н2О — Амегинит/Ameghinite, монокл.
247— а) • 4Н2О, Кернит/Kernite,уст. разорит/rasorite, монокл.,
НМ 2,5, d 1,91, бел. [6]. б) • 5Н2О, Тинкальконит/Tincalconite,
трип, d 1,88, бел. в) • 10Н2О, Тинкаль/Tincal, уст. бура/borax,
монокл., НМ 2,0—2,5, d 1,715, бел. [6]
Na4B10O17 • 7Н2О — Эскуррит/Ezcurrite, трикл.
Na2(B5O8)OH • Н2О — Бирингуччит/Biringuccite, монокл.
Na(BSi3O8) — Ридмернерит/Reedmergnerite, трикл., НМ 6,0—6,5,
^2,55-2,63, бел.
259
I. Неорганические вещества
Продолжение
NaB(Si2O5)(OHJ — Сирлсит/Searlesite, монокл.
Na2Ba(AlSi04L — Баналсит/Banalsite, ромб.
NaBa3(B7Si2016)@HL— Гаррелсит/Garrelsite, монокл.
NaBa3Ca(CO3N • ЗН2О — Маккелвиит/McKelveyite, псевдотриг.
NaBa2Ce2IIFe1II(TiIYSi4O13J(OHJ — Хоакинит/Joaquinite, мо-
монокл., сод. Nb, F~
Na4BaTi™(BSi5O15J — Лейкосфенит/Leucosphenite, монокл.,
бел., сод. Са
Na2BaTiIVMnn(BSi3O10J — Тяньшанит/Tianshanite, гекс.
Na2BaTi2v(Si207J— Батисит/Batisite, ромб.
Na4BeAl(Si4012)Cl — Тугтупит/Tugtupite, тетр.
NaBePO4— Бериллонит/Beryllonite, монокл.
(NaBe4Sbv)O7 — Сведенборгит/Swedenborgite, гекс.
Na2Be(Si03J — Чкаловит/Chkalovite, ромб.
NaBe(Si3O7)OH — Эвдидимит/Eudidymite, монокл.
Na2CO3 — а) • Н2О, Термонатрит/Thermonatrite, ромб., НМ 1,0—
1,5, d'2,255, бел. б) • 10Н2О, Натрон/Natron, уст. природная сода/
native soda, монокл., d 1,45, бел. [6]
NaCa2Al4HCO3(CO3K(OHI0— Тунисит/Tunisite, уст. славянс-
кит/slavyanskite, тетр.
NaCaAl6(PO4L(OH)9 • ЗН2О — Миллисит/Millisite, тетр. (?). Пал-
лит/Pallite — М., сод. Fe
NaCa2Al2(PO4J(OH)F4 • 2Н2О — Моринит/Morinite, уст. ежекит/
jezekite, монокл.
NaCa(Al3Si5016) см. CaAl(AlSi2O8), Na(AlSi3O8)
NaCa2(AlSi04M • 6H2O — Томсонит/Thomsonite, ромб., НМ 5,0—
5,5, d2,1—2,39, бел., сод. Sr [4]. Линтонит/Lintonite — Т. с зел.,
краен, и бел. полосами [1]
NaCa2(Al5Si13036) • 17Н2О — Стильбит/Stilbite, уст. десмин/
desmine, монокл., НМ 3,5—4,0, d2,1—2,2, бел., сод. Ва, Sr
NaCa6Al9Si13046 • 20Н2О — Роджанит/Roggianite, тетр.
Na2Ca(Al2Si3O10J • 7Н2О — Гоннардит/Gonnardite, ромб., НМ 5,
^/2,3, бел., сод. К
260
I. Неорганические вещества
Продолжение табл.
Na2Ca(Al4Si8024) • 6Н2О — Гмелинит/Gmelinite, гекс, НМ 4,5,
^ 2,1, желт.-бел., сод. К, Sr
Na2Ca2(Al6Si9O30) • 8Н2О — Мезолит/Mesolite, монокл., НМ 5,
J2,26, бел., сод. К [4]
Na2Ca5(Al12Si20O64) • 27Н2О — Гарронит/Garronite, тетр., */2,13—
2,17, бел., сод. К, Ва [4]
Na6Ca(Al8Si28072) • 26Н2О — Баррерит/Barrerite, ромб., бел.
Na10Ca5Al6(Si2O5I6Cl6 • 18Н2О — Делхайлит/Delhayelite, ромб.,
сод. К, F", SO \~
Na4Ca14(AlSi7O20K(OHM • 5Н2О — Рейерит/Reyerite, трип, сод. К
Na6Ca2(AlSiO4NS(SO4) — Лазурит/Lazurite, уст. лазоревый (ла-
(лазурный) камень/azure stone, куб., НМ 5—6, d2,4—2,45, ярко-син.
[1, 5]. Ляпис-лазурь/Lapis lazuli — смесь Л. с кальцитом, пиритом
и различными алюмосиликатами [1,5]. Ультрамарин/Ultramarine —
синтетический Л. [5]
NaCaB5O9 • 5Н2О — Пробертит/Probertite, уст. крамерит/kramer-
ite, монокл.
Na2Ca3B5O8(SO4JCl(OHJ — Хейдорнит/Heidornite, монокл.
Na2Ca(CO3J — а) Ньеререит/Nyerereite, ромб, б) • 2Н2О, Пирссо-
нит/Pirssonite, ромб., d 3,0—3,5, бел. в) • 5Н2О, Гейлюссит/Gay-
lussite, уст. натрокальцит/natrocalcite, монокл., НМ 2,5—3,0,
d 1,99-2,04, бел.
Na2Ca2(CO3K- Шортит/Shortite, ромб., НМ 3,5, </2,63, бел.
NaCaCu ^ (AsO4LCl • 5Н2О — Лавендулан/Lavendulan, уст. фрай-
ринит/freirinite, ромб.
NaCaCu^(PO4LCl • 5Н2О — Самплит/Sampleite, ромб.
Na2CaFe4! Al(AlSi7O22)(OHJ — Алюмокатофорит/Alumokato-
phorite, монокл., НМ 5, d 3,2—3,5, сер.-зел., сод. Mg
NaCa^e^1 FeHI(AlSi3OnJ(OHJ — Хастингсит/Hastingsite, мо-
монокл., НМ 5—6, d 3,02—3,45, черн., сод. Mg
Na2CaFe ^ Fe2И(AlS^OjlJ(OHJ — Тарамит/Taramite, монокл.,
сод. Mg, F". Мбозиит/Mboziite — Т., сод. К
NaCaFe4IFeII1(Si4O11J(OHJ— Ферроуинчит/Ferrowinchite, мо-
монокл., т.-кор., сод. Mg, A1
Na12Ca3Fe2n(Si6O18J— Имандрит/Imandrite, ромб.
261
I. Неорганические вещества
Продолжение пгабД
Na3Ca(H2SiO4)PO4— Фосинаит/Phosinaite, ромб.
NaCaMg3Al2(AlSi7O22)(OHJ — Барруаит/Barroisite, монокл.,
сер.-зел., сод. Fe
NaCa2Mg4Al(AlSi30j ^(ОН^ — Паргасит/Pargasite, монокл., НМ
5—6, ^3,1, кор., сод. Fe
Na2CaMg4Al(AlSi7O22)(OHJ — Катофорит/Katophorite (cato-
phorite), монокл., НМ 5, d 3,2—3,5, красн.-кор., сод. Fe
NaCaMg(AlSiO6) — Авгит/Augite, монокл., НМ 5—6, </3,19—3,56,
св.-кор., сод. Fe Ti, К, Mn, Ni, V, Сг
Na13Ca,2Mg]1(Al59Si133O384) * 235Н2О — Фожасит (трад. фоязит)/
Faujasite, куб., НМ 5, d 1,92, бел. [4]
NaCaMg4Al(Si4OnJ(OHJ — Уинчит/Wmchite, монокл., зел.-кор.,
сод. Fe
NaCa2Mg5(AlSi7O22)(OHJ— Эденит/Edenite, монокл., НМ 5—6,
d 3,02—3,45, св.-зел., сод. Fe
NaCa2Mg2(As04K — Берцелиит/Berzeliite, уст. пирроарсенит/руг-
rhoarsenite, куб., желт., сод. Мп
NaCa2Mg4Fein(AlSi3OnJ(OHJ- Роговая обманка/Homblende,
уст. лампроболит/lamprobolite, монокл., НМ 5—6, d 3,02—3,45,
зел.-черн., сод. Fe11, F". Хуанит/Juanite — волокнистая Р. О.
Na2CaMg4FeHI(AlSi7O22)(OHJ — Магнезиокатофорит/Magne-
siokatophorite, монокл., зел.-кор., сод. F~
Na10Ca6Mg18Fe (РО4K6 — Джонсомервиллит/Johnsomervilleite,
трип, сод. Мп
Na2CaMg(PO4J — Брайанит/Brianite, монокл., бел.
Na2CaMg5(Si4OnJ(OHJ— Рихтерит/Richterite, монокл., НМ
5—6, d 2,97—3,45, желт.-фиол., сод. Fe, Мп, Al, F". Магнофорит/
Magnophorite — Р., сод. Ti, К
NaCa^n^AsO^— Манганберцелиит/Manganberzeliite, куб.,
сод. Mg
Na33Ca12Mn l*Q2 Fe 24 (PO4I03 — Филлоуит/Fillowite, триг.
NaCaMn^1 (HSi5O15) — Марстурит/Marsturite, трикл.
(NaCaNb^)O6F — Пирохлор/Pyrochlore, уст. пиррит/pyrrhite,
куб., НМ 4-5,5, rf3,7-5,0, т.-бур., сод. Та, Ti, ОН" [6]. Самире-
сит/Samiresite — П., сод. Pb, U, Ln
262
I. Неорганические вещества
Продолжение табл.
NaCaPO4— Бухвальдит/Buchwaldite, ромб., бел.
Na2Ca(PO4)F — Накафит/Nacaphite, ромб.
Na2Ca(SO4J — а) Глауберит/Glauberite, монокл., НМ 2,5—3,
d2,75—2,85, св.-желт. [6]. б) • 4Н2О, Ваттевиллит/Wattevillite,
ромб, или монокл.
Na10Ca3(SO4)8 • 6Н2О — Гидроглауберит/Hydroglauberite, ромб. (?)
Na2Ca(Si205J • 2,75Н2О — Родсит/Rhodesite, ромб.
NaCa2(Si205JF — Агреллит/Agrellite, трикл.
NaCa4(Si205LF • 8Н2О — Натроапофиллит/Natroapophyllite, ромб.
NaCa2(Si308HH — Пектолит/Pectolite, трикл., НМ 5, я? 2,7—2,8,
бел. Шизолит/Schizolite — П., сод. Мп
Na4Ca3(Si3O8J(OHJ — Комбит/Combeite, трип, сод. F~
Na6Ca5(Si2O5N(OHL— Канасит/Canasite, монокл., сод. К, F~
(NaCaTa^ )O6F — Микролит/Microlite, уст. неотанталит/neotan-
talite, куб., НМ 5,5, d5,2-5,6, желт.-бур., сод. Nb, Ti, U, Bi, ОН" [6]
Na6CaTiIV(Si6018) • H2O — Коашвит/Koashvite, ромб.
Na2CaTiIV(Si207)F2 — Мосандрит/Mosandrite, уст. ринк(ол)ит/
rink(ol)ite, трикл., НМ 5, d2,93—3,03, краен.-кор., сод. Zr, Ln
Na2Ca(U2O7J— Кларкит/Clarkeite, ромб., НМ 4,0—4,5, </6,39,
красн.-кор., сод. РЬ, К, ОН~ [6]
NaCa3(UOf )(CO3KSO4(F) • 10Н2О - Шрёккингерит/Schroeck-
ingerite, уст. дакеит/dakeite, ромб., НМ 2,5, (/2,5, т.-зел.
Na2Ca(VO2+)(CO3K • 6Н2О — Андерсонит/Andersonite, триг.
(Na4CaV*vvyoH32 • 8Н2О — Грантсит/Grantsite, монокл.
(NaCaYin)F6— Гагаринит/Gagarinite, гекс, сод. С1~
NaCaZrIVMnn(SiO4JF — Ловенит/Lavenite, монокл., НМ 6,
d 3,53, желт.
Na6CaZrIV(Si6018) — Цирсиналит/Zirsinalite, триг, сод. Mn, Fe
NaCa2ZrIV(Si04JF — Розенбушит/Rosenbuschite, трикл., сод. Ti
NaCa2ZrIV(Si207H(F) — Вёлерит/Wohlerite (woehlerite), монокл.,
НМ 5,5-6,0, d 3,4, т.-желт.
263
I. Неорганические вещества
Продолжение табд
Na4Ca2(ZrIVSi6017)@HJ— Эвдиалит/Eudialyte, уст. барсановит/
barsanovite, трип, НМ 5—6, d 2,7—3,1, роз., сод. Ln, Fe, Sr, Nb, Ti
К, Cl-
NaCe2nMn^(Si6018HH — Стеэнструпин/Steenstrupine, гекс,
сод. La, P
Na3Cein(Si205K • 6H2O — Сажинит/Sazhinite, ромб.
(NaCeHITiiv)O6- Лопарит/Loparite, ромб., НМ 5,5-6,5,
d 4,6—4,9, черн., сод. Ca, Ln, Nb, Та [6]
НазСе^Т1^(81О4J(СОзKО4(ОН) • 2H2O - Тундрит/Tundrite,
трикл.
Na4Cenl(TiIVSi7018)P04 • 5Н2О — Лапландит/Laplandite, ромб.
NaCl — а) Галит/Halite, уст. каменная соль/rock salt, куб.,
НМ 2,0-2,5, d2,16, бел. [3, 6]. б) • 2Н2О, Гидрогалит/Hydrohalite,
монокл., бел.
NaCrIH(Si03J — Юриит/Ureyite, уст. космохлор/cosmochlore,
монокл., НМ 6, d396, т.-зел.
Na2CuH(CO3J • ЗН2О — Хальконатрон/Chalconatronite, монокл.
Na2Cun(SO4J • 2Н2О — Крёнкит/Kroehnkite, монокл.
NaCu2! (SO4JOH • Н2О — Натрохальцит/Natrochalcite, монокл.
NaF — Вилльомит/Williaumite, куб., d2,5, бел.
NaFeJ!IAl6(BO3K(Si6O18)O3F - Бюргерит/Buergerite, триг., НМ
7,0—7,5, d2,6-2,63, сер.-кор., сод. ОН"
NaFe^Al6(BO3KSi6O18(OHL- Шёрл/Schorl, триг., НМ 7,0-7,5,
af 3,1—3,25, черн., сод. F~
Na2Fe J1 А1(РО4K — а) Уиллиит/Wyllieite, монокл. б) Ферроуилли-
ит/Ferrowyllieite, монокл., сод. Ca, Mn, Mg
NaFenAl5(PO4L(OHN— Бурангаит/Burangaite, монокл., сод. Ca, Mg
Na6FenAl(Si4013J — Науякасит/Naujakasite, монокл.
Na033Fe2n(Al033Si367O10)(OHJ • 4Н2О - Нонтронит/Nontronite,
монокл., НМ 2,5—4,5, d 1,7—1,8, св.-зел. [2]
NaFenFeni(Si205K • 0,5Н2О — Тухуалит/Tuhualite, уст. тухолит/
tucholite, ромб., сод. К
NaFeI1I0Fe^II(Si12O31)(OHI3— Хауиит/Howieite, триг, сод. Mn, A1
264
I. Неорганические вещества
Продолжение табл.
^^^^^^— Рибекит/Riebeckite, монокл., НМ 5,
^3,02—3,42, т.-гол., сод. F~. Крокидолит/Crocidolite, уст. голу-
голубой асбест/blue asbestos — асбестовидный Р. Соколиный глаз/
Hawk's eye — св.-гол. крокидолит, частично замещенный кварцем
[1]. Тигровый глаз/Tigereye — желт.-кор. крокидолит, частично
замещенный кварцем и гётитом [1]
Na3Fe " FeIII(Si4011J@HJ — Арведсонит/Arfvedsonite, монокл.,
НМ6, </3,45,т.-зел.
NaFenPO4— а) Хагендорфит/Hagendorfite, монокл., сод. Са, Мп.
б) Маричит/Maricite, ромб.
NaFe'n(PO4J(OHL • 2Н2О — Цириловит/Cyrilovite, тетр.
NaFe*n(PO4N(OHI0 • 5Н2О — Кидуэллит/KidweUite, монокл.
(NaFein)S2 • 2Н2О - Эрдит/Erdite, монокл.
NaFeHI(SO4J • 6Н2О — Амариллит/Amarillite, монокл.
Na3Feni(SO4K • ЗН2О — Ферринатрит/Ferrinatrite, триг.
NaFe3n(SO4J(OHN — Натрохаросит/Natrojarosite, трип, НМ
2,5-3,5, d 3,1-3,2, т.-желт.
Na2Fein(SO4JOH — а) • 1,5Н2О, Метасидеронатрит/Metasider-
onatrite, ромб, б) • ЗН2О, Сидеронатрит/Sideronatrite, ромб.
NaFeni(Si03J — Эгирин/Agirite (aegirine), монокл., НМ 6,0—6,5,
d 3,4—3,6, зел.-черн. Акмит/Acmite — бур. игольчатый Э.
NaHCO3— Нахколит/Nahcolite, монокл., НМ 2,5, ^2,24, бел.
Na3(HCO3)CO3 • 2Н2О — Трона/Тгопа, монокл., НМ 2,5—3,0,
?/2,15, бел. [6]
Na(H30+)Si205 • 2Н2О — Канемит/Kanemite, ромб.
Na2HPO4 • 2Н2О — Дорфманит/Dorfmanite, ромб., d2, бел.
Na6HPO4(PO4)F • 17Н2О — Натрофосфат/Natrophosphate, куб.
NaHSO4 • Н2О — Маттеуччит/Matteuccite, монокл., d2,l, бел.
NaLiAl2(Al2Si2O10)(OHJ — Эфесит/Ephesite, монокл.
NaLi3Al7(BO3KSi6O18(OHL— Эльбаит/Elbaite, триг, НМ 7,0—7,5,
t/3,1—3,25, желт., сод. F~. Ахроит/Achroite — бцв. Э. [1]. Верделит/
Verdelite — зел. Э. [1]. Индиголит/Indigolite (неправ, indicolite) —
син. Э. [1]. Рубеллит/Rubellite, уст. сиберит/siberite — роз. проз-
прозрачный Э., сод. Мп [1]
265
I. Неорганические вещества
Продолжение та^
Na2LiAlHPO4(PO4)OH — Танкоит/Tancoite, ромб.
Na4Li2Fe2n(Si12O30) — Эмелеусит/Emeleusite, ромб.
Na0 33^! 67Mg2(Si205JF2 — Экторит (трад. гекторит)/НесЮгИе,
монокл.,' НМ 1—2, d2—3, бел., сод. ОН"
NaLiMngI(Si10O28)(OHJ— Намбулит/Nambulite, трикл.
NaLiZr^S^Og^ * HF — Цекцерит/Zektzerite, ромб., сод. Ti
NaMg2Al(Al2Si2O10)(OHJ— Прайсверкит/Preiswerkite, монокл.
NaMg6Al(AlSi30, jJ(OHJ — Натриевый жедрит/Sodium gedrite,
монокл., НМ 5,5-6,0, d2,85-3,57, бур., сод. Fe, Mn, F", С1~
NaMg3Al6(BO3KSi6O18(OHL — Дравит/Dravite, трип, НМ 7,0—7,5,
d 3,03—3,15, кор., сод. F"
NaMgAl(C2O4K • 8Н2О — Жемчужниковит/Zhemchuzhnikovite,
трип, сод. Fe
NaMg19Al12(CO3N 5(SO4L(OHM4 • 28Н2О — Мотукореяит/Motuko-
reaite, гекс.
Na4Mg9Al4Cl12(OHJ2— Кёненит/Koenenite, гекс.
NaMg(Al3Si15036) • 9Н2О — Феррьеит/Ferrierite, ромб.,
НМ 3,0-3,5, б/2,14, бел., сод. К [4]
Na0 7Mg0 7A13 3(Si205L@HL • лН2О — Монморийонит (трад.
MOHTMopkfuioHHTVMontmorillonite, монокл., НМ 1,5—2,5,
d 1,7-2,9, бел. [6]
Na2Mg3Al2(Si4OnJ(OHJ— Глаукофан/Glaucophane, монокл.,
НМ 6, d 3,1—3,3, св.-гол. Кроссит/Crossite — фиол. Г., сод. Fe11,
Fe»1
Na3Mg4Al(Si4OnJ(OHJ— Эккерманит/Eckermannite, монокл.,
сер.-син., сод. Li, Fe, F~
Na6Mg(B3O5)8 • 22H2O — Ривадавит/Rivadavite, монокл.
Na2Mg(CO3J — Айтелит/Eitelite, гекс.
Na3Mg(CO3JCl - Нортупит/Northupite, куб, НМ 3,5-4,0, </2,41,
бел.
Na3Mg(CO3)PO4 — Брадлиит (трад. 6pe^ureHT)/Bradleyite, мо-
монокл., НМ 3,5, d 2,72, бел.
Na6Mg2(CO3LSO4— ТихитДусИйе, куб.
266
I. Неорганические вещества
Продолжение табл.
NaMgF3 — Нейборит/Neighborite, ромб.
NaMg3Fe"I(BO3KSi6O]8(OHL— Ферридравит/Ferridravite, триг.,
НМ 7,0-7,5, </3,25, бур., сод. F"
NaMgFeIH(C2O4K • (8—9)Н2О - Степановит/Stepanovite, триг.
Na2Mg3Fe2П (Si4Oj,J(ОНJ ~ Магнезиорибекит/Magnesioriebeck-
ite, уст. родусит/rhodusite, терновскит/ternovskite, монокл.
NaMg3Mnn(PO4K — Магхагендорфит/Maghagendorfite, монокл.,
сод. Fe
Na2Mg(SO4J • 4Н2О — Блёдит/Bloedite, уст. уортит/warthite, аст-
paxaHHT/astrak(h)anite, симониит/simonyite, монокл., НМ 2,5—
3,0, d 2,25, гол.-бел.
Na6Mg(SO4L— Вантгоффит/Van'thoffite, монокл., НМ 3,5, </2,69,
бел.
Na12Mg7(SO4I3 • 15Н2О — Лёвеит/Loweite (loeweite), триг., НМ
2,5—3,0, ?/2,38, сер.-бел.
Na21Mg(SO4I0Cl3 — Дансит/D'Ansite, куб., </2,59, бел.
NaMg(SO4)OH • 2Н2О — Уклонсковит/Uklonskovite, монокл.
Na2Mg3(SiO3J(Si2O5J • 8Н2О — Лафлинит/Loughlinite, ромб.
Na4Mg(V10O28) • 24Н2О — Хьюмалит/Huemulite, трикл.
NaMn^(Al5Si015) • 2Н2О — Ганофиллит/Ganophyllite, монокл.
или трикл., сод. К, Fe
Na3Mnn(CO3)PO4— Сидоренкит/Sidorenkite, монокл.
Na2MnnFenAl(PO4K— Розмэриит/Rosemaryite, монокл., сод. Са, Mg
Na3Mn4IFe1II(Si4O11J(OHJ— Коцулит/Kozulite, монокл., фиол.,
сод. Al, F"
(Na2MnnMn7v)O16 — Манжироит/Manjiroite, тетр., сод. К
NaMnnPO4— Натрофилит/Natrophilite, ромб.
Na2Mn4J(Si6017) • Н2О — Серанит/Serandite, тетр., сод. Са
NaMn^(Si2O5K(OHM • 2Н2О — Баннистерит/Bannisterite, мо-
монокл., сод. К, Fe, Al
NaNH4HPO4 • 4Н2О — Стеркорит/Stercorite, трикл.
NaNH4SO4 • 2Н2О — Леконтит/Lecontite, ромб.
267
I. Неорганические вещества
Продолжение табл.
NaNO3 — Нитратин/Nitratine, уст. натронная селитра/soda niter,
чилийская (кубическая) селитра/Chile (cubic) saltpeter, триг., НМ
1,5-2,0, </2,27, бел., сод. К, СЮ", Ю3
Na3(NO3)SO4 • Н2О — Дарапскит/Darapskite, уст. нитроглаубе-
рит/nitroglauberite, монокл., НМ 2,5, d2,2, бел.
(NaNbv)O3 — а) Луэшит/Lueshite, монокл., сер. б) Натрониобит/
Natroniobite, монокл. (?)
NaNbv(SiO3JO • 2Н2О — Ненадкевичит/Nenadkevichite, ромб.,
сод. Са, К, Ti, ОН-
Na2Nin(SO4J • 4Н2О — Никельблёдит/Nickelbloedite, монокл.
Na3PO4— Олимпит/Olympite, ромб., d2,5, бел.
Na3Pb 2Т (SO4KC1 — Караколит/Caracolite, монокл.
Na2SO4— а) Тенарит (трад. тенардит)/Т1ге1шхШе, ромб.,
НМ 2,5—3,0, </2,66, бел. [6]. б) • 10Н2О, Мирабилит/Mirabilite,
уст. глауберова соль/Glauber's salt, монокл., НМ 1,5—2,0, d 1,49,
бел. [5, 6]
Na6(SO4JCl(F) — Сульфогалит/Sulfohalite, куб.
Na15(SO4MCl(F) — Гейлит {трад. гельит)/Са1еие, триг., гол.-бел.
Na21(SO4O(Cl)F6— Шайрерит/Schairerite, триг.
Na3(SO4)F — Когаркоит/Kogarkoite, монокл.
(Na4Sb^nAs^n)S17 • 6Н2О — Герстлиит/Gerstleyite, монокл., сод. U
Na2Si205— Натросилит/Natrosilite, монокл., бел.
Na2Si409 • 5Н2О — Макатит/Makatite, ромб.
NaSi7O13(OHK • ЗН2О — Магадиит/Magadiite, монокл. (?)
Na2Si22041@H)8 • 6Н2О — Кенияит/Kenyaite, монокл.
Na4SnTV(Be2Si6016)@HL— CepeHceHHT/Sorensenite, монокл.
Na2Sr2Al2(PO4)F9— Бёггильдит/Boggildite, монокл.
NaSr3CaYin(CO3N • ЗН2О — Доннейит/Donnayite, трикл.
Na3SrLaniZnn(Si6017) — Нордит/Nordite, ромб., сод. Се, Са, Mn, Mg
NaSrPO4— Ольгит/Olgite, триг., сод. Ва
Na3SrThIV(Si8017)@HO— Умбозерит/Umbozerite, аморфн.
268
I. Неорганические вещества
Продолжение табл.
22^442 — Лампрофиллит/Lamprophyllite, мо-
нокл., сод. Ва, F~
(Na2Ti^vFe2n)O16— Фройденбергит/Freudenbergite, монокл.
Na^i^Fe^S^O^^ — Энигматит/Enigmatite (anigmatite,
aenigmatite), трикл.
(NaTi ™ MnnFe 3n Zn " )O38 — Ландауит/Landauite, псевдотриг.
(NaTi2vPb2!)O6(OH) — Плюмбобетафит/Plumbobetafite, куб.,
черн., сод. Nb, Та, Са, F" [6]
Na2TiIV(Si309) • nH2O — Зорит/Zorite, ромб., сод. Al
Na^i^S^Ojj) • 2,5H2O — Пенквилксит/Penkvilksite, монокл. или
ромб.
Na2TiIV(SiO4)O — Натисит/Natisite, тетр.
Na2TiIV(Si205J0 — Нарсарсукит/Narsarsukite, тетр.
Na2Ti 2V (SiO4JO • лН2О — Мурманит/Murmanite, трикл.
Na2TiIV(TiIVSi209) — Лоренценит/Lorenzenite, ромб.
Na2(UO2+J(AsO4J • 5H2O — Натриевый ураноспинит/Sodium
uranospinite, тетр., сод. Са
Na(UOf )(H3O+)SiO4 • 2,5H2O - Натриевый болтвудит/Sodium
boltwoodite, ромб., сод. К
Na(UO2+)PO4 • 4H2O — Натриевый отёнит/Sodium autunite, тетр.
Na4(UO2+N(SO4K(OHI0 • 4Н2О — Натриевый циппеит/Sodium
zippeite, ромб.
Na2(UO2+J(VO4J • 6Н2О — Стрелкинит/Strelkinite, ромб.
(NaUIVTi^v)O6(OH) — Бетафит/Betafite, уст. хатчеттолит/hatchet-
tolite, куб., НМ 4,0—4,5, d3,7—5,0, зел.-кор., сод. Са, Nb, Та, F" [6]
Na(V^08) • 1,5Н2О — Барнсит/Barnesite, монокл.
Na3Yni(Si8019) • 5Н2О — Монтереджанит/Monteregianite, ромб.,
сод. К, Са
NaZn*I(HAsO4JAsO4— Оданиелит/O'Danielite, монокл.
NaZn^(HTeIV03)(TeIV03J • лН2О — Цеманит/Zemannite, гекс,
сод. Fe
Na2Zn2ISi401I — Власовит/Vlasovite, монокл. илитрш., желт.-бел.
269
I. Неорганические вещества
Продолжение табЛ
Na2ZrIV(Si309) — а) • 2Н2О, Катапле(й)ит/Са1ар1еО)Ие, гекс,
6, d2,8, желт, б) • 2Н2О, Гедоннеит/Gaidonnayite, ромб., сер.-бел.
в) • ЗН2О, Илерит/Hilairite, триг.
Na2ZrIV(Si205K • ЗН2О — Эльпидит/Elpidite, монокл., сод. Ti
Na4ZrIV(Si40nJ • 8H2O — Лемуанит/Lemoynite, монокл.
Na5Zr2v(Si6018)Cl • 2Н2О — Петарасит/Petarasite, монокл., сод. ОН~~
Na2Zr^v(Si207H2— Зайдоцерит (трад. cefcio3epHT)/Seidozerite,
монокл., сод. Са, Ti, Mn, F~
NaZrIV(SiO3JOH — Келдышит/Keldyshite, триг. гш/трикл.
Na10Zr4vTi2v(CO3)8O9 — Сабинаит/Sabinaite, монокл.
(NbvFeIH)O4 — Иксиолит/Ixiolite, ромб., сод. Та, Sn, Mn
(Nb2/FeII)O6— a) Колумбит/Columbite, уст. ниобит/niobite,
ромб., НМ 6, rf5,2, черн., сод. Мп, Та, Ln, U, Ti, W, Th [6]. б)
Моссит/Mossite, ?етр., кор.-черн., сод. Мп, Та
^^ — Манганоколумбит/Manganocolumbite, ромб., сод.
Fe, Та [6]
(Nb^Pb")O6— Чанбайит/Changbaiite, триг.
(NbvPbn)O3(OH) — Плюмбопирохлор/Plumbopyrochlore, куб.,
кор., сод. Y, U, Са, F~
(NbvSbI]I)O4— Стибиоколумбит/Stibiocolumbite, ромб., НМ 5,
d5,7, кор., сод. Та
Ni — Никель/Nickel, куб., НМ 3,5, J8,91, бел.
Ni^Al(AlSi3O10)(OH)«— Нимит/Nimite, монокл., НМ 2,5, </2,6-
3,3, зел., сод. Mg, Fe"
Ni^Al2CO3(OHI6 • 4Н2О — Таковит/Takovite, уст. эрлиит/earley-
ite, триг.
i^Al4 5(SO4J 75(OHJ2 • 3,7Н2О — Каррбойдит/Carrboydite, гекс,
сод. СО *-
Ni, _xAs2— Крутовит/Krutovite, куб.
NiAs — Никелин/Niccolite (nickeline), уст. красный никелевый
колчедан/red nickel pyrites, купферникель/kupfernickel, гекс,
НМ 5—6, d7,6—7,8, т.-красн., сод. Fe, Co, Sb, S [6]
270
I. Неорганические вещества
Продолжение табл.
NiAs2 — a) Хлоантит/Chloanthite, уст. белый никелевый колче-
колчедан/white nickel pyrites, куб., сод. Со [6]. б) Раммельсбергит/Ram-
melsbergite, ромб., НМ 5,5—6,0, dl,l, красн.-бел. [6]
NiAs3— Никельскуттерудит/Nickel-skutterudite, куб., сод. Со [6]
Ni3As — Динерит/Dienerite, куб.
Ni5_xAs2~ Орселит/Orcelite, гекс.
NinAs8 — Маукерит/Maucherite, уст. темискамит/temiskamite, тетр.
Ni^AsO^ — а) Ксантиосит/Xanthiosite, монокл. б) • 8Н2О, Анна-
бергит/Annabergite, уст. никелевая охра/nickel ocher, никелевые
цветы/nickel bloom, монокл., НМ 1,5—2,5, d3,07, св.-зел. [6]
Ni(As)S — Герсдорффит/Gersdorffite, уст. никелевый блеск/nickel
glance, куб., НМ 5,5, а? 5,9, сер., сод. Fe, Co, Sb [6]
Ni3Bi2S2— Паркерит/Parkerite, монокл., сод. РЬ
Ni9BiSbS8 — Ошкорнит (трад. гошкорнит)/Наиспесогпйе, тетр.
NiHCO3— Гаспеит/Gaspeite, трикл., желт.-зел., сод. Mg, Fe
Ni^CO3(OHJ • Н2О - Отуэйит/Otwayite, ромб.
Ni3ICO3(OHL • 4Н2О — Саратит/Zaratite, уст. никелевый изум-
изумруд/nickel emerald, куб., НМ 3, d2,6, ярко-зел.
NinCl2 • 6Н2О — Никельбишофит/Nickelbischoflte, монокл., зел.
(Ni2IICuII)S4— Флетчерит/Fletcherite, куб.
(NinNi2lI)S4— а) Зигенит/Siegenite, куб., сод. Со. б) Полидимит/
Polydymite, куб., */4,54—4,81, сер.-черн., сод. Fe, Cu, As, Sb [6]
(NiI1Ni^II)Se4— а) Уилкманит (трад. вилкмани^/Х^йктапке, мо-
нокл. б) Трюстедтит/Trustedtite, триг.
NinO — Бунзенит/Bunsenite, куб., d6,6, желт.-зел.
Ni3Pb2S2 — Шандит/Shandite, триг.
NinS — Миллерит/Millerite, уст. желтый никелевый
(или волосистый) колчедан/yellow nickel (capillary) pyrites, триг.,
НМ 3,0-4,5, </5,2-5,6, т.-желт., сод. Fe, Co, Си [6]
Nin(S2) — а) Ваэсит/Vaesite, куб., т.-сер. [6]. б) Бравоит/Bravoite,
куб., НМ 5,5-6,0, </4,62, т.-сер., сод. Fe [6]
Ni3S2— Хизлвудит/Heazlewoodite, триг, ^i 5,82, желт.
Ni7S6— Годлевскит/Godlevskite, ромб., сод. Fe
271
I. Неорганические вещества
Продолжение табл
NiHSO4— а) • 6Н2О, Никельгексагидрит/Nickel-hexahydrite, мо-
нокл., сод. Mg, Fe. б) • 6Н2О, Ретгерсит/Retgersite, тетр. в) • 7Н2О,
Мореносит/Morenosite, уст. никелевый купорос/ nickel vitriol,
ромб., d\,9, зел.
NiSb — Брайтхауптит/Breithauptite, гекс, d7,5, т.-красн.
NiSb2 — Нисбит/Nisbite, ромб.
Ni(Sb)S — Улльманит/Ullmannite, трикл., НМ 5,0—5,5, </6,65,
св.-сер., сод. Со, Fe, As, Bi [6]
Ni9Sb2S8 — Тучекит/Tucekite, тетр.
NinSe — a) Седерхольмит/Sederholmite, гекс. (f$), сер. б) Мякине-
нит/Makinenite, триг. (у), ^8,4, сер.
Nin(Se2) — а) Пенроузит/Penroseite, куб., сод. Со, Си. б) Куллеру-
дит/Kullerudite, ромб., d6, т.-сер.
NinSeO3 * 2Н2О — Альфельдит/Ahlfeldite, монокл.
Ni2ISi04 — Либенбергит/Liebenbergite, триг., НМ 6—7, */4,4, зел.,
сод. Mg
Ni" Si2O5(OHL — а) Гарньеит/Garnierite, уст. нумеаит/
noumeaite, монокл., d2,3—2,8, зел., сод. Mg [6]. б) Непуит/Nep-
ouite, монокл., зел. в) Пекораит/Pecoraite, монокл., зел. г) Чок-
лит/Chocolite, монокл., т.-кор., сод. Fe
Ni^(Si2O5J(OHJ— а) Виллемсит/Willemsite, монокл., сод. Mg.
б) • 4Н2О, Пимелит/Pimelite, монокл., сод. Mg
Ni4I(Si205K@HJ • 6Н2О — Фалькондоит/Falcondoite, ромб., сод. Mg
NiTe2— Мелонит/Melonite, гекс, dl,3, т.-сер.
Ni(Te)Se — Киткаит/Kitkaite, триг.
Os — Осмий/Osmium, гекс, d22,6, гол.-бел. Иридосмин/Iri-
dosmine (iridosmium), уст. сысерскит/siserskite — сплав О. (до
80%) с иридием, НМ 6,5-7,0, d 18,6-21,6, сод. Pt, Rh, Fe, Cu [6].
Рутениридосмин/Rutheniridosmine (rutheniridosmium) — сплав О.
с иридием и рутением, гекс, сер. [6]
OsAs2 — Омейит/Omeiite, ромб.
Os(As)S — Осарсит/Osarsite, монокл., сод. Ru
Osn(S2) — Эрлихманит/Erlichmannite, куб., ^9,4, зел.-черн.
РЬ — Свинец/Lead, куб., НМ 1,5, d 11,3, т.-сер.
272
I. Неорганические вещества
Продолжение табл.
Pb3As — Афинаит/Atheneite, гекс, сод. Hg
Pb8As3 — Стиллуотерит/Stillwaterite, гекс.
Pb5IAs3II(Cl)O9— Финнеманит/Finnemanite, гекс.
(Pb l6l As 2И )C14O7 — Экдемит/Ecdemite, тетр.
(Pb^As^— Полмурит/Paulmooreite, монокл.
Pb 31 (AsO4)Cl3 — Джорджиядесит/Georgiadesite, монокл.
Pb " (AsO4KCl — Миметит/Mimetite, уст. миметезит/mimetesite,
монокл., НМ 3,5—4,0, d7,0—7,28, желт.-кор. [6]. Бурая свинцо-
свинцовая руда/Brown lead ore — смесь М. с пироморфитом
Pb54(AsO4JCl4O9— Салинит/Sahlinite, монокл.
(PbnAs2n)S4 — Сарторит/Sartorite, монокл.
(Pb ^As 2П )S5 — Дюфренуаит/Dufrenoyite, монокл.
(Pb"As4n)S15 — Грейтонит/Gratonite, триг.
(Pb *'As j" )S22 — Ливейнгит/Liveingite, монокл.
(PbI14As^II)S23— Иорданит/Jordanite, монокл., сод. Tl, Sb
Pb^BSigO^F — Гиалогекит/Hyalotekite, монокл., сод. Са, Ва, ОН"
РЬИВ11П(С1)О2- Перит/Perite, ромб.
(PbHBi2n)S4— а) Галенобисмутит/Galenobismutite, ромб. [6].
б) Сахароваит/Sakharovaite, ромб., сод. Fe, Sb
(Pb2IBi2II)S5- Косалит/Cosalite, ромб.
(Pb у Bi i,11 )S6 — Лиллианит/Lillianite, ромб.
— Канниццарит/Cannizzarite, монокл.
17— Кобеллит/Kobellite, монокл.
PbBi2Se3— Платинит/Platynite, триг., сод. S
(PbllBi^n)Se4— Поубаит/Poubaite, триг., сод. Те2", S2"
(Pb^IBi*1I)Se6SI1 — Вайбуллит/Weibullite, ромб.
(PbnBi 2П )Te2S2 — Алексит/Aleksite, псевдотриг.
РЬПСО3 — Церуссит/Cerussite, уст. свинцовый шпат/lead spar,
белая свинцовая руда/white lead ore, ромб., НМ 3,0—3,5, ^/6,55,
бел., сод. Sr, Zn, Ca [6]
РЬ^(СО3)С12— Фосгенит/Phosgenite, уст. кромфордит/cromford-
ite, роговой свинец/horn lead, тетр., НМ 2—3, flf 6,1, желт.-бел.
273
I. Неорганические вещества
Продолжение табЛ
РЬзЧСОзJ(ОНJ— Гидроцеруссит/Hydrocerussite, гекс, бел.
Pb"(CO3JSO4(OHJ — а) Ледхиллит/Leadhillite, уст. максит/тах*
ite, монокл., НМ 2,5—3,0, d6,5, бел.-гол. [6]. б) Сьюзаннит/Sus-
annite, триг. [6]
РЬПС12 — Котуннит/Cotunnite, уст. роговой свинец/horn lead,
ромб., я?5,8, бел.
Pbn(Cl)F — Матлокит/Matlockite, тетр., зел.-желт.
РЬз!С12О2— Мендипит/Mendipite, уст. чёрчиллит/churchillite,
ромб., dl,\, желт.-бел.
РЬП(С1)ОН — Лаврионит/Laurionite, ромб, или монокл.
РЬ^С13(ОН) — Пенфилдит/Penfieldite, гекс.
РЬ^С14(ОНJ— Фидлерит/Fiedlerite, монокл.
РЬпСг04 — а) Крокоит/Crocoite, уст. маланхроит/malanchroite,
красный свинцовый шпат/red lead spar, красная свинцовая руда/
red lead ore, монокл., НМ 2,5—3,0, d 5,9—6,1, оранж.-красн.
б) • Н2О, Иранит/Iranite, уст. хуниит/khuniite, трикл., желт.
Pb3!Cr04(As04HH — Форнасит/Fornacite, монокл., сод. Си
РЬ2т(СгО4)О — Финикохроит/Phaenicochroite, уст. хроминит/
chrominite, меланохроит/melanochroite, хромовая (или австрий-
австрийская) киноварь/chrome (Austrian) cinnabar, монокл., краен.
Pb^(CrO4J(PO4J • Н2О — Эмбриит/Embreyite, монокл.
Pb*I(FeIIISi3O10)OH - Ягоит/Jagoite, триг., сод. С1"
Pb^GeIV(SO4JO2(OHJ- Итоит/Itoite, ромб.
PbnHAsO4 — Схюлтенит (трад. шультенит)/8сЬи11еЫ1е, монокл.
Pb^(H2Te06)TeIV03— Гердит/Girdite, монокл.
РЬ^(Ю3)С13(О) — Зелигерит/Seeligerite, ромб.
РЬ^AО3JС14О2(ОНJ— Шварцембергит/Schwartzembergite, ромб.
РЬпМоО4 — Вульфенит/Wulfenite, уст. желтая свинцовая руда/
yellow lead ore, тетр., НМ 2,75—3,0, </6,5—7,0, желт., сод. Са, Ln,
W, V, Pb, U [6]
РЬПО — а) Массикот/Massicot, уст. свинцовая охра/lead ocher,
ромб., НМ 2, ?/9,3—9,6, желт. [6]. б) Глёт (свинцовый)/ЬШшве>
уст. литаргит/lithargite, тетр., НМ 2, */9,13, оранж. [6]
274
I. Неорганические вещества
Продолжение табл.
PbIV02— Платтнерит/Plattnerite, тетр., г/9,3, бур.-черн. [6]
?Ъ\1(?О4KС\ — Пироморфит/Pyromorphite, гекс, НМ 3,5—4,0,
J6,7—7,1, желт.-оранж., сод. Ва, Са, V, Fe, As [6]
(РЬ2!РЬ1У)О4— Сурик/Minium, уст. красный свинец/red lead,
тетр., d9, красн.-оранж.
PbI!S — a) Галенит/Galenite (galena), уст. свинцовый блеск/lead
glance, куб., НМ 2—3, d7,4—7,6, т.-сер., сод. Ag, Se2" [6].
б) Виттит/Wittite, монокл., сод. Bi, Se2~
PbnSO4 — Англсит (трад. aHnie3HT)/Anglesite, уст. свинцовый
купорос/lead vitriol, ромб., НМ 3,0—3,5, d 6,2—6,4, бел. [6]
PbI,I0SO4Cl2O8— Сундиусит/Sundiusite, монокл.
PbJ^SO^O — Ланаркит/Lanarkite, монокл.
PbSb — Садбериит/Sudburyite, гекс, сод. Ni
Pb5Sb2— Изомертиит/Isomertieite, куб., сод. Си, As
PbnSbin(Cl)O2- Надорит/Nadorite, ромб.
(PbJ!Sb]f)O7— a) Биндхаймит/Bindheimite, куб., НМ 4,0—4,5,
d 4,6—5,6, желт.-кор., сод. ОН", б) Монимолит/Monimolite, куб.
(PbnSb^n)S4— а) Геттардит/Guettardite, монокл., кор.-черн., сод.
As111, б) Туиннит/Twinnite, ромб.
(Pb"Sb4n)S7- Цинкенит/Zinkenite, гекс, НМ 3, ?/5,3-5,33,
т.-сер.
(Pb^Sb J")S5— Венит/Veenite, ромб., сод. As111
(Pb^Sbgir)S15— Фюлёппит/Fuloppite, монокл.
(Pb^SbJ^Sn — Буланжеит/Boulangerite, монокл., НМ 2,5—3,0,
d6,2, т.-сер., сод. Си, Fe, Zn [6]
(Pb^Sb^^Sjy — a) Плагионит/Plagionite, монокл., черн. б) Тинти-
наит/Tintinaite, ромб., сод. Bi
(Pb^Sbgn)S19— Гетероморфит/Не1еготоф11ке, монокл., черн.
(Pb ^ Sb 'У )S25 — Робинсонит/Robinsonite, трикл.
(Pb"Sb Jn)S21 — Семсиит/Semseyite, монокл.
(Pb}I2SbI1I0I)S27— Стерриит/Sterryite, ромб.
— Плейфэрит/Playfairite, монокл., черн.
275
I. Неорганические вещества
Продолжение табд
70
71
72
73
74
75
76
77
78
79
80
81
82
83
84
85
86
87
89
90
(PbI1I7Sb{I6I)S41 - Мадокит/Madocite, ромб., сод. As111
(PbI1I7SbJI2I)S50- Сорбиит/Sorbyite, монокл., сод. As111
^ — Лонеит/Launayite, монокл.
^^Cl — Дадсонит/Dadsonite, монокл.
Pb3SbTe4— Боровскит/Borovskite, куб.
PbnSe — Клаусталит/Clausthalite, куб., dl,9, сер.-черн.
PbnSe03 — Молибдоменит/Molybdomenite, монокл., черн.
PbnSe04— Керстенит/Kerstenite, ромб., J6,3, бел.
Pb"(SeO4)SO4— Ользакерит/Olsacherite, ромб.
PbnSi03 — Аламосит/Alamosite, монокл., бел.
(PbnSnn)S2- Тиллит/Teallite, ромб., НМ 2,5—3,0, d5,5, черн.
Sb^Su см. (FeIIPbJISn^ISbpS14
РЬиТе - Алтаит/Altaite, куб., </8,1, т.-сер.
РЬпТеО3 — Фэрбанкит/Fairbankite, трикл.
PbnU2O7 • 2Н2О — Вёльсендорфит/Wolsendorfite, ромб., сод. Са
PbIIU7/IO22 • 12Н2О — Вандендриссеит/Vandendriesscheite, ромб.,
т.-желт.
^^17 • 4Н2О - Кюрит/Curite, ромб., НМ 4-5, d7,2,
оранж.-краен. [6]
Pb^V2O7— Шервеит/Chervetite, монокл.
Pb^(VO4KC1 - а) Ванадинит/Vanadinite, гекс, НМ 2,75-3,0, </6,93,
краен., сод. Р, As, Са [6]. б) Эндлихит/Endlichite, гекс, сод. As
PbnWO4 — a) Распит/Raspite, монокл. б) Штольцит/Stolzite, тетр.,
НМ 2,5-3,0, d 7,9-8,3, красн.-бур.
PbnW2O7— Цзисянит/Jixianite, куб., сод. Fe, OH~
Pd — а) Палладий/Palladium, куб., d 12, св.-сер., сод. Pt, Ir.
б) Поларит/Polarite, ромб., сод. Pb, Bi
Pd2As — Палладоарсенид/Palladoarsenide, монокл.
Pd8As3 — Арсенопалладинит/Arsenopalladinite, трикл., сод. Sb
PdBi — Соболевскит/Sobolevskite, гекс.
PdBi2— а) Урванцевит/Urvantsevite, гекс, сод. РЬ. б) Фрудит/
Froodite, монокл.
276
I. Неорганические вещества
Продолжение табл.
Pd2Bi0 2As0 8 — Палладовисмутарсенид/Palladobismutharsenide,
ромб.
PdBiTe — Миченерит/Michenerite, сод. Pt
(Pd3ICu4)Se5— Остербосит/Oosterboschite, ромб.
PdHg — Потарит/Potarite, тетр., сер.
PdNiAs — Маякит/Majakite, гекс.
PdNiSbTe — Гексатестибиопаникелит/Hexatestibiopanickelite, гекс.
Pd3Pb — Звягинцевит/Zvyagintsevite, куб., сод. Pt, Au, Sn
Pd3Pb2— Плюмбопалладинит/Plumbopalladinite, гекс, черн.
PdHS — Высоцкит/Vysotskite, тетр., t/6,6, кор.-черн., сод. Ni, Pt
Pd7Sb3 — Стибиопалладинит/Stibiopalladinite, уст. аллопалладий/
allopalladium, гекс.
PdSbTe — Тестибиопалладит/Testibiopalladite, куб., сод. Bi
Pd17Se15— Палладсеит/Palladseite, куб.
Pd2Sn — Паоловит/Paolovite, ромб.
Pd3Sn — Атокит/Atokite, куб., сод. Pt
PdnTe — Котульскит/Kotulskite, гекс, сод. Bi
PdTe2— Меренскиит/Merenskyite, гекс, сод. Pt, Bi
Pd3_xTe — Китконнит/Keithconnite, триг.
Pd9Te4 — Теллуропалладинит/Telluropalladinite, монокл.
Pr2n(SO4)O2— Техасит/Texasite, ромб.
Pt — Платина/Platinum, куб., НМ 3,5—4,5, d 14—19, т.-сер., сод.
Pd, Ir, Fe, Ni
Pt(As2) — a) Платарсит/Platarsite, куб., сод. S. 6) Сперрилит/Sper-
rylite, куб., НМ 6-7, d 10,6, бел.
Pt(Bi2) — Инсизваит/Insizwaite, куб., сод. Sb
PtBiTe — Масловит/Maslovite, куб.
PtFe — Тетраферроплатина/Tetraferroplatinum, тетр.
Pt3Fe — Изоферроплатина/Isoferroplatinum, куб.
Pt2FeCu — Туламенит/Tulameenite, тетр.
277
I. Неорганические вещества
Продолжение табд
9
10
11
12
13
14
PtnS — а) Брэггит/Braggite, тетр., сод. Pd, Ni. б) Куперит/Cooperite
тетр., </8,8, черн., сод. Pd
Pt4S3— Генкинит/Genkinite, тетр., черн., сод. Pd
PtSb — Штумпфлит/Stumpflite, гекс, сод. Bi
Pt(Sb2) — Геверсит/Geversite, куб., т.-сер.
PtSn — Нигглиит/Niggliite, гекс.
Pt3Sn — Рюстенбургит/Rustenburgite, куб., сод. Pd
PtTe2— Мончеит/ Moncheite, гекс, черн., сод. Pd, Bi
Re — Рений/Rhenium, гекс, d20,5, св.-cep.
Rh — Родий/Rhodium, куб., d \2,4, бел., сод. Pt
Rh(As2) — Холлингуортит/Hollingworthite, куб., сод. Pt, Pd, S
Ru — Рутений/Ruthenium, гекс, d 12,3, бел.
RuAs — Рутенарсенит/Ruthenarsenite, ромб., сод. Ni
RuAs2 — Андуоит/Anduoite, ромб., сод. Os
Run(S2) — Лаурит/Laurite, куб., НМ 7—8, af 6,99, кор.-черн., сод. Os
S — а) Росицкийит (трад. po3Hmarr)/Rosickyite, монокл. (у),
желт.-бел. б) Сера/Sulfur, ромб, (а), НМ 1,5-—2,5, t/2,07, желт.,
сод. Se, Те, As [6]
1
1А
Sb — Сурьма/Antimony, трип, НМ 3,0—3,5, d6,6—6,7, гол.-сер.
SbAsx @,8 < х < 3,0) — Парадокразит/Paradocrasite, уст. алльмонит/
allemontite, мышьяковистая сурьма/arsenical antimony, мон., сер.
Sb(As)S — Гетчеллит/Getchellite, монокл., черн.
SbgnCl2On — Оноратоит/Onoratoite, трикл.
Sb^HO3— а) Сенармонтит/Senarmontite, куб., d5,19, бел. [6]. б)
Валентинит/Valentinite, уст. сурьмяные цветы/antimony bloom,
белая сурьма/white antimony, ромб., НМ 2,5—3,0, d5,76, бел. [6]
Sb^nS3 — а) Метастибнит/Metastibnite, аморфн. б) Стибнит/Stib-
nite, уст. серая сурьмяная руда/grey antimony ore, сурьмяный
(или серый копьевидный) блеск/antimony (grey spear) glance, антй"
монит/antimonite, ромб., НМ 2,0—2,5, d4,5—4,63, т.-сер., сод. Вь
As, Ag, Au [6]
278
I. Неорганические вещества
Продолжение табл.
Sb2nS2O — Кермесит/Kermesite, уст. сурьмяная обманка/antimo-
обманка/antimony blende, красный копьевидный блеск/red spear glance, сурьмя-
сурьмяная киноварь/antimony cinnabar, монокл., т.-красн. [6]
Sbin(SO4)O4(OHJ- Клебельсбергит/Klebelsbergite, ромб.
(SbnlSbv)O4 — Сервантит/Cervantite, уст. сурьмяная oxpa/antimony
ocher, ромб., d 5,82—6,6, желт. [6]
(SbinSb^)O6(OH) - Стибиконит/Stibiconite, куб., св.-желт. [6]
Sb2nTe3 — Теллурантимон/Tellurantimony, трип, d6,5, сер.
ScUIPO4 • 2Н2О — Кольбекит/Kolbeckite, монокл., бел.
Sc2nSi207 — Тортвейтит/Thortveitite, монокл., сер.-зел., сод. Y, Ln
Se — Селен/Selenium, трип, af 4,7, сер.
Se^C^ — Дауниит/Downeyite, уст. селенолит/selenolite, тетр.,
af 3,9, бел.
SiC — Муассанит/Moissanite, гекс. (а), НМ 9,0—9,5, d 3,2, бел.
Карборунд/Carborundum — искусственный М., зел.-черн. [4, 6]
[SiF6],K2— Гиератит/Hieratite, куб., г/2,6, бел.
[SiF6],(NH4J— а) Барарит/Bararite, гекс, НМ 2,5, </2,15, бел.
б) Криптогалит/Cryptohalite, куб., бел.
[SiF6],Na2— Малладрит/Malladrite, трип, t/2,6, бел.
SiO2 — а) Меланофлогит/Melanophlogite, куб., НМ 6,5—7,0, */2,05,
желт.-кор., сод. органические примеси, б) Коэсит/Coesite, мо-
монокл., d 2,91, бел. в) Тридимит/Tridymite, ромб, (а) или гекс. ф),
НМ 7, </2,265 (а), 2,192 (р), бел. [4]. г) Кристобалит/Cristobalite,
тетр. (а) или куб. (р), НМ 6,5, d 2,334 (а), 2,194 (р), бел. Люссаит
(трад. луссатит)/1лд88аШе — волокнистый а-К. д) Стишовит/
Stishovite, тетр., d4,287, бел. е) Кварц/Quartz, трип (а) или гекс.
(Р), НМ 7, d2,648 (a), 2,533 (Р), бел. [4]. Авантюриновый кварц/
Aventurine quartz — краен.-бур. К., сод. гематит, слюды [1]. Аме-
Аметист/Amethyst — фиол., т.-красн., желт, или бцв. К. [1]. Горный
хрусталь/Rock crystal — бцв. прозрачный К. [1]. Дымчатый кварц/
Smoky quartz, уст. раухтопаз/cairngorm (немецк. rauchquarz) —
бур. К. [1]. Карнеол/Carnelian — краен, или краен.-кор. К., сод.
гематит [1]. Лешательеит/Lechatelierite (горная порода) — стек-
стеклообразный переплавленный К., аморфн., d 2,203, сер. Морион/
Morion — черн. К. [1]. Новакулит/Novaculite — бел. мелкозернис-
279
I. Неорганические вещества
Продолжение пгабД
тый К. Розовый кварц/Rose quartz — роз.-красн. К. [1]. Сердолик/
(англ. термин отсутствует) — карнеол (разновидность кварца) или
сардер (разновидность халцедона). Синий кварц/Sapphire quartz -^
К., сод. рутил или роговую обманку [1]. Цитрин/Citrine, уст. запад,
ный {или испанский) топаз/occidental (Spanish) topaz — св.-желт.
К., сод. Fe [1]. Песок/Sand (горная порода) — мелкообломочная
(зёрна 0,05—2,0 мм) рыхлая смесь К., полевых шпатов, слюд и др.
[2]. ж) Халцедон/Chalcedony — волокнистый скрытокристалличе-
ский кварц, НМ 6,5—7,0, d2,57—2,64, сер.-гол. [1]. Агат/Agate -
X. с разноокрашенными полосами [1]. Гелиотроп/Heliotrope, уст.
кровавик/bloodstone — зел. X. с краен, вкраплениями [1]. Кре-
Кремень/Flint, уст. огневой камень (трад. oraeBHK)/firestone — смесь
кварца с X. и (реже) опалом, желт.-бур., НМ ~ 7 [4]. Моховой агат
(трад. moxobhk)/Moss agate — бел. X. с зел. включениями актино-
лита к роговой обманки. Оникс/Опух — X. с чередованием бел.,
сер., т.-кор. и черн. лент и полос, НМ 6,5, d2,6—2,64 [1]. Плазма/
Plasma — т.-зел. X., сод. Fe11 [1]. Празем (трад. npa3)/Prase — зел.
смесь X. с актинолитом. Сапфирин/Sapphirine — гол. X., сод. Mg,
А1 [1]. Сардер (трад. сард)/5а^ — красн.-бур. X., сод. лимонит
[1]. Сардоникс/Sardonyx — X. с краен, полосами [1]. Хризопраз/
Chrysoprase — ярко-зел. X., сод. Ni. Яшма/Jasper — краен, пёстро-
полосчатый X., сод. Fe, Мп [1]. з) • 0,ЗЗН2О, Силгидрит/Silhydrite,
ромб, и) • яН2О, Опал/Opal — разноокрашенная смесь лешателье-
ита (аморфн. разновидность кварца) с мелкокристаллическими
кристобалитом и (реже) тридимитом, НМ 5,0—6,5, d 1,99—2,25 [3].
Арлекиновый опал/Harlequin opal — краен. О. с пятнами других
окрасок [1]. Благородный опал/Precious (или noble) opal — О. с ра-
радужной игрой окрасок [1]. Гейзерит/Geyserite, уст. кремнёвая
(или опаловая) накипь/siliceous (opal) sinter — рыхлый О., отла-
отлагающийся из горячих источников и гейзеров, d 1,8—2,0. Гиалит/
Hyalite, уст. стеклянный опал/water-opal — бцв. прозрачный О.
[1]. Гидрофан/Hydrophane, уст. молочный опал/milk-opal — бел.
непрозрачный О. [1]. Менилит/Menilite, уст. печёночный опал/
liver-opal — сер.-бур. О. Огненный опал/Fire-opal — ярко-красн.-
оранж. прозрачный О. [1]. Перлит/Pearlite, уст. жемчужный блеск/
pearl glance, жемчужная накипь/pearl sinter — аморфн. вулканиче-
вулканический О., состоит из шариков диаметром 1—15 мм, d 1,3—1,6,
красн.-сер. Празопал/Prasopal — зел. О., сод. NiO
[Si(OHN]CO3(SO4), Ca3 • 12Н2О - Томасит (трад. таумасит)/
Thaumasite, гекс, НМ 3,5, d 1,88, бел.
280
I. Неорганические вещества
Продолжение табл.
Sn — а) Олово серое/Tin (grey), куб. (a), г/5,75, сер. б) Олово бе-
белое/Tin (white), тетр. (C), г/7,3, бел.
Sn!I0 — Ромаркит/Romarchite, тетр., d6,2, т.-гол.
Sn^Oj — Касситерит/Cassiterite, уст. оловянный камень/tinstone,
варламоффит/warlamoffite, оловянная руда/tin ore, тетр., НМ 6—
7, </6,98-7,02, красн.-кор., сод. Та, Nb, Fe, W, Se, In [6]
[Sn^COH^LMg - Шёнфлисит/Schoenfliesite, куб.
[SnIV(OHN],Mnn — а) Уикманит (трад. викманит)/\?юктапйе,
куб. б) Тетрауикманит/Tetrawickmanite, тетр.
SnnS — Герценбергит/Herzenbergite, ромб., d 5, бур.
SnIVS2 — Берндтит/Berndtite, триг. или гекс, d 4,5, желт.
SnSb — Стистаит/Stistaite, куб.
(SnnSnIV)S3— Оттеманит/Ottemannite, ромб.
SrAl3(AsO4)SO4(OHN— Кеммлицит/Kemmlitzite, триг.
Sr2Al(CO3)F5 — Стенонит/Stenonite, монокл.
SrAl2(CO3J(OHL • Н2О — Стронциодрессерит/Strontiodresserite,
ромб., сод. Са
SrAl3(PO4J(OHM • Н2О - Гойясит/Goyazite, триг.
Sr2Al(PO4JOH — Гудкенит/Goedkenite, монокл., сер., сод. Са
SrAl3(PO4)SO4(OHN — Сванбергит/Svanbergite, триг., св.-сер.
Sr(AlSiO4J — Слосонит/Slawsonite, монокл.
Sr(AlSi3O8J • 5Н2О — Брюстерит/Brewsterite, монокл., сод. Ва, Са [4]
Sr5(As04KF — Ферморит/Fermorite, уст. стронциоарсенапатит/
strontioarsenapatite, гекс, сод. Са, РО4~, ОН"
Sr2(B14O23) • 8Н2О — Стронциоджинорит/Strontioginorite,
монокл., сод. Са
Sr2(B5O9)Cl • Н2О — Стронциохильгардит/Strontiohilgardite,
монокл.
SrCO3 — Стронцианит/Strontianite, ромб., НМ 3,5, d 3,7, бел., сод.
Са, Ва [4, 6]
SrFe3n(PO4J(OHM • Н2О — Люсуньит/Lusungite, триг.
SrMn2n(VO4J • 4Н2О - Сантафеит/Santafeite, ромб.
281
I. Неорганические вещества
Продолжение mafa
15
16
17
Sr5(PO4KOH — а) Беловит/Belovite, гекс, сод. Се, Na, Ca.
б) Стронциоапатит/Strontioapatite, уст. саамит/saamite, гекс, сол
Ca, F"
SrSO4 — Целестин/Celestite (celestine), ромб., НМ 3,0—3,5,
</3,95-3,97, гол.-бел. [6]
SrVIV(Si207) — Харадаит/Haradaite, ромб.
6
7
10
11
12
(TayAl4)O13F — Симпсонит/Simpsonite, триг., сод. ОН~
(TavB)O4— Бехирит/Behierite, тетр., сод. Nb
(TavBiIU)O4 — Бисмутотанталит/Bismutotantalite, ромб.
(Ta^BiHI)O6(OH) — Бисмутомикролит/Bismutomicrolite, уст.
вестгренит/westgrenite, куб., черн., сод. Ca, Nb [6]
(TayFeH)O6- а) Танталит/Tantalite, ромб., НМ 6,5—7,0, </6,2-
8,2, черн., сод. Mn, Nb [6]. б) Тапиолит/Tapiolite, тетр., НМ 6,0-
6,5, d7,3—7,8, черн., сод. Mn, Nb [6]
(ТаУ_яМпУ_2хре2!)°12 @,08 < х< 0,29) - Уоджинит/Wodginite,
монокл., НМ 5,5—6,0, dl,3, красн.-бур., сод. Nb, Sn [6]
(Та^Мпп)О6— Манганотанталит/Manganotantalite, ромб., dl9
черн. [6]
(TavPbn)O3(OH) — Плюмбомикролит/Plumbomicrolite, куб.,
желт.-кор., сод. Nb, Ti, F~ [6]
(TavSbHI)O4— Стибиотанталит/Stibiotantalite, ромб., НМ 5, rf7,5,
т.-кор., сод. Nb
(Ta^SnIV)O7— Торолит/Thoreaulite, монокл., сод. Nb
(Ta^Sn^)O7— Сукулаит/Sukulaite, куб., сод. Nb
(TavSnn)O3(OH) — Станномикролит/Stannomicrolite, куб., желт.-
кор.,сод. Nb,Ti, F"[6]
1 Те — Теллур/Tellurium, триг., НМ 2,0—2,5, d6,2, сер.-бел., сод. Se
2 TeIVO2 — Теллурит/Tellurite, уст. теллуристая oxpa/tellurium
ocher, ромб, или тетр., d 5,6, желт. Блейкит/Blakeite — кор. Т., сод.
Fe
1 lbwO2 — Торианит/Thorianite, куб., НМ 6,5, d9,7, черн., сод. U,
2 ThIVSiO4 — а) Хаттонит/Huttonite, монокл., d7,1, бел. б) Торит/
Thorite, уст. оранжит/orangite, тетр., НМ 4,5—5,0, J4,4—6,7,
оранж.-черн., сод. U, Y, Ln, Fe, Ca, Mn, P, Al, Ti [6]
282
I. Неорганические вещества
Продолжение табл.
(ThIVTil,v)O6 — Торутит/Thorutite, монокл., сод. U, Са, ОН~
(Th^U^C^ — Уранторианит/Uranthorianite, куб., сер.-кор.
ThIVUIV(Si04J — Ураноторит/Uranothorite, тетр., зел.-черн.
Th3vUIV(SiO4K(OHL — Торогуммит/Thorogummite, уст. макин-
тошит/mackintoshite, НМ 5,5, d 5,43, черн., сод. Pb, Ln, Fe, Na, К
(ThIVYIHTiIV)O5(OH) — Иттрокразит/Yttrocrasite, ромб., НМ 5,5-
6,0, flf 4,8, черн., сод. Ег, Се, Са, U, Fe, W
(TiIVFen)O3 — Ильменит/Ilmenite, уст. менакканит/menaccanite,
титанистый железняк/titanium iron ore, трип, НМ 5—6, af 4,7—
4,78, черн., сод. Mg, Mn [6]
(TiIVFe^)O4 — Ульвёшпинель/Ulvospinel, уст. ульвит/ulvite, куб.,
НМ 7,5-8, d 4,78, т.-кор.
(TiIVFe2H)O5— Псевдобрукит/Pseudobrookite, ромб., т.-кор.
(Ti'vFe4nSbni)O13(OH) - Дербилит/DerbyUte, монокл.
(TiIVMnn)O3 — Пирофанит/Pyrophanite, триг., d4,5, краен. [6]
TiuO — Хонквиит/Hongquiite, куб., */4,8, желт.
TiIV02 — а) Брукит/Brookite, ромб., НМ 5,5—6,0, d4,14, желт.-кор.
[6]. Арканзит/Arkansite — черн. Б. б) Анатаз/Anatase, уст. октаэд-
рит/octahedrite, тетр., НМ 5,5—6,0, d3,9, зел.-желт., сод. Fe, Zn,
Nb [6]. в) Рутил/Rutile, тетр., НМ 6,0—7,5, rf4,2—4,4, красн.-кор.,
сод. Nb [1, 5, 6]. Нигрин/Nigrite (nigrine) — желт.-черн. Р., сод. Fe
(до 11%). Стрюверит/Struverite, уст. ильменорутил/ilmenorutile —
гол.-фиол. Р., сод. Та
(TiIVPbI!)O3 — Македонит/Macedonite, тетр., г/7,5, желт.
TiIV(Te 3VO8) — Уинстанлиит/Winstanleyite, куб.
(Ti^vV4nAsHI)O13(OH) - Томичит/Tomichite, монокл.
(Ti ^V )O9 — Шрейерит/Schreyerite, монокл.
(TIIAsllI)S2 — Лоранит/Lorandite, монокл., НМ 2,0—2,5, rf5,53,
т.-краен.
(Tl*AsHI)S3— Эллисит/Ellisite, триг.
ТЦПО3 — Авиценнит/Avicennite, куб., d 10,1, кор.-черн.
(TlIPbIIAs5II)S9— Хатчинсонит/Hutchinsonite, ромб., краен., сод.
Ag,Cu
283
Неорганические вещества
Продолжение та^
(T\lPbl2lAsl5u)SlQ— Ратит/Rathite, монокл.
T12S — Карлинит/Carlinite, трип, d 8,3, черн.-син.
(TlISbIII)S2— Вайссбергит/WeiBbergite, трикл.
(Tl'Sb^JSg — Пьерроит/Pierrotite, ромб, или монокл., сод. As
(Tl^Sb'I1I)S34— Шабурнит/Chabourneite, трикл.
UIV(MoO4J — Седовит/Sedovite, ромб.
UIV(Mo^O17) • 5Н2О — Моурит/Mourite, монокл.
(UIVNbvFeII)O8 — Печекит/Petscheckite, гекс, сод. Та
(U^Nb рО8 — Льяндраит (трад. лиандратит)/иаг^га1ке, гекс,
сод. Та
(UIVNb^)O6(OHJ — Уранпирохлор/Uranpyrochlore, уст. эллсуор-
тит/elsworthite, куб., ^ 4,82—4,93, черн., сод. Са, Се, Та, F~ [6]
UIVO2 + х @ < jc < 0,67) — Уранинит/Uraninite, уст. ульрихит/ulri-
chite, куб., НМ 5,6-7,0, d8,0-10,9, бур.-черн., сод. Th, Pb, Fe,
Zr, Ra, He, Ar [6]. Клевеит/Cleveite, уст. брёггерит/broggerite —
У., сод. Ln (до 16%). Урановая смолка (или урановая смоляная об-
обманка, урановая смоляная pyaa)/Pitchblende, уст. настуран/nas-
turane — аморфн. стекловидный У.
и^Оз 0,25РЬпО • 1,25Н2О — Фурмарьеит/Fourmarierite, ромб.,
краен.
(UO2+LAlHAsO4(AsO4K • 40Н2О — Арсенураношпатит/Arsenura-
nospathite, тетр.
(UO2+)A1HPO4(OHK • 4Н2О — Ранункулит/Ranunculite, монокл.
(UO2+LA1HPO4(PO4K- а) • 16Н2О, Сабугалит/Sabugalite, тетр.
б) • 40Н2О^ Ураношпатит/Uranospathite, тетр.
(UOf)Al2(PO4J(OHJ • 8Н2О - Фуронгит/Furongite, трикл.
(UOfJAl(PO4JOH • 8Н2О - Тредголдит/Threadgoldite, монокл.
(UOf KА1(РО4J(ОНK - Упалит/Upalite, ромб.
(UOfJAl(VO4J(OH) - а) • 8Н2О, Метавануралит/Metavanuralite,
трикл. б) • 11Н2О, Вануралит/Vanuralite, монокл.
(UO2+K(AsO4J • 12Н2О — Трёгерит/Trogerite (troegerite), тетр. 0)
(UO^+)CO3 — а) Рёзерфордин/Rutherfordite (rutherfordine), ромб.,
d5,2, св.-желт. б) • A,5—2,0)Н2О, Жолиоит/Joliotite, ромб.
284
I. Неорганические вещества
Продолжение табл.
(UO2+JCon(AsO4J • 8Н2О — Метакирхгаймерит/Metakirchhe-
imerite, тетр. (?)
^^ — а) • 8Н2О, Метацойнерит/Metazeunerite,
тетр. б) • A0—16)Н2О, Цойнерит/Zeunerite, тетр.
(UO2+)CuH(OHL— Ванденбрандеит/Vandenbrandeite, уст. урано-
лепидит/uranolepidite, трикл., св.-син.
(UO^+KCu2I(OHI0 • 5Н2О — Рубоит/Roubaultite, трикл.
(UO2+JCun(PO4J— а) • яН2О (п < 8), Метатурбернит/Metatorber-
nite, тетр., d3,5—3,7, зел.-желт. [6]. б) • (8—12)Н2О, Турбернит
(трад. торбернит)/ТогЬегпйе, уст. купроуранит/cuprouranite,
тетр., НМ 2—3, d 3,2—3,6, ярко-зел., сод. Ra [6]
(UO2+JCu^IPb2I(SeIVO3N(OHN • 2Н2О — Демесмекерит/Demes-
maekerite, трикл.
(UOfJCun(SO4J(OHJ • 6Н2О - Иоганнит/Johannite, уст. гил-
пинит/gilpinite, урановый купорос/uranium vitriol, трикл., НМ
2,0-2,5, d3,19-3,3, св.-зел. [6]
(UO2+)Cu44SeIVO3J(OHN • Н2О - Дерриксит/Derriksite, ромб.
(иО2+)зСип(8е1УОз)з(ОНJ • 7Н2О - Мартозит/Marthozite, ромб.
(UO2+JCun(SiO3J(OHJ • 5Н2О — Купросклодовскит/Cuprosk^o-
dowskite, уст. уранохальцит/uranochalcite, урановая зелень/urani-
зелень/uranium green, трикл.
(UO2+)Cun(VO4)OH • 6Н2О — Сенжьеит/Sengierite, монокл.
(UOf JFe2"Al2(PO4LSO4(OHJ • 20Н2О - Кокониноит/Coconi-
noite, монокл. (?)
(UO2+JFen(AsO4J — а) • 8Н2О, Метакалерит/Metakahlerite, тетр.
б) • яН2О (п > 8), Калерит/Kahlerite, тетр.
(UO2+JFen(PO4J • 8Н2О — Бассетит/Bassetite, монокл.
(UO2+LFein(PO4J(SO4JOH • 22Н2О - Сянцзянит/Xiangjiangite,
псевдотетр., сод. А1
(UOfJMnn(PO4J • 10Н2О - Фричеит/Fritzscheite, тетр.
(UO^+)MoO4 • 4Н2О — Умохоит/Umohoite, ромб, или монокл.
(UO^+)Mo2O7 • ЗН2О — Иригинит/Iriginite, монокл.
(UQ2+)NH4PO4 • ЗН2О - Урамфит/Uramphite, ромб. (?)
285
I. Неорганические вещества
Продолжение mafy
(UOfNNi^(SO4K(OHI0 • 16Н2О - Никель-циппеит/Nickel-
zippeite, ромб.
(UO 2+)(OHJ • Н2О — Шёпит (трад. CKynmO/Schoepite, ромб., d$
желт.
(UOfKO(OHL • ЗН2О - Иантинит/Ianthinite, ромб., НМ 2-3,
</5,15,т.-фиол. [6]
(UO2+)Pb^(AsO4J — Халлимондит/Hallymondite, трикл.
(UOfKPb^(AsO4J(OHL • ЗН2О - Хюгелит/Hugelite, монокл.
(UO^+)Pb^(PO4J • 2Н2О — Парсонсит/Parsonsite, трикл.
(UOfJPbn(PO4J- а) • ЗН2О, Девиндтит/Dewindtite, ромб,
б) • 4Н2О, Пржевальскит/Przhevalskite, ромб.
(UO2+KPb2I(PO4J(OHL • ЗН2О — Дюмонит/Dumontite, монокл.
(UOfLPbn(PO4J(OHL • 7Н2О - Ренарит/Renardite, ромб.
(UO^+)PbnSiO4 • Н2О — Казолит/Kasolite, уст. дрогмансит/droog-
mansite, монокл., НМ 4—5, d6, желт.-кор. [6]
(U02+)Pbn(TeIV03J— Моктесумит/Moctezumite, монокл.
(UO^+JFbn(VO4J • 5Н2О — Кюрьенит/Curienite, ромб.
(UOfNSO4(OHI0 • 12Н2О - Уранопилит/Uranopilite, уст. ура-
урановая охра/uranium ocher, монокл., желт.-кор.
(UOfI5Si6O17(OHJ0 • 8Н2О — Соддиит/Soddyite, ромб.
(UO2+)TeO3— Шмиттерит/Schmitterite, ромб.
(UOf)TeJvO7- Клиффордит/Cliffordite, куб., т.-желт.
(UO2+JZnn(AsO4J • 10Н2О — Металодевит/Metalodevite, тетр.
(UOfNZn^(SO4K(OHI0 • 16Н2О - Цинк-циппеит/Zinc-zippeite,
ромб.
UIVSiO4— Коффинит/Coffinite, тетр., НМ 5—6, </5,1, зел., сод.
ОН" [6]
(UIVTa2v')O6(OH) — Уранмикролит/Uranmicrolite, уст. джалмаит/
djalmaite, куб., черн., сод. Nb, F"
(UIVTi2v)O6— Браннерит/Brannerite, монокл. или ромб., НМ 4,5,
^/4,5—4,53, черн., сод. Са, Th, Y, Fe
UIV(UOf K(НМоО4L(МоО4K • 18Н2О - Молуранит/Moluranite,
аморфн.
286
I. Неорганические вещества
Продолжение табл.
(V^Cu^)O10— Штойберит/Stoiberite, монокл.
(VjI!Fen)O4 — Коулсонит/Coulsonite, куб.
У™02 — Парамонтрозит/Paramontroseite, ромб., d4,3, син.-черн.
V2nO3 — Карелианит/Karelianite, трип, af4,8, черн.
V^O5— а) Щербинаит/Shcherbinaite, ромб., d3,3, краен,
б) • ЗН2О, Навахоит/Navajoite, монокл., желт.
VniO(OH) — Монтрозит/Montroseite, ромб., НМ 4,0—4,2, черн.,
сод. Fe [6]
VIVO(OHJ — Даттонит/Duttonite, монокл., роз.
[V^O6(OHJ],SrCa — а) Метадельриоит/Metadelrioite, трикл.
б) • ЗН2О, Дельриоит/Delrioite, монокл., бел.
(VO2+)SO4 • 5Н2О — Минасрагрит/Minasragrite, монокл., т.-гол.
У(&2J — Патронит/Patronite, монокл., d2,65—2,71, зел.-черн. [6]
(VIVSb^n)O5— Стибиванит/Stibivanite, монокл.
(yivyy^Q^ . бн2о _ Бариандит/Bariandite, монокл.
(VinVIV)O2(OHK- Хеггит/Haggite, монокл.
WVIO3— а) • яВ^иО3, Расселлит/Russellite, тетр. б) • Н2О, Тунгс-
тит/Tungstite, уст. вольфрамовая охра/tungsten ocher, ромб. (?),
d5,5, желт. [6]. в) • Н2О, Алюмотунгстит/Alumotungstite, триг.,
сод. А1, ОН", г) • 2Н2О, Меймакит/Meymacite, аморфн., t/5,517,
ярко-желт, д) • 2Н2О, Гидротунгстит/Hydrotungstite, монокл., d4,
желт. [6]
[W^IO6(OHK],CeIH— Церотунгстит/Cerotungstite, монокл.
W^Sj — Тунгстенит/Tungstenite, гекс. w/штрип, НМ 1—2, J7,4—
7,5, сер.-гол.
Y4n(Al2Si2O10)(CO3K • 4Н2О — Кайсихит/Caysichite, ромб., сод.
Са, Ln
YInAsO4 — Черновит/Chemovite, тетр.
Y^n(CO3K • 2Н2О — Локкаит/Loccaite, ромб., сод. Са
YHI(CO3)F — Иттробастнесит/Yttrobastnasite, гекс, желт., сод. Се [6]
YIUCu^(AsO4K(OHN • ЗН2О — Агардит/Agardite, гекс, сод. Са
YUIMn^AsO4(OHL— Ретциан/Retzian, ромб.
287
I. Неорганические вещества
Продолжение ma(jA
8
9
10
11
12
13
14
15
16
17
(YinNbv)O4— a) Иттроколумбит/Yttrocolumbite, ромб., сод. U, Fe
Та. б) Фергюссонит/Fergussonite, уст. брагит/bragite, тирит/tyrite'
тетр. (а) или монокл. (р), НМ 5,0—6,5, d4,2—6,0, зел.-бур., сод
Та, Ln, U [6]
(YHINb^)O6(OH) — Иттропирохлор/Yttropyrochlore, уст. обруче-
вит/obruchevite, куб., кор., сод. Na, Ln, Ca, U, Та, Ti, F~ [6]
YIHPO4— Ксенотим/Xenotime, уст. иттриевый шпат/yttrium spar,
тетр., НМ 4—5, d4,25—4,3, св.-желт., сод. Ln, U, Th, Zr [6]
Y2"Si207 — Таленит/Thalenite, монокл., НМ 6,5, af 4,11—4,23,
желт.-красн., сод. Ln
Y'H(Si04JF — Роулендит/Rowlandite, аморфн., НМ 6, d 4,51,
зел.-кор., сод. Ln, Fe, Mn, ОН"
Y^II(SiO4K(OHK— Иимориит/Iimoriite, трикл.
(YinTav)O4— а) Иттротанталит/Yttrotantalite, монокл. (?), черн.,
сод. Fe, U, Ca, Nb. б) Форманит/Formanite, тетр., НМ 6,5—7,5,
г/5,8, бур.-черн. [6]
(YIIITa2v)O6(OH) — Иттромикролит/Yttromicrolite, уст. ельмит
(трад. хьельмит)/1уе1тие, куб., НМ 5—6, d5,S, зел.-кор., сод. Са,
Nb, Ln, F"
(YniTiIVNbv)O6 — a) Иттроэшинит/Yttroeschynite, уст. прайорит
(трад. приорит)/ргюгке, ромб., НМ 5—6, d5, черн., сод. Ег, Са,
Fe, Th, ОН", б) [Ti > Nb], Поликраз/Polycrase, ромб., НМ 5-6,
*/4,97—5,04, черн., сод. Ег, Се, U, Ca, Th, Та. в) Самарскит/Sa-
marskite, уст. хлопинит/khlopinite, неправ, уранотанталит/urano-
tantalite, ромб., НМ 5—6, d5,7, кор.-черн., сод. Ег, Се, U, Fe, Ca,
Pb, Th, Та, Sn, ОН~. г) [Nb > Ti], Эвксенит/Euxenite, ромб., НМ
6,5, d4,6—5,1, черн.-кор., сод. Са, U, Ln, Th, Та, Fe
(YIIITiIVTav)O6 — Тантэвксенит/Tanteuxenite, ромб., черн., сод.
Се, Са, Nb
YHIVO4— Уэйкфилдит/Wakefieldite, тетр.
Zn — Цинк/Zinc, гекс, dl,\, бел.
(ZnnAl2)O4— Ганит/Gahnite, уст. цинковая шпинель/zinc spinel,
аутомолит/automolite, куб., НМ 7,5—8,0, d4,62, гол.-зел. Дислу-
ит/Dysluite — Г., сод. Мп. Крейттонит/Kreittonite — Г., сод. Fe
ZnnAl2(PO4J(OHJ • ЗН2О — Клеманит/Kleemanite, монокл.
288
I. Неорганические вещества
Продолжение табл.
ZnnAl6(PO4L(OH)8 • 5Н2О — Фаустит (трад. 4>ocTHT)/Faustite,
трикл.
ZnnAl2(SO4L • 22Н2О — Дитрихит/Dietrichite, монокл., бел., сод.
Fe, Мп
Zn3!Al3SO4(OHI3 * 2,5Н2О — Цинкалюминит/Zincaluminite, гекс.
(ZnHAs2n)O4 — JIeftTeHT/Leit(h)eite, монокл.
Og— Райнерит/Reinerite, ромб.
Zn^(AsO4J— a) • 2Н2О, Вариканит/Warikahnite, трикл. б) • 8Н2О,
Кёттигит/Kottigite (koettigite), монокл.
Znu(AsvO3)OH • Н2О — Коритнигит/Koritnigite, трикл.
Zn^AsO^OH — а) Аданин (трад. адамин)/Ас!атке (adamine),
ромб, илитрит., НМ 3,5, </4,34—4,35, желт., сод. Си, Со, Fe [4, 6].
б) • Н2О, Легранит/Legrandite, монокл.
Zn4(BeSi04KS — Гентгельвин/Genthelvite, куб., желт.-бел.
ZnnCO3 — Смитсонит/Smithsonite, уст. галмей (благородный)/
(precious) calamine (англ.) или (edler) galmei (немецк.), цинковый
шпат/zinc spar, трип, НМ 4,0—4,5, dA—5, зел.-бур., сод. Fe, Co,
Си, Mn, Ca, Cd, Mg, Pb [6]
Zn2-ICO3(OHJ — Цинкрозасит/Zincrosasite, монокл., сод. Си
Zn5!(CO3J(OHN— Гидроцинкит/Hydrozincite, уст. цинковые
цветы/zinc bloom, монокл., НМ 2,0—2,5, d 3,6—3,8, сер. [6]
ZnnO — Цинкит/Zincite, уст. красная цинковая руда/red zinc ore,
гекс, НМ 4—5, J5,7, т.-красн., сод. Мп, Fe111 [6]
Zn*J(PO4J • 4Н2О — Хопит (трад. гопеит)/Норейе, ромб, или
трикл., НМ 3,5, d 3,0-3,1, бел.
Zn^(PO4)OH — а) Тарбаттит/Tarbuttite, трикл., dA, сер.-бел.
б) • 1,5Н2О, Спенсерит/Spencerite, монокл.
Zn2IPbII(As04J • 2Н2О — Хельмутвинклерит/Helmutwinklerite,
трикл.
ZnnPb°SiO4 — Ларсенит/Larsenite, ромб.
Zn2IPb4ISiO4(Si2O7)SO4— Квейтит/Queitite, монокл.
ZnnPbn(VO4)OH - Деклуазит/Descloizite, ромб., НМ 3,0-3,5,
^5,9—6,2, краен.-оранж., сод. Си [6]
10-2004
289
I. Неорганические вещества
Окончание rnafa
23
24
25
26
27
28
29
30
31
Zn"S — а) Вюрцит/Wurtzite, гекс, НМ 3,5-4,0, d 3,98, бур.-черн^
сод. Fe, Cd [6]. б) Сфалерит/Sphalerite, уст. цинковая обманка/ **
zinc blende, блэкджек/blackjack, куб., НМ 3,5—4,0, d3,9—4,1,
сер.-бел., сод. Mn, Cd, Co, Ge [6]. Клейофан/Clayophan, уст. ме-
медовая обманка/honeyblende — оранж.-желт. прозрачный С, сод.
Fe [1]. Марматит/Marmatite — черн. С, сод. Fe. Печёнковая (или
скорлуповатая) обманка/hepatic (shelly) blende — смесь С. с вюр-
цитом. в) Полхемусит/Polhemusite, тетр., сод. Hg. г) Матраит/
Matraite, триг.
ZnnSO4— а) • Н2О, Бойлит/Boyleite, монокл., бел., сод. Mg.
б) • Н2О, Ганнингит/Gunningite, монокл., роз.-бел., сод. Мп.
в) Бьянкит/Bianchite, монокл., сод. Fe. г) • 7Н2О, Цинкмеланте-
рит/Zincmelanterite, монокл., сод. Си, Fe. д) • 7Н2О, Госларит/Go-
slarite, уст. цинковый (или белый) купорос/zinc (white) vitriol,
ромб., </1,9, бел.
(ZnnSb2n)O6— Ордоньесит/Ordonezite, тетр.
ZnHSe — Штиллеит/Stilleite, куб., */5,4, т.-желт.
Zn^SiO4— Виллемит/Willemite, триг., НМ 5,5, </3,9—4,2, бел.
(сод. Mn, Fe, Ca, Mg [6]) илижелт. прозрачный [1]
Zn3ISi205@HL— Фрепонтит/Fraipontite, монокл., сод. А1
Zn^l(Si205J@HJ • 4Н2О — Цинксилит/Zincsilite, монокл. (?)
Zn"Si2O7(OHJ • Н2О — Гемиморфит/Hemimorphite, уст. кала-
мин/calamine (англ.) uaugdlmti (немецк.), галмей обыкновенный
(или кремнёвый)/соттоп (siliceous) calamine, кремнистая цинко-
цинковая руда/siliceous zinc ore, ромб., НМ 4,5—5,0, */3,4—3,5, бел. [6]
ZnnWO4— Санмартинит/Sanmartinite, монокл., сод. Fe
ZrIV02— а) Тажеранит/Tazheranite, куб., сод. Ca, Ti. б) Баддлиит,
(трад. бaддeлeит)/Baddeleyite, уст. бразилит/brazilite, монокл.,
НМ6,5, ?/5,4-6,0, бел. [6]
ZrIV(SO4J • 4Н2О — Циркосульфат/Zircosulfate, ромб., */2,8, бел.
ZrIVSiO4— Циркон/Zircon, тетр., НМ 7,5, J4,68—4,7, бур.-желт.,
сод. Ln, Hf, Nb, Fe [4, 6]. Гиацинт/Hyacinth — красн.-кор. U- [U*
Жаргон/Jargon — бцв. или дымчатый Ц. [1]. Малакон/Malacon ~~
стекловидный Ц., НМ 6, d 3,9, гол.-бел., сод. Th, H2O C,0—9,5*)-
Старлит/Starlite — син. Ц. [1]. Циртолит/Cyrtolite — циркон, соД-
U,Th,Y[6]
290
I. Неорганические вещества
названий
указатель
русские названия
дбернатиитКЮЗ
дбихит Си22
Авантюрин Na9a
двгит Na66
двиденнит ТВ
двогадритВ1
дврорит Мп44
Дгардит Y5
Агат Si5x:
моховой Si5x
Аг(в)иларит Ag48
Агреллит Na85
АгриньеитК101
Адамин, Аданин Znl la
АделитСа127
Адмонтит Mg236
Адуляр К 10а
Азопроит Mg42a
Азурит СиЗб
Айкинит Си79а
Айоваит Mg45
Айтелит№155
АйфелитК91
АкаганеитРеЮ7г
Акантит Ag39a
АкатореитМпЮ
Аквамарин Ве2
Акдалаит А1236
Акерманит Са147а
АкмитЫа130
Акрохордит Mg58
Аксаит Mg22a
АктинолитСа150а
Алабандин Мп69
Аламосит РЬ79
тСи^
Алебастр Са193в
Александрит Bel
Рексит РЬ25
АллактитМпП
Pdl5
АллофанА123г
Аллуаит А146г
АллхаритРе107б
Алмаз С1б
Алтаит РЬ82
Алунит К7
Алуноген А138
Альбит Na9a
Альванит А150
Альдерманит Mgl5
Альмандин Fel7
Альстонит Ва13в
Альтхаусит Mg73a
Альфельдит Ni36
Алюминит А1406
Алюмогидрокальцит Са7
Алюмокатофорит Na57
Алюмокопьяпит Fel6
Алюмотунгстит WIb
Амазонит КЮв
Амакинит FelO6
Амальгама Ag21
Амарантит Fel37
Амариллит Nal26
Амблигонит Li2
Амегинит Nal7
Аметист Si5e
восточныйАШ
Амицит К76
Аммониохаросит Fe97
Амосит Fel55
Амфиген К9
Анальцим Na86
Анандит Ва26
Анапаит Са98а
Анатаз Ti76
Ангидрит Са193а
Англезит, Англсит РЬ52
Анд ал ус ит А144а
Андезин Na96
Андерсонит Na95
Анджелеллит Fe26
Андорит Ag35a
Андрадит СаЮб
Андремейерит Ва25
Андуоит Ru3
АнилитСи51
Анкерит Са90
Аннабергит Ni 126
Аннит К38
Анортит Са20а
Анортоклаз Na9B
Анритермьеит Са172
Антарктикит Са68
Антигорит Mg81 a
Антимонит Sb56
Антимонпирсит Ag46a
АнтлеритСи119а
Антониит Си44
Антофиллит Mg36
Антуанит А152а
Апатит Са 18 66
Апачит Си 132
Апджонит Мпб
АплоуитСо13а
Апуанит Fe84
Арагонит Саб 16
Арамайоит Ag426
Арведсонит Na 121
Аргентит Ag396
Аргентопентлендит Fe5
Аргентопирит Fe4a
Аргентохаросит Fe6
Аргиродит Ag20
АрдеалитСаИЗ
Арденнит Mg57A
Арканзит Ti7a
Арканит К98
Армангит As4
Арменит Ва12
Армолколит Mg92
Армстронгит Са274
Аррохадит К83
Арсенат-бел овит Са124
Арсенбраккебушит Fel 18
Арсенобисмит Bi3
Арсеноклазит Мп16
Арсеноламприт As2
Арсенолит As3a
Арсенопалладинит Pd3
Арсенопирит Fe30
Арсенополибазит Ag4a
Арсеносульванит Си28а
Арсенуранилит Са235
291
I. Неорганические вещества
Арсенураношпатит U8
Артинит Mg31a
Арчерит К50
Асбекасит Са58
Асбест, голубой Nal20
Астраханит Nal64
Астролит К1а
Атабаскаит Си56
Атакамит Си45б
Ателестит Bi4
АтокитРс119
АтопитСа194б
Аттапульгит Mg85
АубертитСиЮ
Аугелит А128а
Аурикуприд СиЗО
Аурипигмент As5
Аурихальцит Си 147
АуростибитАиИ
Аустинит Са264
Аутомолит Zn2
Афвиллит Са200г
Афинаит Pd2
Афтитамит К94
АхоитК31
АхроитЫа138
Ацикулит Си79а
АшавалитРеНб
АшаритВ31
АширитСи131
АштонитЫаЮа
Аюин Nal6a
Бабеффит Ва9
Бабингтонит Са93
Бавенит Са50
Бадделеит Zrl6
Баддингтонит N1
Баддлиит2г1б
Базалюминит А141а
Байерит А124а
Байтаунит Са20б
Балканит Agl3
Балл ас С16
Балякинит Си 137а
Бамболлаит Си 1276
Баналсит Na23
Бандилит В7
Баннистерит Nal78
Барарит Si3a
Барбертонит Mg35a
Барбосалит Fe76a
Барбьеит КЮв
БариандитУ12
Барилит ВаЮ
Бариомикролит Ва42
Бариопирохлор Ва38
Барисилит Мп64
Барит Ва39
Баритокальцит Ва13б
Баритоцелестин Ва39
БарнситЫа221
Баррерит Na47
Баррингерит FelO8
Баррингтонит Mg296
Барруаит Na63
BapcaHOBHTNalOl
Бартонит К42
БассанитСа193б
Бассетит U30
Бастинит Мп40
Бастнесит СеЗ
Батисит Na29
Бафертисит Ва44
Бахианит А142
Бацирит Ва56
БаццитВе12
Беарсит Ве4
Бёггильдит Nal99
Бёданит Fel20
Бейерит Са59
Бейкерит Са39А
Бейлиит Mg94
Бейлиссит К62
Беккелит СаббА
Беккерелит Са239
Беллит Ag33A
Беллидоит Си 1286
Беллинджерит Сибб
Бел овит Sri 5а
Бементит Мп84а
Бёмит А1266
Бенитоит Ва46
Бенстонит Ва14
Бераунит Fe79
Берборит Be56
Бергенит Ва51
Берёзовит Сг4а
Берилл Ве2
Бериллит Be 14
Бериллонит Na31
Берлинит А127а
Берманит Мп47
Берндтит Sn7
Берриит Си88
БертонитСиЮб
Бертоссаит Li 10
Бертран(д)итВе15
Бертьеин Fel53a
БертьеитРе144
Берцелианит Си 128а
Берцелиит Na70
Бессмертновит Аи9
Бета-розелит Са69б
Бета-уранофан Са243
Бетафит Na220
Бета- церийфергюссонит
Себ
Бетехтинит Fe61
Беусит Мп59а
Бехирит Та2
Бехоит Ве9
Биберит Со13в
Бидо(кс)ит Ag33
Бийеит Ва48
Бикитаит Li5B
Биккулит СаЗ 1
Биксбиит Мп55
Билинит Fe826
Биллингслиит Ag45
Бильетит Ва48
Биндхаймит РЬ58а
Биннит Fe48
Биотит Кб 1
Бирингуччит Na20
Бирюза Си7
Бисмит Bi86
Бисмоклит Bi6
Бисмутит Bi5
Бисмутомикролит Та4
Бисмутотанталит ТаЗ
Бисмутоферрит Fe34
БиссолитСа150а
Битиит Li9
Битовнит Са20б
Бифосфаммит N5
БичулитСа31
Бишофит Mg346
Бланшардит Си 120а
292
I. Неорганические вещества
Блёди
БлейкитТе2
Блеск
висмутовый Bill
железный Fe 1056
жемчужный Si5n
кобальтовый Со5а
красный копьевид-
копьевидный Sb6
марганцевый Мп69
медный Cul 15
молибденовый Мо4б
никелевый N113
свинцовый РЬ51 а
селеновисмуто-
выйВПЗ
серебряно-медный
Agl7
серебряный Ag396
серый копьевидный,
сурьмяный Sb56
Блэкджек Zn236
Bo6beppHTMg71
Бойлит Zn24a
Бойсит Мп59а
Боксит А123в
БолеитА§16
Боливарит А128в
Болтвудит К ЮЗА
натриевый Na216
Бонаккорит Fe99
БонатгитСиНбв
Борацит Mg26
БоркаритВП
Борнит Fe60
БорнхардитСоП
Боровскит РЬ74
Боронатрокальцит ВЗЗ
БортС1б
Боталлакит Си45а
БотриогенМ§51
^охдановичит Ag7
Брабантит Са225
*Р
оитМ
ЬрагитУ7б
рзи
"Райанит Na74
РайтхауптитЫ130
кб
Браммаллит Nal6
БрандиситСа115
БрандтитСа155
Браннерит U56
Браннокит К57
Брассит Mg55a
Браунит Мп42
Браунмиллерит Са85
БрашитСа112б
Брёггерит U6
Бредигит Са149
Бредлеит Nal57
Брейсуэллит Сг9а
Брецинаит, Бржезинаит
Сг2
БриаритСи61
Бройн(н)ерит Mg29a
Бромаргирит Ag9
Бромеллит Ве8
Бром(ир)ит Ag9
БромлитВа13в
Бронзит Mg786
Брошанит Си 120а
Брукит Ti7a
Бруногайерит Fe89
Бруньятеллит Mg43
Брусит Mg70
Брушит Cal 126
Брэггит Pt8
Брюггенит Cal 146
Брюсит Mg70
Брюстерит Sr8
Буковскиит Fe286
Буланжеит РЬ63
Бунзенит Ni23
БураЫа18в
БурангаитЫаПб
БурнонитСиЮб
Буссенгоит Mg66
Бустамит Мп77б
Бутит Cul 16д
Бутл epHTFe 138
Буттгенбахит Си43
Бухвальдит Na80
Бьоит К61
Бьянкит Zn24e
Бьяребюит ВаЗ 1
Бюргерит Nall3
Бюстрёмит Mg77
Бючлиит К176
Вавеллит А129а
Вагнерит Mg72a
Вад Ва34
ВадеитКШ
Вайбуллит РЬ24
ВайлитСа109а
Вайракит Са22а
Вайрауит Fe45
Вайссбергит Т17
Вайссит Си58
Валентинит Sb46
Валлериит Fe63
Вальстрёмит Ва16
Ванадинит РЬ88а
Ванденбрандеит U19
Вандендриссеит РЬ85
Вантгоффит Nal65
ВануралитШ4б
Вардит Na56
Вариканит Zn9a
Варисцит А127в
Варламоффит Sn3
ВатеритСа61а
Ваттевиллит Na826
Ваэсит Ni26a
ВеберитА114
Вебнерит Ag35a
Вевелит Са62а
ВезиньиитВа21
Везувиан Cal23
ВёлеритМаЮОА
ВелинитМп51
Вёльсендорфит РЬ84
ВенитРЬ61
BepдeлитNal38
Верджилит 1Л5а
Верлит Bi24
Вермикулит Mg82B
Вермландит Cal 19
Версильяит Fe85
Весейит Си75б
Вестгренит Та4
Вестервелдит Fe20
Вивианит Fel Юг
Визерит Мп20
Викингит Ag30
Виккенбургит Cal 7
Викманит Sn5a
Вилкманит Ni22a
Виллемит Zn27
Виллемсит Ni39a
293
I. Неорганические вещества
ВиллиамитСоНа
Вилльомит Nal 12
ВилькеитСа216А
Вильяманинит Си 113а
Вимсит Са40б
Виолан Са146а
ВиоларитРеЮ2
Виридин А144а
Висмут Bil
Висмутин Bill
Витерит Bal 1
ВитлокитСа184
Виттит РЬ51б
Виттихенит СиЗЗ
Витчит В37
Владимирит Cal 106
Власовит Na225
ВокленитСиЮ2
ВокситРе14в
Волковскит Са41а
Волластонит Cal 97
Волынскит Ag8
Вольтаит К43
ВольфеитРеШ
Вольфрамит Fel64a
Вольфсбергит Си 122
Вонсенит Fe736
Воробьевит Ве2
Bp6aHTHgl7
Вудраффит Мп92
ВудхауситСа16
Вулканит Си 136
Вулластонит Cal 97
Вульфенит РЬ46
Высоцкит Pdl4
Вюаньяит Са28
Вюрцит Zn23a
ВюститРеЮ4
Вяйрюненит Ве7
Габриельссонит Fel 17
Гагаринит Na97
Гагеит Мп83
ГадолинитВе16
Галаксит МпЗ
Галенит РЬ51а
Галенобисмутит РЫ7а
ГалитЫа107а
Галлит СибО
Галлуазит А146г
Галмей Znl3,Zn30
благородный Znl3
кремнёвый, обыкно-
обыкновенный Zn30
Галотрихит Fel5
Галургит В22а
Гамагарит Ва27
Ганит Zn2
Ганнингит Zn246
ГаномалитСа191
Ганофиллит Nal71
Гармотом Ваб
Гарньеит Ni38a
Гаррелсит Na24
Гарронит Na46
Гаспеит Nil 6
ГатумбаитСа12
Гатчит Ag52
Гаудейит Си4
Гаусманнит Мп46
ГауэритВ17
Гафнон Hfl
Гаюин Nal6а
Гванахуатит Bi 13
Гвианаит Сг9б
Геверсит Ptll
Гедифан Са37
Гедоннеит Na2266
Гейджит Мп83
Гейзерит Si5n
Гейкилит Mg91
Гейландит Са24а
Гейлит Nal90
Гейлюссит Na53B
Гейровскиит Ag28
Гейтит Са265
Гексагидрит Mg76r
Гексагидроборит Са40г
Гексатестибиопанике-
литРсШ
TeKTOpHTNal41
Гелен ит Са2
Гелиодор Ве2
Гелиотроп Si5>K
Гелландит Са261А
Гельвин Мп21
ГeльитNal90
Гематит Fel056
Гематолит Мп13
Гематофанит Fe 121
Гемафибрит Мп15
Гемиморфит Zn30
Генкинит Pt9
Генрихит Ва49б
Гентгельвин Zn 12
Гёргеиит К23
Гердерит Са54
Гердит РЬ43
Геренит СаПОв
Германит Си47
Герсдорффит Nil3
Герстлиит№193
Герстманит Mg62
Герхардтит Си70
Герценбергит Sn6
Герцинит Fe 11
Гессит Ag51
ГетерогенитСоЮ
Гетеролит Мп90
Гетероморфит РЬ65
Гетеросит Fe 109а
ГётитРеЮ7б
Геттардит РЬ59а
Гетчеллит Sb2
Гиалит Si5n
ГиалотекитРЫ5
Гиалофан К14
Гиацинт Zr3
восточный А123а
ГиббситА124б
Гидценит П5б
Гидраргиллит А1246
Гидроборацит Cal29
Гидрогалит Nal 076
Гидрогематит Fel056
Гидрогётит РеЮ7д
Гидроглауберит Na83
Гидрогроссуляр Са32
Гидродрессерит Bal б
Гидрокалюмит Са9
Гидроксилапатит Cal886
Гидроксилапофиллит К26
Гидроксилбастнесит Се4
Гидроксилгердерит Са55
Гидроксилэллестадит
Са218
Гидромагнезит Mg32a
Гидромусковит К1в
Гидрониоярозит Fe92
Гидроскарброит А18
294
I. Неорганические вещества
Гидрору
Гидр°цинкит2п15
Гиератит Si2
р ийменит Ва52
ГилалитСиПО
Гилдит Fe66
Гилпинит U23
Гинсдалит А136
Гиперстен Mg53
Гиперциннабарит Hg9
Гипс Са193в
Гирксутит СаЮ
ГиролитСа211
Гиттинсит Са272
Гладит Си81
Глаз
кошачий Bel
соколиный, тигровый
Nal20
Глазерит К94
Глина А146в
китайская, фарфоро-
фарфоровая А146в
Глауберит Na82a
Глаукодот Со5в
Глауконит К37
Глаукосферит Си35а
ГлayкoфaнNal52
ГлаукохроитСа165
Глёт, свинцовый РЬ47б
Глушинскит Mg30
Гмелинит Na44
Говлит Са49
ГогманнитРе135в
Годлевскит Ni28
Гойясит Sr4
Голдичит К46в
голдманит Са257
Гом
илит Са89
нардит Na43
1 °ньерит Мп29
Госларит ZnlAjx
ГоуеритВ17
Гошенит Ве2
ГошкорнитМП5
Грамматит Са150б
Грандидьеит Mg7
Грандит Са26
Грантсит Na96
Граутит Мп57в
Графит С 1а
Графтонит Са97
ГрейгитРе81а
ГрейтонитРЫ2
Гремит Cul 376
Гримальдиит Сг9в
Гримселит К97
Гриналит Fel536
Гринокит Cd4a
Гровсит Мп2б
Гроссуляр Са26
Гроутит Мп57в
ГрюнеритРе155
Гудкенит Sr5
ГудмундитРе143
Гулсит Fe73a
Гумбольдтин Fe37
Гумбольдтит Са48
Гумит Mg89
ГунтитСаШ
Гускрикит Са23б
Густавит Ag27
Гюбнерит Мп88
Гюролит Мп40
Дадсонит РЬ73
Дайингит Со9а
Дакеит Na94
Дакьярдит№12
ДаллитСа188а
Данаит Со5в
Даналит Fe32
Данбурит Са47
Даннеморит Мп38
l,HTZnl7
!, °Ргеит К23
^РсейкситВаЗ
1оРтонолитРе150
Даоманит Си27
Дарапиосит К89
Дарапскит№182
Датолит Са48
Даттонит V7
Дауниит Se2
Дашкесанит К19
Девиллин Са77а
Девиндтит U42а
Дезотелит Mg60
Дейвисонит Са14
ДейлиитК112
Деклуазит Zn22
ДелафосситРе51
Делхайлит Na48
Дельриоит V86
Демантоид СаЮб
Демесмекерит U22
Депюжолит Са164
Дербилит Ti4
Дернит Са 186а
Дерриксит U24
Десмин Na41
ДжайпуритСоП
Джалиндит 1п2
Джалмаит U55
Джанеллаит Hg7a
Джеймсонит Fel27
Дженнит Са200д
Джёрбанит А139а
Джефферсонит Са146а
Джиллеспит Ва24
Джимбоит Мп18
Джимтомпсонит Mg84
Джиниит Fe78
Джинорит Са43
Джисмондин Са20г
Джококуит Мп71в
ДжонситК15
Джонсомервиллит Na73
Джорджит Си37
Джорджиядесит РЬ7
Джулголдит Са95
Джурбанит А139а
ДжюрлеитСи114
Диаболит Си98
Диадохит Fel 15
Диалогит Мп22
Диаспор А126а
Диафорит Ag38
Дигенит Си52
Дизаналит Са228
Дикинсонит К92
Дикит А146а
Диксенит Мп52
Диморфит As7
295
I. Неорганические вещества
Динерит Ni9
Диопсид Са146а
Диоптаз Cul31
Дипингит Mg326
Дирит Fe87
Дискразит Ag41
Дислуит Zn2
Дистен А144в
Дитрихит Zn5
Диттмарит Мо65а
Дитцеит Са71
Дихроит Mgl
Добреит BilO
Долерофанит Cul 18
Доломит Са 132
ДомейкитСиН
Донатит Сг4б
Доннейит Na200
Дорфманит Nal34
Дравит Nal46
ДрессеритВа1а
Дрисдаллит Мо5
Дрогмансит U45
ДругманитРе123
Дугласит Fe42
Дундасит А134
Дурангит Na2
Дуфтит Cull
Дюмонит U43
Дюмортьеит А15
Дюранусит As6
Дюфренит Са92
Дюфренуаит РЫ1
Ежекит Na38
Екатеринит Са45
ЕльмитУ14
Еремеевит А14
ЖадСа150, Na8a
Жадеит Na8a
Жаргон Zr3
Жедрит, натриевый
Nal45
Железняк
бурый, игольчатый
FelO76
красный FelO56
магнитный Fe75
титанистый Til
хромистый Сг4а
шпатовый Fe36
Железо Fel
Жемчужниковит Nal47
Жировик Mg826
Жисмондин Са20г
Жозеит Bi23
Жолиоит1Л6б
ЖуравскитСа157
Заварицкит Bi9
Заирит Fe33
Зайдоцерит Na230
ЗвягинцевитРс112
ЗегелеритСа138
Зейбертит Cal 15
Зейригит Са260
Зелень
горная, медная Си35б
урановая U26
Зелигерит РЬ44
Зелигманит Си78
Зёнгеит Gal
3nreHHTNi21a
Зикаит Fe29
Зиннерит Cu29
Золото Аи 1
висмутовое Аи7
серебристое Аи2
Зорит Na209
Зуниит А143
Зуссманит К39
Иантинит U38
Ивакиит Мп31
Идаит Fe58a
Идальгоит А133
ИдокразСа123
Иенит Са94
Известняк Саб 1 г
магнезиальный Cal32
Известь Cal82а
жжёная, негашёная
Cal 82а
ИзокитСаНЗ
ИзоклазитСа187
Изомертиит РЬ56
Изостаннин Си 148
Изоферроплатина Pt6
Изумруд Ве2
восточный А123а
медный Си131
никелевый Nil8
ИиморитУ12
Икерит Са35
Иксиолит Nbl
Икунолит Bi 12
Илезит Мп71б
Илерит Na226B
Иллит К1в
Ильваит Са94
Ильменит Til
Ильменорутил Ti7e
Имандрит Na61
Инверэрит Fel03
Инглишит К78
Индерборит В18
ИндеритВ21
Индианит Са20а
Индиго, медное Cul 12
Индиголит Nal38
Индий Inl
Индит Fe94
ИнеситСа171
Инсизваит Pt3
Иньонит Са42в
Иоганнит U23
Иод(арг)ирит Ag24
Иодобромит Ag9
Иодит Mgl
Иорданит РЫ4
Иордизит Мо4а
Иранит РЬЗбб
Ирарсит 1гЗ
Иригинит U 34
Иридарсенит 1г2
Иридий Irl
платиновый Irl
Иридосмин Osl
ИтоитРЬ41
Иттербит Be 16
Иттробастнесит Y4
Иттробетафит Са2б2
Иттроколумбит Y7a
Иттрокразит Th7
Иттромикролит Y14
Иттропирохлор Y8
Иттротанталит Yl3a
Иттроэшинит Y15a
296
I. Неорганические вещества
Йонбаумит Са39
ЙофортьеитМп81
ЙоханнсенитСа166а
Йохачидолит Са5
Каваиулит Bi22
КадваладеритАПО
Кадмий Cdl
Кадмоселит Cd5
Казолит U45
Каинит К67
Кайсихит Y1
КакоксенРе114
КалаверитАи12а
Калаит Си7
Каламин Zn30
Калафатит К7
Каледонит Си96
Калерит U296
Калиблёдит К65а
Калиборит ВЗО
Калинит Кба
Калиофилит К8а
Калипирохлор К93
Калистронцит К96
КалифорнитСа123
Калицинит К49
Калкинсит Се2
Каллаганит Mg38
Каллаит Си7
Каломель Hg2
Калсилит К8б
Калусит К22
Кальдерит Мп37
Кальциборит Са40а
Кальций-катапле(й)ит
Са273
Кальциокопьяпит СаЮ2
Кальциоураноит Са233
КальцИоферритСа139
^альцИОфольбортитСа82
Кальциртит С276
каль
цит Саб 1г
камень
^азонский К10в
конский Ва39
ГоРоховыйСа61б
Кв К7
коричный Са26
крестовый Fel9
лазоревый (лазур-
(лазурный) Na50
ледяной All6
лучистый Са150а
мыльный Mg826
огневой Si5x
оловянный Sn3
солнечный Na9a
Каммингтонит Mg86
Канавесит В12
Канасит Na89
KaHeMHTNal33
Канит В4
Канкит Fe226
Канниццарит РЬ20
Каноит Мп77а
Канонаит Мп8
Канфилдит Ag49
Каолин (ит) А146в
Каппленит Ва55
КараколитЫа187
КарбоборитВЮ
Карбонадо С16
Карбонат-фторапатит
Са186а
Карбонат-цианотрихит
Сиб
Карборунд Si 1
Карбоцернаит Са61в
Карелианит V4
Карибибит Fe27
Кариопилит Мп84б
Карлинит Т16
Карлфрисит Са223
Карлхинцеит А113
КарминитРе119
Карналлит К63
Карнеол Si5e
Карно(т)ит К107
Кароббиит К34
Каррбойдит Ni4
Карроллит Со9б
КарстенитСа193а
Карфолит Мп9
КассидиитСа181
Кассит Са229
Касситерит Sn3
Катапле(й)ит Na226a
Катоптрит Мп74
Катофорит Na65
Каттье(р)итСо12
КаулситСа21б
Кафетит Са227
Кварц Si5e
авантюриновый, дым-
дымчатый, розовый, си-
синий Si5e
Квасцы
горные К7
железные Fel5
калиевые Кбб
магнезиальные Mgl6
натриевые Na6e
римские Fel5
Квейтит Zn21
Квенстедтит Fe 1 Збг
Кейит Си20
КеккитСа158
Келдышит Na231
Кеммлицит Sri
Кемпит Мп27
Кёненит Nal49
Кенияит Nal97
Кеннедиит Mg90
Кенселит МпбЗ
Кентролит Мп65
Кераргирит Ag 11
Кермесит Sb6
KepmrrNal8a
Керстенит РЬ77
КестеритСи148
Кетсалкотлит Си 149
Кёттигит Zn96
Кеттнерит СабО
Кёхлинит Bi7
Кианит А144в
Кидуэллит Nal24
Кизерит Mg76a
Киллалаит Са200в
Клльхоанит Са200б
Кимрит Ва7
КимцейитСа271
КингитА129б
Кингсмаунтит Са86
Киноварь HglO6
австрийская РЬ38
сурьмяная Sb6
хромовая РЬ38
297
I. Неорганические вещества
Киноит Са80
Киношиталит Ва29
Кирштайнит Са104
Киткаит Ni42
Китконнит Pd22
Клайнит Hg6
Клапротит СиЗЗ
Кларингбуллит Си46
Кларкит Na93
Клаудетит As36
Клаусталит РЬ75
Клебельсбергит Sb7
Клевеит U6
Клейофан Zn236
Клеманит Zn3
Кливлендит Na9a
Клинобисванит Bi26a
Клиноклаз Си22
Клиноптилолит NalO6
Клинохлор Mg2
Клиноштренгит FelO96
Клиноэдрит Са267б
КлинтонитСа115
Клиффордит U51
Клодеит As36
Клокманит Си 126
Кмаит К64
Кнебелит МпЗб
Книповичит Са7
Кнопит Са228
Кноррингит Mg37
Коашвит№91
Кобальт
белый Со2
оловянно-белый СоЗ
черный землистый
Ва34
шпейсовый СоЗ
Кобальтин Со5а
Кобальтокальцит Соб
Кобальтоменит Со 18
Кобальтпентлендит Fe46
Кобальтциппеит Со20
КобеллитРЬ21
Ковеллин Си 112
Когаркоит Nal92
Когенит Fe35
Кожа, горная Mg85
Кокимбит Fel36B
Кокониноит U28
КоктаитСа176
Колдерит Мп37
Коллинсит Са142
Коллофан Са62А
Колманит Са42а
Колорадоит Hg 15
Колумбит Nb2a
Колчедан
белый железный
Fel346
белый никелевый
Ni7a
волосистый Ni25
гребенчатый Fel346
железный Fel34a
желтый никелевый
N125
кобальтовый Со8
кобальтомышьяко-
вый Со5в
копьевидный Fel346
красный никелевый
Ni6
лучистый Fel346
магнитный Fel31
марганцевый Мп70
медный Fe57
мышьяковый Fe30
никелевый FelO3
оловянный Fe70
павлиний медный
Fe60
печёнковый Fel346
серебристый Fe4a
серебряный Fe46
серный Fel34a
Колымит СибЗ
КольбекитБЫ
Кольвецит Си35в
КомаровитСа179
Комбит Na88
Компреньякит К102
Конголит Fe316
Конинкит FelO9r
Конихальцит Са74
Коннеллит Cul 17
Копьяпит Fe83
Кордероит Hgll
Кордиерит Mgl
Кордилит Ва20
Кордьеит Mgl
железный Fe8
Коритнигит2п10
Коркит Fel24
Корнелит Fel366
Корнерупин Mg5
Корнетит Cu75a
Корнубит Cu23a
Корнуоллит Cu236
КорньюитСи133
Коронадит Мп49
Корунд А123а
КосалитРЫ8
Космохлор Nal08
КостибитСо14б
Костовит Аи8
Котоит Mg25
Котульскит Pd20
Котуннит РЬЗО
Коулсонит V2
КоутекитСи17
Коффинит U54
Кохромит Сг1
KoцyлитNal74
Коэнит Fe35
Коэсит Si56
Крайсслит Мп94
Крамерит Na51
КрандаллитСа15
Краусит К466
Краускопфит Ва40б
Краутит Мп39
Креднерит Мп28
Крейттонит Zn2
Кремень 815ж
Кремерсит Fe44
КрёнкитЫаПО
Креннерит Аи 126
КридитСа18
Криолит All6
Криолитионит All 9
Криптогалит Si36
Криптомелан К69
Кристианит Са20а
KpncTHTHgl6a
Кристобалит Si5r
Кровавик 515ж
Кройцбергит А131
Крокидолит Nal20
Крокоит РЬЗба
298
I. Неорганические вещества
Кромфордит РЬ27
Кронстедтит Fe74
]CpoccHTNal52
^рукситСи128в
Крупкаит Си80
КрутаитСи127а
Крутовит Ni5
Крыжановскит Fel 13
КсантиоситЫ112а
КсантитСа123
Ксантоконит Ag3a
Ксантоксенит Са99
Ксантосидерит Fel076
Ксантофиллит Cal 15
Ксенотим Y9
Ксокомекатлит Си 139
Ксонотлит Са202
КтенаситСи119б
Кубанит Fe62
Куланит Ва23
Куллерудит Ni356
Кулькеит Mg4
КуменгеитСиЮО
Кунцит Li56
Куперит Pt8
Купорос
белый 2п24д
железный Fel35e
желтый железный
Fe83
зеленыйРе135е
кобальтовый, крас-
красный Col Зв
марганцевый Мп71г
медный Си 116г
никелевый Ni29B
свинцовый РЬ52
синий Си116г
Урановый ШЗ
Цинковый2п24д
Куприт Си72
Купроартинит Си35г
%провисмутин Си34
кУпрогидромагнезит
Си38
?упРодеклуазитСи111
^У Fe67
?УРориваит Са79
^просклодовскит U26
Купростибит Си 121 '
Купроуранит U216
Купрошпинель Fe52
Купферникель Ni6
Курамит Си57
Куранахит Мпбб
Курнакит Мп55
Курнаковит Mg24
Курчатовит Са128
Куспидин Са207
КусуитСе13
KyTHHaHTAgl2
Кутнагорит Cal 56
Кьюртонит Ва43
Кюрит РЬ86
Кюрьенит U47
Кюстерит Са207
Лабрадор Cal
Лавендулан Na55
Лаврионит РЬЗЗ
ЛавровитСа146
Лавсонит СаЗО
Лазаревичит Си28а
Лазулит Mgl3
Лазурит Na50
Лазурь
железная Fel Юг
медная СиЗб
Лайтакариит Bil4
Лайхунит Fe86
Лакруаит Na3
Лаксманит Си 102
Лампроболит Na71
Лампрофиллит Na204
Ланаркит РЬ54
Лангбайнит К66
Лангбанит Мп50
Лангисит Col
ЛангитСиШг
Ландауит Na207
Ландит МпЗЗа
Лансфордит Mg29B
Лантанит Lai
Лантанобастнесит La2
Лапландит NalO6
Ларанит Т11
Лардереллит В24
Ларнит Cal 99
Ларошит Си92
Ларсенит Zn20
Лаубманит Fe80
ЛаузенитРе136а
Лаурит Ru4
ЛаутаритСа114а
Лаутит Си26
Лауэит МпЗЗг
Лафлинит№169
Лаффиттит Ag23
Лёвеит Nal66
чилийский К90
Левин Са22г
Легранит2п11б
ЛёдН2
Ледхиллит РЬ29а
ЛейкопиритРе21
Лейкосфенит Na27
Лейкофиникит Мп82а
Лейкофосфит К45
Лейтеит Zn7
ЛейтонитК18
Лейцит К9
Леконтит№180
ЛёллингитРе21
Лемуанит Na228
Ленгенбахит Ag26
Леонит К65а
Леонхардит Са22б
Лепидокрокит Fel07B
Лепидолит К52
Лепидомелан К61
ЛессеритВ21
Летовицит N7
ЛеттсомитСи13
Лешательеит Si5e
Лиандратит U4
Либенбергит Ni37
Либерит Li7
Либетенит Си74
Либихит Са237
Ливейнгит РЫЗ
Ливингстонит Hg 13
Лиддикотит Ы8
Лизардит Mg816
Лиллианит РЫ9
Лимонит РеЮ7д
Линарит Си 104
Линдаккерит Си62
Линдгренит Си69
Линдстрёмит Си89
299
I. Неорганические вещества
Линнеит Со8
Линтонит Na40
Липскомбит Fe766
Лироконит Си2б
Лискардит А13
Литаргит РЬ47б
Литидионит К82
Литиофилит Li 17a
ЛитиофоритШб
Литиофосфатит Li 18
Ловенит Na98
Локкаит Y3
Ломон(т)ит Са22в
Лонгбанит Мп50
Лонеит РЬ72
Лопарит NalO4
Лопесит, Лопецит КЗО
Лоранит Т11
Лоренценит Na214
Лосиит Мп23
Лосонбауэрит Мп93
Лосонит СаЗО
Лудламит Fe 11 Ов
Лудлокит Fe23
Лусакит Fel9
Лусонит Си28в
Луссатит Si5r
ЛуэшитЫа183а
Льеврит Са94
Льюсинит А127в
ЛьюиситСа194а
Льюистонит Са186б
Льяндраит U4
Людвигит Mg426
Люнебургит Mg28
Люссаит Si5r
Люсуньит8г13
Лютеит Си2а
Ляпис-лазурь Na50
MaгaдиитNal96
МаггемитРе105а
Магнезиоаксинит Cal 18
Магнезиожедрит Mg3a
Магнезиокарфолит Mgl8
Магнезиокатофорит
Na72
Магнезиокопьяпит Mg52
Магнезиорибекит Nal62
Магнезиоферрит Mg46
Магнезиохромит Mg36
Магнезит Mg29a
Магнетит Fe75
Магнетоплюмбит Мп62
Магний-осумилит К59
Магний-хлорофиникит
Mg20
Магний-циппеит Mg96
Магниоборит Mg23a
Магниотриплит Mg726
Магниофилит Мп59а
Магноколумбит Mg68
Магнофорит Na75
Магнуссонит Мп4
Магхагендорфит Nal63
Мадокит РЬ70
Майенит Са8
Майерсит Agl4
Майкснерит Mg 12
Макаллистерит Mg226
Макатит№195
Макгиллит Мп79
Макгиннессит Mg316
Макдоналдит Ва17
Македонит Ti8
Макиноит Fel32
Макинтошит Th6
МаккейитРе160
Маккелвиит Na25
Маккинстриит Ag39B
Макконнеллит СгЗ
Максит РЬ29а
Макфаллит Cal 73
МалайяитСа221
Малакон Zr3
МаланитСиПЗб
Маланхроит РЬЗба
Малахит Си35б
Малдонит Аи7
Малладрит Si4
Маллар(д)ит Мп71г
Маллит All
Манандонит Lil
Манассеит Mg8a
Манганаксинит Са 154
Манганбаббингтонит
Са159
Манганберцелиит Na76
Манганбрюсит Mg70
Мангангумит Мп82б
Манганит Мп57б
Манган-нептунит К88
Манганобрюсит Мп56
Манганокальцит Мп22
Манганоколумбит Nb3
Манганолангбайнит К70
Манганосит Мп53
Манганостибиит Мп73
Манганотанталит Та7
Манганофиллит Кб 1
Манганохромит Сгб
Манганпиросмалит
Мп84в
Манганфаялит МпЗб
Манганхорнсит Mnl 1
Манганшадлунит Мп35
Мандариноит Fel48
Манжироит Nal75
Мансфилдит А12
Мапимит Fel66
Марганец, землистый
Ва34
Маргарит СаЗ
Маргаросанит Са 189
Мариньякит Се7
Марипозит К2
Маричит Nal226
Мариялит Nal4
Марказит Fe 1346
Марматит Zn236
МарокитСа160
Маррит Ag25
Марстурит Na78
Мартозит U25
Маршит Си65
Масканьит N8
Масловит Pt4
Массикот РЬ47а
Масутомилит К56
Матильдит Ag5
Матлокит РЬЗ1
Матраит Zn23r
МаттагамитСо19
Маттеуччит Nal36
Маукерит1ЧП1
Маунтинит Са198в
Махачкиит СаЗба
Маццит К20
Маякит PdlO
Мбозиит Na59
300
I. Неорганические вещества
МедьСи1
рубиновая Си/2
селенистая Си 128а
Мезитит Mg29a
Мезолит Na45
Мейджорит Mg54
Мейерхофферит Са42б
Меймацит\\аг
Мейонит Са27
Мел Саб 1 г
французский Mg826
Мелаконит Си71
МеланитСаЮб
Меланованадит Са255
Меланостибит Мп75
МеланотекитРе128
Меланофлогит Si5a
Меланохроит РЬ38
Мелантерит Fel35e
Мелилит Са147б
Мелинофан, Мелифа-
нит Са57
Мелоюкозефит Са91
Мелонит Ni41
Мельниковит Fe81a
МенакканитТП
Мендипит РЬ32
Мендосит Na66
Менегинит Си 107
Менилит Si5n
МервинитСа148
Мёрдокит Си94
МеренскиитРсШ
МеркаллитК51
Меркураммонит Hg6
МерлиноитК12
Месселит Са98б
Метаалуноген А138 .
Метаалюминит А140а
Метаанколеит К104
МетаборитШ
МетавануралитиНа
МетаварисцитАШб
метавокситРе14б
Метавольтин К47
Метагенрихит Ва49а
U29a
кирхгаймерит1Л7
Метавачекит Mg93a
Метаотёнит Са240а
Метароссит Са250а
Метасидеронатрит Nal29a
Метастибнит Sb5a
Метатурбернит U21a
Метатюямунит Са246а
Метаураноспинит Са234а
Метаураноцирцит Ва50а
Метахейвиит Са244а
Метацеллерит Са236а
Метациннабарит HglOa
Метацойнерит U18а
Меташодерит А1516
Миаргирит Ag42a
Микроклин КЮв
Микролит Na90
МикситСи31
Миларит К16
Миллерит Ni25
Миллисит Na37
Мимет(ез)ит РЬ8
Минасрагрит V9
Мингуццит Fe38
Миннесотаит Fe 154
Миньюлит К4
Мирабилит Nal886
Мирсит Agl4
Митридатит СаЮО
Михараит Fe55
Миченерит Pd7
Мичерлихит Си42
Мозесит Hg76
Мойхукит Fe64
Моктесумит U46
Молибденит Мо4б
Молибдит МоЗ
Молибдоменит РЬ76
Молибдофиллит Mg74
Молизит Fe40
Молуранит U57
Монацит Се9б
Монетит Са112а
Монимолит РЬ58б
Монит Са62А
Монморийонит Nal51
Моногидрокальцит Са61д
Монсмедит К100
Монтазит Mg86
Монтанит Bi20
Монтбрейит Аи 13
Монтгомериит Са121
Монтебра(з)ит Ш
Монтепонит Cd3
Монтереджанит Na222
Монтичеллит Са145
Монтмориллонит Nal51
Монтрозит V6
Монтройдит Hg8
МончеитР114
МорайншитВеП
Морганит Ве2
МорденитЫаЮа
Мореносит Ni29e
Моринит Na38
Морион Si5e
Морит Fe96
Морлендит Ва8
Мосандрит Na92
Мосонит Fe72
Моссит Nb26
МоттрамитСиШ
Мотукореяит Nal48
Моурит U2
Моховик Si5:ac
Мочевина СЗ
Мошелландсбергит Ag21
Мпоророит А1526
Мрамор Са61г
МрозитСа61е
MyaccaHHTSil
Муллит All
Мунанаит Fel30
Мурит Мп72
MypMaHHTNa213
МурхауситСо13б
Мусковит К1а
Мускоксит Mg47
Мухинит Са249
Мышьяк As 1
белый As3a
желтый As5
Мюрит Ва18
Мякиненит Ni346
Навахоит V56
НагиагитАиЮ
Надорит РЬ57
Надьягат Аи 10
Наждак А123а
301
I. Неорганические вещества
Назинит В28
Накауриит Мп24
Накафит№81
Накипь
жемчужная Si5n
известковая Са61г
кремнёвая, опаловая
Si5n
Накрит А1466
Намбулит№142
Нантокит Си40
Наньлинит Са126
Нарсарсукит Na212
НасонитСа190
Настуран U6
Натисит№211
Натрамблигонит Li2
Натроалунит Na7
Натроапофиллит Na86
Натрокальцит Na53e
НатролитЫаНа
Натромонтебраит Na4
Натрон Na356
Натрониобит Nal836
Натросилит Nal94
Натрофилит Nal76
Натрофосфат Na 135
Натрохальцит Nalll
Натрохаросит N а 12 8
Науманит Ag47
НауякаситЫаШ
Наффилдит Си83
HaxкoлитNal31
Нашатырь N3
Невьянскит Irl
Нейборит№159
Нейит Cu87
Некоит Са198а
Немалит Mg70
Ненадкевичит Nal84
Неотанталит Na90
Нептунит К87
Непуит №386
Несквегонит Mg56
Нефелин К75
Нефрит Са150а
НигглиитРШ
Нигрин ТЛ7в
Никелин Ni6
Никель Nil
Никельбишофит Nil 9
Никельблёдит Nal85
Никельгексагидрит Ni29a
Никельскуттерудит Ni8
Никель-циппеит U36
НилитРеИб
Нимит Ni2
Нингиоит Са247
Нинингерит Mg75
Ниобит Nb2a
НиокалитСа180
Нисбит№31
Ниссонит Mg39
HnTpaTHHNal81
Нитробарит Ва37
Нитроглауберит Nal82
Нитрокальцит Са177
Нитромагнезит Mg67
Нифонтовит В14
Нихромит Сг7
НоблитСа41б
НовакитСи16
Новакулит Si5e
Новацкийит Си 145
Новачекит Mg936
Нозеан Nal66
Нонтронит Nal 17A
Норбергит Mg80
Норденшёльдин Са219
Нордит№201
Нордстрандит А124в
Нордстрёмит Си93
Норсетит ВаЗО
Нортупит Nal 56
Нукундамит Fe56
Нумеаит Ni38
Ньеререит Na53a
Ньюбериит Mg57a
ОберитСиЮ
Обманка
висмутовая Bil5
кадмиевая Cd4a
марганцевая Мп69
медовая Zn236
молибденовая Мо4б
печёнковая Zn236
роговая Na71
серебряная Ag436
скорлуповатая Zn236
сурьмяная Sb6
урановая смоляная Щ
цинковая Zn236
ОбручевитУ8
Овайхиит Ag36
ОверитСа120
Оданиелит Na223
Окартит Fe7
Окенит Са198б
Окерманит Са147а
Оксаммит N2
Оксониохаросит Fe92
Октаэдрит Ti76
Окуэлаит Fel65
Олбриттонит Со7
Олдерманит Mg 15
Оливенит Си21а
Олигоклаз Na9r
Олигонит Fe36
Олимпит№186
Олмстедит К44
Олово
белое Snl6
серое Snla
ОлстонитВа13в
Ольгит Na202
Ользакерит РЬ78
Ольшанскиит В6
Омейит Os2
Омфацит Са146б
Оникс
алжирский, мекси-
мексиканский Саб 1 г
Оноратоит Sb3
OнoфpитHgl0a
Опал Si5n
арлекиновый, благо-
благородный, МОЛОЧНЫЙ,
огненный, печёноч-
печёночный, стеклянный Si5H
Оранжит Th26
Ордоньесит Zn25
Орегонит Fe98
Ориентит Са170
Орицит Са23в
OpceлитNilO
Ортит Са34а
Ортоклаз К 10а
Ортоферросилит Fel49a
Осаризаваит Си9
302
I. Неорганические вещества
ОсарситОвЗ
Осмий Osl
Осмирид 1П
Остербосит Pd8
Остинит Са264
Осумилит К36
Отавит С62
Отёнит Са240б
натриевый Na217
Оггеманит Sn9
0туэйитШ7
^81б
Офит1^81б
Оффретит К80
Охра РеЮ7д
бурая FelO7B
висмутовая Bi86
вольфрамовая W16
железная FelO7B
красная FelO56
молибденовая МоЗ
никелевая N1126
свинцовая РЬ47а
сурьмяная Sb8
теллуристая Те2
урановая U48
• черная Ва34
ОхроитСа135А
0шкорнит1ЧП5
ПабститВа41
Павонит Ag6
Пайгеит Fe73
ПакситСи15
ПалермоитШ9
Палладий Pdla
Палладоарсенид Pd2
Палладовисмутарсенид
Pd6
Паллит Na37
Палыгорскит Mg85
Пальмьеит К95
Цанабаз Fe68
Пандаит Ва37
Пандермит Са44а
Пао.
Пап;
•ловит Pd 18
агоит Са73
Парамелаконит Си48
Парамонтрозит V3
Прагасит Na64
Парисит Са65
Парнауит Си25
Парсеттенсит К71
Парсонсит U41
Парте ит Са20в
Паруэлит Мп86
Паскоит Са253
Патерноит ВЗО
Патринит Си79а
Патронит VIО
ПауэллитСа175
Пахнолит All 8а
Пеганит А127в
Пейнит Са270
Пекоит Си82
Пекораит №38в
Пектолит Na87
Пеллиит Ва15
Пеникисит Ва28
Пенка
медная Са75
морская Mg83
Пенквилксит Na210
Пеннантит Мп2а
Пенроузит Ni35a
Пентагидрит Mg76B
Пентагидроборит В13
Пентагонит Са254
Пентлендит FelO3
Пенфилдит РЬ34в
ПергамитСа182в
Перетаит Са196
Перидот Mg79
Периклаз Mg69
ПеритРЫб
Перлит Si5n
Перлоффит Ва32
Перменжаит Си 125
Перовскит Са228
Персилит Си97
Песок Si5e
Петалит Li6
Петарасит Na229
Петровичит Си64
Пе(т)цит Аиб
Печекит U3
Пиджинит, Пижонит
Mg78a
Пизанит Fel35e
ПизолитСабШ
Пикерингит Mgl6
Пикополит Fe88
Пикотит MglOa
Пикроильменит Mg91
ПикpoлитMg81a
Пикромерит К656
Пикрофармаколит Са141
Пикрохромит Mg36
Пимелит Ni396
Пинакиолит Mg59
Пинчит Hg3
Пираргирит Ag436
Пирит Fel34a
Пироаурит Mg446
Пйробелонит Мп68
Пироксмангит Мп77в
Пироксферроит Fel496
Пиролюзит Мп54б
Пироморфит РЬ49
Пироп Mgl7
Пиросмалит Fel56
Пиростильпнит Ag43a
Пирофанит Ti5
Пирофиллит А145
Пирохлор Na79
Пирохроит Мп56
Пиррит Na79
Пирроарсенит Na70
Пирротин Fel31
Пирсит Ag46
Пирссонит Na536
Пистацит Са34б
Плагионит РЬ64а
Плазма Б15ж
Планшит Си 134
Платарсит Pt2a
Платина Ptl
Платинит РЬ22
Платтнерит РЬ48
Плейфэрит РЬ69
Плеонаст Mg41
Плеонектит Са37
Плюмбаго С1а
Плюмбобетафит Na208
Плюбогуммит А135
303
I. Неорганические вещества
Плюмбомикролит Та8
Плюмбопалладинит Pdl3
Плюмбопирохлор Nb5
Плюмбоферрит Fel22
Плюмбохаросит Fel26
Повеллит Са175
ПознякитСиШб
ПоитРе161
Поларит Pdl6
Полианит Мп54б
Полибазит Ag466
Полигалит К21
Полидимит Ni216
Поликраз Y156
Полилитионит К53
ПолингитКП
Полковичит Fe90
Поллукс, Поллуцит Cs2
Полмурит РЬ6
Полхемусит Zn23e
Портлендит Са183
Потарит Pd9
Поубаит РЬ23
Праз(ем) Si5x
Празопал Si5n
Прайдерит К99
ПрайоритУ15а
Прайсверкит Nal44
Прайсит Са44а
ПраудитСи91
Пренит Са4
Преображенскит В23
Пржевальскит U426
Призматин Mg5
Приорит Y15a
Пробертит Na51
ПрозопитА112
Просперит Са263
Прустит Ag36
Псевдоболит Си99
Псевдобрукит Ti3
Псевдолауэит МпЗЗв
Псевдомалахит Си76
Псиломелан Ва34
Птилолит NalOa
ПуатвенитСиПбб
Пукерит Bi266
Пумпеллиит Са122
ПуналитСа21а
Пурпурит Мп58
ПьемонтитСа174
Пьерроит Т18
РаббиттитСа153
Рабдофан Се9а
Рагенит Fel62
Рагит Bi4
Разорит Na 18а
РайитСи138
Райнерит Zn8
Райхардит М§76д
Раклиджит Bil8
Рамдорит Ag356
Раммельсбергит Ni76
Рамоит К27
Рамсделлит Мп54а
Ранкилит Са244б
Ранкинит Са200а
РансиитСа161
Рансомит Fe65
Рансьеит Са161
Ранункулит U9
Расвумит К41
Распит РЬ89а
Расселлит\?1а
РатитТ15
Раувольфит Си120в
Раухтопаз Si5e
Рауэнталит СаЗбб
Реальгар As8
Реддингит Мп59б
Редингтонит Сг5
РедрутитСи115
Резбаньяит Си86
Рёзерфордин U16а
Рейерит Na49
Рейкебурит Ва42
Рёмерит Fe82a
Ренарит U44
Рений Rel
РёнитСа151
Рёнтгенит Сабб
Реньеит Fe586
Рёсслерит Mg556
Ретгерсит Ni296
Ретциан Y6
РибекитЫаШ
Ривадавит Nal54
Риверсайдит Са216
РивситРеЮО
Ридмернерит Na21
Риккардит Си59
Ринк(ол)ит Na92
Риннеит Fe41
Рихтерит Na75
РишеллитСаЮ1
РобертситСа163
Робинсонит РЬбб
РоблингитСа192
РовеитВ19
Родалькиларит Fe93
Роджинит Na42
Родий Rhl
РодицитСб!
Родонит Мп77г
Родостаннин Fe71
Родохрозит Мп22
Родсит Na84
РодуситШ162
РозаситСи146
Розелит Са69а
Розенбушит NalOO
Розицкит81а
РозмэриитЫа173
Розенханит Са201
Рокбриджит Fe77
Рокесит Си68
Рокюнит Fe39
Романешит ВаЗб
Ромаркит Sn2
Ромбоклаз Fe91
Ромеит Са194б
Ропперит Мп78
Росицкийит81а
Роско(э)лит К108
Россит Са250б
Ростит А1396
РоуитВ19
Роулендит Y11
РоценитРе135б
Рошерит Са51
Ртуть Hgl
роговая Hg2
Рубеллит Nal 38
Рубин А123а
Рубоит U20
Руда
бархатная Си 13
белая свинцовая
304
Неорганические вещества
блёклая мышьяковис-
мышьяковистая Fe48
блеклая серебряная
Fe3
блёклая сурьмянистая
Fe68
болотная FelO76
болотная марганце-
марганцевая Ва34
бурая свинцовая РЬ8
желтая свинцовая
РЬ46
игольчатая Си79а
колёсная Си 106
коралловая Hgl06
красная медная Си72
красная свинцовая
РЬЗба
красная серебряная
Ag36
красная цинковая
Znl6
кремнистая цинковая
Zn30
кубовая К40
медная смоляная
Си133
оловянная Sn3
павлинья медная Fe60
печёнковая Hgl06
почковидная FelO56
пурпуровая медная
Fe60
серая марганцевая
Мп57б
серая сурьмяная Sb5
стекловатая медная
Си72
твердая марганцевая
Ва34
темно-красная сереб-
серебряная Ag43a
Урановая смоляная U6
хРУпкая серебряная
Ag44
черепичная Си72
черная медная Си71
рУзвельтит Bi2
^УиситСа168
^пперит Мп78
рУстамитСа213
Рутенарсенит Ru2
Рутений Rul
Рутениридосмин Osl
Рутеносмирид Irl
Рутил Шв
PyTbenTHgl66
Рюнерсонит Са222
Рюстенбургит Ptl3
Саамит Sri 56
Сабинаит Na232
Сабугалит ШОа
Садбериит РЬ55
СажинитЫаЮЗ
СайбейитВ31
Сайлсит Си67
Сакиит Mg76r
Салеит Mg95
Салинит РЬ9
Салит Са 146а
СамарскитУ15в
Самиресит Na79
Самплит Na56
Самсонит Mnl
Санборнит Ва40а
Санидин К106
Санмартинит Zn31
Сантаклараит Са169
Сантанаит СгЮ
Сантафеит Sri4
СантитКЛЗ
Санхуанит А132
Сапаталит Си8
Сапфир А123а
водный Mgl
Сапфирин Si5x
Сарабауит Са195
CapaTHTNil8
Сард(ер) 515ж
Сардоникс Si5>K
Саркинит Mnl4а
Саркопсид FellOa
Сармьентит Fe28a
СарторитРЫО
Сассолин ВЗ
Сатимолит К74
Саттерлиит Mg48
Саффлорит Со2
СахаитСаШ
Сахамалит Mg33
СахароваитРЫ7б
Сборгит В27
Свабит Са38
Сванбергит Sr6
СварцитСа152
Сведенборгит Na32
Светлозарит Са25
Свинец РЫ
красный РЬ50
роговой РЬ27, РЬЗО
черный С 1а
Свитцерит Мп59в
Седерхольмит Ni34a
Седовит U1
СезаролитМп61
Сейдозерит Na230
Сейняйокит Fel40
Секанинаит Fe8
Селадонит К64
Селен Sel
Селенжозеит Bi 14
Селенит Са193в
Селеновисмутин ВИЗ
Селенолит Se2
Селитра К73
баритовая Ва37
известковая Са177
индийская, калийная
К73
кубическая Nal81
магнезиальная Mg67
натронная Nal81
норвежская Са177
чилийская Nal81
Селлаит Mg40
Семсиит РЬ67
Сенармонтит Sb4a
Сенегалит А1286
Сенжьеит U27
Сенфелдит Cal 10а
Сепиолит Mg83
Сера S16
рубиновая As8
Серанит Nal77
Сервантит Sb8
Сергеевит Cal 34
Сердолик Si5e
Серебро Agl
роговое Ag 11
рубиновое Ag436
305
I. Неорганические вещества
Сёренсенит Nal98
Серицит Kla
Серпиерит Са77б
СесбронитСи140
Сиберит№138
СибирскитСаШ
СиглоитРе12
Сидеразот(ит) Fe95
Сидерит, Сидеродот Fe36
Сидеронатрит Nal296
Сидероплезит Fe36
Сидеротил Fel35r
Сидерофиллит КЗ 5
Сидоренкит Nal72
Сиклерити17б
Силгидрит Si53
Силленит Bi8a
Силлиманит А1446
Сильванит Аи5
Сильвин(ит) К28
Симанит В8
Симониит Nal64
Симплезит Fe24
Симплотит Са251
СимпсонитТа1
Синадельфит Мп12
Сингенит К22
Синкозит Са256
Синхалит Mg6
Синхизит Са64
Сирлсит Na22
Ситапарит Мп55
Скаккит Мп25
Скарброит А17
Скиннерит Си 123
Склодовскит Mg97
Сковеллит Се9а
СколецитСа21а
Скородит Fe22a
СкорцалитРе14а
Скотит Са205
Скунерит МпЗО
Скупит U37
Скуттерудит СоЗ
Славянскит Na36
Слосонит Sr7
Слюда
жемчужная СаЗ
калиевая Kla
магнезиальная К60
обыкновенная Kla
Слюдка, рубиновая
FelO7B
СмайтитРе81б
Смальтин СоЗ
Смарагд Ве2
Смикит Мп71а
Смитит Ag2a
Смитсонит Znl3
Смолка, урановая U6
Смольяниновит Са88
Соболевскит Pd4
Согдианит К58
Сода, природная Na356
Содалит Na 13
Соддиит U49
Созалит Mgl4
Солонгоит В20
Соль
английская Mg76n,
глауберова Nal886
горькая М^76д
каменная NalO7a
эпсомская
Сомольнокит Fel35a
Сонолит Мп85
СонораитРе159
СорбиитРЬ71
Соучекит Си79б
СпанголитСиП
Спекулярит FelO56
Спенсерит Znl86
Сперрилит Pt26
Спёррит Са204
Сподумен U56
Спуррит Са204
Ссайбелиит В31
Ставролит Fel9
Станнин Fe70
Станноидит Fe50
Станномикролит Та 12
Старкиит Mg766
Старлит Zr3
Стеатит Mg826
Стекло, московское
оконное Kla
Стеллерит Са24б
Стенонит Sr2
Стенхуггарит СаЮЗ
СтеньеитСоЮ
Степановит Nal61
CTepKopHTNal79
Стерриит РЬ68
Стефанит Ag44
Стеэнструпин NalO2
Стибиванит VI1
Стибиконит Sb9
Стибиобетафит Са230
Стибиоколумбит Nb6
Стибиопалладинит PdlS
Стибиотанталит Та9
Стибнит Sb56
Стивенсит Mg82a
Стиллуотерит РЬЗ
Стильбит а41
Стистаит Sn8
Стишовит 815д
Стоксит Са220
Страньскийит Си 144
Страшимирит Си21б
Стрел кинит Na219
Стрингемит Са78
Стронцианит Sri 2
Стронциоапатит Sri 56
Стронциоарсенапатит Si9
Стронциоборит В 35
Стронциоджинорит Srtfl
Стронциодрессерит Sr3
Стронциохильгардит Srll
Струвит Mg656
Стрюверит Т17в
Стьюартит МпЗЗ
Суанит Mg23a
Сугилит К86
СукулаитТаИ
СульванитСиНЗ
Сульфоборит В 34
Сульфогалит Nal89
Сундвикит Са20а
Сундиусит РЬ53
Сундтит Ag35
Суниит А143
СуолунитСа210
Сурик РЬ50
железный FelO56
Суринамит А147
Сурьма Sbl
белая Sb46
мышьяковистая SblA
Суссексит В32
Сфалерит Zn236
СфенСа231
Сферокобальтит Соб
306
I. Неорганические вещества
Схёлингит Са76
Схюлтенит РЬ42
Сысерскит Osl
Сьюзаннит РЬ29б
СянхуалитЬШ
Сянизянити31
Тавмавит Са34б
ТаворитШ4
ТадёитСа144
Таджикит Са67
Тажеранит2г1а
Таканелит Мп45
Таковит Ni3
ТаленитУЮ
ТалмесситСа124
Тальк Mg826
Таманит Са98а
Тамаругит Na6a
Танатарит А126а
Тангеит Са82
Танзанит Са34в
TaHKOHTNal39
Таннелит В36
Танталит Та5а
Тантэвксенит Y16
Тапиолит Та5б
Тарамит Na59
Таранакит К5
Тарапакаит К29
Тарбаттит2п18а
Тарновицит, Тарновс-
китСа61б
ТатарскитСа135
Таумасит Si6
Таутолит Са34а
Таффеит MglO6
Тахаранит СаЗЗ
ТахигидритСа136
Тейлорит К72
тейниолит К55
тейнитСи137в
Теллур Tel
черный Аи 10
ГеллурантимонЗЫО
|еллурит Те2
|еллуровисмутин В117
|еллУропалладинит Pd23
|емискамитШ1
1енар(д)итЫа188а
Теннантит Fe48
Тенорит Си71
Терлингваит Hg5
Термонатрит Na35a
ТёрнобумитСеЮ
Терновскит Nal62
Терруггит В9
Терчит Са44б
Тестибиопалладит Pdl6
ТетрадимитВ121
Тетракалсилит К8в
Тетранатролит Nal 16
Тетрауикманит Sn56
Тетраферроплатина Pt5
Тетраэдрит Fe68
Тефроит Мп78
Техасит Рг1
Тешемакерит N4
ТиласитСа125
Тиллиит Са203
Тиллит РЬ80
ТиманитЩ14
Тинаксит К81
Тинкаль№18в
Тинкальконит Nal 86
Тинтинаит РЬ64б
Тинценит Саб
Тирагаллоит Мп76
Тирит Y76
Тиродит Mg61
Тиролит Са75
Тирреллит Си55
Тисонит Се5
Титанит Са231
Тихит№158
Тихоненковит А121
ТлалокитСи150
ТлапаллитСа81
Тоберморит Са182г
Томасит Si6
Томеит Fe36
ТомичитТПО
Томсенолит АН 86
Томсонит Na40
Топаз А148
восточный А123
западный, испанский
Si5e
ТопазолитСаЮб
Торбастнесит Са224
Торбернит U216
ТорианитТЫ
Торит Th26
ТоролитТаЮ
Торогуммит Th6
Торриит Mg98
Тортвейтит Sc2
Торутит ТпЗ
Точилинит Mg50
Травертин Са61г
Траскит Ва45
ТраскоттитСа212
ТреворитРе101
ТрёгеритШ5
Тредголдит U12
Трежерит Ag31
Тремолит Са150б
Трехманит Ag26
Тригонит МпбО
Тридимит Si5B
Трикалсилит К8г
Тримерит Са52
Триплит Мп32а
Триплоидит Мп32б
ТриппкеитСи19
Трипугиит Fel42
Трифан Li56
Трифилин Li 12
Трогталит Со 16а
Трои лит Fe 133
Троллеит А130
Трона Nal32
Трускоттит Са212
Трюстедтит Ni226
Тугариновит Мо2
Тугтупит Na30
Туиннит РЬ59б
Туламенит Pt7
Тулит Са34в
Тунгстенит W3
Тунгстит W16
Тундрит Nal05
Тунисит Na36
ТурбернитШШ
Тургит, Турьит FelO56
Тухолит, Тухуалит Nal 18
Тучекит Ni33
Тыретскит В16
Тюрингит Fe72A
Тюямунит Са246б
307
I. Неорганические вещества
Тяныыанит Na28
Уайартит Са248
УайтитСа137
Уайтманит Mg27
Уваровит Са72
УвитСа117
УзбекитСа142
Уикманит Sn5a
Уиксит К106
Уилкманит Ni22a
УиллиитЫа115а
Уинстанлиит Ti9
Уинчит Na68
УитлокитСа184
Уитморит Fe76e *
Уклонсковит Nal68
Улексит ВЗЗ
Улльманит Ni32
Ульвёшпинель, Ульвит 112
Ульрихит U6
Ультрабазит Ag38
Ультрамарин Na50
Умангит Си54
Умбозерит Na203
Умохоит U33
Унгемахит К84
Уоджинит Таб
УоллиситСиНО
Уордит Na56
Уордсмитит Са 130
УортитЫа164
УпалитШЗ
Уралборит Са40в
Уралолит Са56
Урамфит U35
Уранинит U6
Уранмикролит U55
Уранолепидит U19
Уранопилит U48
Ураноспинит Са234б
натриевый Na215
Ураносферит Bi25
Ураноталлит Са237
Уранотанталит Y15b
Уранотил Са245
Ураноторит Th5
Уранофан Са245
Уранохальцит U26
Ураноцирцит Ва50б
Ураношпатит U106
Уранпирохлор U 5
Уранторианит Th4
Урванцевит Pd5a
Урдит Се9б
Урейит Ag32
УсовитАШ
Уссингит Nal5
Уэвеллит Са62а
Уэдделлит Са62б
Уэйвеллит А129а
Уэйкфилдит Y17
Уэйлендит А16
Уэллсит Ва5а
Уэлшит Са140
Уэрриит Си95
ФабианитВ15
Файткнехтит Мп57а
Фалькондоит Ni40
Фаматинит Си 124
Фармаколит Са109в
Фармакосидерит К40
ФассаитСа146в
Фатерит Саб 1а
Фаузерит Мп71г
Фаулерит Мп77г
Фаустит Zn4
Фаялит Fe 150
Федоровскит В29
Фейхиит Ве5
Фёлькерит Са188б
Фельсит К 10а
Фелыиёбаньит А1416
Фенакит Be 13
Фенаксит К85
Ферберит Fel646
ФерванитРе163б
Фергюссонит Y76
Ферморит Sr9
Фероксигит Fe 107а
Ферригидрит FelO5B
Ферридравит Nal60
Феррикопьяпит Fel39
Ферринатрит Nal27
Феррипирофиллит Fel51
Феррисиклерит Li 13
Ферритунгстит Са96
Ферроаксинит Са84
Ферроактинолит Са107
Ферробрюсит Mg70
Ферробустамит Са105б
Феррогексагидрит
Феррожедрит Fe 10
Феррокарфолит Fel8
Ферропумпеллиит Са87
Ферроселит Fel47
Ферроуиллиит Nal 156
Ферроуинчит Na60
Ферруччит В 2
ФeppьeитNal50
Ферсманит Са232
ФерсмитСа178
Фибролит А1446
Фиброферрит Fel38
Фидлерит РЬ35
Физелиит Ag37
Филлипсит К79
Филлоуит Na77
Финикохроит РЬ38
Финнеманит РЬ4
Фишессерит Аи4
Флайшерит Ge2
Флетчерит Ni20
Флинкит Мп41
Флогопит К60
Флоренсит Се 1
Флюорит Са83
Флюоцерит Се5
ФлюэллитА131
ФоггитСаП
Фоглит Са238
Фожасит Na67
Фольбортит Си Г42
Форманит Y136
Форнасит РЬ37
Форстерит Mg79
Фосгенит РЬ27
Фосинаит Na62
Фостит Zn4
Фосфаммит N6
Фосфоррёсслерит Mg576
Фосфосидерит FelO96
Фосфоферрит Fe 11 Об
Фосфофиллит Fel68
Фосфохальцит Си76
Фосфуранилит Са241
ФошагитСа215
Фоязит Na67
308
I. Неорганические вещества
фрайбергит Fe3
фрайеслебенит Ag34
фрайринит Na55
фРанкеитРе128Б
франклинитРе167
франкоанеллит КЗ
франколитСа186а
франсвиллит Ва53
фребольдитСо15
фремонтит Li2
френцелитВПЗ
фрепонтит Zn28
фресноит Ва47
фриделит Мп84г
фридрихит Си90
фричеит U32
фробергитРе157
фройденбергит Na205
фроловит В5
Фронделит Мп34
Фрудит Pd56
Фрэнкдиксонит Ва22
Фторапатит Са186б
Фторапофиллит К24
Фтороколлофан Са62А
Фукалит Са205
Фуксит К1а
Фукучилит Fe59
Фуркалит Са242
Фурмарьеит U7
Фуронгит U11
Фут(е)итСи117
Фэрбанкит РЬ83
ФэрфилдитСа162
ФэрчайлдитКПа
Фюлёппит РЬ62
Хаапалаит Mg49
Хабазит Са22д
Хагендорфит№122а
Хадемит А1396
ХайдингеритСа109а
ХакманитИа13
Халибит Fe36
Халлимондит U39
Халсит Fe73a
Халцедон Si5>K
ХалькантитСиПбг
ХалькоалюмитСи12
Халькозин Cull5
Халькокианит Си 116а
Халькоменит Си 129
Хальконатрон NalO9
Халькопирит Fe57
Халькосидерит Fe54
Халькостибит Си 122
Халькотрихит Си72
Халькофанит Мп91
Халькофиллит Си5
ХалькоцитСи115
Хамартит СеЗ
Хамбергит Ве5а
Хамберстонит К90
Хаммарит Си84
Хаммерит К68
Ханколит А137
Ханксит К77
Ханнейит Mg64
ХантитСаШ
Харадаит Sri 7
Хардистонит Са269
Харосит К48
Харстигит Be 10
Хастингсит Na58
ХаститСо16б
Хатрурит Са208
Хаттонит Th2a
Хатчеттолит Na220
Хатчинсонит Т14
Хатчит Ag52
XaynHTNall9
Хаулит Са49
Хаусманит Мп46
Хауэрит Мп70
Хёгбумит Mg 11
ХеггитУП
Хеденбергит Са105а
Хедифан Са37
ХедлиитВП9
Хейвиит Са244б
Хейдорнит Na52
ХейитРе129
Хейкокит Fe49
Хеллендит Са261А
Хельмутвинклерит Znl9
Хемусит Mol
Хендерсонит Са259
Хендриксит К109
Хёрлбутит Са53
Хёрнесит Mgl9
Хессонит Са26
Хиастолит А144а
ХибинскитКПО
Хибшит Са32
Хизингерит Fel52
Хизлвудит Ni27
Хиллебрандит Са209
Хильгардит Са46
ХинитСиЮ9
Хинсдалит А136
ХиолитА117
Хлоантит Ni7a
ХлопинитУ15в
Хлоралюминит А19
Хлорапатит Са 185
Хлораргирит Agl 1
Хлорарсениан Мп17
Хлорманассеит Mg9
Хлорманганокалит Мп26
Хлороксифит Си 101
Хлоромагнезит Mg34a
Хлоротил Си24
Хлоротионит КЗЗ
Хлорофиникит Мп89
Хоакинит Na26
Хогтонит К61
Ходжкинсонит Мп96
Ходрашит Си49
Холденит Мп95
Холиит Cd46
Холлендит Ва35
Холлингуортит Rh2
ХолоалитСиЮ8
Хольмквистит Li 15
Хольтедалит Mg736
ХоманитРе135в
Хондроарсенит Мп14а
Хондродит Mg88
Хонквиит Ti6
XonnTZnl7
Хордисит Мо4а
ХотонитК61
Хризоберилл Bel
Хризоколла Си 13 3
Хризолит Mg79
Хризопраз Si5x
Хризотил (-асбест) Mg8lB
Хроматит Са70
Хромдиопсид Са146а
Хроминит РЬ38
309
I. Неорганические вещества
Хромит Сг4а
Хрусталь, горный Si5e
Хуанит Na71
Хуанхэит Ва19
Хуниит РЬЗбб
Хунитоит Са268
Хунчжаоит В226
Хьельмит Y14
Хьюлендит Са24а
Хьюмалит№170
Хьюэллит Са62а
Хьюэттит Са252
Хюбнерит Мп88
Хюгелит U40
Цветы
кобальтовые Со4
никелевые Nil26
сурьмяные Sb46
урановые К105
цинковые Znl5
ЦвизелитРеШ
Цейлонит Mg41
Цекцерит Nal43
Целестин Srl6
Целлерит Са236б
Цельсиан Ва4
Цеманит Na224
Цементит Fe35
Цеофиллит Са214
Церианит Се8
Цериопирохлор Се7
ЦеритСа135А
Церотунгстит W2
Церочухровит СабЗ
Церулеит СиЗ
Церул еолактит Са 13
Церулеофибрит Cul 17
Церуссит РЬ26
Цзисянит РЬ90
Цианотрихит Си 13
Цианохроит К32
Цилиндрит Fe 128A
Цимофан Bel
Цинк Znl
Цинкалюминит Zn6
Цинкенит РЬ60
Цинкит Znl6
Цинкмелантерит Zn24r
Цинкоботриоген Fel70
Цинкокопьяпит Fel71
Цинкрозасит Zn 14
Цинксилит Zn29
Цинк-циппеит U53
Циннабарит Hgl06
Циннвальдит К54
Циппеит К105
натриевый Na218
Циприн Са123
Цириловит Nal23
Циркелит Са275
Циркон Zr3
Цирконолит Са275
Циркосульфат Zr2
Цирсиналит Na99
Циртолит Zr3
ЦиситСи141
Цитрин Si5e
Цоизит Са34в
Цойнерити18б
ЦумебитСиЮЗ
ЦумкоритРе169
ЦумоитВНб
Чалмерсит Fe62
Чанбайит Nb4
Чаоит С2
ЧапманитРе145
Чароит К25
Чевкинит Се 12
Чеймберсит Мп19
ЧермакитСаПб
Чермигит А122
Черниит Си39
Черновит Y2
Черныхит Ва54
Черчиллит РЬ32
Честерит Mg87
ЧилдренитРе13
Чкаловит Na33
Чоклит Ni38r
Чухровит Са261
Шабазит Са22д
Шабурнит Т19
ШадланитРе125
ШайреритЫаШ
Шамозит Fe9
Шандит Ni24
Шанталит Са29
ШаттакитСи135
ШауртеитСаЮ8
Шафарцикит Fel41
Шахнерит Ag22
Шварцембергит РЬ45
Швацит Fe68
Шёгренит Mg44a
Шеелит Са260
Шенвиит Fe47
Шеневиксит Fe47
Шёнит К656
Шёнфлисит Sn4
Шёпит U37
Шервеит РЬ87
Шервудит Са258
ШёpлNall4
Шертелит Mg63
Шессилит СиЗб
Шизолит Na87
Ширмерит Ag29
ШмикитМп71а
Шмиттерит U50
Шнайдерхёнит Fe25
Шнебергит Са194б
ШодеритА151а
Шольцит Са266
Шорломит СаЮб
Шортит Na54
Шпат
атласный Са193в
баритовый Ва39
бурый Са90
гипсовый Са193в
голубой Mgl3
горький Са132
гренландский All6
дощатый Са197
железный Fe36
жемчужный Са132
известковый, исланд-
исландский Са61г
иттриевый Y9
кадмиевый Cd2
калиевый полевой КЮ
карминовый Fel 19
квасцовый К7
кобальтовый Соб
красный свинцовый
РЬЗба
310
. Неорганические вещества
кубовой Са193а
лазоревый (лазур-
(лазурный) Mgl3
ледяной КЮб
малиновый, марган-
марганцевый Мп22
медный Си35б
натриевый полевой
Na9a
олигоновый Fe36
персидский Ва39
плавиковый Са83
свинцовый РЬ26
тальковый Mg29
тяжелый Ва39
цинковый Zn 13
ядовитый Fe30
Шпессартин Мп7
Шпинель MglOa
благородная MglOa
железная Fell
хромистая Сг4
хромовая MglOa
цинковая Zn2
Шпионкопит Си53а
Шпироффит Мп87
ШрейеритТШ
Шрёккингерит Na94
ШтайгеритА149
Штернбергит Fe46
Штефанит Ag44
Штиллеит Zn26
Штихтит Mg356
ШтойберитУ1
Штольцит РЬ89б
ШтоттитСе1
ШтралитСа150а
ШтрелингитСа182б
ШтренгитРе109в
ШтромейеритА§17
^трунц МЗЗб
руцит МпЗЗб
ШтумпфлитРИО
Щ Fe2
Шультенит РЬ42
Шюттеит Hgl2
Щербинаит V5a
Эваит Мп14б
ЭвальдитВа13а
Эвдиалит Na 101
Эвдидимит Na34
днглийские названия
^ernathyite K103
Abichite Cu22
AcanthiteAg39a
Эвклаз ВеЗ
Эвкриптит Li4
ЭвксенитУ15г
Эвлитин Bil5
ЭвхроитСи21в
Эгирин№130
Эглстонит Hg4
Эденит Na69
Эдингтонит Ва5б
Эйтенбогардтит АиЗ
Эканит Са226
Экдемит РЬ5
Экерит Са35
Эккерманит Nal53
Экторит Nal41
Электрум Аи2
ЭлиитСиЮ5
Элит Си76
Эллестадит Са217
Эллисит Т12
Эллсуортит U5
ЭльбаитЫа138
ЭльпасолитА115
Эльпидит Na227
Эмболит AglO
Эмбриит РЬ39
Эмелеусит Nal40
ЭммонситРе158
Эмплектит Cu32
Эмприссит Ag50
Энаргит Cu286
Энделлит А146д
Эндлихит РЬ88б
Эндрьюсит Fe53
Энигматит Na206
Achavalite Fel46
AchiriteCul31
Achroite Nal38
Энстатит Mg786
Эосфорит Mn5
Эпидот Са34б
Эпистильбит Са23в
Эпсомит Mg76д
Эрдит№125
ЭрикаитРе31а
Эрикссонит ВаЗЗ
Эринит Cu5, Cu236
Эрионит К80
Эриохальцит Си41
Эритрин Со4
Эритросидерит Fe43
Эрлиит Ni3
Эрлихманит Os4
Эрубесцит Fe60
Эскеборнит Fe69
Эсколаит Сг8
Эскуррит Nal9
Эсперит Са267а
ЭттингитСа19
Эфесит№137
Эшеллит Nal la
ЭшинитСеП
Югаваралит Са23а
Юнонаит Си85
Юриит Nal08
Юролит Мп40
Ютаит К48
Юталит А127в
Ютенбогордит АиЗ
Явапайит К46а
Яговерит Ва2
Ягоит РЬ40
Якобсит МпЗ 1
Ялпаит Agl8
Ярлит А120
Ярозит К48
Ярославит А125
Ярроуит Си50
Яхонт, красный, синий
А123а
Яшма
Aciculite Cu79a
AcmiteNal30
ActinoliteCal50a
311
I. Неорганические вещества
Adamine, Adamite Znl la
Adelite Cal27
Admontite Mg236
Adular(ia) KlOa
Aegirine Nal30
Aenigmatite Na206
Aeschynite Cell
Afwillite Ca200r
Agardite Y5
Agate Si5*;
moss Si5>K
AgiriteNal30
Agrellite Na85
Agrinierite K101
Aguilarite Ag48
Ahlfeldite Ni36
Aikinite Cu79a
AjoiteK31
Akaganeite FelO7r
Akatoreite MnlO
Akdalaite A1236
Akermanite, Akjaermanite
Cal47a
Akrochordite Mg58
Aksaite Mg22a
Alabandite Mn69
Alabaster Са193в
Alamosite Pb79
Albite Na9a
Albrittonite Co7
Aldermanite Mgl5
Aleksite Pb25
Alexandrite Bel
AlgodoniteCul8
AllactiteMnl7
Allanite Ca34a
Allargentum Ag40
AllchariteFelO76
Alleghanyite Mn80
Allemontite SblA
Alloclasite Co56
AllopalladiumPdl5
Allophan A123r
Almandine, Almandite Fel7
Alstonite Ва13в
Altaite Pb82
Althausite Mg73a
Alum
iron Fel5
magnesia Mgl6
potash, potassium K66
rock K7
Roman Fe 15
soda, sodium Na6B
Aluminite A1406
Aluminocopiapite Fel6
Alumohydrocalcite Ca7
Alumokatophorite Na57
Alumotungstite WIb
Alumstone, Alunite K7
Alunogen A1386
Alvanite A150
Amakinite FelO6
Amalgam Ag21
Amarantite Fel37
Amarillite Nal26
Amazonite К 10b
Amblygonite Li2
Ameghinite Nal7
Amethyst Si5e
oriental A123a
Amicite K76
Ammoniojarosite Fe97
Amosite Fel55
Amphigene K9
Analcime, Analcite Na86
Anandite Ba26
Anapaite ta98a
Anatase Ti76
Andalusite A144a
Andersonite Na95
Andesine Na96
Andorite Ag35a
Andradite CalO6
Andremeyerite Ba25
Andrewsite Fe53
Anduoite Ru3
Angelellite Fe26
Anglesite Pb52
Anhydrite Cal93a
Anigmatite Na206
AniliteCu51
Ankerite Ca90
Annabergite Nil26
Annite K38
Anorthite Ca20a
Anorthoclase Na9e
Antarcticite Саб8
Anthoinite A152a
Anthonyite Cu44
Anthophyllite Mg36
Antigorite Mg81 a
Antimonite Sb56
Antimonpearceite Ag46a
Antimony Sbl
arsenical SblA
white Sb46
AntleriteCull9a
Antoinite A152a
Apachite Cul32
Apatite Ca 1866
Aphthitalite K94
Apjohnite Mn6
Aplowite Co 13a
Apuanite Fe84
Aquamarine Be2
AragoniteCa6l6
Aramayoite Ag426
Arcanite K98
Archerite K50
ArdealiteCall3
Ardennite Mg57A
Arfvedsonite Nal21
Argentite Ag396
Argentojarosite Fe6
Argentopentlandite Fe5
Argentopyrite Fe4a
Argyrodite Ag20
Arkansite Ti7a
Armalcolite Mg92
Armangite As4
Armenite Bal2
Armstrongite Ca274
Arrojadite K83
Arsenate-belovite Cal24
Arsenbrackebuschite Fell8
Arsenic Asl
white As3a
yellow As5
Arsenobismite Bi3
Arsenoclasite Mnl6
Arsenolamprite As2
Arsenolite As3a
Arsenopalladinite Pd3
Arsenopolybasite Ag4a
Arsenopyrite Fe30
Arsenosulvanite Cu28a
Arsenuranospathite U8
Arsenuranylite Ca235
Artinite Mg31a
312
I. Неорганические вещества
Asbecasite Ca58
Asbestos, blue Na 120
AschariteB31
AshtoniteNalOa
Astrak(h)anite Nal64
Astrolite Kla
Atacamite Cu456
Atelestite Bi4
Athabascaite Cu56
Atheneite Pb2
AtokitePdl9
AtopiteCal946
Attapulgite Mg85
AubertiteCulO
Augelite A128a
Augite Na66
Aurichalcite Cul47
Auricupride Cu30
Aurorite Mn44
Aurostibite Aull
Austinite Ca264
Automolite Zn2
Autunite Ca2406
sodium Na217
Aventurine Na9a
Avicennite T13
Avogadrite Bl
Azoproite Mg42a
Azure, copper Cu36
Azurite Cu36
Babefphite Ba9
Babingtonite Ca93
Baddeleyite Zrl6
Bafertisite Ba44
Bahianite A142
Bakerite Ca39A
BalkaniteAgl3
BallasC16
BalyakiniteCul37a
BambollaiteCul276
Banalsite Na23
Bandylite B7
BannisteriteNal78
Bararite Si3a
Barbertonite Mg35a
^arbierite К 10b
°arbosalite Fe76a
°ananditeV12
incite Mg716
Bariomicrolite Ba42
Bariopyrochlore Ba38
Barite Ba39
BarnesiteNa221
Barrerite Na47
BarringeriteFel08
Barringtonite Mg296
Barroisite Na63
Barsanovite NalOl
Bartonite K42
Barylite BalO
Barysilite Mn64
Barytes Ba39
Barytocalcite Bal36
Barytocelestine Ba39
Basaluminite A141a
Bassanite Cal936
Bassetite U30
Bastinite Mn40
Bastnaesite, Bastnasite Ce3
Batisite Na29
Bauxite А123в
Bavenite Ca50
Bayerite A124a
Bayleyite Mg94
Baylissite K62
Bazirite Ba56
Bazzite Be 12
Bearsite Be4
Beckelite СаббА
Becquerelite Ca239
Behoite Be9
Behierite Ta2
BellidoiteCul286
Bellingerite Cu66
Bellite Ag33A
BeloviteSrl5a
Bementite Mn84a
Benitoite Ba46
Benstonite Bal4
Beraunite Fe79
Berborite Be56
Beresovite Cr4a
BergeniteBa51
Berlinite A127a
Bermanite Mn47
Berndtite Sn7
Berryite Cu88
Berthierine Fel53a
Berthierite Fel44
BerthoniteCul06
Bertossaite Li 10
Bertrandite Be 15
Beryl Be2
BerylliteBel4
BerylloniteNa31
Berzelianite Cul28a
Berzeliite Na70
Bessmertnovite Au9
Beta-ceriumfergussonite
Ce6
Betafite Na220
Beta-roselite Ca696
Beta-uranophane Ca243
Betekhtinite Fe61
BeudantiteFel20
Beusite Mn59a
Beyerite Ca59
Bianchite Zii24b
BicchuliteCa31
Bideauxite Ag33
BieberiteCol3B
Bikitaite 1Л56
Bilinite Fe826
Billietite Ba48
Billingsleyite Ag45
Bindheimite Pb58a
Binnite Fe48
Biotite K61
Biphosphammite N5
Biringuccite Na20
Bischofite Mg346
Bismite Bi86
Bismoclite Bi6
Bismuth Bil
Bismuthinite Bill
Bismutite Bi5
Bismutoferrite Fe34
Bismutomicrolite Ta4
Bismutotantalite Ta3
Bityite Li9
Bixbyite Mn55
BjarebyiteBa31
Blanchardite Cul20a
Blende
antimony Sb6
bismuth Bil5
cadmium Cd4a
hepatic Zn236
molybdenum Mo46
313
I. Неорганические вещества
shelly Zn236
silver Ag436
zinc Zn236
Bloedite Nal64
Bloodstone Si5x
Bloom
antimony Sb46
cobalt Co4
nickel Nil26 .
uranium К105
zinc Zn 15
Bobierrite Mg71a
Boehmite A1266
Boggildite Nal99
Bohdanowiczite Ag7
Bohmite A1266
BoleiteAgl6
Bolivarite А128в
Boltwoodite К ЮЗА
sodium Na216
Bonaccordite Fe99
BonattiteCull6B
ВооНиЧеСиПбд
Boracite Mg26
Borax Na 18b
BorcariteBll
BornhardtiteCol7
Bornite Fe60
Boronatrocalcite B33
Borovskite Pb74
BortC16
Botallackite Cu45a
Botryogen Mg51
Boulangerite Pb63
Bournonite Си 106
Boussingaultite Mg66
Boyleite Zn24a
Brabantite Ca225
Bracewellite Cr9a
Brackebuschite Mn67
BradleyiteNal57
Braggite Pt8a
Bragite Y76
Brammallite Nal6
BrandisiteCall5
BrandtiteCal55
Brannerite U56
Brannockite K57
Brassite Mg55a
Braunite Mn42
Bravoite Ni266
Brazilianite Na5a
Brazilite Zrl6
Bredigite Cal49
Breithauptite Ni30
Breun(n)erite Mg29a
Brewsterite Sr8
Brezinaite Cr2
Brianite Na74
BriartiteCu61
Brochantite Си 120a
Broggerite U6
Bromargyrite Ag9
Bromellite Be8
Bromite Ag9
Bromlite Ва13в
Bromyrite Ag9
Bronzite Mg786
Brookite Ti7a
Brownmillerite Ca85
Brucite Mg70
BruggeniteCall46
Brugnatellite Mg43
Brunogeierite Fe89
BrushiteCall26
Buchwaldite Na80
BuddingtoniteNl
Buergerite Nall3
Buetschliite К176
Bukovskyite Fe286
Bunsenite Ni23
Burangaite Nall6
Bustamite Mn776
ButleriteFel38a
Buttgenbachite Cu43
Byssolite Cal50a
Bystromite Mg77
Bytownite Ca206
Cacoxenite Fell4
Cadmium Cdl
Cadmoselite Cd5
CadwaladeriteAllO
Cafetite Ca227
Cahnite B4
Cairngorm Si5e
Calafatite K7
Galaite Cu7
Calamine Znl3, Zn30
common Zn30
precious Zn 13
siliceous Zn30
Calaverite Аи 12a
Calciborite Ca40a
Calciocopiapite CalO2
CalcioferriteCal39
Calciouranoite Ca233
Calciovolborthite Ca82
CalciteCa61r
Calcium-cataple(i)ite
Ca273
Calderite Mn37
Caledonite Cu96
CaliforniteCal23
Calkinsite Ce2
Callaghanite Mg38
Calomel Hg2
Calumetite Cu73
Calzirtite Ca276
Canasite Na89
Canavesite B12
Canfieldite Ag49
Cannizzarite Pb20
Cappelenite Ba55
CaracoliteNal87
Carboborite BIO
Carbocernaite Са61в
Carbonado С16
Carbonate-cyanotrichite
Cu6
Carborundum Sil
Carlfriesite Ca223
CarlhintzeiteA113
Carlinite T16
CarmmiteFell9
Carnallite K63
Carnelian Si5e
CarnotiteK107
Carobbiite K34
Carpholite Mn9
Carrboydite Ni4
Carrollite Co96
Caryopilite Mn846
CassidyiteCal81
Cassiterite Sn3
Cataple(i)ite Na226a
Catophorite Na65
Cattierite Co 12
Caysichite Yl
Celadonite K64
314
I. Неорганические вещества
Cele, Celestite Sri6
Celsian Ba4
Cementite Fe35
CerargyriteAgll
Cerianite Ce8
Ceriopyrochlore Ce7
CeriteCal35A
Cernyite Cu39
Cerochukhrovite Ca63
Cerotungstite W2
Ceruleite Cu3
CeruleofibriteCull7
CeruleolactiteCal3
Cerussite Pb26
Cervantite Sb8
Cesarolite Mn61
Cesbronite Cul40
Ceylanite, Ceylonite Mg41
Chabazite Са22д
Chaboumeite T19
ChalcanthiteCull6r
Chalcedony Si5)K
Chalcoalumite Cu 12
ChalcociteCull5
Chalcocyanite, Chalcokya-
niteCull6a
ChalcomeniteCul29
Chalconatronite NalO9
Chalcophanite Mn91
Chalcophyllite Cu5
Chalcopyrite Fe57
Chalcosiderite Fe54
ChalcosineCull5
ChalcostibiteCul22
Chalcotrichite Cu72
Chalk Саб 1 г
French Mg826
Chalmersite Fe62
Chalybite Fe36
Chambersite Mnl9
Chamosite Fe9
changbaiite Nb4
chantalite Ca29
Chaoite C2
c^apmanite Fel45
charoite K25
^enevixite Fe47
^hernovite Y2
^nykhite Ba54
'-nervetite Pb87
Chessylite Cu36
Chesterite Mg87
ChevkiniteCel2
Chiastolite A144a
Childrenite Fel3
ChioliteA117
Chkalovite Na33
Chloanthite Ni7a
Chloraluminite A19
ChlorapatiteCal85
Chlorargyrite Agll
Chlorarsenian(ite) Mnl7
Chlormanasseite Mg9
Chlormanganokalite Mn26
Chloromagnesite Mg34a
Chlorophaenicite Mn89
magnesium Mg20
Chlorothionite K33
Chlorotile Cu24
ChloroxiphiteCulOl
Chocolite Ni38r
CholoaliteCul08
Chondroarsenite Mnl4a
Chondrodite Mg88
Christianite Ca20a
Christite Hgl6a
Chromatite Ca70
Chromdiopside Cal46a
Chrominite Pb38
Chromite Cr4a
Chrysoberyl Bel
Chrysocolla Cul33
Chrysolite Mg79
Chrysoprase Si5ac
Chrysotile (-asbestos)
Mg8lB
ChukhroviteCa261
Churchillite Pb32
Cinnabar HglO6
antimony Sb6
Austrian, chrome Pb38
Cinnabarite HglO6
Citrine Si5e
Claringbullite Cu46
Clarkeite Na93
Claudetite As36
Clausthalite Pb75
Clay A146b
China, porcelain А146в
Clayophan Zn236
Cleavelandite Na9a
Cleveite U6
ClifforditeU51
Clinobisvanite Bi26a
Clinochlore Mg2
Clinoclas(it)e Cu22
Clinohedrite Ca2676
Clinoptilolite NalO6
Clinostrengite FelO96
ClintoniteCall5
Cobalt
black earthy Ba34
speiss, tin white Co3
white Co2
Cobaltite Co5a
Cobaltocalcite Co6
CobaltomeniteCol8
Cobaltpentlandite Fe46
Cobalt-zippeite Co20
Cochromite Crl
Coconinoite U28
Coesite Si56
Coffinite U54
Cohenite Fe35
Colemanite Ca42a
CollinsiteCal42
Collophanite Ca62A
Coloradoite Hgl5
Columbite Nb2a
Combeite Na88
Compreignacite К102
CongoliteFe316
Conichalcite Ca74
ConnelliteCull7
Cooperite Pt86
Copiapite Fe83
Copper Cul
ruby Cu72
selenium Cul28a
Copperas Fel35e
yellow Fe83
Coquimbite Fel36B
Corderoite Hgll
Cordierite Mgl
iron Fe8
Cordylite Ba20
CorkiteFel24
Cornetite Cu75a
Cornubite Cu23a
CornuiteCul33
315
I. Неорганические вещества
Cornwallite Cu236
Coronadite Mn49
Corundum A123a
Cosalite РЫ8
CosmochloreNal08
Costibite Col46
Cotunnite РЬЗО
Coulsonite V2
Covelline, Covellite Cull2
CowlesiteCa216
CrandalliteCal5
Crednerite Mn28
CreediteCal8
Cristobalite Si5r
CrocidoliteNal20
Crocoite РЬЗба
Cromfordite Pb27
Cronstedtite Fe74
CrookesiteCul28B
CrossiteNal52
Cryolite All6
CryolithioniteA119
Cryptohalite Si36
Cryptomelane K69
Crystal, rock Si5e
Cubanite Fe62
Cumengeite CulOO
Cummingtonite Mg86
Cuprite Cu72
Cuproartinite Cu35r
Cuproauride Cu30
Cuprobismuthinite Cu34
Cuprocopiapite Fe67
Cuprodescloizite Cul 11
Cuprohydromagnesite
Cu38
Cupropavonite Agl5
Cuprosk-f odowskite U26
Cuprospinel Fe52
Cuprorivaite Ca79
CuprostibiteCul21
Curetonite Ba43
Curienite U47
Curite Pb86
Cuspidine, Custerite Ca207
Cyanite А144в
Cyanochroite K32
Cyanotrichite Cul3
Cylindrite Fel28A
Cymophane Bel
Cymrite Ba7
CyprineCal23
Cyrilovite Nal23
Cyrtolite Zr3
D'AchiarditeNal2
Dadsonite Pb73
Dahllite Cal88a
Dakeite Na94
DalyiteK112
Danaite Со5в
Danalite Fe32
Danburite Ca47
Dannemorite Mn38
D'Ansite Nal67
Daomanite Cu27
Darapiosite K89
DarapskiteNal82
Dashkesanite K19
Datolite Ca48
DaubreeiteBilO
Davisonite Cal4
Dayingite Co9a
Deerite Fe87
DelafossiteFe51
Delhayelite Na48
Delrioite V86
Demantoid CalO6
Demesmaekerite U22
Derbylite Ti4
Derriksite U24
Desautelsite Mg60
Descloizite Zn22
Desmine Na41
Despujolsite Cal64
Devilline, Devillite Ca77a
Dewindtite U42a
Diaboleite Cu98
DiadochiteFell5
Dialogite Mn22
Diamond С16
Diaphorite Ag38
Diaspore A126a
Dichroite Mgl
Dickinsonite K92
Dickite A146a
Dienerite Ni9
Dietrichite Zn5
DietzeiteCa71
Digenite Cu52
Dimorphite As7
Diopside Cal46a
DioptaseCul31
Disthene А144в
Dittmarite Mg65a
Dixenite Mn52
Djalmaite U55
DjurleiteCulH
DolerophaniteCull8
Dolomite Cal32
Domeykite Cul4
Donatite Cr46
Donnayite Na200
DorfmaniteNal34
Douglasite Fe42
Downeyite Se2
Dravite Nal46
Dresserite Bala
Droogmansite U45
Drugmanite Fel23
Drysdallite Mo5
Dufrenite Ca92
DufrenoyitePbll
Duftite Cu77
Dumontite U43
Dumortierite A15
Dundasite A134
Durangite Na2
Duranusite As6
Duttonite V7
Dypingite Mg326
Dysanalyte Ca228
Dyscrasite Ag41
Dysluite Zn2
Dzhalindite In2
Eakerite Ca35
Earleyite Ni3
Ecdemite Pb5
EchelliteNalla
Eckermannite Nal53
Edenite Na69
Edingtonite Ba56
Eglestonite Hg4
Ehlite Cu76
Eifelite K91
EiteliteNal55
Ekanite Ca226
Ekaterinite Ca45
ElbaiteNal38
316
I. Неорганические вещества
Electrum Au2
EllestaditeCa217
Ellisite T12
Ellsworthite U5
ElpasoliteA115
Elpidite Na227
Elyite Cul05
EmboliteAglO
Embreyite Pb39
Emeleusite Nal40
Emerald Be2
copper Cul31
nickel Nil8
oriental A123a
Emery A123a
Emmonsite Fel58
Emplectite Cu32
Empressite Ag50
Enargite Cu286
EndelliteA146A
Endlichite Pb886
Englishite K78
Enigmatite Na206
Enstatite Mg786
Eosphorite Mn5
EphesiteNal37
Epidote Ca346
Epistilbite Са23в
Epsomite М^76д
ErditeNal25
Eremeyevite A14
EricaiteFe31a
Ericssonite ВаЗЗ
Erinite Cu5, Cu236
Eriochalcite Cu41
Erionite K80
Erlichmanite Os4
Erubescite Fe60
Erythrite Co4
Erythrosiderite Fe43
EschyniteCell
Eskebornite Fe69
Eskolaite Cr8
Esperite Ca267a
EttringiteCal9
EucairiteAgl9
EuchroiteCu2lB
tuclase Be3
-•^jHLue Li4
tuditalyteNal01
Eudidymite Na34
Eulytin, EulytiteBil5
EuxeniteY15r
Eveite Mnl46
Ewaldite Bal3a
Eye
cat's Bel
hawk's Na 120
Ezcurrite Nal9
Fabianite В15
Faheyite Веб
Faialite Fel50
Fairbankite Pb83
FairchilditeK17a
Fairfieldite Cal62
Falcondoite Ni40
Famatinite Cul24
Fassaite Са146в
Faujasite Na67
Fauserite Mn71r
Faustite Zn4
Fayalite Fel50
Fedorovskite B29
Feitknechtite Mn57a
Feldspar
potash K10
soda Na9a
Felsite KlOa
Felsobanyite A1416
Fenaksite K85
Ferberite Fel646
Fergussonite Y76
Fermorite Sr9
Feroxyhyte FelO7a
Ferricopiapite Fel39
Ferridravite Nal60
Ferrierite Nal50
Ferrihydrite Fe 1 05b
FerrinatriteNal27
Ferripyrophyllite Fe 151
Ferrisicklerite Li 13
Ferritungstite Ca96
Ferroactinolite Ca 107
Ferroaxinite Ca84
Ferrobrucite Mg70
Ferrobustamite Cal056
Ferrocarpholite Fe 18
Ferrogedrite FelO
Ferrohexahydrite Fel35fl
Ferropumpellyite Ca87
FerroseliteFel47
Ferrowinchite Na60
Ferrowyllieite Nal 156
Ferruccite B2
Fersmanite Ca232
FersmiteCal78
Fervanite Fel636
FibroferriteF1386
Fibrolite A1446
Fiedlerite Pb35
Fillowite Na77
Finnemanite Pb4
Fire-opal Si5n
Firestone Si5)K
Fischesserite Au4
Fizelyite Ag37
Fleischerite Ge2
Fletcherite Ni20
Flinkite Mn41
Flint Si5;ac
Florencite Cel
FluelliteA131
Fluocerite Ce5
Fluorapatite Cal866
carbonate Cal86a
Fluorapophyllite K24
Fluorite Ca83
Fluorocollophanite Ca62A
Fluorspar Ca83
Foam, sea Mg83
Foggite Cal 1
FooteiteCull7
Formanite Yl 36
Fornacite Pb37
Forsterite Mg79
FoshagiteCa215
Fourmarierite U7
Fowlerite Mn77r
Fraipontite Zn28
Francevillite Ba53
Franckeite Fel28B
Francoanellite КЗ
Francolite Cal86a
Frankdicksonite Ba22
FrankliniteFel67
FrebolditeCol5
Freibergite Fe3
Freieslebenite Ag34
Freirinite Ba55
317
I. Неорганические вещества
Fremontite Li2
FrenzeliteBiB
Fresnoite Ba47
Freudenbergke Na205
Friedelite Mn84r
Friedrichite Cu90
Fritzscheite U32
Frohbergite Fel57
Frolovite В5
Frondelite Mn34
Froodite Pd56
Froth
copper Ca75
sea Mg83
Fuchsite Kla
Fukalite Ca206
Fukuchilite Fe59
Fuloppite Pb62
Furongite Ull
GabrielssoniteFell7
GadoliniteBel6
Gagarinite Na97
Gageite Mn83
Gahnite Zn2
Gaidonnayite Na2266
Gaitite Ca265
Galaxite Mn3
Galeite Nal90
Galena, Galenite Pb51a
Galenobismutite Pbl7a
Gallite Cu60
GalmeiZnl3, Zn30
edlerZnl3
Gamagarite Ba27
Ganomalite Cal91
GanophylliteNal71
Garnierite Ni38a
Garrelsite Na24
Garronite Na46
GaspeiteNil6
Gatumbaite Cal2
Gaylussite Na53B
GearksutiteCalO
Gedrite, sodium Nal45
Gehlenite Ca2
Geikielite Mg91
Gem
red, blue A123a
Genkinite Pt9
GenthelviteZnl2
Georgeite Cu37
Georgiadesite Pb7
Gerhardtite Cu70
Germanite Cu47
GersdorffiteNil3
Gerstleyite Nal93
Gerstmannite Mg62
Getchellite Sb2
GeversitePtll
Geyserite Si5H
Gianellaite Hg7a
Gibbsite A1246
GilaliteCul30
Gillespite Ba24
Gilpinite U23
Giniite Fe78
Ginorite Ca43
Girdite Pb43
Gismondite Ca20r
Gittinsite Ca272
GladiteCu81
Glance
antimony Sb56
bismuth Bill
cobalt Co5a
copper Cul 15
grey spear Sb56
iron FelO56
leadPb51a
molybdenum Mo46
nickel Ni 13
pearl Si5M
red spear Sb6
selenobismuth Bil3
silver Ag396
silver copper Ag 17
Glaserite K94
Glauberite Na82a
Glaucochroite Cal65
Glaucodot Co5b
Glauconite K37
Glaucophane Nal52
Glaucospherite Cu35a
Glushinskite Mg30
Gmelinite Na44
Godlevskite Ni28
Goedkenite Sr5
Goergeyite K23
Goethite FelO76
GoldAul
bismuth Au7
silvery Au2
Goldichite К46в
Goldmanite Ca257
Gonnardite Na43
Gonyerite Mn29
Goosecreekite Ca236
Gorceixite Ba3
Goshenite Be2
Goslarite ZnlAji
Goudeyite Cu4
GoweriteB17
Goyazite Sr4
GraemiteCul376
Graftonite Ca97
GrammatiteCal506
Grandidierite Mg7
Grandite Ca26
Grantsite Na96
Graphite Cla
GratonitePbl2
Green
copper, mountain
Cu356
uranium U26
Greenalite Fel536
Greenockite Cd4a
GreigiteFe81a
Grimaldiite Сг9в
Grimselite K97
Grossular(ite) Ca26
Groutite Мп57в
Grovesite Mn26
GnineriteFel55
Guanajuatite Bil3
Gudmundite Fe 143
GueriniteCallOB
Guettardite Pb59a
Guildite Fe66
Guilleminite Ba52
Gunningite Zn246
Gustavite Ag27
Guyanaite Cr96
Gypsum Са193в
GyroliteCa211
Haapalaite Mg49
Hackmanite Nal3
Hafnon Hfl
318
I. Неорганические вещества
Hagendorfite Nal22a
HaggiteV13
HaldingeriteCalO96
Haiweeite Ca2446
Halite NalO7a
HalloysiteA146r
Hallymondite U39
HalotrichiteFel5
Halurgite B22a
Hamartite Ce3
Hambergite Be5a
Hammarite Cu84
Hancockite A137
Hanksite K77
Hannayite Mg64
Haradaite Srl7
Hardystonite Ca269
Harmotome Ba6
Harstigite BelO
Hastingite Na58
HastiteCol66
Hatchettolite Na220
HatchiteAg52
Hatrurite Ca208
Hauchecornite Nil5
Hauerite Mn70
Haughtonite K61
Hausmannite Mn46
Hauyn(it)e Nal6a
Hawleyite Cd46
Haycockite Fe49
Heazlewoodite Ni27
HectoriteNaHl
Hedenbergite CalO5a
HedleyiteBil9
Hedyphane Ca37
Heinrichite Ba496
Heintzite B30
Heliodor Be2
Heliotrope Si5*;
HellanditeCa261A
Helmutwinklerite Znl9
Helvite Mn21
HemafibriteMnl5
Hematite FelO56
HematoliteMnl3
HematophaniteFel21
?emimorphite Zn30
jfmusite Mol
Hendersonite Ca259
Hendricksite K109
HenritermieriteCal72 .
Hercynite Fel 1
Herderite Ca54
Herzenbergite Sn6
HessiteAg51
Hessonite Ca26
Hetaerolite Mn90
Heterogenite Co 10
Heteromorphite Pb65
Heterosite FelO9a
Heulandite Ca24a
Hewettite Ca252
Hexahydrite Mg76r
Hexahydroborite Ca40r
Hexatestibiopanickelite
Pdll
Heyite Fel29
Heyrovskyite Ag28
Hibschite Ga32
Hidalgoite A133
Hiddenite Li56
Hieratite Si2
Hilairite Na226B
Hilgardite Ca46
Hiilebrandite Ca209
Hinsdalite A136
Hintzeite B30
Hisingerite Fel52
Hjelmite Y14
Hocartite Fe7
Hodgkinsonite Mn96
Hodrushite Cu49
Hoegbomite Mgl 1
Hoernesite Mgl9
Hogbomite Mgll
Hohmannite Fel35b
Holdenite Mn95
Hollandite Ba35
Hollingworthite Rh2
Holmquistite Li 15
Holtedahlite Mg736
Homilite Ca89
Honeyblende Zn236
Hongquiite Ti6
Hopeite Znl7
Hornblende Na71
Homesite Mgl9
HortonoliteFel50
HowieiteNall9
Howlite Ca49
Hsianghualite Li 11
Huebnerite Mn88
Huemulite Nal70
Hiigelite U40
Hulsite Fe73a
Humberstonite K90
Humboldtine Fe37
Humboldtite Ca48
Humite Mg89
Hummerite K68
Hungchaoite B226
HuntiteCal33
Hureaulite Mn40
Hurlbutite Ca53
Hutchinsonite T14
Huttonite Th2a
Hwanghoite Bal9
Hyacinth Zr3
oriental A123a
Hyalite Si5h
Hyalophane K14
Hyalotekite Pbl5
Hydrargillite A1246
HydroboraciteCal29
Hydrocalumite Ca9
Hydrocerussite Pb28
Hydrodresserite Bal6
Hydroglauberite Na83
Hydrogoethite РеЮ7д
Hydrogrossular Ca32
Hydrohalite NalO76
Hydrohematite Fel056
Hydromagnesite Mg32a
Hydromica K16
Hydromuscovite KIb
Hydroniumjarosite Fe92
Hydrophane Si5h
Hydroscarbroite A18
Hydrotalcite Mg86
Hydrotungstite \?1д
Hydroxylapatite Cal886
Hydroxylapophyllite K26
Hydroxylbastnasite Ce4
Hydroxylellestadite Ca218
Hydroxylherderite Ca55
Hydrozincite Znl5
Hypercinnabar Hg9
Hypersthene Mg53
319
I. Неорганические вещества
Ianthinite U38
IceH2
Idaite Fe58a
IdocraseCal23
Iimoriite Y12
IkunoliteBil2
IlesiteMn716
IlliteKlB
IlmeniteTil
Ilmenorutile Т\1ъ
Ilvaite Ca94
Imandrite Na61
InderboriteB18
Inderite B21
Indianite Ca20a
IndicoliteNal38
Indigo, copper Cull2
IndigoliteNal38
Indite Fe94
Indium Inl
InesiteCal71
Insizwaite Pt3
Inverarite FelO3
Inyonite Са42в
Iodargyrite Ag24
Iodobromite Ag9
Iodyrite Ag24
Iolite Mgl
Iowaite Mg45
Iranite РЬЗбб
Irarsite Ir3
Iridarsenite Ir2
Iridium Irl
Iridosmine, Iridosmium Osl
Irigonite U34
IronFel
-earth, blue Fell Or
Isoclasite Cal87
Isoferroplatinum Pt6
Isokite Cal43
Isomertieite Pb56
IsostanniteCul48
Itoite Pb41
Iwakiite Mn316
Ixiolite Nbl
Jack, black Zn236
Jacobsite Mn31a
Jade Ca 150a, Na8a
Jadeite Na8a
Jagoite Pb40
Jagowerite Ba2
Jaipurite Coll
JalpaiteAgl8
Jamesonite Fel27
Jargon Zr3
Jarlite A120
Jarosite K48
Jasper Si5)K
Jeffersonite Cal46a
Jennite Са200д
Jezekite Na38
Jimboite Mnl8
Jimthompsonite Mg84
Jixianite Pb90
Joaqufnite Na26
Johachidolite Ca5
Johannite U23
Johannsenite Cal66a
Johnbaumite Ca39
Johnsomervilleite Na73
Jokokuite Мп71в
Joliotite U166
Jonesite K15
Jordanite Pbl4
Jordisite Mo4a
Joseite Bi23
Jouravskite Cal57
JuaniteNa71
Julgoldite Ca95
Junitoite Ca268
Junoite Cu85
Jurbanite A139a
Kahlerite U296
Kainite K67
Kaliblodite K65a
Kaliborite B30
Kalicinite K49
Kalinite K6a
Kaliophilite K8a
Kalipyrochlore K93
Kalistrontite K96
Kallaite Cu7
Kalsilite K86
Kaluszite K22
Kanemite Nal33
Kanoite Mn77a
Kanonaite Mn8
Kantite Fe226
Kaolin(ite) А146в
Karelianite V4
Karibibite Fe27
Karstenite Cal93a
Kasolite U45
Kassite Ca229
Katophorite Na65
Katoptrite Mn74
Kawazulite Bi22
KeckiteCal58
Keithconnite Pd22
KeldyshiteNa231
Kemmlitzite Sri
Kempite Mn27
Kennedyite Mg90
Kentrolite Mn65
KenyaiteNal97
Kermesite Sb6
KerniteNal8a
Kerstenite Pb77
KesteriteCul48
Kettnerite Ca60
Keyite Cu20
KhademiteA1396
Khibinskite Kl 10
KhiniteCul09
KhlopiniteY15B
Khuniite РЬЗбб
KidwelliteNal24
Kieserite Mg76a
Kilchoanite Ca2006
Killalaite Са200в
KimzeyiteCa271
Kingite A1296
Kinoshitalite Ba29
Kingsmountite Ca86
Kinoite Ca80
KirschsteiniteCalO4
Kitkaite Ni42
Klaprothite СиЗЗ
Юebelsbergite Sb7
Kleemanite Zn3
Kleinite Hg6
KlockmanniteCul26
Kmaite K64
Knebelite Mn36
Knipovichite Ca7
Knopite Ca228
Knorringite Mg37
KoashviteNa91
320
I. Неорганические вещества
Kobelli Pb21
jCoechlinite Bi7
Koenenite Nal49
Koettigite Zn96
Kogarkoite Nal92
Koktaite Cal76
KolbeckiteScl
Kolwezite Cu35b
IColymite Cu63
KomaroviteCal79
KoninckiteFel09r
Koritnigite ZnlO
KomeliteFel366
Kornerupine Mg5
Kostovite Au8
Kotoite Mg25
Kottigite Zn96
Kotulskite Pd20
KoutekiteCul7
Kozulite Nal74
Kraisslite Mn94
KrameriteNa51
Krausite K466
Krautite Mn39
Kreittonite Zn2
Kremersite Fe44
Krennerite Aul26
KreuzbergiteA131
KroehnkiteNallO
Krupkaite Cu80
KrutaiteCul27a
Krutovite Ni5
KryzhanovskiteFell3
KtenasiteCull96
Kulanite Ba23
Kulkeite Mg4
Kullerudite Ni356
Kunzite Li56
Kupfernickel Ni6
Kuramite Cu57
Kuranakhite Mn66
^rchatoviteCal28
k Mn55
Mg24
^nai
^nah
ahoriteCal56
it
це) Cal
Lacroixite Na3
Laffittite Ag23
Laihunite Fe86
Laitakariite Bil4
Lamprobolite Na71
Lamprophyllite Na204
Lanarkite Pb54
Landauite Na207
Landesite МпЗЗа
Langbanite Mn50
Langbeinite K66
Langisite Col
LangiteCul20r
Lansfordite Mg29e
Lanthanite Lai
Lanthanobastnasite La2
Lapis lazuli Na50
Laplandite NalO6
Larderellite B24
Larnite Cal99
Larosite Cu92
Larsenite Zn20
Laubmannite Fe80
LaueiteМпЗЗг
Laumontite Са22в
Launayite Pb72
Laurionite РЬЗЗ
Laurite Ru4
Lausenite Fel36a
Lautarite Cal 14a
Lautite Cu26
Lavendulan Na55
Lavenite Na98
Lavrovite Cal46a
Lawsonbauerite Mn93
Lawsonite СаЗО
Laxmannite CulO2
Lazarevicite Cu28a
Lazulite Mgl3
Lazurite Na50
LeadPbl
black Cla
horn РЬ27, РЬЗО
red Pb50
LeadhUlite Pb29a
Leather, mountain Mg85
Lechatelierite Si5e
LecontiteNal80
LegranditeZnll6
LeightoniteK18
Leit(h)eite Zn7
Lemoynite Na228
Lengenbachite Ag26
Leonhardite Ca226
Leonite K65a
Lepidocrocite Fe 1 07b
Lepidolite K52
Lepidomelane K61
Lesserite B21
Letovicite N7
Lettsomite Cul3
Leucite K9
Leucophaenicite Mn82a
Leucophosphite K45
Leucopyrite Fe21
Leucosphenite Na27
Levyn(it)e Ca22r
Lewisite Cal94a
Lewistonite Cal 866
Liandratite U4
Liberite Li7
Libethenite Cu74
Liddicoatite Li8
Liebenbergite Ni37
Liebigite Ca237
Lievrite Ca94
LillianitePbl9
Lime Cal82a
Limestone Ca61r
magnesian Cal32
Limonite Ре107д
Linarite CulO4
Lindackerite Cu62
Lindgrenite Cu69
Lindstromite Cu89
Linnaeite, Linneite Co8
Lintonite Na40
Lipscombite Fe766
Liskeardite A13
Litharg(it)e Pb476
Lithidionite K82
Lithiophilite Li 17a
Lithiophorite Li 16
Lithiophosphatite Li 18
Liveingite Pbl3
Liver-opal Si5M
Livingstonite Hgl3
LizarditeMg816
Loadstone Fe75
Loccaite Y3
321
I. Неорганические вещества
Loeweite Nal66
Chile K90
LollingiteFe21
LopariteNal04
Lopezite K30
Lorandite Tl 1
Lorenzenite Na214
Loseyite Mn23
LoughliniteNal69
Loweite Nal66
Lucinite А127в
Ludlamite FellOB
Ludlockite Fe23
Ludwigite Mg426
LueshiteNal83a
Luetheite Cu2
Luneburgite Mg28
LusakiteFel9
Lussatite Si5r
Lusungite Srl3
Luzonite Cu28b
MacDonaldite Bal7
Macedonite Ti8
MacfalliteCal73
Machatschkiite СаЗба
MacKayiteFel60
MackinawiteFel32
Mackintoshite Th6
Madocite Pb70
Magadiite Nal96
Maghagendorfite Nal63
Maghemite FelO5a
Magnesioaxinite Cal 18
Magnesiocapholite Mgl8
Magnesiochromite Mg36
Magnesiocopiapite Mg52
Magnesioferrite Mg46
Magnesiogedrite Mg3a
Magnesiokatophorite Na72
Magnesioriebeckite Nal62
Magnesite Mg29a
Magnetite Fe75
Magnetoplumbite Mn62
Magnioborite Mg23a
Magniophilite Mn59a
Magniotriplite Mg726
Magnocolumbite Mg68
Magnophorite Na75
Magnussonite Mn4
MajakitePdlO
Majorite Mg54
Makatite Nal95
Makinenite Ni346
Malachite Cu356
Malacon Zr3
Malanchroite РЬЗба
Malayaite Ca221
Maldonite Au7
Malladrite Si4
MallarditeMn71r
Manandonite Li 1
Manasseite Mg8a
Mandarinoite Fel48
Manganaxinite Ca 154
Manganbabingtonite Cal 59
Manganberzeliite Na76
Manganblende Mn69
Manganbrucite Mg70
Manganese
earthy Ba34
-hoernesite Mnll
-shadlunite Mn35
Manganfaialite Mn36
Manganhumite Mn826
Manganite Mn576
Mangan-neptunite K88
Manganobrucite Mn56
Manganocalcite Mn22
Manganochromite Cr6
Manganocolumbite Nb3
Manganolangbeinite K70
Manganophyllite K61
Manganosite Mn53
Manganostibiite Mn73
Manganotantalite Ta7
Manganpyrosmalite Мп84в
Manjiroite Nal75
Mansfieldite A12
Mapimite Fel66
Marble Саб 1г
Marcasite Fel346
Margarite Ca3
Margarosanite Cal89
Marialite Nal4
MariciteNal226
Marignacite Ce7
Mariposite K2
Marmatite Zn236
MarokiteCal60
Marrite Ag25
Marshite Cu65
Marsturite Na78
Marthozite U25
Mascagnite N8
Maslovite Pt4
Massicot Pb47a
Masutomilite K56
Matildite Ag5
MatlockitePb31
Matraite Zn23r
MattagamiteCol9
Matteuccite Nal36
MaucheriteNill
Mawsonite Fe72
Maxite Pb29a
Mayenite Ca8
Mazzite K20
McAllisterite Mg226
McConnellite Cr3
McGillite Mn79
McGuinnessite Mg316
McKelveyite Na25
McKinstryite Ag39e .
Meerschaum Mg83
Meionite Ca27
Meixnerite Mgl2
Melaconite Cu71
MelaniteCaiO6
Melanochroite Pb38
Melanophlogite Si5a
Melanostibite Mn75
Melanotekite Fel28
Melanovanadite Ca255
MelanteriteFel35e
Melilite Cal476
Melinophane, Meliphanite
Ca57
Melnikovite Fe81a
Meionite Ni41
Melonjosephite Ca9l
Menaccanite Til
Mendipite Pb32
Mendozite Na66
MeneghiniteCulO7
Menilite Si5n
MercalliteK51
Mercurammonite Hgo
Mercury Hgl
Merenskyite Pd21
322
I. Неорганические вещества
Merlinoite K12
JjenviniteCaHS
Mesitite Mg29a
Mesolite Na45
Messelite Ca986
Meta-aluminite A140a
Meta-alunogen A138a
jvieta-ankoleite K104
Meta-autunite Ca240a
MetaboriteHl
MetacinnabarHglOa
Metadelrioite V8a
Metahaiweeite Ca244a
Metaheinrichite Ba49a
Metakahlerite U29a
Metakichheimerite U17
Metalodevite U52
Metanovacekite Mg93a
Metarossite Ca250a
Metaschoderite A1516
Metasideronatrite Nal29a
Metastibnite Sb5a
MetatorberniteU21a
Metatyuyamunite Ca246a
Meta-uranocircite Ba50a
Meta-uranospinite Ca234a
Metavanuralite U14a
Metavariscite A1276
Metavauxite Fel46
Metavoltine K47
Metazellerite Ca236a
Metazeunerite U18a
Meyerhofferite Ca426
Meymacite Wlr
Miargyrite Ag42a
Mica
common Kla
roagnesian K60
Pearl Ca3
Potash Kla
n%FelO7B
JJichenerite Pd7
JJicle КЮв
lite Na90
i
rs
Ka
raite Fe55
i
^'"lerite Ni25
^'Hisite Na37
Mimet(es)ite Pb8
Minasragrite V9
Minguzzite Fe38
Minium Pb50
iron Fe 1056
Minnesotaite Fel54
Minyulite K4
MirabiliteNal886
Misspickel Fe30
MiBpickel Fe30
cobalt Co5b
Mitridatite CalOO
Mitscherlichite Cu42
MixiteCu31
Moctezumite U46
Mohrite Fe96
Moissanite Si 1
Moluranite U57
Molybdenite Mo46
Molybdite Mo3
Molybdomenite Pb76
Molybdophyllite Mg74
Molysite Fe40
Monazite Ce96
Moncheite Ptl4
MonetiteCall2a
Monimolite Pb586
Monite Ca62A
Monohydrocalcite Са61д
MonsmediteKlOO
Montanite Bi20
Montasite Mg86
Montbrayite Aul3
Montebrasite Li3
Monteponite Cd3
Monteregianite Na222
Montgomeryite Cal21
Monticellite Cal45
Montmorillonite Nal51
Montroseite V6
Montroydite Hg8
Mooihoekite Fe64
Mooreite Mn72
Moorhouseite Co 136
Moraesite Bell
Mordenite NalOa
Morelandite Ba8
Morenosite Ni29e
Morganite Be2
Morinite Na38
Morion Si5e
Mosandrite Na92
Moschellandsbergite Ag21
Mosesite Hg76
Mossite Nb26
MottramiteCulll
Motukoreaite Nal48
Mounanaite Fel30
Mountainite Са198в
Mourite U2
Mpororoite A1526
Mroseite Ca61e
MuiriteBal8
Mukhinite Ca249
MulliteAll
Murdochite Cu94
Murmanite Na213
Muscovite Kla
Muscoxite Mg47
NacaphiteNa81
Nacrite A1466
Nadorite Pb57
Nagyagite Au 10
NahcoliteNal31
Nakauriite Mn24
Nambulite Nal42
Nanlingite Cal26
Nantokite Cu40
Narsarsukite Na212
Nasinite B28
NasoniteCal90
Nasturane U6
NatisiteNa211
Natrambligonite Li2
Natroalunite Na7
Natroapophyllite Na86
Natrocalcite Na53e
NatrochalciteNalll
NatrojarositeNal28
NatroliteNalla
Natromontebrasite Na4
Natron Na356
Natroniobite Nal836
Natrophilite Nal76
Natrophosphate Nal35
Natrosilite Nal94
Naujakasite Nall7
Naumannite Ag47
Navajoite V56
323
I. Неорганические вещества
NealiteFell6
NeighboriteNal59
NekoiteCal98a
Nemalite Mg70
Nenadkevichite Nal84
Neotantalite Na90
Nepheline, Nephelite K75
Nephrite Cal50a
Nepouite Ni386
Neptunite K87
Nesquehonite Mg56
Nevyanskite Irl
Newberyite Mg57a
Neyite Cu87
Niccolite Ni6
Nichromite Cr7
Nickel Nil
Nickelbischofite Nil9
NickelbloediteNal85
Nickel-hexahydrite Ni29a
Nickeline Ni6
Nickel-skutterudite Ni8
Nickel-zippeite U36
Nifontovite В14
NiggliitePtl2
Nigrine, Nigrite Ti7b
Nimite Ni2
Ningyoite Ca247
Niningerite Mg75
Niobite Nb2a
NiocaliteCal80
NisbiteNi31
Nissonite Mg39
Niter K73
sodaNal81
NitratineNal81
Nitrobarite Ba37
NitrocalciteCal77
Nitroglauberite Nal82
Nitromagnesite Mg67
Nobleite Ca416
Nontronite Nal 17A
Norbergite Mg80
Nordenskjoldine Ca219
Nordite Na201
Nordstrandite А124в
Nordstromite Cu93
Norsethite ВаЗО
NorthupiteNal56
Nosean, Noselite Nal66
Noumeaite Ni38a
Novacekite Mg936
Novaculite Si5e
Nowackiite Cul45
Novakite Cul6
Nuffleldite Cu83
Nukundamite Fe56
Nyerereite Na53a
Obruchevite Y8
OcherFel07fl
antimony Sb8
bismuth Bi86,
black Ba34
brown, iron FelO7B
lead Pb47a
molibdic Mo3
nickel Nil26
red Fe 1056
tellurium Те2
tungsten W16
uranium U48
Ochre Ре107д
Ochroite Cal35A
Octahedrite Ti76
O'Danielite Na223
Offretite K80
OjuelaiteFel65
Okenite Cal986
Olgite Na202
Oligoclase Na9r
Oligonite Fe36
OliveniteCu21a
Olmsteadite K44
Olsacherite Pb78
Olshanskyite B6
Olympite Nal86
Omeiite Os2
Omphacite Cal466
Onofrite HglOa
Onoratoite Sb3
Onyx Si5x
Algerian, Mexican
Ca61r
Oosterboschite Pd8
Opal Si5h
harlequin, noble, pre-
precious Si5n
Ophite Mg816
Orangite Th26
OrceliteNilO
Ordonezite Zn25
Ore
black copper Cu7l
bog Fe 1076
bog manganese Ba34
brittle silver Ag44
brown iron Ре107д
brown lead Pb8
chrome iron Cr4a
copper pitchy Cul33
coral HglO6
cube K40
dark red silver Ag436
faded silver Fe3
grey antimony Fe68
Sb56
grey arsenic Fe48
grey manganese Mn576
hard manganese Ba34
hepatic HglO6
magnetic iron Fe75
needle Cu79a
needle iron FelO76
nodular FelO56
peacock copper Fe60
plush copper Cu72
риф1е copper Fe60
red copper Cu72
red iron FelO56
red lead РЬЗба
red silver Ag36
red zinc Znl6
siliceous zinc Zn30
spathic iron Fe36
tile Cu72
tin Sn3
titanium iron Til
velvet(y)Cul3
vitreous copper Cu72
wheel Cu 106
white lead Pb26
yellow lead Pb46
Oregonite Fe98
OrientiteCal70
Oфiment As5
Orthite Ca34a
Orthoclase К 10a
Orthoferrosilite Fel49a
Oryzite Са23в
Osarizawaite Cu9
324
I. Неорганические вещества
Osarsite
iidi
0s3
Osmiri Irl
Osmium Osl
OsumiliteK36
magnesium
Otavite Cd2
Ottemannite Sn9
OtwayiteNil7
OurayiteAg32
Overite Cal20
Owyheeite Ag36
Oxammite N2
Oxoniumjarosite Fe92
Pabstite Ba41
PachnoliteA118a
Paigeite Fe736
Painite Ca270
Palermoite Li 19
Palladium Pd la
Palladoarsenide Pd2
Palladobismutharsenide
Pd6
Palladseite Pdl7
Palmierite K95
Palygorskite Mg85
Panabase Fe68
Pandaite Ba38
Pandermite Ca44a
Pane, moscovian window
Kla
PaolovitePdl8
Papagoite Ca73
Paradocrasite SblA
Paragonite Nala
Paramelaconite Cu48
Paramontroseite V3
paravauxiteFel4r
pargasite Na64
Parisite Ca65
ParkeriteNil4
Parnauite Cu25
ParsettensiteK71
nsite U41
eite Са20в
lite Mn86
coiteCa253
e B30
9
troniteVl0
Paulingite Kl 1
Paulmooreite Pb6
Pavonite Ag6
PaxiteCul5
Pearceite Ag46
Pearlite Si5n
Peastone Саб 16
Pecoraite №38в
Pectolite Na87
Peganite А127в
Pekoite Cu82
Pellyite Bal5
Penfieldite Pb34
Penikisite Ba28
PenkvilksiteNa210
Pennantite Mn2a
Penroseite Ni35a
Pentagonite Ca25,4
Pentahydrite Mg76e
PentahydroboriteB13
PentlanditeFelO3
Percylite Cu97
Peretaite Cal96
PerhamiteCal82B
Periclase Mg69
Peridot Mg79
Perite Pbl6
Perloffite Ba32
PermingeatiteCul25
Perovskite Ca228
Perrotite T18
Petalite Li6
Petarasite Na229
Petrovicite Cu64
Petscheckite U3
Petzite Au6
Pharmacolite СаЮ9в
Pharmacosiderite K40
Phenacite, Phenakite Be 13
Phillipsite K79
Phlogopite K60
Phaenicochroite Pb38
Phosgenite Pb27
Phosinaite Na62
Phosphammite N6
Phosphochalcite Cu76
PhosphoferriteFell06
Phosphophyllite Fel68
Phosphorroesslerite Mg576
Phosphosiderite FelO96
Phosphuranylite Ca241
Phurcalite Ca242
Pickeringite Mgl6
Picotite MglOa
Picotpaulite Fe8
Picrochromite Mg36
Picroilmenite Mg91
PicroliteMg81a
Picromerite K656
Picropharmacolite Cal41
Piedmontite Cal74
Pigeonite Mg78a
Pimelite Ni396
Pinakiolite Mg59
Pinchite Hg3
PinnoiteMg21
Pirssonite Na536
PisaniteFel35e
Pisolite Ca616
Pistacite Ca346
Pitchblende U6
Plagionite Pb64a
Plancheite Cul34
Plasma Si5*:
Platarsite Pt2a
Platiniridium Irl
Platinum Ptl
Plattnerite Pb48
Platynite Pb22
Playfairite Pb69
Pleonaste Mg41
Pleonectite Ca37
Plumbago С la
Plumbobetafite Na208
PlumboferriteFel22
Plumbogummite A135
Plumbojarosite Fe 126
Plumbomicrolite Ta8
Plumbopalladinite Pdl3
Plumbopyrochlore Nb5
PoitviniteCull66
Polarite Pdl6
Polhemusite Zn23e
Polianite Mn546
Polkovicite Fe90
Pollucite, Pollux Cs2
Polybasite Ag466
PolycraseY156
PolydymiteNi216
Polyhalite K21
325
I. Неорганические вещества
Polylithionite K53
PoonahliteCa21a
Portlandite Cal83
Posnjakite Cul206
Potarite Pd9
Poubaite Pb23
PoughiteFel6l
Powellite Cal75
Prase Si5x
Prasopal Si5h
Prehnite Ca4
Preiswerkite Nal44
Preobrazhenskite B23
Priceite Ca44a
Priderite K99
PrioriteY15a
Prismatine Mg5
ProbertiteNa51
ProsopiteA112
Prosperite Ca263
ProuditeCu91
Proustite Ag36
Przhevalskite U426
Pseudoboleite Cu99
Pseudobrookite Ti3
Pseudolaueite МпЗЗв
Pseudomalachite Cu76
Psilomelane Ba34
Ptilolite NalOa
Pucherite Bi266
PumpellyiteCal22
Purpurite Mn58
Pyrargyrite Ag436
Pyrite Fel34a
Pyrites
capillary Ni25
cobalt C08
cockcomb Fel346
copper Fe57
iron Fe 134a
liver Fe 1346
magnetic Fe 131
manganese Mn70
nickel FelO3
peacock copper Fe60
radiated Fe 1346
red nickel Ni6
silver Fe46
silvery Fe4a
spear Fel346
tin Fe70
white iron Fel346
white nickel Ni7a
yellow nickel Ni25
Pyroaurite Mg446
Pyrobelonite Mn68
Pyrochlore Na79
Pyrochroite Mn56
Pyrolusite Mn546
Pyromorphite РЬ49
Pyrope Mgl7
Pyrophanite Ti5
Pyrophyllite A145
Pyrosmalite Fel56
Pyrostilpnite Ag43a
Pyroxferroite Fel496
Pyroxmangite Мп77в
Pyrrhite Na79
Pyrrhoarsenite Na70
Pyrrhotine, Pyrrhotite
Fel31
Quartz Si5e
aventurine, rose, sap-
sapphire, smoky Si5e
Queitite Zn21
Quenselite Mn63
Quenstedtite Fel36r
Quetzalcoatlite Си 149
Quicklime Ca 182a
Quicksilver, horn Hg2
Rabbittite Cal53
RaguiniteFel62
RajiteCul38
Ramdohrite Ag356
Rameauite K27
Rammelsbergite Ni76
Ramsdellite Mn54a
Rancieite Cal61
Rankinite Ca200a
Ranquilite Ca2446
Ransonite Fe65
Ranunculite U9
Rasorite Nal8a
Raspite Pb89a
Rasvumite K41
Rathite T15
Rauchquarz Si5e
Rauenthalite СаЗбб
RauwolfiteCul20B
Realgar As8
Reddingite Mn596
Redingtonite Cr5
RedruthiteCull5
Reedmergnerite Na2l
ReevesiteFelOO
Reichardtite Mg76ji
Reinerite Zn8
Renardite U44
Renierite Fe586
RetgersiteNil296
Retzian Y6
Reyerite Na49
Rezbanyaite Cu86
Rhabdophan(it)e Ce9a
Rhagite Bi4
Rhenium Re 1
Rhodesite Na84
Rhodium Rhl
RhodiziteCsl
Rhodochrosite Mn22
Rhodonite Mn77r
Rhodostannite Fe71
Rhodusite Nal62
Rhomboclase Fe91
RhoniteCal51
Richellite CalOl
Richterite Na75
Rickardite Cu59
RiebeckiteNal20
Rijkeboerite Ba42
Rink(ol)ite Na92
Rinneite Fe41
RivadaviteNal54
RiversideiteCa2l6
Robertsite Cal63
Robinsonite Pb66
Rock, dolomite Cal32
Rockbridgeite Fe77
Rodalquilarite Fe93
RoeblingiteCal92
Roepperite Mn78
Roesslerite Mg556
Roggianite Na42
Rokuhnite Fe39
Romanechite ВаЗб
Romarchite Sn2
RomeiteCal946
Romerite Fe82a
326
I. Неорганические вещества
RontgeniteCa66
ltiteBi2
Roosevelt
RoquesiteCu68
RosasiteCul46
RoscheriteCa51
Roscoelite K108
Roselite Ca69a
RosemaryiteNal73
Rosenbuschite NalOO
Rosenhahnite Ca201
RosickyiteSla
Rossite Ca2506
RoBlerite Mg556
RostiteA1396
Roubaultite U20
Routhierite Hgl66
RoweiteB19
Rowlandite Yl 1
Rozenite Fel356
RubelliteNal38
RubyA123a
RucklidgeiteBil8
RuiziteCal68
RusselliteWla
Rustenburgite Ptl3
RustumiteCa213
Ruthenarsenite Ru2
Rutheniridosmine, Ruthe-
niridosmium Osl
Ruthenium Rul
Ruthenosmiridium Irl
Rutherfordine, Ruther-
fordite U 16a
Rutile П7в
Rynersonite Ca222
SaamiteSrl56
Sabinaite Na232
SabugaliteUlOa
Safflorite Co2
Sahamalite Mg33
Sahlinite Pb9
^infelditeCallOa
^hi
^aiteCal31
**harovaitePbl76
SakiiteMg76r
^a ammoniac N3
^aeitM
rs«eCu67
SallteCal46a
Salt
bitter, English, Epsom
Мё76д
Glauber's Na 1886
rock Na 107a
Saltpeter
baryta Ba37
Chile, cubic Nal81
Indian K73
lime Ca 177
magnesia Mg67
Norwegian Cal77
potash K73
Samarskite Y15b
Samiresite Na79
Sampleite Na56
Samsonite Mnl
Sanbornite Ba40
Sand Si5e
Sanidine K106
Sanjuanite A132
SanmartmiteZn31
Santaclaraite Cal69
Santafeite Srl4
SantanaiteCrlO
SantiteK13
Sapphire A123a
Sapphirine Si5x
Sarabauite Cal95
Sarcopside FellOa
Sard(onyx) Si5>K
Sarkinite Mnl4a
Sarmientite Fe28a
Sartorite PblO
Sassoline, Sassolite B3
Satimolite K74
Satterlyite Mg48
Sazhinite Nal03
Sborgite B27
Scacchite Mn25
Scarbroite A17
Scawtite Ca205
Schachnerite Ag22
Scafarzikite Fel41
SchaireriteNal91
Schaurteite Cal08
Scheelite Ca260
Schertelite Mg63
Schirmerite Ag29
Schizolite Na87
Schmitterite U50
Schneebergite Cal946
Schneiderhohnite Fe25
SchoderiteA151a
Schoenfliesite Sn4
Schoenite K656
Schoepite U37
Scholzite Ca266
Schonite K656
Schoonerite Mn30
Schorl Na 114
Schorlomite CalO6
SchreyeriteTill
Schroeckingerite Na94
SchubneliteFel63a
Schuetteite Hgl2
Schuilingite Ca76
Schultenite Pb42
Schwartzembergite Pb45
Schwazite Fe68
ScoleciteCa21a
Scorodite Fe22a
Scorzalite Fel4a
Scovillite Ce9a
Seamanite B8
Searlesite Na22
Sederholmite Ni34a
Sedovite Ul
Seeligerite Pb44
SegeleriteCal38
Seidozerite Na230
Seinajokite Fel40
Sekaninaite Fe8
Selenite Са193в
Selenium Sel
SelenjoseiteBil4
Selenobismuthinite Bil3
Selenolite Se2
Seligmannite Cu78
Sellaite Mg40
Semseyite Pb67
Senarmontite Sb4a
Senegalite A1286
Sengierite U27
Sepiolite Mg83
SeranditeNal77
SergeeviteCal34
Sericite Kla
Serpierite Ca776
SeybertiteCall5
327
I. Неорганические вещества
Seyrigite Ca260
Shadlunite Fel25
Shandite Ni24
ShattuckiteCul35
Shcherbinaite V5a
Sherwoodite Ca258
Shortite Na54
Siberite Nal38
SiberskiteCalll
Sicklerite Li 176
Siderazot(e), Siderazotite
Fe95
Siderite, Siderodote Fe36
Sideronatrite Nal296
Siderophyllite K35
Sideroplesite Fe36
SiderotilFel35r
SidorenkiteNal72
SiegeniteNi21a
Sigloite Fel2
Silhydrite Si53
Sillenite Bi8a
Sillimanite A1446
Silver Agl
horn Ag 11
ruby Ag436
tellurium Ag51
Simonyite Nal64
SimplotiteCa251
Simpsonite Tal
Sincosite Ca256
Sinhalite Mg6
Sinnerite Cu29
Sinter
calcareous Саб 1 г
opal, pearl, siliceous Si5n
Siserskite Osl
Sitaparite Mn55
Sjogrenite Mg44a
Skinnerite Cul23
Sk-rodowskite Mg97
Skutterudite Co3
Slavyanskite Na36
Slawsonite Sr7
Smaltite Co3
Smithite Ag2a
SmithsoniteZnl3
Smolianinovite Ca88
SmythiteFe816
Soapstone Mg826
Sobolevskite Pd4
Soda, native Na356
SodaliteNal3
Soddyite U49
Sogdianite K58
SohngeiteGal
Solongoite B20
Sonolite Mn85
Sonoraite Fel59
Sorbyite Pb71
S0rensenite Nal98
Soucekite Cu796
Souzalite Mgl4
Spangolite Cull
Spar
alum K7
azure Mgl3
baryta Ba39
bitter Ca 132
blue Mg 13
brown Ca90
cadmium Cd2
calc Ca61r
carmine Fell9
cobalt Co6
copper Cu356
crimson Mn22
cube Cal93a
Greenland All6
gypsum Са193в
heavy Ba39
ice K106
Iceland Ca61r
iron Fe36
lead Pb26
manganese Mn22
oligon Fe36
pearl Ca 132
Persian Ba39
poison Fe30
red lead РЬЗба
satin Са193в
tabular Ca 197
talc Mg29a
yttrium Y9
zinc Znl3
SpeculariteFelO56
Spencerite Znl86
Sperrylite Pt26
Spessartine, Spessartite Mn7
Sphalerite Zn236
SpheneCa231
Spherocobaltite Co6
Spinel MglOa
chrome Cr4a, MglOa
iron Fe 11
precious MglOa
zinc Zn2
Spionkopite Cu53
Spiroffite Mn87
Spodumene Li56
Spurrite Ca204
StainieriteColO
Stannite Fe70
Stannoidite Fe50
Stannomicrolite Та 12
Starkeyite Mg766
Starlite Zr3
Staurolite Fel9
Steatite Mg826
Steenstrupine NalO2
Steigerite A149
Stellerite Ca246
StenhuggariteCalO3
Stenonite Sr2
Stepanovite Nal61
Stephanite Ag44
StercoriteNal79
Sternbergite Fe46
Sterryite Pb68
Stevensite Mg82a
Stewartite МпЗЗд
Stibiobetafite Ca230
Stibiocolumbite Nb6
Stibioconite Sb9
Stibiopalladinite Pdl5
Stibiotantalite Ta9
Stibivanite VI1
Stibnite Sb56
Stichtite Mg356
StilbiteNa41
Stilleite Zn26
Stillwaterite Pb3
Stishovite 515д
Stistaite Sn8
Stoiberite VI
Stokesite Ca220
Stolzite Pb896
Stone
Amazon К 10b
azure Na50
328
I. Неорганические вещества
golognian Ba39
cinnamon Ca26
cross Fe 19
jceA116
radiated Ca 150a
StottiteGel
StrahliteCal50a
StrariskiiteCul44
StrashimiriteCu216
Stratlingite Cal826
StrelkiniteNa219
StrengiteFelO96
Stringhamite Ca78
StromeyeriteAgl7
Strontianite Sri2
Strontioapatite Sri56
Strontioarsenapatite Sr9
Strontioborite B35
Strontiodresserite Sr3
Strontioginorite SrlO
Strontiohilgardite Sri 1
Strunzite МпЗЗб
Struverite Ti7b
Struvite Mg656
StumpflitePtlO
Stutzite Fe2
Suanite Mg23a
Sudburyite Pb55
Sugilite K86
SukulaiteTall
Sulfoborite B34
SulfohaliteNal89
Sulfur S16
ruby As8
SulvaniteCul43
Sundiusite Pb53
Sundtite Ag35a
Sundvikite Ca20a
SuoluniteCa210
Sunstone Na9a
Surinamite A147
Susannite Pb296
Sussexite B32
Svabite Ca38
jvanbergite Sr6
3 Ca25
^ziteCal52
JedenborgiteNa32
rU2i Мп59в
Sylv(in)ite K28
Symplesite Fe24
Synadelphite Mnl2
Synchisite Ca64
Syngenite K22
SzajbelyiteB31
Szmikite Mn71a
Szomolnokite Fe 135a
Taaffeite MglO6
Tacharanite СаЗЗ
TachyhydriteCal36
Tadzhikite Ca67
Taeniolite K55
Takanelite Mn45
Takovite Ni3
Talc Mg826
TalmessiteCal24
Tamanite Ca98a
Tamarugite Na6a
Tanatarite A126a
TancoiteNal39
Tangeite Ca82
Tantalite Ta5a
Tanteuxenite Y16
Tanzanite Са34в
Tapiolite Ta56
Taramite Na59
Taranakite K5
Tarapacaite K29
TarbuttiteZnl8a
Tarnowitzite, Tarnowskite
Саб 16
Tatarskite Cal35
Tautolite Ca34a
Tavorite Li 14
Tawmawite Ca346
Taylorite K72
Tazheranite Zrla
Teallite Pb80
TeineiteCul37B
Tellurantimony SblO
Tellurite Te2
Tellurium Те 1
black Au 10
Tellurobismuthinite Bil7
Telluropalladinite Pd23
Temiskamite Ni 11
Tennantite Fe48
TenoriteCu71
Tephroite Mn78
Terlinguaite Hg5
Ternovskite Nal62
Terruggite B9
Tertschite Ca446
Teschemacherite N4
Testibiopalladite Pdl6
TetradymiteBi21
Tetraferroplatinum Pt5
Tetrahedrite Fe68
Tetrakalsilite К8в
TetranatroliteNall6
Tetrawickmanite Sn56
Texasite Prl
Thadeuite Cal44
Thalenite Y10
Thaumasite Si6
ThenarditeNal88a
Thermonatrite Na35a
Thomaite Fe36
ThomsenoliteA1186
Thomsonite Na40
Thorbastnasite Ca224
ThoreauliteTalO
ThorianiteThl
Thorite Th26
Thorogummite Th6
Thortveitite Sc2
Thorutite Th3
Threadgoldite U12
Thulite Са34в
Thuringite Fe72A
Tianshanite Na28
Tiemannite Hgl4
TigereyeNal20
Tikhonenkovite A121
TilasiteCal25
Tilleyite Ca203
Tin
grey Sn la
white Sn 16
TinaksiteK81
TincalNal8B
Tincalconite Nal86
Tinstone Sn3
Tintinaite Pb646
Tinzenite Саб
Tiragalloite Mn76
Tirodite Mg61
TitaniteCa231
329
I. Неорганические вещества
TlalociteCul50
Tlapallite Ca81
Tobermorite Ca 182r
Tochilinite Mg50
Tomichite TilO
Topaz A148
occidental Si5e
oriental A123a
Spanish Si5e
Topazolite CalO6
Torbernite U216
Tornebohmite CelO
Torreyite Mg98
Traskite Ba45
Travertine Ca61r
Treasurite Ag31
Trechmannite Ag26
Tremolite Cal506
TrevoriteFelOl
Tridymite Si5B
Trigonite Mn60
Trikalsilite K8r
Trimerite Ca52
Triphane Li56
TriphyliteLil2
Triplite Mn32a
Triploidite Mn326
TrippkeiteCul9
Tripuhyite Fel42
Troegerite, Trogerite U15
Trogtalite Co 16a
TroiliteFel33
Trolleite A130
TronaNal32
TruscottiteCa212
Triistedtite Ni226
TscheffkiniteCel2
Tschermakite Cal 16
Tschermigite A122
Tsumcorite Fel69
Tsumebite CulO3
Tsumoite Bil6
Tucekite Ni33
TucholiteNall8
Tugarinovite Mo2
Tugtupite Na30
TuhualiteNall8
Tulameenite Pt7
Tundrite NalO5
Tungstenite W3
TungstiteW16
Tunisite Na36
Tunnelite B36
Tur(g)ite FelO56
Turquoise Cu7
Twinnite Pb596
TychiteNal58
TyretskiteB16
Tyrite Y76
Tyrolite Ca75
Tyrrellite Cu55
Tysonite Ce5
Tyuyamunite Ca2466
Uklonskovite Nal68
Ulexite B33
Ullmannite Ni32
Ulrichite U6
Ultrabasite Ag38
Ultramarine Na50
Ulvite, Ulvospinel Ti2
Umangite Cu54
Umbozeritre Na203
Umohoite U33
Ungemachite K84
UpaliteU13
Uralborite Са40в
Uralolite Ca56
Uramphite U35
Uraninite U6
Uranmicrolite U55
Uranochalcite U26
Uranocircite Ba506
Uranolepidite U19
Uranophane Ca245
Uranopilite U48
Uranospathite U106
Uranosphaerite Bi25
Uranospinite Ca2346
sodium Na215
Uranotantalite Y15b
Uranothallite Ca237
Uranothorite Th5
Uranotile Ca245
Uranpyrochlore U5
Uranthorianite Th4
Urdite Ce96
Urea C3
Ureyite NalO8
Urvantsevite Pd5a
UsoviteAlll
Ussingite Nal5
Utahite K48
Utahlite А127в
Uvarovite Ca72
UviteCall7
Uytenbogaardtite Au3
Uzbekite Cul42
Vaesite Ni26a
Valentinite Sb46
Valleriite Fe63
Vanadinite Pb88a
Vandenbrandeite U19
Vandendriesscheite Pb85
Van'thoffiteNal65
Vanuralite U146
Variscite А127в
Vaterite Саб la
VauqueliniteCulO2
Vauxite Fel4e
Vayrynenite Be7
Veatchite B37
VeenitePb61
VerdeliteNal38
Vermiculite Mg82e
Versiliaite Fe85
Vesignieite Ba21
VesuvianiteCal23
Veszelyite Cu756
Vikingite Ag30
VillamaniniteCull3
Villaumite Nal 12
Vimsite Ca406
Violan Cal46a
ViolariteFel02
Virgilite Li5a
Viridine A144a
Vitriol
blueCull6r
cobalt Co 13b
copper Cull6r
green Fel35e
lead Pb52
manganese Mn71r
nickel Ni29B
red Co 13b
uranium U23
white, zinc Zn24fl
VivianiteFellOr
330
I. Неорганические вещества
Viadiminte CallO6
Vlasovite Na225
VogliteCa238
VoelckeriteCal886
\blborthite Cul42
VolckeriteCal886
Volkovskite Ca41a
Voltaite K43
Volynskite Ag8
Vonsenite Fe736
Vorobyevite Be2
Vrbaite Hgl7
Vuagnatite Ca28
Vulcanite Cu 136
Vysotskite Pdl4
Wad Ba34
WadeiteKlll
Wagnerite Mg72a
Wairakite Ca22a
Wairauite Fe45
WakefieldliteY17
WallisiteCullO
Walstromite Bal6
Wardite Na56
WardsmithiteCal30
Warikahnite Zn9a
Warlamoffite Sn3
Warthite Nal64
Water-opal Si5n
Watersapphire Mgl
Wattevillite Na826
Wavellite A129a
Waylandite A16
WeberiteA114
^bnerite Ag35a
Weddellite Ca626
Weeksite K106
^ehrlite Bi24
weibullite Pb24
^iHte CalO9a
WeiBbergite T17
^issite Cu58
finite Mn51
rryite Cu95
Whewellite Ca62a
WhiteiteCal37
WhitlockiteCal84
Whitmoreite Fe76B
WickenburgiteCal7
Wickmanite Sn5a
Wightmanite Mg27
WilkeiteCa216A
Wilkmanite Ni22a
Willemite Zn27
Willemsite Ni39a
WillyamiteCoHa
Wmchite Na68
Winstanleyite Ti9
Wiserite Mn20
WitheriteBall
Wittichenite Cu33
WittitePb516
Wodginite Ta6
Woehlerite, Wohlerite
NalOOA
WolfeiteFell2
Wolframite Fe 164a
WolfsbergiteCul22
WollastoniteCal97
Wolsendorfite Pb84
Woodhouseite Cal6
Woodruffite Mn92
Wulfenite Pb46
Wurtzite Zn23a
Wustite FelO4
Wyartite Ca248
WyllieiteNall5a
XanthiositeNil2a
XanthiteCal23
Xanthoconite Ag3a
XanthophylliteCall5
Xanthosiderite FelO76
Xanthoxenite Ca99
Xenotime Y9
Xiangjiangite U31
Xocomecatlite Cul39
Xonotlite Ca202
Yaroslavite A125
Yarrowite Cu50
Yavapaiite K46a
Yenite Ca94
YofortieriteMn81
YtterbiteBel6
Yttrobastnasite Y4
Yttrobetafite Ca262
Yttrocerite Ca83
Yttrocolumbite Y7a
Yttrocrasite Th7
YttroeschyniteY15a
Yttrofluorite Ca83
Yttromicrolite Y14
Yttropyrochlore Y8
YttrotantaliteY13a
Yugawaralite Ca23a
Zairite Fe33
Zapatalite Cu8
ZaratiteNil8
Zavaritskite Bi9
Zektzerite Nal43
Zellerite Ca2366
Zemannite Na224
ZeophylliteCa214
Zeunerite U186
Zhemchuzhnikovite Nal47
ZiesiteCul41
Zinc Znl
Zincaluminite Zn6
Zincite Znl 6
Zincmelanterite Zn24r
Zincobotryogen Fel70
Zincocopiapite Fel71
ZincrosasiteZnH
Zincsillte Zn29
Zinc-zippeite U53
Zinkenite Pb60
Zinnwaldite K54
ZippeiteK105
magnesium Mg96
sodium Na218
Zircon Zr3
Zirconolite Ca275
Zircosulfate Zr2
Zirkelite Ca275
Zirsinalite Na99
Zoisite Са34в
Zorite Na206
Zunyite A143
Zussmanite K39
Zvyagintsevite Pdl2
Zwieselite Felll
Zykaite Fe29
331
I. Неорганические вещества
Указатель рудных минералов
Ag
А1
As
Аи
Ва
Be
Bi
С
Са
Се
Со
Сг
Cs
С
Fe
Hg
Ir
К
La
36, 9-11, 24, 39а, 396, 41,
42а, 426, 436, 44, 466, 51
16, 23в, 24а, 246, 26а, 266
1,5,8
1,5,6,10,12а, 126
11,34,39
2, 15, 16
1,11
1а
42а, 42в, 47, 48, 50, 61г, 65,
83, 90, 132, 175, 185, 1866,
1886, 193а, 193в, 228, 231,
2406, 243, 245, 260
3, 7, 96
2, 3, 5а, 5в, 8
6а
2
1, 13,21,22,286,33,356,36,
45а, 456, 52, 71, 72, 78, 79а,
106, 107, 112, 115, 116г, 119,
131, 133, 147
1, 3,9,21,30,36,46,48,57,
58а, 60, 68, 70, 72А, 75, 103,
1056, 1076, 107в, 107д, 1096,
ПОг, 124, 127, 131, 134а,
1346, 164а, 1646, 167
1, 106
1
7,9,28,37,52,54,61,63,67,
69, 73, 75, 107, 108
2
Указатель драгоценных,
Li
Mg
Mn
Mo
Na
Nb
Ni
Os
Pb
s
Sb
Sri
Sr
Та
Th
Ti
U
V
w
Y
Zn
Zr
2,3,5,6,17a
24, 26, 29a, 346, 36, 68, 76a
76д, 826
3, 21, 22, 28, 42, 46, 53-55
576, 69, 70, 78, 84r, 88, 90 '
46
18a, 18b, 35, 79, 82a, 90, 93
104, 107a, 132, 151, 188a
1886, 205, 208, 220
2a, 3
6, 7a, 76, 126, 13, 216, 25
26a, 266, 32, 38a
1
8, 17a, 26, 29a, 296, 46, 47a,
476, 48, 49, 51a, 52, 63, 86
88a
16
4a, 46, 56, 6, 8, 9
12, 16
4, 5a, 56, 6-8, 12
26
1, 5, 7a, 76, 7b
5, 6, 21a, 216, 23, 45
6, 10
16, 1д
76, 8, 9, 136
lla, 13, 15, 16, 22, 23a, 236,
30
16,3
полудрагоценных и поделочных камней
А1
Ва
Be
С
Са
Cs
Си
Fe
23а, 27в, 44а, 44в, 48
46
1-3, 13
16
1,4,26, 346, 34в, 47, 48, 616,
61г, 106, 123, 132, 146а,
150а, 154,231
1
7, 356, 36
17,19
К
Li
Mg
Mn
Na
Si
Ti
Zn
Zr
10a, 10b, 25
2,56
1, 5, 10a, 13, 17, 53, 79, 810,
826, 83
7, 55, 77r
8a, 9a, 40, 50, 120, 138
5e, 5ж, 5и
7в
236, 27
3 ^^
332
II
Химические
элементы. Атомы
1. Названия и символы элементов.
Порядковые номера. Степени окисления
Приведены названия химических элементов, их символы и поряд-
порядковые номера (Z) в Периодической системе, а также степени окисле-
окисления элементов в простых и сложных веществах.
Произношение символов элементов совпадает, как правило, с их
названиями. Исключения указаны верхним индексом (*) и даны в
примечании к таблице.
Представлены характерные (типичные) степени окисления, распо-
расположенные по порядку следования целых рациональных чисел. Про-
Прочерк означает отсутствие данных.
Название, символ
Степени окисления
Азот N*
Актиний Ас
Алюминий А1
Америций Am
Аргон Аг
Астат At
Барий Ва
Бериллий Be
Берютий Вк
Бор В
Борий Bh
Бром Вг
Ванадий V
висмут Bi
Водород Н*
Вольфрам W
^олиний Gd
Га^лий Ga
ГаФний Hf
7
89
13
95
18
85
56
4
97
5
107
35
23
83
1
74
64
31
72
-III, 0, +1, II, III, IV, V
о, +ш
о, +ш
0, +11, III, IV
о
О, +11
0, +11
0, +Ш, IV
-III, 0, +III
-I, 0, +1, V, VII
0, +11, III, IV, V
0, +III,V
-i, о, +i
0, +IV, VI
0,+Ш
о, +ш
0,+IV
333
II. Химические элементы. Атомы
Продолжение табЛ
Название, символ
Гелий Не
Германий Ge
Гольмий Но
Диспрозий Dy
Дубний Db
Европий Ей
Железо Fe*
Золото Аи*
Индий In
Иод1
Иридий 1г
Иттербий Yb
Иттрий Y
Кадмий Cd
Калий К
Калифорний Cf
Кальций Са
Кислород О*
Кобальт Со
Кремний Si*
Криптон Кг
Ксенон Хе
Кюрий Cm
Лантан La
Литий Li
Лоуренсий Lr
Лютеций Lu
Магний Mg
Марганец Мп
Медь Си*
Мейтнерий Mt
Менделевий Md
Молибден Мо
Мышьяк As*
Натрий Na
Неодим Nd
Неон Ne
Нептуний Np
Никель Ni
Z
2
32
67
66
105
63
26
79
49
53
77
70
39
48
19
98
20
8
27
14
36
54
96
57
3
103
71
12
25
29
109
101
42
33
11
60
10
93
28
Степени окисления
0
0, +11, IV
0, +III
0, +III
0,+V
0, +11, III
0,+11, III, VI
0, +1, III
0, +III
-I, 0, +1, V, VII
0, +III, IV
0, +11, III
0, +III
0,+11
0,+1
0, -Ы11, IV
0,+11
-II, I, 0, +11
0, +11, HI
-IV, 0, +11, IV
0,+11
0, +11, IV, VI, VIII
0, -Ы11, IV
0, +III
0,+I
0, +III
0, +III
0, +11
0, +11, IV, VI, VII
0, +1, II
—
0, +11, III
0, +IV, VI
-111,0,+III,V
0,+I
0, +III
0
0, -bill, IV, VI, VII
0, +11, III
334
II. Химические элементы. Атомы
Продолжение табл.
Название, символ
Ниобий Nb
Нобелий No
Олово Sn*
Осмий Os
Палладий Pd
Платина Pt
Плутоний Ри
Полоний Ро
Празеодим Рг
Прометий Рт
Протактиний Ра
Радий Ra
Радон Rn
Резерфордий Rf
Рений Re
Родий Rh
Ртуть Hg*
Рубидий Rb
Рутений Ru
Самарий Sm
Свинец РЬ*
Селен Se
Сера S*
Серебро Ag*
Сиборгий Sg
Скандий Sc
Стронций Sr
Сурьма Sb*
Таллий Т1
Тантал Та
Теллур Те
"Тербий ТЬ
Технеций Тс
Титан Ti
т°рий Th
тУлийТщ
углерод С*
уРани
ФеРмий Fm
41
102
50
76
46
78
94
84
59
61
91
88
86
104
75
45
80
37
44
62
82
34
16
47
106
21
38
51
81
73
52
65
43
22
90
69
6
92
100
Степени окисления
0, +IV, V
0, +11, III
0, +11, IV
0, +IV, VI, VIII
0, +11, IV
0, +11, IV
0, +III, IV, V, VI
0, +11, IV
0, +III, IV
о, +ш
0, +IV, V
0,+11
0, +11, IV, VI, VIII
О,+IV
О, +IV, VII
О, +III, IV
о, +i, и
0,+1
О, +11, IV, VI, VIII
О, +11, III
О, +11, IV
-II, О, +IV, VI
-II, О, +IV, VI
О,+1
О, +III
О,+11
О, +III, V
О, +1, III
О, +IV, V
-И, О, +IV, VI
О, +III, IV
О, +IV, VII
О, +11, III, IV
О,+IV
о, +ш
-IV, I, 0, +11, IV
О, +III, IV, VI
О, +11, III
335
II. Химические элементы. Атомы
Окончание табд
Название, символ
Фосфор Р*
Франций Fr
OropF
Хассий Hs
ХлорС1
Хром Сг
Цезий Cs
Церий Се
Цинк Zn
Цирконий Zr
Эйнштейний Es
Эрбий Ег
Z
15
87
9
108
17
24
55
58
30
40
99
68
Степени окисления
-ш, о, +i, in, v ^Т
0,+1
-1,0
—
-I, 0, +1, III, IV, V, VI, VII
0,+11, III, VI
0,+1
0, +III, IV
0,+11
0,+IV
0, +11, III
0, +III
* Произношение символов некоторых элементов:
Ag — аргентум N — эн
As — арсеникум О — о
Аи — аурум Р — пэ
С — цэ РЬ — плюмбум
Си — купрум S — эс
Fe — феррум Sb — стибиум
Н — аш Si — силициум
Hg — гидраргирум Sn — станнум
2. Относительные атомные массы.
Электронные формулы. Радиусы
Элементы приведены в алфавитном порядке их символов, в левом
нижнем индексе у символов — порядковые номера элементов в Пери-
Периодической системе. Элементы 110—112, 114 и 116, не имеющие пока
названий и символов, представлены в конце таблицы.
Значения относительной атомной массы АТ даны по Международ-
Международной таблице 1997 г. с указанием точности одной-двух значащих цифр
и отвечают природному изотопному составу элементов. Верхним ин-
индексом (*) обозначены радиоактивные элементы, не имеющие ста-
стабильных изотопов. Для этих элементов значения Ат относятся к наи-
наиболее долгоживущим изотопам.
Для элементов 110—112, 114 и 116 вместо значений Ат указаны мас-
массовые числа наиболее долгоживущих изотопов.
336
II. Химические элементы. Атомы
Представленные электронные формулы согласуются с экспери-
экспериментальными данными, в них выделены валентные электроны (нахо-
(находятся вне квадратных скобок). Электронные формулы атомов элемен-
элементов 2-го и последующих периодов сокращены за счет указания симво-
символа предшествующего благородного газа (элемента VIIIA-группы); на-
например, запись формулы атома Ga = [18Аг, Зд?10]^^1 следует читать
1522522/?63523/763^104524/71. В некоторых случаях указано по две равно-
равнозначно возможные электронные формулы (экспериментально под-
подтвержденный выбор отсутствует).
Приведены также атомные, ковалентные и ионные радиусы (гат,
r 9 гион). Прочерк означает отсутствие данных.
Эле-
Элемент
89Ас
47Ag
13AI
18Ar
33As
8;At
79Au
5B
56Ba
4Be
107 Bh
83Bi
97 Bk
з5Вг
6^
2<?a
•
Ar, a. e. м.
227,027750 ± 3
107,8682 ± 2
26,981539 ±5
243,061375 ± 3
39,948 ± 1
74,92159 ± 2
209,98713 ± 1
196,96654 ± 3
10,811 ±5
137,327 ± 7
9,012182 ±3
[267]
208,98037 ± 3
247,070300 ± 6
79,904 ± 1
12,011 ±1
40,078 ± 4
1—-—
Электронная формула
[S6Rn]6dl7s2
[36Kr]4dl05sl
[10Ne]3523/?1
[86Rn]5/77*2
[10Ne]3*23/>6
[18Ar, 3dl0]4s24p3
[54Xe,4fl\5dl0]6s26p5
[54Xe, 4fH]5dl06sl
[2He]2s22pl
[54Xe]6s2
[2He]2s2
—
[54Xe,4/14,5rf10]6s26/>3
[ Rn]5/8-96rf'-°752
[18Ar, 3rfl0]4s24/>5
[2He]2s22p2
[18Ar]452
r
ат
188
145
143
184
174
125
144
98
217
113
—
155
92
197
Радиус, пм
г
ков
171
134
125
97
121
134
88
198
89
—
152
114
77
174
г
ион
Ас3+118
Ag+113
А13+57
Ат2+ 135
Ат4+92
_
As3" 208
As5+46
АГ227
At5+ 57
Au+ 137
Au3+ 91
B3+23
Ba2+ 143
Be2+ 34
—
Bi3+ 96
Bi5+ 74
Bk3+ 98
Bk4+ 87
Br- 196
Br7+ 53
С4" 260
C4+30
Ca2+ 106
337
II. Химические элементы. Атомы
Продолжение табд
Эле-
Элемент
48Cd
58Се
98 Cf
17С1
96 Cm
27Со
24Cr
55Cs
29Cu
!05Db
66Dy
68Er
63EU
9F
Fe
26
100 F
31Ga
64Gd
Ge
,H
l
2He
A, a. e. м.
112,411 ±8
140,115 ±4
251,079580 ±5
35,4527 ± 9
247,070347 ± 5
58,93320 ± 1
51,9961 + 6
132,90543 + 5
63,546 ± 3
262,11376 ± 16
162,50 ±2
167,26 + 3
252,08294 + 2
151,965 ±9
18,9984032 ±9
55,847 + 3
257,095099 ± 8
223,019733 ± 4
69,723 ± 4
157,25 ± 3
72,61 ± 2
1,0078250 ±1
4,002602 ± 2
Электоонная сЬоом\/ла
[36Kr,4^10]552
[54Xe]4/1~25^1~°652
[86Rn]5/10752
[10Ne]3523/M
[86Rn]5/76^/l752
[]8Ar]3</74*2
I Ar]3d54sl
[з^б^1
[lsAr]3d{03sl
[86Rn, 5fi4]6d37s2
[54Xe]4f]06s2
[54Xe]4/12652
[86Rn]5/u752
[254Xe]4/76s2
[2Uc]2s22p5
[ to]3de4s2
18
[86Rn]5/l2752
[s6Rn]7sl
[18Аг, ЗдГ10]^2^1
[54Xe]4/75flf1652
[18Ar, 3flfl0]4^24^2
\sl
Is2
Радиус, пм
149
183
—
—
125
125
265
128
—
177
176
—
204
—
124
—
270
122
180
123
78
128
'ков
141
165
—
99
116
118
235
117
—
159
157
—
185
58
117
—
—
125
161
122
30
32
Гион
Cd2+ 103
Се3+ 107
Се4+ 94
СР+98
Cf+86
Cl- 181
С17+41
Cm3+ 99
Cm4+ 88
Со2+ 82
Со3+ 64
Сг3+64
0^+35
Cs+ 165
Cu+96
Cu2+ 72
Dy3+ 91
?^+89
Es3+ 98
Eu2+112
Eu3+ 98
F-133
Fe2+ 82
Fe3+67
Fm3+ 97
Fr+ 180
Ga+ll3
Ga3+ 62
Gd3+ 97
Ge2+90
Ge4+ 67
H-154
H+-24
338
II. Химические элементы. Атомы
Продолжение табл.
ле-
ент
\%
\о
Hs
п
г
С
Сг
я
[
Lr
Md
rtg
An
Ло
Mt
Ma
Mb
Md
Me
No
-——^
A a. e. м.
178,49 ± 2
200,59 ± 3
164,93032 ± 3
[269]
126,90447 ± 3
114,818 ±1
192,22 ± 3
39,0983 ± 1
83,80 ±1
138,9055 ±2
6,941 ± 2
262,10532 ±6
174,967 ±1
258,09857 ± 12
24,3050 ± 6
54,93805 ± 1
95,94 ± 1
[268]
14,00674 ± 7
22,989768 ± 6
92,90638 ± 2
144,24 ± 3
20,1797 ±6
58,6934 ± 1
259,100931 ± 12
—
Элрктпонняя гЬппмч/пя
[54Xe,4/14]5rf26s2
[ 4Xe, 4fl45d[0]6s2
[54Xe] 4/52
—
[ Kr, 4dl0]5s25p5
[36Ki,4dw]5s25p!
[54Xe, 4fl4]5d76s2
[18Ar]4i'
[l8Ar, 3dl°]4s24p6
[54Xe]5tf'652
[2He]25>
[86Rn, 5/14]6fif'752
[54Xe,4fu]5dl6s2
[86Rn]5/13752
[10Ne]352
Г A t*1 ^ /*/ 5/1 p 2
[ Kr]4^/555I
—
[2He]2522^3
[10Ne]351
[36Kr]4d45sl
[54Xe]4/14652
[2He]2^22/?6
[ Ar]3d84s2
[86Rn]5/14752
156
160
177
—
137
163
136
227
212
188
152
—
173
__
160
124
136
—
71
187
143
182
160
125
—
Радиус, пм
Гков
144
144
158
—
133
150
126
203
189
169
123
_
156
—
136
117
129
—
70
154
134
164
69
115
—
ион
Hf+84
Hg+ 127
Hg2+112
Ho3+ 89
—
1-220
I7+67
In+ 132
In3+ 92
Ir3+ 75
11^66
K+133
La3+ 122
Li+78
Lr3+ 92
Lu3+ 85
Md3+ 96
Mg2+ 78
Mn2+91
Mn7+ 60
Mo4+ 79
Mo6+ 62
—
N3" 132
N5+27
Na+ 98
Nb4+ 74
Nb5+ 69
Nd3+ 104
—
Ni2+ 78
Ni3+ 62
No2+113
No3+ 95
339
II. Химические элементы. Атомы
Продолжение табД
Эле-
Элемент
98*NP
Р
76°S
15Р
1 J
otPa
82Pb
46Pd
61 Pm
84 P°
59Pr
78Pt
*Pu
88 Ra
37Rb
75Re
10*Rf
45Rh
86^
44Ru
Sb
21Sc
Аг, а. е. м.
237,048168 ±2
15,9994 ± 3
190,23 ± 1
30,973762 ± 4
231,0358812
207,2 ± 1
106,42 ± 1
144,912743 ± 4
208,982404 ± 5
140,90765 ± 3
195,08 ± 3
244,064199 ± 5
226,025403 ± 3
85,4678 ± 3
186,207 ± 1
261,10869 ±22
102,90550 ± 3
222,017571 ± 3
101,07 ±2
32,066 ± 6
121,757 ±3
44,955910 ±9
Электронная формула
[S6Rn]5f4-56dl-°7s2
[2Ht]2s22p4
[54Xe,4/l4]5tf66s2
[ Ne]3s23/?3
[ Rn]5f{-26d2-l7s2
[54Xe,4/l45</10]6s26/?2
[36Kr]4</10
[54Xe]4/56s2
[54Xe,4/145tf10]6s26/>4
[54Хе]4/3б52
Г ^^р 4/* IS// пс
L S4"^ ' J J
[86Rn]5/67*2
[86Rn]752
[36Kr]5i'
[54Xe, 4/14]5rf5652
[86Rn, 5/14]6rf2752
[36Kr]4rf855'
[^Xe, 4fH5dw]6s26p6
[36Kr]4rf755'
[10Ne]3.s23/74
[36Kr, 4(iI0]5525/?3
[lsArKdl4s2
Радиус, пм
131
—
135
115
161
175
138
181
167
183
138
151
223
248
137
—
135
—
134
185
182
161
ков
66
126
ПО
158
154
128
163
153
165
129
—
—
211
128
—
125
145
124
104
141
144
¦¦*•»*
ион
Np3+110
Np7+ 85
О2" 132
Os4+ 67
Os8+ 53
P3-212
P5+35
Pa4+95
Pa5+ 89
Pb2+ 132
Pb4+ 84
Pd2+ 86
Pd4+ 64
Pm3+ 106
Po4+ 65
Pr3-^ 106
Pr4" 92
Pt2+ 85
Pt4+ 70
Pu3+ 108
Pu6+81
Ra2+ 152
Rb+ 149
Re4+ 72
Re7+ 60
—
Rh3+75
Rh4+ 67
—
Ru4+ 65
Ru8+ 54
S2- 170
S6+29
Sb3+ 89
Sb5+ 62
Sc3+83
340
II. Химические элементы. Атомы
^—¦—
Эле-
Элемент
~~—-—
]0;sg
Sm
50Sn
38Sr
„Та
15
43ic
52Te
9oTh
22Tl
8|ti
69Tm
«u
23V
74W
54Xe
39Y
70Yb
302n
—
1"
78,96 ± 3
[266]
28,0855 ± 3
150,36 + 3
118,710 ± 7
87,62 ± 1
180,9479 ±1
158,9253413
97,907215 ±4
127,60 ± 3
232,0381 ± 1
47,88 ± 3
204,3833 ± 2
168,93421 ± 3
238,0289 ± 1
50,9415 ± 1
183,84 ±3
131,29 ±2
88,90585 ± 2
173,04 ± 3
65,39 ± 2
91,224 ±2
[I8Ar,3rf10]4.$V
—
[ Ne]3s23p2
[54Xe]4/66s2
[36Kr,4tflo]5s25/>2
[36Kr]5*2
[54Xe, 4/14]5rf36s2
[54Xe]4/8~95rf'~°652
[36Kr]4</55*2
[36Kr,4rf10]5s25/
[86Rn]6rf27s2
[18Ar]3</24s2
[54Xe,4fH5dl0]6s26pl
[54Xe]4/136i2
[86Rd]5/36/'7s2
Г A ri ^ fi -*Л ч1 *•
|^ i пЛ1 J J U ^o
[54Xe,4/14]5^/4652
[36Kr,4^10]5525/?6
[36Kr]4^/1552
[54Xe]4/14652
[18Ar, 3dl0]4s2
[36Kr]4d25s2
Гат
215
—
132
180
141
215
143
178
136
143
180
145
170
175
153
132
137
218
181
194
133
160
Продолжение табл.
Радиус, пм
'ков
117
—
117
166
140
192
134
159
127
137
165
132
155
156
142
123
130
209
162
170
125
145
'ион
Se2" 191
Se5+ 56
Si4" 271
Si4+ 26
Sm2+lll
Sm3+ 100
Sn2+ 93
Sn4+ 74
Sr2+ 127
Ta4+ 68
Ta5+ 64
Tb3+93
Tb4+81
Tc4+ 72
Tc7+ 56
Те2-211
Te6+ Sfi
Iv JU
Th4+ 99
Ti3+ 81
Ti4+ 75
Tl+ 149
Tl3+ 105
Tm3+ 87
U3+ 103
U6+80
у*+61
\й+59
W4+68
Xe8+ 62
У^Юб
Yb2+113
Yb3+86
Zn2+ 83
341
II. Химические элементы. Атомы
Окончание щщ
Эле-
Элемент
'ПО
МП
•112
М14
М16
Аг а. е. м.
[271]
[272]
[277]
[289]
[289]
Электронная формула
—
—
—
—
_
Радиус, пм
—
—
—
—
—
'ков
—
—
—
—
—
Гион
—
—
—
—
3. Изотопы
3.1. Природные изотопы
Приведены относительная атомная масса (Ат) и содержание в при-
природном элементе (мольная доля х) стабильных и радиоактивных изо-
изотопов, встречающихся в природе. Радиоактивные изотопы отмечены
верхним индексом (*).
Изотоп
107Ag
109Ag
27А1
36Аг
38Аг
40Аг
75As
197Au
ioB
"В
130Ва
132Ва
134Ва
135Ва
|36Ва
137Ва
138Ва
Аг, а. е. м.
106,9051
108,9048
26,9815
35,9675
37,9627
39,9624
74,9216
196,9665
10,0129
11,0093
129,9063
131,9050
133,9045
134,9057
135,9046
136,9058
137,9052
х, %
51,35
48,65
100
0,337"
0,063й
99,600"
100
100
18,8
81,2
0,106
0,101
2,417
6,592
7,854
11,230
71,700
Изотоп
9Ве
209Ш
79Вг
81Вг
12С
13С
40Са
42Са
43Са
44Са
46Са
48Са
¦o^cd
•°»Cd
110Cd
luCd
112Cd
Af a. e. м.
9,0122
208,9804
78,9183
80,9193
12,0000
13,0034
39,9626
41,9586
42,9588
43,9555
45,9537
47,9525
105,9065
107,9042
109,9030
110,9042
111,9028
x,%
100
100
50,52
49,48
98,892
1,108 __
96,941
0,647
0,135
2,086
0,004
0,187
1,25
0,89
12,49
12,80
24,13
342
II. Химические элементы. Атомы
Продолжение табл.
Изотоп
_-
used
ii4Cd
i"«Cd
i38Ce
i«Ce
i«ce
»C1
37C1
59Co
»Cr
52Cr
»Cr
54Cr
»3Cs
63Cu
65Cu
•*Dy
•»Dy
160Dy
I61Dy
'«Dy
163Dy
l64Dy
162Er
,64Er
166Er
l67Er
168Er
170Er
15lEu
J^Eu
19F
" -_
Ar a. e. м.
112,9044
113,9034
115,9048
135,9071
137,9060
139,9054
141,9092
34,9689
36,9658
58,9332
49,9461
51,9405
52,9407
53,9389
132,9054
62,9296
64,9278
155,9243
157,9244
159,9252
160,9269
161,9268
162,9287
163,9292
161,9288
163,9292
165,9303
166,9321
167,9324
169,9355
150,9197
152,9212
18,9984
x,%
12,22
28,73
7,49
0,19
0,25
88,48
11,08
75,4
24,6
100
4,31
83,76
9,55
2,38
100
69,17
30,83
0,06
0,10
2,34
18,90
25,50
24,90
28,20
0,14
1,61
33,60
22,95
26,80
14,90
47,77
52,23
100
Изотоп
54pe
56pe
57Fe
58Fe
69Ga
7IGa
*l52Gd
154Gd
155Gd
156Gd
157Gd
158Gd
I6°Gd
70Ge
72Ge
73Ge
74Ge
76Ge
"H
2H
3He
4He
•174Hf
176Hf
177Hf
"8Hf
179Hf
180Hf
l96Hg
l98Hg
199Hg
200Hg
20!Hg
/4r, a. e. м.
53,9396
55,9349
56,9354
57,9333
68,9256
70,9247
151,9198
153,9209
154,9226
155,9221
156,9240
157,9240
159,9270
69,9242
71,9221
72,9235
73,9212
75,9214
1,0078
2,0141
3,0160
4,0026
173,9400
175,9414
176,9432
177,9437
178,9458
179,9465
195,9658
197,9667
198,9682
199,9683
200,9703
x,%
5,84
91,68
2,17
0,31
60,65
39,35
0,20
2,18
14,80
20,47
15,65
24,84
21,86
20,55
27,37
7,67
36,74
7,67
99,985*
0,015*
0,000138"
99,999862°
0,162
5,206
18,606
27,297
13,629
35,100
0,14
10,02
16,84
23,13
13,22
343
II. Химические элементы. Атомы
Продолжение щ^
Изотоп
202Hg
204Hg
165Но
127J
113In
*115In
191Ir
193Ir
39K
мок
41K
78Kr
80Kr
82Kr
83Kr
84Kr
86Kr
*138La
139La
6Li
7Li
175Lu
*176Lu
24Mg
25Mg
26Mg
55Mn
92Mo
94Mo
95Mo
96Mo
97Mo
98Mo
Аг, а. е. м.
201,9706
203,9735
164,9303
126,9045
112,9041
114,9039
190,9606
192,9629
38,9637
39,9640
40,9620
77,9204
79,9164
81,9135
82,9141
83,9115
85,9106
137,9071
138,9063
6,0151
7,0160
174,9408
175,9427
23,9850
24,9858
25,9826
54,9381
91,9068
93,9051
94,9058
95,9047
96,9060
97,9054
x, %
29,80
6,85
100
100
4,23
95,77
38,5
61,5
93,0881
0,119
6,9000
0,35°
2,27*
11,56*
11,55й
56,90й
17,37й
0,089
99,911
7,5
92,5
97,41
2,59
78,60
10,11
11,29
100
15,86
9,12
15,70
16,50
9,45
23,75
Изотоп
юоМо
14N
15N
23Na
93Nb
142Nd
143Nd
*i44Nd
145Nd
i46Nd
148Nd
150Nd
20Ne
21Ne
22Ne
58Ni
60Ni
61Ni
62Nj
64Ni
16Q
17O
18Q
184Os
*186qs
187Os
188Os
189Os
190Os
192Os
31p
204pb
206pb
Аг, а. е. м.
99,9075
14,0031
15,0001
22,9898
92,9064
141,9077
142,9098
143,9101
144,9126
145,9131
147,9169
149,9209
19,9924
20,9938
21,9914
57,9353
59,9308
60,9311
61,9283
63,9280
15,9949
16,9991
17,9992
183,9525
185,9538
186,9557
187,9558
188,9581
189,9584
191,9615
30,9738
203,9730
205,9744
х,°лГ^
9,62
99,635 ^
0,365
100 "
100 ^
27,13 "-
12,18
23,80
8,30
17,19
5,76
5,64
90,92й
0,26й
8,82й
67,76
26,16
1,26
3,66
1,16
99,759
0,037
0,204
0,02
1,58
1,60
13,30
16,10
26,40
41,00 ^
100 __^
1,5
23,6
344
II. Химические элементы. Атомы
Продолжение табл.
Изотоп
^-
2O7pb
208 pb
IO4pd
IO5pd
IM>Pd
IO8pd
nopd
Hlpr
•190pt
192П
I94pt
195К
196pt
I98pt
85Rb
*87Rb
l85Re
*i87Re
IO3Rh
96Ru
98Ru
"Ru
l00Ru
l01Ru
IO2Ru
104Ru
32S
33S
~1ITSb~~
°Sb
Ar, a. e. m.
206,9759
207,9766
101,9056
103,9040
104,9051
105,9035
107,9039
109,9052
140,9077
189,9599
191,9610
193,9627
194,9648
195,9649
197,9679
84,9118
86,9092
184,9530
186,9557
102,9055
95,9076
97,9053
98,9059
99,9042
100,9056
101,9043
103,9054
31,9721
32,9715
33,9679
35,9671
120,9038
122,9042
x, %
22,6
52,3
11,02
11,14
22,33
27,33
26,46
11,72
100
0,001
0,79
32,90
33,80
25,30
7,20
72,165
27,835
37,07
62,93
100
5,52
1,88
12,70
12,60 •
17,00
31,60
18,70
95,02
0,75
4,21
0,02
57,25
42,75
Изотоп
45Sc
74Se
76Se
77Se
78Se
80Se
82Se
28Si
29Si
30Si
144Sm
*l47Sm
*148Sm
149Sm
150Sm
152Sm
154Sm
112Sn
114Sn
ll5Sn
116Sn
117Sn
118Sn
119Sn
120Sn
122Sn
124Sn
84Sr
86Sr
87Sr
88Sr
*180Ta
181Ta
Ar, a. e. м.
44,9559
73,9225
75,9192
76,9199
77,9173
79,9165
81,9167
27,9769
28,9765
29,9738
143,9102
146,9149
147,9148
148,9172
149,9173
151,9197
153,9222
111,9048
113,9028
114,9033
115,9017
116,9030
117,9016
118,9033
119,9022
121,9034
123,9053
83,9134
85,9093
86,9089
87,9056
179,9475
180,9480
x, %
100
0,87
9,02
7,58
23,52
49,82
9,19
92,27
4,68
3,05
3,16
15,07
11,27
13,84
7,47
26,66
22,53
0,97
0,65
0,36
14,53
7,68
24,22
8,58
32,59
4,63
5,79
0,56
9,86
7,02
82,56
0,012
99,988
345
II. Химические элементы. Атомы
Окончаниеi
Изотоп
159^
120Те
122Те
¦123Те
124Те
125Те
126Те
128Те
130Те
•232Jh
46Tl
47Tl
48Tl
49Ti
50Ti
203-n
205T1
169Tm
•234U
•235U
•238U
50y
51V
180\y
182W
183W
184W
186W
Ar, a. e. м.
158,9253
119,9040
121,9031
122,9043
123,9028
124,9044
125,9033
127,9045
129,9062
232,0381
45,9526
46,9518
47,9479
48,9479
49,9448
202,9723
204,9744
168,9342
234,0409
235,0439
238,0508
49,9472
50,9440
179,9467
181,9482
182,9502
183,9509
185,9544
x, %
100
0,096
2,600
0,908
4,816
7,140
18,950
31,690
33,800
100
7,95
7,75
73,45
5,51
5,34
29,524
70,476
100
0,0055
0,7200
99,2745
0,24
99,76
0,13
26,30
14,30
30,67
28,60
Изотоп
124Xe
I26Xe
128Xe
129Xe
130Xe
l31Xe
132Xe
134Xe
136Xe
89y
168Yb
.70уь
171Yb
172Yb
173Yb
174Yb
'7«Yb
64Zn
66Zn
67Zn
68Zn
70Zn
90Zr
91Zr
92Zr
94Zr
96Zr
A^ a. e. м.
123,9059
125,9043
127,9035
128,9048
129,9035
130,9051
131,9041
133,9054
135,9072
88,9059
167,9339
169,9348
170,9363
171,9364
172,9382
173,9389
175,9426
63,9291
65,9260
66,9271
67,9249
69,9253
89,9047
90,9056
91,9050
93,9063
95,9083
0,10°
0,09°
1,91°
26,40"
4,10"
21,20"
26,90°
10,40"
8,90"
100
0,13
3,05
14,30
21,90
16,12
31,80
12,70
48,89
27,81
4,11
18,56
0,63
51,45
11,22
17,15
17,38
2,80
.
a В воздухе.
6 В воде.
346
II. Химические элементы. Атомы
2 радиоактивные изотопы
Приведены наиболее долгоживущие искусственные радиоактив-
изотопы, а также изотопы, используемые в качестве радиоактив-
Н ix индикаторов, и природные радиоактивные изотопы (выделены
Н оифтом). Представлены относительные атомные массы (Ат) и пери-
перины полураспада (Г1/2) изотопов.
Изотоп
¦
227 Ар
^ Ас
l08Ag
ll0Ag
26А1
28А1
243Ат
39Аг
"As
2ioAt
195Au
l98Au
8B
133Ba
140Ва
'Be
l0Be
2!0Bj
*'Вк
"Вг
82Вг
14С
41Са
144Се
Аг, а. е. м.
227,0275
228,0310
107,9060
109,9061
25,9869
27,9819
243,0614
38,9643
72,9238
75,9224
209,9871
194,9650
197,9682
8,0246
132,9060
139,9088
7,0169
10,0135
209,9841
247,0703
76,9214
81,9168
14,0032
44,9560
114,9054
143,9137
7*1/2
21,773 года
6,13ч
127 лет
250 сут
72-105лет
2,24 мин
7,37- 103лет
2,69 года
80,3 сут
26,3 ч
8,1ч
183 сут
2,696 сут
0,769 с
10,73 года
12,79 сут
53,2 сут
1,6-106лет
5,01 сут
1,4- 103лет
57,0 ч
35,34 ч
5,71 • 103лет
1,03- 105лет
162,6 сут
44,6 сут
284,4 сут
Изотоп
251Cf
36С1
247Ст
60Со
51Сг
135Cs
137Cs
64Cu
67Cu
262Db
154Dy
169Er
252Es
150Eu
152Eu
18F
59Fe
6oFe
257Fm
223Fr
67Ga
72Ga
150Gd
152Gd
159Gd
68Ge
Аг, а. е. м.
251,0796
35,9797
247,0703
59,9338
50,9450
134,9059
136,9071
63,9298
66,9277
262,1138
153,9244
158,9257
168,9346
252,0829
149,9197
151,9218
18,0009
58,9350
59,9340
257,0951
223,0197
66,9282
71,9247
149,9187
151,9198
158,9264
67,9281
9,0-102 лет
3,07 • 105лет
1,58-107 лет
5,272 года
27,703 сут
3 • 106лет
30,17 года
12,70 ч
61,8 ч
34 с
1 • 107лет
144,4 сут
9,4 сут
472 сут
36 лет
13,60 года
109,8 мин
44,6 сут
3- 105лет
100,5 сут
22 мин
78,26 ч
14,10 ч
1,8- 106лет
1,1-1014лет
18,6 ч
288 сут
347
II. Химические элементы. Атомы
Продолжение niQ§
Изотоп
3Н(Т)
6Не
174Hf
181Hf
182Hf
194Hg
203Hg
166Ho
129J
114ln
115In
192Ir
194Ir
40K
42K
43K
81Kr
85Kr
137La
138La
140La
9Li
262Lr
174Lu
176Lu
177Lu
258Md
28Mg
53Mn
54Mn
93Mo
Аг, а. е. м.
3,0161
6,0189
173,9400
180,9491
181,9506
193,9654
202,9729
165,9323
128,9050
130,9061
113,9049
114,9039
191,9626
193,9651
39,9640
41,9630
42,9607
80,9166
84,9125
136,9065
137,9071
139,9095
9,0268
260,1053
173,9404
175,9427
176,9438
258,0986
27,9839
52,9413
53,9402
92,9068
7*1/2
12,34 года
0,808 с
2,0- 1015лет
42,4 сут
9- 106лет
260 лет
46,7 сут
1,2- 103лет
1,6 107 лет
8,054 сут
49,51 сут
« 5 • 1014лет
74,08 сут
0,47 года
1,28-109 лет
12,36 ч
22,3 ч
2,1 • 105лет
10,73 года
6-104лет
1,1 • 10плет
40,24 ч
0,178 с
Змин
3,3 года
3,8 • 1010лет
6,71 сут
55 сут
21,0ч
3,7 • 106лет
312 сут
3,5- 103лет
Изотоп
99Мо
13N
22Na
24Na
92Nb
95Nb
147Nd
23Ne
59Ni
63Ni
259No
237Np
15O
186Os
191Os
194Os
32p
33p
231pa
233pa
205pb
210pb
io3pd
107pd
145pm
147Pm
209po
210po
143pr
188ft
190ft
Ar, a. e. м.
98,9077
13,0057
21,9944
23,9910
91,9072
94,9068
143,9101
146,9161
22,9945
58,9344
62,9297
259,1009
237,0482
15,0031
185,9538
190,9609
193,9652
31,9739
32,9717
231,0359
233,0416
204,9745
209,9842
102,9061
106,9051
144,9127
146,9161
208,9824
209,9829
142,9108
187,9594
189,9599
Г1/2^-^
66,02 ч
9,96 мин -"
2,603 года
15,0 ч
3,6- 107лет^
35 сут
2,1 • 1016лет^
10,98 сут
37,6 с
7,5- 104лет^"
100,1 года
58 мин
2,14 -106 лет
122 с
2-1015лет
15,4 сут
6,0 лет
14,31 сут
25,4 сут
3,28 -104лет
27,0 сут _
1,5 • 107лет
27,1 года
17,0 сут
6,5 • 106лет
18 лет
2,623 года____
102 года
138,38 сут ^
13,57 сут__^
10,2 сут
6- 10илет
348
II. Химические элементы. Атомы
Окончание табл.
Изотоп
—
228Ra
83Rb
sORb
87Rb
186Re
l87Re
261 Rf
l0lRh
l02Rh
222Rn
103Ru
IO6Ru
35S
l24Sb
l25Sb
46Sc
79Se
3lSi
i2Si
l46Sm
l4'Sm
l48Sm
b3Sm
lijSn
90Sr
'"Та
18O»,
°Ta
i82Ta
Лг, а. е. м.
192,9630
244,0642
226,0254
228,0311
82,9152
85,9112
86,9092
185,9544
186,9557
261,1087
100,9062
101,9043
222,0176
102,9063
105,9073
34,9690
123,9059
124,9053
45,9550
78,9185
30,9753
31,9740
145,9131
146,9149
147,9148
152,9221
122,9057
125,9077
89,9077
178,9460
179,9475
181,9502
^~1/2
50 лет
8,2-107 лет
1600 лет
5,76 года
86,2 сут
18,8 сут
4,8 • 1010лет
2- 105лет
4- 1010лет
65 с
3,3 года
206 сут
3,824 сут
39,4 сут
367 сут
87,4 сут
60,20 сут
2,7 года
83,8 сут
< 6,5 • 104лет
2,62 ч
~ 650 лет
3- 107лет
1,06- 10плет
7- 1015лет
46,7 ч
129,2 сут
1 • 105лет
28,7 года
1,7 года
> 1 • 1013лет
115,0 сут
Изотоп
157ТЬ
158ТЪ
160ТЪ
98Тс
"Тс
121Те
12зТе
127Те
230Th
232Th
234Th
44Ti
45Ti
204yj
170Tm
171Tm
234U
235JJ
236U
237U
238U
48y
49y
181W
185W
127Xe
88y
90y
169уЬ
65Zn
93Zr
95Zr
Аг, а. е. м.
156,9240
157,9254
159,9272
97,9072
98,9062
120,9050
122,9043
126,9052
230,0331
232,0381
L 234,0436
43,9596
44,9581
203,9739
169,9358
170,9364
234,0409
235,0439
236,0456
237,0487
238,0508
47,9523
48,9485
180,9482
184,9556
126,9052
87,9095
89,9072
168,9352
64,9292
92,9065
94,9080
7~1/2
150 лет
150 лет
72,3 сут
4,2 • 106лет
2,13-105 лет
154 сут
> 1,25- 1013лет
109 сут
7,53 • 104лет
1,40-1010лет
24,1 сут
47 лет
3,09 ч
3,78 года
128,6 сут
1,92 года
2,45-105 лет
7,038-108 лет
2,342 • 107лет
6,75 сут
4,468- 109лет
15,974 сут
330 сут
121,2 сут
75,3 сут
36,41 сут
106,6 сут
64,3 ч
32,0 сут
243,9 сут
1,5- 106лет
64 сут
349
II. Химические элементы. Атомы
4. Энергия ионизации.
Сродство к электрону и протону.
Электроотрицательность
Приведены энергия ионизации (энтальпия отрыва электрона, щ
положительной ионизации) для нейтральных атомов A}), однозардд-
ных и двухзарядных катионов (/2 и /3 соответственно), сродство к
электрону (энтальпия присоединения электрона, или отрицательной
ионизации, Ае) и сродство к протону (энтальпия присоединения про-
протона Ар) для нейтральных атомов, электроотрицательность элементов
(%). Значения, указанные в скобках, получены методом полуэмпири-
ческого расчета. Прочерк означает отсутствие данных.
Эле-
Элемент
Ас
Ag
А1
Am
Аг
As
At
Au
В
Ba
Be
Bi
Bk
Br
С
Ca
Cd
Ce
Cf
Cl
Cm
Co
Cr
Cs
Cu
Энергия ионизации, эВ
>i
5,17
7,58
5,99
5,99
15,76
9,82
9,00
9,23
8,30
5,21
9,32
7,29
6,23
11,81
11,26
6,11
8,99
5,54
6,30
12,97
6,02
7,88
6,77
3,89
7,73
'2
12,06
21,49
18,83
—
27,63
18,63
20,10
20,50
25,15
10,00
18,21
16,74
—
21,76
24,38
11,87
16,91
10,85
—
23,81
—
17,06
15,50
25,10
20,29
20,00
34,83
28,45
—
40,74
28,35
30,06
30,50
37,93
35,84
153,89
25,57
—
36,27
47,93
50,91
37,48
20,08
—
39,61
—
33,50
30,96
34,60
36,83
Сродство, эВ
-1,30
-0,46
—
@,37)
-1,07
-2,79
-2,31
-0,30
@,48)
(-0,38)
-0,95
—
-3,37
-1,27
A,93)
@,27)
-0,52
—
-3,61
—
-0,94
-0,98
-0,39
-1,23
—
—
—
-3,80
—
—
—
-7,30
—
—-
—
—
-5,80
-6,00
—
—
—
—
-5,30
—
—
—
—
—
V
X
1,00
1,42
1,47
A,2)
C,2)
2,11
1,90
1,42
2,01
0,97
1,47
1,67
A,2)
2,74
2,50
1,04
1,46
1,08
A,2)
2,83
A,2)
1,70
1,56
0,86
1,75
350
II. Химические элементы. Атомы
Продолжение табл.
Энергия
'i
5,94
6,11
6,42
5,67
17,42
7,90
6,50
4,07
6,00
6,15
7,90
13,60
24,59
6,83
10,44
6,02
10,45
5,79
9,10
4,34
14,00
5,58
5,39
—
5,43
6,58
7,65
7,43
7,09
14,53
5,14
6,76
5,53
21,56
7,64
6,65
6,27
13,62
8,70
-1 .
ионизации
11,67
11,93
—
11,25
34,97
16,18
—
21,76
20,51
12,10
15,92
54,42
14,90
18,76
11,80
19,10
18,87
17,00
31,62
24,37
11,06
75,64
__
13,90
—
15,04
15,64
16,16
29,60
47,28
14,32
10,72
40,96
18,17
—
—
35,12
17,00
,эВ
'з
22,80
22,70
—
24,70
62,71
30,65
—
32,13
30,71
20,60
34,20
23,30
34,20
22,80
33,00
28,03
26,95
45,72
39,95
19,18
122,45
—
20,96
—
80,14
23,30
27,14
47,45
71,65
25,05
22,10
63,45
35,17
—
—
54,93
25,00
Сродство, эВ
-0,52
-0,52
—
-0,52
-3,49
-0,58
—
—
-0,39
-0,52
-1,74
-0,75
@,22)
@,63)
@,19)
-0,52
-3,08
-0,72
-1,97
-0,47
@,42)
-0,55
-0,59
—
-0,52
—
@,22)
@,97)
-1,18
@,21)
-0,34
-1,13
-0,52
@,22)
-1,28
-1,47
-1,44
—
—
—
-3,70
-3,70
—
—
—
—
—
-2,69
-1,84
—
—
__
-6,30
—
—
—
-4,50
—
—
—
—
—
—
—
—
-4,20
-2,08
—
—
—
-4,90
—
Y
А
1,10
1,11
A,2)
1,01
4,10
1,64
A,2)
0,86
1,82
1,11
2,02
2,10
E,5)
1,23
1,44
1,10
2,21
1,49
1,55
0,91
2,94
1,08
0,97
A,2)
1,14
A,2)
1,23
1,60
1,30
3,07
1,01
1,23
1,07
D,84)
1,75
A,2)
1,22
3,50
1,52
351
II. Химические элементы. Атомы
Окончание
Эле-
Элемент
Р
Ра
РЬ
Pd
Pm
Ро
Рг
Pt
Pu
Ra
Rb
Re
Rh
Rn
Ru
S
Sb
Sc
Se
Si
Sm
Sn
Sr
Та
Tb
Tc
Те
Th
Ti
Tl
Tm
U
V
w
Xe
Y
Yb
Zn
Zr
Энергия ионизации, эВ
'i
10,49
5,89
7,42
8,34
5,55
8,42
5,46
9,00
6,06
5,28
4,18
7,88
7,46
10,75
7,36
10,26
8,64
6,56
9,75
8,15
5,64
7,34
5,69
7,89
5,86
7,28
9,01
6,08
6,83
6,11
6,18
6,19
6,75
7,98
12,13
6,22
6,25
9,39
6,63
19,72
—
15,03
19,43
10,90
19,40
10,55
18,56
—
10,15
27,50
13,06
18,08
21,40
16,76
23,33
16,50
12,80
21,19
16,35
11,07
14,63
11,03
16,20
11,52
15,26
18,60
11,50
13,58
20,43
12,05
11,60
14,65
17,70
21,25
12,24
12,18
17,96
13,13
30,18
—
31,98
32,95
22,30
27,30
21,63
29,02
—
34,20
40,00
26,01
31,06
29,40
28,47
34,83
25,30
24,76
30,82
33,49
23,40
30,50
42,88
21,76
21,90
29,55
28,00
20,00
27,49
29,83
23,70
19,80
29,31
23,84
32,10
20,52
25,50
39,72
22,98
Сродство, эВ
-0,80
—
-1,14
(-1,02)
-0,52
-1,87
-0,52
-2,13
—
—
(-0,42)
-0,15
-1,24
@,42)
-1,14
-2,08
-1,05
@,73)
-2,02
-1,38
-0,52
-1,25
A,51)
-0,62
-0,52
-0,73
-1,96
—
-0,39
-0,50
-0,52
—
-0,64
-0,50
@,45)
@,4)
-0,52
(-0,09)
-0,45
—
—
—
—
—
—
—
—
—
-6,80
—
—
—
-6,50
—
—
—
—
—
—
—
—
—
—
—
-10,80
—
-5,40
—
—
—
—
V
X '¦
2,32
1,14
1,55
,35
1,07
1,76
1,07
,44
1,22
0,97
0,89
1,46
1,45
2,06
1,42
2,60
1,82
1,20
2,48
2,25
1,07
1,72
0,99
1,33
1,10
1,36
2,01
1,П
1,32
1,44
1,П
1,22
1,45
1,40
2,40
1,11
1,06
1,66
1
~
M
—
352
II. Химические элементы. Атомы
5. Распространение в природе
5 1. физическая распространенность
Химические элементы расположены в порядке убывания их физи-
физической распространенности (т. е. их массовых долей) в земной коре.
Радиоактивные элементы, не имеющие стабильных изотопов, обозна-
обозначены верхним индексом (*).
1.0
2. Si
З.А1
4.Fe
5.Са
6.Na
7. К
8.Mg
9.Н
10. Ti
11. Cl
12. P
13. С
14. Mn
15. S
16. N
17. Rb
18. F
19. Ba
20. Zr
21. Cr
22. Ni
23. Sr
24. V
25. Zn
26. Cu
27. W
28. Li
29. Ce
30. Co
31. Sn
32. Y
33. Nd
34. Nb
35. Pb
36. La
37. В
38. Ga
39. Mo
40. *Th
41. Та
42. Cs
43. Br
44. Sm
45. Gd
46. Ge
47. As
48. Be
49. Pr
50. Sc
51. Hf
52. Dy
53. At
54. *U
55. Yb
56. Er
57. Ho
58. Eu
59. Tb
60. Se
61. Lu
62. Sb
63. Hg
64. Cd
65. TI
66. Bi
67. Tm
68. In
69. Ag
70.1
71. Ru
72.0s
73. Pd
74. Те
75. Au
76. Pt
77. Ne
78. He
79. Ir
80. Rh
81. Re
82. Kr
83. Xe
84. *Ra
85. *Pa
86. *Ac
87. *Po
88/Rn
89. *Tc
90. *Np
91.*Pu
92. *Fr
93. *Pm
94. *At
Остальные
элементы
в природе
отсутст-
отсутствуют
Приведены кларки химических элементов, выраженные массовой
долей (%) элемента в земной коре. Элементы расположены в порядке
Убывания физической распространенности.
1.0
2. Si
З.А1
4.Fe
S.Ca
С X т
6-Na
7 iy
7К
Я \ м
о. Mg
9Н
"-
49,50
25,80
7,57
4,70
3,38
2,63
2,41
1,95
0,88
—-—
10. Ti
11.С1
12. Р
13. С
14. Мп
15. S
16. N
17. Rb
18. F
0,410
0,190
0,090
0,087
0,085
0,048
0,030
0,029
0,028
19. Ва
20. Zr
21. Cr
22. Ni
23. Sr
24. V
25. Zn
26. Cu
27. W
0,0260
0,0210
0,0190
0,0150
0,0140
0,0140
0,0120
0,0100
0,0064
28. Li
29. Ce
30. Co
31. Sn
32. Y
33. Nd
34. Nb
35. Pb
Итого:
0,0060
0,0043
0,0037
0,0035
0,0026
0,0022
0,0019
0,0018
99,98%
°стал
ьные элементы (в сумме) — 0,02%.
г-2004
353
II. Химические элементы. Атомы
5.2. Химическая распространенность •
Химические элементы расположены в порядке убывания химиче-
химической распространенности (т. е. их мольной доли, %) в земной коре.
1.0
2. Si
3. Н
4.А1
5.Na
6. Са
7. Fe
8.Mg
55,00
16,35
15,52
4,99
2,03
1,50
1,49
1,42
9. К
10. Ti
11.С
12. С1
13. Р
14. Мп
15. S
16. F
1,100
0,152
0,129
0,095
0,052
0,028
0,027
0,026
17. N
18. Li
19. Сг
20. Rb
21.V
22. Zr
23. Ва
24. Ni
0,0250
0,0160
0,0064
0,0060
0,0049
0,0040
0,0034
0,0032
25. Sr
26. Си
27. Zn
28. Со
29. Be
30. В
Итого:
0,0029
0,0028
0,0015
0,0012
0,0011
0,0006
99,99%
Остальные элементы (в сумме) — 0,01%.
5.3. Элементный состав земной коры
Литосфера
Химические элементы расположены в порядке убывания их массо-
массовой доли (%) в литосфере— твердой оболочке на глубину до
17 км (93,06% массы Земли).
1.0
2. Si
З.А1
4. Fe
5.Са
6. Na
7. К
8.Mg
9.Ti
46,60
27,72
8,13
5,00
3,63
2,83
2,59
2,09
0,44
10. Н
11.Р
12. Мп
13. F
14. S
15. Sr
16. Ва
17. С
18. С1
0,140
0,118
0,100
0,070
0,052
0,045
0,040
0,32
0,020
19. Сг
20. Zr
21. Rb
22. V
23. Ni
24. Zn
25. N
26. Се
27. Си
0,0200
0,0160
0,0120
0,0110
0,0080
0,0065
0,0046
0,0046
0,0045
28. Y
29. Li
30. Nd
31. Nb
32. Co
33. La
34. Ga
35. Pb
Итого:
0,0040
0,0030
0,0024
0,0024
0,0023
0,0018
0,0015
0,0015
99,75%
Остальные элементы (в сумме) — 0,25%.
354
II. Химические элементы. Атомы
ГиДросфера
Химические элементы расположены в порядке убывания их массо-
массовой доли (%) в гидросфере — воде морей и океанов F,91% массы
Земли).
Ь0 85,600
2. Н Ю,780
З.С1 1,987
10. Sr 0,0009
11. В 0,0005
Итого: 99,75%
Остальные элементы (в сумме) — 0,25%.
Атмосфера
Приведено содержание газов в сухом воздухе (вблизи поверхности
Земли) в объемных и массовых долях (%).
Газ
о,
Аг
СО,
Ne
Не
сн4
Объемная
доля
78,09
20,94
0,932
0,0318
0,0018
4,6 • 10
1,5- 10
Массовая
доля
75,52
23,13
1,2853
0,0483
0,0013
7,2-10-5
8,3 • Ю-5
Газ
Кг
н,
N2O
СО
Хе
о,
*
Объемная
доля
1,1 • 10
5,0 • Ю-5
2,5 • Ю-5
1,0- Ю-5
8,5 • 10
2,0 • Ю-7
< 0,0036
Массовая
доля
3,2 ¦ 10
3,5 • Ю-6
3,8 • Ю-5
9,7 • 10
3,9 • Ю-5
3,3 • Ю-7
< 0,0145
* Другие газы - Н20, S02, NH3, HC1, HF, Pb, Hg, I, NO, Rn.
5-4. Жизненно важные элементы
Химические элементы расположены по убыванию их массовой до-
Ли (%) в организме взрослого человека.
13. Si 0,010
14. Zn 0,010
15. Al 0,001
Итого: 99,311%
Остал
ьные элементы (в сумме) — 0,
355
II. Химические элементы. Атомы
6. Открытие элементов
6.1. Исторические периоды развития химии
Исторический
период
1. Предалхимический
до IV в.
2. Алхимический
IV-сер. XVI в.
3. Классический
1551-1750 гг.
1751-1800 гг.
4. Количественный
1801-1869 гг.
5. Современный
1870-1900 гг.
1901-1925 гг.
с 1926
Число
11
13
16
34
63
83
88
114
Известные элементы
Символы
Ag, Аи, С, Си, Fe, Hg, Pb, S, Sb, Sn, Zn
Указанные выше и As, Bi
Указанные выше и Со, Р, Pt
Указанные выше и Ва, Be, Cl, Cr, F, Н,
Mn, Mo, N, Ni, О, Sr, Те, Ti, U, W, Y, Zr
Указанные выше и А1, В, Вг, Са, Cd,
Се, Cs, Er, I, In, Ir, К, La, Li, Mg, Na
Nb, Os, Pd, Rb, Rh, Ru, Se, Si, Та, Tb,
Th, Tl, V
Указанные выше и Ac, Ar, Dy, Ga, Gd,
Ge, He, Ho, Kr, Nd, Ne, Po, Pr, Ra, Rn,
Sc, Sm, Tm, Xe, Yb
Указанные выше и Eu, Hf, Lu, Pa, Re
Указанные выше и Am, At, Bh, Bk, Cf,
Cm, Db, Es, Fm, Fr, Hs, Lr, Md, Mt,
No, Np, Pm, Pu, Rf, Sg, Tc, 110, 111,
112, 114, 116
6.2. Даты и приоритеты открытия
Приведены авторы и даты открытия химических элементов. Авто-
Авторы и даты открытия выделены курсивом; представлены, кроме при-
приоритетных, также ученые, внесшие большой вклад в предсказание,
химическую идентификацию и выделение элементов в свободном ви-
виде, разработку промышленных способов их получения. Для некото-
некоторых элементов авторы и даты открытия не установлены; эти элементы
в виде простых веществ, сплавов или соединений известны с древни*
времен или со средних веков.
356
II. Химические элементы. Атомы
Название
Авторы и дата открытия
Азот
дктиний
Алюминий
дмериций
Аргон
Астат
Барий
Бериллий
Берклий
Бор
Борий
Бром
Ванадий
Висмут
Водород
Вольфрам
Гадолиний
Галлий
Гафний
Гелий
Германий
Гольмий
диспрозий
Дубний
ЕвРопий
К. Шееле A769—1771), Д Резерфорд A772), А. де-Лаву-
азье A775-1777), Ж. Шапталь A790)
А. Дебьерн A899), Ф. Гизель A902)
А. Маргграф A754), X. Эрстед A825), Ф. Вёл ер A827—
1845), А. Сент-Клер-Девилль A854-1856), Ч. Холл
A886), П. Эру A886)
Г. Сиборг, А. Гиорсо и сотр. A945)
Д Рэлей и У. Рамзай A894)
Э. Сегре, Д. Корсон и К. Макензи A940)
К. Шееле и Ю. Ган A774), Г.Дэви A808), Р. Бунзен
A841-1855)
Н. Воклен A798), Ф. Вёлер и А. Бюсси A828), Л. Нильсон
A884), П.ЛебоA898)
Г. Сиборг, А. Гиорсо и сотр. A949)
псевдо-Гебер (XIII—XIV вв.), Л. Гей-Люссак и Л.Тенар
A808), Г.Дэви A808), Ф. Вёлер и А. Сент-Клер-Девилль
A857)
Ю. Ц. Оганесян, Г. Н. Флёров и сотр. A976), Г. Мюнцен-
берг и сотр. A981)
А. Балар A826)
A. дель-Рио A801), Н. Сефстрём A830), Ф. Вёлер A830),
Н. РоскоA865)
— (XV-XVI вв.), Агрикола A550-1556), Василий Вален-
Валентин A599-1602), И. Потт A739)
Г. Кавендиш A766), А. де-Лавуазье и Ж.-Б. Мёнье-де-
ла-Плас A783-1785), Г. Дэви A800)
К. Шееле A781), Ф. де-Элуяр A783), А. Муассан A897)
Ж. Мариньяк A880), Ф. Лекок-де-Буабодран A886)
Д. И. Менделеев A871), Ф. Лекок-де-Буабодран A875)
Д. Костер и Й. Хевеши A923)
П. Жансен A868), Н. Локьер и Э. Франкланд A868-1871),
У. Рамзай и У. Крукс A895)
Д.И.Менделеев A871), К. Винклер A886), В.Ю.Рихтер
A886), Л. МейерA886)
П. Клеве A879)
Ф. Лекок-де-Буабодран A886)
B. А. Друин, Г. Н. Флёров, И. Звара и сотр. A970), А. Гиорсо
и сотр. A970)
Э. Демарсе A896—1901)
357
II. Химические элементы. Атомы
Продолжение табл.
Название
Железо
Золото
Индий
Иод
Иридий
Иттербий
Иттрий
Кадмий
Калий
Калифорний
Кальций
Кислород
Кобальт
Кремний
Криптон
Ксенон
Кюрий
Лантан
Литий
Лоуренсий
Лютеций
Магний
Марганец
Медь
Мейтнерий
Менделевий
Авторы и дата открытия
- C000-2500 лет до н.э.), П.П.Аносов A841)
Г. Бессемер A855), П. Мартен A865), С. Томас A876) '
— E000 лет до н. э), В. Бирингуччо A540), П. Р. Багра-
тионA843)
Ф. Райх и X. Рихтер A863)
Б.Куртуа A811), Л. Гей-Люссак A811—1813), Г.Дэви
A814)
С. Теннант A804)
Ж. МаринъякA878), Ж. Юрбен A907)
Ю. Гадолин A794), Ф. Вёлер A828)
К. Герман A817), Ф. Штромейер A817)
А. Дюамель-де-Монсо A736), А. Маргграф A758),
М. Клапрот A797), Г.Дэви A807), Л. Гей-Люссак и
Л. ТенарA808)
Г. Сиборг, А. Гиорсо и сотр. A950)
Г. Дэви A808), Р. Бунзен A841-1855)
К. Шееле A769—1771), Д. Пристли A774), А. де-Лавуазье
A775-1777), Г. Дэви A800)
/. Брандт A735), Й. Берцелиус A808)
О. Тахений A666), Й. Берцелиус A823),
А. Сент-Клер-Девилль A854)
У. Рамзай и М. Траверс A898)
У.Рамзай и М. Траверс A898), Л. Полинг A933),
Н. БартлеттA962)
Г. Сиборг, А. Гиорсо и сотр. A944)
К. Мосандер A839), Ф. Мутман A902)
Ю.Арведсон A817), Г.Дэви A818), X. Гмелин A818),
Р. Бунзен A841-1855)
А. Гиорсо и сотр. A961—1971), Г Н. Флёров и сотр. A965-
1971)
Ж. Юрбен A907), К. Ауэр A907)
Г. Дэви A808), А. Бюсси A830), Р. Бунзен A841-1855)
К. Шееле, Т. Бергман и Ю. Ган A774), Р. Бунзен A841-
1855)
- E000-3500 лет до н. э.), Агрикола A550-1556), Васи-
Василий Валентин A599—1602)
Г. Мюнценберг и сотр. A987)
Г. Сиборг, А. Гиорсо и сотр. A955)
358
II. Химические элементы. Атомы
Продолжение табл.
Название
Авторы и дата открытия
Молибден
Мышьяк
Натрий
Неодим
Неон
Нептуний
Никель
Ниобий
Нобелий
Олово
Осмий
Палладий
Платина
Плутоний
Полоний
Празеодим
Прометий
Протактиний
Радий
Радон
резерфордий
Рений
Родий
Ртуть
К. ШеелеA778), П. Ельм A783), А. Муассан A895)
— (IV в. до н. э.), Альберт Великий A250), Парацельс (на-
(начало XVI в.), Г. Брандт A733-1735)
А. Дюамель-де-Монсо A736), А. Маргграф A758),
М. Клапрот A797), Г.Дэви A807), Л. Гей-Люссак и
Л. Тенар A808), Р. Бунзен A841-1855)
К. Ауэр {1885), Ф. Мутман A902)
У Рамзай и М. Траверс A898)
3. Макмиллан и Ф. Эйблсон A940), Г. Сиборг и А.Валь
A942)
A. Кронстедт A751), Т. Бергман A775)
4. Хатчетт A801), Г. Розе A844), К. Блумстрандт A866),
Ж. МариньякA866)
Г. Сиборг, А, Гиорсо и сотр. A957—1958), Г. И. Флёров и
сотр. A957-1965)
— D000 лет до н.э.), Р.Бэкон B-я половина XIII в.),
псевдо-Гебер (ХШ-ХГ/вв.), А. Либавий A597), Э. Кохен
A899)
С. ТеннантA804)
У.ВулластонA803)
— (в Европе с XVIII в.), А.де-Ульоа A738), Ф.Ахард
A779), У. Вулластон A804)
Г. Сиборг, Э. Макмиллан и сотр. A940)
М. Склодовская-Кюри и П. Кюри A898)
К. Ауэр A885), Ф. Мутман A902)
Д. Марински, Л. Гленденин и Ч. Кориелл A945)
О. Тан и Л. Майтнер A913—1918), Ф. Содди и Д. Крэнстон
A918)
М. Склодовская-Кюри, П. Кюри и Ж. Бемон A898),
Э. Демарсе A901), А. Дебьерн A910)
Ф. Дорн A900), Э. Резерфорд и Ф. Содди A902), У. Рамзай
A903)
Г. Н. Флёров, И. Звара и сотр. A969—1970), А. Гиорсо и
сотр. A970)
B. Ноддак и И. Такке-Ноддак A925-1928)
У. Вулластон A804)
— B000 лет до н. э.), Г. Брандт A735)
Р. Бунзен и Г. Кирхгофф A861)
359
II. Химические элементы. Атомы
Продолжение табд
Название
Авторы и дата открытия
Рутений
Самарий
Свинец
Селен
Сера
Серебро
Сиборгий
Скандий
Стронций
Сурьма
Таллий
Тантал
Теллур
Тербий
Технеций
Титан
Торий
Тулий
Углерод
Уран
Фермий
Фосфор
Франций
Фтор
К. К. Клаус A844)
Ф. Лекок-де-Буабодран A879), Э. Демарсе A901), Ф. Мут-
манA902)
— E000—3400 лет до н. э.), Агрикола A550—1556)
Й Берцелиус и Ю. ГанA817)
— E000лет до н.э.), Р.Бэкон B-я половина XIIIв.),
псевдо-Гебер (XIII—XIV вв.), Василий Валентин A599—
1602)
— E000—4500 лет до н. э.), В. Бирингуччо A540), Агрико-
Агрикола A550-1556)
Ю. Ц. Оганесян, Г. Н. Флёров и сотр. A974), А. Гиорсо и
сотр. A974)
Д. И. Менделеев A871), Л. Нильсон A879), П. Клеве A879)
А.Крофорд и У.Крукшанк A787), М. Клапрот A793),
Г. Дэви A808), Р. Бунзен A841-1855)
— C000 лет до н. э.), Парацельс (начало XVI в.), Василий
Валентин A599-1602), Г. Брандт A735)
У. КруксA861), К. Лами A862)
А. Экеберг A802), У. Вулластон A809), Й. Берцелиус
A824)
Ф. Мюллер-фон-Рейхенштейн A782), М. Клапрот A798)
К. Мосандер A843)
Э. Сегре и К. Перрьер A937)
У. Грегор A789-1791), М. Клапрот A795-119%
Й. Берцелиус A825), Ф. Вёлер и А. Сент-Клер-Девилль
A825), Л. Нильсон A887)
Й. Берцелиус A828), Л. Нильсон A883)
П. Клеве A879)
— E0тыс. лет до н.э.), А.де-Лавуазье A775—1777),
С. Теннант и У Вулластон A796)
М Клапрот A789), Э. Пелиго A841), А. Муассан A896)
Г. Сиборг, А. Гиорсо и сотр. A952)
Х.Бранд A669), И.Кункель (середина 1670-х гп)»
Р. Бойль A680), А. Маргграф A750), Ф. Вёлер A829>-
А. Шрёттер A847-1849)
М. Пере A939)
К Шееле A771), А. Ампер A810), А. Муассан A886)
360
II. Химические элементы. Атомы
Окончание табл.
Название
Авторы и дата открытия
Хассий
Хлор
Хром
Цезий
Церий
Цинк
Цирконий
Эйнштейний
Эрбий
Г. Мюнценберг и сотр. A984), Ю. Ц. Оганесян и сотр.
A984)
И. Глаубер A648), К. Шееле A774), К. Бертолле A786—
1789), Г. Дэви A810), Л. Гей-Люссак A811—1813)
Н. Воклен A797), М. Клапрот A797), Р. Бунзен A841—
1855)
Р. Бунзен и Г. Кирхгофф A861), К. Сеттерберг A882)
Й. Берцелиус и В.Хисингер A803), М. Клапрот A803),
К. Мосандер A839)
- E000-3000 лет до н.э.). Василий Валентин A599-
1602), А. Маргграф A754), И. Генкель A721), Г. Брандт
A735)
М. Клапрот A789), Й. Берцелиус A825)
Г. Сиборг, А. Гиорсо и сотр. A952)
К. Мосандер A843), Ж. Мариньяк A878)
7. Происхождение русских и латинских
названий и символов элементов
Приведено происхождение (этимология) русских названий хими-
химических элементов, а также (при несовпадении) их латинских назва-
названий. В скобках после латинских названий даны символы элементов,
они образованы первой и одной из последующих букв этих названий.
Сокращения языков
арабск. — арабский
ассир. — ассирийский
феч. — греческий
исп. — испанский
лат. — латинский
нем. — немецкий
русск. — русский
санскр. — санскритский
(древнеиндийский)
тур. — турецкий
франц. — французский
шведск. — шведский
от — от греч азотикос (безжизненный, а — отрицание и зое —
Жизнь). Лат. Nitrogenium (N) — рождающий селитру, от греч. ни-
Щон (селитра) и генес (род, происхождение).
тиний — от греч. актис (луч); по радиоактивности элемента (распа-
(распадается с а- и Р-излучением). Лат. Actinium (Ac).
361
II. Химические элементы. Атомы
Алюминий — от лат. алуминис (род. падеж лат. алумен — квасцы); ц0
содержанию в квасцах. Лат. Aluminium (A1).
Америций — от Америка (часть света); место работы первооткрыват^
лей. Лат. Americium (Am).
Аргон — от греч. аргос (бездеятельный, инертный); по химической
инертности элемента. Лат. Argon (Аг).
Астат — от греч. астатос (неустойчивый); по радиоактивности эле-
элемента (период полураспада 8,1 ч). Лат. Astatium (At).
Барий — от греч. барис (тяжелый); по большой плотности минерала
барит Лат. Barium (Ba).
Бериллий — от греч. бериллос (зеленый драгоценный камень); по окра-
окраске минерала изумруд. Лат. Beryllium (Be).
Берклий — от Беркли (город в США); место работы первооткрывате-
первооткрывателей. Лат. Berkelium (Bk).
Бор — от лат. боракс (бура, белый минерал), восходит к арабск. боурак
или баврак (белый цвет минеральных веществ). Лат. Borum (В).
Борий — в честь Н. Бора. Лат. Bohrium (Bh).
Бром — от греч. бромос (зловонный); по запаху жидкого брома. Лат.
Bromum (Br).
Ванадий — от шведск. Ванадис (имя древнескандинавской богини
красоты); по красивому цвету соединений. Лат. Vanadium (V).
Висмут — от нем. вайсмуттер (белое вещество); по окраске многих
солей. Лат. Bismuthum (Bi) — от бисмут (латинизированный алхи-
алхимический вариант нем. вайсмуттер).
Водород — перевод с лат. Hydrogenium (H), от греч. хидор (вода) и ге-
нес (род, происхождение).
Вольфрам — от нем. вольф (волк) и рам (взбитые сливки, пена). При
выплавке олова примесь вольфрама дает много шлака и понижает
выход олова; по выражению Агриколы, «вольфрам поедает олово,
как волк овцу». Лат. Wolframium (W).
Гадолиний — в честь Ю. Гадолина. Лат. Gadolinium (Gd).
Галлий — от лат. галлу с (галльский петух, символ Франции); по назва-
названию страны и фамилии первооткрывателя (первая часть
фамилии — Лекок, в переводе с франц. петух). Лат. Gallium (Ga).
Гафний — от лат. Гафниа (древнее название Копенгагена); по месту
работы первооткрывателей. Лат. Hafnium (Hf).
Гелий — от греч. Гелиос (Солнце); по открытию в солнечном спектре-
Лат. Helium (He).
Германий — от Германия (страна); по месту работы первооткрывателя.
Лат. Germanium (Ge).
Гольмий — от лат. Голъмиа (древнее название Стокгольма); по
страны (Швеция), где работал первооткрыватель. Лат. H
(Но).
362
II. Химические элементы. Атомы
Диспрозий — от греч. диспроситос (труднодоступный); по трудности
обнаружения. Лат. Dysprosium (Dy).
Яубний —от Дубна (город в России), место работы первооткрывателей
(группа Г. Н. Флёрова). Лат. Dubnium (Db).
Европий — от Европа (часть света); по месту работы первооткрывате-
первооткрывателя. Лат. Europium (Eu).
Железо —возможно, восходит к санскр. гола (металл, руда). Лат. Fer-
rum (Fe) — от ферро (меч).
Золото —одного корня с русск. желтый; по цвету металла. Лат. Aurum
(Аи) — от аурора (утренняя заря); по блеску металла.
Индий — от исп. индиго (ярко-синяя краска); по характерной линии
в спектре. Лат. Indium (In).
Иод — от греч. иодес (фиолетовый); по цвету парообразного иода. Лат.
Iodum (I).
Иридий — от лат. иридис (радуга); по разнообразию окраски соедине-
соединений. Лат. Iridium (Ir).
Иттербий — от шведск. Иттербю (название селения); по месту обна-
обнаружения минерала гадолинит, содержащего скандий, иттрий, лан-
лантаноиды. Лат. Ytterbium (Yb).
Иттрий — см. Иттербий. Лат. Yttrium (Y).
Кадмий — от греч. Кадмея (древняя крепость города Фивы); по месту
нахождения цинковой руды, содержащей кадмий (смесь минера-
минералов сфалерит и смитсонит). Лат. Cadmium (Cd).
Калий — от арабск. алъ-кали (едкое начало золы морских растений);
по свойствам поташа и едкого кали. Лат. Kalium (К).
Калифорний — от Калифорния (штат США); по месту работы перво-
первооткрывателей. Лат. Californium (Cf).
Кальций — от лат. калцис (род. падеж лат. калкс — камень, известняк);
по содержанию в известняке. Лат. Calcium (Ca).
Кислород — перевод лат. Oxygenium (О), от греч. оксис (кислый, кис-
кислотный) и генес (род, происхождение).
Кобальт — от нем. кобольд (домовой, гном); по трудности переработки
(якобы из-за шалости гномов) руд этого металла. Лат. Cobal-
tum(Co).
Кремний — от русск. кремень (твердый камень для высекания огня,
кремнезём). Лат. Silicium (Si) — от лат. силицис (род. падеж лат.
силекс — кремнезём).
криптон — от греч. криптос (тайный, скрытый); по трудности выделе-
ния из воздуха. Лат. Krypton (Кг).
сенон — от греч. то ксенон (нечто странное); по неожиданному от-
крытию как примеси к криптону. Лат. Xenon (Xe).
рий — в Честь П. Кюри и М. Склодовской-Кюри. Лат. Curium
(C)
363
II. Химические элементы. Атомы
Лантан — от греч. лантано (скрываюсь, прячусь); по трудности
ружения. Лат. Lanthanum (La).
Литий — от греч. литое (камень); по открытию в ничем не примеча-
примечательном, похожем на обычный камень минерале петалит (алюмо-
(алюмосиликат). Лат. Lithium (Li).
Лоуренсий — в честь Э. Лоренса. Лат. Lawrencium (Lr).
Лютеций — от лат. Лутециа (древнее поселение на месте современно-
современного Парижа); по месту работы первооткрывателя. Лат. Lutetium
(Lu).
Магний — от лат. магнесиа алъба (белая магнезия); по минералу гидро-
гидромагнезит, содержащему этот металл и найденному древними гре-
греками около города Магнесиа в Малой Азии (ныне город Маниса
в Турции). Лат. Magnesium (Mg).
Марганец — от греч. манганес (очищающий); по осветляющему дейст-
действию (в процессе варки стекла) минерала пиролюзит Лат. Manga-
num (Mn).
Медь — происхождение русского названия не установлено. Лат. Cu-
Cuprum (Си) — от греч. купрос (название острова Кипр); по месту до-
добычи медных руд.
Мейтнерий — в честь Л. Майтнер. Лат. Meitnerium (Mt).
Менделевий — в честь Д. И. Менделеева. Лат. Mendelevium (Md). - *
Молибден — от греч. молибдос (любой материал, оставляющий черную
черту на бумаге, в частности и минерал молибденит). Лат. Molyb-
daenum (Mo).
Мышьяк — от русск. мышь и яд; по применению препаратов мышьяка
для истребления грызунов. Лат. Arsenicum (As) — от греч. арсеШ-
кон (золотисто-желтый); по цвету содержащего мышьяк минерала
аурипигмент
Натрий — от арабск. натрон, или натрун (моющее средство); по при-
применению природной соды и едкого натра для изготовления мыла.
Лат. Natrium (Na).
Неодим — от греч. неос (новый) и дидимос (близнец); по открытию
вместе с празеодимом. Лат. Neodymium (Nd).
Неон — от греч. то неон (нечто новое); по неожиданной окраске
спектра, удивившей сына одного из первооткрывателей (У. PaW-
зая). Лат. Neon (Ne).
Нептуний — от Нептун (название планеты Солнечной системы); п°
месту в Периодической системе за ураном (как планета Нептун л°
удаленности от Солнца следует за Ураном). Лат. Neptunium (Np)«
Никель — от нем. никкель (сокращение бранного слова рудокопо
никколаус); рабочие в XVIII в. принимали за медную руду красны
минерал никелин («фальшивая медь»), из которого, однако, медь
выплавлялась. Лат. Niccolum (Ni).
364
I. Химические элементы. Атомы
Ниобий — от греч. Ниобея (имя дочери Тантала); по близости свойств
ниобия и тантала (см. Тантал). Лат. Niobium (Nb).
Добелий — в честь А. Нобеля. Лат. Nobelium (No).
Олово — происхождение русского названия не установлено. Лат.
Stannum (Sn) — от лат. стагнанс (стоящий на месте; восходит к
санскр. стагс— твердый, стойкий); по большей твердости этого
металла в сравнении со свинцом.
Осмий — от греч. осме (запах); по своеобразному сильному запаху ле-
летучего высшего оксида. Лат. Osmium (Os).
Палладий — от Паллада (название малой планеты, или астероида,
Солнечной системы); по времени открытия элемента вскоре после
обнаружения этого астероида. Лат. Palladium (Pd).
Платина — исп. платина (серебрецо); пренебрежительное название
металла, похожего по внешнему виду на серебро, но не имеющего
полезных свойств последнего — легкоплавкости и ковкости. Лат.
Platinum (Pt).
Плутоний — от Плутон (название планеты Солнечной системы); по
месту в Периодической системе за нептунием (как планета Плутон
по удаленности от Солнца следует за Нептуном). Лат. Plutonium
(Pu).
Полоний — от лат. Полониа (Польша); по родине одного из первоотк-
первооткрывателей (М. Склодовской-Кюри). Лат. Polonium (Po).
Празеодим — от греч. празинос (цвет зелени лука-порея) и дидимос
(близнец); по цвету соединений в отличие от розовой окраски со-
соединений его спутника — неодима. Лат. Praseodymium (Pr).
Прометий — от греч. Прометеус (Прометей; в древнегреческой мифо-
мифологии титан, похитивший огонь у богов Олимпа и передавший его
людям); по синтезу этого элемента в «огне» ядерного реактора.
Лат. Promethium (Pm).
Протактиний — от греч. о протос (предшествующий в ряду) и назва-
названия элемента актиний (см. Актиний); по расположению в одном из
рядов радиоактивного распада перед актинием. Лат. Protactinium
(Ра).
Радий — от лат. радиус (луч); по радиоактивности элемента (распада-
(распадается с ос-излучением). Лат. Radium (Ra).
Радон — от корня названия элемента радий и суффикса -он (по анало-
аналогии с названиями других элементов VIIIA-группы); по образова-
нию при ос-распаде радия. Дат. Radon (Rn).
Резерфордий — в честь Э. Резерфорда. Лат. Rutherfordium (Rf).
ений — от лат. Ренус (Рейн); по названию главной реки Германии,
гДе работали первооткрыватели. Лат. Rhenium (Re),
одий — от Греч# родон (розовый цвет); по окраске соединений. Лат.
Rhodium (Rh).
365
II. Химические элементы. Атомы
Ртуть — вероятно, тюркского происхождения. Лат. Mercurius — Мер*
курий (в древнеримской мифологии имя бога — покровителя под-
подвижной деятельности человека, торговли и путешествий); по под-
подвижности жидкой ртути; символ Hg — от устаревшего латинского
алхимического названия Hydrargyrum (греч. хидраргирос — жидкое,
как вода, серебро, где хидор — вода и аргирос — серебро); по сереб-
серебристому цвету жидкой ртути.
Рубидий — от лат. рубидус (красно-коричневый цвет); по характерным
линиям в спектре. Лат. Rubidium (Rb).
Рутений — от лат. Рутениа (Россия); по названию родины первоотк-
первооткрывателя. Лат. Ruthenium (Ru).
Самарий — от самарскит (минерал, в котором был открыт этот эле-
элемент; сам минерал назван в честь русского геолога В. Е. Самар-
Самарского-Быховца, обнаружившего его на Урале). Лат. Samarium (Sm).
Свинец —происхождение русского названия не установлена Лат.
Plumbum (Pb) — от лат. плумбум (у древних римлян названия спла-
сплавов свинца с оловом; плумбум нигрум — черный свинец, т. е. сплав,
содержащий больше свинца, и плумбум альбум— белый свинец,
т. е. сплав, содержащий больше олова).
Селен —от греч. Селене (Луна); по сопутствованию селена теллуру в
его рудах (как Луна — спутник Земли; см. Теллур). Лат. Selenium
(Se).
Сера — от санскр. сира (светло-желтый); по цвету природной серы.
Лат. Sulfur (S) — от санскр. сулвери (горючий порошок); по горю-
горючести серы.
Серебро — возможно, от ассир. сарпу (светлый); по цвету металла.
Лат. Argentum (Ag) — от греч. аргос (белый, восходит к санскр.
арганта — светлый).
Сиборгий — в честь Г. Сиборга. Лат. Seaborgium (Sg).
Скандий —от лат. Скандиа (полуостров Скандинавия); по месту рабо-
работы первооткрывателя. Лат. Scandium (Sc).
Стронций — от англ. Строншиан (название деревни в шотландском
графстве Аргайлл); по месту обнаружения минерала, содержащего
стронций — стронцианита. Лат. Strontium (Sr).
Сурьма — от тур. сюрме (черная краска для бровей и ресниц); по при*
менению на Древнем Востоке минерала стибнит в косметике. Лат.
Stibium (Sb) — от греч. стиби (черная метка). Устаревшее латин-
латинское название Antimonium — от антимоний (алхимическое назва-
название минерала стибнит).
Таллий — от греч. таллос (ярко-зеленый цвет стеблей травянистых
растений); по характерной линии такого цвета в спектре. Лат-
Thallium (T1).
366
II. Химические элементы. Атомы
Тантал — от греч. Танталос (имя героя древнегреческой мифологии);
по словам первооткрывателя, «как Тантал испытывал муки жажды,
стоя по горло в воде, так оксид данного элемента не способен ре-
реагировать с избытком распространенных кислот». Лат. Tantalum
(Та).
Теллур — от лат. теллурис (род. падеж лат. теллус— мать-земля); по
открытию элемента в золотоносной «земле» (смеси соединений зо-
золота и серебра с теллуром). Лат. Tellurium (Те).
Тербий — см. Иттербий. Лат. Terbium (Tb).
Технеций — от греч. текнетос (искусственный); по впервые прове-
проведенному в лаборатории синтезу химического элемента, отсутст-
отсутствующего в природе. Лат. Technetium (Тс).
Титан — от греч. Титанес (Титаны в древнегреческой мифологии —
боги, отличавшиеся гордым и стойким нравом); по химической ус-
устойчивости минерала рутил. Лат. Titanium (Ti).
Торий — от шведск. торйорд (камень, горная порода; восходит к име-
имени Тор, в древнескандинавской мифологии — бог грома и бури,
изображавшийся с каменным молотом); по открытию элемента
в обычном камне — минерале торит. Лат. Thorium (Th).
Тулий — от греч. Туле (древнее название Северо-Западного побережья
Скандинавии); по месту нахождения минералов, содержащих ту-
тулий. Лат. Thulium (Tm).
Углерод — от русск. рождающий уголь. Лат. Carboneum (С) — от карбо-
нис (род. падеж лат. карбо — древесный уголь, восходит к санскр.
кра — гореть).
Уран — от названия планеты Солнечной системы; по времени откры-
открытия элемента (вскоре после обнаружения планеты Уран). Лат. Ura-
Uranium (U).
Фермий — в честь Э. Ферми. Лат. Fermium (Fm).
Фосфор — от греч. фосфорос (светящийся в темноте, фос — свет и
форос — несущий); по свечению белого фосфора. Лат. Phosphorus
(Р).
Франций — от франц. Франс (Франция); по месту работы первооткры-
первооткрывателя. Лат. Francium (Fr).
Фтор — от греч. фторос (разрушающий); по разъедающему действию
фтора на стекло. Лат. Fluorum (F) — от флуор (текучесть); по ис-
использованию в металлургии минерала флюорит в качестве плавня
(флюса), понижающего температуру плавки.
Кассий — от лат. Хассиа (древнегерманская страна на территории сов-
современной земли Гессен в Германии). Лат. Hassium (Hs).
— от Греч клорос (желто-зеленый цвет увядающей листвы); по
окраске газообразного хлора. Лат. Chlorum (C1).
367
II. Химические элементы. Атомы
Хром — от греч. крома (цвет, краска); по яркой разнообразной окра,
ске соединений. Лат. Chromium (Cr).
Цезий —от лат. цесиус (серо-синий или голубой цвет неба); по окраске"
характерных линий в спектре. Лат. Caesium (Cs).
Церий — от Церера (малая планета, или астероид, Солнечной систе-
системы); по открытию элемента вскоре после обнаружения этого асте-
астероида. Лат. Cerium (Се).
Цинк —нем. цинк (белый металл, восходит к арабск. харасин — металл
из Китая); по месту выработки металла, завезенного в средние века
в Европу. Лат. Zincum (Zn).
Цирконий — от циркон (название минерала, от арабск. заркун — золо-
золотисто-желтый цвет); по окраске драгоценных разновидностей это-
этого минерала. Лат. Zirconium (Zr).
Эйнштейний — в честь А. Эйнштейна. Лат. Einsteinium (Es).
Эрбий — см. Иттербий. Лат. Erbium (Er).
8. Названия элементов на английском,
французском, немецком и испанском
языках
Сокращения грамматических родов: /— женский, т — мужской,
п — средний.
Символ
Ас
Ag
А1
Am
Ar
As
At
Au
В
Ba
Be
Bh
Bi
Bk
Br
Английское, французское, немецкое и испанское названия
actinium, actinium m, Aktinium я, actinio m
silver, argent m, Silber n, plata/
alumin(i)um, aluminium m, Aluminium n, aluminio m
americium, arrmricium m, Amerizium n, americio m
argon, argon m, Argon n, argyn m
arsenic, arsenic m, Arsen n, arsMnico m
astatine, astate m, Astat я, astato m
gold, or m, Gold я, ого т
boron, bore m, Bor я, boro m
barium, baryum m, Barium я, bario m
beryllium, ЬйгуИшт т, Beryllium n, berilio m
bohrium, bohrium aw, Bohrium n, borio m
bismuth, bismuth m, Wismut n, bismuto m
berkelium, ЬегкйНит т, Berkelium n, berquelio m
bromine, brome m, Brom n, bromo m
368
I. Химические элементы. Атомы
Продолжение табл.
Английское, французское, немецкое и испанское названия
carbon, carbone m, Kohlenstoff m, carbono m
calcium, calcium m, Kalzium n, calcio m
cadmium, cadmium m, Kadmium я, cadmio m
cerium, cerium m, Zer я, cerio m
californium, californium aw, Kalifornium я, californio m
chlorine, chlore m, Chlor я, cloro m
curium, curium m, Curium я, curio m
cobalt, cobalt m, Kobalt я, cobalto m
chromium, chrome m, Chrom я, cromo m
caesium, cesium m, Zasium я, cesio m
copper, cuivre m, Kupfer n, cobre m
deuterium, deuterium m, Deuterium «, deuterio m
dubnium, doubnium m, Dubnium n, dubnio m
dysprosium, dysprosium m, Dysprosium n, disprosio m
erbium, erbium m, Erbium n, erbio m
einsteinium, einsteinium m, Einsteinium n, einsteinio m
europium, europium m, Europium n, europio m
fluorine, fluor m, Fluor n, fluor m
iron, fer m, Eisen и, hierro m
fermium, fermium m, Fermium n, fermio m
francium, francium n, Franzium n, francio m
gallium, gallium tn, Gallium я, galio m
gadolinium, gadolinium m, Gadolinium я, gadolinio m
germanium, germanium m, Germanium n, germanio m
hydrogen, hydrogene m, Wasserstoff m, hidrogeno m
helium, helium /w, Helium n, helio m
hafnium, hafnium m, Hafnium я, hafnio m
mercury, mercure m9 Quecksilber n, mercurio m
holmium, holmium m9 Holmium n, holmio m
hassium, hassium m, Hassium n, hasio m
iodine, iode m, Jod n, yodo m
indium, indium m, Indium n, indio m
iridium, iridium m, Iridium n, iridio m
potassium, potassium m, Kalium n, potasio m
krypton, krypton m, Krypton n, cripton m
lanthanum, lanthane m, Lanthan n, lantano m
lithium, lithium m, Lithium n, litio m
lawrencium, lawrencium m, Lawrencium n, lawrencio m
lutetium, lutecium /w, Lutetium n, lutecio m
369
II. Химические элементы. Атомы
Продолжение табЛ
Символ
Английское, французское, немецкое и испанское названия
mendelevium, mendelevium aw, Mendelevium w, mendelevio m
magnesium, magnesium аи, Magnesium w, magnesio m
manganese, manganese аи, Mangan n, manganeso m
molybdenum, molybdene аи, Molybdan n, molibdeno m
meitnerium, meitnerium аи, Meitnerium w, meitnerio m
nitrigen, azote аи, Stickstoff аи, nitrogeno m
sodium, sodium aw, Natrium w, sodio m
niobium, niobium aw, Niob w, niobio m
neodymium, neodyme aw, Neodym «, neodimio m
neon, neon m, Neon n, neon m
nickel, nickel m, Nickel n, niquel m
nobelium, nobelium m, Nobelium n, nobelio m
neptunium, neptunium m, Neptunium л, neptunio m
oxygen, oxygene m, Sauerstoff m, oxigeno m
osmium, osmium m, Osmium n, osmio m
phosphorus, phosphore m, Phosphor m, fosforo m
protactinium, protactinium m, Protaktinium n, protactinio m
lead, plomb m, Blei n, plomo m
palladium, palladium m, Palladium я, paladio m
promethium, promethium m, Promethium n, prometio m
polonium, polonium аи, Polonium n, polonio m
praseodymium, praseodyme m, Praseodym n, praseodimio m
platinum, platine аи, Platin A2, platino m
plutonium, plutonium m, Plutonium at, plutonio m
radium, radium m, Radium n, radio m
rubidium, rubidium аи, Rubidium и, rubidio аи
rhenium, rhenium аи, Rhenium и, renio аи
rutherfordium, rutherfordium аи, Rutherfordium An,ruterfordio аи
rhodium, rhodium аи, Rhodium и, radio аи
radon, radon aw, Radon n, radon aw
ruthenium, ruthenium aw, Ruthenium w, rutenio aw
sulfur, soufre aw, Schwefel aw, azufre aw
antimony, antimoine aw, Antimon n, antimonio aw
scandium, scandium аи, Skandium w, escandio аи
selenium, selenium аи, Selen w, selenio аи
seaborgium, seaborgium аи, Seaborgium w, seaborgio аи
silicon, silicium аи, Silizium w, silicio аи
samarium, samarium aw, Samarium aj, samario aw
370
II. Химические элементы. Атомы
Окончание табл.
Символ
.
Sn
Sr
Т
Та
ТЬ
Тс
Те
Th
Ъ
Т1
Тт
U
V
W
Хе
Y
Yb
Zn
Zr
Английское, французское, немецкое и испанское названия
tin, etain m, Zinn n, estano m
strontium, strontium m, Strontium n, estroncio m
tritium, tritium /и, Tritium и, tritio m
tantalum, tantale m, Tantal «, tantalio m
terbium, terbium m, Terbium n, terbio m
technetium, technetium m, Technetium n, tecnecio m
tellurium, tellure m, Tellur «, telurio m
thorium, thorium m, Thorium n, torio m
titanium, titane m, Titan и, titanio m
thallium, thallium m, Thallium n, talio m
thulium, thulium m, Thulium n, tulio m
uranium, uranium m, Uran n, uranio m
vanadium, vanadium /w, Vanadin n, vanadio m
tungsten, tungstene /w, Wolfram n, tungsteno m
xenon, xenon m, Xenon n, xenon m
yttrium, yttrium m, Yttrium n, itrio m
ytterbium, ytterbium m, Ytterbium я, iterbio m
zinc, zinc m, Zink я, cine m
zirconium, zirconium m, Zirkonium n, circonio m
Молекулы. Ионы
Радикалы
1. Энергия ионизации
Приведены значения энергии ионизации (энтальпии отрыва элект-
электрона, или положительной ионизации, /) для молекул и радикалов.
Вещество
AgF
As2
As4
AsCl3
AsH3
At2
BBr3
BC13
BF3
B2H6
B4Hl0
B5H9
B6Hl0
B10H14
BI3
B2O3
B(OHK
BaCl2
Bal2
BaO
BeF2
/, эВ
11,40
11,00
9,90
11,70
10,06
8,30
10,72
11,60
15,55
11,41
10,40
10,10
9,50
10,70
9,40
14,00
13,50
9,20
8,10
6,97
14,70
Вещество
BeO
Br2
BrF
BrF3
CBr4
CC14
CF4
CH2
CH3
CH4
C2H2
C2H4
с6н6
CH3C(H)O
CH3CN
CH3COOH
CHC13
C5H5N
CH3OH
C2H5OH
CN
/, эВ
10,10
10,53
11,80
12,90
11,00
11,47
15,56
10,40
9,84
12,71
11,41
10,51
9,25
10,22
12,12
10,37
11,35
9,30
10,85
10,47
14,20
Вещество
C2N2
(CN)Br
(CN)C1
(CN)F
(CN)I
CO
co2
cs
cs2
cso
CaCl2
CaO
CeO2
Cl2
C1F
CIO
C1O2
СЮ3
CIO3F
CoO
[Co(COL]
/,эВ
13,37
11,84
12,34
13,32
10,87
14,01
13,79
11,10
10,07
11,18
10,30
6,50
9,50
11,48
12,70
10,40
11,10
11,70
13,60
9,00
8,30
372
I. Молекулы. Ионы. Радикалы
Продолжение табл.
Вещество
[Со2(СО)8]
[Сг(СОN]
CrF2
CrF3
СгО
СгО2
СЮ3
Cs2
CsBr
Csl
Cs2O
CsOH
CuF2
D2
DF
F2
FeBr2
[Fe(C5H5J]
[Fe(COM]
FeCl2
FeF2
FeF3
Ga(O)F
GeBr4
GeCl4
GeH4
Ge2H6
СезН8
H2
HBr
/, эВ
8,20
8,14
10,10
12,20
8,40
10,30
11,60
3,80
7,72
7,25
4,45
7,21
11,30
15,47
16,03
15,69
10,70
6,74
7,95
11,50
11,30
12,50
9,50
10,75
12,12
10,50
10,00
9,60
15,43
11,62
Вещество
HCN
HCOOH
HC1
HF
HI
HN3
HNCO
HNCS
HNO3
HO2
H2O
H2O2
HOF
HS
H2S
H2S2
H2Se
H2Te
HgBr2
HgCl2
Hgl2
h
IBr
IC1
IF
K2
KI
Li2
/,эВ
13,73
11,05
12,74
15,92
10,38
10,74
11,60
10,05
11,03
11,53
12,61
10,90
12,70
10,40
10,47
10,20
9,88
9,14
10,62
11,37
9,50
9,28
9,98
10,31
10,50
9,70
13,50
3,60
8,20
5,15
Вещество
LiBr
LiCl
LiF
LiH
Lil
Li2O
MgBr2
MgCl2
MgF2
Mgl2
[Mn2(COI0]
MnF2
[Mo(CON]
MoO2
MOO3
N2
ND3
NF3
N2F4
NH2
NH3
N2H4
NO
NO2
N2O
Na2
NaCl
Nal
[Ni(COL]
NiCl2
/,эВ
9,40
10,10
11,30
7,85
8,60
6,80
10,65
11,60
13,50
9,57
8,50
11,50
8,23
9,40
12,00
15,58
10,37
13,20
12,00
11,40
10,15
8,74
9,27
9,78
12,89
4,90
8,92
7,64
8,28
11,20
373
I. Молекулы. Ионы. Радикалы
Окончание
Вещество
NiF2
NiO
О2
О3
OF2
ОН
OsO2
OsO3
OsO4
Р4
РС13О
PF3
РН3
р2н4
РЬВг2
РЬС12
PbF2
PbF4
PbO
PbS
PbTe
PdO
PrO2
Rb2
Rbl
RuO2
RuO4
/, эВ
11,50
9,50
12,08
12,52
13,70
13,18
12,20
11,40
12,30
10,80
13,10
9,71
9,98
10,60
10,20
10,30
11,60
10,40
9,00
8,60
8,20
9,10
9,60
3,45
8,00
10,60
12,80
Вещество
s2
SF6
so2
SO2F2
Sb2
Sb4
SbCl3
SbH3
Se2
SeO2
SeO3
SiBr4
SiC
SiCl4
SiF4
SiH4
SiO2
SnBr2
SnBr4
SnCl2
SnCl4
SnF2
SnH4
SnO
SnS
SnSe
/,эВ
9,36
9,43
16,15
12,34
13,30
9,00
8,40
11,00
9,58
8,88
11,50
11,60
10,80
9,20
11,64
15,40
11,40
11,70
10,00
11,00
10,20
12,10
11,50
9,20
10,50
9,70
9,70
Вещество
SnTe
SrCl2
SrO
T2
Te2
TeO2
TiBr4
TiCl4
TiO
TiO2
TIBr
T1C1
T1F
Til
UF6
uo2
uo3
VC13
[W(CON]
wo3
XeF2
XeF4
XeF6
ZnBr2
ZnCl2
ZrO2
9,10
9,70
6,10
15,49
8,29
11,00
10,56
11,70
6,80
10,00
9,14
9,70
10,50
8,47
14,14
5,50
10,40
12,80
8,24
11,70
12,35
12,65
12,19
10,40
11,70
8,00
-—
2. Сродство к электрону
Приведены значения сродства к электрону (энтальпии присоеД»
нения электрона, или отрицательной ионизации, Ае) для молекул
радикалов.
374
II. Молекулы. Ионы. Радикалы
вещество
-—
BF3
BF4
BaO
BaS
BaSe
BaTe
Br2
BrO3
CBr4
CC14
CH2
CH3
C2H4
с6н6
CHClJ
CN
(CN)I
CO2
cs
cs2
ci2
CIO
cio2
cio3
[Cr(COM]
Cro3
CsCl
Cs2o2
F2
-—
4е,эВ
-2,65
< -3,40
-0,57
-0,84
-0,95
-1,43
-2,51
-3,22
-2,06
-2,12
+0,95
-1,08
+1,81
+1,10
-1,76
-3,82
-0,90
>0,00
< —1,46
-1,13
-2,38
-2,20
-3,43
-2,83
-1,20
-4,04
<-l,40
+6,65
-3,08
Вещество
[Fe(COL]
GeBr4
GeCl4
H2
HCN
HCrO4
HNO3
HO2
H2O
HS
HSe
h
IBr
IC1
IO3
KC1
KF
K2O2
LiCl
LiF
Lil
[Mo(COM]
MoOj
N2
NCO
NCS
NCSe
NH2
NO
Ае,эВ
-1,20
-1,60
-0,87
+3,58
< -1,00
-2,40
-2,00
-3,04
-1,78
-2,32
-2,21
-2,58
-2,70
-1,70
-5,50
< -1,27
< -1,26
+6,3
< —1,28
<-l,35
< —1,12
-1,80
-2,59
>2,80
-1,56
-2,17
-2,64
-0,74
-0,02
Вещество
NO2
NO3
N2O
NaCl
NaF
Na2O2
O2
O3
OH
PbCl2
PtF6
Rb2O2
ReO4
S2
s8
SF4
so2
Se2
SeF4
SeO2
SiBr4
SiCl4
SnBr4
SnCl4
TiCl4
UF6
VCI3O
WF4
Де,эВ
-2,50
-3,90
-0,70
< —1,19
< —1,35
+6,15
-0,44
-1,99
-1,83
< -3,20
< -6,77
+6,47
< -2,40
< -2,00
<0,00
-1,20
-1,48
-1,20
<0,00
-1,70
= -2,30
-0,13
0,30
-1,92
-1,57
-1,57
-2,91
-2,03
< -2,30
375
III. Молекулы. Ионы. Радикалы
3. Сродство к протону
Приведены значения сродства к протону (энтальпии присоедине-
присоединения протона Ар) для молекул и радикалов.
Вещество
AsH3
В4Н10
в5н9
В6Н10
CF4
сн2
сн3
сн4
с2н2
ОД
с6н6
СН3С(Н)О
CH3CN
сн3соон
сн3он
с2н5он
^р.эВ
-7,50
-6,20
-7,24
-8,46
-5,20
-8,65
-5,43
-5,30
-6,55
-6,90
-5,63
-8,04
-8,10
-8,16
-7,80
-8,40
Вещество
СО
со2
CsOH
GeH4
н2
НВг
HCN
НСООН
НС1
HF
HI
HNO3
НО2
н2о
HS
H2S
^эВ
-6,21
-4,70
-11,65
-6,04
-4,40
-6,10
-7,40
-7,80
-6,10
-6,85
-6,30
-7,30
-6,40
-7,14
-7,20
-7,40
Вещество
H2Se
КОН
UOH
N2
NCS
NF3
NH2
NH3
NO
NO2
N2O
NaOH
O2
OH
PH3
SiH4
Др,эВ
-7,40
-11,40
-10,40
-5,20
-6,50
-6,60
-8,00
-9,00
> -5,55
-6,60
-5,80 "
-10,70
-4,17
-6,20
-8,07
> -6,35
4. Дипольные моменты
Приведены постоянные дипольные моменты (Д, в дебаях, Д) для
молекул и радикалов. Вещества, у молекул которых дипольные мо-
моменты равны нулю, перечислены в конце таблицы.
Вещество
AsBr3
AsCl3
AsF3
AsH3
Asl3
B4H10
B5H9
B10H14
Р.Д
2,90
1,97
2,82
0,18
1,83
0,56
2,16
3,52
Вещество
B2O3
BaO
BaS
BrCl
BrF
BrF3
BrF5
CC12O
Д.Д
2,50
7,96
10,90
0,57
1,29
1,19
1,51
1,18
Вещество
CH3C(H)O
CH3COOH
CHC13
CH3OH
C2H5OH
(CN)Br
(CN)C1
(CN)F
M
2,69
1,70
1,06
1,71
1,68
2,94
2,80
1,68
--
376
I. Молекулы. Ионы. Радикалы
Окончание табл.
Вещество
(CN)I
со
C(O)F2
CS
C(S)C12
C(S)O
C(Se)O
C(Te)S
C1F
C12F6
C1O2
C12O
C12O7
C1(O)F3
C1O3F
CrCl2O2
CsCl
CsF
Csl
DBr
DC1
Dl
D2O
HBr
HCN
H2CN2
HCNO
HCOOH
H2CS3
HC1
HF
HI
HN3
HNCS
hno3
H2O
H,O2
д,д
3,71
0,11
0,95
0,82
0,28
0,71
0,75
0,17
0,65
0,55
0,78
1,69
0,72
0,02
0,02
0,47
10,42
7,88
12,1
0,83
1,12
0,45
1,87
0,79
2,96
4,24
3,06
1,35
2,13
1,08
1,91
0,42
0,85
1,72
2,16
1,86
2,26
0,93
1,17
Вещество
H2Se
IBr
IC1
IF5
KBr
KC1
KF
KI
LiBr
LiF
LiH
Lil
ND3
NF3
N2F4
NH3
N2H4
NO
NO2
N2O
N2°5
(NO)Br
(NO)C1
(NO2)C1
(NO)F
N(O)F3
(NO2)F
NaCl
Nal
°3
OF2
OH
PBr3
PC13
PC12F3
PC14F
PC13O
PF3
PH3
д,д
0,24
1,21
0,65
2,28
10,41
11,05
7,33
9,20
6,20
6,60
5,88
6,25
1,50
0,24
0,26
1,46
1,83
0,16
0,32
0,17
1,39
1,87
1,83
0,53
1,81
0,04
0,47
10,00
8,50
0,53
0,30
1,65
0,61
0,78
0,68
0,21
2,39
1,03
0,58
Вещество
(PH)F2
PI3
P2I4
PI3O
PN
P(O)F3
P(S)C13
P(S)F3
RbBr
RbF
SBr2O
S2C12
S(C1)F5
SC12O
SCLO,
2 2
SF
SF4
ъ2ь2
С XT
S4N4
so2
S2O
S(O)F2
SO2F2
SbBr3
SbCl3
SbH3
Sbl3
Se2Cl2
SeCl2O
SeF4
SeO2
Se(O)F2
SiF2
TaCl5
TeCl4
T1C1
T1C13
T1F
д,д
1,32
0,34
0,45
1,69
2,75
1,77
1,41
0,63
10,00
8,80
1,47
0,92
1,58
1,44
1,80
1,05
0^63
1,45
1,'б7
1,47
1,62
1,11
3,28
3,93
0,12
0,40
2,10
2,62
1,78
2,70
2,84
1,23
1,20
2,57
4,44
3,93
7,60
377
II. Молекулы. Ионы. Радикалы
Молекулы с нулевым дипольным моментом
А12
А1Вг3
А1С13
A1F3
А113
As2
As4
As4O6
ВВг3
BC13
BF3
В2Н6
B3H6N3
BI3
В(ОНK
BeBr2
ВеС12
BeF2
Bel2
Br2
СВг4
СС14
CD4
CF4
сн4
С2Н2
С2Н4
с6н6
С14
C2N2
со2
cs2
CSe2
Cl2
D2
F2
GaBr3
GaCl3
GaF3
Gal3
GeBr4
GeCl4
GeF4
GeH4
Ge2H6
Gel4
GeO2
H2
HgBr2
HgCl2
Hgl2
h
InBr3
InCl3
InF3
Inl3
N2
N2O4
O2
P2
P4
PBr5
PC15
PF5
p4o6
P4O10
PbCl4
s2
SF6
S2F10
so3
Sb2
Sb4
SbCl5
Se2
SeF6
SeO3
SiBr4
SiCl4
SiF4
SiH4
Si2H6
Sil4
SiO2
SnBr4
SnCl4
SnF4
SnH4
Snl4
Te2
TeF6
TiBr4
TiCl4
Til4
XeF2
XeF4
5. Энергия и длина связи
для двухатомных частиц
Приведены значения энергии атомизации (энергии разрыва свя-
связи Есв), которые отвечают стандартной энтальпии при 298,15 К для
реакций диссоциации молекул и радикалов на нейтральные атомы
(в случае ионов — на нейтральные и заряженные атомы, например,
Аг 2 = Аг + Аг+), а также значения длины связей (/св), соответствую-
соответствующие межъядерным расстояниям. Все вещества считаются идеальными
газами, частицы которых (молекулы, радикалы, ионы) находятся в
невозбужденных электронных состояниях. Прочерк означает отсутст-
отсутствие данных.
Вещество
Ag2
AgBr
AgCl
AgF
Agl
Al2
Есв, кДж/моль
164
184
292
313
359
234
175
/св, пм
268
—
239
228
198
255
247
Вещество
AlBr
A1C1
A1F
All
A1N
A1P
ArJ
Есв, кДж/моль
430
503
675
372
359
217
138
ЧвТпм
229
213
165
254
179
450
378
I. Молекулы. Ионы. Радикалы
Продолжение табл.
Вещество
ArF+
As,
4
AsH
At2
At*
Au2
B2
BBr
BC1
BF
BH
BI
BN
BO
BP
BaBr
BaCl
BaF
Bal
BaO
BaS
BeBr
BeCl
BeF
BeO
BeS
Bi2
Br;
Br2
?'
BrCl
BrF
C2
4
CBr
cci
pp.
Есв> кДж/моль
297
385
267
267
121
234
230
280
434
548
757
338
380
389
807
347
372
448
589
275
565
396
381
389
569
448
380
200
86
194
320
219
233
786
605
531
364
397
339
'ев' ПМ
—
210
—
153
—
—
247
159
188
172
125
123
214
128
120
—
—
268
216
320
194
251
195
180
136
133
174
266
—
228
—
214
176
127
134
146
182
164
112
Вещество
CF
CH
CI
CN"
CN
CN+
CO
co+
cs
cs+
CSe
CaBr
CaCl
CaF
Cal
CaO
CaS
CdBr
CdCl
Cdl
CdS
Ce2
CeF
CeO
ci-
Cl2
C1+
C1F
C1N
CIO
Co2
CoBr
CoCl
CoF
Col
CoO
CoS
Cr2
CrBr
Есв, кДж/моль
545
339
284
1004
762
477
1076
811
714
631
581
322
397
535
285
423
338
157
206
136
< 197
242
582
794
124
243
392
251
259
269
171
329
397
435
284
369
343
154
331
/св, пм
127
112
—
Ill
117
129
113
112
154
—
168
281
244
193
288
182
232
—
—
—
—
306
—
181
199
189
163
161
157
—
—
209
165
—
234
—
379
I. Молекулы. Ионы. Радикалы
Продолжение тщ
Вещество
CrCl
CrF
Crl
CrO
CrS
Cs2
Cs+
CsBr
CsCl
CsF
CsH
Csl
CsO
Cu2
CuBr
CuCl
CuF
Cul
CuO
CuS
CuSe
CuTe
D2
DBr
DC1
DF
DI
DS
Dy2
DyF
Er2
ErF
Eu2
EuF
EuO
EuS
F2
F2
Есв, кДж/моль
367
443
288
457
338
42
50
395
443
514
176
336
296
200
329
382
431
291
267
284
271
192
440
367
433
572
299
354
71
527
75
565
51
523
468
326
121
159
323
/св, пм
—
—
—
163
—
430
470
307
291
235
249
332
—
222
217
205
174
234
173
205
211
235
74
141
128
92
161
134
—
—
—
370
233
141
133
Вещество
Fe2
FeBr
FeCl
FeO
FeS
FrBr
FrCl
FrF
FrI
Ga2
GaAs
GaCl
Gal
GaN
GaP
GaSb
GdF
Ge2
GeH
GeO
GeS
GeSe
GeTe
1H2
H2
1H2
HBr
HC1
HD
HF
HI
HS"
HS
HS+
HSe"
HSe
HT
HTe
He+
Есв, кДж/моль
104
247
350
411
338
380
430
506
322
138
213
476
362
523
230
189
590
277
313
657
551
490
405
-18
436
260
366
432
439
566
298
364
349
359
313
313
442
-238
234
'ев'ИМ
—.
209
163
314
297
239
338
208
220
257
168
201
231
—i
244
159
163
201
214
234
—
74
108
141
128
74
92
161
135
134
138
—
148
74
170
108
380
I. Молекулы. Ионы. Радикалы
Продолжение табл.
веЩество
.-——
ню
HgBr
HgCl
HgF
Hgl
HgO
HgS
HgSe
HgTe
Ho2
HoF
j-
\]
IBr
IC1
IF
IN
In2
InBr
InCl
InF
Inl
IrO
K-,
v'+
K2
KBr
KC1
KF
KH
Kl
КО
KrF+
LaBr
LaCl
Есв, кДж/моль
142
774
87
71
99
129
36
<272
<205
< 166
< 142
83
547
106
153
254
179
212
281
169
104
387
430
523
336
355
57
92
382
425
497
182
325
280
100
188
246
406
464
/св, пм
172
—
—
233
200
249
184
—
—
—
304
194
—
267
—
247
232
191
254
240
—
275
173
392
418
282
267
217
224
305
—
—
175
—
263
247
Вещество
LaF
Lai
Li"
Li2+
Ll2
LiBr
LiCl
LiF
LiH
Lil
LiO
Lu2
LuF
MgBr
MgCl
MgF
MgO
MgS
MnBr
MnCl
MnF
Mnl
MnO
MnS
MoO
N2
N2
N2
ND
NF
NH
NO-
NO
NO+
NS"
NS
NS+
Na2
Na2
Есв> кДж/моль
600
326
92
102
125
423
477
577
235
353
343
142
569
297
318
464
413
309
312
359
447
283
406
292
503
598
945
846
318
297
313
506
632
1051
389
464
506
73
98
/св, пм
203
288
—
267
314
217
202
156
159
239
239
—
192
236
220
175
175
214
—
—
—
—
183
—
110
112
—
132
104
—
115
106
150
144
308
343
381
II. Молекулы. Ионы. Радикалы
Продолжение тобл
Вещество
NaBr
NaCl
NaF
NaH
Nal
NaO
NbO
Nd2
NdF
Ne+ '
NeH+
Ni2
NiBr
NiCl
NiF
Nil
NiO
NiS
ОГ
°2
°2
0\
OD
OF
OH-
OH
OH+
ОТ
P2
P2
PCI
PF
PH
PN
PO
PS
Pb2
PbBr
PbCl
PbF
Есв, кДж/моль
370
411
480
200
290
255
773
< 167
573
71
204
234
360
372
435
292
349
359
—
397
498
646
435
220
463
428
468
437
489
430
289
464
343
731
-544
-335
100
240
300
355
/св, пм
250
236
193
189
271
205
169
311
—
—
—
—
—
214
—
—
—
—
150
134
121
112
97
162
96
97
103
97
189
199
204
159
143
149
«150
186
308
255
218
200
Вещество
Pbl
PbO
PbS
PbSe
PbTe
Pd2
PdO
PmF
Po2
Pr2
PrF
PrO
PtO
PuF
Rb2
Rb+
RbBr
RbCl
RbF
RbH
Rbl
RbO
RuO
S2
S2
S2
SCI
SF
SO
Sb2
Sb+
Sc2
ScBr
ScCl
ScF
Scl
Se2
Se2
Se+
SeO
Есв, кДж/моль
195
372
341
302
245
74
284
540
186
129
580
753
359
540
49
75
387
429
505
165
337
254
490
348
426
522
267
360
522
323
267
113
441
493
599
400
301
309
416
• 423
'ев' ПМ
280
192
229
240
260
257
—
—
—
—
196
173
—
410
444
295
279
227
237
318
—
170
—
189
183
—
161
148
221
—
—
238
223
179
261
—
217
—
165
-
382
II. Молекулы. Ионы. Радикалы
Окончание табл.
~- '"
Вещество
.
Si,
лг
Sit
SiC
SiCl
SiF
SiH
SiO
Sm2
SmF
SmO
SmS
Sn2
SnBr
SnCl
SnF
SnI
SnO
SnS
SnSe
SnTe
SrBr
SrCl
SrF
Sri
SrO
SrS
SrSe
T2
TS
TaF
Tb2
TbF
?2
?2
TeO
?2
h
TiBr
TiCl
TiF
---
ECB> кДж/моль
311
380
439
456
540
302
800
54
536
619
389
196
337
413
472
232
531
465
400
316
331
401
542
263
431
313
247
443
356
603
146
561
263
334
391
288
129
438
494
570
/св> пм
225
—
170
206
160
152
151
—
—
—
—
—
248
229
194
270
183
221
233
252
—
254
208
303
192
244
—
74
—
—
306
—
256
183
330
265
250
230
195
Вещество
Til
TiO
Tl2
TIBr
T1C1
TIF
Til
Tm2
TmF
u2
UF
UO
V2
VBr
VC1
vo
WC1
WF
WO
Xe+
XeF+
Y2
YBr
YC1
YF
YI
YbF
ZnBr
ZnCl
ZnF
Znl
ZnO
ZnS
ZnSe
ZnTe
ZrBr
ZrCl
ZrF
Zrl
ZrO
Есв, кДж/моль
309
666
62
332
371
445
280
54
569
221
724
757
242
439
477
612
421
548
678
100
—
159
483
527
600
433
570
141
225
367
136
272
201
134
96
418
523
623
359
758
'св. ПМ
280
162
—
262
249
208
281
—
—
300
—
—
245
—
—
159
—
183
181
—
184
—
—
241
193
202
—
—
—
—
—
—
—
—
247
230
190
290
171
383
III. Молекулы. Ионы. Радикалы
6. Энергия связи для многоатомных частиц
Приведены значения энергии разрыва связи (Есв) в многоатомн^
молекулах и радикалах, полученные усреднением значений энерп^
для последовательных стадий диссоциации частиц на атом и более
простой нейтральный фрагмент. Например, для метана СН4 расчет
проведен по реакциям:
СН4 —» СН3 + Н,435кДж
СН3 —» СН2 + Н,458кДж
СН2 —> СН + Н,430кДж
СН —» С + Н, 339 кДж
СН,
С + 4Н, 1662 кДж
?СВ(С—Н) = 1662: 4 = 416 кДж/моль
Все вещества считаются идеальными газами, частицы которых на-
находятся в невозбужденных электронных состояниях.
Связь
Ag—F
Al—Br
Al—Cl
Al—F
Al—I
Am—Br
Am—Cl
Am—F
Am—I
As—As
As—Br
As—Cl
As—F
As—H
As—I
Вещество
AgF2
AlBr3
AICI3
A1F3
AII3
AmBr3
AmCl3
AmF3
AmF4
Aml3
As4
AsBr3
AsCl3
AsF3
AsF5
AsH3
Asl3
кДж/моль
«268
358
426
592
285
«389
«452
«572
«519
«318
146
458
322
484
«406
«247
200
Связь
As—О
As=O
Au—Br
Au—Cl
Au—F
Au—I
B—Br
B—Cl
B—F
B—H
B—I
B—0
Ba—Br
Ba—Cl
Ba—F
Вещество
As2O3
As2O3
AuBr3
AuCl3
AuF3
Aul3
BBr3
BC13
BF3
BH3
BI3
B3H3C13N3
B(CH3OK
B(OHK
BaBr2
BaCl2
BaF2
кДж/моль
301
«389
«251
289
«305
-230
367
443
646
382
286
446
536
564^
412
461
574
_—-
384
I. Молекулы. Ионы. Радикалы
Продолжение табл.
Связь
Ва—I
~~Ве^Вг
Ве-С1
Be-F
Be-I
Be—0
Bi—Br
Bi—Cl
Bi-F
Bi—I
Br—F
Br—0
C—Br
c-c
c=c
c==c
C-Cl
C-F
с—н
Вещество
Bal2
BeBr2
BeCl2
BeF2
Bel2
Be(OHJ
BiBr3
BiCl3
BiF3
BiF5
Bil3
BrF3
BrF5
HBrO
CBr4
C(Br)Cl3
C(Br)F3
С^(алмаз)
с2н6
C2H4
C2H2
CBr3cl
CC14
C(C1)F3
CD4
CBr3F
CCI3F
CF4
CH4
CHCI3
HCN
кДж/моль
360
396
464
640
289
537
232
275
-393
-297
168
202
187
201
268
234
291
346
370
712
962
289
306
359
422
449
440
491
416
402
511
Связь
С—I
С—N
C=N
C=N
С—О
c=o
с—s
c=s
C=Se
C—T
Ca—Br
Ca—Cl
Ca—F
Ca—I
Cd—Br
Cd—Cl
Cd—F
Cd—I
Ce—Br
Ce—Cl
Ce—F
Ce—I
Ce=O
Cl—F
Cl—N
Вещество
CI4
C(NH2JO
HNCO
(CN)C1
(CN)F
HCN
HNC
CH3OH
co2
C(S)O
H2CS3
CS2
C(S)O
CSe2
CT4
CaBr2
CaCl2
CaF2
Cal2
CdBr2
CdCl2
CdF2
Cdl2
CeBr3
CeCl3
CeF3
Cel3
CeO2
C1F3
C1F5
C13N
кДж/моль
213
305
615
778
795
933
887
358
804
670
272
578
308
457
425
397
444
559
312
238
275
326
193
«431
500
625
-356
722
207
-142
307
^2004
385
Молекулы. Ионы. Радикалы
Продолжение табЛ
Связь
С1—О
С1=О
Со—С1
Сг—Вг
Сг—С
Сг—С1
Сг—F
Сг—I
Сг=О
Cs—О
Си—Вг
Си—С1
Си—F
D—О
D—S
Dy—Вг
Dy—Cl
Dy—F
Вещество
C12O
нею
C1O2
C1O3
СоС12
CrBr2
СгВг3
[Сг(СОN]
СгС12
СгС13
Сг(С1)О
СгС12О2
CrF2
CrF3
Crl2
Cr(Cl)O
СгС12О2
CrO2
CrO3
Cr(O)F
CrO2F2
Cs2O
CsOH
CuBr2
CuCl2
CuF2
D2O
D2S
DyBr3
DyCl3
DyF3
кДж/моль
207
218
258
238
378
340
299
124
388
336
431
356
486
514
249
519
448
478
479
594
454
276
380
258
303
387
All
373
«377
-444
575
Связь
Dy—I
Er— Br
Er—Cl
Er—F
Er—I
Eu—Br
Eu—Cl
Eu—F
Eu—I
Fe—Br
Fe—С
Fe—Cl
Fe—F
Fe—I
Ga—Br
Ga—Cl
Ga—F
Ga—I
Gd—Br
Gd—Cl
Gd—F
Gd—I
Ge—Br
Ge—С
Ge—Cl
Вещество
Dyl3
ErBr3
ErCl3
ErF3
Erl3
EuBr3
EuCl3
EuF2
EuF3
Eul3
FeBr2
FeBr3
[Fe(COM]
FeCl2
FeCl3
FeF2
FeF3
Fel2
GaBr3
GaCl3
GaF3
Gal3
GdBr3
GdCl3
GdF3
Gdl3
GeBr2
GeBr4
Ge(C2H5L
GeCl2
GeCl4
кДж/моль
«305
«38P
«448
587
«310
«347.
«414.
550
590
«272
343
293
120
396
345
481
«456
279
302
360
«469
246
«418
«485
605
326
276':
«213
«385
349
386
II. Молекулы. Ионы. Радикалы
Продолжение табл.
^—¦
Связь
Ge-F
Ge—Ge
Ge—I
Ge==Se
Ge=Te
H-0
H—S
H—Se
H-Te
Hf-Br
Hf-Cl
Hf—F
Hf-I
Hf=o
Hg-Br
Hg-Cl
Hg-F
Ho—Br
Ho—ci
Вещество
GeF2
GeF4
Ge2H6
Gel2
Gel4
GeSe2
GeTe2
CsOH
HBrO
нею
H2O
KOH
LiOH
NaOH
RbOH
H2S
H2Se
H2Te
HfBr4
HfCl4
HfF4
Hfl4
HfO2
HgBr2
HgCl2
HgF2
Hgl2
HoBr3
HoCl3
HoF3
кДж/моль
481
«452
157
264
212
348
324
513
423
412
464
500
528
502
530
367
«276
«238
«431
495
«649
«360
684
186
227
257
145
«381
«444
583
Связь
Ho—I
I—F
I—0
In—Br
In—Cl
In—F
In—I
Ir=O
К—С
К—О
Kr—F
La—Br
La—Cl
La—F
La—I
Li—О
Lu—Br
Lu—Cl
Lu—F
Lu—I
Mg—Br
Mg—Cl
Mg—F
Mg—I
Mg—О
Mn—Br
Вещество
Hol3
HIO
InBr3
InCl3
InF3
Inl3
IrO2
KCN
K2O
KOH
KrF2
LaBr3
LaCl3
LaF3
Lal3
Li2O
LiOH
LuBr3
LuCl3
LuF3
Lul3
MgBr2
MgCl2
MgF2
Mgl2
Mg(OHJ
MnBr2
кДж/моль
«305
«272
268
231
201
295
326
«444
225
476
438
249
347
50
439
496
630
350
368
442
«410
«477
589
«343
341
391
515
264
398
334
387
, Молекулы. Ионы. Радикалы
Продолжение табЛ
Связь
Mn—C1
Mn—F
Mn—I
Мп—Мп
Мо=О
N—D
N—F
N—Н
N—N
N=N
N—О
N=0
Na—С
Na—О
Вещество
МпС12
MnF2
MnF3
Mnl2
[Mn2(COI0]
МоО2
МоО3
DNO3
ND3
NF3
NH3
(NH)F2
(NH)O2
N2H4
H2N2O2
N2F2
N2H2
HNO2
HNO3
NH2OH
N02
N20
N2O3 -
N2O4
(NO)Br
(NO)C1
(NO)F
NaCN
Na2O
NaOH
кДж/моль
396
488
411
270
108
582
587
432
399
279
391
340
329
253
418
410
548
209
208
264
306
167
335
323
479
531
569
441
253
329
Связь
Nb=O
Nd—Br
Nd—Cl
Nd—F
Nd—I
Ni—Br
Ni—С
Ni—Cl
Ni—F
Ni—I
Np—Br
Np—Cl
Np—F
Np—I
O—F
O—O
0^0
P—Br
P—Cl
P—F
P—H
P—I
P—0
Вещество
NbCl3O
NbO2
NdBr3
NdCl3
NdF3
Ndl3
NiBr2
[Ni(COL]
NiCl2
NiF2
Nil2
NpBr3
NpCl3
NpF3
NpF4
NpF5
NpF6
Npl3
OF2
D2O2
H2O2
°з
PBr3
P(Br)Cl2
PC13
PC12F
PF3
PH3
PI3
p4o6
кДж/моль
661
717
-406
471
620
324
317
143
369
457
252
-397
-460
-586
-561
-519
-477
-326
193
216
214
303
264
297
320
540
505
322
184
«335
388
III. Молекулы. Ионы. Радикалы
Продолжение табл.
Связь
Р-Р
P=S
Pb—Br
Pb—С
Pb—Cl
Pb—F
Pb—I
Pm—Br
Pm—Cl
Pm—F
Pm—I
Pr— Br
Pr—Cl
Pr—F
Pr—I
Pr=O
Pu^Br
Pu-Cl
Pu^p
Вещество
PBr3O
PC13O
P(O)F3
P4
P2C14
p2h4
P2I4
P(S)Br3
P(S)C13
P(S)F3
PbBr2
Pb(C2H5L
PbCl2
PbCl4
PbF2
PbF4
Pbl2
PmBr3
PmCl3
PmF3
Pml3
PrBr3
PrCl3
PrF3
Prl3
PrO2
PtO2
PuBr3
PuCl3
PuF3
PuF4
кДж/моль
506
527
544
201
239
238
259
397
406
414
262
130
353
-243
396
«331
209
-385
-452
615
-305
-418
482
621
339
625
441
388
442
573
-536
Связь
Pu—I
Rb—0
Re—Re
Ru=O
S—Br
S—Cl
S—F
S=O
S—S
S=S
Sb—Br
Sb—Cl
Sb—F
Вещество
PuF5
PuF6
Pul3
Rb2O
RbOH
[Re2(COI0]
RuO2
S2Br2
SC12
S2C12
S(C1)F5
SC12O
SF2
SF6
SO2F2
SC12O
SC12O2
so2
so3
S2O
SO2F2
H2S2
S2C12
S2O
SbBr3
SbBr5
SbCl3
SbCl5
SbF3
SbF5
кДж/моль
-485
-427
-310
236
356
187
490
-217
271
255
193
228
371
284
360
441
421
537
474
517
525
277
264
279
383
260
184
315
249
-440
-402
389
Молекулы. Ионы. Радикалы
Продолжение табЛ
Связь
Sb—I
Sb—Sb
Sc—Вг
Sc—Cl
Sc—F
Sc—I
Se—Br
Se—Cl
Se—F
Se=O
Se—Se
Si—Br
Si—Cl
Si—F
Si—H
Si—I
Si=O
Sm—Br
Sm—Cl
Sm—F
Sm—I
Sn—Br
Sn—С
Sn—Cl
Sn—F
Вещество
Sbl3
Sb4
ScBr3
ScCl3
ScF3
Scl3
SeBr4
SeCl4
SeF4
SeF6
SeO2
SeO3
Se6
SiBr4
SiCl4
SiF4
SiH4
Sil4
SiO2
SmBr3
SmCl3
SmF3
Sml3
SnBr2
SnBr4
Sn(C2H5L
SnCl2
SnCl4
SnF2
SnF4
кДж/моль
195
«121
419
475
608
340
«151
«192
«310
285
425
354
172
310
399
596
322
234
637
«360
«427
595
«285
324
273
226
376
323
456
«414
Связь
Sn—I
Sr—Br
Sr—Cl
Sr—F
Sr—I
T—0
Та—F
Tb—Br
Tb—Cl
Tb—F
Tb—I
Tc—Tc
Те—Br
Те—Cl
Те—F
Те—I
Te=O
Th—F
Ti—Br
Ti—Cl
Ti—F
Вещество
Snl2
Snl4
SrBr2
SrCl2
SrF2
Srl2
T2O
TaF5
TbBr3
TbCl3
TbF3
Tbl3
[Tc2(COI0]
TeBr2
TeBr4
TeCl2
TeCl4
TeF4
TeF6
Tel4
TeO2
ThF4
TiBr2
TiBr3
TiBr4
TiCl2
TiCl3
TiCl4
TiF2
TiF3
кДж/моль
254
«205
405^"
439
551
329
474
597
«410
«477
«615
«339
177
«243
«176
«284
311
«335
330
«121
383
641_
436
393
367
475
458
429
691
632
_--—-~
390
I. Молекулы. Ионы. Радикалы
Окончание табл.
Связь
Ti—I
Ti=O
Tm—Br
Tm—Cl
Tm—F
Tm—I
U—Br
U—Cl
U—F
u=o
V-Br
v-ci
Вещество
TiF4
Til2
Til,
ти4
TiO2
TmBr3
TmClj
TmF3
Tml3
UBr3
UBr4
UBr5
UC13
UC14
UC15
UC16
(UO2)C12
UF3
UF4
UF5
UF6
UI3
(UO2)C12
VBr2
VBr3
VBr4
VC12
«Дж/моль
585
373
313
296
635
= 351
= 418
589
= 251
424
400
335
495
453
417
379
385
608
613
594
526
= 343
519
445
369
328
487
Связь
V=O
W—Cl
w=o
Xe=O
Y—Br
Y—Gl
Y—F
Y—I
Yb—Br
Yb—Cl
Yb—F
Yb—I
Zn—Br
Zn—Cl
Zn—F
Zn—I
Zr—Br
Zr—Cl
Zr—F
Zr—I
Zr=O
Вещество
VC13
VC14
VC13O
vo2
WC12
WC14O
wo2
wo3
XeO3
YBr3
YC13
YF3
YI3
YbBr3
YbCl3
YbF3
Ybl3
ZnBr2
ZnCl2
ZnF2
Znl2
ZrBr4
ZrCl4
ZrF4
Zrl4
гю2
кДж/моль
416
382
577
623
552
521
641
635
84
465
520
633
385
«322
«385
598
«251
270
320
394
205
425
491
650
347
703
391
II. Молекулы. Ионы. Радикалы
7. Строение многоатомных частиц
7.1. Геометрическая форма, длина связей
и валентные углы в частицах
с одним центральным атомом sp-элемента
Представлены многоатомные химические частицы (молекулы, ра.
дикалы, ионы) с общей формулой АВЛ, где А — центральный атом,
В — концевые атомы (группы атомов, лиганды).
Геометрические формы частиц с центральным атомом ^-элемента
12
:ав
ав7
392
III. Молекулы. Ионы. Радикалы
В геометрических формах показаны, кроме химических связей
д_^В, орбитали атома А, содержащие пару валентных электронов
(обозначение, например, :АВ2) или неспаренный электрон (обозначе-
(обозначение -АВ2), а также аксиальные (осевые) позиции концевых атомов В
(обозначение В*) в отличие от экваториальных позиций (обычно свя-
связи А—В и А—В* имеют разную длину).
Экспериментальные данные — длина связей (/св) и валентные углы
молекул и радикалов — отвечают условиям их существования, данные
для ионов — условиям их нахождения в водных растворах или ионных
кристаллах. Многоточие означает отсутствие данных.
Частица
А1Вг3
А1С13
[AICIJ-
A1F3
[A1F4]"
[A1F6]3"
[A1HJ-
[A1(H2ON]3+
AII3
[А1(ОНLГ
:AsBr3
:AsCi3
:AsF3
AsF5
[AsFJ-
•AsH3
•Asl3
^AsO3-
AsO3-
AsS3-
Dn "
BBr3
Bci3
^—
Форма
2
2
4
2
4
11
4
11
2
4
5
5
5
7
11
5
5
5
4
4
2
2
Связь
Al—Br
Al—Cl
Al—Cl
Al—F
Al—F
Al—F
Al—H
Al—0
Al—I
Al—О
As—Br
As—Cl
As—F
As—F
As—F*
As—F
As—H
As—I
As=O
As=O
As=S
B—Br
B—Cl
/CB> nM
227
206
209-214
163
169
181
155
188
244
175
233
216
171
166
171
163-170
151
256
201
175
223
189
174
Валентный угол
Br—Al—Br 120°
Cl—Al—Cl 120°
Cl—Al—Cl 109,5°
F—Al—F 120°
F—Al—F 109,5°
F—Al—F 90°
H—Al—H 109,5°
O—Al—О 90°
I—Al—1120°
O—Al—О 109,5°
Br—As—Br 100°
Cl—As—Cl 99°
F—As—F 96°
F—As—F 120°
F—As—F* 90°
F—As—F 90°
H—As—H 92°
I—As—I 100°
O—As—О...
О—As—О 109,5°
S—As—S 109,5°
Br—B—Br 120°
Cl—B—Cl 120°
393
I. Молекулы. Ионы. Радикалы
Продолжение табц
Частица
BF3
[BFJ-
[ВН4]"
В13
[B(NH3)F3]
во-
во*-
В(ОНK
[В(ОНL]"
ВеВг2
ВеС12
BeF2
[BeF4]2"
Bel2
:BiBr3
:BiCl3
:BiF3
:BiI3
[:::Br(BrJ]-
[::BrF2]+
::BrF3
[::BrF4]~
[:BrF4]+
:BrF5
:вю~
BrO4
Форма
2
4
4
2
4
1
2
2
4
1
1
1
4
1
5
5
5
5
10
6
9
13
8
12
5
4
Связь
В—F
В—F
В—H
В—I
В—N
В—F
В=О
В=О
В—О(Н)
О—Н
В—О
Be—Вг
Be—C1
Be—F
Be—F
Be—I
Bi—Br
Bi—Cl
Bi—F
Bi—I
Br—Br
Br—F
Br—F
Br—F*
Br—F
Br—F
Br—F*
Br—F
Br-F*
Br=O
Br=O
131
140
126
212
160
158
127
132-140
136
95
143-150
191
175
140
155
210
263
248
200
287
250-290
169
172
181
188
170-190
220-250
177
169
178
161
Валентный угол
F—В—F 120°
F—B—F 109,5°
H—В—Н 109,5°
I—B—I 120°
N—B—F«109°
F—B—F«109°
0—В—О 180°
О—В—О 120°
О—В—О 120°
В—О—Н 105°
О—В—О 109,5°
Br—Be—Вг 180°
Cl—Be—Cl 180°
F—Be—F 180°
F—Be—F 109,5°
I—Be—1180°
Br—Bi—Br 100°
Cl—Bi—Cl 100°
F—Bi—F94°
I—Bi—I 98°
Br—Br—Br 180°
F—Br—F 94°
F—Br— F* 86°
F*—Br— F* 188°
F—Br—F90°
F—Br—F...
F—Br—F*...
F—Br—F90°
F—Br— F* 90°
O—Br—0 112°
O—Br—О 109,5°
394
II. Молекулы. Ионы. Радикалы
Продолжение табл.
Частица
СВг4
C(Br)F3
СВг2О
СС14
C(C1)F3
CC12F2
CCI3F
СС12О
CD4
CF4
сн4
CHBr3
СН2Вг2
СН3Вг
СНС13
СН2С12
СН3С1
CHF3
CH2F2
CH3F
^—
Форма
4
4
3
4
4
4
4
2
4
4
4
4
4
4
4
4
4
4
4
4
Связь
С—Вг
С—Вг
С—F
С—Вг
С=О
С—С1
С—С1
С—F
С—С1
С—F
С—С1
С—F
С—С1
С=О
С—D
С—F
с—н
С—Н
С—Вг
С—Н
С—Вг
С—Н
С—Вг
С—Н
С—С1
С—Н
С—С1
с—н
С—С1
с—н
С—F
С—Н
С—F
С—Н
С—F
'св. ПМ
194
191
133
205
113
177
175
133
178
134
176
140
175
117
110
132
109
107
193
109
194
ПО
194
ПО
176
107
177
111
178
ПО
133
109
136
111
139
Валентный угол
Вг—С—Вг 109,5°
Вг—С—Fill0
F—С—F 108°
Вг—С—Вг 110е
Вг—С—0 125°
С1—С—С1109,5°
С1—С—F 110е
F—С—F 109°
С1—С—С1109,5°
F—С—F 109,5°
С1—С—С1112°
С1—С—F 107°
С1—С—С1112°
С1—С—0 124°
D—С—D 109,5°
F—С—F 109,5°
Н—С—Н 109,5°
Н—С—Вг 108°
Вг—С—ВгПГ
Н—С—HI 11°
Вг—С—ВгПГ
Н—С—HI 11°
Н—С—Вг 108°
Н—С—С1108°
С1—С—С1111°
Н—С—Н 112е
С1—С—СИ 12е
Н—С—Н 108°
Н—С—СП 11е
Н—С—F 110е
F—С—F 109°
Н—С—HI 14°
F—С—F 108°
Н—С—HI 10°
Н—С—F 109°
395
I. Молекулы. Ионы. Радикалы
Продолжение
Частица
СН13
СН212
СН31
СН3ОН
C(I)F3
CN2-
(CN)Br
(CN)C1
(CN)F
(CN)I
CO2
CO2-
C(O)F2
CS2
CS2-
C(S)C12
C(S)O
CSe2
C(Se)O
C(Se)S
Форма
4
4
4
4
4
4
1
1
1
1
1
1
2
2
1
2
2
1
1
1
1
Связь
с—н
С—I
с—н
С—I
с—н
С—I
с—н
с—о
О—Н
С—I
С—I
С—F
C=N
C=N
С—Вг
C=N
С—Cl
C=N
С—F
C=N
С—I
с=о
с=о
с=о
С—F
C=S
c=s
c=s
С—Cl
c=s
c=o
C=Se
C=Se
C=O
C=Se
C=S
/св> пм
212
109
212
109
213
110
143
96
215
210
134
123
116
179
116
163
116
126
116
200
117
129
117
132
155
165
160
173
156
115
170
171
116
170
155
Валентный угол
H—С—I 106°
I—С—1113°
H—С—Н 109,5°
I—С—1109,5°
н-с-нпг
Н—С—I 107°
Н—С—Н 109°
Н—С—О...
С—О—Н 109°
I—С—I 109,5°
I—С—F113°
F—С—F 106°
N—С—N 180°
N—С—Вг 180°
N—С—С1 180°
N—С—F 180°
N—С—I 180°
О—С—О 180°
О—С—О 120°
О—С—F 126°
F—С—F 108°
S—С—S 180°
S—С—S 120°
S—С—С1124°
С1—С—СП 12°
S—С—О 180°
Se—С—Se 180°
Se—С—0 180°
Se—С—S 180°
396
I. Молекулы. Ионы. Радикалы
Частица
C(Te)S
[::C1F2]+
::C1F3
:C1F5
C13N:
::C1O~
•:СЮ2
:СЮ+2
:С1Оз
сю;
С12О::
:C1O9F
CIO3F
D2o::
D2s::
GaBr3
GaCl3
[GaClJ-
[GaH4]~
Gal3
—
GeBr4
;GeCl2
GeCl4
[GeCl6]2-
Ge(Cl)F3
^
Форма
1
6
9
12
5
6
6
3
5
4
6
5
4
6
6
2
2
4
4
2
4
3
4
11
4
Связь
C=Te
C=S
Cl—F
Cl—F
Cl—F*
Cl—F
Cl—F*
N—Cl
C1=O
C1=O
C1=O
C1=O
C1=O
0—Cl
C1=O
Cl—F
C1=O
Cl—F
0—D
S—D
Ga—Br
Ga—Cl
Ga—Cl
Ga—H
Ga—I
Ge—Br
Ge—Cl
Ge—Cl
Ge—Cl
Ge—Cl
Ge—F
'св> ПМ
190
156
157
160
170
167
158
176
157
147
141
145
142-145
170
148
167
140
162
97
135
224
209
217
197
246
227
211
211
235
207
169
Продолжение табл.
Валентный угол
Те—С—S 180°
F—Cl—F 100°
F—Cl—F* 90°
F—Cl—F 90°
F—Cl—F* 90°
Cl—N—Cl 108°
0—Cl—0 111°
0—Cl—O118°
0—Cl—0 119°
O—Cl—О 106°
0—Cl—0 109,5°
Cl—О—С111Г
0—Cl—0 114°
0—Cl—F 103°
O—Cl—0 117°
O—Cl—F 101°
D—0—D 105°
D—S—D 92°
Br—Ga—Br 120°
Cl—Ga—Cl 120°
Cl—Ga—Cl 109,5°
H—Ga—H 109,5°
I—Ga—I 120°
Br—Ge—Br 109,5°
Cl—Ge—Cl 107°
Cl—Ge—Cl 109,5°
CIGe—Cl 90°
Cl—Ge—Flll°
F—Ge—F 108°
397
III. Молекулы. Ионы. Радикалы
Продолжение табщ.
Частица
GeF4
[GeF6]2"
GeH4
GeH3Cl
Gel4
GeO2
HBrO::
HCN
HCO3
hcio::
HC1O4
H(i:)O3
HNC
H(N:)O2
HNO3
H2o::
(H3o:)+
H(O::)F
H2(PHO3)
Форма
4
11
4
4
4
1
6
1
2
6
4
5
1
3
2
6
5
6
4
Связь
Ge—F
Ge—F
Ge—H
Ge—H
Ge—Cl
Ge—I
Ge=O
0—Br
0—H
C—H
C=N
c=o
C—0(H)
0—Cl
0—H
C1=O
Cl—0(H)
1=0
I—0(H)
Ns=C
N—H
N=0
N—0(H)
0—H
N=0
N—0(H)
0—H
0—H
0—H
0—H
0—F
P—H
P=0
P—0(H)
/св, пм
167
177
153
152
215
250
163
185
107
115
126
135
169
96
141
164
180
190
119
100
117
144
96
121
141
96
96
95
97
144
139
147
154
Валентный угол
F—Ge—F 109,5°
F—Ge—F90°
H—Ge—H 109,5°
H—Ge—Hill0
H—Ge—Cl 108°
I—Ge—I 109,5°
0—Ge—0 180°
H—0—BrllO°
H—C—N 180°
0—С—О 124°
0—C—O(HI18°
H—0—Cl 103°
0—Cl—0 113°
0—Cl—O(H) 106°
0—I—0 98°
0—I—O(H)...
C—N—H 180°
0—N—O(HI11°
N—0—H 102°
0—N—0 130°
0—N—O(HI15°
N—0—H 102°
H—0—H 105°
H—0—H 109°
H—0—F97°
H—P—0...
0—P—O(HI16° o
O(H)—P—O(H) 102
398
I. Молекулы. Ионы. Радикалы
Продолжение табл.
Частица
Н3Р°4
H2S::
(H3s:)+
hso;
h2so4
HSO3F
H2Se::
H2(Se:)O3
H2Se04
H2Te::
H6Te06
[:::iBr2]-
[»:i(Br)Cl]-
[:::icy-
[::icy+
[::ici4]-
r
Форма
4
6
5
4
4
4
6
5
4
6
11
10
10
10
6
13
12
14
10
Связь
P=O
P—O(H)
S—H
S—H
s=o
S—O(H)
0—H
s=o
S—O(H)
0—H
s=o
S—F
S—O(H)
о—н
Se—H
Se=O
Se—O(H)
0—H
Se=O
Se—O(H)
0—H
Те—Н
Те—O(H)
I—Br
I—Br
I—Cl
I—Cl
I—Cl
I—Cl
I—F
I—F*
I—F
I—F*
I—I
'св> ПМ
152
157
134
135
143-146
156
99
142
153
97
141
153
153
100
146
164
174
100
157
165
100
166
192
271
250
238
255
230
242-260
187
184
183
194
290
Валентный угол
О—Р—О(НI12°
О(Н)—Р—О(Н) 106°
Н—S—Н 92°
Н—S—Н 96°
О—S—О...
О—S—О(Н)...
S—О—Н...
О—S—О 125°
О(Н)—S—О(Н) 100°
S—О—Н 105°
О—S—О 124°
F—S—О(Н) 100°
О—S—О(Н)...
S—О—Н...
Н—Se—Н9Г
О—Se—O(H)...
О(Н)—Se—O(H)...
Se—О—Н...
О—Se—О...
О(Н)—Se—O(H)...
Se—О—Н...
Н—Те—Н 90°
О(Н)—Те—О(Н) 90°
Вг—I—Вг 180°
Br—I—C1180°
Cl—I—C1180°
С1—I—С195°
Cl—I—C190°
F—I—F 90°
F—I—F* 90°
F—I—F72°
F—I—F* 90°
I—I—I 180°
399
!1. Молекулы. Ионы. Радикалы
Продолжение табд.
Частица
:Ю"
I(O)F5
Inl3
KCN
:::KrF2
N3
NCO-
NCS"
:nd3
•:nf2
:nf3
::NH2
:NH3
NH +
:NH2C1
(:nh)F2
:nh2oh
nh3oh+
:no2
•NO2
Форма
5
4
11
11
2
1
10
1
1
1
5
6
5
6
5
4
5
5
5
4
3
3
Связь
1=0
1=0
1=0
I—F
1=0*
I=F*
In—I
С—К
C=N
Kr—F
N=N
C=N
C=0
C=N
c=s
N—D
N—F
N—F
N—H
N—H
N—H
N—H
N—Cl
N—H
N—F
N—H
N—0(H)
0—H
N—H
N—O(H)
0—H
N=0
N=0
/св, пм
182
178
185
182
172
186
262
257
115
189
117
121
117
122
158
103
135
137
103
103
104
102
175
103
140
102
145
96
99
141
97
124
120
Валентный угол
0—I—О 97°
0—I—0 109,5°
0—I—0 90°
F—I—0* 98°
I—In—I 120°
К—С—N 180°
F—Kr—F180°
N—N—N 180°
N—С—О 180°
N—C—S 180°
D—N—D 107°
F—N—F 103°
F—N—F 102°
H—N—H 104°
H—N—H 107°
H—N—H 109,5°
H—N—H 107°
H—N—Cl 104°
H—N—F 100°
F—N—F 103°
H—N—H 107°
H—N—O(H) 103°
N—О—Н 101°
H—N—H ...
H—N—O(H)...
N—О—Н ...
O—N—0 115°
O—N—О 134°
400
I. Молекулы. Ионы. Радикалы
Продолжение табл.
Частица
N0^'
N20
(:NO)Br
(:NO)C1
(NO2)C1
(:NO)F
N(O)F3
(NO2)F
NaCN
<o-
:03
OCN-
::0F2
:PBr3
[PBr4]+
:P(Br)Cl2
:PBr2Q
:pBr(Cl)F
Форма
1
2
4
1
3
3
2
3
4
2
1
6
3
1
6
5
4
5
5
5
Связь
N=0
N=0
N=0
N=N
N=0
N=0
N—Br
N=0
N—Cl
N=0
N—Cl
N=0
N—F
N=0
N—F
N=0
N—F
C—Na
C^N
0=0
0=0
с—о
C=N
0—F
P—Br
P—Br
P—Br
P—Cl
P—Br
P—Cl
P—Br
P—Cl
P—F
'ев' ПМ
110
124
139
113
118
115
214
114
198
121
183
114
151
116
143
118
147
226
115
138
127
135
116
141
222
215
220
204
220
204
220
204
155
Валентный угол
0—N—0 180°
0—N—0 120°
O—N—0 109,5°
N—N—0 180°
0—N—Brll5°
0—N—C1113°
O—N—0 130°
Cl—N—0 115°
O—N—F110°
O—N—F117°
F—N—F 101°
0—N—0 136°
0—N—F112°
Na—C—N 180°
О—О—О 108°
0—0—0 117°
О—С—N 180°
F—0—F 103°
Br—P—Br 101°
Br—P—Br 109,5°
Br—P—Cl...
Cl—P—Cl 100°
Br—P—Cl 100°
Br—P—Br...
Cl—P—F 102°
Cl—P—Br...
F—P—Br...
401
II. Молекулы. Ионы. Радикалы
Продолжение табл
Частица
:P(Br)F2
:PBr2F
PBr3o
:pci3
[РС14]+
РС15
[pci6]-
:P(Ci)F2
:pci2f
рсцо
:pd3
:pf3
pf5
:ph3
ph;
(:ph)F2
:pi3
:P(i)Br2
:Pl2Br
:P(i)Ci2
Форма
5
5
4
5
4
7
11
5
5
4
5
5
7
11
5
4
5
5
5
5
5
Связь
P—Br
P—F
P—Br
P—F
P—Br
P=O
P—Cl
P—Cl
P—Cl
P—СГ
P—Cl
P—Cl
P—F
P—Cl
P—F
P—Cl
P=O
P—D
P—F
P—F
P—F
P—F
P—H
P—H
P—H
P—F
P—I
P—I
P—Br
p T
P—Br
P—I
P—Cl
'се'™
220
155
220
155
206
141
204
198
202
212
207
203
157
204
155
199
146
142
156
153
158
159
141
142
141
158
243
243
220
243
220
243
204
Валентный угол
F—P—F 102°
F—P—Br...
Br—P—F 102°
F—P—Br...
Br—P—Br 108°
Br—P—0 111°
Cl—P—Cl 100°
Cl—P—Cl 109,5°
Cl—P—Cl 120°
Cl—P—Cl* 90°
Cl—P—Cl 90°
Cl—P—F 99°
F—P—F 97°
Cl—P—Cl 99°
Cl—P—F 102°
Cl—P—Cl 104°
Cl—P—0 115°
D—P—D 93°
F—P—F97°
F—P—F 120°
F—P—F* 90°
F—P—F 90°
H—P—H 94°
H—P—H 109,5°
H—P—F 96°
F—P—F 99°
I—P—I 100°
Br—P—I...
Br—P—Br 100°
I—P—I...
I—P—Br 100°
Cl—P—I...
Cl—P—Cl 100°
402
II. Молекулы. Ионы. Радикалы
Продолжение табл.
Частица
^ ¦
:Р12С1
:P(I)F2
?о\-
P(O)F3
[PO2F2]'
[PO3F]2-
psr
P(S)F3
:рьвг2
:PbCl2
PbCl4
[PbCl6]2"
:PbF2
PbH4
:Pbl2
:SBr2o
::sci2
S(C1)F5
:sci2o
sci2o2
::SF2
f:SF3]+
^—¦
Форма
5
5-
4
4
4
4
4
4
3
3
4
11
3
4
3
5
6
11
5
4
6
5
Связь
P—I
P—Cl
P—I
P—F
P=O
P=O
P—F
P=O
P—F
P=O
P—F
P=S
P=S
P—F
Pb—Br
Pb—Cl
Pb—Cl
Pb—Cl
Pb—F
Pb—H
Pb—I
S—Br
S=O
S—Cl
S—Cl
S—F
S—Cl
s=o
S—Cl
s=o
S—F
S—F
4b' ПМ
243
204
247
157
154-156
144
152
147
158
151
159
205
187
154
260
246
243
250
213
186
279
227
145
201
203
158
208
144
201
140
159
150
Валентный угол
I—P—I...
I—P—Cl 100°
I—P—F 99°
F—P—F 98°
0—P—0 109,5°
0—P—F117°
F—P—F 101°
0—P—0 122°
F—P—F 97°
0—P—0...
0—P—F...
S—P—S 109,5°
S—P—F 118°
F—P—F 100°
Br—Pb—Br95°
Cl—Pb—C196°
Cl—Pb—Cl 109,5°
Cl—Pb—Cl 90°
F—Pb—F 90°
H—Pb—H 109,5°
I—Pb—I 95°
Br—S—Br 96°
Br—S—0 108°
Cl—S—Cl 103°
Cl—S—F 90°
F—S—F 90°
Cl—S—Cl 96°
Cl—S—0 106°
Cl—S—Cl 100°
Cl—S—0 124°
F—S—F 98°
F—S—F 98°
403
I. Молекулы. Ионы. Радикалы
Продолжение табд
Частица
:SF4
SF6
:SO2
rSO^-
SO3
SO2-
:S(O)F2
[S(O)F3]+
S(O)F4 •
SO2F2
[SO3F]-
SO3S2-
:s(S)F2
:S(S)O
:SbBr3
:sbci3
SbCl5
[SbCl6]~
:SbF3
[:SbF5]2-
[SbF6]"
:SbH3
Форма
8
11
3
5
2
4
5
4
7
4
4
4
5
3
5
5
7
11
5
12
11
5
Связь
S—F
S—F*
S—F
S=O
S=O
S=O
S=O
S=O
S—F
S=O
S—F
S—F
S=O
S—F*
S=O
S—F
S=O
S—F
S=O
S=S
S=S
S—F
S=S
s=o
Sb—Br
Sb—Cl
Sb—Cl
Sb—СГ
Sb—Cl
Sb—F
Sb—F
Sb—F*
Sb—F
Sb—H
4в> пм
154
164
156
143
152
142
147
141
159
135
144
155
139
158
140
153
142
157
148
199
186
160
188
146
249
233
229
234
221-244
188
202
202
177-195
171
Валентный угол
F—S—F 104°
F—S—F* 90°
F—S—F 90°
0—S—0 119°
0—S—0 105°
0—S—0 120°
O—S—О 109,5°
0—S—F 107°
F—S—F 93°
0—S—F116°
F—S—F 102°
F—S—F118°
F—S—0 124°
0—S—F* 98°
0—S—0 123°
F—S—F 97°
0—S—0 113°
0—S—F 106°
O—S—0 ...
O—S—S ...
S—S—F 108°
F—S—F 93°
S—S—0 118°
Br—Sb—Br98°
Cl—Sb—Cl 97°
Cl—Sb—Cl 120°
Cl—Sb—Cl* 90°
Cl—Sb—Cl 90°
F—Sb—F 95°
F—Sb—F 90°
F—Sb—F* 90°
F—Sb—F 90°
H—Sb—H 92°
404
I. Молекулы. Ионы. Ради
калы
Продолжение табл.
Частица
:SbI3
[Sb(OHNr
[SbS4]3'
:SeCl2O
:SeF4
SeF6
:SeO2
rSeO^-
SeO3
SeO^-
:Se(O)F2
SeO2F2
SiBr4
Si(Br)F3
SiBr2F2
SiCl4
Si(Cl)F3
:SiF2
S*4
[SiF6]2-
Si(H)Br3
SiH3Br
Форма
5
11
4
5
8
11
3
5
2
4
5
4
4
4
4
4
4
3
4
11
4
4
Связь
Sb—I
Sb—O(H)
0—H
Sb=S
Se—Cl
Se=O
Se—F
Se—F*
Se—F
Se=O
Se=O
Se=O
Se=O
Se=O
Se—F
Se=O
Se—F
Si—Br
Si—Br
Si—F
Si—Br
Si—F
Si—Cl
Si—Cl
Si—F
Si—F
Si—F
Si—F
Si—H
Si—Br
Si—H
Si—Br
'ев' ПМ
272
197
100
238
220
161
168
177
169
161
170-176
169
165
158
173
158
169
215
215
156
216
155
202
199
156
159
156
170
149
217
149
221
Валентный угол
I—Sb—199°
0—Sb—0 90°
Sb—0—H...
S—Sb—S 109,5°
Cl—Se—Cl 97°
Cl—Se—0 106°
F—Se—F 100°
F—Se—F* 90°
F—Se—F 90°
0—Se—0 113°
O—Se—0 102°
0—Se—0 120°
0—Se—0 109,5°
0—Se—F 105°
F—Se—F 92°
0—Se—0 126°
F—Se^-F 94°
Br—Si—Br 109,5°
Br^-Si—F110°
F—Si—F 109°
Br—Si—Brlll°
F—Si—F 99°
Cl—Si—Cl 109,5°
Cl—Si—F110°
F—Si—F 109°
F—Si—F 101°
F—Si—F 109,5°
F—Si—F90°
H—Si—Br 108°
Br—Si—Brlll°
H—Si—HI 10°
Br—Si—H 109°
405
I. Молекулы. Ионы. Радикалы
Продолжение mafa
Частица
Si(H)Cl3
SiH2Cl2
SiH3Cl
Si(H)F3
SiH2F2
SiH3F
SiH3I
SiH4
Sil4
Si(I)F3
SiO2
SiO^-
:SnBr2
SnBr4
[SnBr6]2"
:SnCi2
SnCl4
[SnCl5]"
[SnCl6]2"
:SnF2
SnF4
SnH4
:SnI2
Форма
4
4
4
4
4
4
4
4
4
4
1
4
3
4
11
3
4
7
11
3
4
4
3
Связь
Si—H
Si—Cl
Si—H
Si—Cl
Si—H
Si—Cl
Si—H
Si—F
Si—H
Si—F
Si—H
Si—F
Si—H
Si—I
Si—H
Si—I
Si—I
Si—F
Si=O
Si=O
Sn—Br
Sn—Br
Sn—Br
Sn—Cl
Sn—Cl
Sn—Cl
Sn—СГ
Sn—Cl
Sn—F
Sn—F
Sn—H
Sn—I
16ву ПМ
147
201
148
203
148
205
145
156
147
158
146
159
149
244
148
243
239
156
155
157
255
244
259
234
228
236
238
242
206
184
171
278
Валентный угол ,
H—Si—Cl 108°
Cl—Si—СИ 11°
H—Si—НИ Г
Cl—Si—СП 10°
H—Si—HI 10°
Cl—Si—H 109°
H—Si—Fill0
F—Si—F 108°
H—Si—HI 12°
F—Si—F 108°
H—Si—H 109°
F—Si—НПО0
H—Si—НИ Г
I—Si—H 108°
H—Si—H 109,5°
I—Si—I 109,5°
I—Si—F 110°
F—Si—F 109°
0—Si—О 180°
0—Si—О 109,5°
Br—Sn—Br95°
Br—Sn—Br 109,5°
Br—Sn—Br90°
Cl—Sn—Cl 100°
Cl—Sn—Cl 109,5°
Cl—Sn—Cl...
Cl—Sn—Cl*...
Cl—Sn—Cl 90°
F—Sn—F94°
F—Sn—F 109,5°
H—Sn—H 109,5°
I—Sn—195°
406
II. Молекулы. Ионы. Радикалы
Окончание табл.
Частица
Snl4
[Snl6]2'
SnO2
[Sn(OHN]2"
[SnS4]4-
::TeBr2
::ТеС12
:ТеС14
TeF6
:ТеО2
:ТеО^-
ТеО«-
:::XeF2
[::XeF3]+
::XeF4
[:XeF5]+
:XeO3
XeO4
ХеСИ-
0
::Xe(O)F2
:Xe(O)F4
:Xe02F2
"--——
Форма
4
11
1
11
4
6
6
8
11
3
5
11
10
9
13
12
5
4
11
9
12
8
Связь
Sn—I
Sn—I
Sn=O
Sn—O(H)
Sn=S
Те—Br
Те—Cl
Те—Cl
Те—Cl*
Те—F
Te=O
Te=O
Te=O
Xe—F
Xe—F
Xe—F*
Xe—F
Xe—F
Xe—F*
Xe=O
Xe=O
Xe=O
Xe=O
Xe—F*
Xe=O*
Xe—F
Xe=O
Xe—F*
/св, пм
264
284
181
206
237
251
236
233
>233
184
183
188
198
198
183
191
194
190
177
176
174
184-186
176
195
171
190
171
190
Валентный угол
I—Sn—1109,5°
I—Sn—190°
0—Sn—0 180°
O(H)—Sn—O(H) 90°
S—Sn—S 109,5°
Вг—Те—Br 98°
Cl—Те—Cl 150°
Cl—Те—Cl 120°
Cl—Те—Cl* 90°
F—Те—F 90°
0—Те—0 110°
О—Те—О 100°
О—Те—О 90°
F—Xe—F 180°
F—Xe—F* 80-82°
F—Xe—F 90°
F—Xe—F 90°
F—Xe—F* 90°
О—Хе—О 103°
О—Хе—О 109,5°
О—Хе—О 90°
О—Хе—F* 90°
F—Хе—О* 90°
F—Xe—F90°
О—Хе—О 106°
О—Хе—F* 90°
407
II. Молекулы. Ионы. Радикалы
7.2. Геометрическая форма, длина связей,
магнитные моменты и окраска в частицах
с одним центральным атомом df-элемента
Представлены многоатомные химические частицы (молекулы, р^
дикалы, ионы) с общей формулой АВл, где А — центральный атом,
В — концевые атомы (группы атомов, лиганды).
Геометрические формы частиц с центральным атомом ^-элемента
Частица
АВ2
АВ3
АВ4
АВ5
АВ6
АВ7
АВ8
Геометрическая форма
линейная (дигональная)
треугольная (тригональная)
тетраэдрическая
плоскоквадратная
тригонально-бипирамидальная, возможно
квадратно-пирамидальное искажение (атом
А — над центром квадратного основания)
тригонально-бипирамидальная
квадратно-пирамидальная
(атом А — в центре квадратного основания)
октаэдрическая
пентагонально-бипирамидальная
додекаэдрическая
Номер формы
1
2
3
4
5
6
7
8
9
10
Аксиальные (осевые) позиции концевых атомов обозначены В* в
отличие от экваториальных позиций. Известные валентные углы
между связями даны в примечаниях.
Сокращенные обозначения органических лигандов и групп
Ph — фенил С6Н5 phen — 1,10-фенантролин CI2H8N2
acac — ацетилацетонато С5Н7О
Hdmg — диметилглиоксимато
C4H7O2Nj
en — этилендиамин C2H8N2
ру — пиридин C5H5N
bipy — 2,2/-бипиридил (C5H4NJ
Экспериментальные данные — длина связей (/св), валентные
и магнитные моменты (|х, в магнетонах Бора |iB) — для молекул
дикалов отвечают условиям их существования, данные для ионов
408
III. Молекулы. Ионы. Радикалы
условиям их нахождения в водных растворах или ионных кристаллах.
Обозначение «е,» отвечает числу неспаренных d-электронов в указан-
указанных центральных атомах. Многоточие означает отсутствие данных.
Окраска молекулярных веществ дана для конденсированного
(твердого, жидкого) состояния, окраска ионов — для водных раство-
растворов. Расшифровка использованных сокращений цвета приведена в
разделе 1—3.
4acW
[Ag(CNJ]~
[Ag(NH3J]+
[Ag(SO3S'J]3-
[AuBr4]-
[Au(CNJ]-
[Au(CNL]-
[AuCl4]-
[Au(NH3J]+
[Au(NH3L]3+
[Au(OHL]-
[Au(SO3S'J]3-
CdBr2
CdCl2
[CdCl6]4-
CdF2
[Cd(H2ON]2+
Cdl2
[Cd(NH3N]2+
{Cd(OHN]4-
CeBr3
СеСЦ
CeF3
Фор-
Форма
1
1
1
4
1
4
4
1
4
4
1
1
1
8
1
8
1
8
8
2
2
2
Связь
Ag—CA)
Ag nA)
Ag—S'<">
Au—Br<2>
Au—C(l)
Au—C<2>
Au—ClB)
Au—N<'>
Au—N<2>
Au—O<2)
Au—S'<'>
Cd—Br*»
Cd—Cl<"
Cd—ClC)
C(l_p(i)
Cd—O<3>
Cd—I(l>
Cd—N<3>
Cd—O<3>
Ce—Br<7)
Ce—Cl<7>
Ce—F<7>
ПМ
213
188
250
197
224
227
237
221
253
197
255
...
272
258
218
(n-1 )с/-Подуровень
Формула
Ag4d10
Ag4d10
Ag4d10
Aum5</8
Aul5d10
Aum5d*
Aum5d*
Aul5d10
Aum5d*
Aulu5d*
Aul5d{0
Cdu4d10
(Zd^4d^
Cd^4d^
Cdll4d10
Cd^4d^
(Zd^4d^
(Zd^4d^
Bd^4d^
Ct^5d®
Cem5d°
QW
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
D)
D)
D)
Окрас-
Окраска
бцв.
бцв.
бцв.
краен.
бцв.
бцв.
желт.
бцв.
бцв.
желт.
бцв.
бел.
бел.
бцв.
бел.
бцв.
бел.
бцв.
бцв.
бел.
бел.
бел.
409
I. Молекулы. Ионы. Радикалы
Продолжение
Чягтиня
CeF4
Cel3
CoBr2
[Co(C5H5J]
[Co(bipyK]2+
[Co(CNM]3-
[Co(CNN]3-
[Co(COL]-
CoCl2
[CoCl4]2"
CoF2
[CoF6]3"
[Co(H2ON]2+
[CoH2ON]3+
[Co(NCSL]2-
[Co(NH3N]2+
[Co(NH3N]3+
[Co(NO2N]4-
[Co(NO2N]3-
[Co(NO+)(COK]
CrBr3
[Cr(C5H5J]
[Cr(C6H6J]
[Cr(enK]3+
[Cr(bipyK]2+
[Cr(bipyJ(H2OJ]2+
[Cr(CNN]4-
[Cr(CNN]3-
[Cr(CON]
Фор-
Форма
3
2
1
—
8
5
8
3
1
3
1
8
8
8
3
8
8
8
8
3
2
—
—
8
8
8
8
8
8
Связь
Ce—F<6>
Се—1<7>
Co—Br<»
Co—(С,)
Co—N<3>
Co-C<5>
Co—С
Co-C<3>
Co—C<6>
Co—C1<1>
Co—Cl<6)
Co—F<'>
Co—F<3>
Co—O<3>
Co—O<3>
Co—N<6>
Co—N<3)
Co—N<3>
Co—N<3>
Co—N<3>
Co=N<6>
Co—С
Cr—Br<7>
Cr—(Cs)
Cr—(C6)
Cr—N<3>
Cr—N<3>
QT N<3)
Cr—О
Cr—C<3>
Cr—C<3>
Cr—C<3>
ПМ
204
297
232
210
...
189
201
190
181
212
234
172
...
...
...
...
...
...
...
176
183
217
214
...
...
...
207
192
(л-1 ^-Подуровень
Формула
Ce1^0
Сеш5</°
Coll3d7
Cou3d7
Coltt3d6
CoUI3</6
Con3^/7
Coin3J6
Con3fif7
Со1П3^/6
Сои3</7
СоП13^/6
О,огхЪй™
Con3t/7
СгП13^/3
Crll3d4
Cr°3d6
Crm3d3
Crll3d4
Crll3d4
Crll3d4
Cvm3d3
Cr°3^6
0
0
3
1
3
1
0
0
3
3
3
4
3
0
3
3
0
1
0
0
3
2
0
3
2
4
2
3
0
0
D)
...
4,86
...
0
0
...
4,70
5,40
4,90
0
4,30
5,04
0
1,90
0
0
3,94
...
0
3,93
3,27
4,79
3,20
3,72
0
Окрас.
ка
бел.
желт.
зел.
фиол.
син.
зел.
бцв.
бцв.
гол.
син.
роз.
гол.
роз.
син.
син.
желт.
желт.
желт.
желт.
желт.
т.-зел.
краен.
кор.
оранж.
краен.
краен.
син.
желт.
бцв-
--*
410
II. Молекулы. Ионы. Радикалы
Продолжение табл.
Uopthi 1Я
"dU 1 г1ЦС1
CrCl3
[Cr(Cl)O3]-
CrCl2O2
[CrF6]3'
[Cr(H2ON]2+
[Cr(H2ON]3+
««c-[Cr*(H2OLCl2]+
Crl3
[Cr(NCSN]3-
[Cr(NH3N]3+
СЮ3
сю2-
Cr(O)F4
СЮ2Р2
cro3F-
[Cu(bipyK]2+
[Cu(acacJ]
[Cu(CNJ]-
[CuCl2]-
[CuCl4]2-
tc«(H2ON]2+
'Cu(H2OJCl ]2~
tCu(H2OJ(NH3L]2+
^
Фор-
Форма
2
3
3
8
8
8
8
2
8
8
2
3
5
3
3
8
3
1
1
3
8
8
8
С„,ь
Cr—Cl<7>
Cr—Cl
Cr=O
Cr—Cl<8>
Cr=O
Cr—F<3>
Cr—O<3>
Cr-O<3>
Cr—O<3>
Cr—Cl
Cr—1G)
Cr—N<3>
Cr—N<3>
Cr=O<7>
Cr=O<6>
Cr—F<9>
Cr=O*
Cr=O<10>
Cr—F
Cr=O
Cr—F
Cu—NC>
Cu—N*
Cu—N*
Cu—O<6>
Cu—C<"
Cu—Cl<'>
Cu—Cl<6>
Cu—OC)
Cu—Cl<3>
Cu—0*
Cu—N<3>
Cu—0*
Cu—O*
4b.
ПМ
238
219
161
212
158
190
...
201
228
...
163
166
174
157
158
174
161
168
203
223
245
...
192
223
...
228
289
205
259
337
(n-1 )с(-Подуровень
Формула
Сгш3</3
CrV3</o
CrVI3</°
Cr m3d3
Cvll3d4
Cr Ul3d3
Cr m3 d3
Crm3d3
Crm3d3
Cr ^3d3
BY^3d®
Crvl3c/°
Cv^3d®
Bf^3d®
Cull3d9
C\xn3d9
Cul3d10
Cul3d10
Cull3d9
Cuu3d9
Cuu3d9
C\xll3d9
3
0
0
3
4
3
3
3
3
3
0
0
0
0
0
1
1
0
0
1
1
1
1
3,69
0
0
...
4,80
3,85
...
4,03
3,72
3,71
0
0
0
0
0
...
1,95
0
0
...
1,80
1,88
1,89
Окрас-
Окраска
фиол.
оранж.
краен.
т.-зел.
гол.
фиол.
т.-зел.
черн.
фиол.
оранж.
краен.
желт.
краен.
фиол.
краен.
син.
син.
бцв.
бцв.
оранж.
гол.
зел.
т.-син.
411
III. Молекулы. Ионы. Радикалы
Продолжение тобд
час™
[Cu(NH3J]+
[Cu(OHN]4"
DyCl3
DyF3
Dyl3
Erl3
ErF3
Erl3
EuCl3
EuF3
FeBr2
[Fe(C5H5J]
[Fe(enK]2+
[Fe(bipyK]3+
[Fe(phenK]3+
[Fe(acacK]
[Fe(CNN]4"
[Fe(CNN]3-
[Fe(COM]
[Fe(C2O4K]3-
FeCl2
FeCl3
[FeCl4]2"
[FeF6]3"
[Fe(H2ON]2+
[Fe(H2ON]3+
Фор-
Форма
1
8
2
2
2
2
2
2
2
2
1
—
8
8
8
8
8
8
5
8
1
2
3
8
8
8
С,
Cu—NA)
Cu—O<3>
Cu—0*
Dy—Cl<7>
Dy—F<7>
Dy I<7>
Er— Cl<7>
Er— F<7>
?r JG)
Eu—Cl<7>
Eu—F<7>
Fe—Br<"
Fe-(C5)
Fe—N<3>
Fe—N<3>
Fe—NC)
Fe—0<3>
Fe—C<3>
Fe—N<3>
Fe—C<5>
Fe-C*
Fe—O<3>
Fe—Cl<">
Fe—Cl<7>
Fe—Cl<6>
Fe—F<3>
Fe—0<3>
pe oC)
'«•
ПМ
195
280
247
208
282
245
205
280
250
211
224
205
189
200
184
180
217
213
230
{n-1 )с/-Подуровень
Формула
Cull3d9
Dym5d°
Dym5d°
DyU]5d°
Егш5^°
Erm5d°
Evm5d°
Eum5d°
Eum5d°
FQu3d6
FQn3d6
Fen3d6
Ftni3d5
Ftm3d5
Fem3d5
Feu3d6
Fcm3d5
Fe°3d*
Fem3d5
Fell3d6
Fcm3d5
Fell3d6
Felu3d5
FeH3J6
Fem3d5
0
1
0
0
0
0
0
0
0
0
4
0
4
1
1
5
0
1
0
5
4
5
4
5
4
5
0
(ii)
(ii)
(ii)
A2)
A2)
A2)
A3)
A3)
0
5,45
2,20
2,45
5,95
0
2,40
0
5,75
...
...
5,98
5,30
5,90
Окрас.
ка
бцв.
гол.
бел.
бел.
бел.
фиол.
роз.
фиол.
бел.
бел.
зел. .
оранж.
зел.
краен.
краен.
желт.
желт.
краен.
желт.
желт.
бел.
т.-кор-
бцв.
зел.
зел.
бцв.
412
Молекулы. Ионы. Радикалы
Продолжение табл.
Частица
[Fe(H2OLCl2]+
[Fe(NH3N]2+
[Fe(NO+)(CNM]2-
FeO^
FeO^-
FeO3-
FeO2'
GdBr3
GdCl3
GdF3
Gdl3
HfBr4
HfCl4
HfF4
Hfl4
[Hf(OHN]2-
HgBr2
[HgBr4p-
Hg(CNJ
[Hg(CNL]2-
HgCl2
IHgCl4]2-
Wg(H2ON]2+
Hgl,
IHglj-
(Hgl^
Фор-
Форма
8
8
8
2
3
3
3
2
2
2
2
3
3
3
3
8
1
3
1
3
1
3
8
1
2
Fe—O<3>
Fe—СГ
Fe—N<3>
Fe—C<3>
Fe=N*
Fe=O<7>
Fe=OF)
Fe=O<6>
Fe=O<6>
Gd—Br<7>
Gd—Cl<7>
Gd—F<7>
Gd—I<7>
Hf—Br<6>
Hf—ClF)
Hf FF)
Hf lF)
Hf— O<3>
Hg—Br^>
Hg—Br^6)
Hg-C(J)
Hg—C<6>
Hg—Cl<]>
Hg—Cl^6>
Hg—OC)
Hg—0*
Hg-10)
Hg-I<7)
Hg—1F)
ПМ
207
230
...
190
163
180
189
...
165
264
249
210
285
245
233
191
266
241
225
229
234
241
259
275
278
(л-1)с/-Подуровень
Формула
FeII!3J5
Ferf6
Fe</6
Fetf6
Fem3tf5
Fev3</3
Fevl3flf2
Gdul5rf°
Gdni5^°
Gd11^^0
Gdni5J°
HfIV5^/°
Hf^^/0
HfIV5</°
Hgn5^10
Hgn5^10
Hgn5^10
Hgn5^10
Hgn5d10
Hgn5^10
Hgn5^10
Hgn5J10
Hgn5^10
Hgn5^10
5
4
0
0
5
3
2
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
Ц.Ив
5,45
0
0
...
3,88
3,00
A4)
A4)
A4)
A4)
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
Окрас-
Окраска
желт.
бцв.
краен.
краен.
краен.
черн.
краен.
бел.
бел.
бел.
желт.
бел.
бел.
бел.
бел.
бцв.
бел.
бцв.
бел.
бцв.
бел.
бцв.
бцв.
желт.
бцв.
бцв.
413
I. Молекулы. Ионы. Радикалы
Продолжение табл.
Чяртш 1Я
[Hg(NCSL]2"
[Hg(NH3L]2+
[Hg(NO2L]2"
H0CI3
H0F3
H0I3
[IrCl6]3"
[IrCl6]2"
IrF4
IrF6
[Ir(H2ON]3+
LaBr3
LaCl3
LaF3
Lal3
LuBr3
LuCl3
LuF3
[Mn(pyN]2+
[Mn(acacK]
[Mn(CNN]4"
[Mn((CNN]3~
[Mn(CNN]2"
[Mn(COM]"
[Mn(C2O4K]3-
MnCl2
[MnCl4]2"
[MnCl6]4"
Фор-
ма
3
3
3
2
2
2
8
8
3
8
8
2
2
2
2
2
2
2
8
8
8
8
8
5
8
1
3
8
Hg—S<6>
Hg—N<6>
Hg—0<6>
Ho—Cl<7>
Ho—F<7>
Ho—1<7>
Ir—Cl<3>
Ir—Cl<3>
Ir—F<6>
Ir_FC)
Ir—O<3>
La—Br<7>
La—Cl<7>
La—F<7>
La—1<7>
Lu—Br<7>
Lu—Cl<7>
Lu—F<7>
Mn—N<3>
Mn—0<3>
Mn—C<3>
Mn—C<3>
Mn—C<3>
Mn—C<5>
Mn—C*
Mn—0<3»
Mn—Cl<»
Mn—ClF>
Mn—Cl<3>
ПМ
256
211
240
246
206
281
247
196
183
274
259
222
298
256
242
202
...
...
...
187
184
...
220
...
258
(n-1 ^-Подуровень
Формула
Hgrf10
HgJ10
Hgflr10
Нош5</°
Нош5</°
Нош5</°
Irm5d6
lr™5d5
Ir ™5d5
Irvl5</3
Ir'rf6
Laul5d°
Lani5rf°
Lani5rf°
La"'5</°
Luin5^°
MnJ5
Mnm3d4
Mnu3d5
Mnm3d4
Mnw3d3
Mrrl3d*
Mnni3d4
Mnn3d5
Mnll3d5
Mnn3t/5
0
0
0
0
0
0
0
1
1
3
0
0
0
0
0
0
0
0
5
4
1
2
3
0
4
5
5
5
0
0
0
A5)
A5)
A5)
0
1,67
...
3,30
0
0
0
0
0
0
0
0
6,00
4,95
1,80
3,18
3,94
0
4,81
...
5,95
...
Окрас-
Окраска
бцв.
бцв.
бцв.
желт.
бел.
желт.
зел.
краен.
желт.
желт.
бцв.
бел.
бел.
бел.
сер.
бел.
бел.
бел.
роз.
краен
син.
краен.
желт.
бцв.
краен.
роз.
роз.
роз.
414
II. Молекулы. Ионы. Радикалы
Продолжение табл.
ЧЯРТМ! 1Я
lOV/ I rlLJ^Ci
[MnCl6]2-
Mn(Cl)O3
MnF2
[MnF6]2"
[Mn(H2ON]2+
[Mn(H2ON]3+
[Mn(H2OJ(C2O;J]2"
[Mn(NCSN]4"
MnO3~
MnO2"
MnO4
MnO3F
MoBr4
MoBr2O2
[MoBr5OJ"
[Mo(CNM]"
[Mo(CNO]4"
[Mo(CN)8]2"
[Mo(CNLO2]4"
[Mo(CON]
MoCl4
MoCl5
[Мосуз-
[MoCl6]-
MoCL
Фор-
Форма
8
3
1
8
8
8
8
8
3
3
3
3
3
3
8
7
9
10
8
8
3
6
8
8
8
Связь
Mn—Cl<3)
Mn—Cl<6>
Mn=O
Mn—FA>
Mn—FC>
Mn—O<3)
Mn—O<3>
Mn—O'<3>
Mn—0*
Mn—N<3>
Mn=0<6>
Mn=O<6>
Mn=O<6>
Mn=O<16>
Mn—F
Mo—Br<6)
Mo—Br<l7>
Mo=O
Mo—Br<3>
Mo—Br*
Mo=O*
Mo—C<18>
Mo—C<19>
Mo—С
Mo—C<3>
Mo=O'
Mo—C<3>
Mo—Cl<6)
Mo—Cl<5>
Mo—СГ
Mo—Cl<3>
Mo—Cl<3>
Mo—Cl<3>
ПМ
227
206
159
167
...
215
225
...
171
166
163
159
172
239
242
170
255
283
186
...
...
216
220
183
213
223
227
227
246
230
226
(n-1 ^-Подуровень
Формула
MnW
Мп^З*/0
Mnll3d5
Mn™3d3
Mnll3d5
MnHI3flf4
Mnll3d5
Mnll3d5
Mnw3d2
Мп^З^/1
Мп^'З*/0
Mow4d2
MoV{4d0
Mow4dl
Mow4d2
Mom4d3
Mow4d2
Molv4d2
Mo°4de
Mow4d2
Mow4dl
Mom4d3
Mow4dl
3
0
5
3
5
4
5
5
2
1
0
0
2
0
1
0
1
0
0
0
2
1
3
1
0
H.Hb
...
0
...
3,90
5,96
4,90
6,06
1,80
0
0
1,28
0
1,80
0
1,75
0
0
0
2,10
1,54
3,83
...
0
Окрас-
Окраска
краен.
зел.
роз.
желт.
роз.
краен.
роз.
син.
син.
зел.
фиол.
зел.
черн.
т.-зел.
зел.
желт.
черн.
желт.
желт.
бел.
краен.
черн.
краен.
черн.
т.-зел.
415
III. Молекулы. Ионы. Радикалы
Продолжение табц
Чагтииа
МоС12О2
МоС14О
[МоС15О]2-
[MoF6]3"
[MoF6]-
MoF6
[Mo(NCSN]3-
MoO3
МоО2"
Mo(O)F4
[Mo(O)F5]2-
[Mo(O)F5]-
MoO2F2
[MoS4]2-
NbBr5
NbCL
D
NbCl3O
NbF5
[NbF6]-
Nb(O)F3
Фор-
Форма
3
5
8
8
8
8
8
2
3
5
8
8
3
3
6
6
3
6
8
3
с»
Мо_С1B0)
Mo=O
Mo—Cl<21>
Мо=О*
Мб—С1<3>
Мо—СГ
Мо=О
Mo—F<3>
Mo—F<3>
Mo—F<3>
Mo—N<3>
Мо=О<7)
Мо=О<6>
Mo—F<22)
Мо=О*
Mo—F<3>
Mo—F*
Мо=О*
Mo—F^>
Mo—F*
Мо=О*
Мо=ОB3)
Mo—F
Mo=S<6>
Nb—Br<5>
Nb—Br*
Nb—C№
Nb—СГ
Nb—Cl<24>
Nb=O
Nb_pE)
Nb—F*
Nb—F^3>
Nb=O^25>
Nb—F
ПМ
226
170
228
166
240
259
160
200
174
181
...
171
177
182
167
185
203
166
185
203
166
175
182
218
245
242
228
225
229
169
188
184
185
...
187
(г?-1)сУ-Подуровень
Формула
MoVI46/°
l^^o 4d
^/\ct 4d
Mom4d3
Mov4dl
MoVI4^°
Mom4d3
Mo^d0
MoVI4^0
MoVI4J0
Mow4d°
MoVI4^°
MoVI4^°
Mo^4d°
Nbv4J°
Nbv4J°
Nbv4^/^
Nbv4flf ®
Nbv4J°
Nby4d°
0
0
1
3
1
0
3
0
0
0
1
0
0
0
0
0
0
0
0
0
0
0
1,68
1,51
0
3,70
0
0
0
...
0
0
0
0
0
0
0
0
0
Окрас.
ка
желт.
зел.
зел.
кор.
желт.
бцв.
кор.
зел.
бцв.
бел.
желт.
бцв.
бел.
краен.
краен.
бел.
бел.
бел.
бцв.
бел.
416
I. Молекулы. Ионы. Радикалы
Продолжение табл.
чао™.
NdBr3
NdCl3
NdF3
Ndl3
NiBr2
[Ni(C5H5J]
[NiC2H4(PPh3J]
[Ni(enK]2+
[Ni(bipyK]2+
[Ni(HdmgJ]
[Ni(CNL]2"
[Ni(COL]
NiCl2
[NiF6]3"
[NiF6]2"
[Ni(H2ON]2+
[Ni(NCSL]2"
[Ni(NH3N]2+
NiO2~
NpF6
[OsBr6]2"
t°s(C5H5J]
[Os(enKp+
lOs(acacK]
[Os(CNN]4~
I°s(COM]
[OsCl6]2-
[OsCl4N]-
Фор-
Форма
2
2
2
2
1
—
2
8
8
4
4
3
1
8
8
8
4
8
2
8
8
—
8
8
8
5
8
5
Связь
Nd—Br<7>
Nd—Cl<7>
Nd—F<7>
Nd—jG)
Ni—Br*1*
Ni-(C5)
Ni-(C2)
Ni—P
Ni—N<3>
Ni_NC)
Ni—OB>
Ni—C<2>
Ni—CF)
Nj_ci<i>
Ni—F<3>
Ni_FC)
Ni—OC>
Ni—N<2>
Ni—N<3>
Ni=O<7>
Np_F<3)
Os—Br<3>
Os—(C2)
Os—N<3>
Os—O<3>
Os—C<3>
Os—C<5>
Os—Cl<3>
Os—Cl<28>
Os=N*
ПМ
272
258
222
292
221
211
200
220
...
190
186
184
206
...
178
...
...
...
198
251
222
...
...
236
231
160
(n-1 )с/-Подуровень
Формула
Nd"^0
Ndni5</°
Ndin5^°
Ndm5</°
Nitf8
Ni </8
Ni°3t/10
m
Nin3t/8
Ni d8
Ni n3J8
Ni U3 ds
Ni°3^10
Nin3^/8
Ni m3d7
Ni ^3/[/8
Nin3^/8
Nin3</8
NiIV3^6
NpVI6t/0
OsIV5t/4
Osn5t/6
Osin5</5
Osin5^5
Osn5^/6
Os°5t/8
OsIV5t/4
O^Sd2
0
0
0
0
2
2
0
2
2
2
0
0
2
3
0
2
0
2
...
0
2
0
1
1
0
0
2
0
...
...
...
0
3,16
2,88
0
0
2,50
0
3,20
0
3,11
2,10
B7)
1,74
0
1,60
1,81
0
0
1,66
0
Окрас-
Окраска
фиол.
фиол.
роз.
зел.
кор.
зел.
бел.
син.
син.
краен.
желт.
бцв.
желт.
фиол.
краен.
зел.
желт.
син.
черн.
оранж.
краен.
желт.
оранж.
желт.
бцв.
бцв.
оранж.
краен.
*-2004
417
III. Молекулы. Ионы. Радикалы
Продолжение табд
[OsCl5N]2-
[OsCl4(OJ]2-
OsF5
tOsF6]2-
[OsF6]"
OsF6
[Os(H2O)Cl4N]-
[Osl6]2"
[Os(N2)(NH3M]2+
[Os(N)O3]-
OsO4
Os(O)F5
[Os(OJ(OHL]2-
[OsO4(OHJ]2"
[Pd(CNL]2~
[PdC2O4J]2-
[PdCl4]2~
[PdCl6]2-
[PdF6]2-
[Pd(NCSL]2-
[Pd(NH3L]2+
[Pd(NH3N]4+
Фор-
Форма
8
8
6
8
8
8
8
8
8
3
3
8
8
8
4
4
4
8
8
4
4
8
Связь
Os—Cl<3>
Os—СГ
Os=N*
Os—Cl<3>
Os=O*
Os—F<5>
Os—F<3>
Os-F<3>
Os—F<3>
Os—Cl<3>
Os—O*
Os=N*
Os—1C)
Os—N<3>
Oss= NF>
Os=O
Os=O<6>
Os—F<3>
Os—F*
Os=O*
Os—O(H)<3>
Os=O*
Os=O<3)
Os—O(H)
Pd—C<2>
Pd—O<2>
Pd—Cl<2>
Pd—Cl<3>
P(j prC)
Pd—SB)
p,J ]\fB)
Pd—N<3>
ПМ
236
260
175
238
175
172
182
183
234
250
174
...
175
175
171
180
176
174
203
177
...
...
200
200
230
230
210
230
(n-1 )с/-Подуровень
Формула
Osd2
Os^Sd2
Osv5d3
Osw5d4
Osv5rf3
Osm5d2
Os^ed2
Oslv5rf4
Osll5d6
Osmi5d°
Osmi5d°
Os™5dl
Os^d2
OsVIII5rf°
Pd n4d8
Pd U4d*
Pd nAd%
Pd ]V4de
Pd W4d6
Pd n4*/8
Pd ll4d*
Pd W4d6
0
0
1
2
3
2
0
2
0
0
0
1
0
0
0
0
0
0
0
0
0
0
0
0
...
1,48
3,25
...
0
1,64
0
0
0
1,50
0
0
0
0
0
0
0
0
0
0
Окрас-
Окраска
краен.
оранж.
гол.
бцв.
гол.
желт.
краен.
черн.
желт.
желт.
желт.
зел.
роз.
краен.
—
бцв.
желт.
краен.
краен.
желт.
краен.
бцв.
бцв.
¦—
418
Молекулы. Ионы. Радикалы
Продолжены табл.
PrBr3
РгС13
PrF3
РПз
[PtBr4]2-
[PtBr6]2"
[Pt(C2H4)Cl3]-
[PtC2H4(PPh3J]
[Pt(CNL]2-
[Pt(CNN]2-
[Pt(COJCl2]
[PtCO(PPh3K]
[PtCl4]2-
[Ptcg2-
[PtF6]2-
[PtF6]-
[Pt(H2OJI4]
[Ptl4]2-
[Ptl6]2-
[Pt(NH3L]2+
'"Pa«c-[Pt(NH3JBr2]
*Pawc-[Pt(NH3JBr4]
eiPo«c-[Pt(NH3JCl2]
-
Фор1
ма
2
2
2
2
4
8
5
2
4
8
4
3
4
8
8
8
8
4
8
4
8
4
8
4
Pr—Br<7>
Pr—Cl<7>
Pr—F<7>
Pr—1<7>
Pt—BrB>
Pt_BrC)
Pt-(C2)<2>
Pt—Cl
Pt—(C2)<7>
Pt—p
Pt—C<2>
Pt—C<3>
Pt—C<2>
Pt—Cl
Pt_C<«)
Pt—p
Pt—ClB)
Pt—Cl<3>
Pt—F<3>
Pt_F<3)
Pt jC)
Pt—0*
Pt_IB)
Pt—1<3>
pt_ NB)
pt_NC)
pt_NB)
Pt—Br
Pt—Br<3>
Pt—N*
pt_NB)
Pt—Cl
ПМ
271
255
217
290
213
232
210
227
201
...
230
185
235
234
232
191
186
265
210
...
...
207
303
250
205
232
(n-1 )с/-Подуровень
Формула
?Tm5d°
?rm5d°
Prm5</°
Prin5</°
Pt d%
?i™5de
Pt U5d*
Pt°5^10
Pt </8
Pt ^d6
Pt n5 d%
Pto5t/10
p^ 115^/8
Pt ™5d6
Pt lw5de
?ty5d5
Pt ^5d^
Pt U5d*
Ptlv5d6
Pt U5d*
Pt lv5d6
Ptn5^/8
Pt IV5*/6
Pt U5d^
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
1
0
0
0
0
0
0
0
0
B9)
B9)
B9)
B9)
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
Окрас-
Окраска
зел.
зел.
зел.
зел.
кор.
краен.
желт.
желт.
краен.
бцв.
желт.
желт.
краен.
желт.
желт.
бцв.
черн.
черн.
краен.
бцв.
бцв.
краен.
черн.
желт.
419
Молекулы. Ионы. Радикалы
Продолжение табЛ
Час™
4MC-]Pt(NH3JCl2]
[Pt(OHN]2"
[Pt(PPh3K]
[Pt(PPh3J(O2)]
[Pt(PF3L]
PuF6
[ReBr6]2-
[Re(CNN]3-
[Re(CNLN]2"
[ReCl6]2-
Re(Cl)O3
ReCl4O
[ReCl5O]2-
[ReF6]2"
ReF6
ReF,
[Re(H2O)Br4O]"
[Rel6]2"
[Re(NCSN]2"
ReO"
Re(O)F4
ReO3F
Фор-
Форма
4
8
2
2
3
8
8
8
7
8
3
5
8
8
8
9
8
8
8
3
5
3
pt_NB)
Pt—Cl
Pt—0<3>
Pt—p<7>
pt_pCO)
Pt-(O2)
Pt_PF)
Pu_F<3)
Re—Br<3>
Re—C<3>
Re—N(C)<18>
Re—ClC)
Re—Cl<32>
Re=O
Re—Cl<33>
Re=O*
Re—Cl<3>
Re—СГ
Re=O*
Re—F<3>
Re—F<3>
Re—F<19>
Re—F*
Re—Bi<3>
Re=O*
Re—0*
Re—1<3>
Re—N<3>
Re=O<6>
Re—F<33>
Re=O*
Re=OF)
Re—F
ПМ
200
233
196
226
226
201
223
197
250
...
244
153
237
223
170
226
163
242
247
172
183
183
184
251
171
232
...
...
177
186
165
169
186
(n-1 )сУ-Подуровень
Формула
Ptn5d*
PtIV5</6
Pt°5flf10
Pt°5d10
Pt°5*/10
puvi g jo
Re1^3
Reni5J4
Rev5^2
Red\
Re^tf0
Re^d1
Rev5J2
ReIV5J3
Re^^/1
Re^Sd0
Rev5^/2
DpIVCx73
jDglVCr73
ReVII5J°
Re^Sd1
Re^^J0
0
0
0
0
0
0
3
2
0
3
0
1
2
3
1
0
2
3
3
0
1
0
H.Mb
0
0
0
0
0
C1)
3,80
...
0
3,80
0
1,48
...
3,50
...
0
3,70
3,90
0
0
Окрас-
желт.
желт.
желт.
желт.
бцв.
бел.
краен.
зел.
роз.
зел.
бцв.
кор.
зел.
зел.
желт.
желт.
зел.
черн.
зел.
бцв.
гол.
желт.
420
, Молекулы. Ионы. Радикалы
Продолжение табл.
чао™.
[Re(PPh3JCl2N]
[Re(PPh3KCl2N]
[Re(PPh3JCl30]
[Rh(CNN]3"
[Rh(CO)Cl5]2-
[RhCl6]3-
[RhCl6]2-
[RhF6]3"
[RhF6]2"
[Rh(H2ON]3+
[Rh(NCSN]3-
[Rh(NH3N]3+
lRuBr6]2-
[Ru(C5H5J]
[Ru(acacK]
[Ru(COM]
[RuCl6]3-
[RuCl6]2-
[RuCl4N]-
RuF5
[RuF6]2-
[RuF6]-
Фор-
Форма
6
8
8
8
8
8
8
8
8
8
8
8
8
—
8
5
8
8
5
5
8
8
Годои.
Re—Cl<5>
Re=N
Re—P*
Re—P<3>
Re—Cl
Re—P*
Re==N*
Re—P<3>
Re—Cl
Re—Cl*
Re=O*
Rh—C<3>
Rh—C<3>
Rh—Cl
Rh—Cl<3>
Rh—Cl<3>
Rh—FC)
Rh—F<3>
Rh—O<3>
Rh—SC)
Rh—N<3>
Ru—Br<3>
Ru—(С,)
Ru—O<3>
Ru—C<5>
Ru—Cl<3>
Ru—Cl<3>
Ru—С1<34>
Ru=N*
Ru—F<5>
Ru—F*
Ru—F<3>
Ru_pC)
ПМ
238
160
245
246
256
246
179
242
247
160
196
...
...
...
...
221
...
237
...
231
157
183
197
189
(n-1 )of-Подуровень
Формула
Rev5</2
Rev5J2
Rev5</2
RhUI4</6
Rhm4</6
RhHI4^6
RhIV4J5
Rhin4^/6
RhIV4^/5
DUIII4/76
jOUlIIj.yV6
тмЛИилб
RuIV4^/4
Run4^/6
R\xm4ds
Rx\4d*
Rwm4d5
R\xxw4dA
R\jLn4d2
Ruv4J3
RuIV4t/4
Ruv4rf3
2
2
2
0
0
0
1
0
1
0
0
0
2
0
1
0
1
2
2
3
2
3
...
0
0
0
0
...
0
0
0
2,80
0
1,70
0
1,85
2,90
...
3,08
3,70
Окрас-
Окраска
зел.
зел.
зел.
бцв.
краен.
роз.
зел.
краен.
желт.
желт.
краен.
бцв.
черн.
желт.
желт.
бцв.
краен.
желт.
оранж.
зел.
роз.
гол.
421
III. Молекулы. Ионы. Радикалы
Продолжение та^
-—
[Ru(H2O)Cl5]2-
[RuH2O(NH3M]3+
[Ru(NH3N]2+
[Ru(NH3N]3+
[Ru(NH3MCl]2+
[Ru(NH3MOH]2+
[Ru(N2)(NH3M]2+
4
RuO"
RuO4
[RuSO2(NH3LCl]+
ScBr3
ScCl3
ScF3
[Sc(H2ON]3+
Scl3
[Sc(OHN]3"
SmCl3
SmF3
TaBr5
TaCl5
[TaCy-
Фор-
Форма
8
8
8
8
8
8
8
3
3
3
8
2
2
2
8
2
8
2
2.
6
6
8
С.язь
Ru—Cl<3>
Ru—Cl*
Ru—0*
Ru—N<3>
Ru—0
Ru—NC)
Ru—N<3>
Ru—N<3>
Ru—Cl
Ru—NC>
Ru—0
Ru—N<3>
Ru—N*
Ru—N*(N)
RU=OF>
Ru=O<6>
Ru=O<6>
Ru—N<3>
Ru—S*
Ru—Cl*
Sc—Br<7>
Sc—Cl<7>
Sc—F<7>
Sc—O<3>
§c JG)
Sc—0<3>
Sm—Cl<7>
Sm—F<7>
Та—Вг<5»
Та—Br*
Та—С1<5>
Та—Cl*
Та—Cl<3>
ПМ
234
234
210
...
...
...
...
...
...
...
...
212
212
210
179
179
171
217
207
241
247
232
193
268
...
251
212
244
242
227
227
265
(n-1 )с/-Подуровень
Формула
Ruul4d5
Rum4d5
RuJ6
Rum4rf5
Rum4d5
Rum4d5
Rull4d6
Ruvl4d2
Rawu4dl
Ruvm4^o
Rull4d6
Scm3d°
c«IIhjO
Sc*^3d®
Scm3d°
Scni3cf°
Sclll3d°
Smm5d°
Smni5rf°
Tav5rf°
Tav5rf°
Tav5jo
1
1
0
1
1
1
0
2
1
0
0
0
0
0
0
0
0
0
0
0
0
0
1,76
1,95
0
1,88
2,07
1,91
0
...
0
0
0
0
0
0
0
0
C5)
C5)
0
0
0
Окрас-
ка
¦¦¦««,
краен.
бцв.
оранж.
бцв.
желт.
бцв.
оранж.
оранж.
зел.
желт.
краен.
бел.
бел.
бел.
бцв.
бел.
бцв.
—-
желт.
желт.
, ¦
оранж-
бел.
бив.
422
III. Молекулы. Ионы. Радикалы
Продолжение табл.
Частица
ТаСЦО
TaF3
TaFr
ia 5
TbCl3
ты3
[TcBr6]2"
[ТсС16]2"
[Tcl6]2-
TcO4
ThBr4
ThCl4
ThF4
TiBr4
[Ti(C5H5J]
TiCl4
[Ticy3-
mcy2-
TiF4
[TiF6]2-
[Г,(Н2ОN]3+
TU4
TmCl3
TmF3
Tml3
UBr4
№Br4O2p-
^
Фор-,
ма,
3
2
6
2
2
8
8
8 .
3
3 :
3
3
3
—
3
8
8
3
8
8
3
2
2
2
3
8
Связь
Та—С1<36>
Та=О
Та—F<7>
Та—F<5>
Та—F*
Tb—Cl<7)
Tb—I<7>
Тс—Вг<3>
Тс—С1<3>
Тс—1<3>
Tc=O<6>
Th—Br<6>
Th—Cl<6)
fh FF'
Ti—Br<6)
Ti-(C5).
jj—ciF)
Ti-Cl<3>
Ti—Cl<3>
Tl_FF)
Ti—F<3>
Ti-O<3>
Ti I F)
Tm—ClG)
Tm—F<7>
Tm—1<7>
U—Br<6>
U_BrC)
u=o*
ПМ
227
169
190
186
186
248
283
250
...
...
272
258
214
234
...
231
...
235
175
188
255
244
203
279
266
280
170
(n-1 )с/-Подуровень
Формула
Tav5</°
Tam5rf3
Tav5d°
ТЬш5</°
Tbin5J°
Tc lw4d3
Tc iy4d3
Tc W4d3
Tcvu4d0
Thlw6d0
Th IV6</°
Th™6d°
Tlw3do
Tiu3d2
Ti ^3^°
Ti11^1
Ti W3d°
Ti IV3 d°
Ti IV3 d°
Tilu3dl
Ti™3d°
Tmm5d°
Tmm5d°
Tmm5d°
U™6d°
Uwl6d°
0
3
0
0
0
3
3
3
0
0
0
0
0
0
0
1
0
0
0
1
0
0
0
0
0
0
0
0
C7)
C7)
3,94
3,88
4,14
0
0
0
0
0
0
0
1,30
0
0
0
1,75
0
C8)
C8)
C8)
C9)
0
Окрас-
Окраска
бел.
зел.
бел.
бел.
бел.
краен.
желт.
черн.
бцв.
бел.
бел.
бел.
желт.
зел.
бел.
фиол.
желт.
бел.
бел.
фиол.
бур.
желт.
зел.
зел.
бур.
желт.
423
I. Молекулы. Ионы. Радикалы
Продолжение табдш
Чагтиия
UC14
[UC14O2]2"
UF4
[UF6]2"
[UFJ-
UF6
[UF7]3-
[UF7]"
[U(H2O)8]4+
U02
uof
[UO2F5]3"
VBr4
V(Br)Cl2(O)
VBr2(Cl)O
VBr3O
[V(C5H5J]
[V(CNN]4"
[V(CNN]3~
[V(CNO]4~
[V(CNM]3"
Фор-
ма
3
8
3
8
8
8
9
9
10
1
1
9
3
3
3
3
—
8
8
9
8
Связь
U—Cl<6>
и—ci<3>
и=о*
U_FF)
U—F<3>
U—F<3>
U_FC)
U—F<19>
U-F*
U—FA9)
U—F*
и—о
U—F<19>
и—о*
V—Br<6>
V—Br<41>
V—Cl
v=o
V—Br<42>
V—Cl
v=o
V— Br<43>
v=o
V-(C5)
V_CC)
V— C<3>
V—C<19>
V_CC)
V—C*
v=o*
ПМ
253
260
168
206
237
206
200
178
226
176
224
...
196
190
224
176
230
236
212
156
236
212
156
236
156
228
216
215
215
214
231
164
(n-1 )с/-Подуровень
Формула
UIV6rf°
Uv6rf°
Uvl6</°
и^б*/0
и^б^0
rj VIg^/0
Vv3</°
V^3d®
yV^z/O
уИа^З
Y^a^3
Vni3rf2
Wm3d2
Ww3dl
0
0
0
0
0
0
0
0
0
0
0
0
1
0
0
0
3
1
0
0
1
C9)
0
C9)
C9)
D0)
0
C9)
0
C9)
C9)
0
0
...
0
0
0
0
0
...
Окрас*
ка
зел.
желт.
зел.
зел.
СИН.
бел.
зел.
желт.
зел.
бур.
желт.
желт.
краен.
желт.
желт.
желт.
фиол.
желт.
краен-
фиол.
фиол.
_-—
424
I. Молекулы. Ионы. Радикалы
Продолжение табл.
Чягтиия
nClw 1 rtLJ,Gl
(V(CO)el
VC14
[VC13(C1N)]
VC1,O
J
VF5
[VF6]3"
[VF6]2-
[VF6]"
[V(H2ON]2+
[V(H2ON]3+
[V(H2O)F5]2-
[V(H2GMO]2+
[V(H2OLSO4(O)]
[V(NH3MNH2]2+
2
V03-
[VS4]3~
WBr5
^Br2O2
lW(CN)8]3-
Фор-
ма
8
3
3
3
6
8
8
8
8
8
8
8
8
8
1
3
3
6
3
5
10
Связь
V— C<3>
V—Cl<6>
V_QD4)
V=N
V— Cl<45>
v=o
V_FE)
V—F*
V— F<3>
y_FC)
V— F<3>
V_OC)
V_0C)
V_0C)
V—F
V— O<3>
V—O*
v=o*
у qC)
V—O*(SO.)
V=O*
V—N(H3)<3>
V-N(H2)
у=о<!>
v=o<6>
W— Br<5>
W—Br*
W—BrD6)
w=o
W—Br<47>
w=o*
w—с
пм
201
214
214
165
213
160
171
171
...
i6i
...
...
230
230
167
230
...
167
...
175
215
240
240
243
171
260
173
(n-1 )с/-Подуровень
Формула
V°3d5
Vw3dl
Vv3</°
Vv3</°
V^3d®
Vu3d3
yllhj2
Y 1113^2
V{W3dl
Vm3d2
Vy3d°
Vv3c/^
\^3d®
WV5^/^
Wv^5c/^
WVI 5d®
WV5^/^
1
1
0
0
0
2
1
0
3
2
2
1
1
2
0
0
0
1
0
0
1
0
0
0
2,79
0
3,86
2,76
2,74
2,74
0
0
0
1,14
0
0
1,61
Окрас-
Окраска
зел.
краен.
желт.
желт.
бел.
зел.
желт.
бцв.
фиол.
зел.
зел.
син.
син.
краен.
краен.
бцв.
краен.
кор.
краен.
черн.
син.
425
III. Молекулы. Ионы. Радикалы
Продолжение rnafy
Частица
[W(CON]
WC15
WC16
W(C1)F5
WC12O2
WC14O
[WC15O]2-
WF6
[W(NCSN]3~
WO2"
W(O)F4
[WS4]2"
YBr3
YCI3
YF3
«3
YbCl3
YbF3
ZnBr2
[Zn(pyJCl2]
[Zn(CNL]2"
ZnCl2
[ZnCl4]2"
Фор-
ма
8
6
8
8
3
5
8
8
8
3
5
3
2
2
2
2
2
2
1
3
3
1
3
Связь
w—c<3>
W— Cl<5>
w—cr
W— Cl<3>
W— Cl<3>
W—F
W_C1D9)
w=o
W_dD9)
w=o*
W— Cl<3>
w=o
W—F<3>
W— N<3>
w=o<6>
\y_pE0)
w=o*
w=s<6>
Y— Br<7>
Y-C1<7>
Y— F<7>
Y—1G)
Yb—Cl<7>
Yb—F^
Zn—Вг^
Zn—N<6>
Zn—Cl
Zn—C^
zn—a<!>
Zn—Cl<6>
/«.
ПМ
230
226
226
226
225
184
227
171
228
169
...
183
179
183
168
217
263
244
204
280
243
203
221
215
235
202
205
225
(n-1 )с/-Подуровень
Формула
W°5<f6
Wv5rf'
wvi5i/o
wvi5^o
WV5J'
WIII5J3
Wvl5rf°
WVI5rf°
Y"Md°
Yd°
Ym4d°
Yn4d°
Ybm5d°
Ybm5d°
Zn»3rf10
Zn»3rf10
Znrf10
Znrf10
Znrf10
Zn»3rf10
0
1
0
0
0
0
1
0
3
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
1,17
0
0
0
0
1,52
0
3,80
0
0
0
0
0
0
0
E1)
E1)
0
0
0
0
0
0
Окрас-
ка
бел.
т.-зел.
фил.
бцв.
желт.
краен.
зел.
бцв.
зел.
бцв.
бел.
краен.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бел.
бцв.
бел.
бив.
426
Ш. Молекулы. Ионы. Радикалы
Окончание табл.
час™.
ZnF2
[Zn(H2ON]2+
[Zn(H2OJ(NH3L]2+
Znl2
[Zn(N3L]2-
[Zn(NCSL]2-
[Zn(NH3N]2+
[Zn(NH3JCl2]
ZnO$"
[Zn(OHK]-
[Zn(OHL]2"
ZrBr4
ZrCl2
ZrCl3
ZrCl4
[ZrCl6]2-
ZrF3
ZrF4
[ZrF6]2-
[ZrF7p-
4
[Zr(OHN]2-
Фор-
Форма
1
8
8
1
•3
3
8
3
3
2
3
3
1
2
3
8
2
3
8
9
3
8
Связь
Zn—F<]>
Zn—O<3>
Zn—N<3>
Zn—0*
Zn—1<!)
Zn_NF)
Zn—N<6>
Zn—NC>
Zn—N<6)
Zn—Cl
Zn=O<6>
Zn—0<7>
Zn—0<6>
Zr—Br<6>
Zr—ClA)
Zr—Cl<7>
Zr—Cl<6>
Zr—Cl<3>
Zr— F<7>
Zr—F®
2r FC)
Zr_Fd9)
2x l<6>
Zr—0<3>
ПМ
181
...
238
203
215
220
200
198
247
230
230
232
245
193
190
208
200
266
...
(n -1 )сУ-Подуровень
Формула
Znll3d10
Znu3d10
Zn»3</10
Znn3</10
Zn»3</10
Znu3d]0
Znu3d10
Znd10
Znn3d10'
Znll3d10
Znu3d10
ZrIV4J°
Zrn4^2
Zr11^1
Zrw4d°
Zrw4d°
Zrm4dl
Zr™4d°
Zrw4d°
Zvlw4d0
Zr™4d°
Zrlv4d0
e^
0
0
0
0
0
0
0
0
0
0
0
0
2
1
0
0
1
0
0
0
0
0
Ц.Ив
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
Окрас-
Окраска
бел.
бцв.
бцв.
бел.
бцв.
бцв.
бцв.
бел.
бцв.
бцв.
бцв.
бел.
черн.
сер.
бел.
бцв.
сер.
бел.
бцв.
бцв.
оранж
бцв.
427
III. Молекулы. Ионы. Радикалы
A) В—А—В 180°
B) В—А—В 90°
C) В—А—В 90°,
В—А—В* 90°
D) 4Д ех = 1
E) В—А—В 120°,
В—А—В* 90°
F) В—А—В 109,5°
G) В—А—В 120°
(8) С1—Сг—С11130,
О—Сг—ОНО0
(9) F—Сг—О* 100°
A0) О—Сг—О 102°,
F—Сг—F119°
A1) 4/^ = 3
A2) 4/»,е, = 1
A4L/7,е, =
A6H—Мп—О 110°,
F—Мп—О 109°
A7) Вг— Мо—Вг110°,
О—Мо—О 105°
A8) В—А— В 90°,
В—А—В* 90°
A9) В—А— В 72°,
В—А—В* 90°
B0) С1—Мо—С1112°,
О—Мо—О 104°
B1) С1—Мо—С1 87°,
С1—Мо—О* 103°
B2) F—Мо—О* 100°
B3) О—Мо—О 110°,
F—Mo—F 113е
B4) С1—Nb—C1107°,
С1—Nb—0 112°
B5) F—Nb—F 105°
B6) 4/3, ех = 3
B7) 5/1, ^ = 1
B8) Cl—Os—N* 105°
B9) 4/2, ех = 2
C0) Р—Pt—P 101°
Cl—Та—0 112°
C7L/8,^ = 6
C2) Cl—Re—О 108°,
О—Re—0 111°
C3) В—Re—В* 103
C4) Cl—Ru—Cl 86°,
Cl—Ru—N* 105°
C5) 4/5, ex = 5
C6) Cl—Та—Cl 107°,
C9) 5/2, e{ = 2
D0Mf\ex = l
D1) Br—V—О 108°,
Cl—V—С111Г,
Cl—V—О 108°
D2) Вг—V—Brill0,
Br—V—О 108°,
Cl—V—О 108°
D3) Br—V— Brll2°,
Br—V—О 107°
D4) Cl—V— Cl 113°
D5) Cl—V— C11120,
Cl—V—О 107°
D6) Br—W— Br 110°,
O—W—О 105°
D7) Br—W—О* 104е
D8) Cl—W— C11120,
O—W—О 104°
D9) Cl—W—Cl 87°,
Cl—W—O* 102°
E0) F—W—О* 100е
E1) 4/13, ex = 1
7.3. Геометрическая форма, длина связей
и валентные углы в частицах
с несколькими центральными атомами
Представлены многоатомные химические частицы (молекулй я
ионы) АтВл, где атомы А — центральные, а атомы (группы атомов, ли-
ганды) В — концевые.
Экспериментальные данные ддя молекул — длина связей (/св), ва"
лентные углы, а иногда и двугранные углы (а) — отвечают условий
их существования, данные для ионов — условиям их нахождения *
водных растворах или ионных кристаллах. Многоточие означает от*
сутствие данных.
428
I. Молекулы. Ионы. Радикалы
Пространственные изображения геометрических форм частиц
АПА
В А А* В*
А А*В**
QHCJ
3/A A
A A
В
Г А
В*
?
х
7
ул* в**/
\ /А /
10
'А А"
11
I
в* /ё^±7\^в I
i
12
14
17
i I
I i
i i
15
18
21
429
. Молекулы. Ионы. Радикалы
27
28
29
В пространственном изображении геометрических форм показано
расположение атомов А и В и все а-связи А—А и А—В. Символы не-
некоторых атомов А и В (на изображениях) и символы некоторых эле-
элементов (в таблице) отмечены звездочками (*) для идентификации по-
положений этих атомов.
430
II. Молекулы. Ионы. Радикалы
Частица
А12Вг6
[А12Вг7Г
А12С16
А1216
[А12О(ОНN]2-
As4
As4O6
[ASjOjFg]2-
As4S6
Au2Br6
Au2Cl6
B2C14
в2н6
в2о3
b2s3
c2Br2
C:Br6
Форма
19
21
19
19
21
2
31
26
31
18
18
12
19
8
8
2
3
20
Связь
Al—Вг
Al—Вг*
Al—Вг
Al—Вг*
Al—Cl
Al—Cl*
Al—I
Al—I*
Al—O(H)
A1=O*
As—As
As—0
As—F
As=O*
As—S
Аи—Вг
Au—Br*
Au—Cl
Аи—СГ
В—В
В—Cl
в—н
в—н*
B=O
B—0*
B=S
B—S*
Bi—Bi
C=C*
C—Br
C*—Br*
С—С
С—Вг
'ев» ПМ
221
238
226
243
208
230
253
258
175
244
178
181
181
225
359
359
224
233
170
175
120
134
121
131
165
181
288
120
180
180
152
193
Валентный угол
Br—Al—ВгН5"
Br*—A1—Вг* 87°
Br—A1—ВгПЗ"
Br*—A1—Вг* 104"
Cl—Al—C1123"
СГ—А1—СГ 79°
I—A1—1112°
Г—А1—I* 102°
А1—О*—А1132"
As—-As—As 60"
О—As—О 99"
As—О—As 128"
As—0*—As 95°
S—As—SI 14"
As—S—As 100"
Br—Au—Br 90°
Br*—Au—Br* 86"
Cl—Au—Cl 90"
СГ—Аи—СГ 86"
Cl—В—С1119"
a 90"
H—В—Н 122"
H*—B—H* 101°
О—В—О* 180°
В—О*—В 132"
S—В—S* 180"
B—S*—В 96"
Bi—Bi—Bi 60°
С*—С—Br 180"
С—С*—Br* 180°
С—С—Br 109,5"
Br—C—Br 109,5"
431
I. Молекулы. Ионы. Радикалы
Продолжение табл
Частица
CBr3(NO2)
С2С12
С2С14
С2С16
CC13(NO2)
C2F4
C2F6
С2Н2
С2Н4
с2н6
C2N2
C(NO2)F3
С3О2
Форма
17
3
И
20
17
11
20
3
И
20
3
17
29
Связь
С—N*
С—Вг
N*=O*
ппп
1 1 III
с=с
С—Cl
с—сг
с—с
С—С1
С—N*
С—С1
N*=O*
с=с
С—F
С—F*
С—С
С—F
С—Н
С*—Н*
С=С
С—Н
С—Н*
С—С
С—Н
С—С*
С—N*
С—F
N*=O*
С=С*
С=О
/св, пм
122
192
159
120
164
164
130
172
172
157
174
159
173
119
131
132
132
156
132
120
106
106
134
109
109
154
111
. 138
116
116
156
133
121
129
116
Валентный угол
Вг—С—ВгП0°
Вг—С—N* 108°
С—N*—0*111°
О*—N*—О* 134°
С*—С—С1180°
С—С*—СГ 180
С—С—СП 14°
С—С—СП 14°
С—С—С1109,5°
С1—С—С1109,5°
С1—С—С1112е
С1—С—N* 106°
С—N*—0*113°
О*—N*—О* 132°
С—С—F 124°
С—С—F* 124°
С—С—F 109,5°
F—С—F 109,5°
С*— С—Н 180°
С—С*—Н* 180°
С—С—Н 121°
С—С—Н* 121°
С—С—Н 109,5°
Н—С—Н 109,5°
С*—С—N 180°
С—С*—N* 180°
F—С—F110°
F—С—N* 109°
С—N*—0*112°
О*—N*—О* 132°
С—С*—С 180°
О—С—С* 180°
__——
432
II. Молекулы. Ионы. Радикалы
Продолжение табл.
Частица
C(pHJF3
ci2o7
[Со2(СО)8]
сг2о-
Сг3О?0-
Cs2Br2
Cs2Cl2
Cs2F2
Cs2I2
Cu2Cl2
[Cu2Cl6]2-
[Fe2(CO)9]
Fe2Cl6
|Pe2(NOL,2]
Ga2Br6
Ga2ci6
Форма
17
21
23
21
30
6
6
6
6
6
18
25
19
19
19
19
20
Связь
С—P*
С—F
P*—H*
C1=O
Cl—0*
Co—Co
Co—С
Co—С*
Cr=O
Cr—O*
Cr=O
Cr—0*
Cs—Br
Cs—Cl
Cs—F
Cs—I
Cu—Cl
Cu—Cl
Cu—Cl*
Fe—Fe
Fe—С
Fe—С*
Fe—Cl
Fe—Cl*
Fe—N
Fe—I*
N=0
Ga—Br
Ga—Br*
Ga—Cl
Ga—Cl*
Ge—Ge
Ge—H
/св, пм
190
133
143
141
172
252
180
192
160
185
160
170-180
329
311
256
354
211
220
230
246
184
180
211
228
167
258
115
225
235
209
229
241
153
Валентный угол
F—С—F 108°
С—Р*—Н* 92°
H*—P*—H* 97°
O—Cl—О 97°
Cl—O*—Cl 115°
С—Со—С 90°
Cr—О*—Cr 115-120°
O—Cr—0 105-113°
Cr—O*—Cr 136°
Br—Cs—Br 94°
Cl—Cs—C191°
F—Cs—F 79°
I—Cs—I 94°
Cl—Cu—Cl 105°
Fe—C*—Fe 78°
Cl—Fe—Cl 128°
СГ—Fe—Cl* 92°
Br—Ga—BrllO°
Ga—Br*—Ga 93°
Cl—Ga—C1112°
Ga—СГ—Ga 93°
H—Ge—H 109°
433
II. Молекулы. Ионы. Радикалы
Продолжение табл
Частица
H2CN2
HCNO
Н2С2О4
HDS2
HN3
HNCO
HNCS
H2O2
H2S2
Hg2Br2
Hg2Cl2
Hg2F2
[Hg2(H2OJ]2+
Форма
10
3
11
7
4
4
4
7
7
3
3
3
3
Связь
N—С*
C*=N"
N—H
с—н
N*=O*
С—С
C=O
C—O*(H)
s—s
S—H
S—D
N=N*
N*sbN"
N—H
N=C*
C'=O"
N—H
N=C*
c*=s**
N—H
O—O
0—H
s—s
S—H
Hg-Hg*
Hg—Br
Hg*-Br*
Hg—Hg'
Hg—Cl
Hg*-Cl*
Hg-Hg*
Hg—F
Hg*-F*
Hg—Hg'
Hg—О
Hg*-O*
/св, ПМ
135
116
100
117
103
120
154
122
137
206
133
132
124
113
98
121
117
99
122
156
99
145
97
206
133
249-269
271
271
249-269
243
243
249-269
214
214
240-270
215
215
Валентный угол
N—С*—N" 180°
H—N—H113°
a 142°
H—C—N* 180°
C—N*—O* 180°
С—С—О 122°
О—С—О*(Н) 125°
S—S—H 91°
S—S—D91°
N—N*—N" 180°
H—N—N*115°
N—С—О" 180°
H—N—C* 128°
N—C*—S" 180°
H—N—C* 135°
H—О—О 100°
a 119°
H—S—S 92°
a91°
Hg—Hg*—Br* 180°
Hg*—Hg—Br 180°
Hg—Hg*—Cl* 180°
Hg*—Hg—Cl 180°
Hg—Hg*—F* 180°
Hg*—Hg—F 180°
Hg—Hg*—O* 180°
Hg*—Hg—О 180°
434
II. Молекулы. Ионы. Радикалы
Продолжение табл.
Частица
12О5
К2Вг2
К,С12
K2F2
К212
Li2Br2
Li2Cl2
Li2F2
Li2I2
[Mn2(COI0]
[Мо2С18]^-
транс-Ы2?2
4«c-N2F2
N2F4
«Pohc-N2H2 .
4«c-N2H2
N2H4
Форма
3
18
15
6
6
6
6
6
6
6
6
27
24
5
5
14
5
5
14
Связь
Hg-Hg*
Hg-I
Hg*—Г
I—Cl
I—СГ
1=0
I-O*
K—Br
K—Cl
K—F
K—I
Li—Br
Li—Cl
Li—F
Li—I
Mn—Mn
Mn—С
Mn—С*
Mo—Mo
Mo—Cl
N=N
N—F
N=N
N—F
N—N
N—F
N=N
N—H
N=N
N—H
N—N
N—H
1Cb> ПМ
249-269
269
269
239
270
179
194
302
286
235
326
235
223
175
254
292
179
183
214
244
123
140
121
141
149
137
124
105
123
101
145
102
Валентный угол
Hg—Hg*—Г 180°
Hg*—Hg—I 180°
Cl—I—Cl 94°
Cl*—I—Cl* 84°
O—I—О 100°
I—0*—I 139°
Br—K—Br 101°
Cl—K—Cl 98°
F—K—F 88°
I—K—1104°
Br— Li—BrllO°
Cl—Li—Cl 108°
F—Li—F 105°
I—Li—1116°
C—Mn—С 90°
С—Mn—С* 90°
Mn—Mn—С* 180°
Cl—Mo—Cl 90°
Cl—Mo—Mo 90°
N—N—F 106°
N—N—F 114°
F—N—F 103°
N—N—F 101°
a 64°
N—N—H 109°
N—N—H 100°
H—N—H 112°
N—N—H110°
a 90°
435
II. Молекулы. Ионы. Радикалы
Продолжение тщ
Частица
N2Hf
N(NH2)O2
транс-Ы201~
цис-П2О22-
N2O3
N2O4
N2O5
Na2Br2
Na2Cl2
Na2F2
Na2I2
Nb2Br10
O2F2
P4
P2F4
P2H4
P2I4
P4O6
Форма
20
13
5
5
9
11
16
6
6
6
6
26
7
2
14
14
14
31
Связь
N—N
N—H
N—N*
N=O
N*—H*
N=N
N—0
N=N
N—0
N—N*
N*=O
N*=O*
N=0**
2OO
1 II II
222
N=0
N—0*
Na—Br
Na—Cl
Na—F
Na—I
Nb—Br
Nb—Br*
0—0
0—F
P—P
P—P
P—F
P—P
P—H
P—P
P—I
P—0
'св.™
146
98
143
121
101
125
141
175
115
186
120
122
114
178
119
118
121
146
269
254
208
291
244
272
122
158
221
228
159
222
145
221
248
165
Валентный угол
О—N—0 130°
Н*—N*—H*115°
а 128°
0—N—N 120°
0—N—N 90°
N—N*—0 113°
N—N*—0*111°
N*—N—0** 105°
0—N—0* 135°
0—N—0 134°
N—0*—N 109°
а 95°
Br—Na—Br 108°
Cl—Na—Cl 105°
F—Na—F 95°
I—Na—1111°
Br—Nb—Br90°
Br—Nb—Br* 90°
O—O—F 109,5°
а 88°
P—P—P 60°
P—P—F 95°
F—P—F 99°
P—P—H 95°
H—P—Н9Г
P—P—I 90°
I—P—I 102°
0—P—0 99°
P—О—Р 128°
436
II. Молекулы. Ионы. Радикалы
Продолжение табл.
Частица
P4Oio
Rb2Br2
Rb2Cl2
Rb2F2
Rb2I2
[Re2(COI0]
Re2Cll0
[Re2Cl10O]4-
Re2O7
[Ru2Cl10O]4-
S2Br2
S2C12
S2F2
S2F10
S2N2
Форма
32
6
6
6
6
27
26
28
21
28
7
7
7
27
6
5
20
22
28
Связь
P—0
P—0*
Rb—Br
Rb—Cl
Rb—F
Rb—I
Re—Re
Re—С
Re—С*
Re—Cl
Re—Cl*
Re=O*
Re—Cl
Re=O
Re—0*
Ru—0*
Ru—Cl
S—S
S—Br
S—S
S—Cl
s—s
S—F
S—S
S—F
S—F*
N—S
s=s
s=o
s—s
s=o
S—0*
0*—0*
Sb—F
Sb—F*
/св, пм
158
146
315
298
245
339
302
201
201
225
247
186
170
180
180
198
224
193
206
189
164
221
156
156
162
202
146
215
143
150
146
180-190
200-210
Валентный угол
0—P—0 101°
P—0—P 124°
0—P—0*117°
Br—Rb—Br 98°
Cl—Rb—Cl 95°
F—Rb—F 84°
I—Rb—I 101°
C—Re—С 90°
С—Re—С* 90°
Re—Re—С* 180°
Cl—Re—Cl 90°
Cl—Re—Cl* 90°
Re—0*—Re 180°
Cl—Re—Cl 90°
Re—0*—Re 165°
0—Re—0...
Ru—0*—Ru 180°
Cl—Ru—Cl 90°
S—S—Br 105°
a 84°
S—S—Cl 108°
a 85°
S—S—F 108°
a 93°
F—S—F 90°
F—S—F* 90°
S—S—F* 180°
N—S—N 85°
S—S—0 113°
S—0*—0* 122°
Sb—F*—Sb 150°
F—Sb—F 90°
437
II. Молекулы. Ионы. Радикалы
Окончание таб^
Частица
Sef
[Se2(NCSN]2"
Si2Cl6
(SiCl3JO
Si2H6
[Tc2(COI0]
Tef
[Ti2ci9r
[W2Cl10O]4-
[Xe2F3]+
[Xe2Fn]+
Форма
1
18
20
21
20
29
27
1
25
21
28
8
28
Связь
Se—Se
Se—S
Se—S*
Si—Si
Si—Cl
Si—0*
Si—Cl
Si—Si
Si—F
Si—Si
Si—H
Tc—Tc
Тс—С
Те—С*
Те—Те
Ti—Cl
Ti—Cl*
V=0
V—0*
W—Cl
W—0*
Xe—F
Xe—F*
Xe—F
Xe—F*
/св, пм
228
230
300
234
202
164
234
157
232
148
302
200
190
266
221
250
163
182
241
187
190
214
184
221
Валентный угол
Se—Se—Se 90°
Cl—Si—Si 109,5°
Cl—Si—Cl 109,5°
Cl—Si—0* 130°
Cl—Si—СП 10°
Si—Si—Fill0
F—Si—F...
С—Те—С 90°
С—Те—С* 90°
Tc—Tc—С* 180°
Те—Те—Те 90°
...
0—V— 0 93-123°
V—0*—V 145°
W—0*—W 180°
Cl—W—Cl 90°
F—Xe—F* 178°
Xe—F*—Xe 150°
F—Xe—F 90°
Xe—F*—Xe 180°
Термодинамика
1. Энтальпия образования,
энтропия и энергия Гиббса
образования веществ
Представлены термодинамические характеристики: стандартная
энтальпия образования АЯ^98, стандартная энтропия S^9 стандарт-
стандартная энергия Гиббса образования AG^g Для индивидуальных веществ
(атомов, молекул, ионов, радикалов, формульных единиц) в различ-
различных агрегатных состояниях (газообразном, жидком, твердом) и для
веществ в состоянии водного раствора (в этом случае в графе «5^8»
приведена стандартная парциальная энтропия). Данные для некото-
некоторых веществ относятся к упрощенным формулам (в сноске дана точ-
точная формула). Для большинства твердых веществ указана конкретная
кристаллическая система (сингония).
Для электрона приняты следующие значения:
е~ (газ) ег (р-р)
Д#?98 = 0 кДж/моль Ai/?98 = —164 кДж/моль
^98 = 20,869 Дж/(К • моль) 5^98 = -8 Дж/(К • моль)
А(?298 = 0 кДж/моль А(?298 = —157 кДж/моль
Не приведены термодинамические характеристики сильных элект-
электролитов в водном растворе, поскольку они могут быть рассчитаны
суммированием значений для их ионов. Знаком «—» обозначено от-
отсутствие данных.
Принятые сокращения
аморфн. — аморфный р-р — водный раствор
гекс. — гексагональный тв. — твердый
жВДк. — жидкость тетр. — тетрагональный
куб. — кубический триг. — тригональный
монокл. — моноклинный трикл. — триклинный
ромб. — ромбический
439
IV. Термодинамика
Вещество
Ас
Ас2О3
Ag
Ag+
(AgIAgIII)O2
Ag3As04
AgBr
AgBrO3
Ag2C2
AgCN
[Ag(CNJ]-
[Ag(CNJ],K
Ag2CO3
AgCl
[AgCl]
[AgCl2]-
AgClO2
AgClO3
AgClO4
Ag2CrO4
AgF
AgF•2H2O
AgF•4H2O
[AgF]
AgH
[AgHS]
[Ag(HSJ]-
Agl
AgIO3
Ag2MoO4
AgN3
Состояние
газ
куб.
гекс.
газ
куб.
Р-Р
куб.
куб.
газ
куб.
тетр.
ТВ.
триг.
Р-Р
гекс.
монокл.
газ
куб.
Р-Р
Р-Р
тетр.
тетр.
куб.
монокл.
газ
куб.
ТВ.
ТВ.
Р-Р
газ
Р-Р
Р-Р
газ
гекс.
ромб.
куб.
ромб.
Л98.
кДж/моль
+385
0
-2047
+285
0
+ 106
-115
-634
+96
-101
-8
+358
+146
+269
-13
-506
+92
-127
-73
-245
+8
-22
-32
-725
+7
-206
-802
-1389
-240
+306
—
—
+ 159
-62
-169
-838
+309
qO
^298'
Дж/(К ¦ моль)
+ 188
+63
+ 134
+ 173
+43
+73
+28
+276
+257
+ 107
+ 152
—
+ 107
+201
+142
+ 167
+245
+96
+ 155
+231
+ 136
+ 150
+ 162
+218
+236
+84
+168
+264
+26
+205
—
—
+264
+ 115
+ 149
+229
+99
^298.
кДж/моль
+348
0
-1958
+246
0
+77
-37
-545
-77
-97
+74
—
+ 157
+302
+38
-437
+70
-ПО
—73
-215
+75
+71
+88
-635
-20
-188
-670
-1146
-205
+277
+9
-4
+ 110
-66
-92
-750
+378
440
IV. Термодинамика
Продолжение табл.
Вещество
Ag3N
[Ag(NH3J]+
AgNO2
[AgNO2]
AgNO3
Ag2O
[AgOH]
[Ag(OHJ]"
Ag3PO4
Ag2S
[AgSO4]~
Ag2SO4
[Ag(SO3S)]-
[Ag(SO3SJ]3-
Ag2Se
Ag2Se03
Ag2Se04
Ag2Te
Ag2WO4
Al
Al+
Al3+
Al2
AlAsO4 • 2H2O
AlBr
AlBr2
AlBr3
Al2Br6
ЧС3
A1C1
A1C12
AICI3
Состояние
ТВ.
P-P
ромб.
P-P
ромб.
куб.
P-P
P-P
куб.
монокл.
ромб.
P-P
ромб.
P-P
P-P
ромб.
ТВ.
ромб.
монокл.
ТВ.
газ
куб.
газ
Р-Р
газ
ТВ.
газ
газ
газ
монокл.
газ
триг.
газ
газ
газ
монокл.
Д«298.
кДж/моль
+255
-111
-45
—
-124
-31
—
—
-990
-33
-30
-797
-715
—
-1279
-44
-342
-431
-36
-923
+330
0
+913
-531
+462
—
+ 16
-166
-422
-514
-971
-208
-46
-319
-583
-704
^298'
Дж/(К • моль)
—
+246
+ 128
+212
+ 141
+ 121
—
—
+258
+144
+ 151.
+ 136
+200
—
+74
+ 151
+316
+225
+ 155
+253
+ 164
+28
+ 150
-300
+230
__
+240
—
+349
+ 180
+512
+89
+228
+292
+322
+ 111
AGgge,
кДж/моль
—
-18
+ 19
+40
-33
-И
-92
-260
-894
-41
-40
-674
-618
-486
-1027
-51
-310
-338
-42
-841
+289
0
+870
-492
+410
-1709
-25
—
-450
-491
-971
-196
-72
-331
-571
-629
441
IV. Термодинамика
Продолжение maf^
Вещество
А1С13 * 6Н2О
А12С16
[AlCl4],Na
A1F
A1F2+
A1F2
AlF^
A1F3
[A1FJ
[AlFJ-
[A1F5]2~
[A1F6]3"
[AlF6],Na3
A1H
A1H2
AIH3
[A1H4],K
[A1H4],U
[AlH4],Na
All
A1I2
AII3
A12I6
A1N
A1(NH4)(SO4J
A1(NH4)(SO4J • 12H2O
A1(NO3K • 6H2O
A1(NO3K • 9H2O
A1O
A12O3
A12O3 • H2O
A12O3 • 3H2O
A1OH2+
Состояние
триг.
газ
ромб.
газ
Р-Р
газ
Р-Р
газ
триг.
Р-Р
Р-Р
Р-Р
Р-Р
монокл.
газ
газ
гекс.
ТВ.
монокл.
ТВ.
газ
газ
газ
гекс.
газ
газ
гекс.
гекс.
куб.
ТВ.
монокл.
газ
гекс.
аморфн.
аморфн.
Р-Р
АН°98,
кДж/моль
-2693
-1293
-1143
-264
-861
-687
-1191
-1211
-1510
-1524
-1858
-2193
-2533
-3317
+258
-289
-12
-167
-117
-114
+64
-38
-208
-308
-513
+440
-318
-2352
-5944
-2871
-3757
+89
-1675
-2009
-2552
-767
°298>
Дж/(К • моль)
+318
+444
+ 188
+215
-165
—
-59
+277
+66
+8
+40
+47
+21
+238
+ 188
—
+30
+ 129
+88
+ 124
+248
—
+376
+ 190
+585
+227
+20
+216
+697
+468
—
+218
+51
+97
+ 166
-157
д^98,
кДж/моль
-2263
-1209
-1042
-289
-812
—
-1124
-1194
-1431
-1427
-1721
-2008
-2291
-3153
+230
—
+46
-100
-48
-49
+16
—
-260
-304
-567
+409
-287
-2038
-4938
-2204
—
+63
-1582
-1821
-2284
-701
——--
442
IV. Термодинамика
Продолжение табл.
Вещество
AKOH>2
А1(ОНK
[А1(ОНK]
[А1(ОНL]"
А1О(ОН)
А1Р
А1РО4
А1РО4-2Н2О
A1S
A12S3
[A1SO4]+
[A1(SO4J]"
A12(SO4K
A12(SO4K • 6H2O
A12(SO4K • 18H2O
AlSe
Al2Se3
AlTe
Al2Te3
Am
Am3+
AmF3
AmO2
Am2O3
Ar
[At]
Ar+
As
As2
4
-
Состояние
P-P
МОНОКЛ.
триг.
P-P
P-P
ромб, (а)
ромб, (у)
газ
гекс.
ромб.
газ
гекс.
Р-Р
Р-Р
гекс.
МОНОКЛ.
трикл.
газ
гекс.
газ
ТВ.
газ
гекс.
Р-Р
гекс.
куб.
гекс.
газ
Р-Р
газ
аморфн.
газ
триг. (а)
газ
газ
ромб. (($)
AH°98J
кДж/моль
—
-1295
-1290
—
-1490
-1000
-988
= +420
-1734
-2353
+201
-509
-1431
-2337
-3441
-5313
-8879
= +230
-567
= +270
-326
+284
0
—
—
-1081
-1761
0
-12
+ 1514
+ 14
+288
0
+ 194
+ 143
+32
^298'
Дж/(К • моль)
—
+70
—
—
+ 144
+35
+48
—
+91
+ 134
+230
+96
-192
-128
+239
+469
—
—
—
—
—
+195
+72
-159
—
+84
+ 159
+ 155
+59
+ 166
—
+ 174
+36
+242
+330
—
AG°98,
кДж/моль
-907
-1157
—
-1111
-1305
-921
-913
—
-1618
-2111
+150
-492
-1253
-2008
-3100
-4623
—
—
—
—
—
+247
0
-672
-1518
-962
-1674
0
+ 16
+ 1517
—
+247
0
+ 143
-88
—
443
IV. Термодинамика
Продолжение табЛ
Вещество
AsBr3
AsCl3
AsF3
AsF5
AsH2
AsH3
Asl3
AsO
AsO^
AsO^"
As2O3
As2O5
As4O6
As2S3
As2S5
As4S4
At-
At
At2
Au
Au+
AuBr
AuBr3
[AuBr4]"
[Au(CNJ]"
AuCl
[AuClJ-
AuCl3
[AuCl4]-
[AuCl3(OH)]-
Состояние
газ
ромб.
газ
жидк.
газ
жидк.
газ
газ
газ
триг.
газ
Р-Р
Р-Р
куб. (р)
монокл. (а)
ромб.
газ
монокл.
аморфн.
монокл. (а)
газ
газ
газ
ромб.
газ
куб.
Р-Р
ТВ.
ТВ.
Р-Р
Р-Р
ромб.
Р-Р
монокл.
Р-Р
Р-Р
АН 298,
кДж/моль
-130
-193
-271
-315
-921
-957
-1238
+ 159
+66
-80
+70
-664
-892
-666
-664
-925
-1209
-96
-146
-146
-174
+98
+84
0
+368
0
+222
-14
-54
—
—
-35
-174
-118
-325
—
^298'
Дж/(К • моль)
+364
+ 159
+326
+213
+289
+ 181
+353
—
+223
+ 164
+233
-187
-165
+ 117
+ 127
+ 105
+381
+ 164
—
+254
+ 175
+ 187
+276
+ 121
+ 180
+48
+ 128
+98
+ 155
+314
+ 123
+ 108
+257
+ 152
+258
—
кДж/модь
-16(Р
-162
-258
-268
-906
-910
-1181
—
+69
-66
+42
-448
-652
-588
-589
-782
-1098
-95
—
-141
-202
+60
+38
0
+329
0
+ 179
-6
-18
-159
+269
-20
-151
-49
-235
-306
444
IV. Термодинамика
Продолжение табл.
Вещество
AuF
AuF3
Aul
Au2O3
AU2O3 • 3H2O
[Au(OHK]
[Au(OHL]-
AuSb2
AuTe2
В
B+
B2
BBr
BBr2
BBr3
BC1
BC12
BC13
b2ci4
BF
BF2
BF3
1BF4]-
1BF4],K
[BF4],Li
IBF4],Na
IBF4],(XeF+)
BH
hi,
BH2
BH3
D 1»
B2H6
ft 11
B4H10
Состояние
ТВ.
ТВ.
ТВ.
куб.
аморфн.
Р-Р
Р-Р
куб.
монокл.
аморфн.
газ
гекс.
газ
газ
газ
газ
газ
жидк.
газ
газ
газ
жидк.
газ
газ
газ
газ
Р-Р
ромб.
ТВ.
ромб.
ТВ.
газ
газ
газ
газ
газ
дн°98,
кДж/моль
-78
-368
+ 1
-3
-957
—
ь
-13
-12
+4
+562
0
+1369
+846
+239
+70
-205
-239
+185
-61
-404
-427
-491
-117
-501
-1137
-1574
-1886
-1845
-1549
+442
+20
* +92
+35
+68
°298»
Дж/(К-моль)
+87
+ 113
+ 111
+ 134
+243
—
—
—
+ 142
+7
+152
+6
+ 138
+202
+225
+295
+324
+230
+213
+273
+290
+206
+357
+200
+248
+254
+200
+ 157
+139
+ 120
—
+172
+ 188
+232
—
А^298»
кДж/моль
-59
-297
-1
+77
-700
-318
-487
—
-10
+4
+518
0
+1323
+789
+196
+29
-232
-238
+ 157
-74
-389
-387
-461
-145
-513
-1119
-1491
-1791
—
-1743
—
+412
+96
+87
—
445
IV. Термодинамика
Продолжение табА
Вещество
В5Н9
в6н10
в10н14
[ВН4],К
[BH4],Li
B3H6N3
[BH4],Na
BI
BI2
BI3
BN
BO
BO2
B2O3
B(OHK
[B(OHK]
[B(OHL]"
BP
BS
B2S3
Ba
Ba+
Ba2+
BaBr
BaBr2
Состойние
газ
жидк.
газ
жидк.
газ
монокл.
куб.
ромб.
газ
жидк.
куб.
газ
газ
газ
ТВ.
газ
гекс. (а)
куб. ф)
газ
газ
аморфн.
газ
гекс.
газ
трикл.
Р-Р
Р-Р
ТВ.
газ
газ
ТВ.
газ
куб.(а)
газ
Р-Р
газ
газ
ромб.
АН 298,
кДж/моль
+75
+44
+97
+58
+38
-39
-227
-191
-510
-541
-192
+288
+220
+71
-37
+641
-251
—
+6
-293
-1254
-844
-1272
-1013
-1094
-1071
-1343
-101
+253
+67
-239
+ 177
0
+706
-524
-77
-417
-751
298'
Дж/(К • моль)
+276
+184
—
—
—
+ 176
+ 107
+76
+289
+200
+101
+233
+310
+349
+200
+212
+ 15
+7
+203
+229
+78
+280
+54
+303
+89
+ 165
+ 105
+27
+216
+327
+ 106
+ 170
+61
+ 176
+9
—
+348
+149
298»
кДж/моль
+ 177
+ 174
—
—
—
+200
-160
-125
-388
-506
-127
+238
+164
+21
-43
+607
-226
—
-22
-298
-1182
-832
-1193
-951
-969
-969
-1153
-95
+200
+2
-238
+145
0
+666
-548
—
-377
-732
-"
446
IV. Термодинамика
Продолжение табл.
Вещество
ВаВг2 * 2Н2О
Ва(ВгО3J • Н2О
ВаС2
ВаСО3
ВаС1
ВаС12
ВаС12 • 2Н2О
Ва(СЮ3J
Ва(С1О3J • Н2О
Ва(СЮ4J
ВаСЮ4
ВаСг2О7
BaF
BaF2
(BaFe2n)O4
BaGeO3
Ba2Ge04
BaH
BaH2
BaHPO4
(BaHF)O3
Bal
Bal2
H'2H2O
Ba(IO3J
Ba(l03JH20
BaMoO4
Ba3N2
Ba(NO2J
fia(NO3J
BaO
^5
Состояние
МОНОКЛ.
МОНОКЛ.
тетр.
ромб.
газ
газ
ромб.
МОНОКЛ.
ТВ.
МОНОКЛ.
гекс.
ромб.
ТВ.
газ
газ
куб.
гекс.
ТВ.
ТВ.
газ
ромб.
ромб.
ТВ.
газ
газ
ромб.
ромб.
МОНОКЛ.
МОНОКЛ.
тетр.
ТВ.
гекс.
куб.
газ
куб.
тетр.
кДж/моль
-1356
-1003
-82
-1201
-143
-495
-845
-1446
-755
-1048
-789
-1429
-2086
-326
-805
-1192
-1469
-1226
-1840
+ 184
-190
-1818
-1817
+ 15
-323
-610
-1222
-1048
-1296
-1538
-335
-756
-979
-131
-538
-644
оо
^298'
Дж/(К-моль)
+230
+288
—
+ 112
—
—
+ 124
+203
+234
—
+255
+ 153
+235
—
+299
+96
—
—
—
+219
+63
—
—
+362
+ 167
+247
+249
+323
+ 149
—
+214
+235
+70
+78
кДж/моль
-1222
-772
—
-1123
—
-797
-1283
-557
—
-536
-1327
-1910
—
-815
-1142
—
—
—
+ 156
-152
—
—
—
-378
-607
-1104
-886
-1087
-1433
—
-784
-152
-510
-588
447
IV. Термодинамика
Продолжение
Вещество
ВаОН+
Ва(ОНJ
Ва3Р2
Ва3(РО4J
BaS
BaSO3
BaSO4
[BaSO4]
BaSe
BaSeO3
BaSeO4
BaSiO3
Ba2Si04
BaTe
(BaTi)O3
BaWO4
(BaZr)O3
Be
Be+
Be2+
(BeAl2)O4
BeBr
BeBr2
Be2C
Be(CH3COOJ
BeCO3
BeCl
BeCl2
BeCl2 • 4H2O
Be(Cl)F
BeF
Состояние
P-P
газ
ромб.
ТВ.
триг.
газ
куб.
куб.
ромб.
Р-Р
куб.
ТВ.
ромб.
ромб.
ромб.
куб.
тетр.
тетр.
куб.
газ
гекс.
газ
Р-Р
ромб.
газ
газ
ромб.
куб.
ТВ.
ТВ.
газ
газ
ромб, (а)
ТВ.
газ
газ
ДЯ°98,
кДж/моль
-749
-586
-943
-803
-3960
+64
-442
-1030
-1458
—
-364
-1026
-1145
-1608
-2258
-314
-1641
-1634
-2419
+327
0
+ 1233
-404
-2299
+50
-240
-368
-91
-1302
-1024
+ 13
-360
-491
-1848
-570
-208
^298'
Дж/(К ¦ моль)
+56
—
+ 100
+214
+356
+249
+78
+ 121
+ 132
—
+91
+ 151
+ 133
+ 110
+ 176
+57
+ 108
+ 152
+ 125
+ 136
+ 10
+ 142
-197
+66
—
+273
+ 121
+ 16
—
+67
+218
+252
+83
+243
+246
+206
кДж/моль
-7l7"
—
-854
-788
-3743
+18
-437
-947
-1347
-1305
-360
-949
-1032
-1525
-2146
-298
-1554
-1529
-2335
+289
0
+1187
-381
-2177
—
-273
-356
-88
—
-948
+16
-366
-446
-1573
-580
-236
—^
448
IV. Термодинамика
-"¦-¦'
Вещество
BeF
BeF2
[BeF2]
[BeF3]-
[BeF4]2-
BeH
BeH2
Bel2
Be3N2
Be(NO3J
Be(NO3J • 4H2O
BeO
Be(OHJ
[Be(OHK]-
[Be(OHL]2"
BeS
BeSO4
BeSO4 • 2H2O
BeSO4 • 4H2O
BeSeO3
BeSeO4
BeSe04-2H20
BeSeO4 • 4H2O
Be2Si04
Be\VO4
Bi
or
DilTi/i\
Состояние
P-P
аморфн.
газ
тетр.
P-P
P-P
P-P
газ
аморфн.
газ
газ
ромб.
куб.
ТВ.
ТВ.
газ
гекс.
аморфн.
газ
ромб.
тетр.
Р-Р
Р-Р
куб.
тетр.
ТВ.
тетр.
ТВ.
ТВ.
ТВ.
ромб.
триг.
ТВ.
газ
триг.
газ
Р-Р
ДН°98,
кДж/моль
-738
-1022
-784
-1035
-1066
—
__
+321 '
-19
+126
-85
-212
-589
-700
-1936
+ 129
-607
-892
-671
-905
-903
—
—
-235
-1205
-1823
-2425
-848
-947
-1565
-2170
-2145
-1435
+209
0
+918
+81
Продолжение табл.
°298'
Дж/(К ¦ моль)
-99
—
+229
+53
-16
—
—
+ 177
+25
+ 173
+289
+ 130
+50
—
—
+ 198
+14
—
—
. +53
+55
+34
+78
+163
+233
+201
—
+247
+64
+ 115
+ 187
+57
+ 175
-177
AGgge,
кДж/моль
-695
—
-789
-987
-998
-1294
-1587
+291
+16
+116
-134
-213
-538
—
—
+104
-578
—
—
-818
-816
-959
-1115
-233
-1094
-1598
-2081
-801
—
-1828
-2030
-1334
+ 170
0
+877
+92
5-2004
449
IV. Термодинамика
Продолжение
Вещество
Bi2
BiAsO4
BiBr
BiBr3
Bi(Br)O
BiCl
BiCl2+
BiClJ
BiCl3
[BiClJ
[BiOJ-
Bi(Cl)O
BiCl(OHJ
BiF
BiF3
Bil
Bil3
[Bii4]-
Bi(I)O
Bi(NO3K • 5H2O
ВЮ
Bi2O3
Bi(OHK
BiPO4
BiS
Bi2S3
Bi2(SO4K
BiSe
Bi2Se3
BiTe
Bi2Te3
Br"
Br
Состояние
таз
тетр.
газ
газ
ТВ.
ТВ.
газ
Р-Р
Р-Р
газ
куб.
Р-Р
Р-Р
тетр.
ТВ.
газ
куб.
газ
триг.
р-р
ТВ.
трикл.
газ
монокл.
аморфн.
монокл.
газ
ромб.
ТВ.
газ
триг.
газ
триг.
газ
Р-Р
газ
кДж/моль
+225
—
+53
-102
-259
-342
+25
-70
—
-264
-378
—
—
-369
-539
-30
-904
+75
-159
—
-269
-2005
+ 119
-575
-715
-1173
+ 180
-156
-2554
+ 176
-140
+ 179
-79
-219
-122
+ 112
с°
°298»
Дж/(К ¦ моль)
+273
—
+267
+385
—
—
+255
+ 1
—
+356
+ 172
—
—
+ 103
—
+244
—
+275
+234
—
—
—
+246
+ 151
+ 118
+ 123
+285
+200
—
+264
+217
+273
+251
+ 163
+83
+ 175
кДж/moj
+ 178
-614
+ 13
~132
—
—
-1
-59.
-199
-253
-313
-337
-479
-31ft
—
-55
—
+27
-159
-212
—
—
+93
-494
-583
-1058.
+122
-153
-2583
+127
-133
+130
-75
¦—
-239
-104
+82
'
450
IV. Термодинамика
Продолжение табл.
Вещество
Br+
Br2
[Br2]
BrCl
BrF
BrF2
BrF3
BrF5
BrN
BrO
BrOj
Br2O4
c-
C
c+
c2
CBr2
CBr3
CBr4
C(Br)F3
CBr2O
cci
cci2
CC13
cci4
c2cj4
C(C1)F3
CC13F
Состояние
газ
газ
жидк.
Р-Р
газ
газ
газ
газ
жидк.
газ
жидк.
газ
газ
Р-Р
ТВ.
газ
газ
гекс. (а)
куб.(р)
газ
газ
газ
газ
газ
газ
газ
жидк.
газ
газ
газ
газ
жидк.
газ
газ
газ
газ
кДж/моль
+ 1260
+31
0
-1
+ 15
-43
-113
-255
-303
-429
-461
+301
+ 125
-65
+54
+588
+715
0
+2
+ 1810
+838
+268
+ 180
+83
-649
-95
-125
+440
+222
+82
-103
-135
. -12
-695
-477
-285
S298>
ДжДКмоль)
+ 177
+245
+ 152
+ 136
+240
+229
—
+292
+ 178
+319
—
+235
+237
+ 164
—
+ 151
+ 158
+6
+2
+ 155
+199
—
—
+358
+299
+309
—
+224
+266
+300
+310
+216
+341
+284
+301
+310
кДж/моль
+ 1224
+3
0
+4
-1
-58
—
-229
-243
-350
—
+282
+ 108
+20
—
+551
+670
0
+3
+ 1759
+782
—
—
+69
-623
-109
—
+408
+211
+94
-61
-65
+23
-654
-439
-246
451
IV. Термодинамика
Продолжение та§А
Вещество
СС12О
CF
CF2
CF3
CF4
C2F4
CH
CH2
СН3
СН4
С2Н2
С2Н4
с6н6
СНВг3
СН2Вг2
СН3Вг
СН3С(Н)О
сн3соо-
СН3СООН
СНС13
СН2С12
СН3С1
CH(C1)F2
C(H)C12F
C(H)F3
CH2F2
CH3F
CH2I2
CH3I
Состояние
газ
жидк
газ
газ
газ
газ
газ
газ
газ
газ
газ
газ
газ
газ
жидк.
газ.
жидк.
газ
газ
газ
Р-Р
газ
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
газ
газ
газ
газ
газ
газ
газ
жидк.
кДж/моль
-221
-244
+249
-164
-469
-933
-1343
+594
+376
+ 142
-75
+226
+55
+82
+48
+41
-28
-5
-38
-166
-490
-433
-484
-102
-132
-96
-124
-87
-101
-502
-299
-699
-446
-234
+ 119
+ 14
-14
°298»
Дж/(К-моль)
+284
+ 197
+213
+242
+265
+262
+129
+183
+ 181
+ 193
+ 186
+200
+232
+269
+173
+331
+221
+292
+246
+264
+88
+282
+ 160
+296
+203
+270
+ 179
+234 .
+ 145
+282
+292
+260
+247
+223
+310
+254
+ 163
кДж/моль
-20Г
-204
+218
-174
-455
-888
-1257
+561
+363
+ 145
-51
+209
+68
+ 130
+ 124
+32 •
-5
-6
-28
-133
-369
-374
-389
-69
-72
-69
-70
-63
-51
-471
-268
-664
-418
-210
+ 102
+16
+15
452
IV. Термодинамика
Продолжение табл.
Вещество
5 5
СН3ОН
с,н5он
^2 э
С13
С14
CN-
CN
C2N2
(CN)Br
(CN)C1
(CN)F
C(NH2JO
[C(NH2JO]
(CN)I
CO
CO2
[COJ
CO2-
C2OJ-
C(O)F2
CS
CS2
C(S)C12
C(S)O
CSe2
Ca
Ca+
Ca2+
(CaAl2)O4
Ca3(As04J. 4H2O
Состояние
газ
жидк.
газ
жидк.
газ
жидк.
газ
газ
Р-Р
газ
газ
газ
газ
газ
тетр.
Р-Р
газ
газ
газ
Р-Р
Р-Р
Р-Р
газ
газ
газ
жидк.
газ
газ
газ
жидк.
газ
куб. (а)
газ
Р-Р
ромб.
ТВ.
ЛН298.
кДж/моль
+ 139
+99
-202
-240
-235
-277
+385
+307
+ 146
+428
+309
+ 186
+ 138
-12
-333
—
+225
-110
-393
-414
-677
-808
-635
+230
+ 117
+88
—
-142
+257
+219
+ 178
0
+773
-543
-2326
—
9°
°298'
Дж/(К-моль)
+283
+ 178
+240
+ 127
+282
+ 161
—
+392
+ 118
+203
+244
+248
+236
+226
+ 105
+ 176
+257
+ 198
+214
+ 121
-57
+80
+258
+210
+238
+ 151
+299
+231
+263
—
+ 155
+42
+ 161
-55
+ 114
—
кДж/моль
+ 190
+ 181
-163
-167
-168
-174
—
+261
+ 172
+398
+297
+ 165
+ 131
-19
-197
-203
+ 196
-137
-394
-386
-528
-668
-619
+ 179
+67
+64
—
-169
+205
—
+ 144
0
+731
-553
-2209
-4019
453
IV. Термодинамика
Продолжение mafy
Вещество
Са(ВО2J
СаВг
СаВг2
СаВг2 • 6Н2О
СаС2
СаСО3
[СаСО3]
СаС2О4
СаС2О4 * Н2О
СаС1
СаС12
СаС12 • 2Н2О
СаС12 • 6Н2О
Са(С1О4J
СаСЮ4
(СаСг2)О4
СаСг2О7
СаСг2О7 • 4,5Н2О
CaF
CaF2
(CaFe2)O4
CaGeO3
Ca2Ge04
CaH
CaH2
CaHPO4
СаНРО4 • 2Н2О
Са(Н2РО4J
Са(Н2РО4J • Н2О
(CaHf)O3
Cal
Cal2
Состояние
ромб.
газ
газ
ромб.
триг.
тетр.
ромб.
триг.
р-р
монокл.
монокл.
газ
газ
ромб.
ТВ.
триг.
ТВ.
тетр.
ромб.
ТВ.
ТВ.
газ
газ
куб.
тетр.
ТВ.
ТВ.
газ
ромб.
трикл.
монокл.
ТВ.
трикл.
ТВ.
газ
газ
триг.
АН 298.
кДж/моль
-2031
-32
-391
-674
-2503
-62
-1207
-1207
—
-1352
-1670
-98
-467
-794
-1389
-2625
-725
-1379
-2049
-2023
-3362
-277
-779
-1228
-1521
-1295
-1999
+246
-175
-1813
-2403
-3115
-3410
-1811
-0
-232
-538
«о
^298'
Дж/(К-моль)
+ 105
—
+310
+ 134
+305
+70
+88
+92
—
+ 156
+244
+286
+ 114
—
+285
—
+ 134
+ 121
+224
—
+230
+274
+69
+ 145
—
—
+202
+42
+ 111
+ 189
+ 190
+260
—
—
+326
+ 145
**»?
кДж/моль
-1924"
—
-426
-656
-2119
-67
-1127
-1128
-1099
—
-1509
-125
-473
-749
—
-2213
—
-1277
-1936
-1849
—
-303
-788
-1176
-1413
—
—
+218
-136
-1680
-2154
-2812
-305?
—
—
-282
—534
—
454
IV. Термодинамика
Продолжение табл.
Вещество
СаООз)^
Са(Ю3J • 6Н2О
CaMg(CO3J
СаМоО4
Ca(N3J
Ca3N2
Ca(NO3J
Ca(NO3J-4H2O
CaO2
CaOH+
Ca(OHJ
Ca3P2
Ca(PH2O2J
Ca(PO3J
Ca2P2O7
Ca3(PO4J
Ca5(PO4KF
CaS
CaSO3 • 2H2O
CaSO4
CaSO4 • 2H2O
2CaSO4 • H2O
[CaSO4]
CaSe
CaSeO3 ¦ 2H2O
CaSeO4
CaSeO4 • 2H2O
CaSiO3
^a2si04
CaTe
Caleo^
Состояние
монокл.
ромб.
гекс.
тетр.
ромб.
гекс.
куб.
монокл.
газ
куб.
тетр.
Р-Р
газ
триг.
ТВ.
ТВ.
аморфн.
тетр.
монокл.
триг.
гекс.
куб.
гекс.
ромб.
монокл.
триг.
Р-Р
куб.
ТВ.
ТВ.
ромб.
трикл.
монокл.
ромб.
куб.
ТВ.
дя°98,
кДж/моль
-1008
-2785
-2315
-1546
+ 14
-432
-938
-2131
-60
-635
-659
-764
«-550
-985
-494
-1755
-1708
-3333
-4105
-4125
-6888
-482
-1753
-1434
-2023
-3203
-1449
-364
-1609
-1120
-1717
-1635
-2308
-2318
-293
-1123
^298>
Дж/(К • моль)
+230
+424
+ 155
+ 123
—
+105
+ 193
+339
+220
+40
+43
-15
—
+83
+ 145
—
+147
+189
+241
+236
+388
+56
+ 184
+ 107
+ 194
+261
+21
+69
+233
—
+ 185
+82
+ 128
+ 120
+77
—
AG°98J
кДж/моль
-846
-2263
-2152
-1439
—
-369
-743
-1701
-82
-604
-598
-717
—
-897
-475
—
-1532
-3126
-3870
-3889
-6507
-477
-1555
-1322
-1797
-2923
-1310
-360
-1423
-1486
-1550
-2193
-2201
-289
—
455
IV. Термодинамика
Продолжение
Вещество
СаТеОз • 2Н2О
(СаП)О3
Ca(VO3J
CaWO4
(CaZr)O3
Cd
Cd2+
Cd3As2
CdBr
CdBr2
CdBr2 • 4H2O
CdCO3
CdC2O4
CdCl
CdCl+
CdCl2
[CdCl2]
CdF2
Cdl
Cdl2
Cd(IO3J
[CdNO3]+
Cd(NO3J
Cd(NO3J • 4H2O
CdO
CdOH+
Cd(OHJ
[Cd(OHJ]
CdS
CdSO4
Состояние
ТВ.
монокл.
ТВ.
тетр.
ромб.
газ
гекс.
р-Р
тетр.
газ
газ
гекс.
ТВ.
триг.
ТВ.
газ
Р-Р
газ
триг.
Р-Р
газ
куб.
газ
газ
гекс.
ТВ.
Р-Р
ТВ.
ромб.
газ
куб.
Р-Р
триг.
Р-Р
гекс.
ромб.
АН 298,
кДж/моль
-1436
-1662
-2329
-1641
-2721
+ 112
0
-76
-42
+66
-140
-316
-1491
-754
-922
+27
-240
-195
-392
-405
-395
-700
+82
-60
-206
—
-305
-453
-2070
+81
-258
—
-563
—
-152
-933
с°
°298'
Дж/(Кмоль)
—
+94
+ 179
+ 126
+ 100
+ 168
+52
-71
+207
+263
+310
+ 139
+311
+97
—
+251
+32
+286
+115
+ 110
+265
+89
+271
+326
+161
—
-3
—
+393
+233
+55
— '
+88
—
+68
+ 123
кДж/моль
_^ ¦
-1577
-2169
-1534
-2635
+77
0
-78
-36
+26
-172
-297
-1245
-674
_
+1
-220
-198
-344
-356
-398
-651
+34
-107
-204
-373 -•
-187
—
-1653
+58
-228
-272
-474 !
-446
-147
-822
456
IV. Термодинамика
Продолжение табл.
Вещество
5cdS(V8H2O
[CdSO4]
[Cd(SO3S)]
[Cd(SO3SJ]2-
CdSe
CdSeO3
CdSeO4
CdSeO4 • H2O
CdSiO3
CdTe
Ce
Ce3+
Се"®
CeC2
CeCl3
Ce(C104K
CeF2+
CeF3
Ce(NO3K • 6H2O
CeO2
Ce2O3
CeOH3+
Ce(OHK
CePO4
[CePO4]
[CeSO4]+
Ce(SO4J
Ce2(SO4K
Ce2(SO4K • 8H2O
^2(SeO3K
Cf2O3
ci-
_
Состояние
монокл.
P-p
P-P
P-P
гекс.
ТВ.
ТВ.
ТВ.
монокл.
куб.
газ
куб. (а)
Р-Р
Р-Р
тетр.
газ
гекс.
ТВ.
Р-Р
газ
гекс.
трикл.
куб.
триг.
Р-Р
аморфн.
монокл.
р-р
Р-Р
ТВ.
монокл.
трикл.
ТВ.
куб.
газ
Р-Р
ДЯ°98>
кДж/моль
-5188
-981
-723
—
-136
-576
-643
-953
-1189
-108
+423
0
-698
-577
-97
-717
-1029
-917
—
-1213
-1680
-3058
-1090
-1801
-812
-1409
-1939
-1593
-2347
-3955
-6448
—
-1653
-234
-167
^298'
Дж/(К • моль)
+689
+4
+59
—
+97
+ 140
—
—
+97
+92
—
+76
-201
-426
—
—
+ 146
—
—
—
+ 115
—
+62
+ 148
-170
+ 110
+115
—
-59
+201
—
—
+ 153
+56
AG°2QQ,
кДж/моль
-4395
-835
-614
-1142
-137
-498
—
—
-1105
-98
—
0
-676
-508
—
—
-950
—
-979
—
-1601
—
-1025
-1708
-749
-1269
-1816
-1800
-1440
-2121
—
—
-2641
—
-240
-131
457
IV. Термодинамика
Продолжение mafy
Вещество
С1
С1+
С12
[C1J
C1F
C1F5
C12F6
C1N
C12N
C13N
cio-
C1O
C1O2
C1O2
ClOj
C1O3
СЮ4
C12O
C12O7
C1O3F
Cm
Co
Co2+
Co3+
CoAs
CoAs2
Co3(AsO4J • 8H2O
CoBr
CoBr2
CoBr2 • 6H2O
Состояние
газ
газ
газ
Р-Р
газ
газ
газ
жидк.
газ
газ
газ
жидк.
Р-Р
газ
Р-Р
Саз
Р-Р
газ
р-р
газ
газ
жидк.
газ
газ
газ
гекс.
Р-Р
Р-Р
ромб.
ромб.
монокл.
газ
газ
триг.
монокл.
АН 298,
кДж/моль
+ 122
+ 1384
0
-23
-50
-239
-326
-262
+335
+ 176
+84
+230
-107
+ 102
-67
+ 104
-104
+155
-129
+76
+287
+251
-21
+346 A600 К)
+428
0
-59
+25
-51
-98
—
+211
+2
-215
-2020
°298>
Дж/(К • моль)
+ 165
+ 167
+223
+ 121
+218
+311
+562
+376
—
—
—
—
+42
+227
+ 101
+257
+ 164
—
+ 183
+266
+565
—
+279
—
+ 179
+30
-109
-316
+59
+ 100
—
—
+321
+ 134
+375
д^98,
кДж/моль
+ 10?"
+1361
0
+7
-51
-147
-246
-126
—
—
-37
+98
-17
+ 122
-8
—
-9
+94
+399
—
+51
—
+384
0
-56
+78
-49
-97
-3530
—
-39
-201
-1660
458
IV. Термодинамика
Продолжение табл.
Вещество
Со3С
СоС03
[Со(СОL]
[Со2(СО)8]
СоС1
СоС1+
СоС12
СоС12 2 • 6Н2О
Со(СЮ4J ¦ 6Н2О
(Со"Со2")О4
(CollCo2")S4
CoF
CoF2
CoF3
Col
Col2
[Co(NH3M]3+
[Co(NH3N]2+
[Co(NH3N]^
[Co(NH3N]Br2
[Co(NH3MCl]2+
[Co(NH3N]Cl2
[C°(NH3N]C13
tco(NH3MCl]Cl2
[Co(NH3N](NO3K
Co(NO3J
Co(NO3J • 6H2O
CoO
C°A-3H2O
co(OHJ
^
Состояние
ромб.
гекс.
газ
газ
ТВ.
газ
Р-Р
газ
триг.
монокл.
гекс.
куб.
куб.
газ
газ
тетр.
триг.
газ
газ
триг.
Р-Р
Р-Р
Р-Р
куб.
Р-Р
куб.
монокл.
ромб.
тетр.
ТВ.
монокл.
газ
куб.
аморфн.
газ
триг.
АН°298,
кДж/моль
+39
-716
-681
-1428
-1526
+ 152
-224
-84
-311
-2113
-2027
-892
-306
+73
-367
-666
-779
+251
+ 107
-94
—
—
-595
-909
—
-999
-1132
-1023
-1291
-422
-1656
+309
-239
-1451
-251
-537
^298>
Дж/(К-моль)
+ 125
+89
—
I
—
-48
+296
+109
+349
—
+ 103
+274
—
+270
+82
+93
—
+340
+ 159
+318
—
+334
+402
+255
+366
__
+ 192
+474
+53
+201
+82
кДж/моль
+30
-640
—
I
—
-187
-97
-268
-1724
—
-774
-323
—
-378
-621
-707
—
+49
-98
-409
-238
-221
—
-361
—
-576
-588
—
-230
-ИЗО
-215
-1193
-454
459
IV. Термодинамика
Продолжение табд
Вещество
[Со(ОНJ]
СоО(ОН)
CoS
Co(S2)
CoSO4
CoSO4 • 7H2O
[CoSO4]
[Co(SO3S>]
CoSe
CoSeO4 • 7H2O
Co2SiO4
CoWO4
Cr
Cr2+
Cr3+
CrBr
CrBr2
CrBr3
[Cr(CON]
CrCl
CrCl2+
CrCl2
CrCl*
CrCl3
CrCl2O2
(Cr2Con)O4
CrF
CrF2
Состояние
P-P
ромб.
гекс.
куб.
ромб.
монокл.
Р-Р
Р-Р
гекс.
монокл.
ромб.
монокл.
газ
куб.
Р-Р
Р-Р
газ
газ
монокл.
газ
триг.
газ
ромб.
газ
Р-Р
газ
ромб.
Р-Р
газ
гекс.
триг.
газ
жидк.
куб.
газ
газ
монокл.
ДН°98,
кДж/моль
—
-456
-85
-134
-889
-2980
-966
—
-79
-2367
-1411
-1147
+398
0
-180
-212
+ 179
-59
-298'
-164
-400
-1007
-1078
+ 152
—
-134
-395
-546
-246
-544
-516
-529
-597
-1432
+34
-414
-754
^298'
Дж/(К • моль)
—
—
+62
+ 103
+ 118
+406
-39
—
—
—
+159
+ 117
+ 174
+24
+42
-316
—
—
+ 134
—
+ 160
+488
+314
—
—
—
+ 115
-87
—
—
+ 123
+330
+209
+ 135
—
+266
+84
д^98,
кДж/моль
-423
—
-85
-137
-784
-2473
-813
-582
—
-1313
-1041
+353
0
-164
-204
__
—
-285
—
-373
-951
-970
—
-339
—
-356
-466
—
—
-446
-493
-525
-1327
—
-426
-711
460
IV. Термодинамика
Продолжение табл.
Вещество
CrF3
(Cr2nFe)O4
Crl2
Crl3
CrN
Cr2N
CrNH4(SO4J 2 • 12H2O
(Cr2Ni")O4
CrO
CrO2
СЮ3
CrO|-
Cr2O3
Cr2O3 • 3H2O
Cr2O^~
Cr30?o
CrO2F2
сюн2+
Cr(OHJ3>
Cr(OH) +
Cr(OHK
[Cr(OHN]3-
CrS
cr2(SO4K
Cr2Te3
Cs
Cs+
Cs2
CsBO^
Состояние
газ
ромб.
куб.
газ
монокл.
триг.
куб.
ТВ.
куб.
куб.
газ
газ
газ
ромб.
Р-Р
триг.
аморфн.
Р-Р
Р-Р
Р-Р
газ
Р-Р
аморфн.
Р-Р
аморфн.
Р-Р
гекс.
гекс.
ТВ.
газ
куб.
газ
Р-Р
газ
ТВ.
Д«298.
кДж/моль
-906
-1112
-1454
+113
-226
-205
-124
-129
-5562
-1432
+190
-61
-293
-584
-875
-1141
-2026
-1479
—
—
-820
-446
-659
—
-976
—
-176
-3310
—
+78
0
+460
-258
+ 111
-977
^298'
ДжДКмоль)
—
+94
+ 146
—
+ 155
—
+53
+50
+715
+ 120
—
—
+271
+67
+46
+81
+76
+254
—
—
-153
+81
—
+95
—
+65
+288
+209
+ 175
+85
+ 170
+ 133
+284
—
AG°98,
кДж/моль
—
-1042
-1353
—
-230
—
-104
-101
-4563
-1322
—
—
-275
-505
-721
-1059
-1734
-1288
-1846
-2385
—
-418
-576
-624
-847
-312
-179
-2986
—
+51
0
+428
-292
+77
—
461
IV. Термодинамика
Продолжение табд.
Вещество
CsBr
CsBrO3
Cs2CO3
CsCl
CsC103
CsC104
Cs2Cr04
Cs2Cr207
CsF
CsH
CsHCO3
Csl
CsIO3
CsN3
CsNH2
CsNO3
CsO2
Cs2O
Cs2O2
CsOH
Cs2S
Cs2SO4
Cs2Se04
Cu
Cu+
Состояние
газ
куб.
гекс.
газ
ТВ.
газ
куб.(сс)
гекс.
ромб.
ромб.
жидк.
газ
куб.
газ
куб.
ромб.
газ
куб.
куб.
тетр.
тетр.
гекс.
тетр.
газ
гекс.
газ
ромб.
газ
ТВ.
ТВ.
газ
ромб.
ромб.
газ
куб.
газ
Р-Р
дн°98,
кДж/моль
-208
-392
-376
-802
-1127
-245
-443
-407
-443
-1429
—
-358
-556
+ 121
-50
-933
-152
-349
-547
-20
-119
-495
-278
-150
-320
-236
-404
-265
-406
-343
-1104
-1443
-1136
+338
0
+ 1090
+72
«о
D298'
Дж/(К • моль)
+267
+ 117
+ 162
—
+ 189
+256
+ 101
+ 163
+ 175
+229
—
+243
+93
+215
+79
+ 130
+275
+ 123
+167
+ 134
—
+ 146
+65
—
+ 126
—
+118
+255
+84
+146
+410
+212
+218
+166
+33
+161
+42
Дбгэв.
кДж/моль
-240
-379
-285
—
-1039
-263
-415
-305
-314
-1317
-2023
-375
-528
+102
-29
-833
-191
-343
-463
+51
—
-393
-211
—
-276
—
-327
-266
-356
-326
-1044
-1324
-1016
+298
0
+ 1046
+50
462
IV. Термодинамика
Продолжение табл.
Вещество
Си2+
Cu3(As04J • 4Н2О
СиВг
СиВг2
СиВг2 • 4Н2О
CuCN
СиСО3
[СиСО3]
[Си(СО3J]2-
Си2СО3(ОНJ
СиС1
СиС1+
[СиС12]"
СиС12
СиС12 • 2Н2О
[СиС14],К2 • 2Н2О
[CuCl4],(NH4J-2H2O
Си(С1О4J • 6Н2О
СиСЮ4
(Cu2Cu»)Se2
CuF
CuF+
CuF2
CuF2 • 2H2O
CuH
Cul
Си(Ю3J
Cu(IO3J • 0,67H2O
cuMoO4
jCu(NH3)p
Состояние
P-P
ТВ.
газ
куб.
газ
монокл.
ТВ.
монокл.
ТВ.
Р-Р
Р-Р
монокл.
газ
куб.
Р-Р
Р-Р
газ
монокл.
ромб.
тетр.
тетр.
монокл.
ромб.
ТВ.
газ
куб.
Р-Р
газ
куб.
монокл.
газ
газ
куб.
монокл.
трикл.
ТВ.
Р-Р
Д98>
кДж/моль
+66
—
+ 120
-105
+46
-143
-1325
+98
-594
—
—
-1048
+81
-136
—
-278
-21
-216
-819
—
-1460
-1915
—
-98
-13
-508
-262
-276
-538
-1169
+275
+ 153
-68
-411
—
-911
-37
^298'
Дж/(К • моль)
-96
—
+248
+96
—
+ 146
+293
+90
+92
—
—
+222
+237
+87
—
+211
—
+ 108
+ 191
+355
+386
—
—
+216
+69
-64
+260
+69
—
+196
+256
+97
—
—
+ 132
+ 18
AG°98)
кДж/моль
+65
-2732
+79
-101
—
-131
-1079
+ 111
-518
-502
-1049
-901
+53
-119
-71
-244
—
-172
-660
—
-1080
—
-687
-108
—
-488
-222
-283
-488
—
+246
+104
-70
—
-513
-810
-16
463
IV. Термодинамика
Продолжение табл.
Вещество
[Cu(NH3J]+
[Cu(NH3J]2+
[Cu(NH3K]2+
[Cu(NH3L]2+
[Cu(NH3N]Cl2
[Cu(NH3L](NO3J
Cu(NO3J
Cu(NO3J • 3H2O
CuO
Cu2O
CuOH+
Cu(OHJ
[Cu(OHK]"
[Cu(OHL]2"
CuS
Cu2S
CuSO4
CuSO4 • 5H2O
[CuSO4]
Cu2SO4
CuSe
Cu(Se2)
Cu2Se
CuSeO3
CuSeO3 • 2H2O
CuSeO4 • 5H2O
CuSiO3
CuSiO3 • H2O
CuWO4
D
D2
D2O
Dy
Состояние
P-P
P-P
P-P
P-P
тетр.
ромб.
ТВ.
ТВ.
газ
монокл.
куб.
Р-Р
аморфн.
Р-Р
Р-Р
гекс.
ромб.
ромб.
трикл.
Р-Р
ТВ.
гекс.
ТВ,
куб. (а)
ТВ.
ромб.
трикл.
ТВ.
ТВ.
ТВ.
газ
газ
газ
жидк.
газ
гекс.
ДН°98,
кДж/моль
-151
-140
-244
-347
-870
-828
-310
-1217
+320
-156
-171
—
-444
—
-894
-53
-79
-770
-2280
-838
-750
-40
-43
-55
-393
-983
-1951
-1049
-1359
-1030
+222
0
-250
-294
+290
0
^298»
Дж/(К-моль)
+264
+118
+204
+281
—
—
+ 192
—
+231
+43
+92
—
+84
—
+43
+67
+ 121
+112
+301
-18
+ 184
+83
+97
+133
+253
+292
—
—
+87
+ 151
+ 123
+145
+198
+76
+ 196
+75
AG298»
кДж/моль
-65
-31
-73
-112
—
—
-117
—
+292
-128
-148
-130
-359
-492
-658
-54
-86
-662
-1880
-691
-653
-42
-37
-62
-354
-817
—
—
-1208 t
-933
+207
0
-235
-243
+254
0
464
IV. Термодинамика
Продолжение табл.
Вещество
Dy2+
Dy3+
DyBr3
DyCl3
DyF3
Dyl2
Dyl3
Dy2O3
Dy(OHK
Er
Er3+
ErBr3
ErCl3
ErCl3 • 6H2O
ErF3
Erl3
Er2O3
Eu
Eu2+
Eu3+
EuBr2
EuCl2
EuCl3
EuF2
EuF3
Eu2o3
Состояние
P-P
P-P
газ
гекс.
газ
монокл.
газ
ромб.
ТВ.
гекс.
куб. (а)
аморфн.
газ
гекс.
Р-Р
газ
гекс.
монокл.
монокл.
газ
монокл.
гекс.
куб.
газ
куб.
Р-Р
Р-Р
тетр.
газ
ромб,
гекс.
газ
газ
ромб,
куб.
монокл. (а)
АН°98>
кДж/моль
-398
-505
-777
-714
-999
-1197
-1720
-394
-616
-1866
-1885
+317
0
-664
-508
-781
-958
-2838
-954
-1723
-586
-1898
+175
0
-506
-581
-745
-464
-812
-916
-766
-1356
-1620
-1628
-1648
°298'
Дж/(К • моль)
-180
+414
+383
+ 146
+347
+ 121
+218
+ 150
+ 151
+194
+73
-252
+412
+ 158
+399
+345
+121
+218
+ 153
+ 189
+78
-77
-216
+ 168
+323
+170
+ 147
+300
+336
+109
+ 147
AG°2Q8,
кДж/моль
-682
-538
-706
-920
-1187
-1643
-607
-1774
-1757
+281
0
-589
-422
-884
-2418
-944
-1647
+577
-1808
+ 142
0
-500
-554
-727
-471
-773
-837
-772
-1342
-1538
-1534
465
IV. Термодинамика
Продолжение табл.
Вещество
Еи(ОНK
F"
F
F+
F2
Fe
Fe2+
Fe3+
(FeAl2)O4
FeAs2
FeAsO4 • 2H2O
Fe(As)S
FeBr
FeBr2+
FeBr2
FeBr3
Fe2Br6
Fe3C
[Fe(CNN]4"
[Fe(CNN]3"
[Fe(CNN],Ba2 • 6H2O
[Fe(CNN],K3
[Fe(CNN],K4
[Fe(CNN],K4-3H2O
FeCO3
[FeCO3]
[Fe(COM]
FeCl
FeCl2+
FeCl2
Состояние
аморфн.
газ
P-P
газ
газ
газ
газ
куб.
Р-Р
Р-Р
куб.
ромб.
ромб.
трикл.
газ
р-р
газ
трип
газ
гекс.
газ
ромб.
Р-Р
Р-Р
монокл.
ромб.
тетр.
монокл.
триг.
Р-Р
газ
жидк.
газ
Р-Р
газ
триг.
ля°98,
кДж/моль
-1317
-260
-334
+79
+ 1767
0
+417
0
-93
-51
-1975
-44
—
-106
+282
—
-44
-250
-126
-267
-400
+24
+458
+630
-2351
-175
-1188
-1472
-753
—
-732
-764
+251
-194
-149
-342
со
^298»
Дж/(К-моль)
+ 112
+ 145
-14
+ 159
+ 162
+203
+ 180
+27
-105
-279
+ 106
+ 127
—
+ 108
—
-121
+321
+ 138
—
+ 184
—
+ 108
+98
+269
+ 115
+420
+598
+593
+96
-187
+445
+338
+257
-116
+287
+ 118
AG^98, "
кДж/моль
-1177
-267
-280
+62
+ 1743
0
+371
0
-92
-18
-1860
-52
-1260
-110
—
-113
-86
-238
-246
—
+18
+696
+748
-1741
-52
-1088
-1172
-680
-607
-695
-695
+216
-158
-160
-303
466
IV. Термодинамика
Продолжение табл.
Вещество
всГ2-4н2о
VcC\\
FeCl3
FeCl3 • 6Н2О
[FeCl3]
Fe2Cl6
Fe(Cl)O
(Fe2Co»)O4
(FeCu')O2
(Fe2Cu»)O4
FeCu(S2)
FeF
FeF2+
FeF2
FeF3
Fe2F6
(FeIIFeyi)O4
[FeHPO4]+
Fel2
FeMoO4
Fe(NH4J(SO4J • 6H2O
(Fe'"Ni»)O4
Fe095o
FeO
FeO2-
Fe2O3
FeA • 3H2O
FeOH+
FeOH2+
pe(OHJ
lFe(OHJ]
Состояние
монокл.
P-P
газ
триг.
монокл.
P-P
газ
ромб.
куб.
триг.
куб.
тетр.
газ
Р-Р
газ
тетр.
газ
триг.
газ
куб.
Р-Р
газ
триг.
ТВ.
монокл.
куб.
куб.
газ
куб.
Р-Р
триг.
ам.
Р-Р
Р-Р
газ
триг.
Р-Р
АН°98,
кДж/моль
-1552
—
-253
-397
-2224
—
-654
-410
-1140
-530
-963
-181
+47
-370
-390
-661
-821
-1042
-1628
-1118
-1359
+57
-116
-1074
-3922
-1077
-266
+237
-271
-479
-824
-1653
-328
-293
-333
-574
—
°298>
Дж/(К ¦ моль)
+246
—
+344
+ 142
+352
—
+537
—
+ 135
+89
+ 141
+ 118
+240
-130
+265
+87
+304
+98
—
+ 146
-158
+336
+ 170
+ 129
t
+ 132
+57
+236
+61
—
+87
+209
+5
-104
+92
—
AG°298,
кДж/моль
-1272
-291
-248
-332
-1804
-416
-599
—
-1033
-478
-857
-179
+ 14
-332
-400
-618
-813
-972
—
-1015
-1170
-1
-124
-974
—
-969
-245
+205
-251
—
-742
-1399
-291
-243
-493
-459
467
IV. Термодинамика
Продолжение табл.
Вещество
Fe(OHM
[Fe(OHK]-
[Fe(OHK]
[Fe(OHL]2"
[Fe(OHL]"
FeO(OH)
Fe3P
FePO4
FePO4 • 2H2O
FeS
Fe(S2)
FeSO4
FeSO4 • 7H2O
[FeSO4]
[FeSO4]+
Fe2(SO4K
FeSe
Fe2(Se03K
FeSiO3
Fe2Si04
FeTeO3 • H2O
FeWO4
(Fe»'Zn)O4
Fr
Ga
Ga+
Ga3+
GaAs
GaBr
GaBr3
GaCl
Состояние
P-P
P-P
P-P
P-P
P-P
ромб.
тетр.
тетр.
аморфн.
монокл.
гекс. (а)
куб.(р)
ромб, (а)
ромб.
ромб.
Р-Р
р-р
ромб.
гекс.
ТВ.
ромб.
ромб.
трикл.
монокл.
куб.
газ
куб.
газ
ромб.
газ
Р-Р
куб.
газ
ТВ.
газ
Д^298'
кДж/моль
—
—
—
—
—
-559
-163
-1297
-1857
-1889
-101
-174
-151
-928
-3015
-1000
-934
-2581
-75
—
-1195
-1480
-918
-1188
-1171
+73
0
+273
0
-21
-212
-72
-37
-386
-82
^298»
Дж/(К-моль)
—
—
—
—
—
+67
—
+ 101
+ 189
+ 171
+60
+53
—
+ 108
+409
-37
-95
+259
+71
—
+94
+ 145
—
+ 132
+ 152
+ 182
+94
+ 169
+41
+ 162
-321
+64
+252
+ 167
+240
Д<*298.
кДж/моль
-454
-621
-677
-776
-844
-490
—
-1185
-1632
-1658
-101
-163
—
-820
-2510
-847
-785
-2247
-76
-1306
-1118
-1379
—
-1087
-1066
+47
0
+235
0 .
-76
-162
-68
-77
-356
-108
468
IV. Термодинамика
Продолжение табл.
Вещество
GaCl2
GaCl3
GaF
GaF2+
GaF?
GaF3
[GaF3]
Gal
Gal3
GaN
GaO
Ga2O3
GaOH2+
Ga(OH)^
Ga(OHK
[Ga(OHK]
[Ga(OHL]"
GaP
GaPO4
Ga2S3
[GaSO4]+
[Ga(SO4J]-
GaSb
Ga2Se3
Ga2(Se03K
Ga2Te3
Gd
Gd3+
GdCl3
GdCl3-6H2O
Состояние
P-P
газ
газ
ТВ.
газ
P-P
P-P
ТВ.
P-P
газ
газ
ромб.
гекс.
газ
газ
триг.
Р-Р
Р-Р
куб.
Р-Р
Р-Р
куб.
триг.
куб.
Р-Р
Р-Р
куб.
куб.
ТВ.
куб.
газ
гекс.
Р-Р
газ
монокл.
монокл.
АН 298,
кДж/моль
—
-238
-444
-565
-229
-538
-864
-1019
-1208
+ 17
-145
-220
-107
+141
-516
-1104
—
—
-965
—
—
-102
-1413
-510
-1101
-2018
-42
-369
—
-272
+399
0
-684
-690
-1019
-2863
°298'
Дж/(К ¦ моль)
—
—
—
+133
+228
-191
-93
+84
-88
+260
+209
+42
+231
—
+85
—
+113
—
—
+51
+104
+ 161
-185
-148
+76
+ 179
—
+198
+194
+68
-201
+146
+392
ДС298.
кДж/моль
-290
—
—
-493
-254
-477
-783
-941
-1079
-31
-218
-79
+115
—
-1013
-383
-600
-836
-815
-1013
-93
-1297
-505
-922
-1679
-39
-360
-1658
-262
+361
0
-662
-942
-2442
469
IV. Термодинамика
Продолжение табд
Вещество
GdF3
Gdl3
Gd(NO3K • 6Н2О
Gd2O3
Ge
GeIV<4>
Ge2
GeBr
GeBr2
GeBr4
GeCl
GeCl2
GeCl4
GeF
GeF2
GeF4
[GeF5]~
[GeF6]2"
GeH
GeH3
GeH4
Ge2H6
Ge3H8
Gel2
Gel4
GeO
Состояние
газ
гекс.
трикл.
монокл.
газ
куб.
Р-Р
газ
газ
газ
газ
жидк.
газ
газ
газ
жидк.
газ
газ
ромб.
газ
Р-Р
Р-Р
газ
газ
газ
газ
жидк.
газ
жидк.
газ
триг.
газ
жидк.
куб.
аморфн.
газ
АН 298,
кДж/моль
-1180
-618
-3038
-1816
+379
0
—
+482
+ 146
-69
-305
-348
+91
-177
-495
-565
-40
-473
-586
-1190
-1695
-2026
-+280
+238
+90
+ 162
+ 138
+227
+ 192
+51
-92
+68
-136
-152
-237
-46
^298»
Дж/(К • моль)
—
+218
+577
+ 151
+ 168
+31
-657
+253
+257
+318
+396
—
+245
+295
+348
+251
+234
+271
—
+303
+ 125
+ 190
—
—
+90
+297
—
—
—
+334
+ 147
+429
+309
+257
+50
+224
AG^98l
кДж/моль
-611
-2411
-1729
+338
0
-28
+425
+101
-109
-323
—
+60
-189
-457
-498
-70
-484
—
-1150
-1552
-1854
—
—
+113
+209
—
—
—
-5
-92
+18
-149
-154
-212
-73
__ "
470
IV. Термодинамика
Вещество
GeOH3+
Ge(OH)f
Ое(ОН)з
[Ge(OHL]
[Ge(OHM]~
[Ge(OHN]2"
GeS
GeS2
GeSe
GeSe2
GeTe
GeTe2
H-
H
H+
[H+]<5>
H2
HAsO^~
4
H2AsOt
H2As0t
[H3ASO3]
lH3As04]
HBO2
(НВО2K
J![
Состояние
аморфн.
тетр. (а)
триг. (P)
Р-Р
Р-Р
Р-Р
Р-Р
Р-Р
Р-Р
газ
ромб.
куб.
газ
тетр.
газ
ромб.
газ
триг.
газ
газ
газ
газ
Р-Р
газ
Р-Р
Р-Р
Р-Р
Р-Р
Р-Р
Р-Р
р-р
газ
куб.
монокл.
ромб.
газ
ДЯ°98,
кДж/моль
-540
-580
-555
—
—
—
—
—
—
+93
-69
-189
+110
-84
+ 130
-63
+ 187
-25
+161
+ 140
+218
+ 1536
0
0
-4
-689
-911
-721
-914
-749
-907
-562
-804
-794
-2368
-36
Продолжение табл.
^298'
Дж/(К • моль)
—
+40
+55
—
—
—
—
—
—
+234
+66
+87
—
+78
—
+113
—
+91
—
+109
+ 115
+109
0
0
+58
-15
-5
+ 111
+ 117
+ 195
+ 183
+240
+49
+38
+ 150
+ 199
AG°98,
кДж/моль
—
-522
-501
-264
-500
-734
-967
-1154
-1319
+42
-70
-187
—
-85
-62
-28
—
+ 133
+203
+ 1517
0
0
+ 18
-524
-718
-593
-757
-646
-770
-551
-736
-723
-2166
-53
471
IV. Термодинамика
Продолжение табдщ
Вещество
НВгО
[НВЮ]
HCN
[HCN]
НСОз
[Н2СО3]<6>
нс2о4
Н2С2О4
нсоо-
нсоон
[НСООН]
НС1
нею
[НОЮ]
[НС1О2]
НС1О4
НС1О4 • Н2О
НСЮ4
НСг2О7
[Н2Сг04]
HF
[HF]
HF2
[H2Ge03]
HI
[НЮ]
ню3
н5ю6
НМоО4
HN3
HNCO
[HNCO]
Состояние
газ
Р-Р
газ
жидк.
Р-Р
Р-Р
Р-Р
Р-Р
монокл.
Р-Р
газ
жидк.
Р-Р
газ
газ
Р-Р
Р-Р
газ
жидк.
ТВ.
Р-Р
Р-Р
Р-Р
газ
жидк.
Р-Р
Р-Р
Р-Р
газ
Р-Р
ромб.
монокл.
Р-Р
газ
жидк.
газ
жидк.
Р-Р
АН 298,
кДж/моль
-79
-113
+ 134
+ 110
+107
-692
-700
-818
-831
-426
-379
-425
-426
-92
-84
-121
-52
+5
-41
-382
-872
—
-844
-271
-303
-321
-657
—
+24
—
-236
-762
—
+294
+264
-117
-153
—
°298»
ДжДКмоль)
—
+ 142
+202
+ 113
+127
+91
+ 187
+ 117
+ 120
+91
+249
+129
+ 163
+ 187
+236
+146
+ 188
+296
+ 188
—
+ 180
—
+260
+ 174
—
+91
+68
+ 180
+206
+ 120
+117
—
—
+239
+ 141
+238
—
+ 134
AG298»
кДж/моль
—
-82
+ 124
+ 126
+ 119
-587
-623
-688
-702
-352
-351
-362
-373
-95
-71
-80
-28
+92
+78
-758
-1308
-752
-273
—
-298
-581
-730
-1
-99
-142
—
-867
+328
+327
-107
-—
472
IV. Термодинамика
Продолжение табл.
Вещество
HNCS
HNO2
[HNO2]
HNO3
hno5 • зн2о
HN2O2
H3NO4
[HNbO3]?
HO2
H2O
H2O2
[H2O2]
HOF
H(PHO3)-
H(PH2O2)
H2(PHO3)
[H2(PHO3)]
HPO3
HPO2-
H2POj
H2P2O2-
h3po4
2h3po4h2o
W3PO4]
H4P2O7
[H4P2O7]
Hs-
Hs
H2S
Состояние
газ
газ
Р-Р
газ
ЖИДК.
ТВ.
Р-Р
ТВ.
Р-Р
газ
газ
гекс.
жидк.
газ
жидк.
Р-Р
газ
Р-Р
ТВ.
ромб.
Р-Р
аморфн.
Р-Р
Р-Р
Р-Р
жидк.
монокл.
ТВ.
Р-Р
ТВ.
Р-Р
ТВ.
Р-Р
газ
газ
Р-Р
АН 298>
кДж/моль
+ 127
-80
-119
-135
-174
-1096
—
-506
-1039
+24
-242
-292
-286
-137
-187
-191
-94
-969
-615
-952
-965
-977
-1292
-1296
-2279
-1267
-1279
-2862
-1288
-2242
—
« —1800
-18
+ 142
-21
-40
Дж/(К • моль)
+248
+249
+ 153
+267
+ 156
+201
+ 142
+ 100
+230
—
+189
+39
+70
+233
+ 110
+ 143
—
+80
—
—
+79
-33
+90
+ 176
+201
+110
+258
+158
—
+285
-+370
+63
+ 196
+206
+ 121
AG°98,
кДж/моль
+113
-45
-56
-75
-81
-776
+84
-327
-985
—
-229
-234
-237
-106
-120
-134
-831
—
—
-847
—
-1089
-ИЗО
-2015
-1134
-1119
-2483
-1143
—
-2037
-—1550
+ 12
+ 113
—34
-28
473
IV. Термодинамика
Продолжение табд
Вещество
H2S2
H2S4
H2S5
HSO3
HSO4
H2SO4
H2SO4 • H2O
H2S2O7
HSO3S-
[H2SO3S]
HSe"
H2Se
[H2Se]
HSeOj
HSeO4
H2Se03
[H2Se03]
H2Se04
H2SiO3
H2SiO^~
H3Si04
[H4Si04]
[HTaO3]?
HTcO4
HTe-
H2Te
[H2Te]
HTeOj
H2Te03
[H2Te03]
H4TeO^~
Н5Те0б
H6Te06
[H6Te06]
Состояние
газ
жидк.
газ
Р-Р
Р-Р
газ
жидк.
жидк.
ТВ.
Р-Р
р-р
Р-Р
газ
р-р
р-р
Р-Р
ромб.
Р-Р
ромб.
аморфн.
Р-Р
Р-Р
Р-Р
р-р
ТВ.
Р-Р
газ
Р-Р
Р-Р
ромб.
Р-Р
Р-Р
Р-Р
монокл.
Р-Р
Р-Р
ДН°98,
кДж/моль
+ 15
-13
+33
-626
-889
-744
-814
-1128
-1272
-625
-604
+ 16
+30
+ 19
-515
-576
-525
-507
-533
-1188
-1397
-1426
-1462
-1182
-703
+69
+99
+78
-556
-613
-555
-1128
-1158
-1287
-1182
^298'
Дж/(К ¦ моль)
+261
—
—
+ 140
+ 124
+301
+ 157
+212
—
+ 163
+242
+79
+219
+ 164
+ 134
+ 163
—
+208
—
-13
+ 113
+ 179
+230
+ 139
+62
+229
+ 141
+ 139
—
+218
+ 178
+287
—-
+353
AG298.
кДж/моль
—
—
-528
-755
-663
-690
-951
—
-524
-527
+44
+ 16
+22
-411
-451
—
-426
—
—
-1187
-1254
-1310
-1128
-593
+105
+85
+90
-452
—
-474
-866
-928
—
-972
-7707
474
IV. Термодинамика
Вещество
HWOJ
[H2WO4]?
Не
[Не]
Не+
Hf
Hf1VG)
HfC094
HfCl4
HfF4
ню2
НЮ2 • 2H2O
Hf(SO4J
Hf(SO4J • 4H2O
Hg
Hg2+
Hgf
HgBr
HgBr2
Hg2Br2
Hg(CNJ
Hg2CO3
HgCl
HgCl+
HgCl2
Г11
IHgCK]
IHgCy-
Состояние
p-p
p-p
p-p
газ
p-p
газ
газ
гекс.
P-P
куб.
газ
куб.
газ
монокл.
газ
монокл.
аморфн.
ТВ.
ТВ.
газ
жидк.
Р-Р
Р-Р
ГЯ13
газ
ромб.
тетр.
тетр.
ТВ.
газ
Р-Р
газ
ромб.
Р-Р
Р-Р
кДж/моль
—
—
—
0
-2
+2379
+653
0
— ,
-219
-881
-991
-1682
-1931
-225
-1145
—
-2230
-3493
+61
0
+ 171
+ 172
+103
-86
-169
-207
+269
-553
+84
-19
-146
-225
-216
-389
Продолжение табл.
^298»
Дж/(К • моль)
—
—
—
+ 126
+56
+ 132
+ 187
+46
—
+46
+381
+ 191
+325
+ 111
—
+59
—
—
—
+ 175
+76
-32
+85
+272
+312
+ 180
+218
—
+ 174
+260
+75
+295
+ 146
+ 155
+209
AGgga,
кДж/моль
-7728
-952
-965
0
+ 19
+2371
+611
0
-569
-217
-848
-901
-1644
-1829
—
-1088
-1362
—
—
+31
0
+ 164
+ 154
+67
-111
-155
-181
—
-466
+62
-5
-145
-179
-173
-309
475
IV. Термодинамика
Продолжение табд%
Вещество
Hg2Cl2
Hg2Cr04
HgF
HgF2
Hg2F2
Hgl
Hgl2
[Hgl4]2-
Hg2I2
Hg2(IO3J
Hg2(N3J
2Hg(NO3JH2O
Hg2(NO3J-2H2O
HgO
HgOH+
HgS
HgSO4
Hg2SO4
HgSe
HgSeO3
Hg2Se03
Ho
Ho3+
HoBr3
HoCl3
HoF3
Hol3
Ho2O3
I-
I
Состояние
тетр.
ТВ.
газ
газ
куб.
тетр.
газ
газ
тетр. (а)
Р-Р
тетр.
ТВ.
ТВ.
ТВ.
монокл.
ромб.
Р-Р
КУ6.(р)
триг. (а)
ромб.
монокл.
куб.
ТВ.
ТВ.
газ
гекс.
Р-Р
ТВ.
монокл.
газ
ромб.
гекс.
куб.
газ
Р-Р
газ
АН 298»
кДж/моль
-266
—
+3
-294
-421
-490
+ 132
-15
-105
—
-121
_
+594
—
-868
-90
-85
-54
-59
-704
-743
-59
-358
—
+300
0
-707
-842
-979
-1209
-1714
-598
-1881
-195
-58
+ 107
^298'
Дж/(К-моль)
+ 192
—
+248
+266
+ 116
+ 175
+281
+329
+ 184
—
+235
—
+203
—
—
+70
+71
+88
+82
+ 136
+201
+99
+191
—
+ 195
+76
-197
—
+ 146
+347
+ 121
+218
+ 158
+ 169
+ 103
+ 181
4^298,
кДж/моль
-21Г
-618
-18
-290
-372
-436
+88
-56
-103
-215
-111
-177
+750
-564
_
-58
-52.
-48
-51
-590
-626
-53
-288
-327
+265
0
-669
—
-900
-1199
-1637
-588
-1791
-222
-52
+70
476
IV. Термодинамика
Продолжение табл.
Вещество
и
[У
IBr
ICI
i2ci6
IF
IF5
IF7
[I(IJ]-
[I(IJ],Cs
[I(IJ],NH4
[I(I)d,Rb
I3N
I3N • NH3
10;
I2O5
In
In+
In3+
In2
InAs
InBr
InBr3
InCl
•
I r +
2
Состояние
газ
газ
жидк.
ромб.
Р-Р
газ
ромб.
газ
монокл.
трикл.
газ
газ
жидк.
газ
Р-Р
ромб.
ромб.
ромб.
газ
ТВ.
Р-Р
ТВ.
газ
тетр.
газ
Р-Р
газ
куб.
газ
ромб.
ТВ.
газ
куб.
Р-Р
газ
Р-Р
ЛН°98,
кДж/моль
+ 1115
+62
+22
0
+22
+41
-10
+ 17
-35
-180
-94
-834
-883
-944
-53
-361
-216
-345
+287
+146
-220
-183
+239
0
+830
-136
+392
-58
-37
-176
-410
-71
-186
—
-201
—
S298>
ДжДКмоль)
+ 183
+261
+ 137
+ 116
+ 135
+259
—
+247
+98
+334
+236
+329
+215
+346
+236
+238
—
+226
—
—
+ 117
—
+174
+58
+ 168
-265
+272
+76
+260
+112
+167
+248
+95
—
—
—
де;98,
кДж/моль
+ 1072
+19
+16
0
+16
+4
—
-6
-14
-45
-117
-764
-778
-818
-52
-355
—
-338
-126
—
+204
0
+791
-98
+346
-53
-75
-169
-375
-94
-164
-239
—
-375
477
IV. Термодинамика
Продолжение табд.
Вещество
1пС13
[1пшС14],1п
InF
InF2+
Inl
Inl2
Inl3
InO
In2O3
InOH2+
In(OH)^
In(OHK
[In(OHK]
InP
In2S3
[InSO4]+
[In(SO4J]"
In2(SO4K
InSb
In2Se3
In2(Se03K
In2Te
In2Te3
Ir
IrCl2
IrCl3
IrF6
IrO2
IrS2
Состояние
монокл.
ромб.
газ
P-P
газ
ромб.
газ
газ
монокл.
газ
куб.
Р-Р
Р-Р
куб.
Р-Р
куб.
куб.
Р-Р
Р-Р
монокл.
газ
куб.
гекс.
ТВ.
ТВ.
куб.
газ
куб.
ТВ.
газ
гекс.
газ
ромб.
газ
тетр.
куб.
Д/^98,
кДж/моль
-617
-726
-192
—
+83
-102
-21
-116
-224
+386
-924
—
-916
—
-85
-427
-1016
-1932
-2726
-+350
-20
-343
-1794
-80
-191
+669
0
-178
-103
-263
-544
-580
+216
-242
-144
^298'
Дж/(К • моль)
+ 138
+244
+236
—
+268
+ 124
—
—
+209
+236
+104
—
—
+ 107
—
+63
+ 164
-92
-62
+302
—
+86
+195
+320
+ 157
+231
+ 193
+35
+130
+155
+358
—
+59
+62
кДж/моль
-541
-631
-215
-404
+38
-104
—
-217
+364
-828
-315
-528
-780
-736
-74
-413
-859
-1614
-2386
—
-15
-329
-1542
-77
-181
+622*
0
-140
—
-199
-459
—
—
-188
-133
'
478
IV. Термодинамика
Продолжение табл.
Вещество
Ir2S3
к
К+
к2
(K3Ag)O2
KA1(SO4J
KA1(SO4J • 12Н2О
КВО2
К2В4О7
КВг
КВгО3
КСН3СОО
KCN
К2СО3
К2С2О4 • Н2О
K2Ca(SO4J • Н2О
КС1
ксю3
ксю4
К2Сг04
К2Сг207
KCr(SO4J
KcKSO4J. 12Н2О
KF
кн 2°
H2As04
Состояние
ромб.
газ
жидк.
куб.
газ
Р-Р
газ
ромб.
триг.
куб.
газ
триг.
ТВ.
газ
куб.
триг.
монокл.
газ
куб.
монокл.
монокл.
монокл.
газ
куб.
монокл.
ромб.
ромб.
трикл.
триг.
куб.
газ
куб.
ромб.
газ
куб.
тетр.
монокл.
кДж/моль
-245
+89
+2
0
+514
-252
+67
-658
-2470
-6063
-661
-982
-3523
-182
-393,
-358,
-723
+80
-114
-1150
-1645
-3177
-214
-437
-399
-433
-1398
-2068
-2352
-5784
-326
-569
-1165
+ 123
-55
-1187
-966
^298'
Дж/(К • моль)
+97
+ 160
+71
+65
+ 154
+ 101
+250
—
+205
+687
—
+80
+208
+250
+96
+149
—
+253
+ 128
+ 156
—
—
+239
+82
+ 143
+ 151
+200
+291
+240
+708
+226
+67
+ 156
+ 198
+67
+ 155
+ 109
дс^98,
кДж/моль
-224
+61
0
0
+481
-283
+91
—
-2240
-5142
—
-924
-3325
-214
-380
-269
—
+54
-102
-1064
—
-233
-409
-297
-303
-1290
-1888
-2134
-4870
-344
-539
-1023
+ 103
-37
-1042
-867
479
IV. Термодинамика
Продолжение табл.
Вещество
K(HF2)
КН2РО4
К2НРО4
KHSO4
KI
кю3
КЮ4
KMgCl3
KMgCl3 • 6Н2О
KMgF3
K2Mg(SO4J ¦ 6H2O
KMnO4
K2Mn04
K2MoO4
KN3
KNCS
KNO2
KNO3
(KNb)O3
KO2
KO3
K2O
K2O2
KOH
[KOH]
KPO3
K3PO4
K4P2O7
IQPjO, • 3H2O
KReO4
K2S
K2(S3)
K2(S4)
K2(S5)
Состояние
тетр.
ромб.
ТВ.
ромб, (а)
газ
куб.
монокл.
тетр.
ТВ.
ромб.
куб.
монокл.
ромб.
ромб.
монокл.
тетр.
ромб.
монокл.
ромб.
ромб.
тетр.
тетр.
куб.
ромб.
газ
ромб.
р-р
монокл.
куб.
ТВ.
тетр.
тетр.
куб.
ромб.
ромб.
трикл.
ДЯ°98,
кДж/моль
-928
-1569
-1776
-1161
-128
-331
-500
-508
-1086
-2945
-1727
-4538
-829
-1180
-1499
-3
-202
-354
-495
-1346
-284
-261
-363
-440
-232
-425
-477
-1246
-1988
-3202
-4110
-1098
-421
-474
-472
-475
^298'
ДжДКмоль)
+ 105
+ 135
+ 179
+142
+258
+ 104
+ 151
+ 159
—
—
—
+536
+ 172
—
+ 174
+86
+ 124
+ 117
+ 133
+ 122
+ 117
+ 105
+94
+ 120
+244
+79
+92
+ 108
+212
+318
+444
+ 168
+ 113
+ 180
+210
+257
кДж/моль
-860
-1416
-1637
-1033
-168
-325
-417
-397
—
—
—
-3968
-729
—
-1381
+77
-180
-280
-395
-1261
-238
-181
-322
-376
-235
-379
-441
-1155
-1859
-2981
-3718
-995
-406
-460
-458
-465
_- -*
480
IV. Термодинамика
Продолжение табл.
Вещество
К^О3' 2Н2О
[KSOJ-
K2SO4
K2S4O6
K2S2O6(O2)
K2Se
K2Se04
K2Si03
(K2Ti)O3
KVO3
K2WO4
Kr
[Kr]
Kr+
KrF2
La
La3+
UB6
LaC2
[LaCO3]+
LaCl3
LaCl3 • 7H2O
LaF2+
LaF3
Lal3
Ц(МоО4K
Цо3
ЦОНK
^O(OH)
Upo4
Состояние
ТВ.
монокл.
р-р •
газ
ромб.
монокл.
трикл.
куб.
ромб.
ромб.
ТВ.
ромб.
монокл.
газ
Р-Р
газ
газ
газ
гекс.
Р-Р
куб.
тетр.
Р-Р
газ
гекс.
трикл.
Р-Р
гекс.
ромб.
монокл.
триг.
аморфн.
ТВ.
монокл.
ромб.
кДж/моль
-1119
-1257
-1157
-1110
-1438
-1766
-1918
-375
-1120
-1542
-1614
-1170
-1580
0
-15
+1356
+63
+419
0
-707
-130
-79
—
-695
-1062
-3165
—
-1732
-700
-4324
-1793
-1410
-1079
—
-1287
^298'
Дж/(Кмоль)
+ 155
+ 157
+ 147
+365
+ 176
+310
+279
+ 120
+ 180
+ 146
—
—
+ 170
+164
+62
+ 175
—
+ 182
+57
-209
+83
+73
—
+364
+ 146
+463
—
+ 100
+213
+390
+127
+ 145
—
+ 134
кДж/моль
-1025
-1025
-1031
-1048
-1320
-1598
-1699
-360
-1000
-1449
—
—
-1460
0
+ 15
+ 1347
—
+382
0
-686
-127
-80
-1258
-687
-989
-2699
-987
-1654
-695
-4014
-1705
-1286
-1837
-1264
6-2004
481
IV. Термодинамика
Продолжение тщ
Вещество
[LaSO4]+
La2(SO4K
La2(SO4K • 9Н2О
La2Te3
Li
Li+
Li2
LiA102
(LiAs)O3
LiBO2
Li2B4O7
LiBr
LiBr • 2H2O
LiBrO3
Li2C2
Li2CO3
LiCl
LiCl • H2O
LiCIO
LiClO4
LiC104 • 3H2O
LiCrO2
(LiCu)O
(Li2Cu)O2
LiF
(LiFe)O2
LiH
Li(HF2)
Состояние
p-p
ТВ.
гекс.
ТВ.
газ
жидк.
куб.
газ
Р-Р
газ
гекс.
ТВ.
газ
монокл.
тетр.
газ
куб.
ТВ.
ТВ.
ТВ.
монокл.
газ
куб.
куб.
газ
ТВ.
гекс.
ТВ.
ТВ.
ТВ.
газ
куб.
куб.
газ
куб.
ТВ.
ДН°98,
кДж/моль
-1602
-3932
-6655
-786
+ 161
+2
0
+687
-278
+211
-1190
-893
-647
-1018
-3377
-144
-350
-961
-344
-59
-1213
-195
-408
-712
-14
-381
-1298
-926
-391
-781
-332
-616
-766
+ 135
-90
-946
«о
^298»
Дж/(К • моль)
-76
+319
—
+232
+139
+34
+29
+ 133
+ 11
+197
+53
—
+52
+ 158
+225
+69
+113
—
+59
+90
+213
+59
+92
+256
+126
—
+36
—
—
+200
+36
+75
+ 171
+20
+71
кДж/мо^
-145(Г
-3598
—
-776
+128
+ 1
0
+650
-293
+170
-1128
—
-962
-3186
-180
-339
-824
—
-56
-1129
-217
-384
-628
-18
-254
—
-906
—
—
-353
-588
-711
+112
-68
-879
¦"-
482
IV. Термодинамика
Продолжение табл.
Вещество
UHSO4
(U2Hf)O3
Lil
Lil • Н2О
Lil 2H2O
Lil • ЗН2О
Li1MoO4
UN
LiN3
Li3N
LiNH2
LiNO2
LiNO2 • 0,5H2O
LiNO3
(LiNb)O3
LiO
Li2O
Li,O2
LiOH
LiOH • H2O
[LiOH]
Li3PO4
u2s
Li2SO4
Li2SO4 • H2O
Li2Se03 • H2O
Li2Si03
1 . * 3
L'2WO4
(L'22r)O3
Lu
I nu
Состояние
ТВ.
ТВ.
газ
куб.
ТВ.
ТВ.
гекс.
гекс.
газ
ТВ.
гекс.
тетр.
ТВ.
ТВ.
газ
триг.
триг.
газ
газ
куб.
гекс.
газ
тетр.
монокл.
Р-Р
ромб.
куб.
монокл.
монокл.
ТВ.
ромб.
куб.
триг.
ТВ.
газ
гекс.
Р-Р
ДЯ°98,
кДж/моль
-1143
-1798
-80
-271
-592
-893
-1193
-1521
+163
+4
-198
-180
-408
-674
-275
-488
—
+84
-167
-599
-636
-246
-485
-791
-509
-2092
-447
-1436
-1734
-1330
-1653
-1668
-1604
-1743
+428
0
—
ч°
°298>
Дж/(К • моль)
+109
—
+232
+77
—
—
—
+115
+212
+72
+38
—
+84
+279
+88
—
+211
+229
+38
+45
+218
+43
+71
—
+ 105
+63
+ 114
+ 146
—
+76
+92
+ 113
—
+ 185
+51
-192
де°98,
кДж/моль
-1016
—
-123
-268
—
—
—
-1407
+137
+77
-155
—
-335
—
-229
-385
-1271
+60
-187
-562
-571
-252
-439
-684
-1963
-439
-1321
-1559
—
-1561
-1577
-1488
—
+388
0
-653
16-
483
IV. Термодинамика
Продолжение табЛ
Вещество
LuCl3
LuCl3 • 6Н2О
LuF3
Lul3
Lu2O3
Mg
Mg+
Mg2+
(MgAl2)O4
Mg3As2
Mg3(As04J
Mg3Bi2
MgBr
MgBr2
MgBr2 • 6H2O
MgCO3
MgCO3 • 5H2O
[MgCO3]
MgCl
MgCl2
MgCl2 • 6H2O
Mg(C104J
MgCl(OH)
MgCЮ4
MgCЮ4 • 5H2O
(MgCr2")O4
MgCr2O7
MgCr2O7 • 6H2O
MgF
MgF+
MgF2
Состояние
газ
монокл.
ТВ.
газ
ромб.
гекс.
куб.
газ
гекс.
газ
Р-Р
куб.
куб.
ТВ.
триг.
газ
газ
триг.
монокл.
триг.
монокл.
Р-Р
газ
газ
триг.
' монокл.
ТВ.
ТВ.
ТВ.
ТВ.
куб.
ТВ.
ТВ.
газ
р-р
газ
тетр.
ДН°98,
кДж/моль
-675
-950
—
-1100
-1701
-556
-1878
+ 147
0
+891
-462
-2315
-421
-3068
-154
-39
-312
-517
-2408
-1096
-2567
—
-44
-402
-641
-2500
-587
-800
-1344
-2769
-1490
-1957
-3680
-222
-776
-724
-1124
°298'
Дж/(К-моль)
+359
+ 146
+380
+321
+96
+207
+ 110
+149
+33
+ 154
-120
+81
—
+226
—
—
+296
+ 123
+397
+66
+280
—
+233
+271
+90
+366
+218
+83
+123
+322
+119
+218
+457
+221
-33
+258
+57
кДж/моль
-6бГ"
-879
—
-1090
-1624
-550
-1789
+112
0
+849
-455
-2190
—
-2840
—
—
-345
-499
-2054
-1012
-2199
-1002
-70
-406
-592
-2115
-331
-732
-1242
-2378
-1379
-1783
-3161
-248
-746
-731
-1071
, -"
484
IV. Термодинамика
Продолжение табл.
Вещество
(MgF^2")°4
MgH
MgH2
Mgl
Mgb
MgMoO4
Mg3N2
MgNH4As04 • 6H2O
Mg(NH4J(SO4J • 6H2O
Mg(NO3J
Mg(NO3J • 2H2O
Mg(NO3J • 6H2O
MgO
MgOH+
Mg(OHJ
Mg3P2
Mg2P2O7
Mg3(PO4J
MgS
MgSO3
MgSO3 • 6H2O
MgSO4
MgSO4 • H2O
MgSO4 • 4H2O
MgSO4 • 6H2O
M8SO4 • 7H2O
MgSO4]
Mg3Sb2
MgSeO3
%SeO, • 6B,O
%SeO4
Jj8SeQ^-H2O
Состояние
куб.(а)
газ
ТВ.
газ
газ
триг.
ТВ.
куб.
ромб.
монокл.
ТВ.
ТВ.
монокл.
газ
куб.
Р-Р
газ
триг.
куб.
монокл.
ТВ.
газ
куб.
ТВ.
триг.
ромб.
монокл.
монокл.
монокл.
ромб.
Р-Р
триг.
ТВ.
ТВ.
ТВ.
ТВ.
АН 298'
кДж/моль
-1428
+ 170
-77
+53
-170
-364
-1401
-461
-3326
-4294
-790
-1409
-2605
+4
-601
—
-570
-925
-466
—
-3790
+ 139
-347
-1013
-2824
-1280
-1610
-2496
-3086
-3388
-1369
-313
-895
-2702
-974
-1301
ДжДКмоль)
+ 124
+ 193
+31
—
+314
+ 134
+119
+88
—
—
+ 164
—
+453
+221
+27
—
+63
—
+ 155
+189
+240
+46
+92
+351
+92
+ 126
—
+348
+370
-52
—
+322
—
—
AG°98,
кДж/моль
-1317
+ 142
-37
—
-219
-360
-1296
-401
—
—
-589
—
-2072
-21
-569
-628
—
-834
—
—
-3548
+87
-341
-929
-2400
-1166
-1436
—
-2631
-2870
-1212
—
-2266
—
485
IV. Термодинамика
Продолжение табл.
Вещество
MgSeO4 • 4Н2О
MgSeO4 • 6Н2О
Mg2Si
MgSiO3
Mg2Si04
(MgTi)O3
MgWO4
Mn
Mn2+
Mn3+
(MnAl2)O4
MnAs
Mn3(As04J • 8H2O
MnBr
MnBr2
MnBr2 • 4H2O
Mn3C
MnCO3
[Mn(COM]
[Mn2(COI0]
MnCl2
MnCl2 • 4H2O
MnF2
(MnnFe2)O4
Mnl2
(MnuMn^)O4
MnMoO4
Mn3N2
Mn(NH4J(SO4J • 6H2O
Mn(NO3J
Состояние
ТВ.
монокл.
куб.
ромб.
ромб.
триг.
монокл.
газ
куб.(а)
куб. (Р)
куб. (у)
Р-Р
Р-Р
куб.
гекс.
ТВ.
газ
газ
триг.
монокл.
ромб.
триг.
газ
газ
газ
триг.
монокл.
газ
тетр.
куб.
трип
тетр.
ТВ.
ТВ.
монокл.
ТВ.
ДН°98,
кДж/моль
-2195
-2785
-78
-1549
-2172
-1571
-1535
+283
0
+2
—
-220
-100
-2098
-57
—
4-84
-175
-379
-1539
-17
-894
-751
-1610
-264
-481
-1686
-532
-847
-1226
-263
-1385
-1191
-485
-4045
-703
°298>
Дж/(К • моль)
—
+356
+82
+68
+95
+75
+ 101
+ 174
+32
+35
+33
-67
-213
—
+60
—
—
+318
+ 140
+293
+99
+86
—
—
+295
+ 118
+317
+270
+93
—
+ 153
+ 149
+ 132
—
—
+ 167
AG298.
кДж/моль
—
-2329
-77
-1462
-2053
-1483
-1423
+241
0
+ 1
—
-230
-85
-55
-4055
—
-215
-366
-1293
-16
-817
—
—
-276
-440
-1426
-542
-805
—
-264
-1279
-1090
—
—
-503
486
IV. Термодинамика
Продолжение табл.
Вещество
[Vln(NO3J • 6Н2О
MnO
MnO2
MnO4~
MnO4
Mn2O3
Mn2O3 • 3H2O
Mn2O7
MnOH+
Mn(OHJ
MnO(OH)
Mn3(PO4J
MnS
Mn(S2)
MnSO4
MnSO4 • H2O
MnSO4 • 4H2O
MnSO4 • 7H2O
[MnSO4]
Mn2(SO4K
MnSb
MnSe
MnSeO3
MnSeO3 • 2H2O
MnSiO3
Mn2Si04
MnTe
MnWO4
Mo
MoBr2
MoBr3
MoBr4
MoBr5
Состояние
монокл.
газ
куб.
тетр.
Р-Р
Р-Р
куб.
ромб.
жидк.
Р-Р
триг.
монокл.
ТВ.
куб. (а)
куб.
ромб.
монокл.
монокл.
монокл.
Р-Р
аморфн.
гекс.
куб.
ТВ.
ТВ.
трикл.
ромб.
гекс.
монокл.
газ
куб.
ТВ.
ТВ.
ТВ.
ТВ.
АН°98>
кДж/моль
-2372
+ 124
-385
-520
—
-533
-958
-1775
-726
-446
-702
-577
-3066
-214
-245
-1066
-1377
-2257
-3139
-1127
-2768
-50
-149
-695
-1315
-1320
-1730
-111
-1305
+659
0
-121
-170
-189
-215
^298'
Дж/(К • моль)
—
—
+60
+53
+191
+196
+110
+201
+171
+3
+82
—
+300
+78
+54
+112
+ 156
—
—
+3
+259
—
+91
+190
+154
+89
+163
+94
+135
+ 182
+29
+ 142
+ 163
+218
+264
AG298.
кДж/моль
—
—
-363
-465
-449
-440
-880
-1515
-544
-407
-617
—
-2858
-218
-232
-958
-1213
—
—
-987
-2431
—
-154
-637
-1108
-1240
-1632
-115
-1204
+613
0
-109
-142
-155
-172
487
IV. Термодинамика
Продолжение табЛ
Вещество
[Мо(СОN]
МоС12
МоС13
МоС14
МоС15
МоС12О2
MoF6
Mol2
Мо13
Мо14
МоО2
МоО3
МоО3 • Н2О
МоО^-
Mo(O)F4
MoO2F2
[МоО2(ОНJ]
MoS2
N
N+
N2
[NJ
Щ
Щ
NCS"
NF
NF2
NF3
Состояние
газ
ромб.
аморфн.
монокл.
газ
гекс.
газ
монокл.
газ
ТВ.
газ
жидк.
ТВ.
ТВ.
ТВ.
газ
монокл.
газ
ромб.
газ
гекс.
р-р
газ
монокл.
газ
р-р
гекс.
газ
газ
газ
Р-Р
газ
Р-Р
р-р
газ
газ
газ
АН°98,
кДж/моль
-914
-983
-288
-393
-385
-474
-446
-528
-635
-717
-1559
-1586
-47
-61
-82
-13
-590
-363
-745
-851
-1072
-998
-1255
-1310
-1121
—
-234
+473
+ 1883
0
-11
+ 1509
—
+74
+257
+40
-133
°298>
Дж/(К • моль)
+494
+327
+ 113
+ 138
+372
+201
+395
+225
—
—
+350
+260
+ 167
+209
+268
—
+46
+279
+78
—
+ 159
+33
—
—
—
—
+66
+ 153
+ 162
+ 192
+95
+ 197
+ 108
+ 146
+214
+250
+261
AG298>
кДж/моль
-85<Г
-878
-247
-325
-354
-392
-389
-420
—
-1473
-1473
-54
-63
-84
—
-534 '
-346
-668
— •
-950
-838
—
—
-877
1226
+456
+ 1857
0
+18
+1501
+348
+90
+252
+55
~91
'
488
IV. Термодинамика
Продолжение табл.
Вещество
N2F4
NH
NH2
NH3
[NHJ
NH3 • H2O
[NH3 • H2O]
NH3 • 2H2O
2NH3 • H2O
NH}
N2H4
[N2H4]<8>
N2H4 • H2O
NH4Br
NH4Br04
NH4CH3COO
NH4C1
N2H6C12
NH4C1O4
(NH4JCr04
(NH4JCr207
(NH)F2
NH2F
NH4F
NH4(H2AsO4)
NH4(HCO3)
NH4(HF2)
NH4(H2PO4)
<NH4J(HPO4)
NH4(HS)
NH4(HSO3)
N«4(HSO4)
Состояние
газ
газ
газ
газ
жидк.
Р-Р
жидк.
Р-Р
жидк.
жидк.
газ
Р-Р
газ
жидк.
Р-Р
газ
жидк.
куб.
ТВ.
ТВ.
куб.(а)
куб.
ромб.
монокл.
монокл.
газ
газ
гекс.
ТВ.
монокл.
ромб.
тетр.
монокл.
тетр.
ромб.
ромб.
кДж/моль
-5
+340
+ 174
-46
-70
—
-361
-366
-650
-431
+664
-133
+95
+50
—
-205
-243
-271
—
-615
-315
-364
-295
-1287
-1808
-84
-40
-467
-1064
-850
-807
-1446
-1566
-158
-769
-1027
с°
°298»
Дж/(К-моль)
+313
+ 181
+ 195
+192
—
+111
+ 166
+ 179
+233
+268 <
+186
+ 111
+238
+122
+ 138
+264
—
+ 113
+200
__
+95
—
+ 184
+ 173
—
+72
+ 172
+ 121
+ 116
+ 152
—
+98
—
AG298>
кДж/моль
+80
+334
+ 184
-16
—
-27
-254
-263
-493
-267
+709
-79
+159
+149
+ 128
-79
—
-175
—
—
-203
—
-88
-996
-352
-837
-666
-655
-1211
—
-51
—
489
IV. Термодинамика
Продолжение табд.
Вещество
NH4I
NH4IO3
NH4N3
NH4NCS
NH4NO2
NH4NO3
(NH)O2
NH2OH
[NH2OH]<9>
(NH4JSO3 • H2O
(NH4JSO4
(NH4JS2O6(O2)
(NH4JSe04
NH4VO3
NO
NO+
NO2
NO2
NO3
NO3
N2O
N2Or
N2O3
N2O4
N2O5
(NO)Br
(NO)C1
(NOj)Cl
(NO)F
(NO2)F
Состояние
куб.
ромб.
ромб.
монокл.
ТВ.
ромб.
газ
газ
ромб.
Р-Р
монокл.
ромб.
монокл.
монокл.
ромб.
газ
газ
газ
Р-Р
газ
Р-Р
газ
газ
Р-Р
газ
газ
жидк.
газ
гекс.<10>
газ
жидк.
газ
жидк.
газ
жидк.
газ
газ
АН°298,
кДж/моль
-202
-384
+ 115
-58
-238
-366
-78
-51
-115
-98
-1185
-1181
-1648
-874
-1051
+91
+990
-360
-105
+33
-207
+71
+82
—
+83
+9
-19
+11
-43
+82
+52
+53
+28
+ 12
+21
-66
-108
^298'
Дж/(К • моль)
+ 117
—
+ 113
+261
+254
+ 151
+249
+236
+67
+ 167
—
+220
—
+ 141
+211
+ 198
+236
+ 140
+240
+ 147
+253
+220
+28
+312
+304
+209
+356
+ 178
+274
—
+262
—
+272
+272
+248
+260
кДж/моль
-пГ*
—
+274
+ 11
-117
-184
-43
-4
-17
-23
—
-901
—
_
-886
+87
+984
-334
-4
+51
-111
+ 116
+ 104
+146
+ 139
+98
+98
+115
+ 114
+82
—
+67
—-
+54
+63
-51
-66
490
IV. Термодинамика
Продолжение табл.
Вещество
(N0I
N0@2)
(NO2)OF
Na
Na+
Na2
NaA102
NaAl(SO4J12H2O
Na3As04
NaBO2
Na2B4O7
NaBr
NaBr • 2H2O
NaBrO3
Na2C2
Na(CH3COO)
Na(CH3COO) • 3H2O
NaCN
Na2CO3
Na2CO3 • H20
Na2CO3 • 7H2O
ЧС03 • 10H2O
Чс2о4
NaCl
NaClO,
NaClO,
NaClO4
*аС104.н20
NaCr02
Состояние
газ
газ
газ
газ
жидк.
куб.
газ
Р-Р
газ
гекс.
куб.
ромб.
газ
триг.
трикл.
газ
куб.
монокл.
куб.
тетр.
монокл.
монокл.
газ
куб.
монокл.
ромб.
ромб.
монокл.
ТВ.
газ
куб.
ТВ.
куб.
ромб.
монокл.
ТВ.
дя°98,
кДж/моль
+ 100
+71
-26
+ 108
+ 13
0
+611
-240
+ 138
-1133
-5983
-1535
-657
-976
-3291
-151
-361
-953
-343
-19
-709
-1603
+94
-90
-1132
-1432
-3200
-4083
-1321
-181
-411
-306
-338
-382
-678
-857
«о
^298'
Дж/(К • моль)
+283
+253
—
+ 154
+58
+51
+ 148
+59
+230
+71
—
+ 186
+272
+74
+ 190
+241
+87
+ 176
+ 131
+ 111
+ 124
+262
+243
+ 118
+ 135
+ 168
+427
+565
+230
+72
+ 113
+223
+ 142
—
+96
AG°29Q>
кДж/моль
+92
+ 116
—
+77
+ 11
0
+576
-262
+ 100
-1070
—
-1412
-660
-920
-3096
-185
-349
-828
-253
-18
-608
-1334
+67
-80
-1048
-1289
-2716
-3432
-201
-384
-230
-264
-254
—
-794
491
IV. Термодинамика
Продолжение таЪл
Вещество
Na2Cr04
Na2Cr04 • 10H2O
Na2Cr207
NaF
NaFeO2
NaH
NaHCO3
Na(HFJ
NaH2PO4
Na2HPO4
Na2HPO4 • 2H2O
Na2HPO4 • 7H2O
Na2HPO412H2O
Na2H2P2O7
NaHS
NaHSO4
NaHSO4 • H2O
Nal.
Nal • 2H2O
NaIO3
NaMnO4
Na2MoO4
NaN3
NaNCS
NaNH2
NaNO2
NaNO3
(NaNb)O3
NaO2
Na2O
Na2O2
Состояние
ромб.
монокл.
ТВ.
газ
куб.
триг.
газ
куб.
монокл.
триг.
ТВ.
ТВ.
ромб.
монокл.
монокл.
монокл.
триг.
трикл.
монокл.
газ
куб.
трикл.
ромб.
ТВ.
куб.
триг.
ромб.
ромб.
ромб.
газ
триг.
ромб.
куб.
газ
куб.(а)
газ
гекс.
АН 298,
кДж/моль
-1336
-4277
-1967
-294
-577
-698
+ 124
-52
-914
-922
-1545
-1755
-2346
-3821
-5298
-2764
-236
-1132
-1420
-76
-290
-886
-480
-1682
-1454
+20
-176
-124
-359
-257
-469
-1325
-260
-41
-418
-94
-510
с°
Дж/(К • моль)
+ 180
—
+277
+217
+51
+88
+ 188 .
+47
+ 102
+91
+ 127
+150
+221
+434
+636
+220
—
+ 125
+ 170
+249
+99
+ 174
+ 135
+ 160
+459
+71
+ 113
+77
+105
+300
+117
+ 117
+ 116
+272
+75
—
+95
кДж/моль
-1230
—
-1791
-313
-547
-640
+ 103
-32
-816
-854
-1394
-1615
-2088
-3279
-4468
-2522
-1003
-1235
-118
-287
-766
-396
-1583
-1355
+100
-155
-64
-285
-211
-368
-1242
-218
-61
-379
-447
492
IV. Термодинамика
Продолжение табл.
Вещество
NaOCN
NaOH
[NaOH]
NaPO3
Na3PO4
Na3PO412H2O
Na4P2O7
Na4P2O7 • 10H2O
Na2S
Na2(S4)
Na2SO3
Na2SO3 • 7H2O
Na2SO4
Na2SO4 • 10H2O
Na2S2O7
Na2(SO3S)
Na2(SO3S) • 5H2O
Na3Sb
Na2Se
Na2Se03
Na2Se04
Na2Se04 • 10H2O
Na2Si03
Na4Si04
Na2Sn03
Na2Te
Na2Te03
Na2Te03 • 5H2O
(Na2Ti)O3
NaVO3
Na3VO4
4V2O7
Na2WO4
4XeO6
Состояние
триг.
газ
ромб.
Р-Р
ромб.
тетр.
триг.
ромб.
монокл.
куб.
тетр.
триг.
монокл.
газ
ромб, (а)
монокл.
ТВ.
монокл.
монокл.
гекс.
куб.
ТВ.
ромб.
монокл.
ромб.
монокл.
ТВ.
куб.
ромб.
ТВ.
ТВ.
монокл.
куб.
гекс.
куб.
ТВ.
дн°98,
кДж/моль
-120
-211
-425
-470
-1220
-1917
-5480
-3166
-6125
-372
-411
-1090
-3153
-1012
-1388
-4330
-1938
-1117
-2602
-227
-343
-961
-1101
-4056
-1588
-2106
—
-353
-977
-2453
-1592
-1147
-1636
-2919
-1547
-836
«о
°298'
Дж/(К • моль)
+ 125
+236
+64
+48
+96
+ 174
+660
+270
+689
+77
—
+ 146
+450
+345
+ 149
+586
—
+225
+314
—
+ 105
—
+ 117
—
+114
+ 196
—
+ 132
—
—
+ 122
+ 114
+ 190
+318
+ 161
—
AGggg,
кДж/моль
-81
-216
-379
-419
-ИЗО
-1789
-4662
-2947
-5335
-355
—
-1002
-2668
-953
-1270
-3647
—
-1043
-2207
—
-331
—
-971
—
-1464
-1976
-974
-347
—
—
-1497
-1065
-1516
-2722
-1433
—
493
IV. Термодинамика
Продолжение табл%
Вещество
Nb
NbBr5
NbCl5
[NbCl6],K
[NbCl6],Na
NbF5
NbO
NbO2
NbO 7
Nb2O5
Nd
Nd3+
Nd(BrO3K • 9H2O
NdCl3
NdCl3 • 6H2O
NdF3
Ndl3
Nd2O3
NdOH2+
Nd(OHK
Nd2S3
Nd2(SO4K
Nd2(SO4K • 8H2O
Ne
[Ne]
Ne+
Ni
Состояние
газ
куб.
ромб.
газ
монокл.
ТВ.
ТВ.
монокл.
газ
куб.
газ
тетр.
Р-Р
монокл.
газ
гекс.
Р-Р
гекс.
газ
гекс.
монокл.
газ
гекс.
ромб.
гекс.
куб.
Р-Р
гекс.
ромб.
ТВ,
монокл.
газ
р-р
газ
газ
куб.
АН298,
кДж/моль
+722
0
-556
-712
-797
-1262
-1217
-1813
+ 199
-415
-212
-807
-1020
-1897
+327
0
-696
-3583
-721
-1041
-2863
-1293
-1713
-671
-1797
-1808
—
-1404
-1191
-3981
-6382
0
-5
+2087
+424
0
с°
°298'
Дж/(К-моль)
+ 186
+36
+305
+401
+216
—
+ 160
+239
+48
—
+55
+ 151
+ 137
+189
+73
-210
+378
+ 146
+385
+346
+ 121
+213
—
+158
+ 111
+ 134
+289
—
+ 146
+67
+ 158
+ 182
+30
AG^e,
кДж/моль
+677^"
0
-523
-655
-685
—
-1699
+ 169
-388
—
-752
-943
-1764
+292
0
-670
_
-712
-963
-2439
-1284
-1637
-661
—
-1720
-859
-1271
-1159
-3628
—
0 .
+19
+2077
—
+379
0
—--*
494
IV. Термодинамика
Продолжение табл.
Вещество
(NiAl2)O4
Ni3(As04J • 8H2O
NiBr
NiBr2
№3C
NiCO3
NiC2O4
[Ni(COL]
NiCl
NiCl2
NiCl2 • 6H2O
NiF
NiF2
[NiF6],Ca
[NiF6],K2
[NiF6],(NO+J
Nil2
[Ni(NH3L]2+
[Ni(NH3N]2+
[Ni(NH3N]Cl2
tNHNH3N]I2
Ni(NO3J
NKNO3J • 6H2O
NiO
^O3-3H2O
NiOH+
Ni(OHJ
Nis 2
Состояние
P-P
куб.
МОНОКЛ.
газ
газ
триг.
гекс.
ромб.
ТВ.
газ
жидк.
газ
газ
триг.
МОНОКЛ.
газ
газ
тетр.
ТВ.
ТВ.
ТВ.
газ
триг.
Р-Р
Р-Р
куб.
куб.
ТВ.
трикл.
газ
куб.
аморфн.
Р-Р
газ
триг.
Р-Р
триг.
дн°98,
кДж/моль
-54
-1939
—
+181
+20
-220
+36
-689
-863
-586
-630
+ 178
-66
-305
-2109
+74
-326
-657
-1951
-2010
-1116
+ 139
-96
—
—
-997
-789
-430
-2215
+248
-240
-1341
-254
-544
—
-83
S298>
Дж/(К-моль)
-129
+92
—
—
+317
+ 130
+ 106
+86
+ 133
+399
+313
—
+294
+98
+344
—
+269
+74
—
—
—
+ 141
+238
+356
—
—
+ 192
+511
+238
+38
+ 192
+80
—
+53
кДж/моль
-45
-1819
-3482
—
-20
-205
+33
-612
-768
-567
-585
—
-78
-259
-1719
—
-337
-610
—
—
—
—
-95
-195
-253
—
—
-238
-1700
+217
-212
-1080
-220
-459
-418
-80
495
IV. Термодинамика
Продолжение табд.
Вещество
Ni3S2
NiSO4
NiSO4 • 7Н2О
[NiSO4]
NiSb
NiSeO3 • 2H2O
Ni2Si04
NiTe
NiWO4
Np
NpBr3
NpBr4
NpCl3
NpCl4
NpF3
NpF4
Npl3
NpO2
o-
0
0+
02
[02]
05
03
OCN-
OD
OF
0F2
02F
O2F2
OH-
Состояние
триг.
ромб.
ромб.
Р-Р
гекс.
монокл.
ТВ.
гекс.
монокл.
газ
ромб.
гекс.
ТВ.
гекс.
газ
тетр.
гекс.
монокл.
ромб.
газ
куб.
газ
газ
газ
газ
Р-Р
газ
газ
Р-Р
газ
газ
газ
газ
газ
газ
Р-Р
лн°98,
кДж/моль
-203
-873
-2977
-961
-66
-1109
-1430
-54
-1133
+464
0
-725
-765
-904
-788
-992
-1500
-1780
-499
+427
-1030
+107
+249
+ 1569
0
-12
+ 1172
+ 143
-140
+36
+140
-22
+23
+19
-134
-230
^298»
ДжДКмоль)
+ 134
+ 104
+379
-61
+73
+ 197
+ 111
+87
+ 119
+198
+50
+205
+243
+159
—
+201
+ 109
+ 151
+234
—
+83
+158
+161
+155
+205
+111
+205
+239
+107
+190
+214
+247
+260
+277
+ 171
-11
Д6298-
кДж/моль
—197
—763
-2462
-802
-65
-915
-1317
-56
-1028
+420
0
-703
-732
-837
—
-904
-1427
-1690
-502
—
-979
+97
+232
+1547
0
+16
+1166
+163
-97
+32
+110
-5
+37
+58
-129
-157
_—
496
IV. Термодинамика
Продолжение табл.
Вещество
он
он+
от
Os
OsCl3
OsCl4
OsO3
0sO4
Os(S2)
P (краен.)
P
P (черн.)
P+
P2
P4
Р4(бел.)
PBr3
PBr5
PBr3O
PCI
PC12
PCI3
PC15
PC13O
PF
PF2
PF3
PF5
PH
Состояние
газ
газ
газ
газ
гекс.
куб.
ТВ.
газ
газ
монокл.
куб.
аморфн.
газ
ромб.
газ
газ
газ
куб.
газ
жидк.
ромб.
газ
ТВ.
газ
газ
газ
жидк.
газ
тетр.
газ
жидк.
газ
газ
газ
газ
газ
АН 298,
кДж/моль
+39
+ 1318
+35
+790
0
-191
-255
-163
-336
-391
-145
-17
+316
-38
+1337
+ 144
+60
0
-139
-185
-229
-390
-458
+ 150
-44
-287
-319
-375
-445
-560
-597
-47
-431
-919
-1593
+249
со
^298'
Дж/(К ¦ моль)
+184
+183
+ 193
+ 192
+33
—
+ 155
—
+294
+ 134
+55
+23
+ 163
+23
+167
+218
+280
+ 164
+348
+240
—
+360
—
+237
—
+312
+217
+364
+171
+325
+222
+225
—
+273
+293
+196
кДж/моль
+34
+1307
+31
+743
0
—
-158
—
-292
-299
-132
-12
+280
-33
+1293
+103
+25
0
-163
-176
—
-387
—
+ 125
—
-268
-272
-305
-318
-514
-521
-72
—
-897
-1517
+222
497
IV. Термодинамика
Продолжение табл.
Вещество
РН2
РН3
Р2Н4
РН4Вг
РН41
(РНО3J-
Р1з
Р214
PN
РО
ро^-
р2о«-
р4о6
p4o10
P(O)F3
PS
P4S10
P(S)Br3
P(S)C13
P(S)F3
Pa
Pb
Pb+
Pb2+
Pb2
Pb3(As04J
Pb(BO2J
PbBr
PbBr2
Состояние
газ
газ
газ
куб.
тетр.
Р-Р
гекс.
трикл.
газ
газ
Р-Р
Р-Р
газ
жидк.
монокл.
газ
ромб.
триг.
газ
газ
ТВ.
газ
газ
жидк.
газ
тетр.
газ
куб.
газ
Р-Р
газ
ТВ.
ТВ.
газ
газ
ромб.
АН 298.
кДж/моль
+ 126
+5
+21
-128
-69
-969
-46
-83
+99
-27
-1277
—
+1594
-2194
-1640
-3199
-3041
-2984
-1198
+ 125
-364
-256
-381
-331
-1063
0
+ 195
0
+917
-1
+251
—
-1550
+49
-106
-278
(jo
Дж/(К • моль)
—
+210
—
+ 110
+ 123
+ 17
—
—
+211
+223
-220
-105
+347
+284
—
+395
—
+229
+285
+235
+382
+373
+337
—
+299
+52
+ 175
+65
+ 181
+11
+272
—
+ 131
+272
+338
+ 162
AG^98,
кДж/моль
—
+13
—
-48
+2
-812
—
—
+77
-51
-1019
-1924
-1465
-2046
—
-2657
-2698
-1149
+77
-334
-277
-360
—
-1040
0
+162
0
+876
-24
+209
-1579
-1444
+ 10
-142
-262
-—
498
IV. Термодинамика
Продолжение табл.
Вещество
pb(BrO3J
Pb(CH3COOJ
РЬ(СН3СООJ • ЗН2О
рьсо3
рьс2о4
[РЬ(СО3J]2"
PbCl
РЬС1+
РЬС12
[Рьсу
РЬС14
Pb(Cl)F
PbCl(OH)
PbCrO4
PbF
PbF+
PbF2
[PbF2]
[PbF3]-
PbF4
Pb(HCOOJ
PbHPO4
[Pb(HSJ]
[Pb(HSK]~
Pbl
Pbl2
Pb(IO3J
PbMoO4
Pb(N3J
Pb(NO3J
PbO
^
Состояние
ТВ.
ТВ.
монокл.
ромб.
ТВ.
Р-Р
газ
Р-Р
газ
ромб.
Р-Р
газ
жидк.
тетр.
ромб.
монокл.
газ
Р-Р
газ
ромб.
Р-Р
Р-Р
газ
ТВ.
ромб.
монокл.
Р-Р
Р-Р
газ
газ
триг.
ТВ.
тетр.
ромб.
куб.
газ
ромб. О)
тетр. (ос)
АН°298,
кДж/моль
—
-961
-1849
-703
-852
—
+20
—
-174
-359
—
-314
-329
-534
—
-915
-84
—
-438
-679
—
—
-778
-840
-879
-1335
—
—
+133
-8
-178
-489
-1049
+382
-447
+48
-217
-219
рО
Дж/(К • моль)
—
—
—
+ 131
+ 146
—
+259
—
+316
+ 136
—
+385
—
+ 115
—
+169
+249
—
+293
+96
—
—
+334
+ 151
—
+ 137
—
—
+280
+354
+ 175
+323
+ 166
+ 150
+213
+240
+69
+66
AG°98,
кДж/моль
-11
—
—
-629
-750
-1127
-4
-165
-182
-314
-301
-276
—
-485
-480
-817
-109
-312
-445
-628
-597
-844
-737
-745
—-
-1203
-87
-83
+86
-60
-176
-348
-948
+528
-251
+26
-188
-189
499
IV. Термодинамика
Продолжение табд
Вещество
РЬО2
РЬОН+
РЬ(ОНJ
[РЬ(ОНJ]
[РЬ(ОНK]-
РЪ3(РО4J
(Pb2IPbIV)O4
PbS
PbSO4
[PbSO4]
PbSe
PbSeO3
PbSeO4
PbSiO3
Pb2Si04
PbTe
PbTeO3
PbWO4
Pd
Pd2+
PdBr2
PdCl+
PdCl2
[PdCl2]
[PdCl3]-
[PdCl4]2"
[PdCl6]2-
Pdl2
[Pd(NH3JCl2]
PdO
PdO2 • 2H2O
Состояние
тетр.
P-P
гекс.
P-P
P-P
гекс.
тетр.
газ
куб.
ромб.
Р-Р
газ
куб.
ТВ.
ромб.
монокл.
ТВ.
газ
куб.
ТВ.
тетр.
газ
куб.
Р-Р
газ
монокл.
Р-Р
газ
ромб.
Р-Р
Р-Р
Р-Р
Р-Р
монокл.
тетр.
тетр.
аморфн.
АН 298,
кДж/моль
-277
—
-545
—
—
-2655
-723
+ 122
-101
-920
—
+ 117
-103
-533
-617
-1146
-1364
+ 166
-68
-572
-1121
+372
0
—
+109
-107
—
+ 128
-163
—
—
—
—
-63
-429
-119
-676
^298»
Дж/(К • моль)
+72
—
+88
—
—
+353
+211
+252
+91
+149
—
+263
+ 103
+195
+142
+110
+ 187
+271
+ 118
—
+ 168
+ 167
+38
—
—
+ 140
—
—
_
—
—
+297
+231
—
—
+36
+ 113
кДж/моль
-21?"
-226
-452
-401
-572
-2433
-606
+76
-99
-813
-783
+71
-102
-470
-505
-1062
-1253
+120
-69
—
-1020
+334
0
+177
—
-92
+11
—
—
-146
-292
-428
-441
—
—
-498
_- ^
500
IV. Термодинамика
Продолжение табл.
Вещество
pdOH+
pd(OHJ
[pd(OHJ]
PdS
Pm
Pm3+
PmCl3
Po
Po"
Po2
PoO2
Pr
Ргз+
Prcl3
PrClj • 7H2O
PrF3
PrF4
РП3
PrO2
Pr2O3
Ph0n
Pr(OHK
Pt
PtBr2
Р1Вг4
PtCl2
(PtCl4]2-
Состояние
p-p
аморфн.
P-P
тетр.
гекс.
P-P
ТВ.
газ
куб.
P-P
газ
куб.
газ.
гекс.
Р-Р
газ
гекс.
трикл.
газ
гекс.
ТВ.
ТВ.
куб.
триг.
куб. (а)
гекс.
газ
куб.
куб.
ромб,
ромб.
Р-Р
Р-Р
р-р
куб.
АН 298»
кДж/моль
-386
-77
0
-1058
+ 147
0
+145
-251
+356
0
-665
-730
-1036
-3184
-1272
-1762
-2003
-684
-1044
-1833
-5713
-1441
+566
0
-100
-159
-106
-503
-230
«о
°298>
Дж/(К • моль)
+92
+56
+72
-172
+ 140
+ 189
+63
+284
+71
+ 190
+74
-172
+379
+144
+420
+96
+134
+213
+67
+ 130
+488
+96
+192
+42
+53
+ 164
+220
+ 167
+268
AG298.
кДж/моль
-53
-302
-287
-73
0
-703
-979
+109
0
+73
+98
-192
+321
0
-713
-721
-957
-2700
-1678
-1900
-674
-920
-1736.
-5390
-1297
+521
0
-58
-105
-93
-80
-228
-369
-164
501
IV. Термодинамика
Продолжение пщл
Вещество
[Ptcy2-
[PtCl4],K2
[PtCl6],K2
[PtCl4],(NH4J
[PtCl6],(NH4J
[PtCl4],Rb2
Ptl2
Ptl4
PtO
PtO2
Pt(OHJ
[Pt(OHL]2"
(PtnPtIV)Br6
(PtnPtIV)Cl6
(Ptnptlv)l6
PtS
PtS2
Pu
Pu+
Pu3+
Pu4+
PuBr3
PuGl3
PuF3
PuF4
PuF6
PuH2
Pul3
PuO2
Состояние
P-P
тетр.
куб.
тетр.
куб.
ТВ.
ТВ.
аморфн.
газ
газ
гекс.
аморфн.
Р-Р
ТВ.
гекс.
ТВ.
тетр.
триг.
газ
монокл.(а)
газ
Р-Р
Р-Р
ромб.
газ
гекс.
гекс.
газ
монокл.
газ
ТВ;
куб.
ромб.
газ
куб.
ДЯ298,
кДж/моль
-674
-1059
-1252
-803
-984
-1069
-63
-57
+456
+171
-88
-352
—
-261
-336
-168
-82
-109
+346
0
—
—
—
-740
-637
-961
-1552
-1518
-1734
-1705
-1753
-140
-560
-473 A875 К)
-1058
^298'
Дж/(К • моль)
+220
+ 180
+334
—
—
—
+281
—
—
+281
+100
—
+223
+247
—
+55
+75
+177
+55
+183
-129
-364
+191
+ 159
+ 113
+334
+162
+369
+223
+60
+234
—
+82
-928
-1101
—
—
—
—
-59
—
-98
-269
-573
-167
-185
—
-76
-100
+310
0
—
-590
—
-713
—
-892
-1479
-1480
-1645
-1617
-1622
-102
-561
—
-1005
-
502
IV. Термодинамика
Продолжение табл.
Вещество
Ra
г***
Ra2+
RaBr2
RaCl2
RaCl22H2O
Ra(NO3J
RaO
RaSO4
Rb
Rb+
Rb2
RbBr
RbBЮз
Rb2CO3
RbCl
RbC103
RbC104
Rb2cro4
RbF
RbH
RbHCO3
Rb(HF2)
Rbl
RbN3
RbNH2
RbNO3
Rbo^
Состояние
газ
куб.
p-p
ромб.
ромб.
ТВ.
ТВ.
ТВ.
ромб.
газ
куб.
газ
Р-Р
газ
газ
куб.
гекс.
монокл.
газ
куб.
ТВ.
ромб.
ромб.
газ
куб.
газ
куб.
ромб.
ТВ.
газ
куб.
тетр.
ТВ.
трип
тетр.
кДж/моль
+162
0
-530
-782
-869
-1468
-993
-523
-1473
+82
0
+491
-251
+115
-194
-394
-364
-1134
-227
-436
-404
-437
-1411
-345
-554
+134
-59
-958
-920
-149
-334
+4
-110
-490
-263
^298>
ДжДКмоль)
+ 176
+71
+29
+ 155
+ 134
+209
+218
+75
+ 146
+170
+77
+164
+121
+271
+261
+108
+159
+172
+250
+96
+152
+167
+218
+237
+75
+59
+121
—
+269
+118
+120
—
+142
+59
ДС^98,
кДж/моль
+131
0
-556
-762
-821
-1304
-796
-494
-1364
+54
0
+459
-284
+80
-226
-381
-454
-1046
-186
-408
-301
-308
-1301
-362
-523
-34
-858
—
-109
-329
+77
—
-389
-197
503
IV. Термодинамика
Продолжение maSnt
Вещество
Rb2O
Rb2O2
RbOH
Rb2S
Rb2SO4
Rb2Se04
Re
ReBr3
[Re2(COI0]
ReCl5
[ReCl6]2-
[Re3Cl9]
[ReCl6],K2
ReF6
ReO2
ReO3
ReO4
Re2O7
ReS2
Re2S7
Rh
RhCl
RhCl2
RhCl3
[RhCl6]3~
Состояние
газ
куб.
газ
ромб.
газ
ромб.
куб.
газ
ромб.
ромб.
газ
гекс.
ТВ.
газ
куб.
монокл.
р-р
гекс.
куб.
газ
жидк.
куб.
куб.
р-р
газ
ромб.
гекс.
ТВ.
газ
куб.
ТВ.
газ
ТВ.
газ
ТВ.
Р-Р
АН°98,
кДж/моль
-94
-337
-178
-427
-236
-413
-354
-1070
-1436
-1124
+778
0
-165
-1583
-1666
-361
-763
-789
-1312
-1353
-1382
-400
-611
-788
-1115
-1263
-179
-451
+557
0
-68
+ 126
-152 '
+67
-229
—
°298'
Дж/(К • моль)
—
+109
—
+105
+249
+79
+134
—
+197
+200
+189
+37
+184
—
+512
+230
+254
+372
+372
+364
+271
+65
+81
+204
—
+207
+96
+204
+186
+32
+84
+121
+159
+209
Дб298.
кДж/моль
—
-293
—
-351
-237
-364
-339
—
-1317
-1003
+733
0
-141
—
-1473
-252
-628
-567
-1174
-1269
-1270
-347
-532
-696
-1089
-178
-423
+511
0
-50
-112
—
-167
-661
504
IV. Термодинамика
Продолжение табл.
Вещество
Rh2O3
Rh2S3
Rn
Ru
RuCl2
RuCl3
RuF5
RuO2
RuO4
Ru(S2)
s2-
s
s+
Я
s2
Я
Я
я
s8
S2Br2
SCI
SC12
sci4
SA
Состояние
триг.
ромб.
газ
газ
гекс.
ТВ.
газ
гекс.
газ
ТВ.
газ
тетр.
газ
жидк.
монокл.
куб.
Р-Р
газ
монокл. (р)
ромб, (а)
газ
Р-Р
газ
Р-Р
Р-Р
Р-Р
газ
газ
жидк.
газ
газ
жидк.
жидк.
газ
жидк.
АН298,
кДж/моль
-356
-243
0
+657
0
-171
+69
-266
-744
-893
+ 170
-306
-184
-228
-240
-226
+33
+279
«0
0
+ 1279
+30
+128
+26
+23
+21
+ 100
+102
-15
+ 126
-20
-49
-56
-19
-61
°298'
Дж/(К • моль)
+ 106
—
+ 168
+ 186
+29
+167
—
+ 128
—
+ 161
—
+57
+291
+177
+141
+48
-15
+ 168
+33
+32
+ 164
+28
+228
+66
+103
+ 141
+354
+431
—
+239
+282
—
—
+331
+ 167
AG^98,
кДж/моль
-277
—
0
+610
0
-146
—
-196
—
-781
-253
-140
-150
-151
-213
+86
+238
«0
0
+1233
+79
+79
+74
+69
+66
+52
+50
—
+98 -
-28
—
—
-32
-25
505
IV. Термодинамика
Продолжение табл.
Вещество
SC12O
SC12O2
S(C1)O2F
SF
SF2
SF4
SF6
S2FP
SN
S4N4
SO
so2
[SO2]
[SO2 • H2O]<13>
so2.-
so3
so^-
S2O
S2OJ-
s2or
s2o|-
s3or
s4or
s5or
S(O)F2
SO2F2
s2o6(o2J-
SO3S2-
Sb
Sb+
Состояние
газ
жидк.
газ
жидк.
газ
газ
газ
газ
газ
газ
газ
монокл.
газ
газ
ромб.
Р-Р
Р-Р
Р-Р
газ
жидк.
монокл. (а)
Р-Р
газ
Р-Р
Р-Р
Р-Р
Р-Р
Р-Р
Р-Р
газ
газ
Р-Р
Р-Р
газ
триг.
газ
АН°98,
кДж/моль
-213
-246
-364
-378
-564
+76
-296
-770
-1221
-228
+234
+460
+6
-297
-331
-323
—
-636
-396
-468
-455
-909
-56
—
—
—
—
—
—
-565
-858
-1339
-652
+268
0
+1109
°298>
Дж/(К • моль)
+308
+279
+312
+216
—
+228
+258
+290
+291
+290
+222
—
+222
+248
—
+162
+232
-29
+257
+122
+52
+18
+267
+105
+105
+126
+138
+151
+167
+279
+288
+249
+37
+180
+46
+169
кДж/моль
-198
-223
-320
-305
—
+48
-303
-726
-1117
-235
+206
—
-20
-300
—
-301
-538
-487
-371
-373
-369
-744
-86
-598
-791
-967
-958
-1031
-958
-548
-813
-1113
-514
+228
0
+1066
506
IV. Термодинамика
Продолжение табл.
Вещество
Sb2
Sb4
SbBr3
SbCl3
[SbCIJ-
SbCl5
Sb(Cl)O
SbF
SbF3
SbH3
Sbl3
SbO
Sb2O3
Sb2O3 • 3H2O
Sb2O5
Sb(OH)}
[Sb(OHK]
Sb2S3
Sb2(SO4K
(SbIIISbv)O4
Sb2Se3
SbTe
Sb2Te3
Sc
Sc3+
ScBr3
ScCl3
ScF2+
Состояние
газ
газ
газ
ромб.
газ
ромб.
Р-Р
газ
жидк.
монокл.
газ
ромб.
газ
газ
триг.
газ
куб. (а)
ромб, (р)
аморфн.
куб.
Р-Р
Р-Р
ромб.
ТВ.
ромб.
ромб.
газ
триг.
газ
гекс.
Р-Р
газ
ТВ.
газ
триг.
Р-Р
кДж/моль
+239
+ 191
-194
-259
-314
-383
—
-394
-440
-374
-74
-907
+ 145
-8
^98 >
+6
-721
-709
-1543
-1008
—
-774
-158
-2402
-908
-127
+204
-57
+378
0
-632
-544
-752
-686
-941
-960
^298' .
Дж/(К • моль)
+257
+351
+373
+207
+338
+ 184
—
+402
+301
—
+235
+105
+233
+400
+213
+22
+ 132
+141
+216
+125
—
+ 126
+ 182
—
+ 127
+ 197
+268
+234
+ 175
+35
-264
+155
+337
+128
-124
кДж/моль
+ 190
+ 141
-224
-239
-301
-324
-476
-334
-350
—
-100
-834
+148
-62
-96
-20
-641
-632
-1280
-865
-417
-647
-156
—
-796
-121
-153
-55
+336
0
-601
-720
-676
-869
-922
507
IV. Термодинамика
Продолжение тайп%
Вещество
ScF2
[ScF3]
[ScF4]"
Sc2O3
ScOH2+
Sc(OHK
Se2"
Se
Se+
Se^"
Se2
Se6
Se8
SeBr4
SeBr2O
SeCl2
SeCl4
Se2Cl2
SeCl2O
SeF6
SeO
SeO2
SeO^~
SeO3
SeO2"
Si
Si+
Si2
SiBr
SiBr2
SiBr4
Состояние
P-P
P-P
P-P
куб.
P-P
куб.
P-P
аморфн.
газ
триг.
газ
Р-Р
газ
газ
монокл.
ТВ.
ТВ.
газ
монокл.
жидк.
газ
газ
газ
газ
тетр.
Р-Р
тетр.
Р-Р
газ
куб.
газ
газ
газ
газ
газ
жидк.
АН 298,
кДж/моль
-1296
-1635
—
-1909
—
-1376
+64
+5
+228
0
+1175
—
+139
+149
+56
-70
-140
+378
-179
-85
-25
-1117
+55
-127
-226
-509
-167
-599
+452
0
+1244
+593
+181
-43
-420
-461
°298>
Дж/(К • моль)
-33
+20
—
+77
—
+93
-46
+48
+177
+42
+ 175
__
+252
+460
—
—
—
+ 175
+ 184
+ 188
+324
+314
+234
+265
+67
-7
+72
+54
+ 168
+ 19
+ 163
+231
+247
+303
+377
—
298»
кДж/моль
-1235
-1540
-1836
-1819
-812
-1243
+129
+3
+188
0
+1129
+ 114
+89
+87
—
—
+336
-88
-50
-12
-1017
+28
-132
-172
-364
-84
-441
.
+408
0
+1195
+535
+136
-82
-436
__———
508
IV. Термодинамика
Продолжение табл.
Вещество
SiC
SiCl
SiCl2
SiCl3
SiCl4
SiF
SiF2
SiF3
SiF4
[SiF4]2"
[SiF6]2~
[SiF6],Ca
[SiF6],K2
[SiF6],Mg-6H2O
[SiF6],(NH4J
[SiF6],Na2
SiH
SiH2
SiH3
SiH4
Si2H6
Si3H8
SiHCl3
Sil
SiN
Si3N4
SiO
SiO2 (лешательеит)
(коэсит)
fa-тридимит)
fo-кристобалит)
(стишовит)
Состояние
гекс.
куб.
газ
газ
газ
газ
жидк.
газ
газ
газ
газ
Р-Р
Р-Р
тетр.
куб.
монокл.
куб.
триг.
трип
газ
газ
газ
газ
газ
газ
жидк.
газ
газ
газ
гекс.
газ
аморфн.
газ
монокл.
ромб.
тетр.
тетр.
АН°298,
кДж/моль
-63
-65
+ 118
-160
-311
-657
-687
+7
-620
-1000
-1616
—
-2396
-2899
-2966
-4579
-2687
-2689
-2918
+361
+339
+212
+34
+79
+ 121
+92
-513
+220
+486
-744
-99
-902
-321
-906
-909
-908
-861
с°
^298'
Дж/(К • моль)
+ 16
+ 17
+238
+279
+316
+331
+237
+226
+256
—
+282
—
+ 125
—
+236
—
+284
+280
+191
+198
—
—
+205
+274
—
—
+314
—
+217
+ 101
+212
+47
+229
+40
+44
+43
+28
4^298'
кДж/моль
-60
-63
+86
-171
-300
-617
-619
-24
-630
—
-1573
-1612
-2207
—
-2810
—
-2371
-2372
-2757
+327
—
—
+57
+126
—
-482
—
+456
-643
-126
-849
-322
-851
-855
-854
-803
509
IV. Термодинамика
Продолжение mafy
Вещество '
(а-кварц)
SiO2 • Н2О
SiOj"
Si(O)F2
SiS
SiS2
Sm
Sm2+
Sm3+
SmC2
SmCl2
SmCl3
SmCl3 • 6H2O
Sml3
Sm2(MoO4K
Sm2O3
Sm2(SO4K • 8H2O
Sn
Sn(cep.)
8п(бел.)
Sn+
Sn2+<14>
Snlv<15>
SnBr
SnBr+
SnBr2
SnBr4
SnCl
SnCl+
Состояние
триг.
аморфн.
p-p
газ
газ
жидк.
ромб.
газ
триг.
Р-Р
Р-Р
тетр.
газ
ромб.
гекс.
монокл.
ТВ.
ромб.
куб.
монокл.
монокл.
газ
куб. (а)
тетр. (р)
газ
Р-Р
Р-Р
газ
Р-Р
газ
ромб.
газ
ромб.
газ
Р-Р
АН 298,
кДж/моль
-912
-1188
-1353
-935
+113
-157
-205
+208
0
-691
-71
-500
-816
-1053
-2873
-643
-4276
-1826
-1845
-6299
+302
-2
0
+ 1018
-24
-2
+80
—
-121
-268
-314
-406
+43
—
D298'
Дж/(К • моль)
+41
—
-402
+271
+224
+91
—
+183
+70
-75
-212
+95
+316
+126
+ 142
+381
+220
+446
—
+151
+673
+ 168
+44
+52
+ 174
-70
-398
+263
+95
—
+146
+412
—
+252
+109
Дб298.
кДж/моль
-857^""
—
-1027
-951
+61
-159
—
+174
0
-515
-665
-75
-507
-866
-975
-2448
-636
-3975
—
-1727
-5506
+267
«0
0
+975
-27
-2
+40
-138
—
-251
-331
—
+17
-167
510
IV. Термодинамика
Вещество
SnCl2
[SnClJ
[SnCy
SnCl4
[SnCl6],K2
[SnCl6],(NH4J
SnF
SnF+
SnF2
SnF4
SnH
SnH4
SnI
Snl2
Snl4
SnO
SnO2
SnO2 • 2H2O
SnOH+
Sn(OHJ
[Sn(OHJ]
[Sn(OHK]-
[Sn(OHN],Ca
SnS
SnS2
[SnSO4]2-
SnSO4
Sn(SO4J
SnSe
S*(Se03J
Состояние
газ
ромб.
P-P
p-P
газ
жидк.
куб.
куб.
газ
Р-Р
газ
монокл.
газ
газ
газ
газ
газ
монокл.
куб.
газ
тетр.
тетр.
аморфн.
Р-Р
аморфн.
Р-Р
Р-Р
ТВ.
газ
ромб.
триг.
Р-Р
ромб.
ТВ.
газ
ТВ.
ТВ.
• АН298> . !
кДж/моль
-205
-331
—
—
-471
-511
-1482
-1234
-150
—
-452
-649
—
+265
+ 163
+197
+8
-144
-199
+21
-286
-581
-1116
—
-561
' —
—
-1964
+110
-101
-168
—
-887
-1684
+123
-91
-982
Продолжение табл.
^298'
Дж/(К • моль)
—
+ 132
—
—
+366
+265
+371
+431
+242
—
—
—
+314
+213
+229
+271
—
+ 167
+232
+56
+52
+ 155
+47
+ 155
—
—
—
+243
+77
+87
—
—
+ 155
+255
+92
—
AG°298,
кДж/моль
—
-288
-303
-433
-432
-442
-1339
-934
-117
-335
—
+237
+ 188
+ 149
-144
—
-2
-257
-520
-946
-252
-492
-464
-646
—
+63
-99
-159
-782
—
-1451
+75
-90
—
511
IV. Термодинамика
Продолжение табл.
Вещество
SnTe
Sr
Sr+
Sr2+
SrBr2
Sr(BrO3J • H2O
SrC2
SrCO3
SrCl
SrCl2
SrCl2 • 6H2O
Sr(C103J
Sr(C104J
SrCrO4
SrCr2O7
SrF2
(SrFe2)O4
SrH
SrH2
(SrHf)O3
Srl2
Srl2 • 6H2O
Sr(IO3J
Sr(IO3J • H2O
SrMoO4
Sr(NO2J
Sr(NO3J
Sr(NO3J • 4H2O
SrO
Состояние
газ
куб.
газ
куб.(а)
газ
Р-Р
газ
ромб.
монокл.
тетр.
ромб.
газ
газ
куб.
триг.
ромб.
ТВ.
монокл.
ТВ.
газ
куб.
гекс.
газ
ромб.
монокл.
газ
ромб.
триг.
трикл.
ТВ.
тетр.
ТВ.
куб.
монокл.
газ
куб.
АН298,
кДж/моль
+201
-61
+ 164
0
+719
-556
-423
-729
-1014
-84
-1232
-116
-471
-836
+2625
-744
—
-1435
-2053
-778
-1233
-1081
+220
-180
-1827
-271
-568
-2397
-1060
-1313
-1559
-766
-988
-2150
-60
-604
°298'
Дж/(К • моль)
+263
+ 103
+ 165
+53
+170
-27
—
+136
+283
—
+97
+250
+315
+126
+350
—
+247
+142
+229
+290
+82
—
+212
+52
—
+341
+ 159
—
+243
+292
+141 '
+ 176
+ 195
+364
+230
+54
AGgge,
кДж/моль
+ 153
-61
+ 131
0
+678
-571
—
-708
-1244
—
-1152
-142
-459
-791
-2230
—
—
-1332
-1878
-788
-1181
—
+192
-141
—
-322
-565
—
-899
-1097
-1454
-623
-790
-1724
-82
-574
—-—
512
IV. Термодинамика
Продолжение табл.
Вещество
SrO2
SrOH+
Sr(OHJ
Sr(OHJ-8H2O
SrS
SrSO4
SrS2O6 • 4H2O
SrSe
SrSeO3
SrSeO4
SrSiO3
Sr2Si04
(SrTi)O3
SrWO4
(SrZr)O3
T
T2
T2O
TS
Та
TaCl3
TaCl4
TaCl5
TaF5
TaOj
Ta2O5
Tb
Tb3+
TbBr3
TbCl3
Состояние
тетр.
P-P
газ
тетр.
тетр.
куб.
ромб.
гекс.
куб.
ТВ.
монокл.
гекс.
монокл.
куб.
тетр.
монокл.
газ
газ
газ
газ
газ
куб.
куб.
монокл.
газ
монокл.
газ
монокл.
Р-Р
ромб.
газ
гекс.
Р-Р
ТВ.
монокл.
АН°98,
кДж/моль
-637
-782
-564
-957
-3361
-453
-1467
-2911
-387
-1051
-1156
-1646
-2329
-1684
-1656
-2634
+223
0
-252
+145
+782
0
-544
-707
-763
-858
-1828
-1904
-1151
-2048
+389
0
—
-839
-1045
д298>
ДжДКмоль)
—
-6
—
+87
—
+68
+ 111
—
—
+ 127
+113
. +97
+153
+109
+138
+115
+ 128
+153
+204
—
+185
+42
—
—
—
+236
+170
+151
+143
+203
+73
-180
—
+ 146
AG^98,
кДж/моль
—
-733
—
-867
—
-448
-1353
—
—
-969
-1039
-1562
-2215
-1600
-1549
-2549
+208
0
-237
—
+739
0
—
—
—
-750
-1791
-1073
-1913
+350
0
-690
—
-937
7-2004
513
IV. Термодинамика
Продолжение табл.
Вещество
ТЬС13 • 6Н2О
Tb(NO3K • 6Н2О
ТЬО2
ТЬ2О3
Тс
ТсО2
ТсО3
ТсО4
Тс2О7
Те2~
Те
Те+
ТеГ
Те2
ТеВг4
ТеС14
TeF6
Tel4
ТеО
ТеО2
ТеО^-
Th
Th4+
ThBr4
ThC2
ThCl3+
ThCl4
ThCl2O
Состояние
монокл.
монокл.
куб.
куб.
газ
гекс.
монокл.
ТВ.
Р-Р
ТВ.
Р-Р
аморфн.
газ
триг.
газ
Р-Р
газ
монокл.
газ
монокл.
газ
ромб.
газ
газ
ромб.
Р-Р
газ
куб.(а)
Р-Р
газ
ромб.
монокл.
Р-Р
газ
ромб.
ТВ.
АН°98,
кДж/моль
-2871
-3044
-961
-1865
+649
0
-433
-540
-724
-1117
+ 101
+ 11
+192
0
+ 1067
—
+ 167
-209
-207
-324
-1369
-63
+ 173
-59
-329
-533
+576
0
-760
-766
-949
-125
—
-973
-1194
-1236
«о
^298»
ДжДКмоль)
+404
—
+83
+149
+181
+33
+63
+72
-314
+184
-64
—
+ 183
+50
+ 181
—
+268
+71
—
+209
+336
—
+241
+273
+59
+ 13
+190
+53
-330
+438
+234
+69
—
+396
+199
+133
кДж/моль
-2452
—
-903
-1774
+605
0
-381
-460
-630
-938
+174
—
+152
0
+1022.
+163
+117
-125
—
-238
-1273
—
+147
-64
-270
-391
+535
0
-724
-790
-912
-126
-863
-942
-1105
-1163
514
IV. Термодинамика
Продолжение табл.
Вещество
ThF3+
ThFr
ThF}
ThF4
Thl4
Th3N4
ThO2
ThOH3+
Th(OH)f
Th(OH)}
Th(OHL
ThS2
Th(SO4J
Ti
TiBr2
TiBr3
TiBr4
TiCl
TiCl2
T1CI3
TiCl4
T,F2
T,F3
TiF4
OiFe"H,
TiH
Состояние
P-P
P-P
P-P
газ
монокл.
газ
монокл.
ТВ.
газ
куб.
Р-Р
Р-Р
Р-Р
аморфн.
ромб.
ТВ.
газ
гекс.
куб.
газ
ТВ.
газ
куб.
куб.
газ
триг.
газ
триг.
газ
жидк.
газ
газ
ромб.
аморфн.
газ
триг.
газ
АН°98,
кДж/моль
—
—
—
-1674
-2096
-418
-552
-1405
«-510
-1227
-1021
-1274
—
-1772
-627
-2541
+471
0
-385
-336
-551
-551
-619
-185
-303
-517
-541
-732
-761
-805
-654
-1164
-1412
-1649
-1553
-1235
+215
^298'
Дж/(К-моль)
—
—
—
+346
+ 142
+470
+272
+ 179
—
+65
-195
-150
—
+ 144
+96
+ 148
+ 180
+31
+ 126
—
+ 177
+399
+241
+24
+284
+106
+319
+ 140
+352
+252
+261
+287
+103
+134
+312
+106
+215
кДж/моль
-1045
-1357
-1666
-1640
-2002
-363
-548
-1297
—
-1169
-939
-1152
-1354
-1599
-621
-2306
+427
0
-368
—
-527
-570
-591
-181
-312
-473
-527
-665
-724
-738
-662
-1150
-1343
-1559
-1516
-1158
+180
515
IV. Термодинамика
Продолжение табл.
Вещество
TiH2
Til2
Til3
Til4
(TiMnn)O3
TiN
(TiNin)O3
TiO
TiO2
Ti2O3
Ti(OHK
TiO(OHJ
TiP
TiS
TiS2
TiSe
TiSe2
(TiZnn)O3
(TiZn2I)O4
Tl
Tl+
Tl3+
Tl2
TIBr
T12CO3
T12C2O4
T1C1
Состояние
куб.
газ
триг.
ТВ.
газ
куб.
триг.
куб.
триг.
газ
куб.
газ
тетр. (Р)
тетр. (у)
триг.
аморфн.
аморфн.
гекс.
гекс.
триг.
гекс.
гекс.
куб.
куб.
газ
гекс.
газ
Р-Р
Р-Р
газ
газ
куб.
монокл.
монокл.
газ
куб.
кДж/моль
-144
-62
-270
-341
-287
-386
-1358
-338
-1208
+63
-519
-334
^938
044
-1521
-334
—
-283
-269
-425
-237
-309
-1297
-1652
+ 181
0
+789
+6
+ 197
+301
-39
-172
+699
-883
-69
-204
^298»
ДжДКмоль)
+30
+323
+ 148
+192
+433
+246
+ 105
+30
+74
+233
+35
+236
+50
+50
+79
—
—
—
+56
+78
—
—
—
+143
+ 181
+64
+ 175
+129
-192
+287
+268
+123
+ 159
—
+256
+ 111
кДж/моль
-105
-10
-270
-337
-338
-381
-1279
-309
-1120
+33
-490
-334
-883
-889
-1434
—
-1059
—
-267
-430
—
—
—
-1538
+146
0
+750
-32
+215
+254
-77 •
-167
-615
—
-93
-185
516
IV. Термодинамика
Продолжение табл.
Вещество
[Т1С1]
Т1С12+
гпсщ-
Ticij
[Ticy
[Т1С14]-
Т1СЮ3
Т1СЮ4
Т12СЮ4
T1F
[T1F]
T1F3
тн
Т1Ю3
T1N3
T1NCS
T1NO2
TINO3
Т12О
Т12О3
Т12О3 • ЗН2О
тюн
[Т1ОН]
Т1ОН2+
П(ОН)+
ГП(ОНK]
n2s
T12S3
msoj-
T12SO4
Ti2so3s
Состояние
p-p
p-p
p-p
p-p
МОНОКЛ.
P-P
P-P
ТВ.
ромб.
ромб.
газ
ромб.
Р-Р
ТВ.
газ
ромб.
триг.
тетр.
ромб.
куб.
ромб.
газ
гекс.
куб.
аморфн.
газ
ТВ.
Р-Р
Р-Р
Р-Р
Р-Р
триг.
аморфн.
Р-Р
ромб.
ромб.
АН 298,
кДж/моль
-167
+7
—
-179
-315
-351
-518
-134
-138
-957
-154
-327
—
—
+16
-123
-265
-234
+34
-142
-242
+9
-178
-411
-1033
-100
-239
-222
—
—
—
—
-116
-903
-931
—
^298'
Дж/(К • моль)
+179
-69
—
+ 11
+325
+ 103
+202
+169
—
+247
+244
+96
—
• —
+277
+128
+179
+ 126
—
—
+161
+314
+126
+135
+204
+255
+88
+139
—
—
—
—
+ 151
+ 170
+231
—
AGgge,
кДж/моль
-168
+41
-296
-116
-293
-263
-407
-40
—
-863
-208
-306
-313
-515
-30
-125
-190
+301
—
—
-151
-16
-147
-321
-755
-107
-196
-194
-15
-243
-470
-88
—94
-784
-830
-610
517
IV. Термодинамика
Продолжение табл.
Вещество
Tl2Se
Tl2Se04
Т12Те
Tm
Tm3+
TmCl3
TmF3
Tml3
Tm2O3
u-
u
u3+
u4+
UBr3
UBr4
UBr2O
UC2
[U(CO3JO2]2-
[U(CO3KO2]4~
UC13+
UC13
UC14
UC15
UC16
[U(C1)O2]+
UF3+
UFf
UF3
Состояние
тетр.
ромб.
ТВ.
газ
гекс.
Р-Р
монокл.
газ
гекс.
куб.
газ
газ
ромб.
Р-Р
Р-Р
газ
гекс.
газ
монокл.
ТВ.
тетр.
Р-Р
Р-Р
Р-Р
гекс.
газ
тетр.
газ
монокл.
газ
триг.
Р-Р
Р-Р
Р-Р
газ
гекс.
Д^298>
кДж/моль
-58
-629
-89
4-232
0
—
-962
-1295
-582
-1888
—
-524
0
-491
-590
-342
-711
-577
-822
—
-88
—
—
—
-891
-820
-1049
-866
-1253
-1020
-1139
—
—
—
-1096
-1489
°298'
Дж/(К • моль)
+172
+245
+177
+190
+74
-186
+146
—
+218
+139
+203
-200
+50
-153
-346
+205
—
+243
+158
+68
—
—
—
+159
+390
+198
—
+243
+286
—
—
—
+332
+117
А^298»
кДж/моль
-59
-529
-89
+ 197
0
-661
-884
—
-573
-1794
—
+479
0
-489
-550
—
-689
—
-789
—
-90
-2120
-2673
-677
-824
-788
-960
-1144
-1010
-1094
-913
-1223
-1089
-1418
518
IV. Термодинамика
Продолжение табл.
Вещество
UFt
UF4
2UF4 • 5H2O
[UF4]
[UF5]-
UF5
[UF6]2"
UF6
UH3
UI3
UI4
UO2
uo2
uof
uo2,25
UO233
uo3'
UO2(CH3COOJ • 2H2O
UO2CO3
(UO2)C12
UO2F+
(UO2)F2
[UO2F2]
[UO2F3]"
[UO2F4]2~
UOH3+
U(OHL
UO2HPO4
U°2(NO3J
Состояние
P-P
газ
монокл.
ромб.
P-P
P-P
газ
тетр. (р)
P-P
газ
ромб.
куб.
ромб.
газ
ромб.
газ
куб.
Р-Р
Р-Р
ромб.
куб.
аморфн.
монокл.
ромб.
ромб.
ромб.
газ
ромб.
Р-Р
триг.
Р-Р
Р-Р
Р-Р
Р-Р
аморфн.
ТВ.
ТВ.
АН 298,
кДж/моль
_
-1591
-1925
-5367
—
—
-2030
-2039
—
-2137
-2186
-127
-478
-280
-529
«-430
-1085
-1035
-1024
-1131
-1142
-1209
-1225
-1219
-2615
-1696
-992
-1252
-1367
-1650
—
—
—
-827
-1668
-1377
$298'
Дж/(К • моль)
—
+349
+152
+500
—
—
+377
+ 188
—
+376
+228
+64
+238
—
+280
—
+78
+50
-86
+84
+84
—
+99
—
—
+ 146
—
+ 151
-37
+ 140
—
—
—
-115
+67
+276
кДж/моль
-1528
-1560
-1834
-4896
-1832
-2121
-1976
-1929
-2414
-2053
-2058
-73
-482
—
-528
-1032
-967
-961
-1072
-1081
—
-1148
—
—
-1570
-1155
-1270
-1555
-1574
-1869
-2157
-786
-1473
-2112
-1143
519
IV. Термодинамика
Продолжение табл.
Вещество
UO2(NO3J • 2Н2О
UO2(NO3J • 6Н2О
UO2(OH)+
Ш2(ОНJ
UO2(OHJ • Н2О
[UO2(OHJ]
(UO2K(PO4J
UO2SO4
UO2SO4 • ЗН2О
us
us2
U(SO4J
[U(SO4)O2]
[U(SO4JO2]2~
(uyu^Og
V
V2+
v>+
VBr2
VBr3
vc0)8g
VC12
VC13
VC14
V(C1)O
VC13O
VF2
VF3
VF4
Состояние
МОНОКЛ.
ромб.
p-p
ромб.
ромб.
p-p
ТВ.
ТВ.
ТВ.
куб.
ромб.
тетр.
ТВ.
р-р
р-р
ромб.
газ
куб.
р-р
р-р
ТВ.
газ
гекс.
куб.
газ
гекс.
газ
триг.
газ
жидк.
ромб.
газ
жидк.
ТВ.
ромб.
гекс.
Д^298'
кДж/моль
-1979
-3177
-1258
-1535
-1827
-1515
—
-1888
-2790
-314
-533
-525
-2368
-1913
-2818
-3574
+515
0
-227
-263
—
-258
-446
-102
-216
-457
-369
-581
-524
-576
-609
-696
-736
—
-1421
О298»
Дж/(К-моль)
+328
+505
+60
+142
+ 192
+87
—
+155
+264
+78
+111
+110
+161
+54
+113
+282
+182
+29
-135
-238
—
—
+142
+28
+284
+97
+333
+131
+364
+235
+75
+343
+242
—
+98
+123
Дб298,
кДж/моль
-1621
-2594
-1169
-1401
-1639
-1365
-5188
-1726
-2452
-313
-532
-524
-2138
-1721
-2473
-3369
+469
0
-217
-242
-389
—
-412
-100
-226
-411
-360
-512
-491
-504
-559
-659
-669
-707
—
-1328
520
IV. Термодинамика
Вещество
VF5
VI2
VI3
VN
vo
vo2+
vo2
vo^
vo|-
V2O3
V2O5
VOF+
[VOF2]
[VOF3]-
VOH2+
VO(OHJ
[V(SO4)O]
w
WBr2
WBr3
WBr5
WBr6
WBr4O
we
[W(CON]
WC15
wo,
Состояние
газ
ромб.
газ
триг. (а)
газ
куб.
газ
куб.
Р-Р
ромб.
Р-Р
Р-Р
триг.
ромб.
Р-Р
Р-Р
Р-Р
Р-Р
монокл.
Р-Р
газ
куб.
ТВ.
ТВ.
газ
ТВ.
газ
ТВ.
тетр.
гекс.
газ
ромб.
газ
монокл.
газ
куб.
ДН°98,
кДж/моль
-1355
-1481
-22
-256
-46
-217
+150
-432
-489
-713
-650
—
-1218
-1550
—
—
—
—
+850
0
-80
+104
-223
-313
-245
-385
-548
-41
-881
-952
-498
-518
-551
-620
Продолжение табл.
^298'
Дж/(К ¦ моль)
+331
+ 192
—
+ 172
—
+37
+231
+39
-141
+52
-42
—
+99
+131
—
—
—
—
—
+174
+33
+155
+230
+460
+272
+487
+301
—
+36
+501
+332
+432
+230
+406
+301
AGgge,
кДж/моль
-1294
-1378
—
-264
—
-191
+120
-404
-446
-659
-587
-903
-1139
-1419
-745
-1038'
-1327
-462
-887
-1204
+808
0
-71
+ 113
-237
-271
-244
-329
—
-40
-826
-847
-451
-411
-463
-501
521
IV. Термодинамика
Продолжение табл.
Вещество
WC12O2
WC14O
WF6
WI2
wo
wo2
wo3
WO3 • H2O
wo^-
W(O)F4
ws2
Xe
[Xe]
Xe+
XeCl2
XeF2
XeF4
Y
YC12+
YCI3
YCI3 • 6H2O
YF2+
YFJ
YF3
Состояние
газ
ТВ.
газ
тетр.
газ
жидк.
куб.
аморфн.
газ
газ
монокл.
газ
трикл.
газ
р-р
ромб.
Р-Р
газ
монокл.
гекс.
газ
Р-Р
газ
газ
тетр.
монокл.
газ
гекс.
Р-Р
Р-Р
газ
монокл.
монокл.
Р-Р
Р-Р
газ
ромб.
АН 298,
кДж/моль
-701
-789
-612
-689
-1722
-1748
-1750
-5
+439
+88
-590
-293
-843
-906
—
-1172
-1073
-1372
-1445
-213
0
-18
+ 1176
+ 161
-176
-251
+425
0
-702
—
-770
-1025
-2850
—
—
-1263
-1718
со
05 298'
Дж/(К-моль)
+251
+ 132
+364
+213
+342
+253
+223
+ 176
+256
+276
+50
+287
+76
—
__
+ 117
+97
—
—
+68
+ 170
+66
+ 181
—
—
—
+179
+44
-202
—
+351
+138
+372
+317
+ 110
AG298>
кДж/моль
-638
-691
-547
-579
-1633
-1632
-1625
-13
+403
+77
-534
-277
-764
—
-965
-1036
-931
—
—
-204
0
+13
-1167
—
—
—
+385
0
-687
-825
-762
-953
-2431
-994
-1295
-1254
-1647
522
IV. Термодинамика
Продолжение табл.
Вещество
[YFJ
Yl3
YO
Y2O3
YOH2+
Y(OHK
[YSO4]+
[Y(SO4J]-
Yb
Yb2+
Yb3+
YbBr3
YbCl2
YbCl3
YbCl3 • 6H2O
YbF3
Yb2O3
Yb(OHK
Zn
Zn2+
(ZnAl2)O4
2Zn3(As04J • 5H2O
ZnBr
ZnBr2
Zn(CH3COOJ
Zn(CH3COOJ • 2H2O
Zn(CNJ
tZn(CNL]2-
ZnCO3
ZnCl
ZnCl2
Состояние
P-P
гекс.
газ
куб.
P-P
гекс.
P-P
P-P
газ
куб.(а)
P-P
P-P
ТВ.
газ
ромб.
монокл.
монокл.
газ
ромб.
куб.
ТВ.
газ
гекс.
Р-Р
куб.
монокл.
газ
газ
тетр.
тетр.
монокл.
куб.
Р-Р
триг.
газ
газ
тетр.
ДН°98,
кДж/моль
—
-537
-42
-1905
—
-1431
-1597
-2498
+ 152
0
—
—
-794
-445
-772
-962
-2486
-1355
-1657
-1815
—
+ 130
0
-154
-2067
—
+ 102
-186
-330
-1076
-1671
+90
-332
-816
+6
-265
-415
ДжДКмоль)
—
+201
+236
+99
—
+ 103
+75
-15
+ 173
+60
-75
-192
—
+314
+ 120
+ 146
+383
+331
+111
+ 133
—
+161
+42
-111
—
—
—
+300
+ 136
—
—
—
+259
+82
+244
+277
+ 109
AG^98>
кДж/моль
-1596
-532
-69
-1817
-872
-1298
-1449
-2197
+118
0
-510
-657
—
-454
-723
-888
-2065
-1345
-1581
-1727
-1281
+95
0
-147
—
-5222
—
-218
-313
—
—
-427
-734
-21
-269
-369
523
IV. Термодинамика
Продолжение табл.
Вещество
Zn(C104J • 6Н2О
ZnF
ZnF+
ZnF2
ZnH
[Zn(HSJ]
[Zn(HSK]-
Znl2
Zn(IO3J
Z11MOO4
Zn3N2
[Zn(NH3L]2+
[Zn(NH3JCl2]
Zn(NO3J
Zn(NO3J • H2O
Zn(NO3J • 2H2O
Zn(NO3J • 6H2O
ZnO
ZnOH+
Zn(OHJ
[Zn(OH)J
[Zn(OH)J-
[Zn(OHL]2"
Zn3P2
Zn3(PO4J
Zn3(PO4J • 4H2O
ZnS
ZnSO4
ZnSO4 • 6H2O
ZnSO4 • 7H2O
[ZnSO4]
Состояние
гекс.
газ
P-P
газ
тетр.
газ
Р-Р
Р-Р
газ
тетр.
ТВ.
ТВ.
куб.
р-р.
ромб.
ТВ.
ТВ.
ТВ.
тетр.
газ
гекс.
Р-Р
аморфн.
ромб.
р-р
Р-Р
Р-Р
тетр.
монокл.
ромб.
газ
гекс. (р)
куб. (а)
ромб.
монокл.
ромб.
Р-Р
АИ>29в»
кДж/моль
-2121
-157
-478
-497
-764
+228
—
—
-65
-212
—
-116
-23
-677
-699
-495
-804
-1110
-2305
+105
-351
—
—
-644
—
—
—
-195
-2900
—
+204
-195
-209
-980
-2773
-3077
-1060
Й298'
Дж/(К • моль)
—
+233
-70
+254
+74
+204
—
+317
+157
—
+130
—
+298
—
+192
—
—
+410
+225
+44
_
—
+75
—
—
—
—
—
—
+238
+68
+58
+110
+364
+389
-39
AGgge,
кДж/моль
—
-184
-434
-500
-713
+199
-208
-203
-112
-212
-430
-1011
—
-536
—
-299
—
—
-1757
+81
-321
-333
-550
-554
-535
-705
-871
—
—
-3611
+ 155
-193
-204
-869
-2320
-2562
-905
524
IV. Термодинамика
Продолжение табл.
Вещество
ZnSe
ZnSeO3
ZnSeO3 • Н2О
ZnSeO4
ZnSeO4 • H2O
ZnSeO4 • 6H2O
ZnSiO3
Zn2Si04
ZnTe
ZnWO4
Zr
ZrIV
ZrBr3
ZrBr4
ZrC
ZrCl
ZrCl2
ZrCl3
ZrCl4
ZrCl2O
ZrCl2O • 8H2O<16>
Zr(C104L
ZrD2
ZrF3+
ZrF2
ZrF^
ZrF3
ZrF+
ZrF4
Состояние
газ
куб.
ТВ.
ТВ.
ТВ.
ТВ.
трикл.
ромб.
триг.
куб.
монокл.
газ
гекс.
Р-Р
ТВ.
газ
куб.
куб.
аморфн.
аморфн.
газ
газ
гекс.
газ
монокл.
ТВ.
тетр.
ТВ.
ТВ.
Р-Р
газ
ТВ.
Р-Р
газ
Р-Р
газ
монокл.
кДж/моль
+218
-168
-623
-930
-674
-993
-2469
-1232
-1642
-120
-1233
+608
0
—
-636
-643
-759
-197
-303
-531
-326
-603
-754
-867
-981
-1083
-3468
-746
-169
-614
-962
-1188
—
-1663
-1911
«о
^298'
Дж/(К • моль)
+250
+83
+177
—
—
—
—
+90
+131
+83
+141
+181
+39
—
+ 172
+415
+225
+33
+61
+ 100
+308
+337
+ 138
+369
+ 181
+61
—
—
+38
—
+257
+88
—
+303
—
+329
+ 105
кДж/моль
+169
-168
-559
—
—
—
—
-1149
-1528
-117
-ИЗО
+566
0
-524
+608
-664
-724
-193
-276
-482
-340
-592
-685
-832
-890
-993
—
—
-125
-855
-618
-916
-1178
-1176
-1491
-1628
-1810
525
IV. Термодинамика
Окончание табл.
Вещество
Состояние
дн
98,
кДж/моль
298'
ДжДКмоль)
кДж/моль
[ZrF4]
[ZrF5]-
[ZrF6]2-
[ZrF7],(NH4K
ZrH2
Zrl2
Zrl3
Zrl4
ZrN
ZrO2
ZrO, • 2H,0
Zr(OH)f
Zr(OH) +
[Zr(OHL]
ZrO(OHJ
ZrS2
[ZrSO4]2+
Zr(SO4J
Zr(SO4J • H2O
Zr(SO4J • 4H2O
[Zr(SO4J]
[Zr(SO4K]2"
ZrSiO4
P-P
P-P
P-P
куб.
куб.
ТВ.
ТВ.
газ
куб.
куб.
газ
монокл.
аморфн.
Р-Р
Р-Р
Р-Р
Р-Р
аморфн.
триг.
Р-Р
ТВ.
ТВ.
ромб.
Р-Р
Р-Р
тетр.
-3365
-163
-259
-397
-356
-485
-366
-295
-1101
-1721
-ИЗО
-1420
-569
-2244
-2576
-3769
-1990
+337
+35
+ 150
+205
+447
+257
+39
+274
+51
+ 130
-69
+92
+85
-1800
-2106
-2409
-2922
-123
-258
-395
-408
-481
-337
-304
-1043
-1548
-762
-997
-1232
-1465
-1305
-1290
-2049
-2800
-1876
A) [Bi6(OHI2]6+
B) [С16(Н2О)/я(ОН)„]<24-")+
C) [Сг(Н2ОL(ОНJ]
D) [GeO2(OHJ]2"
E) Н3О+ • ЗН2О
F) СО2 • Н2О + Н2СО3
G) [Hf4(H2OI6(OH)8]8+
(8) N2H4 • Н2О
(9) NH2OHH2O
A0) (NO2)NO3
A1) Ро2++ [РоС14]2-
A2) S2F2 + S(S)F2
A3) SO2«H2O
A4) [Sn3(OHL]2++[Sn4(OHN]2+
A5) [Sn(H2ON_n(OH),,]D-)+ + [Sn(OHN]2"
A6) [Zr4(H2OI6(OH)8]Cl8 • 12H2O
526
IV. Термодинамика
2. Энтальпия и энтропия фазовых переходов
Представлены термодинамические характеристики фазовых пере-
переходов в веществах: стандартная энтальпия (А1Г) и стандартная энтро-
энтропия (А5°) при указанных температурах (Г). Для большинства твердых
фаз указана конкретная кристаллографическая система (сингония).
Знаком «—» обозначено отсутствие данных. Список принятых
сокращений см. в разделе IV—1.
Вещество
Ас
Ag
AgBr
AgCN
AgCl
Agl
AgNOj
Ag2S
Ag2SO4
Ag2Se
Ag2Te
A]
AICI3
AIF3
-
Состояние
начальное
куб.
жидк.
куб.
жидк.
куб.
триг
куб.
жидк.
ос-куб.
гекс.
E-куб.
жидк.
ромб.
гекс.
монокл.
ромб.
куб.
ромб.
гекс.
ромб.
монокл.
куб.
жидк.
монокл.
триг.
триг.
триг.
ТВ.
конечное
жидк.
газ
жидк.
газ
жидк.
жидк.
жидк.
газ
гекс.
р-куб.
жидк.
газ
гекс.
жидк.
куб.
куб.
жидк.
гекс.
жидк.
куб.
куб.
жидк.
газ
триг.
газ
жидк.
ТВ.
газ
7;к
1323
3573
1235,08
2443
705
623
728
1823
409
420
827
1799
432,7
482,9
450
453
1118
700
933
406
410
933,52
2773
411
456
465,8
728
1552
ДАЛ
кДж/моль
14,31
293,00
11,95
254,30
9,16
11,72
12,89
182,84
—
6,15
9,41
143,93
2,55
11,55
4,23
—
14,06
7,95
16,74
6,74
0,69
10,92
290,78
—
111,71
35,56
0,63
322,17
AS0,
Дж/(К • моль)
9,71
—
9,67
104,35
13,05
—
17,70
—
—
14,56
11,34
—
5,90
23,85
9,33
—
12,59
11,72
16,74
16,61
1,67
11,72
—
—
—
76,40
0,88
—
527
IV. Термодинамика
, Вещество
[AlF6],Na3
A1N
А12О3
Am
Аг
As
AsH3
As2O3
At2
Au
В
BBr3
B4C
BC13
BF3
B2H6
B5H9
B3H6N3
BN
Состояние
начальное
монокл.
гекс.
гекс.
жидк.
гекс.
куб.
куб.
жидк.
гекс. (а)
куб.
жидк.
монокл.
монокл.
куб.
куб.
ромб.
куб.
жидк.
гекс.
жидк.
гекс.
жидк.
трип
жидк.
ромб.
ромб.
жидк.
монокл.
жидк.
жидк.
ТВ.
гекс. (а)
конечное
жидк.
жидк.
жидк.
газ
куб.
жидк.
жидк.
газ
газ
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
жидк.
газ
жидк.
газ
газ
газ
жидк.
газ
жидк.
газ
газ
жидк.
газ
газ
жидк.
жидк.
7;к
1300
2700
2326
>3273
>873
1565
83,8
87,4
888
156,23
210,68
587
587
551
551
517
1337,58
3220
2348
3973
3973
363,0
2623
285,7
144,79
144,79
172,9
107,7
180,7
333
216,76
3000
Продолжение табл.
ДАЛ
кДж/моль
115,65
67,78
117,15
485,34
—
1437,00
Ы7
6,51
31,80
2,34
17,49
18,41
48,12
24,89
54,60
23,85
12,36
335,05
22,13
519,90
563,80
30,54
104,60
23,85
2,09
23,85
17,99
4,44
14,43
32,22
10,61
75,31
AS°,
ДжДКмоль)
88,95
__
50,88
—
—
—
—
—
35,82
—
—
—
—
—
41,46
9,25
108,74
9,62
127,58
—
— .
—
—
—
—
—
—
—
—
528
IV. Термодинамика
Продолжение табл.
Вещество
в2о3
Ва
ВаСО3
ВаС12
BaF2
Ba(NO3J
BaO
Ва(ОНJ
Ва3(РО4J
BaSO4
Be
(ВеА12)О4
ВеС12
BeF2
Be3N2
BeO
Bi
Состояние
начальное
гекс.
жидк.
ос-куб.
р-куб.
жидк.
ромб.
гекс.
ромб.
куб.
жидк.
куб.
жидк.
куб.
куб.
куб.
ромб.
триг.
ромб.
куб.
гекс.
куб.
жидк.
ромб.
ос-ромб.
C-ромб.
жидк.
тетр.
куб.
куб.
гекс.
гекс.
тетр.
триг.
жидк.
конечное
жидк.
газ
Р-куб.
жидк.
газ
гекс.
куб.
куб.
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
жидк.
жидк.
куб.
жидк.
куб.
жидк.
газ
жидк.
Р-ромб.
жидк.
газ
куб.
жидк.
гекс.
жидк.
тетр.
жидк.
жидк.
газ
723
«2273
643
1000
«2133
1079
1241
1198
1234
«2323
1641
2533
867
1650
«2293
681
1878
1422
1853
1548
1560
2780
2143
676
688
823
403
1076
1673
2473
2373
2853
544,59
1837
кДж/моль
23,01
366,31
0,63
7,66
149,37
18,79
3,05
16,95
15,98
238,49
12,55
347,27
25,10
372,27
57,74
19,20
77,82
—
40,58
—
14,64
295,14
175,73
6,82
8,66
104,60
—
16,74
—
129,29
80,75
11,05
176,98
AST,
Дж/(К-моль)
31,84
—
0,96
7,82
—
17,41
2,47
14,14
12,93
—
7,95
—
29,29
—
26,28
27,82
—
—
25,10
9,41
107,11
—
—
—
—
—
15,56
—
—
—
31,25
20,29
97,07
529
IV. Термодинамика
Продолжение табпш
Вещество
BiCl3
Bi2O3
Bi2S3
Bi2Te3
Br2
BrF3
BrF5
С
CBr4
CC14
CF4
C2N2
CO
co2
cs2
C(S)O
Ca
Состояние
начальное
куб.
жидк.
монокл.
куб.
ромб.
триг.
ромб.
жидк.
ромб.
жидк.
жидк.
куб.(Р)
монокл.
куб.
жидк.
монокл.
куб.
жидк.
монокл.
куб.
жидк.
ТВ.
жидк.
куб.
гекс.
жидк.
куб.
тетр.
жидк.
триг.
жидк.
ос-куб.
р-куб.
жидк.
конечное
жидк.
газ
куб.
жидк.
жидк.
жидк.
жидк.
газ
жидк.
газ
газ
гекс. (а)
куб.
жидк.
газ
куб.
жидк.
газ
куб.
жидк.
газ
жидк.
газ
гекс.
жидк.
газ
газ
жидк.
газ
жидк.
газ
Р-куб.
ЖИДК;
газ
Т,К
505
714
1003
1098
958
858
265,90
332,97
282,0
398,90
313,91
2073
320,1
365,7
462,7
225,5
250,19
349,90
76,22
89,6
145
245,32
252,00
61,52
68,13
81,7
194,674
161,3
319,39
134,33
222,91
716
1115
1768
АН',
кДж/моль
23,47
72,59
—
28,45
79,37
86,61
10,57
29,54
12,03
42,68
30,59
1,88
6,28
4,10
43,51
4,56
2,51
30,00
1,46
0,70
12,59
8,11
23,33
0,63
0,84
6,04
25,23
4,39
26,78
4,73
18,49
1,13
8,66
152,26
AS"
Дж/(К • моль)
46,57
—
—
26,11
76,61
101,00
39,75
88,87
42,68
107,74
97,49
—
—
—
—
—
85,77
—
—
—
—
—
—
—
—
—
—
—
1,59
7,70
86,73
530
IV. Термодинамика
Продолжение табл.
Вещество
Са(ВО2J
СаС2
СаС12
CaF2
(CaFe2)O4
Ca(NO3J
CaO
Ca2P2O7
Ca3(PO4J
CaSO4
Ca2SiO4
(CaTi)O3
Cd
CdBr2
CdCl2
CdF2
Cdl2
Cd(NO3J ¦ 4H2O
CdO
CdS
Ce
CeCl3
CeF,
ci2
Состояние
начальное
ромб.
тетр.
ромб.
ромб.
куб.
тетр.
тетр.
куб.
куб.
тетр.
монокл.
триг.
ромб.
гекс.
монокл.
ТВ.
монокл.
гекс.
жидк.
гекс.
гекс.
триг.
жидк.
куб.
жидк.
гекс.
ромб.
куб.
гекс.
сс-куб.
р-куб.
гекс.
гекс.
тетр.
жидк.
конечное
жидк.
куб.
газ
жидк.
тетр.
жидк.
жидк.
жидк.
жидк.
монокл.
жидк.
монокл.
гекс.
жидк.
ТВ.
ромб.
ромб.
жидк.
газ
газ
жидк.
жидк.
газ
жидк.
газ
жидк.
жидк.
газ
газ
Р-куб.
жидк.
жидк.
жидк.
жидк.
газ
7;к
1435
723
934,6
1055
1423
1692
1493
834
2887
1413
1631
1423
1466
1723
970
1710
1530
594,26
1039,7
638
838
841,7
1237
1345
2026
661
332,5
«1173
958
1003
1077
1095
1703
172,12
239,1
АН",
кДж/моль
73,93
5,56
225,94
28,37
4,77
29,71
108,24
21,34
79,50
6,69
100,83
15,48
—
28,03
1,81
14,18
2,30
6,19
99,58
159,83
20,92
22,18
123,01
22,59
234,30
33,47
32,64
225,10
215,06
2,93
5,18
53,47
55,23
5,64
20,40
AST,
Дж/(К ¦ моль)
51,51
7,70
—
26,87
3,35
17,57
71,67
25,52
27,80
4,73
62,01
11,25
—
17,99
1,88
8,28
1,51
10,42
95,75
—
—
—
16,32
—
—
—
—
—
2,93
4,81
49,45
31,88
—
—
531
IV. Термодинамика
Продолжение табд.
Вещество
C12F6
Cm
Со
СоС12
Сг
СгС12
СгС12О2
Cs
CsCl
Cs2Cr207
CsF
CsNO3
CsOH
Cu
CuCl
CuO
Cu2O
Cu2S
Состояние
начальное
жидк.
гекс.
гекс.
куб.
жидк.
трип
жидк.
куб.
жидк.
ромб.
ромб.
жидк.
куб.
куб.
жидк.
а-куб.
р-куб.
жидк.
ТВ.
куб.
гекс.
куб.
ТВ.
куб.
жидк.
куб.
гекс.
монокл.
куб.
ромб.
гекс.
куб.
конечное
газ
жидк.
куб.
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
газ
газ
жидк.
газ
газ
C-куб.
жидк.
газ
жидк.
жидк.
куб.
жидк.
жидк.
жидк.
газ
гекс.
жидк.
жидк.
жидк.
гекс.
куб.
жидк.
Т,К
284,91
1618
700
1767
3233
1013
1322
2163
2953
1097
1097
390
301,9
301,9
940,8
742,5
918
1575
657
976
427
687
619
1357,7
2813
681
703
1720
1513
376
623
1403
АНТ,
кДж/моль
55,06
14,64
0,45
16,19
376,55
30,96
113,80
16,93
344,31
32,22
251,46
35,15
2,18
78,74
68,28
2,43
20,75
149,33
17,00
10,25
—
13,60
6,74
13,05
304,36
—
10,96
55,65
64,22
3,85
0,84
23,01
AS°,
Дж/(К ¦ моль)
193,30
—
0,63
9,16
117,65
30,96
—
7,95
116,90
—
—
—
7,20
—
—
3,31
22,59
—
—
—
—
—
9,62
—
15,61
32,34
42,38
10,25
1,26
16,32
532
IV. Термодинамика
Продолжение табл.
Вещество
Cu2Se
D2
D2O
Dy
Dy2O3
Er
Eu
Eu2O3
F2
Fe
Fe3C
[Fe(C5H5J]
[Fe(COM]
FeCl2
FeCl3
Состояние
начальное
ос-куб.
гекс.
гекс.
гекс.
жидк.
гекс.
куб.
жидк.
а-куб.
гекс.
жидк.
куб.
жидк.
а-монокл.
монокл.
куб.
жидк.
а-куб.
р-куб.
Y-Куб.
8-куб.
жидк.
ромб.
ТВ.
жидк.
монокл.
жидк.
триг.
жидк.
триг.
триг.
жидк.
конечное
р-куб.
жидк.
жидк.
газ
газ
куб.
жидк.
газ
р-куб.
жидк.
газ
жидк.
газ
р-монокл.
куб.
жидк.
газ
Р-куб.
у-куб.
8-куб.
жидк.
газ
ТВ.
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
газ
газ
7;к
383
18,7
276,963
276,963
276,963
1657
1682
2860
1590
1795
3130
1099
1713
895
45,55
53,451
89,9
1042
1185
1667
1812
«3473
463
451,25
519
253
376
947
1296
580,7
580,7
589
АН0,
кДж/моль
4,85
0,20
6,31
52,77
46,46
4,16
11,06
230,09
0,92
19,90
261,35
9,21
143,50
0,54
0,73
0,51
6,54
1,36
0,90
0,69
15,36
349,59
0,75
64,64
49,79
13,60
37,24
43,01
124,81
43,10
69,04
25,19
AST,
Дж/(К ¦ моль)
12,68
—
22,78
190,54
167,78
2,51
6,57
81,17
0,59
11,09
83,35
8,45
76,73
0,59
—
—
1,34
0,76
0,41
8,49
111,50
1,63
128,45
96,02
—
—
45,69
—
32,84
—
—
533
IV. Термодинамика
Продолжение тайпЛ
Вещество
FeF2
(FenFe2]I)O4
(Fe2Ni»)O4
Fe095O
FeS
Fe2Si04
Fr
Ga
Gd
Ge
GeCl4
GeH4
Gel4
GeO2
H2
HBr
HCN
HD
HF
Состояние
начальное
тетр.
жидк.
куб.
куб.
куб.
а-гекс.
Р-гекс.
куб.
ромб.
куб.
ромб.
тетр.
жидк.
гекс.
куб.
жидк.
куб.
жидк.
жидк.
ТВ.
жидк.
ТВ.
ТВ.
жидк.
тетр. (а)
триг. (р)
гекс.
жидк.
куб.
жидк.
жидк.
гекс.
жидк.
конечное
жидк.
газ
жидк.
ТВ.
жидк.
р-гекс.
куб.
жидк.
жидк.
жидк.
тетр.
жидк.
газ
куб.
жидк.
газ
жидк.
газ
газ
жидк.
газ
газ
жидк.
газ
триг. (Р)
жидк.
жидк.
газ
жидк.
газ
газ
жидк.
газ
7;к
1375
2110
1811
855
1641
411
598
1468
1490
294
275,6
302,93
2676
1535
1585
3545
1210
«3123
356,3
107,4
184,7
298
419
621
1306
1389
13,96
20,28
186,24
206,38
298,80
16,7
292,67
кДж/моль
51,88
224,43
138,07
0,86
31,34
2,38
0,50
32,34
92,17
2,07
2,13
5,59
257,15
3,91
10,05
359,38
36,94
330,91
33,05
0,84
14,06
84,4
14,94
69,5
35,56
43,93
0,12
0,90
2,41
17,61
25,22
0,16
7,49
А С°
До ,
Дж/(К • моль)
—
—
—
1,00
19,00
5,82
0,84
22,01
61,84
6,90
—
18,45
102,05
2,55
6,36
101,55
30,54
106,52
—
—
—
172,4
52,8
120,0
27,20
—
—
—
—
—
84,39
—
25,61
534
IV. Термодинамика
Продолжение табл.
Вещество
HI
HN3
HNO3
н2о
Н2О2
Н(РН2О2)
Н2(РНО3)
Н3РО4
Н4Р2О7
H2S
H2(S2)
H2SO4
H2SO4 • H2O
H2S2O7
H2Se
H2Se04
H2Se04 • H2O
H2Te
He
Hf
Hg
Состояние
начальное
тетр.
жидк.
жидк.
монокл.
гекс.
гекс.
гекс.
жидк.
жидк.
тетр.
ТВ.
ромб.
монокл.
ТВ.
куб.
жидк.
ТВ.
жидк.
монокл.
монокл.
ТВ.
куб.
жидк.
ромб.
ТВ.
ТВ.
жидк.
гекс.
жидк.
гекс.
куб.
жидк.
триг.
жидк.
конечное
жидк.
газ
газ
жидк.
жидк.
жидк.
газ
газ
газ
жидк.
жидк.
жидк.
жидк.
жидк.
жидк.
газ
жидк.
газ.
жидк.
жидк.
жидк.
жидк.
газ
жидк.
жидк.
жидк.
газ
жидк.
газ
куб.
жидк.
газ
жидк.
газ
7;к
222,3
237,8
308,9
231,6
273,15
273,16
273,16
273,16
373,15
272,72
299,7
347
315,50
334
187,61
212,80
183,6
343,9
283,6
281,63
308,37
207,43
231,7
335,6
299
222
271,4
2,0
4,22
2013
2503
«4893
234,288
629,81
ДАЛ
кДж/моль
2,87
19,77
29,71
10,47
6,01
6,01
51,48
45,05
40,66
10,54
9,71
12,84
12,97
9,20
2,38
18,67
7,53
35,15
10,71
19,37
13,35
2,51
19,33
14,43
19,87
4,18
23,22
0,008
0,081
6,74
24,06
575,14
2,33
59,30
AST,
Дж/(Кмоль)
—
—
—
45,23
22,00
22,00
186,91
164,92
108,95
—
—
41,13
—
—
—
—
—
37,78
—
—
—
—
__
—
—
3,35
9,62
117,95
—
94,15
535
IV. Термодинамика
Продолжение табд.
Вещество
HgBr2
HgCl2
Hgl2
HgS
Но
h
IC1
IF5
In
InBr
InBr3
InCl
InCl3
[IninCl4],In
Inl
Ir
IrF6
К
KA1(SO4J •
• 12H2O
KBO2
K2B4O7
Состояние
начальное
тетр.
ромб.
ТВ.
жидк.
тетр.(а)
ромб, (р)
жидк.
трип (а)
гекс.
куб.
жидк.
ромб.
жидк.
монокл.
монокл.
монокл.
тетр.
жидк.
жидк.
ТВ.
жидк.
монокл.
жидк.
жидк.
куб.
жидк.
жидк.
куб.
жидк.
куб.
триг.
ТВ.
конечное
газ
ТВ.
жидк.
газ
ромб. (Р)
жидк.
газ
куб.(р)
куб.
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
жидк.
газ
газ
газ
газ
газ
газ
газ
жидк.
газ
газ
жидк.
газ
жидк.
жидк.
жидк.
т,к
«663
428
553
575,0
404
529
627
617
1701
1743
2980
386,7
457,50
300,34
300,34
282,571
429,78
2297
935
644
926
771
928
1016
2716
4653
326,8
336,7
1033
365
1213
1088
АН°,
кДж/моль
75,48
—
19,41
58,91
2,72
18,83
59,66
4,18
4,69
12,18
240,98
15,77
41,80
11,13
41,55
15,90
3,26
231,84
92,05
105,02
89,96
158,99
192,46
90,79
26,36
612,20
35,98
2,33
80,16
28,03
23,85
104,18
AS0,
ДжДКмоль)
—
—
—
6,74
35,98
—
6,28
2,76
6,99
81,21
40,79
91,13
37,07
—
56,07
7,61
98,95
—
—
—
—
—
—
9,66
131,34
—
6,90
—
—
19,66
536
IV. Термодинамика
Продолжение табл.
Вещество
КВг
KCN
к2со3
КС1
ксю4
К2Сг04
К2Сг207
KF
K(HFJ
KHSO4
KMgCl3
KNCS
KNO3
КОН
K2SO4
Кг
La
Состояние
начальное
куб.
жидк.
куб.
жидк.
монокл.
гекс.
куб.
жидк.
ромб.
ромб.
гекс.
трикл.
монокл.
куб.
жидк.
тетр.
куб.
сс-ромб.
р-ромб.
ТВ.
ромб.
тетр.
ромб.
триг.
ромб.
куб.
жидк.
ромб.
гекс.
куб.
жидк.
гекс.
сс-куб.
р-куб.
конечное
жидк.
газ
жидк.
газ
гекс.
жидк.
жидк.
газ
куб.
гекс.
жидк.
монокл.
жидк.
жидк.
газ
куб.
жидк.
р-ромб.
монокл.
жидк.
тетр.
жидк.
триг.
жидк.
куб.
жидк.
газ
гекс.
жидк.
жидк.
газ
а-куб.
Р-куб.
жидк.
Т, К
1007
1653
907,7
1898
701
1164
1043
1703
574
939
1241,5
530
670,7
ИЗО
1778
469,8
511,9
442
634,2
760
414,6
446,4
402
607,7
517
677
1597
857
1347
115,78
119,93
583
1141
1193
ДАЛ
кДж/моль
29,29
155,23
14,64
157,11
—
27,61
25,52
120,08
13,77
10,25
28,87
—
35,61
28,24
172,80
11,18
6,62
2,05
0,40
53,09
0,13
10,46
5,86
11,72
6,34
9,37
133,89
8,95
37,91
1,64
9,03
0,37
3,56
31,13
AST,
Дж/(К • моль)
—
—
—
—
—
23,60
24,47
—
—
—
—
—
53,05
24,99
—
—
—
—
—
69,87
—
—
14,60
19,16
—
10,46
28,24
—
—
0,63
3,14
4,52
537
IV. Термодинамика
Продолжение табл.
Вещество
Li
LiBO2
Li2B4O7
LiBr
Li2CO3
LiCl
LiF
LiH
Lil
LiNO3
(LiNb)O3
Li2O
LiOH
Li2SO4
Li2Si03
Li4SiO4
Lu
Lul3
Mg
MgBr2
MgCl2
MgCl2 • 6H2O
MgF2
Состояние
начальное
куб.
жидк.
монокл.
тетр.
куб.
жидк.
монокл.
куб.
жидк.
куб.
жидк.
куб.
жидк.
триг.
триг.
куб.
тетр.
жидк.
монокл.
гекс.
куб.
ромб.
монокл.
гекс.
жидк.
гекс.
гекс.
жидк.
триг.
триг.
жидк.
монокл.
тетр.
жидк.
конечное
жидк.
газ
жидк.
жидк.
жидк.
газ
жидк.
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
жидк.
жидк.
жидк.
газ
гекс.
куб.
жидк.
жидк.
жидк.
жидк.
газ
жидк.
жидк.
газ
жидк.
жидк.
газ
жидк.
жидк.
газ
7;к
453,7
1609,8
1122
1191
825
1583
891
883
1653
1118,3
1949,0
953
1443
526,2
1526
1726
744
1198
773
848
1132
1475
1498
1936
3685
1313
921
1368
983
987
1643
390
1563
«2543
АН°,
кДж/моль
3,00
14,31
33,85
120,50
12,13
148,11
44,77
19,54
150,62
27,07
213,38
29,29
170,71
25,61
70,88
58,58
20,96
167,78
—
28,45
12,55
30,12
30,96
19,25
355,91
108,0
8,95
127,40
34,73
43,10
156,23
34,31
58,12
271,96
AS°,
ДжДКмоль)
6,61
—
30,67
—
—
44,81
22,13
—
24,14
30,50
—
48,79
46,02
—
—
—
—
—
—
—
20,08
9,62
97,03
—
9,71
93,47
—
43,68
—
—
37,87
538
IV. Термодинамика
Продолжение табл.
Вещество
(MgFe2)O4
Mg(NO3J ¦ 6H2O
MgO
Mg2P2O7
Mg3(PO4J
MgSO4
Mg2Si
Mg2Si04
Mn
Mn3C
MnCl2
(МпиМп^и)О4
MnS
MnSiO3
Mn2Si04
Mo
MoCl5
MoF6
MoO3
N2
Состояние
начальное
а-куб.
монокл.
куб.
жидк.
монокл.
монокл.
ромб.
куб.
ромб.
а-куб.
Р-куб.
у-куб.
8-куб.
жидк.
ромб.
триг.
жидк.
тетр.
а-куб.
гекс.
р-куб.
трикл.
ромб.
куб.
жидк.
монокл.
жидк.
ромб.
куб.
ромб.
ромб.
жидк.
куб.
гекс.
жидк.
конечное
р-куб.
жидк.
жидк.
газ
жидк.
жидк.
жидк.
жидк.
жидк.
р-куб.
у-куб.
8-куб.
жидк.
газ
гекс.
жидк.
газ
куб.
р-куб.
р-куб.
жидк.
жидк.
жидк.
жидк.
газ
жидк.
газ
куб.
жидк.
газ
жидк.
газ
гекс.
жидк.
газ
Т,К
1230
363,1
3098
3873
1668
1630
1410
1358
2163
980
1360
1411
1518
2324
1583
923
1504
1433
573
593
1888
1596
1600
2897
4983
467
541
263,5
290,73
973
1068
1428
35,61
63,2
77,348
A LJ°
А/г,
кДж/моль
1,46
41,00
77,40
474,47
134,37
120,67
14,64
64,14
86,19
2,23
2,12
1,88
12,06
226,07
12,97
37,53
120,50
20,79
—
—
26,11
40,17
89,62
39,10
592,79
7,53
58,16
—
4,33
271,96
48,91
138,07
0,23
0,72
5,58
Дж/(К • моль)
1,17
—
24,27
_
76,44
74,22
10,46
—
—
2,26
1,55
1,34
7,95
97,48
40,67
—
14,39
—
_
14,48
25,73
55,35
9,62
116,79
—
—
—
14,88
—
45,52
—
—
—
—
539
IV. Термодинамика
Продолжение табл.
Вещество
NH3
N2H4
NH4CI
N2H5C1
NH4NO3
NO
N2O
N2O4
(NO)C1
(NO2)NO3
Na
NaA102
NaBO2
Na2B4O7
NaBr
NaCN
Na2CO3
NaCl
NaC103
NaF
NaFeO2
Состояние
начальное
куб.
жидк.
монокл.
жидк.
а-куб
куб.
ромб.
а-куб.
р-куб.
тетр.
монокл.
жидк.
куб.
жидк.
куб.
жидк.
жидк.
гекс.
куб.
жидк.
гекс.
триг.
трикл.
куб.
жидк.
куб.
жидк.
монокл.
гёкс.
куб.
жидк.
куб.
куб.
жидк.
триг.
тетр.
конечное
жидк.
газ
жидк.
газ
р-куб.
жидк.
а-куб.
р-куб.
тетр.
жидк.
жидк.
газ
жидк.
газ
жидк.
газ
газ
ra3(N2O5)
жидк.
газ
ТВ.
жидк.
жидк.
жидк.
газ
жидк.
газ
гекс.
жидк.
жидк.
газ
жидк.
жидк.
газ
тетр.
жидк.
7;к
195,40
239,8
274,6
386,7
457,6
362
305,5
357,6
398,6
442,8
109,6
121,5
182,3
184,6
262,0
293,9
267,8
305
370,98
1159
740
1238
1014
1028
1663
836,9
1770
753
1124
1074,0
1738
535
1270
1973
1270
1623
ДАЛ
кДж/моль
5,65
23,35
12,66
40,58
4,18
15,23
1,59
1,34
4,23
5,44
2,30
13,78
6,54
16,55
14,65
38,12
25,10
56,90
2,60
86,37
1,30
36,23
81,17
25,52
161,92
8,79
148,07
0,69
29,71
28,66
170,71
22,59
33,14
209,20
2,18
49,20
AST,
Дж/(К-моль)
—
—
—
—
—
—
5,19
3,77
10,63
12,26
—
—
—
—
—
—
—
—
6,99
—
1,76
—
—
—
—
—
—
26,44
26,74
—
42,80
26,44
—
1,72
30,38
540
IV. Термодинамика
Продолжение табл.
Вещество
Nal
Na2MoO4
NaNCS
NaNO3
Na2O
Na2O2
NaOH
Na2S
Na2SO4
Na2(SO3S) • 5H2O
Na2SiO3
Na2Si2O5
Na2WO4
Nb
NbCl5
NbF5
Состояние
начальное
куб.
жидк.
куб.
а-ромб.
Р-ромб.
у-ромб.
ромб.
триг.
ТВ.
а-куб.
Р-куб.
у-куб.
гекс.
ромб.
монокл.
куб.
жидк.
куб.
а-ромб.
Р-ромб.
гекс.
монокл.
ромб.
монокл.
ромб.
куб.
ромб.
куб.
жидк.
монокл.
ТВ.
ТВ.
жидк.
монокл.
жидк.
конечное
жидк.
газ
а-ромб.
Р-ромб.
у-ромб.
жидк.
жидк.
ТВ.
жидк.
р-куб.
у-куб.
жидк.
тетр.
монокл.
куб.
жидк.
газ
жидк.
р-ромб.
гекс.
жидк.
жидк.
жидк.
ромб.
жидк.
ромб.
жидк.
жидк.
газ
ТВ.
жидк.
газ
газ
жидк.
газ
т,к
934
1577
723
858
908
960
580,7
549
579,7
1023
1243
1405
783
516
572,8
594
1663
1453
458
514
1157
321,7
1362
983
1147
861,4
971
2743
5200
456
477,9
477,9
520,7
352,7
507,7
АН°,
кДж/моль
21,76
159,83
61,09
—
—
15,08
18,41
3,39
14,60
—
' 41,84
5,36
—
6,36
6,36
158,57
6,69
—
7,49
23,72
23,43
52,17
_
35,56
35,15
23,85
26,38
718,22
—
35,56
85,35
52,72
12,22
46,44
AST,
Дж/(К-моль)
—
—
—
—
—
—
—
6,15
25,10
—
—
—
37,66
—
11,25
10,75
—
—
—
14,56
20,54
—
38,37
—
30,96
—
—
9,62
135,94
—
—
—
—
34,85
—
541
IV. Термодинамика
Продолжение табдш
Вещество
Nb2O5
Nd
Nd2O3
Ne
Ni
NiCl2
Ni3S2
Np
O2
O3
Os
OsO4
P (краен.)
P4 (бел.)
PBr3
PBr5
РВГ3О
PCI3
Состояние
начальное
монокл.
гекс.
куб.
жидк.
гекс.
куб.
куб.
жидк.
куб.
жидк.
триг.
триг.
триг.
ТВ.
ромб.
ромб.
гекс.
куб.
жидк.
жидк.
гекс.
жидк.
монокл.
жидк.
аморфн.
куб.
жидк.
жидк.
жидк.
жидк.
ТВ.
жидк.
конечное
жидк.
куб.
жидк.
газ
куб.
жидк.
газ
газ
жидк.
газ
жидк.
газ
ТВ.
жидк.
жидк.
гекс.
куб.
жидк.
газ
газ
жидк.
газ
жидк.
газ
газ
жидк.
газ
газ
газ
газ
жидк.
газ
1773
1128
1297
«3353
1395
24,6
24,6
27,102
1728
«3173
1282
1243
823
1081
910
23,90
43,76
54,45
90,188
161,25
3300
«5273
313,8
404,4
689
317,29
530
446,5
379
466
183,1
348,5
АН0,
кДж/моль
102,88
3,03
7Д4
273,04
0,59
0,34
1,80
1,84
17,47
370,38
77,28
202,34
—
24,27
5,61
0,09
0,74
0,44
6,82
10,84
31,76
750,00
14,27
39,75
29,83
2,63
52,22
38,83
54,39
37,99
7,20
30,46
AS0,
ДжДКмоль)
57,66
2,68
5,52
81,71
0,42
—
—
—
10,13
116,19
59,33
—
23,01
—
—
—
—
—
—
9,62
—
—
—
42,51
6,79
98,52
—
—
—
39,3
542
IV. Термодинамика
Продолжение табл.
Вещество
РС15
РС13О
РН3
РА
РАо
Ра
РЬ
РЬВг2
РЬС12
Pb(Cl)F
PbF2
Pbl2
PbO
PbS
PbSO4
Pd
Состояние
начальное
тетр.
ТВ.
жидк.
куб.
жидк.
жидк.
ромб.
ромб.
триг.
триг.
тетр.
куб.
жидк.
куб.
жидк.
ромб.
жидк.
ромб.
жидк.
тетр.
ромб.
куб.
жидк.
триг.
жидк.
тетр. (а)
ромб, (р)
жидк.
куб.
ромб.
монокл.
куб.
жидк.
конечное
газ
жидк.
газ
жидк.
газ
газ
газ
жидк.
жидк.
газ
куб.
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
куб.
жидк.
газ
жидк.
газ
ромб. (Р)
жидк.
газ
жидк.
монокл.
жидк.
жидк.
газ
т,к
453
277,40
379,0
139,4
185,73
448,6
632
695
853
853
1443
1853
«4773
600,85
2018
646
1166
774
1223
879
720
1097
1566
675
1227
761
1159
1808
1350
1139
1443
1827
3213
АН°,
кДж/моль
67,36
13,01
34,35
1ДЗ
14,60
37,66
73,64
20,92
48,12
70,29
14,64
552,00
4,80
177,70
20,92
115,90
23,85
112,17
36,74
2,47
11,92
167,36
21,76
103,76
0,75
29,29
207,23
17,57
16,99
40,17
17,57
332,00
AS",
Дж/(К • моль)
—
—
—
—
—
116,69
—
—
—
—
9,79
—
7,99
87,82
—
31,59
41,80
2,93
10,88
—
—
—
25,27
—
12,55
14,90
29,71
9,62
109,91
543
IV. Термодинамика
Продолжение тайл^
Вещество
Рт
Ро
Рг
РГбОп
Pt
Pu
PuCl3
PuF3
PuF4
PuF6
Ra
Rb
RbBr
RbCl
RbF
Rbl
Состояние
начальное
гекс.
жидк.
куб.
триг.
жидк.
гекс.
куб.
жидк.
ос-куб.
куб.
жидк.
ос-монокл.
Р-монокл.
ромб.
а-куб.
р-куб.
тетр.
жидк.
гекс.
гекс.
монокл.
ТВ.
куб.
жидк.
куб.
куб.
жидк.
куб.
жидк.
куб.
жидк.
куб.
жидк.
куб.
конечное
жидк.
газ
триг.
жидк.
газ
куб.
жидк.
газ
(J-куб.
жидк.
газ
Р-монокл.
ромб.
а-куб.
р-куб.
тетр.
жидк.
газ
жидк.
жидк.
жидк.
жидк.
жидк.
газ
жидк.
газ
газ
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
т,к
1443
«3273
327
527
1235
1069
1204
3783
760
2045
«4073
395
480
588
730
745
913
«3623
1033
1699
1310
324,74
1242
1809
312,5
312,5
969
966
1625
991
1668
1071
1703
929
кДж/моль
12,55
330,00
—
12,55
72,80
3,17
6,89
296,78
9,54
19,66
509,74
3,36
0,64
0,52
0,08
1,86
2,90
343,67
63,60
54,39
42,68
18,64
9,41
162,00
2,26
85,65
75,77
15,48
155,31
18,41
154,47
22,97
165,31
12,51
AST,
Дж/(К • моль)
9,67
—
—
23,81
—
2,97
5,69
78,41
12,55
9,62
124,43
8,57
1,33
0,90
0,11
2,47
3,18
98,11
61,50
32,01
32,58
57,41
9,67
—
7,24
—
—
—
—
—
—
21,09
—
544
IV. Термодинамика
Продолжение табл.
Вещество
RbNO3
RbOH
Re
ReF6
Re2O7
Rh
Rn
Ru
S
s8
S2C12
SC12O
SC12O2
SF6
so2
so3
Sb
Состояние
начальное
жидк.
триг.
куб.
а-ромб.
Р-ромб.
ромб.
гекс.
жидк.
ромб.
куб.
жидк.
ромб.
жидк.
куб.
жидк.
куб.
жидк.
гекс.
жидк.
жидк.
ромб, (а)
монокл.(Р)
жидк.
жидк.
жидк.
ТВ.
ромб.
жидк.
ромб.
жидк.
триг.
куб.
жидк.
конечное
газ
куб.
а-ромб.
Р-ромб.
жидк.
жидк.
жидк.
газ
куб.
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
газ
газ
монокл.(Р)
жидк.
газ
газ
газ
жидк.
жидк.
газ
жидк.
газ
куб.
жидк.
газ
7;к
1600
437
493
564
586
655
3463
«6173
269,7
291,8
306,9
574,7
631,7
2236
«3973
202,2
211,3
2880
«5173
, 717,82
368,7
392,5
411
348,8
342,7
223
197,69
263,1
290,0
317,9
686
903,89
1907
АН",
кДж/моль
150,46
—
—
—
5,61
6,78
33,05
744,00
—
20,92
28,87
64,02
75,73
21,55
496,06
2,90
16,40
25,98
591,49
9,20
3,21
13,74
35,98
31,80
28,03
5,02
7,40
24,92
5,61
40,79
—
19,62
124,39
AS*,
Дж/(Кмоль)
—
—
—
—
—
—
9,62
—
—
—
—
9,62
123,85
—
—
9,62
134,68
12,84
8,70
35,38
87,86
91,21
82,01
—
—
—
19,33
128,32
—
21,71
65,23
545
8-2004
IV. Термодинамика
Продолжение таблщ
Вещество
SbBr3
SbCl3
SbCl5
Sb2O3
Sb2S3
Sb2Se3
Sc
Se
SeCl2O
SeF6
SeO2
Si
SiBr4
SiCl4
SiF4
SiH4
SiO2
кварц
кристобалит
тридимит
Состояние
начальное
ромб.
ромб.
жидк.
гекс.
жидк.
ромб, (а)
куб. (р)
ромб.
ромб.
гекс.
куб.
жидк.
триг.
жидк.
ТВ.
жидк.
ТВ.
жидк.
тетр.
куб.
жидк.
жидк.
куб.
жидк.
куб.
куб.
ТВ.
жидк.
жидк.
триг. (а)
гекс. (р)
тетр. (а)
куб. (р)
ромб, (а)
конечное
жидк.
жидк.
газ
жидк.
газ
куб.( Р)
жидк.
жидк.
жидк.
куб.
жидк.
газ
жидк.
газ
жидк.
газ
газ
газ
газ
жидк.
газ
газ
жидк.
газ
газ
жидк.
жидк.
газ
газ
гекс. (р)
жидк.
куб.(р)
жидк.
гекс. (р)
7;к
369,8
345,5
494
276,0
413
733
928
823,7
890
1609
1814
= 3123
490
958,5
284,0
450,8
226,6
238,4
588
1688
= 3523
425,8
239,21
330,8
177,5
182,9
88
161,3
3223
846
1823
515
2001
390
АН",
кДж/моль
14,69
12,68
45,19
10,04
48,12
6,78
61,71
23,43
54,27
4,01
14,10
314,19
6,69
29,29
4,18
42,68
26,23
18,33
91,21
50,55
355,00
38,07
9,03
29,29
25,73
7,07
0,67
12,13
516,72
1,21
8,54
0,84
7,70
0,17
AST,
Дж/(К • моль)
—
—
—
—
—
8,03
66,48
28,58
61,09
2,51
7,78
101,21
13,56
30,54
14,64
94,56
—
—
149,37
30,00
—
—
—
88,70
—
—
—
—
—
1,42
4,52
1,59
3,85
0,42
546
IV. Термодинамика
Продолжение табл.
. Вещество
Sm
Sm2O3
Sn
SnBr2
SnBr4
SnGl2
SnCl4
Snl2
Snl4
SnO2
SnS
Sr
SrBr2
SrCO3
SrCl2
SrF2
SrO
Sr(OHJ
Та
TaBr5
^
. Состояние
начальное
триг.
куб.
жидк.
куб.
куб.
тетр.
жидк.
ромб.
жидк.
монокл.
ромб.
жидк.
ромб.
жидк.
куб.
жидк.
жидк.
куб.
жидк.
тетр.
ромб.
ТВ.
ос-куб.
р-куб.
жидк.
ромб.
ромб.
куб.
куб.
куб.
тетр.
куб.
жидк.
монокл.
жидк.
конечное
куб.
жидк.
газ
монокл.
тетр.
жидк.
газ
жидк.
газ
ромб.
жидк.
газ
жидк.
газ
жидк.
газ
газ
жидк.
газ
ТВ.
ТВ.
жидк.
Р-куб.
жидк.
газ
жидк.
триг.
жидк.
жидк.
жидк.
жидк.
жидк.
газ
жидк.
газ
>
1190
1345
= 2073
1148
286,4
505,12
2893
505
911
288,5
303
475
520
925
240
387,3
991
417,7
619,0
698
875
1153
878
1041
1663
930
1198
1146
1746
2923
733
3283
5698
539,0
622,0
АН-,
кДж/моль
3,11
8,62
166,41
1,05
2,09
6,99
296,10
7,11
92,05
—
12,55
41,84
12,55
87,86
9,16
34,73
100,42
18,74
56,90
1,88
0,67
31,59
0,84
10,04
141,42
20,08
19,66
16,11
17,99
69,87
22,97
31,28
770,19
44,77
61,07
AS", :
Дж/(К ¦ моль)
2,64
6,40
80,63
0,88
7,36
13,85
102,26
—
—
—
—
—
—
—
—
—
—
—
—
—
0,79
27,41
0,96
9,62
—
—
16,44
14,06
10,88
25,59
28,45
9,62
136,61
—
—
547
18-
IV. Термодинамика
Продолжение табл.
Вещество
ТаС15
TaF5
Tb
Тс
Те
ТеС14
TeF6
ТеО2
Th
ThBr4
Thl4
Ti
TiB2
TiBr4
TiCl4
(TiFe")O3
Til4
Состояние
начальное
монокл.
жидк.
жидк.
гекс.
куб.
жидк.
гекс.
жидк.
трип
жидк.
монокл.
жидк.
ТВ.
ТВ.
ромб.
ос-куб.
Р-куб.
жидк.
жидк.
жидк.
гекс.
куб.
жидк.
гекс.
монокл.
куб.
жидк.
монокл.
жидк.
триг.
гекс.
куб.
жидк.
конечное
жидк.
газ
газ
куб.
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
газ
газ
жидк.
жидк.
р-куб.
жидк.
газ
газ
газ
куб.
жидк.
газ
жидк.
куб.
жидк.
газ
жидк.
газ
жидк.
куб.
жидк.
газ
7;к
489,7
512
502,7
1563
1629
3346
2523
«4573
723,0
1263
497
653
234,3
235,6
1006
1636
2023
«4473
ИЗО
1110
1155
1941
3533
3123
258
311
504
249,05
409,6
1640
379
428
652,7
АН0,
кДж/моль
46,44
54,81
27,61
5,02
10,79
330,89
23,01
650,00
17,49
51,04
18,83
76,99
27,07
8,79
29,06
2,74
16,12
514,46
127,19
120,50
4,26
17,15
421,03
100,42
—
12,89
44,35
9,97
35,98
90,67
9,22
19,83
53,56
AS°,
Дж/(К • моль)
—
—
68,62
3,22
6,65
94,64
9,58
—
24,18
40,42
37,87
—
—
51,51
1,67
7,95
101,67
—
3,68
8,79
118,20
—
—
—
—
55,27
—
—
-
548
IV. Термодинамика
Продолжение табл.
Вещество
TiN
ТЮ
ГЮ2
П2О3
Tl
TIBr
T1C1
T1F
Til
TINO3
T12O
T12S
T12SO4
Tm
и
UBr3
Состояние
начальное
куб.
монокл.
куб.
жидк.
тетр.(у)
монокл.
триг.
гекс.
куб.
жидк.
куб.
жидк.
куб.
жидк.
ромб.
тетр.
ромб.
куб.
жидк.
ромб.
гекс.
куб.
гекс.
триг.
ромб.
гекс.
гекс.
жидк.
ромб.
тетр.
куб.
жидк.
гекс.
гекс.
конечное
жидк.
куб.
жидк.
газ
жидк.
триг.
жидк.
куб.
жидк.
газ
жидк.
газ
жидк.
газ
тетр.
жидк.
куб.
жидк.
газ
гекс.
куб.
жидк.
жидк.
жидк.
гекс.
жидк.
жидк.
газ
тетр.
куб.
жидк.
газ
жидк.
газ
т;к
«3273
1264
2053
3500
2143
433
2103
507
576,8
1748
734
1089
704
1091
355
595
451
715
1106
348
416,7
479,7
576
722,1
773
905
1818
2220
941
1048
1407
4473
1003
1003
A L/°
AIT,
кДж/моль
66,94
3,43
58,58
425,09
66,94
0,90
129,70
0,38
4,08
165,23
15,62
102,93
15,56
103,76
0,38
13,87
—
11,30
104,18
1,00
3,18
9,58
30,29
12,55
—
23,01
16,84
190,67
2,79
4,76
8,52
464,07
46,02
287,02
Дж/(К • моль)
—
2,72
—
—
—
1,88
—
0,75
7,07
93,68
—
—
22,13
—
1,09
23,30
—
—
—
3,01
7,61
—
35,56
—
—
—
9,29
85,90
2,97
4,56
6,07
105,31
—
—
549
IV. Термодинамика
Продолжение табл.
Вещество
UBr4
UC13
UC14
UF4
UF6
V
VC14
VC13O
vo2
V2O5
w
wcis
wci6
WC14O
WF6
wo3
Xe
Состояние
начальное
монокл.
жидк.
гекс.
тетр.
куб.
монокл.
ТВ.
жидк.
ромб.
ромб.
куб.
жидк:
жидк.
жидк.
монокл.
тетр.
ромб.
куб.
жидк.
монокл.
жидк.
гекс.
куб.
жидк.
тетр.
куб.
жидк.
трикл.
монокл.
ромб.
тетр.
куб.
жидк.
конечное
газ
газ
газ
куб.
газ
ТВ.
жидк.
газ
жидк.
газ
жидк.
газ
газ
газ
тетр.
жидк.
жидк.
жидк.
газ
жидк.
газ
куб.
жидк.
газ
жидк.
жидк.
газ
монокл.
ромб.
тетр.
жидк.
жидк.
газ
792
1038
1108
820
863
1118
1309
2003
337
337
2193
3723
426
399,9
340
1913
963
3660
«5953
521
560
500,8
548
620
484
275,2
290,5
291
603
1013
1746
161,30
165,03
АН°,
«Дж/моль
175,31
129,70
263,59
—
193,72
—
42,84
240,58
19,20
49,37
20,93
451,89
37,66
34,73
4,29
56,92
65,10
35,15
823,91
20,92
61,50
14,23
10,88
55,65
7,53
2,09
26,15
—
—
1,72
73,43
0,55
3,02
AS",
Дж/(К • моль)
—
—
—
—
—
—
32,22
—
56,94
—
9,62
122,72
88,70
—
12,43
31,32
69,04
9,62
141,38
—
—
—
—
—
—
7,53
—
—
—
1,63
42,09
—
—
550
IV. Термодинамика
Окончание табл.
Вещество
Y
Yb
Zn
ZnBr2
ZnCl2
ZnF2
Znl2
ZnS
Zr
ZrB2
ZrBr4
ZrCl2
ZrCl4
ZrF4
Zrl4
ZrN
ZrO2
Состояние
начальное
гекс.
куб.
жидк.
а-куб.
Р-куб.
жидк.
гекс.
жидк.
тетр.
тетр.
жидк.
жидк.
тетр.
куб. (а)
гекс.
куб.
жидк.
гекс.
куб.
аморфн.
монокл.
монокл.
тетр.
монокл.
куб.
куб.
монокл.
тетр.
жидк.
конечное
куб.
жидк.
газ
E-куб.
жидк.
газ
жидк.
газ
газ
жидк.
газ
газ
газ
гекс. (р)
куб.
жидк.
газ
жидк.
газ
жидк.
газ
жидк.
монокл.
жидк.
газ
жидк.
тетр.
жидк.
газ
1755
1801
3595
1033
1097
1484
692,7
1179,4
542
566
1006
1775
518
1293
1136
2128
«4613
3473
630
995
604
710
963
1183
691
3253
1448
2973
«4573
ДАЛ
кДж/моль
4,99
11,40
363,34
1,75
7,66
128,87
7,38
115,56
125,94
10,25
129,29
180,33
115,48
13,39
3,94
20,92
582,04
104,60
107,95
26,78
105,86
37,66
—
64,22
121,34
67,36
5,94
87,03
624,25
AS0,
Дж/(К ¦ моль)
2,85
6,32
100,63
1,67
6,99
87,82
10,67
97,61
—
17,41
—
—
—
10,33
3,47
10,04
124,31
—
—
—
—
—
53,30
—
—
4,02
29,50
—
Вещества
в водном растворе
1. Электродные потенциалы
окислительно-восстановительных пар
Электрохимическая полуреакция восстановления некоторой окис-
окисленной формы (атома, молекулы, иона, формульной единицы):
Окисл. форма (Оф) + пе~ = Восст. форма (Вф)
<р° характеризуется значением стандартного потенциала ф° пары Оф/Вф,
измеренным по отношению к стандартному водородному электроду
(рН = 0, давление Н2(г) равно нормальному атмосферному давлению).
Среда водного раствора, если она участвует в полуреакции (и, сле-
следовательно, к ней относится значение ф°), указана обозначениями:
а) кисл. — кислотная среда, либо ионы Н+
Оф + Ш+ + пе~ = Вф
либо кислотная пара Н+/Н2О
Оф + Ш+ + пе~ = Вф + тН2О
б) щел. — щелочная среда, либо ионы ОН"
Оф + пе~ = Вф + ?ОН-
либо щелочная пара ОН~~/Н2О
Оф + wH2O + пе~ = Вф + ?ОН-
в) нейтр. — нейтральная среда, молекулы Н2О
Оф + тН2О + пе~ = Вф
Прочерк в таблице означает кислотную среду, которая не входит
в уравнение полуреакции восстановления.
Все Оф и Вф, находящиеся в водном растворе, считаются гидрати-
рованными. Нейтральные частицы в растворе отмечены нижним ин-
индексом (р) — водный раствор; агрегатное состояние жидких (ж) и га-
газообразных (г) веществ указано, а для твердых веществ опущено.
Кислоты (кислородсодержащие, бескислородные) и их гидроани-
гидроанионы помещены в конец рубрики соответствующего кислотообразую-
кислотообразующего элемента.
552
V. Вещества в водном растворе
Окисленная
форма
Ас3+
Ag+
Ag"
Ag
(Ag'Ag111^
AgBr
AgBЮз
Ag(CH3COO)
AgCN
[Ag(CNJ]~
[Ag(CNK]2-
Ag2CO3
Ag2C2O4
AgCl
Ag2CrO4
Agl
AgIO3
AgN3
AgNCS
[Ag(NH3J]+
AgNO2
Ag2O
Ag2O3
AgOCN
[Ag(OHJ]-
Ag2S (монокл.)
[Ag(SO3J]3~
Ag2SO4
[Ag(SO3SJ]3-
Al3+
[A1F6]3-
+ ne~
3
1
1
1
2
1
1
1
1
1
1
2
2
1
2
1
1
1
1
1
1
2
2
1
1
2
1
2
1
3
3
Восстановленная
форма
Ac
Ag
Ag+
Ag11
Ag2O
Ag + Br-
Ag + ВЮз
Ag + CH3COO-
Ag + CN"
Ag + 2CN"
Ag + 3CN"
2Ag + C02f
2Ag + C202f
Ag + Cl"
2Ag + CrO^~
Ag + Г
Ag +10 3
Ag + N^
Ag + NCS"
Ag + 2NH3(r)
Ag + 2(NH3-H2O)(p)
Ag + NO2
2Ag
(Ag1AgIII)O2
Ag + OCN-
Ag
2Ag + S2"
2Ag + HS"
2Ag + H2S(p)
2Ag + H2S(r)
Ag + 2S0|"
2Ag + S0^"
Ag + 2SO3S2"
Al
A1 + 6F-
Ф°, В
-2,600
+0,799
+1,980
+2,100
+0,599
+0,071
+0,558
+0,640
-0,040
-40,430
-0,510
+0,471
+0,465
+0,222
+0,477
-0,151
+0,355
+0,293
+0,090
+0,164
+0,367
+0,564
+0,342
+0,740
+0,410
+0,563
-0,655
-0,687
-0,066
^-0,037
+0,430
+0,653
+0,004
-1,700
-2,112
Среда
—
—
—
—
щел.
—
—
—
—
—
—
—
—
—
—
—
—
нейтр.
—
щел.
щел.
—
щел.
—
щел.
кисл.
кисл.
—
—
—
—
—
553
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
А10Н2+
А1(ОН)?
А1(ОНK
А1(ОНK (аморфн.)
[А1@НL]-
ос-АЮ(ОН)
у-А1О(ОН)
Am3+
Am™
AmO2
AmO^+
Am(OHK
As
AsO2
AsO^"
AsO\~
As2S3
AsS^
AsS^"
HAsO2(p)
H3As03(p)
H3As04(p)
2At+
At2
+ ne~
3
3
3
3
3
3
3
3
1
2
1
1
3
3
3
3
2
6
3
2
3
3
2
2
2
: Восстановленная
форма
Al
Al
Al
Al
Al
Al
Al
Am
Am3+
Am34"
Am™
AmOj
Am
AsH3(p)
AsH3(r)
As
As
AsO2
AsO^~
2As + 3S2"
2As + 3HS"
2As + 3H2S(p)
2As + 3H2S(r)
As + 3S2"
AsS^ + S2"
As
As
HAsO2(p)
H3AsO3(p)
At2
2At"
f.B
-1,601
-1,496
-1,538
-2,366
-1,538
-2,316
-2,336
-1,544
-1,516
-2,320
+2,250
+ 1,720
+ 1,150
+ 1,640
-2,700
-1,370
-0,238
-1,066
-0,680
-1,572
-0,710
-0,658
-0,609
-0,641
-0,020
+0,009
-0,750
-0,600
+0,234
+0,226
+0,560
+0,586
+0,700
+0,200
Среда
кисл.
кисл.
кисл.
щел.
кисл.
щел.
щел.
кисл.
кисл.
—
—
кисл.
кисл.
щел. '
щел.
кисл.
щел.
щел.
щел.
щел.
щел.
—
щел.
кисл.
кисл.
—
—
кисл.
кисл.
кисл.
кисл.
—
—
554
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
2АЮ-
АЮз
Аи+
Аи1»
[АиВг2]"
[АиВг4]"
[Au(CNJ]-
AuCl
[АиСу
[АиС14]"
[АиС13(ОН)]-
[Au(NCSJ]"
[Au(NCSL]"
Аи2О3
[Аи(ОНL]"
АиО(ОН)
[BFJ-
В(ОНK
[В(ОНL]"
Ва2+
ВаО2
Ве2+
[BeF4]2~
Ве(ОНJ
+ пе~
2
4
1
3
1
2
1
1
1
3
2
3
1
2
6
4
3
3
3
3
3
8
2
2
2
2
2
Восстановленная
форма
At2
At+
AtO"
Аи
Аи
Аи + 2Вг~
[АиВг2]~ + 2Вг
Аи + 2CN"
Аи + С1-
Аи + га-
Аи + 4С1-
АиС1 + ЗС1-
[Auci2]- + га-
Аи + за-
AU + 2NCS"
[Au(NCSJ]- + 2NCS"
2Аи
Аи2О?
Аи
Аи
В(аморфн.) + 4F"
B + 4F-
В(аморфн.)
В
В(аморфн.)
В
[bhj-
Ва
Ba(Hg)EK)
2Н2О + Ва2+
Be
Be + 4HF(p)
Be
Ф°, В.
±0,000
+ 1,400
+0,500
+ 1,691
+1,498
+0,960
+0,800
-0,764
+1,157
+ 1,154
+1,002
+0,924
+0,926
+1,123
+0,690
+0,645
+0,535
+1,640
+0,490
+1,253
+0,622
-1,295
-1,283
-0,900
-0,888
-1,822
-1,810
-1,240
-2,905
-1,570
+2,369
-1,847
-2,042
-2,599
Среда
щел.
КИСЛ.
щел.
—
—
—
—
—
—
—
—
КИСЛ.
—
—
щел.
КИСЛ.
щел.
КИСЛ.
щел.
—
—
КИСЛ.
КИСЛ.
щел.
щел.
щел.
—
—
КИСЛ.
—
КИСЛ.
щел.
555
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
[Ве(ОНL]2"
Biin
[BiClJ-
Bi(Cl)O
Bi(OHK
[Bi6(OHI2]6+
BiO(OH)
Bi2S3
Bk4+
ВГ2(Р)
Вг2(ж)
[Br(BrJ]-
2ВЮ-
BrOj
2BrOj
BrO3
ВгО^
2HBrO(p)
CH3C(H)O(p)
CH3COOH(p)
C2N2(r)
co(r)
co2(r)
2CO2(r)
co2(r)
+ ne~
2
3
3
3
3
18
3
6
1
2
2
2
2
6
10
4
2
2
2
2
2
6
2
2
2
Восстановленная
форма
Be
Bi
Bi + 4C1-
Bi + Cl-
Bi
6Bi
Bi
2Bi + 3S2"
2Bi + 3HS~
2Bi + 3H2S(p)
2Bi + 3H2S(r)
Bk3+
2Br-
2Br"
3Br-
ВГ2(Р)
Br-
Br2
BrO-
HBrO(p)
BrO3
ВГ2(Р)
Вг2(ж)
с2н5он(р)
CH3C(H)O(p)
2CN"
2HCN(p)
CH4(r)
co(r)
H2C2O4(p)
HCOOH(p)
Ф°, В
-2,520
+0,317
+0,168
+0,158
-0,383
+0,215
-0,460
-0,709
-0,741
-0,120
-0,091
+1,600
+1,087
+1,065
+ 1,050
0,434
+1,440
+0,612
+ 1,511
+0,517
+0,538
+ 1,495
+ 1,763
+0,935
+ 1,574
+ 1,595
+0,190
-0,118
-0,236
+0,241
+0,260
-0,104
-0,470
-0,199
Среда
щел.
—
—
кисл.
щел.
кисл.
щел.
—
щел.
кисл.
кисл.
—
—
—
щел.
кисл.
щел.
кисл.
щел.
щел.
кисл.
кисл.
щел.
кисл.
кисл.
кисл.
кисл.
—
кисл.
кисл.
кисл.
кисл.
кисл.
556
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
2C02f
со\-
2НСОз
2Н2СО3(Р)
2HCOj + N2(r)
Са2+
СаО2
Са(ОНJ
Cd2+
[Cd(CNL]2"
[Cd(NH3L]2+
CdOH+
Cd(OHJ
CdS
Ce3+
Ce3+
Ce™
CeO2
Cfiv
C12(p)
C12(r,
cio-
2C1O-
C1O2
C1°2(p)
ao2(r)
+ ne~
2
2
2
2
2
10
2
2
2
2
2
2
2
2
2
3
3
1
1
1
1
2
2
2
2
2
1
1
Восстановленная
форма
со(г)
c2or
нсоо-
ед-
Н2С2О4(р)
2CN"
Са
2Н2О + Са2+
Са
Cd
Cd(Hg)(x)
Cd + 4CN"
Cd + 4(NH3H2O)(p)
Cd
Cd
Cd + S2-
Cd + HS~
Cd + H2S(p)
Cd + H2S(r)
Ce
Се(Нё)(ж)
Ce3+
Ce3+
2C1-
2C1-
2C1-
C12(r)
cio-
C1O2
C1O2
HClO2(p)
Ф°, В
-1,223
-1,210
-1,015
-0,993
-0,386
+0,925
-2,864
+2,222
-3,018
-0,404
-0,352
-1,028
-0,597
-0,178
-0,825
-1,208
-1,239
-0,619
-0,589
-2,483
-1,437
+1,743
+1,293
-1,600
+3,200
+ 1,396
+ 1,358
+0,920
+0,482
+0,681
+0,954
+ 1,032
+1,270
Среда
щел.
щел.
щел.
щел.
кисл.
щел.
—
кисл.
щел.
—
—
—
нейтр.
кисл.
щел.
—
щел.
кисл.
кисл.
—
—
кисл.
—
—
—
—
щел.
щел.
щел.
—
—
кисл.
557
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
2С1О3
С1О3
С1О3
СЮ4
НСЮ(р)
2НС1О(р)
нсю2(р)
Ст4+
Со2+
Со3+
[Co(CNN]3"
(СопСо^)О4
[Co(NH3N]2+
[Co(NH3N]3+
Со(ОНJ
ЗСоО(ОН)
СоО(ОН)
CoS
Сг2+ .
Сг3*
[Cr(CNN]3"
CrCl^
CrO^-
+ ле~
10
2
1
2
8
2
2
2
2
1
2
1
1
2
2
1
2
1
1
2
2
1
1
1
3
Восстановленная
форма
СЮ2
СЮад
нсю2(р)
С1-
С1О3
С1-
С1г(г)
НС1О(р)
Ст3+
Со
Со2+
[Co(CNM]3- + CN"
ЗСо(ОНJ
ЗСо(ОНJ (аморфн.)
Co + 6(NH3H2O)(p)
[Co(NH3N]2+
Со
[СопСо^]О4
Со(ОНJ
Со + S2-
Со + HS-
Co + H2S(p)
Со + H2S(r)
Сг
Сг2+
[Cr(CNN]4"
Сг2+ + 2С1-
Сг(ОНK
[Сг(ОНN]3"
ф°, В
+ 1,470
+0,476
+0,268
+ 1,160
-0,496
+ 1,215
+ 1,386
+0,558
+ 1,189
+0,361
+ 1,494
+ 1,630
+1,645
+3,500
-0,277
+ 1,380
-0,830
-0,160
-0,220
-0,411
+0,178
-0,739
+0,887
+0,189
-0,882
-0,914
-0,294
-0,264
-0,852
-0,409
-1,280
-0,403
-0,125
-0,165
Среда
кисл.
щел.
щел.
кисл.
щел.
кисл.
кисл.
щел.
кисл.
щел.
кисл.
кисл.
кисл.
—
—
—
—
щел.
щел.
нейтр.
—
щел.
щел.
щел.
—
щел.
кисл.
кисл.
—
—
—
—
щел.
щел.
558
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
Сг2О2~
СгОН2+
Сг(ОНJ
Сг(ОН)^
Сг(ОНK
[Сг(ОНN]3-
НСЮ4
Cs+
Cu+
Cu2+
Cu2+ + Br
Cu2+ + 2CN"
Cu2+ + Cl-
Cu2+ + 2C1-
Cu2 +1-
Cu2 + 21-
2Cu2+
[Cu(CNJ]~
CuCl
[CuCl2]-
Cul
[CuI2]~
CuNCS
[Cu(NH3J]+
[Cu(NH3L]2+
2CuO
Cu2O
CuOH+
Cu(OHJ
+ ne~
6
3
2
3
1
1
3
1
1
2
2
1
1
1
1
1
1
1
2
1
1
1
1
1
1
1
2
2
2
2
2
Восстановленная
форма
2Сг3+
Cr
Сг
Сг
Сг(ОНJ
Сг(ОНJ
Cr3*
Cs
Си
Си
Си(Нё)(ж)
Си+
СиВг
[Cu(CNJ]-
CuCl
[СиС12]"
Cul
[Cul2]"
Си2О
си + ген-
Си + ci-
Си + 2С1"
Си + Г
Си + 21"
Си + NCS"
Си + 2NH3(r)
Cu + 2(NH3H2O)(p)
Си + 4NH3(r)
Cu + 4(NH3H2O)(p)
Си2О
2Cu
Си
Си
Ф°, В
+1,333
-0,626
-1,355
-0,516
-1,175
-1,057
+1,363
-2,923
+0,518
+0,338
+0,345
+0,158
+0,657
+ 1,105
+0,551
+0,486
+0,860
+0,690
+0,214
-0,429
+0,124
+0,190
-0,184
±0,000
-0,270
+0,030
-0,120
-0,232
-0,065
+0,669
-0,159
+0,462
-0,366
+0,555
-0,226
Среда
КИСЛ.
кисл.
щел.
кисл.
щел.
щел.
кисл.
—
—
—
—
—
—
—
—
—
—
кисл.
—
—
—
—
—
—
—
нейтр.
—
нейтр.
кисл.
щел.
кисл.
щел.
кисл.
щел.
559
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
2Си(ОНJ
[Си(ОНL]2"
CuS
Cu2S
2D+
2D2O
Dy3+
Dy(OHK
Er3+
Er(OHK
Es3+
Eu2+
Eu3+
Eu(OHK
F(D
F2(r)
Fe2+
Fe3+
Fe3+ + HS"
[Fe(CNN]4"
[Fe(CNN]3"
+ ne~
2
2
2
2
2
2
3
3
3
3
1
2
3
1
3
1
2
2
3
1
1
2
1
Восстановленная
. .c, форма
Cu2O
Cu
Cu + S2-
Cu + HS-
Cu + H2S(p)
Cu + H2S(r)
2Cu + S2"
2Cu + HS"
2Cu + H2S(p)
2Cu + H2S(r)
D2(D
D2(r) + 2OD"
Dy
Dy
Er
Er
Es2+
Eu
Eu
Eu2+
Eu
F"
HF
2F~
2HF
HF2
Fe
Fe
Fe2+
FeS
Fe + 6CN-
[Fe(CNN]4"
Ф°,В
-0,086
-0,132
-0,722
-0,754
-0,133
-0,104
-0,891
-0,923
-0,302
-0,273
-0,044
-0,870
-2,356
-2,780
-2,296
-2,830
-1,500
-3,395
-2,406
-0,550
-2,830
+2,850
+3,030
+2,866
+3,090
+3,013
-0,441
-0,037
+0,771
+ 1,809
-1,728
+0,543
Среда
щел.
щел.
—
щел.
кисл.
кисл.
—
щел.
кисл.
кисл.
—
—
щел.
—
щел.
—
—
—
—
щел.
—
кисл.
—
кисл.
кисл.
—
—
—
щел.
—
—
560
V. Вещества в водном растворе
., Окисленная
форма
[Fe(C2O4K]3-
[FeF6]3"
(FenFe^)O4
FeO|"
FeO^"
Fe2O3
FeOH+
FeOH2+
Fe(OHJ
Fe(OH)^
[Fe(OHN]4"
FeO(OH)
FeS
Fm3+
Ga3+
GaOH2+
Ga(OH)^
Ga(OHK
[Ga(OHL]"
Gd3+
Gd(OHK
Ge2 + ?
GeO
GeO2 (триг.)
[Ge(OHN]2"
H2GeO3(p)
%
H+
+ ne~
1
1
8
3
3
2
2
3
2
3
2
1
2
1
3
3
3
3
3
3
3
2
2
4
2
2
4
4
2
1
1
Восстановленная
форма
[Fe(C2O4J]2- + C2O2-
Fe2+ + 6F"
3Fe
Fe3+
FeO(OH)
2Fe(OHJ
Fe
Fe
Fe
Fe
Fe
Fe(OHJ
Fe + S2"
Fe + HS"
Fm2+
Ga
Ga
Ga
Ga
Ga
Gd
Gd
Ge
Ge
Ge
Ge2 + ?
GeO
Ge
Ge
Ge2 + ?
H-
H(r)
Продолжение табл.
Ф°, В,
+0,020
+0,400
-0,086
-0,914
+ 1,900
+0,720
-0,794
-0,279
-0,019
-0,875
+0,072
-0,762
-0,666
-0,965
-0,997
-1,000
-0,560
-0,505
-0,435
-1,258
-1,326
-2,397
-2,822
-0,240
+0,156
-0,069
+0,052
-0,293
-0,972
-0,129
-0,068
-2,230
-2,107
Среда
—
—
кисл.
щел.
кисл.
щел.
щел.
кисл.
кисл.
щел.
кисл.
щел.
щел.
щел.
—
—
кисл.
кисл.
щел.
щел.
—
щел.
—
кисл.
кисл.
кисл.
кисл.
щел.
кисл.
кисл.
—
—-
561
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
2Н+
2Н+ (рН = 7)
Н2(г) + Са2+
2Н2(Г) + Li+ + А13+
Н2О
2Н2О
Hfiv
ню2
Hf(OH)f
НЮ(ОНJ
Hg2+
Hgf
2Hg2+
[HgBr4]2"
Hg2Br2
[Hg(CNL]2~
Hg2CO3
2HgCl2
[HgCl4]2-
Hg2Cl2
[Hgl4]2"
Hg2I2
HgO
2HgO
2HgO + CO2,-
HgS (куб.)
2HgS (куб.)
Hg2SO4
+ ne~
2
2
2
4
1
2
4
4
4
4
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
Восстановленная
форма
Н2(г)
Н2(г)
СаН2
П[А1Н4]
Н(г)
Н2(г)
Hf
Hf
Hf
Hf
Hg»
2НЕ(Ж)
Hgf
Hgw + 4Br
2Hg()K) + 2Br"
Hg()K) + 4CN-
2НЕ(Ж) + СО2"
Hg2Cl2 + 2C1-
Нё(ж) + 4С1-
2НЕ(Ж) + 2С1"
Hg^ + 41"
2Нё(ж) + 21-
Hg(»
Hgr
Hg2CO3
Hg(x) + S2~
HgEK) + HS-
Hg(x) + H2S(p)
Hgw + H2S(rK
Hgr + 2S2"
Hgr + 2HS"
Hg2+ + 2H2S(p)
Hg2+ + 2H2S(r)
2Hg(x) + SO2-
<pe, В
±0,000
-0,414
-2,157
-1,896
-2,935
-0,828
-1,474
-1,570
-1,680
-2,600
+0,852
+0,796
+0,908
+0,223
+0,142
-0,370
+0,306
+0,657
+0,438
+0,268
-0,038
-0,041
+0,099
-0,599
-0,109
-0,692
-0,724
+0,103
+0,073
-2,199
-2,262
-1,021
-0,962
+0,615
Среда
—
—
—
—
щел.
щел.
—
кисл.
кисл.
щел.
—
—
—
—
—
—
—
—
—
—
—
щел.
щел.
щел.
—
щел.
кисл.
кисл.
¦—
щел.
кисл.
кисл.
—
562
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
Но3+
Но(ОНK
h
2[I(BrJ]-
[I(IJ]~
ю-
210-
IOJ
210 7
IOj
Ю4
ню(р)
2HI0^
H3IOg
H5%)
In3+
InOH2+
In(OH)}
In@HK
In2S3
Ir3*
[IrBr6]2"
[IrCle]3-
[IrCl6]2-
[IrI6]2~
1Ю2
Ir2O3
K+
La3+
U@HK
+ ne~
3
3
2
2
2
2
2
6
10
4
2
2
2
2
2
3
3
3
3
6
3
1
3
1
1
1
6
1
3
3
Восстановленная
форма
Но
Но
21-
I2 + 4Вг"
31"
I-
h
I-
I2
НЮ(р)
ю-
10 з
I-
h
107
IOJ
In
In
In
In
2In+3H2S(p)
2In + 3H2S(r)
Ir
[IrBr6]3-
Ir+6C1-
[IrCl6]3"
[Irl6]3"
Ir3+
2Ir
К
La
La + 30H-
Ф°, В
-2,319
-2,770
+0,535
+0,870
+0,534
+0,484
+0,433
+ 1,081
+0,253
+1,190
+0,196
+1,128
+0,137
+1,653
+0,987
+1,439
+0,700
+ 1,601
-0,338
-0,268
-0,184
-1,066
-0,568
-0,539
+ 1,000
+0,947
+0,720
+ 1,017
+0,480
+0,720
+0,098
-2,924
-2,522
-2,760
Среда
—
щел.
—
—
—
щел.
щел.
кисл.
щел.
кисл.
щел.
кисл.
щел.
кисл.
кисл.
кисл.
щел.
кисл.
кисл.
кисл.
щел.
кисл.
кисл.
—
—
—
—
—
кисл.
щел.
—
—
-
563
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
Li+
Lu3+
Lu(OHK
Md3+
Mg2+
MgOH+
Mg(OHJ
Mn2+
Mn3+
[Mn(GNN]3"
(MnnMn^)O4
MnO2
3MnO2
2MnO2
MnO2
MnO^"
МПО4
Mn2O3
MnOH+
Mn(OHJ
MnO(OH)
MnS
+ ne~
1
3
3
1
2
2
2
2
1
1
2
2
4
2
2
1
2
7
5
3
1
5
2
2
2
1
2
Восстановленная
форма
Li
Lu
Lu
Md2+
Mg
Mg
Mg
Mn
Mn2+
[Mn(CNN]4"
3Mn(OHJ
Mn2+
(MnnMn2n)O4
Mn2O3
Mn(OHJ
MnO(OH)
MnO2
Mn
Mn2+
MnO2
MnO^"
Mn(OHJ
2Mn(OHJ
Mn
Mn
Mn(OHJ
Mn + S2"
Mn + HS"
Mn + H2S(p)
Mn + H2S(r)
Ф°, В
-3,045
-2,255
-2,720
-0,150
-2,370
-2,023
-2,689
-1,192
+1,499
-0,244
-0,324
+1,239
+0,098
+0,139
-0,043
-0,260
+2,308
+0,605
+0,753
-0,194
+1,531
+ 1,725
+0,621
+0,558
+0,355
-0,225
-0,878
-1,566
+0,174
-1,575
-1,607
-0,986
-0,956
Среда
—
—
щел.
—
—
кисл.
щел.
—
—
—
щел.
кисл.
щел.
щел.
щел.
щел.
кисл.
щел.
кисл.
щел.
кисл.
кисл.
щел.
—
щел.
щел.
кисл.
щел.
щел.
—
щел.
кисл.
кисл.
564
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
Мо3+
[Mo(CN)8]3-
[Mo(CNO]4-
МоО2
МоО3
МоО3 • 2Н2О
МоО|-
3N2(r)
N2(r,
2NCO-
2NHJ
N2H+
NH3OH+
2NH3OH+
NH2OH • H2O(p)
2(NH2OH • H2O)(p)
N2H4 • H2O
2NO(r)
2NO2
NO2
2NO2
NO2(r)
+ ne~
3
1
1
4
2
6
6
2
2
6
4
6
4
2
2
2
2
2
2
2
2
2
2
6
1
4
2
1
Восстановленная
форма
Mo
[Mo(CN)8]4~
[Mo(CNO]5"
Mo
MoO2
Mo
Mo
MoO2
2HN3(p)
2NH3(r)
2NHJ ,
N2HJ
2(NH3H2O)(p)
N2H4H2O(p)
2NH3OH+
2(NH2OH • H2O)(p)
^2^2(Г)
H2(r) + 2(NH3H2O)(p)
2NH^
NHJ
N2H^
NH3 H2O(p)
N2H4-H2OW
2(NH3 • H2O)(p)
N2O(r)
N2O1-
N2(r)
NO(r)
N2O(r)
N2Or
NO(r)
HNO2(p)
NO2
Ф'.В
-0,200
+0,726
+0,730
-0,983
+0,537
±0,000
-0,913
-0,772
-3,100
-0,771
+0,272 ,
-0,227
-0,737
-1,119
-1,871
-3,043
-1,750
-0,547
+1,270
+1,334
+1,417
+0,416
+0,805
+0,027
+1,600
+0,722
+0,100
+0,410
-0,453
+0,160
-0,177
+1,046
+1,088
+0,889
Среда
—
—
щел.
кисл.
кисл.
щел.
щел.
кисл.
щел.
кисл.
кисл.
щел.
щел.
кисл.
щел.
щел.
нейтр.
кисл.
кисл.
кисл.
щел.
щел.
щел.
кисл.
щел.
— <;
щел.
щел.
щел.
щел.
кисл.
кисл.
—
565
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма:
2NO3
NOj
2NO3
NO3
2NO3
NO3
2NOj
N2O(r)
N2°4«
HN3(P)
2HNC0(p)
2HNO2
HNO2(p)
2HNO2(p)
H2N2O2(p)
Na+
NaBiO3
Na2O2
Nbv
+ пё
10
2
8
14
8
14
6
3
2
1
8
2
2
8
2
4
2
8
2
4
6
1
4
2
1
2
2
5
, г: Восстановленная
форма
N2(D
HNO2(p)
NH3(r)
NHJ
N2H5
NH3H2O(p)
N2H4H2O(p)
NH3OH+
NH2OH ¦ H2O(p)
NO(r)
NO2
NO2(r)
N2O(r)
N2O4(X)
N2(r)
2NHJ
2HNO2(p)
2NO
2NO2
NH}
C2N2(r)
H2N2O2
N2(D
NO(r)
N2O(r)
Na
Bi111 + Na+
Bi(OHK + Na+
2H2O + 2Na+
4OH- + 2Na+
Nb
<P,B
+1,244
+0,250
+0,930
-0,133
+0,880
+0,824
-0,120
-0,141
+0,725
-0,299
+0,955
+0,010
+0,772
-0,884
+1,116
+0,810
-0,846
+ 1,756
+0,644
+1,051
+1,028
+0,866
+0,660
-0,285
+0,855
+1,453
+ 1,004
+1,302
+2,650
-2,711
+1,808
+0,370
+2,860
+ 1,204
-0,522
Среда
кисл.
щел.
кисл.
щел.
кисл.
кисл.
щел.
щел.
кисл.
щел.
кисл.
щел.
кисл.
щел.
кисл.
кисл.
щел.
кисл.
кисл.
кисл.
кисл.
—
кисл.
кисл.
кисл.
кисл.
кисл.
кисл.
кисл.
—
кисл.
щел.
кисл.
нейтр.
—
566
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
№Оз
Nb2O5
Nd3+
Nd(OHK
Ni2+
[Ni(NH3N]2+
NiOH+
Ni(OHJ
NiO(OH)
NiS
No3+
Np3+
Np4+
NpOj
NpO^
Np(OHK
Np(OHL
NpO2(OH)
NpO2(OHJ
°(D
O(r) + 2H+(pH = 7)
°(D
oi
°2<r)
+ ne~
5
10
3
3
2
2
2
2
1
2
i
3
]
i
i
;
]
]
]
2
2
2
1
2
4
2
1
4
Восстановленная
форма
Nb
2Nb
Nd
Nd
Ni
Ni + 6(NH3H2O)(p)
Ni
Ni
Ni2+
Ni(OHJ
Ni + S2"
Ni + HS"
Ni + H2S(p)
Ni + H2S(r)
No2+
Np
Np3+
Np4+
NpOj
Np
Np(OHK
Np(OHL
NpO2(OH)
H2O
H2O
OH-
HO2
HOj
2H2O
H2O + O(r)
H2O2(p)
O2
2OH-
ф°, В
-0,480
-1,474
-0,599
-2,431
-2,540
-0,234
-0,490
4-0,089
-0,749
+2,252
+0,784
-0,856
-0,888
-0,268
-0,238
+1,400
-1,856
+0,155
+0,739
+1,130
-2,248
-1,756
+0,391
+0,482
+2,430
+0,815
+ 1,602
+0,408
-0,076
+1,229
+0,028
+0,694
-0,560
+0,401
Среда
кисл.
щел.
кисл.
—
щел.
—
нейтр.
кисл.
щел.
кисл.
щел.
—
щел.
кисл.
кисл.
—
—
—
—
—
щел.
щел.
щел.
щел.
кисл.
—
щел.
щел.
щел.
кисл.
кисл.
кисл.
—
щел.
567
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
°3(г)
0F2(D
ОН(Р)
НО2
Н02(р)
Н2°2(р)
[OsBr6]2-
[OsCl6]3-
[OsCy2"
OsO4(p)
OsO4 (монокл.)
OsO4(p) + 6C1-
OsO4
Os(OHL
[OsO2(OHL]2"
[OsO4(OHJ]2-
P (аморфн.)
P4
4(PHO3J^
(PHO3J-
(PH2O2)"
4(PH2O2)-
4PO3,-
?o\-
H(PH2O2)(p)
+ ne~
6
2
6
2
4
1
2
1
1
2
1
3
1
8
8
4
4
4
2
8
2
3
12
12
2
1
4
20
2
4
1
Восстановленная
форма
3H2O
H2O + O2(r)
зон-
он- + о2(г)
H2O + 2F~
OH- + 2F"
Н2О
он-
2ОН-
он(р)
НгО2(Р)
2Н2О
[OsBr6]3"
Os + 6С1-
[OsCl,]3-
Os
Os
[OsCy2-
Os(OHL
Os
Os(OHL
Os
[OsO2(OHL]2-
PH3(r)
4PH3(r)
P4
(PH2O2)-
P (аморфн.)
P4
P4
(PHO3J-
(PH2O2)"
P (аморфн.)
Ф°,В
+1,511
+2,075
+0,683
+ 1,247
+2,176
+1,762
+2,814
+ 1,985
+0,878
-0,240
+1,500
+ 1,764
+0,349
+0,597
+0,449
+0,780
+0,838
+0,010
+ 1,000
+0,170
-0,150
+0,100
+0,025
+0,300
-0,915
-0,046
-0,874
—]
1,650
1,565
1,697
1,820
1,510
1,300
1,432
-0,387
Среда
кисл.
кисл.
щел.
щел.
кисл.
щел.
кисл.
—
щел.
щел.
кисл.
кисл.
_
—
—
кисл.
кисл.
щел.
кисл.
щел.
щел.
щел.
щел.
щел.
щел.
кисл.
щел.
щел.
щел.
щел.
щел.
щел.
щел.
щел.
кисл.
568
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
4Н(РН2О2)(р)
Н^РНОз)^
4Н2(РНО3)(Р)
Н2(РНО3)(Р)
НРО2~
4НРО|"
Н2РО4
4Н2РО4
НзРО4(р)
4Н3РО4(р)
НзРО4(р)
Pav
Pb2+
PbBr2
РЬС12
PbF2
Pbl2
PbO2
PbO2 + SO|-
PbOH+
Pb(OHJ
[Pb(OHK]-
[Pb(OHN]2-
(Pb'1PbIV)O4
+ ne~
4
3
12
2
5
20
5
20
5
20
4
2
5
1
2
2
2
2
2
2
2
2
2
2
2
2
Восстановленная
форма
P4
P (аморфн.)
p4
H(PH2O2)(p)
P (аморфн.)
p4
P (аморфн.)
p4
P (аморфн.)
H(PH2O2)
H2(PHO3)(p)
Pa
Pa4+
Pb
Pb(Hg)(>K)
Pb + 2Br-
РЬ(Нё)(ж) + 2Вг-
Pb + 2C1-
рь(нё)(ж) + га-
гарь + 2F-
Pb(Hg)()K) + 2F-
Pb + 21-
РЬ(НЕ)(ж) + 21"
Pb2+
Pb(OHJ
[Pb(OHK]"
PbSO4
Pb
Pb
Pb
[Pb(OH)J-
3Pb2+
3Pb(OHJ
3[Pb(OHK]"
Ф°,В-
-0,510
-0,454
-0,495
-0,488
-1,447
-1,475
-0,358
-0,377
-0,383
-0,408
-0,382
-0,276
-1,000
-0,100
-0,126
-0,121
-0,277
-0,275
-0,267
-0,262
-0,350
-0,344
-0,379
-0,358
+1,455
+0,386
+0,210
+ 1,685
+0,056
-0,714
-0,538
+0,305
+2,156
+0,587
+0,076
Среда
кисл.
кисл.
кисл.
кисл.
щел.
щел.
кисл.
кисл.
кисл.
кисл.
кисл.
кисл.
—
—
—
—
—
—
—
—
—
—
—
кисл.
щел.
нейтр.
кисл.
кисл.
щел.
щел.
щел.
кисл.
щел.
щел.
569
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
PbS
PbSO4
Pd2+
[PdBr4F
[PdBr6]2"
[PdCl4]2"
[PdCl6]2"
[Pdl4]2"
[PdI6]2~
PdO2
PdOH+
Pd(OHJ
Pm3+
Pm(OHK
Po
PoIV
PoO^-
PoO(OHJ
Pr3+
Priv
Pr(OHK
Ptii
[PtBr4]2"
[PtBr6]2"
[PtCl4]2"
[PtCl6]2"
[Ptl6]2"
+ ne~
2
8
2
2
2
2
2
2
2
2
2
2
2
3
3
2
4
2
4
4
3
1
3
2
2
2
2
2
2
Восстановленная ,
форма
Pb + S2"
Pb + HS"
Pb + H2S(p)
Pb + H2S(r)
PbS
Pb + SO^"
Pb(Hg)()K) + SO2-
Pd
Pd + 4Br"
[PdBr4]2" + 2Br
Pd + 4C1-
[PdCl4]2" + 2C1-
Pd + 4Г
[Pdl4]2" + 21"
Pd(OHJ
Pd
Pd
Pm
Pm
Po2"
Po
Po11
Po
Po
Pr
Ргз+
Pr
Pt
Pt + 4Br-
[PtBr4J2- + 2ВГ
Pt + 4C1-
[PtCl4]2" + 2C1-
[Ptl4]2" + 21-
Ф'.В
-0,956
-0,988
-0,367
-0,338
+0,304
-0,356
-0,350
+0,915
+0,600
+0,993
+0,640
+1,288
+0,180
+0,482
+0,639
+0,954
+0,065
-2,428
-2,836
-1,400
+0,765
+0,879
-0,490
-0,098
-2,462
+2,900
-2,850
+0,963
+0,580
+0,630
+0,811
+0,734
+0,393
Среда
—
щел.
кисл.
кисл.
кисл.
—
—
—
—
—
—
—
—
—
щел.
кисл.
щел.
—
щел.
—
—
щел.
щел.
—
—
щел.
—
—
—
—
—
—
570
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
PtO2
Pt(OHJ
PtS
PtS2
Pu3+
Pu4+
PuO+
PuO2+
PuO3
Pu(OHK
Pu(OHL
Ra2+
Rb+
Re1»
ReIV
[ReCl6]2"
2[ReCl6]2"
ReO2
ReO3
ReO2"
ReO4
+ ne~
2
2
2
2
3
1
1
3
2
1
2
2
3
1
2
1
3
4
1
4
2
4
2
2
7
4
3
Восстановленная
форма
Pt(OHJ
Pt
Pt + S2"
Pt + HS"
Pt + H2S(p)
Pt + H2S(r)
PtS + H2S(r)
Pu
Pu3+
Pu4+
PuO2
Pu3+
Pu4+
PuO^
Pu(OHL
Pu(OHL
Pu
Pu(OHK
Ra
Rb
Re
Re
Re»1
Re
[Re2Cl8]2- + 4C1-
Re
Relv
Re(OHL
Re(OHL
Re
Re»1
Re™
ф°, В
+0,272
+0,237
-0,839
-0,871
-0,250
-0,221
+0,052
-2,031
+0,967
+ 1,156
+ 1,580
+ 1,017
+ 1,042
+0,928
+0,935
-0,331
-2,420
-0,963
-2,916
-2,925
+0,300
+0,264
+0,157
+0,414
+0,756
+0,264
-0,564
+0,399
-0,429
-0,541
+0,369
-0,577
+0,421
+0,510
Среда
щел.
щел.
—
щел.
кисл.
кисл.
кисл.
—
—
кисл.
—
кисл.
кисл.
—
нейтр.
щел.
щел.
щел.
—
—
—
—
—
—
—
кисл.
щел.
кисл.
щел.
щел.
кисл.
щел.
кисл.
кисл.
571
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
Rh3+
RhIV
[RhCl6]3"
[RhCl6]2-
RhO2
RhO2."?
Rh(OHK
Ru2+
Ru3+
RuIV
RuCl3
RuO2
R11O4
RuO4
S
¦ - ¦
2S
3S
4S
5S
(-SCNJ
2SO2(p)
S°2(P)
so2(r)
3SO2(p)
4SO2(P)
5SO2(p)
+ ne'r
3
1
1
3
1
3
1
1
3
3
2
1
1
3
4
1
1
2
2
2
2
2
2
2
4
4
2
6
10
. Восстановленная
форма
ReO2
ReO3
ReO2,"
Rh
Rh3+
Rh + 6C1-
[RhC^]3"
Rh(OHK
Rh(OHK
Rh
Ru
Ru2+
Ru3+
Ru + 3C1-
Ru
RuO2."
RUO4
HS"
H2S(P)
H2S(r)
S2~
sr
sr
sr
sr
2NCS-
HS2O4
s
s
s3or
s4or
s5or
Ф°, В
+0,510
-0,594
-0,924
-0,700
+0,800
+ 1,430
+0,437
+ 1,200
-0,256
-0,768
±0,000
+0,450
+0,230
+0,490
+0,682
-0,254
+0,590
+1,000
-0,476
+0,144
+0,174
-0,654
-0,444
-0,411
-0,381
-0,357
-0,340
+0,770
-0,080
+0,450
+0,451
+0,291
+0,512
+0,418
Среда
кисл.
щел.
щел.
—
—
—
—
—
щел.
щел.
щел.
—
—
—
—
щел.
—
щел.
кисл.
кисл.
щел.
—
—
—
—
—
кисл.
кисл.
кисл.
—
кисл. .
кисл.
572
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
2SO2(p)
2SO2(r)
so2-
2SO^
2SO?T
SOj"
2SO^-
SO2- + Cu2+
s2or
s4or
S2O6(O2J"
so3s2-
HSO3
SbIIIa
Sb
[SbCl4]"
[Sbcy-
[Sb(H2O)(OH5]
2[Sb(H2O)(OH5]
[Sb(H2O)(OHM]
Sb2O3 (аморфн.)
Sb2O3 (куб.)
+ ne~
4
4
4
2
4
8
2
8
6
2
2
8
8
2
2
2
4
4
3
3
3
2
5
4
2
6
6
Восстановленная
форма
so3s2-
SO3S2^
s
s2o2-
so3s2-
HS"
H2S(P)
H2S(r)
HSOj
s2-
s
S°2(P)
so2(r)
s2o2-
so3s2-
CuS
2SO2(p)
2SO3S2-
2SO|"
2S
S
Sb
SbH3(r)
Sb + 4C1^
[SbCl4]- + 2C1-
Sb
Sb2O3 (аморфн.)
Sb(OH)^
2Sb
2Sb
ф°, В
+0,338
+0,390
-0,659
-1,142
-0,589
-0,682
+0,302
+0,309
+0,110
+0,154
-0,674
+0,354
+0,161
+0,159
-0,104
-0,932
-0,244
+0,275
-0,760
+0,419
+0,566
+0,015
+1,961
+0,512
-0,730
+0,476
+0,240
-0,510
+0,170
+0,750
+0,333
+0,629
+0,533
+0,135
+0,122
Среда
кисл.
кисл.
щел.
щел.
щел.
щел.
кисл.
кисл.
кисл.
кисл.
щел.
кисл.
кисл.
кисл.
кисл.
щел.
кисл.
кисл.
щел.
кисл.
кисл.
—
—
кисл.
щел.
кисл.
—
кисл.
' —
—
кисл.
кисл.
кисл.
кисл.
кисл.
573
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
Sb2O5
Sb(OH)+
[Sb(OHN]3"
[Sb(OHN]"
[SbS3]3"
Sb2S3
Sc3+
ScOH2+
Sc(OHK
Se
2Se
SeO^"
SeO2"
HSeO3
H2Se03(p)
Si
[SiF6]2"
SiO2 (триг.)
SiO2 (триг.) + 2Н2(Г)
SiOt
H4Si04(p)
Sm3+
Sm(OHK
+ ne~
4
3
3
2
3
6
3
3
3
2
4
2
2
4
4
4
4
4
4
4
4
3
1
3
Восстановленная
форма
Sb2O3 (куб.)
Sb
Sb
[Sb(OHN]3-
Sb + 3HS-
2Sb + 3S2"
2Sb + 3HS"
2Sb + 3H2S(p)
2Sb + 3H2S(r)
Sc
Sc
Sc
HSe"
H2Se(p)
H2Se(r)
Se2"
Se2"
Se
HSeOj
H2Se03(p)
SeO^~
Se
Se
SiH4(r)
Si + 6F-
Si
SiH4(r)
Si
Si
Sm
Sm2+
Sm
Ф°, В
+0,649
+0,199
-0,649
-0,590
-0,850
-0,714
-0,746
-0,125
-0,096
-2,077
-1,986
-2,663
-0,642
-0,115
-0,082
-0,670
-0,592
-0,341
+1,073
+1,150
-0,001
+0,778
+0,741
-0,148
-1,366
-0,990
-1,138
-1,859
-0,936
-2,414
-1,561
-2,830
Среда
кисл.
кисл.
щел.
—
щел.
—
щел.
кисл.
кисл.
—
кисл.
щел.
щел.
кисл.
кисл.
—
—
щел.
кисл.
кисл.
щел.
кисл.
кисл.
кисл.
—
кисл.
кисл.
щел.
кисл.
—
—
щел.
574
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
Sn2+
[SnCl3]-
[SnCl6]2"
[SnF6]2"
SnO2
SnOH+
Sn(OHJ
[Sn(OHK]-
[Sn(OHN]2"
SnS
Sr2*
Ta2O5
Tb3+
TbIV
Tb(OHK
TCO4
Те
2Te
[TeCy2-
TeO2"
H2Te03
+ ne~
2
2
2
2
4
4
2
2
2
2
4
2
2
2
10
3
1
3
7
3
2
2
4
4
4
Восстановленная
форма
Sn
Sn2+
Sn + 3C1-
[SnCl3]- + 3C1-
Sn + 6F-
Sn
Sn2+
Sn
Sn
Sn
Sn
[Sn(OHK]-
Sn + S2"
Sn + HS"
Sn + H2S(p)
Sn + H2S(r)
Sr
Sr(Hg)w
2Ta
Tb
Tb3+
Tb
Tc
TcO2
Tc(OHL
HTe~
H2Te(p)
H2Te(r)
Te2"
Te2-
Te + 6C1-
Te
Те
Ф°, В
-0,141
+0,154
-0,201
+0,139
-0,250
-0,118
-0,094
-0,078
-0,917
-0,790
-0,875
-0,960
-0,955
-0,987
-0,366
-0,337
-2,888
-1,793
-0,753
-2,391
+2,900
-2,790
+0,472
+0,770
-0,366
-0,956
-0,464
-0,441
-0,902
-0,845
+0,630
-0,412
+0,543
Среда
—
—
—
—
кисл.
кисл.
кисл.
щел.
щел.
щел.
щел.
—
щел.
кисл.
кисл.
—
—
кисл.
—
—
щел.
кисл.
кисл.
щел.
щел.
кисл.
кисл.
—
—
—
щел.
кисл.
575
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
НДеОГ
Н6Те06(р)
Th4+
ThOH3+
Th(OH)f
Th(OH)+
Th(OHL
Ti2+?
Ti3+
Tliv
[TiF6]2"
у-7Ю2 (тетр.)
Ti(OH)f
ГЮ(ОНJ
Tl+
ТГ
Tl3+
Tl3+ + Cl-
TlBr
T1C1
[T1C14]-
T1I
Ti2o3
T12S
Tm3+
Tm(OHK
U3+
u4+
UOJ
uo2+
UOH3+
+ ne~
2
2
4
4
4
4
4
2
3
1
1
4
4
1
4
1
1
2
2
1
1
2
1
4
2
3
3
3
1
1
3
1
4
Восстановленная
форма
ТеО^"
H2Te03
Th
Th
Th
Th
Th
Ti
Ti
Ti2+?
Ti3+
Ti + 6F"
Ti
Ti3+
Ti
TI
Т1(Нё)(ж)
Tl+
T1C1
TI + Br-
Tl + Cl-
T1C1 + 3C1-
[T1C12]- + 2C1-
Tl + I~
2T1+
2T1 + S2"
Tm
Tm
U
u3+
u4+
UOH3+
u3+
и
Ф°,В
+0,401
+ 1,249
-1,875
-1,818
-1,755
-1,663
-2,513
-1,628
-1,208
-0,368
+0,092
-1,190
-1,075
+0,099
-0,860
-0,336
-0,334
+1,280
+1,390
-0,653
-0,556
+0,810
+0,786
-0,761
-0,063
-1,040
-2,278
-2,740
-1,690
-0,631
+0,593
+0,581
+0,007
+0,062
-1,422
Среда
щел.
кисл.
—
кисл.
кисл.
кисл.
щел.
—
—
—-
—
—
кисл.
кисл.
кисл.
—
—
—
—
—
—
—
—
—
щел.
щел.
—
щел.
—
кисл.
кисл.
кисл.
—
кисл.
576
V. Вещества в водном растворе
Продолжение табл.
Окисленная
форма
ио2он+
UO2(OHJ
V2+
v3+
vo2+
vo?
4V03f
V2O5
V(OHK
VO(OHJ
H2V10O?
[W(CN)8]3"
wo2
wo3
woj-
Hw6oir
XeF2(p)
Xe°3(P)
HXeO4
HXeO^"
H4Xe06(p)
Y3*
YOH2+
Y(OHK
Yb3+
Yb3+
Yb(OHK
Zn2+
Zn(CNL]2"
[Zn(NH3L]2+
ZnOH+
Zn(OHJ
+ ne~
2
2
2
1
1
5
1
4
2
1
1
10
1
4
6
6
36
2
6
6
2
2
3
3
3
3
1
3
2
2
2
2
2
Восстановленная
форма
UOH3+
U(OHL
V
V2+
VOH2+
V
vo2+
V4O2-
2VO2+
V(OHJ
V(OHK
10VO2+
[W(CN)8]4"
w
w
w
6W
Xe(r) + 2F"
Xe(r)
Xe(r)
HXeO4
Xe°3(P)
Y
Y
Y
Yb
Yb2+
Yb
Zn
Zn + 4CN"
Zn + 4(NH3-H2O)(p)
Zn
Zn
ф°, В
+0,474
-0,455
-1,125
-0,255
+0,361
+0,164
-0,229
+0,999
-0,740
+0,958
-1,313
-0,436
+ 1,042
+0,457
-0,154
-0,091
-1,055
-0,074
+2,640
+2,120
+ 1,260
+0,940
+2,360
-2,372
-2,193
-2,855
-2,269
-1,518
-2,730
-0,763
-1,260
-1,030
-0,498
-1,243
Среда
кисл.
щел.
—
—
кисл.
кисл.
кисл.
кисл.
щел.
кисл.
щел.
щел.
кисл.
—
кисл.
кисл.
щел.
кисл.
—
кисл.
щел.
щел.
кисл.
—
кисл.
щел.
—
—
щел.
—
нейтр.
кисл.
щел.
577
19-2004
V. Вещества в водном растворе
Окончание.табл.
Окисленная
форма
Zn(OHJ (аморфн.)
[Zn(OHKr
[Zn(OHL]2"
ZnS (куб.)
[ZrF6]2-
ZrO2
Zr(OH)f
ZЮ(OHJ
+ ne~
2
2
2
2
4
4
4
4
-Восстановленная
ц форма
Zn
Zn
Zn
Zn + S2"
Zn + HS"
Zn + H2S(p)
Zn 4- H2S(r)
Zr + 6HF(p)
Zr
Zr
Zr
Ф°,В
-1,222
-1,207
-1,255
-1,500
-1,532
-0,912
-0,882
-1,608
-1,473
-1,355
-2,225
Среда;
щел.
щел.
щел.
—
щел.
кисл.
кисл.
кисл.
кисл.
кисл.
щел.
2. Константы кислотности
кислотно-основных пар
Состояние равновесия обратимой реакции протолиза слабой кисло-
кислоты НА (молекула, ион) в разбавленном @,1—0,001 М) водном растворе
НА+Н2О <=± А- + Н3О+
характеризуется константой кислотности:
*к=[А-][Н3О+]/[НА]=.ДТ)
Значение Кк определяет силу кислоты НА в водном растворе.
Аналогично состояние равновесия обратимой реакции протолиза
слабого основания А- (молекула, ион)
Д- + Н2О <=t HA + OH-
характеризуется к о не тантой основности:
АО=[НА][ОН"]/[А-]=ЛТ)
Значение Ко определяет силу основания А~ в водном растворе.
Для каждой пары кислота НА — основание А~ значения Кк и Ко
связаны соотношением
где Кв — ионное произведение воды (при 25 °С Кв = 1,008 • 10~14).
В таблице приведены значения Кк, а также значения показателей
578
V. Вещества в водном растворе
— Кислота
Ag+¦Н2О
AgOH • Н2О
А13+ • Н2О
А1ОН2+ • Н2О
А1(ОН)+ • Н2О
А1(ОНK • Н2О
Ат3+ • Н2О
AsO+ • Н2О
Аи(ОНK • Н2О
В(ОНK • Н2О
Ва2+ • Н2О
Ве2+ • Н2О
ВеОН+ • Н2О
Ве(ОНJ • Н2О
[Ве(ОНK]- • Н2О
Bi3+ • Н2О
BiOH2+ • Н2О
ВКОН)^ • Н2О
Вк3+ • Н2О
СН3СООН
C(NH3)(NH2)O+
CS(NH3)(NH2)+
Са2+ • Н2О
Cd2+ • Н2О
CdOH+ • Н2О
Cd(OHJ • Н2О
[Cd(OHK]- • Н2О
Се3+ • Н2О
Се4+ • 2Н2О
Cf«+ • Н2О
Ст3+ • Н2О
Со2+ • Н2О
1,02-10-"
9,74 • 103
9,55 • Ю-6
4,68 • Ю-6
1,35 Ю-6
3,16-Ю-8
1,20 • Ю-6
2,00
1,78-Ю-12
7,85 • Ю-7
5,20 • Ю-10
4,40 • Ю-8
4,37 ¦ Ю-14
2,00 • Ю-6
3,16-Ю-8
1,23 • 10-»
3,55 • Ю-'4
2,69 • Ю-2
1,00-Ю-2
3,24 • 10
2,19 • Ю-6
1,74 10
6,61 • Ю-1
3,02
1,70-Ю-'3
2,40 • Ю-8
1,23-Ю-11
1,70 • Ю-14
3,72 • Ю-15
1,00 • Ю-9
6,61
2,40 • 10
1,20-Ю-6
1,26 10"9
11,99
12,01
5,02
5,33
5,87
7,50
5,92
-0,30
11,75
6,11
9,28
7,36
13,36
5,70
7,50
10,91
13,45
1,57
2,00
2,49
5,66
4,76
0,18
-0,48
12,77
7,62
10,91
13,77
14,43
9,0
-0,82
5,62
5,92
8,90
Основание
AgOH
[Ag(OHJ]-
А1ОН2+
А1(ОН)^
А1(ОНK
[А1(ОНL]-
АтОН2+
HAsO2
[Аи(ОНLГ
в4о2-
[В(ОНL]-
[В3О3(ОНL]-
ВаОН+
ВеОН+
Ве(ОНJ
[Ве(ОНK]-
[Ве(ОНL]2"
ВЮН2+
Bi(OH)+
Bi(OHK
BkOH2+
сн3соо-
C(NH2JO
CS(NH2J
CaOH+
CdOH+
Cd(OHJ
[Cd(OHK]"
[Cd(OHL]2"
CeOH2+
Ce(OH)f
СЮН2+
CmOH2+
CoOH+
P*o
2,01
1,99
8,98
8,67
8,13
6,50
8,08
14,30
2,25
7,89
4,76
6,64
0,64
8,30
6,50
3,09
0,55
12,43
12,00
11,51
8,34
9,24
13,82
14,48
1,23
6,38
3,09
0,23
-0,43
5,00
14,82
8,38
8,08
5,10
19*
579
V. Вещества в водном растворе
Продолжение табл.
Кислота
СоОН+ • Н2О
Сг2* • Н2О
Сг3* • Н2О
СЮН2+ • Н2О
Си2+ • Н2О
СиОН+ • Н2О
Си(ОНJ • Н2О
[Си(ОНK]- • Н2О
Dy3+ • Н2О
Ег3* • Н2О
Es3+ • Н2О
Еи3+ • Н2О
Fe2+ • Н2О
Fe3+ • Н2О
FeOH+ • Н2О
FeOH2+ • Н2О
Fe(OH)$ • Н2О
Fe(OHK • Н2О
Fm3+ • Н2О
Ga3+ • Н2О
GaOH2+ H2O
Ga(OH)+ • Н2О
Ga(OHK • Н2О
Gd3+ • Н2О
HAsO2
HAsO?r
HAsO2"
H2As03
H2As04
НзАбОз
H3AsO4
HBrO
HBrO3
1,26-Ю-10
2,51 • Ю-7
1,12 Ю-4
2,82 • Ю-6
4,57 • Ю-8
1,51 • 10-7
1,91 • 10-13
1,38 • 10-14
2,69 • 10-8
3,47 • 10-8
7,24 • 10-6
1,66 10-8
1,82 • 10-7
6,76 • 10-3
8,32 • 10-13
5,50 • 10-4
2,09 • 10-4
4,27 • 10-13
1,58 • 10-4
1,55 • 10-3
3,09 • 10-4
9,55 • 10-5
1,58 • 10
1,51 • 10-8
6,03,-10-10
3,89 • 10-14
3,02 • 10-12
7,41 • 10-13
1,07.- 10-7
5,89- 10-7
5,50 • 10-3
2,06 • 10-9
2,00 • 10-'
9,90
6,60
3,95
5,55
7,34
6,82
12,72
13,86
7,57
7,46
5,14
7,78
6,74
2,17
12,08
3,26
3,68
12,37
3,80
2,81
3,51
4,02
6,80
7,82
9,22
13,41
11,52
12,13
6,97
9,23
2,26
8,69
0,70
Основание.
Co(OHJ
CrOH+
CrOH2+
Cr(OH)^
CuOH+
Cu(OHJ
[Cu(OHK]-
[Cu(OHL]2"
DyOH2+
ErOH2+
EsOH2+
EuOH2+
FeOH+
FeOH2+
Fe(OHJ
Fe(OH)+
Fe(OHK
[Fe(OHL]"
FmOH2+
GaOH2+
Ga(OH)^
Ga(OHK
[Ga(OHL]"
GdOH2+
AsO2
AsO^-
AsO3,-
HAsO^-
HAsO2,-
H2As0j
HjAsOj
BrO-
ЪхО~ъ
4,10
7,40
10,05
8,45
6,66
7,18
1,28
0,14
6,43
6,54
8,86
6,22
7,26
11,83
1,92
10,74
10,32
1,63
10,20
11,19
10,49
9,98
7,20
6,18
4,78
0,59
2,48
1,87
7,03
4,77
11,74
5,31
13,30
580
V. Вещества в водном растворе
Продолжение табл.
'¦Кислота •¦
HCN
HCOJ
НС2О;
Н2СО3
Н2С2О4
нсоон
HCSJ
H2CS3
нею
НС1О2
нсю4
НСг2О7
Н2СгО4
HF
2HF
HF2
H[Fe(CNN]3-
H2[Fe(CNN]2"
HGeOj
H2GeO3
HIO
HIO3
HIO4
Н3ЮГ
H4IOi
H5IO6
HMnO;
HjMogOjg
H4Mo$O26
HN3
HNCO
HNCS
HNO2
4,93 • 10-10
4,68 • 10-"
6,17 • Ю-5
4,27 • Ю-7
6,46 • 10-2
1,78 • lO
1,00 • 10-8
1,00 • 10-3
2,82 • 10-8
l,07-10-2
3,i6-10-7
2,29 • 10-2
9,55
6,67 • Ю-4
2,63 • Ю-3
1,69 lO
6,76 • Ю-5
1,00 • 10-3
1,91 • 10-13
1,86 • Ю-9
2,29-10-"
1,69 • 10-'
2,30 • 10-2
1,05 • 10-15
5,37 • Ю-9
2,82 • 10-2
7,08 10-"
9,77 • 10
1,45 10-2
1,90 lO
3,47 • Ю-4
1,41 • 10-"
5,13-10-4
pKK
9,31
10,33
4,21
6,37
1,19
3,75
8,00
3,00
7,55
1,97
6,50
1,64
-0,98
3,18
2,58
3,77
4Д7
3,00
12,72
8,73
10,64
0,77
1,64
14,98
8,27
1,55
10,15
5,01
1,84
4,72
3,46
0,85
3,29
Основание
CN-
co?r
C2O2"
HCOj
HC2O4
HCOO-
cs^-
HCS;
cio-
C1O2
CrO2-
Cr2O2-
HCrG4
F"
HF2
2F-
[Fe(CNN]4-
H[Fe(CNN]3-
GeO^-
HGeO3
10-
10^
Ю4
н2ю3-
Н3ЮГ
H4tO;
MnO^-
H2Mo8O2^
HjMosO^
NJ
OCN-
NCS-
NO2
4,69
3,67
9,79
7,63
12,81
10,25
6,00
11,00
6,45
12,03
7,50
12,36
14,98
10,82
11,42
10,23
9,83
11,00
1,28
5,27
3,36
13,23
12,36
-0,98
5,73
12,45
3,85
8,99
12,16
9,28
10,54
13,15
10,71
581
V. Вещества в водном растворе
Продолжение табл.
Кислота
HNO3
HN2O2
H2N2O2
HNbO3?
HO2
H2O
Н2О2
н3о+
Н(РНО3)"
Н(РН2О2)
Н2(РНО3)
НРО2"
нр^о3-
НР2О|"
HP3Oto
Н2РО;
h2p2vo2-
Н2Р2О2~
Н2Р303о
Н3РО4
h3p2vo;
Н3Р2О7
н3р3о20-
H4P2rvO6
Н4Р2О7
HPO3F-
H2PO3F
HPO2(NH2J
HPO3(NH2)-
H2PO3(NH2)
hs-
H(S4)-
H(S5)~
2,69 • 10'
2,00 • 10-'2
2,00 • 10~8
4,07 • 10-8
1,58 • 10-5
1,816-10-'6
2,40 • 10-'2
5,551 • 10'
2,57 ¦ 10-7
7,94 • 10-2
1,00 10-2
4,57 • 10-'3
9,55 • 10-"
6,03 • Ю-9
i,oo-io-9
6,17 ¦ 10-8
5,50 • 10-8
1,70-lO
1,00 10-7
7,24 • 10-3
1,55-10-3
3,24 • 10-2
1,00-10
6,46 • 1O-3
1,41 • 10-'
1,58 • 10-5
2,82 • 10"'
1,00,- 10~5
1,00-10"8
1,00 • 10
1,23-10-'3
5,00 • 10-7
2,00 • 10-«
p/CK
-1,43
11,70
7,70
7,39
4,80
15,741
11,62
-1,744
6,59
1,10
2,00
12,34
10,02
8,22
9,00
7,21
7,26
5,77
7,00
2,14
2,81
- 1,49
3,00
2,19
0,85
4,80
0,55
5,00
I 8,00
3,00
12,91
6,30
5,70
Основание
NOj
N2O2"
HN2O2
NbOj
OH-
HO2
H2O
pho^-
PH2O2
H(PHO3)-
po3-
p2o^-
P3Ofo
hpo2-
hp'vo3-
hp2o3-
HP3O^
H2PO4
H2Pivo2-
H2P2O2"
h2p3o30-
H3P'v0^
H3P2O7
PO3F2-
HPO3F-
PO2(NH2J
PO3(NH2J-
HPO3(NH2)"
s2-
(S4)"
(s5r
15,43
2,30
6,30
6,61
9,20
-1,744
2,38
15,741
7,41
12,90
12,00
1,66
3,98
5,78
5,00
6,79
6,74
8,23
7,00
11,86
11,19
12,51
11,00
11,81
13,15
9,20
13,45
9,00
11,00
11,00
1,09
7,70
8,30
582
V. Вещества в водном растворе
Продолжение табл.
Кислота
H2S
HSO7
HSO4
HS2O;
HS2Oe
H2S2O4
H2S2O6
HSO3(NH2)
HSO3(O2)-
HSO3S-
H2SO3S
HSe"
H2Se
HSeOj
HSeO4
H2Se03
HSiO3"
H2SiO2-
H3SiO4
H4Si04
HTaO3?
HTe"
H2Te
HTeOj
H2Te03
H4TeO2-
H5TeO<
H6Te06
HVO|-
H2VO4
H3VO4?
HWO4
H2WO4?
1,05 Ю-7
1,23-10-7
1,12 • 10-2
3,55 • Ю-3
3,98 • Ю-4
5,00 • 10-'
6,31 • lO
7,89 • 10-'
4,00 • 10-'°
1,91 • 10~2
2,51 • 10"'
1,00-io-u
1,55 • lO
4,79 • lO-9
2,19-10-2
2,45 • Ю-3
2,00 • 10~14
1,00-ю-12
1,86 • 10-'2
1,58 • 10-10
2,51 • 10-10
6,76 • 103
2,29 • Ю-3
2,00-10-11
1,35 • lO
1,00 io-15
1,10-10-"
1,90-10-8
7,41 • 10-12
1,12-IO-9
3,24 • lO
2,19-10-4
6,31 • 10-3
6,98
6,91
1,95
2,45
3,40
0,30
0,20
0,10
9,40
1,72
0,60
11,00
3,81
8,32
1,66
2,61
13,70
12,0
11,73
9,80
9,60
12,17
2,64
10,70
3,87
15,00
10,96
7,72
11,13
8,95
4,49
3,66
2,20
Основание
hs-
so?r
so2-
s2o2-
s2o2-
HS2O4
HS2Oi
SO3(NH2)"
SO3(O2J"
so3s2-
HSO3S"
Se2"
HSe-
SeO^"
SeO|-
HSeOj
SiOj-
HSiO3-
H2SiO2~
H3SiO4
TaO3
Te2"
HTe-
TeO|-
HTeO3
H3TeO3"
H4TeO2"
H5Te0i
VO3-
hvo2-
H2VO;
woj-
nwo4
7,02
7,09
12,05
11,55
10,60
13,70
13,80
13,90
4,60
12,28
13,40
3,00
10,19
5,68
12,34
11,39
0,30
2,00
2,27
4,20
4,40
1,83
11,36
3,30
10,13
-1,00
3,04
6,28
2,87
5,05
9,51
10,34
11,80
583
V. Вещества в водном растворе
Продолжение табл.
Кислота
HjXeO^-
Н3ХеО^
Н4ХеО6
Hf(OH)f Н2О
Hf(OH)+ • Н2О
Hg2+ ¦ Н2О
Hgf • Н2О
HgOH+ • Н2О
Hg(OHJ • Н2О
Но3+ • Н2О
Г • Н2О?
1п3+ • Н2О
1пОН2+ • Н2О
In(OH)^ • Н2О
1п(ОНK • Н2О
К+ • Н2О
La3+ • Н2О
Li+ • Н2О
Lu3+ • Н2О
Mg2+ Н2О
Мп2+ • Н2О
NH+
N2H+
N2H2+
Ш3ОН+
Na+ ¦ H2O
NbO+ • H2O
Nd3t • H2O
Ni2+ • H2O
Np3+ • H2O
Np4+ • H2O
NpO^ • H2O
NpOf H2O
1,00-10-"
1,00 • Ю-6
1,00 • Ю-2
1,58 10-'
3,16-10
2,63 • Ю-4
3,31 • Ю-5
8,91 • Ю-5
1,41 • Ю-15
3,09 • Ю-8
3,31 • Ю-5
2,63 • Ю-4
5,75 • 10
7,59 • Ю-6
6,92 • 100
3,47 • Ю-15
2,00-Ю-11
2,29 • Ю-14
4,68 • Ю-8
3,80 • 102
2,57-Ю-11
5,75 • Ю-10
5,89-Ю"9
1,58 10'
9,35 • Ю-7
6,61; Ю-15
3,98
1,26 • Ю-8
1,20:10-и
3,72 • Ю-8
5,01 • Ю-3
1,26 10"9
6,76 • 10~6
11,00
6,00
2,00
0,80
1,50
3,58
4,48
4,05
14,85
7,51
4,48
3,58
4,24
5,12
9,16
14,46
10,70
13,64
7,33
11,42
10,59
9,24
8,23
,20
6,03
14,18
-0,60
7,90
10,92
7,43
2,30
8,90
5,17
Основание
НХеО3-
H-jXeO2;-
HjXeOg
Hf(OH)}
Hf(OHL
HgOH+
Hg2OH+
Hg(OHJ
[Hg(OHK]-
HoOH2+
HIO
InOH2+
In(OH)+
In(OHK
[In(OHL]-
KOH
LaOH2+
LiOH
LuOH2+
MgOH+
MnOH+
NH3 • H2O
N2H4 • H2O
NH2OH • H2O
NaOH
HNbO3?
NdOH2+
NiOH+
NpOH2+
NpOH3+
NpO2(OH)
NpO2(OH)+
P*o
3,00
8,00
12,00
13,20
12,50
10,42
9,52
9,95
-0,85
6,49
9,52
10,42
9,76
8,88
4,84
-0,46
3,30
0,36
6,67
2,58
3,41
4,76
5,77
15,20
7,97
-0,18
14,60
6,10
3,08
6,57
11,70
5,10
8,83
584
V. Вещества в водном растворе
Кислота
[Os(H2OJO4]
[Os(H3O)(H2O)O4]+
[Os(H2O)O4(OH)]-
Ра4+ • Н2О
РаОН3+ • Н2О
pa(OH)f н2о
ра(ОНJ+ н2о
Pa(OH)J • Н2О
РЬ2+ • Н2О
РЬОН+ • Н2О
РЬ(ОНJ • Н2О
Pd2+ • Н2О
Рг3* • Н2О
Ри3+ • Н2О
Ри4+ • Н2О
PuO} • Н2О
РиО2+Н2О
RuO4 • Н2О
SO2 • Н2О
[Sb(H2O)(OHM]
Sb(OH)} • Н2О
Sb(OHK • Н2О
Sc3+ • Н2О
ScOH2+ • Н2О
Sc(OH)^ • Н2О
Sm3+ • Н2О
Sn2+ • Н2О
SnOH+ • Н2О
Sn(OHJ • Н2О
Sn(OH)f Н2О
Sn(OH)+ • Н2О
Sn(OHL • Н2О
[Sn(OHM]- • Н2О
к.
7,95 • Ю-13
1,00 101
1,00 Ю-15
7,24 • 10
4,17-Ю
5,62 • Ю-2
8,91 • Ю-2
3,02 ¦ Ю-5
7,08 • Ю-7
2,00-10-"
9,55 • Ю-12
4,90 • Ю-2
9,55 • Ю-9
1,12 Ю-7
3,09 • Ю-2
2,00 • 10-'°
3,98 • Ю-4
1,00-10-"
1,66 • Ю-2
3,98 • Ю-5
6,92 • Ю-2
1,62 • Ю-12
2,45 • Ю-5
2,00 • Ю-6
3,16-Ю-7
1,55-Ю-8
7,94 • Ю-3
2,88 • Ю-5
3,02 • Ю-10
4,68 • Ю-1
6,03 • Ю-2
5,75 • Ю-10
1,29- Ю-12
12,10
-1,00
15,00
0,14
0,38
1,25
1,05
4,52
6,15
10,70
11,02
1,31
8,02
6,95
1,51
9,70
3,40
11,00
1,78
4,40
1,16
11,79
4,61
5,70
6,50
7,81
2,10
4,54
9,52
0,33
1,22
9,24
11,89
Продолжение табл.
Основание
[Os(H2O)O4(OH)]-
[Os(H2OJO4]
[OsO4(OHJ]2-
РаОН3+
Pa(OH)f
Ра(ОН)+
Ра(ОН)+
Ра(ОНM
РЬОН+
РЬ(ОНJ
[РЪ(ОНKГ
PdOH+
РЮН2+
РиОН2+
РиОН3+
РиО2(ОН)
РиО2(ОН)+
[RuO4(OH)]"
HSOj
[Sb(OHN]-
Sb(OHK
[Sb(OHL]-
ScOH2+
Sc(OH)+
Sc(OHK
SmOH2+
SnOH+
Sn(OHJ
[Sn(OHK]-
Sn(OH)^
Sn(OHL
[Sn(OHM]"
[Sn(OHN]2"
PKO
1,90
15,00
-1,00
13,86
13,62
12,75
12,95
9,48
7,85
3,30
2,98
12,69
5,98
7,05
12,49
4,30
10,60
3,00
12,22
9,60
12,84
2,21
9,39
8,30
7,50
6,19
11,90
9,46
4,48
13,67-
12,78
4,76
2,11
585
V. Вещества в водном растворе
Продолжение табл.
Кислота
Sr2* • Н2О
TaO} • Н2О
Tb3+ • Н2О
ТеО(ОН)+ • Н2О
Th4+ • Н2О
ThOH3+ • Н2О
Th(OHJ+H2O
ТЬ(ОН)з"-Н2О
Ti3+ • Н2О
Ti(OH)f Н2О
Ti(OH)+ • Н2О
Т1+ • Н2О
л3+ • н2о
Т1ОН2+ • Н2О
Т1(ОН)+ • Н2О
Тш3+ • Н2О
и3+ • н2о
и4+ • н2о
ио+2 н2о
uof • н2о
ион3+ • н2о
U(OH)f Н2О
UO2(OH)+ • Н2О
V2*•Н2О
V3* • Н2О
VO2+ • Н2О
VOH2+ • Н2О
VO(OH)+ • Н2О
Y3*•Н2О
Yb3+ • Н2О
Zn2+ • Н2О
ZnOH+ • Н2О
Zn(OHJ • Н2О
6,76 • Ю-14
9,55 • Ю-2
2,34 • Ю-8
3,63 • Ю-4
4,37 • Ю-3
5,01 • Ю-4
4,17-Ю-4
2,82 • Ю-4
5,62 • Ю-3
3,24 • Ю-2
9,77 • Ю-4
6,61 • Ю-14
5,75 • 10-2
2,09 • Ю-2
1,51 • 10~2
3,80 • Ю-8
1,0-Ю-7
3,02 • Ю-2
1,00 Ю-8
6,92 • Ю-3
3,80 • Ю-3
7,24 • Ю-4
5,25 • 10~8
3,47 • Ю-7
1,20 • Ю-3
2,24 • Ю-3
3,02 • Ю-4
8,32 • Ю-4
8,32 • Ю-10
4,27 • Ю-8
2,04 • Ю-8
7,59 • Ю-10
1,29-Ю-12
рКк
13,17
1,02
7,63
3,44
2,36
3,30
3,38
3,55
2,25
1,49
3,01
13,18
1,24
1,68
1,82
7,42
7,0
1,52
8,00
5,16
2,42
3,14
7,28
6,46
2,92
2,65
3,52
3,08
9,08
7,37
7,69
9,12
11,89
Основание
SrOH+
НТаО3?
ТЬОН2+
Н2Те03
ThOH3+
Th(OH)f
Th(OH)}
Th(OHL
ТЮН2+
Ti(OH)}
Ti(OHL
T1OH
T1OH2+
Tl(OH)^
T1(OHK
TmOH2+
UOH2+
UOH3+
UO2(OH)
UO2(OH)+
U(OH)f
и(ОН)з"
UO2(OHJ
VOH+
VOH2+
VO(OH)+
V(OH)^
VO(OHJ
YOH2+
YbOH2+
ZnOH+
Zn(OHJ
[Zn(OHK]-
0,83
12,98
6,37
10,56
11,64
10,70
10,62
10,45
11,75
12,51
10,99
0,82
12,76
12,32
12,18
6,58
7,0
12,48
6,00
8,84
11,58
10,86
6,72
7,54
11,08
11,35
10,48
10,92
4,92
6,63
6,31
4,88
2,11
586
V. Вещества в водном растворе
Окончание табл.
Кислота
Основание
[Zn(OHK]- • H2O
Zr(OH)f H2O
Zr(OH)+ • H20
4,27 • Ю-13
6,17-10-'
1,55-Ю-1
12,37
0,21
0,81
[Zn(OHL]2-
Zr(OH)}
Zr(OHL
1,63
13,79
13,19
3. Константы устойчивости
одноядерных комплексов
Состояние равновесия обратимой реакции образования одноядерного
комплекса [MLJ (заряд здесь и далее не указан) в водном растворе из
центрального атома (комплексообразователя) М и лигандов L
М + лЬ <=t [MLJ
характеризуется общей константой устойчивости:
Значение константы Р„ определяет меру общей устойчивости
комплекса [MLJ в водном растворе.
Состояние равновесия обратимой реакции образования того же
комплекса [MLJ из комплекса [МЬЯ_,]5 содержащего на один лиганд
меньше, и лиганда L
[ML^J + L ?=> [MLJ
характеризуется ступенчатой константой устойчивости:
Значение константы Кп определяет меру устойчивости комплекса
[MLJ по сравнению с устойчивостью исходного комплекса [МЬЯ_,].
Значения констант Кп и Рл для комплекса [MLW] связаны между со-
собой соотношением:
при п = 1
Кп =
Р„_1 — общая константа устойчивости комплекса [MLw_j], т.е.
tMLJ/lMHLr-1
В таблице приведены значения lgPw; для расчета значений ^
(при п > 2) следует пользоваться выражением lgKn = lgPw — lgpw_j.
Комплексы различных атомов М сгруппированы по виду лиганда L.
587
V. Вещества в водном растворе
м
n
Лиганд
Ag1
Аи1
Аи1"
Bi»1
Cd»
Се1»
Со»
Си1
Си"
Fe1"
Hg»
In»1
1
Ni»
Pb"
4
3
2
1
2
4
6
5
4
3
2
1
4
3
2
1
1
2
1
2
2
1
2
1
4
3
2
1
4
3
2
1
4
2
4
Br
8,73
8,00
7,34
4,38
12,46
31,50
9,52
9,42
7,84
6,33
4,45
2,26
3,70
3,32
2,34
1,75
0,38
-0,42
-0,13
5,92
5,86
0,30
0,82
0,55
20,01
18,75
17,33
9,05
-1,25
0,67
1,89
1,30
-8,12
-3,24
3,00
M
Pd"
Pt"
Sn»
Tli
7,111
uIV
uof
Zn"
Лига
Ag1
Ba11
Ca"
Cd»
Ce111
n
3
2
1
4
4
5
4
3
2
1
4
3
2
1
6
5
4
3
2
1
1
1
4
3
2
1
нд СН
2
1
1
1
2
1
3
2
1
toft,
3,30
1,92
1,15
13,10
20,50
1,98
1,66
2,13
1,73
0,90
-0,20
0,60
1,01
0,93
26,20
25,50
23,90
21,20
16,60
9,70
0,18
-0,30
-2,50
-2,90
-2,20
-0,80
[3COO-
0,64
0,74
1,15
0,77
3,15
1,93
3,23
2,65
1,68
M
Cu»
In
Mg"
Mn"
Ni»
Pb»
Sr"
Tl1
Tl1»
uof
Zn»
n
2
1
6
5
4
3
2
1
1
1
2
1
4
3
2
1
1
1
4
3
2
1
2
1
Лиганд C2t
Ag1
Cd"
Co"
Co1"
Cu1
Cu"
2
1
3
2
1
3
2
1
3
2
2
"дРл
3,63
2,23
10,30
9,23
9,08
7,90
5,95
3,51
1,25
1,40
2,12
1,43
8,58
6,48
4,08
2,68
1,19
-0,11
18,30
6,30
4,90
2,61
2,38
1,57
[8N2(en)
7,84
4,70
12,29
10,22
5,63
13,82
10,72
5,89
48,69
10,80
20,13
588
V. Вещества в водном растворе
Продолжение табл.
м
Fe»
Hg»
Mg"
Mn"
Ni"
Tl1
Zn»
Лиганд
Ag1
Cd»
Co»
Cu1
Cu»
Fe»
Hg»
n
1
3
2
1
3
1
3
2
1
3
2
1
1
3
2
1
c5
2
1
4
2
1
2
1
4
3
2
1
4
3
2
1
4
1
3
tgpn
10,76
9,70
7,65
4,34
23,42
0,37
5,67
4,79
2,73
19,11
14,08
7,60
0,30
12,08
10,37
5,71
H5N (py)
4,11
1,97
2,49
2,14
1,27
1,54
1,14
8,70
7,90
6,60
3,90
6,54
5,69
4,38
2,52
6,70
0,71
10,40
M
Ni»
Ni»1
Zn»
n
2
1
3
2
1
3
4
3
2
1
"gpn
10,00
5,10
3,13
2,82
1,78
3,14
1,93
1,61
1,41
1,11
Лиганд (C5H4NJ(bipy)
Ag1
Cd»
Cu"
Fe»
Mg"
Pb"
Zn»
Ли]
Ag1
Au1
Au»1
Cd»
1
3
2
1
3
2
3
2
1
1
1
3
2
1
ганд
4
3
2
2
4
4
3
2
6,80
10,47
8,00
4,50
17,85
14,20
17,58
9,21
4,21
0,50
3,00
13,50
9,80
5,40
CN-
19,42
20,55
19,85
38,30
56,00
17,11
13,92
9,60
M
Co"
Co
Cu1
Fe»
Fe
Hg"
Ni"
Tl»1
Zn»
Ли
Ca"
Cd»
Cu"
La1»
Mg"
Pb"
uof
Ли
Al1"
Ba"
Be»
л
1
6
6
4
3
2
6
5
6
4
3
2
1
4
4
4
3
2
ганд С
1
3
2
1
1
1
2
3
2
ганд С
3
2
1
2
1
"др„
5,18
19,09
64,00
30,30
28,59
24,00
36,90
18,60
43,90
38,97
36,31
32,75
17,00
31,00
35,00
19,62
16,05
11,07
3,20
6,22
10,16
6,91
7,72
3,40
8,20
22,36
18,09
;02-
2
16,30
13,00
2,31
5,91
4,08
589
V. Вещества в водном растворе
Продолжение табл.
м
Cd«
Се1"
Со"
Си"
Fe"
FeUI
La
Mn"
Mn1"
Nd1"
Ni"
NpOf
Pb"
Sr"
JhlV
Tl1
n
2
1
3
2
1
3
2
1
2
1
3
2
3
2
1
3
2
i
1
2
1
3
2
1
3
2
1
3
2
1
2
1
2
1
2
1
4
1
igPn
5,37
3,52
11,30
10,48
6,52
9,70
6,70
4,70
10,30
6,70
5,22
4,52
20,20
16,20
9,40
10,30
н on
7,yU
A 1(\
4,JU
5,80
3,89
19,42
16,57
9,98
>13,50
11,51
7,21
=14,00
7,64
>5,30
7,07
3,30
6,54
4,90
1,90
1,25
29,6
2,03
M
Zn"
Лига
Ag1
Bi
Cd"
Cu»
Hg"
Pb"
Ли
Ag1
Am1»
Au1
Au1"
Bi1»
Cd"
n
3
2
1
3
2
1
igpn
> 12,90
11,89
7,30
8,34
7,55
4,85
нд CS(NH2J
3
6
3
2
1
4
3
4
3
2
3
ганд
4
3
2
1
1
2
4
6
5
4
3
2
1
6
4
13,14
11,94
2,92
2,63
1,58
15,39
12,82
26,30
24,60
21,90
1,77
ci-
5,92
5,40
5,25
3,31
1Д7
11,79
21,30
8,14
6,11
4,98
3,42
3,10
2,43
2,58
2,90
M
Ce1»
Cm»1
Co»
Cr
Cu1
Cu"
Fe»
Fe»1
Ga
Hg»
In»1
Ir
La1"
Mn
Mo™
n
3
2
1
1
1
1
2
1
2
1
3
2
1
2
1
4
3
2
1
4
3
2
1
4
3
2
1
3
2
1
6
1
1
3
2
1
igpn
2,11
2,70
2,00
0,22
1Д7
0,14
-0,11
vr, л. x
0,60
5,42
3,10
-2,10
-0,52
0,95
0,40
0,36
-0,85
0,78
1,78
1,48
-6,80
-4,50
-2,30
0,60
15,22
13,99
13,16
6,76
3,23
2,64
1,72
14,00
-0,15
0,95
-2,69
-0,80
-0,30
590
V. Вещества в водном растворе
Продолжение табл.
м
NpOf
РЬ"
Pd»
Pt"
Pu
Pulv
PuO|+
Sn"
SnIV
Thiv
Tl1
Tl
uof
vo2+
Y"i
n
1
3
2
1
4
3
2
1
4
3
1
1
2
1
3
2
1
1
4
3
2
1
3
2
1
5
4
3
2
1
1
3
2
1
1
1
"gpn
0,21
1,85
2,44
1,62
15,10
13,10
10,60
6,00
16,00
14,48
1,17
-0,25
-0,35
0,10
2,45
2,24
1,51
0,82
-0,51
0,23
0,38
1,38
-0,80
0,25
0,68
17,47
17,00
14,75
12,00
7,50
-0,85
-2,62
-0,92
0,21
0,04
1,26
M
Zn"
ZrIV
n
4
3
2
1
4
3
2
1
Лиганд
Ag1
Alm
Be"
Cd"
Ce1»
Cr1"
Cu»
Fe
Ga111
1
6
5
4
3
2
1
4
3
2
1
3
2
1
1
3
2
1
1
4
3
2
1
3
2
1
; igpn
-1,52
-1,40
0,18
-0,19
1,20
1,50
1,30
0,90
F-
0,38
20,83
20,36
19,03
16,65
12,60
6,98
14,97
12,71
9,94
6,00
1,20
0,53
0,30
3,99
11,02
8,54
5,20
1,23
15,74
13,74
10,74
6,04
13,49
10,72
6,19
M
Gd»1
Ge™
H'
Hg"
In1»
La1"
Mg"
Mn
Ni"
Pb"
Pu1"
Pulv
Sc1"
Sn»
SnIV
Thiv
Tliv
Tl1
UIV
n
1
6
5
2
1
1
3
2
1
1
1
1
1
3
2
1
1
1
4
3
2
1
3
1
6
3
2
1
4
3
2
1
1
6
5
4
"gPn
3,46
25,57
21,84
3,77
3,18
1,56
10,23
7,41
4,63
3,56
1,82
5,76
0,66
3,42
2,27
1,26
7,94
6,77
20,18
17,33
12,88
7,08
10,00
4,85
= 25,00
17,96
13,27
7,28
20,38
16,32
11,74
6,65
0,10
32,21
29,91
28,32
591
V. Вещества в водном растворе
м
uof
vo2+
Zn«
ZrIV
Ли
Са11
Na1
Mg11
,Мпп
Pb11
Ли
Са*1
Fe111
Mg11
Ni11
PuIV
n
3
2
1
4
3
2
1
3
2
1
3
2
1
1
6
5
4
3
2
1
ганд
1
1
1
1
3
2
ганд
5
igPn
24,05
19,82
14,57
13,25
11,89
9,33
4,93
7,15
5,46
3,30
12,14
8,54
4,81
1,26
35,86
31,85
27,17
22,20
16,35
8,89
HCO3
1,26
-0,25
1,16
1,80
5,19
4,77
HPQ2
2,77
10,89
0,72
2,91
2,08
52,00
M
uof
Zn"
n
4
3
2
1
2
1
1
ЛигандH
Al111
Ca11
Fe1»
Thiv
uof
3
2
1
1
4
2
1
3
2
1
Лиганл I-
PuIV
Thiv
uof
Ли
Ag1
Cd"
Co»
1
2
1
3
2
1
ганд
2
1
4
3
2
1
2
|дР„
43,20
33,40
23,70
12,90
18,57
8,43
2,40
2POT
7,60
5,30
3,00
1,41
9,15
8,15
4,30
7,33
5,43
3,00
[,PO4
2,30
3,86
1,89
5,23
3,88
<1,88
HS"
18,45
14,05
20,86
18,49
16,57
9,41
8,77
M
Cu»
Fe11
Hg»
Pbn
Znn
Ag1
Bi»1
Cd11
Cu1
Hg11
In111
Pb11
Продолжение табл.
n
1
3
3
2
2
3
2
3
2
Лиганд
4
3
2
1
6
5
4
1
6
4
3
2
1
2
4
3
2
1
3
2
1
4
3
2
1
'9Pn
5,67
25,90
10,97
8,94
37,72
16,52
15,25
16,10
14,90
I-
13,10
13,68
11,74
6,58
19,10
16,80
14,95
2,89
6,00
5,41
5,00
3,92
2,28
8,76
29,83
27,60
23,82
12,87
2,48
2,56
1,64
3,92
3,42
2,80
1,26
592
V. Вещества в водном растворе
Продолжение табл.
м
Т11
Т1ш
Zn"
Ли!
Ag1
Ва11
Сап
Си11
К1
Mg11
Sr"
Thiv
Tl1
п
4
3
2
1
4
3
2
1
4
3
2
1
1,60
2,00
1,82
1,41
31,82
27,60
20,88
11,41
-0,51
1,26
-1,53
-0,47
анд Юз
2
1
1
6
3
2
1
1
1,90
0 63
V/, \J*J
1,05
0,89
0,82
-0,30
0,72
0,98
11,02
7,18
4,81
2,88
0,50
Лиганд NCS~
Ag1
А11И
Аи1
Аи1»
4
3
2
1
1
2
6
9,67
9,45
8,23
4,75
0,42
23,00
42,04
М
Bi
Cd"
Со"
Сг"'
Си1
Си"
Fe"
Fe1"
п
4
2
6
4
2
1
6
4
3
2
1
4
3
2
1
6
5
4
3
2
1
6
5
4
3
2
4
3
2
1
4
1
6
5
4
3
2
"9р„
42,00
23,00
4,23
3,41
2,26
1,15
-0,08
2,91
2,30
2,40
1,74
2,30
0
-0,7
-0,04
3,80
5,40
6,10
5,80
4,80
3,08
9,27
9,59
10,05
9,90
12,11
6,52
5,19
3,65
2,30
4,53
1,33
3,23
4,23
4,53
4,63
4,33
М
Hg"
In1"
Mn"
Ni"
Pb"
Ru1"
Thrv
Tliv
Tl1
U1V
UOf
V"
vo2+
Zn"
Zrlv
n
1
4
3
2
3
2
1
1
3
2
1
4
3
2
1
1
3
1
1
4
3
2
1
3
2
1
2
1
1
2
1
4
3
2
1
6
5
|дрл
3,03
21,20
20,40
17,60
4,63
3,00
2,58
1,22
1,81
1,64
1,18
0,85
1,90
2,52
1,09
1,78
1,78
1,08
1,70
0
0,20
0,65
0,80
2,18
2,11
1,49
1,90
1,50
2,00
3,68
2,32
3,70
2,20
2,10
1,62
7,90
6,90
V. Вещества в водном растворе
Продолжение табл.
м
п
4
3
2
1
Лиганд
Ag1
Аи1
Аи111
Са11
Cd11
Со»
Со»1
Си1
Си»
2
1
2
4
1
6
5
4
3
2
1
6
5
4
3
2
1
6
5
4
3
2
1
2
1
6
5
4
3
2
1
iQPn
5,80
4,70
3,40
2,00
NH3
7,21
3,37
27,00
30,00
-0,20
5,14
6,80
7,37
6,37
4,92
2,74
4,39
5,13
5,07
4,43
3,50
1,99
35,21
30,80
25,70
20,10
14,00
7,30
10,86
5,93
8,90
11,43
12,90
10,72
7,82
4,27
M
Fe"
Hg»
Li1
Mg»
Mn"
Ni"
Pd"
Pt»
Tl1
Tl
Zn"
л
2
1
4
3
2
1
1
6
5
4
3
2
1
6
2
1
6
5
4
3
2
1
4
4
1
4
3
2
1
4
3
2
1
Л иганд]
Са"
3
2
toft,
2,20
1,40
7,47
6,40
4,80
2,68
-0,30
-3,29
-1,99
-1,04
-0,34
0,08
0,23
9,00
1,30
0,80
8,31
7,89
7,04
5,81
4,26
2,36
30,00
36,00
,92
13,00
11,60
9,30
4,60
8,62
6,92
4,91
2,59
Я2Н4
L Ц
-1,91
-0,80
M
Cd»
Ni»
Zn»
n
1
4
3
2
1
6
5
4
3
2
1
4
3
2
1
Лиганд'
Ag1
Cd»
Cu»
Hg»
2
1
4
3
2
1
2
1
4
Лиганд\
Ag1
Ba»
Bi»1
Ca»
Cd»
Ce»1
Cs1
Fe»1
1
1
1
1
]
j.
>
i
ISPn
-0,16
3,89
2,78
2,40
2,25
11,99
10,75
9,20
7,35
5,20
2,76
3,88
3,78
3,70
3,40
2,83
1,88
3,10
3,81
3,01
1,80
1,65
1,30
13,54
-0,29
0,92
1,26
0,28
-0,31
1,51
1,04
0,01
1,00
594
V. Вещества в водном растворе
Продолжение табл.
м
Hfv
Hg"
Hgf
к1
La
Li1
Mg"
Na1
Pb"
Pulv
Sr»
Thiv
Tl»1
UIV
UOf
Zr™
Ли]
Ag1
n
4
3
2
1
2
1
2
1
1
1
1
1
1
1
1
1
4
3
2
1
1
3
2
1
4
3
2
1
1
4
3
2
1
ганд
3
2
igpn
2,08
1,89
1,51
0,92
0,01
0,35
-0,24
0,08
-0,14
-0,26
-1,45
0,00
-0,59
1,18
1,80
0,54
0,74
1,00
1,11
0,78
0,33
1,10
0,12
0,90
0,18
0,42
0,47
0,36
-1,40
-0,82
-0,26
0,11
0,34
OH-
5,20
3,99
M
А1Ш
Ba»
Be»
Bira
Ca11
Cd»
Ce111
Ce™
Co11
Crln
Cu11
Fe"
n
1
4
3
2
1
1
4
3
1
4
2
1
1
4
z.
l
l
2
1
3
2
1
6
5
4
2
1
4
3
2
1
4
3
2
1
igft,
2,00
32,50
26,00
17,86
8,98
2,22
18,42
18,63
7,48
35,20
15,80
12,43
1,22
9,25
9,68
9,46
6,37
4,60
27,06
14,81
10,49
9,19
4,40
14,41
21,19
27,97
18,45
10,02
15,89
15,00
13,68
6,65
9,60
10,00
9,17
7,25
M
Fe»1
Ga
Gelv
Hg»
Hgf
In»1
La1»
Li1
Lu»1
Mg"
Mn»
Na1
Nd1»
Ni»
Pb»
n
4
3
2
1
6
4
3
2
1
6
5
4
3
2
1
3
2
1
1
4
3
2
1
1
1
1
1
3
1
1
1
3
2
1
3
2
1
igpn
34,49
32,87
21,23
11,83
40,30
38,84
31,65
21,68
11,19
60,91
59,63
54,37
41,09
27,61
13,87
21,20
21,70
10,30
9,00
33,88
29,04
20,17
10,41
3,30
0,17
7,40
2,64
7,81
3,41
-0,48
5,50
12,96
10,21
3,08
13,92
10,83
7,83
595
V. Вещества в водном растворе
Продолжение табл.
м
Pd»
Pt»
Pu'"
PuIV
Sb1»
Sc'"
Sn»
Sn™
Sr»
Thiv
Tl1
Tl1"
ylV
uof
V»
V"'
Y1"
Zn"
Zr™
л
2
1
4
1
1
4
3
2
1
1
3
2
1
6
1
6
3
2
1
1
2
1
2
1
4
2
1
1
¦• 2
1
1
4
3
2
1
4
26,10
12,68
22,67
7,05
9,12
38,30
36,70
24,30
6,07
9,12
11,93
9,01
4,45
63,00
0,82
38,70
27,65
19,87
10,12
0,82
25,37
12,86
25,7
13,78
32,40
15,56
8,84
7,53 .
21,54
11,07
4,92
16,63
15,00
12,90
5,04
54,51
M
n
3
2
1
Лиганд F
Ba»
Ca»
Cd»
Ce»1
Co"
Cu1
Cu»
Fe»1
K1
La»1
Li1
Mg»
Na1
Ni»
Pb»
Sn"
*Sr"
T1r
Zn»
1
1
1
1
1
2
2
1
2
1
2
1
1
1
1
2
1
2
1
2
1
2
1
2
1
Лиганд 15
Ag1
Cd»
3
2
1
2
iQpn
41,32
27,75
14,04
2° 7
4,64
5,60
8,70
17,15
6,10
26,72
12,45
7,60
5,55
2,30
18,57
16,72
3,10
7,20
2,22
7,19
5,82
9,40
6,40
16,40
5,40
1,87
1,69
11,00
8,70
9,00
8,68
5,60
4,19
M
Ce"'
Cu1
Hg"
Tl"'
n
1
3
2
1
3
2
1
4
'др.
8,04
9,36
8,70
7,85
24,96
24,07
22,66
34,00
Лиганд SOl~
Ag1
Al
Ba"
Ca"
Cd"
Ceni
CeIV
Co»
Co»1
Cr»1
Cu»
Er»1
Fe»
Fe
Ga
Gdm
Hg"
Hgf
Ho
In
K1
1
2
I
]
]
]
]
1
1
1
1
1
1
2
1
2
1
1
2
1
2
1
1
2
1
1
1,30
4,90
3,01
2,35
2,43
2,29
3,48
1,78
2,36
1,34
1,60
2,26
3,58
2,20
5,38
4,15
5,06
2,77
3,66
2,44
1,34
2,40
1,30
3,58
5,00
3,04
0,75
596
V. Вещества в водном растворе
Окончание табл.
м
La
Li1
Mg"
Mn"
Na1
Nd
Ni"
NpIV
Pb»
Priii
РцШ
Pu™
Sm»1
Thiv
Tliv
T1i
UIV
uof
n
1
1
1
1
1
1
1
2
1
2
1
1
2
1
1
1
2
1
1
1
2
1
3
"др„
3,50
0,64
2,23
2,26
0,72
3,64
2,32
3,47
2,43
3,47
2,62
3,62
1,62
1,00
3,66
3,66
5,70
3,32
2,40
1,27
5,42
3,24
3,40
M
VO2+
ylH
Yb
Zn"
Zr™
n
2
1
1
2
1
1
1
3
2
1
igpn
2,72
1,48
2,48
3,99
3,34
3,58
2,38
7,64
6,54
3,74
Лиганд SO3S2"
Ag1
Ba"
Ca"
Cd"
Co»
Cu1
Cu"
2
>
3
2
1
3
13,46
8,60
2,33
1,98
6,46
3,94
2,05
13,71
12,27
10,35
13,84
M
Fe»
Fe1"
Hg"
K1
La
Mg"
Mn"
Na*
Ni"
Pb"
Sr"
Tl1
Tl1»
Zn"
n
2
1
1
1
4
3
2
1
4
3
2
1
1
1
2
1
•gpn
12,22
10,27
2,17
3,25
33,61
32,26
30,80
29,27
0,92
2,99
1,79
1,95
1,08
2,06
7,20
6,35
5,13
2,70
2,04
1,91
41,00
4,59
2,29
4. Произведения растворимости
Состояние гетерогенного равновесия между насыщенным водным
раствором малорастворимого сильного электролита МдД, и осадком
того же вещества
характеризуется произведением растворимости ПР:
ПР = [Ма+]т[Ат-]а=АТ)
Приведены произведения растворимости и их показатели
(рПР = -lg ПР) при 25 °С; значения рПР, отмеченные верхним индек-
597
V. Вещества в водном растворе
сом (*), и соответствующие значения ПР отвечают комнатной темпе-
температуре A8-25 °С).
Несоответствие между составом осадка исходного вещества и
ионов в растворе указано с помощью ссылок.
Растворимость веществ рассчитана из математического выражения
дляПР:
Соотношение в
растворе
«катион: анион»
1 : 1
1: 2, 2 : 1
1: 3, 3 : 1
1 : 4, 4 : 1
Растворимость
исходного
вещества, моль/л
Тпр
3л/ПР/4
4л/ПР/27
57ПР/256
Соотношение
в растворе
«катион: анион»
2 : 3, 3 : 2
1:6
3:4
Растворимость
исходного
вещества, моль/л
5л/ПР/108
VnP/46 656
77ПР/6912
Растворимость также пересчитана из единиц моль/л в г/л.
Для электролитов, дающих три разных иона А, В и С B катиона
и 1 анион, 1 катион и 2 аниона), расчетные формулы для раствори-
растворимости будут такими:
а:Ь:с
1:1:1
1:1:2
2:1:2
3:2:2
Растворимость,
моль/л
Шр
4л/ПР/4
Vnp/i6
VnP/432
a:b:c
1:2:6
1:2:8
2:7:2
Растворимость,
моль/л
VnP/186 624
1УПР/67 108 864
ил/ПР/13 176 688
При несоответствии состава осадка исходного вещества и ионов в
растворе значения растворимости рассчитаны по уравнениям реак-
реакций, данных в ссылках.
Значения растворимости малорастворимых сильных электролитов
в воде, определенные указанным способом, являются оценочными.
Для получения более точных значений необходимо учитывать прото-
лиз катионов и/или анионов и комплексообразование между ними
(обычно этот учет повышает растворимость электролитов). Методика
таких расчетов описана в руководствах по аналитической химии
(см., например, Лайтинен Г.-А, ХаррисВ.-Е. Химический анализ.—
М.: Химия, 1979). По этим же причинам экспериментальные данные
по растворимости веществ (раздел VI-1) могут существенно отличать-
отличаться от значений, приведенных в этом разделе.
598
V. Вещества в водном растворе
Вещество
Ас2(С2О4K
Ас(ОНK
Ас(ОНK(аморфн.)
Ag3AsO3
Ag3As04
AgBr
AgBrO,
AgCH3COO
AgCN
Ag2CN2
Ag2CO3
Ag2C2O4
AgCl
AgC102
Ag2CrO4
Ag2Cr207
Agl
AgIO3
AgMnO4
Ag2MoO4
AgN3
AgNCS
AgNCSe
AgNO2
AgOCN
Ag3PO4
Ag2(PO3F)
AgReO4
Ag2S
ПР
2,0 • Ю-2"
1,3 • 10-21
2,1 • 10~19
4,5 • 10-19
1,0 • 10-22
5,0 • 10-»
5,8 • 10-5
4,4 • Ю-3
7,0 • 10-15
7,0 • 10-''
8,7 • 10-12
1,1 • Ю-11
1,8 lO0
2,0 • 10-4
1,2 • 10-12
2,0 • 10-7
2,3 • 10~16
3,2 • 10-8
1,6 Ю-3
2,8 • 102
2,9 • 10-9
1,6 • 10-12
4,0 • 10-'6
3,1 • 10-10
2,0 • 10-8
2,3 • 10-7
1,8 • 10-18
8,9 • 10-"
8,0 • 10-5
7,2 • 10-50
рПР
23,70*
20,89
18,68*
18,35
22,00*
12,30
4,24
2,36
14,16
10,16
11,06
10,96
9,74
3,70*
11,92
6,70
15,64
7,49
2,80*
11,55
8,54*
11,80
15,40*
9,51
7,70
6,64*
17,75
3,05*
4,10*
49,14
Растворимость
моль/л
7,1 • Ю-6
2,6 • Ю-6
9,4 • Ю-6
1,1 • Ю-5
1,4 • Ю-6
7,1 • Ю-7
7,6 • Ю-3
6,6 • Ю-2
8,4 • Ю-8
2,6 • 10-"
1,3 • 10-"
1,4-10-"
1,3 Ю-5
1,4 • Ю-2
6,6 • Ю-5
3,7 • Ю-3
1,5-Ю-8
1,8 • 10-"
4,0 • Ю-2
8,9 • Ю-5
5,4 • Ю-5
1,3 • Ю-6
2,0 • Ю-8
1,8 Ю-5
7,1 • Ю-5
4,8 • 10-"
1,6 • Ю-5
6,1 • Ю-2
8,9 • Ю-3
2,6 • Ю-17
г/л
5,1 • Ю-3
7,3 • 10-"
2,6 • Ю-3
5,1 • Ю-3
6,4 • Ю-4
1,3 • 10-"
1,79
11,07
1,1 • Ю-5
6,6 • Ю-2
3,6 • Ю-2
4,3 • Ю-2
1,9 • Ю-3
2,48
2,2 • Ю-2
1,59
3,6 • Ю-6
5,1 • Ю-2
9,07
3,3 • Ю-2
8,1 • Ю-3
2,1 • 10-"
4,3 • 10-6
2,7 • Ю-3
1,6 Ю-2
7,2 • Ю-2
6,7 • Ю-3
19,01
3,19
6,5 • Ю-15
599
V. Вещества в водном растворе
Продолжение табд.
UvU^ww 1 DvS
Ag2SO3
Ag2SO4
Ag2Se
Ag2SeO3
Ag2Se04
Ag2Te
Ag2WO4
AlAsO4
[AlFJ.Kj.
[AlF4],Na, ,
[AlF6],Na3
A1(OHK
Al(OH)f
A1O(OH)<3>
A1PO4
Am(OHK
Am(OHL
AuBr
AuBr34>
AuCl
AuCl<4>
[AuCl4],Cs
Aul
Aul^
Au2Of
[B(C6H5L],K
[BF4],Cs
[BF4],K
[BF4],Rb
[BH4],Cs
ПР
1,5 • 10-14
1.2-10-5
2,5 • Ю-59
3,1 • 10-16
1,2 • Ю-9
4,7 • Ю-52
5,6 • 10-12
1,6 -10-16
1,6-10-9
1,1 -ДО"8
7,8 • 104
5,7 • lO-32
3,7-Ю-15
1,0 • 10-48
1,7-10-19
2,7 • Ю-20
1,0 • 10-56
5,0 • 10-17
4,0 • 10-36
1,8 • 10~12
3,2 t Ю-25
l,0-10-3
1,6-Д0-23
1,0 -IO6
8,5 • 10-46
2,3 • 10-8
2,0 • Ю-5
2,0 • Ю-3
l,0-10-3
2,5 • 10-7
рПР
13,82*
4,92
58,60
15,51
8,92
51,33
11,25
15,80*
8,80*
7,95
13,11
31,24
14,43
48,00
18,77
19,57*
56,00*
16,30*
35,40*
11,75
24,50*
3,00*
22,80*
46,00*
45,07
7,64*
4,70*
2,70*
3,00*
6,60*
Растворимость
моль/л
l,6 10-5
1,4-10-2
1,8-10-2°
4,3 • Ю-6
6,7 • Ю-4
4,9 • Ю-18
1,1 • 10-4
1,3 10-8
2,8 • Ю-3
1,0 10-4
2,3 • 10-4
6,8 • Ю-9
6,1 • 10-8
4,4 • 10-13
4,1 • 10-10
5,6 • 10-6
2,1 • 10-12
7,1 • 10-9
2,0 • 108
1,3 • 10-6
5,7 • 10-13
3,2 • 10-2
4,0 • 10-12
1,0 • Ю-23
1,2 • 10-12
1,5-10-4
4,5 • Ю-3
4,5 • 10-2
3,2 • 10-2
5,0 • 10-4
Г/Л
4,6 • Ю-3
4,50
5,4-10-18
1,5-Ю-з
2,4 • 10-'
1,7 • 10-15
5,2 • Ю-2
2,1 • 10-*
7,2 • 10-'
1,3 • 10-2
4,9 • 10-2
5,3 • 10-7
4,7 • 10-6
2,6-10-11
5,0 • 10-8
1,7 • Ю-3
6,5 • 10-10
2,0 • 10-6
8,7 • 10-16
3,1 • 10-4
1,7 ¦ 10-'°
14,92
1,3-10-9
5,8 • Ю-2'
5,2 • 10-10
5,4 • 10-2
9,8 • 10-'
5,63
5,45
7,4 • Ю-2
600
V. Вещества в водном растворе
Продолжение табл.
Rpjiipptro
[ВН4],К
[BH4],Rb
Ba3(As04J
Ва(ВЮ3J
BaCO3
BaC2O4
ВаСгО4
BaF2
Ва(Ю3J
BaMnO4
ВаМоО4
Ва2Р2О7
Ва3(РО4J
Ba(PO3F)
BaSO3
BaSO4
Ba(SO3S)
BaSeO3
BaSeO4
BaWO4
Be(OHJ
Be(OHJ6>
Be2SiO4
BiAsO4
Bi2(C2O4K
Bi(Cl)O<7>
Bil3
Bi2O<8>
Bi(OHK
BiO(OH)<3>
ПР
1,3-10-3
2,5 • 10-"
7,8 • 10-51
3,3 • Ю-5
4,9 • Ю-9
1,1 • Ю-7
1,1 • 10-10
1,7-10-6
6,5 • 10-10
2,5 • 10-10
4,9 • 10-9
3,0-10-"
6,0 • Ю-39
4,0 • 10^7
3,3-10-"
1,8 • 100
1,6-10-5
3,1 • 10-7
3,1 • 10-8
1,8 • Ю-9
8,0 • Ю-22
2,1 • Ю-30
6Д1О-
4,4 • 10-'°
4,0 • 10-36
3,4 • 10-36
8,1 • 10-19
5,0 • 10-79
3,0 • Ю-36
4,0 • 10-"°
рПР
2,89*
3660*
50,11*
4,48
8,31
6,96
9,96
5,77
9,19
9,60
8,31
10,52*
38,22*
6,40*
10,48*
9,74'
4,80*
6,51
7,51
8,74
21,10
29,68
42,22
9,36
35,40*
35,47
18,09*
78,30
35,52
39,40
Растворимость
моль/л
3,6 • Ю-2
1,6 • Ю-2
3,7 • 10-"
2,0 • Ю-2
7,0 • Ю-5
3,3 • 10-"
1,0 • Ю-5
7,6 • Ю-3
5,5 • 10-"
1,6 40-*
7,0 • Ю-5
2,0 • 10-"
8,9 • Ю-9
6,3 • 10-"
5,7 • Ю-6
1,3 • Ю-5
4,0 • Ю-3
5,6 ¦ 10-"
1,8 • 10-"
4,2 • Ю-5
5,9 • №-«
1,4-lO4'5
5,3-10-15
2,1 • lO-5
3,3 • 10-8
9,6 ¦ W-10
1,3 Ч05
4,2 • 102
5,8 • 10-10
6,2 10-"
Г/Л
1,94
1,59
2,6 • 10-8
7,94
1,4-Ю-2
7,5 • Ю-2
2,6 • Ю-3
1,33
2,7 • 10
4,1 • lO-3
2,1 • lO-2
8,8 • Ю-2
5,4-10^
1,5 • 10-1
1,2-Ю-з
ЗД-10-3
1,00
1,5-10-1
5,0 • Ю-2
1,6-Ю-2
2,5 • 10~6
6,2 • 10-14
5,9 • 10-13
7,3 • Ю-3
2,2 • lO-5
2,5 • 10~7
7,8 • lO-3
2,0-10-9
1,5 • 10-7
1,5-1O-8
601
V. Вещества в водном растворе
Продолжение табл.
Вршество
BiPO4
Bi2S3
Bi2Se3
Bi2Te3
Ca3(As04J
CaCO3
CaC2O4
CaF2
CaHPOf
Ca(H2PO4)^'°>
Ca(IO3J
CaMg(CO3)<">
CaMoO4
Ca(OHJ
Ca2P2O7
Ca3(PO4J
Ca(PO3F)
CaSO3
CaSO4
CaSeO3
Ca2SiO4
CaWO4
Cd3(AsO4J
Cd(CNJ
CdCO3
CdC2O4
Cd(OHJ
Cd(OHJ(aмopфн.)
CdS
CdSe
CdSeO3
ПР
1,0-10-23
8,9 • 10-'05
2,0 • 10-'2'
2,5 • 10-'43
6,8 • 10-'»
4,4 • 10-9
2,3 • 10-»
4,0-10-"
2,2 • 10-7
1,0 • Ю-3
1,9 • 10-6
3,6 • 10-'6
3,2 • 10"»
6,3 • 10
1,5-10-'7
l,0-10-25
4,0 • Ю-3
3,2 • 10-7
3,7 • Ю-5
4,7 • 10-6
1,2 • 10-'2
1,6 • 10-»
2,2 • lO-33
1,0 • 10-8
2,5 • 10-'4
l,5-10-8
4,3 • 10-'5
2,2 • 10-'4
6,5 • Ю-2»
1,1 • lO-33
5,0 • 10-»
рПР
22,98
104,05
120,70
142,60
18,17*
8,36
8,64*
10,40
6,66
3,00*
5,72
15,44
8,49
5,20
16,82
25,00
2,40*
6,49*
4,43
5,33*
11,92
8,80
32,66*
8,00*
13,60
7,82*
14,37
13,66*
27,19
32,96
8,30*
Растворимость
моль/л
3,2 • Ю-'2
6,1 • Ю-22
2,8 • Ю-25
1,2 • Ю-2»
9,1 • Ю-5
6,6 • Ю-5
4,8 • Ю-5
2,1 • Ю-4
4,7 • Ю-4
6,3 • Ю-2
7,8 ¦ Ю-3
9,8 • Ю-5
5,6 • Ю-5
1,2-10-2
1,6 Ю
3,9 • Ю-6
6,3 ¦ Ю-2
5,7 • 10
6,1 • Ю-3
2,2 • Ю-3
6,7 ¦ Ю-5
4,0 • Ю-5
1,2-Ю-7
1,4 • Ю-3
1,6 • Ю-7
1,2 • 10
1,0 • Ю-5
1,8 • Ю-5
2,5 • Ю-'4
3,3 • Ю-'7
7,1 • Ю-5
г/л
9,8 • 10-'°
3,1 • Ю-'9
1,9 • Ю-22
9,5 • 107
3,6 • Ю-2
6,6 • Ю-3
6,1 • Ю-3
1,7 • Ю-2
6,4 • Ю-2
14,74
3,06
1,8 • Ю-2
1,1 • Ю-2
8,6 • Ю-1
3,9 • Ю-4
1,2 • Ю-3
8,73
6,8 • Ю-2
8,3 • 10"'
3,6 • 10-'
1,2-10-2
14 • Ю-2
7,1 • Ю-5
2,2 • 10"'
2,7 • Ю-5
2,5 • Ю-2
1,5 • Ю-3
2,6 • Ю-3
3,7 • Ю-12
6,2 • Ю-15
1,7-10-2
602
V. Вещества в водном растворе
Продолжение табл.
Bpiiipptro
CdTe
CdWO4
Ce2(C2O4K
CeF3
Ce(IO3K
Ce(IO3L
СеО<|2>
Ce(OHK
CePO4
Co3(AsO4J
[Co(CNN],Ag'
CoCO3
CoC2O4
(Co^o^oy3'
Co(IO3J
[Co(NO2N],Cs3
[Co(NO2N],K3
[Co(NO2]6, (NH4K
[Co(NO2N],Rb3
[Co(NO2N],Tl'
CoO<14>
Co2O3 • 3H2O<15>
Co(OHJ
CoO(OH)B9>
CoS
Co(S2)
CoSeO3
CoWO4
CrAsO4
(Cr2Fe")O416)
Cr2Of>
ПР
8,7 • 10-35
2,0 • Ю-6
2,5 • 10-29
3,2 • 10-'7
3,5 • 10-10
5,0 • 10-'7
9,1 • Ю-23
6,4 • Ю-22
5,1 • Ю-22
7,6 • 10-29
3,9 • 10-26
1,5 10-10
6,3 • 10-8
7,1 • 10-100
1,0-ИН
5,8 • 10-16
4,3 • 100
7,6 • Ю-6
1,5 • 10-15
1,0-Ю-'6
4,3 • 10-15
5,0 • 10-72
1,6 • 10-15
2,5 • 10-
1,8-10-2°
7,3 • Ю-29
1,6- 10-7
3,6 ¦ 10-'°
7,8 • 10-21
3,4 • 10-96
2,7 • 10-7"
рПР
34,06
5,70*
28,60
16,50
9,46
16,30*
22,04
21,19
21,29
28,12*
25,41*
9,82
7,20*
99,15
4,00*
15,24*
9,37*
5,12*
14,82*
16,00*
14,37
71,30
14,80
42,60
19,75
28,14
6,80*
9,44
20,11*
95,47
73,57
Растворимость
моль/л
9,3 • Ю-18
1,4 Ю-3
7,5 • Ю-7
3,3 • 10
1,9-Ю-з
1,8 • 10-"
1,3 • Ю-5
2,2 • Ю-6
2,3 • Ю-11
9,3 ¦ 10-7
1,9 • 10-7
1,2 • Ю-5
2,5 • 10-"
6,6 • 10-6
2,9 • Ю-2
6,8 • Ю-5
2,0 • Ю-3
2,3 • Ю-2
8,6 • lO-5
4,4 • Ю-5
1,0 Ю-5
3,3 • 10-"
7,3 • Ю-6
9,8 ¦ 10-12
1,3-10-19
8,5 • 10-15
4,0 • 10-"
1,9 Ю-5
8,8-10-"
1,4-10-5
8,9 • 10-20
Г/Л
2,2 • 10-'5
5,1 • 10-1
4,1 • 10-"
6,5 • Ю-3
12,62
1,5 • 10-'
2,2 • Ю-3
4,2 • 10-"
5,3 • 10-9
4,2 ¦ 10-4
1,1 • 10""
1,4 • Ю-3
3,7 • lO-2
1,6 • Ю-3
11,95
5,0 • Ю-2
9,0 • 10-'
8,96
5,1 • lO-2
4,2 • 10-2
7,7 • 10""
7,2 • 10-17
6,8 • 10-"
9,0 • 10-'°
1,2 • 10-8
1,1 • 10-'2
7,4 ¦ lO-2
5,8 • Ю-3
1,7 • 10-8
3,2 • lO-3
1,4- 10-17
603
V. Вещества в водном растворе
Продолжение табл.
R Р Н1PPTRO
Cr(OHJ
Сг(ОНK
Сг(ОНK(аморфн.)
Сг(ОНK2)
СгРО4
CrS
CsBrO3
CsC104
CsIO3
CsIO4
CsMnO4
CsReO4
Cu3(As04J
CuBr
CuCN
CuCO3
CuC2O4
Cu2CO3(OHJ
CuCl
Cu"CrO4
Cul
Cu(IO3J
Cu"MoO4
Cu'N3
Cu(N3J
CuNCS
CuO<14>
Cu2O<'>
Cu(OHJ
CuS
Cu2S
ПР
9,7 • 10"'8
7,4 • 10-31
1,1 • Ю-30
1,0 • 10-16
1,0 • 10-"
2,0 • 10-'8
2,0 • Ю-2
4,0 • Ю-3
1,0-10-2
4,4 • JO
9,1 • Ю-5
4,0 • 10-4
7,6 • lO-36
6,6 • 10-9
3,2 ¦ Ю-20
2,4 • Ю-10
2,9 • 10-8
7,8 • 10-34
2,2 • 10-'
3,2 • 10-6
1,1 -10-12
1,4-10-'
1,6-10"9
5,0-10-9
6,4 • 10-10
4,8f-10-15
4,8-10-2'
1,2'10-15
5,6 • Ю-20
1,4-10-36
2,3 • 10-48
рПР
17,01
30,13
29,96
16,00
17,00*
17,70*
1,70*
2,40*
2,00*
2,36*
4,04*
3,40*
35,12*
8,18
19,50*
9,62
7,54
33,11
6,66
5,49
11,96
6,85
8,80
8,30*
9,19*
14,32*
20,32
14,92
19,25
35,85
47,64
Растворимость
моль/л
1,3-Ю-6
1,3 • Ю-8
1,4 • 10"8
1,0-Ю"8
3,2 • 10"9
1,4 • 10-9
1,4 • 10
6,3 • Ю-2
1,0-10-'
6,6 • Ю-2
9,5 • Ю-3
2,0 • Ю-2
3,7 • 10-8
8,1 • Ю-5
1,8-Ю-10
1,5 • Ю-5
1,7 • 10
1,4-10-'
4,7 • 10-4
1,8 • Ю-3
1,0 -10-6
3,3 • Ю-3
4,0 • Ю-5
7,1 • Ю-5
5,4 • 10-4
6,9 • 10-8
1,1 • 10-'
1,7 • 10-8
2,4 • 10-'
1,2-10-'8
8,3 • 10-"
Г/Л
2,1 • 10-4
1,3 • 10-6
1,5 • 10~6
1,0 • 10-*
4,6 • 10-'
1,2-10-'
36,88
14,70
30,78
21,48
2,40
76,62
1,7 ¦ Ю-5
1,2 -Ю-2
1,6 • 10-8
1,9-Ю-3
2,6 ¦ Ю-2
3,0 • lO-5
4,7 • lO-2
3,2 • 10-'
2,0 ¦ 10-4
1,35
8,9 • Ю-3
7,5 • lO
8,0 • lO-2
8,4 • 10-6
8,5 • 10-6
2,4 • 10-6
2,4 • Ю-5
1,1 • 10-'6
1,3 • 10-14
604
V. Вещества в водном растворе
Продолжение табл.
Вещество
CuSe
Cu2Se
CuSeO3
Cu"WO4
DyAsO4
DyF3
ErF3
EuF3
Eu(OHK
FeAsO4
[Fe(CNN],Ag3
[Fe(CNN],Ag4
[Fe(CNN],Ba2
[Fe"(CNN],KFe<27)
FeCO3
FeC2O4
(F^'Fey^Of)
Fe"MoO4
FeO<14>
Fe2O3'9>
Fe2O3 • 3H2O<20>
Fe(OHJ
FeO(OH)<3>
Fe(OH)(aM.)C)
FePO4
FeS
Fe(S2)
FeSe
Fe2"(Se03K
Fe2SiO4
FeWO4
ПР
4,5 • 10-
1,1 • Ю-5'
1,7-10-*
1,0-Ю-5
1,5 • Ю-2"
5,0 • 10-'6
1,6 • 10-'5
3,2 • 10-16
2,8 • Ю-27
5,8 • Ю-2'
1,0 • Ю-22
8,5 • lO-45
3,0 • 10-8
9,7 • lO-2»
2,9-lO^n
2,1 • Ю-7
5,7 • 10-71
2,0 • Ю-8
4,3 • 10-'5
4,1 • 10-60
1,2 • lO-50
7,9 • 10-'6
2,2 • 10-
6,3 • 10-38
1,1 • 10-26
3,4 • 10-17
5,4 • lO-27
1,8-10-2°
2,0 • 10-31
3,7 • 10-30
6,1 • 10-12
рПР
41,35
50,96
7,77*
5,00*
23,82
15,30
14,80
15,50
26,55
20,24*
22,00*
44,07*
7,52*
19,01*
10,54
6,68
70,24
7,70
14,37
59,39
49,92
15,10
41,66
37,20*
25,96
16,47
26,27
19,75
30,70*
29,43
11,22
Растворимость
моль/л
2,1 • Ю-21
6,5 • 10-i«
1,3 • 10-"
3,2 ¦ Ю-3
1,2-Ю-'2
6,6 • Ю-5
8,8 • Ю-5
5,9 • Ю-5
1,0 • 10^7
7,6 • Ю^1
1,4 Ю-6
5,1 • 10-ю
2,0 • Ю-3
4,6 • Ю-7
5,4 • Ю-6
4,6 ¦ 10-"
4,1 • 10"9
1,4-10-"
1,0 ¦ Ю-5
5,0 • 10-21
7,2 • 10^18
5,8 • Ю-6
1,7-Ю-ч
2,2 • Ю-'0
1,0 • 10чШ
5,8-Ю-9
7,3 • Ю-14
1,3 10-ю
2,8 • Ю-7
9,7-10-и
2,5 • Ю-6
г/л
3,0 • 10-19
1,3 • Ю-15
2,5 • Ю-2
9,8 • 10-1
3,7 • 10-'°
1,4 • Ю-2
2,0 • Ю-2
1,2 • Ю-2
2,1 ¦ Ю-5
1,5 • Ю-8 •
7,4 • 10-"
3,3 • Ю-7
9,5 • Ю-1
1,4-10-"
6,2 • 10-"
6,6 • Ю-2
9,4 • Ю-7
3,1 • Ю-2
7,4 • Ю-4
8,1 • Ю-19
1,5 • 10-15
5,2 • 10-"
1,5 • Ю-9
2,0 • Ю-8
1,6 • 10-"
5,1 ¦ Ю-7
8,8 • 10-12
1,8 -Ю-8
1,4 • 10-"
2,0 • Ю-8
7,5 • 10-"
605
V. Вещества в водном растворе
Продолжение табл.
RPIMPPTRO
Ga(OHK
Ga(OH)<2>
GaPO4
GdF3
[GeF6],K2
P-GeO<'2)
GeS
HfF4
[HfF6],K2
НГО<12>
Hf2(aMop<Jm.)B1)
НГО(ОНJ22>
Hg2Br210>
Hg2(CH3COOJ10>
Hg2(CN)f>
Hg2CO3»>
Hg2C2O4»>
Hg2Cl<l0>
Hg2Cr04»>
Hg2HPO4»>
Hg2lf>
Hg2(IO3)$10>
Hg2(NCSJ10>
[Hg(NCSL],Co"
[Hg(NCSL],Zn»
HgO<14>
HgO + Hg<23>
P-HgS
P-HgS + Hg<24>
Hg2SO<»>
ПР
4,1 ¦ 10-36
2,9 • 10-"
3,8 • 10-21
6,3 • 10-'8
3,0 ¦ Ю-5
6,2 ¦ Ю-21
3,0 • Ю-35
3,0 • Ю-25
2,0 • Ю-3
1,2 • 10-64
4,0 • 10-26
1,3-10-2»
7,9 • Ю-23
2,0 • 10-'5
5,0 • 100
8,9 • 10-'7
2,0 • 10-'3
1,5-10-18
1,6 • 10"»
4,0 • 10-'3
5,4 • Ю-2»
2,5 • 10-'4
3,0 • Ю-20
1,5 • 10
2,2 • 10-7
3,3 • Ю-2*
2,7 • 10-24
1,4 -10-45
1,1 • 1O-43
1,0 • 107
оПР
35,39
10,54
20,42
17,20
4,52*
20,21
34,52*
24,52
2,70*
63,92
25,40*
28,89
22,10
14,70
39,30
16,05
12,70
17,82
8,80
12,40*
28,27
13,60*
19,52
5,82*
6,66*
25,48
23,57
44,85
42,96
27,00*
Растворимость
моль/л
6,3 • Ю-10
5,3 • Ю-6
6,2 • 10-"
2,2 • Ю-5
2,0 • Ю-2
3,0 • Ю-5
5,5 • Ю-18
4,1 • Ю-6
7,9 • Ю-2
5,4 • Ю-14
2,2 • 10"»
5,5 • Ю-7
2,7 • Ю-8
7,9 • 10-«
5,0 • Ю-14
9,4 • 10"»
4,5 • Ю-7
7,2 • Ю-7
4,0 • Ю-5
6,3 • Ю-7
2,4 • Ю-10
1,8 • Ю-5
2,0 • Ю-7
1,2-10-з
4,7 • 10
2,0 • 10-»
8,7 • 10-»(HgO)
3,7 • Ю-23
3,3 • 10-22(HgS)
3,2 • Ю-'4
г/л
7,5 • Ю-8
6,4 • Ю-4
1,0 • Ю-8
4,7 • Ю-3
5,18
3,1 • Ю-3
5,7 • Ю-16
1,0 • Ю-3
29,42
1,1 10-"
4,5 • 10
1,3 Ю-4
1,5 • Ю-5
4,1 • Ю-3
2,3-10-"
4,4 • Ю-6
2,2 • Ю-4
3,4 • Ю-4
2,1 • Ю-2
3,1 • Ю-4
1,6-Ю-7
1,4-Ю-2
1,0 • Ю-4
6,0 • Ю-1
2,3 • 10-'
4,4 • Ю-7
l^-lO-^HgO)
8,7 • Ю-21
7,7 • 10-2°(HgS)
1,5-10-"
606
V. Вещества в водном растворе
Продолжение табл.
nI . V >
Rpi IIPPTRO
Hg2SOf
HgSe
Hg2SeO39>
Hg2WOf
HoF3
In(OHK
In2S3
In2Se3
[IrCy,K2
[IrCl6],(NH4J
юр
ir2oy7>
Ir(OH)f»
IrS<26>
KC1O4
KIO4
KReO4
LaAsO4
La2(CO3K
La2(C2O4K
LaF3
La(IO3K
La2(MoO4K
La(OHK
Ьа(ОНK(аморфн.)
LaPO4
La2S3
La2(SO4K
Li2CO3
LiF
ПР
6,2 ¦ Ю-7
2,4 • 10-61
6,3 • 10-'5
1,1 • 1017
6,3 • 10-15
1,3 • 10-37
9,1 • 10-84
5,6 • Ю-92
6,8 • Ю-5
3,0 • Ю-5
1,6 • 10-72
2,0 • 10-48
1,6 • 10-72
1,0 • 105
1,0 • Ю-2
8,3-10^
1,9 Ю-3
3,6 • Ю-22
4,0 • IO-34
2,0 • Ю-28
6,3 • 10-16
6,2 • 10-12
8,2 • Ю-22
3,6 • 10-23
6,5 • Ю-2»
6,9 • Ю-24
5,3 • 10-27
3,0 • Ю-5
1,9 • Ю-3
1,5- Ю-3
рПР
6,21
60,62
14,20*
16,96*
14,20
36,89
83,04
91,25
4,17*
4,52* .
71,80
47,70*
71,80*
75,00*
2,00*
3,08*
2,72*
21,44
33,40*
27,70*
15,20
11,21
21,09
22,44
19,19*
23,16
26,28 ,
4,52*
2,72
2,82
Растворимость
моль/л
7,9 • 10-"
4,9 • Ю-31
7,9 • Ю-8
3,3 • Ю-9
1,2-Ю-4
2,6 • Ю-10
9,7 • Ю-18
2,2 • Ю-19
2,6 • Ю-2
2,0 • Ю-2
1,4-Ю-15
2,6 ¦ Ю-13
1,4 - 10-15
6,3 • 106
1,0 -10-'
2,9 • Ю-2
4,4 • Ю-2
1,9-10-"
8,2 • Ю-8
1,1 • Ю-6
7,0 • Ю-5
6,9 • Ю-4
2,4 • Ю-5
1,1 • Ю-6
7,0 • Ю-6
2,6 • Ю-12
2,2 ¦ Ю-6
4,9 • Ю-2
7,9 • Ю-2
3,8 • Ю-2
г/л
3,9 • 10"'
1,4 • Ю-28
4,2 ¦ Ю-5
2,2 ¦ Ю-6
2,7 • Ю-2
4,4 • Ю-8
3,1 • Ю-15
1,0 • Ю-16
12,42
8,63
3,2 • Ю-13
1,1 • Ю-10
3,8 • Ю-13
1,6-Ю-23
13,86
6,63
12,61
5,3 • Ю-9
3,8 • Ю-5
6,1 • 10-"
1,4 • Ю-2
4,6 • Ю-1
1,8 Ю-2
2,0 • Ю-4
1,3 • Ю-3
6,1 • 100
8,1 • 10-"
27,64
5,81
9,9 • 10-'
607
V. Вещества в водном растворе
Продолжение табл.
RPIIIPPTRO
Li3PO4
LuF3
Lu(OHK
Mg3(As04J
MgCO3
MgC2O4
MgF2
Mg(IO3J
MgNH4PO428>
Mg(OHJ
Mg(OHJ(aмopфн.)
Mg3(PO4J
MgSO3
MgSeO3
MgWO4
Mn3(As04J
MnCO3
MnC2O4
(MnnMn2n)O4'3>
MnuMoO4
MnO<I4>
MnO<12>
МпО2(аморфн.)A2)
Mn2O<5>
Mn2O3 • 3H2O<15>
Mn(OHJ
MnO(OH)B9)
Mn3(PO4J
MnS
Мп5(аморфн.)
ПР
3,2- 10"9
4,0- 10"l5
1,0- 10-2b
2,1 10-20
7,9-10
8,6- Ю-5
6,4-10-9
3,0- 10"'3
2,5- 10-'3
6,8- 102
6,0- 1010
3,9-106
3,0-10
4,4- 10
3,6 Ю-7
1,9- 10-29
4,9- 10-"
5,0- 10-6
9,4- 10"I01
1,2 10
1,5 • 1010
1,0-10-56
1,0-10-5°
1,2-10-84
2,5- 10-7!
2,3-10-'3
1,0-106
1,7- 10-23
1,1-10-'3
2,5 10-'°
рПР
8,49*
14,40
26,00
19,68*
5,10
4,07*
8,19
12,52*
12,60
11,17
9,22*
25,41
2,52*
5,36*
6,44
28,72*
10,31
5,30*
100,03
3,92
9,82
56,00
50,00*
83,92
70,60
12,64
36,00
22,77
12,96
9,60*
Растворимость
моль/л
3,3-Ю-3
1,1 • 10
1,4- Ю-7
4,5- Ю-5
2,8- 10
9,3- 10-3
1,2 -Ю-3
4,2- Ю-5
6,3 Ю-5
1,2- 104
5,3- 10
3,2- 10'6
5,5- Ю-2
2,1 10-3
6,0- 10
7,1- Ю-7
7,0- I0-6
2,2- 10
1,6 10-'°
1,1' Ю-2
3,3- 10
2,1 10"'2
3,3- 10""
2,2- Ю-22
4,9- 109
3,8- Ю-5
4,4- 10"'°
1,1 • Ю-5
з,з- ю-7
1,6 1O-5
Г/Л
3,8- 10-'
2,6 Ю-2
3,1 • Ю-5
1,6- Ю-2
2,4- 10-'
1,04
7,3- Ю-2
1,6-10-2
8,7- 10-3
6,9 10
3,1 • Ю-2
8,5 10-4
5,72
3,2- 10-'
1,6-10"'
3,1 • 10-4
8,0- 10-4
3,2- 10-'
3,6 10-8
23,54
2,4- Ю-2
1,8- 100
2,9 10-9
3,6- Ю-20
1,0- 10-I6
3,4- 10
3,9- 10-8
3,9- 10
2,9- Ю-5
1,4- 10
V. Вещества в водном растворе
Продолжение табл.
Вещество
Mn(S2)
MnSO3
MnSe
Mn"SeO3
Mn2Si04
MnTe
Mn"WO4
MoO<12>
NaIO4
Nb2OP»
Nd2(C2O4K
NdF3
Nd(OHK
Nd2S3
Ni3(AsO4J
[Ni(C4H7O2N2J]<31>
Ni(CNJ
NiCO3
NiC2O4
Ni(C103J
Ni(IO3J
NiO<14>
Ni(OHJ
NiO(OH)<29>
NiS
NiSeO3
Ni"WO4
NpO2(OHJI0>
Pb3(AsO4K
PbBr2
ПР
6,5 • 10-'5
2,6 • 10-7
5,4 • 10-'°
5,4 • 10-8
2,0 • 10-66
4,3- 10-"
3,2 • 10-8
1,0-lO0
3,0 • Ю-3
7,2 • 10-21
5,9 • 10-29
l,3-10-18
5,0 • 10-23
2,3 • 10-'7
3,1 • Ю-26
2,3 • Ю-25
3,0 • Ю-23
1,3-10-7
4,0 • 10-'°
1,0 10-4
1,4-10-8
1,7 • 10-16
1,6 • 10-'4
1,0-lO7
9,3 • lO-22
2,5 • Ю-6
7,9 • 10-'°
2,5 • Ю-22
4,0 • Ю-36
5,0 • 10-5
рПР
14,19
6,59*
9,27
7,27*
65,70
10,37
7,49
50,00*
2,52
20,14
28,23
17,89
22,30
16,64
25,51*
24,64*
22,52*
6,89
9,40*
4,00*
7,85*
15,77
13,80
37,00*
21,03
5,60
9,10
21,60*
35,40
4,30
Растворимость
моль/л
8,1 • Ю-8
5,1 • Ю-4
2,3 • Ю-5
2,3 • 10
7,9 • Ю-23
6,6 • lO-6
1,8 • 10-4
3,3-lO1
5,5 • lO-2
4,2-10-"
8,9 • 10-7
1,5-10-5
l,2-10-6
1.8-10-4
3,1 • Ю-6
3,9 • 10-9
2,0 • 10"8
3,6 • 10-4
2,0 • 10
2,9 • Ю-2
1,5-10-3
3,5 • Ю-6
1,6 10-5
2,5 • 10-'°
3,1- 10-"
1,6 Ю-3
2,8 • 10-5
4,0 • 10-8
3,3 • 10-8
2,3 • Ю-2
Г/Л
9,6 • lO-6
6,9 • Ю-2
3,1 ¦ Ю-3
4,2 • lO-2
1,6-10-2°
1,2 • Ю-3
5,4 ¦ lO-2
4,2 • 10-9
11,72
1,1 Ю-2
4,9 • 10
3,0 ¦ Ю-3
2,3 • 104
7,1 • Ю-2
1,4 Ю-3
1,1 • Ю-6
2,2 • Ю-6
4,3 • lO-2
2,9 • Ю-3
65,96
6,2 • 10-'
2,6 • 10-4
l,5-10-3
2,3 • 10-8
2,8 • 10-9
2,9 • 10"'
8,6 • 10
1,2- 10-5
2,9 • 10-5
8,52
609
V. Вещества в водном растворе
RpiMPPTRr)
' диГг tк ^*1*'_* 1 DV/
РЬ(ВЮ3J
РЬСО3
РЬС2О4
РЬ3(СО3J(ОН)<32>
РЬС12
Pb(Cl)F<33>
РЬ(С1)ОН<33>
РЬСгО4
PbF2
PbHPO4
Pbl2
Pb(IO3J
PbMoO4
Pb(N3J
Pb(NCSJ
PbO<14>
PbO<12>
Pb(OHJ
Pb(OH)<6)
Pb3(PO4J
(Pb^Pb^O,34)
PbS
PbSO4
Pb2(SO4)O • H2O<35>
Pb(SO3S)
PbSe
PbSeO3
PbSeO4
PbTe
PbWO4
PdBr2
ПР
1,6 Ю-4
3,6 • 10-14
7,3-10-11
1,5 • 101
1,7-10-5
2,5 - 10-9
2,0 - 10-14
2,8 • 10-13
2,7 • 10-8
4,0 - 10-12
8,7 • 10"9
2,6 • 10-13
8,5 • 10-16
2,6 • 10"9
2,0 • 10-5
3,8 • 10-16
3,0 • 10-66
5,5 • 106
l,2-10-20
7,9 • 10-43
5,3 - 101
8,7 - 109
1,7 • 10"8
1,5-103
4,0 • 10
6,5 • 10-37
3,0 • 10-12
1,5 10-7
4,1 • lO9
4,5 • 102
2,1 • 10-11
рПР
3,80
13,44
10,14
30,82
4,77
8,60
13,70*
12,55
7,57
11,40
8,06
12,59
15,07
8,59*
4,70*
15,42
65,52*
15,26
19,92
42,10*
50,28*
28,06
7,77
12,82
6,40*
36,19
11,52*
6,82
38,39
11,35
10,68
Продолжение табл.
Растворимость
моль/л
3,4 • 10
1,9-Ю-7
8,5 • Ю-6
1,7-10
1,6 Ю-2
1,3 Ю-3
2,7 • Ю-5
5,3 • Ю-7
1,9 Ю-3
2,0 • 10
1,3-Ю-3
4,0 • 10
2,9 - Ю-8
8,7 • 10
1,7-Ю-2
4,6 • Ю-6
2,6 • Ю-14
5,2 - 10~6
1,1 Ю-10
1,5 10"9
5,1 • 101
9,3 • Ю-15
1,3-10~4
1,6-Ю-3
6,3 • Ю-4
8,1-Ю-19
1,7-10
3,8 • 10
6,4-10-20
2,1 • 10
1,7- 10
г/л
15,83
5,1 • 10
2,5 • 10
1,3-10-2
4,50
3,5 • Ю-1
7,0 • Ю-3
1,7-Ю-4
4,6 • 10
6,1 • Ю-4
6,0 • 10
2,2 • Ю-2
1,1 • 10~5
2,5 • Ю-1
5,53
1,0-Ю-3
6,2 - Ю-12
1,2-10
2,6 - Ю-8
1,2-Ю-6
3,5 • 10"8
2,2 • 10~12
4,0 • Ю-2
8,5 • 10
2,0 • 10
2,3 • 10~16
5,8 • 10
1,3- 10
2,2 • Ю-17
9,6 • 10
4,6 • Ю-2
610
V. Вещества в водном растворе
Продолжение табл.
<
RpillPPTRn
[Pdcy.Kj
[PdCl6],K2
Pd0("t)
PdO<12>
Pd(OHJ
PdS
PoO(OH)<22)
PoS
Po(SO4J
PrF3
Pr(OHK
PtBr\25)
[Pt(CNL],Ba
[PtCl6],Cs2
[PtCl6],K2
[PtCl6],(NH4J
[PtCy,Rb2
[PtCy,Tl2
[PtF6],Cs2
[PtF6],K2
[PtF6],Rb2
PtO*12)
Pt(OHJ
PtS
PuF3
Pu(IO3L
РиО3(аморфн.)<10>
PuO2CO3
Pu(OHK
Pu(OHL
ПР
1,6-10-5
6,0 • 10-6
1,2-10-33
6,5 • 10-71
1,2-Ю-29
7,5 • 10-48
6,3 • Ю-52
5,0 • Ю-29
2,6 • 10-7
1.0-10-17
1,6 10-20
3,0 • 10-41
4,0 • 10-3
3,0 • 10"8
1,1 • Ю-5
9,0 • 10-6
9,0 • 10"8
4,0 • 10-12
2,4 • 10-6
8,4 • 10-13
7,6 • 10-7
1,6-10-72
1,0 Ю-25
1,2-10-61
2,6 • Ю-9
5,0 • 10-13
3,2 • 10-21
1,7-10-13
2,0 • Ю-20
7,0 • 10-56
рПР
4,80*
5,22*
32,92
70,19*
28,92
47,13
51,20*
28,30*
6,59*
17,00
19,80
40,52*
2,40*
7,52*
4,96*
5,05*
7,05*
11,40*
5,62*
12,08
6,12*
71,80*
25,00
60,92
8,59
12,30*
20,50*
12,77*
19,70*
55,16
Растворимость
моль/л
1,6 • Ю-2
1,1 • Ю-2
6,7 • Ю-12
3,0 • Ю-15
1,4 Ю-10
2,7 • 104
1,9 10-"
7,1 • 10-'5
4,0 • 10-3
2,5 • Ю-5
4,9 • 10-6
2,6 • 10-9
6,3 • Ю-2
2,0 • 10-3
1,4 Ю-2
1,3-10-2
2,8 • 10-3
1,0 10-4
8,4 • 10-3
5,9 • Ю-5
5,7 • 10-3
1,4-Ю-15
2,9 • Ю-9
3,5 • 10-31
3,1 • 10-3
1,1 • 10-3
9,3 • 10-8
4,1 • 10-7
5,2 • 10-*
3,1 • 10-12
Г/Л
5,18
4,54
8,2 • 10-'°
4,2 • 10-13
2,0 • 10-8
3,8 • Ю-22
4,9 • Ю-9
1,7 • 10-12
1,61
4,9 • 10-3
9,5 • 10-4
1,3 • 10-6
27,61
1,32
6,81
5,82
1,63
8,2 • 10-2
48,49
2,3 • Ю-2
27,60
3,3 • 10-13
6,7 • 10-7
8,0 • Ю-29
9,4 • 10
1,08
2,7 • Ю-5
1,4 • 10-4
1,5 10-3
9,6 • 10-'°
611
V. Вещества в водном растворе
Продолжение табл.
Вещество
Ra(IO3J
RaSO4
RbBrO3
RbC104
RbIO4
RbMnO4
RbReO4
Re2S<736>
Rh(OHK
RuO<12>
Ru(OHK
Sb2O<37>
Sb2Of>
[Sb(OHN],Na
Sb2S3
ScAsO4
Sc(OHK
[SiF6],Ca
[SiF6],Cs2
[SiF6],K2
[SiF6],Na2
[SiF6],Rb2
SmF3
[SnCl6],Cs2
Snl2
SnO<14>
SnOy2>
Sn(OHJ
Sn(OH)<6>
[Sn(OHN],Ca
ПР
8,8 • 10-10
4,3-10-11
2,0 • Ю-2
2,5 • 10
5,5 • 10
2,9 • 10
9,6 • 10-4
8,8 • 10-129
2,0 • 108
1,0 -10-49
1,0-lO8
4,0 • 102
1,4-10-17
4,0 • 10-8
2,2 • lO"90
1,9 -10-27
8,7 • 108
8,1 • 10-4
1,3 10-5
2,2 • 10-7
3,1 • 10-5
5,0 • 10-7
1,0-106
3,6 • 10"8
8,3 • 10
1,6 lO7
4,8 • 108
5,5 • 107
3,7 • 10-15
2,0 • 10-20
рПР
9,06*
10,37*
1,70*
2,60
3,26*
2,54*
3,02*
128,06
47,70*
49,00*
38,00*
41,40*
16,85*
7,40*
89,66
26,72
27,06
3,09*
4,89*
6,66
4,51
6,30*
16,00
7,44*
5,08*
26,80
57,32
26,26
14,43
19,70
Растворимость
моль/л
6,0 • Ю-4
6,5 • Ю-6
1,4-Ю-1
5,0 • 10
2,3 • Ю-2
5,4 • 10
3,1 • Ю-2
1,1 • Ю-15
5,2-103
5,2-Ю-11
1,4-Ю-10
9,8 • Ю-12
1,8-10"9
2,0-Ю-4
4,6 • Ю-19
4,4 • 104
7,5 • Ю-8
2,8 • 10
1,5 • Ю-2
3,8 • Ю-3
2,0 • Ю-2
5,0 • Ю-3
4,4- 10
2,1 • 10
1,3-10-2
7,4 • 100
1,1 • 102
1,1 • Ю-9
6,1 • Ю-8
1,4- 100
г/л
3,5 • Ю-1
2,1 • 10
30,18
9,25
6,48
11,01
10,40
6,7 • Ю-13
8,0 Ю-11
7,0 • 10"9
2,1 • Ю-8
2,9 • 10"9
5,4 • Ю-7
4,9 • Ю-2
1,6- 106
8,0 • 102
7,2 • Ю-6
5,18
5,98
8,4 • Ю-1
3,71
1,57
9,1 • Ю-3
1,24
4,75
9,9 • 10"8
1,7 -Ю-10
1,7 10
9,3 • Ю-6
3,7-Ю-8
612
V. Вещества в водном растворе
Продолжение табл.
RplllPPTRn
иСЛ-ЦСО 1 DVy
SnS
SnS2
SnSe
SnTe
Sr3(As04J
SrCO3
SrC2O4
SrCrO4
SrF2
Sr(IO3J
SrMoO4
Sr(OHJ
Sr3(PO4J
Sr(PO3F)
SrSO3
SrSO4
SrSeO3
SrSeO4
SrWO4
TbF3
TeO<'2>
Th(C2O4J
ThF4
Th(IO3L
Th(OHL
Th3(PO4L
Th(SO4J
[TiF6],K2
[TiF6],Rb2
TiO<2'>
TiO(OHJ22>
ПР
1 ll
3,0 • Ю-28
2,3 • Ю-58
1,2 • 10-34
3,6 • 10-37
1,3-10-18
5,3 • 10-'°
5,6 • 10-8
2,7 • Ю-5
2,5 • 10-9
3,3 • 10-7
1,6-10-7
3,2 • 10-4
1,0 • 10-31
3,0 • 10-3
6,7-10-"
2,1 • 10-7
1,0 10-6
2,5 • Ю-5
7,1 • 10-9
7,9 • 10-17
3,0 • 10-54
2,0 • Ю-5
5,0 • 10-26
2,5 • 10-'5
7,7 • 10-44
2,6 • 10-79
4,0 • 10-3
5,0 • 10-4
5,5 • Ю-5
1,0 10-29
6,3 • Ю-52
рПР
27,52
57,64
33,92
36,44
17,89*
9,28
7,25*
4,57
8,60
6,48*
6,80
3,49*
31,00*
2,52*
10,17*
6,68
6,00
4,60
8,15
16,10
53,52*
4,70
25,30*
14,60*
43,11
78,59*
2,40*
3,30*
4,26*
29,00*
51,20*
Растворимость
моль/л
1,7-Ю-14
3,9 • Ю-20
1,4-Ю-17'
6,0 • Ю-'9
1,0-Ю-4
2,3 • Ю-5
2,4 • 10
5,2 • Ю-3
8,6 • Ю-4
4,4 • Ю-3
4,0 • 10
4,3 • Ю-2
2,5 • Ю-7
5,5 • Ю-2
8,2 • Ю-6
4,6 • Ю-4
1,0 • Ю-3
5,0 • Ю-3
8,4 • Ю-5
4,1 • Ю-5
6,5 • Ю-12
1,7 • Ю-2
2,9 • Ю-6
4,0 • Ю-4
7,9 • Ю-10
1,7 ¦ Ю-12
1,0-10-'
5,0 • Ю-2
2,4 • Ю-2
1,4 10-'°
1,9-10-"
г/л
2,6 • Ю-12
7,1 • Ю-18
2,7 • Ю-'5
1,5 • Ю-16
5,6 • Ю-2
3,4 • Ю-3
4,2 • Ю-2
1,06
1,1 ¦ 10"'
1,90
9,9 • Ю-2
5,24
1,1 • Ю-4
10,16
1,4-Ю-3
8,5 • Ю-2
2,1 • 10-'
1,15
2,8 • Ю-2
8,9 • Ю-3
1,0 Ю-9
6,98
8,8 • Ю-4
3,7- 10"'
2,4 • Ю-7
1,8 • Ю-9
42,42
12,00
7,97
1,1-10-»
1,9 Ю-9
613
V. Вещества в водном растворе
Продолжение табл.
Вещество
Т1ВгО3
TIBr
Т12СО3
Т12С2О4
Т1С1
Т12СЮ4
тп
Т1Ю3
T1N3
T1NCS
Т12О^17>
Т13РО4
TlReO4
T12S
T12SO3
T12SO4
T12(SO3S)
Tl2Se
Tl2SeO4
Tl2Te
TmF3
UF4
uo2cof
UO2C2Of
(UO2)HAsO49>
(UO2)HPO49>
UO2(IO3J10>
U(OHL
UO2(OH)<'°>
(UO2K(PO4)<39>
ПР
3,9 • 10-4
4,3 • 10-6
4,0 • Ю-3
2,0 • 10-4
1,9 10-4
1,0 10-12
6,6 • 10-8
4,5 • 10-6
2,2 • 10-4
5,8 • 10-4
2,0 • 10-44
6,7 • 10-8
1,2 Ю-5
3,0 • 10"9
6,3 • 10-4
1,5 • 10-4
2,0 • 10-7
2,4 • 102
1,0 • 10-4
4,5 • 10-41
7,9 • 10-16
6,0 • 10-22
6,3 • 10-15
2,0 • 10-4
3,2 10-11
2,1 • 10-11
3,0 • 10-8
1,0 • 10-45
2,0 • 10-15
2,2 • 10-47
рПР
3,41
5,37
2,40*
3,70*
3,72
12,00
7,18
5,35
3,66*
3,24*
43,70
7,17*
4,92*
8,52
3,20*
3,82
6,70*
21,62
4,00
40,35
16,10
21,22*
14,20
3,70*
10,50*
10,68*
7,52*
45,00*
14,70
46,66
Растворимость
моль/л
2,0 • 10
2,1 • Ю-3
1,0 • Ю-1
3,7 • Ю-2
1,4-Ю-2
6,3 • Ю-5
2,6 • Ю-4
2,1 • Ю-3
1,5-Ю-2
2,4 • Ю-2
2,6 • Ю-12
7,1 • Ю-3
3,5 • Ю-3
9,1 • Ю-4
5,4 • Ю-2
3,4 • Ю-2
3,7 • Ю-3
3,9 • Ю-8
2,9 • Ю-2
2,2 • Ю-14
7,4 • Ю-5
1,9 Ю-5
7,9 • Ю-8
1,4 • Ю-2
5,7 ¦ Ю-6
4,6 • Ю-6
2,0 • Ю-3
3,3 • Ю-10
7,9 • Ю-6
1,8-Ю-10
г/л
6,56
5,9 • 10-'
46,88
18,30
3,31
3,3 • Ю-2
8,5 • Ю-2
8,0 • 10
3,65
6,32
1,2 • Ю-9
5,00
1,57
4,0 ¦ Ю-1
26,40
16,97
1,92
1,9 Ю-5
16,11
1,2-Ю1
1,7 • 10
5,9 • Ю-3
2,6 • Ю-5
5,06
2,4 • Ю-3
1,7 • Ю-3
1,21
1,0 • Ю-7
2,4 • Ю-3
1,8 • Ю-7
614
V. Вещества в водном растворе
Окончание табл.
Вещество
vo<14>
vo<4°)
V2O<17>
V2O5 • 3H2O<41>
VO(OH)<10>
(VOK(PO4)<39>
WO У 2)
Y(OHK
YbC2O4
YbF3
Zn3(AsO4J
Zn(CNJ
ZnCO3
ZnC2O4
Zn(IO3J
Zn"MoO4
ZnO<14>
Zn(OHJ
Zn(OH)^6>
Zn3(PO4J
a-ZnS
P-ZnS
ZnSe
ZnSeO3
ZnTe
[ZrFJ.Kj
ZrO<12>
ZrO<2')
ZrO(OH)P>
ZrSiO<42>
ПР
5,4 • 10-20
1,5 10-24
5,3 • 10-75
1,6 - 10-'5
7,1 • 10-23
8,0 • 10-25
l.O-lO-50
3,2 • 10~25
4,5 • 10-25
5,0 • 10-16
1,3 10-27
2,6 • 10-13
5,3 10-"
1,4- 10-9
2,0 • 10-8
3,3 • Ю-5
2,2 • 10-17
3,0 • 10-'6
3,1 • 10-15
9,1 • 10-33
1,2 10-25
7,9 • 10-24
4,7 • 10-27
1,9 • 10-8
7,0 • 10-26
5,0-10-4
1,4-10-64
1,1 • 10-36
1,0 10-31
8,3 • 100
рПР
19,27
23,82
74,28
14,80*
22,15
24,10*
50,00*
24,50
24,35
15,30
26,89*
12,59*
10,28
8,85
7,70*
4,48
16,66
15,52
14,51
32,04*
24,92
23,10
26,33
7,72*
25,16
3,30*
63,85
35,96
31,00
29,08
Растворимость
моль/л
2,4 • Ю-7
7,2 • Ю-9
1,2-10-"
4,4 • Ю-5
2,6 ¦ Ю-8
5,9 • Ю-6
3,3-Ю-11
3,3 • Ю-7
6,7 • Ю-13
6,6 • Ю-5
1,6 • Ю-6
4,0 • Ю-5
7,2 • Ю-6
3,7 • Ю-5
1,7 • Ю-3
5,7 • Ю-3
1,8 • Ю-6
4,2 • 10
5,6 • Ю-8
1,5 Ю-7
3,5 • Ю-13
2,8 • Ю-12
6,9 • Ю-'4
1,4-Ю-4
2,6 • Ю-13
5,0 • Ю-2
5,6 • Ю-14
6,5 • Ю-13
2,1 • Ю-7
2,9 • Ю-15
г/л
1,6 • Ю-5
6,0 • Ю-7
1,8 • 107
1,0-10-2
2,6 • Ю-6
2,3 • Ю-3
7,1 • 10"9
4,6 • Ю-5
1,8 • Ю-10
1,5 • Ю-2
7,8 • Ю-4
4,7 • Ю-3
9,1 • Ю-4
5,7 • Ю-3
7,1 • Ю-1
1,29
1,4-Ю-3
4,2 • Ю-4
5,5 • Ю-6
5,9 • Ю-5
3,4-10-"
2,7 • Ю-10
9,9 • Ю-12
2,7 • 10
5,1 • Ю-11
14,17
6,9 • Ю-12
8,0- 10-"
2,9 • Ю-5
5,3 • Ю-13
615
V. Вещества в водном растворе
0,5М2О(т) + 0,5Н2О
М(ОНK(Т) + 2Н2О
МО(ОН)(Т) + Н2О
AuA
3(T)
2H2O
0,5М2О3(т)+1,5Н2О
М(ОНJ(Т) + 2Н2О
Bi(Cl)O(T) + H2O
3Bi2O3(T)
MA(T)
9H2O
Продолжение табл.
M+ + OH-(M=Ag,Cu)
[М(ОНL]" + Н3О+ (М = Al, Cr, Ga)
М3+ + ЗОН" (М = Al, Bi, Fe)
[AuA3OH]- + H3O+(A=Br,Cl,I)
30H-(M=Au,Mn)
[М(ОНK]" + Н3О+ (М = Be, Pb, Sn, Zn)
Bi111 + Cl- + 2OH-
[Bi6(OHI2]6+ + 6OH-
gf, PuOf, UOf)
(A2" = CO2", C2O2~, СЮ2", HAsO2", HPO2-, SO2", SO2", SeO2",
WOJ")
MA •<-"^ M2+ + 2A~
(M2l< = Ca2+, Hg2+, NpOf, PuOf, UO2+, VO2+)
(A- = Br, CH3COO-, CN", C1-, H2PC>4,1", IO3, NCS-, OH")
CaMg(CO3J(T)
MO2(T> + 2H2O ^» M + 4OH
(M = Ce, Ge, Hf, Ir, Mn, Mo, Pb, Pd, Pt, Ru, Sn, Те, W, Zr)
(М"М^И)О4(Т) + 4Н2О «^ M2+ + 2MIH + 8OH- (M = Co, Mn)
MO(T, + H2O ?=» M2+ + 2OH-
(M = Co, Cu, Fe, Hg, Mn, Ni, Pb, Pd, Sn, V, Zn)
0,5(M2O3 • 3H2O)(T)
(Cr2Fe")O4(T) + 4H2O
0,5M2O3(T) + 1,5H2O
(Fe"Fe^)O4(T) + 4H2
0,5Fe2O3(T)+l,5H2O
0,5(Fe2O3 • 3H2O)(T)
MO
2(T)
2H2O
M111 + ЗОН-(М = Co, Mn)
2Cr3++ Fe2++ 8OH"
M3++ ЗОН-(M = Cr, Ir, Tl, V)
Fe2++ 2FeOH2++ 6OH"
FeOH2+ + 2OH~
FeOH2+ + 2OH~
M(OHJ+ + 2OH-(M = Hf,Ti,Zr)
616
V. Вещества в водном растворе
Окончание табл.
МО(ОНJ(т) + Н2О ?=t MIV + 4ОН- (М = Hf, Po, Ti, Zr)
HgO(T) + Hgw <==» Hg?" + 2OH-
MA4(T) ^=± MIV + 4A-(M = Ir, Pt; A-= Вг, ОН-)
IrS2(T)
KFe[Fe»(CNN](T) <^ K++ Fe3++ [Fe»(CNN]4-
MgNH4PO4(T) <=^ Mg2+ + NH+ + PO|"
MO(OH)(T) + H2O ?=? M + ЗОН-(М = Co, Mn, Ni)
0,5Nb2O5(T)+l,5H2O ?=^ №Оз + Н3О+
[Ni(C4H7O2N2J](T) *=* Ni2++ 2C4H7O2N2
Pb3(CO3J(OHJ(T) <=± 3Pb2+ + 2CO|- + 2OH-
Pb(Cl)A(T) ^=Z Pb2++ Cl-+ A" (A-= F-, OH")
(PbPbIV)O4(T) + 4H2O ?=± 2Pb2++ Pblv + 8OH-
Pb2(SO4)O • H2O(T) <=^ 2Pb2+ + SO2- + 2OH"
Re2S7(T) + 10H2O ^=* 2ReO4 + 7H2S + 2H3O+
0,5Sb2O3(T) + 1,5H2O <=± Sb(OH)^ + OH-
0,5Sb2O3(T) + 3,5H2O <=± [Sb(OHL]~ + H3O+
M3(PO4J
VO2(T) + H2O ?=t VO2+ + 2OH-
0,5(V2O5 • 3H2O)(T) + 3H2O
ZrSiO4(T) + 2H2O
617
Растворимость
веществ в воде
1. Твердые вещества
Представлены экспериментальные данные по растворимости ве-
веществ, являющихся твердыми при температуре растворения.
Растворимость выражена через коэффициент растворимости (к)
в граммах безводного вещества на 100 г воды (г/100 г Н2О). Как пра-
правило, приведена растворимость в холодной B0 °С) и горячей воде
(80 °С); иная температура указана верхним индексом, знак (*) отвеча-
отвечает комнатной температуре A8—25 °С).
Приведен также (через косую линию) состав твердой фазы, т. е.
число молекул воды, приходящееся на 1 формульную единицу веще-
вещества в состоянии стабильного равновесия с насыщенным раствором
при 1 атм и соответствующей температуре. Знак «—» означает, что ве-
вещество не кристаллизуется из раствора.
Изменения формульного состава веществ (в растворе или при
кристаллизации) даны в примечаниях в виде гетерогенного равнове-
равновесия между осадком и насыщенным раствором.
Многоточием обозначено отсутствие данных.
Вещество
AgBrO3
AgCH3COO
[Ag(CNJ],K
AgClO2
AgClO3
AgC104
AgF
AgMnO4
AgNO2
AgNO3
AgReO4
/c,r/100rH2O
20 °C
0,159/0
1,04/0
25/0
0,53/0
18,0325/0
526,6/1
172/2
0,9118/0
0,34/0
227,9/0
0,32/0
80 °C
0,936/0
2,52/0
100/0
50/0
792,840/0
21650/0
l,6929/0
l,3660/0
635,3/0
2,7150/0
Вещество
Ag2SO4
Ag2SeO4
A1C13
A1F3
[A1F6],K3
A1NH4(SO4J
A1(NO3K
A12(SO4K
As2O3(aMopc})H.)A)
p-As2O<'>
/c,r/100rH2O
20 °C
0,79/0
0,118/0
45,9/6
0,5025/l
0,072*/0
7,74/12
73,9/9
36,4/18
3,7/0
1,85/0
80 °C
1,30/0
48,6/6
0,8975/3
53,9/12
132,6/6
73,1/18
10,l100/0
6,16/0
618
VI. Растворимость веществ в воде
Продолжение табл.
Вещество
As2O<2>
[AuBr4],K
[Au(CNJ],K
AuCl<3)
[AuCl4],Cs
[AuCl4],K
[AuCl4],Na
[BF4],Cs
[BF4],K<4>
[BF4],NH44)
[BF4],Na<4>
[BH4],Na
[B(NH3)F3]
в2о<5>
B(OH)<5)
[B2(O2J(OHL],Na2
Ba3(As04J
BaBr2
Ba(BrO3J
Ba(CH3COOJ
BaCl2
Ba(C103J
Ba(C104J
BaF2
BaHAsO4
BaHPO4
Ba(HS)<6)
Bal2
Ba(IO3J
Ba(MnO4J
BaMoO4
Ba(N3J
Ba(NCSJ
Ba(NO2J
Ba(NO3J
/c,r/100rH2O
20 °C
65,8/-
18,315/2
14*/0
68*/2
0,8/0
61,8/0,5
151,2/2
l,617/0
0,44/0
2516/0
10827/0
20,5°/0
3625/0
2,2/-
4,87/0
0,76/6
0,055*/0
98,0/2
0,656/1
71,425/3
36,2/2
33,81/1
289,1/3
0,161/0
0,055*/l
0,015*/0
48,8/4
203,1/7,5
0,03318/l
62,5M/0
0,005823/0
17,317/6
169,325/3
70,4/1
9,05/0
80 °C
75,1/1,67
191,667/2
200/0
19,5/0
40560/0,5
90060/2
6,27100/-
97ioo/_
210100/-
5520/0
9,5/-
23,54/0
120,775/2
3,65/1
73,8/1
52,2/2
84,84/1
495,2/3
0,16230/0
63,9/-
257,1/2
0,197I00/l
75,425/0
213,5/1
26,64/0
Вещество
BaO<7>
BaO<8>
Ba(OHJ
Ba(PH2O2J
Ba(ReO4J
BaS<9>
Ba(S4)
BaSO3
BaS2O6
BaS2O6(O2)
Ba(SO3S)
BaSeO4
BeCO3
BeCl2
BeF2
[BeF4],K2
[BeF4],(NH4J
[BeF4],Na2
Be(NO3J
BeSO4
Ca3(As04J
Ca(BO2)^10)
CaBr2
Ca(CH3COOJ
CaCN2
CaCl2
Ca(ClOJ
Ca(C103J
Ca(C104J
CaCrO4
Ca(HCOOJ
CaHPO4
Ca(H2PO4J
Cal2
Ca(IO3J
CaMg(CO3J
/с, г/100гН2О
20 °C
1,5/-
0,091*/8
3,89/8
28l5/l
8,1330/0
7,86/-
38,415/2
0,02/0
18,7/2
42,83°/4
0,2/1
0,015525/0
0,36°/4
72,8/4
84,625/l
2/0
47,525/0
0,26/0
106,6/4
39,1/4
0,01325/9
0,13/6
143/6
34,7/2
2,525/0
74,5/6
27,9°/3
195,9/2
189/4
13,2/2
16,60/2
0,0225/2
1,17*/1
208,6/6
0,25/1
0,03218/0
80 °C
90,8/-
101,4/8
31100/l
21,5150/0
49,91/-
0,002/0
24,830/2
0,138100/0
77,030/4
5,31OO/O
177,860/4
67,2/2
295/3
33,5/2
147,0/2
33,325/3
354,593/0
226,850/4
14,845/2
17,95/0
0,ll60/0
1,7^0/1
354/0
0,67/0
619
VI. Растворимость веществ в воде
Продолжение табл.
Вещество
Са(МпО4J
Ca(N3J
Ca(NO2J
Ca(NO3J
Са(ОНJ
Са(РН2О2J
Ca(PO3F)
CaS
CaSO4
Ca(SO3S)
CaSeO4
CaWO4
CdBr2
Cd(CNJ
[Cd(CNL],K2
CdCl2
Cd(C103J
CdF2
Cdl2
Cd(NO3J
CdSO4
CeNH4(SO4J
Ce(NO3K
Ce2(SO4K
Ce2(Se04K
CoBr2
CoCl2
Co(ClO3J
Co(ClO4J
CoF2
Co(HCOOJ
Col2
Co(IO3J
[Co(NH3N]Cl3
транс-
[Co(NH3LCl2]Cl
[Co(NH3MCl]Cl2
/c,r/100rH2O
20 °C
33114/4
38,l°/0
88,0/4
129,3/4
0,160/0
15,425/0
0,87*/2
0,02/0
0,206/2
49,3/6
8,318/2
0,218/0
98,4/2
l,715/0
113,4/2,5
264°/2
4,352/0
84,8/0
149,4/4
76,4/2,67
5,33/4
175,525/6
9,66/8
40°/8
113,2/6
52,9/6
135°/6
103,8/6
l,525/4
5,03/2
187,4/6
0,46/6
6,95/0
0,329°/l
0,425/0
80 °C
33825/4
4515/0
151,8/1
358,7/0
0,092/0
12,5100/0
0,102/0
67,940/6
660/2
157,1/0
100100/0
140,4/1
431,465/2
4,525/0
112,8/0
666,3/0
67,2/1
l,0590/4
282,850/6
1,09/4
2,5100/4
240,1/2
97,6/2
318,661/4
11545/6
400/6
0,75/2
12,0450/0
l,0347/0
Вещество
[Co(NH3N](NO3K
Co(NH4J(SO4J
[Co(NH3N]2(SO4K
Co(NO3J
[Co(NO2N],K3
CoSO4
CoSeO4
[Cr(CNN],K3
CrCl3
[Cr(H2OLCl2]Cl
[Cr(NCSN],K3
CrNH4(SO4J
CrO<n>
CrSO4
Cr2(SO4K
CrTl(SO4J
CsAl(SO4J
CsBr
CsBrO3
Cs(CH3COO)
Cs2CO3
CsCl
CsClO3
CsC104
Cs2Cr04
CsCr(SO4J
CsF
Cs2Fe(SO4J
CsGa(SO4J
CsHCO3
Csl
CsIO3
CsIO4
CsMnO4
CsN3
CsNO3
/c,r/100rH2O
20 °C
1,81/0
14,9/6
l,2l7/5
97,3/6
0,917/l,5
36,3/7
54,99'V7
30,96/0
34,925/6
50,625/2
138,89*/4
2,1°/12
167/0
21°/7
6425/18
110,525/12
0,4/12
123,325/0
3,725/0
10n/0
260,515/3,5
186,5/0
6,2/0
1,6/0
71,413/0
625/12
572,925/l,5
78,725/6
0,825/12
209,315/0
85,625/0
2,624/0
2,215/0
0,2319/0
224°/0
23,0/0
80 °C
2,4430/0
33,00/6
211/3
49,3/1
15,740/l2
190/0
5,4/12
214/0
5,335/0
113460/0
250/0
45/0
14,4/0
599,50/0
170,875/0
l,2759/0
307,416/0
134/0
620
VI. Растворимость веществ в воде
Продолжение табл.
Вещество
CsOH
Cs2SO4
Cs2Se04
CsV(SO4J
CuBr2
CuCl2
Cu(C103J
CuF2
Cu(HCOOJ
Cu(IO3J
[Cu(NH3L]SO4
Cu(NO3J
CuSO4
CuSeO4
Dy2(SO4K
Er2(SO4K
Eu2(SO4K
FeBr2
FeBr3
[Fe(CNN],Ba2
[Fe(CNN],H4
[Fe(CNN],K3
[Fe(CNN],K4
[Fe(CNN],Na4
[Fe(CNN],Tl4
FeC2O4
[Fe(C2O4K],K3
FeCl2
FeCl<12>
Fe(ClO4J
Fe(ClO4K
FeNH4(SO4J
Fe(NH4J(SO4J
Fe(NO3J
Fe(NO3K
/с, г/100гН2О
20 °C
385,615/1
178,7/0
24512/0
0,2910/12
126,8/4
72,7/2
164,4l8/6
3,5/2
12,5*/4
0,15/0,67
16,922/1
124,7/6
20,5/5
16,9/5
4,05/8
13/8
2,1/8
115/6
45525/6
0,1415/6
1314/0
46/0
28,0/3
20/10
0,36I8/2
0,07825/2
4,2°/3
68,5/4
91,9/6
80,l°/6
97°/10
6825/12
26,4/6
83,03/6
82,5/9
80 °C
30330/l
210,3/0
131,550/4
96,1/2
33270/4
207,7/3
55,5/5
53,7/5
2,67^/8
5,340/8
l,5440/8
159,775/4
0,7100/6
81,8/0
67/3
62,4/10
3,8I00/2
105100/0
90,7/2
526/-
106,660/6
14260/9
22 iioo/! 2
5270/6
16660/6
104,840/9
Вещество
FeSO4
Fe2(SO4K
GaNH4(SO4J
Ga(NO3K
Ga2(SO4K
Gd2(SO4K
[GeF6],K2
|3-GeO<13>
H3As04
H2C2O4
HIO3
H2(PHO3)
H3PO4
H4P2O7
HSO3(NH2)
H2Se03
H2Se04
H6Te06
[HfF6],K2
[HfF7],(NH4K
HgBr2
Hg(BrO3J
Hg(CH3COO)^14)
Hg2(CH3COOJ
Hg(CNJ
Hg(CNOJ
H|C12
Hg(NCSJ
Hg2SO<15>
Ho2(SO4K
I<16>
?><517>
InBr3
/c,r/100rH2O
20 °C
26,6/7
440*/9
14,525/12
181/9
92/18
2,3/8
0,57518/0
0,43/0
см. As2O5
9,52/2
309,4/0
309°/0
548/0
70923/0
14,7°/0
см. SeO2
566,6/1
50,0530/0
4,75/0
28,1/0
0,55/0
0,14*/2
2510/0
0,7515/0
ll,325/0
0,0ll6/0,5
6,59/0
0,0725/0
0,0425/0
6,5/8
0,03/0
253,4/-
414,1/5
80 °C
43,7/1
l,840/8
2,93100/0
l,0100/0
см. As2O5
84,5/2
472,2/0
69430/0
47/0
см. SeO2
275350/0
106,4/0
2,8/0
1,5/2
100100/-
24,2/0
0,0910%-
3,6^/8
0,22/0
360,8/-
618,960/0
621
VI. Растворимость веществ в воде
Продолжение табл.
Rpmipptrd
InCl3
Inl3
In2(SO4K
[IrCl6],K2
[IrCl6],K3
[IrCl6],(NH4J
[IrCl6],Na3
[Ir(NH3N](NO3K
KA1(SO4J
K2B4O7
KBr
KBrO3
KBrO4
K(CH3COO)
KCN
K2CO3
K2C2O4
K2Ca(SO4J
K2Cd(SO4J
KC1
KC103
КСЮ4
K2Co(SO4J
K2Cr04
K2Cr207
KCr(SO4J
KF
KFe(SO4J
K2Fe(SO4J
KH2AsO4
K2HAsO4
KHCO3
KHC2O4
K(HCOO)
K(HF2)
KH(PHO3)
/с, г/100гН2О
20 °C
195,l22/3
130822/0
117/9
1,25*70
8/0
l,0925/0
21,33l5/12
1,7*70
5,9/12
16,530/8
65,2/0
6,87/0
4,2125/0
255,6/1,5
69,9/0
111/1,5
36,4/1
0,2*71
39,2*72
34,4/0
7,3/0
1,68/0
19,276
63,0/0
12,48/0
12,5125/12
94,2/2
36,525/6
1970
18,8670
33,3/0
331*70
39,2/0
220/0
80 °C
373,7/2,5
2024770
l,12270
4,38/0
71/12
94,6/0
34,28/0
...
380,1/0,5
99,8/0
139,2/1,5
63,6/1
42,347l,5
51,1/0
37,6/0
13,4/0
75,1/0
73,01/0
150,1/0
64,2776
68,3770
16,7'°70
657,6970
114/0
Вршргтвп
KH2PO4
K2HPO4
KHSO3
KHSO4
KI
KIO3
KIO4
KMgCl3
K2Mg(SO4J
KMnO4
K2MoO4
KN3
KNCS
KNO2
KNO3
K2Ni(SO4J
KOCN
KOH
K(PH2O2)
K2(PHO3)
K3PO4
KReO4
K2SO3
K2SO4
K2S2O^18)
K2S2O6
K2S3O6
K2S4O6
K2S5O6
K(SO3F)
K2S2O6(O2)
K2(SO3S)
K2Se04
La(BrO3K
LaCl3
La(NO3K
La2(SO4K
/c,r/100rH2O
20 °C
22,6/0
159,8/3
49/0
51,4/0
144,5/0
8,1/0
0,42/0
39,4*76
18,3/6
6,36/0
184,625/2
49,7*7/0
217/0
306,7/0
31,6/0
5,376
7525/0
112,4/2
20025/0
170/0
98,5/7
l,225/0
107/1
11,1/0
44,5/0
6,64/0
8,8670
14,4270
18,3471,5
6,9*70
4,7/0
155,4/1,67
111,0/0
149/9
97,225/7
113,425/6
2,1425/9
80 °C
70,4/0
267,5670
115*°°/0
121,6100/0
190,7/0
24,8/0
4,44/0
43,875/6
2565/0
105,7*°°/0
40867/0
376/0
168,8/0
45,875/6
162,5/1
178,5673
7,4775/0
111,5/1
21,4/0
107,9/-
63,3l00/0
22,59270
30,17270
32,942°/l,5
...
n47o
312970
118,8*70
230,435/9
170,392/7
0,9675/9
622
VI. Растворимость веществ в воде
Продолжение табл.
Вещество
LiBr
Li(CH3COO)
Li2CO3
Li2C2O4
LiCl
LiClO3
LiC104
Li2Cr04
Li2Cr2O7
LiF
Li2Ge03
Li(HCOO)
Lil
LiMnO4
LiN3
LiNO2
LiNO3
LiOH
Li3PO4
Li2SO4
Lu2(SO4K
MgBr2
Mg(BrO3J
Mg(CH3COOJ
MgCO3
MgC2O4
MgCl2
Mg(ClO3J
Mg(C104J
MgCЮ4
MgHPO4
Mgl2
Mg(IO3J
MgNH4PO4
Mg(NH4J(SO4J
Mg(NO3J
/c,r/100rH2O
20 °C
160,4/2
45,526/2
1,33/0
8,0/0
78,5/1
313,518/0,5
56,12/3
110I8/2
186,530/2
0,2718/0
0,8525/0
39,5/1
165/3
49,9716/3
197,7116/1
73,5l8/0,5
74,5/3
12,8/1
0,03/2
34,6/1
37,8/8
101,1/6
27,318/6
65,625/4
0,18/5
0,0516/2
54,8/6 *
129,918/6
99,2/6
54,825/5
0,15*/3
139,8/8
8,6/4
0,03/6
17,96/6
73,3/6
80 °C
244,8/1
98,251/2
0,8575/0
112,3/1
123,0/3
242/2
0,13535/0
93,8/1
435/1
194,17O/O
15,3/1
30,0/1
13,540/8
11260/6
97,955/4
0,06100/2
65,8/6
280,393/2
109,250/6
66,575/5
0,09/3
185,7/6
16,2100/10
0,011/6
48,32/6
110,1/6
Вещество
Mg(PH2O2)
MgSO3
MgSO4
MnBr2
MnC2O4
MnCl2
MnF2
Mn(NH4J(SO4J
Mn(NO3J
MnSO4
MoO<19>
NH4Br
NH4(CH3COO)
(NH4JCO3
(NH4JC2O4
NH4C1
N2H5C1
N2H6C12
NH4C1O3
NH4C1O4
(NH4JCrO4
(NH4JCr207
NH4F
NH4HCO3
NH4(HCOO)
NH4(HF2)
NH4H(PHO3)
NH4H2PO4
(NH4JHPO4
NH4HS
NH4HSO3
NH4HSO4
NH4I
NH4IO3
NH4IO4
/c,r/100rH2O
20 °C
ll,825/6
0,315/6
35,1/7
146,9/4
0,0325/2
73,9/4
1,06/4
37,l25/6
132,3/6
62,9/5
0,138/0
74,2/0
1484/0
10015/0
4,45/1
37,2/0
17925/0
270,423/0
28,7°/0
24,825/0
37,025/0
35,6/0
82,6/0
21,7/0
143/0
60,15/0
171°/0
35,3/0
69/0
128,l°/0
71,8°/0
10070
172,3/0
2,615/0
2,7l6/0
80 °C
0,41290/3
54,8/1
224,7/2
112,7/2
499/1
45,6/1
2,107/0
119,3/0
22,4/1
65,6/0
11575/0
74,285/0
7O,175/O
115/0
117,6/0
531/0
292,7/0
2603l/0
118,3/0
10670/0
84,760/0
228,8/0
14,5100/0
623
VI. Растворимость веществ в воде
Продолжение табл.
RpillPPTRD
DGLHGV»» 1 DU
NH4Mn04
NH4N3
NH4NCS
NH4NO2
NH4NO3
N2H5NO3
(NH3OH)C1
(NH3OHJSO4
NH4Re04
N2H6SO4
(NH4JSO3
(NH4JSO4
(NH4JS2O6(O2)
(NH4JSO3S
(NH4JSe04
NH4VO3
NaAl(SO4J
Na3AsO4
NaBO^20)
NaB5O8
Na2B4O7
NaBr
NaBrO3
Na(CH3COO)
NaCN
Na2CO3
Na2C2O4
NaCl
NaCIO
NaC102
NaC103
NaClO4
Na2CrO4
Na2Cr207
NaF
Na2GeO3
NaH2AsO4
/c,r/100rhi>O
20 °C
7,9I5/0
20,230/0
170/0
180,1/0
192/0
266/0
8317/0
63,725/0
6,23/0
2,87/0
28,0°/l
75,4/0
58,2°/0
12212/0
0,5215/0
39,72/12
19,116/12
29,5/2
9,24°/5
2,5/10
90,8/2
36,4/0
46,5/3
58,2/2
21,8/10
3,41/0
35,9/0
53,4/5
6417/3
95,9/0
21125/1
84,625/Ю
180/2
4,28/0
23,6/7
179/1
80 °C
27,0740/0
43170/0
30034/0
580/0
213560/0
194100/0
68,590/0
32,34/0
14,39/0
941/0
74,816/0
1O3,31OO/O
1971OO/O
l,650/0
40,845/12
23,430/12
34,l30/2
ll,920/5
24,3/4
118,3/0
75,7/0
153/0
82,555/0
45,1/1
5,71/0
38,1/0
129,950/2,5
! 2260/0
203,9100/0
30075/0
124,7/0
355/2
4,69/0
49,250/7
Rpiiipptro
Na2HAs04
NaHCO3
Na(HCOO)
Na(HF2)
NaH2PO4
Na2HPO4
Na2H2P2O7
NaHS
NaHSO3
NaHSO4
Nal
NaIO3
NaIO4
NaMnO4
Na2MoO4
NaN3
NaNCS
NaNO2
NaNO3
NaOCN
NaOH
Na(PH2O2)
Na2(PHO3)
Na3PO4
Na4P2O7
Na5P3O10
NaReO4
Na2S
Na2SO3
Na2SO4
Na2S2O4
Na2S2O<18>
Na2S2O6
Na2S2O6(O2)
Na2(SO3S)
Na2SeO3
Na2SeO4
/c,r/100rH9O
20 °C
51/12
9,59/0
81,2/2
3,25/0
85,2/2
7,66/12
4,6/6
75,5/3
57,5/0
28,6°/l
179,3/2
9,525/l
10,2/3
144/3
64,715/2
40,8/0
142,625/1
82,9/0
87,6/0
10,7116/0
108,7/1
8325/l
4 \ 90/5
14,525/12
5,50/10
l6,310/6
145,330/0
18,6/9
26,1/7
19,2/10
24,1/2
65,3/0
15,12/2
70,4/0
70,1/5
6037/5
57,225/Ю
80 °C
6530/12
20,2/0
122,260/0
7,590/0
207,3/0
92,4/2
23,5^/6
...
50100/0
296/0
26,6/0
38,850/0
73370/3
6950/2
55l00/0
200/0
135,5/0
149/0
...
314/0
554100/l
68,0/6
54,282/0
173,850/0
49,2/6
29,0/0
43,3/0
88,7/-
49,26/2
229/0
74,875/0
624
VI. Растворимость веществ в воде
Продолжение табл.
Вещество
Na2Si03
NaVO3
Na2WO4
Na4Xe06
Nd(BrO3K
NdCl3
Nd(NO3K
Nd2(SO4K
NiBr2
Ni(CH3COOJ
NiCl2
Ni(C104J
NiF2
Nil2
Ni(IO3J
Ni(NH4J(SO4J
Ni(NO3J
NiSO4
NiSeO4
OsO421>
[PF6],NH4
PbBr2
Pb(BrO3J
Pb(CH3COOJ
PbCl2
Pb(Cl)F
Pb(C102J
Pb(C103J
Pb(ClO4J
PbF2
Pb(HCOOJ
Pbl2
Pb(N3J
Pb(NCSJ
Pb(NO3J
/c,r/100rH2O
20 °C
18,8/9
21Д25/2
73,0/2
0,8/6
75,5/9
98/6
15325/6
7,1/8
131/6
16,6*/4
64,0/6
156,876
2,56/4
148,1/6
1,1374
6,5/6
94,2/6
38,4/7
33,44i5/6
6,44/0
74,8/0
0,9725/0
1,33/1
44,3/3
0,978/0
0,03570
0,095/0
144,318/1
44125/3
0,50770
l,6l6/0
0,07625/0
0,023^/0
0,05/0
52,2/0
80 °C
160,6/...
38,875/2
90,1/2
13245/9
127/6
185576
2,085/8
154/3?
86,275/2
192,945/6
2,58974
187,3/4
1,Q974
21,8/6
172774
66,7/6
74,79/6
3,34/0
221573
2,62/0
0,42100/0
163,/1
0,064270
20ш70
0,3/0
0,09770
0,2ш70
107,4/0
Вещество
Pb(NO3)OH
PbSeO4
PbWO4
m/wz«c-[Pd(NH3JCl2]
Pr(BrO3K
Pr2(C2O4K
PrCl3
Pr(NO3K
Pr2(SO4K
PtBr<22>
[PtBr6],K<23>
[PtBr6],(NH4)<23>
[Pt(CNL],Ba
[Pt(CNL],K2
PtClf>
[PtCl6],Cs<23>
[PtCl6],H2
[PtCl4],K2
[PtCl6],K<23>
[PtCl6],(NH4)<23>
[PtCl6],Na2
[PtCl6],Rb<23)
/w/wwc-[Pt(NH3JCl2]
^c-[Pt(NH3JCl2]
mpaHC-[Pt(NH3JC\4]
«wc-[Pt(NH3JCl4]
[Pt(NH3L]Cl2
[Pt(NO2L],K2
RaBr2
RaCl2
Ra(IO3J
RbAl(SO4J
RbBr
RbBrO3
/c,r/100rH2O
20 °C
19,4*70
0,01325/0
0,0370
0,304l70
91,5/9
0,0225/l0
98,425/7
144i5/6
12,6/8
0,41/я
2,02/0
0,59/0
2,874
33,8/3
142,125/1O
0,02470
140*76
0,93170
0,774/0
0,5/0
53176
0,01470
0,03625/0
0,2625/0
0,1470
0,3370
20ш/1
3,815/0
70,6/2
245,5/2
0,01870
1,6/12
11325/0
2,9325/0
80 °C
163,945/9
141,6/7
302576
3,5/8
lOioo/_
0,36107-
139672
367/3
0,377107
5,31070
3,71/-
1,251°°/-
0,33100/-
0,7i°°/0
3ioo/0
3,0l00/0
l,54100/0
0,17l00/0
25,2/12
191100/0
5,08470
21-2004
625
VI. Растворимость веществ в воде
Продолжение табл.
Вещество
Rb2CO3
RbCl
RbC103
RbC104
Rb2Cr04
Rb2Cr207
RbCr(SO4J
RbF
RbFe(SO4J
RbHCO3
Rbl
RbIO3
RbIO4
RbMnO4
RbN3
RbNO3
RbOH
Rb2SO4
Rb2Se04
RbV(SO4J
[Ru(NO+)Cl5],K2
RuOf>
SbCl^5)
SbF<25>
[SbF6],Na
Sb2O<26>
[Sb(OHN],Na
[SbS3],Na3
[SbS4],Na3
Sc2(SO4K
SeO<27>
[SiF6],Co
[SiF6],Cu
[SiF6],K2
[SiF6],Li2
/c,r/100rH2O
20 °C
223/2
91,1/0
5,4/0
1,0/0
73,6/0
4,96*70
43,427l2
300*71,5
116/1
169270
2,127O
0,65*70
1,12*70
107*70
53,5/0
179*72
48,2/0
159*70
1,6*712
12,0270
1,7170
920/0
444,7/0
128,6/0
0,3*/*
0,1/0
230/9
13,379
64,6*2/5
26422/-
76,822/6
99,7*76
0,11/0
59*72
80 °C
127,2/0
62,8970
9,2/0
95,6670
27,3670
31;997l2
21960/0
4,7670
i
309/0
28247l
75/0
2,03270
1917570
563,6370
66,3*°79
32,2275
47167~
0,38*70
Вещество
[SiF6],Mg
[SiF6], Mn
[SiF6],(NH4J
[SiF6],Na2
[SiF6],Rb2
[SiF6],Sr
Sm(BrO3K
SmCl3
Sm2(SO4K
SnBr<28>
SnCl<29>
[SnCl6],(NH4J
[SnF6],K2
SnI<30>
[Sn(OHN],K<31>
[Sn(OHN],Na<31>
SnSO4
SrBr2
Sr(BrO3J
Sr(CH3COOJ
SrCl2
Sr(C103J
Sr(C104J
SrCrO4
SrF2
Srl2
Sr(IO3J
Sr(MnO4J
SrMoO4
Sr(NO2J
Sr(NO3J
Sr(OHJ
SrSO4
SrS2O6
SrS4O6
/c,r/100rH2O
20 °C
39,3*76
90,4*76
22,7270
0,67/0
0,16/0
2,6*72
62,5/9
93,4/6
2,67/8
85,270
269,8*72
33*70
3,5*71
0,98/0
85*70
61,3*70
18,8*72
100/6
33*71
41,6/0,5
53,1/6
174*78
31027«
0,091270
0,01170
179/6
0,03*71
250*73
0,01*70
65,3/1
70,4/4
0,81/8
0,013/0
13,5/4
2576
80 °C
48,2770
1,96/0
l,35*°70
98,4^/9
99,9576
1,99^/8
31,5*°70
2,95/0
110,5270
50*°70
18,1*°72
175/6
36,1/0,5
93,1/2
0,062770
0,012270
277/6
0,8*°°/0
165*°7l
98/0
8,3/8
0,011970
52*°°/0
64376
626
VI. Растворимость веществ в воде
Вещество
Sr(SO3S)
SrWO4
Tb2(SO4K
[TcF6],K2
ThBr4
ThCl4
Th(NO3L
Th(SO4J
Th(SeO4J
[TiF6],K2
T1A1(SO4J
TIBr
<T12CO3
T12C2O4
T1C1
T1C1O3
T1C1O4
T1F
T1N3
T1NCS
T1NO2
T1NO3
T1OH
T13PO4
T14P2O7
T12S
T12SO4
T12S2O6
Tl2SeO4
T1VO3
UF4
UO2(CH3COOJ
/c,r/100rH2O
20 °C
l,7l3/5
0,14l5/0
3,56/8
l,525/0
65/4
125°/8
190,7/5
1,38/9
0,498°/9
1,28/1
6,4/12
0,048/0
5,23 l8/0
l,4815/0
0,32/0
3,92/0
19,7230/0
24525/0
0,316/0
0,315/0
32,l25/0
9,55/0
34,318/2
0,515/0
4010/0
0,02/0
4,87/0
41,819/0
2,8/0
0,87n/0
0,0125/2,5
7,0715/2
80 °C
39ioo/2
2,5540/8
0,81/4
l,972100/9
...
35,3660/12
0,2568/0
27,2100/0
9,02100/0
1,6/0
36,65/0
81,49/0
28550/0
О^З40/©
95,898/0
111/0
126,19O/O
0,67l00/0
14,61/0
8,5/0
0,21100/0
i \'
Вещество
(-"
(UO2)C2O4
(UO2)F2
UO2(NO3J
(UO2)SO4
U(SO4J
VNH4(SO4J
V2O<32>
[W(CN)8],K4
XeF2
XeO3
YBr3
Y(BrO3K
YC13
YCNOj),
Y2(SO4K
Yb2(SO4K
ZnBr2
Zn(CH3COOJ
ZnCl2
Zn(C103J
Zn(C104J
ZnF2
Zn(HCOOJ
Znl2
Zn(NO3}2
ZnSO4
ZnSeO4
ZrCl2OC3)
ZrF434> "
[ZrF6],K2
[ZrF7],(NH4K
[Zr(H2OL(SO4J]
Окончание табл.
fc,r/100rH2O
20 °C
0,5/3
64,4/0
119,3/6
151,616/3
10,924/4
15,6/12
0,0725/«
12218/2
2,54°/л
36/-
83,330/9
12525/9
75,1/6
96,723/5
7,4716/8
38,4/8
446,4/2
30/2
367/1,5
200,3/4
110,1/6
0,918/4
5,2/2
43218/0
118,8/6
54,1/7
63,625/l
60/8
1,525/-
l,6719/0
18,5/0
80,318/0
80 °C
l,6875/0
74,l100/0
203/6
188,222/3
0,07m/n
4f225/n
lll,375/9
78,1/6
l,9995/8
6,92/8
644,6/0
44,6100/2
549/0
273,250/4
125,250/6
21,2/2
488/0
87170/l
67,2/1
55,3/0
1,3950/-
25100/0
99,14O/O
21*
627
VI. Растворимость веществ в воде
628
As2O3(T) + ЗН2О ?=± 2HAsO2 + 2H2O <=± 2H3AsO3
20°С : As2O5(T) + 5Н2О *=± 2(H3AsO4 • Н2О)(т)
2H3AsO4 + 2H2O
80°С : А^Оэд + 5Н2О = As2O5 • 5Н2О(Т) ?=* 2H3As04 + 2Н2О
АиС13(т) + 2Н2О = АиС13 • 2Н2О(Т) <=± Н[АиС13(ОН)] + Н2О
100°С : M[BF4](T) + Н2О = M[B(OH)F3](T) + HF
M[B(OH)F3] + HF
В2О3(Т) + 5Н2О = 2В(ОНK(Т) + 2Н2О з=* 2[В(Н2О)(ОНK]
80°С : Ba(HSJ(T) + 2Н2О ^± Ва(ОНJ + 2H2St
ВаО(т) + 9Н2О = Ва(ОНJ • 8Н2О(Т) <р± Ва(ОНJ + 8Н2О
2ВаО2(т) + 16Н2О = 2(ВаО2 • 8Н2О)(т)
Ва(НО2J + Ва(ОНJ + 14Н26
20 °С: 2BaS(T) + 14Н2О = Ba(HSJ • 4Н2О(Т) + Ва(ОНJ • 8Н2О(т)
Ba(HSJ + Ва(ОНJ + 12Н2О
80 °С: 2BaS + 14Н2О = Ba(HSJ • 4Н2О(т) + Ва(ОНJ • 8Н2О(т)
2Ва(ОНJ + 2H2St + 10Н2О
Са(ВО2J + 6Н2О = Са(ВО2J • 6Н2О(Т) ?^ Са[В(ОНL]2 + 2Н2О
СЮ3(Т) + Н2О +=? Н2Сг04
80 "С : FeCl3(T) + 2Н2О = FeCl(OHJi + 2HC1
GeO2(T) + H2O ^=? H2GeO3
80 °C: Hg(CH3COOJ(T) + H2O = Hg(CH3COO)OH(T) + CH3COOH
(HgOH)CH3COO + CH3COOH
80 °C: гНвгБО^, + 4H2O = (Hg2JSO4(OHJ(T) + H2SO4 + 2H2O
[Hg2(H2O)OH]2SO4 + H2SO4
VI. Растворимость веществ в воде
1
Н2О
HI + HIO
2(Т)
12О5 + Н2О = 2НЮ3(Т) ?=* 2НЮ3
80 "С : M2S2O5 + Н2О = 2MHSO3(T)
7МоО3(т) + ЗН2О «=* Н6Мо7О24
NaBO2(T) + 2Н2О = NaBO2 • 2Н2О(Т)
2MHSO3
Na[B(OHL]
OsO4(T) -
PtA^-t
80-100
RuO^
SbA3,rtH
*-2H2O <=±
(n + 2)H2O =
•CiMJPtAJ,,
+ 2H2O <=±
hnH2O <=±
[Os(H2OJO4]
PtA4 • иН2О(т) + 2H2O
?=^ [Pt(H2OJA4] +1
., + ^0 ^± M[Pt(]
[Ru(H2OJO4]
[Sb(H2O)BA3]
иН2О
МА
Sb2O5(T) + иН2О = Sb2O5 • лН2О(т)
2[Sb(H2O)(OHM] + (и - 7)Н2О
SeO2(T) + Н2О = H2Se03(T)
H2Se03
7SnBr
2(T)
10Н2О
[Sn3(OHL]Br2 + [Sn4(OHN]Br2 + ЮНВг
7SnCl2(T) + 14Н2О = 7{[Sn(H2O)Cl2] • Н2О}(Т)
[Sn3(OHL]Cl2 + [Sn4(OHN]Cl2 + 10НС1 + 4H2O
20 °C : SnI2{T) +
80 eC : 2SnI2(T) -
M2[Sn(OHN](T)
5V2O5(T) + E«4
H20 *=
I-H2O <=
+ H2O ^
3)H2O =
t [Sn(H2O)I2]
^ (SnOH)I +H[SnI3]
=± M[Sn(H2O)(OHM] + MOH
5(V2O5«H2O)(T) + 3H2O ?=±
^^ H6V10O28 + 5«H2O
4ZrCl2O(T) + 32H2O = 4(ZrCl2O • 8H2O)(T)
[Zr4(H2OI6(OH)8]Cl8 + 12H2O
2ZrF4(T) + 6H2O = [Zr2(H2ONF6]F2(T)
H2[Zr2(H2OJ(OHLF6] + 2HF
629
VI. Растворимость веществ в воде
2. Газы и жидкости
Приведены экспериментальные данные по растворимости газов и
жидкостей в воде при различных температурах (°С, указаны верхним
индексом).
Растворимость газов выражена:
а) объемным коэффициентом растворимости (v) в миллилитрах
вещества на 100 г воды;
б) массовым коэффициентом растворимости (к) в граммах вещест-
вещества на 100 г воды.
Для аммиака NH3 растворимость передана также массовой долей
(и>) в граммах газа на 100 г раствора.
Растворимость газов определена при их парциальном давлении,
равном нормальному атмосферному давлению.
Растворимость жидкостей выражена массовым коэффициен-
коэффициентом растворимости (к) в граммах вещества на 100 г воды.
Взаимодействие между растворяемым веществом и водой оговоре-
оговорено в примечаниях. Изменение формульного состава вещества показа-
показано в виде гетерогенного равновесия между растворяемым веществом
и насыщенным раствором.
Жидкости имеют обозначение «жидк.», остальные вещества — газы.
Вещество
Аг
AsH3
BF^>
Вг2(жидк.)<2>
сн4
C2H2
С2Н4
2. 4
С2Н6
СН3СООН(жидк.)
C2N2
СО
СО23>
С82(жидк.)
Растворимость
v5,24°, 3,3620, 2,494°, 2,2050, 2,0s60, 1,8180
v2020
v 10973°, 1064325
А; 33,2°, 32,225
Аг2,30°, 3,5820, 3,4s40
v5,56°, 3,3120, 3,0125, 2,37"°, 1,95е0,1,7780,1,70100
v 173°, 13110, ЮЗ20, 9325, 8430
v22,6°, 19,15,13,915,12,220, 10,825, 9.830
v9,87°,'4,7220,4,1025, 2,91"°, 2Д860, 1,8380, 1,72100
Смешивается неограниченно
v45020
v3,54°, 2,3220, 2,1425, 1,7740, 1,4960, 1,4380, 1,41100
v 171,3°, 119,410, 87,820, 75,925, 53,0"°, 35,960
Jt0,17920,0,01450
630
VI. Растворимость веществ в воде
Продолэ/сение табл.
Вещество
C(S)O
С1<4>
С12О
н2
НВг
НСМ(жидк.)
НС1
HF
HI
НЫО3(жидк.)
Н2О2(жидк.)
H2S
Н28О4(жидк.)
H2Se
Н2Те
Не
Кг
N2
NH<5>
NO
N2O
Ne
[№(СОL](жидк.)
O2
Растворимость
v 133°, 5420, 40,330
v 461,0°, 229,92°, 201,2525, 143,840, 102,360, 68,380
v99i8
v2,15°, 1,8220, 1,6440, 1,660-100
v 61200°, 5820010, 5330025, 4690050, 34500100
к221,2°, 210,l10, 198,220, 193,025, 171,450, 130,0100
Смешивается неограниченно
v 50700°, 4420020, 4260025, 3860040, 3390060
* 82,3°, 72,020, 69,325, 67,330, 62,840, 59,650, 55,260
Растворяется неограниченно
v4100010
?23410
Смешивается неограниченно
Смешивается неограниченно
v467°, 258,220, 25025, 16640, 1196°, 91,7ю, 81100
*0,71°, 0,3920, 0,3825, 0,2540, 0,1860, 0,1480, 0,12100
Смешивается неограниченно
v3774,27025
А:1,364,0,9825
vl00°
к 0,58°
v 0,978°, 0,86120, 1,010м
vll,0°,5,4025,4,6750
v2,35°, 1,5420, 1,1840, 1,0260,0,9680,0,95100
v 115163°, 7430120, 6079425, 3566050, 2620880
А: 87,5°, 52,62°, 46,225, 22,950, 15,480, 7,410°
w42,8°, 37,810, 33,120, 23,440, 14,16°, 6,280
v7,38°, 4,712°, 3,514°, 2,95^°, 2,7080, 2,6310°
v 130°, 104,85, 87,8ю, 73,815, 62,920, 54,425
vl,23°, l,1625,0,9874
А:0,01810
v4,89°, 3,1020, 2,8325, 2,3140, 1,9560, 1,788°, 1,72100
631
VI. Растворимость веществ в воде
Окончание табл.
Вещество
О3
OF2
РН3
Rn
SF6
so<6>
SO2F2
Xe
Воздух
Растворимость
v50,9°, 28,520, 14,540,8,060
v6,8°,4018
v2720
v51,0°,22,425, 13,050
vl,47°,0,5525
v7979°, 67485, 566510, 393720, 327925, 187740
jfc 22,8°, 19,35, 16,210, 13,515, 11,320, 9,425, 5.440, 4,550,
2,190
v4M16,5
v24,2°,9,725,8,450, 7,1280
v 27,86°, 18.5825
k 0,036°, 0,02225
A)
B)
C)
D)
E)
F)
BF3(r) + 2H2O = BF3-2H2O()K) <=^ H[B(OH)F3]
0 °C :-Вг2(ж) + 7,67H2O = Br2 • 7,67H2O(T) <f=?
<=± HBr+HBrO + 6,67H2O
20-40 °С: Вг2(ж) + Н2О
со2(г)
О°С:С1
HBr + HBrO
H2O
CO2H2O(p)
н2со3(р)
2(Г)
= С12-5,75Н2О(Т)
НС1 + НСЮ + 4,75Н2О
20-80 °C: Cl2(r) + H2O
НС1 + НСЮ
NH
3(r)
H2O
NH3H2O(p)
0-10 'C : SO2(r) + иН2О = SO2 • 7,67Н2О(ж) + (п- 7,67)H2O
SO2nH2O(p)
15-90 °C:SO2(r) + nH2O
SO2/iH2O(p)
632
Плотность воды
и водных растворов
1. Вода при различных температурах
t, °с
0
1
2
4
6
8
10
12
14
16
18
20
22
р, г/л
999,841
999,900
999,941
999,973
999,941
999,849
999,700
999,498
999,244
998,943
998,595
998,203
997,770
f, °С
24
25
26
28
30
32
34
36
38
40
42
44
46
р, г/л
997,296
997,044
996,783
996,232
995,646
995,02
994,37
993,68
992,96
992,21
991,44
990,63
989,79
t,°C
48
50
52
55
60
65
70
75
80
85
90
95
100
Р. г/л
988,93
988,04
987,12
985,70
983,21
980,56
977,78
974,86
971,80
968,62
965,31
961,89
958,35
2. Кислоты и основания
Приведена плотность р растворов кислот и оснований в зависи-
зависимости от содержания растворенного вещества (массовая доля w, мо-
молярная концентрация с) при комнатной температуре A4—20 °С).
р, г/л
w,%
с, моль/л
СР3СООН
999,7
1001,2
1002,6
1004,1
1
2
3
4
0,167
0,333
0,501
0,669
р, г/л
1005,5
1006,9
1008,4
1009,8
1011,2
1012,6
w,%
5
6
7
8
9
10
с, моль/л
0,837
1,006
1,175
1,345
1,516
1,686
633
VII. Плотность воды и водных растворов
Продолжение табл.
р, г/л
1020
1026
1032
1038
1044
1049
1053
1058
1061
1061
1067
1069
и>,%
15
20
25
30
35
40
45
50
55
60
65
70
с, моль/л
2,54
3,41
4,3
5,19
6,08
6,99
7,89
8,8
9,72
10,63
11,54
12,45
НС1
1000
1005
1010
1015
1020
1025
1030
1035
1040
1045
1050
1075
1100
1125
1150
1160
1170
1180
1190
0,36
1,36
2,36
3,37
4,39
5,41
6,43
7,46
8,49
9,51
10,52
15,49
20,39
25,22
30,14
32,14
34,18
36,23
38,32
0,10
0,38
0,66
0,94
1,23
1,52
1,82
2,12
2,42
2,73
3,03
4,57
6,15
7,78
9,51
10,23
10,97
11,73
12,50
НСЮ4
1005
1030
1,00
5,25
0,10
0,54
р. г/л
1060
1095
ИЗО
1165
1205
1250
1300
1355
1410
1475
1540
1605
1675
1005
1021
1036
1050
1070
1096
1118
1123
1000
1005
1010
1015
1020
1025
1030
1035
1040
1045
1050
ш, %
10,06
15,28
20,26
24,94
29,86
34,95
40,10
45,26
50,10
55,17
60,04
64,88
70,15
HF
2
6
10
14
20
28
36
40
HNO3
0,33
1,26
2,16
3,07
3,98
4,88
5,78
6,66
7,53
8,40
9,26
с, моль/л
1,06
1,67
2,28
2,89
3,58
4,35
5,19
6,10
7,03
8,10
9,20
10,37
11,70
1,01
3,06
5,18
7,35
10,69
15,33
20,11
22,40
0,05
0,20
0,35
0,50
0,65
0,80
0,95
1,09
1,24
1,39
1,54
634
VII. Плотность воды и водных растворов
Продолжение табл.
Р> г/л
1055
1085
1115
1150
1180
1280
1365
1380
1385
1390
1395
w,%
10,12
15,13
20,00
25,48
30,00
45,27
59,69
62,70
63,72
64,74
65,84
с, моль/л
1,69
2,61
3,54
4,65
5,62
9,20
12,93
13,73
14,01
14,29
14,57
Н2О2
1002
1006
1013
1020
1028
1035
1043
1050
1057
1065
1073
1080
1088
1096
1104
1112
1003
1009
1020
1036
1
2
4
6
8
10
12
14
16
18
20
22
24
26
28
30
Н3РО4
1
2
4
6
0,30
0,89
1,19
1,80
2,42
3,04
3,68
4,32
4,97
5,64
6,31
6,99
7,35
8,38
9,09
9,81
0,10
0,21
0,42
0,63
р,г/л
1042
1053
1065
1076
1088
1101
1113
1140
1167
1181
ш.%
8
10
12
14
16
18
20
24
28
30
с, моль/л
0,85
1,07
1,30
1,54
1,78
2,02
2,27
2,79
3,33
3,61
H2SO4
1000
1005
1010
1015
1020
1025
1030
1035
1040
1045
1050
1055
1060
1065
1070
1180
1305
1500
1730
1815
1824
1831
1834
1835
0,26
0,99
1,73
2,49
3,24
4,00
4,75
5,49
6,24
6,96
7,70
8,42
9,13
9,84
10,56
25,21
40,25
60,17
80,25
90,12
92,00
93,94
95,12
95,72
0,03
0,10
0,18
0,26
0,34
0,42
0,50
0,58
0,66
0,74
0,83
0,91
0,90
1,07
1,15
3,03
5,36
9,20
14,16
16,68
17,11
17,54
17,79
17,91
635
VII. Плотность воды и водных растворов
Продолжение табл.
р, г/л
1000
1005
1010
1015
1020
1025
1030
1035
1040
1045
1050
1055
1060
1065
1070
1075
1080
1085
1090
1095
1190
1290
1395
1510
1535
998
996
994
992
990
988
w,%
КОН
0,20
0,74
1,30
1,84
2,38
2,93
3,48
4,03
4,58
5,12
5,66
6,20
6,74
7,28
7,82
8,36
8,89
9,43
9,96
10,49
20,37
30,21
39,92
49,95
52,05
NH,
0,05
0,51
0,98
1,43
1,89
2,35
с, моль/л
0,04
0,13
0,23
0,33
0,43
0,54
0,64
0,75
0,85
0,95
]
]
I
1
]
1
]
1,06
1,17
1,27
1,38
1,49
1,60
1,71
1,82
1,94
2,05
4,32
6,95
9,93
13,45
14,24
0,03
0,30
0,57
0,83
1,10
1,36
р, г/л
986
984
/ОТ
982
980
978
976
974
972
970
968
966
964
962
960
958
956
922
914
908
904
902
900
898
1000
1005
1010
1015
1020
1025
1030
1035
1040
ш, %
2,82
3 30
3,78
4,27
4,76
5,25
5,75
6,25
6,75
7,26
7,77
8,29
8,82
9,34
9,87
10,40
20,27
22,75
24,68
26,00
26,67
27,33 ,
28,00
NaOH
0,16
0,60
1,04
1,49
1,94
2,39
2,84
3,29
3,74
с, моль/л
1,63
1 91
i,7i
2,18
2,46
2,73
3,01
3,29
3,57
3,84
4,12
4,41
4,69
4,98
5,27
5,55
5,84
10,97
12,21
13,16
13,80
14,12
14,44
14,76
0,04
0,15
0,26
0,38
0,49
0,61
0,73
0,85
0,97
636
VII. Плотность воды и водных растворов
Окончание табл.
Р. г/л
1045
1050
1055
1060
1065
1070
1075
1080
1085
1090
1095
ш, %
4,20
4,65
5,11
5,56
6,02
6,47
6,93
7,38
7,83
8,28
8,74
с, моль/л
1,10
1,22
1,35
1,47
1,60
1,73
1,86
1,99
2,12
2,26
2,39
Р. г/л
1100
1105
1110
1165
1220
1330
1430
1500
1510
1520
1530
ш, %
9,19
9,64
10,10
15,09
20,07
30,20
40,00
47,33
48,38
49,44
50,50
с, моль/л
2,53
2,66
2,80
4,40
6,12
10,04
14,30
17,75
18,26
18,78
19,31
р,г/л
В(ОНK
1002,2
1005,6
1009,1
1013,6
1
2
3
4
Са(ОНJ
999,8
1000,4
1001,1
0,05
0,10
0,15
H3As04
1005,7
1012,4
1026,0
1039,8
1053,8
1068,1
1082,6
1
2
4
6
8
10
12
р,г/л
1097,5
1112,8
1128,5
1144,7
1161,4
1196,1
1233,1
1282,9
1337,0
1395,9
1460,2
1530,4
1607,0
1690,4
1781,1
14
16
18
20
22
26
30
35
40
45
50
55
60
65
70
НВг
1005,3
1012,4
1026,9
1
2
4
р, г/л
1041,7
1056,8
1072,3
1088,3
1104,8
1121,9
1139,6
1157,9
1196,1
1236,7
1258,0
1315,0
1377,2
1444,6
1517,3
1595,3
1678,7
1767,5
w,%
6
8
10
12
14
16
18
20
24
28
30
35
40
45
50
55
60
65
HCN
759
80
637
VII. Плотность воды и водных растворов
Продолжение табл.
Р,г/л
752
745
738
731
724
717
711
704
697
i
НСООН
1009,4
1019,7
1024,7
1034,6
1044,2
1053,8
1063,4
1073,0
1082,4
1092,0
1101,6
1110,9
1120,8
1129,6
1138,2
1147,3
1156,6
1165,6
1175,3
1181,9
1189,7
1197,7
1204,5
1211,8
0,%
82
84
86
88
90
У V/
92
94
96
98
4
8
10
14
18
22
30
34
38
42
46
*+о
50
54
58
62
66
70
74
78
82
86
90
94
р,г/л
1218,4
НС1О3
1004,4
1010,3
1022,3
1034,4
1046,8
1059,4
1 аи з
1085,6
1099,1
1113,0
1127,3
1141,9
1156,8
HI
1005,4
1012,7
1027,7
1043,1
1058,9
1074,1
1091,8
1109,1
1127,0
1145,6
1164,9
1205,9
1250,3
1273,7
1335,7
1402,9
1475,5
1560
w,%
98
1
2
4
6
8
10
1 1
14
16
18
20
22
24
1
2
4
6
8
10
12
14
16
18
20
24
28
30
35
40
45
50
р,г/л
1655
1770
1901
ню3
1007,1
1015,7
1033,4
1051,7
1070,6
1090,0
1110,0
1130,6
1151,9
1174,0
1196,9
1220,6
1245,0
1270,0
1295,6
1321,8
1390
1464
ню4
1007,6
1016,5
1034,9
1053,9
1073,7
1094,4
1116,1
1138,8
1162,3
1186,5
1211,6
w,%
55
60
65
1
2
4
6
8
10
1 /ч
12
14
16
18
20
22
24
26
28
30
35
40
1
2
4
6
8
10
12
14
16
18
20
638
VII. Плотность воды и водных растворов
Продолжение табл.
р,г/л
1264,7
1293,1
1323,0
1354,5
1387,5
H2S2O6(O
1005
1011
1022
1034
1046
1059
1072
1085
1099
1113
1127
1142
1157
1173
1189
1205
1245
H2SeO4
1005,9
1013,6
1029,1
1044,7
1060,5
1076,6
1093,1
1110,1
1127,6
»,%
24
26
28
30
32
2)
1
2
4
6
8
10
12
14
16
18
20
22
24
26
28
30
35
1
2
4
6
8
10
12
14
16
Р. г/л
1145,5
1163,9
1206,2
1243,8
1287,4
1333,3
1381,9
1433,6
1489,2
1549
1614
1685
1761
1844
1932
2025
2122
LiOH
1010,2
1021,7
1043,7
1065,0
1086,2
1107,4
' XT XJ
N2H4
1000,2
1001,3
1003,4
1005,6
1007,7
1009,9
1012,1
1014,3
18
20
24
28
32
36
40
44
48
52
56
60
64
68
n
76
80
1
2
4
6
8
10
1
2
4 ,
6
8 ,
10
12
14
p, г/л
1016,4
1018,6
1022,8
1026,7
1030,5
1035
1038
1042
1044
1046
1047
1047
1046
1043
1040
1036
1030
1022
1011
1
NH2OH
1000,2
1002,3
1006,5
1010,5
1014,9
1019,2
1023,5
1027,8
1032,2
1036,6
1045,4
1054,4
1059,1
1063,7
j>t%
16
18
22
26
30
35
40
45
50
55
60
65
70
75
80
85
90
95
100
1
2
4
6
8
10
12
14
16
18
22
26
28
30
639
VII. Плотность воды и водных растворов
Окончание табл.
р, г/л
1075,5
1087,5
1099,7
1112,2
1124,9
ш, %
35
40
45
50
55
RbOH
1008,0
1017,4
1036,8
1056,8
1077,4
1098,7
1120,6
1143,2
1
2
4
6
8
10
12
14
so2
1002,8
0,5
р,г/л
1005,6
1008,5
1011,3
1014,1
1016,8
1019,4
1022,1
1024,8
1027,5
1030,2
1032,8
1035,3
1037,7
w, %
1
1,5
2
2,5
3
3,5
4
4,5
5
. 5,5
6
6,5
7
[SiF6],H2
1007
1015
1031
1
2
4
Р,г/л
1048
1065
1082
1100
1117
1136
1154
1173
1212
1252
1293
1314 .
w,%
6
8
10
12
14
16
18
20
24
28
32
34
Sr(OHJB5 °C)
1000,4
1001,8
1003,2
0,1
0,2
0,3
3. Соли
Приведена плотность р растворов солей при различных значениях
массовой доли w растворенного вещества при указанной температуре.
w,%
1
2
4
6
8
10
12
p, Г/Л
AgFA8°C)
1008,8
1019,1
1039,9
1061,3
1083,8
1107,1
1131,6
w,%
14
\(\
10
18
20
25
30
35
40
50
p, г/л
1157,2
1183,7
1211,0
1239,4
1314,6
1400
1480
1580
1850
AgNO3
1
2
4
6
8
10
12
p, г/л
B0 °C)
1007,0
1015,4
1032,7
1050,6
1068,0
1088,2
1108,0
640 .
VII. Плотность воды и водных растворов
Продолжение табл.
w,°A
14
16
18
20
25
30
35
40
50
60
1
2
4
3
10
12
14
16
18
20
22
1
2
4
6
8
10
i л
12
14
16
>
Р. г/л
1128,4
1149,5
1171,5
1194,2
1254,5
1320,5
1393,1
1474,3
1668,0
1910,0
А1Вг3 B0 °С)
1005,7
1013,3
1028,9
1061,9
1079,2
1096,9
1115,0
1133,6
1152,8
1172,5
1192,8
А1С1, A8 °С)
1005,7
1016,4
1034,4
1052,6
1071,1
1090,0
1109,3
1129,0
1149,1
p, г/л
A1NH4(SO4JA5°C)
1
2
4
6
8
10
12
14
16
18
20
22
24
30
A1(NO3K
1
2
4
6
8
10
12
14
16
18
20
24
28
30
32
A12(SO4K
1
1007,9
1016,7
1034,8
1053,3
1072,9
1099,1
1112,1
1132,0
1154,1
1175,7
1 1 ПТ ?
1197,6
1219,7
1242,0
1309,8
A8 °C)
1006,5
1014,4
1030,5
1046,9
1063,8
1081,1
1098,9
1117,1
1135,7
1154,9
1174,5
1215,3
1258,2
1280,5
1303,6
A9 °C)
1009
2
4
6
8
10
12
14
16
18
20
22
24
26
28
P. г/л
1019
1040
1061
1083
1105
1129
1152
1176
1201
1226
1252
1278
1306
1333
BaBr2B0°C)
2
4
6
8
10
12
14
16
18
20
25
30
35
40
Ba(CF
1
2
4
6
1015,6
1033,5
1051,9
1071,0
1090,7
1111,1
1132,3
1154,3
1177,0
1200,6
1263,4
1332,5
1408,7
1492,6
[3COOJA8°C)
1005,9
1013,3
1028,2
1043,3
641
VII. Плотность воды и водных растворов
Продолжение табл.
И>,%р
8
10
12
14
16
18
20
24
28
30
35
40
Р. г/л.
1058,7
1074,5
1090,8
1107,5
1124,6
1142,1
1159,9
1197,0
1235,6
1255,4
1306,9
1360,8
ВаС12B0°С)
2
4 '
6
8
10
12
14
16
18
20
22
24
26
1015,9
1034,1
1052,8
1072,1
1092,1
1112,8
1134,2
1156,4
1179,3
1203,1
1227,7
1253,1
1279,3
Balj B0 °С)
2
4
6
8
ю.
12
1015,4
1033,1
1051,3
1070,1
1089,6
1109,9
w,%.
14
16
18
20
25
30
35
40
. 50
60
Р. г/л
1130,8
1152,5
1175,0
1198,4
1261,0
1328,9
1404
1490
1698
1970
Ba(NO3J A8 °С)
1
2
4
6
8
10
1007,2
1015,1
1032,0
1049,4
1067,4
1086,0
ВеС12 A8 °С)
2
4
6
8
10
12
14
1011,8
1025,1
1038,6
1052,3
1066,3
1080,6
1095,2
Be(NO3J A8 °С)
2
4
6
8
10
12
1010,8
1023,9
1036,1
1049,1
1062,4
1076,1
и>,%
14
16
18
20
22
24
28
Р. г/л
1090,2
1104,6
1119,3
1134,4
1149,0
1165,7
1198,5
BeSO4 B0 °С)
4
6
8
10
12
1034,2
1052,1
1071,3
1090,6
1109,8
СаВг2 B0 °С)
2 .
4
6
8
10
12
14
16
18
20
25
30
35
40
45
50
1015,2
1032,6
1050,4
1068,8
1087,7
1107,1
1127,2
1148,0
1169,6
1191,9
1249,9
1312,5
1381
1457
1541
1635
Са(СН3СООJ A8 °С)
1
2
1004,3
1010,0
642
VII. Плотность воды и водных растворов
w.%
4
6
8
10
12
14
16
18
20
22
P. г/л
1021,5
1033,1
1044,0
1056,3
1067,9
1079,5
1091,2
1102,9
1114,6
1126,3
СаС12BО°С)
1
2
4
6
8
10
12
14
16
18
20
25
28
30
35
40
1007,0
1014,8
1031,6
1048,6
1065,9
1083,5
1101,5
1119,8
1138,6
1157,8
1177,5
1228,4
1260,3
1281,6
1337,3
1395,7
Ca(HCOOJ A8 °C)
1
2
4
6
8
10
1005,6
1012,6
1026,8
1041,3
1056,0
1070,8
w,%
12
2
4
6
8
10
12
14
16
18
20
25
30
35
40
P. г/л
1085,8
Cal2 B0 °G)
1015,0
1032,3
1050,0
1068,3
1087,3
1106,9
1127,3
1148,5
1170,3
1192,8
1253,0
1319,5
1392,8
1473,4
Ca(NO3J A8 °C)
2
4
0
Q
10
12
14
16
18
20
25
30
35
40
45
2
1013,7
1029,1
1044,8
1060,8
1077,1
1093,7
1110,6 >
1127,9
1145,5
1163,6
1211
- 1259
1311
1366
1423
CdBr2 B0 °C)
_
1015,8
4
6
8
10
12
14
16
18
20
25
30
35
40
2
4
6
8
10
12
14
16
18
20
25
30
35
40
45
50
2
4
6
Продолжение табл.
3
P. г/л
1033,9
1052,4
1071,4
1091,0
1111,2
1132,2
1154,0
1176,6
1200,0
1260,5
1328,6
1404,9
1490,2
CdCl2 B0 °C)
1015,9
1033,9
1052,4
1071,5
1091,2
1111,5
1132,4
1154,0
1176,2
1199,2
1260,4
1327,3
1401,0
1483,3
1574,8
1576,2
Cdl2 B0 °C)
1015,3
1032,8
1050,7
643
VII. Плотность воды и водных растворов
w.%
8
10
12
14
16
18
20
25
30
35
40
p, г/л
1069,0
1087,9
1107,5
1127,8
1148,9
1170,9
1193,7
1254,6
1321,9
1396,7
1480,1
Cd(NO3JA8°C)
2
4
6
8
10
12
14
16
18
20
25
30
35
40
50
1015,4
1032,6
1050,2
1068,3
1086,9
1106,1
1126,1
1146,8
1168,2
1190,4
1248,8
1312,4
1382,2
1459,0
1635,6
CdSO4A8°C)
2
4
6
8
10
1018,2
1038,3
1059,0
1080,3
1102,3
wf°A
12
14
16
18
20
25
30
35
40
1
2
4
6
8
10
12
14
16
18
20
25
30
1
2
4
6
8
10
12
14
16
>
p, г/л
1125,0
1148,5
1172,9
1198,2
1224,2
1294,0
1371,4
1455,1
1547,0
CoBr2 A8 °C)
1007
1016
1035
1054
1073
1094
1115
1137
1159
1182
1207
1272
1344
CoCl2A8°C)
1008
1017
1036
1055
1075
1095
1116
1137
1159
w.%
18
20
Продолжение табл.
p, г/л
1182
1205
Co(NO3JA8°C)
1
2
4
6
8
10
12
14
16
18
20
25
30
(
1
2
6
8
1
2
A*
4
6
8
10
12
14
16
18
20
1007
1015
1032
1049
1067
1085
1104
1123
1143
1163
1184
1240
1300
CoSO4 B5 °C)
1007,2
1017,4
1 лсо о
1058,8
1080,0
CrBr3A8°C)
1007,4
1016 2
1 \J Л. \J)Ai
1034,4
1053,2
1072,6
1092,6
1113,2
1134,5
1156,5
1179,4
1203,1
644
VII. Плотность воды и водных растворов
Продолжение табл.
и>,%
24
30
р, г/л
1253,2
1335,5
СгС13A8°С)
1
2
4
6
8
10
12
14
1007,6
1016,6
1034,9
1053,5
1072,4
1091,7
1111,4
1131,6
CrNH4(SO4JA5°C)
9,6
1,1
2,2
3,3
1008,1
1017,2
1035,7
1054,5
Cr(NO3KA5°C)
1
2
4
6
о
5
10
12
14
16
18
20
22
24
26
28
1007
1015
1032
1049
Шоо
1084
1103
1121
1141
1161
1181
1202
1223
1246
1269
w,%
30
Р, г/л
1293
Cr2(SO4KA5°C)
1
2
4
6
8
10
12
14
16
18
20
22
24
26
28
1009,1
1019,1
1039,5
1060,4
1081,7
1103,4
1125,7
1148,6
1172,2
1196,6
1221,8
1247,9
1275,0
1303,2
1332,5
CsBr B0 °С)
1
2
4
6
8
10
12
14
16
18
20
22
24
30
35
40
. 1006,1
1014,1
1030,5
1047,3
1064,7
1082,7
1101,2
1120,3
1140,1
1160,5
1181,7
1203,6
1226,3
1299,7
1367,6
1442,8
w,%
45
50
р, г/л
1526,3
1619,7
CsCl B0 °С)
1
2
4
6
8
10
12
14
\&
18
20
22
24
30
35
40
50
60
1005,9
1013,7
1029,6
1046,1
1062,9
1080,4
1098,3
1116,8
1135,8
1155,5
1175,8
1196,8
1218,5
1288,2
1352,2
1422,5
1585,8
1788,6
Csl B0 °С)
1
2
4
6
8
10
12
14
16
18
20
22
1006,1
1014,0
1030,8
1047,1
1064,4
1082,3
1100,7
1119,8
1139,5
1159,9
1181,1
1203,1
645
VII. Плотность воды и водных растворов
Продолжение табл.
24
30
35
40
45
50
CsNO3
1
2
4
6
8
10
12
14
Cs2SO4
1
2
4
6
8
10
12
14
16
18,
20
22,
24
26
CuBr2
0,2
р, г/л
1225,8
1299,4
1367,8
1443,5
1528,0
1622,8
B0 °С)
1005,6
1013,2
1028,6
1044,4
1060,7
1077,5
1 Г\С\А ?
1094,6
1112,3
B0 °С)
1006,1
1014,4
1031,6
1049,4
1067,6
1087,0
1107,1
1127,5
1148,7
1169,6
1191,3
1213,7
1237,5 1
1264,3
@°С)
1004
0,4 ,
0,6
0,8 .
1
2
4
6
СиС12
1
2
Ф
6
8
10
12
14
16
1Q
20
22
24
26
Cu(NO3
1
2
4
6
8
10
12
14
16
18
20
р, г/л
1007
1011
1014
1018
1036
1072
1113
B0 °С)
1007
1017
1036
1056
1076
1096
1116
1138
1160
1189
1205
1229
1253
1278
JB0°С)
1007
1015
1032
1050
1069
1088
1107
1126
1147
1168
1189
25
р, г/л
1248
CuSO4 B0 °С)
1
2
4
6
8
10
12
14
16
18
[Fe(CNN]
1
2
4
8
10
12
14
16
18
20
[Fe(CNN]
1
2
4
6
8
10
12
14
1009
1019
1040
1062
1084
1107
1131
1155
1180
1206
К3B0°С)
1003,4
1009,0
1020,1
1031,4
1042,7
1054,2
1065,6
1078,9
1089
1101
1113
К4B0°С)
1005,1
1011,9
1025,6
1039,5
1053,6
1067,8
1082,3
1097,1
646
VII. Плотность воды и водных растворов
Продолжение табл.
16
Р. г/л
1112,0
FeCl2 A8 °С)
1
2
4
6
8
10
12
14
16
18
20
25
1007,5
1016,5
1034,8
1053,5
1072,6
1092,3
1112,6
1133,6
1155,1
1177,1
1199,6
1259,6
FeCl3 B0 °С)
1
2
4
6
8
10
12
14
16
18
20
25
30
35
40
45
50
1007
1015
1032
1049
1067
1085
1104
1123
1142
1162
1182
1234
1291
1353
1417
1485
1551
FeNH4(SO4J A5 °С)
1
1007
2
4
6
8
10
12
14
16
18
20
40
Р. г/л
1016
1032
1050
1068
1086
1104
1122
1141
1161
1181
1380
Fe(N03KA8oC)
1
2
4
6
8
10
12
14
16
18
20
25
1006,5
1014,4
1030,4
1046,8
1063,6
1081,0
1098,9
1117,2
1135,9
1155,1
1174,8
1228,1
FeSO4A8 °C)
1
2
4
6
8
10
12
14
16
1008,5
1018,0
1037,5
1057,5
1078,5
1100,0
1122,0
1144,5
1167,5
и>,%
18
20
р, г/л
1190,5
1213,5
Fe2(SO4KA7,5eC)
1
2
4
6
8
10
12
14
20
25
30
35
40
50
1007
1016
1033
1050
1067
1084
1103
1141
1181
1241
1307
1376
1449
1613
HgCl2 B0 °С)
1
2
3
4
5
1006,5
1015,0
1023,6
1032,3
1041,1
InBr3 A8 °С)
1
2
4
6
8
10
12
14
1007,0
1015,5
1032,9
1050,9
1069,5
1088,8
1108,8
1129,5
647
VII. Плотность воды и водных растворов
w.%
16
18
20
30
p, г/л
1150,8
1172,8
1195,6
1323,0
KA1(SO4JA9°C)
1
2
3
4
5
6
1
2
4
6
8
10
12
14
16
18
20
24
28
30
35
40
]
1
2
3
4
1007,9
1017,4
1027,0
1036,9
1046,5
1056,5
KBr B0 °C)
1005,4
1012,7
1027,5
1042,6
1058,1
1074,0
1090,3
1107,0
1124,2
1141,6
1160,1
1198,0
1238,3
1259,3
1314,7
1374,6
fCBrO3 B0 °C)
1005,6
1013,1
1020,6
1028,2
w.%
5
K(CF
1
2
4
6
8
10
12
14
16
18
20
24
28
35
40
50
60
p, г/л
1035,9
13COO)A8°C)
1003,8
1008,9
1019,1
1029,3
1039,5
1049,7
1059,9
1070,3
1080,8
1091,4
1102,2
1124,4
1146,6
1186,8
1216,2
1276,1
1337,2
K2(C4H4O6)B0°C)
1
2
4
6
8
10
12
16
18
20
22
26
30
35
1004,8
1011,4
1024,8
1038,3
1051,9
1065,7
1079,8
1108,7
1123,6
1138,7
1154,0
1185,5
1218,1
1260,6
W,°/
40
50
1
2
4
6
8
10
12
14
16
18
1
2
4
6
8
10
12
14
16
18
20
24
28
35
40
4b
50
53
1
Продолжение табл.
р, г/л
1305,1
1400,1
KCN A5 °С)
1004,1
1009,2
1019,4
1029,7
1040,1
1050,6
1066,2
1071,8
1082,5
1093,1
К2СО3 B0 °С)
1007,2
1016,3
1034,5
1052,9
1071,5
1090,4
1109,4
1129,1
1149,0
1169,2
1189,8
1232,0
1275,6
1354,8
1414,1
1475,9
1540,4
1567,3
К2С2О4A8°С)
1006,1
648
VII. Плотность воды и водных растворов
Продолжение табл.
W,°/c
2
4
6
8
10
12
14
1
2
4
6
8
10
12
14
16
18
20
22
24
1
2
3
4
5
6
0,2
0,4
0,6
0,8
>
p, Г/Л
1013,6
1028,8
1044,1
1059,6
1075,3
1091,2
1107,2
KCl B0 °C)
1004,6
1011,0
1023,9
1036,9
1050,0
1063,3
1076,8
1090,5
1104,3
1118,5 .
1132,3
1147,4
1162,3
KC1O3A8°C)
1004,9
1011,3
1017,8
1024,5
1031,2
1038,0
KC1O4A5°)
1000,4
1001,6
1002,9
1004,1
1,0
1,2
1,4
1,6
1,8
K2CrO4
1
2
4
6
8
10
12
14
16
18
20
24
28
30
32
36
40
K2Cr2O7
1
2
3
4
5
6
7
8
9
10
p, г/л
1005,4
1006,7
1007,9
1009,2
1010,5
A8 °C)
1006,6
1014,7
1031,1
1047,7
1064,7
1082,1
1099,9
1118,1
1136,6
1155,5
1174,8
1214,7
1256,6
1278,4
1301,0
1347,8
1396,3
B0 °C)
1005,2
1012,2
1019,3
1026,4
1033,6
1040,8
1048,1
1055,4
1062,8
1070,3
w,%
11
12
KCr(SO4)
1
2
4
6
8
P, г/л
1077,9
1085,5
2A5°C)
1008,6
1018,2
1037,6
1057,3
1077,3
KFA8°C)
1
2
4
6
8
10
12
14
16
18
20
22
26
KFe(SO4)
1
2
4
6
8
10
12
14
16
18
1007,2
1015,9
1033,4
1051,2
1069,3
1087,7
1106,4
1125,4
1144,8
1164,6
1184,7
1205,2
1247,1
2A5°C)
1008
1017
1034
1052
1071
1090
1110
1130
1151
1173
649
VII. Плотность воды и водных растворов
ш,%
20
KHCOj
1
2
4
6
8
10
КН2РО<
1
2
4
6
8
10
12
14
Р. г/л
1196
A5 °С)
1005,8
1012,5
1026,0
1039,6
1053,4
1067,4
A0 °С)
1007,0
1014,2
1028,4
1042,5
1056,7
1071,1
1086,3
1102;8
KHS A8 °С)
1
2
4
6
8
10
12
14
16
18
20
24
28
35
1004,5
1010,5
1022,4
1034,3
1046,3
1058,3
1070,4
1082,6
1094,9
1107,2
1119,6
1144,7
1170,1
1215,0
v.%.
40
50
Р. г/л
1247,9
1314,4
KHSO4 A8 °С)
1
2
4
6
8
10
12
14
16
18
20
22
24
26
27
]
1
2
4
6
8
10
12
14
16
20
24
28
35
40
1006
1014
1028
1042
1057
1072
1086
1102
1117
1133
1151
1167
1184
1201
1211
KJ B0 °С)
1005,5
1013,0
1028,1
1043,7
1059,7
1076,1
1093,0
1110,4
1128,4
1166,0
1206,0
1248,7
1330,8
1395,9
50
60
1
2
3
4
5
6
Продолжение табл.
>
р, г/л
1545,8
1731,0
КЮ3A8°С)
1007,7
1015,1
1024,5
1033,3
1042,4
1051,5
/11 /-Ч /1С О/"Ч\
1
2
3
4
5
6
1
2
4
6
8
10
12
14
16
20
24
30
1
1006,0
1013,0
1020,0
1027,1
10334,2
1041,4
KN, B0 °С)
1003
1009
1020
1031
1043
1055
1066
1072
1091
1116
1141
1180
KNCSA8°C)
1003,5
650
VII. Плотность воды и водных растворов
Продолжение табл.
W,%-:
г
6
10
14
18
22
26
30
40
50
60
70
Р. г/л
1008,5
1028,8
1049,5
1070,8
1092,7
1115,2
1138,2
1161,8
1220,0
1284,9
1355,4
1430,7
KNO2 A7,5 °С)
1
2
4
6
8
10
12
14
16
18
22
26
30
35
40
50
60
70
1005
, 1011
1024
1037
1049
1062
1075
1088
1102
1116
1144
1172
1203
1242
1284
1378
1484
1598
KNO3 B0 °С)
I
2
1004,5
1010,8
w,%
4
6
8
10
12
14
16
18
20
22
24
p, г/л
1023,4
1036,3
1049,4
1062,7
1076,2
1089,9
1103,0
1118,1
1132,6
1147,3
1162,3
KNa(CH,.CU B0 PO
1
2
4
6
8
10
12
14
16
18
20
22
24
26
28
32
36
1004,9
1011,6
1025,2
1039,0
1053,0
1067,3
1081,8
1096,5
1111,4
1126,5
1141,9
1157,6 !
1173,5
1189,6
1205,9
1239,4
1274,2
K2S A8 °C) !
1
2
4
6
1009
1017
1033
1049
w,%
8
10
12
14
16
18
20
24
28
35
40
45
P, г/л,
1066
1083
1100
1118
1136
1154
1173
1211
1250
1320
1572
1432
K2SO3 A5 °C)
1
2
4
6
8
10
12
14
16
18
20
22
24
26
1007
1016
1032
1049
1067
1085
1103
1121
1140
1160
1179
1199
1220
1240
K2SO4 B0 °C)
1
2
3
4
5
6
1006
1014
1022 ;
1031
1039
1047
651
VII. Плотность воды и водных растворов
W9%
1
8
9
10
K2Si03
1
2
4
6
8
10
12
14
16
18
20
24
28
K2WO4
1
2
4
6
8
10
12
14
16
18
La(NO3)
1
2
4
p, г/л
1056
1064
1073
1081
B0 °C)
1007
1016
1035
1054
1073
1092
1112
1133
1153
1175
1196
1241
1288
A5 °C)
1007,7
1016,4
1034,1
1052,3
1071,1
1090,5
1110,5
1131,2
1152,7
1175,0
3A8°C)
1007,6
1016,7
1035,3
w,%
6
8
10
12
14
16
18
20
22
24
26
28
30
1
2
4
6
8
10
12
14
16
18
22
26
30
35
40
45
1
2
4
p, г/л
1054,5
1074,2
1094,5
1115,3
1136,8
1158,9
1181,7
1205,2
1229,5
1254,7
1280,9
1308
1336
LiBr B0 °C)
1005,5
1012,8
1027,7
1042,9
1058,5
1074,6
1091,0
1107,9
1125,3
1143,2
1180,6
1220,5
1262,9
1320,4
1383,6
1453,5
LiCl B0 °C)
1004,1
1009,9
1021,5
W,°/c
6
8
10
12
14
16
18
20
24
28
32
36
40
42
1
2
4
6
8
10
12
14
16
18
22
26
30
35
40
50
60
1
Продолжение табл.
P. г/л
1033,0
1044,4
1055,9
1067,5
1079,2
1091,0
1102,9
1115,0
1139,9
1165,8
1194,7
1224
1254
1269
Lil B0 °C)
1005,6
1013,1
1028,4
1044,2
1060,4
1077,1
1094,3
1112,0
1130,3
1149,2
1189,0 '
1231,5
1277,2
1339,3
1407,3
1569,2
1774,8
LiNO3 B0 °)
1004,1
652
VII. Плотность воды и водных растворов
Продолжение табл.
w,%
2
4
6
8
10
12
14
16
18
20
22
26
30
35
40
Li2SO4
1
2
4
6
8
10
12
14
16
18
20
22
24
MgBr2
2
4
6
8
р, г/л
1010,0
1022,0
1031,1
1046,5
1059,0
1071,8
1084,8
1098,1
1111,6
1125,4
1139,5
1168,6
1198,8
1239,2
1283,7
B0 °С)
1006,8
1015,5
1032,9
1050,5
1068,4
1086,3
1104,4
1122,8
1141,1
1159,9
1178,9
1198,4
1218,2
B0 °С)
1015,1
1032,4
1050,1
1068,3
w,%
10
12
14
16
18
20
25
30
35
40
45
р, г/л
1087,1
1106,5
1126,5
1147,1
1168,3
1190,3
1248,2
1311
1379
1452
1532
Mg(CH3COOJA8°C)
1
2
4
6
8
10
1004
1010
1032
1033
1045
1056
MgCl2 B0 °С)
2
8
14
20
26
32
1015,0
1065,4
1119,8
1175,7
1235,3
1297,9
MgCrO4A8°C)
2
4
6
8
10
14
16
1018
1038
1059
1080
1102
1147
1170
w,%
20
2
4
6
8
10
12
14
15
18
20
25
30
35
40
50
55
p, г/л
1219
Mgl2 B0 °C)
1014,9
1032,1
1049,8
1078,0
1086,9
1106,5
1126,8
1137,3
1169,5
1192,0
1251,9
1318,0
1391,4
1473,7
1660,0
1776,0
Mg(NO3JB0°C)
2
4
6
8
10
12
14
16
18
20
22
24
1
2
1013,2
1028,5
1044,1
1060,0
1076,2
1092,8
1109,8
1127,2
1144,6
1163,0
1181,5
1200,4
VIgSO4 B0 °C)
1018,6
653
VII. Плотность воды и водных растворов
Продолжение табл.
w,%
4
6
8
10
12
14
16
18
20
22 ,
24
26
МпВг2
1
2
4
6
8
10
12
14
16
18
20
22
24
30
32
МпС12
1
2
4
6
8
Р. г/л
1039,2
1060,2
1081,6
1103,4
1125,6
1148,4
1171,7
1195,5
1219,8
1244,7
1270,1
1296,1
A8 °С)
1007,1
1015,1
1033,2
1051,1
1069,5
1088,6
1108,3
1128,7
1149,8
1171,6
1194,2
1217,6
1241,9
1320,6
1348,9
A8 °С)
1006,9
1015,3
1032,4
1049,8
1067,6
ш,%
10
12
14
16
18
20
22
24
26;
28
30
Mn(NO3
1
2 .
4
6
8
10
12
14
16
18
20
24
28
30
35
40
50
55
MnSO4
Ц
1
2
4
Р. г/л
1085,9
1104,6
1123,8
1143,5
1163,8
1184,6
1206,1
1228,3
1251,1
1274,6
1298,8
JA8°С)
1006,3
1014,0
1029,8
1045,9
1062,4
1079,4
1096,9
1114,9
1133,3
1152,2
1171,7
1212,5
1255,7
1278,1
1336,7
1399,3
1537,8
1614,6
A5 °С)
1008,9
1018,8
1038,9
и>,%
6
8
10
12
14
16
18
20
22
24
26
28
30
¦ . Р> г/л
1059,5
1080,7
1102,5
1124,8
1147,8
1171,4
1195,6
1220,5
1246,1
1272,5
1299,7
1327,7
1356,5
NH4BrA8<>C)
1
2
4
6
8
10
14
18
22
26
30
34
1004,3
1010,0
1021,5
1033,2
1045,1
1057,2
1082,2
1108,1
1135,2
1163,5
1193,3
1224,7
NH4(CH3COO) A8 "С)
1
2
4
6
8
10
12
1000,8
1003,0
1007,4
1011,7
1015,9
1020,0
1024,0
654
VII. Плотность воды и водных растворов
Продолжение табл.
w,%
14
16
18
20
22
24
26
28
30
Р. г/л
1027,9
1031,8
1035,6
1039,3
1042,9
1046,5
1050,0
1053,5
1056,9
(NH4JCO3A5'C)
1
2
4
6
8
10
12
14
16
18
20
24
28
30
35
40
45
1002,6
1006,1
1013,0
1019,0
1026,7
1033,5
1040,3
1047,1
1053,9
1060,7
1067,5
1080,8
1094,0
1100,6
1115,7
1129,4
1141,7
NH4C1 B0 °С)
1
2
4
6
8
10
1001,3
1004,5
1010,7
1016,8
1022,7
1028,6
w,%
12
14
16
18
20
22
26
p, г/л !
1034,4
1040,1
1045,7
1051,2
1056,7
1062,1
1072,6
(N2H6)Cl3B0°C)
1
2
4
6
8
10
12
14
16
18
1002,6
1007,0'
1015,8
1024,6
1033,4
1042,2
1050,9
1059,6
1068,3
1077,0
NH4FA8°C)
1
2
4
6
8
12
14
1003,4
1008,5
1017,8
1026,5
1034,6
1048,7 ;
1054,7
NH4(HCOO) A5 '€)
1
2
4
6
8
10
1001,9
1004,6
1010,1
1015,5
1020,9
1026,2
w,%
12
14
16
18
22
26
30
35
40
45
50
P. г/л
1031,4
1036,6
1041,8
1046,9
1056,8
1066,5
1076,0
1087,4
1098,4
1108,9
1118,9
NH4I-(t8 4:>
1
2
4
6
10
14
18
22
26
30
35
40
50
1005,0
1011,4
1024,4
1037,7
1065,2
1094,2
1124,8
1157,0
1190,8
1226,5
1274,5
1326,4
1442,3
NH4NCS A8 °C>
1
2
4
6
8
10
12
14
1000,9
1093,2
1007,8
1012,4
1017,0
1021,6
1026,3
1030,9
655
VII. Плотность воды и водных растворов
Продолжение табл.
w,%
16
18
22
26
30
38
46
50
58
р, г/л
1035,6
1040,2
1049,5
1058,9
1064,5
1081,8
1100,7
1110,8
1132,2
NH4NO3 B0 °С)
1
2
4
6
8
10
12
14
16
18
20
24
28
30
35
40
50
55
60
1002,3
1006,4
1014,7
1023,0
1031,3
1039,7
1048,2
1056,7
1065,3
1074,0
1082,8
1100,5
1118,6
1127,5
1151,2
1175,4
1225,8
1252,0
1278,5
(NH3OH)C1A7°C)
1
2
4
6
1004,6
1008,4
1016,7
1025,3
8
10
15
20
25
Р. г/л
1034,0
1043,7
1065,5
1088,8
1112,6
(NH4JSO4 B0 °С)
1
2
4
6
8
10
12
14
16
18
20
24
28
30
35
40
50
Na:
1
2
4
6
8
10
12
1004,1
1010,1
1022,0
1033,8
1045,6
1057,4
1069,1
1080,8
1092,4
1103,9
1115,4
1138,3
1160,9
1172,1
1200,0
1227,7
1282,5
>AsO4A7°C)
1009,7
1020,7
1043,1
1065,9
1089,2
1113,3
1137,3
Na2B4O7A5°C)
0,5
1004,2
w,%
1,0
1,5
2,0
2,5
3,0
3,5
p, г/л
1008,4
1013,1
1017,9
1022,6
1027,4
1032,1
_т»_ /лл cnv
Naor ^zu %*,)
1
2
4
6
8
10
12
16
20
24
28
30
35
40
1006,0
1013,9
1029,8
1046,2
1063,1
1080,3
1098,1
1135,2
1174,5
1216,3
1260,8
1284,1
1346,2
1413,8
NaBrO3 B0 °C)
1
2
4
6
8
10
12
14
16
18
20
22
1006,4
1014,7
1030,5
1047,1
1064,1
1081,6
1099,6
1118,3
1137,3
1156,9
1177,1
1197,9
656
VII. Плотность воды и водных растворов
Продолжение табл.
ш.%
24
p, г/л
1219,3
Na(GH3COO) A8 "С)
1
2
4
6
8
10
12
14
16
18
20
22
24
26
28
1003,3
1008,4
1018,6
1028,9
1039,2
1049,5
1059,8
1070,2
1080,7
1091,3
1102 1
X L\JjL) X
1113,0
1124,0
1135,1
1146,2
Na2CO3 B0 °C)
0,2
2,1
4,0
6,0
7,9
9,8
11,6
13,5
15,2
16,9
17,7
Na-
1
2
3
1000
1020
1040
1060
1080
1100
1120
1140
1160
1180
1190
C,O, B0 °C)
1006,4
1014,7
1022,9
4
1
2
4
6
8
10
12
14
16
18
20
22
24
26
1
2
4
6
8
10
14
18
22
26
30
34
38
Af\
40
]
1
2
p, г/л
1031,2
NaCl B0 °C)
1005,3
1012,5
1026,8
1041,3
1055,9
1070,7
1085,7
1100,9
1116,2
1131,9
1147,8
1164,0
1180,4
1197,2
NaClOA8°C)
1005,3
1012,1
1025,8
1039,7
1053,8
1068,1
1097,7
1128,8
1161,4
1195,3
1230,7
1268,0
1308,5
1 1ЛО С
1328,5
NaClO3A8°C)
1005,3
1012,1
w,%
4
6
8
10
14
18
22
26
30
34
38
40 .
NaClO4
1
2
4
6
8
10
12
14
18
22
26
30
34
38
Na2CrO4
1
2
4
6
8
10
12
p, г/л
1025,8
1 f\^f\ *7
1039,7
1053,8
1068,1
1097,7
1128,8
1161,4
1195,3
1230,7
1268,0
1308,5
1328,5
A8 °C)
1005,1
1011,6
1024,7
1038,1
1051,7
1065,6
1079,8
1094,3
1124,1
1155,4
1188,3
1222,7
1259,1
1296,9
A8 °C)
1007,4
1016,3
1034,4
1052,9
1071,8
1091,2
1111,0
22-2004
657
VII. Плотность воды и водных растворов
Продолжение табл.
w,% >
14
16
18
20
22
24
26
. Р, rj/'л
1131,2
1151,8
1172,8
1194,2
1216,0
1238,3
1261,1
Na2Cr,O, (\S °C)
1
2
4
6
о
8
10
12
14
16
18
22
26
30
35
40
45
50
1006
1013
1027
1041
1 ЛС?
1056
1070
1084,
1098
1112
1126
1153
1179
1207
1244
1279
1312
. 1342
NaFA8°C)
1
2
3
4
5
1009,2
1019,8
1030,4
1040,9
1051,5
NajHAsC^ A4 °С)
1
1009,0
ш,%
2
4
6
8
10
12
14
16
NaHCO
1
2
3
4
5
6
7
8
Р. г/л
1017,5
1035,5
1053,3
1075,5
1096,4
1118,0
1140,6
1163,5
>з A8 "С)
1005,9
1013,2
1020,6
1028,0
1035,4
1042,9
1050,5
1058,1
Na(HCOO) A8 °С)
1
2
4
6
8
10
12
14
16
18
20
22
24
1004,9
1011,2
1023,9
1036,8
1049,8
1063,0
1076,2
1089,5
1102,9
1116,4
1130,0
1143,9
1158,0
NaH2PO4 B5 °С)
1
1004,5
и>,%
2
4
6
8
10
Р. Г/ЯС.;,
1012,0
1027,0
1042,2
1057,5
1073,0
Na2HPO4 A8 °С)
1
2
3
4
5
6
NaHSO3
2
4
6
8
10
12
14
16
18
20
24
28
32
36
38
NaHSO4
1
2
4
6
1009
1020
1031
1043
1055
1067
A5 °С>.
1017 ,
1044
1063
1084
1104
1124
1144
1165
1185
1202
1235
1268
1300
1330
1345
B0 °С)
1005,9
1013,7
1029,3
1045,1
658
VII. Плотность воды и водных растворов
Продолжение табл.
8
10
12
14
16
18
20
22
Р. г/л
1061,1
1077,3
1093,7
1110,3
1127,1
1144,1
1161,4
1178,9
Nal B0 °С)
1
2
4
6
8
10
12
16
20
24
28
35
40
50
60
1006,0
1013,8
1029,8
1046,3
1063,3 ^
1080,8
1098,8
1136,6
11 п с а
1176,9
1220,1
1266,3
1355,6
1427,1
1594,2
1803,8
Na2MoO4 A5 °С)
1
2
4
6
8
10
12
14
16
18
1007,8
1016,5
1034,3
1052,6
1071,3
1090,5
1110,2
1130,4
1151,1
1172,4
20
22
NaN3
1
2
4
6
8
10
12
14
16
18
20
22
24
30
NaNCS
1
2
4
6
8
10
14
18
22
26
30
35
40
45
NaNO2
1
р, г/л
1194,3
1216,8
B0 °С)
1004
1010
1022
1034
1047
1059
1072
1085
1099
1112
1126
1140
1155
1202
A8 °С)
1003,8
1009,0
1019,6
1030,3
1041,1
1052,0
1074,1
1096,6
1119,7
1143,3
1167,7
1196
1228
1265
B0 °С)
1005
2
4
?
6
8
ю-
12
14
16
18
20
24
28
32
36
40
NaNO3
1
2
4
6
8
10
12
14
16
18
20
24
28
30
35
40
45
Na3PO4
1
р, г/л .
1011
1024
1038
1052
1065
1078
1092
1107
1122
1137
1168
1198
1230
1264
1299
B0 °С)
1004,9
1011,7
1025,4
1039,2
1053,2
1067,4
1081,9
1096,7
1111,8
1127,2
1142,6
1175,2
1208,5
1225,6
1270,1
1317,5
1368,3
A5 °С)
1008,7
22*
659
VII. Плотность воды и водных растворов
Продолжение табл.
w.%
2
3
4
5
6
7
8
9
10
Na4P2O7
1
2
3
4
P, г/л
1019,4
1029,9
1040,5
1051,5
1062,4
1073,7
1085,0
1096,2
1108,3
B0 °C)
1009
1019
1028
1037
Na2SA8°C)
1
2
4
6
8
10
12
14
16
18
Na2SO3
1
2
4
6
8
10
12
1010
1021
1044
1067
1091
1115
1139
1163
1189
1214
A9 °C)
1007,8
1017,6
1036,0
1055,6
1075,1
1094,8
1114,6
w.%
14
16
18
XT л С Г
Na2bC
1
2
3
4
5
6
7
8
9
10
11
12
13
14
16
Na2(SO
1
2
4
6
8
-40
12
14
16
18
20
24
28
30
p, г/л
1134,6
1154,9
1175,5
LB0 C)
1007,9
1016,4
1025,6
1034,8
1044,1
1053,5
1062,9
1072,4
1081,9
1091,5
1101,2
1110,9
1120,7
1130,6
1150,6
3S)B0 °C)
1006,5
1014,8
1031,5
1048,3
1065,4
1082,7
1100,3
1118,2
1136,5
1155,1
1174,0
1212,8
1253,2
1273,9
w.%
35
40
Na2Si03
1
2
4
6
8
10
12
14
16
18
20
22
24
26
Na2WO4
1
2
4
6
8
10
12
14
16
18
20
22
26
30
34
38
p, г/л
1327,9
1382,7
A8 °C)
1009,4
1020,3
1042,5
1065,2
1088,4
1112,2
1136,5
1161,3
1186,6
1212,3
1238,5
1265,3
1292,6
1320,4
B0 °C)
1007,4
1016,6
1035,4
1054,5
1074,2
1094,4
1115,4
1137,2
1159,8
1183,3
1207,6
1232,8
1286,2
1344,4
1408,4
1478,6
660
VII. Плотность воды и водных растворов
Продолжение табл.
и>,%
NiBr2
1
2
4
6
8
1 Л
Ш
12
14
16
18
20
25
NiCl2
1
2
4
6
8
10
12
14
16
18
20
Ni(NO3
1
2
4
6
8
10
12
Р. г/л
A8-С)
1007,8
1017,0
1035,9
1055,5
1075,8
1 ГЪО/С О
1\)уЬ,у
1118,8
1141,4
1164,8
1188,9
1214,0
1281,5
A8 °С)
1008
1018
1038
1058
1079
1100
1122
1144
1167
1191
1216
ЬA8 °С)
1007
1016
1033
1051
1069
1088
1108
w,%
14
10
18
20
25
30
35
P. г/л
1128
1 НО
114-5
1169
1191
1249
1311
1378
NiSO4A8°C)
1
2
4
6
8
10
12
14
16
18
1009
1020.
1042
1063
1085
1109
1133
1158
1183
1209
Pb(CH3COOJA8°C)
1
2
4
6
8
10
12
14
16
18
20
24
28
30
35
1006,1
1013,7
1029,0
1044,6
1060,5
1076,8
1093,6
1110,9
1128,3
1147,3
1166,3
1206,3
1248,9
1271,1
1330,4
w,%
40
P. г/л
1399,4
Pb(NO3JA5°C)
5
10
15
25
30
1
2
4
6
8
10
12
14
16
18
20
22
24
30
35
40
45
50
1
2
4
6
8
10
1044,9
1093,7
1146,7
1267,8
1335,8
RbBrB0°C)
1005,9
1013,7
1029,7
1046,0
1062,9
1080,3
1098,2
1116,6
1135,6
1155,3
1175,5
1196,5
1218,2
1287,8
1351,9
1422,3
1500,1
1 СОИ А
1586,4
RbCl B0 °C)
1005,6
1013,0
1043,8
1059,7
1076,0
1092,8
661
VII. Плотность воды и водных растворов
Продолжение табл.
w,°/
12
14
16
18
20
22
24
30
35
40
50
1
2
4
6
8
10
12
14
16
18
20
22
24
30
35
40
45
50
60
1
2
Ь
p, г/л
1110,0
1127,8
1145,9
1164,7
1183,9
1203,8
1266,9
1324,1
1385,9
1453,3
1526,8
RbIB0°C).
1005,9
1013,7
1029,6
1046,0
1062,9
1080,4
1098,4
1117,0
1136,2
1156,0
1176,6
1197,8
1219,8
1290,6
1355,9
1428,1
1507,9
1596,9
1809,2
RbNOj B0 °C)
1005,3
1012,5
w,%.
4
6
8
10
12
14
16
18
20
22
Rb,SO4
1
2
4
6
8
10
12
14
16
18
20
22
26
30
[Sn(OHN],
1,3
2,5
5,0
7,5
10,0
12,5
15,1
17,6
p, г/л
1027,2
1042,2
1057,5
1073,1
1089,2
1105,7
1122,7
1140,1
1158,0
1176,3
B0 °C)
1006,6
1015,0
1032,2
1049,9
1068,0
1086,4
1105,2
1124,6
1144,6
1165,2
1186,4
1208,3
1254,2
1302,8
Na2 B0 °C)
1006
1015
1033
1051
1069
1088
1107
1126
w,%
20,1
22,6
25,1
SrBr2
2
4
6
8
10
12
14
16
18
20
25
30
35
40
50
SrCl2
2
4
6
8
10
12
14
16
18
20
25
30
35
p, г/л,-.
1146
1166
1187
B0 °C)
1015,7
1033,7
1052,2
1071,2
1090,7
1110,9
1131,7
1153,2
1175,7
1199,2
1262
1330
1405
1489
1686
B0 °C)
1016,1
1034,4
1053,2
1072,6
1092,5
1113,0
1134,1
1155,8
1178,1
1201
1260
1325 •
1396
662
Vtl. Плотность воды и водных растворов
14%
Srl2
2
4
6
8
10
12
14
16
18
20
30
40
Sr(NO
2
4
6
8
10
12
14
16
18
20
25
30
35
40
Th(NO
1
2
4
6
P. г/л
B0 °C)
1015,4
1033,1
1051,3
1070,1
1089,6
1109,9
1130,8
1152,6
1175,3
1199,0
1329,5
1490,4
3JB0°C)
1015
1031
1048
1065
1083
1101
1119
1138
1158
1179
1233
1290
1352
1419
зLA5вС)
1007,9
1016,9
1035,4
1054,6
w,°/
8
10
12
14
16
18
1
?
3
4
6
7
1
2
3
4
5
1
2
3
>i
4
P. г/л
1074,7
1095,7
1117,6
1140,4
1164,0
1188,5
T1NO3 B5 °C)
1005,6
1014,2
1023,0
.1031,9
1050,1
1059,4
T12SO4 B0 °C)
1007,6
1017,0
1026,5
1036,0
1045,6
(CH3COOJ B0 °C)
1005,5
1012,9
1020,3
1 ЛТ7 О
1027,5
1
2
4
6
8
1008
1017
1036
1054
1072
w,°A
10
12
14
16
18
20
22
24
30
40
50
2
4
6
8
10
12
14
16
18
20
25
30
35
40
50
2
4
6
8
10
12
Продолжение табл.
p, г/л
1091 '<
1110
1129
1149
1171
1194
1218
1243
1322
1466
1649
ZnBr2 B0 °C)
1016,7
1035,4
1054,4
1073,8
1093,5
1113,5
1138,8
1154,4
1175,3
1196,5
1254,3
1317,0
1385,9
1462
1643
ZnCl2 B0 °C)
1016,7
1035,0
1053,2
1071,5
1089,9
1108,5
663
VII. Плотность воды и водных растворов
Окончание табл.
w,%
14
16
18
20
25
30
40
50
60
, 70
Р. г/л
1127,5
1146,8
1166,5
1186,6
1238,0
1292,8
1417,3
1568,1
1749
1962
Znl2 B0 °С)
2
4
6
8
10
12
14
1016
1034
1053
1072
1091
1111
1131
и?,%
16
18
20
25
30
35
40
45
р, г/л
1152
1174
1197
1258
1325
1398
1478
1566
Zn(NO3JA8°C)
2
4
6
8
10
12
14
16
18
1015,4
1032,2
1049,6
1067,5
1085,9
1104,8
1124,4
1144,5
1165,2
и>,%
20
25
30
35
40
50
р, г/л
1186,5
1242,7
1302,9
1367,8
1437,8
1594,4
ZnSO4 B0 °С)
2
4
6
8
10
12
14
16
20
25
30
1019,0
1040,3
1062,0
1084,2
1107,1
1130,8
1155,3
1180,6
1232
1304
1378
Выдающиеся
ученые-химики
Представлены ученые мира — химики, физики, физикохимики и
инженеры-технологи, внесшие земетный вклад в развитие химии.
Для каждого ученого даны имя и фамилия, даты жизни, сведения
о национальной принадлежности и области научной деятельности, ука-
указаны лауреаты Нобелевских премий (для ученых XX в.). Фамилии ино-
иностранных ученых сопровождаются написанием на языке оригинала.
Авогадро (Avogadro) граф, собств. Амедео ди-Кварёнья-и-Черётто
A776—1856). Итальянский физик и химик.
Агрикбла (Agricola), собств. Георгиус Бауэр A494—1555). Немецкий
химик, металлург и минералог.
Альберт Великий (Albertus Magnus), собств. Альберт фон-Болыитедт
A193—1280). Немецкий алхимик, философ и теолог.
Ампер (Ampere) Андре-Мари A775—1836). Французский физик, хи-
химик и математик.
Анбсов Павел Петрович A799—1851). Русский металлург и химик.
Арведсон (Arfvedson) Юхан-Аугуст A792—1841). Шведский химик и
минералог.
Аррёниус (Arrhenius) Сванте-Аугуст A859—1927). Шведский физико-
химик. Нобелевская премия 1903 г.
Арфведсон см. Арведсон.
Астахов Константин Васильевич A904—1975). Русский химик-неор-
химик-неорганик, физикохимик, педагог.
Ауэр (Auer) Карл, барон фон-Вёльсбах A858—1929). Австрийский
химик.
Ахард (Achard) Франц-Карл A753-1821). Немецкий химик и физик.
Багратион Петр Романович A818—1876). Русский инженер, металлург
и химик.
Бал?р (Balard) Антуан-Жером A802—1876). Французский химик.
Бйртлетт (Bartlett) Нил (род. 1932). Английский химик.
Бауэр см. Агрикбла.
Бакётов Николай Николаевич A827—1911). Русский физикохимик.
Беккерёль (Becquerel) Антуан-Анри A852—1908). Французский физик
и радиохимик. Нобелевская премия 1903 г.
Бембн (Bemont) Жан A857—1932). Французский химик.
665
VIII. Выдающиеся ученые-химики
Бергман (Bergman) Турберн-Улаф A735—1784). Шведский химик, фи-
физик и минералог.
Бертоллё (Bertftdllet) Клод-Луи A748—1822). Французский химик.
Берцёлиус (Berzelius) Йене-Якоб A779—1848). Шведский химик и ми-
минералог.
Бессемер (Bessemer) Хенри A813—1898). Английский металлург, изо-
изобретатель и инженер.
Бёттгер (Bottger) Иоганн-Фридрих A682—1719). Немецкий алхимик,
создатель саксонского фарфора.
Бирингуччо (Biringuccio) Ванноччо A480—1539). Итальянский алхи-
алхимик и металлург.
Блумстранд (Blomstrand) Кристиан-Вильхельм A826—1897). Швед-
Шведский химик.
Бойль (Boyle) Роберт A627—1691). Ирландский физик и химик.
Ббльцман (Boltzmann) Людвиг A844—1906). Австрийский физик-тео-
физик-теоретик.
Ббльштедт см. Альберт Великий.
Ббмбаст-фон-Хбэнхайм см. Парацёльс.
Бор (Bohr) Нильс-Хедрик-Давид A885—1962). Датский физик-теоре-
физик-теоретик! Нобелевская премия 1922 г.
Бранд (Brand) Хенниг A625—1692). Немецкий алхимик.
Брандт (Birandt) Георг A694—1768). Шведский химик и минералог.
Брёнстед (Branstedt) Йоханнес-Николаус A879—1947). Датский физи-
кохимик.
Бройль (Broglie) Луи-Виктор де- A892—1987). Французский физик-
теоретик. Нобелевская премия 1929 г.
Бунзен (Bunsen) Роберт-Вильгельм A811—1899). Немецкий химик и
физик.
Буссенгб (Boussingault) Жан-Батист A802—1887). Фразцуский агрохи-
агрохимик и биолог.
Бутлеров Александр Михайлович A828—1886). Русский химик.
БЗкон (Bacon) Роджер A214—1292/94). Английский алхимик, матема-
математик, физик, астроном, философ и теолог; выдающийся ученый
Средневековья.
Бюссй (Bussy) Антуан-Александр A794—1882). Французский химик.
Вааге см. Воге.
Валь (Wahl) Артур (род. 1917). Американский радиохимик.
Ван-ден-Брук (van den Broek) Антониус A870—1926). Голландский
физик и юрист.
Ван-дер-Ваальс (van derWaals) Иоханнес-Дидерик A837—1923). Гол-
Голландский физик-теоретик. Нобелевская премия 1910 г.
Вант-Гофф (Van't Hoff) Якобус-Хенрикус A852—1911). Голландский
химик. Нобелевская премия 1901 г.
666
VIII. Выдающиеся ученые-химики
Василий Валентин (Ba^ius Wentinus, XIV—XV вв.). Немецкий алхимик.
Приписываемые ему сочинения опубликованы в 1599—1602 гг.,
возможно, написаны несколькими ;авторами не раяее 2-й подови-
ны XVI в.
Вёлер (Wohler) Карл-Фридрих A800—1882). Немецкий химик.
Вёнцель (Wenzel) Карл-Фридрих A740—1793). Немецкий химик.
Вёрнер (Werner) Альфред A866—1919). Швейцарский химик. Нобе-
Нобелевская премия 1913 г.
Вйнклер (Winkler) Клеменс-Александер A838—1904). Немецкий химик.
Виноградов Дмитрий Иванович A720?—1758). Русский химик, созда-
создатель русского фарфора.
Вбге (Waage) Петер A833—1900). Норвежский физикохимик и мине-
минералог.
Воклён (Vauquelin) Никола-Луи A763—1829). Французский химик.
Вулластон (Wollaston) Уилльям-Хайд A766—1828). Английский хи-
химик, физик и врач.
Вюрц (Wurtz) Шарль-Адольф A817—1884). Французский химик.
Г?бер (Haber) Фриц A868—1934). Немецкий химик-технолог. Нобе-
Нобелевская премия 1918 г.
Гадолйн (Gadolin) Юхан A760—1852). Финский химик.
Ган (Gahn) Юхан-Готтлиб A745—1818). Шведский химик и минералог.
Ган (Hahn) Отто A879—1968). Немецкий физик и радиохимик. Нобе-
Нобелевская премия 1944 г.
Гёбер (Geber) собств. Джабйр ибн-Хайян G21—815). Арабский алхи-
алхимик и медик. Приписываемые ему сочинения на латинском языке
созданы, по-видимому, позднее разными авторами с условным
именем «псевдо-Гебер» (XIII—XIV вв.).
Гёйзенберг см. Хайзенберг.
Гей-Люсс?к (Gay-Lussac) Луи-Жозеф A778—1850). Французский фи-
физик и химик.
Гёнкель (Henckel) Иоганн-Фридрих A679—1744). Немецкий минера-
минералог, металлург и химик.
Герман (Hermann) Карл-Самуэль-Леберехт (кон. XVIII — нач. XIX в.).
Немецкий химик.
Гесс Герман Иванович A802—1850). Русский термохимик.
Гиббс (Gibbs) Джосайя-Уиллард A839—1903). Американский физико-
физикохимик.
Гйзель (Giesel) Ф. (нач. XX в.). Немецкий радиохимик.
Гибрсо (Ghiorso) Алберт (род. 1915). Американский радиохимик и физик.
Гитбн-де-Морвб (Guyton de Morveau) Луи-Бернар A737—1816); Фран-
Французский химик и юрист.
Гл?убер (Glauber) Иоганн-Рудольф A604—1670). Немецкий химик,
врач и фармацевт.
667
VIII. Выдающиеся ученые-химики
Глёнденин (Glendenin) Лоренс (род. 1918). Американский радиохимик.
Гмёлин (Gmelin) Кристиан-Готтлиб A792—1860). Немецкий химик.
Грёгор (Gregor) Уилльям A761—1817). Английский минералог и химик.
Гулльберг [Гульдберг] (Guldberg) Като-Максимилиан A836—1902).
Норвежский физикохимик и математик.
Гунд см. Хунд.
Дальтон (Dalton) Джон A766—1844). Английский химик и физик.
Дебай (Debye) Питер-Йозеф-Вилхелм A884—1966). Голландский фи-
физик и химик. Нобелевская премия 1936 г.
Дебьёрн (Debierne) Андре-Луи A874—1949). Французский физик и,
химик.
Демарсё (Demanay) Эжен-Анатоль A852—1904). Французский химик.
Джабйр ибн-Хайян см. Гёбер.
Дорн (Dorn) Фридрих-Эрнест A848—1916). Немецкий физик-экспе-
физик-экспериментатор.
Дыоар (Dewar) Джеймс A842—1923). Шотландский физик и химик.
Дэви (Davy) Хамфри A778—1829). Английский химик и физик.
Дюамёль-де-Монсб (Duhamel de Monceau) Анри-Луи A700—1781).
Французский химик, физик, инженер, ботаник и врач.
Ельм (Hjelm) П. (XVIII в.). Шведский химик.
Жанссён (Janssen) Пьер-Жюль-Сезар A824—1907). Французский аст-
астроном и физик-спектроскопист.
Жолиб [Жолио-Кюрй] (Joliot) Фредерик A900—1958). Французский
физик и радиохимик. Нобелевская премия 1935 г.
Жолио-Кюрй (Joliot-Curie) Ирен A897—1956). Французский физик
и радиохимик. Нобелевская премия 1935 г.
Звара (Zvara) Иво (род. 1934). Чешский радиохимик.
Зйнин Николай Николаевич A812—1880). Русский химик.
Зосйма из Панбполиса (Zosimos Panopolitanus), 3507—400. Греческий
ученый, один из основателей алхимии.
Каблуков Иван Алексеевич A857—1942). Русский физикохимик.
Кавецдиш (Cavendish) Хенри A731—1810). Английский химики и физик.
Канниццйро (Cannizzaro) Станислао A826—1910). Итальянский химик.
Кварёнья-и-Черётто см. Авогадро.
Кёкуле (Kekule), собств. Фридрих-Август Кёкуле-фон-Штрадониц
- A829—1896). Немецкий химик.
Кельвин (Kelvin) лорд, собств. Уилльям Тбмсон A824—1907). Англий-
Английский физик и физикохимик.
Кёсом [Кё(е)зом] (Keesom) Виллем-Хендрик A876—1956). Голланд-
Голландский физик.
Кйрхгофф (Kirchhoff) Густав-Роберт A824—1887). Немецкий физик
и химик-спектроскопист.
668
VIII. Выдающиеся ученые-химики
Кистякбвский Владимир Александрович A865—1952). Русский физи-
кохимик.
Клапрот (Klaproth) Мартин-Генрих A743—1817). Немецкий химик и
минералог.
Кларк (Clark) Франк-Уиглсуорт A847—1931). Американский геохимик.
Клаузиус (Clausius) Рудольф-Юлиус-Эмануэль A822—1888). Немец-
Немецкий физик-теоретик.
Кл&ус Карл Карлович A796—1864). Русский химик.
Клёве (Cleve) Пер-Теодор A840—1905). Шведский химик и минералог.
Кбмптон (Compton) Артур-Холли A892—1962). Американский физик.
Нобелевская премия 1927 г.
Кориелл (Coryell) Ч. (XX в.). Американский радиохимик.
Кбрсон (Corson) Дейл (род. 1914). Американский радиохимик и физик.
Костер (Koster) Дирк A889—1950). Голландский физик-спектроско-
физик-спектроскопист.
Кбхен (Cohen) Эрнст-Юлиус A869—1944). Голландский физикохимик.
Крбнстедт (Cronstedt) Аксель-Фредрик A722—1765). Датский химик,
минералог и геолог.
Крбфорд (Crawford) Адер A748—1795). Английский химик.
Круикшенк см. Крукшанк.
Крукс (Crookes) Уилльям A832—1919). Английский физик-спектро-
физик-спектроскопист и химик.
Крукшанк (Cruikshank) Уилльям A745—1810). Английский химик.
Крэнстон (Cranston) Джон (род. 1891). Английский химик.
Кункель (Kunkel) Иоганн A630/38—1703). Немецкий алхимик.
Курнакбв Николай Семёнович A860—1941). Русский химик.
Куртуа (Courtois) Бернар A777—1838). Французский химик и фарма-
фармацевт.
Курчатов Игорь Васильевич A903—1960). Русский физик-ядерщик.
Кучеров Михаил Григорьевич A850—1911). Русский химик.
Кюри И. см. Жолиб-Кюрй.
Кюри М. см. Склодовская-Кюрй.
Кюри (Curie) Пьер A859—1906). Французский физик и химик. Нобе-
Нобелевская премия 1903 г.
Лабаррйк (Labarraque) Антуан-Жермен A777—1850). Французский
фармацевт и химик.
Лавуазье (Lavoisier) Антуан Лоран-де- A743—1794). Французский хи-
химик, основоположник классической химии.
Ламй (Lamy) Клод-Огюст A820—1878). Французский химик.
Л?ури (Lowry) Томас-Мартин A874—1936). Английский химик.
Лебедев Сергей Васильевич A874—1934). Русский химик.
Леблан (Leblanc) Никола A742—1806). Французский химик-технолог.
Лебб (Lebeau) Поль A868—1959). Французский химик.
669
VIII. Выдающиеся ученые-химики
Лекбк-де-Буабодран (Lecoq de Boisbaudran) Франсуа, собств. имя
Поль-Эмиль A838—1912). Французский химик.
Ле-Шателье (Le Chatelier) Анри-Луи A850—1936). Французский фи-
зикохимик и металловед.
Либйвий (Libavius) Андреас A540/50—1616). Немецкий химик и врач.
Лйбих (Liebig) Юстус фон- A803—1873). Немецкий химик.
Лбкьер (Lockyer) Джозеф-Норман A836—1920). Английский астроном.
Ломонбсов Михаил Васильевич A711—1765). Русский ученый-энцик-
ученый-энциклопедист — математик, физик, химик, минералог, геолог, метал-
металлург, инженер-технолог, астроном, экономист, филолог, поэт, ху-
художник и историк.
Лондон (London) Фриц A900—1954). Немецкий физик-теоретик.
Лоренс (Lawrence) Эрнест-Орландо A901—1958). Американский фи-
физик. Нобелевская премия 1939 г.
Лбури см. Лаури.
Льюис (Lewis) Гилберт-Ньютон A875—1946). Американский физико-
химик.
Мййтнер (Meitner) Лизе A878—1968). Австрийский физик и радио-
радиохимик.
Макёнзи (Mackenzie) Кеннет (род. 1912). Американский радиохимик
и физик.
Макмйллан (McMillan) Эдвин-Маттисон A907—1991). Американский
физик и радиохимик. Нобелевская премия 1951 г.
М?лликен (Mulliken) Роберт-Сандерсон A896—1986). Американский
физикохимик. Нобелевская премия 1966 г.
Мйргтраф (Marggraf) Андреас-Зигисмунд A709—1782). Немецкий хи-
химик и металлург.
Мйрински (Marinsky) Джейкоб (род. 1918). Американский химик.
Мариньяк (Marignac) Жан-Шарль A817—1894). Швейцарский химик.
Маркбвников Владимир Васильевич A837—1904). Русский химик.
Мартен (Martin) Пьер A824—1915). Французский металлург и про-
промышленник.
Мёйер (Martin) Лотар-Юлиус A830—1895). Немецкий химик.
Мёйтнер см. Майтнер.
Менделеев Дмитрий Иванович A834—1907). Русский ученый-энцик-
ученый-энциклопедист — химик, физик, гидродинамик, минералог, геолог, ин-
инженер-технолог, астроном, метеоролог, агроном, метролог, эконо-
экономист, педагог и просветитель.
Мёньё-де-ла-Плас (Meusnier de la Place) Жан-Батист-Мари-Клод
A754—1793). Французский математик, химик и военный инженер.
Мбзли (Moseley) Хенри-Гуин-Джеффрис A887—1915). Английский
физик.
670
VIII. Выдающиеся ученые-химики
Мбзли (Moohs) Фридрих A773—1839). Австрийский и немецкий ми-
минералог. ' .
Mop, (Mohr) Карл-Фридрих A806—1879). Немецкий;химику фарма-
фармацевт, i
Мбсандер (Mosander) Карл-Густав A797—1858). Шведский химик.
Муассан (Moissan) Анри A852—1907). Французский химик и фарма-
фармацевт. Нобелевская премия 1906 г.
Мутман (Muthmann) Фридрих-Вильгельм A861—1913). Немецкий
химик.
Мюллер-фон-Рёйхенштейн (Miiller von Reichenstein) Ференц-Йожеф
A740—1825). Венгерский минералог и горный инженер.
Нернст (Nernst) Вальтер-Фридрих-Герман A864—1941). Немецкий
физик и химик. Нобелевская премия 1920 г.
Нйльсон (Nikon) Ларс-Фредрик A840—1899). Шведский химик.
Нобель (Nobel) Альфред-Бернхард A833—1896). Шведский инженер,
химик, изобретатель и промышленник. Основатель фонда между-
международных Нобелевских премий по химии, физике, физиологии и
медицине, литературе и за деятельность по укреплению мира, при-
присуждаемых ежегодно с 1901 г.
Нбдцак (Noddack) Вальтер-Карл-Фридрих A893—1960). Немецкий
физикохимик.
Нбдцак И. см. Такке-Ноддак.
Оствальд (Ostwald) Вильгельм-Фридрих A853—1932). Немецкий фи-
физикохимик и философ. Нобелевская премия 1909 г.
Парацёльс (Paracelsus), собств. Филипп-Ауреоль-Теофраст.
Бомбаст-фон-Хоэнхайм A493—1541). Швейцарский алхимик и врач.
Шули (Pauli) Вольфганг A900—1958). Швейцарский физик-теоретик.
Нобелевская премия 1945 г.
Пелигб (Peligot) Эжен-Мелыпьор A811—1890). Французский химик.
Пере (Регеу) Маргерит A909—1975). Французский радиохимик.
Пёррьер (Perrier) Карло A886—1948). Итальянский минералог.
Писаржёвский Лев Владимирович A874—1938). Русский химик.
Планк (Planck) Макс-Карл-Эрнст-Людвиг A858—1947). Немецкий
физик-теоретик. Нобелевская премия 1918 г.
Пблинг (Pauling) Лайнус-Карл A901—1994). Американский химик,
физик, биохимик, генетик, иммунолог, общественный деятель.
Нобелевские премии 1954 и 1962 гг.
Потт (Pott) Иоганнес-Генрих A692—1777). Немецкий химик.
Пристли (Priestley) Джозеф A733—1804). Английский химик, филолог
и богослов.
Пруст (Proust) Жозеф-Луи A754—1826). Французский химик и фар-
фармацевт.
671
VIII. Выдающиеся ученые-химики
Райх (Reich) Фердинанд A799—1882). Немецкий физик-спектроско-
физик-спектроскопист и минералог.
Рамз?й (Ramsay) Уилльям A852—1916). Английский химик и физик.
Нобелевская премия 1904 г.
Рёзерфорд (Rutherford) Даниел A749—1819). Шотландский химик, бо-
ботаник и врач.
Рёзерфорд (Rutherford) Эрнест A871—1937). Английский физик и ра-
радиохимик. Нобелевская премия 1908 г.
Рио (Rio) Андрес-Мануэль дель- A764—1849). Мексиканский мине-
минералог и химик.
Рихтер Виктор Юльевич A842—1891). Русский химик.
Рихтер (Richter) Еремиас-Беньямин A762—1807). Немецкий химик.
Рихтер (Richter) Хиронимус-Теодор A824—1898). Немецкий химик.
Рбзе (Rose) Генрих A795—1864). Немецкий химик.
Рбско (Roscoe) Хенри-Энфилд A833—1915). Английский химик.
Руэлль (Rouelle) Гийом-Франсуа A703—1770). Французский химик
и аптекарь.
РЗлей (Rayleigh) лорд, собств. Джон-Уилльям Стретт A842—1919).
Английский физик. Нобелевская премия 1904 г.
Сегрё (Segre) Эмилио-Джино A905—1989). Итальянский физик-экс-
физик-экспериментатор. Нобелевская премия 1959 г.
Семёнов Николай Николаевич A896—1986). Русский физик и химик.
Нобелевская премия 1956 г.
Сент-Клер-Девйлль (Sainte-Claire Deville) Анри-Этьенн A818—1881).
Французский химик и инженер.
Сёренсен (Smrensen) Сёрен-Петер-Лауритс A868—1939). Датский фи-
зикохимик и биохимик.
Сётгерберг (Setterberg) К. (XIX в.). Шведский химик.
Сёфстрём (Sefstrom) Нильс-Габриель A787—1845). Шведский химик
и минералог.
Сйборг (Seaborg) Гленн-Теодор A912—1999). Американский радиохи-
радиохимик и физик. Нобелевская премия 1951 г.
Сйджвик (Sidgwick) Невил-Винсент A873—1952). Английский химик.
Склодбвская-Кюрй (SkJodowska-Curie) Мария A867—1934). Польский
и французский радиохимик и физик. Нобелевские премии 1903
и 1911 гг.
Сбдди (Soddy) Фредерик A877—1956). Английский радиохимик и фи-
физик. Нобелевская премия 1921 г.
Сольвё (Solvay) Эрнест-Гастон A838—1922). Бельгийский химик-тех-
химик-технолог, промышленник и филантроп.
Стретт см. Рэлей.
Такке-Нбддак (Tacke-Noddack) Ида-Эва A896—1978). Немецкий фи-
зикохимик.
672
VIII. Выдающиеся ученые-химики
Тахёний (Tacheniu^) Отто (известен 1644—1678). Немецкий химик,
врач и аптекарь.
Тёллер (Teller) Эдвард A908'—2003). Американский физик-ядерщик.
Тенйр (Thenard) Луи-Жак A777—1857). Французский химик.
Тённант (Tennant) Смитсон A761—1815). Английский химик.
Тбмас (Thomas) Сидни-Джилкрист A850—1885). Английский метал-
металлург.
Тбмсон (Thomson) Джозеф-Джон A856—1940). Английский физик.
Нобелевская премия 1906 г.
Тбмсон У. см. Кельвин
Траверс (Travers) Моррис-Уилльям A872—1961). Английский химик.
Ульба (Ulloa) Антонио де- A716—1795). Испанский математик и путе-
путешественник.
Ублластон см. Вулластон.
Фарадёй (Faraday) Майкл A791-—1867). Английский физик и химик.
Фаянс (Fajans) Казимеж A887—1975). Польский физик и химик.
Ферми (Fermi) Энрико A901—1954). Итальянский физик. Нобелев-
Нобелевская премия 1938 г.
Ферсман Александр Евгеньевич A883—1945). Русский геохимик и ми-
минералог.
Флёров Георгий Николаевич A913—1990). Русский физик-ядерщик
и химик.
Фрйнкленд (Frankland) Эдуард A825—1899). Английский химик.
Френкель Яков Ильич A894—1952). Русский физик-теоретик.
Фуркруй (Fourcroy) Антуан-Франсуа A755—1809). Французский химик.
Хййзенберг (Heisenberg) Вернер-Карл A901—1976). Немецкий физик-
теоретик. Нобелевская премия 1932 г.
Хйтчетт (Hatchett) Чарлз A765—1847). Английский химик.
Хёвеши (Hevesy) Йожеф-Дьёрдь A885—1966). Венгерский радиохи-
радиохимик и физик. Нобелевская премия 1943 г.
Хйсингер (Hisinger) Вильхельм A766—1852). Шведский химик и мине-
минералог.
Холл (Hall) Чарлз-Мартин A863—1914). Американский химик и ин-
инженер.
Хунд (Hund) Фридрих (род. 1896). Немецкий физик-теоретик.
Чёдвик (Chadwick) Джеймс A891—1974). Английский физик. Нобе-
Нобелевская премия 1935 г.
Чугаев Лев Александрович A873—1922). Русский химик.
Шапт?ль (Chaptal) Жан-Антуан-Клод, граф де-Шантелу A756—1832).
Французский химик, инженер-технолог, врач и политический де-
деятель.
Шёеле (Scheele) Карл-Вильхельм A742—1786). Шведский химик и
фармацевт.
673
VIII. Выдающиеся ученые-химики
Шбттки (Schottky) Вальтер A886—1976). Немецкий физик.
Шрёдингер (Schrodinger) Эрвин A887—1961). Австрийский физик-тео-
физик-теоретик. Нобелевская премия 1933 г.
Шрёттер (Schrotter) Антон A802—1875). Австрийский химик.
Штрбмейер (Stromeyer) Фридрих A776—1835). Немецкий химик.
Эйблсон (Abelson) Филип-Хауге (род. 1913). Американский физико-
химик.
Эйнштейн (Einstein) Альберт A879—1955). Немецкий физик-теоретик,
основатель современной физики. Нобелевская премия 1921 г.
Экеберг (Ekeberg) Андерс-Густав A767—1813). Шведский химик и ми-
минералог.
Элуяр (Elhuyar) Фаусто де- A755—1833). Испанский химик и мине-
минералог.
Эрленмейер (Erlenmeyer) Рихард-Аугует-Карл-Эмиль A825—1909).
Немецкий химик.
^ (Oersted, 0rsted) Ханс-Кристиан A777—1851). Датский физик.
(Heroult) Поль-Луи-Туссен A863—1914). Французский металлург.
Юрбен (Urbain) Жорж (J872—1938). Французский химик.
ЙЭри (Urey) Харолд-Клейтон A893—1981). Американский физикрхи-
мик. Нобелевская премия 1934 г.
Ян (Jahn) Г.(ХХ&). Английский физик-теоретик.
Приложения
1. Физические постоянные
Гравитационная постоянная G= 6,67259 * 10"~п м3/(кг • с2)
Скорость распространения электромагнитных колебаний в вакууме
с - 2,99792458 • 108м/с (точно)
Магнитная постоянная (магнитная проницаемость вакуума)
ц0 = 4я • 10 Гн/м (точно)
Электрическая постоянная (диэлектрическая проницаемость ваку-
вакуума) е0 = 8,85418782 • 10~12Ф/м
Постоянная Планка
h = 6,6260755 • Ю-34 Дж • с; h/2n = 1,0545727 • 10~34 Дж • с
Атомная единица массы ти « 1,6605402 • 10"7кг
Масса покоя электрона те = 9,1093897 • 10~31 кг
Масса покоя протона тр = 1,6726231 • 107кг « 1836 те
Масса покоя нейтрона тп = 1,6749286 • 10~27кг » 1839 те
Масса покоя мюона /яц = 1,883566 • 10~28кг
Элементарный электрический заряд е = 1,60217733 • 10~19 Кл
Классический радиус электрона ге = 2,817938 • 10~15м
Радиус Бора а0 = 5,2917706 • 10"~п м « 53 пм
Масса атома изотопа !Н 1,673559 • 10~27кг
Масса атома изотопа 2H(D) 3,344548 • 107кг
Масса атома изотопа 4Не 6,646585 • 10"7кг
Постоянная Авогадро NAw = 6,0221367 • 1023 моль^1
Число Авогадро {NAy} ~ 6,02 • 1023 формульных единиц
Постоянная Фарадея F— 9,6485309 • 104Кл/моль
Постоянная Лошмидта NL = 2,686754 • 1025 м
Универсальная газовая постоянная if = 8,314510 Дж/(К • моль)
Нормальные физические условия:
атмосферное давление р0 = 1,01325 • 105 Па (точно)
термодинамическая температура То = 273,15 К (точно)
температура Цельсия /0 = 0 °С
Молярный объем идеального газа при нормальных физических усло-
условиях VM = 2,241108 • 10~2 м3/моль « 22,4 л/моль
675
Приложения
Постоянная Больцмана к= 1,380658 • 10~23Дж/К
Постоянная Стефана-Больцмана а = 5,67051 • 10~8 Вт/(К4 • м2)
Постоянная Вина Ъ - 2,987790 • 10 К • м
Постоянная Ридберга R^ = 1,0973731534 • К^м
Магнетон Бора цв = 9,2740154 • 104 А • м2
Магнитный момент электрона \хе = 9,2847701 • 10~24 А • м2
Стандартное ускорение свободного падения gu = 9,80665 м/с2 (точно)
Средняя плотность сухого воздуха 1,2925 г/л (при н. у.)
Средняя относительная молекулярная масса сухого воздуха 28,966 ти
2. Физические величины и единицы СИ
Величина
Единица СИ
Атомная масса (относительная) АТ
Внутренняя энергия U
Волновое число v
Время т
Давление/?
Дипольный момент/?
Диэлектрическая проницаемость
(относительная) ег
Длина/
Длина волны X
Импульс р
Количество вещества п
Количество теплоты Q
Количество электричества q
Магнитный момент jljl
Масса m
Массовая доля w
Массовая концентрация у,
Молекулярная масса
(относительная) Мт
Мольная доля х
Молярная масса М
Молярный объем VM
Моляльная концентрация ст
Молярная концентрация с
атомная единица массы, а.е.м.
джоуль, Дж
метр в минус первой степени, м
секунда, с
паскаль, Па
кулон-метр, Кл • м
метр, м
метр, м
килограмм-метр в секунду, кг • м/с
моль, моль
джоуль, Дж
кулон, Кл
ампер-квадратный метр, А • м2
килограмм, кг
килограмм на кубический метр,
кг/м3
атомная единица массы, а.е.м.
килограмм на моль, кг/моль
кубический метр на моль, м3/моль
моль на килограмм, моль/кг
моль на кубический метр, моль/м3
676
Приложения
Продолжение табл.
Величина
Мощность Р
Объем V
Объемная доля v
Плотность р
Плотность относительная d
Площадь А
Поверхностное натяжение а
Работа W
Разность потенциалов AV
Сила/*
Сила света /
Скорость реакции v
Сродство к протону Ар
Сродство к электрону Ае
Температура термодинамическая Т
Температура Цельсия t
Теплоемкость С
Теплопроводности коэффициент X
Угол плоский а
Угол телесный со (а)
Химический потенциал вещества \i
Частота v
Электрическая проводимость X
Электрический заряд
(относительный) v±
Электрический потенциал V
Электрический ток /
Электрическое напряжение U
Электрическое сопротивление R
Электродвижущая сила АЕ
Электродный потенциал <р
Энергия Е
Энергия Гельмгольца А
Энергия Гиббса образования
вещества AG
Единица СИ
ватт, Вт
кубический метр, м3
—
килограмм на кубический метр,
кг/м3
—
квадратный метр, м2
джоуль на квадратный метр, Дж/м2
ньютон на метр, Н/м
джоуль, Дж
вольт, В
ньютон, Н
кандела, кд
моль в секунду, моль/с
джоуль, Дж
джоуль, Дж
кельвин, К
градус Цельсия, °С
джоуль на кельвин, Дж/К
ватт на метр-кельвин, Вт/(м • К)
радиан, рад
стерадиан, ср
джоуль на моль, Дж/моль
герц, Гц
сименс, См
элементарный электрический
заряд, э.э.з.
вольт, В
ампер, А
вольт, В
ом, Ом
вольт, В
вольт, В
джоуль, Дж
джоуль, Дж
джоуль на моль, Дж/моль
677
Приложения
Окончание табл.
Величина
Энергия Гиббса реакции AG'
Энергия ионизации /
Энтальпия образования вещества
АН
Энтальпия реакции АН
Энтропия вещества S
Энтропия реакции AS
Единица СИ
джоуль, Дж
джоуль, Дж
джоуль на моль, Дж/моль
джоуль, Дж
джоуль на кельвин-моль,
Дж/(К • моль)
джоуль на кельвин, Дж/К
3. Соотношения между единицами
Приведены соотношения между единицами СИ и внесистемными
единицами.
1 мин (минута)
1ч(час)
1 сут (сутки)
1 год (год)
Время
60 с
60 мин, 3,6- 103с
24 ч, 1440 мин, 8,64 • 104с
365,242 сут, 3,1557 • 107с
Давление
1 атм (физическая атмосфера)
1 мм рт.ст. (миллиметр ртутного
столба)
1 Торр (торр)
1 ат (техническая атмосфера)
1 кгс/м2 (килограмм-сила на квад-
квадратный метр)
1 мм вод. ст. (миллиметр водяного
столба)
1,01325 • 105Па, lOOjtfla, 0,1 МПа,
760 мм рт.ст.
1,33322-102 Па
1,33322- 102Па, 1мм рт.ст.
9,80665 ЧО4 Па
9,80665 Па, 1 • 10 ат
9,806^5 Па, 1 кгс/м2,1 • 10~4ат
Г Д (дебай)
Дщюлышй момент
Т 3,33564-100 Кл-м
1 мк (микрон)
1А (ангстрем)
Длина
1-10м
1-10-10м
Приложения
Окончание табл.
1 т (тонна)
1 кар (карат)
Масса
1-103кг
2-Ю-4 кг
1 л (литр)
Объем
1-10-3м3
Г (градус)
Г (минута)
1" (секунда)
Плоский угол
(я/180) рад («0,0175 рад), 60'
(я/10800) рад (« 2,909 • 10 рад), 60й
(я/648000) рад (~ 4,848 • 10~6 рад)
1 кгс (килограмм-сила)
1 дин (дина)
Сила
9,80665 Н
1 • Ю-5 Н
Энергия
1 эВ (электронвольт)
1 кал^ (термохимическая калория)
1 калм (международная калория)
1 эрг (эрг)
1 кгс • м (килограмм-сила — метр)
1 л • атм (литр-атмосфера)
1 Вт • ч (ватт-час)
- 1,60218 • 109Дж
4,184 Дж (точно)
4,1868 Дж
1 • 10Дж
9,80665 Дж
1,01325 • 102Дж
3,60-103Дж
1 э.е. (энтропийная единица)
Энтропия
| 4,184Дж/К
4. Приставки для образования кратных
и дольных единиц
Приставка
Тера, Т
Гига, Г
Мега, М
Кило, к
Множитель
1012
109
106
103
Приставка
Гекто, г
Дека, да
Деци, д
Санти, с
Множитель
102
10*
ю-1
10
Приставка
Милли, м
Микро, мк
Нано, н
Пико, п
Множитель
ю-3
ю-«
ю-9
ю-12
679
Приложения
5. Латинский и греческий алфавиты
Латинские буквы
Печатные
Аа
ВЬ
Сс
Dd
Ее
Ff
Gg
Hh
Ii
Jj
Kk
LI
M m
Рукописные
Cc
Dd
Wf
%s
li
3i
Kk
?1
Mm
Названия
a
бэ
ЦЭ
ДЭ
э(е)
эф
гэ (жэ)
га (аш)
и
йот
ка
эль
эм
Печатные
Nn
Оо
Рр
Qq
Rr
Ss
Tt
Uu
Vv
Ww
Xx
Yy
Zz
Рукописные
0 о
Pf>
Qi
Яг
§8
$t
Uu
Yv
Ww
X x
Zz
Названия
эн
0
пэ
ку
эр
эс
тэ
У
вэ
дубль вэ
икс
игрек
зет(а)
Греческие буквы
Печатные
Аа
вр
Гу
А8
Ее
ZC.
09
Названия
альфа
бета
гамма
дельта
э псилон
(д) зета
эта
тета
Печатные
И
Кк
АХ
M|i
Nv
5^
Оо
Птс
Названия
йота
каппа
ламбда
ми (мю)
ни (ню)
кси
о микрон
пи
Печатные
Рр
IG
Тт
Yd
Фф
х%
Названия
ро
сигма
тау
и псилон
фи
хи
пси
омега
Список литературы
1. Pure and Appl. Chem. 1984, v. 56, № 5, p. 654.
2. Термические константы веществ. Справочник / Под ред.
В. П. tлушко. — М.: Изд-во ВИНИТИ, 1965 и след.
3. Руководство по неорганическому синтезу / Под ред. Г. Брауэра. —
М.: Мир, 1985-1986.
4. Справочник химика / Под ред. Б. П. Никольского. — Л.: Химия,
1962-1965. 1971.
5. Handbook of Chemistry and Physics. — Cleveland: Chem. Rubber
Co., 1982.
6. Gmelins Handbuch der anorganischen Chemie. — Berlin, 1924.
7. Некрасов Б. В. Основы общей химии. — М.: Химия, 1973.
8. Реми Г. Курс неорганической химии. — М.: Мир, 1972—1974.
9. Турова Н. Я. Справочные таблицы по неорганической химии. —
Л.: Химия, 1977.
10. Ефимов А. И. и др. Свойства неорганических соединений. Спра-
Справочник/А. И. Ефимов, Л. П. Белорукова, И. В. Василькова, В. П. Че-
чев. — Л.: Химия, 1983.
11. ГурвичЛ. В. и др. Энергии разрыва химических связей. Потен-
Потенциалы ионизации и сродство к электрону / Л. В. Гурвич,
Г. В. Караченцев, В. И. Кондратьев. — М.: Наука, 1974.
12. Осипов О. А. и др. Справочник по дипольным моментам /
О. А. Осипов, В. И. Минкин, А. Д. Гарновский. — М.: Высшая школа,
1971.
13. Краснов К. С. и др. Молекулярные постоянные неорганических
соединений / К. С. Краснов, Н. В. Филиппенко, В. А. Бобкова. — Л.:
Химия, 1979.
14. Термодинамические свойства индивидуальных веществ. Спра-
Справочное издание. — М.: Наука, 1978—1983.
15. Наумов Г. Б. и др. Справочник термодинамических величин /
Г. Б. Наумов, Б. Н. Рыженко, И. Л. Ходаковский. — М.: Атомиздат,
1971.
16. Рид Р. и др. Свойства газов и жидкостей / Р. Рид, Д. Праусниц,
Т. Шервуд. — Л.: Химия, 1982.
681
'Список литературы
17. Карапетьянц М. X. Введение в теорию химических процессов.
— М.: Высшая школа, 1981.
18. ДобошД. Электрохимические константы. — М.: Мир, 1980.
191 Альберт А., Сержент Е. Константы ионизации кислот и основа-
оснований. - Л. - М.: Химия, 1967.
20. Назаренко В. А. и др. Гидролиз ионов металлов в разбавленных
растворах / В. А. Назаренко, В. П. Антонович, Е. М. Невская. — М.:
Атомиздат, 1979.
21. Яцимирский К. Б., Васильев В. П. Константы нестойкости комп-
комплексных соединений. — М.: Изд-во АН СССР, 1959.
22. Лурье Ю. Ю. Справочник по аналитической химии. — М.: Хи-
Химия, 1989.
23. Минералы. Справочник / Под ред. Ф. В. Чухрова. — М.: Наука,
1960-1981.
24. Минералогические таблицы. Справочник / Под ред. Е. И. Се-
Семенова. — М., Недра, 1981.
25. Фундаментальные физические константы. — М.: Изд-во стан-
стандартов, 1979.
26. Минералогическая энциклопедия / Под ред. К. Фрея. — Л.:
Недра, 1985.
27. Химический энциклопедический словарь / Под ред. И. Л. Кну-
Кнунянца. — М.: Советская Энциклопедия, 1983.
28. Анорганикум / Под ред. Л. Кольдица. — М.: Мир, 1984.
29. Джонсон Д. Термодинамические аспекты неорганической
химии. — М.: Мир, 1985.
30. Лидин Р. А. и др. Основы номенклатуры неорганических ве-
веществ / Р. А. Лидин, В. А. Молочко, Л. Л. Андреева, А. А. Цветков. —
М.: Химия, 1983.
31. Кан Р., Дермер О. Введение в химическую номенклатуру. — М.:
Химия, 1983.
32. ХьюиД. Неорганическая химия. Строение вещества и реакци-
реакционная способность. — М.: Химия, 1987.
33. Лидин Р. А. и др. Справочник по неорганической химии. Конс-
Константы неорганических веществ / Р. А. Лидин, Л.Л.Андреева,
В. А. Молочко. — М.: Химия, 1987.
34. Шрётер В. и др. Химия. Справочник / В. Шрётер, К.-Х; Лаутен-
шлегер, X. Бибрак. — М.: Химия, 2000.
35. Химическая энциклопедия / Под ред. И. Л. Кнунянца и
Н. С. Зефирова. — М.: Советская Энциклопедия, 1988—1990; Боль-
Большая Российская Энциклопедия, 1992—1998.
36. Номенклатурные правила ИЮПАК по химии. — М.: Изд-во
ВИНИТИ, 1979-1988.
682
Список литературы
37. Lidin R. A. et al. Constants of Inorganic Substances. Handbook /
R. A. Lidin, L. L. Andreeva, V. A. Molochko. — New York: Begell House,
1995.
38. Lidin R. A. et al Reactivity of Inorganic Substanpes. Handbook /
R. A. Lidin, V. A. Molochko, L. L. Andreeva. — New Ybrlc BegeH House,
1996.
39. Lidin R. A. Inorganic Substances. Handbook. — New York: Begell
House, 1996.
40. Block P. et al. Inorganic Chemical Nomenclature. Principles and
Practice / P. Block, W. Powell, C. Fernelius. — Washington: Amer. Chem.
Society, 1990.
41. Суссик-Форнефелъд К. Драгоценные камни и минералы.
Справочник. — М.: Изд-во АСТ-Астрель, 2001.
42. Taschenbuch der Chemie / Herausgeber К. Schwfster. — J^eipzjg:
Fachbuchverlag, 1995.
43. Волков В. А. и др. Выдающиеся химики мира /В. А. Волков,
Е. В. Вонский, Г. И. Кузнецова. — М.: Высшая школа, 1991.
Оглавление
I. Неорганические вещества
1. Классификация 3
2. Номенклатура ИЮПАК 9
2.1. Современные номенклатурные правила 9
2.2. Тривиальные названия веществ и смесей 18
2.3. Несуществующие вещества 22
2.4. Рекомендуемые формулы и названия 24
3. Физические свойства 70
4. Минералы 192
Указатель названий 291
Русские названия B91). Английские названия C11)
Указатель рудных минералов 332
Указатель драгоценных, полудрагоценных и поделочных камней .. 332
II. Химические элементы. Атомы
1. Названия и символы элементов. Порядковые номера.
Степени окисления 333
2. Относительные атомные массы. Электронные формулы. Радиусы.. 336
3. Изотопы 342
3.1. Природные изотопы 342
3.2. Радиоактивные изотопы 347
4. Энергия ионизации. Сродство к электрону и протону.
Электроотрицательность 350
5. Распространение в природе 353
5.1. Физическая распространенность 353
5.2. Химическая распространенность 354
5.3. Элементный состав земной коры 354
5.4. Жизненно важные элементы 355
6. Открытие элементов 356
6.1. Исторические периоды развития химии 356
6.2. Даты и приоритеты открытия 356
7. Происхождение русских и латинских названий и символов
элементов .. 361
8. Названия элементов на английском, французском, немецком
и испанском языках 368
684
Оглавление
III. Молекулы. Ионы. Радикалы
1. Энергия ионизации 372
2. Сродство к электрону 374
3. Сродство к протону 376
4. Дипольные моменты 376
5. Энергия и длина связи для двухатомных частиц 378
6. Энергия связи для многоатомных частиц 384
7. Строение многоатомных частиц 392
7.1. Геометрическая форма, длина связей и валентные углы
в частицах с одним центральным атомом 5р-элемента 392
7.2. Геометрическая форма, длина связей, магнитные моменты
и окраска в частицах с одним центральным атомом
^-элемента 408
7.3. Геометрическая форма, длина связей и валентные углы
в частицах с несколькими центральными атомами 428
IV. Термодинамика
1. Энтальпия образования, энтропия и энергия Гиббса
образования веществ 439
2. Энтальпия и энтропия фазовых переходов 527
V. Вещество в водном растворе
1. Электродные потенциалы окислительно-восстановительных пар .. 552
2. Константы кислотности кислотно-основных пар 578
3. Константы устойчивости одноядерных комплексов 587
4. Произведения растворимости 597
VI. Растворимость веществ в воде
1. Твердые вещества 618
2. Газы и жидкости 630
VII. Плотность воды и водных растворов
1. Вода при различных температурах 633
2. Кислоты и основания 633
3. Соли 640
VIII. Выдающиеся ученые-химики
Приложения:
1. Физические постоянные 675
2. Физические величины и единицы СИ 676
3. Соотношения между единицами 678
4. Приставки для образования кратных и дольных единиц 679
5. Латинский и греческий алфавиты 680
Список литературы 681
685
Справочное издание
Лидин Ростислав Александрович
Андреева Лариса Леонидовна
Молочко Вадим Александрович
КОНСТАНТЫ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Справочник
Зав. редакцией Б. В. Понкратов
Ответственный редактор В. К Бораненкова
Художественный редактор О. В. Матоянц
Технический редактор Н. И. Герасимова
Компьютерная верстка О. И. Колотова
Корректор Я. С. Соболева
Санитарно-эпидемиологическое заключение
№ 77.99.02.953.Д.006315.08.03 от 28.08.2003.
Подписано к печати 31.10.05. Формат 60x90Vu,.
Бумага офсетная. Гарнитура «Ньютон». Печать офсетная.
Усл. печ. л. 43,0. Тираж 3000 экз. Заказ № 2004.
ООО «Дрофа». 127018, Москва, Сущевский вал, 49.
По вопросам приобретения продукции
издательства «Дрофа» обращаться по адресу:
127018, Москва, Сущевский вал, 49.
Тел.: @95) 795-05-50, 795-05-51. Факс: @95) 795-05-52.
Торговый дом «Школьник».
109172, Москва, уд. Малые Каменщики, д, 6, стр. 1А.
Тел.: @95) 911-70-24, 912-15-16, 912-45-76.
Магазины «Переплетные птицы»:
127018, Москва, ул. Октябрьская, д. 89, стр. 1.
Тел.: @95) 912-45-76;
140408, Московская обл., г. Коломна, Голутвин,
ул. Октябрьской революции, 366/2.
Тел.: @95) 741-59-76.
Отпечатано в полном соответствии
с качеством предоставленных диапозитивов
в ОАО «Можайский полиграфический комбинат».
143200, г. Можайск, ул. Мира, 93.
КНИГИ ИЗДАТЕЛЬСТВА «ДРОФА»
Одно из ведущих в России
издательств учебной литературы
предлагает вашему вниманию
литературу для высших учебных заведений.
Серия «СОВРЕМЕННЫЙ УЧЕБНИК»
Уважаемые преподаватели и студенты!
Книги этой серии призваны подвести некоторые итоги работы
российских ученых и педагогов по созданию базовых учебников
для студентов высших учебных заведений.
В рамках данной серии издаются следующие книги
по химии:
ОРГАНИЧЕСКАЯ ХИМИЯ
Под общей редакцией профессора Н. А. Тюкавкиной.
• «Органическая химия». Основной курс. Книга 1.
• «Органическая химия». Специальный курс. Книга 2.
• «Руководство к лабораторным занятиям
по органической химии».
БИОХИМИЯ
В. П. Комов, В. Н. Шведова.
• «Биохимия».
Под общей редакцией профессора В. ("I. Комова.
• «Практикум по биохимии».
БИООРГАНИЧЕСКАЯ ХИМИЯ
Н. А. Тюкавкина, Ю. И. Бауков.
• «Биоорганическая химия».
Под общей редакцией профессора Н. А. Тюкавкиной.
• «Руководство к лабораторным занятиям
по биоорганической химии».
КНИГИ ИЗДАТЕЛЬСТВА «ДРОФА»
Комплект для студентов вузов, обучающихся
по химико-технологическим специальностям
УЧЕБНИК: В. П. Васильев.
• «Аналитическая химия. В 2 кн. Кн. 1. Титриметрические
и гравиметрический методы анализа».
В учебнике изложены теоретические основы титриметрических
и гравиметрического методов анализа, указаны условия и области
применения, их достоинства и недостатки, метрологические харак-
характеристики.
УЧЕБНИК: В. П. Васильев.
"• «Аналитическая химия. В 2 кн. Кн. 2.
Физико-химические методы анализа».
В учебнике изложены теоретические основы физико-химических
методов анализа, указаны области практического применения, их
значение и ограничение, средства и методы оперативного анали-
аналитического контроля, применение тест-методов и сенсоров в анализе.
П О С О Б И Е: В. П. Васильев, Л. А. Кочергина, Т. Д. Орлова.
• «Аналитическая химия. Сборник вопросов, упражнений
и задач».
В сборнике приведены вопросы, упражнения и задачи, связанные
с теоретическим расчетом полноты протекания химико-аналитических
реакций в заданных концентрационных условиях, а также по расчетам
массы навески, концентрации, объемов растворов и т. д.
П О С О Б И Е: В. П. Васильев, Р. П. Морозова, Л. А. Кочергина.
• «Аналитическая химия. Лабораторный практикум».
Практикум состоит из трех частей. Первая часть содержит общие
сведения о технике безопасности и проведении основных химико-
аналитических операций и метрологии анализа. Вторая часть
представляет собой описание 50 работ по химическим методам
анализа. В третьей части изложены основы и техника выполнения
75 работ с применением приборов отечественного производства.