Author: Васильев Б.Т. Отвагина М.И.
Tags: производство серы и её производных химия химическая технология
Year: 1985
Text
Б.Т Васильев
М.И.Отвагина
ТЕХНОЛОГИЯ
СЕРНОЙ
КИСЛОТЫ
S/О ДИ-Ж
3 3 7 3 3 3^ J 2^ Г1 *
БИ&5И&Т.ША
МОСКВА ХИМИЯ 1985
6П7.2
В 191
УДК 661.25
Васильев Б. Т., Отвагина М. И.
Технология серной кислоты. — М.: Химия, 1985,
384 с., ил.
Рассмотрены теоретические основы и аппаратурно-технологическое
оформление всех стадий технологического процесса производства серной
кислоты. Особое внимание обращено на максимальное использование энер-
гетических ресурсов, определение оптимальной единичной мощности тех-
нологических линий, применение новых высокоэффективных аппаратов, соз-
дание безотходной технологии. Показаны перспективные направления тех-
нического развития сернокислотного производства: применение кислорода,
повышенного давления, циркуляционных систем и т. д.
Предназначена для инженерно-технических работников предприятий
практически всех отраслей химической промышленности, а также цвет-
ной металлургии.
384 с., 94 табл., 113 рис., 215 литературных ссылок.
Рецензенты: 1. Докт. техн, наук профессор
И. П. МУХЛЕНОВ.
2. Инженер В. Я. ДРОЗДОВСКИЙ
2802020000-062
---------------62.85
050(01)-85
© Издательство «Химия», 1985
СОДЕРЖАНИЕ
Предисловие ............................................. 6
ГЛАВА I. ОБЩИЕ СВЕДЕНИЯ . ................................. 8
1.1. Развитие и современное состояние сернокислотной про-
мышленности ...................................... 8
1.2. Свойства и применение серной кислоты ... . 13
12.1. Физические свойства водных растворов серной кислоты,
олеума, диоксида и триоксида серы................... 13
1.2.2. Химические свойства диоксида и триоксида серы, серной
кислоты и основные направления ее использования . . 23
1.3. Сырье для производства серной кислоты..........27
13.1. Сера...........................................28
1.3.2. Колчеданы..................................... 35
1.3.3. Диоксид серы металлургических и топочных газов . . 39
1.3.4. Сульфаты............................................. 40
1.3.5. Отработанные кислоты...........................41
ГЛАВА II. ОБЖИГ СЕРОСОДЕРЖАЩЕГО СЫРЬЯ .... 43
11.1, Обжиг колчедана............................. .... 43
II. 1.1. Физико-химические основы обжига колчедана в воздухе 43
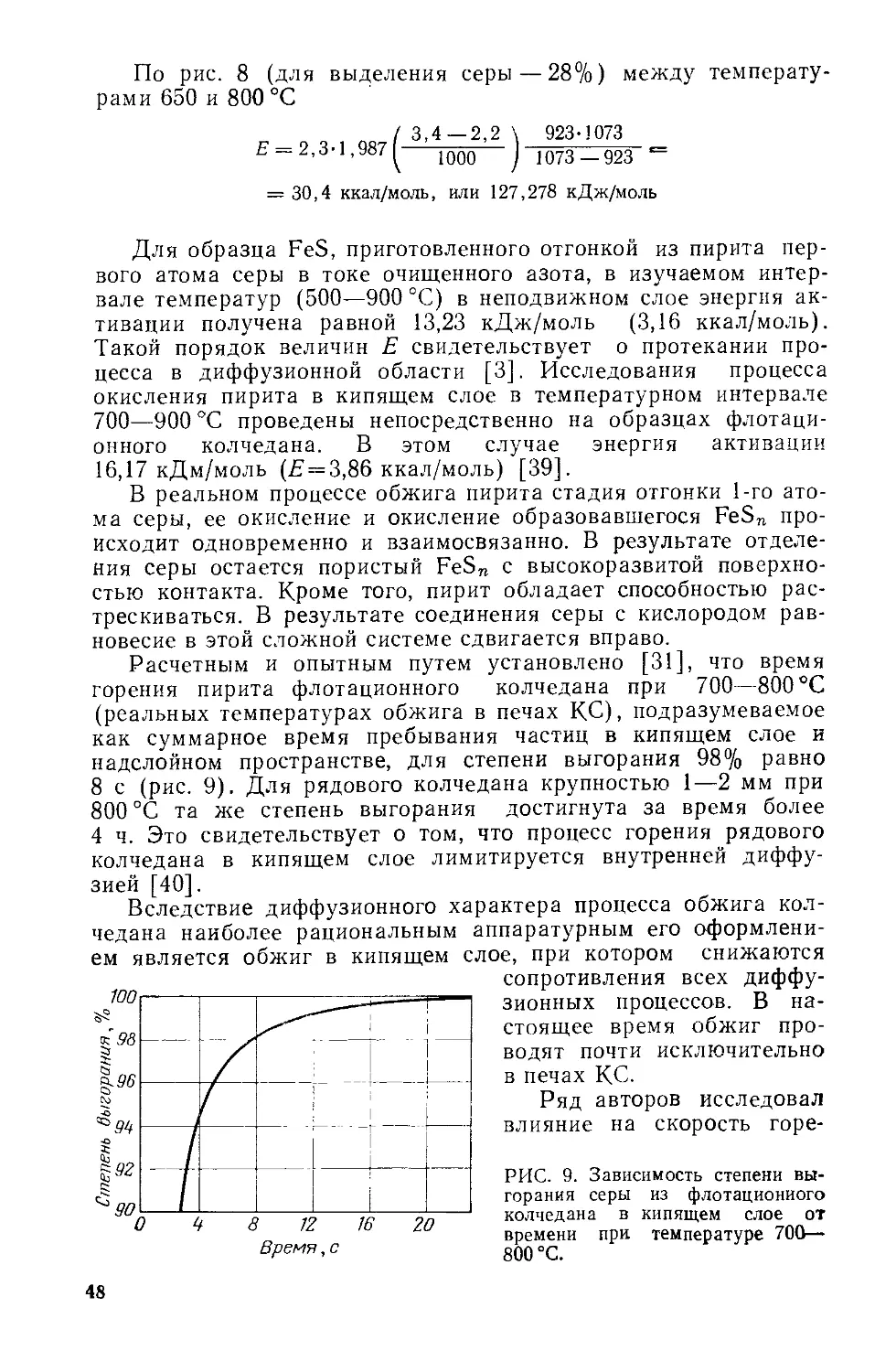
II. 1.2. Поведение примесей колчедана в процессе его обжига 49
II.1.3. Образование триоксида серы и спекание шихты при об-
жиге колчедана . ............................ 54
II. 1.4. Обжиг колчедана при использовании циркулирующего
огарка................................................58
II. 1.5. Основы гидродинамики кипящего слоя колчеданного огар-
ка, интенсивность обжига...................... . 66
II.1.6. Теплообмен в печах КС................. . . 70
II. 1.7. Условия охлаждения обжигового газа.................. 72
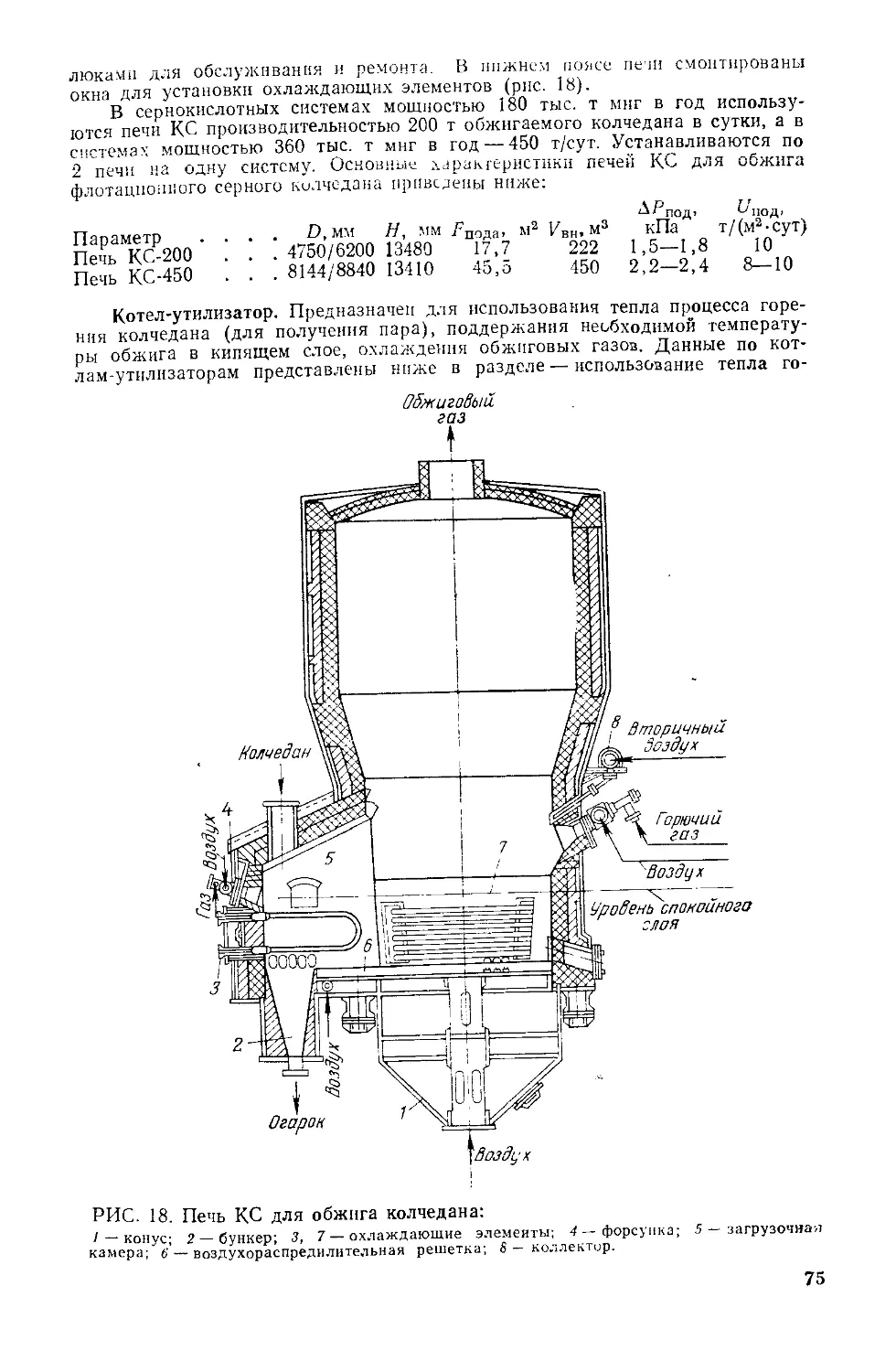
II. 1.8. Технологическая схема и аппаратура отделения обжига 73
II.1.9. Расчет печи КС-450 на воздушном дутье.................80
II.1.10. Зарубежные установки.................. . . 85
II.1.11. Обжиг колчедана в печах КСЦВ......................... 86
II. 1.12. Обжнг колчедана с применением кислорода ... 88
II.2. Сжигание серы . ....................................90
II.2.1. Механизм горения серы ................................93
II.2.2. Влияние повышенного давления на скорость горения серы 99
П.2.3. Печи для сжигания жидкой серы.........................100
11.2.4. Печи для сжигания твердой серы . . .... 107
П.З. Обжиг серной руды.....................................111
П.4. Обжиг сульфатов железа................................112
II.5. Сжигание сероводорода.................................118
П.6. Использование тепла горения серосодержащего сырья 122
II.7. Очистка обжигового газа от огарковой пыли . 124
3
ГЛАВА III. ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫ КОНТАКТНЫМ
МЕТОДОМ.....................................................127
HI.1. Технологические схемы производств в СССР и за рубежом 127
Ш.2. Мокрая очистка обжигового газа.........................138
III.3. Теоретические основы окисления диоксида серы на ката-
лизаторах ...............................................151
III.3.1. Термодинамика окисления диоксида серы . . 151
III.3.2. Ванадиевые катализаторы для окисления диоксида серы 153
III.3.3. Механизм и кинетика окисления диоксида серы . . 157
III.3.4. Окисление диоксида серы при повышенном давлении 163
Ш.4. Контактные аппараты и контактные узлы. Технологиче-
ский режим и особенности эксплуатации . . . 168
III.4.1. Принципиальные технологические схемы контактных
узлов.................................................... 168
Ш.4.2. Технологические режимы работы катализаторов . . 171
Ш.4.3. Типы и особенности контактных аппаратов .... 173
III.4.4. Теплообменники контактных узлов.....................178
Ш.4.5. Расчет контактных узлов .... .... 184
III.5. Сушка газа и абсорбция триоксида серы .... 192
III.5.1. Влажность газов и кислотообмен в цикле сушки-абсорбции 192
III.5.2. Абсорбция триоксида серы............................202
III.5.3. Аппаратура для осушки газа и абсорбции сериого ангид-
рида ................................208
III.6. Очистка отходящих газов и нейтрализация сточных вод 218
Ш.6.1. Аммиачные способы очистки и концентрирования серни-
стых газов........................................ ....... 219
Ш.6.2. Кислотно-каталитический способ очистки газов . . 227
III.6.3. Сульфитно-содовый способ очистки газов . . . 231
Ш.6.4. Причины образования тумана и очистка от него выхлоп-
ных газов.............................................232
III.6.5. Нейтрализация сточных вод..................... . 234
Ш.7. Получение концентрированного и жидкого диоксида серы 235
Ш.8. Получение жидкого триоксида серы и высококонцентри-
рованного олеума............................................240
Ш.9. Получение улучшенных и специальных сортов серной
кислоты........................................ . . 243
Ш.10. Вторичные энергоресурсы . ...................244
ГЛАВА IV. ОСНОВНЫЕ НАПРАВЛЕНИЯ ТЕХНИЧЕСКОГО ПРО-
ГРЕССА В ПРОИЗВОДСТВЕ КОНТАКТНОЙ СЕРНОЙ
КИСЛОТЫ...........................................................245
IV . 1. Тенденции развития . . ...................245
I V.2. Разработка систем с применением давления и кислорода 252
IV .3. Одновременное получение серной кислоты и водорода 262
ГЛАВА V. ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫ НИТРОЗНЫМ
МЕТОДОМ.....................................................267
V.I . Теоретические основы нитрозного процесса .... 268
V.2. Технологический режим башенных систем .... 273
4
V. 3. Применение кислорода в нитрозном процессе . . . 277
V .4. Получение продукционной иитрозилсерной кислоты . . 279
ГЛАВА VI. ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ ИЗ ОТХОДЯЩИХ
ГАЗОВ МЕТАЛЛУРГИЧЕСКИХ ПРОИЗВОДСТВ . . 279
ГЛАВА VII. ИСПОЛЬЗОВАНИЕ ОТРАБОТАННОЙ И РАЗБАВ-
ЛЕННОЙ КИСЛОТЫ...............................297
VI I.1 Регенерация и использование отработанных кислот 297
VII .2. Концентрирование серной кислоты..............301
ГЛАВА VIII. ВСПОМОГАТЕЛЬНОЕ ОБОРУДОВАНИЕ ДЛЯ ПРО-
ИЗВОДСТВА СЕРНОЙ КИСЛОТЫ.....................308
VIII .1. Холодильники и насосы ... 308
VII I.2. Орошающие устройства и брызгоуловители .... 319
VI II.3. Оборудование для хранения и перевозки кислоты . 323
ГЛАВА IX. КОНСТРУКЦИОННЫЕ МАТЕРИАЛЫ, ПОКРЫТИЯ,
ВОПРОСЫ КОРРОЗИИ.......................................325
IX. 1. Виды коррозионных разрушений.......................325
IX.2 . Коррозия металлов, сталей и сплавов в серной кислоте
и олеуме . ....................... . 327
IX.3. Материалы противокоррозионной защиты . . . 331
IX. 4. Материалы для оборудования.........................333
ГЛАВА X. КОНТРОЛЬ И АВТОМАТИЧЕСКОЕ РЕГУЛИРОВАНИЕ
ПРОЦЕССОВ ПРОИЗВОДСТВА СЕРНОЙ КИСЛОТЫ 339
ГЛАВА XI. ТЕХНИКА БЕЗОПАСНОСТИ ........................350
Приложения..............................353
Литература . . 370
Предметныйуказатель .......................377
ПРЕДИСЛОВИЕ
Серная кислота по объемам производства и примене-
ния занимает одно из первых мест среди химических
веществ. Она применяется во многих отраслях промышленности
для получения широкого ассортимента важнейших продуктов.
Объем производства серной кислоты в любой стране может рас-
сматриваться как показатель, который в определенной мере от-
ражает уровень промышленного развития страны.
Непрерывное наращивание выпуска серной кислоты наблю-
дается во всех развитых и развивающихся странах. В 1981 г.
общий уровень мирового производства серной кислоты достиг
139 млн. т. Особенно высоки темпы развития сернокислотной
промышленности в СССР. За два последних десятилетия объ-
ем ее производства в нашей стране возрос почти в 4 раза.
Примерно половина выпускаемой серной кислоты расходуется
на получение минеральных удобрений, обеспечивающих повы-
шение урожайности сельскохозяйственных культур, с другой
стороны — с использованием серной кислоты выпускаются де-
сятки миллионов тонн различных химических продуктов. Та-
ким образом, с полным основанием можно утверждать, что
сернокислотное производство играет важную роль в решении
Продовольственной программы СССР.
Увеличение выпуска серной кислоты сопровождается усо-
вершенствованием ее технологии, аппаратурного оформления
всех стадий производственного процесса, внедрением принци-
пиально новых схем и оригинальных инженерных решений.
Единичные мощности сернокислотных систем за два послед-
них десятилетия повысились со 120 до 360 тыс. т в год при
работе на колчедане и со 100 до 500 тыс. т в год — на сере.
При этом значительно улучшились технико-экономические пока-
затели сернокислотного производства: повысилась степень ис-
пользования серосодержащего сырья, снизились удельные капи-
тальные вложения и эксплуатационные затраты, значительно
повысилась производительность труда.
Одновременно с повышением эффективности производства
на современных сернокислотных системах большое внимание
уделяется решению экологических проблем. Так, внедрение
процесса двойного контактирования с промежуточной абсорб-
цией и црименение новых высокоактивных катализаторов поз-
волило повысить степень окисления диоксида серы в контакт-
ном производстве серной кислоты с 97,5—98,0% до 99,7—
99,8%. При этом примерно в 8—10 раз снизилось содержание
диоксида серы в выхлопных газах.
Современные отечественные сернокислотные системы по
своему техническому уровню, экономической эффективности и
экологическому совершенству не уступают лучшим зарубеж-
ным образцам.
в
В предлагаемой вниманию читателей книге мы стремились
отразить коренные изменения, которые произошли в сернокис-
лотной промышленности за последние годы, показать новей-
шие достижения и перспективы дальнейшего развития техно-
логии и аппаратурного оформления процессов производства
серной кислоты, обобщить богатый опыт эксплуатации серно-
кислотных систем, результаты многочисленных научных иссле-
дований и инженерных разработок.
В книге изложены сведения о свойствах серной кислоты и
промежуточных продуктов, а также о различных видах серосо-
держащего сырья. На современном уровне рассмотрены тех-
нологические процессы получения серной кислоты из различных
видов сырья: обжиг колчедана, сжигание серы и серосодержа-
щих газов, специальная очистка обжиговых газов, каталити-
ческое окисление диоксида серы и абсорбция триоксида серы
с получением верной кислоты. Должное внимание уделено
очистке отходящих газов сернокислотного производства с
целью защиты окружающей среды и утилизации диоксида се-
ры. Дан анализ направлений дальнейшего технического про-
гресса в сернокислотном производстве. Показаны пути исполь-
зования отработанных кислот. Описаны основное и вспомога-
тельное оборудование, конструкционные материалы, применяе-
мые в производстве серной кислоты, отражены методы конт-
роля и автоматизации производства, вопросы техники безопас-
ности. Приведены необходимые справочные данные, методы
важнейших расчетов. Ввиду ограниченного объема книги ряд
вопросов в ней изложен в сокращенном виде, библиографиче-
ские ссылки во многих случаях сокращены до минимума.
Мы надеемся, что эта книга станет полезным практиче-
ским пособием для инженерно-технических работников про-
мышленных предприятий и проектных организаций, даст необ-
ходимую информацию научным работникам, поможет моло-
дым специалистам лучше освоить технологию серной кислоты.
Глава I, разделы 1—6 главы II, разделы 5—10 главы III
и главы IV, V, VII, VIII, XI написаны М. И. Отвагиной и
Б. Т. Васильевым; раздел 7 главы II, разделы 1, 2, 4 главы
III и глава VI — В. И. Явором; раздел 3 главы III —
|В. В. Илларионовым |; глава IX — С. В. Чеховским; гла-
ва X — В. А. Живописцевым.
Выражаем благодарность товарищам по работе, оказавшим
содействие в подборе и подготовке материалов для ряда раз-
делов книги: А. А. Иванову, Б. А. Дубовицкому, В. И. Якуше-
ву, В. А. Колганову, Ю. А. Головачевскому.
Очень признательны профессору И. П. Мухленову и инже-
неру В. Я. Дроздовскому, которые взяли на себя труд внима-
тельно прочитать рукопись книги и дали много полезных сове-
тов авторам.
Все замечания читателей, направленные на улучшение со-
держания книги, будут приняты с благодарностью.
7
ГЛАВА I
ОБЩИЕ СВЕДЕНИЯ
1.1. РАЗВИТИЕ И СОВРЕМЕННОЕ СОСТОЯНИЕ
СЕРНОКИСЛОТНОЙ ПРОМЫШЛЕННОСТИ [1—7]
Производство серной кислоты отражает экономическое
развитие страны. По разнообразию областей примене-
ния серная кислота занимает первое место среди важнейших
продуктов химической промышленности. Ее применяют почти
во всех отраслях народного хозяйства: в химической и нефтя-
ной, легкой и пищевой промышленности; в цветной металлургии,
машиностроении, в сельской хозяйстве и др. В химической про-
мышленности серную кислоту используют для производства ми-
неральных удобрений, кислот и солей, пластических масс, для
сушки газов и на другие цели. В области производства серной
кислоты наша страна всегда находилась в числе передовых
стран.
История сернокислотной промышленности ведется с 1805 г., когда неда-
леко от Москвы был построен химический завод, на котором в свинцовых
«глухих» камерах стали получать из серы 5 т серной кислоты в год. Подоб-
ный завод в Германии был построен на 15 лет позже. В середине XIX в.
сериую кислоту в России вырабатывали иа 40 химических заводах. К 1900 г.
работало 52 завода. Самая крупная установка была пущена в 1873 г. иа
Тентелевском заводе в Петербурге, в 1894 г. и а ией было выпущено около
2 тыс. т кислоты и 1 тыс. т триоксида серы. В 1900 г. иа 52-х сернокислот-
ных заводах было выпущено 74 850 т серной кислоты (в пересчете на моно-
гидрат). Доля контактной кислоты составляла около 5%.
Многие заводы использовали сицилийскую серу. Уже тогда были извест-
ны крупные месторождения сериого колчедана иа Урале и Менее мощные
на Кавказе. Колчедан применяли примерно иа четвертой части заводов. Вво-
зился португальский, испанский (из Рио-Тиито) и греческий (из Солоиик).
Его использовали в качестве балласта на судах, прибывающих из этих стран
в Россию за хлебом. Впервые в качестве серосодержащего сырья колчедан
был применен на Тентелевском химическом заводе для получения олеума
иа первой опытной контактной системе. Первая промышленная установка вве-
дена в эксплуатацию в 1903 г. К 1913 г. работало 6 таких установок мощ-
ностью по 5 тыс. т миг. в год.
Теителевская система, разработанная в России, получила широкое рас-
пространение ие только иа родине, ио и в США, Англии, Японии, Германии,
Румынии, Швеции, Франции, Италии, Норвегии, где в 1916 г. работало 44
теителевских системы. Одиовременио внедрялись меиее совершенные, чем теи-
телевские, установки Грилло — Шредера. Перед первой мировой войной ра-
ботали две системы Маигеймских химических фабрик, где в качестве катали-
затора применяли колчеданный огарок наряду с платиновым катализатором,
который использовали в то время иа контактных системах. В 1913 г. было
выпущено 284 тыс. т серной кислоты. Россия занимала 8-ое место в мире.
США выпустили 2 310 тыс. т.
Рост производств серной кислоты в нашей стране тормозился отсутстви-
ем главного ее потребителя — минеральных удобрений, поскольку существо-
вало ошибочное мнение, что в России иет подходящего сырья для производ-
ства фосфорных удобрений и из отечествеииого сырья можно получить су-
8
перфосфат только с низким содержанием растворимой Р20з. Поэтому вла-
дельцы суперфосфатных заводов ввозили фосфорит из Англии, Марокко и
Америки. В 1913 г. работало 12 суперфосфатных заводов, на которых выпу-
скалось около 87 тыс. т продукции.
В 1917 г. на территории нашей страны было 69 камерных установок,
24 контактных установки Грилло — Шредера, 20 тентелевских и 4 мангейм-
ских. На долю контактной кислоты приходилось около 25% выработки. Во
время гражданской войны в связи с военными действиями и отсутствием
спроса на серную кислоту, ее выработка сильно упала и в период 1918—
1923 г. составляла 13—65 тыс. т. По окончании гражданской войны начался
период восстановления народного хозяйства страны. Уже в 1925—26 годах
производство серной кислоты достигло довоенного уровня. В этот период
число сернокислотных установок уменьшилось вследствие концентрации про-
изводства и закрытия маломощных предприятий. В качестве сырья частично
применяли испанский колчедан, так как доставка сырья с Урала обходилась
дороже. Импорт колчедана был прекращен лишь в 1927 г.
В 1925—26 г. потребность в серной кислоте была удовлетворена только
на 83%, что вызвало необходимость реконструкции действующих и строи-
тельства новых заводов. Первая новая контактная установка была пущена
в 1925—26 г. на Бондюжском заводе. В 1927 г. пущей первый в СССР ба-
шенный цех, работавший на отходящих газах медеплавильного производства*
Полевского завода, в 1928 г. — башенный цех на Чериоречеиском заводе.
К началу I пятилетки (выполнение первого пятилетиего плана началось
1.0Х.28 г.) сернокислотная промышленность располагала 29 контактными,
2 башенными и 33 камерными системами общей мощностью 349 тыс. т.
К концу I пятилетки число контактных установок увеличились до 37, башен-
ных— до 16, а камерных снизилось до 16. Общая мощность сернокислотных
заводов составляла 834 тыс. т, т. е. увеличилась за пятилетие в 2,4 раза-
Это было достигнуто главным образом в результате строительства башенных
систем и интенсификации действующих производств. Для обеспечения выпус-
ка удобрений строили башенные системы, так как они требуют меньших
капитальных затрат и дают возможность получения более дешевой кислоты.
К тому же в то время строили значительно более мощные башенные системы
(40 тыс. т в год), чем контактные (всего на 10—12 тыс. т). Самый крупный
по тому времени башенный цех на Березниковском комбинате был построен
за 11 месяцев. Большим успехом сериокислотчиков был ввод двух башенных
систем на Невском химическом заводе в Ленинграде, целиком построенных
по советским проектам иа отечественном оборудовании.
Годы первой пятилетки явились годами становления советской сернокис-
лотной промышленности. Начало создаваться отечественное оборудование,
развернулись интенсификация производств, освоение новых видов сырья. На
помощь производству пришли научные н учебные нистнтуты. Успехи, достиг-
нутые в развитии сернокислотного производства, в значительной степени
связаны с тесным сотрудничеством науки н производства. Ряд исследований
был проведен в работающих цехах. Технические учебные заведения и уни-
верситеты готовили специалистов и исследователей широкого профиля для
промышленности, в том числе и для сернокислотных производств. Открыва-
лись специализированные техникумы, курсы, ФЗУ.
Необходимые исследования проводились НИУИФом*, где в 1936 г. по
распоряжению наркома тяжелой промышленности Г. К. Орджоникидзе был
организован сернокислотный отдел под руководством профессора К. М. Ма-
лина, возглавлявшего затем работы по серной кислоте более 30 лет. Этот
институт стал головным в отрасли. Исследования проводились также в
УНИХИМе и на ряде кафедр технологических институтов Москвы, Одессы,
Харькова, Ленинграда, Горького и др. Большая работа была проведена по
созданию технической и учебной литературы по серной кислоте. Необходима
* По указанию В. И. Ленина постановлением от 12 сентября 1919 г. при
Высшем Совете народного хозяйства РСФСР на базе существовавшего с
1916 г. Общественного комитета по делам удобрений был создай Научный
институт по удобрениям — НИУ, переименованный впоследствии в НИУИФ1.
* а
Отметить первые книги П. М. Лукьянова, затем К. М. Малина, И. П. Кузь-
миных, Г. К- Борескова, А. Г. Амелина, «Справочник сернокислотчика» и др.
В 1940 г. по производству серной кислоты Советский Союз вышел на
первое место в Европе и второе в мире. Увеличение выпуска серной кислоты
во второй и третьей пятилетках происходило за счет интенсификации произ-
водства в результате поддержания оптимального технологического режима,
разработанного на основе глубоких теоретических исследований, и строитель-
ства новых цехов. Большие успехи были достигнуты в интенсификации ба-
шенного процесса и работы печей обжига колчедана. Гарантированная фир-
мой «Петерсен» интенсивность башенного объема на отечественных системах
была превышена в 10 раз и к 1941 г. была доведена до 200 кг/(м3-сут) и
показана возможность получения на башенных системах 93 %-ной кислоты.
Были сконструированы и построены печи Г и ВХЗ с поверхностью обжига
107 и 140 м2. Основные работы по интенсификации механических печей были
проведены НИУИФом совместно с Невским, Воскресенским, Винницким и
другими заводами. Интенсивность работы печей ВХЗ была доведена до 250—
300 кг на 1 м2 пода печи в сутки.
В 1931 г. 93,5%; кислоты было выработано из рядового колчедана и
2,3% из флотационного. Уже в следующем году из флотационного колчедана
вырабатывалось 36% и из отходящих газов цветной металлургии 4%. В се-
редине 30-х годов обжиг флотационного колчедана был внедрен на всех за-
водах.
В связи с разработкой метода обжига колчедана в кипящем слое, с
1955 г. строятся только печи КС. Первая промышленная печь на 100 т кол-
чедана в сутки была пущена на Воскресенском комбинате. Современные пе-
чи КС имеют производительность 450 т/сут. Для сжигания расплавленной и
отфильтрованной серы ЦКТИ им. Ползунова и Невский химический завод
разработали и освоили высокоинтеисивные циклонные печи СЭТА-Ц-100.
Одновременно с печами специализированными организациями были раз-
работаны котлы-утилизаторы ГТКУ КУКС, ВТКУ и другие и трех- и четы-
рехпольные электрофильтры.
Первые отечественные контактные аппараты К-39 производительностью
40 т/сут (по моногидрату), разработанные НИУИФом и Гипрохимом, были
построены в 1938 г. на Воскресенском химкомбинате. На Красноуральском
медеплавильном заводе в 1953 г. был построен контактный аппарат на
240 т/сут. В середине 60-х годов строились аппараты на 360 т/сут для систем
мощностью 120 тыс. т/год, которыми оснащалась промышленность в годы
VIII пятилетки. В годы IX и X пятилеток были освоены аппараты на 540 и
1000 т/сут для систем на колчедане мощностью 180 н 360 тыс. т/год и на
сере мощностью 1100—1600 т/сут для систем 450—500 тыс. т/год.
До 1932 г. в качестве катализатора в сернокислотном производстве при-
меняли платину. Одесским химическим н Московским им. Менделеева хими-
ко-технологическим институтами были разработаны методы приготовления
ванадиевых катализаторов БОВ и затем БАВ. Работа по созданию новых
катализаторов термостойких, с низкой температурой зажигания, с примене-
нием различных носителей, отличающихся по способам приготовления про-
должаются и в настоящее время. Созданы катализаторы СВД, СВС, ТС,
ИК-1-4, ИК-1-6 и др. Эти работы проводятся НИУИФом, Институтом Ка-
тализа СО АН СССР, УНИХИМом и Ленинградским технологическим инсти-
тутом (ЛТИ), который разрабатывает шариковый катализатор для примене-
ния в кипящем слое.
Для контактных систем мощностью 360 тыс. т/год созданы нагнетатели
производительностью 180 тыс. м3/ч рабочего газа и нагнетатели воздуха для
Печей на 45 и 65 тыс. м3/ч. Для орошения башен внедрены погружные насо-
сы производительностью до 500 м3/ч, а для охлаждения кислот — пластинча-
тые, спиральные, кожухотрубчатые, оросительные антегмитовые, воздушные
холодильники. Большая работа проведена по замене свинца новыми материа-
лами и применению принципиально новых конструкционных материалов.
Сернокислотные системы, работающие по башенному (нитрозному) ме-
тоду, с 1955 г. больше не строятся. Выпуск башенной кислоты в 1980 г. со-
ставил 5% от общего ее выпуска. На период 1985—1990 г. намечено закрыть
10
остальные башенные производства по санитарным соображениям. Возмож-
ные направления развития башенных производств изложены в гл. V.
Использование отходящих газов цветной металлургии всегда было важ-
нейшей народно-хозяйственной проблемой. К концу 1938 г. были построены
контактные установки на всех цинковых заводах. В 1941 г, был введен кон-
тактный цех на медеплавильном заводе мощностью 80 тыс. т/год. Затем
контактные цехн были построены на ряде медеплавильных, никелевых, свин-
цовых и других заводов.
Во время Великой Отечественной войны сернокислотной промышленности
был нанесен большой урон. Часть сернокислотных цехов оказалась на окку-
пированной территории. Потери мощности составили 76%. Часть оборудова-
ния и квалифицированных кадров была эвакуирована на Урал, в Среднюю
Азию и Казахстан. Необходимо было резко увеличить выпуск олеума и ак-
кумуляторной кислоты. Большую роль в снабжении страны кислотой сыграли
коллективы Красноуральского, Кировоградского, Челябинского, Воскресен-
ского и других заводов и специалисты, эвакуированные с заводов Украины
и Центра.
Восстановление разрушенных цехов н строительство новых проводилось
сразу же по мере освобождения временно оккупированных территорий. Уже
в 1944 г. выработка серной кислоты превысила довоенную. В 1949 г. Совет-
ский Союз по производству серной кислоты вышел на второе место в мире.
В 1950 г. было выпущено 2150 тыс. т кислоты, или 130% от выработки
1940 г.
В послевоенные годы еще больше ускорилось техническое перевооруже-
ние сернокислотной промышленности. Возросшая потребность в серной кис-
лоте для производства удобрений, тяжелого органического синтеза, нефтяной
и других отраслях обусловили увеличение доли контактной кислоты, резко
возросла потребность в улучшенных ее сортах. В результате совместного тру-
да коллективов институтов и заводов созданы крупная отрасль промышлен-
ности — производство серной кислоты.
Структура использования серосодержащего сырья со временем изменяет-
ся. Так, в 1960 г. более половины кислоты получали из колчедана, в 1975 г.—
42%, в 1980 г. — 32%, так как возрастает потребление серы и переработка
на серу серусодержащих газов. Доля отходящих газов в сырье для производ-
ства серной кислоты с 1975 г. составляла примерно 18,5%. В ближайшей
перспективе в связи с намеченным быстрым развитием производства кислоты
из серы эта доля будет снижаться. Мощность единичной системы, работаю-
щей на отходящих газах, в настоящее время составляет 180 тыс. т. В целях
использования дешевого отбросного сырья и улучшения охраны окружающей
среды газы цветной металлургии должны всемерно вовлекаться в производ-
ство серной кислоты.
При применении технологического кислорода для плавки цветных метал-
лов концентрация диоксида серы в отходящих газах повышается до 60—
80%, а при подаче кислорода в печи обжига — до 18—22%. Такой газ целе-
сообразно перерабатывать в серную кислоту в смеси со слабыми газами, вы-
деляющимися при различных металлургических переделах.
Сернокислотные системы за три предыдущих пятилетки претерпели зна-
чительные изменения (характеристика современного оборудования дана в
Приложении 1).
В VIII пятилетке вводились системы мощностью 120 и 180 тыс. т/год,
работающие на колчедане с одинарным контактированием. Значительная
часть их впоследствии была переведена на использование серы. В IX пяти-
летке продолжалось строительство систем на колчедане мощностью 180 тыс.
т/год и начато строительство систем на 360 тыс. т в год с одинарным кон-
тактированием (первая система построена в 1973 г. в г. Дорогобуже, послед-
няя— в 1975 г. в г. Ровно) и начато преимущественное строительство мощ-
ных систем с двойным контактированием на колчедане мощностью 360 тыс. т
(первая система построена в 1974 г. в Череповце) н на сере мощностью
450 тыс. т (в 1974 г. в Самарканде). В X пятилетке строились только мощ-
ные современные системы с двойным контактированием: на колчедане мощ-
ностью 360 тыс. т—отечественные и по польским поставкам по лицензий
11
«фирмы «Дорр — Оливер» и иа сере мощностью 450—500 тыс. т — по польской
технологии и польским поставкам.
Характеристика основного технологического оборудования контактных
сернокислотных систем приведена в Приложении I.
В перспективе предусматривается продолжение строитель-
ства систем на сере мощностью 500 тыс. т и более мощных
(600 и 1000 тыс. т) с применением давления и кислорода (см.
гл. IV).
В развитии сернокислотной промышленности, согласно спе-
циализации между странами СЭВ, в последние годы значитель-
ную роль играет Польская Народная Республика, комплектно
поставляющая оборудование для мощных систем по проектам
Гипрохима, институтов ПНР и лицензиям «Дорр — Оливер».
Польские специалисты оказывают техническую помощь в освое-
нии этих систем.
Советским Союзом построены и пущены сернокислотные си-
стемы в Болгарии, Вьетнаме, Индии, Турции, оказывается тех-
ническая помощь по совершенствованию технологии сернокис-
лотного производства на Кубе, в Польше, Венгрии, Чехослова-
кии.
В настоящее время серную кислоту получают в основном на
системах большой единичной мощности (360 и 500 тыс. т/год).
Темпы роста выпуска кислоты на таких системах по сравне-
нию с общим выпуском кислоты на предприятиях Министер-
ства по производству минеральных удобрений видны из следу-
ющих данных (в %):
1975 г. 1978 г. 1979 г. 1980 г. 1982 г.
28 44 53 60 69,3
На отдельных комбинатах строятся по несколько мощных
систем и общий выпуск кислоты доходит до 1,8 млн т в год.
Тенденция укрупнения сернокислотных систем за рубежом
(приведена наибольшая мощность) прослеживается из следую-
щих данных:
Год Мощность, тыс. т/год Фирма, страна, сырье
1973 396 «Томакомаи», Япония, пирит
1974 650 «Монсанто» с ДК, США, отходящие га-
зы
1978 900 «Байер — Лурги», Бразилия, сера
1981 3100 «Монсанто», США, сера
Фирма «Фелпс Додж» закончила строительство завода
мощностью до 1 млн. т в год в Нью Мексико. В 1983—1985 г.
намечено строительство 8-ми установок общей мощностью
4,48 млн. т в год в Марокко (Докорф — Лансфар) по системе
фирмы «Монсанто». Темпы развития производства серной кис-
лоты показаны в табл. 1.
Развитие народного хозяйства нашей страны выдвигает но-
вые и все более повышенные требования к сернокислотной про-
12
Таблица 1. Развитие сернокислотной промышленности
Страна I960 г. 1965 г. 1970 г. 1975 г. 1980 г. 1982 г.
Производство серной кислоты, ТЫС. Т МНС.
США 16200 22600 26785 29166 36599 29359
СССР 5400 8520 12600 18645 23033 23800
Япония 4452 5656 6925 6000 6778 6531
Мировое произ- 51700 71700 89000 108900 143008 130263
водство
Выпуск серной кислоты на душу населения, кг. мнг.
США 90 116 131 136 161
СССР 25 37 50 73 87 —
Удельный вес контактной кислоты в общем объеме производства, %
США 89 95 99 99,7 100
СССР 54 67 78 86 95
Япония 73 77 86 98 — —
мышленности. Необходимо увеличить выпуск улучшенных сор-
тов серной кислоты, предельно снизить вредные выбросы, бо-
лее полно использовать все имеющиеся виды сырья, а также
отходы в виде отработанной кислоты, железного купороса, от-
ходящих слабых газов. Важнейшей задачей является увели-
чение надежности оборудования, что снизит потери сырья и
расходы на ремонты, повысит общую рентабельность.
1.2. СВОЙСТВА И ПРИМЕНЕНИЕ СЕРНОЙ КИСЛОТЫ [3, 4, 8—15]
В химии серной кислотой называют соединение триок-
сида серы с водой H2SO4 (ЗОз-Н2О), а в технике под серной
кислотой подразумевают любые смеси SO3 с водой (мольное
отношение Н2О: SO3 больше 1). Смеси, в которых отношение
меньше 1, называют олеумом, или дымящей серной кислотой.
Серная кислота образует три соединения с водой (H2SO4-H2O,
H2SO4-2H2O и H2SO4-4H2O) и два соединения с триоксидом
серы — SO3 (H2SO4-SO3 и H2SO4-2SO3).
1.2.1. Физические свойства водных растворов
серной кислоты, олеума, диоксида
и триоксида серы
Серная кислота и олеум. Состав водных растворов сер-
ной кислоты характеризуется содержанием в них H2SO4 и
SO3.
Если массовый % H2SO4 равен Пн2во4, то % SO3
П.403 = 0 81 63Пн2бо4 . а Пнг504 = 1.225nSo3
13
В олеуме различают SO3, связанный с водой (в H2SO4) и
не связанный, последний называют свободным. Весь SO3 в
олеуме называют общим. Если % общего SO3 в олеуме FIso.
(общ), то % SO3 (своб)
П5Оз (своб) = 5,4438 [Що3 (общ) — 81,63],
а
nso3 (общ) = 0,1837nso3 (своб) 4-81,63
Свойствам серной кислоты, олеума и промежуточным про-
дуктам их производства (SO2 и SO3) в разных странах посвя-
щены сотни работ. Результаты наиболее достоверных фунда-
ментальных исследований отражены в «Справочнике сернокис-
лотчика» под редакцией проф. К. М. Малина [9].
Серная кислота имеет следующие основные константы:
Молекулярная масса . .................. 98,078
Плотность прн 20 °C, г/см3 .................... 1,8305
Температура плавления (100%-ной), °C . 10,37±0,05
Температура кипения, °C
100%-ной (с разл.)............................. 275±5
98,479 %-ной (макс.)...................... 326±5
Теплота парообразования прн 326,1 °C, Дж/моль 50,124
Теплота плавления (100%-ной), кДж/моль . . 10,726
Теплоемкость прн 25 °C, Дж/(г-К)
98,5 %-ной..................................1,414
99,22 %-ной................................ 1,405
100,39 %-ной...............................1,394
Если рассматривать H2SO4 как соединение гидроксильное,
то структура молекулы представляется формой I, если же при-
нять, что атомы водорода связаны не с отдельными атомами
кислорода, а с радикалом SO4 как целым, то структурная
форма молекулы представляется в виде фо^мы II:
(X /ОН
(У \он
Рентгенометрические определения показали, что в солях
серной кислоты радикал SO4 проявляется как структурная
группа [10].
Стандартные теплоты образования H2SO4 имеют следующие
значения, кДж/моль:
S (тв. ромб) 4- Н2 (г) + 2О2 (г) = H2SO4 (ж) 4-811,86
SO2 (г) 4- Н2О (ж) 4- i/2O2 (г) = H2SO4 (ж) 4- 245,26
SO3 (г) 4- Н2О (ж) = H2SO4 (ж) 4-130,56
SO3 (г) 4- Н2О (г) = H2SO4 (г) 4-95,22
H2SO4 (ж) ----> H2SO4 (г) — 79,2
На рис. 1 представлена диаграмма кристаллизации для си-
стемы Н2О—H2SO4—SO3.
14
РИС. 1. Температура кристаллизации в системе Н20—H2SO4—S03.
От 0% H2SO4 до 64,35% БОзсвоб образуются 6 гидратов. Эти гидраты
являются индивидуальными химическими соединениями, которые взаимно не
растворимы в твердом виде, а образуют эвтектические смеси, т. е. смеси,
имеющие постоянный состав в твердом и жидком состояниях. В области
концентрации SO3 от 64,35% до 100% при кристаллизации образуются твер-
дые растворы. Концентрации растворов кислоты, общее содержание SO3 и
составы твердых фаз, выпадающих в эвтектических точках, даны в Приложе-
нии II.
Между эвтектическими точками располагаются ветви кристаллизации оп-
ределенных соединений трнокснда серы с водой. Эти соединения и соответ-
ствующие им концентрации растворов, их температуры и теплоты плавления
представлены в Приложении III.
Рис. 1 показывает, что в зимнее время при низких темпера-
турах нельзя хранить и перевозить кислоту концентрацией
близкой к чистой SO3: 2SO3-H2O, SO3-H2O и SO3-2H2O, так
как из этих растворов могут выпадать кристаллы. Все товар-
ные сорта серной кислоты соответствуют наиболее низким
температурам ее кристаллизации, т. е. имеют концентрации
близкие к эвтектическим смесям. Температура кристаллизации
серной кислоты и олеума для некоторых их концентраций при-
ведены в Приложении IV.
Ниже приведены температуры кипения серной кислоты:
%H2so4 t, °C %H2SO4 t, °C /6H2SO4 t, °C
45,6 117 75 182 95 297
57,6 134 84,5 223 98 322
66 159 92 274 100 274
Ниже приведены температуры кипения олеума:
t, °C .......... 141,10 133,10 121,10 112,3 87,67 61,0
% SO3 (своб) . . 20 24 30 35 46 62
% SO3 (общ) . . 85,31 86,04 87,14 88,06 90,08 93,03
65,2
65
93,57
Давление паров над 100%-ной H2SO4:
Т, К ........... 523,16 548,16 573,16 598,96 623,16 653,16 673,16
t, °C........... 250 275 300 325 350 380 400
Л кПа .... 8,0 15,3 24 42,3 54,1 60 130,6
15
ё
Е
0,007
0,004
0,003
7,52и
4,512
3,008
1,504
0,752
0,452
j. 0,300
S
- 0,150
ё
§ 0,075
"§ 0,045
0,030
0,015
200
20
Л
2
600
400
0,6
0,4
10
6
4
100
60
40
О 20 40 60 80 100 120 140
Температура, °C
РИС. 2. Зависимость равновесных давлений паров воды над растворами сер-
ной кислоты от температуры.
g КонцентрацияИч&Ол.вжи8тст,%
С;
а РИС. 3. Состав пара над сер-
'Ч ной кислотой при температуре
кипения и нормальном давле-
нии.
Над водными растворами серной кислоты цри температуре
до 100—120°C вплоть до 98,3%-ной H2SO4 в парах присутству-
ют практически только пары воды. Поэтому можно принять,
что в пределах этих концентраций кислот в указанном интер-
вале температуры парциальное равновесное давление паров во-
ды практически равно полному равновесному давлению. Вели-
чины равновесных давлений паров воды представлены на
рис. 2.
При более высоких температурах над концентрированными
растворами серной кислоты наряду с парами воды все в боль-
шем количестве появляются и пары серной кислоты, а также
и SO3 (от разложения H2SO4).
Величины равновесных давлений паров H2SO4 над концент-
рированными растворами серной кислоты при любых темпера-
турах можно рассчитывать по известному уравнению Р в Па:
В
lgP = А — -у-4-2,216
пользуясь следующими значениями коэффициентов А и В [12]:
% H2SO4..................
А........................
В........................
85 90 93 95 98
7,751 7,897 8,170 8,316 8,470
3742 3685 3656 3697 3593
В газовой фазе пары H2SO4 диссоциируют на Н2О и SO3.
При этом соотношение паров Н2О, H2SO4 и SO3 определяется
16
уравнением равновесия
^Н2О^ЗО3
Кр ~ ph2so4
Зависимость константы равновесия от температуры может
быть рассчитана по уравнению (при Р в Па)
500
1g К = 8,0 — -у- + 1,75 1g Т — 5,7- 10-4Т
По преобразованному выражению:
(Рн2оисх - *) (/Чоэисх - *)
*р =------------х---:------
по данным о количестве и составе полного конденсата, полу-
чаемого например, с I м3 объема реального газа, можно рас-
считать равновесные парциальные давления всех компонентов
газовой смеси. Для этого определяются полные количества
(в г) воды (£н2о) и SO3 (g’sog). Так, если паров воды во взя-
том газе оказалось gn о, то на 1 м3 всей газовой смеси при-
ходится объем (в л) исходных водяных паров (£н2о/18) -22,4^
а исходная величина давления (в Па)
10,13-108-gH о-22,4
р__ ИСХ_____________±------
ГН2О — 1000'18
Также определяется и исходная величина T’so8HCX. Подста-
вив найденные таким путем Т’н2оисх и Pso“c* и величину КР а
преобразованное выражение, находят равновесное парциаль-
ное давление H2SO4-A. Равновесные парциальные давления
Н2О и SO3 будут
^н2орави = -Рн2оисх - Рн2зо4рави И Pso3paBH = Pso3acx - Рн2ьо4равн
В парах над олеумом до 39% свободного SO3 кроме SO3
находятся и пары H2SO4, однако для температур, имеющих
место в условиях контактного производства, можно принять,,
что общее давление паров олеума равно равновесному давле-
нию SO3. Данные о давлении паров Н2О, H2SO4 и SO3 над
водными растворами серной кислоты и SO3 над олеумом при-
ведены в Приложении V.
На рис. 3 приведена кривая, позволяющая определять со-
держание H2SO4 в парах при температуре кипения, т. е. кон-
центрацию кислоты, которая получится, если сконденсируются
все пары, образовавшиеся над растворами серной кислоты
различной концентрации. С понижением концентрации кислоты
содержание H2SO4 в парах резко уменьшается. Так, над
80%-ной кислотой в парах содержится менее 1% H2SO4.
Изменение фазового равновесия паров с жидкостью для
смесей Н2О — SO3 при атмосферном давлении показано на
рис. 4. ___
2-584 №*29 ЕЛ ' 17
A?,J%H2SO4
330
320
310
340
e'
<з
e
290^
300
280
92 94 96 98 100
Концентрации H2SC^, %
РИС. 4. Диаграмма кипения растворов серной кислоты при нормальном дав-
лении.
Смесь, соответствующая 98,3 % H2SO4, является азеотропной н имеет
единую температуру конденсации паров и кипения жидкости 336,6 °C. При
небольшом изменении состава в обе стороны от азеотропной точки темпера-
тура начала конденсации пара, называемая точкой росы, значительно отли-
чается от температуры начала кипения раствора. Соответственно отличаются
составы жидкой фазы и полученных из нее паров (пли наоборот). Диаграм-
ма кипения показывает, что при нагревании кислоты, содержащей менее
80% H2SO«, температура кипения лежит ниже 200°C, при этом в пары пере-
ходит исключительно вода; лишь при концентрации кислоты выше 93%
(пунктир на диаграмме) содержание H2SO4 в паре значительно повышается.
При температуре выше 400 °C пары содержат больше SO3, чем H2SO4.
Дальнейшее нагревание вызывает диссоциацию SO3. Выше 700 °C в парах
преобладает SO2, при 1000 °C SO3 диссоциирует почти полностью.
Температуры кипения растворов серной кислоты и олеума,
как и всяких других жидкостей, находятся в зависимости от
давления. Их значения для некоторых концентраций серной
кислоты и олеума приведены в Приложении VI.
Теплоемкость серной кислоты при 20 °C уменьшается от
теплоемкости Н2О до 1,62 Дж/(г-град) {0,335 кал/(г-град)]
для 100%-ной H2SO4. Далее с повышением концентрации SO3
она увеличивается, достигая для жидкого SO3 2,78 Дж/(г-
•град). С повышением температуры теплоемкость водных рас-
творов кислоты возрастает. Значения теплоемкостей для сер-
ной кислоты и олеума некоторых концентраций при различных
температурах приведены в Приложении VII.
Тепловые расчеты, связанные с процессами нагревания и
охлаждения растворов серной кислоты и олеума с приемлемой
для технических целей точностью могут быть проведены с
применением выражения
3 = 0^-/!)
где Q — количество тепла, потребного для нагревания (без учета испарения
воды) или отнимаемого при охлаждении данной кислоты, Дж; G — масса
кислоты, кг; 1\ и /2—количество тепла, потребного для нагревания 1 кг кис-
лоты от 0 до и ti соответственно.
1S
РИС. 5. Интегральные теплоты сме-
шения серной кислоты, жидкого и га-
зообразного трнокснда серы с водой.
На рис. 5 представлены
кривые изменения при
25 °C тепловых эффектов в
расчете на 1 кг H2SO4: тепло-
ты смешения жидкой H2SO4
с водой ((71), теплоты смеше-
ния жидкого SO3 с водой (теп-
лоты образования растворов
серной кислоты и олеума из
жидкого SO3 и воды) — (72;
теплоты смешения газообраз-
ного SO3 с водой (теплоты
образования растворов серной
кислоты и олеума из газооб-
разного SO3 и воды) — (7з.
Все эти величины могут быть
названы также интегральны-
ми теплотами растворения соответственно H2SO4, жидкого SO3.
и газообразного SO3 в воде (см. Приложение VIII).
Для любой концентрации серной кислоты и олеума для лю-
бой абсциссы и данной температуры можно написать следую-
щие соотношения:
U 2 — —()1 из U,— q3 U 3 U 2—9з
где qi — теплота образования H2SO4 из жидкого SO3 н воды; —теплота;
образования H2SO4 нз газообразной SO3 н воды; qs— теплота испарения-
жидкого SO3. Все этн три величины даны в пересчете на 1 кг H2SO4.
Плотность. Плотность растворов серной кислоты (см. При-
ложение IX) необходимо знать при определении объемов ем-
костей, при расчетах гидравлического сопротивления кислото-
проводов и змеевиков холодильников и в ряде других случаев.
Плотность 100%-ной H2SO4 при 20 °C равна 1,8305 г/см3 и из-
меняется с температурой (t в °C) согласно соотношению
р = 1,8517 — 1,1-103/ +2-106z2
Кривая плотности имеет максимум при 98,3% H2SO4, затем:
проходит минимум при 100% H2SO4, достигает другого макси-
мума при 62% свободного SO3 и далее снижается до жидкого-
100%-ного SO3.
От плотности кислоты (и олеума) любой концентрации при
одной температуре можно перейти к плотности при другой тем-
пературе по соотношению
Р2 = Pl ^P ^2 0.)
где pj и р2 — плотности в г/см3 соответственно прн температурах t\ (низшей)
н ti (высшей); Др — изменение плотности на 1 °C в указанном интервале
плотностей.
2*
19
\ nH2soa
/ 100
Теплопроводность (см. Приложение X). Теплопроводность
серной кислоты необходимо знать главным образом при расче-
тах времени ее остывания при хранении в сборниках, при пе-
ревозках в цистернах и т. п. Исходным дифференциальным
уравнением в этих расчетах является
л 1 dT
d[> = -k^r
где q — количество тепла, переносимое за 1 с через 1 см2 площади при гра-
диенте температуры dT[dx.
С приемлемой для технических целей точностью зависи-
мость теплопроводности от концентрации серной кислоты и
температуры можно выразить следующим уравнением
Х= 0,52 + 0,0016/ —1,16 [0,22 +
1 \ 1Эии
где К — коэффициент теплопроводности в Вт/м град; t — температура, °C;
Пн25О4 — концентрация, % H2SO4.
Вязкость (см. Приложение XI). Под вязкостью понимают
силу внутреннего трения в жидкости, ведущую к выравнива-
нию скоростей параллельных потоков текущей жидкости.
Вязкость влияет на режим движения жидкости в трубах и
по поверхности насадок. Ее значения используют при расчетах
гидравлического сопротивления, а также процессов массопе-
редачи. В ряд применяемых в расчетах формул вводят кине-
матический коэффициент вязкости, равный у=ц/р, т. е. отно-
шению вязкости к плотности.
Вязкость серной кислоты, как и всякой жидкости, уменьша-
ется с повышением температуры, особенно значительно в обла-
сти концентрированных растворов. Известные кривые измене-
ния динамической вязкости для растворов серной кислоты и
олеума от температуры имеют экстремумы в областях, близ-
ких к гидратам SO3-2H2O, SO3-H2O и 2SO3-H2O. Максимум
кривой вязкости соответствует 84,5% и 100% H2SO4. Для олеу-
ма максимум кривой вязкости соответствует 55—60% SO3
(своб), далее наблюдается незначительное ее понижение.
Электропроводность. Электропроводность серной кислоты
подчиняется тем же закономерностям, что и электропровод-
ность любого электролита. По мере изменения концентрации
растворов серной кислоты и олеума она имеет несколько экст-
ремумов (максимумов и минимумов).
Это объясняется рядом обстоятельств. С понижением концентрации сер-
ной кислоты увеличивается степень ее электролитической диссоциации, что
повышает число и концентрацию свободных нонов — носителей электрических
зарядов. Однако при очень сильном разбавлении кислоты, хотя электролити-
ческая диссоциация приближается к максимуму, объемная концентрация ио-
нов значительно падает. При большой степени электролитической диссоциа-
ции, но недостаточном разбавлении кислоты, близость друг к другу разно-
именных ионов замедляет их движение во взанмопротнвоположных направ-
лениях.
20
РИС. 6. Зависимость удельной
электропроводности растворов
серной кислоты и олеума от кон-
центрации при 25 °C.
При повышении темпе-
ратуры электролита на 1 °C
электропроводность увели-
чивается примерно на 2—
2,5% вследствие уменьше-
ния гидратации ионов и по-
нижения вязкости раство-
ра. Путем измерения электропроводности можно определить
концентрацию кислоты. Данные об электропроводности рас-
творов серной кислоты и олеума приведены на рис. 6.
Диоксид серы (SO2). При обычной температуре это бес-
цветный газ с резким характерным запахом. Основные его кон-
станты [9] приведены ниже:
Молекулярная масса................................. 64,063
Температура, °C
конденсации ..................................... —10,62
кристаллизации ............................... —75,48
Плотность газа при и. у., г/л...................... 2,9265
Мольный объем при и. у., моль/л.....................21,891
Средняя теплоемкость газообразной SOa в интерва-
ле 0—100 °C, Дж/кг................................. 0,6615
Давление паров над жидким, кПа
при 20 °C...................................... 330,26
при 50 °C.......................................841,13
Теплота испарения, Дж/кг
при —10 °C..................................... 389,65
при 0°C........................................ 380,08
при 20 °C .... 362,54
при 30°C....................................... 353,08
При 20 °C в 1 объеме воды растворяется 40 объемов SO2
с выделением тепла (34,4 кДж/моль). Растворимость в воде
уменьшается с повышением температуры. С повышением кон-
центрации кислоты она вначале уменьшается, достигая мини-
мума при 85,8% H2SO4, затем опять увеличивается. Раствори-
мость SO2 в серной кислоте и олеуме представлена в Прило-
жении XII.
Водные растворы SO2 долгое время рассматривали как рас-
творы сернистой кислоты H2SO3, отсюда возникло и историче-
ски вошло в обиход в технике его название — сернистый ан-
гидрид. Однако в таких растворах находится гидрат SO2-7H2O,
а сернистая кислота не существует, но два ряда ее солей хо-
рошо известны [8].
Диоксид серы легко сжижаемый газ. Жидкий SO2 хорошо
растворяет многие неорганические и органические соединения.
Для сжижения 100%-ного SO2 достаточно после осушки кон-
центрированной серной кислоты сжать его до давления около
21
0,414 Па (4 ат) и охладить. Жидкий сернистый ангидрид хра-
нят и транспортируют в стальных цисте(рнах и баллонах.
Триоксид серы (SO3). При нормальных условиях это бес-
цветный газ. На воздухе он моментально вступает в реакцию
с парами воды, образуя туман из взвешенных в воздухе ка-
пель серной кислоты [4] или ассоциируется в ЗгОв- Основные
константы SO3: молекулярная масса 80,62; температуры: кипе-
ния 44,8 °C; критическая 218,3 °C; плотность 0,633 г/см3.
При каталитическом окислении SO2 триоксид серы образу-
ется с выделением тепла [96,296 Дж/моль (23 ккал/моль)].
Газообразный SO3 сжижается в бесцветную жидкость, в жид-
кой фазе он ассоциируется в утроенные молекулы. В твердом
состоянии SO3 имеет четыре аллотропные формы (а, р, у, б),
отличающиеся структурой и степенью полимеризации.
а-Форма состоит из кольцевых молекул, кристаллы ее имеют вид кристал-
лов льда. Форма р получается из формы а при длительном хранении при тем-
пературе ниже 25 °C. Процесс перехода ускоряется в присутствии даже следов
влаги. Молекулы последующих форм состоят из зигзагообразных цепей, об-
разуемых большим или меньшим числом звеньев — колец. В форме 3 SO3,
кристаллизующегося в виде длинных игл, отдельные цепи изолированы одна
от другой; в форме у они спаяны в плоскую сетку, а в форме б — в объем-
ные структуры. Температура плавления a, fl и у форм равна соответственно
16,8; 31,5 и 62,2 °C. у-Форма получается при охлаждении осушенного жидко-
го SO3. В чистом виде это белый порошок, представляющий собой сильно
полимеризованную форму SO3, строение его подобно строению p-формы, но
цепи образуют сложную структуру. P-Форма отличается от у-формы прост-
ранственным расположением цепей, плавится под давлением при 95 °C.
Нагреванием более конденсированных твердых форм SO3 нельзя полу-
чить обратно a-форму, а тем более жидкую фазу этой формы. Это дости-
гается только через сублимацию в газообразное состояние и дальнейшую кон-
денсацию газа в жидкость.
Ниже приведены теплоты испарения жидкого SO3 при раз-
ных температурах:
t, °C................. 20 25 30 40 50 60 70 80 90 100
Qhch, кДж/кг ... 552 544 535 520 498 481 465 444 427 406
Теплоемкость жидкого триоксида серы при 20 °C составля-
ет 2,78 кДж/(кг-град), средняя в пределах 25—35 °C—
3,324 кДж/(кг-град). Теплоемкость газообразного SO3 в ин-
тервале 25—927 °C определяется по формуле
Ср =58,0 +25,5-10-3Т— 13,52- 1№Т~2
Равновесное давление (упругость) паров над жидким и
твердым SO3 можно рассчитать по уравнению, приведенному
на стр. 16. Коэффициенты А и В в этом уравнении для жид-
кого [9] и твердого [12] SO3 имеют следующие значения:
Коэф- фициент Жидкий SO3 Твердый SO3
для 24— 48 °C для 15— 100 °C для а-формы ДЛЯ 3-формы
А 12,14658 12,08388 14,35918 14,68508
В 2269,3 2249,0 2916,0 3040,0
22
С водой SO3 энергично реагирует с выделением большого
количества тепла ,[9]:
SO3 (г) + Н2О (ж) = 131,1 кДж
Аллотропные формы SO3 менее энергично реагируют с во-
дой, слабо дымят на воздухе и оказывают незначительное
обугливающее действие. Жидкий SO3 смешивается с SO2 во
всех соотношениях, твердый SO3 растворяется в жидком SO2,
не образуя с ним химических соединений. SO3 и моногидрат
серной кислоты смешиваются между собой во всех соотноше-
ниях.
1.2.2. Химические свойства диоксида
и триоксида серы,
серной кислоты и основные
направления ее использования
Диоксид серы (SO2). В химических реакциях он может
•быть как окислителем, так и восстановителем, образует комп-
лексы с аминами и комплексы переходных металлов, в водных
растворах находится в виде гидрата SO2-7H2O. Хотя серни-
стая кислота не существует, хорошо известны два ряда ее со-
лей— бисульфиты, содержащие ион HSO3~, и сульфиты с ио-
нами SO32-. Нагреванием бисульфитов или пропусканием SO2
через их водные растворы получают пиросульфиты (например,
NajSsOs), в которых пиросульфитный ион имеет несимметрич-
ное строение — O2S—SO3.
При нагревании сульфитов с серной кислотой получают ги-
посульфиты (например, Na2S2O3) с тиосульфат-ионом S—О3~
или гидросульфиты (дитионаты), например Na2S2O4, — при
пропускании в их водные растворы SO2 в присутствии цин-
ка [8]. Растворы SO2 и сульфитов имеют в технике широкое
применение как активные восстановители. Известны и другие
сложные соединения, включающие SO2, а также S и иногда
SO42-— так называемые политионаты. С кислородом SO2 реа-
гирует в присутствии катализатора, образуя триоксид серы.
Наиболее широко его применяют в производстве серной кис-
лоты.
Триоксид серы (SO3) —серный ангидрид. Триоксид серы
чрезвычайно бурно соединяется с водой с
тельного количества тепла [9, 12, 13]:
Реакция
выделением значи-
SO3 (г) +Н2О (ж) = H2SO4 (ж)
SO3 (г)+Н2О (r)=H2SO4 (г)
SO3 (ж)+Н2О (ж)=Н25О4 (ж)
Выделение
кДж/моль
130,56
95,36
91,33
тепла
ккал/моль
31,16
22,76
21,80
Пары триоксида серы при введении их в воздух, реагируя
с водяными парами, образуют туман. На этом основывается
применение серного ангидрида в качестве составной части ды-
23
мящих смесей. Он обугливает растительные и животные тка-
ни, отнимая от них воду, является сильным окислителем, при
окисляющем действии в большинстве случаев (например, на се-
ру, фосфор, уголь и др.) он восстанавливается до диоксида
серы. Химическая активность различных форм триоксида серы
понижается по мере повышения их температуры плавления.
Наиболее высокоплавкая форма SO3 отличается химической
инертностью. Твердый триоксид серы растворяется в жидком
диоксиде серы, а жидкий смешивается с последним, не всту-
пая с ним в химические соединения. В любых отношениях три-
оксид серы смешивается с азотной кислотой, образует соеди-
нения со всеми оксидами азота и с триоксидом мышьяка, с ос-
новными оксидами и основаниями соединяется энергично с об-
разованием солей, присоединяя хлорид водорода, дает хлор-
сульфоновую кислоту (HSO3CI), применяемую в производстве
дымящих смесей и в ряде органических синтезов. С аммиаком
триоксид серы дает твердую смесь, содержащую амидосуль-
фоновую кислоту HS3NH2, ее аммонийную соль и другие про-
дукты (сульфамид, сульфамат, имидосульфоновую кислоту).
Эти вещества применяются для пропитки тканей, в мыловаре-
нии, для очистки котлов от накипей и для других технических
целей. Широкое применение SO3 имеет как сульфирующее сред-
ство.
Серная кислота. Это одна из самых сильных кислот. Как
двухосновная кислота она дает средние соли (сульфаты) и
кислые (бисульфаты).
Концентрированная серная кислота проявляет окислитель-
ные свойства за счет понижения валентности атома серы. При
этом, в зависимости от восстановителя, серная кислота может
восстанавливаться до SO2, до S и до H2S. Так:
Си 2H2SO4 (коиц.) — CuSO4 + SO2 2Н2О
При взаимодействии с цинком в зависимости от концентра-
ции H2SO4 и температуры наряду с ZnSO4 получается или SO2,.
или S, или H2S. При взаимодействии концентрированной H2SO4
с углем последний окисляется до СО2, a H2SO4 восстанавли-
вается до SO2. При действии H2SO4 на элементную серу SO2'
появляется и как результат восстановления H2SO4 и как ре-
зультат окисления серы.
Разбавленная серная кислота может окислять только ак-
тивные металлы (находящиеся в ряду напряжений левее во-
дорода). Например, для получения сернокислого цинка приме-
няют реакцию
Zn 4. H2SO4 = ZnSO4 + Н2
Но здесь окисление металла, как и всякой другой кисло-
той, происходит не за счет изменения валентности атома серы,,
а за счет восстановления иона водорода.
Разнообразно применение серной кислоты, основанное наг
24
ее взаимодействии с оксидами металлов, — так в машинострое-
нии железо освобождают от ржавчины
FeO + H2SO4 = FeSO4 + Н2О
Этим же путем получают разнообразные промышленные
сульфаты:
Fe2^3 3H2SO4 = Fe2(SO4)3 -J- ЗН2О
CuO + H2SO4 = CuSO4 + H2O
A12O3 + 3H2SO4 = A12(SO4)3 + 3H2O
Сульфаты железа и алюминия применяют в качестве коа-
гулянтов, сульфат меди — в качестве минеральной краски и
препарата для борьбы с болезнями растений. Двойные сульфа-
ты типа KA1(SO4)2 применяют в крашении, дублении кож,
в производстве лаков, в качестве коагулянтов и др.
Получаемый при взаимодействии серной кислоты с аммиа-
ком сульфат аммония применяют в качестве удобрения. Этот
процесс, в частности, используют при очистке коксовых газов
от аммиака.
В ряде случаев серную кислоту применяют для освобожде-
ния более слабых кислот из солей. Так, в громадных масшта-
бах получают фосфорную кислоту из трикальцийфосфата (фос-
форита) :
Са3(РО4)2 + 3H2SO4 = 2Н3РО4 + 3CaSO4
Взаимодействием этих же веществ в другом соотношении
непосредственно получают удобрение (монокальцийфосфат в
смеси с гипсом):
Са3(РО4)2 + 2H2SO4 = Ca(H2PO4)2-2CaSO4
Вследствие того, что серная кислота при обычных услови-
ях является нелетучей, она вытесняет из солей другие тоже
сильные, но летучие кислоты:
NaNO3 + H2SO4 = HNO3 + NaHSO4
2NaCl + H2SO4 = 2HC1 + Na2SO4
CaF2 + H2SO4 = 2HF + CaSO4
При получении фосфорных удобрений из апатита действием
серной кислоты одновременно освобождают и фосфорную, и
фтористоводородную кислоты:
Ca5(PO4)3F + 5H2SO4 = ЗН3РО4 + HF + 5CaSO4
Серную кислоту применяют и для разложения руд — комп-
лексов различных оксидов металлов. Характерным в этом от-
ношении является процесс производства диоксида титана из
минерала ильменита, состоящего в основном из FeTiO3 с при-
месью РегОз и оксидов ряда других металлов.
В связи со способностью высококонцентрированной серной
кислоты активно присоединять воду (жидкую и пары) ее при-
25
меняют для осушки газов, для концентрирования азотной кис-
лоты и др.
Разнообразное применение это типично неорганическое со-
единение нашло в органических производствах [14, 15]. Так,
в одном из промежуточных процессов производства вискозно-
го волокна серной кислотой разлагают ксантогенат целлюлозы.
Действием серной кислоты на олефины с последующим гидро-
лизом получают спирты. Так, получают этиловый спирт из эти-
лена:
н2о
СН2=СН2 + H2SO4 --> CH3CH2OSO2OH ---> СН3СН2ОН + H2SO4
В широко применяемых процессах нитрования органиче-
ских соединений концентрированная серная кислота входит в.
состав нитрующих смесей; при взаимодействии азотной и сер-
ной кислот возникает ион NO2+ который реагирует с арома-
тическим соединением.
На основе нитропроизводных ароматических соединений по-
лучают сотни различных веществ: взрывчатых, лекарственных,
красителей, пищевых продуктов и др.
Не менее богат комплекс веществ, получаемых и на основе
сульфирования органических соединений. Сущность этого про-
цесса сводится к введению сульфогруппы — SO3H в органиче-
ское соединение вместо атома водорода. Реакцию проводят
концентрированной серной кислотой, олеумом, триоксидом се-
ры и хлорсульфоновой кислотой. На основе сульфирования ор-
ганических веществ ароматического ряда получают множество
лекарственных средств и красителей, а из соединений жирно-
го ряда—разнообразные моющие средства.
Большая часть серной кислоты потребляется в производст-
вах неорганических продуктов — главным обреем минераль-
ных удобрений. В зависимости от особенностей получаемых
продуктов к товарной кислоте предъявляют разные требования
в отношении ее концентрации и допустимого содержания при-
месей. Важно также, чтобы концентрация H2SO4 по возмож-
ности соответствовала низким температурам замерзания кис-
лоты.
С расширением потребности в серной кислоте в ряде произ-
водств (искусственного и синтетического волокон, капролакта-
ма, органических красителей, чистого бензола, титановых бе-
лил, в пищевой и ряде других отраслей промышленности) бы-
стро повышается спрос на улучшенные ее сорта, возрастают
требования в отношении допустимого содержания примесей.
Особенно жестки требования в отношении содержания остат-
ка при прокаливании, железа, оксидов азота, мышьяка, ме-
таллов II группы, селена. Так, увеличение содержания железа
в контактной кислоте, применяемой в производстве вискозного
волокна, с 0,015 до 0,03% уменьшает скорость фильтрации
вискозы в 7—8 раз и ухудшает качество изделий из этого во-
локна (прочность и др.).
26
В настоящее время, в связи с дифференциацией требова-
ний к качеству серной кислоты, кроме технической контактной
кислоты (1-й и 2-й сорта) выпускаются два сорта улучшенной
кислоты (высший сорт и 1-й сорт). Олеум выпускается 3-х
сортов: технический и улучшенный (высший сорт и 1-й сорт).
Кроме того, для отдельных производств выпускаются специ-
альные сорта кислоты и олеума: аккумуляторная и реактив-
ная кислоты, кислота особой чистоты, 65%-ный олеум, а так-
же 100%-ный серный ангидрид. Выпускаются отдельные виды
кислоты со знаком качества.
В настоящее время требования к качеству серной кислоты и
олеума определяются следующими ГОСТами: техническая
кислота и олеум — 2184—77; аккумуляторная кислота — 667—
73; реактивная кислота — 4204—66; кислота особой чистоты —
14262—78.
1.3. СЫРЬЕ ДЛЯ ПРОИЗВОДСТВА СЕРНОЙ КИСЛОТЫ [16—38]
Источниками серосодержащего сырья для производст-
ва серной кислоты являются: руды самородной элементарной
серы; сернистые соединения металлов; сернистые соединения
природных горючих газов, нефти и угля; сульфаты; серосодер-
жащие отходы различных производств.
Суммарные ресурсы так называемой попутной — химически связанной
серы во много раз превышают запасы месторождений самородной серы и на
перспективу станут основной базой для развития отраслей промышленности,
потребляющих это сырье [16].
До 1975 г. основным видом сырья в сернокислотном производстве был
колчедан, на основе которого выпускалось свыше 40% всей кислоты, из серы
33,6%. В 1980 г. доля серы достигла 49,0%. Помимо новых заводов на серу
переводится ряд заводов, ранее использовавших колчедан.
Выпуск кислоты из отходящих газов цветной, черной металлургии и неф-
теперерабатывающей промышленности в общем объеме выпуска кислоты в
1980 г. составлял всего 18,5%. Однако с учетом назревшей необходимости
охраны окружающей среды и экономии сырья абсолютный выпуск кислоты в
перспективе должен увеличиваться. В производство кислоты и других про-
Таблица 2. Структура потребления серосодержащего сырья
в производстве серией кислоты ряда стран
Страны
Виды сырья в % от общего потребления
сера колчедан серосодер- жащие газы прочие
1975 г.| 1980 г. 1975 г.1 1980 г. 1975 г.| 1980 г. 1975 г.| 1980 г.
СССР 33,6 49,1 41,7 32,2 24,4 18,5 0,3 0,2
США 86,0 81,1* 1,0 2,0* — —. 13,0 16,9’
ФРГ 37,5 41,7 28,3 26,4 29,5 31,9 4,2 —.
Япония 17,1 26,3 21,7 13,1 61,2 56,0 — 4,6
* Данные за 1978 г.
27
дуктов будут также вовлекаться газы ТЭЦ, обладающие громадными ресур-
сами серы.
За счет отработанной серной кислоты в настоящее время обеспечивается
5% народнохозяйственной потребности в серной кислоте. Использование раз-
личных видов вторичных кислот будет увеличиваться.
Весьма значительны потенциальные ресурсы колчедана в отвалах обо-
гатительных фабрик. Часть этих отвалов при условии необходимой сушки в
настоящее время может рассматриваться как весомое дополнение к ресурсам
минерального сырья. Структура потребления серосодержащего сырья показа-
на в табл. 2.
1.3.1. Сера
Сера, применяемая в качестве сырья для производства
серной кислоты и других продуктов, получается из ее природ-
ных залежей (в земной коре содержится 0,03% серы), из серо=-
водорода природных газов, газов нефтепереработки, генера-
торных и коксовых газов, из сульфидных руд и диоксида серы.
Общие запасы этого важнейшего серосодержащего сырья на-
много превышают потребности в нем сернокислотной промыш-
ленности.
Свойства серы. Сера S (атомная масса 32,06) в зависимо-
сти от конкретных условий проявляет чрезвычайно многооб-
разные химические и физические свойства. Многообразие хи-
мических свойств и химическая активность серы связано впер-:
вую очередь с ее способностью проявлять и восстановитель-
ные, и окислительные свойства, меняя валентности от —2 до
+6. Разнообразие физических свойств связано с тем, что ее
молекулы в зависимости от температуры и других условий мо-
гут состоять из разного числа атомов с различным их распо-
ложением. Кроме того, в твердом состоянии сера может да-
вать кристаллы различных систем.
Ниже 95,6 °C твердая сера наиболее устойчива в так на-
зываемой форме Sa, кристаллизующейся в ромбической систе-
ме. Почти вся природная сера встречается в виде ромбической
формы желтого цвета. В пределах 95,6—119 °C наиболее устой-
чива форма Sp, кристаллизующаяся в моноклинной системе.
Плотность ромбической серы при 20 °C — 2,07 г/см3. При быст-
ром охлаждении расплавленной серы в холодной воде получа-
ется пластическая (аморфная) сера формы S^. Сера, получен-
ная при быстром охлаждении паров, так называемый серный
цвет, состоит главным образом из этой формы.
Сера обладает очень малой электропроводностью и тепло-
проводностью. Теплоемкость твердой серы составляет 0,67—
0,75 кДж/кг (0,16—0,18 ккал/кг), жидкой при 115,21 °C —
0,99 кДж/кг (0,23624 ккал/кг).
В воде сера нерастворима, хорошо растворима (кроме
аморфной) в сероуглероде и хуже в других органических рас-
творителях — толуоле, бензине, ацетоне, каменноугольной смо-
ле, бромистом этилене и др. При обычной температуре в рас-
творителях сера присутствует в виде колец Ss.
28
При 119 °C и нормальном давлении твердая сера не суще-
ствует; при температуре ниже 110 °C и том же давлении не су-
ществует жидкая сера. При 119 °C моноклинная сера перехо-
дит в Si (жилк.) с поглощением тепла — 1236 кДж/моль
(295 ккал/моль). При 112,8 °C ромбическая сера плавится и
превращается в жидкость соломенного цвета. Вязкость жид-
кой серы 0,01—0,0078 Па-с. Теплоемкость жидкой серы опреде-
ляется по уравнению
ср= 1,84 —1,95-10-зТ
Теплота парообразования при 444,6 °C и нормальном дав-
лении равна 288,1 кДж/кг (68,6 ккал/кг). Начиная со 155—
160 °C, жидкая сера буреет и вязкость ее увеличивается, при
200 °C расплавленная сера становится коричневой и вязкой,
как смола. При дальнейшем повышении температуры вязкость
уменьшается и при 400 °C сера становится легкоподвижной,
а при 444,6 °C и нормальном давлении кипит. В условиях рав-
новесия пары серы состоят из молекул S2, S6 и Ss- При темпе-
ратуре кипения пары содержат 3,8% (об.) S2, 54,6% S6 и
41,6% S8.
Давление паров над жидкой серой в интервале 120—325 °C
описывается уравнением (р в Па, Т в К)
„ 5405,1
1g р = 16,825 — 0,00622387 — —~-
в интервале 325—550 °C lgp= 9,5587 ———
Оксиды и кислородные кислоты серы [10]. Сера обра-
зует четыре нормальных оксида: трноксид серы SOs и диоксид серы SO2 (см.
выше), полуторный оксид серы S2O3 и моиооксид серы SO; кроме того, сера,
образует две перекиси: семноксид серы S2O7 и тетраоксид SO4.
S2O3 получается в виде голубоватых кристаллических чешуек при дейст-
вии серы на совершенно безводный трноксид серы. При попадании влаги
образует темно-голубой раствор, в олеуме растворяется с образованием рас-
творов от голубого до коричневого цвета; коричневые растворы содержат
коллоидную серу. (Данные о SO см. на стр. 30.)
Известны следующие кислородные кислоты и их соли, не имеющие среди,
оксидов серы отвечающих им ангидридов:
Кислота Соль
H2S2O3—тиосерная (неустойчива)
H2S2O2— тиосернистая* *
H2S2O4 — днтиосернистая (гидросериистая)
H2S2O6 — дитноновая
H2S3O6 — тритионовая
H2S4O6 — тетратионовая
FbSsOe — пентатионовая
Нг8бОб— гексатноновая
НгЗхОе—политионовые кислоты**
М>2
М>2
М>2
М'2
S2O3] — тиосульфаты
S20a] — сульфоксилаты
’S2O4] —днтионнты
Д2О6] —дитионаты
M^fSxOe] —политионаты**
* Получается только как промежуточный продукт при различных реакциях, извест-
ны ее эфиры, в водном растворе, вероятно, находится в равновесии с H2S и H2SO3.
* В политионовых кислотах и политионатах х может быть до 10, известны политио-
наты с 20—40 атомами серы.
2»
SO — бесцветный газ, при обычных температурах не реагирует с кислоро-
.дом, реагирует с водой сначала по уравнению 3SO+H2O=H2S+2H2SO3,
затем происходит выделение серы и образование политионовых кислот. SO
получена в 1933 г. Шенком при действии слабого разряда на SOz или смесь
SO2 с парами серы; определена Шенком спектрографически при сгорании се-
ры в избытке ее паров.
Свойства серы, которые необходимы для понимания про-
цесса ее горения, рассмотрены в соответствующем разделе
(см. стр. 91—93).
Сера из самородных руд. Мировые запасы самородной серы
на начало 1977 г. оценивались в 869 млн. т, в том числе досто-
верные и вероятные запасы 359 млн. т, из них 307 млн. т пред-
ставлены карбонатными рудами осадочных месторождений и
52 млн. т — серно-кварцевыми рудами вулканогенных место-
рождений.
Первое место по запасам самородной серы среди промыш-
ленно развитых капиталистических и развивающихся стран при-
надлежит Ираку (335 млн. т, в том числе достоверные и ве-
роятные запасы 83,1 млн. т, содержание серы в руде 23%),
второе место занимает США —штаты Техас, Луизиана, Кали-
форния, Невада (запасы 150 млн. т), затем следуют Чили
(100 млн. т), Мексика (80 млн. т). Месторождение серы в США,
.Мексике, Италии, Палестине, Испании относятся к месторож-
дениям осадочного типа, которые содержат около 70% общих
запасов серы.
К важнейшим месторождениям серы вулканогенного про-
исхождения относятся залежи на Западном побережье Юж-
ной Америки (Чили, Боливия, Перу), а также на островах и
полуостровах, обрамляющих с запада Тихий океан (острова
Японии, Филиппинские острова, Камчатка, Курильские остро-
ва и др.). Руды ряда крупных серных месторождений этого ти-
па отличаются высоким содержанием серы — до 90%.
Наиболее выгодным методом добычи серы из руд является
метод ПВС (подземной выплавки серы), впервые осуществ-
ленный в США (метод Фраша). Он заключается в том, что се-
ру расплавляют непосредственно в месте ее залегания перегре-
той водой, закачиваемой через специально оборудованную до-
бычную скважину, а затем в жидком виде выдавливают на по-
верхность земли сжатым воздухом. Поскольку при температуре
выше 160 °C вязкость серы быстро увеличивается, вода подается
в скважину при 120—159 °C (0,6—0,7 МПа). Этот способ пол-
ностью исключает необходимость предварительной добычи ру-
ды и ее обогащения.
Однако этот метод применим только к залежам, удовлетворяющим ряду
особых требований. Основными из них являются следующие: покрывающие
;рудное тело породы должны быть водонепроницаемы, подстилающие породы
также должны быть или полностью водонепроницаемы или значительно мень-
ше водопроницаемы, чем сам рудный пласт. Глубина залегания рудного тела
при ПВС ие влияет столь значительно на стоимость добычи, как при откры-
той добыче руды. Одиако при очень мелком залегании рудного тела (20—
30 м) возможны осложнения вследствие гидравлического разрыва покрываю-
30
щего слоя. При глубине залегания 600—800 м процесс может стать неэконо-
мичным. Как показала практика, оптимальной глубиной рудного слоя являет-
ся 120—500 м, мощностью — около 10 м. При мощности слоя менее 3 м
экономичность метода становится сомнительной. Хорошим показателем счи-
тается содержание серы в руде не менее 20%.
При лучших показателях залегания руды степень извлече-
ния серы способом ПВС достигает 70%. Степень извлечения не
выше 40% считается неудовлетворительной. Продукт получа-
ется с содержанием серы 99,5—99,9%. Извлекаемую таким об-
разом серу как правило в жидком состоянии и перевозят (на
судах, в железнодорожных или автомобильных цистернах) к
местам потребления.
Наиболее крупным месторождением осадочного типа раньше
были залежи на острове Сицилия. Много месторождений этого
типа разной мощности известно и в СССР. Крупнейшими из них
являются открытые в пятидесятых годах залежи серы в За-
падной Украине (месторождения Роздольское, Яворовское и
др.), а также в Польше. Руда содержит 20—22% элементной
серы, остальное — карбонат кальция с примесями глины и
гипса.
Месторождения серы сильно различаются и по глубине, и
по характеру залегания, и по разбавленности сопутствующей,
породой, и по характеру последней. Техника и методы отделе-
ния серы от породы за длинный период развития серной про-
мышленности претерпели большие изменения.
За рубежом самородную серу добывают в основном мето-
дом ПВС, в СССР широко распространен открытый способ
добычи и флотационно-автоклавный метод переработки. В ка-
честве сырья используют серный концентрат с содержанием
70% серы, вырабатываемой на обогатительной фабрике фло-
тационным методом.
Автоклавный метод. Серный концентрат с обогатительной фабрики на-
правляют в отделение сгущения (обезвоживания), где распределяют по кон-
центратным сгустителям, в которые подают гидролнзованные растворы поли-
акриламида и крахмала. Концентрат проходит две стадии сгущения. Слив'-
концентратных сгустителей I стадии насосами закачивают на сгуститель
II стадии обезвоживания. Слив со II стадии обезвоживания подают на сгу-
стители «хвостов» плавок. Сгущенный концентрат I и II стадий обезвожи-
вания направляют в коллектор, усредняют и насосами подают в скруббер,,
где он подогревается парогазовыми выбросами «хвостов» предыдущих пла-
вок до температуры 40—60 °C, а затем в коллекторы подогретого концентра-
та и распределяют по автоклавам.
Концентрат в автоклавы можно загружать поочередно по двум линиям.
В процессе загрузки подогретого концентрата и специальных реагентов (ос-
ветительный керосин, раствор триполифосфата натрия, раствор жидкого-
стекла), которые способствуют выделению серы из концентрата при авто-
клавном процессе выплавки, в автоклав подают перегретый пар — до дости-
жения необходимой температуры плавления серы. При плавлении концент-
рата в нижней части автоклава образуется слой жидкой серы, над которым-
находится суспензия пустой породы в смеси с неразделенной частью серы
(«хвосты»).
Серу нз автоклава под избыточным давлением 0,20—0,25 МПа сливают
через игольчатую задвижку и по обогреваемому серопроводу поступает в
311
баки, откуда насосами откачивают в механические отстойники. Из отстойни-
ков сера по обогреваемым серопроводам самотеком сливаетси на открытые
площадки склада, где и застывает в монолит. Затем скальными экскавато-
рами ее взрыхляют, перемешивают для усреднения и грузят в открытые ва-
гоны. Часть серы из баков-отстойииков перекачивают в цех очистки, где ее
очищают от примесей органических веществ. В результате получают серу
высшего сорта.
Осевшую иа днище золу в смеси с частью серы удаляют из отстойников
в гранулированном виде (гранулирование в струе холодной воды) на обо-
гатительную фабрику для доизвлечения серы.
По автоклавному методу из руды, содержащей 20% серы,
получают продукт с содержанием 99,5—99,7% серы; общее
извлечение серы из руды составляет 80—85%.
Известны многие примеры организации извлечения серы из руд экстрак-
цией растворителями. Небольшие установки, основанные иа этом принципе,
работают в Италии, Чили, Японии. Однако широкого распространения такие
установки не получили из-за сложности аппаратуры и дороговизны раствори-
телей. По сообщению американской фирмы «Ралеф М. Парсоиос» 6, для это-
го процесса найден дешевый и эффективный растворитель. При этом из 10—
20 %-ной по сере руды извлекают 90% серы чистотой 99,5%.
Сера, получаемая при переработке серных руд, содержит
до 0,5% не растворимых в ней неорганических солей, кислот и
влагу. От этих примесей серу сравнительно легко освободить
дополнительной очисткой. От примесей органических веществ,
мышьяка, селена, частично растворимых в сере, полностью
освободить ее гораздо труднее. Наиболее вредными примесями
.в сере, отрицательно влияющими на процесс ее переработки,
а также на качество получаемой из нее готовой продукции
(в том числе и серной кислоты), являются масла, битумы и
мышьяк.
До 1970 г. сера, получаемая из самородных серных руд глав-
ным образом методом Фраша (США, Мексика, Польша), в об-
щей массе производимой серы занимала около 60%. Но, в связи
с открытием месторождений природных газов, богатых серово-
дородом, а также ростом выбросов сероводорода с промышлен-
ными газами, быстрыми темпами стало расти производство
серы из сероводорода.
Сера из природных газов, нефти и углей. Если бы появи-
лась возможность извлечь всю содержащуюся в них серу, то
потребность в сере основного ее потребителя — сернокислотного
производства была бы значительно превышена. В процессах
коксования и газификации угля сера частично переходит в се-
росодержащие газы. Исходя из уровня расхода угля в СССР
на коксование и содержания в нем серы, ее ресурсы в коксо-
вом газе оцениваются как значительные. Однако фактическая
реализация этих ресурсов для сернокислотного производства
очень низкая, поскольку их используют в качестве энергети-
ческого топлива. В настоящее время серосодержащие соедине-
ния углей и нефти, которые переходят в дымовые газы, пока
не используются по причине очень низкой концентрации в них
SO2.
32
Реально можно говорить об использовании серы, находя-
щейся в виде H2S в природных и попутных газах (растворен-
ных в нефти и выделяющихся при ее добыче), в различных
газах, получающихся при химической переработке нефтей и
углей. Сероводород, извлекаемый из указанных газов, непо-
средственно сжигается до SO2 с целью получения серной кис-
лоты, если она требуется в данном месте. При других услови-
ях сероводород перерабатывают в серу.
Природные газы ряда месторождений содержат значитель-
ные количества сероводорода. Так, газы Лакского месторожде-
ния во Франции содержат 15% H2S, в газах некоторых место-
рождений Канады содержание H2S достигает 40%. Крупные
газовые месторождения со значительным содержанием H2S
имеются и в СССР (в Оренбургской области, в Средней Азии
и др.). Количество серы, которая может быть получена из этих
газов, оценивается примерно в 2 млн. т в год.
Нефти чаще всего являются сернистыми (0,5—2% S) и вы-
сокосернистыми (более 2% S). При различных процессах пе-
реработки нефти получаются углеводородные газы, содержа-
щие 5—10% H2S. Общее количество серы нефтей СССР, кото-
рая может быть получена при имеющейся технике, может обес-
печить работу нескольких крупных сернокислотных систем.
В газах нефтепереработки почти не содержится диоксида угле-
рода, поэтому при алканоламиновой очистке получается почти
100%-ный сероводород.
Природные газы часто наряду с сероводородом содержат
диоксид углерода, который поглощается алканоламинами вме-
сте с сероводородом, поэтому кислые газы представляют смесь
сероводорода как правило более 50% и диоксида углерода.
Сероводород этих газов перерабатывают в элементную серу
обычно по модифицированной схеме Клауса, состоящей из трех
последовательных ступеней окисления сероводорода с проме-
жуточной конденсацией.
На установках типа Клауса выпускают комовую и жидкую
серу. На отдельных установках небольшой мощности серу по-
лучают также в гранулированном виде с размером гранул
2,5—5 мм. Содержание серы в продукте 99,9%.
Большие работы по развитию и усовершенствованию метода
Клауса позволили фирме «Лурги» довести степень извлечения
серы из отходящих газов до 99,0—99,5% и совместно с фран-
цузской фирмой «SNPA» довести разработку метода «сульф-
рен» до промышленного внедрения. Принцип этого метода —
каталитическое превращение H2S и SO2 (после установок Клау-
са) в элементную серу при 120—160 °C с конденсацией и аб-
сорбцией образующейся серы на катализаторе (активный оксид
алюминия). Отработавший катализатор регенерируют при
250—300 °C горячим газом.
В 1970 г. была построена первая крупная установка на ме-
сторождениях природного газа в Лаке на Юге Франции. В на-
3—584
33
стоящее время эксплуатируется более 10 установок в Европе,
Канаде и других странах.
Сера из 8О2-содержащих газов. Основная масса 8О2-содер-
жащих газов — это отходящие газы металлургических произ-
водств. В значительной степени их используют непосредственно
на производство серной кислоты. Однако для ряда географиче-
ских точек переработка таких газов в серную кислоту нецеле-
сообразна и предпочтительно получение из них элементной се-
ры (при концентрации газа выше 5—8% SO2, менее концентри-
рованные газы следует обогащать).
Физико-химические основы процесса восстановления диокси-
да серы различными твердыми или газообразными восстанови-
телями (углем, коксом, оксидом и серооксидом углерода, во-
дородом, метаном и др.) были изучены еще в 30—40-е годы.
В дальнейшем ряд исследований был посвящен разработке
катализаторов, кинетики гетерогенного взаимодействия SO2 с
восстановителями и технологии производства [18—22].
Результаты термодинамических исследований процесса по-
лучения серы из сернистых газов металлургических производств
для 600 различных газовых смесей с использованием 10 газо-
вых восстановителей при различных температурах ведения про-
цесса были рассмотрены на 15 тыс. примеров с помощью вы-
числительных машин [23]. На основе проведенных исследова-
ний [20—23] было установлено, что наиболее простое аппа-
ратурное оформление будет иметь процесс восстановления SO2
до H2S метаном на катализаторе при 600—750 °C (4SO24-
+3CH4 = 4H2S+2H2O + 3CO2 +322,8 кДж) с последующей пере-
работкой H2S в серу по известному способу Клауса.
Способы переработки H2S в серу и серную кислоту по ме-
тоду мокрого катализа отработаны и внедрены в промышлен-
ность. В этой области задачи сводятся к увеличению числа и
мощности производств и повышению степени очистки отходя-
щих газов.
Разработкой процесса получения серы из отходящих газов
путем восстановления SO2 природным газом занимаются мно-
гие зарубежные фирмы, главным образом США [24—26].
Сера из пиритов. Наиболее перспективным в настоящее
время процессом комплексной переработки пиритов с получе-
нием серы является процесс финской компании «Оутокумпу
Оу», который эксплуатируется на серном заводе в Коккола
[30].
Сухой пиритный концентрат (влажность не более 0,02—0,1%) подвер-
гается взвешенной плавке в атмосфере газов от сжигания мазута. Образую-
щиеся газы выходят из печи при 1250 °C и содержат 3—4% S; 2,5—3% О2;
1,5% Н2; 0,8—1,4% H2S; 0,1—0,2% COS; 3,5—4,5% СО; 10—11% СО2; 69—
71% N2 и 200 г/м3 пыли. При охлаждении газов до 350 °C получается пар с
давлением 0,7 МПа. Газы проходят двухступенчатую конверсию по методу
Клауса с промежуточным выделением серы. Серу очищают известковым мо-
локом. Содержание примесей в сере незначительно: менее 0,005% As, менее
0,004% Se и 0,015% нелетучего остатка. Содержание основного вещества до-
стигает 99,98%. Общее извлечение серы из концентратов составляет 90%.
34
Серу направляют потребителям в жидком виде в цистернах или в гранули-
рованном виде. В процессе на 1 т концентрата расходуется 50 кг мазута и
50 кг бензина, который впрыскивается в аптейк печи и над расплавом в от-
стойник серы.
Штейн сжигают в печах КС системы «Лурги», газы направляют на про-
изводство кислоты, огарок (0,5—0,2% S) в гранулированном виде отправ-
ляется в ФРГ. Завод выпускает в год 150 тыс. т элементной серы, 175 тыс. т
кислоты, 370 тыс. т огарка и получает 400 млн. кВт-ч электроэнергии. Доход
предприятия складывается из продажи серы — 60%, энергии — 30% и огар-
ка — 10%.
Процесс внедрен во многих странах. В СССР пущены две установки
-фирмы Оутокумпу. « *
Имеются многочисленные другие методы переработки суль-
фидов в серу, например канадский метод, освоенный на ком-
бинате в Брунсвике, автоклавные методы, выщелачивание
сульфидных концентратов и многие другие, в том числе и по-
лучение серы из слабоконцентрированных сернистых газов
[28].
Качество технической серы в Советском Союзе нормирует-
ся ГОСТ 127—76. Стандарт полностью соответствует рекомен-
дации СЭВ PC 3983—73. В зависимости от применяемого
сырья серу делят на природную и газовую и выпускают следую-
щих видов: комовую, молотую, гранулированную, чешуирован-
ную, литьевую и жидкую. Стандартом предусмотрены 4 сорта
для природной серы — 9995 (т. е. 99,95% S), 9990, 9950,
9920 и 3 сорта для газовой серы — 9998, 9985, 9900.
1.3.2. Колчеданы
По запасам серосодержащих пиритных руд (колчеда-
нов) наша страна стоит на одном из первых мест в мире. Запа-
сы серы в разведанных месторождениях различных колчеда-
нов значительно превышают запасы серы в самородных серных
рудах.
Колчеданами называются рудные минералы, в состав кото-
рых входят сульфиды металлов: железа, меди, кобальта, ни-
келя и многих других. В рудах в зависимости от условий их
-образования наблюдается чрезвычайное разнообразие в соче-
тании сернистых соединений отдельных металлов и комплекс-
ных сернистых соединений двух металлов.
Основой колчеданных руд являются в одних случаях пирит (FeSa), в
других пирротин (Fex-iSx). Если в колчеданной руде (кроме пирита или
пирротина) содержание других, более ценных металлов (медь, никель, ко-
бальт, цинк и др.) недостаточно для их извлечения, то такие руды добыва-
ются для непосредственного использования в сернокислотной промышленно-
сти. При достаточном содержании какого-нибудь одного или нескольких
цветных металлов колчеданные руды добывают и используют в первую оче-
редь для получения этих металлов. Такие руды называют медноколчеданны-
ми, никелевоколчеданными, медноцинковыми и др.
В комплексные колчеданные руды наряду с пиритом входят различные
минералы: сфалерит или цинковая обманка (ZnS), галенит (PbS), халько-
пирит (CuFeS2) и др. Минералы кобальта встречаются чаще в виде кобаль-
томышьяковых и кобальтосернистомышьяковых соединений. В сернистых KO-
S’
35
бальтосодержащих рудах кобальт присутствует главным образом в составе
минералов маннеита (C03S4) и корролита (CoS2). Имеются также залежи
кобальтсодержащих пиритов.
В колчеданных рудах обычно присутствуют многочисленные сернистые
соединения: индия, рения, таллия, соединения селена, теллура, мышьяка, вис-
мута и др., а также примеси свободных благородных металлов (Ag, Au, Pt).
В колчеданную руду входит и так называемая пустая порода, состоящая из
карбонатов и сульфатов тяжелых металлов, кремнезем, глинозем и др.
Серный колчедан на 70—90% состоит из дисульфида желе-
за FeS2 (53,3% серы и 46,7% железа). Встречаются две его
кристаллические модификации: пирит и марказит. Они разли-
чаются по форме кристаллов и некоторым физическим свойст-
вам. Марказит мало распространен в природе, в основном
встречается пирит, поэтому серный колчедан часто называют
пиритом. Пирит кристаллизуется в кубической системе и име-
ет плотность в чистом виде 5,02, а природный — 4,9—5,9 г/см3.
Марказит кристаллизуется в ромбической системе и имеет
плотность соответственно 4,87 и 4,6—4,9 г/см3.
Пирротин, кристаллы которого характеризуются разными отношениями
железа к сере, условно обозначается химической формулой Fex-iSx (чаще
всего от FegS? до FeuSI2). Кристаллическая структура пирротина характери-
зуется гексагональной решеткой. Переменное отношение серы к железу пред-
положительно объясняется тем, что в решетке отдельные места или заняты S
или просто остаются не занятыми (его следует рассматривать как твердый
раствор серы в сульфиде железа). Плотность пирротина 4,58—4,70 г/см3,
твердость около 4. Он магнитен и хороший проводник электричества.
Ресурсы колчедана как сырья для производства серной кис-
лоты повышались параллельно с развитием цветной металлур-
гии, особенно медеплавильной промышленности. По составу
колчеданы отдельных месторождений значительно различают-
ся. Так, содержание серы колеблется от 30 до 51%, железа—
от 18,5 до 45%, меди — от 0,03 до 0,7%, СаО от 2 до 0,015%,
MgO — от 0,5 до 0,05% и т. д. Содержание SiO2 достигает до
5%, А12О3- 0,6%.
Рядовые колчеданы отдельных зарубежных месторождений
содержат 41—50% серы, 38—47% железа, 0,03—0,6% меди,
0,4—3,7% цинка, 0,002—0,5% мышьяка и т. д. Их добывают в
основном как попутный продукт в виде кусков и перед обжи-
гом подвергают дроблению. Значительной роли рядовой колче-
дан не играет.
Сернокислотная промышленность из всех видов пиритного
сырья применяет преимущественно флотационный колчедан.
Методом флотации руды сульфидная часть отделяется от пу-
стой породы и разделяется на фракции, обогащенные по от-
дельным металлам. Так, из колчеданной руды, содержащей
FeS2 и сульфиды меди, в процессе флотации получают медный
концентрат и флотационный колчедан, содержащий в основ-
ном серный колчедан (хвосты флотации). При вторичной фло-
тации флотационного колчедана (хвосты первой флотации) во
вторичные хвосты перейдет главным образом пустая порода,
36
а содержание серы в продукте вторичной флотации (пирит-
ном концентрате) повышается до 38—48%.
Для оптимальных условий дальних перевозок, внутризавод-
скою транспортирования, хранения, дозирования, горения кол-
чедана в печах п, наконец, минимального уноса огарка с об-
жиговыми газами большое значение имеют физические свой-
ства флотационного колчедана. К основным физическим свой-
ствам относятся фракционный состав, гигроскопичность, сыпу-
честь, слеживаемость, удельная, насыпная и истинная плот-
ность, угол естественного откоса, смерзаемость. Физические
свойства флотационного колчедана были подробно освещены в
1935 г. И. Н. Кузьминых. Более подробных исследований этого
вопроса не было сделано, хотя некоторые коррективы и уточ-
нения были внесены в связи с постепенно менявшимся фрак-
ционным составом флотационного колчедана [31].
Флотационный колчедан, совершенно освобожденный от во-
ды, постепенно поглощает ее из влажного воздуха. В течение
5 сут в атмосфере насыщенного парами воды воздуха сухой
флотационный колчедан увлажнялся до содержания воды 2—
2,5%, просто на открытом воздухе за такое же время — до
0,6%. При увеличении влажности колчедана его сыпучесть
уменьшается, а слеживаемость увеличивается. Как показала
практика, колчедан влажностью меньше 0,5% уже настолько сы-
пуч, что он при погрузках и разгрузках очень пылит, а при пере-
возках и внутри цехов «течет» через неплотности вагонов и
других транспортных средств. При влажности свыше 4% он
налипает на стенки бункеров, свыше 6%—комкуется, свыше
11%—превращается в кашеобразную массу, а при 15%—в
пульпу, т. е. вновь приобретает текучесть.
С учетом всего сказанного флотационный колчедан в ме-
сте его получения должен подвергаться сушке. Как показала
практика, в зимнее время во избежание смерзания в колчедане
должно быть не более 3,8% влаги, в летние месяцы допуска-
ется влажность до 8%. В зависимости от влажности колчедана
меняются его угол естественного откоса и насыпная плотность:
Содержание влаги, °/о 0,8 2,8 3,4 4,0 8,2
Насыпная плотность,
кг/л................ 2,12 1,90 1,80 1,80 1,85
Угол естественного отко-
са, град............Около 30 Около 45 — Более 45 —
Насыпная и истинная плотность более мелких фракций кол-
чедана ниже, чем более крупных {31]. Это объясняется тем,
что содержание FeS2 (с большей плотностью) в крупных фрак-
циях выше (содержание пустой породы с меньшей плотностью
выше в мелких фракциях).
Средняя теплоемкость сухого колчедана в интервале тем-
ператур 0—100 °C равна 5,44 кДж/кг (0,130 ккал/кг) [9].
Температура плавления (размягчения) колчедана зависит от
37
его минералогического состава и равняется примерно 642 °C,
при этой температуре колчеданы разлагаются [9]. Некоторые
другие его свойства приведены ниже:
Плотность пирита, г/см
чистого ..................................... 5,02
природного (серного колчедана) .... 4,9—5,2
Твердость природного пирита по Моосу . . 6—6,5
Коэффициент расширения при 20—40 °C, град-1
линейного................................9,1 • 10~6
объемного................................3,4-10“
По средним данным за последние годы на сернокислотные
заводы СССР цветная металлургия поставляет флотационный
колчедан (не перефлотированный следующего состава:
Элемент
Содержание, %
S Fe Zn Си Pb As
40—45 35—39 0,5—0,3— 0,01— 0,1 —
0,6 0,5 0,2 0,15
S1O, Н,0
14—18 4—6
Элемент .... Со Se Те
Содержание, г/т . 50—200 30—60 25—40
Ag Cd Au
10—25 5,5—8,1 0,7—1,5
В настоящее время практически все производство флотаци-
онного колчедана сосредоточено на обогатительных фабриках
Урала и Башкирии. В перспективе его будут выпускать в Ка-
захстане, на Северном Кавказе, в Грузии и Армении.
Требования к качеству колчедана определяются ГОСТ
444—75 на колчедан серный флотационный. Стандарт соответ-
ствует требованиям рекомендаций СЭВ по стандартизации.
Стандартом установлены пять марок флотационного серного
колчедана с содержанием серы сульфидной не менее, %:
КСФ-0 —50; КСФ-1—48; КСФ-2 —45; КСФ-3 — 43; КСФ-4 —
38. Содержание основных примесей должно быть не более, %:
мышьяка — 0,3; фтора — 0,05.
Источником сырья для сернокислотной промышленности
может служить и углистый колчедан.
Содержание S в ископаемых углях колеблется примерно в
пределах от 0,4 до 10% • Сера в углях находится главным обра-
зом в виде пирита и органических соединений (почти поровну
в тех и других) и в значительно меньших количествах в виде
сульфатов.
В угле пирит в значительной части находится в виде жел-
ваков. После околотки и грохочения этот материал (так назы-
ваемый необогащенный углистый колчедан) содержит 30—
40% серы и 12—18% угля. При дальнейшем дроблении и при
отмывке на обогатительных столах получается так называе-
мый обогащенный углистый колчедан, содержащий 42—48%
серы и 5—6% угля.
Особенно целесообразно и экономически выгодно примене-
ние обжига углистого колчедана в смеси с сульфатом железа.
В этом случае (при определенных соотношениях этих компо-
38
нентов в шихте) сульфат железа будет разлагаться целиком за
счет теплоты горения углистого колчедана, а обжиговый газ по
своему составу будет не хуже газа, получаемого от сжигания
безхглистого колчедана в воздухе. К сожалению, этому перс-
пективному сырью пока не уделяется должного внимания. Но
в ближайшие годы это положение должно изменяться в связи
с необходимостью сокращения и в перспективе полной ликви-
дации выбросов вредных газов ТЭЦ.
1.3.3. Диоксид серы металлургических
и топочных газов
На многих металлургических заводах образуется боль-
шое количество газов, содержащих от долей процента до 70%
SO2 — в зависимости от применяемого сырья и технологии.
При концентрации выше 3% SO2 газы условно называются
«крепкими», остальные «слабыми». Использование отходящих
газов цветной металлургии на производство серной кислоты
имеет большое народнохозяйственное значение. Например, на
медеплавильных заводах на 1 т меди теоретически может быть
получено 7—10 т серной кислоты [32].
За последние годы в цветной металлургии внедряются но-
вые прогрессивные методы плавки с применением кислорода —
КФП-, ПЖВ- и КИВЦЭТ-плавки*. Получение при этом высоко-
концентрированных газов дает возможность вовлекать в про-
цесс использования (в основном на получение серной кисло-
ты) одновременно и различные слабые газы.
Гораздо больше, чем на заводах цветной металлургии, вы-
брасывается в атмосферу SO2 с топочными газами ТЭЦ, ГРЭС
и заводских технологических топок. Но проблема использова-
ния этих газов еще более трудна (как с технической, так и с
экономической стороны), чем слабых сернистых газов цветной
металлургии. Поскольку они имеют концентрацию SO2 0,1 —
0,3% (об.), т. е. на 1 т H2SO4 необходимо перерабатывать от
20 до 8 тыс. м3 газа.
До сих пор не реализовано ни одного рентабельного метода
использования SO2 таких газов. Между тем ликвидация вы-
броса громадных масс SO2 становится все более и более не-
обходимой в целях предотвращения загрязнения атмосферы и
водных бассейнов. Эта проблема признана ООН одной из са-
мых актуальных и в последние годы научно-исследовательские
работы в этом направлении ведутся во всех промышленно раз-
витых странах [33]. Многочисленные примененные методы от-
носятся к трем основным направлениям: улавливания и ис-
пользования SO2: абсорбция SO2 растворами и суспензиями,
КФП — кислородно-факельная плавка; ПЖВ — плавка в жидкой ван-
не; КИВЦЭТ — кислородно-взвешенная циклонная электротермическая плав-
ка.
39
адсорбция его твердыми поглотителями и связывание SO2 в
процессе горения топлива, добавляемыми к нему твердыми
поглотителями. По некоторым методам уловленный SO2 оста-
ется в неиспользуемом шламе. В большинстве же рассмотрен-
ных методов ставится задача использования SO2, например
для производства удобрений (сульфат аммония, сложные азот-
но-фосфорные удобрения).
1.3.4. Сульфаты
Ангидрит, гипс, фосфогипс. СССР обладает значитель-
ными запасами сульфатов кальция — гипса (CaSO4-2H2O) и ан-
гидрита (CaSO4), но при существующем балансе серосодержа-
щего сырья в нашей стране нет необходимости применять их
для получения серной кислоты.
Способы получения серной кислоты из сульфата кальция (ангидрита) с
одновременным получением портландцемента были успешно реализованы в
Германии еще в период первой мировой войны. В 60-тые годы один из за-
водов ГДР (г. Косвиг) выпускал в сутки 300 т серной кислоты и 280 т
цемента. Продукция, получаемая из ангидрита, была дешевле, чем из серы
и колчедана на 20 и 15%, а из фосфогипса соответственно на 47 и 42%.
Процесс переработки фосфогипса изучался в СССР, ГДР, ПНР (в опыт-
но-промышленном масштабе на заводе «Косвиг» и комбинате «Визов»),
В странах, располагающих достаточными ресурсами дешевого серосодержа-
щего сырья, производство серной кислоты из фосфогипса оказывается менее
экономичным, чем из серы и колчедана. Удорожающими факторами являются
значительно более высокие расходы электроэнергии, топлива, трудовые и ка-
питальные затраты. Это подтверждают технико-экономические расчеты, вы-
полненные применительно к условиям Советского Союза.
Сульфат железа. В значительных количествах сульфат же-
леза (железный купорос) получают как отход производства,
например диоксида титана, а также в процессе травления ме-
таллов. Так называемые травильные растворы содержат 2,5—
11% свободной H2SO4 и до 15—28% FeSO4-7H2O, считая на
FeSO4. Из травильных растворов FeSO4-7H2O можно выде-
лить, а оставшийся раствор укрепить свежей серной кислотой
и использовать в процессе травления.
Большие количества серной кислоты потребляются в производстве
диоксида титана. При этом на 1 т продукционной ТЮ2 в процессе разложе-
ния ильменита (FeTiOa) получается около 1,25 т сульфата железа (FeSO4)
и 1,8 т так называемой гидролизной кислоты (в пересчете на 100% H2SO4).
Она содержит около 20% H2SO4 и около 15% FeSO4.
Непосредственное использование сульфата железа (железного купороса)
в народном хозяйстве для очистки сточных вод, в качестве ядохимикатов,
для мелиорации солонцовых почв и т. п. далеко не исчерпывает его ресурсов.
По существу, железный купорос является комплексным сырьем — источником
серы и оксида железа. Оксид железа, получаемый из железного купороса в
виде продукта высокой чистоты, может использоваться для изготовления
активных катодных масс, ферритных порошков, полирующих порошков, кра-
сок (сурика) и т. д.
Задача полной и рациональной утилизации сульфата желе-
за (железного купороса) может быть разрешена только при
использовании его для получения серной кислоты, например,
49
в смеси с углистым и (или) серным колчеданом или другими
высококалорийными видами сырья [34]. В 1979 г. в СССР пу-
щена промышленная система для переработки сульфатов же-
леза в смеси с элементной серой в серную кислоту большой
мощности — 360 тыс. т кислоты в год.
Алунит. Алунит [KsSCh-А12(5О4)з-2А12Оз-6Н2О]— сырье
для производства глинозема. От всех видов подобного сырья
(бокситы, нефелины) он отличается высоким содержанием серы.
Обычно алунит содержит примерно по 20% SO3 и глинозема.
При комплексной его переработке с получением глинозема,
серной кислоты, сульфата калия, хлорида натрия и кремневых
отходов в принципе может быть извлечено до 75% серы [35].
При восстановлении алунита парами серы получаются га-
зы, пригодные для производства серной кислоты по полной
схеме — с очисткой от пыли и фтора. В случае применения
циклического метода, по которому сера получается в самом
процессе (при восстановлении SO2), и улавливания отходящих
газов сернокислотного и других производств растворами, обра-
зующимися при выщелачивании восстановленного алунита
[36], процесс его переработки становится практически безот-
ходным.
На одном из алюминиевых заводов, где применено вос-
становление алунита серой, использование серы алунита со-
ставляет около 20%, а основное количество кислоты получают
из привозной серы. В этом случае технически и экономически
целесообразно перевести завод на циклический метод.
1.3.5. Отработанные кислоты
В ряде производств, использующих серную кислоту, она
выходит из процесса в загрязненном или разбавленном (в не-
которых случаях — в загрязненном и разбавленном) виде. От-
работанные кислоты образуются различной концентрацией и с
различным содержанием органических и неорганических при-
месей. Они используются непосредственно или после очистки и
переработки. Эти кислоты следует рассматривать как серосо-
держащее сырье. Доля вторичных кислот в объеме общего по-
требления серной кислоты по ряду стран составляет от 2,5—
4% (Франция, США), примерно до 13% (Япония), в Совет-
ском Союзе — около 6% [34]. Всего у нас используется за год
более миллиона тонн такой кислоты (без учета травильных рас-
творов и кислых гудронов). Общая степень их использования
около 95%. Некоторые данные за 1980 г. (в %) приведены ниже:
Отрасль промышленности Ресурсы Использование
Химическая........................43,1 88
Нефтеперерабатывающая и иефте- 21,2 93
химическая ....................
Коксохимическая....................2,2 ЮР
Прочие ...........................33,5 100
41
Таблица 3. Характеристика отработанной кислоты, %
Производство продуктов Характеристика кислоты
Химическая промышленность
Сода каустическая Полупродукты и красители Диоксид титана Продукты органического теза Сульфоуголь Ацетилен Хлорные соединения Бромэтил Дифенилпропан СИН- 75% H2SO4, примеси CI2, Fe 25—85% H2SO4, нитросоединения 16—20% H2SO4, 15% FeSO4, 2% Fe2(SO4)3, примеси Al, Ti, Ca, Мп н др. 25—30% H2SO4, до 5% органики; 68—72% H2SO4> 1,3—1,8% органики, би- сульфит 40—50% H2SO4, 0,4% органики 75—80% H2SO4, до 6% органики 25—30% H2SO4, 3—4% органики, Fe, CI2 60% H2SO4, органика, FeSO4 63—65% H2SO4, 0,4—0,6% фенола
Коксохимическая и нефтеперерабатывающая промышленность
Алкилирование изобутана, зииа Производство спиртов бен- 82—83% H2SO4, 11% кислых эфиров, 0,2— 4% другой органики 60% H2SO4, до 13% органики
Металлургическая промышленность
Травление металлов 0—10% H2SO4, до 18—20% FeSO4, ингиби- тор коррозии
В химической промышленности отработанная кислота полу-
чается в производстве каустической соды, красителей и полу-
продуктов, хлорсодержащих соединений, продуктов органиче-
ского синтеза, сульфоугля, диоксида титана и других продук-
тов; в нефтеперерабатывающей и нефтехимической промышлен-
ности — в производстве этилового и изопропилового спирта, ал-
килбензина, бензина «калоша», уйатспирита, некаля, сульфано-
ла и др.; в коксохимической промышленности — при очистке и
мойке бензола и нафталина. Характеристика отработанных
кислот дана в табл. 3.
Отработанные кислоты используются в производствах су-
перфосфата, сульфата аммония, для мелиорации солонцовых
почв, травления металлов. Регенерация отработанной кисло-
ты производится методом термического разложения с получе-
нием серной кислоты из сульфатов железа и гидролизной кис-
лоты при разложении их в смеси с серой или колчеданом.
Получаемую в производстве диоксида титана гидролизную кислоту пос-
ле упаривания в одну или две стадии можно использовать в производстве
суперфосфата, сульфата аммония или для травления металлов. После ней-
трализации свободной кислоты железными стружками весь получаемый
сульфат железа можно использовать как товарный продукт.
Кислоты с производств каустической соды и хлорофоса можно исполь-
зовать для осушки хлора, а первую из них также в производстве синтетиче-
ского изопропилового спирта. Кислоту, получаемую в производстве винилхло-
рида, частично используют на обессоливание солончаковых почв. Кислоту с
производства алкилбензина подвергают расщеплению до SO2 с повторным
42
получением серной кислоты. Небольшое количество кислоты с производства
иекаля идет иа производство каучука. Наибольшее количество отработанных
кислот направляется на производство суперфосфата и других минеральных
солей.
Заканчивая рассмотрение различных видов серосодержащего
сырья, следует подчеркнуть, что основным сырьем сернокислот-
ной промышленности является элементарная сера.
Одним из наиболее выгодных видов сырья являются газы
цветной металлургии [46], использование которых важно так-
же с экологических позиций. В отдельных случаях представля-
ется возможной работа крупных потребителей серной кислоты
почти полностью на оборотном сернистом сырье (например,
заводов титановых белил, производств фосфорной кислоты и
концентрированных фосфорных удобрений). В перспективе
должна быть решена проблема использования SO2 топочных
газов или предварительной очистки от серы исходных топлив.
Может быть перспективным использование сероводорода при-
родных газов (после обогащения или в чистом виде) для непо-
средственного получения серной кислоты.
ГЛАВА II
ОБЖИГ СЕРОСОДЕРЖАЩЕГО СЫРЬЯ
11.1. ОБЖИГ КОЛЧЕДАНА [3, 9, 27, 31, 39—54, 74]
11.1.1. Физико-химические основы обжига
колчедана в воздухе
Горение колчедана (пирита) является сложным физи-
ко-химическим процессом, который в зависимости от
внешних условий проходит через ряд последовательных или од-
новременно идущих реакций. Первой фазой горения пирита яв-
ляется его термическая диссоциация:
2FeS3 --> 2FeS -f- S2
При этом образуется газообразная сера ц пирротин, в
котором число атомов серы может быть от FeSi,17 до FeSi.os-
Более ранними исследованиями было доказано, что при 700 °C
FeS и Fe2O3 образуют твердые растворы, которые при охлаж-
дении имеют тенденцию к взаимодействию с образованием
сульфата.
Отгонка серы из FeS2 (в количестве несколько большем, чем
50% от исходной) наблюдается только в расплаве. При нагре-
вании образца флотационного колчедана в токе аргона при
43
580 °C обнаружены остатки пирита и пирротин. При 680 °C
происходит окончательное разрушение кристаллической решет-
ки пирита и пирротин становился преобладающей фазой остат-
ка. Линии троилита (чистого FeS) на рентгенограммах не было
обнаружено и на образцах, отбиравшихся при 740 и 800 °C.
Отношения серы к железу в образцах соответствовали следую-
щим формулам: при 600 °C и FeSi,i3, при 740 °C — FeSi,i0, при
800°C — FeSi,o8. Таким образом, отщепление серы от пирита
.происходит порциями в широком интервале температур.
Остатки от возгонки серы из FeS2 являются пирротинами,
это доказано исследованиями их кристаллической структуры.
Они как и природные пирротины обладают магнитными свой-
ствами.
При низких температурах (250—300 °C) возможно окисление
пирита с образованием сульфата железа:
FeS2 + ЗО„ = FeSOj -f- SO2
Температура начала разложения сульфата равна 167 °C,
выше 300 °C происходит его разложение. При более высоких
температурах окисление пирита проходит до оксидов железа.
При температуре выше 300—400 °C и наличии достаточного ко-
личества кислорода, т. е. в окислительной среде, реакция го-
рения колчедана выражается суммарным уравнением
4FeS2 + 11О2 = 2Fe2O3 -f- 8SO2
а при недостатке кислорода в слабо окислительной среде —
уравнением
3FeS2 + 8О2 = Fe3O4 + 6SO2
Термохимическое уравнение реакции горения FeS2 при
стандартной температуре имеет вид
2-196,5-}-8-70,96—39,0 = 804,68 ккал (3371,6 кДж)
По уравнению Кирхгофа изменение изобарного теплового
эффекта реакции с температурой имеет вид
Д Нт = —801 790 — 14,987 — 0,002Т2 + 5,22 • 105/Г
Термохимические значения тепловых эффектов при горении
FeS2 для различных температур приведены в табл. 4, давле-
ние паров серы на FeS2 — в табл. 5, а над FeS — ниже:
t °C .... 700 800 900 1000 1100 1200
Р мм рт. ст. . .1,85-10-7 6,94-10-« 1,40-10-* 1.77-10'3 15,4-10-3 0,1002
р, Па..........246-Ю"7 923-10-6 186-10-* 235-1Q-3 204,8-10-3 13,320
FeS2 размягчается при 642 °C и, не плавясь, переходит в
FeS, который размягчается при температуре (800 °C), значи-
тельно более низкой, чем температура плавления (1195 °C).
Точки плавления других представляющих интерес соедине-
ний железа: FeO — 1377, Fe3O4— 1527, Fe2O3 — 1560°C.
Медленное окисление колчедана еще до начала их вос-
пламенения. Для колчедана оно наблюдается уже в пределе
44
Таблица 4. Количество тепла, выделяющееся при горении колчедана
Темпера- тура, °C На моль FeSj На 1 кг серы На I1 кг сухой руды (45% S)
1 KKd.l | КДЖ KKd.'i I | кДж ккал | кДж
25 804,680 3369,0 3143,3 13160,3 1414 5920
600 815,750 3415,4 3186,5 13341,2 1434 6004
700 817,725 3423,6 3194,2 13373,4 1437 6016
750 818,700 3427,7 3198,0 13389,4 1439 6025
800 819,680 3431,8 3201,8 13405,3 1441 6033
900 821,670 3440,0 3209,6 13438,0 1444 6046
1000 823,690 3448,6 3217,5 13471,0 1448 6062
Таблица 5. Давление паров серы над FeS2 [11]
Л °C р ^общ ps Ь2 ps ь6 %
мм рт. ст. | кПа мм рт. ст. | кПа мм рт. ст. кПа мм рт. ст. кПа
601 30,0 4,0 29,86 4,0 0,14 0,018 2-Ю-3 0,0002
604 32,0 4,3 31,85 4,2 0,15 0,02 2,3-10-з 0,0003
619 59,5 7,9 59,0 7,8 0,50 0,06 0,01 0,001
626 79,0 10,5 78,3 10,4 0,70 0,09 0,015 0,002
639 121,0 16,1 119,0 15,8 1,95 0,26 0,06 0,008
646 171,5 23,0 167,5 22,3 3,75 0,50 0,13 0,017
654 230,5 30,6 223,5 29,7 6,65 0,88 0,25 0,033
664 249,0 46,4 333,5 44,4 14,80 1,97 0,70 0,093
671 436,0 58,0 413,0 55,0 22,00 2,92 1,15 0,152
676 540,0 71,8 504,5 68,1 33,50 4,45 2,00 0,226
685,5 760,0 101,0 — — — — — —
температуры 170—260 °C [9]. Низший предел температуры
воспламенения определяется началом отщепления первого ато-
ма серы — диссоциации дисульфида железа и воспламенением
отщепившейся серы по уравнению
s + о2 = so2
Температура воспламенения зависит от минералогического
состава, характера примесей, степени измельчения колчедана
и концентрации кислорода в газовой фазе. Различные серни-
стые соединения железа воспламеняются при следующих тем-
пературах, °C: пирротин — 420, пирит — 402, марказит — 378,
арсенопирит — 380, халькопирит — 375. Примеси кварца от 0
до 40% повышают температуру воспламенения с 402 до 418 °C,
добавка 10% угля снижает ее примерно на 50 °C, добавка 10%
огарка практически не изменяет температуры воспламенения.
От степени измельчения колчедана температура воспламенения
зависит следующим образом: при средней степени дробления
0,025 мм температура воспламенения 290 °C; при 0,25 мм —
424 °C; при 0,75 — 426 °C, при 1,5 мм — 428 °C.
Некоторое снижение температуры воспламенения замечено
при повышении влажности газа [13]: с 425 °C при сухом воз-
45
^400
РИС. 7. Дериватограмма нагрева флотационного колчедана
РИС. 8. Зависимость отно-
сительной константы скоро-
сти диссоциации сульфида
железа от температуры при
различной степени выделе-
ния серы.
иа воздухе:
/ — кривая потери масс: 2 — кривая тепловых эффектов; 3 — кривая изменения темпе-
ратуры при нагреве; 4— дифференциальная кривая потери массы.
духе до 397 °C при абсолютной влажности воздуха 198 г/м3.
Температура воспламенения повышается с ростом концентра-
ции SO2 в газовой фазе; отсутствие SO2 соответствует темпе-
ратура 425 °C, при 20% SO2 — 427 °C, при 40 — 435 °C, при
60 — 455 °C, при 80 — 480 °C. Температура воспламенения по-
вышается также с ростом содержания кислорода в газе, по-
ступающем на горение. Такое явление объясняется стимулиро-
ванием процесса образования блокирующей частицы колчеда-
на сульфатной пленки, которая при повышении содержания
кислорода образуется быстрее и получается более прочной
[27].
На рис. 7 представлена дериватограмма нагрева образца флотационного
колчедана на воздухе при атмосферном давлении в открытых платиновых
тиглях на дериватографе МОМ (Венгрия). Скорость нагрева 5 град/мин. На
рисунке выявляются области начала горения — около 340 °C, интенсивного
воспламенения — 420 °C, основного извлечения серы — до 715—730 °C, пол-
ностью процесс заканчивается при 750 °C.
Теоретическая, или максимальная температура горения стан-
дартного колчедана (45% S) на воздухе с получением теорети-
ческой концентрации сернистого ангидрида (15,9%), т. е. при
полном выгорании серы без избытка кислорода в газовой фазе,
равна примерно 1570 °C [3].
46
Практическая температура обжига колчедана в кипящем
слое установлена в пределах 750—850 °C. При этом учитыва-
ется кинетика горения, температура спекания колчедана и дру-
гие факторы. Спекание является результатом того, что при не-
доста!очном и неравномерном доступе воздуха в процессе об-
жига возникают локальные перегревы и появляются FeS п
FeO, которые при 940 °C образуют легкоплавкую эвтектику [4].
Такие продукты обжига колчедана, как Fe2O3 и SiO2 с FeS
легкоплавких эвтектик не образуют. При анализе спеков было
установлено, что они содержат до 14% FeS и до 11% FeO,
а неспекшаяся часть состоит в основном из Fe2O3 и содержит
лишь доли процента FeS и FeO.
Скорость горения является основным показателем процесса
обжига. Знание ее зависимости от различных условий необхо-
димо для разработки рациональной конструкции аппаратуры
и оптимального технологического режима. Кинетика горения
серного колчедана изучалась рядом исследователей с исполь-
зованием различных методов эксперимента.
Применительно к условиям обжига на поду — в неподвижном слое —
фундаментальные исследования проведены в НИУИФе [27, 3]; во взвешен-
ном состоянии для печей пылевидного обжига — в УНИхиме; в условиях
расплава — в МЭИ (Московском энергетическом институте), в кипящем
-слое — в НИУИФе [39, 31] и на кафедре химической технологии МГУ [40].
Исследования процесса термической диссоциации FeS2, т. е.
выделения первого атома серы из пирита, в зависимости от
температуры, проведенные К. М. Малиным [27], показали, что
скорость возрастает с температурой по закону Аррениуса:
А = Л0’ехР (-E/RT)
где Л' — относительная константа скорости; Е—кажущаяся энергия актива-
ции; R- 1азовая постоянная (1,98 ккал/град, или 8,29 кДж/град).
Зависимость относительной константы скорости диссоциа-
ции reS2 от температуры изображена на рис. 8.
Энергия активации для диссоциации FeS2 получена равной
127,3 кДж/моль (30,4 ккал/моль), что свидетельствует о про-
текании процесса в кинетической области [3, 27]. В пределах
температур 1200—1400 °C она равна 113,88 кДж/моль
(27,2 ккал/моль). Таким образом, диссоциация в условиях рас-
плава также проходит в кинетической области.
Пример расчета. При определении численного значения
энергии активации исходят из относительной константы скоро-
сти, за которую принимают изменения степени извлечения серы
(в %) по времени (в с) при разных температурах. Для двух
температур можно написать:
K2/Xi = К0-ехР (—E/RT2)/Ko'exP (—E/RTj)
£ = 2,3£ (lg К2 - 1g /%) • 7\ • Т2/(Т2 - Tt)
47
По рис. 8 (для выделения серы — 28%) между температу-
рами 650 и 800 °C
г- „о по / 3,4—2,2 \ 923-J073
Е~ 2,3-1,987^ [000 ) Ю73 — 923 "=
= 30,4 ккал/моль, или 127,278 кДж/моль
Для образца FeS, приготовленного отгонкой из пирита пер-
вого атома серы в токе очищенного азота, в изучаемом интер-
вале температур (500—900 °C) в неподвижном слое энергия ак-
тивации получена равной 13,23 кДж/моль (3,16 ккал/моль).
Такой порядок величин Е свидетельствует о протекании про-
цесса в диффузионной области [3]. Исследования процесса
окисления пирита в кипящем слое в температурном интервале
700—900 °C проведены непосредственно на образцах флотаци-
онного колчедана. В этом случае энергия активации
16,17 кДм/моль (£ = 3,86 ккал/моль) [39].
В реальном процессе обжига пирита стадия отгонки 1-го ато-
ма серы, ее окисление и окисление образовавшегося FeSn про-
исходит одновременно и взаимосвязанно. В результате отделе-
ния серы остается пористый FeSn с высокоразвитой поверхно-
стью контакта. Кроме того, пирит обладает способностью рас-
трескиваться. В результате соединения серы с кислородом рав-
новесие в этой сложной системе сдвигается вправо.
Расчетным и опытным путем установлено [31], что время
горения пирита флотационного колчедана при 700—800 °C
(реальных температурах обжига в печах КС), подразумеваемое
как суммарное время пребывания частиц в кипящем слое и
надслойном пространстве, для степени выгорания 98% равно
8 с (рис. 9). Для рядового колчедана крупностью 1—2 мм при
800 °C та же степень выгорания достигнута за время более
4 ч. Это свидетельствует о том, что процесс горения рядового
колчедана в кипящем слое лимитируется внутренней диффу-
зией [40].
Вследствие диффузионного характера процесса обжига кол-
чедана наиболее рациональным аппаратурным его оформлени-
ем является обжиг в кипящем слое, при котором снижаются
сопротивления всех диффу-
зионных процессов. В на-
стоящее время обжиг про-
водят почти исключительно
в печах КС.
Ряд авторов исследовал
влияние на скорость горе-
РИС. 9. Зависимость степени вы-
горания серы из флотационного
колчедана в кипящем слое от
времени при температуре 700—
800 °C.
48
ния сернистого сырья компонентов газовой фазы — кислорода ж
диоксида серы. На проблему применения кислорода в серно-
кислотном производстве в СССР впервые было обращено боль-
шое внимание в 1943—1947 гг. по инициативе академика
П. Л. Капицы в связи с его работами по усовершенствованию
кислородных установок. Исследовано [3, 27, 54] влияние кисло-
рода на скорость горения колчедана и FeS. Во всех этих рабо-
тах зависимость скорости горения от концентрации кислорода
имеет следующее выражение
^=ЛС"о2
Установлено, [27], что при сжигании колчедана на поду
при 600 °C в пределах концентрации кислорода 20—50% « =
= 1,2. Позднее та же величина получена [40] при сжигании
FeS при 600—650 °C в кипящем слое; при сжигании FeS в рас-
плаве при 1300 °C и концентрации кислорода 6—18% /1 = 0,9.
Отмечена зависимость п от температуры. Так, при сжигании
колчедана на поду в пределах концентрации кислорода 20—60%
при 550 °C н = 0,75, при 750 °C н = 0,82, а в кипящем слое при
600 °C и концентрации кислорода от 10 до 21% п = 0,65.
При обжиге колчедана с применением кислорода в опытно-
промышленной печи КС [54] производительность печи, подо-
вая и объемная интенсивности процесса увеличивались в пря-
мой зависимости от концентрации кислорода.
Рядом авторов отмечено отсутствие влияния на процесс го-
рения колчедана концентрации диоксида серы в газе. Впервые-
это было показано К. М. Малиным в 1944 г.
11.1.2. Поведение примесей колчедана
в процессе его обжига
Основным компонентом колчедана, как уже указыва-
лось, является дисульфид железа. Но и рядовой, и флотацион-
ный колчедан имеет целый ряд примесей, оказывающих то или.
иное влияние на процесс обжига, на качество получаемых га-
зов, отражающееся на их переработке, или на качество огар-
ков, определяющее возможности и пути их использования.
Все основные примеси к колчедану можно разделить на сле-
дующие группы: породообразующие примеси; сернистые со-
единения элементов подгруппы мышьяка; сульфиды цветных ме-
таллов; селениды и теллуриды и соединения других рассеянных,
элементов.
В состав первой группы примесей входят свободный оксид
кремния, природные силикаты, карбонаты и др. В процессе
обжига карбонаты кальция или магния могут вступать во взаи-
модействие с временно образующимися сульфатами железа,
или цветных металлов:
МеСО3 -р MeSO4 = MeSO4 + СО2 + МеО
4—584
4»
В присутствии свободного SiO2 эта реакция может ограни-
чиваться другой, например
СаСО3 + SiO2 = СаО • SiO2 + СО2
Вновь образовавшиеся сульфаты, например CaSO4, во взаи-
модействие с сульфидами железа и цветных металлов не всту-
пают и при температурах процесса не разлагаются. Поэтому
сульфатная сера этих соединений теряется с огарком или
пылью.
Образование неразложимых в процессе обжига сульфатов
может происходить и другим путем. Так, при медленном охлаж-
дении газа на выходе из печи КС происходит образование
триоксида серы, который с Fe2O3 и другими оксидами (СаО,
MgO), содержащимися в пыли, уносимой газами, дает суль-
фаты.
Очень нежелательной примесью является флюорит, или
плавиковый шпат (CaF2). Между ним и водяным паром, всег-
да имеющимся в газах обжиговой печи, происходит реакция пи-
рогидролиза:
CaF2 + Н2О = СаО ф 2HF
Эта реакция ускоряется в присутствии SiO2, который свя-
зывает СаО в силикат кальция, HF, взаимодействуя с SiO2, об-
разует тетрафторид кремния:
SiO2 4- 4HF SiF4 4- 2Н2О
В зависимости от условий в печи фтор выходит с обжиго-
выми газами на 80—90% в виде HF и на 10—20% в виде SiF4.
Присутствие фтористых соединений в обжиговых газах приво-
дит к необходимости защиты аппаратов последующих отделе-
ний цеха от забивания и разрушения, а также контактной мас-
сы от отравления.
В большинстве видов колчеданного сырья в разных количе-
ствах присутствуют и сульфиды, а также арсениты и антимо-
ниты элементов подгруппы мышьяка (мышьяка, сурьмы и вис-
мута) .
Сульфиды (арсенопирит — FeAsS и антимонит — Sb2S3)
при горении в зависимости от характера газовой среды дают
летучие триоксиды (As2O3 и Sb2O3) и почти не летучие пяти-
оксиды (As2O5 и Sb2O5). Не летучих оксидов образуется тем
больше, чем более окислительной является атмосфера в зоне
обжига. С оксидами тяжелых металлов они дают совсем неле-
тучие арсенаты и антимонаты. Сульфид висмута до 1000 °C
почти не летуч, не летуч и триоксид висмута. В зависимости
от условий обжига с газами уходит 60—80% мышьяка, 20—
40% сурьмы и 5—15% висмута. Так как содержание Sb и Bi
в шихте как правило значительно меньше, чем мышьяка, а
также вследствие значительно меньшей летучести Sb2O3 и
особенно Bi2O3, осаждающихся к тому же уже при сухой очи-
стке, в промывное отделение контактных цехов практически
50
приходит только As2O3 и получаемые там шламы содержат
очень незначительную часть Sb2O3.
Мышьяковые примеси в сернистом сырье создают немало
трудностей в сернокислотном производстве. Во-первых, они
являются ядами для контактных масс, что вызывает необходи-
мость проведения специальной очистки газов. Во-вторых, обра-
зующийся иногда в процессе производства AsH3 (а также и
SbH3) является одним из сильнейших и опасных ядов. Он об-
разуется при взаимодействии мышьяка с водородом, выделяю-
щимся, например, при действии на активные металлы (железо,
цинк) разбавленной кислоты. Наконец, та часть мышьяка, ко-
торая остается в огарке, затрудняет использование огарка в
металлургии, поскольку при окислительном обжиге содержание
мышьяка в огарке в 2—3 раза превышает допустимую норму
(0,05%).
Из соединений цветных металлов в качестве примесей в
шихте присутствуют главным образом сульфиды меди (ковел-
лин— CuS, халькозин — Cu2S, халькопирит CuFeS2), сфалерит,
или цинковая обманка (ZnS), галенит, или свинцовый блеск
(PbS) и др. В условиях окислительного обжига одновалентная
медь, пришедшая в составе халькозина, окисляется до двухва-
лентной.
При низких температурах все эти сульфиды сначала ча-
стично окисляются в сульфаты. При дальнейшем повышении
температуры сульфаты разрушаются (и в результате термиче-
ской диссоциации, и в результате взаимодействия с оставши-
мися сульфидами) с образованием оксидов и SO2. Происходит
и прямое окисление сульфидов до их оксидов и SO2 кислоро-
дом. Определенную роль в окислении сульфидов цветных ме-
таллов играет и образующийся при окислении сульфида же-
леза оксид железа Fe2O3. В результате эти металлы выходят из
печи или в виде оксидов, или в виде сульфатов.
При обжиге в печах КС основная масса огарка уходит из
печи вместе с газом. При медленном охлаждении газа, осо-
бенно в присутствии Fe2O3, в нем образуется SO3, что спо-
собствует значительному превращению оксидов цветных метал-
лов в их сульфаты.
Из рассеянных элементов, содержащихся в колчеданах,
б производстве серной кислоты необходимо учитывать преж-
де всего селен. Минералы селена и его аналога — теллура не
образуют самостоятельных залежей и обычно находятся в ви-
де примесей к аналогичным соединениям серы (или в изоморф-
ной с ними форме, или в виде микроминеральных включений).
При флотации медных руд 60—70% селена и теллура перехо-
дит в пиритную фракцию. По данным сернокислотных заво-
дов, в последние годы в поступающих флотационных колчеда-
нах содержание селена составляет 30—60, а теллура 25—40 г/т.
При обжиге селениды и теллуриды окисляются с образованием
SeO2 и ТеО2. И тот и другой окисел в присутствии оксидов тя-
4'
51
желых металлов могут давать селениты и теллуриты, а частич-
но и селенаты и теллураты.
Из зоны обжига селен и теллур уносятся частично в эле-
ментарном состоянии, частично в виде диоксидов, а также в
виде других соединений. Сведения о температурах плавления
и кипения элементных селена
дены ниже:
Вещество
Температура, °C
плавления
кипения . .
и теллура и их диоксидов приве-
. Se Те SeO2 ТеО2
. 221 449 390 733
. 685 990 — 1275
Из приведенных данных видно, что сорбированный огарком диоксид се-
лена в значительной мере восстанавливается до элементного селена, количе-
ство которого увеличивается с уменьшением температуры (в момент отбора
температура изменялась от 780°C в печи КС до 330°C в электрофильтре).
Проведенные опыты показали, что сорбированный огарковой пылью селен
достаточно прочно удерживается в ней. Так, при 700 °C за 2,5 ч из огарка
улетучилось всего 65,7% селена. Это доказывает, что форма соединений се-
лена в огарке неполностью соответствует диоксиду селена, температура воз-
гонки которого равна 330 °C и указывает на то, что сорбция диоксида се-
лена огарковой пылью сопровождается химическим взаимодействием между
диоксидом селена и компонентами обжигового газа и огарковой пыли. На
сорбцию диоксида селена огарком оказывают влияние концентрация SOj в
газе, температура, а также состав огарковой пыли.
Селен необходимо извлекать из обжиговых газов и потому,
что допустимое содержание его в продукционной контактной
кислоте строго регламентируется, и потому, что он имеет раз-
нообразное применение: в полупроводниковой технике, в сте-
кольной и резиновой промышленности, в ряде фармацевтиче-
ских производств, для легирования некоторых сортов стали
и др.
Выделение селена из колчедана в процессе его обжига за-
висит от степени удаления серы; достаточно полное выделение
селена наблюдается только после удаления свыше 95% серы.
При этом следует отметить, что при высоком содержании FeS
(степень десульфурации 50—95%), выгорание селена почти
прекращается. Это можно объяснить как меньшим сродством
к кислороду у селена, чем у серы, так и взаимодействием суль-
фида железа с образующимся диоксидом селена:
FeS + SeO2 --> FeSe ф- SO2
При обжиге в печах КС в газовую фазу переходит 40—50%
всего селена, поступающего с колчеданом. Распределение по-
терь селена по аппаратам печного агрегата показано в табл.6.
[41].
Зависимость сорбции двуокиси селена огарком из газа от
концентрации сернистого ангидрида в нем [41] приведена в
табл. 7. Выявленный характер зависимости степени сорбции
SeO2 от концентрации SO2 в газе (с наличием максимума), по-
видимому, обусловливается параллельно возрастающей сте-
пенью сульфатизации огарковой пыли.
52
Таблица 6. Распределение потерь селена по аппаратам печного агрегата
Место отбора Потери селена» % Содержание соединений селена, % от общего количества селена в огарке
селей диоксид селена селенит железа (III) селениды железа (II) трудно раствори- мые селе- ниды
Огарок из печи 2,5 60,21 10,06 15,32 14,41 0
Пыль из котла 26,5 63,90 14,76 10,46 9,96 0,92
Пыль из циклона 53,0 66,78 22,07 9,01 2,14 0
Пыль из электро- 18,0 71,08 23,90 5,02 — 0
фильтра
Наиболее значительное влияние на сорбцию ЭеОг огарком
оказывает температура — с ростом температуры до 390—
400 °C она значительно ослаблена. В соответствии с изложен-
ным получение магнетизированного огарка (в форме ЕезСЩ
либо отделение основной массы огарковой пыли от обжигового
газа при высокой температуре позволит уменьшить сорбцию
SeO2 огарком. Повышение степени магнетизации до 81,5%
снижает потери селена с огарком до 36% [41].
Практическое содержание теллура в обжиговых газах не
оказывает особого влияния на их переработку, но извлечение
теллура из-за ряда его ценных свойств является целесообраз-
ным. Если до недавнего времени его применяли в основном в
стекольной, резиновой и химической отраслях промышленно-
сти, то теперь теллур и его соединения стали использоваться в
металлургии, электротехнике, автоматике, полупроводниковой
технике [42].
Распределение теллура (при обжиге колчедана) по тракту
печь — промывное отделение [41] показано в табл. 8. Извлече-
ние теллура целесообразно осуществлять из шламов, собирае-
мых в промывном отделении, технология переработки которых
освоена промышленностью. В связи с этим необходимо вести
обжиг таким образом, чтобы увеличить выход теллура в про-
мывное отделение. Как видно из табл. 8, это достигается либо
Таблица 7. Поглощение SeO2 огарком в присутствии SO2
Концентра- ция SO2 в газе, % (об.) Степень по- глощения SeO2 огар- ком из газа, % Содержание сульфатной серы в огар- ке, % Концентра- ция SO2 в газе, % (об.) Степень по- глощения SeO2 огар- ком из газа, Содержание сульфатной серы в огар- ке, %
0 19,4 0 25,2 15,6 4,2
5,2 26,6 1,6 30,2 13,1 4,3
10,0 29,6 2,0 50,0 12,6 4,5
15,5 25,2 3,2 70,3 10,6 5,1
20,9 16,5 3,7 100,0 7,7 6,0
53
Таблица 8. Распределение теллура при обжиге колчедана
Место отбора с удержание соединений теллура. %
прн окисли- тельном об- жиге в пе- чах КС при магне- ти шрующем обжиге в пе- чах КС (сте- пень магне- тизации 89%) при окислительном обжиге в печи КСЦВ
при воздуш- ном дутье при дутье, обогащен- ном кисло- родом (26%)
Огарок из печи 2,09 1,38 51,80 19,02
Пыль из котла-утилиза- 11,14 5,14 — —
Пыль из циклопа 37,58 20,78 23,25 23,25
Пыль из электрофильтра ' 20,83 23,02 6,42 7,52
Выход в промывное от- деление 28,36 49,68 18,53 50,21
при магнетизирующем режиме обжига, либо при использова-
нии воздушного дутья, обогащенного кислородом.
Из других рассеянных элементов в составе колчеданов присутствуют при-
меси рения, индия, таллия. Все эти элементы в поступающем сырье нахо-
дятся в составе своих сернистых соединений (Re2S7, ReSa, In2S3, InS, In2S,
T12S, T1S, T1S3, TI4S3). В процессах обжига сернистого сырья соединения
указанных элементов испытывают многочисленные превращения: диссоциации
высших сульфидов в низшие (особенно характерно для Re и In), образова-
ние и разложение сульфатов и их взаимодействие с сульфидами (характерно
для In, Т1), образование оксидов вследствие разложения сульфатов и непо-
средственного окисления сульфидов. Конечными продуктами превращений,
по-видимому, являются оксиды и сульфаты вторичного образования.
При расчетах процесса обжига сернистого сырья для получения серной
кислоты нет надобности учитывать реакции, происходящие с соединениями
этих элементов, но надо полагать, что в дальнейшем встанет вопрос о выде-
лении всех этих металлов из огарков, пылей и шламов.
11.1.3. Образование триоксида серы
и спекание шихты при обжиге колчедана
Побочная и нежелательная реакция окисления SO2 до
SO3 протекает при 600—800 °C в условиях каталитического
воздействия оксида железа в присутствии кислорода:
РезОз
SO2 + 0,5O2 4=2: SO3
При 630—640 °C равновесная степень превращения SO2 в
SO3 достигает 65—70%, снижаясь примерно до 20% при 800 °C.
Присутствие в обжиговых газах SO3 ведет к образованию суль-
фатов:
SO3 -р SO2 -р Fe2O3 = 2FeSO4
SO3 -|- 3Fe2O3 = Fe2(SO4)3
54
РИС. 10. Микрофотографии колчедана, обожженного в печи КС при различ-
ной температуре.
В присутствии FeS возможно образование низших оксидов
железа [27]:
5FeSO4 + FeS = 2Fe3O4 + 2SO2
3SO3 + FeS = FeO + 4SO2
Процесс обжига колчедана при 850—900 °C может нару-
шаться спеканием шихты (образуются «козлы»). Предполага-
лось, что спекание связано с образованием эвтектической сме-
си FeS и FeO, состава 60% FeS и 40% FeO, которая имеет
температуру плавления 940 °C. Но размягчение шихты, вызы-
вающее спекание, происходит при температурах ниже этой,
в спеках всегда присутствует FeS в значительных количест-
вах, в то время как в огарке он отсутствует пли содержание
его незначительно. Примесь SiO2, а также Fe2O3 никаких лег-
коплавких систем с FeS не образуют. Степень спекания и проч-
ность спеков значительно увеличивается в присутствии сульфа-
тов железа, причем влияние сульфатов двухвалентного желе-
за более значительно, чем трехвалентного (3).
На микрофотографиях (рис. 10) видно, что при 800 °C на-
блюдается оплавление отдельных частиц шихты, при 1000 °C
заметны уже крупные образования. Образованию спеков спо-
собствуют высокие температуры и наличие FeS и сульфатов.
При нарушении нормального гидродинамического режима в
печах обжига колчедана могут возникать локальные перегревы.
Содержание SO3 в газах в зависимости от условий обжига
и принятого технологического режима составляет 0,3—0,5%. На
рис. 11 приведена зависимость концентрации SO3 в газах от
концентрации SO2
Расчет состава газов обжига. При сжигании любого серосодержащего
сырья в кислородовоздушной смеси любого состава зависимость между со-
держанием кислорода Со, и диоксида серы С so, (в % об.) выражается (без
учета образования SO3) следующим соотношением:
Со2 = n—KCSo2
55
где
вой
РИС. 11. Зависимость между содержанием SO2
и SO3 в газе на выходе из печи КС.
п — содержание кислорода в исходной газо-
смеси (в % об.).
п(т — 1)
К —m 100
т — отношение объема затрачиваемого О2 к
где
объему получаемого SO2.
, Для реакции горения колчедана в воздухе
11 22,4
от = -8~-^ГТ= 1Л064;
п =21;
Я= 1,4064 -0,4064-0,21 = 1,32
где 22,4 и 21,9 — мольные объемы кислорода и двуокиси серы.
Таким образом
Со2 =21—1 ,32-Cso2
Максимальная концентрация:
21
Cso, = 1 32 = 15,9%
Объем сухого обжигового газа при обжиге сульфидного материала
(в м3/кг):
21,9 CSM
с'г- 32 ’ CSo2
Объем сухого обжигового газа на 1 т руды (в м3/кг):
Кгр= 684,4-тЛ-
Cso2
где C-'-s — содержание серы в обжиговом материале, % (при учете образо-
вания SO3 в знаменателе проставляется Cso2-f-Cso ); Cso2—содержание SO2,
% (об.).
Объем диоксида серы в обжиговом газе (в м3/кг):
VSo2 = 0,6844- IO-2-CSM
Объем обжигового газа на 1 т продукции (в м3)
21,9-1000-100 22 347
г'п ~ 98,Пп-С5о2 — nnCso2
где т]п — степень использования SO2 (в продукцию).
Объем воздуха или другой кислородоазотной смеси (в м3/кг):
100+(1,023m — 1) Cso/
V°-P= Vr-P 100
ИЛИ
100+( 1,023m— l)CSOo
VB.n = Vr.n Tm 1
56
Водяные пары поступают в обжиговый газ с сырьем и воздухом или дру-
гой кислородоазотной смесью. Всего на 1 кг руды поступит паров воды
(в м3):
100ш
VPH,O =0.0124 + vI/д
где w — содержание влаги
содержание дутья, м3/м3
в сырье, %; Уд — объем дутья, м3/кг: v — влаго-
<рРнп
р_<рРнп
где ср — относительная влажность, м3/м3; Р — атмосферное давление, Па;
Рпн — давление насыщенного пара при данной температуре, Па.
На 1 т продукции поступит влаги (в м3):
V, п
Гпн2о = ^Рн2о -рГ^-
Объем влажных газов, получающихся при обжиге (в м3/кг):
^в.г — ^с.г “Г ^Н2О
Содержание SO2 в газе обжига (Cso,). объем сухого газа (14), содер-
жание в нем кислорода (Со2), расход сухого воздуха (Ув) на сжигание и
его избыток (а) в расчете на 1 кг серы в колчедане приведены ниже:
Cs(), % .... 15,9 15 14,5 13 12 10 9 8 7,5
J4 м3 .......... 4,30 4,56 4,72 5,265 5,70 6,84 7,60 8,55 9,13
’ % .... 0,0 1,18 1,85 3,82 5,14 7,80 9,1 10,4 11,0
14 м3 ... 4.58 4,84 5,00 5,54 5,98 7,12 7,88 8,33 9,40
а .......... 1,00 1,05 1,10 1,21 1,30 1,55 1,72 1,93 2,05
Выход огарка и степень использования серы сырья. При обжиге колчеда-
на и Других серосодержащих руд образуется огарок, количество которого за-
висит от химического и минералогического состава руды и степени выгорания
серы.
Теоретический выход огарка по уравнению I
2-160
“т= 4-120 =0’67
при обжиге до Fe3O4 ат = 0,64
Так как сера в огарке находится в виде FeS, следует принимать в зна-
менателе 160—0,4 Csor. Тогда выход огарка из сухой руды (колчедана)
160— С5Ф
а== 160— 0,4Csor
где C*s— фактическое содержание серы в колчедане, %; Csor— содержание
серы в огарке, %.
Потери серы с огарком (в %):
аСеог-100
П =
с5ф
Например, при Сфз = 40% и Csor=l%
160 — 40 0,752-100 , ооп/
а~ 160-0,4-1 — °-752 и п~ 40 — 1,88/0
При обжиге колчедана до Fe3O4 выход огарка:
148 —Cs4>
148—0,5Cs'
57
Степень выгорания серы из сульфидного сырья
/ CSor \
₽= 10011 —
где CMs — содержание серы в материале.
11.1.4. Обжиг колчедана при использовании
циркулирующего огарка [3, 39, 43—48]
При обжиге колчедана в атмосфере воздуха или кис-
лорода по суммарному уравнению
FeS2 4-2,75O2= 0,5Fe2O34-2SO2 —842,90 кДж (—207,17 ккал)
27,3% кислорода соединяется с железом и переходит в ога-
рок, а газ при обжиге с применением воздуха разбавляется
азотом. При этом максимальная (теоретическая) концентрация
диоксида серы в газе может быть не выше 15,9%.
Если этот процесс технологически разделить на две стадии,
можно получить концентрированный газ (теоретически до 100%
SO2) без затрат кислорода и огарок в виде магнетита (Fe3O4),
воспользовавшись оксидом железа огарка как переносчиком
кислорода.
Суммарное уравнение реакции I стадии:
FeS2-j- 16Fe2O3 = HFe3O4 + 2SO2 —436,09 кДж (—104,08 ккал)
Во II стадии производится окисление магнетита кислоро-
дом воздуха до оксида железа:
1 lFe3O4 + 2,75О2 = 16.5Fe2O3 ф- 1278,99 кДж (4-305,25 ккал)
Оксид железа возвращается на I стадию.
Термодинамические расчеты (использовались термодинами-
ческие данные источника [11]) показали, что реакция окисле-
ния FeS2 оксидом железа становится термодинамически веро-
ятной при температурах выше 350 °C, причем наибольший эн-
дотермический эффект наблюдается в интервале температур
450—600 °C.
Суммарная энтальпия реакций в двух стадиях равна энтальпии процесса
окисления пирита кислородом. Изменение энтальпии процесса 1-й стадии
можно рассчитывать по следующему термодинамическому уравнению:
53,84-106
ДЯТ = 67 413 4- 75,367 — 0,04472 4-----
изменение изобарного потенциала по уравнению
AZ = 67 413 ф- 3527 — 173,337- 1g 7 ф- 0,04472 ф- 26,9-105
Значения \H = f(t) и для реакции окисления пи-
рита оксидом железа приведены в табл. 9.
Расчет констант равновесия по уравнению
AZ = —19,17-lgKa
дает порядок величин, свидетельствующий о том, что переход серы пирита
в SO2 может быть практически полным.
58
Таблица 9. Значения = и \Z = f(t) реакции окисления
пирита оксидом железа
i, “С - АЧ AZ
ккал/моль i . 1 КДЖ,'МО.1Ь । кка.ч/моль । кДж'МОЛЬ
25 104,08 436,09 48,5 203,22
350 105,93 443,84 1,5 6,28
400 106,20 444,98 —6,5 —27,24
450 106,35 445,60 — 14,5 —60,75
500 107,34 449,75 —21,0 —88,00
600 105,83 443,43 —34,0 — 142,46
700 104,62 438,56 —50,5 —211,60
750 103,72 434,58 —60,0 —251,40
800 102,63 430,02 —68,5 —287,02
900 99,86 418,41 —81,0 —339,40
1000 96,27 403,37 —100,0 —419,00
Изменение энтальпии процесса II стадии подсчитывается по уравнению
Д /7Т = —312 590 — 53,68Г + 0,03872 + 59,45 • 105/Т
изменение изобарного потенциала по уравнению
AZ = —312 590 — 227Т + 123,6257 lg Т — 0,038Г2 — 29,7 • 105/7’
Наличие эндотермического эффекта при взаимодействии
FeS2 с Fe2O3 было установлено также методом термографиче-
ского анализа.
На рпс. 12 представлена термограмма процесса взаимодействия Fe2O3 и
FeS2, полученная при нагревании шихты в виде смеси реагентов при стехио-
метрическом их соотношении. Нагрев проводили в кварцевом тигле при ско-
рости 4 град/мин с продувкой аргоном. Из термограммы следует, что в ин-
тервале температур 500—700 °C наблюдается последовательное появление
двух эндотермических эффектов. Первый, очевидно, вызван термической дис-
социацией пирита. Продукты диссоциации (FeSn и S2 при дальнейшем на-
гревании шихты до 600 °C взаимодействуют с кислородом оксида железа, что
характеризуется наличием второго ярко выраженного эндотермического эф-
фекта, связанного с распадом молекул Fe2O3.
Кинетику взаимодей-
ствия пирита с оксидом
железа изучали в лабо-
раторном реакторе в ус-
ловиях кипящего слоя
(700—900 °C) для флота-
ционного колчедана круп-
ностью 0,2—0,1 мм и
огарка такого же грану-
лометрического состава.
РИС. 12. Термограмма вза-
имодействия FeSO2 и РегО3:
1 кривая тепловых потерь;
2 кривая Изменения темпера-
туры прн нагреве.
Время,мин
59
РИС. 13. Зависимость скорости реакции
окисления пирита от температуры:
1—3 — окисление оксидом железа в атмосфере
азота при степени десульфуризации соответствен-
но 95, 90 и 85%; 4 — окисление кислородом воз-
духа при степени десульфуризации 95%; 5— окис-
ление оксидом железа в атмосфере диоксида се-
ры при степени, десульфуризации 95%.
Экспериментальные данные представ-
лены на графике рис. 13, иа котором по-
казана зависимость скорости реакции от
температуры. Для сравнения на этом же
графике приводятся результаты опытов по
окислению пирита кислородом воздуха, по-
лученные в аналогичных гидродинамиче-
ских условиях. Присутствие диоксида серы
в зоне реакции значительно ускоряет процесс, скорость реакции при этом
практически равна скорости окисления пирита кислородом воздуха.
Скорость реакции окисления пирида оксидом железа в значительной сте-
пени зависит от температуры. Процесс протекает в кинетической области —
среднее значение энергии активации составляет 87,78 кДж/моль
(20 950 кал/моль). При степени десульфуризации 95% наблюдается уменьше-
ние зависимости скорости реакции от температуры, по-видимому, за счет
влияния диффузионного сопротивления и перехода процесса в диффузионно-
кинетическую область. FeS и сера окисляются оксидом железа с меньшей
скоростью, чем FeS2.
Образование H2S при 800—1000 °C в условиях дутья, на-
сыщенного водяным паром, не наблюдалось. По-видимому,
равновесие в системе
2H2S -р О2 ч—> 2Н2О + 1,5S2
сдвигается вправо.
При уменьшении содержания Fe2O3 до соотношения Fe2O3:
:FeS2 = 5 с расчетом восстановления Fe2O3 до FeO выход SO2
соответствует лишь степени перехода Fe2O3 в Fe3O4 и даль-
нейшего раскисления Fe3O4 не происходит, т. е. процесс про-
ходит только до устойчивой формы оксидов железа, наличие
которой подтверждается рядом исследователей.
И. В. Стрежнев, исследовав термодинамически систему FeS, SO2, Fe3O4,
О2 и S2, установил, что в области температур 800—1180 °C устойчивой фор-
мой из оксидов железа является Fe3O4, a FeO становится устойчивой лишь,
начиная с температуры выше 1100 °C.
В работах Г. И. Чуфарова и ряде других работ отмечается, что FeO ие
накопляется в присутствии Fe2O3, так как немедленно проходит восстановле-
ние:
Fe2O3 + FeO = Fe3O4
Несмотря на то, что существование FeO в продуктах реакции восстанов-
ления Fe2O3 при температурах выше 570 °C было подтверждено рентгеногра-
фически, очевидно, что вюстит (твердый раствор FeO и Fe3O4) образуется в
таком состоянии, в котором скорость его превращения в железо превышает
скорость восстановления других оксидов. Полученное железо вступает во
взаимодействие с Fe3O4, образуя FeO, и далее реагирует с Fe2O3 до образо-
вания в конечном итоге Fe3O4.
60
Процесс взаимодействия сульфидов железа с оксидом же-
леза проходит через газовую фазу. Рядом исследователей по-
казано значительное многообразие кажущихся твердофазных
процессов, в действительности протекающих через взаимодей-
ствие твердого вещества с газом или жидкостью или через-
газ — газ. В данном случае участие жидкой фазы исключено,
поскольку точка плавления Fe2O3 находится значительно вы-
ше интервала температур 600—900 °C (плавление огарка фло-
тационного колчедана происходит при 1250—1300 °C).
Отнести процесс к чисто твердофазному нельзя из-за его практически
очень высокой скорости. Поверхность контакта между твердыми веществами
при размере зерен 1—10-3 см составляет 10-4—10-с см2 на 1 см3 реакционной
массы [39], значения коэффициентов диффузии твердого в твердом находятся в
пределах 10-4—10 8 см2/с, а плотность вещества и движущая сила процесса
измеряются величинами порядка единиц, отсюда степень превращения твер-
дых веществ за 1 ч может составить лишь от 1-10—8 до 3—5%.
Несмотря на то что при 600—800 °C давление диссоциации 6Fe2O34=t
==4Fe2O4---O2 составляет от 215,4-10-12 до 172,9-10—4 Па (1,62-10-12—
1,3-10—4 мм рт. ст.), по-видимому, при наличии потребителя атомарного
кислорода диссоциация Fe2O3 проходит как бы в глубоком вакууме — с очень
большой скоростью. И создаются условия для гетерогенного взаимодействия
газообразных атомарного кислорода и паров серы в процессе мономолекуляр-
ного порядка [39].
Присутствие в газовой фазе SO2 ускоряет взаимодействие пирита с огар-
ком вследствие того, что SO2 реагирует с FeS с выделением серы:
SO2 реагирует с FeS с выделением серы:
3FeS + 2SO2 = Fe3O4 + 5S
с Ре20з, образуя SO2. Избыток Fe2O3 не влияет на-
ее с FeS2. Это полностью соответствует работам
показавших, что восстановление
которая далее реагирует
процесс взаимодействия
Г. И. Чуфарова и других исследователей,
Fe2O3 до Fe3O4 идет через образование FeO. Присутствие мерастабильных
соединений FeO приводит к тому, что на некотором участке кривой восстанов-
ления обнаруживается дополнительное (избыточное против стехиометрических
соотношений) количество кислорода, которое и имеет решающее значение в
процессе окисления FeS2. Окисление Fe3O4 в воздухе при температурах выше-
400—450 °C проходит за 0,7—0,8 с.
При окислении углистого колчедана огарком углерод выгорает медлен-
нее, чем сера. В статических условиях (применительно к шахтной печи) в
газовой фазе получается SO2 и СО2, в кипящем слое в газовой фазе содер-
жится значительное количество СО, что, по-видимому, объясняется смеще-
нием равновесия в системе, в результате чего нарушается необходимый
вод кислорода для образования СО;
Согласно уравнению реакции окисления FeS2 оксидом же-
леза теоретически
сида железа на 1
CsK (в %) на 1 т
под-
2-
ок-
в системе должно циркулировать 21,33 т
т FeS2. При содержании серы в колчедане-
FeS2 должно циркулировать огарка
32 (53,4—CSK)
21,33+ ——-------—
CSK
отсюда для стандартного 45%-ного колчедана эта величина
составит 28 т/т. Результаты лабораторных исследований были
проверены в полузаводском масштабе.
На полузаводской установке были обеспечены циркуляция огарка между
реактором и окислителем и циркуляция диоксида серы для создания кипя-
щего слоя в реакторе.
6Г
Циркуляция огарка протекала следующим образом: огарок, отбираемый
через сливную трубу с верхнего уровня кипящего слоя реактора, эжектиро-
вали воздухом и по внешней пневмотранспортной трубе передавали на верх-
ний уровень кипящего слоя окислителя, далее из нижней части окислителя
огарок самотеком через переточную трубу поступал в нижнюю часть кипя-
щего слоя реактора. Циркулирующий диоксид серы из реактора через систе-
му пылеочистки компрессором подавали обратно в реактор. Колчедан та-
рельчатым питателем подавался в середину кипящего слоя реактора с под-
дувкой диоксидом серы через сопло.
Опыты проводили при скорости дутья в аппаратах около 0,15 м/с (в ра-
бочих условиях), давлении в реакторе 3,22—3,99 кПа (25—30 мм рт. ст.) и
в окислителе 266—565 Па (2—5 мм рт. ст.), средних температурах в аппа-
ратах 680—720 °C, средней температуре в транспортной линии 500 °C, скоро-
сти газового потока около 15 м/с, концентрации огарковоздушной смеси
25 кг/м3 и пребывании ее в транспортной трубе в течение 0,7—0,8 с.
Концентрация газа достигала 85—90%. Газовыделения из окислительной
зоны практически не было. В окислитель поступал практически обессеренный
огарок, а захвата диоксида серы горячим огарком не происходило, так как
в существующих рабочих условиях огарок подобен жидкости и не имеет
пустот для заполнения газом. Средние показатели работы установки: содер-
жание серы в огарке из реактора — менее 0,1%, из окислителя — отсутствие
или 0,03%; степень использования серы — 98%, интенсивность реактора — 3 т
45%-ного колчедана с м2 в сутки [43].
Полученные на этой установке данные были использованы
для проектирования крупной промышленной установки на су-
точную производительность 60 т колчедана. В основу аппара-
турного оформления был положен известный принцип «Орто-
Флоу»: реактор и регенератор, размещенные в вертикальной
колонне, имеют внутреннюю пневмотранспортную трубу и пере-
токи.
Строительство установки было начато на одном из предприятий, но было
остановлено в связи с начавшимся среди части работников сернокислотной
промышленности увлечением идеей внедрить в производство серной кислоты
технический кислород, хотя технико-экономические расчеты Гипрохима сви-
детельствовали в пользу огаркового метода получения концентрированного
газа по сравнению с кислородным.
Расчетами Гипрохима и НИУИфа показано, что применение
концентрированного газа, который может быть получен при
окислении колчедана огарком в производстве контактной сер-
ной кислоты, снизит ее себестоимость на 30—40%; при этом
чем выше стоимость электроэнергии, тем больше экономиче-
ский эффект от применения такого газа. Капиталовложения
-снизятся на 38%.
По предварительным расчетам, внедрение описанного метода с дальней-
шим окислением полученного газа кислородом воздуха в производстве ба-
шенной серной кислоты даст следующий эффект: интенсивность башенного
процесса повысится до 1000 кг/(м3-сут), расход азотной кислоты снизится
до 3 кг/т кислоты, значительно уменьшится расход воды и поверхность холо-
дильников сократится примерно на 25%, интенсивность орошения башен при
этом не превысит 20 м3/ч на 1 т продукции.
Возможны различные варианты технологии осуществления
метода обжига с использованием кислорода огарка с получе-
нием газа различной концентрации: с применением пневмо-
<62
транспорта (на обеспечение которого требуются давление око-
ло 0,15 МПа и удельный расход энергии около 10 кВт-ч/т
колчедана вместо 160 кВт-ч/т в случае использования кислоро-
да) и без пневмотранспорта — с передачей огарка через запеч-
ные циклоны [45] и др.
Такой метод передачи огарка может упростить аппаратурное оформление
его транспортирования и при незначительной реконструкции возможен пере-
вод на получение концентрированного газа существующих отделений обжига
колчедана. При строительстве новых заводов следует применять пневмо-
транспортирование.
Применительно к условиям существующих производств
установленные печи кипящего слоя разделяют функционально
на две группы: реакторы и окислители — в соотношении 1:1
или 1:2. Печи оборудуют внешними футерованными циклона-
ми. Огарок циркулирует между печами, окисляясь до гемати-
та в окислителе и восстанавливаясь до магнетита в реакторе.
Весь кислород, подаваемый под решетку окислителя с возду-
хом, передается в реактор огарком по схеме, изображенной на
рис. 14. При наличии циклонов возврата огарка реконструкция
для получения концентрированного газа сводится в основном к
сооружению двух дополнительных футерованных газоходов или
течек для транспортирования огарка между печами. Расчеты
теплового баланса показывают, что совместная работа двух
печей возможна без изменения площади охлаждающих эле-
ментов в печи.
Из расчетов следует, что необходимое для окисления коли-
чество огарка подается в реактор при кратности циркуляции
22—23, что вполне достижимо в печах типа КСЦВ. При этих
пределах циркуляции концентрация SO2 в обжиговых газах
составит 30—45% (об.). Производительность блока может воз-
расти до 1190 т колчедана в сутки или на каждую печь — до
595 т/ сут.
В зависимости от отношения масс огарка и дутьевого возду-
ха изменяется концентрация SO2 в обжиговом газе:
Отношение огарок : воздух, кг/кг
Содержание SO2 в газе, %
при сжигании серы
при сжигании колчедана
10 20 40 80
38,3 49.7 63.2 76,1
31,8 42,5 56,3 70,5
Для получения более концентрированного газа (в пределах
90—100% SO2) и одновременно огарка в виде магнетита для
вновь строящихся производств целесообразно строительство
обжигового агрегата по типу установки для наработки магнит-
ного огарка, работавшей в Воскресенском филиале НИУИФ
[46]. Схема установки представлена на рис. 15.
Колчедан тарельчатым питателем подают в реактор, куда из циклона
поступает огарок. Образовавшийся диоксид серы выводят в коллектор через
газоходы, расположенные по высоте реактора, и направляют потребителю.
Отработанный огарок (магнетит) выводят из нижней части реактора. Часть
огарка направляют в трубопровод готовой продукции, а остальное количест-
во перетекает в окислитель.
63:
ГРИС. 14. Схема блокировки печей
при окислении колчедана огарком
(часть воздуха подается в реактор
для создания кипящего слоя).
Огарок
(Fe2O3)
РИС. 15. Схема опытной установки:
.Г — питатель; 2— реактор с пересыпными полками; 3 — окислитель с КС; 4 — циклон.
Реактор представляет собой гравитационный смеситель, футерованный
шамотом. Внутри его на кирпичных выступах последовательно расположены
конусы, ориентированные вершинами попеременно вверх (центральный) и
вниз (периферийный), на которых колчедан и огарок, ссыпаясь вниз, переме-
шиваются. (Следует отметить, что в процессе окисления огарком не наблю-
дается образования спеков ввиду сильного разбавления серы огарком; со-
держание серы в шихте не превышает 1,5%.) Число конусов рассчитано та-
ким образом, чтобы время контакта компонентов было достаточным для
полного выгорания серы из колчедана и равнялось примерно 7 с.
Окислитель представляет собой печь КС, которая работает при высоких
скоростях газа, что позволяет использовать ее и как пиевмотранспортное
устройство для подачи огарка в циклон 4. Для утилизации тепла в кипящем
слое установлены холодильные элементы. Из циклона огарок через затвор
самотеком поступает в реактор. Пылегазовый поток из окислителя после цик-
лона направляют в санитарный скруббер.
В табл. 10, 11 приводятся результаты расчетов для варианта вывода
продукционного огарка из окислителя.
Процесс окисления пирита огарком или — что то же самое — восстанов-
ления оксида железа пиритом представляет значительный интерес для полу-
чения пиритного огарка, пригодного для использования в черной металлур-
гии с предварительным извлечением цветных металлов. Выход огарка состав-
ляет около 0,7 т/т пирита.
В настоящее время огарок применяют в производстве цемента, дорожном
•строительстве и сельском хозяйстве. При этом исключается использование
его полезных компонентов: железа, цветных и благородных металлов и др.
«64
Таблица 10. Материальный баланс реактора и окислителя
(в т на 1 т 45%-ного колчедана)
CiaiDH иЯЛаНСа | Реактор Окислитель
j приход | расход приход | РАСХОД
Колчедан сухой, всего 1 ,000
порода 0,550
Влага колчедана, 5% 0,052 0,052
Диоксид серы 0,900
Огарок, всего 25,384 25,484 25,484 25,934
Fe2O3 18,000
Fe3O4 17,550
порода 5,076 5,626
избыток (ак=1,1) 2,308 2,308
Воздух, (ав=1,1) 1,930
Азот 1,480
Итого 26,436 26,436 27,607 27,607
В целях комплексного использования сырья и сокращения отходов наиболее
целесообразно перерабатывать пиритные огарки с получением чугуна. Содер-
жание железа в огарках (в оксидной форме) почти в 1,5 раза выше, чем
в железных рудах. Основные трудности их использования в качестве железо-
содержащего сырья заключаются в относительно низком содержании железа
(в сравнении с обогащенными железными рудами)—55%, присутствии
мышьяка, серы, цинка, свинца и сурьмы.
Повышение содержания железа в пиритном огарке может
быть достигнуто путем его обогащения магнитной сепарацией
с использованием типовых магнитных сепараторов. Осуществ-
ление этого способа возможно при условии, что огарок будет в
виде магнетита [47]. Технология получения огарка в виде маг-
нитной фракции при окислении пирита оксидом железа прове-
рялась на промышленной установке (рис. 15). Образующийся
магнетит выгружали из нижней части реактора. При средней
температуре 700—800 °C и времени пребывания реагентов в
Таблица 11. Тепловой баланс реактора и окислителя (температура
в реакторе 700 °C, в окислителе 825 °C)
Статьи баланса Реактор Окислитель
приход расход приход | расход
С колчеданом 2 735
С огарком 5 419 035 4 459 700 4 459 700 5 562 843
Реакция окисления 735 300 2 193 750
Испарение влаги 47 580
С газом 124 740 357 635
С воздухом 10 488
Потери 54 450 66 640
Утилизируемое тепло 676 820
Итого, ккал 5 421 770 5 421 770 6 663 938 6 663 938
Итого, мДж 22 717 22 717 27 922 27 922
5—584
65
РИС. 16. Зависимость обогати-
мости огарка от напряженно-
сти магнитного поля (в Э):
V — выход магнитной фракции; 0 —
содержание железа в магнитной
фракции; 8 —извлечение железа;
v — содержание железа в хвостах.
зоне реакции до 5 с обес-
печивалась степень маг-
нетизации более 95%.
При этом содержание же-
леза достигалось 57—
61% при концентрации серы менее 1%. Для обогащения огарка
не требовался его дополнительный размол.
Данные по обогатимости огарка были получены на установ-
ках Механобрчермета. Степень восстановления до магнетита
оказались в нем более высокой (95%), чем в обогащенной руде
Криворожского ЦГОКа (80—85%), содержание железа по-
вышалось до 65%. Результаты обогащения пиритного огарка,
полученного при окислении им пирита, приведены на рис. 16.
Результаты исследований показали вполне удовлетвори-
тельную обогатимость на сепараторах с низкой напряженностью
магнитного поля. В практике могут быть использованы широ-
ко применяемые в черной металлургии магнитные сепараторы
с напряженностью до 1200—1600 э. Технико-экономические
расчеты подтвердили экономическую эффективность данного
метода переработки пиритных огарков [47, 48].
После извлечения из огарка цветных металлов и других
ценных компонентов (и очистки от мышьяка, если эта очистка
потребуется) он должен быть использован в металлургии.
В Испании, Англии, Франции, ФРГ в разные годы публи-
ковались сообщения об исследованиях процесса окисления
колчедана огарком [39], за последнее время появилась публи-
кация работы румынских исследователей, которые начали изу-
чение этого процесса [74].
11.1.5. Основы гидродинамики кипящего слоя
колчеданного огарка, интенсивность обжига
Принцип кипящего слоя (КС) давно используется для
воздушного обогащения полезных ископаемых, перемешивания
тонкоизмельченных материалов и их транспортирования по
желобам и т. д. В условиях высоких температур этот метод
стал применяться в 20-е годы для газификации угольной мело-
чи в газогенераторах Винклера. В самом широком масштабе
он применен для каталитического крекинга нефти и в органи-
ческом синтезе. При обжиге серосодержащего сырья (колче-
дана) его начали применять в конце 40-х годов в Германии,
США и Советском Союзе.
66
Кипящим или псевдоожиженным называют такое состояние слоя сыпу-
чего зернистого твердого материала, когда при продувании через него газо-
вого потока он становится подобен кипящей жидкости. Если через слой сы-
пучего материала начать продувать газ (воздух), то при малых скоростях
газа происходит его фильтрация через слой и высота слоя на поддерживаю-
щей газораспределительной решетке практически остается неизменной. Когда
скорость газа достигнет некоторой критической величины-—начала псевдо-
ожижения — гидравлическое сопротивление слоя становится равным его ве-
су, слой приобретает текучесть. При дальнейшем увеличении скорости газо-
вого потока высота слоя начинает возрастать и при некоторой новой (вто-
рой) критической величине скорости, твердые частицы начинают уноситься
газовым потоком и переходят в режим пневмотранспорта.
При расчетах процессов в кипящем слое [31] пользуются условной ско-
ростью— w', отнесенной к сечению аппарата, при этой скорости наступает
псевдоожижение, ее называют первой критической скоростью или скоростью
предела устойчивости аы. у; скорость начала уноса частиц из слоя w" назы-
вается второй критической скоростью или скоростью витания. Фактическая,
или рабочая, условная скорость газа w больше w' и меньше w". Отношение
N—wfw' называется числом псевдоожижения.
Для промышленных печей при обжиге флотационного кол-
чедана число псевдоожижения N равно примерно 10—14, при
обжиге рядового колчедана со средневзвешенным диаметром
частиц в слое d«3 мм, 1,3—1,8 [31].
Важным фактором, влияющим на общую структуру слоя, является от-
ношение первоначальной высоты слоя Но к диаметру аппарата. При неболь-
шой величине 7/о/Оап и малой степени расширения в слое образуются ло-
кальные каналы, в которые устремляется газовый поток. При этом не все
частицы в слое оказываются во взвешенном состоянии. На это указывает
меньшее сопротивление слоя по сравнению с расчетным. При значительных
величинах /А,/Вяп возникает явление поршневого эффекта. Как показали
проведенные исследования [49], при Но = О,5 Dan и К=1,75—2,0 кипящий
слой однороден, при К>2,0 однородность слоя нарушается, так же она на-
рушается с увеличением Но. При //o=O,75 Dan однородная структура сохра-
няется только при невысоких степенях расширения (/(=1,25). Увеличение до
7/0>1,0 приводит к тому, что в слое наблюдаются газовые прослойки, слой
становится полностью неоднородным, возникает поршневой эффект.
Однородность кипящего слоя зависит от Но, К и H0!Dan и от грануло-
метрического состава частиц. Она увеличивается с уменьшением диаметра
частиц, так как мелкодисперсные частицы образуют более «вязкий» слой, чем
крупные, но при очень мелких частицах наблюдается неоднородность слоя,
потому что мелкие частицы склонны к слипанию. В кипящем слое целесооб-
разно иметь широкую фракцию ступенчатого состава. Слой кипит при соот-
ветствующих скоростях дутья равномерно, крупные фракции как бы плава-
ют в мелких и при этом меньше истираются, мелкие частицы взаимосвязан-
ные с крупными, в меньшей степени покидают слой. Таким образом, для ши-
рокой фракции характерен меньший пылеуиос и малые скорости дутья, а
следовательно и меньшие энергетические затраты [39].
Полидисперсность слоя характеризуется [50] отношением
начальной скорости псевдоожижения к конечной скорости, ког-
да все частицы переходят в псевдоожиженное состояние. Это
отношение называют числом полидисперсности л. Плотность
слоя (масса огарка в объеме слоя) в условиях устойчивого
кипящего слоя 0,93—1,0 т/м3. Основные характеристики кипя-
щего слоя из частиц огарка размером 0—1 мм при 800 СС при-
ведены в табл. 12.
5* 67
Таблица 12. Основные характеристики кипящего слоя из частиц
огарка размером 0—1 мм при 800 °C
Скорость газового потока, м/с Минималь- ный диаметр частиц, осев- ших в слое ^min* мм Максималь- ный диаметр «закипев- ших» ча- стиц <imax, мм dmin Число псевдоожи- жения частиц Число поли- дисперсно- сти кипящего слоя 1"тах Л .. I ^min
dmax мииималь- ных Nvv.n максималь- ных Л’тах
о,1 0,100 0,575 0,175 30
0,2 0,150 0,8 0,188 30 — —
0,3 0,175 1,0 0,175 30 1,0 0,034
0,4 0,210 1,0 0,21 30 1,3 0,043
0,5 0,235 1,0 0,235 30 1,6 0,055
0,6 0,255 1,0 0,255 30 1,55 0,065
0,7 0,275 1,0 0,275 30 2,25 0,075
0,8 0,300 1,0 0,300 30 2,6 0,088
0,9 0,320 1,0 0,320 29 2,9 0,100
1,0 0,350 1,0 0,350 27 3,3 0,121
Скорость дутья, соответствующая началу псевдоожиже-
ния— пределу устойчивости (п. у.) слоя, может быть опреде-
лена из уравнения (31):
vRen.y
Шп-у = d4
Для ламинарного режима
Re'= 0,0091ф'Аг (при Re < 35)
Для турбулентного режима
Re' = 0,367 (ф'Аг)»,37 (при 70 < Rc 7000)
е3о w'd
где ф = ц______е ; фф — коэффициент формы частиц; Re = — —критерий
gds 7тв—Тг
Рейнольдса; Аг= —-— — критерий Архимеда; d — диаметр частиц, м;
v уг
v — кинетическая вязкость газа, м3/с. Диаметр частиц определяют
d = X(d} — xxdx + •' • 4* xndn
где Xt — массовая доля частиц узкой фракции с диаметром di; ф— фактор
формы — отношение диаметра частиц шаровой формы к расчетному диаметру
частиц произвольной формы того же объема; ф — коэффициент формы — от-
ношение поверхности частиц произвольной формы к поверхности частиц ша-
ровой формы (фф=1/ф).
Для частиц колчедана и огарка характерны следующие зна-
чения важных для процессов в псевдоожиженном слое вели-
чин:
Материал d, мм ф <₽
Флотационный колчедан . . . — 0,54-0,28 0,336 8,8
Огарок . . -0,284-0,071 0,185 23,5
— 3,04-0,5 0,151 44,0
Скорость витания (вторая критическая скорость) определя-
ется из уравнения равновесия сил, приложенных к твердой ча-
68
стице, взвешенной в восходящем потоке газа, которое в крите-
риальном выражении имеет вид
шбит = vReB1II/d4
Re’ = 0,056’ф’Аг (при Re 2)
Re" = 0,152 (ф"Аг)°>175 (при 2 < Re 500)
Для частиц огарка флотационного колчедана различных
размеров d значения w' и w" приведены ниже (в расчетах
принято ут = 3600 кг/м3, ун=И50 кг/м3, /кс = 800°С, фф = 24 для
d=0,1—2 мм и ф = 44 для г/=2,0, уг= 1,43 кгс/м3):
d мм . . . . 0,1 0,2 0,3 0,5 0,8 1,0 1,2 1,5 2,0'
ш' м/с .......... 0,003 0,012 0,027 0,076 0,194 0,305 0,436 0,678 1,21
w" м/с .... 0,093 0,375 0,837 1,5 2,52 3,35 4,05 5,25 7,35
Скорости, соответствующие пределу устойчивости и витания
частиц, снижаются при повышении температуры в связи с из-
менением кинематической вязкости, плотности и критерия Архи-
меда. Например, при повышении температуры от 0 до 800 °C
коэффициент кинематической вязкости возрастает в 10 раз,
плотность снижается в 4 раза, а критерий Архимеда с этим
снижается в 25 раз [31].
Скорость газового потока в кипящем слое, являющаяся од-
ной из основных гидродинамических характеристик слоя, оп-
ределяет и количество обжигаемого колчедана, т. е. интенсив-
ность обжига.
Как показала практика [31], для существования кипящего
слоя в колчедане должно находиться 5—10% крупных частиц,
которые при данном гидродинамическом режиме не выносятся
из слоя. Минимальный диаметр частиц, составляющих слой,
определяет максимально возможную линейную скорость газов
и при заданной концентрации сернистого газа максимальную
подовую интенсивность печи. Диаметр таких частиц называют
определяющим диаметром частиц колчедана. Масса мелких
фракций колчедана, выносимых в надслойное пространство при
соответствующем гидродинамическом режиме, при сгорании в
течение требуемого времени (в соответствии с кинетикой обжи-
га, высокой степенью извлечения серы из колчедана и опти-
мальным размером печи) должно обеспечить температуру на
выходе из печи не выше 900 °C.
Для суточной производительности Всут печи при обжиге
45%-ного колчедана на площади пода печи F можно написать
следующую зависимость:
45* 1000Р17вгВСуТ 1 273 /сл г...
24CSK ‘ 273 = ЗбООшГ
откуда подовая интенсивность в т/(м2-сут)
,, Всут 525-(Дкш
под- F = ₽РВ.Г(273 + /СЛ)
69
объемная интенсивность [в м3/(м2-сут)]
/?сут 525 •CSK
U°5 = V ~ fWE.r (273 + /ср) т
где V—объем печи, м3; /Ср — средняя температура в надслойном простран-
стве; т — время пребывания газов в печи, с.
б^под 273 /ср
Uo6 = F = 273 + ?сл
Пример. При В=450 т/сут, гСл = 750°С, средней температуре в печи
/ср = 825°С, аа = 0,95 м/с, С5к = 4О°/о, (3 = 0,98, т = 8 с, Cso„=14,5% получим
VB.r = 2 м3; {/об = 1,22 т/(м3-сут); С',ГОд = Ю т/(м2-сут)
{/печи = 5сут/{/0б = 450/1,22 = 370 м3
Площадь пода печи
F = Всут/^под = 45 м2
Тепловое напряжение объема печи
Qo6 = 6- 104-{/эб-6-104-1,22 = 73 0Э0 ккал/(м3-ч) или 350 870 кДж/(м3-ч)
II. 1.6. Теплообмен в печах КС
При обжиге серосодержащего сырья в кипящем слое
выделяется значительное количество избыточного тепла, кото-
рое снимается в теплообменных элементах, расположенных в
слое. Несмотря на то, что обжиг колчедана ведут при низких
скоростях газового потока, не превышающих даже для рядо-
вого колчедана 2 м/с, коэффициенты теплообмена для охлаж-
дающих элементов [31] имеют высокие значения: 628,5—
1257 кДж/(м2-ч-град) [150—300 ккал/(м2-ч-град)].
Высокие значения коэффициентов теплообмена объясняются
[50, 51] тем, что теплообмен в данном случае определяется не
толщиной ламинарного слоя газового потока, а толщиной су-
ществующих между поверхностями теплообмена и движущими-
ся частицами тонких ламинарных газовых пленок, средняя тол-
щина которых в основном определяется интенсивностью дви-
жения и концентрацией частиц у поверхности. Уменьшение
толщины пленок (6П) в результате воздействия движущихся
частиц приводит к увеличению коэффициента теплоотдачи со-
гласно уравнению
а = Х/бп
где X — коэффициент теплопроводности газового потока.
Коэффициент теплоотдачи от слоя к поверхности определя-
ется в основном скоростью газового потока, порозностью слоя
и физическими характеристиками ожижаемого материала. На
основе данных промышленных экспериментов коэффициент
теплоотдачи от кипящего слоя огарка серного колчедана к
охлаждающим поверхностям в кипящем слое при псевдоожи-
жении воздухом или обжиговыми газами, содержащими 79—
70
85% азота, может быть рассчитан на основе следующей зави-
симости:
„ - [ (1 — ш I0-4 А,
eKcV j
Для огарка флотационного колчедана при /сл = 750°С а =
= 275 ккал/(м2-ч-град) [.319,8 Вт/(м2-град)].
Внутренний коэффициент теплоотдачи аг от поверхности к
охлаждающему агенту подсчитывается по следующим форму-
лам:
для некипящей воды и пара
для кипящей воды
а2 = 11 б.бР0,2^.7 + 0,5• 10-4
где Рг— критерий Прандтля, который отнесен к средней температуре пото-
ка, так же как и все остальные параметры; Р — давление воды; q — тепло-
вой поток, которым предварительно в расчетах задаются с последующим
уточнением [в ккал/(м2-ч)]
<7= Л'(/сл —/ВСР)
Для утилизации тепла в кипящем слое огарка устанавли-
вают охлаждающие элементы. Наибольшее распространение
получили элементы с естественной циркуляцией V-образного
типа, изогнутые в двух плоскостях. Максимальная величина
тепловоспринимающей поверхности fmax, которая может быть
размещена в слое, для этих элементов составляет 3 м2/м3 слоя
[31].
По величине fmax можно определить максимально возмож-
ную величину Fmax тепловоспринимающей поверхности, прихо-
дящуюся на 1 м2 пода печи при заданной высоте Но спокойно-
го слоя (в м2/м2):
Т'тах 7 Т/р/max
или по тепловому напряжению пода по утилизируемому теплу
^сл и удельной тепловой поверхности охлаждающих элементов
VnoB определить Но с помощью табл. 13 по следующим уравне-
ниям:
Чел ~ 0,0417<2сл(/ПОд
Чел = HofтахЧпов
Пример. Определить необходимую высоту слоя в печи КС при обжиге
флотационного колчедана на воздушном дутье с интенсивностью
10 т/(м2-сут).
Тепловое напряжение пода
Чел = 0,0417<2слС/Под = 0,0417-475 000-10 =200 000 ккал/(м2-ч),
или
838 000 кДж/(м2-ч)
71
Таблица 13. Значения необходимых величин поверхности
охлаждающих элементов F на 1 м2 пода
Показатели Вид колчедана
флотационный | рядовой | углистый
Концентрация кислорода в дутье, % 21 42 63 21 21
Интенсивность б/ПОд, т/(м3-сут) Количество тепла, утилизируемого в слое Qcn на 1 т колчедана, 10 20 30 20 20
Мкал 475 875 970 475 805
МДж Тепловое напряжение по утилизируе- мому теплу <7сЛ на 1 м2 пода в час 1990 3666 4064 1900 3373
Мкал 200 730 1210 400 675
МДж Удельный тепловой поток* к 1 м2 поверхности охлаждающих элемен- тов 9поа в 1 Ч 838 3058 5070 1676 2828
Мкал 150 150 150 100 100
МДж 628 628 628 419 419
Необходимая поверхность охлажде- ния элементов f иа 1 м2 пода, м2 1,33 4,85 8,10 4,0 6,75
* Коэффициент теплопередачи К. при обжиге флотационного колчедана
2/э ккал/(мЛч-град), или 319 Вт/(м2-град), для других колчеданов или 208,8 Вт/(м2-град). Температурный напор А/ во всех случаях 550 180 ккал/(м2-ч-град), °C.
необходимая высота слоя огарка
<7сл 200 000
На = /тах9под = 3-150 000 = °’45 м
Обычно высоту слоя огарка принимают в пределах 1,2—
1,3 м. При обжиге флотационного колчедана на дутье, обога-
щенном кислородом до 42% О2, требуется увеличить высоту
слоя до 1,6 м, а при концентрации кислорода до 63% следует
применить принудительную циркуляцию и холодильные эле-
менты другого типа или при элементах с естественной цирку-
ляцией снижать возможную интенсивность печи почти в два
раза, что приведет к увеличению ее габаритов.
При обжиге рядового колчедана установка в слое элемен-
тов с естественной циркуляцией приводит к необходимости
снижения подовой интенсивности примерно в 1,5 раза.
11.1.7. Условия охлаждения обжигового газа
При обжиге флотационного колчедана в печах с кипя-
щим слоем происходит частичное окисление диоксида серы в
триоксид вследствие каталитического действия мелкодисперс-
ной огарковой пыли в газе, что вызывает необходимость со-
блюдать определенные условия охлаждения обжигового газа
в котлах-утилизаторах.
С целью уменьшения образования SO3 и побочных реакций
сульфатизации огарка необходимо, помимо поддержания вы-
72
сокой концентрации SO2 и высокой температуры газа на вы-
ходе из печи (850—900 °C), быстрое охлаждение обжигового
газа до 450—400 °C, так как именно в диапазоне температур
300—400 °C протекают неблагоприятные реакции. Так, около
630 °C лежит максимум скорости реакции окисления SO2 в SO3
при каталитическом воздействии оксидов железа, а при тем-
пературе около 500 °C наблюдается наиболее интенсивная
сульфатизация оксидов железа [52, 53]. Быстрое охлаждение
газа способствует уменьшению этих явлений.
Как показали данные обследования печей КС с различными
котлами-утилизаторами, практически ничтожное содержание
SO3 в газе за котлом наблюдалось при времени охлаждения
газа в указанных интервалах температур, равном 0,3—0,5 с.
Это тот предел, к которому желательно стремиться при конст-
руировании котлов-утилизаторов. Увеличение содержания SO3
в газе ухудшает электростатическую очистку газа и транспор-
тирование огарковой пыли вследствие ее сульфатизации и по-
вышает потери серы.
Для избежания конденсации паров серной кислоты на по-
верхности труб котлов температуру металла следует поддер-
живать выше точки росы, что для оптимальной концентрации
SO2 (14—14,5%) и возможном при этом содержании SO3,
а также влаги в газе, соответствует температуре 200—220 °C.
Поэтому абсолютное давление пара должно быть не менее
2,5 МПа (25 ат), а с учетом использования пара для получения
электроэнергии — не менее 4,0 МПа (40 ат).
11.1.8. Технологическая схема и аппаратура
отделения обжига
Необходимость создания оптимальных условий обжига
флотационного серного колчедана в кипящем слое, охлажде-
ния обжигового газа и его очистки от пыли предопределяет
принципиальную аппаратурно-технологическую схему печного
отделения. Схема печного отделения, оборудованного печами
КС, работающими на флотационном колчедане, приведена на
рис. 17.
Системой транспортных механизмов колчедан из отделения подготовки
сырья подается непосредственно в бункеры пластинчатых питателей печного
отделения, откуда периодически поступает в бункер тарельчатых питателей.
Тарельчатые питатели с неподвижным спиральным ножом дозируют колче-
дан в печь КС. Воздух, необходимый для горения и создания кипящего слоя,
подают в печь воздуходувкой через дутьевую решетку в количестве, опреде-
ляемом производительностью печи. Необходимая температура обжига в ки-
пящем слое поддерживается установленными в нем тепловоспринимающими
элементами- испарительными и пароперегревательными, которые вместе с
котлом-утилизатором составляют единую систему теплоиспользования.
Обжиговые газы из печи поступают в котел-утилизатор, где охлаждают-
ся и частично освобождаются от наиболее крупных франций выносимого из
печи огарка. После котла-утилизатора обжиговые газы проходят циклоны
грубой очистки, где осаждается основное количество огарка, и поступают на
73
РИС. 17. Схема печного отделения при обжиге колчедана:
1—тарельчатый питатель; 2 — печь КС; 3 —котел-утилизатор; 4 — циклоны; 5 — элект-
рофильтры; 6 — топка для разогрева электрофильтров; 7 — система транспортирования
огарка (редлер или гидроудаление).
тонкую очистку в сухие электрофильтры. Очищенные от огарковой пыли об-
жиговые газы направляют в промывное отделение и далее на переработку в
серную кислоту.
Образующийся при обжиге колчедана огарок выводят из аппаратов печ-
ного отделения с помощью различных разгрузочных устройств в конвейеры с
погруженными скребками (типа Редлер) и передается на склад огарка.
Для розжига печи предусматриваются пусковые (чаще всего газовые)
горелки, а для разогрева сухих электрофильтров — топка. Для этих же целей
в печном отделении устанавливают пусковой дымосос.
Ниже дана краткая характеристика основного технологиче-
ского оборудования печного отделения современного сернокис-
лотного производства.
Бункер для колчедана. Предназначен для создания запаса колчедана не-
посредственно в печном отделении. На каждую печь устанавливается по два
бункера емкостью по 35 м3, что обеспечивает восьмичасовую работу печи.
Бункера снабжены электровибраторами, препятствующими зависанию в них
колчедана.
Питатель пластинчатый. Предназначен для равномерной подачн колче-
дана из бункера. На каждую печь устанавливается по два питателя произ-
водительностью по 25 т/ч. Их габариты: L — 4800 мм, В— 1200 мм.
Питатель тарельчатый (конструкция НИУИФ). Предназначен для равно-
мерной подачи колчедана непосредственно в печь КС. Регулирование числа
оборотов тарелки питателя, а следовательно, и количества подаваемого в
печь колчедана производится с помощью электродвигателя постоянного тока.
На каждую печь устанавливается по два питателя производительностью
65—650 т/сут (180 кг за 1 оборот). Производительность одного тарельчатого
питателя обеспечивает нормальную работу печи в случае выхода из строя
другого.
Печь КС (конструкция Гипрохим). Предназначена для обжига колчеда-
на в кипящем слое, представляет собой сварную цилиндрическую конструк-
цию, футерованную огнеупорным кирпичом. В нижней части печи расположе-
на дутьевая беспровальная подина грибкового типа. Печь снабжена устрой-
ствами для загрузки колчедана, выгрузки огарка, горелками для розжига,
74
люками для обслуживания и ремонта. В нижнем поясе пени смонтированы
окна для установки охлаждающих элементов (рис. 18).
В сернокислотных системах мощностью 180 тыс. т миг в год использу-
ются печи КС производительностью 200 т обжигаемого колчедана в сутки, а в
системах мощностью 360 тыс. т мнг в год — 450 т/сут. Устанавливаются по
2 печи на одну систему. Основные .характеристики печей КС для обжига
флотационного серного колчедана приведены ниже:
Параметр
Печь КС-200
Печь КС-450
. D, мм И, мм
. 4750/6200 13480
. 8144/8840 13410
пода> М2 УВН,М3
17,7 222
45,5 450
^Рпод>
кПа
1,5—1,8
2,2—2,4
О под,
т/(м2-сут)
10
8—10
Котел-утилизатор. Предназначен для использования тепла процесса горе-
ния колчедана (для получения пара), поддержания необходимой температу-
ры обжига в кипящем слое, охлаждения обжиговых газов. Данные по кот-
лам-утилпзаторам представлены ниже в разделе—использование тепла го-
РИС. 18. Печь КС для обжига колчедана:
/ — конус; 2 — бункер; 3, 7 — охлаждающие элементы; 4— форсунка; 5 — загрузочная
камера; 6— воздухораспредилмтельная решетка; 5— коллектор.
75
РИС. 19. Котел-утилизатор типа КС ВТКУ:
/ — печь: — пароперегревательные элементы; 3— испарительные элементы; 4— барабан
котла; 5 — испарительная поверхность котла; 6 — питательный насос.
РИС. 20. Котел-утилизатор типа ГТКУ:
/ — печь; 2 — паропер'гревательные элементы; 3 — испарительные элементы; 4— барабан
котла; 5 — испарительная поверхность котла (типа «труба в трубе»); 6 — питательный
насос.
рении серосодержащего сырья. Котел типа КС ВТКУ изображен на рис. 19,
типа ГТКУ — на рис. 20 (см. также стр. 124).
Циклоны грубой очистки. Являются первой ступенью системы сухой
очистки обжиговых газов. Предназначены для выделения из газового потока
наиболее крупных частиц огарка. Принцип действия — инерционный. В совре-
менных сернокислотных производствах используются укрупненные конические
циклоны марки СК-ЦН-34. На каждый печной блок устанавливается по два
циклона.
Основные характеристики циклонов СК-ЦН-34 для печей различной про-
изводительности (Q) приведены ниже:
Параметр
При Q=200 т/сут
При Q=450 т/сут
D, мм Н, мм
2500 8080
3600 11400
ДР, кПа G, т
0,9—1,0 8,0
0,9—1,0 20,0
Сухие электрофильтры. Предназначены для тонкой очистки обжиговых
газов от огарковой пыли. Процесс улавливания заключается в ионизации га-
за и зарядке взвешенных в нем частиц огарковой пыли, которая затем осаж-
дается иа электродах.
Эффективность работы сухих электрофильтров зависит от целого ряда
факторов: свойств очищаемого газа и улавливаемой пыли, концентрации пы-
ли в обжиговом газе, скорости газа и равномерности его распределения,
электрических параметров электрофильтра. Обжиговые газы, поступающие на
очистку в сухие электрофильтры, в основном содержат частицы пыли диамет-
ром менее 8 мкм. Степень очистки газа в сухом электрофильтре определяется
улавливанием частиц менее 2 микрон. На каждый печной блок устанавливает-
ся по два сухих электрофильтра. Основные характеристики сухих электро-
фильтров приведены ниже:
Производительность печи, т/сут
Тип электрофильтра . . . .
Активное сечение, м2 .
Число полей....................
Скорость обжиговых газов, м/с
Степень очистки, %
Габариты, м ...................
Масса металла, т...............
200
ОГ-4-16
16
4
0,5
99,0—99,3
14,34X3,95X12,4
112
450
УГТ-1-30-3
30
3
0,5
99,0-99,3
12,6x5,0x15,0
120
76
Конвейеры с погруженными скребками. Они являются механическими
транспортирующими устройствами и предназначены для удаления огарка от
аппаратов печного отделения. Конвейер представляет собой закрытый метал-
лической короб прямоугольного сечения, внутри которого движется замкну-
тая тяговая цепь со скребками. Производительность применяемых в серно-
кислотном производстве конвейеров представлена ниже:
Максимальная производительность, т/ч
Скорость дви-
жения цепи, м/с
КПС-2ЭО КПС-320Т КПС-500Т КПС-650Т
12,5 31,5 55 80 0,16
16 40 70 100 0,20
20 50 90 125 0,25
25 63 115 115 0,31
31,5 80 140 200 0,40
Нагнетатель воздуха. Предназначен для подачи в печь КС воздуха, не-
обходимого для горения колчедана и создания кипящего слоя. Основные ха-
рактеристики нагнетателей, применяемых при обжиге колчедана, приведены
ниже:
Параметр . . . . Тип Q, м3/ч Н, кПа п об/мин
Печь КС-200 . . 400-12-3 25000 18 2955
Печь КС-450 . . Э-700-11-2 48500 25 2975
Дымосос. Предназначен для сушки, розжига и разогрева сухих электро-
фильтров. Основные его характеристики приведены ниже:
Параметр ................. Тип Q, м3/ч Н, кПа
Печь КС-200 .... Д-15,5 75000 25
Печь КС-450 .... Д-20 150000 25
Ниже рассмотрены основные показатели технологического
режима обжига колчедана в печах КС (табл. 14).
Температура кипящего слоя и газов. Оптимальной темпера-
турой слоя с учетом теплопотерь, выхода пара и других усло-
вий считают 750—780 °C. Для уменьшения содержания в печ-
ном газе триоксида серы в результате его термического разло-
жения на выходе из печи поддерживают более высокую тем-
пературу газа 850—900 °C, что, как показано выше, обеспечива-
ется за счет догорания части FeS пыли в надслойном простран-
стве. Это связано с необходимостью создания в печи опреде-
ленных гидродинамических условий, определяемых интенсив-
ностью дутья и гранулометрическим составом колчедана.
Концентрация диоксида серы. Малый избыток кислорода в
обжиговом газе способствует уменьшению образования триок-
сида серы, поэтому концентрация диоксида серы должна под-
держиваться в пределах 14—14,5%, что соответствует концент-
рации кислорода около 1,8%. Общее сокращение объема об-
жигового газа за счет снижения коэффициента избытка возду-
ха снижает энергозатраты при его переработке.
Пылеунос и концентрация огарка в обжиговом газе (харак-
теристика огарка дана в табл. 15). Условия выноса огарка из
кипящего слоя зависят от линейной скорости газа w или, при
заданной концентрации газа, —от интенсивности 17Под и опре-
деляющего диаметра частиц огарка dOnp. Максимальная линей-
77
Таблица 14. Основные показатели оптимального технологического
режима обжига флотационного серного колчедана в печах КС
Контролируемый параметр Нормы и техниче- ские показатели
Состав колчедана Расход воздуха, тыс. м3/ч на печь К.С-200 па печь КС-450 Температура в кипящем слое, °C Температура обжигового газа, °C на выходе из печи после котла-утилизатора на входе в сухой электрофильтр Температура обжигового газа на выходе из сухого электрофильтра Концентрация диоксида серы, % на выходе из печи на выходе пз сухих электрофильтров Сопротивление кипящего слоя, кПа для печи КС-200 для печи КС-450 Содержание серы в огарке Разрежение печи, кПа на выходе из печи па выходе из котла-утилизатора на входе в сухой электрофильтр на выходе из сухого электрофильтра Расход питательной воды на котел-утилизатор, т/ч Давление пара в котле-утилизаторе, МПа Температура пара на выходе из котла-утилизатора, °C Удельный расход воздуха, м3/(м2-ч) Интенсивность печи КС подовая, т/(м2-сут) объемная, т/(м3-сут) Содержание огарковой пыли в обжиговом газе, г/м3 По ГОСТ 444—75 18—20 42—44 750+20 850—950 440—450 425—400 320—340 14,0+0.5 11,0—12 10,0—13,0 16,0—18,0 не более 1% 0,15—0,20 0,15—0,20 1,00—1,20 1,90—2,10 2,20—2,30 10-25-25 4,0—4,2 430—450 2300—2500 8—10 0,8—1,0
после печи после котла-утилизатора перед сухими электрофильтрами после сухих электрофильтров Распределение выхода огарка по печному блоку, °/о из печи из котла-утилизатора пз циклонов 300—360 230—280 20—30 0,1-0,2 4—6 15—20 65—75
из сухих электрофильтров Выход пара на 1 т 45%-го сухого колчедана, т 7—10
насыщенного перегретого Продолжительность, с пребывания обжиговых газов в печи охлаждения обжиговых газов в котле-утилизаторе 1,4 1,2 8—9 0,3—0,5
78
Таблица 15, Средний химический и гранулометрический состав
флотационного колчедана и огарка (печи КС)
Химический состав Химический состав
Компоненты колчедан | огарок Компоненты колчедан | огарок
Содержание, % Содержание, %
Сера (общ ) Сера 40—45 0,9—1,0 0,5—1,5 0,4—1,3 Кальций Магний 0,7—0,8 0,95—1,1 0,2—0,3 0,28—0,4
(сульфати.) Железо 35—40 48—55 Содержание, г/т
Медь 0,25—0,5 0,4—0,6 Кобальт 50—200 70—280
Цинк 0,5—0,6 0,7—0,8 Селен 30—60 20—30
Свинец 0,05—0,1 0,07—0,15 Теллур 25—40 20—30
Мышьяк 0,1—0,15 0,15—0,2 Кадмий 5—8 7—10
Кремнезем 13—18 18—25 Золото 0,7—1,9 1—2
Алюминий 0,2—0,3 0,28—0,4 Серебро 10—25 15—35
Фракция, мм Содержание фрак- ции, % Фракция, мм Содержание фрак- ции, %
колчедан | огарок колчедан | огарок
+1,0 0,5 0,3 -0,184-0,1 4,8 12,3
— 1,0+0,5 1,4 0,6 —0,1+0,074 25,7 9,7
—0,5+0,25 1,8 2,8 —0,074+0,05 20,1 18,9
—0,25+0,18 3,2 7,5 —0,05 42,5 47,9
пая скорость газа равна скорости витания w" частиц диаметра
d = ^опр*
Для гидродинамики слоя огарка флотационного колчедана
характерен ламинарный режим дутья и то, что основное коли-
чество частиц имеет диаметр меньше 0,3 мм, отсюда макси-
мальная подовая интенсивность [31]
cso2
б/подтах = 7,25-1О4 ру’сл •а’витопр
где (5 — степень выгорания серы.
Для оптимальных условий обжига, когда
/M= 750°C, ц = 4,15-10~6 кг-с/м2, Cso2 = 14,5% и 0 = 0,98
ивит°пр =1,1-10+2опр; £/подтах =Ю, 5швитопр
Запыленность обжигового газа, выходящего из печи, под-
считывают по уравнению
„ ° » 0,75
2=10х-77—, например Z= 10-98—я—= 368 г/м3
Г в.г
где а — выход огарка, кг/кг колчедана; х — степень выноса огарка нз печи,
%-
Максимальная подовая интенсивность определяется макси-
мально допустимой линейной скоростью газового потока, кото-
79
рой соответствует максимальная запыленность 400 г огарка
флотационного колчедана на 1 м3 газа. Степень выноса огарка
из кипящего слоя и его концентрация в обжиговом газе в за-
висимости от подовой интенсивности печи КС при оптималь-
ных условиях ее работы (/Сл = 750°С; Cso2= 14,5%) на 40%-ном
колчедане показана ниже:
Подовая интенсивность, т/(м2-сут) .... 3 6 10
Линейная скорость газа, м/с.................... 0,285 0,57 0,95
Диаметр наиболее крупных из выносимых частиц,
мм............................................. 0,161 0,227 0,295
Степень выноса огарка из слоя, % .... 80 90 96
Концентрация пыли в газе, г/м3 ............... 300 340 360
11.1.9. Расчет печи КС-450 на воздушном дутье
Исходные данные
Производительность В, т/сут....................................450
Расход сухого колчедана Bcyx, кг/ч.......................... 18750
Содержание, %
серы в колчедане C*s........................................45
влаги в колчедане шк........................................ 6
сульфидной серы в огарке Cors............................... 1
SO2 в сухом обжиговом газе С $02............................14
Температура, °C
колчедана, поступающего в печь..............................10
воздуха, поступающего в печь................................20
в кипящем слое...........................................750
газов на выходе из печи..................................900
газов на выходе из котла.................................450
перегретого пара.........................................440
Давление перегретого пара, МПа................................0,40
Коэффициент теплопередачи в кипящем слое, ккал/(м2-ч-град)
ДЛЯ ИСпарИТеЛЬНОЙ ПОВерхНОСТИ Лисп.........................250
для пароперегревательной поверхности Кпп ................ 220
для испарительного пакета Кку...............................25
Материальный расчет
Все расчеты проведены на сухой колчедан. Объемы газа приведены к
нормальным условиям.
Удельный выход огарка
160—CSK 160 — 45
а~ 160 —0,4Csor ~ 160-0,4-1 = °>72 кг/кг
Степень выгорания серы из колчедана
₽= 100^1 — а- J = 100-^1 — 0,72 = 98,4%
Объем сухих обжиговых газов
45
4-10-2 -pj- = 2,2 мз/кг
Ксг = г'сдбсухР = 2,2-18 750-0,984 = 40 563 м3/ч
80
= 68,4 10-.-——— =68,
/ 100
1+ = 14,4-10-* —
\ CSO2
Объем диоксида серы в обжиговом газе
1Л,о2= 68,4- 10~4-CsK = 68,4-10~4-45 = 0,308 м3/кг
Kso, = Vso2Scyx₽ = 0,308 -18 750-0,984 = 5678 м3/ч
Объем кислорода в обжиговом газе
6,3^-CsK =
= 14,4-10-4 — 6,3] 45 = 0,0542 м3/кг
+)2 = Уо2бсух₽= 0,0542-18 750-0,984= 1000 м3/ч
Объем азота в обжиговом газе
VN2 = 54-10-* + 0,4) CSK =
\ ^^2 /
/ 100 \
= 54-10-* I—14-4-0,4] 45= 1,836 м3/кг
Vn2 = t-N^cyxP = 1,836-18 750-0,984 = 33 885 м3/ч
Объем сухого воздуха (с. в.), поступающего иа обжиг
7 100 \
г'с.в= 68,4-10-М-у,--4-0,4 -CSK =
\ '—-’6)2 /
/ 100 \
= 68,4-10-* I-J4- +0,41-0,45 =2,32 м3/кг
V'c.B = Ус.вбсухР = 2,32-18 750-0,984 = 42 820 м8/ч
Содержание влаги в воздухе
«щн 0,6-0.027
Vb = Р — <ррп = 1 -0,6-0,027 = °’0165 м3/м3
где g — относительная влажность; рп — давление насыщенных водяных па-
ров; Р — атмосферное давление.
Объем влажного воздуха, поступающего на обжиг
ув.в = (1 — vB)• -jc.b = (1 + 0,0165)-2,32 = 2,36 м8/кг
Св.в= 0в.в5Сух₽= 2,36-18 750-0,984 = 43 520 м8/ч
Объем водяных паров в обжиговых газах
100шк
УН2О = Ос.в +0,0124- 100_Шк =
100-6
= 0,0165-2,32 + 0,0124- 1оо^16 = 0,117 м3/кг
Vh2o = VH2oBcyx₽ = 0,117-18 750-0,984= 2160 м3/ч
Объем влажных обжиговых газов
1>вл.г = ь'с.г + ин2о = 2,2 + 0,117 = 2,317 м8/кг
Увл.г= т'вл.г5сух₽= 2,317-18 750-0,984 = 42 723 м8/ч
Концентрация кислорода в обжиговом газе
Со2 = 21—1 ,32CSo2 = 21 — 1,32-14 = 2,5%
6—584
81
Тепловой баланс печи
Приход тепла (расчет на 1 ч)
Тепло, вносимое сухим колчеданом
Qc в =ВсухСс.Л= 18 750-0,12-10 = 22 500 ккал/ч, или 94,2 МДж
Тепло, вносимое влагой колчедана
/ 100 \
Qb.k = 5СуХСн2о'к-1 JOO —а>к —
= 18 750-1 = 11 970 ккал> или 5°Д5 МДж
Тепло, вносимое воздухом
Qb = Ув.вСв^вбсухР = 2,36 0,315 20• 18 785- 0,984 --=
= 267 500 ккал, или 1120,8 МДж
Калорийность сухого 45%-ного колчедана
QKC к = 31,98-45 = 1440 ккал/кг, или 6,03 МДж
Тепло, выделяющееся при сгорании колчедана
Qrop = QKc.KBCyxP = 1440-18750-0,984= 2656 800 ккал, или 1! 132 МДж
Суммарный приход тепла
Qnp = Qc.k 4* Qb.k 4“ Qb + Qrop ~
= 22 500 + 11 970 + 267 500 Д- 26 568 000 = 26 869 970 ккал, или 112 585 МДж
Тепловое напряжение печи
Qnp 26 869 970 , „ „
-==2-=------kqx---= 68 900 ккал/(ч м3), или 288,7 МДж/(ч-м3)
V вн 'jVU
Расход тепла
На испарение влаги колчедана (г — удельная теплота испарения)
/ 100 \
Quon — 1(100 ^к) Qh2O 4” Г1 д 100_К>к 1 j'^cyx =
, I 100 \
= [(100 — 10). 1 + 539,6] I д00_6- — 1 }• 1875 =
= 753510 ккал, или 3157,2 МДж
Количество тепла, вносимое огарком
Qor = бСуХа (ьсл^ог-сл 4“ ЬсуОсКвых) =
= 18 750-0,72-(0,05-0,217-750 4-0,95-0,213-900) =
= 2 585 000 ккал, или 10 831 МДж
Количество тепла, выносимое обжиговыми газами
Qo.r= (QsOj^sOj 4- Co2Vo2 4-Qn,Kn2 4- ChjO^HjO)’^- —
= (0,6-5678 4- 0,38-1000 4-0,359-33 885 4-0,405-2160)-900 =
= 15 179 000 ккал, или 63 600 МДж
Тепловые потери (по опытным данным 1 % от Qnp)
QnoT = 0,01-26 869 970 = 268 700 ккал, или 1125,8 МДж
88
Суммарный расход тепла
Qpacx = Qncn + Qor + Qo.r 4“ Qnor —
= 753 510 + 2 585 000 + 15 179 000 -J- 268 700 =
= 18 786 210 ккал, или 78 714 МДж
Количество тепла, утилизируемого охлаждающими элементами печи
Q ут = Qnp Qpacx —
= 26 869 970 — 18 786 210 = 8 123 760 ккал, или 34038,5 МДж
525CS*
Объемная интенсивность
Uo6 = ₽Vri.r.(273 + /cp)-T
; 900 + 750
Qp =------у----- =826,5 °C
2
525-45
и°б — 0,984-2,36-1099,5-8 — 1 > !57 т/(м3-сут)
Подовая интенсивность (при да=1 м/с)
,, 525Сдкш
С'под=Ткв.г-(273 + /сл)
525-45-1
^П°Д= 0,984-2,36-1023 = 10 т/(м2’сУт)
Линейная скорость обжигового газа в кипящем слое
под 1 0
Wl = 10,5 = 10,5 = 0,95 М/'с
Скорость обжигового газа в расширенной части печи
273 4-273 + 900 7,53
273-рсл ’ О22 273 + 750 ’ 8,142 •°-95— °>92 ’’А-'
Максимальный диаметр частиц огарка, выносимого из печи
, 1 / Й 1 / 4,37-10-"
d= у -4^5 -w2 = у -------45^------0,92= 0,00028 м
Запыленность обжигового газа после печи
а 0,72
ZK.c= 10 (100 — 1]о.гк-с)- — = Ю-(100 — 7,5)- -^2—= 330 г/м:!
где »]KC0.i— степень обеспыливания газа после печи
Расчет основных размеров печи
Площадь верхнего поперечного сечеиня печи КС
п в 450
Гсеч~ t/под ~ 10 ~45 “2
Диаметр нижней цилиндрической части печн
D= 1,13 1,13/45 « 8 м
Площадь пода печи
В пода = В сеч + /ср
6*
83
где /с1> — величина тепловоспрннпмающей поверхности, м2/м3,— принимается
по тепловому расчету и конструктивным соображениям, равной 2,5 м.
Внутренний объем печи (минимальный)
В 450
Vbh^ Uo6 = 1,157 =390 м3
Расчет конвективной поверхности котл a-у тилизатора
Приход тепла
С обжиговыми газами
Qr = 15 179 000 ккал, или 63 600 МДж
Количество тепла, поступающего в котел с огарком
Qor = ^.уйсух^гСоЛг = 0,95 -18 750 0,72 • 0,213 • 900 =
= 2 470570 ккал, или 10351,7 МДж
Итого, приход тепла
Qnp = Qr Д- Qor = 17 649 570 ккал, или 73951,7 МДж
Расход тепла
С огарком, выносимым из котла
Qor = gK y5сухОоДДг = 0,95-18 750- 0,72• 0,192• 450 =
= I 106 750 ккал, или 4637 МДж
Количество тепла, выносимого обжиговыми газами при 450 °C
Qr = (Cso^soj + Со/о2 + СкЛм2 + ChjO^HjoHt =
= (0,556-5678 + 0,354-1000 + 0,33 33 885 + 0,378- 2160)• 450 =
= 6,979 275 ккал, или 29243,2 МДж
Суммарный расход тепла
Qpacx = Q01 + Qr = 1 106 750 + 6 979 275 = 8 086 025 ккал, или 33880,4 МДж
Количество тепла, утилизируемого конвективной поверхностью котла
-Q"yT=Qnp—Qpacx = 17 649 570 — 8 086 025 = 9 563 545 ккал, или 40 071 МДж
Те,мпературиый напор в котле
Д/б—Д/м (900-254)-(450-254)
Л'КУ— — 646 — о/о С
2,316 А77 2,3 Ig Л96~
Величина конвективной тепловоспринимающей поверхности котла-утилиза-
тора при Кку=25 ккал/ч
„ Q"yT 9 563 545
КкуД?ку = 25-378 ~ 1000 м2
Расчет паропроизводительиости печи-котла
Паропроизводительность при получении перегретого пара
р ___ _____Q'yt 4~ Q у т_____
ПП Опп ----Св) 4” ф Окв Св)
8 123 760 4-9 563 545
~^790,3 — 100) 4- 0,05 (263,5 — 100) = 25 320 ккал/4- или 106 МДж/ч
«4
Температурный напор для пароперегревательиой поверхности печи
Д/б — Д'м
Д^пп =------------
А?б
2,3 1g
(750-254)-(750-440) _
Необходимая пароперегревательная поверхность, устанавливаемая в ки-
иящем слое
7)пп Опп *нп) 25 320 (790,3 — 668, /)
"пп== ЯппД^пп = 220-396 = 35 м
Необходимая испарительная поверхность, устанавливаемая в кипящем
-слое
Q'yr — £>пп-(1пп — <нп) 8123760 — 25320 (790,3— 668,7) 2
Яисп = Япп - М " 250 (750 - 250) = 40 м
Суммарная тепловоспринимающая поверхность, устанавливаемая в кипя-
щем слое
Якс = 35 + 40 = 75 м2
Условный удельный выход пара (испарительиость колчедана)
24-2 <2ут 24-(8 123 760 4- 9 563 545)
1000-(tHn —iXB)-S = 1000(699 — 10)-450 = !’43 т/т
11.1.10. Зарубежные установки
Ниже приведены некоторые сведения о работе отдель-
ных представляющих интерес зарубежных установок [31].
Основными зарубежными фирмами, которые строят в различных стра-
нах мира установки по обжигу пиритных концентратов, сериых колчеданов
и других сульфидных материалов, являются фирмы «Лурги» (ФРГ) и
«Дорр—Оливер» (США). Эти фирмы и определяют за рубежом два основ-
ных направления в конструктивном оформлении печных отделений по об-
жигу колчедана. Все другие фирмы (например, «Гюнтер Вальдхаузен»,
«Кребс», «Атаки», «Моитекатиии» и др.) в своих разработках сочетают харак-
терные особенности установок «Лурги» и «Дорр — Оливер».
Общим для указанных фирм является: применение для обжига колчеда-
на только печей с кипящим слоем, значительное повышение единичной мощ-
ности агрегата, отсутствие резервных печей. Для систем производительностью
180 000 т/год моногидрата (540 т/сут) устанавливается одна печь КС, т. е.
одна технологическая линия печного агрегата, при 360 000 т/год (1000 т/сут)—
две печи по 400—450 т/сут. На всех установках с печами КС избыточное
тепло используют для получения энергетического пара. За печами устанав-
ливают котлы-утилизаторы того или иного типа с принудительной или естест-
венной циркуляцией пароводяной эмульсии.
Характерной особенностью установок фирмы «Лурги» является высокая
иитеисивиость печей КС для обжига флотационного колчедана [10—
15 т/(м2-сут)], применение сухой очистки обжигового газа в многопольных
электрофильтрах, установка котлов-утилизаторов водотрубного типа (систе-
мы «Ла-Монт») с многократной принудительной циркуляцией как в котлах,
так и в охлаждающих элементах кипящего слоя. Печи имеют расширение в
верхней части. Газоход расположен сбоку печи и непосредственно примыкает
к котлу. Принципиальной типовой схемой таких установок (как и в Совет-
ском Союзе) является схема: печь — котел — циклоны — электрофильтр.
Установки как правило состоят из одной печи, двух (один резервный)
тарельчатых питателей с радиальным ножом, одного котла-утилизатора, двух
85
параллельных блоков циклонов, двух параллельно работающих электрофильт-
ров. Вывод огарка производится закрытыми, охлаждаемыми водой скребко-
выми конвейерами (типа «Редлер») в увлажнительный барабан, подача воды
в который для увлажнения огарка регулируется дистанционно. Компоновка
редлеров продольная; их резерв не предусмотрен, что обеспечивает мини-
мальное количество транспортеров в печном отделении. До последних лет
в печах «Лурги» отсутствовала форкамера и колчедан подавали по наклон-
ной течке непосредственно в печь, имеющую только беспровальную решетку,
которая сконструирована так, что возможно ее откидывание для очистки.
Затем фирма стала применять небольшие форкамеры для вертикального вво-
да колчедана.
Обжиг производят как правило при концентрации газа 12—13%. Процесс
обжига контролируют главным образом по температуре газа на выходе из
печи, которую регулируют путем изменения подачи колчедана. Установки
фирмы «Лурги» отличаются большой компактностью расположения оборудо-
вания вдоль технологической нитки.
Принципиальная типовая схема установок фирмы «Дорр — Оливер»
печь — котел — циклоны — мокрый промыватель или электрофильтр. Харак-
терными особенностями этих установок являются: низкая интенсивность пе-
чен КС [3—4 т/(м2-сут)j, что связано с обжигом сульфидных материалов
более высокой степени дисперсности (особенно полиметаллических и золото-
содержащих) ; питание печей пульпой; мокрая очистка обжиговых газов
(в аппаратах «Пибоди» или других мокрых промывателях). За последнее
время созданы в основном печи с сухим питанием. Для получения пара уста-
навливают как водотрубные, так и газотрубные котлы-утилизаторы. Печи КС
имеют цилиндрическую форму с неизменным сечением по высоте или с рас-
ширением вверху. Выход газа сверху печи. Огарок выводят из печи как
правило через перелив и собирают от печи, котла и циклонов цепным транс-
портером (с водяным охлаждением), выводящим весь огарок из печного от-
деления. Вывод огарка через перелив, отсутствие форкамеры и возможности
спуска спекшихся кусков, в случае забивки решетки, требует длительной хо-
лодной остановки печи.
Процесс обжига контролируют по температуре слоя, которую регулиру-
ют путем впрыскивания в реактор воды или скрубберной кислоты. Обжиг
ведут при температуре слоя 800 °C с получением газа концентрацией SO?
12-13%.
Сравнение отечественных установок с зарубежными пока-
зывает, что на отечественных установках обжиг ведут с полу-
чением газа более высокой концентрации при высоких интен-
сивности и степени выгорания серы; удачнее решены многие
важнейшие узлы установок: узел загрузки печей — тарельчаты-
ми питателями с неподвижным спиральным ножом и расширя-
ющимся книзу ступенчатым бункером, узел использования
тепла — с перегревом пара в кипящем слое и др.
11.1.11. Обжиг колчедана в печах КСЦВ [31, 51, 52]
При обычном обжиге колчедана в печах КС существование и харак-
тер кипящего слоя огарка, а также интенсивность работы печей обусловлива
ются гранулометрическим составом колчедана, т. е. величиной определяющего
диаметра частиц и содержанием фракции с частицами меиее 5 мкм.
Для большинства флотационных колчеданов определяющий диаметр ча-
стиц равен примерно 300 мкм, а содержание фракции с частицами диаметром
менее 50 мкм составляет 20—25%. Обжиг флотационного колчедана ведут с
интенсивностью 8—10 т/(м2-сут) при концентрации SO? в газе 14—14,5%,
линейная скорость газа в печи при температуре 750 °C находится в пределах
0,8—1 м/с, объемная интенсивность при этом 1—1,25 т/(м3-сут), что соответ-
ствует времени пребывания газов в печи 7—8 с. При этом около 90% всей
86
серы колчедана успевает сгореть в кипящем слое, состоящем из частиц со
средневзвешенным диаметром 0,5—0,6 мм, за время пребывания в нем газа
при высоте слоя 1—1,2 м около 1 с. Остальные 10% серы колчедана со сред-
невзвешенным диаметром 0,08 мм догорают в надслойном пространстве печи
за время пребывания в нем газа около 7 с. Резкое падение скорости горения
FeS в газовой фазе над кипящим слоем, несмотря ня малый размер частиц,
объясняется низкой их концентрацией в объеме газа, и следовательно, очень
низкой относительной скоростью между частицами и газовым потоком и низ-
ким содержанием кислорода в газе.
Скорость газового потока 0,8—1 м/с, согласно расчетам, является макси-
мальной скоростью для частиц диаметром 0,35 мм, а для основной массы
выносимого из кипящего слоя огарка со средневзвешенным диаметром
0,08 мм линейная скорость равна 0,07 м/с. При более дисперсном колчедане
интенсивность печей снижается очень резко. Так, для колчедана, который
дает огарок с определяющим диаметром частиц доли микрона, интенсивность
печи будет не более 1,5—2,5 т/(м2-сут). Применение кипящего слоя при та-
ких низких интенсивностях малоэффективно и даже практически неосущест-
вимо.
Поэтому в конце 60-ых годов были начаты работы [52, 53] по созданию
печей, в которых интенсивность обжига не зависит от гранулометрического
состава колчедана. При этом обжиг должен проводиться в кипящем слое,
существующем при скорости газа выше скорости витания частиц (второй
критической). Такой «искусственный» кипящий слой образуется при пересы-
щении частицами огарка пылегазового потока за счет возврата в кипящий
слой выносимых из него частиц. Пока концентрация возвращаемых частиц
в газовом потоке не достигнет его максимальной пневмотранспортирующей
способности, печь будет работать как пневмотранспортный аппарат. При по-
ступлении все нового количества мелких частиц огарка произойдет пересыще-
ние газового потока огарком и «выпадение» частиц огарка из потока. Но по-
скольку скорость газа в печи превышает скорость витания этих частиц, они
не могут находиться в покое, но и
из-за его пересыщения. Образу-
ется кипящий слой из частиц,
скорость витания которых во
много раз меньше рабочей скоро-
сти газа в печи.
Благодаря возврату более
мелких фракций, средневзвешен-
ный диаметр частнц уменьшается
в 6—7 раз по сравнению с части-
цами кипящего слоя, создаваемо-
го при той же рабочей скорости
и том же гранулометрическом со-
ставе колчедана в обычных усло-
виях, и становится равным сред-
невзвешенному диаметру основ-
ной массы частиц, выносимых из
РИС. 21. Печь КСЦВ для обжига
колчедана:
1—корпус; 2 —футеровка; 3 — свод;
4— засыпка; 5 — крышка печи; 6 — га-
зоход; 7 — циклон возврата; 8 — бун-
кер; 9— клапанный затвор; /б? —ком-
пенсатор; 11 — течка возврата огарка;
12— форкамера для возврата огарка;
13 — окна для охлаждающих элементов;
14, 20 — воздушные коллекторы; 15 —
бункер выгрузки огарка; 16 — опорная
рама; 17 — конус; 18 — воздухораспре-
делительная решетка; 19 — бункер вы-
грузки огарка; 21 — форкамера для
колчедана; 22 — люк для форсунки.
8Т
слоя, т. е. 0,08 мм. Следовательно, относительная скорость газа и часгшг
возрастает почти в 15 раз (от 1 м до 0,07 м/с). Улучшение при этом мае-
сообменных процессов создает возможность снижения температуры обжига.
Снижение температуры обжига без снижения интенсивности печи позво-
ляет обжигать спекающиеся в обычных условиях колчеданы, проводить окис-
лительный сульф атизирующий обжиг различных концентратов (например, пи-
ритно-кобальтовых) и восстановительный магнетизирующий обжиг (при
650—700 °C).
Печь КСЦВ (кипящего слоя с циклоном возврата) имеет две форкаме-
ры: для загрузки колчедана и возврата огарка (рис. 21). Форкамеры обору-
дованы провальными решетками. Воздух подается в печь тремя потоками.
Обжиговый газ через газоход поступает в футерованный циклон возврата,,
уловленный огарок из бункера циклона через клапанной затвор по течке,
снабженной компенсатором, возвращается в печь. Печь снабжена холодиль-
ными элементами. При температуре обжига 580 °C в кипящем слое печи
КСЦВ производительностью 200 т/сут необходимо установить 86 м2 поверх-
ностей: 29 м2 — пароперегревательной и 57 м2 — испарительной, потребная'
тепловоспринимающая поверхность котла-утилизатора составляет 116 м2.
Всего для котлопечного агрегата КСЦВ требуется 202 м2 поверхностей, что-
более чем в 2 раза ниже, чем для котлопечного агрегата КС-200.
Основное количество огарка (80—85%) выводится из кипящего слоя пе-
чи, однако концентрация пыли в газе после циклона, т. е. перед его поступ-
лением в котел-утилизатор, всего 50—70 г/м3 вместо 320—340 г/м3 в газах
из печей КС. Кратность циркуляции огарка в печи КСЦВ определяется из-
уравнения
Kz = ZJZ^
где Zt — запыленность газового потока перед циклоном возврата, г/м3;.
Zor — количество огарка, образующегося при обжиге, г/м3.
Z^Kz^/d3)
Для температуры 400—500 °C Кг равен 36.
В 1972—74 гг. были испытаны и освоены печи КСЦВ-100 н КСЦВ-200 nai
двух заводах, но в дальнейшем иа одном из заводов производство серной
кислоты было переведено на серу, а другой ие был обеспечен мелкодисперс-
ным сырьем. В настоящее время у нас и за рубежом работают две печи
КСЦВ-100 [52, 53].
11.1.12. Обжиг колчедана с применением кислорода
Полупромышленные исследования процесса обжига
флотационного колчедана на воздушно-кислородном дутье бы-
ли проведены в филиале НИУИФ в печах КС с площадью по-
да 2,6 и 2,0 м2 [54]. Обжиговый газ проходит сложную систему
очистки: циклон возврата — газотрубный воздушный теплооб-
менник или кессонированный газоход — второй циклон — элект-
рофильтр. Тепло горения отводили в охлаждаемых водой хо-
лодильных элементах поверхностью 2,7 м2 — в серии опытов
при концентрации газа до 18% SO2 и 4,7 м2 — от 18 до 36%
SO2. Температура кипящего слоя была 720—890 °C. Содержа-
ние кислорода в дутье изменяли в пределах 23—43%. Содер-
жание серы в огарке не превышало в среднем 1%. Опыты ве-
ли непрерывно в течение двух месяцев. Сравнительная харак-
теристика технологических показателей обжига при воздушном,
и кислородно-воздушном дутье дана ниже:
88
Показатели
Расход газа (дутья), всего, м3/ч .
технического кислорода ......................
Подовая интенсивность, т/(м2-сут)
Концентрация в печном газе, %
диоксида серы................................
кислорода ...............................
Содержание в газе после фильтра
пыли, г/нм3..................................
селена, мг/нм3...........................
Воздушное Кислородно-
дутье воздушно*
дутье
2100 2050
— 550
10,5 26,2
14,0 32,5
1,8 1,0
0,05 0,04
8,4 26,2
Основной результат опытов: повышение интенсивности об-
жига в 2,5 раза при практически одинаковом содержании пы-
ли в печном газе. Отмечено трехкратное увеличение выхода
селена в газовую фазу.
Ниже показаны результаты сравнительных расчетов работы
печного отделения на воздушном и воздушно-кислородном
дутье.
Общие данные для обоих вариантов: содержание серы в
колчедане 49%, влаги в колчедане — 6%, серы в огарке—1%;
температура колчедана 10 °C, воздуха и воздушно-кислородной
смеси — 20 °C; температура получаемого перегретого пара
450 °C, давление пара 0,4 МПа; коэффициент теплоотдачи в
кипящем слое 1,17 МДж/(м2-ч-град) [280 ккал/(м2-ч-град)],
коэффициент теплопередачи для котла-утилизатора 0,17 МДж/
/(м2-ч-град) [40 ккал/(м2-ч-град)]. Степень выгорания серы
98,6%, выход огарка 0,695 кг/кг; диаметр нижней зоны печи
7,55 м, верхней — 9,5 м, площадь пода 57,9 м2.
Результаты расчетов:
Показатели Воздушное дутье Кислородо-воз- душное дутье
Производительность печи по 45%-ному колчедану, т/сут 530 650
Концентрация SO2 в газе, % Температура, °C 14,5 17,7
в кипящем слое 680 770
на выходе из печи 710 800
Расход сухого колчедана по 49%-ному, т/ч 20.3 24,9
Подовая интенсивность, т/(м2-сут) 9.2 11,2
Расход влажного воздуха на обжиг, м3/ч 50700 48500
Расход технологического кислорода на обжиг, м3/ч — 2210
Концентрация кислорода в смеси, иду- щей на обжиг, % 21 24,25
Выход влажных обжиговых газов, м3/ч 46680 49040
Концентрация кислорода в сухом обжи- говом газе, оу Количество тепла, утилизируемого в ки- пящем слое 1,85 1,0
ккал/ч 15271400 19076560
кДж/ч 63987166 79930786
Испарительная поверхность в кипящем слое, м2 95 97,2
89
Пароперегревательная поверхность в ки- 59,7
пящем слое, м2.......................
Количество тепла, утилизируемое в кот-
ле
ккал/ч................................. 5 592 000
кДж/ч................................. 23 430 480
Конвективная тепловоспринимающая по- 448
верхиость в котле, м2................
Производительность котла по пару, кг/ч
насыщенному ............................ 36 800
перегретому.............................. 29 900
7 636 000
31 994 840
552
47 200
38 400
Таким образом, применение кислорода от кислородной
станции БР-1 производительностью 12 500 м3/ч 95%-ного кис-
лорода при использовании типового оборудования печного от-
деления без переделок позволит повысить производительность
цеха с 360 до 530 тыс. т/год. Суммарная поверхность теплооб-
менников контактного узла при работе на воздухе составляет
24 900 м2, на кислороде 25 600 м2, т. е. практически не изменя-
ется. Расход теплообменной поверхности на 1 т суточной вы-
работки при работе на кислороде снижается до 25 600:1 600 —
= 16 м2/т. Объем выхлопных газов на 1 т кислоты в 1,5 раза мень-
ше, чем при работе на воздухе, концентрация в них SO2
0,026%.
11.2. СЖИГАНИЕ СЕРЫ
Сера является самым распространенным сырьем для
производства серной кислоты. Оформление процесса окисления
серы до диоксида серы связано с ее многогранными свойства-
ми, поэтому остановимся на них несколько подробнее.
Внешняя валентная оболочка серы с главным квантовым числом 3 со-
держит 6 электронов. Четыре из шести электронов спареиы, два — иет,
поэтому сера в нормальном состоянии двухвалентна. Атом серы имеет то же
число валентных электронов, что и кислород. S2 обладает самым устойчивым
состоянием системы и ее энергетические уровни возбужденного состояния со-
ответствуют энергетическим уровням возбужденного состояния кислорода, но
сера имеет ярко выраженную тенденцию к образованию цепей в связи с
электронной структурой своего атома. Число атомов в молекуле серы от 1
до 20 и более.
Экспериментальные номограммы (модели ионизации), а также термоди-
намические исследования и теоретические расчеты свидетельствуют о том,
что все молекулы Sn (6<«<12) существуют во всех фазах в виде колец
[55]. Предполагается, что все цепочки серы, кроме Ss, являются двухвалент-
ными радикалами, в то время как кольца характеризуются полностью спа-
ренными электронами. Таким образом, кольца соответствуют цепочкам с ко-
ленными группами (такими как, например, Н—S—Н).
Для двухвалентной серы «свободная связь» характеризуется углом круче-
ния 85,30°, углом между связями 106° и длиной связи (2,066 А) [55].
Все исследованные вещества в виде колец, содержащие до 20 атомов,
могут быть выделены в виде чистых, твердых веществ. Небольшие молекулы
в виде цепей и изомеров встречаются в газообразной фазе. Большие моле-
кулы — полимеры и аллотропные соединения — как в твердой, так и в жид-
кой фазах. Структура молекул и их аллотропных соединений отличается
значительным разнообразием (табл. 16).
90
Таблица 16. Физические свойства аллотропов серы
Молекула Цвет Плотность, г/см3 Точка плавле- ния или разло- жения, °C
Ss Оранжево-красный 2,209 50—60
s7 Желтый 2,090 39
Ss-a Желтый 2,069 112,8
s8-p Желтый 1,940 119,6
S8-y Светло-желтый 2,190 106,8—120
S12 Бледно-желтый 2,036 148
Si8 Лимонно-желтый 2,090 128
S20 Бледно-желтый 2,016 124—125
Soo Желтый 2,010 104
Твердая сера. Стабильная форма твердой серы при нормальных темпера-
туре и давлении представляет собой орторомбическую a-серу, состоящую из
коронообразных молекул цпклооктосеры S8 (термодинамически стабильная
форма). а-Сера встречается в твердой, жидкой и газообразной фазах, кри-
сталлизуется в виде нескольких различных кристаллических решеток. Пол-
ностью установлена структура трех аллотропных модификаций. При 95,3 °C
a-сера превращается в моноклинную P-серу, плавящуюся при 119,6 °C; из
растворов, а также из расплава a-серы могут быть выделены игольчатые
кристаллы у-серы, плотность ее 2,19 г/см3, т. е. больше, чем у а- и Р-серы.
На рис. 22 представлена дериватограмма нагрева серы. В табл. 17 приведе-
ны значения давления паров серы.
Таблица 17. Давление паров над серой
Температу- ра, QC Давление Температу- ра, °C Давление
мм рт. ст. | Па атм | Па
106,9 IO-2 0,330 574 5 0,5
141,0 10-1 13,3 644 10 1,0
186,0 1 133 721 20 2,0
244,0 10 133-10 800 40 4,0
328,0 100 133-10-2 833 50 5,0
444,6 760 101-10-3 936 100 10,0
495,0 2 0,2 1035 200 20,0
Таблица 18. Некоторые свойства жидкой серы
Температу- ра, °C Плотность, г/см Вязкость Поверхностное натяжение, кН/м
Пз (дПа) | м2/с
145 1,7836 0,0715 0,0401 58,18
150 1,7797 0,0670 0,0376 57,65
155 1,7758 0,0650 0,3700 57,12
160 1,7718 26,680 15,060 56,60
165 1,7698 169,67 95,87 56,36
190 1,7582 925,70 528,40 54,95
195 1,7550 900,0 512,8 54,66
200 1,7525 800,7 456,9 54,38
300 1,6898 27,1 16,04 48,72
350 1,6608 5,04 3,03 45,89
444,6 1,6018 0,83 0,52 40,54
91
РИС. 22. Дериватограмма нагрева серы:
1 — кривая потери массы; 2 — кривая тепловых
эффектов; 3 — кривая изменения температуры се-
ры при нагреве.
Жидкая сера. Выше температуры
120 °C прн нормальном давлении сера на-
ходится в жидком состоянии. При 159,4 °C
она имеет наименьшую вязкость. Некото-
рые свойства ее представлены в табл. 18.
При 159,4 °C скачкообразно происходит
полимеризация молекул серы. При даль-
нейшем повышении температуры содержа-
ние полимера в равновесной жидкости по-
степенно увеличивается. Длина цепочки по-
лимера проходит максимальное значение
(порядка 10е атомов). Циклооктасера Ss
подвергается термическому разложению до>
линейного дирадикала, который соединяет-
ся с другими кольцами Ss, что ведет к образованию полимера (см. ниже
стр. 98).
После 159,4 °C вязкость серы с возрастанием температуры начинает
очень быстро подниматься, достигая максимума примерно при 190 °C, и пос-
ле этого относительно медленно падает. Повышение вязкости происходит
благодаря одновременному возрастанию концентрации и длины цепочки по-
лимера, а конечное медленное снижение вязкости является результатом про-
тивоположных эффектов возрастания концентрации и уменьшения длины
цепочки.
Давление паров над жидкой серой описывается уравнением (р — в мм
рт. ст., Т — в К):
в интервале 120—325 °C
1g Р= 14,70 — 0,00622387 — 5405,1 /Т
в интервале 325—550 °C
1g Р = 7,43287 — 3268,2/7
Парообразная сера. Теплота парообразования при 7НИП = 444,6°С я ат-
мосферном давлении равна 287,4 кДж/г (68,6 ккал/г). Состав пара при тем-
пературе кипения [9]: 3,8% (об.) S2, 41,8% Ss, 54,6% Ss.
При нагревании происходит постепенное уменьшение концентрации Ss в
равновесных парах серы, сопровождаемое все большим увеличением содер-
жания небольших аллотропов. При температуре около 730 °C основным алло-
тропом является S2 — самая стабильная из небольших по величине молекул
Таблица 19. Термодинамические характеристики парообразной серы
Молекула Реакция Энтальпия ; ТеплоемкоС1Ь, Дж/(моль-град)
ккал/моль кДж/моль
S2 2S(t)—>S2(r) 31,19 130,6 228
S3 2Ss(r)—->3S2(r) 33,87 141,8 269
S4 S4(r)—>2S2(r) 34,85 145,9 311
S5 2S5(r)-+5S2(r) 26,10 109,3 309
S6 3/4S8(r)-^S6(r) 24,34 101,9 354
S7 7/sS8 (r)—>S?(r) 27,13 113,6 408
Ss Ss(r)—>4S2(r) 24,31 101,8 429
92
РИС. 23. Зависимость степени диссоциации
паров серы от температуры.
серы. Известно 17 электронных энергетиче-
ских уровней для Ss, т. е. значительно
больше, чем для О2. Молекула S2 имеет
фиолетовый цвет, энергия диссоциации S2,
полученная на основе спектра ультрафио-
летовых лучей (35 590 см-1) составляет
425 кДж/моль.
В парах серы обнаружены также ал-
лотропные модификации S6, S?, Ss, Ss,
Sio, S,2. Они не присутствуют в газообраз-
ной смеси при равновесном давлении ниже
критической точки (/=1037,8 °C, Р=
= 10,38 МПа (116 атм), у = 0,403 г/см3)
[9]. Эти атомы могут быть получены в
результате электрического разряда. При
критических параметрах содержание алло-
тропной модификации S3 достигает 6%.
Модификация S< встречается в жидкой и
парообразной сере. При 450°C и 2,66 кПа
(20 мм рт. ст.) содержание ее-
составляет 20% всех паров серы, в критической точке от 24 до 40% всех
аллотропных модификаций.
Константы равновесия взаимных превращений [56]
P2s 28 400 P3S 63 710
’8 ~ ~ 4,57T +9>85 18 Ps ~ ~ 4,57T + 20,97
P4S, 92 180
lg p = — 4 57T ' + 30,76
°8 ’
Состав паров серы при различных температурах представлен на рис. 23, а ее-
термодинамические характеристики — в табл. 19.
11.2.1. Механизм горения серы
Горение серы представляет собой сложный процесс в
связи с тем, что сера имеет молекулы с разным числом атомов
в различных аллотропных состояниях и большой зависимостью
ее физико-химических свойств от температуры. Механизм ре-
акции и выход продуктов изменяется как от температуры, так
и от давления кислорода.
Окисление серы происходит еще до ее загорания. При дав-
лении 8,0—22,66 кПа (0,6—170 мм рт. ст.) и температуре 55—
150 °C процесс протекает по цепной реакции. Для каждой
температуры имеются свои минимальные и максимальные дав-
ления кислорода, за пределами которых реакция не идет [57].
При 160—260 °C и нормальном давлении бывает так называе-
мое холоднопламенное горение, характеризующееся очень ма-
лой скоростью реакции [144].
Отдельные стадии процесса горения серы (испарение жид-
кой серы и горение паров в газовой фазе) были подробно ис-
следованы в лабораторных условиях [58]. Исследования про-
цесса испарения жидкой серы проводили при температурах от
120 до 440 °C, т. е. в пределах между точками плавления и ки-
93
пения серы. Линейная скорость газа, пропускаемого над рас-
плавленной серой, была от 0,026 до 0,26 м/с (расчет на нор-
мальные условия).
Определена зависимость интенсивности испарения жидкой
серы от скорости газа (V) и температуры. Для различных
температур формулы для ее расчета имеют следующий вид:
у^зоо °с _ 500У°>58; ^400 °с = 407 500У°>515;
К1440°с=2 105 000V°,8
На интенсивность испарения серы значительное влияние
имеет температура. Так, при повышении температуры от 120
до 180 °C она возрастает в 5—10 раз, а от 180 до 440 °C —в
300—500 раз. Интенсивность испарения при скорости газа
0,104 м/с определяют по следующим формулам:
^(120-140 °C) _ 8,745 —2600/Т; дДио-гоо°C) _ 7>346 _ 2025/7";
^(200-440 Ю) = 10,415 — 3480/7’
Чтобы определить интенсивность испарения серы при лю-
бой температуре от 120 до 440 °C и линейной скорости газа в
пределах 0,026—0,26 м/с, ее находят сначала для скорости га-
за 0,104 м/с по этим формулам и пересчитывают на другие ско-
рости [59]:
1g К/= Ig^' + nlg^'/v')
где K'i и /<"1 — рассчитанное и искомое значения интенсивности испарения;
v'— скорость, равная 0,104 м/с; v"— скорость, для которой определяется
коэффициент /<!•
в результате исследования кинетики окисления паров серы
при 650—1100 °C [58] было установлено, что константу скоро-
сти реакции окисления серы до SO2 можно найти из уравнения
lgK=B-4/T
подставляя следующие значения коэффициентов А и В:
для температур 650—850 °C А = 2510, В = 3,49; для 850—
1100 °C А = 1875, В = 2,92.
С использованием этих данных при заданных степени окис-
ления х и составе газа длительность процесса окисления т опре-
деляется из уравнения
а—начальная концентрация паров серы; b—начальная концентрация кис-
лорода.
При высоких температурах скорость химической реакции
окисления серы больше скорости физических процессов [59],
поэтому скорость процесса горения определяется процессами
массо- и теплоотдачи (протекает в диффузионном режиме).
С уменьшением размера капель сокращается время их испаре-
ния. Мелкое распыление частиц серы и равномерное их распре-
94
деление в воздушном потоке увеличивает поверхность контак-
та, облегчает нагрев и испарение частиц.
В более поздних работах [60—64] изучалось горение от-
дельных капель серы. Измерение константы времени горения
капель серы проводили с применением так называемого мето-
да следа, заключающегося в экспонировании на фотопленку
следа горящих капель, который определяет длину полета ка-
пель от момента их воспламенения до полного выгорания. От-
дельные капли серы вводили в поток горячего (450 °C) воз-
духа, движущегося со скоростью 1,91—6,1 м/с. Установлено,
что константа горения практически не зависит от начального
диаметра капель и равна 1,04 мм2/с. Эффективность процесса
горения определяется временем полного сгорания каждой от-
дельной частички серы.
Эти исследования с использованием новейших методов экс-
перимента привели к разработке принципиально новой теории
горения — был установлен «взрывной» характер горения и изу-
чены основные его закономерности.
Время прогрева капель серы исследовали в интервале тем-
ператур 155—1200 °C. Установлено, что, несмотря на непосто-
янство физических свойств серы, температура поверхности кап-
ли повышается линейно. Время прогрева при (сР=1200°С со-
кращается в 5 раз по сравнению с /ср=1000°С. Оно определя-
ет время подготовки ее к горению. Значительное сокращение
этого времени возможно прежде всего за счет улучшения ка-
чества распыливания и повышения температуры среды.
Время испарения капель существенно зависит от темпера-
туры: при ее повышении от 1000 до 1600 °C время сокращается
вдвое. Для капель различного начального диаметра Д, при (СР =
= 1200 °C получены следующие значения времени прогрева
(тпр) и испарения (т!1СП):
с/н, мм
Тпр, С
Тисп, С
0,01 0,1 1
0,0041 0,407 40,74
0,0001’5 0,0149 1,49
2
163
5,96
Существенно и то, что для мелких капель время испарения
значительно меньше времени их пребывания в топочной каме-
ре. Мелкие капли успевают полностью испариться перед вос-
пламенением или в зоне воспламенения.
Процесс горения отдельных капель серы изучали по кинограммам и ос-
циллограммам. Световой сигнал от горящей капли воспринимался фотодат-
чиком и преобразовывался в нем в фототок, передаваемый на усилитель, а
затем на шлейфовый осциллограф Я-102. Процесс горения снимали на кино-
пленку.
Анализ осциллограмм (которые характеризуют светимость при горении
капель во времени) показал, что процесс горения капель серы можно разде-
лить на три периода: инкубационный период, период интенсивного горения и
период догорания. Инкубационный период характеризуется медленным нара-
станием величины фототока. Происходит слабое голубое свечение капли се-
ры. В конце этого периода начинаются слабые выбросы пламени и пилооб-
разное изменение фототока на осциллограмме (рис. 24). Период интенсивного
горения начинается резким нарастанием величины фототока и в течение все-
95
Время.с
РИС. 24. Осцилограмма светимо-
сти капель серы при горении (I,
II, III — периоды горения).
го периода происходит его скач-
кообразное изменение. Процесс
горения капель серы сопровож-
дается выбросами пламени дли-
ной до 5 см (рис. 25), причем
продолжительность каждого из
выбросов очень мала — всего
0,1—0,2 с. Одновременно могут
быть от одного до трех выбро-
сов — протуберанцев. Период догорания характеризуется быстрым уменьше-
нием фототока. Капля серы догорает спокойно без выбросов пламени.
По осциллограммам было определено время интенсивного
горения в зависимости от начального диаметра капли. Получе-
но следующее выражение:
т= 0,148dHs
Пропорциональность продолжительности времени интенсив-
ного горения кубу начального диаметра капель означает, что
определяющим фактором прн горении являются процессы, про-
текающие внутри капли и приводящие к выбросу пламени.
При 120 °C сера представляет собой кольцо Ss, начиная с 159,4 °C оно
подвергается термическому разложению до линейного дираднкала, который
соединяется с другими кольцами Ss, образуя полимер S*x. При повышении
температуры полимер разлагается [61] с соответствующим изменением эн-
тальпии:
S*x ----> S*x_8-J-S-(ж)
S*x $*х-в + $в (ж)
S*x-2 + S2 (ж)
ДЯ = —16,8 кДж (—4 ккал)
ДЯ = 21 кДж (5 ккал)
ДЯ= 96,6 кДж (23 ккал)
Учитывая незначительное содержание Ss и Sj в жидкой сере [60] и что
положительному значению термохимического теплового эффекта соответст-
вует отрицательное изменение энтальпии, можно говорить о выделении боль-
шого количества тепла при раз-
ложении полимера. Это ведет к
интенсивному парообразованию
внутри капли, внешне же прояв-
ляется в форме «взрывов» внутри
капли, приводящих к выбросам
горящих паров серы — выбросам
пламени. «Взрывы» внутри капли
и выбросы пламени происходят
в течение всего периода интенсив-
ного горения [61].
Изучение осциллограмм по-
казало, что первый период горе-
ния составляет примерно 45% от
суммарного времени горения ка-
пель серы, второй период — 25%
и третий — 30%.
РИС. 25. Фотография взрывного
горения капли серы.
S6
По приведенной здесь формуле время интенсивного горения
капли диаметром 2 мм составляет 1,18 с, суммарное время го-
рения составляет 1,18:0,25 = 4,72 с. Если бы горение капель се-
ры происходило без «взрывов» внутри капли и выбросов пла-
мени, то время горения можно было бы определить по формуле
тИсп = ^н2/Д по диаграмме I—t для серы температура в зоне го-
рения будет порядка 1000 °C, а константа горения для этих ус-
ловий /<=0,49 мм2/с. Отсюда время горения капли диаметром
2 мм будет составлять 8,2 с. Таким образом, суммарное уве-
личение скорости процесса горения капель серы за счет перио-
да интенсивного горения интенсифицируется в 8,2:4,72 =
= 1,74 раза. Увеличение скорости горения капли серы выброса-
ми пламени по сравнению с обычным горением может быть оп-
ределено из следующего равенства:
0,45-1-0,25(1 4-х) 4-0,30 = 1,74, отсюда х«3
Это говорит о том, что процесс горения паров серы в фа-
кельном выбросе идет в три раза быстрее, чем с поверхности
капли.
Результаты исследований взрывного горения при повышен-
ных температурах (700—1600 °C, диаметр капель в пределах
0,4—2,5 мм) описываются уравнением Аррениуса. Энергия ак-
тивации для первоначальной температуры окружающей среды
7850 Дж/моль.
Полученные результаты показывают, что процесс горения
капель серы протекает в диффузионной области. Температура
окружающей среды незначительно влияет на константу рав-
новесия, так же как и скорость потока воздуха, если она выше
3,5 м/с. При повышении температуры окружающей среды про-
исходит незначительное увеличение скорости горения капель
серы за счет диффузионной составляющей горения. На взрыв-
ное горение повышение температуры почти не влияет, так как
интенсивность взрывного горения капель серы определяется
лишь скоростью перегруппировки молекулы жидкой серы, из-
менить которую можно лишь увеличив или уменьшив темпера-
туру на поверхности капли, а она при горении постоянна и рав-
на температуре кипения 444,6 °C.
Результаты экспериментального изучения горения отдель-
ных капель при повышенных температурах позволили рассчи-
тать значения константы скорости горения /< и величины кон-
станты скорости испарения Б:
t, °C......................1360
К, мм2/с...................1,49
Б, мм2/с...................0,59
1460 1560 1659 1730
1,55 1,60 1,63 1,66
0,66 0,75 0,82 0,91
На рис. 26 показаны схема горения, соответствующая обычному диффу-
зионному горению капли серы, по которому протекают I и III периоды го-
рения, и схема горения капли серы в период интенсивного горения, при ко-
тором происходят выбросы горящих паров серы. Горение капли серы по пер-
вой схеме идет в приведенной пленке диаметром dap. К зоне горения с по-
верхности капли переносятся пары серы, а с внешней поверхности пленки —
7—584
97
II
РИС. 26. Схема горения капель серы (I—III — периоды горения).
кислород. Во внутренней части пленки между поверхностями горения и кап-
ли находятся лишь продукты реакции и пары серы, а с наружной стороны —
только окислитель н продукты горения.
При горении капли серы по второй схеме кроме обычного диффузионно-
го горения идет горение факела выброшенных «взрывом» внутри капли па-
ров серы, протекающее втрое быстрее. В начальном участке факела присут-
ствуют только пары серы, в центральной части — пары серы и продукты го-
рения. По мере удаления от центра капли происходит уменьшение централь-
ной части факела и увеличение наружной его части. В результате интенсив-
ного парообразования внутри капли происходит выброс паров серы. При пе-
ресечении поверхности горения пары серы воспламеняются, и продукты сго-
рания выносятся за пределы ядра факела. Ввиду интенсивного перемешива-
ния паров серы и окислителя, происходящего в результате впрыска паров
серы в среду окислителя, время горения выброшенных паров серы, как уже
сказано, невелико (0,1—0,2 с). Поскольку длительность периода догорания не
зависит от начального диаметра капли, то очевидно выбросы пламени про-
исходят до тех пор, пока масса горящей капли не станет равной некоторой
критической, и капля серы спокойно догорает.
Итак, анализ осциллограмм и кинограмм процесса горения
серы показал, что внутри капли серы протекает разветвленная
цепная реакция. Согласно открытию Н. Н. Семенова, происхо-
дит образование активных частиц — атомов, радикалов, моле-
кул, которые обладают избытком энергии. Авторами теории
«взрывного» горения серы [61] предлагается следующий воз-
можный механизм протекания цепной реакции:
s8
S—Se s. -ф S8
Sx
Sx + S8*
Sx + S8*
S8 + я ~
•s-se-s.
• S -ф Se—S—S8-—полимер' Sx*
► S8 -ф S8*—зарождение цепи
> 2S8 + S8*
* S8 + S8*
V
продолжение цепи
S8* -ф M --> S8 -ф M—обрыв цепи
Для зарождения цепи необходимо образование возбужденной частички,
несущей избыток энергии, которая будет использована в последующих хими-
ческих превращениях. При повышении температуры в капле полимер S*x
разлагается с образованием одной невозбужденной молекулы S8 и одной
возбужденной S*8, так как этот процесс экзотермичеи. Возбужденная моле-
кула S*8, сталкиваясь с полимером 5Л, передает ему избыток энергии и пере-
98
ходит в невозбужденное состояние. Это приводит к разложению полимера с
образованием одной возбужденной и одной невозбуждеиной молекулы.
Продолжение цепи обеспечивается также переносом дополнительного ко-
личества энергии с поверхности горящей капли полимером S*s к невозбуж-
денным молекулам Ss. В результате образуются новые возбужденные моле-
кулы S*8. Обрыв цепи может осуществляться при столкновении возбужден-
ной молекулы S*s с посторонней молекулой М.
Описанная разветвленная цепная реакция протекает очень
интенсивно и ведет к накоплению паров серы и их перегреву
выше точки кипения, так как поверхностное натяжение оболоч-
ки капли создает внутри нее давление несколько выше атмос-
ферного. Некоторое время сохраняется равновесие, но затем
оболочка капли рвется и пары серы выбрасываются наружу.
Диффузионный режим горения переходит во взрывной. Таким
образом, горение капель серы протекает как в диффузионном,
так и в взрывном режиме, причем оба процесса идут одновре-
менно.
Характеристику скорости горения капель серы К (в мм2/с)
можно представить как алгебраическую сумму скоростей
взрывного и диффузионного горения: К=К13з+Кл»ф.
11.2.2. Влияние повышенного давления на скорость
горения серы
Изучение процесса горения капель серы усложняется
тем, что одновременно проходят два процесса — горение испа-
ряющихся с поверхности капли паров серы в диффузионном
режиме и горение выброшенных взрывом изнутри капли па-
ров серы во взрывном режиме [64], причем выгорание капли
в последнем режиме при атмосферном давлении происходит в
несколько раз быстрее.
Представляло интерес определить влияние давления возду-
ха на скорость горения капель серы. Исследования проводили
в барокамере при изменении давления от 0 до 1,5 МПа
(15,3 ат). Воспламенение капли происходило самопроизвольно
при введении ее в микропечь. Температуру в печи измеряли
термопарой, время горения определяли по электросекундомеру
с точностью +0,01 с. Процесс горения снимался на кинопленку.
При атмосферном давлении
взрывное горение явно выражено,+2,6
при давлении 0,6 МПа (6,12 ат) на- 1
блюдается лишь один выброс горя- g
щих паров серы, а при 1,2 МПа
(12,25 ат) взрывное горение вооб-
go,s
РИС. 27. Зависимость констант скорости 0
горения капель серы от давления.
7
99
ще отсутствует и выгорание серы идет в чисто диффузионном
режиме.
На рис. 27'представлены результаты исследования зависи-
мости. скорости горения серы (температуру в микропечи под-
держивали равной 800 °C) от давления.
Для определения скорости горения серы при температурах,
отличающихся от 800 °C, необходимо пользоваться уравнением
Аррениуса, принимая энергию активации, равной 7850 Дж/моль
(1873,5 ккал/моль). Константа скорости горения /( (в мм2/с)
представлена как алгебраическая сумма констант взрывного
Квз и диффузионного Кдиф горений. Константа скорости диффу-
зионного горения возрастает пропорционально давлению. Кон-
станта скорости взрывного горения при возрастании давления
уменьшается по экспоненте и при давлении 1,0 МПа (10,2 ат)
практически равна 0. Тем не менее, при повышении давления
суммарная скорость процесса горения капель серы возрастает.
Выявленные закономерности описываются следующими урав-
нениями:
Квз= 0,78-ехр(— 1.59Р)2,54 мм2/с
КЛ,Ф = 1,21Р-}-0,23 мм2/с
К = 1,21Р0,78-ехр (— 1,59)2,м + 0,23 мм2/с
Проведены исследования по горению капель серы при повы-
шенных температурах и давлениях и различной степени рас-
пиливания серы при различной температуре и давлении [61,
62].
Степень выгорания диспергированной жидкой серы (п, %)
б циклонной камере под давлением может быть определена по
формуле [63]
L
п = ЮО
где L — суммарная длина потока газа; L* — длина пути потока газа, необхо-
димая для полного выгорания серы.
11.2.3. Печи для сжигания жидкой серы
Серу сжигают в основном в жидком состоянии, также
существуют печи для сжигания твердой, комовой серы (глав-
ным образом загрязненной). Для сжигания жидкой серы наи-
более распространены горизонтальные форсуночные печи, обо-
рудованные распыливающими форсунками.
Горизонтальная форсуночная печь представляет собой сварной футеро-
ванный барабан с плоским днищем и жестким корпусом. Форсунки обычно
вмонтированы в прямоугольную топочную камеру. Для подвода воздуха слу-
жит приваренный к камере диффузор. Наружный диаметр печи 6,3 м, внут-
ренний— 5,3 м, объем печного пространства — 310 м3, длина—15,2 м. Про-
изводительность по сере достигает 300 т/сут и более. Печь работает в комп-
лексе с вспомогательным оборудованием для фильтрования серы и использо-
вания тепла горения серы.
100
Действующие в зарубежной сернокислотной промышленности форсуноч-
ные печи, разработанные и применяемые фирмами «Лурги» (ФРГ), «Монсан-
то» и «Хемико» (США), «Хенд бэкходо» (Япония), «Кребс» и «Юджин Кюль-
ман» (Франция), «Целлеко» (Швеция) и другими, различаются производи-
тельностью и типом установленных форсунок, наличием или отсутствием экра-
нов внутри печной камеры, расположением входных отверстий для подачи
воздушного дутья в печь, устройствами для перемешивания потоков воздуха
с парами серы, а также оборудованием для рационального использования
тепла процесса горения серы.
Удельный объем печных камер в расчете на 1 т сжигаемой серы у печей
некоторых из зарубежных фирм конструкций составляет: «Хемико»—1,43,
«Техас гильф» — 0,75, «Целлеко» — 0,14 м3/сут. Печи фирмы «Кребс» имеют
длину Ими диаметр — 7 м. Фирма «Юджин Кюльман» разработала конст-
рукцию серусжигающей установки производительностью 200 т/сут, работаю-
щей под давлением до 0,6 МПа. Разрабатывается система для производства
серной кислоты под тем же давлением мощностью 1800 т/сут, в которой уста-
навливается одна печь производительностью по сере 600 т/сут [65].
Главными техническими задачами при конструировании аг-
регатов для обжига серы являются обеспечение высокого теп-
лового напряжения в печной камере, максимально полного
окисления паров серы в диоксид серы, эффективного использо-
вания вторичных энергоресурсов (тепла горения серы), полу-
чения газа заданной концентрации с минимальным содержани-
ем вредных примесей.
К вредным примесям в печном газе относятся не только
обычные контактные яды (они могут поступать вместе с недо-
статочно чистым сырьем), но также такие вещества, как три-
оксид серы, оксиды азота, продукты неполного сгорания серы,
неуспевшая окислиться сера. Присутствие их в газе зависит
целиком от технологического режима работы серосжигающих
установок.
В современных серосжигающих печах тепловое напряжение
в среднем достигается равным 21 • 104—16,5-106 кДж/(м3-ч) [5-
• 104—4-Ю6 ккал/(м3-ч)]. Температуру в печах поддерживают
в зависимости от требований, предъявляемых к получаемому
газу, соображений по сохранности футеровки печи и эффек-
тивности теплоиспользования. При сжигании одного и того же
количества серы получают тем более концентрированный газ,
чем меньше объем газа и выше его температура.
На рис. 28 показана приближенная зависимость между тем-
пературой и концентрацией газа, образующегося при адиаба-
тическом сжигании серы в воздухе, имеющем температуру
0 °C [59], на рис. 29 зависимость между температурой в печи,
расходом воздуха на 1 кг серы и концентрацией газа [65].
Нижний предел температуры печи был определен исследо-
ваниями по сжиганию серы в кислороде для сульфит-целлю-
лозного производства, где нежелательной примесью в газе яв-
ляется триоксид серы. Установлено, что при 350—400 °C со-
держание SO3 в газе составило около 35%, при 600—650°C—
7%, при 700—750 °C — 4% и при 900 °C и выше присутствия
SO3 не обнаружено, поскольку при этих температурах проис-
ходит его термическая диссоциация.
101
РИС. 28. Зависимость между температурой и концентрацией газа:
/ — концентрация кислорода в газе, % (об.); 2 — концентрация SO2. % (об.).
РИС. 29. Зависимость температуры (теоретической) в печи (/) и расхода
воздуха (2) на сжигание 1 кг серы от концентрации SO2 в газе.
При высоких температурах происходит взаимодействие
между кислородом и азотом воздуха с образованием в газе
нежелательной примеси — оксидов азота. В связи с тем, что за
последние годы получили широкое развитие сернокислотные
производства с так называемой «короткой» схемой, а также в
связи с увеличением числа потребителей высококачественной
кислоты возникли затруднения, связанные с наличием в кис-
лоте оксидов азота.
Содержание оксидов азота (N2O3) в кислоте и олеуме со-
гласно ГОСТу должно быть не более 0,0005, что соответству-
ет концентрации N2O3 в газе менее 2 мг/м3.
Для достижения таких норм, а также при получении кисло-
ты специальных сортов, приходится вводить в продукционную
кислоту денитратор в виде дорогостоящего гидразинсульфата.
Образование оксидов азота становится заметным при тем-
пературе выше 1300 °C (в некоторых случаях появление их
отмечается и при более низкой температуре в печи). Влияние
кислорода, присутствующего в печном газе, на окисление азо-
та особенно велико при высоких температурах.
Подробные исследования процесса генерации оксидов азо-
та проведены [68] на сернокислотной системе большой мощ-
ности, оборудованной форсуночной печью для сжигания 20,8 т
серы в час. Температура подаваемого в печь воздуха 240—
250 °C, диаметр отверстия форсунки 9,5 мм, время пребывания
газа в печи 2,2 с. Сернокислотная система работает на жид-
кой сере по обычной «короткой» схеме с двойным контакти-
рованием. Содержание оксидов азота определяли в газовой фа-
зе— до и после сушильной башни, контактного аппарата, аб-
сорберов А-1 и А-2 и в жидкой фазе — в кислоте абсорберов,
102
сушильной башни и в товарной кислоте. Газ после серной пе-
чи не содержит диоксида азота, содержание оксида азота со-
ставляет 40—100 мг/м3 и возрастает с повышением температу-
ры в печи.
Равновесная Сравн и фактическая Сфакт концентрации окси-
да азота в газах от сжигания серы при различных температу-
рах приведены ниже (значения Сфакт получены при обследо-
вании промышленной печи производительностью 20,8 т/ч):
t, °C . .
Сранн, МГ/М3
Сфакт, МГ/М3
. 900 1020 1100 1200 1300 1400 1500
. 180 415 680 1175 1927 2760 4950
. — 40 60 100 — — —
После 1 стадии абсорбции в газе N2O3 не обнаружено, после контактного
аппарата его концентрация составляла в среднем 2 мг/м3. Это явление авто-
ры объясняют принципиальной возможностью окисления NO до NO2 при тем-
пературах выше 60—70 °C, т. е. на выходе из абсорбера А-1. В кислоте аб-
сорбера А-1 N2O3 не обнаружено. На 2-ой стадии абсорбции N2O3 полностью
поглощается и концентрация его в кислоте А-2 составляет 0,003—0,005%, в
сушильной и товарной кислоте содержание N2O3 было в пределах 0,0001—
0,0005% (кислота от абсорберов непрерывно перетекает в сборник сушильной
башни, откуда частично передается на склад).
Основными местами появления окислов азота в обследованной сернокис-
лотной системе являются печь, где происходит окисление азота при горении
серы, и вторая стадия технологического процесса, где наблюдается частичное
(около 2 относительных процентов) окисление NO в NO2. Накопление N2O3
наблюдалось в кислоте абсорбера А-2 и сушильной башни.
Для восстановления оксидов азота на 1 т кислоты в сушильную башню
добавляют 1,0—1,5 г сульфата гидразина. Оксиды азота восстанавливаются
по реакции:
3N2H4-H2SO4 + 2N2O3 = 3H2SO4 + 5N2 ф- 6H2O
Остаточное содержание оксидов азота в товарной кислоте составляет
менее 0,0005%.
Для предотвращения образования оксидов азота фирма
«Лурги» (ФРГ) вводит в практику работы некоторых сернокис-
лотных заводов двухступенчатый процесс сжигания серы, схе-
ма которого приведена на рис. 30.
В печи предварительного сжигания
серы (форпечь) оксиды азота не обра-
зуются благодаря дефициту кислорода.
Печной газ, выходящий из форпечи,
содержит диоксид серы и пары серы.
Газ охлаждают до определенного уров-
ня в котле-утилизаторе № 1, установ-
ленном за форпечью, и направляют в
печь дожигания серы, где обеспечены
условия для полного перевода всей ос-
тавшейся в печном газе неокислившейся
серы в диоксид серы. Благодаря отно-
сительно низкой температуре дожига-
ния серы, окислы азота в печном газе
практически отсутствуют.
РИС. 30. Схема двухступенчатого про-
цесса сжигания серы фирмы «Лурги»:
I -- печь для предварительного сжигания се-
ры; 2, 4 — котлы-утилизаторы; 3 — печная ка-
мера дожигания серы.
Возди.х
103
Количество воздуха, подаваемого в печь дожигания, определяется желае-
мой концентрацией SO2 в газе. С помощью автоматических систем регулиро-
вания различных технологических параметров и концентрация SO2 в печном
газе', и температура могут поддерживаться на одном и том же уровне при
разных загрузках серы в печь.
Процесс двухступенчатого сжигания серы позволяет предотвращать об-
разование оксидов азота, обеспечивает полное сгорание серы, повышает на-
дежность работы серосжигающих агрегатов и аппаратов сушильного, кон-
тактного и абсорбционного отделений сернокислотного производства [65].
Для сжигания жидкой серы успешно применяют циклонные
печи, разработанные с учетом эффективного воздействия на
процесс турбулизации парогазовой смеси. Особенность этих
печей состоит в том, что материал, подвергаемый тепловой об-
работке, подают в печь тангенциально, создавая аэродинамиче-
ский вращающийся поток, аналогичный потоку в циклонах.
Аппараты такой конструкции используют в различных энерго-
технологических процессах.
Циклонные печи для сжигания серы впервые разработаны
в СССР (ЦКТИ им. И. И. Ползунова совместно с Невским хи-
мическим заводом и другими предприятиями) и внедрены в
нескольких вариантах, отличающихся числом камер, способа-
ми ввода воздуха и серы, устройством пережимных колец и
др. [69].
Печь циклонного типа представляет собой полую камеру с тангенциаль-
ным вводом жидкой серы и воздуха. Благодаря вращательному движению
газового потока со скоростью 100—120 м/с в циклонной камере создаются
благоприятные условия для тепло- и массообмена паров серы с воздухом,
возрастает скорость горения серы.
Сжигание серы (1200—1300 °C) ведут с небольшим избытком воздуха
й газ, содержащий 16—18%
циклонной печи достигает
4,6-106 Вт/м3 [4-Ю6
ккал/(м3-ч)], а объем ап-
парата уменьшается в 30—
40 раз по сравнению с объ-
емом факельной форсуноч-
ной печи такой же произ-
водительности. Достоинства
камерной циклонной печи,
кроме указанных выше: по-
стоянная концентрация SO2
в получаемом газе, простое
регулирование процесса го-
рения серы и его автомати-
зация, малая затрата вре-
мени и горючего материала
на разогрев н пуск печи
после длительной останов-
РИС. 31. Циклонная печь
для сжигания серы:
/ — форкамера; 2, 4 — пережим-
ные кольца; 3, 5 — камеры до-
жигания; £ —футеровка; 7 —
воздушный короб; 8, /0 — фор-
сунки для подачи серы; 9, 11 —
сопла для подачи воздуха.
104
кн (5—6 ч вместо 2 сут, необходимых для разогрева и пуска факельных
печей в аналогичных условиях).
Циклонные печи для обжига серы генерируют оксиды азота в гораздо
меньшем количестве, чем обычные топки энергетических котлов. Это проис-
ходит из-за больших скоростей в циклонной печи при малом времени пребы-
вания газов в зоне высоких температур.
Циклонные печи для сжигания серы могут быть как горизонтальными,
так и вертикальными. Одна из конструкций горизонтальной циклонной печи
схематично представлена на рнс. 31, Печь снаружи имеет воздушный короб
(рубашку) для снижения температуры наружной обшивки и подогрева по-
ступающего в печь воздуха. В форкамеру через две группы сопел тангенци-
ально подают первичный воздух, а через механическую форсунку — жидкую
серу. Здесь происходит испарение и частичное сгорание паров серы. В пер-
вую камеру дожигания через форсунку дополнительно вводят жидкую серу,
а через сопла — часть вторичного воздуха. Окончательное дожигание паров
серы происходит во второй камере, куда направляют дополнительное количе-
ство воздуха.
ЦКТИ совместно с Белгородским котлостроительным заво-
дом разработан энерготехнологический агрегат циклонного ти-
па производительностью (по сжигаемой сере) 100 т/сут
(СЭТА-Ц-100), состоящей из циклонной печи и котла-утилиза-
тора. Такие агрегаты эксплуатируются на нескольких заводах.
Разрабатываются агрегаты на 200 и 300 т/сут.
Важнейшим оборудованием печей для сжигания жидкой се-
ры являются форсунки, которые должны обеспечить тонкое и
равномерное распыление жидкой серы, хорошее смешение ее
с воздухом в самой форсунке или за нею, быстрое регулирова-
ние расхода жидкой серы с сохранением необходимого соот-
ношения ее с воздухом, устойчивость определенной формы и
длины факела, а также иметь прочную конструкцию, надежную
и удобную в эксплуатации. Для бесперебойной работы форсу-
нок важно, чтобы сера была хорошо очищена от золы и биту-
мов. Форсунки бывают механического и пневматического дей-
ствия.
Механические форсунки работают под давлением, которое создается на-
сосом, нагнетающим расплавленную серу. Форсунку обогревают паром прн
140 °C, что обеспечивает наибольшую текучесть серы н предохраняет форсун-
ку от температурных деформаций. Для бесперебойной работы механических
форсунок давление в серопроводе перед пнмн поддерживают в пределах
0,3—0,4 кПа.
В форсунках пневмотического действия сера, поступающая самотеком из
напорного бака, распиливается сжатым воздухом или паром. Чтобы обеспе-
чить свободное поступление жидкой серы, напорный бак устанавливают на
высоте 4—5 м над уровнем форсунок. Воздух, предварительно подогретый до'
150—200 °C. очищенный от пыли и осушенный, подают в форсунку под дав-!
ление 0,4—0,6 МПа. Расход воздуха для таких форсунок на 1 кг серы со--
ставляет 0,1 м3. : 1
В настоящее время в нашей стране эксплуатируется более'
20 печей циклонного типа. Эти печи по сравнению с факель-’
ными печами имеют почти на два порядка более высокое теп-
ловое напряжение топочного объема [69]. .
Для уточнения расчетов камерных циклонных печей бьрли
проведены необходимые исследования. В опытах по распыли-
1Ш5
ванию жидкой серы в факеле двухкамерной циклонной топки
производительностью 150 т/сут измеряли среднюю скорость
воздуха в соплах, температуру газов в топке и концентрацию
SO2 на выходе из печи, которая изменялась от 13,9 до
21,0% (об.). Дисперсность распыла жидкой серы центробеж-
ными форсунками предварительно определяли на форсуноч-
ном стенде. Установлено, что средний характеристический диа-
метр капель составил 0,09—0,12 мм, а средний поверхностный
бо»О,2 мм.
При обработке результатов исследований с использованием
известных закономерностей для сжигания жидкого топлива и
аэродинамики закрученой струи получены расчетные уравне-
ния для сжигания распыленной жидкой серы в циклонной
печи [63]. Процесс горения распыленной жидкой серы в фа-
келе печи определяется горением единичных капель. Длина
пути потока газов L* (в м), необходимая для полного выгора-
ния распыленной серы, составляет
L* =
где 6о—средний диаметр капель, мм; v — скорость потока, м/с; Б — констан-
та скорости испарения, равная —б/д20/Л; x=llv, I — длина пути потока газов,
ла котором происходит выгорание распыленной серы; С — константа.
В промышленных печах 6 = 0,1 мм, при этом С=143 [67],
что соответствует выгоранию серы в топочном объеме печи на
99,5%. С помощью этой зависимости можно установить необ-
ходимые размеры печи при создании новых конструкций или
определить степень выгорания распыленной серы в топочном
объеме имеющейся печи.
Расчет L* для различных значений коэффициента избытка
воздуха а, определенной скорости воздуха, например при
ц = 35 м/с позволяет определить значение критического средне-
го диаметра капель серы 6Кр. При 60<6Kp в топке будет обес-
печиваться полное выгорание диспергированной жидкой серы,
а при 6о>6Кр — неполное.
Настоящая методика определения степени выгорания дис-
пергированной жидкой серы может быть использована также
для расчета двухкамерных циклонных печей производитель-
ностью 100, 200 т/сут и более.
Одним из новых направлений в технике сжигания жидкой
серы за рубежом является использование так называемого
вибрационного горения. При таком горении факел периодиче-
ски изменяет свою форму и размеры, иногда совсем исчезая.
Одновременно с той же частотой колеблются все параметры
процесса — давление в камере, скорость и состав парогазовой
смеси, температура и др.
Вибрационное горение возможно при любом виде топлива: твердом, жид-
ком, газообразном. Частота колебаний может составлять от нескольких до
тысяч в секунду, причем возможно одновременное появление колебаний низ-
кой и высокой частоты. В некоторых случаях пульсация горения может быть
использована вместе с ультразвуковыми волнами для интенсификации про-
106
цесса горения и теплообмена. При этом существенно увеличивается теплоиа-
пряжение и скорость горении.
По некоторым методам, предложенным за рубежом, жидкую серу сжи-
гают, периодически впрыскивая ее в камеру горения. Каждая порция серы
сгорает мгновенно — вспышками, и частота колебаний газового столба, обра-
зующегося в камере, равна нлн кратна частоте впрыскивания жидкой серы.
В специальных камерах для увеличения амплитуды пульсации пламени уста-
навливают клапаны, которые препятствуют обратному выбросу газов при
вспышке.
11.2.4. Печи для сжигания твердой серы
В процессе сжигания твердой серы исключаются ее
предварительное плавление и последующие трудоемкие опера-
ции отстаивания и очистки. Однако содержащиеся в твердой
сере примеси и загрязнения затрудняют процесс сжигания, сни-
жая его интенсивность.
Сжигание твердой серы в печах — двухстадийный процесс.
Вначале происходит плавление твердой серы, а затем ее испа-
рение и взаимодействие паров серы с кислородом воздуха. Теп-
ла, выделяющегося при горении паров серы, более чем достаточ-
но для расплавления и испарения поступающей в печь твердой
серы.
По конструктивным особенностям печи для сжигания твер-
дой серы можно разделить на ванные (отражательные, с барбо-
тажным слоем), с псевдоожиженным (кипящим) слоем, комби-
нированные и т. п.
Ванная отражательная серная печь представляет собой футерованную
камеру (ванну), где находится расплавленная сера. Негорючие прнмеси, на-
ходящиеся в сере, постепенно накапливаются и загрязняют под камеры. Для
получения из загрязненных сортов серы относительно чистого диоксида серы
используют печи ванного типа с барботажным слоем.
Первичный воздух (х 1 %) должен иметь скорость, обеспечивающую ин-
тенсивное барботирование и турбулизацию слоя жидкой серы. Барботажный
слой представляет собой систему, в которой жидкая сера является сплошной
фазой, а воздух — дисперсной. Частицы серы, попадающие в этот слой, быст-
ро нагреваются и плавятся. Температура барботажного слоя находится в
пределах 300—380 °C, лишь на границе фаз жидкая сера — парогазовая смесь
она достигает 440—450 °C. При этой температуре начинается испарение серы
с поверхности. Относительно невысокая температура, которая поддерживает-
ся в слое расплавленной серы, ограничивает горение тяжелых фракций орга-
нических соединений (температура горения выше 300—380°C), содержащихся
в сере.
Для сжигания паров серы над уровнем барботажного слоя вводят вто-
ричный воздух — через коллектор по тангенциально направленным каналам.
Чтобы обеспечить турбулизацию газового потока по всей высоте печи соот-
ношение последней к диаметру выдерживают в пределах 4:1—5:1. Для
этой же цели на некоторых ванных печах с барботажным слоем предусмот-
рен пережим.
Вследствие удаления загрязнений со шлаком серные пары получаются
более чистыми, чем в ванных печах, работающих на загрязненной сере. Для
удаления шлака предусмотрено переливное устройство. В выгружаемом шла-
ке содержится до 50% серы, поэтому его можно использовать в качестве
кислотоупорного строительного материала или сжигать в других печах. При
тепловом напряжении камеры горения 7,123-10® кДж [1.7-106 ккал/(м3-ч)]
получают газ устойчивой концентрации 14—15% SO2.
107
РИС. 32. Печь ЖКС для сжИ-
гания серы (с жидкокипящим
слоем):
/ — загрузочная труба; 3 — устрой-
ство для поддержания уровня слоя;
3 — надслойная решетка; 4 — нако-
питель; 5 — регулятор числа оборо-
тов.
Для сжигания загряз-
ненной серы (содержа-
щей до 0,5% мышьяка)
успешно используется
печь с жидким кипящим
слоем (ЖКС) на химиче-
ском заводе в Эстонской
ССР. Конструкция печи
показана на рис. 32. Так
как температура возгон-
ки соединений мышьяка,
а также селена и некото-
рых углеводородов, ле-
жит выше температуры
кипения серы, отгоняе-
мые пары серы сжигаются, а примеси остаются в шламе, кото-
рый непрерывно выводится из печи.
Для сжигания твердой серы иногда применяют печи КС, ис-
пользуя для создания взвешенного слоя песок, шамотную
крошку. Печи КС применяют и для сжигания твердой серы в
смеси с цинковым концентратом в любых соотношениях.
В зарубежных разработках технологии сжигания твердой серы особое
внимание уделяют использованию турбулентного смешении частиц твердой
серы с потоками воздуха [65]. Соотношение между массами подаваемых в
печь воздуха и серы поддерживают в пределах от 4,3 до 13. -Содержание
серы с размерами кусков менее 0,18 мм составляет 80%, а массовое соотно-
шение между серой и воздухом составляет от 3 до !/з. Такое соотношение
обеспечивает достаточное распыление серы и предохраняет от возможности
взрыва. Смесь твердой серы с воздухом подают с такой скоростью, чтобы
обеспечить устойчивое пламя горелки. Как и в случае сжигания жидкой
серы, скорость газа выбирают ие ниже 4,7—5,5 кг/(м2-с), что позволяет сжи-
гать твердую серу в печах малого объема [0,24-10-7 м3/(кг-с)]. Критерий
Рейнольдса должен быть выше критического — в пределах 30 000—50 000
[59].
Для подачи и дозирования твердой серы в печи (ванные,
кипящего слоя) обычно применяют стационарные и передвиж-
ные шнековые питатели пли герметичные роторные питатели.
Шнековый питатель полностью заполняется серой, что уменьшает про-
никновение в пего газа. Помимо того, в бункере над винтом шнека создает-
ся затвор из кусковой серы высотой не менее 0,5—0,8 м. Тарельчатые пита-
тели для подачи кусковой серы не применяют, поскольку возможно загора-
ние серы в питателе и выброс ее из бункера.
Для получения при обжиге серы чистого и сухого газа
в НИУИФе разработана [69] печь принципиально новой конст-
рукции— ПГС (предварительной газификации серы — рис. 33).
108
РИС. 33. Печь ПГС (с предварительной газификацией серы):
1 — испаритель; 2—плавильник: 3 — циклонная камера сжигания; 4 — вводы воздуха на
дожигание; 5 —камеры дожигания.
Печь представляет собой футерованный вертикальный цилиндрический
реактор с конической нижней частью, снабженной штуцером для вывода
шлама. Первичный воздух поступает в ванну для расплавленной серы, вто-
ричный — подается в надванное пространство. Реактор снабжен установлен-
ным соосно с ним цилиндрическим обечайкой-плавильником, образующим со
стенкой реактора кольцевой зазор. В верхней части обечайки-плавильника,
выведенной из печи, имеются отверстия для загрузки серы и вывода водя-
ных паров н возгонов, нижняя часть, закрытая решеткой, помещена в ванне.
Температура в испарителе 350—400 °C, в зоне обжига — 600—1100 °C.
Расход воздуха на испарение 1 т серы 100—280 м3/ч, на сжигание — первич-
ного и вторичного — по 2700—2500 м3/ч. Концентрация SO2 в газе 13—14%.
Печь работает следующим образом. После обычного разогрева ее запол-
няют жидкой серой до заданного уровня, затем подают первичный п вторич-
ный воздух. При этом в зависимости от давления, под которым работает
печь, в обечайке-плавильнике устанавливают определенный уровень жидкой
серы, который превышает уровень серы в корпусе печи на величину, соответ-
ствующую избыточному давлению. Таким образом образуется гидрозатвор,
109
so2
РИС. 34. Опытный комбинированный обжиговый
аппарат БКС (с барботажным КС):
1— корпус барботажного испарителя; 2— охлаждающая
рубашка; 3 — уровнемер; 4 — штуцер для разгрузки; 5 —
барботер; 6, 8, 10 — коллекторы ввода кислорода; 7 —
вихревая беспровальная решетка: 9, 11 — охлаждающие
элементы; 12 — штуцер для отбора газа; 13 — отбойиая
решетка; Ti—Те — термопары.
что позволяет без герметизации узла загрузки
питать печь твердой серой.
Нагрев и плавление серы ведут за счет теп-
ла обжиговых газов, омывающих обечайку-пла-
вильник, и частично за счет тепла горячей серы
(340—360 °C), находящейся в нижнем конце
этого аппарата. При этом происходит интенсив-
ное образование паров серы, которые затем сжи-
гают до SOj в токе вторичного воздуха в коль-
цевом зазоре между корпусом печи и обечайкой-
плавильником. Твердая сера, проходя обечайку
сверху вниз, нагревается и плавится, а содержа-
щиеся в ней влага и возгоны, например легколе-
тучие органические примеси, испаряются и выво-
дятся из верхней части обечайки-плавильника, не
смешиваясь с обжиговым газом. Минеральные и
высококипящие примеси постепенно оседают и
скапливаются в конической части, откуда выво-
дятся в виде шлама.
Таким образом, печь имеет сравнительно
простую конструкцию, компактна, может рабо-
тать ва любой сере, вплоть до сильно загрязнен-
ной, под давлением до 9,81 кПа (1000 мм вод. ст.) и давать практически
чистый и сухой газ.
Для получения высококонцентрированного диоксида серы
при сжигании серы в кислороде разработан способ, предусмат-
ривающий газификацию серы в барботажном слое и последую-
щее сжигание ее паров в кипящем слое инертного материала.
Схема опытного комбинированного аппарата БКС представлена на
рис. 34. Пары серы, образующиеся в испарителе, куда подается 5—7% всего-
кислорода, сгорают в кипящем слое при раздельной рассредоточенной по вы-
соте аппарата подаче кислорода и отводом избыточного тепла в холодиль-
ных элементах.
Для утилизации тепла в сернокислотных системах, работаю-
щих на сере, наибольшее распространение получили водотруб-
чатые котлы-утилизаторы (рис. 35) с естественной циркуля-
цией— СЭТА-Ц (разработка ЦКТИ) и ОИ-70-0Ю (поставки
ПНР), характеристика которого приведена ниже:
Выход пара, т/ч...............................63—68
Площадь, м2
котла (общая)............................... 1409
испарительной поверхности .................. 1043
пароперегревательной поверхности . . . 366
экономайзера................................ 1920
Давление пара, МПа (ат).........................4,0 (40);
Температура пара, °C......................... 440
Скорость газа, м/с........................... 5.5
Масса котла, т............................... 300’
ПО
РИС. 35. Котел-утилизатор типа ОИ-70:
1— печь; 2 — пароперегревательная поверхность котла; 3 — испарительная поверхность
котла; 4 — барабан котла; 5 — экономайзер.
11.3. ОБЖИГ СЕРНОЙ РУДЫ
Разрабатывается процесс прямой термической перера-
ботки серных руд в серную кислоту, а также в серную кислоту
и серу, минуя стадию получения серы [70].
В филиале НИУИФ руду с карбонатной основой и дальневосточную вул-
каногенную руду обжигали во вращающемся барабане диаметром 1 м и дли-
ной 7,5 м. Сырье загружалось в виде кусков размером до 100 мм. Обжиг
вели при 350—550 °C с недостатком воздуха и дожиганием паров после
очистки обжиговых газов от пыли. Это позволило снизить потери серы от
сульф атизации известняка, достигнуть извлечения серы из сырья 96—99% и
отказаться от сухого электрофильтра.
Опыты проведены с получением в качестве продукции серной кислоты
или серной кислоты и серы. В случае использования руд с карбонатной осно-
вой дополнительно получали обессеренный сухой известняк, пригодный для
получения стройматериалов и для применения в сельском хозяйстве.
Схема термической переработки серной руды сводится к следующему:
руду обжигают в противотоке с воздухом, образующийся огарок выгружают
при 250—300 °C и направляют на утилизацию. Газ на выходе из барабанной
печи (350—450 °C) содержит 20% SO2, пары серы, 20—30 г/м3 пыли, следы
сероводорода, пары воды. После сухого пылеуловителя содержание пыли
снижается до J—3 г/м3. Далее газ в смеси с воздухом подают в камеру
дожигания паров серы, где температура достигает 800—900 °C. Дальнейшую
переработку обжигового газа в серную кислоту проводят, например, по типо-
вой длинной схеме получения кислоты контактным методом. Если после пы-
леулавливания сконденсировать пары серы, получается серная кислота и сера.
Показатели процесса термической переработки серных руд
приведены ниже (содержание вредных веществ в газовых вы-
бросах и сточных водах не превышало ПДК):
И1
Степень извлечения серы, %......................98
Интенсивность обжига, т/(м’-сут)................Ю
Содержание SO2 в газе после камеры дожига, °/о • 12—14
Пылевынос из барабана, г/м3.....................20—30
Выход серы на 1 кг серы, окисленной до SO.,
кг..............................................1—5
Таким образом, достигнута в 10 раз более высокая интен-
сивность обжига, чем при обжиге колчедана в печах КС. Полу-
чаемая серная кислота соответствует требованиям ГОСТа, сера
не содержит органических примесей и легко доводится до сорта
9999, огарок представляет собой сухой известняк высшего сор-
та, пригодный для получения извести, цемента, а также для из-
весткования почв.
Термический метод обжига серной руды автотермичен для
руд с содержанием серы не менее 8% и влажности не более
10%. Возможность одновременного получения серной кислоты
и жидкой серы может дать большой экономический эффект на-
родному хозяйству. Результаты исследований используются для
внедрения разработанной технологии в промышленность.
Согласно последним разработкам, обжиг серной руды про-
водили в поступающем прямотоком предварительно подогретом
до 700 °C (за счет отходящих газов) воздушном дутье при
1100—1200°С в восстановительной среде, поддерживая моль-
ное соотношение оксид/диоксид углерода равным 0,01—0,05.
На 1 т руды, содержащей 20% S и 80% кальцита, подавали
895 м3 воздуха и 24 м3 природного газа. В результате обжига
получили газ, содержащий 13% SO2, 19,4% СО2, 0,4% СО и из-
весть, содержащую 75% активной СаО. Общие потери се-
ры 0,3%.
11.4. ОБЖИГ СУЛЬФАТОВ ЖЕЛЕЗА [70—73]
1; Процесс выделения SO2 из сульфата железа можно
вести в одну стадию—без предварительного’обезвоживания и
В1Две стадии — с предварительным обезвоживанием. Если суль-
фат извлекают из раствора в виде FeSO4-H2O, то предваритель-
ное обезвоживание не требуется, так как в этом случае содер-
жание воды в исходном материале составляет 10—11%. После
сушки и дегидратации FeSO4-7H2O в нем часто остается при-
мерно такое же количество воды. В исходном FeSO4-7H2O со-
держание воды составляет не менее 46%, а с адсорбированной
водой еще более.
На рис. 36 приведена дериватограмма сушки и обжига семи-
вбДного сульфата железа [72]. Эндотермический эффект до
1,00 °C соответствует потере гигроскопической влаги; эффекты
в.,интервале температур до 220—300°C соответствуют потерям
6 молекул воды. В пределах 300—320 °C теряется и последняя
молекула воды. При раздельных процессах разложения и суш-
ки, в аппарат разложения требуется подавать меньше топлива
и воздуха или топочных газов, что дает возможность получать
из печи разложения более концентрированный до SO2 газ.
РИС. 36. Дериватограмма нагре-
ва 7-ми водного сульфата желе-
за:
1 — кривая потерн массы; 2 — диффе-
ренциальная кривая прямого нагрева;
3— температурная кривая прямого на-
грева; 4 — дифференциальная кривая
потеря массы.
Оформление процесса разло-
жения сульфатов железа опреде-
ляется целями, которые при этом
ставятся, а также местными ус-
ловиями. Но во всех случаях
процесс должен быть организован
так, чтобы образующийся газ был
пригоден для получения серной
кислоты. Если, кроме того, ста-
вится задача получения чистого
огарка, то разложение надо вести
за счет теплоты сжигания чистого
газа или чистой серы в воздухе.
Целесообразно конечно выбирать
по возможности н более чистый
сульфат железа (купорос). Для
этого, по-видимому, будет более
пригоден купорос из травильных
растворов, чем отбросный купорос
от производства титановых белил.
Если задача получения чистого
огарка не ставится, то в качестве
источника тепла можно применять
и газ от обжига угля в воздухе,
жен также совместный обжиг купороса с пиритом, углистым колчеданом,
и грязной серой. Во всех случаях, где для этого есть возможность, целе-
сообразно использование отбросного нагретого воздуха. В случае примене-
ния в процессе серосодержащих веществ (сероводород, сера, колчедан) мож-
но получать более концентрированные по SO2 газы. При разложении суль-
фата с помощью высокотемпературного твердого инертного теплоносителя
(огарка) можно получать 100%-ный SO2.
Огарок следует подогревать газами от сжигания газообразного топлива.
При этом получающийся от разложения сульфата огарок может найти разно-
образное применение, а газы после нагрева огарка, останутся еще вполне
пригодными для сушки сырого купороса или для других целей.
Для исключения обратного соединения SO3 с огарком при понижении
температуры по тракту газа реактор необходимо выполнить в виде печи КС
с циклоном возврата, чтобы огарок в основном отбирался из самой печи (из
кипящего слоя).
Вопросам сушки и разложения сульфатов посвящено очень
большое число работ как зарубежных, так и отечественных.
Наиболее значительной работой за последние годы можно счи-
тать проведенные в НИУИФе исследования В. И. Якушева, до-
веденные до внедрения на сернокислотной системе большой
мощности.
Исследованиями процесса дегидратации семиводного сульфата железа
методом изотермической сушки продолжительностью до 26 ч установлено не-
прерывное удаление воды без образования промежуточных кристаллов. Ди-
8—584
И»
«фрактограммы конечных соединений при температурах 60, 80, 100, 120 °C
представлены веществом FeOHSO4. Образование моногидрата сульфата же-
леза подтверждается лишь в момент достижения потерь массы 35% и не-
значительной (до 60 мин) выдержке после этого. Затем моногидрат пол-
ностью переходит в FeOHSO4. В интервале 200—300 °C удаление 6 молей
происходит за 15—30 мин с образованием тех же продуктов, что и прн 60—
120 °C. Количественное соотношение этих продуктов зависит от длительности
сушки.
С учетом полученных данных схема термохимических прев-
ращений (60—400°C) описывается следующими реакциями:
60—300 “С
FeSO4-7H2O ------► FeSO4-H2O + 6Н2О
2FeSO4-H2O -f- 0,5О2 = 2FeOHSO4 + Н2О
300—400 “С
FeSO4 H2O -------► FeSO4 -|- Н2О
300—400 °C
2FeOHSO4 --------► Fe2O(SO4)2 + Н2О
Энергии активации (Е) процесса дегидратации для различ-
ных температурных интервалов (А/), рассчитанные с учетом
термогравиметрических данных, представлены ниже:
Л/, °C................... 40—100 100—200 200—340
Е, кДж/моль
(ккал/моль) . . . 95,5 (22.8) 157,1 (37,5) 166,0 (39,6)
Для изучения процесса термического разложения серосодер-
жащих отходов в качестве сульфатов железа использовали вы-
сушенную при 150—180 °C смесь семиводного и одноводного
сульфатов железа. Данные ТВА показали, что после сушки по-
лучено соединение FeSO4-1,36Н2О. Установлено, что процесс
термической диссоциации сульфатов железа в атмосфере возду-
ха описывается следующими реакциями:
200—260 °C
FeSC4-l,36H2O -------► FeSO4-H2O + 0,36Н2О
260—320 °C
FeSO4 Н2О ------> FeSO4 Н2О
360—460 °C
4FeSO4 + О2 ------► 2Fe2O(SO4)2
460-575 °C
5Fe20(S04)2 ------> 2Fe40(S94)5 + Fe2O3
575—800 °C
Fe4O(S34)5 ------->- 2Fe2O3 4- 5SO3
750—800 °C
SO3 ► SO2-[-0,5O2
Эти процессы являются основными при разложении сульфа-
тов железа. Вероятность протекания данных реакций подтвер-
ждается результатами термодинамического анализа.
При разработке технологии использования серосодержащих
отходов — сульфатов железа и углистого колчедана для произ-
водства серной кислоты, для лабораторных исследований были
114
РИС. 37. Зависимость степени обессеривания
от продолжительности обжига при различных
температурах:
/ — сульфат железа; 2 —шихта; 3 — углистый колче-
дан.
использованы сульфаты железа — от-
ходы производства пигментной дву-
окиси титана и обогащенный углистый
колчедан.
Образец углистого колчедана содержал
(в %): Soam —44,81; С — 5,30; Н2О —0,91; Fe
(на Fe2O2) — 56,94; СаО — 0,20; MgO — 0,04;
As — 0,0012; Си — 0,008; Si — 4,68; остаток не-
растворимый в соляной кислоте — 2,95%. Суль-
фаты железа (смесь из отвала хранилища се-
миводного сульфата железа и солей после упар-
ки гидролизной серной кислоты) по основным
компонентам содержали (в %): 5сульфатн —
18,76; Fe06m—31,60; Н2ОСвоб—31,80; H2SC>4cbo6—•
до 6,00.
Для исследования процесса термического
разложения сульфатов железа в присутствии
углистого колчедана смесь серосодержащих
отходов (шихта) при условиях автотермично-
сти (5су.1ьфатн/5сульфидн= 1 : 1,7) была подверг-
нута термической обработке в псевдоожижен-
ном слое. Обжигались образцы с размерами
частиц 0,5—0,25 мм и 2—1 мм, характерны-
ми для серосодержащих отходов. В качестве
ожижающего агента использовали воздух.
Для сравнения при тех же температурах в кипящем слое разлагали отдель-
но сульфат железа и углистый колчедан. Исследования проводили в темпе-
ратурном интервале 600—800 °C при продолжительности обжига от 5 до-
300 с.
С учетом результатов опытов процесс термического разло-
жения сульфатов железа при сжигании углистого колчедана
суммарно можно описать следующими реакциями:
4FeSO4- Н2О --► 2SO2 -% 2SO3 -% 2Fe2O3 -% 4Н2О
4FeS3 + 1Ю2 ---> 8SO2 -% 2Fe2O3
2C + 3O2 ---> 3CO2
___________________2SO3 --->- 2SO2 + O2_____________________________
4FeSO4-H2O + 4FeS2 + 14O2 + 3C -------------------------------------> 12SO2 -% 4Fe2O3 + 3CO2 + O2 -% 4H2O
Зависимость степени обессеривания сульфата железа, шихты
и углистого колчедана (0,5—0,25 мм) от времени обжига при
различных температурах (600, 650, 700, 800°С) представлена на
рис. 37.
Значительное отставание степени обессеривания сульфата железа (иа
15—20%) по сравнению с обессериванием шихты и углистого колчедана с
увеличением продолжительности обжига с 5 до 300 с сохраняется при тем-
пературах 600 и 650 °C. Продолжительность обжига свыше 120 с при 700 °C
и 5 с при 800 С не оказывает существенного влияния на степень обессерива-
ния. Так, при 700 °C за 120 с степень обессеривания образцов (а) находится
8*
115-
в пределах 98,12—98,91 %, а при 800 °C и продолжительности обжига т=5 с
а=96,3—97,8%. Увеличение степени обессеривания шихты объясняется, по-ви-
димому, тем, что разложение сульфатов железа проходит через стадию об-
разования SOg, а кислород в момент его выделения более активен, чем кисло-
род воздуха. Кислород, образующийся из сульфатов железа, окисляет около
10% поступающего колчедана.
Результаты лабораторных исследований были обработаны по методу наи-
меньших квадратов на машине «Раздан-3» с получением регрессионных урав-
нений, выражающих зависимость степени обессеривания (а, %) от темпера-
туры (/, °C) и времени (т, с) для сульфатов железа:
а2 = 3851,694 — 17,46014/ %- 0,322257т + 26 403-10~3/2 —
— 2,58- 10~4т2 — 1,3-10'5/3 — 2,92- 10-4/т -
ДЛЯ ШИХТЫ (5сульфати/5цирити—1 : 1,68) :
а2 = —239,20 %- 89,374 10'2/ + 13,322• 10~2т — 58,960• 10~6/2 -16,815-10~3Д
.для углистого колчедана:
а3 = —306,229 %- 1,0672/ + 25,609-10~2т — 70,072 • 10~5/2 — 33,410 • 10~5 Д
Уравнения справедливы в интервале температур 600—800 °C и прн про-
должительности обжига 5—300 с. Степень обессеривания частиц шихты раз-
мером 2—1 мм при температуре до 800°C ниже на 5—6%.
Скорость реакций определяли по количеству SO2, выделив-
шегося в газовую фазу из навески за определенный промежуток
времени. Полученный характер зависимости In К—1/7-104 —
прямая линия, показывает, что скорости реакций при обжиге
шихты, углистого колчедана, термическом разложении сульфа-
тов железа подчиняются уравнению Аррениуса. Энергия акти-
вации в кДж/моль (ккал/моль) составляет: для сульфата же-
леза— 90,0 (21,5); для шихты — 83,0 (19,8); для углистого кол-
чедана 63—125,7 (15—30).
па рис. оо представлены типичные кривые диффсрснциалыю-термического
(ДТА) н термовесового (ТВА) анализов семиводного н одноводного сульфа-
тов железа. Для исследованного образца FeSO4-H2O (вид а) определены
4 глубоких эндотермических эффекта: при 100 °C — потеря гигроскопической
н большей части кристаллизационной воды; при 320 °C — потеря последней
РИС. 38. Кривые днфференцпальнотермпческого (/) и термовесового (2)
анализов семиводного (п) п о щоводного (б) сульфатов железа.
116
Воздух
РИС. 39. Технологическая схема отделения подготовки и обжига сульфатов
железа:
2 —топка; 2— сушильный барабан; 3 — батарейный циклон; 4— тарельчатые питатели;
5 — печь КС-100; 6 — теплообменник; 7 — циклон; 8 — электрофильтр; 9, 10 — баки для
приготовления пульпы; Ц — напорный бак.
молекулы воды; при 540 °C — окисление сульфата до FeSOi, что сопровож-
дается небольшим прибавлением массы; при 700 °C максимальный эффект —
процесс разложения. Значительные потери массы одноводного сульфата же-
леза (б), наблюдаемые до 330°C, и эндотермический эффект при 120°C
обусловлены высокой исходной влажностью и кислотностью образца.
Опытно-промышленные исследования термического разложе-
ния сульфатов железа при сжигании углистого колчедана про-
ведены в печном отделении одного из сернокислотных цехов.
Использовали сульфаты железа — отход производства пигмент-
ного диоксида титана и углистый колчедан. Обжиговый газ пе-
рерабатывали в серную кислоту контактным способом по длин-
ной схеме. Огарок отправляли на цементный завод, где исполь-
зовали его в производстве цемента.
Принципиальная технологическая схема отделения подго-
товки сульфатов железа к обжигу и отделения обжига пред-
ставлена на рис. 39.
Сульфаты железа (семиводиый и соли после упаривания гидролизной
серной кислоты) для обеспечения нормальных условий их транспортирования
в сушильный барабан смешивают с ретуром — сухой шихтой, состоящей из
смеси сухого сульфата железа и колчедана. Сушку шихты ведут топочными
газами от топки в барабане. Отходящие газы после циклона выбрасываются
в атмосферу. Высушенную шихту тарельчатым питателем подают в печь
КС-100. Обжиговый газ после охлаждения в теплообменнике и сухой очистки
в циклоне и электрофильтре поступает в промывное отделение сернокислот-
ной системы. Подаваемый на дутье воздух нагревают до 300—350 °C за счет
охлаждения обжигового газа после печи. При организации раздельной дози-
ровки в качестве ретура при сушке сульфатов железа используют высушен-
ный сульфат железа.
Температуру кипящего слоя поддерживали в пределах 720—
860 °C, газы выходили пз печи при 780—830 °C. Содержание
117
диоксида серы в обжиговом газе после печи составляло 11,0—
15,4%, кислорода —2,6—6,3%, диоксида углерода 0,6—3,3%,
триоксида серы — до 0,1 %- Оксид углерода и сероводород не
обнаружены. Содержание серы в огарке после печи 0,45—1,02%,
углерод выгорает на 87,0—91,5%.
Условия автотермичного ведения процесса разложения сухих
сульфатов железа при сжигании смеси углистого и флотацион-
ного колчеданов обеспечиваются при соблюдении соотношения
Зсульфатн : 8сУльфндн= 1: 1,7—2,0. С увеличением доли углистого
колчедана в смеси расходный коэффициент по сульфату железа
увеличивается с 430 кг (применение флотационного колчедана)
до 793 кг на 1 т серной кислоты при использовании только уг-
листого колчедана.
На той же установке проведены испытания процесса пере-
работки сульфатов, подаваемых в печь КС в виде пульпы.
Пульпу готовят в баке или накопителе при 64—85 °C. Плав иасосом по-
дают в напорный бак или непосредственно в форсунку печи КС-100.
Полученный на основе семиводного сульфата железа и солей после упа-
ривания гидролизной серной кислоты плав (пульпа) при содержании 12,9—
16,8% H2SC>4cbo6; 41,1—45,8% HzSOtoBin; 38,0—43,4% FeSCU имел плотность
1,68—1,86 т/м3, кинематическую вязкость (1—2) • 10~6 м2/с, отношение
Ж/Т=1,6—2,4. Обжиг плава проводили при температуре кипящего слоя 690—
870 °C, температура газа на выходе из печи изменялась в пределах 720—
810 °C. Состав газового потока после печи: 11,0—15,0% SO2; 0,1—0,2% SO3;
10,0—16,0% Н2О; 2,1—4,3% О2; 1,4—3,9% СО2; остальное — Ы2; СО, Н2—ие
обнаружены. Содержание серы в огарке после печи не превышает 1,5%.
Использование серы в качестве восстановителя позволяет получить об-
жиговый газ с содержанием диоксида серы 16—20%. Испытания показали
принципиальную возможность термического разложения пульпы при сжига-
нии серы в печи КС.
На основе полученных данных построен промышленный цех
производства серной кислоты мощностью 1000 т/сут с двойным
контактированием. Серу сжигают в кипящем слое инертного
материала, куда вводят пульпу сульфатов. Использование суль-
фатов дало возможность работать со сниженным расходным
коэффициентом по сере, так как примерно 20% кислоты полу-
чается за счет сульфатов, и утилизировать отходы производст-
ва в виде сульфатов.
11.5. СЖИГАНИЕ СЕРОВОДОРОДА [9, 12]
Сероводород является сырьем для получения серной
кислоты (а также серы, получаемой по методу Клауса). Основ-
ные его константы [9] приведены ниже:
Молекулярная масса.................................... 34,08
Критические константы
температура, °C.................................... 100.4
давление, МПа (атм) ........................... 8,72(88,9)
плотность, г/см3................................... 0,310
Теплота плавления при —83,53 °C, кДж/моль
(ккал/моль)..................................... 2,380(0,568)
Теплота сгорания при атмосферном давлении с образо-
ванием SO2 и Н2О, кДж/кг (ккал/кг).............. 572,81(136,71)
118
Предельно допустимая концентрация сероводорода в воздухе
производственных помещений 10 мг/м3, в атмосферном воздухе
населенных пунктов 50 мг/м3, обнаруживается по запаху при
концентрации 2,3 мг/м3. Взрывоопасные концентрации сероводо-
рода в воздухе от 4,3 до 45,5% (об.). Температура самовоспла-
менения в смеси с кислородом составляет 220—235 °C, в смеси
с воздухом — 346—379 °C [9].
Максимальная скорость горения сероводорода (около
40 см/с) достигается в смеси, содержащей около 11% H2S; во
влажной газовой смеси (1,6% паров воды) скорость горения
уменьшается примерно на 25%.
Растворимость Р сероводорода в воде показана ниже:
t, °C............ 10 20 25 40 50 60 80 100
Р, мл/л .... 3399 2582 2282 1669 1392 1190 917 810
Сероводород является примесью газов природного, попут-
ного, коксового, генераторного и газов нефтепереработки. Обыч-
но эти газы содержат 0,3—1,5% H2S; имеются отдельные ме-
сторождения попутного газа, где концентрация H2S достигает
20%. Такой газ может быть переработан непосредственно в
серную кислоту по методу «мокрого катализа».
Сжигание сероводорода до SO2 проходит по реакции
H2S 1,5О2 = SO2 -|- Н2О 523,33 кДж/моль (124,9 ккал/моль)
При этом на 1 кг вещества выделяется следующее количе-
ство тепла (в МДж и ккал): чистый H2S— 15,420 (3680); сго-
рающая S—116,425 (3920); получаемый SO2 — 8,212 (1960).
Содержание кислорода в обжиговом газе при подаче воздуш-
ного дутья составляет
Со2 = 21 — 1,42SO2
и предельная (теоретическая) концентрация SO2, получаемого
по рассматриваемой реакции, равна 14,78%. Состав газа приве-
ден в табл. 20.
Температура газа /г на выходе из печи сжигания приближен-
но рассчитывается по следующей формуле, выведенной из
уравнения теплового баланса (формула выведена без учета
потерь тепла, передаваемого в окружающую среду 1 м3 серово-
дородного газа):
__ /с -р Ыь 167а
г— . а
1 + 6 — 200
где 6 — объем воздуха, затрачиваемого на сжигание 1 м3 исходного газа, м3.
Температуру в печи сжигания сероводорода поддерживают
обычно в пределах 900—1000°С, так как при более высокой
температуре и наличии избыточного кислорода возможна фик-
сация азота из воздуха с образованием нежелательной приме-
си NO в кислоте. Оксид азота может появляться в печном газе
119
Таблица 20. Состав газа, получаемого при сжигании сероводородного газа
в смеси с воздухом (в исходном газе 4% Н2О, в воздухе 1,5% Н2О)
Газ, содержащий 85% H2S Газ, содержащий 6% H2S
расход воздуха на м3 газа, м3 избыток воздуха а состав обжигового газа, % расход воздуха на м3 газа, м3 избыток воздуха а состав обжигового ' газа, %
so2 О2 I Н2О SO2 I о2 | н2о
6,164 1 12,61 0 14,38 0,435 1 4,27 0 7,58
7 1,14 11,22 2,28 13,14 0,5 1,15 4,08 0,91 7,31
8 1,30 9,91 4,43 11,78 0,6 1,38 3,82 2,17 6,54
10 1,62 8,04 7,50 9,83 0,7 1,61 3,59 3,28 6,62
12 1,95 6,76 9,60 8,51 0,8 1,84 3,39 4,26 6,33
14 2,27 5,83 11,12 7,55 0,9 2,07 3,21 5,14 6,07
16 2,6 5,13 12,28 6,82 1,0 2,3 3,05 5,93 5,84
также в результате сгорания примеси газа — синильной кис-
лоты
2HCN + 3,5О2 = 2NO + 2СО2 + Н2О
Поэтому вести сжигание сероводорода предпочтительнее при
невысоких температурах и подавать воздух ступенчато, тогда
синильная кислота при недостатке кислорода сгорает с образо-
ванием азота:
2HCN -4- 2,50, = N, + 2С0, + Н„0
РИС. 40. Схема двухступенчатой моноэтаноламнновой очистки газов:
/ — абсорбер I ступени; 2 — абсорбер II ступени; 3 — брызгоуловитель; 4 — отгонная ко-
лонна I ступени; 5 — отгонная колонна II ступени; 6 — сборник флегмы; 7 — холодиль-
ники; 8 — теплообменники; 9 — кипятильник; 10 — конденсатор.
120
Для обогащения слабых газов применяется в основном мо-
ноэтаноламиновый метод — одно или двухступенчатый, разрабо-
танный институтом Гипрогазоочистка [12]. Технологическая
схема двухступенчатого моноэтаноламинового способа обога-
щения изображена на рис. 40.
Исходный газ поступает последовательно в два абсорбера, затем в брыз-
гоуловитель и направляется на дальнейшую переработку. Абсорбер I ступе-
ни орошается 25—30%-ным раствором моноэтаноламина при 25—35 °C. Аб-
сорбер II ступени орошается при той же температуре 5—12%-ным раствором,
который поглощает остатки сероводорода и диоксида углерода и одновре-
менно улавливает пары этаноламина, увлекаемые газом из абсорбера I сту-
пени— вследствие высокого давления паров над концентрированным раство-
ром. Концентрированный раствор моноэтаноламина, содержащий поглощение
H2S и СОг, из абсорбера I ступени подается насосом или под давлением газа
(если газ находится под давлением) в отгонную колонну I ступени через теп-
лообменник.
Следует отметить, что абсорбционная способность водных растворов эта-
ноламинов по отношению к H2S и СО2 очень высока: 0,5 моля H2S или СО2
соединяются с одним молем этаноламина; особенно высокой поглотительной
способностью обладает моноэтаноламин NH3CH2CH2OH. Содержащиеся в га-
зе аммиак, смола и ароматические углеводороды не взаимодействуют с эта-
ноламинами.
Перед поступлением в отгонную колонну раствор подогревают в тепло-
обменнике за счет тепла регенерированного раствора, вытекающего из отго-
ночной колонны I ступени. В колонне десорбция HzS и СОг из раствора про-
исходит при температуре 115—120 °C, создаваемой за счет тепла вторичного
пара, который образуется в кипятильнике, обогреваемом глухим паром.
В нижнюю часть отгонной колонны поступают одновременно пары из отгон-
ной колонны второй ступени.
Парогазовая смесь из колонны I ступени поступает в конденсатор, где
охлаждается водой до 36—40 °C. При этом большая часть водяных паров
конденсируется, конденсат отделяется от газа в сборнике флегмы и возвра-
щается в отгонные колонны первой и второй ступени. Кислые газы, содержа-
щие H2S и СО2, направляются на использование. Раствор из абсорбера
II ступени через теплообменник поступает в отгонную колонну II ступени
на регенерацию, затем через холодильник возвращается в абсорбер II сту-
пени. Регенерация в колонне II ступени происходит при температуре 125—
130 °C, создаваемой за счет вторичного пара из соответствующего кипятиль-
ника.
Сероводородный газ, выделяемый при очистке технологи-
ческих или других газов, подразделяют на концентрированный
(90—94% H2S) и газ низкоконцентрированный (3—7% H2S).
Схема печного отделения для сжигания концентрированного
газа включает печь, котел-утилизатор и вентиляторы.
Печь, ввиду высокой взрывоопасности и токсичности образующихся сме-
сей, оборудуется мембранным клапаном-отсекателем, который автоматически
прекращает поступление сероводородного газа в печь при погасании в ней
пламени или нарушениях подачи воздуха. Импульсом к прекращению подачи
газа служит падение давления воздуха в трубке, соединяющей напорный
патрубок вентилятора для подачи воздуха и мембранное пространство кла-
пана-отсекателя.
Сероводородный газ подается в печное отделение под давлением 9,81—
11,77 кПа (1000—1200 мм вод ст.), температуру в печи поддерживают в
пределах 900—1000 °C, обжиговые газы охлаждают в котле-утилизаторе до
450—470 °C, при этом на 1 т кислоты образуется 0,7 т пара давлением
1,2 МПа.
121
Более совершенным агрегатом для сжигания сероводородно-
го газа является агрегат ПКС-10/40 (печь-котел для сероводо-
рода), в котором печь и котел-утилизатор объединены. При этом
значительно улучшились условия теплообмена и использования
тепла, сократился расход конструкционных материалов, упрос-
тилось обслуживание.
Агрегат имеет котел вертикального типа, водотрубный, двухбарабанный
с естественной циркуляцией. Он оборудован двумя горелками для подвода в
топку сероводородного газа и одной горелкой для растопочного газа, снаб-
жен двойным кожухом, внутри которого проходит воздух, поступающий за-
тем в печь.
Состав сжигаемого сероводородного газа: 91 % H2S; 6% СО2; 1 % Н2; 2%
углеводородов( С„Н„). Состав газа после котла: 10% SO2; 0,2% SO3, 74%
N2; 4,3% О2; 11,5% водяных паров.
Техническая характеристика котла ПКС-10/40 [9]
Паропроизводительность, т/ч................ 10
Давление пара, МПа.........................3,5—4,0
Температура, °C
перегретого пара .......................... 400—450
газа после печи............................. 1300
газа после котла............................. 520
Сопротивление по газовому тракту, Па (мм
вод. ст.).................................... 981(100)
Расход на сжигание, м3/ч
сероводородного газа................... 1600
воздуха..................................... 13000
Давление сероводородного газа, кПа (мм вод.
ст.).......................................9,81—11,77
(1000—1200)
11.6. ИСПОЛЬЗОВАНИЕ ТЕПЛА ГОРЕНИЯ СЕРОСОДЕРЖАЩЕГО
СЫРЬЯ
Обжиг серосодержащего сырья является экзотермичес-
ким процессом, при котором выделяется значительное количест-
во избыточного тепла. При обжиге колчедана в печах КС избы-
точное тепло горения утилизируется охлаждающими элемента-
ми, устанавливаемыми в кипящем слое, а тепло отходящих об-
жиговых газов — в котлах-утилизаторах, устанавливаемых за
печами КС. Охлаждающие элементы кипящего слоя вместе с
котлом-утилизатором оставляют единый циркуляционный кон-
тур.
Тепло процесса обжига используется главным образом для
получения пара. Причем, пар может быть получен как насы-
щенный, так и перегретый, т. е. пар энергетических парамет-
ров, пригодный для выработки электроэнергии. При сжигании
1 т серного колчедана в печах КС может быть получено 1,4 т
насыщенного или 1,2 т перегретого пара, что в пересчете на 1 т
серной кислоты составляет соответственно 1,15 т насыщенного
и 1 т перегретого пара. Основные параметры вырабатываемого
пара: насыщенный — Р = 4,0 МПа (40 ат), /=250°С; перегре-
тый— Р = 4 МПа (40 ат); /=440°C. При получении насыщен-
122
ного пара в кипящем слое устанавливают только испаритель-
ные элементы, а при получении перегретого — дополнительно
и пароперегревательные элементы, в которые из барабана котла
подается насыщенный naps
При конструировании и эксплуатации котлов-утилизаторов
необходимо соблюдать два основных требования: время пребы-
вания обжиговых газов в котле должно составлять 0,3—0,5 с
и давление пара в барабане поддерживаться не менее 2,5 МПа.
Минимально возможное время пребывания обжиговых газов
в котле определяется необходимостью максимально быстрого
охлаждения их до 430—450 °C для устранения побочных реак-
ций образования SO3 и сульфатизации огарковой пыли. При
давлении пара в барабане котла менее 2,5 МПа температура
металла будет ниже точки росы серной кислоты, что приведет
к конденсации ее паров на поверхностях нагрева и последующе-
му выходу их из строя.
В сернокислотных производствах, работающих на колчеда-
не, применяются два основных типа котлов-утилизаторов с есте-
ственной циркуляцией — газотрубчатые и водотрубчатые.
В вертикальных газотрубчатых котлах-утилизаторах теплообменные по-
верхности монтируют из унифицированных газотрубных секций типа «труба в
трубе». По внутренним трубам проходит обжиговый газ, а в кольцевом про-
странстве— нагреваемая и испаряемая вода. Концы двойных труб вварены
в нижние и верхние коллекторы, которые опускными и подъемными трубами
подсоединены к барабану котла. Конструктивно котлы-утилизаторы типа
ГТКУ могут быть одно- и двухходовыми. Устанавливаются они за печами
КС различной производительности — от 100 до 450 т/сут. Наибольшее рас-
пространение получили котлы ГТКУ-Ю/40-440 для печей КС-200 и
ГТКУ-25/40-440 для печен КС-450 (см. рис. 20).
Опыт эксплуатации газотрубчатых котлов в нашей стране
показал, что внутренние поверхности газовых труб необходимо
регулярно (примерно каждые 2—3 мес.) очищать от огарковых
отложений. Кроме того, котлы этого типа недостаточно герме-
тичны и имеют повышенное гидравлическое сопротивление. На
ряде заводов котлы ГТКУ-25/40-440 реконструированы с заме-
ной газотрубчатого блока на водотрубчатый ширменного типа.
Более эффективными в эксплуатации являются водотрубча-
тые котлы-утилизаторы, разработанные ЦКТИ им. И. И. Ползу-
нова совместно с Белгородским заводом энергетического маши-
ностроения. В котлах этого типа обжиговые газы проходят в
межтрубном пространстве, а охлаждающая пароводяная эмуль-
сия циркулирует внутри тепловоспринимающих устройств —
ширм, экранов и конвективных пучков.
В сернокислотных системах, работающих на колчедане, при-
меняются водотрубчатые котлы-утилизаторы КУКС и УККС,
КС ВТКУ (см. рис. 19). В отличие от газотрубчатых для их
изготовления требуется примерно в 2 раза меньше металла,
находящегося под давлением; практически полностью герметич-
ны; обладают незначительным гидравлическим сопротивлением,
123
Таблица 21. Характеристика котлов-утилизаторов
Показатели Газотрубчатые КУ к печам Водотрубчатые КУ к печи КС-450
2КС-200 | КС-450
Тип котла ГТКУ-Ю/40 ГТКУ-25/40 КС-450 ВТКУ
Поверхность котла, м2
общая 368 617 1070
испарительная 15 34 35
пароперегревательная 17 43 43
Масса котла, т ПО 200
Скорость газа в котле, м/с 20 20 3,5
Перепад давления, кПа 0,8—1,0 0,8—1,0 0,4—0,6
Давление пара, МПа 4,0 4,0 4,0
Температура пара, °C 450 450 450
Выход пара, т/ч 10,0—12,5 25 25
а также не нуждаются в чистке теплообменных поверхностей
е течение года.
В сернокислотных системах, работающих на сере, наиболь-
шее распространение получили водотрубчатые котлы-утилиза-
торы с естественной циркуляцией — СЭТА-Ц (разработка
ЦКТИ) и ОИ-70-010, поставки Польской народной республики
(см. рис. 35).
Основные параметры котлов-утилизаторов (КУ), устанавли-
ваемых за печами КС сернокислотных производств, приведены
в табл. 21.
11.7. ОЧИСТКА ОБЖИГОВОГО ГАЗА ОТ ОГАРКОВОЙ
ПЫЛИ [3, 4, 9, 75—77]
Обжиговый газ, поступающий на переработку, необходи-
мо тщательно очищать от пыли, которая снижает качество про-
дукционной серной кислоты, засоряет последующую аппарату-
ру, повышает ее гидравлическое сопротивление и создает ряд
других трудностей при эксплуатации. После сухой очистки ос-
таточная запыленность обжигового газа не должна превышать
0,1—0,2 г/м3.
Движение газа от печей КС в котлах-утилизаторах сопро-
вождается изменением направления на 180° и снижением ско-
рости с 15—20 до 3—5 м/с. При этом в бункер котла выпадает
20—25% огарка, а остальные 75—80% (примерно 210—
250 г/м3) улавливаются при сухой очистке [3]. Гранулометри-
ческий состав огарка (пыли) широкий — 10—300 мкм, поэтому
применяют ступенчатую очистку газа механическими и электри-
ческими способами. Наиболее крупные частицы огарка выделя-
ют из газового потока при использовании сил инерции в цикло-
нах. Существуют различные типы циклонов.
Наиболее совершенным является циклон ЦН-15 конструкции НИИОГАЗ
[9, 75—77]. Коэффициент полезного действия циклона ri (в %) определяют
124
как массовое отношение пыли, уловленной в циклоне бул, к пыли, поступив*
шей GBX за то же время:
j£L.100= Gbx-G^.1oo
G=x
где Gbux — масса пыли на выходе из циклона, кг.
Скорость газа в циклонах 7—20 м/с при гидравлическом сопротивлении
400 Па соответствует степени очистки от пыли размером 5—20 мкм 50—
99,5% [4]. После печей КС-450 устанавливают два циклона СК-ЦН-34 ди-
аметром 3600 мм. Запыленность газа после таких циклонов ие превышает
20—22 г/м3 и г] составляет около 90% [4].
Увеличение диаметра циклона снижает т|, но сокращает требуемое число
циклонов и, соответственно, подсос воздуха через запирающее устройство
под бункерами каждого блока. Подсос воздуха в местах спуска огарка обра-
зует поток навстречу уловленному огарку и может свести т] к нулю, если
подсос достигает 10—15% объема очищаемых газов. Наибольшая герметич-
вость циклонов обеспечивается при работе под давлевием или разрежением
до 2,5 кПа. Сокращение подсосов воздуха является важвым фактором по-
вышения качества сухой очистки обжиговых газов. Установка для сухой
очистки газов и конструкция циклонов показавы ва рис. 41.
После циклонов тонкую очистку обжигового газа осущест-
вляют в сухих электрофильтрах. Газ проходит между верти-
кальными электродами, один из которых заземлен (осадитель-
ный),^ другой соединен с отрицательным полюсом (корониру-
РИС. 42. Схема основных систем су-
хих электрофильтров:
а — трубчатый электрофильтр; б — пла-
стинчатый электрофильтр (стрелки показы-
вают направление потока электронов); V —
напряжение, приложенное к электродам;
— радиус трубчатого осадительного
электрода; г — радиус коронирующего
электрода; Н — расстояние между корони-
рующим и пластинчатыми электродами;
d — расстояние между коронирующими
электродами.
РИС. 41. Конструкция одиночного циклова НИИОГаза (а) и циклона
«СПОТ» (б).
125
тощий). Осадительные электроды бывают трубчатые и пластин-
чатые и вокруг них образуется корона — область характерного
свечения и звука. Лучшие условия для улавливания пыли обес-
печивают трубчатые осадительные электроды — благодаря пре-
имуществу в распределении электрического поля, однако их
применяют редко из-за высокой металлоемкости и трудностей
при встряхивании электродов. Основные системы сухих электро-
фильтров представлены на рис. 42.
Под действием электрического поля высокого напряжения у поверхности
коронирующих электродов в газах образуются ионы и электроны, сообщаю-
щие частицам пыли электрический заряд. Благодаря ионизации газов и за-
рядке частиц пыль переносится к осадительным электродам, оседает на них
и отдает им свой заряд. Обеспыленные газы выходят из фильтра, а уловлен-
ная пыль при встряхивании электродов ссыпается в бункер.
В печных отделениях используют горизонтальные по направлению дви-
жения газа многопольные пластинчатые сухие электрофильтры типа ОГ-3-15
и ОГ-4-16, УГТ-1-30-3 для очистки обжиговых газов при температуре до
400—450 °C и скорости газов 0,5—0,6 м/с и ниже. Электрофильтр питают по-
стоянным током от выпрямителей, предварительно повысив напряжение от
220—280 до 80—100 тыс. В. С печами КС устанавливают автоматизирован-
ные электроагрегаты с селеновым выпрямителем типа АФАС-80-250,
АФАС-80-400. Агрегат АФАС-80-250 позволяет получать постоянный ток
250 мА и напряжение 80 кВ с периодическим поиском возможного макси-
мального напряжения. Также выпускаются электроагрегаты типа АИФ, АУФ
и АТФ, снабженные полупроводниковыми выпрямительными устройствами.
Степень очистки газа зависит от многих факторов: от
свойств газа и пыли, загрязненности пылью электродов, скоро-
сти газа и равномерности его распределения и, самое главное,
от напряжения и силы тока.
Если повышается температура газа, то снижается напряжение на коро-
нирующих электродах, которое можно поддерживать без пробоя. Пробойное
напряжение примерно обратно пропорционально абсолютной температуре
газа. Однако при температуре ниже 275 °C возможна конденсация SO3, а
при температуре выше 425 °C на коронирующих электродах появляются твер-
дые наросты — «колбасы», что снижает очистку газа; кроме того, деформиру-
ются металлические конструкции. Влияние влажности газа на напряжение в
электрофильтре обратно влиянию температуры. Чем крупнее пыль, тем легче
и быстрее она улавливается в электрофильтре. Химический состав пыли влия-
ет на электросопротивление (проводимость частиц), например при повышен-
ном содержании оксидов и сульфидов свинца и цинка, проводимость частиц
снижается и ухудшается работа электрофильтра.
Для снижения конечной запыленности следует повышать
напряжение или увеличивать поверхность осаждения. Повыше-
ние содержания пыли, даже крупных фракций, повышает про-
странственный заряд, приводит к загрязнению электродов, па-
дению силы тока (запиранию короны) и ухудшению очистки,
так как ток начинает переноситься не ионами газа, а медленно
перемещающимися частицами. Увеличение напряжения на коро-
ширующих электродах повышает степень очистки газа от пыли
в электрофильтре в соответствии с уравнением [3]
2,3х 1g —
326
где Е — напряженность поля, В/см; V — разность потенциалов, В; х — рас-
стояние от центра трубы до точки измерения напряжения, м; R и г радиус
трубы и короиирующего электрода, м.
Скорость движения (дрейфа) частиц w (в см/с) радиусом1
от 1 до 50 мкм определяется по уравнению
0J1E2,-
w ----------
В
где Е—напряженность поля, В/см; г—радиус частицы, см; р, — динамиче-
ская вязкость газа, г/(см-с).
Фактическая скорость вдвое меньше рассчитанной по этому
уравнению. Теоретическую степень очистки газа г] в электро-
фильтре определяют по уравнению:
т] — 1 — ехр (—wf)
Значение коэффициента f для электродов различных видов оп-
ределяют по формулам:
2L L LS
t wR ' wH ? wQ
трубчатые пластинчатые шестигранные
где L, R, И и S — длина электрополя, радиус трубы, расстояние между оса-
дительным и короиирующим электродами и активный периметр осадительного'
электрода, м; ш — скорость газа, м/с; Q — площадь поперечного сечеиия оса-
дительного электрода, м2.
Хорошая очистка газов от пыли достигается при тщатель-
ном монтаже сухих электрофильтров, включении их в работу
после прогрева от пусковой топки и при стабильной работе всей
системы. Прогрев сухого электрофильтра до подачи в него об-
жигового газа способствует предохранению корпуса от корро-
зии. Это достигается также уплотнением термоизоляции в ко-
робах между ребрами жесткости на корпусе электрофильтра,,
например типа УГТ-Т-30, периодическим прокручиванием за-
порных устройств.
ГЛАВА III
ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫ КОНТАКТНЫМ
МЕТОДОМ
111.1. ТЕХНОЛОГИЧЕСКИЕ СХЕМЫ ПРОИЗВОДСТВА В СССР
И ЗА РУБЕЖОМ [78—87]
U аибольшее распространение в СССР и за рубежом:
получили системы производства серной кислоты из
газов от сжигания серы и обжига колчедана. Производство сер-
ной кислоты при использовании в качестве сырья колчедана осу-
ществляют по полной, так называемой, классической схеме. Та-
кая схема с одинарным контактированием изображена на
127,
Сырье
Кислота
на склад
РИС. 43. Схема производства серной кислоты из колчедана контактным
1, 12 — нагнетатели; 2 — печь КС; 3 — котел-утилизатор; 4 — циклон; 5 — сухой электро-
рофильтры; 9 — увлажнительная башня (в новых системах, работающих в испаритель-
лообменник; 14 — контактный аппарат; 15 — ангидридный холодильник (экономайзер);
ки; 19 — трубчатый холодильник; 20 — сборники кислоты.
рис. 43. Основные стадии процесса по данной схеме: обжиг кол-
чедана— очистка и осушка 502-содержащего газа — контактное
окисление SO2 в SO3 — абсорбция образовавшегося триоксида
серы.
Колчедан поступает в обжиговую печь, куда подают воздух. Образовав-
шийся БОг-содержащий (сернистый) газ охлаждают в котле-утилизаторе,
очищают от пыли в циклоне и сухом электрофильтре и направляют в про-
мывное отделение. Мокрую очистку газа от остатков пыли и вредных для
ванадиевых катализаторов примесей ведут в промывных башнях первой
ступени мокрых электрофильтров, увлажнительной башне и второй ступени
электрофильтров (8). Показанная на схеме увлажнительная башня имеется
на ряде действующих заводов, для вновь проектируемых установок ее не пре-
дусматривают за исключением тех случаев, когда в газах присутствует фтор
илн применяемая вода имеет температуру выше 30 °C, что связано с тем,
что в настоящее время в СССР и за рубежом работу промывных отделений
перевели на испарительный режим [87].
Затем газ освобождают от влаги в сушильной башне, а от брызг и тума-
на серной кислоты — в брызгоуловителе. Башни орошают серной кислотой по
циклу: сборник — насос — холодильник—башня — сборник (при работе холо-
дильника под давлением). Очищенный н осушенный сернистый газ нагнета-
телем подают в контактное отделение. Все оборудование до нагнетателя ра-
ботает под разрежением, после нагнетателя — под давлением.
В контактном отделении исходный сернистый газ нагревается в теплооб-
менниках до температуры зажигания катализатора и поступает иа окисле-
ние в контактный аппарат. При окислении на слоях катализатора темпера-
тура его повышается, поэтому газ охлаждают между слоями в промежуточ-
ных теплообменниках, а из последнего слоя образующийся триокснд серы
направляют на охлаждение во внешний теплообменник и ангидридный холо-
дильник и далее на абсорбцию SO3 в олеумный и моногидратный абсорберы.
Затем, после очистки от брызг и тумана серной кислоты в брызгоуловителе,
128
Олеум
на склад
способом:
фильтр; 6 — первая промывная башня; 7 — вторая промывная башня; 8 — мокрые элект-
ном режиме, таких башен нет); 10 — сушильная башня; 11 — брызгоуловителй; 13 — теп«
16 — олеумный абсорбер; 17 — моногидратный абсорбер; 18 — оросительные холодильни*
выхлопные газы выбрасывают в атмосферу с содержанием 0,15—0,3% SOj.
Вновь строящиеся сернокислотные цеха с одинарным контактированием
должны оборудоваться установкой улавливания SO2 из выхлопных газов до
его остаточного содержания 0,03%.
В процессе работы концентрации и температуры кислот в промывном
отделении повышаются за счет улавливания небольшого количества SO3 и
охлаждения газа. Для поддержания стабильного режима организован пере-
ток кислоты из увлажнительной башни в сборник 2-й промывной башни, из
последней — в сборник 1-й промывной башни, а в сборник увлажнительной
башни непрерывно добавляется вода. Циркулирующие кислоты пропускают
через холодильники. При поглощении кислотой влаги из газа в сушильной
башне концентрация кислоты снижается, а в процессе абсорбции SO3 кон-
центрация олеума и моногидрата в башнях повышается. Для поддержания
стабильного режима применяют кислотооборот между сушильной и абсорб-
ционной башнями и в систему добавляют воду.
При использовании данной схемы получают следующую продукцию: оле-
ум, серную кислоту концентрацией 92—94% H2SO4 и разбавленную промыв-
ную кислоту, которую на некоторых заводах осветляют и закрепляют про-
дукционной кислотой до 75 или 93% H2SO4.
По аналогичной полной схеме получают серную кислоту из
серы в тех случаях, когда сера содержит вредные для катализа-
тора примеси, например мышьяк. Если сера чистая, то для по-
лучения серной кислоты применяют короткую схему. Ниже
приведено краткое описание варианта с одинарным контакти-
рованием.
По этой схеме расплавленную отстоенную и отфильтрованную серу по-
дают на сжигание в печь, куда поступает воздух, осушенный в сушильной
башне. Образовавшийся сернистый газ после печи охлаждают в котле-утили-
заторе и пароперегревателе от 1000—1200 до 400—450 °C и направляют в
контактное отделение. Окисление SO2 производят в 5-слойном контактном
S—584 129
аппарате. Реакционный газ охлаждают после I слоя в пароперегревателе,
после II слоя — в теплообменнике, после III и IV слоев — поддувом воздуха.
После V слоя газ охлаждают во внешнем теплообменнике и ангидридном хо-
лодильнике и направляют в абсорбционное отделение, аналогичное полной
схеме.
Если сера содержит органические вещества (остатки флотореагентов) то
при их сгорании образуются пары воды и затем сернокислотный туман, за-
трудняющий абсорбцию триоксида серы. Для уменьшения количества тумана
абсорбцию иногда ведут в горячем режиме — при повышенной температуре
кислоты в башне от 70—80 до ПО—140 °C. Для поддержания такого режима
необходимо усиление футеровки аппаратуры и применение специальной схе-
мы с ретуром [78].
В связи с необходимостью снижения выбросов в атмосферу
соединений серы и повышения степени извлечения целевого про-
дукта, в последнее десятилетие в нашей стране и за рубежом
получила распространение технологическая схема с двойным
контактированием (ДК). Вариант короткой схемы установки
ДК, работающей на сере, приведен на рис. 44, а полной схемы
на колчедане — на рис. 45 [78—87]. Метод ДК позволяет до-
стичь того же минимального содержания SO2 в выхлопных га-
зах сернокислотного производства, что и после химической очи-
стки.
Метод основан на известном принципе Ле-Шателье, согласно
которому удаление одного из компонентов реакционной смеси
сдвигает равновесие реакции в сторону образования этого ком-
понента. Сущность метода заключается в проведении процесса
окисления диоксида серы с выделением триоксида серы в до-
полнительном абсорбере. На первой стадии проводят частичное
окисление SO2 и после охлаждения газа абсорбируют образо-
вавшийся SO3, а выходящую из промежуточного абсорбера га-
зовую смесь нагревают и направляют на вторую стадию окисле-
ния, затем газ вновь охлаждают и абсорбируют SO3.
РИС. 44. Схема производства серной кислоты из серы по методу ДК:
/ — серная печь; 2 — котел-утилизатор; 3 — экономайзер; 4—пусковая топка; 5, 6 — теп»
лообменники пусковой топки; 7 — контактный аппарат; 8 — теплообменники; *9 — сушиль-
ная башня; 10, 11— первый и второй моногидратные абсорберы; 12 — сборники кислотыв
13 — выхлопная труба.
130
РИС. 45. Схема отечественной системы ДК на колчедане:
1, 3 — первая н вторая промывные башни; 2 — оросительный холодильник; 4 — мокрые
электрофильтры; 5, 6 — увлажнительная и отдувочная башни (в новых системах» рабо-
тающих в испарительном режиме, увлажнительных башен нет); 7 — сушильная башня;
в — волокнистые фильтры; 9 — воздушные холодильники; 10 — нагнетатель; 11 — брызго-
уловитель; 12 — теплообменники; 13 — сборники; 14 — погружные насосы; 15 — контакт-
ный аппарат; 16 ~ олеумный абсорбер; 17 — моногидратный абсорбер I ступени; 18 — мо-
ногндратиый абсорбер II ступени.
Первая промышленная установка ДК была пущена в эксплуатацию в
начале этого столетия Союзом Мангеймских химических фабрик [1] с целью
только экономии дорогостоящего платинового катализатора. Но, поскольку
дополнительные затраты не окупались, метод не получил распространения и
вскоре был забыт. В начале 70-х годов метод был вновь возрожден в связи
с усилением требований по охране окружающей среды тенденциями значи-
тельного увеличения единичных мощностей и концентрации производств по
выпуску кислоты на больших комбинатах.
Метод ДК наряду со снижением содержания SO2 в выхлоп-
ных газах позволяет перерабатывать более концентрированные
газы, что дает значительный экономический эффект. Напри-
мер, если вместо газа, содержащего 7,5% SO2, перерабатывать
9 — 9,5%-ный газ, производительность системы возрастает на
20—25%. При этом по сравнению с использованием химических
методов очистки производительность труда возрастает на 30—
40%, снижаются удельные капитальные затраты — на 13—15%
и себестоимость продукции — на 13—16%.
Для газа, полученного от обжига колчедана в воздухе, об-
ласть оптимальных концентраций находится в интервале 9,0—
9,5% SO2, а для газа от сжигания серы — 10—11% SO2.
9*
131
Метод ДК в современном аппаратурном оформлении позво-
ляет получить степень конверсии, равную 0,995—0,999. Остаточ-
ное содержание SO2 при этом составляет 0,02—0,05%. Химичес-
кие способы очистки позволяют снизить содержание SO2 в от-
ходящих газах в соответствии с парциальным давлением SO2
над поглотительными растворами до 0,02%-
По методу ДК на первой ступени процесса на двух-трех сло-
ях катализатора степень конверсии составляет 0,9—0,95. Содер-
жание SO2 в газе после промежуточного абсорбера — около 1%.
Большой избыток кислорода позволяет на второй стадии про-
цесса получить степень конверсии на одном слое катализатора
до 0,95 и более, на двух слоях — до 0,98.
Суммарную степень конверсии при ДК определяют по фор-
муле
•’Общ = Х1 + (1 *1) Х2
где .V] и х-2 — степени конверсии на первой и второй ступенях процесса.
Концентрация SO2 и О2 после промежуточной абсорбции
находят из уравнений
а(1—хх) Ь—0,5ахх
а' = ! —1,5ахх b' = 1 — 1,1ахг
Концентрацию этих компонентов в выхлопных газах опре-
деляют из аналогичных уравнений, только вместо Xi использу-
ют значение хОбщ.
Получение серной кислоты по методу ДК несколько слож-
нее, чем при одинарном контактировании из-за большей тепло-
обменной поверхности, что вызвано необходимостью двукратно-
го нагревания газа до температур реакции, а также наличия
дополнительного абсорбера. Кроме того, при ДК предъявляют-
ся высокие требования к очистке газа, выходящего из проме-
жуточного абсорбера, от брызг и тумана серной кислоты и осу-
шке исходного газа. Необходимая теплообменная поверхность
в установках ДК зависит от концентрации SO2 в исходном га-
зе и от технологической схемы контактного узла. Изменение
температурного режима в слое катализатора существенного
влияния на эту величину не оказывает.
Установки ДК различаются общим количеством слоев ка-
тализатора, распределением их по ступеням и схемами теплооб-
мена между газовыми потоками. Число слоев катализатора в
контактных аппаратах систем ДК принимается равным 4—5,
распределение слоев по стадиям может быть, например, 2 + 2,
или 3+1 и т. д. Расчеты показывают, что схема 2 + 2 требует
наибольшего расхода катализатора и теплообменной поверхно-
сти. Для схем 3+1 и 3 + 2 суммарная поверхность теплообмен-
ников примерно одинакова, но в схеме 3 + 2 масса загружаемого
катализатора примерно на 15% меньше. Кроме того, два слоя
катализатора на второй ступени обеспечивают меньшую чув-
ствительность процесса к изменению условий эксплуатации.
132
РИС. 46. Схема узла ДК фирмы «Лурги»:
/ — фортеплообменник; 2 — теплообменники; 3 — контактный аппарат; 4 —абсорбер.
Поэтому в СССР была принята схема 3 + 2. Для упрощения
этой схемы перед V слоем охлаждение можно проводить не в
теплообменнике, а путем поддува части холодного газа, посту-
пающего из промежуточного теплообменника, что незначитель-
но изменяет содержание SO2 в выхлопных газах. Температуры
газовых потоков, поступающих на промежуточную и конечную
абсорбцию, ниже, чем при одинарном контактировании.
Высокие технологические показатели и отсутствие необхо-
димости в очистке выхлопных газов являются основой широко-
го применения схем ДК- В связи с повсеместным возрастанием
интереса к методу ДК разработаны разнообразные варианты
технологических схем, принципиальные отличия которых про-
являются прежде всего в компоновке контактного и абсорбци-
онного отделений [78—80]. Условно все схемы можно разделить
на схемы, работающие на холодном сернистом газе (после про-
мывки и осушки), и схемы, работающие на горячем газе. Для
удобства рассмотрения схем внешние теплообменники, состоя-
щие из двух последовательно включенных аппаратов, на рисун-
ках изображены в виде одного аппарата.
Схемы на холодном газе. Технологическая схема узла ДК,
построенного фирмой «Лурги» по разработкам фирмы «Байер»,
представлена на рис. 46.
В данной схеме принят вариант слоев катализатора 3+1. Нагревание
газа, поступающего на первую стадию катализа, осуществляется в фортепло-
обменнике, теплообменниках после IV, I и II слоев катализатора, а газа, вы-
ходящего после первого абсорбера, — в фортеплообменнике и теплообменнике
после III слоя. Степень превращения газа с содержанием 9,0—9,5% SO2
после первой стадии катализа 90—92% и общая 99,5%. Одним из способов
регулирования режима в процессе работы контактного аппарата является из-
менение объема исходного газа, поддуваемого после I слоя. Оба фортеплооб-
менника — небольшие по размеру, легкозаменяемые — предохраняют от об-
разования конденсата серной кислоты, сульфатов н коррозии в следующих
за ними, более крупных теплообменниках.
Нагревание газа, выходящего из первого абсорбера, в теплообменнике
после одного только III слоя уменьшает теплопередачу и увеличивает по-
верхность теплообмена:
133
где А — безразмерный параметр, характеризующий мощность теплообменни-
ка (2.1— всех теплообменников схемы, 24 = 5,8); К — коэффициент теплопе-
редачи, Вт/(м2-град); F—поверхность теплообмена, м2; Vo — объем газа, м3;
Ср —теплоемкость газа, Дж/(м3-град).
При коррозии в фортеплообменниках в трубки поступает газ
с содержанием 9—9,5% SO2, что снижает степень превраще-
ния, как и поддув исходного газа после I слоя.
Технологическая схема узла ДК, разработанная фирмой
«Парсонс» (США) для варианта слоев 3+1, представлена на
рис. 47.
Нагревание газа, поступающего на первую стадию катализа, осуществ-
ляется в теплообменниках после III и I слоев катализатора, а выходящего
после первой абсорбции — в теплообменниках после V, IV и I слоев (после
I слоя установлено два параллельных теплообменника). Между II и
III слоями установлены газовоздушные теплообменники. Степень превраще-
ния на первой стадии катализа 97%, общая — 99,8—99,9% при содержании
в исходном газе 8,5% SO?. Концентрация SO2 невысокая, отвод тепла после
II слоя воздухом нерационален для схемы ДК, а поверхность теплообменни-
ков высокая (24 = 5,9). Не исключается конденсация кислоты во внешних
теплообменниках и необходимость ежегодной замены катализатора I слоя для
достижения высокой степени превращения.
Технологическая схема узла ДК сернокислотной системы,
построенной в СССР по проекту и поставкам ПНР (лицензия
фирмы «Дорр — Оливер») имеет вариант слоев катализато-
ра З+Д.
Нагревание газа, поступающего на первую стадию катализа, производит-
ся в теплообменниках после III и I слоев, а газа, выходящего из первого
абсорбера, — в теплообменниках после IV и II слоев. Температура газа на
входе в первый абсорбер 200 °C, во второй — 170 °C. При содержании в газе
8,5% SO2 проектная степень превращения на первой стадии катализа 93%,
общая — 99,5%, а поверхность теплообменников на 10% меньше, чем в схе-
мах фирм «Лурги» и «Парсонс». Во внешнем теплообменнике перед второй
стадией абсорбции нагревается низкоконцентрированный газ, что исключает
большое снижение степени превращения при коррозии трубок.
Технологическая схема узла ДК отечественной системы с
вариантом слоев 3 + 2 представлена на рис. 48.
Нагревание газа, поступающего на первую стадию катализа, осуществ-
ляется в теплообменниках после III и I слоев, а газа из промежуточной аб-
сорбции— в фортеплообменнике после III слоя и теплообменниках после V,
IV и II слоев. Расчетная степень превращения для газа с содержанием 9%
SO2 составляет 99,7—99,8%, поверхность теплообменников относительно не-
велика (24 = 5,2), а применение двух слоев на второй стадии катализа спо-
собствуют повышению надежности контактирования.
А'з вторую
абсорбцию
РИС. 47. Схема узла ДК
фирмы «Парсонс»:
1 — теплообменник; 2 — контакт-
ный аппарат; 3 — газовоздушный
теплообменник; 4 — абсорбер.
131
SO2 '7^ *'777/77
РИС. 48. Схема узла ДК отечественной системы на сере:
1—4 — теплообменники; 5 — контактный аппарат.
Для переработки газа с более высоким содержанием SO2
схема, приведенная на рис. 48, видоизменяется с целью повыше-
ния устойчивости I слоя.
Исходный газ нагревают в теплообменниках после III и II слоев, а газ
после промежуточной абсорбции — в теплообменниках после V, IV и I слоев.
В теплообменнике после I слоя теплообмен между газом, поступающим на
I слой и выходящим из I слоя, отсутствует.
Зарубежные и отечественные схемы различаются организа-
цией теплообмена, обеспечивающего автотермичность процесса,
способами предотвращения коррозии теплообменников, числом
слоев катализатора на первой и второй стадиях катализа. Эти
три фактора тесно связаны между собой, однако теплообмен
при нагреве исходного газа в теплообменнике за счет охлажде-
ния низкоконцентрированного газа перед второй абсорбцией
нецелесообразен, так как при возможной в этих условиях кор-
розии трубок существенно повышается содержание SO2 в отхо-
дящих газах.
Защита теплообменников от коррозии и повышение тепловой
устойчивости системы ДК возможно путем проведения горячей
абсорбции, подогрева газа после промежуточного абсорбера
в фортеплообменнике или рекуператоре за счет тепла высоко-
температурного газа, или других источников — водяного пара,
электроэнергии. В отечественных схемах принято нагревание
газа после промежуточной абсорбции в фортеплообменнике, в
основном газом, выходящим из контактного аппарата. В значи-
тельной мере тепловая устойчивость схем ДК определяется со-
стоянием теплоизоляции, поэтому необходимо ее качественное
выполнение и поддержание в исправности при эксплуатации.
Схемы на горячем газе. Технологическая схема узла ДК
фирмы «Парсонс», работающего на горячем газе от сжигания
серы, имеет вариант слоев 3+1.
Исходный газ перед поступлением на I слой охлаждается в теплообмен-
нике. Газ из первого абсорбера нагревается в теплообменнике до и после
I слоя. После II слоя газ охлаждается в пароперегревателе, после III и
135
so2
РИС. 49. Схема узла ДК на газе от сжигания серы (проект ПНР):
1 — теплообменники; 2— контактный аппарат; 3 — фортеплообменник; 4 — газовоздушные
теплообменники; 5 — экономайзер; 6 — абсорбер.
IV слоев — в экономайзерах. Подогрев газа с первой стадии абсорбции в
теплообменнике при температуре до 620 °C уменьшает количество теплооб-
менников и их стоимость. В схеме облегчается возможность поддерживать
оптимальную степень превращения на первой стадии катализа, так как нет
необходимости в высокой температуре III слоя для нагрева газа перед
IV слоем.
На рис. 49 представлена технологическая схема узла ДК,
работающего на газах от сжигания серы на ряде заводов СССР
по проекту и поставкам ПНР, с вариантом слоев 3+2.
Газ из печи поступает на I слой после охлаждения в котле-утилизаторе.
После первой стадии абсорбции газ нагревается в фортеплообменнике, рас-
положенном за III слоем и в теплообменниках после II и I слоев. Для ох-
лаждения газа перед первой стадией абсорбции до 226 °C применяют также
газовоздушные теплообменники, а перед второй стадией абсорбции — эконо-
майзер; требуемая поверхность теплообменников невелика (24=4,9). Сте-
пень превращения при работе на газе с содержанием 9,5% SO2 на первой
стадии катализа составляет 92—95%, и общая — 99,4—99,8%. Высокая тем-
пература газа, поступающего на абсорбцию, уменьшает опасность осаждения
тумана в теплообменниках, однако увеличение влажности газа при окисле-
нии органических примесей серы повышает точку росы паров серной кисло-
ты и количество тумана, образование тумана возрастает также при сниже-
нии эффективности демистеров.
Схемы получения серной кислоты из чистой серы гораздо
проще, чем полные схемы с переработкой холодного газа, по-
ступающего в контактное отделение. В короткой схеме ДК газ
нагревается только перед второй стадией катализа, что повы-
шает тепловую устойчивость системы, снижает поверхность
теплообмена (SA— от 5,2—5,9 до 4,9), повышает надежность
управления режимом работы контактного и абсорбционного от-
делений.
Ориентировочные температуры газа перед промежуточной и
конечной абсорбцией в схемах ДК при различной концентрации
136
исходного газа (температура газа после компрессора и абсор-
беров 60 °C) приведены ниже [3]:
6
б'зОг- % • •
Т, °C . .
153 168
9
204
10
220
11
12
248
7
В схемах, работающих на горячем газе, очистка от тумана
так же важна, как и в схемах на холодном газе, и применение
горячего режима абсорбции может быть средством повышения
надежности работы теплообменников и снижения вредных вы-
бросов в атмосферу.
Технология серной кислоты за рубежом существенно не от-
личается от отечественной, но в схемах есть значительные раз-
личия в аппаратуре.
Обжиг сырья проводят в печах КС с промывкой газа в испарительном
режиме. В промывном отделении широко применяют трубу Вентури и аппа-
рат «Свемко», промывную кислоту фильтруют; охлаждают ее только во вто-
рой стадии промывки—в холодильниках «Сигри» [75]. Отдувку SO2 прово-
дят не только из сушильной, но и из промывной кислоты, что повышает из-
влечение серы. На некоторых заводах вместо второй промывной и увлажни-
тельной башен ставят газовые холодильники и вместо двух — одну ступень
электроочистки; известна система с подачей колчедана в виде пульпы с до-
бавлением промывной кислоты в печь КС [75]; выхлопные газы чаще всего
очищают в бисульфитных установках. За рубежом все шире используют вто-
ричные энергоресурсы; применяют насосы и холодильники, устойчивые при
температуре кислоты 120 °C, различные усовершенствованные насадки пра
плотности орошения до 35—37 м3/(м2-ч) [75].
Схема получения серной кислоты из сероводорода методом
мокрого катализа представлена на рис. 50 [12]. Метод мокрого
катализа получил свое название в связи с тем, что окисление
диоксида серы на ванадиевом катализаторе проводят при зна-
чительном содержании в газе паров воды — около 7%.
Газы, содержащие сероводород, бывают концентрированны-
ми (до 90% H2S) и слабыми (6—10% H2S). Процесс перера-'
ботки сероводорода состоит из следующих стадий: сжигание се-
РИС. 50. Схема производства серной кислоты из сероводородного газа вы-
сокой концентрации:
7 —фильтр; 2 — вентилятор; 3 — печь; 4 — котел-утилизатор; 5 —контактный аппарат:
б — холодильник; 7 — башня-конденсатор; 8 — электрофильтр; 9 — циркуляционный сбор*
ник; /0 —насос.
137 .
роводорода, контактное окисление SO2 в SO3 и его выделение
из газов.
При высокой концентрации H2S схема его переработки соответствует
рис. 50. Очищенный в фильтре воздух вентилятором подают в печь для сжи-
гания сероводорода. Образовавшийся сернистый газ охлаждают в котле-ути-
лизаторе от 1000 до 400—450 °C и подают в контактный аппарат. Между
слоями катализатора реагирующую смесь газов охлаждают добавлением хо-
лодного неосушенного воздуха. Из контактного аппарата прореагировавший
газ поступает в насадочную колонну — башню-конденсатор, орошаемую сер-
ной кислотой. Температура орошающей кислоты на входе в башию 50—60 °C,
на выходе 80—90 °C. Большая часть триоксида серы поглощается в башне-
конденсаторе, а меньшая часть (30—35%) соединяется с парами воды и
образует сернокислотный туман, который затем улавливают в мокром элект-
рофильтре.
Схема получения серной кислоты из слабого сероводородного газа от-
личается от описанной схемы тем, что воздух в печь подают после его нагре-
вания в теплообменниках газом после слоев катализатора (аналогично корот-
кой схеме, работаюшей на сере), а процесс конденсации SOa проводят в бар-
ботажном конденсаторе типа концентратора «Хемико». Газ последовательно
проходит три камеры барботажного аппарата, в которых температура сни-
жается от 230—240 до 100 °C и концентрация кислоты от 93,5 до 30% H2SO4.
Так как в барботажном конденсаторе тепло отводится испарением воды, то
поверхность холодильников сокращается в 15 раз по сравнению с башней-
конденсатором. Концентрация SO2 перед контактным аппаратом установок
мокрого катализа 2,5—5,5%, степень превращения SO2 в SO3 97,5—98,5%.
Для получения кондиционной серной кислоты из отработан-
ных кислот их подвергают термическому разложению в печи.
Для этой цели кислоту вместе с топливом подают в печь, где при тем-
пературе около 1200 °C органические примеси разлагаются по реакции [12]:
2H2SO4 4- С = 2SO2 + 2Н2О + СО2
Образующийся сернистый газ охлаждают в рекуператоре, нагревая воз-
дух, подаваемый в печь, а затем перерабатывают по классической схеме.
Если в образовавшемся сернистом газе отсутствуют примеси, вредные для
сернокислотного катализатора, то целесообразно использовать более простую
схему мокрого катализа.
Серную кислоту можно получать из топочных газов ТЭЦ по
схеме, включающей: систему сухой очистки газов от пыли, кон-
тактный аппарат, конденсатор-теплообменник, систему мокрой
очистки от брызг и тумана серной кислоты.
Опытная установка по такой схеме испытана при работе под давлением
до 0,4 МПа и использовании катализатора СВД в виде колец размером
18X18X4 мм и гранул. При содержании в газе 0,03—0,17% SO2 степень
превращения составила 82—95% [82]. Для получения серной кислоты из низ-
коконцентрированных газов различных отраслей промышленности могут при-
меняться разнообразные методы предварительного обогащения SO2 и после-
дующей его переработки известными способами. Возможно и гщименение ме-
тода конденсации SO2 с получением жидкого диоксида серы. В процессе из-
влечения SO2 и его концентрирования удаляют вредные для контактной
массы примеси [75]. Данные о рентабельном производстве по такой схеме
отсутствуют.
111.2. МОКРАЯ ОЧИСТКА ОБЖИГОВОГО ГАЗА [4, 9, 12, 75, 87—91]
Основы процесса очистки газа. После сухой очистки об-
жиговый сернистый газ проходит промывное отделение, где очи-
щается от остатков пыли и SO3, а также от примесей, которые
138
отравляют ванадиевые сернокислотные катализаторы и загряз-
няют кислоту—мышьяк, фтор и др. Из промывных кислот це-
лесообразно извлекать ценные металлы — селен, теллур и др.
Содержание пыли в газах, поступающих в промывное отде-
ление сернокислотного производства, не должно превышать
0,2 г/м3. Эта пыль практически полностью вымывается серной
кислотой в промывных башнях. Несмотря на наличие отстой-
ников (сборников) в циклах промывных башен, примеси, вымы-
ваемые из газа кислотой, осаждаются и выкристаллизовывают-
ся в башнях, электрофильтрах, кислотопроводах, распылителях,
холодильниках и т. д. Поэтому оборудование промывного отде-
ления периодически тщательно очищают — пропаривают и про-
мывают.
Содержание железа, взвешенных частиц и твердого остатка
после прокаливания в промывной кислоте зависит от содержа-
ния пыли в газе на входе в промывное отделение и режима мок-
рой очистки. При запыленности газа 0,05 г/м3 и выводе про-
мывной кислоты в количестве около 2°/о от выработки моногид-
рата, содержание в ней железа составляет 0,022%. Осадок
промывной кислоты представляет собой в основном соединение
Ее2(5О4)з-9Н2О. Повышение запыленности газа в значительной
мере влияет на качество продукции при закреплении промыв-
ной кислоты, так как вся пыль улавливается кислотой. На
практике отсутствие осаждения сульфата железа при закрепле-
нии промывной кислоты достигается при запыленности газа ме-
нее 0,1 г/м3.
Содержание SO3 в газах от обжига колчедана в печах КС
не превышает 0,5%, как правило, оно находится в пределах
0,1—0,3%. В газах от сжигания серы содержится незначитель-
ное количество SO3 — менее 0,1%. Триоксид серы соединяется
с парами воды с образованием паров серной кислоты, которые
конденсируются при охлаждении в промывных башнях. Образу-
ющийся туман серной кислоты частично поглощается в промыв-
ных башнях, что может повышать концентрацию промывных
кислот, а полностью выделяется в мокрых электрофильтрах.
Содержание тумана серной кислоты в газе на входе в контакт-
ный аппарат не должно превышать 5 мг/м3, так как туман вы-
зывает коррозию металла и попадание образовавшихся сульфа-
тов на I слой катализатора.
В газах после печей КС содержится 300—400 мг/м3 мышья-
ка. С повышением концентрации SO2 в газах снижается содер-
жание кислорода и увеличивается содержание мышьяка [85].
В газах от сжигания сильно загрязненной серы перед промыв-
кой может содержаться до 80 мг/м3 и более мышьяка [21]. По
установленным нормам после промывного отделения допускает-
ся не более 0,02 г As2O3 на 1 м3 газа, а перед контактным ап-
паратом мышьяк должен полностью отсутствовать. Часть три-
оксида мышьяка в газо- и парообразном состоянии растворя-
ется в промывной серной кислоте. В кислоте, вытекающей из
139
РИС. 52. Зависимость растворимости диоксида селена и триоксида мышьяка
от температуры промывной кислоты.
РИС. 51. Зависимость растворимости триоксида мышьяка в серной кислоте
до температуры и концентрации кислоты.
сборника первой промывной башни, может содержаться около
1% (20 г/л) As2O3 [12, 75]. При охлаждении этой кислоты
часть мышьяка выпадает в осадок, так как растворимость
As2O3 уменьшается с понижением температуры (рис. 51) [75].
Выпадающий осадок мышьяка оседает в холодильниках, кис-
лотопроводах и аппаратуре и может нарушать ритмичность
процесса. Большая часть поступивших с газом соединений
мышьяка конденсируется и растворяется в сернокислотном ту-
мане, который затем улавливается в электрофильтрах.
В колчедане содержится 0,002—0,02% селена, который при
обжиге в печах КС примерно на 45% остается в огарке и пыли,
а также переходит в газ в виде SeO2. Диоксид селена из газо-
и парообразного состояния частично («50%) переходит в сер-
ную кислоту, орошающую башни, а частично («50%) в серно-
кислотном тумане. Растворимость SeO2 в серной кислоте вы-
сока и возрастает с повышением температуры (рис. 52). Диок-
сид серы, растворенный в промывной кислоте, восстанавливает
диоксид селена по реакции
SeO2 4- 2SOa 4- 2Н2О = Se| 4- 2H2SO4
Металлический селен выпадает в осадок в аппаратуре про-
мывного отделения, особенно в мокрых электрофильтрах, где
улавливается сернокислотный туман.
J4Q
Фтор попадает в обжиговый газ при обжиге сырья, где он
содержится в виде CaF2:
CaF2 + Н2О <=> СаО + 2HF
Колчедан содержит 0,003—0,04% CaF2, а после его обжига
в печах КС газы содержат 8—20 мг/м3 фтора. Степень выделе-
ния фтора в газ составляет 20—60% [86]. Выделение фтора в
газ можно сократить до 1—2 мг/м3 при низкотемпературном
обжиге (600°C и ниже). Фторид водорода, взаимодействуя с
кремнеземом сырья, образует четырехфтористый кремний:
SiO2 + 4HF <—> SiF4 + 2Н2О
Обжиговый газ содержит 80—90% фтора в виде HF и 10—
20%—в виде SiF4 [9]. Фтор интенсивно разрушает аппаратуру
и катализатор, взаимодействуя с металлами и диоксидом крем-
ния. Остаточное содержание фтора после очистки газа не долж-
но превышать 1 мг/м3. Вопросы, связанные с очисткой обжиго-
вого газа от соединений фтора, подробно рассмотрены в раз-
деле, посвященном получению серной кислоты из отходящих
газов металлургических производств. Большая часть фтора пог-
лощается из газов кислотой в промывных башнях, а некото-
рая— с туманом извлекается в мокрых электрофильтрах.
Туман образуется при механическом дроблении жидкости и
конденсации паров. Конденсация паров происходит на поверх-
ности и в объеме, если пересыщение пара выше критического
значения. Расчетом можно определить условия предотвращения
образования тумана.
Пример [75]. Газ, содержащий 22,8 г/м3 паров серной кислоты, при тем-
пературе 200 °C проходит через 95%-ную кислоту при температуре 120 °C.
В результате охлаждения газа на поверхности кислоты конденсируется
9,2 г/м3 пара. На выходе из аппарата, в котором происходит контакт газа с
кислотой, в газе будет содержаться 22,8—9,2=13,6 г/м3 (2,37 мм рт. ст.) па-
ров серной кислоты. Возникающее пересыщение, вычисляемое по формуле
s=p : ра, равно 2,37 : 0,824 и составляет 2,87, где 0,824 — давление насыщенно-
го пара H2SO4 над 95%-ной серной кислотой при 160 °C [12].
Критическое пересыщение, соответствующие 160 °C, составляет 2,8, т. е.
возникающее пересыщение превышает критическое значение, а следовательно,
на выходе из аппарата образуется туман серной кислоты.
Если температуру газа понизить не до 160, а до 180 °C, то при этом
5,64 г/м3 (0,98 мм рт. ст.) паров H2SC>4 конденсируется на поверхности кис-
лоты. На выходе газ будет содержать 22,8—5,64=17,16 г/м3 (2,98 мм рт. ст.)
паров H2SO4. При этом возникающее пересыщение 5=2,98:1,977=1,5,
где 1,977 — давление насыщенного пара H2SO4 над 95%-ной серной кислотой
при 180 °C.
Критическое пересыщение при 180 °C составляет 2,45, следовательно, воз-
никающее пересыщение ниже критического значения и туман не образуется.
Туман лишь частично (на 30—50%) поглощается в промыв-
ных башнях, а окончательно выделяется только в мокрых элек-
трофильтрах. Механизм отделения части тумана в мокрых элек-
трофильтрах и пыли в сухих электрофильтрах одинаков. Капли
тумана абсорбируют образовавшиеся под действием электричес-
кого поля ионы газа, заряжаются, движутся к осадительным
141
электродам, отдают им свои заряд и стекают в виде жидкости.
Для повышения степени очистки в мокрых электрофильтрах
туман укрупняют снижением температуры и концентрации
кислоты во второй промывной и увлажнительной башнях. При
этом содержание H2SO4 в капле не изменится, т. е.
^1Р1^1=
где V, р, С — объем капли тумана, плотность и концентрация кислоты (1 и
2 —до и после укрупнения).
Если в 1-й промывной башне C1 = 75°/q, H2SO4, а в увлажни-
тельной башне С2=5% H2SO4, то увеличение диаметра частиц
определяется из соотношения
di - У С2ра - У 5-1,032
Следовательно, при снижении концентрации кислоты, раз-
меры и скорость движения капель в электрическом поле уве-
личиваются почти в 3 раза. При отсутствии в схеме увлажни-
тельной башни для повышения степени очистки газа от тумана
устанавливают дополнительную ступень мокрых электрофильт-
ров или уменьшают скорость газа. Вместе с туманом в промыв-
ном отделении выделяется пыль, мышьяк, селен и другие при-
меси.
Изучается очистка газа от вредных для катализатора приме-
сей твердыми сорбентами, например мышьяка — цеолитами или
силикагелем при 350—400 °C. При этом не потребовалось бы
охлаждать и увлажнять обжиговый газ в промывном отделении,
а затем вновь сушить и нагревать его для окисления в контакт-
ном отделении. Но такая очистка разработана только в лабо-
раторном масштабе.
Режим работы промывного отделения. Схемы мокрой очист-
ки обжиговых газов могут отличаться друг от друга в зависи-
мости от вида сырья, содержания в нем примесей, требований
к качеству продукции и других условий. Наиболее полная схе-
ма применяется для очистки газов от обжига колчедана
(рис. 53).
Обжиговый газ после сухой очистки поступает в 1-ю промывную башню,,
орошаемую серной кислотой концентрацией 50—60% H2SO4. Здесь газ в ос-
новном очищается от пыли, охлаждается, прнмеси частично улавливаются,
а частично переходят в туман. Вторая промывная башня орошается кисло-
той концентрацией около 20% H2SO4. Здесь газ дополнительно очищается и
охлаждается, происходит частичное осаждение и укрупнение частиц тумана.
Основная часть тумана улавливается на 1-й ступени мокрых электрофильт-
ров. В увлажнительной башне газ орошается кислотой концентрацией до 5%
H2SO4 и охлаждается с укрупнением тумана. На 2-й ступени электрофильт-
ров улавливается оставшийся туман. Далее газ обезвоживают в сушильной
башне с брызгоуловителем. Кислота из башен стекает в сборник. Циркули-
рующая кислота разогревается за счет теплоты испарения воды и поглощая
триоксид серы, а также тепла обжигового газа, поэтому ее пропускают через
холодильники.
Часть кислоты из цикла 1-й промывной башни направляют на извлечение
селена из образовавшегося селенового шлама. Благодаря поглощению триок-
142
РИС. 53. Схема очистного отделения для газов, получаемых при обжиге
колчедана:
/ — первая промывная башня; 2 — вторая промывная башня; 3 — первый мокрый электро-
фильтр; 4 — увлажнительная башня (в новых системах, работающих в испарительном
режиме, таких башен нет); 5 — второй мокрый электрофильтр; 6 — сушильная башня;
7 — брызгоуловитель; 8 — холодильники кислоты; 9 — сборники кислоты.
сида серы из газа и испарению воды концентрация кислот в башнях повы-
шается, поэтому для поддержания стабильного режима добавляют воду в
сборник увлажнительной башни, откуда избыток кислоты перетекает в сбор-
ник 2-й промывной и затем 1-й промывной башен.
Концентрация кислоты в увлажнительной и 2-й промывной башен уста-
навливается в зависимости от концентрации кислоты в 1-й промывной баш-
не, которая определяется в основном соотношением SOs и воды в газах, а
также заданной концентрацией отбираемой промывной кислоты. Температура
кислоты в последней башне должна быть возможно ниже, чтобы с газами
уходило меньше влаги, количество которой в дальнейшем влияет на концент-
рацию продукционной серной кислоты и выход олеума по отношению к обще-
му выпуску продукции.
Количество промывной кислоты в пересчете на моногидрат составляет
2—3% от общей выработки при обжиге колчедана в печах КС. Количество
промывной кислоты (в %) от общей выработки системы определяют по фор-
му.де
100-T]'-Cso3
G— ncso2 + П'СзОз
где т)', 1] — коэффициенты использования SO3 н SO2 в продукции системы
(практически т)'— 1); Cso3 и Cso2—концентрация SO3 и SO2 в газе, %.
Концентрация промывной кислоты зависит от содержания в газе триок-
сида серы и режима очистки. Избыток кислоты 1-й промывной башни после
фильтрации передают на концентрирование, либо на закрепление олеумом
или моногидратом до 75 или 93% H2SO4 и отправляют потребителю.
При испарительном режиме поддерживается более высокая
температура и (или) более низкая концентрация кислоты, оро-
шающей 1-ю промывную башню, чем при обычном режиме.
В этом случае в 1-й промывной башне газ охлаждается без
холодильников — за счет испарения воды, которая конденсиру-
ется во 2-й промывной башне, где увеличивается выделение
тепла и, как следствие, требуемая поверхность холодильников.
Интенсивная конденсация паров воды во 2-й промывной башне
143
приводит к укрупнению тумана, поэтому отпадает необходи-
мость в увлажнительной башне. Испарительный режим целе-
сообразно применять при повышенных запыленности и содержа-
нии мышьяка в газе, так как на 1-й промывной башне нет хо-
лодильников и с повышением температуры кислоты возрастает
растворимость триоксида мышьяка.
Пример. Определить температуру кислоты в 1-й промывной башне при
испарительном режиме, если известно: состав газа — 79% N2, 8% Оз, 10%
SO2, 3% НзО; расход газа— 116 000 м3/ч; температура газа на входе в баш-
ню— 350 °C, на выходе из башни — 80 °C; концентрация кислоты — 40%
H2SO4.
Средняя теплоемкость газа в интервале температур 80—350 °C:
С= 0,312 • 0,79+0,314 • 0,08+0,358 0,03+0,43 0,1 = 0,32 ккал/м3 = 1,34 кДж/м3.
Количество тепла, расходуемое на испарение воды:
Q = 1,34-116 000-(350 —80) = 4,2-10’ кДж/ч
Количество испаряемой воды:
4,2-10’
q = —sKFfj— = 1,86-104 кг/ч = 18,6 т/ч = 23 200 м3/ч
где 2260 — теплота испарения воды, кДж/кг.
Нагрузка по газу на выходе из башни:
116 000 4- 23 200 = 139 200 м3/ч
Состав газа на выходе из башни: 66,5% N2, 6,7% О2, 8,4% SO2 и 18,4%
Н2О.
Давление паров воды в газе:
760-18,4= 140 мм рт. ст. = 1,37 кПа
Такое давление паров воды над 40%-ной серной кислотой соответствует
температуре около 69 °C [4].
Результаты аналогичных расчетов температуры для разных
концентраций серной кислоты при испарительном режиме 1-й
промывной башни приведены ниже:
£наЗО4, %
Т'назод/С .
Тгаза вых, С
30 35 40 45 50 55 60
63 66 6 9 74 80 85 93
75 77 80 83 85 90 95
Результаты расчета промывного отделения, работающего в
обычном и испарительном режиме контактной системы произ-
Таблица 22. Состав газа перед промывным отделением и его расход
Компоненты Содержание, % Расход газа на 42 т/ч кислоты
сухой газ | влажный газ м3 | кг
so2 13,5 12,76 10270 29 430
SO3 0,01 0,009 7 25
о2 3,5 3,31 2261 3 800
n2 82,99 78,6 63136 [79 000
Н2О — 5,24 4210 3 380
Итого: 80282 115 635
144
Таблица 23. Технологический режим промывного отделения
Обычный режим Испарительный режим
1-я башня 2-я башня 1-я башня 2-я башня
Показатели вход ВЫХОД ВХОД ВЫХОД ВХОД ВЫХОД вход выход
Температура, °C
газа 350 85 85 40 350 120 120 40
кислоты 60 84 35 45 80 80 35 60,5
Концентрация кисло- ты, % 50 51 21 21 50 52 5 5
водительностью 1000 т моногидрата в сутки, или 42 т/ч, приве-
дены в табл. 22 и 23 [87].
Баланс воды промывного отделения описывается соотноше-
нием:
^вх.ч 4* ~ 4” ^вых.ч
где Швх. ч и — количество воды, поступающей с газом и добавляемой в
сборник последней башни; шп и w вых. ч количество воды, выводимой с про-
мывной кислотой и уносимой с выходящими из промывного отделения га-
зами.
При получении 42 т/ч серной кислоты баланс воды (табл.
24) характеризуется приведенными ниже данными.
Обычный режим. В 1-ю промывную башню поступает с газом 3380 кг
воды в виде пара. При промывке из кислоты испаряется 1680 кг воды, кото-
рая вместе с парами воды, поступившими в 1-ю башню (5060 кг), направ-
ляется во 2-ю промывную башню, где 1360 кг паров воды конденсируется.
В сборник 2-й башни для баланса добавляется 320 кг воды. Вода сконден-
сированная (1360 кг) и добавленная (320 кг) передается в сборник 1-й про-
мывной башни. Из 2-й башни 3700 кг воды (в виде пара) с выходящим га-
зом поступает в мокрые электрофильтры.
Испарительный режим. В 1-ю башию с газом поступает 3380 кг воды.
При промывке из 1-й башни испаряется 11 000 кг воды. Сюда же из 2-й
башни поступает сконденсированная (10 130 кг) и добавленная для баланса
(870 кг) воды, Испарившаяся из 1-й башни вода (14 380 кг) направляется
во 2-ю башню, где 10 130 кг ее конденсируется. Выходящие из 2-й башни
пары воды (4250 кг) с газом поступают в мокрые электрофильтры.
Несмотря на то, что при испарительном режиме поверх-
ность холодильников во 2-й промывной башне больше, чем при
обычном режиме, испарительный режим более прогрессивен как
в технологическом, так и экономическом отношении. В этом
случае не требуется увлажнительная башня со сборником, на-
сосом и коммуникациями, а благодаря укрупнению тумана по-
вышается степень очистки газа в мокрых электрофильтрах, что
дает возможность снизить капитальные затраты. Коэффициент
теплопередачи холодильников 1-й промывной башни в основ-
ном зависит от слоя инкрустаций и шлама, для чистых поверх-
10—584 145
Таблица 24. Результаты расчета повержности оросительных
холодильников и расхода воды
Показатели Обычный режим Исполнительный режим
•Количество тепла, отводимого в хо- лодильниках, МДж/ч
1-й башни 25,4 —
2-й башни 8,3 33,2
общее 33,7 33,2
Температура, °C кислоты в холодильниках
1-й башни (вх/вых) 84/60 45/35
2-й башни (вх/вых) 60,5/45
воды в холодильниках
1-й башни (вх/вых) 25/40 —
2-й башни (вх/вых) Средняя разность температур в хо- 25/30 25/40
лодпльниках, °C
1-й башни 29,5
2-й башни Коэффициент теплопередачи холо- 12,5 15,25
дильннков, кДж/(м2-ч-град)
1-й башни 542 ——
2-й башнн 835 835
Поверхность холодильников, м2
1-й башни 1200 —
2-й башни 793 2600
общая 'Расход воды в холодильниках, м3/ч 1993 2600
1-й башни 405 —.
2-й башни 396 530
общий 801 530
иостей К=542 кДж/(м2-ч-град). Однако поддерживать чистоту
холодильников очень трудно. Поэтому практически при работе
:на запыленном газе поверхность холодильников при испаритель-
ном режиме может быть даже меньше, чем при режиме с холо-
дильниками 1-й промывной башни, хотя средняя разность тем-
ператур при испарительном режиме меньше. Тепловой баланс
отделения представлен в табл. 25.
Фиктивная скорость газа в промывных башнях составляет
s0,8—I м/с, плотность орошения 15—20 м3/(м2-ч) и выше. Для
'Сильно запыленных газов с повышенным содержанием приме-
сей (особенно фтора) применяют «водный» режим промывки,
при котором концентрация кислоты в цикле 1-й промывной
башни составляет 10—15% H2SO4 и ниже. Это позволяет повы-
сить степень очистки газов [88].
Аппаратура промывного отделения. При переработке серо-
содержащих газов по классической (длинной) схеме перед по-
ступлением на контактирование они проходят мокрую очистку
в промывном отделении, которое включает промывные башни
и мокрые электрофильтры.
346
Таблица 25. Тепловой баланс промывного отделения (МДж/ч)
Обычный режим Испарительный режим
Показатели 1
1-я башня | 2-я башня 1-я башня | 2-я башня
Приход тепла
с газом 38,8 9,44 38,8 13,4
при конденсации — 3,15 — 24,2
Расход тепла
с газом 9,44 4,44 13,3 4,44
при испарении 3,95 —• 25,5 —
Тепло, отводимое в холо- 25,4 8,30 — 33,2
днльннках
Первая промывная башня (рнс. 54) представляет собой полую стальную'
колонну, внутри выложенную рольным свинцом толщиной 3—5 мм, кислото-
стойкими материалами — полннзобутиленом, фаолитом и др. и футерованную-
кислотоупорной керамикой. При повышенном содержании фтора ее футеруют
углеграфитовымн блоками. Башню устанавливают на фундаменте из кисло-
тоупорного материала. Для повышения равномерности распределения газа
внутри башни из кирпича выкладывают сужающееся устройство — пережим.
Кислоту для орошения подают насосом из сборника в коллекторы, рас-
положенные на крышке башнн, откуда она поступает в 10—20 распылителей.
С повышением числа распылителей возрастает доля смоченной поверхности,
поэтому в некоторых случаях целесообразно дополнительно устанавливать,
распылители на боковой поверхности башнн нлн располагать их в 2—3 яруса
по высоте. Применяют центробежные, ударные, щелевые и другие типы рас-
пылителей [9].
Вторая промывная (рнс. 55), а также увлажнительная башни, как и 1-я
промывная башня заключена в стальной корпус, выложенный кислотостойки-
ми материалами н футерованный керамикой. Башнн заполнены насадкой —
керамическими илн фарфоровыми кольцами Рашига для увеличения поверх-
ности контакта газа н жидкости. Снизу укладывают несколько рядов крупных
колец 80—120 мм, а затем на весь объем загружают более мелкие кольца —
размером 50 мм. Раньше кольца укладывали рядами в шахматном порядке.
С ростом производительности установок н размеров башен их укладка на-
садкой требует много ручного труда, поэтому применяют засыпку колец вна-
вал. Незаполненное пространство
над насадкой имеет высоту около
1 м. Здесь размещены распыли-
тели кислоты. Внизу насадка рас-
полагается на колосниковой ре-
шетке, опирающейся на столбики
из кирпича. На входе имеется
газовая коробка (только на ста-
рых заводах, так как без газовых
коробок надежнее защита от кор-
розии), а на входе кислоты, для
ее равномерного поступления н
распределения установлен напор-
ный бачок. Кислота вытекает из
башнн через ннжннй штуцер в
РИС. 54. Первая промывная баш-
ня:
/ — корпус; 2 — распылители кислоты;
3 — коробка со штуцером для отвода
кислоты; 4 — футеровка; 5 — смотровое
стекло.
10*
147
сборник, откуда насосом через холодильники подается на орошение. Уста-
навливают два или три насоса (один резервный) с самостоятельными кнс-
лотопроводами.
В СССР, США и других зарубежных странах для промывки газа широко
применяют аппарат «Свемко» (рис. 56). Он состоит из двух частей (верхней
и нижней), заключенных в одном корпусе. Нижняя часть — полая, орошается
брызгалами, верхняя часть имеет тарелки с отбойниками. Газ при движении
снизу вверх соприкасается с промывной кислотой, стекающей с отбойников и
образуется газожидкостный пенный слой. Аппарат «Свемко» выполняет роль
1-й (нижняя часть) и 2-й (верхняя часть) промывной башии. Интенсивная
очистка при этом позволяет работать на запыленном газе с одной ступенью
мокрых электрофильтров и без увлажнительной башни.
За рубежом, в основном в ФРГ, распространен скруббер Вентури для
мокрой очистки газов. Этот аппарат изготовляют с одной вертикальной тру-
бой Вентури (рис. 57) или в двухступенчатом исполнении — с добавлением
горизонтальной трубы Вентурн, что повышает интенсивность очистки.
В ФРГ и Японии для охлаждения газа после 1-й промывной башни при-
меняют газовые холодильники (вместо 2-й башни). В них газ движется по
трубам, а охлаждающая вода между труб. Кислота из 1-й промывной башни
отстаивается в сборниках, а при повышенной запыленности дополнительно
устанавливают отстойники (сгустители), в которых скорость движения неве-
лика и примеси успевают осаждаться.
Для охлаждения промывной кислоты применяют погружные, ороситель-
ные и кожухотрубчатые холодильники, выполненные из антегмита — пропи-
танного специальными смолами графита (графитопласт АТМ-1). Интенсив-
ность таких холодильников повышается при многоходовом исполнении (хо-
лодильники типа «Сигри»),
Электрическую очистку газов в промывном отделении проводят в мок-
рых электрофильтрах. Сотовый мокрый электрофильтр изготовляют из освии-
РИС. 55. Вторая промывная башня:
/ — корпус: 2 — футеровка; 3 — насадка (кольца); -/ — распылители; 5 —решетка; 6
столбики; 7 — сборник кислоты: 8 — холодильник.
148
РИС. 57. Промыватель Вентури:
1 — скруббер; 2 — брызгоуловитель.
РИС. 56. Аппарат «Свемко»:
1 — корпус; 2 — смотровой люк; 3 — брызгалы; /—тарелка; 5 — отбойник брызг; 6—лю-
ки для осмотра и установки тарелок.
цованной стали. На входе газа установлена распределительная решетка, а
внутри осадительные электроды из шестигранных свинцовых труб и корони-
рующие электроды из стальной освинцованной проволоки диаметром 1,8—
2,0 мм в форме «звездочки». Электроды подвешены к верхней раме, укреп-
ленной на опорных изоляторах к обогреваемой кварцевой трубе. В настоящее
время свинец заменяют другими кислотостойкими материалами, например
титаном. При наличии в газе фтора необходимы сплавы титана с палладием
или молибденом. Осадительные электроды изготовляют из винипласта, поли-
пропилена. Норма центровки винипластовых труб составляет ±5 мм. Эффек-
тивна установка игольчатых свинцовых коронирующих электродов [89], что
позволяет повысить газовую нагрузку на 20—5О°/о-
Хорошая работа мокрых электрофильтров достигается при отсутствии
отклонений в режиме работы промывных башен, регулярной периодической
промывке горячей водой или пропарке, исправном состоянии оборудования и
шиберных затворов. Для возможности промывки устанавливают не менее
двух параллельных секций или самостоятельных односекционных электро-
фильтров. Скорость газа в электрофильтре с трубчатыми (сотовыми) осади-
тельными электродами до 1 м/сек, с пластинчатыми — до 0,5 м/сек.
Применяют мокрые электрофильтры типа М — однопольный, двухсекци-
онный (мокрый); типа ШМК — однопольный, односекционный (пластинчатый,
мокрый, кислотный) и др. [9]. При нормальной работе мокрых электро-
149
шльтров ШМК выходное напряжение составляет 60 кВ, удельный ток коро-
ны 0,24—0,4 мА/м, степень очистки газа составляет 97,0—99,8% [89]. Основ-
ным показателем эффективной работы мокрых электрофильтров является от-
сутствие в газе после них серпокислотного тумана н мышьяка. Для визуаль-
ного определения отсутствия в газе тумана после очистки в торцах прямого
участка газохода устанавливают стекла, возле одного из которых есть под-
светка электролампой. При отсутствии тумана газоход хорошо просмат-
ривается.
Извлечение селена из обжигового газа. Селен относится к
редким рассеянным элементам, который все более широко при-
меняется в народном хозяйстве (электро- и радиотехнике и др.).
Степень извлечения селена из сырья в производстве серной кис-
лоты достигает 30—60% и зависит от режима работы цеха и
установленного оборудования. Примерный баланс селена одно-
го из сернокислотных цехов представлен на рис. 58.
Процесс извлечения селена состоит из следующих стадий:
поглощение 5еО2 из газа кислотой, восстановление SeO2 до ме-
таллического селена, выделение селена из кислоты. Первая и
вторая стадии совмещаются с очисткой газа. Скорость восста-
новления диоксида селена возрастает при снижении концентра-
ции серной кислоты, повышении температуры и увеличении
концентрации диоксида серы в кислоте.
Металлический селен в виде бедного шлама (до 5% Se)
осаждается из кислоты в аппаратуре промывного отделения или
при фильтрации промывной кислоты, в виде богатого шлам.’
(до 50% Se) —из тумана в мокрых электрофильтрах. Шлам из
промывной кислоты и конденсата мокрых электрофильтров от-
фильтровывают, промывают водой и 5%-ным раствором соды
и сушат. Для повышения степени восстановления диоксида се-
лена следует конденсат и кислоту перед фильтрацией нагре-
вать до 90—100 °C. Схема одной из действующих установок
извлечения селенового шлама показана на рис. 59 [90].
По этой схеме получают «усредненный» селенистый шлам, для чего кон-
денсат мокрых электрофильтров передают в цикл промывных башен. Кислоту
из сборника 1-й промывной башни после охлаждения до 20—30 °C подают на
Колчедап
(W07.Se)
Обжиговая
печь ___________
~707.Se
Следы Se-
Промывные I
башни L
Se
Мокрые элек-
трофильтры
54%Se
~50 % S е (потери
в огарке и пыли (богатый шлам)
сулил электрофильтров) £y%Se 77%Se(now(w с прамь,вной
(бедный шлам) кислотой)
РИС. 58. Баланс селена в производстве контактной серной кислоты.
150
РИС. 59. Схема извлечения
селенистого шлама из про-
мывной кислоты:
/ — холодильник; 2 - фильтр
патронный керамический П К Ф -
40А-ТС; — дозатор; 4 — цент-
рифуга; 5—вакуумная сушил-
ка; 6 — г.ульпатор; 7 — сборник
•осветленной кислоты.
Киспота промывная
В Смесительную установку
«густительную фильтрацию
В патронный керамический
фильтр ПКФ-40А-ТС. На-
чальное содержание твер-
дой фазы в кислоте до
фильтрации 0,5—5 кг/м3.
По мере накопления шла-
ма в фильтре, его в виде
лульпы сбрасывают обрат-
иым толчком воздуха под
давлением в пульпатор. Осветленная кислота поступает в сборник. Пульпа
в баке-репульпаторе нейтрализуется содовым раствором и по 1 м3/ч через
дозатор поступает в отстойную центрифугу ОГШ-202К.-3. Фугат после цент-
рифуги подается в сборник 2-й промывной башни, а осадок идет на вакуум-
ную сушилку. Производительность фильтра-сгустителя около 2 м3/ч по от-
фильтрованной кислоте при степени ее осветления 95—96%. Продолжитель-
ность заполнения фильтра шламом 10—14 дней. Шлам центрифуги содержит
около 27% влаги.
Схема установки извлечения селена на автоматическом
фильтрпрессе показана на рис. 60 [91].
Кислота 1-й промывной башни (6,4—20,5 м3/ч) отводится на фильтрацию
нз сборника в фильтр ФПАКМ-10ДП. Осветленная кислота частично идет на
склад для закрепления, частично возвращается в 1-ю башню. Производи-
тельность по фильтрату 10 м3/ч, степень осветления кислоты 90% при содер-
жании твердой фазы в кислоте 5—7 кг/м3 н содержании в осадке 35% воды.
Высокая производительность и возможность полной автоматизации процесса
извлечения селена позволили рекомендовать фильтр ФПАКМ-10ДП в каче-
стве базового для сернокислотных производств.
111.3. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛЕНИЯ ДИОКСИДА СЕРЫ
НА КАТАЛИЗАТОРАХ [92—115, 126]
ill.3.1. Термодинамика окисления диоксида серы
Реакция окисления диоксида серы в триоксид
SO2 0,5О2 ч -•* $О3 Q
обратима и степень окисления газа любого состава строго оп-
ределяется температурой и парциальными давлениями компо-
нентов реакции:
Pso3 d In Кр —ЛИ
= ^so,-Po2°’5 ’ dT = RT2
На основе данных по стандартным теплотам образования
[И] изменениям энтальпий компонентов относительно значе-
ний при 298,15 1\ с помощью ЭВМ рассчитаны величины тепло-
151
Таблица 26. Значения энтальпий и констант равновесия
реакции окисления SO2
Темпера- тура» °C Энтальпия Константа равновесия Кр Температура, СС Энтальпия Константа равновесия Кр
ккал/моль 1 кДж/моль 1 ккал/моль 1 кДж/моль
400 23 309 97 665 539,4 550 23 179 97 120 22,2
450 23 268 97 500 158,0 600 23 131 96 920 9,8
500 23 225 97 313 55,5 650 23 082 96 713 —.
вого эффекта и константы равновесия реакции окисления SO?
в интервале 400—625 и 650 °C [94]. Полученные уравнения име-
ют следующий вид:
—ДЯТ = 22671,67 + 4,423Т —8,571-1О3?2 + 6,256-1 С-'Т3 - 1,777-1О-9?4
953,786
Кр=-----у----—2,226? + 1,873-1С-гТ —0,683-К-;Т3 +
+ 1,294-10"10?3 + 0,662
Для технических расчетов может быть использовано пред-
ложенное нами уравнение
Значения энтальпии и константы равновесия реакции окис-
ления диоксида серы приведены в табл. 26.
Равновесные степени превращения. Под степенью превраще-
ния понимают отношение количества окисленного SO? к коли-
честву его в исходной газовой смеси. Максимальная степень
превращения при заданных условиях (температуре и исходных
концентрациях реагирующих компонентов) достигается в усло-
виях равновесия.
Обозначим через а и b исходные парциальные давления SO?
и Ог и через хр равновесную степень превращения. Для состоя-
ния равновесия с учетом уменьшения объема газовой смеси при
протекании реакции выражения для парциальных давлений при-
мут следующий вид:
а—ах ах Ь — 0,5ах .
Ps°2 = 1 — 0,5ах : ₽so3 = 1 —0,5ах ’ Р°2 = 1 —0,5 ’
ах (1 —0,5ах)°,в
= а (1 — х) (6 — 0,5ох)°,в
Это выражение справедливо при общем давлении 1 атм
(0,098 МПа). При общем давлении Ратм в знаменателе появля-
ется Р0’5, поскольку Р в членах парциальных давлений SO?
152
РИС. 60. Схема установки извлечения
селенистого шлама на автоматическом
фильтпрессе:
/ — сборник кислоты I промывной башни; 2 —
автоматический фильтрпресс ФПАКМ-10 ДП;
3 — вакхум-сушилка.
и SO3 взаимно сокращаются. Урав-
нение преобразуется в удобную
для расчетов степени превраще-
ния форму:
х=_________........
1/" 1 — 0,5ах
К₽+ V Р(Ь-—0,5ах)
Это уравнение определяет х
в неявном виде, что, однако, не
слишком усложняет расчет, обычно требующий двух повторно-
стей.
Уравнения для определения Кр и х можно преобразовать
так, чтобы между этими величинами была явная зависимость,
и находить Др, задаваясь значениями х:
х । Г 1 — 0,5ах
1 —х V Р(Ь—0,5ах)
или после логарифмирования в сочетании с предложенным на-
ми уравнением получим выражение для температуры (в °C):
I = ---------------1-------------------------- = X / О , X
х 1 —0.5ах
ig П—Г + 0,5 1g -b_0>5ax- + 0,5 1g (1/Р) + 4,877
Рассчитанные с помощью ЭВМ по этому уравнению значения
равновесных степеней конверсии в температурном интервале
400—650 °C для различных начальных парциальных давлений
SO2 и О2 при нормальном давлении приведены в Приложе-
нии XIII.
Ш.3.2. Ванадиевые катализаторы для окисления
диоксида серы
Окисление диоксида серы в настоящее время проводят
гетерогенно на ванадиевых катализаторах, которые к концу 30-х
годов полностью вытеснили платиновые.
В СССР почти одновременно было разработано три техно-
логических процесса изготовления катализаторов, один из них,
предложенный Г. К- Боресковым [92, 93], был внедрен в про-
мышленность. Этот катализатор (БАВ) до 1965 г. был единст-
венным и его продолжали выпускать до конца 70-х годов. Не-
достатком катализатора было то, что он изготовлялся как по-
лупродукт, превращавшийся в истинный катализатор при об-
работке низкоконцентрированным диоксидом серы, в процессе
которой хлор замещался на сульфатную группу и выделялся
153
в атмосферу. Эта операция (насыщение) проводится после
загрузки катализатора в контактный аппарат.
Чистый пятиоксид ванадия обладает слабой каталитической
активностью, резко возрастающей в присутствии солей щелоч-
ных металлов [92]. Их промотирующая роль обусловлена обра-
зованием низкоплавких пиросульфованадатов. Активный ком-
понент в условиях катализа находится в расплавленном состоя-
нии [93].
Термографические и рентгенофазовые исследования систем
V2O5—K2SO4 и V2O5—K2S2O7 [92] обнаружили образование
в них соединений, близких по составу к 1,2 V2O5 K2O-SO3 или
КгО-25О3, и наличие эвтектики с температурой плавления ни-
же 430 °C в первой системе. Полученные данные дали основа-
ние к разработке нового, насыщенного катализатора СВД [94].
Катализатор СВД изготовляется путем смешения кремне-
земистого носителя'^даатомита с содержанием не более 3%
А120з, тонко измолотого пятиоксида ванадия и раствора
KHSO4, последующего гранулирования и прокаливания гранул.
В дальнейшем, взамен измельченного пятиоксида ванадия
было предложено применять гидратированный пятиоксид вана-
дия [95], а также добавление в формуемую массу поверхност-
но-активных веществ. При таком способе изготовления повы-
шается влагоемкость массы. Это приводит при сушке и прока-
ливании гранул к увеличению пористости и, следовательно, ак-
тивности, к снижению насыпной плотности катализатора.
Стремление повысить активность при низких температурах
привело к разработке катализатора СВС [95] и катализатора
Института катализа — ИК-1-4. В отличие от катализатора СВД,
эти катализаторы производятся с использованием в качестве
носителя осажденного силикагеля при применении гидратиро-
ванного пятиоксида ванадия по несколько отличающимся меж-
ду собой технологическим схемам.
Применение этих катализаторов при концентрации газа 8—
9% SO2 позволяет снизить температуру на входе в I слой ката-
лизатора до 405—410 °C.
Катализаторы с повышенной активностью при низких тем-
пературах рекомендуется загружать в качестве запалов в
I слой, а также в нижние по ходу газа слои, работающие при
температурах ниже 440°C. В связи с этим может быть снижена
температура на входе в I слой, благодаря чему соответственно
понижается температура на выходе из слоя, что позволяет
вести переработку более концентрированных газов, не опасаясь
термической инактивации катализатора.
Для переработки газов повышенной концентрации (10—11 °/о
SO2) был разработан катализатор ТС (термостабильный), бо-
лее устойчивый к термической инактивации, чем СВД. Катали-
затор ТС отличается от СВД тем, что в качестве носителя ис-
пользуется модифицированный диатомит. Модифицирование
осуществляется обработкой слабыми растворами солей переход-
154
ных металлов IV периода или сульфата ванадия с последующим
прокаливанием при температуре до 700 °C в течение 2—3 ч. При
этом происходит образование ситалоподобных структур, пре-
пятствующих превращению кремнезема в а-кристаллобалит, ко-
торый появляется при термической инактивации катализато-
ра [96—98].
В ЛТП разработан шариковый износоустойчивый катализа-
тор для работы во взвешенном слое. Его получают пропиткой
растворами ванадата и сульфата калия шарикового алюмосили-
кагеля с определенным содержанием AI2O3 и последующей тер-
мообработкой, при которой, в зависимости от температуры и со-
держании вводимого KNO3, создается определенная пористая
структура. При этом с повышением размера гранул значение
среднего оптимального радиуса пор возрастает [99, 120].
В последнее время разработаны катализаторы (ИК-1-6,
МСВ — с малым содержанием ванадия и др.), характеризую-
щиеся существенно более высокой активностью в области низ-
ких температур, которые проходят полупромышленные или
опытные испытания [100—102]. При использовании этих ката-
лизаторов в качестве запалов и в нижних слоях контактных
аппаратов намечается сокращение общего расхода катализато-
ра. Катализатор МСВ [100] обладает высокой активностью
при низких температурах и средней — при высоких. Низкая
стоимость, малое содержание ванадия (в 2—4 раза меньше,
чем в обычных катализаторах) и высокая активность делают
этот катализатор перспективным для промышленности.
Для переработки газов с повышенной концентрацией SOa
и под давлением были созданы ванадиевые катализаторы но-
вых типов, обладающие повышенной термостабильностью или
пониженной температурой зажигания. Текстура их зерен обеспе-
чивает высокоразвитую доступную внутреннюю поверхность —
с большим объемом транспортных пор и тонкими рабочими по-
рами, примыкающими к транспортным порам. Катализаторы
разрабатывались в НИУИФ и испытывались совместно с ХПИ,
МХТИ и СКТБ катализаторов.
Разработан трубчатый катализатор СВД с пониженным гид-
равлическим сопротивлением (размер трубок: d = 8+l мм, 1 =
= 10 мм, бет = 2—2,5 мм), катализаторы образцов № 24, 31, 36,
КД-катализатор давления (в виде колец) и др. Удельная по-
верхность катализаторов: СВД — 5 м2/г, КД—18 м2/г, № 24—
57,2 м2/г, № 31 — 19,3 м2/г.
Для работы под давлением и при использовании концентри-
рованного газа предпочтительнее применение катализатора с
низким гидравлическим сопротивлением и высокой активностью
при низких температурах — кольцеобразного или трубчатого с
высокой степенью использования поверхности.
Степень использования поверхности катализатора можно
условно оценить по толщине наружного слоя, принимая, что он
работает полностью. Эту толщину, как показали исследования,
155
без существенной погрешности можно принять равной 0,6 мм.
Так, для гранул СВД с J = 8 мм и / = 25 мм степень использова-
ния массы составляет 31%, для d = 5 мм и /=10 мм — 49%, для
более мелких гранул — 51%. Для трубчатого катализатора
с —Ю мм, </вн = 3—8, /=15—25 мм и 6 = 2 мм степень ис-
пользования составляет 63,2%. При всех указанных значениях
размеров эффективность слоя трубок, с учетом увеличения т,
в 1,23 раза выше, чем слоя стандартных гранул.
За рубежом поставщиками катализаторов для производства серной кис-
лоты являются фирмы «BASF» (ФРГ), которая выпускает ванадиевые ката-
лизаторы свыше 60 лет, «Monsanto Environmental Chemicals Systems» (США),
«American Cyanamid Со» (CHIA), «Catalist and Chemicals Inc» ' (CHIA),
«Iskra industry Co, Ltd» (Япония), «YSC Chemicals RTZ» (Великобритания),
«Kemira» (Финляндия), «Haldor Topsoe» (Дания), «Saint Gobain и Krebs»
(Франция) и др.
Наряду с катализаторами фирмы «BASF» широкое использование полу-
чили катализаторы фирмы «Monsanto Env. Chem. Sys.». В настоящее время
свыше 50% всей серной кислоты, выпускаемой капиталистическими
странами, получают с катализаторами этой фирмы. Катализа-
тор типа 210 характеризуется высокой стабильностью и сохраняет удовлет-
ворительную активность в условиях длительной эксплуатации в производстве
серной кислоты практически из всех известных видов сырья. Кроме того, его
применяют для очистки низкоконцентрированных газов тепловых электро-
станций с получением серной кислоты концентрацией 70% H2SO4 при ката-
литическом окислении сернистых газов с содержанием 0,2—1,0% SO2 (про-
цесс разработан этой фирмой). Низкотемпературный катализатор Т-516
предназначен специально для загрузки на первый слой аппарата. Другой
низкотемпературный катализатор — фирмы «ISC Chem RTZ» имеет темпера-
туру зажигания 360—370 °C и обеспечивает оптимальную конверсию при тем-
пературе 430 °C.
Датская фирма «Haldor Topsoe» выпускает ванадиевой катализатор на
диатомитовом носителе, промотированиый оксидом калия (3 моля К2О на
1 моль V2O5). Общее содержание V2O5 составляет 8%, форма катализато-
ра — таблетки размером 6X6 мм с удельной поверхностью 2,1 м2/г. Выпуска-
ются также кольцеобразные катализаторы, отличающиеся вдвое меньшим гид-
равлическим сопротивлением: VK38, VK38A и VK 7— низкотемпературный
для переработки слабых газов (1—2% SO2) с температурой зажигания
370 °C.
Финская фирма «Kemira» выпускает гранулированные термостабильные
катализаторы с drp = 4—5 мм (RHV=49 и RHV = 59) и drp = 6,8—10 мм
(RHV=67 и RHV=107), сохраняющие активность до 700 °C [141].
Удельные загрузки катализатора при работе сернокислотных
установок на сере составляют примерно 180 л/(т-сут), при пе-
реработке пиритных концентратов — от 180 до 220—240 л/(т-
•сут), при использовании газов обжига цинковых и медных
концентратов удельная загрузка катализатора увеличивается и
составляет 250—300 л/(т-сут), иногда до 500 л/(т-сут). Для
загрузки в первый слой (по ходу газа) применяются катализа-
торы низкотемпературных модификаций, а также термостабиль-
ные катализаторы в виде комбинированной загрузки [141]. Ха-
рактеристика катализаторов, применяемых в промышленности
и в опытных условиях, приведены в разд. III.3.4.
156
111.3.3. Механизм и кинетика окисления диоксида серы
Со второй половины 60-х годов в СССР проведены ин-
тенсивные исследования ванадиевых катализаторов. Изучены
диаграммы состояния систем: V2O5—K9S2O7 [102,105] и VOSO«
[109*], влияние толщины слоя активного компонента на сте-
пень его использования, исследованы механизм и кинетика окис-
ления диоксида серы [104].
В первой системе установлено присутствие трех соединений:
ЗКгЗзОуV2O5, SICSsOj-VzOs и ICSsOyVsOs, разлагающихся инконгруэнтно-
при температурах соответственно 315—330, 365—380 и 405—400 °C [101, 103,
105].
Согласно последним данным о влиянии различных щелочных металлов
на активность катализаторов следует, что калий оказывает максимальное
влияние, чем и обусловливается его применение.
Поскольку активный компонент ванадиевых катализаторов
в температурной области их применения находится в расплав-
ленном состоянии, возникает специфическая особенность в ме-
ханизме их действия. Катализаторы работают как абсорбцион-
ные и процесс окисления протекает внутри слоя активного ком-
понента. В области высоких значений поверхности реакция про-
текает во всем объеме расплава вследствие его малой величи-
ны, со снижением поверхности катализатора толщина пленки,
расплава увеличивается и скорость реакции лимитируется диф-
фузией газообразных компонентов в объеме расплава. Толщина
пленки, при которой ее объем используется полностью при ра-
боте катализатора, составляет при 485°C 0,06 мкм (600 А), при
420 °C 0,2 мкм (2000 А) [102, 104]. Такая оценка дается при
допущении равномерного распределения плава компонента по
поверхности катализатора.
Представление о механизме реакции базируется на резуль-
татах исследования кинетики реакции стационарного состава
активного компонента [104].
Схема процесса может быть сформулирована следующим
образом:
1) 2V5+ + О2- + SO2 у—» 2V4+ 4- SO3 1
2) 2V4+4-l/2O2 --> 2V5+4-O2- J A
В первой стадии достигается равновесие, а вторая стадия
является медленной и определяет скорость процесса.
Предлагаемая схема является окислительно-восстановитель-
ной и соотношение между двумя ступенями окисления ванадия^
в условиях стационарного состояния катализатора определяет
его активность.
Стационарный состав катализатора не зависит от концентра-
ции кислорода в газовой фазе и определяется только соотно-
шением концентраций SO2 и SO3. Установлено, что при обра-
ботке катализатора инертным газом в отсутствии кислорода-
наблюдается окисление четырехвалентной формы ванадия, со-
держание которой возрастает после подачи реакционной смеси
15Z
до равновесного состояния. При справедливости рассмотренно-
го механизма (А), скорость каталитической реакции должна
равняться скорости окисления катализатора кислородом и быть
меньше скорости восстановления. В действительности, в область
температур выше 420 °C скорость каталитической реакции мно-
го больше скорости восстановления катализатора. В связи с
этим вероятен механизм, в котором процесс протекает по пути,
не связанном с изменением валентного состояния ванадия. Схе-
му такого процесса можно представить в следующем виде:
1) V2O5-nSO3 + SO2 q^,V2O5-(n-l)SO3-SO2 + SO3 1
2) V2O5 (n-l)SO3-O2 «=>: V2O4-nSO3 Б
3) V2O3-(n — 1) SO3 SO2O2 + SO2 iV2O5-nSO3 4-SO3 I
В этом случае скорость каталитической реакции должна
быть пропорциональна доле активного компонента в окислен-
ной форме и по этому механизму каталитическая реакция про-
текает в присутствии триоксида серы в газовой фазе.
Скорости окисления четырехвалентного ванадия кислородом
.и каталитической реакции в отсутствии триоксида серы близки
и при малых степенях превращения процесс протекает по окис-
лительно-восстановительному механизму, который может быть
представлен схемой:
1) V2O4-nSO3 V2O4 (n—2)SO3 + 2SO3
2) V2O4-(n-2) О3 4-1/20, -> V2O5-(n-2)SO3
3) V2O5-(W—2) SO3SO2SO3 * V2O4-nSO3
Стадия 1 в условиях протекания каталитической реакции на-
лодится в равновесии. Стадия 2 является сложной и определя-
ет скорость протекания реакции. Порядок этой реакции по кис-
лороду равен 1. Стадия 3 проходит с большой скоростью, что
практически приводит к полному восстановлению ванадия.
Таким образом, кинетические закономерности достаточно
сложны. Исследованию кинетики окисления диоксида серы на
ванадиевых катализаторах посвящено большое число работ, в
которых предложены различные уравнения для расчета массы
катализатора, загружаемого в контактные аппараты [104—106,
108, 114].
В СССР применяют уравнение Института катализа:
г ~ ’ <Pso2 + A>so3 I1 I ApPso/o20’5
(1)
Постоянная А изменяется в пределах 0,8—1,0 в зависимос-
ти от типа катализатора и температуры.
Разнообразие кинетических уравнений обусловлено сложным характером
кинетических закономерностей реакции окисления диоксида серы. По суще-
ству, ни в одной из работ не была изучена кинетика во всей области усло-
вий, реализуемых в промышленных аппаратах [104].
Наиболее полные исследования проведены в Институте катализа СО АН
СССР. Следует отметить ряд интересных работ МХТИ им. Д. И. Менделее-
ва, посвященных экспериментальной проверке кинетических уравнений [109].
158
Область условий протекания реакции в промышленных ап-
паратах: концентрация диоксида серы 4—12%, кислорода 6—-
13%. При двойном контактировании их содержание на второй'
стадии снижается примерно до 1 и 4% соответственно. Темпера-
турный интервал 400—600°C. Обычно процесс ведут до степе-
ни превращения диоксида серы 98,0% при одинарном и 99,8%
при двойном контактировании.
Подробное изучение зависимости скорости реакции от кон-
центрации SO2, SO3 и Ог показало, что в области температур
выше 470 °C во всем интервале степеней превращения наблю-
дается первый порядок реакции по кислороду. Скорость реак-
ции является функцией отношения /%о3:/%о2- С повышением,
концентрации кислорода может наблюдаться порядок реакции
ниже первого [104].
Понижение температуры существенно усложняет зависи-
мость скорости реакции от концентрации. В области низких,
температур и степеней превращения скорость реакции пропор-
циональна концентрации кислорода, не зависит от концентра-
ции SO2 и сильно тормозится SO3.
Работа всех слоев катализатора в промышленных аппара-
тах описывается кинетическим уравнением (1), кроме начала,
первого слоя, где применимо уравнение, предлагаемое Институ-
том катализа, описывающее процесс при допущении, что весь
ванадий находится в четырехвалентном состоянии:
/ %> — 1 \
,2)-
Kt, Кг, Кз являются сложными комбинациями констант скоростей и равнове-
сий отдельных этапов процессов, идущих по ассоциативному и окислительно-
му механизму.
При нанесении значений констант в зависимости от темпе-
ратуры на график в координатах Аррениуса получаются два
излома. Первый для разных катализаторов расположен в пре-
делах 420—450 °C, второй — 520—530°C [102]. Энергия актива-
ции при низких температурах для высокотемпературного ката-
лизатора (СВД) составляет примерно 188,5 кДж/моль
(45 ккал/моль), и излом соответствует 440°C. В температурном
интервале до 520 °C энергия активации составляет примерно
83,8 кДж/моль (20 ккал/моль) и становится равной нулю при
более высоких температурах.
Для низкотемпературного катализатора все точки изломов
сдвинуты примерно на 20 °C в сторону более низких темпера-
тур, причем энергия активации в низкотемпературной области
составляет около 125,7 кДж/моль (30 ккал/моль). В остальных
температурных областях она такая же, как у СВД.
Применение кинетических уравнений к расчету необходимо-
го времени соприкосновения для достижения заданной степени
конверсии проводится при учете работы катализатора в кон-
тактном аппарате в адиабатических условиях,, т. е. без отвода
159
выделяемой теплоты реакции. Это приводит к непрерывному
нагреванию слоя по мере продвижения газа. Степень нагрева
пропорциональна степени превращения и концентрации диокси-
да серы в газе.
С точностью, достаточной для технического расчета, можно
принять, что на диаграмме температура — степень превраще-
ния, количество выделенного тепла, а следовательно и темпера-
тура разогрева слоя, будут линейно изменяться с конверсией.
Вывод приближенного уравнения температуры разогрева слоя
приводится в [92]. Эта температура равна:
t = -|- Хх
где t — конечная температура в слое; /о — начальная температура газов при
входе в слой; х — степень конверсии; Л = Д//-а1С? или Z= 10,1 а/уСр; а — объ-
емное содержание диоксида серы в исходной газовой смеси; у — плотность
газовой смеси при нормальных условиях; Ср — средняя теплоемкость газовой
смеси.
Для газовых смесей с различным содержанием диоксида се-
ры Cso2 значения Л приведены ниже:
Cso2, %.................. 7 8 9 10 11 12 14 17
X, кДж/(м3-град) . . .835 935 1056 1170 1260 1352 1560 1890
X, ккал/(м3-град) . . . 199 225 252 279 302 324 373 450
Влияние внутренней диффузии. В реальных условиях кон-
тактного процесса влияние внешнедиффузионных факторов на
скорость реакции незначительно — менее 3%. Диффузионное
сопротивление уменьшается с ростом массовой скорости газо-
вого потока при высоких парциальных давлениях реагентов,
при малых значениях скоростей реакции и размера зерна ка-
тализатора [101, 102].
В промышленных катализаторах внутренняя поверхность
зерен в десятки раз больше наружной поверхности. Поэтому
скорость переноса реагирующих веществ к внутренней поверх-
ности оказывает большое влияние на протекание контактного
процесса.
В промышленных условиях для обеспечения высокой ско-
рости реакции обычно поддерживают избыток кислорода. По-
этому парциальное давление кислорода слабо изменяется при
варьировании степени превращения, а следовательно, и вдоль
радиуса зерна. Если принять, что коэффициенты диффузии SO2
и SO3 примерно одинаковы, то для данного процесса задача
расчета влияния внутренней диффузии может быть сведена к
анализу диффузионно-кинетического уравнения для одного ком-
понента— диоксида серы [114, 126]:
/ d2c 2 dc\ „
£>эф + — • -jT] = w (Q
•с граничными условиями: при r = 0 dcldr—Q
при г = /? С = С„
•где С — концентрация SO2 на расстоянии г от центра зерна, моль/см3 (кон-
центрация в зоне реакции); Сп — концентрация SO2 у поверхности зерна,
360
моль,'смг; —скорость реакции, отнесенная к единице объема зерна,
моль/(см3-с); — эффективный коэффициент диффузии SO2, определяю-
щий перенос вещества в пористой структуре, см2/с; R3 — радиус зерна ката-
лизатора, см, определенный как /?3 = 3V/S (Г и S — объем и наружная по-
верхность зерна катализатора).
Расчет влияния внутренней диффузии на процесс показал
[111], что в широком интервале всех параметров степень ис-
пользования катализатора не зависит от х и снижается с при-
ближением к равновесию. Это объясняется тем, что скорость
обратной реакции имеет порядок выше первого [ПО, 102]. За-
висимость скорости реакции от х можно приближенно предста-
вить в виде уравнения первого порядка:
w = КРЬ (хр —х)
где b—мольная доля кислорода в исходной смеси.
Уравнение можно преобразовать к виду
W==K1~^T RT (cso, — CpsoJ
(CPso2—равновесная концентрация SO2), что формально соот-
йетствует кинетическому уравнению первого порядка с констан-
той скорости равной RT [114].
Промышленные ванадиевые катализаторы характеризуются
большим радиусом пор (> 1000 А= 10~7 м), что обеспечивает
молекулярный характер диффузии. В этом случае коэффициент
диффузии при давлении связан соотношением
Dp = DJ^/P
где D- — коэффициент диффузии при Р=0,1 кПа.
Для реакции первого порядка степени использования ката-
лизатора может быть выражена аналитически через параметр
Тиле, который с учетом выражения для ш и Dp равен
V /~~ЬР RT уКГ
S | aPt ’ 22,4 ' D3
где .У = 8,2 ГПа/( моль-град); — константа, см3/(г-с• Па); у — кажущаяся
ПЛОТНОСТЬ, Г СМ".
Скорость реакции окисления на катализаторе промышленно-
го зернения. При изучении влияния внутридиффузионного тор-
можения на скорость окисления SO2 [112] установлено, что
в довольно широком интервале всех параметров степень исполь-
зования катализатора практически не зависит от степени прев-
ращения х и несколько уменьшается с приближением к равно-
весию. С ростом начальной концентрации кислорода и сниже-
нием концентрации SO2 величина ф увеличивается и, следова-
тельно, снижается ц. При переходе в область внутренней диф-
фузии порядок по кислороду уменьшается. С повышением на-
11—584
161
чальных концентраций кислорода и диоксида серы степень ис-
пользования катализатора уменьшается.
При проведении инженерных расчетов возможно использо-
вание кинетического уравнения (1) с поправкой константы ско-
рости реакции на степень использования катализатора. Степень
использования катализатора зависит от отношений концентра-
ций кислорода и диоксида серы в исходном газе, общего давле-
ния и температуры:
^набл — КкинЧ Р ’ Т)
Степень использования в зависимости от состава газа и дав-
ления [126] для различных катализаторов, начальных концент-
раций, температур и давлений укладывается на одну зависи-
мость, аппроксимируемую функцией
/ ab^P^ \ ( ct
'1='1ст[ а^ьр Пст-*,19^ йр j
где Цст — степень использования в стандартных условиях (7,5% SO2, 11%
О2, атмосферное давление).
Данная зависимость справедлива в интервале отношения
а/b примерно от 0,1 до 1,5. При значениях а/&<0,1 следует
ожидать изменения кинетических закономерностей. В этом
случае реакция протекает по первому порядку по SO2 и нулево-
му по О2 и не зависит от концентрации SO3. При а/&>1,5 не-
обходимо учитывать влияние обратимости реакции на степень
использования, приводящее к ее понижению.
Теоретические расчеты показали, что степень использования
катализатора на II ступени контактирования в 2—3 раза ниже,
чем на I ступени, за счет изменения состава газа. Результаты
исследований Института катализа [126], проведенных цирку-
ляционно-проточным методом для катализатора ИК-1-1 (разме-
ры гранул: диаметр — 0,5 см, длина 1 см), представлены в
табл. 27 и 28. Значения Кнабл при различных температурах рас-
считываются по зависимости
[ Е 7 1 1 \]
А* на б л — К* ехР I р I Т* т I
где К* — константа скорости при опорной температуре Т*.
Таблица 27. Значения Краб и т] при различных составах
исходной смеси и температурах
О. % Ь, % t, °C a/b А'наб.т см:'(г с ат) ^ЭКСП п расчет
0,96 4,23 420 0,23 0,44 0,37 0,34
0,99 8,00 420 0,12 0,23 0,19 0,26
1,54 6,28 420 0,25 0,46 0,38 0,36
7,50 11,00 420 0,68 0,75 0,59 0,57
1,06 6,12 440 0,17 0,46 0,22 0,23
0,93 5,28 460 0,18 0,48 0,15 0,19
7,5 11,0 485 0,68 1,50 0,26
П Р И 5 е ч а н и е. В кинетической области Х42о = 1,2. X4as = 5,8 см3/(г-с-ат)
162
1 а блица 28. Характеристика катализаторов СВД и ИК-1-4
Показатели Температу- ра. °C Катализаторы
СВД гра- | ИК-1-4 1 гранулы ИК-1-4
d, мм ___ 5X10 5хЮ 8х8> 2,8
Тнас, Г/СМ3 — 0,67 0,65 0,60
\каж, Г/СМ5 — 1,1а 1,1 5,0 1.1 5,5
Дкпв, см3/(г-с-ат) 485 4,9
420 0,75 1,1 1,5
Кнабл, см3/(г-с-ат) 485 1,7 1,8 2,3
420 0,3 0,8 0,9
V] 420 0,68 0,55 0,61
285 0,35 0,37 0.42
D3i, см2/с 420 0,027 0,036 0,052
485 0,047 0,052 0,076
Таблица 29. Значения наблюдаемой энергии активации (Диабл)
Катализатор £набл> h Дж 'моль (ккал/моль) г,, к т2, к
T<Tt T2>T>Tt | т>т2 х<0,6 | х>0,6
СВД 197(47) 38,6(14) 0 733 713 813
ИК-1-4 125,7(30) 54,5(13) 0 713 693 803
Т\, Т2 — точки перелома в арреннусовских координ атах; х - -степень превращения.
В табл. 29 приведены значения £Набл, а в табл. 30 —харак-
теристики некоторых катализаторов, применяемых в промыш-
ленности.
III.3.4. Окисление диоксида серы при повышенном
давлении
Влияние давления на скорость реакции возможно оце-
нить в кинетической области, где практически отсутствует влия-
ние физических факторов. Повышение давления влияет как на
скорость процесса, так и на состояние равновесия. Скорость ре-
акции и выход продукта с повышением давления увеличиваются
за счет повышения действующих концентраций SO2 и О2 и уве-
личения движущей силы процесса.
Увеличение равновесной степени превращения с повышением
давления при низких температурах (/с440°С) мало — менее
0,5% на 1 МПа (10 ат), когда велико значение константы рав-
новесия; при высоких температурах (/>600 °C) это увеличение
достигает 30%. Экспериментальные данные ЛТП, полученные в
интервале рабочих температур для газа, содержащего 10% SO2
11*
163
Таблица 30. Характеристика катализаторов
Марка Страна Форма Размеры, мм
d н
ИК-1-6 СССР Гранулы 5 4 1
ИК-1-б 7—:
ИК-1-6 » 6 7—1
ИК-1-6 » Кольца, 12 8—S
ИК-1-4 » трубки Гранулы 5 7—1
ИК-1-4 » Кольца, 12 8—S
свс трубки Кольца, 5 7—1
СВД СССР трубки Кольца, 5 7-1
КС-6 ПНР труЬкИ » 6 10
КС-4 » » 4 10
КНТ-4 4 10
АС ГДР Шарики 6—8
БАСФ- ФРГ Гранулы 5-5,5 7—1
04—10 БАСФ- » 5—5,5 7—1
04—11 «Мопсап- США 5,7
то»-210 «Монсан- » 8,0 8
то»-516 Франция 5,0 8—1
— Содержание v2o5> % Насыпная плотность, кг/л Лпабл’ смУ(с-ат) Степень превраще- ния (в ст. усл.)
485 °C, х=70% 420 °C, х=90% 485 °C 420 °C
~.5 ^а. -0,6—0.7 2,3—2,7 0,85—1 , 1 86—88 62—65
5 7,5—9 0,6—0,7 2.3-2.7 0785—1,1 _—8Ь —6273
5 7,5—9 0,6—0,7 2,3—2,7 0,85—1,1 86 58,0
5 6,5—9 0,56-0,6 2,3—2,7 0,85—1,1 86—90 61,8
5 6,5—9 0,65 1,85 0,77 80—82 50—45
5 6,5—9 0,56—0,6 80—82 50—55
5 7,5—9 0,6 2,0—2,16 0,8—0,9 80—82 45—50
5 6,5—7,5 0,61 1,96 0,33 84—86 17—22
'
5,6 0,48 1,18 0,37 75—78 20—22
5,6 0,50 1,8 0,56 75—78 20—22
5,6 0,53 1,7 0,7 75—78 20—22
5,0 0,60 1,58 0.4 72—75 17—20
5 6,0 — — — 83,7 15—20
5 8,0 -7- — —• 88,0 15—20
8,3 0,91 1,14 0,33 83,0 15—20
7,0 0,77 1,80 0,42 83,0 15—20
0 9,0 0,58 2,08 0,41 86,2 25
и 18,9% Оо, при давлении 0,1, 0,3, 0,5, 0,8 и 1,0 МПа, обработа-
ны по уравнению Борескова — Иванова и рассчитаны на ЭВМ
(см. Приложение XIV).
Для описания процесса под повышенным давлением была
проведена проверка возможности использования известных кине-
тических уравнений, полученных при атмосферном давлении. Из
большого числа имеющихся в настоящее время уравнений вы-
браны наиболее часто применяемые для инженерных расчетов
контактных аппаратов, а также представляющих интерес с точки
зрения механизмов, на основании которых они выведены. Про-
верка проведена для ряда уравнений, в том числе: 1 —Бореско-
ва— Иванова, 2 — Борескова — Иванова, модифицированного
авторами, 3 — Эклунда, 4 —Иваненко — Торочешникова — Сал-
тановой, 5 — Шимичека, 6 — Марса — Мессена, 7 — Померанце-
ва [114].
Результаты экспериментальных исследований обрабатывали
по специальной программе, предусматривающей оптимизацию
всех параметров уравнения, критерий оптимальности 7? миними-
зировался:
п
R — (®расч ®эксп)2
Уравнения 1—4, несмотря на некоторые отличия, практически
с одинаковой точностью (значения 7? очень близки — соответст-
венно 0,459, 0,447, 0,490 и 0,453) описывают экспериментальные
данные зависимости скорости реакции от концентрации реаги-
рующих веществ. Численные значения энергии активации в со-
ответствующих температурных интервалах для этих уравнений
близки к значениям, полученным из зависимости скорости пря-
мой реакции от температуры (Eii0-52о= 101—110 кДж/моль).
Другая группа уравнений — уравнения 5—7 несколько лучше
описывают экспериментальные данные (7? имеет меньшие значе-
ния— соответственно 0,373, 0,329, 0,286), но численные значения
энергии активации получаются значительно выше (£'440-520 =
= 164—214 кДж/моль).
Существенным недостатком этой группы уравнений является
тс, что при значениях х->0 скорость реакции стремится к беско-
нечности, что противоречит физическому смыслу. Следует отме-
тить, что зависимость lg K=f(T) уравнения 7 по сравнению с
другими уравнениями гораздо ближе приближается к линейной,
и величины энергии активации, вычисленные по этому уравне-
нию, больше, чем для других уравнений, отличаются от значе-
ний энергии активации, определенных из зависимости скоростей
прямой реакции от температуры.
Например, Е (в кДж/моль) по уравнению Борескова (2-му) при темпе-
ратурах 420—440 °C равна 273, по 7-му уравнению — 374, при 440—520 соот-
ветственно 105 и 214, при температуре выше 520 °C — 8 и 143.
Кроме того, для всех рассмотренных уравнений отмечается
зависимость константы скоростей реакции от давления, кроме
165
7-го уравнения, т. е. механизм реакции на самом деле несколько
более сложен, чем представленный при выводе этого уравнения.
Исходя из физического смысла кинетических параметров и
данных экспериментальных исследований, при расчете промыш-
ленных контактных аппаратов для окисления газа различного
состава и при различном давлении следует использовать кине-
тическое уравнение Института катализа, при этом наблюдаемая
константа скорости определяется выражением:
/ аР0 \°35
^набл ~ ^вабл. сТ-!,19
где Лнабл. ст — наблюдаемая константа скорости реакции при стандартных
условиях, рассчитанная на единицу объема катализатора.
Влияние давления на величину йнабл и степень использова-
ния гранул катализатора ИК-1-1 при 485 °C [126] показано
ниже:
Р, МПа . . .
Йнабл, см3/(г-с-ат)
П................
1 2 4 7 9
1,5 0,86 0,73 0,59 0,47
0,29 0,17 0,14 0,12 0,09
Как уже сказано, в последнее время разработаны ванадие-
вые катализаторы для переработки газов с повышенной концент-
рацией по SO2 и под давлением, обладающие повышенной тер-
мостабильностью, с существенно более высокими активностями
в области рабочих температур. Данные испытаний катализато-
ров для повышенных давлений приведены в табл. 31.
Расчеты, проведенные на основе теоретических и эксперимен-
тальных исследований по влиянию давления, подтверждают воз-
можность переработки диоксида серы без промежуточной аб-
сорбции (одностадийное контактирование) с общей степенью
Таблица 31. Данные обследований работы промышленных катализаторов
под давлением
Катализатор К2о V2O5 hV2O6, % Удельная поверх- ность, М2; Г Температура 420 СС Температура 485 °C
0,98 МПа 1,47 МПа 0,98 МПа 1,47 МПа
w | k w | k .. 1 k ш | k
СВД 3:1 6,5 3,41 0,0180,391 0,067 0,567 0,072 1,45 0,1302,636
свс 2,4:1 12,0 9,50 0,076 0,622 0,088 0,785 0,088 1,34 0,096 1,722
ИК-1-4 3:1 9,3 10,80 0,075 0,662 0,086 0,678 0.092 1,527 0,132 2,442
мсв, диатомит 9:1 2,4 3,36 0,056 0,448 0,075 0,664 0.047 0,941 0,056 1,039
МСВ, аэроснл 9:1 27,4 27,40 0,072 0,592 0,087 0,703 0,049 1,014 0,075 1,607
а1 — скорость реакции, отнесенная к I г катализатора, мл^г-с); k — константа ско-
рости в уравнении Борескова, мл/(г-с-ат).
166
Таблиц а 32. Температура газа на входе в I слой
Давление. МПа Концентрация SO2. °/о
8 9 1 10 11
0.5 440 383 364 348
0.7 400 378 359 342
1,0 398 375 353 336
превращения 99,8%, что с трудом достигается.. на системах—с.
двойным контактированием, работающих при обычном давлении.
Однако максимально возможная концентрация SO2 в исходном
газе при проведении процесса под давлением до степени превра-
щения 99,8% без промежуточной абсорбции будет определяться
допустимой температурой в слоях катализатора ввиду низкой
каталитической активности катализаторов в области темпера-
тур ниже 380 °C.
Значения температур, соответствующих равновесной степени
превращения 0,998 при давлении в системе 1,0 МПа, приведены
ниже:
Cs02, % ..............8 9 10 И 12
... 400 393 386 379 372
Учитывая, что температура газа на входе в последний слой
катализатора несколько ниже приведенных, можно сделать вы-
вод, что максимально возможная концентрация диоксида серы
в исходной реакционной смеси не должна превышать 10%. Не-
обходимые температуры газа на входе в первый слой катализа-
тора, рассчитанные так, чтобы температура в конце слоя состав-
ляла 600 °C, представлены в табл. 32.
Из приведенных данных следует, что цри концентрации в ис-
ходном газе выше 9% должна быть обеспечена принудительная
стабилизация температуры в конце первого слоя катализатора.
При этом в слой загружают такое количество катализатора
(без запаса), чтобы при минимально возможной температуре на
входе в I слой температура на выходе из него составляла 590 °C.
При падении активности катализатора в процессе эксплуатации
температуру на входе в слой следует определять таким образом,
чтобы в конце слоя она была 590 °C. В этом случае необходима
специальная система автоматической стабилизации режима. Оп-
тимальные технологические режимы работы контактного аппара-
та на катализаторах ИК-4 и СВС под различным давлением
при переработке газа, содержащего 9% SO2 и 12% Ог, с дости-
жением степени превращения 0,998, показаны в табл. 33 (хк —
конечная степень превращения, и tK — температура в начале и
в конце слоя, Ск — необходимый расход катализатора в л на 1 т
H2SO4 в сутки).
Таким образом, при переработке 9%-ного газа в трехслойном
контактном аппарате под давлением до 1 МПа с достижением
конечной степени превращения 0,998 возможно использование
167
Таблица 33. Оптимальные технологические режимы контактного аппарата
№ слоя Параметры слоя Давление, МПа
0,5 1 0,75 | 1,0
I Д'к 0,858 0,869 0,877
с 385 380 380
/к 601 599 601
Ск 41 25 19
II 0,991 0,992 0,992
с 401 403 412
tK 434 434 441
ск 61 45 29
III А" к 0,998 0,998 0,998
С 375 375 384
tK 377 376 385
Ск 95 87 56
Всего Ск 197 157 104
систем с одностадийным контактированием. Однако при созда-
нии безотходной сернокислотной системы для достижения степе-
ни конверсии 0,9995 и при работе под давлением необходимо две
стадии окисления.
Окисление высококонцентрированного SO2 техническим кис-
лородом под повышенным давлением целесообразно ввиду отсут-
ствия в исходной смеси инертных газов. Однако градиент уве-
личения выхода с повышением давления непрерывно снижается.
Для данной реакции выбор оптимального давления будет обус-
ловлен экономическими показателями.
111.4. КОНТАКТНЫЕ АППАРАТЫ И КОНТАКТНЫЕ УЗЛЫ.
ТЕХНОЛОГИЧЕСКИЙ РЕЖИМ И ОСОБЕННОСТИ ЭКСПЛУАТАЦИИ
[9, 80, 116—129]
III.4.1. Принципиальные технологические
схемы контактных узлов
Технологическая схема и аппаратура контактного узла
зависит от вида применяемого сырья, способов отвода тепла ре-
акции, производительности установки и других факторов.
При получении серной кислоты из чистой серы или сероводо-
рода по короткой технологической схеме промывное отделение
отсутствует, газ после печи и котла-утилизатора подают непо-
средственно в контактный аппарат. В контактных узлах, рабо-
тающих на газах от обжига колчедана, отходящих газах метал-
лургических и других производств перед поступлением в кон-
тактный аппарат газовый поток нагревают от 40—70 до 420—
440 °C в теплообменниках за счет тепла прореагировавшего
газа.
168
Ряд построенных ранее сернокислотных производств на раз-
личном сырье, а также новых — на отходящих газах с содержа-
нием 3—6% SO2, используют схему контактного узла с одинар-
ным контактированием. Новые производства на сере и колчеда-
не строятся по схеме двойного контактирования с контактными
аппаратами с 4—5 слоями катализатора. На рис. 61 представле-
на схема контактного узла с одинарным контактированием,
включающая 4-слойный аппарат с промежуточными теплообмен-
никами [116].
Очищенный и осушенный сернистый газ подается газодувкой, нагревает-
ся во внешнем и промежуточных теплообменниках и поступает на I слой кон-
тактного аппарата. Пройдя все слон катализатора с промежуточным охлаж-
дением в теплообменниках, прореагировавший газ покидает контактный ап-
парат, охлаждается во внешних теплообменниках и направляется на абсорб-
цию образовавшегося SO3. Оптимальный температурный режим поддержива-
ют с помощью байпасных газоходов с задвижками на теплообменниках, ко-
торые обычно устанавливают последовательно по ходу газа, иногда — перед
двумя последними слоями — параллельно. Максимальная степень превраще-
ния SO2 в контактном аппарате достигает 98,0—98,5%.
При двойном контактировании (ДК) после первой стадии ка-
тализа из газовой смеси поглощается образовавшийся SO3 и на
вторую стадию катализа поступает неокисленная часть исходно-
го SO2. Степень превращения по схеме ДК составляет 99,5—
99,8%. При этом степень превращения на первой стадии ката-
лиза 93—95% и на второй — 95—97%. Схема контактного узла
ДК представлена на рис. 62.
Перед поступлением на I слой контактного аппарата газ нагревают в
теплообменниках до 420—440 °C (наиболее часто применяются выносные
теплообменники). После прохождения 3 слоев катализатора газ охлаждают
РИС. 61. Схема контактного узла с одинарным контактированием:
у _ турбогазодувка; 2 — брызгоуловитель; 3 — внешний теплообменник; 4 — контактным
аппарат: -5 — топка; 6 — теплообменник пускового подогревателя; 7 — пусковая газодув-
ка; 5 — термопары.
169
РИС. 62. Схема контактного узла с ДК:
Л 2, 5, 6 — теплообменники; 3 — первая сту-
пень контактирования; 4 —вторая ступень
контактирования.
в теплообменнике и направляют на пер-
вую стадию абсорбции. Далее газ на-
гревают в теплообменниках контактного
узла н направляют на вторую стадию
катализа. Обычно обе стадии катализа
конструктивно располагают в одном
контактном аппарате. Варианты слоев
на 1 и 2 стадиях катализа: 3+1, 2+2,
3+2 или 4+1.
Работа установок ДК часто затрудняется на второй стадии
недостаточной конверсией, что снижает общую степень превра-
щения в контактном аппарате. Зависимость максимальной об-
щей (конечной) степени превращения от степени превращения
на первой и второй стадиях катализа показана на рис. 63 и 64.
При использовании газов от сжигания серы (рис. 63), содержащих 10%
SOs, можно достичь хк = 99,8% при Х]>92,7% или хк=99,9% при Xi = 95,7%
(температура газа на входе на вторую стадию 430°C). Для газов от обжига
колчедана (см. рис. 64) для тех же условий хк = 99,8% при х1=94,3% или
хк=99,9 при Xi>96,6%. Чем выше концентрация SO2 до контактного аппа-
рата, тем больше должна быть степень превращения на первой стадии для
достижения заданной конечной степени превращения.
На практике температура газа на входе во вторую стадию
катализа находится в пределах 420—430 °C при конечной степе-
ни превращения 99,5—99,8%. Для достижения более высоких
степеней превращения (не менее 99,9%) необходимы катализа-
торы с высокой активностью при низких температурах (400—
420 СС) и зернами меньшего размера.
Степень превращения на второй стадии катализа и конечную
степень превращения можно увеличить применением интенсифи-
цирующих факторов, например, добавлением к газу кислорода
после первой стадии абсорбции, особенно в тех случаях когда
его содержание в газе ниже 5%. Для газов от обжига колчеда-
на, содержащих не более 8—9% SO2, и газов от сжигания серы,
содержащих не более 9—10% SO2, добавление значительного
количества кислорода (до 20%) дает небольшие изменения сте-
пени превращения на второй стадии (не более 0,5—1%), что при
высокой степени превращения на первой стадии приводит к не-
большим изменениям конечной степени превращения. Для по-
вышения надежности работы целесообразно применение на вто-
рой стадии контактирования двух слоев катализатора с проме-
жуточным охлаждением. Это дает возможность увеличить сте-
пень превращения от 97,4 до 98,5%, а конечную степень превра-
щения— от 99,74 до 99,84%. Однако, чем меньше начальная кон-
центрация SO2 и выше степень превращения на первой стадии
катализа, тем меньше эффект от наличия двух слоев на второй
стадии. Поэтому за рубежом на второй стадии катализа чаще
170
устанавливают один слой катализатора и стремятся достигнуть
максимально возможной степени превращения на первой стадии
катализа, например, на первой стадии количество слоев увеличи-
вают до четырех, что в итоге дает систему 4+1.
На второй стадии катализа устанавливать более двух слоев
катализатора нецелесообразно, так как при приближении про-
цесса к равновесию нельзя существенно повысить степень пре-
вращения SO2 в SO3. Кроме того, установка третьего слоя дает
дополнительное сопротивление, что вызывает повышенный рас-
ход электроэнергии и увеличение стоимости аппарата.
111.4.2. Технологические режимы работы
катализаторов
Эксплуатационные качества катализатора в наибольшей
степени определяются его активностью, гидравлическим сопро-
тивлением, механической прочностью, продолжительностью сро-
ка службы.
РИС- 64. Зависимость степени превращения
РИС. 63. Зависимость конечной
степени превращения хк от
степени превращения на пер*
вой и второй Х2 стадиях
контактирования для газов от
сжигания серы.
Тг — температура газа па входе во
вторую стадию контактирования:
а — концентрация SO2 перед первой
стадией контактирования.
на второй стадии контактирова-
ния х2 от температуры при различном числе слоев катализатора:
/ — один слой; 2 — два слоя (7’р1«7’р2 = 420 °C, ,Г1 = 90%): 3 — равновесная кривая для
газа с содержанием 10% SO? (х, = 90%).
171
Таблица 34. Комбинированная загрузка катализаторов
в контактный аппарат диаметром 8 м
№ слоя Одинарное контактирование, 3G0 т,сут (CSO2=7,5%. Л'к 98.0%) Двойное контактирование, -120 т/сут (^SOo —9.0%, хк~-99,8%)
ТИП катализатора высота слоя, мм объем катализа- тора, М3 тип катализатора высота слоя, мм объем катализа- тора, м3
I ИК 1—4 СВД 100 350 5,4 16,0 СВИТ СВД 150 650 7.2 30.4
II СВД 400 19,0 СВД 550 25,6
III СВД 500 23,2 СВД 450 20.8
IV ИК 1—4 450 21,2 СВД 500 23,2
V ИК 1—4 500 23,2 СВИТ 120 5.8
СВД 260 12,1
Итого
Удельная
загрузка
2300 108
300 л/т
2680 125,1
285 л/т
Область применения низкотемпературных катализаторов —
верхняя часть I слоя, IV и V слои. Область применения высоко-
температурных катализаторов— нижняя часть I слоя, II и
III слои. Комбинированная загрузка контактного аппарата ката-
лизатором обеспечивает надежную его работу в течение дли-
тельного срока эксплуатации. Приме-р комбинированной загруз-
ки катализаторов в схеме контактного узла ОК и ДК приведен
в табл. 34 [116].
Оптимальное содержание SO2 в газах от обжига колчедана,
поступающих на первую стадию катализа в систему ДК, состав-
ляет 8,5—9,0%, в газах от сжигания серы— 10—10,5%. Присни-
Таблица 35. Показатели работы промышленных
Содержание SO2, % 1-я стадия катализа
температура по слоям, °C *1, %
I 1 II 1 III
j: i Газы от обжи 8,5 414—598 463—540 468—494 92,8 8,85 418—598 465—539 461—489 92 5 9,2 418—600 465—540 463—492 91,0 Газы от ежи 9,5 435—585 450—512 435—456 95,0 9,5 440—580 448—510 440—460 94,8 9,5 435—585 452-514 436—457 94 5
172
женин концентрации SO2 существенно возрастает требуемая по-
верхность теплообменников, а при повышении — уменьшается
концентрация кислорода в газе и общая степень превращения.
При окислении сернистых газов рекомендуются следующие оп-
тимальные соотношения SO2 и О2 (%) [9]:
CSo2................ 7 13 15 19 22 25 32 39 47 54
С02 ...........II 14 15 17 19 20 23 27 31 34
Показатели технологического режима работы промышлен-
ных контактных аппаратов ДК приведены в табл. 35. На вторую
стадию катализа поступают газы с содержанием примерно 0,5—
0,9% SO2. Оптимальный температурный режим окисления диок-
сида серы на второй стадии катализа систем ДК может изме-
няться в интервале 420—530 °C [129]. При этом значение опти-
мальных температур окисления низкоконцентрированного газа
увеличивается с повышением концентрации кислорода, а при из-
менении содержания SO2 сохраняется на прежнем уровне.
Системы, работающие на газах от сжигания серы, в среднем
имеют более стабильные и высокие значения степени превраще-
ния в контактном аппарате (99,5—99,8%) по сравнению с систе-
мами, работающими на газах от обжига колчедана (99,4—
99,6%), так как газы от сжигания серы содержат больше кисло-
рода. Практически загрузка контактной массы при двойном кон-
тактировании по сравнению с одинарным уменьшается. В систе-
мах, работающих на газах от сжигания серы, при одинарном
контактировании загрузка катализатора составляет 220—240,
при ДК— 170 — 210 л/(т-сут) кислоты; в системах, работающих
на газах от обжига колчедана, при одинарном контактирова-
нии — 300—330, при ДК — 270—290 л/(т-сут) [129].
111.4.3. Типы и особенности контактных аппаратов
В современном сернокислотном производстве наиболее
широко применяются контактные аппараты с горизонтальными
стационарными слоями катализатора и отводом тепла в вынос-
контактных аппаратов ДК
2-я стадия катализа ХК, % Расход ка- тализатора на ! т кис- лоты, л/сут
температура по слоям, °C *2, %
IV | V
га колчедана
433—458 434—456 433—458 418—421 424—427 420—422 95,8 94,7 94,2 99,7 99,6 99,5 290
гания серы 430—441 42С—423 94,0 99.70
430—445 432—448 422—425 425—428 96,0 95,5 99.80 99,7 213
173
РИС. 65. Контактный аппарат с добавлением холодного газа после первого»
слоя производительностью 540 т/сут:
!— V — слои контактной массы; 1—3 — промежуточные теплообменники; 4 — смесители;
5 — слои кварца (15—20 мм).
ных теплообменниках. Применяются также контактные аппара-
ты с внутренними теплообменниками (типов К-39, К-58-5,
КЦТ) либо с поддувом воздуха или газа (рис. 65, 66) [9].
При работе по короткой схеме на газах от сжигания серы
или сероводорода применяется охлаждение газа между слоями
в пароперегревателях, в газовоздушных теплообменниках или
174
РИС. 66. Контактный аппарат с вы-
носными теплообменниками произво-
дительностью 1000 т/сут:
I——слои контактной массы; Г—слой
кварца.
РИС. 67. Контактный аппарат ОТС с отводом тепла серой:
1 — гильзы; 2 —трубки; 3 —жидкая сера: 4 — корпус: .5 — днище; 6 — колосники; 7 — ка-
тализатор; 3 — футеровка; 9— трубная рещетка; 10 — крышка.
поддувом воздуха, что значительно упрощает конструкцию кон-
тактного узла.
Для устойчивой работы контактного аппарата необходимо
равномерное, распределение газа и температур по сечению аппа-
рата, достаточная мощность теплообменников, надежная схема
регулирования, простота обслуживания и ремонта и др. Наи-
большая равномерность температур и концентраций газа в ап-
парате достигнута при использовании выносных теплообменни-
ков. В контактных аппаратах производительностью 500 и
1000—1500 т/сут перегородки между слоями катализатора могут
быть плоскими или сферическими, связанными стойками с несу-
щими балками, или опирающимися на центральную колонну.
Контактные аппараты типа К-39 имеют следующие недостатки: ремонт
теплообменников и замена трубок возможны только при демонтаже верхней
части аппарата; диаметр трубных решеток достигает 6—7 м и при этом воз-
растает сопротивление межтрубного пространства из-за увеличения числа ря-
дов труб; низкий коэффициент теплопередачи — 7—9,3 Вт/(м2-град)
[6—8 ккал/(м2-ч-град)] из-за малых скоростей газа в трубках; неравномер-
ность температур и концентраций газа по сечению аппарата. При наличии в
аппаратах К-39 горизонтальных теплообменников возможно их ремонтировать
без демонтажа решеток и повысить коэффициент теплопередачи 11,6—
14,0 Вт/(м2-град) [10—12 ккал/(м2-ч)], однако при этом также усложняется
конструкция аппарата, сохраняется неравномерность параметров в слоях, при
шахматном расположении труб возрастает сопротивление межтрубного про-
странства из-за окалины.
В аппаратах КПТ катализатор расположен в кольцевом пространстве
-между корпусом аппарата и центральными теплообменниками. В них меньше
потери тепла и газ охлаждается более равномерно, чем в аппаратах К-39, а
.ремонт центральных теплообменников возможен без выгрузки катализатора.
175
Таблица 36. Характеристика контактных аппаратов
Показатели Одинарное контактирование Двойное контактирование
К-39-4 КИТ | К-58-5
Производительность, т/сут Концентрация SO2, % 240 180—240 240 360 540 1030 1100 1500
7,5 5,0—6,5 7,5 7,5 7,5 7,5 9 0 9,5 99.8
Степень превращения, °/о 97,5 98,0 ' 98,0 98,0 98,0 98,0 99,6
Объем газа, тыс. м3/ч Габариты (диаметрХ Хвысота) 32 36 31,5 47 71 136 120 150
6,8X18 7,4X17 6,5X17,35 8X17,8 9X20,5 12x28,1 14X27,5 13,4x27,5
Масса металла, т 217 147 170 245 340 600 550 550
Загрузка катализато- ра по слоям, м3 72 67 75,6 113,4 164,7 324 300 300
I 16,8 14,4 13,2 19,8 29,7 56,5 69 58,5
II 14,4 12,0 12,0 18,0 27,0 51,5 54 65,5
III 19,2 19,0 16,8 25,2 32,4 72,0 54 72 +
IV 21,6 21,6 15,6 23,4 35,1 67,0 61,5 52,0
V —— — 18,0 27,0 40,5 77,0 61,5 52,0
Поверхность теплооб- менников после слоев, м2
I 1400 1150 — — 3860 3770
II 960 700 1400 1800 2530 4400 3860 1515
111 400 100* 70* 250 680 — 3860x2-!- 4816x2-1-
+ 1100 + 1135
IV — — 70* 250 340 1100
V 2000 2700 2000 2600 2960 4400X2 3860X2 Экономайзер
* Пласшнчатыс теплообменники.
К недостаткам этих аппаратов относится усложнение внутренних конструк-
ций перегородками „ карманами у центральных теплообменников.
Показатели наиболее широко применяемых в СССР контакт-
ных аппаратов для окисления SO2 приведены в табл. 36. Совре-
менные контактные аппараты большой мощности — более
1000 т/сут (по серной кислоте) имеют диаметр 12—14 м и высо-
ту 27—31 м, в них загружается около 300 м3 катализатора. С по-
вышением габаритов контактных аппаратов снизилась их удель-
ная производительность, увеличилась неравномерность парамет-
ров слоев, потребовалось усиление опор, снизилась надежность
конструкции. Эти обстоятельства вызывают необходимость но-
вых конструкторских решений для снижения расхода металла и
материалов, повышения однородности параметров в слоях, сни-
жения сопротивления, исключения перегревов катализатора, уп-
рощения ремонта и повышения надежности работы контактного
узла.
В нашей стране испытываются кассетный контактный аппарат (катали-
затор помещен в кассеты из проволоки), аппарат с внутренним теплообменом
[116], с вертикальным слоем [185], аппарат нестационарного окисления (с из-
менением направления движения газа), с кипящим слоем катализатора, аппа-
раты, работающие на концентрированном SO2 с применением давления, кис-
лорода, по схеме тройного контактирования, циркуляционным и комбиниро-
ванным схемам [129].
В НИУИФ совместно с Гинцветметом разработан контактный аппарат
для переработки газов повышенной концентрации — вплоть до 66,7% SOj
[124]. Схема аппарата ОТС — с отводом тепла серой представлена на
рис. 67.
В качестве охлаждающего агента для отвода избыточного тепла реак-
ции окисления применена сера, заключенная в запаянные трубки. Верхняя
часть трубок, в которой происходит конденсация паров серы, отделена от ре-
акционного пространства. Газ поступает в аппарат сверху, проходит через
зазоры между трубками и гильзами; далее он попадает на слой катализа-
тора непосредственно или через выносной теплообменник — для увеличения
температуры за счет тепла прореагировавших газов.
Гильзы закреплены в трубной решетке. Зазор между ними и трубками
рассчитывается по условиям теплопередачи так, чтобы скорость газа в зазоре
была оптимальной.
Конденсирующиеся в верхней части трубок пары серы, отдавая через
стеики трубок тепло конденсации, нагревают поступающий газ. Жидкая сера
стекает в нижнюю часть трубок, расположенную в зоне катализатора, где
испаряется за счет тепла реакции окисления, тем самым охлаждая катализа-
тор. Температура в зоне катализа поддерживается автоматически, так как
при температуре ниже 444,6 °C сера перестает кипеть и трубки отключаются,
с повышением температуры увеличивается движущая сила (Д/) и увеличи-
вается количество передаваемого тепла.
Использование аппарата ОТС, согласно расчетам, позволяет
путем использования высокотемпературного теплоносителя —
серы увеличить степень конверсии по сравнению с традиционны-
ми методами конверсии на 1,5—1,8% вследствие снижения гра-
диента температур между стенками трубок и серединой слоя,
позволяет исключить возможность инактивации катализатора
при возрастании скорости газов, поскольку рабочая температура
охлаждающего агента совпадает с температурой зажигания ка-
тализатора.
12—584
177
При использовании тепловых трубок можно вести окисление
в 1—3 слоях катализатора с выносными теплообменниками или
без них (в зависимости от концентрации исходного газа). Труб-
ки могут быть установлены в аппарате любой конструкции. Оп-
тимальной является конструкция аппарата с вертикальным рас-
положением катализатора (в вертикальных коробах) [9], при
этом число трубок сокращается по сравнению с обычными аппа-
ратами на порядок.
Сравнение аппарата ОТС с вертикальным слоем катализа-
тора с аппаратами, установленными на системах ПНР (мощ-
ность— 500 тыс. т/сут), показывает значительные его преиму-
щества:
Аппарат...................ПНР ОТС
Диаметр, м................ 16 9
Высота, м................. 32 28
Теплообменники............Выносные Внутренние
Расход металла на аппарат ОТК в два раза меньше, чем на
аппарат ПНР.
Проектно-конструкторскими отделами двух фирм — Канады и
ФРГ — найдены перспективные конструкции реакторов для высо-
копроизводительных сернокислотных установок мощностью до
5 тыс. т/сут: кассетные аппараты с радиальным потоком газа че-
рез вертикально расположенные кольцевые слои катализатора
и аппараты с горизонтальным секционированием каждого слоя
катализатора, где, благодаря увеличению количества проходов
для газа и более равномерной работе всего катализатора в слое,
удается примерно в 2 раза повысить количество конвертируемо-
го газа. Анализ особенностей новых разрабатываемых конструк-
ций контактных аппаратов позволяет заключить, что с целью
создания высокопроизводительных установок мощностью от 1 до
5 тыс. т/сут большое внимание уделяется обеспечению длитель-
ной эффективной работы катализатора как в первом, так и в ос-
тальных слоях. Чтобы улучшить работу слоя катализатора
(в первую очередь первого слоя), предлагаются форконтактные
аппараты принципиально новой конструкции контактной камеры,
например кассетные реакторы с радиальным потоком газа через
вертикально секционированный слой [118].
111.4.4. Теплообменники контактных узлов
Удельная площадь теплообменной поверхности зависит
от схемы контактного узла, концентрации SO2, коэффициентов
теплопередачи и др. В схемах ДК сернистый газ дважды нагре-
вают до температуры зажигания катализатора — перед I и
II стадией катализа, поэтому возрастают требования к надежно-
сти работы теплообменной аппаратуры. На 1 т/сут вырабаты-
ваемой серной кислоты требуется до 20 м2 теплообменной по-
верхности при работе на газах от сжигания серы или обжига
колчедана и до 40—60 м2 при работе на отходящих газах.
178
Теплообменники, в которых исходный газ нагревается за
счет тепла газового потока после последнего слоя катализатора,
называют внешними, теплообменники между слоями—проме-
жуточными. Они могут быть внутри контактного аппарата —
внутренние и вне контактного аппарата — выносные. Контакт-
ный узел обычно работает без подвода постороннего тепла —
автотермично. Поверхность внешнего теплообменника определя-
ется безразмерным параметром — А из соотношения [9]:
л_ __________^д__1
V0Cp - Ххк-Д/П 1
где Л’— коэффициент теплопередачи, ккал/м2-час-град; F—поверхность теп-
лообмена, м2; Vo — расход газа, м3/ч (объем газа приведен к нормальный
условиям); Ср — истинная теплоемкость газа при средней температуре в теп-
лообменнике, ккал/м3-град; t0, t,:— температура газа на входе — выходе из
контактного аппарата; Д/п— снижение температуры из-за теплопотерь, °C;
А — адиабатический разогрев газа, °C; х,-— конечная степень превращения,
доли.
Значения А в зависимости от концентрации SO2 при t0=
= 40 °C, /к = 430 °C, А/п = 20°С и хк = 0,98 приведены ниже:
Cs02, %............. 2 3 4 5 6 7 8 9 10
А................... 9,0 4,72 3,13 2,19 1,4 1,22 0,94 0,73 0,55
Наибольшие значения А соответствуют газам с низкой кон-
центрацией SO2 (2—4%), для автотермичной переработки кото-
рых нужно увеличение мощности теплообменников. При повы-
шении поверхности теплообменников следует учитывать возра-
стание потерь тепла в окружающую среду и влияние их на ве-
личину А. Результаты расчета поверхности внешнего теплооб-
менника контактного узла производительностью 240 т/сут при
различных концентрациях SO2 и потерях тепла (116) приведены
в табл. 37. [/С в ккал/(м2-ч-град)].
С учетом колебаний концентрации SO2, загрязнения и разру-
шения трубок берут запас поверхности теплообмена в пределах
25—40% расчетного значения. Для теплообменников с сегмент-
ными перегородками оптимальная скорость газа в трубках 6—
8 м/с, в межтрубном пространстве — 5—6 м/с. В большинстве
случаев по трубкам проходит горячий газ, а в межтрубном про-
странстве— холодный. Коэффициент теплопередачи составляет
Таблица 37. Зависимость площади поверхности внешнего теплообменника
от концентрации и потерь тепла
Содержание в газе SO2, % Pacxoi га- за, м3/ч мп. °C Л Г, м2
Л'-!0 /<-20
8 30 500 20 0.94 1 040 520
40 1,11 1 270 635
3 82 000 20 4.72 12 700 6 З.эО
40 7,15 19 200 9 000
179
8,1—10,3 Вт/(м2-град) [7—8 ккал/(м2-ч-град) ] при сопротивле-
нии 1—1,5 кПа. При производительности 360—1000 т/сут в теп-
лообменнике оставляют сегменты незаполненные трубками и ко-
эффициент теплопередачи увеличивается до 11,6—15,0 Вт/(м2-
•град) [10—13 ккал/(м2-ч-град)] без существенного повыше-
ния сопротивления. Наличие сегментных перегородок приводит
к отклонению потока от идеального обтекания труб; поперечное
сечение для прохода газа оказывается переменным из-за ци-
линдрической формы аппарата; между обечайкой, трубками и
перегородкой образуются байпасные потоки. Под влиянием аг-
рессивных веществ на поверхности теплообменника откладыва-
ются сульфаты железа. Вышеуказанные причины приводят к
снижению коэффициента теплопередачи на 60—70%, увеличе-
нию сопротивления аппарата [116].
Коэффициент теплопередачи определяют по уравнению:
1 еаха2
— , --- X . - а
ах 1 еос2
где Я] и «2 — коэффициенты теплоотдачи; е — поправочный коэффициент.
Для газовых теплообменников термическим сопротивлением стенки мож-
но пренебречь. Коэффициенты теплоотдачи рассчитывают по следующим
уравнениям:
а = NtA/d
для газа, идущего по трубкам
Nu = 0,023Re°,sPrM
для газа, идущего в межтрубном пространстве труб, расположенных в
шахматном порядке
Nu = 0,33Re°,6Pr°,33
где Nu— критерий Нуссельта (Nu = ad/%); Re — критерий Рейнольдса
(Re=K.’d/v); Рг — критерий Прандтля (Pr=36OO-Co-v/%); a — коэффициент
теплоотдачи, Вт/(м2-град), [ккал/(м2-ч-град)]; d — диаметр трубки, м (для
газа в трубках — внутренний диаметр, для межтрубного пространства-—на-
ружный диаметр); Л — теплопроводность газа, Вт/(м2-град),
[ккал/(м-ч-град)]; w— скорость газа, м/с; v — кинематическая вязкость га-
за, м2/с; Со — теплоемкость газа; ккал/(кг-град), кДж/кг-град.
Скорость газа в трубках — wTP и межтрубном пространстве —
щмт определяют по формулам:
V V
_________1 о_________________________v о______
^Р- 3600*0,785-nd2Ba ’ Шмт- / dH X
3600 • D 1—-/-
где п — число трубок; dm и dK— внутренний и наружный диаметр трубок, м;
D — наружный диаметр теплообменника, м; t — шаг между трубками, м
(обычно /=1,2—1,3).
При расчете коэффициента аг вводят поправочный коэффи-
циент е = 0,3—0,4, учитывающий отклонение газового потока от
поперечного и проскок части газа в зазорах. Установлены зна-
180
чения коэффициентов ai и аг в зависимости от скорости газа
для труб диаметром 25, 50 и 75 мм [9]. Диаметр теплообменни-
ков для контактного узла производительностью 1000 т/сут дости-
В теплообменниках с перекрестным током газа (без перего-
родок) в межтрубном пространстве скорость газа можно увели-
чить до 6—8 м/с, в трубках до 7—10 м/с. Коэффициент тепло-
передачи достигает 18—25 ккал/(м2-ч•град) при сопротивлении
1,5—2 кПа [9]. В качестве внешних указанные теплообменники
целесообразно включать последовательно (два аппарата), тогда
средняя разность температур увеличится от 0,7—0,75 до 0,88—
0,95 ее величины при полном противотоке.
Характеристика теплообменника с перекрестным ходом [116]
приведена ниже:
Расход газа, тыс. м3/ч.............................. 136
Площадь поверхности теплообмена, м2 3860
Трубки
число, мм...................................... 3280
диаметр, мм......................................57X3.5
длина, мм......................................... 7000
Диаметр аппарата, мм ............................... 5500
Доля газа в межтрубном пространстве . . . 0,7—1,0
Скорость газа, м/с
в трубках................................... 6,0
в межтрубном пространстве................4,5—6,3
Коэффициент теплопередачи
ккал/(м2-ч-град)................................ 16—22
Вт/(м2-град)................................18,6—25,6
Общее сопротивление, кПа........................ 0,981
Характеристика теплообменников установки ДК мощностью
1500 т/сут, работающей по короткой схеме на сере с охлаждени-
ем между IV и V слоями воздухом, приведена в табл. 38.
Во внешних теплообменниках, в отличие от остальных рабо-
тающих при более высоких температурах, возможно образование
сульфатов и коррозия как в трубном, так и в межтрубном про-
странстве. Трубки теплообменника могут оказаться полностью
забитыми сульфатом железа (у=1 г/см3). В результате корро-
зии обнаруживаются течи, пропуски газа в трубки, что уменьша-
ет степень использования SO2 и увеличивает вредные выбросы в
Таблица 38. Характеристика теплообменников установки ДК
мощностью 1500 т/сут на сере
Теплооб- менник после слоя По- верх- ность, м2 Диа- метр, мм Высо- та, мм Трубки Температура, °C
d, мм н, мм п, шт. по трубкам между трубок
вход ВЫХОД
вход ВЫХОД
I 3770 4000 12500 54/4 7900 2666 585 450 251 430
г 1515 3600 8200 57/3 4000 2120 512 435 147 251
III 1135 3600 7200 57/3 3000 2120 456 397 60 147
IV 4816 4500 13000 57/3 7900 3406 300 200 45 150
V 4816 4500 13000 57/3 7900 3406 397 300 150 256
181
атмосферу. Во внешних теплообменниках при температуре около
250 °C и нарушении осушки в газе присутствуют пары серной
кислоты и температура стенки труб может быть ниже точки
росы.
Зависимость точки росы от содержания паров воды в газе
перед контактным узлом представлена ниже (для технологиче-
ских расчетов рекомендуется принимать температуры на 10 °C
выше):
СН2О’ %<°6 » /, сс СН2О’ п»(об > t, =С t, С СН2О' г, эс
0,01 103 0,07 138 0,15 154 0,35 174
0,02 из 0,08 141 0,16 156 0,40 177
0,03 121 0,10 146 0.20 161 0,50 182
0.04 127 0,11 147 0,22 163 0,75 192
0,05 131 0,12 149 0,25 165 1,00 199
0,06 135 0,14 153 0,30 170
Конденсация кислоты происходит в большей степени в труб-
ках у входа холодного газа. Температуру стенки трубок опреде-
ляют по формуле
_ «А + Ма
СТ ~ CCj + <х2
где ai и а2—коэффициенты теплоотдачи трубного и межтрубного простран-
ства, Вт/(м2-град) [ккал/(м2-ч-град)]; t\ и t2—температура SO3 и S02
в рассматриваемом месте трубного пучка, °C.
Температура стенки труб повышается при байпасировании
части холодного газа мимо теплообменника, но это уменьшает и
коэффициент теплоотдачи в межтрубном пространстве. Конден-
сация кислоты происходит в трубках главным образом при пере-
работке низкоконцентрированного сернистого газа, так как при
этом выделяется мало тепла, и при нарушении нормы осушки.
В случае выхода газа из трубок теплообменника сверху кон-
денсат, стекая по трубкам, задерживается потоком газа, вызы-
вает их коррозию, забивание сульфатом, рост сопротивления.
Конденсация паров серной кислоты может усиливаться в период
пуска контактного аппарата, когда температура последних слоев
составляет 330—350 °C. Например, при подаче газовой смеси по
пусковой схеме через теплообменник: неизбежно конденсируется
кислота в трубках, поэтому использование внешнего теплообмен-
ника в этой схеме целесообразно только в период разогрева
контактного узла на воздухе и при нормальном режиме работы..
В переходном пусковом режиме следует часть холодного газа
подавать минуя внешний теплообменник — по линии байпаса.
Температуру газа на входе в абсорбер (^абс) —после внешне-
го газового теплообменника ориентировочно определяют по фор-
муле
абс = + 27 ха
где t0 — температура газа на входе в контактный узел, °C; х— степень пре-
вращения, доли; а — исходная концентрация SO2, %.
182
При проектировании можно предусмотреть повышение темпе-
ратуры стенки труб внешнего теплообменника на 10—15 °C, за
счет байпасирования части газа мимо дополнительного малога-
баритного фортеплообменника, установленного последовательно
с основным внешним теплообменником. В этом случае байпаси-
руемая часть газа значительно больше, чем при байпасировании
двух теплообменников.
В системах мощностью 450 тыс. т в год (поставки ПНР) в
теплообменнике, установленном после сушильной башни перед
I абсорбером для охлаждения газа за счет подогрева холодного
газа, наблюдается конденсация серной кислоты. Кислота появ-
ляется из-за наличия влаги в газе и конденсируется на стенках
труб в месте входа холодного воздуха в межтрубное простран-
ство.
В системах на сере содержание влаги Сн2о в газе больше,
чем на колчедане за счет влаги, образующейся при сгорании уг-
леводородов Су_в — примесей серы:
Cv-B, % . . . . — 0,03
CH2O.% (об.) . . 0,01 0,015
/конд, °C ... . ЮЗ 108
0,04 0,06 0,1 0,2 0,3
0,018 0,028 0.045 0,085 0,13
112 118 128 142 150
Таким образом, при использовании серы, например сорта
9990, содержащей 0,06% органических примесей, содержание па-
ров воды в газе вдвое превышает норму, а температура конден-
сации на 10 °C выше, чем для систем на колчедане.
Для исключения конденсации проводят байпасирование теп-
лообменника после IV и V слоев, что существенно уменьшает
количество воздуха и коэффициент теплопередачи в межтруб-
ном пространстве. Кроме того, для уменьшения скорости возду-
ха и соответственно коэффициента теплопередачи в самом хо-
лодном сечении теплообменника можно увеличить высоту каме-
ры для ввода воздуха с 1,2 до 2 м. Байпасирование одного теп-
лообменника позволяло увеличить температуру стенки теплооб-
менника IV на 11 °C по сравнению с обычной схемой. При этом
/Ст превышает точку росы для газа влажностью 0,02%. Повыше-
ние высоты камеры до 2 м дает повышение температуры до
127 °C, что позволяет работать без конденсации кислоты на газе
влажностью 0,04%. Можно работать при значительном содер-
жании в газе органических примесей (более 0,1%), повышая
температуру газа на II абсорбции. Тогда байпасирование тепло-
обменников после слоев катализатора будет производиться сле-
дующим образом:
Показатели После IV и
\ слоев
(/абс=200 °с)
Якам, М 1,2 2
/ст, °C 104 116
После IV слоя
Па6с = 200 °C)
После IV слоя
(С,бс=230°С)
12,2 2
115 127
1,2 2
130 144
Для повышения тепловой устойчивости систем ДК иногда ис-
пользуют подогрев газа после промежуточного абсорбера в фор-
183
теплообменнике горячим газом, выходящим из контактного ап-
парата, затем в основном внешнем теплообменнике — газами,
выходящими из фортеплообменника при температуре 350—
400 °C, либо проводят I стадию абсорбции в горячем режиме
при температурах выходящего газа 95—140 °C, что, однако, свя-
зано с затруднениями из-за повышенной агрессивности среды
при температурах выше 70—80 °C. Применяется специальная
схема горячей абсорбции (температура кислоты НО—140 °C), по
которой циркуляционный насос работает при температуре не бо-
лее 80 °C с возвратом охлажденной кислоты в смесительный ба-
чок после абсорбера и соответствующей химической защитой
оборудования [78].
Для разогрева и пуска контактного узла используют пусковой подогре-
ватель, который состоит из топки и теплообменника. Воздух или сернистый
газ нагревают в межтрубном пространстве теплообменника, по трубкам кото-
рого проходят горячие топочные газы. Контактные узлы производительностью
ди 540 т/сут оборудованы дымососом для протягивания топочных газов в
дымовую трубу, а производительностью 1000 т/сут—вентилятором высокого
давления, и дымосос не требуется. Для повышения степени использования
тепла топочных газов — экономии топлива целесообразно устанавливать по-
следовательно два теплообменника. Рационально использование электроподо-
гревателя.
В СССР для контактных узлов выпускаются нагнетатели раз-
личных марок [9]. Максимальная производительность отечест-
венных нагнетателей составляет 100—180 тыс. м3/ч и напор
27,4—39,2 кПа. Контактную массу из контактных аппаратов сов-
ременных заводов выгружают с помощью водокольцевых ва-
куум-насосов [9].
III.4.5. Расчет контактных узлов
По условиям осуществления процесса окисления SO2 и
принципу теплоотвода контактные аппараты можно разделить на
следующие группы:
1. Аппараты со стационарными слоями катализатора и про-
межуточным теплообменом (наиболее широко применяемые);
2. Аппараты со стационарными слоями катализатора и непре-
рывным теплообменом;
3. Аппараты с кипящими слоями катализатора и непрерыв-
ным теплообменом;
4. Аппараты с нестационарным режимом окисления и тепло-
отвода в слоях катализатора.
Для расчета контактного узла выдается задание по произво-
дительности, составу газа, числу стадий, скорости газа, типу
контактной массы, степени превращения. Расчетом по составлен-
ному материальному и тепловому балансу определяется: режим
температур, концентраций и степеней превращения контактного
узла, диаметр аппарата и высота слоев катализатора, поверх-
ность теплообменника и размеры теплообменников, гидравличе-
ское сопротивление.
184
Каждый контактный аппарат имеет определенную устойчи-
вость, т. е. способность сохранять стационарное состояние при
изменении входных параметров в определенном интервале зна-
чений. Условие устойчивости одного верхнего слоя катализатора
с промежуточным теплообменником имеет вид
di к , , 1
Ли' < 1 " А
dt'K
где ~м,~ —параметрическая
я* н
чувствительность слоев
катализатора, показы-
вающая, насколько изменится температура газа на выходе из слоя при из-
менении его температуры на входе на 1 °C; А— параметр промежуточного
теплообменника (см. стр. ).
Байпасирование части газа мимо теплообменника не изменя-
ет область устойчивых режимов, и для расчета устойчивости ап-
парата можно пользоваться этим выражением.
Расчет параметрической чувствительности производят с по-
мощью диаграммы т—х, на которую наносят расчетную кривую
для слоя при значениях начальной и конечной степени превра-
щения (л-ц и л‘к) и температуры в начале слоя tn и определяют
необходимое время контакта т. Затем строят линию tK'=tH+ At
и определяют х'к; при определенном т получают изменение Дл'к.
Исходя из полученного хк, рассчитывают f к и вычисляют
•— б:
Для контактного аппарата с промежуточными теплообмен-
никами предел устойчивости будет 1 + 1/А = 2,15, для контактно-
го аппарата с вводом холодного газа после I слоя — 2,37. При
двукратном запасе катализатора «запас устойчивости» аппарата
с промежуточными теплообменниками составляет 20 °C, т. е.
при снижении температуры газа на входе в I слой больше, чем
на 20СС, аппарат затухнет. При устойчивой работе I слоя II и
последующие слои работают также устойчиво. В аппаратах с
промежуточным вводом холодного воздуха или отводом тепла
внешними теплоносителями (вода, пар) отсутствует теплообмен
между исходным и прореагировавшим газом, поэтому их устой-
чивость значительно выше.
При расчетах оптимального режима принимается равномер-
ное распределение температур и концентраций в поперечном се-
чении слоя. На практике по разным причинам имеются отклоне-
ния от средней температуры, что может приводить к снижению
степени превращения, поэтому необходим избыток контактной
массы, компенсирующий неравномерность параметров в аппа-
рате.
Для снижения неравномерностей в контактном аппарате ус-
танавливают смесители, направляющие лопатки и другие уст-
ройства, повышающие равномерность подвода, распределения и
отвода газовых потоков. В этом аспекте большой интерес пред-
185
ставляют работы по гидродинамическому и математическому мо-
делированию, на основе которых в последние годы получила
развитие теория масштабного перехода в химической техноло-
гии. Теория масштабного перехода основана на представлении о
том, что решающим фактором, обусловливающим снижение’эф-
фективности аппаратов при увеличении их размеров, является
возникновение различных гидродинамических неоднородностей,
в первую очередь, — неравномерностей распределения потоков по1
сечению аппаратов ,[122].
Степень использования катализатора в конце каждого слоя
больше, чем в начале, при этом изменение степени превращения
до оптимальной кривой (Ах/) и после нее (Ах/7) связаны соот-
ношением
d (dx/dx) Xi^ d (dt,'dt) xt
----dt---- =----dt----SXi
Параметры, удовлетворяющие этим условиям, находят путем
подбора.
Массу катализатора для загрузки по слоям контактного ап-
парата (Vt) определяют по формуле
V^CiV^
где С, — коэффициент запаса; Vo — расход газа, ма/с; т— время контакта, с.
Коэффициент запаса учитывает ряд поправок: на снижение
активности катализатора в процессе эксплуатации, на устойчи-
вость работы аппарата, на неравномерность распределения и
и смешения потоков газа.
Фактическая продолжительность контакта на второй стадии
катализа систем ДК больше по сравнению с расчетной на
I слое — в 1,5 раза и на II слое — в 2 раза.
Используют также поправку на фактическую активность ка-
тализатора (Ci), отличающуюся от стандартной:
Cj = Кст/ К а
где Лет — константа скорости стандартного образца; Кн — константа скоро-
сти фактическая — по паспорту нли контрольному испытанию катализатора.
Диаметр контактного аппарата находят в соответствии с за-
данной скоростью газа или гидравлическим сопротивлением сло-
ев катализатора, которое определяется по уравнению [9]
где ДР—перепад давления слоя, кге/м2; f — коэффициент сопротивления;
р — плотность газа, кгс-с2/м4; U — лииейная скорость газа, м/с; S — внешняя
удельная поверхность слоя зерен, м2/м3; ;е — доля свободного объема (пороз-
иость слоя); Н—высота слоя зерен, м.
Коэффициент сопротивления зависит от критерия Рей-
нольдса:
f = 8/C/Re + Кя
где Re=4(7/Sv (v — кинематическая вязкость, м2/с).
186
Значения коэффициентов Кст и /<1Г для катализаторов СВД в
виде гранул и таблеток:
Коэффициенты.....................Яст Ки
Гранулы СВЛ ...... 8—9 0.6—0,65
Таблетки..........................6—7 0,5—0,55
При Re = 50—500 величина f может быть аппроксимирована
с точностью до 10% выражениями:
/ = 4,00-Re~+2ti (таблетки и гранулы)
/ = 4,20-Re-0,3 (кольца)
Гидравлическое сопротивление слоя (ДР, Па) можно с доста-
точной точностью определить и по более простой формуле
[9, 12]:
ДР= ббЗО-уоРоАДН
где у — плотность газа при средней температуре в слое, кг/м3; w— фиктив-
ная скорость газа, считая на живое сечение аппарата при средней темпера-
туре в слое (для гранулированного ванадиевого катализатора wе+0,4—
—0,45 м/с); И — высота слоя катализатора, м; 6630 — коэффициент, выведен-
ный на основе практических данных.
В сернокислотных системах, работающих на сере по корот-
кой схеме, наблюдается ускоренный рост гидравлического сопро-
тивления первого слоя катализатора, вследствие осаждения на
нем твердых частиц, поступающих с газом. На основе анализа
динамики роста гидравлического сопротивления промышленных
аппаратов [128] было получено эмпирическое уравнение, опи-
сывающее увеличение гидравлического сопротивления Р в Па со
временем (/ в мес.):
/ rcso с3 \
1 — 0,294- 10-«-К ----Р2— -I
где К — коэффициент, равный 76 м-1 (это среднее значение без учета вы-
бросов); V — газовая нагрузка, №/ч; Cso2—концентрация диоксида серы на
входе в контактный аппарат, % (об.); С3 — содержание золы в отфильтро-
ванной сере, % (масс.); S — сечение слоя катализатора, м2. Значения V, Cso..,
С берутся усредненными за период от пуска системы до момента t.
Результаты проведенных исследований показали, что для ра-
боты без пересева I слоя гранулированного катализатора в тече-
ние двух лет (увеличение гидравлического сопротивления в
5 раз) зольность серы не должна превышать 0,0015%. Отмечен
существенный выигрыш от применения в I слое колец 12X12
или гранул диаметром 8 мм. Результаты расчета оптимальных
режимов 4 и 5-слойных контактных аппаратов с промежуточны-
ми теплообменниками приведены в табл. 39.
Пример упрощенного расчета. Рассчитывается контактный аппарат про-
изводительностью 500 тыс. т/год, работающего по схеме ДК с вариантом
слоев 3 + 2 на газах от сжигания серы с содержанием 9% SO2 при степени
превращения 99,85%. Число рабочих дней в году — 333. Охлаждение газа
187
Таблица 39. Оптимальный режим контактных аппаратов
Слой Параметры Одинарное контакти- рование Двойное контакти- рование (34*2)
а=7.5 6=10,5 д = 9 £’=12 я=8 6=10 0=9 6=9 а=10 6=8
I Л'к 0,707 0,686 0,656 0,695 0.646 0.615
Ги 440 440 430 430 425 420
Л 591 586 596 577 588 591
т 0,613 0,571 0,724 0,50 0,53 0,67
II \’к 0.92 0,875 0,879 0,864 0,833 0,807
7, г 451 482 470 484 485 479
Тк 497 522 526 523 532 532
т 0.834 0,428 0,542 0,37 0,43 0,62
III W 0.971 0.949 0,957 0,94 0,92 0,90
Т„ 436 450 442 454 461 459
Л 446 4ОО 462 471 482 484
т 1,271 0,771 1,094 0,65 0,74 1,06
IV 0,971 0,949 0,957 0 0 —
Л’к 0,98 0.974 0.98 0,956 0,944 0,929
Л, 429 436 432 430 430 430
Тк 431 442 438 445 454 462
т 1,418 1,025 1,616 0,28 0,46 0,89
V Л’к — 0,98 — 0,968 0,963 0.97
т„ —- 429 —. 420 432 420
Тк — 430 — 431 433 421
т — 1,101 — 0,04 0,09 0,50
S.v 0,98 0,98 0,98 0,998 0,997 0,997
4,136 3,896 3,976 1,84 2,25 2,34
уд — — — 5.5 4.8 4.2
т - время соприкосновения, с; .4 — параметр теплообменника.
после I, II, III слоев — в теплообменниках, после IV слоя — добавлением воз-
духа, после V слоя — в экономайзере (см. рис. 49). Катализатор гранулиро-
ванный СВД, верх I слоя — СВС.
Объем газа (при нормальных условиях), поступающего в контактный
аппарат
500 000-1000-21,9
333-24-98-0,09-0,9985 = 160000 м3/ч
где 21,9 и 98 — мольный объем SO2 и молекулярная масса серной кислоты;
333 и 24 — число рабочих дней в году и часов в сутках; 0,09 и 0,9985 — со-
держание SO2 в газе и степень превращения, доли единицы.
На основе этих данных рассчитан приведенный в табл. 40 материальный
баланс контактного аппарата.
Внутренний диаметр контактного аппарата:
D== V3600-0,785^
где V—расход газа, м3/ч; w— линейная скорость газа, м/с (принимается
0,25—0,3 м/с)
„ 1Л 160 000
F 3600-0,785-0,3 — Id,/ м
188
Таблица 40. Материальный баланс контактного аппарата
Первая стадия катализа
Приход | Расход
компонент кг | ..з 1 1 о 1 0 ! i м3 j “ <1
so. 41200 14400 9 2000 700 0,46
о2 27300 19200 1 9 17500 12350 8,05
n2 158000 126410 79 158000 126400 82,54
so3 — — — 49000 13700 8,95
Всего: 226500 160000 226500
Вторая стадия катализа
Приход Расход
компо- нент газ на IV слой о/ , 0 воздух на V слой кг М3 0/ /О
кг | м3 кг | м3
so. 2000 700 0,48 57 20 0,0134-
О, 17500 12350 8,5 3150 2200 20163 14210 9,5
N 2 158000 126400 90,02 10400 8300 168400 134700 90,1
so3 — — — — — 2430 680 0,4
Всего: 177500 13550 191050
Наружный диаметр контактного аппарата с учетом футеровки составит
14 м.
Повышение температуры за счет тепла реакции при полном окислении
9%-ного SO2 составляет 252°C.
Температурный режим определен с учетом выбора конечных температур-
в слоях (?к = С + ЛхХ) такими, чтобы достигаемая степень превращения на
I слое была 10%, а на последних слоях на 0,5% ниже равновесных. Степень
превращения SO2 по слоям контактного аппарата и температурный режим
приведены в табл. 41. Общая степень превращения составляет
=0,95 + (1 — 0,95)-0,97 = 0,9985
Протекание процесса ДК изображено на диаграмме t—х (рис. 68).
Таблица 41. Температура и степень превращения
по слоям контактного аппарата
Слой Температу- ра. СС Степень пре- вращения на вы- ходе из слоя, доли Слой Температу- ра. °C Степень пре- вращения на вы- ходе из слоя, доли
на входе на выходе на на входе выходе
1-я стадия катализа 2-я стадия катализа (9% SO2, 12% О,) (0,48% SO2, 8,5% О2) I 430 596 0.656 IV 435 449 0,94 II 470 526 0,879 V 430 431 0,97 III 442 460 0 95
18»
Газ, идущий на IV слой при
РИС. 68. Диаграмма t — X контактного
аппарата ДК:
/—/ — адиабаты; Л’рР Л*л9 — равновесные кривые.
Требуемую поверхность теплообменни-
ков ориентировочно можно определить
приняв условно коэффициент теплопереда-
чи К = 50,28 кДж/(м2-ч-град)
12 ккал/(м2-ч-град)] и теплоемкость газов
Ср= 1,42 кДж/м3 (0,34 ккал/м3).
В теплообменнике после I слоя газ ох-
лаждается от 596 до 470 °C. Тепловая на-
грузка теплообменника:
Q= 160 000-0,34-(596 —470) =
= 6 860 000 ккал/ч (288 ГДж/ч)
этом нагревается на
160 000 (596— 470)
139 300
т. е. при входе в теплообменник
ность температур:
596 ----> 470
160 185
430 -<--- 285
он имеет 430—145=285 °C. Средняя раз-
166 4- 185
А/ср =-----£----= 175,5 °C
Площадь поверхности нагрева
теплообменника составляет
Q 6 860 000
F= КЫ = 12-175,5
= 3080 м2
Аналогично рассчитанная поверхность теплообменников составляет: пос-
ле II слоя — 1540 м2, после III слоя (фортеплообменник) — 1800 м2 и газо-
воздушные теплообменники — 4850 м2.
Точное определение габаритов теплообменников и коэффициентов тепло-
передачи возможно лишь при их полной конструктивной разработке с учетом
существующих стандартов и поправок на среднюю разность температур по
схеме тепловых потоков.
Для расчета требуемого объема катализатора фиктивное время сопри-
косновения (т) определяют, используя диаграммы [9, с. 522—527], либо
уравнение Борескова — Иванова, по которому вначале определяют значение
dxjdx для нескольких участков слоя. Затем строят график (dt/dx)—х, пло-
щадь которого соответствует времени соприкосновения, либо рассчитывают
аналитическим путем по формуле
Vi (dx/dx)B 4- (dr/dxj, д
2 •
(dr/dx'in-t -Г (dx!dx\n
ф 2
Для достижения необходимой точности при расчете аналитическим путем
количество и интервалы участков слоя подбирают так, чтобы каждое после-
. дующее значение dxfdx не превышало предыдущее более, чем в -~2 раза.
Уравнение Борескова — Иванова для определения значений dx/dx имеет
вид:
dx а 1—0,5ах 1—0,2х 1
dx ~~ kc ~b — 0,сах 1—х х- 1—0,5ах
_1 — Кр(1 — х)2 ‘6—0,5ах_
где а, Ь, х — начальные концентрации SO2, О2 и степень превращения, доли
единицы; kc— константа скорости, с_1-Па-1; Кх— константа равновесия,
Па-0-5; т — время соприкосновения, с.
190
Таблица 42. Значение л по участкам I слоя катализатора
(верх СВС, низ СВД)
Участок Степень превращения, Температура. °C т. с
в начале 1 в конце в начале 1 в конце
1 0 0.05 430 443 0,12
2 0,05 0,1 443 452 0,04
3 0,1 0,2 452 480 0,04
4 0.2 0,3 480 506 0,022
5 0,3 0,4 506 531 0,05
6 0,4 0,5 531 556 0,05
7 0,5 0,6 556 581 0,07
8 0,6 0,656 581 596 0.06
2т=0,452
Для I слоя в начале I участка (хо=О, /=430 °C) значение dt/dx=3,3,.
а в конце участка (xi = 0,05, /=443 °C), dx/dx=l,5.
3,3+ 1,5
т = 0,05-------= 0,12
Значения т для участков I слоя катализатора приведены в табл. 42.
Таким же способом рассчитано время соприкосновения на остальных
слоях.
Высота I слоя составляет
Н1 = 0,3-0,452-4 ~ 0,54 м s; 540 мм
где 0,3 — скорость газа, м/с; 0,452 — время соприкосновения, с; 4 — коэффи-
циент запаса.
Аналогично определяем #2=330 мм, #3=460 мм, #4=320 мм,.
Дб=400 мм. Для улучшения равномерности распределения газа принимаем-
#2—#4=400 мм.
Удельный расход катализатора (g) составляет
0,785•13•72 (540 + 400 + 460 + 400 + 400) • 1000
g =----------------------1^50-------------------= 218 л/(т • сут)
Результаты расчета загрузки катализатора в контактный аппарат мощ-
ностью 500 тыс. т серной кислоты в год приведены в табл. 43.
Гидравлическое сопротивление I слоя определяем по приведенной ранее
формуле. Скорость газа в рабочих условиях при Р=1,1 ат (0,1078 МПа) и.
430+596
/ср=-----L---= 513 °C
(513 + 273)
ш= 0,3 t ' = 0,79 м/с
Плотность у=0,59 кг/м3 определена из соотношения
aVso2 + *Vo2 + C?N2 273
v = 100 ‘ 273 +г ‘1 ’1
где Cso2 = 2,86%; Co2 = 1,43%; Cn3=1,25%.
Сопротивление I слоя высотой 0,54 м составляет
ДР= 6630-0,59°>’-0,791>7-0,54 = 1550 Па
Сопротивление остальных слоев рассчитывают аналогично.
19t*
Таблица 43. Загрузка катализатора (расчетная)
Слой Расход газа, м3/с т, с Коэффициент запаса Расход катали- затора, м3
I 44,4 0,45 4,0 80,2
II 44,4 0,54 2,0 48,1
III 44,4 0,80 1,3 63.2
IV 38,8 0,80 1,5 46.5
V 41,7 0,70 2,0 58.5
Пособием для упрощенных расчетов отдельных стадий контактного
окисления диоксида серы служат и другие источники [128].
III.5. СУШКА ГАЗА И АБСОРБЦИЯ ТРИОКСИДА
СЕРЫ [3, 4, 12, 130, 131]
111.5.1. Влажность газов и кислотообмен
в цикле сушки-абсорбции
В контактных системах, работающих по схемам сухого
катализа, газ перед контактным узлом подвергается очистке от
паров воды.
Пары воды не оказывают вредного влияния на работу вана-
диевой контактной массы, если газы, содержащие эти пары, по-
ступают в контактный аппарат при сравнительно высокой темпе-
ратуре (порядка 400°C). Но если в контактный узел подавать
газ с тем содержанием воды, с каким он выходит после мокрой
очистки, то практически очень осложнится процесс абсорбции с
получением олеума. Кроме того, если в контактный узел посту-
пает холодный газ, содержащиеся в нем водяные пары вместе
с SO3 могут давать пары H2SO4, которые при осаждении на
стенках труб теплообменника будут его разрушать.
Опыт работы показывает, что при учете этих обстоятельств,
особенно второго из них, допускаемое содержание паров воды в
газах после сушки должно быть порядка 0,08 г/м3. Разумеется,
содержание паров воды в газах на выходе из сушильной башни
не может быть меньше величины, определяемой давлением па-
ров воды над кислотой, орошающей башню при данной темпе-
ратуре (табл. 44).
Из этих данных следует, что при орошении сушильной баш-
ни кислотами концентрацией 90—95% и температуре 35—50 °C
норма содержания паров воды в газах после сушки 0,08 г/м3,
или 0,01% (об.), вполне достижима. Но при использовании в ка-
честве сырья серы влажность газа (Сн,о) значительно увеличи-
вается за счет сгорания углеводородов (Су-В).'
Cv-в в сере, % (масс.) 0.03 0.04 0,06 0.1 0.2 0,3
Сн2о в газе, % (об.) 0,015 0,018 0,028 0,045 0,085 0,13
Поэтому при использовании газов от сжигания серы осушку
газа стараются проводить более концентрированной кислотой.
192
Таблица 44. Давление паров Н2О над серной кислотой
90%-ная кислота 95 %-ная кислота
Температу- давление паров давление паров I
i ВО - ьг ! < ВОЛЫ. Г'М'
ММ ’’!. С Г. i J!a 1 ММ р 1. С 1. J !,а
35 0,0179 2.38 0,019 0,00150 0.2 0.0016
40 0.0265 3.52 0.0285 0,00235 0,312 0,00242
45 0,0395 5,25 0.0426 0,00370 0,49 0.004
50 0.0580 7,70 0,062 0,00877 1,16 0,0094
Над такой кислотой (около 98% H2SO4) существует некоторое,
хотя и очень малое, парциальное давление паров H2SO4. В зави-
симости от температуры пары H2SO4 и Н2О могут образовать
некоторое количество тумана.
При поглощении паров воды серной кислотой выделяется
большое количество тепла, вследствие чего кислота нагревается
и частично испаряется. Пары кислоты, смешиваясь с более хо-
лодным газом, поступающим на осушку, конденсируются с обра-
зованием тумана. Туман серной кислоты уносится газовым пото-
ком и вызывает разрушение аппаратуры, расположенной по
схеме после башен. Поэтому допустимое содержание тумана в
газе после его осушки строго регламентируется — оно не должно
превышать 5 мг/м3 сухого газа. В табл. 45 приведены данные о
содержании тумана в газе после сушильных башен контактных
сернокислотных заводов в зависимости от температуры и кон-
центрации серной кислоты [12].
Из приведенных данных видно, что в случае, если сушильная
башня одна, для ее орошения при 35—40 °C в принципе могут
применяться кислоты концентрацией H2SO4 в пределах 90—
98%. Практика работы показывает, что для орошения следует
.применять кислоты концентрацией 93,5—98,5%.
Если устанавливаются две последовательные сушильные башни, то пер-
вая из них орошается 93±0,5%-ной, а вторая 98—98,5%-ной H2SO4. При не-
обходимости вывода из системы слабой кислоты (например 76%-ной кисло-
ты для суперфосфатного цеха или 70%-ной кислоты, подаваемой на упарива-
ние до 92,5—94,0% для достижения возможно большего выхода олеума) пер-
вая сушильная башня орошается кислотой, имеющей концентрацию вводимой
кислоты.
Если продукция выпускается только в виде 92,5—94%-ной кислоты, мо-
жет быть установлен один абсорбер, если же выпускается также олеум, то
два абсорбера. Один абсорбер, а также второй из двух абсорберов должны
Таблица 45. Содержание тумава (в мг/м3)
Концентра- ция кисло- Tbi , % Температура, °C
40 1 60 | 80 100
90 0.6 2 6 23
95 3 11 33 115
98 9 19 56 204
13—584
193
орошаться кислотой, над которой давление паров SO3 и Н2О практически
равно 0, что диктуется требованиями полноты абсорбции. Этим требованиям
удовлетворяет только 98%-ная кислота. Первый абсорбер при работе систе-
мы с выпуском олеума орошается олеумом с концентрацией, близкой к про-
дукции (24—18,5% SO3 своб.). Такой олеум обладает и наименьшим корро-
зионным действием, чем олеум более низких и более высоких концентраций.
При схеме с двойным контактированием олеумный абсорбер может быть
установлен также в шунт.
Температура газа на входе в сушильную башню должна
быть 25—30°C (но не выше 35°C); при более высокой темпера-
туре с газом вводится много водяных паров и получение всей
продукции в виде олеума становится невозможным. В сушиль-
ной башне температура газа повышается примерно до 50 °C. На
входе в олеумный абсорбер ее поддерживают в пределах 60—
100°C (после ангидридного холодильника). На некоторых заво-
дах (особенно в случае отсутствия ангидридного холодильни-
ка) эта температура выше — доходит до 180 °C. В этом случае
надо увеличивать орошение олеумного абсорбера, что приводит
к росту нагрузки на холодильники этого абсорбера. Температу-
ра газа после олеумного абсорбера достигает 50 °C. Температу-
ру орошающих кислот поддерживают в пределах 35—45 °C,
а вытекающих из башен — 50—60 °C.
При повышенной влажности газа (выше 0,07%), например
при получении серной кислоты из серы по «короткой» схеме, для
уменьшения образования тумана абсорбцию ведут только в мо-
ногидратном абсорбере при высокой температуре орошающей
кислоты (80—90 °C на входе в абсорбер и 110—120 °C на выхо-
де). С повышением температуры уменьшается возникающее
пересыщение паров серной кислоты и туман не образуется или
же его образование значительно уменьшается [12]. На одном из
заводов через олеумный абсорбер пропускают до 30% всего по-
ступающего на абсорбцию газа (при 275—300°C). После сме-
шения выходящего из олеумного абсорбера газа (температура
56 °C) с остальной частью газа, который при 225—240 °C на-
правляют в моногидратный абсорбер. Указанная схема при
влажности газа перед контактным аппаратом 1,8 г/м3, или
0,22% (об.), позволяет получить в виде олеума не менее 20%
продукции.
На наших заводах обычно устанавливают одну сушильную
башню и два абсорбера (последний абсорбер орошается
98%-ной кислотой), на зарубежных — одну сушильную башню,
орошаемую 93 или 98%-ной кислотой. Если на системе не полу-
чают олеум, то устанавливают один абсорбер, орошаемый
98%-ной кислотой, если же имеются два абсорбера, олеумный
абсорбер иногда устанавливаются в шунт.
На современных заводах сушильные и абсорбционные башни
оборудованы фильтрами для улавливания из газа брызг кисло-
ты: на системах ПНР устанавливается дополнительный слой на-
садки, проволочные сетки; на сушильных башнях систем, рабо-
тающих на сере, — полипропиленовые патроны, на колчедане —
194
полимерные фильтры из фторпласта в виде сеток объемного
плетения. На всех абсорбционных башнях устанавливаются пат-
ронные фильтры с фторином.
В большинстве случаев сушильные и абсорбционные башни
имеют объединенный кислотооборот.
Количество воды, поступающее с газами из промывного от-
деления в сушильные башни при работе цеха на газах от обжи-
га пирита, а также на загрязненной сере, в расчете на 1 т (1 кг)
продукционного SO3 составляет в кг (г)
<ГВн2О'18 /Cso2il-80 22 500^0
G- 1000 (р_фрН2о)22Л / ;00-22,4 = Csopi (Р - <Р^н2о)
соответственно на 1 т (кг) H2SO4
18 400<рРН2о
~ Сьо2Ц (Р — Ч Рн2о)
где Р — полное давление газовой смеси перед сушильной башней, Па;
Рц2О~ полное давление паров воды при определенной температуре, Па;
Д— степень насыщенности водяных паров; Cso2—содержание SO2, считая на
сухой газ, %; 1] —степень использования SO2 в продукции, %.
Концентрация газа, при которой обеспечивается заданная
концентрация продукции, определяется из следующего выра-
жения;
1000 —ПзОч 22,5срРН|>о
nso3 Cso2n(P —ф) Рн2о
где П so3 —содержание общего SO>, в заданной продукции, %.
Левая часть выражения показывает массу Н2О в кг на 1 т
продукционного SO3, в правой части стоит масса Н2О в кг в рас-
чете на 1 т SO3, приходящего с газами (см. предыдущее выра-
жение). Решая уравнение в отношении CsOg, получаем
22,5<рРн,оПзо3
С5°2 > т] (Р — фРн„0) (100 — П5о3)
По этому выражению определяется минимальная величина
обеспечивающая получение продукции заданной концентрации.
Например, стандартный олеум (85,3% SO3 общ., 20% SO3 своб.) можно
получить (при условиях после промывной башни: <р = 1,0; Z = 30°C, т. е.
^>Н,О=31,8; Р = 745 мм рт. ст.) только при концентрации SO2 не меньше
5,9%. При тех же условиях стандартная кислота (92,5% H2SO4; 75,5% SO3)
может быть получена при концентрации SO2 не меньше 3,15%, наиболее сла-
бую кислоту (75% HjSOa), предусмотренную ГОСТом, можно получить при
концентрации SO2 не меньше 1,6%,.
Кислотооборот (в т H2SO4) в цикле сушки-абсорбции в рас-
чете на 1 т продукции H2SO4 составляет
6Пмн,504ПкН25о4
Л= 100 000 (Пмн2зо4 — Пкн2зо4)
13
195
Кислота
Кислота
Олеум Разбавленная
б сушильная кислота в
РИС. 69. Схемы кислотооборота между сушильными и поглотительными
башнями:
а — без ввода кислоты со стороны; б — с вводом кислоты со стороны, без отвода разбав-
ленной кислоты; в — с вводом кислоты со стороны и отводом разбавленной кислоты;
г — с вводом кислоты со стороны и концентрированием разбавленной сушильной кисло-
ты; д — с вводом кислоты со стороны, отводом разбавленной кислоты и установкой до-
полнительной поглотительной башни; / — сушильные башни; 2 — поглотительные башни
для 98%-ной кислоты; 3—’поглотительные башии для олеума; 4 — концентратор; 5 —
дополнительная башня с подачей кислоты в башии 2 нлн 3.
где G — масса воды, улавливаемой в сушильной башне на 1 т H2SO4 про-
дукции, кг; Пмн25О4 и Пнн2зо4 — содержание H2SO4 в кислоте, идущей из
абсорбера в сушильную башню, и во встречной кислоте соответственно, %.
Эта величина характерна для случая, когда вся необходимая
дополнительная вода для образования продукции подается в
циркуляционные баки абсорбционных башен, а из сушильной
башни продукция не выдается. При выпуске продукции в виде
92,5%-ной кислоты из сушильной башни величина кислотообо-
рота будет (А—1) т. При подаче части или всей необходимой
воды в сборник сушильной башни кислотообо,рот соответственно
возрастает. Примеры некоторых схем кислотооборота приведены
на рис. 69.
Кислоты поступают в башни через отдельные холодильники,
так как сушильная башня орошается кислотой при более низкой
температуре, чем кислота для орошения абсорбционных башен
(табл. 46).
Необходимые концентрации кислот в цикле орошения каж-
дой башни поддерживают путем вывода из этих циклов или
ввода в них соответствующих кислот. Так, часть 94—95%-ной
кислоты из цикла сушильной башни передают в сборник моно-
196
гидратных абсорберов, а взамен нее вводят в сборник сушиль-
ной башни 98,3%-ную кислоту из цикла моногидратного абсор-
бера. В сборник олеумного абсорбера также вводят 98,3%-ную
кислоту из цикла моногидратного абсорбера, а часть 20%-кого
олеума отводят из цикла олеумного абсорбера па склад. По-
скольку в олеумном абсорбере обычно поглощается больше SO3,
чем необходимо для выпуска продукции в виде олеума, часть
олеума из цикла олеумного абсорбера направляют в сборник
моногидратного абсорбера.
Оптимальную концентрацию (98,3% H2SOi) в сборнике мо-
ногидратного абсорбера поддерживают регулированием подачи
в этот сборник олеума или воды. Воду добавляют, если в посту-
пающих на осушку газах содержится меньше влаги, чем требу-
ется по балансу воды.
Кислоту, выводимую из цикла сушильной башни, для осво-
бождения от растворенной SO2 пропускают через отдувочную
башню, в низ которой подают воздух. По выходе из башни воз-
дух вместе с отдутой SO2 вводят в газопровод перед сушильной
башней.
Если часть продукции должна быть выпущена не в виде
олеума, а в виде 92,5—94%-ной кислоты, то такую кислоту
можно отобрать из цикла сушильной башни или из цикла моно-
гидратного абсорбера. В последнем случае отбираемую 98,3 %-
ную кислоту направляют в смеситель для разбавления до тре-
буемой концентрации (93—94% H2SC>4).
' Если олеум требуется выпускать периодически или в не-
больших количествах, то устанавливают небольшой олеумный
абсорбер с обводным газопроводом, так что через этот абсорбер
пропускают лишь часть газа, причем его количество регулируют
в соответствии с необходимым выпуском олеума; если олеум не
выпускают, то весь газ пускают в моногидратный абсорбер, ми-
нуя олеумный абсорбер.
Схема сушильно-абсорбционного отделения упрощается, если
вся продукция выпускается .в виде 92,5—94 %-ной кислоты.
В этом случае олеумный абсорбер можно не устанавливать и
абсорбцию SO3 вести в моногидратных абсорберах. Продукци-
онную кислоту выводят из цикла моногидратного абсорбера
Таблица 46. Распределение температур в сушильно-абсорбционном
отделении
Аппарат Температура кислоты, °C Температура газа, °C
на входе на выходе на входе | на выходе
Сушильная башня 35—40 50—55 30—35 45
Олеумный абсорбер 35—40 55—60 100—200 60—70
Моногидратный абсор- 55—65 85—90 200—220 60—65
бер Моногидратный абсорбер при ДК 62—64 70 170—180 70—75
197
(разбавляя ее до требуемой концентрации водой в смесителе)
.или сушильной башни.
При отборе продукционной кислоты из сушильной башни
осушку газа иногда ведут в двух последовательно соединенных
по газу башнях: первая орошается 92—94%-ной, а вторая 94—
96%-ной кислотой. В сборник второй башни вводят моногидрат,
а избыток кислоты из цикла второй башни выводят в сборник
первой башни; продукцию отбирают из цикла первой башни.
В ряде случаев в абсорбционную систему вводят кислоту со
стороны для закрепления ее до олеума. Количество вводимой
кислоты определяется балансом системы по воде; это количест-
во может быть увеличено, если кислоту из сушильной башни не
передавать в абсорбционные башни, а выводить из системы.
Холодильники кислоты устанавливают на напорной линии
насосов (работа под «давлением»), или между башней и сборни-
ком или, реже, на всасывающей линии насосов; в этих случаях
(работа под «заливом») холодильники работают под небольшим
давлением, что целесообразно с точки зрения плотности соеди-
нений. Однако при работе под «заливом» скорость кислоты в хо-
лодильниках, а следовательно, и коэффициент теплопередачи
ниже, чем при работе под «давлением»; кроме того при работе
под «заливом» из холодильников трудно удалять кислоту при
остановках. Поэтому работа под «давлением» предпочтительнее.
В качестве холодильников наиболее распространены ороситель-
ные, спиральные, пластинчатые; применяют также (главным об-
разом, для олеума) вертикальные пленочные и горизонтальные
кожухотрубчатые холодильники.
При осушке обжигового газа серной кислотой скорость аб-
сорбции паров воды определяется скоростью их диффузии через
газовую пленку. Количество Q паров воды, диффундирующих
через эту пленку, т. е. абсорбируемых серной кислотой (в кг/ч),
выражается уравнением [12]
Q = КРЬР
где К — коэффициент абсорбции, кг/(м2-ч-Па) [кг/(м2-ч-мм рт. ст.)]; F —
поверхность соприкосновения фаз (поверхность насадки), м2; ДР — средне-
логарифмическая разность давлений в начале и в конце процесса (движущая
сила абсорбции), Па (мм рт. ст.).
Движущую силу абсорбции рассчитывают по формуле
„ Р1'—р2'
2,3 1g р^,_р^,
где Р'1, Р'2— парциальное давление абсорбируемого газа в начале и в кон-
це процесса абсорбции, Па (мм рт. ст.); Р"\, Р"?—равновесное давление
абсорбируемого газа над жидкостью в начале и в конце процесса, Па
(мм рт. ст.).
Если равновесное давление абсорбируемого газа очень мало
по сравнению с его парциальным давлением в газовой фазе, то
198
часто определяют время соприкосновения газа с насадкой, необ-
ходимое для понижения парциального давления абсорбируемого
газа (движущая сила абсорбции) от Р\ до Pi'!. Это время т
(в с) рассчитывают по уравнению
т~ Л' 1п Р/
где р= 17S— гидравлический радиус насадки, м; V — свободный объем на-
садки, м3/м3 (см. Приложение XV); S — удельная поверхность насадки, м2/м3
(см. Приложение XV); К'— коэффициент абсорбции, м/с; Р'} и Р'2—парци-
альное давление абсорбируемого газа в начале и в конце процесса, Па
(мм рт. ст.).
При абсорбции в башнях с насадкой поглощение газов проис-
ходит на поверхности насадки, орошаемой жидким абсорбентом.
Поэтому чем больше поверхность насадки, тем полнее и быстрее
протекает абсорбция. Однако с увеличением поверхности насад-
ки возрастают размеры абсорбционных башен и повышается их
стоимость, в связи с чем большое значение имеют способы по-
вышения эффективности абсорбционного процесса при мини-
мальной поверхности насадки, в частности путем увеличения
коэффициента абсорбции, который в большой степени зависит
от скорости газа.
Коэффициент абсорбции в кг/(м2-ч-Па) или в кг/(м2-ч-мм
рт. ст.) рассчитывают по уравнению
К = Kowm
где Ко—константа, численно' равная коэффициенту абсорбции прн скорости
газа 1 м/с; w— фиктивная скорость газа в башне (без учета наличия в ней
насадки), м/с; т — коэффициент, равный 0,5 при ламинарном потоке и 0,8
при турбулентном потоке.
При увеличении скорости газа повышается интенсивность аб-
сорбции. Например, при повышении скорости газа вдвое коэф-
фициент абсорбции возрастает в 1,75 раза. Поэтому производи-
тельность абсорбционных башен может быть значительно повы-
шена путем увеличения количества газа, пропускаемого через
них за единицу времени. Но при этом возрастают унос брызг и
гидравлическое сопротивление башни, что в большинстве случа-
ев является основным препятствием для повышения производи-
тельности существующих абсорберов.
Повышение гидравлического сопротивления абсорбционных
башен при увеличении скорости (объема) проходящего газа вы-
ражается уравнением
ЛР2 = AP, (tt’2M)2
где ХРг — гидравлическое сопротивление башни при скорости газа в насадке
гд2, Па (мм рт. ст.); Р,— то же при скорости газа Wi, Па (мм рт. ст.);
Ш1 и к'2 — скорости газа в насадке, м/с.
199
Ниже приведены значения константы
воды серной кислотой при 50 °C:
/Со абсорбции паров
Концентрация H2SO4,
% 80 85 90 93 95 97 98
Константа Ко-10'1 при давлении в Па 1,9 2,2 2,5 2.6 2.8 2.9 3.0
.То же в мм рт. ст. 250 300 330 350 370 390 400
С изменением температуры в пределах 10 °C величина Ко
меняется незначительно. При повышении концентрации серной
кислоты константа абсорбции возрастает, одновременно увели-
чивается движущая сила абсорбции, так как уменьшается давле-
ние насыщенных паров воды над серной кислотой. Благодаря
этому поверхность насадки в сушильной башне может быть
уменьшена.
Ниже приведены результаты расчета необходимой поверхно-
сти F насадки в сушильной башне при различной концентрации
орошающей серной кислоты (расчет сделан для газа, содержа-
щего 7% SO2, при скорости газа в насадке башни 0,6 м/с и про-
изводительности контактной системы 1 т/ч серной кислоты):
Концентрация H2SO4, % • 90 91 92 93 95 97 98
Поверхность насадки F, м2 1500 1356 1240 11S6 1114 1072 1030
При повышении концентрации серной кислоты до 93% H2SO4
поверхность насадки, необходимая для осушки газа, уменьшает-
ся. Дальнейшее повышение концентрации кислоты не дает зна-
чительного эффекта в смысле уменьшения размеров сушильной
башни. В то же время, количество моногидрата, передаваемого
из абсорбционного в сушильное отделение для повышения кон-
центрации сушильной кислоты, значительно возрастает. В связи
с этим увеличиваются расход электроэнергии и потери SO2 с от-
ходящими газами.
Пример расчета сушильной башни [12].
Исходные данные для расчета:
Производительность А, т/ч H2SO4....................... 10
Концентрация SO2 в газе, %............................ 7
Концентрация кислоты, орошающей сушильную башню С,
% H2SO4................................................... 95
Температура, °C
газа на входе в башню................................... 32
кислоты на входе и выходе................................ 40
Давление паров воды в газе, Па (мм рт. ст.)
на входе в башню...................................... 4735 (35.6)
на выходе из башни ............................... 10,1 (0,076)
Разрежение в системе Рр (до газодувки), Па (мм рт. ст.) 2926 (22)
Барометрическое давление Р, Па (мм рт. ст.) . . . 101,08 ( 760)
Скорость газа в насадке ш, м/с........................ 0.8
Поверхность насадки находим по формуле
F = QJK.&P
200
Количество паров воды (в кг/ч), поглощаемых из газа, определим по
уравнению
V (Р/ — Р2') Л1н2о
Q = (Р — Р-/ — Ро) RT
где V — объем сухого газа, приведенный к нормальным условиям, м3/ч.
Если принять степень окисления х = 0,98 и полноту поглощения SO3 в
абсорберах 7 = 0,99, то при а = 0,07
ЛР7 10000-22,4 ",
V = Л1н2яо/«7— 98,08-0,07-0,98-0,99 = 33 640 м -/ч
Подставляя в расчетную формулу известные и найденные значения вхо-
дящих в нее величин, получаем:
33 640-(35,6 —0,076)-18
Q= (760—22 —35,6)-22,4 “ 1360 кг/ч
Коэффициент скорости абсорбции паров воды (для 95%-иой кислоты по-
данным, приведенным на стр. 200, Ко = 0,037):
К = 0,037-0,80.8 = 0,031 кг/(м2-ч-мм рт. ст.) — 2,35-10-4 кг/(м2-ч-Па)
Равновесное давление паров воды над 95 %-ной серной кислотой при
40 =С составляет 0,002 мм рт. ст. (при Р'я^Р"?)- Подставив значения.
P'i = 35,6, P"i = 0,076, Р'2=Р"2=0,002 в уравнение для ДР, находим:
, (35,6 —0,002)—(0,076 —0,002)
ДР = -------------35 6 — 0 002--------- = 3,3 мм Рт- ст- — -4 к44а
2,3 lg 0,076 —0,002
Таким образом, поверхность насадки
1360
F = 0,031 -5,8 = 7580 м2
Из опыта эксплуатации известно, что насадка башни обычно использует-
ся не полностью, поэтому вводим коэффициент запаса 1,20. Тогда поверхность,
насадки в рассчитываемой сушильной башне должна быть равна
F= 7580-1,20= 9100 м2
Если выбрать насадку в виде правильно уложенных колец размером
50X50 мм (согласно Приложению XV поверхность 1 м3 такой насадки равна
ПО м3), то общий объем насадкн составит
Ен= 9100/110= 82,8 м3
Внутренний диаметр сушильной башни
1/ 4V\ I Г 4-33 640 (273 + 40)-760
V mo-3600 = V 3,14-0,8-3600-273 (760 —22) = 4,2 м
где V) — объем газа при температуре t и барометрическом давлении Р.
Высота насадки
„ 41% 4-82,8
И ~ лДв2 — 3,14-4,22 ~ 6,02 м
Если производительность цеха увеличить на 75% (до 17,5 т/ч), то при
соблюдении всех принятых условий количество воды Q, поглощаемой в су-
шильной башне, также увеличится на 75% и будет составлять 2380 кг/ч.
201
Тогда скорость газа в насадке сушильной башни, размеры которой установ-
лен!'! нашим расчетом, составит
к/ = 0.8-1,75 = 1,4 м/с
а коэффициент скорости абсорбции
К = 0,037-1,4°,8 = 0,0485 кг,/(м2-ч-мм рт. ст.) = 9,15 кг/(м2-ч-кПа)
Количество паров воды в газе после сушильной башни рассчитываем нз
уравнения
л р _ Q _
~ KF - ____ Р,’— Р’
Подставив в это уравнение значения Q=2380, К=0,0485, £=7580,
£[ = 35,6, Р'2=Р"2=0,002, получим
2380 (35,6 — 0,002) — (£/'— 0,002)
0,0485-7580 = 35,6— 0,002
2,3 1g Р1»_ 0,002
.Откуда
£/' = 0,118 мм рт. ст. = 15,8 кПа или 0,0153% (об.)
что соответствует содержанию воды 0,0153% (об.).
Гидравлическое сопротивление башни при этом значительно увеличится:
ДР2= ДРр (1,40/0,8)2 = ДРрЗ.05
т. е. гидравлическое сопротивление увеличится более чем в 3 раза.
111.5.2. Абсорбция триоксида серы
Как уже указывалось выше, газообразный триоксид
серы наиболее полно абсорбируется 98,3%-ной серной кислотой,
при меньшей или большей концентрации H2SO4 способность ее
поглощать SO3 ухудшается. Над кислотой, содержащей менее
98,3% H2SO4, в газовой фазе находятся пары воды, над кисло-
той, содержащей более 98,3% H2SO4— триоксид серы. Полнота
абсорбции SO3 в значительной степени зависит и от температу-
ры серной кислоты: чем ниже температура, тем выше степень
абсорбции.
При обработке полученной газовой смеси, содержащей SO3,
кислотой концентрацией менее 98,3% H2SO4 часть триоксида
серы соединяется с парами воды, образуя туман серной кисло-
ты, который плохо улавливается в обычной абсорбционной аппа-
ратуре, и в основном уносится отходящими газами в атмосферу.
При этом на выходе из выхлопной трубы виден туман (абсор-
бер «газит»). Чем ниже концентрация серной кислоты и выше
ее температура, тем больше выделяется из нее паров воды, обра-
зуется больше тумана и выше потери SO3. При обработке кон-
тактного газа кислотой, концентрация которой более 98,3%
H2SO4, триоксид серы поглощается не полностью, так как из
этой кислоты выделяется SO3. В этом случае отходящие газы
202
также уносят в атмосферу часть триоксида серы, который с вла-
гой воздуха образует туман серной кислоты.
Таким образом, в обоих рассмотренных случаях абсорбция
SO3 ухудшается и выделяется туман H2SO4, причем характер его
неодинаков. При абсорбции SO3 менее концентрированной кис-
лотой (<98,3% H2SO4) туман образуется непосредственно в аб-
сорбере и виден у самой кромки выхлопной трубы. В потоке
газа, движущегося от входа в абсорбер к выходу из него, части-
цы тумана укрупняются, и он приобретает белый цвет. При оро-
шении абсорбера более концентрированной кислотой (>98,3%
H2SO4) туман образуется после смешения отходящих газов с
влагой атмосферного воздуха и становится заметным на некото-
ром расстоянии от кромки трубы. В момент образования части-
цы тумана имеют очень малые размеры и цвет тумана, вначале
голубоватый, переходит в белый после укрупнения частиц.
Поскольку при соприкосновении SO3 с серной кислотой, со-
держащей менее 98,3% H2SO4, абсорбции сопутствует образова-
ние тумана, обычные уравнения, описывающие процесс абсорб-
ции, в данном случае неприменимы. Это особенно наглядно
подтверждается тем, что с повышением температуры полнота
поглощения SO3 серной кислотой, имеющей концентрацию ниже
98,3% H2SO4, очень резко снижается, а при определенной (кри-
тической) температуре абсорбция SO3 вообще прекращается.
Давление паров воды над кислотой, возрастающее с повышени-
ем температуры, при критическом ее значении настолько велико,
что весь SO3, соединяясь с парами воды, полностью превраща-
ется в туман. При содержании в газе 5% SO3 критическая тем-
пература с увеличением концентрации H2SO4 повышается сле-
дующим образом:
Концентрация H2SO4, %...................85 90 95
Критическая температура абсорбции, °C . . 105 144 198
Если концентрация серной кислоты выше 98,3%, то при со-
прикосновении ее с серным ангидридом протекает обычный про-
цесс абсорбции. В этом случае справедлива расчетная формула
Q= ЛТАР
где Q — количество абсорбируемого SO3, кг/ч; К — коэффициент абсорбции,
кг/(м2-ч-Па) [кг/(м2-ч-мм рт. ст.)]; F — поверхность насадки, .м2; АР — дви-
жущая сила абсорбции, равная
PF-Pz"
где Р'1 и Р"2—парциальное давление абсорбируемого газа в начале и кон-
це процесса, Па (мм рт. ст.); P"i, Р"2 — равновесное давление абсорбируе-
мого газа над жидкостью при входе и выходе жидкости, Па (мм рт. ст.).
Коэффициент абсорбции при поглощении SO3 серной кисло-
той может быть определен по формуле
К = Кош».8
203.
"РИС. 70. Зависимость Ко от концентрации при различной температуре кис-
лоты.
РИС. 71. Зависимость степени абсорбции SO3 в моногпдратном абсорбере от
концентрации кислоты при различной температуре.
где Ко— коэффициент, зависящий от концентрации и температуры кислоты;
w — фиктивная скорость газа в абсорбере (без учета заполнения его насад-
кой), м/с.
Зависимость коэффициента Ко от концентрации и температу-
ры кислоты показана на рис. 70. Из этого рисунка видно, что
при 60 °C и концентрации H2SO4 98,3% (т. е. 80% SO3 общ.)
величина Ко составляет 0,175, а при абсорбции олеумом, содер-
жащим 20% SO3 (своб.), т. е. 85,3% SO3 (общ.) До=О,115.
На рис. 71 приведены расчетные данные о зависимости степе-
ни абсорбции триоксида серы в моногпдратном абсорбере от
концентрации и температуры орошающей кислоты. Для кислоты
концентрацией менее 98,3% H2SO4 учитывались потери SO3 в
виде тумана серной кислоты, образующегося из паров воды и
SO3, и в виде паров H2SO4 (испарение серной кислоты). При
большей концентрации орошающей кислоты учитывались только
потери в виде SO3 (неполнота абсорбции) и в виде паров
H2SO4 (испарение кислоты). Из этого рисунка видно, что
98,3%-ная серная кислота обладает наиболее высокой абсорб-
ционной способностью. С понижением и повышением концентра-
ции H2SO4 степень абсорбции кислоты уменьшается тем более
резко, чем выше температура кислоты.
На рис. 72 приведена зависимость степени абсорбции триок-
сида серы в олеумном абсорбере, орошаемом 20%-ным олеумом,
от температуры при различном содержании SO3 в газе. Из этих
данных видно, что с повышением температуры степень абсорб-
ции SO3 сильно уменьшается и при определенной температуре
(84 °C при 7,5% SO3 в газе и 76 °C при 5% SO3) абсорбция пол-
ностью прекращается. Максимальное содержание SO3 св. в полу-
чаемом олеуме при заданном содержании SO3 в газе, поступаю-
204
щем на абсорбцию, зависит от температуры абсорбции серного
ангидрида, так как содержание SO3 (св.) определяется равновес-
ным давлением SO3 над олеумом.
Максимальная концентрация олеума (Сол), достигаемая при
различной температуре (t) абсорбции (содержание SO3 в газе
7%) показана ниже:
t °C ....... 2Э 30 40 50 60 70 80 90 100
СоЛ, % SO3 (св.) . . . 50 45 42 38 33 27 21 14 7
Количество олеума, которое можно получить в системе, зави-
сит также от температуры перед сушильной башней, так как
она определяет содержание паров в газе, поступающем в су-
шильную башню, и, следовательно, количество воды, поглощае-
мой в ней. На рис. 73 приведена зависимость выхода олеума от
температуры газа перед сушильной башней при различной кон-
центрации SO3 в газе.
Скорость газа в абсорберах принимается 0,8—1,0 м/с, плот-
ность орошения олеумного абсорбера — 10—12 м3/м2, моногид-
ратных — 16—20 м3/м2.
Исследования влияния давления на процесс абсорбции три-
оксида серы моногидратом проведены в пленочном абсорбере
с фиксированной поверхностью контакта фаз и в барботажном
аппарате [131].
Для системы триоксид серы — серная кислота (моногидрат)
принято считать, что скорость массопередачи определяется ско-
ростью массоотдачи в газовой фазе. Коэффициент массопереда-
чи определяет коэффициент диффузии, для случая молекуляр-
ной диффузии он обратно пропорционален давлению. В реаль-
ных аппаратах степень турбулизации газовой фазы очень велика
и турбулентная диффузия превалирует над молекулярной. По-
этому значение коэффициента массопередачи с ростом общего
давления падает нелинейно. Несмотря на уменьшение коэффи-
циенты массопередачи с ростом давления скорость абсорбции
увеличивается за счет повышения движущей силы.
Температура олеина
на выходе ,°C
РИС. 73. Зависимость выхода олеума от температуры газа перед сушиль-
ной башней при различной концентрации SO3 в газе.
РИС. 72. Зависимость степени абсорбции SO3 в олеумном абсорбере от тем-
пературы при различном содержании SO3 в газе.
205
Давление, МПа
РИС. 74. Зависимость скорости абсорбции от
давления в тарельчатом (/) и насадочном (2)
абсорберах.
Исследования подтвердили, что
объемные коэффициенты массопереда-
чи нелинейно уменьшаются с увеличе-
нием давления для всех типов таре-
лок в барботажных аппаратах и наса-
дочных башнях в соответствии с урав-
нением
К =
Например, в случае использования тарелок провального типа
и ситчатых тарелок с переливом, показатель степени п = 0,57—
0,6, а для насадочных аппаратов п = 0,2. При постоянной массо-
вой скорости газовоздушного потока скорость абсорбции увели-
чивается с ростом давления (рис. 74) в соответствии с уравнени-
ем [131]:
и = Я2№-°,5
Установлено, что скорость процесса и коэффициент массопе-
редачи нелинейно увеличиваются с ростом массовой скорости
при всех значениях давления. При этом влияние массовой скоро-
сти тем более значительно, чем выше давление. Так, скорость
абсорбции при атмосферном давлении пропорциональна массо-
вой скорости в степени 0,8, а при давлении 1,0 МПа в степе-
ни 0,88.
Увеличение скорости абсорбции в барботажном аппарате по
сравнению с насадочным аппаратом связано с более интенсив-
ным обновлением поверхности контакта фаз при повышенном
давлении в условиях барботажного режима.
Выход олеума и распределение абсорбции SO3 по абсорбе-
рам. В олеуме с содержанием П8о3 процента общего SO3 на
1 масс. ед. SO3 приходится воды
100-nSo,
а= nSO3
Так, для стандартного 20%-го (по свободному SO3) олеума
эта величина равна
100 — 85,3!
85“31
= 0,172
Если отношение поглощаемой в сушильных башнях воды к
поглощаемому в абсорбционных башнях триоксиду серы больше
0,172, то вся продукция не может быть получена в виде стан-
дартного олеума, если то же отношение меньше 0,172, то вся
продукция системы может быть выпущена с концентрацией
выше стандартного олеума. Но продукцию выпускают обычно в.
206
виде стандартной кислоты или стандартного олеума, при этом в
систему добавляют воду. Вместо добавочной воды можно вво-
дить в систему со стороны разбавленную серную кислоту, в це-
лях повышения ее концентрации.
В периоды, когда возрастает спрос на стандартный олеум,
для увеличения его выхода обычно в систему вводят со стороны
92,5%-ную кислоту.
В общем случае выход концентрированной продукции из си-
стемы при вводе в нее менее концентрированной кислоты описы-
вается уравнением [9]
100а
nS°3— (а-1)-100
1 “4“ о “I- ги
п SO3
где IIsOgH П'зо3% общего SO3 в получаемой и во вводимой (более слабой
кислоте) соответственно; а — отношение общего количества получаемой кис-
лоты к количеству кислоты, производимой системой за счет газа; а — содер-
жание Н2О в кг на 1 кг SO3, поступающего на сушку-абсорбцию
(a = G/1000).
100 nso3 — (1 + а) Пзо3П'5о3
“= 100-(П5о3 — П'зо3)
Если влага из системы полностью удаляется (а = 0) с по-
мощью концентрирования сушильной кислоты до стандартной,
которая опять возвращается в систему, то выражение превраща-
ется в следующее:
100- nSo3 — nso3 n'So3
а'= I00-(nso3-n'so3) ~
При Пзо3=85,31% и n'sos =75,1 %, а' = 2,1. В последнем слу-
чае на 1 т стандартного олеума, получаемого из газа, образуется
1,1 т такого же олеума за счет ввода 92,5 %-ной кислоты со сто-
роны. Выход олеума в этом случае не зависит от влажности га-
зов, поступающих на сушку.
Если выводимая слабая кислота не подвергается упарива-
нию, а используется как таковая, например в производстве удоб-
рений, то с ней из системы на 1 кг SO3 продукции удаляется SO3
n"so3
100—n"so3'a
В этом случае выход олеума будет
100-nso3 — nso3n'so3 n’So3
= nSOs-n'so3 “ 100-li"so8'a
Величины а" во всех случаях значительно больше а'. Это
значит, что вывод воды из системы со слабой кислотой с одно-
временным вводом в систему 92,5%-ной кислоты значительно
повышает выход олеума.
Получение всей продукции системы в виде стандартного оле-
ума, а тем более выпуск дополнительного количества олеума за
207
счет ввода 92,5%-ной кислоты могут бЬггь практически реализо-
ваны только при соответствующих размерах абсорберов. Необ-
ходимой величине а соответствует вполне- определенная вели-
чина 0 — доля абсорбции триоксида серы в первом (а следова-
тельно, и во втором абсорбере):
100а Q ( (10) + (а — 1)
пЗОз-р+ П'ьОз
где FIso3—содержание SO3 в конечном продукте, %; а — общий выход олеу-
ма, %; Пзо3 —содержание SO3 в кислоте передаваемой из второго абсор-
бера в первый, %.
Из последнего выражения получается
(П=о3 — n'so3)
₽- 100a’nso3 (100 — n'so3)
Из этого выражения, например при risos=85,31 (20%-ный
олеум) и ITso3=80 (98%-ная H2SO4), получается 0 = 0,31 а.
При а=1, т. е. при работе системы без ввода кислоты со сто-
роны, в случае выпуска всей продукции в виде олеума 0 = 0,31,
а при а = 2,1 0 = 0,66. Отсюда следует, что для повышения выхо-
да олеума при вводе кислоты со стороны необходима повышен-
ная производительность олеумного абсорбера.
При повышении температуры газа всего на 3 °C (от 32 до
35 °C) и концентрации SO2 в газе 7% выход олеума понижается
на 20% (от 100 до 80%). Выход олеума свыше 100% достигает-
ся при вводе в абсорбционное отделение (со стороны) концен-
трированной серной кислоты (92,5% H2SO4) вместо недостаю-
щей воды.
III.5.3. Аппаратура для осушки газа
и абсорбции серного ангидрида
Для осушки газа и абсорбции SO3 применяют почти ис-
ключительно насадочные башни. В последние годы ведутся мно-
гочисленные исследования по замене их другими видами абсор-
беров (барботажными и распиливающими).
Насадочные абсорберы. Насадочные абсорберы представляют собой баш-
ни, загруженные насадкой из тел различной формы (кольца, седла и др.).
Насадку укладывают на колосниковую решетку. Газ поступает в башню че-
рез штуцер в подколосниковом пространстве и отводится сверху (большей
частью через штуцер в крышке). Кислоту подают на орошение через устрой-
ство, обеспечивающее равномерное распределение орошения по всему попе-
речному сечению башни. Отводится кислота снизу.
В моногидратных абсорберах может оказаться целесообразным приме-
нение прямотока вместо противотока, что позволяет работать с большими
(до 10 м/с) скоростями газа; при этом интенсифицируется массообмен и
снижается гидравлическое сопротивление.
Кислота стекает по насадке в основном в виде пленки. Соприкосновение
газа с кислотой происходит главным образом на смоченной поверхности на-
садки, покрытой текущей пленкой.
208
РИС. 75. Сушильная башня и моногидратные абсорберы:
1 — стальной корпус башни; 2 — футеровка; 3 — лаз для загрузки насадки; 4— брызго-
уловнтель; 5 — распределительная плита; 6 — колосниковая решетка.
РИС. 76. Олеумный абсорбер:
1— колосниковая решетка; 2 — стальной корпус; 3—насадка; 4 — смотровое стекло; 5 —
распылитель; 6 — лаз для загрузки насадки.
В сернокислотном производстве применяют керамические (иногда фар-
форовые) насадки, причем наиболее распространены кольца Рашнга, загру-
женные в навал или в укладку. В навал загружают кольца небольших раз-
меров (25 мм или 35X35 мм — для загрузки верхней части башен). Кольца
больших размеров (50 мм) на наших заводах загружают обычно в укладку,
в шахматном порядке. На зарубежных заводах практикуют загрузку больших
колец (50 и 80 мм) в навал. Загрузка в навал упрощает процесс заполнения
башни насадкой, однако при этом удельная поверхность ниже, а сопротив-
ление выше, чем при загрузке в укладку; поэтому последний способ пред-
почтительнее.
В зарубежной практике применяют также кольца с крестообразной пере-
городкой и кольца с прободенными стенками (кольца Палля). Кольца с
крестообразной перегородкой, загружаемые в укладку или в навал, сложны
в изготовлении и обладают низким свободным объемом. Кольца Палля, за-
гружаемые обычно в навал, обладают меньшим сопротивлением и несколько
большей эффективностью по сравнению с кольцами Рашига тех же размеров,
однако эти кольца дороги и сложны в изготовлении. Последнее относится и
к применяемым иногда при загрузке в навал седлообразным насадкам.
Сушильные башни и моногидратные абсорберы (рис. 75) представляют
собой стальной цилиндр, футерованный кислотоупорной керамикой. Поддер-
14—584
209
жпвающая решетка из андезитовых нли керамических колосников опирается
на столбы из кислотоупорного кирпича. На поддерживающей решетке уста-
навливают несколько рядов крупных колец (150, 120, 100 и 80 мм), на кото-
рые укладывают основной слой насадки из колец 50 мм. Орошающую кисло-
ту подают посредством чугунной распределительной плиты или других
устройств.
Олеумные абсорберы выполняют аналогично сушильным башням и моно-
гидратным абсорберам, но оросительное устройство изготовляют из стали.
Применяют также стальные иефутерованиые олеумные абсорберы с поддер-
живающим устройством из стальных балок (рис. 76).
Плотность орошения выбирают исходя из условий, необходимых для до-
•Стпжения удовлетворительной смоченности насадки и требований теплового
баланса. При регулярных насадках с точки зрения их смоченности желатель-
но применение плотностей орошения 10—12 м/ч. Из требований теплового ба-
ланса плотность орошения выбирают с таким расчетом, чтобы закрепление
кислоты в моногидратном абсорбере и разбавление ее в сушильной башне
было в пределах 0,3—0,5%; этому соответствует повышение температуры
кислоты в башне 10—20 °C. В олеумиых абсорберах закрепление олеума до-
пускают на 1—2% SO3 (своб.). Обычно плотность орошения поддерживают
.следующих пределах: в сушильных башнях 8—15 м3/(м2-ч), в абсорбционных
башнях 10—20 м3/(м2-ч).
Барботажные абсорберы. В барботажных абсорберах поверхность кон-
такта между фазами развивается потоком газа, распределяющегося в жид-
кости в виде пузырьков н струек. Такое движение газа (барботаж) осуществ-
ляется большей частью в аппаратах колонного типа с тарелками различных
конструкций [130].
В барботажных абсорберах применяют тарелки перекрестного илн про-
вального (беспереливного) типа. На первых из них движение газа н жидко-
сти осуществляется перекрестным током; эти тарелки имеют специальные пе-
реливные устройства для перетока жидкости с одной тарелкн на другую.
Из тарелок этой группы наиболее распространены колпачковые н ситчатые.
В тарелках провального типа переливные устройства отсутствуют, так что
газ и жидкость проходят через одни и те же отверстия.
Распыливающие абсорберы. В прямоточных распыливающих аппаратах
используют высокие скорости гззз (20—30 м/с и выше), что ведет к знячи-
тельной интенсификации абсорбции; при этом вся жидкость уносится с газом
и отделяется от него в отдельном сепараторе; распыление жидкости осу-
ществляется за счет кинетической энергии движущегося с большой скоростью
газового потока. Из различных видов этих аппаратов в сернокислотном про-
изводстве испытывались форсуночный абсор-
бер Вентури и абсорбер APT (абсорбер рас-
пиливающего типа).
Абсорбер Вентури имеет форму расходо-
мерной трубы Вентури (вследствие чего аб-
сорбер и получил свое название) и состоит
из сужающейся части (конфузора), узкой
части (горловины) н расширяющейся части
(диффузора). Жидкость подается через фор-
сунки в горловину илн конфузор. Газ, с боль-
шой скоростью пройдя через горловину, по-
степенно снижает скорость в диффузоре и
направляется в сепаратор. Наличие диффузо-
ра обеспечивает переход кинетической энергии
газа в энергию давления с минимальными по-
терями. В 1981 г. фирма «Лургн» (ФРГ)
РИС. 77. Аппарат APT:
1 — распределительная камера; 2— распыливающие
коиуса; 3 — абсорбционная камера; 4 — сепарацион-
ное устройство; 5 — отверстия в отбойном цилиндре;
6 _ отбойный цилиндр.
210
ввела в эксплуатацию (в г. Орджоникидзе) систему мощностью 220 тыс. т
серной кислоты в год на отходящих газах цинкового завода, применив вместо-
башеи во всех отделениях абсорберы Вентури. Но использование аппарата
Вентури для осушки газа и абсорбции SO3 нецелесообразно, поскольку эти
аппараты в одну ступень не могут обеспечить требуемую степень осушки га-
за (0,01% об. Н2О) и степень абсорбции SO3 (0,999) без резкого уве шче-
ния энергетических затрат, кроме того, неизбежен сравнительно большой брыз-
гоунос.
Аппарат APT (рис. 77) отличается отсутствием диффузора и имеет пле-
ночную подачу орошения: газ проходит сверху вниз через сужающийся кни-
зу конус (конфузор), по стенкам которого стекает кислота. В аппарате APT
можно осуществить несколько ступеней распиливания, устанавливая два
(или более) конуса. Однако в аппарате с двумя ступенями распиливания
сопротивление в 2 раза выше, чем в одноступенчатом, а число единиц пере-
носа увеличивается при этом лишь в 1,7 раза; таким образом, вторая ступень
распиливания менее эффективна, чем первая.
Сравнение различных типов абсорберов. Основными преиму-
ществами насадочных абсорберов являются их небольшое сопро-
тивление, возможность работы при изменении газовой нагрузки
в широких пределах и небольшой брызгоунос. Однако в услови-
ях сернокислотного производства они обладают тем недостат-
ком, что требуют циркуляции больших количеств кислоты (до
нескольких сот кубических метров в час) и отвода тепла в вы-
носных холодильниках с невысоким [150—250 ккал/(м2-ч-
•град)] коэффициентом теплопередачи. Кроме того, насадочные
абсорберы при больших нагрузках по газу (десятки тысяч ку-
бических метров в час) громоздки и требуют высоких капиталь-
ных затрат.
Недостатками других, более интенсивных аппаратов (скоро-
стные прямоточные распыливающие абсорберы, барботажные
абсорберы) являются значительное сопротивление, ограничен-
ный диапазон изменения газовой нагрузки и повышенный брыз-
гоунос. Скоростные прямоточные распыливающие абсорберы
проще и дешевле насадочных и имеют меньшие габариты. Их
применение позволяет снизить капитальные вложения (по срав-
нению с насадочными), но связано с повышением расхода элек-
троэнергии (вследствие высокого сопротивления) и не устраня-
ет циркуляцию кислоты с отводом тепла в выносных холодиль-
никах. Применение этих аппаратов, по-видимому, целесообразно
в качестве первой ступени абсорбции (олеумного абсорбера).
Перспективными следует считать аппараты, в которых не
требуется циркуляции кислот и может быть осуществлен внут-
ренний отвод тепла. К таким аппаратам относятся трубчатые
пленочные абсорберы прямоточного типа [130], работающие с
высокими скоростями газа (до 40 м/с) по принципу нисходяще-
го или восходящего прямотока. Другим видом таких аппаратов
являются рассмотренные выше барботажные абсорберы с внут-
ренним отводом тепла. Основными их достоинствами являются
осуществление внутреннего отвода тепла с высоким коэффициен-
том теплопередачи (в 4—5 раз выше, чем в выносных холодиль-
никах) и резкое сокращение количества перекачиваемых кислот.
14'
211
Вследствие этого значительно упрощается и удешевляется схе-
ма абсорбционно-сушильного отделения. Несмотря на высокое
сопротивление барботажных абсорберов и возрастание вследст-
вие этого расхода энергии на протягивание газа, общий расход
энергии по сравнению с насадочными абсорберами ниже в ре-
зультате экономии энергии на перекачку кислот. Таким обра-
зом, применение барботажных абсорберов должно вести
к уменьшению капитальных вложений и эксплуатационных за-
трат.
Пример расчета олеумного и моногидратного абсорберов
Исходные данные
Количество поступающего на абсорбцию газа (при н. у.), м3/ч 134000
Содержание SO3 в поступающем газе, % (об.)..............7,5
Температура поступающего газа, °C.......................120
Степень извлечения SO3 из газа, %.......................99,95
Насадка — кольцами в укладку, размером, мм..............50X50
Расчет олеумного абсорбера. Принимаем степень извлечения SO3 в оле-
умном абсорбере 70%, тогда объем поглощенного в этом абсорбере SO2
будет Vji/iZ, объем газа после абсорбера
У2 = (1 — у^) = 134 000(1 —0,075-0,7) = 127 000 м3/ч
а содержание в нем SO3
, Т1У1 — К1У1? yi(l —г)
У*~ У2 - 1-У1г
0,075 (1 — 0,7)
1 —0,075-6,7 = °’0238 (2’38% об->
где Vj — объем поступающего газа (134 000 м3/ч); iji— объемная доля SO$
в поступающем газе (0,075); z— доля SO3, поглощенная в олеумном абсор-
бере (0,7).
Выбираем приведенную скорость газа (при н.у.) 1,1 м/с и определяем
необходимую площадь поперечного сечения абсорбера (в расчете на средний
расход газа (134 000+127 000)/2= 130 500 м3/ч) Г
130 500
S= 3600-1,1 = 33 м2
чему соответствует диаметр 6,48 м.
Принимаем башню с внутренним диаметром 6,27 м (диаметр по кожуху
6,5 м), площадь сечения S=31 м2. Тогда приведенная скорость газа
130 500
wo = 3600-31 = 1>17м/сек
Принимаем плотность орошения 20 м3/ч, тогда количество орошения со-
ставит 20-31=620 м3/ч при плотности олеума 1900 кг/м3
L= 620-1900= 1 180 000 кг/ч
Определяем закрепление олеума в башне и его нагрев. Количество по-
глощенного SO3 равно
80 80 „ „
= 22 4 У1У1г — "22~4 '' 13^ -0,075= 25 200 кг/ч
Концентрация вытекающего олеума составляет (при начальной концент-
рации 20% SO3 своб., т. е. при массовой доле х2=0,2)
Lx.+ Wa 1 180 000-0,2 4.25 000
Xj — L-\-Wk ~ 1 180 000 4 25 200 = °,216 (21,6% SO3 своб.)
212
Принимая температуру газа после абсорбера 50 'С, находим отвод тепла
при охлаждении газа [теплоемкость 0,32 ккал/(м3-град) или
1,34 кДж/(м2-град)]
О, = 134 000-0.32 (120—50) = 3 000 000 ккал/ч = 12 570 000 кДж/г
Теплота растворения SOa равна
Q2 = 25 200- 172 = 4 330 000 ккал/ч = 18 142 000 кДж/ч
где дифференциальная теплота растворения SO3 в 20%-ном олеуме равна
172 ккал/кг = 722 кДж/кг.
Общее количество выделяемого тепла
Q = Qt -% Q2 = 3 000 000 -% 4 330 000 = 7 330 000 ккал/ч = 30 712 000 кДж/г
Нагрев олеума [теплоемкость 0,34 ккал/(кг-град), или 1,43 кДж/(кгХ
Хград)]
Q 7 330 000 „
Д/= Lc = 1 180000-0,34 =18’3 С
Если принять начальную температуру олеума 45 °C, то его конечная
температура будет 45 +18,3 = 63,3 °C.
Равновесное давление SO3 над поступающим олеумом (20% своб. SO3,
45 °C) составляет Р*2=0,0064 бар = 0,64 кПа, а над уходящим олеумом
(21,6% своб. SO3, 63 °C) P*i =0,0248 бар, 2,48 кПа. Парциальное давление
SO3 (при общем давлении Р=1 бар) в поступающем газе Р!=0,076 бар =
= 7,6 кПа, в уходящем газе /% = 0,0238 бар = 2,38 кПа.
Движущая сила внизу абсорбера Pi—P*i = 0,076—0,0248 = 0,0512 =
= 5,12 кПа, а вверху абсорбера Р2—Р*2 = 0,0238—0,0064 = 0,0174 бар =
= 1,74 кПа.
Средняя движущая сила
0,0512 —0,0174 „
(Р— Р’)ср =---------q Q5J2 = 0,0316 бар =3,16 кПа
2’3 lg 0,0174
Число единиц переноса
Рх— Р2 0,076 — 0,0238
(Р — Р*)ср =' 0,0316 =1.66
Для насадки кольцами 50 мм в укладку имеем е = 0,735, <2=110 м2/м3.
Для 20%-ного олеума при средней температуре (45 + 63,3)/2 = 54,1 °C имеем
рж=1850 кг/м3, цж = 11,2-10~3 Па-с.
Средняя скорость пленки
у v v
v <-+> — I/ Зрж ( 3600<z ) ~
3f 1850-9,81 / 20 у
— 1/ 3-11,2-Ю-3 \ 3600-110 J =°>12 м/с
Количество удерживаемой жидкости (проверено в эксперименте по NH3)
6r nh3= 'V0,41 = 0,0103-20°,« = 0,039
Относительная скорость газа
к>0 . . 1,17
шотн - е — йгКн3 + 1>51'ср = 0,735 —0,039 + 1,5-0,12 = 1,86 м/сек
213
Коэффициент массоотдачи
Р --= 57,8-1,86°.74 = 91,4 кг/(м2-ч-бар) = 9,14 кг,(м2-ч-МПа)
Для 20%-ного олеума при 54,1 °C имеем Ко=3, Ki=0,53,
Кг = 5,1—0,0417-104,5 = 0,74, при Ch,so4 = 104,5%. Таким образом коэффициент
массопередачи
К= РК0К]К2 = 91,4-3-0,53-0,74= 107,5 кг/(м2 • ч • бар) = 10,75 кг/(м2-ч-МПа)
Принимаем число точек подачи орошения на 1 м2 п = 40, находим коэф-
фициент ухудшения
п 40
Vy = пЬ = 40Д-19 = 0>68
Эффективная поверхность контакта
Куу 20-0,68 _ , _х
аэф — p^-qv = 0,0194 4- 0,0086-20 = /1/Ч
Объемный коэффициент мяссопередячи при коэффициенте запаса f=2
Ка3л, 107,5-71 „ „
Кх = j— =---------s-----= 3820 кг/(м3-ч-бар) = 38,20 кг/(м3-ч-МПа)
7 z
Высота единицы переноса
36ООЛ4К 3600-80-1,2
Л= 22,4KV(P—Р2) = 22,4-3820(1 —0,023) = 4-14 м
где приведенная скорость газа на входе в абсорбер
134000
ay° = 3600-31 = 1’2 м/с
Необходимая высота насадки
Н= Nh = 1,66-4,14= 6,9 м
Можно также предварительно найти объем насадки
WA 25 200
Van~ Kv(P—Р*)ср — 3820-0,0316 — 207 м3
откуда высота насадки:
Расчет моногидратного абсорбера. Объем газа перед абсорбером
1%= 127 000 м3/ч, начальная концентрация г/!==0,0238. Объем газа после аб-
сорбера находим исходя из степени поглощения 99,95% по отношению к ис-
ходному газу, поступающему в олеумный абсорбер:
1% = 134 000(1 -0,075-0,9995) = 124 000 м3/ч
Содержание SO3 в уходящем газе
0,075(1 —0,9995)
У2 ” ।___Q Q75-0 9995 = ^*^^90405 бар = 4,05 Па (0,00405%)
Количество поглощенного SO3
80
— 22,4 =
80
= ~22 4 (127 000-0,0238— 124 000-0,0000405)= 10750 кг/ч
214
Принимаем абсорбер такого же диаметра (6,27 м), как олеумпый; пло-
щадь сечения S = 31 м2. Приведенная скорость газа (в расчете на средний
расход (127 000+124 000) : 2= 125 5000 м3/ч)
125 500
, =',12 м с
u
Количество орошения при плотности орошения 20 м-/ч составляет
20-31=620 м3/ч или при плотности моногидрата 1840 кг/м3 /, = 620-1 840 =
= 1 140 000 кг/ч.
Массовая доля SO3 в выходящей кислоте составляет (при орошении
98,3%-ной H2SO4, т. е. х2=0,8024)
1140 000-0,8024 4-10 750
1140 000 4- 10 750 - 0,8042
(98,5% H2SO4)
Теплота растворения SO3 равна
10 750-285= 3 070 000 ккал/ч = 12 863 300 кДж/ч
Пренебрегая изменением температуры газа, находим нагрев кислоты
[теплоемкость 0,348 ккал/(кг-град), или 1,46 кДж/(кг-град)]
3 070 000
М —------------------7 7 °C
— 1 140 000-0,348 ~ 1,1 °
При начальной температуре кислоты 45 °C ее конечная температура бу-
дет 45 + 7,7 = 52,7 °C.
Равновесным давлением SO3 над кислотой можно пренебречь. При общем
давлении Р=1 бар=100 кПа парциальное давление SO3 в поступающем газе
Pi = 0.0238 бар, 2,38 кПа, в уходящем газе /32 = 0,0000405 бар = 4,05 Па.
Число единиц переноса
0,0238
=2,3 1g 0 0000405 = 6,37
Коэффициент массопередачи и высоту единицы переноса находим ана-
логично олеумному абсорберу. Относительная скорость газа будет 1,79 м/с.
Коэффициент массоотдачи р = 88,8 кг/(м2-ч • бар) =8,9 кг/(м2-ч-МПа). Объем-
ный коэффициент массопередачи Д+ = 9480 кг/(м3-ч • бар) =94,8 кг/(м3-ч-МПа)
(при Ко=3, Ki = K2=l, / = 2). Высота единицы переноса /г=1,54 м. Необходи-
мая высота насадки
И = 6,37-1,54 = 9,8 .м
Пример расчета отдувочной башни
Исходные данные
Количество отдуваемой кислоты, т/ч .... 31
Степень отдувки, %................................99,9
Объем воздуха для отдувки, м3/ч................... 4250
Скорость воздуха, м/с......................... 0,8
Температура воздуха/кислоты, °C...................25/40
Содержание SO2 в газе, %..........................7,5
Расчет
Сечение башни
4250 (273 4- 32,5) ,
3600-273-0,8 = 1,6эм; Дьн=1,5м
где 32,5 — средняя разность температур в башне.
215
Плотность орошения башни
31 000
1810-1,65 = 10 м3/(м2’4)
Парциальное давление SO2 перед башней
7,5-760/100= 57 мм рт. ст. =7,6 кПа
Растворимость SO2 при Р = 57 мм рт. ст. и 40 °C
1,7-57/760= 0,1275 г/100 г
Общее количество SO2 в кислоте, подаваемой на отдувочную башню
0,1275-31 000/100 = 39,5 кг или 0,6172 кмоль
Молекулярная масса 93,63%-ной кислоты
98-0,9363 + 18-0,0637 = 92,9 кг/кмоль
Количество молей кислоты в отдуваемой кислоте
31 000/92,9= 333,7 кмоль
Отдувается SO2
39,5-0,999= 39,46 кг, или 0,6165 кмоль
Остается SO2 в кислоте
39,5 — 39,46= 0,04 кг, или 0,0005 кмоль
Концентрация SO2 в жидкой фазе:
до отдувки после отдувки
0,6165 0,0005
х2 = 333 7 = °’001847 *i = ззз 7 = 0,0000015
Парциальное давление SO2 в газовой фазе на входе в башню + =0,
на выходе
39,5-22,4-760
Р2 =----64-4250----= 2,5 мм рт. ст. = 0,33 кПа
Равновесное давление SO2 над кислотой, вытекающей из башни
, 0,04-100-760
Рг = ~gj QQQ. д у = 0,0576 мм рт. ст. илн 0,0077 кПа
Константа фазового равновесия трх = Р'!х
0,000077
тРЛ = 0,0000015 = 51 ’33 бар = 5133 кПа
0,076
тРгх2= '0+01847 =41’15 бар = 4115 кПа
51,33 + 41,16
тРхср =--------2------= 4®.24 бар = 4624 кПа
Средняя движущая сила процесса массопередачи при отгонке
._ (0,076— 0,0033) —(0,000077 —0)
Д Рср = -------------- 0 0727---------~ = 0 >0160 бар = 1,6 кПа
2,3 lg 0,000077
216
Коэффициент массопередачи в газовой фазе
/ 1 \-0,395 [J
fW = 5-85’4 d^-) А«НЖз-.У°,’»
где а — удельная поверхность контакта, а = 110 м2/м3; я=с/ЭЕВ/0,025 =
=0,027/0,025=1,08: /—высота насадки; /=0,05 м; U — плотность орошения,
М3/(м2-ч)
/ 0 05 \-о,395 Ю
fW = 5,85• 110 ‘ 1 ’081,45’2171"1,1)7’ 10 Ч- 1ТЗ"'0,80’733 =
= 428,45 кмольДм3-ч• бар) = 4,28 кмоль/(м3-кПа)
Коэффициент массопередачи в жидкой фазе
₽р= 1 1,6-/70,768/-°,185= 11,6-1О°,768 - 5О-о>185 = 33 ч"1
33-1810
—д2~89—= 848 кмольДм3-ч)
Коэффициент массопередачи
1 1
Kv = 1 mP.vcP = 1 46,24 =
₽PV + Ру 428,45 + 643
= 13,51 кмольДм-ч-бар) и 0,13 кмольДм-ч-кПа)
Высота насадки
GSO2 0,6165
Н = KybPcpS = 13,51-0,016-1,65 = 2>45 м
Высоту насадки следует увеличить с учетом поглощения водяных паров
при отдувке SO2. Давление водяных паров в воздухе при 25 °C и насыщении
70%
23,756-0,7= 1663 мм рт. ст. =2,216 кПа
Поступит в башию водяных паров с воздухом
15,63
4250- ~7qq_ie Q3' = 95 м3, или 76,4 кг
Парциальное давление водяных паров на входе в башню
95-760 „„
425Q— = 17 мм рт. ст. = 1,7 мПа
Парциальное давление водяных паров на выходе из башни в соответст-
вии с нормой регламента (0,01% Н2О)
0,01-760 „ „ . „
---IOO----— 0,076 мм рт. ст. = 7,6 кПа
Равновесное давление паров над 93,6%-ной кислотой 0,002 мм рт. ст.
(0,266 Па)
Средняи движущая сила абсорбции:
ДРср_ (17 - 0.002)-(0 076 - 0.002) _ 3 _ ,,,
2,3 lg 0,074
217
Коэффициент массопередачи
К— о,037-F0,8 = 0,037-0,86 = 0,032 кг/(м3-ч-мм рт. ст.) = 3,2 кг/(м2-ч-Па>
Объем насадки для колец 50X50 в укладку (/-'=110 м2/м3, см. Прило-
жение XV):
76,4 6,9
1Лнас = 0,032-110-3,14 = 6,9 м3; Янас = 1(65 —4,2м
Для лучшего распределения кислоты следует добавить 0,5 м насадки из
колец 25X25 в навал.
111.6. ОЧИСТКА ОТХОДЯЩИХ ГАЗОВ И НЕЙТРАЛИЗАЦИЯ
СТОЧНЫХ ВОД [132—139]
Обезвреживанию отходящих сернистых газов различных
производств и утилизации полученных при этом продуктов уде-
ляется значительное внимание как у нас, так и за рубежом.
Ежегодный выброс оксидов серы (SO2 и, в меньших количе-
ствах, SO3) в нижние слои атмосферы превышает 150 млн. т
серы; из них 60—80% выбрасываются с продуктами сгорания из
котлов и печей, а остальное — преимущественно агломерацион-
ными установками черной металлургии, предприятиями химиче-
ской и нефтехимической промышленности [132]. Основными
источниками загрязнения атмосферы диоксидом серы являются
электростанции, сжигающие сернистые угли или мазут; их вы-
бросы в 60 раз превышают выбросы сернокислотных произ-
водств.
Хотя удельный вес сернокислотного производства в общем
масштабе загрязнения атмосферы диоксидом серы невелик (тем
более — в связи с повсеместным быстрым переходом на метод
двойного контактирования), все-таки проблема очистки выхлоп-
ных газов для старых и маломасштабных заводов весьма акту-
альна.
В производстве серной кислоты из различного сырья выхлоп-
ные газы могут содержать:
из колчедана — кроме азота и кислорода, диоксид и триоксид
серы, туман, брызги и пары серной кислоты;
из природной серы по короткой схеме — обычно наблюдает-
ся повышенное содержание сернокислотного тумана;
из сероводорода по методу мокрого катализа — в выхлопных
газах отсутствует триоксид серы, но также возможно повышен-
ное содержание тумана серной кислоты;
из отходящих газов цветной и черной металлургии — кроме
тумана и брызг серной кислоты, а также диоксида и триоксида
серы некоторое количество углеводородов или продуктов их тер-
мического разложения и осмоленпя, фтористых соединений и
других примесей в зависимости от состава газов, перерабаты-
ваемых на данном предприятии.
В связи с возросшими требованиями по охране окружающей
среды, введена жесткая норма по выбросам вредных веществ.
218
Предельно допустимые концентрации (ПДК) некоторых ве-
ществ приведены в Приложении XXI.
Рассмотрим способы очистки отходящих газов, которые в на-
стоящее время применяются или имеют перспективы для при-
менения в сернокислотной промышленности. К ним в первую
очередь относятся аммиачные кислотно-каталитический и суль-
фитно-содовый способы.
111.6.1. Аммиачные способы очистки
и концентрирования сернистых газов
Все способы очистки отходящих газов с применением
аммиака можно разделить на два класса: жидкостные (мокрые)
способы и сухие способы.
Основой почти всех жидкостных аммиачных способов явля-
ется процесс поглощения диоксида серы из газов раствором
сульфит-бисульфита аммония. В зависимости от дальнейшей об-
работки полученного раствора жидкостные аммиачные способы
подразделяются на циклические и нециклические. Циклические
способы, в свою очередь, делятся на паровые и комбинирован-
ные. Среди нециклических способов выделена большая группа
аммиачно-кислотных способов.
Сухие способы — немногочисленны; их можно разделить на
две группы: твердофазные и газовые.
Жидкостные аммиачные способы. Во всех жидкостных ам-
миачных способах схема поглощения SO2 из газов сульфит-би-
сульфитным раствором, а также последующая дополнительная
очистка газов от тумана и брызг — одинакова. Большой вклад
в изучение физико-химических основ этого процесса, а также
в развитие аммиачных способов очистки и концентрирования
диоксида серы был внесен 3. П. Розенкнопом [133] и
Б. А. Чертковым Г134—136, 138].
Аппаратурная разработка узла очистки отходящих газов
от SO2 растворами сульфит-бисульфита аммония включает аб-
сорбер распыливающего типа APT ,[137]. Степень очистки га-
зов от SO2 в этих аппаратах составляет 80—90%; содержание
диоксида серы на выхлопе из электрофильтра при соблюдении
установленного режима не превышает 0,025—0,035% (об.).
Нециклические способы. Процесс абсорбции SO2
раствором сульфит-бисульфита аммония можно выразить сле-
дующими уравнениями:
(NH4)2SO3 4- SO2 4- Н2О = 2NH4HSO3
NH4HSO3 4- NH3 = (NH4)2SO3
Для наиболее полного поглощения SO2 из газов в растворе
должно поддерживаться определенное мольное отношение рас-
творенного диоксида серы к эффективному аммиаку, равное
примерно 0,7. При таком соотношении SO2: NH3 (эфф.) равно-
весное давление SO2 и NH3 над этим раствором минимально,
219
что позволяет наиболее полно поглощать SO2 из газовой смеси
при минимальных потерях NH3. Общая концентрация солей
[ (NH4)2SO3+NH4HSO3] в орошающем растворе поддержива-
ется на уровне 500—600 г/л.
Сернокислотный туман, SO3 и брызги H2SO4, имеющиеся в
выхлопных газах, частично взаимодействуют в абсорбере с по-
глощающим раствором, образуя сульфат аммония:
SO3 + 2NH3 + Н2О = (NH4)2SO4
H2SO4 + 2NH3 = (NH4)2SO4
Неуловленные частицы тумана H2SO4, а также туман ам-
монийных солей и брызги уносимого раствора окончательно
улавливаются в электрофильтре.
Для восполнения расхода аммиака и поддержания в раство-
ре оптимального отношения SO2/NH3 (эфф.), в цикл абсорбции
непрерывно вводится аммиачная вода или газообразный аммиак.
Избыток образующегося раствора сульфит-бисульфита аммония
непрерывно выводится из системы и направляется на дальней-
шую переработку, в зависимости от выбранного способа утили-
зации этого раствора.
Первым, наиболее простым, путем утилизации растворов
сульфит-бисульфита аммония является его непосредственное ис-
пользование только в некоторых отраслях промышленности, на-
пример в кожевенном производстве, при флотации руд и в не-
которых других отраслях.
Другой способ использования сульфит-бисульфита аммония
состоит в том, что полученные после абсорбера APT растворы,
содержащие примерно 500—600 г/л растворенных солей, допол-
нительно закрепляются (в специальных насадочных колоннах
или в колонне с провальными тарелками) очищенным от пыли
и примесей обжиговым газом (7—12% SO2) до содержания в
них солей (в основном бисульфита аммония) 800—850 г/л. По-
лученный раствор отправляется в качестве готового стандарт-
ного продукта различным потребителям, например, в производ-
ство капролактама или для получения жидкого диоксида серы.
Одним из вариантов частичной утилизации раствора суль-
фит-бисульфита аммония является процесс его термического
разложения при высокой температуре в обжиговых печах сер-
нокислотного цеха с выделением SO2 в общий поток обжиго-
вых газов. В этом случае аммиак, затраченный на очистку от-
ходящих газов, не используется. При высокой температуре в пе-
чи он, в основном, превращается в азот.
Если в составе предприятия, на котором эксплуатируется
цех с аммиачной очисткой выхлопных газов, имеются цеха про-
стого суперфосфата, можно применить упрощенный аммиачно-
сульфатный способ очистки отходящих газов. При этом раство-
ры сульфит-бисульфита аммония направляются на разложение
в промывное отделение сернокислотного цеха. Выделяющийся
при разложении концентрированный диоксид серы выдувается
220
из промывной кислоты обжиговым газом и с общим потоком га-
за уходит на дальнейшую переработку в сернокислотную систе-
му. Промывная кислота с примесью образовавшегося сульфата
аммония выводится из системы и передается в производство
простого суперфосфата.
Одним из наиболее применяемых в нашей сернокислотной-
промышленности вариантов использования сульфит-бисульфит-
ных растворов является разложение их в специальной колонне
концентрированной серной кислотой [136]. При этом протекают
реакции:
(NH4)2SO3 + H2SO4 = (NH4)2SO4 + H2SO3
2NH4HSO3 4- H2SO4 = (NH4)2SO4 + 2H2SO3
2NH4HSOs <—> (NH4)2SO3 + H2SO3
H2SO3 <=> tso2 + H2O
В результате получается 40%-ный раствор сульфата аммо-
ния и выделяется 100%-ный диоксид серы, который отдувают из;
раствора с помошью острого пара (при 90—100 °C). Иногда от-
дувку SO2 ведут воздухом. Диоксид серы возвращают в серно-
кислотную систему или направляют на сжижение, а раствор1
сульфата аммония нейтрализуют аммиаком (избыток кислоты)
и передают в отделение выпарки и кристаллизации, где из него-
получают стандартный кристаллический продукт. Такие уста-
новки очистки отходящих газов запроектированы и построены
на многих крупных сернокислотных производствах.
Разложение сульфит-бисульфита аммония серной кислотой с
получением 100%-ного SO2 и кристаллического (NH4)2SO4 про-
изводится в больших масштабах на нескольких заводах.
Циклические способы. Во всех описанных выше ам-
миачно-кислотных способах выделение поглощенного из отходя-
щих газов SO2 в концентрированном виде сопровождается по-
лучением эквивалентного количества аммиачных солей. В цик-
лических способах основная цель заключается в концентриро-
вании диоксида серы при многократном повторном использова-
нии поглотителя.
Наиболее широко применим классический паровой или, как.
его еще называют, аммиачно-циклический способ. Сущность,
его заключается в том, что полученный в результате абсорбции
диоксида серы из отходящих газов раствор сульфат-бисульфита.
аммония (в основном состоящий из бисульфита аммония) под-
вергается нагреву с помощью острого пара. При этом реакция
SO2 + (NH4)2SO3 % Н2О «=> 2NH4HSO3
смещается влево; из раствора выделяется SO2 и в нем увели-
чивается содержание сульфата аммония. Десорбированный ди-
оксид серы может быть направлен в сернокислотную систему
или на сжижение, а охлажденный регенерированный раствор*
(Возвращается в цикл очистки отходящих сернистых газов.
22 и
04dLUSH.4oid SG3
РИС. 78. Схема установки концентрирования диоксида серы аммиачным ме-
тодом:
/ — поглотительная башня; 2 — фильтр; 3 — конденсатор; 4 — подогреватель; 5 — отгонная
колонна; 6 — кипятильник; 7 — холодильная башня; 8, 10 — холодильники; 9— сушильная
башня; // — выпарной аппарат; 12 — солеотделители; 13 — центрифуга.
Паровой классический способ подробно исследован у нас в
стране [134] и внедрен в промышленность (рис. 78). Этот спо-
соб концентрирования слабых сернистых газов применяется так-
же в Англии, США и ряде других стран.
Основным недостатком аммиачно-циклического способа при
использовании его для обогащения низкоконцентрированных
сернистых газов является большой расход пара на отгонку SO2
(до 10 т на 1 т SO2). Для устранения этого недостатка в
НИУИФе разработан усовершенствованный способ, позволяю-
щий сократить расход пара в несколько раз. Сущность этого
способа, называемого моноаммонийфосфатным, заключается в
том. что в циркулирующий раствор сульфит-бисульфита аммо-
ния в определенной точке вводят фосфорную кислоту для повы-
шения относительного содержания бисульфита в растворе. Это
приводит к резкому возрастанию равновесного давления SO2
над раствором и соответствующему сокращению расхода пара.
Образующийся при этом фосфат аммония выпадает из охлаж-
денного раствора после достижения предела его растворимости
в данной солевой системе. После отделения кристаллов моно-
аммонийфосфата к раствору добавляют аммиак и возвращают
раствор в цикл орошения абсорбционных аппаратов.
•222
Возможен комбинированный димоноаммонийфосфатный спо-
соб, который мало разработан, но представляет определенный
интерес для предприятий основной химии, на которых
имеется производство серной кислоты и сложных удобрений.
Способ основан на способности диаммонийфосфата поглощать
SO2 из газовой смеси с образованием моноаммонийфосфата и
бисульфита аммония:
(NH4)2HPO4 4- SO2 4- Н2О =?=* ХН4Н2РО4 + NH4HSO3
Используя высокую растворимость этих солей и подбирая,
оптимальное соотношение между NH3 и Р2О5, можно произво-
дить абсорбцию SO2 при пониженной температуре раствора и
его отгонку при нагреве насыщенного раствора примерно до
100 сС, т. е. осуществить циклический процесс.
Можно также обрабатывать полученный после абсорбции
смешанный сульфит-бисульфит-фосфатный раствор избытком
фосфорной кислоты для выделения SO2 в концентрированном
виде. Для заводов, имеющих в своем составе цех по производст-
ву аммофоса, такая схема предельно проста, поскольку она ба-
зируется на растворах, отбираемых и возвращаемых в основной
производственный цикл.
Принципиальная схема процесса сводится к следующему. Аммофосную-
пульпу отбирают из основного цикла и подвергают дополнительной сатура-
ции аммиаком до мольного отношения NH3: НзРС>4=1,5—1,6. Затем пульпу
фильтруют и фильтрат направляют на орошение абсорбционной колонны..
Далее к раствору добавляют фосфорную кислоту в количестве, необходимом
для перевода оставшегося диаммонийфосфата в моноаммонийфосфат и для;
разложения бисульфита аммония по реакции
NH4HSO3 4- Н3РО4 = NH4H2PO4 4- SO2 + Н2О
Раствор после обработки фосфорной кислотой поступает на отгонную ко-
лонну для полного удаления S03 в токе водяного пара или воздуха. Горячую-
пульпу после отгонной колонны возвращают в цех аммофоса.
В большинстве описанных выше аммиачных способов в каче-
стве конечного продукта получается сульфат аммония. Для то-
го, чтобы избежать затруднений при утилизации больших коли-
честв этого продукта, являющегося низкоконцентрированным
азотным удобрением, можно применить для очистки газов цик-
лический сульфат-бисульфатный процесс [136], по которому
сульфат аммония подвергается термическому разложению. Этот
способ основан на том, что при нагревании сульфата аммония
до 250—300 °C часть аммиака выделяется в газовую фазу с об-
разованием плава бисульфата аммония:
(NH4)2SO4 <—> NH3 + NH4HSO4
Если выделившийся аммиак вернуть на очистку газов и по-
лучить раствор сульфит-бисульфита аммония, а плав бисульфи-
та использовать для разложения этого раствора по реакциям
(NH4)2SO3 + 2NH4HSO4 = SO2 + 2(NH4)2SO4 4- H2O
NH4HSOs 4- NH4HSO4 = SO2 + (XH4)2SO4 + H2O
223
то можно получить 100%-ный диоксид серы и вновь сульфат
аммония, т. е. замкнуть цикл. Сульфат-бисульфатный способ
довольно сложен в аппаратурном оформлении процесса терми-
ческого разложения (NH4)2SO4 и пока промышленного распро-
странения не получил.
К этой же группе относится и комбинированный аммиачно-
известковый способ [132]. По этому способу газообразный ам-
миак впрыскивают непосредственно в очищаемые от SO2 газы
до поступления их на установку обезвреживания. При этом SO2
реагирует с аммиаком в газовой фазе с образованием сульфи-
та и бисульфита аммония. Далее газы направляют в два по-
следовательно установленных абсорбера, орошаемых раствором
сульфит-бисульфата аммония, в которых улавливаются образо-
вавшиеся сульфоаммиачные продукты. Избыток раствора из
абсорбера направляют в реактор, в который одновременно по-
дают острый пар и известковое молоко. В реакторе протекают
следующие реакции:
(NH4)2SO4 + Са(ОН)2 = CaSO4 + f 2NH3 + 2Н2О
NH4HSO3 + Са(ОН)2 = CaSO3 + ]NH3 + 2H2O
(NH4)2SO3 4- Ca(OH)2 = CaSO3 + f 2NH3 + 2H2O
Аммиак и водяной пар отсасывают из реактора и с добавле-
нием свежей порции аммиака подают в голову процесса. Пуль-
пу из реактора охлаждают в холодильнике и отфильтровывают
•от шлама в центрифуге. Часть маточного раствора поступает в
цикл орошения абсорберов, а другую направляют в сборник для
приготовления известкового молока. Осадок сбрасывают в от-
вал или используют в качестве строительного материала.
По другому варианту раствор из абсорбера сначала подают
в отгонную колонну, где при нагревании из него выделяется
часть поглощенного SO2, и затем в реактор для взаимодействия
с известью. Таким образом можно примерно 60% SO2 получить
в виде товарного продукта, а 40% —в виде сульфит-сульфатно-
го шлама.
Сухие аммиачные способы. Сухих способов связывания SO2
с применением аммиака в отличие от жидкостных, известно
очень мало. В основном предлагается подавать NH3 в газовую
фазу и полученные твердые продукты реакции (сульфит, пиро-
сульфит, сульфат, аминосульфат и др.) улавливать в электро-
фильтре. Можно подобрать условия (температура, соотношение
NH3 и SO2, влагосодержание), когда связывание SO2 происхо-
дит с достаточной полнотой. Однако утилизация полученного
продукта и переработка его в сульфат аммония довольно
• сложны.
Чтобы избежать дополнительной переработки продукта улав-
ливания предлагается сначала проконвертировать SO2 в SO3 на
дешевом катализаторе, затем добавлять в газовую фазу NH3 и
получать сразу сульфат аммония. Из литературы известен так-
же твердофазный аммиачный способ извлечения SO2 из газов,
'.224
когда поглотителем служит предварительно насыщенная ам-
миаком торфяная масса [139].
Расчетные формулы
1. Определение содержания диоксида серы в газах, поступающих на
очистную установку, а также общего объема отходящих газов.
Если известна производительность сернокислотного цеха, а также вели-
чина потерь SO? и серной кислоты в процессе производства, то общее коли-
чество (в кмоль/ч) диоксида серы в газах после контактного аппарата может
быть рассчитано по формуле
4-1000(1 — х)
GSO2= 24-98-П
а его объем (в м3/ч)
Vso2= Gso2'22,4
где Gso„—количество иепроконтактированного SO2 в газах после контакт-
ного аппарата, кмоль/ч; Vso, — объем иепроконтактированного SO2, м3/ч;
А — производительность цеха по серной кислоте (без учета промывной кис-
лоты), т/сут моногидрата; П — коэффициент, учитывающий величину потерь
SO2 и кислоты после промывного отделения, включая неполноту контакти-
рования, доли единицы; х— степень контактирования, доли единицы.
Далее, если обозначить через С — содержание SO2 в газе перед кон-
тактным аппаратом в °/о (об.), через С' — содержание SO2 в газе после мо-
ногидратного абсорбера в % (об.), то последнюю величину, с учетом умень-
шения объема газа за счет связывания кислорода газовой смеси при контак-
тировании, а также с учетом уменьшения объема газа в результате погло-
щения SO3 при абсорбции, можно рассчитать следующим образом.
Перед контактированием в 100 м3 обжигового газа содержится С м3
SO2 и (100—С) м3 азота и кислорода. После контактирования объем SO2,
SO3, 1N2 и О2 (в м3) будут соответственно равны:
VSo2=(l-x)-C; Vso3=x-C; Vn2,o2 = 100 - С-0,5х-С
После абсорбции SO3 общий объем газовой смеси (в м3) составит
Izr c = VN-2 о2 + ^so2= 100—С — 0,5х-С + (1 — х)-С = 100 — 1,5х-С
а содержание SO2 в отходящих газах (в % об.)
VSo2-100 (1 — х)-С-100
С’= = 100 —1,5х-С
Из этого уравнения можно получить известную формулу для определе-
ния степени контактирования по изменению объемного содержания SO2 в
газовой смеси до и после контактирования (в долях единицы)
100 (С—С')
х== С (100 — 1,5С')
Общий объем отходящих газов ЕОбщ при данном содержании SO2 в га-
зах после моногидратного абсорбера составляет (в м3/ч)
Vso2’ 100
1''об1Ц =---------
или, подставляя в это уравнение значения Vso2h С', получим
Д-1000 (1 — х)-22,4 (100 — 1,5х-С)-100
V°бЩ = 24,98-П (1 — х)-С-100
9,55-4(100 — 1,5хС)
У°бщ— п.с
15—584
225
2. Определение количества аммиака, необходимого для поглощения ди-
оксида серы в аппаратах APT.
Расход аммиака на поглощение сернистого ангидрида из отходящих га-
зов (в кг/ч 100%-ного NH3) равен
Gso/Tl7
°NH3 = s/C
где т]— степень улавливания SO2 в аппаратах APT, доли единицы; S/C—
молярное отношение SO2 к NH3 (эфф.) в циркулирующем растворе суль-
фит-бисульфита аммония, доли единицы.
Если учесть, что аммиак расходуется еще на связывание в сульфат ам-
мония примесей SO3, тумана и брызг серной кислоты, поступающих с отхо-
дящими газами, и обозначить нх суммарное содержание через «К» (в г/м3),
то расход NH3 на эту статью составит (в кг/ч 100%-ного NH3)
А-3000-34-К
Gnh3(k) = 1000-98-24
где 3000 — средний объем отходящих газов, приходящийся иа 1 т выраба-
тываемой серной кислоты, м3.
В окончательном виде дополнительный расход аммиака (в кг/ч) соста-
вит
Gnh3(k> =0,0433-А-К
Общий расход аммиака на установке улавливания (в кг/ч) будет равен
/ OsoAl-l7 \
Gnh3(o6ih) — (Gnh3 -|- Gnh3(kj) 1 >03 = ^/с -|- 0,0433АХу 1,03
где 1,03 — коэффициент, учитывающий 3%-ные потери NH3.
3. Определение количества серной кислоты, необходимой для разложе-
ния раствора сульфит-бнсульфнта аммония.
При взаимодействии раствора сульфит-бисульфита аммония с серной
кислотой происходит образование сульфата аммония и выделяется диоксид
серы. На разложение одного моля сульфита аммония требуется одни моль
серной кислоты, а на разложение одного моля бисульфита аммония необхо-
димо затратить 0,5 моля серной кислоты. Таким образом, если в растворе
сульфит-бисульфита аммония, поступающего на разложение, содержится у
молей сульфита и z молей бисульфита аммония, то стехиометрический расход
серной кислоты а (в молях) на разложение 1 л такого раствора составит
а=у+0,5 z=0,5 (2у+г)
Общий расход серной кислоты (в л/ч) по уравнениям можно рассчитать
по формуле
QaM-100 Qa-9,8
<?H2S04=1ooo-Ch2so1Y= Ch2so4Y
где Qh2SO4— общий расход серной кислоты на разложение раствора суль-
фит-бисульфита аммония, л/ч; Q — расход раствора сульфит-бисульфита ам-
мония, л/ч; а — стехиометрический расход серной кислоты, моль/л сульфит-
бисульфита аммония; М — молекулярная масса серной кислоты, г/моль;
CH2SO4—концентрация серной кислоты, %; у — плотность серной кислоты,
кг/л.
Обычно разложение проводится с некоторым избытком серной кислоты
против стехиометрии. В этих случаях расчетное количество H2SO4 соответст-
венно увеличивается.
4. Определение количества сульфата аммония, вырабатываемого на уста-
новке очистки отходящих газов.
Выход сульфата аммония (кристаллического в кг/ч) на установке очистки
отходящих газов сернокислотного цеха, можно подсчитать по формуле
GSO,*1‘132
G(NH4)2so4 = 5^2
226
После подстановки и сокращения, в окончательном виде формула при-
мет вид:
28,1-А(1 — х) т)
G(NH4),SO4 — П-S/C
без учета потерь в процессе выпарки, кристаллизации и сушки.
5. Определение расходной нормы серной кислоты на 1 т кристаллическо-
го сульфата аммония.
Расходную норму серной кислоты (в т моногидрата) на 1 т кристалли-
ческого сульфата аммония можно рассчитать по уравнению
Дн280Л
H2SO4 М(ХН4)25О4П1
где Mh2so4> ^f(NH4)2SO4—молекулярные массы серной кислоты и сульфата
аммония; К — коэффициент, учитывающий окисление раствора сульфит-би-
сульфита аммония до сульфата аммония, кислородом газа в растворе,
доли единицы; П| — коэффициент, учитывающий потери сульфата аммония в
процессе его получения, упарки раствора, кристаллизации и сушки.
Если принять потери сульфата аммония в процессе его получения рав-
ными 5%, а самоокисление раствора сульфит-бисульфита аммония до суль-
фата в размере 10% (в зависимости от концентрации SO2 в очищаемом газе,
температуры и состава сульфит-бисульфита аммония, степень окисления мо-
жет колебаться в пределах от 5 до 15% от поглощенного SO2), то расходная
норма серной кислоты в т на 1 т (KH4)2SO4 составит
98-0,90
°H2so4 = 132-0,95 ~°’7т/т
111.6.2. Кислотно-каталитический способ
очистки газов
Кислотно-каталитический способ улавливания SO2 из
газов низкой концентрации основан на возбуждаемой ионами
металлов переменной валентности (Си, Fe, Мп) цепной реак-
ции окисления SO2 в жидкой фазе до серной кислоты. Роль
катализатора в этой реакции заключается в превращении в
активную форму кислорода, поступающего вместе с SO2 в жид-
кую фазу [136]. Механизм цепного процесса окисления SO2
объясняется действием монотионовой кислоты HSO3. Последняя
находится в равновесии или переходит в дитионовую кислоту,
которая часто образуется наряду с серной кислотой в окисли-
тельном процессе. Ион-радикал монотионовой кислоты перехо-
дит в дитионовую кислоту:
SO3- + Н+ ----> HSO3 2HSO3 --------> H2S2Oe
Действие монотионовой кислоты может быть представлено
в следующем виде:
HSO3 + О2 + so32- + Н2О ---> 2SO42- + 2Н+ + ОН
Радикал ОН генерирует новый ион монотионовой кислоты:
ОН + SO32- ---> SO3 %- ОН so3- 4- Н + -->-HSO3
и снова начинается цепь реакции.
15* 227
Согласно работам Н. Н. Семенова, образующийся при пере-
мене валентности свободный радикал монотионовой кислоты
дает новые радикалы:
SOs -|- О2 * SO5
Радикал кислоты Каро SO5~ вступает в реакцию
SOs- + SO3*- --> SCV- + SO3-
B результате взаимодействия иона кислоты Каро с ионом
сульфита образуется серная кислота
SO32-4-SO32----> 2SO42-
Ион-радикал SO3~ вновь начинает цепь реакций.
Н. Н. Семенов подтверждает возможность образования мо-
нотионовой кислоты тем, что при разрядке иона SO32~ на элек-
троде появляется вначале ион-радикал SO3_, который образу-
ет затем ион дитионовой кислоты S2O62-. Следы дитионовой
кислоты в получаемой серной кислоте были обнаружены при
изучении каталитической активности природного пиролюзита
[136]. Предполагается, что образование дитионовой кислоты
происходит в момент растворения пиролюзита в серной кисло-
те, содержащей диоксид серы.
Предложена схема реакций
2МпО2 + 3SO2 --> MnSO4 -|- MnS2Oc
MnS2O6 4- H2SO4 -> MnSO4 4- H2S2O6
Из дитионовой кислоты образуется монотионовая кислота:
H2S2Oe 2HSO3
Она может присоединять кислород и начинать новую цепь
реакций:
2HSO3 + О2 + 2Н2О -> 2H2SO4 + 2ОН
Радикал ОН окисляет двухвалентный марганец:
2MnSO4 + 2ОН 4- H2SO4 --> Mn2(SO4)3 + 2Н2О
Mn2(SO4)3 + SO2 + 2H2O -> 2MnSO4 + 2H2SO4
Сопоставление катализаторов различных типов дано
в табл. 47 [скорость абсорбции SO2 в моль-107/(мин-см2)].
Наиболее эффективным катализатором является природная
марганцевая руда и пиролюзит. Многочисленные исследования
показали [138], что при отсутствии в газах веществ, отравляю-
щих катализатор (продукты неполного сгорания, фенолы и
др.), этот процесс протекает эффективно. Необходимо также,
чтобы в газах имелось благоприятное соотношение между О2 и
SO2, объемное отношение О2: SO2 должно быть около 35.
228
Таблица 47. Сравнение различных типов катализаторов
Катализатор Концентрация. % капли, мкм Скорость ,i ГччтициИ so, '
катализа- тора SO2 в газе
MnSO4 0,025 0,030 700 0.32
0,050 0,012 700 0,53
0,100 0,020 700 1,00
Fe2(SO4)3 5,3 0,030 760 0,13
FeSO4 0,5 0,036 790 0.07
MnSO4 + Fe2(SO4)3 0,05+0.266 0,012 770 0,45
MnSO4+CuSO4 0,05+0,0005 0,025 780 0,46
NiSO4 0,10 0,035 700 0
Отходящие газы сернокислотного производства после мно-
гостадийной их обработки в основном технологическом процес-
се не содержат, помимо SO2 и SO3, каких-либо других твердых
или газообразных примесей, которые могут оказать вредное
воздействие на процесс извлечения SO2. Это обстоятельство
дало основание внедрить кислотно-каталитический способ для
очистки отходящих газов. Впервые в крупном масштабе он был.
испытан на установке производительностью 20 000 м3/ч.
В НИУИФе были проведены исследования по усовершенст-
вованию технологии и аппаратурного оформления кислотно-ка-
талитического способа применительно к очистке отходящих
газов контактных систем. В частности, улучшен контакт жидко-
сти с катализатором и уменьшен его расход, изменены гидро-
динамические условия работы абсорберов, выявлена оптималь-
ная концентрация образующейся кислоты и др.
Лимитирующей стадией процесса является стадия поглоще-
ния из газовой смеси трудно растворимого кислорода. Поэтому
более пригодным для данного процесса оказался абсорбер, в ко-
тором можно в максимальной степени интенсифицировать мас-
сопередачу в жидкой фазе при сравнительно небольшом увели-
чении гидравлического сопротивления. Этому требованию отве-
чают абсорберы с обычной кольцевой насадкой, с прямоточным
движением контактирующих фаз. При прямотоке можно осуще-
ствить процесс при высокой плотности орошения без захлебы-
вания и без резкого возрастания гидравлического сопротивления
аппарата. Технологическая схема процесса представлена на
рис. 79.
РИС. 79. Схема очистки отхо-
дящих газов кислотно-катали-
тическим способом:
/ — первый абсорбер; 2 — фильтры;
3 — второй абсорбер; 4 — брызгоу.чо-
витель.
22»
Отходящий газ контактной системы подается в два последовательно рас-
положенных насадочных абсорбера. Линейная скорость газа в сечении абсор-
бера составляет 0,8—1 м/с. Движение фаз в абсорбере осуществляется по
принципу прямотока. Плотность орошения абсорбера составляет 15—
20 м3/(м2-ч). В первом по ходу газа абсорбере циркулирует более концент-
рированная серная кислота (15—25%-ная), а во втором — кислота концентра-
цией 5—10%. Свежую воду для компенсации испарения и расхода на обра-
зование кислоты подают в циркуляционный сборник 1-го абсорбера, а избы-
ток образующейся кислоты передают в циркуляционный сборник 1-го абсор-
бера и оттуда выводят из системы. Часть орошающей кислоты (10—15%)
перед поступлением иа насадку абсорбера проходит через контактный
фильтр, где происходит взаимодействие жидкости с пиролюзитом и обогаще-
ние ее активными ионами марганца. Концентрация Мп в кислоте поддержи-
вается на уровне 0,03—0,10%, время пребывания газа в активной зоне 15—
20 с. Очистка газа от SOa может быть обеспечена на 60-^-70%.
Основные расчетные показатели для установки производи-
тельностью по газу 75 000 м3/ч приведены ниже:
Исходная концентрация SO2 в газе, % 0^13
Степень улавливания SO2, %.........................85
Количество поглощенного SO2, кг/ч.................238
Количество образующейся 30%-ной кислоты, кг/ч . 1220
Расход воды, кг/ч
иа образование кислоты........................855
для компенсации испарения .................. 3000
Расход Мп, кг/ч.................................—1,21
Расход пиролюзитовой руды (степень использования
60%), кг/ч........................................3,2
Концентрация Мп в продукционной кислоте, % . 0,1
Диаметр абсорбера (линейная скорость газа 1 м/с),
м................................................5,75
Высота насадки в каждом абсорбере, м . 7
Расход кислоты на орошение [А = 15 м3/(м!-ч)], м3/ч 396
Гидравлическое сопротивление каждого абсорбера,
кПа...............................................0,6
Расход кислоты иа контактный фильтр (15%), м3/ч 60
Площадь сечения контактного фильтра, м2 . 6
Основным недостатком в работе таких установок является
коррозия металлической аппаратуры из-за трещин в свинцовой
оболочке. При коррозии металла и растворении его в кислоте,
выделяющийся водород способствует появлению восстановлен-
ных соединений серы (сероводород и др.), в присутствии кото-
рых каталитическая реакция окисления SO2 в жидкой фазе
тормозится. Требуется длительное время и повышенный расход
пиролюзита, чтобы ликвидировать вредное действие яда и вос-
становить процесс каталитического окисления SO2.
Наряду с улавливанием SO2 в абсорберах установки одно-
временно происходит и достаточно полное (на 60—90%) вымы-
вание из газа сопутствующих кислых примесей (SO3, тумана и
брызг H2SO4).
Оптимальные показатели технологического режима очистки
отходящих газов по кислотно-каталитическому способу приведе-
ны ниже:
230
Концентрация SO2 в газе, %
исходная .............................................
конечная .........................................
Средняя степень улавливания, %........................
Скорость газа в абсорберах, м/с.......................
Плотность орошения абсорберов, м3/(м2-ч) . . . .
Высота насадки в абсорберах, м........................
Характер движения газа и жидкости в абсорберах
Концентрация кислоты, % H2SO4
в 1-м абсорбере...................................
во 2-м абсорбере .................................
Концентрация Мп в кислоте
в 1-м абсорбере.......................................
во 2-м абсорбере .................................
Температура, °C
поступающего газа.................................
орошающих кислот..................................
Размер насадки (керамические кольца в укладку), мм
Доля кислоты, пропускаемой через контактные фильтры, %
Скорость подъема кислоты в фильтре, м/ч . . . .
Высота слоя пиролюзита в фильтре, м...................
0,15 — 0,20
0,022—0,03
85
О 8
25
8
Противоток
15—20
5—10
0,10—0,15
0,02—0,05
60—70
25—30
50X50
15
10
1,5
Ш.6.3. Сульфитно-содовый способ очистки газов
Диоксид серы из отходящих газов сернокислотного про-
изводства поглощается сульфитно-содовым раствором. При этом
протекают реакции
Na2CO8 -J- 2SO2 + Н2О = 2NaHSOg + СО2
2Х’а2СО3 4- SO, 4- Н,0 = 2NaHCO, 4- Na„SO,
Na2SO3 4- SO2 4- Н2О = 2NaHSOs
Отходящий газ после брызгоуловителя моногидратных абсор-
беров поступает на поглощение SO2 в абсорбер установки очист-
ки. Газовая нагрузка установки 15000 м3/ч. Поступающий газ
содержит 4,675 г/м3 SO2, степень очистки 99,5%, концентрация
отходящего газа не более 0,005% SO2.
Исходный сульфитно-содовый раствор концентрацией 1,19—1,25 г/см3 с
рН=9—12 у=1,16—1,20 г/см3 насосом подают в напорный бачок абсорбера,
а после абсорбера он стекает обратно в сборник. При рН=7 раствор перека-
чивают в циркуляционный сборник, откуда направляют для доукрепленпя на
орошение скрубберов Вентури, одновременно сюда же подают 6—8%-ный
газ. После скруббера Вентури брызги улавливают во втором скруббере и
циклоне-брызгоуловителе, далее газ подают вентилятором в нижнюю часть
абсорбера. Температура поступающего в абсорбер газа 25—40 °C, раствора —
до 45 °C.
На 1 т готовой продукции с содержанием 36,6% бисульфита натрия (в
готовой продукции содержится также 1% Na2SOa) расходуется: 194 кг каль-
цинированной соды, 360 кг диоксида серы (по балансу — 234 кг, что соот-
ветствует 83,7 м3 100%-ного SO2, или 3097 м3 7%-ного), 12 кВт-ч электро-
энергии, 0,14 Гкал пара, 0,7 м3 воды.
Ниже приведена краткая характеристика оборудования.
Абсорбер: dBH = 3000 мм; // = 6414 мм; насадка — кольца Рашига ряда-
ми— от 120 до 50 мм; IzHac = 21,2 м3; //нас = 3000 мм; футеровка — кислото-
упорный кирпич, обложенный полиизобутиленом на Арзампте-5; плотность
орошения 10 м3/(м2-ч); расход раствора 70 м3/ч; распределение раствора по
насадке осуществляется через 5 распылителей. Брызгоуловитель абсорбера:
231
<1 = 3200 мм; /7=1600 мм; насадка — мелкие кольца Рашига. Скрубберы Вен-
тури (2 шт.): материал — оргстекло; конфузор d = 400 мм; диффузор d =
= 4500 мм; горловина d = 900 мм. Циклон-брызгоуловитель: тип — вертикаль-
ный прямоточный; d = 612 мм, Н=2500 мм, материал — оргстекло. Вентилятор
(2 шт.); производительность 3500 м3/ч; материал — стеклотекстолит. Цирку-
ляционные сборники: обогрев — паром через змеевик.
В стадии освоения находятся две такие установки, производительностью
по газу 65000 м3/ч каждая. Абсорбция SO2 из отходящих газов сернокислот-
ного производства проводят в аппарате APT, для укрепления раствора пре-
дусмотрен барботажный четырехполочный абсорбер. Барботажный абсорбер
представляет собой колонну с ситчатыми тарелками и охлаждающими эле-
ментами для отвода тепла реакции диоксида серы с сульфит-бисульфитным
•раствором. Во избежание пересыщения раствора и выпадания на первой та-
релке по ходу газа кристаллов пиросульфита натрия сухой газ перед подачей
из компрессорного отделения в абсорбер увлажняется в увлажнительной
башне, затем газ проходит циклон-брызгоуловитель и поступает в абсорбер.
Этот способ очистки применяется также в ФРГ и Японии.
111.6.4. Причины образования тумана
и очистка от него выхлопных газов
Образование тумана. Выхлопные газы контактных сер-
нокислотных заводов при определенных условиях могут содер-
жать тонко распыленные частицы серной кислоты. Этот аэро-
золь серной кислоты с размерами частиц примерно 0,5—10 мкм
принято называть «кислотным туманом». Если его содержание
в отходящем газе выше 35 мг/м3, его можно видеть невоору-
женным глазом. Чем мельче частицы тумана, тем легче он ви-
ден. Возможно присутствие в тумане более мелких и более
крупных частиц. Частицы серной кислоты крупнее 10 мкм при-
сутствуют в газах, по-видимому, в результате механического
уноса кислоты из абсорбера, такие частицы мало влияют на
.видимость выхлопного газа. Капельки кислоты указанного раз-
мера легко оседают на стенках газоходов и выхлопных труб и
не участвуют в загрязнении атмосферы, за исключением случа-
ев, когда на сернокислотных установках работают с высокой
скоростью газового потока на выхлопе.
Источниками образования тумана серной кислоты могут
быть триоксид серы, сама кислота и вода.
Выхлопные газы, содержащие SO3, вследствие неполноты
абсорбции, образуют туман при соприкосновении с влагой атмо-
сферного воздуха. Кислотный туман может образоваться в аб-
сорбере при соприкосновении со слабой или холодной кислотой.
При абсорбции кислотой повышенной концентрации возрастает
парциальное давление паров SO3, вследствие чего он будет вы-
водиться из абсорбера. Туман серной кислоты может также об-
разоваться, когда газы подвергаются охлаждению перед абсорб-
цией, как это происходит в производстве олеума. Перечисленные
выше туманы, как правило, состоят из частиц мельчайших раз-
меров и избавление от них является весьма трудной проблемой.
Туман серной кислоты образуется в результате конденсации
232
ее паров, возникающих при испарении горячей кислоты абсорб-
ционной башни. Парциальное давление паров серной кислоты:
над кислотой возрастает с ростом температуры и концентрации
кислоты. Хотя количество паров серной кислоты в обычных ус-
ловиях эксплуатации мало, но оно может оказаться совершенно
достаточным, чтобы образовался явно видимый туман.
Туман образуется также при наличии паров воды в газах,
поступающих в контактный аппарат. Обычно это связано с пло-
хой работой сушильной башни. При эффективной работе су-
шильной башни влажность газов должна снижаться до 80 мг/м3
и механический унос брызг серной кислоты должен отсутство-
вать. На установках, сжигающих серу, туман может возникнуть
вследствие присутствия воды, образующейся при горении при-
месей углеводородов в сере.
На установках, регенерирующих SO2 из кислых гудронов,
туман, образовавшийся в системе мокрой очистки, не улавлива-
ется полностью в электрофильтрах. Этот туман проходит через-
сушильные башни и контактный аппарат и вновь возникает, ког-
да газы охлаждаются в абсорбционной башне. Совершенно оче-
видно, что просачивание пара или воды внутри системы способ-
ствует образованию тумана.
Очистка газов от тумана серной кислоты. Санитарные уста-
новки, рассмотренные в предыдущем разделе, рассчитаны глав-
ным образом на удаление SO2 из отходящих газов, но в этих си-
стемах не достигается высокоэффективное удаление частиц ту-
мана крупностью менее 10 мкм; чем меньше частица тумана,
тем менее вероятно их поглощение раствором. Механически ув-
леченные частицы размером крупнее 10 мкм абсорбируются рас-
твором в скруббере с образованием сульфата аммония.
Для удаления тумана серной кислоты отходящих газов ре-
комендуют применять рассмотренные ниже аппараты.
Скруббер Вентури. Есть указания, что при обработке газа водой из рас-
чета 0,57—0,76 л/м3 в выхлопных газах после этого аппарата остается 17—
100 мг/м3 тумана серной кислоты. При этом гидравлическое сопротивление
аппарата составляет 225—380 мм вод. ст., 2,25—3,80 кПа.
Сепараторы с плотным слоем насадки. В этих аппаратах используются
частицы песка, кокса и других сыпучих материалов, волокнистое полотно,
которые задерживают частицы тумана или вызывают коагуляцию вследствие
интенсивной турбулизации газа в малых пространствах между слоями на-
садки. Для этой же цели применялись промышленные (стандартные) наса-
дочные материалы. Слой высотой 30 см из элементов насадки седельного ти-
па (седла Берля) размером 2,5 см является эффективным для удаления час-
тиц тумана среднего размера при скорости газа порядка 3 м/с.
Для удаления тумана применялись крупные фильтрующие установки, на-
саженные слоями точно отсортированной коксовой мелочи. Волокнистое по-
лотно с нитями различного диаметра применяется для этой цели в очень, ог-
раниченной степени, вследствие тенденции материала к слежнванню и сли-
панию.
Механические коагуляторы. Удаление кислотного тумана (за исключением
таких мельчайших частиц тумана, которые образуются на установках, выпу-
скающих олеум) происходит с помощью фильтров из многослойной стальной
сетки и фильтров из пористой керамики.
23»
Работа на отделителях, изготовленных из проволочной сетки, обычно
проводится в две ступени: в первой нижней ступени сетка сжата до плот-
ности 0,2 кг/л, во второй — до меньшей плотности. Сетки помещены в верти-
кальной трубе на расстоянии в несколько сантиметров одна от другой. Ниж-
няя сетка (высокой плотности) действует как коагулятор, а проскочившие
через нее коагулированные частицы удаляются на верхней сетке.
Скорость газов в этих аппаратах достигает 3,3—5,4 м/с. Прн скоростях
ниже 3,3 м/с кинетическая энергия частиц, по-видимому, слишком мала, что-
бы способствовать коагуляции, а прн более высоких скоростях улавливание
частиц тумана осложняется. Сопротивление в этом аппарате достигает
750 Па. На установках, выпускающих 98%-ную кислоту, выхлопной газ, про-
пущенный через такой отделитель, неизменно содержал 17 мг/м3 тумана сер-
ной кислоты. Туман олеумных установок пока не удалось улавливать никаки-
ми механическими коагуляторами.
Так как уловленный туман представляет собой крепкую серную кислоту
(выше 96% H2SO4), то при выборе проволочной сетки надо учитывать воз-
можность коррозии. Затраты на такие фильтры невелики. Стоимость уловлен-
ной кислоты обычно полностью покрывает эти затраты в течение одного года.
Фильтры из керамики. Для удаления кислотного тумана весьма эффек-
тивны фильтры из пористых керамических труб, например, так называемые
фильтры Бринка. Они имеют трубы длиной несколько метров, диаметром не-
сколько сантиметров при толщине стенки 9,5—10 мм. Трубы монтируются в
горизонтальной трубной решетке. Верхние края труб открыты, нижние за-
крыты. Газы направляются по трубам сверху вниз и выходят через пористые
стенки. Для керамических трубчатых фильтров требуется значительно боль-
шая фильтрующая поверхность, чем для фильтров из проволочной сетки.
Фильтровальные трубы состоят из равномерных частиц глинозема (или
аналогичного кислотоупора), скрепленных связующим средством, обеспечи-
вающим пористую структуру труб. При поломке труб расходы по текущему
ремонту значительно выше, чем при работе с проволочными фильтрами. За-
траты на них также значительно выше. Чтобы получить на керамическом
фильтре такую же степень очистки от тумана серной кислоты, как на прово-
лочном фильтре, рабочее сопротивление должно составить 2,0—2,5 кПа, зна-
чительно возрастают эксплуатационные расходы.
Электрофильтры, для улавливания частиц тумана серной кислоты из хо-
лодного SO2-содержащего газа в системах мокрой очистки широко применя-
ются трубчатые электрофильтры. В ннх удовлетворительно улавливаются
мелкие частицы тумана, но установка электрофильтра требует больших капи-
тальных вложений.
Электрофильтры применялись для очистки выхлопных газов, содержащих
серную кислоту. В ряде случаев стальные трубчатые электрофильтры оказа-
лись непригодными: трноксид серы или пары серной кислоты проскакивали
через фильтр в газообразной форме п на выхлопе образовывали видимый ту-
ман. В этих условиях удовлетворительно работают свинцовые трубчатые
электрофильтры, если обеспечить предварительное увлажнение газов.
Звуковые агломераторы. Работа звуковых агломераторов основана на
том, что звуковые волны приводят мелкие частицы аэрозоля в состояние
вибрации, и они коагулируют с образованием в несколько раз более крупных
частиц. Эти более крупные частицы могут быть удалены из газового потока
при помощи обычных циклонов. На одной пз сернокислотных установок
очистка проходила на 90% и содержание тумана на выходе составляло 70—
100 мг/м3.
111.6.5. Нейтрализация сточных вод
При нормальной работе сернокислотного цеха вода из
холодильников для кислот не должна содержать вредных при-
месей. Она считается условно чистой и может сбрасываться в
водоемы. Но в случаях утечки кислоты из холодильников и их
234
ремонта вода становится кислой и сбрасывать се в водоемы
нельзя.
Наиболее рациональный способ очистки кислых стоков заключается в
организации системы водооборота со станцией нейтрализации в цикле- При
атом вода от всех холодильников поступает в приемные баки, откуда наси-
сами подается на |раднрны для охлаждения, затем собирается в сборники и
прессами передастся на .холодильники.
При обнаружении кислотности воды автоматически включается станция
нейтрализации, и в воду добавляются нейтрализующие добавки (мел, из-
весть, известковое молоко). Для восполнения потерь воды за счет испарения,
проливов и т. д. в цикл водооборота систематически добавляется свежая во-
да. Система водооборота устраняет возможные сбросы кислых вод, а также
сброс чистых, но теплых обедненных кислородом вод, отрицательно дейст-
вующих на флору и фауну водоемов. Водооборот организован на большин-
стве давно работающих и на всех новых заводах.
В некоторых сернокислотных цехах для нейтрализации кислых стоков
имеются местные станции нейтрализации, включающие сборник с мешалкой
и баки для хранения содового или известкового раствора.
На нейтрализацию кислые стоки поступают по трубам со специальными
клапанами, автоматически открывающимися по команде от датчика-сигнали-
затора кислотности воды; также автоматически открывается клапан с нейтра-
лизующим раствором и включается мешалка. Количество нейтрализующего
раствора регулируется по pH-метру, установленному иа трубопроводе для
выходящей из сборника воды. Из сборника нейтрализованная вода посту-
пает в канализацию условно чистых стоков или в шламонакопитель завод-
ской станции нейтрализации.
111.7. ПОЛУЧЕНИЕ КОНЦЕНТРИРОВАННОГО И ЖИДКОГО
ДИОКСИДА СЕРЫ
Концентрированный газообразный и жидкий диоксид
серы широко используется в промышленности для получения
сульфитов, в производстве моющих средств, в холодильной тех-
нике, в легкой, пищевой и других отраслях промышленности.
Диоксид серы, предназначенный для этих целей, получают глав-
ным образом из отходящих газов, и лишь в отдельных случа-
ях— из газов, образующихся при сжигании серы или при обжи-
ге серного колчедана.
Из многих предложенных методов концентрирования газов с
низким содержанием SO2 наибольшее применение получил цик-
лический метод с использованием жидкого абсорбента, в пер-
вую очередь — аммиака, по которому SO2 поглощается аммиач-
ной водой с образованием раствора сульфит-бисульфита аммо-
ния (см. выше). Поглотительный раствор обрабатывают острым
паром пли нагретым воздухом, если не требуется получение
100%-ного SO2. В некоторых случаях для выделения SO2 рас-
твор обрабатывают серной, азотной или фосфорной кислотой.
Газ после конденсации паров и осушки направляют на сжиже-
ние.
Перспективным способом получения концентрированного
SO2 (до 95—98%) может быть окисление колчедана огарком,
описанные в гл. II.
Представляет интерес циклический магнезитовый метод извлечения диок-
сида серы из низкоконцентрированных газов. В этом процессе поглотителем
235
служит водная суспензия MgO. В первой стадии процесса диоксид серы из-
влекается из газа в орошаемой поглотителем башне с насадкой по следую-
щим реакциям:
MgO + H2O=Mg(OH)2
Mg(OH)2 + SO2 + 5НгО = MgSO3-6H2O
Плохо растворимый в воде шестиводный сульфит магния отфильтровы-
вают и сушат топочными газами в кипящем слое при 160—180 °C. Затем су-
хую соль нагревают топочными газами в кипящем слое вначале до 500, по-
том до 900—1000 °C. В этих условиях сульфит магния разлагается с выде-
лением SOa и образованием MgO, который охлаждают и возвращают в про-
цесс. Таким способом получают газ, содержащий около 20% SO2, осталь-
ное — компоненты топочных газов. Способ используется также для получе-
-яия чистого оксида магния.
Чистый диоксид серы обычно получают из серы и триокси-
да серы. При этом серу обрабатывают олеумом. Растворенный
в нем триоксид серы реагирует с серой по уравнению [141]
2SO3 4- S = 3SO2
Этот процесс экономичен при организации его в контактном
^сернокислотном цехе, поскольку можно использовать олеум,
циркулирующий в системе. Часть растворенного в олеуме SO3
расходуется на образование SO2. Образующийся при этом бо-
лее слабый олеум возвращается в цикл олеумного абсорбера.
Взаимодействие серы и триоксида серы происходит в реакторе, представ-
ляющем собой котел, снабженный теплоизоляцией, в который сверху по цент-
ральной трубе поступает твердая сера. Олеум, содержащий 30% SOj (своб.)
и подогретый до 100 °C, поступает через днище реактора и вытекает по пат-
рубку в верхней части реактора уже при содержании 5—10% SO3. Образую-
щийся при окислении серы SO2 вместе с выделяющимся из олеума SO3 по-
:следовательно проходит два фильтра, заполненных серой, с которой реагиру-
ет газообразный триокснд серы. Для удаления из диоксида серы остатков
SO3 газ пропускают через два абсорбера с насадкой, орошаемой моногидра-
том, затем фильтруют для удаления брызг и кислотного тумана и комприми-
руют для снижения SO2.
Процесс уже несколько десятилетий используется в промыш-
ленности, но в литературе практически отсутствуют сведения об
изучении его физико-химических основ. В НИУИФе проведен
ряд лабораторных исследований, направленных на совершенст-
вование способов производства чистого концентрированного ди-
оксида серы.
Кинетику взаимодействия S с SO3 и механизм процесса изу-
чали в лабораторных реакторах с мешалкой. Концентрация
олеума была от 5 до 30% SO3 (св.), температура в зоне взаимо-
действия 70—100 °C. В олеум впрыскивали жидкую серу, кото-
рая при температурах ниже точки ее затвердевания (119 °C)
превращалась в шарики диаметром 1,5—6 мм.
Константу скорости процесса рассчитывали по уравнению
т = psD/kCSCl3
т — время, необходимое для полного протекания взаимодейст-
вия, с; ps — плотность серы, равная 64 кмоль/м3; D — диаметр
236
шарика серы, м; k— константа скорости, отнесенная к единице
фаз, м/с; Csos—концентрация SO3 (св.), кмоль/м3.
Зависимость константы скорости от температуры показана
ниже:
t, °C ................70 80 90 100
lg k.................. 4.85 4.50 4.25 3.90
Значение энергии активации, равной 19,5 ккал/моль
(81,6 кДж/моль), свидетельствует о протекании процесса в ки-
нетической области.
Опытами было установлено протекание процесса через про-
межуточное соединение — S2O3— дитриоксид: S+SO3 = S2O3, ко-
торый, гидролизуясь, выделяет серу по реакции
2S2O3 + 2Н2О + 2SO3 = S + 3SO2 + 2H2SO4
Наличие серы визуально наблюдается по появлению характер-
ной синей окраски растворов серы в олеуме [139]. Соединение
S2O3 образует устойчивые растворы в олеуме при содержании
SO3 (св.) выше 10%, при более низкой концентрации S2O3 не
образуется, по-видимому, в этих условиях происходит его пол-
ный гидролиз.
Скорость образования диоксида серы из промежуточного со-
единения возрастает с повышением температуры (концентрация
олеума не оказывает заметного влияния):
Температура, °C ............... 70 80 90 100
Степень разложения S2O3, % 15 28 50 85
Энергия активации процесса разложения S2O3 (образования
SO2) составляет 13,6 ккал/моль (57,2 кДж/моль). Технологиче-
ская схема процесса представлена на рис. 80.
Олеум, концентрацией 25% SO3 (св.) нагревается последо-
вательно в двух теплообменниках типа «труба в трубе» отрабо-
танным олеумом и паром до 120 °C и направляется в реактор,
куда подается также жидкая отфильтрованная сера. В реакторе
поддерживается температура 95—100 °C. Отработанный олеум,
пройдя теплообменник, гидрозатвор и сборник, возвращается на
закрепление. Образовавшийся диоксид серы поступает в наса-
дочный моногидратный абсорбер, орошаемый 98,3 %-ной серной
кислотой. Очищенный газ в виде сухого высококонцентрирован-
ного (до 100% SO2) диоксида серы направляется потребителю.
Ориентировочные технико-экономические сравнения серо-
олеумного способа с аммиачно-циклическим показали сокраще-
ние капитальных вложений на 12,5%, сокращение расхода пара
в 2 раза, трудозатрат на 24%, а также сокращение расхода
воды.
Наиболее целесообразна организация получения диоксида
серы на предприятиях, где имеется производство олеума, по-
скольку может быть использован олеум, циркулирующий в си-
стеме: использование — закрепление.
237
3 T 5 6 / 8 э -J
РИС. 80. Технологическая схема получения 100%-ного диоксида серы:
I, 2 — подогреватели; 3 — сборник отработанного олеума; 4 — гидрозатвор; 5 — реактор;
6 _ насос для жидкой серы; 7—сборник жидкой серы; 8 — сборник кислоты; 9 — моно-
гидратный абсорбер; 10 — насос кислотный; 11 — холодильник; 12 — брызгоуловитель.
Сжижение диоксида серы. Для получения жидкого диоксида
серы газообразный концентрированный SO2 после предвари-
тельной осушки сжимают в компрессоре до давления 0,4 МПа
(около 4 ат) и затем охлаждают до 20 °C в холодильнике-кон-
денсаторе. Сжиженный таким образом диоксид серы поступает
в сборник-хранилище, откуда SO2 разливают в баллоны или
цистерны. Несжиженная в конденсаторе часть диоксида серы
вместе с примесями азота и кислорода возвращается в абсорб-
ционную башню установки для концентрирования или исполь-
зуется для получения серной кислоты, сульфитов и др.
Диоксид серы можно сжижать и без предварительной осуш-
ки его серной кислотой — проводя компримирование газа в не-
сколько ступеней. Сначала из газа конденсируются водяные
пары, которые таким образом выводятся из системы, затем
сжижается диоксид серы. Жидкий SO2 получают и из газов с
концентрацией 6—7% SO2, но при этом требуется давление
свыше 1,96 МПа (20 ат).
Для практических целей в расчетах при производстве жид-
кого SO2 удобно пользоваться номограммой (построенной по
данным Юшманова Е. И.), по которой можно определить ос-
новные технологические параметры процесса сжижения
(рис. 81).
Пример пользования номограммами.
Исходные данные: Р = 0,9 МПа; t= 15°C; Cso =60%.
На виде а точка пересечения для принятых t и Р дает иа ординате спра-
ва концентрацию отходящего газа — 30% SO2 (доля 0,3). На виде б точка
пересечения поднимающейся линии 0,3 с горизонталью 0,6 (шкала справа)
дает на абсциссе долю сжиженного SO2— 0,7. Опускаясь от той же точки
пересечения (вид б) параллельно кривым, подходим к правой ординате, и иг.
238
РИС. 81. Номограммы для расчета процес-
са сжижения диоксида серы:
а — для определения доли SO2 в отходящем газе;
б — для определения доли сжиженного SO2; в —
для определения расхода газа на 1 кг жидкого
SO2 и расхода электроэнергии на I т жидкого
SO2 в зависимости от давления и расхода газа;
г — для определения оптимального (по расходу
электроэнергии) давления.
виде в проводим горизонтальную линию до пересечения с кривой 1, -затем,
опускаясь вертикально к абсциссе, находим на ней расход газа на 1 кг жид-
кого SO2 — 0,6 м3, а при пересечении с лучом 0,9 МПа на ординате справа
находим теоретический расход электроэнергии — 57 кВт-ч иа 1 т сжиженно-
го SO2.
На виде г по исходной доле SO2 в газе (0,6) и исходной температуре
(15 °C) находим оптимальное давление газа (1,0 МПа), при котором будет
минимальный расход электроэнергии.
111.8. ПОЛУЧЕНИЕ ЖИДКОГО ТРИОКСИДА СЕРЫ
И ВЫСОКОКОНЦЕНТРИРОВАННОГО ОЛЕУМА
Высококонцентрированный (100%-ный) триоксид серы
широко применяется в разнообразных технологических процес-
сах, кроме того, из него получают реактивную серную кислоту.
Основные способы получения 100%-ного триоксида серы:
1. Отгонка SO3 из 20%-ного или более концентрированного
олеума в аппаратах, обогреваемых топочными газами. Способ
применяется обычно на заводах органического синтеза.
2. Отгонка SO3 из олеума циркулирующего в абсорбционном
отделении сернокислотного производства с использованием теп-
ла газов, поступающих из контактного отделения, или топочных
газов.
Большой практический интерес представляет окисление
100%-ного SO2 в среде чистого кислорода на ванадиевом ката-
лизаторе, оно связано с использованием дорогостоящих исход-
ных веществ.
На рис. 82 изображена схема установки для получения
100%-ного триоксида серы на сернокислотных производствах.
Горячий газ, содержащий SOj, направляется из контактного отделения
в межтрубное пространство теплообменника-испарителя, по трубам которого
протекает олеум, предварительно нагретый в теплообменнике. Далее охлаж-
денный газ направляется на абсорбцию по обычной схеме контактных си-
стем.
Вытекающий из испарителя горячий олеум с пониженным содержанием
триоксида серы поступает в теплообменник, где отдает тепло олеуму, идуще-
му из абсорбционного отделения, а затем передается в сборник первого
(олеумного) абсорбера, где вновь насыщается триоксидом серы до первона-
чальной концентрации. Газообраз-
ный ЗОз, выделившийся при нагре-
вании олеума, отводится в кон-
денсатор, откуда жидкий SO3 по-
ступает в сборник. Сборник снаб-
жен водяной рубашкой, в кото-
рую из резервуара поступает во-
да, подогретая острым паром до-
30—40 °C. Это исключает возмож-
Зоба Пар
3 абсорбцион-
ное отбе- г-*-п
Л ° ни?
И шелотопроообо
после олеумного:
абсорбера
\3 сборник
олеумного
абсорбера
РИС. 82. Схема установки для
получения 100%-ного триоксида-
серы:
1 — теплообменник-испаритель; 2 — оле-
умный теплообменник: 3 — конденсатор
SO3; 4 — сборник для жидкого SOsj
5 —резервуар для получения теплой
воды.
240
ность замерзания и кристаллизации гриоксида серы. Следует отметить, что-
при нагревании технического кристаллического триоксида серы он не пла-
вится, а непосредственно переходит в газообразное состояние (возгоняется).
Стопроцентный трноксид серы кристаллизуется уже при
температуре 16,8 °C, поэтому его получение и перевозка связа-
ны с большими трудностями, и вместо пего в некоторых случа-
ях применяется высокопроцентный олеум, содержащий 65%
SO3 (св.). В обычных условиях технический триоксид серы по-
сле замерзания самопроизвольно полимеризуется. После этого
перевести его в жидкое состояние нагреванием при атмосфер-
ном давлении не представляется возможным, поскольку SO3
возгоняется часто со взрывом. Это затрудняет применение три-
оксида серы, так как дозировать и перевозить твердый SO3
практически невозможно.
Чтобы сохранить триоксид серы в жидком состоянии при
охлаждении ниже температуры замерзания 16,8 °C и, таким об-
разом, предотвратить полимеризацию SO3 (что важно для его
хранения и перевозки), к нему добавляют стабилизаторы, на-
пример В9О3 или различные борсодержащие соединения —
Na2B4O7, ВС13, BF3, KBF4, NaBF4, В(ОСН3)3, BF3O(CH3)2,
NOBF4. Концентрация стабилизатора составляет от 0,01 до 2%
(в расчете на SO3) в зависимости от его состава и темпера-
туры.
Классический стабилизатор В2О3-|-(CH3)2SO4 содержит от
0,005 до 0,1% В2О3 и от 0,05 до 1% (CH3)2SO4, что соответст-
вует соотношению (CH3)2SO4: В2О3 от 7: 1 до 10: 1 [9, 12, 125].
Имеется несколько иностранных патентов, в которых в ка-
честве стабилизаторов предложены соединения галогенов, со-
единения Sb, Sr, Si, органо-силикаты, NPC13-SO2C1, NPC13CH2—
NPC13C6H5 (0,5—2,5%), диметил-оксалат (0,1—2%), SOC12-
• (CH3)2SO3, Na2SO4, КСгОз и др. [125].
Наиболее широкое распространение в качестве стабилиза-
тора SO3 получил борный ангидрид В20з- Процесс стабилиза-
ции состоит в следующем. К жидкому триоксиду серы, содер-
жащему не менее 99,6% SO3 (остальное влага), в закрытом со-
суде добавляют 0,7—1,0% (в расчете на SO3) сухого борного
ангидрида (влажность борного ангидрида не более 0,3%). По-
сле перемешивания смесь нагревают до 60—70 °C и выдержи-
вают при этой температуре 3 ч.
Жидкий триоксид серы, стабилизированный борным ангид-
ридом, в закрытой таре из углеродистой стали не полимеризу-
ется в течение многомесячного хранения зимой при температу-
ре до —30 °C. Стальная тара не оказывает вредного влияния
на продукт и заметного разрушения тары при перевозках не
наблюдается.
Высококонцентрированный олеум. Олеум с содержанием
65% свободного SO3 применяется в производстве анилиновых
красителей и некоторых других производствах. Температура
16—584
241
РИС. 83. Схема получения 65%-ного олеума:
/ — отгонный аппарат; 2 — конденсатор SO3: 3 — теплообменник олеум — олеум; 4, 5—
напорные баки; 6 — реактор; 7 — сборник 65%-ного олеума; 8 — холодильник; 9 — резер-
вуар; 10 — железнодорожная цистерна.
кристаллизации такого олеума минус 0,35 °C, в связи с этим он
удобен для перевозок. Приготавливают его насыщением 18—
20%-ного или более концентрированного олеума либо моногид-
рата газообразным или жидким SO3, получаемым при терми-
ческом разложении 25—20%-ного олеума за счет тепла топоч-
ных газов или тепла газов контактного узла [3, 9, 12]. Схема
.получения 65%-ного олеума приведена на рис. 83.
Часть олеума поступает в испаритель, который обогревается газами из
контактного узла. Обычно температура газа на входе в испаритель 220—
225 °C, на выходе около 180 °C. Отгонка SO3 из олеума проводится до со-
держания в нем 18—15% SO3 (св.). Газообразный SO3 сжижается в конден-
саторе и через напорный бак поступает в реактор, куда одновременно из на-
порного бака подается технический олеум. В реакторе, снабженном мешал-
кой, образуется 65%-пый олеум, который сливается в сборник и перекачи-
вается в резервуар, откуда загружается в цистерны.
Для снижения температуры в реакторе до 90—100 °C из сборника через
холодильник непрерывно подается ретур 65%-ного олеума. Отработанный
•олеум из испарителя проходит теплообменник олеум — олеум, где отдает свое
тепло олеуму, направляемому в испаритель.
Имеется еще несколько схем получения 65%-ного олеума с
использованием как топочных газов, так и газов контактного
узла; с получением только 65%-ного олеума или с одновремен-
ным получением жидкого SO3; с получением только жидкого
SO3 или с одновременным получением безводной серной кисло-
ты. Имеются также способы получения 65%-ного олеума через
высококонцентрированный SO2, окисляемый кислородом на ва-
надиевом катализаторе.
242
111 .9. ПОЛУЧЕНИЕ УЛУЧШЕННЫХ И СПЕЦИАЛЬНЫХ СОРТОВ
СЕРНОЙ КИСЛОТЫ
Основное количество серной кислоты вырабатывается
в виде технической контактной. В 1980 г. было выпущено
76,7% такой кислоты, а также 9,7% контактной улучшенной
кислоты; 4,1% олеума технического, 2,4% олеума улучшенно-
го, 0,8% аккумуляторной и реактивной кислоты и 6,3% башен-
ной кислоты (от общей выработки).
Для производства улучшенной контактной кислоты и улуч-
шенного олеума аппаратуру и коммуникации сушильно-абсорб-
ционного отделения изготовляют из кислотостойких материалов
(холодильники и кислотопроводы из стали Х18Н12М.2Т и
Х18Н10Т), увеличивают поверхность холодильников кислоты и
повышают качество очистки газа в мокрых электрофильтрах от
мышьяка.
Чистые сорта серной кислоты приготовляют из моногидрата,
или получают в специальных абсорберах из газа после олеум-
ного абсорбера, так как в нем газ очищается от оксидов азота,.-
которые образуются в печах сжигания серы (при грубом распы-
ле серы и высоких температурах в зоне обжига).
Аккумуляторная кислота применяется в качестве электроли-
та в аккумуляторах. Качество ее определяется ГОСТ 667—73.
Большинство заводов выпускает контактную серную кислоту,,
которая после удаления из нее диоксида серы (в отдувочных,
башнях или смесителе—тщательно очищенным воздухом) удо-
влетворяет требованиям на аккумуляторную кислоту. После от-
дувки SO2 для окисления органических примесей (если требует-
ся) добавляют небольшое количество перекиси водорода. На
некоторых заводах работают специальные абсорбционные уста-
новки для получения аккумуляторной кислоты из газа, отбирае-
мого после олеумного абсорбера, и дистиллированной воды, ко-
торую получают в аппарате с паровым обогревом. Воздух очи-
щают в четырех последовательно установленных баках. Первый
по ходу воздуха бак имеет насадку из стеклянной ваты и слу-
жит фильтром, второй — залит водой, третий — кислотой, чет-
вертый— имеет насадку из стеклянных шариков и служит брыз-
гоуловителем. Эти баки, дистиллятор и все коммуникации к ним
выполняются из меди, абсорбер и брызгоуловители в цикле аб-
сорбции защищены футеровкой. Бак-смеситель, где 98%-ная
кислота разбавляется дистиллированной водой до стандартной
концентрации, снабжен свинцовым змеевиком.
Перевозится аккумуляторная кислота в железнодорожных
цистернах или контейнерах со специальным кислотоупорным по-
крытием или футеровкой.
Реактивная серная кислота выпускается по ГОСТ 4204—77
трех сортов: химически чистая (х. ч.), чистая для анализа
(ч. д. а.) и чистая (ч). Получают ее из 100%-ного триоксида се-
ры и дистиллированной воды. Возможно также применение га-
16-
24$
зов контактного отделения. До последнего времени установки по
получению реактивной кислоты оснащались барботажными
эмалированными аппаратами мощностью 4 тыс. т/год (по япон-
ской технологии). Новые отечественные установки на 7,5 тыс.
т/год оснащаются пенными абсорберами с провальными тарел-
ками и подвижными теплосъемными элементами. Тарелки аб-
сорберов, выносные и встроенные холодильники изготовляются
из фторопласта.
Небольшое количество серной кислоты согласно ГОСТ
14262—78 выпускается в виде продукта особой чистоты.
11 1.10. ВТОРИЧНЫЕ ЭНЕРГОРЕСУРСЫ
К вторичным энергоресурсам (ВЭР) производств кон-
тактной серной кислоты относятся: физическое тепло обжиговых
газов и огарка, тепло, выделяющееся при окислении диоксида
серы и абсорбции триоксида серы. Физическое тепло огарка не
используется из-за низкой температуры основной части выводи-
мого огарка.
При использовании тепла газов (850—1050 °C) от обжига
флотационного колчедана (12,5—14,5% SO2) в котлах-утилиза-
торах типов ГТКУ-Ю/40, ГТКУ-25/40, КС-200 ВТКУ, КС-450
ВТКУ, КУКС-200, OS-26 (ПНР) на 1 т моногидрата получают
0,6—0,7 Гкал (2,5—2,9 ГДж) пара давлением 4 МПа, перегре-
того (440 °C) или насыщенного (250°C). При использовании
тепла газов (1000—1100°С) от сжигания серы (12—16% SOz)
в котлах-утилизаторах типов СЭТА-Ц-100, СКУ-14/40, ОИ-70
(ПНР) на 1 т моногидрата получают 0,5—0,8 Гкал (2,1 —
3,4 ГДж) пара давлением 4 МПа (перегретого — 400 °C и насы-
щенного— 250 °C) и давлением 2,5 МПа (насыщенного —
220 °C). И в том, и в другом случае температура газа на выходе
из котла находится на уровне 450 °C.
Тепло, выделяющееся при окислении диоксида серы в систе-
мах на сере, используют на получение пара (часть его теряет-
ся на стадии абсорбции). При работе на колчедане использова-
ние тепла окисления предусмотрено для подогрева питательной
воды только на системах одинарного контактирования мощно-
стью 360 тыс. т/год (поставки ПНР по лицензии Дорр — Оли-
вер).
ВЭР в виде перегретого пара используют для получения
электроэнергии только в тех случаях, когда его количество су-
щественно превышает потребность предприятия для технологи-
ческих и санитарно-технических нужд. Насыщенный пар после
РОУ под давлением 1—1,3 МПа при температуре 180—185 °C
используется технологическими цехами минеральных удобре-
ний. Насыщенный пар под давлением 0,6 МПа при 160 °C идет
для подогрева серопроводов при фильтрации серы, в серных и
мазутных форсунках используется при пуске систем, в колон-
нах разложения на установках улавливания отходящих газов
и на различные теплофикационные нужды заводов.
244
Количество пара, поступающего в общезаводские сети, и
его распределение по цехам и на отдельные операции на боль-
шинстве заводов не измеряются. О достаточности производимо-
го в данный момент пара судят по поддержанию постоянного
давления в общезаводской паровой сети. Давление пара в си-
стеме регулируют включением п изменением мощности котлов
ТЭЦ или котельной завода, работающих на природном топли-
ве, а также сбросом пара сернокислотных цехов в атмосферу,
например в летний период, когда не используется пар на отоп-
ление.
За рубежом также уделяют большое внимание глубокому использова-
нию ВЭР. Так, по данным фирмы Лурги тепло кислот сушильно-абсорбцион-
ного отделения (температура 110 °C) утилизируются с получением подогре-
той до 80—90 °C воды, которую применяют для обогрева помещений, для
промывки фильтров целлюлозных фабрик, в производстве фосфорной кисло-
ты, для дистилляции морской воды. Отвод тепла осуществляется в тефлоно-
вых пластинчатых холодильниках с анодной защитой и в кожухотрубчатых —
со стеклянными трубками. Еще более гибким решением для использования
вторичного тепла кислот при 140 °C является непосредственное получение
пара низкого давления — около 0,15 МПа. В дальнейшем предусматривается
увеличение давления пара при помощи компрессора (примерно до 0,5 МПа)
для расширения области его применения. Тепло выхлопных газов сернокис-
лотных установок и частично кислот сушильно-абсорбционного отделения ис-
пользуют для концентрирования промывных кислот (от 20 до 70% H2SO4),
которые затем направляют в производство суперфосфата. Разрабатываются
способы утилизации тепла кислот в промывном отделении.
ГЛАВА IV
ОСНОВНЫЕ НАПРАВЛЕНИЯ ТЕХНИЧЕСКОГО ПРОГРЕССА
В ПРОИЗВОДСТВЕ КОНТАКТНОЙ СЕРНОЙ КИСЛОТЫ
[142—160]
I V.1. ТЕНДЕНЦИИ РАЗВИТИЯ
За последнее десятилетие почти во всех странах мира
(особенно в ряде развивающихся стран) производст-
во серной кислоты значительно увеличилось, что обусловлено
развитием отраслей промышленности, потребляющих серную
кислоту (производство минеральных удобрений, химическая,
нефтеперерабатывающая промышленности, черная и цветная
металлургия и др.). Мировое производство серной кислоты в
1982 г. составило 140 млн. т против 89 млн. т в 1970 г. Увели-
чение выпуска серной кислоты сопровождалось техническим
прогрессом производства.
Основными направлениями технического прогресса в серно-
кислотном производстве являются:
рост единичных мощностей технологических линий (систем);
разработка принципиально новых эффективных технологиче-
ских систем и их аппаратурного оформления, снижение метал-
245
«я*
лоемкости и энергетических затрат на производство, т. е. созда-
ние материале- и энергосберегающих систем;
уменьшение выбросов вредных веществ в атмосферу с вы-
хлопными газами — создание практически безотходных серно-
кислотных систем.
Увеличение мощности единичных технологических линий по-
зволяет уменьшить удельные капитальные вложения и эксплуа-
тационные затраты, повысить производительность труда. По
этим показателям эффективно также строительство нескольких
технологических линий на одном предприятии (концентрация
производств). В соответствии с этим во всех странах за послед-
ние 15 лет возросла единичная мощность сернокислотных си-
стем, повысилась концентрация сернокислотных систем на од-
ном предприятии.
Так в СССР за этот период мощность сернокислотных систем на колче-
дане (здесь и далее — в расчете на 100%-ную H2SO4—моногидрат) возросла
с 120 до 360 тыс. т/год, а на сере со 100 до 500 тыс. т/год. За рубежом наи-
более крупные сернокислотные системы на колчедане эксплуатируются в Япо-
нии — 420—430 тыс. т/год, на сере — в США и ряде развивающихся стран
Африки — 600—700 тыс. т/год.
В СССР имеются предприятия, на которых работают несколько серно-
кислотных систем общей мощностью свыше 1,5 млн. т/год, в США — свыше
2 млн. т/год.
Указанный рост единичных мощностей технологических ли-
ний достигнут в основном путем увеличения геометрических
размеров аппаратов при сохранении примерно тех же скоростей
газовых потоков и тех же значений гидравлического сопротивле-
ния всей системы в целом. Это привело к необходимости созда-
вать аппараты очень больших размеров и при достижении не’
которого предела — к усложнению внутренних конструкций ап-
паратов. Вся аппаратура становится чрезвычайно громоздкой и
сложной в эксплуатации (увеличиваются простои системы и рас-
ходы на ремонт), возрастают удельные металле- и материало-
емкость систем. Так, диаметр контактного аппарата сернокис-
лотной системы на колчедане мощностью 360 тыс. т/год равен
14 м, высота — 28 м.
Выполненные расчеты показали, что дальнейшее увеличение
мощности систем таким путем технически и экономически неце-
лесообразно. Нужны новые технические решения увеличения
мощности систем. Несмотря на то, что переход современных
мощных систем с одинарного на двойное контактирование по-
зволило в 4—6 раз снизить содержание диоксида серы в выхлоп-
ных газах (степень контактирования возросла с 98 до 99,5—
99,8%), увеличение мощности систем и концентрация сернокис-
лотных систем на одном предприятии привели к значительным
суммарным выбросам диоксида серы. Так, сернокислотная си-
стема мощностью 500 тыс. т/год даже при степени контактиро-
вания 99,5—99,8% выбрасывает с выхлопными газами порядка
от 1600 до 700 т диоксида серы в год. При работе двух и более
таких систем на одном предприятии выбросы диоксида серы
246
увеличиваются настолько, что даже на системах ДК становится
сложным соблюдение установленных санитарных норм (ПДК)
по диоксиду серы (особенно с учетом общего фона вредных вы-
бросов на предприятии).
Строительство установок химической очистки отходящих га-
зов требует дополнительных капитальных вложений, а также
значительных эксплуатационных и особенно трудовых затрат.
Кроме того, оно не всегда возможно из-за отсутствия необхо-
димого спроса на образующиеся побочные продукты.
Вопросы охраны природы от загрязнений промышленными
выбросами приобрели в последние годы особую актуальность
в связи с их пагубным воздействием на животный и раститель-
ный мир, на здания и сооружения. Особенно большой вред на-
носит диоксид серы, выбросы которого во всем мире исчисля-
ются десятками миллионов тонн, в том числе и от контактных
сернокислотных систем. Требования охраны окружающей сре-
ды являются решающим фактором в определении перспектив-
ности развития каждого направления в промышленности. Наря-
ду с этим, выбросы ди- и триоксида серы, брызг и тумана сер-
ной кислоты с отходящими газами являются невосполнимыми
потерями производства, уменьшающими степень использования
сырья.
Поэтому совершенствование сернокислотного производства
в направлении дальнейшего повышения степени контактирова-
ния (т. е. степени использования серы) снижения выбросов ди-
оксида серы приобретает важное народнохозяйственное и при-
родоохранное значение.
Для дальнейшего совершенствования сернокислотного про-
изводства в настоящее время большое значение приобретает
снижение удельной металлоемкости сернокислотных систем,
снижение расхода энергии, использование вторичных энергоре-
сурсов.
Снижение удельной металлоемкости может быть достигнуто
увеличением в аппаратах сернокислотной системы массовой
скорости газовых потоков и концентрации диоксида серы в пе-
рерабатываемом газе, применением новых интенсивных процес-
сов и аппаратов, оптимальной компоновкой аппаратов системы,
рациональной схемой и аппаратурным оформлением теплооб-
мена в контактном аппарате (за счет уменьшения поверхности
теплообменников). Улучшение энергетических показателей си-
стем возможно путем повышения концентрации диоксида серы
в перерабатываемом газе, применения эффективных новых тех-
нологических схем и аппаратов, за счет более полного использо-
вания реакционного тепла (вторичных энергоресурсов).
В настоящее время в Советском Союзе эксплуатируются сер-
нокислотные системы двойного контактирования ДК на колче-
дане производительностью 360 тыс. т/год и на сере производи-
тельностью 500 тыс. т/год, определяющие технический уровень
сернокислотного производства страны.
247
Системы ДК не только обеспечивают снижение содержания
SO2 в выхлопных газах за счет достижения более высоких зна-
чений окисления диоксида серы в контактных узлах (до 99,5—
99,8%), но и позволяет перерабатывать более концентрирован-
ный по SO2 газ (до 10%). В результате производительность си-
стемы повышается на 20—25%.
Отечественные сернокислотные системы ДК производитель-
ностью 360 тыс. т/год (см. рис. 45) по техническому уровню со-
ответствуют лучшим зарубежным системам на колчедане. В них
комплексно использован весь отечественный опыт совершенст-
вования и интенсификации сернокислотного производства. Печ-
ные отделения оснащены мощными печами для обжига колче-
дана в кипящем слое — КС-450, производительностью 450—
500 т/сут колчедана с утилизацией тепла его горения — получе-
нием пара энергетических параметров (450 °C; 4,0 МПа), ис-
пользуемого для производства электроэнергии и для технологи-
ческих нужд теплофикации. Очистка обжигового газа от пыли
производится в 3-х польных электрофильтрах УГТ-3-30. Про-
мывные отделения работают в испарительном режиме. Кислоты
в циклах орошения сушильных башен и абсорберов охлажда-
ются в аппаратах воздушного охлаждения. Используются по-
гружные насосы. Степень окисления SO2 в контактных аппара-
тах составляет 99,6—99,8%.
Все технологические аппараты расположены на нулевой от-
метке, а не на постаментах, как на старых системах, что умень-
шает объем строительных работ, снижает расход энергии на по-
дачу кислоты на орошение башен. Системы имеют автоматизи-
рованное управление технологическим процессом — АСУ ТП.
Технологические показатели работы этих систем (в расчете на
1 т моногидрата) приведены ниже:
Расход колчедана (45%-иом по сере), кг . . . 795—800
Расход электроэнергии, кВт-ч................ 174
Выход пара (450 °C; 4,0 МПа)............... 0,74
Сернокислотные системы (см. рис. 44), работающие на сере
(проект и поставка ПНР), также соответствуют современному
техническому уровню. В них используют камерные форсуноч-
ные печи, производительностью 500—550 т серы в сутки. Тепло
горения серы и окисления SO2 утилизируется в системе водо-
трубного котла-утилизатора (с воздушными теплообменниками,
экономайзерами, пароперегревателями). Охлаждение кислот
производится в спиральных или пластинчатых теплообменниках.
Система имеет компактную планировку.
Технологические показатели работы систем (в расчете на
1 т моногидрата) приведены ниже:
Степень окисления SO2, %............................До 99,8
Расход серы, кг.................................... 339
Расход электроэнергии, кВт-ч........................ 94
Выход пара (450 °C, 4,0 МПа)....................... 0,8
248
Однако, рассмотренные системы имеют ряд существенных
недостатков. Эти системы определяют современное техническое
состояние сернокислотного производства, но не могут рассмат-
риваться как перспективные для дальнейшего развития серно-
кислотного производства.
Недостатками их являются: высокая удельная металлоем-
кость, которая для систем на колчедане составляет 19,6 кг на
1 т годовой мощности, а для систем на сере — 9,0 кг; высокие
удельные энергозатраты; недостаточное использование тепла
реакции; большие материальные и трудовые затраты на экс-
плуатацию производств серной кислоты.
Работы по дальнейшему техническому развитию сернокис-
лотного производства ведутся в следующих направлениях:
разработка метода получения серной кислоты из концент-
рированного газа (до 50—70% SO2) с использованием техни-
ческого кислорода (трехступенчатой конверсией); разработка
мощных систем на сере, работающих под давлением, и цикли-
ческих систем, работающих под давлением и с применением
технического кислорода.
Повышение концентрации диоксида серы является одним из
важнейших факторов интенсификации сернокислотного произ-
водства, поскольку пропорционально повышению концентрации
SO2 увеличивается производительность сернокислотной систе-
мы при одновременном снижении потерь тепла реакции. Но при
этом для достижения удовлетворительных выбросов диоксида
серы с выхлопными газами необходимо иметь трех- и четырех-
ступенчатое контактирование и абсорбцию.
Из-за высокого удельного тепловыделения при окислении
концентрированного газа и невозможности отвода тепла из зо-
ны реакции использование контактных аппаратов только с филь-
трующими слоями катализатора затруднено и малоэффективно.
Поэтому при разработке процесса производства серной кислоты
из концентрированных газов (до 50—70% SO2) для первой сту-
пени конверсии SO2 применен контактный аппарат с одним ки-
пящим слоем износоустойчивого катализатора. Изотермичность
кипящего слоя и высокие коэффициенты теплоотдачи обеспечи-
вают возможность окисления концентрированного диоксида се-
ры на 60—75% без перегрева катализатора и эффективное ис-
пользование тепла реакции. После первой абсорбции триоксида
серы газовая смесь разбавляется воздухом до концентрации
15—18% SO2 и подается на последующее окисление по схеме
ДК в контактный аппарат со стационарными слоями катализа-
тора.
Обобщенные технологические показатели работы контактно-
го узла для переработки концентрированного газа, полученные
на опытной установке, приведены в табл. 48.
Расчеты показали, что интенсивность работы аппаратов в та-
кой системе повышается не менее, чем в 2,5—3 раза. Система,
как видно из таблицы, может обеспечить высокие показатели
249
Таблица 48. Показатели работы опытной установки
Показатели Стадии конверсии На выходе из установки
I 1 п 1 Ш
Количество газа на вхо- де, м3/г кислоты Состав газа, % (об.) 360 360* 280 275
SO2 63 15,7 1,2 0,04
о2 31,6 22,5 18,8 18,4
Время контакта, с 2,2 4,5 0,5 —
Степень окисления, % 75 * Добавлено 255 м3 воздуха. 94 97 99,95
процесса как по степени окисления SO2, так и по остаточному
содержанию его в выхлопном газе. Сложность строительства и
эксплуатации такой системы заключается в необходимости
иметь кислородную установку, требующую дополнительных ка-
питальных вложений и эксплуатационных затрат.
Для переработки запыленных газов, полученных от обжига
колчедана, и отходящих газов цветной металлургии, представ-
ляет интерес так называемая короткая схема на колчедане —
схема СО. Как известно, промывное отделение сернокислотного
производства на колчедане является капиталоемким. При его’
эксплуатации возникают серьезные трудности, поскольку требу-
ется очистить отжиговый газ от всех примесей (огарковая пыль,
мышьяк, фтор, туман серной кислоты), и аппараты отделения
работают в условиях требующих специальной коррозионной за-
щиты. В схеме СО заложены максимальные резервы упрощения
аппаратурно-технологического оформления отделения очистки
обжиговых газов. В ней отсутствуют промывные и сушильные
башни и мокрые электрофильтры (рис. 84).
Проведенные исследования и опытные работы показали, что
влияние содержащихся в обжиговом газе вредных примесей
(As, HF, огарковая пыль, Н2О) на катализатор и, следователь-
но, на весь процесс, может быть устранено.
Показана возможность достаточно полной фиксации мышь-
яка огарком при окислительном обжиге с получением обжиго-
вого газа концентрацией не выше 12% SO2 (содержание As в
обжиговом газе около 2 мг/м3) и достаточно тонкой очистки
обжигового газа от огарковой пыли в сухих электрофильтрах
(до 50 мг/м3). Присутствие в обжиговом газе паров воды не
оказывает вредного влияния на процесс каталитического окис-
ления диоксида серы на катализаторе и препятствует взаимо-
действию фтористого водорода, содержащегося в обжиговом
газе, с носителем катализатора.
В схеме СО устраняются основные несоответствия энергети-
ческого и технологического аспектов работы контактных систем
на колчедане, связанные с необходимостью охлаждения, увлаж-
250
5
РИС. 84. Короткая схема ДК для переработки газа от сжигания колчедана
(СО):
/ — печь КС; 2 — котел-утилизатор; 3 — циклон; 4 — сухой электрофильтр; 5 — контакт-
ный аппарат КС I ступени; 6— теплообменник I ступени; 7 — абсорбер-конденсатор;
5 —сборник 93%-ной кислоты; 9, 16 — волокнистые фильтры; 10— мокрый электрофильтр;
// — турбогазодувка; 12 — брызгоуловитель; 13 —- теплообменник П ступени; /‘/—кон-
тактный аппарат II ступени; 15— абсорбер; 17 — сборник 98%-ной кислоты; 18 — пуско-
вой подогреватель.
нения и последующих осушки и нагрева газовой смеси. В систе-
ме СО обжиговые газы после сухих электрофильтров направля-
ются в контактный аппарат с кипящим слоем специального ка-
тализатора КС (1-ая стадия контактирования). Остаточная огар-
ковая пыль в обжиговом газе проходит через слой катализато-
ра КС и улавливается в насадочном конденсаторе, орошаемом
крепкой кислотой, после чего газ через теплообменники посту-
пает в контактный аппарат со стационарными слоями катали-
затора (2-я стадия контактирования) и затем в абсорбционную
башню.
Проведенные испытания опытно-промышленной системы СО
производительностью 150 т/сут на Гомельском химзаводе подт-
вердили ее эффективность при условии применения на первой
стадии окисления SO2 контактных аппаратов с кипящим слоем
катализатора КС. Ниже приводится характеристика обжигово-
го газа перед входом в контактный аппарат «КС» на опытно-
промышленной установке:
Температура, °C............................300
Концентрация SO2, %........................9—11
Содержание огарковой пыли, мг/м3...........^50
Содержание соединений мышьяка, мг/м3 . . . <2
Количество газа, тыс. м3/ч.................14—18
В аппарат КС загружался специально приготовленный ката-
лизатор КС фракционного состава 0,4—1,2 мм. Общая степень
окисления SO2 составляла 99,5—99,7%- Такие системы перспек-
тивны для переработки газов, полученных при обжиге колчеда-
на, и отходящих газов предприятий цветной металлургии.
251
IV.2. РАЗРАБОТКА СИСТЕМ С ПРИМЕНЕНИЕМ ДАВЛЕНИЯ
И КИСЛОРОДА
Применение повышенного давления на всех стадиях
производства серной кислоты является наиболее перспективным
направлением развития сернокислотной промышленности, так
как при этом обеспечиваются следующие положительные фак-
торы улучшения технологических показателей сернокислотных
систем:
в соответствии с принципом Ле-Шателье увеличивается вы-
ход SO3 при взаимодействии SO2 и О2 на катализаторе (реак-
ция в газовой фазе идет с уменьшением объема). Возрастает
степень использования сырья, уменьшаются выбросы вредных
веществ (SO2) в атмосферу. Может быть достигнута степень
конверсии диоксида серы 99,95—99,99%. Становится возмож-
ным создание практически безотходного производства серной
кислоты;
объемы перерабатываемого газа уменьшаются пропорцио-
нально давлению, что позволяет создавать мощные системы с
малыми размерами аппаратов. Диаметры аппаратов системы
мощностью 700—750 тыс. т/год при давлении 1,0—1,2 МПа не
превышает 3,5—3,6 м (в обычной системе мощностью 450—
500 тыс. т/год диаметр контактного аппарата равен 13 м, а аб-
сорберов 8,5 м);
удельная металлоемкость системы снижается в 2,5—3,0 раза.
Сокращается производственная площадь, занятая сернокислот-
ной системой;
все оборудование сернокислотной системы мощностью 700—
750 тыс. т/год под давлением 1,0—1,2 МПа может быть полно-
стью изготовлено, собрано и испытано на машиностроительных
заводах и поставлено в собранном виде на строительную пло-
щадку для монтажа, что ускоряет и удешевляет монтаж систе-
мы. Габаритные размеры обычных сернокислотных систем зна-
чительно превышают допустимые нормы транспортировки к ме-
сту монтажа. Такое оборудование перевозят в виде деталей-за-
готовок и собирают и сваривают на месте, при этом обеспечивать
хорошее качество сборки, сварки и футеровки на стройпло-
щадке труднее, чем при полном изготовлении всего аппарата на
машиностроительном заводе. На сборку аппаратов из деталей-
заготовок расходуется много дополнительного времени, что зна-
чительно удлиняет сроки монтажа системы. Капитальные ремон-
ты крупногабаритных аппаратов требует более длительного
времени, чем требуется при ремонте или полной замены мало-
габаритного аппарата;
аппараты сернокислотного производства, работающие под
повышенным давлением, подлежат котлонадзору. К ним предъ-
являются требования повышенной прочности и герметичности.
Их изготовление и испытания на заводе-изготовителе обеспечи-
вает повышенную надежность работы отдельных аппаратов и
252
РИС. 85. Технологическая схема получения серной кислоты из серы с при-
менением повышенного давления, разработанная фирмой «Южин — Кюльман»-
(Франция):
/ — воздушный фильтр; 2 — сушильная башня; 3 — компрессор; 4 — печь для сжигания
серы; 5 — котел-утилизатор: 6 — газовый фильтр; 7 — контактный аппарат I ступени кон-
тактирования; 8 — теплообменники; 9 — промежуточный абсорбер; 10 — контактный ап-
парат II ступени; 11— экономайзеры; 12 — конечный абсорбер; 13—паровая турбина;
14 — газовая турбина.
всей сернокислотной системы. Улучшаются культура производ-
ства и условия работы обслуживающего персонала;
резко снижается расход катализатора — в 6—7 раз по срав-
нению с обычной системой;
увеличивается скорость горения серы, окисления диоксида
серы, абсорбции триоксида серы, что позволяет применять для1
этих процессов новые интенсивные аппараты.
Важным преимуществом сернокислотных систем, работаю-
щих под повышенным давлением, является возможность полу-
чать непосредственно в производстве серной кислоты триоксид,
серы и высококонцентрированный олеум с содержанием до 65%
свободного SO3, получение которых в настоящее время возмож-
но лишь на специальных производствах олеума.
В семидесятые годы опытно-промышленные и промышлен-
ные испытания различных вариантов сернокислотного производ-
ства под давлением проводились во Франции, Канаде, Японии,
США и других зарубежных странах. В последнее время в ряде
стран строятся промышленные сернокислотные системы под
давлением [158].
В 1972 г. французские фирмы Кребс и Южин — Кюльман на
заводе в г. Пьер-Бенит (вблизи Лиона) пустили в эксплуатацию
разработанную ими первую промышленную систему на сере
под давлением 0,55 МПа мощностью 575 т/сут (200 тыс.
т/год)—процесс РСИК. Технологическая схема системы
Южин — Кюльман приведена на рис. 85.
25$
Воздух сжимается компрессором до 5,5 (0,55 МПа), проходит сушиль-
ную башню и поступает в печь, куда также подается расплавленная сера.
В процессе сжигания серы образуется газ концентрацией 12% SO2. Из печи
газ направляется в котел-утилизатор, проходит газовый фильтр и затем
при температуре 430 °C направляется в контактный аппарат. На первой ста-
дии конверсии в процессе ДК работают три слоя катализатора, на второй
стадии — один. Необходимые температурные режимы в слоях поддерживают-
ся при помощи соответствующих теплообменников. Общая степень конверсии
на двух стадиях составляет 99,85—99,9%.
Выходящий из конечного абсорбера газ при 80 °C проходит через два
теплообменника, нагреваясь до 500 °C, а затем поступает на турбину для
сброса давления с получением энергии и в экономайзер для рекуперации
тепла. Выхлопной газ при 150 °C через трубу выбрасывается в атмосферу.
Турбина находится на одном валу с компрессором и покрывает две трети
энергии, требуемой для работы компрессора, а одну треть — паровая тур-
бина.
Загрузка ванадиевого катализатора в контактный аппарат — 42 тыс. л
(70 л па 1 т суточной производительности, против 200 л в обычной системе),
съем пара (440 °C, 4,0 МПа)—0,975 т на 1 т выпускаемой кислоты, расход
электроэнергии 55 кВт-ч/т.
По данным фирмы, удельная металлоемкость системы уменьшена в
2,5 раза, занимаемая производственная площадь по сравнению с обычной си-
стемой— в 3,5 раза. Удельные капитальные вложения снижены на 25%.
Оригинальное решение сернокислотной установки, работаю-
щей с применением повышенного давления, предложено фир-
мой «Кеметик интернациональ» (Канада). Согласно канадской
схеме, число аппаратов, обеспечивающих функционирование
сернокислотной установки, меньше и последовательность неко-
торых стадий процесса, а также расположение оборудования не-
сколько иные, чем в обычном контактном способе получения
серной кислоты.
На рис. 86 приведена схема опытно-промышленной установки произво-
дительностью 250 т/сут (на сере), испытанной в Канаде. Воздух, поступаю-
щий в систему для сжигания серы и окисления SO2 в SO3, проходит через
фильтр и при помощи компрессора сжимается до давления 0,78 МПа. Сжа-
тый воздух проходит две ступени осушки: грубую — в конденсаторе-охлади-
теле (конденсат периодически выводится из этого аппарата) и тонкую — в
сушильно-отдувочном агрегате. На его орошение из абсорбционного отделе-
ния поступает концентрированная серная кислота со значительным содержа-
нием растворенного SO2. В качестве такого агрегата в системе применена
обычная башня с насадкой, хотя и отмечается, что вместо нее могут быть
использованы и аппараты других типов, включая скрубберы Вентури. Су-
шильно-отдувочный агрегат работает при температуре 40—70 °C под давле-
нием 0,78 МПа, причем часть кислоты, минуя холодильник, поступает на
орошение через боковой ввод аппарата, а другая часть после охлаждения в
холодильнике подается на орошение сверху.
После тонкой осушки газовоздушная смесь поступает в брызгоуловитель,
из него — на вторую ступень компрессора, где сжимается до давления
2,8 МПа, а затем направляется в печь, куда через форсуночное устройство
впрыскивается жидкая сера. На выходе из печного агрегата концентрация
SO2 в газе поддерживается равной 9% (об.), а температура — 400—430 °C.
Для отделения возможных механических примесей газ пропускается че-
рез газовый фильтр и поступает в 3-х слойный контактный аппарат, где про-
исходит конверсия SO2 в SO3 (степень конверсии 99,7%). Затем газ охлаж-
дается до 200 6С в экономайзере и поступает в холодильник-конденсатор, где
конденсируется 80% содержащегося в нем SO3 и более 28% оставшегося не-
окисленным SO2. В абсорбере, орошаемом 97—98%-ной серной кислотой, из
газа практически полностью удаляются SO2 и SO3.
254
3 атмосферу
Серная кислота
РИС. 86. Принципиальная схема сернокислотной установки производитель-
ностью 250 т/сут фирмы CIL (Канада):
/ — печь для сжигания серы; 2 — котел-утилнзатор; 3 — воздушный фильтр; 4 — сушиль-
ная башня; 5 — сборник кислоты; 6 — компрессор; 7 — промежуточный холодильник в,
воздушном компрессоре; 8 — реактор с первым слоем катализатора; 9 — встроенные теп-
лообменники контактного узла; 10 — реактор со вторым н третьим слоями катализатора;
И — экономайзер; 12 — абсорбер; 13 — брызгоуловнтель; 14 — выносной теплообменник;
15— расширительная турбина для хвостовых газов.
Сконденсированный SO3 добавляют полностью или частично к кислоте,
циркулирующей в системе орошения абсорбера. Отбор готовой продукцию
осуществляется после прохождения ею специального устройства для сниже-
ния давления. Предусмотрена возможность вывода из системы жидкого SO3
(после холодильника-конденсатора). Для получения олеума изменяется режим
работы холодильника-конденсатора (на орошение впрыскивается холодная
серная кислота).
После абсорбера выхлопной газ нагревается в теплообменниках контакт-
ного аппарата, вступает в теплообмен с газами установки для сжигания серы,
а затем расширяется в рекуперационной газовой турбине и сбрасывается в-
атмосферу. Газовая турбина покрывает 85% мощности, требуемой для рабо-
ты двух компрессоров, а остальные 15% требуемой мощности — за счет паро-
вой турбины.
Содержание растворенного в орошающей кислоте SO2 повышается с
0,0008% (на входе в абсорбер) до 0,008% (на выходе из него). Абсорбер
снабжен высокоэффективным осадителем тумана. Потери SO, составляют
55,8 кг/сут, или 0,2 кг на 1 т производимой кислоты, что соответствует общей
степени конверсии SO2 — 99,9%-
Особенностью процесса производства серной кислоты под повышенным
давлением, разработанного фирмой CIL, является ступенчатое изменение дав-
ления в сушильном (0,8 МПа) и абсорбционном (2,8 МПа) отделениях про-
изводства серной кислоты. Разность давлений в аппаратах используется для-
отдувки растворенного SO2 воздухом и в сушильном отделении. Процесс кон-
версии газа является одностадийным, однако применение повышенного дав-
ления существенно увеличивает эффективность использования серы в произ-
водстве серной кислоты. Объединение циклов орошения сушильной башни и
абсорбера и разница в давлениях в сушильной башне и абсорбере позволяет
иметь всего один циркуляционный насос для их орошения.
Выход пара энергетических параметров в данной системе достигает 1,4 т
на 1 т продукционной кислоты. Фирма считает, что капитальные вложения-
на создание данной системы на 20—25% меньше соответствующих вложений
на эквивалентную систему обычного типа ДК, а удельная металлоемкость-
снижается в 3,5—4 раза.
255.
Таблица 49. Сравнительные показатели по выбросам SO2
Процесс Концентрация SO3 в выхлопных га- зах, % Выбросы SO2 на 1 т продукцион- ной кислоты, кг
Одинарное контактирование 0,15—0,25 13—15
Двойное контактирование с проме- жуточной абсорбцией 0,03—0,05 2—3
Процесс под давлением Южин — Кюльман 0,015 0,6—1,2
Канадский процесс под давлением 0,003 0,2
Все рассмотренные системы под давлением имеют значитель-
но меньше выбросов SO2 с выхлопными газами и приближают-
ся к практически безотходным или являются таковыми, что вид-
но из табл. 49.
В НИУИФ совместно с организациями-соисполнителями —
ЛТИ им. Ленсовета, МИХМ, М.ХТИ им. Д. И. Менделеева,
ХПИ, ППИ и др. — на основе проведенных исследований всех
процессов технологии серной кислоты и опытных работ разра-
ботаны эффективные сернокислотные системы на сере под по-
вышенным давлением — прямоточная и циклическая с примене-
нием кислорода.
Прямоточная система, разработанная НИУИФ — МИХМ
(рис. 87) использует турбокомпрессорный агрегат ГТТ-12 азот-
нокислотной системы АК-72.
Воздух в турбокомпрессорном агрегате сжимается в 2-х ступенях до
1,2 МПа и направляется в печь для сжигания серы, куда через форсунки по-
дается также расплавленная сера. Образовавшийся в результате горения об-
жиговый газ с содержанием 11—12% SO2 проходит котел-утилизатор, где
охлаждается до температуры 420—430 °C и направляется в контактный узел.
Газ проходит последовательно 3 контактных аппарата (каждый с одним сло-
ем катализатора) с установленными после них теплообменниками и направ-
ляется в промежуточный абсорбер, где образовавшийся триоксид серы погло-
щается с образованием серной кислоты. Затем газ нагревается в теплообмен-
никах и поступает в контактный аппарат второй стадии контактирования.
Конечная степень конверсии 99,92—99,95%. Во втором абсорбере происходит
поглощение SO3, образовавшегося на второй стадии конверсии, после чего газ
выбрасывается в атмосферу.
Затем газ нагревается в теплообменниках контактного узла до 500—
-550 °C и поступает в топку, где сжигается природный газ в таком количестве,
чтобы поднять температуру газа до 700°C, н направляется в турбину турбо-
компрессорного агрегата ГТТ-12, где отдает свою энергию для работы ком-
прессора.
В этих условиях работа турбины полностью покрывает потребность в
энергии компрессорной группы агрегата ГТТ-12. Получается замкнутая энер-
готехнологическая система. Газ после турбины проходит теплообменник или
экономайзер и выбрасывается через выхлопную трубу.
При повышении давления растет растворимость диоксида се-
ры в кислоте. Поэтому при абсорбции триоксида серы под дав-
лением 1,1 МПа в абсорбере происходит также растворение в
кислоте непроконвертированного диоксида серы. При выводе
продукционной кислоты из сушильной башни из нее воздухом
256
17—584
РИС. 87. Схема производства серной кислоты под давлением (прямоточная):
/ турбокомпрессорный агрегат ГТТ-12; 2 контактные аппараты; 3 — серная печь; 4—котел-утилизатор; 5 - сушильная колонна; 6 — аб"
сорберы; 7 — сборники серной кислоты; 8 — пусковой подогреватель; 9 — теплообменники; 10 — экономайзеры.
Таблица 50. Основные технико-экономические показатели
сернокислотных систем
Показатели Система
под давлением (прямоточная) без давления (поставки ПНР)
Мощность, тыс. т/год 740 500
Капитальные вложения, % 122 100
в основное производство 95 79
в общезаводское хозяйство 27 21
Удельные капитальные вложения, %
всего 77,3 100
в основное производство 79 79
Себестоимость 87 100
Численность трудящихся, чел. 80 107
Трудозатраты, чел.-час/т 0,20 0,39
Приведенные затраты, % 92 100
Металлоемкость, кг/т 5,014 8,603
всего в основное производство 2,83 6,418
Выбросы SO2 в атмосферу, кг/т 0,3 1,97
выдувается растворенный в абсорбционной кислоте диоксида
серы, за счет чего увеличивается общий процент конверсии. Вы-
брос диоксида серы на 1 т продукционной кислоты составляет
примерно 0,3 кг, т. е. система является практически безотход-
ной.
Выполненное Гипрохимом по исходным данным НИУИФ»а
ТЭО на строительство сернокислотной системы под давлением
по прямоточной схеме мощностью около 700 тыс. т/год (систе-
ма НИУИФ — МИХМ) подтвердили технико-экономическую
эффективность этой системы (табл. 50). Расчеты показали так-
же, что в системе НИУИФ — МИХМ топливно-энергетические
затраты на производство кислоты значительно ниже (на 36,5%),
чем в действующих современных сернокислотных системах на
сере (проект и поставка ПНР), что видно из табл. 51.
Так как удельная металлоемкость основного производства
системы НИУИФ — МИХМ значительно ниже (в 2,5 раза), чем
в сравниваемой системе без давления, то также значительно ни-
же будут энергозатраты на создание этих систем и на единицу
производственной мощности (1т), что видно из табл. 52.
Максимальные резервы интенсификации открываются при
реализации циркуляционных схем производства серной кислоты
под давлением с применением кислорода [8, 9, 10]. В циркуля-
ционной системе комплексно используются все факторы повы-
шения интенсивности и приближения к безотходной технологии:
концентрированные газы, оптимальные температуры, активные
и устойчивые в работе катализаторы, повышенное давление, ин-
тенсивные аппараты с кипящим слоем и с пенным слоем и, на-
конец, наиболее прогрессивная схема с рециклом по газу, обес-
печивающая энергетически и экологически совершенное произ-
водство.
258
Таблица 51. Топливно-энергетические затраты на производство 1 т H2SO,
Показатели Система под давле- нием, прямоточная (740 тыс. т/год) Система без давле- ния (поставки ПНР. 500 тыс. т/год)
Энергетические затраты электроэнергия, кВт-ч (т у. т) 14,2(0,00497) 75(0,02625)
пар (Р=0,6 МПа, /=158 °C), 0,13(0,02249) 0,15(0,02595)
Гкал (т у. т) пар (/’=1,5—1,7 МПа, /=220°C), 0,0011(0,00019) —
Гкал (т у. т) вода оборотная, м3 (т у. т) 56,9(0,01877) 67,23(0,02218)
вода химочищенная, м3 (т у. т) 1,22(0,000512) 1,1(0.000462)
Топливо, природный газ (Q = 0,195(0,0279) 0,014(0,002)
= 8480 ккал'м3), Гкал (т у. т) Сжатый воздух (Р=0,6—0,8 МПа), 2,2(0,00007) 2,2(0,00007)
м3 (т у. т) Сера (топливо), т (т у. т) 0,332(0,105) 0,335(0,1061)
Итого, т у. т. 0,1799 0,1830
Вторичные энергоресурсы (ВЭР) — 0,796(0.1377) 0,68(0,1176)
пар (Р = 4 МПа, / = 440°С), Гкал т у. т. Итого за вычетом ВЭР, т у. т 0,0422 0,0654
т у. т — тонн условного топлива.
В случае сжигания серы в кислороде при любых концентра-
циях SO2, вплоть до 60%, можно сохранить постоянное (необхо-
димое) соотношение С)2: SO2. Применение изотермических реак-
торов кипящего слоя способствует проведению процесса при
температуре, приближающейся к оптимальной, с полным ис-
пользованием внутренней поверхности катализатора и достиже-
нию высокой степени превращения за один цикл. При этом ре-
цикл по газу позволяет создать практически безотходное произ-
водство. Становится возможным уменьшить число слоев в кон-
тактном аппарате до одного, число ступеней контактирования и
абсорбции — до одной. Полностью исключаются из системы про-
межуточные теплообменники. При сочетании перечисленных
Таблица 52. Энергозатраты на создание сернокислотных систем, т у. т
Показатели Система под давлением, 740 тыс. т/год Система без давления, 500 тыс. т/год
на создание системы на единицу мощности иа создание системы на единицу мощности
Изготовление металла 2935,2 0,003968 4327,6 0,008655
Изготовление футеровоч- ных материалов 436,6 0,00059 1280,0 0,00256
Изготовление аппаратов 1834,9 0,002479 2973,9 0,005947
Итого 5206,7 0,007037 8581,5 0,01716
17;
259
преимущества циркуляционных схем с известными достоинства-
ми реакторов КС для переработки высококонцентрированных
газов под давлением стало возможным создание высокоинтен-
сивной сернокислотной системы большой единичной мощности
с высокими технологическими, энергетическими и экономиче-
скими показателями.
Для производства высококонцентрированного диоксида се-
ры сжиганием серы в кислороде разработан принципиально
новый способ, предусматривающий газификацию серы в барбо-
тажном слое и последующее сжигание паров серы в кипящем
слое инертного материала, охлаждаемом при помощи теплооб-
менной насадки (см. рис. 34).
Разработанная НИУИФ совместно с ЛТИ им. Ленсовета
технологическая схема циркуляционной сернокислотной систе-
мы, предусматривающая проведение технологического процес-
са по замкнутому циклу под давлением с применением техни-
ческого кислорода, представлена на рис. 88.
Газификацию серы проводят при температуре 600—700 °C и давлении
1,5 МПа в испарителе, куда подается кислород (5—7% от общего расхода
его в системе). Пары серы сжигают в печи с кипящим слоем инертного зер-
нистого материала при 700—800°C. Сюда же подают и весь кислород, необ-
ходимый для образования диоксида серы, а впоследствии — и триоксида се-
ры. Общий избыток кислорода составляет 0,5—2,0% от стехиометрического.
Температура в печи поддерживается в результате размещения в кипящем
слое теплообменных элементов котла-утилизатора. Газовая смесь, содержа-
щая 65—66% SO2, поступает в циркуляционный контур, включающий тепло-
обменник, однополочный контактный аппарат КС-7 и пенный абсорбер, кото-
рые работают под давлением 1,0 МПа. Циркуляцию газовой смеси осуществ-
ляют при помощи инжектора, использующего энергию газовой смеси, выходя-
щей из печи. Теплообменные нзсэдки, расположенные в зппзрзтзх выполни-
ют функции пароперегревателя и испарителя котла-утилизатора.
В контактном аппарате КС при 1,0 МПа 500—550 °C степень превраще-
ния SO2 в SO3 составляет 92—95%. Из контактного аппарата газовая смесь,
пройдя теплообменник, поступает в абсорбер, где улавливается SO3. Затем
газовая смесь, содержащая SO2, О2, N2, засасывается инжектором и возвра-
щается в цикл. Около 0,5% газовой смеси для исключения накопления инер-
тов направляется в малогабаритную установку очистки хвостовых газов, со-
стоящую из контактного аппарата и абсорбера, после чего выбрасывается в
атмосферу. Кроме того, в установку очистки поступает газ из десорбера, где
производится отдувка воздухом диоксида серы, растворенного в продукцион-
ной кислоте.
Степень использования диоксида серы в системе составляет
99,995—99,999%, выбросы диоксида серы не превышают 0,02—
0,03 кг на 1 т 100%-ной кислоты (мнг), т. е. система является
практически безотходной. Система энергетически совершенна.
Практически полное использование тепла реакции обеспечива-
ет производство 1,25—1,3 т пара на 1 т мнг.
Удельная загрузка катализатора составляет около 4,5 кг на
1 т мнг суточной выработки. Диаметр всех аппаратов циркуля-
ционной системы мощностью 700 тыс. т/год близок к 3,5 м, т. е.
они все транспортабельны по железной дороге, что позволяет
полностью их изготавливать на машиностроительных заводах и
поставлять на строительные площадки.
260
РИС. 88. Схема производства серной кислоты из серы под давлением 1,5—1,0 МПа (по циклической схеме и с использованием
кислорода):
I — печь дожита серы; 2 — котел-утилизатор; 3 — инжектор; 4 — контактный аппарат КС: 5 — теплообменник; 6 — экономайзер: 7. /'> — тумано-
брызгоуловителн- 8 — абсорбер: 9 — холодильник кислоты; // — труба; /’--контактный аппарат очистки; 13 - десорбер: 14 — абсорбер (конечный):
15. 18 — насосы кислотные: 16, /9 — сборники кислоты; 17, 29 — воздуходувки: 21 — топка подогревателя; 22 — подогреватели пусковой. 23 — шла-
монакопптель; 24 — плавилка серы; 25 — непаритель-окиелнтель серы; 26 — воэдухоразделнтельная установка.
Рассмотренные эффективные безотходные сернокислотные
системы, работающие под повышенным давлением, являются
новым перспективным этапом технического прогресса сернокис-
лотного производства.
В 1982 г. на заводе в г. Ли-Крик (США, штат «Северная Каролина»),
принадлежащем американской фирме «Техасгульф», пущена в эксплуатацию
крупнейшая в мире сернокислотная система на сере мощностью 3100 т/сут
(1 млн. т/год). Проект системы выполнен фирмой «ААонсанто». При проекти-
ровании этой системы использованы новые технические решения. Отмечается
высокая энергетическая эффективность производства, обеспечивающего па-
ром собственные компрессоры и выдающего тепловую энергию для нужд
производства фосфорсодержащих продуктов. Теплообменная аппаратура кон-
тактного и абсорбционного отделений выполнена с таким расчетом, чтобы
предотвратить конденсацию тумана серной кислоты по газовому тракту.
В проекте предусмотрены высокоэффективные туманоуловители, а также спе-
циальные системы контроля содержания оксидов серы в выхлопных газах.
Особое внимание уделено энергосберегающим системам, предназначенным
для обеспечения эффективной работы такой мощной установки. Для охлаж-
дения циркуляционных кисло г применены кислотные холодильники с анти-
коррозионной анодной защитой. В системе используется тепло, выделяющееся
на стадии абсорбции триоксида серы. С целью уменьшения размеров аппара-
тов система запроектирована для работы при несколько повышенном давле-
нии (0,07—0,08 МПа) и с более высокими скоростями газа в аппаратах по
сравнению с действующими системами. В ряде зарубежных стран (Швеция,
Англия, США и др.) последние годы уделяется пристальное внимание более
полному использованию вторичных энергоресурсов. Построены сернокислотные
системы, в которых тепло абсорбции триоксида серы используется для пред-
варительного нагрева воды, подаваемой в котел-утилизатор, или же для це-
лей теплофикации. Указывается, что использование этого способа обеспечи-
вает значительную экономию и окупается в течение 6 месяцев.
Таким образом, основными направлениями технического про-
гресса производства серной кислоты являются: создание мате-
риало- и энергосберегающих систем большой мощности, обеспе-
чение высокой надежностью работы каждого аппарата и уст-
ройства системы и всей системы в целом, снижение удельных
выбросов вредных веществ с выхлопными газами.
Путями решения этих проблем являются: применение повы-
шенного давления и повышенной концентрации диоксида серы,
эффективных катализаторов, внедрение новых интенсивных ап-
паратов, работающих при повышенных скоростях газа, более
полное использование теплоты всех реакций на всех стадиях
производства, использование коррозионно стойких материалов,
автоматизации управления производством.
IV.3. ОДНОВРЕМЕННОЕ ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ
И ВОДОРОДА
В связи с постоянным удорожанием органических топ-
лив, являющихся основой современного энергопроизводства
(в первую очередь, нефти и природного газа), запасы которых
ограничены и постепенно исчерпываются, возникла проблема
их экономии и, в конечном итоге, замены.
В последнее время в промышленно развитых странах начал-
ся постепенный переход к новой энергетической системе, харак-
262
РИС. 89. Технологическая схема получения водорода термоэлектрическим
разложением воды в «замкнутом» сернокислотном цикле:
/ — блок электролиза; 11 — блок термолиза; /У/— блок разделения газов; / — электро-
лизер; 2—сборник кислоты; 3 — концентратор; 4, 7 — сепараторы; 5 —реактор; 6 — испа-
ритель; 8 — компрессор; 9, 10 — конденсаторы; 11— турбогенератор.
теризующейся расширением использования ядерных возобнов-
ляемых источников энергии при сохранении в энергобалансе су-
щественной роли органических топлив. В этой новой энергети-
ческой системе универсальным энергоносителем, который может
передавать энергию от ядерных и других энергоисточников мно-
гочисленным и разнообразным потребителям, заменяя таким
образом органическое газожидкостное топливо, будет водород,
получаемый из воды. Это чистое в экологическом отношении
топливо, поскольку практически единственным продуктом его
сгорания является вода.
При проработке возможных способов эффективного и эконо-
мичного получения водорода из воды (за рубежом и в СССР)
было установлено, что наиболее перспективным для опытно-
промышленного освоения является получение водорода термо-
электрохимическим разложением воды в сернокислотных цик-
лах.
Проведенные исследования и опытные работы позволили
разработать так называемый замкнутый сернокислотный цикл
получения водорода термоэлектрохимическим разложением во-
ды с использованием второго теплообменного контура высоко-
температурного ядерного реактора, в котором товарным продук-
том является водород и кислород, сырьем — вода, а серная кис-
лота находится в цикле. Принципиальная схема замкнутого
сернокислотного цикла изображена на рис. 89.
Схема включает три блока: термолиза серной кислоты, электролиза и
разделения газовой смеси.
Концентрированная серная кислота (95—96%-ная) подвергается терми-
ческому разложению (термолизу) за счет какого-либо внешнего источника
тепла (в частности, тепла второго контура высокотемпературного ядерного
реактора) в испарителе и каталитическом реакторе. В испарителе серная
263
кислота испаряется и диссоциирует на SO3 и Н2О при 450—500 °С. В реак-
торе при 850—900 °C триоксид серы на специальном (КД) катализаторе вос-
станавливается до диоксида серы по реакции
so3 + Н2О -----> SO2 + 0,5О2 +- Н2О
Суммарная реакция термолиза
К,/
H2SOtf ---> S02 + 0,502+H20 (термолиз)
Образовавшаяся газовая смесь, содержащая SOa, SO3, НгО и Ог, охлаж-
дается в концентраторе (тепло используется для концентрирования серной
кислоты, поступающей из блока электролиза), где из нее кислотой практиче-
ски полностью абсорбируется триоксид серы. Далее, газовая смесь, пройдя
через сепаратор (где из нее отделяются брызги и туман серной кислоты),
поступает в конденсатор для выделения воды. Оставшаяся смесь диоксида
серы и кислорода разделяется на последовательных ступенях компримирова-
ния и конденсации. При этом диоксид серы сжижается. Далее он направляет-
ся в блок электролиза, а сжатый кислород проходит турбогенератор (для
использования энергии сжатия газа) и направляется потребителю. В элект-
ролизер, который заполнен 50—60%-ной серной кислотой, через каталитиче-
ский анод подаются жидкий диоксид серы и вода. В процессе электролити-
ческого разложения воды с деполяризацией анодного процесса диоксидом
серы образуется водород и серная кислота:
SO2 + H2O —SO3+H2
SO3 + Н2О ---> H2SO4 (электролиз)
Водород проходит через диафрагму в катодное пространство и выводит-
ся оттуда потребителю. Образующаяся в анодном пространстве 50—60%-ная
серная кислота выводится из электролизера и направляется в аппарат кон-
центрирования. После концентратора закрепленная до 95—96% кислота на-
правляется в испаритель, и цикл повторяется. Каждая молекула циркулирую-
щей кислоты за один цикл дает, таким образом, одну молекулу водорода.
Напряжение на ячейке электролизера сернокислотного цикла равно
0,7—1,0 В; это примерно в 3 раза меньше, чем при щелочном электролизе
воды, что делает энергетически и экономически эффективным получение во-
дорода рассматриваемым способом (расход электроэнергии на 1 м3 водорода
составляет около 2 кВт-ч, вместо примерно 6 кВт-ч при щелочном электро-
лизе).
Выполнен большой объем исследований по разработке ката-
лизаторов для термического разложения серной кислоты и по
кинетике процесса термолиза кислоты. Исследования показали,
что перспективным катализатором является оксид железа, на-
несенный на термостабильный носитель. В этом случае носитель
для катализатора должен обладать пористой структурой с пре-
обладанием крупных транспортных пор (0,1—1,0 мкм), а в про-
цессе изготовления катализатора должно быть обеспечено фор-
мирование соответствующей крупнопористой структуры.
В качестве носителя рекомендованы диатомит и активный
оксид алюминия (у-А12О3). Проведенные исследования показа-
ли также перспективность модифицированного (хромистой кис-
лотой) железохромоксидного катализатора. Оптимальный же-
лезохромоксидный катализатор содержит в своем составе 14—
18% Сг2О3 и 86—82% Fe2O3. Оптимальный состав достигается
обработкой железохромоксидной основы 25—35%-ным раство-
ром хромовой кислоты. В фазовом отношении железохромо-
264
РИС. 90. Технологическая схема одновременного получения водорода и сер-
ной кислоты термоэлектрохимическим разложением воды в «разомкнутом»
сернокислотном цикле:
I — блок электролиза; 11—блок термолиза; III — блок разделения газов; / — электроли-
зер; 2 — концентратор; 3~ реактор; 4 — испаритель; 5, 7 — конденсаторы; 6 — компрес-
сор; 8 — сепаратор; 9 — сборник кислоты.
ксидный катализатор представляет собой твердый раствор ок-
сида хрома в оксиде железа.
На ослове дальнейших исследований и расчетов разработан
новый «разомкнутый» сернокислотный цикл одновременного
производства водорода п серной кислоты термоэлектрохимиче-
ским разложением воды.
Такой сернокислотный цикл может работать как с исполь-
зованием тепла ядерного реактора или другого источника вы-
сокотемпературного тепла, так и без них. Сущность «разомкну-
того» цикла состоит в том, что в цикл вводится сера, являющая-
ся с одной стороны источником энергии для термического раз-
ложения триоксида серы, а с другой — сырьем для получения
товарной кислоты. Образующийся в цикле за счет ввода серы
дополнительный диоксид серы позволяет получать дополнитель-
но количество водорода и товарную серную кислоту, выводимую
из цикла. Принципиальная схема «разомкнутого» сернокислот-
ного цикла изображена на рис. 90.
В испарителе за счет подводимого тепла (температура 450—500 °C) про-
исходит испарение серной кислоты и диссоциация ее паров на SO3 и Н2О.
Из испарителя газовая смесь поступает в реактор, куда также подается жид-
кая сера. Сера испаряется и вступает во взаимодействие с триоксидом серы
по реакции
2SO3 + S --> 3SO2
Количество серы, подаваемой в реактор, должно соответствовать стехио-
метрическому ее отношению к SO3 по данной реакции. При этом выделяется
тепло, и температура газовой смеси повышается до 850 900 °C.
После реактора газовая смесь, состоящая из SO2 и Н2О, поступает в
концентратор, куда подается 50—60%-ная серная кислота, полученная в
электролизере. После концентратора газовая смесь направляется в конден-
265
сатор, где конденсируются пары воды. Затем газ (SO2) компремируется и
подается в электролизер, где проходит та же реакция, что и в «замкнутом»
цикле (только будет подаваться в 1,5 раза больше SO2, чем в «замкнутом»
цикле за счет диоксида серы, полученного от разложения циркулирующей
серной кислоты и от поданной в цикл серы).
Из электролизера полученный водород подается потребителю, а серная
кислота, выход которой соответствует количеству введенной в цикл серы,
выводится из цикла как товарная непосредственно после электролизера или
после концентратора.
В «разомкнутом» цикле исключается необходимость приме-
нения высокотемпературного теплоносителя, т. е. его осущест-
вление не связано с наличием, в частности, высокотемператур-
ного атомного реактора. Этот способ одновременного получения
водорода и товарной серной кислоты представляет большой ин-
терес для химической промышленности, так как для крупных
заводов по производству сложных минеральных удобрений, в
состав которых входит производство аммиака, он позволит иск-
лючить необходимость в постороннем источнике водорода (при-
родный газ) и получить одновременно на том же оборудовании,
кроме водорода, и серную кислоту, практически с полным ис-
пользованием серы и без выхлопных газов. При этом необходи-
мость в строительстве контактной сернокислотной системы от-
падает. Комбинация стадий двух описанных сернокислотных
циклов — «замкнутого» и «разомкнутого» — позволяет создать
разомкнутые сернокислотные циклы термоэлектрохимического
разложения воды с получением в различных соотношениях во-
дорода, серной кислоты и кислорода.
Технико-экономические расчеты показали, что в «разомкну-
том» цикле затраты энергии на получение водорода примерно
на 30% меньше, чем в «замкнутом» цикле. Проведенные иссле-
дования и расчеты показывают перспективность проведения
всех процессов сернокислотных циклов термоэлектрохимическо-
го разложения воды с получением водорода или водорода и сер-
ной кислоты при повышенном давлении. Проведение процессов
при повышенном давлении позволит значительно уменьшить
размеры аппаратов и, следовательно, снизить капитальные вло-
жения в строительство термоэлектрохимических предприятий по
производству водорода и серной кислоты, повысить эффектив-
ность электролиза серной кислоты, значительно упростить аппа-
ратурное оформление процессов разделения продуктов реакции
в цикле, снизить затраты на транспортирование продукционно-
го водорода. Возможно применение давления в пределах 5—
40 ат (0,5—4 МПа).
ГЛАВА V
ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫ НИТРОЗНЫМ
МЕТОДОМ [162—170]
Первая (нитрозная) башенная система в нашей стра-
не была пущена по лицензии Петерсена в 1927 г.,
с 1955 г. башенные системы больше не строились. Удельный
вес башенной кислоты в общем объеме выпуска кислоты в
1980 г. составил у нас 5%, в США такое соотношение было
принято уже в 1965 г., а к 1980 г. составило менее 1%.
На современном уровне развития сернокислотного производ-
ства башенный процесс утратил свою значительную роль, кото-
рую он играл до 50-х годов, и был вытеснен крупномасштаб-
ным технически более совершенным контактным процессом,
важным преимуществом которого является отсутствие загрязне-
ния атмосферы оксидами азота.
Быстрая послевоенная переориентация на контактные произ-
водства исключила из общих планов развития башенных про-
изводств, несмотря на их достоинства, при использовании в ка-
честве сырья колчедана, к которым относятся: предельная про-
стота аппаратурного оформления и проведения технологического
процесса, более низкие капитальные вложения и эксплуатаци-
онные затраты, отсюда — более низкая себестоимость (примерно
на 10—15% ниже контактной кислоты), возможность строи-
тельства завода в короткие сроки и эффективного использова-
ния высококонцентрированного диоксида серы и др. Башенная
кислота, кроме основных потребителей — промышленности удоб-
рений и металлургии, всегда имела специфических потребите-
лей, например в текстильном производстве для протравливания
тканей (из-за ее относительно малой коррозионной агрессивно-
сти), при обработке некоторых руд и т. п.
В настоящее время только для получения удобрений требу-
ются десятки миллионов тонн серной кислоты. Требования к
качеству кислоты для этих целей соответствуют стандартам на
башенную кислоту. Следовательно, можно не расходовать Чи-
стую концентрированную контактную кислоту, которую в произ-
водствах удобрений предварительно разбавляют в специальных
смесительных установках, а применять башенную.
На сегодня оптимальный режим башенного процесса доста-
точно изучен, проектные показатели по интенсивности перекры-
ты в 5 и более раз. Кроме того, разработаны методы повыше-
ния концентрации обжиговых газов, в том числе с применением
кислорода, освоено строительство крупногабаритных башен и
другой абсорбционной аппаратуры, которая может быть успеш-
но использована и для башенного процесса. Все это создает
предпосылки для развития башенных производств на новой ос-
нове.
267
РИС. 91. Схема семибашениой системы:
/ — денитрационпая башня; 2, 3 — первая и вторая продукционные башни; 4— окисли-
тельная башня (окислительный объем, орошаемый); 5—7—абсорбционные башни; 8 —
электрофильтр.
Непременным условием для возобновления строительства
башенных сернокислотных систем является резкое снижение
выбросов оксидов азота и серы с выхлопными газами. За по-
следние годы разработаны процессы, обеспечивающие решение
этого вопроса, однако требуется опытно-промышленная провер-
ка этих процессов. В настоящее время проводится проектная
проработки сернокислотной башенной системы на колчедане
мощностью 180 тыс. т/год. Если закладываемые в ней новые
технологические процессы, направление на снижение содержа-
ния оксидов азота и серы в выхлопных газах, подтвердятся —
целесообразно рассмотрение вопроса о строительстве новых ба-
шенных систем.
Принципиальная технологическая схема современной семи-
башенной системы получения серной кислоты нитрозным мето-
дом представлена на рис. 91.
Для производства башенной кислоты не требуется специальной очистки
газа. В настоящее время все заводы работают на сере, но и при работе на
колчедане гаэ очищался только от пыли.
Аппаратурное оформление башенного процесса не сложно: диоксид серы
перерабатывается в 7—8 футерованных башнях с керамической насадкой,
одна из башен — полая является регулируемым окислительным объемом.
Известны различные схемы орошения башен [3, 9, 12]. Башни имеют сбор-
ники кислоты, холодильники, насосы, подающие кислоту в напорные баки над
башнями. Перед двумя-тремя последними башнями устанавливается хвос-
товой вентилятор. Для очистки отходящих газов от тумана серной кислоты
после последней—санитарной башни или перед ней имеется мокрый электро-
фильтр и 100-метровая выхлопная труба.
Оксиды азота, необходимые для процесса, получают из азотиой кислоты,
вводимой в систему.
V.I. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ НИТРОЗНОГО ПРОЦЕССА
Физико-химические основы процесса детально изучены
советскими учеными К. М. Малиным, И. Н. Кузьминых,
В. С. Епифановым, Н. И. Смысловым, В. Н. Шульцем, А. В. Ба-
268
леевым, Т. 1-1. Куниным, Ю. М. Соловьевым и рядом др. [3, 9,
12, 161, 169]. (Ранее проведенные в этом направлении «клас-
сические работы» Люнге, Берля, Мюллера, Рашита, Абеля, Со-
реля дали ряд ценных результатов по свойствам различных сер-
ноазотных соединений, но не вскрыли механизм кислотообра-
зования и не сыграли существенной роли в развитии производ-
ства.)
В нитрозном процессе окисление диоксида серы осущест-
вляется при помощи оксидов азота, которые являются перенос-
чиками кислорода. При этом высшие оксиды азота (диоксид
NO2 и трихлорид N2O3) восстанавливаются до оксида азота
(NO). Оксид азота вновь окисляется до высших оксидов кисло-
родом. В процессе окисления диоксида серы существенную роль
играет нитроза, которой в технике называют раствор оксидов
азота в водных растворах серной кислоты. При растворении в
водных растворах серной кислоты (концентрация 73% H2SO4)
оксиды азота в зависимости от степени их окисления образуют
нитрозилсерную кислоту:
N2O3 + 2HaSO4 = 2HNSO5 + Н2О + 20,6 ккал (86,3 кДж)
или нитрозилсерную и азотную кислоты:
2NO2 + H2SO4= HNSO5 + HNO3 + 5,7 ккал (23,9 кДж)
При нормальной работе в газах башенных систем степень
окисления оксидов азота не больше, чем это соответствует фор-
муле N2O3.
Большое значение в нитрозном процессе имеет концентрация
исходной серной кислоты, т. е. кислоты после удаления из нее
всех окислов азота. Зная содержание H2SO4 и N2O3 в нитрозе,
Таблица 53. Изобарные потенциалы реакций нитрозного процесса
Реакция az353, k
ккал/моль | кДж/моль
2NO + 02= 2NO2 —14 420 —60 500
SO2+H2O = H2SO3 + 1580 +6 620
NO + NO2+H2O=2HNO2 —6 410 —26 860
H2SO3+2HNO2= H2SO4+2N0+H20 —27 460 —115 000
NO2+NO + 2H2SO4=2HNSO5+H2O —48 000 —201 120
hnso5+h2o=h2so4+hno2 —20 800 —83 600
N2O3+H2O = 2HNO3 —6 400 —26 800
HNO2+H2SO4=HNSOs+H2O +2 300 +9 640
2HNO2+ SO2—>Нг5О4 + 2N0 —39 470 — 163 500
S02+N02—*SO3 + NO —32 475 — 134 000
hno3+so2—>hnso5 —20 800 —83 600
hno2+so2—>hnso4 — 1 000 —4 190
HNSO4+HNO2—i-HNSOs+NO —1 800 —7 540
2SO2+N2O3+O2+H2O=2HNSO5 +4 320 + 18 000
2HNSO5+SO2+2H2O—>H2SO4+2NO +7 000 +29 150
269
эту концентрацию можно рассчитать по формуле
А= 100^(100 — 0,66)
где А — содержание H2SO4 в исходной кислоте, %; У— содержание H2SO.
в нитрозе по данным анализа, %; В — содержание N2O3 в нитрозе по данным
анализа (в пересчете на HNO3), %.
Механизм кислотообразования [162]. Результаты расчетов
изобарных потенциалов, проведенных для температуры 80 °C,
как средней в продукционной зоне, приведены в табл. 53. Из
полученных расчетных данных следует, что реакция образова-
ния H2SO3 в этих условиях невероятна, а поглощение SO2 нит-
розой нужно отнести к случаю физической абсорбции, что со-
гласуется с результатами ряда исследований о том, что SO2
растворяется в H2SO4 без химического взаимодействия. Схема
кислотообразования в нитрозном процессе выглядит следую-
щим образом:
SO2 (г) SO2 (р-р)
HNSO5 + Н2О =?=* H2SO4 + hno2
2HNO2 + SO2 (р-р) --> H2SO4 + 2NO (p-P)
NO (p-p) < > NO (r)
2NO (г) + O2 (r) -> 2NO2(r)
(NO + NO2) (r) (NO + NO2) (p-p)
(NO + NO2) (p-p) + H2SO4 <—>: HNSO5 + HNO2
Скорости газа и плотности орошения. Увеличение линейной
скорости газа в интервале 0,2—0,7 м/с повышает коэффициент
Г>^ПАПХТТТТТТ СГЛ птглттп™ rsArvz.,, м.хчтт гтхчттттхчхч
vrkvpvein аиоирицнн ич>2 опачаос vDicipcc, oaicivi медленнее, спи-
рость свыше 0,7 м/с не влияет на коэффициент скорости абсорб-
ции. Коэффициент скорости абсорбции SO2 К[в г/(м2-ч-Па)]
определяется уравнением
К = Awrb
.4 — постоянная; ьаг — линейная скорость газа, м/с; b — показатель, завися-
щий от плотности орошения q следующим образом:
<7, м3/м2-ч..................... 12,6 31,5 50,5
Ь .............................. 0,315 0.339 0,523
Влияние плотности орошения на коэффициент скорости абсорб-
ции определяется уравнением
К= Aqm
Значение показателя степени tn зависит от соотношения
между относительными долями сопротивления со стороны газо-
вой и жидкой фаз в общем сопротивлении. На основании экспе-
риментальных данных значения т при плотности орошения в
этом уравнении для различных линейных скоростей газа равны:
wit м/с....................... 0,52 0,64 0,73 0,80 0,90
т ......................... 0,785 0,800 0,8435 0,8652 0,8800
270
Концентрации исходной серной кислоты и газа. Температу-
ра процесса. С повышением концентрации серной кислоты ско-
рость поглощения SO2 нитрозой вначале медленно, затем очень
быстро повышается и достигает резко выраженного максимума
при концентрации кислоты э/ 70 ^П2'^х^4**±Н2О). С- дальнейшим
повышением концентрации до 84,5% (H2SO4-II2O) скорость по-
глощения понижается до минимума. Затем скорость поглощения
SO2 с повышением концентрации кислоты вновь медленно воз-
растает.
Окисление абсорбированного диоксида серы осуществляется
продуктами гидролиза нитрозилсерной кислоты. Наиболее высо-
кая степень поглощения SO2 при концентрации кислоты 57%
H2SO4 объясняется тем, что при этой концентрации степень гид-
ролиза нитрозилсерной кислоты достигает 100%. С увеличением
содержания H2SO4 в нитрозе сверх 57% скорость поглощения
SO2 понижается вследствие уменьшения степени гидролиза нит-
розилсерной кислоты. Понижение же скорости поглощения SO2
с уменьшением содержания H2SO4 в нитрозе ниже 57%, по-ви-
димому, связано с уменьшением содержания в ней HNO2, опре-
деляющего скорость процесса окисления SO2.
С повышением температуры скорость поглощения SO2 нитро-
зой увеличивается, причем характер этой зависимости изменяет-
ся при 100—НО °C. Возможно, что до этой температуры реакция
определяется скоростью гидролиза нитрозилсерной кислоты, а
при более высокой температуре и достижении полного гидроли-
за— скоростью взаимодействия SO2 с продуктами гидролиза.
Скорость взаимодействия диоксида серы с нитрозой прямо
пропорциональна его содержанию в газе. Такая зависимость на-
блюдается при любых условиях, так как скорость реакции в га-
зовой фазе прямо пропорциональна содержанию диоксида серы
в ней, а скорость поглощения жидкой фазой должна быть пря-
мо пропорциональна разности между содержанием SO2 в газо-
вой фазе и на границе раздела фаз, где оно равно нулю. Таким
образом, концентрация SO2 в газе влияет в продукционной зоне
на движущую силу абсорбции, в абсорбционной — на объем га-
за на единицу продукции и, следовательно, на объем аппара-
туры.
Большое влияние на скорость процесса оказывает повыше-
ние концентрации кислорода. Это объясняется тем, что с повы-
шением содержания кислорода в газе увеличивается скорость
его поглощения жидкостью и скорость окисления образующего-
ся оксида азота в жидкостной пленке. В результате содержание
инертного газа в жидкостной пленке уменьшается, а содержание
активного по отношению к SO2 компонента увеличивается, что
и ведет к ускорению процесса окисления диоксида серы в жид-
костной пленке.
Нитрозность кислоты. В современных башенных системах
нитрозность кислоты достигает 15—19% (в пересчете на HNO3).
Значительное влияние на степень окисления SO2 в жидкой фазе
271
имеет присутствие в нитрозе свободной азотной кислоты ;[162—
164]. При содержании азотной кислоты до 1,5% активность нит-
роз повышается на 30%. Дальнейшее увеличение содержания
азотной кислоты перестает сказываться на росте активности
нитрозы, что связано с уменьшением степени гидролиза нитро-
зилсерной кислоты при замене части воды свободной азотной
кислотой.
Скорость восстановления азотной кислоты в нитрозах зави-
сит от концентрации исходной серной кислоты и растет с ее сни-
жением. Оптимальным условием для перевода азотной кислоты
в нитрозилсерную по уравнению SO2+HNO3 = HNSOs является
узкий интервал концентраций серной кислоты 75,5—78%, в ко-
тором при большой скорости восстановления азотной кислоты
скорость образования нитрозы становится максимальной. По-
вышение температуры увеличивает активность азотной кислоты
так же, как нитрозы.
Скорость поглощения оксидов азота серной кислотой зависит
от скорости газового потока до достижения скорости газа
0,8 м/с. Дальнейшее увеличение скорости газового потока не
сказывается на увеличении скорости поглощения оксидов азота
вследствие прекращения влияния на процесс диффузии газа че-
рез газовую пленку.
Поглощение оксидов азота. В условиях нитрозного процес-
са оксиды азота присутствуют в виде NO, NO2 и N2O3.
Растворимость оксида азота в водных растворах серной кис-
лоты незначительна. Так, при нормальном давлении и темпера-
туре 20 °C концентрация NO в растворах составляет:
Концентрация H2SO4, % . . . . 100 45 24 0
Содержание NO, %............. 0,00255 0,00203 0,00519 0,00965
Растворимость NO в нитрозе при нормальном давлении, тем-
пературе 40 °C и различной концентрации исходной кислоты по-
казана ниже:
Содержание HNSO5, %
Растворимость, %
при концентрации H2SO4 75%
при концентрации H2SO4 92%
6 8 10
0,17 0,26 0.28
0,28 0,31 0,32
Скорость поглощения оксидов в виде N2O3 почти в 2 раза
выше, чем NO2. С повышением температуры скорость поглоще-
ния окислов азота серной кислотой уменьшается.
Скорость поглощения N2O3 серной кислотой возрастает с
повышением концентрации кислоты:
Концентрация серной кислоты, % 73,4
Коэффициент скорости поглоще-
ния
кг/(м2-ч-мм рт. ст.) . . . 8,5
кг/(м2-ч-кПа) .... 1,14
76,6 80,8 84 95,6
8,8 9.0 9,5 10,5
1,17 1,20 1,27 1,34
272
Избыточное содержание NO не оказывает влияния на про-
цесс поглощения оксидов азота, эквимолекулярное соотношение
между NO и NO2 (N2O3) является оптимальным для поглоще-
ния оксидов азота серной кислотой и процесса окисления SO2.
Потери оксидов азота с отходящими газами слагаются из
статических потерь, обусловленным давлением оксидов азота
над нитрозой, орошающей последнюю башню, и потерь, завися-
щих от технологических дефектов — несоблюдения оптимальных
условий ведения процесса. Уменьшение статических потерь воз-
можно при повышении концентрации кислоты, орошающей по-
следнюю башню, до 80% H2SO4, дальнейшее повышение кон-
центрации кислоты сказывается незначительно [12].
Характер зависимости скорости поглощения окислов азота
серной кислотой от скорости газа и плотности орошения насад-
ки показывает, что основное влияние на скорость поглощения
оказывают химические процессы, протекающие в жидкой фазе,
а не диффузионные процессы в газовой и жидкостной пленках.
О том же свидетельствует повышение скорости поглощения ок-
сидов азота с увеличением концентрации серной кислоты и по-
нижением температуры, так как при этом уменьшается гидро-
лиз нитрозилсерной кислоты.
Денитрация нитрозы. Для уменьшения потерь оксидов азо-
та и получения продукции высокого качества, оксиды азота из
нее должны быть удалены возможно более полно. Скорость де-
нитрации серной кислоты снижается с повышением концентра-
ции кислоты и возрастает с повышением температуры. Скорость
денитрации кислоты, содержащей окислы азота в виде N2O5,
значительно больше, чем содержащей N2O3. Это объясняется
образованием нитрозилсерной кислоты при взаимодействии SO2
и HNO3, вследствие чего давление оксидов азота над нитрозой
сильно повышается. Нитроза, в которой оксиды азота находятся
в виде смеси N2O3 и N2O5, денитруется еще быстрее.
Практически в денитрационной башне не удается полностью
удалить оксиды азота из кислоты. Для некоторых же потреби-
телей серной кислоты их присутствие недопустимо. Поэтому
разработаны методы удаления оксидов азота из башенной кис-
лоты при добавлении к ней реагентов. Наиболее эффективными
реагентами, восстанавливающими растворенные оксиды азота
до NO или до азота, оказались сульфат аммония, формалин,
амидосульфоновая кислота и карбамид, которые добавляют в
кислоту в небольших количествах.
V.2. ТЕХНОЛОГИЧЕСКИЙ РЕЖИМ БАШЕННЫХ СИСТЕМ [3, 9, 12]
Непременными условиями нормальной работы башенных
систем является постоянство объема поступающего обжигового
газа и концентрации в нем диоксида серы.
В современных башенных системах достигнута высокая ин-
тенсивность равная 220—250 кг/(м3-сут) (100%-ную кислоту в
18—584
273
расчете на единицу суммарного объема всех башен). Практиче-
ски на действующих заводах расход азотной кислоты составля-
ет 15—18 кг/т. Продукционная серная кислота выпускается с
минимальным содержанием оксидов азота (0,03%), во второй
продукционной башне кислота менее денитрироваиная — содер-
жит до 0,5% оксидов азота.
Плотность орошения башен обычно составляет 10—
15 м3/(м2-ч).
Кратность орошения (отношение общего расхода кислоты,
орошающей все башни, к выходу готовой продукции), которая
определяется по данным материального баланса, обычно со-
ставляет 30—50. Чем интенсивнее работает система, тем мень-
ше кратность орошения при одинаковой плотности орошения.
Согласно стандарту концентрация башенной кислоты долж-
на быть не менее 75% H2SO4. Температура кристаллизации та-
кой кислоты —51 °C, поэтому практически исключается воз-
можность ее замерзания при перевозке и хранении в зимнее
время.
Башенные сернокислотные заводы могут выпускать более
концентрированную кислоту, удовлетворяющую по качеству бо-
лее широкий круг потребителей и более удобную для перевоз-
ки. Однако с повышением концентрации H2SO4 в первой башне
(денитраторе) уменьшается степень денитрации кислоты, а в
продукционных башнях снижается скорость окисления SO2 п
т. д. Орошение башен кислотой пониженной концентрации (ме-
нее 75% H2SO4) нецелесообразно вследствие ухудшения усло-
вий абсорбции оксидов азота и увеличения их потерь. Кроме
того, при концентрации ниже 75% H2SO4 кислота вызывает
усиленную коррозию стальной и чугунной аппаратуры.
Кислота поступает на орошение первой абсорбционной баш-
ни при 45—55 °C. В результате выделения тепла при абсорбции
оксидов азота и конденсации паров воды кислота нагревается
на 15—20 °C и выходит из первого абсорбера при 60—75 °C. Эта
кислота поступает на орошение денитратора и продукционных
башен. Температура кислоты, вытекающей из денитрационной
башни, зависит главным образом от концентрации в ней H2SO4
и от температуры обжигового газа, подаваемого в денитратор.
Чем выше эта температура, тем полнее денитрируется серная
кислота, что имеет существенное значение для работы послед-
ней абсорбционной башни.
Температура кислоты, орошающей последнюю абсорбцион-
ную башню, должна быть как можно ниже; она определяется
температурой охлаждающей воды, подаваемой в оросительные
холодильники. По нормам технологического режима темпера-
тура кислоты, орошающей последнюю башню системы, не долж-
на превышать 40 °C. При этом создаются хорошие условия для
абсорбции оксидов азота, а на температурный режим продукци-
онных башен низкая температура кислоты, поступающей из по-
следней абсорбционной башни, влияет незначительно.
274
Нитрозность кислоты, орошающей продукционные башни,
должна обеспечивать практически полную переработку диокси-
да серы в серную кислоту: содержание SO2 в газе, выходящем
из последней продукционной башни, не должно превышать
0,05то. С повышением нитрозиости орошения интенсивность пе-
реработки SO2 в башнях возрастает. Поэтому в современных
башенных системах нитрозность кислоты, орошающей продук-
ционные башии, достигает 15—19%. Однако с увеличением нит-
розности кислоты интенсивность переработки SO2 повышается
только до определенного предела, по достижении которого далее
не изменяется. Таким образом, в производственных условиях
нецелесообразно значительно увеличивать нитрозность кислоты,
поскольку это может привести к увеличению потерь оксидов азо-
та с отходящими газами.
Азотооборот, т. е. количество оксидов азота (в кг HNO3 на
1 т продукции), выделяющихся в газовую фазу в продукцион-
ной зоне, зависит от кислотооборота (расхода орошающей кис-
лоты), температуры и нитрозиости орошающей кислоты. В ба-
шенных системах, интенсивность которых достигает 200—
250 кг/(м3-сут), азотооборот составляет 700—900 кг/т.
Новый метод доработки диоксида серы. В продукционной
зоне обычно перерабатывается около 90% SO2, дальнейшая пе-
реработка ложится на абсорбционную зону, естественно, ухуд-
шая ее работу. Кроме того, низкие температуры и высокие
плотности нитроз не позволяют полностью провести окисление
остаточного диоксида серы, и выхлопные газы содержат до
0,3% so2.
В филиале НИУИФ разработан и опробован на опытной ба-
шенной системе производительностью 30 т/сут так называемый
бензитрозный цикл орошения, обеспечивающий практически
полное окисление SO2. Метод основан на контакте безнитрозных
12—50%-ных растворов серной кислоты с нитрозными газами,
выходящими из продукционной зоны [163—165]. Скорость окис-
ления SO2 при использовании безнитрозного цикла в 2—3 раза
выше, чем скорость окисления нитрозами. Окислителями SO2
являются оксиды азота нитрозных газов, вступающие в контакт
с водными растворами серной кислоты, или азотная кислота,
вводимая в эти растворы.
Между продукционной и абсорбционной зонами нитрозные газы прохо-
дят через абсорбер, орошаемый 12—45%-ными (оптимально 40—50%-ными
водными растворами серной кислоты, содержащими 0,3—0,5% HNO3. До
абсорбера концентрация SO2 соответствовала 0,6—1,2%, степень переработки
ее составила 98,7—100%, концентрация оксидов азота не менялась.
Повышение концентрации серной кислоты до 70—71% и образование
слабых нитроз привело к снижению степени окисления SOs до 71—73%. Ко-
эффициент скорости окисления SO2 для интервала концентрации орошающих
кислот 12—45% H2SO4 составил 1800—2000 кг/(м3-ч-атм), при повышении
концентрации до 70% он снизился до 500 кг/(м3-ч-атм). Вся вода, необхо-
димая для кислотообразования в продукционной зоне подавалась в сборник
абсорбера и затем в виде водных растворов серной кислоты поступала в го-
ловные башни.
18*
275
Содержание оксидов азота в выхлопных газах в среднем было 0,14%,
что позволило снизить расход азотной кислоты до 4 кг/т мнг, или до 0,066%.
Создание на башенных системах безнитрозного цикла явля-
ется эффективным средством ликвидации потерь SO2 и одно-
временно может рассматриваться как метод уменьшения по-
терь оксидов азота. Наиболее целесообразным является комби-
нирование цикла воднокислотной доработки диоксида серы по-
сле продукционной зоны с водно-кислотным методом глубокого
улавливания оксидов азота, организуемым между абсорбцион-
ной зоной и санитарной башней.
Новый метод улавливания оксидов азота. Для очистки от
оксидов азота выхлопных газов башенного процесса разработан
эффективный метод, основанный на поглощении N2O3 серной
кислотой, a NO2 водой [166, 167].
Для реализации метода очистки сернокислотная система пе-
реводится на режим переокисления, при котором на входе в аб-
сорбционную зону в газах поддерживается избыточное содержа-
ние NO2 против необходимого для образования эквимолекуляр-
ной смеси N2O3. Содержащийся в газе N2O3 поглощается серной
кислотой в абсорбционной зоне как обычно, а избыточный NO2
улавливается воднокислотным раствором в дополнительной
башне, устанавливаемой перед санитарной башней. Перед до-
полнительной башней газовый поток разделяется и 3/4 его на-
правляется на водную отмывку NO2. При этом образуется NO:
3NO2 + Н2О ---> 2HNO3 + NO
После водной отмывки газ, содержащий NO, смешивается в
смесителе-брызгоуловитсле с оставшейся 1/4 газового потока, со-
держащего NO2, в результате получается эквимолекулярная
смесь — N2O3, которая улавливается в санитарной башне.
Метод опробован в филиале НИУИФ на опытной башенной
системе производительностью 30 т/сут.
Для перевода системы на режим переокисления температура орошающей
продукционную зону нитрозы была повышена с 65 до 71—73 °C, а нитроз-
иость — с 6 до 10—12% (в пересчете иа HNO3). При стабильном режиме
концентрация кислот в водно-кислотном цикле составила 4—6% H2SO4 и
1,5% HNO3. Всю воду (500—517 кг на 1 т продукции) вводили в циркуляци-
онный сборник водно-кислотного цикла.
Была достигнута степень поглощения оксидов азота 85—90% из газов,
содержащих 0,3—0,4 NO3. Содержание оксидов азота в выхлопных газах на
1 т моногидрата составило 0,03—0,05%, что соответствует их расходу 3—
4 кг, в то время как при обычном режиме работы системы оно достигало
16 кг. Кроме того, при обычном режиме в выхлопных газах содержание SO2
колебалось в пределах 0,1—0,4%, при новом режиме оно приближалось к ну-
лю. Резко сократился вынос сернокислотного тумана — с 70—100 мг/м3 газа
до 4—10 мг/м3. Максимальная степень разбавления кислоты санитарной баш-
ни брызгами и парами воды не превышала 2%, что не сказывалось на рабо-
те башни.
Получение концентрированной кислоты в башенных систе-
мах. В башенных системах обычно выпускается кислота кон-
центрацией 75% H2SO4. Получение в тех же башенных системах
276
более концентрированной серной кислоты достигается путем ис-
пользования тепла обжигового газа, поступающего в башенную
систему, для упаривания башенной серной кислоты до 92,5 или
90,5%-ной H2SO4; кислота такой концентрации удовлетворяет
многих потребителей [12j. Количество кислоты, подаваемой на
орошение первой денитрационноп башни, уменьшают настолько,
чтобы температура кислоты в этой башне повысилась до
200 °C. Тогда в нижней части башни происходит интенсивное
упаривание серной кислоты.
Естественно, что условия работы башенной системы при выпуске кон-
центрированной кислоты усложняются, так как в одной и той же башне про-
изводится и денитрация кислоты и ее концентрирование. Между тем, с повы-
шением концентрации серной кислоты скорость процесса ее денитрации быст-
ро падает, а потому возрастает нагрузка на вторую продукционную башню.
Кроме того, при уменьшении количества кислоты, орошающей первую башню,
и повышении температуры этой кислоты значительно ухудшается процесс
теплопередачи в первой башне. Поэтому важно наличие большой поверхности
насадки при достаточной ее кислотостойкости и термостойкости.
Практика работы башенных систем показывает, что поверхность насадки
в первой башне должна составлять 1500 м2 на 1 т продукционной серной
кислоты в час [12]. Важно создать достаточно высокую плотность орошения
денитрационной башни, так как количество кислоты, поступающей на оро-
шение этой башни, значительно меньше, чем прн обычной работе системы.
Повышение плотности орошения достигается путем уменьшения диаметра
башнп.
Концентрация кислоты, получаемой в башенных системах,
тем больше, чем выше температура обжигового газа и чем ниже
содержание в нем диоксида серы. Последнее объясняется тем,
что с уменьшением концентрации сернистого ангидрида увели-
чивается объем газа на единицу продукции, а следовательно,
возрастает общее количество тепла, поступающего с обжиговым
газом. Концентрация кислоты, получаемой в башенных систе-
мах, очень сильно зависит от температуры и при содержании в
обжиговом газе 8% SO2 возможность получения концентриро-
ванной кислоты при температуре 330 °C исключается.
При выпуске концентрированной кислоты охлаждение обжи-
гового газа в первой башне происходит сравнительно медленно,
так как орошающая кислота в нижней части башни имеет вы-
сокую температуру (до 200 °C). В этих условиях создается низ-
кое пересыщение паров серной кислоты и туман образуется в
незначительном количестве. Поэтому в отходящих газах содер-
жится очень мало тумана и нет необходимости в установке
электрофильтра в конце системы.
V.3. ПРИМЕНЕНИЕ КИСЛОРОДА В НИТРОЗНОМ
ПРОЦЕССЕ
Применение кислорода на всех стадиях процесса — от
получения сернистого газа высокой концентрации до его перера-
ботки в серную кислоту — позволит весьма значительно интен-
сифицировать работу башенного производства и сократить вы-
бросы оксидов азота в атмосферу до санитарных норм.
277
Таблица 54. Показатели применения кислорода в башенном процессе
Вид сырья Дутье Концентрация so2, % Объем производ- ства, тыс. т/год (мнг.) Капиталь- ные в ложе- НИЯ, % Себестоимость, % Приведенные за- траты. %
о удельные |
Колчедан Воздушное 9 360 100,0 100,0 100,0 100,0
Колчедан Воздушно-кисл О' родное 25 960 144,4 54,6 100,0 87,0 100,0 99.0
Сера Воздушное 12 180 100,0 100,0
Сера Воздушно-кисло- родное 45 450 155,2 62,2 99,5 96,5 95,5
Сера Воздушно-кисло- родное с ретуром • 70 775 176,0 41,0 90.8
газа
Научно-исследовательские и опытные работы, проведенные
в НИУИФ в 1965—1972 гг. показали, что использование 60—
70%-ного (по SO2) газа вместо 8—12%-ного позволяет интен-
сифицировать процесс со 180—200 до 3000—3500 кг на 1 м3 на-
садки в сутки и снизить выбросы оксидов азота с 12—17 до
1 кг на 1 т моногидрата и менее [169]. При применении газа
концентрацией выше 60% мощность системы увеличится с 180
до 1550 тыс. т мнг в год. Но такое увеличение выпуска кисло-
ты потребует строительства нескольких кислородных станций,
что снижает технико-экономические показатели производства.
Ориентировочные технико-экономические показатели были рассчитаны
для производства, имеющего в своем составе одну типовую кислородную
станцию КТК-35-3, в котором в кислородно-воздушной среде проводится об-
жиг колчедана с получением 25%-ного газа, или сжигание серы — с получе-
нием 45%-ного газа, либо процесса ведется на 70%-ном в среде ретурного
газа. Основой для расчетов послужили испытания, проведенные в опытном
цехе филиала НИУИФ [170], которые показали, что в зависимости от ука-
занных выше концентраций сернистого газа иа базе оборудования цеха мощ-
ностью 360 тыс. т/год на колчедане выработка может быть увеличена до-
960 тыс. т/год на базе цеха мощностью 180 тыс. т иа сере — соответственно
до 450 и 775 тыс. т/год.
С учетом затрат на расширение складов сырья и готовой продукции, на-
сосного оборудования и холодильников перевод производства на 25%-ный газ
при работе на колчедане потребует дополнительных капитальных вложений
в размере 44,4% от стоимости оборудования, зданий и сооружений объектов
основного производства типовой схемы, прирост выработки составит 167%, на
сере при 70%-иом газе — капитальные вложения увеличатся на 76%, а при-
рост выработки составит 330%.
Результаты расчетов приведены в табл. 54.
Таким образом, применение кислорода приведет к сниже-
нию удельных капитальных вложений тем в большей степени,
чем выше концентрации газа, снизятся себестоимость и приве-
денные затраты по основному производству.
278
V.4. ПОЛУЧЕНИЕ ПРОДУКЦИОННОЙ НИТРОЗИЛСЕРНОЙ
КИСЛОТЫ
Концентрированные безводные растворы нитрозилсер-
ной кислоты применяются в промышленности органического
синтеза, например, в производстве капролактама из толуола.
Чистая нитрозилсерная кислота при нормальных условиях представляет
собой белые гигроскопические кристаллы, расплывающиеся на воздухе, с тем-
пературой плавления 73 °C. Вполне устойчива лишь при растворении в без-
водной серной кислоте, в разбавленной кислоте она подвергается гидролизу
с образованием азотистой кислоты:
HNSO5 + НаО ч—H2SO4 + HNO2 + 8900 ккал (37 290 кДж)
Степень гидролиза не зависит от величины общей нитрозности при не-
больших ее значениях. При большой общей нитрозности (содержание окси-
дов азота в пересчете на П20з) выделяющаяся при образовании нитрозил-
серной кислоты вода снижает концентрацию серной кислоты, что в свою оче-
редь ведет к увеличению степени гидролиза. Степень гидролиза нитрозилсер-
ной кислоты при обычной температуре в зависимости от содержания H2SO4
в исходной кислоте имеет значения:
Содержание H2SO4, % . . 98 95 92 90 87 80 70 57
Степень гидролиза, % . . 1,1 40 7,3 12,4 19,4 27,7 49,8 100
С повышением температуры степень гидролиза увеличивается. Растворе-
ние кристаллической нитрозилсерной кислоты в водных растворах серной кис-
лоты происходит с поглощением тепла.
Нитрозилсерную кислоту (кристаллы или в виде концентрированных без-
водных растворов) можно получить двумя методами [164, 168]:
1. В двухстадийном процессе первоначально получают эквимольную
смесь оксидов азота (N2O3), которую в последующей стадии абсорбируют
концентрированными растворами серной кислоты или олеумом (эквимольную
смесь получают взаимодействием 35—65%-ных водных растворов HNO3 и
8-68% SO2).
Взаимодействие между реагентами описывается суммарным уравнением
NaO3 + 2H2SO4 + SO3 ---> 2HNSO5 + H2SO4
2. При непосредственном взаимодействии 100%-ных диоксида, серы и
азотной кислоты:
SO2 + HNO3 -—> HNSO5
Реакцию проводят при сильном охлаждении реагентов (до ±5 °C) или
с разбавлением реакционной смеси различными инертными растворителями,
так как взаимодействие нитрозилсерной кислоты с азотной может сопровож-
даться взрывом по реакции
HNSO5 + HNO3 H2SO4 + 2NO
ГЛАВА VI
ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ ИЗ ОТХОДЯЩИХ
ГАЗОВ МЕТАЛЛУРГИЧЕСКИХ ПРОИЗВОДСТВ [171—189]
U аряду с серой и колчеданом для производства сер-
* " ной кислоты используют отходящие газы цветной
металлургии в медной, свинцово-цинковой, алюминиевой и ни-
кель-кобальтовой промышленности. Цветная металлургия явля-
ется одним из значительных поставщиков серной кислоты в
274
СССР — около 24% от общего выпуска (с учетом использова-
ния серы для закрепления сернистых газов).
Характеристика отходящих газов цветной металлургии. В производстве
меди около 90% выпускаемой продукции приходится на долю пирометаллур-
гического способа [171]. Переработка медных концентратов, содержащих
15—40% серы, в большинстве случаев заключается в плавке сырья (часто
добавляют обжиг) и конвертировании штейнов. В процессе образуются боль-
шие объемы отходящих газов (например, 50—60 тыс. м3/ч, при высокой тем-
пературе (900—1300 °C) с содержанием пыли 20 -300 г/м3.
Концентрация SO2 в газах печи КС составляет 11—16%, шахтной печи —
4—6%, конверторов — 0—12% (в среднем 3—4%), отражательной печи —
0,5—2,5% [80]. Наибольшее количество сернистых газов (около 50%) с низ-
ким содержанием SO2 (менее 3—3,5%) образуется в медной промышленно-
сти при плавке сырья в отражательных печах и в никель-кобальтовой про-
мышленности (43%) при плавке руд в шахтных печах.
Концентрация SO2 в газах конверторов низкая и колеблется в широких
пределах вследствие периодичности процесса. Она снижается из-за подсосов
воздуха под напыльники. Эти газы иногда закрепляют газами от сжигания
серы в серосжигающих установках. Для снижения подсосов воздуха приме-
няют усовершенствованные напыльники и автоматические запорные устрой-
ства, что повышает содержание SO2 до 7—8%. Газы печей отражательной
плавки в большинстве случаев не используют из-за низкой концентрации SO2,
однако с применением воздушно-кислородного дутья концентрация SO2 воз-
растает [172], и это создает возможность переработки газов в серную кисло-
ту [173] (такой процесс осуществлен на заводе «Онахама» в Японии).
Внедрение процессов автогенной плавки сульфидов тяжелых цветных
металлов позволяет получать сернистые газы с содержанием до 80—90% S02
и 2—6% О2. На одном из комбинатов многие годы применяют автогенный
процесс кислородно-факельной плавки (КФП). Концентрированные сернистые
газы КФП проходят охлаждение и сухую очистку от пыли, где разбавляются
воздухом до 25—30% SO2, и после смешения с конверторными газами при
содержании 6—7% SO2 перерабатываются в серную кислоту по схеме оди-
нарного контактирования. Строительство второго комплекса КФП на этом
комбинате с новым сернокислотным цехом ДК и реконструкция существую-
щего сернокислотного цеха на ДК позволяют увеличить степень использова-
ния серы из газов от 60 до 95%. Проходят промышленную проверку процес-
сы автогенной плавки в жидкой ванне (ПЖВ), кислородно-электротермиче-
ский (КИВЦЭТ) взвешенной плавки (ВП) [174].
В производстве цинка применяют в основном гидрометаллургический
способ, в котором цинковые концентраты, содержащие в среднем 29—34% S.
обжигают в печах КС с применением дутья, обогащенного кислородом. От-
ходящие газы печей КС при использовании кислорода содержат до 10—12%
SO2 и 8—10% О2, а также 60—130 г/м3 пыли.
В производстве свинца как правило осуществляют спекание концентра-
тов с флюсами, шахтную плавку агломерата и рафинирование чернового свин-
ца. Сера на 80—85% удаляется во время обжига н спекания в агломераци-
онных машинах. При подаче дутья в агломашнну сверху отходящие газы со-
держат 2—2,5% SO2, при подаче дутья снизу—4—5% SO2, а при рециркуля-
ции части газов — 6—6,5% SO2 и 8 г/м3 пыли.
При освоении агрегатов КИВЦЭТ в свинцово-цинковой промышленности
возможно получение газов, содержащих 30—60% SO2, 5—15% СО2, 1—7%
О2, 3—4% Н2О, и 0,01—0,05% SO3 [175].
В производстве никеля и кобальта руду плавят в шахтных печах, кон-
вертируют на файнштеин, который обжигают и выплавляют никель в элект-
ропечах. Около 60% серы, содержащейся в шихте, выделяется в газы, со-
держащие до 0,2% SO2. Конверторные газы, содержащие 2—2,5% SO2 (а при
внедрении совершенных иапыльников и дросселей — 3—4% SO2), в ряде слу-
чаев перерабатывают в серную кислоту, однако уровень использования серы
остается весьма низким. При освоении агрегата непрерывного конвертирова-
ния (АНК) возможно получение газа содержащего 6,2—11,2% SO2 [174].
280
В производстве алюминия из бокситов, содержащих менее 1% S, образу-
ются низкоконцентрнрованные сернистые газы, которые не используются.
При обжиге и восстановлении алунитов серой газы содержат: 24% SO2,
3,5% О2, 11% Н2О, 2,5% СО2, 59% N2. При сухой очистке эти газы разбав-
ляются до 7—8% SO-. и поступают в сернокислотный цех. Газы от печей
спекания при мокром способе подачи шихты и подсосе воздуха в печь содер-
жат до 1% SO2 [176]. Возможно эффективное обогащение этих газов для
последующего получения серной кислоты [177].
В производстве олова, молибдена, вольфрама, ртути и некоторых других
тяжелых цветных металлов также возможно перерабатывать сернистые га-
зы, хотя объемы их выпуска во много раз уступают объему выпуска таких
продуктов, как медь, цинк, свинец.
Обжиг сульфидного сырья в кипящем слое повышает интенсивность про-
цесса и концентрацию SO2, но увеличивает запыленность обжигового газа.
Во многих случаях пыль газов в цветной металлургии (например, содержа-
щая свинец) труднее улавливается, чем колчеданная. Это повышает опас-
ность забивания газоходов от металлургических агрегатов до сернокислотно-
го цеха сульфатами, шламом, конденсатом серной кислоты.
Содержание триоксида серы и паров серной кислоты в отходящих газах
может изменяться в широких пределах вследствие разнообразия металлурги-
ческих процессов, типов печей, составов сырья. В автогенном процессе на
влажной шихте (ПЖВ) отходящие газы могут содержать до 30% влаги
(против примерно 6% Н2О в газах от обжига колчедана), что повышает тем-
пературу коррозионно-безопасного уровня газоохладителя примерно на 30 °C,
повышает отложение в газоходах сульфатов, затраты на сухую и мокрую
очистку.
Отходящие газы цветной металлургии содержат в своем составе много
примесей, в их числе рассеянные редкие элементы — рений, селен, германий,
теллур, галлий, индий, таллий, благородные металлы — золото, серебро, пла-
тину, извлечение которых имеет большое народнохозяйственное значение.
Вместе с тем, имеются и примеси, которые отравляют ванадиевый катализа-
тор, увеличивают содержание твердого остатка в промывных кислотах, из-
меняют цвет товарной серной кислоты, оказывают интенсивное коррозионное
воздействие на оборудование. Газы содержат такие примеси в следующих
концентрациях, мг/м3: As — до 30, F — 20—50, Se—10—20, Hg—10—15;
сульфаты и окислы Zn, Pb, Си, Cd, Fe 0,2—0,6 г/м3, органические вещества
0,1—0,3%. В газах иногда содержится до 2 г/м3 As и до 0,5 г/м3 F.
Производство серной кислоты в цветной металлургии.
В цветной металлургии основная задача заключается в получе-
нии цветных металлов, а сернистые газы являются только по-
путным продуктом. Получаемая серная кислота примерно на
20% расходуется в цехах электролиза и для других нужд пред--
приятий, выпускающих цветные металлы, а стоимость серной
кислоты намного меньше стоимости основной продукции — ме-
талла. Это обстоятельство длительное время приводило к недо-
статочному вниманию со стороны металлургов, к качеству сер-
нистого газа (по составу) и объему его использования для
производства серной кислоты. Требования экономики, охраны
природы и материальное стимулирование в значительной мере
способствуют увеличению заинтересованности металлургов в
выпуске серной кислоты.
Перед непосредственным поступлением в сернокислотное
производство отходящие газы проходят систему охлаждения и
пылеочистки в металлургических пределах. Для такой подго-
товки газов устанавливают котлы-утилизаторы, пылевые каме-
ры, циклоны, рукавные фильтры и др.
281
Во многих случаях пыль содержит большой процент цветных, редких и
благородных металлов и поэтому является оборотной. При высокой эффек-
тивности аппаратов пылеулавливания возможно селективное разделение и
извлечение указанных металлов.
Сернокислотные цеха в цветной металлургии имеют более
низкую мощность, чем в промышленности удобрений, что свя-
зано с необходимостью бесперебойной переработки поступаю-
щего газа круглый год при наличии резерва мощности, а так-
же ремонтов оборудования.
Особенностью производства серной кислоты из газов цвет-
ной металлургии является его зависимость от режима метал-
лургического передела. Несмотря на непрерывное ведение ме-
таллургических процессов (конвертора работают поочередно,
по графику) объемы газов, поступающих в сернокислотный
цех, не стабильны, запыленность и концентрация SO2 изменя-
ются в значительно более широких пределах, чем в автоном-
ных сернокислотных цехах. Для устойчивого ведения техноло-
гического режима получения серной кислоты широкие колеба-
ния входных параметров нежелательны, так как могут вызы-
вать ряд отрицательных явлений. Например, при снижениях
концентраций возможно переохлаждение нижних слоев катали-
затора и потеря его активности. Низкая и нестабильная кон-
центрация SO2 в конверторных, агломерационных и других
газах приводит к нарушению автотермичности контактного уз-
ла и необходимости работы с подогревом, создает напряжен-
ность теплового баланса и затруднения повсеместному внедре-
нию процесса ДК.
Для создания устойчивости в работе и повышения эффектив-
ности сернокислотных производств необходимо расширение
внедрения автогенных процессов с получением концентрирован-
ных сернистых газов, строительство силосов накопления огарка
для стадии электролиза при капитальных ремонтах обжигового
цеха, оснащение металлургических агрегатов эффективными
газоохлаждающими и газоотводящими системами, устраняющи-
ми разбавление газов атмосферным воздухом, улучшение сухой
и мокрой очистки газов от пыли и вредных примесей и др.
Полная технологическая схема производства серной кислоты
при работе на колчедане или отходящих газах металлургиче-
ских производств не имеет принципиальных отличий, но в цвет-
ной металлургии склад сырья, подготовка, обжиг концентрато-
ров и пылеулавливание как правило обслуживаются персоналом
металлургического передела.
Поступающие в сернокислотный цех после сухой очистки га-
зы проходят промывное, контактное и сушильно-абсорбционное
отделения. При схеме одинарного контактирования выхлопные
газы должны проходить также химическую очистку. В схемах
ДК требования, предъявляемые к промывному отделению, такие
же, как в схемах одинарного контактирования, а химическая
очистка выхлопных газов не требуется. На рис. 92 показана
282
схема классической сернокислотной системы цеха, работающего
на отходящих газах медеплавильного завода.
Отходящие газы при температуре 180—250 °C поступают в промывное
отделение и Поспелова гельно проходят Фообашню. первую промывную баш-
ню. первую ступень мокрых электрофильтров МП-12. вторую промывную
башню и вторую ступень мокрых электрофильтров МСШ. Форбашня и пер-
вая промывная башня полые, вторая промывная башня с насадкой. В про-
мывном отделении ввиду присутствия фтора применяют «водный» режим про-
мывки газа. Форбашия работает в испарительном режиме при концентрации
кислоты 10—15% H2SO4. Вытекающая из форбашни кислота проходит сгу-
ститель и поступает в сборник, откуда насосом подается на орошение. Вы-
текающая из первой промывной башни кислота проходит отстойник и посту-
пает в сборник, откуда насосом через оросительные холодильники подается
на орошение. Из отстойника и сгустителя шлам выпускают в приямок, а от-
туда в ливненакопителн. Циркуляция кислот на второй промывной башне
осуществляется также, как и иа первой.
Промывное отделение цеха состоит из 4 самостоятельных параллельных
систем, идентичных по оборудованию. Промывная кислота концентрацией
10—15% H2SO4 с высоким содержанием вредных примесей является нестан-
дартным продуктом и сбрасывается на очистные сооружения. После отстаи-
вания в ливненакопителях очистных сооружений промывную кислоту нейтра-
лизуют известковым молоком, а частично передают на кучное выщелачива-
ние. Осадок в виде шламов периодически отгружают на свинцовый завод.
После промывного отделения газ поступает на осушку в сушильно-аб-
сорбционное отделение цеха, состоящее нз 2 параллельных ниток оборудова-
ния. Газ проходит первую и вторую сушильных башни и брызгоуловитель,
а затем поступает в контактно-компрессорное отделение, где установлено
3 нагнетателя, в том числе один резервный. После нагнетателя газ проходит
фильтр-брызгоуловитель и нагревается в 3 внешних теплообменниках и
2 внутренних теплообменниках контактного аппарата и поступает на I слой
катализатора. Охлаждение газа после I слоя осуществляется за счет подду-
ва части более холодного газа, после II слоя — на одном из наружных теп-
лообменников, а после III и IV — во внутренних теплообменниках. После
V слоя газ охлаждается в 2 наружных теплообменниках и ангидридном хо-
лодильнике, проходит олеумный и моногидратный абсорберы, брызгоулови-
тель и выхлопные газы выбрасываются через трубу в атмосферу.
Производительность каждого из четырех контактных аппа-
ратов составляет 270 т/сут (100% H2SO4), газовая нагрузка до-
стигает 40—45 тыс. м3/ч. Содержание SO2 перед контактным
аппаратом по проекту 7,5%, а практически колеблется довольно
Таблица 55. Показатели работы контактного аппарата
Показатели Слой и тип катализатора
форслой (БАВ+СВД) и слой I (СВС) слой II (СВД) Слой III (СВД+СВС б. у.) Слой IV (БАВ) слой V (СВС)
Температу- ра, °C Степень превраще- ния, % 435—566 75,5* 475—540 87,5—88,0 440—469 96,7—96,9 435—440 97,6—97,9 435—425 98.0—98,4
* Степень превращения рассчитана по температурному режиму.
283
РИС. 92. Схема сернокислотной системы с одинарным контактированием, ра-
1— форбашня; 2 — I промывная башня; 3 — 1 ступень электрофильтров; 4— II промывная
вители; 9, 10 — олеумныи и моногидратный абсорберы; 11 — контактный аппарат; 12—
17 — нагнетатель; 18 — теплообменники.
значительно, и при ремонте печи КФП цех работает на конвер-
торном газе с содержанием около 3% SO2. В табл. 55 приведе-
ны показатели работы контактного аппарата при содержании в
газе 5,5—6% SO2 и 17—18% О2, удельный расход катализатора
составляет 290 л/(т-сут).
Очистка газов от мышьяка и фтора. В промывном отделении
газ очищается от пыли, сернокислотного тумана, вредных при-
месей, (мышьяк, фтор и др.) и из него извлекают ценные ком-
поненты (рений, селен и др.). Для мокрой очистки отходящих
газов, как и для абсорбции SO3, широко используют полые и
насадочные башни. При повышенном содержании в отходящих
газах пыли и вредных примесей скорость газа в промывных
башнях снижают от 0,8—1,0 до ~0,5 м/с, устанавливают до
3 башен, иногда рекомендуют три ступени мокрых электро-
фильтров. Каждая башня орошается «на себя», а избыток кис-
лоты передается в сборник предыдущей башни, куда стекает и
конденсат мокрых электрофильтров. В сборник последней баш-
ни добавляется вода. Технологический режим промывного от-
деления по температурам отходящих газов и кислот такой же,
как и на газах от обжига колчедана, а концентрация кислот в
среднем ниже, так как для улавливания примесей часто приме-
няют так называемый режим водной промывки (5—15%
H2SO4).
Примеси мышьяка и селена частично растворяются в про-
мывной кислоте, но в основном переходят в состав сернокислот-
ного тумана и улавливаются в мокрых электрофильтрах. Содер-
жание мышьяка в растворах промывного отделения может до-
284
ботающей на отходящих газах медеплавильного производства:
башня; 5—II ступень электрофильтров; 6, 7 — I и II сушильные башни; 8 — брызгоуло-
сгуститель; 13— отстойник; 14— сборники; 15 — насосы; 16— ангидридный холодильник;
стигать 1 °/о As2O3, что вызывает его кристаллизацию, а при не-
достаточной очистке газа мышьяк отравляет ванадиевые ката-
лизаторы. Срок службы, сернокислотных катализаторов на от-
ходящих газах в 1,5—2 раза меньше, чем на газах от обжига
колчедана [178].
Если при обжиге колчедана содержание фтора в газах перед
промывным отделением составляет всего 8—20 мг/м3, то в сме-
си газов КФП и конверторов — 50—80 мг/м3, а на выходе из пе-
чи КФП— до 500 мг/м3, так как внедрение автогенных процес-
сов повышает не только концентрацию диоксида серы, но и его
примесей. Фтор оказывает коррозионное воздействие на мате-
риалы, разрушает керамическую футеровку газоходов, башен и
насадку (что требует применения дорогостоящей углеграфито-
вой футеровки), при попадании его в контактный аппарат про-
исходит отравление и разрушение катализатора, сопровождаю-
щееся ростом сопротивления. При содержании в газе перед кон-
тактным аппаратом более 3 мг/м3 фтора катализатор требует-
ся заменять ежегодно.
При концентрациях HF в газе менее 1,5—2 г/м3 максималь-
ная концентрация фтора в жидкой фазе не превышает 1%, а
парциальное давление его над такими растворами очень мало.
Поэтому введение химических реагентов в поглотитель не ока-
зывает существенного влияния на скорость абсорбции [88].
Следовательно, при низких концентрациях фтористых соедине-
ний скорость химического взаимодействия их с водой не лими-
тирует скорость абсорбции, а добавление реагентов (Ыа2СОз>
NaSO4, K2SO4 и др.) малоэффективно и требует дополнитель-
285
ной аппаратуры для выделения образующихся гелевидных
осадков (если F не связан в SiFe~ осадок не выпадает).
Температура слабо влияет на скорость абсорбции фтори-
стых соединений. Повышение температуры в 4 раза приводит
к увеличению коэффициента массопередачи всего в 1,2 раза. Од-
нако с повышением температуры возрастает давление паров
фтористых соединений над растворами, например с повышени-
ем температуры от 40 до 60 °C парциальное давление HF над
5%-ной фтористоводородной кислотой возрастает в 3 раза [12],
поэтому в целом абсорбцию целесообразно осуществлять при
более низких температурах.
Увеличение контакта фаз, путем повышения активной высо-
ты полых абсорберов до 6—8 м улучшает очистку газов от HF,
но дальнейшее увеличение этой высоты влияния не оказывает
[88].
Растворимость HF достигает минимума при 93% H2SO4, а
SiF4 поглощается серной кислотой с концентрацией не более
63% H2SO4 [88]. Растворимость смеси HF и SiF4 в растворах
серной кислоты улучшается при снижении ее концентрации и
температуры. SiF4 и HF хорошо растворимы в воде. Поглоще-
ние SiF4 водой возможно по следующим реакциям:
SiF4 4- Н2О «=> 4HF 4- SiO2
4HF + 2SiF4 <—> 2H2SiF6
3SiF4 4- 2H2O 4^7» 2H2SiF6 + SiO2
Наибольшее повышение степени очистки таких газов от фто-
ра возможно путем увеличения поверхности контакта фаз и
улучшения гидродинамических условий абсорбции. При нали-
чии в системе трех промывных башен, вторую и третью целесо-
образно загружать насадкой из колец Рашига или Инталокс
100X100 мм.
В абсорберах распиливающего типа очистку газов водой
можно интенсифицировать за счет увеличения степени дробле-
ния жидкости и повышения плотности орошения. При умень-
шении диаметра капли от 4,2 до 2,4 мм концентрация HF в
капле возрастает в 3—4 раза. Для этой цели необходимо при-
менять форсунки с большой поверхностью разбрызгивания
жидкости, например центробежные, фторопластовые (или поли-
этиленовые) с наклонными прорезями, чем достигается увели-
чение доли смоченной поверхности и равномерность распреде-
ления жидкости.
Плотность орошения в распиливающих абсорберах на неко-
торых старых заводах составляет 5—10 м3/(м2-ч), однако при
таких низких нагрузках очистка газов затрудняется. Плотность
орошения промывных башен целесообразно увеличивать до 20—
30 м3/(м2-ч), что значительно улучшает качество промывки га-
за, уменьшает вероятность проскока части газа вне контакта
с жидкостью. Плотность орошения достаточна, если разность
286
температур выходящего из башни газа и орошающей жидкости
не превышает 1—2 °C.
Значительный опыт очистки фтористых газов накоплен в
алюминиевой промышленности, где широко применяется как
сухая очистка — через слой глинозема с возвратом его в произ-
водство алюминия [181], так и мокрая — водой, например в
скруббере с ситчатыми тарелками норвежской фирмы «Электро-
кемикс».
Очистка промывной кислоты. Промывные кислоты сернокис-
лотных цехов заводов цветной металлургии — один из основных
источников загрязнения сточных вод мышьяком, ртутью, цин-
ком, селеном, хлором, фтором и другими примесями, наиболее
опасной из которых является мышьяк. Проблема очистки про-
мывных кислот от мышьяка осложняется необходимостью ути-
лизации ценных компонентов кислоты — рения, селена, кадмия,
меди, цинка и др. Рений при промывке газов переходит в рас-
твор серной кислоты, и затем извлекается из этого раствора по
специальной технологии. Селен, содержащийся в газе в виде
SeO2, растворяется в промывной кислоте, образуя селенистую
кислоту НгЗеОз, которая на специальных установках восстанав-
ливается диоксидом серы до металлического селена.
Фильтрация промывной кислоты с извлечением ценных ком-
понентов имеет важное значение для улучшения условий очист-
ки газов, снижения забивки аппаратуры и газоходов, уменьше-
ния их коррозии и эрозии, получения кондиционной серной кис-
лоты (по примесям) при последующем закреплении ее до то-
варной продукции. (В некоторых случаях промывную кислоту
сбрасывают на очистные сооружения и дополнительно расходу-
ют нейтрализующие реагенты.)
Фильтрация промывной кислоты освоена на одном из нике-
левых заводов на свечевых фильтрах с выделением цинка и
кадмия и полным использованием промывной кислоты в цехе
электролиза никеля. На одном пз медеплавильных заводов ос-
воена установка извлечения шлама на автоматическом фильтр-
прессе ФПАКМ (35% влаги). Высокая производительность
фильтра (по фильтрату 10 м3/ч) и возможность полной автома-
тизации позволили рекомендовать его в качестве базового для
сернокислотных цехов [182].
По пиролюзитному методу очистки промывных кислот трех-
валентный мышьяк окисляют до пятивалентного с образовани-
ем арсенатов марганца, которые осаждают известковым моло-
ком, а кеки с содержанием 5—7 As и других примесей направ-
ляют на захоронение. В промышленности применяют комбини-
рованный сульфидно-пиролюзитный метод очистки кислоты от
мышьяка. В присутствии SO2 кислоту очищают раствором
сульфидов натрия с образованием нерастворимого и неядови-
того сульфида мышьяка. Организация извлечения мышьяка из
кислот может быть ускорена при использовании его для нужд
народного хозяйства.
287
РИС. 93. Схема сернокислотной системы с двойным контактированием, ра-
/— труба Вентури; 2— II промывная башня; 3 — электрофильтры; 4 — сушильная баш-
бер; 8 — газодувка; 9 —- теплообменники; 10— контактный аппарат; 11— отстойник; 12 —
Эффективно применение упарки промывных кислот. При
этом отгоняется хлор и фтор, а в осадок выпадают арсенаты
цинка и железа, и повышается концентрация серной кислоты.
Для упарки промывных кислот возможно использование тепла
выхлопных газов. В некоторых случаях целесообразно промыв-
ной кислотой увлажнять пылящие концентраты, В настоящее
время разрабатывается ионообменная очистка промывных кис-
лот. В практике все же наиболее широко применяется нейтра-
лизация промывных кислот известковым молоком с выделени-
ем осадка CaSO4.
Аппаратура промывного отделения. В промывных отделени-
ях используется разнообразная аппаратура, изготовленная из
титана, свинца, антегмита, полиизобутилена, фаолита, полиэти-
лена, винипласта и других материалов. В последние годы ис-
пытан новый мокрый электрофильтр типа БВК (без влияния
кромок), производительность которого в 3 раза больше обыч-
ных мокрых электрофильтров, а габариты в 5 раз меньше [186].
Важным фактором интенсификации улавливания примесей
является замена устаревшего абсорбционного оборудования бо-
Таблица 56. Показатели работы абсорберов для очистки
фторсодержащих газов
Абсорбер Эффектив- ность очист- ки, % Скорость га- за, м/с Сопротив- ление, Па Производи- тельность по газу, тыс. м3/ч
Распиливающий полый 50—70 0.47—0,53 200—300 30—40
Распиливающий наса- 70—80 0,47—0,53 300—500 0,47—0,53
д ОЧНЫЙ
Вентури 85 40—51* 900—1600 59—64
АПН (1 с 2-мя слоями) 95—99,6 3,5—4,5 1400—1960 25—32
Абсорбер ГДР (1 с 4-мя 90—94 2.0 1500 10—40
тарелками)
Скруббер Дойля 75—85 15—30** 1300—1500 10—50
* В горловине. *’ На выходе из сопла.
ботающей на отходящих газах медеплавильного производства в США:
ня; 5 — отдувочная башня; 6 — двухступенчатый аппарат Вентури; 7 — конечный абсор-
ороснтельные холодильники; 13 — сборники; 14— кожухотрубчатые холодильники.
лее эффективным. В табл. 56 приведена сравнительная характе-
ристика существующих и разрабатываемых аппаратов для улав-
ливания фтористых соединений.
Все действующие абсорберы имеют сравнительно низкую эффективность
(степень очистки 50—85% на один аппарат) и установка того или иного ап-
парата диктуется обычно его надежностью. Наиболее распространенным кон-
структивным недостатком распыливающих абсорберов является неравномер-
ность распределения газа по сечению колонны, что подтверждается замерами
температур на наружной поверхности, где перепад по сечению башни состав-
ляет 5—8 °C.
Среди разработанных абсорбционных аппаратов для промывки газов ка-
чественно выделяется абсорбер с плавающей насадкой (АПН), у которого
коэффициент массопередачи равен 40000—50 000 ч-1, благодаря чему в од-
ном аппарате с двумя слоями достигнута степень очистки 95—99,6%. АПН
широко применяется за рубежом и в нашей стране принят к широкому внед-
рению для очистки фтористых газов в производстве удобрений [179].
Пенные абсорберы, аппараты Вентури, APT отличаются повышенными
сопротивлением и брызгоуносом, либо узким диапазоном рабочей скорости
газа. Однако имеется положительный опыт использования аппарата Вентури
на одном из металлургических заводов в нашей стране [180] и во многих
производствах за рубежом, поэтому необходимо изучать возможность рас-
ширения области применения этого аппарата.
На работу абсорбера большое влияние оказывает присутствие твердых
частиц в газах и образование осадков — шлама. Повышенная запыленность
газов, поступающих в промывное отделение, приводит к эрозии кислотоупор-
ной футеровки газоходов и аппаратов, насадки, забиванию форсунок, нерав-
номерному распределению жидкости и газа. Во многих случаях установки
фильтрации промывной кислоты в сернокислотных производствах не освое-
ны, а содержание фтора в промывной кислоте не нормируется и превышает
1 г/л. Тогда резко возрастает коррозия свинца.
По проекту фирмы «Лурги» в СССР пущена сернокислотная
система ДК с очисткой газа в абсорберах Вентури и башне с
кремнийсодержащей насадкой для частичного связывания фто-
ра химическим путем.
Метод ДК. На заводах цветной металлургии в сернокислот-
ных цехах все шире внедряется метод ДК. На рис. 93 приведе-
на схема ДК (с вариантом слоев 2+2) на отходящих газах
медеплавильного производства, пущенная в эксплуатацию в
США в 1974 г. по разработкам фирмы «Лурги» [175]. Произ-
водительность установки по газу 200 тыс. м3/ч.
19—584
289
РИС. 94. Схема контактного узла с аппаратом КЦТ системы электроцинко-
вого завода:
1 — выносные теплообменники I стадии процесса; 2 — спиральный теплообменник; 3 —
контактный аппарат КЦТ; 4 — выносные теплообменники II стадии процесса; / — слои
катализатора.
В качестве I промывной башии применяют трубу Вентури, иа II стадии
абсорбции — двухступенчатый аппарат Веитури. Отдувка SOa из промывной
и сушильной кислот проводят в башнях. В промывном отделении установле-
ны высокоскоростные компактные электрофильтры и оросительные холодиль-
ники. В сушильио-абсорбционном отделении кислоту охлаждают в кожухо-
трубчатых холодильниках. Брызги улавливают в брызгоуловителях, встроен-
ных в башни, а после промежуточной абсорбции — в слое насадки «Инталокс»
высотой 2 м. Автотермичиость процесса обеспечивается при повышенной тем-
пературе промежуточной абсорбции. Основные операции автоматизированы.
В нашей стране система ДК впервые была пущена в экс-
плуатацию на отходящих газах одного из заводов цветной ме-
таллургии в 1973 г. В 1979 г. после реконструкции все 5 сер-
нокислотных систем этого завода были переведены на схему
ДК. На 1-й и 2-й системах использован контактный аппарат
типа К-39-5, на 3—5-й — типа КЦТ. Схема контактного узла
этой системы приведена на рис. 94.
Диоксид серы после нагнетателя направляют в межтрубные пространст-
ва двух выносных теплообменников после III слоя катализатора, а затем
через трубки верхнего теплообменника подают иа I слой контактного аппа-
рата КЦТ. После II и III слоев газ охлаждают в трубках теплообменников
и направляют на I стадию абсорбции. После I стадии абсорбции газ нагрева-
ют в выносных теплообменниках II степени, спиральном теплообменнике,
межтрубном пространстве иижнего теплообменника КЦТ и направляют иа
IV и V слои катализатора. После V слоя газ охлаждают в выносных тепло-
обменниках и направляют на II стадию абсорбции.
Контактный аппарат диаметром 8 м и высотой 18 м перерабатывает
27—28 тыс. м3/ч с содержанием 6—9% SO2 в автотермичиом режиме — без
дополнительного подогрева. Степень превращения составляет 99,6—99,8%,
удельный расход катализатора 273 л/(т-сут) [184].
При окислении SO2 иа II стадии катализа значения оптимальных темпе-
ратур увеличиваются с повышением концентрации кислорода, а при измене-
290
иии содержания SOs сохраняются на прежнем уровне [183]. На II стадии
катализа количество катализатора, рассчитанное по кинетическому уравне-
нию, рекомендуется увеличивать для I слоя в 1,5 раза и для II слоя —
в 2 раза [126]:
Для систем ДК, которые работают на отходящих газах, со-
держащих 9—12% SO2 и 11,5—9% О2, оптимальный вариант
слоев 44-1. При этом для газа, содержащего 12% SO2, газ меж-
ду III и IV слоями катализатора охлаждают воздухом для по-
вышения скорости окисления. Для 9%-ного SO2 подача воздуха
прекращается, III и IV слои работают как один, и схема аппа-
рата преобразуется в 34-1. Количество катализатора рассчиты-
вают на 12%-ный SO2, а поверхность теплообменников — на
9%-ный SO2.
Ниже приведен оптимальный технологический режим работы
контактного аппарата для переработки отходящих газов цвет-
ной металлургии с различным содержанием диоксида серы и
кислорода по схеме ДК [484].
1 стадия катализа
Исходный состав газа 12%SO„ 9%О. 9%SO,, 11,5%О,
Слой I хк 0,55—0,47 0,707
Тк-Тк 410—437—590 420—598
Слой II Хк 0,731 0,874
Гн-Тк 470—557 480—522
Слой III Хк 0.801 0,910
Тн-Тк 501—524 480—489
Слой IV хк 0,932 0.901
Тя-Тк 433—475 480—489
У- 0,21
II стадия катализа
Исходный состав газа 0,8%S08,7,5%02 0,9SO«, 8,4 % О-
Слой V Хк 0,971 0 978
Ти-Тк 427—450 396—423
Уг 1,04 0,877
Здесь х к—конечная степень превращения, доли; Т н и Т к — начальная и конечная
температура, °C; у в'л у г—доля воздуха (40 °C) и газа.
Особенности эксплуатации контактного узла. При окислении
диоксида серы отходящих сернистых газов в контактный аппа-
рат попадают примеси, отравляющие ванадиевый катализатор.
В контактных массах во всех слоях обнаруживают мышьяк,
фтор, селен, ртуть, сульфаты и окислы цинка, свинца, меди, кад-
мия, железа. Механизм воздействия на катализатор мышьяка и
фтора такой же, как и при окислении газов от обжига колчеда-
на. Сульфаты и окислы цинка и меди снижают активность ка-
тализаторов, образуя двойные соли типа MeSC^-^SC^. Приме-
си газа также механически экранируют поверхность зерен ка-
тализатора при их адсорбции, капиллярной конденсации или
осаждения в порах, затрудняя доступ реагирующих веществ к
активным центрам.
19*
291
Недостаточная очистка газов при повышенном содержании
примесей часто является причиной существенного снижения
степени превращения диоксида серы в контактном аппарате.
Наибольшему воздействию примесей подвергается первый по
ходу газа слой катализатора. Для снижения воздействия вред-
ных примесей реакционной смеси на I слой в контактном аппа-
рате целесообразно устанавливать форслой отработанного ката-
лизатора, что увеличивает срок службы I слоя и тепловую
устойчивость контактного узла [126].
Наибольшей коррозии подвергается теплообменник, распо-
ложенный первым по ходу газа после первой стадии адсорбции.
Для защиты от сернокислотной коррозии громоздких (с пло-
щадью поверхности до 5000 м2) и дорогостоящих теплообмен-
ников после промежуточной стадии абсорбции специалисты од-
ного из алюминиевых заводов разработали и установили паро-
газовый фортеплообменник, включив его в паровую схему кот-
ла-утилизатора. Фортеплообменник с площадью поверхности
нагрева 114 м2 собран из стальных спиралей (сталь 20) котла-
утилизатора (диаметр труб 45X4,5 мм) и обеспечивает нагрев
технологического газа от 80 до 160—180 °C, т. е. до коррозион-
но безопасного уровня. Давление пара на входе в форподогре-
ватель 343,2 кПа, температура 260 °C. Установка парогазового
фортеплообменника перспективна и для других систем, так как
его работа более надежна по сравнению с газовыми теплооб-
менниками или рекуператорами.
Компоновка контактного узла (расположение теплообмен-
ников, газоходов, компенсаторов, дросселей, смесителей) суще-
ственно влияет на распределение газовых потоков, степень
превращения, размер капитальных вложений. Высокая эффек-
тивность работы контактного аппарата может быть достигнута
лишь при создании необходимых условий для равномерного
подвода, распределения и отвода газового потока, при подборе
соответствующих распределительных устройств. Например, в
контактном аппарате при выходе потока из слоя со стороны,
противоположной входу, распределение потока будет равномер-
нее, чем при выводе потока со стороны входа. При входе и вы-
ходе газа с одной стороны для улучшения равномерности рас-
пределения газа внутри аппарата необходимо установить рас-
пределительные короба.
Для тепловой устойчивости контактного узла важное значе-
ние имеет качество теплоизоляции. Присоединение к корпусу
контактных аппаратов площадок, лестниц, лифтов, штырей для
крепления изоляции и других металлических элементов намно-
го увеличивает тепловые потери. Практически теплопотери ча-
сто превышают проектные нормы в 1,5—3 раза и достигают
12,6—21,0 ГДж/(м2-ч) [300—500 ккал/(м2-ч)]. Для наружной
теплоизоляции необходимо использовать более качественную
минеральную вату — прессованные маты, применять их уклад-
ку с перекрытием швов при общей толщине изоляции контакт-
292
ного аппарата до 500 мм. Целесообразно заменить крепление
изоляции со штырями на бандажное, а площадки устанавли-
вать на опоры, не примыкающие к корпусу аппарата.
Для повышения эффективности работы огневых подогрева-
телей целесообразно подключать к ним два теплообменника,
что способствует снижению температуры выбрасываемых то-
почных газов до 100—150 °C. На некоторых комбинатах уста-
новлены электрические подогреватели, эффективность работы
которых на газе с низкой (и часто колеблющейся) концентра-
цией SO2 выше, чем огневых. Электрические подогреватели
вводятся в работу за 30—40 мин и работают длительное вре-
мя при содержании в газе 1,5—2% SO2 без остановки контакт-
ных аппаратов. Электроподогреватель сравнительно небольшой
мощности (800 кВт) может обеспечить нагрев 50 000 м3/ч газа
на 30 °C [185].
Пусковой подогреватель предназначен для пуска и остановки систем, од-
нако при низкой или колеблющейся концентрации SO2 его часто включают
на постоянную работу, что приводит к большим затратам топлива при низ-
кой степени использования тепла (примерно 50%) в результате высокой тем-
пературы выбрасываемых газов (300—350 °C).
Экономика производства. Получение серной кислоты из от-
ходящих газов является высокорентабельным производством.
В табл. 57 показана структура цеховой себестоимости 1 т сер-
ной кислоты ряда медеплавильных заводов, в которой основ-
ными слагаемыми являются затраты на сырье (сера в газах),
расходы на содержание и эксплуатацию оборудования и цехо-
вые расходы.
Себестоимость серной кислоты существенно зависит от ви-
да и стоимости перерабатываемого сырья (табл. 58). В этом
аспекте использование газов цветной металлургии экономиче-
ски более эффективно, так как стоимость 1 т серы в отходящих
газах в среднем примерно в 4—7 раз ниже, чем в колчедане и
природной сере. Однако пока в цветной металлургии для по-
лучения серной кислоты используют не более 40% диоксида
серы, выделяющегося при металлургическом переделе [188].
Таблица 57. Структура себестоимости (в %) серной кислоты
на отдельных медеплавильных заводах
Статьи затрат 1-й вариант 2-й вариант 3-й вариант
Сырье (стоимость газа) 53 18,5 25
Вспомогательные материалы 7 2,5 1.1
Энергетические затраты 9 14,3 24
Зарплата 2 4 4,4
Расходы по содержанию и эксплуа- тации оборудования 20 46 32
Цеховые расходы 9 14,7 13,6
Цеховая себестоимость 100 100 100
293
Перспективы развития цветной металлургии тесно связаны с
увеличением полноты и комплексности использования сырья,
уменьшением загрязнения окружающей среды, созданием ма-
лоотходной технологии всего производства, включая и серно-
кислотное. Для решения этих задач необходимо совершенство-
вание существующих и разработка новых процессов и оборудо-
вания металлургического передела, пылеулавливания и произ-
водства серной кислоты. Например, внедрение автогенной плав-
ки и непрерывного конвертирования котлов-утилизаторов,
совершенных напыльников, скоростных электрофильтров, газо-
плотного оборудования и коммуникаций позволяет повысить
степень извлечения серы в серную кислоту.
При добавлении к газам автогенной плавки конвертерных
газов (или воздуха) до соотношения O2:SO2=1, можно полу-
чить смесь, содержащую не более 16% SO2 и перерабатывать
ее в серную кислоту по прямоточной многоступенчатой схеме,
без дополнительного применения кислорода [189]. Методы
двойного и тройного контактирования, циркуляционные и ком-
бинированные схемы при использовании кислорода, повышен-
ного давления, кипящего слоя, тепла ВЭР, специальных ката-
лизаторов позволяют повысить эффективность переработки
концентрированных газов автогенной плавки при получении
серной кислоты, а также высокочистых серосодержащих про-
дуктов— 100%-ного SO3, жидкого SO2 и серы.
В конце 60-х годов были проведены полупромышленные испытания сер-
нокислотной системы, по переработке газов автогенной плавки. Газы авто-
генной плавки с содержанием 75—85% SO2 после сухой и мокрой очистки
(по типовой схеме) через электроподогреватель подавали в контактный узел,
куда добавляли воздух или кислород. Контактный узел был оборудован ап-
паратами с кипящими слоями катализатора.
Испытания подтвердили принципиальную возможность и эффективность
переработки высококонцентрированных сернистых газов автогенной плавки.
Степень превращения SO2 при концентрации 12—20% SO2 на одном слое со-
ставила 70—80%, при 29—49% SO2 на трех слоях достигнута степень пре-
вращения 70—90% и на пяти слоях 95—96%. С повышением концентрации
SO2 до 45% оказалось возможным снижать температуру на входе в кипящий
слой до 60 °C.
Направление по переработке газов автогенных металлургических процес-
сов в серную кислоту изучается и за рубежом. Расчетные данные фирмы
«Норд Дойче Аффинери» (ФРГ) показывают снижение капитальных вложе-
ний и эксплуатационных затрат при переработке в серную кислоту концент-
рированных газов медеплавильного завода производительностью (по меди)
100 тыс. т/год [189]. При повышении концентрации SO2 в интервале 10—16%
Таблица 58. Себестоимость серной кислоты, получаемой
из различного сырья (условные единицы)
Сырье Затраты на сырье Стоимость пе- реработки Себестоимость
Сера 2,0 0,6 2,6
Колчедан 1,3 I 2,3
Отходящие газы 0,3 I 1,3
294
РИС. 95. Схема сушильно-абсорбционного отделения:
/ — регулятор уровня; 2— насосы; 3 — промежуточный абсорбер; 4 — второй абсорбер;
5 — сушильная башня; 6 — холодильник.
снижение затрат наибольшее, так как при этом для окисления диоксида серы
не требуется добавления кислорода. Однако при получении более концентри-
рованных газов затраты на переработку концентрированных отходящих газов
снижаются.
Перспективы развития производства. На одном из медных
заводов нашей страны внедряется анодная защита кожухотруб-
чатых холодильников. С применением таких холодильников
сушильно-абсорбционное отделение может быть переведено на
новый режим и схему, изображенную на рис. 95.
Серная кислота последовательно проходит сушильную башню, хвосто-
вой и промежуточный абсорберы. Температура кислоты в башнях повышает-
ся, самая высокая — на выходе из промежуточного абсорбера—103 °C. Кис-
лоту охлаждают до 60 °C в холодильнике с анодной защитой и возвращают
на орошение сушильной башни. Других холодильников в схеме нет. Продук-
ционную кислоту выводят из цикла сушильной башни. Концентрацию кисло-
ты в сушильной башне и промежуточном абсорбере поддерживают добавле-
нием воды.
Высокая температура кислоты повышает движущую силу теплопередачи
и поверхность холодильников уменьшается в 2 раза. Недостаток схемы за-
ключается в тяжелых условиях работы насоса после промежуточного абсор-
бера.
Для переработки отходящих газов с низким содержанием
(1—3%) на одном из медеплавильных заводов проходит опыт-
но-промышленную проверку способ нестационарного окисле-
ния. Этот способ разработан в институте Катализа СО АН
СССР с целью снижения капитальных и эксплуатационных за-
трат в производстве серной кислоты из низкоконцентрирован-
ных сернистых газов металлургических и других производств.
В нестационарном способе конверсия диоксида серы осущест-
вляется только за счет тепла химической реакции. Неподвиж-
ный слой катализатора предварительно разогревают до 420—
520 °C и процесс конверсии ведут в нестационарном режиме —
при периодическом изменении мест ввода и вывода сернистых
295
газов при помощи клапанов. Концентрация диоксида серы на
выхлопе остается на уровне действующих сернокислотных це-
хов с одинарным контактированием.
Фирма «Лурги» также уделяет большое внимание перера-
ботке металлургических газов с низким содержанием SO2 —
менее 4%.
Продажа кислоты, получаемой из газов, содержащих меиее 6—7% SO2,
всегда связана с определенным убытком. Однако, даже с учетом этого, наи-
более эффективно из газов получение именно серной кислоты (по сравнению
с другими продуктами), хотя при этом и возникают две проблемы, связан-
ные с достижением автотермичиости систем и обеспечением водного баланса.
Для переработки газа с содержанием 2% SO2 в 93 и 98,5%-иую кислоту
температура газа на входе в сушильную башню не должна превышать 22 и
17 °C, соответственно. Для решения проблемы водного баланса устанавлива-
ют сушильную форбашию, орошаемую 30—60%-иой серной кислотой, которую
затем концентрируют в дополнительном аппарате Вентури (за счет тепла
выхлопных газов и тепла, выделяющегося при абсорбции) и возвращают на
орошение форбашни. Такая система является идеальным буфером при коле-
баниях состава и количества отходящих газов металлургических производств.
Отходящие газы от печей обжига молибдена (10 000 м3/ч) концентрацией
0,8—1,5% SO2 перерабатывают иитрозиым методом на одной из установок
ФРГ, что значительно снижает капитальные вложения по сравнению с кон-
тактным способом.
Проблему переработки высококонцентрированных сернистых
газов фирма «Лурги» разрабатывает в нескольких вариантах.
1. Подача одной части высококонцентрированных сернистых газов иа
I слой, а другой—иа II слой. При этом иа I слое предусматривается окис-
ление 9%-ного (по SO2) газа. Это достигается благодаря поддуву воздуха
дополнительным нагнетателем, после сушки в автономной сушильной башие.
2. Применение контактного аппарата с кипящим слоем катализатора.
3. Применение термостойких катализаторов, пригодных для работы при
температурах 650—670 °C.
Повышение концентрации SO2 и стабильности объемов отхо-
дящих газов металлургических производств является непремен-
ным условием дальнейшего повышения эффективности сернокис-
лотного производства на их основе. Реконструкция и техниче-
ское перевооружение предприятий цветной металлургии позво-
ляет увеличить выпуск серной кислоты из отходящих газов и
степень извлечения серы, что будет также способствовать охра-
не природы и повышению степени использования сырья.
Удельные капитальные вложения в строительство сернокис-
лотного цеха на отходящих газах почти на 30% меньше, чем на
колчедане, потому, что стоимость склада сырья, печного отделе-
ния и сухого пылеулавливания относится к затратам на метал-
лургический передел [75]. Капитальные вложения распределя-
ются следующим образом: промывное отделение — 52%, кон-
тактное— 23%, абсорбционное—14% и склад кислоты—11%.
Удельные капитальные вложения снижаются с увеличением
мощности цеха.
ГЛАВА VII
ИСПОЛЬЗОВАНИЕ ОТРАБОТАННОЙ И РАЗБАВЛЕННОЙ
КИСЛОТЫ
VII.1. РЕГЕНЕРАЦИЯ И ИСПОЛЬЗОВАНИЕ
ОТРАБОТАННЫХ КИСЛОТ
В современной химической индустрии широко исполь-
зуются эффективные технологические процессы, ос-
нованные на применении серной кислоты в качестве реагента
или катализатора. Во многих случаях при этом образуются
значительные количества отходов — отработанной серной кисло-
ты (ОСК) и кислых гудронов (кг). Неуклонное развитие хими-
ческой и нефтехимической промышленности сопровождается
увеличением таких отходов. j
Эти отходы представляют собой многокомпонентные системы, включаю-
щие, кроме водных растворов серной кислоты различной концентрации, раз-
нообразные органические и неорганические примеси: эфиры, спирты, кетоны,
сульфо- и карбоновые кислоты, сульфоны, а также продукты вторичных
процессов — смолы, асфальтены, карбены и др., хлор, хлорид водорода, окси-
ды азота, азотную кислоту, сульфаты металлов, сульфат и бисульфат аммо-
ния, металлоорганические и другие соединения.
Всего в настоящее время в нашей стране насчитывается более двухсот
видов отработанной серной кислоты, в которых содержится около ста видов
органических и неорганических примесей.
Общее количество образовавшихся ОСК в 1983 г. в нашей
стране превышало 2 млн. т (в пересчете на моногидрат), т. е.
составляло около 10% от общего производства серной кислоты
в Советском Союзе. Поэтому проблема утилизации и регенера-
ции ОСК имеет важное народнохозяйственное значение как
средство увеличения ресурсов серосодержащего сырья и серной
кислоты, а также защиты охраны окружающей среды.
Исходя из качественного состава и количества ОСК сло-
жились следующие основные направления ее утилизации — не-
посредственное использование ОСК (с предварительной очист-
кой от примесей и концентрированием разбавленных ОСК) и
термическое расщепление ОСК и КГ с получением серной кис-
лоты.
Так, ОСК от производства каустической соды используется в производ-
ствах простого суперфосфата и сульфата аммония; диоксида титана — в про-
изводствах простого суперфосфата и фосфорной кислоты; хлорных соедине-
ний— в производствах простого суперфосфата, сульфата аммония, при трав-
лении металлов; сульфоугля — в производстве серной кислоты; алкилбензо-
ла — на обработку известковых почв и т. д.
ОСК и КГ с большим содержанием органических соединений подверга-
ют термическому расщеплению с получением серной кислоты, которую воз-
вращают в производство, где образуются ОСК и КГ.
297
РИС. 96. Схема печного агрегата
термического разложения отрабо-
танной кислоты:
1 — напорный бачок; 2 — печь расщеп-
ления; 3 — печь дожигания; 4— обд>\
ваемый газоход; 5 — теплообменник.
Следует отметить, что не существует какого-то одного уни-
версального метода очистки ОСК. Выбор его определяется
прежде всего качественным составом ОСК. Это может быть
экстракция примесей, высаливания их, отдувка газообразных
примесей, коагулирование, ионный обмен, дробная кристаллиза-
ция, адсорбция и др. Среди описанных в отечественной и зару-
бежной литературе способов регенерации ОСК и КГ наиболь-
ший интерес представляют два — термическое расщепление и
концентрирование ОСК, поскольку эти методы применимы прак-
тически ко всем видам ОСК и КТ и имеют широкое промыш-
ленное распространение. Различают два вида термического
расщепления ОСК и КГ — высокотемпературное и низкотемпе-
ратурное.
Высокотемпературное расщепление—-весьма эффективный
и достаточно универсальный метод, получивший широкое рас-
пространение в промышленности СССР и за рубежом
(рис. 96). Обычно процесс высокотемпературного расщепления
ОСК и КГ проводят при температуре 900—1200 °C. Необходи-
мую температуру процесса поддерживают сжиганием топлива,
предпочтительно серосодержащего. Обычно для этих целей ис-
пользуют сероводород, серу, сернистый мазут, природный газ.
Помимо тепла сгорания топлива, тепловой режим расщепления
поддерживается за счет окисления углеводородов, содержащих-
ся в отработанной кислоте.
Суммарно этот процесс может быть выражен следующим
уравнением реакции
H2SO4 -f- CnHm + (л 0,25m —0,5) О2 < SO2 лСО2 -|- (0,5m + 1) Н2О
В Советском Союзе разработана и внедрена на ряде пред-
приятий эффективная технологическая система получения сер-
ной кислоты из ОСК от процессов алкилирования и из КГ про-
изводства жидких парафинов (процесс «Парекс» на базе высо-
котемпературного расщепления с использованием в качестве
топлива сероводорода или серы). Образующийся при термиче-
ском разложении КГ диоксид серы перерабатывается по длин-
ной схеме в высококачественный олеум, который возвращается
в цикл процесса «Парекс». Избыток серной кислоты в виде то-
варной продукции отправляется потребителям. Технологическая
298
схема такого производства, использующего отбросный серово-
дород, представлена на рис. 96. (
Процесс расщепления проводят в печи при температуре 1200 °C, которая
достигается за счет сжигания сероводорода и горения содержащихся в отра-
ботанной кислоте органических примесей. Печь представляет собой интенсив-
ный трехкамерный котел циклонного типа. В первую камеру подают кислый
гудрон (или отработанную кислоту), сероводород и воздух, во вторую — се-
роводород и воздух для полного разложения КГ. При этом КГ или ОСК раз-
лагаются на воду, кислород и диоксид серы, органическая часть окисляется
до диоксида углерода. Газ после печи охлаждается до 600—650 °C в рубашке
газохода, а затем до 300 °C в теплообменнике воздухом, который направ-
ляется в печь. Дальнейшая переработка полученного в печи обжигового газа,
содержащего SOs (степень разложения серной кислоты около 97%), в серную
кислоту осуществляется по известной классической схеме с промывным от-
делением.
В этой системе приняты новые высокоэффективные технические решения,
которые позволили сделать ее практически бессточной и безотходной. В про-
мывном отделении вместо традиционных оросительных холодильников внед-
рена прогрессивная башня-холодильник. Охлаждение кислоты ведут атмос-
ферным воздухом. Это позволило вывести из системы избыток влаги и таким
образом получить необходимое количество олеума.
Сочетание башни-холодильника в промывном отделении и аппаратов воз-
душного охлаждения крепких кислот в сушильно-абсорбциоином отделении
позволило полностью отказаться от использования воды для охлаждения
кислот, в результате чего отпала необходимость в строительстве системы
водооборота с насосами, градирнями, водяными коммуникациями, станцией
нейтрализации и т. д.
С целью устранения выбросов диоксида серы с выхлопными газами в си-
стемах применены схема двойного контактирования или установки химиче-
ской очистки (в случае одинарного контактирования).
Для переработки КГ, отличающихся высоким содержанием
органических веществ (15—90%) и повышенной вязкостью, ис-
пользуют процессы низкотемпературного расщепления. Они ме-
нее энергоемки и дают возможность утилизировать органиче-
скую массу сернокислотных отходов с получением полезных
продуктов. Эти процессы основаны на химическом взаимодейст-
вии сернокислотных отходов с углеводородами, которые играют
роль восстановителя и теплоносителя. Нестабильные промежу-
точные соединения, образующиеся при этом взаимодействии,
расщепляются с выделением диоксида серы. Температура, при
которой проводят процессы низкотемпературного расщепления,
находится в пределах 150—350 °C (в зависимости от состава
КГ).
Сера, входящая в состав серной кислоты и органической
массы, распределяется между продуктами низкотемпературного
расщепления. Основная часть серы переходит в диоксид серы,
который может быть направлен на переработку в серную кисло-
ту, на производство 100°/0-ного диоксида серы или на получение
серы. Другая (меньшая) часть серы переходит в углеводород-
ный остаток — кокс.
Установки иизкотемпературиого расщепления имеются за рубежом. Фир-
ма «Хемико» (ФРГ) разработала процесс регенерации кислого гудрона в го-
ризонтальных вращающихся печах при 250—350 °C. Конечными продуктами
являются диоксид серы и высокосериистый кокс. Английская фирма «Майли»
299
разработала процесс разложения кислого гудрона в шнеке-реакторе при 230—
250 °C с последующим нагревом в специальной реторте до 340—350 °C цир-
кулирующего кокса за счет тепла дымовых газов и тепла сжигания летучих
веществ и части кокса. Недостатком процесса является низкая концентрация
диоксида серы в обжиговом газе (около 2,5%).
Представляет интерес разработанный за рубежом способ переработки
кислых гудронов с получением кокса, когда коксованию подвергается предва-
рительно нейтрализованный сернокислотный отход.
Особое место среди множества различных видов отработан-
ных кислот занимает гидролизная серная кислота — отход про-
изводства пигментного диоксида титана. Это объясняется боль-
шим объемом таких отходов и их специфическими составами.
Состав гидролизной серной кислоты изменяется в зависимости
от используемого сырья. Усредненный состав: 22,0% H2SO4;
11,50% FeSO4; 1,06% MgSO4; 1,08% TiOSO4; 0,92% Fe2(SO4)3;
0,78% A12(SO4)3; 0,21% MgSO4; 0,05% CaSO4, остальное —
вода.
Наиболее целесообразным методом регенерации гидролиз-
ной серной кислоты является одно- или двухступенчатое ее кон-
центрирование (соответственно 20—22 до 50—57 и с 50—57 до
72% H2SO4) в аппаратах с погружным горением, освоенное на
отечественных предприятиях. Однако увеличение концентрации
гидролизной кислоты свыше 55% H2SO4 приводит к образова-
нию мелких кристаллов сульфатов железа, что вызывает силь-
ное пересыщение раствора. Это значительно осложняет ее филь-
трацию. Поэтому как правило гидролизную кислоту концентри-
руют до содержания H2SO4 около 55%. После фильтрации
упаренная гидролизная серная кислота содержит 55,0% H2SO4;
1,43% FeSO4-H2O; 2,0% A12(SO4)3; 0,03% TiOS(J4; остальное —
вода.
Регенерированную (упаренную и отфильтрованную) гидро-
лизную серную кислоту используют в смеси с чистой крепкой кис-
лотой в определенном соотношении в произодствах экстрак-
ционной фосфорной кислоты, простого суперфосфата, сульфата
аммония. Выделенный при фильтровании упаренной гидролиз-
ной кислоты осадок — сульфат железа также является серосо-
держащим отходом, поскольку в его состав входит 45—55%
FeSO4; 2—6% Fe2(SO4)3; до 16% H2SO4; остальное — вода.
В основном этот отход направляется в отвалы, загрязняющие
окружающую среду. Развитие производства пигментного диок-
сида титана еще более усугубляет проблему утилизации как
упаренной гидролизной кислоты, так и сульфатов железа.
В нашей стране разработаны и внедрены в промышленность
методы использования гидролизной серной кислоты в производ-
ствах экстракционной фосфорной кислоты и простого суперфос-
фата. Разработан и внедрен также метод переработки сульфа-
тов железа в серную кислоту путем термического разложения
их при одновременном сжигании жидкой серы в печах КС-ЦВ
(«кипящего слоя с циклоном возврата). Полученный обжиговый
газ, содержащий 14—16% диоксида серы, перерабатывают в
300
серную кислоту по классической длинной схеме с промывным
отделением.
Отработанные серные кислоты, образующиеся в хлорной
промышленности и содержащие растворенный хлор, очищают
от него отдувкой воздухом, после чего их можно использовать
в производстве фосфорных удобрений. Кислоты, содержащие
оксиды азота, очищают с карбамидом, который восстанавлива-
ет их до элементарного азота. Указанные методы разработаны
и внедряются в промышленности.
В настоящее время около 96% всех ОСК утилизируется
рассмотренными в этом разделе методами.
VII.2. КОНЦЕНТРИРОВАНИЕ СЕРНОЙ КИСЛОТЫ
Серная кислота в больших количествах находит приме-
нение как водоотнимающее средство: при концентрировании
азотной кислоты, в производстве нитроцеллюлозы, при нитро-
вании углеводородов, для осушки промышленных газов, при
очистке нефтепродуктов, в производстве синтетических спир-
тов и во многих других производствах. При этом образуется
разбавленная серная кислота, которую затем концентрируют
упариванием или смешивают с более крепкой кислотой или с
олеумом с целью получения кислоты нужной концентрации.
Разбавленные растворы серной кислоты можно концентри-
ровать простым упариванием, так как при температуре кипе-
ния ее вплоть до содержания в растворе примерно 80% H2SO4
в пары выделяется практически только вода. Теоретически
упариванием водных растворов можно получить серную кислоту
концентрацией 98,3% (азеотропная смесь), практически же кон-
центрацию кислоты доводят не более чем до 96%. С повышени-
ем концентрации раствора серной кислоты температура кипения
его непрерывно повышается. Но она резко уменьшается с пони-
жением давления. Это дает возможность, применяя разрежение,
обеспечить большую разность температур между упариваемой
кислотой и теплоносителем.
При концентрировании серной кислоты протекают два основ-
ных процесса: передача тепла кислоте и испарение воды. Рас-
ход тепла складывается при этом из следующих статей [9]:
Qi — тепло, необходимое для нагревания кислоты от исход-
ной температуры до температуры концентрирования;
Q2 — тепло дегидратации, необходимое для удаления воды
из разбавленной серной кислоты (численно равно дифференци-
альной теплоте разбавления);
Q3 — тепло, расходуемое на испарение удаляемой воды (теп-
лота парообразования);
Q4 — потери тепла в окружающую среду.
При упаривании серной кислоты одновременно с испарени-
ем воды происходит также испарение H2SO4, приводящее к ее
потерям. Количество испаряемой серной кислоты тем больше,
301
чем выше содержание H2SO4 в растворе. В современных кон-
центрационных установках испарение кислоты относительно не-
велико. Поэтому в общем тепловом балансе оно обычно не учи-
тывается.
Количество тепла, требуемое для нагревания серной кислоты, можно вы-
числить по формуле
Q1=G(ZZ2—Z/j)
где G — масса нагреваемой кислоты, кг; Ht и Н2—количество тепла, требуе-
мое для нагревания 1 кг кислоты от О °C до исходной температуры tt и до
температуры концентрирования tz, кДж/кг (ккал/кг).
Тепло, необходимое для удаления воды из кислоты, определяют по фор-
муле
Q2 = 272
100 — а
150—а
100 — Ь
150 — b
где Q2—тепло, требуемое для удаления воды (в расчете на 1 кг H2SO4)
кДж/(ккал); а — начальная концентрация кислоты, % H2SO4; Ь — конечная
концентрация кислоты, % H2SO4.
Более точно Qi определяют с учетом температуры, при которой происхо-
дит упаривание:
Г 412ЛТ2 + 76 (0,585Л12 -J- 0,164) (/ — 15) 1
[ Л12 4-0,35 + М2 4-0,235 ] —
r412M1-J-76 (0,585^4-0,164) (/—15) 1
“[^4-0,35 + ^4-0,235 ]
где М,— отношение содержания воды и H2SO4 в исходной кислоте; Mi—то
же, в конечной (концентрированной) кислоте.
Установка с концентратором капельного типа. Установка со-
стоит из двух распыливающих аппаратов, имеющих форму труб
Вентури. Схема установки изображена на рис. 97.
Концентрируемая кислота поступает через дозатор во вторую (по ходу
газа) трубу Вентури. Затем в циклоне кислота сепарируется и самотеком на-
правляется в концентратор, выполненный также в виде трубы Веитури.
Сконцентрированная до 92,5—95% серная кислота отделяется в циклоне и
при 180—220 °C стекает в холодильник. Горячий топочный газ, при помощи
которого происходит дробление жидкости на капли размером 100—400 мкм
и упаривание кислоты, поступает в концентратор Вентури при 850—900 °C.
В трубе он охлаждается до 220—230 °C и выходит из второго циклона при
температуре 150 °C. Воздух в установку подается высоконапорной воздуходув-
кой, создающей перед топкой напор 1700 мм вод. ст. (166,8 кПа). Скорость
газового потока в концентраторе около 150 м/с.
Капельный концентратор Вентури состоит из двух усеченных конусов раз-
ной длины, общая длина трубы 2500 мм. Диаметр горловин 1300 мм, диаметр
отверстий на входе и на выходе газов жидкостной смеси 650 мм. Корпус ап-
парата выполнен из листов углеродистой стали толщиной 10 мм и внутри
имеет футеровку толщиной 130 мм из кислотоупорного кирпича. В качестве
подслоя под футеровку укладывается листовой свинец, а на участке со сто-
роны входа газа, где наиболее высокая температура, труба гомогенно освин-
цовывается на толщину 3 мм. Подача разбавленной серной кислоты в трубу
Вентури производится при помощи четырех сопел, расположенных на перифе-
рии конфузора. За работой этих сопел наблюдают через смотровые окна,
установленные на газоходе перед трубой. Для охлаждения труба Вентури
снабжена водяной рубашкой.
302
РИС. 97. Схема концентрирования серной кислоты в трубах Вентури:
/ — топка; 2 — насос; 3 — холодильник кислоты; 4 — труба Веитури (концентратор); 5,
7 — циклоны-сепараторы; 6 — труба Вентурн (туманоуловитель); « — дозатор; 9 — напор-
ный бак.
Туманоуловитель Вентури работает и как форконцентратор, и как подо-
греватель кислоты; кислота концентрируется в нем от 68—70 до 74—77%
H2SO4 и нагревается на 10—12 °C. При эксплуатации установки предпочита-
ют раздельную подачу разбавленной серной кислоты: частично в туманоуло-
витель и частично непосредственно в концентратор. При этом происходит пе-
рераспределение расхода тепла так, что температура выходящего газожид-
костного потока из концентратора становится более низкой (195—200°C).
Благоприятное распределение потока кислоты повышает коэффициент исполь-
зования тепла из-за снижения температуры выходящей в холодильник про-
дукционной кислоты и понижения температуры газов на выходе из тумано-
уловителя до 135 °C.
Производительность установки составляет 350 т/сут. При ра-
боте на мазуте содержание тумана серной кислоты в газах по-
сле концентратора составляет 5—8 г/м3, на газообразном топ-
ливе— всего до 1—3 г/м3. При этом в выхлопных газах перед
электрофильтром содержится до 0,7—0,5 г/м3 тумана серной
кислоты.
Расчетные (на 1 т моногидрата) расходные коэффициенты
на получение серной кислоты концентрацией 92,5% при пита-
нии установки 68%-ной кислотой при температуре 120 °C сле-
дующие:
Топливо — газ [41190 кДж/м3 (9830 ккал/м3)], м3 . 44,5
Вода при 23°C, м3....................................6,5
Электроэнергия, кВт-ч...............................16,6
303
РИС. 98. Схема установки для концентрирования гидролизной кислоты от
производства титановых белил:
1 — сборник гидролизной кислоты; 2 — центробежные насосы; 3 — оросительный теплооб-
менник; 4 — концентратор; 5 — эрлифт; 6 — отстойник; 7 — центрифуга; 8 — транспортер
для удаления кристаллов; 9— сборник для пуска установки; 10 — взрывная мембрана;
И — погружная горелка; /2 — осевой вентилятор; 13 — выхлопная труба.
Установка с трубой Вентури является компактной, и более
высокопроизводительной и требует меньших капитальных за-
трат по сравнению с установкой с барботажными концентра-
торами.
Осуществление процесса при больших скоростях газового
потока позволяет вести концентрирование на незначительном,
весьма коротком расстоянии от сопел, а также избежать пере-
грева кислоты и выводить ее из аппарата при более низкой
температуре, чем в барботажных концентраторах. Благодаря
этому снижаются расход топлива на концентрирование и рас-
ход воды на охлаждение продукционной кислоты. Более низ-
кая температура кислоты уменьшает степень ее разложения и
туманообразование, что облегчает очистку газа.
Установки с погружными горелками. Такие установки полу-
чили применение прежде всего для упаривания очень разбав-
ленной серной кислоты до средней концентрации (55—75%
H2SO4). В случае необходимости дальнейшее концентрирова-
ние производят в установках другой конструкции, так как при-
менение погружного горения приводит к разложению серной
кислоты.
304
Такой способ сжигания топлива нашел применение в уста-
новках английской фирмы «Нордак» и в нашей промышленно-
сти для упаривания гидролизной серной кислоты, являющейся1
отходом производства диоксида титана (титановых белил).
Схема установки представлена на рис. 98.
Раствор гидролизной серной кислоты, содержащей, например, 16%
H2SO4, 8,5% FeSO4, 1—1,5% TiSO4, 2—3% прочих сульфатов (остальное во-
да), при температуре 80 °C из сборника центробежным насосом перекачива-
ют в ванну оросительного теплообменника, где он циркулирует при помощи-
насоса, который подает ее на орошение. В этом теплообменнике, изготовлен-
ном из свинцовых труб, орошающий раствор гидролизной кислоты частично
упаривается (до 24% H2SO4) за счет тепла парогазовой смеси, поступающей1
из концентратора. Парогазовая смесь прн температуре 120 °C поступает в-
трубы оросительного теплообменника, где охлаждается до 80 °C и далее ухо-
дит в вытяжную трубу.
Подача кислоты нз ванны оросительного теплообменника в концентратор
автоматически регулируется в завнснмости от температуры раствора, нахо-
дящегося в концентраторе. В нем поддерживают концентрацию гидролизной-
кислоты около 55% H2SO4, прн температуре не выше 120 °C. Прн этих усло-
виях растворимости сульфата железа (железного купороса) понижается, он-
кристаллизуется в виде FeSO4-H2O и вместе с кристаллами других сульфа-
тов в виде пульпы осаждается на дно концентратора. Для улучшения усло-
вий крнсталлнзацнн эту пульпу непрерывно перемешивают воздушной струей
нз погружной трубы эрлифта, с помощью которого пульпа транспортируете®
в отстойник. В отстойнике кристаллы осаждаются на коническом дне аппа-
рата, а осветленный раствор по переливной трубе поступает в выпарной ап-
парат II ступени (на схеме не показан), где может производиться дальней-
шее концентрирование серной кислоты до 75—78% H2SO4.
Отстойник в нижней части аппарата имеет рубашку для охлаждения
пульпы, поступающей в центрифугу. Полученные кристаллы выгружаются на.
транспортер и попадают в сушилку для получения сухой соли. Концентратор
рис. 99 представляет собой сосуд с коническим дном, изготовленный из угле-
родистой стали. Внутри аппарат гуммирован кислотостойкой резиной и фу-
терован кислотоупорным кирпичом. Погруженные в жидкость горелки закреп-
лены на крышке концентратора.
Камера сгорания имеет огнеупорную футеровку. Смешению горючего
газа с воздухом способствует завихритель. Вокруг горелки размещают цир-
куляционную трубу с прямоугольным отверстием в верхней части. Ее уста-
навливают на аппарате с таким расчетом, чтобы расстояние между уровнем
кислоты и нижним концом погруженной трубы горелки было около 670 мм.
Горячие газы прн температуре 1300—1400 °C нз горелки барботируют через
раствор, поднимаются в кольцевое пространство между трубой и горелкой,
и выбрасываются через прямоугольные отверстия циркуляционной трубы;
при этом тепло, отдаваемое газами при охлаждении нх до 125 °C, расходует-
ся на выпаривание воды нз кислоты и нагрева поступающего раствора.
Установка снабжена средствами автоматизации, обеспечивающими посто-
янство уровня раствора в ванне оросительного теплообменника (изменением
подачи гидролизной кислоты), постоянство уровня раствора в концентраторе
(путем регулирования выхода раствора из отстойника) и стабилизацию тем-
пературы в концентраторе (с помощью регулирования подачи исходной кис-
лоты нз ванны оросительного теплообменника). Регулирование подачи газа
производится в зависимости от уровня в дозировочном устройстве и коррек-
тируется с соблюдением необходимого соотношения газа с воздухом. Авто-
матический контроль безопасности горения осуществляется с помощью фото-
электрического прибора, который контролирует наличие факела в камере сго-
рания. В случае погасания пламени прибор отсекает подачу газа.
На одной из установок обрабатывают в сутки 125 г гидро-
лизной кислоты и получают при двухступенчатом концентриро-
20—584
305
РИС. 99. Концентратор с погружной
горелкой:
I — стальной корпус; 2 — кислотоупорная
футеровка; 3 — предохранительная мембра-
на; 4 — парогазовый сборник; 5 — камера
горения жидкого топлива; 6 — барботаж-
ная труба.
вании 18—19 т 75—78%-ной сер-
ной кислоты с незначитель-
ным содержанием сульфатов.
Кроме этого получают 15—16 т
одноводного сульфата железа с
содержанием 4—6% SiO2, 4%
H2SO4 и примесями других суль-
фатов.
Отходящие из установки газы
содержат 0,3 г/м3 SO2 и 0.1 г/м3
H2SO4.
Комбинированные методы
концентрирования. В литературе
[4] в качестве примера комбинирования процесса концентриро-
вания серной кислоты с другими производствами описан такой
технологический комплекс: концентрирование азотной кисло-
ты — производство серной кислоты нитрозным методом — кон-
центрирование серной кислоты.
В башенных сернокислотных системах продукция выпускается в виде
76%-ной H2SO4. На образование 1 т моногидрата и его разбавление до 76%
H2SO4 затрачивается 500 кг воды:
10ОО.10 I 1 ЛОО \
1 VVV 1и /1 VVV \
98 + ( 0,76 — 100j = 50° кг
За счет влаги колчедана и воздуха в систему на 1 т H2SO4 поступает с
обжиговыми газами около 60 кг воды. Недостающее количество воды
(500—60=440 кг) обычно в систему добавляется.
На заводах, где наряду с башенными системами имеются установки кон-
центрирования азотной и серной кислот, в башенную систему можно вместо
воды вводить 68%-ную H2SO4— отработанную кислоту после концентриро-
вания азотной кислоты и довести ее в нитрозном процессе до 76%-ной.
На 1 т H2SO4 в продукции башеииой системы при этом можно ввести сле-
дующее количество 76 %-ной серной кислоты:
440
1000
0,68
1000
0,76
= 2,85
т
или 4,2 т 68%-ной отработанной серной кислоты. Такой кислотооборот позво-
ляет уменьшить общий расход топлива на коицеитрироваиие 68%-ной серной
кислоты до 93% H2SO4.
Смешение кислот. В некоторых случаях целесообразно по-
лучать серную кислоту нужной концентрации смешением более
концентрированной кислоты с менее концентрированной.
Для получения 1 кг серной кислоты средней концентрации (Пс, % H2SO4)
из кислот более высокой (Пв, % H2SO4) и более низкой (Пн, % H2SO4) тре-
буется (в кг)
306
концентрированной кислоты
Пс — Пн
Пв пн
кислоты низкой концентрации
Цл — Пс
Пв пн
т. е. для смешения концентрированной н разбавленной кислот их следует
брать в соотношении
Пс — Пн
Пв — Пс
При смешении кислот выделяется дифференциальная теплота смешения
Q, которую можно определить в расчете на 1 кг кислоты требуемой средней
концентрации по формуле [4]:
„ Г 100— Пс 100 —Пн / 100— Пв I
<?~2’72 150 —Пс +ОнПн 150—Пн — 0 —сн)Пв- 150_Пв
где Q„ — массовая доля в смеси кислоты низкой концентрации.
Температура
концентрирования, °C
РИС. 100. Номограмма для определения общего количества тепла для кон-
центрирования кислоты (1 ккал=4,1868 кДж).
20*
307
Тепло испарения воды (на 1 кг испаренной Н2О) может быть вычислено
шо формуле
Q3= 83,9 3/З65—/
где t—температура упаривания, °C.
Потери тепла в окружающую среду Q4 зависят от устройства концентра-
ционной установки, режима ее работы, производительности и других условий.
Количество воды (в кг), которое необходимо удалить из разбавленной серной
кислоты, вычисляется по формуле
G= 100В — —-т-
I а о
где В — масса получаемой концентрироваииой кислоты, кг.
Общее количество тепла, требуемого для концентрирования
(без учета потерь), может быть определено по номограмме
(рис. 100).
Например (см. пунктир на рисунке): от точки, соответствующей началь-
ной концентрации кислоты 76% H2SO4, от левой оси ординат ведут нисхо-
дящую параллель с наклонной линией до пересечения с вертикалью, опущен-
ной из точки, отвечающей конечной концентрации кислоты 92% H2SO4 (на
верхней шкале). Из точки пересечения наклонной и вертикали проводят го-
ризонтальную линию до ее пересечения с вертикалью, иосстановленной из
точки, соответствующей 220 °C — температура концентрироиания (см. на
нижней оси абсцисс). Затем ведут восходящую наклонную параллель до пе-
ресечения ее с правой осью ординат. Точка на этой оси (примерно 260 тыс.
ккал, или около 1,1 МДж) соответствует количеству тепла, требуемого для
получения 1 т концентрированной (92%-иой) серной кислоты (из 76%-ной).
По номограмме может быть определен лишь примерный рас-
ход тепла однако с достаточной для заводской практики точно-
стью.
ГЛАВА VIII
ВСПОМОГАТЕЛЬНОЕ ОБОРУДОВАНИЕ
ДЛЯ ПРОИЗВОДСТВА
СЕРНОЙ КИСЛОТЫ
VI11.1. ХОЛОДИЛЬНИКИ И НАСОСЫ
Для производства серной кислоты характерно выделе-
ние значительного количества тепла. При получении
1 т продукта по классическому контактному методу из системы
необходимо вывести около 1,6 млн. ккал (6,7 ГДж) тепла, од-
на часть которого выводится в печном отделении — через охлаж-
дающие элементы печи, котел-утилизатор, в виде естественных
потерь и т.п., другая — при охлаждении кислоты в холодильни-
ках системы ее циркуляции в технологическом цикле башен
308
Таблица 59. Тепловой баланс башен контактной сернокислотной
системы, тыс. ккал/ч (тыс-кДж/ч)
Приход тепла | Расход тепла 1
Цикл промывных башен
Тепло охлаждения га- за от 390 до 43 °C . . Тепло образования 50 %-ной кислоты . 11425(48842) 545(2282) Теплота испарения воды Отводится в холо- дильниках промывной башни 1370(5737) 10600(44387)
Итого . . . 11970(50124) Итого . . . 11970(50124)
Цикл сушильной башни
Теплота конденсации водяных паров . . Теплота образования 94%-ной кислоты . 2260(9464) 2900(12144) Отводится в холо- дильниках .... 5160(21607)
Итого . . . 5160(21607) Итого . . . 5160(21607)
Цикл I стадии абсорбции
Тепло охлаждения га- за с 200 до 60 °C . Теплота образования 98 %-ной кислоты . 5760(24120) 11190(46858) Отводится в холо- дильниках олеумиой и I моногидратной башен 16950(70978)
Итого . . . 16950(70978) Итого . . . 16950(70978)
Цикл 11 стадии абсорбции
Тепло охлаждения га- за с 200 до 60 °C . Тепло образования 98 %-ной кислоты . 5180(21690) 650(2722) Отводится в холо- дильнике II моногид- ратной башни . . . 5830(24413)
Итого . . . 5830(24413) Итого . . . 5830(24413)
Всего отводится тепла в холодильниках серной кислоты . . 38540(161380)
(в аппаратах промывного и сушильно-абсорбционного отделе-
ний) [3, 9, 12].
В табл. 59 приведен тепловой баланс башен контактной сер-
нокислотной системы мощностью 360 тыс. т/год, работающей на
9 %-ном газе.
Количество тепла, отводимого в холодильниках, зависит от
концентрации исходного газа. Поскольку при промывке газа
тепло выделяется в основном за счет его охлаждения, то при
охлаждении низкоконцентрированных газов цветной металлур-
гии требуется устанавливать дополнительную поверхность ох-
лаждения. В табл. 60 приведены усредненные данные по удель-
ной поверхности холодильников ряда контактных сернокислот-
ных производств, работающих на различном сырье.
309
Таблица 60. Удельная поверхность холодильников, в м2 на 1 т/сут миг
Вид системы (по сырью) Промывные башни Сушильные башии Абсорбци- онные башни Всего
Системы иа сере 1,05 1,91 3,85 3,88 4.9 8,48
короткая схема полная схема 2,69
Системы на колчедане 3,52 2,43 4,4 10,35
Системы на отходящих газах цветной металлур- гии 5,7 2,7 3,7 12,1
Следует отметить, что в сернокислотных производствах на-
блюдается значительный разброс в используемой удельной по-
верхности холодильников, объясняемый конструктивными осо-
бенностями холодильников, климатическими условиями, качест-
вом охлаждаемой воды и эффективностью эксплуатации. Так,
для производств, работающих на колчедане, при средней удель-
ной поверхности 10,35 м2/(т-сут) колебания находятся в преде-
лах 5—15 м2/(т-сут), в производствах серной кислоты из отхо-
дящих газов цветной металлургии при средней величине
12 м2/(т-сут) —от 7 до 21 м2/(т-сут).
Оросительные холодильники. Оросительные холодильники
состоят из прямых, расположенных друг над другом труб и со-
бираются из нескольких параллельных секций.
Над верхними трубами расположены оросительные устройства в виде
треугольных и прямоугольных желобов, с треугольными прорезями иа верх-
них кромках; иногда для лучшей организации стекания и равномерной пода-
чи воды по всей длине труб (по нижней образующей) устанавливают успо-
коительные гребенки. Под холодильником установлен поддон для сбора и от-
вода стекающей иоды.
В большинстве случаев холодильники собирают из труб диаметром 100—
150 мм с длиной прямых участков 9—24 м. Число труб по вертикали выбира-
ют из теплового расчета, конструктивных соображений и удобства компо-
новки, обычно не более 12—14 рядов, в некоторых случаях 20—22 ряда. Ми-
нимальное расстояние между трубами составляет 200—300 мм. Для удобства
ремонта холодильник составляется из отдельных секций с расстоянием меж-
ду секциями 800 мм. Поверхность секций в зависимости от материала, разме-
ра и числа труб составляет 80—288 м2. Коэффициент теплопередачи холо-
дильников около 150—200 ккал/(м2-ч-град) [174—232 Вт/(м2-град)].
Оросительные холодильники имеют простую конструкцию,
но отличаются низкой эффективностью использования охлаж-
дающей воды, большой металлоемкостью, требуют больших
производственных площадей, при установке их в помещении соз-
даются условия, приводящие к сильной увлажненности воздуш-
ной среды, к тумано- и парообразованию, при установке их вне
помещения возникает угроза в зимнее время замерзания воды
в оросительных устройствах, кроме того затрудняется ремонт
холодильников. За последнее время их заменяют на более эф-
310
фективные: кожухотрубчатые, спиральные, пластинчатые, воз-
душные.
Кожухотрубчатые холодильники. Переход на кислотостойкие
стали расширяет возможности применения выпускаемых про-
мышленностью нормализованных холодильников кожухотрубча-
того типа TH. Кожухотрубчатые холодильники в последние годы
стали широко применять для охлаждения концентрированной
кислоты и главным образом олеума.
При разности температур между корпусом и пучком труб до 50 °C при-
меняют холодильники жесткого типа, при разности температур выше 50 °C —
холодильники снабжаются компенсаторами. Наибольшее распространение
имеет вертикальный холодильник, в котором кислота движется в межтруб-
ном пространстве сплошным потоком, а охлаждающая вода свободно стекает
пленкой по внутренним стенкам труб. По высоте холодильника установлены
горизонтальные перегородки и охлаждаемая кислота совершает частичное
поперечное движение в межтрубном пространстве, что улучшает теплообмен.
Кислота подается под большим напором, чем вода. Для изготовления холо-
дильников применяются трубы 38X2,5 мм, поверхность теплообмена состав-
ляет 220—620 м2, при этом диаметр корпуса бывает в пределах 1,2—1,7 м.
Кожухотрубчатые холодильники очень компактны, поставляются в собранном
виде, достаточно герметичны, не требуют дорогостоящих поддонов. Но в иих
не удается создать высокую скорость кислоты и равномерное распределение
воды по всем трубам. Кроме того, весьма сложен их ремонт.
Коэффициент теплопередачи в зависимости от скорости кислоты рассчи-
тывают по уравнению К=1165 кА765. Для типовых кожухотрубчатых холо-
дильников типа ТЛ с поверхностью 40 м2 при скорости кислоты и воды 0,12—
0,19 м/с коэффициент теплопередачи составляет 120—190 ккал/(м2-ч-град)
[146—220 Вт/(м2-град)]. Общий вид такого холодильника представлен иа
рис. 101.
За последние годы внедрены ко-
жухотрубчатые холодильники с труб-
чаткой из графитопластовых (антег-
митовых) труб—холодильники «НЭЗ»
(Новочеркасского электродного заво-
да) и подобные им «Сигри» (табл.
61), установленные на ряде вновь по-
строенных мощных сернокислотных
системах и предназначенные для ох-
лаждения разбавленных кислот про-
мывных башен.
Разработаны в освоении кожухо-
трубчатые холодильники с фторпла-
стовыми трубками диаметром 2,5—
6,5 мм и толщиной стенки 0,25—
0,64 мм.
РИС. 101. Кожухотрубчатый холодильник из
графитопласто — антегмита (F= 102 м2, dTp=
=32/42 мм).
311
Таблица 61. Основные показатели антегмитовых кожухотрубчатых
холодильников
Показатели Холодильники
«Сигри» | «нуз»
Поверхность теплообмена, м2 107 102
Число труб 253 433
Диаметр труб, мм 32X5 32x5
Длина труб, мм 4900 3810
Диаметр корпуса, мм 762 1120
Число ходов 1 1
Температура кислоты, °C на входе 60 51 39
на выходе 30 29 36
Температура воды, °C иа входе 17 24 21
на выходе 23 32 24
Скорость кислоты, м/с 0,93 0,91 0,08
Коэффициент теплопередачи, ккал/(м2-ч-град) 460 665 104
Вт/(м2-град) 535 770 120
В США несколько сернокислотных систем для охлаждения крепких кис-
лот оснащены кожухотрубчатыми холодильниками из фторопласта, имеющи-
ми трубчатку из 2500—3100 трубок диаметром 2,5 мм и длиной 1—3,3 м, с
поверхностью теплообмена 50 м2 [193]. Коэффициент теплопередачи холо-
дильников из фторпласта 240—300 ккал/(м2-ч-град) [278—348 Вт/(м2-град)].
В этих холодильниках положительным является отсутствие коррозии, стои-
мость их сравнима с аппаратами из нержавеющих сталей.
Спиральные холодильники. Спиральные холодильники ис-
пользуются на некоторых заводах для охлаждения нитрознои
кислоты. Холодильники выпускались заводами химического ма-
шиностроения с поверхностью охлаждения 35—45 м2. С 1976 г.
были пущены около 15 контактных систем на сере (по постав-
кам ПНР), в которых установлены спиральные холодильники
поверхностью по 80 и 100 м2.
Этн холодильники имеют два спиральных канала, которые выполнены
глухими по ходу кислоты и открытыми со стороны воды, что позволяет про-
изводить систематическую очистку водяных каналов. Холодильник поверх-
ностью 80 м2 имеет длину канала 60 м, высоту 1,4 м, ширину 25 мм и тол-
щину стеикн 4 мм.
Движение жидкостей в каналах холодильника противоточное, что повы-
шает эффективность использования воды. Важным преимуществом спираль-
ных холодильников является их компактность и возможность пропускания
жидкостей с высокими скоростями [194]. Расчетное значение коэффициента
теплопередачи составляет 700 ккал/(м2-ч-град) [812 Вт/(м2-град)].
Пластинчатые холодильники. Выпускаемые промышленно-
стью разборные пластинчатые холодильники относятся к наи-
более интенсивным типам теплообменных аппаратов; в последнее
время они получили широкое распространение [194]. Тепло-
обменная поверхность представляет собой гофрированные пла-
стины с поперечными или «в елку» гофрами. Пластины с рези-
новыми прокладками по контуру сжимаются двумя плитами и
312
‘РИС. 102. Общий вид и схема работы разборного пластинчатого холодиль-
щика.
компануются в секции. Охлаждаемая и нагреваемая жидкости
проходят по каналам между пластинами. Общий вид и схема
работы пластинчатого холодильника представлены на рис. 102.
Усредненные показатели работы холодильника поверхностью
160 м2 при работе на моногидрате приведены ниже:
Расход кислоты и воды, м3/ч....................150 и 230
Скорость кислоты и воды, м/с..................0,46 и 0,71
Температура, °C
кислоты на входе и выходе...................56 и 34
воды на входе и выходе......................26 и 36
Коэффициент теплопередачи ккал/(м2-ч-град)
и Вт/(м2-град)................................ 980 и 1140
Расчет. Ниже приведен примерный расчет коэффициента теплопередачи
пластинчатого холодильника (по РТМ-26-01, введен в действие в 1978 г.).
Исходные данные
Холодильник для кислоты сушильной башни F=160 м2
Расход кислоты на холодильник, t/=100 м3/ч=0,0278 м3/с
Концентрация кислоты — 93,45%
Температура кислоты: //=50, //' =—40 °C воды: /2/=И, /г"=23°С
По табл. 2 Р Т М
Число пластин в холодильнике 320 шт.
Число зазоров для прохода (320—2) : 2=159 шт.
Толщина стенки пластины 6=0,001 м.
Длина L = l,37 м. Ширина В=0,5 м
Эквивалентный диаметр канала йэ = 0,00585 м.
Площадь поперечного сечения канала для прохода жидкости /1 = 0,00134 м2.
Плотность р! = 1807,5; р2= 1000 кг/м3.
Удельная теплоемкость Ci = 0,37, C'i = 0,36 ккал/(кг-гр ад) [1,55 и
1,51 кДж/(кг-град)].
Коэффициент теплопроводности Л, Вт/(м-град) — (см. расчет).
Кинематическая вязкость V! = 10,9 сПз = 10,9 мПа-с.
313
Расчет
Число пластин в холодильнике
160
0?5
= 320 шт.
Число зазоров для прохода жидкости
320 — 2
2
= 159 шт.
50 + 40
1г =------j-----= 45 °C
300
У1 = —3— = 100 м3/ч = 0,0278 м3/с
Pl = 1807,5 кг/м3
67 = 0,37 ккалДкг-град) = 1,55 кДж/(кг-град)
/ t \ С
= 0,447 +0,0014/—(0,22+ |5qq ) Ю0 =
= 0,276 ккал/(м-ч-град) = 0,320 Вт/(м-град)
vx = 10,9 сПз = 10,9 мПа-с
10,9
v = -lgxL г-3,6 = 0,0217 м2/г= 6,03-10-в м2/с
1ои/»□
н2о
р= 998,8 кг/м3 С = 1 ккалДкг-град)
X = 0,5 ккал/(м ч • град) v = 1,0-10"6 м2/с
H2SOt (ст.)
45 + 17
^ат =-----£----= 31 °C рст = 1819,3 кг/м3
Сст=0,36 ккал/(кг-град) = 1,51 кДж/(кг-град)
/ 31 \
Я,ст = 0,447+ 0,0014-31 — (0,22+ — -0,935 =
= 0,265 ккал/(м-г-град) = 0,307 Вт/(м-град)
Н2О (ст.)
рст = 995,7 кг/м3; C=l; vCT= 8,3- 10~6 м2/с
Хст=0,53 ккал/(мг• град) = 2,23 кДжДмг-град).
Тепловой баланс
<2= Ух-Ci (<i' = у.-с2
^=0,0278-1807,5 = 50,25 кг/с
50,25-0,37-(50 —40) = у2-1 -(23 — 11)
50,25-0,37-10
У2 =--------]2------= 15,5 кг/с
314
HzSOt
Скорость охлаждаемой рабочей среды
у 0,0278
wi = ft™ — 0,00134-159 — 0,13 м/с
Критерий Рейнольдса
Rex
Wld3
Vi
0,13-0,00585
6,03-10-6 — 12t)>u
0,276
стенки
0,36-8,3-10-«-1819,3-3600
о одк — 73,85
0,25
I = 15,388
Движение жидкости турбулентное, поскольку Re>50.
Критерий Прандля среды
C1V1P13600 0,37-6,03-10-«-1807,5-3600
Рг1 = А, “ ~
Критерий Прандля
Ргст =
Критерий Нуссельта для кислоты
По табл. 5 РТМ С=0,0978; п=0,73
(рг \0.25
-д----)
НГСТ1 /
= 0,0978-126°>73-52,6°>43
Коэффициент теплоотдачи кислоты
Nu.A, 15,388-0,276
ах = —------= —Q 00585—~ 726,0 ккал/(мг-ч-град) = 835 Вт/(м2-град)
Н2О
Скорость охлаждающей воды
у2 0,0155
а’2=-Т1й' = 0,00134-159 = 0,073 м/с
Критерий Re2
w2d3 0,073-0,00585
Re2 - v — 1-10-“ — 427
Критерий Рг2
1-1-10-6-999,8-3600
рг2= о,5 =7,2
Критерий РгСт 2
1-8,3-10-6-995,7-3600
Ргст2= о,53 =5,6
Критерий Нуссельта для воды
(7 2 \°,25
-ТГс- = 20
5,6 )
Коэффициент теплоотдачи воды
20-0,5
“2= ”0,00585 = 1710 ккал/(м2'4 • град) = 1984 Вт/(м2-град)
315
По таблице 6РТМ — термические сопротивления от загрязнений:
серной кислоты 6l/Zl = 0,00005 м2-град/Вт
воды речной б2А2=0,00017 м2-град/Вт
По табл. 7 РТМ — термические сопротивления пластин
6СТ 63
-т— = —г?- • 10-6 = 0,000004 м2 • град/Вт
AqJ IО
Коэффициент теплопередачи
' 1 1 V1
= -ggg- +0,00005 + 0,000004 + 0,00017 + — д84~ I = 520 Вт/(м2 • град)
или
/ 1 1 V1
К — ( 72g + 0,00019 + I = 480 ккал/(м2-ч-град)
Пленочные холодильники. В пленочных холодильниках обе
жидкости стекают вдоль вертикальной поверхности тонкой плен-
кой. Преимуществом таких холодильников являются минималь-
ные затраты энергии на перекачку жидкостей. Коэффициент
теплопередачи 500—600 ккал/(м2-ч-град) [580—696 кДж/(м2-
•град)] [195]. Разработаны 3 типоразмера двухпленочных хо-
лодильников с поверхностью теплообмена 100, 150 и 200 м2, ко-
торые серийно изготавляются заводами химического машино-
строения. Пленочные холодильники установлены на нескольких
сернокислотных заводах цветной металлургии, они широко при-
меняются для охлаждения олеума. Холодильники могут быть
выполнены в кожухотрубчатом или листовом исполнении. Для
промывной кислоты разработаны холодильники поверхностью
50 м2 с применением полиэтиленовой пленки [198].
Холодильники с воздушным охлаждением. Применение воз-
душного охлаждения вместо водяного в ряде районов может
быть вызвано ограниченными водными ресурсами. Существен-
ным является также резкое уменьшение попадания загрязнен-
ных сточных вод в реки и другие водоемы. Но воздушные хо-
лодильники расходуют 40 кВт-ч электроэнергии на 1 т охлаж-
даемой кислоты, что примерно на 3 кВт-ч выше суммарного
расхода электроэнергии на перекачивание воды при водяном
охлаждении. Большой опыт применения аппаратов воздушного
охлаждения накоплен в нефтеперерабатывающей промышлен-
ности, на заводах синтетического спирта, синтетического каучу-
ка, капролактама и др.
Выпускаются нормализованные аппараты воздушного
охлаждения (АВО) горизонтального типа (АВГ), зигзагообраз-
ные (АВЗ, ГОСТ 13934—68) и малой производительности
(АВМ, ГОСТ 13935—68). В нашей сернокислотной промышлен-
ности с 1973 г. внедрены холодильники АВЗ на четырех круп-
ных предприятиях [196]. Общий вид аппаратов воздушного
охлаждения типа АВЗ показан на рис. 103.
316
РИС. 103. Общий вид аппарата воздушного охлаждения типа АВЗ:
/—3 — привод вентилятора; 4 — коллектор; 5 — колесо вентилятора; 6 — узел увлажнения,.
7 — диффузор; 8 — металлоконструкция; 9 — жалюзи; J0 — теплообменная секция.
Аппараты воздушного охлаждения состоят из ряда прямоугольных сек»
цин, включающих поперечнооребренные металлические трубы. Число труб в
секции 4, 6 и 8; секции труб в холодильниках АВЗ расположены под острым
углом друг к другу и к горизонтальной опорной площадке. Секции смонтиро-
ваны на раме и закреплены с одного конца. Опорная рама вместе с секция-
ми смонтирована на бетонной опорной конструкции. На отдельной раме уста-
новлен вентилятор. Воздух проходит через межтрубное пространство секций,
кислота, протекающая внутри труб, охлаждается за счет теплообмена через-
ребристую поверхность труб.
В производстве контактной серной кислоты рекомендуется-
применять холодильники в следующем исполнении [9]: Б1 —
внутренняя труба из стали 10 — для олеумного абсорбера; Б2 —
внутренняя труба из стали Х18Н10Т — для моногидратного аб-
сорбера; БЗ — внутренняя труба из стали Х17Н13М2Т — для су-
шильной башни.
Расчетный коэффициент теплопередачи аппарата поверхно-
стью 363 м2 для случая охлаждения 900 м3/ч серной кислоты,
концентрацией 98% с 64 до 45 °C составляет в ккал/(м2-ч-град)
[Вт/(м2-град)]:
отнесенный к единице оребренной поверхности—15,58
[18,1]
отнесенный к внутренней гладкой поверхности труб — 305
[355]
317
Таблица 62. Усредненные показатели работы холодильников АВЗ
Кислота, аппарат Расход кислоты, мЗ/ч Скорость кислоты, м/с Температура, °C Коэффици- ент тепло- передачи
кислоты воздуха ккал Вт
на входе на выходе на входе 1 на выходе ес СП U. м S м2-град
Олеум, 4-ходовой 431 1,41 76,3 67,8 19,6 60,4 239 278
Сушильная, 4-ходо- 350 1,14 66,2 55,5 20,5 48,0 246 286
вой
Моногидрат, 4-ходо- 385 1,28 66,9 56,0 21,6 41,7 251 292
вой
Моногидрат, 8-ходо- 201 1,31 68,7 51,0 21,6 41,7 212 247
вой
На 1000-тонных системах для охлаждения кислот сушильной
башни, олеумного абсорбера и двух ступеней моногидратных
абсорберов применены холодильники АВЗ с поверхностью FBh =
= 390 м2 и FH = 7500 м2. Всего установлено 16—18 аппаратов
4-х и 8-ходового исполнения. Параметры их работы показаны
в табл. 62.
Насосы. В сернокислотной промышленности применяются
горизонтальные центробежные, одноступенчатые насосы типа X,
консольные, с рабочими колесами одностороннего входа и по-
гружные типа ХП.
Таблица 63. Характеристика насосов
Обозначение типоразмеров Производи- тельность, м3/ч Напор, м столба жидкости Число обо- ротов в мин Мощность двигателя, кВт Масса, кг
2АХ-4И 20 53 2900
2Х-4П 20 53 2900
ЗХ-6П 45 54 2900
4Х-6И 90 85 2900 __
5Х-6Ф 90 33 1450
8Х-9И-1 200 46 —
8Х-9И-1а 350 32 — — —
ЗХП-6А или Е 45 45 2900 28 310
4ХП-9А или Е 90 49 2900 40 350
5ХП-6А или Е 162 49 1500 75 620
7ХП-9А 288 42 1500 100 720
9ХП-9Е 530 37 960 132 —
9ХПА-9Е-1 530 37
9ХПА-9И 600 28 960 200 —
Примечание. Насос X — для химических жидкостей; ХП — погружной для хи*
мнческнх жидкостей; первая цифра — диаметр входного патрубка в мм, уменьшенный
в 25 раз; вторая цифра — коэффициент быстроходности, уменьшенный в 10 раз; А — уг-
лероднстая сталь или чугун; Е — сталь типа ЭИ-448; И — сталь типа ЭИ-943; П — пласт-
масса; Ф — фарфор.
318
Насосы 8Х-9И, 4Х-6И, 2АХ-4И эксплуатируются в промыв-
ном отделении. Их особенностью является наличие импеллера,
на основном диске рабочего колеса, который, наряду с сальни-
ком, служит для уплотнения вала.
Погружные насосы типа ХП эксплуатируются в абсорбцион-
но-сушильном отделении. Они не имеют сальниковых уплотне-
ний или заменяющих их устройств, которые являются наиболее
уязвимой деталью любого центробежного насоса. Погружные
насосы устанавливают непосредственно на сборниках, поэтому
отпадает необходимость в дополнительной площади пола, в си-
фонах и арматуре на всасывающих кислотопроводах. Погруж-
ные насосы обладают значительными экономическими и техни-
ческими преимуществами по сравнению с горизонтальными
центробежными насосами. Характеристики некоторых насосов
приведены в табл. 63. Некоторые сведения о насосах для про-
изводства серной кислоты помещены также в гл. VIII.
VIII.2. ОРОШАЮЩИЕ УСТРОЙСТВА И БРЫЗГОУЛОВИТЕЛИ
В сушильных и абсорбционных башнях сернокислотно-
го производства применяют преимущественно неразбрызгиваю-
щие оросители с так называемой многоточечной подачей кисло-
ты— плиты, желоба, перфорированные коллекторы [200].
Перфорированный коллектор типа «Дорр — Оливер». Уста-
новлены на некоторых системах поставки фирмы «Поимекс»
(ПНР) в башнях диаметром 9 м. Ороситель состоит из уложен-
ного по диаметру башни составного (из трех частей) толстостен-
ного чугунного коллектора £) = 600 мм с боковыми коническими
отверстиями, в которые вставлены заглушенные на торце труб-
чатые отводы с обращенными вверх отверстиями. Над отверсти-
ями помещены отражатели струй. Все устройство смонтировано
на кольцевом выступе башни и засыпано насадкой на глубину
около 1 м. Питание оросителя осуществляется насосами, под-
ключаемыми с двух сторон коллектора. Ороситель прост по
конструкции и способу питания, но при его эксплуатации воз-
никает угроза зарастания отводов и отверстий сульфатами. Де-
монтаж и очистка трубчатых отводов осложнены заглублением
оросителя в слой насадки. Масса оросителя составляет 11 т.
Желоба типа «Кребс» (фирма «Полимекс»). Установлены в
основном на башнях диаметром 8,5—9 м, выполнены из чугун-
ных П-образных секций с торцевыми фланцами и литыми боко-
выми штуцерами, между которыми на фланцах смонтированы
трубчатые вставки, обеспечивающие вертикальное положение и
параллельность желобов. Оросительные трубки (около 1 тыс.
шт. длиной 700—1000 мм, прямые и отогнутые с различными
углами отгиба) установлены в донных отверстиях желоба и
имеют наверху съемную фторпластовую диафрагму, определя-
ющую расход кислоты через каждую трубку. Трубки заглубля-
319
ют в слой брызгоулавливающей насадки на 500—700 мм. Цент-
ральный желоб (или заменяющая его опорная балка) установ-
лен по диаметру башни, перпендикулярно к нему расположены
20 желобов. Центральный желоб изготовлен из спецстали, ос-
тальные желоба чугунные. Масса желоба 10 т.
Система питания желобов включает внешний напорный бак
(D — 2 м, /7 = 3—4 м), к которому присоединен вводимый внутрь
'башни магистральный коллектор, изготовленный из спецстали в
виде трубы (£> = 600 мм), разветвляющейся внутри башни (по
•числу желобов) и имеющей симметрично спаренные отводы
(£) = 300 мм) с диафрагмами в начале отвода и кассетными пер-
форированными уловителями загрязнений на конце отводов.
Общая масса желобов и коллектора питания составляет около
27 т.
Устройство сложно по конструкции, сборка и демонтаж их
осложнены наличием большого числа резьбовых соединений.
Желоба устанавливают совместно с брызгоуловителями (обыч-
но фильтрующего типа), допустимый брызгоунос после кото-
рых не должен превышать 20 мг/м3.
Напорно-сливная плита НИУИФ [199, 200]. Установлена в
башнях диаметром 3—9 м. Изготовлена из листовой спецстали
или чугуна. Плита состоит из огороженных бортами и разде-
ленных межбортовыми каналами подвешенных к крышке сек-
торов с приваренными (или запрессованными в днище при чу-
гунном исполнении оросителя) патрубками, опирающимися на
торец насадки. Бачок питания секторов плиты — типа «Паук»
(7)=1—1,6 м, // = 0,8—1 м) присоединен трубами из спецстали
к внешнему напорному баку (7) = 2 м, //=2 м) или непосред-
ственно к насосам. Патрубки плиты заглушены сверху, забор-
ное отверстие расположено в цилиндрической части трубки,
что обусловливает подачу кислоты насосами с минимальным
разбрызгиванием.
У оросителей этой конструкции отсутствуют резьбовые со-
единения, съемные узлы и детали, а также заглубление трубок
в слой насадки. Стационарно закрепленные на секторах плиты
патрубки (они могут быть выполнены как съемные, например
в чугунных плитах) нижними концами опираются на предва-
рительно выровненный слой насадки (подсыпки) такого же
размера, как основная насадка. Этот слой является вторичным
после плиты распределителем жидкости. Масса плиты из спец-
стали для башен D = 8 м составляет 8—9 т (6=5 мм), а из чу-
гуна— 18 т (6 = 20 мм), масса питательного бачка 0,8—1 т
<200].
К другим типам оросителей сернокислотных башен относятся [200]:
щелевые брызгалки, разбрызгивающие звездочки и механические форсунки.
Щелевые брызгалки в настоящее время применяют как правило
в башнях промывного отделения. Их выполняют в виде вводимых через
крышку башни заглушенных снизу свинцовых или (чаще) фторпластовых
труб, имеющих придонные боковые прорези. Предпочтительными следует счи-
тать брызгалки с увеличенным числом отверстий, выполненных с учетом влия-
320
ния углов наклона верхней н нижней грани прорези и ее высоты для обес-
печения высокой равномерности и полноты смачнвання насадки.
Разбрызгивающие звездочки применяют лишь в производст-
ве серной кислоты по нитрозному методу. Ороситель выполнен как вращаю-
щийся от электропривода, закрепленный на вертикальном валу разорызги-
вающий диск с ребрами различной протяженности, к оси которого из кониче-
ской воронки с диафрагмой подводится кислота.
Механические форсунки, цельнофакельные и с полым факелом
разбрызгивания, используют в первых промывных башнях, в нижней части
скрубберов Свемко (поставки фирмы «Полтмекс» ПНР), а иногда и в элект-
рофильтрах.
Брызгоуловители на сушильных и абсорбционных башнях.
Необходимая степень очистки газа зависит прежде всего от ко-
личества брызг и тумана после башни, которое определяется
температурой и концентрацией кислоты, типом и состоянием
кислотораспределителей.
Современные сернокислотные системы оснащены брызгоуло-
вителями с волокнистыми фильтрующими слоями, расположен-
ными вертикально или горизонтально, которые встроены в баш-
ню либо являются выносными патронными или кассетными ап-
паратами. На старых сернокислотных заводах в качестве брыз-
гоуловителей установлены насадочные башни, которые целесо-
образно применять в сочетании с переливными плитами, генери-
рующими значительное количество брызг. При эксплуатации
усовершенствованных плит степень очистки в насадочных баш-
нях-брызгоуловителях находится на уровне 20—30%.
В системах с одинарным контактированием аппараты для
улавливания брызг и тумана серной кислоты устанавливают по-
сле сушильной башни и конечного абсорбера, а в системах
ДК — также и после промежуточного абсорбера. Суммарное со-
держание брызг (частицы диаметром 3 мкм и более) и тумана
(частицы диаметром менее 3 мкм) серной кислоты перед кон-
тактным аппаратом не должно превышать 5 мг/м3, после абсор-
беров— 20—50 мг/м3.
Брызги эффективно улавливаются в инерционных брызгоуло-
вителях, характеризующихся высокими скоростями газа (1,5—
4,6 м/с) при толщине нити в фильтрующем слое 30—80 мкм и
гидравлическом сопротивлении слоя толщиной 150 мм, равном
200—700 Па. Для повышения степени улавливания брызг и ту-
мана серной кислоты от 80—95 до 90—95% в инерционном
фильтре устанавливают два слоя фильтрующего материала,
при этом сопротивление пропорционально возрастает. В систе-
мах на сере (поставки ПНР) удовлетворительно работают де-
мистеры с горизонтальными слоями полимерных сеток объем-
ного плетения.
В зарубежной практике для очистки от брызг и тумана широко исполь-
зуют диффузионные свечевые фильтры Бринка со стекловолокнистыми гид-
рофобными фильтрующими материалами (диаметр 6—9 мкм, толщина слоя
50 мм) при скорости газа 0,1—0,3 м/с. Степень улавливания в них брызг
100%, а тумана — 99,9%. Фильтры Бринка фирмы «Монсанто» (США) ши-
роко распространены за рубежом, но стоимость их высока, а гидравлическое
сопротивление достигает 4 кПа [75, 199].
21—584
321
В стадии внедрения в промышленность находится комбини-
рованный двухступенчатый фильтр инерционно-диффузионного
типа. Первая ступень — инерционная (скорость газа 3,5 м/с,
степень очистки 85%), вторая ступень —диффузионная (ско-
рость газа 1,5 м/с, степень очистки 95%). Сопротивление филь-
тра около 2,5 кПа [75]. В отечественных инерционных фильт-
рах чаще применяют фторопластовую стружку, расположенную
в вертикальных патронах. В таких фильтрах скорость газа
находится в пределах 1,1—1,5 м/с, сопротивление 0,8—1,5 кПа,
Степень очистки от брызг достигает 90% (при исходном содер-
жании брызг не более 1 г/м3) и от тумана—50%. Высокораз-
витая поверхность фильтров достигается расположением филь-
трующих элементов вертикально по цилиндрической поверхно-
сти полигонного слоя (рис. 104) или в виде патронов (рис. 105,
106). Фильтры, в которых фильтрующий слой уложен между
металлическими сетками, являются самоочищающимися. Их
устанавливают внутри башни или сверху в надстройке либо де-
лают выносными.
В качестве фильтрующих материалов применяются:
1. Фторпластовая стружка размерами (0,1—0,2) X (0,1—0,2) мм. Толщина
слоя 50 мм, пористость слоя 90%, перепад давления 1,0—1,5 кПа), скорость
фильтрации 1,3—1,5 м/с.
2. Фторин (ТУ 6-06-9-30—80). Ширина не менее 150 см, толщина
8±1,5 мм, диаметр волокна 70—80 мкм, воздухопроницаемость 65—15 м3/м2
при перепаде давления 50 Па, пористость 88—90%.
3. Полипропиленовый войлок (ТУ 17-14-77—79). Толщина 10 мм, диаметр
волокна 60—70 мм, пористость 88—90%. Перепад давления 0,8—2,0 кПа,
РИС. 104. Фильтр с вертикальным фильтрующим слоем:
1 — корпус; 2 — фильтрующий слой; 3 — гидрозатвор; 4 — элемент фильтрующего слоя;
5 — прокладка между сетками; ^ — волокно; 7—сетка.
РИС. 105. Патронный фильтр с вертикальным фильтрующим слоем:
а — элемент патронного фильтра (патрон); б — волокнистый фильтрующий слой; 1—во-
локно; 2 — сетка; 3 — гидрозатвор.
322
РИС. 106. Схема встроенного в
башню брызгоуловители патронно-
го типа с вертикальным фильтру-
ющим слоем:
1 — корпус; 2 — фильтровальный пат-
рон-, — фильтрующий слой; 4 — опор-
ная плита.
скорость фильтрации 1,3—-1,5 м/с.
Применяют для сушильных башен.
4. Фторпластовая сетка (по-
ставки ПНР). Леска диаметра
0,25—0,5 мм. Имеются 1 или
2 горизонтально расположен-
ных слоя; высота фильтрующих
слоев на сушильных башнях
350 мм, на абсорбционных — 150—
200 мм; скорость фильтрации 2,5—
4 м/с, перепад давления 0,5—
1,0 кПа.
5. Стеклоткань (поставки ПНР). Патроны диаметром 0,6 м и высотой
1 м имеют 7 фильтрующих слоев, число патронов 27, скорость фильтрации
0,87 м/с, перепад давления 0,3—0,5 кПа.
С целью повышения степени очистки от брызг и тумана раз-
рабатываются принципиально новые фильтрующие материалы
с гидрофобной пропиткой, а также конструкции фильтров, при-
менительно к диффузионному режиму работы при скорости
0,1—0,3 м/с.
VIII.3. ОБОРУДОВАНИЕ ДЛЯ ХРАНЕНИЯ И ПЕРЕВОЗКИ
КИСЛОТЫ
Оборудование для хранения и розлива кислоты [9, 12].
Готовая продукция выпускается непрерывно. Отгрузку же кис-
лоты ведут периодически, поэтому на каждом сернокислотном
заводе имеется склад готовой продукции (рис. 107), располо-
женный в здании или под навесом, предохраняющим от атмо-
сферных осадков верхнюю часть баков-хранилищ, где распола-
гаются люки, распределительные вентили, сифоны и т. д.
Баки готовой продукции представляют собой горизонтальные или (чаще)
вертикальные цилиндрические резервуары емкостью до 3000 м3, изготовленные
из листовой стали. Общая емкость баков на складе рассчитывается иа хра-
нение не менее чем 10-суточной продукции цеха. Обычно устанавливают не-
сколько баков, чтобы можно было производить их чистку и ремонт без оста-
новки цеха. Вдоль баков прокладывается железнодорожный путь "й имеется
специально оборудованная площадка, у которой устанавливают цистерны
для налива кислоты. При заполнении цистерны предусмотрен санитарный от-
сос газов. Концентрированную серную кислоту, содержащую выше 72%
H2SO4, башенную, техническую кислоту и олеум хранят в стальных нефуте-
рованных баках. Баки для олеума имеют тепловую изоляцию и обогреваются
специальными паровыми элементами. Стальные баки для хранения кислоты
более низкой концентрации (улучшенной, аккумуляторной и химически чис-
той) футеруют кислотоупорной керамикой.
В северных районах, где в зимнее время температура воздуха может
быть значительно ниже температуры замерзания серной кислоты, все баки
готовой продукции размещают в отепленном помещении. В средней полосе
и в южных районах баки склада кислоты располагаются вне помещений.
Олеум транспортируется в специальных обогреваемых цистернах.
21*
323
РИС. 107. Схема склада серной кислоты:
1— поглотительный сборник паров олеума; 2, 3 — резервуары для олеума и концентри-
рованной кислоты; 4, 5 — иасосы для перекачивания олеума и концентрированной кис-
лоты; 6 — теплообменник для нагрева олеума; 7 — желоб для сбора проливов кислоты
из сальников насосов; 8 — уткн для подачи кислоты в цистерны; 9 — вакуум-сборник;
10 — кран-укосина; 11— траверса с трубами для подачи кислоты и ее отсасывания иа
цистерн; 12 — цистерны для олеума н концентрированной кислоты; / — олеум; II— кон-
центрированная кислота; /// — вакуумная линия; /V — кислота из поглотительного сбор-
ника; V — линия воздушника; VI — отсос проливов кислоты от сальников насосов.
На складах устанавливают также смесительные установки
для приготовления 92—94 %-ной кислоты и аккумуляторной
кислоты, приспособление для розлива аккумуляторной кислоты
в бутыли и для упаковки этих бутылей.
Оборудование для перевозки серной кислоты. В соответствии
с требованиями потребителей серную кислоту разливают в тару
различной емкости и устройства. Большей частью ее перевозят
на дальние расстояния в железнодорожных цистернах грузо-
подъемностью до 50 т. При отправке небольших партий местным
потребителям пользуются автоцистернами, контейнерами, сталь-
ными бочками емкостью от 0,2 до 1 т и, наконец, стеклянными
бутылями емкостью от 30 до 45 л; аккумуляторную и реактив-
ную кислоты разливают также в стеклянные бутыли емкостью
до 1 л.
Железнодорожная цистерна представляет собой сварной цилиндр, при-
крепленный к раме вагона, имеющий купол для залива кислоты, осмотра и
очистки ее. Цистерна снабжена соответствующими устройствами для подачи
внутрь воздуха и кислоты, а также для слива кислоты. Разгружают цистер-
ну при помощи сифона или сжатым воздухом. В последнем случае через
верхний штуцер ее соединяют с источником сжатого воздуха; кислота выли-
вается по трубе, доходящей до дна цистерны.
324
Если цистерна загрязнена, то ее перед наливом очищают на специальной
установке. Цистерны из-под нефтепродуктов перед наливом в них серной кис-
лоты пропаривают, промывают горячей водой и продувают воздухом. При
попадании влаги в цистерну серная кислота разбавляется и вызывает корро-
зию цистерны. Поэтому все люки и краиы должны быть герметично закрыты
как во время следования цистерны с кислотой, так и порожняком. Акатериал,
из которого изготовляют цистерны, должен быть возможно более однород-
ным во избежание образования гальванических пар, действие которых вызы-
вает коррозию.
В обычных стальных железнодорожных цистернах из углеродистой стали
(Ст. 3 и Ст. 5) перевозят олеум, концентрированную контактную кислоту,
башенную кислоту и меланж. Более слабую серную кислоту перевозят в
стальных цистернах, покрытиях изнутри свинцом или специальными кисло-
тоупорными материалами (полиизобутиленом, винипластом и др.). Для акку-
муляторной и улучшенных сортов серной кислоты применяют цистерны из
кислотостойкой стали.
Стеклянные бутыли для отправки потребителям помещают в корзины или
обрешетки. Промежуток между бутылью и стенкой корзины или переклади-
нами обрешетки заполняют соломой или древесной стружкой.
На каждую цистерну составляется паспорт, в котором указаны сорт сер-
ной кислоты, основные аналитические данные, дата отгрузки и вес. Бочки,
бутыли и другую более мелкую тару снабжают ярлыком (биркой); на ярлы-
ке указывают характеристику и вес серной кислоты.
ГЛАВА IX
КОНСТРУКЦИОННЫЕ МАТЕРИАЛЫ, ПОКРЫТИЯ,
ВОПРОСЫ КОРРОЗИИ
IX.1. ВИДЫ КОРРОЗИОННЫХ РАЗРУШЕНИЙ
борудование сернокислотного производства подверга-
'-'ется почти всем известным видам и типам коррози-
онного воздействия. В разрабатываемых в настоящее время но-
вых процессах производства серной кислоты под давлением бу-
дет наблюдаться и более сложный процесс коррозии — под на-
пряжением.
Коррозия — это процесс химического или электрохимического
воздействия агрессивной среды на материал, приводящий к раз-
рушению металла или изменению физико-химических характе-
ристик неметаллических материалов.
Химическая коррозия протекает в неэлектролитах и сухих
газах или с материалами, взаимодействие которых с агрессив-
ной средой протекает без образования на их поверхности двой-
ного электролитического слоя. Газовая коррозия, протекающая
в сухих газах при отсутствии слоя жидкости на поверхности,
может рассматриваться как электрохимический процесс, в ко-
тором оксидная пленка — окалина выполняет функции электро-
лита. В процессе газовой коррозии на поверхности металла об-
разуется оксидная пленка, защитные свойства которой зависят
от прочности связи с поверхностью металла, прочности самой
325
пленки, ее пористости и других физико-механических характе-
ристик.
В технологических процессах производства серной кислоты
при взаимодействии кислоты с неметаллическими материала-
ми основным видом коррозии принято считать химическую кор-
розию. Химическая стойкость неорганических материалов в кис-
лых средах определяется кислотостойкостью основных оксидов.
При этом неорганические вещества и материалы со значитель-
ным содержанием кристаллических структур более кислото-
стойки, чем аморфные вещества и материалы того же химиче-
ского состава. На практике о химической стойкости материала
неорганического происхождения в данном случае судят по
комплексу свойств, изменяющихся в результате его взаимодей-
ствия с 98%-ной серной кислотой: изменению его прочностных
характеристик, пористости и проницаемости.
Химическая стойкость материалов органического происхож-
дения, кроме химического состава вещества определяется
структурой материала. При оценке химической стойкости этих
материалов важную роль играет изменение физико-механиче-
ских свойств: степени полимеризации (вулканизации), плотно-
сти проницаемости, склонности к деструкции под воздействием
агрессивных сред и др. Кроме того, при оценке возможности
применения того или иного полимера необходимо учитывать
условия его эксплуатации — в качестве самостоятельного за-
щитного покрытия или как непроницаемого подслоя под футе-
ровку. Естественно, в последнем случае степень воздействия аг-
рессивной среды на него снижается.
Электрохимическая коррозия представляет собой сложный
многоступенчатый процесс с цепью химических реакций, харак-
теризуемый анодным и катодным процессами, протекающими
взаимосвязанно. Известно, что поверхность любого даже самого
чистого металла гетерогенна из-за различной ориентации кри-
сталлов и фаз, на ней всегда есть участки с различными элект-
родными потенциалами, которые в растворе электролита будут
представлять собой систему короткозамкнутых гальванических
пар. Применяемые в производстве серной кислоты металлы тер-
модинамически не стабильны и способны легко вступать во вза-
имодействие с раствором электролита. Коррозионная стойкость
металлов и сплавов определяется образованием на их поверхно-
сти абсорбционных и фазовых слоев, тормозящих протекание
анодного и катодного процессов. Эти металлы и сплавы на их
основе получили название пассивирующихся.
Способность поверхностных пленок тормозить протекание
коррозионного процесса не универсальна. Так, углеродистая
сталь весьма устойчива в олеуме и 98%-ной серной кислоте при
20 °C, но в разбавленных растворах серной кислоты корродиру-
ет со скоростью более 100 мм/год из-за непрерывного образова-
ния и растворения пассивной пленки. Образование устойчивых
пассивных пленок в среде серной кислоты различной концентра-
326
ции позволило успешно и рационально применять металлы и
сплавы в производстве этой кислоты.
Высокая коррозионная стойкость нержавеющих сталей ос-
нована на явлении пассивности. Пассивность — это состояние
высокой коррозионной стойкости металла или сплава (в усло-
виях, когда с термодинамической точки зрения они являются
вполне реакционноспособными), вызванное избирательным тор-
можением анодного процесса. Пассивность нержавеющих сталей
зависит от содержания в них хрома как основного легирующе-
го элемента. Наименьшее содержание хрома, обеспечивающее
сталям пассивное состояние, практически составляет 12%.
С увеличением содержания хрома коррозионная стойкость ста-
лей в окислительных средах резко возрастает. Для придания
высокой устойчивости нержавеющие стали легируют хромом,
никелем и молибденом, а также медью, ниобием и другими
элементами, повышающими пассивность и улучшающими фи-
зико-механические характеристики сталей.
Сопротивление материалов действию растворов серной кис-
лоты, а следовательно, и длительность эксплуатации оборудо-
вания зависят от условий воздействия агрессивных сред, их
температуры, концентрации, скорости движения и наличия аб-
разивных частиц. В настоящее время еще нет единых нормати-
вов и требований к противокоррозионной защите оборудования,
которые обязывали бы принимать то или иное решение в зави-
симости от коррозионных условий эксплуатации. Но предусмот-
рено увеличение расчетной толщины стенок аппаратов на 1 мм
для компенсации коррозии под влиянием агрессивной среды.
Технологические среды сернокислотных производств агрес-
сивны по отношению к металлическим и неметаллическим ма-
териалам, причем коррозионное воздействие различно на раз-
ных стадиях технологического процесса. Растворы серной кис-
лоты средних концентраций (20—60% H2SO4) при температу-
ре от 40 до 80 °C (кислота промывных и увлажнительных ба-
шен) обладают высокой коррозионной активностью по отноше-
нию к металлическим материалам ввиду их высокой электро-
проводности и степени диссоциации, но не оказывают разру-
шающего действия на кислотостойкие полимерные материалы.
Серная кислота высоких концентраций (90% H2SO4 и выше)
при температуре от 40 до 80 °C (продукционная и сушильная
кислоты, моногидрат и олеум) разрушают большинство орга-
нических материалов, но не обладают высокой агрессивностью
по отношению к сталям и сплавам, благодаря невысокой элек-
тропроводности и сильным окислительным свойствам.
IX.2. КОРРОЗИЯ МЕТАЛЛОВ, СТАЛЕЙ И СПЛАВОВ
В СЕРНОЙ КИСЛОТЕ И ОЛЕУМЕ
Имеющиеся в литературе [203—209] обширные сведе-
ния по коррозионной стойкости металлов и сплавов в серной
кислоте неоднородны. Расхождение многих данных связано с
327
различием в методиках испытаний, но главным образом с раз-
личием коррозионной активности кислоты, взятой для испыта-
ния, которая зависит от способа ее производства (башенная
или контактная, из серы или из колчедана, с отдувкой SO2
или без нее).
Коррозионную стойкость чистых металлов, сталей и сплавов
устанавливают в соответствии с ГОСТ 13819—68 по десяти-
балльной шкале. В качестве основной характеристики корро-
зионной стойкости нержавеющих сталей принята скорость кор-
розии, выраженная в миллиметрах в год. Однако при опреде-
лении общей равномерной коррозии часто пользуются массо-
вым показателем скорости коррозии, т. е. определяют потерю
массы образца за определенный промежуток времени, отнесен-
ный к единице площади [г/(м2-ч)]. Пересчет массовых потерь
на линейные (мм/год) производят по формуле
8,76К
п =------
где П — проницаемость (глубинный показатель коррозии), мм/год; у — плот-
ность металла, г/см3; К — потеря массы, г/(м2-ч).
Ниже приводятся некоторые данные по коррозионной стой-
кости чугунов, углеродистых сталей, нержавеющих сталей и
сплавов, полученные нами экспериментально для растворов
серной кислоты и олеума различных концентраций при различ-
ных температурах.
1. Чугуны. Чугуны применяют для изготовления насосов, арматуры, тру-
бопроводов, холодильников, отдельных элементов и оборудования, предназна-
ченных для эксплуатации в присутствии серной кислоты концентрацией бо-
лее 70% при температуре 30—70 °C.
В концентрированных растворах серной кислоты иа поверхности чугуна
образуются труднорастворимые сульфаты и оксиды железа, которые надеж-
но защищают его от дальнейшего разрушения. Максимальная скорость кор-
розии чугуна наблюдается в серной кислоте концентрации 50% и ниже.
При наличии в кислоте свободного SO3 (10—24%) чугун более коррози-
онно стоек, чем углеродистая сталь. В серной кислоте с высоким содержани-
ем SO3 (более 10%) наблюдается растрескивание чугуна, объяснимое прони-
канием в поры чугуна триоксида серы, в результате чего протекает реакция
с образованием диоксида кремния. Объем продуктов реакции значительно
превышает первоначальный объем, что и приводит к образованию трещин.
Чугун с шаровидным графитом обладает лучшими механическими свой-
ствами, чем серый чугун, и более высокой коррозионной стойкостью. К чугун-
ным сплавам, обладающим высокой стойкостью в растворах серной кислоты,
относится ферросилид, содержащий 14,5—18% кремния и сплав «антихлор»,
дополнительно легированный 3,5—5,0% молибдена. Эти сплавы устойчивы в
растворах серной кислоты прн температуре кипения; даже в этом случае
скорость коррозии не превышает 0,15 мм/год. Ферросилид и антихлор не при-
меняются в среде олеума из-за склонности к растрескиванию.
2. Углеродистые стали. Углеродистые стали не устойчивы в растворах
серной кислоты концентрации ниже 65%. Окислительные свойства этих рас-
творов, повышение температуры растворов интенсифицирует процесс корро-
зии. С повышением концентрации кислоты до 75% и выше скорость корро-
зии снижается, а в присутствии оксидов азота, сопутствующих башенному
процессу производства серной кислоты, скорость коррозии углеродистой ста-
ли устанавливается иа уровне 0,1 мм/год. Углеродистая сталь устойчива в
328
98%-ной серной кислоте при обычной температуре, однако хранение и транс-
портировка кислоты в стальных емкостях приводит к повышенному содержа-
нию в ней железа, что делает кислоту непригодной для целого ряда потре-
бителей. Углеродистая сталь устойчива в олеуме, благодаря чему его пере-
возят в стальных цистеинах. На коррозионную стойкость углеродистой стали
в концентрированных кислотах большое влияние оказывает движение кис-
лоты.
Стальные корпуса аппаратов сушильно-абсорбционного отделения подвер-
гаются сквозной коррозии в тех местах, где футеровка имеет «пустошовку»,
т. е. незаполненный замазкой шов. Наварка металлических заплат на повреж-
денное место не предотвращает коррозии. Однако, если при остановке башни,
закачать в поврежденное место силикатную замазку и наварить «карман»,
также заполнив его силикатным раствором, коррозия на данном участке пре-
кратится.
Углеродистые стали подвержены интенсивной коррозии в случае разбав-
ления кислоты. Так, в стальных нефутерованных хранилищах серной кислоты
наблюдается интенсивная коррозия корпуса при частых опорожнениях аппа-
рата, так как остающаяся на стенках кислота, сорбируя влагу воздуха, раз-
бавляется.
3. Нержавеющие стали. Нержавеющие стали достаточно широко и успеш-
но применяются в сернокислотном производстве. С увеличением мощности си-
стем и совершенствованием технологии производства серной кислоты, количе-
ство и ассортимент используемых нержавеющих сталей возрастают.
На скорость коррозии нержавеющих сталей существенное влияние ока-
зывает наличие примесей, содержащихся в серной кислоте. В Приложении
XVI приведены результаты испытаний нержавеющих сталей в серной кислоте.
Из представленных данных следует: наибольшей коррозионной стойкостью
обладает сталь 06ХН28МДТ (ЭИ-943), однако область ее применения весьма
ограничена — в 20%-ной H2SO4 до 75 °C и в 30%-ной до 70 °C. При высоких
концентрациях серной кислоты (более 80%) сталь ЭИ-943 стойка при тем-
пературе до 90 °C.
При концентрации серной кислоты более 80% и обычной температуре
стали 08Х22Н6Т (ЭП-53), 08Х21Н6М2Т (ЭП-54), 10Х17Н13М2Т (ЭИ-448) и
12Х18Н10Т (ЭЯ-1Т) являются коррозионностойкими.
Наличие растворенного в серной кислоте SO2 увеличивает коррозию не-
ржавеющих сталей (табл. 64).
Наряду с деформируемыми сталями и сплавами при изготовлении насо-
сов, арматуры, трубопроводов, форсунок, решеток и отдельных деталей обо-
рудования широко используются литейные стали и сплавы. Их коррозионная
стойкость в серной кислоте как правило мало отличается от стойкости дефор-
мируемых материалов. В малоагрессивных растворах серной кислоты приме-
няются углеродистая сталь, ферросилид, чугун серый и высокопрочный (с ша-
ровидным графитом). Однако наиболее часто в производстве серной кислоты
используются литейные нержавеющие стали и сплавы. Скорость коррозии
сталей в серной кислоте и олеуме, а также области применения литейных
материалов в растворах серной кислоты приведены в Приложениях XVI—
В настоящее время разработан новый перспективный литейный конструк-
ционный материал — сталь марки 90Х28МФТАЛ (ТУ 2606-1231—79) для ма-
Таблица 64. Скорость коррозии нержавеющих сталей в 92 %-ной
серной кислоте с различным содержанием SO2, мм/год
Марка стали / = 50°С / = 70 °C
7.8% SO2 | без SO2 3,35% SO2 | без SOa
06X21Н5Т (ЭП-53) 1,275 1,02 2,248 1,786
08Х21Н6М2Т (ЭП-54) 0,204 0,128 1,807 1,134
12Х18Н10Т (ЭЯ-1Т) 0,159 0,127 1,2826 0,683
329
лоагрессивных сред производства серной кислоты и других технологических
сред [208]. Наряду с экономнолегированным составом (не содержит никеля)
сталь 90Х28МФТАЛ обладает хорошими литейными и технологическими
свойствами. Имеются две области концентраций серной кислоты, в которых
новая сталь обладает высокой коррозионной стойкостью—до 35% H2SO4
при температуре 60 °C и в концентрированной кислоте при температуре 60—
80 °C. При этом скорость коррозии не превышает 0,3 мм/год.
Достоинством нового литейного материала является его высокое сопро-
тивление гидроабразивному износу. В связи с этим сталь 90Х28МФТАЛ ре-
комендована для изготовления проточной части пульповых насосов и показа-
ла при испытаниях высокую коррозионную и эрозионную стойкость, что обес-
печивает эксплуатационную надежность и высокий ресурс работы насосов.
4. Никель и его сплавы можно успешно применять в растворах серной
кислоты. Монель — сплав никеля с медью, характеризуется большой однород-
ностью и высокими механическими свойствами. Хастеллой — сплав, содержа-
щий в качестве основных компонентов никель, молибден, железо и другие
элементы, отличается хорошими механическими свойствами и высокой корро-
зионной стойкостью. Ранее известные коррозионностойкие сплавы на основе
никеля имеют следующий состав: монель — 70% Ni, 30% Си, хастеллой А и
В — Н70М27Ф, хастеллой С — Х15Н55М16В (ЭП-567) и другие (ГОСТ
5632—72). При обычной температуре монель устойчив в серной кислоте и
применяется для изготовления теплообменников, насосов.
С развитием химической промышленности потребовались и были разра-
ботаны новые сплавы: Ni — Fe — Cr — Мо и Ni — Fe — Cr — Mo—Си как
деформируемые, так и литые, отличающиеся высокой коррозионной стой-
костью в серной кислоте (скорость коррозии их не превышает 0,25 мм/год).
При увеличении содержания молибдена до 29% и выше коррозионная стой-
кость сплавов на основе никеля повышается, однако образующиеся при этом
молибдениты никеля заметно снижают пластичность сплава и затрудняют его
сварку. Дополнительным преимуществом этих сплавов является то, что на
их коррозионную стойкость не оказывает существенного влияния присутст-
вие диоксида серы.
Наилучшей коррозионной стойкостью в серной кислоте различной кон-
центрации в широком интервале температур обладает сплав Хастеллой В или
аналогичный отечественный сплав Н70М27Ф (ЭП-496). Однако невысокие
технологические свойства значительно ограничивают его использование как
конструкционного материала.
Сплавы 03ХН60МБ (ЭП-758) и ХН54МДСЛ, разработанные в послед-
ние годы, обладают высокой коррозионной стойкостью в серной кислоте при
повышенных температурах. Сплав ЭП-758 применим практически в серной
кислоте любой концентрации при температуре вплоть до 90 °C. Новый литей-
ный сплав ХН54МДСЛ (ТУ 2601-295—79) применим при 100 °C в серной кис-
лоте концентрации до 30% и 65—98%, при более низких температурах сплав
стоек в кислоте любой концентрации [208]. Необходимо отметить, что сплав
ХН54МДСЛ характеризуется хорошими литейными свойствами — жидкоте-
кучестью, малой склонностью к трещинообразованию, что позволяет исполь-
зовать его при изготовлении литых деталей сложной конфигурации — проточ-
ной части химических насосов, арматуры и др. Наряду с коррозионной стой-
костью этот сплав обладает высоким сопротивлением гидроабразивному из-
носу в средах, содержащих взвеси твердых частиц (пульпах).
Высокой коррозионной стойкостью в серной кислоте обладают сплавы
Н70М26Л и Н65М30Л, которые используют для отливки труб, насосов, ар-
матуры.
5- Свинец. Свинец используют в качестве конструкционного материала
для изготовления химической аппаратуры, предназначенной для работы в
растворах серной кислоты при ее производстве, хранении и перевозке. Для
изготовления химической аппаратуры применяют свинец С2, содержащий не
менее 99,92% РЬ и обладающий высокой коррозионной стойкостью в раство-
рах серной кислоты концентрацией от 5 до 85% при температурах до 80°C.
Стойкость свинца в растворах серной кислоты объясняется образованием на
его поверхности пленки, состоящей из труднорастворимого сульфата свинца.
330
Концентрированная серная кислота способна растворять сульфат свин-
ца, поэтому свинец рекомендуется применять при концентрации кислоты не
более 85% и температуре не выше 100 °C. Следует учитывать, что поврежде-
ние сульфатной пленки на свинце, например при эрозии, вызванной потоками
жидкостей с взвесями, скоростными потоками чистых жидкостей и даже пото-
ками газов с брызгами кислоты, также может привести к коррозионному
разрешению свинца.
6. Медь. Медь отличается достаточной коррозионной стойкостью в сер-
ной кислоте при условии, что концентрация раствора не превышает 80%, в
этом случае скорость коррозии при 20 °C не превышает 0,1 мм/год. При бар-
ботаже кислорода через раствор серной кислоты скорость коррозии меди рез-
ко возрастает.
Коррозионная стойкость сталей и сплавов в олеуме. В лите-
ратуре мало освещены процессы коррозии в олеуме, что по
всей видимости связано с экспериментальными трудностями и
высокими требованиями по технике безопасности. В Приложе-
нии XVI приведены результаты коррозионных испытаний угле-
родистой стали (Ст. 3) и наиболее распространенных нержа-
веющих сталей в олеуме. Опыты проводились в течение 100 ч
при ежесуточной смене раствора. Как следует из приведенных
данных, с увеличением концентрации олеума от 11,5 до 24%
SO3 (своб.) заметного изменения скорости коррозии всех ис-
пытанных материалов не наблюдается. При этом различие в
скоростях коррозии высоколегированных нержавеющих сталей
и экономнолегированных нержавеющих сталей незначительно.
Общей закономерностью является рост скорости коррозии с
увеличением температуры олеума от 100 до 160 °C.
IX.3. МАТЕРИАЛЫ ПРОТИВОКОРРОЗИОННОЙ ЗАЩИТЫ
Высокая агрессивность серной кислоты по отношению
к чистым металлам, сталям и сплавам потребовала применения
для аппаратурного оформления сернокислотного производства
полимерных материалов, кислотоупорных вяжущих на основе
фенолоформальдегидных смол и жидкого стекла, материалов
на основе каучуков и других.
Противокоррозионная защита основного технологического
оборудования осуществляется путем применения комплекса
материалов, каждый из которых выполняет определенные
функции. В случае применения технологического оборудова-
ния сложной конструкции (например, Пой промывной башни)
противокоррозионная защита состоит из подслоя рольного
свинца, подслоя полиизобутилена, подслоя асбеста и двуслой-
ной футеровки кислотоупорным кирпичом на силикатной замаз-
ке с расшивкой швов замазкой арзамит.
Функции каждого слоя заключаются в следующем. Подслой свинца яв-
ляется непроницаемым подслоем, предохраняющим стальной корпус аппара-
та от воздействия серной кислоты. Его применяют в наиболее ответственных
и нагруженных механически узлах и аппаратах. Подслой полиизобутилена
выполняет функцию второго непроницаемого эластичного подслоя, который,
повышая деформативность конструкции, дополнительно герметизирует под-
слой свинца. Поскольку верхний температурный предел применения полинзо-
331
бутилена равен +60°C, поверх него наклеивают на жидком стекле листовой
асбест, который снижает температурное воздействие на подслой и дополни-
тельно придает эластичность конструкции.
Футеровочное покрытие выполняется из штучных кислотоупорных мате-
риалов на диабазовой или андезитовой замазке. Общая толщина покрытия
рассчитывается из условия совместной работы корпуса аппарата, подслоя и
футеровки, а также ее статической устойчивости. Учитывая пористость футе-
ровки и низкий коэффициент ее термического расширения применяют двух- и
трехслойные футеровочные покрытия, достигающие толщины 230 мм и более.
В условиях работы промывного отделения сернокислотного производства по-
следний, внутренний слой футеровки выполняется на силикатной замазке с
расшивкой швов замазкой арзамит. Это мероприятие предохраняет силикат-
ную замазку от вымывания слабыми растворами кислот и повышает непро-
ницаемость швов. Однако, несмотря на комплекс мероприятий, непроницае-
мость футеровки в большинстве случаев не достигается.
Полимерные материалы находят все более широкое приме-
нение в практике противокоррозионной защиты и вытесняют
традиционный и дорогостоящий свинец.
Проводятся поисковые работы по замене свинцовых осадительных элект-
родов мокрых электрофильтров на винипластовые и стеклопластиковые.
К числу наиболее распространенных материалов, применяемых в качестве
непроницаемого подслоя, относится полиизобутилен. Мягкий полиизобутилен
ЯПСГ и жесткий полиизобутилен ПСГ выпускаются по ТУ 38-105203—70.
Оклейка пластинами полиизобутилена производится на клее 88-Н, СН-57 и
СН-58. Полиизобутилен устойчив в серной кислоте концентрации не выше
60% до температуры 60 °C.
В настоящее время разработано и широко применяется в качестве не-
проницаемого подслоя под футеровку, а в некоторых случаях и как само-
стоятельное покрытие, латексное покрытие «Полан». Покрытие «Полан» пред-
ставляет собой композицию, наносимую на металлическую поверхность мето-
дом воздушного распыления в 10—15 слоев с сушкой каждого слоя при
температуре 25—30 °C. Расход «Полана» — 6 кг иа 1 м2 защищаемой поверх-
ности. При этом образуется сплошное высокоэластичное бесшовное покрытие.
«Полан» может с успехом применяться в серной кислоте концентрации ие вы-
ше 60% до температуры 100 °C, а также для защиты железобетонных по-
верхностен.
Наиболее распространенные замазки, применяемые в сер-
нокислотном производстве, представляют собой вяжущие, за-
творяемые на водном растворе жидкого стекла. Ускорителем
твердения является кремнефторид натрия, наполнителем слу-
жит диабазовая или андезитовая мука. Силикатные замазки ус-
тойчивы в серной кислоте любых концентраций вплоть до тем-
пературы кипения.
Замазка «Арзамит» представляет собой полимерную замазку на основе
фенолоформальдегидных смол с наполнителем — молотым графитом, содер-
жащим отвердитель. Замазка устойчива в серной кислоте концентрацией не
выше 70% при температуре до 115 °C. Следует напомнить, что в процессе
полимеризации замазки изменяются в объеме и растрескиваются при толщи-
не швов более 7 мм. Замазки иа основе эпоксидных и полиэфирных связую-
щих применяются реже. Из них предпочтительнее полиэфирные замазки, об-
ладающие более высокой химической и термической стойкостью. К их недо-
статкам следует отнести сложность производства работ с ними, так как при
приготовлении растворов требуется точная дозировка и введение в строгой
последовательности двух или трех компонентов — отвердителя, катализатора
и окислителя.
332
Штучные кислотоупорные изделия широко применяются в
сернокислотном производстве. В зависимости от сорта они име-
ют кислотостойкость 95—97%, водопоглощение 9—7% и предел
прочности при сжатии 30—40 МПа (300—400 кгс/см2).
С 1970 г. отечественной промышленностью начат выпуск шпунтованных
и фасонных кислотоупорных изделий по ТУ 21-УССР-73—77 и
ТУ 21-РСФСР-465—77. Применение этих изделий повышает надежность про-
тивокоррозионной защиты за счет повышения устойчивости футеровки и ка-
чества швов. Перспективными для сернокислотных башен представляются
крупноблочные кислотоупорные изделия, предназначенные для выполнения
«опор под насадку, которые выпускают по ТУ 21-УССР-74—77.
Резины и резиновые технические изделия не находят широ-
кого применения в сернокислотных производствах и применя-
ются главным образом в виде прокладочных материалов для
гуммированных насосов, а также гуммированной и шланговой
запорной арматуры в условиях промывного отделения.
В серной кислоте концентрации выше 60% могут применяться резины на
«основе фторкаучуков, например ИРП-1225, ИРП-1227 и ИРП-1345. Однако
эти резины вследствие невысоких показателей физико-механических свойств,
значительной трудности крепления их к металлической поверхности, невысо-
кой деформативностн применяются главным образом как прокладочные ма-
териалы в пластинчатых н других холодильниках.
Резины на основе изопренового, нитрильного, этилен-пропиленового, ме-
тилметастнрольного н бутилового каучуков устойчивы в серной кислоте кон-
центрацией не выше 60%. Так, в 40%-ной серной кислоте при 70 °C устойчи-
вы резины марок 1434, 50-3042, 1481, ИРП-1287, 1348, 4004 и 3825.
В 60%-ной серной кислоте при 70 °C — резины 1348, 1481, 51-3042, ИРП-1287,
11-18 и 1334; при 100°С — резины 1481, 51-3042, ИРП-1287 и 11-18.
Все вышеуказанные резины могут быть рекомендованы к применению,
главным образом, в виде формованных изделий, т. е. вкладышей арматуры,
клапанов и т. д.
IX.4. МАТЕРИАЛЫ ДЛЯ ОБОРУДОВАНИЯ
На рис. 108 представлена схема рационального приме-
нения нержавеющих сталей и материалов химической защиты
в сернокислотной системе мощностью 360 тыс. т в год с воздуш-
ными холодильниками. Ниже приведены экспликация и харак-
теристика оборудования (материал, масса) этой системы:
1 — конвейер; 2 — электровибратор; 3 — пересыпное устройство; 4 — питатель
тарельчатый; 5 — печь (3 шт., 12Х18Н10Т, 1320 кг); 6 — пересыпное устрой-
ство с пода печн (3 шт., 12Х18Н10Т, 1800 кг); 7—пересыпное устройство с
перелива печн (3 шт., 12Х18Н10Т, 1800 кг); 8— двойной секторный затвор
(6 шт., 12Х18Н10Т, 816 кг); 9 — ловушка для крупных фракций огарка
(60 шт., 12Х18Н10Т, 4380 кг); 10 — котел-утилизатор (3 шт.); 11 — циклон
(12 шт.); 12— двойной затвор «мигалка» (9 шт., 12Х18Н10Т, 1315 кг);
13— электрофильтр (6 шт.); 14 — топка для разогрева электрофильтров
(1 шт., 12Х18Н10Т, 18 кг); 15—I промывная башня (1 шт.), 16— насос цент-
робежный 8Х-9И-1 (6 шт., 06ХН28МДТ, 180 кг); 17—сборник I и II про-
мывных башен (3 шт., 06Х28НМДТ, 480 кг): 18 — оросительный холодильник
(34 шт.); 19—II промывная башня (1 шт.); 20— электрофильтр (4 шт.);
21 — гидрозатвор (1 шт.); 22 — насос центробежный 2АХ-44-1 (5 шт.,
Ю6Х28НМДТ, 185 кг); 23 — сборник для отфильтрованной кислоты (1 шт.);
24 — пульпатор (2 шт.); 25— насос центробежный 4Х-6И-1 (2 шт.,
©6Х28НМДТ, 130 кг); 26— фильтр патронный (2 шт.); 27—сборник к олеум-
333
GO
W
На склад
РИС. 108. Схема производства серной кис-
лоты на колчедане мощностью 360 тыс. т в
год. Применение спецсталей в технологиче-
ском процессе (см. текст на стр. 333 и 336).
335
ному абсорберу (I шт.); 28—II моиогидратиый абсорбер (1 шт.,
08X2IH6M2T, 9460 кг); 29— иасос погружной 9ХП-9Е-1 (16 шт.,
10Х17Н13М2ТЛ, 9600 кг); 30 — кислотопроводы (12Х18Н10Т, 28110 кг);
31— холодильник воздушный (24 шт., 12Х18Н9Т— 11280 кг, 10Х17Н13М2Т—
208440 кг, 12Х18Н10П — 2460 кг); 32 — напорный бак ко II моногидратному
абсорберу (1 шт.); 33 — кислотопроводы (08Х22Н6Т, 42500 кг); 34 — олеум-
ный абсорбер (1 шт.); 35— холодильник к олеумному абсорберу (5 шт.);
36— брызгоуловитель (2 шт.); 37 — сборник к I и II моногидратиым абсор-
берам (1 шт.); 38— моногидратный абсорбер (1 шт., 08Х21Н6М2Т, 9460 кг);
39 — напорный бак к I моногидратному абсорберу (2 шт., Вст. Зсп5 +
+ 10Х17Н13М2Т—1640 кг, 10Х17Н13М2Т — 440 кг); 40 — иасос погружной
4ХП-9Е-2 (2 шт., 10Х17Н13М2ТЛ, 250 кг); 41 — сборник к отдувочной башне
(1 шт., 10Х17Н13М2ТА — 220 кг, Вст. сп5 + 10Х17Н13М2Т —820 кг); 42 —
отдувочная башня (1 шт., 10Х17Н13М2Т — 260 кг, 12Х18Н9Т — 60 кг);
43 — кислотопроводы (0,8Х22Н6Т— 46550 кг); 44 — напорный бак к сушиль-
ной башне (1 шт.); 45— сушильная башня (1 шт., 10Х17Н13М2Т, 9460 кг);
46— кислотопроводы (10Х17Н13М2Т, 20020 кг); 47—насос погружной
5УП-6Е-2 (2 шт., 10Х17Н13М2Т, 720 кг); 48 — смеситель (1 шт., 06Н28МДТ,
52 кг); 49 — сборник к смесителю (1 шт., Вст. сп5+10Х17Н13М2Т — 820 кг,
10Х17Н13М2Т — 220 кг); 50 — нагнетатель (1 шт.); 51 — фильтр-брызгоуло-
витель (1 шт., 12Х18Н10Т, 350 кг); 52 — теплообменник (4 шт.); 53—тепло-
обменник (2 шт., 12Х18Н10Т, 247440 кг); 54 — контактный аппарат (1 шт.,
12Х18Н10Т, 95180 кг); 55 — теплообменник (1 шт.); 56 — центрифуга (2 шт.,
12Х18Н10Т, 1200 кг); 57 — вакуум-сушилка (2 шт., Вст. сп5+12X18H1QT —
2380 кг, 12Х18Н10Т-—2630 кг); 58 — пусковой подогрев № 2 (1 шт.); 59 —
пусковой подогреватель № 1 (1 шт., 12Х18Н10Т, 26350 кг); 60 — топка
(1 шт.); 61 — насос центробежный 6Х-9Е (4 шт., 10Х17Н13М2Т, 120 кг);
62— кислотопроводы 08Х21Н6М2Т, 16000 кг); 63 — резервуар (4 шт.,
10Х17Н13М2Т, 120 кг).
В печном отделении, работающем иа колчедане, где наиболее распростра-
ненным видом коррозии является газовая коррозия, в основном применяется
сталь 12Х18Н10Т — благодаря универсальности ее свойств, сочетающих жа-
ростойкость и коррозионную стойкость.
^)то XTZQ ЛТОП1. Пдт/Аиаи ТТ !гатг<7 TZ ГТ ПТГИОГТОГТТПЛ ТТ г». П/ЛЧПЛ11 А^ППНАППТ,
О' 1 Ы j 1 VZ1 14. llyXlXTl Vll V11X1IM XI U VJ 1 XI, JJClkZkJ"
тающем на сере. Жидкая сера не является сильно агрессивной средой, однако
в большинстве случаев сера, поступающая иа обжиг, содержит значительное
количество примесей, состав и содержание которых постоянно меняется и су-
щественно влияет на коррозию. Испытания нержавеющих сталей, проведен-
ные в печном отделении сернокислотного цеха в течение 8 мес., показали, что
стали 08Х22Н6Т (ЭП-53) н 08Х21Н6М2Т (ЭП-54) не устойчивы в плавлеиной-
технической сере, скорость коррозии их составляла 0,37—0,28 мм/год. Следо-
вательно, узлы оборудования, работающие в контакте с плавленой серой, сле-
дует изготовлять из стали 12Х18Н10Т. В газовой фазе над плавленной серой
достаточно устойчивой является углеродистая сталь.
Корпуса аппаратов печного отделения выполнены из стали и футерова-
ны шамотным кирпичом. В промывном отделении корпус первой промывной
башни защищают на всю высоту рольным свинцом, оклеивают полиизобути-
леном или по свинцу наносят композицию «Полан», затем футеруют кислото-
упорным кирпичом на андезитовой или диабазовой замазке с расшивкой
швов замазкой арзамит. Корпус второй промывной башни защищают свин-
цом по днищу и на высоту 1200 мм, затем оклеивают полиизобутиленом или
иа весь корпус наносят «Полан». Затем башню футеруют кислотоупорным
кирпичом на силикатной замазке с расшивкой швов замазкой арзамит.
Крышки башенной аппаратуры промывного отделения защищают гомогенным;
свинцеванием, что при качественном выполнении работ создает достаточно
надежное покрытие. Однако более перспективным представляется примене-
ние иа крышках полимерных защитных покрытий или крышек из кислото-
стойкого полимербетона.
Сборники кислот защищают полиизобутиленом или <Поланом» (во всех
случаях применение «Полана» предпочтительнее), с последующей футеровкой
336
кислотоупорным кирпичом иа силикатной замазке с расшивкой швов замаз-
кой Арзамит.
Традиционным материалом оросительных холодильников являлся свинец.
Однако вследствие дефицитности свинца в настоящее время его почти ие-
применяют, а оросительные холодильники промывного отделения выполняют
из аптегмита, представляющего собой наполненную графитом фенолоформаль-
дегидиую или бакелитовую смолу, отвержденную в прессформе. Наряду с
теплообменниками их антегмита находят применение и оросительные тепло-
обменники из стекла и армированного стекла. Ответственной частью ороси-
тельных холодильников являются поддоны, которые представляют собой же-
лезобетонные емкости с установленными в них секциями оросительных холо-
дильников. Поддоны защищают полиизобутиленом или «Полаиом» с после-
дующей футеровкой кислотоупорным кирпичом по диабазовой замазке с
расшивкой швов замазкой арзамит.
Электрофильтры имеют стальной корпус, футерованный аналогично вто-
рой промывной башне. Осадительные электроды выполнены в виде свинцо-
вых шестигранных труб. Известны случаи применения полимерных материа-
лов для изготовления осадительных электродов и корпусов электрофильтров.
Наиболее перспективным является применение стеклопластиков для осади-
тельных электродов.
Коммуникации промывного отделения выполнены из стальных освинцо-
ванных труб, бронированного полипропилена, фторпласта. Одиако полипропи-
леновые коммуникации недостаточно надежны из-за частых обрывов поли-
пропилена по фланцам. При изготовлении фторпластовых коммуникаций тре-
буется проводить отбортовку фторпласта по фланцам с нагревом в пресс-
форме. Выполнять повороты и отводы из фторпласта ие удается. В условиях
промывного отделения устойчивой нержавеющей сталью является только
сталь 06Х28МДТ (ЭИ-943), которая используется для изготовления вставок
и переходов освинцованных труб, насосов, штуцеров и арматуры. Коррозион-
иостойки в этих условиях и высоколегированные сплавы на никелевой осно-
ве, одиако из-за дефицитности компонентов и высокой стоимости применение-
этих сплавов ограничено.
В контактном узле могут использоваться хромистые стали, содержащие
более 12% хрома, одиако из-за низкой технологичности этих сталей в кон-
тактном отделении, так же как и в печном, применяется сталь 12Х18Н10Т.
Наиболее рационально использовать здесь стали, экоиомнолегированные по-
иикелю, ио обладающие высокой жаростойкостью и жаропрочностью в серо-
содержащих средах. Корпус контактного аппарата футерован шамотом, иефу-
тероваииые части аппарата защищаются металлизацией алюминием, т. е. на-
пылением алюминия, расплавленного в пламени пропановой горелки, или при
помощи электродугового аппарата. Трубы выносных теплообменников али-
тируются.
Полки контактного аппарата в условиях воздействия горячего сернистого
газа и триоксида серы испытывают значительные нагрузки контактной мас-
сы. Несмотря иа широкий ассортимент жаропрочных сталей, устойчивых в
среде диоксида серы, применение стали 12Х18Н10Т в этих условиях оказы-
вается наиболее оправданным.
В условиях сушильио-абсорбциоииого отделения применимы стали
08Х22Н6Т, 08Х21Н6М2Т, 12Х18Н10Т и 10Х17Н13М2Т, одиако области их
применения ограничены верхним температурным пределом коррозионной стой-
кости. В среде сушильной и отдувочной башен при температуре выше 50 °C
устойчива сталь 10Х17Н13М2Т, которая применяется для изготовления ком-
муникаций кислоты, поступающей на холодильники. Коммуникации, установ-
ленные после холодильников, могут быть выполнены из экономиолегирован-
ных сталей 08Х22Н6Т или 08Х21Н6М2Т.
Стальные корпуса башенной и емкостной аппаратуры сушильно-абсорб-
ционного отделения футерованы кислотоупорным кирпичом на силикатной за-
мазке. В качестве подслоя применяют асбест, однако целесообразность его
использования спорна, так как наклеенный иа жидком стекле на корпус ап-
парата он не обеспечивает необходимой деформативности. Распределитель-
ные решетки в сушильных башнях обычно выполнены из чугуна, ио иаибо-
22—584
337
.лее надежными являются решетки из стали 10Х17Н13М2Т. В олеумном аб-
сорбере распределительные решетки выполнены из углеродистой стали, а в
мопогидратных абсорберах — из чугуна.
Коммуникации сушильно-абсорбционного отделения выполнены из чугу-
на, однако они мало надежны и оказывают отрицательное влияние на каче-
ство выпускаемой кислоты. Коммуникации 1-го моногидратного абсорбера до
холодильника целесообразно выполнить из стали 10Х17Н13М2Т, а коммуни-
кации от холодильника до абсорбера — из стали 08Х21Н6М2Т. Цикл второго
моногидратного абсорбера наиболее рационально выполнить из сталей
08Х22Н6Т и 08X21Н6М2Т.
Оросительные холодильники сушильного и моногидратного циклов как
правило выполнены из чугуна, а олеумного цикла — из углеродистой стали
(Ст. 20). Кожухотрубчатые, спиральные, воздушные и пластинчатые холо-
дильники сушильного цикла должны быть изготовлены из стали
10Х17Н13М2Т. Такие же холодильники моногидратного цикла должны быть
нз стали 12Х18Н10Т.
Защиту оборудования установки улавливания отходящих газов сернокис-
лотных производств целесообразно рассмотреть на примере озонокаталитиче-
ской установки, поскольку в ней используется большинство материалов. Аб-
сорберы и циркуляционные сборники защищены аналогично оборудованию
промывного отделения, т. е. стальной корпус оклеен полиизобутиленом в два
слоя с проваркой швов или защищен композицией «Полан» и затем футеро-
ван кислотоупорным кирпичом на силикатной замазке с расшивкой швов за-
мазкой арзамит. Коммуникации изготовляют из освинцованной стали, перехо-
ды, тройники, штуцера и другую арматуру—-из стали 06ХН28МДТ. Приме-
нение полимеров и гуммировки не желательно, потому что старение полимер-
ных материалов может интенсифицироваться от воздействия окислителей и
пиролюзита. Электрофильтры защищены рольным свинцом. Коммуникации
озона выполнены из стали 06Х22Н6Т.
Установки сульфитно-бисульфитной очистки не отличаются по защите
оборудования и коммуникаций от установок улавливания отходящих газов
озонно-каталитическим способом. Газоходы этих установок изготовлены из
алюминия или титана.
На ритмичную работу сернокислотного производства существенно влияют
правильный выиор насосов и условия их эксплуатации. Применение в серно-
кислотном производстве насосов с кислотостойкими покрытиями или из не-
металлических материалов дает значительную экономию легированной стали
при увеличенной химической стойкости и долговечности. Насосы изготовляют
с гуммированной прочной частью, из пластмасс и фарфора. Пластмассовые
насосы марки 1,5Х-4П, ЗХ-6П н др. Целиноградского насосного завода пред-
назначены для перекачивания чистой серной кислоты плотностью до
1300 кг/м3 при температуре 60 °C. Корпуса этих насосов, а также передние
и задние крышки изготовлены из полипропилена и фенолита, рабочие коле-
са— из пластмасс с запрессованной металлической втулкой. Для перекачи-
вания серной кислоты любой концентрации при температуре до 80 °C можно
применять фарфоровые насосы типа X — Ф Славянского керамического за-
вода. Детали проточной части этих насосов выполне<чы из фарфора и для
.защиты от механических повреждений заключены в металлический корпус
(см. Приложение XIX).
338
ГЛАВА X
КОНТРОЛЬ И АВТОМАТИЧЕСКОЕ РЕГУЛИРОВАНИЕ
ПРОЦЕССОВ
ПРОИЗВОДСТВА СЕРНОЙ КИСЛОТЫ
Технико-экономические показатели производства сер-
ной кислоты и показатели качества продукции зави-
сят прежде всего от точности соблюдения технологического ре-
жима. Поэтому ведение автоматических методов контроля и ре-
гулирования процессов, т. е. автоматизация производства, имеет
большое народнохозяйственное значение. В химической, в част-
ности — в сернокислотной промышленности автоматизация кон-
троля и управления особенно важна, так как в ходе химических
процессов возможно выделение в атмосферу производственных
помещений и окружающую среду вредных веществ в виде газов,,
паров, пыли и др.
Производство серной кислоты является непрерывным. Все ос-
новные аппараты технологической схемы соединены последова-
тельно. При перебоях в работе одного аппарата нарушается ре-
жим работы последующих аппаратов. Так, при уменьшении
концентрации диоксида серы в газе, поступающем на контакти-
рование, понижается температура в контактных аппаратах и
уменьшается степень превращения. Чтобы восстановить нор-
мальный режим и повысить степень окисления SO2 до требуе-
мой нормы, газовые потоки приходится регулировать соответ-
ствующими задвижками. При этом в абсорбционном отделении
в связи с уменьшением количества поглощаемого SO3 необходи-
мо изменять количество кислоты, передаваемой из очистного
отделения в сборник при моногидратном абсорбере, и количе-
ство моногидрата, направляемое в сборник олеума.
Следует подчеркнуть, что при строгом соблюдении техноло-
гического режима длительное время не требуется дополнитель-
ного регулирования. Известны случаи, когда в течение многих
суток отдельные узлы сернокислотных систем непрерывно рабо-
тали в стабильном режиме. Действительно, при постоянстве
объема и концентрации компонентов газовой смеси, поступаю-
щей в контактное отделение, температурный режим контактных
аппаратов не изменяется. Следовательно, сохраняются постоян-
ные условия контактирования и абсорбции. Поэтому количест-
ва кислоты, передаваемой из абсорбционного отделения в про-
мывное и возвращаемой обратно, и кислоты, циркулирующей
между абсорберами, остаются постоянным, концентрация кисло-
ты не изменяется и сохраняется высокая степень абсорбции.
В производстве серной кислоты нитрозным методом при постоянстве ос-
новных параметров — расхода газа, концентрации в нем диоксида серы, рас-
хода азотной кислоты, подаваемой в систему, при бесперебойной работе на-
сосов и другого оборудования — также иет необходимости в каком-либо ре-
гулировании башенного процесса.
22* 33S<
При нормальной работе сернокислотного производства об-
служивающий персонал только следит за технологическим ре-
жимом и регистрирует его параметры. Отсюда иногда делается
.неправильный вывод, что автоматизация управления производ-
ством серной кислоты не дает экономического эффекта, по-
скольку при этом трудовые затраты снижаются незначительно.
Однако экономический эффект внедрения автоматизации в про-
изводство серной кислоты определяется главным образом улуч-
шением условий труда, уменьшением расхода сырья, электро-
энергии, воды, улучшением других параметров, повышением ин-
тенсивности процесса, поскольку автоматизированный процесс
можно вести при наиболее высоких (оптимальных) показателях.
Поддерживать такие показатели при ручном регулировании
практически невозможно, так как даже незначительные откло-
нения от оптимального режима могут приводить к нарушению
автотермичности процесса или большим производственным по-
терям.
Контроль производства. Задача контроля производства за-
ключается в своевременном обнаружении отклонений от уста-
новленного режима, что позволяет быстро устранить их и пред-
отвратить нарушения режима на других стадиях процесса.
Методы контроля можно условно подразделять на ручные и автомати-
ческие. К ручным методам контроля обычно относят проведение химических
анализов. Вначале отбирается проба сырья, полупродукта или продукта, за-
тем производится химическая обработка пробы и делаются соответствующие
вычисления. Поэтому во многих случаях результаты химического анализа
получают через несколько часов с момента отбора пробы. В то же время,
для всех непрерывных процессов, какими являются получение серной кисло-
ты и ее концентрирование, своевременное обнаружение отклонений парамет-
ров технологического режима от установленных оптимальных норм имеет
решающее значение.
При автоматических методах контролн измерения производится в основ-
ном непрерывно. Приборы автоматического контроля не только указывают, но
и сигнализируют об отклонении измеряемого параметра от заданного значе-
ния. Они являются также элементами системы автоматического регулирова-
ния. Регистрация показаний может производиться на значительном расстоя-
нии от места замера — дистанционно. Это позволяет при установке приборов
возле рабочих мест сосредоточить регистрацию всех основных показателей в
одной точке—в пункте управления. Таким образом, становится возможным
одновременный контроль работы обслуживающим персоналом на каждом
участке цеха или отделения и начальником смены — всего цеха или отделе-
ния непосредственно из пункта управления. Поэтому автоматический контроль
производства серной кислоты применяется все более широко и вытесняет
другие методы контроля. Однако для некоторых показателей пока отсутству-
ют надежные автоматические методы измерения, поэтому ручные, в частно-
сти химические, методы контроля еще распространены в сернокислотной
-промышленности.
Контролируемые и регулируемые параметры всех основных
•отделений сернокислотного производства приведены в Прило-
жениях XX—XXII.
Автоматическое регулирование процесса обжига колчедана
в печах КС. Важнейшими показателями процесса получения
диоксида серы, определяющими устойчивую работу всего сер-
340
3. КгазоВо-
РИС. 109. Схема автоматизации печного агрегата по температуре:
/ — датчик температуры; 2 — датчик давления; 3— исполнительный механизм; 4 — регу-
лятор разрежения; 5 — регулятор температуры; 6 — регулятор уровня кипящего слоя;
7, 9 — регуляторы расхода воздуха; 8 — расходомер; 10 — ограничитель сигнала; 11 — ре-
гулятор числа оборотов двигателя питателя.
нокислотного производства, являются постоянство объема по-
лучаемого газа и концентрации в нем SO2. Постоянство объ-
ема обжигового газа обеспечивается подачей в печь заданного
количества воздуха. Поддерживать постоянную концентрацию
диоксида серы в газе сложнее, так как она зависит не только
от количества поступающего в печь сырья, но и от многих дру-
гих факторов: степени измельчения сырья, содержания в нем
серы, влаги, различных примесей, условий обжига и т. д.
На рис. 109 представлена система автоматического регули-
рования печи КС по разности температур газов после печи и
в кипящем слое, однозначно и почти линейно связанной с кон-
центрацией диоксида серы в пределах 13,5—16% SO2. Опти-
мальная разность температур автоматически поддерживается
регулятором, корректирующим задания регулятору, стабилизи-
рующему число оборотов тарельчатого питателя и корректиру-
ется по расходу общего воздуха, подаваемого в печь.
Промышленная эксплуатация системы регулирования печи
КС по разности температур показала, что отклонения концент-
рации диоксида серы составляют ±0,25—0,35%. Существенно
стабилизировался температурный режим процесса, улучшились
технологические показатели, повысилась производительность
труда на участке обслуживания печей и котлов-утилизаторов,
снизилось содержание сульфидной серы в огарках и пыли.
Автоматическое регулирование промывки обжигового газа.
Очищенный от пыли обжиговый газ промывается разбавленной
серной кислотой в первой и второй промывных башнях при
341
От газоанашзатзра зеред
юнтмтным аппара тт*
РИС. ПО. Система регулирования промывного отделения:
7 — исполнительный механизм; 2 — увлажнительная башня; 3 — датчик температуры;
4 — I промывная башня; 5, 7 — электрофильтры; 6 — II промывная башня; 8—корректи-
рующий регулятор; 9 — датчик измерителя уровня; 10 — регулятор уровня; // — стабили-
зирующий регулятор температры; 12 — датчик концентрации; 13 — регулятор концент-
рации.
сравнительно низкой температуре. В этих условиях основные
примеси газа переходят в туман, который частично осаждается
в промывных башнях и полностью — в увлажнительной башне
и мокрых электрофильтрах. Кислота, накапливающаяся в баш-
не и электрофильтрах, передается во вторую башню, а из нее
в первую. Концентрация H2SO4 в увлажнительной и второй
промывной башне определяется концентрацией кислоты в пер-
вой промывной башне, температурным режимом промывного
отделения и другими условиями. В соответствии с этим постро-
ена схема автоматизации промывного отделения, представлен-
ная на рис. 110.
Температуру кислоты на входе во вторую промывную (или
увлажнительную) башню стабилизирует регулятор, воздейству-
ющий на подачу воды на холодильники этой башни. Регулятор
получает задание от корректирующего регулятора в зависимо-
сти от температуры газа перед сушильной башней и концентра-
ции SO2 перед контактным аппаратом и от требуемого соотно-
шения между выпуском олеума и технической кислоты.
Концентрация кислоты первой промывной башни регулиру-
ется перетоком кислоты из второй промывной башни. Уровни
кислот в сборниках регулируются: первой промывной башни —
передачей избытка кислоты на склад, второй промывной баш-
ни— подачей разбавленной кислоты из цикла увлажнительной
башни, увлажнительной башни — добавлением воды.
Автоматизация контактного отделения. Основным возмуща-
ющим воздействием промышленных контактных узлов являет-
ся изменение концентрации SO2 в перерабатываемом газе. Эго
возмущение возникает в печном отделении вследствие недо-
342
статично надежной работы механизмов печных агрегатов, а
также из-за колебаний качественного состава колчедана — со-
держания серы, влаги и т. и. Возмущения по концентрации
SO2 для контактного узла являются наиболее неблагоприят-
ными, так как приводят к отклонениям температурного режи-
ма от оптимального. Поэтому автоматизация управления ре-
жимом контактного узла в первую очередь должна обеспечи-
вать автоматическую стабилизацию этого показателя.
Для оптимального ведения технологического режима кон-
тактного аппарата необходимо также автоматически стабили-
зировать температуры газа перед слоями катализатора. Иссле-
дования работы контактных узлов показывают, что автомати-
ческая стабилизация температуры перед всеми слоями катали-
затора, кроме первого, не является обязательной. Достаточно
стабилизировать температуру газа на входе в последние два
слоя катализатора. Кроме того, для обеспечения устойчивой
работы аппарата необходима автоматическая стабилизация
температуры газа на входе в первый слой катализатора на
уровне не ниже температуры «зажигания». Схема автоматиза-
ции пятислойного контактного аппарата с поддувом свежего
газа после первого слоя приведена на рис. 111.
Концентрация газа на входе в аппарат поддерживается на заданном
значении путем изменения подсоса воздуха перед отдувочной башней. Ре-
гулятор получает импульс от газоанализатора. Температура газа на входе в
первый слой регулируется дроссельной заслонкой, изменяющей количество хо-
лодного газа, поступающего мимо выносного теплообменника непосредственно
РИС. 111. Система регулирования контактного аппарата с поддувом свежего
газа после первого слоя:
/ — отдувочная башня; 2 — сушильная башня; 3 — газодувка; 4 — датчик газоанализато-
ра; 5 — теплообменник; 6 — исполнительный механизм; 7 — датчик температуры; 10—12 —
регуляторы температуры; 13— регулятор концентрации; 14 — переключатель режимов.
343
в контактный аппарат. Температура газа на входе в IV и V слои катализа-
тора регулируется дроссельными заслонками, изменяющими количество газа;,
подаваемого в соответствующий встроенный теплообменник перед IV и
V слоями.
При работе системы автоматической стабилизации концен-
трации диоксида серы перед контактными аппаратами сущест-
венно снижаются колебания концентрации SO2 как на входе в
аппарат, так и на выходе из системы.
При постоянстве температуры (и объема) газа на входе в
первый слой контактной массы температура на выходе из это-
го слоя зависит только от концентрации SO2 в поступающем
газе. Поэтому, наряду с регулированием концентрации SO2 по
импульсу газоанализатора, возможно регулирование по кос-
венному параметру — температуре после первого слоя.
В отходящих газах цветной металлургии концентрация SO2
колеблется в пределах 5—8,5%, поэтому регулирование ее пу-
тем подсоса воздуха в газоход исключается. Стабилизация
температурного режима контактирования в этом случае дости-
гается за счет поддержания соответствующей температуры на
входе в нижний внутренний теплообменник аппарата. При по-
вышении концентрации SO2 в газе регулирующая система
должна автоматически снижать температуру газа, поступаю-
щего в этот теплообменник, чтобы отводился избыток тепла,
выделившегося при окислении диоксида серы повышенной кон-
центрации. В случае понижения концентрации SO2 автомати-
ческая система изменяет задание регулятору, и температура
газа на входе в указанный теплообменник повышается.
Автоматизация сушильно-абсорбционного отделения. Рас-
сматриваемый объект управления подвергается воздействиям
возмущений, основными из которых являются изменения кон-
центрации триоксида серы в газах, степень абсорбции в олеум-
ном абсорбере и температура перед сушильной башней. Коле-
бания содержания влаги в газах сушильной башни зависят от
температуры газа на выходе из печей, от температуры окру-
жающей среды и режима работы промывного отделения. Коле-
бания содержания триоксида серы в газах абсорбционных ба-
шен зависят от содержания диоксида серы в газах, поступаю-
щих в контактный аппарат, от режима работы и состояния
контактного аппарата.
Основными параметрами, определяющими ход технологиче-
ского процесса в сушильно-абсорбционном отделении, являют-
ся концентрации орошающих кислот. Оптимальные концентра-
ции кислот достигаются принудительным распределением по-
токов кислот по циркуляционным сборникам сушильных башен
и абсорберов, что приводит к значительным изменениям уров-
ней в сборниках.
На заводах колебания температуры газа на входе в олеум-
ный абсорбер не меньше ±4 °C; это вызывает колебания тем-
пературы олеума на выходе из абсорбера и существенные из.-
344
менения степени абсорбции на данной стадии. Стабилизация
температуры газа на входе в олеумный абсорбер может умень-
шить влияние этого фактора. Поддержание температуры олеу-
ма на выходе из башни может быть обеспечено путем стабили-
зации температур газа и кислоты на входе в абсорбер или по-
средство?»! изменения интенсивности орошения. Однако послед-
нее нежелательно, так как изменение интенсивности орошения
существенно влияет и на степень абсорбции.
Сушильно-абсорбционное отделение является сложным объ-
ектом регулирования с большим числом прямых и обратных
связей и восемью регулируемыми параметрами: четырьмя кон-
центрациями кислот и четырьмя уровнями. В каждом цикле
орошения имеется несколько звеньев (абсорбер, холодильник,
сборник) со сложными динамическими характеристиками. Уст-
ранение влияния указанных выше возмущающих факторов на
заданный режим реализуется путем управления клапанами и
задвижками, установленными на технологических трубопрово-
дах и газоходах. Однако, поскольку изменения режима тесно
взаимосвязаны между собой, управление каким-либо одним
клапаном приводит к изменению всех параметров, определяю-
щих данный режим, что сильно затрудняет ручное управление
процессом.
На рис. 112 показана схема автоматизации сушильно-аб-
сорбционного отделения (САО) сернокислотного цеха, работа-
ющего по схеме ДК с выпуском продукции в виде сушильной
кислоты, олеума и сушильной кислоты, либо одного олеума.
Вариант выпуска продукции устанавливается заданием регу-
лятору выпуска олеума на склад.
Концентрация олеума (Кол) регулируется изменением подачи моногид-
рата первого моногидратного абсорбера в циркуляционный сборник олеумно-
- о шорник сушильной
башни
РИС. 112. Система регулирования сушильно-абсорбционного отделения по
схеме ДК:
1 — сборник отдувочной башни; 2— сборник сушильной башни; 3 — сборник первого
моногидрата; 4— сборник олеума; 5— сборник второго моногидрата; 6 — исполнительный
механизм; 7 — датчик концентрации кислоты; 8 — регулятор концентрации; 9 — датчик
уровня; 10 — регулятор уровня; // — датчик измерителя расхода; 12 — регулятор расхода
«ислоты.
345
РИС. ИЗ. Система автоматического согласования нагрузок печного и кон-
тактного отделений:
/ — печь КС; 2— котел-утилизатор; 3 — циклон; 4 — электрофильтр; 5 — коллектор газа;
6— задатчик регулятора; 7—измеритель расхода газа; 8— регулятор расхода газа; 5—*
исполнительный механизм; 10— газодувка: 11— контактное отделение; 12 — датчик дав-
ления; 13 — корректирующий регулятор; 14 — стабилизирующий регулятор; 15 — возду-
ходувка.
го абсорбера. Постоянство концентрации кислоты моногидратиых абсорберов
регулируется подачей воды в сборники этих абсорберов. Концентрация су-
шильной кислоты (Кек) регулируется изменением подачи моногидрата перво-
го моногидратного абсорбера в сборник сушильной башни. Уровень в олеум-
иом сборнике поддерживается воздействием на подачу олеума в сборник пер-
вого моногидратного абсорбера, а уровень в сборнике первого моногидрат-
ного абсорбера — изменением подачи кислоты сушильной башни в этот сбор-
ник. Уровень во втором сборнике регулируется подачей избытка кислоты в
сборник отдувочной башни, а уровень в первом сборнике — сбросом избытка
кислоты на склад. Уровень в сборнике второго моногидратного абсорбера
поддерживается передачей избытка кислоты во второй сборник.
При одностадийном контактировании нет второго моногид-
ратного абсорбера. Система автоматического регулирования
(САР) отделения абсорбции в этом случае аналогична выше-
изложенной для отдувочной и сушильной башен, первого мо-
ногидратного и олеумного абсорберов.
Комплексная автоматизация производства. Схема комплекс-
ной автоматизации контактного производства серной кислоты
при обжиге колчедана включает все решения по автоматизации
отдельных участков сернокислотного производства, приведенные
выше (см. рис. 109—112). При работе сернокислотных систем
возникает задача согласования нагрузок печного и кислотного
участков. Одна из схем автоматизации, позволяющая решить
эту задачу, приведена на рис. 113.
Схема работает следующим образом. В случае технологической необхо-
димости нагрузка контактного отделения изменяется при помощи задатчика
регулятора 10 расхода газа. При изменении потребления газа контактным от-
делением изменяется манометрический режим в коллекторе газа. Это измене-
ние отслеживается главным регулятором двухконтурной системы регулирова-
ния. В зависимости от нагрузок печей КС этот регулятор корректирует ра-
боту вспомогательных регуляторов расхода воздуха в печь таким образом,
чтобы выход образующегося обжигового газа стал равен его потреблению.
346
О математическом моделировании. Методы математическо-
го моделирования являются важным современным средством
исследования процессов химической технологии. Эти методы
позволяют выбрать оптимальные размеры и конструкцию ап-
паратов, определить оптимальные режимы протекающих про-
цессов, построить наилучшую систему управления этими про-
цессами.
Метод математического моделирования основывается на следующем.
Пусть существуют две физические системы, которые ведут себя в некотором
отношении аналогичным образом, тогда более удобную для исследования си-
стему назовем моделью нли аналогом. Возможны различные виды аналогий
между системами:
геометрические аналогии, при которых подобными являются размеры
рассматриваемых систем (примером геометрического аналога системы будет
служить ее макет);
физические аналогии, при которых процессы в системах не отличаются
по физической природе, но сами системы отличаются, например размерами
(примером физических моделей могут служить опытные установки технологи-
ческих процессов);
математические аналогии, при которых технологическая система и ее мо-
дель описываются одинаковыми математическими зависимостями (уравне-
ниями).
Таким образом, математической моделью (математическим описанием
процесса) называется совокупность формул (а также таблиц, графиков), ко-
личественно описывающая зависимости между различными параметрами про-
цесса. Этими параметрами могут быть, например, скорости химических пре-
вращений, концентрации реагентов, температуры, расходы, давления компо-
нентов реакций, геометрические размеры аппаратов и т. п.
Математическим моделированием процесса называется исследование его
математического описания с целью решения задач конструирования, выбора
режимов и управления процессом. Математическое моделирование сложного
процесса осуществляется с помощью аналоговых и цифровых вычислительных
машин.
Основной проблемой математического моделирования является получение
достаточно точного математического описания процесса. Обычно такие опи-
сания сложных процессов весьма громоздки, что затрудняет дальнейшее их
исследование. Таким образом, математическое описание процесса должно
представлять разумный компромисс между желаемой точностью и слож-
ностью получаемых выражений.
Существуют два метода составления математической модели. Аналити-
ческий метод основан на изучении процессов тепло- и массообмена и физи-
ко-химических закономерностей процесса. В этом случае математическая мо-
дель состоит из кинетических уравнений, уравнений материального и тепло-
вого балансов, уравнений процессов тепло- и массопередачи. Аналитическая
модель процесса может быть весьма точной, но получение ее связано с дли-
тельной теоретической и экспериментальной работой. Существенное достоин-
ство аналитических моделей заключается в пригодности их при проектирова-
нии новых процессов.
Вторым методом является экспериментальный метод получения матема-
тического описания, состоящий в исследовании действующих аппаратов с
целью получения необходимых зависимостей между параметрами. Получение
точного математического описания экспериментальным методом обычно за-
труднительно. Кроме того, экспериментальная математическая модель при-
годна только для того аппарата, иа котором проводились эксперименты.
Основные технологические агрегаты сернокислотного про-
изводства в течение последнего времени являлись объектом ма-
тематического моделирования. В первую очередь к таким агре-
347
гатам были отнесены печи КС и контактный аппарат, затем су-
шильно-абсорбционное отделение и промывное отделение.
Для печей кипящего слоя были получены уравнения зависи-
мости концентрации диоксида серы на выходе из печи от основ-
ных параметров на входе в печь — расхода колчедана, его влаж-
ности и гранулометрического состава, расхода воздуха. С ис-
пользованием полученной математической модели была разра-
ботана система автоматического регулирования печей кипящего
слоя типа КС-200 и КС-450.
Математическая модель контактного аппарата со стационар-
ными слоями катализатора разработана Боресковым Г. К- и
Слинько М. Г. с сотр. На основе этой модели установлены оп-
тимальные условия загрузки в реактор катализатора и опти-
мальный температурный режим работы реактора. Модель реак-
тора использовалась также для построения системы автомати-
ческого регулирования.
Математическое моделирование процессов химической тех-
нологии позволяет глубже изучать работу агрегатов, разраба-
тывать оптимальные конструкции аппаратов и изыскивать пути
интенсификации действующих процессов.
Автоматизированные системы управления. На протяжении
последнего десятилетия ЦИНИКА и НИУИФ были выполнены
значительные работы по созданию и внедрению АСУ ТП, пред-
назначенной для оперативного управления сернокислотными
производствами.
АСУ ТП «Купол». Система предназначена для оперативно-
го контроля и управления крупнотоннажными производствами,
состоящими из нескольких технологических линий большой
мощности. Система относится ко второму уровню, основные ее
функции: автоматический централизованный контроль и управ-
ление; учет; анализ производства.
Структура управления двухуровневая, иерархическая, исхо-
дит из необходимости централизации контроля и управления,
оперативного обнаружения и устранения отклонений от регла-
мента и согласования режимов технологических переделов, а
также вывода людей из непосредственного контакта с агрессив-
ной средой производственной зоны.
Технически, в отличие от первой системы, которая была ре-
ализована на ЭВМ УМ-1, все тиражируемые системы были вы-
полнены на ЭВМ М-6000 АСВТ и разработанном ЦНИИКА
комплексе унифицированных диспетчерских средств, включаю-
щих пульт управления, мнемощит сигнализации, щит устройств
графической регистрации, стойку оперативных измерительных
приборов, устройств ручного ввода информации и цифровой ин-
дикации и устройств логической обработки информации.
Система состоит из нескольких автономных технических под-
систем: информационно-диспетчерской подсистемы контроля,
реализованной на унифицированных средствах диспетчериза-
ции; информационно-вычислительной подсистемы контроля.
348
анализа, управления и рекомендаций, выполненной на элект-
ронной вычислительной машине М-6000; подсистемы производ-
ственной разговорной связи.
Алгоритмы математического обеспечения АСУТП «Купол»
реализуют: централизованный оперативный контроль и диспет-
черское управление; расчет технико-экономических показателей;
составление производственно-технологической документации;
учет работы оборудования; анализ предаварийных ситуаций;
оценку деятельности сменного персонала; выбор оптимального
технологического режима контактного узла; непосредственное
цифровое управление; обмен данными с АСУ верхнего уровня
(АСОДУ).
В результате внедрения систем «Купол» в отрасли за деся-
тилетие было достигнуто резкое увеличение доли автоматизиро-
ванных сернокислотных производств — с 5% в 1970 г. до 35%
в 1980 г.
Прежде всего система решает один из основных вопросов уп-
равления в химии: она позволяет своими техническими средст-
вами централизовать управление и, как следствие, сократить
численность оперативного персонала. Кроме того, удается под-
нять качество управления технологическим процессом, благода-
ря более полному и более оперативному представлению диспет-
черу хода технологического процесса на мнемосхеме, устройст-
вах регистрации и сигнализации; более рациональному ведению
процесса на основе рассчитываемых на ЭВМ технико-экономи-
ческих показателей и оценок работы технологического персона-
ла; более тщательному соблюдению регламента и лучшему
контролю за состоянием оборудования.
Все это позволило увеличить выпуск продукции в среднем'
на 0,3—0,5% и снизить материальные и энергетические затраты,
на 1,2%. Сокращение численности персонала за счет централи-
зации управления, увеличение выпуска продукции и снижение
затрат позволили получить предприятиям существенный эконо-
мический эффект.
АСУ ТП «Вектор». В отличие от АСУ «Купол», являющей-
ся системой второго уровня, объединяющей управление всем-
сернокислотным производством, АСУ «Вектор» предназначена
для управления одной или несколькими мощными технологиче-
скими линиями. Она представляет собой систему первого уров-
ня, т. е. наряду с централизованной частью сбора и представ-
ления информации, включает всю низовую систему локальной
автоматизации. В состав АСУ входит ЭВМ типа М-6000, назна-
чение которой реализация алгоритмов, функционирующих в
темпе с процессом.
Основной принцип, положенный при разработке АСУ «Век-
тор», что и определяет ее особенность,— минимизация щитовых
приборов. Подавляющая часть информации выходит на опера-
тора через вызывные приборы и терминалы ЭВМ — телевизион-
ный индикатор СИД-1000. Задатчики регуляторов и дистанци-
34»
• онное управление регулирующими органами сосредоточены в
одном центральном пункте управления.
АСУ ТП «Вектор» внедрена в промышленную эксплуатацию
в 1976 г., одновременно с пуском одного из производств. Бла-
годаря этому достигнут существенный экономический эффект-
срок пуска и освоения проектной мощности нитки сокращен в
2—2,5 раза. В части сокращения обслуживающего персонала
практически повторяются результаты, достигнутые при внедре-
нии АСУ «Купол».
ГЛАВА XI
ТЕХНИКА БЕЗОПАСНОСТИ
На производство серной кислоты распространяются
«Правила безопасности для производств основной хи-
мической промышленности», согласованные с Госстроем СССР
4 января 1979 г. (письмо № АБ-49-20/0), с ПК профсоюза рабо-
чих химической и нефтехимической промышленности 18 декабря
1978 г. (Постановление секретариата, протокол № 26) и утверж-
денные Госгортехнадзором СССР 28 августа 1979 г. (протокол
№ 38), Министерством химической промышленности 23 марта
1979 г. (письмо № Н-2970-79 от 22 марта 1979 г.).
В соответствии с указанными правилами для действующих
и вновь вводимых в эксплуатацию производств серной кислоты
должны быть разработаны и утверждены в установленном по-
рядке технологические регламенты, согласно которым и следу-
ет вести технологический режим производства.
Все производственные цехи, отделения, участки производст-
ва серной кислоты должны иметь инструкции по безопасному
ведению процесса и безопасной эксплуатации оборудования, со-
ставленные в соответствии с технологическими регламентами и
указанными выше «Правилами». Инструкции по каждому рабо-
чему месту должны утверждаться главным инженером пред-
приятия.
Все инженерно-технические работники производства долж-
ны проходить аттестацию в порядке, установленном Положени-
ем об аттестации работников, проверке знаний и допуске пер-
сонала к самостоятельной работе на предприятиях, в организа-
циях и учреждениях химической промышленности. Все рабочие
вновь принятые на работу, а также переводимые на другую ра-
боту, обязаны пройти инструктаж по правилам внутреннего
распорядка и обучение безопасным методам работы в соответ-
ствии с имеющимся «Положением». Знания рабочих по вопро-
сам техники безопасности и пожарной безопасности должны
проверяться специальной комиссией.
'350
Таблица 65. Предельно-допустимые концентрации (ПДК) газов, паров
и пыли (СН 245—71), мг/м3
Вещества В воздухе ра- бочей зоны производствен- ных помещении В атмосферном воздухе населен- ных мест
максимальная разовая среднесуточная
Диоксид серы 10 0,5 0,05
Сероводород 10 0,008 0,008
Триоксид серы, серная кнс- 1 0,3 0,1
лота (туман, пары) Оксиды азота 2 0,4 0,4
Азотная кислота Гидриды мышьяка 0,3 — 0,003
Фторсодержащие соеднне- 0,5 0,02 0,005
ния (на F) Диоксид селена 0,1 — —
Селен аморфный 2 — —-
Озон Оксид углерода 0,1 20 3 1
Хлор 1 0,1 0.03
Соляная кислота (на HCI) 5 0,2 0,2
Аммиак 20 0,2 0,2
Пыль огарковая и колче- данная Пыль пятпоксида ванадия 4 0,5 0,002
Ртуть металлическая 0,01 — 0,0003
При эксплуатации сернокислотного производства нужно-
помнить, что серная кислота является агрессивным веществом,
и при попадании на кожу человека вызывает ожоги. Поэтому
необходимо в соответствии с инструкциями всегда работать в
защитной спецодежде, рукавицах, а при обслуживании и ре-
монте кислотопроводов, кислотных насосов, внутри башен —
пользоваться защитными очками. Оборудование необходимо со-
держать в исправном состоянии, на фланцах кислотопроводов
и сальниках кислотных насосов должны быть установлены за-
щитные кожуха, вращающиеся части оборудования должны
иметь ограждения.
Для исключения опасности выделения вредных веществ в
окружающую среду необходимы качественное изготовление и
монтаж оборудования, строгое выполнение графиков планово-
предупредительного ремонта, выполнение норм технологиче-
ского режима, инструкций по технике безопасности. При ава-
рийных ситуациях может происходить выделение диоксида и
триоксида серы, паров и тумана серной кислоты. Поэтому каж-
дый рабочий должен иметь на рабочем месте противогаз. При
нормальном состоянии оборудования и при выполнении норм
технологического режима содержание вредных веществ в возду-
хе рабочей зоны и в атмосферном воздухе населенных мест не
должно превышать предельно допустимых концентраций,
(табл. 6’5).
351
Нужно проявлять особое внимание при работе с серой. Кус-
ковая сера воспламеняется при 250—270 °C, порошкообразная—
при 230 °C. Осевшая серная пыль взрывоопасна, температура
ее самовозгорания 205—207 °C. Взвешенная в воздухе серная
пыль фракции 150 мкм имеет нижний предел взрывоопасности
17,6 г/м3, беззольная сухая пыль — 2,3 г/м3. Пары серы с воз-
духом образуют взрывоопасную смесь. Поэтому во избежании
возможных «хлопков» при пусках серная печь должна быть
разогрета до 800 °C. Все электрооборудование склада комовой
серы должно быть во взрывобезопасном исполнении.
Котлы-утилизаторы должны эксплуатироваться в соответ-
ствии со специальными инструкциями — как аппараты, работа-
ющие под давлением.
Устройство и эксплуатация газовых сетей, мазуто- и серо-
проводов, топок для сжигания жидких и газообразных горю-
чих веществ (мазута, серы, природного газа, сероводорода и
т. д.) должны соответствовать требованиям «Правил безопас-
ности в газовом хозяйстве», эксплуатационной инструкции.
Емкости (баки, хранилища) серной кислоты необходимо
устанавливать в специальные поддоны с бортами высотой не
менее 15 см. Поддоны должны иметь слив или устройство для
перекачивания кислоты в соответствующую емкость.
Запрещается работать на неисправном оборудовании, пу-
скать в эксплуатацию производственное оборудование без ог-
раждений, звуковой или световой сигнализации, контрольно-
измерительных приборов, блокировок, обеспечивающих безопас-
ность его обслуживания.
Регулярно следует проводить проверку знаний обслуживаю-
щего персонала по технике безопасности на каждом рабочем
месте.
23—584
ПРИЛОЖЕНИЯ
t. ОСНОВНОЕ ТЕХНОЛОГИЧЕСКОЕ ОБОРУДОВАНИЕ
В ПРОИЗВОДСТВЕ КОНТАКТНОЙ СЕРНОЙ кислоты
Годы Мощность, тыс. т Мнг в год Процесс Сырье Аппарат
наименование |производительность [размеры, м ЧИСЛО
До 1966 120 Одностадийное контактирование Колчедан Печь КС-200 200 т/сут (колч.) Контактный аппа- 4700 м3/ч рат (5 слоев) Сушильная башня » Олеумный абсор- » бер Моногидратный » абсорбер Дв-6,2; Д„-4,75; //-13,5 Д-8; //-19 Д-5,5; //-15 Д-5,5; //-12 Д-5,5; //-15 1 1 1 1 1
1966— 1970 180 Одностадийное контактирование Колчедан Печь КС-200 См. выше Контактный аппа- 70000 м3/ч рат (5 слоев) Сушильная башня 70000 м3/ч Олеумный абсор- » бер Моногидратный » абсорбер См. выше Д-9; //-25 Д-6,5; //-15 Д-6,5; //-12 Д-6,5; //-15 2 1 1 1 1
360 То же То же Печь КС-450 450 т/сут (колч.) Контактный аппа- 136000 м3/ч рат (5 слоев) Сушильная башня > Олеумный абсор- > бер Дв-9,84; Д„-9,14; //-13,4 Д-12; //-28 Д-8 Д-5; /7-12 2 1 1 1
Годы Мощность, ТЫС. Т MIIF в год Процесс Сырье
1971—
1975
360 Двойное контакта- Колчедан
роваине
200 То же Сера
450 То же То же
Продолжение
Аппарат
наименование
производительность [размеры, м
число
Моиогидратный » абсорбер Д-8; //-20 1
Печь КС-450 См. выше См. выше 2
Контактный аппа- 125000 м3/ч Д-12—14; /7-28 1
рат (5 слоев) Сушильная башня » Д-8; //-20 1
Олеумный абсор- 125000 м3/ч Д-8; //-20 1
бер Моиогидратный » абсорбер Д-8; //-20 1 + 1
Печь СЭТЛ-Ц-100 100 т/сут Д-1,6; /7-3—5 2
Контактный аппа- 60000 м3/ч Д-10; //-20 1
рат (5 слоев) Сушильная башня » Д-5,5 1
Моиогидратный абсорбер » Д-5,5 1
Печь СЭТА-Ц-100 См. выше См. выше 5
Контактный аппа- 136000 м3/ч рат (5 слоев) Д-14; // 32 1
Сушильная башня » Д-8; //-20 1
Олеумный абсор- » бер » 1
Моиогидратный >.< абсорбер 1 +
SOO To же, ПНР To же
1976— 360 Двойное контакта- Колчедан
1980 ровапие, ПНР
360 То же
То же
500 То же
Сера
Печь форсуночная Контактный аппа- 160000 м»/ч Д-5,5; Д-10 1 Д-13,5; Д-20 1
рат (5 слоев) Сушильная башня » Д-8,5; Д-18 1
Моногпдратный абсорбер » Д-8,5; Д-18 1-]-1
Печь КС-450 450 т/сут (колч.) Д.-9.84; Д„-9,14; Д-13,4 2
Контактный аппа- рат (4 слоя) 125000 м3/ч Д-13,5; Д-20 1
Сушильная башня » Д-8; Д-18 1
Олеумный абсор- бер Д-8; Д-18 1
Моногпдратный абсорбер » Д-8; Д-18 1 + 1
Печь КС-450 См. выше
Контактный аппа- 125000 м’/ч
рат (5 слоев)
Сушильная башня 125000 м’/ч
Олеумный абсор- »
бер
Моногпдратный »
абсорбер
См. выше 2
Д-14; /7-28 1
Д-8; //-20 1
Д-8; Д-20 1
Д-8; //-20 1-|-1
См. ныше
II. СОСТАВ ТВЕРДЫХ ФАЗ В ЭВТЕКТИЧЕСКИХ ТОЧКАХ СИСТЕМЫ
Н2О — H2SO4 — SO3
Содержание
Темпера-
SO3 (своб.), % тура, ‘-С Характеристика точек Состав твердой фазы
0 0,0 Температура плавления Н20
37.55 —73,10 Эвтектическая точка H2SO4-4H2O+H2O
57.64 —28,36 Температура плавления H2SO4-4H2O
67.80 —47,46 Эвтектическая точка H2SO4 • 4Н2О + H2SO4 • 2Н2О
69,70 —42,70 Эвтектическая точка H2SO4-3H2O + H2SO4-2H,O
72,13 —39,51 Температура плавления H2SO4-2H2O
73.68 —39,87 Эвтектическая точка H2SO4-2H2O+H2SO4-H2O
84,48 8,56 Температура плавления H2SO4-H2O
100,00 10,37 Температура плавления H2SO4
15,81 — 10,15 Эвтектическая точка H2SO4 + H2SO4-SO3
44.79 35,15 Температура плавления H2SO4-SO3
61 8 1,00 Эвтектическая точка H2SO4-SO3 + H2SO4-2SO3
62,0 1,20 Температура плавления H2SO4-2SO3
64.35 — 1,10 Эвтектическая точка H2SO4-2SO3 + tb. p-p SO3
100,00 16,8 Температура плавления y-SO3
III. СОСТАВ РАСТВОРОВ СЕРНОЙ КИСЛОТЫ, ТЕМПЕРАТУРА
И ТЕПЛОТА ПЛАВЛЕНИЯ СОЕДИНЕНИЙ, РАСПОЛАГАЮЩИХСЯ
НА ВЕТВЯХ КРИСТАЛЛИЗАЦИИ МЕЖДУ ЭВТЕКТИЧЕСКИМИ
ТОЧКАМИ ДИАГРАММЫ КРИСТАЛЛИЗАЦИИ СИСТЕМЫ
Н2О — H2SO4 — SO3
Концентрация раствора Формула соединения Температу- ра плавле- ния, °C Теплота плав- ления, кДж/моль
45,58% H2SO4 H2SO4-6,5H2O —52,88 34,29
57,64% H2SO4 H2SO4-4H2O —28,36 30,664
65,79% H2SO4 H2SO4-3H2O —36,31 24,011
73,13% H2SO4 H2SO4-2H2O —39,47 18,254
84,48% H2SO4 H2SO4-H2O 8,48 19,452
100,0% H2SO4 H2SO4 10,31 10,728
44,79% SO3 (св.) H2SO4 SO3 35,55 —
62,0% SO3 (св.) H2SO4-2SO3 1,2 —-
IV. ТЕМПЕРАТУРА КРИСТАЛЛИЗАЦИИ (fKP) СЕРНОЙ КИСЛОТЫ
И ОЛЕУМА ДЛЯ НЕКОТОРЫХ КОНЦЕНТРАЦИЙ (С) H2SO4 И SO3(cb.)
Серная кислота Олеум
Ch2so4- /0 t . °C кр’ CH2SO4> 2% 4 / °C кр’ CSO3(CB)’ % *кр> % CSO3(cB)’ 0/ 0 f °C кр*
70,0 —42,0 92,0 —17,5 10 — 1,5 26 15,5
75,0 —29,5 93,0 —27,0 15 —9,3 30 21,8
80,5 1,7 94,0 —31,9 17 —5,8 40 33,7
85,0 8,0 97,0 —7,0 18 —2,8 45 35,0
88,5 0,5 98,0 —0,7 20 2,5 50 31,7
356
Продолжение
Серная кислота Олеум
/0 I / сс i со.’ •кр' | 4 кр’ с5Оз(св)- | '0 1 SP’ -0 CSOS<CB>’ '° 1 t °C кр’
89,0 — 1,4 98,5 1,8 22 7,4 60 7,6
90,0 —5,5 99,0 4,5 24 11,9 61,8 1 ,о
91,0 -11,5 100 10,37 25 13,7 65 —0,35
V. ОБЩЕЕ ДАВЛЕНИЕ ПАРОВ (В ММ РТ. СТ.) НАД СЕРНОЙ
КИСЛОТОЙ И ОЛЕУМОМ (1 ММ РТ. СТ. = 133,33 Па)
Концент- рация Температура, °C
20 40 60 80 100 | 120 140 160 180 200
0 17,5 55,3 Серная 149 кислота (в 435 760 % H2so4)
10 16,6 52,9 143 337 720 — —
20 15,4 48,6 133 314 678 —
30 13,2 41,7 116 273 590 —
40 9,95 31,8 87,3 211 574 — —
50 6,20 20,3 58,0 143 326 670 —
55 4,43 14,8 43,0 108 253 522 — —
60 2,87 9,85 29,3 75,3 178 377 760 —
65 1,61 5,65 18,6 47,0 114 251 525
70 0,723 2,75 9,12 26,0 67,0 153 332 665
75 0,284 1,14 3,98 12,0 32,0 76,5 173 354 685
80 0,084 0,381 1,47 4,77 13,9 35,6 85,5 188 378 735
85 0,026 0,125 0,411 1,77 5,39 14,5 36,3 82 169 340
90 0,005 0,027 0,120 0,450 1,49 4,19 11,2 27,7 59 120
95 __ 0,002 0,013 0,061 0,237 0,79 2,4 6,5 15,9 36,7
98,3 2-10-4 10-» 5 • 10~3 0,02 0,07 0,22 0,65 1,62 3,55 7,76
100 8-10"4 5-10*? 0,027 0,117 0,43 1,38 3,99 10,31 24,65 55,1
Олеум [в % SO3 (св.)]
15 — 2,0 7,4 22 60 148 331 692 —
18 0,78 2,5 10,8 33,2 —
20 0,8 3,3 12 39 107 267 606
25 1,5 5,8 22 71 191 477 —
30 2,0 9,1 36 115 312
35 3,6 15 59 191 .
65 85 295
100 190 600 — — —
VI. ТЕМПЕРАТУРА КИПЕНИЯ
СЕРНОЙ КИСЛОТЫ И ОЛЕУМА
Ch2SO4> % • . . . 90 92 94 96 98 99 100
^кип . . . 256 273 292 314 336 320 290
Q03 (св ), % • • . . 16 18 20 22 24 26 28
^кии . . . 151 146 141 137 133 129 125
357
VII. ТЕПЛОЕМКОСТЬ РАСТВОРОВ СЕРНОЙ КИСЛОТЫ
Теплоемкость серной кислоты в кал/(кгград) (1 кал=4,19 Дж)
Концентрация H2SO4, % Температура, °C Концентра- ция H2SO4, % Температура, °C
20 | 40 60 | 80 20 40 60 I 80
80.0 448 460 465 477 92,5 373 380 391 399
82,5 446 453 458 465 95,0 354 364 370 382
85 438 443 446 452 97,5 341 353 358 366
87,5 420 425 433 436 100 355 343 351 359
90 396 405 415 420
Теплоемкость олеума при 30 °C:
Концентрация SO3 (св.), °/о • Теплоемкость, кал/(кг- град) . 20 25 30 40 50 60
. 320 319 320 325 324 380
VIII. ТЕПЛОТА ОБРАЗОВАНИЯ ВОДНЫХ РАСТВОРОВ СЕРНОЙ
КИСЛОТЫ И ОЛЕУМА ИЗ ГАЗООБРАЗНОГО SO3 И ВОДЫ
В ККАЛ/КГ Н2О (1 ККАЛ =4,19 кДж)
Концентра- ция Температура, °C
0 | 50 1 ЮО 1 150
40 Серная кислота (в с 278 291 '0 H2SO4) 306 —
50 383 401 422 —
60 514 540 569 —
80 902 948 1000 —
90 1212 1276 1349 —
91 1251 1317 1393 —
92 1290 1359 1437 —
93 1332 1404 1485 —
94 1375 1450 1535 —
95 1421 1500 1586 —
96 1469 1548 1641 —
97 1520 1604 1699 —
98 1573 1669 1758 —
99 1631 1720 1823 —
100 1693 1785 1892 —
18,3 Олеум 1903 [в % SO3 2023 (св.)] 2155 2287
20 1926 2046 2184 2327
25 2002 2128 2256 2416
30 2074 2186 2353 2516
40 2262 2398 2590 2755
50 2547 2685 2890 3067
60 2934 3078 3290 3468
IX. ПЛОТНОСТЬ СЕРНОЙ КИСЛОТЫ И ОЛЕУМА В Г/СМ3
Концентра- ция Температура, СС
20 1 25 I 40 60 80 90
5 1,0317 Серная кислота 1,0300 (в % H2SO4) 1,0240 1,0140 1.0022 0,9955
40 1,3028 1,2991 1,2879 1,2732 1,2589 1,2589
90 1,8144 1,8091 1,7933 1,7729 1,7525 1,7428
91 1,8195 1.8142 1,7986 1,7783 1,7581 1,7485
358
Продолжение
Температура, СС
Концентрация | 90 1 25 1 40 ! fif! ! 80 ! 90
92 1,8240 1,8188 1,8СЗЗ 1,7832 1,7633 1.7546
93 1,8279 1,8227 1,8074 1.7876 1,7681 1,7583
94 1,8312 1.8260 1,8110 1,7914 1,7720 1.7624
95 1,8337 1,8286 1,8137 1,7944 1,7751 1.7656
96 1,8355 1,8305 1,8157 1.7965 1.7773 1,7680
97 1,8364 1,8314 1,8166 1,7976 1,7785 1.7695
98 1,8361 1,8310 1.8163 1,7978 1,7786 1,7698
99 1,8342 1,8292 1,8145 1,7958 1,7778 1.7693
100 1,8305 1,8255 1.8107 1,7925 1,7765 1,7686
Олеум* [в % SO3 (см.)]
10 1,867 1,863 1,844 1,829 1.810 —
15 1,884 1,880 1,862 1.847 1,827 —
18 1,894 1,890 1,872 1,857 1,837 —
20 1,902 1,898 1,879 1,864 1,843 —
25 1,918 1,915 1,897 1,880 1,858 —
30 1 ,935 1,932 1,914 1,895 1,872 —
35 1,950 1,947 1,928 1,909 1,884 —
40 1,965 1,961 1,940 1.919 1,894 —
45 1,978 1,974 1.950 1,927 1,901 —
50 1,989 1,984 1,957 1,933 — —.
60 2,000 1,994 1,958 (1,916) — —
65 2,001 1,992 1,948 (1,897) — —
* Плотность приведена не для 40. а дл? г 45 °C.
X. ТЕПЛОПРОВОДНОСТЬ И ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ
РАСТВОРОВ СЕРНОЙ КИСЛОТЫ
Теплопроводность в Вт/(м град)
Концентра- Температура, °C
ЦИЯ H2SO4, % —20 | 0 | 20 \ 40 | 60 | 80 | 100 | 120
98 0,306 0,330 0,342 0,353 0,376 0,388 0,4
92 0.296 0,320 0,344 0,353 0,376 0,390 0,402 0,425
75 0,348 0,365 0,383 0,4 0,423 0,448 0.47 0,432
60 0,383 0,416 0,430 0,44 0,464 0,5 0,522 0,544
Поверхностное натяжение в кН/м
Концентра- ция H2SO4, % Температура, °C
—20 } ° 1 18 ! 20 40 60 80 100 120
8 27,8 — — 73,58 76,13 — — — —
41 — — 77,80 — — — — — —
60 77,3 76,7 — 76,1 75,4 74,5 73,6 72,7 71,8
75 74,1 73,6 — 73. 1 72.6 72,1 71,6 71.1 70,6
85 — 67,61 —.
92 63 61,9 — 61,4 60 9 60,3 59,7 59,1 58,5
98 — 55,9 — 55,1 54,3 53,7 53,1 52.5 51,9
359
XI. ВЯЗКОСТЬ СЕРНОЙ КИСЛОТЫ И ОЛЕУМА В мПа-с
Вязкость концентрированных растворов серной кислоты
Концентра- ция H-SO,, % Температура, °C
—12,2 ° 10 1 2« 1 32 43 1 60 100
88 Тв. 49,0 41,8 24,9 16,4 12,4 8,0 3,4
90 Тв. 47,0 38,9 23,9 15,8 12,0 7,9 3,8
92 72 45,0 35,5 22,6 15,0 п,з 7,7 3,9
94 71,0 44,5 34,0 22,0 15,0 11,3 7,9 3,9
96 72,5 46,0 34,2 22,9 15,4 11,8 8,2 3,9
98 — 51,0 37,0 24,4 16,7 12,5 8,7 3.8
100 — — 43,0 27,5 19,0 14,0 9,0 3,8
Вязкость олеума
Содержание SO3 (св.), % Температура, °C Содержание йО3 (св.), % Температура, °C
25 45 60 | 80 25 I45 | 60 | 80
18 29,0 15,0 10,1 6,5 40 49,6 21,7 13,5 7,9
20 25 29,8 32,9 15,4 16,7 10,4 11,2 6,6 7,0 50 57,6 23,2 13,2 7,7
30 37,6 18,5 12,0 7,4 60 51,8 18,5 9,9
XII. РАСТВОРИМОСТЬ ДИОКСИДА СЕРЫ (В %) В ВОДЕ,
СЕРНОЙ КИСЛОТЕ И ОЛЕУМЕ (ПРИ НОРМАЛЬНОМ ДАВЛЕНИИ SO2)
Концент- Температура, °C
рация ю | 20 | 30 | 40 1 50 | 80 1 100
0 15,30 Серная кислота (в % H2SO4)
10,50 7,50 5,60 4,50 2,00 1,40
10 12,30 8,72 6,40 4,57 3,72 1,67 1,28
20 11,28 7,79 5,66 4,11 3,32 1,47 1,15
30 10,25 6,85 5,04 3,66 2,92 1,28 1,02
40 9,25 5,81 4,17 3,20 2,44 1,09 0,89
50 8,25 4,90 3,76 2,73 2,13 0,96 0,76
55 7,75 4,31 3,26 2,47 1,80 0,89 0,69
60 7,25 3,94 3,05 2,27 1,77 0,81 0,62
65 6,72 3,68 2,74 2,01 1,53 0,74 0,55
70 6,11 3,24 2,46 1,72 1,38 0,67 0,49
75 5,49 2,86 2,23 1,64 1,25 0,61 0,425
80 4,84 2,63 1,98 1,43 1,16 0,58 0,365
85 4,50 2,34 1,80 1,36 1,13 0,57 0,335
90 4,72 2,52 1,96 1,49 1,16 0,62 0,37
95 5,80 3,02 2,23 1,66 1,38 0,745 0,42
100 6,99 3,82 2,72 2,02 1,72 0,99 0,54
Олеум [в % SO3 (св.)]
5 7,91 4,29 3,10 2,31 2,05 1,18 0,64
ГО 8,86 4,80 3,49 2,60 2,35 1,75 1,02
15 9,85 5,35 3,89 2,92 2,45 1,85 1.11
360
Продолжение
Концент- рация Температура, °C
10 i 20 | 30 ! 4U i 50 80 100
20 10,87 5,94 4,31 3,26 2,71 2,07 1,24
25 11,93 6,57 4,57 3,62 3,00
30 13,02 7,24 5,17 3,98 3,29
40 15,37 8,70 6,07 4,78 3,92
50 17,74 10,32 7,02 5,64 4,61 — —
Примечание. Для нахождения растворимости прн давлении, отличном от нор-
мального, приведенные данные следует ное давление SO2 в газе в мм рт. ст.). умножать на 0,00142 PSQ (PSO2 — парциал'ь-
XIII. ЗАВИСИМОСТЬ РАВНОВЕСНЫХ СТЕПЕНЕЙ КОНВЕРСИИ
ОТ ТЕМПЕРАТУРЫ ДЛЯ ГАЗОВ ОТ ОБЖИГА КОЛЧЕДАНА
И СЖИГАНИЯ СЕРЫ В ВОЗДУХЕ*
Температу- ра, СС Обжиг колчедана Сжигание серы
с=0,075 fe=0,ll о=0,08 5=0,09 а=0,10 6=0,0675 о=0,09 5=0,12 0*0* IIII С «О 0=0,12 5=0,09
400 0,993 0,991 0,989 0,991 0,990 0,989
410 0,990 0,989 0,985 0,989 0,989 0,987
420 0,986 0,984 0,977 0,986 0,987 0,981
430 0,983 0,980 0,972 0,983 0,980 0,979
440 0,979 0,976 0,962 0,981 0,979 0,974
450 0,976 0,970 0,958 0,978 0,972 0,969
460 0,970 0,963 0,946 0,971 0,969 0,959
470 0,960 0,959 0,934 0,966 0,960 0,949
480 0,958 0,949 0,923 0,960 0,952 0,940
490 0,948 0,940 0,910 0,950 0,944 0,929
500 0,939 0,928 0,893 0,940 0,933 0,912
510 0,927 0,911 0,878 0,929 0,920 0*898
520 0,910 0,898 0,859 0,918 0,909 0,882
530 0,898 0,881 0,838 0,900 0,891 0,866
540 0,880 0,859 0,814 0,882 0,878 0,843
550 0,860 0,839 0,791 0,862 0,855 0,819
560 0,839 0,819 0,767 0,841 0,831 0,796
570 0,818 0,796 0,738 0,820 0,809 0^770
580 0,790 0,770 0,711 0,799 0,785 0,743
590 0,761 0,741 0,681 0,762 0,759 0*716
600 0,733 0,711 0,652 0,746 0,729 о’б8б
610 0,705 0,683 0,622 0,719 0,700 0,656
620 0,675 0,654 0,591 0,690 0,669 0,627
630 0,644 0,620 0,572 0,658 0,640 0^596
640 0,604 0,589 0,529 0,627 0,606 0*567
газе соответственно диоксида серы
и кислорода
* а и b — содержание в исходном
В объемных долях.
361
XIV. ЗАВИСИМОСТЬ РАВНОВЕСНЫХ СТЕПЕНЕЙ ПРЕВРАЩЕНИЯ
ОТ ДАВЛЕНИЯ И ТЕМПЕРАТУРЫ (РАСЧЕТ НА ЭВМ)
Температу- ра, °C Давление, МПа 0,1 | 0,3 I 0,5 | 0,8 | 1,0
400 0,9950 0,9971 0,9978 0,9982 0,9984
420 0,9918 0.9953 0,9963 0,9971 0,9974
440 0,9869 0,9924 0,9941 0,9953 0,9958
460 0,9797 0,9882 0,9908 0,9927 0,9935
480 0,9654 0,9821 0,9860 0,9889 0,9901
500 0,9550 0,9735 0,9793 0,9836 0,9853
520 0,9357 0,9617 0,9700 0,9761 0,9786
540 0,9105 0,9460 0,9576 0,9666 0,9696
560 0,8786 0,9257 0,9413 0,9529 0,9577
580 0,8399 0,9001 0,9206 0,9360 0.9423
600 0,7943 0.8687 0,8949 0,9148 0,9230
620 0,7427 0,8316 0.8638 0.8888 0,8992
640 0,6862 0,7888 0,8274 0,8579 0.8708
660 0,6267 0,7411 0,7860 0,8221 0,8376
XV. характеристика промышленных насадок
Размеры насадок
(наружный дна-
метрхвысо-
таХтолщниа
стенок), мм
Удельная
поверхность,
м2/м3
Свободный
объем, доля
Эквивалент-
ный диа-
метр, м
Число штук
в 1 м3
Масса
1 м3, кг
Кольца керамические в укладку
50x50x5 ПО 0,735 0,027 8500 650
80x80x8 80 0,72 0,036 2200 670
1 ЛЛ ч/ 1ЛЛ\/ 1 Л £Л л та л лло ТЛЕЛ
Л W 1 W /\ 1 V VV U1 V
Кольца керамические в навал
25 x 25 x3 200 0,74 0,015 50 000 530
50x50x5 90 0,785 0,035 6 000 530
Кварц кусковой
12—25 167 0,47 —
50 63 0,46 —
75 43 0,45 — —
150 29 0,44 — — —
XVI. СКОРОСТЬ КОРРОЗИИ СТАЛЕЙ В СЕРНОЙ КИСЛОТЕ, ММ/ГОД
Сталь 08Х22Н6Т (ЭП-53)
Концентра- Температура, °C
ЦИЯ H2SO4, % 20 30 1 60 1 80 90
0,2 0,437 3—10 -
1,0 0,336 3—10 3—10 — —
5 3—10 3—10 3—10
40 3—10 3—10 3—10 .
92 0,127 0,506 0,675 1,837 2—3
96 0,067 0,087 0,122 0,165 1—3
98 0,045 0,094 0,122 0,154 1,435
362
Сталь 08X21Н6М2Т (ЭП-54)
Концентра- ция H-SO4, Температура. °C
20 40 1 5и 70 80 90
0,5 0,327 1,228 4,583
3 0, 124 3.560 3—10 10 — —
5 3,428 3—10 3—10 10 — —
10 3—10 3—10 3—10 10 — —
40 10 10 — — — —
80 7,854 10 — — — —
92 0, 122 0.431 0,527 1,837 1—3 10
94 0,101 0.303 0.477 0,664 1—3 10
96 0,113 0,201 0,323 0,578 1—3 10
98 0,035 0.С82 0,110 0,163 1,427 10
Сталь 12Х18Н10Т (ЭЯ-1Т)
Концентра- ция H2SO4, % Температура, °C
20 50 1 60 1 80 90 | 100
0,2 0,372 3—10 3—10 10 10 10
1,0 0,235 1,684 1,735 4,482 10 —
2,0 0 401 3,516 3—10 10 — —
5.0 4,432 3—10 3—10 10 — ——
20 5,848 10,445 — — — —
40 3—10 3—10 10 —— — —
60 3—10 3,124 3,445 5,378 10 —
93 0,248 0,444 0,521 1,560 6,314 10,548
96 1,354 1,748 2,875 5,471 8,163 —
98 0,107 0,124 0,232 0,743 4,837 —
Сталь 10Х17Н13М2Т (ЭИ-448)
Концентра- ция H2SO4, % Температура, °C
20 50 1 70 I 80 | 90
1 1,034 1,003 2,331 3—10 3—10
5 0,833 0,127 0,732 3—10 3—10
10 0,885 1,222 1,785 3—10 3—10
20 0,118 1,544 2,765 3—10 3—10
40 4,244 6,832 6—10 6—10 6—10
60 4,415 5—10 5—10 5—10 —
93 0,042 0,056 0,064 0,303 —.
94 0,037 0,063 0,164 0,747 1,828
98 0,024 0,47 0,105 0,167 4,324
363
Сталь 06ХН28МДТ (ЭИ-943)
Концентра- ция HsSO«, % Температура, °C
20 50 60 70 1 75 1 80 1 90
О 0,08 0,011 0,025 0,105 0,123 0,242 0,561
10 0,096 0,016 0,043 0,108 0,137 0,202 0,808
20 0,083 0,089 0,118 0,123 0,135 0,773 1,328
30 0,043 0,044 0,076 0,078 0,42 0,84 1,635
40 0,073 0,081 0,092 0,096 0,124 0,422 1,758
50 0,071 0,093 0,101 0,123 0,146 0,512 1,848
60 0,063 0,072 0,096 0,098 0,103 0,134 1,373
80 0,067 0,067 0,094 0,088 0,112 0,124 1,272
90 0,052 0,085 0,083 0,085 0,097 0,113 0,272
92 0,048 0,64 0,085 0,092 0,096 0,125 0,276
94 0,037 0,039 0,082 0,092 0,095 0,123 0,262
98 0,030 0,039 0,064 0,067 0,069 0,084 0,102
XVII. СКОРОСТЬ КОРРОЗИИ СТАЛЕЙ В ОЛЕУМЕ
Материал Содержание SO3 (св.), % Температу- ра, °C Скорость коррозии, мм/год Материал Содержание SO3 (св.), % Температу- ра, °C Скорость коррозии, мм/год
Ст. 3 08Х22Н6Т 08Х21Н6М2Т 12Х18Н10Т I.0X17H13M2T 08ХН28МДТ 24 100 0,101 Ст. 3 0,096 08Х22Н6Т 0,089 08Х21Н6М2Т 0,088 12Х18Н10Т 0,075 10Х17Н13М2Т 0,025 08ХН28МДТ 18 100 0,114 0,083 0,056 0,040 0,024 0,021
Ст. 3 08Х22Н6Т О8Х21Н6М2Т 12Х18Н10Т 10Х17Н13М2Т 08ХН28МДТ 24 130 0,534 Ст. 3 0,105 08Х22Н6Т 0,095 08Х21Н6М2Т 0,097 12Х18Н10Т 0,089 10Х17Н13М2Т 0,037 08ХН28МДТ 18 130 0,184 0,081 0,061 0,041 0,035 0,029
Ст. 3 08Х22Н6Т 08Х21Н6М2Т 12Х18Н10Т 10Х17Н13М2Т 08ХН28МДТ 24 160 7,65 Ст. 3 1,024 08Х22Н6Т 0,237 08Х21Н6М2Т 0,145 12Х18Н10Т 0,097 10Х17Н13М2Т 0,089 08ХН28МДТ 18 160 0,463 0,124 0,097 0,094 0,075 0,062
Ст. 3 08Х22Н6Т 08Х21Н6М2Т 11,5 100 0,124 12Х18Н10Т 0,082 10Х17Н13М2Т 0,086 06ХН28МДТ 11,5 100 0,041 0,039 0,021
364
XVIII. ОБЛАСТИ ПРИМЕНЕНИЯ ЛИТЕЙНЫХ МАТЕРИАЛОВ
В СЕРНОЙ КИСЛОТЕ
Марка стали или сплава Условия эксплуа- тации I । Марка стали 1 или сплава Условия эксплуа- тации
концент- рация кислоты, % темпера- тура, °C концент- рация КИСЛОТЫ, % темпера- тура, °C
0Х23Н28МЗДЗТЛ 0—100 До 70 До 100 До 100 Х18Н12МЗТЛ, Олеум 10Х18Н9ТЛ, 10Х18Н12МЗТЛ До 100
Х23Н28МЗДЗТЛ 98 Олеум
Х17Н13М2ТЛ 90—94 До 60 Сплав С-15 (фер-0—90 До 100
Х17Н13МЗТЛ 98 До 100 росилид)
Олеум До 100
Ст. 25Л, Ст. 35 90—94 До 20
Х18Н10ТЛ 90—94 До 50
Х18Н9ТЛ 98 До 100 Чугун СЧ18-36 90—94 До 20
98 До 20
Олеум До 20
XIX. МАТЕРИАЛЫ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ИЗГОТОВЛЕНИЯ
ПРОТОЧНОЙ ЧАСТИ НАСОСОВ
Материал или покрытие деталей проточной части Условное обозначение материала Материал или покрытие деталей проточной части Условное обозначение материала
Углеродистая сталь и чу- А Ферросилид л
гун Титан т
Бронза и цветные спла- Б Пластмасса п
ВЫ Резиновое покрытие ме- р
Хромистая сталь типа Д талла
марок Х28, Х34* Керамика, фарфор ф
Хромоникелевая сталь К Графит г
типа марки Х18Н9Т Покрытия из смолы, за- У
Хромоникельмолибде- Е щитные оболочки
новая сталь типа марки Х18Н12МЗТ (ЭИ-448) Хромоникелькремнистая М сталь типа марки 15Х18Н12С4ТЮ (ЭИ-654) Хромоникельмолибде- И номедистая сталь типа марок Х20Н25МЗД2Л, 0Х23Н28МЗДЗТ (ЭИ-943) Покрытия из эмали и стекла э
* Марки нержавеющих сталей соответствуют ГОСТ 5632—72.
365
XX. КОНТРОЛИРУЕМЫЕ И РЕГУЛИРУЕМЫЕ ПАРАМЕТРЫ
ПРИ ОБЖИГЕ КОЛЧЕДАНА В ПЕЧАХ КС
Измеряемая величина Место отбора импульса Верхний предел измеряемой величины Тип датчика Тип вторич- ного прибора Тип регуля тора
Температура,
°C
кипящего В зоне обжига 900 Термопара Потенцио- ПР3.21
слоя ТХА метр ксп 3
отходящих После печи КС 900 То же КСП 4
газов Перед котлом- 900 » То же
утилизатором Перед цикло- 470 » »
ном
Перед электро- фильтром 430 390 » »
После электро- фильтра »
390
по полям Бункера » »
электро- Трубопровод 104 тхк »
фильтра питатель- ной воды перегрето- го пара питательной воды Трубопровод пара 440 То же »
Объемный рас- ход, м3/ч
природно- Газопровод к — ДАШ ПВ4 ПР3.2Г
го газа растопочной
топке
воздуха в Трубопровод ЛГЛЛЛ ‘tUUUU ДМП ПВ4 ПР3.22
печь КС воздуха перед нагнетателем 6000
воздуха в То же То же То же То же
форкамеру печи КС
Расход пере- Трубопровод 38 ДМ ПВ4 ПР3.21
гретого пара, пара
т/ч Скорость вра- Двигатель при- 1500 Тахогенера- Привод Привод,
щения двига- теля питателя колчедана, об/мин Давление, кПа вода питателя тор Д-1 ТЭ-1 ПМУ
природно- Трубопровод — Труба им- тммп —
го газа газа пульсная
воздуха На выходе из нагнетателя 29 0,4 То же То же
насыщен- Трубопровод ДМП ПВ4 —
ного пара пара (бараба- на котла) 0,55
питатель- Трубопровод То же пвю ПР3.21
ной воды питательной
перегрето- воды Трубопровод 0,4 То же пвю ПР3.21
го пара перегретого пара
366
П родолжение
Измеряемая величина Место отбора импульса Верхний предел измеряемой гсличины Тип датчика Тип вторич- ного прибора | i Тип | регуля- !
Разрежение После печи -ыоо дмп ПВ4 ПР3.21
отходящих га- После КУ 1500 Труба им- Тахомер —
зов, Па После циклона 2000 пульсная То же ТММП То же
После СЭФ 2500 » —
Перед нагие- 16000 » » —
тателем В топке разо- » » —
Уровень, мм грева СЭФ В барабане дмпк ПВ-10Э ПР3.21
Сопряжение котла-утилиза- тора Трубопровод 16,0 То же То же То же
кипящего слоя, кПа Содержание воздуха в печь Газопроводы 14,5 Газоанали- ксп-з »
SO2 после пе- чи КС, % Уровень кол- после печи КС и котла-утили- затора Бункер колче- Верхний, затор ДТ Датчик
чедана в бун- керах, м дана нижний ДЭ-63Л1
XXI. КОНТРОЛИРУЕМЫЕ И РЕГУЛИРУЕМЫЕ ПАРАМЕТРЫ
В ПРОМЫВНОМ И АБСОРБЦИОННОМ ОТДЕЛЕНИЯХ
Измеряемая величина Место отбора импульса Верхний предел измеряемой величины Тип датчика Тип вторич- ного прибора Тип регуля тора
Температура, °C орошаю- щей кисло- ты Кислотопровод кислоты на орошение I ПБ 65 Термометр Потенцио-
11 ПБ 30 тем То же метр КСМ4 То же
СБ 42 »
ОА 50 » »
МА 55 —
вытекаю- щей кисло- ты Кислотопровод кислоты из аб- сорбера 1 ПБ 75 тем КСМ4
П ПБ 50 То же То же
СБ 55 »
О А 60 »
МА 70 » —
367
Продолжение
Измеряемая величина Место отбора импульса Верхний предел измеряемой величины Тип датчика Тип вторич- ного прибора Тип регуля- тора
в сбории- Сборник ках кисло- I ПБ ты II ПБ СБ ОА МА газа на Трубопровод входе в газа иа входе абсорбер в I ПБ II ПБ СБ ОА МА газа иа вы- Трубопровод ходе из аб- газа на выходе сорбера из I ПБ II ПБ СБ ОА МА Разрежение га- Перед I ПБ зов по техно- логическому Перед II ПБ тракту, ПА Перед СБ _ После СБ давление га- Трубопровод зов по техно- после иагнета- логическому теля тракту, кПа Газопровод пе- ред О А Газопровод Перед МА Г азопровод после МА Запыленность Коллектор сточных вод, сточных вод pH Концентрация Сборник орошающих кислот, % I ПБ H2SO4 11 ПБ Трубопровод кислоты иа входе в СБ ОА МА Уровень кисло- Сборник I ПБ ты в сборни- Сборник II ПБ ках, м Сборник СБ Сборник ОА Сборник МА 65 ТСМ 45 То же 50 » 60 » 60 » 369 ТСМ 99 То же 40 200 70 J00 ТСМ 40 То же 45 70 60 2600 Труба им- пульсная 2850 т0 Же 5000 » 6500 » пл - ipyoa им- пульсная 16 То же 13,0 » 3,5 » 2,6 — Датчик pH — Концентра- томер 50 КНЧ-1 20 95 КНЧ-1 20SOg То же (св.) 98,6 » 2,0 Пьезомет- рическая трубка с датчиком мсп КСМ4 — То же — » — » — » — КСМ4 — То же — » — » — КСМ4 — То же — » — » — » — Тягомер — тммп То же — » — » — НИМ —- То же — » — » — » — Прибор ПВ 10 ПР3.21 То же ПВ 10 ПР3.21 То же То же » » ПВ 10 »
368
Продолжение.
Измеряемая вели- чина Место отбора импульса Верхний предел измеряемой величины Тип датчика Тип вторичного । прибора Тип регуля- тора
Расход, м3/ч кислоты на Трубопровод кислоты I ПБ 20,0 ИР-51 — —
склад То же, СБ 21,5 » — —
олеума на склад Трубопровод кислоты 4,6 — —
воды в аб- сорбцион- ное отде- ление Трубопровод воды 10,0 Дифмано- метр ДМП Прибор ПВ4
воды в промывное отделение То же 5,0 То же То же
XXII. КОНТРОЛИРУЕМЫЕ И РЕГУЛИРУЕМЫЕ ПАРАМЕТРЫ
В КОНТАКТНОМ ОТДЕЛЕНИИ
Измеряемая величина Место отбора импульса Верхний предел из меряемой величины Тип датчика Тип вторич- ного прибора Тип регуля тора
Температура Трубопровод
технологиче- газа перед ских газов, °C I слоем 440 Термопара Потенцио- ПР3 21
II слоем III слоем IV слоем V слоем Трубопровод после I слоя 480 460 435 430 620 тхк Термопара метр КСП-3 Потенцио-
II слоя III слоя IV слоя V слоя Внутри I слоя До н после 560 500 460 435 500 До 500 тхк тхк метр КСП-4 КСП-4
теплообменни- ков контактно- го узла Объемный рас- ход, хг/ч технологи- Трубопровод 125000 Дифмано- Прибор
веского га- газа перед су- за шильной баш- ней воздуха Перед огду- 40000 метр дсп ДАШ ПВ 4 ПВ 4
на разбав- войной башней
пение
24—584
369
Продолжение
Измеряемая вели- чина Место отбора импульса Верхний предел измеряемой величины Тип датчика Тип вторичного прибора Тип регуля- тора
Концентрация SO2, % Трубопровод газа перед су- шильной баш- ней 9,5 Г азоанали- затор ДТ Прибор кед ПР3.21
Трубопровод газа на выхо- де из моногид- ратного абсор- бера 0,02 Г азоанали- затор ПГУ-2 Потенцио- метр КСП-3
ЛИТЕРАТУРА
1. Лукьянов П. М. История химических промыслов и химической промыш-
ленности России до конца XIX века/Под ред. С. И. Вольфковича. М.,
Изд-во АН СССР, 1948. Т. 1, 544 с.
2. Лукьянов П. М., Соловьева А. С. История химической промышленности
СССР, М., Просвещение, 1966. 254 с.
3. Малин К. М., Аркин И. Л., Боресков Г. К., Слинько М. Г. Технология
серной кислоты. М. — Л., Госхимиздат, 1950. 570 с.
4. Амелин А. Г. Производство серной кислоты. М., Химия, 1967. 472 с.
5. Научно-исследовательский институт по удобрениям и инсектофунгицидам
им. проф. Я- В. Самойлова. Юбилейный сборник. М., Химия, 1969. 162 с.
6. Sulphur, 1978, N 139, р. 18; 1981, N 155, р. 48; 1984, N 170, р. 39.
7. Меренкова Т. М. — Хим^ пром, за рубежом, 1983, № 10 (250), с. 1—18.
8. Коттон Ф., Уилкинсон дж. Основы неорганической химии. Нер. с англ.
М., Мир, 1979. 678 с.
9. Справочник сериокислотчика/Под ред. К. М. Малина. 2-е изд. М., Химия,
1971. 746 с.
10. Реми Г. Курс неорганической химии. Пер. с ием. М., Мир, 1972. Т. 1,
686 с.
11. Карапетянц М. X. Химическая термодинамика. 3-е изд. М., Химия, 1975.
536 с.
12. Амелин А. Г. Технология серной кислоты. 2-е изд., перераб. М., Химия,
1983. 360 с.
13. Термодинамические свойства индивидуальных веществ. Справочное изда-
ние. В 4-х т./Сост. Гурвич Л. В., Вейц И. В., Медведев В. А. и др.
3-е изд. М., Наука, 1978. Т. 1, кн. 2, 328 с.
14. Несмеянов А. Н., Несмеянов Н. А. Начала органической химии. М., Хи-
мия, 1970. Кн. 2, 824 с.
15. tasullo Н„ Oscar Т. Sulfuric Acid Use and handling. N. Y., 1965. 312 p.
16. Минеральные ресурсы промышленно развитых капиталистических и раз-
вивающихся стран иа начало 1978 года/Под ред. В. Н. Полуэктова. М.,
Всесоюзи. геол, фонд, 1979. 444 с.
17. Советский Союз. Политико-экономический справочиик/Сост. В. А. Голи-
ков. М., Политиздат, 1982. 169 с.
18. Авербух Т. Д. и др.— Хим. пром., 1971, № 3, с. 200—203.
19. Отвагина М. И., Сретенская Н. С. — Цветные металлы, 1972, № 6,
с_ 23___24.
20. А. с. 362632, 1972 г. (СССР).
21. Отвагина М. И., Сретенская Н. С., Буриченкова Н. Г. — Тр.НИУИФ,
1975, вып. 225, с. 194—199.
370
22. Отвагина Al. /7.. Сретенская И. С., Васина О. Д. — Цветные металлы...
1977, № 6, с. 24—25.
23. Кипнис А. Я. и др. — Havq. тр. (Гипроникель), вып. 62, Л., Гипроникель,
1975. с. 16—27.
24. Alining Congr J. 1969. v. 55. N 6, p. 38.
25. World Mining, 1970. N 10, p. 37.
26. Яенковский ,V1. .4. Природная сера. M., Химия, 1972. 240 с.
27. Далин К. М., Боресков Г. К., Пейсахов И. Л. и др. Технология серной
кислоты и серы. М.— Л., Госхимиздат, 1941. 520 с.
28. Борбат В. Ф., Добросельская Н. П., Михайлов В. В. Производство эле-
ментарной серы из серных руд и при комплексной переработке сульфид-
ных концентратов. М., «Цветметинформация», 1971. 90 с.
29. Отвагина А1. И., Сретенская И. С., Иванов И. М.— В кн.: Техническая
и экономическая информация. Промышленность удобрений и серной кис-
лоты. Переработка серосодержащего сырья/Под ред. К. М. Малина. М.,
НИУИФ, 1966, № 3—4, 192 с.
30. Sulphur, 1964, N 50, р. 33—38; 1974, N 118, р. 19—34.
31. Терновская А. И., Коренберг Я. Г. Обжиг серного колчедана в кипящем-
слое. М., Химия, 1971. 198 с.
32. Гудима И. В., Шейн Я. П. Краткий справочник по металлургии цветных
металлов. М., Металлургия, 1975. 535 с.
33. Sulphur, 1978, N 137, р. 26—30; 1979, N 142, р. 26—29.
34. Филатов Ю. В., Якушев В. И., Кандауров К. С., Михайловская Ф. Р. —
Тр.НИУИФ, 1976, вып. 227, с. 21—29.
35. Добросельская И. П., Гудима И. В., Васильев Б. Т. Утилизация серни-
стых газов заводов цветной металлургии. М., Металлургия, 1976. 160 с.
36. А. с. 322944, 1972 г. (СССР); 360836, 1972 г. (СССР).
37. Быховер Н. А. Научно-технический прогресс и проблемы минерального
сырья. М., Недра, 1979. 223 с.
38. Загряцкая Л. М. и др. — Кокс и химия, 1980, № 2, с. 51.
39. Отвагина М. И. Автореф. канд. дис. М., НИУИФ, 1957.
40. Малец А. М. и др. — ЖХП, 1963, № 11, с. 30—33.
41. Епифанов В. С., Кабанова Г. Б. — ЖХП, 1972, № 9, с. 32.
42. Чижиков Д. М., Счастливый В. П. Теллур и теллуриды. М., Наука, 1966-
160 с.
43. Отвагина М. И. — Металлург, и хим. пром. Казахстана, 1960, № 1,
с. 76—85.
44. Отвагина М. И., Голованева А. И. — В кн.: Техническая н экономическая
информация. Промышленность удобрений и серной кислоты. Переработка
серосодержащего сырья/Под ред. К. М. Малина, М., НИУИФ, 1966,
№ 3—4. 192 с.
45. А. с. 648513, 1978 г.; 431119, 1974 г. (СССР).
46. Букин В. В., Отвагина М. И., Малашкина С. А.—Тр.НИУИФ, 1977,
вып. 230, с. 133—137.
47. Юров П. П., Отвагина А1. И., Овчинников Б. П. и др. — Цветные метал-
лы, 1972, № 5, с. 78—80.
48. Отвагина М. И., Еремин О. Г., Васильев Б. Т., Епифанов В. С. — В реф.
сб. НИУИФ: Промышленность минеральных удобрений и серной кисло-
ты. М„ НИИТЭХИМ, 1974, вып. 7, с. 15—19.
49. Альтшуллер В. С., Сеченов Г. П. Процессы в кипящем слое под давле-
нием. М., Изд-во АН СССР, 1963. 214 с.
50. Гельперин И. И., Айнштейн В. Г., Кваша В. В. Основы техники псевдо-
ожижения. М., Химия. 1967. 664 с.
51. Терновская А. И., Васильев Б. Т., Дубовицкий Б. А. и др. — ЖПХ, 1972,
№ 3, с. 188—193.
52. Терновская А. Н„ Васильев Б. Т., Дубовицкий Б. А. и др. — Тр.НИУИФ,
1975, вып. 225, с. 5—12.
53. А. с. 491812, 1975 г. (СССР).
54. Ануров В. В., Попов А. Е., Епифанов В. С. и др. — В реф. сб. НИУИФ:
Промышленность минеральных удобрений и серной кислоты. М., НИИТЭ-
ХИМ, 1977, вып. 5, с. 4—7.
24*
371
55. Mayer В, — Chem. Rev., 1976, v. 76, N 3, p. 367—387.
56. Rieke I. M„ Barro R. F. — Canad. J. Phys., 1969, N 21, p. 2423—2427.
57. Семенов И. H. О некоторых проблемах химической кинетики и реакцион-
ной способности. М., Изд-во АН СССР, 1958. 686 с.
58. Цейтлин А. И.— В кн.: Тр. НИОХИМ, Л., Госхимиздат, 1959, т. 12,
с. 85—92.
59. Шварцштейн Я- В., Кузьмин Г. А. Получение сернистого газа из эле-
ментарной серы. М., Химия, 1972. 157 с.
60. Шелякин А. П., Васильев Б. Т., Воротников А. Г. — В реф. сб. НИУИФ:
Промышленность минеральных удобрений и серной кислоты. М.,
НИИТЭХИМ, 1976, вып. 9, с. 5—6.
61. Шелякин А. П„ Васильев Б. Т. и др. — Докл. СО АН СССР. Физика го-
рения и взрыва. 1980, № 2, с. 138—140.
-62. Шелякин А. П., Васильев Б. Т., Воротников А. Г. — ЖПХ, 1980, т. 53,
№ 4, с. 813—816.
63. Шелякин А. П., Клепач А. С.. Васильев Б. Т. — ЖПХ, 1984, № 4, т. 57,
с. 919—921.
64. Шелякин А. П. Автореф. канд. дис. М., МХТИ, 1979.
65. Васильев Б. Т., Добросельская Н. П. — Хим. пром, за рубежом, 1977,
№ 8 (176), с. 23—33.
66. Шелякин А. П., Васильев Б. Т., Воротников А. Г. и др. — Хим. пром.,
1979, № 9, с. 49—50.
67. Шелякин А. П. — Докл. СО АН СССР. Физика горения и взрыва, 1984,
№ 2, с. 53—55.
68. Явор В. И., Сазонов С. Ф„ Ким И. А., Иванова И. Д.— Цветная метал-
лургия, 1979, № 17, с. 37—39.
69. А. с. 715915, 1980 г. (СССР).
70. А. с. 1063770, 1983 г. (СССР).
71. А. с. 545579, 1977 г. (СССР).
72. Якушев В. И. Автореф. канд. дис. М., МХТИ, 1978.
73. А. с. 644724, 1979 г. (СССР).
74. Исследование процесса окисления пиритов оксидами железа в псевдо-
ожиженном слое. Сообщение 1. Grigoriu J., Calistru С., Balasian J.,
Capac D. Cercetarea procesului de oxidare a piritelor en oxizi de fier «Rev.
chim.» (RSR), 1982, v. 33, № 12, p. 1118—1121 (рум.; рез. русск., нем.,
англ., фр.). Сообщение 2. Grigoriu J., Calistru С., Balasian 1. Studiul
procesului de oxidare a piritelor en oxizi de fier in strat fluidizat «Rev.
chim.» (RSR), 1983, v. 34, N 2, p. 135—137 (рум.; рез. русск., аигл.).
75. Амелин А. Г., Яшке Е. В. Производство серной кислоты. М., Высшая
школа, 1980. 245 с.
76. Справочник по пыле- и золоулавливанию/Под ред. А. А. Русаиова. М.,
Энергия, 1975. 296 с.
77. Ужов В. Н„ Вальдберг А. Ю. Подготовка промышленных газов к очист-
ке. М., Химия, 1975. 216 с.
78. Резницкий И. Г. — Цветные металлы, 1978. № 3, с. 21—22.
79. Балашов А. А., Васильев Б. Т., Козлов В. П. и др. — Тр.НИИУИФ, 1975,
вып. 225, с. 69—80.
80. Электрофильтры в цветной металлургии/Под ред. А. А. Гурвица. М.,
Металлургия, 1982. 136 с.
81. Васильев Б. Т., Борисов В. М., Терентьев Д. Ф., Львова И. С. — Хим.
пром., 1974, № 4, с. 276—280.
82. Воротников А. Г., Васильев Б. Т., Борисов А. И. и др. — Тр. НИУИФ,
1975, вып. 225, с. 135—142.
83. Бернацкий Ю. П., Раздорских Л. М., Дегтева В. И. и др. — Тр.
НИУИФ, 1975, вып. 225, с. 183—190.
84. Солодянкина Н. Л., Борисов В. М., Скоробогатов В. А. и др. — Хим.
пром., 1981, № 3, с. 27—29.
85. Амелин А. Г. — Тр. НИУИФ, 1971, вып. 218, с. 62—71.
86. Раздорских Л. М„ Епифанов В. С., Хусес Я. Э. и др. — Тр. НИУИФ,
1975, вып. 225, с. 29—32.
87. Kovalevski Z. — Przem. chem., 1980, v. 59, № 7, p. 389—390.
372
88. Галкин Н. П„ Зайцев В. А., Серегин М. Б. Улавливание и переработка
фторсодержащпх газов. М., Атомиздат, 1975. 239 с.
89. Кирицев И. А. — Хим. пром., 1975, № 9, с. 40—43.
90. Орешин 10. И., Епифанов В. С., Коняхина Л. В. и др. — В реф. сб.
НИУИФ: Промышленность минеральных удобрений и серной кислоты
М., НИИТЭХИМ, 1979, вып. 7. с. 1—3.
91. Успенский Д. Д.. Жук Н. Н„ Шулятьев Н. В. и др. — В реф. сб. НИУИФ:
Промышленность минеральных удобрений и серной кислоты. М.,
НИИТЭХИМ, 1979, вып. 7, с. 4—5.
92. Боресков Г. К. Катализ в производстве серной кислоты. М. — Л., Гос-
химиздат, 1954. 348 с.
93. Илларионов В. В. Ванадиевые катализаторы для контактного производ-
ства серной кислоты. М., Госхимиздат, 1963. 176 с.
94. А. с. 107200, 1957 г.; 116093, 1958 г.; 422445, 1974 г.; 432921, 1974 г.
(СССР).
95. Малкиман В. И. Автореф. канд. дис. Л., ЛТИ, 1969.
96. А. с. 422445, 1974 г. (СССР).
97. А. с. 432921, 1974 г. (СССР).
98. Масленников Б. М., Капилевич С. Б., Спиридонова Н. В., Лаба-
дюк И. А.— ДАН СССР, 1976, т. 227, Ns 6, с. 1416—1417.
99. Мулленов И. П., Добкина Е. И., Дерюжкина В. И., Сорока В. Е. Тех-
нология катализаторов. Л., Химия, 1979. 308 с.
100. Томишко М. М. Автореф. канд. дис. М., НИУИФ, 1981.
101. Масленников Б. М., Илларионов В. В., Губарева В. И. и др. — ДАН
СССР, 1978, т. 238, № 6, с. 1411—1414.
102. Иванов А. А., Полякова Г. М. Механизм и кинетика каталитических
процессов. Новосибирск. Ин-т катализа, СО АН СССР, 1977. 81 с.
103. Глазырин М. П., Красильников В. И., Ивакин А. А. — ЖНХ, 1980, т. 25,
№ 12, с. 3368—3373.
104. Боресков Г. К, Буянов Р. А., Иванов А. А. — Кинетика и катализ, 1967,
т. 8, № 1, с. 153.
105. Иванов А. А., Боресков Г. К-, Буянов Р. А. и др. — Кинетика и катализ,
1968, т. 9, Ns 3, с. 560—564.
106. Harris J. Z., Normann J. R.— Ind. End. Chem., Proc., Des. Devel., 1972,
v. 11, p. 564.
107. Иваненко С. B. — В кн.: Сернокислотный катализ. Материалы междуна-
родной школы. Новосибирск, 1982, Ч. 2, с. 37—45.
108. Чваковский С. П. Автореф. канд. дис. М., НИОПИК, 1973.
109. Иваненко С. В., Салтанова В. П., Торочешников И. С. и др. — Изв. ву-
зов. Химия и хим. технол., 1973, т. 6, № 12, с. 1862—1864; Проблемы ка-
тализа. Тр. МХТИ, 1973, № 90, с. 80.
ПО. Боресков Г. К, Бесков В. С., Иванов А. А. — ДАН СССР, 1969, т. 183,
с. 856.
111. Иванов А. А., Боресков Г. К-, Бесков В. С. — Пористая структура ката-
лизаторов и процессы переноса в гетерогенном катализе. Новосибирск.
Ин-т катализа СО АН СССР, 1970. 205 с.
112. Балашов А. А., Иванов А. А. — Тр. НИУИФ, 1975, вып. 225, с. 91—97.
ИЗ. Никитский В. П. Автореф. канд. дис. М., МХТИ, 1979.
114. Иванов А. А., Беляева Н. П. — В кн.: Сернокислотный катализ. Материа-
лы Международной школы. Новосибирск, 1982. Ч. 2, с. 3—20.
115. Васильев Б. Т., Доброселъская Н. П., Масленников Б. М. — Хим. пром,
за рубежом, 1979, № 2 (вып. 194), с. 40—57.
:116. Козлов В. IE, Балашов А. А., Васильев Б. Т., Добросельская Н. П. Теп-
лообменное оборудование контактного отделения и новые типы контакт-
ных аппаратов для переработки сернистых газов цветной металлургии.
М., ЦНИИцветмет экономики и информации, 1979. 56 с.
117. А. с. 432096, 1974 г. (СССР).
118. Садиленко А. К-, Козлов В. П., Ху вес Я. Э., Балашов А. А. Контактное
отделение сернокислотного цеха. М., Химия, 1972. 96 с.
119. Добросельская Н. П., Лаврентьева Г. Ф. — Цветная металлургия, 1979,
№ 4, с. 61—63.
373
120. Катализ в кипящем слое/Под ред. И. П. Мухленова и В. М. Померанце-
ва. М, Химия, 1978. 238 с.
121. Отвагина Л1. И., Терентьев Д. Ф., Двор В. И., .Мегвинов А. А. — В реф.
сб. НИУИФ: Промышленность минеральных удобрении п серной кисло-
ты. М., НИИТЭХИМ, 1970, вып. 5—6, с. 42—46.
122. Масштабный переход в химической промышленности/Под ред. А. М. Ро-
зена. М., Химия, 1980. 319 с.
123. Козлов В. П„ Явор В. И. — Тр. НИУИФ. 1977, вып. 230, с. 72—74.
124. А. с. 958319, 1982 г. (СССР).
125. Pincovschi, Е. Sehnologia acidulni sulfuric si a compusilor intermediari.
Bucuresti. Ed. tehnica, 1967. 392 p.
126. Боресков Г. K-, Иванов А. А. и dp. — В кн.: Кинетические уравнения для
расчета промышленных контактных аппаратов производства серной кис-
лоты. Новосибирск, Ин-т катализа, СО АН СССР, 1980, с. 1—30.
127. Расчеты химико-технологических процессов/Под ред. И. П. Мухленова.
Л., Химия, 1982. 300 с.
128. Угначев В. И-, Петровская Г. И., Козлов В. П. и др. — Тр. НИУИФ,
1984, вып. 244, с. 162—174.
129. Сорока В. Е., Явор В. И. Новые системы производства серной кислоты
из металлургических газов, серы и колчедана. М., ЦНИИцвегмет эконо-
мики и информации, 1979. 68 с.
130. Рамм В. М. Абсорбция газов. 2-е изд. М., Химия, 1976. 768 с.
131. Шемраев Н. В., Тошинский В. И., Васильев Б. Т. — В реф. сб. НИУИФ:
Промышленность минеральных удобрений и серной кислоты. М., НИИ-
ТЭХИМ, 1981, вып. 3. с. 18—19; в кн.: Материалы XII Всесоюз.
науч.-техн. конф. «Технология неорганических веществ и минеральных
удобрений», Чимкент, 1981. Т. 2, с. 169—171.
132. Сигал И. Я- Защита воздушного бассейна при сжигании топлива. Л.,
Недра, 1977. 294 с.
133. Розенкноп 3. П. Извлечение двуокиси серы из газов. М., Госхимиздат,
1952. 192 с.
134. Чертков Б. А. Автореф. докт. дне. М., МХТИ, 1964.
135. Кулешова А. А., Чертков Б. А-, Сафонов А. В. — В реф. сб. НИУИФ:
Промышленность минеральных удобрений и серной кислоты. М.,
НИИТЭХИМ, 1973, вып. 5, с. 9—17.
136. Чертков Б. А. и др. Получение серной кислоты из отходящих газов кис-
лотно-каталитическим способом. Обзорн. информ., М., НИУИФ, 1974.
56 с.
137. Терновская А. И.— Хим. пром., 1962, № 7, с. 501.
138. Бродский Ю. И., Балычева К. В. Современные методы очистки дымовых
газов от сернистого ангидрида и их экономика. Сер.: Промышленная са-
нитария и санитарная очистка газов. М., ЦНИИТЭнефтехим, 1973. 89 с.
139. Сальнюк А. П., Шавинская И. Г., Горшков В. П. Анализ методов очист-
ки газовых выбросов от сернистого ангидрида и сероводорода. Обзорн.
информ. ВНИПИСЕРА, М„ НИИТЭХИМ, 1981. 33 с.
140. Кафаров В. В. Принципы создания безотходных химических производств.
М., Химия, 1982. 288 с.
141. Habashi Г. Dugdale К. — Z. tschr. anorg. u. allg. Chem. 1971, Bd. 380,
N 3, S. 322—325.
142. Кириллова Ж. В., Перфильев В. М., Сущее В. С. Использование отрабо-
танной серной кислоты в СССР и за рубежом. Обзорная информация,
Сер.: Минудобрения и серная кислота, М., НИИТЭХИМ, 1984 г., 26 с.
143. А. с. 882594, 1981 г. (СССР).
144. Васильев Б. Т-, Добросельская Н. П. — Хим. пром, за рубежом, 1980,
№ 10 (214), с. 35—45.
145. Васильев Б. Т„ Воротников А. Г., Илларионов В. В., Филатов Ю. В.—
Тр. НИУИФ, 1979, вып. 235, с. 55—70.
146. Васильев Б. Г., Добросельская И. П. — Цветные металлы, 1977, № 7„
с. 27—29.
374
147. Васильев Б. Т., Масленников Б. М., Каграманов Г. Г. и др. — Вопросы
атомной науки и техники. Сер.: Атомно-водородная энергетика и техно-
логия. М„ 1979, вып. 1 (5), с. 148—152.
148. Васильев Б. Т„ Каграманов Г. Г., Славинский А. В. — Вопросы атомной
HclVhM И ТЕХНИКИ. Grp-- АТОМНО'ВОДОрОдНаЯ ЭНсрГСТИКа И 1 ех ПОЛОГИ л,
1981, вып. 2 (9), с. 59—63.
149. Васильев Б. Т., Новиков А. А., Спиридонова И. В. и др. — Вопросы
атомной науки и техники. Сер.: Атомно-водородная энергетика и техно-
логия, 1982, вып. 3 (13), с. 26—27.
150. Добросельская Н. И., Видякин Н. И., Васильев Б. Т. Производство сер-
ной кислоты из газов с повышенной и высокой концентрацией двуокиси
серы в цветной металлургии. М., ЦНИИцветмет экономики н информа-
ции, 1978. 57 с.
151. Кафаров В. В., Золотарев В. В., Михайлов Г. М.— Хим. пром., 1981,
№ 9, с. 36—39.
152. Сорока В. Е., Васильев Б. Т., Кочергин Ю. А. — Сб. Гетерогенные ката-
литические процессы. Тр. ЯТИ. Л., ЛТИ, 1975, с. 10—15.
153. Васильев Б. Т., Борисов А. И., Воротников А. Г. и др. — Тр. НИУИФ,
1975, вып. 225, с. 115—128.
154. А. с. 644525, 644526, 1979 г. (СССР).
155. Епифанов В. С., Сафонов А. В., Набатов В. В. и др. — В реф. сб.
НИУИФ: Промышленность минеральных удобрений и серной кислоты.
М., НИИТЭХИМ, 1974, вып. 8, с. 12—16.
156. Епифанов В. С., Хрящев С. В., Терентьев Д. Ф. и др. — Хим. пром. 1977,
№ 2, с. 2.
157. Масленников Б. М„ Васильев Б. Т„ Спиридонова Н. В. — Вопросы атом-
ной науки и техники. Сер.: Атомно-водородная энергетика и техноло-
гия, 1981, вып. 2 (9), с. 23—25.
158. Sulphur, 1981, № 153, р. 15.
159. Sulphur, 1982, № 161, р. 13—14.
160. Sulphur, 1982, № 162, р. 27.
161. Нейперт К. В., Смыслов Н. И., Бернацкий Ю. П. — Тр. НИУИФ. 1961,
вып. 2, с. 1—9.
162. Соловьев Ю. М. Автореф. канд. дис. М., МХТИ, 1970.
163. Лобова 31. В., Епифанов В. С., Смыслов Н. И. — ЖПХ., 1973, т. 46,
№ 6, с. 1334—1336.
164. Лобова М. В. Автореф. канд. дис. М., НИУИФ, 1974.
165. А. с. 389011, 1973 г. (СССР).
166. Епифанов В. С., Соловьев Ю. М. и др. Использование отработанной сер-
ной кислоты в нитрозном сернокислотном производстве. Тезисы докла-
дов Всесоюзного совещания «Утилизация жидких сернокислотных отхо-
дов», Пермь, 1984 г., 54 с.
167. Громов А. П., Епифанов В. С. — Хим. пром., 1981, № 8, с. 38.
168. А. с. 258063, 1970 г. (СССР).
169. Смыслов Н. И., Епифанов В. С., Копылов В. А. и др. — Хим. пром.,
1973, № 5, с. 40.
170. Козловский Э. М. и др. — В кн.: Экономика и научная организация тру-
да в химической промышленности. М., НИИТЭХИМ, 1978, № 3, 48 с.
171. Осмулькевич В. А. Производство серной кислоты из технологических га-
зов предприятий цветной металлургии. М., Металлургия, 1971, 95 с.
172. Отвагина М. И., Купряков Ю. П., Артемов Н. Н. и др. — Цветные ме-
таллы, 1971, № 7, с. 5—6.
173. Двор В. И., Отвагина М. И., Терентьев Д. Ф. и др. — В реф. сб. НИУИФ:
Промышленность минеральных удобрений и серной кислоты. М.,
НИИТЭХИМ, 1971, вып. 6, с. 11—16.
174. Зубарев В. И., Равданис Б. И., Фигурнов И. В.— Цветные металлы,
1978, № 6, с. 1—3.
175. Снурников А. П. Комплексное использование сырья в цветной металлур-
гии. М., Металлургия, 1977. 272 с.
176. Беньяш Е. Я. и др. — Тр. ВНИИцветмета, 1975, № 25, с. 247—252.
177. А. с. 322944, 1972 г. (СССР).
375
178. Отвагина М. И., Явор В. И., Сретенская Н. С., Шарифов М. Ю. — В реф-
сб НИУИФ: Промышленность минеральных удобрений и серной кисло-
ты. М„ НИИТЭХИМ, 1972, вып. 4, с. 16-20.
179. Серманизов С. С., Тарат Э. Я-, Балабеков О. С. и др. — Хим. пром.»
1979, № 8, с. 35—37.
180. Козлов Г. С., Ведерников В. Б., Сабанцев Б. И. и др. — Цветные ме-
таллы, 1978, № 3, с. 18—19.
181. Дубчак Р. В. Зарубежная практика очистки газов от фтористых соеди-
нений при производстве алюминия. М., ЦНИИцветмет экономики и ин-
формации, 1978. 30 с.
182. Амелин А. Г., Алешин А. М.— ЖПХ, 1982, т. 55, № 11, с. 2421—2428.
183. Иванова И. Д., Явор В. И., Еремин О. Г. — Тр. Гинцветмета, 1978»
№ 44, с. 117—121.
184. Явор В. И., Муслимов А. М., Иванова И. Д. и др. — Цветные металлы,
1980, № 2, с. 37—39.
185. Явор В. И., Новожилов В. Н. Совершенствование способов переработки
металлургических газов на серную кислоту. М., ЦНИИцветмет эконо-
мики и информации, 1981. 36 с.
186. резницкий И. Г., Добросельская И. И. Производство серной кислоты из
отходящих газов цветной металлургии. М., Металлургия, 1983. 136 с.
187. Явор В. И., Иванова И. Д., Сазонов С. Ф. — Цветные металлы, 1978,
№ 11, с. 50—52.
188. Явор В. И-, Иванова И. Д., Ким И. А. — Цветная металлургия, 1981,
№ 21, с. 25—28.
189. Ulrich X. F., Sander И. В. — AIME. Annual Meeting, Atlanta, Georgia,
1977, March, N 8, p. 2—39.
190. A. c. 1003880, 1983 г. (СССР).
191. Кофман В. Я. Новые тенденции в производстве серной кислоты. Экспр.
информ. Сер. XV. Химические производства, контроль и опробование
сырья и продуктов цветной металлургии. М., ЦНИИцветмет экономики и
информации, 1982, № 6, 7 с.
192. Жохова Т. И., Стерлин В. И., Лембриков В. М. — Тр. НИУИФ, 1976,
вып. 227, с. 13—17.
193. Удыма И. Г. Аппараты с погружными горелками. 2-е изд. М.. Машино-
строение, 1973. 271 с.
194. Живайкин Л. Я-, Васильев Б. Т., Шварцштейн Я. В. и др. — Хим. пром.,
1976, № 10, с. 51—53.
195. Sulphur, 1971, N 92, р. 44; 1972, N 99, р. 17.
196. Барановский И. В., Коваленко Л. М., Ястребенецкий А. Р. Пластинчатые
и спиральные теплообменники. М., Машиностроение, 1973. 288 с.
197. Вертикальный кожухотрубный теплообменник пленочного типа. Информ,
о науч.-техн, сотрудничестве СЭВ, 1972, № 35, с. 480.
198. Шехтман А. А., Бляхер И. Г., Штерензон А. Л. и др. — Хим. пром.,
1975, № 6, с. 460—461.
199. А. с. 378698, 1973 г. (СССР).
200. Головачевский IO. А., Васильев Б. Т. — В реф. сб.: Промышленность ми-
неральных удобрений и серной кислоты. М., НИИТЭХИМ, 1979, вып. 1,
с. 14—18.
201. Явор В. И., Колганов В. А. Улавливание брызг и тумана серной кислоты
в сернокислотном производстве. М., ЦНИИцветмет экономики и инфор-
мации, 1984. 32 с.
202. Яшке Е. В., Филатов Ю. В., Колганов В. А., Недоборов Ю. П. — Хим.
пром., 1981, № 7, с. 35—37.
203. Клинов И. Я. и др. Химическое оборудование в коррозионно-стойком
исполнении. Справочник. М., Машиностроение, 1970. 589 с.
204. Коррозия и защита химической аппаратуры. Справочное руководство.
Т. 4. Производство серной кислоты и фосфорных удобрений/ПоД ред.
А. М. Сухотина и В. С. Зотикова. Л., Химия, 1970. 272 с.
205. Туфанов Д. Г. Коррозионная стойкость нержавеющих сталей п чистых
металлов. Справочник. 4-е изд., М., Металлургия, 1982. 352 с.
376
206. Томашев Н. Д., Чернова Г. П. Коррозия и коррозионно-стойкие сплавы.
М., Металлургия, 1973. 232 с.
207. Малышева Г. В., Чудновский Е. М., Башкиров В. А. — Защита металлов,
1982. т. 18. № 4, с. ”641—643.
208. Добролюбов В. В., Киселев В. Д„ Петровская В. .4. и ор. — Вопросы
атомной науки и техники. Сер.: Атомно-водородная энергетика и техно-
логия, 19/9. 1 (5). с. 144—147.
209. Бернштейн И. М„ Васильев Б. Г., Голант А. И. и др. Автоматизация
управления сернокислотным производством. М., Химия, 1975. 246 с.
210. Кафаров В. В., Михайлов Г. В. Введение в инженерные расчеты хими-
ческих реакторов с неподвижным слоем катализатора. М., МХТИ, 1969.
158 с.
211. Бесков В. С. Моделирование химических процессов и реакторов. Ново-
сибирск, СО АН СССР, 1971, Т. 1, 111 с.
212. Михайлов Г. В., Витков В. С., Живописцев В. А. — Хим. пром., 1981,
№ 6, с. 372.
213. Страус В. Промышленная очистка газов. Пер. с англ. М., Химия, 1981.
616 с.
214. Зайцев П. Л1., Владимирская Г. Н., Кельман Ф. Н., Макарова Е. И. Ана-
литический контроль в производстве серной кислоты. М., Химия, 1979.
280 с.
215. Кушелев В. П. Основы техники безопасности на предприятиях химиче-
ской промышленности. М., Химия, 1977. 280 с.
ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ
Абсорбер (ы)
барабанные 210
башенные 193, 194
Вентури 288
гидравлическое сопротивление 199
моногидратные 204 сл., 353 сл.
насадочные 206, 208 сл.
олеумные 204 сл., 209 сл., 353 сл.
плотность орошения 212, 215
работы контроль 367 сл.
— показатели 288
•— регулирование 267 сл.
распылительные 210, 288
сопоставление 211
тарельчатый 206, 288
тепловой баланс 309
Абсорбция
абсорбента концентрация 202
горячая 184
движущая сила 198, 203, 213
диоксида серы 202 сл., 219 сл.
извлечения степень 204 сл., 212
константа Ко 200
массопередачи коэффициент 214 сл.
в нитрозном процессе 270
паров воды 193, 194, 198 сл.
плотность орошения 212, 215
скорость 198, 199, 201, 202
температура критическая 203
триоксида серы 202 сл.
число единиц переноса 213
Автоматизация производства 339 сл.
АСУ 348 сл.
датчики 366 сл.
Автоматизация производства
комплексная 346 сл.
контактного отделения 342 сл.
обжига колчедана 340, 341
приборы вторичные 366 сл.
промывного отделения 341, 342
регуляторы 366 сл.
сушильио-абсорбционного отделе-
ния 344 сл.
схемы см. Схемы автоматизации
Агломераторы звуковые 234
Адсорбция мышьяка цеолитами 142
Башни промывные
конструкция 147, 148
насадка 362
плотность орошения 212, 274
работы режим 142 сл.
тепловой баланс 309
Башни сушильные
насадки поверхность 200
производительность 353 сл.
работы режим 193, 194
размеры 353 сл.
расчет 200 сл.
скорости газа 200
тепловой баланс 309
Борескова—Иванова уравнение 190
Брызгалки щелевые 320, 321
Брызгоуловители 231, 232, 321 сл.
Ванадиевые катализаторы
активность 157, 186
БАВ 153
377
Ванадиевые катализаторы
выгрузка 184
загрузка 156, 186, 260
ИК 154, 155, 163 ел., 172
иностранных фирм 156, 164
коэффициент запаса 186
масса расчетная 158, 159
МСВ 155, 166
плотность 163
поверхность 155, 163, 166
приготовление 154, 155
распределение по слоям 132, 133
расход 191, 253
СВД 154 сл., 163 сл., 172
содержание пятиоксида ванадия
164
состав 154, 157
степень использования 155, 156,
166, 186
температура разогрева слоя 160
трубчатые 155, 156
ТС 154
энергия активации 163, 165
Вентури аппараты
абсорберы 288, 290
гидравлическое сопротивление 233
концентратор 302
промыватель 148, 149
скруббер 148, 149, 232, 233
Водород, получение в сернокислот-
ном цикле
замкнутом 262 сл., 266
разомкнутом 265, 266
Возгонка серы из колчедана 44 сл
Вязкость
олеума 20, 360
серной кислоты 20, 360
серь; жидкой 29, 91, 92
Гидравлическое сопротивление
абсорбционных башен 199, 230
Вентури скруббера 233
коагуляторов 234
контактных аппаратов 186, 187,
191
фильтров 234, 321 сл.
Гипс 40
Горение серы 93 сл.
Гудроны кислые 297 сл.
Да вление паров
воды
в газе сушильных башен 200, 201
над серной кислотой 193
над диоксидом серы (жидким) 21
зависимость от температуры 16
над олеумом 17, 357
расчет 16, 17
над серной кислотой 15 сл., 357
— серой 29, 91, 92
серы над дисульфидом железа 45
Двойное контактирование 130 сл.,
171 сл., 247 сл., 251, 288 сл.
Диоксид серы
абсорбция 202 сл., 219 сл., 231
выброс в атмосферу 218, 256, 258
жидкий, получение 235 сл.
конверсия см. Окисление диоксида
серы
концентрирование 221 сл.
магнезитовый метод 235
серо-олеумный метод 237
сульфит-бисульфитом аммония
223, 224, 235
концентрированный, получение
235 сл.
металлургических газов 279 сл.
окисление см. Окисление диоксида
серы
растворимость
в воде 360
— олеуме 360, 361
— серной кислоте 360
свойства 21 сл., 152, 235
сжижение 238 сл.
топочных газов 39, 40
транспортирование 22
хранение 22
чистый (из серы и триоксида се-
ры) 236, 237
Дисульфид железа 35, 38
горение 43 сл.
диссоциация 46 сл.
окисление огарком 58 сл.
Г-1 Q& QO
inivjMMVib им, uu
энергия активации диссоциации 47,
48
энтальпия окисления огарком 152
Катализаторы
ванадиевые см. Ванадиевые ката-
лизаторы
кислотно-каталитической очистки
газов 228, 229
КС 251
термического разложения серной
кислоты 264
Кислотооборот сушильно-абсорбцион-
ного узла 193 сл.
Кислоты отработанные 41 сл., 237 сл.
Клауса метод 33
Коагуляторы 233, 234
Коллектор перфорированный 319
Колчедан
горение, скорость 47 сл.
микроструктура (обожженного) 55
обжиг см. Обжиг колчедана
окисление огарком 58 сл., 235
примеси 49 сл., 140 сл.
ресурсы 35
рядовой 36
378
Колчедан
свойства 37, 38, 43 сл.
состав 38, 79
углистый 115, 116
флотационный 36 сл.
Конвейеры 77
Конверсия диоксида серы см. Окис-
ление диоксида серы
Константа
абсорбции г.аров воды Ко 200
скорости
взаимодействия диоксида серы и
серы 236, 237
горения серы 94, 97 сл.
диссоциации сульфида железа 46
47
окисления диоксида серы 166
равновесия
диссоциации серной кислоты 16,
17
окисления диоксида серы 151 сл.
Контактная масса см. Ванадиевые
катализаторы
Контактный (ые) аппарат(ы)
с вертикальным слоем катализато-
ра 177, 178
габариты 176, 353 сл.
гидравлическое сопротивление 186,
187, 191
диаграмма t — х 190
диаметр, расчет 186, 188, 189
загрузка катализатора 176 сл., 191,
192
кассетный 177, 178
.с кипящим слоем катализатора 177
конструкции 173 сл.
контактирования время 190, 191
материальный баланс 189
моделирование 186
нестационарного окисления 177
с отводом тепла серой 175, 177
— поддувом газа после I слоя 343
производительность 175, 176,
353 сл.
с промежуточным теплообменом
185
работы режим 168, 172, 173, 177,
188, 291
разогрев 184
распределение слоев по стадиям
132 сл.
теплопередача 175
устойчивость 185
характеристика техническая 176
Контактные отделения (узлы)
автоматизация 342 сл.
байпасирование газа 82, 83
с двойным контактированием 169,
170
контроля параметры 369, 370
с одинарным контактированием 169
Контактные отделения (узлы)
пуск 184
расчет 184 сл.
регулирования параметры 369, 370
тбп.юпотеои 292
эксплуатация 291 сл.
Концентрирование серной кислоты
комбинированное 306
в концентраторах капельного типа
302 сл.
— — с погружными горелками
304 сл.
расчет 301, 302
смешением 306 сл.
Котлы-утилизаторы 75, 76, 84, ПО,
111, 122, 123, 124, 244
Коррозия металлов 292, 362 сл.
Коэффициент (ы)
гидравлического сопротивления
186, 187
запаса катализатора 186
массопередачи 206, 214, 215, 217,
218
расширения температурного (кол-
чедана) 38
скорости абсорбции 198 сл., 270
теплообмена в печи КС 70
теплоотдачи теплообменников
180 сл.
теплопередачи
б кипящем слое 70, 71, 89
— контактном аппарате 175
расчет 190
в теплообменниках 180 сл.
— холодильниках 145, 146, 175,
179 сл., 190, 310 сл., 317
теплопроводности 20
формы частиц 68, 69
Массопередача 206, 214, 215, 217, 218
Материальный баланс
контактного аппарата 189
печи КС 81
промывного отделения 144, 145
реактора окисления колчедана
огарком 65
селена в производстве серной кис-
лоты 150
Моделирование контактных аппара-
тов 186
Мокрый катализ 137 сл.
Монотионовая кислота 227, 228
Мышьяк, содержание в обжиговом
газе 139, 140
Нагнетатели 77, 184
Насадки башен 362, 365
Насосы 318, 319
Нейтрализация сточных вод 234, 235
Нитрозилсерная кислота 279
379
Обжиг
колчедана см. Обжиг колчедана
серной руды 111, 112
сульфатов железа 112 сл.
Обжиг колчедана 43 сл.
автоматизация 340, 341
влияние примесей 49 сл.
выгорание серы, степень 89
интенсивность 10, 79, 80
с применением кислорода 49,
88 сл., 366, 367
огарок колчедана см. Огарок кол-
чедана
в печах КС 48, 49, 78
----КСЦВ 86 сл.
показатели оптимальные 78
расчет 57
регулирование 366, 367
тепловыделение 45
углистого 115
установки зарубежные 84, 85
утилизация тепла 122 сл.
с циркуляцией огарка 58 сл.
Обжиговые газы
запыленность 77, 79, 139
влажность
перед контактированием 192
— сушкой 195
диоксида серы содержание 63, 131,
176
мышьяка содержание 139, 140
огарка содержание 77
осушка 192 сл.
охлаждение 72 73 75 76
очистка 76
мокрая 138 сл.
моноэтаноламиновая 120, 121
от мышьяка 284 сл.
—• пыли 124 сл.
— селена 140, 150 сл.
степень 126
от фтора 284 сл.
промывка, автоматизация 341, 342
соотношение диоксида серы и кис-
лорода оптимальное 173
состав
перед контактированием 251
— промывкой 144
расчет 55 сл.
точка росы 182, 183
триоксида серы содержание 139
тумана содержание 139, 193
фтора содержание 141
Огарок колчедана
выход 89
концентрация в обжиговом газе 77
обогащение 65, 66
как окислитель 58 сл.
состав средний 79
циркуляция 61 сл., 87, 88
380
Окисление диоксида серы
под давлением 163, 165 сл., 177
зависимость от температуры 171
катализаторы см. Ванадиевые ка-
тализаторы
кинетика 157 сл.
механизм 157 сл.
нитрозой 270 сл.
равновесие 151, 152
скорость 161 сл., 166
стадии 157, 158
степень равновесная 132 сл., 152,
153, 164, 169 сл., 248, 361, 362
— под давлением 252
— по слоям катализатора 189
термодинамика 151 сл.
Олеум 13, 14
выпуск 243
высококонцентрированный, получе-
ние 241, 242
выход при абсорбции 206
получение, условия 195, 197
свойства 14 сл., 157 сл.
Орошающие устройства 319 с л.
«Орто-Флоу», принцип 62
Отработанная серная кислота
концентрирование 301 сл.
расщепление высокотемпературное
298 сл.
Отходящие газы
выброс в атмосферу суммарный
218
диоксида серы содержание 129,
131, 132
кислорода содержание 132
оксидов азота содержание 276
очистка
аммиачная жидкостная 219 сл.,
— сухая 224, 225
дпаммонийфосфатная 223
кислотно-каталитическая 227 сл.
показатели 230, 231
расчет 225 сл.
степень 219
сульфит-бисульфитиая 224
сульфитно-содовая 231, 232
от тумана серной кислоты 233 сл.
состав 218
ПДК 119, 351
Печь (и)
барабанная 111
с барботажным слоем 109
ваниы 107
кипящего слоя (КС)
высота слоя 71, 72
гидродинамика 66 сл.
группы (типы) 63
с жидким слоем 108
интенсивность 10, 69, 70, 79, 80
Печь (и)
кипящего слоя
конструкция 74, 75
материальный баланс 80, 81
охлаждающие элементы 71
производительность 69, 353 сл.
размеры 83, 84, 353 сл.
расчет 80 сл.
скорости газа критические 67 сл.
температурный режим 77
тепловой баланс 82, 83
теплообмен 70 сл.
типы (группы) 63
характеристика слоя 67 сл.
с циклоном возврата (КСВВ)
86 сл.
объем удельный 101
для сжигания
сероводорода 121, 122
серы жидкой 100 сл.
— твердой 107 сл.
СЭТА-ц-100 354, 355
для обжига '* ’ ’
колчедана 66 сл.
серной руды 111, 112
сульфата железа 117, 118
для окисления колчедана огарком
63 сл.
тепловое напряжение 101, 107
теплоиспользование 122 сл.
форсунки 105
форсуночные 100
циклонные 104 сл.
Пирит см. Дисульфид серы
Пирротин 35, 36, 45
Питатели 74
Плотность
диоксида серы 21
катализаторов ИК, СВД 163
кипящего слоя колчедана 67
колчедана 37, 38
марказита 36
олеума 19, 359
пирита 36, 38
пирротина 36
серной кислоты 14, 19, 358, 359
сероводорода 118
серы 28, 29
сульфата железа 181
Поверхностное натяжение
серной кислоты 359
серы жидкой 91
Производство серной кислоты
контактной см. Производство кон-
тактной кислоты
иитрозной см. Производство нит-
розиой кислоты
Производство контактной кислоты
автоматизация см. Автоматизация
производства
и водорода 262 сл.
Производство контактной кислоты
из газов автоклавной плавки 294,
295
__ — конпеитриоованных 62 сл.,
131 249 250 296
— — металлургических произ-
водств 279 сл.
под давлением 252 сл.
с двойным контактированием
130 сл., 147 сл., 151, 171 сл.,
247, 248, 288 сл.
капитальные вложения 131, 258
катализаторы см. Ванадиевые ката-
лизаторы
колчедана расход 248
— обжиг см. Обжиг колчедана
контактное отделение см. Контакт-
ное отделение
контроль 240, 366 сл.
короткая схема 250, 251
коррозия оборудования 325 сл.
металлоемкость 247, 252, 258
мощность единичная 6, 10, 246, 247
нестационарным способом 295, 296-
оборудование см. по видам аппа-
ратов: Абсорберы, Башни про-
мывные и т. д.
из отработанной кислоты 138,
298 сл.
пара выход 248, 259
приведенные затраты 258
производительность труда 131
промывное отделение см. Промыв-
ное отделение
противокоррозионные материалы
331
регулируемые параметры 366 сл.
себестоимость 131, 258, 278
из сериых руд 111, 112
— серы 129, 130, 248
совершенствование 245 сл.
из сульфатов 118
сушильно-абсорбционное отделение-
см. Сушильно-абсорбционное,
отделение
схемы см. Схемы производства
техника безопасности 350 сл.
утилизация тепла 122 сл., 259
энергозатраты 248, 258 сл., 293
энергоресурсы 244, 245
Производство нитрозной (башенной)
кислоты
денитрация нитрозы 273
интенсивность 273
капитальные вложения 278
с кислородом 277 сл.
кислотообразования механизм 270
кислоты концентрация 270, 274
концентрированной 276, 277
нитрозность кислоты 271, 272, 275
орошение башен
3811
Производство нитрозной (башенной)
кислоты
орошение башен
безнитрозное 275, 276
кратность 274
плотность 270, 274
поглощение оксидов азота 272, 273
работы режим 270, 273 сл.
расход азотной кислоты 274
схема семибашенная 268
улавливание оксидов азота 276
Промывное отделение
башни см. Башни промывные
контроля параметры 367 сл.
материальный баланс 144, 145
регулируемые параметры 367 сл.
режим работы 142 сл.
схема 147
тепловой баланс 147
Растворимость
диоксида селена в серной кислоте
140
— серы в воде, серной кислоте,
олеуме 21, 360, 361
мышьяка в серной кислоте 140
оксидов азота в серной кислоте 272
серы 28
.Расчет
абсорберов
моногидратного 214, 215
олеумного 209 сл.
бЗШНЦ О Т Д 'DO ЧП 0И 21м СТ
выхода огарка 57
— олеума при абсорбции 206 сл.
гидравлического сопротивления 191
давления паров равновесного 16,
17
загрузки катализатора 158, 159,
191, 192
количества промывной кислоты 143
контактных аппаратов 186 сл.
— узлов 184 сл.
концентрирования кислоты 301,
302, 306 сл.
котла-утилизатора 84
материальных балансов см. Мате-
риальный баланс
очистки отходящих газов 225 сл.
печи кипящего слоя 68 сл., 80 сл.
сжижения диоксида серы 238 сл.
состава обжиговых газов 55 сл.
степени использования сырья 57
температуры газа на выходе из пе-
чи 119
— кислоты в 1-й промывной башне
144
теплового баланса см. Тепловой ба-
ланс
теплообменников 133, 134, 190
Растворимость
холодильников пластинчатых 146,
313 сл.
энергии активации 47, 48
циклонов 125
Реактор окисления колчедана огар-
ком 62, 64
Ресурсы сырья 30 сл., 41, 42
Селен 51 сл.
извлечение из обжигового газа 150,
151
-----промывной кислоты 151, 153
содержание в колчедане, обжиго-
вом газе 140
шлам селеновый 150, 151, 153
Сепараторы 233
Сера
автоклавная 31. 32
аллотропные формы 90, 91
возгонка из колчедана 44 сл.
выплавка подземная 30, 31
из газов цветной металлургии 34
---- природных 32
испарение 93 сл.
месторождения 30, 31
из нефти 32 сл.
— пиритов 34, 35
ресурсы 30, 32
самородная 30 сл.
свойства 28 сл., 90 сл.
из серосодержащих газов 32, 34
сжигание см. Сжигание серы
ОС
wp 1 а ии
степень извлечения из сырья 31, 33
из угля 32 сл.
экстрагирование растворителями 32
Серная кислота
азеотропная смесь с водой 18
аккумуляторная 243
башенная (нитрозная) 267 сл.
вязкость 360
гидролизная 300
давление паров 357
диссоциация 16, 17
концентрирование 301 сл.
коррозионное воздействие на ста-
ли 292, 362 сл.
особо чистая 244
отработанная 297 сл.
пары
пересыщение 141
состав 16 сл.
применение 25, 26
производство см. Производство
серной кислоты
реактивная 243, 244
регенерация 297 сл.
свойства 14 сл., 24 сл., 256 сл.
себестоимость 131, 258, 278, 293,
294
382
Серная кислота
содержание оксидов азота 103
сорта 27
структура молекулярная 14
сушильная, концентрация 192, 193
термолиз 263
транспортирование 324, 325
улучшенная 243
хранение 323, 324
Сернистый ангидрид см. Диоксид
серы
Серный ангидрид см. Триоксид серы
Сероводородные газы 33
горения скорость 119
растворимость в воде 119
переработка 118 сл.
содержание H>S 121
«Сигрн» холодильник 148
Системы сернокислотные см. Схемы
производства
Скрубберы 148, 149, 232, 233, 288
Стабилизаторы триоксида серы 241
Сточные воды, нейтрализация 234,
235
Сульфат железа 41
нагрева дериватограмма 112, 113
температура разложения 44
Сульфит-бисульфит аммония 220, 221
Сушильно-абсорбционное отделение
344 сл.
автоматизация 344 сл.
башни см. Башни сушильные
кислотооборот 193, 195 сл.
температурный режим 194, 197
Схема (ы)
автоматизации
контактного узла 344, 346
печного агрегата 341
промывного отделения 342
сушильно-абсорбционного отде-
ления 345. 346
горения серы 97, 98
двойного контактирования, узлов
134 сл., 170
извлечения селена из промывной
кислоты 151, 153
кислотооборота между сушильной
и поглотительной башнями 196
контактного узла 134 сл., 169, 170,
290
концентрирования кислоты 303,
304
обжига сульфатов железа 117
окисления колчедана огарком 64
очистки отходящих газов, кислот-
но-каталитической 229
— сероводородных газов, моноэта-
ноламиновой 120
печного отделения 73, 74
получения высококонцентрирован-
ного олеума 241, 242
Схемы (ы)
------триоксида серы (100%-ного)
240
npoiP.RC’tCTRa см. Схемы произвол*
СТВ2 Серной КИСЛОТЫ
промывного (очистного) отделения
143
сжигания серы, двухступенчатого
103
сушильно-абсорбционного отделе-
ния 295
термического разложения отрабо-
танных кислот 298
Схемы производства серной кислоты
«Байер—Лурги» 12
большой единичной мощности 12
под давлением 253 сл.
с двойным контактированием 130.
251, 288
на газе горячем 135 сл.
— — цветной металлургии 282 сл
«Дорр-Оливер» 12
«Кеметик Интернационалы» 254 сл.
из колчедана 127 сл., 131 сл.
«Монсанто» 12
НИУИФ —ЛТИ 260 сл.
НИУИФ—МХТИ 256 сл.
с одинарным контактированием
131, 169, 284, 285
ПНР И, 12
из сероводородного газа 137
— серы 129, 130
«Томакомаи» 12
на холодном газе 133 сл.
«Южин—Кюльмаи» 253, 254
Сырье серосодержащее см. также по
видам сырья (колчедан, сера,
серосодержащие газы)
алунит 41
ангидрит 40
гипс 40
гидроны кислые 297 сл.
кислоты отработанные 41 сл.
колчеданы 35 сл.
структура потребления 11, 27
сульфат железа 40, 41
фосфогипс 40
Теллур 52 сл
Температура
абсорбции критическая (трпоксида
серы) 203
воспламенения железа соединений
45
горения колчедана 46, 47
кипения
диоксидов селена, теллура 52
олеума 15, 18, 357
селена 52
серной кислоты 14, 15, 18, 357
теллура 52
383-
Температура
кристаллизации
конденсации диоксида серы 21
кристаллизации
диоксида серы 21
олеума 15, 356, 357
серной кислоты 15, 274, 356, 357
трноксида серы (100%-ного) 241
плавления
диоксидов селена, теллура 52
железа соединений 44
колчедана 37
селена 52
серной кислоты 14, 356
серы 91
теллура 52
разложения
серы 91
сульфата железа 44
размягчения пирита 44
Тепловой баланс
башен контактной системы 309
печей КС 82, 83
промывного отделения 147
расчет 18
реактора и окислителя колчедана
огарком 65
‘Теплоемкость
диоксида серы 21
колчедана 37
олеума 18, 358
серной кислоты 14, 18, 358
серы 28, 29, 92
Теплообмен
в кипящем слоем 70, 71, 79
— контактном аппарате 175
расчет 190
в теплообменниках 180 сл.
— холодильниках 145, 146, 175,
179 сл., 190, 310 сл., 317
‘Теплообменники
байпасирование газов 282, 283
гидравлическое сопротивление 180,
181
защита от коррозии 135
конденсация кислоты 182, 183
контактных узлов 178 сл.
коррозия 181
мощность 133, 134
с перекрестным током газа 181
поверхность 134, 136, 176, 178, 179,
181, 190
расчет 133, 134, 190
с сегментными перегородками 179
скорость газа 179, 180
температура стенки 182, 183
теплопередачи коэффициент 145,
175, 179 сл., 190, 310 сл., 317
Теплопроводность серной кислоты 20,
359
Теплота
горения колчедана 45
испарения диоксида серы 21
образования
олеума 358
серной кислоты 14, 358
парообразования
серной кислоты 14
серы 29, 92
плавления
серной кислоты 14
сероводорода 118
растворения триоксида серы 23,
213, 215
сгорания сероводорода 118, 119
смешения серной кислоты и олеума
с водой 19
Триоксид серы
абсорбция 202 сл.
выброс в атмосферу 218
жидкий, получение 240, 241
образование при обжиге 54 сл.
свойства 22 сл.
содержание в обжиговом газе 139
стабилизаторы 241
температура кристаллизации
(100%-ного) 241
Туман серной кислоты
образование 141, 193, 202, 203,
232 сл.
улавливание 232 сл.
Турбокомпрессор ГТГ-12 256
Фильтры
гидравлическое сопротивление 234
механические 151, 194, 195, 234,
321 сл.
электрические см. Электрофильтры
Флюорит, влияние на обжиг колчеда-
на 50
Форсунки 105, 321
Фортеплообменник 292
Фосфогипс 40
Фраша метод 30, 32
Фтор, выделение при обжиге колче-
дана 50
Холодильник (и)
антегмитовые 312
с воздушным охлаждением 316 сл.
кожухотрубчатые 148, 311
оросительные 310, 311
пластинчатые 312, 313
пленочные 316
поверхность удельная 310
«Сигри» 148
спиральные 312
Циклоны 76, 124, 125, 232
3 84
Шлам селеновый 150, 151, 153
Электроподогреватели 293
Электропроводность
олеума 20, 21
серной кислоты 20, 21
серы 28
Электрофильтры
мокрые 141, 142, 148, 234
сухие 76, 125 сл.
Энергия активации
взаимодействия серы и триоксида
серы 237
Энергия активации
дегидратации сульфита железа 114
диссоциации дисульфида железа
47, 48
катализаторов 163, 165
колчедана углистого 116
окисления сульфата железа 116
разложения дитриоксида серы 237
расчет 47, 48
Энтальпия реакции
окисления диоксида серы 152
— пирита оксидом железа 58, 59
разложения полимеров серы 96
БОРИС ТИХОНОВИЧ ВАСИЛЬЕВ МАРИАННА ИВАНОВНА ОТВАГИНА ИБ № 1028 Сдано в набор 12,11.84. Подп. в печ.
ТЕХНОЛОГИЯ СЕРНОЙ КИСЛОТЫ 22.03.85. Т-07569. Формат бумаги бОХЭО’Аб- Бумага тип. № 1. Гарн. литературная. Печать высокая. Усл. печ. л. 24,0. Усл. кр.-отт. 24,0. Уч.-изд. л. 30,0. Тираж 6500 экз. Заказ № 584. Цена 1 р. 90 к. Изд. № 2010.
Редактор М. В. МИНИКС Художник Б. А. КОТЛЯР Художественный редактор Н. В. НОСОВ Технический редактор Ордена «Знак Почета» издательство «Химия». 107076, Москва. Стромынка, 21. Типография № 11 Союзполнграфпрома при Государственном комитете СССР по делам издательств, полиграфии и книжной торговли. Москва, 113105, Нагатинская ул., д. 1.
В. М. СКИТИНА
Корректор
Т. С. ВАСИНА