Text
химия и жизнь
Научно-популярный журнал Академии наук (TUP 1968
Ка обложке — фото И. Бека и
Л. Фомичева к статье «Стекло».
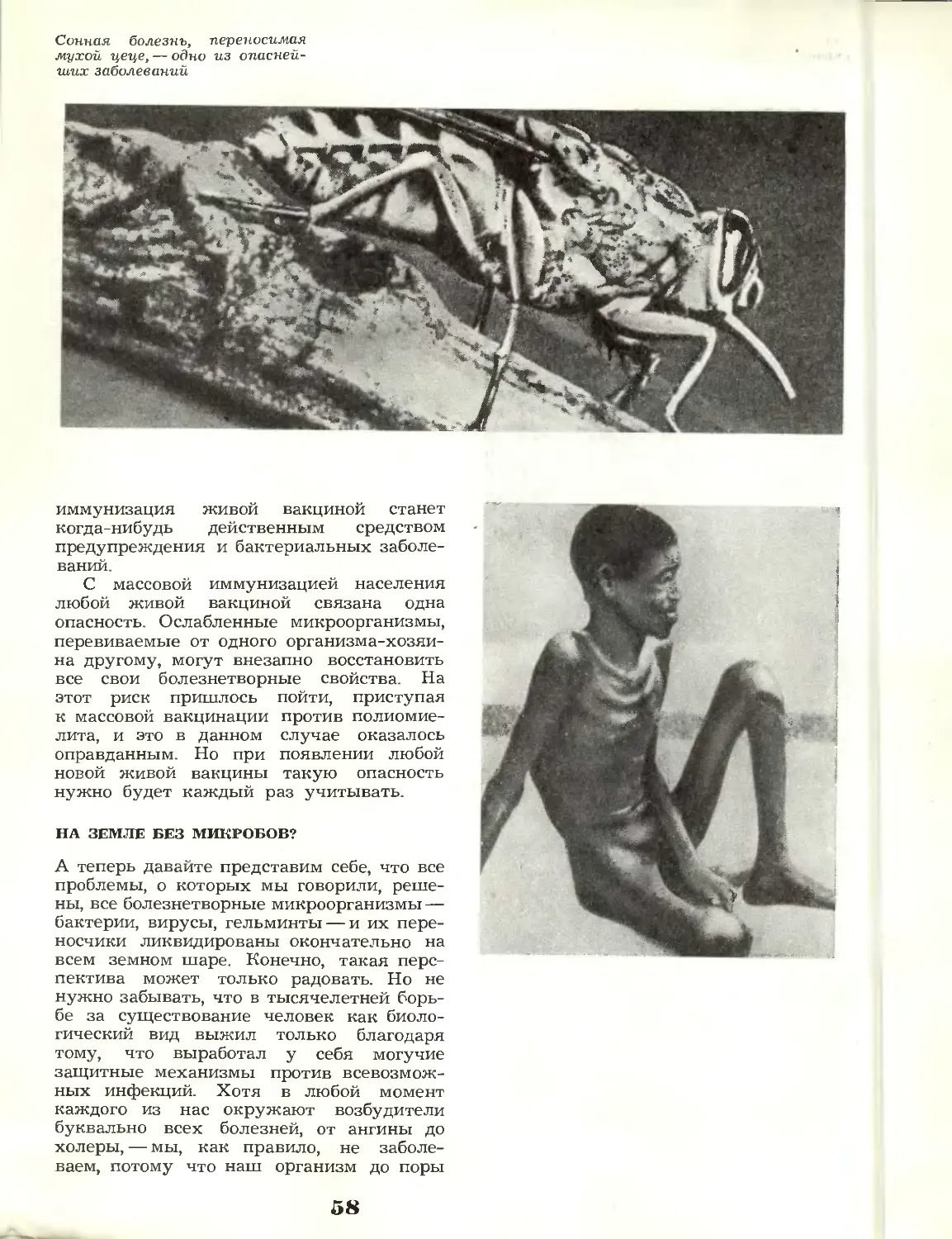
Инфекционные болезни
преследуют человека с незапамятных
времен. Эта египетская стела,
на которой изображен больной
с парализованной в результате
полиомиелита ногой, относится
к 18-й династии A580—1350 гг.
до н. э.). О путях искоренения
заразных болезней на Земле и о
связанных с этим научных и
социальных проблемах
рассказывают в этом номере журнала
американские ученые М. Кац и
X. Копроески и советский
эпидемиолог О. В. Бароян
ЕЖЕМЕСЯЧНЫЙ
НАУЧНО-
ПОПУЛЯРНЫЙ
ЖУРНАЛ
АКАДЕМИИ
НАУК СССР
ХИМИЯ И ЖИЗНЬ
До 4
АПРЕЛЬ 1968
ГОД ИЗДАНИЯ 4-й
Редакционная коллегия:
И. В. Петрянов-Соколов
(главный редактор),
IL Ф. Баденков,
Н. М. Жаворонков,
B. А. Каргин,
C. В. Кафтанов,
Н. К. Кочетков,
Л. И. Мазур,
Б. Д. Мельник,
B. И. Рабинович
(ответственный секретарь),
П. А. Ребиндер,
М. И. Рохлин
(зам. главного редактора),
C. С. Скороходов,
Б. И. Степанов,
A. С. Хохлов,
М. Б. Черненко
(зам. главного редактора),
Н. М. Эмануэль
Редакция:
Б. Г. Володин,
Д. А. Глейх,
B. Е. Жвирблис,
A. Д. Иорданский,
О. И. Коломийцева,
О. М. Либкин,
B. В. Станцо,
Т. А. Сулаева,
И. М. Чаплина,
B. К. Черникова
Художественный редактор
C. С. Верховский
Технический редактор
Э. С. Язловская
Корректоры:
Ю. И. Глазунова,
Е. И. Сорокина
При перепечатке ссылка на журнал
«Химия и жизнь» обязательна.
Адрес редакции:
Москва В-333,
Ленинский проспект, 61.
Телефоны:
135-52-29,
135-32-41,
135-63-91.
Подписано к печати 6/III-68. Т. 04619. Бумага
84 ^ 108'., . Печ. л. 6,0. Усл. печ. л. 10,08 ~ 1 вкл.
Уч.-изд. л. 11,27. Тираж 142 500. Заказ 2271. Цена 30 Коп.
Московская типография № 2 Главполиграфпрома
Комитета по печати при Совете Министров СССР,
Москва, проспект Мира, 105.
10
12
15
16
18
19
27
37
41
К 98-летию со дня рождения
Владимира Ильича Ленина
Два документа с двумя
комментариями
Первый комментарий: это
было в тысяча девятьсот
девятнадцатом
Второй комментарий: горючие
сланцы — значение и
перспективы
Что вы знаете и чего не знаете
о горючих сланцах
Экономика и производство
Что дешевле сжечь
Полезные советы и пояснения к ним
Материал тысячи
возможностей
О плащах «болонья»
Из писем в редакцию
Наши консультации
Проблемы и методы современной
науки
Разрезанные молекулы
Классика науки
Атомы, лучи, кванты
Погода и организм
Обыкновенное вещество
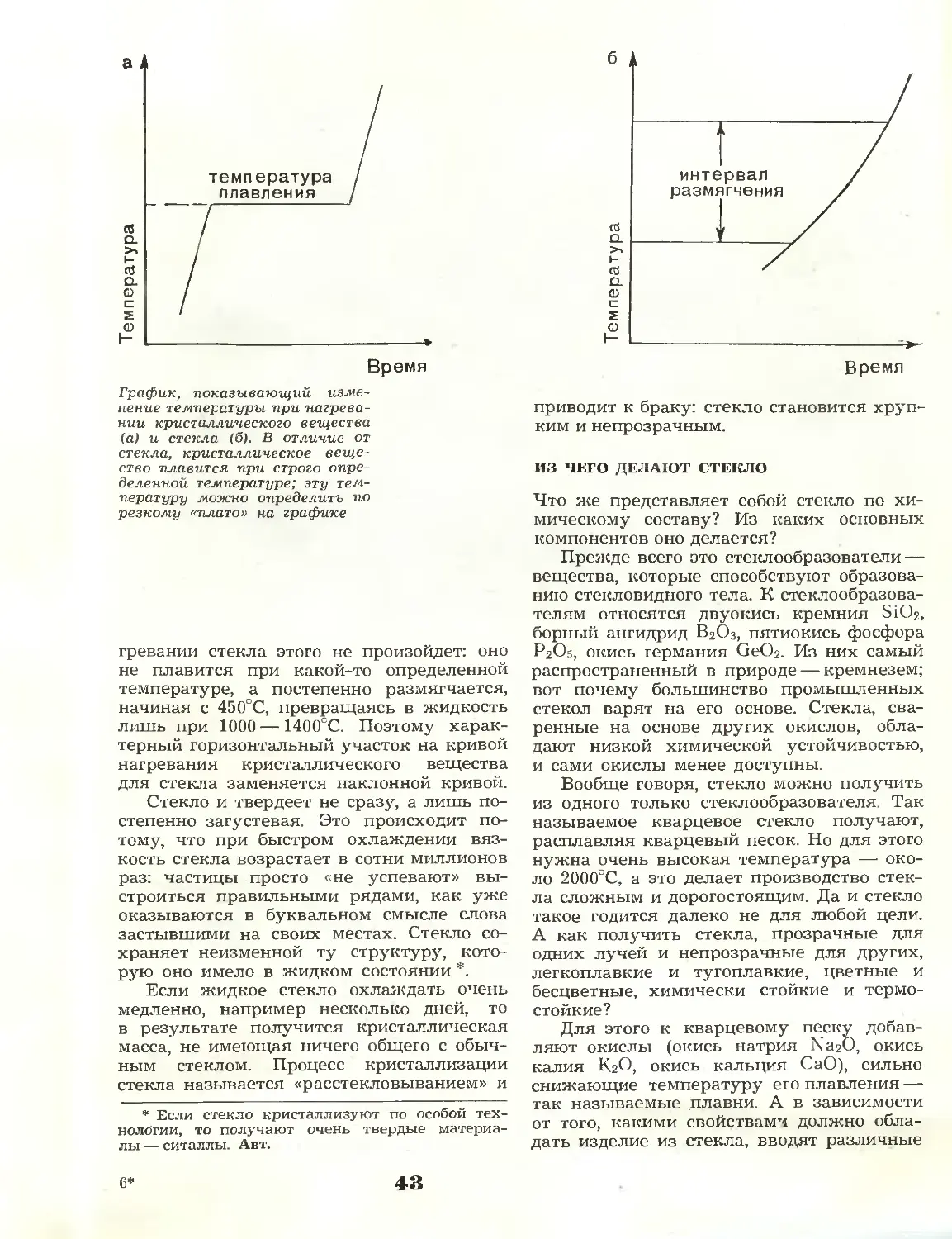
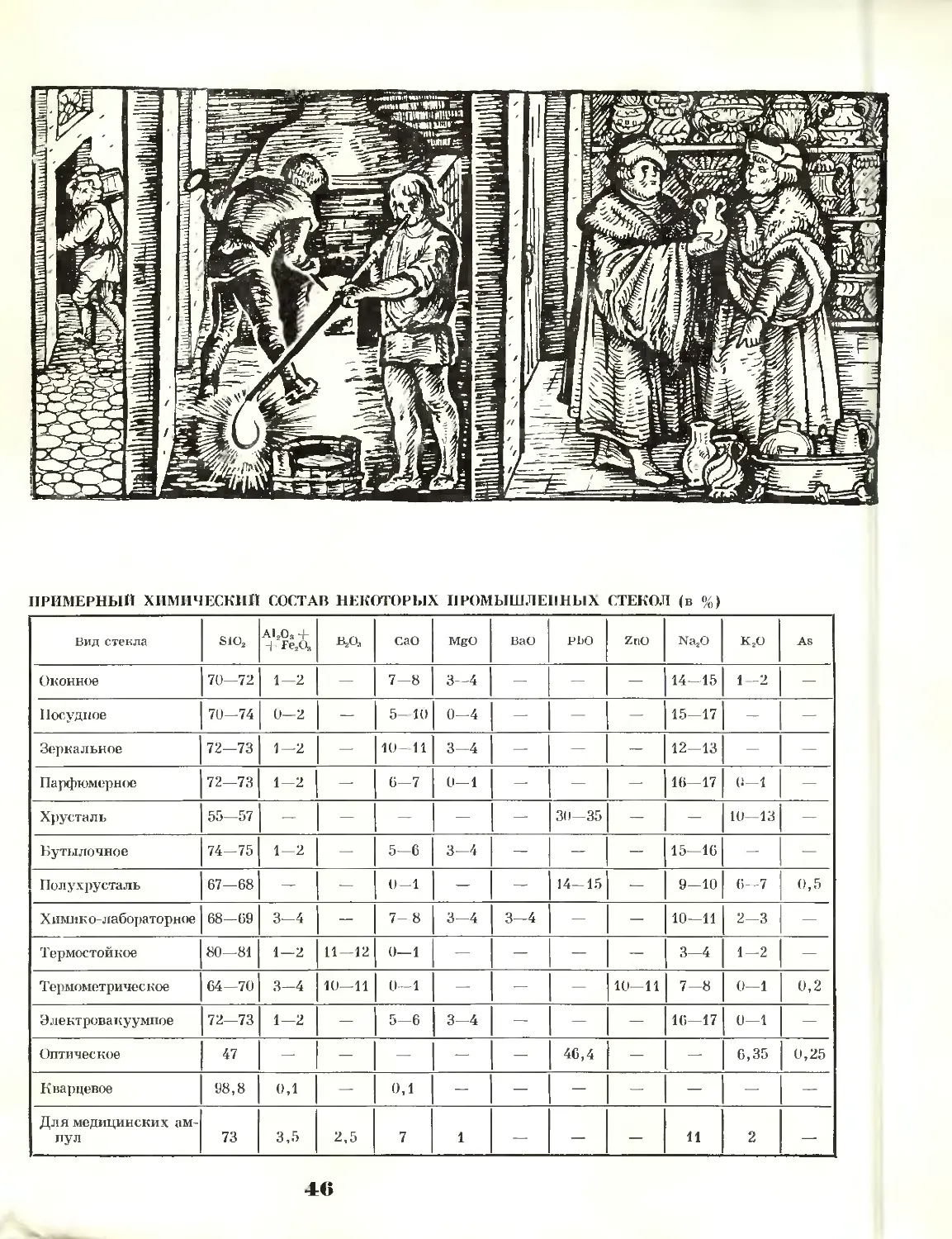
Стекло
В. А. Волков
В. С. Файнберг
С. Н. Блохина
В. А. Войтович
М. И. Ушакова
A. А. Баев
Л. И. Пономарев
М. Назиров
B. Б. Дмитриев,
Т. К. Трунова
53 Информация
54 Искоренение инфекций: точка
зрения биолога
59 Комментирует действительный
член АМН СССР О. В. Бароян
Наука — производству
61 Ни километра без резины —
Живые лаборатории
66 Волчье лыко
68 Новости отовсюду
Полезные советы и пояснения к ним
70 О забытых рецептах
Игра
72 Не будьте легковерными
Живые лаборатории
74 Яд лягушки кокой — самый
сильный небелковый яд
77 За ядовитыми лягушками в
джунгли Колумбии
Клуб Юный химик
80 Бандиты и старый учитель
81 Задачи на растворы
82 Секреты сплавов
86 Что такое Нобелевская премия
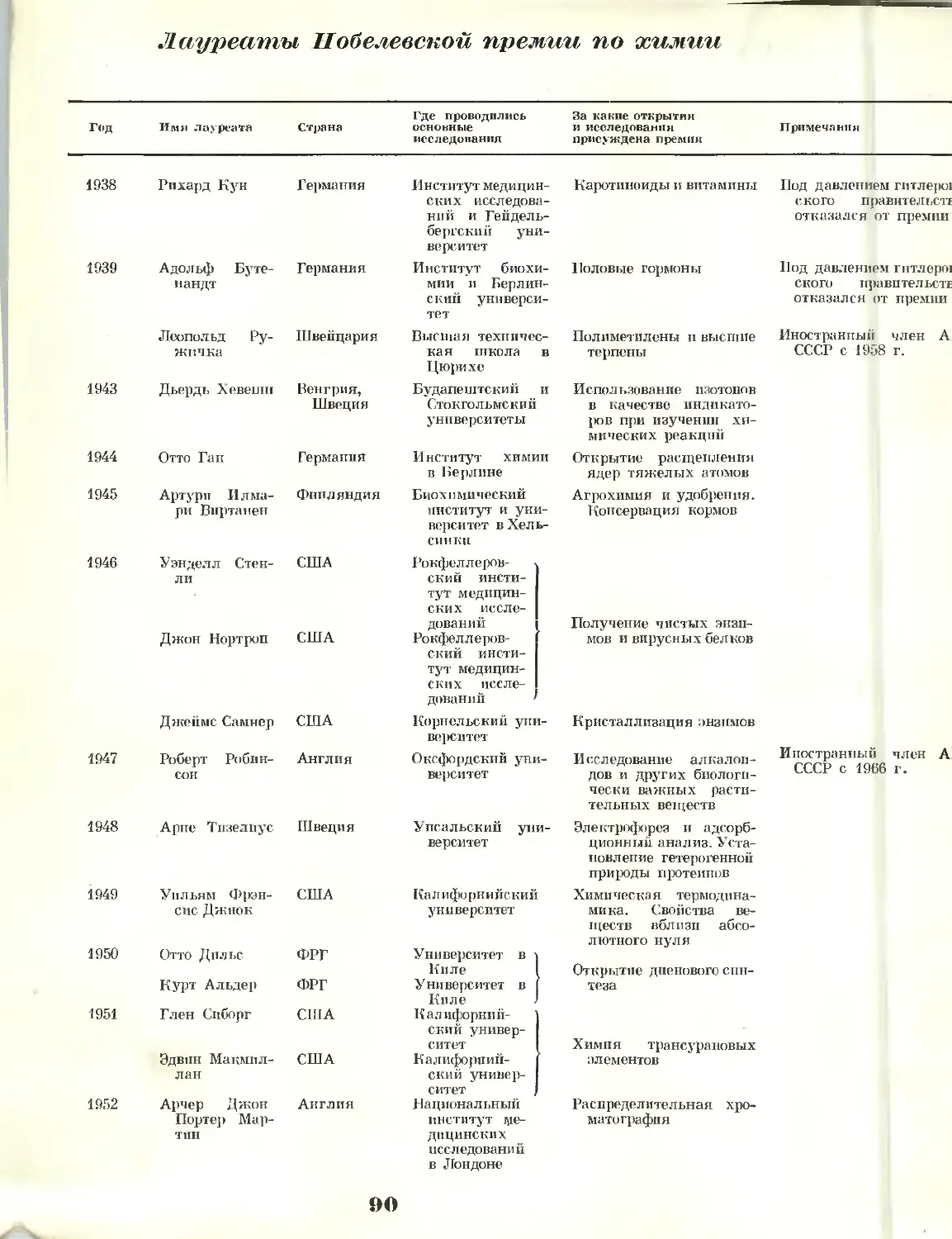
88 Лауреаты Нобелевской премии
по химии
93 Французский — для химиков— Т. Н. Комровская
М. Кац,
X. Копровски
Л. Е. Виницкий
М. Мазуренко
П. П. Дятлов
Г. Гур
И. Л. Кнунянц,
Н. А. Лошадкин
М Лзтам
Д. В. Пальчиков
О. Коломийцева
К 98-ЛЕТИЮ СО ДНЯ РОЖДЕНИЯ
ВЛАДИМИРА ИЛЬИЧА ЛЕНИНА
Два
документа
с двумя
комментариями
Первый комментарий:
это было
в тысяча девятьсот
девятнадцатом
Владимир Ильич Ленин всегда проявлял
глубокий интерес к химической науке и
промышленности. В библиотеке Ленина в
Кремле можно видеть труды Ломоносова,
Ферсмана, Прянишникова, Чугаева. С
именем Ленина связаны становление первых
советских научно-исследовательских
химических институтов и первые шаги
советской химической промышленности, в том
числе организация химической
переработки горючих сланцев.
В декабре 1918 года при Высшем Совете
Народного Хозяйства был создан Главный
сланцевый комитет во главе с
выдающимся русским ученым Иваном Михайловичем
Губкиным. Уже весной 1919 года в
Поволжье, в районы залегания сланцев
отправились геологи, а в июле — августе того же
года выехали Губкин и другие
руководители комитета, чтобы помочь экспедиции.
Ленина эти работы очень интересовали:
в годы гражданской войны Советская
власть, отрезанная в течение длительного
времени от донецкого угля и бакинской
нефти, остро нуждалась в топливе.
В июле 1919 года Владимир Ильич
обратился к руководителю
научно-технического отдела ВСНХ Н. П. Горбунову с
просьбой: «Выяснить, что сделано по
организации добычи горючего из сланцев Сыз-
райского уезда и казанской нефти». В ответ
на этот запрос Ленина и была написана
докладная записка, хранящаяся ныне в
Центральном государственном архиве
народного хозяйства СССР.
В своей записке И. М. Губкин изложил
основные результаты разведочных работ,
а также свои соображения по дальнейшему
развитию сланцевого дела. Владимир
Ильич отнесся к этим соображениям с
большим вниманием и выполнил просьбу
Губкина о признании рабочих и служащих
Главного сланцевого комитета
работающими на оборону: вскоре он подписал декрет,
по которому рабочие и служащие Глав-
сланца, независимо от возраста, считались
призванными на военную службу с
оставлением на местах своей работы.
В октябре 1919 года в химической
лаборатории Главсланца в гор. Осташкове были
получены из сланца первые образцы
керосина и других продуктов. Ленин пригласил
к себе Губкина, осмотрел образцы и долго
беседовал с ученым. В конце беседы,—
вспоминал Губкин, — Владимир Ильич
сказал: «Вот вам мой телефон, вот
телефон секретаря. Когда нужна будет помощь,
обращайтесь ко мне непосредственно...».
1*
3
ПРЕДСЕДАТЕЛЮ СОВЕТА НАРОДНЫХ КОМИССАРОВ
ТОВ. ВЛАДИМИРУ ИЛЬИЧУ ЛЕНИНУ.
Во исполнение Вашего поручения, переданного в
Главный Сланцевый Комитет Заведывающим Научно-Техническим
Отделом тов.Н.П.Горбуновым, сообщаю нижеследующее.-
Горючие сланцы Волжского района расположены в двух
местах: в районе гор. Симбирска и в районе гор, Сызрани.
О их существовании было давно известно и в науке и у мест-
ных людей. Но практического значения в промышленной аизни
страны они до сих пор еще не получили. Тля*™ »«—.. -
го уеада я пока не касаюсь, так как в запросе, переданном
мяе от заведываящего Н.Т.О. тов. Н.П.ГОРБУНОВА был поставлен
только вопрос о Волжских горючих сланцах. Вели бы явилась
необходимость осветить я эту сторону деятельности Главсланца,
в его распоряжении имеется богатый материал и по разработке
сапропелем.-
Председатель Коллегии -^
Главного Сланцевого Комитета sft <у*/я^--, •
В конце 1919 года на Сызранском ме- ванная весной 1921 года в Химический
сторождении близ села Кашпир заложили институт им. Л. Я. Карпова. Здесь, в част-
первый сланцевый рудник. К разработке ности, удалось получить из сланцев ихти-
способов получения из сланцев различных ол, не уступающий лучшим заграничным
ценных продуктов была привлечена Цент- образцам. Большую работу по исследова-
ральная химическая лаборатория ВСНХ, нию химического состава сланцев разных
возглавляемая А. Н. Бахом и преобразо- месторождений и продуктов их переработ-
4
UNITED NATIONS ЩШ NATIONS UNIES
AIDE-MEMOIRE
UNITED NATIONS SYMPOSIUM ON THE
DEVELOPMENT AND UTILIZATION OF OIL SHALE RESOURCES
to be held in Tallinn, USSR,
26 August to 9 September 1968.
Organized by the United Nations and the
Government of the Union of Soviet Socialist Republics
ПАМЯТНАЯ ЗАПИСКА
СИМПОЗИУМ ООН ПО РАЗРАБОТКЕ И ИСПОЛЬЗОВАНИЮ
ГОРЮЧИХ СЛАНЦЕВ
состоится в Таллине, СССР,
с 26 августа по 9 сентября 1968 года.
Симпозиум проводит Организация Объединенных Наций
и Правительство Союза Советских Социалистических Республик
ки проводил Н. Д. Зелинский и его
сотрудники.
16 октября 1922 года В. И. Ленин писал
в Президиум ВСНХ: «Тов. Красин прислал
мне письмо, в котором сообщает о
крупнейших успехах группы инженеров во
главе с тов. Губкиным, которая с
упорством, приближающимся к героическому, и
при ничтожной поддержке со стороны
государственных органов, из ничего развила
не только обстоятельное научное
обследование горючих сланцев и сапропеля, но и
научилась практически приготовлять из
этих ископаемых различные полезные про-
5
дукты, как-то: ихтиол, черный лак,
различные мыла, парафины, сернокислый
аммоний и т. д. Ввиду того что эти работы,
по свидетельству т. Красина, являются
прочной основой промышленности^ которая
через десяток, другой лет будет давать
России сотни миллионов, я предлагаю:
1. Немедленно обеспечить в финансовом
отношении дальнейшее развитие этих
работ. 2. Устранить и впредь устранять
всяческие препятствия, тормозящие их, и
3. Наградить указанную группу инженеров
Трудовым орденом Красного Знамени и
крупной денежной суммой».
ЧЕМ ЗАМЕНИТЬ НЕФТЬ?
Ни одно полезное ископаемое не может
сравниться по своему значению с
горючими ископаемыми — важнейшим
источником энергии и ценнейшим химическим
сырьем. Они дают нашей стране свыше
96% потребляемой энергии. Из них
получают подавляющее большинство
продуктов органического синтеза, полимеров,
красителей, ядохимикатов, сотни других
нужных веществ.
Важнейшее место среди горючих
ископаемых сейчас занимает нефть. Стоимость
нефти, выкачиваемой за год из недр земли,
в полтора раза превышает стоимость
годовой добычи всех остальных видов
минерального сырья. Каждые 10—15 лет
потребление ее удваивается. Но богатства
земных недр не безграничны. Например,
США обеспечены разведанными запасами
нефти всего на 9 лет. Все глубже уходят
буры в поисках черного золота и все реже
его находят.
По некоторым расчетам, уже в
ближайшие годы человечеству придется садиться
на голодный нефтяной паек, а к 2050 году
нефтепродукты практически исчезнут из
топливной диеты. Поэтому ученые уже
сейчас ищут, чем можно заменить нефть.
А можно ли вообще ее заменить?
Каменный уголь, как это общепризнано,
является хорошим энергетическим топливом, но
8 февраля 1923 года Президиум ВЦИК
утвердил постановление Совнаркома о
награждении работников сланцевой
промышленности орденом Трудового Красного
Знамени.
В своих воспоминаниях академик
И. М. Губкин отмечал: «Раз
заинтересовавшись топливом, Ленин уже не бросал этой
проблемы, а постоянно обращался к ней,
искал решения вопроса, направлял работу
ученых...»
В. А. ВОЛКОВ
он малопригоден для получения
углеводородного сырья. В этой связи все большее
внимание научных и промышленных
кругов привлекают горючие сланцы.
Свидетельство тому — международный
симпозиум ООН по добыче и переработке
горючих сланцев, который будет проведен в
этом году в столице Советской Эстонии.
Здесь соберутся химики, технологи,
энергетики, горняки, экономисты — сотни
ученых из десятков стран.
Горючие сланцы — одно из величайших
сокровищ земных недр. Они встречаются
на всех континентах. Мировые ресурсы
органического углерода,
аккумулированного в сланцах, превышают запасы всех
других видов топлива, вместе взятых.
ЧТО ТАКОЕ ГОРЮЧИЕ СЛАНЦЫ?
Ответить на этот вопрос не очень легко.
Сланцы разных месторождений имеют
разную геологическую судьбу, они не
похожи друг на друга ни внешним видом, ни
химическим составом. Сланцы бывают
желтые, зеленые, красноватые,
коричневые, черные. Одни из них расслаиваются
на тонкие легкие листочки, подобные
бумаге, другие представляют собой
монолитную плотную породу.
Известны месторождения, где залежи
сланца образуют сплошные километровые
толщи; в других же местах мощность пла-
Второй комментарий:
горючие сланцы—
значение и перспективы
в
стов измеряется всего несколькими
сантиметрами, а то и миллиметрами.
Горючие сланцы образовались из
донных отложений древних водоемов.
Иногда морское дно, поднявшись,
становилось сушей, а затем вновь опускалось.
Пласты сланца чередовались с пластами
угля. Такие месторождения, похожие на
слоеные пироги, встречаются в Китае,
Югославии, Испании, Южной Африке.
Жизнь зародилась и развилась сначала
в водоемах и лишь много позже шагнула
на сушу. Поэтому горючие сланцы в общем
старше своих более известных братьев —
каменных углей. Есть сланцы, которые
насчитывают полмиллиарда лет — это самые
древние горючие ископаемые на земном
шаре.
Различие в происхождении углей и
сланцев проявляется в различии их
состава. Прежде всего для сланцев
характерно преобладание минеральной массы
над органической. Минеральная масса
состоит в основном из карбонатов и
алюмосиликатов. Обнаруживаются следы
десятков других элементов, в том числе
некоторых редких. Многие сланцы содержат в
заметных количествах уран. Из сланцевой
золы можно получить разнообразные
полезные продукты — цемент, шлаковату,
известь, удобрения.
В неорганическую матрицу сланца
вкраплены крохотные, в несколько
микронов, лепешки органического
вещества — керогена. Несмотря на то, что его
содержится очень мало — настолько мало.
что многие сланцы даже не горят, хоть и
называются горючими, — именно
органическое вещество составляет главную
ценность этого ископаемого.
Органическое вещество сланца состоит
из гигантских полимерных молекул,
строение которых достоверно не установлено.
Молекула керогена слишком велика и
слишком сложна, чтобы ее можно было
изучать непосредственно. Поэтому сделаны
попытки определить природу керогена
косвенным путем: молекулу разбивают на
осколки, по строению которых судят о
структуре исходного вещества. При
перегонке— нагревании без доступа воздуха —
молекулы керогена расщепляются с
образованием более простых молекул газа и
смолы (в этом и заключается сущность
переработки сланца). Основная масса
смолы большинства сланцев состоит из
циклических соединений. Отсюда можно было
бы заключить, что кероген сланца, так же
как и органическое вещество углей,
слагается из ароматических колец, связанных
между собой в различных комбинациях.
Другой способ расшифровки строения
сложных соединений — их осторожное
окисление. Известно, что ароматические
соединения при окислении в определенных
условиях всегда образуют бензолкарбоно-
вые кислоты различного строения.
Например, из нафталина получается фталевая
кислота:
окисление
нафталин
:—СООН
я >— СООН
фталевая кислота
Естественно, что образования бензол-
карбоновых кислот следовало ожидать и
при окислении керогена. Но тут ученых
ожидал сюрприз: в продуктах окисления
органического вещества сланца — в
отличие от углей — бензолкарбоновые кислоты
практически отсутствуют. Это
свидетельствует в пользу линейного строения
молекул керогена. А появление циклических
структур в продуктах разложения сланца
объясняется их синтезом в процессе
перегонки.
Кероген сланцев отличается от
органического вещества углей не только
строением, но и химическим составом. Особенно
важна разница в содержании водорода.
В расчете на органическое вещество уголь
содержит 3—5% водорода, сланец —
9—12%, нефть—11—13% (остальное
приходится главным образом на углерод и
частично на кислород, серу и азот).
Следовательно, кероген по элементарному составу
ближе к жидким топливам, чем к твердым.
И действительно, при сухой перегонке до
70% керогена переходит в жидкий
продукт— смолу. Остальная часть
превращается в газ, воду и твердый остаток.
Сланцевая смола и нефть похожи обычно,
как сестры-близнецы, хотя нередки и
исключения. При разложении углей в смолу
превращается в среднем всего лишь
20—30% их органического вещества, а
многие угли, бедные водородом (их
называют «тощими»), вовсе не дают жидких
продуктов.
Таким образом, сланец — не совсем
обычное горючее ископаемое. По
физическим свойствам, по методам добычи и пер-
7
вичной переработки, это, несомненно,
твердое топливо. По химическому составу
органического вещества, по целям
переработки и характеру продукции сланец стоит
в одном ряду с нефтью.
Нельзя представлять себе сланец в виде
каменной губки, пропитанной смолой или
нефтью. Его часами можно держать в
кипящем бензоле или ацетоне, и в раствор
не перейдет ни капли смолы по той
простой причине, что она не присутствует в
сланце, а образуется при его разложении.
Выход смолы из лучших сланцев не
превышает 16—20%, а в большинстве
случаев 5—13%, что соответствует
содержанию в полезном ископаемом 10—20%
органического вещества. При переработке
эстонских сланцев, принадлежащих к
лучшим в мире, 100 вагонов подают сланец на
завод и только 20 возвращаются с товарной
продукцией. Перевозить на дальние
расстояния топливо с таким количеством
балласта невыгодно. Его нужно
перерабатывать на месте добычи, но даже это не
всегда оправдано: нужно добыть,
раздробить, нагреть до 500е С 1000 кг сланца,
уловить продукты разложения, охладить и
вывезти в отвал 750 кг бесполезного
остатка— и все это для того, чтобы получить
лишь 180 кг смолы!
Не меньшие трудности возникают и при
сжигании сланца. Электростанция одной и
той же мощности потребляет его в три раза
больше, чем угля. Количество золы при
этом возрастает в десятки раз, что
осложняет ее улавливание и удаление,
увеличивает износ труб, котлов и засорение
воздушного бассейна.
Использование горючих сланцев
требует изобретательности, упорного поиска,
талантливой инженерной мысли. *
СОВЕТСКИЕ СЛАНЦЫ
В Советском Союзе свыше 100
месторождений горючих сланцев — в Прибалтике,
на Украине, в Поволжье, Казахстане и
других районах.
Отечественное сланцевое дело уходит
корнями в далекое прошлое. Еще в 1697 г.
Петр I издает указ об отправке для
исследования в Голландию образцов ухтинского
горючего сланца (из бассейна Печоры).
В 1792 г. в «Трудах Вольного
Экономического общества» петербургские ученые
А. И. Энгельгардт и И. Г. Георги впервые
описали эстонские сланцы — «буроватую
легкую слоистую землю»: «Горит она сама
с желтым пламенем и густым дымом и
огонь тогда можно содержать одними
земляными глыбами, что ночью пастухи и
делают. Сей огонь дает много жара, но
противный имеет запах»...
В 1916 г., когда Петроград оказался
отрезанным от английского угля, была
предпринята попытка использовать
прибалтийские сланцы для получения
светильного газа. Из Эстонии в Петроград
доставили 22 вагона сланца. 50 лет спустя в
честь этого события, которое считается
началом отечественной сланцевой
промышленности, в Кохтла-Ярве был установлен
памятник — вагонетка, с помощью которой
были добыты первые куски сланца.
Особенно большой размах получили
исследования сланцев после установления
Советской власти. Работа ученых в этой
области получила поддержку и высокую
оценку В. И. Ленина. Как вспоминал
впоследствии академик И. М. Губкин,
«развитию сланцевого дела в Советской стране
В. И. Ленин помогал вплоть до своей
смерти и защищал его всею силою своего
авторитета».
Теперь в СССР на нескольких мощных
предприятиях, из которых крупнейшим
является комбинат им. В. И. Ленина в
Кохтла-Ярве, ежегодно перерабатывают
миллионы тонн сланца. Из него получают газ»
моторное и котельное топливо, шпалопро-
питочное масло, дорожный битум,
электродный кокс, серу, гипосульфит,
ядохимикаты, бензол, растворители, лаки,
полимерные клеи, синтетические дубители,
лекарственные препараты,
стройматериалы и многие другие продукты.
Наибольшее значение имеют сланцы
Прибалтийского бассейна — на территории
ЭССР и Ленинградской области. Они
отличаются высоким качеством, расположены
близко к поверхности, в густонаселенном
промышленном районе, удаленном на
тысячи километров от источников угля,
нефти и газа, и играют важную роль в
снабжении Северо-Запада страны топливом и
химическим сырьем.
Прибалтийский сланец —
светло-коричневый слоистый камень, дающий при
перегонке 18—20% смолы. В отличие от нефти
и от смол большинства других сланцев она
состоит в основной своей массе не из
углеводородов, а из кислородсодержащих
соединений — фенолов, кетонов, сложных
эфиров, строение которых еще далеко не
8
выяснено. Эти особенности состава смолы
делают ее уникальным химическим
сырьем, но они же создают трудности для
исследователей и технологов, так как
изучение и переработка такого продукта не
может проводиться по схемам,
разработанным для нефти и других сланцевых смол.
Поиски наилучших путей использования
смолы не прекращаются и уже дали
значительные результаты.
Крупных успехов добились советские
инженеры и в области энергетического
использования сланца. Его потребляют
теперь многие теплоэлектростанции и, в
частности, известный всей стране
энергетический гигант — Прибалтийская ГРЭС
мощностью 600 тыс. квт.
По размаху исследований, по
масштабам добычи, переработки и использования
горючих сланцев Советский Союз далеко
опередил другие государства, и не
удивительно, что именно наша страна выбрана
местом проведения международного
симпозиума, который, будем надеяться, станет
важной эпохой в изучении этого топлива
будущего.
Кандидат технических наук
В. С. ФАЙНБЕРГ
Что вы знаете и чего не знаете
о горючих сланцах
Щ Мировые запасы органического
углерода, заключенного в
различных видах топлива, составляют: в
нефти — 10 и т, в угле — 1013 т,
в сланце — 1017 т.
■ Месторождения горючих
сланцев известны в Австралии,
Австрии, Англии, Аргентине,
Афганистане, Бирме, Болгарии, Бразилии,
Греции, Израиле, Индии,
Иордании, Ирландии, Испании, Италии,
Йемене, Канаде, КНР, Конго
(Киншаса), Коста-Рике, Ливане, Мали,
Мальгашской республике,
Марокко, Никарагуа, Новой Зеландии,
Норвегии, ОАР, Панаме, Перу,
Польше, Сальвадоре, Сирии,
Сомали, СССР, США, Таиланде,
Турции, Уругвае, Франции, ФРГ,
Чехословакии, Чили, Швейцарии,
Швеции, Эквадоре, ЮАР и
Югославии.
■ В Шотландии, в местечке
Торбан Хилл, были найдены когда-то
сланцы с выходом смолы 55%.
Месторождение быстро
истощилось, но термин «торбаниты»
закрепился за очень богатыми
сланцами, дающими выход смолы
свыше 30%. Месторождения торбани-
тов встречаются в Австралии,
Аляске, Южной Африке. Запасы их
относительно невелики.
■ Первый исторический
документ, имеющий отношение к слан-
цепереработке, — английский
патент, взятый в 1694 г.
Промышленная переработка сланца началась
во Франции в 1838 г. — раньше,
чем переработка нефти. Само
слово petroleum («каменное масло»)
означало когда-то сланцевую
смолу и лишь впоследствии так стали
называть нефть.
■ Подземная газификация и
перегонка твердых топлив, идею
которой выдвинули еще Менделеев
и Рамзай, десятки лет привлекает
внимание ученых разных стран.
Горючие сланцы подвергались
подземной переработке в
промышленных масштабах в Швеции
с 1942 по 1960 г.
■ В США разработан метод
подземной перегонки сланцев с
помощью ядерного взрыва, который
должен образовать подземную
реторту высотой 300 м и
диаметром 120 м, вмещающую свыше
10 млн. т раздробленного сланца.
Из такой реторты можно получить
700 тыс. т смолы.
Щ Слово «ихтиол» означает
«рыбье масло». Однако эта целебная
мазь получается не из рыб, а при
перегонке некоторых видов
горючих сланцев, богатых серой.
Месторождений таких сланцев
известно немного: в СССР (Поволжье)
и в Австрии (Тироль).
■ Только одно сланцевое
месторождение Грин Ривер в США
содержит в три раза больше
потенциального жидкого топлива, чем
все разведанные нефтяные
месторождения мира, и в 39 раз
больше, чем нефтяные месторождения
США. При потреблении нефти на
предполагаемом уровне 1980 г.
сланцы Грин Ривер обеспечат
США жидким топливом в течение
368 лет. В пересчете на газ
потенциальные запасы этого
бассейна составляют 170 трилл. куб. м.,
что в 8 раз больше мировых
запасов газа и в 21 раз больше запасов
США.
Щ Прибалтийский горючий сланец,
имеющий мировую известность,
называется иногда «кукерсит» —
по имени местечка Кукерс (ныне
Кукрузе), где пласты сланца
выходят на поверхность. Теперь
Кукрузе является составной частью
города Кохтла-Ярве — центра
Эстонского сланцевого бассейна.
Кукерсит имеет возраст около
500 млн. лет. Ниже него залегают
пласты так называемого диктионе-
мового сланца, который старше
кукерсита на несколько десятков
миллионов лет — это,
по-видимому, самое древнее горючее
ископаемое на Земле.
Щ В Советском Союзе из горючих
сланцев получают свыше 40 видов
различных продуктов.
£ Химия и Жизнь, № 4
9
ЭКОНОМИКА
И ПРОИЗВОДСТВО
Что дешевле сжечь
Вся деятельность человечества,
все виды производства
неразрывно связаны с процессами
превращения энергии — из
химической в тепловую, из
тепловой в механическую, из
электрической в тепловую или
механическую и т. д. Какой же
из существующих источников
энергии наиболее выгодный? На
этот вопрос ответить
невозможно. Если бы такой источник
вдруг обнаружился, то,
очевидно, не было бы смысла
применять все остальные. Можно
говорить лишь о том, какой из
источников энергии выгодно
(или возможно) применять в
данном конкретном случае. А в
результате применения
различных источников энергии должен
быть достигнут максимальный
суммарный
народнохозяйственный эффект. Говоря строгим
языком, необходимо
оптимальное соотношение между
трудовыми затратами на извлечение
энергии и ее потребление.
ЧТО УЧИТЫВАТЬ?
Источников энергии много.
Чтобы сравнить их между собой,
нужно прежде всего знать, как,
по каким параметрам
сравнивать. В самом деле, как
сравнить киловатт-час
электроэнергии с литром бензина? Имеет ли
смысл сопоставлять стоимость
кубометра газа и тонны угля?
И тем не менее сопоставимый
показатель существует. Это
стоимость работы, на которую
затрачена энергия. Правда, в
зависимости от вида работы ее
стоимость будет выражаться в
различных единицах. Скажем,
Экономист С. Н. БЛОХИНА
если речь идет о механической
работе, то она будет выражаться
в рублях за киловатт-час, если
тепловой — то в рублях за
килокалорию. Но сложность не
в единицах — есть переводные
коэффициенты от одной
единицы к другой. Главная сложность
в том, что у каждого способа
превращения энергии — свой
коэффициент полезного
действия. Например, у электромотора,
преобразующего электрическую
энергию в механическую, КПД
приближается к 0,9, а КПД
бензинового двигателя обычно не
превышает 0,3. И это
необходимо учитывать.
КПД преобразования — не
единственный критерий
экономической целесообразности
применения того или иного
источника энергии. Весьма важна и
стоимость самого
преобразователя энергии, особенно когда он
дорог (для примера назовем
двигатель внутреннего
сгорания). Нельзя забывать и о
воздействии силовой установки на
окружающую среду и людей.
Это относится не только к
ядерным источникам энергии, но и
к источникам, использующим
такие «классические» топлива,
как уголь, сланцы, нефтяные
продукты. Ведь при сжигании
этих веществ образуется
большое количество токсических
веществ, загрязняющих
атмосферу.
В том случае, когда речь
идет о транспортной установке,
необходимо, кроме того,
учитывать вес запаса топлива и
самого двигателя.
Нужно помнить и о
стоимости транспортировки топлива
(или другого вида энергии) к
месту потребления. Во многих
случаях она автоматически
учитывается ценами на топливо и
энергию (в разных районах —
разные цены). И, наконец,
приходится учитывать и расходы,
связанные с ремонтом
оборудования.
ПОЧЕМ КИЛОКАЛОРИЯ?
Почему-то бытует такое
представление, будто самый
дешевый вид энергии — зто
электричество. Так ли это? Обратимся к
цифрам.
Давайте сравним, сколько
стоит 1 ккал тепла, полученная
из электричества и из разных
видов топлива (с учетом тех
факторов, о которых говорилось
в предыдущей главе).
Килокалория тепла, полученная из
электрической энергии, обходится
приблизительно в 0,0025
копейки, а полученная при сжигании
бензина — всего в 0,00069
копейки, в три с лишним раза
дешевле! А если сжигать дизельное
топливо, то стоимость одной
килокалории уменьшится еще
примерно в два раза. Что же
касается газа, то у него эта
величина еще меньше: всего
0,0002 копейки (в 12 раз
дешевле, чем тепло, полученное из
электроэнергии). Но это —
только в случае получения тепла.
А ведь большая часть энергии
расходуется в виде
механической работы.
Как же проектировщику
быстро проанализировать, какой из
источников энергии наиболее
целесообразен в том или ином
случае? Для этого нужна преж-
ю
де всего методика, по которой
можно было бы
систематизировать технико-зкономические
показатели источников энергии.
Такая работа была проведена
сотрудниками кафедры
промышленной статистики
Московского
экономико-статистического института.
Оказалось, что стоимость
единицы работы (или тепла)
можно выразить несложной
формулой:
^М£
^рем
п
где: С* — стоимость единицы
работы (или тепла); Р — цена
единицы топлива; Н —
теплотворность топлива; т] —
коэффициент полезного действия
двигателя; С- —стоимость
машины-преобразователя; С —
стоимость ремонтов машины за
весь срок службы; п — число
ремонтов; N — мощность
машины; R — ресурс машины.
Сравнив значения С* для
различных топлив, можно
определить, в каком из
сравниваемых вариантов 1 киловатт-час
или 1 килокалория обойдется
дешевле. А чтобы узнать,
насколько одна машина
экономически выгоднее другой, нужно
разность величин С* умножить
на мощность и время работы
машины.
Для примера вернемся к
упомянутым ранее источникам
энергии: электричеству,
бензину, дизельному топливу и газу,
но уже для случая превращения
этой энергии в механическую.
Пусть двигатель имеет
мощность 20 квт. Стоимость 1 квт-ч
механической работы,
полученной из электроэнергии, составит
2,25 копейки (по цене для
промышленных предприятий);
стоимость 1 квт-ч, полученного при
работе двигателя внутреннего
сгорания на бензине, равна
1,9 копейки, на дизельном
топливе — 0,9 копейки, а на газе —
0,4 копейки. Как видите,
соотношение заметно изменилось в
пользу электричества, хотя оно
и осталось самым дорогим.
Для двигателей мощностью в
несколько киловатт
электрическая энергия окажется уже
значительно выгоднее энергии,
вырабатываемой бензиновым
двигателем. Но главная причина
повсеместного распространения
электродвигателей на
промышленных предприятиях
заключается в том, что они компактны,
безвредны, а их КПД высок. Не
ставить же у каждого станка
турбину!..
НА ЧЕМ ОСТАНОВИТЬСЯ?
Если речь идет о стационарной
установке, где вес не имеет
значения, то приведенная формула
дает однозначное решение. Для
транспортной машины этой
формулы уже недостаточно — вес
запаса топлива и двигателя
машины влияет на экономичность
всей транспортной установки в
целом. Ведь автомобиль,
самолет, локомотив вынуждены
затрачивать энергию на
перевозку не только полезного груза, но
и двигателей, и запаса топлива.
Например, годовой ущерб от
одного килограмма лишнего веса
(т. е. сумма средств,
перерасходованных за год при
увеличении Беса конструкции на 1 кг)
у пассажирских самолетов
ИЛ-18 и АН-10 превышает
300 рублей.
Если и вес силовой
установки, и стоимость единицы
энергии у одного из сравниваемых
вариантов будет меньше, чем у
другого, то решение не
вызывает затруднений. А как быть,
если у одного двигателя
стоимость единицы энергии меньше,
а у другого — меньше вес?
В этом случае проектировщику
нужно выбрать такую силовую
установку и, соответственно,
такой вид топлива, чтобы
суммарные расходы на топливо и на
машину за весь срок службы
были наименьшими.
Этот выбор нелегок —
величины, входящие в уравнение, не
постоянны, а изменяются в
зависимости от мощности,
требуемого срока службы, количества
выпускаемых двигателей. А вес
двигателя зависит, в свою
очередь, от тех же мощности и
срока службы, от вида топлива.
Для того чтобы
проектировщикам было удобнее
ориентироваться среди множества топлив
и источников энергии,
предложены таблицы, которые
облегчат оптимальный выбор топлива
и силовой установки. (Заметим,
что существует около тысячи
источников энергии и несколько
десятков преобразователей.)
Фрагментом такой таблицы мы
и заканчиваем статью. В этой
таблице символом G обозначен
удельный вес двигателя (то есть
отношение веса к мощности) с
запасом топлива на 5 часов.
Двигатель внутреннего сгорания (ресурс 5000 часов номинальной мощности)
Марка топлива
Бензин А-72
1 Газ
| Дизельное топливо . .
Интервал мощности, л. с.
0—20
G
1 4,15
5,7
9.9
с*
0,0196
0,0042
0,0095
20-40
G
4,0
5,0
8,5
с*
0,0190
0,0040
0,0090
40-100
G
3,85
5,3
6,0
с*
0,0180
0.0038
0,0085
100—300 | 300—500 1
G
3,5
4,9
5,0
с*
0,0172
0,0035
0,0080
G
3,2
4,6
4,5
с* 1
0,0170
0,0033
0,0075 |
2*
и
TtTVTrrvrvrr^
■■«■
ГГГТ
-^JJJiJji
iAAi
ПОЛЕЗНЫЕ СОВЕТЫ
И ПОЯСНЕНИЯ К НИМ
Материал
тысячи возмоэюностеи
До наших дней сохранилось
несколько сооружений,
построенных еще в глубокой древности,
долговечность и прочность
которых овеяны легендами. Это.
например, Беслецкий мост в
Сухуми, Татартубскии минарет в
Северной Осетии, некоторые
старинные здания в Таллине.
Теперь мы знаем секрет
древних строителей: в известко-
во-песчаный вяжущий раствор
они добавляли природные
полимеры — яичный или молочный
белок, кровь животных. Именно
зти вещества и придали
сооружениям столь поразительную
стойкость.
У читателей может
возникнуть законный вопрос: неужели
современная химия не нашла
еще достойной замены этим
веществам? Конечно, такая
замена существует. Это поливинила-
цетатная эмульсия (в
дальнейшем будем называть ее
сокращенно — ПВАЭ). Если ее ввести
в какое-нибудь современное
вяжущее вещество (например,
портланд-цемент), то оно будет
способно выдержать
конкуренцию с вяжущими материалами
древних строителей, а если
смешать цемент, песок, воду и ПВАЭ
и склеить этой массой два
куска бетона, то образовавшийся
монолит удастся разорвать где
угодно, но только не по
клеевому шву!
ЧТО ЖЕ ТАКОЕ
ПОЛИВИНИЛАЦЕТАТНАЯ
ЭМУЛЬСИЯ?
Это взвесь (дисперсия)
шарообразных частиц полимера по-
ливинилацетата в воде. Сам
полимер получается из ацетилена
и уксусной кислоты (ее, в свою
очередь, тоже получают из
ацетилена) в результате
следующих реакций:
СНзСПОН- СН _ СН >
СН3СООСН = СН2 полимеризация.
Но это еще ничего не говорит
о том, каким образом
приготовляют саму эмульсию. А об этом
стоит подробно рассказать.
Разберемся сначала, почему
ПВАЭ устойчива? Почему она
даже при длительном хранении
не расслаивается на воду и
собственно полимер? Ведь средний
размер частиц этой эмульсии
около одного микрона, а из
коллоидной химии известно, что
взвеси гидрофобных веществ
(а поли вини лацетат — как раз
вещество гидрофобное)
устойчивы лишь в том случае, если
размер частиц не превышает одной
десятой микрона.
Дело все в том, что
поверхность каждого
микроскопического поливинилацетатного
шарика покрыта тончайшим слоем
гидрофильного вещества —
поливинилового спирта. Именно
эта пленка и не дает шарикам
слиться воедино.
Но каким образом удается
каждую невидимую
невооруженным взглядом капельку
одного вещества покрыть
тончайшим слоем другого?
ЛЛЛЛлАЛЛАЛАЛЛ
л •••
i»»^
ч»ь>
ч»*
1«
ч»*
^•*
«•*
•Чек.
-«•►
■*•*
Z»*-
>*
2 е*
•«•*
^•►/ч
••••••••••
ттутгггггг
fis /1
H /я
J? 1L
К^ёГт
^—4*^"Ч-—
ВШУ й А
-_ W Л.ЛЛААЛАЛЛ^ЛАЛЛЛ*ЛЛЛЛАЛ*лАЛлЛ»ЛАЛЛА*ЛЛЛЛЛлЛ^
# ••• w ^.» ••••••••■•••••••■*••••• •■«•••••••■•• #«ту
2*с *?► ^=^\ ^^ «•*
J •'*XEtrrxi«yS* * ^ aa JTi a * * * * алла л* ► 4 rA л А£А л ЖАА*А ?aaaa*AAaaAAAAAAaAa Жл< • £ ч I VJjft* даааш ал Л.
• r•••• • • ••£
ттгт»ттттт*
Часто бывает, что
сложнейшие на первый взгляд задачи
решаются чрезвычайно просто.
В нашем случае этим
решением оказалась так называемая
эмульсионная полимеризация.
Эмульсионная
полимеризация состоит в следующем.
Сначала готовят эмульсию
мономерного винилацетата (это
жидкость, нерастворимая в воде) в
водном растворе поливинилового
спирта. Для этого мономер
вливают тонкой струей при
энергичном перемешивании в
раствор: каждая капелька винил-
ацетата покрывается тончайшим
слоем поливинилового спирта.
Потом вводят инициатор
полимеризации — перекись
водорода — и нагревают эмульсию.
Полимеризация начинается в
каждой капельке, каждая капелька
превращается в твердую
частицу полимера, а поливиниловый
спирт так и остается на ее
поверхности.
Теперь расскажем, какие
превращения происходят с ПВАЭ
при ее использовании. Почти во
всех случаях ПВАЭ необходимо
превратить в твердое тело, чаще
всего в пленку. Для этого нужно
удалить воду — или испарить
ее, или отсосать пористой
подложкой (или и тем и другим
способом одновременно). По
мере потери воды частицам
полимера становится все «теснее»,
пока наконец они не окажутся
так плотно прижатыми друг
к другу, что из водной
эмульсии образуется твердое тело.
Но свойства этого тела —
прежде всего механические и
оптические — сильно зависят от
температуры, при которой
удалялась вода. Если температура
была ниже 30е С, то из ПВАЭ
(уж таково ее свойство)
образуется хрупкая мутная масса.
Что же делать? Работать с
ПВАЭ при температуре выше
30° С? Это явно неудобно. Есть
другой выход —
пластифицировать эмульсию, добавить в нее
вещество-пластификатор, от
которого полимер набухает,
делается мягче. Если к 100
весовым частям ПВАЭ добавить
6 — 8 весовых частей дибутил-
фталата, промешать 20 — 30
минут, а потом оставить на сутки
для «созревания», то
полученная композиция называется
пластифицированной
эмульсией. Твердые тела из нее
получаются монолитными,
механически прочными, прозрачными;
они хорошо прилипают к
различным материалам, обладают
стойкостью к солнечному свету
и кислороду воздуха. Устойчивы
они также к действию многих
органических растворителей и,
в частности, нефтепродуктов.
К сожалению,
пластифицированная ПВАЭ, обретя
способность образовывать пленки при
комнатной температуре, теряет
хл а достой кость: при
замораживании и последующем
оттаивании она необратимо портится.
(Для непластифицированной
эмульсии замораживание не
страшно: при оттаивании она
восстанавливает свои структуру
и свойства полностью.) Кроме
того, дибутилфталат снижает
твердость и теплостойкость
пленки, увеличивает ее
ползучесть.
Этих недостатков не имеют
так называемые временные
пластификаторы. Это органические
жидкости, которые в момент
образования пленки действуют
подобно дибутилфталату, но в
отличие от него через некоторое
время бесследно исчезают из
пленки, испаряются. Поэтому
пленка становится и гомогенной,
и эластичной, и в то же время
сохраняет все свои лучшие
свойства.
Для временной
пластификации ПВАЭ используют диэти-
ленгликоль, триэтиленгликоль,
простые и сложные зфиры этих
спиртов. Практика показала, что
лучше всего применять смесь
временного и постоянного
пластификаторов.
Внешне пластифицированна'я
18
змульсия практически не
отличается от непластифицирован-
ной. Однако их легко можно
распознать. Для этого несколько
капель ПВАЭ размазывают
тонким слоем на обычном оконном
стекле и дают высохнуть. Если
при этом образуется
прозрачная эластичная пленка —
эмульсия пластифицированная, если
хрупкая, матовая — нет.
Никогда не бывает, чтобы
какой-то материал был
одинаково хорош для любой цели.
А у ПВАЭ есть еще одно
замечательное качество: она очень
легко модифицируется.
Действие тепла, окислителей, поверх-
ностноактивных веществ,
различных добавок позволяет очень
гибко менять ее свойства.
КЛЕЙ ДЛЯ БУМАГИ
И ФОТОКАРТОЧЕК
Обычно для склеивания бумаги
используется или силикатный,
или казеиновый конторский
клей. Силикатный клей
обладает рядом недостатков: оставляет
пятна, быстро стареет и
приклеенное перестает держаться,
клеевой шов хрупок; написанное
чернилами обесцвечивается, а
фотографическое изображение
от него быстро выцветает.
Казеиновый клей, хотя и не дает
столь хрупкой пленки и не
разрушает красителей, тоже
оставляет заметные следы; кроме
того, много возни и с его
приготовлением.
Всех этих недостатков
лишена поливинилацетатная
эмульсия. Она дает совершенно
незаметный, очень прочный,
эластичный и не стареющий
шов (недаром ее все шире
применяют полиграфисты при
изготовлении переплетов); ПВАЭ
не разрушает красителей,
фотографическое изображение от нее
В начале этой заметки мы
назвали поли вини л ацетатную
эмульсию «материалом тысячи
возможностей», а пока что
упомянули только об одной области
ее применения — для
изготовления вяжущих растворов. Где же
еще ее применяют?
Даже простое перечисление
областей использования ПВАЭ
заняло бы несколько страниц.
Ее добавляют в бетон, из
которого делают полы
машиностроительных предприятий: такие
полы не раскалываются при
случайных ударах, не
отскакивают от основания, не пылят.
Штукатурка, содержащая ПВАЭ,
прочно держится на стенах и
потолке, не пачкает. Краски,
изготовленные на основе ПВАЭ,
не выцветает.
Поливинилацетатная эмульсия незаменима при
мелком ремонте обоев, для
их прочного прикрепления
вдоль окон, дверей, потолка, для
наклейки этикеток на
стеклянные банки.
КЛЕЙ ДЛЯ ДЕРЕВА
Трудно найти лучший клей для
дерева, нежели ПВАЭ. Столяр,
хоть раз поработавший с ним,
не захочет уже больше
возвращаться к традиционному
столярному клею. С помощью
ПВАЭ можно приклеить
оторвавшуюся паркетную клепку,
отремонтировать окно, дверь.
КЛЕЙ ДЛЯ ОБУВИ,
ЧУЛОК
С помощью ПВАЭ можно
произвести мелкий ремонт кожаной
обуви. А сколько неприятностей
доставляет женщинам
«убежавшая» петля? И здесь хороша
ПВАЭ: петлю можно закрепить
капелькой эмульсии (правда,
не хуже обычных масляных, но
в отличие от последних их
можно наносить прямо на влажную
поверхность, высыхают они
всего за 2 — 3 часа, емкости с
остатками краски легко отмываются
просто водой. Без ПВАЭ не
обходится и текстильное
производство: она используется при
изготовлении знаменитых
нетканых материалов, постоянно
«накрахмаленных» воротничков
и т. д. и т. п.
Поливинилацетатная
эмульсия может сослужить хорошую
службу и дома.
Инженер
Ь. А. ВОЙТОВИЧ
при стирке чулки не следует
долго держать в воде).
КЛЕЙ ДЛЯ КЕРАМИЧЕСКОЙ
ПЛИТКИ
Обычно керамическую плитку
прикрепляют к стенам с
помощью цементного раствора
(иногда используют и густотертую
масляную краску). Однако
такое соединение не вполне
надежно. С помощью ПВАЭ
керамическую плитку можно
укрепить буквально «намертво».
КЛЕЙ ДЛЯ...
ГВОЗДЕЙ
Жителям блочных и панельных
домов часто приходится ломать
голову над тем, как прикрепить
к бетонной стенке выключатель,
розетки, как повесить картину.
Вот и приходится под всякую
малость пробивать в стенке
шлямбуром гнездо для деревян^
ной пробки.
ПВАЭ позволяет избежать
Пять из тысячи
14
этой трудоемкой и
малоприятной операции: достаточно
приклеить к бетонной стене
деревянный брусок (соединение
получается достаточно прочным)
и вбить в него гвоздь или
шуруп.
После всего сказанного нет
особой нужды приводить новые
доказательства того, что поли-
винилацетатная эмульсия — это
материал тысячи возможностей.
В последние годы большую
популярность приобрела одежда.
изготовленная из ткани
«болонья». Плащи, спортивные
куртки и даже плавки делают из
нее. А что такое «болонья»
знают немногие.
Эти изделия существенно
отличаются от изделий из
хлопчатобумажных или смешанных
тканей, пропитанных
специальными химикатами или
прорезиненных — покрытых с изнанки
резиновой пленкой. «Болонья»
имеет ряд преимуществ перед
ними: она прочна, стойка к.
климатическим воздействиям,
наконец, она гораздо легче прочих
плащевых материалов. Плащ из
«болоньи» весит 350—400
граммов, в то время как средний вес
плаща из хлопчатобумажных
тканей колеблется в пределах
800—1500 граммов. Название
«болонья», как нетрудно
догадаться, пришло к нам из
Италии, где впервые была сделана
зта ткань.
Ткань плащей «болонья» —
это капрон (реже — нейлон),
пропитанный полиакриловыми
или полиэфирными смолами и
силиконами. Нанесенное на
ткань не смачивающееся
водой покрытие состоит из двух
или трех слоев, его наносят
Тем более что мы перечислили
их далеко не все.
Более того. Этому
замечательному материалу всегда
можно найти тысяча первое
применение—
От редакции. Статья
В. А. Войтовича достаточно
убедительно доказывает
замечательные возможности поливи-
нилацетатной змульсии. В на-
на изнаночную сторону
материала.
Первый слой делается из
основного пленкообразователя. Это
очень вязкая жидкость. Ее
изготовляют, растворяя в этил-
ацетате смесь полимера и
сополимера акриловой кислоты.
Сюда же добавлены полиизоци-
анат — для «сшивания»
структуры смолы — и белая сажа —
для придания пленке матовости.
Высокая вязкость нужна для
того, чтобы не получилось
сквозной пропитки. Этот слой
непроницаем для воды, он служит
главным «водоизолятором».
Второй слой — тот же плен-
кообразователь, но менее
вязкий. Его наносят, чтобы придать
поверхности ткани приятную на
вид и на ощупь структуру. На
водопроницаемость второй слой
влияет мало. На этом процесс
пропитки двухслойных (более
дешевых) материалов
заканчивается.
Третий слой наносят,
главным образом для гарантии
качества, для того, чтобы пленка
была более равномерной.
Иногда на лицевую сторону ткани
наносят еще и четвертый слой
пленкообразователя,
содержащий 3—5% металлической
пудры разных цветов. После того
шей стране налажено ее
крупнотоннажное производство (ГОСТ
10002 — 62) для нужд самых
разнообразных отраслей народного
хозяйства. Однако эта же статья
доказывает, что ПВАЭ
незаменима не только на производстве,
но и в быту. Редакция надеется,
что торговые организации
подумают о том, чтобы в
хозяйственных магазинах можно было бы
всегда приобрести поливинил-
ацетатную эмульсию.
как все слои нанесены и
высушены, для того чтобы плащевая
ткань не слипалась и была
приятной на ощупь, ее изнаночную
и лицевую стороны
обрабатывают специальным гидрофобизи-
рующим составом — раствором
силикона. Такая обработка
приводит к тому, что ткань совсем
уже не смачивается водой и к
ней почти не прилипает грязь.
Эти свойства сохраняются в
течение 3—4 лет.
Свойства плащевой ткани
«болонья» определяются
свойствами ее полиамидной основы
и полимерных материалов
покрытия. Напомним, что капрон
устойчив к действию
минеральных кислот, щелочей, водных
растворов мыл и моющих
средств, а также к действию
плесени и микроорганизмов.
Теми же свойствами
обладает и ткань «болонья», она легка,
прочна, практична, но в отличие
от капрона «болонья»
совершенно неустойчива к действию
органических растворителей,
особенно уайт-спирита, три-
хлорэтилена, тетрахлорзтилена.
Эти вещества растворяют
полимерное покрытие, поэтому
химической чистке (в обычном
понимании этого слова) плащи
«болонья» подвергать нельзя.
О плащах „болонья
15
Полимерная пленка делает
зту ткань непроницаемой для
воды. Но, к сожалению, не
только для воды, но и для воздуха.
Поэтому плащи из «болоньи»
следует использовать только по
прямому назначению, то есть
пользоваться ими в сырую
погоду для защиты от дождя.
(Кстати, капроновое волокно и
полимеры пропитки под
действием прямых солнечных лучей
постепенно разрушаются,
поэтому если плащ носить в
солнечную погоду, то он быстро придет
в негодность.)
Подвергать «болонью»
химической чистке нельзя, но ее
можно стирать в мыльных
растворах или применяя
нейтральные моющие средства,
такие как «Новость», «Березка»,
«Мир». Вода должна быть не
горячей C0—40° С). Стирать еле-
ИЗ ПИСЕМ В РЕДАКЦИЮ
■ «ПУТЬ К БЕССМЕРТИЮ?»
В сентябрьском номере нашего
журнала за прошлый год была
опубликована заметка «Путь к
бессмертию!». Автор этой
заметки И. С. Фипимоненко
высказывает смелое предположение, что
«до потопа» люди могпи жить по
нескольку тысячелетий, так как
в их пище содержалось очень
мало радиоактивного изотопа
калия К40.
Внешне эта заметка была
логически безупречной. Однако она
была основана на ряде
допущений, справедливость которых мы
предложили проанализировать
читателям. Ниже мы приводим
выдержки из наиболее
интересных откликов.
Мне кажется, что в статье «Путь
к бессмертию?» автор И. С. Фили-
дует в обильной пене, сильно
загрязненные места смочить
моющим раствором и оставить
изделие полежать некоторое время
A5—20 мин). Сильных
механических воздействий следует
избегать. Стирая «болонью», не
стоит применять жесткие
щетки, сильно тереть и
отжимать ее.
После стирки плащ следует
прополоскать сначала в теплой
C0—40е С), а потом холодной
A5—20е С) воде. После
полоскания воде дают стечь и, не
отжимая плаща, вешают его на
плечики. В таком положении он
и сушится. Не рекомендуется
сушить изделие из «болоньи»
при высокой температуре и под
действием прямых солнечных
лучей. После просушивания
плащи «болонья» можно гладить
с лицевой стороны и только ела-
ИЗ ПИСЕМ В РЕДАКЦИЮ
моненко неправильно
истолковывает годы. По всей вероятности,
«до потопа» люди считали
продолжительность жизни в днях, а не
в годах; если пересчитать, то оно
так и получится: царь жил
36 000 лет = в году 360 дней
умножить на 100 лет, или 28 800 лет =
= 360 • 80 лет и т. д.
Оля АНТОНОВА, Москва
...Скорее всего цифры,
приведенные шумерийскими писцами,
не характеризуют возраст
древних царей, выраженный в наших
годах, а содержание КгО в
каменном угле не характеризует
количества К40 в их пище.
Массивы каменного угля — это
окаменевшая биомасса гигантских
древних лесов с весьма мало Г;
примесью останков шумерийских
царей.
Л. И. ЛЕВЕНСОН, Ташкент
бо нагретым утюгом. Лучше
пользоваться утюгом с
терморегулятором (установив ручку
терморегулятора на делениях
«капрон» или «искусственный
шелк»). От сильного нагревания
капрон, как и прочие
полиамиды, плавится.
В заключение несколько слов
о ремонте плащей «болонья».
Если в плаще появились
небольшие разрывы и дырки, их
можно закрепить с помощью клея
КП-1, разработанного в Научно-
исследовательском технохими-
ческом институте бытового
обслуживания (НИТХИБ). Пока
этот клей поступает только
в ремонтные мастерские и
комбинаты бытового
обслуживания.
Кандидат химических наук
М. И. УШАКОВА
ИЗ ПИСЕИ В РЕДАКЦИЮ
...Не первый взгляд логичные
построения авторе, увы,
эфемерны: они безнадежно рушатся от
соприкосновения с любым из
ряда научно достоверных фактов.
Начнем с того, что с*до
потопа» в земной коре радиоактивного
калия было не меньше, а
больше, чем во времена
исторические... Ведь нет и не предвидится
данных, что на протяжении
истории Земли в ней нарождался
вторичный К40 или что он поступал
из Космоса. Протекал только
процесс распада первоначального, со
времен формирования Земли,
запаса К40. Его период
полураспада равен 1,3 млрд. лет,
следовательно, если считать возраст
Земли 5 млрд. лет, то на заре
своей истории она имела в 10 раз
больше К40, чем теперь... Стало
быть, следуя логике заметки,
необходимо признать, что шумерий-
16
ские цари больше нашего
вкушали K40i равно и других
радиоизотопов, содержащихся в
растительных и животных тканях...
Предположим, что все это
так, — возразит воинствующий
оппонент. — Но как объяснить
низкое содержание калия в
каменном угле, резко выделяющееся
на фоне высокого содержания
в золе растений? Именно в золе.
Так как если бы автор сопоставил
золу растений с золой угля, то
в ней оказалось бы не 0,2% КгО,
а в 5—30 раз больше.
Однако не в этом суть дела.
Прежде всего, неужели автор
всерьез полагает, что древние
шумеры жили в каменноугольном
периоде или где-то поблизости?
Нет, автор не грешен в такой
ереси. Поскольку ему известно,
что каменноугольный период
начался лет 275 миллионов назад
и длился 50—55 миллионов лет.
Так почему же автор привлекает
каменный уголь в качестве
главного вещественного
доказательства того, что во садах ли, в
огородах шумерийских царей и их
подданных произрастали плоды
с низким содержанием
радиоактивных веществ?
...Таким образом, надо
отвергнуть одно из допущений,
сформулированных в редакционном
послесловии: не существует связи
между содержанием К40 в
каменном угле и в пище «допотопных»
людей. Не более состоятельны
и остальные три допущения.
...Итак, заметку ссПуть к
бессмертию?» следует рассматривать
как предумышленную, учиненную
в сговоре с редакцией журнала
мистификацию. Бесспорно
остроумную — дающую неплохую
пищу для моциона мысли. Но и
только.
Доцент Д. Н. ФИНКЕЛЬШТЕЙН,
Свердловск
■ КАК ЗАКОНЧИЛАСЬ
ОДНА ДУЭЛЬ
В декабрьском номере нашего
журнала за 1966 год была
напечатана статья «История одной
дуэли», в которой рассказывалось
об ожесточенной дискуссии,
разгоревшейся в 1962—1963 гг. между
двумя группами швейцарских
химиков. Спор произошел из-за
«кетолактона» — вещества,
которое два ученых (И.-Р. Нав и
А. В. Грамполов) выделили из
эфирного масла жасмина, и
которого три других ученых (Э. Де-
моль, Э. Ледерер и Д. Мерсье)
не обнаружили.
«Дуэль» эта закончилась
мирно. Объединенными усилиями обе
группы химиков установили, что...
все по-своему были правы: хотя
эфирное масло жасмина и
содержало кетолактон, но это
вещество было очень трудно обнаружить
и выделить в чистом виде. В
конце статьи, в частности, говорилось:
«...что-то не слышно, чтобы кто-
нибудь из ее участников (то есть
участников «дуэли». — Ред.)
занялся изучением структуры
злополучного вещества. Так иногда
бывает: после того как соперники
помирились, они могут и забыть
о предмете раздора...».
Спустя некоторое время после
выхода журнала в свет редакция
получила от сотрудника
Всесоюзного научно-исследовательского
института синтетических и
натуральных душистых веществ
кандидата химических наук Л. А.
Хейфица письмо, адресованное ему
Э. Демолем — одним из
участников «химической дуэли».
Выдержки из этого письма Э. Демоль
любезно разрешил опубликовать
в нашем журнале.
«Дорогой доктор Хейфиц!
51 хочу Вам сказать, как я был
рад, получив от Вас экземпляр
«Химии и жизни» № 12, 1966 г.
Журнал я получил несколько
ранее письма, но увидев рисунок
дуэли на стр. 50, сопровожденный
хорошо знакомыми мне
химическими формулами, я без труда
понял, что эта статья касается
меня! 51 ее немедленно попросил
перевести. И вот каковы мои
впечатления:
Прежде всего — это подлинное
восхищение, вызванное уровнем
журнала. Насколько я знаю, ни
в Швейцарии, ни во Франции нет
ни одного научно-популярного
журнала, в котором бы научные
работы анализировались на
основе первоисточника. Далее меня
равным образом поразили
большая объективность и здравый
смысл статьи в «Химии и жизни».
Не подлежит сомнению, что такой
подход будет способствовать
раскрытию талантов будущих
больших ученых, читающих этот
журнал. Наконец, я должен Вам
сказать, что статья в «Химии и
жизни» помогла мне высоко оценить
тонкость вашего юмора, юмора
советских людей!
Однако я не согласен по двум
пунктам:
1. Количество кетолактона во
фракциях, которые я исследовал
с помощью масс-спектрометрии,
составляло всего 4—6% (а не 4—
14%, как указано на стр. 53).
2. Достоинство ученого
заставило меня предпринять изучение
этого гадкого кетолактона.
Результатом этого явилась
публикация, которую я высылаю вместе
с письмом. Лишь после появления
последней статьи я согласился
положить мои пистолеты в ящик!
Этот спор отчетливо
показывает, что поиски все более и
более полной объективной истины
являются первым долгом
ученого. И если это необходимо для
решения какой-либо отдельной
проблемы, ученого не должно
пугать сотрудничество с теми, кто
в обычной обстановке мог бы
быть его «конкурентом». Никакие
соображения — личного,
коммерческого или политического
престижа — никогда не должны
препятствовать поиску научной
истины в чистом виде. Поэтому я
полностью согласен с заключением
статьи в «Химии и жизни», где
говорится, что научная мысль
имеет большую ценность, чем
личность ученого».
О Химия и Жизиь, № 4
17
НАШИ КОНСУЛЬТАЦИИ НАШИ КОНСУЛЬТАЦИИ НАШИ КОНСУЛЬТАЦИИ НАШИ
■ КАЛИЙ ЗАКАЛИВАЕТ
Существуют ли химические
способы защиты садов и огородов от
зимних и весенних заморозков!
А. М. МИХАИЛОВ,
гор. Жуковский
Один из самых важных факторов,
повышающих морозоустойчивость
растений, — это их способность
сохранять влагу. Ткани,
испытывающие недостаток влаги или
слишком быстро ее испаряющие, легче
повреждаются заморозками.
Для нормального обмена влаги
в растении необходимо
поддерживать определенную степень
набухания коллоидов клеток — тургор.
И здесь важная роль принадлежит
одному из главных элементов
питания растений — калию.
Калий не только является
составной частью растения, но и
активно участвует в синтезе и
накоплении необходимых растению
углеводов. Органическое вещество
создается растением в ходе
фотосинтеза из углекислоты и воды
при участии световой энергии.
Основной процесс образования
углеводов — восстановление
углекислоты с выделением кислорода:
6Н2С03 - C6R12Oe BOo .
глюкоза
Первым продуктом
восстановления углекислоты является
муравьиная кислота НСООН, затем
формальдегид НС НО, который в
дальнейшем образует глюкозу.
В этом восстановительном
процессе калий и принимает активное
участие.
Переход от простейших
углеводов типа глюкозы к более
сложным, в том числе крахмалу и
клетчатке, происходит также в
присутствии калия. Некоторые злаки
(например, гречиха) вообще не
образуют крахмала, если в их хлоро-
филльных зернах отсутствует
калий.
Калий оказывает влияние и на
распределение белков в тканях
растений — его много в зонах роста,
им богат камбий. Установлено, что
калий имеет большое значение
для синтеза белковых веществ,
если азотистое питание поступает в
аммиачной форме. Образование
в растении простых и сложных
белковых веществ тесно связано с
присутствием в нем ферментов.
А образование многих ферментов
весьма затрудняется при
недостатке калия.
Большое влияние оказывает
калий и на физическое состояние
коллоидов, образующих
протоплазму и входящих в состав
клеточных стенок; степень набухания
этих коллоидов зависит от
присутствия в растворе катионов, причем
калий (в противоположность
кальцию и магнию) значительно
способствует их набуханию. Легко
проникая в клетки растения, калий
разрыхляет протоплазму и тем
самым облегчает поступление воды
в растение, создает осмотическое
давление в клетке и повышает тур-
гор. Этим и можно объяснить
повышение морозоустойчивости (а
также засухоустойчивости)
растений, хорошо обеспеченных
калием.
Поэтому один из самых
надежных «химических» способов
уберечь растения от мороза —
своевременное внесение в
достаточных количествах калийных
удобрений.
Ф. П. КАЩЕНКО,
Агрохимическая
лаборатория Московского
общества охраны природы
■ хотим подготовиться
ПОЛУЧШЕ!
Люда РОМАНЧЕНКО из города
Гвардейска Калининградской
области пишет: «В вашем журнале
(№ 5, 1967) в рубрике «Хотите
подготовиться к экзаменам
получше!» был опубликован список
литературы, помогающей успешно
сдать экзамены в вуз. Но как
достать указанные книги!
Посоветуйте...»
С этим же вопросом к нам
обращаются и многие другие
ребята.
Отвечает консультант П. И.
СТАРОСЕЛЬСКИЙ.
При Академии педагогических
наук СССР работает
Государственная научная библиотека по
народному образованию имени К. Д.
Ушинского. В ней открыт
межбиблиотечный абонемент,
обслуживающий периферийные школьные
библиотеки.
По запросу любой школьной
библиотеки работники абонемента
посылают по указанному адресу
форму «Обязательства
своевременного возвращения книг».
Заполнив бланк обязательства,
можно вместе с ним послать в
библиотеку свой первый заказ.
Библиотека в соответствии с ее профилем
при первой же возможности его
удовлетворит.
Адрес библиотеки имени
Ушинского: Москва, Ж-17, Большой
Толмачевский переулок, 3.
Кроме того, Магазин
педагогической книги (Москва, К-9, улица
Пушкина, 7) высылает по
требованию имеющиеся в продаже
учебники и учебные пособия
наложенным платежом.
18
ПРОБЛЕМЫ И МЕТОДЫ
СОВРЕМЕННОЙ НАУКИ
Разрезанные молекулы
Доктор биологических наук
А. А. БАЕВ
Высшим пилотажем науки можно было бы назвать сложнейшие методики>
используемые для исследования структуры молекул биополимеров - бел-
кое и нуклеиьовыу кислот. Одйк из признанных мастеров этого высокого
искусства - советски? учены? А.А.Баев, недавно завершивший работы по
расшифровке строения одной из транспортных рибонуклеиновых кислот -
тРНК (об этом открытии мы рассказывали в I' 7 журнала). Сейчас группа
А.А.Баева, используя весь арсенал отработанных и во многом
усовершенствованных методов исследования, продолжает изучать тРНК, но уже на
качественно новом уровне - выясняя взаимосвязь между структурой тРНК
и ее функциями в клетке. Это - новее направление исследований,
представляющее собой оригинальный вклад в мировую науку.
Основная задача молекулярной
биологии— изучение связи между химической
структурой и биологической функцией.
Например, исследуя главный белок мышцы —
актомиозин, молекулярный биолог
стремится выяснить, от каких химических и
физических его свойств зависит
способность мышечного волокна сокращаться,
что происходит с актомиозином при
сокращении и т. д. Этим молекулярная
биология и отличается прежде всего от
классической биохимии первой половины этого
столетия, изучающей химический состав
живого вещества и химические процессы,
составляющие основу жизнедеятельности.
При этом внимание
исследователя-биохимика направлено на превращения
главным образом низкомолекулярных
соединений — Сахаров, жиров, аминокислот и
пептидов. Объектом же молекулярно-био-
логических исследований служат
гигантские молекулы биополимеров — белков и
нуклеиновых кислот. Благодаря своей
сложной физико-химической природе эти
вещества наделены такими свойствами,
которые позволяют изучать на уровне их
молекул уже не только чисто химические,
но и простейшие биологические функции,
которые ранее исследовались лишь на
клетках и на целом организме. Один
только пример для пояснения:
наследственность, проявляющаяся у живых существ
в воспроизведении себе подобных, на
уровне молекул сводится к процессу
копирования молекул ДНК, который и
исследуют молекулярные биологи.
В этой, статье речь пойдет о
транспортных РНК (тРНК) и их изучении с позиций
молекулярной биологии, о том, какие
химические и физические их свойства и
каким образом позволяют им выполнять
свои функции в биосинтезе белка.
3*
19
тРНК: МОЛЕКУЛА-ПЕРЕНОСЧИК
В первом приближении функцию тРНК в
клетке можно описать очень кратко и
просто: участвуя в белковом синтезе, тРНК
соединяются с аминокислотами и
переносят их в строящуюся белковую цепь.
Но это — лишь первое приближение.
Когда мы начинаем прослеживать
превращения тРНК в клетке шаг за шагом, сразу
становится ясно, что при этом происходят
многие и притом очень различные по
своей природе процессы. Так, присоединяя
аминокислоту, тРНК взаимодействует со
специфическим ферментом
(активирующим ферментом аминоацил-тРНК-синте-
тазой), который катализирует эту
реакцию. Затем тРНК связывается с
рибосомой и с информационной РНК,
взаимодействует со многими различными
ферментами.
Таким образом, выполняемый тРНК
перенос аминокислоты в белковую цепь
на самом деле состоит из многих
последовательно происходящих процессов. В
целом все они носят циклический характер:
после того, как доставленная тРНК
аминокислота включена в нужное место
белковой цепи, тРНК освобождается и вновь
готова участвовать в тех же процессах.
Таким же свойством многократно
выполнять одно и то же действие обладают
ферменты; однако считать тРНК ферментом
мы не можем: она не является ни
белком — катализатором, ни коферментом,
составляющим часть фермента. Более
всего тРНК сходна по своей роли в
клеточных процессах с
метаболитами-переносчиками — такими, как щавелевоуксусная
кислота в цикле трикарбоновых кислот
или аргинин в цикле образования
мочевины. Но от них тРНК отличается
полифункциональностью: как мы видели, она
участвует не в одной, а во многих
отдельных реакциях.
,Г 20
Р
30 у
2Н 2Н Y
V-У-л -А'
?н
ААЦУ-ц^
Ц-Ц-Ц А Р'т т*ц
*У-Р-А
;7Р
/Г-г-р-у-щ
г \-ч-
• р
•Л
•а
А
- а
-А
и,
и,
Л-В-АЛИ44
Р
.Мб.
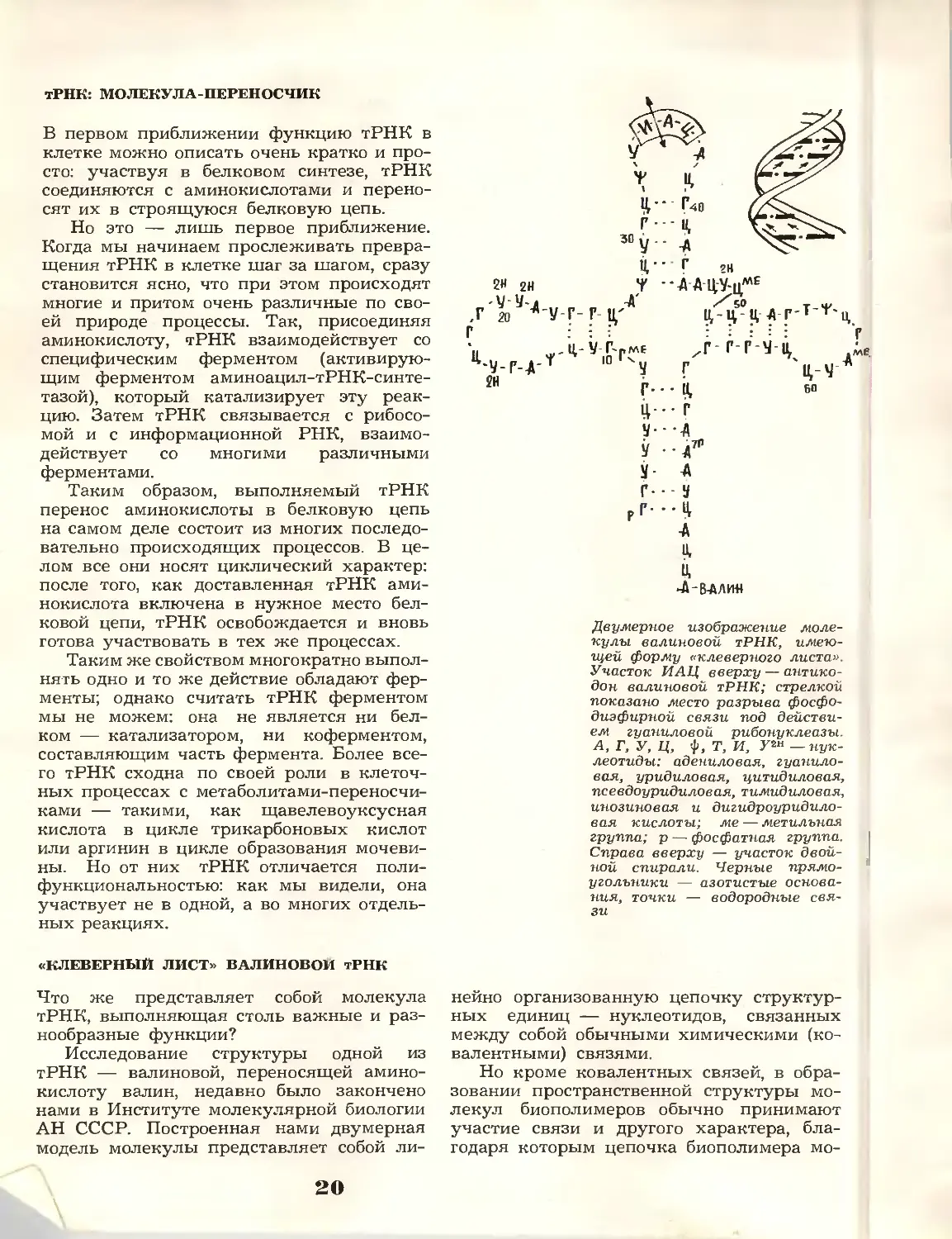
Двумерное изображение
молекулы еалиновой тРНК,
имеющей форму «клеверного листа».
Участок ИАЦ вверху — антико-
дон еалиновой тРНК; стрелкой
показано место разрыва фосфо-
диэфирной связи под
действием гуаниловой рибонуклеазы.
А, Г, У, Ц, ф, Т, И, У2Н — нук-
леотиды: адениловая, гуанило-
вая, уридиловая, цитидиловая,
псевдоуридиловая, тимидиловая,
инозиновая и дигидроуридило-
вая кислоты; ме — метильная
группа; р — фосфатная группа.
Справа вверху — участок
двойной спирали. Черные
прямоугольники — азотистые
основания, точки — водородные
связи
«КЛЕВЕРНЫЙ ЛИСТ» ВАЛИНОВОМ тРНК
Что же представляет собой молекула
тРНК, выполняющая столь важные и
разнообразные функции?
Исследование структуры одной из
тРНК — валиновой, переносящей
аминокислоту валин, недавно было закончено
нами в Институте молекулярной биологии
АН СССР. Построенная нами двумерная
модель молекулы представляет собой
линейно организованную цепочку
структурных единиц — нуклеотидов, связанных
между собой обычными химическими (ко-
валентными) связями.
Но кроме ковалентных связей, в
образовании пространственной структуры
молекул биополимеров обычно принимают
участие связи и другого характера,
благодаря которым цепочка биополимера мо-
20
жет сворачиваться в сложный клубок
определенной формы. Это прежде всего
более слабые и неспецифические
водородные связи, действующие между
азотистыми основаниями по принципу,
установленному в прошлом десятилетии М. Уотсоном
и Ф. Криком. Согласно этому принципу
адениловая кислота образует
комплементарную (взаимно дополняющую) пару с
уридиловой, а гуаниловая — с цитидило-
вой.
Зная последовательность нуклеотидов
в цепочке молекулы валиновой тРНК,
можно попытаться определить, какие
участки молекулы будут «сшиты» между
собой водородными связями. Оказывается,
в молекуле валиновой тРНК такие
комплементарные группы нуклеотидов
расположены, как правило, далеко одна от
другой. Например, нуклеотиды, занимающие
в молекуле положения с 1 по 7,
комплементарны нуклеотидам 67—73,
расположенным на другом конце молекулы.
В результате водородные связи,
сгнивающие между собой удаленные отрезки
цепи, придают молекуле тРНК сложную
конфигурацию, напоминающую
клеверный лист. Образуются четыре двухтяже-
вых участка, один свободный конец и три
петли, не содержащие оснований,
которые могли бы спариться по правилу
Уотсона и Крика. Эти петли, не образующие
двойных тяжей, и являются податливыми
частями молекулы.
«Клеверный лист», конечно, можно
считать только очень грубым подобием
реальной структуры молекулы валиновой
тРНК: в действительности молекула не
расположена на плоскости, а имеет
трехмерную конфигурацию. Но пока наши
представления о трехмерной форме
молекулы тРНК еще очень неясны. Можно
лишь предполагать, что полностью
свободны только верхняя петля молекулы тРНК
и ее концевой участок. Две другие петли,
видимо, как-то связаны либо между собой,
либо с другими частями молекулы.
СТРУКТУРА И ФУНКЦИЯ
Итак, мы теперь в общих чертах
представляем себе пространственное
расположение молекулы тРНК. С другой
стороны, мы знаем, какие функции выполняет
тРНК в процессах жизнедеятельности
клетки. Можно предположить, что для
выполнения этих функций нужна именно
такая структура, какую и имеет тРНК. Но
для молекулярного биолога такого
элементарного заключения недостаточно.
Прежде всего, хотя форма молекул всех
тРНК (а их, во всяком случае, не менее
20 — по числу аминокислот, входящих в
состав белка, а скорее всего гораздо
больше) почти или даже совершенно одинакова,
их химическое строение — природа
нуклеотидов и последовательность их в
молекуле — у индивидуальных тРНК резко
различна.
В настоящее время мы знаем
последовательность расположения нуклеотидов в
цепи нескольких тРНК. За последние два
года описаны первичные структуры ала-
ниновой, двух сериновых, тирозиновой,
валиновой и фенилаланиновой тРНК.
Однако знание этой первичной структуры
еще не дает в руки исследователя ключ к
изучению связи между структурой и
функцией: функциональная роль тех или
иных частей молекулы все еще остается
неясной. К тому же в большинстве
случаев мы не знаем химических и
физико-химических свойств тех веществ, с
которыми тРНК вступает во взаимодействие. Так,
нам неизвестно химическое строение
ферментов, с которыми связана тРНК; мы не
знаем структуры рибосом, с которыми она
образует комплекс.
Исключением являются реакции тРНК
с аминокислотами и с информационной
РНК. В первом случае точно известно, что
аминокислота присоединяется к
концевому адениловому нуклеотиду тРНК (ее
карбоксильная группа образует сложно-
эфирную связь со свободной гидроксильной
группой рибозы аденозина). В отношении
же информационной РНК предполагают,
что при взаимодействии с тРНК между их
комплементарными основаниями
образуется комплекс согласно правилам Уотсона и
Крика. Положение участка тРНК,
реагирующего с информационной РНК, сейчас
точно известно. Этот участок, или, как его
называют, антикодон, расположен в центре
верхней петли молекулы тРНК и состоит
из трех нуклеотидов. Они комплементарны
к нуклеотидам кодона — участка
молекулы информационной РНК,
определяющего включение в синтезируемый белок
определенной аминокислоты.
Кодоны аминокислот теперь
достоверно известны. Например, включение в
белок аминокислоты аланина задается ко-
донами ГЦУ, ГЦЦ, ГЦА или ГЦГ (Г —
21
сокращенное обозначение нуклеотида
гуанина, Ц — цитозина, У — урацила и А —
аденина). В соответствии с этим антикодо-
ном аланиновой тРНК служит тройка
нуклеотидов ИГЦ. Структура этих анти-
кодонов доказана прямым анализом.
Вот пока и все наши сведения
относительно нуклеотидов тРНК, участвующих
в тех или иных реакциях.
НЕМНОГО ФАНТАЗИИ
Там, где ученый не располагает фактами,
он прибегает к гипотезе, которая, конечно,
не может заменить экспериментально
доказанной истины, но позволяет
осмысливать и обобщать разрозненные факты,
намечать пути опытного решения проблемы.
На основании всего того, что нам
известно о связи структуры и функции
биополимеров (прежде всего — ферментов),
мы можем утверждать, что каждый
химический и физико-химический процесс,
в котором участвует такая молекула,
осуществляется строго определенной ее
частью. Естественно предположить, что
каждый такой участок, который можно
было бы назвать действующим центром,
содержит определенные химические
группы, служащие исполнителями данной
реакции, и что такой центр должен иметь
строго определенную пространственную
организацию. Вот как обстоит дело,
например, при взаимодействии фермента и
его субстрата. На верхнем рисунке
показан активный центр рибонуклеазы —
фермента, расщепляющего фосфодиэфирные
связи РНК, — и взаимодействующая с
ним часть молекулы РНК. Вы видите, что,
во-первых, форма активного центра
фермента точно соответствует форме
субстрата и что, во-вторых, активные
химические группы фермента (направление их
действия показано стрелками) занимают
точно определенное положение по
отношению к тем участкам молекулы
субстрата, которые являются мишенью атаки со
стороны фермента.
Нечто подобное должно происходить
и в том случае, когда тРНК, присоединяя
аминокислоту, взаимодействует с
активирующим ферментом (а эта реакция
интересует нас в первую очередь). Пока мы не
знаем, как на самом деле происходит это
взаимодействие; но логика подсказывает,
что оно должно подчиняться тем же
закономерностям.
К,*
*-/\
Сущего *ер/*е«^
Вверху — комплекс, образуемый
ферментом рибонуклеазой и
частью молекулы РНК — ди-
нуклеотидом, состоящим из
остатка цитидиловой кислоты
и какого-либо другого
нуклеотида (R). Видно, что
конфигурация активного центра
фермента соответствует конфигурации
субстрата (как форма перчатки
соответствует форме руки).
Стрелками указаны
направления атаки активных групп
фермента на фосфодиэфирную
связь. Внизу — гипотетическая
схема комплекса, образуемого
тРНК с активирующим
ферментом. Действующий центр тРНК
на схеме образован азотистым
основанием (хотя в принципе
не исключено и участие в нем
фосфатных групп и сахара)
^s
22
Более того, мы можем предположить,
что из трех составных частей нуклеотидов
РНК — остатка фосфорной кислоты,
сахара (рибозы) и основания — только
последняя может определять избирательность
реакции тРНК и фермента. Фосфатные
остатки и рибоза во всех звеньях молекулы
тРНК совершенно одинаковы. Основания
же различны по своей химической
природе, обладают разными
функциональными группами, неравномерно расположены
по длине молекулы тРНК. Поэтому
именно азотистым основаниям мы склонны
приписать главную роль в реакциях тРНК.
Можно представить себе, что
взаимодействие тРНК с активирующим
ферментом происходит примерно так, как это
изображено на нижнем рисунке (в
отличие от верхнего это лишь принципиальная
схема, которая не отвечает никакой
действительной реакции).
Итак, для того чтобы установить связь
между структурой и функцией тРНК,
нужно прежде всего отыскать нуклеотиды,
участвующие в той или иной реакции. Это
уже новое направление в изучении тРНК,
которое рождается в лабораториях на
наших глазах — функциональная
топография, то есть исследование той
функциональной нагрузки, которую несут
отдельные нуклеотиды или их совокупности
в молекуле тРНК.
Поиски на этом направлении
осложняются особенностями пространственной
организации молекулы тРНК. Дело в том,
что, как мы уже говорили, в естественном
состоянии удаленные друг от друга части
ее нуклеотидной цепи оказываются
сближенными. Поэтому в линейно развернутой
молекуле отдельные «кусочки»
действующего центра реакции могут оказаться
в разных местах. Действительной
конфигурации молекулы тРНК мы не знаем,
нуклеотиды или их группы мы
вынуждены отыскивать на линейно развернутой
молекуле, и это создает большие
трудности в решении задачи.
ПУТИ И ПОДХОДЫ
К структурно-функциональному изучению
тРНК, в частности к исследованию ее
реакции с активирующим ферментом, можно
подходить по-разному. Один из
возможных путей — химическая модификация
молекулы тРНК. Для этого подбирают
достаточно специфическую химическую
реакцию, воздействующую на отдельные
нуклеотиды, и наблюдают, как это
отзывается на способности тРНК присоединять
аминокислоту — на ее акцепторной
функции. В большинстве случаев акцепторная
функция при этом в той или иной степени
утрачивается. Если известно, какое
именно звено в молекуле тРНК изменено, то
можно сделать вывод о его возможной
роли в акцепторной функции.
Существует много специфических
реакций, которые нашли применение при
функциональных исследованиях у нас и за
рубежом. Однако до сих пор все они
проводились на препаратах суммарной
тРНК — смеси многих различных тРНК.
В этих условиях нельзя было выделить
продукт реакции и установить точно, какие
же части молекулы изменены. Между тем,
как вытекает из всего сказанного, именно
расположение модифицированных звеньев
и служит решающим фактором в
изменении функции. Зная, какое основание
подверглось химической модификации, но не
зная его положения в молекуле, нельзя
ничего сказать о причине функционального
изменения.
Только недавно химическую
модификацию тРНК стали изучать на
индивидуальных препаратах. Это сделали,
например, на аланиновой тРНК американцы
Р. Холли и М. Бростоф. Пока эти
исследования только подтвердили
предположение, что в молекуле тРНК реагируют
прежде всего нуклеотиды, расположенные
в петле антикодона, и свободный конец
тРНК. Почему так получается, понятно:
эти участки молекулы не защищены
водородными связями и открыты действию
химических агентов.
Но химические модификации — не
единственный способ, который может
привести нас к пониманию связи структуры
и функции тРНК. Есть и другой подход. Он
заключается в том, чтобы тем или иным
образом рассечь молекулу тРНК на куски
и исследовать по отдельности их
способность взаимодействовать с активирующим
ферментом. Такой подход можно назвать
«методом разрезанной молекулы». Он был
придуман коллективом нашей лаборатории
и в первое время казался нам подлинным
открытием. Мысль о нем возникла еще
давно и окончательно сформировалась,
когда мы убедились в возможности
расшифровать последовательность
нуклеотидов валиновой тРНК. Предвидя успешное
23
завершение этого исследования, мы
поставили перед собой задачу: найти и заранее
отработать свои пути изучения функции
тРНК на основе точно известной
структуры. Тогда и возникла мысль испытать
функциональную (прежде всего
акцепторную) способность обломков молекулы
тРНК, которые мы научились получать
и состав которых был нам точно известен.
Правда, затем наступило некоторое
разочарование. Оглядевшись, мы заметили,
что нечто подобное было уже сказано или
сделано другими (не новая ситуация для
современной молекулярной биологии!).
Может быть, самым ярким таким
примером могут служить опыты М. Ниренберга
и П. Ледера (США), проведенные совсем
с другой целью — еще раз проверить
правильность расшифровки кода
информационной РНК. Авторы этих опытов брали
рибосомы, тРНК с присоединенной к ней
меченой аминокислотой и, внося в
реакционную смесь искусственно
приготовленные тройки нуклеотидов, соответствующие
кодонам информационной РНК, наблюдали
за ходом связывания тРНК с рибосомой.
Оказалось, что тринуклеотиды усиливают
это связывание, и притом специфически:
каждая тРНК «отзывается» только на тот
тринуклеотид, который является ее ко-
доном.
В этих экспериментах имитировалась
самая начальная стадия белкового
синтеза— момент присоединения тРНК,
«нагруженной» аминокислотой, к рибосоме. При
обычном течении белкового синтеза за
этим следует включение аминокислоты
в строящуюся белковую цепь. Здесь этого
завершающего акта не происходило из-за
отсутствия нужных для этого ферментов
и вообще многих условий, необходимых
для синтеза белка. Но для нас важно
другое. Оказывается, и маленький кусочек
информационной РНК — всего около Viooo
ее цепи — способен, пусть частично, но все
же выполнять функцию целой молекулы.
Использование разработанного нами
метода было намечено как главный путь
изучения функциональной топографии
тРНК. Пока еще рано говорить, насколько
применим такой подход к ее сложной
молекуле. Не исключено, что создать
«работоспособные» структуры из обломков
линейной молекулы вообще невозможно.
В этом случае избранный нами путь скоро
может закончиться тупиком. Только опыт
и многочисленные, упорные попытки
способны дать окончательный ответ на этот
вопрос. Однако уже на первых шагах
исследований в этом направлении нам
удалось получить результаты, которые
интересны сами по себе, независимо от того,
окажется ли плодотворным метод
разрезанной молекулы в целом.
РАЗРЕЗАННАЯ МОЛЕКУЛА
Мы уже говорили, что область антикодона
валиновой тРНК, как и всех других
тРНК,— самый уязвимый участок
молекулы. Именно его атакуют прежде всего
различные ферменты, способные разрывать
те или иные фосфодиэфирные связи.
Применяя один из них — рибонуклеазу, гидро-
лизующую связи по остаткам гуаниловой
и инозиновои кислот, и делая это в
заведомо неблагоприятных для фермента
условиях, нам удалось разорвать только
одну-единственную связь в молекуле
валиновой тРНК и именно связь между
остатками инозиновои и адениловои кислот
в пределах антикодона.
В результате молекула разрывается на
две половины почти равной длины. Эти
половины можно разделить и посмотреть,
сохраняют ли они способность
присоединять в присутствии надлежащего
фермента аминокислоту валин, как это делает
целая молекула тРНК. (Само собой
разумеется, что валин способен присоединяться
только к той половине молекулы тРНК,
которая несет концевую адениловую
кислоту; но важно выяснить, нужна ли для
его присоединения к этой половине
молекулы другая ее половина.)
Практически этот интересный
эксперимент, имеющий принципиальное значение
для понимания общих закономерностей
функционирования тРНК, мы проводим
так. Берем чистый препарат валиновой
тРНК и определяем его способность
присоединять валин, меченный
радиоактивным углеродом (С14-валин). Количество
присоединенной аминокислоты можно
выразить в импульсах счетчика на
миллиграмм препарата в минуту. 1 мг валиновой
тРНК у нас присоединял такое количество
С14-валина, которое дает в минуту
50 000 импульсов.
Потом мы подвергаем валиновую тРНК
действию гуаниловой рибонуклеазы, о
которой мы говорили выше. Фосфодиэфирная
связь между остатками инозиновои и
адениловои кислот разрывается. При помощи
24
Схема опыта с разрезанной
молекулой. А — акцепторная,
НА — неакцепторная половина
9ВАЛИНОВАЯ тРНК
АКЦЕПТОРНАЯ АКТИВНОСТЬ
50000 и/ип./zvihh мг
А 3 НА Расщепление гуаниловои
| РИБОНУКЛЕАЗОЙ
УУУ^~ Разделение половин на ионо-
ф ОБМЕННИКЕ
Я * °рнк
А НА тРНК
зооооимп/минуиг ОПРЕДЕЛЕНИЕ
АКЦЕПТОРНОЙ АКТИВНОСТИ
4 +
НЕТ НЕТ
Выделение продуктов
ГИДРОЛИЗА
Y
СМЕШЕНИЕ П0Л0ВИН/О5РАЗО-
С» ВАНИЕ СЛИТНОЙ МОЛЕКУЛЫ
?1пАиТп /ми« мг Определение акцел-
50000имп/лчш мг Юрной дшвности
-о—о— Разделение смеси на
1 * И0НОО5/ИЕННИКЕ
^ нАЕт метки ^/ДЕЛЕНИЕ ПОЛОВИН
Определение метки
500С0ил^п//иин-/иг
ионообменника мы отделяем полученные
половины молекулы друг от друга и от ва-
линовой тРНК, оставшейся нерасщеплен-
ной. Теперь можно снова определить
акцепторную активность, то есть способность
каждой фракции присоединять валин.
Оказывается, что если нерасщепленная
валиновая тРНК сохраняет акцепторную
активность практически на прежнем
уровне, то половины молекулы ее совершенно
утрачивают. Присоединять валин
неспособна даже половина, содержащая
концевую адениловую кислоту, хотя она,
казалось бы, и могла это делать!
Затем мы проделываем очень простую
операцию (тем не менее это и есть
кульминация всего опыта). Мы смешиваем
растворы обеих половин молекулы тРНК и снова
определяем акцепторную активность
смеси. Многократные опыты показывают, что
способность присоединять валин
полностью восстанавливается. Это — самый
неожиданный и важный результат
эксперимента.
Но, может быть, при смешивании
растворов половины молекулы тРНК
попросту вновь соединяются, и полную
акцепторную активность, замеченную нами,
проявляют обыкновенные, не разрезанные
молекулы?
Чтобы это проверить, мы и проводим
заключительную часть эксперимента.
Смесь половин молекулы, уже
«заряженную» аминокислотой, мы снова
пропускаем через ионообменник. Разорвать фосфо-
диэфирную связь ионообменник не в
состоянии— это не фермент. И мы снова
получаем разделенные половины молекулы
(что было бы невозможно, если бы
химическая связь была восстановлена), а
меченая аминокислота, как и следовало
ожидать, оказывается привязанной к той из
них, которая содержит концевую
адениловую кислоту. Значит, химического
соединения половин молекулы в нашем опыте
не происходит.
Как можно истолковать наш опыт?
Прежде всего совершенно очевидно, что
для присоединения аминокислоты
необходимы обе половины молекулы, хотя сама
химическая реакция присоединения
происходит только в одной из них.
По-видимому, обе половины молекулы нужны для
взаимодействия с активирующим
ферментом, соединение с которым предшествует
реакции тРНК с аминокислотой. Можно
заключить, что участок молекулы,
реагирующий с ферментом, охватывает обе
половины молекулы тРНК, хотя мы и не
знаем, как далеко он распространяется и
какие нуклеотиды в него входят.
У нас есть все основания думать, что
конфигурация половин, ведущих
самостоятельное существование (и по
существу являющихся новыми молекулами),
резко отличается от той формы, которую
они имели в составе исходной молекулы
тРНК. В этих половинах (особенно в
неакцепторной) сохраняется очень мало
водородных связей, которые и придают им
в составе исходной молекулы тРНК
характерную конфигурацию. Скорее всего эти
молекулы в растворе имеют форму мало
упорядоченных клубков. Это
обстоятельство не может не иметь значения при
взаимодействии половинок с ферментом,
поскольку точное соответствие
конфигурации фермента и субстрата — совершенно
необходимая предпосылка каталитической
реакции.
Когда же мы снова смешиваем
половинки молекулы, то, как показали наши
физико-химические измерения, ее
нормальная форма в какой-то степени
восстанавливается — образуется «сшитая»
молекула, хотя одна из ее связей так
и остается разорванной. Мы можем с зна-
4 Химия и Жизнь, № 4
25
Конфигурация молекулы тРНК
и ее половин
ГУДОИЛОВАЯ
РНК-АЗА
ПРОИЗОШЕЛ
РАЗРЫВ
СВЯЗИ
Молекула
сохраняет
ПРЕЖНЮЮ
<РОРМУ
Половины
РАЗАЕЛЕНЫ
Их ФОРМА
ИЗМЕНИЛАСЬ
Нагревание
Нити
ОБРАЗУЮТ
КЛУБОК
чительнои долей вероятности представить
себе, что при этом происходит в растворе,
когда благодаря тепловым движениям
половины молекулы приходят в контакт
друг с другом. Сами по себе водородные
связи слабы (их свободная энергия
примерно в 10 раз меньше энергии обычной
химической связи) и не отличаются высокой
избирательностью. Но когда они занимают
целые обширные участки молекулы, эти
слабые и неспецифические взаимодействия
становятся сильными и специфическими.
Энергия их оказывается достаточной для
того, чтобы преодолеть силы
отталкивания отрицательно заряженных фосфатных
остатков и беспорядочные тепловые
движения. Как выяснилось, связи эти
настолько специфичны, что каждая половина
находит своего партнера даже и в том
случае, когда в растворе присутствуют
половины молекул других тРНК (а такие
опыты были сделаны).
Все это приводит нас к мысли, что уже
в растворе, содержащем половины
молекул валиновой тРНК, происходит ее
самосборка. Это второе очень важное следствие
описанного опыта. Такой процесс — не
единственный в своем роде; мы можем
найти примеры, показывающие, что
самосборка молекул биополимеров,
разорванных на части,— их общее свойство.
Будущее покажет, можно ли
исследовать функциональную активность
валиновой тРНК, переходя от половин ее
молекулы к более мелким обломкам. Предстоит
еще попытаться проделать аналогичные
опыты с другими тРНК; попробовать
получить гибридные молекулы, состоящие
из половин разных тРНК. Если это не
удастся, придется придумывать
что-нибудь другое. Нужно трезво учитывать
возможность неудач и не огорчаться ими:
наука редко делает приятные подарки. Но
мы не сомневаемся, что рано или поздно
все трудности будут преодолены, и
механизм функционирования транспортных
РНК будет раскрыт во всех своих деталях.
НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ
ХИРУРГИЧЕСКИЕ ИНСТРУМЕНТЫ
ИЗ СИНТЕТИЧЕСКИХ
МАТЕРИАЛОВ
Инструменты, изготовленные из
ультрамида — смолы на основе
поликонденсации себациновой
кислоты с гексаметиленд
намином, — обладают свойством,
необходимым хирургам, — они
просвечиваются рентгеновскими
лучами и оставляют на снимках
только совсем слабые тени, не
затемняющие операционного поля.
Ультрамид дешев и легко
стерилизуется. Из него можно
изготовлять инструменты для
одноразового пользования.
Инструменты из ультрамида герметически
запаковывают в пленку из
синтетического материала и
стерилизуют облучением. Такие
инструменты, так же как шприцы для
одноразового использования,
можно употреблять при
катастрофах и несчастных случаях.
ЗЕЛЕНАЯ ПИЩЕВАЯ КРАСКА
С давних пор в некоторых
странах приготовляют зеленый
краситель для тканей следующим
способом: размолотые зерна
зеленого кофе оставляют на ночь
в яичном белке. Когда химики
исследовали этот раствор, они
обнаружили, что красящее
вещество— виридиновая кислота,
которая образуется при
взаимодействии содержащейся в зернах
кофе хлорогеновой кислоты с
белком.
Немецкие ученые разработали
способ получения синтетической
виридиновой кислоты, основанный
на взаимодействии хлорогеновой
кислоты с аммиаком или
карбонатом аммония.
Так как новый синтетический
краситель состоит из
биологически разлагаемого белка и
природной кислоты, встречающейся
во многих растениях и не опасной
для человека, ученые
рекомендуют применять виридиновую
кислоту как краску для пищевой
промышленности. Ярко-зеленая
интенсивная окраска виридиновой
кислоты обогатит палитру красок
пищевых продуктов, для
окрашивания которых в зеленый цвет до
сих пор разрешалось использовать
только хлорофилл.
26
КЛАССИКА
НАУКИ
Атомы, лучи, кванты
Кандидат физико-математических наук
Л. И. ПОНОМАРЕВ,
гор. Дубна
Конец прошлого и начало нашего века
часто называют героическим периодом
физики. Это было время, когда каждый год
приносил неожиданные открытия,
фундаментальность которых очевидна даже
сейчас, более полувека спустя. Одно из таких
открытий связано все с той же трубкой
Это — третья статья из серии, посвященной
квантовой механике. Первые две были
напечатаны в № 1 и 2 за этот год.
Крукса: в 1895 году Вильгельм Конрад
Рентген A845—1923), изучая катодные
лучи, обнаружил новое излучение, которое
возникало в том месте анода, куда падал
пучок электронов.
Свойства этого излучения были
необычны, даже пугающе необычны: оно без
труда лронизывало человеческое тело и даже
проникало сквозь закрытые дверцы
сейфов. Только в 1912 году немецкие физики
Фридрих и Книппинг по предложению
4*
27
Макса фон Лауэ A879—1960) пропустили
эти лучи через кристалл и обнаружили
у них способность к интерференции и
дифракции. А это означало, что Х-лучи (как
их вначале назвал Рентген) — не поток
частиц, а волны, только очень короткие:
всего от 10"' до 10 ~10 см.
Несколько месяцев спустя, в 1896 году,
Антуан Анри Беккерель A852—1908)
открыл новый тип излучения, еще более
странный: это излучение возникало
самопроизвольно в куске урановой руды и
состояло из положительно заряженных
частиц, которые Резерфорд назвал а
-частицами. Они оказались вчетверо тяжелее
атомов водорода, причем заряд их был
равен двум зарядам электрона.
Некоторые вещества (например ZnS)
начинали светиться, если на них попадал
пучок «-частиц. Это позволило все тому
же Уильяму Круксу в 1903 году изобрести
спинтарископ — прибор, который позволял
видеть вспышки от единичных о. -частиц,
попадавших на экран из сернистого цинка.
Эти два открытия хорошо известны,
и мы о них только напомнили.
АТОМЫ
В начале века в физике бытовали самые
разные и часто фантастические представ-
28
«...Вся совокупность научных данных не
оставляет места для сомнения в существовании атомов
и молекул.»
В. И. Ленин, 1908 г.
ления о строении атома. Например, Линде-
ман, ректор Мюнхенского университета,
в 1905 году утверждал, что «...атом
кислорода имеет форму кольца, а атом серы —
форму лепешки». Но большинство
физиков пришло к выводу, что прав
Дж. Дж.Томсон: атом — это равномерно
заряженный положительный шар диаметром
Ю~8 см, внутри которого плавают
отрицательные электроны (или корпёсли, писали
в русских изданиях начала века), размеры
которых 103 см. Сам Джи-Джи — как его
называли ученики — относился к своей
модели без энтузиазма. А некоторые
физики представляли себе атом совсем иначе.
Одни об этом говорили вслух: среди них
были Джонстон Стоней, который еше
в 1891 году предполагал, что «...электроны
движутся вокруг атома, подобно
спутникам планет»; Жан Перрен, который
в 1901 году пытался представить себе
«нуклеарно-планетарную структуру
атома»; японский физик Нагаока и сэр
Оливер Лодж, утверждавшие в 1902 году, что
«...пространства внутри атома
чрезвычайно громадны по сравнению с величинами
самих, образующих его, электрических
ядрышек. Другими словами, атом
представляет своего рода сложную
астрономическую систему, подобную кольцу
Сатурна».
Другие, например, Петр Николаевич
Лебедев, доверяли подобные мысли только
своему дневнику. В 1887 году он
предполагал, что частота излучения атомов
определяется частотой обращения электрона
по орбите. А голос Николая Морозова был
заперт в стенах Петропавловской крепости.
Но ни один сторонник идеи
планетарного атома не мог доказать главного:
устойчивости системы, состоящей из
положительной сердцевины и электронов,
которые вокруг нее вращаются.
Действительно, на круговой орбите
электрон движется ускоренно и,
следовательно, по теории Максвелла — Лоренца,
должен терять энергию на излучение. Зная
размеры атома (-^Ю-8 см), легко оценить
скорость (—2-108 см/сек) движения
электрона по орбите и величину центростреми-
тельного ускорения ( -^Ю25 см/сек2). При
таких ускорениях излучение должно быть
настолько интенсивным, что уже через
10 ~8 сек электрон упадет на
положительный центр притяжения. Ничего похожего
в природе не происходит: атом не только
устойчив, но и восстанавливает свою
структуру после разрушений.
Это и был основной аргумент в пользу
модели Томсона, с точки зрения чистой
логики вполне убедительный. Однако в
физике уже более двухсот лет принято
правило: окончательный выбор между
гипотезами вправе сделать только опыт. Такой
опыт поставил в 1909 году Эрнст Резер-
форд A871—1937) со своими
«мальчиками».
Представьте себе крупного и шумного
человека, который принужден сидеть
в темной комнате и, глядя в микроскоп,
считать на экране спинтарископа вспышки
(сцинтилляции) от я-частиц. Работа
изнурительная: уже через две минуты глаза
устают. Ему помогают опытный исследо-
29
«Разрушимость атома, неисчерпаемость его,
изменчивость всех форм материи и ее движения
всегда были опорой диалектического
материализма.»
В. И. Ленин, 1908 г.
ватель Ганс Гейгер и двадцатилетний
лаборант Эрнст Марсден. Их прибор
несложен: ампула с радием-С, испускающим
ос-частицы, диафрагма, которая выделяет
из них узкий пучок и направляет его на
экран из сернистого цинка, и микроскоп,
через который наблюдают сцинтилляции
«-частиц на экране. Место появления
очередной сцинтилляции предугадать
нельзя — они возникают беспорядочно, но так,
что в целом на экране получается довольно
резкое изображение щели диафрагмы.
Однако, если на пути а -частиц
поставить металлическую фольгу, то вместо
резкого изображения щели на экране
возникает размытая полоса. Эта полоса была
лишь немного шире изображения щели,
полученного в первом случае: з-частицы
отклонялись от прямого пути в среднем
всего на 2°. Однако несложный расчет
показал: для того чтобы объяснить даже
такие небольшие отклонения, нужно
допустить, что в атомах фольги могут
возникать огромные электрические поля —
свыше 200 000 в/см.
В положительном шаре атома Томсона
таких напряжений быть не может.
Столкновения с электронами также не в счет:
ведь по сравнению с ними а -частица,
летящая со скоростью 20 км/сек,— все равно,
что пушечное ядро рядом с горошиной.
И все же пути ос-частиц искривлялись.
В поисках разгадки Марсден предложил
проверить: а не могут ли а -частицы
отражаться от фольги назад? С точки зрения
модели Томсона, опыт вполне
бессмысленный: пушечное ядро не может отразиться
от горошины. Результат был
неожиданным, но вполне убедительным, хотя
поверить в это было трудно: а -частицы
отражались от фольги.
Прошло два года. За это время Гейгер
и Марсден сосчитали более миллиона
сцинтилляций и доказали: отражается назад
примерно одна а -частица из 8000.
Только теперь, 7 марта 1911 года,
Манчестерское философское общество — то
самое, президентом которого был когда-то
Джон Дальтон — услышало доклад Рэзер-
форда: «Рассеяние ос- и ?-лучей и строе-
ние атома». В тот день слушатели узнали,
что атом подобен солнечной системе: он
состоит из ядра и электронов, которые
вращаются вокруг него на расстояниях
Ю~8 см. Размеры ядра очень малы — всего
10 ~13 — 10 ~12 см, но в нем заключена
практически вся масса атома. Заряд ядра
положителен и по величине равен примерно
половине атомного веса элемента.
Сравнение с солнечной системой не случайно:
диаметр солнца A,4 -10° км) примерно во
столько же раз меньше размеров
солнечной системы F • 109 км), во сколько
диаметры ядер (-^10~12 см) меньше размеров
атома (~~10~а см).
Мы настолько привыкли к новым
понятиям, что объясняя электронику,
ссылаемся на телевизор, а рассказывая о
механике, приводим в пример паровоз.
Поэтому сейчас нам трудно понять тогдашнее
недоумение людей, по силе ума подобных
Резерфорду. Действительно, ведь все так
прозрачно: просто * -частица отражается
от ядер атомов. И к этой картине мы
привыкаем с детства. Но чтобы нарисовать
ее в первый раз, необходима смелость,
добытая большим трудом. Прежде, чем эта
картина стала известна каждому,
пришлось не только сосчитать свыше
миллиона сцинтилляций: нужно было (как
вспоминал недавно Гейгер) «...преодолеть такие
трудности, смысл которых мы сейчас даже
понять не в состоянии»; нужно было
сначала в течение десяти (!) лет доказывать,
что z -частицы — не что иное, как атомы
гелия, потерявшие два электрона.
Доказать было непросто, и Шведская академия
наук хорошо понимала это, когда в 1908
году присудила Резерфорду Нобелевскую
премию за исследование химической
природы *-частиц. Обо всем этом постепенно
забыли: результат был важнее и проще,
чем путь, к нему приведший.
Сообщение Резерфорда физики
приняли сдержанно. Сам он в течение двух лет
также не очень сильно настаивал на своей
модели, хотя и верил в безошибочность
опытов, которые к ней привели. Причина
была все та же: если верить
электродинамике, такая система существовать не
может. Приходилось выбирать: либо
электродинамика, либо планетарный атом. И
физики молча выбрали первое. Молча, потому
что опыты Резерфорда нельзя было ни
забыть, ни опровергнуть. Физика атома
зашла в тупик. И чтобы выйти из него,
нужен был Нильс Бор.
«Новейшие открытия естествознания — радий,
электроны, превращение элементов —
замечательно подтвердили диалектический материализм
Маркса...»
В. И. Ленин, 1913 г.
ЛУЧИ
Независимо от гипотез о строении атома,
физики рано поняли, что знания о нем
можно получить, изучая его линейчатый
спектр. (Так музыкант по тону струны
определяет ее длину, а инструмент узнает
по аккорду). В физике всякое изучение
в конечном итоге сводится к измерению.
Поэтому прежде всего необходимо было
научиться измерять длины волн как можно
точнее, то есть еще пристальнее, чем
Фраунгофер, исследовать структуру
линейчатого спектра.
На призменном спектрографе Кирхгофа
и Бунзена этого сделать уже было нельзя.
Стеклянную призму в нем сменила
дифракционная решетка, которую
значительно усовершенствовал Генри Роулэнд
A848—1901) — представитель тогда еще
молодой американской науки.
С помощью этого прибора в течение
нескольких десятилетий трудами Карла
Рунге A856—1927), Фридриха Кайзера
A853—1940) и особенно лаборатории
Фридриха Пашена A865—1947) в Тюбингене
были точно измерены десятки тысяч
спектральных линий различных элементов
и аккуратно записаны в длинные таблицы.
(К 1913 году общее число работ по
спектральному анализу перевалило за 50 000.)
В частности, оказалось, что знаменитая
желтая линия D в спектре натрия состоит
из двух очень близко расположенных
линий: D! = 5895,9236 А и D2 = 5889,9504 А.
Но высшая задача любой науки не
в том, чтобы накапливать факты, а в том,
чтобы установить связи между явлениями
и найти их причину. Всем было ясно, что
в этих длинных таблицах заключена
огромная информация о структуре атома.
Но как ее оттуда извлечь? Вероятно, такие
же чувства испытывали египтологи до
Шампольона, глядя на иероглифы.
Первый шаг всегда труден и незаметен.
Поэтому об Иоганне Якобе Бальмере
A825—1898), который впервые обнаружил
30
какие-то связи в этом хаосе чисел, мы
знаем очень мало. Известно, что был он
" школьным учителем в одном из
швейцарских кантонов и было ему 60 лет, когда он
пришел к своему открытию. Он заметил,
что четыре линии в видимой части спектра
водорода расположены не беспорядочно,
а образуют серию, которую можно описать
одной формулой:
Лп — Ло- п2 ■ - 4 '
где п = 3, 4, 5, 6, Х0= 3645,7 А.
Это простое соотношение заслуживает
всяческого внимания. Дело в том, что
оно — точное, в чем каждый желающий
может легко убедиться сам.
Такие совпадения не могут быть
случайными, и потому открытие Бальмера
не затерялось в архивах.
В 1888 году Рунге заметил, что формула
Бальмера упрощается, если в нее вместо
с
длины волны подставлять ее частоту v=у:
А в 1890 году шведский физик Иоганн
Роберт Ридберг A854—1919) предложил
более общую формулу, чем Бальмер:
^=cR(^-i)-
«...Диалектический материализм настаивает на
временном, относительном, приблизительном
характере всех этих вех познания природы
прогрессирующей наукой человека. Электрон так же
неисчерпаем, как и атом, природа
бесконечна, но она бесконечно существуе т...»
В. И. Ленин, 1908 г.
(Здесь: с = 3 • 1010 см/сек — скорость света,
тип — целые числа, а число R =
= 109 677,576 см называется с тех пор
постоянной Ридберга для атома водорода).
Полагая в этой формуле m = 2, можно
вычислить всю серию Бальмера, измеренную
впоследствии вплоть до п = 31. В общем
случае частоту любой линии в спектре
водорода можно записать в виде разности
двух чисел — термов Тт и Т п
v=Tm-Tn,
где TV -jjr ' Т пг=-ц2- ' a m и п —
целые числа.
Продолжая работы Ридберга, молодой,
рано умерший швейцарский ученый
Вальтер Ритц A878—1909) в 1908 году
сформулировал так называемый комбинационный
принцип: частоту v произвольной линии
в спектре любого атома можно
представить как разность двух термов Тт и Тп
vmn = Tm Тп ,
даже в том случае, когда отдельный терм
Т п уже нельзя записать в таком простом
виде, как для атома водорода.
На первый взгляд, в этом нет никакого
выигрыша: просто от набора частот мы
перешли к набору термов. Однако это не
так: попытайтесь прочесть книгу, в
которой нет промежутков между словами, и вы
сразу почувствуете разницу. Особенно,
если эта книга на неизвестном языке.
Кроме того, чисел стало значительно меньше:
чтобы определить частоты 50 линий
водорода, которые были известны в начале
века, достаточно задать десяток термов.
Неожиданно в хаосе чисел
обнаружилась система. Беспорядочный набор линий
распался на серии. В непонятной книге
стали различать отдельные слова. В
простейшем случае — в атоме водорода
удалось разглядеть даже буквы, из которых
они составлены. Однако смысл слов и
происхождение букв по-прежнему оставались
неизвестными: иероглифы еще не
заговорили, хотя и не казались теперь столь
загадочными.
31
Это стремление осмыслить структуру
спектра, действительно, напоминало
попытку почти вслепую расшифровать
незнакомый текст. Утомительная работа
длилась больше четверти века, и отсутствие
общей идеи отталкивало от нее многие
глубокие умы. Необходимо было найти
ключ к шифру. Это сделал Нильс Бор в
1913 году.
КВАНТЫ
Излучение возникает внутри атома,
однако, покинув его, существует независимо.
Иногда оно состоит из волн одинаковой
длины — такое излучение называют
монохроматическим. Линейчатый спектр атома
состоит из набора монохроматических
лучей, и наборы эти различны для разных
атомов.
До сих пор нас интересовала только
одна характеристика волн — их частота v.
Однако лучи — сложное явление, и
свойства их нельзя свести только к частоте
излучения. Солнечный луч прозрачен, но
вполне материален, — он даже имеет вес:
каждую минуту на 1 см2 поверхности
земли падает 2 • Ю5 г света. На первый
взгляд неощутимо мало, но это означает,
что за год на Землю упадет 80 000 тонн
солнечных лучей (и это всего лишь две
миллиардных доли — 2 -1(Г9 от общего
потока, излучаемого Солнцем). Эти тонны
лучей осуществляют круговорот веществ
в природе, так что в конечном итоге вся
жизнь на Земле возможна только под
Солнцем.
Действие излучения легче всего
сопоставлять с морскими волнами,
набегающими на берег: после работ Христиана
Гюйгенса A629—1695) и Огюстена Жана
Френеля A788—1827) такая аналогия
стала бесспорной. Каждый год приносил
новые этому доказательства: в явлениях
интерференции, дифракции и поляризации.
В 1873 году Джемс Клерк Максвелл A831—
1879) теоретически предсказал, что свет,
падая на поверхность тел, должен
оказывать на них давление (также в полном
согласии с нашей аналогией). Световое
давление— очень тонкий эффект, но Петр
Николаевич Лебедев A866—1912) в 1899
году все-таки обнаружил его
экспериментально. Казалось, теперь волновая
природа света доказана настолько надежно, что
всякие дальнейшие опыты для ее проверки
не имеют смысла.
К счастью, опыты в физике ставят не
только для проверки теорий. И в то время,
когда Лебедев завершал свой знаменитый
опыт, уже существовал другой опыт, столь
же тщательный, но более непонятный.
В 1887 году Генрих Рудольф Герц A857—
1894) (тот самый, который доказал
волновую природу электромагнитного излучения
и тем самым справедливость всей
электродинамики Максвелла) обнаружил явление,
которое впоследствии назвали
фотоэффектом. Суть его в следующем: если свет
ртутной лампы (теперь мы такие лампы
называем кварцевыми) направить на металл
натрий, то с поверхности металла
вылетают электроны. В конце века большая
часть физиков уже ясно сознавала, что
атсм сложен, и потому само по себе это
явление никого не удивило. Довольно
быстро все согласились с тем, что
электроны в опыте Герца вылетают из атомов
натрия под действием излучения
кварцевой лампы.
Странно и непонятно было другое:
законы этого явления, которые установили
Филипп Ленард A862—1947) и Александр
Григорьевич Столетов A839—1896) на
рубеже XX века. Эти ученые измеряли
число выбитых электронов и их скорость
в зависимости от интенсивности и частоты
падающего излучения.
Как мы уже знаем, лучи, которые
возникают внутри атомов, различаются между
собой не только длиной волны А , но также
амплитудой А. Причем интенсивность луча
I измеряется квадратом амплитуды: I =|А|2.
Это ясно видно на спектрограммах:
некоторые линии там значительно ярче
других, например, в желтом дублете натрия
линия D2 вдвое ярче линии Di.
Наш предыдущий опыт и знания о
волнах подсказывают нам, что действие волн
тем заметнее, чем больше их амплитуда.
Чтобы убедиться в этом, достаточно выйти
на берег моря во время шторма.
Интенсивность излучения можно увеличить и по-
другому: увеличивая число излучающих
атомов. Поэтому, если вместо одной
ртутной лампы взять две, три, десять, то
энергия излучения и его интенсивность
возрастет во столько же раз. Естественно
ожидать, что и скорость выбитых электронов
вырастет в такой же пропорции.
Но скорость электронов оставалась
прежней, менялось лишь число их — вот
первая несообразность, которая ожидала
ученых в конце опытов. Зато эта скорость
82
зависела от частоты падающего излучения
и притом сильно. Кварцевая лампа
излучает фиолетовые и ультрафиолетовые
лучи. Но оказалось, что если вместо них на
поверхность натрия направить пучок
красных лучей, то электроны не вылетят
вообще. «Если излучение—волновой
процесс (а это строго доказано), такого не
может быть», — утверждали одни. «Но
ведь это происходит!» — возражали
другие.
Если бы несколько прибрежных утесов
неожиданно обрушились на ваших глазах,
почти наверное вы бы стали искать
внешние причины такой катастрофы. Конечно,
волны моря постепенно размывают берег,
и время от времени утесы рушатся, но все
знают, как редко это бывает. Однако, если,
обернувшись к морю, вы обнаружите там
военный корабль, который ведет по берегу
пальбу из орудий главного калибра, вы
сразу догадаетесь, что причина внезапных
разрушений не волны, а снаряды, хотя их
энергия и меньше, чем общая энергия
морских волн. Однако энергия волн
равномерно распределена по всему побережью,
и нужны века, чтобы мы увидели
результаты их ежедневной работы. По сравнению
с этой работой энергия снаряда ничтожна,
зато она сосредоточена в малом объеме
и выделяется мгновенно. Если к тому же
снаряд достаточно велик — он разрушит
утес. Последнее важно: действительно, все
свойства снаряда, кроме размеров,
присущи и пуле, однако сокрушить скалу ей
не под силу.
Примерно так рассуждал Эйнштейн,
когда предложил свое объяснение явлений
фотоэффекта. Он знал об открытии Планка,
но для Эйнштейна с его непредвзятой
манерой мышления гипотеза о квантах света
не казалась столь ужасной, как самому
Планку. Поэтому он был первый, кто не
только поверил в нее, но и применил для
объяснения новых опытов. Эйнштейн
утверждал: свет не только испускается
квантами, как того требовала гипотеза
Планка, но и распространяется так же —
квантами. Потому свет, падающий на
поверхность металла, подобен не морским
волнам, но артиллерийским снарядам.
Причем каждый такой снаряд-квант может
выбить из атома только один электрон.
Согласно Планку (вспомните первую
статью), энергия Е снаряда-кванта равна
liv. По мысли Эйнштейна, часть ее Р
расходуется на то, чтобы вырвать электрон из
атома, а остальная часть — на то, чтобы
разогнать его до скорости v, т. е. сообщить
IT1V2
ему кинетическую энергию Т = -у-. Оба
эти утверждения можно коротко записать
в виде простого уравнения:
mv2
Стоит принять эту гипотезу — и все
явления фотоэффекта проясняются.
Действительно, пока размеры снарядов малы
(красный свет), они не могут выбросить
электрон из атома (hv< P)y как бы много
'*> --$
z5* V£>
Рисунок
художника
ДЮБУ
(Франция)
5 Химия и Жизнь, № 4
33
мы их не посылали. Если же мы начнем
увеличивать их размеры (фиолетовый
свет), то в конце концов их энергия станет
достаточной для выбивания электронов
(hv > Р). Но по-прежнему их скорость
будет зависеть только от величины
квантов (т. е. частоты ^), а не от их числа.
Шестнадцать лет спустя глубокую
простоту уравнения Эйнштейна Шведская
академия наук отметила Нобелевской
премией. Но в 1905 году, когда уравнение было
написано впервые, на него нападали все,
даже Планк. Он любил Эйнштейна и
потому, убеждая прусское министерство
просвещения пригласить его на работу в
Берлин, просил «...не слишком сильно ставить
ему в упрек» гипотезы относительно
явлений фотоэффекта.
Планка можно понять: только что
вопреки своим убеждениям и желанию он
ввел в физику квант действия h. Лишь
постепенно он осознал неизбежность зтого
шага, но даже в 1909 году признавался
Эйнштейну: «Я еще плохо верю в
реальность световых квант». Однако дело было
сделано: как говорил Эйнштейн двадцать
лет спустя, «...Планк посадил в ухо
физикам блоху», и она не давала им покоя, хотя
они и пытались не замечать ее. Во всяком
случае Планк постарался ввести квант
действия так, чтобы не пострадала
волновая оптика — здание чрезвычайной
красоты, созданное в течение двух столетий.
Поэтому, согласно Планку, свет только
испускается квантами, но
распространяется по-прежнему как волна-—только
в этом случае удавалось сохранить все
результаты волновой оптики.
А Эйнштейн поступал так, как будто
до него вообще не существовало физики,
или, по крайней мере, как человек, ничего
не знающий об истинной природе света.
Здесь сказалась замечательная
особенность Эйнштейна: в совершенстве владея
логикой, он больше доверял интуиции
и фактам. Для него не было случайных
фактов в физике. Поэтому в явлениях
фотоэффекта он видел не досадное
исключение из правил волновой оптики, а сигнал
природы о существовании еще
неизвестных, но глубоких законов.
Так уж случилось, что исторически
сначала были изучены волновые свойства
света. Только в явлениях фотоэффекта
физики впервые столкнулись с его
корпускулярными свойствами. У большинства
из них инерция мышления была настолько
велика, что они отказались этому верить.
«Не может быть!» — повторяли они
подобно фермеру, увидевшему жирафа впервые
в жизни.
Эйнштейн, конечно, знал историю
оптики не хуже других. Но его независимый
ум равнодушно относился к ее праву
первородства. Для него не имели значения все
прежние заслуги оптики, если они не
могли объяснить единственный, но
бесспорный опыт. Он глубоко, почти религиозно,
верил в единство природы, и для него
один такой опыт значил не меньше, чем
вся история оптики. А его честность не
позволила ему пройти мимо неугодного
факта.
В науке по-настоящему опасны только
неверные опыты: опытам принято верить.
Но любую гипотезу всегда тщательно
проверяют. Даже если она окажется ложной,
опыты, которые опровергли ее, часто
приводят к результатам более ценным, чем
сама гипотеза. Проверили и гипотезу
Эйнштейна — она оказалась истинной.
В 1911 году Роберт Милликен,
проверяя уравнение Эйнштейна, определил из
него величину постоянной Планка h. Она
совпала с тем значением, которое получил
Планк из теории теплового излучения.
А вскоре поставили опыт, идея которого
в точности аналогична картине
разрушения утесов на берегу моря. И снова
оказался прав Эйнштейн, а не признанный
авторитет волновой оптики.
Конечно, Эйнштейн не отрицал, что она
все-таки существует. И не оспаривал
опытов, которые доказывали волновую
природу света. Просто он довел возникшее
противоречие до конца и предоставил
разрешать его следующему поколению
физиков.
Несмотря на единодушные протесты,
мысль о квантах света не погибла, и
восемь лет спустя дала могучие всходы. Это
произошло в 1913 году, когда в
лабораторию Резерфорда пришел застенчивый
и неторопливый датчанин Нильс Бор.,
34
ОКОНЧАТЕЛЬНАЯ ПОБЕДА
АТОМИСТИКИ
Долгое время на атомистику
смотрели просто как на
«...любопытную гипотезу, допустимую с
точки зрения нашей
познавательной способности». А философ и
физик Эрнст Мах A838—1916)
прямо называл всех атомистов ссоб-
щиной верующих». Его можно
понять: человеку трудно вообразить
себе нечто, далее принципиально
неделимое. И все же в начале
века идея об атоме победила
окончательно: разум оказался
способным понять даже то, чего он не в
состоянии представить. И
случилось это гораздо раньше, чем
через 300 лет, как предсказывал
Людвиг Больцман A844—1906).
Но победа эта все-таки немного
запоздала: после работ Томсона и
Резерфорда понятие с<атом»
потеряло свой прежний смысл. Стало
ясно — атом сложен и делим,
хотя для этого нужны силы,
намного большие, чем химические.
«К сожалению, законы природы
становятся вполне понятными
только тогда, когда они уже не
верны», — говорил Эйнштейн. Это
не означает, конечно, что
одновременно с этим законы теряют и
все свое значение: независимо от
дальнейших успехов науки
доказательство реальности атома (даже
в старом смысле ато[хос —
неделимый) навсегда останется
одной из самых важных ее побед.
Окончательное утверждение
атомистики также связано с
именем Эйнштейна: в том же 1905
году независимо от польского
физика Мариана Смолуховского
A872—1917) он дал
математическое описание броуновского
движения. Эту теорию подтвердил
экспериментально Жан Перрен,
который в 1909 году предпринял
систематические и тщательные
исследования броуновского
движения. И до Перрена многие
физики: голландец Карбонэль в
1880 году, француз Гуи в 1-888
году и другие ученые —
утверждали, что истинная причина этих
движений — толчки молекул
жидкости, которые сами невидимы
даже в лучший микроскоп.
Удивительные по изяществу опыты
Перрена не просто доказали
справедливость этих утверждений. Из них
следовало нечто большее:
непонятное движение частиц в
жидкости есть точная модель истинного
движения невидимых молекул,
увеличенная в несколько тысяч
раз. Поэтому, изучая броуновское
движение частиц, мы тем самым
получаем наглядную картину
движений невидимых молекул.
(Точно так же как знание свойств
радиоволн дает нам представление
о волнах света и даже о
рентгеновских лучах.)
После этих работ гипотезу об
атомах признали все, даже
знаменитый враг ее Вильгельм Оствальд
A853—1932). А в 1909 году тот же
Резерфорд, который доказал
сложную структуру атома, вместе
с Болтвудом дал и наиболее
убедительное доказательство
атомистической структуры вещества. Вот
как это произошло.
Уже давно было замечено, что
в минералах, содержащих
радиоактивные вещества — торий, уран,
радий — скапливается гелий.
Измерили даже, что из 1 г радия в
год выделяется 39 мм3 гелия.
После установления природы а
-частиц ничего чудесного в этом
факте не было. Но Резерфорд на этом
не остановился: он сосчитал число
а -частиц, которое вылетает в
секунду из 1 мг радия. Оно
оказалось большим, но вполне
определенным: 3,4 .107 частиц/мг . сек,
т. е. один грамм радия
выбрасывает за год 3,4-107-3,16 .Ю7.103 =
= 1,07 ■ 1018 ос-частиц. Все эти а-ча-
стицы, захватив по два электрона,
превращаются в атомы гелия и
занимают объем 39 мм3.
Следовательно, в 1 см3 содержится L =
= 2,56 . 1019 атомов. Но ведь это и
есть то самое число Лошмидта,
которое он вычислил на основании
молекулярно-кинетической
гипотезы! Действительно, один грамм-
атом гелия (как и любого
одноатомного газа) занимает объем
22,4 литра и содержит 6,02-1023
атомов, т. е. в 1 см3 помещается
атомов:
6,02-1028
Совпадение убедительное.
Но человеку присуща
необъяснимая потребность: прежде чем
признатв что-то окончательно,
увидеть это что-то своими глазами.
(Строго говоря, для этого нет
никаких оснований: мы постоянно
становимся жертвами оптических
обманов.) Эту любопытную
потребность человеческого познания
вполне удовлетворил в 1911 г.
Чарлз Томсон Рис Вильсон A869—
1959). После пятнадцати лет усилий
он создал свою знаменитую
камеру, которая позволяла
проследить движение отдельных а
-частиц по туманным следам, которые
они оставляли. Конечно, значение
этого изобретения было не в том,
что оно успокоило капризы
человеческой психики, а в том, что в
руках у физиков был теперь
новый инструмент для исследования
структуры атома.
Мы напомнили сейчас далеко
не все опыты, которые в конечном
итоге убедили всех: да,
действительно, число N атомов в грамм-
молекуле любого вещества
конечно, хотя и очень велико. Как и
число людей на земле, это число N не
может быть дробным. Более того,
число Авогадро N = 6,02497 . 1023
мы знаем сейчас значительно
точнее, чем число жителей Земли.
«Если бы в результате какой-то
мировой катастрофы все
накопленные научные знания вдруг
оказались бы уничтоженными и к
грядущим поколениям живых существ
перешла бы только одна фраза, то
какое утверждение, составленное
из наименьшего количества слов,
принесло бы наибольшую
информацию? Я считаю, что это —
атомная гипотеза (можете называть ее
не гипотезой, а фактом — это
ничего не меняет): все тепа состоят
из атомов — маленьких телец,
которые находятся в беспрерывном
движении, притягиваются на
небольшом расстоянии, но
отталкиваются, если одно из них плотнее
5*
35
прижать к другому. В одной этой
фразе содержится невероятное
количество информации о мире,
стоит лишь приложить к ней
немного воображения и чуть
соображения».
Эти слова принадлежат
Ричарду Фейнману, нашему
современнику, Нобелевскому лауреату
1965 года по физике. И хотя они
почти дословно повторяют
Демокрита, понятия и образы, которые
мы с этими словами связываем
теперь, — совсем другие: за 25
столетий об атоме узнали много
нового. Это было непросто —
просты только результаты науки, и они
не зависят от личности
исследователя — в этом их ценность.
АТОМЫ И ПУСТОТА
Даже люди,, легко гнущие
подковы, признают, что атомы тверды: в
детстве им ведь тоже
приходилось расшибать коленки об углы.
Поэтому очень трудно
представить себе, что атом — такой же
пустой, как пространство между
Землей и Солнцем, и в то же
время необычайно устойчивый.
Известно, например, что вода
останется водой даже под
давлением в 10 000 атмосфер. Это
очень большое давление: так
примерно будет давить слон, если
его поставить на площадку в
1 см2. Площадь одного атома
равна A0Г8 смJ = 10~16 см2,
ТЕХНОЛОГИ, ВНИМАНИЕ!
ЕЩЕ ОДНА ПРОЗРАЧНАЯ
ПЛАСТМАССА.
Японская фирма ссДжапан
синтетик резин» выпускает в виде
таблеток и порошков прозрачную
пластмассу на основе сополимера
акролеина, бутадиена и стирола.
Этот материал перерабатывается
литьем под. давлением,
выдавливанием и другими традиционными
видами переработки пластиков.
Изделия из этого сополимера
отличаются механической прочностью
и поверхностной твердостью.
Строго выполняя требования
технологического режима, можно и из от-
т. е. на один атом давит сила
~107 г/см2.10 6 см2 = 10"9 г. Вес
атома примерно 10~23 г,
следовательно, он выдерживает вес,
который в сто миллионов миллионов
(в 1014) раз превышает его
собственный. Это все равно, как если
бы на того же слона
взгромоздить сотню Эверестов.
Все это удивительно, но не
мешает атомам быть пустыми,
поразительно пустыми: все ядра
атомов, из которых построен Эверест,
можно упаковать в один мешок.
Правда, мешок этот Земля не
выдержит: он сразу же провалится к
ее центру, настолько он будет
тяжел.
ДИФРАКЦИОННАЯ РЕШЕТКА
Неизвестно, как обернулась бы
история атома, если бы физики не
изобрели дифракционную
решетку. Принцип действия решетки
основан на явлении дифракции, то
есть на способности волн огибать
препятствие, если оно сравнимо с
их длиной. Волны различной
длины огибают препятствие
по-разному, что позволяет разделить их и
точно измерить. Благодаря этому
прибору в спектроскопии
достигнуты точности измерений, даже
для физики удивительные. Уже в
начале века удавалось разделить
две линии в видимом спектре,
если их длины волн отличались друг
от друга хотя бы на 10~3 А, т. е.
ТЕХНОЛОГИ, ВНИМАНИЕ!
ходов этого производства получать
изделия с высокой степенью
прозрачности.
«Japan Plastics Age» A067, №3)
СЕРА — КАТАЛИЗАТОР
Монохлоруксусная кислота —
вещество, широко применяемое в
промышленности органического
синтеза. Она нужна в
производстве гербицидов, красителей,
косметических товаров, а также в
качестве консервирующего средства
для кормов и овощей. Недавно на
заводе имени Г. Димитрова в Бра-
зв
всего на 10 п см, при общей
длине видимого спектра — 5000 А
(сейчас точность повышена до
10 А).
Это действительно очень мало:
представьте себе, что вы захотели
измерить длину экватора с
точностью до метра. Ясно, что в этой
попытке нет нужды, да и особого
смысла тоже, просто потому что
результат такого измерения будет
зависеть от каждого муравейника
на пути. Но в спектроскопии
подобные усилия представляют не
только спортивный интерес, и
дальнейшая история атома
убедительно это доказала вопреки
недоверию и насмешкам, которые
эти усилия подчас сопровождали.
Кстати о метре. Знаменитый
платино-иридиевый стержень с
двумя рисками, отлитый по
решению Конвента и хранящийся под
стеклянным колпаком в
Международном бюро мер и весов в
Севре близ Парижа, оказался
неточным. Поэтому спектроскописты
предложили новый эталон метра:
1 650 763,73 длины волны
оранжевой линии криптона (Кг-86) в
вакууме. Эталон этот с 1958 года
принят во всем мире.
ТЕХНОЛОГИ
тиславе разработан новый
непрерывный способ производства
этого вещества. Способ основан на
реакции хлорирования уксусной
кислоты в присутствии серы как
катализатора. Процесс происходит
во время непрерывной
циркуляции маточного раствора,
получаемого при кристаллизации моно-
хлоруксусной кислоты; в
последнюю добавляют свежую уксусную
кислоту и серу. На кристаллизацию
подают продукт хлорирования,
содержащий 65—70% монохлорук-
сусной кислоты.
«Chemicky prumysl» A967, №7)
Погода и организм
М. НАЗИРОВ
Рисунки
Ю. ВАЩЕНКО
Осел мечется и громко кричит — будет дождь-
Верблюд фыркает — к бурану...
Собаки валяются перед ненастьем и ветром...
Куры купаются в песке — к дождю...
Свинья к теплу чешется...
Беспокойное поведение животных и птиц
почти всегда говорит о близком
наступлении ненастья, мороза или ветра; ленивое,
спокойное состояние — примета
приближающегося тепла. То же относится и к
человеку. Перед ненастьем нам становится
душно, клонит ко сну, часто (особенно
у больных — например, ревматизмом)
появляется ломота или боль в костях и
суставах, звон в ушах.
Частота некоторых заболеваний
изменяется в зависимости от времени года.
Различные поражения кожи,
инфекционные катары кишечника, детский спиналь-
ный паралич (полиомиелит) — все эти
недуги чаще встречаются летом. Зимой или
весной наблюдается учащение случаев
базедовой болезни, сердечных приступов,
язЕенной болезни — не говоря уже о
простуде; весенним максимумом
характеризуются туберкулез, экзема и др.)
Погодой определяется и число
несчастных случаев того или иного рода в
различных городах, снижение
производительности труда рабочих, просчеты служащих
банков, нарушение сна. А верные себе
англичане подметили даже связь между
изменением погоды и сменой кабинета
министров...
Каким же образом погода действует на
организм животных и человека, вызывая
раздражения, которые отражаются на их
поведении?
ПОГОДА ДЕЙСТВУЕТ...
Не все представляют, что на поверхность
человеческого тела воздух давит с силой
свыше 16 тонн. Но, на наше счастье,
природа снабдила организм примерно
такой же силы встречным, так называемым
внутренним давлением, которое и
нейтрализует колоссальное внешнее давление.
(Вот почему космонавты, выходя за
пределы атмосферы, вынуждены создавать
внутри скафандров повышенное давление,
призванное противодействовать давлению
изнутри организма.4
37
Давление воздуха характеризуется
довольно сильными непериодическими
колебаниями, связанными с изменением
погоды. Эти колебания составляют в среднем
10—20 миллиметров ртутного столба, или
примерно 15—25 граммов на квадратный
сантиметр, что соответствует весу
приземного слоя воздуха толщиной в 100—■
200 метров.
Раньше предполагали, что колебания
атмосферного давления оказывают на
организм чисто механическое воздействие. Так,
знакомое многим ощущение глухоты и
боли в ушах, возникающее в самолете
с набором высоты, вызвано понижением
атмосферного давления, в результате чего
барабанная перепонка выпячивается; при
понижении атмосферного давления газы,
находящиеся в желудочно-кишечном
тракте, расширяются — это может
сопровождаться ухудшением аппетита и
нарушением процесса пищеварения.
Однако колебания давления оказывают
на организм и косвенное влияние. Так, при
понижении атмосферного давления
воздух, содержащийся в капиллярах почвы,
расширяется и выделяется в нижние слои
атмосферы. А почвенный воздух содержит
повышенное количество радона, который,
в свою очередь, оказывает на
человеческий организм сильнейшее воздействие;
в такой же обратной зависимости от
давления находится и интенсивность
космического излучения.
А вот чувствительность к фену
(теплому и сухому ветру, дующему с гор),
выражающаяся в появлении головной боли,
чувства неуверенности и страха, зудящих
болей, мелькания в глазах, шума в ушах,
головокружений, сердцебиений и в
падении работоспособности, оказалась
результатом воздействия на организм
«барических волн» (то есть волн, подобных
звуковым, но вызванных различными
динамическими процессами,
протекающими в атмосфере). Эти волны могут
восприниматься осязательными рецепторами
и рецепторами ушного лабиринта;
рецепторы же эти связаны с высшими отделами
вегетативной нервной системы,
управляющими процессами обмена в живом
организме.
Температура воздуха сильно влияет
на процессы теплообмена; она испытывает
еще более резкие, чем давление,
непериодические колебания, которые подчас
оказываются для организма весьма
неожиданными. Известны, например, «запоздалая
зима» — в первую половину февраля;
«мартовская зима» — во вторую декаду
марта; холодные дни в середине мая и
даже середине июня. Встречаются также
периоды возврата тепла: так называемое
бабье лето в конце сентября и теплые дни
в начале января.
Влажность воздуха оказывает,
пожалуй, самое существенное влияние на
организм. В метеосводках обычно указывают
относительную влажность, то есть
процентное отношение наблюдаемой влажности
воздуха к максимально возможной при
данной температуре. Воспринимаемая
температура тем выше, чем выше влажность
воздуха: при одной и той же температуре
влажный воздух кажется «теплее» сухого.
В нормально вентилируемом помещении
так называемая зона комфорта (условия,
при которых человек чувствует себя
хорошо) определяется следующими
соотношениями между температурой и
влажностью воздуха:
20°С и 85% относительной влажности
25°С и 60% » »
30°С и 44% » »
35°С и 337о' » »
Высокая влажность воздуха
благоприятствует росту многих микроорганизмов;
поэтому при влажном воздухе (например,
в тропиках) опасность воздушной
инфекции выше. Образующийся в промышлен-
38
ных районах при стопроцентной влажности
воздуха туман может поглощать
различные газы, которые вступают в химические
реакции с водой: известно немало случаев
массового отравления людей
образующимися при этом ядовитыми химическими
соединениями.
Облачность, являющаяся как бы
«приподнятым» туманом, оказывает влияние
прежде всего на интенсивность солнечной
радиации, а о роли Солнца для всего
живого-—-говорить не приходится. Не
исключена возможность и чисто
психологического воздействия облачности (особенно
сплошной) на самочувствие человека.
Некоторые жалобы, связанные с
метеорологическими явлениями, сразу же
прекращаются, как только начинаются
дожди и грозы. Причина этого заключается
в том, что дождь очищает воздух от
вредных газов и микробов, смывает пыль;
возможно также, что вода закупоривает
почвенные капилляры, прекращая тем
самым выделение из них газов. Однако
моросящий дождь, так же как и туман,
может иногда играть роль
эпидемиологического фактора, особенно при сильном
ветре, когда с поверхности загрязненных
водоемов в воздух поднимаются
мельчайшие капельки воды, несущие в себе
мириады микроорганизмов.^
Ветер тоже оказывает на организм
сильное воздействие, охлаждая его. Так,
при температуре 20°С насыщенный влагой
воздух, движущийся со скоростью 3 м/сек,
кажется таким же холодным, как
неподвижный воздух при температуре 14°С; но
при высокой влажности и температуре
охлаждающее действие ветра снижается
и совершенно исчезает при максимальной
влажности и 35°С.
ОРГАНИЗМ РЕАГИРУЕТ...
Какое же звено конкретно связывает
многочисленные метеорологические процессы
с соответствующими биологическими
реакциями?
Это совсем не простая проблема.
Можно с уверенностью сказать разве, что
главная точка приложения
«метеорологических сил» — это вегетативная нервная
система, ибо она, с одной стороны,
неразрывно связана с наружным покровом
и слизистыми оболочками организма,
а с другой — со всеми внутренними
органами, регулируя их деятельность.
Другой из возможных механизмов
влияния погоды на живые существа
связан, по-видимому, с прямым воздействием
на процессы обмена веществ, которые на
молекулярном уровне управляются
многочисленными ферментами. Например,
гликолиз (распад углеводов в отсутствие
кислорода) представляет собой широко
распространенный в животном и
растительном мире ферментативный процесс.
Оптимальная производительность ферментов
(в том числе и гликолитических) зависит
от окислительно-восстановительного
потенциала среды в такой же степени, как
и от ее кислотности и температуры;
поэтому при недостатке кислорода процессы
расщепления углеводов проходят легче,
чем при нормальном его поступлении;
в свою очередь, парциальное давление
кислорода зависит от погодных и
климатических факторов. Аналогичное действие
оказывает и ультрафиолетовая радиация,
интенсивность которой находится в прямой
зависимости от климата и состояния
погоды. И вообще — в атмосфере протекает
немало физико-химических процессов и
содержится немало примесей, способных
оказывать непосредственное воздействие
на ферментные системы организма.
Механизмы воздействия погоды на
живой организм могут оказаться самыми
неожиданными; их число, по-видимому,
достаточно велико, и не исключено, что на
один и тот же метеорологический фактор
различные системы реагируют
одновременно и по-разному.
Вместе с тем было бы неверным
рассматривать действие каждого из элементов
погоды в отрыве от другого. Погода — это
сложнейший комплекс явлений как в
масштабах данной местности, так и
масштабах всей Земли в целом и даже ее
ближайшего космического окружения.
Сегодня биометеорология исследует
воздействие на организм человека
атмосферного электричества, ионов воздуха,
электромагнитных волн, солнечной радиации;
изучают биологическое действие
космических лучей, а также солнечной активности;
особенно живо обсуждается в последнее
время биологическое воздействие
радиоактивных веществ, химических
окислительно-восстановительных примесей,
аэрозолей: предметом многочисленных
исследований служат процессы теплообмена
в организме человека, особенно влияние
терморегуляции на сердечную
деятельность и кровообращение; растет интерес
к процессам, протекающим на
поверхностных биологических мембранах клеток
и их ядер, и к их связи с изменением
внешних условий.
Все это свидетельствует о том, что для
исчерпывающего ответа на поставленный
в начале статьи вопрос нужно и погоду
и организм рассматривать как единое
целое, нужно одновременно проследить
тысячи связей...
Но все же — почему перед дождем
«осел мечется и громко кричит»?
Всякий живой организм обладает
неповторимым по своей сложности и
тонкости механизмом регулирования,
выработавшимся на протяжении миллионов лет
эволюции. С его помощью организм
стремится ликвидировать нарушения,
вызванные в нем изменением внешних условий,
и располагает для этого широким
арсеналом методов. Примером может служить
терморегулирование. Как только
температура среды, непосредственно
воздействующей на наружный покров тела, выходит
за пределы «зоны комфорта»,
незамедлительно изменяется интенсивность
циркуляции крови, процессов сгорания,
выделения пота.
Этот автоматический контроль
непрерывно осуществляется через нервную
систему и рецепторные центры, весьма
чувствительные к изменениям
температуры, давления, химического состава
воздуха и т. п. А между нервной системой
и рецепторными центрами, между мозгом
и, например, кончиками пальцев человека
насчитывается до 800 своеобразных
ступеней усиления. Понятно поэтому, что
информация, передаваемая регулирующей
системой, может искажаться из-за
разнообразнейших влияний окружающей среды
(в том числе и метеорологических), что,
в свою очередь, приводит к ошибкам
управления. Именно эти ошибки и
воспринимаются мозгом как сигналы о
предстоящем изменении погоды. И так как
сигналы эти не могут быть
проанализированы так же однозначно, как, скажем,
световые или звуковые сигналы, то мозг
воспринимает их как неопределенные,
скрытые сигналы опасности: животное
беспокоится, мечется; человек испытывает
чувство неуверенности, тоски, страха...
«Осел мечется и громко
кричит — будет дождь...» Эта па-
родная примета позволяет
предсказывать непогоду. Но каков
механизм действия этого «бюро
прогнозов»?
Любой живой организм (в
том числе и организм осла)
представляет собой
сложнейшую саморегулирующуюся
систему. Главная задача этой
системы состоит в том, чтобы,
несмотря на меняющиеся внешние
условия, ее параметры
сохранялись неизменными. Говоря
попросту, осел стремится
приспособиться к любым, даже самым
неблагоприятным условиям.
На вклейке изображена
схема механизма,
осуществляющего терморегуляцию. Как только
внешние воздействия A)
изменяют температуру системы B),
это сразу же отмечается
особыми нервными клетками —
датчиками температуры C);
сигналы от этих клеток усиливаются
специальными отделами мозга
D) и затем вызывают
изменение интенсивностей процессов
сгорания E), потоотделения F),
кровообращения G) и т. д.
Наиболее тесно связаны друг
с другом и с окружающей ере-
дой нервные центры. Поэтому
на стадии усиления регулирую-
щие сигналы могут искажаться
из-за других внешних
воздействий, например резкого
изменения давления воздуха,
электрического состояния атмосферы
и т. д. (8); регуляция
нарушается, и живое существо
испытывает тревогу и беспокойство.
Надо подчеркнуть, что в
действительности все системы
регуляции теснейшим образом
связаны между собой; связаны между
собой и все процессы,
приводящие к изменению погоды.
Поэтому дело обстоит таким
образом, что весь организм в целом
реагирует на всю погоду в
целом
-ю
ОБЫКНОВЕННОЕ
ВЕЩЕСТВО
Стекло
В. Б. ДМИТРИЕВ,
Т. К. ТРУНОВА
Рисунки
И. ЗАХАРОВОЙ,
Е. СКРЫННИКОВА
Мы привыкли к стеклу, как привыкли ко многим
вещам, постоянно окружающим нас. Уже не
удивляют нас прекрасные зеркальные окна,
цветные витражи... Только на выставках да в
ювелирных магазинах иногда поражаемся мы
искусству стеклоделов, а в остальных случаях обычно
просто не обращаем внимания на стекло —
обычный ведь бытовой материал!
Что мы знаем о стекле? То, что оно очень
прозрачно, хорошо отмывается, не
пропускает воздуха, не реагирует с активными
химическими веществами; знаем, что из
него делают экраны телевизоров, окна,
лампы, вазочки, очки, рюмки; заметили,
что совсем недавно появился стеклянный
кирпич.
А между тем стекло уже далеко не тот
материал, который был известен на
протяжении веков. Ему научились придавать
новые, порой невероятные свойства:
например, необычайную прочность; способность
служить и изолятором, и
полупроводником; защищать и от радиации, и от
ослепительного света при атомных вспышках...
Но прежде чем рассказывать обо всех
современных областях применения стекла,
надо ответить на несколько вопросов.
КАК ВОЗНИКЛО СТЕКЛО
Кто изобрел стекло? На этот вопрос
невозможно ответить. Ученые предполагают,
что стекло как таковое было впервые
получено в незапамятные времена каким-то
неизвестным гончаром, покрывавшим
глиняную посуду глазурью, по своему составу
мало чем отличавшейся от стекла. Для
этого подсохшие изделия из глины
обмазывали смесью песка, соды и извести,
добавляя иногда различные красящие
вещества; потом их обжигали, и, может быть,
гончар заинтересовался случайно
полученным сгустком глазури. Он расплавил смесь
песка с содой и другими материалами, из
которой изготовляли глазурь, и вполне
правдоподобно, что именно так была
открыта новая отрасль производства —
стеклоделие.
Можно предположить, что родиной
стеклоделия был Ближний Восток. Здесь,
недалеко от Фив, было найдено самое древ-
Одно из замечательнейших
свойств стекла, отличающих его
от других материалов, состоит
в том, что оно способно
поддаваться самым разнообразным
способам обработки. Стекло
можно пилить, сверлить,
обтачивать на токарном станке,
шлифовать, полировать, реэать...
Но, пожалуй, самое
замечательное свойство стекла — это то,
что его можно отливать,
формовать на центробежных
машинах, штамповать, прокатывать
и, наконец, выдувать. Кроме
того, стекло можно сваривать
само с собой и с различными
металлами. На цветной вклейке
вы видите отдельные этапы
изготовления стеклянной колбы
кинескопа телевизора на
автоматической линии. Вот из
питателя «капля» стекломассы
подается в форму, в которой
прессуется экран кинескопа
(фото 1); в это время из другого
питателя вытекает еще одна
капля, из которой будет
изготовлен конус трубки. Пока еще
капля не заполнила всей формы
(фото 2), но при следующем
ходе стола на нее опустится
верхняя матрица. Экран готов
(фото 3). С огромной скоростью
вращается форма (фото 4);
центробежные силы «размазывают» по
ее поверхности расплавленное
стекло, которое после
охлаждения превратится в конус
трубки. Механические руки
осторожно поворачивают колбу, и
автомат вваривает в нее ножку
анода (фото 5). Наконец, после
ряда промежуточных операций
и специальной термической
обработки, экран и конус
встречаются на электрогазосварочном
автомате и герметично
свариваются (фото 6)
О Химия и Жизнь, № 4
41
•-Si
o-O
l-Na
Как ни странно, но до сих пор
среди ученых нет единого
мнения об истинной структуре
стекла. По одной гипотезе (рисунки
слева), структура стекла
подобна структуре кристаллического
тела: она представляет собой
сетку, в узлах которой
расположены атомы, ионы или группы
атомов. Но в отличие от
кристаллической сетки
структурная сетка стекла неправильная
(считается, что примерно такой
же, но только подвижной
структурой обладает и жидкость). На
рисунке изображены проекции
структур кристаллического
кварца (а), кварцевого (б) и
обычного натриевого (в) стекла.
По другой гипотезе (рисунок
справа) стекло можно
рассматривать как скопление
микрокристаллических образований —
кристаллитов, крайне малых
и сильно деформированных
структурных образований.
Предполагают, что в центре
структура кристаллита очень
близка структуре
соответствующей кристаллической решетки,
а граничные области имеют
массу искажений — они
аморфны. На рисунке изображена
структура стекла; а —
кристаллиты кварца, б — тетраэдры
Si04, в — натрий. Существуют
и другие точки зрения на
строение стекла
нее изделие из стекла — бусина, возраст
которой исчисляется в 5 500 лет! Позднее
в Риме производство стекла было развито
довольно широко: римские мастера
изготовляли изумительной красоты
стеклянные вазы, кубки и самые разнообразные
безделушки, как бы сделанные из
драгоценных камней.
В средние века центром мирового
стеклоделия стала Венеция. Венецианские
мастера делали из стекла тончайшие изделия,
расписывали их эмалями, покрывали
позолотой, украшали узорами из трещин,
создавали узоры из цветных стеклянных
нитей, закатанных в стекло. Секрет
изготовления венецианского стекла хранился
в строжайшей тайне: всех стеклянных дел
мастеров заставляли жить на острове Му-
рано, близ Венеции, в полной изоляции от
внешнего мира; предлогом служила
забота... о пожарной безопасности города.
И хотя раскрытие профессиональной
тайны каралось смертью, секреты
венецианских мастеров потом стали известны
во Франции, затем в Германии и в Англии,
а к XVII веку стекольные заводы
существовали во многих странах мира.
ЧТО ТАКОЕ СТЕКЛО?
Стекло — твердое вещество, получившееся
в результате охлаждения расплава. Но
переход в твердое состояние в этом
случае происходит особым образом, не
согласующимся с нашими представлениями
о затвердевании жидкостей. При
затвердевании расплавов большинства веществ
молекулы занимают совершенно
определенные места и образуют так называемую
кристаллическую решетку; все ее ячейки
имеют одинаковую форму — куба, призмы
и т. д. В стекле же нет решетки,
характерной для кристаллических веществ; нет
регулярного повторения одних и тех же
структурных элементов. Но и полного
хаоса тоже нет в стекле — во многих
отношениях оно похоже на жидкость, в
которой в отличие от газа существует так
называемый ближний порядок.
Стекло не имеет определенной
температуры плавления. Если мы возьмем
кристаллы, например, поваренной соли и
нагреем их до температуры плавления, то
соль сразу, скачкообразно, из твердого
состояния превратится в жидкость. При на-
±2
a A
Q.
Q.
О
2
б А
температура
плавления
Время
График, показывающий
изменение температуры при
нагревании кристаллического вещества
(а) и стекла (б). В отличие от
стекла, кристаллическое
вещество плавится при строго
определенной температуре; эту
температуру можно определить по
резкому «плато» на графике
гревании стекла этого не произойдет: оно
не плавится при какой-то определенной
температуре, а постепенно размягчается,
начиная с 450°С, превращаясь в жидкость
лишь при 1000 — 1400°С. Поэтому
характерный горизонтальный участок на кривой
нагревания кристаллического вещества
для стекла заменяется наклонной кривой.
Стекло и твердеет не сразу, а лишь
постепенно загустевая. Это происходит
потому, что при быстром охлаждении
вязкость стекла возрастает в сотни миллионов
раз: частицы просто «не успевают»
выстроиться правильными рядами, как уже
оказываются в буквальном смысле слова
застывшими на своих местах. Стекло
сохраняет неизменной ту структуру,
которую оно имело в жидком состоянии *.
Если жидкое стекло охлаждать очень
медленно, например несколько дней, то
в результате получится кристаллическая
масса, не имеющая ничего общего с
обычным стеклом. Процесс кристаллизации
стекла называется «расстекловыванием» и
* Если стекло кристаллизуют по особой
технологии, то получают очень твердые
материалы — ситаллы. Авт.
О.
>^
О.
G)
с
G)
интервал
размягчения
Время
приводит к браку: стекло становится
хрупким и непрозрачным.
ИЗ ЧЕГО ДЕЛАЮТ СТЕКЛО
Что же представляет собой стекло по
химическому составу? Из каких основных
компонентов оно делается?
Прежде всего это стеклообразователи —
вещества, которые способствуют
образованию стекловидного тела. К стеклообразова-
телям относятся двуокись кремния Si02,
борный ангидрид В203, пятиокись фосфора
Р2О5, окись германия Ge02. Из них самый
распространенный в природе — кремнезем;
вот почему большинство промышленных
стекол варят на его основе. Стекла,
сваренные на основе других окислов,
обладают низкой химической устойчивостью,
и сами окислы менее доступны.
Вообще говоря, стекло можно получить
из одного только стеклообразователя. Так
называемое кварцевое стекло получают,
расплавляя кварцевый песок. Но для этого
нужна очень высокая температура —
около 2000°С, а это делает производство
стекла сложным и дорогостоящим. Да и стекло
такое годится далеко не для любой цели.
А как получить стекла, прозрачные для
одних лучей и непрозрачные для других,
легкоплавкие и тугоплавкие, цветные и
бесцветные, химически стойкие и
термостойкие?
Для этого к кварцевому песку
добавляют окислы (окись натрия Na20, окись
калия К20, окись кальция СаО), сильно
снижающие температуру его плавления —
так называемые плавни. А в зависимости
от того, какими свойствам:* должно
обладать изделие из стекла, вводят различные
6*
43
Внутренний вид современной
стекловаренной печи: «влеты»
горелок (а), отверстия для вы-
хода дымовых газов (б), окна
для отбора стекломассы (в),
свод печи (г)
добавки: чтобы придать стеклу блеск —
окись свинца, для повышения
механической прочности и химической
устойчивости— окись алюминия и т. д.
Как говорят специалисты, все эти
окислы вводятся в состав стекла различными
сырьевыми материалами. Сода Ыа2СОз
вводит в стекло окись натрия, мел СаСОз —
окись кальция, поташ К2СО3 — окись
калия. Кварцевый песок, сода, мел, поташ,
поступившие на стекольный завод,
проходят в специальных цехах обработку: они
просушиваются, измельчаются,
просеиваются и затем смешиваются в
определенном соотношении; получается однородная
смесь— «шихта».
В ЧЕМ ВАРЯТ СТЕКЛО?
Хотя в состав шихты и входят
компоненты, сильно снижающие температуру ее
плавления, она все же еще остается
высокой— 1200—1500°С. Поэтому варят стекло
в специальных печах.
Современные стекловаренные печи —■
это гигантские сооружения, площадь
которых достигает несколько десятков и даже
сотен квадратных метров, а емкость —
пятисот и более тонн стекломассы.
Отапливаются такие печи мазутом, газом или
электричеством.
Бассейн стекловаренных печей
разделяется на две части: варочную и вырабо-
точную, которые сообщаются между собой
узким тоннелем — «протоком». С одного
конца в печь непрерывно поступает шихта;
пройдя варочную часть, она превращается
в жидкий расплав, затем медленно
перетекает в выработочную часть и поступает на
формование.
Может возникнуть вопрос: для чего,
собственно, разделяют бассейн на две
части? Дело в том, что при температуре
варки стекломасса настолько жидка, что ее
невозможно ни выдувать, ни прессовать,
ни вытягивать. В выработочной же части
печи, где температура на 200 — 300°С ниже,
чем в варочной, стекломасса несколько
охлаждается, становится более вязкой
и уже пригодна для формования.
44
КАК ВАРЯТ СТЕКЛО?
Варка стекла — дело не столь простое, как
может показаться на первый взгляд.
Получить хорошее стекло — значит не
только расплавить шихту и добиться
образования стекла как такового, но и суметь
сделать его действительно прозрачным.
Но прежде чем шихта превратится
в прозрачную однородную массу, в ней
произойдет целый ряд сложных физико-
химических превращений. Вряд ли нам
удастся проследить за всеми стадиями
стекловарения, остановимся только на
основных.
При нагревании шихты в первую
очередь испаряется содержащаяся в ней влага.
Затем начинается разложение сырьевых
материалов:
Na2C03 -> Na20 <- С02 | ,
К2СОэ->К20 , С02; ,
СаС03 -> СаО -, С02 ] .
Газообразные продукты разложения
улетучиваются из шихты, а оставшиеся
окислы натрия, кальция, калия вступают
в реакцию с песком, образуя сложные
соединения — силикаты:
Na20 Ь Si02 -> Na2Si03 ,
К20 Ь Si02 -> KgSiOg,
СаО + Si02 -* CaSi03 .
Приведенная нами схема упрощена. На
самом деле при варке происходят гораздо
более сложные процессы, и каждый
силикат образуется в результате большого
числа разнообразных химических реакций.
На этом этапе, в интервале температур
800 — 1200°С, шихта представляет собой
всего лишь сплав силикатов. Лишь после
того, как эта смесь расплавится и ее
компоненты растворятся друг в друге, стадия
стеклообразования закончится. Но это
совсем не то стекло, к которому мы
привыкли: оно все пронизано бесчисленным
множеством пузырей. Чтобы осветлить
стекломассу, ее выдерживают при температуре
1300—1500°С. В более горячем (и,
следовательно, менее вязком) расплаве пузырькам
газа легче подняться на поверхность. Для
ускорения этого процесса в шихту вводят
специальные добавки, так называемые
осветлители; при высокой температуре
они интенсивно выделяют газы в виде
крупных пузырей, которые быстро
поднимаются вверх, захватывая на своем пути
задержавшиеся в стекломассе мелкие
пузырьки.
Одновременно с осветлением протекает
еще одна стадия варки стекла —
гомогенизация. Дело в том, что еще в самом начале
варки, после растворения силикатов и
песка, стекломасса получается химически
и физически неоднородной. Она
представляет собой как бы соты из мельчайших
ячеек, которые отличаются друг от друга
по составу и свойствам. Поэтому
гомогенизация стекла, то есть его превращение
в однородную массу,-—задача не менее
важная, чем освобождение стекломассы от
включенных в нее газов. Лишь после этого
стекломасса готова и поступает в вырабо-
точную часть печи.
А теперь перешагнем через таинство
изготовления изделий из стекла и расскажем о некоторых
наиболее интересных областях применения этого
замечательного материала.
ОСТОРОЖНО! НЕ КАНТОВАТЬ!
Эта надпись знакома всем. Ее можно
встретить на ящиках с посудой и приборами,
телевизорами и зеркалами, оконными
стеклами и елочными игрушками... И на
каком бы языке ни была эта надпись, все
знают, что с грузом надо обращаться
осторожно, потому что рядом ставят клеймо —
стилизованное изображение стеклянной
рюмки. Это клеймо говорит о том, что
содержимое ящика столь же хрупко, как
и изображенный на нем предмет.
Представление о стекле, как самом
непрочном материале, настолько
укоренилось, что само это слово стало синонимом
слова «хрупкий». Но из стекла делают не
только рюмки. Взять, например,
иллюминаторы подводных лодок — ведь они тоже
стеклянные. Элементарный расчет
показывает, что сила давления на их поверхность
может достигать несколько сот
килограммов. И стекло выдерживает! Не правда ли,
это никак не вяжется с нашими
привычными представлениями об этом
материале...
А иллюминаторы космических
кораблей? Они не только выдерживают
огромный перепад давлений, вибрацию и
тепловые нагрузки, но и рассчитаны на
встречу с мелкими метеоритами. И это опять
стекло!
Но каким образом стеклу удается
придать такие свойства? Природа стекла
такова, что оно остается хрупким при любом
составе. Поэтому борьба с хрупкостью ве-
J-5
примерный химический
Вид стекла
Оконное
Посудное
Зеркальное
Парфюмерное
Хрусталь
Бутылочное
Полухрусталь
Химико- лабораторное
Термостойкое
Термометрическое
Электровакуумное
Оптическое
Кварцевое
Для медицинских
ампул
Si02
70—72
70—74
72—73
72—73
55—57
74—75
67—68
68—09
80—81
64—70
72—73
47
98,8
73
СОСТАВ НЕКОТОРЫХ ПРОМЫШЛЕННЫХ
А120, +
Н Fe2G3
1—2
0—2
1—2
1-2
—
1—2
—
3-4
1—2
3-4
1—2
—
0,1
3,5
В203
—
—
—
—
—
-
—
—
11—12
10—11
—
—
—
2,5
СаО
7—8
5- 10
10 И
6—7
5—6
0-1
7—8
0—1
0—1
5—6
—
0,1
7
MgO
3—4
0—4
3—4
0—1
—
3-4
—
3—4
-
-■
3—4
—
—
1
ВаО
—
—
—
—
—
—
—
3-4
—
—
—
—
—
—
РЬО
-
—
—
—
30 -35
—
14 15
—
—
—
—
46,4
—
—
СТЕКОЛ (в %)
ZnO
—
-
—
—
—
—
—
—
—
10—11
—
—
—
—
Na20
14 -15
15—17
12—13
16—17
—
15—16
9—10
10—11
3—4
7—8
16-17
—
—
11
к2о
1 2
0- 1
10 -13
-
6-7
2—3
1—2
0-1
0—1
6,35
—
2
As
—
-
-
■-
-
—
0,5 1
-
—
0,2 1
—
0,25
—
—
4G
дется хитрыми, «обходными» маневрами.
Помните, как режут листовое стекло? Для
этого специальным инструментом
(«алмазом») на его поверхность наносят еле
заметную невооруженным глазом царапину.
Затем лист кладут на край стола —
небольшое усилие, и лист сломан, причем излом
проходит точно по риске. Значит,
неглубокая риска (ее глубина составляет всего
несколько процентов толщины самого
стекла) предопределяет место разрушения.
При тщательном исследовании даже
самого гладкого стеклянного листа на его
поверхности можно обнаружить сетку
микроскопических «рисок». Правда, никто
специально не царапал это стекло; его
поверхность неизбежно повреждается в
процессе производства и перевозки, а при
нагрузке любой из дефектов становится
очагом разрушения.
И верно: стоит лишь избавиться от
этих микроскопических дефектов,
например стравить тонкий поверхностный слой
плавиковой кислотой, как прочность
стеклянного листа возрастет в 3—4 раза.
Это отличный метод упрочнения стекла.
Но беда в том, что протравленный на
заводе лист во время транспортировки снова
царапается, теряет прочность. Не
предлагать же хозяйкам мыть окна плавиковой
кислотой! Следовательно, поверхность
листа необходимо сделать не только
идеально гладкой, но и очень плотной.
Этого удается добиться так называемой
закалкой: готовый стеклянный лист
нагревают до температуры, близкой к
температуре размягчения, а затем резко
охлаждают, погружая в жидкость или обдувая
воздухом. После такой обработки
прочность листа возрастает в 5 — 6 раз, а его
поверхность становится настолько
плотной, что не царапается даже
металлическими предметами.
Что же происходит со стеклом при
закалке? При резком охлаждении лист
остывает неравномерно — сначала поверхность,
затем внутренние слои. Также
неравномерно происходит и сжатие: поверхностный
слой оказывается уплотненным и в
дальнейшем противостоит разрушающим лист
растягивающим напряжениям.
К этому же результату — уплотнению
тонкого поверхностного слоя — приводит
и так называемая химическая закалка.
Для этого готовые стеклянные изделия
помещают на несколько минут в ванну
с расплавом лития. В расплаве на
поверхности стекла происходит обмен ионов
натрия на ионы лития; образовавшийся
отличный от основной массы тонкий
поверхностный слой находится в напряженном
состоянии, даже еще большем, чем при
обычной закалке. Таким способом
упрочняют не только листовое стекло, но и
изделия сложной конфигурации.
Ну а как же все-таки делают
иллюминаторы подводных лодок и космических
кораблей? Как делают пуленепробиваемое
стекло?
Секрет прост: стекло делают
многослойным. В некоторых случаях
используют пакеты из стеклянных листов
толщиной всего 0,05 миллиметра — тоньше
обычной бумаги. Один такой лист не очень
прочен, но 50 листов, склеенных особым клеем
воедино, запросто противостоят огромному
давлению, перепаду температур, ударам
пуль и метеоритов. Многослойные пакеты
применяются и для более прозаических
целей: для остекления витрин
промышленных зданий, автомобилей, самолетов *.
Иначе говоря, наше представление
о стекле как о самом хрупком материале
не совсем верно. Недалеко, наверное, то
время, когда мы вообще забудем о том,
что стекло хрупко...
ХРУСТАЛЬНЫЙ ДВОРЕЦ
Сегодня в «хрустальных дворцах» живут
не только волшебники. Современная
строительная техника сделала реальностью
сказочную мечту: сейчас все чаще можно
встретить дома, почти целиком
построенные из стекла.
Но удобно ли жить и работать в таком
«хрустальном дворце»? Нет, не удобно!
В ясную погоду в таком доме обычно
нестерпимо светло и жарко: солнечные лучи
нагревают полы, обстановку, но тепло не
выходит наружу, так как стеклянные
стены — прекрасный теплоизолятор.
Возникает так называемый парниковый эффект.
Плохо и другое. Жить и работать в
таком доме неуютно: люди чувствуют себя
как в витрине универмага, когда нет
уголка, в котором можно было бы скрыться от
нескромного взгляда.
* Простейший — трехслойный — пакет такого
рода носит название «триплекс». Такое стекло
получило распространение во время второй
мировой войны. — Авт.
47
И все же мы можем нарисовать
картину хрустального дворца недалекого
будущего, картину, которая кажется несколько
фантастической несмотря даже на то, что
в ней не будет ни одной детали, которая не
была бы уже изобретена.
Стены нашего хрустального дворца
в зависимости от его назначения должны
пропускать или поглощать лучи той или
иной области спектра. Например, стены
жилого дома должны пропускать
ультрафиолетовую радиацию и задерживать
(особенно на жарком юге) тепловое
инфракрасное излучение; стены музеев и
книгохранилищ должны задерживать
ультрафиолет, разрушающий краски, бумагу...
Свойство поглощать или пропускать те
или иные лучи можно придать стеклу
с любой основой — фосфатному,
силикатному. Чтобы силикатное стекло не
задерживало биологические активные
ультрафиолетовые лучи, оно должно содержать
минимальное количество соединений
трехвалентного железа и совершенно не
должно содержать окислов хрома, свинца,
титана. Поэтому всю предварительную
обработку сырья приходится проводить в
аппаратах, изготовленных из материалов, не
содержащих железа; варят такое стекло
в печах со специальной футеровкой. А вот
соединения двухвалентного железа делают
стекло непрозрачным для инфракрасных
лучей.
Стены хрустального дворца должны
защищать его жителей и от яркого
солнечного света. Но,— скажете вы,— зачем тогда
вообще делать стены стеклянными? Разве
может быть стекло и прозрачным и
непрозрачным одновременно?!
Представьте себе — да! Для этой цели
могут служить так называемые фотохром-
ные стекла *, способные менять свою
окраску и прозрачность автоматически,
в зависимости от освещенности. В тени,
в необлученном состоянии такое стекло
прозрачно и пропускает около 90
процентов видимого света — столько же, сколько
и обычное оконное стекло. Но стоит только
поместить его на солнце, как через 30
секунд его пропускная способность снизится
до 50 процентов, а еще через 22 секунды —
до 28 процентов. В таком состоянии оно
имеет серую или серовато-коричневую
окраску, поглощая лучи всего видимого
спектра. А когда освещение ослабевает,
стекло снова начинает светлеть и через
1 — 2 минуты становится прозрачным.
Такие удивительные свойства стеклу
придают мельчайшие частички галоидного
серебра, равномерно распределенные
в стекломассе. Молекулы галоидного
серебра обладают способностью под
действием света переходить в новое,
возбужденное состояние. Этот переход сопровож-
* См. «Химия и жизнь», 1965, № 7—8.
48
дается изменением спектра поглощения,
и частички начинают поглощать новый,
отличный от первоначального диапазон
лучей — стекло меняет окраску.
Стены, сделанные из фотохромного
стекла, можно затемнять и по желанию.
Для этого на его поверхность следует
нанести тонкую прозрачную токопроводя-
щую пленку, а металлическую окантовку
присоединить к источнику энергии.
Изменяя величину тока, протекающего по
пленке, можно менять температуру листа,
что повлечет за собой и изменение свето-
пропускания (для фотохромных стекол
прозрачность — функция не только
освещенности, но и температуры).
Из таких же панелей можно собирать
и внутренние перегородки дворца. На них
можно наносить с помощью фотохромных
красителей возникающие и исчезающие
рисунки, а также рисунки, меняющие свой
цвет.
Никаких печей и отопительных
батарей в комнатах не будет — их заменят
панели из микропористого стекла, через
которые будет подаваться теплый (или
холодный) воздух.
Торшеров, ламп, люстр во дворце тоже
не найти. Мягкое рассеянное освещение
обеспечат стеклянные панели с люминес-
цирующими слоями.
Системы отопления, освещения и
регулировки светопропускания можно будет
питать электроэнергией, вырабатываемой
стеклянными преобразователями
солнечной энергии, размещенными на крыше
дворца.
И, наконец, прилегающие к зданию
дорожки будут также из стекла,
подсвечиваемого ночью — снизу или с боков.
Это будет прекрасный дворец. Такой,
о котором веками мечтали люди...
СТЕКЛЯННАЯ СКОВОРОДА
Граненый стакан растрескивается, если
после холодной воды в него налить
кипяток. Тот же результат будет, если в
нагретый толстостенный стеклянный сосуд
налить холодной воды. Это свойство стекла
хорошо известно; пользуясь стеклянной
посудой, мы стараемся избегать резких
«тепловых ударов».
А вот толстая зеленоватая сковорода
спокойно подставляет свои бока пламени
горелки и не трескается. Почему? Чтобы
ответить на этот вострое, прежде всего надо
выяснить, что происходит со стеклом при
резких сменах температуры.
В тот момент, когда в горячий стакан
наливают холодную воду, различные слои
его стенок из-за плохой теплопроводности
охладятся в разной степени. Температура
внутренней поверхности стакана резко
упадет, а его внешний слой останется
горячим: перепад температуры вызовет
в стекле неравномерные напряжения.
Величина этих напряжений
непосредственно связана с коэффициентом
теплового расширения стекла: чем меньше этот
коэффициент, тем легче стекло переносит
резкие изменения температуры. Именно
из такого стекла и делают жаростойкую-
посуду.
Самое, термостойкое — кварцевое
стекло, представляющее собой чистый
кремнезем Si02. Стакан из этого стекла можно
нагреть до светло-красного каления и
затем бросить в холодную воду. Почти
мгновенное изменение температуры от 1000°С
до комнатной температуры для него
совершенно безопасно.
Кварцевое стекло обладает самым
малым коэффициентом теплового
расширения из всех известных в природе веществ.
Если нагреть на 100°С изготовленную из
обычного стекла палочку длиной 10
сантиметров, то в результате теплового
расширения она удлинится на 100 микронов.
Такая же палочка из кварцевого стекла
даст приращение длины только на 5
микронов — в 20 раз меньше.
Однако, несмотря на это замечательное
свойство, кварцевое стекло сравнительно
мало распространено, и совершенно не
встречается в быту. Это объясняется
трудностями, с которыми связано
производство такого стекла и изделий из него. Даже
при 2000°С кварцевое стекло имеет
консистенцию густого теста, и поэтому при
формовании изделий приходится применять
давление около 4—5 атмосфер.
По этой же причине в кварцевом стекле
остается много газовых пузырьков,
делающих его непрозрачным или
малопрозрачным. Удалить эти пузырьки — очень
сложная техническая задача. Все это делает
кварцевое стекло очень дорогим
материалом, используемым только для
специальных целей.
Из этого положения есть один
остроумный выход. Первоначально варится
стекло, содержащее не только двуокись
кремния, но и окись натрия или калия
49
и окись бора. Такое стекло варится при
сравнительно низкой температуре, а затем
путем особой химической обработки
(выщелачивания) примеси растворяются в
кислоте и удаляются. Выработанные таким
образогд стекла называют кварцоидными
и кварцевидными.
Но и они дороги.
Ученые давно задумывались над тем,
как получить дешевое стекло, стойкое
в химическом и тепловом отношении.
Особенно нуждались в таком стекле химики.
В 1896 году в этом направлении начал
работать профессор Петербургского
университета В. Е. Тищенко. Он впервые ввел
в состав стекла окись бора, которая
сообщила стеклу повышенную тепловую и
химическую стойкость; вместе с тем такое
стекло можно было варить почти при той
же температуре, что и обычное. С тех пор
рецепты теплостойких стекол претерпели
различные изменения в соотношении
составных частей, но в основе своей и по сей
день остались все теми же.
ВЛИЯНИЕ НАИБОЛЕЕ ВАЖНЫХ ОКИСЛОВ НА ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА СТЕКЛА
]
Окисел
Двуокись кремния Si02
Окпсь алюминия А1203
Борный ангидрид В203
Окись натрия Na20
Окись калия КгО
Окись лития Li20
Окись бария ВаО
Окись цинка ZnO
Окись свинца РЬО
Влияние окисла
Стеклообразователь. Снижает коэффициент линейного расширения, повышает
термостойкость, химическую устойчивость и электрическое сопротивление
стекла. При введении больших количеств Si02 стекло становится очень
тугоплавким.
В присутствии Si02 служит стеклообразователем, предотвращает
кристаллизацию стекла, повышает его химическую и термическую устойчивость,
снижает коэффициент линейного расширения. Введение больших количеств А12Оэ
сильно повышает тугоплавкость стекла.
Служит хорошим стек л ообра зова те лем, снижает склонность стекла к
кристаллизации п уменьшает вязкость при высоких температурах. В203 снижает
коэффициент линейного расширения стекла и повышает его термостойкость.
Сильно снижает тугоплавкость стекла и уменьшает его склонность к
кристаллизации. Повышает коэффициент линейного расширения стекла и,
соответственно, уменьшает его термостойкость. Кроме того, Na20 снижает
химическую устойчивость стекла и его электрическое сопротивление.
Снижает тугоплавкость стекла, повышает коэффициент линейного расширения
и снижает термостойкость. Сильно уменьшает способность стекла к
кристаллизации, снижает его электрическое сопротивление.
Снижает тугоплавкость стекла даже в большей степени, чем Na20 и К20.
Повышает коэффициент линейного расширения стекла и снижает его
электрическое сопротивление.
Снижает тугоплавкость стекла, но в меньшей степени, чем Na20, K20 и Li20.
Повышает электрическое сопротивление стекла и его коэффициент
линейного расширения. Снижает склонность стекла к кристаллизации.
При введении в стекло в количестве до 5—10% снижает его тугоплавкость,
повышает термостойкость. Излишнее количество способствует
кристаллизации стекла.
Улучшает оптические свойства стекла, придает блеск и поглощает
радиоактивное излучение.
50
Из боросиликатного стекла делаются
в основном все термостойкие изделия,
которые работают в условиях резкой смены
температур. Например, раскаленные до
150—200°С стеклянные оболочки мощных
электрических ламп, установленных на
открытом воздухе, не разрушаются при
охлаждении дождем и снегом. Водомерные
стекла паровых котлов и многие другие
стеклянные предметы и детали постоянно
испытывают резкие смены температур на
100—200°С. Наконец, лабораторная посуда,
трубы, кастрюли и сковородки, в которых
можно приготовить обед, тоже делаются из
этого замечательного стекла.
Стекло — материал воистину неисчерпаемых
возможностей. Все, о чем мы только что рассказали,
лишь очень поверхностно характеризует
многообразие областей его применения. Поэтому
закончим нашу статью подборкой коротких заметок —
информации, дающих более полное представление
о том, как стекло вошло в плоть и кровь
современной техники.
ш ^
BhSSSSbSi
щ
Щ%!^Ш
щ
ГША
СТЕКЛЯННЫЙ
ТЕРМОМЕТР
Обычное стекло — прекрасный
электроизоляционный материал.
И мало кто знает, что существует
стекло-полупроводник.
Например, стекло, содержащее
As2Se3 и As2Fe3, по своим
электрическим характеристикам —
полупроводник с высоким
отрицательным термическим
коэффициентом сопротивления. Это значит,
что при увеличении температуры
электрическое сопротивление
такого стекла резко падает.
Полупроводящее стекло
используют для определения
температуры в активной зоне атомного
реактора. Преимущество
стеклянного термометра перед обычными
термопарами состоит в том, что
его сопротивление не меняется
под действием облучения.
ЛИТР... СТЕКЛА
Хотя мы говорим, что стекло по
своей внутренней структуре
похоже на жидкость, при комнатной
температуре оно совсем на нее не
похоже. Но вот стекло,
содержащее мышьяк, серу и большое
количество бора, — это жидкость,
затвердевающая (и
приобретающая свойства обычного стекла)
при температуре значительно
ниже нуля. Такое стекло
действительно можно отмерять литрами...
РУБИН ИЛИ СТЕКЛО?
«Сердцем» лазера первое время
служил кристалл рубина. Но
получить такой кристалл не так-то
просто: он должен быть достаточно
большим и, кроме того, идеально
однородным.
А вот сейчас в качестве
лазерных материалов используют
стекло, содержащее около 6
процентов окисла неодима — Nd2Os. Если
в рубине активным ионом служит
трехвалентный хром, то в неоди-
мовом стекле эту функцию
выполняет трехвалентный неодим.
КАКАЯ БАНКА
ЛУЧШЕ?
В 1965 году в Брюсселе состоялся
VII Международный конгресс по
стеклу. Один из докладов,
зачитанных перед этим высоким
собранием, был посвящен...
обыкновенной консервной банке.
Дело в том, что, по
наблюдениям авторов доклада, световые лучи
с длиной волны около 500
миллимикронов неблагоприятно влияют
на вкусовые качества консервов.
Поэтому было предложено делать
консервные банки из стекла, со-
51
держащего Fef Mn, Cr, Ti, V и Се.
Такое стекло сильно поглощает
лучи с длиной волны 500
миллимикронов.
ОСТОРОЖНО,
РАДИАЦИЯ!
Ученые, работавшие с
радиоактивными объектами, обратили
внимание на то, что под действием
больших доз излучения стекло
темнеет, теряет свою
прозрачность. Это наблюдение послужило
толчком к созданию специальных
стекол — индикаторов радиации:
такие стекла темнеют
пропорционально интенсивности и
продолжительности облучения.
РАКЕТА ЛЕТИТ В ЦЕЛЬ
Один из способов точного
наведения ракеты на цель состоит в том,
что в ее головке устанавливают
аппаратуру, чувствительную к
инфракрасным (тепловым) лучам.
Горячие выхлопные газы двигателя
цели (например, самолета) как бы
притягивают к себе управляемый
снаряд.
Но работе «инфракрасного
наводчика» может помешать и
обычное световое излучение. Поэтому
наводящую головку ракеты
закрывают специальным стеклянным
колпаком, совершенно
непроницаемым для лучей видимой части
спектра, но почти не
поглощающим инфракрасные лучи.
ЯРЧЕ ТЫСЯЧИ СОЛНЦ...
Один из поражающих факторов
ядерного взрыва — мощная
световая вспышка, способная ослепить
человека, находящегося даже на
большом расстоянии от эпицентра
взрыва. Защитить глаза тем более
трудно, что в боевой обстановке
сам момент взрыва почти
невозможно предвидеть.
Вместе с тем можно защитить
глаза от светового импульса с
помощью очков с фотохромными
стеклами: эти стекла мгновенно
темнеют на ярком свету.
СТЕКЛЯННЫЙ
УСИЛИТЕЛЬ
Специальное ванадиевое стекло
используют в качестве основной
части каскадных
фотоумножителей.
«Сердцем» таких приборов
обычно служит
эмиттер—электрод, на поверхность которого
нанесен слой какого-нибудь металла
или окисла. Этот слой обладает
особым свойством: квант
излучения или элементарная частица,
ударившись о его поверхность,
выбивает из нее несколько
электронов; эти -электроны, ускоряясь
электрическим полем, ударяются о
другой эмиттер и в свою очередь
выбивают из него новые
электроны. Таким образом, число
электронов непрерывно растет, и фото-
ток увеличивается.
Стекло в качестве эмиттера —
еще одна неожиданная область
применения этого замечательного
материала.
ФОТОПЛАСТИНКА
БЕЗ ЭМУЛЬСИИ
Блоки специального
светочувствительного стекла (оно получается
при введении в стекломассу от
0,001 до 1 процента коллоидных
частиц благородных металлов и
0,5 процента специальных
добавок, при облучении интенсивно
испускающих электроны) позволяют
получать объемные цветные
изображения. Этот удивительный
«фотоматериал» проявляют и
фиксируют... в печи при температуре
лишь немного ниже температуры
размягчения стекла. При этом
коллоидные частички, рассеянные
прежде в массе блока и поэтому
невидимые, собираются в
довольно крупные группы, способные
отражать свет. Группировка частиц
происходит вокруг нейтральных
атомов, возникших из ионов при
экспонировании блока на свету.
ПРОЗРАЧНАЯ ПАМЯТЬ
В электронных приборах
(например, в системе цветного
телевидения) необходимо порой задержать
какой-нибудь сигнал на доли
секунды и затем передать его
дальше. Сейчас в таких линиях
задержки в качестве рабочего элемента
предлагают использовать много-
композиционные стекла, например
калиево-свинцово-силикатные.
ЗА ОКНОМ — РАДИАЦИЯ
Не всегда телекамера пригодна
для наблюдения за
радиоактивными объектами, например
атомными реакторами. В этом случае в
толстые защитные стенки
реакторных помещений вставляют не
менее толстые стекла, которые
задерживают опасное излучение, но
сами при этом не темнеют. Таким
свойством обладают стекла на
основе тяжелых металлов.
ИНФОРМАЦИЯ ИНФОРМАЦИЯ ИНФОРМАЦИЯ ИНФОРМАЦИЯ ИНФОРМАЦИЯ ИНФОРМАЦИЯ
Современное состояние
исследований в области химии инертных
газов. Апрель. Москва. (Научный
совет по неорганической химии
АН СССР)
X Симпозиум по ликвационным яв-
^" лениям в стеклах. Апрель. Ленин-
5 ш град. (Институт химии силикатов
I ft АН СССР)
ш О Совещание по комплексному ис-
q x пользованию солевых богатств за-
U х лива Кара-Богаз-Гол. Апрель.
Ашхабад. (Институт химии АН Туркм.
ССР)
Всесоюзная конференция по
химическим реакторам. Май. Киев.
(Институт физической химии АН
УССР)
Применение низкотемпературной
плазмы в технологии тугоплавких
соединений. Май. Киев. (Институт
проблем материаловедения АН
УССР)
IV семинар ло жаростойким
покрытиям. Май. Ленинград.
(Институт химии силикатов АН СССР)
V совещание по металловедению,
физико-химии и металлофизике
сверхпроводящих материалов.
Май. Москва. (Институт
металлургии АН СССР)
Конференция по получению и
анализу веществ особой чистоты.
Май. Горький. (Горьковский
университет, Лаборатория
стабилизации полимеров АН СССР)
О
а.
<
I"
5 со
Международный симпозиум по
хромато-масс-спектрометрии. Май.
СССР, Москва.
VI симпозиум по газовой
хроматографии. Май. ГДР, Берлин.
IV европейский симпозиум
Европейской федерации химической
технологии. Май. Бельгия,
Брюссель.
Международная конференция по
каучуку. Май. Западный Берлин.
Ill международный конгресс по
цитологии. Май. Бразилия, Рио-
де-Жанейро.
VI всемирный конгресс по
плодовитости и бесплодию. Май.
Израиль, Тель-Авив.
Международная конференция по
химии. Май. Франция, Париж.
Международные дни химического
машиностроения. Май. Франция,
Париж.
28-й международный конгресс по
алкоголю и алкоголизму. Май.
США, Вашингтон; Канада,
Монреаль и Торонто.
В ближайшее время
выходят в издательствах:
«М и р»:
Р. Бреслоу. МЕХАНИЗМЫ
ОРГАНИЧЕСКИХ РЕАКЦИЙ. 1 р. 06 к.
П. де ла Map, P. Боптон. ЭЛЕК-
ТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ
К НЕНАСЫЩЕННЫМ СИСТЕМАМ.
1 р. 50 к.
К. Ниденцу, Дж. Даусон. ХИМИЯ
БОРАЗОТНЫХ СОЕДИНЕНИЙ. 1 р.
2В к.
А. Барнард. ТЕОРЕТИЧЕСКИЕ
ОСНОВЫ НЕОРГАНИЧЕСКОЙ ХИМИИ.
2. р. 36 к.
СОВРЕМЕННАЯ КВАНТОВАЯ
ХИМИЯ (под редакцией О. Синаног-
лу). 1 р. 64 к.
Р. Бельчер. СУБМИКРОМЕТОДЫ
АНАЛИЗА ОРГАНИЧЕСКИХ
ВЕЩЕСТВ. 1 р. 14 к.
3. Амис. ВЛИЯНИЕ
РАСТВОРИТЕЛЕЙ НА СКОРОСТИ И
МЕХАНИЗМЫ ХИМИЧЕСКИХ РЕАКЦИЙ. 2 р.
«X и м и я»:
А. А. Аскадский. ФИЗИКО-ХИМИЯ
ПОЛИАРИЛАТОВ. 1 р. 20 к.
С. В. Генепь и др. ПРИМЕНЕНИЕ
ПОЛИМЕРНЫХ МАТЕРИАЛОВ В
КАЧЕСТВЕ ПОКРЫТИЙ. 1 р. 05 к.
Ф. X. Джейл. ПОЛИМЕРНЫЕ
МОНОКРИСТАЛЛЫ. 3 р. 13 к.
В. Г. Жиряков. ОРГАНИЧЕСКАЯ
ХИМИЯ. 93 к.
Е. М. Капайтан. СМАЗОЧНЫЕ
МАСЛА ДЛЯ РЕАКТИВНЫХ
ДВИГАТЕЛЕЙ. 89 к.
В. В. Кафаров. МЕТОДЫ
КИБЕРНЕТИКИ В ХИМИИ И ХИМИЧЕСКОЙ
ТЕХНОЛОГИИ. 1 р. 08 к.
Р. Бейтс. ОПРЕДЕЛЕНИЕ рН. 2 р.
19 к.
ик
А. Б. УШАКОВ, Москва: Будут ли
еще проводиться в Советском
q ^ Союзе международные химиче-
о- £ ские выставки!
оЗЕ
В связи с успехом выставки
«Химия в промышленности,
строительстве и сельском хозяйстве»
A965 год) такие выставки решено
проводить в Москве регулярно.
В Торговой палате СССР
сообщили, что ближайшая выставка
намечена на 1970 год.
53
со°реД^нн2йТаукЙ Искоренение инфекций:
тонка зрения
биолога
Доктор медицины М. КАЦ,
доктор медицины X. КОПРОВСКИ
Это было в Москве, на IX Международном конгрессе по микробиологии, В
зале университетского клуба шло заседание одного из симпозиумов.
Только что кончился перерыв на обед, гомон в зале не утихал,
запоздавшие участники с шумом пробирались на свои места. А тем временем
председатель уже предоставил слово очередному докладчику.
Как только прозвучала первая фраза доклада, зал удивленно затих.
Потому что это была фраза из бессмертного "Декамерона11 Боккаччо:
«Славную Флоренцию постигла смертоносная чума, посланная праведным
гневом божиим на смертных...>?
Авторами доклада были сотрудники Института анатомии и биологии в
Филадельфии (CILA) Майкл Кац и Хилари Копровсни. 1/1 хотя такое начало
было довольно неожиданным, оно оказалось как нельзя более уместным: в
докладе, изложение которого мы публикуем, речь шла о том, возможно
ли полностью искоренить с лица Земли грозные эпидемические
заболевания, много веков повергавшие в ужас целые страны.
54
Чума—«черная смерть», которой мы
обязаны появлением на свет
«Декамерона»,— сейчас полностью исчезла в Европе.
Почему это произошло, мы не знаем.
Чумная палочка все еще опасна для человека —
об этом свидетельствуют несчастные
случаи в лабораториях при неосторожном
обращении с ее культурами. Чумная
блоха — один из переносчиков болезни — все
еще живет среди нас и все еще может быть
заражена чумным микробом. Правда,
исчезло другое звено в цепи
распространения инфекции — черная крыса, которая
сейчас встречается только в некоторых
портовых районах. Но остались ее
сородичи, например бурая крыса, которая тоже
может переносить чумных блох.
И тем не менее эпидемии чумы сейчас
не грозят нам. То, что мы не можем назвать
причин этого, показывает, как мало мы
знаем о природе эпидемических
заболеваний и как поэтому трудно наметить
биологически обоснованный путь к их полной
ликвидации.
ПОЛЬЗА И ВРЕД САНИТАРИИ
До последнего времени единственным
способом приостановить распространение
многих заразных болезней были санитарно-
гигиенические мероприятия. Чем выше
санитарный уровень жизни, чем лучше
жилищные условия, действеннее контроль
за питьевой водой и продуктами питания,
тем меньше опасность заболевания. Вот
лишь один пример. Когда-то видное место
среди инфекционных болезней во всем
мире занимали детские расстройства
дизентерийного характера. В 1901—1905 гг.
в Бостоне (США) они в летнее время
уносили от 600 до 800 детей в месяц. А 30 лет
спустя в те же месяцы в Бостоне умирало
от таких расстройств лишь по 20 детей.
Элементарные санитарные мероприятия —
контроль за качеством продаваемого
молока, улучшение гигиенического состояния
жилищ — могут принести не менее
эффективные результаты и в других странах,
особенно слаборазвитых, где детские
поносы до сих пор косят детей тысячами.
Правда, есть у санитарии и оборотная
сторона. При высоком санитарном уровне
среды человек впервые сталкивается
с заразным началом в гораздо более
позднем возрасте, чем в странах с плохими
санитарными условиями. А некоторые
заболевания протекают в детстве куда
легче, чем у взрослых, и после них
остается стойкий иммунитет. Например, во
время эпидемии гепатита в Нью-Дели
(Индия) в 1955—1956 гг. наименее
подверженными болезни оказались жители
городских трущоб. Такая же зависимость
установлена и для полиомиелита.
Но отказываться от улучшения
санитарных условий только на этом основании
было бы, тем не менее, неразумно. В
конце концов против полиомиелита у нас есть
теперь эффективная вакцина, а гепатит
далеко не так опасен, как десятки других
заболеваний, распространение которых
было приостановлено благодаря
санитарным мерам.
КОГДА БЕССИЛЬНЫ ЛЕКАРСТВА
В прошлом многие заразные болезни легко
удавалось обуздать с помощью противо-
микробных лечебных и профилактических
препаратов. К сожалению, в последнее
время лекарства все чаще и чаще
оказываются бессильными против возбудителей
заболеваний. Неуклонно растет число
микроорганизмов, приспособившихся к
действию лекарств: к ним сейчас
откосятся, например, менингококки, гонококки,
стрептококки. А пенициллин? Какие
радужные надежды возлагались на него
в борьбе с болезнями, которые вызывают
стафилококки! Теперь же история
пенициллина звучит как настоящая повесть
о потерянном рае.
Причина такого положения —
неумеренное и неконтролируемое применение
лекарств, и прежде всего антибиотиков.
Повинна в этом и сама эффективность этих
средств, из-за которой мы меньше
заботимся о предупреждении болезней.
Так или иначе заболеваемость многими
болезнями в последнее время
увеличилась. Среди таких болезней — малярия,
которая, казалось, уже находится на грани
исчезновения. Всего несколько лет назад
эту болезнь — одну из самых
распространенных, от которой страдают 140 млн.
людей и ежегодно умирает 1,5 млн., — можно
было предотвратить ежедневным или
еженедельным приемом лекарств. Но недавно
в Камбодже и в Колумбии появились
штаммы малярийного плазмодия,
устойчивые ко всем лекарствам, кроме хинина.
И поскольку хинин слишком токсичен^
чтобы его можно было применять как
профилактическое средство, приходится
55
признать, что сейчас существуют
разновидности малярии, предотвратить которые
мы бессильны.
ВОЙНА — ПЕРЕНОСЧИКАМ
Борьба против переносчиков заразного
начала — один из эффективнейших
методов искоренения инфекционных болезней.
На целых огромных территориях земного
шара применение ДДТ позволило
полностью истребить комара-анофелеса —
главного переносчика малярийных
плазмодиев. Теперь эти районы избавлены от
малярии.
Однако и здесь сложилось примерно
такое же положение, как и с
антибиотиками: по мере того как насекомые —
переносчики болезней вырабатывают
устойчивость против инсектицидов, бороться
с ними становится все труднее.
Кроме того, нужно иметь в виду, что
если будут уничтожены, например, все
комары-анофелесы, то переносчиками
малярии могут стать новые виды комаров,
которые тем самым заполнят
образовавшийся «экологический вакуум».
И все-таки, несмотря на это, проблема
борьбы с комарами не так уж сложна.
Хуже обстоит дело с переносчиками других
заболеваний, например водяными
улитками, которые переносят тяжелое глистное
заболевание шистозоматоз. Есть множество
химических средств, которыми можно
уничтожить улиток; но любое из них
губительно и для всей остальной водной
фауны и неизбежно превратит водоем
в безжизненную пустыню.
В таких случаях необходимы
принципиально новые способы борьбы с
переносчиками. Например, возможно применение
физического метода. Если нагреть
прибрежные воды рек и озер, зараженных
шистозоматозом, то все живые существа
в них, в том числе и улитки-переносчики,
погибнут, а вдали от берега водная фауна
и флора останутся нетронутыми.
Существуют и в некоторых случаях
уже успешно применяются генетические
способы борьбы. Например, в местах
распространения насекомых-переносчиков
выпускают большие количества специально
выращенных стерильных самцов или же
особей, дающих в потомстве преобладание
самцов. И в том и в другом случае
численность переносчика с каждым поколением
снижается.
56
ПРОБЛЕМЫ ИММУНИЗАЦИИ
Могучее средство искоренения заразных
болезней — искусственное создание у
населения иммунитета к ним, достигаемое
путем массовой вакцинации. Особенно
эффективен этот метод в борьбе с такими
болезнетворными организмами, которые
создают длительный иммунитет. К ним
относится, например, вирус полиомиелита.
Это заболевание исчезло в некоторых
странах только благодаря массовой
иммунизации. В будущем можно ожидать
появления вакцин и против других вирусов,
создающих длительный иммунитет,
например вирусов кори или краснухи.
Труднее будет разработать
иммунизационные методы борьбы с вирусными
заболеваниями органов дыхания:
вызывающие их вирусы или слишком
разнообразны, или же не создают длительного
иммунитета.
Бактерии, к сожалению, тоже не создают
стойкого иммунитета, и поэтому борьба
с ними путем иммунизации не столь
перспективна. Правда, вакцинирование
оказалось эффективной мерой ликвидации
дифтерии и столбняка. Например, в
британской армии до начала
противостолбнячных прививок, во время первой мировой
войны, на 1000 раненых приходилось три
случая столбняка; а за всю вторую
мировую войну среди британских солдат было
отмечено всего 35 случаев столбняка, да
и то в 15 из них оказалось, что солдаты по
тем или иным причинам не проходили
иммунизацию. Но не нужно забывать, что
в данном случае иммунизация направлена
не против самой инфекции, а против
токсинов, вырабатываемых возбудителем
болезни, и помочь ликвидации
болезнетворного начала она не может.
В последнее время исследователи
пытаются использовать в борьбе против
бактериальных заболеваний метод
иммунизации живой вакциной, который сейчас
широко применяется против вирусных
болезней (вспомним тот же полиомиелит).
Живых вакцин против бактерий пока
почти нет, но некоторые эксперименты
в этом направлении вселяют известные
надежды. Например, оказалось, что можно
предотвратить опасную стафилококковую
инфекцию у новорожденных, если сразу
же после рождения заразить их одним из
штаммов стафилококка, который обычно
заболевания не вызывает. Может быть,
Сонная болезнь, переносимая
мухой цеце, — одно из опасней-
тих заболеваний
иммунизация живой вакциной станет
когда-нибудь действенным средством
предупреждения и бактериальных
заболеваний.
С массовой иммунизацией населения
любой живой вакциной связана одна
опасность. Ослабленные микроорганизмы,
перевиваемые от одного
организма-хозяина другому, могут внезапно восстановить
все свои болезнетворные свойства. На
этот риск пришлось пойти, приступая
к массовой вакцинации против
полиомиелита, и это в данном случае оказалось
оправданным. Но при появлении любой
новой живой вакцины такую опасность
нужно будет каждый раз учитывать.
НА ЗЕМЛЕ БЕЗ МИКРОБОВ?
А теперь давайте представим себе, что все
проблемы, о которых мы говорили,
решены, все болезнетворные микроорганизмы —
бактерии, вирусы, гельминты — и их
переносчики ликвидированы окончательно на
всем земном шаре. Конечно, такая
перспектива может только радовать. Но не
нужно забывать, что в тысячелетней
борьбе за существование человек как
биологический вид выжил только благодаря
тому, что выработал у себя могучие
защитные механизмы против
всевозможных инфекций. Хотя в любой момент
каждого из нас окружают возбудители
буквально всех болезней, от ангины до
холеры, — мы, как правило, не
заболеваем, потому что наш организм до поры
58
Антисанитария — источник приятиям придается большое
эпидемий. Поэтому разносто- значение в борьбе с заразными
ронним гигиеническим меро- заболеваниями
до времени успешно нейтрализует
попадающие в него микроорганизмы.
Если же мы ликвидируем все
инфекции, то не утратит ли человечество за
ненадобностью через несколько поколений
эти защитные механизмы? Тогда человек
падет жертвой первого же нового патогена,
который может* появиться, скажем, в
результате мутации. А если какие-то
болезнетворные организмы будут занесены на
Землю с других планет? Ведь эта
возможность уже сейчас вполне реальна...
Поэтому мы считаем, что ставить
вопрос о полной ликвидации инфекций можно
будет только тогда, когда уровень наших
знаний позволит отчетливо представить
себе все возможные последствия. И
главным соображением при разработке любой
программы искоренения болезней должно
быть прежде всего сохранение
экологического равновесия.
Рисунок
В. УМНОВА
Фото из журнала
«Курьер ЮНЕСКО»
Комментирует директор Института
эпидемиологии и микробиологии
им. //. Ф. Гамалея, действительный член
Академии медицинских наук СССР
О. В. БАРОЯН
Проблема ликвидации заразных
заболеваний и освобождения
человечества от наиболее массовых
и опасных инфекций в настоящее
время выдвигается как одна из
ведущих проблем современной
микробиологии и современного
общества в целом. Объясняется
это различными причинами. С
одной стороны, достижения
последних десятилетий в области
биологической науки позволяют более
научно обоснованно подходить к
претворению в жизнь этой
многовековой мечты человечества.
С другой стороны, социальный
прогресс, который имел место на
протяжении последних 50 лет во
многих странах, значительно
облегчил решение этой проблемы.
Действительно, за последние
несколько десятилетий в
экономически развитых странах уже не
регистрируются такие в прошлом
опасные и массовые заболевания,
как чума, холера, оспа, малярия,
паразитарные тифы, дифтерия,
полиомиелит и многие другие.
Однако эти инфекции еще
свирепствуют во многих странах Азии,
59
Африки и Латинской Америки,
что создает непрерывную угрозу
их проникновения в другие
страны.
Поэтому доклад американских
ученых М. Каца и X. Копровски,
посвященный биологическому
аспекту ликвидации заразных
заболеваний, представляет
несомненный интерес. Дело в том, что в
проблеме борьбы с инфекциями
и ликвидации некоторых из них
на современном уровне наших
знаний высказаны две гипотезы.
Первая считает возможной, как
принято говорить, «эрадикацию» —
искоренение инфекций, то есть
полную ликвидацию возбудителя
заболеваний как биологического
вида; вторая ограничивается
требованием резкого снижения
заболеваемости, при котором
клинически выраженные формы
заболевания отсутствуют, хотя его
возбудитель еще продолжает
циркулировать в человеческом
обществе. В социальном плане эти
решения очень близки: и в том и в
другом случае речь идет об
отсутствии в человеческом обществе
того или иного заболевания со
всеми его тяжелыми
последствиями. Но дискуссия идет о другом —
о принципе биологического
подхода. Можно ли вообще
ликвидировать эволюционно установившийся
на протяжении веков
биологический вид и каких последствий
можно ожидать, если бы это удалось?
Справедливости ради надо
признать, что хотя эпидемии
инфекционных заболеваний
известны человечеству с незапамятных
времен, повсеместно
ликвидировать хотя бы один возбудитель
заболевания до сих пор не
удалось. Есть много оснований
полагать, что если многократно
иммунизировать все население земного
шара против оспы, то эта антро-
понозная — €счисто человеческая»
инфекция могла быть
ликвидирована в полном смысле слова, и
ее возбудитель как биологический
вид был бы обречен на гибель.
Что же касается других вакцин,
то они часто направлены не
против самого возбудителя, а против
выделяемых им вредоносных
токсинов. Поэтому даже когда такое
заболевание не проявляется,
возбудитель определенное время
продолжает циркулировать в
иммунных (защищенных) организмах.
Некоторые исследователи, в
том числе и авторы доклада,
считают, что ликвидация возбудителя
вообще опасна, так как она может
нарушить сложившийся
экологический баланс между микробом —
возбудителем болезни и
человеком — хозяином. В значительной
степени сторонники этой точки
зрения правы. Однако
абсолютизировать ее было бы неправильно.
Например, малярия, вызываемая
плазмодием, ликвидирована во
многих странах, и никакого вреда
населению ликвидация
биологического вида плазмодиев не
принесла. С другой стороны, можно
и в самом деле поставить вопрос:
а нужно ли ликвидировать,
скажем, такой микроорганизм, как
кишечная палочка? Да, она в очень
редких случаях может вызывать
тяжелые заболевания. Но не
приведет ли ее ликвидация к
активизации всей кишечной флоры
человека и не могут ли в результате
появиться такие болезни, которые
ранее вообще не были известны?
В решении таких спорных
вопросов нужен конкретный,
вдумчивый и биологически
обоснованный подход.
Слабая сторона доклада — его,
так сказать, социологическая
стерильность. Еще с древнейших
времен эмпирические
наблюдатели улавливали непосредственную
связь между появлением
эпидемий и различными социальными
потрясениями: войнами, засухой,
наводнениями и, как следствие,
голодом. Значительная часть
биологов считает, что хотя природа
инфекционного заболевания —
биологическая, но движущими
силами эпидемий являются
социальные процессы. Это подтвердила
и вторая мировая война, во время
которой видимое
эпидемиологическое благополучие нарушалось
и эпидемии появлялись даже в тех
районах, где отдельные инфекции
казались уже ликвидированными.
Конечно, эпидемиологическое
благополучие достигнуто не
только в СССР. Осуществление
крупных коммунальных и социальных
мероприятий позволило
ликвидировать многие инфекции в
отдельных географических зонах
мира. Это проблема в первую
очередь социологическая, но и
эпидемиолог не должен о ней
забывать.
Как для медика, для меня
важна другая сторона вопроса —
логичность и обоснованность
постановки глобальной цели
освобождения человечества от эпидемий.
Сейчас уже не вызывает
сомнений, что ликвидация инфекций в
глобальном масштабе может быть
достигнута только при самом
широком международном
сотрудничестве медиков, биологов и служб
государственного или
общественного здравоохранения. Сейчас в
рамках Всемирной организации
здравоохранения сделаны первые
попытки создать департамент по
глобальной борьбе с инфекциями.
Есть все основания полагать, что
широкое международное
сотрудничество, построенное на
взаимном доверии, а главное — на
осознании безграничной гуманности
поставленной цели, может дать
успешные результаты и значительно
снизить заболеваемость во
многих развивающихся странах, где
население еще тяжело страдает
от инфекций.
Заключая, можно сказать, что
хотя в проблеме ликвидации
инфекций и существуют
дискуссионные положения, курс на резкое
снижение инфекционных
заболеваний с точки зрения
современной биологической науки вполне
обоснован. Достижения советской
медицины на протяжении 50 лет —
наглядное подтверждение этому.
00
НАУКА — ПРОИЗВОДСТВУ
Ни
километра
без
резины
Кандидат технических наук
Л. Е. ВИНИЦКИЙ
Рисунки
Б. АКУЛМНМЧЕВА
Изделия из резины нужны
электротехникам и химикам, медикам и строителям,
вообще — всем. Из резины делают соски
и игрушки, обувь и шины, шайбы и шланги.
Железная дорога — а именно она
перевозит сейчас больше 60% всех грузов и
пассажиров— тоже не может работать без
многочисленных изделий из резины.
Несмотря на всю несхожесть, резиновые
изделия обладают одним общим
свойством— эластичностью. Это значит, что они
способны к высоким обратимым
деформациям. Кусочек резины можно увеличить
в размере в несколько раз, и если оставить
его в покое, то он быстро придет к
исходному состоянию. И при этом, чтобы
деформировать этот кусочек, нужно затратить
относительно небольшие усилия. Иначе
говоря, модуль упругости резин невелик:
он в 104—105 раз меньше модуля
упругости стали.
Основа всякого резинового изделия —
это эластомеры: натуральный или
синтетические каучуки. Используя различные
каучуки и прочие компоненты резины,
можно получать изделия с очень
непохожими свойствами. Так, резины могут
отличаться по прочности в 10 раз, а по
жесткости — даже в 20 раз; одни стойки к самым
агрессивным средам, другие растворяются
в обыкновенной воде; есть резины
электроизоляторы, а есть проводники.
§
ВСЕ НАЧАЛОСЬ С ФАЭТОНА
Хотя резина известна уже больше столетия,
бурное развитие резиновой
промышленности началось лишь в нашем веке.
И причиной этого было появление
автомобильного транспорта. Высокие скорости,
большая маневренность,
комфортабельность оказались недостижимыми без
резиновых пневматических шин.
Правда, еще с XVIII столетия для
снижения шума и уменьшения тряски на
городских фаэтонах, каретах, омнибусах,
а позднее и на крестьянских телегах стали
ставить стальные рессоры. А когда
кончилась эпоха лошадиной тяги и начался
нынешний скоростной век, одних рессор стало
недостаточно.
Но еще раньше автомобильного
появился рельсовый железнодорожный транспорт.
Зачем же резина на железных дорогах?
Там же стальные колеса и стальные
рельсы... И все же железнодорожный
транспорт — один из крупнейших потребителей
резины. И пусть вас убедит в этом далеко
не полный перечень резиновых деталей,
без которых не может обойтись транспорт:
это тепло-звукоизоляционные уплотнения
окон и дверей, резиновые и резино-метал-
лические амортизаторы, резиновые
шланги и рукава, диэлектрические маты,
теплостойкие и морозостойкие
уплотнители, упругие подрельсовые прокладки
и многое, многое другое.
Резиновые изделия на железных
дорогах СССР начали широко применять
25—30 лет назад. И сегодня нормальная
работа железных дорог была бы просто
невозможна без использования резиновых
деталей.
Вряд ли в одной статье можно хотя бы
охарактеризовать все эти детали.
Ограничимся лишь описанием некоторых из них.
61
КАК СЭКОНОМИТЬ КОЖУ
В любом пневматическом или
гидравлическом устройстве есть уплотнители,
предотвращающие утечку газов и жидкостей.
А тормозная система как раз и работает на
пневматике или на гидравлике. Добавим
к этому, что в каждом локомотиве и
вагоне — своя тормозная система. Теперь
должно быть ясно, почему уплотнителям стоит
посвятить отдельную главу.
Требований к уплотнителям много. Они
должны сохранять работоспособность при
температурах от —60 до + 60°С, обладать
минимальной ползучестью, большой
гибкостью, стойкостью к смазочным маслам,
свету, озону. Только при этих условиях
уплотнения будут герметичными, а
тормоза — надежными...
Еще лет тридцать назад уплотнители
делали из кожи. И чтобы оснастить
уплотнителями тормозные приборы одного
только вагона, требовалось до полутора шкур
взрослой коровы! И лишь когда развилось
производство отечественного маслостойкого
хлоропренового каучука, многие
тормозные уплотнители стали изготовлять из
резины. Это было большим подспорьем для
кожевенно-обувной промышленности.
Но хлоропреновые каучуки тридцатых
годов были недостаточно морозостойкими,
а в наших климатических условиях это
серьезный недостаток. Поэтому в то время
полностью заменить резиной кожу не
удалось. Это было достигнуто уже в
послевоенные годы, когда наша химическая
промышленность освоила бутадиеннит-
рильные каучуки повышенной
морозостойкости. Только тогда перестали делать
дорогие и трудные в изготовлении
кожаные уплотнители, и благодаря этому
ежегодные затраты на железнодорожное
оборудование снизились более чем на
100 000 руб. Некоторые резиновые
уплотнители показаны на рис. 1.
Сложнее дело с уплотнителями
двигателей на локомотивах. Они должны
сохранять уплотняющие свойства до 150—250°С!
А резины на основе «обычных» каучуков
ограниченно теплостойки: их долговечность
при температуре выше 70°С невелика.
Надежные маслотеплостойкие
уплотнители железнодорожных двигателей можно
сделать на основе каучуков, содержащих
фтор. Резины из новых фторкаучуков
прекрасно сопротивляются износу и
подолгу сохраняют эластические свойства
при температурах 150—200°С.
62
РЕЗИНА ПОД КОЛЕСАМИ
Всем известно, что деревянные шпалы
быстро разрушаются. Причин много: здесь
и воздействие влаги, микробов, и смена
температур, и разрушающее действие
динамических нагрузок при прохождении
+\ поездов. Через несколько лет деревянные
шпалы приходится менять.
Железобетонные шпалы, естественно,
более прочны и долговечны. Предполагают,
что срок их службы будет не менее
30—40 лет. Но в отличие от деревянных
железобетонные шпалы менее упруги.
И этот недостаток может восполнить
резина.
Между рельсом и шпалой помещают
амортизирующие (а заодно и
электроизолирующие) прокладки из резины, которые
воспринимают вибрации,
передающиеся на шпалу при контакте колеса с
рельсом.
Замена шпал на отечественных
железных дорогах началась несколько лет назад
и будет полностью закончена лишь в
следующем десятилетии. И если бы
потребовалось поставить резиновые прокладки
-на все железнодорожные пути, то
пришлось бы построить несколько новых
заводов резинотехнических изделий и
соответствующее число предприятий,
производящих каучук и компоненты резиновых
изделий только для прокладок. Оказалось,
впрочем, что для их изготовления можно
частично использовать регенерат (т. е.
продукт вторичной переработки вышедших
из строя резиновых изделий). Регенерат
в 4—5 раз дешевле каучука, и в то же
время прокладки, содержащие до 30%
регенерата, обладают требуемыми
изоляционными и механическими свойствами:
об этом свидетельствует многолетний
опыт.
МОДУЛЬ, ГИСТЕРЕЗИС И ТРЯСКА
Дома мы пользуемся подушками из перьев
и пружинными матрацами. Впрочем,
губчатая, пористая или пенистая резина
успешно конкурируют как с перьями, так
и с пружинами. И сейчас множество
матрацев и подушек в пассажирских вагонах,
так же как и сидения машинистов
локомотивов, делают из пенистых и губчатых
резин. Они намного легче пружинных, не
боятся моли и влаги, не подвержены
коррозии. В течение ближайших нескольких
лет все пассажиры спальных вагонов
будут пользоваться исключительно
матрацами и подушками из полимерных
материалов. Но это, как говорится, цветочки...
В куда более сложных условиях
динамических нагрузок находятся
амортизаторы железнодорожных локомотивов и
вагонов.
При укладке рельсов между
отдельными участками оставляются зазоры. Это
делается потому, что рельсовая сталь (как
и все другие реальные материалы)
расширяется при повышении температуры
и сжимается при ее снижении. Когда
колесо наезжает на рельсовый стык,
возникают удары, перерастающие при большой
скорости в вертикальные колебания,
вибрации (знакомую всем тряску) и шум. Это
отнюдь не идет на пользу пассажирам,
и одними матрацами здесь не помочь. Но
помимо неприятного воздействия на
пассажиров колебания ведут к разрушению
подвижного состава и пути. И колебания
надо устранять.
При трогании с места или резком
торможении пассажир автомобиля,
троллейбуса или поезда испытывает неприятное
ощущение, вызываемое действием
горизонтальных нагрузок. И эти воздействия
необходимо смягчать, так же как и уси-
63
л
**§
1Г М И111111Л111Г1МIIIIU
niii iimiuhii i HMiniiiiiiiiiiiMiiiiiiiiMiiimmm >
гистерезис
2
График изменения свойств
амортизаторов в зависимости от
модуля и гистерезиса резины
Колесо с резиновылш
амортизационными элементами.
Благодаря вертикальным
перемещениям резино-металлических
элементов при наезде колеса на
стыки и другие неровности по-
глощается энергия колебаний
и снижаются звуковые
вибрации, вызывающие шум
лия, возникающие в поперечном
направлении. При движении поезда возникают
колебания и вибрации различной частоты
и амплитуды, действующие в различных
направлениях. Наиболее полно удается
гасить их с помощью резиновых
амортизаторов. Немудрено, что вес резиновых
деталей в пассажирских вагонах скоростных
линий достигает 2,5% общего веса вагона
Амортизационные свойства резины
определяются в первую очередь значениями
ее модуля (об этом говорилось в начале
статьи) и упругого гистерезиса. Под
гистерезисом (в наиболее простом изложении)
понимается способность материала (или
конструкции) возвращать обратно лишь
часть воспринятой энергии. У резин
величина гистерезиса колеблется от 0,05 до
0,7, в то время как, например, у стали она
близка к нулю. А способность поглощать
энергию вибраций, ударов и т. п. тем
больше, чем больше величина гистерезиса.
Благодаря низкому модулю, высокому
гистерезису и малому удельному весу
резины исключительно, хорошо поглощают
энергию — в 25—30 раз лучше, чем сталь.
Сюда же нужно присовокупить и то,
что резина достаточно надежно крепится
к металлу, не требует смазки, стойка к
коррозии. Процесс разрушения резинового
изделия происходит не мгновенно, а во
времени. Это позволяет избежать аварий,
которые сопутствуют внезапному
разрушению, характерному для металлических
деталей.
Модуль и гистерезис по-разному
влияют на срок службы и амортизацию. Так,
из графика (рис. 2) видно, что с
увеличением гистерезиса возрастает
амортизационная способность большинства железно-
04
дорожных амортизаторов, но
одновременно снижается долговечность. В то же время
рост модуля, увеличивая срок службы
изделия, ухудшает его амортизационные
характеристики. Поэтому в каждом
конкретном случае выбирается определенная
резина, обладающая оптимальными
свойствами. Лучшие резины — на основе
натурального каучука и каучуков
регулярного молекулярного строения. Эти каучу-
ки СКД (цис-полибутадиеновый) и СКИ
(полиизопреновый) серийно выпускаются
в Советском Союзе.
Несколько лет назад у нас появились
комфортабельные «бесшумные» трамваи
(например, трамваи маршрута № 5 в
Москве). Пассажиры не чувствуют в них
тряски, шум значительно приглушен. Все
это достигнуто благодаря применению
колес с резиновыми
элементами-вкладышами (рис. 3). Рельсовый транспорт с такими
колесами не только комфортабелен, но и
долговечен. Колесами с резиновыми
вкладышами оборудованы также вагоны
метрополитена, «электричек» и некоторые
вагоны дальнего следования.
Широко распространены резиновые
или резино-металлические рессоры (рис. 4).
Если пружинные амортизаторы, вместо
которых используют такие рессоры, выходят
из строя ежегодно, то на европейских
железных дорогах устройства с резиновыми
элементами служили 12—15 лет без
замены.
Грузовой локомотив весит около 230—
280 тонн. Эту колоссальную нагрузку
воспринимают всего четыре пары резиновых
конусов (рис. 5).
С увеличением скоростей движения на
железных дорогах возникла
необходимость в создании еще более «мягких»
амортизационных устройств. Так,
предложено использовать в качестве
амортизатора воздух, заключенный в резино-ткане-
вую оболочку. И тут не лишне упомянуть,
что такие конструкции будут работать
лишь с надежными резиновыми
уплотнениями.
Для восприятия энергии ударов при
формировании составов, а также при
торможении, движении под уклон и т. д.
используют специальные устройства —
поглощающие аппараты. Во многих из них
амортизаторы — это комплекты резино-
металлических элементов (рис. 6).
Составы, оборудованные такими поглощаюши-
ми аппаратами, успешно эксплуатируются
« 5
4
Резиновая рессора колокольного
типа: 1 — корпус; 2 —
резиновый элемент; 3 — сердечник
5
Резиновый конус —
амортизатор центральной опоры
локомотива. Вертикально
расположенная пара конусов воспринимает
нагрузку в десятки тонн
ё
tTT^eii ш
без ремонта и замены элементов уже в
течение шести лет.
Мы не останавливались подробно на
многих резиновых изделиях и деталях,
применяемых на железнодорожном
транспорте для самых различных целей.
Впрочем, это и не входило в задачу автора,
который пытался лишь подтвердить давно
уже очевидный специалистам факт:
современному поезду без резины не проехать и
километра...
ЖИВЫЕ
ЛАБОРАТОРИИ
Волчье лыко
Поглощающие аппараты с рези-
по~ металлическими элементами
В конце апреля, после долгой
зимы, все устремляются в лес,
поражающий после зимнего
однообразия обилием красок.
В это время и цветет волчье
лыко — волчеягодник, или волч-
ник, или дафна (Daphne mezere-
um L.), единственное в средней
полосе древесное растение,
зацветающее ранней весной, до
появления листьев, яркими и
довольно крупными цветками,
а не сероватыми сережками
(как, например, ольха, орешник,
береза).
Слово «дафна» по-гречески
означает «лавр». Оно
происходит от древнегреческого мифа,
рассказывающего, как Аполлон
полюбил красавицу Дафну, и
она, спасаясь от преследования
бога, превратилась в лавровое
деревцо. Многие
средиземноморские родственники нашего
волчьего лыка — вечнозеленые,
и их листья и плоды
действительно похожи на лавр.
Вечнозеленая лавровая дафна растет
и у нас, в Крыму.
Наш волчеягодник
распространен на очень большой
территории СССР: в лесах
Европейской части, на Кавказе, в
Сибири — до самого Байкала.
Это небольшой кустарник,
скорее — карликовое деревцо, до
1—1,5 м высоты. Тонкие
прутики его веточек весной сплошь
усыпаны пучками
ярко-розовых цветков, каждый из
которых очень похож на цветок
сирени. У него такая же
трубочка с тычинками, сидящими
внутри, но их не по две, как у
сирени, а по четыре.
Погода весной непостоянна,
и драгоценную пыльцу в
раскрытом цветке волчника может
залить водой. Но этого не
происходит: капли дождя не могут
попасть в трубку венчика,
потому что отверстие ее очень узко,
и воду не пускает внутрь
воздух, находящийся в трубке.
А насекомым он не мешает
запустить внутрь цветка свой
хоботок. Цветки волчника
посещают несколько видов пчел,
мухи-цветочницы,
бабочки-крапивницы.
Цветки волчника имеют очень
нежный своеобразный аромат.
Интересно, что цветы его бли-
06
жайших родственников (а их
целых 50 видов) пахнут совсем
иначе: волчник альпийский —
ванилью, лавровый и волчник
Филиппа — фиалкой,
полосатый — сиренью, волчник
Благи — гвоздикой.
Кора и листья волчника
совсем лишены запаха, но
животные не трогают растение, так
как оно очень ядовито. Так же
как и у липы, кора волчника
очень легко обдирается
длинными узкими плетями — лыком.
Но разорвать их поперек редко
кому удается: они очень прочны
и гибки. Такой же гибкостью
обладают стволик и ветки
волчника. Это очень выгодно
растению: зимой снег плотно
придавливает ствол к земле и
закрывает его своим пушистым
покровом.
Кора волчника на вкус очень
горькая; неприятный вкус
долго остается во рту, даже если
только прикоснуться к ней
языком. Химики, исследовавшие
кору волчьего лыка,
обнаружили в ней глюкозид дафнин
С15Н16О9. Горький вкус дафнина
и предохраняет растения от
поедания животными.
Кроме дафнина в коре
волчника содержится желтое
красящее вещество, воск, камедь,
сахар, минеральные соли и
желтая смола мезереин, присутствие
которой и делает волчник
ядовитым. Мезереин раздражает
слизистые оболочки, вызывает
жжение во рту, острое
желудочное расстройство, которое может
окончиться смертью. А если
мезереин попадет на кожу,
появляются краснота и волдыри.
Раньше кору волчьего лыка
употребляли наружно как
нарывное средство. К сожалению,
и в наши дни это любимое
средство знахарей, применение
которого часто ведет к
отравлению.
Волчник называют еще и
волчеягодником. К сентябрю это
деревцо, совсем невзрачное
летом, снова становится
декоративным: созревают
ярко-красные ягоды, так и манящие их
отведать. Но тому, кто по
неосторожности или неопытности
попробует «волчьих ягод»,
грозит очень сильное отравление.
Так же как кора и листья,
сочные плоды и семена волчника
содержат дафнин и мезереин.
Академик П. С. Паллас в своем
«Путешествии по разным
провинциям Российского
государства», вышедшем в 1776 г.,
рассказывал, что красные ягоды
волчника, известные в Сибири
под именем дикого перца,
«употребляют двояко: вместо
рвотного дают детям от кашля, а
здешние женщины, награждая
недостаток румян, сими
ягодами натирают щеки, отчего оне,
по причине острого сока,
краснеют и почти рдеют. Мужики,
вынув зернышки и растолокши
оных тридцать, принимают
вместо лекарства, к чему весьма
крепкий потребен желудок, а
корень, своей остротой все
растение превосходящий, пользует
от зубной болезни».
Как же распространяются
столь ядовитые семена? Ведь
животные избегают даже
прикасаться к листьям волчника и
уж подавно не трогают его
плодов!
Но, оказывается, есть и
исключения. Дрозды без всякого
вреда для себя склевывают
яркие плоды и разносят их
семена на довольно далекие
расстояния. Каким образом они
избегают действия яда — непонятно.
Из спелых ярко-красных
ягод волчника можно получать
красную краску, а из коры —
желтую. В Гималаях из луба
волчника коноплевого делают
так называемую непальскую
писчую бумагу. А на
декоративные качества волчника
давно обратили внимание садоводы:
известны две его садовые
формы.
М. МАЗУРЕНКО,
Главный ботанический сад
АН СССР
67
НОВОСТИ ОТОВСЮДУ . НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ
ЖЕЛЕЗО ИЗ ДЫМА
Дым, выбрасываемый трубами
теплоэлектроцентралей, содержит
немало ценных веществ, в том
числе и железо. В Польше на
электростанции «Явожно-И» с
успехом испытан аппарат,
улавливающий железо из дыма. При
включении этого аппарата
возникает вращающееся
электромагнитное поле, под действием
которого и происходит осаждение
частиц металла. Так польскими
инженерами сразу «убиты два
зайца»: атмосфера
предохраняется от загрязнения и
одновременно из дымного облака добывается
металл.
ПРИКЛЕЕННЫЙ КОСМОНАВТ
Когда космонавт работает в
открытом космосе, он должен
каким-то способом прикрепиться
к корпусу корабля. Системы
крепления до сих пор представляют
собой сложную задачу для
конструктора.
Журнал «Chemische Rundschau»
A967, № 17) предлагает новую
оригинальную конструкцию
сиденья, легко прикрепляющегося
к стенке корабля с помощью
особого клея. Клей изготовляется на
высокоактивной мономерной циа-
нисто-акрилатной основе. Клей
упаковывают в капсулы, которые
загружаются в подставки сиденья.
Когда требуется закрепиться
в выбранном месте снаружи
корабля, космонавт приставляет
каждую подставку к стенке
корабля, нажимает на
соответствующее устройство, и капсула
с клеем разрывается.
Выделившийся клей схватывается в
течение 10 секунд и прочно
прикрепляет сиденье к кораблю
независимо от угла соединения корпуса
и подставки.
ИСКУССТВЕННЫЙ ПЕРЛАМУТР!
До сих пор искусственный
перламутр получали в основном из
гуанина (СбН^40), довольно
редкого и дорогого органического
вещества, который добывается из
чешуи пресмыкающихся и рыб.
В последнее время
неоднократно пытались получать
перламутр и из неорганических
веществ с коэффициентом
преломления от 1,9 до 2,9 (это
коэффициент преломления перламутра) —
основного карбоната свинца или
двуокиси титана. Однако
воспроизвести эффект перламутрового
блеска полностью долгое время
не удавалось.
Журнал «Chemie-Industrit»
A967, № 1) сообщает, что в Италии
предложен новый способ
обработки основного карбоната свинца,
при котором благодаря
сочетанию определенной температуры
и кислотности возникает
кристаллическая структура со всеми
особенностями натурального
перламутра.
ЛУЧШЕ ХЛОРЕЛЛЫ!
Французские химики исследовали
состав голубовато-зеленой
водоросли, растущей в водах
африканского озера Чад, и получили
ошеломляющие результаты: она
содержит в себе углеводы, белки,
жиры, витамины А, В2/ В с, В,2 и С,
то есть почти все необходимые
для питания компоненты. Кроме
того, водоросль отличается
высокой урожайностью: за год она
дает с гектара 42 тонны
питательной массы (урожай пшеницы
с одного гектара — 2,5—3 т).
Жители близлежащих африканских
государств издавна употребляли
водоросль в пищу. По
питательности и урожайности водоросль
далеко превосходит хлореллу,
которая в настоящее время
успешно культивируется в Японии.
Во Франции предполагают со
временем начать промышленное
производство питательных смесей
на основе водоросли озера Чад,
испытание которых на животных
и птицах прошло успешно и дало
хорошие результаты.
ПИВО ДЛЯ КУР
Оказывается, и куры не могут
устоять перед этим напитком.
Более того, сухие пивные отстой,
входившие в рацион птиц,
настолько благоприятно влияли на
них, что яйценоскость кур
повысилась на 5%i а из снесенных ими
68
НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ
яиц вывелось на 9% больше
цыплят. Как сообщает журнал
«Feedstuff» A967, № 38), какое-то, пока
еще неизвестное, вещество в
пивных отстоях повышает фертиль-
ность кур и индюков.
ФОТОГРАФИЯ
ПОД ОБЛУЧЕНИЕМ
Оригинальный способ
«омоложения» ценных старых фотографий
и фотодокументов описан во
французском журнале «Science et
vie» A967, № 598). Фотокарточку
помещают... в ядерный реактор,
где она подвергается интенсивной
бомбардировке нейтронами. Под
действием такой обработки
серебро, входящее в состав
вещества, образующего
фотоизображение, превращается в
радиоактивный изотоп, испускающий
бета-лучи. Время жизни этого
изотопа измеряется минутами.
Поэтому сразу после облучения снимок
кладут на очень мелкозернистый
негативный материал. Под
действием бета-излучения на этом
негативе возникает новое
изображение, значительно более
четкое, чем на старом снимке.
ТЕРМОС
из полиэфирной пленки
К сведению будущих покорителей
лунных просторов: уже сейчас
можно изготовить сосуд из
нового теплоизоляционного
материала, в котором жидкость будет
сохраняться горячей в течение всей
лунной ночи, равной по
продолжительности 14 земным суткам.
Этот материал, по сообщению
журнала «Design news» A967,
№ 19), состоит из 100 слоев алю-
минизированной полиэфирной
пленки и 100 слоев «бумаги» из
стекловолокна, чередующихся
между собой. Алюминизированная
пленка, так же как и зеркальное
стекло в сосуде Дьюара, отражает
лучистую энергию, а «бумага» из
стекловолокна служит прокладкой
между слоями пленки.
Новый теплоизоляционный
материал будет использован для
изготовления контейнеров,
которые защитят приборы,
доставленные на Луну, от резкой смены
температуры лунной атмосферы.
АЗОТ ОКРАШИВАЕТ АЛМАЗЫ!
Южноафриканские ученые
установили, что желтую окраску
алмазам придает примесь
соединений азота. При синтезе
искусственных алмазов соединения азота
используются как катализаторы.
Так как желтые алмазы
встречаются и в природе, очевидно и
естественный процесс их образования
связан с каталитическим
действием этих соединений.
СИГАРЕТНЫЕ ФИЛЬТРЫ
С ИОНООБМЕННОЙ СМОЛОЙ
Серьезная угроза для здоровья
людей — все более
увеличивающееся накопление изотопа поло-
ния-210 в животных и растениях,
так как, внедряясь в организм, он
приводит к разрушению костных
тканей. Один из возможных
источников заражения поло-
нием-210— курение: в организм
попадает полоний-210,
содержащийся в листьях табака. Журнал
«Angewandte Chemie» A967, № 5)
сообщает, что применение фильт^
ра, наполненного ионообменной
смолой, которая используется для
обессоливания морской воды,
позволило значительно сократить
содержание полония-210 в дыму
сигарет. Обычные фильтры
пропускают 50% полония, фильтр с
ионообменной смолой
задерживает более 90% полония-210 из
сигаретного дыма.
ЛИТИЕВЫЕ АККУМУЛЯТОРЫ
Журнал «Science Journal» A967,
№ 11) сообщает об испытаниях
новых так называемых литиевых
аккумуляторных батарей. Ученые
считают, что легкий литиевый
аккумулятор может стать одним
из лучших портативных
источников тока. Катод сделан из литий-
теллурового сплава, анодом
служит чистый литий. Электролит —
смесь галогенидов лития.
Полная перезарядка
аккумуляторов занимает не более 15
минут. Удельная мощность новых
батарей достигает 1100 ватт на
1 кг веса, КПД — 75—80% и
зависит от того, как быстро проходит
зарядка и перезарядка.
Предполагают, что такие
аккумуляторы смогут быть
использованы в комбинации с
топливным элементом для подачи тока
в жилые помещения и
учреждения. Топливные элементы запасают
энергию на длительное время, а с
помощью литиево-теллуровых
аккумуляторов можно получать
ток высокой мощности, когда это
понадобится.
Рисунки
Р. МУСИХИНОЙ
09
ПОЛЕЗНЫЕ СОВЕТЫ
И ПОЯСНЕНИЯ
К НИМ
О забытых рецептах
Бытовая химия разнообразна. Мы широко пользуемся
синтетическими моющими средствами, изделиями из пластмасс,
пятновыводителями, полиролями, пастами для чистки посуды,
растворителями. Но пока нельзя сказать, что промышленность, производящая
химические препараты бытового назначения, дала нам палочку-
выручалочку на все случаи жизни. Существующие пробелы
частично восполняются старыми рецептами, многовековым
опытом матерей и бабушек. И этим опытом не следует пренебрегать.
Сколько таких «бабушкиных рецептов» могли бы прислать в
редакцию читатели «Химии и жизни»! Мне кажется, что журнал
окажет немалую услугу своим читателям, собрав с их помощью
и опубликовав такие рецепты. Повторяю, этим опытом не стоит
пренебрегать, многие из старинных рецептов окажутся полезными
и в наш химический век. В качестве первого материала такого рода
предлагаю несколько известных мне старых рецептов.
БЫЛ ТАКОЙ ЭПИЗОД
Собираясь на дачу, я сунул в
чемодан с бельем походную
аптечку. В дороге раскрылась
склянка с йодом, йод залил
рубашку из белого шелкового
полотна. В химчистку ее не
приняли (хотя, насколько мне
известно, обесцветить йод не
так уж сложно — раствором
гипосульфита, например);
окрасить тоже отказались. Довод
один: шелковое полотно,
дескать, краску не принимает.
— Не горюй, — сказала лиф-
П. П. ДЯТЛОВ, пенсионер,
в прошлом химик
терша, — и шелк-полотно
окрасим.
И действительно окрасила.
— Чем, бабушка, красила?
— А луковой шелухой.
Раньше ей на пасху яйца красили,
и сейчас еще в деревнях таким
отваром красят варежки,
шарфики белые, а девчата — и
волосы в рыжий цвет.
После «луковой» окраски
сорочка выглядела неплохо.
Ведь в луковой шелухе есть
фенольные соединения, они и
окрашивают ткань. А роль
дубителя — вещества,
«прикрепляющего» краску к ткани,
скорее всего сыграла небольшая
добавка кальцинированной
соды. Может быть, старушка
была еще более зрудирована в
химии и технологии крашения
и в качестве дубителя
применила глауберову соль. Я
удивлялся лишь одному — что об
этом простом и старом
средстве не знали в солидном
предприятии, именуемом фабрикой
химической чистки и крашения.
НАРУЖНАЯ ПЛЕНКА ЯЙЦА
Вы помните, как ваша
бабушка хранила яйца впрок? В те
времена холодильников и в
помине не было, и скорее всего,
она пользовалась таким
физико-химическим способом. Яйца
протирали влажной тряпочкой,
сушили на воздухе, а затем
дважды покрывали их тонким
слоем вазелина или глицерина.
Потом завертывали в бумагу и
хранили яйца долгое время в
обычных домашних условиях.
Вазелин или глицерин закры-
70
вали поры в скорлупе,
прекращали доступ воздуха, и
яйцо консервировалось.
У этого способа один
недостаток: при варке такие яйца
давали неприятную, жирную
на ощупь накипь, в кухне
пахло химией. Но можно
модифицировать этот способ, применив
вместо органических веществ
раствор силикатного клея
(содержимое стограммовой
бутылочки растворяется в литре
воды). Способ консервации тот
же, а запаха — нет.
ВСЯК СЕБЕ ХИМИК
Угощала меня старушка
огурцами солеными. Крепкие,
пахучие, чуть пряные на вкус
огурцы сами просились на стол!
— А знаешь, чем я их
консервировала? Горчицей, — и
поделилась секретом.
Чайной ложки горчицы,
разведенной в воде, вполне
достаточно для банки емкостью
в три литра. С такой добавкой
огурцы и без стерилизации
долго сохраняют вкус и цвет,
остаются крепкими, а кроме
того, приобретают слабо
выраженный, но очень приятный
горчичный привкус. Горчица
здесь работает и как пряность,
и как антисептик.
Изобретательница или,
точнее, хранительница этого
способа говорила мне, что мастера
разносолов используют химию
довольно широко: кто кладет
при консервировании
салициловую кислоту, кто аспирин,
кто еще что-то. Не знаю,
каковы на вкус соленья с этими
приправами, но горчица — это
вещь!
СТАРО КАК МИР
Холстами отбеленными
славилась Русь. А чем белили?
Персолем? Нет, солнцем. Мятые
моченые холсты расстилали на
траве у рек и озер, и солнце
своими лучами (главным
образом ультрафиолетовыми)
белило холсты. Распространяться
об этом не стоит, но мораль
ясна: чем бы вы ни стирали
белье, постарайтесь сушить его
на солнце.
КАК УДАЛИТЬ РЖАВЫЕ
ПЯТНА
Белое белье при стирке иногда
приобретает рыжие пятна,
пятна ржавчины. Бороться с ними
крайне трудно: ни
многократная стирка, ни синтетические
моющие средства не помогают.
Но выход есть. Нужно смочить
ржавое пятно теплой водой и
посыпать его щавелевой
кислотой. Ее кристаллы тщательно
растирают, добавляя еще
несколько капель воды. Не знаю
точно, какие реакции при этом
происходят. Скорее всего, идет
частичное восстановление
трехвалентного железа до
двухвалентного. Бурая окись
превращается в светло-зеленую
закись. Кроме того, образуются
бесцветные комплексные
соединения. В результате пятна
бледнеют, приобретают светло-
светло-зеленую окраску, а
после кипячения или двух-,
трехкратного повторения всей
процедуры полностью исчезают.
Говорят, что щавелевую
кислоту можно заменить более
доступной — лимонной (она
продается в бакалейных
отделах продовольственных
магазинов), но ни мной, ни моими
домашними зтот способ пока
не опробован.
ЧТО ТАКОЕ «ТИНОЛЬ»?
В годы НЭПа у
Китайгородской стены был базар. От
Москвы-реки до
Политехнического музея стояли палатки. Чего
только здесь не продавали!
Я в то время работал монтером,
часто приходилось паять
провода, причем качество спая
тщательно контролировалось.
С оловом было трудно, и меня,
как и других монтеров,
выручал «тиноль» — гуталинообраз-
ная паста, продававшаяся на
«развале». Тиноль наносили
поверх места спая и грели
пламенем свечи. Спай получался
прочным. Я узнал, что в состав
тиноля входили олово,
канифоль и какое-то масло. Но как
его приготовляют, я так и не
узнал, хотя у Китайгородской
стены с помощью тиноля паяли
чайники и кастрюли прямо на
глазах.
Прошло много лет. Сейчас,
если мне нужно что-либо
запаять, я ищу кислоту, олово,
паяльник. А было так просто:
свеча и тиноль. Понимаю, что
для промышленности он, может
быть, и не нужен, но для
домашних, не очень
ответственных дел зта паста и сейчас
нашла бы применение. Очень уж
удобно работать с ней.
Может быть, кто-нибудь из
прочитавших эту заметку
помнит, как делается тиноль?
Рисунки
Р. МУСИХИНОЙ
71
ИГРА
Не будьте
легковерными
Писатели-фантасты обычно отталкиваются
от науки. К сожалению, иногда они делают
это настолько энергично, что наука, получив
мощный толчок, кувырком летит из их
произведений.
Печально, когда такого рода фантазия
направляется не в пространство — время, а
на нашу грешную Землю и преобразует наш
мир по мелочам. На первый взгляд это
выглядит очень здорово; чем плохи, например,
таблетки для питания: принял один грамм —
и сыт целый день. Хотите так питаться?
Не соглашайтесь, читатель! Ведь одного
углерода вы теряете за сутки по меньшей
мере 200 граммов, а мы с вами не растения,
к фотосинтезу мы, увы, не приспособлены...
Тем, кто хочет поупражняться в
распознавании подобных «таблеток», и
предлагается публикуемый ниже рассказ. Какие,
по-вашему, ошибки допустил его автор?
Проверить правильность ваших
умозаключений вы сможете, заглянув на
страницу 92.
ТРИУМФ ДИМЫ ОВСЮГОВА
Подходя к конференц-залу минут за пять
до начала своего доклада, Дима
Овсюгов услышал гул. «Ну и набралось
народу,— подумал он. — Повеселиться пришли!
Какой-то мэнээс без степени1 собрался
ниспровергать основы. Ладно, смейтесь,
только последним смеяться буду я!»
В 10 часов 00 минут 21 июля 2078 года
за председательским столом появился, как
обычно, директор института.
— Сегодня мы заслушаем доклад
научного сотрудника лаборатории
преобразования энергии Вадима Александровича
Овсюгова «О возможности создания регре-
tuum mobile2». Пожалуйста, тише!
Дима глубоко вдохнул — будто нырять
собрался — и начал читать.
— В науке давно уже и, как многие
1 Мэнээс без степени — младший научный
сотрудник, не имеющий ученой степени (научн -
быт.).
2 Perpetuum mobile — вечный двигатель (лат.).
думают, окончательно, утвердилось
мнение, что построить вечный двигатель
невозможно. (Председатель: «Тихо!») На чем
основано это мнение? На многочисленных
неудачных попытках создать perpetuum
mobile и на отсутствии удачных попыток.
Был даже сформулирован закон
сохранения энергии; таким образом,
невозможность создания вечного двигателя
узаконена.
Однако (Дима повысил голос)
внимательный анализ экспериментального
материала, на основании которого был
установлен так называемый закон сохранения
энергии (председатель схватил
колокольчик), показывает, что не было предпринято
каких-либо попыток построить вечный
двигатель, в котором один вид энергии
преобразовывался бы в другой. Была,
впрочем, попытка соединить обмотки
электродвигателя и динамомашины, имеющих
общий вал. В этом случае происходит
преобразование механической энергии в
электрическую и наоборот. Однако и неудача
с таким вечным двигателем ничего не
доказывает (голос из зала: «Он рехнулся!»).
Надо думать, что выигрыш энергии при
одном превращении компенсируется
потерей при другом.
Колокольчик не помогал. Председатель
встал и постучал сорокавосьмицветной
авторучкой по бутылке с нарзаном.
— Каждый сможет высказаться во
время обсуждения, — прокричал он.
— Я постараюсь, — произнес Дима в
наступившей тишине, — на конкретном
примере показать несостоятельность доводов
противников вечного двигателя.
Каждому школьнику известно, что
если к электродам, погруженным в
раствор электролита, подвести водород и
кислород, то между электродами возникнет
электродвижущая сила — ЭДС. Такая
система может давать ток. Это топливный
элемент, который был самым
распространенным источником энергии лет сто назад.
ЭДС кислородно-водородного топливного
элемента—1,23 вольта. Если можно
получать кислород и водород электролизом
72
воды при напряжении меньше чем
1,23 вольта, то это значит, что удастся
построить вечный двигатель — потому что
тогда на производство кислорода и
водорода пойдет меньше энергии, чем
получится при их использовании в топливном
элементе. Но можно ли разложить воду
при напряжении меньше 1,23 вольта?
Утверждают, что нельзя...
Аргументация? Пожалуйста! Если
можно получать кислород и водород при более
низком напряжении, можно создать
вечный двигатель, подавая эти газы в
топливный элемент. Итак, почему невозможно
построить вечный двигатель? Потому что
нельзя получать кислород и водород при
напряжении ниже 1,23 вольта. Почему
невозможно получать кислород и водород
при более низком напряжении? Потому
что тогда можно построить вечный
двигатель. Порочный круг замкнулся! Между
тем достаточно поставить простейший
опыт, чтобы убедиться, что вода
разлагается при любом напряжении.
Дима нажал кнопку. Два многоцелевых
кибера3 ввезли демонстрационный стенд
и удалились, чуть слышно шурша поли-
пергидролевыми гусеницами.
— Здесь установлены вольтметр и ги-
перотклонометр4, а также источник тока
и сосуд со щелочью, в который опущены
два платиновых электрода. Напряжение
источника измеряется вольтметром и
подается на электроды. В цепь электродов
последовательно включен гиперотклоно-
метр. Итак, я подаю на электроды всего
одну десятую вольта. Ток может пройти
между электродами только в том случае,
если происходит разложение воды. Сейчас
я замкну цепь, следите за отклонометром!
Стрелка отклонометра резко дернулась,
остановилась на шестом делении, затем
стала ползти назад и окончательно
остановилась на третьем делении. Минуту или
две в зале стояла мертвая тишина. Затем
какой-то старичок, чувствуя, что почва
привычных представлений уходит из-под
ног, сдавленно крикнул: «Стрелку заело!».
Снисходительно улыбнувшись, Дима вы-
3 Многоцелевой кибер — полифункциональное
кибернетическое устройство, применяемое для
подметания улиц, переноски тяжестей и
составления отказов на заявления о выдаче авторских
свидетельств (фант.)
4 Гиперотклонометр ■— прибор, позволяющий
измерять малые электрические токи по
отклонению большой железной стрелки (фант.).
ключил и снова включил рубильник.
Стрелка вернулась к нулю, затем поползла
вправо и уткнулась в третье деление.
— Этот опыт, который следовало бы
поставить лет двести назад, не оставляет
сомнений, что водород и кислород могут
быть получены при достаточно низком
напряжении. До создания вечного двигателя
остался один шаг.
Собственно говоря, нужно только
создать в электролизере над каждым из
электродов инертную атмосферу, — азота,
например, или гелия. До сих пор все как-то
упускали из вида, что напряжение
разложения воды зависит от концентрации
кислорода и водорода в газовой смеси над
растворами. Чем больше мы разбавим эти
газы, тем меньше напряжение разложения.
Кислород и водород, которые
выделяются на электродах электролизера и раз^
бавляются инертным газом, нужно
пропускать через мембраны, проницаемые
только для водорода или только для
кислорода. А разделенные газы направить
к соответствующим электродам топливного
элемента. Теперь эти газы не разбавлены,
для них напряжение разложения в
точности равно 1,23 вольта. Значит, и ЭДС
топливного элемента — такая же. Вот откуда
берется выигрыш энергии!
Остальное, как говорят футболисты,
дело техники (Дима, окрыленный успехом,
позволил себе некоторую игривость
изложения).
Мы построили действующую модель
вечного двигателя мощностью 25 ватт
(кибер ввез на тележке модель). Потребитель
тока — лампочка. Из сказанного ранее
должно быть ясно, что для пуска вечного
двигателя достаточно продуть газовые
камеры топливного элемента водородом и
кислородом. Сейчас я это сделаю!
Дима открыл два крана. Послышалось
шипение, тут же загорелась лампочка. Зал
ахнул. Дима закрыл краны. Лампочка
продолжала гореть — минуту, другую,
третью — в полной тишине. Потом кто-то
начал аплодировать, и вот уже
аплодировали все, вскакивали с мест, что-то
кричали...
Когда Овсюгов выходил из института,
он услышал: «Дима, погоди...»
Обернулся— и увидел сияющие глаза Лены
Крутояровой... Проходивший мимо
многоцелевой кибер сделал вид, что ничего не
замечает.
Г. ГУР.
73
%i*
Вот ок, драгоценный охотничий сильный из известных сейчас
трофей — лягушка кокой, кожа ядов
которой таит в себе самый
**.
*
74
ЖИВЫЕ
ЛАБОРАТОРИИ
Яд лягушки кокой —
самый сильный
небелковый яд
Не так давно в журнале «Journal
of the American Chemical Society»
была опубликована одна из
последних работ известного
американского химика и
биохимика Б. Виткопа и его сотрудников
по расшифровке строения
«самого сильного из известных до
сих пор ядов». Авторы
выражали «глубокую благодарность
миссис М. Лэтам, которая
организовала и непосредственно
возглавила трудное и опасное
путешествие» в Южную Америку
за источником этого яда.
«Красочное описание экспедиции, —
сообщалось далее в статье, —
предполагается опубликовать в
журнале Национального
географического общества». Именно
зта статья об одной из
экспедиций М. Лэтам за редкими
животными и предлагается
читателю на страницах журнала
«Химия и жизнь». Бесспорно,
особый интерес в этом
повествовании представляет рассказ
о ловле лягушек Phyllobates lati-
nasus (Phyllobates bicolor), из
кожного экстракта которых
было выделено в очищенном виде
действующее начало яда,
названное батрахотоксином.
Ранние сведения о кожном
секрете маленькой черной
лягушки кокой, по токсичности
превосходяще м кураре, были
опубликованы еще в 1869 году.
Однако большие трудности,
Академик
И. Л. КНУНЯНЦ,
кандидат химических наук
Н. А. ЛОШАДКИН
связанные с получением этого
яда в достаточных количествах,
делали до самого последнего
времени тщетными любые
попытки выделить токсические
основы яда и расшифровать
химическую природу его
действующего начала. Трудности
возникали в первую очередь в
связи с тем, что «источник» яда
чрезвычайно мал (обычно
взрослая лягушка достигает в длину
всего 2—3 см и весит немногим
более 1 г). В среднем из 100
лягушек можно получить
примерно 275 мг «сырьевого» экстракта,
из которых при последующей
очистке удается выделить около
1 мг очищенного яда. Кроме
того, отыскать крошечных
лягушек у самой земли, в густых
зарослях джунглей, конечно,
очень трудно.
И все же экспедиции М.
Лэтам удалось собрать сотни и
тысячи лягушек кокой. Но тут
возникли новые затруднения.
Попытка перевезти живых
лягушек на самолете из Колумбии
в Вашингтон окончились
неудачей. Тогда было решено готовить
на месте исходный экстракт,
который мог быть доставлен в
лабораторию без потери
активности яда. С этой целью
М. Лэтам была разработана
следующая методика: лягушки
умерщвлялись с помощью
эфира, кожа их немедленно
удалялась и резалась на мелкие
кусочки; затем при комнатной
температуре в течение
нескольких часов проводилась
обработка кожи 70-процентным
метанолом. Полученный в
результате упаривания экстракта в
вакууме и высушивания сухой
плотный остаток сохранял
активность в течение нескольких
месяцев. Из этого остатка в
лаборатории Б. Виткопа с
помощью специально
разработанных способов очистки, которые
включали в себя
последовательную экстракцию органическими
растворителями и
препаративные хроматографические
методы, удалось выделить продукт,
который был идентифицирован
как очищенное основное
действующее начало яда кокой.
В дальнейшем с помощью
тонкослойной хроматографии
удалось выделить три фракции,
имеющие одинаковый состав.
Они были названы батрахоток-
синами «А», «В» и «С».
Детально охарактеризовать свойства
каждой фракции не удалось,
так кад они были получены в
очень небольших количествах:
в распоряжении исследователей
было всего 6 мг батрахотокси-
на «В» и 1 мг батрахотокси-
на «С».
Особый интерес
представляют исследования структуры и
химических свойств яда кокой.
75
Определен молекулярный вес
вещества — 399,24 — что
соответствует строению молекулы
C24H33NO4 (для батрахотоксинов
«А» и «В» предполагается
строение C24H35NO5). Полученный
препарат хорошо растворим в
воде и органических
растворителях: ацетоне и твине-80 (по-
лиоксиэтилен- [20] -моноолеат).
В растворе он не теряет
физиологическую активность. С
помощью ионообменных смол
было показано, что в яде
отсутствуют кислотные группы и
имеется слабоосновная группа,
содержащая атом азота.
Для изучения тонкой
структуры яда кокой были
использованы современные
физико-химические методы анализа: масс-
спектроскопия, ядерный
магнитный резонанс, инфракрасные
и ультрафиолетовые спектры
поглощения. В результате
высказано предположение, что яд
кокой содержит стероидную
циклическую структуру с
несколькими заместителями:
Предполагается, что эти
заместители (R и R') содержат
NO-группу, связанную с
радикалом, в состав которого входят
четыре атома углерода. В
состав заместителей могут также
входить метильная или
альдегидная группы.
Физиологическая активность
очищенного препарата батрахо-
токсина очень высока —
бесспорно, самая высокая из всех
известных в настоящее время
небелковых ядов. Очищенный
Спимок резко
«преувеличивает» размеры кокой. На самом
препарат яда кокой оказался в
несколько раз токсичнее кураре,
паралитического яда тарихоток-
сина (выделенного из
эмбрионов калифорнийского тритона)
и тетродотоксина (выделенного
из рыбы фугу), примерно в
50 раз сильнее нейротоксина
кобры и в 500 раз — яда
морского огурца. Батрахотоксин в
тысячи раз превосходит
токсичность такого яда, как цианистый
натрий.
Все эти сравнения сделаны
на основе сопоставления токсо-
доз, полученных при парэнте-
ральном (внутривенном,
внутримышечном и подкожном)
введении мышам перечисленных
ядов. Подобная оговорка не
случайна, так как для яда кокой
характерна явно выраженная
видовая чувствительность.
Например, оказалось, что кролики
и собаки примерно в 100 раз
более чувствительны к этому
яду, чем мыши, в то время как
лягушки и жабы подвержены
деле это создание умещается в
чайной ложке
действию только очень высоких
доз (смертельные дозы для них
примерно в тысячи раз выше,
чем для мышей).
У пораженных животных
(мыши, кошки) наблюдался
паралич двигательной и
дыхательной мускулатуры. При
подкожном введении летальных доз
смерть животных наступала
уже через несколько минут.
Фармакологическое изучение
показало, что механизм
действия яда кокой сходен с
действием кураре *. По-видимому, яд
оказывает действие и на
центральную нервную систему.
Изучение этого интереснейшего
вещества продолжается.
* См. «Химия и жизнь», 1965,
№ 3.
76
За ядовитыми
лягушками—
в джунгли Колумбии
Марта ЛЭТАМ
Тропический ливень хлестал по
тростниковой крыше моей
хижины. Я препарировала за
столиком партию лягушек Phyllo-
bates latinasus — кокой, как
называют их местные индейцы.
Из кожи лягушек предстояло
затем выделить экстракт
чрезвычайно сильного яда. Занятая
работой, я не могла и подумать,
что через какие-то полчаса буду
изнемогать от боли и мне чудом
удастся спастись от смерти.
Дверь хижины была
открыта; я видела, как вздувшаяся от
дождей река Сан-Хуан несется
мимо деревушки Плайя де Оро
с ее пальмами и глинобитными
хижинами. Эту деревушку я
выбрала в качестве базы для
своей экспедиции, которая в
колумбийских джунглях
занималась охотой за редкими
животными, в первую очередь за
лягушками кокой.
НЕСЧАСТНЫЙ СЛУЧАЙ
Дождь — самая обычная погода
в Чоко, одной из провинций
Колумбии. В здешнем климате,
теплом и влажном, превосходно
чувствуют себя обитатели
лесной подстилки и среди них
черная с желтыми полосками
лягушка кокой. Это создание
столь мало, что умещается в
чайной ложке, однако его кожа
таит в себе самый сильный из
известных сейчас ядов. Веками
индейцы Чоко отравляли этим
ядом стрелы для своих
духовых ружей. Подобные яды,
например, кураре из Южной
Америки и строфантин из Африки
стали основой лекарств, широко
применяемых в хирургии и при
лечении сердечных болезней.
А яд кокой? Имеет ли он
медицинскую ценность? На этот
вопрос пытались дать ответ
исследователи из американского
Национального института
здравоохранения, давшего мне заказ
на большую партию кокой.
/ Я взяла в руки очередную
I влажную лягушку и щелкнула
ножницами. И вдруг — как это
могло случиться? — острие
ножниц оцарапало мой палец.
Я стала быстро высасывать
кровь из ранки и почувствовала
во рту привкус металла.
Спазма сдавила мне горло,
по лицу струились капли пота.
Задыхаясь, я опустилась на
раскладушку, повторяя: «Дышать!
Дышать!..» В течение часа меня
трясло, как в лихорадке. Почти
силой я вливала себе в рот
томатный сок — единственную
жидкость, которая нашлась в
хижине.
На пороге хижины
появились промокшие до костей
индейцы. Они протягивали мне
свою дневную добычу —
лягушек, завернутых в зеленые
листья. Надо было сосчитать их и
заплатить охотникам.
До сих пор не понимаю, как
мне удалось остаться в живых.
По-видимому, дело было в том,
что в ранку попал сырой,
неконцентрированный яд, и я
быстро высосала его из пальца.
Постепенно спазмы ослабели.
Через два часа я снова была на
ногах, заплатила за
принесенных лягушек и рассортировала
их по клеткам.
МОЯ ПРОФЕССИЯ — ОХОТА
Моя профессия — охота за
редкими животными, которые
представляют интерес для научного
изучения. Я специализируюсь
по мелким обитателям джунглей
и горных районов: птицам,
обезьянам, змеям, грызунам. Но
более всего мне памятны
ядовитые лягушки, которых мы
ловили в колумбийских болотах.
О том, что яд этих лягушек
очень силен, я узнала в 1961
году от индейцев провинции Чоко
во время моей экспедиции за
огромными земляными
червями. Местные охотники принесли
мне тогда 50 лягушек кокой.
Я отправила их самолетом
доктору Б. Виткопу, в Вашингтон.
Это были первые живые
лягушки кокой, отправленные за
пределы Колумбии.
«Из 50 экземпляров, которые
были посланы, — рассказывал
мне впоследствии Виткоп, — мы
получили живыми только семь.
Шесть из них не дожили до
следующего утра, а седьмая
была еле жива. К сожалению,
активное начало яда разрушается
под действием ферментов сразу
же после смерти животного».
Из единственной живой
лягушки ученые выделили очень
небольшое количество яда, до-
77
Главное в работе с кокой —
осторожность и еще раз
осторожность!
статочное, однако, чтобы
разжечь их интерес. Во время
следующей экспедиции я послала
уже не лягушек, а сырой яд,
выделенный из 2400 животных.
Из этого сырья было получено
около 30 мг чистого
кристаллического яда — его хватило бы
для умерщвления 3 000 000
мышей!
И вот я снова отправляюсь
в джунгли Чоко. На этот раз
меня сопровождает фотограф
Тор Айгеланд и мой
четырнадцатилетний сын Билли. У меня
снова заказ на лягушек кокой и
гигантских земляных червей,
обитающих на склонах Анд.
ПЕРВЫЕ ПРИГОТОВЛЕНИЯ
С высокого берега реки
Сан-Хуан нас криками приветствовали
мои друзья по предыдущим
путешествиям. Они помогли нам
разгрузить лодку, провели в
хижину. Здесь мы подмели пол,
разложили постели и,
сраженные усталостью после долгого
пути, мгновенно уснули.
Наутро мы вывесили
объявление о том, что будем покупать
гигантских тараканов, обезьян,
муравьедов, и, конечно,
ядовитых лягушек. Не успела я
оглянуться, как Билли заполучил
обезьянку и голубого попугая.
К концу недели в Плайя де
Оро обычно съезжаются
индейцы из лесных поселений.
Раньше они приносили много
лягушек. Я надеялась договориться
с ними и на этот раз.
Утром в воскресенье с улицы
донесся крик Билли: «Индейцы
идут!» Я вышла из хижины и
с радостью приветствовала
своего старого друга Кимико,
который когда-то учил меня
отыскивать в джунглях лягушек.
ЛОВЦЫ ПОДРАЖАЮТ
ЛЯГУШКЕ
«Пойдешь с нами ловить
кокой?», — спросила я Кимико.
Мой гость обменялся
испытующими взглядами со своими
спутниками, долго молчал и
только затем ответил коротким
и гордым кивком головы. На
следующий день мы
отправились в джунгли. Кимико со всем
своим семейством показывал
дорогу, за ними шли Билли, я
и Тор с фотоаппаратами.
Малютку-лягушку трудно
разглядеть в темной зелени.
Как же находят ее индейцы ?
Мы остались на тропе и стали
наблюдать за Кимико. Он
присел в болоте, поднес руку к лицу
и, быстро-быстро постукивая по
щеке, начал свистеть, издавая
звуки, напоминающие голос
лягушки: «чи-чи-чи-чи-чи». С
минуту он посидел молча, потом
над болотом снова послышался
его призыв.
«Чи-чи-чи-чи-чи», —
откликнулась лягушка. Но откуда
исходил ответ? Мое ухо не могло
уловить даже направления
звука. Между тем Кимико не зевал.
Он подпрыгнул с ретивостью,
78
не уступающей лягушачьей, и
приземлился на четвереньки.
В воздухе молнией мелькнула
его рука... Затем охотник сорвал
лист и свернул его в кулек. Он
положил туда пойманную
лягушку, закупорив один конец
комком грязи и завязав
травинкой другой.
Охота продолжалась.
Индейцы внимательно вслушивались
в звуки джунглей, определяя
направление и расстояние до
желанной добычи. Слишком
далеко для одного прыжка? Они
отползли чуть-чуть,
остановились, засвистели снова.
Невидимая кокой ответила и вскоре
оказалась в руках охотников.
Через некоторое время я стала
обладательницей 25 лягушек.
СИЛЬНЕЕ САМОГО
СИЛЬНОГО ЯДА
Мы наблюдали охоту столь же
древнюю, как культура племен,
населяющих здешние места.
Когда-то индейцы охотились на
кокой перед тем, как выйти на
тропу войны. Теперь они
используют отравленные стрелы
лишь для охоты на зверя.
Я рассказала Билли и Тору,
как делают такие стрелы — эту
процедуру мне демонстрировал
когда-то Кимико. Лягушку
насаживают на острую палочку и
держат над пламенем костра.
Кожа лягушки начинает
выделять яд, и охотник обмакивает
в него наконечник стрелы, на
котором имеются спиральные
насечки. В эти насечки и
проникает яд. Одной лягушки
хватает, чтобы отравить 50 стрел
для духового ружья.
Высушенный яд остается смертельным
в течение 15 лет.
Пойманные нами лягушки
были в тот же день
препарированы. Я усыпляла лягушку
эфиром, затем снимала с нее
кожу с помощью ножниц и
пинцета. Именно в такой
момент, несколькими днями
позже, забыв осторожность, я
пренебрегла пинцетом, что стоило
мне нескольких часов мучений.
Разрезанные на кусочки
шкурки я опускала в спирт, затем
разливала раствор по
бутылкам.
Именно из этого экстракта
был получен кристаллический
яд, который оказался в десять
раз сильнее яда японской рыбы
фугу, самого сильного из
известных ядов.
«Не исключена возможность,
что из яда кокой можно
получить хороший лечебный
препарат. Подобные яды уже
используются как сердечные
стимуляторы», — сказал мне доктор
Виткоп и добавил: «Ничего
нельзя знать заранее. Во всяком
случае, это очень интересное
вещество, оно заслуживает
серьезного внимания».
НОВОЕ ПУТЕШЕСТВИЕ
Каждый день индейцы
приходили в Плайя де Оро с
кульками из листьев, наполненными
лягушками кокой. Приносили
они и других животных: менее
токсичных, но более красивых
«пестрых» лягушек, птиц,
мелких позвоночных. Иногда мы
ходили в джунгли вместе с
охотниками. Нас поражало, что
даже их детишки ловко и очень
умело добывают лягушек.
Однажды мы отправились на
долбленых каноэ к истокам реки
Тадозито. Вода Тадозито
кристально чистая, а над рекой
смыкаются ветви деревьев.
Какие-то гигантские белые цветы,
длинные водяные лилии и
экзотические орхидеи делали берега
необыкновенно красивыми. Врг-
мя от времени нам попадались
хижины, окруженные
пальмами и банановыми деревьями.
СЛУХИ О ЖАБЕ-ПТИЦЕЕДЕ
НЕ ПОДТВЕРДИЛИСЬ
Отдохнув в одном из таких
поселений, мы отправились к
большому болоту у истоков
реки. Нашим проводником был
молодой местный вождь. Он вел
нас через сказочный
тропический лес, или, если хотите,
через настоящую зеленую преис-
подню. То и дело нам
приходилось прокладывать путь с
помощью мачете.
На болоте мы надеялись
кроме кокой изловить жабу,
которая, как мне рассказывали,
поедает птиц величиной с
цыпленка и одно прикосновение к
которой стоит жизни. Я уже
много лет безуспешно пыталась
найти эту «sap о de lorn a» —
горную жабу. Не повезло мне и на
этот раз. Может быть,
удивительная жаба и живет в болотах
Тадозито, но нам она на этот
раз не попалась. Зато кокой
водились здесь в изобилии. Через
несколько часов охоты у меня
было уже около 150 лягушек —
больше я вряд ли смогла бы
обработать.
Лягушки кокой окрашены
здесь несколько по-иному:
полоски вдоль спины у них не
желтые, а ярко-оранжевые.
Наше путешествие сильно
затянулось. И когда после
десятичасового пешего перехода мы
подошли к берегу Сан-Хуан, у
меня дрожали колени и по лицу
струился пот. Ноги у нас были
исцарапаны, одежда
пропиталась грязью, и мы умирали от
усталости. Плайя де Оро на той
стороне реки казалась самым
желанным местом на земле.
И все же по возвращении
пришлось сразу же взяться за
дело: надо было приготовить
экстракт яда лягушек...
Сокращенный перевод с
английского Т. ХЕЙФЕЦ
(из журнала «National
Geographic», май 1966 г.)
70
Клуб
Юный
химик
ВИКТОРИНА
Бандиты и старый учитель
1 V 8с Li Mn Те
fen Cu Co TeF6
PdCl2 Zn Ni В
Na InCl3 TeF6
ЬЪ Tb CdCl2 Ci_
Tb Se H20
Ге Sb TeF6 1
Pd Cd Ar
V Cs( 1
Ba FeCl2
l 111 Li InCl3
В небольшом городке Н. за один месяц
было ограблено два магазина. Начальник
городского угрозыска капитан Чибис
подозревал, что главарь банды грабителей —
некто Морковкин, недавно досрочно
освобожденный из заключения. На запрос
о нем Чибису сообщили, что Морковкин
был осужден за кражу, в заключении
хорошо работал и много читал, книги брал
главным образом по химии.
Несколько дней спустя капитан заметил
на стене одного из домов странную
записку. Дворник вспомнил, что видел на том
же месте похожие записки уже два раза,
но думал, что это балуются ребята. Узнав,
когда это было, Чибис удивился: оба раза
записки» появлялись незадолго до
ограбления магазина.
Не шифрованная ли это записка —
ведь Морковкин в заключении усиленно
сыил штудировал химию! Однако, как ни
пытался капитан расшифровать текст, ничего
осмысленного не получалось. Тогда Чибис
отправился за помощью к своему старому
учителю химии Петру Павловичу.
На следующее утро Петр Павлович
позвонил Чибису и сказал: «Двадцать
седьмого в полночь будет ограблен или
пятый, или третий магазин».
Двадцать седьмого в двадцать четыре
часа банда Морковкина была задержана
при попытке ограбления магазина № 3.
Как удалось старому учителю найти
ключ к шифру?
80
ХОТИТЕ ПОДГОТОВИТЬСЯ
К ЭКЗАМЕНАМ ПОЛУЧШЕ!
Задачи на растворы
И в школе, и на вступительных экзаменах
в вузы приходится решать задачи по
растворам. Эти задачи бывают разной сложности.
В этом номере журнала вам предлагаются
«рядовые» задачи. Но даже темг кто
считает, что такие задачи им по плечу, прорешать
их все же стоит — лишняя тренировка перед
экзаменами никогда не повредит...
Задачи подготовлены Д. В.
ПАЛЬЧИКОВЫМ.
ЗАДАЧА № 1
Определите нормальность раствора
азотной кислоты, если титр этого раствора
равен 0,0063 г/мл.
ЗАДАЧА № 2
Сколько граммов гидрата окиси железа
образуется при взаимодействии 200 мл
0,5 н. раствора хлорного железа и 100 мл
2 н. раствора едкого кали?
ЗАДАЧА № з
Сколько граммов хлористого серебра
выпадет в осадок при взаимодействии 20 мл
соляной кислоты плотностью 1,050 г/мл
с 50 г 5%-ного раствора фторида серебра?
ПРОКЛЯТЫЕ КАЛОРИИ
Костя где-то здорово ошибся в расчетах.
С четырьмя литрами даже ледяной воды
ему никак не похудеть. Судите сами:
количество тепла, необходимое для
нагревания четырех литров воды от 0 до 37
градусов, равно 4 • 1000 • 37 = 148 000 кал =
=148 ккал. А 1 кг свинины дает щ>—^+
. B9,97 >: 9000)
+ - Ym 3242,9 ккал. И в организме
остается 3242,9—148 = 3094,9 ккал. Чтобы
ЗАДАЧА № 4
Удельный вес серной кислоты 1,84 г/мл.
Определите ее молярность и
нормальность.
ЗАДАЧА № 5
500 г 10%-ного раствора нитрата бария
вступили в реакцию с 200 мл 2 н. раствора
серной кислоты. Сколько граммов
сульфата бария образовалось?
ЗАДАЧА № 6
Сколько граммов меди выделится на
катоде, если пропустить через раствор
хлорной меди ток силой 10 а в течение одного
часа?
ЗАДАЧА № 7
В каком объемном отношении нужно взять
0,8 н. и 0,3 н. растворы для приготовления
лз них 0,4 н. раствора?
ЗАДАЧА № 8
Сколько 50%-ного раствора следует
прибавить к 10 т 20%-ного раствора, чтобы
приготовить 30%-ный раствор?
Решение задач — на стр. 84
похудеть, Костя должен был получать
2500 ккал, значит, со свининой он получал
3242,9 — 2500 = 742,9 ккал лишних. А
чтобы эти лишние килокалории тратились на
нагревание воды, Косте пришлось бы вы-
742,9
пивать не четыре, а 37 ~ 20 литров
ледяной воды ежедневно!
Но мой друг все же похудел — от
ангины все худеют...
Ответ на вопрос
прошлого номера
81
Имитация диаграммы состояния
сплава типа свинец — олово. На
фотографии состав смеси
изменяется по горизонтали, а тем-
пература — по вертикали.
Поверхность раздела жидкой и
твердой фаз отмечена
стрелками, она воспроизводит линию
Та — Тв на рис. 1
НАШ ПРАКТИКУМ
Секреты сплавов
Обычно сплавы (например, сплав двух
каких-нибудь металлов) исследуют так.
Готовят ряд сплавов с различным
соотношением компонентов, изучают
физико-химические свойства каждого из образцов
(скажем, хотя бы температуру плавления),
эти данные наносят на график, по оси
абсцисс которого откладывают состав, а
по оси ординат — свойство (в нашем
случае — температуру плавления), и затем
отдельные точки соединяют между собой
непрерывной линией. В результате
получается так называемая диаграмма состояния
(рис. 1).
Зачем нужны диаграммы состояния?
Дело в том, что свойства сплавов (совсем
не обязательно только сплава металлов —
это может быть сплав любых веществ)
изменяются не случайно, а строго
закономерно. Поэтому по диаграмме состояния можно
очень быстро и точно найти состав такого
сплава, который обладал бы точно
заданными свойствами (или наоборот, получив
диаграмму состояния, можно сразу же
решить, удастся ли на основе данных
компонентов вообще получить сплав с
заданными свойствами).
Более того. Диаграмма состояния по-
82
ЮО%А
100% Б
Ю0%А
Ю0%Б
Пример простейшей диаграммы
состояния. По оси абсцисс
отложен состав смеси — от 100%
чистого вещества А слева до
100% чистого вещества Б
справа. Та — температура
плавления чистого вещества А; Тс —
температура плавления чистого
вещества Б. Температура
плавления вещества А с примесью
небольшого количества
вещества Б ниже Та; точно так же
температура плавления
вещества Б с примесью небольшого
количества вещества А ниже
Т Б. Смесь, обладающая
минимально возможной
температурой плавления (она обозначена
точкой «a»), wocur название
эвтектики, а Тэ —эвтектической
температуры. Эвтектика
замечательна тем, что она
кристаллизуется сразу вся, в то время
как кристаллизация смесей
другого состава происходит
более сложным образом —
сначала выделяются кристаллы
одного из веществ, а затем
кристаллы эвтектики. Смеси
любого состава затвердевают
полностью при эвтектической
температуре Тэ
Пример более сложной
диаграммы состояния. Вещества
А и Б образуют в точке «б»
химическое соединение В; это
соединение образует эвтектики
«а.» и «в» с веществами А и Б
соответственно. Такая система
характеризуется двумя эвтекти-
ческими температурами ТЭ и
Тэ; температуры плавления
веществ А и Б, а также их
соединения В, в общем случае
различны (при этом Тв может
даже превышать Та и Тб), но
они могут быть и одинаковыми.
На рисунке изображен как раз
случай, когда Та = Т г, = Т в
зволяет судить о тонких процессах,
протекающих в системе при разных
температурах. Например, диаграмма состояния
позволяет обнаружить образование
химических соединений (рис. 2).
Но обычный метод составления
диаграмм состояния имеет и некоторые
недостатки. Во-первых, процесс
изготовления и исследования каждого из
образцов достаточно трудоемок. Во-вторых,
этот метод не позволяет получить картину
самого процесса кристаллизации.
Зачастую, например, большой слиток
получается неоднородным — состав его внешних
слоев отличается от состава сердцевины.
Поэтому, чтобы получить однородный
слиток, приходится тщательно подбирать
режим кристаллизации, а для этого
приходится каждый раз распиливать пробный
слиток, полировать и травить кислотой
поверхность спила, а затем изучать ее под
микроскопом. Таким путем, разумеется,
можно получить сведения лишь об
отдельных этапах кристаллизации — наблюдать
процесс в его динамике принципиально
невозможно.
Но существует очень интересный
способ одновременно и непрерывно следить
за кристаллизацией сплава и наблюдать
фактически готовую (правда, довольно
приблизительную) диаграмму состояния.
Само собой разумеется, для этой цели
используется не сам сплав, а его модель.
Модель эта представляет собой ячейку,
состоящую из двух покровных стеклышек
от микроскопа, склеенных между собой
с двух противоположных краев (рис. 3).
Между этими стеклышками оставляют
тонкий плоский зазор; в этот зазор с двух
сторон вводят по капле разных
прозрачных легкоплавких органических веществ
(например, гексахлорэтана, четырехброми-
88
холодный
стеклянная
ячейка
поверхность
раздела шидной и
твердой фаз
горячий
3
Прозрачная ячейка, состоящая
из двух покровных стеклышек,
скрепленных между собой
с двух сторон. В щели со
сторон А и Б вводятся разные
вещества, которые дают
непрерывный ряд смесей разного
состава
4
Схема устройства,
позволяющего получать диаграмму
состояния и одновременно
наблюдать рост кристаллов разного
состава
стого углерода, камфоры). Веществам дают
частично смешаться — так, чтобы состав
жидкости непрерывно изменялся от одного
края ячейки к другому,— и затем
полученную модель помещают под микроскоп. На
столике микроскопа должны быть два
латунных блока — один горячий (например,
обогреваемый током), а другой холодный
(охлаждаемый проточной водой). Ячейку
кладут на блоки склеенными сторонами
и ждут, пока вдоль нее не установится
постоянный градиент температуры (рис. 4).
Спустя некоторое время под микроскопом
можно будет увидеть готовую диаграмму
состояния, подобную изображенной на
рисунке в начале статьи.
Если при этом равномерно перемещать
модель в сторону холодного блока, то под
микроскопом можно будет одновременно
наблюдать и рост кристаллов самого
различного состава.
Таким способом удалось воочию
увидеть, как внутри слитка возникают зоны
мелких кристаллов. Оказалось, что когда
сплав охлаждается, то затвердевание
начинается с наружной поверхности слитка
и образуются так называемые дендриты
(то есть древовидные кристаллы), которые
внедряются внутрь горячей сердцевины.
Мелкие ветви этих кристаллов
оплавляются, переносятся к центру слитка и
образуют там сплав, отличающийся по своему
составу от состава внешнего слоя.
Этот метод позволит, по-видимому, не
только моделировать процессы
кристаллизации сплавов: его можно в принципе
использовать и для точной идентификации
веществ. Например, если два вещества
совершенно идентичны, то на снимке
получится идеально горизонтальная линия,
а если вещества различны (хотя и
плавятся при одной и той же температуре — при
той же температуре может плавиться и их
смесь, что видно из рис. 2), то это можно
будет сразу же обнаружить по
характерным изломам границы раздела фаз.
По материалам журнала «Scientific American»
Решение задач
(См. стр. 81)
ЗАДАЧА № 1
Найдем сначала массу азотной кислоты,
содержащейся в 1 л раствора:
ш = 1000-0,0063 — 6,3 г.
Поскольку грамм-эквивалент азотной
кислоты равен 63 г, то нормальность взятого
раствора подсчитать нетрудно:
m 6,3
г-экв
63
Следовательно, азотная кислота — деци-
нормальная.
ЗАДАЧА № 2
Такие задачи удобнее решать в
грамм-эквивалентах. Определим число
грамм-эквивалентов хлорного железа:
пг-экв= 0,2.0,5 = 0,i .
Во втором растворе содержится 0,1-2 =
= 0,2 г-экв КОН.
Напишем уравнение реакции:
0,1 г-экв 0,2 г-экв х г-экв
FeCl3 + 3 КОН =i Fe(OHK-T-3KCl.
3 г-экв 3 г-экв 3 г-экв
84
В недостатке — хлорное железо; по нему
и решаем задачу:
0,1-3
х = —тр~ = 0,1 г-экв Fe(OHK
Теперь остается выразить это число
в граммах. Молекулярный вес гидрата
окиси железа 107; значит, грамм-эквива-
107
лент его равен -у- = 35,67.
Итак, образовалось 35,67 -0,1 = 3,567 г
Fe(OHK.
ЗАДАЧА № 3
По удельному весу определим процентную
концентрацию соляной кислоты (см.
школьный задачник, табл. 1). При d"= 1,050 г/мл
концентрация равна 10,17%.
20 мл раствора соляной кислоты весят
20-1,050 = 21 г.
В этих 21 г чистой соляной кислоты
содержится 21 • 0,1017 = 2,14 г.
Теперь найдем вес фторида серебра:
50 • 0,05 = 2,5 г, а затем напишем
уравнение реакции:
2,14 г 2,5 г х г
НС1 + AgF = I AgCl + IJF
36,5 г 127 г 143,5 г
Решаем задачу по фториду серебра,
поскольку он в недостатке.
2,5-143,5
х =
ЗАДАЧА № 4
127
= 2,824 г.
Один литр серной кислоты весит 1000 •
•1,84= 1840 г.
По удельному весу найдем процентную
концентрацию серной кислоты (школьный
задачник, табл. 2). Она равна 95,6%.
В растворе содержится 1840 -0,956 =
= 1759,04 г 100%-ной H2S04.
Теперь найдем молярность серной кис-
1759,04
лоты: ■
98
17,95.
И, наконец, найдем нормальность
серной кислоты. Так как грамм-эквивалент
H2S04 равен 49 г, то нормальность равна
ЗАДАЧА № 5
В первом растворе содержится 500 ■
•ОД = 50 г азотнокислого бария. Так как
грамм-эквивалент серной кислоты равен
49 г, то во втором растворе содержится
0,2-2-49 = 19,6 г H2S04.
Теперь напишем уравнение реакции:
50 г 10,6 г х г
Ва (NG3J -f HaS04 = I BaS04 + 2HN03.
261 г 98 г 233 г
Найдем недостающее вещество.
50
Ba(N03J : ^ = 0,19 (в недостатке);
H-SO-
19,6
98
= 0,2 (в избытке).
Задачу решаем по нитрату бария:
50'233 = 44,6 г BaS04.
х = -
ЗАДАЧА № 6
261
Зная силу тока I (в амперах) и время t
протекания тока (в секундах), можно найти
количество электричества Q по формуле
Q = It.
Q = 10 • «О • «О = 36 000 кулонов.
Грамм-эквивалент меди 64/2 = 32 г.
Определим массу выделившейся меди:
32-36 000
■ = Н,9 г.
96 Ш
ЗАДАЧА № 7
Есть несколько вариантов- решения этой
задачи, но проще всего решать ее по
правилу смешения.
0,8 0,3
\ /
0,4
/ \
0,1 0,4
Следовательно, на один объем 0,8 н.
раствора необходимо взять четыре объема 0,3 н.
раствора, чтобы приготовить из них 0,4 н.
раствор.
ЗАДАЧА № 8
Эту задачу также решаем по правилу
смешения:
50 20
\ /
30
/ \
10 20
Значит, на 10 весовых частей 50%-ного
раствора следует взять 20 весовых частей
20 % -ного. Иными словами, соотношение
равно 1: 2.
Итак, количество 50 % -ного раствора
равно ~2 = о т..
85
Что такое
Нобелевская премия
О. КОЛОМИЙЦЕВА
Рисунок И. ЛИВШИЦ
Наш журнал неоднократно печатал материалы о лауреатах Нобелевской
премии по химии (статьи о работах Н.Н.Семенова, Д.Кроуфут-Хотчкин,
М.Ф.Перутца, М.Снлодовсной=Кюри). Редакция получает много писем, в
которых читатели спрашивают: сколько всего было Нобелевских
лауреатов по химии? когда выдана первая премия? кто такой Нобель'?
Отвечаем.
3 сентября 1864 года, в полдень,
предместье Стокгольма Гелен-
борген потряс ужасающей силы
взрыв. На месте, где еще
несколько минут назад высилась
фабрика нитроглицерина,
принадлежавшая изобретателю
динамита шведскому инженеру
Альфреду Нобелю, осталась
огромная воронка, медленно
наполнявшаяся водой. Под
развалинами соседнего флигеля
нашли тело младшего брата
Альфреда — Оскара Нобеля.
Погиб при катастрофе и самый
близкий друг изобретателя —
химик Хетцман.
Катастрофа сильно
подействовала на Нобеля. Он
продолжает научные исследования, но
выглядит разбитым,
угнетенным. А между тем объем
выпускаемой продукции динамита
растет. Автор изобретения
полагал, что его открытие будет
оказывать помощь людям в
горных работах, в строительстве.
В своих статьях он утверждал,
что в тот день, когда две армии
поймут, что они при помощи
взрывных средств способны
уничтожить одна другую за
несколько секунд, — навсегда
замолкнут орудия, прекратятся
все войны.
Но история развивалась
иначе. Началась франко-прусская
война. Бомбы, начиненные
смертоносным взрывчатым
веществом, падали по обе стороны
линии фронта. Динамит стал
массовым средством уничтожения
н<;
людей, он сеял смерть. И на
этих страданиях наживался
шведский капиталист Альфред
Нобель...
Постепенно Нобель осознает
меру своей ответственности
перед человечеством. Пытаясь
хоть отчасти «сквитать свой
долг», он финансирует мирные
организации и съезды. В 1895
году в Париже Нобель составляет
завещание, согласно которому
основная часть его громадного
состояния должна быть
использована на ежегодные премии его
имени. В завещании подробно
определено, кому эти премии
могут быть вручены:
ПЕРВАЯ — предназначается
автору самого значительного
открытия или изобретения в
области физики;
ВТОРАЯ — присуждается
автору самого крупного открытия
или усовершенствования в
области химии;
ТРЕТЬЯ — дается тому, кто
сделал в истекшем году
важнейшее открытие в области
физиологии или медицины;
ЧЕТВЕРТАЯ — вручается
автору литературного
произведения, наиболее ярко
воплотившего «идеальную идею»
своего времени;
ПЯТАЯ — присуждается
пацифистской организации или
отдельному лицу,
проявившим максимум усилий для
организации мирных съездов
и конгрессов.
Через год после смерти
Нобеля, в апреле 1900 года, это
завещание было утверждено
специальным королевским эдиктом.
В 1901 году были присуждены
первые премии.
За шестьдесят с лишним лет
вокруг процедуры присуждения
Нобелевских премий возникло
много традиций. В области
физики и химии премии
присуждает Шведская академия наук.
В области литературы —
Шведская королевская академия.
Выбор лауреата в области
физиологии и медицины — право
Стокгольмского института
медицины и хирургии. Премией
мира награждает комиссия из
пяти лиц, выбираемая
норвежским стортингом.
Как определяются лауреаты
года?
За полгода до присуждения
премий Шведская академия
наук обращается примерно к
восьмистам людям — крупнейшим
специалистам в своей области,
прежним лауреатам
Нобелевских премий, и спрашивает их
мнение: кто наиболее достоин
эвания нового лауреата
Нобелевской премии? До первого
марта собирают ответы.
Чтобы избежать преждевременных
дискуссий, названные имена
хранятся в строгой тайне. В
сентябре собирается пленум
Академии, идут жаркие прения — и
в предпоследний четверг
октября наконец происходят выборы
лауреатов. Процедура
происходит в парадном зале Дома
биржи в Стокгольме. Согласно воле
Нобеля, шведские ученые
участвуют в выборах бесплатно.
Но по традиции после
присуждения премий каждый член
Нобелевского комитета получает
от управляющего биржей по
серебряному талеру — на оплату
обеда в расположенном
напротив подвальчике-ресторане.
Говорят, ученым премии
присуждаются с меньшими спорами,
чем писателям: очевиднее
конкретные результаты.
Десятое декабря, годовщина
смерти Альфреда Нобеля, —
самый торжественный день.
Король вручает лауреатам
почетные дипломы, медали и чеки на
получение премий. Потом в
«золотом зале» Стокгольмской
ратуши проходит пышный прием.
По правилам, награжденный
должен получить Нобелевскую
премию лично. Если же он не
может прибыть на торжества,
премия вручается
дипломатическому представителю
государства, гражданином которого
является награжденный.
87
Лауреаты Нобелевской премии по химии
Год
Имя ла>реата
Страна
Где проводились
основные
исследования
За какие открытия
и исследования
присуждена премия
Примечания
1901
19U2
1903
1904
1905
1906
1907
1908
1909
1910
1911
1912
1913
1914
1915
1918
В 191G,
Якоб Гендрик
Вант-Гофф
Эмиль Фишер
Сванте Август
Аррениус
Уильям Рамзай
Адольф фон
Байер
Анри Муассан
-Эдуард Бюхнер
Эрнест Резер-
форд
Вильгельм
Фридрих
Оствальд
Отто Баллах
Мария Склодов-
ская-Кюри
Франсуа Огюст
Виктор Гринь-
яр
Поль Сабатье
Альфред Вер-
нер
Теодор Уильям
Ричарде
Рихард Виль-
штеттер
Фриц Габер
~1917, 1919, 1924,
Голландия
Германия
Швеция
Англия
Германия
Франция
Германия
Англия
Гермапия
Германия
Польша,
Франция
Франция
Франция
Швейцария
США
Германия
Германия
1933, 1940,
Берлинский
университет
Берлинский
университет
Стокгольмский
университет
Университетский
колледж в
Лондоне
Мюнхенский ушт*
верситет
Парижский
университет
Сельскохозяйственный колледж
в Берлине
Университет
Виктории в
Манчестере
Лейпциге кий
университет
Университет в Гет-
тпнгене
Пари же кий
университет
Университет в
Наши
Университет в
Тулузе
Университет в
Цюрихе
Гарвардский
университет
Мюнхенский
университет
И пститут
физической химии и
электрохимии в
Берлине
1941 и 1942 годах Но
Иностранный чл.-корр.
Петербургской АН с
1895 г.*
Иностранный ч л. -корр.
Петербургской АН с
1899 i\
Почетный член
Петербургской АН с 1913г.
Иностранный чл.-корр.
Петербургской АН с
1904 г.
Законы химической
динамики и
осмотического давления в
раствора х
Изучение Сахаров и
пуринов
Теорпя
электролитической диссоциации
Открытие инертных
газов в атмосфере и па-
хождение их места в
периодической системе
Работы по органическим
красителям и гидро-
ароматнческим
соединениям
Изучение и выделение
элемента фтора.
Применение оригинальной
электрической дуговой
печи
Исследования в области
биологической химии
и открытие
внеклеточной ферментации
Изучение распада
элементов и химия
радиоактивных веществ
Катализ, химическое
равновесие и скорости
реакций
Работы в области алици-
клических соединений
Открытие радия и
полония, выделение
металлического радия,
изучение природы радия
и его соединений
Открытие реакции его
имени
Гидрирование
органических соединений в
присутствии
мелкодисперсных металлов
Теория комплексных
соединений
Точное определение
атомных весов многих
элементов
Химия красящих веществ
растительного мира,
особенно хлорофилла
Синтез аммиака из азота
и водорода
Нобелевская премия по химии не присуждалась.
Чл .-корр. Российской АН
с 1922 г. Почетный
член АН СССР с 1925 г,
Чл.-корр. Петербургской
АН с 1896 г.
Чл.-корр. Петербургской
АН с 1907 г.
Почетный член АН СССР с
192Н г.
88
Лауреаты Нобелевской премии по химии
Имя лауреата Страна
Где проводились
основные
исследования
За какие открытия
и исследования
присуждена премия
Примечания
Вальтер Герман Германия
Нернст
Фредерик Содди Англия
Фрэнсис У иль- Англия
ям Астон
Фриц Прегль
Рихард Зигмон-
Теодор Свел-
берг
Генрих Отто
Внланд
Адольф Biih-
даус
Австрия
Германия
Швеция
Германия
Германия
Артур Гарден Англия
Ганс Карл Ав- Швеция
густ Симон
фон Эйлер-
Хелппн
Ганс Фишер
Карл Бош
Германия
Германия
Фридрих Гус- Германия
тав Бергнус
Ирвинг Ленг- США
мюр
Гарольд Клей- США
тон Юри
Фредерик Жо- Франция
лно-Кюрп
Ирен Жол но- Франция
Кюри
Петер Позеф Голландия
Вильгельм
Дебай
Уолтер Норман Англия
Хеуорс
Пауль Каррер Швейцария
Берлинский
университет
Оксфордский
университет
Трпнитн-колледж,
Кембридж
Университет в
Граце
Геттингенский
университет
Уисальскнй
университет
Мюнхенский
университет
Геттингенский
университет
Лондонский
университет и
институт Листера
Институт по
изучению
витаминов в
Стокгольме
Мюнхенский
университет
Фирма «Бадише
анилин унд
сода фабрик»
Фирма «И. Г.
Фарбенпнду-
стри»
Фирма «Дженерал
Электрик»
Колумбийский
университет
Парижский
университет
Парижский
университет
Институт физики
и Берлинский
университет
Бирмингемский
университет
Цюрихский
университет
Термохимия
Химия радиоактивных
веществ,
происхождение и природа изотопов
Масс-спектрометрическое
открытие изотопов
большого числа
нерадиоактивных
элементов и установление
закона «целых чисел»
Микроанализ
органических веществ
Коллоидная химия
Работы в области
дисперсных систем
Исследования желчных
кислот и аналогичных
веществ
Строение стеринов и
образование витамина D
из эргостерпна под
действием УФ-облучения
Ферментация Сахаров и
изучение энзимов
ферментации
Ферментация Сахаров и
изучение энзимов
ферментации
Строение красящих
веществ крови и
растений. Синтез гемина Ф
Разработка методов
химии высоких давлений
Химия поверхностных
явлений
Открытие тяжелого
водорода
Синтез новых
радиоактивных элементов
Рен т геностру кту рный
анализ, дифракция
электронов, дипольные
моменты и строение
молекул
Углеводы и витамин С
Каротиноиды, флавины
и витамины А и В«
Чл.-корр. АН СССР с
1924 г.
Иностранный член АН
СССР с 1966 г.
Иностраннып член АН
СССР с 1927 г.
Чл.-корр. АН СССР с
1947 г.
Чл.-корр. АН СССР с
1947 г.
Иностранный член АН
СССР с 1924 г.
89
Лауреаты Нобелевской премии по химии
Год
Имя лауреата
Страна
Где проводились
основные
нсследокания
За какие открытия
и исследования
присуждена премия
Примечания
1938
1939
1943
1944
1945
1946
1947
1948
1949
1950
1951
1952
Рихард Кун
Адольф Буте-
нандт
Леопольд Ру-
жпчка
Дьердь Хевешн
Отто Ган
Артури И л
мари Внртанен
Уэнделл
Стенли
Джеймс Самнер
Роберт
Робинсон
Германия
Германия
Швейцария
Венгрия,
Швеция
Германия
Финляндия
США
Джон Нортроп США
США
Англия
Арне Тизелиус Швеция
Уильям
Фрэнсис Джиок
Отто Дильс
Курт Альдер
Глен Спборг
Эдвин Макмил-
лан
Арчер Джон
Порте])
Мартин
США
ФРГ
ФРГ
США
США
Англия
Институт
медицинских
исследований и Ген дел ь-
бергский
университет
Институт
биохимии и
Берлинский
университет
Высшая
техническая школа в
Цюрихе
Будапештский и
Стокгольмский
университеты
Институт химии
в Берлине
Биохимический
институт и
университет в
Хельсинки
Рокфеллеровский
институт
медицинских
исследований
Рокфеллеровский
институт
медицинских
исследований
Корнельский
университет
Оксфордский
университет
Упсальский
университет
Калифорнийский
университет
Университет в
Киле
Университет в
Киле
Калифорнийский
университет
Калифорнийский
университет
Национальный
институт
медицинских
исследований
в Лондоне
Каротиноиды и витамины
Половые гормоны
Полиметплены и высшие
терпены
Использование изотопов
в качестве
индикаторов при изучении
химических реакций
Открытие расщепления
ядер тяжелых атомов
Агрохимия и удобрения.
Консервация кормов
Получение чистых
энзимов и вирусных белков
Кристаллизация ;>нзпмов
Исследование
алкалоидов и других
биологически важных
растительных веществ
Электрофорез и
адсорбционный анализ.
Установление гетерогенной
природы протеинов
Химическая
термодинамика. Свойства
веществ вблизи
абсолютного нуля
Открытие диенового
синтеза
Химия трансурановых
элементов
Распределительная
хроматография
Под давлением гнтлерся
с кого правнтельст!
отказался от премии
Под давлением гитлеро!
ского правительств
отказался от премии
Иностранный член А
СССР с 1958 г.
Иностранный член А
СССР с 1966 г.
90
Лауреаты Нобелевской премии по химии
Год
1953
1954
1955
1956
1957
1958
1959
1960
19G1
1962
1963
1964
1965
1966
Имя лауреата
Ричард Лоренс
Миллингтон
Снндж
Гермап Штау-
дингер
Лайнус Карл
Полинг
Винсент дю
Виньо
Николай
Николаевич
Семенов
Сприл Норман
Хнншелвуд
Александр
Тодд
Фредерик Сенд-
жер
Ярослав Гей-
ровский
Уиллард Ф.
Лнбби
Мелвин
Кельвин
Джон Каудерп
Кендрыо
Макс
Фердинанд Перутц
Карл Циглер
Джулио Натта
До1Х)ти Кроу-
фут-Хотчкпн
Роберт Вудворд
Роберт Сендер-
сон Маллн-
Страна
Англия
ФРГ
США
США
СССР
Англия
Англия
Англия
ЧССР
США
США
Англия
Англия
ФРГ
Италия
Англия
США
США
Где проводились
основные
исследования
Роуэтовский
исследовательский
институт
Фрайбургский
университет
За какие открытия
и исследования
присуждена премия
Распределительная
хроматография
Химия
высокомолекулярных веществ
Калифорнийский Природа химической свя-
технологический зи и строение комп-
институт
лексных соединений
Корнельскнй уни- Биохимические соедпие-
верситет
Институт хими- 1
ческой
физики АН СССР
Оксфордский
университет j
Кембриджский
университет
К ембриджский
университет
Институт поляре
графин АН ЧСС
К ал ифо рнип ский
университет
Калифорнийский
университет
Кембриджский
университет
Кембриджский
университет
Институт
исследования
угля в
Мюнхене
Миланский
технологический
институт
Сомервилл-колледж, Оксфорд
Гарвардский уш
верситет
Чикагский ун]
верситет
ния серы. Первый
синтез полипептидного
гормона
Механизмы химических
\ реакции
Нуклеотиды и нуклео-
тидные ко-эвзимы
Строение протеинов, в
частности инсулина
Полярография
;р
Радиоуглеродное
датирование
Фотосинтез
Строение глобулярных
белков
Химия и технология
высокомолекулярных
соединений
Рентгеноструктурное
определение строения
витамина В12 и других
важных
биохимических объектов
I- Развитие искусства
органического синтеза
п- Развитие метода
молекулярных орбит. Иссле-
Прпмечання
Иностранный
СССР с 1958
Чл .-корр. АН
1929 г., акад
Иностранный
СССР с 1958
Иностранный
СССР с 19G6
Иностранный
СССР с 1966
член АН
г.
СССР с
. с 1932 г.
член АН
г.
член АН
г.
член АН
г.
Рональд Нор- Англия
риш
Джордж Портер Англия
Манфред Эйген ФРГ
Кембриджский
университет
Королевский
институт в
Лондоне
Институт
Макса Планка в
Геттингене
дование природы
химической связи и
электронного строения
молекул
Сверхскоростные
химические реакции
91
Исправленная ошибка
(ВМЕСТО РЕДАКЦИОННОЙ ПОПРАВКИ К
НАПЕЧАТАННОМУ)
В 1966 году в № 8 и 9 нашего
журнала была опубликована
статья известного
американского биохимика Джорджа Уолда
«Происхождение жизни». Эта
статья открывалась
предисловием, написанным советским
коллегой автора — академиком
Александром Евсеевичем Браун-
штейном. Представляя
читателям автора статьи, академик
Браунштейн отметил, в
частности, что Уолд — лауреат
Нобелевской премии.
Как только номер нашего
журнала вышел в свет, в
редакции раздался звонок:
— Говорят из редакции
журнала «Наука и жизнь». Мы
готовим к печати статью Уолда
(речь шла о статье
«Детерминизм, индивидуальность и
проблема свободной воли»,
опубликованной в № 1 и 2 «Науки и
жизни» за 1967 год). У вас
написано, что Уолд — Нобелевский
лауреат, а насколько нам
известно, он этой премии не
получал. Уточните, пожалуйста,
откуда зти сведения...
Без особого воодушевления
звоним академику Браун-
штейну:
— Александр Евсеевич, вы
писали, что Уолд — лауреат
Нобелевской премии. Это
действительно так?
На другом конце провода
искреннее удивление:
— А что, разве ему ее не
присуждали? Не может быть!
Впрочем, я проверю.
И проверка показала
(напоминаем, дело было осенью
1966 года), что Джордж Уолд
не получал Нобелевской премии.
Налицо был самый
обыкновенный журнальный «ляп»...
Но прошел всего лишь год
с небольшим, и мы прочли в
газетах, что за работы по
изучению биохимии зрения Дж. Уол-
ду вместе с двумя другими
учеными — Холденом Хартлингом
(США) и Рагнаром Гранитом
(Швеция) — присуждена
Нобелевская премия 1967 года... Сама
жизнь исправила нашу ошибку,
о которой мы сообщаем с
очевидным опозданием.
Не будьте легковерными
(См. стр. 72)
До полного триумфа Диме Овсюгову
оставалось совсем немного — устранить всего
лишь две ошибки в своих рассуждениях. Но
в том-то вся и загвоздка, что одну из них
устранить никак нельзя...
Вот эти ошибки.
1. Опыт с разложением воды, который
демонстрировал Дима Овсюгов, ничего
не доказывает, поскольку электроды были
просто опущены в раствор, но не
изолированы от воздуха. Поэтому на одном из них
мог выделяться кислород, а на другом —
ионизироваться кислород воздуха. Таким
образом, ток мог проходить через
электролизер и без разложения воды. Но это еще
полбеды...
2. Теперь эти газы не разбавлены.
Напряжение разложения воды, как и ЭДС
топливного элемента, зависит не от того,
насколько кислород и водород разбавлены
инертным газом, а только от их
парциальных давлений (парциальное давление — это
давление, которое имел бы данный газ,
если бы он при той же температуре
занимал весь объем смеси). Парциальные же
давления газов по обе стороны мембран,
проницаемых для них, одинаковы. Поэтому
ЭДС топливного элемента будет в лучшем
случае равна напряжению разложения
воды в электролизере, но никак не больше!
Значит, и этот вечный двигатель, как и все
его предшественники, работать не будет...
92
УЧИТЕСЬ
ПЕРЕВОДИТЬ
Французский—
для химиков
Прежде всего, проверьте перевод предложений,
помещенных в предыдущем номере.
1. В лесохимических лабораториях общества
«Прожиль» исследуются новые области
применения уже известных инсектицидов и веществ,
убивающих грибок: таких, как пентахлорфенол,
хлорокись меди, этиленбисдитиокарбаминовая
кислота, гексахлорбензол.
2. Знание числа оптических электронов (тех,
которые находятся на внешней орбите) помогает
определить валентность элементов:
одновалентных — с 1 или 7 электронами, двухвалентных —
с 2 или 6, трехвалентных — с 3 или 5,
четырехвалентных — с 4.
3. Исследовательские работы общества «Пьер-
фит» в области органических производных
фосфора направлены на изучение макромолекул с
двух- и трехмерной решеткой на основе фосфора,
из которых изготовляются прозрачные,
бесцветные и негорючие пластмассы; кроме того, в
настоящее время завод «Пьерфит» разрабатывает
метод придания огнестойкости целлюлозе, дереву,
бумаге и текстилю.
4. Суспензоиды — это разновидности
гидрофобных коллоидов, не адсорбирующих воду;
например, хлористое серебро, которое можно
получить методом Бредига (электрогол) или путем
химической реакции (колларгол).
5. Применение современных методов анализа,
таких как полярография и спектрография в
ультрафиолетовых лучах, позволило получить
практически чистое вещество A0—12 частей
примесей на миллион).
ХИМИЧЕСКИЕ СИМВОЛЫ
Зная словообразовательные элементы,
заимствованные из греческого и латинского языков,
значительно легче понять французские
научно-технические тексты.
Кроме зтих элементов, во французских
текстах из области химии читатель встречает
хорошо известный ему комлекс общепринятых
международных символов и названий химических
элементов. Примерно 50% этих названий
образованы с помощью суффикса -ium, произносящегося
по-французски как «йом» и имеющего русский
аналог — ий. Этот способ очень продуктивен и
используется при наименовании новых
элементов, как например: kourtchatovium — курчатовий,
mendelevium — менделевий.
Однако многие французские названия
химических элементов, приведенные ниже, имеют
некоторые особенности и не всегда совпадают с
соответствующими названиями на русском языке.
Символ Название Символ Название
Ag
As
Au
С
F
Fe
H
К
Mg
Mil
элемента
Argent
Arsenic
Or
Carbone
Fluor
Fer
Hydrogene
Potassium
Magnesium
Manganese
Na
О
Pb
s
Sb
Sn
w
Zn
элемента
Sodium
Ox у gene
Plomb (произносится
pic)
Soufre*
Antimoine
Etain
Tungstene
Zinc (произносится
zsk)
Некоторые элементы имеют по два названия:
одно из них совпадает с общепринятым
международным, другое употребляется только во
французском языке. Символы у этих элементов тоже
двойные. Это элемент гафний — Hafnium (Hf) или
Celtium (Ct) и бериллий — BeriHium (Be) или
Glucinium (GI). Производные от названий этих
* Наряду со словом soufre во французском
языке имеется его дубликат греческого
происхождения thio-, который образует много
производных: thioacide — тиокислота, thiokol —
полисульфидный каучук, тиокол, thiophenol — фенилмер-
каптан, тиофенол и т. д.
элементов часто образуются именно от их
французских дублетов (glucine — окись бериллия).
кислоты и соли
При чтении французских химических текстов
иногда могут возникнуть трудности в переводе
названий солей. Эти названия во французском
языке образуются с помощью латинских
суффиксов -ate, -ite и -иге, которые в латинском
языке образуют названия кислотных остатков *.
Суффикс -ate образует названия солей
кислородных кислот с максимальной валентностью
кислотообразующего элемента. Ему соответствует
русский суффикс -ат. Например:
bromate — соль бромноватой кислоты, бромат;
nitrate — соль (или эфир) азотной кислоты,
нитрат;
phosphate — соль (или зфир) фосфорной
кислоты, фосфат
Суффикс -ite образует названия солей
кислородных кислот со средней или минимальной
валентностью кислотообразующего элемента. Ему
соответствует русский суффикс -ит. Например:
chlorite — соль хлористой кислоты, хлорит;
nitrite — соль (или эфир) азотистой кисло-
нитрит;
phosphite — соль (или зфир) фосфористой
кислоты, фосфит;
chromite — соль (или эфир) хромистой
кислоты, хромит (а также хромистый
железняк).
Суффикс -иге образует названия солей
бескислородных кислот. В русском языке ему
соответствует суффикс — ид. Например:
bromure •— соль бромистоводородной
кислоты, бромид;
chlorure — соль соляной кислоты, хлорид;
titanofluorure — соль титанофтороводородной
кислоты.
ной соли. Такое название как во французском,
так и в русском языке образуется сочетанием
двух или нескольких слов. При этом в
большинстве случаев французское определяющее слово
становится определяемым и наоборот *.
arsenite neutre de potas-—
sium
bromate de potassium —
broinate de sodium —
bromure d'ammonium —
bromure
bromure
bromure
bromure
bro inure
bromure
chlorate
d "argent
chromique
t'erreux
ferrique
cuivreux
cuivrique
d'ammonium
rhlorite de sodium —
chlorure d'alluminium —
chromate mercureux —
chromate mercurique —
chromite de potassium —
iodure d'argent —
iodure chromique —
iodure ferreux —
iodure mercurique —
nitrate d'argent —
nitrate t'erreux -—
nitrate ferrique —
nitrite de potassium —
phosphite monosodique —
phosphite disodique
titanate de barium
средний мышьякови-
стокислый калий;
бромноватокислый
калий;
бромноватокислый
натрий;
бромистый аммоний,
бромид аммония;
бромистое серебро;
трехбромистый хром;
бромистое железо;
бромное железо;
бромистая медь;
бромная медь;
хлорноватокислый
аммоний;
хлористокислый
натрий;
хлористый алюминий,
хлорид алюминия;
хромовокислая закись
ртути;
хромовокислая окись
ртути
хромит калия;
йодистое серебро;
трехйодистый хром;
йодистое железо;
двуйодистая ртуть;
азотнокислое серебро;
азотнокислая закись
железа;
азотнокислая окись
железа;
азотистокислый калий,
первичный кислый
фосфор и сток ис л ый
натрий;
вторичный кислый
фосфористокислый
натрий;
титанат бария.
Зная значение суффиксов, образующих
типовое название групп солей во французском языке,
можно легко перевести название любой конкрет-
* Эти суффиксы могут иметь и другие
значения. Например, слово aldehydate означает вообще
продукт присоединения аммиака или аминов
к карбонильной группе альдегидов; titanite — зто
название минерала, представляющего собой тита-
носиликат кальция, а слово micanite (от mica —
слюда) — название одного из
электроизоляционных материалов. Таким образом, опознать
названия солей по указанным суффиксам можно лишь
«посмотрев в корень» слова — он должен
означать название элемента, образующего соль
данной группы.
Если вы встретите такое словосочетание, в
котором первым словом будет уже известное вам
типовое название соли, а вторым — слово acide
(кислота), то переводить его надо так:
iodure d'acide — йодангидрид;
bromure d'acide — бромангидрид;
chlorure d'acide — хлорангидрид;
chlorure de I'acide
benzene sult'onique — бензолсульфохлорид.
Как вы уже заметили, в вышеприведенных
примерах прилагательные, образующиеся от на-
* Правда, некоторые названия переводятся
дословно: nitrure de bore — нитрид бора, но такие
случаи редки.
04
Место склейки
звания металла, могут иметь два суффикса: -еих
и -ique, причем первый суффикс отражает
меньшую валентность, а второй — большую.
Например:
titaneux — содержащий трехвалентный титан;
titanique — содержащий четырехвалентный
титан;
chromeux — содержащий двухвалентный хром;
ehromique — содержащий трехвалентный хром;
chloreux — хлористый;
chlorique — хлорноватый.
Здесь уместно заметить, что в последние годы
русский химический язык имеет тенденцию
«освободиться» в названиях солей от суффиксов,
отражающих степень валентности, и перейти на
международный способ ее выражения. Например,
chlorure cuivreux (хлористая медь) и chlorure
cuivrique (хлорная медь) записываются как
хлорид меди (I) и хлорид меди (II). В названиях же
кислот можно придерживаться традиционных
суффиксов -истая и -ная: acide azoteux —
азотистая кислота; acide azotique — азотная кислота.
Для того чтобы закрепить прочитанный
материал, переведите следующие отрывки из
журнальных статей, обращая внимание на знакомые
вам слова и словосочетания.
1. Dans la plupart des pays du nionde le role de
fertilisant du sol estattribue au triplet: azote, phos-
phore, potassium; ma is cT a pros la nouvelle ecole de
professeur Homes («La Nature», Novembre 1964) et
d'autres chercheurs, il faut associer a N, P et К
trois autres elements fondamentaux: soufre,
magnesium et calcium, pour avoir une fumure dite equili-
bree. Pendanl Iongtemps Tazote et la potasse etaient
i'ouruis aux cultures sous forme de sulphates d'am-
inonium et de potassium, renter man t respectivement
24 et 18 pour 100 de soufre.
2. Atteinte par la penurie de soufre, l'industrie
ehimique s'est orientee vers des for mules ou Ies
elements considered comme essentfels (N, P, K) se
trouvaient concentres. С'est ainsi que rammoniac
anhydre, l'acide phosphor ique, Ies phosphates el
nitrates d'ammonium ont ete substitues aux engrais
traditionnels, en eliminant ainsi 1c soufre, consi-
clere comme une «impurete».
3. I/etude par diffraction electronique des filmes
d"oxyde a niontre que lorsque le inetal est chauffe
dans Pair a em iron cent trente degres, on obtient
Ies figures de diffraction qui correspondent a Poxy-
de stanneux. Aux temperatures plus elevees, il se
produit une transformation en oxyde stamiique. II
est probable que le i'ilme forme a Pair aux
temperatures ordinaires est constitue par de Poxyde
stanneux.
Старший преподаватель
Московского института
химического машиностроения
Т. Н. КОМРОВСКАЯ
95
Заочная
читательская
конференция
1968 года
Уважаемый читатель! Редакция журнала
«Химия и жизнь» обращается к Вам с просьбой
ответить на ряд вопросов, поставив галочки в
соответствующих кружочках в разделах I, II и III.
Например, если Вы ждете от химии помощи
в быту, работаете в совхозе и окончили среднюю
школу, поставьте галочки против вопросов 1-3,
II-3 и III-6; если Вы работаете в заводской
лаборатории, одновременно учитесь в химическом
вузе и хотите, чтобы журнал помогал Вам в
работе и учебе, отметьте кружочки против
пунктов 1-1, 1-2, II-l, II-2, II-6, Ш-4 и Ш-6; если Вы
химик с ученой степенью, работаете в
лаборатории и любите фантастику, поставьте галочки
против пунктов 1-5, II-1, III-1 и Ш-2 и т. д. —
так, чтобы в каждом из разделов I—III было
отмечено не менее одной строки.
Если у Вас есть какие-нибудь конкретные
замечания или пожелания — изложите их на
свободном месте. Затем аккуратно отрежьте
страницу, сложите ее и опустите в почтовый ящик;
марку наклеивать не обязательно, хотя и
желательно...
Спасибо
I. ЧЕГО ВЫ ЖДЕТЕ ОТ ЖУРНАЛА
«ХИМИЯ И ЖИЗНЬ»?
О 1-1- Помощи в работе.
О 1-2. Помощи в учебе.
О 1-3. Полезных сведений для дома.
О 1-4. Удовлетворения любознательности.
О 1-5. Занимательного досуга.
II. ЧЕМ ВЫ ЗАНИМАЕТЕСЬ?
О П-1. Работаете (или работали) в лаборатории.
О П-2. Работаете (или работали) на
предприятии.
О И-3. Работаете (или работали) в колхозе,
совхозе.
О П-4. Работаете (или работали) в учреждении.
I О П-5. Обучаете (или обучали) химии.
О И-6. Учитесь (или собираетесь учиться
дальше).
III. ВАШЕ ОБРАЗОВАНИЕ?
I О Ш-1. Доктор или кандидат наук.
I О Ш-2. Высшее химическое,
О Ш-3. Высшее нехимическое.
О Ш-4. Студент-химик.
I О Ш-5. Студент-нехимик.
I О Ш-6. Среднее законченное.
О Ш-7. Среднее незаконченное.
Место склейки
Линия сгиба
-а
К
со
В
СО ш
и S
р в
о **
W £» се
со 5
Ю В >>
<**
*н *
S 4 21
Кроссворд
До сих пор наш журнал кроссвордов не
печатал. С пониманием относясь к
пристрастию отдельных наших читателей к
кроссвордам, мы тем не менее полагали,
что научно-популярный журнал призван
скрашивать досуг читателям иными
способами. Но целая серия писем с просьбой
печатать кроссворды и с кроссвордами
собственного изготовления побудили нас один
раз отступить от традиции...
По горизонтали:
1. Установка с демпфирующим устройством.
8. Источник химических знаний. 10. Теоретик,
отличающийся крайней педантичностью. 11.
Золотисто-коричневая жидкость со специфическим
запахом. 13. Тонкая газопроницаемая прослойка,
выполняющая отчасти теплозащитные функции.
17. Сестра матери известного химика. 18.
Роговое образование фиксированной формы и цвета.
19. Стеклянный или фарфоровый сосуд для
сыпучих тел. 20. Средство разрешения
неразрешимой научной проблемы. 23. Инструмент для
манипуляции со сложными смесями
органических веществ. 25. Период фазового перехода
гидрида кислорода. 27. Куполообразное сооружение,
не оборудованное устройством противопожарной
безопасности. 29. Мелкодисперсная смесь с
высоким содержанием белковых веществ. 30.
Группа домов, включающая в себя здание известного
химического вуза. 31. Истинный
первооткрыватель реакции Гриньяра.
По вертикали:
2, Инструмент, с помощью которого были
зафиксированы некоторые положения квантовой
химии. 3. Препарат, употребляемый как химиками,
так и биологами. 4. Отравляющее вещество.
5. Совокупность элементов, включающая по
меньшей мере одну подгруппу. 6. Нагревательный
прибор. 7. Сложная смесь органических веществ.
9. Изделие из медного сплава. 12. Юный химик.
14. Горючее. 15. Руководитель химического
факультета одного из столичных вузов. 16.
Развернутый профиль. 21. Представитель приматов.
22. Помощник алхимика. 23. Мера длины, не
вошедшая в систему СИ. 24. Исходный продукт для
приготовления мелкодисперсной смеси с высоким
содержанием белковых веществ. 26. Очень
крупный химик. 28. Один из продуктов деятельности
химической лаборатории. 29. Пакля.
«Ежели кушанье, которым я
угощаю вас нынче,
приготовлено неудачно, то повинен в этом
не столько мой повар, сколько
химия, находящаяся еще в
пеленках»,— говорил мсье д'Аста-
рак, герой романа Анатоля
Франса «Харчевня королевы
Гусиные Лапы», алхимик
XVIII века. А. Франс — не
единственный писатель, в
произведениях которого можно найти
размышления о веществе и его
превращениях. О химии писали
Овидий и Руссо, Гете и
Достоевский. Этим «химическим»
страницам литературной
классики посвящена статья
И. Г. Жирнаускаса, которая
будет опубликована в следующем
номере журнала.
Элемент плутоний и
«химические профессии» микробов, ре -
ставрация древней керамики и
необыкновенная разновидность
воды — вот темы некотопыпг
других статей пятого номера.