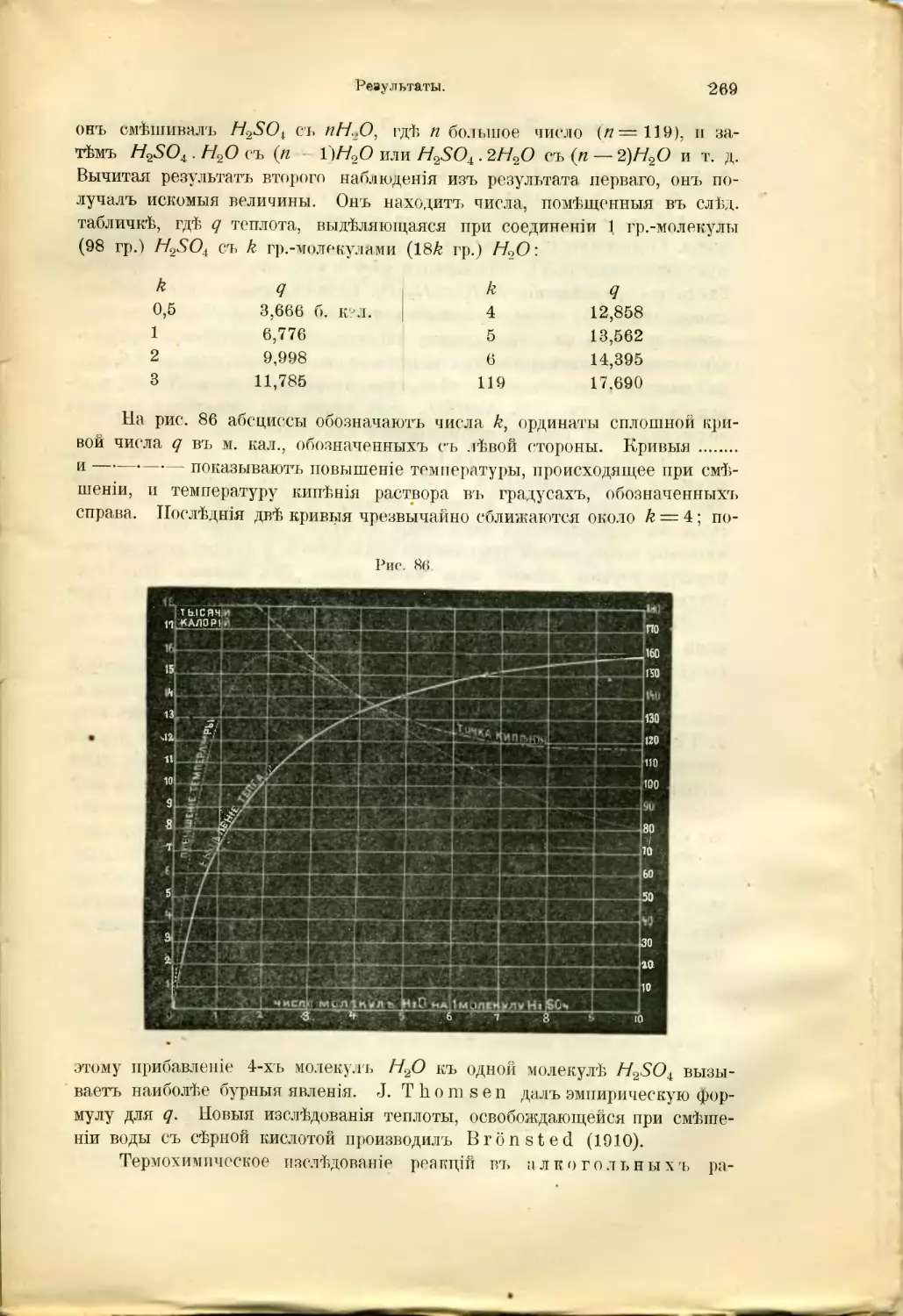
Text
изик
О. Д. ХВОЛЬСОНА.
ТОМЪ ТРЕТІИ.
Ученіе о теплотѣ.
ИЗДАНІЕ ТРЕТЬЕ.
Пересмотрѣнное и значительно дополненное.
Съ 220 рисунками въ текстѣ.
С.-ПЕТЕРБУРГЪ.
Изданіе К. Л. РИККЕРА.
Невскій проспектъ, 14.
1912.
Типографія Эд. Бергмана, Юрьевъ, Лифляндія.
Предисловіе къ третьему изданію.
Это изданіе существенно отличается отъ предыдущихъ:
нѣкоторыя статьи замѣнены другими и во всѣхъ главахъ вне-
сены добавленія, относящіяся къ изслѣдованіямъ, появившимся
послѣ выхода въ свѣтъ второго изданія.
Приношу глубокую и сердечную благодарность Ѳ. Ѳ. Со-
колову, съ величайшею тщательностью не только читавшему
корректуры, но и постоянно обращавшему мое вниманіе на
разнаго рода промахи.
О. Хвольсонъ.
Спб., Апрѣль 1912 г.
ОГЛАВЛЕНІЕ ІП-го ТОМА.
отдѣлъ девятый.
Ученіе о теплотѣ.
Глава первая. Введеніе.
§ 1. Тепловая энергія . . . ................
§ 2. Температура............... . . .......... ......
§ 3. Температурные коеффиціенты.......... ........................
§ 4. Нѣкоторыя предварительныя свѣдѣнія . . ...................
СТР.
1
5
9
12
Глава вторая. Термометрія.
§ 1. Задача термометріи . ... .... .......... . . . 15
§ 2. Газовый термометръ............. 18
§ 3. Термометры съ жидкостями . 25
§ 4. Термометры ртутные; ихъ изготовленіе. . . . . . 28
§ 5. Калибрированіе термометровъ.............32
§ 6. Вліяніе свойствъ стекла и ртути, а также внѣшнихъ физическихъ
причинъ на показанія ртутныхъ термометровъ..................................37
§ 7. Поправка на выступающій наружу ртутный столбикъ ................40
§ 8. Сравненіе ртутныхъ термометровъ между собою и съ нормальнымъ
водороднымъ.................................................................41
§ 9. Термометры для спеціальныхъ цѣлей...............................44
§ 10. Вѣсовой термометръ ........................................... 47
§ 11. Другіе способы измѣренія не очень высокихъ температуръ .... 49
§ 12. Пирометры. Измѣреніе высокихъ температуръ...................... 52
§ 13. Оптическая пирометрія.................. ... . ... .59
§ 14. Термоэлектрическіе пирометры................................ 62,
§ 15. Измѣреніе весьма низкихъ температуръ. 70
§ 16. Термостаты......................................................72
Литература......................................................74
Глава третья. Зависимость размѣровъ и давленія тѣлъ отъ
температуры.
§ 1. Температурные коеффиціенты размѣровъ твердыхъ тѣлъ........79
§ 2. Методы опредѣленія коеффиціентовъ расширенія твердыхъ тѣлъ. . 82
§ 3. Результаты измѣренія расширенія твердыхъ тѣлъ.............90
VI
СТР
§ 4. Вліяніе температуры на объемъ анизотропныхъ тѣлъ; расширеніе
кристалловъ . . /..........................................................95
§ 5. Обзоръ способовъ опредѣленія теплового расширенія жидкостей.
Расширеніе ртути .................................................... 101
§ 6. Тепловое расширеніе и термическій коеффиціентъ давленія воды. . 112
§ 7. Тепловое расширеніе и термическій коеффиціентъ давленія другихъ
жидкостей 124
§ 8. Тепловое расширеніе и термическій коеффиціентъ давленія газовъ.
Теорія 128
§ 9. Тепловое расширеніе и термическій коеффиціентъ давленія газовъ.
Опыты 135
Литература..........................•..........................149
Глава четвертая. Теплоемкость.
§ 1. Введеніе. . . . ........................ .... 154
§ 2. Теплоемкость воды................................... . . 158
§ 3. Способъ Ьаѵоіеіег и Ьаріасе’а................................... 166
§ 4. Способъ ледяного калориметра Германа и Вшіьеп’а . . 167
§ 5. Способъ Раѵге’а и ЗіІЪегтапп’а.................................. 171
§ 6. Способъ смѣшенія ... . . .............. . . 173
§ 7. Способъ охлажденія .... . . 185
§ 8. Способъ конденсаціи паровъ.......................... .... 187
§ 9. Различные способы опредѣленія теплоемкостей. ... ... 188
§ 10. Теплоемкость твердыхъ и жидкихъ тѣлъ . . . . . 190
§ 11. Теплоемкость газовъ .... .... . . . . . . 199
§ 12. Теплоемкость газовъ при постоянномъ давленіи . . . 203
§ 13. Теплоемкость газовъ при постоянномъ объемѣ . . ... 211
§ 14. Опытныя опредѣленія величины к — С&: . . . ... 216
§ 15. Связь между теплоемкостью тѣлъ и ихъ молекулярнымъ или атом-
нымъ вѣсомъ.............. ...................................... . • 228
Литература............. ............................ .... 244
Глава пятая. Переходъ различныхъ формъ энергіи въ энергію
тепловую. Термохимическія явленія.
§ 1. Источники тепла.............................................. 251
§ 2. Основныя положенія термохиміи ... ... . . . 256
§ 3. Термохимическіе методы изслѣдованія ..................... - . 263
§ 4. Нѣкоторые результаты термохимическихъ изслѣдованій . . 2б7
Литература.............................................. • 272
Глава, шестая. Охлажденіе тѣлъ
§ 1. Введеніе. . . . ... . . 273
§ 2. Законъ Ньютона................ . . . 276
§ 3. Законъ Ппіоп&'а и Реііѣ........................................277
§ 4. Формулы Зіеіап’а, Ьогепг’а, КоееНі, Ѵіоііе’я, Терешина и др. Охлаж-
деніе твердыхъ тѣлъ въ жидкостяхъ.................. ... . ... . 284
§ 5. Численныя величины для скорости охлажденія . .... 286
Литература.................................................... 287
Глава седьмая. Теплопроводность
§ 1. Введеніе. . . . . . ................... . . 288
§ 2. Понятіе о математической теоріи теплопроводности . . ... 290
§ 3. Рѣшеніе нѣкоторыхъ простыхъ задачъ, относящихся къ теплопро-
водности ЗОО
VII
СТР.
§ I. Опытное изслѣдованіе относительной теплопроводности твердыхъ
тѣлъ.......................................................................308
§ 5. Опредѣленіе абсолютной теплопроводности твердыхъ тѣлъ . . . . 317
§ 6. Теплопроводность анизотропныхъ тѣлъ...........................327
§ 7. Теплопроводность жидкостей.......... ................. . 331
§ 8. Теплопроводность газовъ....................................... 338
§ 9. Температурный скачекъ на границѣ двухъ тѣлъ . . . 350
Литература............................................ ... 353
Глава восьмая. Основы термодинамики.
§ 1. Введеніе................................................... 358
§ 2. Первое начало......................... - . • 360
§ 3. Механическій эквивалентъ теплоты.................. • 362
§ 4. О выраженіяхъ вида Хйх + Ѵ(1у гдѣ X и У функціи отъ х и у . 378
§ 5. Величины, опредѣляющія состояніе вещества...................381
§ 6. Обратимые и необратимые процессы............. ... ... 384
§ 7. Круговые процессы. Графическія изображенія . 395
§ 8. Теплота, получаемая тѣломъ............................ • • 398
§ 9. Формулы, основанныя на первомъ началѣ ... . . 404
§ 10. Круговой процессъ Карно .... .............. .... 405
§ 11. Второе начало термодинамики; основанія работъ Сагпоі и Сіаибіие’а. 409
§ 12. Второе начало термодинамики; работы Тіютеоп’а, Воіігтапп'а и др.;
регреішші тоЫІе второго рода.......................................... . 420
§ 13. Абсолютная шкала температуръ, предложенная \Ѵ. Тііошбоп’омъ
(ЕогсІ Кеіѵіп)..............................................................423
§ 14. Формулы, основанныя на второмъ началѣ. . . . .... 425
§ 15. Энергія тѣла. Формула КігсйѣоН’а...................... . 429
§ 16. Энтропія и ея свойства............................ ... 432
§17. Свободная энергія и термодинамическій потенціалъ................438
§ 18. Система, состояніе которой опредѣляется многими перемѣнными;
условія равновѣсія системы................................................ 441
§ 19. Заключеніе. . . . . ...................................443
Литература. . .... ......................... . 445
Глава девятая Приложенія термодинамики къ явленіямъ,
нами уже разсмотрѣннымъ.
§ 1. Идеальные газы ... . . . . • 448
§ 2. Реальные газы .... . . . . . ... 458
§ 3. Газовый термометръ............... . . . .......... 463
§ 4. Поверхностное натяженіе.................... . . . 464
§ 5. Энергія и энтропія твердыхъ и жидкихъ тѣлъ...................467
§ 6. Истинная теплоемкость по Сіаиэіие’у............. .... 467
§ 7. Теплоемкости с? и сѵ для тѣлъ твердыхъ и жидкихъ........... 468
§ 8. Адіабатическое измѣненіе состоянія жидкихъ и твердыхъ тѣлъ . 470
§ 9. Растяженіе твердыхъ тѣлъ................................. 473
§ 10. Давленіе лучистой энергіи и законъ Стефана . .... 476
§11. Гипотеза Нернста .... ................. .... 479
Литература............................ . . ... .181
Глава десятая. Переходъ изъ твердаго состоянія въ жидкое
и обратно. Приложеніе термодинамики къ общему случаю
перехода вещества изъ одного состоянія въ другое.
§ 1. Общія замѣчанія. Фаза......................... ... .... 483
§ 2. Точка плавленія. Идеи Тамманна.................................... 485
§ 3. Точка плавленія сплавовъ. ... . . . ... 490
ѵш
СТР.
§ 1. Переохлажденіе.................... . 493
§ 5. Измѣненіе объема тѣлъ при плавленіи............................494
§ 6. Приложеніе термодинамики къ общему случаю перехода вещества
изъ одного состоянія въ другое ... ............................... . 498
§ 7. Вліяніе давленія на точку плавленія ..... .... 502
§ 8. Теплоемкости С и с твердыхъ и жидкихъ тѣлъ . . . 510
§ 9. Скрытая теплота плавленія......................................510
§ 10. Скрытая теплота аллотропическихъ превращеній; вліяніе давленія
на температуру превращенія . . . .... . . . . . 514
Литература.....................................................517
Глава одиннадцатая. Переходъ изъ жидкаго и твердаго
состоянія въ газообразное и обратно.
1.
2.
3.
4.
5.
6.
7.
8.
Испареніе и ожиженіе . ... .... ... 520
Кипѣніе..................................................... 524
Сфероидальное состояніе............... .... . 530
Скрытая теплота испаренія и кипѣнія........................ ... 532
Приложеніе началъ термодинамики къ явленіямъ испаренія жидкостей 550
Сгущеніе газовъ.................... . ......................558
Испареніе твердыхъ тѣлъ . . ... . . . . 570
Диссоціація . . ... . . .... 575
Литература. ... . ... . . ... 576
Глава двѣнадцатая. Свойства насыщенныхъ паровъ.
Ги грометрія.
§ 1. Введеніе.......................................................581
§ 2. Методы опредѣленія упругости насыщенныхъ паровъ................582
§ 3. Измѣренія упругости насыщеннаго пара, произведенныя до Ке^паиіі 584
§ 4. Опредѣленія Ке^паиіі и Ма^ппе’а упругости насыщеннаго пара . . 588
§ 5. Измѣренія упругости насыщеннаго пара, произведенныя послѣ Ке^папН 591
§ 6. Формулы для упругости насыщеннаго пара........................596
§ 7. Зависимость упругости насыщеннаго пара отъ формы поверхности
жидкости и отъ внѣшнихъ силъ, дѣйствующихъ на эту поверхность.............604
§ 8. Вычисленіе удѣльнаго объема и плотности насыщенныхъ паровъ . 608
§ 9. Опытныя опредѣленія плотности и удѣльнаго объема насыщенныхъ
паровъ .... . . ................ . . . . . . 610
§ 10. Теплоемкость с насыщенныхъ паровъ . .......... ... 619
§ 11. Теплоемкость с насыщенныхъ паровъ . . . ............625
§ 12. Законъ Ваііоп’а.............................................. 625
§13. Гигрометрія.................... . . .......... ... 629
Литература. ... .... ............ ... , . 637
Глава тринадцатая. Ненасыщенные пары. Критическое
состояніе. Ученіе о соотвѣтственныхъ состояніяхъ.
§ 1. Введеніе................... . . . . . . 642
§ 2. Теплоемкость ненасыщенныхъ паровъ...............................643
§ 3. Плотность, упругость и тепловое расширеніе ненасыщенныхъ паровъ 645
§ 4. Формула Ѵап-(іег-\ѴааІ8’а................... . ... 650
§ 5. Формула Сіаившб’а и другія..................................... 657
§ 6. Критическая температура и критическое состояніе •.............. 664
§ 7. Экспериментальное изслѣдованіе критическаго состоянія вещества 674
§ 8. Ученіе о соотвѣтственныхъ состояніяхъ . . 684
Литература............ 695
IX
Глава четырнадцатая. Равновѣсіе соприкасающихся
веществъ. Правило фазъ. Растворы.
СТР.
§ 1. Введеніе.....................................................699
§ 2. Кріогидраты..................................................701
§ 3. Правило фазъ.......................... ... ... 704
§ 4. Термодинамическая теорія слабыхъ растворовъ по Ріапск’у. . . . 714
§ 5. Растворимость................................................719
§ 6. Осмотическое давленіе и диффузія въ растворахъ. . ...........723
§ 7. Теплота растворенія и разбавленія................ . . 725
§ 8. Диссоціація и двойной обмѣнъ въ растворахъ . 733
§ 9. Упругость пара и точка кипѣнія растворовъ . 735
§ 10. Затвердѣваніе растворовъ . . .... . . . 748
Литература. . . .................. . . .... 754
Предметный указатель . . .758
Указатель русскихъ авторовъ ... . . . . 762
Указатель иностранныхъ авторовъ. . . 764
ГЛАВА ПЕРВАЯ.
Введеніе.
§ 1. Тепловая энергія. Въ т. I мы познакомились съ понятіемъ
объ энергіи; мы видѣли, что энергія проявляется въ различныхъ фор-
махъ, которыя раздѣляются на двѣ группы. Къ первой группѣ относятся
различныя формы энергіи кинетической, существеннымъ признакомъ ко-
торой представляется движеніе вещества: вторую группу составляютъ
разнообразныя формы энергіи потенціальной, количественно опредѣляемой
въ зависимости отъ расположенія вещества. Мы указали на воз-
можность несуществованія потенціальной энергіи, всѣ случаи которой,
можетъ быть, сведутся когда-нибудь къ пока еще неизвѣстнымъ формамъ
энергіи кинетической. Въ предыдущихъ двухъ томахъ нами были по-
дробно разсмотрѣны слѣдующія формы энергіи:
1) Кинетическая энергія движущагося тѣла: она измѣряется жи-
вою силою
7=2^ ......... (1)
тѣла, гдѣ т масса, ѵ скорость тѣхъ частей, на которыя мы мысленно
раздѣляемъ тѣло. Точнѣе мы напишемъ
У = і ѵ-сіт.......................(2)
гдѣ интегрированіе распространено на всѣ элементы йт массы тѣла.
2) Потенціальная энергія массъ, притягивающихся по закону Нью-
тона. Она измѣряется разностью П^о — й/, гдѣ Жо наибольшее значе-
ніе, котораго можетъ достигнуть потенціалъ двухъ массъ другъ на друга
при крайнемъ физически возможномъ ихъ сближеніи, П/ значеніе того
же потенціала при данномъ расположеніи массъ. Въ случаѣ одной си-
стемы матеріальныхъ точекъ, величина 117 представляетъ потенціалъ си-
стемы самой на себя.
3) Лучистая энергія (т. II), которая представляется энергіей особаго
рода движенія, распространяющагося въ эфирѣ.
4) Энергія упруго измѣненнаго тѣла. Нѣкоторые частные случаи этой
формы энергіи были нами указаны въ т. I.
Теперь мы приступаемъ къ изученію энергіи тепловой, которую мы
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. III, изд. 3-е. 1
2
Введеніе.
считаемъ за кинетическую энергію движенія частицъ или молекулъ. За-
пасъ тепловой энергіи выражается формулою (1)
<3 = * 2 ...................(з)
если за единицу тепловой энергіи принять ту, которая въ абсолютной
системѣ единицъ вообще принимается за единицу какого бы то ни было
рода энергіи, т.-е. ту, которая эквивалентна единицѣ работы (т. I). Та-
кую единицу мы будемъ называть механическою единицею тепло-
вой энергіи или просто теплоты. Въ формулѣ (3) подъ т
слѣдуетъ подразумѣвать массы всѣхъ тѣхъ мельчайшихъ частицъ тѣла,
которыя въ данный моментъ движутся со скоростями ѵ, вообще неодина-
ковыми. Современное ученіе о сложномъ составѣ молекулъ не только
химическихъ соединеній, но и простого вещества въ твердомъ, жидкомъ
и газообразномъ (съ немногими исключеніями) состояніи, заставляетъ
насъ считать то движеніе, живою силою (1) котораго измѣряется запасъ
тепловой энергіи въ тѣлѣ, состоящимъ изъ движенія молекулъ, а можетъ
быть и нѣсколькихъ связанныхъ между собою молекулъ, движущихся
какъ одно цѣлое, и изъ внутренняго «интрамолекулярнаго» дви-
женія составныхъ частей молекулы, движущихся безъ разрыва той связи,
которая называется химическимъ сродствомъ и соединяетъ ихъ въ одно
цѣлое. Впрочемъ мы должны считать весьма вѣроятнымъ, что при не-
прерывныхъ столкновеніяхъ частицъ между собою, какъ слѣдствіе ихъ
движенія, должно весьма часто происходить раздробленіе сложныхъ ча-
стицъ и молекулъ на ихъ составныя части. Допущеніе такихъ раздробленій
играетъ важную роль въ теоріи нѣкоторыхъ физическихъ явленій и мы съ
нимъ встрѣтимся напр. при изложеніи современнаго ученія объ электролизѣ
(разложеніе вещества, введеннаго въ замкнутую электрическую цѣпь).
Тепловая энергія есть энергія движенія неправиль-
наго, безпорядочнаго (ип^еогдпеЬ); это движеніе представля-
етъ крайнюю противоположность движенію даннаго тѣла (системы моле-
кулъ), какъ цѣлаго, при которомъ скорости всѣхъ частицъ тѣсно
связаны между собою: въ кинематикѣ доказывается, что въ каждый, дан-
ный моментъ скорость ѵ частицы складывается изъ скорости по-
ступательнаго движенія, общаго всѣмъ частицамъ, и скорости ѵ2 враща-
тельнаго движенія съ нѣкоторою угловою скоростью со около оси, парал-
лельной направленію скорости ѵъ причемъ положеніе оси и скорость
одинаковы для всѣхъ частицъ. Существуютъ и другіе случаи правиль-
наго, т.-е. упорядоченнаго (^еогйпеі) движенія частицъ тѣла, хотя и не
движущагося, какъ цѣлое. Въ видѣ примѣра можно указать на сложное
движеніе струны, дающей, кромѣ основного, еще рядъ добавочныхъ то-
новъ; далѣе — на аналогичный сличай движенія звучащаго столба воз-
духа въ трубѣ, на движеніе пластинки (Хладніевы фигуры), или вообще
на движеніе частицъ какой бы то ни было среды при распространеніи
въ ней звуковыхъ колебаній; наконецъ, сюда же относятся движенія ча-
стицъ, соотвѣтствующія вихревымъ движеніямъ, и т. д.
Тепловая энергія.
3
Тепловое движете—наименѣе правильное: оно не подвержено, на-
сколько извѣстно, никакимъ условіямъ, связывающимъ величины и на-
правленія движенія частицъ, по крайней мѣрѣ, если эти частицы не со-
сѣднія. Не трудно понять, что именно такое движеніе должно быть на-
иболѣе вѣроятнымъ. Дѣйствительно, представимъ себѣ систему дви-
жущихся частицъ, причемъ характеръ движенія не обусловленъ никакими
заданіями. Для каждой частицы всѣ направленія движенія въ данный мо-
ментъ одинаково возможны, а потому и одинаково вѣроятны. Въ этомъ
случаѣ наиболѣе вѣроятнымъ является движеніе вполнѣ безпорядочное,
при которомъ, если число частицъ весьма велико, всѣ направленія
движенія встрѣчаются приблизительно одинаково часто. Безпрерыв-
ныя столкновенія частицъ между собою должны способствовать устано-
вленію такого равномѣрно-безпорядочнаго движенія. Всякое другое рас-
предѣленіе скоростей должно быть менѣе вѣроятнымъ, а наименѣе вѣро-
ятнымъ является такое распредѣленіе скоростей, при которомъ система
движется какъ цѣлое. Равномѣрно-безпорядочное движеніе
устанавливается само собою. Всякое упорядоченное движеніе
вызывается опредѣленными внѣшними причинами, вліяющими на систему
частицъ. Разъ такое движеніе системы установилось, оно, въ силу ос-
новныхъ законовъ механики (инерціи), можетъ продолжаться неопредѣ-
ленно долго. Но если существуетъ малѣйшая причина, мѣшающая без-
препятственному продолженію упорядоченнаго движенія, то должно обна-
ружиться стремленіе къ переходу системы отъ упорядоченнаго движенія
къ движенію равномѣрно-безпорядочному, какъ болѣе вѣроятному. Обрат-
наго стремленія не существуетъ: равномѣрно-безпорядочное движеніе ча-
стицъ лишь при исключительныхъ условіяхъ можетъ перейти въ движе-
ніе упорядоченное.
Нетрудно было бы провести аналогію съ толпою людей, въ которой
порядокъ установить трудно и онъ легко разстраивается. Упорядо-
ченное движеніе вызывается исключительными обсто-
ятельствами и легко разстраивается, т.-е. имѣетъ стрем-
леніе къ переходу въ движеніе равномѣрно-безпоря-
дочное. какъ въ наиболѣе вѣроятное.
Прилагая сказанное къ движенію тепловому, которое и есть дви-
женіе равномѣрно-безпорядочное, мы получаемъ слѣдующій весьма важ-
ный выводъ:
Тепловое движеніе частицъ есть движеніе наибо-
лѣе вѣроятное. Всякое не-тепловое движеніе матеріи
должно имѣть стремленіе къ переходу въ движеніе
тепловое. Такой переходъ вызывается малѣйшими причинами, раз-
страивающими не-тепловое, т.-е. болѣе или менѣе упорядоченное дви-
женіе. Иначе:
Не-тепловая энергія движенія матеріи имѣетъ
стремленіе перейти въ энергію тепловую. Такой переходъ
мы наблюдаемъ при всякомъ ударѣ, при треніи и т. д. Энергія
1*
4
Введеніе.
тепловая лишь при исключительныхъ условіяхъ, такъ
сказать, искусственно, можетъ быть преобразована въ
не-тепловую энергію движенія матеріи.
Что нужно понимать подъ «исключительными условіями будетъ вы-
яснено впослѣдствіи (см. термодинамику).
Внутренній строй матеріи опредѣляется съ одной стороны интен-
сивностью теплового движенія частицъ, съ другой — тѣми еще неразга-
данными причинами, которыя дѣйствуютъ между частицами и которыя
получили для наглядности названіе «силъ сцѣпленія». Подъ вліяніемъ
этихъ причинъ сохраняется нѣкоторое среднее разстояніе между части-
цами тѣлъ твердыхъ, и отчасти тѣлъ жидкихъ. При ихъ отсутствіи или
достаточной малости, частицы тѣлъ удалились бы другъ оть друга на
разстоянія, которыя зависѣли бы только отъ внѣшнихъ, условій, т.-е. на-
личности свободнаго пространства, и отъ ньютоновскихъ силъ взаимнаго
кажущагося притяженія между частицами. На допущеніи отсутствія силъ
сцѣпленія основана, какъ мы видѣли, кинетическая теорія идеальныхъ га-
зовъ (т. I). тепловымъ движеніемъ частицъ которыхъ опредѣляются и
объясняются ихъ свойства.
Первоначальное представленіе о теплотѣ получается на основаніи
особаго рода ощущенія, вызываемаго тѣлами, до которыхъ мы дотроги-
ваемся или которыя находятся близко отъ насъ. Эти ощущенія распре-
дѣляются по своей интенсивности въ непрерывный рядъ, идущій какъ
бы отъ нѣкотораго нуля въ обѣ стороны. Ощущенія, соотвѣтствующія
двумъ частямъ этого ряда, качественно различны; они называются ощу-
щеніями тепла и холода. Положеніе нуля зависитъ отъ случайнаго
теплового состоянія частей нашего тѣла, воспринимающихъ ощущенія.
Параллельно съ измѣненіемъ теплового ощущенія, вызываемаго матеріей,
наблюдаются измѣненія разнообразныхъ другихъ ея свойствъ. Относи-
тельно сущности причины, обусловливающей какъ эти ощущенія, такъ и
эти свойства, т.-е. относительно сущности теплоты, существовали въ раз-
ное время различныя теоріи. Если не считать мнѣнія отдѣльныхъ лицъ,
то можно сказать, что до сороковыхъ годовъ ХІХ-го столѣтія теплота
считалась за особаго рода вещество, за одно изъ «невѣсомыхъ», отъ на-
личнаго запаса котораго въ тѣлѣ зависитъ тепловое состояніе этого по-
слѣдняго. Нѣкоторыя подробности изъ исторіи возникновенія новаго уче-
нія, разсматривающаго теплоту, какъ форму кинетической энергіи, будутъ
указаны въ главѣ, посвященной термодинамикѣ, всецѣло опирающейся,
какъ мы увидимъ, на два начала, изъ которыхъ первое и заключается
въ томъ, что теплота есть форма энергіи, межд^ тѣмъ какъ нѣкоторый
намекъ на второе начало заключается въ томъ, что выше было сказано
о тепловомъ движеніи, какъ наиболѣе вѣроятномъ движеніи частицъ и о
стремленіи другихъ формъ кинетической энергіи матеріи переходить въ
энергій) тепловую.
Съ измѣненіемъ запаса тепловой энергіи мѣняются почти всѣ свой-
ства матеріи, а потому намъ приходилось уже въ предыдущихъ двухъ
Температура.
5
томахъ указывать на зависимость большого ряда явленій отъ теплового
состоянія матеріи. Въ видѣ примѣра укажемъ хотя бы на зависимость
поверхностнаго натяженія жидкостей, скорости звука, коеффиціента пре-
ломленія и т. д. отъ теплового состоянія матеріи. Большое число сюда
относящихся данныхъ было приведено въ ученіи о газахъ, въ особен-
ности, въ главѣ, посвященной кинетической теоріи газовъ. Выведенное
или указанное раньше мы, вообще говоря, въ этой части нашего курса
повторять не будемъ, за исключеніемъ тѣхъ случаевъ, когда болѣе по-
дробный разборъ намъ дастъ возможность обобщить то, что уже было
изложено.
Различные отдѣлы ученія о теплотѣ еще тѣснѣе между собою свя-
заны, чѣмъ отдѣлы другихъ физическихъ ученій, хотя бы напр. ученія
о лучистой энергіи. Въ особенности это относится къ тѣмъ отдѣламъ, съ
которыхъ по необходимости приходится начинать изученіе тепловыхъ
явленій: въ главѣ объ измѣреніи температуры, какъ самой основной изъ
величинъ, встрѣчающихся въ ученіи о теплотѣ, мы почти непрерывно
имѣемъ дѣло съ явленіемъ теплового расширенія тѣлъ; главу же о тепло-
вомъ расширеніи тѣлъ неудобно излагать ранѣе разсмотрѣнія способовъ
измѣренія температуръ. Чтобы выиги изъ этого затрудненія, мы предпо-
сылаемъ обѣимъ главамъ краткій обзоръ нѣкоторыхъ понятій и фактовъ,
впрочемъ, болѣе или менѣе извѣстныхъ изъ элементарнаго курса физики.
На нѣкоторые изъ нихъ уже было указано въ началѣ т. I и мы неодно-
кратно на нихъ ссылались въ т. I и т. II; подробное же ихъ изученіе
помѣщено ниже въ различныхъ главахъ этого тома.
§ 2. Температура. Ощущеніе даетъ намъ представленіе о возмож-
ности у одного даннаго тѣла различныхъ степеней нагрѣтости. кото-
рыя мы можемъ представить себѣ расположенными въ непрерывный рядъ.
Степень нагрѣтости тѣла характеризуется терминомъ «температура».
Сравненіе температуръ двухъ различныхъ тѣлъ на основаніи ощущенія
при соприкосновеніи нашего тѣла къ тѣламъ невозможно. Температуры
двухъ различныхъ тѣлъ называются одинаковыми, если при взаимномъ
ихъ соприкосновеніи не мѣняется ихъ температура, т.-е. степень нагрѣ-
тости : при этомъ предполагается, что тѣла при соприкосновеніи не дѣй-
ствуютъ другъ на друга химически. Въ противномъ случаѣ равенство
температуръ двухъ тѣлъ обнаруживается равенствомъ каждой изъ нихь
съ температурою третьяго тѣла. Изъ двухъ тѣлъ М и А/, не дѣйствую-
щихъ химически другъ на друга, обладаетъ болѣе высокою температурою
то тѣло, которое при соприкосновеніи (смѣшеніи) тѣлъ /И и А/ охлажда-
ется. При этомъ другое тѣло непремѣнно нагрѣвается, если только со-
прикосновеніе тѣлъ не вызываетъ перемѣны состоянія одного изъ нихъ
или обоихъ. Въ противномъ случаѣ одно изъ двухъ тѣлъ можетъ сохра-
нить свою температуру Гнапр. если горячее тѣло помѣстить въ ледъ
при 0° или весьма холодное тѣло въ воду при 0°). Въ этомъ случаѣ из-
мѣненіе температуры другого тѣла укажетъ, которое изъ нихъ обладало
болѣе высокой температурой. Впрочемъ, бываютъ случаи, когда смѣшеніе
6
Введеніе.
тѣлъ 7И и 7Ѵ не даетъ намъ отвѣта на вопросъ о томъ, которое изъ нихъ
было теплѣе; это тѣ случаи, когда при смѣшеніи температуры обоихъ
тѣлъ уменьшаются (ледъ и ЫаСГ). Смѣшеніе тѣлъ /14 и не можетъ
вызвать повышенія температуръ обоихъ тѣлъ, если только эти тѣла не
дѣйствуютъ химически другъ на друга.
Болѣе глубокое изслѣдованіе понятія о температурѣ можно найти
въ книгѣ М а с Гі’а Віе Ргіпсіріеп йег ЛѴаегтеІейге», Беіргі^ 1896
(стр. 39—57) и въ замѣчательной статьѣ Н. Н. Шиллера «Возникно-
веніе и развитіе понятія о температурѣ», Кіевъ 1899 г.
Впослѣдствіи мы увидимъ, что существуетъ возможность дать слѣ-
дующее опредѣленіе понятія о болѣе высокой температурѣ: тѣло А обла-
даетъ болѣе высокою температурою, чѣмъ тѣло В, если
существуетъ возможность какими бы то ни было ма-
нипуляціями перенести теплоту отъ А къ В безъ того,
чтобы этотъ переходъ сопровождался какими-либо из-
мѣненіями въ другихъ тѣлахъ.
При достаточно тѣсномъ соприкосновеніи (смѣшеніи) дв^хъ или нѣ-
сколькихъ тѣлъ всегда само собою устанавливается равенство ихъ
температуръ. Въ этомъ заключается одинъ изъ результа-
товъ упомянутаго выше стремленія къ равномѣрно-
безпорядочному движенію, при которомъ среднее значеніе жи-
вой силы движенія частицъ, опредѣляющей, какъ мы предполагаемъ, тем-
пературу, одинаково во всѣхъ частяхъ системы. Это особенно ясно,
когда тѣла /14 и Л/ по природѣ одинаковы.
Въ т. і мы указали на температуру, какъ на одно изъ понятій,
встрѣчающихся въ физикѣ, которыя не могутъ называться величинами,
и потому не могутъ быть измѣрены. Въ непрерывномъ ряду темпера-
туръ мы можемъ только отмѣтить опредѣленныя точки или репёры (фран-
цузское слово, часто употребляемое на русскомъ языкѣ, напр. на-
шими геодезистами); это даетъ намъ возможность построить шкалу тем-
пературъ и при ея помощи измѣрять температурные интервалы. Репе-
рами служатъ температуры таянія льда и кипѣнія воды при внѣшнемъ
давленіи въ 760 мм. ртутнаго столба, а также и другія «постоянныя»
температуры.
К і с И а г сі 8 и СйигсйШ (Хеіі8сйг. 1. РЬуз. Сйет. 26 р. 690, 1898,
28 р. 313, 1899), затѣмъ Кісйагсіз и ЛѴе1І8 (іЬід. 56 р. 348, 1906)
и Ріс1іагсІ8 и ѴѴгеде (іЬісІ. 61 р. 313, 1907) указали цѣлый рядъ
такихъ постоянныхъ температуръ, которыя могутъ служить постоянными
точками въ шкалѣ температуръ. Онѣ соотвѣтствуютъ тѣмъ нонварі-
антиымъ состояніямъ системы тѣлъ, о которыхъ будетъ сказано впо-
слѣдствіи. Особенный интересъ представляетъ «точка превращенія >
соли Ха2804 + ЮН20, которая находится при 32°,383 водородной шкалы
(см. ниже). Въ главѣ XIV мы эти работы подробно разсмотримъ.
Всякое такъ называемое «измѣреніе температуры» есть въ сущности
опредѣленіе по шкалѣ интервала или разстоянія измѣряемой темпера-
Температура.
7
туры отъ одной изъ реперъ. Шкала сама состоитъ изъ ряда репёръ,
распредѣленныхъ внутри температурнаго интервала, ограниченнаго двумя
главными репёрами, а также въ обѣ стороны отъ нихъ, внѣ этого интер-
вала. Установивъ реперы опредѣленнымъ образомъ, мы называемъ тем-
пературный интервалъ между двумя сосѣдними репёрами однимъ
градусомъ.
Весьма существеннымъ является вопросъ о способѣ распре-
дѣленія реперъ, совокупность которыхъ составляетъ термоме-
трическую шкалу. Строго научный, т.-е. раціональный методъ по-
строенія такой шкалы былъ указанъ ЛѴ. Т Ь о ш 8 о п’ омъ (Ь о г (1 К е 1 ѵ і и) ;
съ этою шкалою, которая получила названіе абсолютной Томсо-
новской шкалы температуръ, мы познакомимся впослѣдствіи. Те-
перь намъ важно лишь запомнить, во-первыхъ, что раціональная шкала
температуръ существуетъ, и, во-вторыхъ, что шкалу водороднаго
термометра въ широкихъ предѣлахъ можно считать за тождествен-
ную съ абсолютною шкалою Томсона.
Въ слѣдующей главѣ мы увидимъ, что существуетъ возмож-
ность практически осуществить или построить темпера-
турную шкалу, исходя изъ тѣхъ законовъ лучеиспу-
сканія, которые были подробно разсмотрѣны въ т. II.
Напомнимъ, какъ получаются температурные промежуточные и внѣш-
ніе реперы, т.-е. какъ строится температурная шкала такъ называемаго
водороднаго термометра, оставляя пока въ сторонѣ вопросъ о практиче-
скомъ выполненіи этой задачи. О водородномъ термометрѣ уже было
упомянуто въ т. Г.
Обозначимъ черезъ Ѵ1 объемъ даннаго количества водорода при
температурѣ тающаго льда и произвольномъ давленіи /?, и черезъ Ѵ2 объ-
емъ того же газа подъ тѣмъ же давленіемъ р при температурѣ паровъ
воды, кипящей подъ давленіемъ 760 мм. Пусть далѣе число равныхъ
температурныхъ интерваловъ, на которое мы желаемъ раздѣлить весь
интервалъ между тѣми главными репёрами, которымъ соотвѣтствуютъ объ-
емы Ц и Ѵ2. Раздѣлимъ разность Ѵ2 4 на Л' равныхъ частей и
примемъ за одинъ градусъ то измѣненіе температуры, которое увеличи-
ваетъ взятый объемъ водорода при неизмѣнномъ давленіи р на одну та-
кую часть. Если объемъ V водорода равенъ
ѵ= V, + і ..................(4)
то мы можемъ принять, что его температура на і градусовъ выше (если
і >> О) или ниже (при і < О) температуры таянія льда.
Въ шкалѣ Цельзія М=100, 14 и Ѵ2 соотвѣтствуютъ температу-
рамъ, условно принимаемымъ равными 0° и 100°. Отличіе шкалъ Рео-
мюра и Фаренгейта отъ шкалы’Цельзія извѣстно изъ элементар-
наго курса физики.
Вмѣсто того, чтобы наблюдать объемъ даннаго количества водорода
8
Введеніе.
при постоянномъ давленіи р, предпочитаютъ по нѣкоторымъ причинамъ
наблюдать измѣняющееся съ температурою давленіе р при постоян-
номъ объемѣ V. Пусть рг и давленія водорода при двухъ главныхъ
реперахъ; если
Р == Рі + і ~ ........
то температура на I градусовъ выше или ниже температуры таянія льда.
Итакъ, равныя приращенія объема или давленія
водорода даютъ намъ возможность отмѣтить темпера-
турные репёры и такимъ образомъ построить шкалу
температуръ.
Международная Коммиссія Мѣръ и Вѣсовъ 3 (15) октября 1887 г.
въ Парижѣ еще точнѣе установила принципъ опредѣленія нормальной
температурной шкалы, а именно: начальное давленіе рх водо-
рода должно равняться давленію ртутнаго столба въ
1 м. вышины (1,3158 атмосферы) и самое наблюденіе должно
вестись соотвѣтственно формулѣ (4,а), т.-е. при постоян-
номъ объемѣ, а не соотвѣтственно формулѣ (4).
Приборы, служащіе для измѣренія температуръ, называются тер-
мометрами. Они будутъ разсмотрѣны въ слѣдующей главѣ.
Большой интересъ представляетъ вопросъ о возможности введенія
понятія о температурѣ пустоты. Е. ЛѴіейешапп (АѴіеЛ. Апп.
34 р. 448, 1888) первый указалъ на возможность такого расширенія по-
нятія о температурѣ. Рѣшеніе вопроса далъ Ріапск (1897—1901), ко-
торый ввелъ новую величину — температуру лучистой энергіи.
Онъ разсмотрѣлъ случай стаціонарнаго состоянія лучистой энергіи въ
пустотѣ, полагая, что всѣ лучи прямолинейно поляризованы и монохро-
матичны. Исходя изъ электромагнитной теоріи свѣта, онъ показалъ, что
за абсолютную температуру7 Т такой пустоты слѣдуетъ принять вели-
чину, опредѣляемую равенствомъ
(Апп. й. РЙѴ8. (4) 1 р. 115, 1900\ Здѣсь п число колебаній для данныхъ
лучей, с скорость свѣта, К напряженіе лучистой энергіи, а и Ь двѣ мі-
ровыя постоянныя, изъ которыхъ а имѣетъ размѣръ (время X гра'
дугъ), Ь размѣръ (работа X время). Въ- системѣ сантиметръ-граммъ-се-
кунда-градусъ Цельзія Ріапск находитъ (Апп. й. Рйуз. (4) 6 р. 188,
1901; Ѵогіев. пеЬ. сі. Тйеогіе йег ЛѴаегтезігаІіІшщ, р. 164, 1906)
—27
Ь = 6,548 . 10 эргъ X сек.
к - * = 1.346 . Ю~“ ...........М
а градусъ
Основываясь на этихъ двухъ постоянныхъ, на скорости свѣта и на
постоянной всемірнаго притяженія, Ріапск построилъ «естествен-
Температурные коеффиціенты.
9
ную» систему единицъ, не зависящую отъ размѣровъ или свойствъ
какихъ-либо тѣлъ (эталоны длины) или веществъ (вода).
До сихъ поръ мы предполагали, что каждая построенная нами шкала
температуръ можетъ служить для измѣренія температуры всѣхъ тѣлъ.
Существуетъ, однако, возможность поступить и иначе, а именно постро-
ить для всякаго тѣла (вещества) свою особенную, только для него при-
годную шкалу температуръ, которыя называются приведенными
температурами. Исходною точкою служитъ при этомъ критиче-
ская температура (т. I) даннаго вещества, которая принимается равною
единицѣ. Пусть она равна Тс по абсолютной шкалѣ; тогда приве-
денная температура т, соотвѣтствующая абсолютной температурѣ Г, равна
Т
т = ....................
* с
Когда температуры различныхъ веществъ одинаковы въ обычномъ
смыслѣ слова, ихъ приведенныя температуры совершенно различны. Въ
гл. XIII мы увидимъ, какое значеніе имѣютъ эти приведенныя температуры.
§ 3. Температурные коеффиціенты. Съ измѣненіемъ температуры
тѣла (матеріи) мѣняются, вообще говоря, всѣ его свойства; иначе говоря,
всевозможныя физическія свойства, съ которыми мы имѣемъ дѣло, суть
функціи температуры і. Но температура еще не опредѣляетъ состоянія
тѣла, которое, какъ мы видѣли (г. I), вообще характеризуется двумя ве-
личинами. Положимь, что одна изъ нихъ есть температура. другую обо-
’значимъ черезъ х. Пусть г нѣкоторая физическая величина, которая
есть функція состоянія (т. I), т.-е. мѣняется съ измѣненіемъ со-
стоянія тѣла. Въ общемъ случаѣ имѣемъ
г = .......................(5)
Допустимъ, что і мѣняется, м е ж д) тѣмъ какъ х остается
неизмѣннымъ, и пусть г0, и г2 частныя значенія, соотвѣтству-
ющія і — 0°, и /2°, такъ что
^о=/(О,х), ^і=/(^іЛѢ г2=/(^,х);
полагаемъ > 1\. Въ этомъ случаѣ величина
т.-е. отношеніе средняго измѣненія величины г при повышеніи темпера-
туры на 1° въ интервалѣ между и /2° къ значенію величины при 0°,
называется среднимъ температурнымъ кое ффиціен томъ
величины г, между температурами 4°и^° при х = Соп8І. Усло-
віе х = Соп8І. на практикѣ весьма часто сводится къ условію р = Соіі8і.,
т.-е. мы наблюдаемъ вліяніе температуры на вещество, находящееся подъ
постояннымъ давленіемъ. Бываютъ и исключенія, въ особен-
ности для газообразныхъ тѣлъ, въ которыхъ роль величины х можетъ
играть напр. объемъ ѵ.
10
Введеніе.
Полагая = 0°
фиціентъ между 0° и
и 4 = /°, получаемъ средній температурный коеф-
/°
1 г — г0
“ г0 ’ і
{ К І<> = І АІ, Хг - X и х^= х Лх, имѣ-
(7)
Полагая въ (б)
емъ средній температурный коеффиціентъ между температурами і и і-\- Лі,
равный
1 Лх.
Аі'
предѣлъ этой величины, т.-е.
1
а =
’сіх
(11
'х = СОП8І.
(7, а}
называется температурнымъ коеффиціентомъ величины х
при температурѣ і и при условіи х — Гопзі. Когда не мо-
жетъ быть сомнѣнія насчетъ того, какая величина х остается постоян-
ною при измѣненіи температуры, пишутъ просто
Понятно, что въ общемъ случаѣ
а = д (і, х)............................................(8,&)
т.-е. что а зависитъ отъ температуры і и отъ величины лг, или что а
также есть нѣкоторая функція состоянія.
Если а отъ і не зависитъ, то (8) даетъ х = аіх$ -ф С. Но х = г0
при і = 0, слѣд. С — х0 и потому
г = г0 (1 4- а/).....................(9)
Если х, какъ функція отъ і, можетъ быть представлена въ видѣ ряда
х = х0 [1 + Аі + Ві2 + СР + . . . ........................(10)
гдѣ коеффиціенты Д, В, С... опредѣляются хотя бы эмпирически, то (8) даетъ
а = д _|_ 2 В/-ф-3 СУ2 +.......................................(11)
Наоборотъ, если температурный коеффиціентъ выраженъ въ видѣ ряда
и = -ф -ф “Н..................................................(12)
то вытекающее изъ (8) выраженіе для (Іх даетъ приращеніе г2 — хг ве-
личины х при переходѣ отъ къ ^>° въ видѣ
4
<г2—^=^0 аЛі = г0 а0 (і2 — іг) (42~ 42)+ (43 —^і3) + (13)
Если = 0, '= то гі — го, и Для г = имѣемъ
х = г0 (1 + аі -|- «і/2 + -1 а.2/8 . (14)
X о
Температурные коеффиціенты
11
что вытекаетъ и непосредственно изъ сравненія НО) и (11). Само со-
бою разумѣется, что температурные коеффиціенты, въ общемъ случаѣ,
какъ функціи температуры, сами обладаютъ опредѣленными температур-
ными коеффиціентами. Вмѣсто величины (8) разсматриваютъ иногда
величину
, 1 (іг
а
г аі
(15)
Обратимся къ нъкоторымъ частнымъ случаямъ.
I. Пусть г = /, гдѣ / одинъ изъ линейныхъ размѣровъ тѣла
и пусть х — р, такъ что измѣненіе температуры происходитъ при посто-
янномъ внѣшнемъ давленіи; величина
1 аі
10 <11.......................
называется линейнымъ к о еффиці е нтомъ расширенія (< тепло-
вого; прибавляется только въ рѣдкихъ случаяхъ, когда возможно недора-
зумѣніе) тѣла или вещества, изъ котораго тѣло состоитъ. При
а = Сопзі. имѣемъ, согласно (9),
I = 4) (1 "4"
II. Пусть г = ѵ, т.?е. объему даннаго
опять х — р. Величина
.......................(17)
количества вещества и пусть
і аѵ
а = тт .
аі
(18)
называется, для краткости, коеффиціентомъ расширенія ве-
щества (напр. воды, ртути, мѣди). При а = Сопзі. имѣемъ
ѵ = ѵ0 Ц + «О..................(19)
Если (16) обозначить черезъ «/, (18) черезъ то, какъ извѣстно
изъ элементарнаго курса физики, для изотропныхъ тѣлъ приблизительно
аѵ — 3 аі.............................................(20)
Выводя величину а по формулѣ (16) или (18), мы за величину х,
которая при измѣненіи температуры должна оставаться постоянною, при-
няли давленіе р. Вообще говоря, это имѣетъ существенное значеніе
только хля газообразныхъ тѣлъ.
III. Пусть г = р, т.-е. давленію,
дится. Тогда величина
1 ар
а = .
Ро
подъ которымъ тѣло нахо-
......................(21)
есть температурный коеффиціентъ давленія, зависящій,
конечно, отъ выбора той величины х, которая при измѣненіи температуры
должна оставаться постоянною. Величина (21) имѣетъ особый интересъ
для газообразныхъ тѣлъ, когда за х принятъ объемъ ѵ. т.-е. когда нагрѣ-
ваніе газа происходить при постоянномъ объемѣ.
12
Введеніе.
Для газообразныхъ тѣлъ введемъ вмѣсто (18) и (21) символи-
ческія обозначенія
_ 1 Ісі/ѵ
а>ѵ Ѵо \ (11
— 1 №р\ ..............
ар- р0\аі)ѵ
гдѣ буква, поставленная внизу подъ второю, скобкою, обозначаетъ ту ве-
личину. которая при нагрѣваніи остается постоянною. Величину ар весьма
неудачно иногда называютъ ко еффиціентомъ расширенія газа
при постоянномъ объемѣ; точное названіе должно быть: тем-
пературный коеффиціентъ давленія при постоянномъ
объемѣ. У словно мы можемъ его короче назвать температу р -
нымъ коеффиціентомъ давленія.
Для идеальныхъ газовъ, строго слѣдующихъ законамъ Бойля
и Гей-Люссака, имѣемъ
= а,р .......... (23)
Дѣйствительно, мы видѣли (т. I), что уравненіе состоянія такихъ
газовъ опредѣляется равенствомъ рѵ — ПТ = /?(273 + і\ гдѣ /? для
даннаго количества даннаго газа величина постоянная. Это уравненіе даетъ
273/?
!(іѵ\ __ # •
\сИ) р
\ !р
Подставляя эти величины въ
/?
ѵ
(22), мы находимъ, что
аѵ — ар - 273 ........................
Выбравъ водородъ за тѣло, которое должно послужить намь
для построенія температурной шкалы, мы принимаемъ, что въ опредѣ-
ленныхъ предѣлахъ, а именно при не очень большихъ давленіяхъ, водо-
родъ почти обладаетъ свойствами идеальнаго газа. Для него ар дѣйстви-
тельно почти постоянное число, но оно больше аѵ (для другихъ газовъ
аѵ ар) и мы видѣли выше, что Международная Коммиссія Мѣръ и Вѣ-
совъ опредѣлила, чтобы построеніе нормальной температурной шкалы
производилось путемъ наблюденія измѣненія давленія водорода, на-
грѣваемаго при постоянномъ объемѣ. Это и соотвѣтствуетъ спеціальному
предположенію, что для водорода именно ар = Сопзі.
§ 4. Нѣкоторыя предварительныя свѣдѣнія. Единица коли-
чества теплоты, т.-е. единица тёпловой энергіи можетъ быть вы-
брана различно. На стр. 2 мы уже упомянули о механической единицѣ
теплоты, эквивалентной единицѣ работы и соотвѣтствующей приращенію
живой силы движенія частицъ тѣла на одну единицу. Такимъ образомъ,
Предварительныя свѣдѣнія
13
напр. эргъ, мегаэргъ и джуль суть единицы количества теплоты (т. Г). Если
количество теплоты С? выражено въ механическихъ единицахъ и /? работа,
эквивалентная тепловой энергіи <2, то мы имѣемъ численное равенство
<2 7?.............(25)
Если выражено въ другихъ единицахъ, то
(2 = АЯ=±Й........ (26)
гдѣ Е механическій эквивалентъ теплоты, А — термическій эквивалентъ
работы. Не входя пока ни въ какія подробности, мы назовемъ малой
калоріей то количество теплоты, которое нагрѣваетъ одинъ граммъ
чистой воды отъ 0° до 1°. При разборѣ вопроса о теплоемкости воды
мы дадимъ болѣе точное опредѣленіе этой величины. Большая ка-
лорія содержитъ 1000 малыхъ калорій. Мы считаемъ излишнимъ вво-
дить два термина: теплоемкость и удѣльная теплота. Мы будемъ гово-
рить о теплоемкости опредѣленнаго тѣла или опредѣленной
совокупности разнородныхъ тѣлъ, нагрѣваемыхъ, какъ одно цѣлое, и о
теплоемкости опредѣленнаго вещества, которая и называется иногда удѣль-
ною теплотою, и которая равна теплоемкости тѣла, состоящаго изъ этого
вещества и обладающаго единицею вѣса.
Если для нагрѣванія тѣла отъ до /2° требуется единицъ тепла,
то величина
называется среднею теплоемкостью
температурами и 62°- Полагая = 7,
вмѣсто С?. имѣемъ въ предѣлѣ
тѣла въ промежуткѣ между
і2 -- I + Ді и вставляя ЛС?
С ~ сГі
(28, а)
= сМ................(28,6)
с называется теплоемкостью тѣла при температурѣ і.
Чтобы нагрѣть тѣло отъ /х° до требуется количество теплоты
Р =сйі ......... (29)
^1
Если С теплоемкость однороднаго тѣла, р его вѣсъ, с теплоемкость
вещества, изъ котораго оно состоитъ, то
С = ср.................(29, а)
Если тѣло сложное и величины рі и Сі относятся къ одной изъ его
однородныхъ частей, то
С 2 Рі<і........ (30)
14
Введеніе.
Количество тепла потребное для нагрѣванія тѣла, а слѣд. и
теплоемкость тѣла, зависятъ отъ тѣхъ условіи,
при которыхъ происходитъ нагрѣваніе. Одно ука-
заніе на повышеніе температуры, напр. отъ /° до (/ + 1)°, еще не
опредѣляетъ собою того измѣненія состоянія, которому тѣло подверглось,
ибо, какъ мы видѣли, состояніе тѣла опредѣляется двумя величинами,
изъ которыхъ одна можетъ быть температура і, а другая — какая нибудь
величина х, могущая мѣняться независимо отъ Л Количество тепла зави-
ситъ отъ измѣненій величинъ / и х, а потому и теплоемкость зависитъ
огъ того, какъ при нагрѣваніи мѣняется х. Въ частныхъ случаяхъ мы
можемъ имѣть х р или х = ѵ. Теплоемкости, соотвѣтствующія слу-
чаямъ р = Соп8І. и ѵ = Сопзі., т.-е. теплоемкость ср при постоян-
номъ давленіи и теплоемкосгь сѵ при п о с т о я н н о м ъ объемѣ
представляютъ еще болѣе частные случаи. Когда говорятъ о теплоем-
костяхъ твердыхъ и жидкихъ тѣлъ, то почти всегда имѣютъ въ виду ве-
личину ср.
Съ нѣкоторыми свойствами теплоемкостей ср и сѵ для газовъ мьі
уже познакомились въ т. I. Между прочимъ тамъ была выведена формула
ср — сѵ = и была введена величина к = Ср'-Сѵ, встрѣчающаяся
напр. въ формулѣ для скорости звука въ газахъ щ. II).
Понятіе о скрытой теплотѣ плавленія и испаренія (или ки-
пѣнія) извѣстно изъ начальнаго курса физики.
Переходъ тѣлъ изъ твердаго состоянія въ жидкое сопровождается
иногда внезапнымъ измѣненіемъ объема, такъ что щнное вѣсовое ко-
личество вещества обладаетъ при одной и той же температурѣ (темпера-
турѣ плавленія) въ твердомъ и жидкомъ состояніяхъ не одинаковыми
объемами. Въ этомъ отношеніи особенно замѣчательны ледъ и вода;
послѣдняя при замерзаніи расширяется. Если черезъ ѵл и ѵв обозна-
чить объемы одного и того же вѣсового количества льда и воды при 0°,
то, по новѣйшимъ изслѣдованіямъ,
= ^,9167 ѵл I (зі)
ѵл = 1,0909 I
Расширеніе при замерзаніи составляетъ, слѣдовательно, около 9,1°/0.
Теплота, какъ форма энергіи, можетъ получиться только на счетъ
уже существующаго запаса другой формы энергіи и съ своей стороны
можетъ исчезнуть, только перейдя въ другую форму энергіи. При этомъ
тѣло, теряющее часть своего запаса тепловой энергіи, совершаетъ нѣко-
торую работу. Терминъ «источникъ тепла» является не вполнѣ уста-
новившимся. Строго говоря, источниками тепла могутъ быть только запасы
другой энергіи, напр. энергіи движенія, химической, электростатической
(зарядъ) и т. д. Принято, однако, иногда называть источниками теплоты
тѣ явленія, которыя сопровождаютъ переходъ другой формы энергіи
въ энергію тепловую или которыя такому переходу способствуютъ. Та-
кимъ образомъ принято называть источниками теплоты горѣніе, треніе.
Предварительныя свѣдѣнія
15
ударъ и т. д., хотя истинные источники суть въ первомъ случаѣ хими-
ческая энергія, во второмъ и третьемъ — энергія движенія тѣлъ тру-
щихся или соударяющихся, или, по крайней мѣрѣ, одного изъ нихъ.
Лучистая энергія также можетъ быть источникомъ тепловой энергіи, а
именно, когда поверхность тѣла способна поглощать падающую на нее
лучистую энергію. Переходъ лучистой энергіи въ тепловую былъ раз-
смотрѣнъ нами въ ученіи о лучистой энергіи (т. П, гл. 2). Обратный
переходъ тепловой энергіи въ лучистую будетъ нами разсмотрѣнъ ниже.
Въ явленіяхъ превращенія разныхъ формъ энергіи въ энергію тепловую
и обратно играетъ важную роль то стремленіе къ переходу отъ упорядо-
ченнаго движенія частицъ вещества къ равномѣрно-безпорядочному, о
которомъ было сказано выше. Ей не противорѣчитъ стремленіе тепловой
энергіи переходить въ энергію лучистую, ибо конечнымъ результатомъ та-
кого перехода представляется равномѣрное распредѣленіе всей энергіи,
существующей въ доступной нашему наблюденію вселенной, по всѣмъ
частямъ послѣдней.
Считаемъ не лишнимъ напомнить, что мы, ради соблюденія строгой
точности и послѣдовательности, совсѣмъ не вводимъ термина «лучистая
теплота» ; послѣдняя есть не что иное, какъ инфракрасная лучистая энер-
гія, подробно изученная нами въ т. II, гдѣ ея мѣсто. Нельзя не пожа-
лѣть, что даже въ нѣкоторыхъ новѣйшихъ курсахъ физики встрѣчается
глава «о лучистой теплотѣ» въ той части курса, которая посвящена уче-
нію о теплотѣ. Объ этомъ вопросѣ мы уже говорили достаточно по-
дробно въ т. II.
ГЛАВА ВТОРАЯ.
Термометрія.
§ 1. Задача термометріи. Въ предыдущей главѣ мы познакомились
съ понятіями о температурѣ и о шкалѣ температуръ. Мы упомянули
что существуетъ вполнѣ раціональная шкала АѴ. Т Ьі о т 8 о п’а, которую
можно назвать абсолютною, и что отъ нея лишь незамѣтно отличается
нормальная шкала водороднаго термометра, съ устройствомъ котораго
мы познакомимся ниже. Мы увидимъ, что устройство водороднаго тер-
мометра настолько сложно, что имъ можно пользоваться лишь въ исклю-
чительныхъ случаяхъ. Для обыкновеннаго измѣренія температуръ необ-
ходимо имѣть болѣе удобные и простые приборы, дающіе возможность
опредѣлить въ каждомъ данномъ случаѣ ту температуру, которую указы-
валъ бы водородный термометръ, еслибы существовала возможность вос-
пользоваться имъ при данныхъ обстоятельствахъ.
Задача термометріи и заключается въ устройствѣ приборовъ (термо-
метровъ), которые могутъ служить для этой цѣли, въ тщательномчэ и все-
стороннемъ изученіи свойствъ этихъ приборовъ и въ опредѣленіи тѣхъ
16
Термометрія.
условій, которыя необходимо соблюдать, пользуясь ими, и тѣхъ способовъ
вычисленій, которые даютъ возможность перейти отъ непосредственныхъ
показаній прибора къ показаніямъ водороднаго термометра, или, какъ го-
ворятъ, ввести поправки къ отсчетамъ, непосредственно произве-
деннымъ на приборѣ. Устройство термометровъ основано на слѣдую-
щемъ. Положимъ, что 5 какая-либо физическая величина, которая при
заданныхъ добавочныхъ условіяхъ является нѣкоторою функ-
ціею температуры Г, такъ что можно положить
5=7(0.......................(1)
Допустимъ, что существуетъ возможность измѣрить величину 5 при
различныхъ температурныхъ условіяхъ, и пусть 50 и 5]00 ея численныя
значенія при 0° и 100°. Положимъ, что при температурѣ Г, которую мы
желаемъ опредѣлить, наша величина имѣетъ значеніе 5, и пусть
5 Зо-Н5100 ' ..............(2)
Тогда мы назовемъ величину і температурою, показываемой термо-
метромъ, устройство котораго основано на наблюденіи величины 5 при
данныхъ условіяхъ. Полагая / —- О, 1, 2, 3 ... 99, 100, мы
получаемъ температурную шкалу, которая при 0° и 100° совпадаетъ со
шкалой нормальной. Остальныя же точки шкалы (реперы — стр. 6) не
совпадаютъ съ точками шкалы нормальной, т.-е. температура
І = 100 .................(3)
*^100 ’ ^0
отсчитанная на нашемъ приборѣ, не совпадаетъ съ истинною температу-
рою Г, которую указалъ бы при тѣхъ же условіяхъ водородный термо-
метръ на основаніи формулъ
/, = р0+Г'’і«-Й..................(4>
7 100 Р ...... (5)
Аоо — А)
гдѣ р0, р100 и р давленіе при постоянномъ объемѣ даннаго количества
водорода при 0°, 100° и при измѣряемой температурѣ. Величина *
Ч = Т— і .......... (6)
составляетъ поправку, т.-е. величину, которую слѣдуетъ приба-
вить къ показаніямъ термометра, чтобы найти истинную температуру Т
по нормальной шкалѣ, тождественной, въ предѣлахъ ошибокъ наблю-
деній (0°,00Г), со шкалою абсолютною. Поправка ?? = 0 при 0° и при 100°;
она, вообще говоря, достигаетъ наибольшаго значенія при нѣкоторой тем-
пературѣ, лежащей между 40° и 69°.
Если 5 есть линейная функція истинной температуры Г, то по-
правка г/ о при всѣхъ температурахъ. Но величина 5, которая обла-
Задача термометріи.
17
дала бы такимъ свойствомъ, до сихъ поръ еще не найдена. Про упру-
гость р водорода, находящагося при постоянномъ объемѣ, мы должны
сказать, что она весьма мало отличается отъ линейной функціи темпера-
туры, измѣренной по абсолютной шкалѣ Томсона, что и даетъ намъ
право считать нормальныя температуры Г, вычисленныя по формулѣ (5).
тождественными съ температурами абсолютной шкалы.
Устраивая термометръ, мы можемъ по нашему усмотрѣнію выбрать
величину 5 и то тѣло, на которомъ измѣненія величины 5 будутъ на-
блюдаться. Замѣтимъ, что 5 можетъ быть напр. длина, объемъ, давленіе,
плотность, величина изгиба или поворота при измѣненіи геометрической
формы тѣла, электрическое сопротивленіе, термоэлектродвижущая сила
и т. д. Тѣло можетъ быть газообразное, жидкое и твердое. Наиболѣе
часто наблюдается измѣненіе объема, причемъ за тѣло (вещество) обык-
новенно берутъ ртуть.
Устройство водороднаго термометра, какъ увидимъ ниже, настолько
сложно, что для опредѣленія поправокъ ц = Т — і нѣтъ возможности
сравнивать показанія каждаго изготовляемаго хорошаго термометра, дол-
женствующаго служить для точныхъ наблюденій, съ термометромъ водо-
роднымъ. Вмѣсто этого сравниваютъ (компарируютъ) изслѣдуемый термо-
метръ съ такъ называемымъ нормальнымъ термометромъ, ка-
ковой долженъ находиться при всякой физической лабораторіи. Нормаль-
ные термометры суть такіе, для которыхъ поправки ц съ достаточною точ-
ностью извѣстны. Существуютъ два способа получить нормальный тер-
мометръ и поправки у къ нему:
1. Поправки т) опредѣлены опытомъ, т.-е. путемъ сравненія по-
казаній нормальнаго термометра съ показаніями водороднаго термометра
непосредственно или черезъ рядъ (не длинный) промежуточныхъ термоме-
тровъ, изъ которыхъ первый былъ сравненъ съ водороднымъ термометромъ.
2. Термометръ изготовляется по строго опредѣленнымъ прави-
ламъ, при соблюденіи которыхъ мы можемъ быть увѣрены, что поправки щ
будутъ имѣть при различныхъ температурахъ і вполнѣ извѣстныя значе-
нія, разъ навсегда опредѣленныя. Къ такого рода нормальнымъ термо-
метрамъ относятся ртутные термометры, приготовленные изъ нѣкоторыхъ,
строго опредѣленныхъ сортовъ стекла, напр. изъ такъ называемаго твер-
даго французскаго (ѵегге (іиг) или изъ іенскаго стекла 16ш или 59ІП.
Выборъ величины 5, далѣе тѣла, на которомъ наблюдаются измѣне-
нія этой величины, и, наконецъ, самаго устройства термометра опредѣля-
ется тѣми спеціальными цѣлями, для которыхъ приборъ назначается, а
также тою обстановкою, при которой придется имъ пользоваться. Термо-
метръ, непригодный для однѣхъ цѣлей, можетъ быть весьма удобнымъ
для другихъ, и наоборотъ. Одно изъ свойствъ, достиженіе котораго почти
всегда желательно — это чувствительность термометра, которая
сводится къ слѣдующимъ двумъ свойствамъ: термометръ долженъ обна-
руживать малыя измѣненія температуры (напр. до 0°,005) и онъ долженъ
быстро принимать ту температуру, которая при его помощи измѣряется.
КУРСЪ ФИЗИКИ О. X в О Л Ь С О Н А. Т. III. изд. 3-е. 2
18
Термометрія.
Обзоръ исторіи термометріи можно найти въ упомянутой выше книгѣ
Масіі’а: Біе Ргіпсіріеп йег ЛѴаегтеІеііге (стр. 2 38 и 58—64).
§ 2. Газовый термометръ. Газовый термометръ состоитъ изъ сте-
кляннаго, фарфороваго или металлическаго резервуара шаровидной или ци-
линдрической формы, наполненнаго опредѣленнымъ сухимъ газомъ. Этотъ
резервуаръ можетъ быть помѣщенъ въ тающій ледъ (0°), въ пары кипя-
щей воды (около 100°), а также въ то пространство или въ ту среду,
температуру Р которой требуется опредѣлить. Смотря по роду газа, мы
Рис. 1.
имѣемъ термометры воздушный, водородный, азотный и *т. д. При по-
мощи особаго манометра измѣряются давленія р0> Аоо и Р газа ПРИ тем"
пературахъ 0°,100° и /°, причемъ объемъ газа остается почти вполнѣ
постояннымъ.
Преимущества газоваго термометра заключаются, помимо особыхъ
преимуществъ водороднаго термометра, о которыхъ было сказано выше,
въ той быстротѣ, съ которою расширяются газы при нагрѣваніи, а слѣд.
и возрастаетъ ихъ давленіе, если препятствовать такому расширенію.
Послѣднее отъ 100—400 разъ больше расширенія твердыхъ тѣлъ, въ
150 разъ больше расширенія стекла и въ 20 разъ больше расширенія
ртути. Вотъ почему расширеніе резервуара при нагрѣваніи сравнительно
мало вліяетъ на показанія термометра. Далѣе, газовый термометръ при-
Газовый термометръ.
19
годенъ отъ самыхъ низкихъ до самыхъ высокихъ температуръ, въ осо-
бенности, если онъ наполненъ водородомъ.
Газовый термометръ по устройству тождественъ съ приборомъ, слу-
жащимъ для измѣренія коеффиціентовъ расширенія аѵ и давленія ар;
этотъ приборъ будетъ описанъ въ главѣ третьей. Два коеффиціента аѵ и ар
опредѣляются, какъ мы увидимъ, двумя различными способами: въ пер-
вомъ наблюдается расширеніе газа при почти постоянномъ давленіи; во
второмъ — давленіе газа при почти постоянномъ объемѣ. Оказывается,
что и для измѣренія температуръ можно пользоваться этимъ приборомъ
двумя способами. Однако на практикѣ предпочитаютъ второй способъ,
т.-е. наблюдаютъ измѣненія давленія газа, какъ сказано выше.
На рис. 1 представленъ газовый термометръ Ве^папіі.
Онъ состоитъ изъ стекляннаго резервуара Л, соединеннаго трубкою СІЕ
съ ртутнымъ манометромъ, прикрѣпленнымъ къ вертикальной доскѣ, плос-
кость которой перпендикулярна къ плоскости рисунка. Этотъ манометръ
изображенъ отдѣльно съ правой стороны рисунка. Онъ состоитъ изъ
двухъ параллельныхъ трубокъ ЕН (гдѣ Е конецъ трубки сІЕ на лѣвомъ
рисункѣ") и содержащихъ ртуть, которая можетъ быть прилита черезъ
отверстіе или выпущена черезъ кранъ К въ сосудъ V. На трубкѣ ЕН
находится около а горизонтальная черта; термометры Т и Т служатъ
для опредѣленія температуры различныхъ частей манометра.
Шаръ А наполняется совершенно сухимъ газомъ черезъ трубку /?,
которая соединена съ высушивающимъ аппаратомъ и съ насосомъ,
служащимъ для многократнаго выкачиванія и впусканія газа въ ре-
зервуаръ А.
Способъ наблюденія понятенъ изъ предыдущаго. Сперва помѣща-
ютъ шаръ въ тающій ледъ и, прибавляя или выливая ртуть, доводятъ ее
въ колѣнѣ ЕН до черты а. Обозначимъ черезъ Н барометрическое дав-
леніе, къ которому прибавлена или изъ котораго вычтена небольшая раз-
ность высотъ ртути въ трубкахъ ЕН и .//<, такъ что Н есть давленіе
газа, когда А находится въ тающемъ льдѣ. • Затѣмъ помѣщаютъ резер-
вуаръ А въ то пространство, температуру х котораго требуется измѣрить
и, приливая ртуть, вновь приводятъ уровень ртути къ чертѣ а. Поло-
жимъ, что барометрическое давленіе въ этомъ случаѣ равно Н'; разность
уровней ртути въ трубкахъ ЕН и Ж, т.-е. вертикальное разстояніе между а
и нѣкоторой горизонтальной плоскостью у, обозначимъ черезъ Л. Тогда
давленіе Л/3, подъ которымъ находится газъ при искомой температурѣ х,
равно Н± Н' + И.
Пренебрегая пока всякими поправками и допуская, что газъ обла-
даетъ постояннымъ температурнымъ коеффиціентомъ ар, мы имѣемъ
Н^На + арХ)......... (7)
откуда
Н, — Н
Х~ Нар
(8)
2*
20
Термометрія
Это же выраженіе получается изъ (4), гдѣ р^-Н, р = Т=х и
далѣе Аоо = Ро (1 + 100ар); слѣд.
Аоо Ро _ „ _ н
100 -Р^Р~ПаР-
Коеффиціентъ ар считается для даннаго газа извѣстнымъ; мы уви-
димъ, что онъ опредѣляется изъ той же формулы (7), если принять
вмѣсто х температуру въ 100°, или близкую къ ней и намъ извѣстную
температуру паровъ кипящей воды, въ которыхъ и помѣщается ре-
зервуаръ А.
Формула (8) даетъ лишь весьма грубое приближеніе къ истинной
искомой температурѣ, и притомъ по тремъ причинамъ:
1. Объемъ резервуара А мѣняется при нагрѣваніи, такъ что объемъ
газа не есть величина постоянная.
2. Газъ, находящійся въ такъ называемомъ вредномъ п.р о -
странствѣ б/Еа, не подвергается тому же нагрѣванію, какъ газъ въ А,
3. Коеффиціентъ ар нельзя считать постояннымъ для не-водород-
наго термометра.
Пренебрегая третьимъ обстоятельствомъ, мы составимъ уравненіе
для опредѣленія х. Пусть V объемъ сосуда А и трубки до точки сі
при 0°; у коеффиціентъ расширенія матеріала, изъ котораго сдѣланъ
сосудъ; ѵ объемъ вреднаго пространства; ух коеффиціентъ расширенія
стекла, изъ котораго сдѣлана часть НЕа\ і температура вреднаго про-
странства въ первомъ опытѣ (когда резервуаръ А во льду), 4 — во
второмъ. При первомъ опытѣ газъ занимаетъ объемъ V -|- ѵ (1 + у^);
если бы весь газъ находился при 0°, то онъ занялъ бы объемъ
1 + 7^
1 арі
при давленіи . . . Н.
Во второмъ опытѣ объемъ газа равняется V (1-|- ух) + ѵ (1 -|- у^);
если бы онъ весь находился при 0°, то онъ занималъ бы объемъ
ѵ
1 - при давленіи . . . Нг.
1 і
Два объема при давленіяхъ Н и Нх относятся къ одной и той же
температурѣ 0°, и потому по закону Бойля:
Ѵ-{-ѵ
1 +7і*
1 + аРі.
[ 1 + 1 + ар?і]
Нх. . . (9)
Изъ этой формулы получается искомая температура х.
Вводя для краткости величину
мы имѣемъ
„ _ у_ г і -Ь тЛ _ н 1 -Ь /і*]
У 1 1 + 1 + ар* 1 ’
ар(Н—а)—Нху..............
(Ю)
Газовый термометръ.
21
Если резервуаръ сдѣланъ изъ стекла, то въ о равно у. Фор-
мула (10) переходитъ въ (8), если пренебречь вреднымъ пространствомъ ѵ
(тогда б = 0) и расширеніемъ резервуара А (у = 0).
КЛрр (1901) далъ подробныя правила для пользованія газовымъ
термометромъ. И. Лебедевъ (1899) произвелъ въ Главной Палатѣ
Мѣръ и Вѣсовъ весьма точное изслѣдованіе водороднаго термометра.
При выводѣ нашихъ формулъ мы предполагали, что взятый газъ
слѣдуетъ законамъ Маріотта и Гей-Люссака. Болѣе точная тео-
рія должна обращать вниманіе на отступленія газовъ отъ этихъ законовъ.
Съ этой теоріей мы познакомимся въ гл. IX.
Многочисленныя измѣненія въ устройствѣ газоваго термометра (Еи(1-
Ьег^’а, Ма^пиз’а, Еескпа^еГя, еіпйо 1 (Га) имѣютъ нынѣ уже
только историческій интересъ. Обращаемся къ описанію газоваго термо-
метра, устроеннаго и изученнаго Р. Сйар-
Рис. 2. р и і 8 въ Международномъ Бюро Мѣръ и- Вѣ-
совъ около Парижа. Эта классическая работа
положила, вмѣстѣ съ работами ОиіНаите’а,
Регпеі’а и др., основанія термометріи, какъ
точной науки.
Мы начнемъ описаніе прибора съ мано-
метра, изображеннаго на рис-. 4; этотъ мано-
метръ соединенъ съ резервуаромъ при помощи
тонкой трубочки с. Онъ содержитъ въ себѣ со-
единеніе барометра съ манометромъ и даетъ
возможность опрёдѣлить упругость газа, нахо-
дящагося въ резервуарѣ при помощи двухъ отсчетовъ,
какъ пользуясь приборами Е е п а и 1 і и др., приходится дѣлать
четыре отсчета: два для опредѣленія высоты ртутнаго столба въ
барометрѣ и два для измѣренія разности высотъ ртутныхъ столбовъ въ
манометрѣ. Приборъ Сііаррпіз состоитъ изъ четырехъ трубокъ Р,
т, ггі и п, содержащихъ ртуть. Средняя часть Р отдѣльно изобра-
жена на рис. 5. Какъ видно, трубки пг' и п вполнѣ отдѣлены другъ отъ
друга сплошною перегородкою. Трубка с проходитъ черезъ эту перего-
родку и слѣд. соединяетъ газовый резервуаръ съ весьма узкимъ простран-
ствомъ, находящимся въ п надъ ртутью. Трубки т и т непосредственно
соединены между собою тоненькой трубкой, какъ показано на рисункѣ.
Трубка О соединена съ т, и наконецъ трубка п соединена съ т и О
при помощи горизонтальной трубки, находящейся налѣво отъ сі. Кра-
номъ а можно прекратить сообщеніе между т и Р; кромѣ того можно
прекратить сообщеніе между трубкой п и трубками т и О при помощи
коническаго конца винта, если вращать рукоятку Ь.
Трубку Р можно перемѣщать вверхъ и внизъ при помощи салазокъ;
закрѣпивъ послѣднія, можно придавать трубкѣ Р малыя перемѣщенія,
вращая головку винта И. Къ перегородкѣ Р прикрѣплено внутри трубки п
весьма малое остріе, видное на рис. 5. Въ ртуть трубки пг погружена
Рис. з.
между тѣмъ
22
Термометрія,
барометрическая трубка ВК', въ верхней части В находятся два изо-
гнутые внизъ черные крючка, вродѣ изображеннаго на рис. 3. Всю
трубку ВК можно опускать и поднимать при помощи винта 5 и тѣмъ
самымъ доводить уровень ртути въ В до соприкосновенія съ Ястріемъ
одного изъ этихъ крючковъ, причемъ мѣняется объемъ пустого простран-
ства надъ ртутью.
Изъ этого описанія понятно, что п и т замѣняютъ манометръ въ
приборѣ Ке^паиИ, между тѣмъ какъ т'В представляетъ барометръ,
нижній уровень ртутнаго столба котораго не приходится измѣрять въ
Рис. 5.
Рис. 4.
трубкѣ т. Разность уровней ртути АВ даетъ намъ сразу упругость газа,
находящагося въ резервуарѣ.
Когда температура газа въ резервуарѣ установилась, и желаютъ
опредѣлить его упругость, то доводятъ уровень А ртути въ п до сопри-
косновенія съ маленькимъ остріемъ, поднимая или опуская трубку О.
Этимъ достигается крайнее уменьшеніе вреднаго пространства. Упомя-
нутое выше измѣненіе объема пустого пространства въ В очевидно слу-
житъ для провѣрки того, насколько это пространство дѣйствительно ли-
шено слѣдовъ воздуха. Вертикальныя разстоянія уровней ртутныхъ стол-
бовъ измѣряются при помощи катетометра (т. I). Резервуаръ газоваго
Газовый термометръ.
23
термометра СЬарриіз представляетъ собою цилиндрическій сосудъ изъ
иридистой платины съ закругленными концами, длиною въ 1,1 метръ; внѣш-
ній діаметръ его 36 мм.; толщина стѣнокъ 1 мм.; емкость болѣе одного
литра. *Къ одному концу прикрѣплена трубочка, длиною въ 50 мм., ко-
торая при помощи платиновой трубочки въ 1 м. длины и 0,7 мм. вну-
тренняго діаметра соединена съ манометромъ. Конецъ ея с виденъ на
рис. 4 и 5. Объемъ вреднаго пространства не составляетъ и 0,001 части
емкости резервуара.
Резервуаръ помѣщался въ горизонтальномъ положеніи внутри одного
изъ двухъ чановъ, игравшихъ въ то же время роль компараторовъ,
т.-е. служившихъ для непосредственнаго сравненія газоваго термометра
съ опредѣленными ртутными термометрами. По формѣ чаны напомина-
ютъ полуцилиндры съ горизонтальными образующими (вродѣ корыта);
стѣнки у нихъ двойныя. Не входя въ подробное ихъ описаніе, замѣтимъ,
что однимъ изъ нихъ пользовались при невысокихъ температурахъ. Вну-
тренній чанъ наполняется водою, какъ и наружный, причемъ вода под-
держивается при постоянной температурѣ. Ртутные термометры помѣ-
щаются во внутреннемъ чанѣ, параллельна резервуару. Весь приборъ
покрывается стеклянною крышкою, черезъ которую можно произво-
дить отсчитыванія ртутныхъ термометровъ. При наблюденіяхъ ниже 0°
внутренній чанъ наполняется алкоголемъ, а наружный — охлаждаю-
щей смѣсью.
Второй чанъ или компараторъ (у обоихъ приборовъ имѣются нѣко-
торыя общія части) служитъ для наблюденій въ парахъ кипящей воды.
Онъ также имѣетъ двойныя стѣнки, но закрывается иолуцилиндрическою
крышкою, въ которую вставлены четыре вертикальныя трубки, имѣющія
также двойныя стѣнки. Въ эти трубки вставляются изслѣдуемые ртутные
термометры. Небольшой водяной манометръ, придѣланный сбоку крышки
прибора, служитъ для опредѣленія того небольшого избытка упругости
пара надъ атмосфернымъ давленіемъ, который всегда существуетъ въ по-
добныхъ приборахъ. Опредѣливъ высоту барометра на приборѣ, изобра-
женномъ на рис. 4 (при этомъ трубки т и п разобщаются вращеніемъ
рукоятки &), мы будемъ знать упругость пара, а отсюда, пользуясь из-
вѣстными таблицами, и температуру паровъ. СііарриІ8 производилъ
опыты съ водородомъ, азотомъ и углекислымъ газомъ, наполняя ими ре-
зервуаръ газоваго термометра. Какъ увидимъ далѣе, СЬарриіз сравни-
валъ показанія трехъ газовыхъ термометровъ между собою и съ показа-
ніями ртутнаго термометра изъ твердаго французскаго стекла (ѵегге (іпг).
Сравненіемъ шкалъ различныхъ газовыхъ термометровъ занимался
впервые Ке^паиИ. Во всѣхъ этихъ шкалахъ точки 0° и 100° совпа-
даютъ и вопросъ заключается въ опредѣленіи разностей показаній для
температуръ промежуточныхъ или лежащихъ ниже 0° или выше 100°.
К е п а и И изслѣдовалъ этотъ вопросъ въ различныхъ направленіяхъ,
изучая не только вліяніе рода газа, но и вліяніе начальнаго давленія,
подъ которымъ газъ находится, напр. при 0°, а также сорта стекла, изъ
24
Термометрія.
котораго изготовленъ резервуаръ. Результаты опытовъ Ве^папіі
слѣдующіе :
1. Вліяніе сорта стекла сравнительно незначительно; оно вызыва-
етъ разность показаній лишь въ0°,1 при 200°, въ 0°,22 при 300° и въ 0°.51
при 350°, если одинъ изъ сравниваемыхъ резервуаровъ состоитъ изъ обык-
новеннаго стекла, а другой изъ хрусталя.
2. Вліяніе давленія, подъ которымъ находится газъ, также неве-
лико. Мѣняя это давленіе отъ 0,5 до 2-хъ атмосферъ, Ке^паиіі получилъ
разности показаній, не превышавшія 0°,2 въ предѣлахъ между 0° и 324°.
3. Показанія воздушнаго и водороднаго термометровъ отличаются
между собою на малыя величины. Углекислота и сѣрнистый газъ даютъ
болѣе замѣтныя отступленія, доходящія для послѣдняго до 3° при темпе-
ратурѣ въ 300°, сравнительно съ термометромъ воздушнымъ.
Результаты Ке^паиіі были поколеблены несравненно болѣе точ-
ными работами Сйарриів, методъ котораго былъ изложенъ выше. Онъ
нашелъ, что шкалы термометровъ водороднаго и азотнаго весьма мало
другъ отъ друга отличаются, между тѣмъ какъ углекислый газъ даетъ
отступленія, значительно превышающія ошибки наблюденій, неизбѣжныя
при современныхъ точнѣйшихъ измѣреніяхъ, какъ это видно изъ ниже-
слѣдующей таблички:
Показанія термометровъ, наполненныхъ
водородомъ: азотомъ: углекислымъ газомъ
0° 0°,000 0°,000
20° 20,009 20,043
40° 40,011 40,059
100° 100,000 100,000.
Если допустить, что азотъ и углекислый газъ слѣдуютъ формулѣ
Сіаивіпб’а, уже упомянутой въ т. I (мы возвратимся къ ней ниже),
то получается слѣдующее продолженіе этой таблички:
н со2
200° 199°,93 199°,3
500° 499°,6 498°,4.
Результаты опытовъ Сйарриів заставили Международную Коммис-
сію Мѣръ и Вѣсовъ остановиться на томъ опредѣленіи нормальной шкалы,
которое было приведено на стр. 8.
Ольшевскій сравнивалъ показанія газовыхъ термометровъ, на-
полненныхъ водородомъ, азотомъ, кислородомъ и углекислымъ газомъ при
весьма низкихъ температурахъ. Вотъ нѣкоторыя изъ его чиселъ:
— 32°,5 — 118°,6 — 151°
ТѴ2 — 33°,0 — 119°,1 — 152°
При температурѣ — 150° для кислороднаго и при — 128° для угле-
кислаго термометровъ разница показаніи сравнительно съ термометромъ
Термометры съ жидкостями.
25
водороднымъ составляетъ 2°. Весьма вѣроятно, что при — 150° шкала
водороднаго термометра еще мало отличается отъ абсолютной шкалы
Томсона и что даже при — 220° отступленіе не превышаетъ 2°.
Къ газовымъ термометрамъ могутъ быть причислены дифференціаль-
ные термоскопы, устройство которыхъ извѣстно изъ элементарнаго курса
физики. Иногда ими пользуются, чтобы обнаружить малѣйшую разницу
температуръ въ двухъ пространствахъ, напр. сосудахъ, содержащихъ жид-
кости, въ которыя и погружаются два резервуара термометра.
Весьма чувствительный дифференціальный термометръ былъ постро-
енъ А. Тоеріег’омъ. Удобства этого прибора обнаружились при ра-
ботѣ М. Т о е р 1 е г’а надъ опредѣленіемъ плотности паровъ и газовъ.
§ 3. Термометры съ жидкостями. Измѣреніе температуръ при по-
мощи термометровъ съ жидкостями основано на наблюденіи объема, за-
нимаемаго жидкостью внутри сосуда, состоящаго изъ резервуара и при-
паянной къ нему капилярнои трубки, причемъ жидкость наполняетъ ре-
зервуаръ и часть трубки. Резервуаръ бываетъ шаровидный, продол-
говатый или, въ рѣдкихъ случаяхъ, иной формы. Трубка всегда, а ре-
зервуаръ почти всегда дѣлаются изъ стекла. Трубка снабжена шкалою,
которая нанесена или на самой трубкѣ, или на особой пластинкѣ, заклю-
ченной вмѣстѣ съ капилярной трубкой въ другую, болѣе широкую трубку.
Какъ жидкости употребляются въ термометрахъ ртуть, алкоголь и толу-
олъ и лишь въ рѣдкихъ случаяхъ другія вещества. Увеличеніе объема
жидкости въ термометрѣ обнаруживается тѣмъ, что конецъ жидкаго стол-
бика въ трубкѣ перемѣщается вдоль шкалы на линейную величину, ко-
торой соотвѣтствуетъ нѣкоторый внутренній объемъ Аѵ. представляющій
видимое или кажущееся расширеніе жидкости, и показывающій, насколько
жидкость при нагрѣваніи расширилась болѣе, чѣмъ сосудъ, въ которомт»
она находится. Докажемъ, что кажущійся коеффиціентъ расширенія у
жидкости равенъ разности между истиннымъ коеффишентомъ -расшире-
нія а жидкости и коеффиціентомъ расширенія р оболочки.
Положимъ, что повышеніе температуры АІ вызвало увеличеніе
емкости той части оболочки, которая занята жидкостью при 0°; далѣе
истинное увеличеніе жидкости пусть будетъ Аѵ± и кажущееся Аѵ. Въ та-
комъ случаѣ Аѵ = Аѵг — Аѵ%. Раздѣливъ это равенство на ѵ^АІ. гдѣ ѵ$
объемъ жидкости при 0°, и перейдя къ предѣлу, имѣемъ
1 (1ѵ 1 йѵѵ 1_ (Іѵ^
ѵ0 (11 Ѵо (11 Ѵо (11
На основаніи формулы (18) стр. 11 первый членъ есть /, второй а,
третій /?, а потому имѣемъ
у = а — $...........................(И)
ч*го и требовалось доказать. Изъ этого слѣдуетъ, что законъ наблюдае-
маго расширенія жидкости есть какъ бы результатъ совмѣстнаго прояв-
ленія двухъ законовъ истиннаго расширенія жидкости и оболочки.
26
Термометрія.
Замѣтимъ, что при выводѣ формулы (11) мы пренебрегли расшире-
ніемъ той части трубки, которая успѣла наполниться жидкостью при на-
грѣваніи послѣдней отъ 0° до наблюдаемой температуры.
Схема приготовленія термометра извѣстна: наполнивъ резервуаръ и
часть трубки надлежащимъ количествомъ жидкости, погружаютъ приборъ
въ тающій ледъ и въ пары кипящей воды, намѣчаютъ черты 0° и 100°,
раздѣляютъ разстояніе между зтими чертами на 100 равныхъ линей-
ныхъ частей и продолжаютъ шкалу ниже 0° и выше 100°. Отсчеты,
произведенные по шкалѣ термометра, построенной такимъ образомъ, да-
дутъ намъ, однако, весьма невѣрные результаты, вслѣдствіе цѣлаго ряда
причинъ, вліяющихъ на показанія прибора и требующихъ введенія соот-
вѣтствующихъ поправокъ.' Роль этихъ причинъ и способы введенія
поправокъ въ особенности выяснилъ и разработалъ Опіііаише. Всѣ
обстоятельства, вызывающія погрѣшности въ показаніяхъ термометровъ,
можно разбить на пять группъ, которыя и разсмотримъ.
I. Геометрическія свойства прибора. Объемъ трубки
между чертами 0° и 100° долженъ быть раздѣленъ на части одинаковой
емкости, не потому, чтобы мы ожидали одинаковыя кажущіяся при-
ращенія объема жидкости при одинаковыхъ повышеніяхъ температуры
по нормальной шкалѣ водороднаго термометра, а потому, что только раз-
дѣленіе трубки на части одинаковой емкости представляетъ нѣчто вполнѣ
опредѣленное, когда выбраны жидкость и матеріалъ (сортъ стекла)
оболочки термометра, нѣчто такое, отъ котораго мы затѣмъ уже можемъ
искать вполнѣ опредѣленный переходъ къ нормальной шкалѣ. Раздѣле-
ніе разстоянія между 0° и 100° на равныя линейныя части тогда только
соотвѣтствуетъ раздѣленію трубки на части одинаковой емкости, когда
внутренній каналъ трубки вполнѣ нилиндриченъ. Таковымъ геоме-
трическимъ свойствомъ трубка, однако, никогда не обладаетъ съ матема-
тическою точностью, а потому необходимо изслѣдовать трубку и опредѣ-
лить для каждаго дѣленія шкалы термометра его положеніе на другой,
фиктивной шкалѣ, дѣленія которой соотвѣтствовали бы одинаковымъ по
емкости частямъ трубки. Манипуляція, при помощи которой изслѣдуется
каналъ трубки, называется калибрированіемъ.
П. Физическія свойства жидкости и оболочки, не
зависящія отъ внѣшнихъ воздѣйствій на приборъ.
1. Волосность вліяетъ на показанія термометра, когда діаметръ
трубки очень малъ.
2. Когда жидкость смачиваетъ стѣнки трубки (алкоголь), то
термометръ, охлаждаясь, показываетъ слишкомъ низкія температуры, такъ
какъ часть жидкости остается на стѣнкахъ трубки.
3. Если термометръ погруженъ въ среду, температура которой не-
прерывно мѣняется и должна быть опредѣляема черезъ извѣстные про-
межутки времени, то въ каждый щнный моментъ температура термо-
метра будетъ отставать отъ температуры среды и слѣд.
ее показывать невѣрно. Величина отставанія зависитъ отъ теплопро-
Термометры съ жидкостями.
27
водности оболочки и жидкости, отъ ихъ массы и отъ быстроты измѣненія
температуры.
4. Емкость резервуара постепенно уменьшай гея втеченіе иногда
весьма большого промежутка времени (многіе годы) послѣ изготовленія
(выдутія) шарика. Вслѣдствіе этого двѣ основныя точки (0° и 100°) по-
степенно перемѣщаются, а потому и всѣ дѣленія шкалы мало-по-малу
мѣняютъ свое значеніе. Объясняется это молекулярными перемѣщеніями,
происходящими въ стеклѣ втеченіе долгаго времени послѣ того, какъ
стекло, размягченное для выдутія шарика, охладилось. Необходимо какъ
можно чаще опредѣлять истинное положеніе двухъ основныхъ точекъ на
шкалѣ термометра.
III. Вліяніе внѣшнихъ физическихъ причинъ на по-
казанія термометровъ. Сюда относятся:
1. Вліяніе измѣненій температуры. Всякое нагрѣваніе
и послѣдующее затѣмъ охлажденіе термометра вызываетъ временное «при-
н и ж е н і е основныхъ точекъ, вслѣдствіе того, что резервуаръ нескоро
принимаетъ тотъ объемъ, который соотвѣтствуетъ болѣе низкой темпера-
турѣ. Это явленіе напоминаетъ упругое послѣдѣйствіе (т. I), и можетъ
быть названо термическимъ послѣдѣйствіемъ.
2. Вліяніе внѣшнихъ давленій на резервуаръ, повышаю-
щихъ показанія термометровъ. Такое давленіе производится жидкостью,
въ которую погруженъ резервуаръ термометра, а также воздухомъ.
3. Вліяніе силы тяжести на жидкость, вызывающее вну-
треннее давленіе на резервуаръ, понижающее показанія термометра.
Это вліяніе зависитъ отъ показанія термометра, т.-е. отъ длины жидкаго,
давящаго столба, и отъ его положенія; оно наибольшее при вертикаль-
номъ положеніи термометра.
IV. Вліяніе расположенія термометра относительно
среды, температуру которой требуется опредѣлить. Во многихъ слу-
чаяхъ нѣтъ возможности погрузить весь термометръ въ эту среду, или по-
тому. что онъ въ ней не вмѣщается, или потому, что это лишило бы
насъ возможности видѣть конецъ жидкаго столба и сдѣлать отсчетъ. Такъ
называемы «выступающій столбикъ», находящійся внѣ изслѣдуе-
мой среды, обладаетъ иной температурой, чѣмъ среда; онъ вслѣдствіе
этого обыкновенно укороченъ, что и влечетъ за собою необходимость
ввести поправку на выступающій столбикъ.
V. Вліяніе законовъ расширенія жидкости и обо-
лочки на показанія термометра. Необходимо знать поправки, служащія
для перевода показаній даннаго термометра къ нормальной шкалѣ термо-
метра водороднаго. Объ этомъ было уже сказано на стр. 16 и мы ви-
дѣли, какими способами эти поправки могутъ сдѣлаться извѣстными.
Когда выбрана опредѣленная жидкость, то величина
поправокъ для каждаго дѣленія шкалы термометра за-
виситъ уже только отъ сорта стекла, изъ котораго
приготовленъ термометръ.
28
Термометрія.
Рис. 7.
а\
Рис. 6.
Всего въ этомъ перечнѣ указано 10 причинъ, вліяющихъ на пока-
занія термометровъ съ жидкостями.
§ 4. Термометры ртутные; ихъ изготовленіе. Преимущества ртути
передъ другими жидкостями, служащими для наполненія термометровъ,
слѣдующія :
1. Очищеніе ртути производится сравнительно легко, такъ что можно
быть увѣреннымъ, что различные термометры наполняются вполнѣ одина-
ковою жидкостью.
2. Ртуть не смачиваетъ стекла, вслѣдствіе чего исчезаетъ одно изъ
десяти приведенныхъ выше обстоятельствъ, на вліяніе котораго было бы
весьма затруднительно ввести соотвѣтствующую поправку.
3. Ртуть остается жидкою въ сравнительно весьма широкихъ пре-
дѣлахъ температуръ.
Трубка для термометра должна быть тщательно выбрана, ибо ея ка-
налъ долженъ по возможности меньше отступать отъ цилиндрической формы.
Для изученія геометрическихъ свойствъ канала вво-
дятъ въ него столоикъ ртути, длину котораго измѣ-
ряютъ въ различныхъ мѣстахъ трубки. Выбираются
такія трубки, въ которыхъ эта длина весьма мало мѣ-
няется при перемѣщеніи ртути отъ одного конца
трубки до другого.
Способъ наполненія термометра ртутью понятенъ
изъ рис. 6; поперемѣнно нагрѣвая и охлаждая резер-
вуаръ мы вводимъ въ него ртуть, пока весь воздухъ
не будетъ изъ него выгнанъ. Затѣмъ выливаютъ лиш-
нюю ртуть изъ сосуда И и, нагрѣвая стекло подъ этимъ
сосудомъ, оттягиваютъ трубку въ тонкое остріе. На-
грѣвъ термометръ немного выше той температуры, до
которой должна идти его шкала, запаиваютъ трубку;
около верхняго конца послѣдней обыкновенно оста-
вляютъ небольшое вздутіе, какъ видно на рис. 7, на
которомъ представленъ готовый термометръ, шкала
котораго нанесена на самомъ стеклѣ.
При выборѣ размѣровъ резервуара и діаметра ка-
нала трубки пользуются слѣдующими соображеніями.
1. Для увеличенія чувствительности термоме-
тра, въ смыслѣ способности обнаруживать малыя тем-
пературныя измѣненія, слѣдуетъ брать резервуаръ
большой и трубку тонкую.
При слишкомъ тонкой трубкѣ- задерживается перемѣщеніе ртути
вслѣдствіе внутренняго тренія.
3. При большомъ резервуарѣ термометра уменьшается чувствитель-
ность въ смыслѣ способности быстро воспринимать температуру окружа-
ющей среды.
4. При большомъ резервуарѣ термометръ отнимаетъ много тепла
2.
Ртутные термометры.
29
отъ того тѣла, температуру котораго требуется опредѣлить, чтб иногда
можетъ повлечь за собою замѣтное пониженіе этой температуры.
Смотря по назначенію термометра, должны получить перевѣсъ тѣ
или другія соображенія при выборѣ размѣровъ резервуара и трубки. Въ
хорошихъ французскихъ термометрахъ емкость резервуара примѣрно въ
60 разъ превышаетъ емкость трубки между дѣленіями 0° и 100°; толщина
стѣнокъ резервуара 0,5—0,7 мм.; длина одного градуса около 6 мм.
Предполагая, что точки 0° и 100° должны помѣщаться на шкалѣ
термометра, разсмотримъ способы ихъ первоначальнаго опредѣленія, ко-
торые въ то же время суть способы, по которымъ впослѣдствіи произво-
дится опредѣленіе ихъ новаго положенія, постепенно измѣняющагося
(стр. 26 II, 4 и III, 1). Сперва опредѣляется каждый разъ положеніе 100°.
I. Опредѣленіе точки 100° на шкалѣ термометра.
100° есть температура кипѣнія чистой воды придавленіи въ 760 мм. ртут-
наго столба, температура котораго 0°, а слѣд. плот-
ность ртути 13.59593, притомъ подъ широтою 45°.
Для приведенія къ другимъ шпротамъ можетъ
служить формула : ^45 = 1 — 0,00259 С08 2<р.
Въ Петербургѣ это отношеніе равно 1,00128,
въ Москвѣ — 1,000942.
На рис. 8 изображенъ простой приборъ
— кипятильникъ, служащій для опредѣленія
точки 100°. Онъ состоитъ изъ мѣднаго сосуда Р.
надъ которымъ .находится широкая трубка А,
окруженная и прикрытая цилиндромъ В. до верх-
ней крышки котораго трубка А не доходитъ.
Пары воды, кипящей въ Р, поднимаются по А.
опускаются въ пространство между А и В и
Рис. 8.
выходятъ черезъ трубку Р наружу. Манометръ т служитъ для опредѣ-
ленія избытка давленія паровъ надъ атмосфернымъ давленіемъ. Термо-
метръ вставляется при помощи пробки въ отверстіе а, причемъ резерву-
аръ не долженъ касаться поверхности воды; въ то же время конецъ
ртутнаго столбика долженъ весьма мало выступать наружу. Послѣ про-
должительнаго кипѣнія воды отмѣчается положеніе конца ртутнаго столба,
или дѣлается отсчетъ, когда положеніе основной точки провѣряется на
готовой шкалѣ. Показанія барометра и манометра т опредѣляютъ упру-
гость паровъ, по которой узнаютъ,ихъ температуру, пользуясь готовыми
таблицами. Конечно и здѣсь должны быть введены тѣ поправки на дав-
леніе, о которыхъ будетъ сказано ниже.
Болѣе сложными приборами пользуются въ учрежденіяхъ, занимающихся
изготовленіемъ наилучшихъ термометровъ. Такъ въ Физико-Техническомъ
Императорскомъ У чрежденіи въ Шарлоттен бургѣ около Берлина (Ееісйя-
апбіаіі) употребляется приборъ, въ которомъ между прочимъ верхняя
часть наружнаго цилиндра сдѣлана изъ стекла, вслѣдствіе чего отсчетъ
можетъ быть сдѣланъ въ то время, какъ весь термометръ находится въ
30
Термометрія.
парахъ воды. Поправка (какъ мы увидимъ, всегда сомнительная) на вы-
ступающій столбикъ отпадаетъ. Пары образуются въ отдѣльномъ кипя-
тильникѣ, изъ котораго (ши переводятся въ приборъ, содержащій воду.
Кромѣ того принимаются особыя мѣры, чтобы весьма точно опредѣлить пере-
вѣсъ упругости пара надъ давленіемъ атмосферы. Регпеі, ^е^еги
СгитІісЬ подробно описали всѣ детали изготовленія «нормальныхъ»,
т.-е. образцовыхъ термометровъ въ Шарлоттенбургѣ.
Рис. 9.
Рис. іо.
Рис. 11.
Весьма интересенъ приборъ, который построилъ Р. СйарриІ8
для Международнаго Бюро Мѣръ и Вѣсовъ около Парижа. Этотъ приборъ
изображенъ на рис. 9, 10 и 11: съ лѣвой стороны (9) внѣшній видъ
прибора, съ правой наверху (10) вертикальный разрѣзъ верхней части
цилиндра А; съ правой стороны внизу (11) изображенъ горизонтальный
разрѣзъ черезъ трубку В. Приборъ состоитъ изъ котелка С, въ которомъ
вода приводится въ кипѣніе. Пары проходятъ черезъ трубку О въ подшип-
никъ Мг (рис. 9 и 11), имѣющій форму кубика и соединенный при помощи
трубки В съ такимъ же подшипникомъ ТИ2. Трубка В, раздѣленная пе-
регородкою на двѣ части, можетъ вращаться около своей оси между непо-
Ртутные термометры.
31
движными подшипниками, какъ это ясно видно на рис. 11. Съ трубкою В
соединена часть Л, состоящая изъ цилиндра, имѣющаго двойныя стѣнки,
какъ показано на рис. 10. Внутреннее пространство соединено съ М17
наружное съ М2 (рис. 11). Подшипникъ /И2 соединенъ съ внутренней
трубкою холодильника Е, черезъ внѣшнюю оболочку котораго протекаетъ
холодная вода. Сгустившійся паръ проводится черезъ трубку К ко дну
котелка С.
Испытуемый термометръ помѣщается въ верхней части цилиндра А;
онъ виситъ на крючечкѣ и проходитъ черезъ трубку, вставленную въ
отверстіе крышки цилиндра и черезъ направляющую часть Р (рис. 10).
Отсчитываніе производится при помощи зрительной трубочки Л.
Приборомъ можно пользоваться въ двухъ положеніяхъ: одно изо-
бражено на рисункѣ; другое положеніе получается, если повернуть ци-
линдръ А и трубочку В около оси послѣдней на 90°.
линдръ А приметъ горизонтальное положеніе
и ляжетъ на вилообразную поставку № Такимъ
образомъ можно избѣгнуть необходимости вводить по-
правку на внутреннее давленіе ртутнаго столба. Ма-
нометръ Н служитъ для опредѣленія избытка упру-
гости паровъ въ М± надъ атмосфернымъ давленіемъ.
Паръ проходитъ по трубкѣ Л въ и черезъ В
(рис. 11) во внутреннюю трубку цилиндра А; далѣе
онъ "идетъ черезъ отверстія въ Р, спускается по на-
ружной оболочкѣ цилиндра А и черезъ В (рис. 11)
проходитъ въ М2, и наконецъ въ Е сгущается въ жид-
кость. Какъ сказано, этотъ же приборъ служитъ и для
частыхъ провѣрокъ положенія верхней основной точки
на готовыхъ термометрахъ.
При этомъ ци-
Рис. 12
в
[I. Опредѣленіе точки 0° на шкалѣ термометра. По-
ложеніе нижней основной точки опредѣляютъ, погружая термометръ въ
тающій снѣгъ. Тщательное изученіе явленія термическаго послѣдѣйствія
привело къ слѣдующему правилу: опредѣленіе точки 0° должно быть
сдѣлано немедленно послѣ опредѣленія точки 100°; термометръ, выну-
тый изъ паровъ кипящей воды, должешь быть опущенъ въ тающій ледъ,
какъ только онъ успѣетъ охладиться примѣрно щ 50°.
На рис. 12 изображенъ простой приборъ, служащій для опредѣленія
нижней основной точки. Металлическій сосудъ А наполненъ снѣгомъ
или скобленнымъ льдомъ, который непремѣнно слѣдуетъ облить водой,
чтобы между кусочками льда не оставался воздухъ. Избытокъ воды, а
также вода, образующаяся при таяніи льда, вытекаетъ черезъ отверстіе,
находящееся въ нижней части сосуда. Мѣсто для термометра получаютъ
заранѣе, втыкая деревянную палочку въ ледъ.
Въ Шарлоттенбургѣ (Ееісйвапвіаіі) пользуются приборомъ, состоя-
щимъ изъ двухъ стеклянныхъ колоколовъ, вставленныхъ одинъ въ другой,
отверстіями вверхъ. Оба снабжены трубками для вытеканія воды. Вну-
32
Термометрія.
тренній сосудъ и промежутокъ между обоими сосудами наполняются ско-
бленнымъ льдомъ. Приборъ Международнаго Бюро Мѣръ и Вѣсовъ имѣетъ
подобное же устройство, но въ немъ промежутокъ между двумя сосудами
весьма узкій и въ этомъ промежуткѣ находится слой воздуха. Ледъ дол-
женъ быть по возможности чистъ и ни въ какомъ случаѣ не долженъ
содержать слѣдовъ соли.
§ 5. Калибрированіе термометровъ. Изготовляя термометръ, слѣ-
дуетъ предварительно выбрать по возможности цилиндрическую трубку,
перемѣщая въ имѣющихся длинныхъ трубкахъ ртутный столбикъ при-
мѣрно въ 70 мм. длины. Для лучшихъ термометровъ выбираютъ такую
трубку, въ которой длина этого столба не мѣняется болѣе, чѣмъ на 1 мм.
Калибрированіе (стр. 26) производится на готовыхъ термоме-
трахъ; калибрированіе трубки до изготовленія термометра и нанесеніе
уже исправленной шкалы не представляетъ никакихъ выгодъ и нынѣ
Рис. 13.
оставлено. Калибрированіе термометровъ, снабженныхъ шкалою изъ мо-
лочнаго стекла почти невозможно. То же самое относится къ термоме-
трамъ, не снабженнымъ на концѣ маленькимъ расширеніемъ (см. рис. 7,
стр. 28) и не содержащимъ слѣдовъ воздуха, при полномъ отсутствіи ко-
тораго невозможно отдѣлить столбика ртути.
На рис. 13 изображенъ приборъ, который въ Шарлоттенбургѣ слу-
жилъ для калибрированія. Доска ВВ вращается около горизонтальной
оси и можетъ быть наклонена на желаемый уголъ къ горизонту при по-
мощи дуги Т и закрѣпляющаго винта. Одинъ пли два микроскопа ММ
перемѣщаются вдоль салазокъ 55. Изслѣдуемый термометръ кладется на
двѣ подставки іі, которыя могутъ быть приподняты или опущены и ко-
торыя прикрѣплены къ бруску ; этотъ брусокъ можно немного пере-
мѣщать и вращать вдоль поверхности доски ВВ. Такимъ образомъ можно
установить ось термометра параллельно салазкамъ 55, причемъ горизон-
Калибрированіе термометровъ.
33
гальная нить окулярнаго микрометра микроскопа, перемѣщаемаго вдоль 55,
должна совпадать съ осью трубки, всѣ дѣленія которой должны быть оди-
наково отчетливо видны, разъ микроскопъ установленъ на одно изъ нихъ.
Существуетъ цѣлый рядъ различныхъ способовъ калибриро-
ванія термометренной трубки и мы не можемъ здѣсь войти въ подробное
ихъ разсмотрѣніе; ограничиваемся указаніемъ на нѣкоторые простѣйшіе
способы, не могущіе, впрочемъ, давать очень точныхъ результатовъ. Даль-
нѣйшія подробности можно найти въ сочиненіяхъ, посвященныхъ спеці-
ально лабораторнымъ работамъ, а также въ статьяхъ, указанныхъ въ
концѣ этой главы въ обзорѣ литературы. Простые способы калибриро-
ванія предложили Оау-Ь.иззас, ЕидЬег^, Наіівігоет и Вез-
зеі. Наиболѣе точный способъ ВеззеГя былъ разработанъ Оеіііп-
^еп’омъ; важныя работы по вопросу о калибрированіи сдѣлали далѣе
ТЬіез еп, Магеск, Вгоск, Вепоіі и О и і 11 а п т е. Мы огра-
ничимся разсмотрѣніемъ двухъ способовъ Ѳау-Ьи8 8ас’а.
1. Первый способъ (тау-Ьпзяас’а. Достаточно указать на
основную идею этого способа, могущаго дать лишь общее понятіе о гео-
метрическихъ свойствахъ капилярнаго канала. Отдѣлимъ столбикъ ртути
въ нѣсколько сантиметровъ длины (способа, коимъ достигается такое от-
дѣленіе, мы не описываемъ) и будемъ его передвигать вдоль трубки такъ,
чтобы при каждомъ новомъ положеніи одинъ изъ его концовъ занялъ то
положеніе, которое передъ тѣмъ было занято его другимъ концомъ. Та-
кимъ образомъ вся трубка раздѣлится на равнообъемныя части неодина-
ковой длины. Раздѣляя эти длины, каждую на опредѣленное число рав-
ныхъ частей, получимъ шкалу, дѣленія которой соотвѣтствуютъ прибли-
зительно одинаковымъ внутреннимъ объемамъ. Этимъ простѣйшимъ спо-
собомъ пользовался напр. Ке^паніі при изготовленіи своихъ тер-
мометровъ.
II. Второй способъ Сгау-Ьи88ас’а. Формулируемъ прежде
всего точнѣе задачу, которую требуется рѣшить. Положимъ, что для
щннаго термометра были опредѣлены точка таянія льда и точка кипѣнія
воды и что первая оказалась находящейся у дѣленія а0 шкалы, вторая —
у дѣленія 100 -|- а]00. Идеальная шкала, дѣленія которой мы ищемъ, на-
чинается у дѣленія а0 и кончается у дѣленія 100 + аюо шкалы термо-
метра и слѣд. имѣетъ длину 100 -(- а100 — а0 дѣленій этой же шкалы.
Объемъ трубки, соотвѣтствующій идеальной шкалѣ, раздѣляемъ мысленно
на 100 равныхъ частей; соотвѣтствующія имъ 99 черточекъ, располо-
женныя между дѣленіями а0 и 100 -|- а100 термометренной шкалы, и со-
ставятъ, вмѣстѣ съ этими двумя конечными дѣленіями, искомую идеаль-
ную шкалу. Пусть одно изъ чиселъ 1, 2, 3, 4,.99. Обозна-
чимъ черезъ (7Ѵ) положеніе АЛтой черты идеальной шкалы на термоме-
тренной шкалѣ. Въ такомъ случаѣ, вообще
№ = ......... (12)
Задача и заключается въ опредѣленіи величинъ
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Г. III. изд. 3-е.
3
34
Термометрія.
Величины адг называются поправками; это тѣ величины, ко-
торыя слѣдуетъ прибавить къ температурамъ, наблюденнымъ по термоме-
тренной шкалѣ, чтобы получить температуры по идеальной шкалѣ. До-
пустимъ напр., что 30-ое дѣленіе идеальной шкалы приходится на дѣле-
ніи 30,12 терм. шкалы; тогда а30 = + °Л2 5 слѣд. поправка равна - 0,12
и наблюденная температура въ 30° въ дѣйствительности равна 30—|—
0,12) = 29°,88. Если 70-ое дѣленіе идеальной шкалы приходится
на дѣленіи 69,91 терм. шкалы, то а70 — — 0.09 5 слѣд. поправка равна
4- 0,09 и наблюденная температура 70° должна быть замѣнена числомъ
70 -|- 0,09 = 70°,09. Способъ Сгау-Ьиззас’а, впрочемъ еще раньше
предложенный НеппегѴомъ, заключается въ слѣдующемъ. Отдѣлимъ
ртутный столбикъ, длина котораго мало отличалась бы отъ длины п дѣ-
леній шкалы, гдѣ п содержится цѣлое число к разъ въ числѣ 100, такъ что
кп 100...........................................................(13)
Установимъ столбикъ послѣдовательно въ к положеніяхъ, при кото-
рыхъ нижній (ближайшій къ 0°) конецъ находился бы на дѣленіяхъ 0, п,
2я, Зп . . . . , (к — 2)п, (к Г)п шкалы, а верхній близъ дѣленій л,
2я, 3/г, 4я......(к — 1)л, кп (= 100), и пусть точныя положенія верх-
няго конца находятся на дѣленіяхъ п + дь 2/г —|— Зп + д3.........(к —
1)/г-|-д^_1, 100 -Р && Произвольную изъ величинъ <5 обозначимъ
черезъ <5у; это можетъ быть величина положительная и отрицательная.
Допустимъ, что всѣ искомыя адг суть величины малыя и что длина стол-
бика не измѣнится вовсе, если его передвинуть на величину «дг, т.-е.
если его начало устанавливать не на дѣленіяхъ 0, п, 2п и т. д., но на
дѣленіяхъ а0, (и) = л 4~ «и, (2^ = 2п 4" , (Зл) = Зл 4~ «зп и т- Д-,
иначе говоря на нулевомъ, л-омъ, 2л-омъ и т. д. дѣленіяхъ искомой иде-
альной шкалы.
Изъ самаго способа полученія величинъ бу явствуетъ, что к разъ
взятый объемъ ртутнаго столбика заполняетъ 100 4"2 Дѣленій термо-
метренной шкалы; но 100 дѣленій этой шкалы (отъ 0 до 100) равны
100 4- а0 '•— а100 дѣленіямъ искомой шкалы, а слѣд. к разъ взятый объемъ
ртутнаго столбика заполняетъ 100 4-* «о — аіоо равнообъемныхъ
дѣленій этой искомой шкалы. Отсюда слѣдуетъ, что объемъ ртутнаго
столбика равенъ емкости
100 4- ао аюо +2
к
дѣленій искомой шкалы. Введемъ для краткости обозначеніе
«о _ «юо 4” 2
- к ....................................<І4>
Принимая во вниманіе (13), получимъ, что объемъ ртутнаго
столбика равенъ емкости
п +/?
Калибрированіе термометровъ.
35
дѣленіи искомой шкалы. При маломъ можно считать/^ дѣленій
тождественными на обѣихъ шкалахъ, а отсюда слѣдуетъ, что длина
ртутнаго столбика, во всѣхъ его положеніяхъ, укоро-
ченная (исправленная) на $ дѣленій, равна длинѣ п дѣ-
леній искомой шкалы. Это даетъ возможность опредѣлить поло-
женіе дѣленіи (/г), (2//), (3//) и т. д. искомой шкалы, для которой начало
(0) = а0 и конецъ (кп) = (100) = 100 «юо-
Какъ сказано выше, мы предполагаемъ, что длина п столбика
въ его первомъ положеніи не измѣнится, если мы его начало пере-
двинемъ отъ 0 термометренной шкалы къ 0 искомой шкалы, т.-е. къ дѣ-
ленію а0. Тогда конецъ столбика придется на дѣленіи а0 4~ п 4“ а
конецъ исправленной длины столбика у дѣленія а0 4“ п 4“ —Р- На
основаніи сказаннаго выше, здѣсь и должно находиться /г-тое дѣленіе
искомой шкалы. Итакъ
(«) = п -Ь а0 — 0 + |
а слѣД- . . . .................(15)
ап = «о — 0 ’
что и даеть поправку ап для перехода отъ наблюденныхъ /г°
къ исправленнымъ тг° ап.
Длина п 4~ <52 столбика не измѣнится, если мы начало помѣстимъ у
/г-таго дѣленія искомой шкалы, т.-е. у (//)-таго дѣленія данной шкалы.
Тогда конецъ исправленной длины придется на дѣленіи (гі) + п 4“ ^2 — Р*
съ которымъ и должно совпасть 2/г-тое дѣленіе искомой шкалы. Итакъ
(2п) = (п) + п 4- ; вставивъ сюда (гі) изъ (15), получимъ
(2 л) = 2л + а0 — 20+ <5.2 |
«= а0 — 2/У -|- д] -|“ <5-2 і
Конецъ исправленной длины ртутнаго столбика, начало котораго на-
ходится при дѣленіи (2/7), будетъ находиться у дѣленія (2п) + п-\- д3 -/?,
съ которымъ должно совпасть 3/г-тое дѣленіе искомой шкалы. Слѣд.
(3/г) = (2/г) 4" 4" — Л Вставляя сюда (16), имѣемъ
(3//) = 3/г 4- п0 — 3/? 4“ 4~ <5‘2 4~
а3/г = а0 4" 4- ^2 4" Й3
.Іегко видѣть, какъ слѣдуетъ идти дальше. Полагая, что р цѣлое
число, получаемъ общее выраженіе для положенія р/г-таго дѣленія иско-
мой шкалы и для величины арп :
Р .
(рп) - - рп + а0 - Р/?4~2
1
Р
арп = «о — Р$ 4-Е дІ
1
...................(18)
3*
36
Термометрія .
Такимъ образомъ найдена поправка — арп для дѣленій т 2 гц Зп
и т. д. Полагая въ (18) р = й, имѣемъ
фгі) = кп + а0 - +2
гдѣ 2 6і безъ знаковъ означаетъ, что берется сумма всѣхъ О/. Но &я = 1ОО,
согласно (13); вставляя еще /?, см. (14), получаемъ
(ЮО)= 100 + а100,
какъ и должно быть. Если поправку къ дѣленію рп термометрен-
ной шкалы обозначить черезъ урп, то (18) даетъ
Р
7рп ~ Р& — «о 2 й/....................(1уА>
1
Если термометръ показываетъ /ш°, то слѣдуетъ записать темпера-
туру рп + урп.
Вопросомъ о способѣ Сгау-Ьизбас’а занимался В. В. Лерман говъ.
Не вдаемся ни въ какія дальнѣйшія подробности, относящіяся къ
многократному калибрированію при помощи нѣсколькихъ ртутныхъ стол-
биковъ различной длины (Л различное) или съ однимъ столбикомъ, при-
чемъ одно калибрированіе начинается, какъ было сказано, съ дѣленія О,
а другія напр. съ дѣленій 5°, 10° и т. д.
Изъ другихъ способовъ калибрированія представляетъ интересъ по
своей сравнительной простотѣ способъ Наііеіго еш’а. Принципъ, на
которомъ онъ основанъ, изложенъ въ «Руководствѣ къ практикѣ физиче-
скихъ измѣреній > Ф. Кольрауша, С.-Петербургъ 1891, стр. 75 (способъ не
названъ) и въ извѣстномъ учебникѣ Миеііег’а (Мпеііег-Роиіііеі),
8-ое изданіе подъ редакціей Е. РТаипсіІег’а, т. П, отдѣл. 2, стр. 57—59
(1897 г.). Когда величина адг? см. (12) стр. 33, найдена для ряда раз-
личныхъ А/, то эти же величины для промежуточныхъ дѣленій могутъ
быть опредѣлены по графическому методу. Для этого чертятъ коорди-
натныя оси на листѣ бумаги, раздѣленномъ на квадратныя клѣтки. На
оси абсциссъ откладываютъ дѣленія 7Ѵ шкалы термометра; на оси орди-
натъ — величины адг, для удобства въ удесятеренномъ масштабѣ про-
тивъ масштаба дѣленій М Соединивъ полученныя такимъ образомъ
точки плавною кривою, мы можемъ допустить, что ея ординаты дадутъ
намъ величины для всѣхъ дѣленій шкалы термометра.
Въ Международномъ Бюро Мѣръ иВѣсовъ въ Парижѣ въ настоящее время
примѣняются новые методы Сгиіііаиш е’а и Т11 і е 8 е п’а, описанные
въ «Тгаѵапх еі Мётоіге8» этого Бюро. Г-жа Тагпагісіег (1904), ра-
ботающая въ Бюро, дала прекрасный обзоръ новѣйшихъ методовъ въ
статьѣ, къ которой Ѳпіііаите написалъ предисловіе.
Въ § 3, стр. 25, мы помѣстили обзоръ тѣхъ десяти обстоятельствъ,
которыя вліяютъ на показанія термометровъ съ жидкостями и заставля-
ютъ насъ вводить соотвѣтствующія поправки. На стр. 28 было указано,
Ртутные тррмометры.
37
что одно изъ этихъ обстоятельствъ, а именно смачиваніе стѣнокъ трубки
жидкостью, въ ртутныхъ термометрахъ роли не играетъ. Изъ остаю-
щихся, такимъ образомъ, девяти поправокъ мы пока разсмотрѣли только
одну, поправку на калибръ канала. Обращаемся къ бѣглому обзору
остальныхъ поправокъ.
§ 6. Вліяніе свойствъ стекла и ртути, а также внѣшнихъ физи-
ческихъ причинъ на показанія ртутныхъ термометровъ.
I. Волосность вызываетъ запаздываніе въ показаніяхъ термо-
метра и ставитъ предѣлы для чувствительности термометра, не давая воз-
можности пользоваться трубками съ чрезмѣрно тонкими каналами. Вели-
чина поверхностнаго давленія не одинакова во всѣхъ частяхъ трубки,
т.-е. при различныхъ температурахъ, такъ какъ ширина трубки не вездѣ
одинаковая; далѣе она зависитъ отъ того, поднимается или опускается
ртуть,’ ибо отъ этого зависитъ форма мениска и величина краевого угла
(т. I). Съ измѣненіемъ поверхностнаго давленія мѣняется и емкость
резервуара. Малѣйшая нечистота ртути вызываетъ весьма замѣтное
отставаніе въ показаніяхъ термометра. СгиіПапте рекомендуетъ про-
мывать трубку кипящей водой до изготовленія термометра; этимъ сни-
мается внутренній слой стекла, полурастворенный въ водѣ, покрывающей
стѣнки канала вслѣдствіе гигроскопичности стекла.
II. Отставаніе показаній термометра, погруженнаго въ среду,
температура которой непрерывно мѣняется. Пусть Т перемѣнная темпе-
ратура среды, і наблюденная температура, которую можно считать за из-
вѣстную намъ, хотя бы графически построенную функцію времени г.
Тогда имѣемъ формулу
т -'+ ‘ *...........................<1в>
гдѣ с постоянная, зависящая отъ свойствъ резервуара термометра. Ее
можно опредѣлить, наблюдая температуры і термометра, погруженнаго
въ среду съ постоянною температурой 1\. Если начальное значеніе і,
то имѣемъ
откуда
По Тйіевеп’у колеблется отъ 7 до 30 сек. для различныхъ тер-
мометровъ.
Математическую теорію вопроса о показаніяхъ термометра, подвер-
женнаго быстро мѣняющимся температурамъ, развилъ Нет^еееіі, ос-
новываясь на уравненіяхъ теоріи теплопроводности (см. ниже).
ІП. Перемѣщеніе основныхъ точекъ. Выше мы на
стр. 27 указали на двѣ причины, вызывающія перемѣщеніе основ-
ныхъ точекъ: 1) прогрессивное непрерывное поднятіе нуля, продолжаю-
38
Термометрія.
щееся иногда втеченіе многихъ лѣтъ послѣ изготовленія термометра,
и 2) временное приниженіе нуля, вызываемое всякимъ нагрѣваніемъ, за
которымъ слѣдуетъ постепенное возвращеніе нуля къ прежнему положе-
нію. Повидимому, однако, въ обоихъ случаяхъ дѣйствуетъ одна и та же
причина, проявленіе которой мы на стр. 27 назвали термическимъ по-
слѣдѣйствіемъ. Приготовленіе термометра сопровождается нагрѣваніемъ
стекла до его размягченія, которое и можно разсматривать, какъ причину
сравнительно огромнаго приниженія нулевой точки, постепенно затѣмъ
поднимающейся. Сильное охлажденіе вызываетъ отрицательное прини-
женіе, т.-е. временное поднятіе нулевой точки. Вообще можно сказать,
что всякое измѣненіе температуры вызываетъ сперва быстрое, а затѣмъ
медленное, но продолжительное измѣненіе емкости резервуара термометра.
Такъ, при охлажденіи, емкость резервуара получается сначала слишкомъ
большою, вслѣдствіе чего конецъ ртутнаго столба при 0° оказывается
приниженнымъ.
Приниженіе основныхъ точекъ было весьма тщательно изслѣдовано
въ Шарлоттенбургѣ (Ееісішапзіаіі) и въ Международномъ Бюро около Па-
рижа. Мы лишь вкратцѣ укажемъ на нѣкоторые результаты.
1. Приниженіе исчезаетъ тѣмъ быстрѣе, чѣмъ выше температура,
которую имѣлъ термометръ передъ погруженіемъ въ тающій ледъ. Вотъ
почему слѣдуетъ, опредѣляя положеніе нормальныхъ точекъ, возможно
быстро переносить термометръ изъ паровъ кипящей воды въ тающій ледъ.
2. Измѣненія основныхтэ точекъ въ значительной степени умень-
шаются, если подвергнуть готовый термометръ продолжительному (нѣ-
сколько недѣль) догрѣванію или отжиганію въ парахъ сѣры, ртути или
даже кадмія. На догрѣтыхъ французскихъ термометрахъ имѣется над-
пись «гесші»,
3. Величина прогрессивнаго измѣненія, а также временныхъ при-
ниженій, въ высокой степени зависитъ отъ сорта стекла. Не годится
стекло, называемое хрусталемъ и содержащее свинецъ, а также не го-
дятся всѣ тѣ стекла, въ составъ которыхъ входятъ К и Ыа одновременно.
Особыя преимущества представляютъ тугоплавкія стекла французское
стекло ѵегге сіиг и нѣкоторые сорта іенскаго стекла, въ особенности
№№ 59ш и 16ш.
4. Не подлежитъ сомнѣнію, что приниженіе основныхъ точекъ уже
существуетъ въ то время, какъ термометръ показываетъ какую-либо тем-
пературу /, и что слѣд. каждой температурѣ і соотвѣтствуетъ особое по-
ложеніе основныхъ точекъ или особое приниженіе нуля. Отсюда
является необходимость вводить поправку на приниженіе нуля
при всякомъ отсчетѣ термометра. Только вводя эту поправку, получаемъ
согласные результаты при измѣреніи температуръ одновременно съ весьма
различными по составу стекла и величинѣ приниженія термометрами,
(лиіііаите далъ таблицу приниженій нуля для различныхъ і и при-
томъ для термометровъ изъ ѵегге (Іиг; приниженіе доходитъ почти до
0° 1 при / = 100°. Тйіебеп, Воеіісйег и др. дали эмпирическія
Ртутные термометры.
39
формулы, напр. вида такъ, для іенскаго стекла № 16ш
ВоеѣѣсЬег находитъ % = 0,00071/ -ф- 0,00008/2.
8 с И о И (въ Іенѣ) устроилъ (1897) термометръ, резервуаръ кото-
раго состоитъ изъ стекла, термическое послѣдѣйствіе котораго мало
(№ 16ІП); внутри резервуара впаянъ маленькій стерженекъ изъ стекла,
обладающаго большимъ термическимъ послѣдѣйствіемъ (№ 335ш). Два
дѣйствія на постоянную точку компенсируются и, какъ показали изслѣ-
дованія НоИшапп'а, нагрѣваніе до 300° не вызываетъ въ этихъ тер-
мометрахъ никакого замѣтнаго приниженія.
Вопросомъ о перемѣщеніи основныхъ точекъ занимался еще Маг сЬІ8.
IV. Вліяніе давленій на показанія ртутныхъ тер-
мометровъ. Внѣшнее давленіе, обыкновенно слагающееся изъ давле-
ній атмосферы и (если измѣряется температура жидкости) гого столба
жидкости, который находится выше резервуара термометра, повыша-
етъ показанія послѣдняго. Повышеніе вызванное давленіемъ въ
1 мм. ртутнаго столба (0° и широта 45°) называется коеффиціен-
т о м ъ в н ѣ пг н я г о д а в л е н і я.
Внутреннее давленіе вызывается ртутнымъ столбомъ и зависитъ отъ
его длины, температуры и наклона къ горизонту; оно вызываетъ умень-
шеніе показаній термометра. Уменьшеніе /?/, вызванное, какъ выше,
давленіемъ въ 1 мм., называется к о е ф ф и ц і е н т о м ъ внутрен-
няго давленія.
Внѣшнее давленіе Р, отличающееся отъ нормальнаго въ 760 мм.,
вызываетъ необходимость ввести поправку 7е = ~ $е(Р 760).
Если длина ртутнаго столбика, считая отъ средины резервуара, при
измѣряемой температурѣ /° равна //, плотность ртути равна д. при /° и <50
при 0°, наклонъ стержня къ горизонту есть а, то необходимо ввести поправку
Ті = А 8ІП «•
Вся поправка у на давленіе равна
<5,
7 = ^іІіх 8ІП« ~ ™0)................(20)
()о
Эта поправка увеличивается, когда въ термометрѣ находятся слѣды
газа, сжимаемаго при повышеніи температуры.
Коеффиціентъ @е опредѣляется при помощи особыхъ приборовъ, въ
которыхъ наблюдаются показанія термометра, подвѣшеннаго въ глице-
ринѣ внутри вертикальнаго цилиндра, поперемѣнно соединяемаго съ внѣш-
нимъ воздухомъ и съ воздушнымъ насосомъ. Величина колеблется
для различныхъ термометровъ между 0°,0001 и 0°,0004. Для нормаль-
наго термометра № VII въ Шарлоттенбургѣ = 0°,0001522; для термо-
метровъ изъ ѵегге йпг $е = 0°,0001207.
Коеффиціентъ нѣсколько больше такъ какъ къ расширенію ре-
40
Термометрія.
зервуара присоединяется сжатіе самого ртутнаго столба. Приблизительно
можно принять
0,0000154.
Непосредственное опредѣленіе производится путемъ наблюденій
термометра при 100° въ вертикальномъ и горизонтальномъ положеніяхъ,
для чего и можетъ служить приборъ, изображенный на рис. 9 стр. 30.
Въ Шарлоттенбургѣ устроенъ спеціальный приборъ для опредѣленія
Для вышеупомянутаго термометра № VII было найдено = 0,0001621;
связь между @е и /?/ оказалась согласною съ тою, какая получается, если
принять во вниманіе сжатіе ртути.
§ 7. Поправка на выступающій наружу ртутный столбикъ. Не
всегда возможно погрузить весь термометръ въ ту среду, температуру Т
которой требуется измѣрить. Въ этомъ случаѣ температура ртутнаго
столбика, выступающаго наружу, уже не 7, а потому и его длина иная,
чѣмъ въ случаѣ, еслибы весь термометръ находился внутри данной среды.
Тогда необходимо ввести поправку, которая растетъ вмѣстѣ съ разностью
между температурою Т и температурою О' внѣшняго воздуха, и съ дли-
ною выступающаго столбика или съ числомъ п градусовъ, помѣщаю-
щихся на этомъ столбикѣ. Эта поправка б можетъ имѣть значительную
величину. Если обозначимъ коеффиціентъ кажущагося расширенія ртути
въ стеклѣ черезъ а, среднюю температуру выступающаго столбика че-
резъ т и, наконецъ, температуру, которую показываетъ термометръ, че-
резъ Л то очевидно искомое
Т = і 4- б = і + па (Т — г)..................(21)
Когда Т г большая величина, то въ послѣднемъ членѣ можно напи-
сать і вмѣсто Т, т.-р. положить
Т = і па (і — т)......................(21,а)
Формула (21) даетъ болѣе точное выраженіе
і пат
1 па
Къ сожалѣнію, нѣтъ способа точнаго опредѣленія средней температуры г
выступающаго столбика. Иногда помѣщаютъ рядомъ съ этимъ столби-
комъ другой термометръ такъ, чтобы его резервуаръ приходился рядомъ
съ срединою длины столбика и принимаютъ температуру, показываемую
этимъ термометромъ, за г. НоН2шапп полагаетъ, что, опредѣливъ та-
кимъ образомъ т, слѣдуетъ въ (21) или (21,а) принять для а уменьшенное
число « = 0,000135. АѴпеІІпег далъ болѣе точную формулу для о;
выводъ ея основанъ на законахъ статическаго распредѣленія температуры
въ цилиндрахъ (стержняхъ), нагрѣваемыхъ съ одного конца. Она имѣ-
етъ такой видъ
0.6755/7 | Р
I Я
Ртутные термометры.
И
гдѣ $ температура окружающаго воздуха. М число дѣленій шкалы на
единицѣ ея длины, р периметръ, у площадь поперечнаго сѣченія трубки
термометра. Сравнительно простой способъ слѣдующій: вмѣсто (21,а)
пользуются формулою
Т = і + 0,000156 (п — - &)............(22)
гдѣ /? число постоянное и опредѣляется эмпирически, сравнивая темпера-
туры Т и і термометра, сперва вполнѣ погруженнаго въ данную среду,
а затѣмъ имѣющаго выступающій столбикъ длиною въ п дѣленій его шкалы.
Остроумный способъ для введенія поправки о быль предложенъ
О и і 11 а и т е’омъ; мы не будемъ его разсматривать, но замѣтимъ, что
этотъ способъ весьма усовершенствовалъ МаЬІке. Другой способъ далъ
Асіагп (1907). Всѣ указанные способы не могутъ дать точныхъ значе-
ній для искомой поправки о, а потому слѣдуетъ при точныхъ измѣре-
ніяхъ избѣгать выступающаго столбика, замѣняя, въ крайнемъ случаѣ,
ртутный термометръ термоэлектрическою парою или пользуясь, гдѣ можно,
термометрами съ укороченною шкалою (см. § 9).
§ 8. Сравненіе ртутныхъ термометровъ между собою и съ нор-
мальнымъ водороднымъ. Чтобы перейти отъ показанія і даннаго термо-
метра къ показанію Т водороднаго термометра, необходимо къ і при-
бавить нѣкоторую поправку см. (6) стр. 16, гдѣ
П = Т — і........................(23)
Поправки /д переводящія показанія термометра по его идеаль-
ной шкалѣ къ нормальной водородной шкалѣ, зависятъ для ртут-
ныхъ термометровъ исключительно только отъ рода
стекла.
Многіе ученые занимались сравненіемъ шкалъ ртутныхъ термоме-
тровъ между собою и со шкалою воздушнаго или водороднаго термоме-
тровъ. Теоретически различіе между этими шкалами выясняется слѣдую-
щимъ образомъ. Пусть Ѵо объемъ при 0° резервуара и трубки до черты 0°;
ѵ0 объемъ одного дѣленія шкалы (идеальной) при 0°; а100 и ат средніе
коеффиціенты расширенія ртути межд) 0° и 100° и между 0° и Т°:
^юо и Рт тѣ же величины для стекла. Видимое расширеніе ртути при
нагрѣваніи отъ 0° до 100°, т.-е. объемъ ртути, поднимающейся выше
нуля, очевидно равенъ 100 І/о (а100 — /?100). Онъ заполняетъ 100 дѣленій
шкалы, изъ которыхъ каждое имѣетъ емкость ѵ0 (1 + 1ОО/?1оо). Отсюда
получается равенство
Ц) каіоо Лоо).= М1 + 1СЮ/?100).
Когда термометръ нагрѣтъ до истинныхъ Г°, то выше нуля поднимается
объемъ ртути Ѵ()Т (ат - 9^), заполняющій і дѣленій шкалы, изъ кото-
рыхъ каждое обладаетъ емкостью Ѵо (1 Отсюда слѣдуетъ, что
(а7 — /?г) = С1 Н”
Раздѣливъ это равенство на предыдущее, получаемъ
42
Термометрія.
т _ аюо — Аоо 1 + Т^т
ат — Рт 1 + 1ОО/?іоо
(24)
Послѣдній множитель весьма мало отличается отъ единицы, такъ что
всегда можно положить
-г _ і а100__ЛоО
— ат — рт
. • (25)
Законы расширенія ртути и стекла различны, а потому множитель при і
не равенъ единицѣ и слѣд. і не равно Т.
Средніе коеффиціенты расширенія могутъ быть представлены въ
видѣ эмпирическихъ выраженіи
аТ = “о + «іТ+ «-зТ2,
Ѵт = Л + № +
Вставляя эти выраженія и соотвѣтствующіяп ри Г = 100° въ (25). получаемъ
у-___________л («о I 4~ 1СЮ — л?і) —|- ЮО2 (а2 — Ръ)
. (%-&) + Т(сЧ-^)+ ’
Произведемъ дѣленіе, принимая во вниманіе, что и р± малы сравни-
тельно съ а0 и Ро; получаемъ
Т = Яі + ООО - Г) -А + Ц002 - гъ —А
«0 --------------------- р0 «0 р0
Въ скобкахъ можно положить і вмѣсто
Т и тогда для искомой поправки
у получается
9/ = Т — і = I (іоо — і) —— ~-
а0 - Ро
Для ртути можно положить
1 + (юо + о“2" о2
«1 — Р1
• (26)
аѵ = 18116 . 10~аг = 115
ІО-10: а2 = 212 . 10 ~ 13-
Для стекла 81. СгоЬаіп
Р$ = 2142 . 10 “ 8 ; & = 237 . 10 ~ 10 ; Л -- 0.
Отсюда ясно, что для і между 0° и 100° поправка ^<0, т.-е. і>Т\ всѣ
дѣленія идеальной шкалы термометра расположены выше нормальной
шкалы. При і 100° поправка дѣлается положительною, т.-е. показанія
ртутнаго термометра слишкомъ низки.
Для сравненія ртутныхъ термометровъ между собою служатъ нынѣ
особые приборы, компараторы, которые могутъ быть горизонтальные и
вертикальные. Горизонтальный компараторъ, служившій Сііарриіз
для сравненія ртутныхъ термометровъ съ водороднымъ и другими газо-
выми термометрами, былъ описанъ на стр. 23. Онъ можетъ служить и для
сравненія ртутныхъ термометровъ межд^ собою. Постоянство темпера-
туры воды, протекающей черезъ компараторъ, поддерживается особыми
приборами, называемыми т е р м о с т а т а м и. Въ Шарлоттенбургѣ нахо-
Ртутные термометры.
43
дятся два компаратора, одинъ вертикальный, другой горизонтальный.
Ихъ описали Тйіевеп, Всііееі и 8еіі въ концѣ 1895 г.
В е § п а и И сравнивалъ между собою показанія воздушнаго и раз-
личныхъ ртутныхъ термометровъ при температурахъ выше 100°.
18і(1 о г Ріегге первый показалъ (1842), что между 0° и 100°
различные ртутные термометры даютъ неодинаковыя показанія. Позже
Вескпа^еі сравнивалъ ртутный (изъ тюрингенскаго стекла) и воз-
душный термометры между 0° и 100° и нашелъ, что между 40° и 50°
ртутный термометръ показываетъ выше на 0,2°. Методическія сравне-
нія ртутныхъ и газоваго термометровъ, при точномъ о п р е дѣлені и
химическаго состава стекла первыхъ изъ нихъ, произве-
дены АѴіеЬе и ВоеНсйе г’омъ, М а г е с к’омъ, О и і 11 а и т е’омъ,
ГйарриІ8 и* въ самое послѣднее время совмѣстно Т И і е 8 е іГомъ,
8 с 11 ее Гемъ и 8е11. АѴіеЬе далъ таблицу для сравненія хода тер-
мометровъ изъ іенскаго стекла, твердаго французскаго стекла и англій-
скаго хрусталя; ХѴіеЬе и ВоеіісЬег, а также Магеск сравни-
вали ртутный термометръ изъ іенскаго стекла съ воздушнымъ. О и і 1 -
Іаише составилъ таблицу, дающую разности показаній термометровъ
изъ твердаго хрусталя и изъ твердаго французскаго стекла (ѵегге диг).
СйарриІ8 сдѣлалъ важнѣйшій шагъ: по способу, описанному на
стр. 23, онъ сравнилъ показанія ртутнаго термометра изъ ѵегге (Іиг съ
показаніями водороднаго термометра и тѣмъ самымъ свелъ шкалу ртут-
наго термометра къ нормальной шкалѣ, которая, какъ было сказано, не-
замѣтно отличается отъ абсолютной томсоновской шкалы (стр. 7). На-
конецъ, ТЬіевеп, 8сйее1 и 8е11 сравнили (въ ПІарлоттенбургѣ)
между собою термометры изъ іенскихъ стеколъ 1бІИ и 59ш (боросиликатъ)
и изъ французскаго ѵегге (іиг. Огиеігтасйег (1895) и въ особен-
ности Ьегоке (1899) непосредственно сравнили показанія ртутнаго тер-
мометра изъ стекла 59ш съ показаніями газоваго термометра. Ь е ш к е
находитъ между 100° и 200° поправки, которыя при 200° доходятъ до 0°,67.
Такимъ образомъ, въ настоящее время можно пере-
вести къ нормальной температурной шкалѣ показанія
термометровъ изъ четырехъ сортовъ стекла: изъ твердаго французскаго
хрусталя, изъ твердаго стекла ѵегге (іиг и изъ іенскихъ стеколъ 16П1 и 59ІП.
Приводимъ наибольшія разности между показаніями этихъ термо-
метровъ.
при
(Фр. тв. хруст.) — (Ѵегге (Іиг) =^= 0°,031 50°
(Ѵегге (Іиг) — (77) о0,233 25°
+ 0°,107 40°
(Ѵегге (іиг) - (№ 16ІП). . . = — 0°,0129 50°
(Ѵегге <іиг) — (№ 59ІП). . . = + О°,О769 50°
(№ 16ш) — (№ 59,п) . . . . = Д- 0°,0899 50°
Приводимъ еще графическое изображеніе результатовъ сравненія
трехъ ртутныхъ и двухъ газовыхъ и СО2) термометровъ съ нормаль-
44
Термометрія.
нымъ водороднымъ, произведеннаго С11 а р р и і 8. На рис. 14 ось абс-
циссъ представляетъ шкалу водороднаго термометра; ординаты даютъ
отступленія шкалъ пяти другихъ термометровъ. Каждое дѣленіе на
абсциссѣ равно 10°, а на ординатѣ 0,05°:
Рис. 14.
Весьма тщательно сравненіе термометровъ изъ ѵегге (Іиг и приве-
деніе ихъ шкалы къ водородной произвели АѴаісІпег и Шскіпзоп
(1907); точность, достигнутая ими, не допускаетъ ошибки, превышаю-
щей 0,002°.
§ 9. Термометры ДЛЯ спеціальныхъ цѣлей. Разсмотримъ устрой-
ство нѣкоторыхъ сортовъ термометровъ съ жидкостями, отличающихся
отъ обыкновеннаго ртутнаго термометра, разсмотрѣннаго выше.
I. Термометры съ укороченною шкалою. Сокращеніе
длины термометра представляется всегда желательнымъ; оно умень-
шаетъ ломкость самого прибора и. главное, длину выступающаго стол-
бика при многихъ измѣреніяхъ. Когда термометръ долженъ быть чувстви-
теленъ, т.-е. имѣть длинные градусы, и въ то же время служить для
опредѣленія высокихъ температуръ (напр. до 300°), то онъ получилъ
бы огромную длину (до метра), еслибы на его шкалѣ были нанесены
всѣ дѣленія, начиная отъ 0°. Укорачиваютъ также термометры, съ
которыми постоянно приходится измѣрять температуры, колеблющіяся
въ не широкихъ предѣлахъ. Полагаемъ, что основныя двѣ
точки (0° и 100°) должны находиться на шкалѣ термо;
метра; мы слѣд. не относимъ сюда термометровъ, въ которыхъ, какъ
напр. въ комнатныхъ, помѣщена только часть шкалы, нанесенная пу-
темъ простого сравненія даннаго термометра съ хорошимъ готовымъ
термометромъ.
1. Термометръ, служащій для гипсометрическихъ цѣлей, т.-е.
для опредѣленія температуры кипѣнія воды на возвышенныхъ точкахъ,
изображенъ на рис. 15. На его шкалѣ помѣщается точка 0°; затѣмъ
Ртутные термометры.
45
слѣдуетъ вздутіе /?, которое наполняется ртутью при повышеніи темпе-
ратуры, хотя бы до 80°, и наконецъ идетъ продолженіе шкалы до 105°.
Термометръ для калориметрическихъ цѣлей (при спо-
служитъ для измѣренія температуръ между 15° и 25°.
нанесены дѣленія около 0°; далѣе идетъ вздутіе, по-
15°—25°, второе вздутіе и наконецъ дѣленія примѣрно
2.
собѣ смѣшенія)
11а его шкалѣ
томъ шкала отъ
отъ 95°—105°.
3. Для измѣренія высокихъ температуръ служатъ термо-
метры, на которыхъ помѣщены: дѣленія около 0°, вздутіе,
около 100° и далѣе еще одно или нѣсколько вздутій,
смотря по тому, въ какихъ предѣлахъ находятся из-
мѣряемыя температуры. Для опредѣленія основныхъ
точекъ выше 100° могутъ служить температуры ки-
пѣнія нафталина (С10778) и бензофенола
(С6/75)2СО (дифенилкетона). С г а 118 опредѣлилъ
эти точки для различныхъ атмосферныхъ давленій;
при нормальномъ давленіи въ 760 мм. первое вещество
кипитъ при 218°, второе - при 306°.
4. Термометръ АѴаІТегсі іп’а. Въ 1840 г.
былъ построенъ АѴ а 1 і е г (1 і п’омъ гермометръ, ко-
торый онъ назвалъ метастатическимъ, изображен-
ный на рис. 16. Въ немъ вся шкала вмѣщаетъ не
болѣе 3 или 4 градусовъ, столь длинныхъ, что можно
производить отсчеты до 0,001°. Абсолютное значеніе
этихъ градусовъ можетъ быть измѣнено по желанію,
смотря по тому, около какой температуры прихо-
дится производить измѣреніе; достигается это пе-
реводомъ излишняго количества ртути въ верхній
резервуаръ ВО, Трубка оканчивается наверху от-
тянутою и согнутою частью С. Если желаютъ на-
блюдать высокія температуры, то нагрѣваютъ А нѣ-
сколько выше этихъ температуръ, причемъ ртуть
изъ конца С выливается въ резервуаръ ВО. Чтобы
къ болѣе низкимъ температурамъ, слѣдуетъ перевернуть
Рис. 15.
105
100
95Г
90
?5
н
А
дѣленія
Рис. 16.
О
В
А
термо-
переити
метръ, причемъ конецъ С будетъ погруженъ въ ртуть, находящуюся въ ВО,
и затѣмъ охлаждать резервуаръ А. Длина градуса, очевидно, должна мѣ-
няться въ зависимости отъ количества ртути, участвующей въ расшире-
ніи, а слѣд. она должна мѣняться въ зависимости отъ того, какую
мы температуру наблюдаемъ и сколько слѣд. ртути находится въ ВО.
Возникающее отсюда значительное затрудненіе мѣшало этому термометру
получить болѣе широкое распространеніе. Однако недавно бсЬеигег-
К е 81 п е г показалъ, какимъ образомъ можно ввести необходимую по-
правку, послѣ чего термометръ \ѴаИег(1іп’а можетъ оказаться весьма
удобнымъ и полезнымъ инструментомъ. Усовершенствованіемъ этого тер-
мометра занимались Ретпеі и въ особенности Вескшапп, Верхняя
46
Термометрія.
часть термометра Вескпіапп’а изображена на рис. 17. Подвергая тер-
мометръ легкимъ сотрясеніямъ, можно заставить падать капли ртути изъ
верхней части резервуара въ нижнюю. Впослѣдствіи (1905) Вескшапп
еще измѣнилъ и усовершенствовалъ свой термометръ.
II. Термометры съ алкоголемъ и другими жидко-
стями и термометры съ не стеклянными резервуа-
рами. Преимущество алкоголя передъ ртутью заключается только въ
томъ, что онъ при весьма низкихъ температурахъ, при ко-
Рис. 17. торыхъ ртуть затвердѣваетъ, остается жидкимъ. Недостатки
алкогольнаго термометра состоять, во-первыхъ, въ смачива-
ніи стѣнокъ трубки (стр. 26), и, во-вторыхъ, въ невозмож-
ности опредѣлить верхнюю основную точку, такъ какъ алко-
голь кипитъ при 79°. Послѣдній недостатокъ устраняется,
если вмѣсто алкоголя взять толуолъ, жидкость, коеффиціентъ
расширенія которой мало мѣняется съ температурой; онъ
можетъ быть добытъ въ весьма чистомъ видѣ, кипитъ при 111°
и не затвердѣваетъ даже при - - 80°. Толуолъ былъ впервые
предложенъ Л у г и н и и ы м ъ.
Сііарриіз нашелъ, что различные толуоловые тер-
мометры даютъ вполнѣ согласные между собою результаты
(нѣсколько сотыхъ градуса до — 70°). Онъ сравнилъ также
алкогольные и толуоловые термометры съ термометромъ во-
дороднымъ. Отступленія оказались весьма значительными,
но, какъ сказано, для толуола они вполнѣ постоянны.
Л о 11 у и XV Іі і I е также сравнивали алкогольный термометръ съ
термометромъ воздушнымъ. КоМгаизсЬ указалъ на нефтяной эфиръ
(Реігоіаеіііег), какъ на жидкость, пригодную Для термометровъ. Онъ
при — 188° еще не затвердѣваетъ; при — 188° его объемъ равенъ лишь
4 б объема при 0° и 3/4 объема при ф- 30°. НоІЬогп и Ваийаіп (1901)
занимались приготовленіемъ такихъ термометровъ. В а и (1 а і п пользо-
вался при этомъ жидкостью, которая при 15° обладаетъ плотностью 0,647.
Рис. 18.
Она оставалась вполнѣ прозрачною до тем-
пературы жидкаго воздуха (около — 190°).
Ваіу и Сіюгіеу, а затѣмъ ХѴіеЬе
предложили замѣнить ртуть сплавомъ
изъ К и 2Ѵа для измѣренія высокихъ тем-
пературъ (до 550°).
М а г с Ь і 8 устроилъ ртутный термо-
метръ съ платиновымъ резервуа-
ромъ, въ которымъ основныя точки оказались дѣйствительно постоян-
ными и не было замѣтно «приниженія > нуля при нагрѣваніи до 100°.
III. Максимумъ и минимумъ термометры. Устройство
максимумъ-минимумъ термометра ВиіііегІогсГа показано на рис. 18.
Максимумъ температуры, бывшій втеченіе заданнаго времени, отсчи-
тывается на ртутномъ термометрѣ АВ, въ которомъ стальной штифтикъ 5
Вѣсовой термометръ.
47
толкаетея къ В ртутнымъ столбомъ при его удлиненіи и остается на
мѣстѣ, когда ртуть идетъ назадъ. Минимумъ опредѣляется на алкоголь-
номъ термометрѣ СО, въ которомъ стеклянное тѣльце р, передвигается къ О,
когда конецъ жидкаго столба при охлажденіи дой-
детъ до его лѣваго конца. При повышеніи тем-
пературы алкоголь проходитъ мимо которое
остается на мѣстѣ.
Медицинскій термометръ, служащій для из-
мѣренія температуры тѣла человѣка, содержитъ
пузырекъ воздуха между короткимъ ртутнымъ
столбикомъ и остальною массою ртути. При на-
грѣваніи термометра этотъ столбикъ передвигается;
при охлажденіи онъ затѣмъ остается на мѣстѣ.
Весьма распространенъ нынѣ, особенно въ
Германіи, термометръ, который изображенъ на
рис. 19. Резервуаръ АР и часть трубки РН на-
полнена алкоголемъ (или креозотомъ) ; далѣе идетъ
ртутный столбъ ВНС и наконецъ опять алкоголь,
отчасти наполняющій резервуаръ О. Стеклянныя
тонкія трубочки, содержащія по кусочку желѣз-
ной проволоки, передвигаются концами В и С
ртутныхт> столбовъ, оставаясь на мѣстѣ, когда В
или С отъ нихъ удаляются. При помощи маг-
нита можно передвинуть оба указателя до кон-
цовъ В и С ртутнаго столба, когда начинается
новый періодъ времени, для котораго требуется
опредѣлить максимальную и минимальную температуры.
§ 10. Вѣсовой термометръ. Способъ примѣненія вѣсового термо-
метра тѣсно связанъ со способомъ опредѣленія коеффипіентовъ расши-
Рис. 20.
ливаютъ
ренія жидкостей, а также стекла, что будетъ нами раз-
смотрѣно въ слѣдующей главѣ. Вѣсовой термометръ (рис. 20)
состоитъ изъ стекляннаго резервуара гп, снабженнаго вытяну-
тою и согнутою трубочкою, подъ
отверстіемъ о которой помѣща-
ется чашечка с. Для удобства по-
мѣщаютъ резервуаръ въ металли-
ческій мѣшочекъ(сѣтку),прикрѣп-
ленный къ кольцу (рис. 21), кото-
рое вмѣстѣ съ другимъ кольцомъ,
поддерживающимъ чашечку О,
составляетъ одно цѣлое съ ру-
кояткою С.
Рис. 21.
Сперва опредѣляютъ вѣсъ р всего прибора (съ чашечкой,
сѣткой и рукояткой), не содержащаго вовсе ртути. Затѣмъ на-
ртуть въ О и путемъ послѣдовательнаго нагрѣванія и охлажде-
48
Термометрія.
нія резервуара А вполнѣ наполняютъ его и всю трубку ртутью, вы-
тѣснивъ весь воздухъ. Далѣе окружаютъ приборъ тающимъ льдомъ,
оставляя кончикъ трубки въ ртути, находящейся въ 29. Минутъ черезъ
двадцать выливаютъ ртуть изъ чашечки 29, которую помѣщаютъ на ея
мѣсто и затѣмъ взвѣшиваютъ весь приборъ, не обращая вниманія на то,
что при комнатной температурѣ часть ртути перельется въ чашечку 29.
Вычтя изъ вѣса прибора вѣсъ р пустого, получаемъ вѣсъ Ро ртути, за-
полняющей термометръ до отверстія трубки при 0°. Величины 7% и р
можно считать разъ навсегда извѣстными для даннаго термометра.
Чтобы измѣрить температуру і какого-либо пространства, наполня-
ютъ приборъ ртутью при 0°, такъ что вѣсъ ртути Ро, и затѣмъ помѣща-
ютъ его въ данное пространство. Полагаемъ, что і > 0°; тогда часть
ртути, наполнявшей сосудъ при 0°, выльется въ чашечку 29. Эту ртуть
выливаютъ и опредѣляютъ вѣсъ всего прибора. Вычтя изъ этого вѣса
вѣсъ пустого прибора, получаемъ вѣсъ Р^ ртути, наполняющей резерву-
аръ и трубку при 2°.
Допустимъ, что средніе коеффиціенты расширенія ртути и стекла
между 0° и 2° извѣстны, какъ функціи температуры 2. Найдемъ связь
между величинами р, Ро, Рь и 2. Пусть д0 плотность ртути при 0°.
Объемъ І/о резервуара и трубки былъ при 0° заполненъ ртутью,
вѣсъ которой равнялся Ро. Отсюда слѣдуетъ, что
При 2° этотъ объемъ сдѣлался равнымъ
Этотъ объемъ былъ заполненъ Р; вѣсовыми единицами ртути, нахо-
дившейся при температурѣ 2. Объемъ этой ртути при 0° равенъ Р;: д0,
а при 2° онъ равенъ
Р(
А (1 + «/).
°0
Приравнивая это выраженіе объему V; и сокративъ на д0, получа-
емъ искомую связь
РЛ1'+2^) = Ро (1 + 2^).................(27)
Эта формула даетъ
Мы предположили, что и извѣстны, какъ функціи температуры 2;
взявъ для и значенія, соотвѣтствующія приблизительно извѣстному 2,
вычислимъ 2 по формулѣ (28) и затѣмъ вычислимъ его вновь точнѣе,
подставивъ для и значенія, соотвѣтствующія найденному 2. Такое
вычисленіе можно повторить и въ третій разъ.
Термоскопы.
49
Наша формула значительно упростится, если ввести средній коеф-
фиціентъ уі кажущагося расширенія ртути. Единица объема ртути
при 0° заняла при /° дѣйствительный объемъ 1 а/, который, вслѣд-
ствіе расширенія оболочки, какъ будто уменьшился въ 1 -ф- ^і разъ, при-
чемъ онъ далъ кажущійся объемъ 1 + у^і. Итакъ
1 4" і
• (29)
При весьма малыхъ расширеніяхъ отсюда и получается у* =
см. (11) стр. 25. Вмѣсто (27) имѣемъ теперь
(30)
откуда
Приблизительно
1
С , и тогда
_ р0 - Рі
ТІРІ
(31)
можно принять у; за величину постоянную, равную
р ___р
.......................(32)
Коеффиціентъ С можетъ быть опредѣленъ разъ навсегда наблюде-
ніемъ при 100°: если Р100 вѣсъ ртути, остающейся въ приборѣ при 100°,
то имѣемъ изъ (32), положивъ і = 100,
С=100
'о Рюо
С и Ро въ (32) суть величины постоянныя для даннаго прибора, а
потому мы найдемъ искомую температуру опредѣляя только вѣсъ
ртути, наполняющей приборъ при і° и вычисляя і по формулѣ (32).
§ 11. Другіе способы измѣренія не очень высокихъ температуръ.
Термоскопы. Разсмотримъ еще нѣкоторые способы, примѣнявшіеся
также для измѣренія не очень высокихъ температуръ, оставляя пока во-
просъ о приборахъ, служащихъ для измѣренія весьма высокихъ темпера-
туръ ; строгаго разграниченія провести, конечно, нельзя.
I. Термоэлектрическій способъ. Въ т. 11 мы уже имѣли
случай познакомиться съ понятіемъ о термоэлектричествѣ. Если спаять
двѣ проволоки изъ металловъ Л4 и 7Ѵ и концы ихъ присоединить къ про-
водамъ, идущимъ къ чувствительному гальванометру, то въ замкнутой
такимъ образомъ цѣпи появляется токъ, если температура і спая метал-
ловъ /И и не равна температурѣ /0 тѣхъ мѣстъ, гдѣ эти металлы при-
соединены къ проводамъ, почти всегда мѣднымъ. Электродвижущая
сила Е, а слѣд. и пропорціональная ей, при неизмѣнномъ общемъ сопро-
тивленіи цѣпи, сила тока I могутъ быть выражены въ видѣ опредѣлен-
ной квадратичной функціи температуръ і и /0. Въ этомъ заключается
законъ Авенаріуса (въ Кіевѣ), неправильно иногда приписываемый
Т а і і’у. Видъ этой функціи слѣдующій :
Е = а (і — і0) + Ь (Р — V)..............(33)
КУРСЪ ФИЗИКИ О. X В О Л ь С О Н А. Т. III, изд. 3-е.
4
50
Термометрія.
Если предположить, что мѣста, гдѣ металлы М и М присоединены
къ проводамъ, находятся въ тающемъ льдѣ, то и мы получаемъ
фориулу + ....................(34)
которая, дѣйствительно, для многихъ термоэлектрическихъ «паръ» съ до-
статочною точностью выражаетъ законъ термо электродвижущихъ силъ.
Коеффиціенты а и Ь должны быть эмпирически найдены сравненіемъ
показаній гальванометра, служащихъ мѣрою величинъ Д съ показаніями
иного, уже изслѣдованнаго измѣрителя температуръ, напр. ртутнаго или
газоваго термометра. Для измѣренія температуры какой-либо среды по-
мѣщаютъ въ ней спай металловъ Ж и окружаютъ мѣста ихъ соеди-
ненія съ проводами, идущими къ гальванометру, тающимъ льдомъ, и по
формулѣ (34) опредѣляютъ температуру і. Считаемъ излишнимъ входить
здѣсь въ какія-либо подробности, тѣмъ болѣе, что въ настоящее время
разсматриваемый способъ получилъ большое примѣненіе при измѣреніи
высокихъ температуръ, о чемъ будетъ сказано ниже. Для обычныхъ и
не слишкомъ высокихъ температуръ, между 0° и 200° Раішег (1905)
изучилъ термоэлементъ, состоящій изъ мягкаго желѣза и новаго сплава
«Айѵапсе» (55% Си, 44,4% А7, 0,6% Ре). Онъ нашелъ, что съ помощью
этого термоэлемента можно опредѣлять отсчитываемыя отъ о0 темпера-
туры съ относительной точностью въ 0,04%.
II. Электрическое сопротивленіе г данной проволоки
есть функція температуры, которую можно предварительно изучить, со-
ставивъ для нея эмпирическую формулу или таблицы, или, наконецъ,
изобразивъ ее графически. Если такую проволоку, свернутую въ видѣ
катушки, чтобы она занимала меньше мѣста, помѣстить въ то простран-
ство, температуру і котораго надо опредѣлить и измѣрить ея сопротивле-
ніе г, то этимъ опредѣлится и искомое і. Къ этому способу мы также
еще возвратимся въ статьѣ о пирометрахъ. На аналогичномъ принципѣ
основано устройство болометра, описаннаго нами раньше (т. II).
Зависимостью электрическаго сопротивленія отъ температуры часто
пытались воспользоваться для построенія телетермометра, который
позволялъ-бы измѣрять температуру удаленныхъ точекъ, напримѣръ, на
глубинѣ моря. Такіе аппараты были построены Зіешепз’омъ. Вгаип’омъ,
Риііщ’емъ, Кписізеп’омъ и др.
III. Мезііп (1902) предложилъ измѣрять температуру по вели-
чинѣ электродвижущей силы элемента Ьаіітег Сіагк’а (т. IV. нор-
мальные элементы), помѣщеннаго въ изслѣдуемое пространство.
IV. Вегійеіоі предложилъ интересный способъ опредѣленія тем-
пературы газа по его коеффиціенту преломленія п\ преиму-
щество эгого способа заключается въ томъ, что вліяніе температуры на
оболочку никакой роли не играетъ. Мы видѣли (т. II), что для даннаго
п — 1 д ,
газа , гдѣ а плотность газа, не зависитъ отъ того, будетъ ли а
(1
мѣняться вслѣдствіе измѣненія давленія или вслѣдствіе измѣненія темпе-
Термоскопы..
51
ратуры. Лучъ свѣта разлагается при помощи толстой пластинки 3 а -
тіп’а (т. II) на два луча, проходящіе черезъ двѣ параллельныя трубки,
закрытыя стеклянными пластинками, и наполненныя однимъ и тѣмъ же
газомъ. Пройдя трубки, лучи интерферируютъ (опускаемъ подробности),
давая рядъ полосъ. Отмѣчаютъ положеніе центральной полосы, когда
газь въ обѣихъ трубкахъ находится при одинаковомъ давленіи и темпе-
ратурѣ. Затѣмъ средняя часть одной изъ трубокъ помѣщается въ ту
среду, температуру которой требуется измѣрить, напр. окружается осо-
бымъ сосудомъ, содержащимъ пары какой-либо кипящей жидкости : концы
трубки охлаждаются водою. Интерференціонныя линіи перемѣщаются, а
выкачивая газъ изъ другой трубки, можно ихъ привести въ прежнее по-
ложеніе. Тогда плотность газа въ этой второй трубкѣ равна средней
плотности газа въ первой. Вегіііеіоі даетъ формулы для вычисленія
отсюда температуры Т средины первой трубки, когда еще извѣстна тем-
пература і ея концовъ. Опыты надъ парами алкоголя, воды и ани-
лина дали хорошіе результаты, причемъ измѣряемыя Т были около 78°,
100° и 184°.
V. Термоскопы, основанные на наблюденіи плавле-
нія различныхъ легкоплавкихъ смѣсей и сплавовъ.
Соіетап приготовилъ серію смѣсей воды съ глицериномъ, замерзаю-
щихъ при опредѣленныхъ температурахъ между — 37° и 0°, и рядъ
сплавовъ парафина съ другими веществами, плавящихся между ф 5° и
-ф- 38°. По номеру смѣси, еще не замерзающей, ели сплава, дѣлающагося
жидкимъ, можно приблизительно судить о температуръ.
VI. Рядъ приборовъ основанъ на расширеніи твердыхъ тѣлъ и
притомъ главнымъ образомъ на неодинаковости расширенія
различныхъ твердыхъ тѣлъ. Если наложить другъ на друга
двѣ полоски или ленты изъ различныхъ металловъ и спаять или скле-
пать ихъ во всю длину, чтобы получилась одна полоска, прямая или
согнутая, то форма этой полоски будетъ мѣняться съ измѣненіемъ темпе-
ратуры, вслѣдствіе того, что длина двухъ ея составныхъ частей, вообще
говоря, будетъ измѣняться неодинаково. Полоска при нагрѣваніи изгиба-
ется въ ту сторону, гдѣ находится металлъ, который менѣе расширяется,
а при охлажденіи въ сторону того металла, который болѣе сжимается,
т.-е. въ сторонуг противоположную. На рис. 22 изображена такая сложная
полоска, прямая при нѣкоторой температурѣ. Полагая, что свѣтлая по-
лоса обозначаетъ металлъ съ большимъ коеффиціеитомъ расширенія, мы
увидимъ, что при нагрѣваніи полоска А А приметъ форму ВВ, а при
охлажденіи форму СС. Вмѣсто двухъ металлическихъ полосокъ можно
также взять одну изъ эбонита, другую изъ слоновой кости.
На рис. 23 представленъ такъ называемый металлическій термометръ
В г е §• и еі. Три тонкія полоски изъ серебра, золота и платины спаяны во всю
длину, такъ что золото приходится между болѣе расширяющимся серебромъ
и менѣе расширяющеюся платиной. Всей полоскѣ, которая при нагрѣваніи
закручивается въ сторону платины, придана форма винтовой линіи, которая
4*
52
Термометрія.
подъ стекляннымъ колоколомъ прикрѣплена однимъ концомъ къ точкѣ А.
Къ другому концу придѣлана горизонтальная стрѣлка, остріе которой при
измѣненіяхъ температуры перемѣ-
щается вдоль круговой шкалы МѴ,
на которой нанесены дѣленія по
Рис. 23.
Рис. 22.
сравненію съ показаніями другого,
напр. ртутнаго термометра.
Существуетъ множество раз-
личныхъ термометровъ и термо-
графовъ, основанныхъ на томъ же
принципѣ. Термографами пользу-
ются на метеорологическихъ станціяхъ для болѣе или менѣе непрерыв-
наго записыванія температуры воздуха.
§ 12. Пирометры. Измѣреніе высокихъ температуръ. Приборы,
служащіе для измѣренія высокихъ температуръ (напр. выше 300°), назы-
ваются пирометрами, а соотвѣтствующій отдѣлъ экспериментальной
физики — пирометріей. Вопросу о точномъ измѣреніи высокихъ темпе-
ратуръ посвящается теперь много работъ; это вопросъ, стоящій на оче-
реди, послѣ того какъ обыкновенная термометрія, измѣряющая темпера-
туры между 0° и 100° и недалеко отъ этихъ предѣловъ, сдѣлала, благо-
даря работамъ Сгпіііаите’а, СЛіарриів, ТЬіеяеп’а, РегпеСа,
НоІЬогп и О ау и др., тѣ успѣхи, о которыхъ выше было сказано, и
которые даютъ возможность измѣрять указанныя температуры съ точ-
ностью до немногихъ тысячныхъ долей градуса.
•Въ различное время было предложено весьма большое число пиро-
метрическихъ способовъ, изъ которыхъ однако лишь немногіе могутъ
дать сколько-нибудь надежные результаты. Въ этомъ параграфѣ мы да-
димъ бѣглый обзоръ всѣхъ этихъ способовъ, кромѣ термоэлектрическаго
и Оптическаго, которые будутъ разсмотрѣны отдѣльно.
I. Ртутный термометръ. Ртуть кипитъ при 357°, а потому,
казалось бы, ртутный термометръ не можетъ служить для измѣренія тем-
пературъ, лежащихъ выше 357°. Однако Регзоп нашелъ, что ки-
питъ только при 450°, когда она находится подъ давленіемъ въ 4 атмосф.
и при 500°, когда давленіе равно 30 атмосф. На основаніи этого факта,
были устроены термометры, въ которыхъ въ трубкѣ надъ ртутью оста-
вленъ газъ, не дѣйствующій на ртуть, напр. 7Ѵ, сжимающійся, когда ртут-
ный столбикъ поднимается; онъ производитъ давленіе на и не даетъ ей
закипать. Приготовляя термометры изъ тугоплавкаго стекла, можно имѣть
приборы, дающіе весьма точные результаты и въ то же время вполнѣ за-
Пирометры.
53
атмосферъ; на немъ можно измѣ-
Рис. 24.
измѣренія высокихъ температуръ,
служивающіе названія пирометровъ. Въ Шарлоттенбургѣ (ЕеісПвапвіаІѢ)
устроенъ особый приборъ для сравненія такихъ термометровъ; жидкостью
служитъ расплавленная смѣсь двухъ селитръ и (точка
плавленія около 230°), которая только при 600° начинаетъ замѣтно испа-
ряться. Изслѣдованія М а 111 к е показали, что если пользоваться его ви-
доизмѣненіемъ способа Сгиіііаите’а для поправки на температуру
выступающаго столбика (стр. 40), то можно производить измѣренія при
помощи ртутныхъ термометровъ до температуры 500° и даже выше съ
точностью до 0,1°.
М і е Іі 18 въ Америкѣ устроилъ ртутный термометръ, содержащій
углекислый газъ при давленіи въ 20
рять температуры до 550°; этотъ тер-
мометръ былъ изслѣдованъ въ Ееісіія-
апзіаіі въ Шарлоттенбургѣ.
Бпіоиг (1900) построилъ тер-
мометръ, оболочка котораго была сдѣ-
лана изъ кварца, и который былъ
наполненъ оловомъ. Онъ можетъ
служить для измѣренія температуръ
до 900°.
II. Газовый пирометръ.
Р о и і 11 е I первый воспользовался
газовымъ термометромъ (стр. 18) для
опредѣленія весьма высокихъ темпе-
ратуръ, замѣнивъ сравнительно легко-
плавкое стекло, изъ котораго обык-
новенно дѣлается резервуаръ, плати-
ною. Далѣе Ее^паиН пользо-
вался воздушнымъ термометромъ для
введя въ него нѣкоторыя измѣненія. Резервуаръ А (рис. 24) съ труб-
кою аг могъ быть отдѣленъ отъ манометра ссіе/; на концѣ трубки нахо-
дился кранъ г. Ее^паиН поступалъ слѣдующимъ образомъ: резерву-
аръ А и трубка аг наполнялись сухимъ газомъ; затѣмъ резервуаръ по-
мѣщался въ среду, температура которой требовалось опредѣлить, причемъ
кранъ г на концѣ трубки оставался открытымъ, такъ что расширяющійся
газъ могъ свободно выходить изъ резервуара. Черезъ нѣкоторое время
кранъ закрывался, резервуаръ съ трубкой вынимались изъ упомянутой
среды, окружались тающимъ льдомъ и присоединялись къ манометру.
Способъ соединенія при помощи муфточки съ винтами понятенъ изъ
рисунковъ {а) и (6). Наконецъ кранъ открывался и ртуть въ колѣнѣ, съ
которымъ соединенъ резервуаръ, вновь доводилась до той верхней черты,
до которой она доходила ранѣе присоединенія резервуара. Въ другомъ
колѣнѣ она тогда стояла ниже. Не входимъ въ дальнѣйшія подробности
и въ указаніе формулы, аналогичной (10) стр. 20.
Ні.СІаіг-ВеѵіПе и Т г о о 81 показали въ цѣломъ рядѣ ра-
54
Термометрія.
ботъ, что платина при высокихъ температурахъ пропускаетъ черезъ себя
газы и слѣд. какъ матеріалъ для резервуара газоваго пирометра не го-
дится. Съ тѣхъ поръ стали употреблять резервуары изъ фарфора.
Веѵіііе и Т г о о 81 занимались усовершенствованіемъ пирометра съ
фарфоровымъ резервуаромъ и, между прочимъ весьма тщательно изучили
свойства фарфора изъ Вауепх и опредѣлили его коеффиціентъ расшире-
нія, который между 1000° и 1400° оказался равнымъ 0,000016 или 0,000017;
около 1500° онъ возрастаетъ до 0,00002. Резервуаръ обыкновенно упо-
треблялся шаровидный.
Значительно подвинутъ былъ вопросъ новѣйшими работами Ноі-
Ъ о г п’а и \Ѵ і е п’а. Они, во-цервыхъ, употребляли фарфоровый сосудъ
продолговатый, приспособленный для введенія въ него термоэлектриче-
скаго элемента, о чемъ будетъ сказано въ § 14; во-вторыхъ, они обра-
тили вниманіе на важное значеніе глазури, покрывающей резервуаръ
снаружи (глазурь на внутренней поверхности оказалась неудобною, такъ
какъ она даетъ пары) и, наконецъ, они наполняли резервуаръ настолько
разрѣженнымъ газомъ, что даже при высшихъ достигнутыхъ ими темпе-
ратурахъ (1400°) давленіе этого газа оставалось меньшимъ давленія ат-
мосферы. Вслѣдствіе этого расплавленная глазурь вгонялась внѣшнимъ
давленіемъ въ поры фарфора, которыя она закупоривала, не давая внѣш-
нему воздуху проникнуть во внутрь резервуара. Если же давленіе вну-
три послѣдняго больше атмосфернаго, то газъ, пройдя черезъ поры ре-
зервуара, легко пройдетъ и черезъ слой жидкой глазури, плавящейся
около 1000°. Фарфоръ совершенно размягчается при 1500° и потому
НоІЬогп и УѴіеп производили опыты съ резервуарами, изготовлен-
ными изъ болѣе тугоплавкой глины и наполненными азотомъ. НоІ-
Ьогп и Ѵаіепііпег (1906) могли при помощи такого прибора из-
мѣрять температуры до 1600°.
НоІЬогп и Вау усовершенствовали газовый пирометръ. Они поль-
зовались тремя резервуарами: первый состоялъ изъ Іенскаго стекла 59П1
^боросиликатъ) и былъ назначенъ для температуръ между 200° и 500°;
второй состоялъ изъ глазированнаго фарфора, а третій изъ сплава пла-
тины и иридія. Р. ГЬарриіз (1902) точнѣе изслѣдовалъ тепловое рас-
ширеніе фарфора, играющее важную роль во второмъ приборѣ.
Тгаѵегз и Лацпегосі (1903) нашли, что при высокихъ темпе-
ратурахъ водородъ разлагаетъ стекло, фарфоръ и даже кремневую кислоту.
Поэтому они сдѣлали попытку примѣнить къ измѣренію весьма высокихъ
температуръ гелій, помѣщенный въ кварцевый сосудъ. Но эта идея ока-
залась невыполнимой, такъ какъ гелій диффундируетъ сквозь кварцъ,
какъ мы это видѣли въ т. I (гл. VI).
III. Опредѣленіе плотности паровъ. Вмѣсто того, чтобы
наблюдать упругость газа, находящагося въ резервуарѣ пирометра, можно
путемъ взвѣшиванія опредѣлять плотность газа или пара какого-
либо вещества, введеннаго въ резервуаръ.
Тгоойі и Веѵіііе пользовались способомъ Ьпшае (т. I);
Пирометры.
55
фарфоровый сосудъ съ вытянутымъ отверстіемъ (вѣсъ сосуда извѣ-
стенъ), содержащій немного іода, помѣщается въ среду, температуру
которой требуется измѣрить. Излишекъ іода испаряется; черезъ нѣко-
торое время запаиваютъ отверстіе резервуара, вынимаютъ послѣдній, да-
ютъ ему охладиться и взвѣшиваютъ его. Зная нормальную плотность О
паровъ іода, легко опредѣлить искомую температуру х изъ формулы
(і = 1,293
I Н 1 кх
у 760 ’ 1 4- ах
760 ’ 1 + аі
гдѣ V объемъ, к коеффиціентъ расширенія резервуара: Н давленіе ат-
мосферы, а слѣд. и паровъ іода въ моментъ, когда запаивается отверстіе;
Н' давленіе и і температура воздуха, когда производилось первое взвѣ-
шиваніе резервуара; а коеффиціентъ расширенія паровъ и (1 разность
вѣса резервуара, содержащаго пары іода и вѣса его же, наполненнаго
воздухомъ, въ граммахъ. Ке§*паиИ бралъ ртуть вмѣсто іода и послѣ
опыта, когда резервуаръ охладился, собиралъ и взвѣшивалъ жидкую
ртуть, образовавшуюся изъ тѣхъ паровъ, которые при нагрѣваніи остава-
лись въ резервуарѣ. Ке^папИ наполнялъ также цилиндрическій ре-
зервуаръ водородомъ, количество котораго, остающееся въ резервуарѣ
при опредѣляемой температурѣ, онъ прогонялъ черезъ накаленную трубку
содержащую окись мѣди. Струею сухого воздуха онъ прогонялъ образо-
вавшіеся пары воды въ стеклянныя трубки, наполненныя пемзою, смо-
ченною сѣрною кислотой. По увеличенію вѣса этихъ трубокъ, очевидно,
можно было опредѣлить количество водорода, оставшагося въ резервуарѣ;
а отсюда и температуру послѣдняго.
V. М а у е г и его ученики выработали пирометрическій способъ,
основанный на методѣ опредѣленія плотности паровъ, носящемъ названіе*
способа V. • М а у е г’а и разсмотрѣнномъ нами раньше (т. I): по этому
способу удавалось производить опредѣленія температуръ и плотности
до 1700°.
ТѴ. Давленіе и диссоціація паровъ. По Сгаііе’у
кипѣніе сѣры или ртути подъ давленіемъ можетъ служить для опредѣле-
нія температуръ. Ьату устроилъ < мраморный пирометръ», въ кото-
ромъ упругость диссоціаціи, т.-е. упругость выдѣляющейся СО2 служитъ
мѣрою температуры.
V. Способъ смѣшенія (калориметрическій). Этотъ спо-
собъ къ которому мы возвратимся впослѣдствіи, служитъ обыкновенно
для опредѣленія теплоемкостей при помощи точныхъ температурныхъ из-
мѣреній ; но онъ, наоборотъ, можетъ служить и для измѣренія темпера-
туры, если теплоемкость употребляемыхъ нами тѣлъ хорошо извѣстна..
Пусть Р вѣсъ опредѣленнаго тѣла /14, напр. куска платины, желѣза и т. д.,
с теплоемкость вещества, изъ котораго оно состоитъ; С теплоемкость ка-
лориметра, взятаго цѣликомъ, т.-е. металлическаго сосуда, воды въ немъ,
мѣшалки и термометра; і температура воды. Помѣстимъ тѣло М въ
среду, температуру х которой мы желаемъ опредѣлить, и когда оно при-
56
Термометры.
метъ эт} температуру, опустимъ его быстро въ воду калориметра, кото-
рая нагрѣется до нѣкоторой температуры Ѳ. Въ такомъ случаѣ имѣемъ
равенство
Рс(х— Ѳ) = С(Ѳ — О-Ь-Д...................(35)
гдѣ А то количество теплоты, которое калориметръ успѣлъ потерять луче-
испусканіемъ до момента отсчета температуры Ѳ. Ниже мы увидимъ,
какъ эта величина опредѣляется.
Попытки опредѣленія высокихъ температуръ этимъ способомъ нача-
лись весьма давно (съ 1802 г.). Р о и і 11 е і (1836) первый разработалъ этотъ
способъ, изслѣдовавъ до 1200° теплоемкость платины, изъ которой и дѣ-
лаютъ обыкновенно тѣло АГ. Работы Р і о п с 11 о п’а надъ теплоемкостью
желѣза даютъ возможность тѣло М дѣлать изъ желѣза; предлагали также
М дѣлать изъ Л7 или изъ кварца. Существенный источникъ погрѣшно-
стей заключается въ неизбѣжной потерѣ тепла тѣломъ при перенесеніи
или даже паденіи (не всегда } добномъ) его изъ среды, температуру х ко-
торой требуется опредѣлить, въ воду калориметра.
VI. Измѣненіе размѣровъ твердыхъ тѣлъ. Существу-
етъ большое число пирометровъ, основанныхъ на расширеніи твердыхъ
тѣлъ съ температурою и назначенныхъ для техническихъ цѣлей, гдѣ осо-
бенной точности въ измѣреніи высокихъ температуръ не требуется. Въ
послѣднее время занимались этимъ вопросомъ Ье СЬ.аіе1іег,Ріоп-
сЬоп и Селивановъ. Первый изучалъ расширеніе различныхъ ме-
талловъ, фарфора, кварца и др. веществъ при высокихъ температурахъ;
второй старался приложить методъ Еігеаи (см. гл. III) къ измѣренію
высокихъ температуръ, а послѣдній изучалъ расширеніе платины.
Нѣкоторою извѣстностью пользовался одно время пирометръ АѴебц-
•\ѵоо(Га, основанный на свойствѣ глиняныхъ непрокаленныхъ цилин-
дриковъ уменьшаться въ діаметрѣ при накаливаніи: онъ не можетъ дать
даже приблизительна точныхъ указаній, такъ какъ уменьшеніе діаметра
зависитъ не только отъ температуры, до которой цилиндрикъ былъ на-
грѣтъ, но и отъ продолжительности нагрѣванія.
VII. Плавленіе и кипѣніе тѣлъ. Серія чистыхъ метал-
ловъ, сплавовъ или иныхъ тѣлъ, плавящихся при различныхъ температу-
рахъ, можетъ дать указаніе на температуру среды ; такое же указаніе можно
получить, наблюдая кипѣніе опредѣленныхъ жидкостей, особенно если
при этомъ мѣнять внѣшнее давленіе. Первымъ способомъ пользовался
Р г і п 8 е р , приготовивъ серіи сплавовъ Аи — Л^, Рі — А<? и Аи Рі;
А р р о 11 пользовался серіей сплавовъ изъ мѣди и олова. Интересный
способъ опредѣленія высокихъ точекъ плавленія предложилъ Л о 1 у,
' устроивъ приборъ, названный имъ мель дометромъ: платиновая
проволока нагрѣвается постепенно усиливающимся токомъ, пока весьма
малое количество вещества, положеннаго на него, не расплавится. Ка-
либрированіе производится при помощи веществъ, точки плавленія кото-
рыхъ извѣстны. Измѣряются сила тока или удлиненіе проволоки. К а т -
Пирометры.
57
$ау и Еишогрііороиіой показали удобопримѣнимость этого при-
бора.
VIII. Электрическое сопротивленіе проволоки можетъ
служить мѣрою температуры, до которой она нагрѣта. На этомъ осно-
вано устройство цѣлаго ряда пирометровъ. Возможность пользоваться
этимъ способомъ находится въ тѣсной связи съ развитіемъ работъ, по-
священныхъ вопросу о зависимости сопротивленія даннаго проводника
отъ температуры і; этотъ вопросъ будетъ подробнѣе разсмотрѣнъ въ т. IV.
Изслѣдованія С а 11 е п (1 а г’а показали, что для нѣкоторыхъ металловъ
можно положить
— #о(1 4" ................(36)
гдѣ /?0 и сопротивленія при о0 и при /°, а и 3 постоянные коеффи-
ціенты.
Особою извѣстностью пользовался пирометръ 8 і е ш е п §’а, изобра-
женный на рис. 25. Платиновая проволока намотана на огнеупорный ци-
Рис. 25.
линдръ и припаяна къ мѣднымъ проводамъ; платиновый ци-
линдръ, закрытый съ одного конца, окружаетъ платиновою <.
проволоку; онъ, какъ видно изъ рисунка, надѣтъ на желѣз-
ный цилиндръ. Основной вопросъ о томъ, не вызываютъ ли
сильныя накаливанія постояннаго измѣненія въ сопротивле-
ніи проволоки былъ изученъ въ 1870 г. особой Коммиссіей
Британской Ассоціаціи. Самая проволока была введена въ
одну изъ вѣтвей моста Витстона, о которомъ уже1 было ска-
зано въ т. П. 8 і е т е п 8 приспособилъ свой приборъ и
для нѣкоторыхъ случаевъ измѣренія невысокихъ темпера-
туръ; въ особенности извѣстно его примѣненіе для измѣ-
ренія температуръ на большихъ глубинахъ въ океанѣ.
Наиболѣе полное изученіе вопроса принадлежитъ Саі-
1 е п (1 а г’у. Онъ показалъ, что повторныя накаливанія не
мѣняютъ сопротивленія проволоки изъ совершенно чи-
стой платины, такъ что при каждомъ возвращеніи къ
той же температурѣ получается всегда одно и то же сопро-
тивленіе. О аПепсіаг сравнивалъ показанія пирометра
съ показаніемъ газоваго термометра, помѣстивъ проволоку
н ирометра внутри резервуара послѣдняго. Онъ нашелъ, что
если вмѣсто (36) принять линейную зависимость
которая даетъ
= Яо(1 + аі}
(37)
/ = 100
''100 /'О
(38)
то истинная температура Т получается по формулѣ
Т=і-\- о
/ і V
\100 /
і ’
100
(39)
58
Термометрія.
гдѣ о постоянное число, которое можно опредѣлить для данной проволоки
и которое близко къ 1,54. ѲгіТТііЬз нашелъ, что формулы (38) и (39)
еще болѣе точны, чѣмъ полагалъ самъ С а 11 е п б а г. Самая проволока
въ пирометрахъ С а 11 епб аг’а была намотана на азбестовую бумагу.
Для опредѣленія о СаПепйаг и (ігіИі іЬ8 рекомендуютъ наблю-
деніе въ парахъ сѣры, точка кипѣнія которой 444,53° + 0,082°Л при да-
вленіи въ 760 + И мм. НоІЪогп и ЛѴіеп находятъ, однако, что фор-
мула СаПепдаг’а не точна; противъ этого возражалъ Саііепйаг
(1899), основываясь на весьма точныхъ измѣреніяхъ.
В г а и п также изслѣдовалъ платиновый пирометръ, сравнивая его
съ газовымъ пирометромъ, резервуаръ котораго былъ сдѣланъ изъ фар-
фора.
Дальнѣйшія изслѣдованія производили О е лѵ а г и Р1 е ш пі і п Я',
Неусоск и ЭДеѵіІІе, Тогу, Віскзоп (1897), Сйгее (1900)
ТЪіезеп (1903), Ейдѵагдз (1905) и СатрЬеІІ (1905). Изъ нихъ
ІЭ і с к 8 о п предложилъ формулу вида (А? 4~ #)2 - р(і-\- Ь), въ которой а, Ь
и р постоянныя числа и которая хорошо согласуется съ наблюденіями
различныхъ, названныхъ выше ученыхъ.
Р. СЬарриіз и Нагкег (1900) также изслѣдованіи платиновый тер-
мометръ; они подтвердили формулу С а Не и да г’а, причемъ б оказалось
равнымъ 1,54 при температурахъ между — 23° и -р 45°; при болѣе вы-
сокихъ температурахъ, до 100°, эта формула даетъ результаты, неточные
до 0°,01. Они находятъ, что температурою кипѣнія сѣры, равной 445°,27,
весьма удобно можно пользоваться какъ третьей основной точкой. Наг-
кег (1904) одинъ довелъ изслѣдованіе до 1000° и нашелъ О — 1,49 —1,51.
Наконецъ, Тгаѵегз и Олѵуег (1905) изучили платиновый термометръ
между -р 34° и —190° и сравнили его съ водороднымъ термометромъ. Они
нашли чрезвычайно большое значеніе о = 1,9. НоІЪогп (1901) непо-
средственно сравнивалъ платиновый термометръ съ водороднымъ; онъ на-
ходитъ, что сопротивленіе /? выражается формулою
= А>0 [ 1 4- 0,1103934/ 4- О,000000988/2 .
ЛѴаідпег и Вигдезз (1909) нашли, что если пользоваться чи-
стой платиной, то формула Саііепдаг’а даетъ отъ 0° до 1100° ошибки,
не превышающія 1° при 1100°. Нечистая Рі, а также Р(1 даютъ менѣе
точные результаты.
Въ 1896 г. былъ построенъ Арріеуаг сГомъ платиновый термометръ,
въ которомъ температура измѣряется сопротивленіемъ платиновой прово-
локи, причемъ отсчеты на Витстоновомъ мостѣ даютъ непосредственно тем-
пературы. Сравненіе платиноваго термометра ОгіГИіІів’а съ ртут-
нымъ термометромъ, которымъ пользовался Коѵѵіаіні при своихъ рабо-
тахъ, произвели ЛѴаійпег и М а 11 о г у.
IX. Акустическіе способы. Изъ другихъ способовъ упо-
мянемъ еще нѣкоторые. Мы видѣли (т. II), что скорость V звука
Пирометры
59
въ газахъ при /° выражается формулою
Ѵ= К, 1 Г+ аЛ
гдѣ Ио скорость при 0° и а — 0,00365 — коеффиціентъ расширенія газовъ.
Если закрытая съ одного конца труба имѣетъ длину /0 при 0°, то она
издаетъ при 0° звукъ, число колебаній 2Ѵ0 котораго равно
^=21„............................
При /° она даетъ тонъ, число колебаній котораго равно
(41)
21 ~ 2/0(1 + да)
гдѣ [3 коеффиціентъ линейнаго расширенія вещества трубки. Измѣряя Ао
и можно найти искомое і. Такой пирометрическій способъ былъ
предложенъ Са§піаг(1-Еаіои г’омъ, С11 а л і а г й ’омъ и позже А. М.
Меуег’омъ. Въ послѣднее время 8. Тоіѵет-Ргевіоп изучалъ во-
просъ объ акустическомъ измѣреніи температуръ. О и і л к е построилъ
(1897) акустическій термометръ, основанный на измѣреніи длины волны
звука въ трубкѣ, температуру которой желаютъ измѣрить. Длина волны
опредѣляется по способу, основанному на интерференціи звука, и самый
приборъ напоминаетъ по своему устройству приборы 0 и і п с к е и К о е -
пі^’а, описанные въ т. П.
§ 13. Оптическая пирометрія. Этимъ названіемъ мы обозначаемъ
совокупность пирометрическихъ методовъ, основанныхъ на изученіи
свойствъ лучей, испускаемыхъ тѣлами, температуры которыхъ требуется
измѣрить.
Сюда же мы относимъ неподходящій подъ это опредѣленіе, уже опи-
санный нами (стр. 50) методъ В. Вегійеіоі, который усовершенство-
вавъ (1902) свой методъ, сдѣлалъ его пригоднымъ для измѣренія высо-
кихъ температуръ. Онъ замѣнилъ одну изъ упомянутыхъ выше стеклян-
ныхъ трубокъ фарфоровою и ввелъ еще нѣкоторыя измѣненія, на ко-
торыхъ мы не останавливаемся. Этимъ приборомъ онъ опредѣлилъ
точки кипѣнія селена, кадмія и цинка и точки плавленія серебра и
золота.
Переходя къ чисто оптическимъ пирометрамъ, укажемъ сперва на
нѣкоторыя старыя работы, въ которыхъ цвѣтъ и спектръ тѣлъ,
нагрѣтыхъ выше температуры, при которой только начинается ихъ свѣ-
ченіе (красное каленіе), служатъ указателями ихь температуры. Р о и і 1 -
1 е I измѣрялъ температуру раскаленной платины при помощи воздушнаго
термометра и составилъ табличку, въ которой указанъ ея двѣтъ при раз-
личныхъ температурахъ. Весциегеі въ обширной работѣ старался ос-
новать фотометрическую пирометрію, измѣряя* силу свѣта, испускаемаго
60
Термометрія.
нагрѣтымъ тѣломъ и прошедшаго черезъ красное, зеленое или синее
стекло. Онъ нашелъ, что всѣ непрозрачныя тѣла испускаютъ при одина-
ковыхъ температурахъ одинаковый свѣтъ. Этотъ результатъ подтвердилъ
позже Сгоѵа. Ѵіоііе, Ъе СйаЁеІіег, Веяоісі и др. сравнивали
температуру и силу свѣта нагрѣтыхъ тѣлъ. СІІайзіопе и Оелѵаг
сравнивали температуру съ общимъ характеромъ спектра, Г і е ѵ е 2
съ длиною спектра, которая съ повышеніемъ температуры увеличи-
вается.
Новая эра для оптической пирометріи настала въ 1^99 г., когда вь
основу температурныхъ измѣреній были положены тѣ законы лучеиспу-
сканія, которые подробно были изложены въ т. П; напомнимъ, вкратцѣ,
необходимое. Лучеиспускательная способность /:(Л, Т) абсолютно чер-
наго тѣла (т. е. такого, которое поглощаетъ всѣ лучи), какъ функція длины
волны Я и абсолютной температуры Т, нѣкоторое время выражалась фор-
мулою АѴ і е п’а
с
Е(к, 1) = Сл~5е '-Т...................(42)
см. т. И. Какъ мы видѣли, эта формула не можетъ считаться справедли-
вою вообще и должна быть замѣнена формулою Р1 а п с к’а или форму-
лою Ьиштег’а и 4аЪпке. Но внутри области видимыхъ лучей
даже до очень высокихъ температуръ (по Ьитшег'у, до 5000°) фор-
мула АѴ і е п’а смѣло можетъ быть примѣнена. Она даетъ
}^Е — у — С ..............................(42ча)
л 1
гдѣ Л отъ Т не зависитъ и натуральный логариѳмъ. Далѣе во Н томѣ
были изложены слѣдующіе законы.
Законъ АѴіеп’а:
. Т____| = 2940 (абсол. черн. тѣло)
т | = 2630 (платина)
(43)
Здѣсь Лт та длина волны, для которой лучеиспускательная способность Е
максимальная. Этотъ максимумъ Ет для абсолютно чернаго тѣла слѣдуетъ
второму закону АѴ і еп’а :
Ет =ВТ°.......................(43, а)
гдѣ В постоянная.
Законъ 8 і е і' а п’а для интегральнаго лучеиспусканія абсолютно чер-
наго тѣла: ос
у*Е(&Т)ал= СТ*.......................(44)
О
Постоянныя с и А въ (42) и (43) связаны уравненіемъ
с — ЪЛт Т = 5А
(45)
Оптическая пирометрія.
61
Полагая для абсолютно чернаго тѣла Т = 2900, мы получаемъ
(7 = 52^7=1450 .............
(45.67)
Напомнимъ, что лучеиспусканіе всякаго тѣла, окружен-
наго непроницаемою оболочкою, тождественно съ лу-
чеиспусканіемъ абсолютно чернаго тѣла, если принять, что
оболочка и всѣ находящіяся въ ней тѣла находятся при одной и той же
температурѣ (т. II).
Если е есть испусканіе произвольнаго тѣла и а —его погло-
щеніе, то, по закону КігсЫіоІГа (т. II),
е = аЕ. . . ..........(45/)
Это даетъ Ірл = - + ^Е и. слѣдовательно, на основаніи (42,а),
І^е = 1$а + / — ...... (45,с)
Формулы (42 л), (43) и (44) имѣютъ 'силу только для абсолютно чер-
наго тѣла. Если-же мы примѣняемъ эти формулы къ произволь-
ному тѣлу и по наблюденному излученію (для опредѣленной 2) вычис-
ляемъ температуру, то мы получаемъ такимъ образомъ не истинную
температуру тѣла 7, но такую температуру которую имѣло-бы аб-
солютно черное тѣло, если-бы его излученіе (для той-же 2) было
тождественно съ наблюденнымъ. Эту температуру ТА называютъ чер-
ной температурой тѣла (Ъіаск Ьосіу іеиірегаіліге). Выведемъ урав-
неніе, связывающее черную температуру Ед съ истинной температурой Т.
Вмѣсто (42л) мы должны теперь написать:
V—...................................(45,^)
Такъ какь мы принимаемъ, что Е при такъ-же велико, какъ е при 7°,
то Е въ (45,сГ) равняется І^л въ (45,с). Это даетъ :
14500
л
1 \
ТАІ
(45л)
1
7
если замѣнить с его значеніемъ изъ (45,а). Если принять, что для дан-
ной 2 поглощеніе а не зависитъ отъ температуры, то получается про-
стое уравненіе
1---* = Соп8І...............(45,/)
Тд 7
Если для даннаго тѣла найдены непосредственнымъ измѣре-
ніемъ температуры 7 и 7д, то (45/) и (45л) даютъ отношеніе испу-
сканія е даннаго тѣла къ испусканію Е абсолютно чернаго тѣла при
62
Термометрія.
той-же температурѣ; именно,
. е 14500/ 1
л (г
1 \
Тд)^
• (45,^)
откуда и получается искомое отношеніе
е
Е=-а = 1 — г.........................(45/)
гдѣ г означаетъ отражательную способность тѣла. Такого рода
опыты были впервые сдѣланы Н о 1 Ь о г и’омъ и Н е п п і ц’омъ (1905) для
Рі, Аи и А§. Они изучали испусканіе не для опредѣленныхъ Л, но для
отрѣзковъ спектра, «центры тяжести» которыхъ точно совпадали съ
0,643д (красная), 0,550/і (зеленая") и 0,474,а (голубая;. Для платины
были опредѣлены Т и Тд для семи температуръ между ^=681° и і =
= 1573°. При этомъ уравненіе (45,/) для краснаго свѣта дало :
Т— 1 р,0000507.
‘А 1
Такимъ образомъ, поглощеніе а дѣйствительно оказалось отъ 7 не
зависящимъ. Формула (45,§) даетъ :
= 0,319.
Е
Слѣдовательно, испусканіе платиной красныхъ лучей равняется 0,319
ихъ испусканія абсолютно чернымъ тѣломъ. На^еп и К и Ь е п 8 нашли
для Л — 0,643 значеніе 1 г, равное 0,340 (т. II), что хорошо со-
гласуется съ (45,/і). Для зеленыхъ лучей оказалось =0,340, для го-
е Е
лубыхъ =0,368.
Для золота и серебра НоІЬогп и Неппі^ получили слѣ-
е
дующія величины Е :
Лучи: Золото Серебро
красные 0,127 0,080
зеленые 0,258 0,071.
При одной и той-же температурѣ въ красномъ свѣтѣ
испусканіе платины равняется приблизительно 1/8, зо-
лота — х/8 и серебра — 1 14 абсолютно чернаго испу-
сканія.
Всѣ работы, относящіяся къ оптической пирометріи, мы раз-
дѣлимъ на нѣсколько группъ.
I Работы \Ѵапиег’а (1900—1901) и Кету (1904). АѴаппег
построилъ пирометръ, теорія когораго основана на формулѣ (42,а). Если
Оптическая пирометрія
63
Ео и То два сопряженныя значенія, то эта формула даетъ
, Е с I 1 1 \ , .
— Л ( То~~ т)................(46)
На основаніи формулъ (43) и (45) ЛѴаппег полагаетъ с— 14500. Пи-
рометръ ДѴаппег’а построенъ такъ, что въ него попадаютъ только лучи
длины волны 2 = 0,6563^; въ сущности это спектрофотометръ, служа-
щій для непосредственнаго сравненія двухъ лучеиспускательныхъ способ-
ностей Е и Е$. Лучеиспусканіе Е^ получается отъ лампочки накаливанія
(6 вольтъ), при чемъ постоянство величины Е^ провѣряется при помощи ами-
лацетатовой лампочки. Температура Го, соотвѣтствующая лучеиспуска-
нію Е$, опредѣляется разъ навсегда при помощи сравненія съ лучеиспу-
сканіемъ абсолютно чернаго тѣла. Такъ какъ с, 2 и То извѣстны, то (46)
даетъ искомую температуру Т тѣла, когда Е: Е^ опредѣлено фотометри-
ческимъ способомъ. Разсматриваемый пирометръ можетъ служить, напр.,
для опредѣленія температуры доменныхъ печей и вообще во всѣхъ слу-
чаяхъ, когда можно принять, что лучеиспусканіе тѣла несущественно от-
личается отъ лучеиспусканія абсолютно чернаго тѣла. Нагітапп (1904)
показалъ, что пирометръ АѴаппег’а для очень тонкихъ накаленныхъ
проволокъ не даетъ хорошихъ результатовъ, такъ какъ этом} мѣшаютъ
диффракціонныя явленія (т. Л).
На существенно другомъ принципѣ основанъ абсорбціонный
пирометръ Регу (1904). На основаніи формулы (42) мы имѣемъ
для даннаго 2 (опредѣляемаго краснымъ стекломъ) напряженіе
а
т ..................(46, а)
Это напряженіе дѣлается равнымъ напряженію і постояннаго источника,
лучи котораго проходятъ черезъ поглощающій слой; толщина х послѣд-
няго можетъ быть измѣнена и измѣрена. Въ этомъ случаѣ
— Ьх
і = /е ........ (46,0
гдѣ Ь коеффиціентъ поглощенія вещества упомянутаго слоя. Изъ (46,а)
и (46,Ь) слѣдуетъ, что величины х и 1 : Г связаны линейнымъ уравне-
ніемъ вида
х—р—Ят........................(46,0
Когда р и д эмпирически опредѣлены, можно вычислить 7 по измѣрен-
ному х. Слой перемѣнной толщины х состоитъ изъ двухъ клинообраз-
ныхъ, подвижныхъ пластинокъ, подобныхъ тѣмъ, которыми пользуются
въ компенсаторахъ, входящихъ въ составъ различныхъ оптическихъ
приборовъ (т. II).
64
Термометрія.
II. Методы, основанные на примѣненіи формулы
кгпТ—А. В. А. Михельсонъ (въ Москвѣ, 1887) первый произвелъ измѣ-
реніе температуры, опредѣливъ длину волны , соотвѣтствующую макси-
мальному лучеиспусканію Е, Но мы видѣли (т. II), что данная имъ фор-
мула приводитъ къ соотношенію Т — Соп8І.. которое въ настоящее
время не можетъ считаться справедливымъ.
Ьитшег и Ргіп^зйеіт (1899), АѴаппег (1900) и 8іе-
лѵагі (1901) пользовались правильной формулой кт Т = А = Соп8І. для
опредѣленія температуры Т лучеиспускающихъ тѣлъ. Такъ какъ для аб-
солютно чернаго тѣла А = 2940, для платины А — 2630, то весьма
вѣроятно, что соотношеніе ктТ = Соп8І. примѣнимо и къ другимъ тѣ-
ламъ, и что А всегда имѣетъ нѣкоторое среднее значеніе между двумя
вышеприведенными. Смотря по тому, насколько максимальное лучеис-
пусканіе, соотвѣтствующее именно лучамъ близко къ пропорціональ-
ности Г5 или Г6, можно судить о томъ, приближается ли разсматривае-
мое тѣло по своимъ свойствамъ къ абсолютно черному тѣлу или къ пла-
тинѣ. По формуламъ
1 1 ‘ ~ 2940 ~ 2630
/ = . и / = ,
/ к
'*т '*т
можно, во всякомъ случаѣ, опредѣлить два крайнія значенія для Т.
Этимъ способомъ Ьппітег и Ргіп^зііеіт (1899) опредѣляли пре-
дѣльныя значенія для абсолютныхъ температуръ различныхъ источниковъ
свѣта (дуговая лампа 3750°--4200°, лампа ЬІегпзѴа 2200° -2450°, го-
рѣлка Ауэра 2200° 2450° и др.). Распредѣленіе энергіи они измѣряли
болометромъ (т. II).
Въ солнечномъ спектрѣ максимумъ интенсивности находится при-
близительно въ желтыхъ лучахъ. Если положить кт == 0,5/х, то для тем-
пературы солнца получается круглымъ числомъ 6000°.
ЗсЬийіег (1905) опредѣлилъ температуру фотосферы въ 6700°,
а температуру поглощающаго слоя въ 5450°. Негігвргипд’ (1905)
получилъ для температуры вну треннеи поверхности солнца приблизи-
тельно 10000° съ возможной погрѣшностью въ + 1000°.
Въ послѣднее время занимались вопросомъ о температурѣ солнца
МіІІосЬаи и Еегу (1906- 1909), СоЫепг (1907), Гольдгаммеръ
п др. Температуру звѣздъ опредѣляли \Ѵ іі 8 і п ц и БсЬеіпег
(1909), Когйтапп (1910) и Неррег^ег (1910). Мы не можемъ
останавливаться на этихъ весьма интересныхъ работахъ и ограничиваемся
указаніемъ литературы.
Ьіітшег и Ргіп^вЬеіт (1901) показали, какимъ обра-
зомъ можно соединить спектрофотометрическій методъ \Ѵ а п п е г’а
(стр. 63) съ только-что описаннымъ болометрическимъ, чтобы получить
болѣе тѣсныя границы для искомой температуры. Въ томъ же году
Ьиштег построилъ свой интерференціальный фото-пирометръ, который
былъ изображенъ въ томѣ II и описанъ, какъ фотометръ. Если примѣ-
нять этотъ приборъ для измѣренія отношенія Е: Е^ въ (46), то онъ оче-
Оптическая пирометрія.
65
Рис. 26.
видно можетъ служить для опредѣленія Т и такимъ образомъ играть
роль пирометра. Примѣнимость формулы Т = А къ опредѣленію тем-
пературы пламенъ изслѣдовали Ьиттег и Ргіп^зЬеіт (1902) и
біелѵагі (1902). Послѣдній полагаетъ, что эта формула для пламенъ
вполнѣ примѣнима: для свѣтящагося пламени онъ находитъ А = 2280.
III. Пирометръ НоІЬогіГа и КигіЪаит’а. Этотъ приборъ
(рис. 26) состоитъ изъ зрительной трубки, объективъ Ц которой даетъ,
за отверстіемъ діафрагмы О, изобра-
женіе раскаленной поверхности, тем-
пературу которой надо измѣрить. На
томъ же мѣстѣ находится угольная
нить лампочки накаливанія (6 вольтъ),
которая на рисункѣ повернута на 90°.
Черезъ окуляръ А2 наблюдаются уголь-
ная нить и раскаленная поверхность.
Посредствомъ измѣненія сопротивле-
нія ГГ въ цѣпи, въ которой дѣйству-
етъ электродвижущая сила Е, яр-
кость лампочки усиливаютъ до тѣхъ
поръ, пока она не исчезнетъ на свѣт-
ломъ фонѣ, на которомъ она сначала
казалась темной. Соотвѣтствующая сила тока измѣряется приборомъ 5
(прецизіонный амперметръ). При температурахъ отъ 600° до 800° измѣ-
ренія производятся непосредственно; для температуръ свыше 800° пе-
редъ'окуляромъ помѣщается красное стекло. Сопротивленіе помѣщено
на столбикѣ, поддерживающемъ зрительную трубку и можетъ быть измѣ-
нено простымъ поворотомъ кольца. Калибрированіе прибора произво-
дится при помощи абсолютно чернаго тѣла (т. II), температура котораго из-
мѣряется термоэлементомъ. Такимъ способомъ для всякой силы тока, ука-
занной на 5, получается соотвѣтствующая температура, приблизительно
до 1500°; на шкалѣ 5 температуры нанесены непосредственно. Если из-
мѣряемая температура выше, то свѣтъ слѣдуетъ ослабить. Для этого
служатъ дымчатыя стекла, или двукратное отраженіе отъ призмъ (Р на
рис. 26), или трехкратное отраженіе. Коеффиціентъ ослабленія ср опре-
дѣляется разъ навсегда изъ наблюденій надъ чернымъ тѣломъ по формулѣ
которая вытекаетъ изъ (46;. Здѣсь с= 14500, Л = 0,643 (красное стекло),
Го обозначенная на зрительной трубкѣ «ослабленная» температура, а Т
истинная температура чернаго тѣла. Если ср извѣстно, то (47) даетъ
искомое Г, если температура Го была отсчитана на приборѣ. При двухъ
отраженіяхъ можно дойти до 2800°, при трехъ — до 6000°, тогда какъ
лампочка накаливанія доведена лишь до 1500° (То). Кегпзѣ (1903)
употребилъ подобный же методъ для измѣренія высокихъ температуръ.
КУРСЪ ФИЗИКИ О. X в О Л Ь С О Н А. Т. III, изд. 3-е. 5
66
Термометрія.
КпгІЬапт примѣнилъ вышеописанный пирометръ для измѣренія
температуры пламенъ (1902); точность его метода оспаривалъ Ъит-
т е г (1903), но К и г 1Ь а и т возражалъ послѣднему. Ограничиваемся
указаніемъ литературы.
IV. Законъ 8 іе іа п’а и второй законъ АѴіеп’а. 81 е-
і а п первый пытался вычислить температуру Т солнца на основаніи дан-
наго имъ закона. Новое вычисленіе было выполнено V аг Ь и г §’омъ
(1899) ; онъ нашелъ Т = 6490°.
Далѣе Тегу (1902) въ цѣломъ рядѣ работъ показалъ, какимъ обра-
зомъ, на основаніи закона 8іеіап’а, могутъ быть произведены измѣре-
нія температуръ, при условіи, когда лучеиспусканіе разсматриваемаго
тѣла можетъ быть принято за лучеиспусканіе абсолютно чернаго тѣла.
Онъ построилъ простой пирометръ въ видѣ зрительной трубы. Въ фо-
кусѣ объектива (изъ плавиковаго шпата) находится спай термоэлемента
желѣзо константанъ; измѣряется такимъ образомъ сила термоэлектриче-
скаго тока. Въ электрически накаляемой печи находится кусокъ извести,
лучеиспусканіе которой, очевидно соотвѣтствующее черному тѣлу, слу-
житъ для калибрированія пирометра. Температура печи измѣряется тер-
моэлементомъ Ье СЬаіеІіег (платина и платина-иридій). Законъ
біеіап’а оказался вѣренъ въ предѣлахъ 900°—1500°. Этимъ пиро-
метромъ Р е г у измѣрялъ температуры раскаленныхъ тѣлъ, въ особен-
ности различныхъ окисловъ. Въ то же время онъ измѣрялъ лучеиспус-
каніе этихъ тѣлъ при помощи прибора, вполнѣ сходнаго съ описаннымъ
выше приборомъ НоІЬогп’а и КигІЪаиш’а. Позже (1904) онъ еще
усовершенствовалъ свой пирометръ.
V. Температурная шкала, о с н о в а н н а я на т е оріи лу-
чеиспусканія. Въ началѣ 1903 г. появилась въ высшей степени ин-
тересная работа Ьитшег’а и Ргіп^зйеіт’а. въ которой окон-
чательно доказано, что на основаніи законовъ лучеиспусканія можно
измѣрять абсолютныя температуры до 2300°, по крайней мѣрѣ по тремъ
методамъ; этимъ расширена извѣстная до сихъ поръ область точныхъ
пирометрическихъ измѣреній на 1000°. Еигашет и Ргіп^яйеіш
пользовались одновременно тремя измѣрительными приборами:
1. Плоскій болометръ, для измѣренія интегральнаго луче-
испусканія (44), слѣдующаго закону біеіап’а.
2. С п е к т р о б о л о м е т р ъ для опредѣленія фу нкціи Е (л, Т). Она
даетъ Лт и Ет\ однако значеніе1 Л = для котораго Е принимаетъ
максимальное значеніе Ет, не можетъ быть опредѣлено точно. Поэтому
они вовсе не пользовались формулой (43) Лт Т = Л, а только формулой
(43,а) для максимума энергіи.
3. Спектрофотометръ для измѣренія яркости для пяти различ-
ныхъ Л, а именно 0,62—0,59—0,55—0,51—0,49^. Температура Т можетъ
быть вычислена по формулѣ (42), или по какой-либо другой формулѣ,
приложимой къ видимой области (см. т. II), если для даннаго Л наблю-
дать яркость Е.
Термоэлектрическіе пирометры
67
Сначала для этихъ трехъ приборовъ опредѣлялись коеффиціенты
пропорціональности, при помощи раскаленнаго абсолютно чернаго тѣла,
температура котораго была измѣрена термоэлементомъ. Затѣмъ это тѣло
доводилось до гораздо болѣе высокой температуры (напр. до 2325°), которая
измѣрялась по всѣмъ тремъ способамъ. Измѣренія дали : интегральнаго лу-
чеиспусканія въ среднемъ 2330°, максимальной энергіи 2325°, яркости
2320°. Изъ этихъ опытовъ слѣдуетъ, что на основаніи законовъ луче-
испусканія практически возможно построить температурною шкалу. Если
считать температуру пропорціональной корню четвертой степени изъ ин-
тегральнаго лучеиспусканія чернаго тѣла и если принять разность тем-
пературъ между точкой замерзанія и точкой кипѣнія воды равной 100°,
то получается температурная шкала, тождественная со шкалою идеаль-
наго газоваго термометра и теоретической, практически однако не осу-
ществимой шкалой Т іі о т 8 о п’а.
Въ послѣднее время появился рядъ прекрасныхъ обзоровъ мето-
довъ оптической пирометріи, принадлежащихъ Вау и О г 81 г а п сГу
(1904), ѴѴаісІпег’у и Впг^езз’у (1905) и Ікіё (1905).
Въ заключеніе упомянемъ,, что различные изслѣдователи прилагали
методы оптической пирометріи для опредѣленія температуры воль-
товой дуги. Сюда относятся измѣренія \Ѵаппет’а, Ѵегу, Ьиш-
шет’а и Ргіп^зйеіт’а, Еёгу и, наконецъ, АѴаійпег’аи Виг-
§е8 8’а (1904), которые примѣнили три метода и получили нижеслѣду-
ющіе результаты :
пирометръ НоІЬогп-КигІЬаиш’а . . . 3690°
„ ѴѴаппег’а . .......................... 3680°
„ ЬеСйаіеІіег........................ 3720°
Эти числа означаютъ абсолютныя и при томъ «черныя > температуры.
§ 14. Термоэлектрическіе пирометры. На стр. 50 мы напомнили,*
въ чемъ заключается термоэлектрическій методъ измѣренія температуръ.
Его примѣнимость къ высокимъ температурамъ начала выясняться, бла-
годаря работамъ Ье Сйаіеііег, Вагиз’а, НоІЬогп’а и ХѴіеп’а
и др. На стр. 49 была приведена формула (33) Авенаріуса, даю-
щая термоэлектродвижущую силу, когда спаи находятся при температу-
рахъ и при = 0° имѣемъ болѣе простую формулу (34) стр. 50.
Ропіііеі (1836) первый воспользовался термоэлектрической парой
Ре- -Рі для измѣренія высокихъ температу ръ. Желѣзная трубка (рис. 27) или
стволъ Ьа/ закрытъ съ одной стороны желѣзнымъ дномъ с, къ серединѣ
котораго припаяна платиновая проволока, идущая вдоль оси трубки, на-
полненной магнезіей или азбестомъ, чтобы проволока не могла коснуться
внутренней стѣнки трубки. Конецъ платиновой проволоки присоеди-
ненъ къ зажимному винту I: другой зажимъ т соединенъ съ самою
трубкою. При помощи этихъ зажимовъ пирометръ вводится въ цѣпь,
содержащую гальванометръ. Конецъ ствола, гдѣ находится спай, вста-
вляется въ среду, температуру которой хотятъ измѣрить. Л о 1 1 у
5*
68
Термометрія.
употреблялъ пару Рі — Си, Вео’паиіі и Козеііі вновь Рі — Ре,
не получая хорошихъ результатовъ.
Въ 1863 г. появилась обширная работа ВесциегеГя, изслѣдо-
вавшаго элементъ Рі — Рск Онъ вставилъ тонкую фарфоровую трубку
аЪ (рис. 28) въ болѣе широкую трубку АВ, также фарфоро-
вую. Черезъ тонкую трубку проведена палладіевая проволока т,
а внѣ ея, но внутри широкой трубки — платиновая про-
волока п. Концы двухъ проволокъ скручены другъ съ дру-
гомъ. Обѣ проволоки соединены съ проводами, идущими къ
гальванометру, а мѣста соединенія находятся внутри стеклян-
ныхъ согнутыхъ трубокъ, окруженныхъ тающимъ льдомъ. Трубка
АВ была вставлена въ печь, такъ что ея середина, гдѣ нахо-
дилось мѣсто соединенія проволокъ изъ Рі и Рй, подвергалась
наибольшему нагрѣванію. Весциегеі калибрировалъ пока-
Рис. 27.
Рис. 28.
в
Ь т
занія своего пирометра при помощи воздушнаго пирометра,
фарфоровый резервуаръ котораго вставлялся въ трубку АВ че-
резъ открытый при этомъ конецъ В, Оказалось, что темпера-
тура і и сила У термоэлектрическаго тока связаны эмпириче-
скою формулою вида
І ’
Весциегеі воспользовался своимъ пирометромъ для опре-
дѣленія точекъ плавленія металловъ; объ этомъ будетъ ска-
зано ниже.
Я с й і и 2 обстоятельно изучилъ термоэлектрическую пару Ре — Рі,
устроивъ для ея калибрированія газовый (Л/) пирометръ, резервуаръ ко-
тораго составлялъ желѣзный цилиндръ, соединенный однимъ концомъ съ
манометромъ. На другомъ концѣ вставлена въ дно цилиндра трубка,
внутренній, закрытый конецъ которой находился близъ центра самаго
резервуара. Въ эту трубку вводилась пара Ре — Рі, такъ что спай на-
ходился какъ разъ въ центрѣ резервуара, но все-таки не въ наполняю-
щемъ его газѣ. Изъ другихъ работъ выдаются изслѣдованія Т а і Ь’а,
В г а и п’а и др.
Вопросъ о термоэлектрической пирометріи получилъ новый толчокъ,
благодаря работамъ Ье Сйаіеііег. изучавшаго пару изъ платины и
сплава платины съ 10° 0 родія. Для калибрированія онъ воспользовался
рядомъ точекъ плавленія и кипѣнія, для которыхъ онъ принялъ числа,
отчасти передъ тѣмъ ^опредѣленныя ѴіоПе’емъ. Эти числа суть: вода
100°, свинецъ (плавл.) 323°, — 358°, Хп — 415°, 5— 448°, 8е— 665°,
Термоэлектрическіе пирометры.
69
А§ - 945°, Аи — 1045°, Си — 1054°, Рсі — 1500° и Рі — 1775°. Онъ на-'
шелъ, что элементъ Рі — (Рі, РК) отличается особымъ постоянствомъ,
т.-е. и послѣ многократныхъ накаливаній даетъ одн} и ту же электро-
движущую силу е, если возвращаться къ прежней температурѣ спая.
Эта сила е, однако, не выражается формулою Авенаріуса; до 300°
она выражается болѣе сложною формулою,, но зато между 300° и 1200°
можно положить е = А Ві, гдѣ А и В постоянныя числа. Ь е СЬа-
іеііет находитъ, что при помощи его элемента можно измѣрять темпе-
ратуру до 1200° съ ошибкою ’ около 10°.
Ваги8 произвелъ обширное изслѣдованіе термоэлектрическаго пи-
рометра, одна изъ проволокъ котораго платиновая, а другая состоитъ изъ
сплава платины съ 20% иридія. Половина его книги, посвященной
пирометріи, занята описаніемъ и методомъ калибрированія этого пиро-
метра и сравненіемъ его съ парою Ь е СЬаіеІіег. В а г и 8 подробно
описываетъ три рода приборовъ, служащихъ для калибрированія пиро-
метра. Первый родъ служитъ для наблюденія не очень высокихъ, а вто-
рой родъ для наблюденія высокихъ точекъ кипѣнія различныхъ веществъ,
каковы: нафталинъ, камфора, дифениламинъ, бензофенолъ, ртуть и сѣра
съ одной стороны, РЬ, Тлі, Ссі, Ві, 8Ь и 8п съ другой. Третій родъ при-
боровъ служитъ для калибрированія пирометра при высокихъ точкахъ
плавленія алюминія, золота и палладія. Перечисляя преимущества тер-
моэлектрическаго пирометра, В а г и 8 , между прочимъ, указываетъ на
слѣдующія обстоятельства: можно измѣрять температуру чрезвычайно
маленькаго пространства; можно измѣрять температуры до точки плавле-
нія платины и даже выше, если помѣстить спай въ огнеупорную обо-
лочку и пользоваться металлами въ жидкомъ видѣ; показанія пирометра
постоянны до 0,1% въ теченіе нѣсколькихъ лѣтъ; эти показанія полу-
чаются почти моментально.
Въ 1892 и 1895 годахъ появились работы НоІЬотп’а и ѴѴіеіГа,
о которыхъ ужо было упомянуто на стр. 54. Они изслѣдовали элементъ
Ье Сйаіеііег (платина и сплавъ платины съ 10% родія), сравнивая
его показанія непосредственно съ показаніями воздушнаго термометра.
Отъ фарфороваго резервуара послѣдняго шли двѣ трубки въ противопо-
ложныхъ направленіяхъ; черезъ эти трубки были проведены проволоки
пирометра, спай котораго находился въ центрѣ резервуара. Одна изъ
трубокъ была соединена съ ртутнымъ манометромъ обыкновеннаго устрой-
ства. Коеффиціентъ расширенія фарфора былъ опредѣленъ и оказался
равнымъ 0,0000044 и не зависящимъ отъ температуры. НоІЬогп и
АѴіеп убѣдились, что многократное нагрѣваніе пирометра до 1400° не
вызываетъ въ немъ никакихъ измѣненіи, и что температура і можетъ
быть выражена, какъ функція электродвижущей силы е, формулой вида
і -Ае Ве2 4- Се*........................(48)
гдѣ Л, В и С постоянныя, имѣющія, однако, для различныхъ экземпля-
ровъ пирометра неодинаковыя значенія. Если е выразить въ микроволь-
70
Термометрія.
тахъ (см. т. IV), то для одного экземпляра найдено, напримѣръ,
І = 13,76г - 0,004841г2 + 0,000001378г3
въ предѣлахъ отъ 400° до 1440°. Позже НоІЬогп и Ьал (1899 и 1900)
непосредственно сравнили элементъ Ье Сйаѣеііег съ газовымъ тер-
мометромъ; Ьіпдеск и Еоіііе (1900), а также Вау и АІІеп
(1904) изслѣдовали этотъ элементъ при высокихъ температурахъ.
Уголь вредно дѣйствуетъ на этотъ пирометръ; поэтому послѣдній
слѣдуетъ помѣщать въ фарфоровыхъ трубкахъ. Точность измѣренія до-
ходитъ до + 5° при 1000°. На рис. 29 показано внутреннее устройство пи-
рометра Ье Сііаѣеііег въ томъ "видѣ, который ему придали мастер-
скія Каізег’а и Зсйпіісіі’а въ Берлинѣ и Негаеиз’а въ Ганау
(Папай), по указаніямъ Н о 1 -
Іэ о г п’а и АѴ 1 е п’а. Одна изъ
проволокъ проходитъ черезъ ка-
пиллярную фарфоровую трубку;
кромѣ того обѣ проволоки окру-
жены фарфоровыми трубками.
Вмѣстѣ съ пирометромъ изгото-
вляется гальванометръ (ГАгзоп-
ѵаГя, шкала котораго непосред-
ственно даетъ температуру спая пирометра и доходитъ до 1500°.
Локи Мс. Сгае воспользовался элементомъ Ье Сйаіеііег
для опредѣленія точекъ плавленія цѣлаго ряда неорганическихъ солей.
Вскоепі^еб построилъ переносный пирометръ, состоящій изъ термо-
электрической пары Ье Гііаіеііег съ милливольтметромъ АѴ е 8 -
1 о п’а (т. IV). Ь ау и А Не п (1904) дошли до 1600°; Віетепз и
Наізке (1904) построили самопишущій термоэлектрическій пирометръ.
§ 15. Измѣреніе весьма низкихъ температуръ. Для измѣренія
тѣхъ весьма низкихъ температуръ, которыхъ нынѣ удалось достигнуть,
благодаря возможности ожиженія такихъ газовъ, какъ воздухъ, водо-
родъ и т. д., служатъ газовые термометры и термоэлектрическіе эле-
менты. АѴгоЫехѵзкі сравнивалъ показанія водороднаго термометра
и термоэлектрическаго элемента мѣдь-нейзильберъ при температурахъ 100°,
0°, — 102°,9 и — 131°; послѣднія двѣ температуры получаются въ жид-
комъ этиленѣ, когда онъ кипитъ при давленіи атмосферномъ и при да-
вленіи въ 30 мм. ртутнаго столба. Изъ этого сравненія онъ нашелъ,
что температура і и отклоненія гальванометра, которыя могли считаться
мѣрою электродвижущихъ силъ г, связаны уравненіемъ
І = 7,3256г — 0,12749г2 0,0073998г3 .... (49)
по виду и даже по расположенію знаковъ напоминающимъ уравненіе (48)
стр. 69. Величины г отрицательны, когда температура спая, слу-
жащаго для измѣренія температуръ ниже 0°, т.-е. ниже температуры дру-
гого спая нейзильберовой проволоки съ мѣдною проволокою, идущею къ
Измѣреніе низкихъ температуръ.
71
гальванометру. Принявъ формулу (49), XV г о Ы е лѵ 8 к і измѣрила, при
помощи водороднаго термометра и термоэлемента температуры жидкаго
кислорода и азота, кипящихъ при атмосферномъ давленіи, и нашелъ обо-
ими способами совершенно одинаковыя температуры : 184°, 1 и 193°,2.
Такимъ образомъ формула (49) вѣрна въ широкихъ предѣлахъ отъ + 100°
до — 190°. Ниже - 200° оба прибора дали несогласные результаты, и
XV г о Ъ1 е м 8 к і полагалъ, что невѣрный результатъ даетъ водородный
термометръ вслѣдствіе того, что температура — 200° близка къ той, при
которой водородъ можетъ находиться въ жидкомъ состояніи.
018 х е аѵ 8 к і пришелъ, однако, къ другому выводу, сравнивъ, между
собою газовые термометры, наполненные водородомъ, азотомъ, кислоро-
домъ и окисью азота. Послѣдніе три термометра дали при 150° по-
казанія, отличавшіяся отъ показаній водороднаго термометра не болѣе,
чѣмъ на 1° или 2°; между тѣмъ окись азота можно привести въ жидкое
состояніе при — 93°,5, кислородъ при — 118°,8 и азотъ при — 146°.
Отсюда слѣдуетъ заключить, что водородный термометръ и ниже 200°
даетъ вѣрные результаты. Остается, однако, важный результатъ, что
термоэлементомъ Си — нейзильберъ можно измѣрять температуры до —190°.
Тгаѵегв и Лаоиегой (1903) предложили пользоваться гелі-
емъ при измѣреніи весьма низкихъ температуръ. Они нашли, что во-
дородный термометръ показываетъ при температурѣ жидкаго кислорода
на ОД° меньше термометра съ геліемъ, полагая, что при 0° въ обоихъ
термометрахъ давленіе равнялось 1000 мм. Впрочемъ ОІехелѵекі еще
раньше (1896) сравнилъ термометры съ водородомъ и съ геліемъ; онъ
не нашелъ разности въ ихъ показаніяхъ до 210°.
ХѴіікоАѵекі построилъ приборъ для измѣренія весьма низкихъ тем-
пературъ ; главная часть прибора — посеребренная платиновая проволока
(діаметръ 0,06 мм., длина отъ 2 до 3 метровъ), электрическое сопротивле-
ніе которой опредѣляется. По сравненію съ водороднымъ термометромъ
составлена табличка сопротивленій 7? въ зависимости отъ температуры Г.
Вотъ нѣкоторыя числа:
і 7? 7?
50° 1105,9 100° 778,9
0° 1000,0 — 150° 661,5
50° 891,4 180° 588,0
7? выражено въ омахъ; ѴѴ і I к о лѵ 8 к і утверждаетъ, что точность измѣре-
ній доходитъ до о ’ 05°.
Категііп^к 0ппе8 (1897) воспользовался термоэлементомъ мѣдь-
нейзильберъ для измѣренія весьма низкихъ температуръ: показанія этого
элемента онъ тщательно сравнилъ съ показаніями водороднаго термометра.
Позже (1903) онъ воспользовался термоэлементомъ константанъ-
сталь и дошелъ до температуры въ 210°. В е лѵ а г (1905) изслѣдо-
валъ термоэлементъ нейзильберъ-платина при нижайшихъ дости-
72
Термометрія.
жимыхъ температурахъ, доходя до температуры въ 14,4° абс. (— 258,6°)
испаряющагося подъ низкимъ давленіемъ твердаго водорода. Онъ на-
шелъ, что при измѣреніяхъ этимъ термоэлементомъ температуръ въ пре-
дѣлахъ отъ 6° абс. до 35° абс. примѣнимо уравненіе вида Е=аТ-\-ЬТ2,
гдѣ Е - электродвижущая сила и Т — абсолютная температура, если
при этомъ одинъ спай находится въ кипящемъ водородѣ (20,5° абс.).
НоІЬогп и \Ѵіеп изслѣдовали зависимость между сопротивле-
ніемъ платиновой проволоки, а также между величиною е термоэлек-
тродвижущей силы пары желѣзо-константанъ и температурою і, указы-
ваемой водороднымъ термометромъ. Оказалось, что между 0° и — 190°
І = — 258,3 + 5,0567-ау 0,005855^2,
гдѣ выражено въ омахъ (для проволоки, которую они изслѣдовали).
Далѣе они нашли, что между 0° и — 190°
I = — 0,0178с - 0,0000008784с2,
гдѣ с выражено въ микровольтахъ (т. IV). ЬайепЪиг^ и Кгие^еі
пользовались трехчленнымъ уравненіемъ. Меіііпк (1905) нашелъ, что
до — 197° можно пользоваться трехчленнымъ уравненіемъ, которое, од-
нако, при еще болѣе низкихъ температурахъ оказывается непригоднымъ.
Реііаі (1901) воспользовался явленіемъ Пельтье (т. IV) для измѣренія
низкихъ температуръ.
Еоѣііе (1902) показалъ, что термометръ, содержащій продажный
пентанъ, весьма удобенъ для измѣренія низкихъ температуръ. Въ
позднѣйшей работѣ (1904) онъ сообщилъ результаты изслѣдованія этого
термометра. Оказалось, что онъ даетъ возможность измѣрять темпера-
туры около — 190° съ точностью до + 0,02°. йіеЬегі и КііЬп
изготовляютъ такіе термометры, которыми можно пользоваться до - 200°.
На возможность примѣненія нефтяного э ф и р а ѵ же было ука-
зано на стр. 46.
Жидкій воздухъ кипитъ, смотря по содержанію кислорода въ
немъ, между— 182°,4 и 195°,7, причемъ его плотность колеблется въ ши-
рокихъ предѣлахъ между 0,791 и 1,131. Вейп и КіеЪііг воспользова-
лись системою поплавковъ различной средней плотности, чтобы по из-
вѣстному способу (т. I) опредѣлять плотность, а слѣд. и температуру ки-
пящаго воздуха.
Обзоръ всѣхъ работъ по вопросу объ измѣреніи низкихъ темпера-
туръ (за время отъ 1890 до 1902 г.) составилъ Зііеагег.
§ 16. Термостаты. Терморегуляторами или термостатами называются
приборы, при помощи которыхъ поддерживаютъ въ данной, обыкновенно
жидкой средѣ опредѣленную заданную температуру въ теченіе необходи-
маго, иногда весьма продолжительнаго времени. Подробности объ устрой-
ствѣ термостатовъ можно найти, напр.. въ книгѣ О 8 і а 1 б , Наші- шій
НиеИзЬисй яиг АизіиеЬгшщ рЬузісо-сйетізсЪег Ме88ип<?еп. Ьеіргія 1893,
стр. 60—78.
Термостаты.
73
Вобепйіеіп изслѣдовалъ и подробно описалъ различные термо-
статы для температуръ между 100° и 700°. Ограничиваемся описаніемъ
одного изъ самодѣйствующихъ термостатовъ, регулирующихъ притокъ газа
къ горѣлкѣ, подогрѣвающей данную среду. Схема прибора изображена на
Рис. 31.
рис. 30. Въ подогрѣваемую среду, напр. въ сосудъ съ водой, подъ кото-
рымъ находится зажженная газовая горѣлка, помѣщается резервуаръ А,
наполненный съ воздухомъ и соединенный съ и — образной трубкой, въ
нижней части которой находится ртуть. Газъ протекаетъ изъ А черезъ
тонкую трубку, нижнее отверстіе а которой находится на небольшомъ раз-
стояніи отъ ртути, когда температура Т резервуара именно та, которую
желаютъ поддерживать. Черезъ трубку В газъ проходитъ къ горѣлкѣ.
Когда температура среды поднимается выше Т, то воздухъ въ Л расши-
ряется, ртуть въ правомъ колѣнѣ поднимается и закрываетъ отверстіе а
газоприводнои трубки. Чтобы горѣлка при этомъ не погасла, проводятъ
къ ней газъ еще черезъ другую трубку, снабженную краномъ, лишь чуть-
чуть открытымъ: такую трубку можно вставить между В и А. Когда
среда охлаждается до Г°, отверстіе а открывается и пламя горѣлки уве-
личивается. Дальнѣйшія работы о термостатахъ указаны вгь литературѣ.
Термостаты играютъ большую роль при бактеріологическихъ изслѣ-
дованіяхъ. Относящіеся сюда приборы (ГАг8-опѵаГя, ЬаиІепзсЫае-
§ег’а, АІішапіГа, Огнянникова (Врачъ№32,1890), К расильчика
(Апп. бе ГІП8І. Разіеиг. 3 р. 166, 1889), Курчинскаго (Врачъ № 30,
1892), КеісІіегГа и др. отчасти описаны въ книгахъ: Г ейсслеръ,
Курсъ клинической бактеріологіи, Спб. 1893, стр. 8—11 и Габричев-
скій, Руководство къ клинической бактеріологіи, Спб. 1893, стр. 59—63.
Если температура Т равна температурѣ кипѣнія какого-либо веще-
ства, то можно пользоваться термостатомъ А п (1 г е а е, изображеннымъ
на рис. 31 и помѣщаемымъ непосредственно въ данную среду. Упомя-
нутое вещество помѣщается въ закрытомъ колѣнѣ А надъ ртутью: когда
74
Термометрія.
температура среды дѣлается выше Г, то вещество закипаетъ, вслѣдствіе
чего отверстіе газоприводной трубки закрывается. При помощи этого тер-
мостата можно удерживать температуру постоянною въ предѣлахъ до 0°,04.
Коловратъ- Червинскій (1909) построилъ замѣчательный тер-
мостатъ для высокихъ температуръ; этотъ приборъ даетъ возможность
цѣлыми днями удерживать температуру до 1000° настолько постоянною, что
колебанія ея не превышаютъ 2°— 3°.
Кн. Голицынъ построилъ термостатъ, который даетъ возмож-
ность около 200° удерживать температуру постоянною въ предѣлахъ отъ
0,01° до 0,003°.
ЛИТЕРАТУРА.
Изъ общихъ сочиненій по термометріи укажемъ :
В Ф. Лугининъ. Лекціи о термометріи. Москва, 1892 (литографир.),
Н. Г. Егоровъ. Современное состояніе термометріи. Временникъ Главн. Палаты
Мѣръ и Вѣсовъ 2 р. 55, 1895.
Оиіііаите. Тгаііё ргаіідие де Іа ТЬегпаотёігіе (іе ргёсізіопз. Рагіз, 1889.
Статьи Вепоіі, Магек’а, Регпеі, Оиіііаите и СНарриів въ Тгаѵапх еі Мёш. ди
Вигеаи іпіегпаі. дез роідз еі тезигез 1—6 и 10
Статьи Регпеі, Зае^егь, ОитІісН’а и др. въ АЫіапсІІ. (іег рЬуз. іесііп. Кеісѣзап-
зіаіі 1, Вегііп, 1894.
УЛМо. Модегп Меіеогоіо^у. Глава II.
Къ § 1.
К. ІНотвоп (Ьогй Кеіѵіп). ЕдіпЬ. Тгапз. 20 р. 270, 1851.
Къ § 2.
Рерпаиіі. Мёш. бе ГАсад. 21 р. 168, 1847.
Карр. Аип. (1. РЬуз. (4) 5 р. 905, 1901; дисс. Коепі&зЪег^, 1901.
И. Лебедевъ. Временникъ Гл. Палаты Мѣръ и Вѣсовъ 4 стр. 57, 1ку«.
Міу. Ро^. Апп. ДиЪеІЬд. р. 82, 1874.
РидЪег^. Ро&&. Апп. 44 р. 119, 1838.
Ма^пив. Ро^. Апп. 55 р. 1, 1842.
Рескпа^еі. Ро^. Апп. 123 р. 155, 1864.
ѴѴеіпНоШ. Ргодг. а. Сйетпіігег ѲехѵегЬезсІшІо, 1873.
Р. СНарриів. Тгаѵаих- ди Виг. дез Р. еі Мез. 6, 1888; Ріііі. Ма§. (5) 50
р 433, 1900.
Регпеі. АЫіапсІІ. д. рКуз.-іесКп. КеісКзапзі. 1, 1894.
ОІвхегивЫ. \Ѵ. А. 31 р. 58, 1887.
А. Тоеріег. УѴ. А. 56 р, 609, 1895; 57 р. 325, 1896.
М. Тоеріег. УѴ. А. 57 р. 310, 1896.
Къ § 3.
Оиіііаите. Тгаііё ргаіідие де Іа ТЬегтотёігіе де ргёсізіоп Рагіз, 1889; Тгаѵ.
ди Виг. дез Р. еі Мез. 5 и 6.
Къ § 4 и 5.
Лермонтовъ. Вопросы Физики. 1907. р. 335.
Регпеі, Заерег ипд ОитІісН. АЫіапдІ. д. Рйуз.-ТесЬп. Кеісіізапзі. 1, 1894; Іпзіг.
15 р. 2, 41, 81, 117, 1895.
Литература.
75
Калибрированіе термометровъ:
Погре апй Киескег. Вер. оГ ВгіііеЬ Аяяое.. ёоиіііатріоп, 1882. Содержитъ об-
зоръ способовъ.
Веззеі. Рор\ц\ Апп. 6 р. 287, 1826.
Тіііезеп. СаіТе Верегі. 15 р. 285, 677, 1879. См. также Іпеіг. 15 р. 46, 1895.
Магек. СагГе Верргі. 15 р. 300, 1879; Тгаѵ. еі Мёт. (іи Виг. сіее Р. еі Мее. 2
р. 35; 4 р. 18; 5 р. 1.
А. ѵ. Оеіііпреп. Соггесііоп сіег ТЬегтотеіег. Вограі (Юрьевъ), 1865
\ѴИ(1. Вегісііі йЬ. сі. АгЬеііеп хиг ВеГогт сіег есіпѵеіх. ГТгтааеее. Хйгісіі, 1868.
Рогп. бсЬгій. сі. рііуе.-оекопот. Ѳее. хи Коепі^еЬег^. 13, 1872.
Неппегі. Тгаііё сіее Тісргтотёігее р. 184, 1758.
Вепоіі. Тгаѵ. еі Мёт. сіи Вигеаи сіее Р. еі Мее. 2 р. 35, 1882.
Вгоск. Тгаѵ. еі Мёт. сіи Вигеаи сіее Р. еі Мее. 5. 1886.
Г-жа Тарнаридеръ. Описаніе методовъ калибрированія термометровъ. Съ пре-
дисловіемъ Оиіііаите'ѣ. Москва, 1904.
Напзеп. АЫіапсіІ. 6. еаесііе. Оее. сі. \Ѵіее. 15, 1874.
Сагі. СагГе Верегі. 1.
Лермантовъ. Ж. Ф. X. О. 10 р. 244, 1878.
Къ § 6.
Іігіевеп. Ѵег^ІеісЬип^ сіег ОиескеіІЬегіКегт. Меігопотіесііе Веііга^е 3, Вегііп, 1881.
Нег^езеіі. Меіеого1о§\ Хіясііг. 14 р. 433, 1897.
Оиіііаите. Тгаііё сіе Іа ТЬегтотёігіе, р. 328
Воеііскег. Іпеіг. 8 р. 409, 1888.
Магсігіз. С. К. 124 р. 443, 189 < ; Хіесііг. рііуе. Сііет. 29 р. 1, 1899; 37 р. 553,
605, 1901 ; Лоигп. Йе рііуе. (3) 7 р. 573, 1898; 8 р 193, 1899.
Но#тапп. Іпеіг. 17 р. 257, 1897.
Къ § 7.
Ноііхтапп ЫеЫ^’е НапсіхѵоегіегЬисІі <1. СЪетіе, 7 р. 368.
ѴѴиеІІпег. ЬекгЬисЬ сі. Ехрегітепіаіркуяік, 2 р. 386, 1896 (5-ое изданіе); См. Ьап-
йоіі. ОатрГіепеіоп Ьотоіо^ег ѴегЬіпсІипр:еп, Вопп 1868.
Оиіііаите. беапсее сіе Іа 8ос. іг. сіе рііуе. 1891 р. 17.
Макіке. Іпеіг. 13 р. 85, 1893; 14 р. 76, 1894.
АЛат. Іпеіг. 27 р. 101, 1907.
Къ § 8.
Ткіезеп, 8с1іеІІ ипй 8еІІ. Іпеіг. 15 р. 433, 1895. •
Ре^паиіі. Мёт. сіе ГАсасі. 21 р. 239, 1847.
А. Ріегге. Апп. сі. сЫт. еі рЬуе. (3) 5 р. 427, 1842.
Кескпа&еі. Р\ Апп. 123 р. 115, 1864.
ѴЛеЬе ипй Воеіісігег. Іпеіг. 10 р. 233, 1890.
Скарриів. Тгаѵ. е( Мёт. сіи Виг. сіее Р. еі Мее. 6, 1888.
Магек. Іпеіг. 10 р. 283, 1890.
Тігіезеп, 8скееІ ип(І 8е11. Іпеіг 15 р. 433, 1895; \Ѵ. А. 58 р. 168, 1896.
ѴЛеЬе. Іпеіг. 10 р. 435 1890.
Огиеігтаскег. Іпеіг. 15 р. 250, 1895.
Ьетке. Іпеіг. 19 р. 33, 1899.
\Х/аі(Іпег и Г)іскіп8оп. Виіі. Виг. о! Яіапсі. 3 р. 663, 1907; Іпеіг. 28 р. 375, 1908.
Къ § 9.
Сга/і8. Сііет. Вег. 20 р. 709, 1887; Хаіигр (англ.) 26 р. 466, 1882.
ѴѴаІ/епііп. Виіі. сіе Іа Кое. ^ёоіо^. сіе Ргапсе 13 р 118, 1841—1842. С. В. 1840
р. 292: 1842 р. 63; Ро&ег. Апп. 57 р. 541, 1842.
8скеигег-Ке8іпег. С. В. 121 р. 553, 1895.
76
Термометрія.
Регпеі. АЬкапбІ. бег Веіскзапзіаіі 1 р. 14, 1894; Іпзіг. 15 р. 7, 1895.
Весктапп. Хізскг. Г. ркуз. Сііет. 2 р. 638, 1888; 15 р. 672, 1894; 21 р. 252,
1896; 40 р. 142, 1902; 44 р. 193, 1903; 51 р. 329, 1905.
Огиеіхтасііег. Іпзіг. 16 р. 171, 1896.
СІіарриІ8. Агсіі. бе 8с. ркуз. (3) 28 р. 293, 1892.
/оНу. Ро^. Апп. биЬеІЪ. р. 82, 1874.
ѴСкііе. Ргос. Асаб. оі Агі апб Йсіепсез 21 р. 1, 45, 1885.
КоИІгаизск. \Ѵ. А. 60 р. 463. 1897.
НоІЬогп. Апп. б. Ркуз. (4) 6 р. 255, 1901.
Ваийаіп. С. К. 133 р. 1207, 1901.
Ваіу апй Сііогіеу. Вегі. Вег. 27 р. 470, 1894.
ѴѴіеЬе. 2ізс1іг. б. Сгіазіпзігшп.-Іпбизігіе 4 р. 1, 1894.
МагМ.8. б. бе ркуз. (3) 4 р. 217, 1895.
Риіііег/огй. ЕбіпЬ. Тгап8. 3, 1794; ОіІЬегі’з Апп. 17.
Къ § 11.
Раітег. Ркуз. Веѵ. 21 р. 65, 1905.
$іетеп8. Ьиш. ёіесіг. 28 р. 602, 1888.
Вгаип. Еіекігоіескп. Хеіізскг. 1888 № 8.
Риіщ. АѴіеп. Вег. 98 р. 1502, 1889; Верегі. б. Ркуз. 26 р. 733, 1890; 27 р. 301, 1891.
Вегікеіоі. б. бе ркуз. (3) 4 р. 357, 1895; С. В. 120 р. 831, 1895; 126 р. 410, 1898.
Соіетап. Ргос. РЫ1. 8ос. (тіаз^охѵ. 15 р. 94, 1884.
Къ § 12.
Ваги8. Меззип^ кокег Тетрегаіигеп. Ьеіргщ, 1892 (Монографія, содержащая
всю литературу пирометріи).
Ваги8. Ьез рго&гёз бе Іа Ругошеігіе. Варр. рге88. аи Соп^гёз. іпіегпаі. бе р1іу8. I
р. 148, Рагіе 1900.
Ье Сігаіеііег еі Воийоиагсі. Ѵёеиге без іешрёг. ёіеѵёез. РагІ8 190о.
Регзоп. С. В. 19 р. 757, 1844.
МаИІке. Іпзіг 12 р. 402, 1892; 14 р. 73, 1894; Скет. Вег. 26 р. 1815, 1893.
ЫіеИІ8. б. Атег. Скет. 8ос. 16 р. 396, 1894.
Ии/оиг. С. В. 130 р. 775, 1900.
Роиіііеі. С. В. 3 р. 782, 1836.
Рерріаиіі. Веіаііоп без Ехрёгіепсез 1 р. 168, 1847.
Оеѵіііе еі Тгоозі. С. В. 45 р. 821, 1857; 49 р. 239, 1859; Апп. скіт. еі ркуз. (3)
58 р 257, 1860; Вегі. Вег. 1857 р. 73.
НоІЬогп и. Рау. \Ѵ. А. 68 р. 817, 1899; Апп. б. Ркпз. (4) 2 р. 505, 1900; Атег.
б. оі 8с. (4) 8 р. 165, 1899.
НоІЬогп и. Ѵаіепііпег. Вегі. Вег. 1906 р. 811.
Р. СКаррш.8. Ркіі. Ма^. (6) 3 р. 243, 1902.
Рерпаиіі. (§ 11, III). Апп. бе скіт. еі ркуз. (3) 63 р. 39, 1861.
V. Меуег. Вегі. Вег. 11 р. 1867,2253, 1878; 12 р. 1426, 1879; Віп^іег'з боигп. 231
р. 330, 1878; 232 р. 418, 1879.
Сга/І8. Каіиге (англ.) 26 р. 466, 1882.
Ьату. С. В. 69 р. 347, 1869 ; 70 р. 393, 1870; Біп&іег’з боигп. 194 р. 209, 1869;
195 р. 525, 1870.
Роиіііеі. С. В. 3 р. 782, 1836.
Ріопскоп. С. В. 102 р. 1454, 1886; Апп. скіт. еі ркуз. (6) 41 р. 33, 1887.
Ье Скаіеііег. С. В. 107 р. 862, 1888; 108 р. 1046, 1096, 1889; 111 р. 123, 1890.
Ріопскоп. (§ 11, VI), С. В. 108 р. 992, 1889.
Селивановъ. Ж. Ф X. О. 23 р. 152, 1891.
Оапіеі. боигп. ВоуаІ. 8ос. Ьопбоп 11 р. 309; Ркіі. Ма§. (2) 10 р. 191, 268, 297,
350, 1831 ; (3) 1 р. 197, 261, 1832.
Литература.
77
Ргіпзер. Ьопсіоп Тгапз. 1827; Апп. сЫт. еі рЬуз. (2) 41 р. 247, 1829; Ро^. Апп.
13 р. 576, 1828; 14 р. 529, 1828
Арроіі. МіііЬеіІ й. (ЗехѵегЬеѵегеіпз ги Наппоѵег, 1855 р. 345.
СаІІепсІаг. Ргос. Е. 8ос. 41 р. 231, 1886; Тгап8. К. 8ос. 178, А р. 161, 1887; 182,
А р. 119. 1891; РЫІ. Ма&. (5) 32 р. 104, 1891; 33 р. 2?0, 1892; 47 р. 191, 1898; 48
р. 519, 1899.
8іетеп$. РЫІ. Ма&. (5) 42 р. 150, 1871; Ргос. К. 8ос. 19 р. 443, 1871; Ріп&іег’з
Лоигп. 198 р. 394, 1В7О; 209 р. 419, 1873.; 217 р. 291, 1875.
Огі//іі1г8. Ргос. К. 8ос. 1890 (Декабрь); Тгапв. [К. 8ос. 179 р. 119, 1891.
НоІЪогп шиі ѴМеп. \Ѵ. А. 47 р. 107, 1892; 56 р. 360, 1895.
Вгаип. ЕІекігоіесЬп. ХізсЬг. 9 р. 421, 1888.
Веи'аг апсі Еіетіп^. РЫІ. Ма&. (5) 40 р. 97, 1870.
Тогу. РЫІ. Ма&. (5) 50 р. 421, 1900.
СНгее. Ргос. К. 8ос. 57 р. 3, 1900.
Е(кѵаг(І8. СопІгіЬ. ДеГГ. РЬуз. ЬаЬог. 2 №8; Ргос. Атег. Акай, о! Агіз апй 8с. 40
р. 549, 1905.
СатрЪеІІ. РЫІ. Ма^. (6) 9 р. 713, 1905.
Піе8еп. Іпзіг. 23 р. 363, 1905.
Р. СНарриіз и. Т. А. Нагкег. РЫІ. Тгапз. 194, А р. 37, 1900; Тгаѵ. еі Мёт. (іи
Вигеаи іпіегп. йез Р. еі Мезигез 12, 1900; *І. йе рЬуз. (3) 10 р. 20, 1901.
Нагкег. РЫІ. Тгапз. 203 р. 343, 1904; Ргос. Е. 8ос. 73 р. 217, 1904.
1гаѵег8 апй (шуег. ХізсЬг. Г. рііуз. СЬет. 52 р. 437, 1905.
НоІЬогп. Апп. (1. Рііуз. (4) 6 р. 242, 1901.
Неусоск апй Неѵіііе. Тгапз. Сііет. 8ос. 1895.
Иіск8оп. РЫІ. Ма&. (5) 44 р. 445, 1897. .
ѴѴаісІпег ипй Виг§е88. Рііуз. Ееѵ. 28 р. 467, 1909; Виіі. Виг. оі* 8іапй. 7 р. 1, 1911.
АррІеуапІ. РЫІ. Ма^. (5) 41 р. 62, 1896.
ѴѴаісІпег апй Маііогу. РЫІ. Ма&. (5) 44 р. 165, 1897.
Са^піагй-Ьаіоиг. С. К. 4 р. 28. 1837.
А. М. Меуег. Ро&&. Апп. 148 р. 287, 1873.
Оіапіагй. С. К. 78 р. 128, 1874; Ро^. Апп. 153 р. 158, 1874.
Іоіѵег Рге8іоп. РЫІ. Ма&. (5) 32 р. 58, 1891.
()шпке. V. А. 63 р. 67, 1897.
Тоіу. Ргос. К. ІгізсЬ. Асай. (3) 2 р. 98.
Ратзау апй Еитогр1іорои1о8. РЫІ. Ма&. (5) 41 р. 360, 1896.
Къ § 13.
Вегікеіоі. Апп. (1е сЫш. еі рііуз. (7) 26 р. 58, 1902.
РоиШеі. С. Е. 3 р. 782, 1836.
Весдиегеі. С. Е. 57 р. 681, 1863: Апп. сЫт. еі рііуз. (4) 1 р. 120, 1864.
Сгоѵа. С. Е, 87 р. 322, 979, 1878; 90 р. 252, 1880; Апп. сЫт. еі рііуз. (5) 19
р. 472, 1880; й. йе рііуз. (1) 8 р. 196, 1879.
Ѵіоііе. С. Е. 92 р. 866, 1204, 1881; 96 р. 1033, 1883; Апп сЫш. еі рііуз. (10)
р. 289, 1877.
Ье Скаіеііег. <1. сіе рііуз. (3) 1 р. 185, 1892.
Вехоіа. А. 21 р. 175, 1884.
Реіѵаг апсі ОІа(І8іопе. Сііет. Келѵз 28 р. 174, 1873.
Еіеѵех. Виіі. Асай. Е. йе Ве1&. (3) 7 р. 348, 1885.
НоІЪогп и. Неппцг. Вегі. Вег. 1905 р. 311.
ѴЦаппег. Рііуз. 2ізсЬг. 1 р. 226, 1900; 3 р. 112, 1901.
Нагітапп. РЬуз. Ееѵ. 19 р. 452, 1904.
ѴѴаппег. Апп. й. РЬуз. (4) 2 р. 141 1900.
Віечѵагі. РЬуз. Ееѵ. 13 р. 257, 1901 ; 15 р. 306, 1902; РЬуз. 2ізсЫ. 4 р. 1. 1902.
78
Термометрія.
Ьиттег и. Ргіп%8Ііеіт. Ѵегіі. а. а. рііуе. бее. 1 р. 230, 1899; 3 р. 36, 1901;
Рііуе. Хіескг. 3 р. 97, 233, 1901—1902.
НоІЬогп и, КигІЬашп. Вегі. Вег. 1901 р. 712; Іпеіг. 22 р. 55, 1902; Б. А. 10
р. 225, 1903.
8іе/ап. Вег. \Ѵіеп. Ак. 79, II р. 391, 1879.
Ьиттег и. Ргіпр8ііеіт Ѵегіі. аеиіесіі. рііуе. Ѳее. 5 р. 3, 1903.
8іеіѵагі. Рііуе. Кеѵ. 13 р. 257, 1901, 15 р. 306, 1902, Рііуе. 2іес1іг. 4 р. 1, 1902.
Ьиттег и. Ргіп^зііеіт. Ѵегіі. ЛеніесЬ. рііуе. Ѳее. 1 р. 230, 1899; 3 р. 36, 1901;
Рііуе. Яіесііг. 3 р. 97, 233, 1901 1902.
Ьиттег. Ѵегіі. аеиіесіі. рЬуе. Ѳее. 3 р. 142, 1901 ; Рііуе. Хіескг. 3 р. 219, 1902.
8сИи8іег. Аеігорііуе. Л. 21 р. 258. 1901.
Неггзргип^. Хіесііг. Г. хѵіее. Рііоіодтаріііе 3 р. 173, 1905.
МПІосИаи еі Еегу^ С. К. 143 р. 505, 570, 731, 1906; 146 р. 252, 372, 1908.
МіІІосНаи. Л. бе Р1іу8. (4) 6 р. 389, 1907; 8 р. 347, 1909.
СоЫеп8. Рііуе. Кеѵ. 24 р. 307, 1907.
Гольдгаммеръ. Апп. а. Рііуе. (4) 25 р. 905, 1908.
УѴіІ8Іпр и. 8скеіпег. РиЪІ. РоіеЛаш. оЪеегѵ. 19 № 1 (№ 56), 1909; Аеіг. Хасііг. 183
р. 97, 1909.
ѴѴіІ8Іп%. Аеігорііуе. Л. 32 р. 130, 1900.
ИогЛтапп. Г. К. 149 р. 557, 662, Ю38, 1909; 150 р. 448, 669, 1910.
Неррегрег. \Ѵіеп. Вег. 119 р. 197, 1910.
Ьитттег и. Ргіпр8кеіт. Рііуе. Хіесііг. 3 р. 234, 1902.
КигІЬаит. Рііуе. 7іес1іг. 3 р. 186, 332, 1902.
Негп8і. Рііуе. Хіесііг. 4 р. 733, 1903.
ѴѴагЬигр. Ѵегіі. аеиіесіі. рііуе. Ѳее. 1 р. 50, 1899.
Регу. С. К. 134 р. 977, 1201, 1902; Апп. сіііт. еі рЬуе. (7) 27 р. 433. 1902, Л. а.
рііуе. (4) 2 р. 97, 1903; 3 р. 32, 701, 104.
Рау апй Ѵап Озігаші. Аеігорііуе. 3. 19 р. 1, 1904.
ѴѴаісіпег апй Вигре88. Рііуе. Кеѵ. 19 р. 241, 1904.
Къ §14.
Ье Скаіеііег. С. К. 102 р. 819, 1886; Виіі. 8ос, сіііт. Рагіе 44 р. 482, 1886; 47
р. 2, 300, 1887 ; Л. ар рііуе. (2) 6 р. 23, 1887; 8ігіёте Соп^гёе, Іпаиеігіе аи §ае, Рагіе,
Іюнь 1888.
Ваги8. Меееип# Ііоііег Тетрегаіигеп, Ьеіргі^ 1892, р. 41—92; Ріііі. Мад. (5) 29
р. 141, 1890; 8І11. Лоигп. 39 р. 478, 1890.
НоІЬогп ипа УХ/іеп. \Ѵ. А. 47 р. 107. 1892; 56 р. 360, 1895.
Роиіііеі. С. К. 3 р. 782, 1836.
Ьоііу. Ріііі. Ма^. (3) 19 р. 391, 1841.
Рерпаиіі. Кеі. Лее Ехрёг. 1 р. 246 (1845, Рагіе 1847.
Ро8еііі. Апп. сЪіт. еі рііуе. (5) 17 р. 177, 1879.
Е. Весдиегеі. Апп. сіііт. еі рііуе. (3) 68 р. 49, 1863.
8скіпх. Ѳіп^іег’е Лоигп. 175 р. 85, 1865; 179 р. 436; 1866.
Таіі. Тгапе. К. 8ос. ЕЛіпЪ. 27 р. 125, 1872—73.
Вгаип. Ріііі. Ма$. (5) 19 р. 495, 1885.
Негаеи8 ипЛ КаІ8ег & 8скті(іі. Іпеіг. 15 р. 373, 1895.
НоІЬогп и. Рау. см. литературу къ § 12.
Ыпсіеск и. Роіке. Іпеіг. 20 р. 285, 1900.
Рау апй АІІеп. Рііуе. Кеѵ. 19 р. 177, 1904.
8іетеп8 и. НаІ8ке. Іпеіг. 24 р. 350, 1904.
Ьокп. Мс. Сгее. АѴ. А. 55 р. 95, 1895.
8скоепі]'е8. Агсіі. 8с. рііуе. (4) 5 р. 136, 1898.
Векп и. КіеЫіг. Апп. а. Рііуе. (4) 12 р. 421, 1903.
8кеагег. РЬуе. Кеѵ. 15 р. 243, 1902.
Объемъ твердыхъ тѣлъ.
79
Роіке. Іпзіг. 19 р. 143, 1899; 22 р. 192, 1902.
Реііаі. С. В. 133 р. 921, 1901.
Къ § 15.
ѴУгоЫе'Шзкі. АѴ. А 25 р. 371, 1885.
Оізгеѵѵзкі. \Ѵ. А. 31 р. 58, 1887.
Тгаѵег8 апй Зациегой. Ргос. К. Ьос. 70 р. 484, 1902; 2ізс1іг. Г. ркуз. Сііет. 45.
р. 385, 1903.
Ѵ(/'іікоі2)8кі. РЫ1. Ма&. (5) 41 р. 312, 1896.
Категііп^іі Оппез. 2ііііп#8ѵег8І. Коп. Акай. ѵ. \Ѵеі. Атзіегйат 1896—97, р. 37.
79; 12 р. 625, 1903; Сотт. ітот. іке ЬаЪ. Ркузісз, Ьеійеп № 27; ВеіЪІ. 21 р. 21, 1897,
НоІЬогп ипа Уіеп. Вегі. Вег. 1896 р. 673; XV. А. 59 р. 213, 1896; Іпзіг. 16 р. 344,
1896; 17 р. 142, 1897; 28 р. 759, 1904.
ЬайепЬиг^ и. Кгие^еі. Скет. Вег. 32 р. 1818, 1899.
Меіііпк. Ѵегзі. К. Ак. ѵоп ХѴеі. 1904—1905 р. 212, 221; Сотт. Рку&. ЬаЪ.
Ьеуйеп № 93.
Иетѵаг. Ргос. К. 8ос. 76 р. 316, 1905.
Векп и. КіеЫіх. Апп. й. Ркуз. (4) 12 р. 421, 1903.
81геагег. Ркуз. Веѵ. 15 р. 243, 1902.
Роіке. Іпзіг. 19 р. 143, 1899; 22 р. 192, 1902; 24 р. 47, 1904.
Реііаі. С. В. 133 р. 921, 1901.
Къ § 16.
АпЛгеае. XV. А. 4 р. 614, 1878.
Оитіісіг. Іпзіг. 18 р. 317, 1898.
Роіке. Іпзіг. 19 р. 143, 1899; 20 р. 14, 33, 1902.
Войепзіеіп. 2ізскг. ркуз. Скет. 30 р. 113, 1899.
бону. 3. йе рку8. (3) 6 р. 479, 1897.
ОзіимМ. Регіойізске Егзскеіпшщеп Ъеі йег Аиііоезип^ йе» Скготн. Аккапйі.
еаеске. Ѳез. 26 № 2 р. 40.
Саііігіп. 2ізскг. іиг сотргіт. и. Пиеззі^е (іазе 3 № 4.
УТеіпкоІД. Апп. й. Ркуз. (4) 5 р. 943, 1901.
Вгайіеу апЛ Вгочѵпе. й. ркуз. Скет. 6 р. 118, 1902.
Сеег. й. ркуз. Скет. 6 р. 85, 1902.
Коловратъ-Червинскій. й. йе Ркуз. (4) 8 р. 495, 1909; Іпзіг. 29 р. 295, 1909.
ГЛАВА ТРЕТЬЯ.
Зависимость размѣровъ и давленія тѣлъ отъ температуры.
§ 1. Температурные коеффиціенты размѣровъ твердыхъ тѣлъ. На
стр. 9 мы дали общую формулу (6) для средняго температурнаго коеффи-
ціента между двумя данными температурами и 4 и формулу (7,&) для
температурнаго коеффиціента при опредѣленной данной температурѣ
эти формулы относились къ произвольной физической величинѣ г, мѣня-
ющейся при заданныхъ добавочныхъ условіяхъ, въ зависи-
мости отъ температуры.
Обращаемся къ случаю, когда г представляетъ одну изъ величинъ,
опредѣляющихъ геометрическіе размѣры твердаго тѣла, т.-е. длину /,
80
Объемъ и давленіе тѣлъ.
поверхность 5 или объемъ ѵ. Добавочнымъ условіемъ обыкновенно явля-
ется въ этомъ случаѣ постоянство внѣшняго давленія, подъ которымъ тѣло
находится. Что же касается вліянія температуры на давленіе, произ-
водимое тѣломъ на окружающую его оболочку, т.-е. вліянія, упомянутаго
въ заголовкѣ этой главы, то мы будемъ разсматривать таковое только для
тѣлъ газообразныхъ и жидкихъ.
Мы предположимъ, что разсматриваемое твердое тѣло изотропно (т. I)
и слѣд. вліяніе температуры на линейные размѣры его не зависитъ отъ
направленія послѣднихъ. Случай анизотропнаго тѣла будетъ разсмотрѣнъ
впослѣдствіи. Положимъ, что /0 и Іі (или просто Л разстояніе при 0°
и /° двухъ точекъ твердаго тѣла, т.-е. то, что во многихъ случаяхъ мо-
жетъ быть названо длиною твердаго тѣла. Мы можемъ написать
/=/(0...........................(1)
Эмпирически можно эту функцію представить въ видѣ
/ = /0(1+Дг‘-|-5^-|-С/з + ...).............(2)
На основаніи общей формулы (6) стр. 9 имѣемъ для средняго
коеффиціента линейнаго расширенія выраженіе’
гдѣ 4 и 4 значенія длины I при температурахъ 4 и (2) и (3) даютъ
<ч,2 - А 4- В(4 4- 4) 4- С(і* + 44 +42) 4-................(4)
Если 4 = 0 и 4 = 4 то получаемъ для средняго коеффиці-
ента между 0° и /°
аі = А 4-В^4-а24-.....................(5)
Для коеффиціента линейнаго расширенія при /° имѣемъ на основа-
ніи (16) стр. 11
а = А 4- 2ВгД-ЗС/24- ...
(6)
что получается и изъ (4), если положить 4 —' 4 ^4 и потомъ Аіх = 0
и 4 -- 4 или проще 4 = 4 = Если коеффиціентъ а данъ, какъ функ-
ція температуры, а ~ /(I), въ частномъ случаѣ, вида
а = а0 4~ 4" <М2 +.........................(7)
то вообще
а въ частномъ случаѣ
I — /0? 1 4- 4~ 9
I 2
4- у асіі^.......................(8)
о.
«1^+1 «2^3+---1 . . . . (9)
о I
Объемъ твердыхъ тѣлъ.
81
Для удлиненія /2 — /15 соотвѣтствующаго повышенію температуры отъ
4
Д° 4» имѣемъ /2- 4 = /0
ай/, и въ частномъ случаѣ
4
4 — 4(4 4)
к
«о + 2 "Ь 4) + 3 «2(42+ 44 + 42) + • • •
Но сравненіе (9) и (2) показываетъ, что а0 = Л, = В, * а2 = С
и т. д., и потому (4) даетъ
4 4 — 4аі,з(4 4).........................(ю)
Полагая опять 4 = 0 и 4 = 4 получаемъ I — /0 = 4аЛ или
/ = 4(1 + «/)...........................(И)
Для поверхности 5 и для объема ѵ можно написать формулы, вполнѣ
аналогичныя формуламъ отъ (2) до (11), съ тою только разницею, что
вмѣсто различныхъ а появятся коеффиціенты или у поверхностнаго или
объемнаго расширенія. Для изотропной среды Д = 2а и у — За,
см. стр. 11. Иногда разсматриваютъ вмѣсто величинъ (16) и (18), стр. 11,
которыя перепишемъ такъ
величины
_____ I (11 1 йѵ
а____10 (1і ’ ? ѵ0 йі
, ___ 1 (11 ,____ 1 (ІѴ
а I М ' ? ѵ йі
....................(12)
....................(13)
Замѣтимъ, что если у' = За' = Сопйі., то получается
I = 10еа 1 \ ѵ — ѵ^еу *....................(14)
Относительно теплового расширенія твердыхъ тѣлъ мы сдѣлаемъ одно
важное замѣчаніе. Расширеніе твердаго однороднаго тѣла М (рис. 32)
происходитъ во всѣхъ его частяхъ совершенно свободно, безъ появленія
внутреннихъ натяженій или давленій. Такъ, напр., расширеніе мысленно
выдѣленной внутри тѣла части А не вызываетъ давленія на остальную
часть тѣла ВВВ. Это явствуетъ изъ того, что изъ однороднаго твердаго
тѣла можно при всякой его температурѣ, не слишкомъ близкой къ точкѣ
плавленія, искусственно выточить любую внутреннюю часть безъ измѣ-
ненія остальной части ВВВ (допускаемъ отсутствіе чисто техническихъ
трудностей). Еслибы при какой-либо температурѣ часть А давила на
часть ВВВ, то вынутіе части А повлекло бы за собою уменьшеніе по-
лости, чего, однако, не наблюдается. Отсюда слѣдуетъ, что масса ВВВ при
нагрѣваніи сама располагается въ томъ пространствѣ, которое на рисункѣ
КУРСЪ ФИЗИКИ О. ХВ О Л Ь С О Н А. т. III, изд. 3-е. 6
82
Объемъ и давленіе тѣлъ.
ограничено извнутри и извнѣ пунктиромъ, безъ понужденія со стороны
расширяющейся части А. Такое же совершенно измѣненіе массы ВВВ
было бы вызвано нагрѣваніемъ и въ случаѣ отсутствія части А. Изъ ска-
заннаго вытекаетъ, что если нагрѣвать полое тѣло, то по-
Рис. 32.
Рис. 33.
лостъ его расширяется настолько же. насколько она
расширилась бы, еслибы она была наполнена тѣмъ же
веществомъ, изъ котораго [состоитъ полое тѣло (обо-
л о ч к а). Мы уже неоднократно пользовались этимъ положеніемъ, начиная
со стр. 20.
§ 2. Методы опредѣленія коеффиціентовъ расширенія твердыхъ
тѣлъ.
I. Методъ Ь а р ] а с е’а и Ьаѵоійіет. Къ первымъ точнымъ
опредѣленіямъ линейнаго расширенія тѣлъ относятся измѣренія, произве-
денныя Ьаріасе’омъ и Ьаѵоізіет.
Рис. 34.
вленнаго на разстояніи 200
Ихъ методъ выясняется изъ схематическаго
рис. 33. Стержень кі, приготовленный изъ ис-
пытуемаго вещества, помѣщается на двухъ
валикахъ въ металлическій ящикъ, подъ ко-
торымъ находится печка. Конецъ к упи-
рается въ неподвижный вертикальный бру-
сокъ, не отмѣченный на рисункѣ. Ко-
нецъ I упирается въ вертикальный стер-
жень о/, неизмѣнно связанный со зритель-
ною трубою аЬ, могущей вращаться около
точки о. Черезъ эту трубу можно видѣть
дѣленія вертикальнаго масштаба, устано-
женіе котораго совпадаетъ съ нитью окуляра Ь,
м. отъ трубы и опредѣлить то мѣсто /, изобра-
Ящикъ, въ которомъ находится кі, наполняютъ тающимъ льдомъ, до-
водятъ оі до соприкосновенія съ кі, и дѣлаютъ отсчетъ на шкалѣ. Затѣмъ
ящикъ наполняютъ масломъ или водою и нагрѣваютъ жидкость до нѣко
торой температуры, которую опредѣляютъ при помощи ртутныхъ термо-
метровъ. Стержень кі, удлиняясь, перемѣщаетъ оі въ положеніе от, вслѣд-
ствіе чего и труба аЬ поворачивается около оси о на уголъ, равный Іот.
Наблюдатель видитъ теперь уже вмѣсто / другое дѣленіе 5 шкалы. Если
Объемъ твердыхъ тѣлъ.
83
удлиненіе Іт стержня кі обозначить черезъ Д то ясно, что /5 : Л=/о\ оі.
Удлиненіе /1 оказалось, такимъ образомъ, увеличеннымъ въ 744 раза. Зная
длину стержня, удлиненіе Л и повышеніе температуры, легко опредѣ-
Рис. 35.
лить средній коеффиціентъ расширенія между 0° и температурою і воды
или масла.
Самый приборъ изображенъ на рис. 34. Испытуемый стержень ле-
житъ на валикахъ, поддерживаемыхъ стеклянными брусками I. На от-
дѣльномъ рисункѣ о' представляетъ сѣченіе стержня, г валикъ. Одинъ
Рис. 36.
конецъ стержня упирается въ неподвижный брусокъ е\ другой же его
конецъ опирается на брусокъ ІЬ, вращающійся, вмѣстѣ съ трубою А,
около оси аа.
6*
84
Объемъ и давленіе тѣлъ.
Ьаѵоізіег и Ьаріасе опредѣлили при помощи этого прибора
коеффиціенты линейнаго расширенія различныхъ металловъ, а также раз-
личныхъ сортовъ стекла.
II. Методъ Коу и Ватзсіеп’а. Методъ Кашжіеп’а, кото-
рымъ въ 1784 г. воспользовался Еоу для опредѣленія коеффиціента рас-
ширенія мѣръ, служившихъ для англійскихъ градусныхъ измѣреній, за-
ключается въ слѣдующемъ. На крѣпкихъ ножкахъ установлены парал-
лельно другъ другу три ящика; крайніе ящики А и С (рис. 35)
остаются во время опытовъ наполненными тающимъ льдомъ, между тѣмъ
какъ въ средній В наливаются вода или масло, нагрѣваемыя до опредѣленной
температуры. Укороченный разрѣзъ средняго ящика изображенъ на рис. 36.
Въ каждомъ изъ трехъ ящиковъ помѣщенъ брусокъ, причемъ брусокъ въ
среднемъ ящикѣ В и есть тотъ, коеффиціентъ расширенія котораго тре-
буется опредѣлить. Къ его концамъ прикрѣплены объективы В' и В"
двухъ зрительныхъ трубъ; окуляры С и С" присоединены къ концамъ
бруска, находящагося въ ящикѣ С, между тѣмъ какъ на брускѣ въ А по-
мѣщены два кольца А' и Д", въ центрѣ которыхъ перекрещиваются нити,
освѣщенныя зеркальцами или собирательными стеклами. Значки А' и А”
и окуляры С и С" остаются во все время опыта неподвижными.
Брусокъ въ среднемъ ящикѣ В правымъ концомъ упирается въ осо-
бый механизмъ, дающій возможность, вращая головку винта У, нѣсколько
передвигать весь брусокъ по направленію его длины. На другомъ концѣ
имѣется масштабъ, ноніусъ и микрометренный винтъ, при помощи кото-
рыхъ можно перемѣщать объективъ В" въ сторону на опредѣленную ве-
личину, причемъ точность измѣренія доходитъ до 0,003 мм., что соста-
вляло приблизительно 1: ІО6 часть длины бруска (около 2 метровъ). На-
блюденія производились слѣдующимъ образомъ. Брусокъ въ В сперва тоже
окружался тающимъ льдомъ, и затѣмъ при помощи винта и микроме-
тра с/сі объективы В' и В" устанавливались такъ, чтобы точки пересѣче-
нія нитей А' и А" совпадали съ вертикальными нитями окуляровъ С'
и С". Затѣмъ наливали въ ящикъ В жидкость и нагрѣвали ее до
опредѣленной измѣряемой температуры і; брусокъ въ В удлинился, объ-
ективъ В" сдвинулся налѣво и вмѣстѣ съ нимъ изображеніе нитей А"
въ фокальной плоскости окуляра С" сдвинулось также налѣво. Нѣкото-
рое, хотя и весьма малое смѣщеніе изображенія произошло и въ оку-
лярѣ С\ такъ какъ объективъ В' находился не на самомъ концѣ бруска.
При помощи винта приводятъ сперва пересѣченіе нитей А' на нить
окуляра С' и затѣмъ уже перемѣщаютъ объективъ В" направо, пока и
въ окулярѣ С' пересѣченіе нитей значка А" не совпадетъ съ верти-
кальной нитью окуляра С", Величина, на которую приходится сдвинуть
объективъ В", и которая измѣряется микрометромъ с/(1, равна удлиненію
части бруска, находящейся между вертикальными плоскостями, проходя-
щими черезъ оптическія оси обѣихъ зрительныхъ трубъ. Зная длину
этой части бруска, удлиненіе и температуру /, уже легко получить сред-
ній коеффиціентъ линейнаго расширенія между 0° и /°.
Объемъ твердыхъ тѣлъ.
85
III. Методъ Гиезз’а и СгІаігеГя. Интересенъ приборъ, по-
строенный механикомъ Р и е 8 8’омъ, при помощи котораго (11 а і г е 1
опредѣлялъ коеффиціенты расширенія различныхъ твердыхъ тѣлъ. Вер-
тикальный стержень изъ испытуемаго вещества помѣщается внутри мѣд-
ной трубки, окруженной сосудомъ, въ которомъ можно быстро мѣнять
температуру, пропуская струю пара или струю воды. Стержень опира-
ется снизу на микрометренный винтъ, а сверху на короткое плечо ры-
чага, длиннымъ плечомъ котораго является стрѣлка, остріемъ своимъ ука-
зывающая на дѣленія вертикальной дуговой шкалы. При помощи микро-
метреннаго винта перемѣщаютъ стержень послѣ каждаго нагрѣванія или
охлажденія въ такое положеніе, чтобы стрѣлка указывала на нуль дѣле-
нія. Число оборотовъ головки микрометреннаго винта опредѣляетъ иско-
мое измѣненіе длины стержня.
IV. Методъ дифференціальный. В о г (1 а, изучая стержни,
служившіе для французскихъ градусныхъ измѣреній, воспользовался спо-
собомъ, предложеннымъ В е - Ь и с’омъ. Платиновый стержень АВ (рис. 37),
длиною въ 12 футовъ, расположенъ рядомъ съ мѣднымъ А'В'. На АВ
имѣется шкала дѣленій, на А'В' ноніусъ къ этой шкалѣ. Концы А и А со-
единены неподвижно. При нагрѣваніи мѣдь сильнѣе расширяется, чѣмъ
платина, конецъ В' скользитъ вдоль АВ, и отсчетъ на ноніусѣ мѣняется.
Такіе отсчеты производились при 0° и при 100°. Зная коеффиціентъ расшире-
нія платины, можно отсюда опредѣлить коеффиціентъ расширенія мѣди.
Этимъ способомъ воспользовались В и ] о п § и Реііі, изучая тепловое
расширеніе различныхъ тѣлъ; длина стержней въ ихъ опытахъ равня-
лась только 1,2 м. •
V. Методъ вѣсового термометра. Въ § 10 предыдущей
главы, стр. 17, мы познакомились съ вѣсовымъ термометромъ и показали,
какимъ образомъ онъ можетъ служить для измѣренія температуры і, когда
извѣстны средніе коеффиціенты кубическаго расширенія а/ и между 0°
и /° жидкости (ртути), которою термометръ наполнялся, и вещества
Рис. 37.
(стекла), изъ котораго онъ самъ сдѣланъ; для этого служатъ формулы
(28) или (31) стр. 48 и 49. Допустимъ, однако, что коеффиціентъ расшире-
нія жидкости былъ опредѣленъ какимъ-либо способомъ, и что мы из-
мѣряемъ температуру і, до которой приборъ нагрѣвается, при помощи
другого термометра, напр. воздушнаго: тогда манипуляція, описанная на
стр. 48, дастъ намъ коеффиціентъ кубическаго расши-
ренія оболочки на основаніи формулы (27) стр. 48.
Р( (1 + іа() = Ро (1 + ................(15)
86
Объемъ и давленіе тѣлъ.
въ которой Ро и Р/ вѣса ртути, наполняющей приборъ при 0° и
Формула (15) даетъ
Рі (1 + — Ро
Л— р„<
(16)
Рис. 38.
Приборъ, по устройству тождественный съ вѣсовымъ термометромъ, •
можетъ однако служить и для опредѣленія коеффиціента кубическаго
расширенія всякаго твердаго
тѣла, если его можно помѣ-
стить внутри прибора (какъ
это показано на рис. 38), при-
давъ ему форму цилиндра или
параллелепипеда. Вѣсъ р этого
тѣла и его плотность при 0°
должны быть извѣстны, равно какъ и коеффиціенты и расширенія
ртути и стекла ; изъ нихъ опредѣляется предварительно вышеизложен-
нымъ способомъ для даннаго сорта стекла. Обозначимъ опять черезъ Ро
и Р* вѣсъ ртути, наполняющей при 0° и свободное пространство вну-
три прибора, и черезъ <50 плотность ртути при 0°. Объемъ прибора, за-
п р
нятый испытуемымъ тѣломъ и ртутью при 0°, равенъ а слѣд.
«о о0
при /° этотъ объемъ дѣлается равнымъ
ІР
\^0
+ Г°) (ім
Онъ теперь наполненъ объемомъ тѣла и оставшеюся въ приборѣ
ртутью, вѣсъ которой равенъ Рѵ Объемъ тѣла при равенъ ? (1 + х^),
гдѣ Лу искомый средній коеффиціентъ кубическаго расширенія тѣла между 0°
р
и /°; объемъ ртути равенъ 1 С1 ~Ь «/)• Мы имѣемъ слѣдующее равенство :
IР ^о\ Р
Р й В1 = /7 О + хі^ 4“ Л (1 + а/О • • (17)
\и0 ѵ0 / и0
изъ котораго и опредѣляется искомая величина Этимъ способомъ
пользовались Р п 1 о п и Реііі при опредѣленіи коеффиціентовъ куб.
расширенія различныхъ металловъ. Ртуть можно замѣнить и другою
жидкостью.
VI. Способы Маіійіе8еп’а и Корр’а. Мы узнаемъ коеф-
фиціентъ кубическаго расширенія твердаго тѣла, если опредѣлимъ его
плотность при различныхъ температурахъ, ибо плотность обратно про-
порціональна объему, занятому даннымъ количествомъ вещества. Плот-
ности и при 0° и /° связаны равенствомъ
х/ __ _
і 1 -|- и/
(18)
Обеъмъ твердыхъ тѣлъ.
87
гдѣ средній между 0° и 1° коеффиціентъ кубическаго расширенія. На
этомъ основаны методы МаііЬіевеп’а и Корр’а. МаііЬіевеп
поступалъ слѣдующимъ образомъ. ("перва онъ опредѣлилъ коеффиціенты ли-
нейнаго расширенія стеклянныхъ стержней и затѣмъ, по способу Ѵрхимеда,
пользуясь кусками того же стекла, плотность воды при различныхъ тем-
пературахъ. Наконецъ онъ опредѣлялъ потерю вѣса испытуемыхъ тѣлъ
въ водѣ, нагрѣтой до различныхъ температуръ, т.-е. по способу Архи-
меда опредѣлялъ плотность этихъ тѣлъ при различныхъ температурахъ.
Корр опредѣлялъ плотность цѣлаго ряда металловъ, минераловъ и
стеколъ при различныхъ температурахъ по способу флакона, примѣнен-
ному для твердыхъ тѣлъ.
ЛІІ. Методъ Еіхеан. Остроумный методъ Рігеаи, нынѣ
получившій широкое примѣненіе благодаря работамъ Вепоііи А Ъ Ь е,
основанъ на принципѣ, который будетъ понятенъ изъ рис. 39, пред-
ставляющаго приборъ Р і 2 е а и въ простомъ видѣ. Три винта, изъ кото-
рыхъ на рис. изображены только два и которые нынѣ дѣлаются изъ сплава
платины съ 10% иридія, проходятъ черезъ круглую пластинку близъ ея
краевъ, составляя треножный столикъ, на который кладется тѣло, ли-
нейный коеффиціентъ расширенія котораго требуется опредѣлить. На
верхніе тупые концы винтовъ кладется 'сте-
клянная пластинка, причемъ длина винто-
выхъ ножекъ, расположенныхъ выше столика,
регулируется такимъ образомъ, чтобы между
нижнею поверхностью стеклянной пластинки
и верхнею поверхностью тѣла оставался тон-
кій слой воздуха. Эта поверхность тѣла шли-
фуется не вполнѣ плоскою (въ первоначаль-
номъ методѣ Р і 2 е а и), но напр. нѣсколько выпуклою. Если освѣтить при-
боръ сверху однороднымъ (монохроматическимъ) свѣтомъ, то въ тонкомъ
слоѣ воздуха обнаруживаются интерференціонныя полосы, напр. въ видѣ
колецъ Ньютона, если поверхность тѣла выпукла въ серединѣ; въ об-
щемъ случаѣ эти полосы представляются въ видѣ темныхъ и свѣтлыхъ
кривыхъ линій. Когда поверхности стекла и тѣла совершенно плоски,
но не вполнѣ параллельны другъ другу, то полосы представляютъ пря-
мыя линіи, параллельныя другъ
плоскостей.
Темная полоса получается
Л
воздуха равна т , гдѣ т цѣлое
Хи
другу и прямой пересѣченія двухъ
въ тѣхъ мѣстахъ, гдѣ толщина сі слоя
число и Л длина волны взятаго одно-
роднаго свѣта; для сосѣдней полосы, находящейся по одной сторонѣ отъ
нея, слѣдуетъ вмѣсто т взять т — 1, а для сосѣдней по другой сто-
ронѣ т + 1. Если температура і станетъ возрастать, то толщина сі слоя
воздуха измѣнится на величину Д равную разности линейныхъ расши-
реній винтовыхъ ножекъ, выступающихъ выше столика, и тѣла, поло-
женнаго на столикъ. Вслѣдствіе постепеннаго измѣненія толщины сі бу-
88
Объемъ и давленіе тѣлъ.
детъ происходить непрерывное перемѣщеніе всей системы полосъ по на-
правленію отъ тѣхъ мѣстъ, гдѣ <1 больше, къ тѣмъ мѣстамъ, гдѣ сі меньше,
если сі при нагрѣваніи увеличивается; если же сі при нагрѣваніи умень-
шается, т.-е. если тѣло сильнѣе расширяется, чѣмъ ножки, то движеніе
полосъ произойдетъ въ обратную сторону. Если сосчитать число М по-
лосъ, проходящихъ при нагрѣваніи прибора отъ /°г до мимо какого-
либо значка, нанесеннаго на нижнюю поверхность стекла или мимо точки
пересѣченія нитей окуляра зрительной трубы, служащей для наблюденія,
то нетрудно найти искомый коеффиціентъ линейнаго расширенія а тѣла.
Пусть коеффиціентъ линейнаго расширенія винтовыхъ ножекъ равенъ 3
(мы увидимъ ниже, какъ онъ опредѣляется); длину винтовыхъ ножекъ
отъ поверхности стола обозначимъ черезъ А; высоту изслѣдуемаго тѣла
черезъ /; очевидно Ь немногимъ больше I. Наконецъ положимъ, что тем-
пература измѣнилась на т° = — іг. Измѣненіе Л толщины сі очевидно
равно Л/отсюда ясно, что
+ л = + — Іат.................(19)
Хи
откуда и опредѣляется искомое а. Знаки + показываютъ, что равно
Хи
правой сторонѣ формулы (19) или обратной разности Іат Ь^т, смотря
по тому, которая изъ нихъ положительна.
Если пользоваться желтымъ свѣтомъ натріевой горѣлки, то =
Хи
= 0,000294 мм.; такое измѣненіе толщины сі уже вызываетъ перемѣщеніе
полосъ, при которомъ одна полоса становится на мѣсто сосѣдней. Мы
можемъ однако наблюдать перемѣщеніе полосъ на 0,1 ихъ взаимнаго раз-
стоянія; отсюда слѣдуетъ, что величина Л можетъ быть опредѣлена съ
точностью до 0,00003 мм. Е і г е а и размѣстилъ на поверхности стекла
10 точекъ, Вепоіѣ 25 точекъ, служившихъ для точнаго опредѣленія
малыхъ перемѣщеній цѣлаго ряда полосъ. Среднее изъ всѣхъ измѣреній
давало величину перемѣщенія полосъ до дробной части ихъ взаимнаго
разстоянія.
Формула (19) не вполнѣ точна, такъ какъ при выводѣ ея мы не
приняли во вниманіе, что съ измѣненіемъ температуры мѣняется длина
волны 2 въ воздухѣ. Поправку на это обстоятельство ввести не трудно.
Для опредѣленія величины поднимаютъ столикъ выше и наблю-
даютъ интерференціонныя полосы, появляющіяся между поверхностью
столика (на которое никакое тѣло не положено) и нижнею поверхно-
стью стекла.
Вепоіі подвергъ методъ Еігеаи весьма тщательному изученію
и во многомъ его усовершенствовалъ; онъ изложилъ результаты своихъ
работъ въ двухъ обширныхъ сочиненіяхъ.
Для средняго коеффиціента линейнаго расширенія винтовъ изъ
Объемъ твердыхъ тѣлъ.
89
сплава Рі и 10% /г онъ находитъ
а, = (8539,6 + 2,298/) 10 “9. '
Весьма большой интересъ представляетъ методъ Р і ъ е а и въ той
формѣ, которую ему придалъ АЪЬе. Приборъ АЪЬе былъ описанъ, а
впослѣдствіи (1898) и усовершенствованъ РиИгісЪ/омъ; АЬЬе поль-
зуется двумя или тремя сортами лучей, испускаемыми свѣтящейся Гейс-
леровой трубкой и имѣющими различныя длины волнъ. Это даетъ ему
возможность избѣжать утомительнаго счета полосъ, проходящихъ мимо
значковъ, пока нагрѣвается приборъ, т.-е. втеченіе иногда нѣсколькихъ
часовъ. По методу АЬЬе достаточно измѣрить при температурахъ
и 4 разстояніе значка отъ ближайшей середины между двумя полосами
для двухъ или, лучше, для трехъ различныхъ А.
Не имѣя возможности входить въ дальнѣйшія подробности, ограни-
чиваемся краткимъ описаніемъ устройства прибора АЬЬе. Интерференці-
онный приборъ изображенъ на рис. 10. О представляетъ пластинку изъ
испытуемаго вещества; Р стеклянная пластинка, плоскости которой не
вполнѣ параллельны (уголъ между ними 20х), вслѣдствіе чего лучи, пада-
ющіе сверху перпендикулярно къ нижней сторонѣ пластинки и отразив-
шіеся отъ верхней стороны, отклоняются въ сторону и не примѣшива-
ются къ интерферирующимъ лучамъ, отраженнымъ отъ нижней поверх-
ности пластинки Р и отъ верхней тѣла О. Значкомъ служитъ посере-
бренный кружокъ т. На рис. 41 показанъ вертикальный разрѣзъ
черезъ весь приборъ, а внизу горизонтальный разрѣзъ верхней его
части. Интерференціонный приборъ Т находится внутри сосуда 6, тем-
пература котораго можетъ быть измѣнена. Лучи Гейслеровой трубки А
отражаются призмочкой р по направленію /
вертикально внизъ при помощи призмъ Рг
и Р2. На обратномъ пути они попадаютъ въ
зрительную трубу Р\ которая и служитъ для
наблюденія интерференціонныхъ полосъ. Эти
полосы представляютъ систему параллельныхъ
другъ другу прямыхъ, такъ какъ слой воз-
духа между Р и О (рис. 40) ограниченъ двумя
плоскостями, которыя располагаютъ не вполнѣ
параллельно другъ другу (т. II).
Приборомъ АЬЬе пользовались, кромѣ
РиНгісЬ’а, еще АѴеійтапп, Кеітегсіез,
8 с Ь е е 1 и др. Въ послѣднее время АЬЬе
ввелъ новое усовершенствованіе, замѣнивъ столикъ полымъ цилиндромъ,
вырѣзаннымъ изъ кварца параллельно оптической оси. Высота цилиндра
(вѣрнѣе кольца) 10 мм., внутренній діаметръ 25 мм. Онъ лежитъ на
пластинкѣ изъ кварца и таковая же служитъ ему крышкой. Внутри
кольца помѣщаются испытуемыя пластинки. Остальное понятно изъ пре-
дыдущаго. Новыя работы по вопросу о расширеніи кварца будутъ раз-
и затѣмъ направляются
Рис. 40.
90
Объемъ и давленіе тѣлъ.
смотрѣны ниже. 8сЬее1 (1904) и Аугез (1905) присоединили къ
этому аппарату особое приспособленіе, позволяющее производить измѣре-
нія также и при температурѣ жидкаго воздуха.
Т п і I о п помѣстилъ на верхнюю поверхность испытуемаго тѣла
пластинку изъ алюминія, толщина которой около 0,4 длины винтовъ, рас-
положенныхъ надъ столикомъ. Въ этомъ случаѣ расширеніе пластинки
и винтовъ одинаковое, такъ что смѣщеніе интерференціонныхъ полосъ
вызывается только расширеніемъ испытуемаго тѣла.
Могіеу и Во^егв измѣряли тепловое расширеніе металличе-
скихъ стержней, пользуясь интерференціоннымъ способомъ, напоминаю-
щимъ способъ Місііеізоп’а съ которымъ мы познакомились въ т. П.
Рис. 41.
§ 3. Результаты измѣренія расширенія твердыхъ тѣлъ. Сопоста-
вимъ нѣкоторые результаты измѣреній, произведенныхъ надъ изотроп-
ными твердыми тѣлами тѣми методами, которые были разсмотрѣны
въ § 2.
Первый, опредѣлявшій коеффиціентъ расширенія въ зависимости отъ
температуры, былъ Наіізігоет; онъ выразилъ длину стержней изъ
стекла и изъ желтой мѣди въ видѣ эмпирической функціи вида (2) стр. 80,
изъ которой, какъ мы видѣли, легко получается и коеффиціентъ расши-
ренія а въ видѣ (6) или, что то же самое, (7) стр. 80.
Расширеніе твердыхъ тѣлъ.
91
МаНкіезеп опредѣлилъ постоянныя А и В формулы (2) для цѣ-
лаго ряда металловъ; это даетъ возможность опредѣлить средніе коеффи-
ціенты линейнаго расширенія п100 между 0° и 100°.
Ье С Ь а 1 е 1 і е г опредѣлилъ средній коеффиціентъ линейнаго расши-
ренія между 0° и высокой температурой Т\ приводимъ нѣко-
торыя числа для сравненія съ числами а40 найденными Рігеап,
1О7а4о 107а^ т
Мягкое желѣзо 120 145 1000°
Мѣдь 170 200 1000°
Никкель .... 127 182 1000°
Платина .... 90 113 1000°
Алюминій . . . 231 315 600°
Ьётегау (1900) указалъ на то, что произведеніе а7\ гдѣ Т аб-
солютная температура плавленія, имѣетъ приблизительно оди-
наковое значеніе (около 0,02) для большинства металловъ. На суще-
ствованіе подобной зависимости указывали уже раньше Рісіеі и позже
РапауеП (1905).
Ѳіаігеі нашелъ, что если металлическій стержень изъ продажнаго
(тянутаго) матеріала многократно нагрѣвать и охлаждать, то
первыя нагрѣванія даютъ слишкомъ малыя, а первыя охлажденія слиш-
комъ большія числа для коеффиціентовъ а/. Эти числа идутъ какъ бы
другъ другу навстрѣчу и лишь послѣ многихъ нагрѣваній и охлажденій
они дѣлаются между собою равными. Такъ для стали первое нагрѣваніе
дало а - 0,00101, первое охлажденіе а 0,00132: третье охлажденіе
а = 0,00129, четвертое нагрѣваніе а = 0,00122. Объясняется это вну-
треннимъ натяженіемъ, вызваннымъ способомъ приготовленія проволоки и
существующимъ въ ней стремленіемъ къ уменьшенію длины.
НоІЪогп’и Вау произвели (1900) весьма тщательное опредѣленіе
коеффиціентовъ расширенія Рі, Рсі, А& №, стали, Константина (сплавъ)
и сплава Рі - ./г; такое же опредѣленіе произвелъ 8сЬееі (1902) для
Рі, Р&, фарфора, іенскаго стекла 59ЙІ (боросиликатъ) и кварца, бсііееі
получилъ слѣдующі е результаты :
Рі ... 4 = /0(1 + 8,806 .10 Ч + 0,00195 . 10 V2).
Рсі . . . Ц = /0(1 + 11,612 .10 Ч + 0,00323 . 10 6/2).
Стекло 59ІП . . . Ц = /0(1 + 5,608 . 10“Ч + 0,00290 . 10 V2).
Въ послѣднее время появилось большое число работъ по вопросу о
тепловомъ расширеніи тѣлъ при низкихъ температурахъ. Этимъ
вопросомъ занимались Аутез (1905, Л/, А§), бііеагег (1905, Л/), Во-
гезу (1906—1908, Аи, Си, Л^, 5/?, Ссі, Ві, Ре, Рі, 8п, РЬ, 8е, Хп стекло
и др.), Неппіп^ (1907, металлы, сплавы, стекла), 8с1іее1 и Неизе
(1907, Рі), Каштегііп^іі Оппез и Сіау (1907, Рі), 8сЬее1
(1907. Рі, Рсі) и др. Вообще говоря, а уменьшается съ пониженіемъ тем-
пературы; но во многихъ случаяхъ найдены разнаго рода неправиль-
ности, напр. максима или минима величины а. Большую роль играетъ?
92
Объемъ и давленіе тѣлъ.
несомнѣнно, чистота изслѣдованнаго матеріала. Такъ, напр., ІЭотзеу
.нашелъ сперва для Аи четыре максима и четыре минима величины а;
но впослѣдствіи оказалось, что для вполнѣ чистаго Аи величина а мѣ-
няется плавно.
Весьма тщательное изслѣдованіе зависимости а отъ температуры и
давленія для металловъ произвелъ Пг ііпеІ8 еп (1910). Онъ изслѣдовалъ
примѣнимость формулы
аѵ = дъ...........................(22, а).
аі
которую далъ ТЬіезеп (1908, и е постоянныя, Т абсолютная темпе-
ратура). Онъ нашелъ, что е періодическая функція атомнаго вѣса, мак-
сима которой совпадаютъ съ минима величины а и съ максима атом-
наго объема.
Результаты изслѣдованія расширенія кварца будутъ изложены ниже.
ВаЫапіег изучалъ вліяніе растяженія металлическихъ
проволокъ на ихъ коеффиціентъ линейнаго теплового расширенія; оказы-
вается, что этотъ коеффиціентъ увеличивается, если проволоку под-
вергать натяженію. ЬаЫаікіег показалъ однако, что это измѣненіе
является прямымъ слѣдствіемъ уменьшенія модуля Юнга (т. I) т.-е. уве-
личенія растяжимости при повышеніи температуры. Если нагрѣть натя-
нутую проволоку, то къ удлиненію отъ нагрѣванія прибавляется удлине-
ніе вслѣдствіе увеличившейся растяжимости, что и даетъ кажущееся уве-
личеніе коеффиціента расширенія. ВаЫапйег даетъ слѣдующую формулу
Р I 1
«9 - О-'— I
8(і-і)\Ее
1 \
Еі)
(21)
которую легко вывести. Въ ней средній коеффиціентъ расширенія
между температурами і и I' для проволоки ненатянутой, для про-
волоки натянутой грузомъ Р: 8 площадь поперечнаго разрѣза проволоки;
и Еу модули Юнга при температурахъ [ и і'. Ясно, что а2 > сср
если Еу «С Е*.
81оііе (1907) далъ теоретическую формулу
1 +
(іа
(ір
(і-Нп
(22, Ь)
Здѣсь р натяженіе при постоянной температурѣ і\ 4 температура
плавленія, с температурный коеффиціентъ модуля всесторонняго сжатія (т.Г).
Замѣчательную особенность представляетъ каучукъ. Натянутая
каучуковая полоска или трубка укорачивается при нагрѣваніи, т.-е. ея ко-
еффиціентъ линейнаго расширенія а по направленію растяженія
отрицателенъ. Это явленіе открылъ ѣ о и 1 е. Если черезъ сильно растя-
нутую каучуковую трубку пропустить струю горячаго пара, то она укора-
чивается на замѣтную величину. Взегкеп показалъ, что даже при
сравнительно небольшомъ натяженіи, когда удлиненіе равно 0.1 перво-
Расширеніе твердыхъ тѣлъ.
93
начальной длины, коеффиціентъ «уже отрицателенъ, а именно а= — 0,00012.
Когда длина увеличена въ 2,3 раза противъ нормальной, то а = — 0,00051.
Еслибы можно было приложить формулу (21) ВаЫапсІег’а къ каучуку,
для котораго а9 < а19 ибо > 0, а2 < 0, то пришлось бы заключить,
что для каучука^/ > ЕІ9 т.-е. что модуль Юнга растетъ съ температурою.
Но опыты Кпввпег’а показали, что удлиненіе каучука, натянутаго гру-
зомъ, значительно увеличивается вмѣстѣ съ температурою. Отсюда ясно,
что модуль Юнга, какъ и слѣдуетъ ожидать, съ повышеніемъ темпера-
туры уменьшается и что слѣд. формула О а Ы а п сі е г’а къ каучуку не-
примѣнима.
Дѣло разъясняется опытами Лебедева, который нашелъ, что плот-
ность растянутаго каучука съ повышеніемъ температуры уменьшается,
несмотря на уменьшеніе его длины. Отсюда слѣдуетъ, что натянутый
каучукъ имѣетъ положительный коеффиціентъ расширенія по напра-
вленію, перпендикулярному-къ его длинѣ, т.-е. къ направленію растяги-
вающей силы. Это указываетъ, что растянутый каучукъ есть тѣло ани-
зотропное, такъ что его можно было бы разсматривать въ слѣдующемъ
§ 4, гдѣ мы встрѣтимся еще и съ другими случаями разнозначныхъ въ
различныхъ направленіяхъ коеффиціентовъ расширенія. М. Сапіопе и
О. Сопііпо нашли, что объемъ растянутаго каучука имѣетъ положитель-
ный температурный коеффиціентъ. Кромѣ того Кипсіі доказалъ, что
растянутый каучукъ обладаетъ свойствомъ дихроизма, чѣмъ уже непосред-
ственно доказывается его анизотропность.
бсйишасйег, Ройгі и Могіія (въ Пулковѣ) нашли въ 1849 г.,
что ледъ при охлажденіи ниже 0° сжимается, и что слѣд. расширеніе Н2О
происходитъ только отъ 4° до 0°, и затѣмъ внезапно въ моментъ затвер-
дѣванія. Для коеффиціента линейнаго расширенія льда они нашли число
0,0000518. Позднѣйшія изслѣдованія Ріиескег’а и (Зеізвіег’а дали
число 0,0000528. В е а г, изслѣдовавшій для большого числа тѣлъ рас-
ширеніе между — 188°,7 (жидкій воздухъ) и + 17°, нашелъ для коеффи-
ціента линейнаго расширенія льда « = 0,000027, т.-е. приблизительно
половину числа, относящагося къ промежутку между 0° и — 20°. Для
твердой ртути онъ нашелъ За = 0,0000887 между—38°,8 и — 188°,7.
8 с й о 11 нашелъ, что стекло, быстро охлажденное, и слѣд. имѣющее
внутреннія натяженія, обладаетъ большимъ коеффиціентомъ расширенія,
чѣмъ стекло медленно охлажденное и потому болѣе изотропное. Въ 1894 г.
появилось обширное изслѣдованіе Всйоіі’а и ХѴіпкеІтап п’а о зави-
симости коеффиціента кубическаго расширенія а стеколъ отъ ихъ со-
става. Они изслѣдовали 30 сортовъ іенскаго стекла и нашли, что числа а
колеблются въ весьма широкихъ предѣлахъ между а == 0,0000110(41 В2О3
и 59^лО) до а = 0,0000337 (5757О2, 13К2О, 13іѴа26,12Д/2О3 и 5ХпО\ При
этомъ оказалось возможнымъ приблизительно вычислить а для каждаго
сорта стекла на основаніи формулы вида
а = а1х1 + а2х2 + а3х3 + . . . ,
94
Объемъ и давленіе тѣлъ.
гдѣ аъ а2, . вѣсовыя количества различныхъ веществъ, входящихъ
въ составъ вѣсовой единицы стекла; хг, х2, х3, . . . характерныя для
этихъ веществъ постоянныя. Такъ напр. 107х равно 10,0 для Ыа2О, 8,5
для 5,0 для Д/2О3, 3,0 для РЬО, 1,8 для ХпО, 0,1 для М§0 и т. д.
Присутствіе Ыа2О и К2О особенно сильно увеличиваетъ коеффиціентъ
расширенія стекла.
МаЙЬіезеп изслѣдовалъ тепловое расширеніе сплавовъ. Онъ
нашелъ, что при всѣхъ температурахъ расширеніе сплава равно суммѣ
расширеній составныхъ частей, отдѣльно взятыхъ при тѣхъ же темпера-
турахъ, иначе что коеффиціентъ объемнаго расширенія а сплава, въ объ-
емѣ ѵ котораго содержатся объемы . . . , , составныхъ
частей, коеффиціенты расширенія которыхъ а2, а3, . . . . «/, . . . , есть
среднее изъ величинъ а/, вычисляемое по т. наз. формулѣ смѣшенія, т.-е.
а = = »
ѵ
или ѵа = Яѵіаі. Правильность этой формулы подвердилъ напр. Зіайі-
Ь а § е п для магналія (сплавъ АІ и Расширеніе сплавовъ Си — АІ
и Си — 8Ь изслѣдовалъ Ье ГЬаіеІіег.
Нѣкоторыя вещества обнаруживаютъ при расширеніи особенности.
8ѵе(1е1іи8 находитъ для Ее и стали аномальности около 660° и 730°,
а именно аномальное сжатіе при нагрѣваніи и таковое же расширеніе
при охлажденіи. Положеніе двухъ температуръ зависитъ отъ содержанія
угля. Аномальное расширеніе желѣза изслѣдовалъ также Ье СЬаІеІіег.
(диіііаите изслѣдовалъ тепловое расширеніе различныхъ сплавовъ
А? и стали. Сплавъ, содержащій 35,7°/0 А7, обладаетъ наименьшимъ
коеффиціентомъ расширенія (въ 10 разъ меньше, чѣмъ у Рі\ а именно
средній коеффиціентъ между 0° и /° равенъ (0,877 + 0,001272^)10 6; плот-
ность этого сплава 8,098. Ему удалось приготовить такую проволку, рас-
ширеніе которой между 0° и 26° оказалось въ 61 разъ меньше расши-
ренія платины.
Этотъ результатъ подтвердили СЬагру и Огепеі (1902).
Коеффиціенты расширенія а эбонита и гуттаперчи весьма
быстро возрастаютъ съ температурой. КоЫгаивсЬ нашелъ для эбонита
а = 7700.10 8между 17° и 25°, и а == 8420.10 между 25° и 30°. В и 8 8П ет
нашелъ для гуттаперчи:
і 10° 20° 30° 40°
108а 18200 19830 21500 23200.
Расплавленное и опять затвердѣвшее іодистое серебро имѣетъ,
какъ показалъ Г і г е а и, отрицательный коеффиціентъ кубическаго расши-
ренія а при всѣхъ температурахъ отъ — 10° до + 70°, т. е. оно сжи-
мается при нагрѣваніи и расширяется при охлажденіи: Гігеаи нашелъ
что 108а = — 417 и ІО8 = — 4.2. Послѣднее число показываетъ,
(II
Объемъ анизотропныхъ тѣлъ.
95
что а стремится къ нулю при пониженіи температуры, и что при I = — 60°
вѣроятно а = О, т.-е. плотность іодистаго серебра наименьшая.
В о <1 хѵ е 1 ] показалъ, что уменьшеніе объема продолжается до 142°;
при этой температурѣ плотность іодистаго серебра имѣетъ максимумъ;
при дальнѣйшемъ нагрѣваніи іодистое серебро опять расширяется и это
расширеніе продолжается и выше точки плавленія (527°).
Кристаллы правильной системы (т. I) изотропны, а потому мы здѣсь
же можемъ упомянуть объ особенностяхъ двухъ веществъ, принадлежа-
щихъ къ этой системѣ.
Для алмаза Вігеаи нашелъ коеффиціентъ кубическаго расши-
ренія а равнымъ = 1686 + 43
При I = — 38°,8 получается а = 0, а при і < - 38°,8 имѣемъ а < О
Отсюда слѣдуетъ, что алмазъ имѣетъ максимумъ плотности при і =
= — 38°,8.
Для закиси мѣди Рігеан нашелъ
Ю9а = — 284 4- 69,2Л
При і >* 4°,1 имѣемъ а >* 0; при і = 4°,1 получается а — 0 и, на-
конецъ, при і <С 4°,1 имѣемъ а < 0. Отсюда слѣдуетъ, что закись мѣди
обладаетъ наибольшею плотностью при і = 4°,1, т. е. почти при той же
температурѣ, какъ и вода.
Замѣчательно мало тепловое расширеніе аморфнаго (плавленнаго)
кварца; его измѣряли НоІЬогп и Неппіп§ (1903). Всйееі (1903),
СЬарриіз (1903), Вогзеу (1906—1908), МіисЬіп (1907), Еапііаіі
(1910), Кау (1910) и др. НоІЬогп и Непиів^ нашли между 0°
и 1000° величину 106а = 0,54; 8сЬее1 для той же величины, 0,322
между 0° и 100°, СЬ.арриІ8— 0.385. Позже 8 с Ь е еі Ц907) далъ между
Ю0° и — 190° формулу
/ /0 (1 + 0,217.10 -Ч + 0,002379.10 ЧР).
Въ 1907 г. онъ нашелъ максимумъ плотности при — 80°; выше 0° по-
лучается линейная зависимость I отъ і. К а п й а 11 нашелъ максимумъ
величины а при + 500° и минимумъ при 950°.
Въ заключеніе статьи о тепловомъ расширеніи изотропныхъ твер-
дыхъ тѣлъ укажемъ, что въ Шарлоттенбургѣ (КеісЬапвіаІі) предпринятъ
рядъ опредѣленій коэффиціентовъ расширенія различныхъ стеколъ, метал-
ловъ и т. д.
§ 4, Вліяніе темературы на объемъ анизотропныхъ тѣлъ; расши-
реніе кристалловъ, МіІ8сЬет1ісй первый открылъ, что анизотропные
кристаллы, т.-е. всѣ, кромѣ кристалловъ правильной системы, при нагрѣ-
ваніи неодинаково раширяются въ различныхъ направленіяхъ. Онъ за-
мѣтилъ это, измѣряя при различныхъ температурахъ двугранный уголъ у
одного изъ реберъ кристалла известковаго шпата, при чемъ оказалось,
что этотъ уголъ съ повышеніемъ температуры измѣняется. Это озна-
чаетъ, что кристаллъ, расширяясь, не остается подобнымъ самому себѣ,
96
Объемъ и давленіе тѣлъ.
а такой результатъ не могъ бы получиться, еслибы кристаллъ расши-
рялся по всѣмъ направленіямъ одинаково. Чтобы опредѣлить и самые
коеффиціенты расширенія, МіізсЬегІісЬ опредѣлилъ вмѣстѣ съ О и -
1 о п ^’омъ коеффиціентъ у кубическаго расширенія кристалла. Чтобы по-
нять вычисленія М і і 8 с Ь е г 1 і с Ь’а, разсмотримъ вкратцѣ вопросъ о рас-
ширеніи анизотропныхъ тѣлъ и выведемъ нѣкоторыя формулы.
Допустимъ, что въ анизотропной средѣ существуютъ три взаим-
но перпендикулярныя направле-
нія. по которымъ коеффиціенты
линейнаго расширенія суть
аь а2, аз> и допустимъ далѣе,
что эти направленія имѣютъ
слѣдующую важную особенность:
частицы, расположенныя вдоль
геометрической прямой, парал-
лельной одному изъ этихъ на-
правленій, остаются на этой
прямой: иначе говоря, физиче-
ская нить частицъ не мѣняетъ
своего направленія при измѣ-
неніи температуры, если нить
параллельна одному изъ этихъ
направленій. Коеффиціенты
Рис. 42.
а2 и а3 мы назовемъ главными.
Проведемъ изъ произвольной точки О (рис. 42) координатныя оси по
тремъ упомянутымъ направленіямъ, и пусть Л4(х, у, г) положеніе какой-
либо точки при 0°. При /° она займетъ новое положеніе ЛГ(^, у, ^).
координаты котораго опредѣлятся изъ условій
г = х(1 + а^)
V - = А1 + «2^
С = 1 “|“ Ц3О
(22)
Прямая ОМ = г переходитъ въ ОМ' = р; отсюда слѣдуетъ, что при
измѣненіи температуры мѣняется не только длина, но и направленіе
физической нити частицъ. Полагая
р = г(1 + ^)...........................(23)
мы назовемъ /? коеффиціентомъ линейнаго расширенія по направленію
0/14, составляющему углы др, тр и ѳ съ координатными осями. Взявъ сумму
квадратовъ равенствъ (22), и подставивъ х = гсоздо, у — гсоз'ір, г = гсозе,
получаемъ
— г-\( 1 + н1Л)2со829 -|-(1 а2/)2С082ір + (1 + а3Г2)со82ѳ].
При малости величинъ аі можно пренебречь ихъ квадратами; тогда
получается = Г2 2г2/(а1со82до «2соз2ір + а3С082 0).
Объемъ анизотропныхъ тѣлъ.
97
Равенство (23). возвышенное въ квадратъ, даетъ такимъ же спо-
собомъ
р2 = г2 2г2
Изъ сравненія послѣднихъ двухъ формулъ слѣдуетъ:
= о^соз2^ Ц- а2С082тр 4“ а3С0828
(24)
Вообразимъ три взаимно перпендикулярныя направленія съ коеф-
фиціентами линейнаго расширенія А, А и /?3, составляющія съ коорди-
натными осями углы 9^152,з> Ѵі,2,з> 61,2,8- Напишемъ для трехъ $ формулы
вида (24); сложивъ ихъ, получаемъ немедленно:
+ ^2 + Л ----- а1 + а2 4“ а8.......................(25)
Сумма коеффиціентовъ линейнаго расширенія по
произвольнымъ тремъ взаимно перпендикулярнымъ на-
правленіямъ есть величина постоянная, равная суммѣ
трехъ главныхъ коеффиціентовъ.
Проведемъ черезъ О прямую, составляющую равные углы со съ
осями координатъ, такъ что <р — у = В = со. Такъ какъ со82д? 4" со82ір +
4~ СО820 = 1, ТО имѣемъ 3 СО82С0 = 1 ИЛИ СО8С9 =
1
Ѵз
, откуда со = 54°44'.
КоеффиціейТъ линейнаго расширенія {У, соотвѣтствующій этому на-
правленію, получаемъ изъ (24), подставивъ со82д> = С082/ф = со820 = 1 :
3
Р' = (аі 4" 4" «з)...................(26)
о
По направленію со коеффиціентъ расширенія ра-
венъ среднему значенію трехъ коеффиціентовъ расши-
ренія по тремъ взаимно перпендикулярнымъ на-
правленіямъ.
Вырѣжемъ изъ нашей среды прямоугольный параллелепипедъ, сто-
роны котораго при 0° равны Іъ 12 и /3; объемъ его при 0° равенъ Ѵо =
= 444- Пусть объемъ при /° равенъ V; полагая
Ѵ=У0(1+^)....................(27)
мы назовемъ у коеффиціентомъ кубическаго расширенія. При /° размѣры
4, 4 и 4 превратились въ 4 (1 + АО* 4 (1 4~ АО и 4 (1 4~ АО 5 ихъ
произведеніе равно V. Подставляя въ (27) это произведеніе, а также
Ѵо = 444, получаемъ:
і -|- уі = (і 4- АО (і 4~ АО (і 4~ АО-
Произведя перемноженіе, отбросимъ произведенія Малыхъ величинъ А’^
другъ на друга и сократимъ на і. Тогда остается 7 = А 4“ А 4“ А, что
вмѣстѣ съ (25) и (26) даетъ
7 = А 4" А 4“ А — аі 4- а2 4- аз = 3А • • • • (28)
КУРСЪ ФИЗИКИ О. X В О Л Ь С О Н А. т. III, изд. 3-е. 7
98
Объемъ и давленіе тѣлъ.
Коеффиціентъ кубическаго расширенія есть вели-
чина опредѣленная для даннаго анизотропнаго тѣла,
равная суммѣ коеффиціентовъ линейнаго расширенія
по тремъ взаимно перпендикулярнымъ направленіямъ,
или равная утроенному среднему коеффиціенту /?' по направленію со,
указанному выше.
Въ одноосной анизотропной средѣ коеффиціентъ расширенія
имѣетъ одинаковую величину по всѣмъ направленіямъ, перпендикуляр-
нымъ къ оси. Если Ох взять по направленію оси, то направленія
осей Оу и Ог можно выбрать произвольно. Главныхъ коеффиціентовъ
расширенія два: сц по направленію оси и а2 перпендикулярно къ оси.
Формулы упрощаются, ибо н3 = а2. Вмѣсто (24) имѣемъ очевидно
= ахСО82ф + а28ІП2ф.....................(29)
ибо ось Оу можно расположить въ плоскости, проходящей черезъ Ох и
направленіе ОМ. Вмѣсто формулы (28) имѣемъ теперь
Г = Рі +/?2-|-/?з = «і+2а2 = 3^.............(30)
Возвращаемся къ опытамъ МіізсііегіісЬ’а, нашедшаго, что дву-
гранный уголъ кристалла известковаго шпата измѣняется при нагрѣваніи
отъ 0° до 100°, и опредѣлившаго затѣмъ еще коеффиціентъ кубическаго
расширенія у. Измѣреніе двуграннаго угла показало МііесііегіісіГу,
что кристаллъ сильнѣе расширился вдоль оси, чѣмъ перпендикулярно къ
ней, а именно, что
і іоой! = х оО342
1 + 10002
или, въ виду малости а3 и а.2, проще 1 + ЮО (ах — о2) = 1,00342, т.-е.
ах — а2 — 0,0000342.
Измѣреніе у дало второе уравненіе у = ах + 2а2 = 0,0000196.
Изъ двухъ уравненій получается ах = 0,0000293, а2 = — 0,00000487.
Такимъ образомъ оказалось, что известковый шпатъ при нагрѣваніи
расширяется по направленію оси и сжимается по направленію, перпен-
дикулярному къ оси.
Послѣ МіібсйегіісЬ'а вопросомъ о тепловомъ расширеніи кри-
сталловъ занимался Ріа И. Приборъ, которымъ онъ пользовался, изо-
браженъ на рис. 43. На изслѣдуемый кристаллъ Ь надавливается пру-
жиною У конецъ короткаго плеча рычага, вращающагося около оси Р\
къ концу длиннаго плеча Н прикрѣплено зеркало О. Ось Р рычага ле-
житъ на выступѣ Е кольца /?, надѣтаго на столбъ В, вдоль котораго на-
несено дѣленіе, дающее возможность опредѣлить высоту оси Р надъ
основаніемъ А всего прибора. Вращеніе зеркала О около оси Р на-
блюдалось по способу трубы и шкалы (т. I); это вращеніе опредѣ-
ляло разность расширеній кристалла Ь и столба В, вызванныхъ нагрѣ-
Объемъ анизотропныхъ тѣлъ.
99
ваніемъ всего прибора. Расширеніе столба В разъ навсегда опредѣля-
лось, а потому изъ наблюденій могъ быть полученъ искомый коеффиці-
ентъ линейнаго расширенія кристалла Ь.
Ріаіі подтвердилъ результаты МИвсІіегІісЬ’а; онъ нашелъ,
что нѣкоторые кристаллы расширяются сильнѣе, чѣмъ какой-либо изъ
металловъ, и что для нѣкоторыхъ кристалловъ коеффиціентъ расширенія
въ опредѣленныхъ направленіяхъ отрицателенъ.
Рис. 43.
Замѣтимъ, что для такихъ кристалловъ тепловое расширеніе
равно нулю во всѣхъ направленіяхъ, параллельныхъ образующимъ
конуса, уравненіе котораго
^сов2^ -|- о2со82др 4" «зСО82^= О,
см. (24). Для одноосныхъ кристалловъ, у которыхъ одна изъ величинъ
или «2 отрицательна, тепловое расширеніе равно нулю по всѣмъ напра-
вленіямъ. составляющимъ съ осью уголъ <р, для котораго, см. (29),
СС^СО82ф 4" «28ІП29) = О,
откуда
^9> = 1 — ч
к «2
Сжатіе вообще очень мало; поэтому РI а і I полагалъ, что величина у
всегда положительна, т.-е., что объемъ кристалла всегда увеличивается съ
повышеніемъ температуры. Далѣе Ріа И нашелъ, что для кристалловъ
гексагональной системы замѣчается постоянное соотношеніе между
ихъ оптическими и термическими свойствами: отрицательные кристаллы
(т. ІІ) расширяются сильнѣе вдоль оси, чѣмъ перпендикулярно къ ней,
между тѣмъ какъ для положительныхъ кристалловъ имѣетъ мѣсто обрат-
7*
100
Объемъ и давленіе тѣлъ.
ное. Для кристалловъ квадратной системы такого соотношенія не на-
блюдается.
Наиболѣе тщательно изслѣдованіе теплового расширенія кристалловъ
было произведено Рігеаи по его способу, положенному на стр. 87.
Приводимъ нѣкоторые изъ его результатовъ.
Для кристалловъ правильной системы (тѣла изотропныя) расширеніе
по всѣмъ направленіямъ одинаковое; особенности, которыя представля-
ютъ алмазъ и закись мѣди, уже были указаны на стр. 95.
Для кристалловъ одноосныхъ (гексагональная и квадратная системы)
«2 = а3. Рігеаи измѣрялъ а1} а2 и /?'; послѣдняя величина могла быть
вычислена по формулѣ (30), дающей — * (аі “Ь 2а2). Вотъ нѣкото- 108/?' (набл.). 10*0' (вычисл.).
рые примѣры: 108ах 108а2
Цирконъ . . . . . . 4430 2330 3040 3030
Смарагдъ . . . ... — 106 137 57 56
Известковый шпатъ . 2621 — 540 507 514
Кварцъ . . ... 781 1419 1206 1206
Вепоіі изслѣдовалъ по < способу Еі 2 е а и расширеніе известко-
ваго шпата и кварца и опредѣлилъ зависимость коеффиціентовъ и а2
отъ температуры, представивъ ихъ въ видѣ ат — 4~ Ьгі. = а2-\- Ь2і.
Примѣненіе кварца въ приборѣ РиИгісІГа (стр. 89) заста-
вило заняться тщательнымъ измѣреніемъ теплового расширенія этого ве-
щества, и притомъ параллельно оптической оси. Это расши-
реніе измѣряли Рігеаи (1866), Вепоіі (1888) Веітегдея (1896)
8сйее1 (1902) и Вапсіаі] (1905). Положимъ, что I есть длина пла-
стинки кварца, вырѣзанной параллельно оптической
оси, /0 — ея длина при 0° и 4 = 4 С1 “Н Въ слѣдующей таблицѣ
сопоставлены найденныя этими учеными значенія для величины а; рядомъ
даны температуры, въ передѣлахъ между которыми производились наблю-
денія и къ которымъ относятся соотвѣственныя формулы.
Рігеаи. .
Вепоіі. .
Веітегйев
8сЬее1. .
Вапйаіі .
2° — 60°
6° — 80°
5° — 220°
16° - 100°
16° — 250°
а = (7,10 4- 0,00885/) . 10“ 6
а = (7,161 0,00801/) . 10“ 6
а — (6,925 4- 0,00819/) . 10“ 6
а = (7,144 4- 0,00815/) . 10“ 6
а = (7,170 4- 0,00810/) . 10“ 6
Если мы положимъ а = а0 4- /?/, то коеффиціентъ расширенія при /°
будетъ равенъ = а0 4~ 2/?/. На это слѣдуетъ обратить вниманіе, такъ
какъ нѣкоторые изъ этихъ излѣдователей даютъ а, другіе — Ме-
жду 16° и 250° по В а П(1а ІГю, слѣдовательно, <^=(7,170 4- 0,01620/).10‘ 6
Для промежутка между 250° и 470° В а п сі а 11 даетъ выраженіе
а, = [11,25 4- 0,0165 (/ — 250) 4- 0,0000566 (/ — 250)2 4~
4- 0,000000134 (/ — 250)3] . 10“6
Объемъ жидкостей.
101
Въ промежуткѣ между 470° и 505° возрастаетъ съ необычайной
быстротою, причемъ и послѣдняя формула является непригодной.
Объ особенныхъ свойствахъ сплавленнаго іодистаго серебра мы уже
говорили на стр. 94. Для кристалловъ Л^/, принадлежащихъ къ гекса-
гональной системѣ, Рігеаи нашелъ при 40°
щ = — 0,00000397, = + 0,00000065.
Эти числа даютъ для коеффиціента у кубическаго расширенія
у = Щ 4- 2а2 = — 0.00000267.
Отсюда слѣдуетъ, что и кристаллическое іодистое серебро при на-
грѣваніи сжимается. Мы не затрогиваемъ сложнаго вопроса о положе-
ніи осей трехъ главныхъ расширеній аь и а3 въ двуосныхъ кри-
сталлахъ.
Теоріей вопроса о тепловомъ расширеніи кристалловъ занимался
Федоровъ. Въ своемъ «Курсѣ Кристаллографіи» (С. П. 1901) онъ
на стр. 338 упоминаетъ такой способъ изслѣдованія термическаго рас-
ширенія кристалловъ: поверхность кристалла покрывается слоемъ благо-
роднаго металла, на которомъ воспроизводится диффракціонная
рѣшетка (т. II). При нагрѣваніи кристалла происходитъ смѣщеніе
спектровъ, которое и даетъ возможность опредѣлить величину расшире-
нія кристалла.
Къ статьѣ о расширеніи анизотропныхъ тѣлъ можетъ быть отне-
сенъ, какъ было сказано на стр. 93, вопросъ о вліяніи температуры на
растянутый каучукъ. Сюда, пожалуй, можно отнести и вопросъ о рас-
ширеніи нѣкоторыхъ неоднородныхъ и какъ бы анизотропныхъ тѣлъ,
какъ, напр., дерева. Ѵіііагі нашелъ, что для различныхъ сортовъ
дерева поперечное тепловое расширеніе отъ 5 до 25 разъ больше расши-
ренія продольнаго.
§ 5. Обзоръ способовъ опредѣленія теплового расширенія жид-
костей. Расширеніе ртути. Для жидкостей приходится разсматривать
только объемное расширеніе, а потому подъ коеффиціентомъ расширенія а
жидкостей всегда подразумѣвается коеффиціентъ кубическаго (объ-
емнаго) расширенія. Способы опредѣленія величины а для жидкостей
можно раздѣлить на двѣ группы.
I. Въ способахъ первой группы мы непосредственно наблюдаёмъ
разность между расширеніемъ жидкости и расширеніемъ того сосуда, въ
которомъ она находится; коеффиціентъ расширенія этого со-
суда долженъ быть извѣстенъ. Къ этимъ способамъ относится:
1. Способъ обыкновенный, термометренный: жидкость наполняетъ
резервуаръ и часть трубки, тщательно калибрированной; наблюдается из-
мѣненіе уровня жидкаго столба въ трубкѣ при измѣреніи температуры.
2. Способъ вѣсового термометра.
3. Способъ флакона, по существу почти не отличающійся отъ пре-
102
Объемъ и давленіе тѣлъ.
дыдущаго, такъ какъ оба способа сводятся къ опредѣленію измѣненія
плотности жидкости при измѣненіи температуры.
II. Ко второй группѣ относятся способы опредѣленія величины а,
которые можно назвать способами гидростатическими. Сюда относятся:
4. Способъ сообщающихся сосудовъ, въ которыхъ, какъ извѣстно,
высоты жидкостей обратно пропорціональны ихъ плотностямъ.
5. Способъ, основанный на измѣреніи потери вѣса опредѣленнаго
тѣла М въ жидкости при различныхъ температурахъ. Коеффиціентъ
расширенія тѣла М долженъ быть извѣстенъ.
Изъ указанныхъ здѣсь пяти способовъ выдѣляется способъ четвер-
тый, способъ сообщающихся сосудовъ, какъ единственный непо-
средственный способъ опредѣленія теплового расширенія жидкостей,
не требующій предварительнаго опредѣленія того же коеффиціента для
другого вещества. Огромное значеніе этого способа заключается въ слѣ-
дующемъ: если исключить способъ пятый, весьма рѣдко примѣнявшійся,
то оказывается, что остальные три способа, которыми на дѣлѣ постоянно и
пользуются, требуютъ предварительнаго опредѣленія коеффиціента расшире-
нія Р сосуда, обыкновенно стекляннаго. Такое опредѣленіе можетъ быть, од-
нако; сдѣлано только путемъ наблюденія расширенія въ
этомъ сосудѣ жидкости, коеффиціентъ расширенія а кото-
рой уже извѣстенъ. Чтобы выйти изъ этого «сігсиіпзѵіііо-
8118», мы должны, хотя бы для одной какой-либо
жидкости, опредѣлить а инымъ способомъ; тогда мы
будемъ имѣть возможность при помощи этой жидкости
опредѣлить /? для сосуда, а потомъ и а для всякой дру-
гой жидкости.
Способъ сообщающихся сосудовъ, который еще извѣстенъ
подъ названіемъ способа Биіоп^’а и Реііі, примѣнялся названными
учеными, а затѣмъ и другими исключительно только для
ртути и для воды. Теорія этого способа заключается въ слѣдующемъ;
Къ жидкостямъ очевидно примѣнима формула (18) стр. 86, связывающая
плотности и при 0° и при /°
Рис. 44
гдѣ аЁ средній коеффиціентъ объемнаго расширенія жидкости между 0° и /°.
Положимъ, что одна и та же жидкость находится въ двухъ сообща-
ющихся сосудахъ А и В (рис. 44), причемт, температура жидкости въ
сосудѣ А равна 0°, а въ сосудѣ В равна /°. Высоты Ао и жидкихъ
столбовъ обратно пропорціональны плотностямъ б/0 и жидкости, т.-е.
біо
Но
Объемъ жидкостей.
103
Это равенство и формула (31) даютъ
№
= Ао
Формула (32) выражаетъ, что столбъ жидкости, высота котораго Иі и
температура /, уравновѣшиваетъ столбъ, температура котораго 0°, если
высота й0 послѣдняго равна /^:(! + «//). Высоту Ао можно назвать
приведенною къ 0° высотою жидкаго столба. Можно еще
сказать, что жидкіе столбы Ло при 0° и при /° гидростатически экви-
валентны и могутъ быть замѣнены другъ другомъ, безъ измѣненія про-
изводимаго ими давленія.
Важно имѣть въ виду, что < приведеніе къ 0°» здѣсь происходитъ
необычное: Ло и величины линейныя, между тѣмъ какъ средній
между 0° и /° коеффиціентъ кубическаго (объемнаго) расширенія.
Рис. 45.
Если въ сообщающихся сосудахъ столбы имѣютъ температуры і^Т
и высоты И} и то мы имѣемъ:
\-\-атт~ \ + аіі......................<33)
Приведенныя высоты, опредѣляющія гидростатическое давленіе, должны
быть равны между собою.
Приборъ, которымъ пользовались В и 1 о н и Реііі, изображенъ
на рис. 45. АВВ' А' сообщающіеся сосуды, содержащіе ртуть; АВ окру-
жено тающимъ льдомъ, А'В' находится въ широкомъ цилиндрѣ, напол-
ненномъ масломъ, температуру котораго можно мѣнять, усиливая или
ослабляя топку въ находящейся подъ нимъ печкѣ. Температура і въ со-
судѣ А'В' опредѣлялась при помощи воздушнаго термометра О'Е', снаб-
104
Объемъ и давленіе тѣлъ.
женнаго манометромъ Н'К'. Кромѣ того имѣлся еще ртутный вѣсовой тер-
мометръ ЕЕ, который, однако, очевидно не могъ служить для измѣренія
температуры, такъ какъ имъ можно пользоваться только, зная уже коеф-
фиціентъ расширенія ртути, для опредѣленія котораго производился
самый опытъ. Термометръ ЕЕ служилъ лишь для сравненія. Къ опы-
тамъ В и 1 о п ^’а и Р е I і і непосредственно прилагается формула
(32), дающая
п‘ =
(34)
Разность высотъ — Ло въ А и Л, а также высота Ло измѣрялись при
помощи катетометра (т. I), изобрѣтеннаго В и 1 о п §*’омъ и Р е 1 і і именно
при выполненіи этого опытнаго изслѣдованія.
Результаты, полученные В и 1 о п ^’омъ и Р е і і і, помѣщены въ
слѣдующей табличкѣ:
Температура і Средній коефф. Температура Температура по фик-
по воздушному расширенія по вѣсовому тивному ртутному
термометру. для ртути. термометру. термометру.
0° — 0° 0°
100° 0,0001802 100° 100°
200° 0,0001843 202°,99 204°,61
300° 0,0001887 307°,48 314°,15.
Значеніе чиселъ первыхъ двухъ столбцовъ понятно; второй столбецъ по-
называетъ, что для ртути растетъ съ температурою. Числа третьяго
столбца вычислены въ предположеніи, что кажущееся расширеніе
ртути въ стеклѣ остается и выше 100° тѣмъ же, какимъ оно получается
изъ наблюденій между 0° и 100°, каковыя температуры опредѣлялись воз-
душнымъ термометромъ. Наконецъ, въ четвертомъ столбцѣ помѣщены
температуры, указываемыя такимъ ртутнымъ термометромъ, въ которомъ
наблюдалось бы абсолютное расширеніе ртути, причемъ опять-таки,
допускалось, что а/ = а100.
Не останавливаясь на опытахъ Міііігег’а, давшихт» между 1,5° и
22° слишкомъ малое число « = 0,000174, перейдемъ къ классическимъ
опытамъ Ве§паи 1і, произведеннымъ по двумъ способамъ. Приборъ,
которымъ пользовался Ке^паиИ при опытахъ по первому способу, изо-
браженъ на рис. 46. Двѣ трубки іа и іа', содержащій ртуть и открытыя
сверху, соединены между собою горизонтальною трубкою, въ которой
около О сдѣлано отверстіе на верхней ея сторонѣ. Отъ нижнихъ кон-
цовъ вертикальныхъ трубокъ идутъ двѣ горизонтальныя трубки другъ
другу навстрѣчу; къ ихъ концамъ прикрѣплены вертикальныя стеклян-
ныя трубочки, соединенныя при помощи изогнутыхъ трубокъ ѵ и затѣмъ
одною трубкою съ резервуаромъ У, въ который накачивался нагнетатель-
нымъ насосомъ сгущенный воздухъ приблизительно до давленія въ 2 ат-
мосферы. Это давленіе регулировалось такимъ образомъ, чтобы оно могло
поддержать столбы ртути въ трубкахъ іа и іа и чтобы въ то же время
Объемъ ртути
105
въ двухъ вертикальныхъ трубкахъ, расположенныхъ ниже ѵ, оставались
небольшіе столбики ртути. Правая трубка іа окружена широкимъ сосу-
домъ, черезъ который непрерывно протекала вода изъ трубки, изобра-
женной въ правомъ верхнемъ углу ;
она протекала черезъ особую трубку,
снабженную воронкою, до дна со-
суда, а съ поверхности уходила по
сифону сс.
Лѣвая трубка іа' окружена была
болѣе широкимъ сосудомъ, наполнен-
нымъ масломъ, подогрѣваемымъ снизу
особою печью. Мѣшалка, снабжен-
ная системою горизонтальныхъ крыль-
евъ и приводимая въ движеніе при
помощи шнурка, перекинутаго че-
резъ неподвижные блоки, служитъ
для непрерывнаго перемѣшиванія
масла. Температура масла опредѣля-
ется при помощи газоваго термометра,
длинный резервуаръ котораго виденъ
съ лѣвой стороны; онъ снабженъ
трубкою А съ манометромъ, не изо-
браженнымъ на рисункѣ. Горизон-
тальный разрѣзъ черезъ лѣвый ши-
рокій сосудъ изображенъ отдѣльно
въ Е'и, гдѣ видны и крылья мѣшалки.
Весь приборъ какъ бы виситъ на желѣзномъ стержнѣ СРР, вращаю-
щемся около оси С, вдѣланной въ каменную стѣну; этотъ стержень сво-
бодно проходитъ черезъ два кольца Р, Р, также вдѣланныя въ стѣны и
опирается на винты, головки которыхъ видны въ Р, Р. При помощи этихъ
винтовъ можно привести стержень СРР въ горизонтальное положеніе.
Нижнія трубки проходятъ черезъ кольца, расположенныя на нижнихъ кон-
цахъ четырехъ стержней Т и также при помощи винтовъ приводятся
въ горизонтальное положеніе. Вершины ртутныхъ столбиковъ въ і и і на-
ходятся на одинаковой высотѣ, такъ какъ трубки наверху соединены
между собою, какъ было сказано, выше. Давленіе въ V и количество
ртути регулировались такимъ образомъ, чтобы въ отверстіи О посреди
верхней горизонтальной трубки была видна капля ртути. Обозначимъ
температуры ртути: въ правой трубкѣ черезъ /, въ лѣвой черезъ 7, и
въ двухъ стеклянныхъ трубкахъ ниже ѵ черезъ г. Высоты ртутныхъ
столбовъ, измѣряемыя отъ оси нижней горизонтальной трубки, обозначимъ
такъ: съ лѣвой стороны столбъ /7, съ правой Н'\ эти величины почти
равны между собою ; далѣе въ стеклянныхъ трубкахъ ниже ѵ съ лѣвой
стороны А, съ правой И'. Давленіе воздуха въ сосудѣ V уравновѣшива-
етъ съ одной стороны разность давленій столбовъ Н и А, съ другой
106
Объемъ и давленіе тѣлъ.
разность давленій столбовъ Н' и А7. Если всѣ эти столбы привести къ 0°,
пользуясь формулой (32), то разности приведенныхъ столбовъ слѣва и
справа должны быть равны между собою. Это даетъ намъ равенство:
Н И _____ Н' И' (35)
1-|-ат Т 1 -+- ат т 1 + а^і 1 - атт
Здѣсь ат, и средніе коеффиціенты объемнаго расширенія ртути
между 0° и Г°, 0° и /°, 0° и т°. Подставивъ предварительно въ (35) вмѣсто
аі и ат числа, найденныя Ви 1 оп^’омъ и Реііі, Е е п а и 11 получилъ
рядъ значеній для а/ при различныхъ Т. Изъ этихъ чиселъ онъ вывелъ
болѣе точныя значенія коеффиціентовъ а1 и ат и, вставляя ихъ въ рядъ
уравненій вида (35), повторилъ все вычисленіе и нашелъ окончательныя
значенія для а у при различныхъ Т.
Второй способъ Е е п а и 11 ближе .подходитъ къ способу
Лпіоп^’а и Реііѣ; его легко понять при помощи схематическаго
рис. 47. Ртутные столбы, находящіеся въ АВ и А'В' при температурахъ
Т и I соединены трубкой СС'О'О, средняя часть С'Е которой настолько
гибка, что она не мѣшаетъ удлиненію внизъ желѣзной трубы АВ при ея
нагрѣваніи. Боковыя горизонтальныя трубки ЕЕ и Ю оканчиваются вер-
тикальными стеклянными трубками, въ которыхъ и находятся верхніе
Рис. 47.
концы ртутныхъ столбовъ. Высоты столбовъ обозначимъ слѣдующимъ
образомъ: аЬ - 77, а'Ь' = Н’; надъ Е и О находятся столбы А и И': вер-
тикальное разстояніе точекъ а и а\ т.-е. а" а' пусть равно А7'. Это вы-
сота ртутнаго столба, помѣщающагося въ С'О'. Температуры трехъ стол-
бовъ ртути А, А7 и И" (въ СО7) можно считать одинаковыми и равными т-
Гидростатическія давленія слѣва и справа на ртуть, находящуюся въ СС'
одинаковы, а потому должны быть равны и суммы высотъ ртутныхъ
Объемъ ртути.
107
столбовъ съ той и другой стороны, если ихъ привести къ 0°. Это даетъ
намъ равенство
Н Л Н' Л' Л"
(36)
Изъ этого равенства В е § п а и И опредѣлилъ величины тѣмъ же спо-
собомъ послѣдовательныхъ приближеній, какой выше былъ изложенъ въ
связи съ равенствомъ (35).
Какъ результатъ всѣхъ своихъ наблюденій, Ке^паиіі вывелъ
слѣдующую эмпирическую формулу для средняго коеффиціента рас-
ширенія ртути между 0° и Г°:
аг— 0,00017905 -|-0,00000О0252Г.
(37)
Средній коеффиціентъ между 0° и 100° получается отсюда равнымъ
«і00 = 0,00018157,
между тѣмъ какъ Бпіоп^и РеШ нашли число 0,00018018.
Если ат= а-\- ЬТ, то коеффиціентъ расширенія а при темпе-
ратурѣ Г равенъ а~а-\-2ЬТ. Изъ таблицы, данной Ке^паиИ,
приводимъ нѣкоторыя числа:
Температура по
воздушному
термометру.
т
0°
20°
50°
80°
100°
140°
200°
240°
280°
300°
Средній коефф
расширенія
между 0° и Г°.
а?
0,00017951
18027
18102
18153
18254
18405
18506
18607
18658
Коефф. расши-
ренія при тем-
пературѣ Т.
а
0,00017905
1«0о1
18152
18304
18405
18606
18909
19111
19313
19413
Температура по
чисто ртутному
термометру.
0°.000
19°,776
49,650
79,777
100,000
140,776
202,782
244,670
287,005
308,340
Въ послѣднемъ столбцѣ помѣщены температуры, которыя указывалъ
бы термометръ, основанный на наблюденіи одного только расширенія
ртути въ предположеніи что а = ат = Сопъі. = а100, т.-е. что расшире-
ніе ртути при всѣхъ температурахъ равно тому, которое наблюдается при
ея нагрѣваніи отъ 0° до 100°.
Работы Ке^паиН подверглись къ критическому разбору со сто-
роны Вескпа^еГя, Войска, ХѴиеНпег’а, Менделѣева,
Ьеѵу и Вгосй'а.
108
Объемъ и давленіе тѣлъ.
Кескп а е 1 приходитъ къ заключенію, что а? должно быть пред-
ставлено въ видѣ трехчлена
(іт= а “I- ЬТ сТ2 ........ (38)
и вмѣсто (37) пишетъ
ат= 0,00018018 + 0,00000000,94 Т + 0,00000000005Г2.
В о 8 8 с 11 а полагаетъ, между прочимъ, что слѣдуетъ разсматривать
для ртути коеффиціентъ расширенія
т.-е. въ знаменателѣ перваго множителя писать ѵ вмѣсто ф0. Это зна-
читъ, что расширеніе сіѵ при каждомъ весьма маломъ нагрѣваніи (с№) слѣ-
дуетъ сравнивать не съ объемомъ ѵ0, который ртуть имѣла при 0°, но съ
тѣмъ объемомъ, который она имѣетъ при данной температурѣ і. Объ
этомъ мы уже упомянули на стр. 81, см. (13), гдѣ величина (39) обозна-
чена черезъ у'. В о с 8 с Ь а полагаетъ, что для ртути а' = Соп8і., и
что слѣд. объемъ ея ѵ есть показательная функція температуры Т вида
а'1
ѵ = ѵ§е ,
см. аналогичную формулу (14) стр. 81. Во 88 с На находитъ, что на-
блюденія К е п а и 1 і даютъ число
а = 0,01)018077.
УѴиеІІпег приходитъ къ тому же заключенію, какъ и В е с к -
па^еі, а именно, что слѣдуетъ для «^принять формулу вида (38), при-
чемъ у него <2 = 0,000181163, Ь = 0,000000011554, с — 0,000000000021187.
Эти величины даютъ для ат и а нѣсколько иныя числа, чѣмъ приведен-
ныя выше, данныя самимъ Ве^папіі. Однако отступленія не велики ;
такъ, \Ѵие11пег находитъ
а100 = 0,00018253.
Менделѣевъ вновь предложилъ двучленную формулу
ат = 0,0001801 -4- 0,000000027,
которая весьма мало отличается отъ формулы (37) Ее^паиИ. Далѣе
Ь е ѵу вывелъ изъ наблюденій В е п а и И трехчленную формулу вида (38)
и, наконецъ, Вгосй въ 1883 г. ввелъ цѣлый рядъ поправокъ въ вы-
численія Ве^паиИ. Вгосіі также предлагаетъ трехчленное выра-
женіе вида (38), принимая
а — 0,000181792, Ь — 0,000000000175, с = 0,00оо00000035116.
Объемъ ртути,
109
Впослѣдствіи В г о с 11 ввелъ еще одну, весьма впрочемъ небольшую по-
правку. Для средняго коеффиціента а100 онъ нащелъ при этомъ
«юо = 0,00018210.
Изъ самостоятельныхъ опредѣленій расширенія ртути, произведенныхъ
послѣ Ве^папИ, упомянемъ сперва о работѣ Т Ь. і е 8 е п’а, 8 с Ь е е Гя
и 8е1Гя, которые изслѣдовали это расширеніе въ стеклянныхъ сосудахъ,
опредѣливъ коеффиціентъ расширенія послѣднихъ на трубкахъ, сдѣлан-
ныхъ изъ одинаковыхъ съ этими сосудами сортовъ стекла. Они нашли
«юо = 0,00018245. Полагая, что температура Т выражена въ градусахъ
водороднаго термометра, они находятъ
ат = 0,00018161 + 0,0000000078 Г.
Дальнѣйшее прекрасное изслѣдованіе, произведенное въ Вигеаи бе
РоіЙ8 еі Мёвитеь, принадлежитъ СЬарриіб, воспользовавшемуся ме-
тодомъ вѣсового термометра. Стеклянный сосудъ изъ ѵегге йиг имѣлъ
длину, равную 106 см., внѣшній діаметръ его равнялся 40 мм., внутрен-
ній — 36 мм. СЬарриів изслѣдовалъ сперва продольное расширеніе
сосуда между 0° и 100° и вычислилъ отсюда объемное расширеніе стекла.
Затѣмъ было опредѣлено расширеніе ртути путемъ взвѣшиванія выливав-
шейся при нагрѣваніи (отъ 0°) ртути. Окончательно СЬарриіб полу-
чилъ выраженіе вида (38):
ат = 0,000181690 + 0,000000002591 Т+ 0,00000000011456 Г2.
Кромѣ того СЬарриіб вычислилъ коеффиціентъ расширенія ртути
изъ своихъ прежнихъ сравненій показаній ртутнаго термометра изъ ѵегге
йиг съ водороднымъ термометромъ, принимая для расширенія ѵегге йиг
тѣ результаты, которые онъ теперь получилъ для иного сосуда. При этомъ
онъ получилъ слѣдующую формулу, относящуюся къ промежутку отъ — 20°
до 4-100°:
аг = 1,815405. ІО-4+ 0,195130. 10~8Г + 1,00917.1О '-1ОГ2 —
— 2,03862.10- 13Г3.
Для объемовъ V ртути (І/о — 1) первая изъ этихъ двухъ формулъ даетъ
слѣдующія значенія:
т V Т V
— 20° 0,996364 + 50° 1,009091
10 0,998183 60 1,010916
0 1,000000 70 1,012743
+-10 1,001817 80 1,014575
20 1,003634 90 1,016412
30 1,005451 100 ’ 1,018254
40 1,007270
110
Объемъ и давленіе тѣлъ.
Вторая (четырехчленная) формула даетъ числа, отличающіяся отъ этихъ
не болѣе, чѣмъ на 4 единицы послѣдняго десятичнаго знака.
Измѣренія ТЬіе 8еп’а, 8сЬ.ееГя и 8 е 1 Гя, а также работы
СЬарриіз относятся, такимъ образомъ, къ первой изъ двухъ группъ
способовъ, упомянутыхъ на стр. 101, ибо непосредственно измѣрялась раз-
ность расширеній жидкости и того сосуда, • въ которомъ она находилась.
Къ этой группѣ способовъ мы теперь и обратимся.
Если обозначить истинный коеффиціентъ расширенія жидкости1 че-
резъ а, кажущійся — черезъ /, и коеффиціентъ расширенія сосуда че-
резъ /?, и если относить всѣ три коеффиціента къ одной и той же тем-
пературѣ А то, какъ было доказано на стр. 25, см. формула (11)
« = 7 + ........................(40)
То же самое соотношеніе можно принять и межд} средними коеффиціен-
тами расширенія и Дѣйствительно, допустимъ, что мы наблю-
даемъ расширеніе жидкости по обыкновенному термометренному способу:
имѣется приборъ, по формѣ вполнѣ сходный съ обыкновеннымъ ртутнымъ
термометромъ, т.-е. состоящій изъ шаровиднаго или продолговатаго сте-
кляннаго сосуда и трубки, снабженной шкалою и весьма тщательно про-
калибрированной. Наполнивъ сосудъ и часть трубки испытуемой жид-
костью, опредѣляютъ положеніе конца жидкаго столбика въ трубкѣ при
температурахъ 0° и і°. Предварительные опыты взвѣшиванія прибора пу-
стого и затѣмъ наполненнаго ртутью при 0° даютъ намъ объемъ со-
суда и части трубки, которые при 0° были наполнены испытуемой жид-
костью; такимъ же образомъ взвѣшиваніе даетъ намъ объемъ ѵ0 одного
дѣленія шкалы при о0- Допустимъ, что при нагрѣваніи жидкости отъ 0°
до конецъ столбика перемѣстился на п дѣленій шкалы. Положимъ, да-
лѣе, что 1/0 и ѵ0 превращаются при /° въ Ѵі и
Средній коеффиціентъ кажущагося расширенія опредѣляется
на основаніи предположенія, что стѣнки сосуда и трубки вовсе не рас-
ширились, и что слѣд. объемъ жидкости Ѵо увеличился только на ве-
личину пѵ^ итакъ мы имѣемъ
Ѵ0 + пѵ0=Ѵ0(1+Г/і).......................(41)
Въ дѣйствительности жидкость занимаетъ при і0 объемъ
Ѵ/+ пѵі= Ѵо(1 -|- /?/) -|- ^0(1 -|- /?//) = (І/о-|- /гг/0)(1 -|- /?/).
Слѣд. средній коеффиціентъ истиннаго расширенія опредѣляется ра-
венствомъ
(Ѵо“Н я^0)(1 /?/) — ^о(1 +
Замѣняя первый множитель его значеніемъ (41), и сокращая на Ѵо, полу-
чаемъ 1 -ф- а/ = (1 4- ^)(1 + 7іі); отсюда
«, = !>, + ?, + №......................(12)
Объемъ ртути.
111
Въ этой вполнѣ точной формулѣ можно пренебречь послѣднимъ членомъ,
т.-е. положить
аі = Рі + Ѵі
(43)
вполнѣ аналогично (40).
Зная для даннаго прибора, достаточно измѣ>
ѵ ѵ пѵо
рить п и по формулѣ у
фиціентъ а*.
вычислить чтобы узнать искомый коеф-
Величина опредѣляется изъ предварительныхъ опытовъ со ртутью
Рис. 48.
при помощи той же формулы (43), въ кото-
рой сі/ извѣстно изъ разсмотрѣнныхъ выше
опытовъ надъ ртутью, и у/ вычисляется на
основаніи наблюденій по только что приведен-
ной формулѣ.
На рис. 48,а изображенъ простой дила-
тометръ, на рис. 48,Ь дилатометръ О 81 -
тга 1 (Га съ добавочной трубкой, служащей для
быстраго наполненія прибора испытуемой жид-
костью ; въ послѣднюю погружаютъ верхній ко-
нецъ перевернутаго прибора и вытягиваютъ
воздухъ изъ него высасываніемъ изъ добавоч-
ной трубочки. Эту трубочку закрываютъ сур-
гучомъ, особымъ краномъ или придавленной къ
отверстію пластинкой послѣ того, какъ изъ нея
вытекла лишняя жидкость; такимъ образомъ
весьма удобно наполнить трубку до желатель-
ной черты. Чтобы при нагрѣваніи прибора до /°
не имѣть дѣла съ длиннымъ выступающимъ
столбикомъ, О 8 1 лѵ а 1 (і помѣщаетъ вдоль трубки
рядъ вздутій, емкости которыхъ должны быть из-
Рис. 49.
вѣстны ; такой дилатометръ изображенъ на рис. 49.
Производя измѣренія при различныхъ температурахъ і, можно опре-
дѣлить какъ функцію температуры вида
Ѵо/
— «о +
если извѣстно, какъ фунція температуры. Коеффиціентъ расширенія а
при іР опредѣлится по формулѣ а = а0 ф- 2а^-]- За2Р.
Вѣсовой дилатометръ по устройству и методу употребленія тож-
дественъ съ вѣсовымъ термометромъ, разсмотрѣннымъ на стр. 47. Мы вы-
вели для него формулу (27) стр. 48
а іі) = Ро(1 ф-
гдѣ Ро и вѣса жидкости, наполняющей сосудъ при 0° и /°, и и
средніе коеффиціенты расширенія жидкости и стекла между 0° и /°. Про-
дѣлавъ опытъ со ртутью, для которой а* извѣстно, найдемъ повто-
ривъ затѣмъ опытъ съ испытуемой жидкостью, мы найдемъ для нея
112
Объемъ и давленіе тѣлъ.
На стр. 101 и 102 былъ помѣщенъ обзоръ способовъ опредѣленія те-
плового расширенія жидкостей. Изъ этихъ способовъ мы разсмотрѣли пер-
вый, второй и четвертый; на третьемъ и пятомъ мы не останавливаемся,
въ виду очевидной простоты теоріи этихъ способовъ.
§ 6. Тепловое расширеніе и термическій коеффиціентъ давленія
воды. Весьма большой интересъ представляетъ вопросъ объ измѣненіи
объема даннаго количества воды или, иначе, вопросъ объ измѣненіи плот-
ности воды въ зависимости отъ температуры. Интересъ этого вопроса
основанъ, во первыхъ на томъ, что водою пользуются при многихъ ме-
трологическихъ изслѣдованіяхъ, напр. при опредѣленіи удѣльныхъ вѣсовъ
по способу гидростатическому (т. I), во-вторыхъ на той важной роли, ко-
торую вода играетъ въ природѣ и, наконецъ, въ-третьихъ, на той замѣ-
чательной особенности, которую представляетъ расширеніе воды, имѣю-
щей максимумъ плотности около 4°, т.-е. расширяющейся, какъ при на-
грѣваніи, такъ и при охлажденіи, если то и другое начинать съ этой
температуры.
Коепі^еп, Н-п (І8оп,8ои1ег1ап(1, ѵ ап Ь а а г идр. ста-
рались объяснить расширеніе воды ниже 4°, исходя изъ опредѣленныхъ
представленій о молекулярномъ строеніи воды и льда ѵсм. т. 1, ученіе о
жидкостяхъ ).
О существованіи температуры наибольшей плотности воды было из-
вѣстно уже Флорентійскимъ академикамъ, открывшимъ это свойство воды
около 1670 г. Точныя опредѣленія температуры наибольшей плотности
воды были впервые произведены около начала ХІХ-го столѣтія. Эти опре-
дѣленія производились по тремъ различнымъ способамъ.
1. Способъ НаПйігое ш’а; этотъ способъ основанъ на опре-
дѣленіи плотности воды при различныхъ температурахъ путемъ опредѣле-
нія потери вѣса въ этой водѣ нѣкотораго тѣла, коеффиціентъ расшире-
нія. а слѣд. и плотность котораго извѣстны при тѣхъ же различныхъ
температурахъ. НаПзігоет опредѣлялъ потерю вѣса въ водѣ сте-
кляннаго шарика: кромѣ того онъ изслѣдовалъ тепловое расширеніе
трубки, приготовленной изъ того же сорта стекла, какъ и шарикъ. Объ-
емъ Ѵі шарика при /° могъ быть выраженъ формулою вида Ѵ(= Уо(1 4~
4~ аі 4~ Ы2): потеря вѣса Р; того же шарика въ водѣ при /° формулою
вида Рі = Ро(1 + + СР). Раздѣляя Р{ на Ѵ7, Наіібігоет
находилъ плотность воды при /°, выраженную черезъ плотность б/0 =
= Ро: Ѵо при 0°.Оказалось, что
(1І = 4- 0,000052939/ 0,0000065322Р 4~ 0,00000001443Р).
Эта формула даетъ наибольшую плотность при 4°,108, равную 1.00010824,
если положить б/0=1. Этимъ же способомъ пользовался МаііЬіезеп,
который, однако, избѣжалъ одного изъ возможныхъ источниковъ погрѣшно-
стей въ опытахъ НаНйігое ш’а, опредѣляя потерю вѣса въ водѣ куска
стекла, отрѣзаннаго отъ того же стекляннаго стержня, коеффиціентъ рас-
ширенія котораго онъ измѣрялъ.
Объемъ и давленіе воды\
113
II. Способъ Норе и КишіогсГа заключается въ слѣдующемъ: въ
боковую стѣнку вертикальнаго сосуда, наполненнаго водою, вставленъ
рядъ горизонтально расположенныхъ'термометровъ; резервуары ихъ нахо-
дятся въ водѣ на оси сосуда, одинъ надъ другимъ, причемъ одинъ изъ
нихъ располагается около дна сосуда и одинъ недалеко отъ поверхности
воды. Весь сосудъ подвергается медленному охлажденію, во время кото-
раго слѣдятъ за показаніями всѣхъ термометровъ. Слои воды всегда рас-
полагаются такимъ образомъ, что болѣе плотные опускаются ко дну со-
суда, а наименѣе плотные поднимаются къ поверхности. Когда темпера-
туры і слоевъ всѣ выше температуры х наибольшей плотности воды, мы
имѣемъ внизу наиболѣе холодный, а у поверхности наиболѣе теплый слой;
когда-же і сдѣлается меньше искомаго х, то наоборотъ, наиболѣе холод-
ная вода располагается у поверхности воды, а наиболѣе теплая — около
дна сосуда. Изучая переходъ отъ одного распредѣленія температуръ къ
другому, можно опредѣлить температуру х, какъ это видно изъ рис. 50,
на которомъ показаны результаты опытовъ, произведенныхъ В е р г е I г.
Ординаты изображаютъ температуры четырехъ термометровъ, изъ кото-
рыхъ № 1 нижній, а № 4 верхній, какъ функціи времени; О А общая на-
чальная температура всѣхъ термометровъ. На рисункѣ ясно видна пере-
мѣна въ распредѣленіи температуръ: сначала № 1 имѣетъ наиболѣе низ-
кую температуру, а потомъ № 4. Для опредѣленія искомой температуры х
В е р г е і г поступилъ такъ: онъ взялъ, во-первыхъ, среднюю изъ темпе-
ратуръ, при которыхъ происходятъ рѣзкіе переходы кривыхъ къ направ-
ленію почти параллельному оси абсциссъ; во-вторыхъ среднюю изъ ор-
динатъ точекъ пересѣченія кривыхъ между собою; въ третьихъ — сред-
нюю изъ точекъ пересѣченія четырехъ кривыхъ съ кривою (не начерчен-
ною) средней температуры всей массы воды и, наконецъ, въ четвертыхъ —
среднюю изъ полученныхъ такимъ образомъ трехъ величинъ. Оконча-
тельно В е р г е і г нашелъ для температуры х наибольшей плотности воды
х = 3°,987.
Этимъ способомъ пользовались Т г а 11 е 8, В и ш { о г й , Н а 11 -
еігоет и, впослѣдствіи, Г. Ехпег, Ь. ЛѴеЬег и Сорреі. Ехпег
измѣрялъ температуры слоевъ воды при помощи термоэлектрическихъ
паръ и нашелъ х = 3°,945; ЛѴеЬег нашелъ х между 4°,08 и 4°,09,
число, по всей вѣроятности, слишкомъ высокое. Сорреі (1894 и 1903)
КУРСЪ ФИЗИКИ О. X В О Л Ь С О Н А. Т. III, изд. 3-е. 8
114
Объемъ и давленіе тѣлъ.
особенно тщательно устранившій различные источники погрѣшностей,
нашелъ
х = 3°,98
по водородному термометру (около 4°,005 по ртутному;.
III. Способъ дилатометра; это обычный способъ изслѣдо-
ванія расширенія жидкости въ сосудѣ, имѣющемъ видъ термометра, раз-
смотрѣнный на стр. 111. Этимъ способомъ расширеніе воды изучали
Вергеіг, Ріегге, Корр, ЛѴеійпег, Козеііі, Мппке
и, въ послѣднее время, бсйееі. Коеффиціентъ расширенія сосуда дол-
женъ быть извѣстенъ. Чтобы опредѣлить тем-
пературу х наибольшей плотности, О е р г е I 2
воспользовался слѣдующимъ графическимъ спосо-
бомъ. На оси Ой (рис. 51) онъ откладывалъ тем-
пературы воды, на ординатахъ кажущіеся объемы
воды въ термометренномъ сосудѣ. Такимъ обра-
зомъ онъ получилъ кривую, напоминающую па-
раболу. Истинные объемы получатся, если къ
кажущимся объемамъ прибавить увеличенія ем-
кости сосуда. Для этого онъ провелъ прямую Ос
такъ, чтобы ея ординаты йс равнялись увеличеніямъ емкости сосуда при соот-
вѣтствующихъ температурахъ. Точка і касанія касательной псі. параллель-
ной Ос. и опредѣляетъ своею абсциссою Оа искомую температуру х. ибо ей со-
отвѣтствуетъ наименьшая ордината іЬ на осяхъ ѴОс. Вергеіг провелъ
рядъ хор,дь, параллельныхъ Ос. и затѣмъ прямую, проходящую черезъ
ихъ середины, принявъ, что точка пересѣченія кривой съ этой прямой и
есть искомая точка А
К о р р, весьма тщательно изслѣдовавшій расширеніе воды, нашелъ
х = 4°,08. Наиболѣе точныя изслѣдованія сдѣланы въ послѣднее время
Кг еі Піитомъ и, въ особенности, бей ее Гемъ по способу дилато-
метра. Изъ нихъ первый нашелъ 3°,973, а второй 3°,960 по водородному
термометру. Эти числа мало отличаются отъ числа 3°,98, найденнаго
С о р р е I (см. выше).
Вліяніе растворенныхъ въ водѣ веществъ на темпера-
туру х наибольшей плотности изслѣдовали О е р г е 12, К а г 81 е п, В о -
зеѣіі, Вепсіег, Р. Ленцъ, ЕйсіогГ, Ьизаппа, Виггоіа,
Сорреѣ, Реіііпеііі и М а г о 1И, № о г 1 (эфиръ), Сіпеііі и Мо-
г е 11 о (алкоголь) и др. Оказывается, что присутствіе растворенныхъ ве-
ществъ въ водѣ понижаетъ температуру наибольшей плотности воды.
Такъ, напр., Вергеіи находитъ слѣдующія числа (р число граммовъ
вещества въ 997,45 гр. воды):
р X р X
Морская вода. — 3°,67 /с2со8 . . . 37,039 — 3°,95
ЫаСІ. . . . 12,346 + 1,19 74,078 — 12,41
37,039 — 4,75 Ыа;>СОъ . 37,039 — 7,01
74,078 16.00 74,078 — 17,30
Объемъ и давленіе воды.
115
СаС1.2 .
К25О4 .
Ыа^ЗО^.
Р
6,173
24,692
74,078
74,078
37,039
X
+ 3,24
4- 0,06
— 10,43
— 8,37
— 4,33
Алкоголь
Н2ЗО, .
Р
74,078
12,346
24,692
37,039
2,30
0,60
1,92
5,02
Пониженіе Дх температуры х приблизительно пропорціонально ко-
личеству р раствореннаго вещества, какъ это видно изъ нижеслѣдующихъ
чиселъ Е о 8 е Н і, относящихся къ . растворамъ ЫаСІ. Здѣсь р число
граммовъ, растворенныхъ въ 100 гр. . Дх р Дх Р 0,5 1° 2,00 1 2,23 2,23 2 4,58 2,29 3 7,24 2,41 Дх Среднія значенія для разлі воды. А Дх р Дх Р 4 9,63 2,41 6 15,07 2,51 7 17,69 2,53 8 20,62 2,58 ічныхъ солей равны: •
Дх ^аС^ СаСІ-2 К2СО* = 2.40 1,61 2.21 2Ѵа2СО3 /С2$О4 2,93 1.70 Ыа2ЗО± 2,27.
Р Сорреі (1899—1903) опредѣлилъ м о л е к у л я р н о е пониженіе
температуры наибольшей плотности, т.-е. величину О: т, гдѣ О наблю-
денное пониженіе, а т число граммъ-молекулъ соли, растворенныхъ въ
1000 гр. воды. Для КС/, ЫаСІ и Р^ЬСІ онъ нашелъ для величины О: т сред-
нія значенія, равныя 11,7, 13,3 и 11,7; ІлСІ дало 6,0 и І^Н±СІ число 7,2.
Бромиды дали большее пониженіе, чѣмъ хлориды, а іодиды большее, чѣмъ
бромиды.
Р. Ленцъ опредѣлилъ температуру х для растворовъ смѣсей
М§С/2, КС/. СаЗО^ Мё30, и ЫаСІ различной плотности, составлявшихъ
какъ бы искусственную морскую воду. При плотностяхъ этихъ раство-
ровъ, мѣнявшихся отъ 1,00710 до 1,03812, Р. Ленцъ нашелъ, что тем-
пература х мѣняется отъ -|~ 2°,2 до — 5°,3.
Би8аппа и Вигяоіа нашли для чистой воды вѣроятно слиш-
комъ высокое число х = 4°,15, а для растворовъ КЫО& ЫсМО%, Ва(РЮ3)2
и т. д. различныя болѣе низкія температуры. Такъ, напр., для раствора
3,3365 гр. въ 100 гр. воды, плотность котораго 1,02803, они
нашли х = 0°,52. Тишіігг (1910) нашелъ, что для слабыхъ ра-
створовъ этиловаго спирта температура х наибольшей плотности
лежитъ выше, чѣмъ для чистой воды; при увеличеніи крѣпости ра-
створа, х понижается и для 4,775 гр. спирта на 100 гр. воды х такое же,
какъ для чистой воды.
8*
116?
Объемъ и давленіе тѣлъ*
Ѵап сіег АѴ а а 18 теоретически нашелъ, что съ увеличені-
емъ внѣшняго давленія температура х наибольшей плотности должна
гіонижаться, такъ какъ сжимаемость воды увеличивается при ея охлаж-
деніи ниже 4°.
Пользуясь числами Сггавзі (т. Г), онъ находитъ, напр., что при
давленіи въ 10,5 атмосф. х = 3°,4. Опыты А ш а $ а і подтвердили
этотъ результатъ; вотъ нѣкоторыя изъ его чиселъ (р давленіе въ ат-
мосферахъ) :
р — 41,6 93,3 144,«
х = 3°,3 2°,О 0°,6.
Рис. 52.
На рис. 52 изображены изотермы воды для температуръ отъ 0° до 10°.
данныя Аша§аі. На оси абсциссъ отложены объемы, на ординатахъ
давленія. При р = 1 (близъ оси
абсциссъ) наименьшій объемъ со-
отвѣтствуетъ изотермѣ 4°; здѣсь
же изотермы попарно пересѣка-
ются, ибо объемы одинаковы при
3° и 5°, при 2° и 6°, при 0° и 8°.
Но по мѣрѣ увеличенія давле-
нія р (слѣдуетъ мысленно про-
вести прямыя параллельно оси
абсциссъ) мѣняется порядокъ
изотермъ; наименьшее ѵ соот-
вѣтствуетъ все болѣе понижаю-
щейся температурѣ и при наи-
большемъ давленіи, соотвѣтствующемъ верхнему краю рисунка, наимень-
шій объемъ приходится при 0°.
Ьибаппа произвелъ рядъ опытовъ, чтобы обнаружить вліянія да-
вленія р (атмосф.) на температуру х для растворовъ. Вотъ нѣкоторые
изъ результатовъ его опытовъ:
Вода чистая......................х = 4°, 10 0,0225 (р — 1)
1,30 гр. КМОь въ 100 гр. Н2О . , х = 1,84 — 0,0124 (р -1)
1,44 „ ЫаСІ « « « « . . х = 0,77 - - 0,0110(/2—1)
5,20 „ Си80± « « « « . . гѵ=—0.14 — 0.0053 (/?—1)
Чѣмъ ниже х при р = 1, тѣмъ менѣе вліяніе давленія на х.
* Покончивъ съ вопросомъ о температурѣ наибольшей плотности воды,
перейдемъ къ работамъ, относящимся вообще къ расширенію
В'оды; для практики особый интересъ представляетъ расширеніе воды
между 0° и 30°.
На стр. 112 мы уже привели эмпирическую формулу Наіі-
81 г о е ш'а для плотности воды, какъ функціи температуры і.
1 Корр находитъ, что объемъ воды между і = 25° и і = 100° не
можетъ быть выраженѣ одною эмпирическою формулою вида
Ѵі = 1 4- аі Ы? + сі*...................(44)
Объемъ и давленіе воды.
117
и даетъ различныя численныя величины коеффиціентовъ а. Ь и с для
трехъ температурныхъ промежутковъ 25°—50°, 50°—75° и 75°—100°.
Подобнымъ же образомъ Н е п г і с і даетъ три значенія трехъ коеффиціен-
товъ для интерваловъ 28°—50°, 50° —80° и 80°—-100°.
Весьма тщательныя измѣренія въ предѣлахъ между 0° и 100° про-
изводилъ Возеііі. Въ послѣднее время появился рядъ новыхъ изслѣ-
дованій расширенія воды, произведенныхъ Т Ъ і е 8 е п’омъ, Магек’омъ.
БсЬееГемъ, Сйарриіз, КгеіШп^’омъ, <1 е Ьаппоу и др. Тем-
пература приведена у этихъ наблюдателей къ водородному термометру;
Тйіезеп, а также Магек производили свои изслѣдованія по спо-
собу I — гидростатическому (взвѣшиваемое тѣло у обоихъ состояло изъ
горнаго хрусталя), остальные ученые по способу III — дилатометриче-
скому. Принимая объемъ и плотность при 3°,960 равными 1, 8 с 11 е е 1
находитъ: У1ОО = 1?043466; ^100 = 0,958345.
Въ предѣлахъ отъ 0° до 33° бсііееі находитъ
= Ѵо (1 -Н аі + Ы* + сР + еі%
гдѣ
а=—6427.10“"8, Ь = 85053. 1О“”10, с = — 67898. 10"“12, е = 40121. ІО""14.
Кгеііііп^ находитъ наибольшую плотность при 3°,973, и далѣе
а = — 6533,61.10“"8 6=86505.10“10, с = —74392.10“12, е=50024.10“14
Числа ТЬіезеп’а, Магек’а, ЗскееГя и наконецъ Кгеіі-
Ііп^’а весьма близки другъ къ другу, какъ видно изъ слѣдующей та-
блицы, въ которой объемъ при 4° принятъ равнымъ 1.
Магек. Тйіе зеп. ВсЬееІ. Кг еііііп^.
0° 1,000123 1,000132 1,000125 1,000128
1° 069 072 069 071
2° 030 030 030 030
3° 007 006 007 008
4° ООО ООО ООО ООО
5° 008 008 008 008
10° 267 270 269 270
16° 866 873 866 868
• 20° 1769 1771 1764 1766
25° 2940 2934 2930 2935
30° 4347 4346 4344 4350
33° — — < 5313.
Если объемъ при 0° принять равнымъ единицѣ, то бсііееі нахо-
дитъ минимумъ объема при 3°,960, равнымъ 0,9998748.
Для плотности воды приведемъ слѣдущую табличку:
ТЬіейеп. Магек. 8 с Ь е е 1. Скарриій. 1892 СЬарриіе. 1897
0° 0,9998696 0,9998767 0,9998748 0,9998681 0,9998674
5° 0,9999916 0.9999919 0.9999918 0.9999916 0.9999918
118
Объемъ и давленіе тѣлъ
Тйіезеп. М а г е к. 8 с Ъ е е 1. Скарриіе. СЬарриіе.
1892 1896
10° 0,9997296 0,9997327 0,9997309 0,9997285 0,9997272
15° 0,9991290 0,9991347 0,9991347 0,9991289 0,9991285
20° 0,9982327 0,9982339 0,9982399 0,9982327 0,9982328
25° 0,9970749 0,9970683 0,9970781 0,9970741 0,9970726
30° 0.9956731 0,9956720 0,9956746 0,9956787 0,9956755
40° — — — 0,9922443 0,9922471.
IV. Способъ сообщающихся сосудовъ. Въ 1897 г. по-
явилась работа ТЬіеяеп’а, ЗсйееГя и БіеезеІЬогзГа, изслѣдовав-
шихъ расширеніе воды по способу Биіоп^’а и Р е ѣ іѣ, т.-е. по способу
сообщающихся сосудовъ. Для плотности <5 они даютъ эмпирическую формулу
(;-3,98)* /4-283 (44 }
503570 * ?+67,26
Дальнѣйшія изслѣдованія ТЬіевеп’а по тому же методу появились
въ 1904 г.; они относятся къ температурамъ между 50° и 100°. Онъ на-
шелъ, что формула
й _ (/ — 3,98)2 і-\- 343
— 568290~~ ’ /-[-72,74
приложима отъ 25° до 100°. Еще лучше согласуется съ наблюденіями
формула
3,982)2 /+ 273 350 — /
— 466700 ‘ /-|-67 * 365- /’
Тйіевеп приводитъ, какъ окончательный результатъ всѣхъ сво-
ихъ измѣреній, таблицу, изъ которой мы выписываемъ нѣкоторыя числа:
1 0° (1 - <5)1О6 133 і 25° (1 — <5)106 2931 і 70° (1 — д)106 22192
1° 74 30° 4328 75° 25114
2° 32 35° 5942 80° 28169
3° 8 40° 7756 85° 31351
4° 0 45° 9756 90° 34657
5° 8 50° 11930 95° 38082
10° 273 55° 14269 100° 41625
15° 20° 874" 1771 60° 65° 16763 19406 102° 43074.
(Зп^ііеіто (1899) также пользовался способомъ сообщающихся со-
судовъ для изслѣдованія теплового расширенія жидкостей.
Изъ новѣйшихъ работъ упомянемъ изслѣдованіе Р1 а 1 о, Вотке
и Нагѣіп^’а (1900 г., между 0° и 60°), произведенное по методу гидро-
статическому и Ландезена (въ Юрьевѣ, 1902), опредѣлившаго по спо-
собу дилатометра измѣненіе объема воды между 30° и 80°. Принимая за
объемъ и давленіе воды.
119
единицу объемъ при 0°, Ландезенъ находитъ напр. такія числа для
объема воды:
30° 1,00421 50° 1,01194 70° 1.02254
35° 588 55° 1484 75° 2560
40° 767 60° 1691 80° 2882.
45° 970 65° 1965
Многіе ученые старались выразить эмпирическими формулами объ-
емъ воды, какъ функцію температуры. Кромѣ обыкновеннаго алгебраиче-
скаго многочлена (44) стр. 116, были предлагаемы и другія формулы, бо-
лѣе сложныя. Такъ МаііЬіевеп далъ формулу
Ѵі — 1 — — 4) -|- Ь(і — 4— (\і — 4)3,
гдѣ для і между 4° и 82° постоянныя а = 258 . ІО-8, Ь = 54724 . 1О~10,
с=7178 . 10~п. Козеііі предложилъ болѣе общую формулу вида
Ѵі = 1 + а(і — 4)а4- Ь(і — 4)^4- С(і — 4)Л
гдѣ а, Ь, с, а, /? и у постоянныя числа.
Вопросомъ о расширеніи воды весьма много занимался Д. И. М е н д е -
лѣевъ. Въ статьѣ «Объ измѣненіи плотности воды при нагрѣваніи* (1891)
онъ предложилъ формулу, дающую плотность воды для температуръ отъ
— 10° до + 200° (опыты опредѣленія этой плотности ниже 0° и выше 100°
будутъ изложены ниже):
^ = 1-
А(В-\-іХС— О
(45)
Постоянныя оказались равными: Л = 1,9, В = 94,1 и С= 708,5.
Въ позднѣйшей работѣ Д. И. Менделѣевъ (1895) разсматриваетъ
послѣднія изъ вышеупомянутыхъ работъ (кромѣ работы Ктеііііп ^’а) и на-
ходитъ, что въ предѣлахъ между 0° и 80° плотность воды
можетъ быть представлена формулою вида
й/=1
4 + Він
(4б)
гдѣ температура по водородному термометру, А = 122420, В= 1180,2,
такъ что
<У( = 1_ — =1- «•“О88«Ѵ„^
122420 + 1180,2^ 108,825 -|- Ін
Новое изслѣдованіе, которое въ 1897 г. опубликовали ТЫебеп
НсЬееІ и Оіезз еійогві (стр. 118) привело Д. И. Менделѣева
120
Объемъ и давленіе тѣлъ.
къ формулѣ, подобной (45): онъ пишетъ ее въ видѣ
я _ 1 _ О2
(46, М
гдѣ Л = 118932, В— 1366.75 и С = —4.13.
Если медленно охлаждать воду, то, какъ мы увидимъ ниже, можно
довести ея температуру до — 10° безъ того, чтобы она затвердѣла.
Вергеіг, Ріегге и ДѴеідпег изслѣдовали измѣненіе объема
при такомъ «переохлажденіи» воды ниже 0°; оказывается,
что расширеніе, наблюдаемое при охлажденіи воды отъ 1° до 0°, про-
должается и при дальнѣйшемъ ея охлажденіи, какъ видно изъ слѣ-
дующихъ чиселъ:
і В ертеіг. Ріегге. АѴ е і а п е г.
4- 4° 1,0000000 1,0000000 1,0000000
0° 1,0001269 1,0001183 1,0001360
— 4° 1,0005619 1,0005565 1,0005490
— 8° 1,0013734 1,0012709 1,0013487
10° — 1,0018034 1,0019070.
При —10° объемъ воды такой же, какъ при -|-2Оо,5.
АѴаіегзІоп изслѣдовалъ расширеніе воды, заключенной въ тол-
стостѣнной трубкѣ при температурахъ отъ 100° до 320°, вводя поправку
на потерю испарившейся жидкости. Н і г п изучалъ ‘ расширеніе воды
между 100° и 200°, уравновѣшивая давленіе ртутнымъ столбомъ высотою
въ 10 м. Въ обоихъ опытахъ мы имѣемъ дѣло съ расширеніемъ воды,
находящейся подъ значительнымъ давленіемъ. Принимая объемъ воды
при 4° равнымъ единицѣ, ХѴаіегзіоп находитъ слѣдующія числа для
объема Ѵі воды при температурахъ і
І і Уі
100° 1.0433 260° 1.2896
140° 1,0813 300° 1,4181
200° 1,1612 320° 1,5098.
Нігп, результаты опытовъ котораго заслуживаютъ большаго довѣ-
рія, выразилъ объемъ V/ между 100° и 200° эмпирическою формулою вида
Ѵі = 1 + аі + Ы? + сР + (іі\
а = О,О3Ю867875 Ь = 0,0б30073653
с = 0,0^28730422 (і = — 0,0п6645703.
Это даетъ (Ѵо = 1):
і Уі і Уі
100° 1,04315 160° 1,10149
140° 1,07949 200° 1.15777
Объемъ и давленіе воды.
121
Числа Нігп’а показываютъ, что коеффиціентъ расширенія а воды
быстро растетъ съ повышеніемъ температуры. Между 100° и 120° имѣемъ
« = 0,00080; между 180 и 200° оказывается а — 0,00155, что составляетъ
уже почти половину коеффиціента расширенія газовъ.
Во всѣхъ предыдущихъ опытахъ вода предполагалась чистою и не
содержащею воздуха. Плотность воды, содержащеіі воздухъ,
между 0° и 20° нѣсколько меньше плотности чистой воды; выше 20° эта
разница дѣлается незамѣтной. Наибольшая разность равна 0,0000034 при 8°.
Тепловое расширеніе растворовъ изслѣдовали ОегІасЬ,
Магі^пас, Кгешегз, Р. Ленцъ и Н. Рѣзцовъ, ЕогсЬ, (1е
Ь а п п о у , Ландезенъ, Ваитііаиег, К г е і і 1 і п и ір. Боль-
шинство названныхъ ученыхъ изучали растворы солей, кислотъ и сахара ;
послѣдніе два — смѣси воды съ алкоголемъ. Никакіе простые законы
или правила при этомъ не обнаружились, кромѣ факта, что растворы кис-
лыхъ солей КН80± и МаН80± болѣе расширяются, а растворы основ-
ныхъ солей К>80± и Ыа.>8О± менѣе, чѣмъ растворы кислоты Н28О±. Для
солей фосфорной кислоты растворъ основной соли имѣетъ наибольшій,
растворъ кислоты наименьшій коеффиціентъ расширенія. Р. Ленцъ и
Н. Рѣзцовъ изслѣдовали расширеніе морской воды.
Ландезенъ (1904) изслѣдовалъ растворы КСІ, К28О±, М§80±.
СН^СООЫа, ІлСІ, (тростниковый сахаръ) и СО(А772)2 (мочевина).
Обращаясь къ вопросу о вліяніи давленія на тепловое
расширеніе воды, замѣтимъ, что о немъ уже было сказано въ
т. 1. Покажемъ прежде всего, какая связь существуетъ между зави-
симостью коеффиціента расширенія отъ давленія и зависимостью коеф-
фиціента сжатія отъ температуры. Обозначимъ черезъ ар средній коеффи-
ціентъ расширенія между температурами 0° и /° при давленіи въ р атмо-
сферъ, такъ что сц будетъ обозначать коеффиціентъ расширенія при
р = 1 атмосф.; далѣе обозначимъ черезъ коеффиціентъ сжатія при
температурѣ /° и черезъ /?0 коефф. сжатія при 0°. Пусть Ѵр д объемъ при
давленіи р и температурѣ ^°, и І/і,о объемъ при нормальномъ давленіи
и 0°. Разсмотримъ два перехода отъ К,о къ Ѵрі.
1. Нагрѣемъ жидкость отъ 0° до I® при давленіи въ 1 атмосф.;
объемъ превратится въ ІА,о (1 -ф- «10; увеличивая при температурѣ і дав-
леніе до р атмосф., мы получимъ объемъ
Ѵр,і — аі0(1 — А/7)-
2. Увеличимъ при 0° давленіе до р атмосф., вслѣдствіе чего объемъ
превратится въ Ѵі,о (1 — /?0), и затѣмъ нагрѣемъ жидкость отъ 0° до /°
при постоянномъ давленіи р\ ея объемъ сдѣлается равнымъ
Ѵрд = 1А,о(1 ^Р){ 1 -р «рО-
Сравнивъ два выраженія для величины мы получаемъ равенство
+ = 1 — /?о , ..............(47)
1 -|- арі і. _
122
Объемъ и давленіе тѣлъ.
Изъ этого равенства слѣдуетъ, что если > /?0, то ар < и, наобо-
ротъ, если то
Если коеффиціентъ сжатія увеличивается (умень-
шается) съ повышеніемъ температуры, то коеффиці-
ентъ теплового расширенія уменьшается (увеличива-
ется) съ повышеніемъ давленія.
Понятно, что вмѣсто 0° мы могли бы взять произвольную началь-
ную температуру и вмѣсто 1 атмосферы — произвольное начальное
давленіе /?0.
Мы видѣли (т. і), что для всѣхъ жидкостей, кромѣ воды, сжимае-
мость съ повышеніемъ температуры ѵвеличивается; отсюда слѣдуетъ,
что коеффиціентъ расширенія всѣхъ жидкостей, кромѣ
воды, при увеличеніи давленія уменьшается.
Для воды @ уменьшается отъ 0° до 60° и затѣмъ начинаетъ расти.
Отсюда слѣдуете, что между 0° и 60° коеффиціентъ расширенія
воды растетъ, а выше 60° уменьшается при возрастаю-
щемъ давленіи.
Съ этимъ вполнѣ согласуются результаты опытовъ Ата^аі; при-
боръ. которымъ онъ пользовался, описанъ въ т. 1 Ландезенъ нахо-
дите, что при 50° величина а независите отъ давленія.
Опыты А т а д а I даютъ возможность рѣшцть интересный вопросъ
о термическомъ коеффиціентѣ давленія воды, характери-
зующемъ увеличеніе давленія воды, нагрѣваемой при
постоянномъ объемѣ. Объ этомъ коеффиціентѣ уже было упомя-
нуто на стр. 11, гдѣ онъ для газовъ былъ обозначенъ черезъ ар, см. (22);
мы къ нему еще возвратимся въ термодинамикѣ.
На стр. 12 мы доказали, что для идеальныхъ газовъ термическій
коеффиціентъ давленія есть величина постоянная, равная термическому
коеффиціенгу объема. Для жидкостей, кромѣ воды, термическій ко-
еффиціентъ давленія приблизительно обратно пропорціоналенъ началь-
ному давленію, подъ которымъ жидкость находилась до нагрѣванія. Для
выясненія этого обстоятельства обозначимъ черезъ 7/ средній термиче-
скій коеффиціентъ давленія между 0° и /°, такъ что, если при 0° на-
чальное давленіе равнялось оно при 1° равно
р = Ро (і 4- Тіі)........................
откуда
I .......................(50)
V = СОП8І.
Термическій коеффиціентъ давленія при температурѣ і равенъ
йр
(11
Формула (4») даетъ для увеличенія давленія
Р—Ро = Ро7іІ ......... (51)
Объемъ и давленіе воды.
123
Мы увидимъ въ слѣдующемъ параграфѣ, что для изслѣдован-
ныхъ жидкостей, кромѣ воды, это увеличеніе давленія
приблизительно пропорціонально і и отъ начальнаго
давленія не зависитъ. Это значитъ, что приблизительно
Р^і=с . . . '.............(52)
гдѣ С постоянное число, т.-е. 77 обратно пропорціонально начальному
давленію р0. Для жидкостей представляетъ поэтому интересъ не вели-
чина 77, но скорѣе величина С, такъ что вмѣсто (48) слѣдуетъ разсма-
тривать равенство
Р — Ро + Сі ......... (53)
Для идеальныхъ газовъ, наоборотъ, = Сопзі = и потому
увеличеніе давленія р — /?0 пропорціонально начальному давленію /?0, или
обратно пропорціонально объему ѵ газа, при которомъ происходитъ на-
грѣваніе. Дѣйствительно, равенства рѵ = /? (273 -|- і) и р^ѵ = 273
даютъ при вычитаніи
_ № _ і
Р Ро— ѵ — Ро 273 •
Величина С можетъ быть вычислена, если извѣстны средній коеф-
фиціентъ расширенія между 0° и и коеффиціентъ сжатія Д при /°.
Обозначимъ черезъ Ѵо объемъ жидкости при 0° и начальномъ давленіи /70.
Нагрѣемъ жидкость до ^°, не мѣняя давленія; объемъ сдѣлается равнымъ
І/о (1 + а^)- Подвергнемъ ее теперь нѣкоторому давленію р, не мѣняя
температуры і. Объемъ сдѣлается равнымъ
Уо (1 + а/) [1 — Л (Р - РоЛ-
Выберемъ давленіе р такъ, чтобы получился прежній объемъ 1/0; тогда
имѣемъ
(1а/О[1 —&(Р Ро) | = 1 •
Но р есть давленіе жидкости, нагрѣтой отъ 0° до при постоян-
номъ объемѣ Ѵо, слѣд.
Р = Ро О 4- 7/0 = Ро + Сі-
Предыдущее равенство даетъ теперь
(1 + а,/) (1 - = I.
откуда
С=~=ДІТМ).......................(64)
Величины аг извѣстны при различныхъ начальныхъ давленіяхъ /?0,
и величины /3/ при различныхъ температурахъ Л слѣд. можно вычислить
величины С и давленія р жидкости при различныхъ температурахъ і,
если нагрѣваніе происходитъ при постоянномъ объемѣ и на-
124
Объемъ и давленіе тѣлъ.
чальное давленіе /?0 при 0° дано. Приводимъ интересную табличку ве-
личинъ р въ атмосферахъ, вычисленную Аша( для воды:
V Ро(О°) 5° 10« 200 300 400 50° 600 700 80° 900 100°
1.0000 1 — 3,7 34,5 92,4 171,5 272,2 395,5 512,0 665,0 820.5 986,5
0,9995 10,5 8,4 13,8 45,3 103,7 183,0 284,5 405,0 535,0 678,5 833,5 1000,0
0,9985 29,7 28,0 34,2 66,9 126,5 207.0 309,5 427,5 560,0 705,0 860,0 —
0,9975 49,0 48,0 54,5 89,0 149,5 231,0 333,5 453,0 586,5 731,0 887,0 —
0,9950 99,0 100,2 107,5 145,0 207,5 291,5 396,5 517,0 651,5 798,0 956,0 —
0,9900 201,0 205,7 216,8 260.0 327,0 415.0 622,5 647,0 784.5 934,5 — —
0,9800 416,0 427,8 445,0 500,0 578,0 674,0 790,0 922,0 — — — —
0,9700 647,0 666,0 691,5 758,0 847,0 954,0 — — — — — —
0:9600 895,5 923,5 654,5 — — — — — — — — —
0.9500 1170 — 1247 1344 1450 1596 1716 — — — — —
Въ первомъ столбцѣ помѣщены тѣ постоянныя объемы, при кото-
рыхъ происходило нагрѣваніе; они, понятно, уменьшаются съ возрастані-
емъ начальнаго давленія /?0, при которомъ вода находилась при 0°. Не-
правильности, которыя вода представляетъ при нагрѣваніи и при сжима-
ніи, рѣзко выражены въ этой табличкѣ. Такъ напримѣръ давленіе р
уменьшается при нагрѣваніи отъ 0° до 5°, когда начальное давленіе р§
не очень велико и возрастаетъ при большихъ /?0. Изъ таблички видно,
что если воду, находящуюся при 0° и давленіи р0 = 1, при постоянномъ
объемѣ нагрѣть до 100°, то ея давленіе дойдетъ до 986.5 атмосферъ.
Числа приведенной таблички показываютъ, что для воды С = р^ =^=
= (р — р0): і далеко не постоянное число ; увеличеніе р — р0 давленія
не пропорціонально і и зависитъ отъ начальнаго давленія р$ при 0°,
какъ видно изъ слѣдующей таблички:
Величины С = Ро?} =- - д л я воды.
РоОО- 1 -50 ОО_іоо()О—200 00—30° 00—40° 0«—50° 00—60° 0°—70° 0°—.80° 0°—90° 00—100°
0,27 1,67 3,05 4,26 5.42 6,58 7.30 8,30 9,10 9,85
10,5 — 0,33 1,74 3,11 4,31 5,50 6,58 7,49 8,35 9,14 9,87
29,7 — 0,45 1,86 3,23 4,43 5,60 6,63 7,58 8,44 9,22 —
49,0 — 0,55 2,00 3,35 4,55 5,69 6,73 7,67 8,52 9,31 —
99,0 0,24 0.85 2,30 3,62 4,81 5,97 6,97 7,90 8,74 9,50 —
210,0 0,94 1,58 2,95 4,20 5,35 6,43 7,43 8,33 9,17 — —
416,0 2,36 2,90 4,20 5,40 6,45 7,48 8,32 — — — —
647,0 3,80 4,45 5,55 6,66 7,54 — — — — — —
895,5 5,60 5,90 — — — — — — — — —
1170 — 7,62 8,53 9,51 10,53 11,17 — — — — —
Числа эти обозначаютъ среднее давленіе воды при нагрѣваніи на 1°
отъ 0° (когда начальное давленіе /?0) до /°. Непостоянство величины С
весьма рѣзко выражено при малыхъ і и небольшихъ /?0. При большихъ I
величина С приближается къ постоянству.
§ 7. Тепловое расширеніе и термическій коеффиціентъ давленія
другихъ жидкостей. Тепловое расширеніе различныхъ жидкостей было
предметомъ изслѣдованій многихъ ученыхъ: Вергеіг, Гіегге, Корр,
Нігп, ГгапкепЬеіт, Лугининъ, 2ап<1ег и др. Оказалось
Объемъ и давленіе жидкостей.
125
вробще возможнымъ выразить объемъ V жидкости эмпирическою фор-
мудрю вида ѵ = 2 + аі + Ьі2 + сі.................(55)
въ предѣлахъ отъ 0° до температуры кипѣнія жидкости при нормальномъ
давленіи. Постоянныя я, Ъ. с имѣютъ для различныхъ жидкостей весьма
различныя значенія, и пока не удалось найти простой зависимости междл
этими числами и химическимъ составомъ вещества. Общимъ правиломъ
оказывается, что расширеніе жидкостей растетъ вмѣстѣ
съ температурою, т.-е. что Ь и с величины положительныя.
Нѣкоторыя правильности, относящіяся къ молекулярнымъ объемамъ
жидкостей при точкахъ кипѣнія, будутъ упомянуты ниже.
Нігп измѣрялъ коеффиціенты расширенія нѣкоторыхъ жидкостей
для температуръ, лежащихъ выше ихъ точекъ кипѣнія, пользуясь спосо-
бомъ, упомянутымъ на стр. 111; онъ изслѣдовалъ алкоголь до 160°, эти-
ловый эфиръ до 120°, терпентинное масло до 160°, сѣроуглеродъ и хло-
роэтиленъ (С2С/4) до 150°. Объемы онъ выразилъ эмпирическою фор-
мужио вида ѵ = ! + аі + + сі.А +
Коеффиціенты расширенія жидкостей при высокихъ температурахъ,
вообще, весьма велики и иногда превышаютъ коеффиціентъ расширенія
газовъ (0,0036). Такъ, напр., Д. И. Менделѣевъ еще до Н і г п’а
нашелъ, что коеффиціентъ расширенія этиловаго эфира при 190° до-
ходитъ до 0,0054.
Средній коеффиціентъ расширенія С32 между 40° и 80° равенъ 0,00141,
между 120° и 160° онъ уже равенъ 0,00226. Еще большими коеффиці-
ентами расширенія обладаютъ ожиженные газы, какъ показали опыты
Ггіоп’а, Андреева, Тйііогіег, Сггішаісіі и Рісіеі. Приво-
димъ числа Андреева для жидкихъ 5О2, СО2 и ТѴ2О.
Средніе коеффиціенты расширенія жидкихъ:
между температурами 5О2 со2 МО
— 10° И 5° 0,00190 0,00190 0,00475 —
— 5° и 0° 194 200 492 0,00428
0° и 5° 198 210 540 422
5° и 10° 202 220 629 484
10° и 15° 206 230 769 656
15° и 20° 210 240 975 872
Расширеніе жидкихъ СО2 и Ы2О даже при низкихъ температурахъ
больше расширенія газовъ. ТЬііогіег находитъ, что средній коеффи-
ціентъ расширенія жидкой СО2 между 0° и 30° доходитъ до 0,017 (объемъ
увеличивается наполовину). Огіоп находитъ, что коеффиціентъ рас-
ширенія жидкой ЗО2 равенъ 0,001734 при 0°, и доходитъ до 0,009571
при 130° (критическая температура 156°). Наконецъ Рісіеі нашелц
для коеффиціента расширенія жидкаго ацетилена огромное число 0,01.
На стр. 122 мы указали, что коеффиціенты расширенія а
126
Объемъ и давленіе тѣлъ.
жидкостей (кромѣ воды) уменьшаются при увеличеніи
давленія, что и подтвердилось опытами Атадаѣ надъ одиннад-
цатью жидкостями; въ то же время оказалось, что при большихъ давле-
ніяхъ исчезаетъ зависимость коеффиціента расшире-
нія а отъ температуры. Въ видѣ примѣра приводимъ табличку
для этиловаго эфира; давленіе р дано въ атмосферахъ.
а . ІО6 для этиловаго эфира.
р 0°—20° 200—40° 40°—60° 600—80° 80°—100° 100°—138° 1380—198
50 1511 1687 1779 1947 2112 — —
100 1445 1523 1649 1782 1904 — —
200 1319 1390 1469 1522 1614 1749 2156
100 1153 1193 1225 1250 1305 1327 1436
600 1045 1060 1074 1086 1098 1115 1165
800 958 961 985 981 962 983 1008
900 926 931 940 926 928 923 946
1000 900 900 905 894 888 880 890
Другой рядъ опытовъ еще болѣе рѣзко подтверждаетъ указанное
правило, какъ показываетъ слѣдующая табличка:
а , , ІО6 для этиловаго эфира.
Р 0° - 20° 20° — 50°
1000 894 905
1500 752 788
2000 680 699
2500 633 620
3000 579 571-
На стр. 124 было указано, что величина р07/= (гдѣ
средній термическій коеффиціентъ давленія при нагрѣваніи жидкости при
постоянномъ объемѣ отъ 0° до /°,р0 начальное давленіе ир при /°)
есть величина для жидкостей, кромѣ воды, близкая къ постоянству. По
формулѣ (54) стр. 124 можно вычислить величины С—р^/ и давленіе р. При-
водимъ табличку давленій р въ атмосферахъ для этиловаго эфира, анало-
гичную табличкѣ для воды на стр. 124:
V Р<№) 10° 20° 30° 40° 50° 60° 70° 80° 90° 100°
1,000 1 101 200 299 396 493 588 684 778 870 962
0,990 71 176 280 383 484 584 683 781 878 — —
0,980 150 258 365 472 577 681 784 886 988 — —
0,970 239 351 462 572 681 790 899 1005 — — —
0,960 338 455 570 684 797 911 — — — — —
0,950 448 569 690 809 927 — — — — — —
ЧИНЪ На основаніи С: ЭТИХЪ чиселъ составлена слѣдующая табличка вели-
Объемъ и давленіе жидкостей
127
р—р°
С = р07і= - ( г
для этиловаго эфира.
Ро < 00—100 00—20° 00—30° 00—40° 0°—50° 00—60° 0°—70° 0°—80° 0°—90° 00—100”
1 10,00 9,95 9,93 9,90 9,86 9,80 9,76 9,71 9,66 9,61
71 10,50 10,45 10,40 10,33 10,26 10,20 10,14 10,09 — —
150 10,80 10,75 10,73 10,65 10,62 10,57 10,51 — — —
239 11,20 11,15 11,10 11,05 11,02 11,00 10,93 — — —
338 11,70 11,60 11,53 11,48 11,46 — — — — —
448 12,10 12,10 12,03 12.00 — — — — — —
Эти числа показываютъ, что увеличеніе р— р° давленія для эфира при-
близительно пропорціонально повышенію і температуры и мало зависитъ
отъ начальнаго давленія; совершенно другой результатъ дала намъ
табличка на стр. 124 для воды. у
Сагпаягі (1903) вычислилъ средній коеффиціентъ расширенія а 7
ртути между 22,8° и /° при давленіяхъ до 3000 атмосферъ. Мы приве-
демъ нѣкоторыя значенія величины а. ІО4 для различныхъ температуръ Л
52,8° 110° 150,3° 191,8°
1 атмосфера 1,809 1,817 1,827 1,830
1000 1,769 1,785 1,781 1,782
2000 1,692 1,757 1,723 1,732
3000 1,574 1,721 1,651 1,681
Многіе ученые старались замѣнить формулу (55) другою, съ мень-
шимъ числомъ постоянныхъ, или, по возможности, основанною на какихъ
либо теоретическихъ соображеніяхъ, или отличающеюся большею про-
стотой. Такъ напр. предлагалась формула
Ѵ=еаі,
гдѣ постоянная а различна для различныхъ жидкостей; но эта формула
не удовлетворяетъ опытнымъ даннымъ.
Большой интересъ представляетъ формула Д. И. Менделѣева
>/=т4м.........................,м)
отъ которой жидкости отступаютъ приблизительно такъ же, какъ газы
отступаютъ отъ формулы Гей-Люссака. Она представляетъ какъ
бы первое приближеніе, относясь къ своего рода «идеальнымъ» жидко-
стямъ. Для различныхъ жидкостей ' Д. И. Менделѣевъ находитъ к
между 0,00080 и 0,00155.
Теоретически вывели формулу (56) Д. П. Коноваловъ и Ьиіііег.
6. ВегіЬеІоі (1899) далъ для молекулярнаго объема V(объ-
емъ одной граммъ-молекулы) жидкости формулу
11,177
V— & л. тлитРамъ .... (56,а)
128
Объемъ и давленіе тѣлъ.
Здѣсь Тс абсолютная критическая температура; Рс критическое давленіе
(гл. XIII) въ атмосферахъ. Эта формула оказалась справедливой для цѣ-
лаго ряда жидкостей. Полагая Т = 273 мы видимъ, что зависимость V
отъ і здѣсь та же самая> какъ и въ формулѣ (56) Менделѣева.
Формулу подобную (56) предложилъ ЛѴиеПпет для нѣкоторыхъ
жидкостей (алкоголь, С52, ХпСІ^ въ тѣсныхъ предѣлахъ температуръ,
напр. отъ 10° до 30°. Авенаріусъ предложилъ формулу
Ѵ=а+ Ь\%(ТС — і)..................(57)
гдѣ Тс критическая температура жидкости. Жукъ нашелъ, что съ этою
формулою хорошо согласуются наблюденія надъ этиловымъ алкоголемъ
(С2НъО). Къ подобной же формулѣ пришелъ Сггітаісіі.
Маііеі и РтіейетісЫі902) придали формулѣ Авенаріуса видъ
V = а — Ь\%(А — і)...............(57, а)
въ которой а, Ь и А постоянныя. Оказалось, что для 25 жидкостей и до
температуръ, которыя на 30°—40° ниже критической, эта формула спра-
ведлива. Постоянная А оказалась на нѣсколько градусовъ выше крити-
ческой температуры. Отношеніе а : Ь всегда близко къ 3,78.
НеііЪогп вывелъ теоретически формулу
ѵ=н—\ ................<58)
Г I і VI8
[1—к\ек — 1 /]
гдѣ к и л двѣ постоянныя. 3 а е § е г предложилъ формулу
Ѵ=А + в\~*........................(59)
1 — гг
въ которой А и В двѣ постоянныя, а коеффиціентъ расширенія газовъ и
8 термическій коеффиціентъ капиллярной постоянной (т. I). Для ртути
А== 0,95262, В= 0,0738, € = 0,00013.
К а п к і п е предложилъ формулу
18у= — А + ВТ—....................(60)
гдѣ Т абсолютная температура, т.-е. Г = 273 -|-^
§ 8. Тепловое расширеніе и термическій коеффиціентъ давленія
газовъ. Теорія. Мы назвали идеальными такіе газы, которые строго
слѣдуютъ законамъ Бойля и Гей-Люссака; уравненіе состоянія,
связывающее объемъ ѵ, давленіе р и температуру мы писали для та-
кихъ газовъ въ видѣ рѵ = Р7\ гдѣ Т= - + абсолютная температура,
Объемъ и давленіе газовъ.
129
а коеффиціентъ теплового расширенія идеальныхъ газовъ. Такое зна-
ченіе буквы а мы сохранимъ и въ этой главѣ, т.-е. мы
обозначимъ черезъ а предѣльное значеніе, къ которому стремятся коеф-
фиціентъ теплового расширенія аѵ (при постоянномъ давленіи) и терми-
ческій коеффиціентъ давленія ар (при постоянномъ объемѣ) по мѣрѣ при-
ближенія свойствъ газовъ къ свойствамъ газа идеальнаго (см. ниже).
Измѣнимъ прежнее значеніе буквы /?, обозначая черезъ /? величину,
равную прежней 7?: а; тогда уравненіе состоянія идеальнаго газа при-
метъ видъ
= 7?(1 + а/).................(61)
Когда газъ нагрѣвается при постоянномъ давленіи/?, т.-е. свободно
расширяется, то его объемъ ѵ есть функція температуры и величину
аѵ=А{^\ ................(62)
\с“' )р = Сопеі.
мы называемъ просто коеффиціентомъ расширенія газа при
температурѣ і.
Когда газъ нагрѣвается при постоянномъ объемѣ ѵ, то его давленіе
р ееть функція температуры и тогда величину
а„= 1 ................(63)
Ро \ )ѵ=. С0П8І.
мы называемъ термическимъ коеффиціентомъ давленія при
температурѣ/. Для идеальныхъ газовъ, какъ было доказано на
стр. 12,
аѵ=ар = а......................(64)
Для реальныхъ газовъ аѵ и ар отличаются другъ отъ друга, и оба пред-
ставляютъ функціи состоянія газа, т.-е. они зависятъ напр. отъ р и /.
Для среднихъ коеффиціентовъ мы особыхъ обозначеній вводить
не будемъ, т.-е. мы положимъ
I.................(65)
^=М1+-а/) |
гдѣ теперь аѵ и ар средніе коеффиціенты между 0° и /°; понятно, что
и они суть функціи состоянія, т.-е. напр. величинъ р и і.
Слѣдуетъ помнить, что аѵ (коеффиціентъ объема) относится къ по-
стоянному /?, а ар (коеффиціентъ давленія) — къ постоянному ѵ. Легко
ошибиться, такъ какъ въ ученіи о теплоемкости газовъ мы привыкли къ
обозначеніямъ сѵ и ср> гдѣ сѵ относится къ случаю постояннаго % ср —
къ случаю постояннаго р.
КУРСЪ ФИЗИКИ О ХВОЛЬСОНА. т. III, изд. 3-е.
9
130
Объемъ и давленіе тѣлъ.
Нѣкоторые опыты даютъ величину среднюю между аѵ и ар; мы ее
обозначимъ черезъ а'. Эти опыты имѣютъ нынѣ уже только историческій
интересъ: при производствѣ этихъ опытовъ мѣняли и ѵ и р
Прежде чѣмъ перейти къ опытнымъ опредѣленіямъ величинъ аѵ и ар,
разсмотримъ теоретически вопросъ объ ихъ зависимости отъ ѵ и р.
Легко можно доказать, что ар или < аѵ, смотря по тому, въ ко-
торую сторону газъ уклоняется отъ закона Бойля. Допустимъ, что при
0° объемъ и давленіе равнялись г>0 и р0: нагрѣемъ газъ до /° при посто-
янномъ давленіи /?0, причемъ объемъ сдѣлается равнымъ
•^ = ^1 + аѵі).
Если же нагрѣть газъ отъ 0° до при постоянномъ объемѣ ѵ0, то по пу-
чится давленіе
р = р0(1 + «рО-
При одной и той же температурѣ і мы сперва имѣемъ величины р0,
ѵ, а потомъ р, ѵ0, причемъ р > р0. По закону Бойля рѵ^=р^ѵ; по-
слѣднія два выраженія даютъ
' /™0 = ...................(66)
Р<Р 1 + аѵі
Съ увеличеніемъ давленія для всѣхъ газовъ, кромѣ водорода, уменьшается
произведеніе упругости на объемъ, т.-е. рѵ^<іроО\ для Н имѣемъ на-
оборотъ рѵ^ > р^ѵ. Отсюда слѣдуетъ, что для всѣхъ газовъ, кромѣ
водорода, для водорода должно быть ар ^>аѵ.
Весьма интересно разсмотрѣть, какія указанія на свойства величинъ
аѵ и ар даютъ уравненія состоянія реальныхъ газовъ, предложенныя вза-
мѣнъ формулы (61). Между этими уравненіями первое мѣсто занимаетъ
уравненіе Ѵап (1 ег ХѴааІз’а, съ которымъ мы уже встрѣчались (т. I)
^=^0 4-«О....................(67)
Здѣсь а, Ь. /? и а постоянныя числа: а зависитъ отъ силъ, дѣй-
ствующихъ между частицами газа, Ь — отъ объема, который занятъ мо-
лекулами газа (ихъ сферами частичныхъ дѣйствій); /? постоянная, раз-
личная для различныхъ газовъ; а постоянная, одинаковая для всѣхъ га-
зовъ и равная коеффиціенту расширенія идеальныхъ газовъ. При а —
= Ь = 0 формула (67) переходитъ въ (61). Найдемъ ар и аѵ для газа,
уравненіе состоянія котораго имѣетъ видъ (67). Пусть т'о и р0 относятся
къ 0°, тогда (67) даетъ
[ро + Л | (®о — Ь) = /?.................(68)
При нагрѣваніи до упругость возрастаетъ до р, если объемъ оста-
Объемъ и давленіе газовъ
131
ется равнымъ г/0; (67) даетъ теперь
(р + (^0- Ь) = Н(1 + аІ)...................(69)
\ «'о'/
Если же нагрѣть газъ до при постоянномъ давленіи р0, то ѵ0 перейдетъ
въ ѵ, и (67) приметъ видъ
(р0 + (ѵ — Ь) = /?(1 Ц- аі).......................(70)
Искомыя величины ар и аѵ равны
а =Р--Р^ а =
Р Р.І ’ Ѵ
ѵ —
ѵ01
Раздѣляя (69) на (68), получаемъ
а
(1 4"
откуда
аР
а
Р<А>2
Іа
(71)
Въ добавочномъ членѣ можно, при не очень большихъ р0, положить
РоѴц = /?; тогда получается
а/’==і1 + Т°а.........................(72)
\ "-0 /
Раздѣляя (70) на (68), имѣемъ, сокративъ на р0,
Л_|_ а *) = (14- 0<1+«0.
\ РоѴ7 \ Роѵо I
Раскроемъ скобки, сократимъ и приведемъ подобные члены къ общему
знаменателю; тогда получимъ
аѵ0 Ьаѵ02 . аѵ Ьаѵ2 . , Л . а \ / Ь\
ѵ Ч-------о о = г/о4- — ч “Г а^о 1 4- 2 11 I-
Ро^о Ро® ^0 Ро^0 Ро^о' \ Ро^о / \ Ѵ0І
Перенеся три первыхъ члена справа налѣво и взявъ ѵ — ѵ0 за
скобки, получимъ для искомаго аѵ сложное выраженіе вида
гдѣ
. . (73)
9*
132
Объемъ и давленіе тѣлъ.
Если въ М подставить ѵ = ѵ0 (1 + аѵі) и пренебречь послѣднимъ
членомъ, то получается
2Ѵ=1 а ........................(14;}
РоѴ^ И +аѵі)
Если пренебречь всѣми членами, въ которыхъ встрѣчается произве-
деніе аЬ, и если произвести дѣленіе М на то получается приближен-
ное выраженіе
(Ху —
- . а Г 1
1 + —: 1 Н------:--
\ 1 "Н аѵІ
(75)
Сравнивъ съ (71), видимъ, что
. / а Ь\ , .
аѵ = ар + — 2/Т т л — «.............(76)
р \Р0ѵ0Ѵ + аѵі) ѵ0) Ѵ 7
Формулы (72), (75) и (76) приводятъ къ цѣлому ряду выводовъ, съ кото-
рыми мы ниже сравнимъ результаты опытовъ.
При а = Ь = О имѣемъ аѵ = ар = а, какъ и должно быть.
Когда а = О и Ь >> 0, то
аѵ
ар=а
1-Н»
®о/
(77)
При а = 0 имѣемъ, см. (67),
рѵ = /?(1 -(- аі) + др,
т.-е. произведеніе рѵ растетъ при возрастающемъ давленіи.
1. Если — 0, то п р о и з в е д е н і е рѵ р а ст е тъ при возраста-
ющемъ давленіи; = а; аѵ<ар, далѣе «^величина посто-
янная; «^уменьшается съ увеличеніемъ давленія (ибо ѵ^
уменьшается). Для водорода можно положить а= 0; для него рѵ растетъ
при возрастающемъ давленіи (т. I);. слѣд. для водорода мы
должны ожидать на основаніи формулы Ѵап сіег АѴааіз’а
(Хр = СопзЕ, аѵ<^ар и аѵ уменьшающееся съ увеличеніемъ
давленія.
Положимъ, что для нѣкотораго газа Ь = 0 и а > 0. Тогда
а
а
Ро^о2 (1 + <Ѵ)
(78)
, ><х.
Объемъ и давленіе газовъ.
133
Формула (67) даетъ
рѵ = /?(1 -|-аО— а;
ѵ
эта формула показываетъ, что съ увеличеніемъ давленія произведеніе рѵ
уменьшается (ибо ѵ уменьшается).
2. Если 6 = 0, то /^уменьшается съ возрастающимъ
давленіемъ:величины % и ар удовлетворяютъ неравен-
ству аѵ > ар а.
Полагая, что а >> 0 и 6 > О, мы получаемъ слѣдующіе результаты:
величина ар отъ Ь вовсе не зависитъ и если только а не нуль, то, какъ
видно изъ (71) или (72), ар должно расти вмѣстѣ съ давленіемъ и быть
больше а.
3. Для всѣхъ газовъ, кромѣ в о д о р о д а (я = 0), ар > а; да-
лѣе для всѣхъ газовъ ар растетъ при возрастающемъ да-
вленіи.
Температура і не входитъ въ выраженіе для а/?, если только а не за-
виситъ отъ температуры, что указывало бы на неполноту формулы V а п
Де г УѴ ааіз’а.
4. Коеффиціентъ ар для всѣхъ газовъ не зависитъ
отъ температуры і, если только величина а отъ і не за-
в и-с итъ.
Формула (75) показываетъ, что аѵ уменьшается, если і растетъ и
притомъ
5. Коеффиціентъ аѵ для всѣхъ газовъ, кромѣ водо-
рода (я = 0), уменьшается съ повышеніемъ температуры.
Для водорода % отъ температуры не зависитъ.
Зависимость аѵ отъ р въ общемъ случаѣ весьма сложная; для слу-
чая водорода (а = 0), какъ мы видѣли, см. (77) и № 1, аѵ уменьшается
при увеличеніи давленія. При не очень большихъ давленіяхъ, когда
можно принять (75) и когда вліяніе величины а больше вліянія величины
Ь, величина аѵ должна увеличиваться вмѣстѣ съ давленіемъ, т.-е. съ умень-
шеніемъ г/0. Нетрудно однако видѣть, что при большихъ давленіяхъ коеф-
фиціентъ аѵ долженъ начать убывать съ возрастаніемъ р. Обратимся къ
точной формулѣ (73). Величину 7И можно написать въ видѣ
М = І1 ч- Ьр°\ = (1 4- АРо) (1 - Вр0\
\ Ро^о)7 \ Ро^оІ
Эта величина имѣетъ, при А >* В, максимумъ и при нѣкоторомъ р0
начинаетъ убывать. Если для простоты положить ѵ = ѵ0, то
1 ~. “7, -1 ~Ар°(і - 2Вр°у
(Ро'Ѵо) \ РоѴО)
Эта величина имѣетъ минимумъ и при нѣкоторомъ р0 начинаетъ
расти Изъ сказаннаго ясно, что при нѣкоторомъ р0 слѣдуетъ ожидать,
что аѵ начнетъ убывать.
134
Объемъ и давленіе тѣлъ.
6. Для водорода аѵ уменьшается съ увеличеніемъ
давленія; для другихъ газовъ аѵпри небольшихъ давле-
ніяхъ вѣроятно растетъ, а начиная отъ нѣкотораго да-
вленія непремѣнно уменьшается съ возрастающимъ
давленіемъ.
Можно составить обзоръ всѣхъ результатовъ, вытекающихъ изъ фор-
мулы Ѵап <1 ег ЛѴааІв’а:
I. Для водорода: ар = а = СОП8І; аѵ < ар, отъ і не зависитъ и
уменшается, когда р растетъ.
II. Для всѣхъ газовъ, кромѣ во до род а: аѵ >> ар >> а; ар
отъ і не зависитъ (если а отъ I не зависитъ) и растетъ вмѣстѣ съ р;
аѵ уменьшается, когда і растетъ ; при увеличеніи давленія аѵ при малыхъ
давленіяхъ растетъ, если а велико въ сравненіи съ Ь, и во всякомъ слу-
чаѣ убываетъ при очень большихъ давленіяхъ.
Нѣкоторые ученые (А п (і г е 8, Аша^аі) изслѣдовали нѣсколько
иные коеффиціенты, чѣмъ разсмотрѣнные выше аѵ и ар, опредѣляемые
формулами (65), въ которыхъ ѵ0 и р0 всегда относятся къ 0°. Допустимъ,
что при і)0 объемъ и упругость равнялись и р±, и что при нагрѣваніи
до 4° ПРИ постоянномъ рг объемъ ѵ1 переходитъ въ г/2, а при постоян-
номъ упругость рг переходитъ въ р2. Тогда новые коеффиціенты а'ѵ
и а‘р опредѣлятся изъ равенствъ
ѵ2 = Ѵі [1 + а‘ѵ (і2 -<)] | (79)
Легко найти выраженіе для а'р на основаніи формулы (67). если по
стоянный объемъ обозначимъ черезъ ѵ (безъ значковъ):
ІР1 + л) О = + а^)
\ ѵ I
(рэ + (у — Ь} = /?(1 н- а4)
Раздѣливъ второе равенство на первое, получаемъ на основаніи вто-
рого равенства (79)
а
а
ргѵ2] 1 + а?!
(80)
При ^ = 0.это уравненіе переходитъ въ (71).
Мы увидимъ ниже, что нѣкоторые опыты, въ особенности надъ СО2,
приводятъ къ результатамъ, несогласнымъ съ формулою (67) Ѵап (іег
АѴ а а 18’а. Въ т. I была уже упомянута формула СI а и 8 і и 8’а,
которую можно разсматривать, какъ видоизмѣненіе формулы Ѵап (іег
\Ѵ а а 18’а. Если ввести абсолютную температуру Т — 1 + і, и вмѣсто а/?
а
Объемъ и явленіе газовъ.
135
писать /?, то послѣднюю формулу можно написать въ видѣ
РТ а
ѵ Ь ѵ2
С1аи8іп8 принимаетъ, что величина а обратно пропорціональна 7,
и вмѣсто ѵ2 вставляетъ (у + с)2, такъ что получается формула
нт а
п = —-------
ѵ — Ь Т {у ф- г)2
(81)
содержащая, кромѣ /?, три постоянныя Ь, с и (1.
Впослѣдствіи С1 а и 8 і и 8 остановился на уравненіи состоянія
Р = 1 — АТ -—В ...... (82)
ЦТ ѵ — Ь (т» + с)2
въ которомъ, кромѣ /?, имѣется пять постоянныхъ Ь, с, п, А и В
8 акта и предложилъ для СО2 уравненіе состоянія
р_ ЦТ КЕ т..................(83)
ѵ Ь ѵ + с
съ четырьмя постоянными Ь, с, К и Е
Ограничимся выводомъ выраженія для ар на основаніи первой фор-
мулы С1аи8ІИ8’а (81). Она даетъ, если постоянный объемъ обозначить
черезъ Ѵц.
/?7о (I
Ро = / т і ѵ>’
ЦТ (1
р =
ѵ0 Ь Т (ѵ + ЕР
Вычитая первое равенство изъ второго, вставляя Т 70=/ и раз-
дѣляя на получаемъ
К . 1 (8П
7 РР РРРѵ і>) РЛіРо + с)2 Т
Формула Сіаизіпв’а приводитъ къ результату, что ар
уменьшается съ возрастающею температурою Т,
Понятно, что тотъ же результатъ вытекаетъ и изъ формулы (71),
если вмѣстѣ съ Сіаивіпв’омъ допустить, что величина а обратно про-
порціональна Т.
§ 9. Тепловое расширеніе и термическій коеффиціентъ давленія
газовъ. Опыты. Первыя точныя опредѣленія коеффиціента расширенія
газовъ а0 были произведены Ѳау-Ьи88ас’омъ. Онъ наполнялъ шаръ А
(рис. 53) и часть трубки АВ, снабженной дѣленіями, испытуемымъ сухимъ
газомъ, отдѣленнымъ отъ наружнаго воздуха каплею ртути, положеніе
136
Объемъ и давленіе тѣлъ.
которой наблюдалось, когда шаръ и трубка до капли были сперва окру-
жены тающимъ льдомъ, а потомъ кипящею водою; температура послѣд-
ней измѣрялась термометрами Т и Р. Емкость шара и дѣленій трубки
были извѣстны. Изъ своихъ опытовъ Сгау-Ьияяас нашелъ
аѵ = 0,00375
(85)
для всѣхъ газовъ и также для паровъ (эфира); послѣдній результатъ даже
приблизительно не вѣренъ, какъ показали уже опыты Еіаи^ег^иев’а,
Рис. 53.
нашедшаго, что влажный воздухъ сильнѣе расширяется, чѣмъ сухой.
Число, почти одинаковое съ числомъ 6гау- Ъи я 8 а с’а, нашелъ Ваі-
іоп, а именно % = 0,00373; далѣе Ьопіопя и Реііі при своихъ
опытахъ надъ расширеніемъ ртути (стр. 103). косвенно вывели, что число
(85) дѣйствительно вѣрно.
Число (85) слишкомъ велико, какъ показалъ впервые ВисІЬег^
(1837); источникъ погрѣшностей въ опытахъ Сг ау - Ь и 8 8 ас’а былъ ука-
занъ М а яп ия’омъ (1842); онъ заключается въ томъ, что ртутная капля
представляетъ ненадежный затворъ для испытуемаго газа и что, смотря
по обстоятельствамъ, или часть раза выходитъ наружу, проходя между
ртутью и стекломъ трубки, или нѣкоторор количество наружнаго воздуха
входитъ во внутрь прибора.
ЕиДЬегя производилъ свои изслѣдованія двумя способами. Пер-
вый способъ даетъ нѣкоторую величину а', среднюю между аѵ и ар, мы
познакомимся съ этимъ способомъ ниже въ той формѣ, которую ему при-
далъ КеяпаиН. Второй способъ ЕийЬегя’а даетъ величину ар ; его
приборъ тождественъ съ газовымъ термометромъ, описаннымъ на стр. 18
въ томъ видѣ, который ему придалъ Ее^папН. Приборъ ЕисІЬегя’а
отличался отъ прибора Ее^папН болѣе простымъ устройствомъ; кромѣ
того ЕисІЬегя не вводилъ поправки на объемъ воздуха, находящагося
въ трубкѣ, соединяющей резервуаръ съ манометромъ. Въ точной фор-
мулѣ (9) стр. 20 у Е и а Ъ е г я’а не доставало вторыхъ членовъ въ скоб-
кахъ. Резервуаръ помѣщался сперва въ тающій ледъ, а затѣмъ въ пары
Объемъ и давленіе газовъ.
137
кипящей воды, такъ что температура, которая въ ур. (9) обозначена че-
резъ х, была извѣстна. Обозначая ее черезъ полагая ѵ = 0 и сокра-
щая на V, получаемъ вмѣсто (9)
Я(1 4- арІ) = //і(1 +
откуда и получается
ЕийЬег^ нашелъ по обоимъ способамъ одно и то же число для
а' и «р. а именно
а' = ар = 0,003646
вмѣсто 0,00375, найденнаго Оау -Ьиззас’омъ.
Ма^п и8 производилъ измѣренія по второму способу Ки сі Ь е гц’’а
и нашелъ
ар = 0,00366Ь.
Обращаемся къ классическимъ работамъ Ее^паиИ надъ расши-
реніемъ газовъ. Е е и а и 1 і опредѣлялъ интересующіе насъ коеффи-
ціенты тремя способами, видоизмѣняя два изъ нихъ, такъ что можно го-
ворить о пяти серіяхъ наблюденій, произведенныхъ по различнымъ
способамъ.
Способъ I Д, тождественный съ первымъ способомъ К и (1Ь е г ^’а,
даетъ нѣкоторую среднюю величину а', ибо газъ въ двухъ сравниваемыхъ со-
стояніяхъ имѣетъ различные ѵ и р. Сущность этого способа будетъ по-
Рис. 54. Рис. 55.
нятна изъ рис. 54 и 55. Цилиндрическій резервуаръ АВ (у Еий-
Ъег^’а шаръ) снабженъ капилярной трубкой, изогнутой подъ прямымъ
угломъ и оканчивающейся въ 22. Резервуаръ помѣщался сперва въ па-
рахъ кипящей воды, для чего служилъ приборъ, уже описанный нами на
138
Объемъ и давленіе тѣлъ.
стр. 29. Трубка АС присоединялась къ высушивающимъ трубкамъ С и С',
наполненнымъ кусочками пемзы, смоченной крѣпкой сѣрной кислотой;
Р насосъ. Чтобы высушить резервуаръ и наполнить его сухимъ газомъ,
Ке^паиИ до тридцати разъ выкачивалъ изъ него газъ и затѣмъ мед-
ленно вновь впускалъ въ него свѣжій газъ. Полчаса спустя послѣ послѣдняго
наполненія снималась соединяющая трубка около О и запаивалось от-
верстіе О трубки АСО; въ этотъ моментъ отмѣчалось барометрическое
давленіе Н и соотвѣтствующая ем^ температура і паровъ кипящей воды.
Приборъ затѣмъ вынимался изъ кипятильника, перевертывался, концомъ
СО опускался въ ртуть (рис. 55) и закрѣплялся при помощи рамки ЛКѴ<2<2',
тарелки ЕЕ' и винта V, какъ показано на рисункѣ. Кончикъ О запаян-
ной трубки отламывался подъ ртутью и резервуаръ АВ окружался таю-
щимъ льдомъ или снѣгомъ, положеннымъ на тарелку ЕЕ'; газъ сжимался
и ртуть поднималась вверхъ. Черезъ часъ закрывалось отверстіе О при
помощи маленькой ложечки К, содержащей воскъ и прикрѣпленной къ тп,
и записывалось барометрическое давленіе Н'. Затѣмъ ледъ удалялся и
посредствомъ катетометра измѣрялась высота И ртутнаго столба въ при-
борѣ. Для этого служилъ стержень і. нижнее остріе котораго доводилось
до соприкосновенія съ поверхностью ртути: длина стержня была извѣстна,
такъ что оставалось измѣрить вертикальное разстояніе верхняго острія і
отъ уровня ртути въ АВ. Давленіе, подъ которымъ находился газъ при ^°,
равняется, такимъ образомъ, Н' Л, что существенно отличалось отъ Н.
Далѣе взвѣшивался приборъ съ вошедшею въ него ртутью; вѣсъ ртути
обозначимъ черезъ Р; наконецъ опредѣлялся извѣстнымъ способомъ коеф-
фиціентъ у расширенія стекла, причемъ приходилось опредѣлить и вѣсъ Р
ртути, наполняющей весь приборъ при 0°. Пусть б плотность ртути
при 0°. Мы имѣемъ газъ сперва при
р
объемѣ (1 + . . . давленіи Н . . . температурѣ Р.
а потомъ тотъ же газъ при
Р Р'
объемѣ ... давленіи Н' Л . . . температурѣ 0°.
Обозначая въ этомъ случаѣ коеффиціентъ
имѣемъ очевидно
расширенія черезъ а',
или
с_(1.±ъ0
Р — Р'
6
Р (і 4- /О н
(Р -ргХН'—К)
^6)
откуда и получается а .
Способъ ІЛ В отличался отъ предыдущаго
при 0° и мало отличались другъ отъ друга.
тѣмъ, что объемы газа
Достигалось это тѣмъ,
О
Объемъ и давленіе газовъ.
139
что трубка бралась болѣе длинная, такъ что ртуть, поднимаясь, не вхо-
дила въ шаровидный резервуаръ. На рис. 5б показанъ видоизмѣненный
приборъ. Посреди трубки находилась нѣсколько расширенная часть, въ
которой и помѣщался верхній уровень ртутнаго столба; при измѣреніи
длины столба А, приходилось ввести поправку на капилярную депрес-
сію. Формула та же (86), но она даетъ величину, которую можно при-
нять равною ар.
Способъ II, А представляетъ усовершенствованіе второго спо-
соба ВиІЪег^’а. Приборъ не что иное, какъ описанный нами на
стр. 18 и изображенный на рис. 1 газовый термометръ. Тѣ же манипу-
ляціи, которыя были описаны въ указанномъ мѣстѣ, приводятъ къ фор-
мулѣ (9), въ которой, однако, вмѣсто х слѣдуетъ вставить извѣстную намъ
температуру Т паровъ воды, кипящей въ резервуарѣ М,
Такимъ образомъ мы имѣемъ формулу
\ 1 арі} \ 1 + арТ 1 +• арІ1)
(значеніе буквъ см. стр. 19 и 20). Вводя, какъ и на стр. 20. величину
= ѵ_ / 14- _ 1 4-
ѵ । і 14~ ^р^і 14~ ^рі I
получаемъ, соотвѣтственно формулѣ (10) на стр. 20. если положить х = Г.
_//1(1 + ?П ЯН-0
р ~ ( Н О) Т
(8Н)
Величина ар заключается въ самомъ о: но такъ какъ величина о
малая, то достаточно при ея вычисленіи принять ар = 0,00367 и затѣмъ
на основаніи (88) вычислить болѣе точное значеніе этого коеффиціента.
Способъ II. В отличался отъ предыдущаго только примѣненіемъ
иначе устроеннаго манометра.
Способъ III. Этотъ способъ даетъ коеффиціентъ расширенія аѵ,
такъ какъ газъ расширяется при постоянномъ или, по крайней мѣрѣ,
почти постоянномъ давленіи. Приборъ, которымъ пользовался Е е -
^паиіі, отличался отъ описаннаго на стр. 18 и изображеннаго нарис. 1
иначе устроеннымъ манометромъ. Трубка р (рис. 57) соединяетъ ре-
зервуаръ съ манометромъ, погруженнымъ въ воду, которая непрерывно
перемѣшивается мѣшалкою оо'; ея температура опредѣляется термоме-
тромъ. Лѣвое колѣно манометра имѣетъ расширенную часть, снабженную
дѣленіями и тщательно прокалибрированную. Въ нижнихъ частяхъ двухъ
колѣнъ манометра находятся краны г и г'; послѣдній отдѣльно изобра-
женъ въ разрѣзѣ въ В'. Онъ даетъ возможность, смотря по его положе-
нію, соединить оба колѣна только между собою (боковой каналъ вверхъ),
оба колѣна сразу открыть (каналъ направо), открыть только лѣвое колѣно
(налѣво) или только правое колѣно (внизъ). Когда резервуаръ находится
14П
Объемъ и давленіе тѣлъ
въ тающемъ льдѣ, доводятъ ртуть
чество газа взято такое, что при
въ лѣвомъ колѣнѣ до черты на; коли-
этомъ давленіе газа мало отличается
Рис. 56.
отъ атмосфернаго, такъ что въ обо-
ихъ колѣнахъ ртуть находится почти
на одномъ уровнѣ. Обозначимъ че-
резъ V объемъ резервуара и черезъ ѵ
объемъ соединительной трубки до
черты па, оба объема при 0°; пусть
далѣе у коеффиціентъ расширенія
стекла резервуара и трубки, Н да-
вленіе газа при 0°, мало отличаю-
щееся отъ барометрическаго, такъ
какъ уровни ртути въ обоихъ колѣ-
нахъ почти одинаковые; наконецъ
пусть і температура части трубки до
черты аа. Газъ занимаетъ объемъ V
при 0° и ѵ (1 + уі) при ^°. Если
бы онгь весь находился при 0°. то онт» имѣлъ бы
Рис. 57.
объемъ
Ѵо +
V (1 4- у/)
1 -|—
при давленіи Н.
Нагрѣвая затѣмъ резервуаръ въ парахъ кипящей воды до нѣкоторой
температуры 7, даютъ газу свободно расшириться, выпуская ртуть изъ
обоихъ колѣнъ манометра такъ, чтобы уровни ртути въ нихъ были по
возможности одинаковые. Газъ, расширяясь, перейдетъ въ лѣвое колѣно
манометра и наконецъ заполнитъ его до нѣкоторой черты /?, на высотѣ
которой уровень ртути приблизительно будетъ находиться и въ правомъ
колѣнѣ. Пусть ѵ' объемъ соединительной трубки и лѣваго колѣна мано-
метра до черты ,5 при 0°, Н' давленіе, подъ которымъ газъ находится и
которое мало отличается отъ барометрическаго, и слѣд. также отъ Н.
Газъ занимаетъ во второй части опыта объемъ (1 + 7?^ при и
ѵ (1 + 7^і) при температурѣ іг, Если бы температура газа равнялась 0°,
то онъ занималъ бы объемъ
1 7^" Г • 1 “Ь 7^1 • гг/
Ц) 1 _ц п т + ѵ 1 и / ПРИ Давлен1и Н •
По зикону Бойля имѣемъ
1 + гМ
і 4“
1 + 7Т , , 1_+ 7^і \ ...
1 + аѵ^ 1 Н- аіА/
отсюда
ЯЧ1 +7П
ѵ (і 4- /01 , ’
(89)
Объемъ и давленіе газовъ.
141
И здѣсь можно съ правой стороны для аѵ сперва подставить при-
ближенное выраженіе, напр., аѵ = 0,00367, и вычислить %, затѣмъ вста-
вить болѣе точное выраженіе и повторить вычисленіе.
Пять серіи опытовъ, произведенныхъ Ве^паиіі по разсмотрѣн-
нымъ способамъ, дали для воздуха слѣдующіе результаты :
Воздухъ.
Способъ І,Л а' 0,0036623 . . ѵ и р мѣняются.
Способъ 1.5 ар — 0,0036633 . . . ѵ почти постоянное.
Способъ II,А ар = 0,0036679 . . . ѵ постоянное.
Способъ 11,5 ар = 0,0036650 . . . ѵ постоянное.
Способъ ПІ аѵ = 0.0036706 . . . р постоянное.
Если взять среднее изъ трехъ значеній ар и сопоставить его съ по-
слѣднимъ числомъ, то получается
ар = 0,0036653 |
ар — 0,0036706 ]
(90)
Ее^паиіѣ изслѣдовалъ, кромѣ воздуха, рядъ другихъ газовъ,
причемъ получилъ слѣдующія значенія для ар и аѵ (числа для воздуха
повторены) :
Термическій коеф- фиціентъ давленія. (ѵ = Сопеѣ). Коеффиціентъ тепло- вого расширенія. (р = СОП8І.).
ар
Азотъ ..... 0,0036682 —
Водородъ 36678 0,0036613
Окись углерода . . 36667 36688
Углекислый газъ . . 36896 37099
Ціанъ 36821 38767
Закисъ азота . . . 36763 37195
Сѣрнистый газъ . 36696 39028
Хлористый водородъ 36812 —
Воздухъ 36653 36706
Вісйагсіз и Магк (1903) произвели весьма точное опредѣленіе
величинъ аѵ для Н2, Ы2 (не чистый) и СО2 между 0° и упомянутой на
стр. 6 постоянной температурой 32°,383 превращенія сѣрнонатровой соли.
Они нашли при давленіяхъ р:
Ы2 (не чистый) СО2
р 743 745 738 мм.
аѵ 0,003659 0,003660 0,003727
Что различные газы
было доказано Ее^паиИ
имѣютъ неодинаковые коеффиціенты ар
слѣдующимъ нагляднымъ опытомъ. Три
142
Объемъ и давленіе тѣлъ.
трубки 1г. И и і (рис. 58) соединены внизу между собою. Въ В и В'
трубки продолжаются горизонтально (не изображено) и ведутъ къ двумъ
резервуарамъ одинаковой емкости, содержащимъ различные газы въ та-
Рис. 58.
кихъ количествахъ, что ртуть въ НВ и !і' В' доходитъ до одной
высоты оо, когда оба резервуара находятся при 0°. Если на-
грѣть оба резервуара, въ і прилить столько ртути, чтобы ртуть
въ ІгВ опять доходила до уровня о, то ртуть въ И'В' будетъ
стоять выше или ниже этого уровня. На рисункѣ изображенъ
случай, когда справа находится воздухъ, слѣва углекислый газъ;
послѣдній расширяется сильнѣе перваго.
Числа К е § п а и 1Ь показываютъ, что для водорода ар ,
между тѣмъ какъ для всѣхъ другихъ газовъ аѵ >* ар. Въ пре-
дыдущемъ параграфѣ мы видѣли (стр. 134, I и II), что именно
такія отношенія и слѣдуетъ ожидать на основаніи формулы
Ѵап (1 ег ЛѴ а а 1з’а. Этимъ въ то же время подтвержда-
ется, что для водорода можно пренебречь постоянною а въ
этой формулѣ.
Л о 11 у нашелъ слѣдующія значенія для ар :
Водородъ . . 0,0036562
Азотъ. . . . 36677
Воздухъ . .
36695
Кислородъ . . 0,0036743
Углекисл. газъ 37060
Закись азота . 37067
СйарриІ8 изслѣдовалъ 27, ./V и СО2 при помощи прибора, опи-
саннаго на стр. 22 ^рис. 4 и 5); онъ нашелтэ:
ар
Водородъ .... 0,00366254
Азотъ................. 367466
СО2 .................. 372477
ЛѴ. НоІІтапп (1898) нашелъ для воздуха
аѵ — ар = 0,00000589.
Д. И. Менделѣевъ указалъ, что значеніе ар для воздуха, най-
денныя Ма&пий’омъ, Ее^паиН и ЛоНу. дѣлаются весьма близ-
кими другъ другу, если ввести поправку на измѣненіе силы тяжести въ
зависимости отъ широты мѣста наблюденія и еще нѣкоторую другую не-
большую поправку. Тогда получаются слѣдующія числа:
Ма§піі8 . .
Ее^паиН. .
Зоііу . . ,
Не исправлено. Исправлено.
ар для воздуха.
0.0036678 0,0036700
36650 36694
36696 36702.
Объемъ и давленіе газовъ.
143
Еескпа^еі нашелъ для воздуха ар = 0.0036682. Асіѵепіолѵвкі
(1909) нашелъ для ЫО величину аѵ = 0,0037074 между 0° и 140°.
Пользуясь формулою (71) стр. 131
=+ Аа)
а.
можно вычислить коеффиціентъ а для идеальныхъ газовъ. Возьмемъ
н&пр. число ар для азота; среднее изъ чиселъ Ее^паиіі и Л о 11 у
равно ар = 0,003668. Если за единицу объема принять объемъ ѵ0 ки-
лограмма газа при 0° и при давленіи въ 1000 мм., то изъ опытовъ
Ее^паиіі и А т ааI (т. I) надъ сжимаемостью азота полу-
чается а = 0,00303. Если же давленіе измѣрять въ атмосферахъ и за
единицу объема принять объемъ газа при 0° и давленіи въ 760 мм., то
а = 0,76 . 0,00303 = 0,0023. Въ этомъ случаѣ р0 =1, ѵ0 = 1. и слѣд.
ар = (1 4- а) а, откуда
0,003668
1,0023
= 0,0036609.
и дѣй-
Для водорода мы должны имѣть ар = а (стр. 134,1);
ствительно, для водорода среднее изъ чиселъ Ма^пив’а. Ее^паиіі и
«Іоііу равно 0,003661.
Новѣйшія изслѣдованія дали
иное число; сюда относится уже
Новыя числа суть:
однако для
упомянутое
о-р для /72.
водорода нѣсколько
опредѣленіе С1Ь а р р и і 8.
а —
(^р
1 —а
Сііарриів (1ь88).........
Каттегііп^й Оппев (1901)
Тгаѵегв апй Задиегой (1903)
Тгаѵег8 апй Ладиегосі (1903)
Для гелія:
Тгаѵегв аий <Іадиего(1 (1903)
0,00366254 . . . при 0° давл. 1000 мм.
0,0036627 . . . „ 0° „ 1000 „
0,00366255 ........ 0° „ 700 „
0,0036627 . . . „ 0° „ 500 „
0,00366255 . . . при 0° давл. 700 мм.
Весьма замѣчательно совпаденіе чиселъ Сііарриів и Тгаѵегв и
Я а ди его (Га для водорода, и тождество чиселъ, найденныхъ послѣдними
изслѣдователями для водорода и гелія. Они полагаютъ, что это число
остается неизмѣннымъ при всѣхъ начальныхъ давленіяхъ, которыя
меньше 1000 мм.
Ьейис (1909) вычислилъ истинныя и среднія значенія величинъ
% и ар для 20-ти газовъ, а именно для 77, А, СО, О, АО, СН^
СО2, С2776, А2О, С2772, 77С/, С2А2, С/73С/, С/, СН^Н2. 8О2,
Для триметиламмонія онъ находитъ напр.
аѵ = 0,004122, ар = 0,004038.
Обращаемся къ опытнымъ опредѣленіямъ зависимости ар и аѵ отъ
144
Объемъ и давленіе тѣлъ.
давленія и отъ температуры. Теоретическія предсказанія на основаніи
формулъ Ѵап йег ДѴааІв’а и Сіаивіиз'а изложены на стр. 134,
I и II и на стр. 135.
А. Зависимость ар и % отъ давленія р. Ве^паиіі
изслѣдовалъ зависимость ар отъ начальнаго давленія /?0 и 0°. Приводимъ
нѣкоторыя изъ его чиселъ для воздуха и для С02.
Воздухъ.
Начальное давл. ЮОар Начальное давл.
А> при 0°. ЮОар
Ро при 0°.
109,72 мм. 0,36482 760,00 мм. 0,36650
174,36 0,36513 1678,40 99 0,36760
266,07 » » 0,36542 2144,14 99 0,36894
374,67 5» 0,36587 3655,56 99 0,37091.
Углекислый газъ.
Начальное давленіе р0 при 0°. ЮОа^.
758,47
901,09
1742,73
3589,07
мм.
0,36856
0,36943
0,37523
0,38598.
Числа для воздуха при слабыхъ давленіяхъ мало вѣроятны, но во
всякомъ случаѣ эти опыты показываютъ, что ар растетъ вмѣстѣ съ да-
вленіемъ /?, согласно формулѣ (71) стр. 131 и выводу II стр. 133.
Меіапсіег изслѣдовалъ ар для воздуха, С02 и Н2 при давленіяхъ
ниже атмосфернаго. Онъ нашелъ, что для воздуха и СО2 величина ар
уменьшается вмѣстѣ съ р, но, достигнувъ минимума значенія (для воз-
духа при 170 мм., для СО2 при 56 мм.), при дальнѣйшемъ уменьшеніи
давленія опять начинаетъ возрастать. Для Н2 Меіапсіег находитъ
непрерывное возрастаніе ар при убываніи давленія отъ атмосфернаго до
9.3 мм. Эти результаты нуждаются въ провѣркѣ; они противорѣчатъ
нашимъ теоретическимъ выводамъ (ар — Сопеі для Н2 и ар убываетъ
вмѣстѣ съ р для остальныхъ газовъ). .Возможно, что въ опытахъ Ме -
Іапсіег’а оказалось вліяніе газоваго слоя, пристающаго къ стѣнкамъ ре-
зервуара (т. I) и постепенно освобождающагося при слабыхъ давленіяхъ.
Па вліяніе этого слоя указалъ Гйарриі'8. Каізег указалъ на влія-
ніе пыли при опытахъ опредѣленія величинъ ар и аѵ\ каждая пылинка
окружена слоемъ сгущеннаго газа, который при нагрѣваніи освобожда-
ется. Ее^паиіі изслѣдовалъ также зависимость аѵ отъ давленія.
Первые опыты при небольшихъ давленіяхъ дали для водорода почти не
мѣняющееся аѵ\ для воздуха, СО2 и 8О2 оказалось, что аѵ растетъ при
увеличеніи давленія:
Объемъ и давленіе газовъ.
145
со2
Р аѵ
760 мм. 0,0037099
2520 „ 0,0038455
Р
760 мм. 0,0037099
987 „ 0,0039804.
5О2
Для изслѣдованія аѵ при болѣе высокихъ давленіяхъ К е п а и И
пользовался особымъ способомъ. Два латунные сосуда А и В (рис. 59),
объемы которыхъ при 0° равны и І/2, соединены съ резервуаромъ I/,
содержащимъ сгущенный газъ. Сосудъ А помѣщается въ тающій ледъ, В въ
Рис. 59.
Г' ~~"Р
пары кипящей воды. Черезъ нѣкоторое время закрываются краны г и г',
сосуды А и В отвинчиваются и взвѣшиваются. Вѣсъ пустыхъ сосудовъ
извѣстенъ, слѣд. получаются вѣса Р± и Р2 газа, содержащагося въ А
при 0° и въ В при і° (около 100°) ; общее давленіе обозначимъ черезъ р.
Пусть у коеффиціентъ расширенія латуни и <5 вѣсъ куб. см. газа при 0°
и 760 мм. Тогда
Р‘ = Ѵ‘д 7» •
Р2 = Ц><5
Р 1 + ГІ
760 1 4- аѵГ
откуда
/Л Ѵ2 , . \ 1
% ~ (^2 ’ И (1 + I
Давленіе р, получающееся изъ перваго уравненія, должно быть исправ-
лено въ виду отступленія газа отъ закона Бойля.
Такимъ способомъ Ведтіаиіі нашелъ:
Воздухъ. Углекислый газъ.
Давленіе р Давленіе р %
3844,3 мм. 0,0037242 4167,7 мм. 0,0039956
6505,3 „ 37688 4333,9 „ 40061
КУРСЪ ФИЗИКИ О. X в о л ь С О Н А. г. III. изд. 3-е. 10
г
146
Объемъ и давленіе тѣлъ.
Воздухъ. Углекислый газъ.
Давленіе р % Давленіе р ос^,
10335,4 „ 37825 7115,6 „ 42269
10879.7 „ 37984 8545,5 „ 44064
12833,2 „ 37979 8784,8 „ 44081
14248,5 „ 38422 12271,4 „ 48577.
И эти числа вполнѣ подтверждаютъ, что аѵ возрастаетъ вмѣстѣ съ р,
пока р не очень велико, какъ того требуетъ теорія (стр. 134).
Переходимъ къ замѣчательнымъ работамъ А п й г е я’а и А т а -
а 4, изслѣдовавшихъ величины ар и аѵ до весьма высокихъ давленій.
А п (1 г е лѵ 8 опредѣлялъ ар и аѵ д л я углекислоты. Приводимъ сперва
числа ар для различныхъ начальныхъ давленій р0 и различныхъ нагрѣ-
ваній отъ 0° до /°.
і — 6°,5 1 64° 1 — 100°
А> атмосфер. аР а ССр а ар а
16,42 — 0,004754 0,01018 0,004700 О,00у65
21,48 0,00537 0,01104 0,005237 0,01019 0,005138 0,00955
\ 25,87 0,00588 0,01080 0,005728 0,01007 0,005610 0,00950
30,37 — — 0,006357 0,00996 0,006177 0,00930
33,53 0,00734 0,01111 0,006973 0,01000 0,006741 0,00931
Вторые столбцы содержатъ величины а, вычисленныя по формулѣ (71),
въ которой принято а = 0,00366. Для болѣе высокихъ давленій
А п (1 г е лѵ 8 опредѣлялъ увеличеніе давленія при нагрѣваніи отъ = 64°
до 4 = Ю0° (при 0° газъ превратился бы въ жидкость); онъ пользо-
вался слѣдовательно формулою (79) стр. 134 и опредѣлялъ величину ар\
т.-е. среднее значеніе коеффиціента между 64° и 100°, отнесенное
къ давленію при 64°.
Рі а/ а Рі &р а
21,42 0,003526 0,00999 48,40 0,004367 0,00916
28,65 3718 956 67,65 5392 921
35,29 3956 968 94,27 7029 783.
42,74 4166 918
Величины а вычислены по формулѣ (80) стр. 134.
Всѣ приведенныя числа подтверждаютъ, что ар растетъ вмѣстѣ съ р.
Приводимъ значенія коеффиціента аѵ для С0.2, по наблюденіямъ
Апйгелѵз’а, для различныхъ давленій р (въ атмосф.) и различныхъ
нагрѣваній отъ 0° до /°.
р 1 = 7°,5 і = 64» І = 100°
12,01 0,004620 — —
16,22 5200 — —
17,09 — 0,005136 0,004994
Объемъ и давленіе газовъ.
147
р і = 70,5 і = 64° і = 100°
20,10 6070 5533 5324
24,81 • 7000 6204 5922
27.69 7820 6737 6369
31,06 8950 7429 6968
34,39 10970 8450 7762.
Для высокихъ давленій Ап(1 г е лѵ 8 опредѣлялъ величину аѵ по
формулѣ (79) стр. 134 и притомъ также въ предѣлахъ между 4 = 64°
и 4=100°, т.-е. среднія значенія между этими температурами, отне-
е н н ы я къ объему при 64°. Онъ получилъ слѣдующія числа:
Р Р Р
17,09 0,003572 31,60 0,004187 64,96 0,006512
20,10 3657 34,49 4266 81,11 8033
22,26 3808 40,54 4596 106,9 13150
24,81 3892 46,54 4946 145,5 18220
27,69 4008 54,33 5535 223,0 8402
Эти числа показываютъ, что величины аѵ растутъ вмѣстѣ съ давле-
ніемъ р; послѣднее число показываетъ, однако, что при очень большихъ
давленіяхъ аѵ опять начинаетъ убывать. Сравненіе чиселъ аѵ и ар для
одинаковыхъ р и і показываетъ, что всегда аѵ > ар. Все это вполнѣ
согласно съ нашими выводами изъ формулы V ап (1 е г \Ѵ а а 1 8’а
(стр. 134, II).
А ш а а I изслѣдовалъ зависимость величины ар отъ давленія р для
воздуха, О, Н, СО2 и этилена. Для водорода ар постоянно до
/7=700 атмосферъ; далѣе ар медленно убываетъ до 1800 атмосферъ и
затѣмъ опять остается постояннымъ до /? = 2800 атм. Для О, IV, СО2
и этилена замѣчается возрастаніе ар вмѣстѣ съ р до нѣкотораго
максимума, за которымъ ар уменьшается при возрастаніи давленія р.
Это уменьшеніе объясняется тѣмъ, что произведеніе р^ въ знаменателѣ
выраженія (71) имѣетъ при нѣкоторомъ высокомъ давленіи минимумъ.
Максимумъ ар приходится для СО2 при 155 атмосф., для азота при 400 ат-
мосф. и для кислорода при 600 атмосф. приблизительно.
А ш а а і изслѣдовалъ далѣе величину аѵ для тѣхъ же газовъ. Для
водорода аѵ непрерывно уменьшается съ увеличеніемъ давленія, доходя
до 0,00218 при 1000 атмосф. между 0° и 100°. Для остальныхъ газовъ
аѵ сперва увеличивается вмѣстѣ съ р и затѣмъ опять уменьшается. Такъ
для СО2 между 40° и 50° величина аѵ/ (отнесенная къ объему при 40°)
растетъ до огромнаго числа 0,07566 при /740 = 90 атмосф., и убываетъ до
0,00191 при р40 = 1000 атмосф. Все это вполнѣ согласно съ нашими вы-
водами на стр. 134.
В. Зависимость ар и аѵ отъ температуры Л Опыты Ке-
^паиіі привели къ тому результату, что ар для воздуха и для СО2 не
10*
148
Объемъ и давленіе тѣлъ.
зависитъ отъ температуры. Для 8О2 онъ находитъ, что ар уменьшается
съ повышеніемъ температуры, между тѣмъ какъ по формулѣ V а и (1 е г
АѴааІв’а ар не должно зависѣть отъ і (стр. 134;. Ѵап сіег Ѵ\гааІ8
полагалъ возможнымъ объяснить этотъ результатъ отдѣленіемъ газа, при-
ставшаго къ стѣнкамъ резервуара при его нагрѣваніи. Однако опыты
Апсігелѵз’а надъ СО2 показываютъ, что ар несомнѣнно уменьшается
при повышеніи температуры. Такъ напр.
между 0° и 6,5° . . . ар = 0,00537
« 0° и 64° . . . =0,00524
« 64° и 100° ... = 0,00497.
Этотъ результатъ противорѣчитъ формулѣ Ѵап сіег АѴааІз’а
но, какъ мы видѣли на стр. 135, онъ согласенъ съ формулою 01 аи-
8 і и з’а, который нашелъ, что для СО2 изъ опытовъ А п сі г е лѵ 8’а полу-
чаются слѣдующія значенія для постоянныхъ его формулы (81):
= 0,003688, 6 = 0,000843, (і = 2,0935, с = 0,000977,
такъ что уравненіе состоянія углекислаго газа имѣетъ видъ
— 0,0036887' 2,0935
р — V — 0,000843 ‘ Т{ѵ + 0.000977)2
СЬаррпіз также нашелъ, что ар уменьшается съ повышеніемъ темпе-
ратуры для И и СО2 К со2
ар
между 0° и 20° 0,00367641 0,00373275
« 0° и 40° 567 3029
« 0° и 100° 166 2477.
Эти числа также согласны съ формулою С1аи8ІП8’а (84) стр. 135.
Опыты Апйтелѵе’а, приведенные на стр. 146, показываютъ, что
аѵ уменьшается съ возрастаніемъ температуры, что опять-таки согласно
съ нашими выводами на стр. 134. Къ тому же результату приводятъ
опыты Аша^аі надъ СО2 и 8О2 при давленіи въ 1 атмосферу:
5О2 со2
аѵ
10°— 60° 0,003904 0°— 50° 0,003714
10°—150° 3832 0°—150° 3706
10°—250° 3798 0°—250° 3703.
ЛѴі1ко\Ѵ8кі изслѣдовалъ величину аѵ для воздуха до весьма
низкой температуры (—145°) и при различныхъ давленіяхъ. Оказалось, что
Литература.
149
согласно предыдущему, аѵ увеличивается съ пониженіемъ температуры и
при низкихъ температурахъ. Приводимъ нѣкоторыя изъ чиселъ, которыя
далъ \Ѵііколѵ8кі для аѵ . 1Об:
р атмосф. 1000 160 —35°,0 -780.5 —1030,5 —130° —1400 —1450
15 379 382 — — — — 420 427
25 388 392 — 411 422 443 463 479
30 392 398 — 420 434 462 492 519 (р= 29)
40 402 408 — 438 461 508 632 —
50 410 419 430 457 487 569 — —
80 431 446 467 512 557 607 — —
100 441 458 489 537 579 — — —
120 449 465 501 550 577 — — —
130 — 468 — 551 581 — — —
Въ заключеніе замѣтимъ, что въ 1894 г. появилась работа Е Ваіу
и \Ѵ. К аш 8 а у я о тепловомъ расширеніи весьма разрѣженныхъ газовъ.
Они нашли, что съ уменьшеніемъ давленія величина аѵ для убываетъ,
для О2 увеличивается. При давленіи въ 1,4 мм. для кислорода получа-
ется аѵ = 1/233; ниже 0,7 мм. эта величина еще увеличивается. Для
азота междз 5 и 1 мм. оказывается % = 1/зо4-
4ацпего(і и Вето! (1904—1905) опредѣляли среднее значеніе ар
между 0° и температурой плавленія золота, которую они нашли равной
1067,4°. для ТѴ2, О2, воздуха, СО и СО2. Въ слѣдующей таблицѣ даны
результаты этихъ опредѣленій.
начальное давленіе при 0° среднее значеніе ар между 0° и 1067,4°
м. 200—230 мм. 0,0036643
О2 180—230 « 0,0036654
воздухъ 230 « 0,0036643
СО 230 « 0,0036638
240 0,0036756
со2 170 « 0.0036713.
ЛИТЕРАТУР V
Къ. § 2.
Ьаѵоізіег еі Ьаріасе. См. Віоі, Тгаііё де рііуеідпе 1 р. 151, Рагіе 1816; йсітѵѵеі^-
§ег’е Доигп. 25 р. 355, 1819.
Ноу. РЫ1. Тгапе. 1785; Франц. переводъ Ргопу, Рагіе 1787 (изд. Бісіоі).
Оіаігеі. Ро§&. Апп. 160 р. 497, 1877.
Вогсіа. см. Віоі, Тгаііё бе рііуе. 1, р. 164, Рагіе 1816.
Ое ѣис. РЫ1. Тгапе. 88; Д. Де Рііуе. Де Веіатёіѣгіе 18 р. 363.
Ниіопр еі Реііі. Апп. сЫт. еі рііуе. (2) 2 р. 254, 1816; 7 р. 113, 1818; ОПЬ.
Апп. 58 р. 254, 1818.
150
Объемъ и давленіе тѣлъ.
МаШііезеп. Ркй. Тгапв. 1 р. 231, 1866; Ркіі. Ма&. (4) 31 р. 149, 1866; 32 р. 472,
1866; Ро%%. Апп. 128 р. 512, 1866; 130 р. 50, 1867.
Корр. ЫеЬ. Апп. 81 р. 1, 1852; РЫ1. Ма&. (4) 3 р. 268, 1852; Апп. скіт. еі ркуз.
(3) 54 р. 338, 1858.
Ріхеаи. Апп. скіт. еі ркув. (4) 2 р. 143, 1864; 8 р. 335, 1866; Ро^. Апп. 123
р. 515, 1864; 128 р. 571, 1866.
Вепоіі. Тгаѵ. еі Мёт. <1. Впг. без Р. еі Ме8. 1, 1881; б р. 3, 1888; б. сіе ркув.
(2) 8 р. 253, 1889.
Риі/гісіі. Іпвіг. 13 р. 365, 1893; 18 р. 261, 1898.
Тиііоп. Ргос. К. 8ос. 63 р. 208, 1898; йівскг. Т. ркуз. Скет. 30 р. 529, 1898.
Ѵ&еісіттіапп. ЛѴ. А. 38 р. 474, 1889.
РеітегсІез. Аивбекпип^ бев Оиаггев, Візв. бепа, 1896.
Вскееі. Апп. б. Ркуз. (4) 9 р. 837, 1902; Іпвіг. 23 р. 90, 1903; 24 р. 285, 1904
Аугез. Ркуз. Веѵ. 20 р. 38, 1905.
Могіеу апд Рорегз. Ркуз. Веѵ. 4 р. 1, 106, 1896.
Къ § 3.
Наіілігоет. (ИГЪ. Апп. 36 р. 60, 1810.
Ьётпегау. С. К. 131 р. 1291, 1900.
Рісіеі. См. Моиззоп, Ьекгкиск б. Ркувік, 3-ье нзд. 2 р. 335, 188, и С. Ь. 'МеЬеі
Апп. бег Ркуз. (4) 18 р. 868, 1905.
Рапауе//. Апп. б. Ркуз. (4) 18 р. 210, 1905.
Аугез. Ркуз. Веѵ. 20 р. 38, 1905.
ВИеагег. Рку8. Веѵ. 20 р. 52, 1905.
Иогзеу. Ркув. Веѵ. 23 р. 246, 1906; 25 р. 88, 1907; 27 р. 1, 1908.
Вскееі. Ѵегк. б. б. ркуз. Оев. 1907 р. 3, 24, 718.
Всігееі ипсі Неизе. Ѵегк. б. б. ркуз. Ое8. 1907 р. 449; Рку8. Хеіівскг. 8
р. 756, 1907.
Каттегііпрк Оппез и Сіау. Ѵег8І. К. Ак. ѵ. АѴеі. 16 р. 243, 1907; Сотт. Ркув.
ЬаЪ. Ьеібеп 8ир1. № 17 р. 1.
Неппіщг. Ѵпп. б. Рку8. (4) 22 р. 631, 1907.
Сгйпеізеп. Апп. б. Ркуз. (4) 33 р. 33, 65, 1910.
Ткіезеп. Ѵегк. б. б. ркуз. Сев. 1908 р. 410.
Маіііііезеп, см. къ § 2.
Ье СИаіеІіег. С. В. 108 р. 1096, 1889; 128 р. 1444, 1899; 129 р. 331, 1899.
Сіаігеі, см. къ § 2.
НоІЬогп и. Нау. Вегі. Вег. 1900 р. 1009; В. А. 4 р. 104, 1901; 8І11.’ б. (4) 11
р. 374, 1901.
НаЫапдег. Ро^. Апп. 140 р. 672, 1868.
Віоііе. Оі. Ріпяка Ѵегі. 8ос. Рогк. 49, 1907.
В]’егкеп. \Ѵ. А. 43 р. 817, 1891.
Лебедевъ. Ж. Ф. X. О. 13 р. 246, 1881.
Сапіопе е Сопііпо. Вепб. В. Іпві. Ьотк. бі 8с. е Іеіі. (2) 33 р. 215, 1900.
ВсНитасНег, Роіггі ипсі Могііх. Мёт. бе ГАсаб. бе 8і.-Рёіегвк 4 р. 297, 1850.
Нечѵаг. Ргос. В. 8ос. 70 р. 237> 1902.
Ріиескег ітд Оеіззіег. Ро&&. Апп. 86 р. 238,1852.
Ре^паиіі. Апп. скіт. еі ркув. (3) 4, 1842; Мёт. бе ГАсаб. 21 р. 205, 1847.
УѴіпкеІтапп ипд Всігоіі. \Ѵ. А. 51 р. 736, 894.
МаііЫезеп (сплавы). Ро^г. Апп. 130 р. 50, 1867.
ВіаМіа^еп. Мескап. 7ір-. 1901 р. 21.
Вѵесіеііиз. Кгііівске Ьаеп&еп ипб Тетрегаіигаепбегип&еп бев Еізепв, Ьрваіа, 1896;
Ркіі. Ма&. (5 46 р. 173, 1890.
Оиіііаите. С. В. 124 р. 176, 752, 1897; 125 р. 235, 1897; 136 р. 303, 356,
1903; Агск. 8с. ркуз. (4) 15 р. 253, 433 и т. д., 1903; б. бе ркуз. (3) 7 р. 264, 1898.
Литература.
151
Скагру еі Огепеі. С. В. 134 р. 540, 1902.
ПоОиіеІІ. Ргос. К. 8ос. 25 р. 280, 1877; 31 р. 291, 1881; 32 р. 540, 1881; 33
р. 143, 1882.
Еігеаи. С. К. 64 р. 314. 771, 1867; Ро&&. Апп. 132 р. 292, 1867.
Тійезеп ипй 8скееІ. Іпзіг. 12 р. 293, 1892.
НоІЪогп и. Неппіпр. Апп. (1. Рііуе. (4) 10 р. 446, 1903.
Р. СКарриіз. Ѵегіі. Ыаіигі. Оее. Ваееі. 16 р. 173, 1903.
8скееІ. ѴегЬ. (1. (1. рііуз. Ѳез. 1907 р. 3, 24, 718.
Міпскіп. Рііуе. Веѵ. 24 р. 1, 1907.
Рапйаіі. Рііуе. Веѵ. 30 р. 216, 1910.
Кау. РЫІ. Ма^. (6) 20 р. 718, 1910.
Къ § 4.
Міізскегііск. Ро§&. Апп. 1 р. 125, 1824; 10 р. 137, 1827; 41 р. 213, 448, 1837;
Апп. сЫт. еі рЬуе. (2) 25 р. 108, 1824; 32 р. 111, 1826.
Р/а#. Ро^л Апп. 104 р. 171, 1858; 107 р. 148, 1859.
Еіхеаи. С. В. 60 р. 1161, 1865; 62 р. 1101, 1866; 64 р. 314, 771, 1867; Ро^.
Апп. 126 р. 611, 1865; 128 р. 565, 1866; 132 р. 292, 1867.
Вепоіі. Тгаѵ. еі Мёш. би Виг. іпі. бе Р. еі Ме8. 6 р. 1, 1888.
8скееІ. Апп. 6. Рііуе. (4) 9 р. 837, 1902; Іпегг. 23 р. 90, 1902; \Ѵіее. АЫіапбІ.
(1. рііуе.-іесііп. Веісііеапеі. 4, НеГі I, р. 35, 1903.
Рашіаіі. Ркуе. Веѵ. 20 р. 10, 1905.
Федоровъ. ХеііесЬг. 1 Кгуеіаііо^г. 28 р. 483, 1897.
Къ § 5.
Риіощг еі Реііі. Апп. сЫт. еі рЪуе. 7 р. 127, 1818.
Міііігег. Ро^. Апп. 80 р. 55, 1850.
Рерпаиіі. Вёіаііопе бее ехрегіепсее, 1 р. 271, 1847; Мёт. бе ГАсаб. 21, 1847.
Во88ска. Ро&^. Апп. Ег&Ьб. 5 р. 276, 1871.
УХ/иеІІпег. Ро&&. Апп. 153 р. 440, 1874.
Менделѣевъ. Ж. Ф. X. О. 7 р. 75, 1875; 3. бе рііуе. 5 р, 259, 1876.
Ьеѵу. Аиебе1тип& бее ОискеіІЬеге. ВІ88. Наііе, 1881.
Вгоск. Тгаѵ. еі Мёт. би Виг. бее Р. еі М. 2, 1883.
Рескпа^еі. Р. Апп. 123 р. 115,1864.
Ткіе8еп, 8скееІ ипд 8еІІ. Іпеіг. 16 р. 49, 1896.
Скарршз. Тгаѵ. еі Мёт. би Виг. іпі. без Роібе еі Ме8. 13, 1907; Л. бе Р1іу8. (4)
4 р. 12, 1905.
Къ § 6.
НаІІ8ігоет. Ро&&. Апп. 1 р. 129, 1824.
Маіікіе8еп. Ро^. Апп. 128 р. 512, 1866.
Рит/огй. (ііІЪ. Апп. 20 р. 369, 1805.
Норе. Апп. сЫт. еі рііуз. (1) 53 р. 272, 1805.
Оергеіх. Апп. сЫт. еі рііуе. (2) 62 р. 5, 1836; 68 р. 296, 1838; 70 р. 5, 1839.
Тга11е8. СгіІЬ. Апп. 27 р. 263, 1807.
Ехпег. МТеп. Вег. 68 р. 463, 1873.
Ь. ѴРеЬег. III Вег. бег СоттІ88. гиг Ѵпіеге. 6. беиіесііеп Мееге, р. 1 ; ВеіЪІ. 2-
р. 696, 1878.
Сорреі. Апп. сЫт. еі рііуз. (7) 3 р. 246, 1894 ; 28 р. 145, 1903.
Ріегге. Апп. сЫт. еі рііуе. (3) 15 р. 325, 1845; см. Егапкепкеіт. Апп. сЫт. еі
рііуе. (3) 37 р. 74, 1873; Ро&&. Апп. 86 р. 451, 1852.
Корр. Ро^. Апп. 72 р. 1, 223, 1847; 92 р. 42, 1854.
ѴѴеіапег. Ро^. Апп. 29 р. 300, 1866.
доііу. Вег. Миепск. Асаб. 1864 р. 141.
152
Объемъ и давленіе тѣлъ.
Дозеііі. Ро&&. Апп. Ег^Ьб. 5 р. 273, 1871; Аііі беі Іпві. Ѵепеіо (3) 13, 1868;
Апп. сііпп. еі рііуе. (4) 17 р. 370, 1869.
Мипске. См. СгеЫег’е рііуе. ДѴоегіегЬисІі, статью \Ѵаегте, Аиебеішип^.
ЗсНееІ, \Ѵ. А. 47 р. 441, 1892; Іпеіг. 17 р. 331, 1897.
Кгеіііііцу. Аиебеііпип^ бее ХѴаеееге, Иіее. Вегііп, 1892; ВеіЫ. 18 р. 58, 1894.
Наибольшая плотность растворовъ:
Рергеіх. Апп. сЫт. еі. рііуе. (2) 62 р. 5, 1836; 70 р. 49, 1839; 296, 1839.
Ка/8іеп. Кагеіеп’е АгсЫѵ Г. Міпегаі. 19 р. 1, 1846; 20 р. 3, 1846.
Розеііі. См. выше.
Вепдег. А. 22 р. 179, 1884; 34 р. 872, 1887.
Р. Ленцъ. Мёт. бе ГАсаб. бе 8і.-РеіегеЬ. (7) 29 № 4, 1882.
РиедогД. Ро&&. Апп. 114 р. 63, 1861.
Ьизаппа е Виххоіа. Хиоѵо Сітепіо (3) 35 р. 31, 1894.
Сорреі. Апп. сіііт. еі рііуе. (7) 3 р. 268, 1894; С. К. 124 р. 533, 1897; 128
р. 1561, 1899; 132 р. 1218, 1901; Апп. сіііт. еі рііуе. (7) 28 р. 203, 1903.
Реіііпеіи е Магоііі. Віѵ. 8сіепі.-Іпбиеі. 28 р. 64, 1896; ВеіЫ. 21 р. 182, 1897.
Когі. МаапбЫ. ѵ. Ыаіиигѵ. 20 р. 79, 1896.
Сіпеііі. Ы. Сіт. (4) 2 и 3, 1895—96.
Могеііо. Ы. Сіт. (4) 6 р. 198, 1897.
Титтіігг. ХѴіеп. Вег. 119 р. 393, 1910.
Вліяніе давленія на температуру наибольшей плотности:
Ѵап (іег Ѵааіз. Сопііпиііаег бее ^аеі. и. Пиеее. 2иеі. Ьеіргі^, 1881 ; ВеіЫ. 1
р. 511, 1877.
Ата^аі, С. В. 116 р. 779, 946, 1893.
Ьизаппа. Киоѵо Сітепіо (4) 2 р. 233, 1895.
Новыя работы о расширеніи воды:
ТШезеп. Варрогг бе Іа Сопіег. &ёп. бее Р. еі Мее. 8ері. 1889, р. 111.
Магек. \Ѵ. А. 44 р. 170, 1891.
Вскееі. См. выше.
Кгеііііп^. См. выше.
Ре Ьаппоу. С. В. 120 р. 866, 1895.
Скарриіз. Тгаѵ. еі Мёт. б. Виг. бее Р. еі Мее. 6, 1888; 13, 1907; Агсіі. 8с.
рііуе. (3) 20 р. 1, 1888; \Ѵ. А. 63 р. 202, 1897.
(лщгііеіто. Вепб. В. Ас. беі Ьіпсеі (5) 8, 2 8ет. р. 271, 310, 1899.
Ткіезеп, Вскееі ипй Ріеззеікогзі. \Ѵ. А. 60 р. 340, 1897; Іпеіг. 17 р. 87, 1897;
АЫіапбІ. б. рЬуе.-іесЬп. Веісііеапеіаіі 3 р. 1—70, 1900; Іпеіг. 20 р. 345, 1900.
Ткіевеп. ХѴіее. АЫіапбІ. б. рііуе.-іесіт. ВеісЬеапеіаІГ 4 р. 1, 1904.
Ріа іо, Ротке ипй Нагііп^. \Ѵіее. АЫі. б. к. Хогт* АісЬи^з. Коттіе. 1900
Ней II.
Ландезенъ. Труды Общества Естеств. при Императ. Юрьевск. Универс. XI,
Юрьевъ, 1902.
Д. И. Менделѣевъ. Ж. Ф. X. О. 13 р. 183, 1891; Ріііі. Ма$. (5) 33 р. 99, 1892;
Времен. 2 р. 133, 1895; 3 р. 133, 1896.
ѴѴаіегзіоп. РЫ1. Ма^. (4) 21 р. 401, 1861; 26 р. 116, 1863.
Нігп. Апп. сіііт. еі рііуе. (4) 10 р. 32, 1867.
Расширеніе растворовъ:
Оегіаск. 8рес. Оеуѵ. бег ^еЪгаеисІіІ. 8а1г1оееип^еп. РгеіЬег^, 1895.
Магірргас. Агсіі. 8с. рЬуе. (2) 39 р. 217, 273, 1870; ЪіеЫ&е Апп. 8ирр1. 8 р. 370.
Кгетегз. Ро§’&. Апп. 105 р. 367, 1858.
Р Ленцъ и Рѣзцовъ. Извѣстія С.-П. Технолог. Института. 1880 и 1881 р. 239.
Литература. 153
Рогсіг. 2івсЬг. рЬув. СЬет. 18 р. 675, 1895; XV. А. 55 р. 191, 1895.
Ое Ьаппоу. ХівсЬг. рЬув. СЬет. 18 р. 443, 1895.
ВаитКаиег. Ро§^. Апп. ПО р. 659, 1860.
Кгеііііщг. Аиебеітип^ бев ХѴаввегв и т. д. Вівв. Ег1ап§-еп, 1892.
Ата^аі. Апп. сЫт. еі рЬув. (6) 29 р. 559, 1893.
Ьагиіезеп. ВсЬгіііеп бег ХаіигГ. Сев. ап сі. ІІпіѵ. биг|‘елѵ. 14 р. 1904.
Къ § 7.
Оергеіх. Апп. сЫт. еі рЬув. (2) 70, 1839.
Корр. Ро&у. Апп. 72 р. 1, 223, 1847; ЫеЬ. Апп. 93 р. 129; 94 р. 257; 95 р. 307
1855; 98 р. 367, 1867, 1856; Апп. сЫт. еі рЬув. (3) 47 р. 412, 1855.
Ріегге. Апп. сЫт. еі рііуз. (3) 15 р. 325, 1845; 19 р. 193 1847; 21 р. 336,
1847; 30 р. 5, 1850; 31 р. 118, 1851; 33 р. 199, 1851 ; ЫеЫ^’в Апп. 56 р. 139, 1845;
64 р. 159, 1848; 80 р. 225, 1851.
РгапкепИеіт. Ро§^. Апп. 72 р. 422, 1847.
Лугининъ. Апп. сЫт. еі рЬув. (4) 11 р. 453, 1867; ЫеЬ. Апп. 8ирр1. 5
сі. 295, 1867.
Хапдіег. ЫеЬ. Апп. 214 р. 138, 1882; 223 р. 56, 1884.
Нігп. Апп. сЫт. еі рЬув. (4) 10 р. 32, 1867.
Д. И. Менделѣевъ. Горный журналъ 1861; ЫеЬ. Апп. 119 р. 1, 1861.
Огіоп. Апп. сЫт. еі рЬуз. (3) 56 р. 5, 1859.
Андреевъ. ЫеЬ. Апп. ПО р. 1, 1859; Апп. сЫт. еі рЬув. (3) 56 р. 317, 1859.
Іігііогіег. Апп. сЫт. еі рЬув. (2) 60 р. 427, 1835.
Огітаісіі. 3. сіе рЬув. (2) 5 р. 29, 1886; Аііі сіеі Ыпсеі (4) Вепб. 2, I р. 231
1885—86; Аііі беІГАсаб. Саіапіа (3) 18 р. 273, 1885.
Рісіеі. АгсЬ. 8с. рЬув. 34 р. 362, 1895.
Ата^аі. Апп. сЫт. еі рЬув. (6) 29 р. 559, 1893.
Сагпагхі. X. Сіт. 5 р. 180, 1903.
Менделѣевъ (Законъ расширенія жидкостей). Ж. Ф. X. О. 6. Отд. хим. р. 1, 1882;
16, Отд. Физ. р. 292, 474, 1884; СЬет. Вег. 17 р. 129, 1884; РЫ1. Ма^. (5) 33 р. 29,
1892; Апп. сЫт. еі рЬув. (6) 2 р. 271, 1884.
Коноваловъ. Ж. Ф. X. О. 18, Отд. хим. р. 295, 1886.
Ьиіігег. ЕівсЬг. рЬув. Сііеіп. 12 р. 524, 1893.
О. ВегіНеІоі. С. В. 128 р. 606, 1899.
ХѴиеІІпег. Роі^ц\ Апп. 133 р. 1, 1868.
Аѵепагіиз. Виіі. бе ГАсаб. сіе 8і.-РеіегвЬ. 10 р. 697, 1877; Ж. Ф. X. О. 16 р. 242,
400, 1884.
Жукъ. Ж. Ф. X. О. 13 р. 239, 1881; 16 р. 304, 1884; 17 р. 13, 1885.
Маііеі еі Ргіедгісіі. АгсЬ. 8с. рЬув. (4) 15 р. 50, 1902.
НеіІЪогп. 2і8сЬг. рЬув. СЬет. 7 р. 367, 1891.
Рапкіпе. ЕбіпЬ. Хедѵ. РЫ1. боигп. ОсюЬег 1849; 8сіепі. Рарегв р. 13.
Къ § 8.
Ѵап де г ѴРааІз. Сопііпиііаеі бев ^авіоегті^еп ипсі Пиевзі^еп Хивіапбев. Ьеір-
1881.
Ьедис. Апп. сЫт. еі рЬув. (7) 15 р. 95, 1898.
Сіаизіиз. XV. А. 9 р. 337, 1880; 14 р. 279, 692, 1881.
Ваггаи. С. В. 101 р. 1145, 1885.
Къ § 9.
Сау-Ьи$8ас. Апп. сЫт. еі рЬув. (1) 43 р. 137, 1802 (ап X); СіІЬ. Апп. 12, 1802;
см. Віоі. Тгаііё бе рЬувідие 1 р. 182, 1816.
Ріащгег&иез, см. ѲеЫег’в рЬув. ХѴоегіегЬисЬ 1 р. 625, 1825.
Оаііоп. Мет. оГ іЬе МапсЬевіег РЫ1. 8ос. 5 р. 3, 599.
154
Теплоемкость.
Оиіопр, еі Реііі. Апп. сЫт. еі рііуе. (2) 2 р. 240, 1816; 7 р. 117, 1818.
РидЬег^. Ро^. Апп. 41 р. 271, 1837; 44 р. 119, 1838.
Ма^пиз. Ро&&. Апп. 55 р. 1, 1842.
Ре^паиіі. Мёт. сіе ГАсасІ. 21 р. 1, 1847; Апп. сЫт. еі рііуе. (3) 4 р. 5, 1842;
5 р. 52, 1842; Ро^. Апп. 55 р. 141, 391, 557, 1842; 57 р. 115, 1842.
№11у. Ро&§. Апп. ДиЬеІЪсІ. р» 82, 1874.
Діскагдз и. Магк. Хіесѣг. 1. рііуе. Сііетіе 43 р. 475, 1903; Ргос. Атег. Аее. 38
р. 417, 1903.
Скарриіз. Тгаѵ. еі Мёт. Ни Вигеаи (Ые Р. еі Мее. 6, 1888.
ІГ. НоНтапп. АѴ. А. 66 р. 224, 1898.
Каттегііпрк Оппез. Соттипісаі. о! іііе ЬаЬог. оГ Ьеісіеп № 60, 1901.
Ігаѵегз и. Зациегосі. Хіесііг. Г. рііуе. Сііетіе 45 р. 385, 1903.
Д. И. Менделѣевъ. Вег. сііет. Оее. 10 р. 81, 1877.
Рескпа^еі. Ро&§. Апп. 123 р. 127, 1864.
Адѵепіочѵзкі. Виіі. Сгасохѵ. 1909 р. 742.
Ата^аі. Апп. сЫт. еі рііуе. (4) 28 р. 274, 1873.
Меіагиіег Ьа Ыіаіаііоп 4ее §аг. Гельсингфорсъ, 1889; АѴ. А. 47 р. 135
1892; Асіа 8ос. Йсіепі. Реші. 19, 1891: 20, 1894; 33, 196; Воііяташі-Рееіесіігіі'і
р. 789, 1904.
Сііарриіз. (Вліяніе пыли). АѴ. А. 8 р. 1,1879.
Каізег. АѴ. А. 34 р. 607, 1888.
Ре^паиіі. (Высокія давленія). Мёт. сіе ГАсасІ. 26 р. 567, 1862.
Апдгеірз. РЫІ. Ма§. (5) 3 р. 63, 1877.
Ата^аі. (Высокія давленія). Апп. сЫт. еі рііуе. (4) 29 р. 252, 1873; (5) 22
р. 353, 1881.
Сіаизіиз. АѴ. А. 9 р. 337, 1880.
Ѵ^іікоірзкі. Ехігаіі сіи Виіі. (1е ГАсасІ. де Сгасоѵіе 1891 р. 181; ВеіЫ. 16
р. 176, 1892.
Ваіу апд. Ратзау. РЫІ. Ма§. (5) 37 р. 301, 1894.
^диегод еі Регоі. С. К. 138 р. 1032, 1904; 140 р. 1542, 1905; АгсЬ. д. ес. рііуе.
еі наіиг. (4) 20 р. 28, 128, 506, 1905.
Ьедис. С. К. 148 р. 1173, 1909.
ГЛАВА ЧЕТВЕРТАЯ.
Теплоемкость.
§ 1. Введеніе. Теплота есть форма энергіи и, какъ таковая, не
можетъ измѣниться количественно; но она ѵюжетъ образоваться изъ дру-
гихъ формъ энергіи, а также, исчезая какъ теплота, перейти въ другія
формы энергіи. Теплота, такимъ способомъ образующаяся или исчезаю-
щая, а также теплота, передаваемая отъ одного тѣла къ другому, или
отъ одной части даннаго тѣла къ другой, представляетъ нѣкоторую фи-
зическую величину, которая можетъ быть количественно сравниваема съ
другою величиною того же рода: отсюда является представленіе о воз-
можности измѣрить количество теплоты, образующейся, исчезающей или
переходящей отъ одного тѣла къ другому. Для этого должна быть вы-
брана опредѣленная единица количества теплоты и должны быть выра-
ботаны способы сравненія даннаго количества теплоты съ этой единицей.
Введеніе.
155
Настоящая глава посвящена двумъ вопросамъ: вопросу о выборѣ
практически удобной единицы тепла и вопросу о количествѣ те-
плоты, потребномъ для нагрѣванія различныхъ тѣлъ отъ заданной перво-
начальной температуры до другой заданной окончательной, т.-е. вопросу
о теплоемкости тѣлъ. Отдѣлъ физики, занимающійся измѣреніемъ
количествъ теплоты, играющихъ роль въ различныхъ физическихъ явле-
ніяхъ, называется калориметріей; приборы, которыми при этомъ
приходится пользоваться, называются калориметрами. Исторію раз-
витія калориметріи можно найти въ книгѣ МасЬ’а <'Ргіпсіріеп сіег ХѴаег-
шеІеЬге Ьеіргі§, 1896, р. 153—182.
На русскомъ языкѣ существуетъ капитальное сочиненіе В. Ф. Лу-
гинина и 1. Н. Щукарева Руководство къ калориметріи», Москва
1905, переведенное на французскій языкъ («Мёйюйев ііе саіогітеігіе еіс»,
Рагій, А. Негтапп, 1908).
Важнѣйшія величины, измѣреніемъ которыхъ занимается калориме-
трія, суть слѣдующія:
1) теплоемкость; 2) скрытая теплота плавленія или отвердѣванія:
3) скрытая теплота испаренія (кипѣнія) или ожиженія; 4) скрытая те-
плота измѣненія молекулярнаго строя твердыхъ тѣлъ, напр. при переходѣ
моноклиномѣрнои сѣры въ октаэдрическую; 5) теплота смѣшенія двухъ
жидкостей, индифферентныхъ другъ относительно друга или химически
взаимодѣйствующихъ (алкоголь и вода); 6) теплота растворенія и разба-
вленія растворовъ; 7) теплота, выдѣляемая или поглощаемая при раз-
личныхъ химическихъ реакціяхъ, между прочимъ теплота горѣнія; 8) те-
плота. получаемая какъ результатъ опредѣленной работы: 9) теплота,
получаемая при превращеніи въ нее остальныхъ формъ энергіи: лучи-
стой. электрической (зарядъ и токъ) и др.
Калориметрія можетъ измѣрять лишь тѣ количества теплоты, кото-
рыя при опредѣленныхъ условіяхъ исчезли, возникли или перемѣстились.
Она не можетъ опредѣлить полнаго запаса тепловой энергіи, заключаю-
щагося въ данномъ тѣлѣ при опредѣленныхъ заданныхъ условіяхъ.
На стр. 13 мы сказали все необходимое относительно терминоло-
гіи. которой мы будемъ держаться. Мы будемъ отличать < теплоемкость
тѣла» (напр. калориметра) и теплоемкость вещества», напр. мѣди, воды,
азота и т. д. Формулы отъ (27) до (30) стр. 13 опредѣляютъ теплоем-
кость среднюю и теплоемкость при опредѣленной температурѣ, количе-
ство теплоты <2, потребное для нагрѣванія тѣла, а также зависимость
теплоемкости С сложнаго тѣла, отъ вѣсовъ Рі составныхъ частей и тепло-
емкостей Сі вещества, изъ котораго эти части состоятъ, см. (30) стр. 13.
.........................(і)
Принимая, пока безъ всякихъ болѣе точныхъ указаній, теплоемкость
воды равной единицѣ, мы видимъ, что р^і равна вѣсу воды, погло-
щающей при нагрѣваніи такое же количество теплоты, какъ и данное
156
Теплоемкость.
сложное тѣло. Вотъ почему нѣмецкіе ученые назвали величину С весьма
удачно водянымъ эквивалентомъ (АѴа88ег\ѵегШ) даннаго тѣла.
Если теплоемкость с тѣла есть функція температуры, которую
можно представить въ видѣ
с = с0 + аі + Ьі2................ . . . (2)
то количество теплоты, потребное для нагрѣванія тѣла отъ і^ до і%\
равно
4
0= / с<іі — с0(і2 4) -і- а — ^2)4- I (і-і— Л8>- • (з)
4
Средняя теплоемкость сг между температурами и /2° равна
с — = го ? (4 + 4) Н—л (42 + 44 + 42) • (4)
Отсюда средняя теплоемкость сі между 0° и і"
4 = со + 4 аі+ I- Ьі2.......................о)
о
Чтобы нагрѣть тѣло отъ 0° до /°, потребно количество (^теплоты, равное
<2; = Сіі = С()і 4- * аі2 -І- *- №.............(6)
Атомною теплоемкостью вещества Сд называется тепло-
емкость этого вещества, взятаго въ вѣсовомъ количествѣ, равномъ атом-
ному его вѣсу. Пусть с теплоемкость вещества. А его атомный вѣсъ
тогда атомная теплоемкость
сА = Ас.............................................................(7)
Аналогично, величина
= №.............................(Л;
гдѣ молекулярный вѣсъ вещества, называется молекулярною
теплоемкостью вещества.
Теплота (^, притекающая къ тѣлу, вообще говоря, раздѣляется на
три части. Первая часть расходуется на внутреннюю работу; она
особенно велика при температурахъ плавленія и кипѣнія или вблизи
этихъ температуръ. Вторая часть (?2 тратится на внѣшнюю работу при
расширеніи тѣла, подвергнутаго всестороннему давленію. Наконецъ, третья
часть идетъ собственно на повышеніе температуры, т.-е. на увеличе-
ніе живой силы движенія молекулъ и атомовъ.
Сіаавіиз предложилъ называть истинною теплоемкостью
(лѵайге ЛѴаегтесарасііаеѣ) величину, измѣряемую количествомъ теплоты,
Введеніе.
157
расходуемой только на нагрѣваніе тѣла при повышеніи его
температуры на 1°.
Терминъ «теплоемкость» принадлежитъ Ігѵіпе’у, ученику Віаск’а;
Г адо линъ въ Або ввелъ въ 1784 г. терминъ удѣльная теплота».
Обращаемся къ фундаментальному вопросу о выборѣ единицы
количества теплоты. Теоретическая единица количества тепла,
которую можно назвать еще механическою единицею, равна ко-
личеству теплоты, эквивалентному одной единицѣ работы. Въ С. О, 5.
системѣ единица работы есть эргъ <т. I): эквивалентное ему количество
теплоты представляетъ единицу количества теплоты, также называемую
эргомъ. Милліонъ эрговъ составляютъ мегаэргъ, 10 мегаэрговъ
равны д ж у л ю.
Измѣрить теплоту каждый разъ эквивалентною ей работою практи-
чески невозможно. Приходится выбрать практическую единицу
тепла, которую мы обозначимъ черезъ д. Мы увидимъ, что наука, къ со-
жалѣнію, еще не достигла желаемой точности въ опредѣленіи этой основ-
ной единицы. Въ прежнее время, когда точность измѣренія различныхъ
физическихъ величинъ еще не достигла той степени, до которой она
дотла въ настоящее время, можно было ограничиться обычнымъ опредѣ-
леніемъ практическихъ единицъ теплоты, большой и малой кало-
ріи, какъ количествъ теплоты, потребныхъ для нагрѣванія одного кило-
грамма и одного грамма чистой воды на 1°. Въ т. I мы видѣли, что
если принять 426 килогр.-метра работы эквивалентными одной большой
калоріи, то оказывается, что приблизительно малая калорія равна
41,6 мегаэрга и джуль равенъ 0,24 малой калоріи. Но затрудненіе осо-
баго рода и, вслѣдствіе этого, нѣкоторая неопредѣленность результатовъ
проистекаютъ отъ неустановившагося до сихъ норъ точнаго опредѣленія
калоріи; это является слѣдствіемъ неизвѣстности, въ которой
мы все еще отчасти находимся, по вопросу о зависи-
мости теплоемкости воды отъ температуры.
Конечно было бы легко остановиться на одномъ изъ нижеслѣдую-
щихъ опредѣленій калоріи:
Большая калорія равна количеству тепла, потребному для нагрѣва-
нія 1 килограмма чистой воды
1^ отъ 0° до 1° (Ке^паиіі), или
1° 1°
2) отъ 4° до 5° или отъ 14 до 15 (Мах\ѵе11), или
3) отъ 15° до 16° (около этихъ температуръ производятся обыкно-
венно калориметрическія измѣренія), или
4) отъ 0° до 100°, дѣленному на сто (Випзеп, 8 с И и 11 е г
и АѴ а г 11г а).
Опредѣленіемъ калоріи могло бы служить условіе, чтобы она равня-
лась опредѣленному, заданному числу джулей, напр., 4,2 джуля; затѣмъ
пришлось бы уже отыскать ту температуру, которой эта калорія соот-
158
Теплоемкость.
вѣтствуетъ. Мы увидимъ, что такого рода предложеніе было сдѣлано, но
что пришлось отъ него отказаться.
Оставляя пока разборъ способовъ опредѣленія теплоемкости тѣлъ,
обратимся къ основному, какъ видно изъ предыдущаго, вопросу о тепло-
емкости воды.
§ 2. Теплоемкость воды. Въ настоящее время мы имѣемъ уже
большое число (около 20-ти) работъ по вопросу о зависимости теплоем-
кости с воды отъ температуры; и тѣмъ нр менѣе вопросъ этотъ нельзя
считать окончательно рѣшеннымъ, ввиду несогласія межд} собою ре-
зультатовъ этихъ работъ. Первые Г) е Ьис, Еіаи^ег^иез и Пге
нашли, что с уменьшается, когда і растетъ. Позже В. е и т а п п вы-
велъ изъ своихъ наблюденій, что, наоборотъ, с растетъ съ і и что сред-
няя теплоемкость между 27° и 100° равна 1,0127, если при і = 27° при-
нять с = 1.
Первыя обширныя измѣренія величины с были сдѣланы К е & -
іі а и 1 і; его опыты простирались до 190°. Онъ пользовался способомъ смѣ-
шенія : хотя подробности, относящіяся къ этому способу, будутъ изложены
ниже, но мы считаемъ возможнымъ здѣсь же описать его приборъ, тѣмъ бо-
лѣе, что сущность способа смѣшенія извѣстна изъ элементарной физики.
Приборъ Ведпаиіі состоитъ изъ калориметра ге (рис. 60) и
толстостѣннаго сосуда С. вт» которомъ происходитъ нагрѣваніе воды до
высокихъ температуръ. Въ калориметрѣ находится мѣшалка тп и ре-
наверху калориметръ оканчивается трубочкой е,
снабженной дѣленіями. Емкость калориметра до
нулевого дѣленія въ е, а также емкость дѣленій
трубочки были извѣстны. Температура воды въ С
измѣрялась термометрами г, т; трубочка Т съ
краномъ /? соединяетъ сосудъ С съ калориме-
тромъ ; она проходитъ черезъ стѣнку аЬ, че-
резъ которую постоянно течетъ вода опредѣлен-
ной температуры для устраненія непосредственнаго
нагрѣванія калориметра сосудомъ С, Кранъ г
служитъ для выпусканія воды изъ калориметра.
Опытъ производился слѣдующимъ образомъ: ка-
лориметръ наполнялся водою до опредѣленной
черты: вѣсовое ея количество было въ такомъ
случаѣ извѣстно. Затѣмъ выпускалось нѣкоторое
количество воды черезъ кранъ г и взвѣшивалось;
отсюда получался вѣсъ воды, оставшейся въ ка-
лориметрѣ. Затѣмъ открывался кранъ /? и впускалось такое количество
горячей воды, чтобы вода опять доходила до какого-либо дѣленія трубки е.
При этомъ вода въ калориметрѣ непрерывно перемѣшивалась. Термоме-
тры і и г давали начальныя температуры двухъ смѣшиваемыхъ коли-
чествъ воды и окончательную температуру смѣси. Понятно, что вводи-
лись всѣ необходимыя поправки, о которыхъ будетъ сказано впослѣд-
зервуаръ термометра
Рис. во.
Теплоемкость воды
159
ствіи. Ве§-паи1і вывелъ изъ своихъ наблюденій, что теплоемкость с
воды при температурѣ і равна
с = 1 + 0,00004/ -|- 0,0000009/2.
Отсюда средняя теплоемкость между 0° и /°, см. (2) и (5) стр. 156,
= 1 + 0,00002/ 4- 0,0000003/2.
Воззсйа нашелъ, что если перевести температурныя опредѣленія
Ве^паиіі къ показаніямъ воздушнаго термометра, то результаты этихъ
наблюденій можно представить болѣе простою формулою
с = 1 4- 0,00022/,
которая даетъ с= 1,022 при 100° и с = 1,044 при 200°. Весьма стран-
нымъ представляется указаніе ѴеИеп’а будто почти всѣ числа Ее^-
паиіі вычислены невѣрно на основаніи данныхъ опытовъ, подробно ука-
занныхъ въ мемуарахъ Ее^паиіі, и что во многихъ случаяхъ вмѣсто
возрастанія теплоемкости съ температурой получается ея убываніе.
Въ 1870 г. появились почти одновременно три работы: Нігп’а,
Ріаипйіег’а и Ріаііпег’а и, наконецъ, Зашіп’а и А тайгу.
Нігп пользовался способомъ, который будетъ указанъ ниже; онъ
нашелъ измѣняемость величины с, которая въ 50 разъ превосходитъ най-
денную Ее^паиИ. Принимая с = 1 при /=1°, онъ находитъ, напр.,
с = 1,050 при /=9°, с = 1,033 при/=12°, с = 1,071 при /= 13°,5 ит. д.
Ріанікііег и Ріаііпег нашли максимумъ теплоемкости около 7°. Я а -
тіп и А т а и г у (способъ электрическаго тока, см. ниже) опредѣляли с
между 0° и 75°, и.нашли с = 1 4~ 0,00110/4~ 0,0000012/2, т.-е., напр.,
/=0 10° 50° 75° 100°
с= 1 1,011 1,053 1,089 1,122
И эти числа возрастаютъ несравненно быстрѣе, чѣмъ тѣ, которыя на-
шелъ Ее^паиіѣ. Изъ позднѣйшихъ опредѣленій величины с мы выдѣлимъ
прежде всего работы Ми епсЬЬ аи8 е п’а, Непгі с И 8 еп’а, Ваит-
§аг!пег’а, Пегова, Еарр’а, ЗоЬаппвоп’а и г-жи 8іато. При-
водимъ сперва эмпирическія формулы, которыми эти ученые полагали воз-
можнымъ выразить результаты своихъ наблюденій:
МиепсІіЬаивеіі: с — 1 4- 0,000425/... между 17° и 64°.
Непгісйвеп: с — 1 4- 0,0003156/ 4- 0,000004045/2... междуь23° и 99°.
Ваит^агіпег: 1 4-0,000307/... между 1° и 98°.
Пегова: с= 1 4-0,0011/ г 0,000006/2... между 0°и 24°(между
2° и 5°,5 другая, болѣе сложная формула).
Еарр : с= 1,039925—0,007068/4-О,00021255/2— 0,000001584/3
между 0° и 100°, причемъ средняя теплоемкость между 0° и 100°
принята равною единицѣ.
Г-жа 81 а т о : с = 1 0,001255/.
160
Теплоемкость
Для сравненія сопоставимъ результаты наблюденій для различныхъ
температуръ, полагая вездѣ с = 1 при 0°.
5° 10° 20° 40° 60° 80° 100°
Ее^паиіѣ: 1,00022 1,00049 1,00116 1,00304 1,00564 1,00896 1,01300
В088СІіа: 1,00110 1,00220 1,00440 1,00880 1,01320 1,01760 1,02200
Латіпи Ашаигу: 1,00554 1,01112 1,02248 1,04592 1,07032 1,09568 1,12200
Ваит^агѣпег: 1,00154 1,00307 1,00614 1,01228 1,01842 1,02456 1,03070
Неі ПГІСІ18ОП: 1,00168 1,00356 1,00793 1,01910 1,03349 1,05114 1,07201
МиепсЫіаиееп: 1,00151 1,00302 1,00604 1,01208 1,01812 1,02415 1,03019
Г-жа 8іато: 1,00628 1,01255 1,02510 1,05020 1,07530 1,10040 1,12551
6еГ08а: 1,00565 1,01160 1,02440 —
Еарр: 0,9716 0,94999 0,9335 0,9576 0,9989 0,9852 0,8409
<1о1іапп8оп: 1,0000 1,00о9 1,0170 1,039
Сравненіе этихъ чиселъ показываетъ, какъ громадны разности между
опредѣленіями различныхъ ученыхъ. Дальнѣйшія изслѣдованія произво-
дили Реіііпеііі, Кееееп, ѴеНеп и В г и е 8 с Ь. Изъ нихъ V е 1 -
іеп получаетъ минимумъ с = 0,9734 при 43°,5, полагая с0 = 1.
Обращаемся къ другой группѣ работъ, произведенныхъ за послѣднее
время, а именно къ работамъ Еоаѵ 1 ап(Га, ЬіеЬі^’а, Вагіоіі и
бЧгассіаіі, ОгИіііІіе’а, Оіеіегісі, Ьийіп’а, Вагпез и Саі-
Іепсіаг, 8сЬп8Іег и банной, и наконецъ, Ееупо 1 (1 е’а и
М о о г Ъ у.
Е о аѵ 1 а п (1 произвелъ замѣчательный рядъ опредѣленій механическаго
эквивалента тепла Е, которыя мы подробно разсмотримъ ниже. При этомъ
онъ нашелъ, что величина Е, эквивалентная количеству теплоты, потреб-
ному для повышенія температуры вѣсовой единицы воды на 1°, зависитъ
отъ самой температуры воды. Понятно, что величина Е пропорціональна
теплоемкостямъ с. Для Е въ к и логр.-метрахъ (на широтѣ Бальти-
моры) онъ нашелъ такія числа:
1= 5° ІО» 15о 20° 25° 300
Е = 429,8 428,5 427,4 426,4 425,8 125,6.
Приводимъ еще одну таблицу, въ которой Е выражено въ д ж у -
ляхъ (ІО7 эрговъ^
І = 140 16° 180 200 220 24° 25°
^=4,192 4.187 4.183 4.179 4,176 4,174 4,173.
Эти числа показываютъ, что величина с уменьшается при по-
вышеніи температуры и имѣетъ около 30° минимумъ. Не-
посредственныя измѣренія по способу смѣшенія подтвердили этотъ резуль-
татъ и показали, что между 30° и 100° величина с весьма медленно
увеличивается. Если среднюю теплоемкость между 0° и 10° при-
нять равной единицѣ, то средняя теплоемкость между 28° и 100° равна
0,9933. Результаты ЕоАѴІапсГа были подтверждены на приборѣ Еоаѵ-
1 а п (Га ЬіеЬі§’омъ.
Теплоемкость воды.
161
Ьау, Регпеі и наконецъ ЛѴаійпег и М а По ту ввели различ-
ныя поправки въ числа Волѵіапсі’а. ЛѴаідпег и Маііогі даютъ
слѣдующія числа:
10° 15° 20° 25° 30° 35°
4,195 4,187 4,181 4,176 4,175 4,177 дж.
Между 15° и 25° можно положить
Сі = Г1б [1 — 0,00026 (І— 15)].
Если положить с1б = 1, то получаются такія числа:
5° 10° 15° 20° 25° 30° 35°
1,0042 1,0019 1,0000 0,9983 0,9972 0,9967 0,9969.
Минимумъ находится при 32°, между тѣмъ какъ неисправленныя
числа В о лѵ 1 а п (Га даютъ 29°. Вагіоіі и бігассіаіі весьма тщательно
измѣряли величину с между 0° и 30° . Принимая с = 1 при 15°, они нахо-
дятъ, что с=.а — Ы — гдѣ а = 1,00688, # = 556Ю“6, (1 =
= 615.10~8, е= 1015.ІО 9, /=13.10—9. Эти числа даютъ для с минимумъ
около 20°. ОгПППіъ (методъ электрическій, см. ниже § 9) выводитъ
изъ своихъ опредѣленій величины Д что между 15° и 25° с=1 —
— 0,000266(/ — 15°), если принять с=1 при 15°. Окончательно (тгіТ-
1 і IЬ 8 находитъ такія числа для Е:
15° 20° 25°
4,19г* 4,192 4,187 дж.
Ашев даетъ въ своемъ отчетѣ исправленныя имъ числа
4,190 4,184 4,179 'дж.
Віеіегісі изъ подобныхъ же опредѣленій находитъ, что с имѣетъ
минимумъ около 30°, равный 0,9872 (принимая с=1 при 0°). и затѣмъ
растетъ до 1,0306 при 100°. Средняя теплоемкость между 0° и 100°
равна 1,0045. Ьи(1іп находитъ формулу
С = 1 — 0,0007667^ + 0,0000196/® — 0,0000001162е3,
которая даетъ минимумъ с = 0,9914 при 25°, затѣмъ с =1 при 62°, максимумъ
с —1,0053 при 85° и наконецъ с— 1,0033 при 100°. Позже (1896) Ьи-
сі і п ввелъ еще нѣкоторыя поправки въ свои вычисленія и нашелъ,
что средняя теплоемкость воды между 0° и 100° равна ея теплоемкости
между 0° и 1°.
Въ 1899 г. появилась работа СаПевдаг’а и Вагпез’а, которые
заставляли протекать струю воды черезъ трубку; вдоль оси этой трубки
была натянута проволока, черезъ которую пропускался электрическій токъ
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. Ш, изд. 3-е. И
162
Теплоемкость.
Количество теплоты, выдѣлявшейся въ проволокѣ, могло быть вычислено
весьма точно; нагрѣваніе воды измѣрялось термоэлектрическимъ элемен-
томъ и отсюда могла быть найдена теплоемкость воды. Въ предѣлахъ
между 0° и 60° названные ученые* нашли
с = 0,9982 + 0,0000045(2^ — 40)2,
что даетъ минимумъ с при 40°. Впослѣдствіи Вагпев далъ формулу
с = 0,99733 ф- 0,0000035(37,5 - І)2 + 0,00000010(37,5 — /)3.
Отъ 5° до 37,5° надо послѣдній членъ взять съ плюсомъ, а отъ
37,5° до 55° съ минусомъ. Выше 55°
с = 0,99850 + 0,000120(/ — 55) -|- 0,00000025(/ — 55)2.
йсЬпвіег и Ѳаппоп опредѣлили Е для 19°,1 и нашли Е —
= 4,1905 дж. Ашев ввелъ нѣкоторыя поправки и далъ число Е =
= 4.185 дж.
Интересное изслѣдованіе произвелъ Шеіегісі (1905) надъ тепло-
емкостью воды между 100° и 300°. Онъ воспользовался ледянымъ
калориметромъ Випзеп’а. Воду онъ нагрѣвалъ въ припаянной квар-
цевой трубочкѣ, которую онъ затѣмъ пустую нагрѣвалъ до той-же
температуры, чтобы опредѣлить поглощаемую ею теплоту. Принимая
среднюю калорію между 0° и 100° равной единицѣ, онъ получилъ для средней
теплоемкости воды ст между 0° и Е и для теплоемкости при /° слѣду-
ющія выраженія, имѣющія силу въ предѣлахъ отъ 35° до 300°:
ст = 0,99827 — 0,00005184^ + 0,00000069 Г212
Сі = 0,99827 — 0,00010368^ + 0,0000020736^.
По этимъ формуламъ получаются слѣдующія значенія для ст и сі :
і — 100° 140° 180° 220° 260° 300°
ст 1,0000 1,0046 1,0113 1,0203 1,0315 1,0449
Сі 1,0086 1,0244 1,0468 1.0758 1.1115 1,1538
Яапке (1910) находить минимумъ с при 27°; полагая с =*= 1 при
15° онъ находитъ с = = 1,00560 при 2°, с = 0,99869 при 27° и с- = 1,00048
при 46°.
Мы разсмотрѣли важнѣйшія работы, относящіяся къ опредѣленію
теплоемкости воды. Теперь является вопросъ, каковы положительные, точ-
ные результаты этихъ изслѣдованій? Въ 1900 и 1901 гг. появились че-
тыре работы, которыя имѣли цѣлью опредѣлить эти результаты на осно-
ваніи лучшихъ изслѣдованій. Эти четыре работы слѣдующія: АѴ а г -
Ьиг^, рефератъ объ единицѣ теплоты (Лейпцигъ 1900); Атее и
СггИііІЬз напечатали по реферату въ «Каррогів ргёзепѣёз аи Соп-
^гёз іпіегпаііопаі де рііузіцие» (Рагіз 1900); наконецъ 6 гі Иіійв’омъ
Теплоемкость воды.
163
было сдѣлано въ Лидсѣ четыре доклада, которые появились особой кни-
гой подъ заглавіемъ «Тйе іЬеттаі теазигетепі оі епег^у» (Сат-
Ьгій§е 1901).
Дѣло идетъ главнымъ образомъ о рѣшеніи слѣдующихъ вопросовъ:
1. Какъ великъ механическій эквивалентъ какой-
либо опредѣленной калоріи? Для 15°-калоріи (водородный тер-
мометръ) этотъ вопросъ въ настоящее время, повидимому, рѣшенъ. А ш е 8 ,
СггіИііЬіб и УѴ а г Ъ и г § находятъ, что лучшія изъ до сихъ поръ произ-
веденныхъ изслѣдованій дают^ слѣдующій результатъ
/:1б = 4,188 джуля.
причемъ только послѣдняя цифра сомнительна на одну единицу.
Въ 1907 г. была учреждена при Нѣмецкомъ Физ. Обществѣ особая
коммиссія по вопросу объ единицахъ и обозначеніяхъ въ формулахъ (Аив-
8СІШ88 Гпег ЕіпЪеііеп шій Рогтеі^тоеввеп, обычно для краткости обозна-
чаемый А. Е. Е.). Въ 1908 г. эта коммиссія вывела, какъ наиболѣе вѣроят-
ное, то-же самое число 4,188; но въ формулировкѣ своихъ выводовъ она,
почему то, приводитъ (1908 и 1910) число
Е1б = 4,189 джуля = 427.2 клгр.-м.
Джуль = 0,23865 мал. 15° калоріи.
*
II. Какъ измѣняется теплоемкость с воды въ наи-
болѣе важномъ для калориметріи промежуткѣ между 10°
и 25° ? И этотъ вопросъ можетъ считаться рѣшеннымъ. 0гіІП11і8 даетъ
результаты лучшихъ изслѣдованій въ слѣдующей таблицѣ:
Вагіоіі и 81 г а с с і а і і. Ь и а і п. К о лѵ 1 а п а. ОгіИііЬз. С а 11еп4 аг и Вагпез.
10° 1,0018 1,0010 1,0019 — 1,0021
11 13 08 14 — 16
12 09 06 10 — 11
13 05 04 07 1,0006 07
14 02 02 03 03 03
15 1,0ѵ00 1,0000 1,0000 1,0000 1,0000
16 0,9998 0,9998 0,9ЭУб 0,9997 0,9997
17 97 97 93 94 94
18 96 96 90 91 90
19 95 95 86 88 88
20 94 94 83 85 85
21 93 93 81 82 83
22 93 93 79 79 80
23 94 92 76 76 77
24 95 92 74 73 75
25 97 93 72 70 74
30 1.0010 0,9996 0,9967 — 0,9969
35 — 1,0003 0,9969 — 0,9967
11*
164
Теплоемкость.
Особенно замѣчательно совпаденіе чиселъ въ послѣднихъ трехъ столб-
цахъ, причемъ слѣдуетъ замѣтить, что соотвѣтствующія работы произво-
дились по совершенно различнымъ способамъ.
ХѴагЬпг^, который разсматривалъ только первыя четыре работы,
принимаетъ, какъ среднее значеніе:
ІО» 150 20°
с = 1,0016 1,0000 0,9989
и полагаетъ между -|-100 и +20°:
с = 1 — 2,7. 10~4(^ — 15) + 10~5(7— 15)2.
III. Какъ измѣняется теплоемкость с воды между 0°,
и 100°? Сюда присоединяются частные вопросы: при какой темпера-
турѣ с достигаетъ минимума и какъ велика средняя теплоем-
кость воды между 0° и 100°? Удовлетворительный отвѣтъ на главный
вопросъ до сихъ поръ еще не полученъ; значенія для с при высокихъ
температурахъ, найденныя различными учеными, сильно между собою раз-
нятся. Если положить с0 = і, то напр. Ѵеііеп получилъ Гюо — 0,9846,
Віеіегісі — Сюо = 1,0306: разница составляетъ 41/2%. Работы Саі-
1 е п й а г’а и В а г п е а’а дали для Е слѣдующія числа (приведенныя Сг г И -
П1Ь з’омъ къ водородному термометру).
5° 4,2130 джуля 40° 4,1769 джуля 75° 4,1912 джуля
10 4,1991 45 4,1776 80 4,1946
15 4,1912 50 4,1785 85 4,1979
20 4,1851 55 4,1806 90 4,2014
25 4,1805 60 4,1828 95 4,2050
30 4,1780 65 4,1854
35 4,1774 70 4,1881 Среднее 4,1887
Температура і, при которой с достигаетъ минимума, еще весьма не-
опредѣленна, какъ и всегда въ подобныхъ случаяхъ. Мы видѣли выше,
что по числамъ Колѵіапй’а і близко къ 30°. Саііепйаг и Вагпез
нашли сперва ^ = 40°, позже Вагпез нашелъ 37°,5 (стр. 162).
Для отношенія средней теплоемкости с0___юо воды между 0° и 100°
къ значенію с15 при 15° ЛѴ агЬиг^ даетъ слѣдующія числа:
Изъ опытовъ Ьи йіп’а...........= 1,0052
^іб
« Біеѣегісі. . . . =10103
сіб
« <То1уи(лгіПИ1і8’а -°-=1—= 0,9957
<ЛБ
К е у п о 1 <18 и М о о г Ь у даютъ, какъ среднее значеніе между 0° и 100°,
Теплоемкость воды.
165
величину 2: = 4,1833 джуля. Если взять у Воѵѵіапй’а величину для
Е при 15°, то получится
-== 0,9988.
сіб
ВеЪп (1905) изъ своихъ опытовъ получилъ:
Со~100 = 0,9997.
г1б
ѲгіІПіЬв вводитъ поправку; онъ находитъ Е — 4,1836 джуля и
Со—100 г 008
Г1Б
Коммиссія А. Е. Р. (1908) приходитъ къ заключенію что
со-100 = с1б.
Изъ чиселъ Саііепсіаг’а и Вагпев’а Сгг ИШЬ 8 находитъ сред-
нюю величину 2: = 4,1854 джуля. Вагпев находитъ, что г0—1Оо = с16.
Итакъ, повидимому, можно утверждать, что средняя
теплоемкость с0___юо воды между 0°и100° эквивалентна 4,184
джуля, причемт> ошибка не превышаетъ О,О5°/о и что Со—юо приблизи-
тельно равно с16.
IV. Какую величину слѣдуетъ принять за единицу
теплоты и какой номенклатуры держаться въ калоримет-
ріи? СггИШЬз сдѣлалъ сперва (1896) слѣдующія предложенія:
1. Механическая единица теплоты есть джул ь = ІО7 эрг.
Это опредѣленіе очевидно чисто теоретическое.
2. Термометрическая единица теплоты р ав н а 4,2 джуля.
3. Количество теплоты, нагрѣвающее 1 гр. воды отъ
9Ѵ20 ДО Ю1/./, равно термометрической единицѣ теплоты.
Далѣе СггИШЬв предложилъ называть термомъ то количество те-
плоты, которое требуется для нагрѣванія 1 гр. воды на 1°; такимъ обра-
зомъ термъ есть функція температуры. Опредѣленный нормальный
термъ (зіашіагсі ІЬегш) онъ предложилъ называть «Волѵіапсі». По выше-
изложенному «КоѵѵіаінЬ равнялся бы терму при 10°.
Но позже (1901) СгіИШЬз существенно измѣнилъ пункты 2 и 3.
Новѣйшія, выше изложенныя изслѣдованія привели его къ тому резуль-
тату , что 4,2 джуля соотвѣтствуютъ терму въ 7°,5; эта температура прак-
тически значенія не имѣетъ, такъ какъ она слишкомъ низка. Поэтому
онъ отказался отъ «круглаго» числа 4,2 и высказалъ слѣдующія пред-
ложенія :
1. Термометрическая единица теплоты есть то коли-
чество теплоты, которое нагрѣваетъ 1 гр воды отъ 17°до
18° по парижской водородной шкалѣ.
2. Эта единица теплоты равняется 4.184 джуля.
166
Теплоемкость.
3. Та же единица теплоты соотвѣтствуетъ средней
теплоемкости воды между 0° и 100°.
Названія «Волѵіапй» онъ при этомъ не употребляетъ, хотя казалось
бы вполнѣ цѣлесообразнымъ сохранить названія «термъ» и Ко\ѵ1ап(1
. (термъ при 17°).
Теплоемкость с воды ниже 0° изслѣдовали То ш ша8і пі и С а г -
бапі и, кромѣ того, МагііпеШ; первые доходили до 10°. послѣд-
ній до —6°. Обѣ работы показали, что с увеличивается при пониженіи
температуры і ниже 0°. Числа Магііпеііі оказываются довольно со-
гласными съ эмпирическою формулою Вагіоіі и Яѣгассіаѣі. приве-
денной на стр. 161. Приблизительно с увеличивается на 0,0005 при по-
ниженіи I на 1° (с= 1 при ^ — 0°). При і=— 6°,2 имѣемъ с = 1,0032.
В а г п е 8 и Сооке (1902) опредѣлили с до — 5°,5 ; они нашли, что
кривая, изображающая между 0° и 100°, правильно продолжается
и ниже 0°. Для I — —-5° они нашли с= 1,0159, положивъ с16=1.
Теплоемкость с, о которой мы говорили, представляетъ для тѣлъ
твердыхъ и жидкихъ теплоемкость при постоянномъ давленіи, со-
отвѣтственно величинѣ ср для газовъ, ибо измѣренія с производятся при
почти постоянномъ атмосферномъ давленіи. Вычисленіе теплоемкости сѵ
при постоянномъ объемѣ производится для твердыхъ и жидкихъ тѣлъ на
основаніи теоретической формулы, которая будетъ выведена ниже. Ради
полноты разбора вопроса о теплоемкости воды приведемъ величины сѵ для
воды по вычисленіямъ Вагіоіі и бѣгассіаіі; какъ и прежде (стр. 161)
принято с=1 (точнѣе ср — 1) при 15°.
І = 0° 5° 10° 15° 20° 25° 30° 35°
6^= 1,00592 1,00380 1,00046 0,99683 0,99320 0.98984 0,98697 0,98490
При 4° очевидно сѵ = ср; при всѣхъ другихъ температурахъ сѵ < ср
§ 3. Способъ Ьаѵоізіег и Ьаріасе’а. Обращаясь къ способамъ опредѣ-
ленія теплоемкости тѣлъ, мы сперва разсмотримъ лишь тѣ способы, кото-
рые пригодны для тѣлъ твердыхъ и жидкихъ.
Способъ таянія льда, которымъ пользовались Ьаѵоівіет и Ьа-
р 1 а с е, основанъ на опредѣленіи тепла, отданнаго тѣломъ при охлажденіи,
путемъ измѣренія количества льда (при 0°), расплавленнаго этою отдан-
ною теплотою. Приборъ Ьаѵоівіег и Ьаріасе’а состоитъ изъ трехъ
металлическихъ сосудовъ, вставленныхъ одинъ въ другой (рис. 61). Во
внутренній сосудъ, сдѣланный изъ проволочной ткани, помѣщается испы-
туемое тѣло, температуру котораго обозначимъ черезъ і\ искомую тепло-
емкость тѣла обозначимъ черезъ с. Промежутки между этимъ сосудомъ и сосу-
домъ В, а также между В и А, наполнены толченымъ льдомъ, лежащимъ
также на крышкахъ, покрывающихъ два внутренніе сосуда. Вода, образо-
вавшаяся при плавленіи льда и вытекшая черезъ г, взвѣшивается. Пусть
ея вѣсъ р; скрытая теплота плавленія льда = 80; слѣд. мы имѣемъ сі = 80/7.
Раздѣляя с на вѣсъ тѣла, получимъ теплоемкость вещества,
изъ котораго состоитъ тѣло, если оно однородно. Ледъ въ сосудѣ В дол-
Способъ Германа и Випееп’а.
167
женъ быть предварительно смоченъ водою. Способъ этотъ имѣетъ только
историческій интересъ и точныхъ результатовъ дать не можетъ.
Рис. 61.
Неодинаковая теплоем-
кость различныхъ веществъ
обнаруживается на остроум-
номъ опытѣ ТупдаІГя: на
восковую плитку СО ^рис. 62)
кладутся шарики одинаковаго
вѣса, приготовленные изъ
различныхъ металловъ и пред-
варительно нагрѣтые до оди-
наковой температуры. Воскъ
подъ шариками плавится, при-
чемъ желѣзный шарикъ бы-
стрѣе другихъ проходитъ черезъ
воскъ и падаетъ внизъ; нѣ-
сколько позже за нимъ слѣдуетъ шарикъ мѣдный; оловянный выходитъ
нижнею частью изъ воска, но не выпадаетъ; менѣе другихъ углубляются
въ воскъ шарики висмутовый и свинцовый, теплоемкости которыхъ наи-
меньшія. Противъ этого опыта можно возразить, что шарики, имѣя раз-
ные объемы, расплавляютъ неодинаковыя количества воска, углубляясь
на равную величину. Поэтому Д. Л а ч и н о в ъ замѣнилъ сплошные ша-
рики полыми, причемъ радіусы полостей были выбраны такъ, чтобы всѣ
шарики имѣли одинаковый радіусъ внѣшней поверхности и одинако-
вый вѣсъ.
§ 4. Способъ ледяного калориметра Германа и Випзеп'а. Этотъ
способъ основанъ также на опредѣленіи количества льда, превращеннаго
въ воду тою теплотою, которую отдало испытуемое тѣло, охладившись
отъ извѣстной намъ первоначальной температуры & до 0°. Количество
расплавленнаго льда измѣряется, однако, не взвѣшиваніемъ образовав-
шейся воды, но путемъ опредѣленія уменьшенія объема, сопровождаю-
щаго плавленіе льда. Это уменьшеніе ѵ объема можетъ быть опредѣлено
двумя способами : непосредственно волюмомстрически, или взвѣшиваніемъ
ртути, заполняющей образовавшійся объемъ ѵ (способъ Всііиііег’а и
ѴѴ а г 11і а).
Когда 1 гр. льда при 0° плавится, то получается уменьшеніе объема
въ 0,09070 куб. см.; при этомъ ледъ поглощаетъ 80,025 мал. кал.
Отсюда слѣдуетъ, что уменьшеніе чю объема, вызванное притокомъ
одной малой калоріи, равно
= 0,0011334 куб. см.
80,025 л
Если наблюдалось уменьшеніе ѵ объема, то число (? малыхъ кало-
рій, отданныхъ тѣломъ, равно съ другой стороны = гдѣ
168
Теплоемкость.
Сі его средняя теплоемкость между 0° и /°. Равенство Сіі = ѵ:іѵ даетъ:
_ ѵ ___ ѵ __________882,304г/
Сі~ ѴОІ “О^О11334/“ І ...... (9)
Здѣсь ѵ должно быть выражено въ куб. см. Раздѣляя на вѣсъ
тѣла (въ граммахъ), получаемъ среднюю теплоемкость вещества, если тѣло
однородное. Если опредѣлять Р ртути, заполняющей объемъ т/, то имѣ-
емъ Р = ѵд, гдѣ б плотность ртути.
Одной малой калоріи соотвѣтствуетъ вѣсъ /7 = ^(5, т.-е.
/7 = 0,01544 гр. ртути,
причемъ за малую калорію принята часть той теплоты, которая нагрѣ-
ваетъ 1 гр. воды отъ 0° до 100°. Очевидно 0 = Р: р = с^і, откуда
Р Р
С* рі 0,01544^ ’ * ’ * . (10)
Если вмѣсто испытуемаго тѣла взять сперва воду, то величина р мо-
жетъ быть и непосредственно предварительно опредѣлена.
Вііпзеп принялъ /7 = 0,01541 мгр.; Ѵеііеп (1884) нашелъ
р = 0,01547. ѴѴагЪиг^ полагаетъ однако, что приведенное нами число
йсЬиІІег’а и ЛѴагІЬ’а наиболѣе точное. Оіейегісі (1905) пользо-
вался значительно большимъ числомъ р = 0,015491.
Идея ледяного калориметра принадлежитъ московскому ученому Гер-
ману. который въ 1834 г. въ статьѣ «О пропорціи, въ которой теплота
соединяется съ химическими элементами» описалъ приборъ, изображен-
ный на рис. 63. Указаніе на работу Германа, равно какъ рисунокъ
и описаніе прибора заимствуемъ изъ книги В. Ф. Лугинина «Описаніе
различныхъ методовъ опредѣленія теплотъ горѣнія органическихъ сое-
диненій». Москва, 1894. Приборъ Германа состоялъ изъ стеклян-
наго сосуда АА (рис. 63), черезъ крышку котораго проходятъ тонко-
стѣнный латунный цилиндръ ВВ, трубка съ поршнемъ О/Э и трубка СС,
снабженная дѣленіями и прокалибрированная. Сосудъ АА весь наполня-
ется смѣсью льда и воды. Испытуемое вещество предварительно нагрѣ-
вается въ сосудѣ ЕЕ до температуры, показываемой термометромъ, и за-
тѣмъ быстро вносится въ сосудъ ВВ, какъ показано на рисункѣ. Пор-
шень ОО служитъ для того, чтобы до начала опыта довести воду въ СС
до нулевого, верхняго дѣленія. Когда испытуемое тѣло охлаждается
до о0, то часть льда въ АА расплавляется и соотвѣтствующее уменьше-
ніе ѵ объема обнаруживается пониженіемъ уровня воды въ трубкѣ СС.
Въ 1847 г. НегзсЬеІІ, не зная о работѣ Германа, указалъ на
подобный же способъ опредѣленія теплоемкостей и, наконецъ, въ 1870 г.
В и п 8 е п построилъ свой ледяной калориметръ, изображенный на рис. 64
въ одной изъ видоизмѣненныхъ его формъ. Онъ состоитъ изъ стеклян-
наго резервуара Ѵ7Ѵ7. соединеннаго съ трубкою С^Е; резервуаръ ѴСѴУ
Способъ Випееп’а.
169
наполненъ чистою водою, трубка (№ ртутью, которая наполняетъ также
ЕИР. Въ резервуаръ Ѵ7Ѵ7 входитъ открытая сверху трубка Р^ которая
закрывается пробкою К. Горизонтальная трубка /?. лишь частью изобра-
женная на рисункѣ, снабженная дѣленіями и весьма тщательно прокали-
брирована. При помощи крана Л можно прибавлять ртуть и такимъ обра-
Рис. 64.
зомъ приводить ее до начала опыта къ нулевому дѣленію трубки /?, т.-е.
до мѣста, находящагося вблизи праваго ея конца. Весь приборъ помѣ-
щается въ сосудѣ 5, наполненномъ чистымъ снѣгомъ или смѣсью воды
и льда. Сосудъ 5 находится во второмъ сосудѣ Л, содержащемъ дурные
проводники тепла или толченый ледъ.
Прежде всего слѣдуетъ часть воды въ Ѵ7Ѵ/ превратить въ ледъ.
Для этого достаточно влить въ трубу Р7 нѣсколько алкоголя и затѣмъ
вставить въ нее пробирный стаканчикъ, содержащій смѣсь СаСЦ и снѣга.
Черезъ нѣкоторое время образуется ледяная масса Е; тогда вынимаютъ ста-
канчикъ и при помощи пропускной бумаги высушиваютъ трубку РЕ
Можно поступить иначе, а именно пропускать втеченіе нѣкотораго вре-
мени черезъ Р7 струю охлажденнаго алкоголя. Для этого пользуются при-
боромъ, схематически изображеннымъ на рис. 65. Трубка Са представля-
етъ отдѣльно трубку Р/ рисунка 64; пробки и трубки соединяютъ Са съ
сосудами А и В, какъ показано на рис. 65. Сосудъ А содержитъ алко-
голь, сосудъ В сначала пустъ; оба сосуда окружены охлаждающей
170
Теплоемкость.
смѣсью изъ поваренной соли и снѣга. Высасывая воздухъ попере-
мѣнно изъ трубокъ а и Ь, заставляютъ холодный алкоголь многократно
протекать черезъ трубку Са, пока вокругъ нея не образуется ледяная
масса Е (рис. 64).
Когда тѣмъ или фугимъ способомъ достигнуто образованіе льда Е,
наливаютъ въ Р} нѣкоторое количество воды, вслѣдствіе чего вокругъ
образуется тонкій слой воды, сообщающійся съ На дно У кладутъ
иногда кусокъ ваты, чтобы падающее въ Р/ тѣло не могло пробить дна.
Вода, налитая въ V, еще тѣмъ полезна, что нижніе ея слои, отнимая те-
плоту отъ испытуемаго тѣла, сначала немного нагрѣваются, но во вся-
комъ случаѣ менѣе, чѣмъ до 4°. Вслѣдствіе этого они остаются внизу
и, съ своей стороны, передаютъ полученную ими теплоту содержимому
сосуда ІГІГ.
Когда вода налита въ У и ртуть въ Р доведена до желаемаго дѣле-
нія, опускаютъ испытуемое тѣло, предварительно нагрѣтое до /°, въ РЕ
Часть льда Е растаетъ, объемъ уменьшится и конецъ ртутнаго столбика
въ Р перемѣстится налѣво, положимъ на п дѣленій. Если емкость одного
дѣленія равна со, то ѵ = по), и слѣд. по формулѣ (9) получимъ
882.304/76)
сі =
/
170
Теплоемкость.
смѣсью изъ поваренной соли и снѣга. Высасывая воздухъ попере-
мѣнно изъ трубокъ а и Ь, заставляютъ холодный алкоголь многократно
протекать черезъ трубку Са, пока вокругъ нея не образуется ледяная
масса Е (рис. 64).
Когда тѣмъ или фугимъ способомъ достигнуто образованіе льда Е,
наливаютъ въ Р} нѣкоторое количество воды, вслѣдствіе чего вокругъ
образуется тонкій слой воды, сообщающійся съ На дно У кладутъ
иногда кусокъ ваты, чтобы падающее въ Р/ тѣло не могло пробить дна.
Вода, налитая въ V, еще тѣмъ полезна, что нижніе ея слои, отнимая те-
плоту отъ испытуемаго тѣла, сначала немного нагрѣваются, но во вся-
комъ случаѣ менѣе, чѣмъ до 4°. Вслѣдствіе этого они остаются внизу
и, съ своей стороны, передаютъ полученную ими теплоту содержимому
сосуда ІГІГ.
Когда вода налита въ У и ртуть въ Р доведена до желаемаго дѣле-
нія, опускаютъ испытуемое тѣло, предварительно нагрѣтое до /°, въ РУ.
Часть льда Е растаетъ, объемъ уменьшится и конецъ ртутнаго столбика
въ Р перемѣстится налѣво, положимъ на п дѣленій. Если емкость одного
дѣленія равна со, то ѵ = по), и слѣд. по формулѣ (9) получимъ
882.304/76)
сі =
/
Способъ Раѵге’а и бПЪегшапп’а.
171
Соединеніе широкой трубки съ капилярною въ приборѣ, которымъ
пользовался Випвеп, было нѣсколько иначе устроено, чѣмъ показано
на рис. 64; капилярная трубка 5 (рис. бб) проходила черезъ пробку к,
которую можно было нѣсколько поднимать или опускать и этимъ приво-
дить конецъ ртутнаго столбика въ горизонтальной части трубки 5 до же-
лаемаго начальнаго положенія. Въ этомъ приборѣ ш = 0,0<ю07733 куб.
см., такъ что вычислялось по формулѣ
0,068213л
Чувствительность прибора Випвеп’а весьма велика; 0,4 гр. ла-
туни, нагрѣтой до 37° и опущенной въ РЛ заставляетъ ртуть въ /? пе-
ремѣститься на 20,3 дѣленій.
ЗсЬиІІет и АѴагІІіа видоизмѣнили устройство калориметра Вип-
8 е п’а и между прочимъ замѣнили горизонтальную трубку /? изогнутой
трубкой АВ (рис. 67), наполненной ртутью до конца В, который погру-
жался въ плоскую чашечку со ртутью. Вѣсъ этой чашечки измѣрялся до
и послѣ опыта, чѣмъ и опредѣлялся вѣсъ Р ртути, втянутой въ калори-
метръ. Формула (10) стр. 168 даетъ въ этомъ случаѣ искомую теплоем-
кость С/ Точность этого способа, какъ показалъ В. Ф. Лугининъ, въ
гри раза превосходитъ точность способа В и п 8 е п’а.
Способомъ 8 с 11 и 11 е г’а и ЛѴ а г і На пользовался также ѵ о п Т Ь а п ,
въ значительной степени измѣнившій устройство самаго калориметра.
Дальнѣйшія видоизмѣненія ввели Біеѣегісі, Воу8, Кипи (1904) и
Сгетіеп (1905); послѣдній устроилъ удобный лекціонный приборъ.
Ьіпсіпег (1902) далъ подробныя указанія, какъ слѣдуетъ пользо-
ваться ледянымъ калориметромъ, чтобы получить наиболѣе точные ре-
зультаты.
§ 15. Способъ Гаѵге’а и 8і1Ьегшапп’а. Ртутный калориметръ на-
званныхъ ученыхъ изображенъ на рис. 68. Онъ состоитъ изъ большого
чугуннаго или стекляннаго сосуда, соединеннаго со стеклянною трубкою 2?,
снабженною дѣленіями и нрокалибрированною. Сверху находится широ-
кая трубка съ поршнемъ, приводимымъ въ движеніе при помощи ^руко-
ятки В. Сбоку входятъ во внутрь сосуда одна или двѣ металлическія
трубки А, закрытыя съ внутренняго конца (см. пунктиръ на рисункѣ).
Весь сосудъ долженъ быть наполненъ ртутью, входящей также и въ
трубку О. Труба Ь служитъ для отсчитыванія дѣленій, противъ которыхъ
останавливается ртуть. При помощи поршня и рукоятки В доводятъ
ртуть въ началѣ каждаго опыта до нѣкотораго дѣленія трубки 7), лежа-
щаго недалеко отъ ея начала съ правой стороны.
Весь приборъ вставляется въ ящикъ и окружается дурными провод-
никами тепла. Если въ одну изъ боковыхъ трубокъ А ввести тѣло, которое
является источникомъ тепла, или которое теплѣе ртути въ Л, то эта ртуть
расширяется и конецъ ртутнаго столбика въ О перемѣщается влѣво
172
Теплоемкость,
на нѣкоторое число дѣленій, которое обозначимъ черезъ п. Необходимо
знать число дѣленій М, соотвѣтствующихъ одной калоріи, выдѣлившейся
въ боковой трубкѣ А, въ которую обыкновенно наливаютъ немного ртути
и затѣмъ вставляютъ въ нее стеклянный тонкостѣнный стаканчикъ. Въ
послѣдній вводятъ, какъ показано на рисункѣ, конецъ пипетки, содержа-
щей въ Е опредѣленное количество воды, которую нагрѣваютъ спиртовою
Рис. 68.
лампочкою до кипѣнія. Затѣмъ перевертываютъ пипетку, вращая ее около
трубочки, вставленной въ калориметръ, такъ чтобы вода влилась въ ста-
канчикъ А, Когда она охладится, опредѣляютъ маленькимъ термоме-
тромъ ея температуру і, и число дѣленій, на которыя перемѣстилась
ртуть въ если р вѣсъ воды и Т температура кипѣнія, то вода от-
дала р(Т—I) единицъ тепла. Отсюда слѣдуетъ, что одна единица тепла
вызываетъ перемѣщеніе ртути въ О на
дѣленій. Если въ другомъ опытѣ ртуть въ О перемѣстилась на п дѣле-
ній, то мы заключаемъ, что въ трубкѣ А выдѣлилось число ф единицъ
тепла, равное
л = пр(Т і)......................(10а)
Приборъ этотъ можетъ служить для опредѣленія теплоемкости,
хотя не всегда, удобно опредѣлить температуру і, до которой охладилось
тѣло въ А, Приборъ главнымъ образомъ назначался для измѣренія
Способъ смѣшенія.
173
количествъ тепла, выдѣляющихся при различныхъ химическихъ про-
цессахъ.
Яатіп видоизмѣнилъ приборъ Еаѵге’а и ^іІЬегтапп’а, при-
давъ ему болѣе удобную форму. Калориметръ Яатіп’а описанъ въ егн
курсѣ физики (напр. изд. 3-ье, часть II, 1878 г. стр. 17*).
§ 6. Способъ смѣшенія. Наиболѣе важнымъ изъ всѣхъ способовъ
опредѣленія теплоемкости слѣдуетъ признать способъ смѣшенія, такъ какъ
имъ наиболѣе часто пользуются. Этимъ способомъ впервые воспользо-
вался Рихманъ въ С.-Петербургѣ (1750). Сущность его заключается
въ слѣдующемъ. Калориметръ состоитъ изъ металлическаго цилиндриче-
скаго сосуда, въ который вливается вѣсовое количество р воды; въ
водѣ находится мѣшалка и термометръ. Испытуемое тѣло нагрѣва-
ется до опредѣленной температуры Т и затѣмъ по возможности бы-
стро погружается въ воду калориметра, которая подвергается непре-
рывному перемѣшиванію. Пусть і первоначальная температура воды
и Ѳ окончательная температура или, какъ говорятъ, температура
Т
смѣси. Обозначимъ черезъ среднюю теплоемкость тѣла между
Ѳ° и Г°, черезъ с® среднюю теплоемкость воды между и Ѳ°, че-
резъ е19 с2, с8 теплоемкости калориметрическаго сосуда, мѣшалки и термо-
метра, черезъ с' теплоемкость корзиночки или сосудика, въ которомъ на-
ходится испытуемое тѣло, если оно порошкообразное или жидкое; если
гѣло твердое, то особой для него оболочки не требуется и слѣд. с' = О.
Далѣе обозначимъ черезъ д то количество тепла, которое потерялъ кало-
риметръ отъ момента, когда была опредѣлена температура / воды до мо-
мента, когда былъ сдѣланъ отсчетъ температуры Ѳ, вслѣдствіе неодина-
ковости температуръ самого калориметра и окружающаго воздуха. Иногда
Т <^і и Ѳ < і; тогда д можетъ быть и величиною отрицательною;
иногда получается д < 0, хотя Г > А но зато і много меньше температуры
воздуха. Приравнивая количества тепла, потерянное тѣломъ и пріобрѣ-
тенное калориметромъ, получаемъ равенство
(^+И(7'-Ѳ) = (^Ѳ + с1 + ^+с3)(Ѳ - /) + <7 • • • (11)
Оставляя пока вопросъ о способахъ опредѣленія нѣкоторыхъ вели-
чинъ, входящихъ въ это равенство, въ особенности важнѣйшей величины д9
разсмотримъ устройство нѣкоторыхъ калориметровъ. На рис. 69 изобра-
женъ приборъ К е п а и И, состоящій изъ калориметра О и аппарата
для предварительнаго нагрѣванія испытуемаго тѣла до температуры Т.
Калориметръ О состоитъ изъ латуннаго сосуда, который въ приборѣ В е -
^паиіі повѣшенъ на шнуркахъ между тремя столбиками. Въ насто-
ящее время пользуются калориметрами, состоящими изъ нѣсколькихъ
вставленныхъ одинъ въ другой латунныхъ сосудовъ, между которыми оста-
ется слой воздуха. На рис. 70 изображено внутреннее устройство такого
калориметра; сосуды отдѣлены другъ отъ друга треугольными кусками
174
Теплоемкость.
дерева или пробки. Иногда калориметръ вставляется еще въ двустѣнный
сосудъ, причемъ промежутокъ между стѣнками послѣдняго заполненъ водою.
Калориметръ О (рис. 69) отдѣленъ отъ остальной части прибора
стѣнкою Н, опущенною внизъ. Напрѣваніе тѣла происходитъ въ парахъ
воды, кипящей въ перегонномъ кубѣ 5, изъ котораго пары по трубкѣ е
проходятъ въ нагрѣвательный аппаратъ; затѣмъ они по трубкѣ а входятъ
въ сосудъ съ водою. Нагрѣвательный аппаратъ изображенъ на отдѣль-
Рис. 70.
Рис. 69.
номъ рисункѣ. Испытуемое тѣло с помѣщается на шнуркахъ въ среднемъ
вертикальномъ каналѣ прибора, въ особой оболочкѣ или безъ таковой,
смотря по роду тѣла, какъ было сказано выше. Иногда температура 7
тѣла опредѣляется особымъ термометромъ; но ее можно также опредѣ-
лить по таблицамъ температуры кипѣнія воды, зная барометрическое да-
вленіе. Пары воды заполняютъ пространство рр, отдѣленное отъ внѣш-
ней оболочки АА слоемъ вещества, дурно проводящаго теплоту. Когда
нагрѣваніе испытуемаго тѣла можно считать оконченнымъ, поднимаютъ
стѣнку А, пододвигаютъ калориметръ подъ нагрѣвательный аппаратъ, вы-
нимаютъ задвижку гк, даютъ тѣлу упасть въ калориметръ, который бы-
стро вновь отодвигаютъ въ сторону, спускаютъ стѣнку А, приводятъ въ
движеніе мѣшалку ^она на рис. 69 не изображена) и слѣдятъ за темпера-
турою по термометру і погруженному въ воду калориметра.
Описанный приборъ подвергся многимъ измѣненіямъ. Такъ напр.
помѣщаютъ калориметръ на особыхъ салазкахъ или рельсахъ, чтобы удоб-
, Способъ смѣшенія.
175
нѣе было передвигать его въ ту и другую сторону. Снаружи онъ дол-
женъ быть тщательно отполированъ, чтобы уменьшить потерю тепла лу-
чеиспусканіемъ ; полезно позолотить его внѣшнюю поверхность.
Приборъ К е п а и 1 і (рис. 69) даетъ возможность нагрѣвать тѣло
только до нѣкоторой температуры Г. близкой къ 100°. Для опредѣленія
средней теплоемкости тѣлъ въ другихъ» температурныхъ предѣлахъ, К е -
папИ построилъ приборъ, изображенный на рис. 71. Испытуемое тѣло К
помѣщается внутри наклонной трубки АВ, окруженной водою или охла-
Рис. 71.
ждающеи смѣсью; рдтп мѣшалка, V калориметръ. Открывъ пробку В и
отпустивъ шнурокъ, который виденъ съ» правой стороны, мы заставимъ
тѣло К упасть въ калориметръ. Первоначальная температура тѣла опре-
дѣляется термометромъ Т.
В. Ф. Л у г и н и н ъ построилъ нѣсколько весьма удобныхъ» прибо-
ровъ. Одинъ изъ нихъ отличается тѣмъ, что въ немъ передвигается не
калориметръ, а нагрѣватель. Дальнѣйшее его видоизмѣненіе, описанное
въ 1896 г., изображено на рис. 72. Этотъ приборъ спеціально предна-
значенъ для опредѣленія теплоемкости жидкостей между температурой,
близкой къ ихъ точкѣ кипѣнія, и температурой комнатной. Нагрѣваніе
происходитъ въ парахъ различныхъ жидкостей, соотвѣтственно подобран-
ныхъ. Калориметръ А (около 200 куб. см.) установленъ неподвижно на
эбонитовомъ треугольникѣ внутри двустѣннаго сосуда С, наполненнаго
водою. О деревянный брусокъ, установленный на винтовыхъ ножкахъ.
Мѣшалка состоитъ изъ горизонтальной пластинки, имѣющей форму от-
крытаго кольца: она снабжена отверстіями и стержнемъ, въ который
вставленъ» кусокъ слоновой кости е. Около / этотъ стержень легко скрѣп-
ляется съ шатуномъ» я, приводимымъ въ движеніе^ эксцентрикомъ /; не-
большой электромагнитный двигатель вращаетъ верхнее1 колесо. Внутри
176
Теплоемкость.
калориметра находится корзиночка изъ металлической сѣтки; въ нее па-
даетъ испытуемое тѣло, которое такимъ образомъ остается въ центрѣ ка-
лориметра и не мѣшаетъ движенію мѣшалки. Теплоемкость этой сѣтки
должна быть прибавлена къ многочлену въ скобкахъ съ правой стороны
равенства (11). Подвижной нагрѣватель установленъ на четырехъ коле-
сахъ, катящихся по рельсамъ; стержни также снабжены колесиками.
На круглое отверстіе платформы ѴѴ помѣщенъ сосудъ К съ жидкостью,
Рис. 72.
которая подогрѣвается двойною кольцевидною газовою горѣлкою. Пары
проходятъ по трубкѣ Е въ пространство, окружающее средній каналъ на-
грѣвателя Е и затѣмъ черезъ О къ холодильнику У, откуда жидкость
стекаетъ обратно въ черезъ холодильникъ непревывно протекаетъ
сгруя воды. Жидкость, образующаяся особенно въ началѣ опыта въ Е,
стекаетъ по трубкѣ М ко дну сосуда К. Трубка Е и сосудъ Е окру-
жены войлокомъ и снаружи никкелированной латунью. Стержни о и рр
придаютъ всей системѣ большую устойчивость. Свинцовый грузъ 5 слу-
житъ противовѣсомъ.
Испытуемое тѣло помѣщается въ средній каналъ нагрѣвателя, за-
крытый сверху и снизу. Нижній конецъ автоматически и моментально
открывается на малую часть секунды раньше паденія тѣла, которое по-
мѣщается внутри ложковидныхъ щипцовъ, соединенныхъ со стержнемъ,
выступающимъ наружу черезъ верхнее дно средняго канала. Если на-
Способъ смѣшенія
177
давить на верхній конецъ (кнопку) этого стержня, то щипцы открыва-
ются (въ такомъ положеніи они показаны на рисункѣ) и тѣло выпада-
етъ; одновременно открывается заслонка, закрывающая нижнее дно.
Твердыя тѣла помѣщаются непосредственно между щипцами; жид-
кости помѣщаются въ яйцевидныхъ стеклянныхъ или серебрянныхъ обо-
лочкахъ. Температура, до которой нагрѣваются тѣла, опредѣляется осо-
бымъ термометромъ, показаннымъ на рисункѣ. Въ 1901 г. Лугининъ
ввелъ новыя усовершенствованія въ своемъ приборѣ.
Рис. 73.
На рис. 73 изображенъ нагрѣватель Кеитапп’а, которымъ поль-
зовался въ своихъ работахъ Р а р е. Онъ состоитъ изъ двустѣннаго ко-
нусовиднаго сосуда аааа, въ которомъ сдѣланы круглый вырѣзъ тт внизу
и четыре внутреннія отверстія ШШі. Другой конусовидный сосудъ ЬЬЬ
помѣщенъ внутри перваго; въ него впаянъ котелокъ сс\ онъ вращается
около оси и также имѣетъ четыре отверстія А, которыя приходятся
противъ отверстій внѣшняго сосуда при томъ его положеніи, которое изо-
бражено на рисункѣ. Черезъ ось проходитъ термометръ //. Пары прохо-
дятъ черезъ трубу § въ сосудъ ЬЬЬ; черезъ отверстія й они переходятъ
въ наружный сосудъ а и затѣмъ выходятъ черезъ трубу к. Испытуе-
мое тѣло помѣщается въ котелкѣ сс. Когда оно достигло постоянной тем-
пературы Г, поворачиваютъ внутреннюю часть ЬЬЬ на 180°, вслѣдствіе
чего тѣло выпадаетъ изъ котекла сс черезъ вырѣзъ тт въ калориметръ,
пододвинутый подъ нагрѣватель.
Простой нагрѣватель и калориметръ для веществъ, имѣющихся въ
небольшомъ количествѣ, построилъ К о р р.
Н. А. Гезехусъ предложилъ въ 1889 г. новый калориметрическій
принципъ, построивъ воздушный калориметръ. Принципъ устройства этого
прибора слѣдующій : калориметръ, содержащій нѣкоторое количество воды,
вставленъ въ резервуаръ воздушнаго термометра, снабженнаго маноме-
тромъ. Нагрѣтое до Г° тѣло погружаютъ въ воду калориметра, темпе-
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. III, изд. 3-е. 12
178
Теплоемкость.
ратура котораго /°, и прибавляютъ тотчасъ столько холодной воды, чтобы
температура смѣси осталась равною что и обнаруживается неизмѣн-
ностью показаній манометра. Если р вѣсъ, г температура и с теплоем-
кость (при /°) прибавленной воды, то теплоемкость х тѣла получится изъ
равенства
х (Т — = рс (і — т).
Вѣсъ воды калориметра и теплоемкости его различныхъ частей вовсе
знать не нужно. Приборъ Н. А. Гезехуса изображенъ на рис. 74.
Рис. 74.
ЛѴаіегтап усовершенствовалъ
методъ Н. А. Гезехуса. Маре-
нинъ (1908) измѣрялъ при помощи
этого калориметра теплоемкость нѣко-
торыхъ сплавовъ. В. Преображен-
скій построилъ дифференціальный воз-
душный калориметръ.
Термометръ удобно употре-
блять съ перемѣннымъ количествомъ
ртути въ нижнемъ резервуарѣ, постро-
енный по принципу ЛѴаИегйіп’а и
В е с к т а п п’а (стр. 45). Весьма важ-
ное усовершенствованіе ввели й а е § е г
и біеіплѵеііг (1903). Они показали,
что точность калориметрическихъ из-
слѣдованій значительно увеличивается,
если измѣрять температуру калориметра
при помощи платиноваго термометра, а
его теплоемкость тѣмъ электрическимъ
способомъ, который будетъ разсмотрѣнъ ниже.
Вегіііеіоі предложилъ употреблять винтообразную мѣшалку ,
которую не приходится поднимать и опускать, но лишь вращать около
вертикальной оси.
Нетпві и ЫпЛешапп (1910) построили калориметръ для из-
мѣренія с при низкихъ температурахъ. Онъ состоитъ изъ мѣднаго, тол-
стостѣннаго, продолговатаго сосуда (вѣсъ 500 гр.), помѣщеннаго въ пу-
стотѣ. Температура измѣряется термоэлементами, спаи которыхъ нахо-
дятся внутри стѣнки. Мѣшалки въ этомъ приборѣ ненужно. Этотъ при-
боръ даетъ среднія значенія с между двумя температурами.
Для опредѣленія с при заданной, низкой температурѣ ^гпві (1910)
построилъ рядъ приборовъ, въ которыхъ испытуемое вещество нагрѣва-
ется отъ заданной температуры, примѣрно, на 1° при помощи электриче-
скаго тока. Количества тепла опредѣляется сопротивленіемъ проволоки
и приложенной электродвижущей силой (т. IV).
До сихъ поръ мы предполагали всегда, что жидкостью въ калори-
Способъ смѣшенія.
179
метрѣ является вода, Бедѵаг (1904) построилъ калориметръ, въ кото-
ромъ вода замѣнялась твердой углекислотой (—78°), жидкимъ
воздухомъ (—188°) и жидкимъ водородомъ (—252,5°). Тепло-
емкости вводившихся въ калориметръ тѣлъ опредѣлялись по объемамъ
образовывавшагося газа и по теплотѣ испаренія употреблявшихся при
измѣреніяхъ веществъ.
Прежде пытались также замѣнять воду иными жидкостями, напр.
толуоломъ, ртутью ит. д.
Для опредѣленія величинъ г1? с2 и с' въ уравненіи (11) можно поль-
зоваться таблицами, въ которыхъ указаны теплоемкости веществъ, изъ
которыхъ сдѣланы калориметръ, мѣшалка и оболочка ; вѣсъ отдѣльныхъ
частей долженъ быть извѣстенъ. Большой точности при опредѣленіи ст
и с2 не требуется. Теплоемкость с3 термометра можно опредѣлить непо-
средственно, погружая его нагрѣтымъ въ особый маленькій калориметръ.
Можно также вычислить с3 по формулѣ с3 = 0,46г/, гдѣ ѵ объемъ части
термометра, погруженной въ калориметръ. Эта формула основана на томъ,
что случайно единицы объема ртути и стекла обладаютъ почти одина-
ковой теплоемкостью, близкой къ 0,46. Объемъ ѵ опредѣляется по уве-
личенію вѣса стаканчика съ водой, поставленнаго на чашку вѣсовъ,
когда въ воду погружается часть ѵ термометра.
Вѣсъ р воды въ калориметрѣ полезно опредѣлять послѣ опыта (взвѣ-
шивая его вмѣстѣ съ тѣломъ, вѣсъ котораго извѣстенъ), такъ какъ при
паденіи тѣла въ воду трудно избѣжать нѣкоторой потери воды вслѣдствіе
ея разбрызгиванія.
Обращаемся къ вопросу объ опредѣленіи величины д — тепла, по-
теряннаго калориметромъ, см. ур. (11) стр. 173. Замѣтимъ, что темпера-
тура калориметра, мѣняющаяся отъ і до Ѳ, не должна отличаться отъ
температуры г окружающаго воздуха болѣе, чѣмъ на 5°, и только въ
случаѣ, когда калориметръ содержитъ много воды (500—1000 гр.), можно
допустить нѣсколько большую разность температуръ.
В и ш 1 о г д. предложилъ пользоваться слѣдующимъ способомъ для
уменьшенія потери тепла д. Положимъ, что предварительные опыты или
приближенный подсчетъ дали для ожидаемаго нагрѣванія Ѳ — і нѣкоторую
г 1
величину??. Тогда охлаждаютъ калориметръ до температуры —-- г/,
такъ чтобы его окончательная температура сдѣлалась равною Ѳ = т -|- ??,
т.-е. чтобы въ началѣ опыта калориметръ былъ бы настолько же холод-
нѣе окружающаго воздуха, насколько онъ въ концѣ опыта дѣлается теплѣе
его. Сперва онъ будетъ получать, а потомъ отдавать теплоту. Однако,
эти два количества тепла не равны между собою, и д поэтому не будетъ
равно нулю, такъ какъ нагрѣваніе калориметра идетъ сначала весьма
быстро, а затѣмъ уже гораздо медленнѣе. Отдача тепла воздуху будетъ
гораздо продолжительнѣе, чѣмъ полученіе теплоты изъ него, и потому
12*
180
Теплоемкость.
окажется д > 0. Гораздо лучше брать і = г - такъ чтобы окон-
П I 1
нательная температура калориметра равнялась У = т + г/.
О
И этотъ способъ не можетъ, однако, дать надежныхъ результатовъ,
тѣмъ болѣе, что понятіе о температурѣ Ѳ смѣси представляется на прак-
тикѣ мало яснымъ и опредѣленнымъ. Дѣло въ томъ, что когда мы вво-
димъ нагрѣтое тѣло въ калориметръ, вода котораго имѣетъ начальную
температуру то термометръ, опущенный въ эту воду, вообще говоря,
сперва быстро поднимается,
достигаетъ нѣкоторой наи-
высшей температуры и за-
тѣмъ начинаетъ падать. Это
паденіе, сперва неправиль-
ное, дѣлается съ нѣкото-
раго момента равномѣр-
нымъ. Имѣя дѣло съ не-
прерывно мѣняющейся тем-
пературой, мы находимся въ
затрудненіи относительно
выбора величины Ѳ въ урав-
неніи (11) стр. 173. Поступаемъ слѣдующимъ образомъ. Обозначимъ те-
перь черезъ Ѳ ту температуру, до которой нагрѣлся бы калориметръ, если
бы онъ былъ окруженъ абсолютными непроводниками тепла, т.-е. во
время опыта вовсе не терялъ бы теплоты черезъ лучеиспусканіе (# = 0).
Въ такомъ случаѣ ур. (11) принимаетъ видъ
(4 + сЭ(7’-Ѳ) = (^?-Ьс14-с2Н-с3)(Ѳ-0. • • (12)
и весь вопросъ сводится къ опредѣленію температуры Ѳ. Для разъясне-
нія вопроса обратимся къ рис. 75, заимствованному изъ учебника Миеі-
1ег-Роиі11еі-Ріаип(11ег’а. Положимъ, что ординаты кривой О ВС
<д)сь абсциссъ гдѣ-нибудь ниже ОА\ представляютъ тѣ значенія темпера-
туры калориметра, какъ функціи времени, которыя наблюдались бы при
отсутствіи всякой потери тепла лучеиспусканіемъ. Кривая сперва под-
нимается и, начиная отъ нѣкоторой точки В, дѣлается параллельной оси
абсциссъ. Ординаты точекъ прямой ВС, очевидно, и представляютъ ис-
комую температуру Ѳ. Кривая ООЕЕ выражаетъ наблюденный ходъ
температуръ; точка Е съ максимальной ординатой соотвѣтствуетъ мо-
менту, когда калориметръ получаетъ столько же теплоты отъ погружен-
наго въ него тѣла, сколько онъ теряетъ лучеиспусканіемъ. Начиная отъ
этого момента, потеря превышаетъ притокъ, и начиная отъ точки Е, по-
лучается часть кривой ЕЕ, которую можно принять за прямую; здѣсь
притокъ тепла нуль и калориметръ вмѣстѣ съ тѣломъ правильно охлаж-
дается. Изъ рисунка ясно, что максимальная наблюденная температура
(ордината точки 29) никоимъ образомъ не можетъ служить для опредѣле-
Способъ смѣшенія.
181
нія величины Ѳ, ординаты точки В. Обозначимъ черезъ Ѳп ординату
точки Е, т.-е. наблюденную температуру, начальную въ ряду темпера-
туръ, убывающихъ равномѣрно; пусть далѣе ВЕ = Л убыль температуры
калориметра вслѣдствіе лучеиспусканія и испаренія отъ момента по-
груженія въ него тѣла до момента отсчета температуры Ѳл. Очевидно
мы имѣемъ
Ѳ = Ѳп + Л.........................(13)
и весь вопросъ сводится къ опредѣленію величины Л. Разсмотримъ два
способа опредѣленія Л.
Способъ I требуетъ наблюденія температуры г окружающаго воз-
духа. Назовемъ время ОН первымъ періодомъ, время послѣ Н вторымъ
періодомъ. Наблюдаемъ показанія термометра, начиная отъ момента по-
груженія нагрѣтаго тѣла, черезъ равные промежутки времени, напр., че-
резъ каждыя 10, 20, 30 или 60 сек., смотря по обстоятельствамъ; назо-
вемъ такой промежутокъ времени интерваломъ и. Температуры, наблю-
денныя въ первомъ періодѣ, обозначимъ черезъ Ѳо, Ѳ1? Ѳ2, . . . , і, ѲЛ,
такъ что Ѳо = і равно температурѣ калориметра въ моментъ погруженія
тѣла, а Ѳп есть ордината точки Е. Температуры во второмъ періодѣ обо-
значимъ черезъ $0, — ь очевидно, = Ѳп и, по условію,
#о — = Л — ^2 - • • • = ^т— 1 -- = V,
гдѣ ц наблюденное пониженіе, температуры втеченіе равныхъ временъ о.
Обозначимъ, далѣе, черезъ г2, . . . , гп наблюденныя темпера-
туры окружающаго воздуха въ моменты, лежащіе посреди интерваловъ о
перваго періода, черезъ г среднюю температуру воздуха въ теченіе вто-
рого періода и, наконецъ, черезъ $ среднюю изъ величинъ до &т.
Такъ какъ во второмъ періодѣ избытокъ температуры калориметра
надъ температурою воздуха, равный $ — г, вызвалъ во время о пониже-
ніе температуры калориметра у, то мы заключаемъ, что избытокъ въ 1°
вызоветъ во время а пониженіе
$ — г ’
а избытокъ въ х° пониженіе, равное дх. Величины
Ѳо + ©і ©і -(- Ѳ2 Ѳ2 Ѳ3 "Ь
2 —2-------~2--------------гз--.------2-------<14)
представляютъ средніе избытки за интервалы а перваго періода; умно-
жая эти разности на р, мы получимъ потери температуры калориметра
въ отдѣльные интервалы о, а взявъ сумму этихъ потерь, мы найдемъ ис-
комую величину 4, входящую въ (13) и равную полной потерѣ темпера-
туры калориметра за первый періодъ. Итакъ мы имѣемъ
/Ѳ0+Ѳх ©, + ©2 ѳ„_1 + ѳп \ ц
л = 2------Н--------2-----*2 + - • • +-----2-------• • •
182
Теплоемкость.
Вставляя это въ (13), находимъ Ѳ, входящее въ уравненіе (12).
Приведемъ примѣръ, данный Ріаипйіег’омъ. Въ немъ і = 10°,00;
/г = 10, т = 5; о = 1 мин. Наблюденія и выводы помѣщены въ слѣд.
таблицѣ:
Отсчеты на тер- Среднія тем- Средняя Вычислен.
Время. мометрѣ кало- пературы въ температура „Избытки". потеря тем-
риметра. интервалы а. воздуха. пературы.
0 Ѳо = / = 10,00 10,90 Ті =12,05 — 1,15 — 0,023
А ч: 1 = 11,80 12,25 т2 = 12,05 4-0,20 + 0,040
2 Ѳ2 = 12,70 13,05 т3 = 12,05 1,00 0,020
.2 *р, 3 Ѳ3 = 13,40 13,65 ч =12,05 1,60 0,032
ф с 4 Ѳ4 = 13,90 14,08 т5 =12,05 2,03 0,041
5 Ѳ5 = 14,25 14,38 тб = 12,05 2,38 0,047
3 и 6 Ѳ6 = 14,50 14,55 т7 =12,05 2,50 0,050
л ф 7 Ѳ7 = 14,60 14,63 т8 = 12,03 2,60 0,052
1—1 8 Ѳ8 = 14,65 14,62 =12,02 2,60 0,052
9 Ѳ9 = 14,63 14,62 т10 = 12,02 2,60 0,052
1 10 Ѳ10 = #о = 14,6О А = 0,396
•2 11 12 13 #2 = 14,55 #2 = 14,50 > #3 = 14,45 # = 14,50 т = 12,00 # — т = 2,50
ф । р П = 0,05 е _ _ о ,02.
сч 1 1 14 #4 = 14,40
Во второмъ періодѣ пониженіе въ одну минуту равно 0°,05, при
среднемъ избыткѣ # — т = 2°,50 ; отсюда пониженіе р при избыткѣ въ
1° равно р = 0°,02. Помножая «избытки», т.-е. величины (14), помѣщен-
ныя въ пятомъ столбцѣ, на р, получаемъ числа послѣдняго столбца, т.-е.
потери температуръ втеченіе десяти интерваловъ перваго періода. Ихъ
сумма и есть искомое Д = 0°,396. Въ нашемъ случаѣ Ѳп = Ѳ1о = 14°60,
слѣд. искомое Ѳ = 14°60 + 0°,396 = 15°,00.
Способъ П принадлежитъ В е §• п а и И; опубликовалъ его
впервые Наипйіег. Этотъ способъ, наиболѣе точный, имѣетъ еще то
преимущество, что вовсе не требуетъ наблюденія температуры окружаю-
щаго воздуха. Температура калориметра должна наблюдаться еще вте-
ченіе нѣкотораго числа к интерваловъ времени и до погруженія въ него
нагрѣтаго тѣла, такъ что всего получаются три періода, состоящія изъ
к + п -|~ т равныхъ интерваловъ времени о. Температуры, наблюден-
ныя въ первый періодъ, обозначимъ черезъ ^0, 4 . . . і; послѣдняя
температура перваго періода = і = Ѳо не можетъ быть наблюдаема и
получается вычисленіемъ. Температуры и въ первомъ и въ треть-
емъ періодахъ составляютъ ариѳметическія прогрессіи и пусть теперь
/о --- —- ^2 — --- ^3 — •
. . _ ^0 — 4—1
— 4—2 “ 4—1 — |
= #3 = --- = 'Ѵ-1 =
Способъ смѣшенія.
183
Температура I воды въ моментъ погруженія нагрѣтаго тѣла вычи-
сляется по формулѣ
= = = • • • (15)
Пусть теперь і' средняя изъ величинъ /0, . І&—ь и
средняя изъ величинъ $0, $х, $2 . . . ,
Измѣненію температуры отъ і' до соотвѣтствуетъ измѣненіе въ по-
терѣ температуры во время одного интервала о, равное разности вели-
чинъ и ^2. Отсюда слѣдуетъ, что если температура калориметра из-
мѣнится на 1°, то потеря температуры за время о измѣнится на величину
_ Ѵ2 — Ѵі
~ »' — I'
(16)
Если въ какой-либо интервалъ б температура калориметра равня-
лась напр. г°, т.-е. превышала среднюю температуру і' на г — I' граду-
совъ, то потеря температуры во время о должна была превышать по-
терю при температурѣ і' на величину (г — і') д, т.-е. потеря равна
= + . • • (17)
Формулою (17) воспользуемся, чтобы вычислить потери темпера-
туры въ различные интервалы второго періода, во время которыхъ тем-
пературы равнялись
Ѳо+Ѳі ®1 + ®2 ®2 + +
—2~’ —2—> —!—’•••’ ---------------2---- • • • Г18)
гдѣ Ѳо = = Л Вставляя эти выраженія въ (17) вмѣсто г, получаемъ
потери температуръ, сумма которыхъ и составитъ искомую величину 3
въ (13). Такимъ образомъ легко получается
/1 = (Ѳі -Н «2 + в3 -ь ... + 4----_4-^.(і9)
Эта формула иногда называется формулою Ее^паиІі-РТаипсІІег’а.
Приведемъ примѣръ вычисленія величины 3. Первый періодъ со-
стоялъ изъ десяти интерваловъ а; втеченіе первыхъ девяти температура
правильно возрастала отъ 14°,645 до 14°,660; отсюда
14,645 — 14,660
= —- 9
= — 0°,0017,
(15) даетъ
I = е0 == 14,660 4- 0,0017 = 14,662.
184
Теплоемкость.
Во второмъ періодѣ наблюдались температуры (первая только-что
нами вычислена)
Ѳо = 14,662 ©1 = 15,08 Ѳ2=17,92 Ѳ3 = 18,06 ©4 = 18,065 ©6 = 18,065.
Затѣмъ начался третій періодъ и температура пала втеченіе шести
интерваловъ отъ #0 = ©б = 18,065 до $в = 18,02. Отсюда получаемъ
18,065 — 18,02 .
% =------2---------= + 0°,0075.
О
Среднія температуры перваго и третьяго интерваловъ суть
і' = 14,°65 = 18,°04.
Вставляя найденныя величины и п = 5 въ (19) получаемъ
А — (15,08 -|- 17,92 + 18,06 -|- 18,065 18?06^.^~ 14,662 —
или Л = 0,0245. Наконецъ (13) даетъ
Ѳ = 18,065 + 0,0245 = 18,0895.
Ріаипсііег совѣтуетъ охлаждать калориметръ до опыта настолько,
чтобы температура поднималась во всѣхъ трехъ періодахъ. Вопро-
сомъ объ охлажденіи калориметра занимались въ послѣднее время Ноі-
Ъеіп и, въ особенности, АѴасіблѵоіЧІі (1897).
Несомнѣнно, что погрѣшности, зависящія отъ потери тепла калори-
метромъ ни въ какомъ случаѣ не могутъ быть вполнѣ точно исключены.
Ноішап (1895) сдѣлалъ попытку совершенно исключить по-
терю тепла калориметромъ; съ этой цѣлью онъ предложилъ
окружать калориметръ оболочкой, въ которой одновременно возбуждалось
тоже нагрѣваніе, которое имѣлось въ калориметрѣ. Однако Ноішап
никакихъ опытовъ не сдѣлалъ. Независимо отъ Н о 1 т а п’а практиче-
ски воспользовались этой идеей В і с й а г (1 8 и Ь а га Ь (1905), а
Вісйагйв, Непдегбоп и Р о г Ъ е 8 еще ее улучшили и примѣнили
при многочисленныхъ калориметрическихъ измѣреніяхъ. Нагрѣваніе обо-
лочки можетъ производиться различными способами, напр. приливаніемъ
горячей воды. Лучшимъ оказывается химическій методъ: кало-
риметръ окружается натріевымъ растворомъ, въ который вводится такое
количество сѣрной кислоты, чтобы жидкость нагрѣлась настолько-же,
какъ и вода въ калориметрѣ. Произведенные опыты показали, что та-
кимъ способомъ получаются вполнѣ постоянные результаты.
Биронъ (1909) показалъ, какъ слѣдуетъ видоизмѣнить формулу (19)
для случая калориметра весьма малыхъ размѣровъ.
Способъ охлажденія.
185
Магі^пае предложилъ видоизмѣненіе способа смѣшенія для
жидкосте й; этимъ способомъ пользовался напр. Р е г г о і.
§ 7. Способъ охлажденія. Формула, опредѣляющая температуру
охлаждающагося тѣла, какъ функцію времени, будетъ выведена ниже.
Но мы уже теперь можемъ воспользоваться этою формулою, тѣмъ болѣе,
что результатъ, къ которому она насъ приведетъ, представляется а ргіогі
довольно вѣроятнымъ и нагляднымъ. Помѣстимъ тѣло, поверхность ко-
тораго 5, температура въ пространство, температура котораго г, и бу-
демъ считать время г, начиная отъ этого момента. Пусть далѣе с те-
плоемкость тѣла и И испускательная способность его поверхности, из-
мѣряемая количествомъ тепла, которое съ единицы поверхности излуча-
ется въ единицу времени, когда разность температуръ тѣла и окружаю-
щаго пространства равна 1°. Спустя время г послѣ начала охлажденія
тѣла, его температура будетъ равна
з/г
і = г -|- (і^ — т) е с 2...................(20)
гдѣ е основаніе натуральныхъ логариѳмовъ. Формула (20) даетъ і =
при х — 0, и і = т при 2 = <х>. Для другого тѣла получимъ то же са-
мое пониженіе температуры отъ до і въ другое время опредѣля-
емое формулою
і = т -|- (/0 — т) е еі \
гдѣ и е2 поверхность, испускательная способность и теплоемкость
второго тѣла. Изъ послѣднихъ двухъ формулъ получается
8І12
с
8уІІу2у
С 8І12
откуда - = .
Если поверхности обоихъ тѣлъ одинаковы по размѣрамъ и физиче-
скимъ свойствамъ, то И = 5 = и тогда получается
с ____ 2
Сі ~ ’
т.-е. теплоемкости тѣлъ пропорціональны временамъ, потребнымъ для
одинаковаго охлажденія тѣлъ отъ /0 до і; этотъ результатъ и а ргіогі пред-
ставляется понятнымъ, такъ какъ при одинаковыхъ и і теплоемкости
с и Су пропорціональны количествамъ теплоты д и которыя тѣла
должны потерять лучеиспусканіемъ.
Чтобы сдѣлать 5 = и А = А3 приходится оба тѣла помѣщать одно
послѣ другого внутри одного и того же тонкостѣннаго металлическаго
или стекляннаго сосудика, и въ немъ наблюдать охлажденіе. Если у те-
плоемкость сосудика, то вмѣсто с должно въ (20) стоять с у, вмѣсто Су
получимъ + У, такъ что послѣднее уравненіе принимаетъ видъ
с -I- У = 2
откуда Сі - с + — 7
(21)
186
Теплоемкость.
Если второе тѣло однородное, то получимъ теплоемкость вещества,
раздѣливъ сі на вѣсъ тѣла.
Методъ охлажденія былъ предложенъ въ 1796 г. ТоЬіав Мау-
ет’омъ; имъ пользовались О и 1 о п $ и Реііі, Беіагіѵе и М а г -
сеѣ и, въ особенности, Ве^паиіі. Приборъ Ке^паиіѣ изображенъ
на рис. 76. Испытуемое тѣло наполняетъ (въ видѣ порошка)
Рис. 76. золоченый серебряный цилиндръ ф, внутри котораго нахо-
дится резервуаръ термометра. Цилиндръ ѵ помѣщается въ
металлическомъ, вычерненномъ внутри цилиндрѣ р, окру-
женномъ во время опыта тающимъ льдомъ или водою, имѣ-
ющею постоянную температуру. При помощи трубки г выкачи-
ваютъ нѣсколько разъ воздухъ изъ сосуда р, вновь наполняя его
каждый разъ сухимъ воздухомъ. Наконецъ еще разъ произво-
дятъ выкачиваніе, чтобы давленіе остающагося вполнѣ сухого
воздуха не превышало 1 мм. Весь приборъ помѣщается сперва
въ теплую воду; когда температура въ ^установится, вынима-
ютъ приборъ изъ воды, погружаютъ его въ болѣе холодную
среду, обыкновенно въ тающій ледъ, и наблюдаютъ пониженіе
температуры черезъ равные промежутки времени. Повторяя
тотъ же опытъ съ опредѣленнымъ вѣсовымъ количествомъ воды
‘въ г/, мы будемъ знать с, и слѣд. (21) даетъ намъ Для изслѣ-
дованія жидкостей можно, вмѣсто сосуда ѵ, пользоваться сте-
кляннымъ сосудомъ асі, отдѣльно изображеннымъ на рис. 76.
Въ болѣе простыхъ приборахъ воздухъ изъ цилиндра
р не выкачиваютъ, и до опыта погружаютъ весь приборъ въ
большой сосудъ съ тающимъ льдомъ, или проще съ водою при комнатной
температурѣ. Сосудъ ѵ съ испытуемымъ тѣломъ нагрѣваютъ отдѣльно
въ горячей водѣ, и затѣмъ, высушивъ, помѣщаютъ въ цилиндръ р.
Способъ охлажденія по разнымъ причинамъ не даетъ надежныхъ
результатовъ. Оказывается, что для порошкообразныхъ тѣлъ скорость
охлажденія зависитъ отъ ихъ плотности, т.-е. отъ способа насыпки (съ
вколачиваніемъ или безъ него). Далѣе термометръ показываетъ темпе-
ратуру центральныхъ частей испытуемаго вещества; если оно плохо
проводитъ теплоту, то эта температура можетъ значительно отличаться
отъ температуры поверхности, и тогда наши формулы уже перестаютъ быть
точнымц. Далѣе необходимо имѣть въ виду, что потеря тепла охлажда-
ющимся тѣломъ происходитъ не только лучеиспусканіемъ, но и пото-
ками воздуха, вызванными разностью температуръ между ѵ и р, т.-е. такъ
называемой конвекціей; кромѣ того, теплота и непосредственно пе-
редается черезъ воздухъ, обладающій нѣкоторою теплопроводностью. Кон-
векцію можно уменьшить, разрѣжая воздухъ, но теплопроводность его,
какъ мы увидимъ впослѣдствіи отъ разрѣженія не мѣняется. Н і г п
пользовался способомъ охлажденія для опредѣленія теплоемкостей жид-
костей при высокихъ температурахъ. Формула (20) непригодна, когда
разность температуръ тѣла и окружающаго пространства велика, и по-
Способъ конденсаціи паровъ.
187
тому онъ выражалъ температуру і охлаждающагося тѣла нѣкоторою
эмпирическою функціею времени г, основываясь на наблюденіяхъ; от-
сюда онъ опредѣлялъ скорость ѵ охлажденія по формулѣ ѵ = для раз-
личныхъ температуръ і. Если для другого вещества, помѣщеннаго въ
ту же оболочку, при той же температурѣ і скорость охлажденія равна
то мы имѣемъ (с + 7) -р у) гдѣ с, с± и у имѣютъ преж-
нее значеніе.
В е р а и 1 і построилъ приборъ подъ названіемъ термокалори-
метра, также служащій для опредѣленія теплоемкости тѣлъ по способу
охлажденія. Самъ Ее^паиіі не далъ подробнаго описанія его которое
можно найти въ «Сотъ йе рйувідие йатіп’а и Вонѣу, напр. въ
изд. 3-емъ т. II, стр. 29.
Интересное видоизмѣненіе способа охлажденія предложилъ Тере-
шинъ; оно примѣнимо къ металлическимъ проволокамъ. Горизонтально
натянутая проволока накаливается электрическимъ токомъ; грузикъ, при-
крѣпленный къ ея серединѣ, опускаясь, даетъ возможность опредѣлить
температуру проволоки. По скорости охлажденія проволоки, наблюдае-
маго послѣ размыканія тока, можно опредѣлить ея теплоемкость. Г-жи Сер-
добинская и Емельянова опредѣлили этимъ способомъ теплоем-
кость платины и золота.
§ 8. Способъ конденсаціи паровъ. Если тѣло, теплоемкость кото-
раго с и температура ввести въ пространство, наполненное насыщен-
ными парами какой-либо жидкости, температура которыхъ Т^> і, то
часть пара осядетъ на поверхности тѣла въ жидкомъ состояніи, пока
тѣло не нагрѣется до температуры Т. Если скрытую теплоту испаренія
обозначить черезъ Л и вѣсъ образовавшейся жидкости черезъ /?, то тѣло
получило рХ единицъ тепла, и слѣд.
с (Г— і) = рХ.....................(22)
Зная Г, і и Л, можно опредѣлить с, измѣряя увеличеніе р вѣса
тѣла при помѣщеніи его въ парахъ. На этомъ основаны паровые ка-
лориметры, одновременно предложенные йоіу и Випвеп’омъ. Зоіу
построилъ также дифференціальный паровой калориметръ, о которомъ бу-
детъ сказано ниже. Дальнѣйшія видоизмѣненія парового калориметра
принадлежатъ АѴігIя’у и Щукареву (въ Москвѣ); на нѣсколько
другомъ принципѣ основанъ приборъ К е е 8 е п’а.
Мы опишемъ паровой калориметръ Випзеп’а, изображенный на
рис. 77. Пары воды проходятъ изъ котла А черезъ сѣтку, задерживаю-
щую жидкія капельки, въ паровую камеру В; въ верхнюю часть камеры
вставленъ конусъ изъ пемзы съ каналомъ для выхода пара. Сбоку уста-
новлена труба г, соединенная съ вертикальной трубой, въ которой го-
ритъ большое газовое пламя. Происходящая вслѣдствіе этого тяга за-
ставляетъ пары, выходящіе изъ В, направляться въ трубу г, а не под-
ниматься наверхъ, что дѣйствовало бы вредно на находящіеся сверху
188
Теплоемкость.
вѣсы С. Испытуемое тѣло помѣщается въ цилиндръ изъ платиновой
сѣтки; нижняя часть этого цилиндра состоитъ изъ платиновой жести,
представляя чашечку, въ которой собирается жидкость, осѣвшая на по-
верхности тѣла. Тѣло привѣ-
Рис. 77. шивается на тонкой платиновой
ренія Л можно принять равною Л =
При опредѣленіи Р слѣдуетъ і
вѣсъ Ро опредѣлялся въ воздухѣ, а
торыхъ меньше плотности воздуха,
наго слѣдуетъ вычесть 0,000636г/
см. Опытъ производятъ сперва съ
проволокѣ къ чашкѣ чувстви-
тельныхъ вѣсовъ. Опредѣляютъ
его вѣсъ Ро и температуру і\
затѣмъ его быстро вводятъ въ
камеру В, уже наполненную на-
сыщенными парами. При по-
мощи гирьки И и крючечка о
придаютъ тѣлу и проволокѣ по-
ложеніе, обозначенное пункти-
ромъ; при этомъ проволока ка-
сается пемзы, всасывающей ка-
пельки воды, могущей осѣсть
на проволоку около верхняго
отверстія камеры В. Черезъ нѣ-
которое время снимаютъ гирьку
И и взвѣшиваютъ тѣло; это пов-
торяютъ нѣсколько разъ, пока
не получится постоянный вѣсъ Р;
тогда Р — Ро= р т.-е. равно
вѣсу жидкости, образовавшейся
на поверхности тѣла.
Температуру Т паровъ опре-
дѣляютъ по барометрическому
давленію; скрытую теплоту испа-
= 536,5 4- 0,7 (100 — Г).
шести поправку вслѣдствіе того, что
Р — въ парахъ воды, плотность ко-
Изъ вѣса непосредственно найден-
гр., гдѣ ѵ объемъ тѣла въ куб.
пустымъ платиновымъ цилиндрикомъ,
чтобы опредѣлить его теплоемкость, а потомъ уже съ цилиндрикомъ, со-
держащимъ испытуемое тѣло. Подробное описаніе паровыхъ калориме-
тровъ Л о 1 у, Вппвеп'а и АѴігія’а и способа ими пользоваться можно
найти въ лекціяхъ (литографированныхъ) В. Ф. Лугинина, Москва,
1893. Щукаревъ значительно упростилъ калориметръ Л о 1 у.
§ 9. Различные способы опредѣленія теплоемкостей. Разсмотримъ
еще нѣкоторые методы опредѣленія теплоемкостей, изрѣдка употребляв-
шіеся и представляющіе нѣкоторый интересъ.
I. Способъ электрическаго тока. Если черезъ прово-
локу, сопротивленіе которой те/ омовъ, пропустить токъ въ і амперовъ,
Различные способы
189
то втеченіе одной сек. въ ней выдѣлятся джулей тепля, гдѣ джуль
эквивалентенъ ІО7 эргамъ. Принимая теплоемкость воды при 15° равною
единицѣ, имѣемъ по ВолѵІапсГу, что джуль = 0,2387 мал. калоріи. Ко-
личество д тепла, выдѣляющагося въ проволокѣ, равно слѣд.
д = 0,2387/2,г2/ мал. кал.
Вмѣсто этой формулы можно написать
д = мал. кал.,
гдѣ е разность потенціаловъ у концовъ проволоки, выраженная въ воль-
тахъ. Этимъ выдѣленіемъ тепла можно воспользоваться, чтобы опредѣ-
лить теплоемкость жидкостей. Въ сосудъ (калориметръ), содержащій
испытуемую жидкость, вводятъ спирально свернутую проволоку, пропу-
скаютъ черезъ нее токъ и наблюдаютъ повышеніе температуры жидкости.
За величинами і и необходимо слѣдить во время опыта, ибо мѣня-
ется во время опыта вслѣдствіе измѣненія температуры жидкости. Не-
обходимо принять во вниманіе, что теплота распредѣляется между жид-
костью (вѣсъ р, теплоемкость х), калориметромъ, мѣшалкою, термометромъ
и проволокою, и что во время опыта часть теплоты теряется лучеиспу-
сканіемъ. Если с сумма теплоемкостей названныхъ тѣлъ, кромѣ самой
жидкости, і начальная, Т окончательная исправленная температура, то
^ = (/?х + с)(7'—/),
гдѣ г продолжительность (въ секундахъ) дѣйствія тока. Это уравненіе
даетъ искомую теплоемкость х жидкости. Чтобы сравнить теплоемкости
двухъ жидкостей, изъ которыхъ одна можетъ быть вода, пропускаютъ
одинъ и тотъ же токъ послѣдовательно черезъ двѣ одинаковыя прово-
локи, помѣщенныя въ двухъ калориметрахъ, содержащихъ испытуемыя
жидкости. Для двухъ жидкостей имѣемъ
(рх с) (Т — Г) = 0,2387/2^
(Ріхі + сі) (^і — ^і) = 0,2387/^г,
откуда опредѣляется отношеніе х: х±. Начальныя температуры і и 4
могутъ быть и одинаковыя. Ріаипйіег воспользовался этимъ спосо-
бомъ для сравненія теплоемкостей различныхъ жидкостей съ теплоем-
костью воды. Впослѣдствіи онъ замѣнилъ проволоки стеклянными, спи-
рально свернутыми трубками, наполненными ртутью, чтобы избѣжать бо-
ковыхъ отвѣтвленій тока въ самой жидкости. Этимъ же способомъ поль-
зовались йатіп и йоііаппбоп (при изслѣдованіи теплоемкости воды
стр. 159) и бсіііатр (другихъ жидкостей).
К е г е а п о измѣрялъ время, втеченіе котораго различныя жид-
кости одинаково нагрѣваются.
II. Спос объ Апйтелѵв’а и Нігп’а. Теплоемкости двухъ жид-
костей могутъ быть сравнены наблюденіемъ повышеній ихъ температуръ,
190
Теплоемкость.
вызванныхъ однимъ и тѣмъ же количествомъ теплоты д. На этомъ ос-
нованъ способъ, предложенный еще въ 1845 г. Апйгелѵв’омъ; имъ
пользовался Нігп при своихъ опредѣленіяхъ теплоемкости воды(стр. 159).
Приборъ Нігп’а состоялъ изъ большого термометровиднаго сосуда, содер-
жащаго воду, заполняющую также часть трубки, на которой проведены
двѣ черты. Предварительно нагрѣваютъ сосудъ настолько, чтобы вода
въ трубкѣ стояла выше верхней черты. Затѣмъ даютъ ему охладиться;
въ моментъ, когда конецъ жидкаго столбика доходитъ до верхней черты,
погружаютъ сосудъ въ испытуемую жидкость, перемѣшиваютъ ее, выни-
маютъ сосудъ, когда конецъ столбика доходитъ до нижней черты и опре-
дѣляютъ повышеніе температуры испытуемой жидкости. Ріаипсііег
построилъ подобный же приборъ со ртутью. Магі^пас бралъ испыту-
емыя жидкости въ такихъ количествахъ, чтобы повышенія ихъ темпера-
туры были одинаковыя; этимъ онъ избавился отъ необходимости вво-
дить поправку на потерю теплоты лучеиспусканіемъ: всѣ жидкости
получали одинаковое количество теплоты д — д*.
ОитІісЬ. и ѴѴіеЬе (1898), а также Ріаилйіег (1899) усо-
вершенствовали этотъ методъ.
ПІ. Способъ Віаск’а и ТЬотвеп’а. Принципъ тотъ же,
какъ и въ предыдущемъ способѣ, но одинаковыя количества тепла полу-
чаются сжиганіемъ опредѣленнаго количества газа. ТЬош8еп напол-
нялъ калориметръ примѣрно литромъ жидкости и сжигалъ въ его центрѣ
одинаковое во всѣхъ опытахъ количество водорода. Такъ какъ при этомъ
нагрѣваніе происходитъ равномѣрно, то Тіютвеп могъ совершенно
исключить потерю тепла лучеиспусканіемъ, пользуясь способомъ К и ш -
Іо гд’а (стр. 179).
Коноваловъ пользовался, какъ источникомъ тепла, смѣсью сѣр-
ной кислоты и воды, а Биронъ тщательно разработалъ этотъ методъ.
§ 10. Теплоемкость твердыхъ и жидкихъ веществъ, Существуетъ
весьма большое число изслѣдованій теплоемкостей различныхъ твердыхъ
и жидкихъ веществъ. Результаты этихъ изслѣдованій, а также указаніе
обширной литературы можно найти въ таблицахъ БапсіоІѴа и Воегп-
віеіп’а. Здѣсь мы разсмотримъ немногіе изъ результатовъ, добытыхъ
различными учеными, оставляя пока въ сторонѣ все отно-
сящееся къ вопросу о связи между теплоемкостью ве-
щества и его химическимъ составомъ, атомнымъ или моле-
кулярнымъ вѣсами и т. под. (законы Риіоп^’а и Реііі, Кеи-
шапп’а, Корр’а и т. д.). Этотъ вопросъ мы разсмотримъ послѣ статьи
о теплоемкости газовъ.
Наибольшею теплоемкостью изъ всѣхъ изслѣдован-
ныхъ до сихъ поръ тѣлъ обладаетъ водородъ. Одно и то
же простое вещество обладаетъ, вообще говоря, въ различныхъ ал-
лотропическихъ формахъ (т. I) неодинаковою теплоемкостью.
Такъ Ве^папИ нашелъ для различныхъ состояній углерода слѣ-
дующія теплоемкости:
Твердыя и жидкія тѣла.
191
Животный уголь . . 0,26085 Графита естественный 0,20187
Древесный уголь . . 0,24150 Граф. изъ домен. печи 0,19702
Коксъ изъ камен. угля 0,20085 Графитъ ретортный . 0,20360
Коксъ изъ антрацита . 0,20171 Алмазъ 0,14687.
ІЭеІагіѵе и Магсеі нашли для алмаза даже число 0,1192.
АѴпеІІпег нашелъ для графита 0,2019, для алмаза 0.1468;
далѣе для
Кристаллич. мышьяка . 0,0830 Кристаллич. селена. . 0,0840
Аморфнаго мышьяка 0,0758 Аморфнаго селена . . 0,0953.
Для свѣже сплавленной сѣры Ве^папіі нашелъ теплоемкость
с = 0,1844; втеченіе двухъ лѣтъ теплоемкость постепенно понижалась
до 0,1764; для естественной кристаллической сѣры онъ нашелъ с = 0,1776.
Красный и бѣлый фосфоръ обладаютъ почти одинаковымъ с = 0,251.
Вп8 8у нашелъ, что вязкая сѣра (выше 157°) обладаетъ большею тепло-
емкостью, чѣмъ сѣра жидкая, для которой с = 0,232. Такъ, между 160°
и 264° среднее значеніе с = 0,300, а между 232°,8 и 264° даже с = 0,324.
Плотность (твердость) даннаго вещества также вліяетъ на его
теплоемкость с. Такъ Ке^папіі нашелъ для куска мягкой мѣди с =
= 0,0950; послѣ обработки молотомъ оказалось с = 0,0936; для мягкой
стали онъ нашелъ 0,1165, для твердой 0,1175; для твердаго (быстро ох-
лажденнаго) стекла 0,1923, для мягкаго 0,1937. Уплотненіе вызываетъ,
вообще, уменьшеніе теплоемкости вещества.
Одно и то же вещество обладаетъ въ твердомъ и въ жид-
комъ состояніяхъ весьма различною теплоемкостью с. какъ видно изъ
слѣдующихъ чиселъ, гдѣ для воды и брома прибавлено еще с для паровъ:
Тверд. Жидк. Парообр. Тверд. Жидк.
н2о 0,502 1,000 0,477 8п 0,0562 0,0637
Вг 0,0843 0,1051 0,0555 РЬ 0,0314 0,0402
Нё 0,0314 0,0333 — Нафталинъ 0,3992 0,4824
8 0,203 0,234 —• Бензолъ 0,319 0,322
СаС12 0,345 0,555 — 0,278 0,413.
А. Цингеръ и И. Щегляевъ нашли слѣдующія интересныя
числа для эбонита, пробки и пальмоваго дерева, входящихъ въ составъ
нѣкоторыхъ калориметровъ :
Эбонитъ. Пробка. Пальмовое дерево.
с — 0,3387 0,4852 0,4194.
Теплоемкости, какъ видно, необыкновенно большія.
Температура имѣетъ весьма большое вліяніе на теплоемкость
тѣлъ. На стр. 156 мы^привели связь между эмпирическими формулами
для теплоемкостей с при данной температурѣ, — средней меледу 0° и
/° и с' — средней между /г° и і2°:
192
Теплоемкость.
с — со 4“ аі 4“ Ы?
?і = с0 + * аі + ЬР
о
с' = со 4~ 9 (Л + 4) + “5“ (Л2 +• ^14 4- 42)
& о
(23)
Зависимость этихъ величинъ отъ температуры разсмотрѣна нами
для воды въ § 2. Уже Биіоп^ и Реѣіѣ нашли, что теплоемкость
многихъ тѣлъ увеличивается съ повышеніемъ температуры; они нашли
слѣдующія числа для с100 и с300:
Ре ^100 0,1098 ^800 0,1218 Ар Г100 0,0559 ^800 0,0611
Си 0,0949 0,1013 Рі 0,0335 0,0355
7.П 0,0927 0,1015 Стекло 0,177 0,190.
В ё (1 е опредѣлялъ среднія теплоемкости между тремя температур-
ными интервалами, а именно приблизительно отъ 15° до 100°, до 170°
(для Ре 142°) и до 210° (для Ре и Си 247°): на основаніи формулы (23)
для с4 онъ могъ отсюда опредѣлить с0, а и Ь. Оказалось, что 6 = 0, т.-е.,
что с = с0 4~ аі^ гдѣ с0 и а имѣютъ слѣдующія значенія :
со а со а
Ре 0,1053 0,000071 РЬ 0,0286 0,000019
Си 0,0910 0,000023 • 7,п 0,0865 0,000044
8п 0,0500 0,000044 8Ь 0,04603 0,000021
Для Ре получаются отсюда при различныхъ / такія числа
і = 0° 100° 200° 400°
с = 0,1053 0,1195 0,1337 0,1479
Сі - 0,1053 0,1124 0,1195 0,1266.
Ву$ігоет опредѣлилъ среднюю теплоемкость до і= 300° для
нѣкоторыхъ металловъ и нашелъ слѣдующія числа:
і Чугунъ. Сталь литая. Ре чистое. Серебро. Платина.
0° 0,12768 0,11782 0,111641 0,05698 0,032386
150° 0,13140 0,12190 0,115949 0,05800 0,032950
300° 0,14070 0,13216 0,126719 0,06055 0,034750.
Важный вопросъ 0 теплоемкости платины въ зависимости отъ / былъ
изученъ многими учеными. Р о и і 11 е 1 нашелъ а= 0,0323 4 -0,0000041/.
АѴеіпЬоЫ нашелъ для Рі возрастаніе величины до і = 250°, за-
тѣмъ убываніе, опять слабое возрастаніе и наконецъ постоянное когда
і росло отъ 700° до 950°. Ѵіоііе получилъ до і = 1177°
а = 0,0317 4- 0,000006/,
Твердыя и жидкія тѣла.
193
и слѣд. с = 0,0317 0,000012Л Это даетъ с — 0,0317 при о0 и с = 0,0557
при ^ = 2000°. Для Р(1 ѴіоНе нашелъ с = 0,05820-Д- 0,00002^ до 1265°.
Далѣе онъ нашелъ, что теплоемкость золота мало мѣняется съ темпера-
турой. Среднія теплоемкости оказались такія:
с100 — 0,0324 ; ^боо — 0,0326 ; ^ѳоо — 0,0345 ; Сіооо — 0,0352.
РіопсЬоп также изслѣдовалъ рядъ металловъ до высокихъ тем-
пературъ; для теплоемкости с онъ нашелъ:
і Ее № Со
0° 0,05758 0,11012 0,10836 0,10584
100° 0,05864 0,11682 0,11283 0,11107
500° 0,06648 0,17623 0,13274 0,14616.
Весьма замѣчательна зависимость с отъ і для желѣза: (О 600°
наблюдается правильное возрастаніе с съ температурою по формулѣ
с = 0,11012 + 0,000050633/^-И 0,000000164/2.
Отъ 600° до 720° теплоемкость мѣняется по другому закону, отчасти зна-
чительно уменьшаясь. При 700° имѣемъ с = 0,3243, а при 720° только
с = 0,218, и это число остается постояннымъ между 720° и 1000°; отъ
1000° до 1200° имѣемъ с = 0,1989. Замѣчательно, что какъ разъ при
700° желѣзо теряетъ способность намагничиваться. Этимъ вопросомъ за-
нимались позже Нагііеу и Нагкег (1905). Для средней теплоем-
кости ст желѣза между 0° и Нагкег находитъ слѣдующія величины:
і
200°
300
Ст
0,1175
0,1233
і
400°
500
Ст
0,1282
0,1338
I Ст
600° 0,1396
700 0.1487
I Ст
800° 0,1597
900 0,1644
I ст
1000° 0,1557
1100 0,1534.
ОЬегіюГГег (1907) опредѣлилъ с для желѣза до 1500°; оказалось,
что средняя теплоемкость с между 0° и /° равна 0,1221 при ^ = 250°.
Она растетъ до 0,1698 при /" = 800° и затѣмъ медленно убываетъ до
0,1667 при ^= 1500. Ьесйег (1907) изслѣдовалъ Ыі до 720° и Ре
до 950°. Для № онъ нашелъ максимумъ с при 320° и минимумъ при 400°;
для Ре — медленное возрастаніе с до 650°, быстрое до 740° и быстрое
уменьшеніе до 950°.
Веки изслѣдовалъ теплоемкость различныхъ металловъ и графита
при очень низкихъ температурахъ (до —186°). Онъ нашелъ,
особенно для графита, очень быстрое убываніе с съ пониженіемъ тем-
пературы, какъ видно изъ слѣдующихъ чиселъ:
/ — + 18о оо _ 790 _ і8о°
с = 0,1730 0,1610 0,111 0,041
Еще дальше пошелъ Оехѵаг (1905). воспользовавшійся своимъ
упомянутымъ выше калориметромъ съ твердой СО2 (— 78°), жидкимъ
воздухомъ (— 188°) и жидкимъ водородомъ (— 252,5°). Онъ изслѣдовалъ
алмазъ, графитъ и ледъ. Въ слѣдующей таблицѣ приведены
среднія теплоемкости между данными температурами:
КУРСЪ ФИЗИКИ О. хв О Л Ь СО Н А. Т. III, изд. 3-е.
13
194
Теплоемкость.
4-18»-----78° —78°------188° —188°------252,6
Алмазъ . . 0,0794 0,0190 0,0043
Графитъ . . 0,1341 0,0599 0,0133
Ледъ . . . 0,463 (огъ —18° до —78°) 0,285 0,146.
Въ § 15 мы увидимъ, что для алмаза с при 985° достигаетъ вели-
чины 0,459; эта величина въ сто разъ больше наименьшей изъ вели-
чинъ, полученныхъ О е лѵ а г’омъ. Съ тѣмъ-же калориметромъ Г) е ’ѵѵ а г
изслѣдовалъ еще 19 различныхъ веществъ (нейзильберъ, латунь, Те, 5,
8е, ЫаСІ, СаС12, МН^СІ, нафталинъ, параффинъ, А&І. А§Вг, А^СІ и проч.)
и опредѣлилъ для нихъ ст между —188° и различными иными темпера-
турами. Также Тіійеп занимался опредѣленіемъ с при низкихъ тем-
пературахъ; онъ выразилъ с формулой
. ЬР
с — с° + 1 _|_ >
гдѣ а и Ь двѣ постоянныя. Дальнѣйшія изслѣдованія зависимости ве-
личины с отъ темйературы для металловъ производили въ послѣднее
время ОаеФе (1902), АФІег (хромъ, 1902), Всйпіііг (1903), 8іпес-
кег (1905); Огйпеібеп (1908), Ма^пие иЬіпсІетапп (1910)
и Ма^ппз (1910). Изъ нихъ (Згйпеізеп находитъ, что отношеніе
коеффиціента расширенія къ теплоемкости металла отъ температуры
почти независитъ. Теплоемкость тѣлъ при весьма низкихъ тем-
пературахъ изслѣдовали въ послѣднее время Р о г с Ь. и Е о г сі -
теуег (1906), Еогсіпіеуег и ВегпоиіПі (1907), Еискеп (1909),
Еісііагсіз п Йаскзоп (1910) и, въ особенности Еегпвѣ и его уче-
ники Ма^пиз, Ьіпбетапп и КогеІ (1910, 1911). Эти ученые
изслѣдовали, отчасти при помощи прибора, упомянутаго на стр. 178,
РЬ, А§, Хп, Си, АІ, А§СІ, РЬСІ%, 8, }, а также большое число органи-
ческихъ веществъ; они доходили до температуры кипящаго водорода
(около 23° абс.). Оказалось, что с быстро уменьшается до са-
мыхъ низкихъ температуръ и, повидимому, стремится къ нулю
при температурахъ, которыя близки къ абсолютному нулю.
Теплоемкость кварца растетъ по Ріопсйоп’у отъ 0,1737 до 0,305
при повышеніи температуры отъ 0° до 400°; отъ 400° до 1200° она оста-
ется постоянно равною 0,305. Н. Г. ЛѴеЪег изучалъ зависимость с отъ
і для С. В и 8і; приводимъ нѣкоторыя изъ его чиселъ.
Воръ. Кремній. Графитъ. Алмазъ.
1 с і с і с і с
— 390,6 0,1965 — 390,8 0,1360 — 500,3 0,1138 — 50°,5 0,0635
+ 26,6 0,2382 + 21,6 0,1697 — 10,7 0,1437 — 10,6 0,0955
76,7 0,2737 57,1 0,1833 4-10,8 0,1604 + 10,7 0,1128
125,8 0,3069 '86,0 0,1901 61,3 0,1990 58,3 0,1532
177,2 0,3378 128,7 0,1964 138,5 0,2542 140,0 0,2218
233,2 0,3663 232,4 0,2029 249,3 0,3250 247,0 0,3026
I 641,9 0,4454 606,7 0,4408
977,9 0,4670 985,0 0,4589
Твердыя и жидкія тѣла.
195
Теплоемкость алмаза съ повышеніемъ температуры увеличивается
въ семь разъ; разница между с для графита и алмаза составляетъ 80%
при —50° и только 1,7% при 980°. ѴіоПе находитъ, что выше і =
= 1000° средняя теплоемкость графита между 0° и /° равна с = 0,355
4- О,ОООО6Л
Кипг (1904) изслѣдовалъ с для древеснаго угля до высокихъ темпе-
ратуръ ; онъ нашелъ с = 0,243 при 435°, с = 0,363 при 1000° и с = 0,382
при 1297°. Ьіпйпет (1903) нашелъ возрастаніе с съ температурою
для многихъ минераловъ.
Твердыя органическія вещества изслѣдовали й е Нееп, В а -
ѣеііі, Не§8 и Богаявленскій (1904). Послѣдній нашелъ, что
весьма малыя примѣси сильно вліяютъ на с кристаллическихъ органиче-
скихъ веществъ, въ особенности вблизи точки плавленія. Чѣмъ меньше
примѣсей, тѣмъ меньше и с. Для вполнѣ чистыхъ веществъ с мало
зависитъ отъ температуры и с = /(/) есть функція линейная.
ЛѴіе^апй (1907) и 8сЫеіі (1907) сравнивали с при различ-
ныхъ аллотропическихъ состояніяхъ. Они подтвердили правило, которое
теоретически вывелъ В і с й а г я, а именно, что болѣе плотная мо-
дификація обладаетъ меньшею теплоемкостью. ЛѴіе-
$ а п й изслѣдовалъ С, В, 5/, Р, 5, А$, Зе, Те и 8п\ БсЪІеіі на-
шелъ, что къ различно обработаннымъ сортамъ Рі и Л7 примѣнимо то
же правило.
Вісііагг (1893, 1899, 1906) далъ остроумную теорію, объясняю-
щую тѣ особенности, которыя представляетъ теплоемкость твердыхъ тѣлъ.
Мы къ ней возвратимся въ § 15.
Тйіезеп (1908) полагалъ, что с можетъ быть выражено пока-
зательной функціей абсолютной температуры.
Ве^паиіі, Нігп, Бе-Нееп, КеІ8, 8сЫИ, ЗсЬиеПег
и многіе другіе ученые изслѣдовали теплоемкости с различныхъ жид-
костей. И для жидкостей, вообще говоря, с возрастаетъ съ темпера-
турою. Нігп доходилъ до 160°, Ое-Нееп до температуръ, лежащихъ
выше критической. Для алкоголя Нігп нашелъ такія числа
і = 0° 80° 120° 160°
г = 0,42292 0,71123 0,85942 1,11368.
□ е-Нееп находитъ внезапное пониженіе теплоемкости при пере-
ходѣ черезъ критическую температуру, какъ видно изъ слѣдующихъ чиселъ:
1 С 1 С
Эфиръ. . . . 180° 1,041 Бромист. этилъ 215° 0,852
— ... . 185° 0,547 — — 220° 0,233
Амиленъ. . . 170° 1,500
— . 175° 0,773
Не приводимъ другихъ результатовъ, которые можно найти въ та-
блицахъ ЬапйоИ’а и Воегп8Іеіп’а. Ясѣ И Г высказалъ предпо-
13*
196
Теплоемкость.
ложеніе, что для жидкостей с есть линейная функція температуры і
и что для гомологовъ она можетъ быть представлена графически парал-
лельными прямыми. Курбатовъ (1903) показалъ, что это предполо-
женіе не вполнѣ вѣрно. Онъ нашелъ, что для нормальныхъ жидкостей
с = /(/) изображается кривой съ малой кривизной; для гомологовъ съ
почти одинаковымъ молекулярнымъ вѣсомъ с = /(^) выражается форму-
лами, которыя весьма мало между собой различаются.
ОгіИііЬ.8 весьма тщательно изслѣдовалъ величину с для ани-
лина, которымъ онъ совѣтуетъ пользоваться какъ калориметрическою
жидкостью, вмѣсто воды. Онъ находитъ
с = 0,5156 Н- 0,0004 (І — 20) + 0,000002 (/ — 20)2,
причемъ за единицу тепла принятъ «ролэндъ», т.-е. «термъ^> при 15° (см.
стр. 165). Вагіоіі, однако, находитъ для с числа, замѣтно отличаю-
щіяся отъ чиселъ Огі ѣііѣііз’а; предложеніе пользоваться анилиномъ
онъ находитъ непрактичнымъ въ виду способности анилина поглощать
большія количества воды изъ влажнаго воздуха. Курбатовъ (1902)
также изслѣдовалъ анилинъ и нашелъ очень сложную зависимость с
отъ температуры. Средняя теплоемкость растетъ отъ 22° до 137°, убы-
ваетъ до 158° и затѣмъ снова возрастаетъ.
Ртуть представляетъ ту странную особенность, что ея теплоем-
кость с убываетъ съ повышеніемъ температуры. Этотъ
результатъ былъ найденъ АѴіпкеІ шапп’омъ, который далъ для с
между 19° и 142° формулу с = 0,03336 — 0,0000069А Реііегйоп и
Нейеііив выразили сомнѣніе въ справедливости факта уменьшенія с
при повышеніи /, но опыты Масса г і и МіІІЬаІег’а вполнѣ под-
твердили этотъ фактъ. Принимая при I = 0° число Р е И е г 8 о п’а
0,033266, МіНЬаІег даетъ формулу с — 0,033266 — 0,0000092А Сред-
нія изъ чиселъ АѴіпкеІшап п’а (до 140°), Массагі и Міі-
IЬ. а 1 е г’а таковы :
0° 20° 60° 100° 140° 180° 200°
С — 0,03333 0,03319 0,03290 0,03262 0,03233 0,03203 0,03189.
Новѣйшія опредѣленія Вагіоіі и бігассіаіі (между 0° и 30°)
хорошо согласуются съ числами АѴіпкеІтапп’а и Массагі.
В а г п е 8 и Сооке находятъ для ртути между 0° и 84° (по
шкалѣ азотнаго термометра).
с = 0,0333458 — 1,074 . 10“^-|- 0,00385 . ІО”^2
причемъ за единицу принята 15°,5 — калорія. Курбатовъ (1908) из-
слѣдовалъ с для до 306° и нашелъ минимумъ между 200° и 250°.
Теплоемкость нѣкоторыхъ переохлажденныхъ жидкостей изслѣдо-
валъ Ь. Вгпппег.
Велѵаг (1901) и А11 (1904) опредѣляли с для ожижженныхъ га-
зовъ. Ведѵаг нашелъ для жидкаго азота с = 0,43. Для жидкаго
Твердыя и жидкія тѣла.
197
водорода онъ сперва (1901) далъ число с — 6; позднѣйшія измѣре-
нія (1905) привели его къ числу с — 3,4.
Весьма любопытно, что Мс. ІпіобЬ (1907) нашелъ для жид-
каго ацетилена теплоемкость, нѣсколько большую теплоемкости
воды. Ваѣѣеііі Ц908) изслѣдовалъ с щя жидкостей, затвердѣвающихъ
при низкихъ температурахъ (С52, эфиръ, спирты, толуолъ и др.) до —140°.
Теплоемкость сплавовъ изслѣдовалъ Ве^паиіі; онъ нашелъ,
что теплоемкость С многихъ сплавовъ можетъ быть вычислена по фор-
мулѣ смѣшенія, т.-е. допуская, что составныя части сплава сохраняютъ
тѣ теплоемкости, которыми онѣ обладали въ свободномъ состояніи. Если Сі
теплоемкости, р[ вѣса составныхъ частей, то
с _ ЗРіРі _ Р1<Л + р2с2 + рас8 + . . .
С- 2Рі - Р1^р2 + р3 .... (24)
Законъ, выраженный этой формулой, иногда называется закономъ
Меитапп’а. Сюда относятся, напр., сплавы РЬ8п, РЬ8п^ РЬ8Ь, Ві8п,
Ві8п2, Ві8п28Ь, Ві8п28Ь7,п2, Вргіп^ нашелъ, что формула (24) прило-
жима для жидкихъ сплавовъ вида РЬр8Пд, гдѣ р и д равны 1,2, .... 6
при температурахъ, значительно превышающихъ температуру плавленія.
Зато въ предѣлахъ отъ 100 до 360° формула (24) для нихъ непригодна :
наблюденное среднее С оказалось гораздо больше вычисленнаго по
формулѣ (24). Нѣчто подобное замѣтилъ 8ргіп^ и для легкоплавкихъ
сплавовъ и амальгамъ. Такъ, напр., для сплава Ьірролѵііг’а онъ на-
шелъ значенія для С, которыя при 28° щходили до С — 0,0634, тогда
какъ формула (24) даетъ С = 0,0365. Однако, М а г о 1 і о получилъ для
этого сплава С = 0,0354. АиЬеІ объясняетъ такое уклоненіе чиселъ
8ргіп§’’а тѣмъ, что Зргіпд пользовался способомъ охлажденія, не-
примѣнимымъ къ твердымъ тѣламъ.
Можно было ожидать, что при низкихъ температурахъ получится С
болѣе согласное съ формулою (24), что и было подтверждено опытами
8 с к и е г’а, который изслѣдовалъ рядъ легкоплавкихъ сплавовъ и амаль-
гамъ 8п, РЬ, Ыа и К. Оказалось, что формула (24) приложима къ
легкоплавкимъ сплавамъ въ предѣлахъ отъ — 80° до + 20°. То же са-
мое относится къ амальгамамъ Т,п2Н^ РЬ^Н^, къ десятипроцентной на-
тровой и къ 10,58 процентной калійной амальгамамъ. Другія амальгамы
даютъ С близкія къ вычисленнымъ по формулѣ (24) только при темпе-
ратурахъ і >* — 40°. Ниже — 40° получаются отклоненія, доказываю-
щія, что при этихъ температурахъ часть ртути затвердѣваетъ, выдѣляя
скрытую теплоту. Теплоемкость нѣкоторыхъ сплавовъ Ре и 8Ь, а также
Ре и АІ изслѣдовалъ ЬаЬогйе; онъ подтвердилъ формулу (24).
Н. Н. Бекетовъ опредѣлилъ теплоемкость палладія (25,094 гр.),
поглотившаго 710 объемовъ водорода (т. I), т.-е. 0,1418 гр. Если прило-
жить къ этому сплаву палладія и водорода формулу (24), то получается
для теплоемкости с водорода въ томъ его состояніи, въ которомъ онъ на-
ходится въ палладіи, число с = 5,88.
198
Теплоемкость.
Белѵаг (1873) находитъ значительно меньшее число с = 3,5. Такъ
какъ, какъ мы видѣли, для жидкаго водорода получилось с = 3,4,
а для газообразнаго водорода (см. § 12) также ср = 3,4, то Ве-
\ѵаг заключаетъ, что теплоемкость водорода въ газообразномъ, жидкомъ
и окклюдированномъ состояніяхъ одна и та-же.
Вита8 (1911) изслѣдовалъ с для сплавовъ Ре и М, для кото-
рыхъ существуетъ температура превращенія (т. IV). Оказалось что при
этой температурѣ происходитъ внезапное пониженіе теплоемкости.
Ви88у и Виі^пеі впервые показали, что формула (24) даетъ
для смѣсей жидкостей вообще слишкомъ малыя значенія. 8 с Ь и е 11 ет
показалъ, однако, что къ смѣсямъ жидкостей, индифферентныхъ другъ
къ другу, формула (24) приложима, напр., къ смѣсямъ хлороформа и С52,
хлороформа и бензина, С32 и бензина. Къ смѣсямъ же, содер-
жащимъ алкоголь, формула (24) совершенно неприложима, какъ
показали почти одновременно бсііиеііег, Виргё и Ра§е. Такъ
для смѣсей алкоголя и хлороформа С иногда на 15% больше вычислен-
наго. Для смѣсей алкоголя и воды получается иногда С > 1, т.-е. те-
плоемкость смѣси больше теплоемкости каждой изъ составныхъ частей.
ЬесЬег, Ра^ііапі и 2еіѣегшапп нашли подобные же
результаты для смѣсей метиловаго, пропиловаго и изобутиловаго алко-
голей съ водою.
Теплоемкость растворовъ изслѣдовали РеГ8оп, 8сЬие1-
Іег, 1 ТЬотзоп, Магі^пас, ЛѴіпкеІтапп, Вревскій,
Биронъ, Ма^іе, Ри8сЫ, МаІЬіав, Дорошевскій и Ра-
но вскій (1908), ЗсЫевіп^ег (1909) и др. Оказалось, что тепло-
емкость растворовъ не можетъ быть вычислена по формулѣ (24). Пусть с
теплоемкость раствореннаго вещества, напр., твердой соли, и допустимъ,
что р гр. вещества растворены въ 100 гр. воды. Тогда формула
100 ре
100 + р.......................
(25)
дала бы намъ теплоемкость раствора, вычисленную по правилу смѣшенія.
Наблюденное С меньше С'; въ нѣкоторыхъ случаяхъ теплоемкость (100 4- р)
гр. раствора оказывается даже меньше числа 100, т.-е. меньше теплоем-
кости тѣхъ 100 гр. воды, которые входятъ въ растворъ.
М а 1Ь і а 8 далъ формулу С =
а 4- п
Ь 4- іг
с, гдѣ с теплоемкость
ра-
створителя (для воды с = 1), п число эквивалентовъ растворителя на 1 эк-
вивалентъ растворимаго; а и Ь постоянныя, зависящія отъ раствори-
маго. Такъ, напр., для
а Ь а Ь
2,5 7,4 ЫаСІ 11,45 20
НСІ 1,97 9,23 ЫН^О. 5,33 12,55
ШНО 4,0 31,4 Сахара 8,78 19,77
Твердыя и жидкія тѣла. — Газы
199
МаѣЫав показалъ, что его формула приводится къ (25), если до-
пустить, что теплоемкость с растворимаго перешла при раствореніи въ
а
с = с и что при этомъ его эквивалентъ
увеличился въ Ь разъ.
Д. II. Коноваловъ измѣрилъ теплоемкости смѣсей анилина и диметил-
анилина съ уксусной, масляной и пропіоновои кислотами, Биронъ —
растворовъ сѣрной кислоты. Вегійеіоѣ, Таттапп, Р и 8 с 111 идр.
дали теоретическій разборъ вопроса о теплоемкости растворовъ. Ривсы
высказалъ предположеніе, что въ растворахъ часть воды измѣняется та-
кимъ образомъ, что для нея теплоемкость равна теплоемкости льда (0,5).
Ма^і.е пришелъ къ тому заключенію, что формула (25) должна
быть примѣнима ко всѣмъ растворамъ не электролитовъ, что онъ
и доказалъ въ цѣломъ рядѣ работъ. Для растворовъ электролитовъ онъ
даетъ формулу
с = с0 + а — Ьр..................(26)
гдѣ с0 обозначаетъ теплоемкость чистаго растворителя; а и Ь двѣ по-
стоянныя и р степень диссоціаціи раствореннаго электролита. Эта формула
превосходно согласуется съ результатами, полученными Т Ь о ш 8 е п’омъ.
Въ заключеніе замѣтимъ, что V а пЧ - Н о И въ своихъ лекціяхъ по
теоретической и физической химіи, часть III, теоретически выводитъ
формулу, данную Ваккег’омъ, которая даетъ возможность вычислить
теплоемкость с жидкости, если извѣстны теплоемкость при постоянномъ
объемѣ ея пара (см. ниже), скрытая теплота испаренія и коеффиціентъ
расширенія при температурѣ испаренія. Для ртути и эфира по этой фор-
мулѣ получаются числа, весьма близкія къ наблюденнымъ.
§ 11. Теплоемкость газовъ. Количество теплоты, потребное для
нагрѣванія газовъ, вообще въ гораздо большей степени, чѣмъ для тѣлъ
твердыхъ и жидкихъ, зависитъ отъ тѣхъ условій, при которыхъ происхо-
дитъ самое нагрѣваніе. Это объясняется способностью газовъ къ произ-
вольно большому расширенію. Мы увидимъ впослѣдствіи, что теплота С),
поглощенная тѣломъ, тратится на нагрѣваніе, т.-е. на увеличеніе кине-
тической энергіи движенія частицъ и атомовъ, на внутреннюю ра-
боту и на работу внѣшнюю. Для твердыхъ и жидкихъ тѣлъ эта третья
часть, вообще говоря, весьма мала и на практикѣ нагрѣваніе почти
всегда происходитъ при одинаковыхъ условіяхъ, а именно при постоян-
номъ внѣшнемъ давленіи. Для газообразныхъ тѣлъ, особенно если ихъ
температура находится весьма далеко отъ точки ожиженія, вторая часть
весьма мала, но зато часть третья, расходуемая на внѣшнюю работу, мо-
жетъ быть и нулемъ и весьма большою положительною величиною, когда
газъ расширяется, а также и величиною отрицательною, когда газъ под-
вергается сдавливанію.
Между различными значеніями, которыя можетъ принимать тепло-
емкость газа, представляютъ особый интересъ величины с? и сѵ — тепло-
емкостей при постоянномъ давленіи и при постоянномъ объемѣ, съ кото-
200
Теплоемкость.
рыми мы уже встрѣчались неоднократно. Для идеальныхъ газовъ,
болѣе полную теорію которыхъ мы разберемъ ниже, мы вывели въ т. ]
нѣкоторыя формулы, которыми намъ пришлось уже пользоваться, напр., въ
ученіи о звукѣ. Если упругость, объемъ и абсолютную температуру вѣ-
совой единицы обозначить черезъ /?, ѵ и Т, то для идеальныхъ газовъ
рѵ = КТ...............................(27)
гдѣ постоянная величина, т.-е. не зависящая отъ состоянія газа. Если
за единицы объема и давленія принять куб. метръ и давленіе въ 1 ки-
логр. на 1 кв. м. поверхности, то
.......................(27,а)
гдѣ <5 удѣльный вѣсъ газа по отношеніи къ воздуху. Въ т. [ была вы-
ведена формула
ср — сѵ = .....................(28)
гдѣ А термическій эквивалентъ работы, т.-е. приблизительно —; ср и сѵ
относятся къ одному килограмму вещества. Вставивъ (27,а) въ (28), по-
лучаемъ
Произведенія срд и сѵд представляютъ теплоемкости объема газа,
равнаго объему одного килограмма воздуха. Если черезъ ѵ0 обозначить
этотъ послѣдній объемъ, то срд: ѵ0 и Сѵ^: ѵ0 представляютъ теплоем-
кости единицы объема газа, которыя мы обозначимъ черезъ ?р
и уѵ. Формула (29) даетъ
7 -7Ѵ= °’°688
р ѵ ѵ0
(30)
т.-е. разность теплоемкостей при постоянномъ давленіи и при постоян-
номъ объемѣ, отнесенныхъ къ единицѣ объема, есть величина постоян-
ная для всѣхъ идеальныхъ газовъ, взятыхъ, конечно, при одинаковыхъ
давленіи и температурѣ. При 0° и 760 мм. имѣемъ ф0 = 0,7733 и слѣд.
7р - = о = 0,0889 ...........(31)
1 V, < < Од
Оставляя единицы объема и давленія неопредѣленными, мы полу-
чаемъ общую формулу
Л/?
гдѣ 7? постоянная формулы (27) и Фо объемъ вѣсовой единицы воз-
духа при давленіи и температурѣ разсматриваемой единицы объема газа.
Газы.
201
Изъ формулы (29) получается для идеальныхъ газовъ
Су -- Ср
0.0688
д
(32)
II о этой формулѣ можетъ быть вычислено ср, если
сѵ найдено.
Мы видѣли (т. I), что молекулярный вѣсъ р газа равенъ = 28.886
Помножая (29) на //, мы получаемъ слѣва молекулярныя теплоемкости
р и а справа постоянное число:
с,, П — с,. ѵ = 0,0688 X 28,88 = 1,987 .(33)
Разность молекулярныхъ теплоемкостей при посто-
янномъ давленіи и при постоянномъ объемѣ для иде-
альныхъ газовъ есть величина постоянная, близкая
къ двумъ малымъ или большимъ калоріямъ, если взяты
граммовъ или д килограммовъ газа, гдѣ молекулярный вѣсъ газа (для
водорода = 2).
Отношеніе : сѵ мы обозначимъ черезъ к. Эта величина входитъ
въ формулу для скорости звука V (т. II),
ѵ I ' *
гдѣ сі масса единицы объема газа.
Въ т. I была выведена формула Р о і 8 8 о п’а
рѴк — Соп8і....................(35)
связывающая р и ѵ для случая адіабатическаго измѣненія состоя-
нія идеальнаго газа, т.-е. такого измѣненія, при которомъ газъ не всту-
паетъ въ тепловой обмѣнъ съ окружающими его тѣлами. Сюда отно-
сится случай внезапнаго сжатія или расширенія газа. Объемъ ѵ и аб-
солютная температура Т связаны при этомъ формулою (т. I)
7^—1 = Соп8І .... ... (36)
Обозначимъ черезъ У весь запасъ кинетической энергіи движенія,
заключающійся въ единицѣ вѣса даннаго газа. Этотъ запасъ состоитъ
изъ энергіи }и поступательнаго движенія молекулъ, изъ энергіи враща-
тельнаго движенія молекулъ и изъ энергіи интрамолекулярныхъ движеніи
атомовъ или группъ атомовъ, входящихъ въ составъ молекулъ. Въ т. I
мы вывели формулу
4 3
7 = 2 (/г-0....................
дающую отношеніе энергіи поступательнаго движенія ко всему запасу
энергіи въ газѣ. По существу 7„ не можетъ быть больше слѣд. к — 1
2 5
не оолыпе 3 или - 1С60.................(38)
202
Теплоемкость.
Величина к не можетъ превышать числа 1,666 . . .
Для одноатомныхъ газовъ можно положить т.-е.
к
к= „.............................(39)
о
л <- и 5
и наоборотъ, если мы для такихъ газовъ найдемъ «= — , то это озна-
О
чаетъ, что Зи = У, т.-е. что энергія вращательнаго движенія атомовъ
или не существуетъ (нуль или ничтожно мала), или отъ температуры
не зависитъ. &
Для двухъ и многоатомныхъ газовъ С 7 и слѣд. к < . М а х -
о
лѵ е 11, Во 11гшапп и др. старались теоретически вывести зависимость
величины к отъ числа п атомовъ, входящихъ въ составъ молекулы. Для
двухатомныхъ газовъ получается
7
к = г = 1,40 ........................(40)
5
если допустить, что разстояніе двухъ атомовъ, входящихъ въ составъ
молекулы, не можетъ измѣниться; въ противномъ же случаѣ мы должны
имѣть
4
к= = 1,33........................ . (41)
о
Съ увеличеніемъ числа п должно уменьшаться отношеніе а
слѣд. должно уменьшаться и число к Въ одноатомныхъ газахъ = 7;
3 7 4 1
въ двухатомныхъ если к = & ; если же к — то = 2
Формула (37) показываетъ, что если для какого-либо газа к не зависитъ
отъ температуры, то и отношеніе остается постояннымт> при на-
грѣваніи газа. Это означаетъ, что притекающая теплота распредѣляется
въ постоянномъ отношеніи между энергіей поступательнаго движенія мо-
лекулъ и энергіей остальныхъ, въ газѣ существующихъ движеній, напр.
3 2
въ отношеніи - : = 3 : 2 въ двухатомныхъ газахъ, для которыхъ к =
О О
= 1,40, или въ двухъ равныхъ частяхъ, когда к = 1,33. Къ этому во-
просу мы возвратимся въ § 15.
§ 12. Теплоемкость газовъ при постоянномъ давленіи. Первыя
опредѣленія теплоемкости ср для различныхъ газовъ произвели Сгалѵ-
Тогсі, Ьаѵоізіег и Ьаріасе, СІётепЬ и Везоттез и бау-
Ьи8 8ас. Результаты, полученные этими учеными, были, однако, весьма
мало точны. Въ 1812 г. появилась классическая работа ВеІагосЬе и
Вёгагй'а, давшихъ впервые результаты, заслуживающіе довѣрія.
Приводимъ нѣкоторыя числа ср для различныхъ газовъ но опредѣ-
леніямъ Веіагосйе’а и ВёгагсГа.
Газы.
203
ср СР
Воздухъ . . 0,2669 Ѵзотъ . 0,2754
Кислородъ . . . . . 0,2361 Углекислый газъ. . . 0,2210
Водородъ.... . . 3,2936 Окись углерода . . . 0,2884;
Окись азота . . . . 0,2369 Этиленъ . 0,4207
Послѣ ВеІагосЬе’а и Вёгагсі’а и до Ее^папіг произво-
дили опредѣленія теплоемкости газовъ НаусгаіЧ, Оеіагіѵе и М а г -
с е I, Арз’оііп, 8иегшепп и Л о и 1 е.
Въ 1862 г. появилась классическая работа Ее^паиИ, къ которой
мы и обращаемся. Приборъ, которымъ пользовался Ее^паиіі, изобра-
Рис. 78.
женъ на рис. 78. Испытуемый газъ находился въ большомъ металличе-
скомъ резервуарѣ А, вмѣстимостью около 35 литровъ, въ сгущенномъ со-
стояніи. Изъ А газъ протекалъ непрерывной струей по трубкамъ въ на-
грѣвательный приборъ С, затѣмъ въ калориметръ О, откуда онъ свободно
выходилъ въ воздухъ. Резервуаръ А помѣщался въ большомъ сосудѣ,
наполненномъ водою, температура которой во время опыта оставалась
постоянною. Вѣсовое количество Р газа, протекшаго черезъ калори-
метръ, опредѣлялось по уменьшенію давленія Н газа въ резервуарѣ А,
На основаніи предварительныхъ опытовъ была опредѣлена зависимость
количества газа І2 въ резервуарѣ А отъ его давленія Н \ эта зависимость
могла быть выражена эмпирической формулой вида
& = а + ЬН + сН\
204
Теплоемкость.
гдѣ а, Ь и с три постоянныя. Съ уменьшеніемъ давленія Н въ резерву-
арѣ А должна была бы уменьшиться и скорость теченія газа черезъ при-
боръ. Чтобы достигнуть равномѣрнаго теченія газа во все время опыта,
Ве^паиіѣ помѣстилъ въ/ особый регулирующій приборчикъ, отдѣльно
изображенный въ У7, и кромѣ того открытый манометръ пг, соединенный
съ трубкою. Регуляторъ Р состоитъ изъ винта, оканчивающагося снизу
конусомъ и имѣющаго головку, снабженную дѣленіями, отсчетъ которыхъ
производится при помощи указателя, поставленнаго сбоку. Вращая го-
ловку винта, можно было болѣе или менѣе открывать отверстіе, черезъ
которое проходилъ газъ и тѣмъ регулировать давленіе Д, которое газъ
имѣлъ до вступленія въ нагрѣватель С и избытокъ котораго надъ атмо-
сфернымъ давленіемъ измѣрялся манометромъ пг; показанія послѣдняго
должны были сохраняться постоянными во время опыта.
Въ нагрѣвателѣ С газъ проходилъ черезъ змѣевикъ, состоявшій изъ
оловянной трубки въ 10 м. длины и 8 мм. внутренняго діаметра. Ке§-
паиіі убѣдился непосредственными опытами, что газъ, пройдя змѣе-
викъ, вполнѣ принималъ температуру окружающей его жидкости, служа-
щей для его нагрѣванія. Сосудъ С содержалъ масло, подогрѣваемое снизу,
и непрерывно перемѣшиваемое круглою мѣшалкою. Термометромъ, не
• показаннымъ на рисункѣ, опредѣлялась температура Т масла, а слѣд. и
газа. Изъ С газъ проходилъ по трубкѣ черезъ вертикальную стѣнку,
также не показанную на рисункѣ, въ калориметръ О. Послѣдній содер-
жалъ четыре круглыхъ, плоскихъ металлическихъ сосуда, соединенныхъ
между собою вертикальными трубками. Спиральныя перегородки превра-
щали каждый изъ четырехъ сосудовъ въ спиральный каналъ; пройдя че-
ре«л> ати сосуды, т.-е. по всѣмъ оборотамъ четырехъ каналовъ. газъ
вполнѣ принималъ температуру воды, налитой въ калориметръ, содержа-
вшій еще мѣшалку и термометръ. Масло въ С нагрѣвалось до 100° или
до 200°; для опредѣленія теплоемкости при низкихъ температурахъ,
Ве^панИ замѣнялъ масло охлаждающей смѣсью, температура которой
равнялась — 30°.
Маленькій манометръ пг служилъ для опытовъ при давленіи, близ-
комъ къ атмосферному. Чтобы измѣрить ср при большихъ давленіяхъ /л
Ве^папіі доводилъ давленіе въ резервуарѣ А до 10 атм., замѣнялъ пг
большимъ ртутнымъ манометромъ и помѣщалъ капилярную трубку на
концѣ трубки, выступающей изъ калориметра. Такимъ образомъ, онъ до-
водилъ давленіе р газа, протекающаго черезъ приборъ, до 4-хъ атмо-
сферъ и это давленіе оставалось постояннымъ въ С и 2?, такъ какъ пе-
реходъ давленія газа къ атмосферному совершался только внутри и около
отверстія капилярнои трубки, черезъ которую газъ вытекалъ.
Въ нѣкоторыхъ опытахъ В е^паиіі помѣщалъ регулирующій при-
борчикъ Р не на пути газа между А и С, но у выхода газа изъ калори-
метра, достигая такимъ образомъ равномѣрнаго теченія газа черезъ при-
боръ. При этомъ давленіе р газа равнялось давленію РІ въ резервуарѣ и
слѣд. постепенно уменьшалось. Но расширеніе газа, соотвѣтствующее
Газы.
205
этому уменьшенію давленія, происходило въ А; черезъ калориметръ газъ
протекалъ при постоянномъ давленіи, такъ что и въ этомъ случаѣ опре-
дѣлялась величина ср. При вычисленіи теплоемкости ср необходимо при-
нять во вниманіе, что калориметръ во время самаго опыта теряетъ те-
плоту вслѣдствіе лучеиспусканія и пріобрѣтаетъ теплоту вслѣдствіе те-
плопроводности тѣхъ частей, которыми онъ соединенъ съ нагрѣвателемъ С.
Ходъ полнаго наблюденія поэтому долженъ быть слѣдующій. Когда тем-
пература нагрѣвателя С установилась, наблюдаютъ втеченіе десяти ми-
нутъ черезъ каждую минуту температуры Ѳ калориметра и т окружаю-
щаго воздуха; положимъ, что Ѳо и го среднія изъ десяти значеній этихъ
величинъ, <5Ѳ0 среднее измѣненіе температуры калориметра, положитель-
ное, когда Ѳ растетъ. Въ такомъ случаѣ можно положить <5Ѳ0 — К +
-|- а (г0 Ѳо), гдѣ К повышеніе температуры калориметра, вызванное
притокомъ тепла черезъ теплопроводность. Послѣ десятаго наблюденія
начинаютъ пропускать газъ черезъ калориметръ, наблюдай черезъ каждую
минуту температуры калориметра и окружающаго воздуха. Взявъ ариѳ-
метическія среднія сосѣднихъ отсчетовъ, получаютъ среднія температуры
• • • > калориметра и среднія температуры г3, . . . , тп
окружающаго воздуха за каждую изъ п минутъ, втеченіе которыхгь про-
должалось пропусканіе газа черезъ калориметръ. Послѣ прекращенія по-
тока газа продолжаютъ наблюденія еще втеченіе десяти минутъ, и пусть
теперь Ѳо' и среднія значенія, 6ѲО' среднее измѣненіе температуры
калориметра втеченіе одной минуты. Соотвѣтственно первому равенству
имѣемъ теперь <5Ѳ0' = К +• а (г0' - Ѳо'). Изъ двухъ уравненій находятъ
величины К и а. Затѣмъ составляютъ для каждой изъ п минутъ, вте-
ченіе которыхъ газъ проходилъ черезъ калориметръ, величину +
п
гдѣ * = 1,2,3, . . . . , п. Сумма величинъ дѲ^ т.-е. 2
1
составитъ повышеніе температуры калориметра, происшедшее не оть
протекающаго черезъ него газа; эта сумма, которая, впрочемъ, можетъ
быть и величиною отрицательною, должна быть вычтена изъ темпера-
туры Ѳ", наблюденной въ концѣ я-той минуты, когда былъ прекращенъ
потокъ газа, чтобы узнать повышеніе температуры калориметра, вызван-
ное газомъ. Пусть Ѳ' температура калориметра въ моментъ, когда тече-
ніе газа началось, и С теплоемкость калориметра. Въ такомъ случаѣ ка-
лориметръ получилъ отъ газа теплоту С (Ѳ" — <5 Ѳ/ — Ѳ'). Вѣсовое ко-
личество Р газа охладилось отъ начальной температуры Т нагрѣвателя
до температуры калориметра, которая въ отдѣльныя минуты равнялась
в1? Ѳ2, . . . . , Ѳп. Въ этомъ случаѣ газъ отдалъ столько же тепла,
какъ еслибы вся его масса охладилась до средней изъ этихъ п темпера-
2ѲІ
туръ, которую обозначимъ черезъ-----. Мы получаемъ такимъ образомъ
равенство
206
Теплоемкость.
/
Рсо\1 — = С ((/' — — ѲД
Р \ П I
которое и служить для опредѣленія ср.
Результаты опытовъ К е § п а и И мы изложимъ ниже.
Въ 1876 г. появилась работа Е. Ѵ/іе <1 е т ап п’а, котором> уда-
лось опредѣлить ср для различныхъ газовъ и при различныхъ темпера-
турахъ, пользуясь приборомъ весьма небольшихъ размѣровъ. Суще-
Рис. 79.
ственнымъ представляется въ этомъ приборѣ нагрѣваніе и охлажденіе
газа не въ длинныхъ змѣевикахъ, но въ небольшихъ, сравнительно, сосу~
дахъ, наполненныхъ мѣдными или серебряными стружками; при этомъ
газъ соприкасается съ огромною поверхностью, служащею для его нагрѣ-
ванія или охлажденія. Приборъ Е. ДѴі е (1 е т ап п’а изображенъ на
рис. 79. Газъ находится въ каучуковомъ пузырѣ С, изъ котораго онъ
вытѣсняется по способу ВеІагосЬ е’а и В ё г а г (Га: вода льется
изъ О въ Д, причемъ воздухъ переходитъ изъ А въ В. Водяные мано-
метры Р и Р' опредѣляютъ давленіе въ А и В. Количество газа, вы-
текшаго изъ С, опредѣляется по вѣсу воды, перешедшей въ Л, по пока-
заніямъ манометровъ Р и Р', и по температурѣ газа, которая измѣряется
въ приборѣ термометромъ і. Газъ проходитъ черезъ стклянку /7,
содержащую сѣрную кислоту или ртуть, для того, чтобы можно было
удобно слѣдить за скоростью теченія газа, и затѣмъ черезъ сосудъ У, на-
полненный стеклянными шариками, для удержанія кислоты на случай,
Газы.
207
еслибы слѣды ея примѣшались въ Н къ газу. Далѣе газъ проходитъ че-
резъ нагрѣватель Т7, состоящій изъ мѣдной трубки длиною въ 11 см. и
шириною въ 4 см., наполненной мѣдными стружками; она окружена во-
дою или расплавленнымъ параффиномъ; /? мѣшалка, Т термометръ. Изъ
нагрѣвателя газъ вступаетъ въ крошечный серебряный калориметръ /И,
установленный на цилиндрѣ К, сдѣланномъ изъ металлической сѣтки и
находящемся внутри сосуда Л, между двойными стѣнками котораго про-
текаетъ вода изъ по направленію Ы$8іід. Высота калориметра 5,5 см.,
ширина 4,2 см., толщина серебряной стѣнки 0,35 мм.: калориметръ со-
держалъ всего 60 гр. воды.
На отдѣльномъ рисункѣ ЛГ показано поперечное сѣченіе калори-
метра. Въ немъ находится маленькая мѣшалка г и три серебряные верти-
кальные цилиндрика а, /9 и у, высота которыхъ 41 мм., ширина 9 мм.;
эти цилиндрики вполнѣ наполнены серебряными стружками. Газъ всту-
паетъ снизу въ цилиндрикъ а, затѣмъ сверху въ снизу въ у и, нако-
нецъ, черезъ трубку р выходитъ наружу. К е § п а и И нашелъ слѣдую-
щія значенія для среднихъ теплоемкостей различныхъ газовъ межд}
20° и 200°:
теплоемкость при постоянномъ давленіи, отнесенная
къ равнымъ вѣсамъ къ равнымъ объемамъ
(для воды г^ = 1)
ср срд
Воздухъ 0,2375 ’ 0,2375
Азотъ •0,2438 0,2365
Кислородъ 0,2175 0,2405
Водородъ 3,4090 0,2359
Окись углерода .... 0,2450 0,2376
Окись азота 0,2317 0,2406
Закись азота 0,2262 0,3447
Хлоръ 0.1210 0,2964
Углекисл. газъ ... 0,2169 0,3307
Амміакъ 0,5084 0,2996
Сѣрнистый газъ. . . . 0,1544 0,3414
Метанъ 0,5929 0,3277
Этиленъ 0,4045 0,3909
Хлорист. этилъ С2НЪСІ . 0,2238 0,6096
Въ послѣднемъ столбцѣ помѣщены числа гдѣ <5 плотность газа
относительно воздуха, т.-е. теплоемкости равныхъ объемовъ
газа, причемъ эти объемы выбраны равными объему вѣсовой единицы
воздуха.
Числа послѣдняго столбца, относящіяся къ газамъ, далекимъ отъ на-
сыщенія, каковы Л4>> Ог, А/2, СО и ЛЮ, почти равны между собою. Это
даетъ намъ право высказать слѣдующій законъ:
Одинаковые объемы идеальныхъ газовъ облада-
ютъ при д а н н омъ давленіи одинаковою теплоемкостью.
Одинаковые объемы газовъ содержатъ, по закону квогадро (т. I),
208
Теплоемкость.
одинаковое число молекулъ, а потому изъ сказаннаго слѣдуетъ, что мо-
лекулярная теплоемкость всѣхъ идеальныхъ газовъ
одна и та же.
Для простыхъ двухатомныхъ газовъ отсюда получается такой резуль-
татъ: ат о м н ая т е пл о е м ко с т ь всѣхъ простыхъ двухатом-
ныхъ идеальныхъ газовъ одна и та же.
ср Атомный вѣсъ. Атомная теплоемкость.
о2 0,2175 16 3,480
0,2438 14 . 3,413
/У2 3,4090 1 3,409
Числа, полученныя Е. ѴѴіейетапп’омъ, оказываются большею
частью весьма близкими къ числамъ В е п а и И, если ввести поправку
на зависимость теплоемкости воды отъ температуры, которая была не
одна и та же у названныхъ наблюдателей.
По введеніи этой поправки получаются такія числа:
Ср между 0° и 200°.
Ке^паиИ. Е. ѴѴіесІетап и.
Воздухъ . . . - 0,2386 0,2391
Водородъ.... 3,424 3,413
Окись углерода . 0,2426 0,2461
Углекислый газъ . 0,2171 0,2175
Закись азота. . . 0,2272 0,2271
Этиленъ .... 0,4058 0,4186
Амміакъ .... 0,5106 0.5314.
Тишіігг (1900) нашелъ для водяного пара
ср = 0,4741.
Зависимость теплоемкости ср отъ температуры изслѣдовали Ве-
д’папіі и Е. ѴѴіейетапп. Ве^паиіі нашелъ что для воздуха
и водорода ср отъ температуры не зависитъ. Такъ онъ нашелъ
для воздуха среднія теплоемкости
отъ — 30° до -|- 10° ср = 0,23771
0° до 100° 0,23741
0° до 200° 0,23751,
Е. ѴѴіейетапп также нашелъ, что ср для воздуха, водорода и
окиси углерода отъ температуры не зависитъ. Тотъ же результать
подтвердилъ АѴ ііколѵзкі для воздуха при весьма низкихъ температу-
рахъ, пользуясь способомъ, подобнымъ способу Ве^паиіі и Е. АѴіе-
йетапп'а; но первоначально онъ измѣрялъ температуру газа помощью
термоэлемента. Онъ также нашелъ, что для воздуха ср до — 140° не за-
виситъ отъ і. НоІЬогп и А и 8 1 і п (1905) первые изслѣдовали тща-
тельно зависимость ср отъ температуры для V, О и воздуха; они также
Газы.
209
пользовались термоэлементомъ. Найденныя ими значенія средней теплоем-
кости ср были слѣдующія:
азотъ кислородъ воздухъ
между 20° и 440° 0,2419 0,2240 0,2377
между 20° и 630° 0,2464 0,2300 0,2426
между 20° и 800° 0,2497 — —
Между 0° и і° средняя теплоемкость ср равняется
ср = с0 (1 Н- 0,00004/).....................(4 , а)
Совершенно другой результатъ получается для газовъ, легко ожи-
жаемыхъ. К е § п а и 11 нашелъ для СО2
между — 30° и 10°
10° и 100°
4- 10° и 210°
ср = 0,1843
0,2025
0,2169
Отсюда можно найти теплоемкости ср при различныхъ температу-
рахъ для СО2: при 0° ср = 0,1870 100° 0,2145
200°
0,2396.
Съ повышеніемъ температуры величина ср быстро растетъ. Е. ѴПе-
й е т а п п даетъ такія формулы:
0° 100° 200°
Углекислый газъ. ср — 0,1952 4- 0,000229/ 0,1952 0,2169 0,2387
Этиленъ. . . . Ср = 0,3364 4- 0,000825/ 0,3364 0,4189 0,5015
Закись азота . . Ср = 0,1983 4- 0,000230/ 0,1983 0,2212 0,2442
Імміакъ.... ср — 0,5009 4- 0,000310/ 0,50ОУ 0,5319 0,5629
Разность величинъ ср при 0° и 200° доходитъ для этилена ДО 49%.
НоІЬогп и Неппіп^ также изслѣдовали СО2 и для ис тинной
теплоемкости ср при /° нашли слѣдующія значенія:
/—0° 100° 200° 400° 600° 800°
Ср = 0,2028 0,2161 0,2285 0,2502 0,2678 0,2815
Эти числа даютъ формулу:
ср = 0,2028 4- 0,0001384/ — 0,00000005/2.
НоІЬогп и Неппіп^ (1905) опредѣлили отношеніе среднихъ
теплоемкостей водяного пара (/? = 1 атм.) и воздуха и вычислили эту ве-
личину для водяного пара, принимая для воздуха формулу (43,а) и под-
ставляя между 20° и 200° число Ке^паиН 0,2355. Они получили
слѣдующія числа:
водяной паръ водяной паръ
между воздухъ
ПО0—270° 1,940 0,4639
110°—440° 1,958 0,4713
КУРСЪ ФИЗИКИ 0 ХВОЛЬСОНА. Т. Ш, нзд. 3-е. 14
210
Теплоемкость.
между
110°— 620°
110°—820»
водяной паръ
воздухъ
1,946
1,998
водяной паръ
0,4717
0,4881
Въ позднѣйшей работѣ НоІЪогп и Неппіп§ опредѣлили ср для
СО2, и ВОДЯНОГО пара до 1400°. При 1400° они получили для углекислаго
газа 0,303 (0,201 при 0»), для азота 0.288 (0.235 при 0°) и для водяного
пара 0,668 (0,469 при 0°).
Зависимость теплоемкости ср отъ давленія р была изслѣдована
Ве^папіі для воздуха, водорода и СО2. Оказалось, что теплоем-
кость ср названныхъ газовъ отъ давленія не зависитъ.
Однако, опыты <Іо1у, о которыхъ будетъ сказано ниже, уже заставляютъ
усомниться въ справедливости этого результата и ему совершенно проти-
ворѣчатъ результаты опытовъ Ь и 8 8 а п а, опубликованныхъ въ рядѣ ста-
тей, начиная съ 1894 г. Приборъ Ьи8 8апа состоялъ изъ двухъ же-
лѣзныхъ цилиндровъ А и В, изъ которыхъ первый содержалъ испытуе-
мый газъ, второй былъ наполненъ ртутью. Поднимая и опуская попе-
ремѣнно тотъ или другой цилиндръ, можно было перегонять газъ изъ
А въ В и обратно, причемъ газъ проходилъ черезъ нагрѣватель и черезъ
калориметръ при своемъ теченіи изъ А въ В; обратно изъ В въ А онъ
проходилъ непосредственно. Въ первыхъ опытахъ Ьи88апа доводилъ
давленіе газа въ приборѣ до 45 атмосф., изслѣдуя воздухъ, водородъ, ме-
танъ, углекислый газъ, этиленъ и окись азота. Онъ нашелъ, что для
всѣхъ газовъ теплоемкость ср быстро растетъ при увеличеніи давленія р,
и что ср можетъ быть выражено эмпирической формулой
ср = а ф- Ь(ѵ — 1).................. . . (44)
Значеніе постоянныхъ а и Ь слѣдующее:
а Ь
Воздухъ. . . 0,23707 0,001498
Водородъ . . 3,4025 0,013300
Метанъ . . . 0,5915 0,003463
а Ь
Углек. газъ . 0,20130 0,0019199
Этиленъ . . 0,40387 0,0016022
Окись азота . 0,22480 0,0018364.
Давленіе р выражено въ атмосферахъ. Эти числа даютъ слѣдую-
щее возрастаніе величины ср въ процентахъ при увеличеніи давленія отъ
1 атмосф. до 41 атмосф.:
Воздухъ..............21%
Водородъ...........15°/0
Метанъ...............23%
Углекисл. газъ . . . 38%
Этиленъ................12%
Окись азота .... 33%
Для теплоемкости ур единицы объема Ьи $ 8 апа даетъ формулу вида
7р = а' + Ь' (р — 1) + с‘(р — I)2...........................(45)
гдѣ напр. для воздуха а' — 0,00039078, Ь'= 0,00027523, С'~ 0,0000020614
Измѣнивъ нѣсколько устройство своего прибора, Ьи.88апа изслѣ-
довалъ Ср при давленіяхъ, доходившихъ до 106 атмосф. и при темпера-
Газы.
211
бурахъ отъ 73° до 210°. Первый рядъ опытовъ при 78° и давленіяхъ отъ
31,5 103,25 атм. далъ для воздуха формулу
ср = 0,23702 + 0,0015504(р 1) — 0,0000019591(р — I)2.
Если результаты этихъ работъ окажутся достовѣрными, то они бу-
дутъ имѣть весьма большое значеніе. Ьиззапа изслѣдовалъ также
(1896) ср для углекислаго газа при различныхъ і и р. Приводимъ нѣко-
торыя изъ чиселъ для ср (р выражено въ атмосферахъ):
р 13,2° 38,0° 67,6° 98,1° 114,9°
24,25 — 0,2882 0,2465 — —
54.10 0.7301 0,3257 0,2753 — —
61,70 0,8900 0,4384 0,3227 0.3172 0,3133
75,80 1,4713 0,7325 0,4842 0,4615 0,3854
85,40 2,1096 0,9954 0,5972 0,5324
86,90 — — 0,6832 — —
Въ позднѣйшей работѣ (1897) Ьиззапа получилъ вообще нѣсколько
меньшую зависимость ср отъ р.
Молекулярныя теплоемкости = рсрп ср7Ѵ—р,сѴ1 гдѣ//
молекулярный вѣсъ. На стр. 208 уже было указано, что идеальные газы
имѣютъ одинаковую молекулярную теплоемкость. Помножая атомныя
теплоемкости кислорода, азота и водорода на 2, получаемъ молекулярныя
теплоемкости при постоянномъ давленіи:
(?2 ^2 ^2
с^р = 6,96 6,83 6,82
Другія числовыя величины будутъ приведены ниже. Величина срр ==
= рср растетъ съ температурою, какъ и ср. ЪеСЬаіеІіег полагаетъ,
что для всѣхъ газовъ и паровъ можно положить
р,р 6,5 -р- аТ......................(46)
гдѣ Т абсолютная температура и а постоянная, которая для //2, /Ѵ2, О2 и
СО близка къ 0,0010; для болѣе сложныхъ газовъ а больше этого числа, напр.
СО2 С2Н± СНСІэ (С2НЪ\О
(эфиръ)
а = 0,0071 0,0084 0,0137 0,0305 0,0510 0,0738.
Формула (46) даетъ при очень высокихъ температурахъ весьма боль-
шія числа для молекулярныхъ теплоемкостей. Мы познакомимся въ слѣ-
дующемъ параграфѣ съ опытами, которые для ср,ѵ дѣйствительно даютъ
большія числа при очень высокихъ температурахъ. Связь между срр и
по крайней мѣрѣ для идеальныхъ газовъ, дана формулою (33) стр. 201.
Общій вопросъ о теплоемкости паровъ будетъ разсмотрѣнъ
впослѣдствіи.
§ 13. Теплоемкость газовъ при постоянномъ объемѣ. Всѣ спо-
собы опредѣленія теплоемкости сѵ могутъ быть раздѣлены на три группы.
14*
212
Теплоемкость.
Къ группѣ I относится опредѣленіе сѵ на основаніи вычисленія прй По-
мощи формулы, опредѣляющей величину разности ср — сѵ; эта формула
даетъ сѵ, когда ср извѣстно. Группу II составляютъ непосредственныя
опытныя измѣренія величины сѵ. Къ группѣ III мы относимъ всѣ спо-
собы опытнаго опредѣленія величины к — ср : сѵ\ зная к и ср мы най-
демъ сѵ. Въ этомъ параграфѣ мы разсмотримъ только первыя двѣ группы.
I. Опредѣленіе сѵ на основаніи формулы для ср — сѵ.
Для идеальныхъ газовъ мы имѣемъ формулу, см. (28) и Г29) стр. 200,
0,0688
Сѵ — ср ^4/? — ср ...........(47)
гдѣ д плотность относительно воздуха. Принимая для воздуха ср — 0,2388,
получаемъ для него (<5 = 1) сѵ = 0,2388 0,0688 = 0,1700.
Такимъ же образомъ мы вычислимъ сѵ и для нѣкоторыхъ другихъ
газовъ; зная ср и сѵ, мы можемъ вычислить к = ср : сѵ, а слѣд. также
отношеніе энергіи поступательнаго движенія ко всему запасу энергіи
У въ газѣ, пользуясь формулой. (37) стр. 202.
Такимъ образомъ получаются напр. слѣдующія числа:
й ср сѵ к = с-р- Сѵ ' У 3 = -(А-1).
Воздухъ . . . 1 0,2388 0,1700 1,404 0,606
Кислородъ . . 1,1056 0,2185 0,1563 1,398 0,597
Азота .... 0,9713 0,2446 0,1738 1,407 0,611
Водородъ . . . 0,0693 3,4240 2,4269 1,408 0,614
Окись углерода . 0,9678 0,2442 0,1732 1,410 0,615.
Ве^паиіі и Е. \Ѵ і е а е ш а п п нашли : что ср для воздуха, во-
дорода и окиси углерода отъ температуры не зависитъ. Формула (47)
показываетъ, что и сѵ для названныхъ газовъ отъ темпера-
туры не зависитъ. Для СО2 и другихъ газовъ ср растетъ съ тем-
пературою; соотвѣтственно должно расти и сѵ, если только формула (47)
къ даннымъ газамъ приложима. Числа Е. \Ѵ іе сіе таи п’а, приведенныя
на стр. 209, даютъ
сѵ к ''и. У •
Углекислый газъ . . - I 0° 100° 0,1493 0,1722 1,303 1,263 0,4545 0,3945
Закись азота . . . . I 0° 100° 0,1530 0,1760 1,295 1,256 0,442 0,384
Амміакъ I 0° 1 100° 0,3853 0,4163 , 1,299 1,277 0,448 0,413
Этиленъ ..... ^ ( 0° 1000 0,2658 0,3483 1,266 1,202 0,399 0,303.
Еслибы независимость ср отъ р, найденная Ве^паиіі. дѣйстви-
Газы.
213
тельно имѣла мѣсто, то на основаніи формулы (47) и сѵ должно было бы
быть независимымъ отъ р. Если вѣрны результаты, найден-
ные Ьиззапа, то сѵ должно расти вмѣстѣ съ да-
вленіемъ р.
Формула (33) даетъ приближенно
С[Л,Ѵ — СП,р
Числа для приведенныя на стр. 212, даютъ для молеку-
лярной теплоемкости при постоянномъ объемѣ:
О2 ТѴ2 Я2
4,96 4,83 4,82.
формула (46) приложима только къ газамъ, мало отклоняющимся
отъ законовъ Бойля и Гей-Люссака. Ниже будетъ выведена фор-
мула, относящаяся ко всѣмъ тѣламъ природы, а именно:
л^(іѵ (ір
ср ~ Сѵ ~ АТ аі аі...................
гдѣ А, какъ и въ (47), термическій эквивалентъ тепла, Т абсолютная темпе-
ратура.
Р ’
Для идеальныхъ газовъ рѵ=К1, откуда ѵ — ,р — — ,— =
ар п р- ѵ ѵ <и
-г. — —, и слѣд. ср — сѵ — АТ —= АП (такъ какъ РТ сокра-
Ссь О рі)
щается съ рѵ), т.-е. получается (47). Согласно принятому нами обозна-
ченію, имѣемъ (стр. 129)
(іѵ йр
ІЙ — ѵ0иѵ — Роар ’
гдѣ ѵ0 и р0 относятся къ 0°, а0 коеффиціентъ объемнаго расширенія,
ар термическій коеффиціентъ давленія. Вмѣсто (47) можемъ написать
ср — сѵ = АТѵорйаѵар..............(49)
Пользуясь формулою (48) или (49), можно вычислить одну изъ те-
о (іѵ (ір
плоемкостеи ср или сѵ, если извѣстны другая и величины ., и .
іл/і/ аі1
Такъ поступали Ата^аі и АѴііко^ькі, какъ мы увидимъ ниже.
II. Непосредственное опытное опредѣленіе ве-
личины сѵ. Такія опредѣленія были сдѣланы о 1 у при среднихъ,
МаІІагсГомъ и Ье СЬаѣеІіег и др. при очень высокихъ темпе-
ратурахъ.
Л) Опыты Лоіу. На стр. 187 мы изложили принципъ парового
калориметра и описали приборъ Випзеп’а. Пользуясь тѣмъ же прин-
ципомъ, Я о 1 у построилъ дифференціальный паровой калориметръ, при
помощи котораго онъ измѣрялъ теплоемкость сѵ газовъ, опредѣляя коли-
чество тепла, потребнаго для ихъ нагрѣванія, когда они находятся въ
замкнутомъ со всѣхъ сторонъ пространствѣ, а именно внутри полаго ме-
214
Теплоемкость.
таллическаго шара. Приборъ Л о 1 у изображенъ на рис. 80. Къ коро-
мыслу весьма чувствительныхъ вѣсовъ привѣшены два тонкостѣнные мѣд-
ные шара, емкостью каждый около 158 куб. см. и вѣсомъ въ 92,2 гр. Ихъ
теплоемкости сдѣланы совершенно равными при помощи маленькихъ ку-
сочковъ мѣди, прибавленныхъ къ тому изъ нихъ, теплоемкость котораго
Рис. 80.
сперва оказалась меньшею. Въ одинъ изъ ша-
ровъ накачивался газъ до давленія въ 27 м. ртут-
наго столба; изъ другого шара выкачивался воз-
духъ или онъ наполнялся газомъ при нормальномъ
давленіи. Оба шара вводились въ паровую камеру
и затѣмъ на вѣсахъ опредѣлялась разность р вѣ-
совыхъ количествъ воды, осѣвшихъ на шарахъ.
Эта разность отдала свою скрытую теплоту рк на
нагрѣваніе газа, ибр для нагрѣванія шара и дру-
гихъ придаточныхъ частей требуются одинаковыя
количества теплоты съ той и другой стороны.
Если і первоначальная температура шаровъ, Т тем-
пература пара и д разность вѣсовыхъ количествъ
газа, содержащихся въ двухъ шарахъ, то имѣемъ,
см. (22) стр. 187, дсѵ (Т — і) = рА, откуда и полу-
чается искомая теплоемкость сѵ. Я о 1 у нашелъ
для воздуха и углекислаго газа довольно быстрое
возрастаніе величины сѵ съ давленіемъ. Для воз-
духа онъ далъ эмпирическую формулу сѵ —
= 0,17151 + 0,02 788р, гдѣ о плотность воздуха от-
носительно воды, такъ что р = 0,001293 при давленіи въ одну атмос-
феру. Для СО2 ЭГоІу далъ сперва формулу сѵ = 0,16577 + 0,2064р, а
потомъ болѣе сложную сѵ = 0,1650 4“ 0,2125р + 0,3400р2, гдѣ р плот-
ность этого газа относительно воды. При давленіи въ 1 атмосф*. получа-
ется сѵ = 0,1654; при 21,66 атмосф. сѵ = 0,17386. Опыты съ водо-
родомъ обнаружили малую зависимость сѵ отъ давленія. Мы упомянули
на стр. 214, что А т а § а 1 и \ѴіікоіѴ8кі воспользовались форму-
лою (48) для вычисленія величины ср. Опыты 3 о 1 у даютъ сѵ при вы-
сокихъ давленіяхъ, при которыхъ ср опредѣляется не легко. Пользуясь
эмпирической формулой для сѵ, которую <1 о 1 у далъ для СО2 и сооствен-
V (ІѴ йр к .
ными опредѣленіями величинъ -77 и , Ашааі вычислилъ ср и к =
ср : сѵ при различныхъ температурахъ (до 100°) и при давленіяхъ до
200 атмосф. Оказалось, что при 50° величина ср имѣетъ максимумъ
около 100 атм., а именно ср — 1,4161. При тѣхъ же температурѣ и дав-
леніи величина А достигаетъ весьма большого значенія к — 4,633. ѴѴіі-
ко\ѵ8кі вычислилъ сѵ для воздуха при различныхъ р, пользуясь
формулою
(Г*®
(ір
— АТ а? • •
. (50)
Газьт.
215
которая будетъ выведена въ главѣ, посвященной основамъ термодина-
мики. Затѣмъ онъ при помощи формулы (48) нашелъ сѵ и наконецъ к
для различныхъ і и различныхъ плотностей д воздуха, отнесенныхъ къ
нормальной плотности (0° и 760 мм.). Вотъ нѣкоторыя изъ его чи-
селъ для к
<5 = 10 30 60 100
0° 1,42 1,44 1,53 1,60
— 60° 1,42 1,49 1,58 1,72
— 100° 1,44 1,53 1,71 2,10
— 120° 1,45 1,56 1,79 —
— 140° 1,38 1,46 1.54 1,80.
Повидимому, к достигаетъ максимума при —120°. Ьіпсіе также
вычислилъ ср для в о з д у х а при низкихъ і и большихъ р. Полагая
ср — 0,237 при і = 0° и р = 1 атм., онъ находитъ напр. ср = 0,846
при і = — 100° и р = 70 атм.
В) Опыты МаПагсі’а и Ье Сііаіеііег и др. Теплоемкость
сѵ при весьма высокихъ температурахъ опредѣляли М а 11 а г сі и
Ье СЬаіеІіег путемъ наблюденія максимальнаго давленія взрывчатыхъ
газовыхъ смѣсей во время взрыва. Это давленіе даетъ возможность вы-
числить температуру,* а отсюда и теплоемкость смѣси, такъ какъ количе-
ство тепла, выдѣляющагося при взрывѣ, извѣстно на основаніи термохи-
мическихъ изслѣдованій. Примѣшиванія одинаковыхъ объемовъ О2, Л/2,
Н2 или СО ко взрывчатой смѣси (напр. гремучему газу) дало одинако-
вое пониженіе максимальной температуры, откуда слѣдуетъ, что тепло-
емкость сѵ этихъ газовъ одинаковая до 2700°. При обыкновенной
температурѣ молекулярная теплоемкость этихъ газовъ приблизи-
тельно равна (см. стр. 213)
сціѵ = 4,9.
М а 11 а г д и Ье Сйаіеііег нашли, что сѵ не зависитъ отъ да-
вленія, даже если послѣднее доходитъ до 6000 атмосф. Ьъ температу-
рою і теплоемкость с^ѵ быстро возрастаетъ по слѣдующимъ формуламъ:
О2, /Ѵ2, Н2, СО. , с^ѵ = 4,8 4- 0,0006/
СО2...............с^ѵ = 6,50 4- 0,00774/
Н2О (паръ) . . . С^ѵ = 5,78 4- 0,00572/.
Ѵіеіііе и Вегіііеіоі въ общемъ подтвердили эти результаты;
они находятъ при высокихъ температурахъ (/>>2000°)
для СО2 . ... Ср Ѵ = 19,1 +- 0,0030 (/ — 2000)
для Н2О (паръ) . с/ьѵ = 16,2 4“ 0,0038 (/ — 2000).
Формула МаПагсі’а и Ье Сйаіеііег даетъ для СО2
при 2000° . . . с^ѵ = 21,98
при 3000° . . . с ' = 29,72,
216
Теплоемкость.
между тѣмъ какъ формулы Ѵіеіііе’а и ВегіЪеІоІ (1884) и Ьап-
§* еп’а (1903) даютъ при тѣхъ же двухъ температурахъ числа 19,1 и 22,1.
Изъ опытовъ Е. ЛѴіейета пп’а (стр. 213) получается для СО2
при 0° и 100° теплоемкости = 6,54 и 7,48, что хорошо согласуется
съ формулою М а 11 а г (Га и Ь е Сііаіеііег, дающей соотвѣтственно
числа 6,50 и 7,27.
§ 14. Опытныя опредѣленія величины к = ср : сѵ. Если для дан-
наго газа возможно непосредственными опытами найти величину &, то
мы будемъ знать сѵ, если величина ср была найдена.
Можно и непосредственно найти ср и сѴі если извѣстно к и если
можно допустить, что газъ по своимъ свойствамъ не слишкомъ удаля-
пг х 0,0688 ,
ется отъ идеальнаго газа. Мы видѣли, что ср —сѵ= $— см. (29)
стр. 200, гдѣ Л плотность газа относительно воздуха. Мы знаемъ далѣе,
что молекулярный вѣсъ р, — 28,88(5 (т. I), слѣд.
0,0688 X 28,88 1,987
Ср °ѵ ~ ' и. ~ р,
Пользуясь равенствомъ ср = ксѵ, получаемъ отсюда:
1,987
Сѵ “ 1)
_ 1,987/г
СР ~ — 1)
(51)
По этимъ формуламъ можно вычислить ср и если к найдено.
Примѣромъ послужитъ намъ ниже вычисленіе ср и сѵ для паровъ ртути.
Существуетъ нѣсколько способовъ опытнаго опредѣленія величины к\
мы ихъ разсмотримъ послѣдовательно.
I. Способъ СІетепЬ и Ееяогтея’а. Подробную исторію
этого способа изложилъ Мапепѵгіег. Вообразимъ нѣкоторое количе-
ство газа при первоначальномъ объемѣ г/0, давленіи р0 и абсолютной
температурѣ То. Измѣнимъ внезапно объемъ газа такъ, чтобы пере-
ходъ его въ новое состояніе, опредѣляемое величинами ѵ, р и Г, могъ
считаться адіабатическимъ. Затѣмъ доведемъ газъ до первоначальной
температуры То, нагрѣвая или охлаждая его при постоянномъ объемѣ ѵ.
Мы имѣемъ, такимъ образомъ, три состоянія газа
I ^0 Р)
П ѵ р
Ш ѵ Р1
I
Т I Переходъ адіабатическій.
70 ? Измѣненіе при пост, объемѣ.
Новое давленіе въ третьемъ состояніи обозначено черезъ рг. На-
блюдая три давленія р0, р и ръ можно вычислить к. При этомъ слѣду-
етъ отличать два случая, смотря по тому, произвели ли мы адіабатиче-
ское сжатіе или расширеніе. Въ первомъ случаѣ ѵ < г/0, слѣд. р > р0
и Рі > Ро, ибо въ I и Ш температуры одинаковы; далѣе Г > Го, ибо
Газы.
217
при сжатіи газъ нагрѣвается, поэтому рг < р. Полагая въ этомъ случаѣ
Ро = р — и Рі= Р — имѣемъ такую схему :
А. Газъ былъ подвергнутъ сжатію:
I А р0—р — И А
V А
П V р Т И>Ьі . . (Л)
V
Ш V Р1=Р—К А р0<Рі<р-
Неравенство И < Лх слѣдуетъ изъ р0 < Ръ т.-е. Р — к < р —
В Газъ былъ подвергнутъ расширенію. Легко сообра-
зить, что мы теперь имѣемъ такую схему:
і А Т0 1
А V
ц V Р Т И <111 А
ІП V Рі=Р + ^і А р0>Рі>р-
Мы дадимъ три вывода формулы, по которой вычисляется к по на-
блюденнымъ давленіямъ. Первый выводъ даетъ строго точную формулу;
онъ очень простъ, но основанъ на формулѣ Р о і 8 8 о п’а. Второй выводъ
не пользуется этой формулой, но зато онъ болѣе сложенъ; этотъ выводъ
обыкновенно приводится въ учебникахъ. Наконецъ мы предлагаемъ тре-
тій выводъ, который нѣсколько проще второго и, какъ кажется, даетъ по-
лезное для начинающихъ освѣщеніе разсматриваемой здѣсь манипуляціи.
Выводъ 1. Переходъ I — II адіабатическій, слѣд. по формулѣ
Роі8 8оп’а, см. (35) стр. 201, р$ѵ^ — рѵк. Состоянія I и III характе-
ризуются одинаковой температурой Го, слѣд. по формулѣ Бойля =
=р±ѵ. Эти два равенства даютъ
(2о\к—Р и ^0—а
\ V I р0 ѵ р ’
Р_ = /А ?
А \РоI ’
1„Р
к = ^= ................(62)
[А 1&А — 1Оо
Ро
откуда
и слѣд.
Формула (52) и есть вполнѣ точная формула для
Упрощая (52), мы отличимъ случаи (Л) и (В),
указано выше.
А. Случай сжатія: р$—р— А, Рі—Р —
ѵг = р^-\-И — отсюда имѣемъ
вычисленія к
на которые было
слѣд. р — р0 + к,
218
Теплоемкость.
Разлагая логариѳмы въ рядъ и останавливаясь на первыхъ членахъ,
, И И — кл
получаемъ к — ? : —~, или
Л == т.—тг .... . . (53)
Л—4 7
В. Случай расширенія :р0=/? +А,/?!=/? +слѣд./?=р0—
А=А + Аі—Л.
Аналогично предыдущему выводу найдемъ
И
" ......................(54)
Выводъ 2, обыкновенно приводимый въ учебникахъ. Обозначимъ
черезъ х повышеніе температуры газа при внезапномъ уменьшеніи его
объема на ~ -тую долю, гдѣ абсолютная температура газа ; такое умень-
7 о
шеніе объема какъ разъ равно увеличенію объема отъ нагрѣванія на 1°
при постоянномъ давленіи. Если килограмму газа при 70° придать коли-
чество тепла сѵ, не мѣняя его объема, то онъ нагрѣется до (70 + 1)°,
т.-е. на 1°. Если мы ему при р = СопвС придадимъ количество тепла ср,
то онъ также нагрѣется на 1°, а объемъ его увеличится на 2, -тую долю.
7 о
Сожмемъ его теперь до прежняго объема, т.-е. на -тую долю: онъ на-
7 о
грѣется еще на х°, т.-е. всего на (1 + х)°. Объемъ остался прежній,
но газъ получилъ количество тепла ср. Повышенія температуры должны
относиться, какъ полученныя количества тепла, т.-е. ср : сѵ = (1 Д- х) : 1,
откуда
к = 1 4- х...... . .... (а)
Обращаемся къ случаю (Д), схема котораго помѣщена на стр. 217.
( остоянія I и Ш даютъ по закону Бойля — —- — , откуда
Рі
Уо—ѵ^Рі—Ро
Рх
Переходъ отъ П къ Ш произошелъ при ѵ — Сопйѣ., слѣд.
‘ О Р1
откуда
Г— Г0 р — а
то Рі
(?)
При переходѣ отъ 1 къ Ц произошло относительное сжатіе, равное
ѵ0 — ѵ . „ „
-----, вызвавшее повышеніе температуры Т — 10, между тѣмъ какъ отно-
ѵо
сительное сжатіе 7, вызываетъ повышеніе температуры на х°. Приблизи-
ло
тельно можно считать малыя повышенія температуры пропорціональными от-
носительнымъ уменьшеніямъ объема, т.-е. положить (Т— 70): х : і .
г>0 /0
Газы.
219
Отсюда _ _
х= —
Въ силу (а), (/9) и (у), получаемъ отсюда х — к — 1 =-—— и
Рі—Ро
ь=Р^_Р2
Рі —Ро'
Но въ нашемъ случаѣ р0 — р — И; рѵ = р — и слѣд. к = ѵ~~, .
Пг іЪу
Такимъ образомъ, выведена формула (53) для случая (Л). Аналогично
легко вывести и (54) для случая {В).
Выводъ 3. Предположимъ, что опять имѣемъ дѣло съ случаемъ (Л),
когда сперва сжатіе вызвало нагрѣваніе газа, а потомъ газъ охладился до
первоначальной температуры. Пусть полное количество тепла, отдан-
ное газомъ при переходѣ отъ первоначальнаго состоянія I къ окончатель-
ному ПІ. Легко найти два выраженія для (^. Переходъ отъ I къ II про-
изошелъ адіабатически, т.-е. безъ теплового обмѣна между газомъ и окру-
жающими предметами. При переходѣ отъ 11 къ III газъ при ѵ — Соп$1.
охладился отъ Т до Го; слѣд.
<2 = ^(Г—Го)....................(а)
Можно непосредственно перейти отъ I къ ПІ, сжимая газъ при
постоянной температурѣ Го отъ объема г/0 до объема ѵ. Приблизительно
(см. ниже точнѣе) можно принять, что это малое сдавливаніе произошло
при постоянномъ давленіи р0; работа г, которая при этомъ была произ-
ведена, равна г — (т>0 — ѵ)р0 = роѵо = - - гдѣ /? постоян-
но--------------------------------------п0
ная формулы рѵ = РТ. Очевидно ф = Лг = Л/?Г0 Ѵ . По закону
По
О е V Ръ -- V Рі--Ро т. ДО
Ь о и л я — = —, откуда---= ~. Вставляя эту величину и АН —
ѵо Рі н0 ру
— Ср— сѵ, получаемъ
Сѵ)го^о . ,...........
Рі
Сравнивая это съ (а), имѣемъ сѵ (Т — То) (с„ — сѵ}Т0~—От-
г ' Рі
сюда
то Рі —Ро
тт Р ѵ Т — То р — рл
Но-^ = —, слѣд. —---------і-і; отсюда
10 Рі 'О Рі
к-і=Р^Ру. Рт^=Р^Рі . . М
Рі Рі— Ро Рі— Ро
и і.
к=Р_Т^Ро^=
Рі—Ро к — ЬІ
220
Теплоемкость
Коли для работы г принять болѣе точное выраженіе г — — =
Ро
— , то отсюда получилось бы приближенное выраженіе
Ро
г = 11 + = /?7о ,
\ Ро ) Ро
и для <3, вмѣсто (/9),
^ = (ср~-сѵ)ТоР^~Ро
Ро
Это даетъ, вмѣсто (у),
к І = Р^Р1 = ѣ. р-н
Рі—Ро'Рг Ь Нір — Ігі
Второй множитель можно принять рапнымъ единицѣ, ибо И и Н1
малы сравнительно съ р (при умноженіи пренебрегаемъ величинами 1гкг
и Ах2 сравнительно съ рк и рк^, и тогда получается для к прежнее выраженіе.
Н. НегЬг далъ болѣе глубокій анализъ опытовъ Сіе тепѣ и І)е-
богтее’а, разсматривая болѣе общій случай, чѣмъ тотъ, который соот-
вѣтствуетъ этимъ опытамъ. Разборъ Н. Н е г і г’а помѣщенъ въ учебникѣ
физики А. ХѴиеІІп ег’а (ЬейгЬисЬ йег ЕхрегітепіаІрЪувік), изд. 5-ое, Т. И.
(Сіе Ьеііге ѵоп йег ДѴаегте) 1896 г. стр. 541 и 543. Теоріей способа
С1 е шеп і и В е 8 о гш е 8’а занимался такж^ Рлѵуп^ейа\ѵ. Приборъ
Гіетепі и Вевогте 8’а, въ которомъ приблизительно происходятъ два
измѣненія состоянія газа, указанныя въ схемѣ (А), стр. 217, такъ что к
можетъ быть вычислено по формулѣ (53) стр. 218, изображенъ на рис. 81.
Онъ состоитъ изъ большого шаровиднаго/' стекляннаго сосуда, снабжен-
наго горлышкомъ съ металлической оправой. Краны г и пг даютъ воз-
можность соединять шаръ съ внѣшнимъ воздухомъ. Сбоку находится ма-
нометръ. За крывъ
кранъ г, вытягиваютъ черезъ ш немного воздуха изъ
шара, вслѣдствіе чего въ манометрѣ поднимается ве-
щной столбъ высотою к. Теперь воздухъ обладаетъ
объемомъ т/0, равнымъ емкости шара, температурою
Го окружающаго пространства и давленіемъ /?0 =
— р — Л, гдѣ р барометрическое давленіе, выражен-
ное высотою водяного столба. Впрочемъ р не вхо-
дитъ въ окончательную формулу, изъ которой видно,
что к и Лг могутъ быть измѣрены въ произвольныхъ
единицахъ. Затѣмъ открываютъ кранъ г; внѣшній
воздухъ устремляется во внутрь шара; вслѣдствіе
чего находящійся въ немъ воздухъ сжимается до
меньшаго объема г/, а температура возрастетъ до Г,
когда давленіе внутри шара сдѣлается равнымъ барометрическому р, т.-е.
когда вода въ трубкѣ манометра будетъ имѣть высоту нуль. Въ этотъ
моментъ закрываютъ кранъ г. Наконецъ воздухъ охлаждается до перво-
Газы.
221
начальной температуры 70, безъ измѣненія объема т/; давленіе дѣлается
равнымъ Рі= р — А1? гдѣ А3 вновь указывается манометромъ.
Въ одномъ изъ своихъ опытовъ С1 е т епI и В е8ог те 8 наблю-
дали А = 188 мм., Ах = 49 мм. Это даетъ по формулѣ (53)
188 _188_1
188—49 І39
Изложенный способъ по разнымъ причинамъ не можетъ дать точ-
ныхъ результатовъ. Сжатіе не происходитъ вполнѣ адіабатично и газъ
успѣваетъ потерять нѣкоторое количество тепла до момента закрытія
крана г. Вслѣдствіе этого въ шаръ входитъ больше воздуха, чѣмъ бы
слѣдовало, и р1=р — Аг получается слишкомъ большимъ, слишкомъ
малымъ, а потому и А слишкомъ малымъ. Далѣе фэрмула (53), какъ
мы видѣли, приближенная: оказывается, что она также даетъ слишкомъ
малое А. Наконецъ, весьма трудно уловить моментъ, когда давленіе внутри
шара равно барометрическому р. Воздухъ, врываясь во внутрь шара,
доводитъ давленіе до величины, которая больше р; вслѣдствіе этого начи-
нается обратное движеніе воздуха и вообще цѣлый рядъ колебаній давленія.
Способомъ Сіетепі и О е 8 о г т е з’а пользовались прежде всего
Сгау-Ьи88ас и ЛѴеІіег, ЛѴеівЪасІі, Нігп, Ма88оп и Б г е 8 е г.
Они пользовались способомъ {В) (стр. 218), при которомъ начальное да-
вленіе рв газа больше атмосфернаго р, такъ что происходило адіабатиче-
ское расширеніе газа. Вычисленіе производилось по точной формулѣ (52),
которая въ этомъ случаѣ даетъ
к = Ш = \%(р + К) — \$р
Ш Ш (ЛИ) —(р + Аі) *
Ѳау-Ьп88ас и XV е И е г нашли такимъ способомъ для воздуха А = 1,376,
ЛѴеІ8ЬасЬА = 1,4024, Нігп А = 1,3845; Мая8о п для воздуха А = 1,419
для углекислаго газа А = 1,30. I) г е 8 е г получилъ для воздуха А = 1,425
пользуясь ртутнымъ манометромъ.
Сагіп нашелъ, что числовое значеніе, получаемое для А, зависитъ
отъ времени г, втеченіе котораго остается открытымъ кранъ сообщающій
сосудъ со внѣшнимъ воздухомъ. Увеличивая постепенно г отъ весьма
малыхъ значеній, онъ замѣтилъ, что для А получаются сперва непра-
вильно колеблющіяся значенія, затѣмъ величины постоянныя и, наконецъ,
при дальнѣйшемъ увеличеніи г, числа для А начинаютъ убывать. С а г і п
принялъ для А тѣ числа, которыя въ нѣкоторыхъ предѣлахъ измѣненія
времени т остаются постоянными. Такимъ образомъ онъ нашелъ:
к к
Воздухъ . 1,41 Амміакъ . . . . 1,328
Кислородъ . . . . . 1,41 Углекислый газъ . . 1,291
Азотъ . 1,41 Закись азота. . . 1,285
Водородъ . . . . 1,41 Сѣрнистый газъ. . 1,262
Окись углерода , . 1,41 Этиленъ , . . . 1,257
222
Теплоемкость
КоЫгаизсЬ и Коепѣ^еп измѣряли постепенно мѣняющееся
въ сосудѣ давленіе, при помощи прибора, основаннаго на принципѣ ме-
таллическаго барометра; Воепі^еп слѣдилъ за показаніями этого при-
бора, снабженнаго зеркальцемъ, при помощи трубы и шкалы. КоЫ-
гаивсЬ получилъ для воздуха слишкомъ малое число к = 1,302. Весьма
тщательно произведенные опыты Воепі^еп’а дали для воздуха к =
= 1,4053; для СО2 к = 1,3052.
Видоизмѣненіе этого способа представляютъ опыты Р а ц п е I, ко-
торый сжималъ воздухъ ртутью, внезапно вступающей въ сосудъ. Его
опыты дали для воздуха к = 1,4083.
II. Способъ Аззшапп’а и Р. Миеііег’а. Представимъ себѣ
17-образную трубку, оба колѣна которой содержатъ ртуть; заставимъ
ртуть совершать малыя колебанія внутри неподвижно установленной
трубки, и пусть Т время колебанія. Если на обѣ вѣтви трубки наса-
дить полые стеклянные шары, открытые снизу, такъ что ъоздухъ надъ
ртутью и воздухъ въ соотвѣтствующемъ шарѣ составитъ замкнутое цѣ-
лое, то время колебанія ртути будетъ иное, ибо колебаніе будетъ сопро-
вождаться поперемѣннымъ сжатіемъ и разрѣженіемъ каждой изъ двухъ
массъ воздуха, находящихся надъ ртутью. Обозначимъ новое время ко-
лебанія черезъ Тх, Допуская адіабатичность сжатій и разрѣженій воз-
духа, можно доказать, что
гдѣ ѵ объемъ газа въ каждой изъ вѣтвей, р его упругость и д площадь
поперечнаго сѣченія трубки. Если объемы и ѵ2 съ щухъ сторонъ не
равны, то вмѣсто ѵ слѣдуетъ вставить 2ѵгѵ2\(ѵу + т/2). Опыты Р. Миеі-
іег’а дали для воздуха к= 1,4046, углекислаго газа 1,265, НСІ— 1,398,
8О2— 1,256, 8Н2 — 1,276, — 1,262, С2Н±- 1,243. Весьма подроб-
ное опытное и теоретическое изслѣдованіе этого метода произвелъ Нагѣ-
тапп (1905).
Ш. Способъ Ьиттег’а и Ргіп^вііеіт’а. Для адіабати-
ческихъ измѣненій состоянія газа были выведены формулы рѵк — РуѴук
и Тѵк~г = (см. т. I). Изъ этихъ двухъ формулъ получается связь
между упругостью и абсолютной температурой
Эта формула даетъ
(55)
Ьишшег и Ргіпдвііеіт помѣстили мѣдный полый шаръ (ем-
кость 90 литровъ) въ большой сосудъ съ водою; внутри шара находился
Газы.
223
весьма чувствительный болометръ (т. II) для измѣренія температуръ.
Температура Т газа, наполнявшаго шаръ, была извѣстна (температура
воды), равно какъ и его давленіе р, которое было больше атмосфер-
наго рг. Шаръ внезапно открывался, давленіе дѣлалось равнымъ ръ а
температура, измѣряемая болометромъ, равной 7\. Вводя всѣ необходи-
мыя поправки, названные ученые нашли (1898) для /г, вычисленнаго по
формулѣ (55), слѣдующія числа:
Воздухъ Кислородъ. Углекисл. газъ. Водородъ.
к = 1,4025 1,3977 1,2995 1,4084.
Макоуѵег (1903) нашелъ по этому способу для водяного пара
к = 1,305 и для воздуха к = 1,401.
IV. Способъ Лашіп’а и Кі ска г (Га. опредѣленное количе-
ство газа, абсолютная температура котораго Го, объемъ ^0, давленіе /?0,
нагрѣвается платиновою проволокою, черезъ которую проходитъ электри-
ческій токъ, втеченіе опредѣленнаго времени, одинъ разъ при постоян-
номъ объемѣ, причемъ получается температура 7\ и давленіе рг (объемъ г>0),
другой разъ при постоянномъ давленіи, причемъ температура дѣлается
равной 72, объемъ (давленіе /?0). Количество тепла, отданное прово-
локой газу въ обоихъ случаяхъ одинаковое, а потому имѣемъ сѵ (Тх Го) =
= ср (?2 — То), откуда
гг, "Г РоРр -г А А 'Г № . гугртптгя
Ко /о —— у 12 р^ » отсюда
к __ (А — а) А
(А—^о)Ро'
Яатіп и Кісііагсі нашли слѣдующія числа:
Воздухъ. Водородъ. Углекисл. газъ.
к = 1,41 1,41 1,29.
V. Способъ, основанный на опредѣленіи скорости
звука. Въ т. П была выведена формула для скорости V звука:
гдѣ р упругость газа, т.-е. давленіе на единицу поверхности, выражен-
ное въ единицахъ вѣса (силы), д масса единицы объема газа, и к =
= ср : сѵ. Зная скорость звука въ газѣ, можно найти к по формулѣ
к = — V2 = ~ V2.........................(56)
Р ёР
гдѣ § ускореніе силы тяжести, О вѣсъ единицы объема газа. Для воз-
духа при 0° и 760 мм. давленія имѣемъ, принявъ метръ и килограммъ
224
Теплоемкоеіѣ.
за единицы длины и вѣса, 9,81, р = 10333, О= 1,293; для скорости звука
м
примемъ среднее число изъ наилучшихъ наблюденій — І/= 331,74 --
сек.
при 0°. Вводя эти величины въ (56), получаемъ для воздуха к = 1,4047.
Если принять Ср = 0,2350, то получимъ сѵ = ср : к = 0,1673.
Числа Ке^паиіі для скорости звука въ другихъ газахъ даютъ:
Н2 СО2 Ы2О ЬН*
к = 1,396 1,368 1,361 1,239.
1Э и 1 о п для сравнненія скоростей звука въ различныхъ газахъ за-
ставлялъ одну и ту же трубу (длина волны Л = соп8І.) звучать, наполняя
ее различными газами, и опредѣлялъ отношеніе чиселъ колебаній получа-
емыхъ тоновъ, которое равно отношенію скоростей V и Ѵр Онъ на-
шелъ такимъ способомъ для воздуха к — 1,405, для водорода к = 1,394,
для углекислаго газа к = 1,326, для этилена к = 1,228. Отношеніе V: Ѵ±
можетъ быть опредѣлено и по способу пыльныхъ фигуръ КипсІГа (т. II)
и этимъ способомъ нынѣ наиболѣе часто пользуются для опредѣленія ве-
личины к, а затѣмъ иногда и величинъ ср и сѵ при помощи формулъ (51)
стр. 217. Кипсіі и АѴагЬиг^ опредѣляли по этому способу к для
ртутныхъ паровъ и нашли к — 1,666 или к = 1,675, если ввести
одну поправку, указанную йігескег’омъ. При помощи формулъ (51)
стр. 217, втэ которыхъ = 200, получаются отсюда для паровъ ртути
ср = 0,0247; сѵ = 0,0148.
На стр. 202 мы видѣли, что для одноатомныхъ газовт> к = 1.666 :
плотность ртутныхъ паровъ, какъ извѣстно, указываетъ на ихъ одно-
атомность, и мы видимъ, что опыты К и и (1 Га и АѴ а г Ь и г ^’а впол нѣ
подтверждаютъ этотъ выводъ. Отсюда слѣдуетъ, что въ парахъ ртути
вся энергія движенія заключается въ энергіи поступательнаго движенія
атомовъ. Энергія вращательнаго движенія атомовъ или вовсе не суще-
ствуетъ, или ничтожно мала, или отъ температуры не зависитъ.
К а і 8 е г пользовался способомъ пыльныхъ фигуръ К и п (1 Га, изу-
чая вліяніе ширины трубы на скорость въ ней звука; это вліяніе было
еще замѣтно даже при ширинѣ трубы, равной 82 мм. Производя опыты
съ различно широкими трубами, Каівег могъ исключить вліяніе ши-
рины. Для воздуха онъ нашелъ к — 1,4106.
АѴиеІІпег опредѣлялъ тѣмъ же способомъ к для воздуха. СО,
СО2, А^О, и С2Н± при 0° и при 100°. Онъ нашелъ слѣдующія числа:
Воздухъ. СО со2 Ы2О Л^З С2Я4
0° 1,40526 1,4032 1,3113 1,3104 1,3172 1,2455
100° 1,40513 1,3970 1,2843 1,2745 1,2791 1,1889.
Во всѣхъ случаяхъ к уменьшается съ повышеніемъ температуры;
для воздуха к повидимому отъ температуры не зависитъ.
Зігескег изслѣдовалъ А", С/, 23г, СІИ, ВгН. СМ и 5г/, опре-
Газы.
225
дѣлилъ для нихъ к и, по формулѣ (51) стр. 117, ср и сѵ. Напр. для па-
ровъ Вг онъ нашелъ к = 1,293, что даетъ ср = 0,05480, между тѣмъ
какъ Ве^паиіі нашелъ непосредственно 0.0555. Сарзііск опредѣ-
лилъ к для большого числа паровъ и газовъ, вводя поправку на укло-
неніе ихъ отъ закона Бойля. Онъ нашелъ между прочимъ слѣду-
ющія числа:
к к разн.
СкЦ 1,313 СН.АСІ 1,279 | 0,060
1,182 СН2С12 1,219 {
С2НІ 1,250 0,065
С82 1,239 СНСІЛ 1,154 I
Къ весьма замѣчательнымъ результатамъ пришелъ ѴѴіікоѵУбкі,
который опредѣлялъ к для воздуха при І : = 0° и — 78°,5 и подъ давле-
ніемъ р отъ 10 до 100 атм. Онъ нашелъ слѣдующія числа:
р атм. = 0° і = — 78°,5
10 к = 1,43 к = 1,48
50 1,53 1,79
100 1,64 2,30.
Зіеѵепз (1901) измѣрялъ скорость звука въ воздухѣ при темпе-
ратурахъ до 1000° и въ различныхъ парахъ при 100° и выше; такимъ
способомъ онъ нашелъ для к слѣдующія значенія :
Воздухъ . . . 0° к = 1,4006 С52 . . . . 99°, 7 к = 1,234
„ . 100° 1,3993 Бензолъ . . . 99°,7 1,105
,, .... 950° 1,34 Хлороформъ. . 99°,8 1,150
Эфиръ .... 99°, 7 1,112 Уксусн. кислота 136°,5 1,147
Метилов. спиртъ 99°, 7 1,256 [одъ .... 185°,5 1,303.
Этилов. спиртъ. 99°,8 1,134
Комбинируя полученныя имъ числа съ числами С а р 8 1 і с к’а,
81 е ѵ е п 8 находитъ:
ед к = 1,182 ] Разн.
с2нъон к = 1,134 ] 0,048
СНі к = 1,313 ]
снАон к — 1,256 ] 0,047
Результатъ, найденный 81 е ѵ е п 8’омъ для воздуха, не былъ под-
твержденъ Каіейпе. Послѣдній нашелъ при 900° величину к — 1,39,
слѣд. почти полную независимость к отъ температуры.
Ѵаіепііпег (1903) опредѣлилъ к для паровъ азота при тем-
пературѣ жидкаго воздуха (около —192°). Онъ нашелъ при слабомъ
давленіп то же число, какъ и при обыкновенной температурѣ. Когда
пары почти насыщены и ихъ давленіе близко къ 2 атм., то к на 5 проц.
больше. Для ср и сѵ онъ находитъ при указанной низкой температурѣ
КУРСЪ ФИЗИКИ О ХВОЛЬСОНА. Т. ПІ, изд. 3-е. 15
226
Теплоемкость.
Сѵ = 0,1769 -к 0,000322р — 0,0346 ,
Ср = 0,2476 + 0,000451/? — 0,0346 ,
гдѣ 5 давленіе насыщенныхъ паровъ.
Тгеіѣи (1903) измѣрилъ величину к для различныхъ паровъ и на-
шелъ слѣдующія числа:
к
насыщенный водяной паръ (100°) 1,3290
перегрѣтый п (110°) 1,3301
п 99 (120°) 1,1329
п п (130°) 1,1319
насыщен. алкоголевый 99 (78°) 1,1390
„ эѳировый 99 (35°) 1,1122
К о с Ь (1907) произвелъ обширное и весьма интересное опредѣлв'
ніе к для сухого воздуха, лишеннаго примѣси СО2 при 0°
и —79,3° и при давленіяхъ отъ 1 до 200 атм. Изъ полученныхъ
имъ результатовъ выписываемъ слѣдующія числа: Давленіе: 1 25 50 100 150 200 атм.
0°: 1,470 1,527 1,636 1,721 1,803
— 79,3°: 1,405 1,566 1,763 2,187 2,435 2,277.
При — 79,3° величина к имѣетъ максимумъ при давленіи
около 150 атм. Впослѣдствіи (1908) Коей ввелъ поправку, которая
увеличила приведенныя числа на 0,6% при 100 атм. и обѣихъ темпера-
турахъ, на 13,% при 200 атм. и 0°, и на 2 % при 200 атм. и — 79,3°.
Гіігбіепаи (1908) нашелъ, что между 0° и 500° к для воздуха
постоянно, для СО2 убываетъ на 3,5%, для 8О2 убываетъ на 4,8%.
VI. Способъ Мапеиѵгіег. Представимъ себѣ объемъ газа ѵ,
находящійся при давленіи /?; измѣнимъ этотъ объемъ на малую вели-
чину Дѵ и притомъ адіабатически, и обозначимъ черезъ Дрд соотвѣт-
ствующее измѣненіе величины р. Формула рѵк — Сопеі. даетъ ѵкДрд +
-|- крѵк~ гДѵ = 0 или
ѵ Др д + крДѵ = О......................(а)
Произведемъ то же самое измѣненіе Дѵ объема изотермически, т.-е.
при постоянной температурѣ, и обозначимъ соотвѣтствующее измѣненіе
давленія черезъ Дрі- Равенство рѵ = Солеѣ даетъ
ѵДрі + р^Дѵ = О......................($)
Перенося въ (а) и (/?) вторые члены направо, и раздѣляя эти равен-
ства почленно, получаемъ
к ................................(54
Лрі
Формула (57) можетъ быть обобщена для всѣхъ тѣлъ и тогда она
Газы.
227
называется формулою Ке есІГа. Мапеиѵгіег построилъ приборъ, да-
ющій возможность измѣрить величину Арц, соотвѣтствующую малому адіа-
батическому сжатію Аѵ; величина Арі получалась вычисленіемъ Онъ
находитъ:
Воздухъ. СО2
к = 1,3924 1,298 1,348.
Позже Мапеиѵгіег и Роигпіег нашли (1897) для ацетилена
к —.1,273.
Въ заключеніе этого параграфа замѣтимъ, что Мапеиѵгіег далъ
подробный обзоръ методовъ опредѣленія величины к и результатовъ,
полученныхъ различными учеными (за время 1812—1895 г.).
§ 15. Связь между теплоемкостью тѣлъ и ихъ молекулярнымъ
или атомнымъ вѣсомъ. Пиіопд* и Реѣіѣ опредѣлили теплоемкости с
для ряда металловъ и для сѣры; помноживъ эти числа на атомные вѣса
А тѣхъ же тѣлъ, они нашли, что произведеніе Ас есть величина посто-
янная, приблизительно равная 3. Они изслѣдовали Ві, РЬ, Рі, Аи, 8п,
Ар, Хп, Си, Ыі, Ре и 5. Вотъ нѣкоторыя изъ чиселъ, данныхъ назван-
ными учеными:
с А сА с А сА
РЬ 0,0293 103,5 3,032 Си 0,0949 31,7 3,008
Аи 0,0298 98,5 2,935 Ре 0,1100 28 3,080
Аё 0,0557 54 3,007 8 0,1880 16 3,008.
Приблизительное равенство произведеній Ас выражаетъ знаменитый
законъ (точнѣе — правило) В и 1 о п^’а и Реѣіѣ: произведеніе
атомнаго вѣса твердыхъ элементовъ на ихъ теплоемкость
есть величина, одинаковая для всѣхъ этихъ элементовъ.
Произведеніе Ас можно разсматривать, какъ то количество тепла, кото-
рое потребно, чтобы нагрѣть А килогр. вещества на 1°, напр. (принимая
для А числа Виіоп^’а и РеііЬ) 98,5 килогр. золота, 28 килогр. же-
лѣза, 16 килогр. сѣры и т. д. Но эти вѣсовыя количества химически эк-
вивалентны, т.-е. содержатъ одинаковое число атомовъ. Отсюда слѣдуетъ,
что для нагрѣванія одного атома названныхъ веществъ на 1° требуется
одинаковое количество теплоты, которое служитъ мѣрою атомной тепло-
емкости. Поэтому законъ В и 1 о п ^’а и Р е і і 1 можно формулировать еще
такимъ образомъ: атомная теплоемкость для всѣхъ твердыхъ
элементовъ одинакова. Обширныя изслѣдованія Ке^паиИ надъ
теплоемкостью тѣлъ дали ем} возможность точнѣе высказаться объ
этомъ законѣ.
Удвоеніе атомныхъ вѣсовъ, въ необходимости котораго убѣдились
химики послѣ В и 1 о п ^’а и Реііі, привело къ удвоенію и того постоян-
наго числа, которому приблизительно равны произведенія Ас. Въ ниже-
слѣдующей табличкѣ помѣщены числа с, А и Ас для ряда элементовъ,
данныя АѴие Ппег’омъ въ его учебникѣ; въ третьемъ столбцѣ названы
ученые, опредѣлявшіе с.
15*
228
Теплоемкость.
с А Ас
Алюминій . 10,2143 Ве§паи1і \ 0,2270 Віс1іаг<І8 27,04 5,79 6,14
Бромъ тверд. (- -7«° до 30°). 0,0843 Ве^папіі 79,76 6,72
Висмутъ . . 0,0308 « 208,4 6,42
Желѣзо . . 0,1138 « 55,88 6,36
Золото Іодъ . . . 0,0324 « 0,0541 « 196,7 126,53 6,36 6,84
Иридій . . 0,0323 Ѵіоііе 192,5 6,14
Кадмій . . . . 0,0548 Випкеп 111,5 6,11
Калій . . . 0,1662 ЗсЬиег 39,03 6,48
Кальцій . . 0,1704 Випееп 39,91 6,80
Кобальтъ. . 0,1067 Ве^паиіі 58,6 6,25
Литій . . . 0,9408 « 7,01 6,58
Магній . . /0,2450 Корр '/0,2519 Ьогепг 24,3 5,95 6,12
Марганецъ . 0,1217 Ве^паиИ 54,8 6,67
Мѣдь . 0,0935 « 63,18 5,91
Мышьякъ . / 0,0814 « ‘ / 0,0830 ЛѴ и е 11 п е г 74,9 6,10 6,21
Натрій 0,2830 8 с 11 и е г 23 6,51
Никкель . . 0,1082 Ве^паиіѣ 58,6 6,39
Олово. . . 0,0559 Випвеп 118,8 6,63
Палладій. . . 0,0593 Ке^паиіі 106,35 6,31
Платина . . 0,0324 « 194,3 6,29
Ртуть (—78° ДО —40°) . 0,0319 « 199,8 6,38
Ртуть жидкая 0,0330 ХѴіпкеІта пп — 6,60
Селенъ . . 0,0762 Ве^паиіѣ 78,87 6,01
Свинецъ . . 0,0314 « 206,39 6,48
Серебро . . 0,0570 « 107,66 6,13
Сурьма . . / 0,0508 « /0,0523 Корр 119,6 6,08 6,23
Цинкъ . . . . . . 0,0935 Випвеп 65,1 6,10
Приведенныя числа показываютъ, что произведеніе Ас колеблется
около нѣкотораго средняго числа, приблизительно равнаго 6,30. Совер-
шенно не слѣдуютъ этому правилу при обыкновенной температурѣ прежде
всего углеродъ, кремній и боръ. Для нихъ получаются такія числа:
Углеродъ. с А Ас
Древесный уголь ... . 0,241 11,96 3,13
Графитъ . 0,2018 2,42
Алмазъ . 0,1128 « 1,35
Кремній.
Графитообразный. ... . 0,181 28,3 5,12
Кристаллическій .... . 0,165 « 4,67
Плавленный . 0,138 « 3,89
Теплоемкость и молекулярный вѣсъ.
229
Боръ. с А Ас
Аморфный . . 0,254 10,9 2,77
Графитообразный. . . . 0,235 « 2,56
Кристаллическій . . . . . 0,230 « 2,51
Однако изслѣдованія Н. Е. ЛѴ е Ь е г’а показали, что теплоемкость
этихъ трехъ веществъ быстро растетъ съ температурою, причемъ произ-
веденіе Ас приближается къ числу 6, какъ видно изъ слѣдующей таблички:
Ѵлмазъ Температура. . . 985° С 0,4589 Ас 5,49
Графитъ . . . . 985° 0,4674 5,60
Воръ . 233°,2 0,3663 3,99
« красное каленіе 0,50 5,45
Кремній кристалл. . . 232°,4 0,2029 5,74.
Нѣчто подобное относится и къ бериллію. Ье СЬаіеІіег нахо-
дить для атомной теплоемкости углерода слѣдующія выраженія:
Отъ 0° до 250° .... Ас = 1,92 0,0077/.
Отъ 250° до 1000° .... Ас = 3,84 + 0,00246/.
Моінзап и Оаиііег показали, что атомная теплоемкость чистаго
бора при 400° равна 6,4. Длѣ сѣры и фосфора получаются различ-
ныя числа, смотря по состоянію вещества. Для сѣры с колеблется между
0,163 (естеств. кристаллы, по Корр’у) и 0.1844 (свѣже расплавленная,
по Ке^паиіі); соотвѣтственно Ас колеблется между 5,22 и 5,90. Для
желтаго фосфора йе^паиіі находитъ с — 0,1740 между 10° и —78°,
А = 30,96, такъ что Лс=5,39; между тѣмъ Корр даетъ между 13° и
36° число с = 0,202, т.-е. Ас = 6,26.
Весьма интересную работу о зависимости атомной теплоемкости Ас
отъ температуры опубликовалъ Вейп. Онъ находитъ для Ас слѣдующія
числа въ различныхъ температурныхъ интервалахъ:
+ 100° до + 18° + 18° до - 79° — 79° до — 186°
РЬ 6,4 6,2 6,0
Рі 6,3 6,1 5,4
1г 6,2 5,8 5,1
Рсі 6,3 6,0 5,2
Са 6,0 5,6 1,5
№ 6,4 5,8 1,3
Ре 6,3 5,6 1,0
АІ 6,0 5,3 4,2
8Ь 6,0 5,8 5,5
8п 6,5 6,1 5,8
С(і 6,3 6,0 5,6
Аё 6,0 5,9 5,4
1п 6,1 5,8 5,2
230
Теплоемкость.
4- 100° до + 18°
6,1
2,4
С
4- 18° до — 79° — 79° до — 186°
5,7 4,6
1,7 0,9.
Если мы примемъ для углерода наименьшее изъ чиселъ, най-
денныхъ Ве\ѵаг’омъ (стр. 194), именно величину средней теплоемкости
алмаза между — 188° и 252,5°, равную 0,0043, то мы получимъ Ас~ 0,052
— величину, въ 100 съ лишнимъ разъ меньшую, чѣмъ слѣдуетъ по пра-
вилу Виіоп^’а— Реііі.
Воп1зс1іе\ѵ находитъ (частью при помощи вычисленій), что для
алюминія Ас имѣетъ слѣдующія значенія:
I =600° 300° 0° —100° —200° -—250°
Ас — 8,10 6,58 5,64 5,12 4,35 3,86.
Многочисленныя опредѣленія атомной теплоемкости металловъ и
ниже упоминаемой молекулярной теплоемкости соединеній были произве-
дены Тіісіеп’омъ.
Кісііагг (1904) показалъ теоретически, что для смѣси двухъ
газовъ, для которыхъ отношеніе теплоемкостей равно кг и к" * это от-
ношеніе к не вычисляется по правилу смѣшенія, но что 1 : (к— 1) есть
линейная функція плотности <5 смѣси. Пусть д' и д" плотности состав-
ныхъ частей, причемъ <Г, <5" и (5 отнесены къ 0° и 1 атм. давленія. Тогда
1 _<5 — д' 1 1
к — 1“ Ъ"— Ь' ’ к''— 1 + 8' к!— 1 ’ ‘ ‘ ('57,а)
Корр (1966) изслѣдовалъ смѣси О2 съ СО2 и аргона съ СО2; резуль-
таты измѣреній вполнѣ подтвердили справедливость этой формулы. а -
соЬй (1904) опредѣлялъ к для смѣсей кислорода и озона; считая фор-
мулу (5 7. а) справедливой, онъ вычислилъ для чистаго озона &=1,29.
Котовичъ (1908) далъ формулу
л
, — 1)р' Н- к"(к' — 1) р
(к"-1)р'-і-ік'-1)р"'
. . (57, Ь)
въ которой рх и р.2 парціальныя давленія составныхъ частей смѣси. Ее можно
написать въ видѣ
Р Р' . Р"
к — 1~~к'—1'к'' — Ѵ
гдѣ р=р' р". Принимая во вниманіе, что
+ /') = й'Р' + &"р",
легко убѣдиться, что формулы Котовича и Кісйагга тождественны.
Правиломъ Биіопд’а и Реііі въ нѣкоторыхъ случаяхъ можно
пользоваться для опредѣленія атомнаго вѣса элементовъ. Для хлористаго
индія принималась формула ІпС12. которая дала Іп = 76. Это число не
подходитъ къ періодической системѣ и Менделѣевъ принялъ формулу
ІпСІъ, которая даетъ Іп =114. Для индія с= 0,057; А = 76 даетъ
Ас = 4,3, тогда какъ А = 114 дастъ величину Ас = 6,5. Такимъ обра-
зомъ правило Виіоп^’а и Реііі оказалось рѣшающимъ при опредѣле-
ніи атомнаго вѣса индія.
Теплоемкость и молекулярный вѣсъ
231
Обращаемся къ вопросу о теоретическомъ значеніи закона О иіоп ^’а
и Реііі. Нами уже было указано (стр. 156), что теплота с, погло-
щаемая тѣломъ при нагрѣваніи на 1°, тратится на увеличеніе живой силы
движенія частицъ, на внутреннюю работу и на внѣшнюю работу; послѣд-
няя для твердыхъ и жидкихъ тѣлъ весьма мала и мы ею пренебрегаемъ.
Въ такомъ случаѣ имѣемъ с — /17 + ДН и Ас — АД} + АДН, гдѣ Д7
тратится на увеличеніе живой силы, ДН на внутреннюю работу. Вели-
чина /17 равна истинной теплоемкости С по терминологіи Сіаизіив’а
(стр. 156), такъ что мы имѣемъ
Ас — АС-\-АДН........................ (58)
Мы видѣли (т. I), что молекулы газовъ обладаютъ при одинаковыхъ
температурахъ одинаковою живою силою, пропорціональною абсолютной
температурѣ. Отсутствіе обмѣна энергіи между соприкасающимися тѣ-
лами, температура которыхъ одинакова, заставляетъ распространить это
положеніе и на жидкія и твердыя тѣла. Въ такомъ случаѣ тратится оди-
наковое количество тепла на увеличеніе живой силы одного атома какого
бы то ни было вещества при его нагрѣваніи на 1°, т.-е. истинная
атомная теплоемкость всѣхъ элементовъ одна и та же.
Отсюда ясно, что и произведеніе АС должно быть одно и то
же для всѣхъ элементовъ, ибо АС есть количество тепла, потреб-
ное для увеличенія живой силы атомовъ, при нагрѣваніи эквивалент-
ныхъ количествъ вещества, т.-е. содержащихъ одинаковое количество ато-
мовъ, на 1°.
Произведеніе истинной теплоемкости на атомный
вѣсъ должно быть величиной постоянной для всѣхъ эле-
ментовъ. Сіаизіиз считаетъ величину С вообще вполнѣ постоян-
ною для даннаго элемента, т.-е. не мѣняющейся ни съ температурой, ни
съ переходомъ элемента изъ одного состоянія въ другое; всѣ измѣненія
теплоемкости с, или точнѣе сѵ, онъ приписываетъ измѣненію внутрен-
ней работы.
Законъ Виіоп^’а и Реѣіѣ, говорящій, что Ас приблизительно оди-
наково для всѣхъ твердыхъ элементовъ, заставляетъ насъ допустить, что
въ твердыхъ элементахъ внутренняя работа, соверша-
емая между одинаковымъ числомъ атомовъ, или при-
ходящаяся на одинъ атомъ, приблизительно одна и та
же, и въ этомъ заключается теоретическое значеніе названнаго закона.
Воіігшапп, ВісЬагг, 8іаі§-т иеііег, Еіпвіеіп, Тйіе-
8 е п, Ье\ѵі8 и др. пытались теоретически вывести правило Ас = 6 для
твердыхъ элементовъ. ВісЬагг доказалъ, что Ас для твердаго состо-
янія должно быть ровно вдвое больше, чѣмъ для газообразнаго, когда
газъ состоитъ изъ отдѣльныхъ атомовъ и слѣд. к = 5 : 3; при этомъ слѣ-
дуетъ положить с = сѵ. Далѣе мы имѣли формулу (стр. 217).
1,987
СР Сѵ ~ и.
232
Теплоемкость.
гдѣ — молекулярный вѣсъ и слѣд.. для одноатомныхъ газовъ тожде-
ственно съ А. Если положить // = А и ср = то изъ обоихъ уравне-
ній получится Ас = 6. Это должно быть справедливо для всѣхъ ме-
талловъ, пары которыхъ одноатомны (напр. ртуть). Вообще Віскатя
находитъ, что Ас приблизительно равно 6, когда перемѣщенія атомовъ
малы сравнительно съ ихъ взаимнымъ разстояніемъ. Въ противномъ слу-
чаѣ возможны значительныя отступленія; въ этомъ случаѣ с особенно
сильно зависитъ отъ температуры. Тѣла съ малымъ атомнымъ объемомъ
(атомный вѣсъ дѣленный на плотность), каковы Ве, Во, и С, а также
тѣла съ малымъ атомнымъ вѣсомъ даютъ для Ас слишкомъ малыя вели-
чины. Въ первомъ случаѣ разстоянія атомовъ малы; во второмъ пе-
ремѣщенія могутъ быть велики, вслѣдствіе незначительности массы ато-
мовъ. Этотъ теоретическій выводъ подтверждается фактами. АѴ і е а п сі
(1907) и ВоМапсІ (1906) дали дальнѣйшее теоретическое развитіе
идей Віскагя’а.
Новую, весьма остроумную теорію далъ Еіпзіеіп (1907, 1911).
Основанная на электронной теоріи (т. IV) и на теоріи лучистой энергіи,
данной Ріапск’омъ (т. II и IV), она приводитъ къ формулѣ
__
Л п е 7 И/
Ас = 37? .—~ ' 2...................(57, с)
ѵт-ч^
въ которой 7? постоянная уравненія состоянія идеальныхъ газовъ, рав-
ная 1,985 въ системѣ граммъ—калорія; Т абсолютная температура, а нѣ-
которая постоянная, находящаяся въ зависимости отъ лучеиспуска-
тельной способности вещества. Формула (57,г) даетъ г —0
при Т = 0. При высокихъ температурахъ получаемъ Ас = 3/?. ч т о
весьма близко къ числу Ас=Ь. Опыты ЭДегпбі’а и его учени-
ковъ (стр. 194) опредѣленія с при весьма низкихъ температурахъ служили
также для провѣрки формулы Еіизіеіп’а. Опыты Ма^пив’а пока-
зали, что (57, г) необходимо замѣнить формулою
а М\2
с \ 77 3
Ас = 3%і а 4 ............(57,сі)
“ т и
\е — 1/
Такъ, напр. получились для свинца # = 58, 6 = 0,000078, для се-
ребра # = 162, 6 = 0,000048, для А§С # = 168, 6 = 0,000022, для РЬСІ
#= 172, 6 = 0,000018.
Позднѣйшія изслѣдованія Ы е г п 8 і’а и Ь і п (1 е ш а и п’а (1911) за-
ставили этихъ ученыхъ замѣнить формулу (57, г) болѣе сложною
Теплоемкость и молекулярный вѣсъ.
233
въ которой находится только одна постоянная и которая хорошо согла-
суется съ наблюденіями для РЬ, Си, АІ и А&
Ьаештеі (1905) указалъ, что, въ силу значительной зависи-
мости теплоемкости отъ температуры, значеніе с = 6,2 имѣетъ силу для
различныхъ элементовъ при различныхъ температурахт> и что можно
число 6,2 замѣнить любымъ числомъ изъ промежутка
3,5—9,5, если каждый разъ относить опредѣленное число къ соотвѣтству-
ющей ему опредѣленной температурѣ. Если для твердыхъ элементовъ
отнести всѣ числа къ т е м п е р а т у р ѣ п л а в л е н і я, то получается слѣ-
дующая интересная таблица :
Элементъ Темпер. плавленія Удѣльная теплоемкость при этой температурѣ А Ас
ы 190° 1,3 7 9,45
Ыа ЮО 0,36 23 8,28
АІ 700 0,35 27 9,45
8 120 0,25 32 8,00
М 1600 1,166 59 9,79
Си 1100 0,145 64 9,28
7.п 420 0,142 65 9,23
Вг —7 0,114 80 9,12
Элементъ Темпер. плавленія Удѣльная теплоемкость при этой температурѣ А Ас
1040 0,082 108 8,87
са 315 0,066 112 7,39
РЬ 330 0,0413 207 8,55
Среднее 8,85
Значенія Ас здѣсь приблизительно настолько-же отклоняются отъ
средняго значенія, какъ и числа таблицы на стр. 229.
Г. Е. Кеитапп нашелъ въ 1831 слѣдующій закона,, представляю-
щій какъ бы обобщеніе закона Л и 1 о п ц’а и Р е ѣ і ѣ: произведеніе
теплоемкости химически подобно составленныхъ слож-
ныхъ тѣлъ на ихъ молекулярный вѣсъ есть величина
приблизительно постоянная. Ке^паиіі, Раре и Корр
подтвердили этотъ законъ для многихъ группъ химическихъ соединеній.
Приведемъ немногія изъ этихъ группъ; с теплоемкость, // молекуляр-
ный вѣсъ.
Соединенія типа РО.
с /хс
М§0 0,24394 40,3 9,83
МпО 0,15701 70,8 11,14
МО 0,15880 74,6 11,86
СиО 0,14201 79,2 11,27
2п0 0,12480 81,1 11,13
Н§0 0,05179 215,8 11,19
РЬО 0,05119 222.4 11,38
Среднее 10,97.
234
Теплоемкость.
С !< дс
Соединенія типа Т?2О3.
0,17000 159,8 27,2
Сг2О^ 0,17960 152 27,4
Л$2О3 0,12768 197,8 25,3
8ь2оя 0,09009 287,8 25,9
Ві2О-л 0.06053 464,8 28,1
Среднее 26,8.
Соединенія типа НС12.
мёсі2 0,19460 95,1 18,5
СаСІ. 0,16420 110,7 18,2
8гС12 0,11990 158,1 19,0
ВаС12 0,08957 207,7 18,6
7,пСІ.> 0,13618 135,9 18,6
8пС12 0,10161 189,6 19,3
НёС12 0,06889 270,6 18,7
РЪС12 0,06641 277,2 18,4
МпСІ.г 0,14250 125,6 17,9
Среднее 18,58.
Соединенія типа /?7ѴО3.
кыоъ 0,23875 101 24,1
0,27821 85 23,6
Аё1ѴОя 0.14352 169,7 24,4
Среднее 24,03.
Соединенія типа А2^О4.
К,8О4 0,10910 174 33,1
^28О4 0,23115 142 32,8
Среднее 32,95.
Приводимъ среднія значенія молекулярныхъ теплоемкостей дс для
соединеній различнаго типа:
Типъ. Типъ. І1С
РО 11,0 Рі. 19,4
ро2 14,0 рйо8 24,0
ро8 18,8 РМ2О6 38,2
Р%08 26,9 Р8О4 26,4
Р8 11,9 Р28О4 32,9
Р8. 18,1 рсо3 21,4
РСІ 12,7 Р2СО8 29,1
РС12 18,7 РЗО^ЪНъО 78,3
/У 13,4 РЗО^іН.,0 97,4.
Вопросъ о зависимости величины /хс отъ состава тѣлъ долгое время за-
нималъ ученыхъ. 'I о 111 е высказалъ впервые въ 1844 г. законъ, ниже приве-
Теплоемкость и молекулярный вѣсъ.
235
денный; ѴѴоезіуп вновь на него указалъ въ 1848 г., но только въ
1864 г. этотъ законъ былъ окончательно формулированъ К о р р’омъ
и подтвержденъ огромнымъ матеріаломъ, добытымъ его собственными из-
слѣдованіями.
Законъ Яоиіе’я и Корр’а: молекулярная теплоем-
кость твердыхъ соединеній равна суммѣ атомныхъ
теплоемкостей элементовъ, входящихъ въ составъ
этихъ соединеній.
цс = 2 піаісі......................(59)
гдѣ и с относятся къ соединенію; теплоемкость, аі атомный вѣсъ и
слѣд. атомная теплоемкость одного изъ элементовъ, входящихъ въ
составъ соединенія, щ число атомовъ этого элемента въ одной молекулѣ
соединенія, такъ что /г = піа-г Корр принимаетъ атомную теплоём-
кость всѣхъ элементовъ, кромѣ О, 77, /7, В, 5/, С, 5 и Р, равною 6,4.
Соединенія типа даютъ для 5 теплоемкость 11,9—6,4 = 5,5, а
соединенія типа 7?52 Даютъ (18,1 - 6,4): 2 = 11,7 : 2 = 5,85. Окончательно
Корр принимаетъ для 5 число 5,4. Атомная теплоемкость кислорода
получается изъ соединеній:
типа/?25О4 . . . (32,9 —6,4X2 —5,4): 4 . . . 3,7
. . . 11,0—6,4....................4,6
/?О2 ... (14,0 —6,4): 2..............3,8
/?О3 .... (18,8 — 6,4): 3.............4,1
АоО3 .... (26,9 — 6,4 X 2) : 3........4,7.
Корр принимаетъ 4, какъ среднее для атомной теплоемкости твер-
даго кислорода, т.-е. входящаго въ составъ твердыхъ химическихъ сое-
диненій. Для С принимается число 1,8, найденное для алмаза. Оконча-
тельно Корр останавливается на слѣдующихъ числахъ для элементовъ.
для которыхъ атомная теплоемкость не равна 6.4: Атомная Атомная
теплоемкость. теплоемкость.
0 4,0 С 1,8
н 2,3 8і 3,8
н 5,0 8 5,4
в 2,7 Р 5,4.
Принимая эти числа и число 6,4 для всѣхъ остальныхъ элементовъ, можно
вычислить теплоемкости с различныхъ твердыхъ соединеній
по формулѣ (59) ; результаты оказываются приблизительно вѣрными.
8 і е р Ъ а и М е у е г (1900) указалъ на то обстоятельство, что раз-
смотрѣнный здѣсь законъ (молекулярная теплоемкость равна суммѣ атом-
ныхъ теплоемкостей) тѣмъ точнѣе оправдывается, чѣмъ ближе данное со-
единеніе слѣдуетъ другому закону: < молекулярный объемъ равенъ суммѣ
атомныхъ объемовъ». Ѵап АиЪеі (1901) оспариваетъ этотъ взглядъ.
Для жидкихъ соединеній законъ ОАиІе’я и Корр’а вовсе не
оправдывается.
236
Теплоемкость.
ЛѴіпкеІтапп нашелъ, что можно вычислить теплоемкость г раз-
личныхъ сортовъ стеколъ по формулѣ ср=^Сірі, гдѣ р[ вѣсовыя коли-
чества, Сі теплоемкости веществъ (напр. ХпО, 8іО2, К2О,СаО и т. д.)
входящихъ въ составъ стекла, и р 2 Рь т-"е- п0 формулѣ, приложимой
къ сплавамъ (стр. 197). бгагпіег нашелъ еще въ 1852 г. и Корр
подтвердилъ впослѣдствіи, что теплоемкость твердой воды, входящей
въ составъ гидратовъ солей, равна теплоемкости льда. Дѣйствительно
табличка на стр. 235 даетъ:
(Я80^7Н2О}—7?5О4 = 97,4— 26,4=71—ЧН2О; слѣд. для Н2О цс = 10,1
(ДбО4Ѣ7//2О)—(Д8О4 5Л/2О)=97,4—78,3=19,1=2/72О; слѣд. для Н2О/хс=9,6
Среднее цс = 9,85; но для воды ц,= 18, слѣд. г = 0,55. Для льда с — 0,5.
На стр. 198 мы привели изслѣдованіе Н. Н. Бекетова, кото-
рый нашелъ для атомной теплоемкости твердаго водорода, поглощеннаго
палладіемъ число 5,88: оно совершенно расходится съ числомъ 2,3, ко-
торое принимаетъ Корр.
Кеіз и 8 с 11 і И нашли нѣкоторые интересные результаты для
теплоемкостей органическихъ жидкостей. К е і 8 нашелъ, что
молекулярныя теплоемкости веществъ, составляющихъ гомологическій
рядъ, даютъ приблизительно одинаковыя разности. Такъ въ ряду Спир-
товъ СпН2П^_2^ молекулярная теплоемкость //с растетъ въ среднемъ на 9,69
при увеличеніи п на единицу; въ ряду кислотъ СпН2ПО2 это возрастаніе
равно 8.38, такъ что прибавленіе СН2 въ различныхъ рядахъ вызываетъ
неодинаковое увеличеніе молекулярной теплоемкости.
8 с 11 і { Гу удалось открыть цѣлый рядъ интересныхъ фактовъ отно-
сительно величины теплоемкости с и, въ особенности, ея зависимости отъ
температуры. Если выразить с въ видѣ с = с0 + Ы, то с0, и въ еще
большей мѣрѣ Ь, оказываются общими для цѣлыхъ рядовъ органическихъ
соединеніи. Ограничиваемся двумя примѣрами.
Ар ом ат и ч е с кі е у гл е в одо р о д ы:
Жирныя кислоты:
Бензолъ
Толуолъ
Метаксилолъ
Параксилолъ
Этилбензолъ
Псевдокумолъ
Мезитиленъ
с=0,3834ф-0,001043^
с=0,3929+0.001043^
Муравьиная
Уксусная
Пропіоновая
Масляная
Изомасляная
Валеріановая
с=0,4966+0,000709^
г=0.4440+(),001418/
с=О,4352+0,001418Л
Прояилбевзолъі 04000+00010Ш
Цимолъ I
Замѣчательно, что для муравьиной кислоты Ь какъ разъ равно по-
ловинѣ того Ь, которое получается для остальныхъ кислотъ.
Болѣе сложная связь между теплоемкостью жидкости и другими фи-
Теплоемкость и молекулярный вѣсѣ.
237
зическими величинами была указана А. Надеждинымъ. Къ его ра-
ботѣ мы возвратимся ниже. МасЬе (1901) показалъ, что теплоем-
кость с жидкости должна быть приблизительно равна
{войной истинной теплоемкости ея пара. Мѣрою послѣд-
ней служитъ сѵ. Дѣйствительно оказывается, что для ряда жидкостей с
приблизительно равно 2с ѵ.
Обращаясь къ тѣламъ газообразнымъ, можно было бы для
нихъ ожидать особенно простыхъ и ясныхъ соотношеній между тепло-
емкостью и атомнымъ или молекулярнымъ вѣсомъ. Можно было бы ду-
мать, что теплоемкость сѵ при постоянномъ объемѣ и представляетъ
истинную ихъ теплоемкость въ смыслѣ С1 а и 8 і и з’а, которая, будучи
помножена на молекулярный вѣсъ, есть величина постоянная для всѣхъ
газовъ. Такое заключеніе основано на представленіи о малой величинѣ
внутренней работы въ газахъ. Истинная теплоемкость, помноженная на
атомный вѣсъ, по теоріи (стр. 233), должна быть величиною посто-
янною для всѣхъ газовъ, а потому мы въ правѣ ожидать, что произведе-
ніе теплоемкости сѵ на молекулярный вѣсъ р есть величина, пропорціо-
нальная числу п атомовъ, входящихъ въ составъ частицы газа; произве-
деніе ^сѵ равно молекулярной теплоемкости при постоянномъ объемѣ, а
потому мы для всѣхъ газовъ можемъ ожидать
^=^’ = СоП8І.........................(60)
п п
Такъ напр. для всѣхъ двуатомныхъ газовъ и паровъ, каковы /72, О2,
А/2, С72, Вг2, Л, СО, Л/О, НСІ, ВгСІ, мы должны имѣть с^ѵ = Соп81; то
же самое относится къ трехатомнымъ СО2, МО, 5О2, Н23 и т. д. Вели-
1
чину — можно назвать среднею атомною теплоемкостью при по-
стоянномъ объемѣ. Такъ какъ газы, взятые въ вѣсовыхъ количествахъ,
пропорціональныхъ молекулярнымъ вѣсамъ ц, занимаютъ одинаковые
объемы или, что то же самое, въ одинаковыхъ объемахъ газовъ заклю-
чается одинаковое число молекулъ (законъ Авогадро, т. I). то ожи-
даемое равенство молекулярныхъ теплоемкостей ^сѵ для газовъ съ
одинаковымъ числомъ п атомовъ въ молекулѣ сводится къ равенству те-
плоемкостей уѵ такихъ газовъ, взятыхъ въ одинаковыхъ объемахъ; изъ (60)
слѣдуетъ, что : п должно быть одинаковое для всѣхъ газовъ.
По формулѣ (31) стр. 201 разность ур — есть величина одинако-
вая для всѣхъ газовъ, равная
7р — ?ѵ = 0,0688 ...............(61)
если положить ѵ0 = 1, т.-е. если всѣ газы брать въ объемахъ, равныхъ
объему вѣсовой единицы воздуха при данныхъ температурѣ и давленіи,
каковой объемъ для удобства и принятъ равнымъ единицѣ. При такомъ
выборѣ единицы объема имѣемъ, см. (29) стр. 200
7р — дСр; = дсѵ................(62)
238
Теплоемкость
молекулярныя же теплоемкости равны
== ~~ 28,88ур • == = 28,88/^ • • • (63)
ибо /і = 28,886. Для разности двухъ молекулярныхъ теплоемкостей вы-
текаетъ отсюда формула (33") стр. 201
Ср,,р ср,,ѵ = 1,^87................(64)
Мы ожидаемъ найти уѵ : п одинаковымъ ція всѣхъ газовъ; (60), (62)
и (63) показываютъ, что въ такомъ случаѣ и срЛ) : п также должно быть
одинаковымъ для всѣхъ газовъ, и кромѣ того ур : п и с^р : п — рср : п
также одинаковымъ для тѣхъ газовъ, которые слѣдуютъ законамъ Бойля
и Гей-Люссака. Соединяя все вышеизложенное, можно сказать:
Мы въ правѣ ожидать, что средняя атомная тепло-
емкость при постоянномъ объемѣ, т.-е. величина
: п — срѵ : /г, гдѣ п число атомовъ, входящихъ въ со;
ставъ молекулы газа, одна и та же для всѣхъ газовъ-
или что 7Ѵ : и, гдѣ теплоемкость единицы объема
газа при постоянномъ объемѣ, величина одинаковая
для всѣхъ газовъ. Для газовъ, слѣдующихъ законамъ
Бойля и Гей-Люссака можно ожидать, что и соотвѣт-
ствующія теплоемкости при постоянномъ давленіи,
т.-е. величины цср : п и срр\п и ур'.п окажутся величи-
нами одинаковыми для всѣхъ газовъ.
Какъ частный случай получаемъ отсюда:
Теплоемкости уѵ и ур двуатомныхъ газовъ, каковы
//2, О2, СО, ЫО, отнесенныя къ одинаковымъ объе-
мамъ, должны быть равны между собою, и то же самое
должно, понятно, относиться и къ молекулярнымъ
теплоемкостямъ ср/ѵ и с^р, которыя въ 28,88 разъ больше
Уѵ м ур (если послѣднія отнесены къ объему вѣсовой
единицы воздуха), или къ атомнымъ теплоемкостямъ,
равнымъ 0,5 ср,ѵ и 0,5 с^р. Только этотъ послѣдній выводъ подтверж-
дается опытомъ для немногихъ газовъ, какъ мы это уже видѣли на стр. 207.
Наблюденія Ве^паиИ дали для величины срд — ур, см. (62), числа,
которыя мы вновь выписываемъ, прибавивъ два числа для СО и 1\Ю.
7р 0?^ с^р 0,5 [лср 7р 0,^ Ср}р — 6,5 ^ср
О2 0,2405 3,480 со 0,2376 3,430
0,2365 3,413 КО 0,2406 3,476.
0,2359 4,409
Средняя молекулярная теплоемкость ср р при постоянномъ давленіи
для этихъ пяти газовъ равна 6,88 ; средняя атомная теплоемкость 0,5 срр
равна 3,44. Изъ формулы (64), или принимая во вниманіе величины сѵ
Теплоемкость й молекулярный вѣсъ.
239
найденныя изъ опытовъ, мы получаемъ среднюю молекулярную теплоем-
кость при постоянномъ объемѣ равною 4,90; средняя атомная тепло-
емкость 2с равна 2,45. Этимъ, однако, почти и ограничивается согласіе
опытныхъ данныхъ съ тѣми теоретическими выводами, къ которымъ мы
пришли выше. Стоитъ только разсмотрѣть числа, относящіяся къ С/2, Вг2,
/2, НСЦ НВг и др., чтобы замѣтить значительныя отступленія; такъ для
С12 имѣемъ с^ѵ = 3,10.
Точно также вовсе не оправдывается постоянство величины с„ ѵ: п
для всѣхъ газовъ, какъ видно изъ слѣдующей таблицы:
п сѵ ѵ — №ѵ С{л,ѵ • п к-Ср
Гр
1 200 0,0147 2,94 2,94 1,66
О2 2 32 0,1544 4,95 2,47 1,405
^2 У 28 0,1735 4,86 2,43 1,405
«2 V 2 2,4263 4,85 2,43 1,405
со 28 0,1848 4,89 2,44 1,403
по 30 0,1662 4,99 2,49 1,394
1 сі2 71 0,0873 6,20 3,10 1,323
Вг2 99 160 0,0428 6,84 3,42 1,292
4 99 254 0,0257 6,52 3,26 1,307
на 99 36,5 0,1392 5,08 2,54 1,394
НВг 99 81 0,0573 4,64 2,32 1,431
і ш 99 128 0,0394 5,04 2,52 1,397
сн V 162,5 0,0389 6,32 3,16 1,317
ВгЗ 99 1 207 0,029 6,14 3,07 1,33
со2 < | 00 1 3 44 0,1486 6,54 2.18 1 1.311 |
( ЮО» и 0,1695 “ 7 7,48 2,49 | 1,284 )
< ( 00 1 1000 » » 44 99 0,1513 0,1737 6,66 7,64 2,22 \ 2,55 / 1,311 ) 1,274 1
5О2 » 64 0,1237 7,92 2,64 1,248
» 34 0,1933 6,57 2.13 1,258
( 0° 4 1 17 0,3803 1 6,46 1,61 1,317 ч
1 1000 1 0,4159 1 7,07 1 1,77 1,279 )
сні 1 5 16 0,4495 7,19 1,44 1,319
с2н6 < { 00 6 28 ' 0,2702 7,57 1,26 1 1,245 1
| 1000 99 99 0,3523 9,86 1,64 1 1,189 ।
Е. ѴѴіейетапп опредѣлилъ теплоемкости для паровъ различ-
240
Теплоёмкость.
ныхъ жидкостей. Изъ его наблюденій получается слѣдующая таблица,
приведенная къ 0°.
Пары п Ц — №ѵ сіі,ѵ • п сѵ
Сѣроводородъ С82 3 ' 76 0,1054 8,01 2,67 1,248
Хлороформъ ССІ^Н . . 5 119,4 0,1178 14,05 2,81 1,139
Бромистый этилъ С2775Вг . 8 169 0,1168 12,70 1,59 1,159
Ацетонъ С3Н€іО. 10 58 0,2636 15,29 1,53 1,132
Бензолъ .... 12 78 0,1981 15,46 1,29 1,129
Уксусный эфиръ С^Н^О2 • 14 88 0,2394 21,07 1,50 1,094
Эфиръ С^Н^О . 15 74 0,3455 25,57 1,70 1,078
Числа предпослѣдняго столбца обѣихъ таблицъ показываютъ, что
средняя атомная теплоемкость при постоянномъ объемѣ вовсе не одина-
кова для различныхъ газовъ; она колеблется между 1,26 и 3,42. Эле-
менты какъ бы распадаются на двѣ группы: Н, О, и Н@, СІ, Вг, 3,
изъ которыхъ вторая имѣетъ большія численныя значенія этой величины,
чѣмъ первая.
Мы должны отсюда заключить, что и для газовъ истинная теплоем-
кость не совпадаетъ съ теплоемкостью и что, слѣдовательно, исходная
точка нашихъ разсужденій неправильна.
Ветіііеіоі полагаетъ, что элементы (газы и пары) раздѣляются
на ч е т ы р е группы, для которыхъ срр и сиѵ имѣютъ слѣдующія
значенія: сн п с„ 7.
1 группа, одноатомные газы 5 3
2 группа, двуатомн. газы, не диссоціирующіеся 8,6 4,8
3 гр., двуатомн. газы, подверж. диссоц.(С7, Вг, У) 6,8 6,6
4 группа, четырехатомные пары (Р, и др.) 13,4 11,4.
Эти числа показываютъ, что приблизительно с^ѵ - п = 3.
По мнѣнію 8 о к п с к е измѣненіе теплоемкости съ температурой
объясняется интрамолекулярною работою ; съ этимъ вполнѣ
согласуется тотъ фактъ, что теплоемкость одноатомныхъ паровъ Н§ отъ I
не зависитъ.
На стр. 202 мы упомянули о попыткахъ опредѣлить зависимость ве-
личины к отъ числа п молекулъ. Эти попытки не могли увѣнчаться
успѣхомъ, такъ какъ послѣдній столбецъ таблицы стр. 241 показываетъ,
что для одинаковаго п величина к принимаетъ различныя значенія.
Еслибы законъ В и 1 о п и Р е 1 і і прилагался къ газамъ въ смыслѣ
постоянства величины цсѵ : п, то зависимость к отъ п была бы очень
простая. Дѣйствительно. (64) можно написать въ видѣ (пишемъ 2 вмѣ-
сто 1,987) сѵ — сѵ = . Прибавивъ сюда = В, гдѣ В поетоян-
р М п
ное число, получаемъ
Теплоемкость и молекулярный вЬсъ*
24І
2 4- пВ
с"-~ т
пВ
2
пВ'
Для паровъ ртути п = 1
слѣд. вообще для газовъ
и к = 1,666 = (стр. 225); отсюда В = 3 и
о
^=1+о2
1 ЗП
4
Эта формула дала бы к = — — 1,33 для двухатомныхъ газовъ; на-
О
блюденіе даетъ для большинства этихъ газовъ к = „ = 1,40, и число,
5
близкое къ 1,33 для С1.2 и ВпІ. Для п = 3 мы должны были бы имѣть
к =1,22. что также не согласно съ опытами. Подобныя же изслѣдованія
производили, Зіаі^тпеііег и РізсИег (1905). Послѣдній пред-
ложилъ формулу
5
6я ‘
а итапп выводитъ, основываясь на нѣкоторыхъ соображеніяхъ
которыхъ не станемъ приводить, формулу
, _ и + 5
«4-3’
7 4
которая для п = 2 даетъ к = - , для п — 3 число к — - и для п = 4
9 5 3
число к= „ = 1,286. ВоНгшапп занимался вопросомъ о зависимости
к отъ формы атомовъ для одноатомныхъ газовъ. Неизвѣстность, въ ко-
торой мы находимся относительно характера интрамолекулярныхъ движе-
ній и ихъ зависимости отъ строенія частицы, не даетъ намъ возможно-
сти теоретически разобрать вопроса о теплоемкости сложныхъ тѣлъ. По-
видимому, для послѣднихъ существуетъ большее разнообразіе возможныхъ
случаевъ, чѣмъ для твердыхъ элементовъ, для которыхъ вѣроятное пред-
положеніе приблизительно одинаковой внутренней работы весьма упро-
щаетъ вопросъ. Дальнѣйшія теоретическія изслѣдованія производили
Воупіоп (1901) и Яеапв (1901).
Л ИТЕРАТУР А.
Къ § 1.
МасН. Оіе Ргіпсіріеп сіег ХѴаегтеІеІіге, Ьеіраі^. 1896, р. 153—210.
Заимствуемъ изъ этой книги литературу, относящуюся къ возникновенію кало-
риметріи :
НісКтапп. №оѵі Сопппелі. Асасі. Реігор. 1 р. 152, 1750; 3 р. 309, 1753; 4
р. 241, 1758.
КгаДі. СоиітеіН. Асасі. Реітор. 14 р. 218, 233, 1744—1746.
Воегііаѵе. Еіет. СЪетп. 1 р. 268, 1732.
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. Ш, изд. 3-е, 16
242
Теплоемкость*
Віаск. Ьесіигев оп ѢЬе Еіетепів о! Скетівігу, ЕдіпЫіг^Ь, 1803; нѣмеіШ. пере-
водъ СгеІГя, НатЪиг§\ 1804.
Ігѵіпе. Еввау оп скетісаі викіесів. Ьопдоп, 1805.
ѴѴіІке. Коп^. Ѵеіепвк. Асасі. Куа. НапсІІ. 1772, 1781.
Сга^когй. Ехрегітепів апсі ОЬвегѵаііопв оп Ѵпітаі Неаі. Ьопдоп, 1778.
ЬатЬегі. Тепіатеп де ѵі саіогіз. Асіа Неіѵеііса. 2, Вавііае 1775; Руготеігіе,
Вегііп, 4779.
Сасіоііп. Ыоѵ. Асіа В. 8ос. Прваііепв. 5, 1784.
РіскагсІз. Хівскг. ркув. Скет. 36 р. 356, 1902.
Къ § 2.
Ре Ыис. См. ѲеЫег’в Ркувісаі. ХѴоегіегЪ. 2-е изд. 9 р. 844.
Ріаиуег^иез. Лоигп. де ркуз. (Ре Іа Меііегіе) 77 р. 283.
[]ге. Аппаіз. о! ркііов. 10 р. 273, 1817.
Р. Ыеитапп. Ро§&. Апп. 23 р. 40, 1831.
Ке&паиіі. Апп. скіт. еі рііуз. (2) 73 р. 35, 1840; Мёт. де ГАсад. 21 р. 730, 1847.
Во88СІга. Ро§^. Апп. Ликеікд. р. 549, 1874.
Ѵеііеп. \Ѵ. А. 21 р. 45, 1884.
Нігп. С. К. 70 р. 592, 831, 1870.
Р/аипсіІег ипсі Ріаііпег. Рор’р’. Апп. 140 р. 574; 141 р. 537, 1870.
№тіп еі Агпаигу. С. В. 70 р. 66 , 1870.
МиепсЫіаизеп. XV. А. 1 р. 592, 1877; 10 р. 284, 1880 (въ статьяхъ ѴРиеІІпег а).
Непгіскзеп. XV. А. 8 р. 83, 1879.
Ваит&агіпег. XV. А. 8 р. 648, 1879 (въ статьѣ Р/ашиНег’а).
Сегоза. В. Ас. деі Ьіпсеі (3, а) 10 р. 75, 1881; ВеіЫ. 6 р. 222, 1882.
Рарр. Вівв. Еиегіск, 1883.
}окаппзоп. біѵегві&і аі К. Ѵеі. Асад. Ебгкапді. 48 р. 325 1891-; ВеіЫ. 16 р.
508, 1892.
Магіе Віато. Віввегі. Йиегіск, 1877; ВеіЫ. 3 р. 344, 1879.
Рснѵіагкі. Ргос. оі Ыіе Атег. Асад. о! агів апд вс. 15 р. 75, 1879—1880; 16
р. 38, 1880-1881; Ргос. В. 8ос. 61 р. 479, 1897.
ЬіеЫрг. 8Ш. Я. 26 р. 57, 1883.
Ѵеііеп. XV. А. 21 р. 31, 1884; Оівв. Вопп, 1883.
Вагіоіі е Вігассіаіі. Киоѵо Сіт. (3) 32 р. 19, 97, 215, 1892; 34 р. 64, 1893; Веп-
діс. деі В. ІП8І. Ьоткагдо (2) 26, 1893; 28, 1895.
Кеезеп. XV. А. 18 р. 369, 1883.
Огі//іікз. Тгапе. В. 8ос. Ьопдоп 184, А р. 361, 1893; 186, А р. 268, 1895.
Ріеіегісі. XV. А. 33 р. 417, 1888; 37 р. 494, 1889; Ѵегкапді. д. д. ркув. Сее. 6
р. 228, 1904; Ркуз. Хівскг. 5 р. 661, 1904; Апп. д. Ркув. (4) 16 р. 653, 1905.
Ѵ/аісіпег апсі Маііогу. Ркув. Веѵ. 8, 193, 1899; Ргос. К. 8ос. 61 р. 479. 1897.
Ретеі. ѴіегіеЦакгввскг. д. МаіигЬ Ѳев. іп Йіігіск. 41, 140, 1896.
Шу. Ркіі. Тгапв. 186, А р. 322, 1895.
Реіііпеііі. Апп. деі В. Іві. Теспісо ді Вагі 17, 1898.
Атез. Варрогів, ргёз. аи Соп&гёв іпіегпаі. де ркувідие I р. 181, Рагів, 1900.
Огі//іік8. Варрогів, ргёв. аи Соп^гёв іпіегпаі. де рку8І^ие I р. 214, Рагів, 1900.
Огі//Ші8. Тке ікегшаі теавигетепі о( Епег&у. Саткгід&е 1901.
Реупоісіз апсі МоогЬу. Ркіі. Тгапв. 190, А р. 301, 1897; Ргос. В. 8ос. 61
р. 293, 1897.
Векп. Вегі. Вег. 1905 р. 72 ; Аппаі. д. Ркув. (4) 16 р. 653, 1905.
Вскизіег апсі Оаппоп. Ркіі. Тгапв. 186, А р. 415, 1895; Ргос. В. 8ос. 57 р. 25,1894.
}апке, Бісс., Вовіоск, 1910
Коммиссія А. Е. Р. Ѵегк. д. д. ркуз. Ѳез. 9 р. 96, 1907; 10 р. 584, 1908; 12
р. 476, 19 і0.
Рау. Ркув. Ве\. 6 р. 193, 1898; Ркіі. Ма$. (5) 46 р. 1, 1898..
Литература.
243
ІлиПп. Бізз. 2иегісЬ, 1895; Агсіі. 8с. рііуз. 34 р. 507.
ВгиезсН. Бізз. Еозіоск. 1894,
Саііепсіаг агиі Вагпез. Ргер. Вгіі. Аззос. 1899, 8есі. А.; Еіесігісіап 43 р. 775,
1899; Рііуз. Ееѵ. 10 р. 202, 1899; Ргос. Е. 8ос. 67 р. 238, 1900; Йізсііг. і. рііуз. Сііет.
32 р. 153, 1900.
Саііегкіаг. Еер. Вгіі. Аззос. (Ваз^олѵ. 1901 р. 34.
Вагпез. Ргос. Е. 8ос. 67 р. 238, 1900.
Вагпез апсі Ьезіег Сооке. Рііуз. Ееѵ. 15 р. 65, 1902.
Ѵ^іпкеітапп. НапсІЬисІі сіег Рііузік, II, 2 р. 338, 1896.
ОгіДіИіз (Выборъ единицы тепла). РЫІ. Ма&. (5) 40 р. 431, 1895.
Вагіоіі е Вігассіаіі (вода ниже 0°). Киоѵо Сіш. (3) 31 р. 133, 1892.
Магііпеііі. Аііі (I. Е. Асай. сіі Тогіпо. 25, р. 565, 1890.
Тоттазіпі е Сагйапі. Хиоѵо Сіш. (3) 21 р. 185, 1887.
Вагіоіі е Вігассіаіі. (Величина гѵ). Иноѵо Сіш. 36 р. 127, 1894; ЕепДіс. Е. Іпзі.
БотЬагДо (2) 27, 1894; ВеіЫ. 19 р. 47, 1895.
ХѴагЬиг^. Ееіегаі неЪег сііе ХѴаегтееіпкеіі, Ееіргщ 1900; Рііуз. Хеіізсііг. 1 р.
• 171, 1900.
Къ § 3.
Ьаѵоізіег еі Ьаріасе. Мёт. Де ГАсай. Еоуаіе, Рагіз 1780; Оѳнѵгез Де Ьаѵоі-
зіег 2 р. 283.
Д. Лачиновъ. Ж. Ф. X. О. 12 р. 131, 1880.
Къ § 4.
Германъ (Негтапп). Зап. Импер. Моск. Общ. Испыт. Природы 3, 1834.
Випзеп. Ро&&. Апп. 141 р. 1, 1870; 142 р. 616, 1871.
ЗсИиІІег ипй 'Х'агіИа. XV. А. 2 р. 359, 1877.
Лугининъ. Методы опредѣленія теплотъ горѣнія. Москва, 1ь94 р. 73. Нѣмецкій
переводъ, Берлинъ 1897.
Ыеіегісі. XV. А. 33 р. 417, 1888.
Воуз. РЫІ. Ма§. (5) 21 р. 214, 1886.
Кипг. Аппаі. сі. Рііуз. (4) 14 р. 315, 1904.
Сгётіеи. Л. Де Рііуз. (4) 4 р. 105, 1905.
Пап. XV. А. 13 р. 84, 1881.
ВоиізсНехм. Бізз. Хнегісіі, 1900; ВеіЫаеііег 25 р. 178—182, 1901.
Ьіпйпег. Рііуз. /ізсііг. 3 р. 237, 1902.
Къ § 5.
Гаѵге. Апп. сЫт. еі рЬуз. (3) 36 р. 5, 1852; 37 р. 416, 1852; 40 р." 293, 1854;
(4) 26 р. 385 ; 27 р. 265, 1872;' 29 р. 87, 1873; (5) 1 р. 438, 1874
Къ § 6.
Гісіітапп. Хоѵі Соттені. АкасІ. Реігороі. 1 р. 152, 1750 г.
Керпаиіі. Апп. сЫт. еі рііуе. (2) 73 р. 5, 1840; (3) 63 р. 1, 1861 ; Ро^. Апп.
122 р. 272, 1864.
Лугининъ. Ж. Ф. X. О. 16, отд. хим. р. 569. 1884; Іпзіг. 16 р. 130, 1896; Д. Де
рііузідпе (3) 10 р. 5, 1901.
Г. Кеитапп. Ікщц. Апп. 23 р. 1, 1831.
Раре. Ро^. Апп. 120 р. 351, 1863.
Корр. ЬіеЪ. Аппаі. 8ирр1. 3, 1864—65.
Н. А. Гезехусъ. Ж. Ф. X. О. 19 р. 432, 1887; Д. Де рііуз. (2) 7 р. 489, 1888.
Маренинъ. Ж. Р. Ф.-Х. Общ. 40 р. 393, 1908.
Ѵ/аіегтап. РЫІ. Мая. (5) 40 р. 413, 1895; Рііуз. Ееѵ. 4 р. 161, 1896; Іпзіг. 16 р.
121, 1896.
Лерег ипй Віеіпъѵеііг. Ѵегіі. Денізсіі. рііуз. Сее. 5 р. 353, 1903.
16*
244
Теплоемкость.
В. Преображенскій. Ж. Ф. X. О. 15 р. 67, 1883.
Иехмаг. Ргос. К. 8ос. 74 р. 123, 1904; 76 р. 325, 1905; Ргос. 11. Іпзііі. 14 р. 398,
1894; М-те Сигіе, Еесііегсііез виг Іез йиЪзіапсез Касііоасііѵез, 2-ѳ ё(1іі. р. 100.
Ыегпві и. Ыпйетапп. Вегі. Вег. 1910 р. 247.
Ыегпві. Вегі. Вег. 1910 р. 262.
Р/аипбІег. Рода. Апп. 129 р. 102, 1866.
НоІЬеіп. Яізсііг. рііуз. Сііет. 21 р. 178.
\Х;а(І8г2)огіН. 8111. Л. (4) 4 р. 265, 1897.
Ноітап. Ргос. Атег. Акай. 31 р. 252, 1895.
Рісііагсів апб ЬатЬ. Ргос. Атег. Акасі. 40 р. 657, 1905.
РісНаг(І8) Непсіегвоп апсі Виг^евз. Хізсііг. Г. рЬуз. Сііетіе 52 р. 551, 1905.
Магі^пас. Агсіі. 8с. рііуз. (2) 39 р. 217, 1870; 55 р. 113, 1876.
Реггоі. АгсЬ. 8с. рііуз. (3) 32 р. 145, 254, 337, 1894.
Биронъ. Ж. Р. Ф.-Х. Общ., Отд. Хим. 1909 р. 1406.
Къ § 7.
ТоЫа8 Мауег. Оезеіге ипй Мосіійсаііопеп сіез АѴаегтезіоПез. Егіапдап, 1796.
Пиіоп^ еі Реііі. Апп. сіііт. еі рЬуз. (2) 10, 1819.
Беіагіѵе еі Магсеі. Апп. скіт. еі рііуз. (2) 75, 1840: (3) 2, 1841.
Ре^паиіі. Апп. сЫт. еі рііуз. (2) 73 р. 5, 1840; (3) 9 р. 327, 1843; Рода. Апп.
62 р. 55, 1844.
Нігп. Апп. скіт. еі рііуз. (4) 10, 1867.
Терешинъ. Зап. Инст. Путей Сообщ. въ С.-Петерб. 1899.
Сердобинская и Емельянова. Ж. Ф. X. О. 33 р. 23, 1901; Прилож. 25 р. 680, 1901.
Къ § 8.
Му. Ргос. К. 8ос. 41 р. 352, 1887; 47 р. 218, 1889.
Випвеп. АѴ. А. 31 р. 1, 1887.
ѴШх. АѴ. А. 40 р. 438, 1890.
Иеевеп. АѴ. А. 39 р. 131, 1890.
БсНиекагеъѵ. АѴ. А. 59 р. 229, 1896.
Къ § 9.
Р/аипбІег. АѴіеп. Вег. 59 р. 145, 1869; 100 р. 352, 1891.
Кергеапо. С. К. 128 р. 875, 1899.
БсНІатр. АѴ. А. 58 р. 759, 1896.
Апбгеъѵв. Апп. сіііт. еі рііуз. (3) 14 р. 92, 1845.
Нігп. С. К. 70 р. 592, 831, 1870.
Магі&іас. См. къ § 6.
Оитіісіі ипй ѴТіеЬе. \Ѵ. А. 66 р. 530, 1898.
Р/аипсІІег. АѴ. А. 67 р. 439, 1899.
Віаск. См. ЕівсИег, СезсЫсІііе сіег Рііузік, т. VII.
ТІготвеп. Рода. Апп. 142 р. 337, 1871; Л. сіе рііуз. 1 р. 35, 1873.
Коноваловъ. Ж. Ф. X. О. 30 р. 355, 1898; Сііет. СігЪІ. 2 р. 699, 1898.
Биронъ. Ж. Ф. X. О. 30 р. 355, 1898; Сііет. СігЫ. 2 р. 700, 1898.
Къ § 10.
Еерпаиіі. Апп. сіііт. еі рііуз. (3) 1, 1841; Рода. Апп. 53 р. 60, 243, 1841.
Оеіагіѵе еі Магсеі. Рода. Апп. 52 р. 120, 1841.
ѴѴиеІІпег ипй Веііепбог//. Рода. Апп. 133 р. 293, 1868.
Би88у. С. В. 123 р. 305, 1896.
Керргаиіі (плотность вещества). Апп. скіт. еі рііуз. (2) 73, 1840; (3) 9, 1843;
Рода. Апп. 51 р. 44, 1840; 62 р. 53, 1844.
ѴѴіпкеІтапп. \Ѵ. А. 49 р. 401, 1893.
Литература.
245
Зубовъ. Ж. Ф. X. О. 28 р. 22, 1896.
Цингеръ и Щегляевъ. Ж. Ф. X. О. 27 р. 30, 1895.
Оиіощг еі Реііі. Апп. сЫт. еі рЬуз. 7 р. 113, 1818.
Вёбе. Мёт. соигоппёз де ГАсасІ. де Вгихеііез, 27.
Вузігоет. беГѵегз. К. Ѵеі. Ак. РогЬапдІ. 17 р. 307, 1860.
РоиіЦеі. С. В. 21 р. 782, 1845.
УХ/еіпкоІб. Род*д*. Апп. 149 р. 186, 1873.
Ѵіоііе. С. К. 85 р. 543, 1877 (Рі); 87 р. 981, 1878 (Рб); 89 р. 702, 1879 (Уг и Аи)
120 р. 868, 1895 (графитъ).
Ріопскоп. С. К. 102 р. 1122, 1886 (металлы); 106 р. 1344, 1888 (кварцъ).
Оаебе. Бізз. ЕгеіЬиг^ і. Вг. 1902; РЬуз. ХізсЬг. 4 р. 105, 1902.
Абіег. Візз. 2йгісЬ. 1902.
Нагкег. РЫІ. Ма&\ (6) 10 р. 430, 1905.
Бсктііх. Ргос. К. 8ос. 72 р. 177, 1903.
Біиескег. АѴіеп. Вег. 114 р. 657, 1905.
Векп. АѴ. А. 66 р. 236, 1898; В. А. I. р. 257, 1900.
Ріібеп. Ргос. К. 8ос. 66 р. 244, 1900.
И. Р. ѴРеЬег. Ро^К- Апп. 154 р. 367, 1875.
Ілпбпег. Дисс., Егіап^еп, 1903.
Кипг. Апп. д. РЬуз. 14 р. 309, 1904.
Бе Нееп. Виіі. Акад. К. Ъеі^. 5 р. 757, 1883.
Ваіеііі. АШ. К. Гзі. Ѵепеі. (3) 3 р. 35, 1886.
Не88. АѴ. А. 35 р. 410, 1888.
Богоявленскій. Записки Общ. Е. въ Юрьевѣ 13, 1904.
ОЬегко#ег. Дисс. Аасііеп, 1907.
Ьескег. ѴегЬ. д. д. рііуз. Осз. 1907 р. 647; АѴіеп. Вег. 117 р. 111, 1908.
ѴѴі&тб. Апп. д. РЬуз. (4) 22 р. 99, 1907.
Бскіеіі. Дисс. МагЬигд, 1907; Апп. д. РЬуз. (4) 26 р. 201, 1908.
Ріскагх. АѴ. А. 48 р. 708, 1893; 67 р. 704, 1899; МагЬиг^ег Вег. 10]). 194, 1906.
(1гііпеІ8еп. Апп. д. РЬуз. (4) 26 р. 211, 393, 1908; 33 р. 65, 1910.
Ма^пи8 и. Ьіпбетапп. 2ЫсЬг. 1. ЕІекігосЬешіе 16 р. 269, 1910.
Марпи8. Апп. д. РЬуз. (4) 31 р. 597, 1910.
Рогск и. Иогбтеуег. Апп. д. РЬуз. (4) 20 р. 423, 1906.
Иогбтеуег и. ВегпопіИі. ѴегЬ. д. д. рЬуз. Оез. 1907 р. 175.
Еискеп. РЬуз. 2еіізсЬг. 10 р. 86, 1909.
Ріскагб8 а. баск8оп. 2ізсЬг. к рііуз. Сііет. 70 р. 414, 1910.
Иегп8І, Коге/ и. Ьіпбетапп. Вегі. Вег. 1910 р. 247.
Иепі8і. Вегі. Вег. 1910 р. 262; 1911 р. 306.
Ьіпбетапп. Вегі. Вег. 1911 р. 316.
Ыегпзі и. Ьіпбетапп. Вегі. Вег. 1911 р. 494.
Ткіе8еп. ѴегЬ. д. д. рЬуз. Ѳеь. 1908 р. 410, 415, 604, 947.
Теплоемкость жидкостей:
Ре^паиіі. Мёш. де ГАсад. 26 р. 270, 1862.
Нігп. Апп. сЫт. еі рЬуз. (4) 10 р. 32, 1867.
Бе Нееп. Виіі. Ас. К. де Ве1&. (3) 15 р. 522, 1888; ВеіЫ. 12 р. 650, 1888.
Реі8. АѴ. А. 13 р. 447, 1881.
8скі//. ІлеЬ. Апп. 234 р. 300, 1886; 2ізсЬг. [. рііуз. сііет. 1 р. 376, 1887.
Бскиеііег. Ро§-§-. Апп. Ег^Ьд. 5 р. 116, 192, 1871.
ОгіЩікз. РЫІ. Ма^. (5) 39 р. 47, 1895.
Кунбатовъ. Ж. Ф. X. О. 34, хнм. отд. р. 766, 1902; 35, хим. отд. р. 119, 1903.
Вагіоіі. Кепдіс. К. Іпзі. ЬотЪагд. (2) 28, 1895: Хиоѵо Сіт. (4) 2 р. 347, 1895.
Ѵ&іпкеітапп. Ро&§\ Апп. 159 р. 163, 1876.
Вагіоіі е Бігассіаіі. Ыиоѵо Сіт. (4) 1 р. 291, 1895.
Иассагі. Мет. д. К. Асаб. ді Тогіпо 23 р. 594, 18.
246
Теплоемкость.
Реііегзоп шій Нейеішз. Л. Г. ргасі. СЪетіе. Ыеие Еоі^е. 24 р. 135, 1881.
Курбатовъ. Ж. Р. Ф. X. Общ., Отд. Хим., 40 р. 811, 1908.
МіШіаІег. \Ѵ- А. 36 р. 897, 1889.
Ватез апй Сооке. Рііуз. Веѵ. 16 р. 65, 1903; Вер. Вгіі. Аееос. ВеИазі (1902)
р. 530, 1903.
Вгиппег. С. В. 120 р. 912, 1895.
АП. Аппаі. 4. Рііуз. 13 р. 1010, 1904.
Беъѵаг. Ргос. К. 8ос. 68 р. 361, 1901 ; 76 р. 325, 1905.
Бехѵаг (Н2 въ Ра). Тгапз. В. 8ос. ЕЛіпЪ. 1873.
Бшпаз. Агсіі. 8С. рЬув. еі паі. (4) 27 р. 352, 453, 1909.
Мс. Іпіозк. Л. рііуе. сііет. 11 р. 306, 1907.
ВаііеІИ. Рііуз. 2ізс1іг. 9 р. 671, 1908; Л. Ле Рііуз. (4) 7 р. 881, 1908; ВепЛіс. В.
Асс. Л. Ілпсеі (5) 16, I р, 243, 1907; Ы, Сіт. 13 р. 418, 1907.
Ре^паиіі (сплавы). Апп. сіііт. еі рііуз. (3) 1 р. 129, 1841; Ро&&. Апп. 53 р. 60,
88, 243, 1841.
Бскиег. ЛѴ. А. 46 р. 177. 1892.
АиЬеІ. РЪуе. 2ізс1іг. 1 р. 452, 1900.
ЬаЬогйе. Л. Ле рііуз. (3) 5 р. 547, 1896; С. В. 123 р. 227, 1896.
Н. И. Бекетовъ. Ж. Ф. X. О. 11, отд. хим. р. 2, 1879; Сііет. Вег. 12 р. 686, 1879.
Виззу еі Виі^пеі. Апп. сЫт. еі рііуз. (4) 4 р. 5, 1865.
Биргё апй Ра&е. РЫ1. Ма&. (4) 38, 1869; Ро&&. Апп. Ег^Ь. 5 р. 221, 1871.
Ьесііег. \Ѵіеп. Вег. 76 р. 1, 1877.
Ра^Напі. Киоѵо Сіт. (3) 12 р. 229, 1883.
Хеііегтапп. Л. Ле рііуе. 10 р. 312, 1881.
Теплоемкость растворовъ:
Бсішеііег. Ро§&. Апп. 136 р. 70, 1869.
У. Тііотзеп. Ро$&. Апп. 142 р. 337, 1871.
Магі&пас. Апп. сЫт. еі рііуз. (4) 22 р. 385, 1871 ; (5) 8 р. 410, 1876.
Ѵ&іпкеітапп. Ро^. Апп. 149 р. 1, 1873.
Вревскій. Ж. Ф. X. О. 31 р. 164, 1899
Биронъ. Ж. Ф. X. О. 31 р. 171, 1899; 40 р. 339, 1908.
МаНііаз. Л. Ле рііуе. (2) 8 р. 204, 1889; С. В. 107 р. 524, 1888.
Ма&е. Рііуз. Веѵ. 9 р. 65, 1899; 13 р. 91, 1901; 14 р. 193, 1902; 25 р. 171, 1907;
Рйуз. 2ізсЬг. 1 р. 233, 1900; 3 р. 21, 1901 ; 4 р. 156, 1902.
РизсИІ. ЛѴіеп. Вег. 109 р. 981, 1901.
Д. Коноваловъ. Ж. Ф. X. О. 25, отд. хим. р. 216, 1893.
Таттапп. 2І8Сііг. рііуз. Сііет. 18 р. 625, 1895.
ВегіИеІоі. Апп. сЫт. еі рііуе. (5) 4 р. 43, 1875.
Дорошевскій и Роковскій. Ж. Р. Ф. X. Общ. отд. хим. 10 р. 860, 1908; 41 р.
958, 1110, 1909.
ЪМезіп^ег. РЬув. 2еііес1іг. 11 р. 210, 1910.
Къ § 11.
СІ. Махіѵеіі. Хаіиге (англ.) 11 р. 357, 1875; 16 р. 242, 1877; Всіепііііс рареге
2 р. 418.
Воіігтапп. Ро&§\ Апп. 160 р. 175, 1877.
Къ § 12.
Сгахѵ/огй. См. беЫег'з Рііуе. АѴоегіегЪ. 10, 1 АЬіІі. р. 683, 1841.
Ьаѵоізіег еі Ьаріасе. Оеиѵгее Ле Ьаѵоіеіег, 2.
СІётепі еі Безогтез. Лоигп. Ле рііуеідие (Ле Іа Меііегіе) 39.
Сау-Ьиззас. Апп. сЫт. еі рііуз. 81 р. 98, 1812.
Беіагоске еі Вёгагй. Апп. сЫт. еі рііуз. 85 р. 72, 1813.
НаусгаД. ОіІЬ. Апп. 76, 1824; ЕЛіпЪ. Рійі. Тгапе. 10, 1824—26.
Литература.
247
Оеіагіѵе еі Магсеі. Ро^. Апп. 10 р. 363, 1827: 16 р. 340, 1829; 52 р. 126, 1841;
Апп. сіііт. еі рііуе. (2) 75, 1840.
Виегтапп. Род1^. Апп. 41 р. 474, 1837.
Ьоиіе. Ріііі. Тгапе. 1852 р. 65.
Ре^паиіі. Мёт. сіе ГАсапб. 26 р. 58, 1862.
Е. ѴРіейетапп. Ро^. Апп. 157 р. 1, 1876.
УѴіікогѵзкі. б. бе рііуе. (3) 5 р. 123, 1896; Ріііі. Ма^. (5) 42 р. 1, 1896.
НоІЬогп и. Аизііп. Вегі. Вег. 1905 р. 175; \Ѵіее. АЫіапбІ. б. рііуе.-іесііп. Кеісііе-
апеі. 4 р. 133, 1905; Рііуе. Кеѵ. 21 р. 209, 1905.
НоІЬогп и. Неппіп^. Апп. б. Рііуе. (4) 18 р. 739. 1905; 23 р. 809, 1907.
Титіігх. \Ѵіеп. Вег. 108 р. 1395, 1900.
Ьи88апа. Хиоѵо Сіт. (3) 36 р. 5, 70, 130, 1894; (4) 2 р. 327, 18У5; 3 р. 92, 1896;
б р. 81, 1897; 7 р. 61, 365, 1898.
Ье Сііаіеііег. С. К. 104 р. 1780, 1887; Хіесііг. рЬуе. Сііет. 1 р. 456. 1887.
Къ § 13.
Ре^паиіі. См. § 12.
Е. УѴіейетапп. См. § 12.
Ьоіу. Ргос. В. 8ос. 41 р. 352, 1886; 47 р. 218, 1889; 55 р. 390, 1894; Ріііі. Тгапе.
182 А. р. 73, 1892; 185 р. 943, 1894; Сііетіс. Мехѵе. 58 р. 271, 1888.
Ата^аі. С. К. 121 р. 863, 1895; 122 р. 120, 1896; б. бе рііуе. (3) 5 р. 114, 1896.
УМікочѵзкі. См. § 12.
Ьіпйе. Миепсіі. Вег. 1897 р. 485.
Маііагй еі Ье Сііаіеііег. С. к. 91 р. 825, 1880; 93 р. 145, 962, 1014, 1076, 1881;
Аппаіее бее Міпее (8) 4 р. 274, 1883.
Ѵіеіііе. С. К. 96 р. 1358, 1883.
ВегНгеІоі еі Ѵіеіііе. С. К. 98 р. 545, 601, 770, 852, 1884; Апп. б. Сіііт. еі Рііуе.
(6) 4 р. 13, 1885.
Ьап^еп. ЕогесІіші^еагЬеііеп бее Ѵегеіпе беиіесііег Іп&ещеиге, НеГі 8 р. 1, 1903.
Къ § 14.
Сіётепі еі Ое8огте8. боигп. бе рііуе. (бе Іа Меііегіе) 89 р. 321, 428, 1819.
Мапеиѵгіег (Исторія способа Сіётепі и Вееогтее’а) б. бе рііуе. (3) 4 р. 341, 1895.
Н. Негіх. См. ХѴиеІІпег, ЬеІігЪ. бег Ехрегітепіаірііуеік 2 р. 541, 1896 (изд. 5-ое).
Внууп^ейаи'ш. б. бе рііуе. (3) 6 р. 129, 1897.
Сау-Ьи88ас и ѴѴеІіег. Апп. сЫт. еі рііуе. (1) 20, 1822.
ѴѴеІ88Ьас1і. Сіѵіііп&епіеиг. Хеие РоЫе 5 р. 46, 1859.
Нігп. Тііёогіе тёсапісре бе 1а сііаіеиг. 1 р. 103, Рагіе, 1875 (изд. 3-ье).
Ма88оп. Апп. сіііт. еі рііуе. (3) 53, 1858.
А88тапп. Ро^§\ Апп. 85 р. 1, 1852.
Нагітапп. Аппаі. б Рііуе (4) 18 р. 252, -1905.
Оге8ег. См. ЬекгЪ. бег Ехрегіт.-РІіубік ѵоп Киеір. 4.
Сагіп. Апп. сіііт. еі рііуе. (3) 67, 1862; (4) 20 р. 1869.
КоігІгаи8с1і. Ро^. Апп. 136 р. (518, 1869.
Роепі^еп. Ро§*^. Апп. 141 р. 552, 1870 ; 148 р. 580, 1873.
Радиеі. б. бе рііуе. (2) 4 р. 30, 1885.
Р А. Миеііег. \Ѵ. А. 18 р. 94, 1883.
Ьиттег ипй Ргіп^кеіт. \Ѵ. А. 64 р. 555, 1898 Подробно будетъ напечатано
въ изданіяхъ йтіікеопіап Іпеіііиііоп, \Ѵае1ііп$іоп.
Макоіѵег. Ріііі. Ма&. 6) 5 р. 1903.
Ьатіп еі рісііагй. С. К. 71 р. 336, 1870.
Кипйі. Роз’&. Апп. 127 р. 487, 1865; 135 р. 347, 1868.
Кипйі ипй УѴагЬиг^. Ро^. Апп. 157 р. 353, 1876.
Зігескег. АѴ. А. 13 р. 20, 1881; 17 р. 85, 1882,
248
Теплоемкость.
КаІ8ег. XV. А. 2 р. 218, 1877.
ѴѴиеІІпег. XV. А. 4 р. 321, 1878.
Сарзііск. Ргос. К. 8ос. 57 р. 322, 1895; РЫІ. Тгапз. 185, А р. 1, 1894; 186,
А р. 567, 1895; СЬет. Ме\ѵз 68 р. 39, 1893.
Каіекпе. Апп. 6. РЬуз. (4) 11 р. 225, 1903.
Уликою 8кі. ВиИ. іпіегп. сіе Сгасоѵіе 1899 р. 138.
8іеѵеп8, ѴегЫ 6. сІеигзсЬ. рііуз. Оез. 3 р. 56, 1901 ; В. А. р. 285, 1902.
Ѵаіепііпег. МйпсЫ Віігип^зЬег. 1903 р. 691; Апп. <1. Рііуз. (4) 15 р. 74, 1904.
Тгеііх. Дисс., Вопп 1903.
Коск. МйпсЬ. Вег. 23, II р. 379, 1907; 28 р. 67, 1908; Апп. 6. Рііуз. (4) 26 р. 551,
1908; 27 р. 311, 1908.
Рйгзіепаи. Апп. а. Рііуз. (4) 27 р. 737, 1908; X егЫ 4. (I. рііуз. Оез. 1908 р. 968;
1909 р. 137.
Мапеиѵгіег. (Новый способъ). С. К. 120 р. 1398; 1895; Апп. сЫт. еі рііуз. (7)6
р. 321, 1895; Іпзіг. 16 р. 91, 1896.
Мапеиѵгіег еі Роигпіег. С. К. 123 р. 228, 1896; 124 р. 183, 1897.
Мапеиѵгіег (Обзоръ способовъ). Л. сі. рііуз. (3) 4 р. 445, 1895.
Ваііеііі. Карр. ргёз. аи Соп&гёз іпіегпаі. бе рЬузідие 1 р. 682, Рагіз 190<>.
Къ § 15.
Риіощ? еі Реііі. Апп. сЫт. еі рііуз. 10 р. 395, 1819.
Ре^паиіі. Апп. сЫт. еі рііуз. (2) 73 р. 5, 1840; (3) 1 р. 129. 1841: 9 р. 322, 1843,
Ро^. Апп. 51 р. 44, 213, 1840; 53 р. 60, 243, 1841; 62 р. 50, 1844.
Ріскаг(І8. Сііет. Хелѵз 65 р. 97.
Векп, XV. А. 66 р. 236, 1898; О. А. 1 р. 257, 1900.
Вопі8ске,ш. Візз. Хиегісіі. 1900; ВеіЫ. 25 р. 178, 1901.
ТіШеп. Ргос. К. 8ос. 66 р. 244, 1900; 71 р. 220, 1903; 73 р. 226, 1901; Сііет.
Хехѵз 89 р. 165, 1904.
Кіскагг (Смѣси). Апп. сі. Рііуз. (4) 19 р. 639, 1906; МагЬиг^. Вег. 1904 р. 57.
Карр. Дисс. МагЬиг^, 1907.
Кошовичъ. Ж. Р. Ф.-Х. Общ. 40 р. 16, 1908.
}асоЬ8. Дисс. МагЬиг^, 1904.
Ѵіоііе. С. К. 89 р. 702, 1879.
Вип8еп. Ро^. Апп. 141 р. 1, 1870.
Вскиех. XV. А. 46 р. 177, 1892.
Корр. ЬіеЪ. Апп. 8ирр1. 3 р. 1, 290, 307, 1864—65.
Ьогепг. XV. А. 13 р. 422, 1881.
Ѵ/іпкеІтапп. Ро&$. Апп. 159 р. 152, 1876.
Н. Р. УѴеЬег. Ро^. Апп. 154 р, 367, 1875.
Ье Скаіеііег. С. К. 116 р. 1051, 1893.
МоІ88ап еі Оаиііег. Апп. сЫт. еі рііуз. (7) 7 р. 568, 1896.
СІаи8Іи8. Ро&$. Апп. 116 р. 100, 1862.
Яіскагг. XV. А. 48 р. 708, 1893; 67 р. 704, 1899; ѴегЫ 6. сІеиізсЬ. рііуз. Оез. 1
р. 47, 1899; ІМаіинѵізз. КипбзсЬаи 9 р. 221, 237, 1894; РезізсЬг. 6. рЫІ. Еакиіі. яи
ОгеИзхѵаІсІ (ги ЕЬгеп ѵ. Н. Ьітргісііі) 1900; Вег. (1. Оез. гигВеібгсІ. 0. Ыаіипѵ. МагЬиг^
1904 р. 61, 1906 р. 185; ХізсЬг. 1 апог^. СЬетіе 58 р. 356, 1908; 59 р. 146, 1908.
Зігеіпіх. Апп. 6. РЬуз. (4) 8 р. 847, 1902.
Ые/. Меуег. ХѴіеп. Вег. 109 р. 405, 1901; В. А. 2 р. 135, 1900.
Воіігтапп. ХѴіеп. Вег. 63 р. 731, 1871.
Еіпзіеіп. Апп. 6. РЬуз. (4) 22 р. 180, 1907; 34 р. 170, 1911.
Ткіезеп. ѴегЬ. 6. 6. рііуз. Оез. 1908 р. 410, 415, 604.
Ма^пи8 и. Ышіетапп. 2ізсЬг. I. ЕІекігосЬетіе 16 р. 269, 1910.
Ма^пи8. См. Кегп8І, Л. бе РЬуз. (4) 9 р. 729, 1910.
Кегп8і и, ііпсіетапп, Вегі. Вег. 1911 р. 494.
Литература.
219
Ьіпсіетапп. Вегі. Вег. 1911 р. 316.
Ѵ^іе^апд. Рііуз. 2ізсЬг. 8 р. 344, 1907; 9 р. 66, 1908; Апп. сі. РИуз. (4) 24 р. 601,
1907; МагЬигдег Вег. 1906 р. 185.
Рокіапд. Рііуз. Хізсііг. 7 р. 832, 1906; 8 р. 512, 1907.
Ьеъоіз. 2І8СІ1Г. Г. шюг§\ СЪетіе 55 р. 200, 1907; 4. Атег. сііет. 8ос. 29 р. 1165-
1516, 1907.
ЬИттек Апп.*с1. Рііуз. (4) 16 р. 551, 1905.
Е. Е. Иеитапп. Ро^. Апп. 23 р. 32, 1831.
Раре. Ро^. Апп. 120 р. 337, 579, 1863; 122 р. 408, 1864; 123 р. 277, 1864.
}оиІе. РЫ1. Ма^. (3) 25 р. 334, 1844.
ЧѴоезіуп. Апп. сЫт. еі ркув. (3) 23 р. 295, 1848; Ро^г. Апп. 76 р. 129, 1849.
Ѵап АиЬеІ. 3. сіе рііуе. (3) 10 р. 36, 1901.
ѴМпкеІтапп (законъ Зоиіе’я и Корр’а). \Ѵ. А. 49 р. 401, 1893.
Оатіег. С. К. 35 р. 278, 1852.
Реіз. \Ѵ. А. 13 р. 447, 1881.
8скір\ ІЛеЬ. Апп. 234 р. 300, 1886.
А. Надеждинъ. Ж. Ф. X. О. 16 р. 222, 1884.
Маске. \Ѵіеп. Вег. 110 р. 176, 1901.
Вегікеіоі. С. К. 124 р. 119, 1897.
8окпске. Миепсіі. Вег. 27 р. 337, 1897.
Иаитапп. ЬіеЪ. Апп. 162, 1872.
Воіігтапп. С. К. 127 р. 1009, 1898.
8іаі%тие11ег. \Ѵ. А. 65 р. 655, 670, 1899.
Ризскі. АѴіеп. Вег. 112 р. 1230, 1903.
Різскег. ТИзсІіг. 1. Маііі. и. Рііуе. 51 р. 126, 1905.
Е. ѴРіесІетапп. АѴ. А. 2 р. 195, 1877.
Воупіоп. Рііуе. Кеѵ. 12 р. 353, 1901.
Лапз. РЫ1. Ма^. (6) 2 р. 638, 1901.
ГЛАВА ПЯТАЯ.
Переходъ различныхъ формъ энергіи въ энергію тепловую.
Термохимическія явленія.
§ 1, Источники тепла. Теплота, какъ форма энергіи, можетъ быть
получена только преобразованіемъ изъ запаса другой, уже имѣющейся
формы энергіи, причемъ образующаяся теплота д количественно должна
быть эквивалентна исчезнувшей энергіи е другого рода. Если измѣ-
рять д и е эквивалентными единицами, т.-е. такими, которыя при затратѣ
даютъ одинаковыя количества работы, то мы имѣемъ простое равен-
ство д = е. Различныя формы энергіи, изъ которыхъ образуется энер-
гія тепловая, представляютъ т. наз. источники тепло т ы. Относи-
тельно этихъ источниковъ укоренилась нѣсколько неправильная термино-
логія, а именно иногда называютъ < источниками теплоты тѣ явленія,
которыя <> б у сл о в л и в а ю т ъ или сопровождаютъ переходъ энер-
гіи е въ тепловую д. Такъ напр. постоянно причисляютъ ударъ и
треніе къ источникамъ теплоты, хотя мы имѣемъ здѣсь дѣло съ пере-
ходомъ кинетической энергіи движенія цѣлыхъ тѣлъ въ энергію тепло-
250
Теплоемкость.
вую, каковой переходъ происходитъ при ударѣ и при треніи; источ-
никомъ здѣсь служитъ энергія движенія тѣлъ. Подобнымъ же образомъ
указаніе на «горѣніе тѣлъ», на «химическія реакціи», какъ
на источники тепла, не вполнѣ точно : истиннымъ источникомъ является
здѣсь потенціальная химическая энергія разнородныхъ тѣлъ. Сжатіе
тѣлъ, какъ искусственно вызванное, напр. въ воздушномъ огнивѣ, такъ и
само собою образующееся вслѣдствіе взаимнаго тяготѣнія частицъ тѣлъ
(^небесныя свѣтила), также не должно быть причислено къ источникамъ те-
плоты. Въ первомъ случаѣ источникомъ служитъ движеніе сдавливаю-
щаго поршня или, если идти далѣе назадъ, та энергія, на счетъ кото-
рой поршень былъ приведенъ въ движеніе; во второмъ случаѣ мы имѣ-
емъ потенціальную энергію притягивающихся массъ, которая прежде
всего переходитъ въ энергію движенія частицъ.
Многіе случаи образованія теплоты изъ другихъ формъ энергіи уже
разсмотрѣны нами или будутъ разсмотрѣны въ тѣхъ отдѣлахъ нашего
курса, которые трактуютъ именно объ этихъ формахъ энергіи. Въ этой
главѣ мы даемъ обзоръ различныхъ случаевъ образованія тепловой энер-
гіи, прибавляя немногое къ тому, что нами уже было разсмотрѣно раньше.
На одномъ только случаѣ, который раньше не приходилось разсматри-
вать, мы здѣсь остановимся подробнѣе, именно на случаѣ перехода химиче-
ской энергіи въ энергію тепловую, т.-е. на случаѣ такъ наз. т е р м о х и м и -
ч е с к и х ъ явленій.
Мы считаемъ извѣстными понятія объ эквивалентности теплоты и
работы, о механическомъ эквивалентѣ Е теплоты и термическомъ эквива-
лентѣ работы А = 1: Е, Эти понятія были выяснены въ т. I и мы ими не-
однократно пользовались въ предыдущихъ главахъ этого тома. Разборъ
способовъ опредѣленія величины Е будетъ помѣщенъ ниже
Разсматривая случаи превращенія энергіи, мы въ этой, а также въ
слѣдующей гл. VI совершенно оставляемъ въ сторонѣ все, что находится
въ той или другой связи съ т. наз. вторымъ началомъ термодинамики.
Составимъ обзоръ случаевъ перехода различныхъ формъ энергіи въ
энергію тепловую.
I. Энергія движенія тѣлъ. Если масса т движется со скоростью
то энергія е движенія равна — тѵ^ если элементы ат массы т движутся
1 С
съ различными скоростями, то ^ = - I ѵ2ат, гдѣ интегралъ распростри-
Сі I
йенъ на всю движущуюся массу. Для случая вращенія мы имѣли фор-
мулу е = Адо2, гдѣ К моментъ инерціи тѣла относительно оси враще-
Сі
нія, со угловая скорость (т. I). Если т и ѵ выражены въ С. О. 5. еди-
ницахъ, то е выразится въ эргахъ: ІО7 эрговъ = 0,24 мал. калоріи. Для
случая поступательнаго движенія одного тѣла имѣемъ поэтому
1 .л 12/т>2 .
д = . 10 ' . 0,24 мал. кал. — мал, кал, . . . (1)
Источники тепла.
251
Для случая вращающагося тѣла
д = * Кео2. ІО-7.0,24 ѵіал. кал. = мал. кал. ... (2)
Для общаго случая движенія тѣла
12 і ѵЦт
д = - 10у - мал. кал..................(3)
Если только часть энергіи движенія перешла въ тепловую, причемъ
скорости Ѵо и соо перешли въ ѵ или со, то д вычисляется по формуламъ
12ш(^02 — ^2)
д =-----— мал. кал.
12 АГ(соо2—ш2)
д — --- мал. кал.
10 .... (4)
12 I (г>02 — г*2) сіпг
д ’ —--------мал. кал.
И. Лучистая энергія. Когда лучистая энергія распростра-
няясь. доходитъ до эфира, наполняющаго промежутки между части-
цами матеріи (по принятой нами терминологіи, т. II) то она отчасти,
а иногда и вся переходитъ въ энергію тепловую; въ этомъ случаѣ гово-
рятъ, что лучистая энергія была поглощена даннымъ тѣломъ. Та-
кое поглощеніе можетъ закончиться на весьма небольшомъ разстояніи
отъ поверхности тѣла; но оно можетъ также продолжаться на всемъ
пути прохожденія лучей черезъ тѣло. Въ первомъ случаѣ говорятъ о
поверхностномъ, во второмъ о внутреннемъ поглощеніи
лучистой энергіи. Какъ при всякомъ притокѣ тепловой энергіи къ тѣлу,
такъ и въ этомъ случаѣ, часть поглощенной энергіи тратится на вну-
треннюю и, въ общемъ случаѣ, на внѣшнюю работу. Кромѣ того часть
лучистой энергіи, можетъ быть, и непосредственно переходитъ въ другія
формы энергіи, напр. въ энергію химическую.
Какая доля лучистой энергіи поглощается тѣломъ, зависитъ отъ
спеціальныхъ свойствъ, а именно отъ т. наз. поглощательной способности
послѣдняго. Этотъ вопросъ былъ разсмотрѣнъ въ т. П.
Непосредственныхъ способовъ измѣренія лучистой энергіи не суще-
ствуетъ. Для ея измѣренія необходимо превратить ее, по возможности
цѣликомъ, въ энергію тепловую, которую затѣмъ и измѣряютъ.
Интересный примѣръ превращенія лучистой энергіи въ тепловую,
часть которой тутъ же тратится на работу, представляетъ радіометръ,
изобрѣтенный въ 1873 г. Сгоокез’омъ. Обыкновенный радіометръ со-
стоитъ изъ стекляннаго шаровиднаго или грушевиднаго сосуда (рис. 82),
252
Термохимія.
изъ котораго по возможности выкачанъ воздухъ. На вертикальномъ остріѣ,
находящемся внутри прибора, лежитъ стеклянная шапочка, къ которой
Рис. 82.
прикрѣплены четыре вертикально располо-
женныя слюдяныя или алюминіевыя пла-
стинки, вычерненныя съ одной стороны
сажей. Если на этотъ приборъ падаютъ
лучи солнца пли иного источника лучистой
энергіи, то подвижная часть начинаетъ
быстро вращаться, и притомъ такъ, что
не вычерненныя стороны пластинокъ дви-
жутся впередъ.
Для объясненія вращенія крыльевъ
радіометра были предложены различныя
гипотезы. Такъ Кеупоісів полагалъ,
что на вычерненной сторонѣ происходитъ
испареніе слѣдовъ жидкости (воды, ртути),
п что движеніе вызывается упругостью
образующихся паровъ. 2 о е 11 п е г допу-
скалъ испареніе самаго стекла, алюминія
или сажи подъ вліяніемъ падающихъ на
нихъ лучей. Нѣкоторые ученые полагали,
что въ радіометрѣ играютъ роль электри-
ческія явленія. Всѣ эти гипотезы въ на-
стоящее время оставлены и движеніе при-
писывается вліянію слѣдовъ газа, оставшагося внутри радіометра. Вычер-
ненная сторона сильнѣе нагрѣвается, чѣмъ блестящая, вслѣдствіе чего мо-
лекулы газа отскакиваютъ отъ первой съ большею скоростью, чѣмъ отъ
второй. Онѣ получаютъ какъ бы ударъ отъ черной стороны, которая по
закону равенства дѣйствій и противодѣйствій при этомъ подвергается да-
вленію, заставляющему ее отступать назадъ. Что силы, вращающія радіо-
метръ дѣйствительно внутреннія, доказывается тѣмъ, что если радіометръ
заставить плавать, то крылья вращаются въ одну сторону, стеклянная обо-
лочка въ противоположную.
Оопіе (1899) измѣрилъ величину давленія, дѣйствующаго на крылья
радіометра. Для случая, когда источникъ находится на разстояніи 50 см.
отъ радіометра, онъ нашелъ слѣдующія давленія, выраженныя въ 10 5 дина
на кв. сантиметръ: лампочка Н е 1 п е г - А11 е п е с к а (т. II) 7—8, горѣлка
А и е г’а 40—50, аргантовая горѣлка 70—80 и т. д. Давленіе газа въ радіо-
метрѣ было менѣе 0,0027 мм.; при большей упругости газа давленіе, выз-
ванное свѣтомъ было меньше. Подобные же результаты нашелъ В і е с к е.
Указаніе на обзоръ обширной литературы, почти цѣликомъ отно-
сящейся къ 1874—1879 г., можно найти ниже (см. также т. II).
III. Энергія электрическаго тока. Переходъ энергіи
электрическаго тока въ энергію тепловую будетъ разсмотрѣнъ въ т. IV.
Ради полноты приведемъ относящуюся сюда формулу
Источники тепла.
253
е2
д — (\2Аі?гі — 0,2ѣіеі = 0,24 і мал. кал.
(5)
гдѣ і сила тока въ амперахъ, г сопротивленіе въ омахъ того проводника,
въ которомъ появляется теплота е электродвижущая сила, дѣйствую-
щая на этотъ проводникъ или разность потенціаловъ на его концахъ-
выраженная въ вольтахъ, и, наконецъ, і время (въ секундахъ), втеченіе
котораго токъ проходилъ черезъ проводникъ.
IV. Потенціальная энергія тѣлъ, притягивающихся
по закону всемірнаго тяготѣнія. Массы пі и т , находящіяся
на разстояніи р другъ отъ друга, притягиваются съ силою
= С _2 ДИН...........................(6)
V
гдѣ С = 1 : 14900000, если т и пі' выражены въ граммахъ, а р въ сан-
тиметрахъ (т. I). Потенціалъ Ѵ7 ихъ друга на друга (т. I) равенъ
..................................................................(7)
Когда разстояніе уменьшится отъ р0 до р и потенціалъ соотвѣт-
ственно отъ НТо до Ѵ7, то потерянна я энергія е, равная произве-
денной работѣ г, равна
Въ случаѣ двухъ отдѣльныхъ массъ пі и т' потенціальная энергія
переходитъ сначала въ энергію движенія этихъ массъ и, при отсутствіи
сопротивляющейся среды, она только при соудареніи тѣлъ переходитъ въ
энергію тепловую. Если даны два однородные шара (или два шара,
плотности которыхъ суть функціи разстоянія точекъ отъ ихъ центровъ),
радіусы которыхъ и Т?2, и если центры шаровъ находятся на разсто-
яніи р друга отъ друга, то теплота д, которая можетъ развиться, если
эти шары, взаимно притягиваясь, дойдутъ до соприкосновенія, равна
піт' тпі'\ ЪЗАСпіт ( 1 1\
-г) 0|”' = 10’ <9)
Мы назвали потенціаломъ системы самой на себя величину
ту 1 ѵ.уі пгпі
г.....................................(10)
гдѣ знакъ 22 обозначаетъ, что каждая частица системы должна быть
комбинирована со всѣми остальными частицами. Если система перей-
детъ изъ начальнаго расположенія въ новое и при этомъ ея потенціалъ
на самое себя измѣнится отъ Ѵ70 до то силы взаимнаго тяготѣнія ча-
стицъ произведутъ работу ІѴ0. Если вся система состоитъ изъ раз-
розненныхъ отдѣльныхъ частицъ или даже молекулъ, непрерывно между
собою сталкивающихся, и слѣд. по свсем) строенію напоминаетъ газъ
Массагі-
МетГй. К. Дипц.
254
Термохимія.
или паръ, то можно допустить, что вся работа П/— П/о дастъ въ резуль-
татѣ теплоту такъ что
/IV/ IV/, 24(ІГ—ІГо)
^==(Ц7—и/0) эрговъ—- - н мал. кал. . . (11)
Если IV7 обозначаетъ максимальное значеніе, до котораго можетъ дойти
потенціалъ системы самой на себя, то запасъ е потенціальной энергіи
въ системѣ вообще равенъ
ѴГ.........................(12)
Онъ дѣлается равнымъ нулю при Й7 = Ѵ7т, т.-е. когда система достигла
наибольшаго возможнаго сгущенія. При безконечно разрозненномъ на-
чальномъ состояніи системы имѣемъ ІѴ'о = 0, такъ что вся теплота, вы-
дѣлившаяся при образованіи системы изъ безконечно разрознен-
наго состоянія, равна
24 Ѵ7т ,іа,
д = эрговъ = -д мал- кал........................
причемъ теплота, образовавшаяся на счетъ другихъ формъ энергіи, напр.
химической, не принята во вниманіе.
Для однороднаго шара мы вывели формулу (т. Т) Ѵ7 =
16 4
= СгіЧ&Рр Вводя массу М = — лкк(\ мы получаемъ
15 3
ІГ/-3^2
5/? ’
(14)
Формула (13) даетъ намъ теплоту образованія однород-
наго шара изъ безконечно разрозненнаго состоянія:
_72СТИ2
Я “ 5,109/?
мал. кал.
(15)
гдѣ масса Л4 шара и его радіусъ /? должны быть выражены въ граммахъ
и сантиметрахъ; С = 1 :14900000.
Если шарь, радіусъ котораго /?, сгустится и мы новый радіусъ обо-
значимъ черезъ /?', то при этомъ сгущеніи выдѣлится количество те-
плоты, равное
72СЛЕ/1 1\
Ч = ‘5 лоф .............(16)
1 гѵ п — 1 п
Если радіусъ уменьшился на — тую долю, т.-е. если /? = ^ к, то
72С/И2 п 7,
« = 5Д05(^і)Л ................(1”
Если вставить численное значеніе С и выразитъ д въ большихъ кало-
ріяхъ, то получается
0,9 7/И2 „
1О'«(п-1)/? 00лыи-калор.............(18)
Источники тейла
255
Весьма вѣроятно, что главный источникъ солнечной теплоты
и слѣдуетъ искать въ томъ, что масса солнца продолжаетъ сгущаться.
По формулѣ (18) можно приблизительно вычислить, какое количество те-
плоты должно выдѣлиться, если радіусъ солнца уменьшится напр. на
0,0001 своей величины; тогда п = 10000. Вставляя вмѣсто М массу
солнца въ граммахъ, и вмѣсто А? его радіусъ въ сантиметрахъ, получа-
емъ количество теплоты, которое могло бы нагрѣть массу воды, равную
массѣ солнца, на 2860°. Этого количества тепла хватитъ примѣрно на
2290 лѣтъ при томъ тепловомъ лучеиспусканіи, которымъ нынѣ обла-
даетъ солнце.
V. Энергія электрическаго заряда. Вопросъ о пе-
реходѣ энергіи заряда въ энергію тепловую будетъ разсмотрѣнъ въ
т. IV. Ради полноты приводимъ здѣсь выраженіе для количества д те-
плоты, выдѣляющейся при разрядѣ, если таковой не сопровождается по-
сторонней работой:
Е2
д — 0,12 ѴЕ — 0,12 = 0,12с V2 мал. кал.......(19)
гдѣ V потенціалъ въ вольтахъ, до котораго заряженъ проводникъ, с его
емкость въ фарадахъ и Е его зарядъ въ кулонахъ.
VI. X и м и ч е с к а я э н е р г і я. Ея переходъ въ энергію тепловую
мы разсмотримъ въ слѣдующихъ параграфахъ этой главы.
VII. Молекулярная энергія. Можно указать на цѣлый
рядъ случаевъ возникновенія тепловой энергій, которые не могутъ быть
отнесены къ вышеуказаннымъ и въ которыхъ источникомъ тепла явля-
ется энергія молекулярная. Укажемъ на нѣкоторые изъ этихъ случаевъ.
1. При переходѣ насыщеннаго пара въ жидкость, или жидкости вь
твердое тѣло выдѣляется «скрытая теплота. Это явленіе мы впо-
слѣдствіи разсмотримъ подробно.
2. При уменьшеніи поверхности жидкости произво-
дится работа молекулярными силами, обусловливающими возникновеніе
поверхностнаго натяженія (т. I). Мы ниже разсмотримъ это явленіе и
покажемъ, что напр. при уменьшеніи поверхности данной массы воды на
1 кв. см. выдѣляется 10~6 малой калоріи.
3. Измѣненіе объема или длины твердаго тѣла также
можетъ сопровождаться переходомъ потенціальной молекулярной энергіи
въ энергію тепловую.
4. Интересный случай выдѣленія тепла наблюдается, когда сухой
порошокъ смѣшивается съ какою-либо жидкостью. Это
явленіе открылъ Ропіііеі (1822); имъ занимались очень многіе уче-
ные, напр. Лпп^к (1865), Меіеепет, Сапіопі (1866), Ьа^ег^геп
(1899), АѴіесІетапп и Ьіійекіпд (1885), Магііпі Ц896—1904),
ВеНаіі (1900), ЬіпеЬаг^ег (1901), Ратке (1902), Веііакі и Рі-
паггі (1902). 8сЬлѵа1Ъе (1905) и др.
256
Термохимія.
Полный указатель литературы находится въ работѣ Зсйѵ^аіЬе.
Подробное сопоставленіе всѣхъ теорій сдѣлано въ послѣдней работѣ М а г-
ііпі (1904).
По мнѣнію нѣкоторыхъ ученыхъ, причина выдѣленія тепла заклю-
чается въ уплотненіи жидкости, вызванномъ молекулярными силами. М а г -
і і п і полагалъ, что жидкость на поверхностяхъ зеренъ затвердѣваетъ, при-
чемъ выдѣляется скрытая теплота плавленія. Р а г к 8 нашелъ, что прибавле-
ніе воды къ кремневой кислотѣ, песку или порошку стекла при 7° вызыва-
етъ выдѣленіе количества теплоты, которое пропорціонально поверхности
всѣхъ зеренъ, и въ среднемъ равно 0,00105 мал. калоріи на 1 кв. см. по-
верхности. Изслѣдованія Веііаіі и Гіпагяі не согласуются съ этими
результатами. 4 и п к впервые замѣтилъ, что вода при температурѣ
ниже 4° вызываетъ не нагрѣваніе песка, но его охлажденіе, что говоритъ
въ пользу теоріи сжимаемости, такъ какъ, какъ мы увидимъ ниже (гл. IX
§ 8), вода при сжатіи нагрѣвается при температурѣ выше 4° и охлажда-
ется при температурѣ ниже 4°. 8сЬііѵа1Ье (1905) подвердилъ это на-
блюденіе для песка и кремнезема. При 4° онъ не нашелъ никакого из-
мѣненія температуры при смачиваніи. Максимумъ развитія теплоты на-
ходится при вполнѣ опредѣленномъ соотношеніи смѣшиваемыхъ веществъ.
Наибольшее ея развитіе онъ нашелъ при смѣшеніи 10 гр. кремнезема съ
20 гр. воды при 16,3°. Количество развивавшейся при этомъ теплоты
достигало 6,16 мал. калорій.
VIII. Интраатомная энергія. Соединенія радія непре-
рывно выдѣляютъ теплоту. Р. Ситіе и А. ЬаЪогде находятъ, что
одинъ граммъ чистаго хлористаго радія выдѣляетъ въ одинъ часъ около
100 малыхъ калорій. Предполагаютъ, что источникомъ этой теплоты слу-
житъ интраатомная энергія. Допуская, что химическій атомъ въ дѣй-
ствительности обладаете сложными, строеніемъ, можно себѣ представить,
что въ немъ существуетъ и запасъ» особаго рода внутренней, ему прису-
щей энергіи.
§ 2. Основныя положенія термохиміи. Совокупность щухъ или
большаго числа химически разнородныхъ веществъ, способныхъ вступить
въ химическую реакцію, и взятыхъ въ такихъ количествахъ, въ какихъ
они входятъ въ эту реакцію, обладаетъ нѣкоторымъ запасомъ потенціаль-
ной химической энергіи, которая можетъ быть измѣрена количествомъ
теплоты выдѣляющейся во время этой реакціи. Изслѣдованіемъ» те-
пловыхъ» явленій, сопровождающихъ химическія реакціи, занимается тер-
мохимія. Она составляетъ отдѣлъ химіи и подробно излагается въ
курсахъ химіи, а также въ отдѣльныхъ ей посвященныхъ сочиненіяхъ.
Однако общія ея положенія, методы, которыми она пользуется, и нѣко-
торые изъ добытыхъ ею результатовъ представляютъ большой интересъ и
для физики, а потому мы считаемъ необходимымъ хотя бы вкратцѣ ихъ
изложить.
Термохимія имѣетъ большое значеніе для техники, добывающей не-
обходимые ей запасы энергіи путемъ сжиганія различныхъ горючихъ ма-
Основныя положенія.
257
теріаловъ, и для физіологіи, разсматривающей различныя явленія, проис-
ходящія въ тѣлѣ животныхъ, теплота которыхъ является результатомъ
опредѣленныхъ химическихъ реакцій.
Явленія растворенія, стоящія на рубежѣ явленій химическихъ
и физическихъ, также сопровождаются выдѣленіемъ или поглощеніемъ те-
пла ; они неразрывно сопровождаютъ многія химическія реакціи, а потому
обыкновенно также разсматриваются въ работахъ, посвященныхъ термохи-
міи. Мы, однако, здѣсь не будемъ останавливаться на явленіяхъ раство-
ренія, отнеся ихъ къ тѣмъ главамъ этого тома, въ которыхъ вообще раз-
сматривается переходъ тѣлъ изъ одного состоянія въ другое.
Укажемъ сперва, какимъ образомъ изображаются результаты термо-
химическихъ изслѣдованіи въ видѣ уравненій. Для этого пишутъ слѣва
химическія формулы веществъ, имѣвшихся до реакціи, справа формулы
веществъ, явившихся какъ результатъ реакціи, плюсъ то количество д
теплоты, которое выдѣлилось во время реакціи. Напр.:
С -ф- О2 = СО2 4“ д . ..........(20,а)
Иногда формулы ставятъ въ скобкахъ
(С) + (О2) = (СО2) + ^.................0ЭД
Когда самый ходъ реакціи не можетъ подлежать сомнѣнію, пишутъ
формулы веществъ, вступающихъ въ реакцію, рядомъ въ скобкахъ, от-
дѣляя ихъ запятыми, напр.
(ЯС/, ЫаНО)^д.....................(20,с)
Пользуясь числовыми результатами термохимическихъ изслѣдованій,
необходимо обращать вниманіе на то, въ какихъ единицахъ выражена те-
плота д и къ какимъ количествамъ реагирующихъ веществъ она
относится. Теплота д выражается въ малыхъ или въ большихъ калоріяхъ;
О 81 а 1 (1 выражаетъ д въ особой единицѣ, которую онъ обозначаетъ
черезъ К, и которая равна количеству теплоты, потребному для нагрѣва-
нія 1 гр. воды оть 0° до 100°. Приблизительно К = 100 мал. кал. =
— 0,1 больш. кал.
Теплоту д относятъ или кь опредѣленному" и всегда одинаковому
вѣсовому количеству одного изъ веществъ, вступающихъ вь реакцію,
или къ граммъ-молекулѣ всѣхъ этихъ веществъ, т.-е. къ /х граммамъ каж-
даго изъ нихъ, гдѣ /х ихъ молекулярный вѣсъ. Такъ напр. можно харак-
теризовать тепловыя явленія, сопровождающія окисленіе и горѣніе тѣлъ,
указывая то количество тепла д, которое выдѣляется при окисленіи вѣ-
совой единицы тѣла или при затратѣ вѣсовой единицы кислорода, или
при окисленіи ц граммовъ вещества, гдѣ ц молекулярный вѣсъ послѣд-
няго. Такъ напр. теплота горѣнія этилена (С2Я4) въ нѣкоторыхъ сочи-
неніяхъ приводится равною 11,88 б. кал., въ другихъ равною 333,3 б. кал.
Первое число относится къ 1 гр. этилена, второе къ 28 гр., ибо молеку-
лярный вѣсъ /х этилена равенъ 28.
КУРСЪ ФИЗИКИ О ХВОЛЬСОНА. Т. III, изд. 3-е.
17
258
Термохимія.
Въ таблицахъ ЬапдоИ’аи Воегпвіеіп’а приведены теплоты.
горѣнія въ б. калоріяхъ на 1 килогр. вещества. Въ таблицахъ В. Ф.Лу-
г и ни на даны числа въ мал. калоріяхъ на 1 гр. и въ большихъ кало-
ріяхъ на одну граммъ-молекулу (,а граммовъ^ вещества. Въ курсахъ хи-
міи (ОзѣхѵаЫ, ЭДегп$і и др.) почти всегда относятъ д къ граммъ-мо-
лекулѣ, и то же самое всегда подразумѣвается, когда результатъ термо-
химической реакціи пишется въ видѣ уравненія, см. (20, я, &, с); такъ
въ (20. а) С и О2 обозначаютъ 12 гр. углерода и 32 гр. кислорода, въ (20, с)
НСІ и ИаНО указываютъ, что реакція произошла между 36.4 гр. хло-
ристаго водорода и 40 гр. ѣдкаго натра.
Тепловой эффектъ многихъ реакцій зависитъ отъ количества
воды, въ которой вещества растворены. Мы имѣемъ важный частный
случай, когда это количество воды столь велико, что дальнѣйшее ея при-
бавленіе уже не вліяетъ на тепловой эффектъ реакціи. Въ этомъ слу-
чаѣ прибавляютъ буквы Ад (адпа) къ формуламъ веществъ. Такъ напр.
равенство
КНОАд-\- НСІАд — КСІАд 13,7 б. кал.
обозначаетъ, что при смѣшеніи 56 гр. КНО и 36,4 гр. НСІ, взятыхъ вь
разбавленныхъ растворахъ, выдѣляется 13,7 б. калорій; писать Н2О съ
правой стороны излишне, ибо образовавшаяся вода, примѣшиваясь къ
большему количеству (Л#), никакого теплового эффекта не вызываетъ.
Тепловой эффектъ реакціи зависитъ отъ того, находились ли веще-
ства въ твердомъ, жидкомъ или газообразномъ состояніи; поэтому О 8 1 -
лѵ а 1 (1 предложилъ обозначать формулы жидкостей обыкновеннымъ шриф-
томъ, газовъ — курсивомъ и твердыхъ тѣлъ — жирнымъ шрифтомъ.
Химическая реакція можетъ происходить съ выдѣленіемъ или съ
поглощеніемъ теплоты. Въ первомъ случаѣ она называется экзотер-
мическою, во второмъ эндотермическою (#<0). Къ эндотерми-
ческимъ реакціямъ относится напр. образованіе С82:
С 4- 82 — С82— 19 б. к.,
т.-е. 12 гр. углерода соединяются съ 64 гр. сѣры, поглощая при этомъ 19
б. кал. Образованіе О3 (озона), С12О, НС И2О. ИО2, Аи} и др. проис-
ходитъ эндотермически.
Основаніемъ термохиміи служитъ законъ Гесса (Нее 8, 1840),
гласящій, что полное количество тепла, выдѣляющееся
при переходѣ группы веществъ А въ группу веществъ В,
не зависитъ отъ способа этого перехода, т.-е. отъ рода
и числа промежуточныхъ реакцій, если только физиче-
ское состояніе (въ обширномъ смыслѣ слова) группъ А
и группъ В во всѣхъ случаяхъ перехода одно и то же. За-
мѣчательно, что этотъ законъ, которымъ, очевидно, выражается частный
случай принципа сохраненія энергіи, былъ найденъ и вполнѣ точно фор-
мулированъ раньше открытія этого принципа. Огромное значеніе закона
Основныя положенія.
259
Гесса заключается въ томъ, что онъ даетъ возможность в ы ч и с л и т ь
теплоты, соотвѣтствующія такимъ реакціямъ, которыя непосредственно на-
блюдать невозможно. Приведемъ нѣсколько примѣровъ.
Опредѣлить теплоту образованія СО изъ угля и кислорода. Непо-
средственныя наблюденія даютъ теплоты образованія СО2 изъ С и изъ
СО, а именно С + 20 = СОа + 97
СО-Ь О = СО2 + б8
(всѣ количества тепла мы будемъ далѣе выражать въ большихъ кало-
ріяхъ). По закону Гесса теплота образованія С02 изъ С и 02 должна
равняться теплотѣ образованія СО изъ С и О, сложенной съ теплотой
образованія С02 изъ СО и О. Отсюда слѣдуетъ, что
С+ О = СО + 29.
Удалось опредѣлить это число и болѣе непосредственнымъ способомъ,
причемъ оно оказалось весьма близкимъ къ теоретическому.
Замѣтимъ, что послѣднее равенство получается вычитаніемъ преды-
дущихъ двухъ другъ изъ друга. Вообще законъ Гесса даетъ возмож-
ность производить надъ термохимическими уравненіями такія же манипу-
ляціи, какъ надъ уравненіями обыкновенными; мы можемъ ихъ склады-
вать и вычитать, а также переносить въ нихъ члены съ одной стороны
на другую.
Приведемъ еще интересный примѣръ опредѣленія теплоты образо-
ванія ангидрида 5О3. Если сжигать смѣсь РЬО и 5 въ кислородѣ, то
образуется РЬ80± и выдѣляется #=165,5. Итакъ
+54-30-- РЛ504 4 165,5
Если РЬО растворить въ разбавленной Н280±, то получается
РЬО^Н28О4Ад = РЬ80± + Ад 4 23.3.
Вычтя это равенство изъ предыдущаго, получимь
5 4 30 4 Ад = Н280±Ад + 142,2.
Наконецъ при раствореніи 503 въ водѣ получается
503 4~ Ад = Н280±Ад 4 41,1.
Если это уравненіе вычесть изъ предыдущаго, то получится
5 4 ЗО = 5О3 + 101,1.
Такимъ образомъ найдена теплота образованія 503 изъ 5 и 03.
Законъ Гесса даетъ возможность вычислить теплоту # о б р а-
зованія органическихъ веществъ, если извѣстна ихъ
теплота горѣнія ф. Дѣйствительно пусть <2 сумма теплотъ горѣ-
нія составныхъ частей соединенія; въ такомъ случаѣ по закону Гесса
<7 = # + О откуда
д=^—(^..........................(21)
17*
260
Термохимія.
Величина <?' легко вычисляется, если положить на каждый атомъ
//, С и 5 соединенія такія количества теплоты:
Н С 8
33,75 94,3 71,1.
Такъ напр. при сгораніи граммъ-молекулы этиловаго алкоголя С2Н$О,
молекулярный вѣсъ котораго 46, имѣемъ теплоту горѣнія граммъ-моле-
кулы 340; между тѣмъ теплота горѣнія составныхъ частей С?' = 94,3 X 2
4- 33,75 X 6 — 391. Отсюда теплота образованія граммъ-молекллы этило-
ваго алкоголя # = <2' — <2 = 391 340 = 51.
Вычисляя такимъ способомъ теплоту образованія находятъ иногда
величины отрицательныя; въ такомъ случаѣ самое явленіе образова-
нія вещества происходитъ эндотермически. Такъ напр. теплота горѣнія
С52, С2Н± оказывается больше суммы теплотъ горѣнія составныхъ частей.
Приведемъ еще одинъ примѣръ прямого опытнаго подтвержденія за-
кона Гесса. Даны 1 гр.-мол. НН3, 1 гр.-мол. НСІ и большое количество
воды; ихъ можно превратить въ растворъ 1 гр.-молекулы НН^СІ въ той
же водѣ и притомъ двумя путями: 1) можно соединить газы /Ѵ/73 и НСІ
и образовавшійся твердый нашатырь растворить въ водѣ; 2) можно от-
дѣльно растворить въ водѣ ИН3 и НСІ и затѣмъ произвести соеіиненіе
въ растворѣ. Тепловые эффекты видны изъ нижеслѣдующаго:
Первый путь:
(/ѴЯ3, НСІ) = 42,1
(НН^СІ,ад) = — 3,9
(ИН3, НСІ, ад} = 38,2
Второй путь:
(ИН3,ад) = 8,4
(НСІ, а#) = 17.3
(ЫН3ад, НСІад) — 12,3
(НН3, НСІ, ад) = 38,0.
Числа получаются, дѣйствительно, почти одинаковыя.
Зная теплоты образованія различныхъ соединеній, мы можемъ вы-
числить, сколько теплоты выдѣляется или поглощается при опредѣленной
реакціи. Возьмемъ напр. реакцію полученія дѣйствіемъ На на М$С12,
которая происходитъ по формулѣ
М^С12 + 2^ = ^аСІ + Мё.
Теплота образованія М^С12 равна 151,0: для ИаСІ она равна 195,4;
отсюда слѣдуетъ, что при образованіи 2ИаСІ-\- изъ 2На, 2СІ и
выдѣляется больше тепла, чѣмъ при образованіи М^С12 ~|~ 2Мг, на вели-
чину 195,4 X 2 151,0 = 239,8, и это количество теплоты должно выдѣ-
литься при разсматриваемой реакціи.
Тепловой эффектъ, сопровождающій опредѣленную химическую реак-
цію и непосредственно наблюдаемый при опытахъ, вообще говоря не мо-
жетъ служить мѣриломъ той потенціальной химической энергіи, которая
исчезла во время реакціи. Самая реакція почти всегда сопровождается цѣ-
лымъ рядомъ физическихъ явленій, которыя также происходятъ съ выдѣ-
леніемъ или поглощеніемъ тепла. Нѣкоторыя изъ этихъ явленій могутъ
Основныя положенія
261
быть приняты во вниманіе, такъ что можетъ быть введена соотвѣтствую-
щая поправка для полученія теплового эффекта, соотвѣтствующаго
чисто химическому явленію. Въ другихъ же случаяхъ введеніе поправки
невозможно, и та величина, которую мы получаемъ на основаніи опытовъ,
выражаетъ результатъ совокупности нѣсколькихъ явленій, которыя отдѣ-
лить другъ отъ друга пока еще невозможно. Разсмотримъ тѣ явленія,
которыя сопровождаютъ химическія реакціи и имѣютъ вліяніе на наблю-
даемый тепловой эффектъ.
I. Если вещества до реакціи были тверды, а послѣ реакціи получа-
ются тѣла жидкія или газообразныя, или если вообще до и послѣ
реакціи состояніе тѣлъ неодинаковое, то переходъ тѣлъ изъ
одного состоянія въ другое долженъ былъ сопровождаться тепловыми эф-
фектами, отдѣлить которые весьма часто невозможно. Мы видѣли на
стр. 259, что С + О СО 4~ 29 и СО + О = СО2 Ц- 68. Присоединеніе
перваго атома О къ С даетъ 29, присоединеніе второго 68 б. кал. Весьма
вѣроятно, что первое число . меньше второго вслѣдствіе перехода твер-
даго С въ газообразное состояніе.
II. Тепловой эффектъ д реакціи зависитъ отъ состоянія, въ кото-
ромъ находились тѣла до реакціи. • Это между прочимъ относится и къ
аллотропическимъ видоизмѣненіямъ, если таковыя существуютъ.
Такъ напр. при горѣніи угля получается:
Аморфный уголь . . 97 (Раѵге и ЗіІЬегтапп).
Графитъ..........94,8 (Вегійеіоі).
Алмазъ . , . . . 94,3 (В е г і Ь е 1 о I).
Послѣднее число и было нами принято на стр. 259 при вычисленіи
теплотъ образованія различныхъ веществъ. Для теплоты горѣнія сѣры
имѣемъ:
Свѣже расплавленная 5 . . . . 69,3
Моноклиномѣрная 5..............71,7.
III. Величина д зависитъ отъ состоянія, въ которомъ находятся про-
дукты реакціи. Такъ при соединеніи 2 гр. водорода и 16 гр. кислорода
выдѣляется 67,52 б. кал., если продуктъ реакціи Н2О, является въ жид-
комъ видѣ. Понятно, что если результатомъ соединенія получатся пары,
хотя бы и при той же температурѣ, какую раньте имѣла вода, то д бу-
детъ меньше.
IV. Реакціи часто сопровождаются распаденіемъ молекулъ
элементовъ, вступающихъ въ реакцію. Тепловой эффектъ этого распаде-
нія остается неизвѣстнымъ. Такъ напримѣръ соединеніе водорода и кис-
лорода сопровождается распаденіемъ молекулы О2, и тепловой эффектъ
д — 67,52 есть результатъ двухъ реакцій: О2 = О-|-О-}-яи Н2-\~ О =
= Н2О -\-у. Величина д = 67,52 ~у + причемъ х, вѣроятно, вели-
чина отрицательная. Точно также при соединеніи 1 гр. водорода съ
35,4 гр. хлора выдѣляется 22 б. кал., причемъ происходитъ разложеніе
262
Термохимія.
молекулъ Н2 и С/2. Принято писать (/7, СІ) = 22, но было бы точнѣе
написать
(Я2, С12) — (Н, Н) — (СІ, СГ) = 22 X 2 = 44.
V. Внѣшняя работа, положительная или отрицательная, имѣ-
етъ вліяніе на д. если она сопровождаетъ реакцію. Если реакція про-
исходитъ при постоянномъ внѣшнемъ давленіи (напр. атмосферномъ) и
при этомъ изъ твердыхъ или жидкихъ тѣлъ образуются газы (7,п Н^80^),
то теплота, потраченная на расширеніе, должна быть прибавлена къ на-
блюденному д\ если изъ газовъ образуются жидкости или твердыя тѣла,
то наблюденное д должно быть уменьшено. Такъ, при реакціи Н2 + О —
= Н2О наблюдается д ~ 68,4, когда образуется жидкая вода: внѣшняя
работа эквивалентна 0,88 б. кал. и потому исправленное д ~ 68,4 — 0,88 —
= 67,52 б. кал. Изъ сказаннаго ясно, что тепловой эффектъ д реакціи
зависитъ отъ внѣшняго давленія и неодинаковъ, смотря по тому, проис-
ходитъ ли реакція при постоянномъ объемѣ (дѵ) или при постоянномъ
давленіи (др). Отъ одной величины, впрочемъ, легко перейти къ другой ;
разница между ними не велика.
Такъ напр. для реакціи горѣнія метана (С774) имѣемъ дѵ = 212,4,
др = 213,5.
VI. Въ наблюденную величину д необходимо ввести поправку, когда
температуры і тѣлъ, входящихъ въ реакцію, и продуктовъ реак-
ціи не одинаковы.
VII. Термическій эффектъ д химической реакціи есть функція той
температуры і, при которой реакція происходитъ, т.-е.
которую имѣютъ тѣла, входящія въ реакцію, и которую окончательно
принимаютъ ея продукты. Эту функцію легко найти. Пусть сумма мо-
л окулярныхъ теплоемкостей веществъ Л, вступающихъ въ реакцію,
равна а сумма тѣхъ же теплоемкостей для веществъ В, которыя
образовались, равна и пусть д± и д2 тепловые эффекты реакціи
при температурахъ и і2. Мьі можемъ двумя путями перевести группу
тѣлъ А, находящихся при въ группу тѣлъ В при і2°. Можно прове-
сти реакцію при и затѣмъ нагрѣть ея продукты до 4° ; ПРИ этомъ си-
стема отдастъ количество тепла дх — (і2— \ но можно также
сперва нагрѣть группу А до і2 и затѣмъ произвести реакцію, въ како-
вомъ случаѣ будетъ выдѣлено количество тепла д2 — (/2— іг) На-
чальное и окончательное состоянія одинаковы, слѣд. эти два количества
тепла должны быть равны; отсюда получаемъ
^=(4—4) 2 ѵ'іс'і | .... (22)
Измѣненіе теплового эффекта реакціи въ зависимости отъ темпера-
туры пропорціонально разности теплоемкостей тѣлъ до и послѣ реакціи.
Мы видѣли на стр. 235, что если соединяются твердыя тѣла, образуя
твердое тѣло, то сумма молекулярныхъ теплоемкостей остается безъ из-
Основныя положенія. - Методы изслѣдованія
263
мѣненія. Отсюда слѣдуетъ, что тепловой эффектъ реакціи, происходящей
между твердыми тѣлами, образующими твердыя же тѣла, отъ тем-
пературы не зависитъ.
Насчетъ механизма выдѣленія тепла при химическихъ реакціяхъ су-
ществуютъ различныя гипотезы. КісЬагйз (1902) высказалъ мысль, что
основною причиною выдѣленія тепла является работа, совершаемая при томъ
сжатіи вещества, которое сопровождаетъ соединеніе двухъ веществъ.
Онъ вводитъ представленіе о сжимаемыхъ атомахъ, состоящихъ изъ ядра
и оболочки; такое представленіе вполнѣ согласуется съ тѣмъ новымъ
ученіемъ о сложности атомовъ, которое возникло въ послѣднее время.
МііНег-ЕггЬасЬ (1870—1881) первый указалъ на связь между
количествомъ выдѣляющейся теплоты и сжатіемъ, • сопровождающими
химическія реакціи. Кісйагсіз независимо отъ него высказалъ и
развилъ эту мысль. Онъ изслѣдовалъ прежде всего хлористыя и броми-
стыя соединенія и пришелъ къ выводу, что работа, которую необходимо
затратить для сжатія, происходящаго при образованіи твердаго и жидкаго
вещества, приблизительно пропорціонально выдѣляемой теплотѣ. Онъ за-
ключилъ отсюда, что работа сжатія и представляетъ глав-
ный источникъ теплоты, выдѣляющейся при химиче-
скихъ реакціяхъ.
§ 3. Термохимическіе методы изслѣдованія. Калориметры, кото-
рыми пользуются при термохимическихъ изслѣдованіяхъ, можно раздѣ-
лить на двѣ группы; первою группою пользуются при наблюденіи реакцій,
происходящихъ въ жидкостяхъ; вторая группа служитъ для изученія реак-
ціи горѣнія твердыхъ, жидкихъ или газообразныхъ тѣлъ. Весьма важно,
чтобы во всѣхъ случаяхъ изучаемая реакція происходила по возмож-
ности быстро.
Для наблюденія реакцій, происходящихъ въ жидкостяхъ, употребляютъ
различно устроенные калориметры. Иногда наливаютъ одну изъ жидко-
стей въ калориметръ, помѣщая другую жидкость въ пробирный стакан-
чикъ, дно котораго пробиваютъ, когда установилось тем-
пературное равновѣсіе. Иногда помѣщаютъ второе веще-
ство, твердое или жидкое, въ тонкостѣнный стеклянный ша-
рикъ внутри жидкости, налитой въ калориметръ, и въ над-
лежащій моментъ разбиваютъ шарикъ. ВегѣЬеІоѣ помѣ-
щаетъ одну жидкость въ калориметръ, другую въ колбу съ
широкимъ горломъ, которую онъ захватываетъ деревянными
щипцами, чтобы перелить ея содержимое въ калориметръ.
На рис. 83 изображенъ калориметръ <1. Т11 о ш 8 е п’а;
двѣ жидкости помѣщены, одна надъ другой, въ различ-
ныхъ сосудахъ, снабженныхъ мѣшалками г и 7? и термо-
метрами і и Т. Жидкости смѣшиваются, если поднять
стержень ѵ. Оба сосуда защищены металлическими ци-
линдрами (не изображенными) отъ теплового дѣйствія
Рис. 83.
окружающихъ предметовъ. Калориметръ Еаѵге’а и ЗіІЬегтапп’а,
264
Термохимія.
изображенный на рис. 68 стр. 172, спеціально назначался для термохими-
ческихъ работъ. Смѣшиваніе жидкостей, сопровождающееся химической
реакціей, происходило въ боковой трубкѣ А; количество выдѣлившейся
теплоты опредѣлялось по формулѣ (10,&) стр. 172.
Наблюденіе теплового эффекта реакціи усложняется, когда въ ре-
зультатѣ получаются, между прочимъ, тѣла газообразныя, которыя необ-
ходимо охладить до температуры калориметра. Вегіііеіоі производитъ
въ этомъ случаѣ реакцію въ цилиндрическомъ платиновомъ или стеклян-
номъ сосудѣ, погруженномъ въ воду калориметра. Отъ верхней части бо-
ковой поверхности цилиндра идетъ трубка-змѣевикъ, нѣсколько разъ об-
ходящая цилиндръ и входящая въ небольшую камеру, въ которой оста-
ются капли жидкости, увлеченныя газомъ; изъ этой камеры газъ по осо-
бой трубкѣ выходитъ изъ калориметра наружу.
Обращаемся къ способамъ измѣренія теплотъ горѣнія. Такія
измѣренія производили впервые Ьаѵоівіег и Ьаріасе при помощи
ледяного калориметра: затѣмъ Сга^ѵЕогй, Баііоп и Витіогй
пользовались водянымъ калориметромъ, заставляя газообразные продукты
горѣнія, происходившаго подъ калориметромъ, проходить черезъ него по
змѣевику. Б е р г е г значительно усовершенствовалъ этотъ приборъ. Пер-
выя точныя измѣренія были сдѣланы Бпіоп^’омъ и послѣ его смерти
опубликованы его ассистентомъ С а Ь а г Ѵомъ. Дальнѣйшія почти одно-
временныя изслѣдованія принадлежатъ А п й г е лѵ з’у и Г а ѵ г е’у и 8 і 1 -
Ьегшапп’у. Апйге дѵ8 смѣшивалъ газъ
сь необходимымъ для его сгоранія кисло-
родомъ и производилъ мгновенный взрывъ
при помощи тонкой платиновой проволоки,
которую онъ накаливалъ электрическимъ
токомъ. Сосудъ со смѣсью газовъ помѣ-
щался въ водѣ калориметра.
Весьма обширныя изслѣдованія теп-
лотъ горѣнія производили Еаѵге и 8 і 1 -
Ь е г ш а п п ; приборъ, которымъ они поль-
зовались. изображенъ на рис. 84. Горѣніе
происходило въ мѣдномъ сосудѣ Л, при-
крѣпленномъ къ крышкѣ калориметра аа,
въ которой сдѣланы отверстія для термо-
метра, для кольцеобразной мѣшалки //.
и еще большое отверстіе посреди. Кало-
риметръ аа установленъ на пробковыхъ
ножкахъ въ сосудѣ б/, который находился
въ сосудѣ ее\ промежутокъ между аа и (1
наполненъ пухомъ, между (I и ее водою.
Кислородъ вводился въ сосудъ А черезъ
трубку О; газы, теплоту горѣнія которыхъ требовалось опредѣлить, черезъ
наклонно поставленную трубку В. Когда требовалось направить струю
Методы изслѣдованія.
265
кислорода на медленно горящія твердыя тѣла, то кислородъ вводился че-
резъ трубку В. Газообразные продукты горѣнія проходятъ по змѣевику
$8К и выходятъ черезъ отверстіе е; жидкіе продукты собираются въ ци-
линдрикѣ К. Широкая труба, покрытая стекломъ, и зеркало М даютъ
возможность наблюдать во время опыта горѣніе, происходящее въ А.
Жидкости сжигались въ маленькихъ лампочкахъ: сѣра и уголь въ пла-
тиновыхъ цилиндрикахъ, снабженныхъ сѣтчатымъ дномъ.
Дальнѣйшія усовершенствованія описаннаго прибора ввели <Г Т Ь о пі -
зеп, 8 іо Ьш апп, Вегіііеіоі и, въ особенности. В. Ф. Луги пинъ,
калориметръ котораго подробно описанъ въ его сочиненіи, указанномъ
ниже. Камера, въ которой происходитъ горѣніе въ приборѣ Лугинипа,
стеклянная, снабженная металлическимъ дномъ.
Ледяной калориметръ Випзеп’а (стр< 167) служилъ для
опредѣленія теплоты горѣнія водорода. Имъ пользовались ЗсЬиНег и
ДѴагіЬа (стр. 171) и нѣсколько позже Тйап. Приводимъ, для сравне-
нія, числа (въ б. калоріяхъ), полученныя различными наблюдателями для
теплоты горѣнія 1 гр. водорода.
Еаѵге и ВіІЬегтап п 34,095
Апйгелѵз....... 33,534
1 ТЬотзеп. . . 34,217
ЗсЬиІІег и ѴѴагіЬа 34,199
Т к а п . . . . . 34,230
ВегіЬеІоі . . . . 34.600.
На граммъ-молекулу приходится двойное количество тепла.
Во всѣхъ разсмотрѣнныхъ способахъ горѣніе поддерживалось прито-
комъ струи кислорода. Другой способъ былъ предложенъ Ьеѵіз Т И о пі -
8 е п’омъ, впервые примѣненъ Г 1 а п с 1 а п (Томъ и затѣмъ разработанъ
8 іойтап п’омъ. Онъ заключается въ сжиганіи изслѣдуемаго вещества
на счетъ кислорода х л о р н о в а т о - к и с л а г о кали (бертолетовой соли).
ЗіоЬшапп помѣщаетъ смѣсь этой соли, испытуемаго тѣла и индиф-
ферентнаго вещества (МпО<> и пемза), служащаго для замедленія реакціи,
въ платиновый цилиндръ, находящійся внутри латуннаго цилиндра, окру-
женнаго водою калориметра. Смѣсь зажигается особымъ фитилемъ, а по
окончаніи горѣнія 81 о Ь т а п п даетъ водѣ проникнуть во внутрь латун-
наго цилиндра, вслѣдствіе чего раскаленный платиновый цилиндръ и его
содержимое охлаждаются, а образовавшійся КСІ растворяется. В. Ф. Лу-
ги нинъ полагаетъ, что способъ Зіойтапп’а не даетъ точныхъ ре-
зультатовъ, но что этотъ способъ можетъ быть усовершенствованъ.
Обращаемся къ способу опредѣленія теплотъ горѣнія, впервые пред-
ложенному Вегійеіоі (1881) и извѣстному подъ названіемъ способа
калориметрической бомбы. Сущность этого способа заключается
въ слѣдующемъ. Стальной, замкнутый со всѣхъ сторонъ сосудъ (бомба)
выложенъ внутри слоемъ платины, на которую не дѣйствуютъ продукты
горѣнія, и .которая сама не окисляется; въ немъ помѣщается испытуемое
.вещество въ платиновой чашкѣ, поддерживаемой платиновыми стержнями.
Бомба наполняется кислородомъ, сгущеннымъ до давленія въ 25 атмосф., и
помѣщается внутри калориметра Мгновенное сжиганіе (взрывъ) произво-
266
Термохимія.
дится электрической искрой или накаливаніемъ при помощи тока желѣзной
проволоки, сгорающей въ кислородѣ; при этомъ раскаленныя частицы окиси
желѣза падаютъ на испытуемое вещество, чѣмъ и вызывается взрывъ.
Съ помощью этого прибора было произведено огромное число наблюденій
самимъ Вегіііеіоі и его учениками, въ особенности В. Ф. Лугини-
нымъ, давшимъ наиболѣе полное описаніе бомбы и самого способа на-
блюденія въ сочиненіи, указанномъ ниже; изъ него заимствуемъ рису-
нокъ и описаніе.
Рис. 85.
Калориметрическая бомба
въ томъ видѣ, въ какомъ она
употребляется нынѣ, изображена
на рис. 85. Наружная часть аа
представляетъ стальной тигель;
ЬЬ платиновая внутренняя обо-
лочка ; ее платиновая крышка,
(1(і(і и еее остальныя крышки,
изъ которыхъ послѣдняя привин-
чивается, какъ показано на ри-
сункѣ. Черезъ крышку прохо-
дитъ изолированный стержень
//, нижняя часть котораго окру-
жена огнеупорной эмалью, защи-
щенной отъ непосредственнаго
дѣйствія пламени ^платиновымъ
цилиндромъ оо. Каналъ // и
трубка Ь служатъ для накачи-
ванія кислорода; вращая головку
к винта и опуская гайку
можно закрыть отверстіе канала
// и тѣмъ самымъ герметически
закрыть бомбу. Испытуемому
веществу придаютъ, если оно
твердое, форму лепешки д и по-
мѣщаютъ его въ платиновую ча-
шечку р; между платиновыми
стержнями г и 5 помѣщается тонкая желѣзная проволока, которая касается
лепешки д, Теплоемкость бомбы опредѣляется вычисленіемъ по вѣсу вхо-
дящихъ въ ея составъ матеріаловъ, или сжиганіемъ въ ней вещества, те-
плота горѣнія котораго извѣстна, или, наконецъ, сжигая послѣдовательно
два различныя количества одного и того же вещества и мѣняя при этомъ
количество воды въ калориметрѣ. Въ послѣднемъ случаѣ получаются два
уравненія, изъ которыхъ можно опредѣлить теплоту горѣнія и теплоем-
кость калориметра.
Количество вещества берется такое, чтобы на его сжиганіе трати-
лось около 20% находящагося въ бомбѣ кислорода. Если вещество жид-
Методы изслѣдованія. Результаты.
267
кое, то его помѣщаютъ въ‘особый платиновый стаканчикъ, на устройствѣ
котораго не останавливаемся. ВегіЬеІоі показалъ, какимъ образомъ
слѣдуетъ пользоваться бомбой, когда испытуемое вещество содержитъ 5
или С/, такъ чтобы получились вполнѣ опредѣленные продукты горѣнія,
а именно, кромѣ СО2 и Н2О, въ первомъ случаѣ только водная сѣрная
кислота, во второмъ — соляная кислота, растворенная въ водѣ. Когда
опредѣляется теплота горѣнія газовъ, слѣдуетъ брать количество кисло-
рода, близкое къ тому, которое необходимо для полнаго сгоранія. Даль-
нѣйшія изслѣдованія калориметрической бомбы и наилучшаго способа
ея примѣненія производили Зіоігтапп и Зубовъ (1904). Маѣ-
1 е г, французскій инженеръ, построилъ калориметрическую бомбу, въ ко-
торой платиновая оболочка замѣнена слоемъ особаго рода бѣлой эмали,
не страдающей ни отъ высокой температуры, ни отъ дѣйствія веществъ,
образующихся при взрывѣ. Она значительно дешевле бомбы Вегіѣе-
ІоЬ, цѣна которой весьма высока. Лае§ег и 8іеіп\ѵеЬг (1903)
показали, что теплоемкость калориметра можетъ быть весьма точно опре-
дѣлена электрическимъ способомъ; объ этомъ уже было упомянуто при
описаніи калориметровъ: они пользовались этимъ способомъ, работая
съ калориметрическою бомбою Вегійеіоі. Въ двухъ позднѣйшихъ
работахъ (1905 и 1906) Яае^ег и біеіплѵеѣг опубликовали даль-
нѣйшія свои изслѣдованія относительно калориметрическихъ измѣре-
ній теплотъ сгоранія и тщательное изслѣдованіе относительно калибровки
бомбы Вегійеіоі въ электрическихъ единицахъ помощью платиноваго
термометра.
§ 4. Нѣкоторые результаты термохимическихъ изслѣдованій. Въ
предъидущихъ двухъ параграфахъ мы привели изъ области термохиміи
немногія указанія на ея основныя положенія и на методы, которыми она
пользуется, выбирая то, что должно представить интересъ для физики.
Что же касается до результатовъ термохимическихъ изслѣдованій, пред-
ставляющихъ огромный численный матеріалъ, то мы ограничиваемся ука-
заніемъ на немногіе факты, опять-таки могущіе представить интересъ
для физики.
Образованіе солеи. Теплота выдѣляющаяся при смѣшеніи
кислоты и основанія, слагается изъ двухъ частей, изъ которыхъ одна
зависитъ только отъ кислоты, другая только отъ основанія: это значитъ,
что первая часть для данной кислоты остается одна и та же, каково
бы ни было- основаніе, а вторая, въ такомъ же смыслѣ, не зависитъ отъ
рода кислоты.
Замѣтимъ слѣдующія важныя числа: при раствореніи въ сѣрной
кислотѣ
1 гр. Тлі выдѣляются 1635 мал. калорій.
1 гр. Си » 881 мал. калорія.
Те и ло та д одинакова д л я всѣхъ солей, о б р а з у ю-
щихся при смѣшеніи сильной ОДНООСНОВНОЙ кислоты
268
Термохимія.
съ сильнымъ основаніемъ. Такъ при смѣшеніи кислотъ НСІ,
НВг, Ш, НИО*, НСЮ*, НВгОъ НЮ3 съ ЫаНО, КНО, Ва(НО)2, Са(НО)2
и др. получаются количества теплоты, колеблющіяся въ тѣсныхъ предѣ-
лахъ между 13,7 и 14,1 б. кал. Исходя изъ представленія о диссоціаціи
электролитовъ, находящихся въ растворѣ (т. I), объясняютъ это явленіе
тѣмъ, что кислота, основаніе и соль диссоціированы, такъ что при смѣ-
шеніи первыхъ двухъ происходитъ всегда одна и та же реакція 770-}-
-|- Н~ Н2О. Если напр. смѣшать растворы КН О и НСІ, то мы имѣемъ въ
растворѣ до смѣшенія вещества К, ОН, Н, СІ, а послѣ смѣшенія веще-
ства К. СІ, Н2О. Болѣе слабыя одноосновныя кислоты даютъ д иногда
нѣсколько большее, иногда нѣсколько меньшее. Такъ для уксусной кис-
лоты д — 13,3, для муравьиноіі 13,4, для ціанистаго водорода (НСК) д ~ 12,8.
Съ постоянствомъ величины д для многихъ солей находится въ связи
т.наз.законъ т е р м <> н е йтр а л ьн о ст и соляныхъ растворовъ,
найденный Ней й’омъ и гласящій, что смѣшеніе нейтральныхъ солей не
сопровождается тепловыми явленіями, если только двойной обмѣнъ не со-
провождается выдѣленіемъ осадка.
Тщательнѣйшее изслѣдованіе относительно теплоты нейтрализаціи
сильныхъ кислотъ и основаній было произведено Вегійеіоі и <1. Т Ь о т -
8 е п’омъ. Позже такія изслѣдованія были произведены АѴ о е г ш а п’омъ
(1905), который воспользовался ледянымъ калориметромъ. Онъ устано-
вилъ, что теплота нейтрализаціи 5 между 0° и 32° въ сильной степени
зависитъ отъ температуры и можетъ быть представлена выраженіемъ вида
5 = 50—аі. Отъ концентраціи 5 зависитъ лишь для весьма концентриро-
ванныхъ растворовъ.
Интересно, что для аналогичныхъ соединеній элементовъ, располо-
женныхъ въ одномъ столбцѣ періодической системы, иногда получаются
теплоты д образованія, правильно растущія или убывающія съ возраста-
ніемъ атомнаго вѣса элемента. Такъ въ ряду ІлСІ, ИаСІ, КСІ, М&С12,
СаС12, 8гС12, ВаС12 теплота д правильно растетъ отъ 93,8 до 194,7. Въ
ряду М^О, СаО, 8г0, ВаО величина д уменьшается отъ 143,9 до 124,2.
Гидратизація солей сопровождается выдѣленіемъ теплоты, ко-
торую можно опредѣлить, растворяя вь большомъ количествѣ воды сперва
безводную соль, а потомъ гидратъ. Такъ напр. при раствореніи граммъ-
молекулы СаС12 (111 гр.) выдѣляется 16,0 б. кал.; при раствореніи
СаС12 6/72О п о г л о щ а ю т с я 4,3 б. кал. Отсюда слѣдуетъ, что ги-
дратизація хлористаго кальція сопровождается выдѣленіемъ 16,0 —(- 4,3) =
= 20,3 б. кал.
Теплоту,выдѣляющуюся при образованіи сплавовъ, измѣряли Лу-
ги н инъ и Щу каре въ (Си-\-АГ) и Васке г (Хп~\- Си). Послѣдній
нашелъ максимумы выдѣленія теплоты при образованіи сплавовъ, соот-
вѣтствующихъ формуламъ СиХп2 и СиХп.
Смѣшеніе Н28О± съ водою было изслѣдовано весьма многими
учеными, между прочимъ Ріаипсіі ег’омъ. Чтобы опредѣлить д для
случаевъ смѣшенія Н28(Э^-\~ Н2О, Н28О±-\~ %Н2О, Н28О±-[-%Н2О и т. д.,
Результаты.
269
онъ смѣшивалъ Н28О^ съ пН.,О, гдѣ п большое число (//=119), и за-
тѣмъ Н28О±. Н2О съ (п Ѵ>Н2О или Н28О±. 2Н2О съ (п — 2)Н2О и т. д.
Вычитая результатъ второго наблюденія изъ результата перваго, онъ по-
лучалъ искомыя величины. Онъ находитъ числа, помѣщенныя въ слѣд.
табличкѣ, гдѣ д теплота, выдѣляющаяся при соединеніи 1 гр.-молекулы
(98 гр.) Н28О± съ к гр.-молекулами (18& гр.) Н2О\
к я к я
0,5 3,666 б. К?л. 4 12,858
1 6,776 5 13,562
2 9,998 6 14,395
3 11,785 119 17.690
На рис. 86 абсциссы обозначаютъ числа ординаты сплошной кри-
вой числа д въ м. кал., обозначенныхъ съ лѣвой стороны. Кривыя.....
и------ . . показываютъ повышеніе температуры, происходящее при смѣ-
шеніи, и температуру кипѣнія раствора въ градусахъ, обозначенныхъ
справа. Послѣднія двѣ кривыя чрезвычайно сближаются около к = 4; по-
Рис. 86
этому прибавленіе 4-хъ молекулъ Н2О къ одной молекулѣ Н28О± вызы-
ваетъ наиболѣе бурныя явленія. 4. Тііопізеп далъ эмпирическую фор-
мулу для д. Новыя изслѣдованія теплоты, освобождающейся при смѣше-
ніи воды съ сѣрной кислотой производилъ Вгопзіесі (1910).
Термохимическое изслѣдованіе реакцій въ а л кого л ь н ы х ъ ра-
270
Термохимія.
створахъ произвели Т а н а т а р ъ и П и с а р ж е в с к і й. Окисленіе метал-
ловъ и образованіе галоидныхъ солей было изслѣдовано Гаѵге’омъ, 8і1-
Ьегтапп’омъ, Апсіг екя’омъ и др.
Число эндотермическихъ реакціи довольно велико; на
стр. 258 были упомянуты нѣкоторыя изъ нихъ. Укажемъ еще на слѣду-
ющія. Образованіе Н2О2 изъ Н2О сопровождается поглощеніемъ 23,2 б. кал.;
при образованіи (СТѴ)2 поглощаются 64,4 б. кал. Любопытный случай на-
блюдается при смѣшеніи ЫаНО съН28 О4. Если къ раствору ЫаНО прибавить
столько кислоты, чтобы образовалась нейтральная соль Ыа28О±, то выдѣ-
ляется # = 31,4 на 1 гр.-молекулу кислоты. При дальнѣйшемъ прибавле-
ніи кислоты происходитъ поглощеніе тепла, доходящее до 3 б. кал.;
оно можетъ быть объяснено тѣмъ, что въ растворѣ часть Ыа28О± пере-
ходитъ въ кислую соль ЫаН80±. Это одинъ изъ немногихъ случаевъ
эндотермической реакціи, происходящей самопроизвольно.
Горѣніе. Температура горѣнія не можетъ быть вычислена по ко-
личеству д выдѣляющагося тепла и теплоемкости продуктовъ горѣнія
Такъ напр. при горѣніи водорода величина д такъ велика, что она на-
грѣла бы образовавшіеся пары воды до 6700°; но пары воды при зна-
чительно болѣе низкой температурѣ разлагаются, а потому ясно, что тем-
пература горѣнія должна быть много ниже. Изъ опытовъ ВипзеіГа
слѣдуетъ, что температура горѣнія водорода въ чистомъ О2 около 1790°.
ВегкепЬивсЪ (1899) находитъ максимальную температуру пла-
мени бунзеновской горѣлки равною 1820°. О новыхъ оптическихъ спо-
собахъ измѣренія температуры пламенъ было сказано въ главѣ второй.
Опредѣленія теплотъ горѣнія органическихъ соединеній привели къ
нѣкоторымъ результатамъ, представляющимъ общій интересъ. Такъ напр.
Г ТЬотзеп нашелъ, что въ нѣкоторыхъ случаяхъ теплота горѣнія
углеводородовъ можетъ быть вычислена, какъ линейная функція числа
атомовъ углерода, числа атомовъ водорода, числа простыхъ и числа двой-
ныхь связей. На стр. 261 мы видѣли, что аллотропическія видоизмѣне-
нія С и 5 имѣютъ различныя теплоты горѣнія. То же самое относится
къ Р; переходъ желтаго фосфора въ красный сопровождается поглоще-
ніемъ 27,3 б. кал., а потому теплота горѣнія для желтаго фосфора больше,
чѣмъ для краснаго. Метамеры, т.-е. соединенія, частицы которыхъ имѣ-
ютъ одинаковый составъ, но различное строеніе, даютъ различныя те-
плоты д горѣнія. Приводимъ два примѣра
Я
Уксусная кислота . . . . Муравьинокислый метилъ. . . 3505 4157
Пропіоновая кислота .... Я 4670
Уксуснокислый метилъ сянво2 5344
Муравьинокислый этилъ . . . 5279.
Полимеры, частицы которыхъ состоятъ изъ одинаковыхъ относитель-
Результаты.
271
ныхъ количествъ составныхъ частей, даютъ правильно возрастающія теп-
лоты горѣнія, какъ видно изъ слѣдующихъ чиселъ для ряда СпН2п
д Разности. д Разности.
Этиленъ С2Н± 333,4 Парамиленъ С10//20 1582 156X5
Пропиленъ 192,7 159,4 Цетенъ 2481 150X6
Изобутиленъ 650,6 157,9 Метамиленъ С^ОНІО 3059 145X4.
Амиленъ Сб//10 804,2 153,6
Теплота образованія для СпН2п равна 17,3+7,9//, что для
этилена (п — 2) даетъ отрицательное число. Подобныя правильно возраста-
ющія теплоты горѣнія замѣчаются во многихъ другихъ гомологическихъ
рядахъ. Приведемъ еще два примѣра. Для углеводородовъ ряда СпН2п^
Я Разности.
Метанъ сн, 211,9
Этанъ анв 370,4 158,5
Пропанъ с3н. 529,2 158,8
Триметилметанъ с4н10 687,2 158,0
Тетраметилметанъ СЬН12 847,1 159,9
Гексанъ с6ни 999,2 152,1.
Теплота образованія равна 14,4 + 7,9//.
Для одноатомныхъ спиртовъ приводимъ числа
8іо Ьтапп’а:
я Разности.
Метиловый спиртъ ся4 0 168,5
Этиловый ан.о 324,6 156,1
Пропиловый » С3Ни 0 481,1 156,5
Изобутиловый » с.н^о 637,6 156,5
Ѵмиловый » сън^о 793,4 155,8
Октиловый » СъНщО 1262,0 156,6X3
Цетиловый 2510,9 156,1X8.
Во всѣхъ трехъ приведенныхъ рядахъ разности почти одинаковы: при-
бавленіе СН2 вызываетъ увеличеніе теплоты горѣнія примѣрно въ 158 б. кал.
Такъ какъ теплота горѣнія элементовъ, изъ которыхъ состоитъ СН2,
равна 165,9, то и оказывается, что теплота образованія увеличивается на
7,9 б. кал. на каждое прибавленное СН2.
Законъ Вегіііеіоі. Въ 1867 г. ВегіЬеІоі высказалъ законъ,
который онъ затѣмъ положилъ въ основаніе термохиміи и вообще хими-
ческой механики и который извѣстенъ подъ названіемъ принципа на-
ибольшей работы: всякая химическая реакція идетъ въ такомъ на-
правленіи, въ которомъ происходитъ наибольшее выдѣленіе тепла. Впо-
слѣдствіи Вегійеіоі прибавилъ условіе: при отсутствіи притока внѣшней
энергіи. Подъ вліяніемъ посторонней энергіи реакція можетъ происходить
и въ противоположномъ направленіи.
Но г 8 іш а пп, й аіЬк е, Н еішйо Иг, ВоНгшапп и др. утвер-
'272
Термохимія
ждаютъ однако, что принципъ Ветіііеіоі не выдерживаетъ ни теорети-
ческой, ни экспериментальной критики. Разборъ этого интереснаго во-
проса можно найти вгь книгѣ КетпзЬ’а ТЬеогеІійсЬе СЬетіе, 1893,
стр. 536—542. Пе Еогсгапд (1904) въ двухъ интересныхъ работахъ
показалъ, что законъ ВегіЬеІоѣ долженъ быть замѣненъ инымъ, кото-
рый онъ называетъ „Ргіпсіре ди тахітит де сЬаІеиг 1гап8І:огтаЫе“.
Таблицы результатовъ термохимическихъ изслѣдованій можно найти
въ таблицахъ ЬапдоИ’а и Воегпніеіп’а въ статьяхъ ВегіЬеІоі,
Р Тошйеп’а, ВіоЬтапп’а, въ книгахъ В. Ф. Лугинина, ^аи-
тапп’а. Овідѵаід’а. и друг.
ЛИТЕРАТУРА.
Къ § 1.
Обзоръ литературы о радіометрѣ можно найти въ книгѣ: Ѵ&іпкеітапп, Напсі-
ЬисЬ (Іег Рйуеік II, 2 р. 262—264, Вгееіаи 1896 (содержитъ 110 указаній).
Сгоокез. Ргос. К. 8ос. 22 р. 32, 373, 1874; 24 р. 276, 1876; 25 р. 304, 1877; 28
р. 29, 1878; РЫІ. Тгапз. 164 р. 501, 1875; 165 р. 519, 1876; 166 р. 326, 1877; 170 р. 87
1880; РЫІ. Ма&. (5) 1 р. 395, 1876; 2 р. 374, 1876.
РеупоІсВ. РЫІ. Ма§. (5) 2 р. 231, 1876; РЫІ. Тгапе. 166 р. 725. 1877.
Хоеііпег. Ро^. Апп. 160 р. 154, 296, 459, 1877.
Ропіе. \Ѵ. А. 68 р. 306, 1899.
Ріеске. XV. А. 3 р. 142, 1878; 69 р. 119, 1899.
Рауіеі^іі. Хаі. 81 р. 69, 1909.
Теплота, выдѣляющаяся при смачиваніи порошковъ:
Роиіііеі. Апп. сЫт еі рііуе. 22 р. 141, 1822.
Зип^к. Ро^. Апп. 125 р. 292, 1865.
МеІ88пег. V7. А. 29 р. 114, 1886.
Сапіопі. Кепд. К. І8І. ЬотЪагсІо 8 р. 135, 1866.
Магііпі Аііі К. І8І. Ѵепеіо (7) 8 р. 502, 1897; 9 р. 927, 1898; 63 р. 915, 1904;
Хиоѵ. Сіт. (4) 7 р. 396, 1898; 9 р. 334, 1899; 10 р. 42, 1899; 11 р. 353, 1900; РЫІ. Мад.
(5) 44 р. 205, 1897; (6) 5 р. 595, 1903.
Скарриіз. XV. А. 19 р. 21, 1883.
ХѴіедетапп и. Ьиедескіп^. \Ѵ. А. 25 р. 145, 1885.
Соге. РЫІ. Ма§. (5) 37 р. 306, 1894.
Егсоііпі. Хиоѵ. Сіт. (4) 9 р. 110, 446, 1899.
Веііаіі. Аііі сіеі. К. І8І. Ѵепеіо 59 II, 1900; Хиоѵ. Сіт. (4) 12 р. 296, 1900.
ЫпеЪаг^ег. РЬу8. Ееѵ. 13 р. 48, 1901.
Рагкз. РЫІ. Мак. (6) 4 р. 240, 1902.
Ьарегртеп. ВШап^. К. 8ѵ. Акасі. Напсіі. 24, II, 1899.
МеВеп8. Апп. сЫт. еі рѣуе. (5) 3 р. 522, 1874.
Таіе. РЫІ. Ма&. (4) 20 р. 508, 1860.
ВеІІсЛі е Ріпаггі. Аііі сіеі В. І8І. Ѵепеіо 61 р. 503, 1902; 63 р. 915, 1904; РЫІ.
Ма§. (6) 4 р. 240, 1902.
ЗсІтшаІЪе. Апп. (1. РЬуз. (4) 16 р. 32, 1905.
Хлористый радій:
Ситіе еі ЬаЬогсІе. С. В. 136 р. 673, 1903.
Къ §§ 2 и 3
По термохиміи имѣется на русскомъ языкѣ:
Янъ (Лаки). Основанія термохиміи. Переводъ Н. С. Дрентельна. Спб. 1893.
Литература.
273
Изъ иностранныхъ :
У. Потзеп. ТЬегтосЬетіесЬе ѴпіегенсЬип^еп. Ьеіргі^ 1882—86 (четыре части).
Главы въ учебникахъ физической химіи Озіъѵаіб’а,, Ыегпзій и <р.
Віоктапп. 2І8сЬг. Г рЬув. СЬет. 10 р. 411, 1892.
Зубовъ. Ж. Р. Ф.-Х. О., 36, часть хим. р. 275, 1904.
Вегікеіоі. Тііегтосііітіе, Рагіе, 1897.
Таблицы, относящіяся къ теплотѣ горѣнія и къ теплотѣ образованія:
Ьапбоіі шкі Воегпзіеіп. РЬуеік.-сЬетізсЬе ТаЪеІІеп. 3-ое изд., Вегііп 1905, р. 416
(только теплоты горѣнія).
В. Лугининъ. Описаніе различныхъ методовъ опредѣленія теплотъ горѣнія орга-
ническихъ соединеній. Москва, 1894. (Нѣмецкій переводъ: Вегііп, 1897). Таблицы со-
держатъ теплоты горѣнія и образованія и указаніе литературы для приблизительно
одной тысячи веществъ.
О. Незз. Ро&&. Апп. 56 р. 463, 593, 1842.
МиІІег-ЕггЬаск. Ро&§. Апп. 139 р. 287, 1870; 149 р. 33, 1873; 154 р. 196, 1874;
\Ѵ. А. 13 р. 522, 1881.
Ріскагбз. ХізсЬг. 1*. рЬув. СЬешіе40р. 169, 597, 1902; Ргос. Атег. Асад. 37 р. 1, 1901.
Ме^ег и. 8іеіпъѵекг. ѴегЬ. (1. (1. рЬув. Сее. 5 р. 50, 353, 1903; 2І8сЬг. I. рЬув.
СЬет. 53 р. 153, 1905; Апп. д. РЬу8. (4) 21 р. 23, 1906.
Обширную литературу далѣе не приводимъ. Наибольшее число работъ принадле-
житъ слѣдующимъ ученымъ: Еаѵге и ВіІЬегтапп, Е Ткотзеп, Вегікеіоі, В. Лугининъ
Віоктапп, Маіі^поп. Подробныя литературныя указанія можно найти также въ книгѣ,
И. Осиповъ. Теплота горѣнія и т. д. Харьковъ, 1893.
Къ § 4.
'Моегтапп. Апп. (1. РЬув. (4) 18 р. 775, 1905.
Вгдпзіеб. 2І8сЬг. 1. рЬув. СЬет. 68 р. 693, 1910.
Р/аипбІег. ЛѴіеп. Вег. 71, 1875. *
У. Ткотзеп. Ро&&. Апп. 90 р. 278, 1853.
ВегкепЬизск. \Ѵ. А. 67 р. 649, 1899.
Іанатаръ и Писаржевскій. Ж. Ф. X. О. 29, отд. хим. р. 185, 1897.
По вопросу о температурѣ горѣнія см.
Курнаковъ. О вычисленіи температуръ горѣнія. Горный Журналъ, ноябрь 1892 г.
(Указана литература вопроса).
Лугининъ и Щукаревъ. АгсЬ. 8С. рЬуя. (4) 15 р. 49, 1903.
Васкег. Ргос. В. 8ос. 68 р. 9, 1901; СЬет. Мемъ. 83 р. 49, 1901.
Ьетоиіі. Апп. (1. СЫт. еі рЬув. (8) 1 р. 496, 1904; 5 р. 1, 1905.
Ое Еогсгапб. С. К. 139 р. 905, 908, 1904.
ГЛАВА ШЕСТАЯ.
Охлажденіе тѣлъ.
§ 1. Введеніе. Въ предыдущей главѣ былъ данъ обзоръ источниковъ
теплоты, т.-е. случаевъ возникновенія тепловой энергіи изъ другихъ формъ
энергіи, и нѣсколько подробнѣе разсмотрѣнъ одинъ изъ относящихся
сюда случаевъ, а именно переходъ химической энергіи въ тепловую. Слѣ-
довало бы подобнымъ же образомъ разсмотрѣть и случаи перехода теплоты
въ другія формы энергіи. Но мы этого дѣлать не будемъ, во первыхъ,
КУРСЪ ФИЗИКИ О ХВОЛЬСОНА. Т. III, изд. 3. 18
274
Охлажденіе.
такъ какъ эти переходы. < тносясь къ различнымъ отдѣламъ физики, разо-
браны въ соотвѣтствующихъ мѣстахъ нашего курса, и во вторыхъ, такъ
какъ общій вопросъ о затратѣ тепловой энергіи на производство работы,
результатомъ которой и можетъ явиться другая форма энергіи (напр. дви-
женіе тѣлъ), представляя нѣкоторыя, весьма важныя особенности, будетъ
подробно разсмотрѣнъ въ гл. восьмой.
Въ этой главѣ мы разберемъ явленіе охлажденія тѣлъ, отчасти
представляющее случай перехода теплоты въ другую форму энергіи, а
именно въ энергію лучистую, но въ то же время почти неминуемо
сопряженное еще съ явленіями конвекціи и теплопроводности, какъ бу-
детъ сказано ниже.
Представляемъ себѣ тѣло, нагрѣтое до нѣкоторой температуры Го и
затѣмъ, при опредѣленной заданной обстановкѣ, предоставленное самому
себѣ. Допускаемъ, что этой новой обстановкѣ соотвѣтствуетъ болѣе низ-
кая температура Ѳ, которую тѣло и принимаетъ черезъ нѣкоторый, хотя
бы и весьма большой или, теоретически говоря, даже безконечно боль-
шой промежутокъ времени. Температура Ѳ, къ которой стремится тѣло,
и можетъ быть названа температурой окружающей среды. Иногда бы-
ваетъ удобнымъ принять Ѳ = 0, т.-е. вести счетъ температуры отъ этой
температуры. Тогда приходится разсматривать только избытокъ тем-
пературы тѣла надъ температурой окружающей среды, т.-е. величину,
стремящуюся съ теченіемъ времени къ нулю. Охлаждающееся тѣло мо-
жетъ быть окружено жидкостью или газомъ; мы будемъ разсматривать,
главнымъ образомъ, второй случай. *
Потеря теплоты охлаждающимся тѣломъ, которое окружено газомъ,
происходитъ по четыремъ причинамъ:
1) Тѣло теряетъ теплоту вслѣдствіе ея превращенія въ лучи-
стую эн ергію: выражаясь точнѣе, мы должны сказать, что тѣло больше
теряетъ теплоты вслѣдствіе его лучеиспусканія, чѣмъ оно получаетъ те-
плоты, возникающей на счетъ той лучистой энергіи, которая испускается
совокупностью всѣхъ окружающихъ тѣлъ и поглощается поверхностью тѣла.
2) Потеря тепла происходитъ подъ вліяніемъ силы тяжести, дѣй-
ствующей на газъ, который окружаетъ тѣло, и вызывающей восходящіе
потоки нагрѣтаго газа, бывшаго въ соприкосновеніи съ поверхностью тѣла.
Этотъ газъ непрерывно замѣняется другимъ, притекающимъ съ боковъ и
снизу. Такимъ образомъ устанавливается теченіе газа, уносящее теплоту
отъ поверхности тѣла. Этотъ способъ перемѣщенія теплоты, т.-е. ея уносъ
подвижною средою, называется конвекціей.
3) Газъ, окружающій тѣло, обладаетъ теплопроводностью и потому
часть теплоты уходитъ черезъ газъ безъ превращенія въ другую форму
энергіи. Мы увидимъ въ слѣдующей главѣ, что теплопроводность
даннаго газа отъ его плотности не зависитъ, что она оста-
ется неизмѣнною до весьма высокой степени разрѣженія газа. Хотя те-
плопроводность газовъ сравнительно невелика, она однако играетъ важную
роль въ явленіяхъ охлажденія.
Законъ Ньютона
275
4) Невозможно помѣстить тѣло свободно въ газовой средѣ, а потому
всегда происходитъ нѣкоторая убыль тепла вслѣдствіе теплопроводности
тѣхъ тѣлъ, которыя удерживаютъ охлаждающееся тѣло въ его положеніи.
Четвертую изъ перечисленныхъ здѣсь причинъ потери теплоты мы
вовсе разсматривать не будемъ. Опыты охлажденія слѣдуетъ вести такъ,
чтобы эта потеря была по возможности мала.
Конвекцію можно уменьшить, помѣщая охлаждающееся тѣло въ зам-
кнутое пространство, въ которомгь газъ по возможности разрѣженъ. Но
во всякомъ случаѣ играетъ роль въ явленіяхъ охлажденія,
кромѣ лучеиспусканія, еще теплопроводность окружаю-
щаго газа. При охлажденіи тѣла въ неразрѣженномъ газѣ присоеди-
няется сюда еще конвекція. Изъ всего сказаннаго явствуетъ, что охлаж-
деніе тѣлъ представляетъ въ общемъ случаѣ крайне сложное явленіе; не-
удивительно, что законы этого явленія еще далеко не выяснены: оно за-
виситъ отъ слишкомъ большого числа разнообразныхъ факторовъ, выяс-
нить отдѣльное вліяніе которыхъ невозможно. Въ особенности сложными
представляются явленія конвекціи, зависящія отъ рода и состоянія окру-
жающаго газа, отъ формы оболочки, окружающей газъ, если таковая су-
ществуетъ, и отъ положенія тѣла въ этой оболочкѣ. Явленіе еще услож-
няется, если окружающій газъ самъ по себѣ находится въ движеніи, напр.
въ случаѣ охлажденія тѣла на открытомт, воздухѣ. Дальнѣйшее осложне-
ніе проистекаетъ отъ той роли, которую въ явленіяхъ охлажденія играетъ
внутренняя теплопроводность самого охлаждающагося тѣла.
Теплота теряется съ поверхности тѣла, къ которой она должна притекать
пзвнутрп : поэтому внутренія части тѣла должны имѣть болѣе высокую
температуру, чѣмъ поверхностные слои, такъ что вообще о температурѣ
охлаждающагося тѣла и говорить нельзя. Къ этому вопросу мы возвра-
тимся въ слѣдующей главѣ, а здѣсь мы предположимъ, что охлаждаю-
щееся тѣло столь мало или столь хорошо проводитъ теплоту, что въ каж-
дый данный моментъ можно пренебречь разностью между температурами
различныхъ его точекъ и принять для всего тѣла одну и ту же непре-
рывно мѣняющуюся температуру.
Въ этой главѣ мы разсматриваемъ только явленія правильнаго охла-
жденія, не сопровождаемыя побочными явленіями, напр. химическаго ха-
рактера. Когда охлаждается напр. желѣзо, то при опредѣленныхъ тем-
пературахъ замѣчается остановка въ охлажденіи и даже повышеніе тем-
пературы. Эти явленія рекалесценціи имѣютъ химическія причины.
Изъ вышеизложеннаго ясно, что слѣдуетъ отличать законы
лучеиспусканія и законы охлажденія, зависящаго не только
отъ лучеиспусканія, но и отъ теплопроводности газовъ, а обыкновенно
еще и отъ конвекціи. Существуютъ наблюденія, несомнѣнно служившія
къ изученію законовъ лучеиспусканія: это наблюденія съ термоэлектри-
ческимъ столбикомъ или съ болометромъ, установленнымъ въ сторонѣ отъ
тѣла, температура котораго была извѣстна, могла быть измѣняема по про-
изволу и удерживаема постоянною втеченіе времени, достаточнаго для
18*
276
Охлажденіе.
производства наблюденія. Непосредственныя наблюденія надъ температу-
рою охлаждающагося тѣла, понятно, могли привести только къ законамъ
охлажденія. Нѣкоторые ученые старались найти теоретическіе или
эмпирическіе законы охлажденія, въ которыхъ отдѣльно выразились бы
потери тепла лучеиспусканіемъ и дѣйствіемъ окружающаго газа.
§ 2. Законъ Ньютона, Количество (2 теплоты, теряемое поверх-
ностью 5 тѣла во время т, выражается формолю
= . . .............Ц)
гдѣ коеффиціентъ і/ измѣряется количествомъ тепла, которое теряется еди-
ницей поверхности въ единицу времени. Законъ Ньютона выражаетъ, что
V пропорціонально разности температуръ Т тѣла и Ѳ окружающей среды:
Ч = Ѳ)..............................(2)
гдѣ А постоянное число. Но этому закону имѣемъ
р = Л(Г~Ѳ)5г........................(3)
Величину 1г мы назовемъ коеффиціентомъ внѣшней те-
плопроводности; эта величина измѣряется тѣмъ количествомъ тепла,
которое теряется единицей поверхности тѣла въ единицу времени, когда
втеченіе этого времени поддерживается разность температуръ Т—Ѳ=1°.
Величину И можно было бы назвать лучеиспускательною способностью
поверхности если бы охлажденіе происходило въ пустотѣ. На законъ
Ньютона слѣдуетъ смотрѣть, какъ на эмпирическій законъ охла-
жденія, причемъ И, въ самомъ общемъ случаѣ, содержитъ въ себѣ всѣ
четыре части (стр. 274), на которыя распадается теплота, теряемая тѣломъ.
Практическая примѣнимость этого закона ограничивается случаемъ, когда
разность Т -Ѳ не превышаетъ 5°, и во всякомъ случаѣ нельзя смотрѣть
на А, какъ на величину, не зависящую отъ абсолютныхъ значеній тем-
пературъ Т и она растетъ примѣрно на 1% при повышеніи обѣихъ
температуръ на 1°.
Выведемъ законъ пониженія температуръ при допущеніи закона
Ньютона. Весьма малое количество тепла теряемое тѣломъ въ
малый промежутокъ времени Лг, приблизительно равно
= Ѳ)5/Іг............................Г4)
Время г будемъ считать отъ начала охлажденія, когда температура
тѣла равнялась То. Величина /іф равна также — сД Г, гдѣ с теплоемкость
охлаждающагося тѣла, и — ДТ весьма малое пониженіе температуры во
время Дт. Выраженіе (4) для тѣмъ точнѣе, чѣмъ меньше время Дт,
втеченіе котораго разность Т—Ѳ, въ дѣйствительности непрерывно мѣняю-
щаяся, принимается постоянною. Равенство й(Г—Ѳ)8Дт =—сД Т, дающее
будетъ тѣмъ точнѣе, чѣмъ меньше Дт. Въ предѣлѣ получаемъ точное вы-
Законъ Ньютона. — Законъ Дюлонга и Пти
277
. СІТ И8 _ СІТ А5 , ~
раженіе (/—в). Оно даетъ ? =-----— ат. Отсюда имѣемъ
г (ІТ Н8 г. Та О
ибо т = 0 соотвѣтствуетъ Т= Го; интегрируя, получаемъ
"ІЙ 5*? ф ф II
и наконецъ Л5 Г=Ѳ+(Т0-Ѳ> (5)
При т = 0 имѣемъ Т = Го, при т = оо получаемъ Т — Ѳ, т.-е. температура
тѣла асимптотически приближается къ температурѣ Ѳ окружающаго про-
странства. Если принять Ѳ = 0, т.-е. разсматривать только избытки
Т и Го температуры тѣла надъ температурою окружающей среды, то
вмѣсто (5) получается
Т=Тое~~с~т.......................(6)
Замѣтимъ, что (5) выражаетъ также законъ нагрѣванія тѣла,
имѣющаго начальную температуру Го, и помѣщеннаго въ среду съ болѣе
высокою температурою Ѳ; въ этомъ случаѣ слѣдуетъ написать (5) въ видѣ
Т=Ѳ ^—Т^е~ст ........................(7)
Говоря о численныхъ значеніяхъ величины А, выражаютъ обыкно-
венно (2 въ малыхъ калоріяхъ, 5 въ кв. см. и время г въ минутахъ;
тогда А измѣряется числомъ малыхъ калорій, теряемыхъ кв. сантиме-
тромъ поверхности въ одну минуту. Наблюденіе температуры охлажда-
ющагося тѣла даетъ возможность вычислить И формулѣ
Н = .............................(8)
легко получающейся изъ (б)
§ 3. Законъ Дюлонга и Пти. Прежде чѣмъ приступить къ изло-
женію классическихъ опытовъ Виіоп^’а и Реііі надъ охлажденіемъ
тѣлъ введемъ понятіе о скорости V охлажденія. Температура Т охлаж-
дающагося тѣла есть нѣкоторая функція времени т. такъ что вообще
можно написать Т =- / (г). Величину
Ѵ = -/(т) = -^........................ )
мы назовемъ скоростью охлажденія. Количество /1(2 тепла, те-
ряемое во время /1т, равно, см. (1) стр. 276, ?;5Лт, гдѣ т] именно та
величина, которую мы ищемъ и для которой законъ Ньютона до-
пускаетъ простую форму (2) стр. 276. Во всякомъ случаѣ ц содержитъ Г,
и слѣд. мѣняется во время /1т, а потому послѣдняя формула, въ кото-
рой щ считается не зависящимъ отъ т, будетъ тѣмъ точнѣе, чѣмъ меньше /1т.
Въ предѣлѣ имѣемъ точное выраженіе
278
Охлажденіе.
Величина : сіт называется тепловымъ потокомъ, исходящимъ
отъ тѣла. Съ другой стороны очевидно
(1$ = — сЛТ....................(11)
гдѣ с теплоемкость тѣла; отсюда — сйТ — т.-е.
Ѵ= — ^=ѵ8 ........ (12)
аг с
Послѣдняя формула даетъ
т/ (л о\
3 1/= 3 ,1г..................П31
•
Искомая величина пропорціональна скорости охлажденія V. Для (К^
имѣемъ выраженіе, см. (10),
б/ф = сѴсіт......................(14)
и наконецъ имѣемъ очевидную связь между тепловымъ потокомъ и ско-
ростью охлажденія
У = сѴ.........................(15)
тонкостѣнный
Рис. 87.
Формула (13) показываетъ, что для изученія закона
охлажденія тѣлъ можно опредѣлять изъ опытовъ ско-
рость охлажденія Ѵ—йТ.йт. Такъ и поступали Виіоп^ и
Р е ѣ і ѣ. Приборъ, которымъ они пользовались, изображенъ на рис. 87.
Большой сосудъ наполненъ водой; внутри воды помѣщается мѣдный
шаръ В, вычерненный внутри. Его радіусъ около 15 см.;
онъ снабженъ цилиндрическимъ горлышкомъ, на которое
ставится стеклянный .цилиндръ і, соединенный при по-
мощи трубки г съ воздушнымъ насосомъ. Во внутрь
шара В вставляется резервуаръ Т большого термометра,
предварительно сильно нагрѣтаго и показывающаго, какъ
всякій термометръ, свою собственную температуру. Этотъ
резервуаръ и представляетъ тѣло, охлажденіе котораго
наблюдалось. Вставивъ нагрѣтый термометръ, покрывъ
его цилиндромъ I и выкачавъ воздухъ до давленія 2—3 мм.,
13 и 1 о п у и РеііЬ наблюдали температуру охлаждаю-
щагося шарика. Они полагали, что вліяніе оставшагося воз-
духа ничтожно, и что наблюдаемое охлажденіе происходитъ исключительно
только отъ лучеиспусканія. По это невѣрно, такъ какъ теплопроводность
газа отъ его плотности не зависитъ; мы увидимъ ниже, какъ велико было
охлаждающее дѣйствіе газа, остававшагося въ разсматриваемыхъ опытахъ
внутри шара В, Изслѣдовавъ охлажденіе «въ пустотѣ», □ и 1 о п § и
Р е 1 і і производили ряды наблюденій, когда шаръ В былъ наполненъ
различными газами, причемъ давленіе и температура газа мѣнялись въ
Законъ Дюлонга и Пти.
279
широкихъ предѣлахъ. Такимъ образомъ они надѣялись совершенно от-
дѣлить вліяніе лучеиспусканія отъ вліянія окружающаго газа. Непосред-
ственно наблюдалась температура Т охлаждающагося тѣла (черезъ каж-
дую минуту) и температура 0 окружающей оболочки, равпая темпера-
турѣ воды въ большомъ сосудѣ. Обозначимъ избытки температуръ
черезъ і, такъ что _ р____у
Для опредѣленія скорости V при различныхъ Ѳ и і, Виіоп^ и
Ре Ш поступали слѣдующимъ образомъ. Формулу (6), относящуюся къ
избыткамъ, можно написать въ видѣ
л. — са
і = і^е
Наблюденные большіе избытки і не выражаются, однако, такою
функціею времени г, такъ какъ законъ Ньютона непримѣнимъ при боль-
шихъ і. Поэтому Л и 1 о п и Р е і і ѣ приняли чисто эмпирическую
зависимость _ (пт । ,зт2\ , х
7 = + ..................(17)
и изъ наблюденій опредѣляли для каждаго отдѣльнаго опыта значеніе
трехъ постоянныхъ А, а и /?. Формула (17) даетъ
/У/
V = — 7 = (а + 1]%А.................. (18)
аг
Дай/? извѣстны, слѣд. по этой формулѣ могла быть вычислена скорость V.
Прежде всего В и 1 о п и Р е Н1 изслѣдовали вліяніе массы М и
поверхности 5 охлаждающагося тѣла. Они опредѣлили скорости Ц. Ѵ2
и охлажденія въ неразрѣженномъ воздухѣ, при различныхъ
избыткахъ і отъ I = 20° до I = 100°, трехъ шариковъ, діаметры кото-
рыхъ равнялись 2, 1 и 7 см. Оказалось, что при всѣхъ і отношеніе
Ц : І/2 = 2,11, а отношеніе Іф: = 3,80. Отсюда слѣдуетъ, что за-
конъ измѣненія V въ зависимости отъ і одинъ и тотъ* же для всѣхъ
шариковъ, т.-е. отъ 714 и 5 не зависитъ. Подобнымъ же образомъ они
сравнили скорости V охлажденія термометренныхъ резервуаровъ различ-
ной формы, наполненныхъ различными жидкостями. И здѣсь оказалось,
что отношеніе скоростей, взятыхъ при одномъ и томъ же избыткѣ і, отъ
этого избытка не зависитъ. Такъ напр. скорость Ѵф для шарика, напол-
неннаго водой, составляла" при всѣхъ I лишь 0,454 скорости Ѵ2 для ша-
рика, наполненнаго ртутью. Но когда Л и 1 о п и Реііі стали срав-
нивать скорости охлажденія стекляннаго резервуара съ блестящею, ни-
чѣмъ не покрытою поверхностью и стекляннаго шарика посеребреннаго,
то оказалось, что отношеніе скоростей охлажденія не одно и то же при
различныхъ і.
Изъ всего сказаннаго слѣдуетъ, что скорость V охлажденія тѣла,
окруженнаго газомъ, можетъ быть представлена въ слѣдующемъ видѣ:
V пг I/(е, і, 0) -ф- ср (е, р, і, $)].........(19)
гдѣ пг зависитъ отъ массы 714 и оть поверхности 5 охлаждающагося
280 Охлажденіе.
тѣла и, кромѣ того, отъ его формы и состава; далѣе е величина, харак-
теризующая родъ поверхности (стекло, серебро и т. д.), к зависитъ отъ
рода газа, р упругость газа. Первый членъ въ скобкахъ долженъ теоре-
тически опредѣлять скорость охлажденія въ пустотѣ, второй равенъ уве-
личенію скорости, вызванному присутствіемъ газа. На дѣлѣ первый членъ,
опредѣленный Би Іонномъ и Рѳііі, равенъ скорости охлажденія въ
газѣ, упругость котораго хотя и равна всего 2—3 мм., но теплопровод-
ность котораго такая же, какъ у газа неразрѣженнаго.
Обращаемся къ опытамъ Биіоп^’а и Реііі, произведеннымъ въ
весьма разрѣженномъ воздухѣ, въ «пустотѣ» по ихъ выраженію.
Оказалось, что скорость охлажденія при всѣхъ і увеличивается въ
1.16 разъ, когда температура 0, а слѣд. и температура Т увеличивается
на 20°. Это значитъ, что V увеличивается въ геометрической прогрессіи,
когда Ѳ растетъ въ ариѳметической прогрессіи, и что въ выраженіе #),
которое мы ищемъ, входитъ множитель вида а®. Кромѣ того, V зави-
ситъ отъ і, а потому V въ «пустотѣ» выражается формулою вида
V = гр (і) а®......................(20)
Такъ какъ V увеличивается въ 1,16 разъ, когда Ѳ увеличивается на 20°,
то я20 = 1,16, откуда 2о/-
а = |/ 1,16 — 1.0077 ....................(21)
Зависимость V оть /, т.-е. видь функціи гр(і) былъ опредѣленъ Он-
іо п ^’омъ и Р е 1 і I теоретически на основаніи слѣду ющихъ соображе-
ній. Скорость V охлажденія тѣла есть разность между скоростью Ц. съ
которою тепловая энергія тѣла передается окружающему эфиру, и ско-
ростью Ѵ2, съ которой тепловая энергія тѣла растетъ, образуясь изъ по-
тока лучистой энергіи, испускаемаго окружающей оболочкой. Ц есть
функція отъ Т = і + Ѵ2 есть функція отъ 0, и эти двѣ функціи
должны быть одинаковы, т.-е. можно положить
Р) — Р(Р) .... (22)
ибо V — 0 при всѣхъ б/, когда ^=0. Сравнивая это съ (20), получаемъ
Р (і -р- Ѳ) — Р (Ѳ) = гр (/) а®. При Ѳ — 0 имѣемъ Р (^) — Р (0) = тр (/").
Вычитая это изъ предыдущаго, получаемъ Р (і + 0} — Р(і) — Р (Ѳ) +
+ ЛО) = V (0 1).
Если Ѳ и і обмѣняются значеніями, то мы имѣемъ
Е(Ѳ)- Г(0 + ^(0) = Ѵ(^(^ - 1).
Лѣвыя части послѣднпхгь двухъ равенствъ одинаковы, слѣд.
—1) ~ (0) (а*—1) или .
а1 — 1 а° — 1
Ѳ и і совершенно произвольны, а потому ясно, что при всѣхъ значеніяхъ
ѵ « , , V . V’ (/) Л
перемѣнной г этадрооь имѣетъ одно и то же значеніе, т.-е. что . - А,
а1 — 1
гдѣ А постоянное число. Отсюда ір(/) -- А (аі— 1) и слѣд., см. (20),
Законъ Дюлонга и Пти.
281
Ѵ=АаЧаі — 1) = А^а1 — аР} . . . (23)
гдѣ А зависитъ отъ формы, массы и состава охлаждающагося тѣла и
отъ величины и отъ рода (величина ё) его поверхности. Формула (23) и
выражаетъ т. наз. законъ Дюлонга и Пти.
Переходимъ къ опытамъ охлажденія въ пространствѣ, наполненномъ
газомъ. Скорость V охлажденія состоитъ теперь изъ двухъ частей
.................(24)
изъ которыхъ первая равна выше найденному Ѵ17 т.-е.
Ѵ1 = Ааѳ(аі — 1) = А(аг — аѳ)...... (25)
Вторую часть мы въ формулѣ (19) символически выразили такъ:
Ѵ2 = тд> (е, к. р, і, Ѳ)........(26)
Значеніе буквъ приведено выше. Для опредѣленія величины Ѵ2 В и -
I о п и РеІИ наблюдали скорость V охлажденія въ газѣ при тѣхъ
условіяхъ, т.-е. при тѣхъ значеніяхъ А и Ѳ. при которыхъ раньше была
опредѣлена скорость Ц въ пустотѣ». Вычитая Ц изъ V, они полу-
чали скорость І/2.
Производя наблюденія со стекляннымъ шарикомъ непокрытымъ и
съ шарикомъ посеребреннымъ, они нашли для Ѵ2 одинаковыя въ обоихъ
случаяхъ значенія. Отсюда слѣдуетъ, что Ѵ2 отъ е не зависитъ: охлаж-
дающее дѣйствіе газа не зависитъ отъ рода поверхности тѣла. Если
предварительные опыты показали, что V зависитъ отъ е, то это объяс-
няется тѣмъ, что Ц находится въ зависимости отъ е, и что множитель А
мѣняется съ измѣненіемъ лучеиспускательной способности поверхности тѣла
Дальнѣйшіе опыты показали, что скорость Ѵ2 при данномъ избыткѣ I
не зависитъ отъ Ѳ. Вмѣсто (26) мы можемъ теперь написать
І/2 = тд (&, р, I)....................(27)
Далѣе В и 1 о п и Реііі опредѣляли скорость Ѵ2 при различныхъ
давленіяхъ р газа. Оказалось, что при всѣхъ избыткахъ і скорость Ѵ2
увеличивается въ 1,36 разъ, когда давленіе р увеличивается въ 2 раза и
когда окружающій газъ есть воздухъ. Если р перейдетъ въ р‘ — 2пр. то
Ѵ2 перейдетъ въ V/= (1,36)^14? Это даетъ
Рр = !§• «1^1,36, •
или
. 14' 1^1,36. р' _ р' . [р'\№ .. Ѵё (р'\°^
!§• т7 = т о - 0,4э1§-=1§ Г . Отсюда “ = ,
ь Ѵ2 1ц2 р Р \Р/ ^4 \Р/
т.-е. скорости охлажденія пропорціональны степени 0,45 упругостей воз-
духа. Итакъ вообще
Ѵ2 = тар (к, і)рс . ... . . (28)
гдѣ с, однако, оказалось зависящимъ отъ к, т.-е. отъ рода газа. В и-
1 о п и Реііі нашли слѣдующія значенія показателя с:
282
Охлажденіе.
С с
Воздухъ...........0,45 Углекислый газъ . 0,517
Водородъ .... 0,38 Маслородный газъ 0,501.
Наконецъ В и 1 о п и Р е і і і изслѣдовали завігсим<>сгь скорости
отъ избытка і = Т — Ѳ, Оказалось, что скорость Ѵ2 увеличивается вч»
2,35 раза, когда I увеличивается въ 2 раза. Совершенно какъ въ пре-
дыдущемъ случаѣ, мы выведемъ отсюда, что Ѵ2 пропорціонально нѣко-
]о’2 35
торой степени п избытка /, причемъ п = = 1,232. Оказалось, что
этотъ показатель отъ рода газа не зависитъ. Окончательно имѣемъ теперь
= 5^1,232.....................................................(29)
гдѣ В и с зависитъ отъ рода газа и. кромѣ того. В зависитъ отъ массы,
формы и состава охлаждающагося тѣла. Вставивъ (25) и (29) въ (24),
получаемъ окончательно
Ѵ=- Аа^а* — Г) + Вр'В™. . . . (30)
гдѣ а = 1,0077; зависимость В и с отъ разныхъ обстоятельствъ только-
что была указана; коеффиціентъ А отъ рода газа не зависитъ, но зато
онъ зависитъ отъ рода поверхности охлаждающагося тѣла.
Количество теплоты, теряемое тѣломъ въ единицу времени,
равно 0 = сѴ, гдѣ с теплоемкость тѣла и V принимается постояннымъ
втеченіе единицы времени: количество д теплоты, теряемое единицей
поверхности въ единицу времени въ пустотѣ, равно
<7 ? ^5 (а1 -а^ = т(ат . (31)
о о о
гдѣ Т = Ѳ + /, какъ прежде, температура тѣла. Роиіііеі нашелъ
для поверхности, покрытой сажей, т = 1,146. Реггеі, основываясь на
опытахъ ЫісІіоГя, вычисляетъ /тг = 1,085. Мы увидимъ ниже, что эти
числа слишкомъ велики.
Опыты В и 1 о п ^’а и Р е і і і были критически разобраны весьма
большимъ числомъ ученыхъ, работы которыхъ не оставляютъ сомнѣнія
въ томъ, что формула (30) не выражаетъ закона природы, что ей можно
придать лишь значеніе формулы эмпирической. Ве Іа Ргоѵояіауе
и Веяаіпя первые повторили опыты Виіоп^’а и Реііі; они изу-
чили охлажденіе посеребренныхъ, позолоченныхъ, вычерненныхъ, а также
ничѣмъ не покрытыхъ стеклянныхъ резервуаровъ термометровъ. Кромѣ
того они мѣняли форму того сосуда, внутри котораго происходило охлаж-
деніе. Они нашли, что множитель А. дѣйствительно постоянный для не
покрытаго стекла, зависитъ для покрытаго стекла отъ температуры. Такъ
они нашли, что для резервуара, покрытаго серебромъ, А = 0,00870 при
150° и А = 0,01090 при 63°. Множитель В не вполнѣ одинаковъ для
различныхъ поверхностей. Особенно важнымъ представляется открытый
ими фактъ, что при слабыхъ давленіяхъ р охлаждающее дѣйствіе газа
Законъ Дюлонга и Пти.
283
перестаетъ быть пропорціональнымъ рс. Существуютъ два давленія рх
и между которыми это дѣйствіе постоянно, т.-е. отъ р не зависитъ;
величины и р2 различны, смотря по формѣ и размѣрамъ пространства,
въ которомъ совершается охлажденіе.
Изслѣдованіемъ степени примѣнимости формулы Впіоп^'а и Ре-
1і1, и вообще ея критикою занимались Норкіпв, 8 о г е к, ЛѴ11 -
йеіту, Ргарег, Мас-Гегіапе, Егісвоп, Ьап^іеу, Ѵіоііе,
(дгаеѣг, К а г г , Л а т і п и Кісйагсі, Кіѵіёге, Зіеіап и въ
послѣднее время Сотрап. Слѣдуетъ однако имѣть въ виду, что нѣко-
торые ученые критиковали формулу Виіоп^’а и Реііі, какъ выража-
ющую закона» охлажденія, а другіе лишь первую часть формулы, разсма-
тривая ее, какъ выраженіе нѣкотораго закона лучеиспусканія. Такъ,
I) г а р е г измѣрялъ лучеиспусканіе металлической проволоки, нагрѣвае-
мой электрическимъ токомъ, и нашелъ, что напр. лучеиспусканія при 800°.
1200° и 1600° относятся между собою, какъ 1:5:16. между тѣмъ какъ
законъ Оикп^’а и Реііі далъ бы отношенія 1:21,5:462,2. Наибо-
лѣе важный критическій разбора опытовъ В и 1 о п ^’а и Р е ѣі ѣ при-
надлежитъ Віеіап’у. который обратилъ вниманіе на -вліяніе теплопро-
водности газа, остававшагося вт» сосудѣ при опытахъ въ т. наз. пустотѣ.
8іеі‘ап вычислилъ, какая доля величины К наблюденной Впіоптомъ
и Реѣіѣ въ ихъ < пустотѣ», вызывалась теплопроводностью газа, оставав-
шагося вт» сосудѣ; онъ при этомъ воспользовался формулою, которая бу-
детъ выведена въ слѣдующей главѣ. Результаты его вычисленій для
двухъ рядовъ наблюденій Выіоп^’а и Реѣі Ь приведены въ нижеслѣ-
дующей табличкѣ; эти наблюденія относились къ стеклу и къ серебру
при Ѳ = 20°. Числа третьяго столбца относятся къ резервуару посере-
бренному. Въ четвертомъ столбцѣ помѣщены скорости охлажденія, вы-
званныя теплопроводностью газа и очевидно одинаковыя для обѣихъ по-
верхностей. Въ послѣднихъ двухъ столбцахъ помѣщены исправленныя
скорости охлажденія, которыя соотвѣтствовали бы дѣйствительной пу-
стотѣ. Итакъ при Ѳ = 20° имѣемъ :
Избытокъ. і V, наблюденныя ИиІоптомъ и Регіг. Поправка. Истинныя V въ пустотѣ.
Стекло Серебро Стекло Серебро
240° 12,40 2,18 0,99 11,41 1Д9
200 8,58 1,53 0,79 7,79 0,74
160 5,67 1,02 0,61 5,06 0,41
120 3,56 0,62 0,44 3,12 ОДЯ
100 2,74 0,47 0,36 2,38 0,11
80 1,99 0,34 0,28 1,71 0,06
60 1,40 0,24 0,20 1,20 0,04.
Для стекла поправка доходитъ до 16%, для серебра же она коле-
блется между 45% и 84%, т.-е большая часть наблюденнаго
охлажденія вызывалась теплопроводностью газа, оста-
вавшагося в ъ с о с у д ѣ! Въ дальнѣйшія подробности критическаго
284
Охлажденіе.
разбора опытовъ Оиіоп^’а и Реііі, сдѣланнаго 8іеіап’омъ, мы не
входимъ. Опыты С г о о к е в’а , (см. ниже въ статьѣ о теплопроводности
газовъ) еще рѣзч ? указываютъ на роль слѣдовъ газа, окружающихъ охла-
ждающееся тѣло.
Большинство авторовъ, упомянутыхъ на стр. 283, высказывались про-
тивъ примѣнимости формулы В и 1 о п ^’а и Р е I і I и противъ того, чтобы
первая ея половина могла быть принята, какъ законъ лучеиспусканія.
По мнѣнію Огаеіг’а, слѣдуетъ признать этотъ законъ неприложимымъ
даже при низкихъ температурахъ. Ѵіоііе произвелъ большой рядъ из-
слѣдованій надъ лучеиспусканіемъ раскаленныхъ тѣлъ. Въ одной изъ
этихъ работъ онъ полагалъ возможнымъ удержать формулу В и 1 о п ^’а и
Р е і і Ь, считая однако величину а за нѣкоторую функцію избытка такъ
что при і =^= 800° величина а = 1,0233, при і = 1775° оказалось уже
а = 1,0144.
§ 4. Формулы ЗіеТап’а, ѣогепх’а, Возеііі, Ѵіоііе’я, Терешина и др.
Охлажденіе твердыхъ тѣлъ въ жидкостяхъ. Въ т. II мы уже указали
на различныя формулы, выражающія законы лучеиспусканія. Эти
же формулы представляютъ и законы охлажденія тѣлъ въ пусто т ѣ. При-
ведемъ болѣе полный обзоръ формулъ, относящихся собственно къ охлаж-
денію тѣлъ; въ нихъ Т и Ѳ обозначаютъ абсолютныя температуры
тѣла и окружающей оболочки.
Формула 8іе1'ап’а для количества д теплоты, испускаемаго еди-
ницей поверхности въ единицу времени, такова:
д = о(Г4 —......................* . (32)
гдѣ, какъ и въ (31), Т температура тѣла, 0 температура окружающаго про-
странства или, точнѣе, окружающей оболочки. Мы видимъ, что по 81 е -
Іап’у д пропорціонально разности четвертыхъ степеней абсолютныхъ
температуръ тѣла и оболочки.
Если О мало сравнительно съ Т, то можно пользоваться упрощен-
ною формулою
д = вТ1.......................(32, а)
Воікшапп, Голицынъ, Сггаеій, 8сЬпееЪе1і,8с]і1еіег-
шасЬег, Воііотіеу, Реггеі, Віѵіёге и др. занимались изслѣ-
ваніемъ примѣнимости формулы 81 е I а п’а. Сюда же относится болѣе тео-
ретическая работа СЬгівііапзеп’а. Ьишшег и Ргіп^вііеіт до-
казали (1897), что формула біеіап’а вполнѣ точно выражаетъ законъ
лучеиспусканія (охлажденія въ пустотѣ) для абсолютно чернаго
тѣла (т. II).
Далѣе ограничиваемся перечнемъ формулъ:
Реггеі: д = б(Тп — Ѳп), гдѣ п колеблется между 3,6 и 4,2.
ВовеШ: д = аТ* (Т — 0) — Ь (Г — 0).
Н. Р. АѴ еЬ ег: д = А (еа?Т — еа®Ѳ").
Есііег: д = А (Т - - 0) еа(Т - Ѳ\
Охлажденіе твердыхъ тѣлъ въ жидкостяхъ.
280
Г. Я. Терешинъ предложилъ двѣ формулы:
д = АеаТ(Гі — Ѳ*),
д = ВеаТ\Т^ - іА\
Болѣе сложныя формулы были предложены ѴіоПе’емъ.
Всѣ приведенныя формулы относятся къ охлажденію въ пустотѣ,
ибо онѣ, какъ сказано, выражаютъ законы лучеиспусканія. Фор-
мулы, которыя выражали бы дѣйствительные законы охлажденія и
которыя были бы аналогичны формулѣ (30), стр. 282, В и 1 о п д’а и Р е -
ііі, были предложены ЛѴіІЬе 1 ту, ОЬегЬеск’омъ, Ботепг’омъ и
Терешинымъ. Формула ЛѴ і 1Ь е 1 т у весьма сложна ; формула Б о -
тепг’а имѣетъ слѣдующій видъ 5
д = о (Г4 — 04) + Л (Т — ѲУ..............(33)
гдѣ Л зависитъ отъ формы и размѣровъ охлаждающагося тѣла; она отли-
чается отъ формулы (32) 81 е I а п’а лишь добавочнымъ членомъ. Б. ЛѴ. Н а г і -
тапп (1904) опубликовалъ многочисленныя наблюденія надъ теплоотда-
чей раскаленныхъ нитей. Изъ этихъ наблюденій Терешинъ (1905) вы-
велъ, что формула Б огепг’а (33) справедлива для широкаго температур-
наго интервала отъ 200° до 1500°. Самъ Терешинъ ранѣе (1897) пред-
ложилъ слѣдующія двѣ формулы:
д = Аеа1\Ті - Ѳ*) + а (Г—
д = ВеаГІ(Р — Ѳ*) -Н Ь (Т —
Беев замѣнилъ число 4 почти равнымъ ему числомъ 1,26. В. ЛѴа§-
пег (1902) нашелъ, что формула Богепг’а не выдерживаетъ критики,
такъ какъ показатель при различныхъ обстоятельствахъ различенъ. Такъ
какъ первый членъ формулы Богепя’а относится только къ абсолютно
черному тѣлу, то понятно, что двучленная формула (33) не можетъ вы-
ражать общаго закона охлажденія. Всѣ разсмотрѣнныя до сихъ поръ фор-
мулы относятся къ случаю, когда охлаждающееся тѣло находится въ пу-
стотѣ или въ неподвижномъ воздухѣ. Охлажденіе въ потокѣ воздуха
изслѣдовали экспериментально ОЬегЬеск (1895), теоретически Б о г е п г
(1881) и для нѣкоторыхъ спеціальныхъ случаевъ Воиввіпевд (1902).
Для вертикальной проволоки въ горизонтальномъ воздушномъ потокѣ
ОЬегЬеск находитъ, что скорость охлажденія пропорціональна скорости
и плотности воздуха.
Охлажденіе твердыхъ тѣлъ въ жидкостяхъ изслѣдовали теорети-
чески ОЬегЬеск, Богепг и Воивзіпевц. Послѣдній находитъ, что
для тѣла произвольной формы потеря тепла въ покою щейся жид-
кости выражается формулою
д — Лу0’233 &0’533 ^0,46" . у} 1,233
гдѣ у коеффиціентъ расширенія, к коеффиціентъ теплопроводности (см.
гл. VII), с теплоемкость жидкости. Если жидкость течетъ параллельно
плоской поверхности тѣла, то д пропорціонально квадратному корню изъ
28о
Охлажденіе.
скорости теченія. Затѣмъ Воиййіпезц (1905) значительно обобщилъ
свои изысканія и развилъ формулы для охлажденія тѣлъ любой формы,
поверхность которыхъ повсюду выпукла. Спеціально онъ изслѣдовала^
случаи, когда тѣло представляетъ собою эллипсоидъ, пластинку, иглу,
сферу и эллиптическій цилиндръ.
Опытныя изслѣдованія охлажденія гѣлъ въ покоющейся жиакости
производили Огоѵе и Эаіапсіег, въ движущейся 8ег, біапѣоп и
Роговскій.
§5. Численныя величины для скорости охлажденія. Мас Гегіапе
изслѣдовалъ охлажденіе мѣднаго шара, діаметромъ въ 4 см., помѣщеннаго
внутри сосуда, между двойными стѣнками котораго находилась вода при
комнатной температурѣ. Шаръ былъ окруженъ невысушеннымъ возду-
хомъ при нормальномъ давленіи; температура его измѣрялась при помощи
термоэлектрическаго элемента. Для количества ц теплоты, теряемой въ
1 минуту однимъ кв. сантиметромъ поверхности, когда
разность температуртэ тѣла и оболочки равна /°, онъ на-
шелъ слѣдующія числа, выраженныя въ малыхъ калоріяхъ, для по-
лированной и для вычерненной поверхности мѣднаго шара:
і Поверхн. полирована. • Поверхн. вычернена. (‘тношеніе.
5° о,оюб8; X 5 0,01512 X 5 0,707
10° о,оіпб; X 10 0,01596 X Ю 0,699
20° 0,01206 X 20 0,01734 X 20 0,695
30° 0,01272; X 30 0,01836 X зо 0,693
40° 0,01320 х 40 0,01914 X 40 0,693
60° 0,01396 ' X 60 0,01968 X 60 0,690
Аналогичные опыты производили Місйоі и Воіѣотіеу. Если
написать ц въ видѣ = Иі, то величина /? возрастаетъ съ повышеніемъ
температуры. Къ тому же результату приводятъ формулы В и 1 о п д^а и
Реііѣ. Въ т. II., мы привели результатъ опытовъ ЗІеіап’а и Сіігіз-
Ііапзеп’а относительно потери тепла поверхностью тѣла, покрытаго
сажей и находящагося въ весьма разрѣженномъ воздухѣ. Эти опыты
даютъ числовыя значенія коеффиціентовъ т и о въ формулахъ (31) и (32):
т = 0,8670, б = 7,26 X Ю-11 (см. т. II). Обозначимъ теперь черезъ А?
число малыхъ калорій, теряемыхъ въ 1 минуту кв. сантиметромъ вычер-
ненной поверхности при 7°, когда разность температуръ тѣла и обо-
лочки і = Т—Ѳ= 1°. Вышеприведенныя числа пг и о даютъ для Лр
слѣдующія значенія
т Впіоп^ и Реііі йіеіап
0° Ло = 0,006625 0,005876
30° ^зо — 0,008339 0,008015
100° ^іоо = 0,01427 0,01500
^100 2,1534 2,553.
Опыты Мас Еегіапе’а, произведенные въ неразрѣженномъ воз-
духѣ, даютъ числа приблизительно вдвое большія.
Литература.
287
ЛИТЕРАТУРА.
Подробныя литературныя указанія по вопросу объ охлажденіи можно найти
въ книгѣ:
С. Терешинъ. Къ вопросу о зависимости лучеиспусканія отъ температуры. С. П.
1896 ; Ж, Ф. X. О. 29 р. 169, 22г, 277, 1897; 30 р. 15, 1898.
Менѣе полныя указанія въ сочиненіяхъ:
Реггеі. 8І11. 3. (3) 38 р. 3, 1889; 39 р. 137, 1890.
О. Хвольсонъ. О современномъ состояніи актинометріи. Прилож. къ 69-му тому
Записокъ Импер. Акад. Наукъ. № 4, С. П. 1892.
Къ § 2.
Хеи'іоп. Орпеспіа Маіііешаііса 2 р. 423, Ьаиеапае еі Оепеѵае, 1744.
Къ § 3.
Оиіощг еі Реііі. Апп. сіііт. еі. рііуе. (2) 7 р. 225. 337. 1818; Всіпѵеі^ег’з
Зонгп. 25.
Роиіііеі. С. К. 7 р. 39. 1838; Тауіог’е 8с. Мешоіге 4
/. Хісігоі. Ргос. К. 8ос. ЕЗіпЬ. 1889—70 р. 207.
Реггеі. Виіі. рЫІоеорІі. 8ос. оі АѴазЫп&іоп 5 р. 83, 1883; 8Ш. 4. 38 р. 3, 1889.
Ре Іа Ргоѵо8іауе еі Резаіпз. Апп. сіііт. еі рііуе. (3) 12 р. 129, 1844; 16 р. 337,
1846; 22 р. 358, 1848; С. К. 38 р. 440, 1854; Ро^. Апп. 68 р. 235, 1846; 69 р. 367, 1846.
Норкіп8. РЫ1. Тгапе. 1868 р. 379.
8огеі. АгсЪ. 8с. рііуе. (2) 44 р. 220; 45 р. 222, 1872; 52 р. 89; 55 р. 217, 1876; (3)
1 р. 86. 1879.
ѴТШіеІту. Ро&&. Апп. 84 р. 119, 1851.
Ргарег. 8сіепііі. Метоіге, р. 44.
Мас-Регіапе. Ргос. К. 8ос. 32 р. 465, 1875.
Ргіс8оп' СопігіЬнііоп іо іііе Сепіеппіаі ехЫЬіііоп, 1872 р. 49; Ыаіиге р. 106, 187;
Ьапргіеу. Хаі. АсаЗ. о! Ріііі аЗеІрЫа, Осі. 1876.
Ѵіоііе. С. К. 88 р. 171, 1879; 92 р. 866, 1204, 1881; 96 р. 1033, 883; 105 ро 1632,
1883; 4. Зе рііуе. (3) 1 р. 298, 1893.
Огаеіх. №. А. 11 р. 923, 1880.
Хагг. Ро^х. Апп. 142 р. 123, 1871.
Ьатіп еі РісііапЬ С. К. 75 р. 105, 453, 1872.
Ріѵіёге. С. К. 95 р. 452, 1882.
8іе/ап. №іеп. Вег. 79, II р. 391, 1879.
Сотрап. С. К. 136 р. 813, 1902. 1901 ; 4. Зе рііуе. (4)1 р. 708, 1902; Апп. Зе сіііт.
еі рііув. (7) 26 р. 488, 1902.
Къ § 4.
8іе/ап. №іеп. Вег. 79, II р. 391, 1879; 4. Зе рііуе. 10 р. 317, 1881.
Воіігтапп. №. А. 22 р. 31, 291, 1884.
Голицынъ. №. А. 47 р. 479, 1892; Ріііі. Ма§\ (5) 35, 1893.
Сгаеіх. №. А. 11 р. 913, 1880; 36 р. 857, 1889.
8с1гпееЬеІі. №. А. 22 р. 432, 1884.
8сКІеіегтасИег. №. А. 26 р. 287, 1885; 34 р. 630, 1888; 36 р. 349, 1889.
Воііотіеѵ. Ргос. Е. 8ос. 42 р. 357,1887; Ріііі. Тгапе. 178 р. 429, 1887; 184 р. 591, 1893.
Реггеі. 8І11. 4. (3) 38, 1889; 39 р. 132, 1890. *
Ріѵіёге. С. К. 95 р. 452, 1882; 4. Зе рііуе. (2) 3 р. 473, 1884.
СНгІ8ііап8еп. №. А. 19 р. 267, 1883.
Ьиттег и Ргіпррііеіт. №. А. 63 р. 395, 1897.
Ро8еііі. Аііі 3. Е. Ас. 3. Ьіпсеі (3) 2 р. 64, 174, 1878; Апп. сіііт. еі рііуе. (5)
17 р. 177, 1879.
И. Р. ѴРеЬег. Вегі. Вег. 1888 (2) р. 565. 930.
Есііег. №. А. 40 р. 531, 1890.
288
Теплопроводность.
А. ДО. Нагітапп. РЬув. 2І8СІіг. 5 р. 582, 1904.
С. Терешинъ. 1 с. р. 95; Извѣстія С. П. Технологич. Института 1893 р. 253;
1897 р. 1; Ж. Р. Ф. X. О. 37 р, 15, 1905; Рііуе. Хіескг. 6 р. 217, 1905.
ѴШІгеІту. Ро&§. Апп. 84 р. 119, 1851.
ОЬегЬеск. \Ѵ. А. 7 р. 271 1879.
Ьогепх. \Ѵ. А. 13 р. 422, 582, 1881.
/?. Ѵ&а&гег. ИІ88. ХиегісЬ 1902; ВеіЫ. 27 р. 534, 1903.
Ьеев. РЫ1. Ма#. (5) 7 р. 429, 1889.
Ьогепх. АѴ. А. 13 р. 422, 582, 1881.
ОЬегЬеск. АѴ. А. 7 р. 271, 1879: 56 р. 397, 1895.
Воиввіпевд. С. К. 132 р. 1382, 1901; 133 р. 257, 1901; 138 р. 1134, 1189, 1904;
140 р. 15, 65, 1905; 4. де рііуе. (4) 1 р. 65, 71, 1902.
Огоѵе. Ро^. Апп. 71 р. 194, 1847; 78 р. 366, 1849; 80 р. 366, 1849.
Оаіапйег. 61. к. Ѵеіепек. Ак. Роегѣапді. 8іоск1іо1пі 33 р. 29, 1876.
8ег. Тгаііё дее р1іу8. іпдиеігіеііе I р. 160, 1888.
8іапіоп. Тгапв. К. 8ос. Ьопдоп 190, А р. 67, 1897.
Роговскій. Диссертація, Петерб. 1903; С. К. 136 р. 1391, 1903.
Къ § 5.
Мас Еегіапе. Ргос. К. 8ос. 20 р. 90, 1871 ; Ркіі. Ма§. (4) 43, 1872.
Мскоі. Ргос. К. 8ос. ЕдіпЬ. 1869—70, р. 207.
Воііотіеу. Ркіі. Тгапе. 178 р. 429, 1887.
ГЛАВА СЕДЬМАЯ.
Теплопроводность.
§ 1. Введеніе. Запасъ тепловой энергіи различныхъ соприкасаю-
щихся тѣлъ или различныхъ частей одного и того же тѣла остается безъ
измѣненія, если эти тѣла или эти части одного тѣла находятся при оди-
наковой температурѣ и если никакой затраты этого запаса энергіи на
производство какой бы то ни было работы не происходитъ. Въ даль-
нѣйшемъ мы всегда будемъ предполагать отсутствіе такой посторонней
траты энергіи. Исключеніе представляетъ поверхность тѣла, гдѣ, какъ
мы видѣли (т. II), происходитъ постоянная потеря тепловой энергіи,
переходящей въ энергію лучистую и, въ то же время, поглощеніе лу-
чистой энергіи, испускаемой окружающими тѣлами, и превращеніе ея
въ энергію тепловую. Мы видѣли, что непосредственно наблюдается
только разность между испускаемой и поглощаемой энергіей, и только ее
мы будемъ разсматривать, какъ тепловую энергію, потерянную у поверх-
ности тѣла, если эта разность не равна нулю. Запасъ тепловой энергіи
въ данномъ тѣлѣ или въ данной части тѣла не остается постояннымъ,
когда соприкасающіяся тѣла или когда части одного и того же тѣла обла-
даютъ различною температурою, т.-е. различною среднею живою силою
движенія частицъ. Въ этомъ случаѣ происходитъ передача тепловой
энергіи по направленію отъ мѣста болѣе нагрѣтаго къ мѣсту менѣе на-
грѣтому, устанавливается, выражаясь образно, потокъ тепловой энергіи по
направленію убывающихъ температуръ Такое явленіе передачи или по-
Введеніе.
289
тока теплоты называется внутреннею теплопроводностью или
просто теплопроводностью.
Проведемъ мысленно черезъ тѣло плоскость, и пусть о площадь ма-
лой, ограниченной части этой плоскости. Если малая часть тѣла, непо-
средственно съ одной стороны прилегающая къ о (такъ что о часть ея
поверхности), получаетъ втеченіе нѣкотораго времени т количество д теп-
ловой энергіи отъ сосѣдней съ нею малой части тѣла, прилегающей къ а
съ другой стороны, то мы будемъ это выражать словами: количество д
теплоты протекло черезъ часть б плоскости по направленію, перпенди-
кулярному къ этой плоскости.
Механизмъ внутренней передачи тепловой энергій, т.-е. механизмъ
теплопроводности можно себѣ представить двояко. Передача тепла, т.-е.
энергіи движенія частицъ, можетъ происходить непосредственно, какъ
слѣдствіе непрерывныхъ столкновеній частицъ между собою. Если въ со-
сѣднихъ слояхъ тѣла энергія движенія различная, то непрерывныя столк-
новенія частицъ повлекутъ за собою увеличеніе энергіи въ томъ слоѣ,
гдѣ она меньше, и, наоборотъ, уменьшеніе ея тамъ, гдѣ она больше.
Передача тепла можетъ, однако, происходить и иначе, а именно пу-
темъ междучастичныхъ радіацій. Каждая частица внутри тѣла непре-
рывно передаетъ свою энергію окружающему ее эфиру, заполняющему
междучастичныя пространства, вызывая въ немъ потоки лучистой энергіи;
въ то же время убыль ея энергіи движенія непрерывно пополняется до-
стигающими ее потоками лучистой энергіи, исходящими отъ всѣхъ сосѣд-
нихъ частицъ. Энергія движенія частицы остается безъ измѣненія, когда
средняя энергія всѣхъ окружающихъ частицъ одна и та же, т.-е. когда
частицы обладаютъ одинаковой температурой. При неравномѣрномъ рас-
предѣленіи температуръ происходитъ постепенная передача энергіи. По-
ложимъ, что стержень нагрѣвается съ одного конца, и пусть А и В два
сосѣдніе слоя молекулъ, расположенные въ поперечныхъ сѣченіяхъ
стержня. Если энергія частицъ въ слоѣ А больше, чѣмъ въ слоѣ В, то
на слой В падаетъ со стороны слоя А болѣе интенсивный потокъ лучи-
стой энергіи, чѣмъ потокъ, испускаемый слоемъ В по направленію къ А.
Вслѣдствіе этого должна увеличиться энергія частицъ слоя В, т.-е. пре-
взойти энергію частицъ слѣдующаго, сосѣдняго съ нимъ слоя С. Тогда
между слоями В и С повторится то, что происходило между слоями А и
В, т.-е. произойдетъ увеличеніе энергіи частицъ слоя С и т. д.
Неизвѣстно, которымъ изъ этихъ двухъ способовъ происходитъ ВН> -
тренняя передача тепла; можетъ быть, обоими способами одновременно.
Но, какимъ бы способомъ ни происходила передача энергіи отъ мѣстъ бо-
лѣе энергичнаго движенія къ мѣстамъ движенія менѣе энергичнаго, —
самый фактъ этой передачи, постоянно и вездѣ само
собою происходящей, можетъ быть разсматриваемъ,
какъ простѣйшій примѣръ того стремленія къ равно-
мѣрно безпорядочному распредѣленію движеній ча-
стицъ, о которомъ было сказано на стр. 3.
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. III, изд. 3.
19
290
Теплопроводность.
Быстрота, съ которой теплота внутри тѣлъ передается отъ слоя къ
слою, зависитъ прежде всего отъ вещества, изъ котораго состоитъ тѣло. Раз-
личныя вещества, или, какъ обыкновенно говорятъ, различныя тѣла обла-
даютъ неодинаковою теплопроводностью. Они, какъ извѣстно, раздѣляются
на дурные, посредственные и хорошіе проводники тепла,
между которыми, понятно, рѣзкихъ границъ не существуетъ. Къ хорошимъ
проводникамъ относятся металлы, къ дурнымъ газы, жидкости (кромѣ Н^)
и многія твердыя тѣла, упомянутыя ниже. Теплопроводность зависитъ
отъ состоянія тѣла и мѣняется, напримѣръ, вмѣстѣ съ его температу-
рою ; будучи измѣряема нѣкоторою опредѣленною величиною, она оказы-
вается функціею состоянія тѣла.
§ 2. Понятіе о математической теоріи теплопроводности. При не-
равномѣрномъ распредѣленіи температуры і внутри тѣла, величина і пред-
ставляется функціей координатъ х, у, г точекъ этого тѣла, т.-е. функціей
точки (т. I). Пусть
і = / (х, у, г)............ Н)
Поверхности одинаковой температуры, уравненіе которыхъ
/(х,у, г) = Сопьі....................(2)
называются изотермическими поверхностями. Двѣ такія по-
верхности не могутъ пересѣкаться, такъ какъ температура, по физиче-
скому своему значенію, есть функція однозначная; кромѣ того она есть
функція вездѣ конечная и внутри тѣлъ твердыхъ, каковыя мы только и раз-
сматриваемъ, непрерывная. У поверхности тѣлъ мы допускаемъ разрывъ
этой функціи, внезапный ея переходъ въ величину, которую мы назовемъ
тепы ера ту рой $ окружающаго пространства. Для простоты
мы послѣднюю обыкновенно будемъ считать равною нулю, т.-е. отъ нея
будемъ вести счетъ температуръ. Температурное состояніе тѣла можетъ
быть двоякое: перемѣнное и стаціонарное. Перемѣннымъ называется
такое состояніе, при которомъ распредѣленіе температуръ мѣняется съ
теченіемъ времени г; въ этомъ случаѣ і есть функція трехъ координатъ
ивремени: і = Р(х,у,г, г).....................(3)
Стаціонарнымъ называется температурное распредѣленіе, не мѣ-
няющееся со временемъ, такъ что і является въ общемъ случаѣ функціею
только трехъ перемѣнныхъ. Стаціонарное состояніе характеризуется не-
прерывнымъ теченіемъ теплоты, причемъ всякій элементъ тѣла въ данное
время столько же получаетъ теплоты черезъ одну часть всей поверхности,
сколько онъ черезъ другую часть теряетъ. Если тѣло изолировано, т.-е.
вся его поверхность окружена пространствомъ съ вездѣ одинаковою темпе-
ратурою $, то единственное возможное стаціонарное состояніе есть то,
при которомъ і = т.-е. всѣ точки имѣютъ одинаковую температуру,
равную температурѣ окружающаго пространства. Стаціонарное не-
равномѣрное состояніе возможно только въ случаѣ, когда тѣло
находится въ соприкосновеніи съ такъ называемыми источниками тепла.
Теорія.
291
поддерживающими или всю поверхность тѣла при опредѣленныхъ и при-
томъ не вездѣ одинаковыхъ температурахъ, или только нѣкоторыя части
поверхности при вездѣ одинаковыхъ или неодинаковыхъ температурахъ,
причемъ остальныя части поверхности теряютъ теплоту въ окружающее
пространство вслѣдствіе ея перехода въ лучистую энергію.
Основанія математической теоріи теплопроводности были положены
Роигіег и Роівзоп’омъ. Задача этой теоріи въ самомъ общемъ слу-
чаѣ, заключается въ опредѣленіи вида функціи (3), или, въ частномъ
случаѣ, когда ищется стаціонарное тепловое состояніе, вида функціи (1)
при заданныхъ условіяхъ. Эти условія могутъ быть весьма
различны; во всякомъ случаѣ должны быть даны форма тѣла и его
физическія свойства, играющія роль въ явленіяхъ теплопроводности, т.-е.
величины к и /г, о которыхъ будетъ сказано ниже, а также, въ случаяхъ
перемѣннаго температурнаго состоянія, плотность й и теплоемкость с.
Когда требуется найти стаціонарное состояніе, то добавочныя усло-
вія относятся къ опредѣленнымъ мѣстамъ поверхности тѣла, темпе-
ратура которыхъ, искусственно поддерживаемая, какъ было сказано выше,
должна быть дана.
Въ задачахъ на перемѣнное температурное распредѣленіе должны
быть еще извѣстны начальныя условія, т.-е. должно быть дано
распредѣленіе температуръ въ какой нибудь моментъ времени, начиная
отъ котораго и требуется изслѣдовать ходъ измѣненія температуры то-
чекъ тѣла. Въ частныхъ случаяхъ начальныя условія пли условія у по-
верхности могутъ быть весьма простыя. Начальное условіе можетъ быть
напримѣръ і = Соп§1. ; тогда на поверхность тѣла, всѣ точки котораго
находятся при одинаковой температурѣ, начинаютъ дѣйствовать источники
тепла. Замѣтимъ, что эти источники сами могутъ быть перемѣнными, т.-е.
температуры, которыя они поддерживаютъ въ заданныхъ мѣстахъ поверх-
ности тѣла, могутъ быть функціями времени. Особый интересъ пред-
ставляютъ случаи, когда эти температуры суть періодическія
функціи времени.
Мы имѣемъ простыя условія, при полномъ отсутствіи источниковъ
тепла у поверхности тѣла, въ задачѣ объ охлажденіи тѣла, первоначальное
температурное распредѣленіе котораго дано. Здѣсь идетъ рѣчь о полномъ
рѣшеніи задачи, которая на стр. 277 была рѣшена для маленькаго тѣла,
температура котораго принималась равною температурѣ его поверхности.
Разнаго рода задачи, относящіяся къ теплопроводности, представляютъ
весьма большія трудности, и рѣшеніе ихъ относится скорѣе къ курсу ма-
тематики, чѣмъ къ курсу физики. Основанія, на которыхъ построено
рѣшеніе этихъ задачъ, сравнительно весьма просты и не зависятъ
отъ нашихъ взглядовъ на сущность тепловыхъ явле-
н і й. Въ этомъ заключается тотъ признакъ, который заставляетъ насъ
относить теорію теплопроводности, созданную Г о и г і е г, къ отдѣламъ
математической физики, о характерѣ которыхъ было сказано въ т. I.
Чтобы объяснить простое основаніе теоріи Роигіег, введем ь
19*
292
Теплопрововодность.
сперва понятіе опаденіи температуры. Проведемъ внутри тѣла
прямую Ох (рис. 88) и пусть х разстояніе любой точки на этой прямой
отъ избраннаго начала О. Температура і точекъ прямой Ох можетъ
быть разматриваема, какъ функція отъ х, т.-е. для этихъ точекъ
можно положить і = /(х). Возьмемъ простѣйшій случай равномѣрнаго
измѣненія температуръ вдоль Ох. а именно уменьшенія ихъ по напра-
вленію Ох. Въ этомъ случаѣ і есть линейная функція отъ х и можетъ
быть написана въ видѣ і = а Ц- Ьх. гдѣ а температура точки О и Ь ве-
разстояніе которыхъ отъ О равно х± и х2.
личина отрицательная, равная
уменьшенію температуры на еди-
ницу длины прямой Ох. Поло-
жительная величина = — Ь.
т.-е. положительная разность
температуръ двухъ точекъ пря-
мой Ох. отстоящихъ другъ отъ
друга на единицу длины, назы-
вается паденіемъ темпера-
туры вдоль прямой Ох. Оно
является мѣрою быстроты, съ
которой температура мѣняется
вдоль прямой Ох. Пусть и
4 температуры точекъ А и В.
Въ этомъ случаѣ паденіе @ равно
Р=-і>=
— хг х2 - хг
Мы полагали, что 4» слѣд. @ величина положительная.
Положимъ теперь, что вдоль Ох температура I есть какая нибудь
функція отъ х. т.-е. что і—^х~). Если точки А и В опять обладаютъ
температурами и /2, то величина
/? = -
х2 --хг
О)
представляетъ среднее паденіе температуры между А и В
по направленію Ох. Положимъ далѣе, что точки А и В близки другъ
къ другу, что О А =х, ОВ = х-\- Дх, и что температуры точекъ Аи В суть
і и Въ такомъ случаѣ среднее паденіе температуры между А и
5РавН0 = _Ді
? (х-\-Дх)— х Дх
(’танемъ безконечно уменьшать разстояніе АВ = Дх; предѣлъ, къ
которомл стремится /9, т.-е. величина
(ІХ
(5)
Теорія.
293
называется паденіемъ температуры въ т о ч кѣ А по направ-
ленію Ох.
Проведемъ черезъ А и В плоскости перпендикулярно къ Ох и вы-
дѣлимъ изъ нихъ около А и В столь малыя равныя части сд и чт0
температуру можно считать одинаковой во всѣхъ точкахъ каждой изъ
плоскостей сл и о2. Допустимъ сперва, что паденіе Д имѣетъ одно и то
же значеніе во всѣхъ точкахъ между А и В, т.-е. что і линейная функ-
ція отъ х, и слѣд. /? выражается формулою (4). Количество теплоты 7,
которое во время т протекаетъ черезъ къ б2, пропорціонально площади а
этихъ малыхъ плоскостей и пропорціонально г, если допустить, что тем-
пературы и і2 не измѣнились втеченіе времени Далѣе д должно зависѣть
отъ вещества, изъ котораго состоитъ тѣло. Мы знаемъ, что д = 0, если
/? = 0, и что д тѣмъ больше, чѣмъ быстрѣе температура уменьшается по
направленію Ох. Отсюда ясно, что д есть функція паденія /3 между
А и В. Допустимъ, что д пропорціонально паденію $
температуры. На этомъ допущеніи, а ргіогі впрочемъ весьма вѣро-
ятномъ, и основана прежде всего математическая теорія теплопроводности ;
опыты подтвердили результаты этой теоріи и тѣмъ самымъ доказали и
правильность этого допущенія. Все сказанное выражается формулою
д = 1гот^=—кот ---------................(6)
•^2 ~ ' X}
гдѣ к множитель пропорціональности, зависящій отъ вещества тѣла. Этотъ
множитель к называется коеффиціентомъ внутренней тепло-
проводности даннаго вещества. Физическое значеніе этого коеффи-
ціента получается слѣдующимъ образомъ. Положимъ, что въ частномъ
случаѣ х2— х1 — 1. б=1. т=1, — ^2 = 1°: въ такомъ случаѣ имѣемъ
численное равенство д = к. Отсюда вытекаетъ такое опредѣленіе: коеф-
фиціентъ внутренней теплопроводности измѣряется тѣмъ количествомъ те-
плоты, которое протекаетъ въ единицу времени черезъ единицу поверх-
ности по направленію, къ ней перпендикулярному, когда температура по
этому направленію равномѣрно уменьшается на 10 при переходѣ отъ одной
точки къ другой, отстоящей отъ нея на единицу длины, или, проще, когда
паденіе температуры по этому направленію равно единицѣ.
Изъ этого опредѣленія ясно, что численное значеніе коеффиціента к
должно зависѣть отъ выбранныхъ нами основныхъ единицъ длины
массыМи времени Г,т.-е. кдолжно обладать опредѣленнымъ размѣромъ.
Въ т. I мы подробно познакомились съ ученіемъ о размѣрѣ физиче-
скихъ величинъ. Въ ученіи о теплотѣ мы впервые встрѣчаемся съ вели-
чиною, которая различными наблюдателями и составителями таблицъ вы-
ражается въ различныхъ единицахъ, однако опредѣленнымъ образомъ ос-
нованныхъ на единицахъ А, /14 и Т. Поэтому намъ необходимо опредѣ-
лить размѣръ величины к. За единицу количества тепла мы приняли то
количество, которое нагрѣваетъ единицу массы воды, находящейся въ
опредѣленномъ физическомъ состояніи, на 1°. Чтобы нагрѣть массу пь
294
Теплопроводность.
воды на /° требуется количество тепла д = ті. Отсюда слѣдуетъ, что
Ф = Л4.............................(7)
Для другого вещества имѣемъ д — стіу гдѣ с теплоемкость этого ве-
щества. При нашемъ выборѣ единицы тепла, когда для воды с — 1, не-
зависимо отъ единицъ Л, Ж и Г, величина с есть простое число, т.-е.
теплоемкость — нулевого размѣра. Полагая х2 — х3 = х, —
4-4- у. І і Ц X та
— г2 = г, мы можемъ написать ц = кот , откуда к — 1 . Величи-
х т ат
на х размѣра а размѣра А2, наконецъ т размѣра Т: такимъ образомъ
получимъ размѣръ коеффиціента к внутренней теплопроводности:
[к\ = м. ,
т -е
[*І= ........................(8)
Величину к выражаютъ иногда въ С. О. 5. единицахъ, а иногда въ
единицахъ (мм., мгр., сек.); въ таблицахъ ВапсІоІѴа и В о е г п 81 е і п’а,
къ сожалѣнію, приведены величины к, выраженныя въ послѣднихъ еди-
ницахъ, т.-е. к измѣрено числомъ единицъ тепла, равныхъ 0,001 мал. ка-
лоріи (1 мгр. воды на 1°), протекающихъ въ 1 сек. черезъ 1 кв. мм. по-
верхности, когда паденіе температуръ по направленію, перпендикулярному
къ этой поверхности, составляетъ 1° на протяженіи 1 мм. По правилу,
изложенному въ т. [, мы находимъ
к—= * і°00”Т- =ы„к "ь
10 мм. сек. мм. сек.
см. сек.
Численное значеніе к въ системѣ (мм., мгр., сек.) въ
100 разъ больше, чѣмъ въ С. О. 5. системѣ. Мы встрѣтимся
ниже съ величиной ѣ
гдѣ о плотность, с теплоемкость вещества. Послѣдняя величина нулевого
размѣра, размѣръ плотности М : А3 (т. I); принимая еще во вниманіе
(8), мы находимъ размѣръ величины а2\
/ 2
[«2]= т..........................(9,«)
Отсюда ясно, что численное значеніе я2въ системѣ (мм.,
м гр., с е к.) т а к ж о въ 100 разъ больше, чѣмъ въ С. О. 5. с и -
стемѣ. Величины к и а2 суть функціи состоянія тѣла, т.-е. зависятъ
напр. отъ температуры тѣла и отъ давленія, подъ которымъ оно нахо-
дится ; лишь въ первомъ приближеніи можно эти величины считать по-
Теорія.
295
стоянными для даннаго вещества. Вставляя въ формулу (6) для паденія
температуръ точное выраженіе (5), мы находимъ:
д =— кбг .............................V10)
сіх
Направленіе х можетъ быть выбрано вполнѣ произвольно, а потому
ясно, что послѣдняя формула опредѣляетъ количество тепла, протека-
ющаго во время г черезъ произвольный элементъ поверхности о (распо-
ложенный гдѣ и какъ угодно внутри тѣла) по направленію, пер-
пендикулярному къ а.
У поверхности тѣла происходитъ потеря тепла вслѣдствіе перехода
теплоты въ лучистую энергію, вслѣдствіе конвекціи (стр. 274) и вслѣд-
ствіе теплопроводности окружающаго газа. Теорія теплопроводности ис-
ходитъ изъ закона ЫеАѴІоп’а, т.-е. допускаетъ, что количество# тепла,
теряемаго во время т элементомъ о поверхности тѣла, пропорціонально
избытку температуры і элемента а надъ температурою в окружающей
среды; кромѣ того можно положить # пропорціональнымъ о и г, если эти
двѣ величины весьма малы. Мы имѣемъ д = Нбтл(і -У), гдѣ Умножитель
пропорціональности, называемый внѣшнею теплопроводностью;
онъ очевидно измѣряется тѣмъ количествомъ тепла, которое теряется еди-
ницей поверхности въ единицу времени, когда избытокъ і—0=1°. Въ
дальнѣйшемъ мы будемъ вести счетъ температуръ отъ температуры окру-
жающей среды, т.-е. мы положимъ 0. Тогда получается
д = коті.................. . (11)
Слѣдуетъ помнить, что эта формула перестаетъ быть примѣнимой
при />5°, если И принимать за величину, не зависящую отъ і. Прини-
мая во вниманіе формулу (7), и то, что размѣръ о равенъ У2, мы находимъ
Формулы (8) и (12) даютъ размѣръ отношенія У : к
Р1= 1 1..................(13)
I к ] Ь
При стаціонарномъ состояніи величина #, опредѣляемая фор-
мулами (Ю) и (11), не зависитъ отъ времени г. Количество теплоты С,
протекающее черезъ единицу поверхности въ единицу вре-
мени, назовемъ тепловымъ потокомъ: мы имѣемъ:
внутри тѣла Г)__ Я __ у .
аг (іх'
у поверхности
-- кі.
296
Теплопроводность.
При перемѣнномъ тепловомъ состояніи д есть функція времени т.
Въ весьма малое время Ат протекаютъ внутри тѣла и черезъ его поверх-
ность количества тепла :
Ад ~ — кб М Ат7 Ад — НбіАт.
сіх
Средній тепловой потокъ во время Ат равенъ (2=1 . Предѣлъ
этой величины при безконечно маломъ Ат называется тепловымъ по-
токомъ въ моментъ времени т; онъ равенъ
Внутри тѣла имѣемъ опять
а
Ъ поверхности:
а
сід____ & сіі
СІТ СІХ
(15)
ат
(16)
1
б
1
б
Тепловой потокъ внутри тѣла пропорціоналенъ паденію темпера-
туры, у поверхности - температурѣ, которая въ окружающей средѣ равна
нулю. Для сід имѣемъ :
(ІІ
внутри тѣла сід = Обсіт — кб — .................
у поверхности сід = Обсіт —кбісіт .... (18)
На поверхности б соприкосновенія двухъ тѣлъ, теплопроводности ко-
торыхъ кг и &2, а температуры и мы должны имѣть
1 СІІ] *. (ІІсу
кг , 1 =к?
1 сіх сіх
(18л)
если х направленіе нормали къ о; это выражаетъ, что на поверхности б
не происходитъ ни накопленія, ни убыли теплоты.
Тепловой потокъ имѣетъ въ изотропномъ тѣлѣ на-
правленіе нормали п къ изотермической поверхности
/ = Соп8І. Дѣйствительно, пусть дхі ду и дг отнесенныя къ единицѣ вре-
мени слагаемыя теплового потока; въ такомъ случаѣ тепловой потокъ д
по величинѣ равенъ
+ • (18-0
Формула (17) даетъ
д= кб\ — + .г -Н т — — ... (18.Г)
7 ' \(ІХ ] 1 \ сіу у 1 \ сіг сіп
Векторъ . какъ извѣстно, нормаленъ къ поверхности
какъ слагаемыя д.\, ду. д2 пропорціональны величинамъ
і — Сопя!: а такъ
сіі сіі сіі
сіх ’ сіу йг
то понятно, что и векторъ д нормаленъ къ той же поверхности.
Теорія.
297
Если тѣло имѣетъ форму тонкой плоской пластинки, то
возможенъ случай, когда теплота распространяется только въ двухъ из-
мѣреніяхъ, параллельныхъ поверхностямъ пластинки. Въ этомъ случаѣ
можно положить і == /(х, у); вмѣсто изотермическихъ поверхностей, имѣ-
Рис. 89.
емъ линіи і — СопбЬ., которыя назовемъ изотермами. Въ изотроп-
ной пластинкѣ тепловой потокъ вездѣ перпендикуляренъ къ изотермамъ.
Большой интересъ представляетъ случай, когда пластинки со-
стоятъ изъ разнородныхъ частей. Въ этомъ случаѣ происхо-
дитъ преломленіе изотермъ на границѣ этихъ разнородныхъ ча-
стей. Пусть МЫ (рис. 89) граница частей Рг и пластинки, теплопро-
водности которыхъ кА и к2 5 изотерма і = Сопзі. Проведемъ ось х по
направленію АЫ- ось у нормальна къ МЫ\ (р± и <р2 углы между нор-
малью и изотермою АВ и АС. Тепловые потоки въ и Р2 около точки А
обозначаемъ черезъ ^/и формула (18,//) даетъ
Г18.^)
Числа около скобокъ указываютъ, къ какой части пластинки при-
надлежитъ точка, лежащая около А. Такъ какъ температуры съ обѣихъ
сторонъ отъ МЫ одинаковы, то мы должны имѣть
(18,г)
29«
Теплопроводность.
(18,я) даетъ
(18/)
Такъ какъ д1±_АВ, то мы имѣемъ, см. (18,г/),
(СІІ \ / (11 \
), : Щ
= СОП8І. .
(18*0
1^2 = Яі,у : 72,X = (
(іа,Ь) и (18,Л даютъ теперь
І87_і _
к-
Этою формулою опредѣляется законъ п р е л о м л е н і я изотермъ.
Выведемъ то общее условіе, которому должна въ перемѣнномъ те-
пловомъ состояніи удовлетворять температура і, какъ функція четырехъ
величинъ х, у, г и г, см. (3) стр. 290. -Пусть точка А (рис. 90) имѣетъ
координаты х, у, г и температуру I; проведемъ параллельно координат-
нымъ осямъ безконечно малые отрѣзки прямыхъ АН = Дх, АО = Ду,
АВ = А%, и построимъ на нихъ параллелепипедъ АВСОРЕСН. Опредѣ-
лимъ избытокъ чз) теплоты, втекающей въ него во время 4г, надъ тепло-
той, вытекающей изъ него въ то же время. Черезъ АВСО втекаетъ ко-
личество тепла , .
= — ІіАг
ух о (И
Значекъ х, поставленный снизу, указываетъ, что а и , относятся
къ элементу поверхности, координата х котораго равна координатѣ х
точки А : вмѣсто о мы написали АВСО = Ду Дг. Черезъ противополож-
ную сторону ЕРСН вытекаетъ количество тепла
сіі \
/х н- \х
о ѵ (іі ѵ
Здѣсь уже другое; оно получается изъ предыдущаго замѣною х на
гѵ-|-_1х. По теоремѣ Тайлора имѣемъ, если отбросить безконечно ма-
лыя величины высшихъ порядковъ,
ДуДг.
Ях + Ах — &Ат
Такимъ образомъ
хД-Дх
б/2/ л
сіх* Лх-
Ях + ІХ -
Дх\ ДуДг.
Вычитая отсюда дх, получаемъ часть искомаго количества теплоты
остающагося въ параллелепипедѣ,
Ях — Ях -_1х = /г/%2
Теорія.
299
Аналогично опредѣлимъ еще двѣ части того же искомаго количес тва
тепла іе/, разсматривая количества ду и д2 тепла, втекающія черезъ АВЕН
и АНОО, и количества ду + ду и дг-\-Дх вытекающія черезъ СЕОО и
СЕЕО. Получаемъ:
сРі (Ш
ду — ду^\у — к ДхДуАхАт, ц. дг + Лг=к Ах Ду Дх Дт.
Для іѵ находимъ, сложивъ эти три величины,
, / лч . ач , ач\ . . . .
Масса /и параллелепипеда равна /г = дАх Ау Аг: оставшееся въ немъ
количество тепла вызываетъ повышеніе температуры Аі, причемъ =
Рис. оо.
= с/г Аі, гдѣ с теплоемкость вещества. Вставивъ /г и сравнивъ это
выраженіе те/ съ предыдущимъ, получаемъ:
/ срі ач
( йх2 + йу2 ’
сіг2 I
Ах Ау Аг Ат = с$Ах Ау Аг Аі.
Раздѣляя на с$Ах Ау Аг Аг. и переходя къ предѣлу, считая Ат безко-
нечно малымъ (пропорціональность Ад времени Ат тѣмъ точнѣе, чѣмъ
меньше Ат), находимъ:
/ сРі (Еі . йЧ \ (Іі
* сіх2 ’ сіу2 ’ Ля21 (1г
к
а1 =
(19)
300
Теплопроводность.
Для сличая стаціонарнаго теплового состоянія, когда і отъ г
не зависитъ, имѣемъ знаменитое уравненіе
(12і і_ _1_ 614
СІХ2 ' б/у2 ’ сі?2
(20)
§ 3. Рѣшеніе нѣкоторыхъ простыхъ задачъ, относящихся къ те-
плопроводности. Роигіег и РоІ88оп указали пути рѣшенія задачъ
на перемѣнное или стаціонарное тепловое
состояніе тѣлъ. Мы можемъ здѣсь за-
няться рѣшеніемъ лишь немногихъ про-
стѣйшихъ задачъ.
I. Задача о стаціонарномь
т е п л о в о м ъ с о с т о я н і и стѣны. Дана
стѣна или пластинка, ограниченная двумя
параллельными плоскостями АВ и СО
(рис. 91), края которыхъ находятся столь
далеко отъ разсматриваемаго мѣста, что
плоскости можно принять безконечно боль-
шими ; толщина стѣны сі. Стороны АВ
и СО удерживаются впродолженіе долгаго
времени при температурахъ и /2, при-
чемъ пусть Требуется опредѣлить
стаціонарное тепловое состояніе стѣны,
т.-е. температуру і, какъ функцію коорди-
натъ точекъ стѣны.
Примемъ начало О координатъ въ плоскости АВ и проведемъ ось х
перпендикулярно къ плоскостямъ АВ и СО. Такъ какъ всѣ части стѣны
ничѣмъ другъ отъ друга не отличаются, то ясно, что точки, лежащія на
плоскости, параллельной АВ, напр. на СИ, имѣютъ одинаковую темпера-
туру, или что изотермическія поверхности (стр. 290") суть плоскости, па-
раллельныя сторонамъ стѣнки. Отсюда слѣдуетъ, что і отъ у и г не за-
виситъ, т.-е. что
сіі
сіх
= В. т.-е.
У равненіе (20) даетъ въ этомъ случаѣ
і — АА~Вх
(Рі
СІХ2~
(21)
гдѣ А и В двѣ постоянныя величины, которыя можно найти на основаніи
условій, что і = А при х = 0 и I — яри х = (1. Итакъ = А, і2 =
= А -|- Всі = ^ + ЕМ- Отсюда А = и В= ^2 - Оконча-
тельно имѣемъ . ,
1 = іг— 1 2 х .... (22)
Для паденія температуры по направленію х находимъ
сіі ___ „______-12
сіх ~~ сі
(22,а)
Задачи.
301
Температура есть линейная функція отъ х. паденіе вездѣ одинако-
вое. Замѣтимъ, что полученное нами рѣшеніе, строго говоря, является
лишь перефразировкой основного нашего допущенія о пропорціональности
между количествомъ д протекающаго тепла и паденіемъ температуры.
Іакъ какъ теплота вездѣ течетъ отъ АВ къ СО по направленію Ох, не
мѣняясь количественно, то ясно, что мы получаемъ одно и то же д, гдѣ
бы мы ни помѣстили элементъ о плоскости, перпендикулярной къ Ох.
Но если д = Сопзі., то и паденіе должно быть ш стоянно, т.-е. мы мо-
жемъ прямо написать — В. Если отложить ОЕ = и ЬЕ = то
прямая ЕЕ изобразитъ законъ измѣненія температуры въ стѣнѣ: темпе-
ратура точекъ плоскости ОН равна і = АѴ. Формула (21) относится къ
случаю, когда к отъ і не зависитъ. Для случая стѣны легко разобрать
и случай, когда к = <р(Е). Мы должны во всякомъ случаѣ имѣть д =
— Гоп8І., т.-е. что д не зависитъ отъ х.
Но тогда (10) даетъ к
/А М
или ах
аі
СІХ
— В.
- В, гдѣ В постоянное число.
Положимъ напр.
к = к0 (1 + аі)
(23)
гдѣ /г0 значеніе величины к при і = О. Тогда мы имѣемъ к0(1-]-аі) =
= в, к0 (і + аі) аі = вах, ах
к0 I (1 —1~ аі) аі — В I сіх —1~ А.
гдѣ А постоянное число. Наконецъ имѣемъ отсюда
к^і + * = Л + Вх.....................(24)
Величины А и В опредѣлятся, какъ прежде. Полученная формула
показываетъ, что для случая, когда имѣетъ мѣсто (23), прямая ЕЕ (рис. 91)
замѣняется дугою параболы, проходящей черезъ точки Е и Е.
II. Задача о стаціонарномъ тепловомъ состояніи
стержня. Однородный стержень АВ (рис. 92) имѣетъ площадь попе-
речнаго сѣченія 5, периметръ поперечнаго сѣченія р, длину /, коеффиці-
енты внутренней и внѣшней теплопроводности к и к. Концы А и В
удерживаются при температурахъ и 4, считаемыхъ отъ температуры
окружающей среды. Требуется найти стаціонарное распредѣленіе тем-
302
Теплопроводность.
пературъ въ стержнѣ, полагая сѣченіе 5 столь малымъ, что для всѣхъ
его точекъ можно принять одну и ту же температуру і, т.-е. допуская,
что і = Р(х), гдѣ х разстояніе сѣченія 5 отъ начала А.
Проведемъ безконечно близкія сѣченія СР и ОО. и напишемъ, что
количество тепла дъ входящее въ отрѣзокъ СРРО стержня черезъ СР,
равно количеству д%, выходящему изъ него черезъ ОС, сложенному съ
б/Г
кх
количествомъ #3, которое теряется черезъ боковую поверхность о того
же отрѣзка. Итакъ мы имѣемъ дг — д2 #3. Черезъ СР втекаетъ ко-
личество тепла = — к8Т
аі
что паденіе —
; значекъ х внизу обозначаетъ опять,
взято для сѣченія, разстояніе котораго отъ А равно х.
Черезъ сѣченіе РО вытекаетъ
д2 = — кзт
= - к8т
ах]х-\-Лх
б/х2
Лх\
членами высшихъ порядковъ мы пренебрегаемъ. Черезъ боковую поверх-
ность уходить количество тепла ^3 = Ао/г: но о=рДх. слѣд. #3 -^крітАх.
Вставляя найденныя дъ д2 и д3 въ равенство дѵ — д2 + получаемъ,
послѣ сокращенія одинаковыхъ членовъ и раздѣленія на к8тЛх,
(Рі кр
(іх2 к$
(25)
Этому уравненію должна удовлетворять искомая температура і, какъ
функція отъ х. Введемъ обозначеніе
а2=К.Р . . . ..........(26)
кз
Для круглаго стержня, радіусъ сѣченія котораго /?, имѣемъ
5 = л/?2, р — 2л/?, и слѣд.
“2=^...........................<27»
* А
Размѣръ величины ѣ равенъ А \ периметръ р размѣра А, площадью
/ѵ
размѣра А2 слѣд. размѣръ величины а2
М = ...........................(28)
5 равненіе (25) напишемъ въ видѣ
(І2І
“ 9 = (Рі . . . . (29)
йх2
Такому линейному уравненію съ постоянными коеффиціентами и
безъ послѣдняго члена, т.-е. безъ члена, содержащаго только х, удовле-
творяетъ функція вида і — еах. Вставляя ее въ (29) и сокращая на еах.
получаемъ а2 = а2. Отсюда два значенія для а:
Задачи.
303
/ Ігр
^ = -о = -|/ «.,=
Полное рѣшеніе уравненія (29) будетъ
і — Ае' ах + Ве ах
Іір
(30)
или
—1 НР
і = Ае '
1 кр
* к8
(31)
гдѣ А и В постоянныя, значеніе которыхъ опредѣляется изъ условія, что
і = 4 при х = о, и і = при х — I. Эти условія суть
іг = А + В
/2 = Ае~~а1 -|- Веа1
(31, а)
Опредѣливъ отсюда Л и В и вставивъ ихъ въ (30), получаемъ пол-
ное рѣшеніе нашей задачи. Формула (28) показываетъ, что величина ах
нулевого размѣра, какъ и слѣдуетъ, ибо эта величина является показа-
телемъ -степени, т.-е. отвлеченнымъ числомъ.
Для весьма длиннаго стержня, одинъ конецъ котораго нахо-
дится при температурѣ а другой столь удаленъ, что его температура
остается равною температурѣ нуль окружающей среды, формула упро-
щается. Теоретически мы должны положить, что і = 0 при х = оо.
Но еах безпредѣльно возрастаетъ, когда х растетъ, а потому послѣднее
условіе даетъ В = 0. Далѣе і = при х — 0 ; это даетъ А = такъ
что окончательно
1 = іое~ к8Х ......... (32)
Покажемъ, какъ опредѣлить А и В въ (30), когда конецъ х = О
удерживается при температурѣ і0, а конецъ х = 1 остается сво-
боднымъ въ окружающей средѣ, принимая самъ собою нѣкото-
рую неизвѣстную температуру ір Первое условіе даетъ
А —В = .............(33)
Количество д тепла, притекающаго къ тому основанію стержня, для
котораго х = /, равно
г; оно должно равняться тому количе-
7
ству, которое теряется основаніемъ 5; отсюда
। г = кзхір или
I
\=МІ9 .
I
• • (34)
Формула (30) даетъ
, | — аАе а1 аВеа1.
304
Теплопроводность.
Вставляя эти два выраженія въ (34), находимъ
А(ак — Н)ё~а1 - В(ак-\~К) еа1 — Ъ . . . (35)
(33) и (35) опредѣляютъ искомыя А и В.
Докажемъ важную теорему о температурахъ трехъ
равностоящихъ другъ отъ друга сѣченій. Пусть 0.,
и температуры трехъ сѣченій Р, <2 и Р (рис. 92), разстоянія кото-
рыхъ отъ конца А равны г, г -|- (і и г + 2(1. По формулѣ (30) имѣемъ
= Ае~аг + Веаг, Ѳ2 = Ае а(г+а) Веа(-2+а>,
03 = Де—а^+2а) Веа(г+2а)
Отсюда
уі -Нз _ ^е-аг^_^е~2аау^_Веаг ц _
— Ае~а(г+а) _|_ ^о(г+ф
_ Ае-^+Ѵ (еаа 4- е~аа) + Ве^+Ф (е~аіі + еаа) _ аа _аа
Ае~а(2+гі>_|_ Веа(г+а) ~ 6 г е
Величина г сократилась, равно какъ коеффиціенты А и В.
Отсюда слѣдуетъ, что дробь (^ -(- : &2 щя даннаго стержня за-
виситъ только отъ его физическихъ свойствъ (к и /г). отъ геометриче-
скихъ свойствъ его сѣченія (5 и р) и отъ разстоянія (1, на которомъ на-
ходятся другъ отъ друга три сѣченія; эта дробь не зависитъ
ни отъ длины / стержня, ни оть температуръ и і2
его концовъ, ни отъ того мѣста на стержнѣ, гдѣ вы-
браны три сѣченія. Если слѣд. взять другія три сѣченія на тѣхъ
же другъ отъ друга разстояніяхъ, и если ихъ температуры #4, или
#8, и т. д., то
4' А 4— А А 4~ А п (1 лг!
1 У 3 = - ЦТ - = - 7 „ ~ — . . = еа(і + е аа = 2п . . . (36)
А А А
гдѣ п постоянное число. Равенство
2п = еа(і 4- е~а(і .... . . . (37)
даетъ е2аа - - 2пеа(і 4~ 1 = о, еа(і = п + V гі? 1.
Оба корня суть величины другъ другу обратныя, ибо (п— V /г2—1) 1 =
— п V п2 — 1; отсюда слѣдуетъ, что одинъ корень равенъ еаа , дру-
гой равенъ е~аа, и дѣйствительно равенство (37) показываетъ, что еаа
и е а(і удовлетворяютъ одному и тому же уравненію. Величина еа(1 > 1:
отсюда ясно, что
еа(і — п-\- Vп2 — 1...................(38)
Кривая, выражающая зависимость і = /(х), выпукла къ оси х-овъ,
отсюда слѣдуетъ, что < I (А + А) или, что 4- А»): А больше 2.
Поэтому п > 1 и корень мнимымъ быть не можетъ.
Задачи.
305
Ш. Задача о стаціонарномъ тепловомъ состояніи
шарового слоя. Шаровой слой, ограниченный поверхностями Зіи52
(рис. 93), радіусы которыхъ гх и г2, обладаетъ коеффиціентомъ теплопро-
водности к. Поверхности и 52 удерживаются при постоянныхъ тем-
пературахъ и /2; требуется найти стаціонарное состояніе шарового
слоя, т.-е. температуру і въ любой
его точкѣ. Введемъ полярныя ко-
ординаты г, у, ір съ началомъ въ
центрѣ. По причинѣ симметріи,
ясно, что і есть функція одного г,
т.-е. что изотермическія поверхности
суть концентрическія шаровыя по-
верхности съ общимъ центромъ
въ С. Итакъ мы имѣемъ і = /(г);
найдемъ условіе, которому должна
удовлетворять эта функція. Про-
ведемъ двѣ безконечно близкія ша-
ровыя поверхности 5 и У и пусть 5
имѣетъ радіусъ г и температуру і.
На поверхности 5 возьмемъ эле-
ментъ о, который въ полярныхъ
координатахъ равенъ б = г2ътд)Лд)Лу, и пусть о' элементъ поверхности У,
вырѣзанный изъ нея тѣмъ же тѣлеснымъ угломъ а при С, какъ и б ; ясно,
что б' = (г + ^)28ІПфб/д?бйр = (г2 -|- 2гДг)$т(рЛфЛ'ір, если пренебречь ква-
дратомъ величины /1г. Тѣлесный уголъ а вырѣзаетъ изъ шарового слоя, ле-
жащаго между 5 и 5', элементъ объема, черезъ боковую поверхность котораго
теплота вовсе не протекаетъ, ибо паденіе температуры по направленіямъ,
перпендикулярнымъ къ радіусамъ г, равно нулю; теплота течетъ только
по направленіямъ радіусовъ. Отсюда ясно, что количество дг теплоты,
протекающей черезъ о, равно количеству дг . протекающему черезъ о'.
Мы имѣемъ
д г *•кбт
| = — ЛГГ28ІП<)Р^дР<Йр
Точно такъ же
дг-\-\г =
Вставляя а' = (г2 -Н 2г/1г)8Іпд^Лр и |
чаемъ: '
Лг I
Лг, полу-
ЛМ
Лг2
Яг+Лг = — (г2 + 2гЛг)8т^ад>(Іір )
Перемножая почленно и отбрасывая малыя высшаго порядка, по-
лучаемъ
дг±дг = — кт8іпдЛ(рЛц> г I I
кт.
//2/ I
Аг^г2^Лг\.
’ Лг2
КУРСЪ ФИЗИКИ О. X в О Л ь С О Н А. Т. III, изд. 3-е.
20
306
Теплопроводность.
Приравниваемъ дг и \г, сокращаемъ одинаковые члены и дѣ-
лимъ все на —ктг*ыхир(1(р(і'ѵДг; тогда остается
й + — ;г =0...............................<39)
(1г2 г (1г
Вотъ условіе которому должна удовлетворять функція і = /(г). За-
мѣтимъ, что (39) можно получить изъ (20) простымъ преобразованіемъ,
полагая і — /(г), гдѣ г2 = х2 -ф- ѵ2 ф- г2. Чтобы рѣшить уравненіе (39),
(іі /опх । 2г а і о аг А
полагаемъ = г; тогда (39) даетъ ф- - = О, или ф- 2 ? = о.
Отсюда
(іг
. г
сіг ____,
---
гдѣ С постоянное. Далѣе имѣемъ отсюда 4- 21^г = С, или І^гг2 = С
Если логариѳмъ постояненъ, то и самая величина постоянна. Обозначимъ
ее черезъ — В; итакъ гг2 = — В. Отсюда
_ В
г (1г г2
(40)
Это даетъ
гдѣ А постоянное;
отсюда
^ = Д-|- —
1 г
(41)
Такимъ образомъ законъ зависимости і отъ г найденъ. Постоян-
ныя А и В опредѣляются изъ условій, что і=і\ при г = г1; и і = /2
В в
при г — г%. Это даетъ = Д + — , /2 = Д ф- . Отсюда найдемъ А
<1 '2
и В, и вставимъ эти величины въ (41). Тогда получаемъ окончательно
/ = Г<2Ѣ ~ ГА*± _|_ Г1Г2^1 ~~ 1 (42)
г2 — Гі г2 — гг ’ г
Опредѣлимъ полное количество теплоты ($, протекающее въ еди-
ницу времени черезъ поверхность 5. Очевидно,
<2
, Л (11 . 1 п ^11
— — кЗ -г = — \лкг~ .
(1г (1г
<11 і\г» (А — /2) і ѵ
Но паденіе температуры — слѣд.
ф = ^пк (Іі - /2)
Г1Г2
г2 — Гі
. (43)
Это количество, какъ и слѣдуетъ, не зависитъ отъ радіуса г по-
Задачи.
307
верхности 5. Замѣтимъ, что задачу можно рѣшить еще проще, исходя
изъ очевиднаго факта, что С) не должно зависѣть отъ г, т.-е. что
одно и то же количество тепла должно послѣдовательно пройти черезъ
всѣ шаровыя поверхности различныхъ радіусовъ г. Въ этомъ случаѣ
ясно, что количество д тепла, проходящее во время г черезъ опредѣ-
ленную часть о шаровыхъ поверхностей, должно быть обратно про-
порціонально г2. Но д пропорціонально произведенію к на паденіе тем-
пературы ; слѣд. это произведеніе должно быть обратно пропорціонально г2,
т.-е.
мы должны имѣть
аі _ С
аг ~ г*
уравненіе (40), гдѣ С.к — В. Мы даже сразу получили болѣе об-
уравненіе, ибо (44) даетъ возможность разобрать случай, когда к
. (44)
— уравненіе, разобрать которое нетрудно.
стаціонарномъ тепловомъ состояніи
с л о я. Безконечно длинный цилиндрическій слой
т.-е.
щее
зависитъ отъ температуры, напр., когда к = к[} (1 -|- аі). Тогда имѣемъ
-МЦ-«0^ =
IV. Задача о
цилиндрическаго
ограниченъ цилиндрическими поврхностями, радіусы круговыхъ сѣченій
которыхъ Гі и г2, и ось которыхъ общая. Внутренняя (г3) и внѣшняя (г2)
поверхности поддерживаются при температурахъ іх и і2; требуется опре-
дѣлить стаціонарное тепловое состояніе слоя. Если г разстояніе точки
слоя отъ его оси, то ясно, что і — /(г), т.-е., что изотермическія поверх-
ности суть поверхности цилиндровъ, общая ось которыхъ совпадаетъ съ осью
цилиндрическаго слоя. И эту задачу можно, какъ предыдущую, рѣшить
тремя способами. Разсматривая теченіе теплоты черезъ элементъ объема
слоя, ограниченный безконечно близкими 1) двумя цилиндрическими по-
верхностями радіусовъ г и г + /1г, 2) двумя
лярными къ оси и 3) двумя плоскостями,
можно вывести уравненіе
ач , 1 М
—— — — — О
аг* г аг
плоскостями, перпендику-
проходящими черезъ ось,
. . (45)
Это же уравненіе можно вывести и изъ (20), расположивъ ось г — овъ
вдоль оси слоя, и полагая гдѣ г2 = х2 + .У2. Но проще всего мы
найдемъ і, исходя изъ очевиднаго факта, что количество теплоты, про-
ходящей въ единицу времени черезъ любую цилиндрическую поверхность
5, радіусъ которой г и длина /, и ось которой совпадаетъ съ осью слоя,
не зависитъ отъ г. Величина поверхности 5 прямо пропорціональна г,
слѣд. количество д, протекающее во время г черезъ заданную по величинѣ
часть о поверхностей 5. обратно пропорціонально г. Отсюда слѣдуетъ, что
гдѣ С постоянное число. Легко разобрать это уравненіе, полагая к =А0Ц +
+ аі). Если к постоянное, то (45) получается непосредственно изъ (46).
20*
308
Теплопроводность.
Положимъ для этого случая С : к = В; тогда имѣемъ , или і —
= — А или
і = А — В\%г..............(47)
Постоянныя А и В опредѣляются изъ равенствъ
іг—А — В\^гг, і2 = А В\%г2.
Опредѣливъ отсюда А и В, получаемъ окончательно:
х ^2—_Ь~ Іот /4к)
^2 — ^0 %г2—................. ?
Количество тепла, протекающаго въ единицу времени черезъ по-
верхность 5 (радіусъ г, длина /), равно
^= -к8^ = — к2лгІ М = 2пкгІ.
(ІГ (ІГ
4 4 1
1^2 *г 9
или
2лкІ
г
1^-
^2)
(49)
Величина г, какъ и должно быть, сократилась.
Ограничиваемся разборомъ этихъ четырехъ задачъ, относящихся къ
стаціонарному тепловому состоянію. Задачъ на перемѣнное тепловое со-
стояніе. представляющихъ весьма большой интересъ, мы рѣшать не бу-
демъ; онѣ представляютъ болѣе значительныя математическія трудности.
§ 4. Опытное изслѣдованіе относительной теплопроводности твер-
дыхъ тѣлъ. Мы укажемъ на нѣкоторые опыты, основанные на тепло-
проводности тѣлъ, и затѣмъ перейдемъ къ способамъ опредѣленія отно-
шенія коеффиціентовъ к теплопроводности различныхъ тѣлъ. Въ элемен-
тарныхъ учебникахъ физики приводятся различные опыты, основанные
на большей или меньшей теплопроводности тѣлъ. Сюда относится влія-
ніе металлическихъ сѣтокъ на распространеніе горѣнія газовъ и осно-
ванная на этомъ вліяніи предохранительная лампа В а ѵ у; далѣе опытъ
кипяченія воды и даже плавленія свинца въ бумажномъ мѣшечкѣ и т. д.
Теплопроводность играетъ главную роль и въ опытѣ Тгеѵеііап’а; этотъ
опытъ заключается въ слѣдующемъ. Берутъ латунную трехгранную призму,
снабженную деревянной ручкой (рис. 94) и имѣющую жолобъ вдоль од-
ного изъ реберъ, и сильно нагрѣваютъ ее. Потомъ ее кладутъ, какъ по-
казано на рисункѣ, на горизонтальный свинцовый цилиндрикъ такъ, что
она опирается на него въ двухъ точкахъ. Затѣмъ даютъ призмѣ легкій
боковой толчекъ, такъ что она, колеблясь, начинаетъ поперемѣнно опи-
раться то на одну, то на другую точку. Холодная призма послѣ немно-
гихъ колебаній останавливается въ прежнемъ положеніи. Горячая же
призма продолжаетъ. столь быстро колебаться, что она издаетъ довольно
высокій звукъ. Притомъ амплитуда колебаній такъ мала, что на главъ
Твердыя тѣла.
309
нельзя замѣтить движенія призмы. Объясняется это явленіе слѣдующимъ
образомъ. Каждый разъ, когда призма, нѣсколько повернувшись въ сто-
рону, касается свинцоваго цилиндра одною точкою, она передаеть послѣд-
нему нѣкоторое количество тепла. Вслѣдствіе этого происходитъ нагрѣ-
ваніе поверхности свинца, и такъ какъ послѣдній не принадлежитъ къ
Рис. 94.
самымъ лучшимъ проводникамъ тепла, то происходитъ расширеніе свинца,
т.-е. подъ точкою опоры призмы внезапно образуется выпуклость. Легко
понять, что образованіе этой выпуклости должно вліять на призму, какъ
толчекъ снизу вверхъ, какъ нѣкоторое подбрасываніе. Когда призма за-
тѣмъ качнется въ другую сторону, опираясь другой точкой, то произой-
детъ то же самое, т.-е. она вновь получитъ толчекъ снизу вверхъ. Эти
быстро слѣдующіе другъ за другомъ толчки поддерживаютъ колебательное
движеніе призмы, настолько быстрое, что призма издаетъ звукъ. Опытъ
не удается, если вмѣсто свинца взять лучшій проводникъ тепла, напр.
мѣдь. Теплота, переданная мѣди, быстро въ ней распространяется, вы-
зывая слишкомъ слабое мѣстное нагрѣваніе, а слѣд. и слабое расширеніе.
Зато свинецъ можно замѣнить каменною солью, горнымъ хрусталемъ и
нѣкоторыми другими минералами. Призма, напротивъ, должна состоять
изъ матеріала, хорошо проводящаго теплоту.
А. С. Поповъ придумалъ любопытное видоизмѣненіе этого опыта.
На горизонтальную металлическую пластину кладется тонкій слюдяной
листъ съ нѣсколько приподнятыми краями. Если положить на него на-
грѣтый металлическій цилиндръ, то цилиндръ начинаетъ катиться взадъ и
впередъ отъ одного края къ другому. Выпуклости, поддерживающія дви-
женіе цилиндра, образуются здѣсь на слюдяной пластинкѣ. Усѣченный
конусъ при тѣхъ же условіяхъ катится вокругъ своей геометрической вер-
шины. Согнутая въ дугу плоская металлическая пластинка качается въ
ту в и другую сторону. Первоначальный легкій толчекъ вызываетъ во
всѣхъ случаяхъ движеніе, которое затѣмъ продолжается, пока разность
температуръ превосходитъ 60°—70°. Металлическая пластинка подъ слю-
дянымъ листомъ необходима для охлажденія послѣдняго. Если ее замѣ-
310
Теплопроводность
нить стекломъ, то вслѣдствіе сильнаго нагрѣванія слюды движеніе быстро
прекращается.
Прежде чѣмъ перейти къ экспериментальнымъ изслѣдованіямъ тепло-
проводности, мы разсмотримъ нѣсколько методовъ, служащихъ для того,
чтобы на плоскомъ тѣлѣ сдѣлать видимымъ расположеніе хотя-бы од-
ной изотермы. Вёпагтопі покрывалъ пластинку тонкимъ слоемъ
воска, который частью расплавлялся, причемъ граница плавленія его да-
вала изотерму. Ниже (§ 6) мы увидимъ, какимъ образомъ V о і і видо-
измѣнилъ этотъ методъ. Иной способъ заключается въ пользованіи двой-
ными солями Си2}2 • и 2А&І. которыя при опредѣленной тем-
пературѣ мѣняютъ окраску. Первая (мѣдная) соль при 70° внезапно мѣ-
няетъ свою окраску изъ темнокрасной на черную и при нѣсколько низ-
шей температурѣ -- изъ свѣтлокрасной на темнокрасную. Если смѣсью
такой соли и лака покрыть пластинку, то при неоднородномъ нагрѣваніи
получаются двѣ рѣзкія изотермы. Вторая (серебряная) соль мѣняетъ свою
окраску при 45° изъ свѣтложелтой на оранжевую. Кісііагг (1902) и въ
особенности О. Невв (1906) пользовались этимъ методомъ для экспери-
ментальнаго воспроизведенія изотермъ въ тѣхъ различныхъ случаяхъ, ко-
торые поддаются теоретическому разбору.
Переходимъ къ способамъ сравненія коеффиціентовъ к для различ-
ныхъ веществъ. Еще Роигіег построилъ приборъ подъ названіемъ кон-
тактнаго термометра для сравненія теплопроводностей различныхъ тѣлъ.
Первые опыты точнаго опредѣленія величины к принадлежатъ Р ё с -
I е 1. Его приборъ состоялъ изъ цилиндра, содержавшаго вѣсовое коли-
чество Р воды при температурѣ і\ дномъ цилиндра служила испытуемая
металлическая пластинка. Ея нижняя поверхность касалась нагрѣтой воды,
налитой въ другой большій сосудъ. Эта вода имѣла нѣкоторую темпера-
туру Т^>і Теплота передавалась черезъ металлическую пластинку водѣ
въ цилиндрѣ, температура которой въ опредѣленный промежутокъ времени
поднималась до і'. Изслѣдуя скорость нагрѣванія воды въ цилиндрѣ,
Р ё с 1 е 1 могъ опредѣлить количество ц тепла, проходящее въ единицу
времени черезъ пластинку при различныхъ разностяхъ температуръ Т— Л.
По теоріи
, Лі . Т—Г
а = — кз -т- = — кз — г--..................(50)
йх (1 '
гдѣ 5 площадь основанія, (1 толщина пластинки, см. (22, а) стр. 300. Пер-
вые опыты дали однако д почти независимымъ отъ (і. Этотъ странный
результатъ Р ё с 1 е і правильно объяснилъ тѣмъ, что водяные слои, непо-
средственно прилегающіе къ двумъ сторонамъ поверхности металлической
пластинки, плотно къ ней пристаютъ, и вмѣстѣ съ ней представляютъ
систему, теплопроводность которой почти не зависитъ отъ толщины ме-
таллической пластинки; главную роль играютъ приставшіе слои воды,
весьма плохо, сравнительно съ пластинкою, проводящіе теплоту. Р ё с 1е 1
построилъ тогда болѣе сложный приборъ, въ которомъ было устранено
только-что указанное обстоятельство. Верхній сосудъ, содержавшій опре-
Твердыя тѣла.
311
дѣленное вѣсовое количество воды, былъ окруженъ болѣе широкимъ сосу-
домъ. Промежутокъ между сосудами заполненъ плохо проводящимъ ве-
ществомъ, а внизу пробковымъ кольцомъ, къ которому прикрѣплена, испы-
туемая метал іическая пластинка, составляющая такимъ образомъ дно верх-
няго сосуда и касающаяся воды, налитой въ нижній сосудъ. Обѣ по-
верхности пластинки непрерывно обтираются щетками, которыя и сни-
маютъ приставшій слой воды. Опыты, произведенные съ этимъ прибо-
ромъ, показали, что 7 дѣйствительно обратно пропорціонально толщинѣ сі
пластинки. Этимъ подтверждается правильность теоріи, допускающей,
что количество д пропорціонально паденію температуры. Опредѣливъ д,
Р ё с 1 е 1 могъ опредѣлить и численное значеніе коеффиціента к, поль-
зуясь формулою (50).
Роигіег и Рёсіеі изслѣдовали теплопроводность тѣлъ, -взятыхъ
въ формѣ пластинокъ. Саіѵегі и ^ѣпков опредѣляли количество те-
плоты, передаваемое короткимъ стержнемъ.
Переходимъ къ опытамъ, произведеннымъ со стержнями, нагрѣ-
ваемыми съ одного или съ двухъ концовъ
наго теплового состоянія. Законъ распре-
дѣленія температуръ и нѣкоторыя его свой-
ства выведены на стр. 301 -304.
Сюда относится прежде всего опытъ
Іп^епііоиз’а (или Ііі^еп-Наизя’а):
рядъ одинаковыхъ по толщинѣ стержней,
приготовленныхъ изъ различнаго матеріала,
вставленъ въ горизонтальномъ положеніи
рядомъ въ боковую стѣнку сосуда, содер-
жащаго горячую, или, лучше, кипящую
воду. Поверхность стержней покрыта тон-
кимъ слоемъ воска, который таетъ, начи-
ная съ концовъ, ближайшихъ къ сосуду
съ водою. Черезъ достаточный промежу-
токъ времени плавленіе воска останавливается, причемъ длина х части
стержней, на которой воскъ растаялъ, тѣмъ больше, чѣмъ лучше стер-
жень проводитъ теплоту. Этотъ опытъ можетъ даже служить для прибли-
зительнаго опредѣленія отношенія коеффиціентовъ к±: к2 двухъ стержней.
Пусть и х2 длины частей этихъ стержней, на которыхъ воскъ раста-
ялъ, температура воды и і температура, таянія воска. Формула (32)
даетъ і = іое~а^, і = гдѣ
до достиженія ими стащонар-
Рис. 95.
/гр 2 Ігр ,
, , х^, откуда
1
И (охлажденіе у поверхности воска), периметръ р и площадь 5 сѣченія у
всѣхъ стержней одинаковы. Два выраженія для і даютъ аххг = а2х2 или
кѵ___Ху-
^2 ~ ^22 ’
312
Те п л опрово д ность.
Коеффиціенты теплопроводности прямо пропорціональны квадратамъ
разстояній, на которыхъ произошло плавленіе воска.
Весьма удобное для лекцій видоизмѣненіе прибора Іп^епііоив'а
было предложено Н. А. Гезехусомъ. Стержни устанавливаются на-
клонно (рис. 95) и загнутыми концами погружаются въ кипящую воду.
Поверхность стержней покрывается слоемъ параффина, а на верхнія ихъ
части насаживаются небольшія параффиновыя подушки, покрытыя согну-
тыми мѣдными пластинками, какъ показано на рисункѣ. Во время опыта
эти подушки опускаются внизъ до того мѣста, температура котораго сдѣ-
лалась равною температурѣ плавленія параффина.
Для демонстративныхъ цѣлей весьма удобный приборъ былъ постро-
енъ Ѳ. Ѳ. Петрушевскимъ. Этотъ приборъ изображенъ на рис. 96.
М мѣдный изогнутый прутъ, верхній конецъ котораго подогрѣвается пла-
менемъ газовой горѣлки. Нижній конецъ вставленъ въ мѣдную трубку А,
служащую резервуаромъ термоскопа, снабженнаго трубкою С, которая со-
держитъ жидкость; трубочка (і служитъ для предварительнаго всасыванія
жидкости изъ сосудика Р. Другая система РА'й'С'Р' отличается отъ
МАсІСР только тѣмъ, что прутъ Р сдѣланъ изъ желѣза. Чѣмъ лучше
прутъ проводитъ теплоту, тѣмъ больше опускается жидкость въ соот-
вѣтствующей трубкѣ.
Другой приборъ, могущій служить для сравненія коеффиціентовъ к
и А различныхъ стержней былъ устроенъ мною. Онъ изображенъ на
рис. 97. Четыре металлическіе стержня ЬЬ вставлены концами въ че-
тыре кипятильника А, снабженные холодильниками С. Въ А кипитъ
вода; черезъ с протекаетъ вода, проведенная изъ резервуара В по труб-
камъ, не изображеннымъ на рисункѣ. Посреди каждаго изъ стержней
сдѣлано углубленіе, въ которое наливается ртуть и вставляется резер-
вуаръ маленькаго термометра і. Когда достигнуто стаціонарное состоя-
ніе, опредѣляютъ температуру, указываемую этими термометрами. Пусть
Т и і избытки температуры въ Л и въ одной изъ точекъ I надъ температу-
рою окружающаго воздуха. Условія (31,а) стр. 303 принимаютъ видъ
А + В=Т Ае~а1 + Веа1—Т.
Отсюда
Теа1 Т
А = Л1_ в = —±—1.
1-|-еа* і-|-^^
Температуру і въ средней точкѣ мы найдемъ, если вставимъ А и В
и кромѣ того х — — въ (30). Такимъ образомъ получаемъ :
аі
в 2
і = 2Т—~- ,
1 + еа1'
Отсюда
7'4- , ГНр 2 , I Т‘ Р
е = I " О = Г йН1* I
Твердыя тѣла
313
Наконецъ имѣемъ •
п Л, 7-1-/Г2—/2
гдѣ С величина одинаковая для всѣхъ стержней и знакъ обыкновен-
наго логариѳма. Т также одинаково для всѣхъ стержней, но і зависитъ
отъ матеріала (й) стержня и отъ вещества, покрывающаго его поверх-
ность (Л). Наблюдая і, можно при помощи послѣдней формулы найти
отноіпеніе величинъ к для стержней изъ различнаго матеріала, но одина-
коваго поверхностнаго слоя, или отношеніе величинъ 1г для различныхъ по-
верхностныхъ слоевъ, покрывающихъ стержни изъ одинаковаго матеріала.
Рис. 96.
Рис. 97.
Болѣе точный способъ сравненія коеффиціентовъ к былъ предло-
женъ Віоі. Этотъ способъ основанъ на формулѣ (36) стр. 304, относя-
щейся къ температурамъ Ѳъ 02, Ѳ3 трехъ равноотстоящихъ другъ отъ
друга сѣченій стержня, нагрѣваемаго хотя бы съ одного конца, и достиг-
шаго стаціонарнаго теплового состоянія. Взявъ на такомъ стержнѣ нѣ-
сколько разъ по три точки, раздѣляя каждый разъ сумму температуръ край-
нихъ точекъ на температуру средней точки, мы получимъ нѣсколько зна-
ченій величины 2п, которыя дѣйствительно оказываются довольно близ-
кими другъ къ другу. Беремъ ихъ среднее значеніе 2п. Изъ формулы
(38) стр. 304, въ которой сі разстояніе наблюдаемыхъ точекъ, а вели-
чина а дана въ (2б), получаемъ:
“ = | Е = ?Ч"+І "2~1]'
514
Теплопроводность.
Для другого стержня получимъ такимъ же способомъ
“> = |/Л^‘ = <і,18:[", + І ѵ“’
Если стержни одинаковыхъ размѣровъ и покрыты одинаковымъ ве-
ществомъ, напр. вычернены и если разстояніе точекъ взято одно- и то же,
то р—рг, 5 = 1г = 1г± п — Возвысивъ послѣднія два равенства
въ квадратъ и раздѣливъ ихъ другъ на друга, получаемъ формулу
к,х_ ]§•(/? + V п2—1)12
V «і2—1)1
(51)
которая даетъ возможность вычислить отношеніе коеффиціентовъ тепло-
проводности двухъ веществъ.
Опыты производилъ по этому способу прежде всего ГЭ е 8 р г е і 2. При-
боръ, которымъ онъ пользовался, изображенъ на рис. 98. Конецъ А го-
Рис. 98.
ризонтально расположеннаго стержня АВ нагрѣвается лампой С. На рав-
ныхъ разстояніяхъ другъ отъ друга сдѣланы въ стрежнѣ углубленія, въ
которыя налита ртуть и опущены резервуары термометровъ. Линія, про-
веденная пунктиромъ, показываетъ распредѣленіе температуръ при ста-
ціонарномъ состояніи стержня.
Этимъ же способомъ пользовался Неітегзеп для изслѣдованія
теплопроводностей различныхъ матеріаловъ. Существенное улучше-
ніе ввелъ Ьап^Ъегд, замѣнившій термометры, вставленные въ углубле-
нія, термоэлектрическимъ элементомъ, который прикладывался къ различ-
нымъ мѣстамъ стержня. Кромѣ того онъ замѣнилъ толстые стержни, ко-
торые изслѣдовалъ ІЭевргеіг, проволоками и, наконецъ, онъ воспользо-
вался формулою Р о і 8 8 о п’а для стаціонарнаго состоянія безконечно длин-
наго стержня, одинъ конецъ котораго находится при температурѣ въ
Твердыя тѣла.
315
случаѣ, если к и И величины не постоянныя, но функціи температуры
вида к == к0 (1 + аі), к — к0 (1 + /Зі). Тогда вмѣсто (32) і = іое~ах получа-
ется слѣдующая формула
'=[1 - 2 4КР ~ 2а) \іое~ах + 10? - 2а) і^е~ах.
Весьма тщательно изслѣдовали теплопроводность по этому же спо-
собу ХѴіейетапп и Ргапи. Испытуемая проволока ЬЬ (рис. 99) по-
мѣщалась внутри стекляннаго колокола, снабженнаго металлическимъ
дномъ и горлышкомъ, черезъ которое проходила трубка к, въ которой и
помѣщался нагрѣваемый конецъ проволоки. Нагрѣваніе производилось
парами кипящей воды, проходившими черезъ металлическую коробку т;
трубка Л служила для отвода паровъ. Температура і различныхъ точекъ
проволоки измѣрялась термоэлементомъ, проволоки котораго были прове-
дены черезъ стеклянную трубку п. Эта трубка проходила черезъ трубку г,
въ которой она могла двигаться, не пропуская воздуха. Особое устрой-
Рис. 99.
ство термоэлемента давало возможность всегда одинаковымъ образомъ при-
кладывать его къ проволокѣ ЬЬ. Боковая трубка съ краномъ давала воз-
можность выкачать воздухъ изъ стекляннаго колокола и производить на-
блюденія въ пустотѣ. Весь приборъ помѣщался въ большомъ металличе-
скомъ ящикѣ, наполненномъ водою, температура которой не мѣнялась во
время опыта. Термоэлементъ состоялъ изъ желѣза и нейзильбера. Всѣ
испытуемыя проволоки были покрыты слоемъ серебра, чтобы придать имъ
одинаковый коеффиціентъ внѣшней теплопроводности А.
Въ нижеслѣдующей табличкѣ приведены результаты опытовъ ЛѴіе-
йешапп’а и Егапг’а. Во второмъ столбцѣ помѣщены величины 2я,
въ третьемъ относительныя значенія коеффиціентовъ А, причемъ для се-
ребра принято А = 100. Послѣдній столбецъ содержитъ относительныя
значенія коеффиціентовъ л электропроводности для тѣхъ же ме-
талловъ. Для серебра было положено Л = 100. Приводимъ эти интерес-
ныя числа, хотя и относящіяся къ другому отдѣлу физики, въ виду важ-
ности результата, къ которому приводитъ сравненіе послѣднихъ двухъ
316
Теплопроводность.
столбцовъ: теплопроводность металловъ приблизительно
пропорціональна ихъ электропроводности.
2п к А 2п к Л
Серебро. . . 2,0556 100 100 Желѣзо . . 2,393 11,9 13,0
Мѣдь . . . . 2,026 73,6 73,3 Свинецъ . . 2,443 8,5 10,7
Золото . . 2,086 53,2 58,5 Платина . . . . 2,597 8,4 10,3
Латунь . . 2,200 23,1 21,5 Нейзильберъ . 2,772 6,3 —
Цинкъ — 19,0 24,0 Сплавъ Розе . 3,434 2,8 —
Олово . . 2,264 14,5 13,6 Висмутъ . . , 4,565 1,8 I,9
Позже (1859) АѴіесіетапп вновь произвелъ подобныя же изслѣ-
дованія надъ различными сплавами и металлами, причемъ онъ самъ опре-
дѣлялъ и электропроводность для тѣхъ же веществъ. Приводимъ нѣкото-
рыя изъ его чиселъ:
к Л Л А
8 част. Си + 1 часть 2п 27,3 25,5 3 част. 8п + 1 часть Ві 10,1 9,0
6,5 , » 1 1 » » 29,9 30,9 1 „ » 1 1 „ 5,6 4,3
4,7 , » 1 » » 31,1 29,2 1 » „ 1 з „ „ 2,7 2,0
2,1 » » 4" 1 » » 25.8 25,4
Подобные же опыты производили Ѳиіііапсі, Еіііп^зііаизеп и
ЭДегпзІ и др. Р. КоМгаивсЬ нашелъ для закаленной (А)и мягкой (А,)
стали отношеніе к : = 0,56. Для ихъ электропроводностей оказалось
отношеніе Л : = 0,60. Дальнѣйшіе результаты сравненія величинъ к и Л
будутъ приведены ниже. Интересный методъ опредѣленія отношенія
ку : к2 теплопроводностей двухъ тѣлъ далъ АѴ. Ѵоі^і (1898). Этотъ
методъ основанъ на формулѣ
(51,бі)
изотер-
послѣд-
К =
к2 1%д)2
(см. (18,^) стр. 298) гдѣ и углы, образуемые произвольной
мой на линіи раздѣла обѣихъ частей пластинки съ нормалью къ
ней. Упомянутый методъ состоитъ въ слѣдующемъ: изъ сравниваемыхъ
матеріаловъ вырѣзываютъ двѣ одинаковыя пластинки въ формѣ прямо-
угольныхъ треугольниковъ и склеиваютъ ихъ по діагонали, такъ что обра-
зуется прямоугольная пластинка. Поверхность ея покрываютъ элеадино-
цой кислотой (съ примѣсью воска и терпентина) и затѣмъ пластинку при-
кладываютъ одной изъ узкихъ сторонъ къ мѣдному бруску, нагрѣтому до
70°—90°. Линія плавленія, соотвѣтствующая 44°—45°, очень ясно видна
и совпадаетъ съ соотвѣтственной изотермой. На границѣ (діагональ
пластинки) линія плавленія имѣетъ переломъ, причемъ углы и (р2
можно очень точно измѣрить. Формула (51,а) даетъ тогда искомое отно-
шеніе кг : к2. По этому способу Р. А. Всйиіге (1902) сравнивалъ
теплопроводность различныхъ сплавовъ Ві 4“ РЬ, Ві -ф- 8п и 8п + Хп съ
теплопроводностью чистыхъ РЬ, ВЦ 8п и 2,п. Оказалось, что к для сплава
Хп — 8п можно вычислить по правилу смѣшенія (объемы) изъ к щя Хп
Твердыя тѣла.
317
и 8п. Наоборотъ, малѣйшая примѣсь РЬ или 8п къ Ві вызываетъ умень-
шеніе А, хотя чистые РЬ и 8п гораздо лучше проводятъ, чѣмъ ВІ, Со-
вершенно аналогичную зависимость обнаруживаютъ и
электропроводности тѣхъ же сплавовъ. По способу Ѵоі^і’а
Роске (1899) сравнивалъ теплопроводность различныхъ стеколъ.
§ 5. Опредѣленіе абсолютной теплопроводности твердыхъ тѣлъ.
Опредѣленіе к въ абсолютныхъ единицахъ сводится къ нахожденію коли-
чества тепла, протекающаго черезъ поперечное сѣченіе тѣла въ данное
время и при данномъ паденіи температуры. Мы будемъ выражать к въ
С. О. 8. единицахъ, т.-е. измѣрять эту величину числомъ малыхъ калорій,
протекающихъ въ 1 сек. черезъ кв. см. поверхности, когда паденіе пер-
пендикулярно къ этой поверхности равно 1° на 1 см. длины. Опредѣле-
ніе абсолютнаго значенія к представляетъ большія затрудненія, на кото-
рыя было указано при описаніи опытовъ Рёсіеі <цтр. 310), давшихъ
результаты, весьма далекіе отъ вѣрныхъ; такъ Рёсіеі находитъ для
мѣди число А, которое почти въ 6 разъ меньше вѣрнаго. Но той же при-
чинѣ не привели къ надежнымъ результатамъ и опыты О и 1 о п &’а съ
полымъ шаромъ, наполненнымъ льдомъ и помѣщеннымъ въ среду съ тем-
пературою въ 100°, причемъ опредѣлялось количество льда, растаявшаго
въ заданное время; к могло быть вычислено по формулѣ (43) стр. 306
(1)и1ои§ пользовался менѣе точной формулой). Существуетъ однако
цѣлый рядъ болѣе точныхъ способовъ опредѣленія к въ абсолютной мѣрѣ,
основанныхъ на наблюденіи стаціонарнаго или перемѣннаго теплового со-
стоянія тѣлъ различной формы. Теорія большинства изъ этихъ методовъ
основана на формулахъ, которыя нами выведены не были, а потому и са-
мые методы не могутъ быть разобраны детально. Ограничиваемся ука-
заніемъ на важнѣйшіе изъ этихъ методовъ. При этомъ мы укажемъ
также на результаты опредѣленія зависимости коеффиціента к отъ тем-
пературы.
[. Методъ Р о г Ь ев’а. Одинъ конецъ длиннаго стержня нагрѣ-
вается до температуры і0. При стаціонарномъ состояніи температура і
на разстояніи х отъ этого конца опредѣляется формулою (32) стр. 303,
і = і^е~ах, гдѣ а' = ^/~ . Измѣряя температуру / въ различныхъ
точкахъ, можно вычислить величины /0 и а, которыя, такимъ образомъ,
будемъ считать извѣстными. Количество д теплоты, протекающее въ
единицу времени черезъ то поперечное сѣченіе 5 стержня, которому со-
отвѣтствуетъ данное х, равно
<7 - к$ — = акзі^е ~~ах .... . . (52)
сіх
Это количество теплоты равно тому, которое теряется въ единицу
времени поверхностью той части стержня, которая находится за раз-
сматриваемымъ сѣченіемъ, т.-е. отъ х = х до х — 1. Разсмотримъ безко-
318
Теплопроводность.
нечно малый отрѣзокъ этой части: пусть длина его сіх\ тогда его объ-
емъ 8(іх, его теплоемкость дсзгіх, гдѣ о плотность, с теплоемкость мате-
ріала, изъ котораго сдѣланъ стержень. Его температуру обозначимъ че-
резъ і. Г о г Ь е 8 полагалъ, что количество теплоты, теряемое этимъ от-
рѣзкомъ въ безконечно малый промежутокъ времени сіт черезъ его боко-
вую поверхность, равно тому количеству дд теплоты, которое этотъ же
отрѣзокъ потеряетъ во время сіт, свободно охлаждаясь въ воздухѣ и обла-
дая втеченіе времени сіт тою же температурою і. ЕогЬев нагрѣвалъ
болѣе короткій стержень изъ того же матеріала, такого же сѣченія 5 и
съ такимъ же поверхностнымъ слоемъ, и наблюдалъ его охлажденіе въ
воздухѣ. При этомъ получалась перемѣнная температура какъ нѣко-
торая функція времени г
І = д)(т\
Очевидно дд равно произведенію теплоемкости дсзсіх отрѣзка на
пониженіе температуры аі, происходящее во время сіт т.-е. дд =
= — $с8(іхсіі— — цеху/(т)сіхсіт. Величина — =
аі
ат
есть скорость ѵ
охлажденія при данной температурѣ I, см. (9) стр. 277. Опытъ даетъ
намъ величину ѵ для различныхъ і, а потому мы можемъ положить ѵ =
—/(/). Теперь имѣемъ дд — $с8ѵахат. Это количество тепла теряетъ
разсматриваемый отрѣзокъ во время ат и при стаціонарномъ состояніи:
слѣд. онъ въ единицу времени теряетъ количество осзѵах тепла. Вся
часть стержня отъ х = х до х = I теряеть въ единицу времени
і
д^=8()С у ѴаХ.
X
• Величина ѵ есть функція температуры; но такъ какъ і извѣстно для
каждаго х, то можно ѵ представить, какъ функцію отъ х, и вычислить
интегралъ, хотя бы при помощи графическаго способа. Обозначимъ его
численное значеніе черезъ Р, Тогда д = 8осР и (52) даетъ ак8І^е~~ах=
= 8@сР, откуда
к= ЯсР =®сР
аІе^~~ах аі
(53)
По этой формулѣ и найдется к. Е о г Ь е 8 изслѣдовалъ по этому
способу чугунъ. Мѣняя х, онъ могъ вычислить к для различныхъ сѣче-
ній, а слѣд. и для различныхъ температуръ. Онъ нашелъ слѣдующія числа
для к въ С. О. 8. системѣ (размѣръ величины указанъ въ (8) стр. 2940:
0° 50° 100й 150° 200° 275°
к = 0,207 0.177 0,157 0,145 0,136 0,124----
см. сек.
Е о г Ь е 8 принималъ р и с независимыми отъ температуры, въ чемъ
заключался важный источникъ погрѣшностей. Въ дѣйствительности к
врядъ-ли убываетъ такъ быстро съ температурою. Таіі и въ особен-
320
Теплопроводность.
к 105/ 103Л к 105Л 103Л
Мѣдь . 1,0405 65,13 1,6 Олово . 0,1510 8,33 1,8
Цинкъ . . 0,303 18,00 1,7 Свинецъ. . 0,0810 5,06 1.6
Латунь . . 0,2625 16,47 1,7 Сурьма . . 0,0420 2,47 1,7
Желѣзо. . 01587 9,41 1,7 Ртуть . 0,0201 1,06 1,8
Пропорціональность между к и Л вполнѣ подтверждается этими числами.
III. Методъ Е. ^итапп’а. Стержень изъ испытуемаго мате-
ріала нагрѣвается съ одного конца до достиженія стаціонарнаго состоянія.
Затѣмъ удаляется источникъ тепла и наблюдаются черезъ каждыя 8 се-
кундъ температуры двухъ точекъ, лежащихъ вблизи концовъ стержня. Те-
орія показываетъ, что сумма и разность этихъ двухъ температуръ даютъ
возможность отдѣльно вычислить коеффиціенты к и к. Можно замѣнить
стержень кольцомъ, одно мѣсто котораго сперва нагрѣвается; при охлаж-
деніи кольца наблюдаютъ температуры двухъ точекъ, діаметрально проти-
воположныхъ и находящихся на различныхъ разстояніяхъ отъ того мѣста,
которое сперва непосредственно нагрѣвалось. Размѣры сѣченія кольца
должны быть малы, сравнительно съ его діаметромъ. Пусть о длина оси
кольца, 4 и температуры одной и температуры другой точки въ
моменты и г2. Тогда к и к получаются изъ формулъ
1 ьД+й.'
5 Ті— Г2
Гранитъ.
0і010!М й?-)’
сек.
гр.
Могутъ быть взяты также и шары, причемъ наблюдаются темпера-
туры въ центрѣ и у поверхности. Дурные проводники изслѣдовались въ
к
формѣ шаровъ. Г. е и ш апп опредѣлялъ величину а2 — , см. (9") и (9,а)
стр. 294, гдѣ р плотность, с теплоемкость вещества.
Каменный уголь. Сѣра. Ледъ. Песчаникъ,
ь
— 1= 0,00116 0,00126 0,01145 0,01357
рг
к = 0,00030 — 0,00573
см. сек.
Н. Е. УѴ еЪ е г производилъ измѣренія по способу Е. М еииі апп’а,
пользуясь кольцами. Дурнымъ проводникамъ онъ придавалъ форму круг-
лыхъ толстыхъ пластинокъ, охлажденіе которыхъ и наблюдалось. Н е с 11 і
Ц903) примѣнилъ этотъ методъ къ плохимъ проводникамъ. Чрезвычайно
тщательное теоретическое изслѣдованіе этого метода и его эксперимен-
тальной приложимости къ хорошимъ проводникамъ опубликовалъ Сгіа^е
(1905). Онъ находитъ, что этотъ методъ можетъ давать результаты точные до
1
процента.
2
Твердыя тѣла.
321
IV. Методъ А и § 8 і г о е т’а. Одинъ конецъ длиннаго стержня
или середина такого стержня поперемѣнно нагрѣвается струею пара и за-
тѣмъ охлаждается холодною водою. Черезъ нѣкоторое время, когда на-
грѣванія и охлажденія были періодически повторены достаточное число
разъ, оказывается, что и въ другихъ точкахъ стержня температура пра-
вильно колеблется между двумя опредѣленными, но для различныхъ то-
чекъ различными предѣлами. Теорія показываетъ, что наблюдая періоди-
чески измѣняющіяся температуры въ двухъ точкахъ стержня, можно вычи-
слить величину к.
Подробный критическій разборъ способа Ап^вігоеш’а былъ сдѣ-
ланъ Вита8. Между прочимъ Ап^вігоет принимаетъ плотность р
и теплоемкость с вещества за величины, не зависящія отъ температуры.
к
А п 81 г о е т находитъ для а- = — :
мѣдь а2 = 1,163(1 —и,00151УГ)
желѣзо а2 = 0.2409(1 — 0,002874/) ».
Если для рис вставить ихъ значенія изъ опытовъ В ё (1 е’а,
см. стр. 192, то получается:
мѣдь /г = 0,9394(1 0,001065^), желѣзо А = 0,1842(1—0,001562В.
Н. \Ѵ е Ь е г произвелъ рядъ изслѣдованій по способу А п 81 г о е т’а,
видоизмѣненному Г. Иеитапп’омъ: оба конца стержня поперемѣннно
нагрѣваются и охлаждаются, причемъ нагрѣваніе одного конца произво-
дится одновременно съ охлажденіемъ другого. Наблюдая температуру се-
редины и еще двухъ точекъ стержня, можно вычислить 1г и к. Нае^-
81 г о е т производилъ сравнительныя измѣренія по способамъ Ап -
,8ІгоепГа и Е. Иеитапп’а (методъ кольца).
V. Методъ Р. КоЫгаиес й’а (1899). Этотъ ученый далъ весьма
интересный методъ для опредѣленія отношенія теплопроводности къ
электропроводности тѣлъ. Такъ какъ величину Л можно весьма точно из-
мѣрить (т. IV), то здѣсь получается способ'ь опредѣленія величины к въ
абсолютныхъ единицахъ. Въ простѣйшемъ видѣ этотъ способъ состоитъ
въ слѣдующемъ: стержневидное тѣло, боковая поверхность котораго не
отдаетъ теплоты, подвергается дѣйствію электрическаго тока, которымъ и
нагрѣвается. Послѣ того, какъ наступитъ равновѣсіе, измѣряютъ въ трехъ
мѣстахъ стержня три температуры иъ и2 и и три потенціала ѵ19 ѵ2
и (т. IV) или вѣрнѣе разности этихъ величинъ. Въ такомъ случаѣ
оказывается, что
А = 2 И1^2 ~~ ^з) ~
А (®1— (^2—^8) (®8 —^1)
Если упомянутыя три точки взять на одинаковомъ другъ отъ друга
разстояніи, а именно такъ, чтобы и1 = и^ и если положить и2— и1 —
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. III, изд. 3-е. 21
322
Теплопроводность.
= и., — ил = и, ѵг — = 2(г/1 — ѵ.^ = (2^ — ѵ.3) = К то получается
к 1 V2
к ІГ
к
причемъ 3 , оудучи зависимо отъ температуры, представляетъ среднее зна-
к
ченіе изъ всѣхъ между температурами и иг = и3.
Лае^ег и Ві$8е11іог8І развили теорію этого метода и опредѣ-
лили для 23 металлическихъ стержней значеніе 2 : к при температурахъ
18° и 100°. Измѣривъ электропроводность 2, можно было найти теплопровод-
ность к для этихъ температуръ, а также температурный коеффиціентъ
теплопроводности. Послѣдній оказался положительнымъ для Л/, Аи, Рі,
Рсі, Константина и манганина; онъ отрицательный для Си, Л^, Ыі, 7,п,
Сй, РЬ, 8п, Ре, Ві и для стали. Для чистыхъ металловъ онъ вообще
очень малъ. Значенія для к : 2, найденныя для чистыхъ метал-
ловъ при одинаковой температурѣ, весьма мало между собой
разнились, хотя значенія 2 и & мѣнялись въ весьма широкихъ предѣлахъ
(отъ единицы къ десяти). Значительно большія величины для к : 2 были
найдены для Ре, Ві, Константина и манганина. Температурный коеффи-
ціентъ для к : 2 оказался положительнымъ и для чистыхъ металловъ при-
близительно равнымъ 0,004; эта величина соотвѣтствуетъ температурному
коеффиціенту электрическаго сопротивленія (1 : 2).
VI. Другіе методы. КігсЫіоИ и Напвегоапп изслѣдо-
вали перемѣнное тепловое состояніе въ металлическихъ кубахъ, ребра ко-
торыхъ имѣли длину, равную 140 мм. На одну изъ вертикальныхъ сто-
ронъ куба направлялась струя воды, температура которой была на нѣ-
сколько градусовъ выше или ниже первоначальной температуры куба.
Три канала, доходившіе до оси куба, перпендикулярной къ этой сторонѣ,
давали возможность слѣдить за измѣненіемъ температуры въ трехъ вну-
треннихъ точкахъ куба. Температуры измѣрялись термоэлектрическимъ
способомъ. Весьма сложная теорія даетъ возможность найти на основа-
ніи этихъ наблюденій величины к. КігсЬЬоіІ п Н ап 8 е ш апп нашли,
А
что для желѣза, свинца и олова величина а- = съ повышеніемъ
температуры уменьшается, для мѣди увеличивается, для цинка отъ тем-
пературы не зависитъ.
Многіе ученые пользовались подобными же методами, напр. Г. А
ЗсЬиІге. Какъ КігсЫіоН и Напвешапп, такъ и Р. А. бсііиіге
допускали, что омываемая водой часть поверхности тѣла въ
точности принимаетъ температуру воды. Сггиепеізеп
(1900) первый показалъ, что это допущеніе неправильно и по
слѣдующей причинѣ: у омываемой поверхности образуется тонкая непо-
движная водяная пленка, которая вызываетъ замѣтную разницу между
температурами воды и поверхности тѣла, (тгиепеівеп видоизмѣнилъ
способъ Р. А. Всйиіге’а такъ, что въ вышеупомянутомъ допущеніи уже
Твердыя тѣла.
323
не было надобности. Онъ опредѣлялъ также отношеніе к: Л (теплопро-
водности къ электропроводности) и подтвердилъ, что для сплавовъ (Си— №)
и не чистыхъ металловъ это отношеніе имѣетъ большія значенія, чѣмъ
для металловъ чистыхъ.
8сІіаііІе1Ьег§ег (1902) измѣрялъ температурные скачки между
поверхностью стержня и водой, помѣщая одинъ конецъ стержня въ воду
при 6°,1, другой въ паръ при 98°,55, пока не наступало равновѣсіе. Ока-
залось, что концы стержня имѣли температуры 12°,75 и 94°,07. Темпе-
ратурные скачки составляли такимъ образомъ 6°,65 и 4°,48.
Огйпеійеп замѣнилъ обливаніе водой нагрѣваніемъ посредствомъ
лучеиспусканія накаленной платиновой пластинки; этимъ методомъ поль-
зовался ОіеЬе (см. ниже). Позже Сггйпеіееп (1905) развилъ теорію
обоихъ методовъ и далъ графическій методъ для вычисленій.
8сйап1е1Ьег^ег измѣряль к для мѣди также и по способу
Е. К о Ъ1 г а и 8 с й’а и нашелъ въ среднемъ к = 0,943 С. О. 5. единицъ.
Ь. Ьогепг (въ Копенгагенѣ) измѣрялъ теплопроводность по двумъ
способамъ. Первый изъ нихтэ подобенъ способу ЕогЬез’а (стр. 317), съ
тою однако разницею, что онъ принялъ для скорости охлажденія стержня
свою формулу, которая приведена на стр. 285. см. (33). Второй способъ
заключается въ слѣдующемъ: весь стержень помѣщается въ пространство,
температура котораго можетъ быть измѣнена и доведена до 100°. Въ
этомъ пространствѣ происходитъ затѣмъ дальнѣйшее нагрѣваніе стержня
съ одного конца, причемъ измѣряются при помощи термоэлементовъ тем-
пературы и равноотстоящихъ другъ отъ друга точекъ. Пусть темпера-
туры эти іъ онѣ получаются, какъ нѣкоторыя функціи.вре-
мени г. Удаливъ источникъ нагрѣванія, Ьогепг наблюдалъ темпера-
туры ' тѣхъ же точекъ во время охлажденія стержня.
Теорія даетъ слѣдующее : пусть і2 + 4 + • • • + і — + 4 ~Н • • • 4"
— і п—і = 5‘, — і2 -ф- іп — іп—і ;== 4, і± — і2 і' п — I'п—і = -4 ; тогда
2 _ к _ р /аз азу
а ~~ де ~ Л—4' б// / ’
гдѣ I разстояніе точекъ другъ отъ друга, которое въ опытахъ Ьогепг’а
равнялось 2 см. Измѣненіе температуры пространства, въ которомъ
находился стержень, давало возможность найти к при различныхъ тем-
пературахъ.
Приводимъ нѣкоторыя изъ чиселъ, найденныхъ Ьотеп г’омъ и Кігсіі-
ЬоіГомъ и Паи 8 етапп’омъ; всѣ величины въ С. О. 8, единицахъ.
Ьогепг. КігсЫіоИ и Напветапп. 15°
0° 100°
Мѣдь . . Магніи . . 0,7198 0,3760 0,7226 0,3760 0,4152 Разные сорта 7.п,
Алюминій . 0,3445 0,3619 0,2545' I .. .. 0,1418
Цинкъ . . — '— — II .. .. 0,0964
Желѣзо . . 0,1665 0,1627 0,1446 ш .. 0,1375
21*
324
Теплопроводность.
Ъогепг. КігсЬЬоП и Напвешапп.
00 100° 15°
Олово . . 0.1528 0,1432 0,0793
Свинецъ . 0,0836 0,0764
Нейзильберъ 0,0700 0,0887
Сурьма . 0,0442 0,0396
Висмутъ . 0,0177 0,0174
По Ьогепг’у к для нѣкоторыхъ металловъ растетъ, для другихъ
убываетъ, для не мѣняется при повышеніи температуры. Абсолютныя
измѣренія величины к производили также 6гау, Наіі (для стали) и др.
Разсматривая результаты, найденные различными учеными, легксм
видѣть, что относительно зависимости теплоемкости отъ тем-
пературы, т.-е. относительно величины а въ формулѣ к=к^(1 -ф- аі) еще
существуетъ огромная неувѣренность. Особенно страдаютъ противорѣ-
чіями болѣе раннія наблюденія. Такъ, Е. Ьепг нашелъ, что для Си, Ре,
латуни и нейзильбера а положительное и почти равно соотвѣтственнымъ
коеффиціентамъ электропроводности 2; такъ для желѣза онъ нашелъ
а = 0,00405, тогда какъ Ь о г е п 2 даетъ а < 0. О 8 ш о п (1 нашелъ, что
для чугуна между 100° и 200° теплопроводность к на 15% больше, чѣмъ
между 60° и 90°. Я нашелъ для мѣди а = 0,000469, для латуни а =
— 0.000886, тогда какъ Ь о г е п 2 даетъ соотвѣтственно а = 0,000039 и
а = 0,002445.
Выше уже было упомянуто, что для чистыхъ металловъ Яае^ег
и ВІ88еИіог8І нашли для а очень малыя значенія, частью положи-
тельныя, частью отрицательныя, бігапео (1898) также нашелъ, что
для Си и Ре а должно быть очень мало. Только для трехъ сплавовъ и
для висмута 3 а е § е г иТ)І88е11іог8І нашли большія значенія для а.
Для висмута а =— 0,002. СгіеЪе (1903) изслѣдовалъ теплопровод-
ность висмута при низкихъ температурахъ и нашелъ слѣдую-
щія значенія (въ С. О, 8. единицахъ) :
+ 18° — 79° —186°
к = 0,0192 0,0252 0,0558
Первыя два числа даютъ а — — 0,003. СгіеЬе пользовался мето-
домъ Сггиепеівеп’а, причемъ, однако, по мысли эгого же ученаго на-
грѣваніе одной .изъ поверхностей производилось не потокомъ воды, но
лучеиспусканіемъ раскаленнаго платиноваго листа. Ѳіа^е (1905) опре-
к
дѣлилъ температурные коэффиціенты для величины а2 = — и нашелъ
для Ре, Си, А§, РЬ, 8п, 7лі, стали и нейзильбера небольшія отрицатель-
ныя значенія.
Что касается отношенія к: 2 теплопроводности къ электропроводно-
сти, то мы выше уже привели результаты важнѣйшихъ, относящихся сюда
изслѣдованій. Укажемъ еще, что Кіе128сЬ нашелъ, что для мѣди, со-
держащей фосфоръ или мышьякъ (до 5%), значеніе к: 2 меньшее, чѣмъ
Твердыя тѣла.
325
для чистыхъ металловъ, тогда какъ мы видѣли, что для сплавовъ были
найдены большія значенія. Послѣднія подтвердили также ѵап АпЪеІ
и Раіііоі (1895) для константана, алюминіевой бронзы и сплава Ее 4- №
С е 11 і е г нашелъ, что для различныхъ сортовъ угля к: Л имѣетъ весьма
различныя значенія. Съ возрастаніемъ температуры к-.Х растетъ и для
чистыхъ металловъ главнымъ образомъ [потому, что Л убываетъ. Для
висмута Даецег и ВІ88е1йог8І нашли относительно малый тем-
пературный коеффиціентъ 0,0015. 6 і е Ь е , напротивъ, нашелъ, что
между 4 18° и — 186° для висмута не мѣняется и слѣд. к и Л обла-
даютъ одинаковыми температурными коеффиціентами. Ь о г е п г полагалъ,
что к: Л пропорціонально абсолютной температурѣ, но это приблизительно
вѣрно только для нѣкоторой группы чистыхъ металловъ (Си, Аи, А& №,
Хп, са, РЬ, 8гі).
Подробный обзоръ всѣхъ работъ по вопросу о теплопроводности ме-
талловъ опубликовали НоІЪогп и ЛѴ і е п (1896).
Дѣйствіе магнитнаго поля на теплопроводность тѣлъ будетъ
разсмотрѣно въ т. IV.
VII. Методы измѣренія к для дурныхъ проводниковъ
тепла. Ограничиваемся, главнымъ образомъ, указаніемъ литературы, кото-
рая помѣщена ниже. Теплопроводность пластинокъ изслѣдовали НегвсйеП
(минералы), Ту п <і а 11 (дерево), Ь ап § (камни, кирпичъ), А п (1 г елѵ8 (ледъ),
Норк іп8 (минералы, воскъ), Ьее8 (минералы, дерево), Сіігівііапзеп
(стекло и мраморъ), О д (і о п г (стекло), Георгіевскій (строевые мате-
ріалы) и другіе.
Ь о сі $ е предложилъ такой методъ: стержень разрѣзанъ на двѣ части ;
однпнъ конецъ одной части нагрѣвается, и изслѣдуется распредѣленіе
температуръ въ другой части, сперва, когда она непосредственно касается
первой, а потомъ, когда между обѣими частями помѣщенъ слои изъ испы-
туемаго вещества. Видоизмѣненіемъ этого способа пользовались Ь е е 8 и
ѴЪгоІіоп. Неітегзепи ЬіИго'ѵѵ пользовались методамъ Віоі-
Везргеія (стр. 314), 8тііЬ и КпоН—методомъ А п § 8 і г о е т’а (ре-
знна и гутаперча). Р. Неитапіц ЗіеЕап, В. ЛѴеЪег, Таша^аѵа,
8 і а д 1 е г и Н. М е у е г изслѣдовали различныя тѣла въ формѣ шаровъ,
кубовъ или цилиндровъ. Ьогсі Кеіѵіп и Мпггау помѣщали ‘парал-
лелепипеды изъ различныхъ минераловъ нижнимъ основаніемъ въ распла-
вленное олово; верхнее основаніе охлаждалось водою. При помощи термо-
элементовъ, введенных ъ въ боковые каналы, измѣрялась температура внутри
параллелепипеда.
СйгІ8Ііап8еп (1881) далъ слѣдующій методъ для опредѣленія от-
ношенія величинъ к для дурныхт проводниковъ. Изъ трехъ параллель-
ныхъ мѣдныхъ пластинокъ А, В, С, двѣ крайнія А и С удерживаются
при температурахъ и Пластинки изъ сравниваемыхъ веществъ за-
полняютъ оба промежутка. Когда наступитъ равновѣсіе, измѣряютъ тем-
пературу мѣдной пластинки В. Если и (1> разстоянія мѣдныхъ пла-
326
Теплопроводность.
стинокъ, и слѣд. толщины испытуемыхъ пластинокъ, то искомое отно-
шеніе кг: к2 выражается формулой
/іД ^‘2 (з
к2 сі2 — і2
Рааійогп сравнилъ по этому способу теплопроводности стекла и
воздуха.
V о і § I омывалъ одну сторону испытуемой пластинки струею холод-
ной воды, а другую сторону приводилъ въ соприкосновеніе съ опредѣ-
леннымъ количествомъ теплой воды. Наблюдая скорость охлажденія этой
воды, можно вычислить к для пластинки. Ѵепвке (1891) и Роске
(1899) опредѣляли этимъ способомъ к для стекла.
Ліѵеп (1905) нагрѣвалъ цилиндрическое тѣло, пропуская электри-
ческій токъ по проволокѣ, натянутой вдоль оси цилиндра. Затѣмъ онъ
измѣрялъ термоэлементомъ разность температуръ 0 между двумя точками,
находившимися на разстояніяхъ а и Ь отъ оси. Если д есть развив-
шееся въ проволокѣ на сантиметръ за секунду количество теплоты, то
к = <1 —
2л а
Подобнымъ методомъ пользовался Ь е е 8 для опредѣленія к при весьма
низкихъ температурахъ. Приводимъ нѣсколько его чиселъ { Т — абсолют-
ная температура, к выражено въ С. 0. 8. единицахъ).
Т 120° 180° 240°
Ледъ 0,0062 0,0058 0,0052
Нафталинъ 0,0013 0,0011 0,0009
Анилинъ 0,0011 0,00086 0,0007
Глицеринъ 0.00078 0.00082 0,00076
Значительный интересъ. также и для геофизики, представляетъ во-
просъ о теплопроводности снѣга. Опредѣленіемъ ея занимались Р. е и -
тапп (1862), Ап(1гелѵ8 (1886), Н.) е 181 гоет (1889), Абельсъ (1892)
и ^П88оп (1901). Н) е І8ІГ0 ет нашелъ к — 0,000508 С. О. 5. при
плотности 6 = 0,183. Но это число повидимому слишкомъ велико. На
большое вліяніе, которое должна имѣть плотность снѣга, указалъ В о е й -
ковъ. А б е л ь с ъ нашелъ
к = 0.006862. С. О. 8.
йапвзоп пользовался методомъ С Ьгі 8 (іа п 8 еп’а ; для сравненія
служила пластинка стекла. Снѣгъ замѣнялся водою, для которой прини-
малось число Ьеев’а (1898) к = 0,00147 С. О. 5. при 11°, такъ что
окончательно снѣгъ сравнивался съ водою. Лап88оп нашелъ въ С. 0.8.
единицахъ
к = 0.00005 + 0,00196 + 0,006д4.
При 6 = 0 получается значеніе к для воздуха.
Анизотропныя тѣла.
327
О кай а (1905) опредѣлялъ к и д на различныхъ глубинахъ снѣго-
вого слоя. Полученныя имъ величины (0,00028 и 0,00045) лучше со-
гласуются съ формулой к б е л ъ с а , нежели съ формулой 4 а и 8 8 о п’а.
Многіе ученые опредѣляли к для с м ѣ с и рг и /л2 частей двухъ ве-
ществъ, теплопроводности которыхъ кх и к2. Ьеез (1900) находитъ, что
к не получается по правилу смѣшенія, но по формулѣ
* = кМі” + РЛ") : (»і + Л>),
гдѣ п постоянная.
М а х іѵ е 11 далъ выраженіе для удѣльнаго электрическаго
сопротивленія к неоднородной среды, состоящей изъ вещества съ
удѣльнымъ сопротивленіемъ к2, въ которомъ расположено весьма большое
число весьма малыхъ шаровъ, имѣющихъ удѣльное сопротивленіе кх, а
именно:
+ к2 -у- р(кг — к2)_ &
2^ + к2 — 2р (кг — к^
(см. Тгаііё й’ёіесігісііё еі йе та^пёіІ8ше. Рагіе 1885 I р. 496, гдѣ
множитель к2 пропущенъ). Здѣсь р означаетъ отношеніе объема шаровъ
къ общему объему. Совершенно аналогичная формула должна суще-
ствовать также и для теплопроводности, если вмѣсто к, к± и к2 подста-
вить обратныя теплопроводностямъ величины. Ь і 8 е Меііпет (1906)
провѣрила формулу МахлѵеІГа для ртутной мази (ЬТщ. Нуйгаг^угі) опре-
дѣливъ теплопроводность чистаго жира и мази (р = 1 ) но методу
40
С Ііг і 8 1 і а п 8 е п’а. Согласованіе съ формулой М а х ѵѵ е 1 Га получилось
прекрасное.
§ 6. Теплопроводность анизотропныхъ тѣлъ. Теплопроводность
анизотропныхъ тѣлъ, напр. кристалловъ всѣхъ системъ, кромѣ правиль-
ной. въ различныхъ направленіяхъ неодинакова. Математическая теорія
распространенія тепла въ кристаллахъ была дана Инка ш е Гемъ, 8 і о -
кез’омъ и Ьашё. Мы ограничиваемся указаніемъ на главнѣйшій ре-
результатъ. Если внутри и з о т р о п н а г о тѣла какая-либо точка С могла
бы сдѣлаться источникомъ теплоты, распространяющейся отъ нея во всѣ
стороны, то изотермическія поверхности представили бы поверхности кон-
центрическихъ сферъ съ общимъ центромъ въ С. Въ кристаллахъ при
тѣхъ же условіяхъ изотермическія поверхности представили бы подоб-
ные эллипсоиды съ общими осями и общимъ центромъ въ С. Для
кристалловъ одноосныхъ, т.-е. квадратной и гексагональной системъ, по-
дучаются эллипсоиды вращенія, для кристалловъ двуосныхъ — эллипсоиды
трехосные. Въ общемъ случаѣ слѣдуетъ отличать три главные коеф-
фиціента теплопроводности ки к2 и к.л, соотвѣтствующіе направленіямъ
осей эллипсоида. Направленія тепловыхъ потоковъ вообще
не совпадаютъ съ нормалями къ изотермическимъ
поверхностямъ.
Первые опыты, доказавшіе, что теплопроводность тѣлъ въ разлпч-
328
Теплопроводность.
ныхъ направленіяхъ можетъ быть неодинаковою, принадлежатъ Бе Іа
Кіѵе’у иПе СапйоНе’ю; но они относились къ дереву и о нихъ
мы скажемъ виже.
Подробное опытное изслѣдованіе теплопроводности кристалловъ было
сдѣлано 8ёиагтоптомъ по слѣдующему способу. Изъ кристалла онъ
вырѣзалъ пластинку, въ серединѣ которой просверливалъ отверстіе; черезъ
отверстіе онъ вводилъ тонкую серебряную трубочку, изогнутую на нѣко-
ромъ разстояніи отъ пластинки подъ прямымъ угломъ. Горизонтально
расположенная пластинка покрывалась тонкимъ слоемъ воска, смѣшаннаго
со скипидаромъ; затѣмъ нагрѣвалась горизонтальная часть трубки и воз-
духъ продувался черезъ трубку. Такимъ образомъ середина пластинки
нагрѣвалась горячимъ воздухомъ; теплота отъ этого мѣста распространя-
лась во всѣ стороны и воскъ плавился. Та часть поверхности, на ко-
торой воскъ расплавился, была ясно видна и послѣ охлажденія пла-
стинки ; оказалось, что она ограничена эллипсомъ. Измѣряя длину
полуосей этого эллипса, и повторяя опытъ съ пластинками, вырѣзанными
изъ кристалла въ различныхъ направленіяхъ, можно было построить изо-
термическій эллипсоидъ, и найти направленія и относительныя вели-
чины его осей.
М е у е г замѣнилъ воскъ слоемъ двойной іодистой соли мѣди и ртути
(СщЛ2. которая ниже 70° имѣетъ яркокрасный цвѣтъ, а выше 70°
дѣлается темнобурой. Воепі^еп показалъ, что достаточно до нагрѣва-
нія сильно дохнуть на поверхность пластинки: слой влаги при нагрѣваніи
испаряется, а предѣлы, до которыхъ испареніе распространилось, легко
замѣтить, посыпая пластинку плауновымъ порошкомъ (ЬусороШит), кото-
рый затѣмъ стряхивается съ сухихъ мѣстъ. Такимъ образомъ контуръ
получается весьма рѣзкій.
Нагрѣваніе можно производитъ и другими способами, напр. касаясь
середины пластинки сильно нагрѣтымъ металлическимъ остріемъ; можно
также ввести проволоку черезъ отверстіе, сдѣланное посреди пластинки,
и затѣмъ черезъ проволоку пропустить сильный электрическій токъ.
Если пластинка толстая, то послѣдній способъ нагрѣванія, а также
способъ 8 ё п а г ш о п Г а даютъ контуръ яйцевидный, а не эллиптическій.
Это объясняется тѣмъ, что нагрѣваніе исходитъ не изъ одной точки, но
изъ всѣхъ точекъ отрѣзка прямой; въ этомъ случаѣ изотермическая по-
верхность уже не будетъ эллипсоидомъ.
ѴопЬап^, Л^іппеіаг, Раре, Туіійаіі, Воепіуеп и др.
изслѣдовали большое число различныхъ кристалловъ. Оказалось, что въ
кристаллахъ правильной системы изотермическая поверхность есть шаръ;
въ одноосныхъ кристаллахъ она дѣйствительно является эллипсоидомъ
вращенія, причемъ ось вращенія всегда совпадаетъ съ оптическою осью
кристалла (т. II). Этотъ эллипсоидъ можетъ быть продолговатымъ или
сплюснутымъ, совершенно какъ волновая поверхность для необыкновен-
наго луча. Вь большинствѣ случаевъ, но не всегда, характеръ эллипсои-
довъ термическаго и оптическаго одинаковый, т.-е. оба продолговаты
Анизотропныя тѣла.
329
или оба сплюснуты. Но бываютъ исключенія; такъ напр. известковый
шпатъ и бериллъ имѣютъ продолговатые эллипсоиды термическіе и
сплюснутые оптическіе; для корунда имѣетъ мѣсто обратное. Это зна-
читъ, что направленію наибольшей скорости распространенія тепла
соотвѣтствуетъ направленіе наименьшей скорости необыкновеннаго луча
и наоборотъ.
Способъ 8 ё п а г пі о п Га даетъ возможность опредѣлить отношеніе
скоростей распространенія тепла въ различныхъ направленіяхъ внутри
кристалла. Опредѣленія абсолютнаго значенія величины к для кристал-
ловъ производили ТисЬвсЬтісІі и Ьеез. Тпсйьсіітіді пользо-
вался способомъ Н. Г. ДѴ е Ъ е г’а (см. ниже теплопроводность жидкостей).
< >нъ нашелъ слѣдующія числа :
Кварцъ. Известковый шпатъ.
к к
|| оси 0,02627 0,00960 гр.
Подъ угл. въ 45° съ Осью 0,02120 0.00863 „„ ~ ѵ&.ѵѵІЬ
1 къ оси 0,01597 0,00787.
Для каменной соли к = 0,01 по всѣмъ направленіямъ. Ь е е 8 поль-
зовался способомъ Ъ о д § е’а, упомянутымъ на стр. 325. Онъ нашелъ для
каменной соли к = 0,0133; далѣе:
II оси
л_ оси
Кварцъ.
0,0299
0,0158
Известковый шпатъ.
0,0100
0,0084 см.сек.
гр.
Приводимъ для нѣкоторыхъ одноосныхъ кристалловъ отношеніе
кг • && гдѣ к^ относится къ направленію вдоль оси, к2 — перпендику-
лярно къ оси:
ЗУ ЗУ ІО
Графитъ . . около 4 Доломитъ . . 1,10
Сурьма . . . . 2,56 Турмалинъ . . 1,35
Інатазъ . . 1,80 Кварцъ . . 0,58
Теллуръ. . . 0,66 Смарагдъ . . 0,81
Киноварь . . . 0,72 Идокразъ . . 0,90
Для кристаллическаго висмута нашли одновременно:
Ьолѵпйб (1903)
1 = 0,704
к2
Реггоі (1903) К = о 745
к2
йае^ег (1906) нашелъ значительно меньшее число 0,671.
ЛѴ. Ѵоі^і далъ (1897) остроумный способъ измѣренія отношенія
теплопроводностей къ к2 и к3 вгь кристаллѣ», заключающійся въ слѣдую-
330
Теплопроводность.
темъ (этотъ методъ существенно одинаковъ съ методомъ изслѣдованія
изотермъ, разсмотрѣннымъ на стр. 310). Вырѣжемъ изъ кристалла пла-
стинку параллельно одной изъ трехъ плоскостей, содержащихъ двѣ изъ
трехъ осей эллипсоида, и положимъ, что стороны прямоугольной пла-
стинки составляютъ углы въ 45° съ направленіями этихъ осей хх, уу
рис. 100 слѣва), которымъ соотвѣтствуютъ напр. значенія к± и к2, Раз-
рѣжемъ пластинку по направленію перевернемъ одну половину и
склеимъ обѣ половины такъ, какъ показано на рис. 100 справа. Покроемъ
пластинку тонкимъ слоемъ легкоплавкаго вещества; V о і і совѣтуетъ,
какъ уже было сказано выше, пользоваться элаидиновои кислотой (Еіаі-
йіпваиге) съ примѣсью 0,1 — 0,5 воска и скипидара. Если нагрѣвать
пластинку со стороны а, то по причинамъ симметріи прямая сф во
всякомъ случаѣ представитъ направленіе теплового потока, идущаго отъ
точки а къ точкѣ /9. Изотермы, какъ мы видѣли (стр. 327), составля-
ютъ съ потокомъ уголъ не равный 90°, а потому на нашей пластинкѣ
изотермы представятся въ видѣ линій, имѣющихъ переломы въ точкахъ
прямой аД, какъ показано на рис. 101. Если уголъ между касательными
въ этихъ точкахъ обозначить черезъ (/\ то
1 +
1
</
2
Ч ’
2
гдѣ два знака относятся къ двумъ случаямъ к2 > к} и к2 < кі. Уголъ (/
легко измѣряется, такъ какъ изотермы (предѣлъ расплавившагося слоя)
весьма рѣзко замѣтны. Для кварцевой пластинки, вырѣзанной парал-
лельно оси, уголъ д около 30°. Неодинаковое к въ различныхъ напра-
вленіяхъ наблюдается не только у кристалловъ, но и въ сжатомъ стеклѣ
(8 ё п а г пі о п і), въ некристаллическихъ минералахъ, имѣющихъ и лосю >-
стп спайности, и въ особенности въ деревѣ, которое представляетъ тѣло
неоднородно-анизотропное.
Опыты Ие Іа Еіѵе’а и Ое С а пйоііе'я, ТупйаІГя, КпоЪ-
Іаисіі’а, ГогЬез’а, Ьев«’а, (тгеівв’а, В. Лхгинина и др., про-
изведенные частью по способу бёпагшопі’а, частью по способу Віоі-
Вевргеіг (стр. 311), показали, что к наибольшее по направленію во-
Жидкости.
331
локонъ дерева, наименьшее перпендикулярно къ волокнамъ, причемъ слѣ-
дуетъ отличать направленія по радіусу поперечнаго сѣченія ствола де-
рева и перпендикулярно къ радіусу. Такъ напр. Ье8 8 находитъ, пола-
гая для мрамора к = 100 (приблизительно к = 0,0018 С. О. 8. по Е о г Ь е з’у):
|| волокнамъ . .........
» || радіусу .
_1_ » Д_ »
Кленъ. Дубъ.
19,2 16,1
8,6 7,5
8,5 8.6.
ЕогЬез нашелъ для сосны || волокнамъ к =0.00030 С. О. 5., д_ къ
волокнамъ к = 0.000088 С. О. 8. В. Л у г и н и н ъ изслѣдовалъ ходъ тем-
пературы внутри деревьевъ втеченіе года.
§ 7. Теплопроводность жидкостей. Изслѣдованіе теплопроводно-
сти жидкостей представляетъ особыя затрудненія вслѣдствіе ихъ удобо-
подвпжности, вызывающей конвекцію тепла болѣе теплыми частями жид-
кости, поднимающимися наверхъ. Поэтому теплопроводность жидкостей
можетъ быть изслѣдована только путемъ нагрѣванія жидкости сверху или
ея охлажденія снизу, она во всякомъ случаѣ весьма мала, что доказы-
вается напр. слѣдующимъ опытомъ. Въ пробирный стаканчикъ налива-
ютъ холодную воду и кладутъ въ нее касочекъ льда, обернутый прово-
локой, чтобы онъ оставался на днѣ стаканчика. Нагрѣвая воду въ верх-
ней части стаканчика, можно ее довести до кипѣнія безъ того, чтобы
ледъ растаялъ.
Изслѣдованія теплопроводности жидкостей были главнымъ образомъ
произведены по двумъ существенно различнымъ методамъ. Въ первомъ
изъ нихъ подвергается нагрѣванію сверху или охлажденію снизу жид-
кій вертикальный столбъ, стаціонарная пли перемѣнная тем-
пература котораго изслѣдуется въ различныхъ горизонтальныхъ слояхъ.
Во второмъ методѣ жидкость помѣщается въ видѣ тонкаго слоя между
двумя горизонтальными металлическими пластинками, температуры кото-
рыхъ наблюдаются ; это методъ жидкаго слоя или ж и д к о й п л е н к и
(ЬатеІІепшеНіосІе). Кромѣ того существуютъ еще особые методы \Ѵіп-
кеішапп’а и бгаеіг’а.
I. М е т о д ъ жидкаго столба. Первые опыты были произве-
дены по методу жидкаго столба. Кит іо г(1 вывелъ изъ своихъ наблю-
деній, что вода вовсе не обладаетъ теплопроводностью. Однако позднѣй-
шіе опыты Ы і с йоізоп’а, Ми г г ау, Ріскеі, Т. Тйопізоп’а и др.
доказали существованіе внутренней передачи тепла въ вертикальномъ
жидкомъ столбѣ, нагрѣваемомъ сверху. Первые болѣе точные опыты
произвелъ Юейргеіг, стараясь примѣнять къ жидкостямъ свой ме-
тодъ, разсмотрѣнный выше (стр. 314). Въ деревянный цилиндрическій
сосудъ наливалась вода и въ него вставлялся мѣдный сосудъ, дно кото-
раго касалось поверхности воды. Въ этотъ сосудъ наливалась горячая
вода, которая возобновлялась черезъ каждыя 5 минута. Шесть горизон-
тальныхъ термометровъ были вставлены въ боковд ю стѣнку цилиндра,
332
Теплопроводность.
такъ что ихъ резервуары лежали на оси цилиндра. Стаціонарное состо-
яніе устанавливалось черезъ 36 часовъ. Оказалось, что температура мо-
жетъ быть выражена формулою / = Ае~ах, гдѣ х вертикальная коорди-
ната слоя. РааІ2о\ѵ воспользовался тѣмъ же методомъ, но онъ опре-
дѣлялъ величину 2п — (рг + : 02, см. (36,а), ограничиваясь распредѣ-
леніемъ жидкостей въ рядъ по у бывающимъ теплопроводностямъ. Воі-
іотіеу наливалъ горячую воду непосредственно на деревянную до-
щечку, плававшую на поверхности водяного столба. Недостатокъ ме-
тода Иезргеіг и его послѣдователей заключается между прочимъ въ
томъ, что деревянная стѣнка цилиндра также проводить теплоту къ ниже
лежащимъ слоямъ жидкаго столба, такъ что наблюдаемое нагрѣваніе не
вызывается одною теплопроводностью жидкости. Спеціально методъ
Воііотіеу'я содержитъ еще иные источники погрѣшностей; поэтому
неудивительно, что онъ для воды находитъ к = 0.0002 С. О. 5., между
тѣмъ какъ вѣрное число должно быть примѣрно въ 6 разъ больше.
Опыты СЪ г ее, опредѣлявшаго температуру различныхъ слоевъ жид-
каго столба при помощи платиновой проволоки, электрическое сопро-
тивленіе которой измѣрялось, дали также мало между собою соглас-
ные результаты; однако среднее изъ его опредѣленій, а именно к —
= 0,00124 С. О. 8. для воды при 18°, слѣдуетъ признать вѣроятно до-
вольно близкимъ къ истинѣ.
А п § 8 і г о е ш опредѣлялъ к для ртути, пользуясь своимъ спосо-
бомъ періодическаго нагрѣванія и охлажденія, который былъ описанъ на
стр. 321; ртуть наполняла стеклянную вертикальную трубку, діаметромъ
въ 37,6 мм. Ап^ьѣгоет находитъ при 50° для ртути к=0,0177С. 0.8.
Ьипсіциізі, пользуясь тѣмъ же методомъ, впервые (1869) далъ надеж-
ныя числовыя значенія величины к для различныхъ жидкостей; онъ
также помѣщалъ жидкости въ вертикальныя стеклянныя трубки.
Н. Р. \Ѵ е Ь е г вывелъ изъ наблюденій Ь и п (1 ц и і 8 і’а нѣсколько
другія числа для раствора 2.п8О±, вводя болѣе точное числовое значеніе
теплоемкости этого раствора. Такъ для раствора, плотность котораго 1,382,
онъ находитъ к = 0.001437.
Теплопроводность р ту т и опредѣлялъ В е г е 1 по способу <охран-
наго цилиндра », о которомъ уже было упомянуто на стр. 319. Его приборъ изо-
браженъ на рис. 102. Онъ представляетъ собою ледяной калориметръ Впп-
8еп’а (стр. 169), резервуаръ котораго удлиненъ въ видѣ трубки АВ; длина
трубки, считая отъ Л, равняется 20 см., діаметръ 1,3 см. Трубка проходитъ че-
резъ горизонтальную желѣзную пластинку, подъ которой находится ледъ, ок-
ружающій и самый сосудъ калориметра. Стеклянная трубка АВ окружена бо-
лѣе широкой (діаметръ 6 см.) и нѣсколько болѣе высокой трубкой, содержащей,
какъ и АВ, ртуть. Эта трубка покрыта крышкой, черезъ которую проходятъ
три трубки: черезъ двѣ изъ нихъ вступаютъ, а черезъ третью выводятся
наружу пары кипящей воды. Четыре горизонтальныя желѣзныя прово-
локи 1, 2, 3, 4 проникаютъ до середины трубки АВ; онѣ изолированы
Жидкости.
333
тродвижущая сила котораго
Рис. 102.
КС
и только ихъ концы (въ АВ) оставлены непокрытыми. Каждая пара
проволокъ даетъ вмѣстѣ со ртутью термоэлектрическій элементъ, элек-
служитъ для измѣренія разности тем-
пературъ двухъ точекъ. Предваритель-
ными опытами В е г § е 1 убѣдился, что
всѣ точки горизонтальнаго слоя въ трубкѣ
АВ имѣютъ одну и ту же температуру.
Когда было достигнуто стаціонарное те-
пловое состояніе, онъ измѣрялъ количе-
ство С} теплоты, которое передавалось ка-
лориметру въ единицу времени, наблю-
дая перемѣщеніе конца ртутнаго столбика
въ тонкой горизонтальной трубкѣ, какъ
было объяснено на стр. 170. По формулѣ
п_к8(і1 -/2)
а
гдѣ х площадь поперечнаго сѣченія трубки
АВ, іг — разность температуръ двухъ
ея точекъ, находящихся на разстояніи сі
другъ отъ друга, вычислялась величина к.
Для средней температуры 50° всего столба,
Вег^еі получилъ 6 = 0,02015. Величина ф одна и та же во всѣхъ
сѣченіяхъ трубки АВ. Измѣряя въ различныхъ отрѣзкахъ этой
трубки, В е г е і могъ найти зависимость к оть температуры. Оказа-
лось, что въ формулѣ 6 = 60(1с^), температурный коеффиціентъ а =
= 0,001267. Между 0° и 300° онъ нашелъ а = 0,00045. Такимъ
образомъ оказывается, что теплопроводность ртути у м е н ь ш а е т с я
съ повышеніемъ температуры.
В е г е 1 опредѣлилъ к для ртути еще другимъ способомъ: ртут-
ный столбъ АВ былъ укороченъ и расширенъ, а количество передан-
ной теплоты измѣрялось уменьшеніемъ вѣса ледяного цилиндра, который
снизу касался желѣзной пластинки, служившей основаніемъ ртутнаго
столба. Этотъ способъ далъ к = 0,02001. Трудно сказать, были ли въ
опытахъ В е г е 1 устранены вертикальныя теченія ртути въ трубкѣ АВ.
Опыты \Ѵас ІізпіиіЬ’а показалц, что такія теченія несомнѣнно суще-
ствуютъ въ столбахъ менѣе плотныхъ жидкостей, нагрѣваемыхъ сверху.
ЛѴас1і8ти11і пользовался окрашенными жидкостями, которыя при на-
грѣваніи обезцвѣчиваются, напр. слабымъ растворомъ іодистаго крахмала,
синій цвѣтъ котораго исчезаетъ при температурѣ между 30° и 70°, зави-
сящей отъ концентраціи раствора. При нагрѣваніи жидкости сверху ясно
обнаруживалось образованіе вихревыхъ движеній, въ которыхъ болѣе хо-
лодная жидкость поднималась, болѣе теплая опускалась. Эти движенія
не прекращались, когда жидкій столбъ окружался охраннымъ цилин-
334
Теплопроводность.
дромъ по способу Вег^еі. Опыты АѴасйбиіиіІГа заставляютъ во-
обще отказаться отъ способа жидкаго столба.
II. Методъ жидкой пленки. Сгпііітіе первый воспользо-
вался этимъ способомъ, помѣстивъ слой жидкости между обращенными
Другъ къ другу горизонтальными основаніями двухъ полыхъ конусовъ.
Черезъ верхній конусъ пропускалась струя пара, между тѣмъ какъ ниж-
ній, обращенный вершиною внизъ, и снабженный водянымъ манометромъ,
служилъ воздушнымъ термометромъ. (Іиііігіе сравнивалъ нагрѣваніе
воздуха въ случаѣ, когда основанія конусовъ касались другъ друга, и
когда между нпми находился слой жидкости. Онъ нашелъ, что глице-
ринъ проводитъ теплоту въ 3.84 раза, алкоголь въ 10 разъ и хлороформъ
въ 12 разъ хуже, чѣмъ вода, и что растворы солей лучше проводятъ
теплоту, чѣмъ вода. 'Весьма точное опредѣленіе величины к и ея темпе-
ратурнаго коеффиціента было произведено Ьеез’омъ (1898І для нѣсколь-
кихъ жидкостей. Онт> нашелъ такія числа:
к (С. 0.5.) а (между 25° и 45°)
Вода <11°) ..... . 0,00147 - 0.0055
Метиловыя алкоголь (11°) . 0,00052 0,0034
Этиловый алкоголь (11°) . 0,00046 —0,0058
Глицеринъ (20°) .... 0,00070 - 0,0044
Уксусная кислота (11°). . 0,00043 —
Методъ жидкой пленки былъ развить Н. Е. АѴ е Ъ е г’омъ. Двѣ
мѣдныя круглыя пластинки помѣщены горизонтально одна надъ другой,
въ разстояніи нѣсколькихъ миллиметровъ другъ отъ друга. Промежутокъ
наполнялся испытуемой жидкостью, которая держалась въ немъ капил-
лярными силами. Вся система опускалась на горизонтальную поверх-
ность большого куска льда; постепенное измѣненіе температуры верхней
пластинки измѣрялось термоэлектрпческимъ столбикомъ. Эти измѣренія
даютъ возможность вычислить к для промежуточной жидкой пленки.
ЬіОгЬег^ показалъ однако, что формула, которою при этомъ пользо-
вался Н. В. АѴ е Ь е г, должна быть замѣнена болѣе сложною, и что по-
этому и числовые результаты, данные АѴеЬег’омъ, должны быть измѣ-
нены. Такъ, напр. АѴеЬег находитъ для воды, полагая к = к0(1 -ф- а^),
к = 0,00120 а = 0,00786.
между тѣмъ какъ по вычисленіямъ ЬотЬег§э’а изъ наблюденій АѴе-
Ьег’а получается
к = 0,000138 а — 0,00494.
Поэтому остается сомнительнымъ и законъ, найденный АѴеЬег’омъ:
величина к: бс, гдѣ б удѣльный вѣсъ и с теплоемкость единицы объ-
ема жидкости, имѣетъ для всѣхъ жидкостей приблизительно одно и то
же значеніе. Въ позднѣйшей работѣ (1885) АѴеЬег разобралъ теорети-
ческое значеніе своего закона и подтвердилъ его на 46 жидкостяхъ.
Жидкости.
335
Между прочимъ ЛѴеЬег приходитъ къ результату, что теплопровод-
ность жидкостей не должна зависѣть отъ ихъ внутренняго тренія. Этотъ
результатъ былъ подтвержденъ ЛѴасІізтиіЬ’омъ, который для чистой
воды при 4°,1 находитъ к — 0,00129, а для воды, содержащей 1% жела-
тины, достаточной для ея застыванія, въ двухъ опытахъ к = 0,00131 и
к = 0.00128, т.-е. такое же число, какъ и для чистой воды. Для 5% ра-
створа получается уже к = 0,00116.
Въ 1893 г. Н. Р. ЛѴеЬег измѣнилъ свою формулу; онъ нашелъ,
что величина
к _3 т ~ ,
I = е = Соп8і.
ос I с
Здѣсь т молекулярный вѣсъ жидкости. Ѵап АиЬеІ показалъ, что этотъ
законъ не подтверждается числами, данными Ьееа’оыъ для чистыхъ
жидкостей (вода, глицеринъ, уксусная кислота) и для ихъ смѣсей.
І)е Нееп нѣсколько измѣнилъ способъ \ѴеЬег’а: онъ взялъ бо-
лѣе толстыя мѣдныя пластинки и измѣрялъ при помощи трехъ термоэле-
Рис. 103.
ментовъ паденіе температуры въ нижней пластинкѣ и температуру верх-
ней. Дальнѣйшее видоизмѣненіе представляетъ уже упомянутый выше
методъ Сіігізііапзеп’а, употреблявшаго, вмѣсто двухъ, три мѣдныя
пластинки (радіусъ 13,14 см., толщина 9 мм.), отдѣленныя другъ отъ
друга маленькими кусочками стекла. Вся система ставится на мѣдный
сосудъ А (рис. 103), черезъ который протекаетъ холодная вода, а на
верхнюю пластинку ставится такой же сосудч, В съ протекающей черезъ
него теплой водой. Три ртутные термометра, вставленные сбоку въ
мѣдныя пластинки, служатъ для опредѣленія ихъ температуръ іъ і2 и 4-
Въ промежуткахъ между пластинками помѣщаются слои тѣхъ двухъ ве-
ществъ, теплопроводности к± и к2 которыхъ желаютъ сравнить. Если
и (12 толщины этихъ слоевъ, то очевидно
ь ^1 4 ___ и
а, а2 '
откуда
/?] (Аі Аз!
СІ2 (^ — Л2)
336
Жидкости,
Болѣе точная формула выведена Сйгібііапбеп’омъ и АѴіпкеІ-
пі а пп’омъ. В. В. Станкевичъ изслѣдовалъ теплопроводность боль-
итого числа органическихъ жидкостей по способу С1ігІ8ііап8е п’а.
НеппеЬег^ сравнивалъ по тому же способу теплопроводности к смѣ-
сей воды и алкоголя и нашелъ для нихъ к меньше, чѣмъ для воды, и
больше, чѣмъ для алкоголя. Его опыты не подтверждаютъ закона АѴ е -
Ьег’а. йае^ег сравнивалъ по тому же способу теплопроводности со-
ляныхъ растворовъ съ теплопроводностью стекла, заполнявшаго одинъ
изъ промежутковъ. Для измѣренія температуръ онъ пользовался термоэле-
ментами. Его опыты, показавшіе, что для растворовъ солей к меньше, чѣмъ
для чистой воды, подтверждаютъ законъ АѴеЬег’а. АѴасйзтиІІі
производилъ опыты по способу Н. Г. АѴ е Ь е г’а. Ею числа указыва-
ютъ на отсутствіе связи между к и внутреннимъ треніемъ въ жидкостяхъ.
Существуетъ множество видоизмѣненій способа жидкой пленки. Такъ
АѴасЬзпіиіІі (1901) помѣщаетъ жидкость между двумя параллельными
мѣдными пластинками, изъ которыхъ верхняя нагрѣвается потокомъ воды,
а нижняя находится на кускѣ льда. Количество теплоты <2, прошедшее
въ единицу времени черезъ жидкость, измѣряется количествомъ раста-
явшаго льда и к вычисляется изъ формулы
/= = .-0
-------- ^2 5
гдѣ (1 толщина жидкой пленки, 5 ея поверхность, і± и температуры
обѣихъ мѣдныхъ пластинокъ. АѴ а с й 8 ш и 111 показалъ, что примѣнені-
емъ его метода можно одновременно опредѣлять вмѣстѣ съ к также и
удѣльную электрическую проводимость Л. По этому- методу Егііг КоЬ1 -
гаизсіі (1904) опредѣлилъ величины к и Я для воды и растворовъ КСк
Н^ВО^ и трихлору ксусной кислоты (ССІ^СООН). Онъ нашелъ, что к и
Я уменьшаются съ уменьшеніемъ концентраціи и что для различныхъ
растворовъ большему Я соотвѣтствуетъ также большее к.
Интереснымъ способомъ пользовались Мііпег и СЬаіІоск,
мѣняя толщину пленки, такъ что по вышеупомянутой формулѣ можно
было вычислить к изъ двухъ наблюденій, есла извѣстна были раз-
ность сі! —
В. АѴеЪег (1903) нагрѣвалъ жидкость сверху при помощи сосуда,
содержавшаго жидкій нараффинъ, въ которомъ находилась катушка изъ
никелиновой проволоки, черезъ которую пропускался электрическій токъ.
Подъ жидкостью находился тающій ледъ. Внутри жидкости помѣщались
одинъ надъ другимъ спаи термоэлемента, который указывалъ величину
4 — 4- С вычислялось по силѣ тока и разности потенціаловъ по за-
кону" Джуля (т. IV). В. АѴеЪег нашелъ для к слѣдующія значенія
въ С. 0.8, единицахъ:
к к
Вода .... 0,00131 Глицеринъ . . 0,000656
Керосинъ . . 0,000382 Ртуть.... 0,0197
Жидкости.
337
ПІ. Способы АА’іпкеІтапп’а и Сггаеіг’а. АѴіпкеІтапп
помѣстилъ жидкость въ промежутокъ между двумя концентрическими мѣд-
ными цилиндрами. Наружный цилиндръ окружался смѣсью льда и воды,
причемъ кольцеобразная мѣшалка, снабженная щетками, непрерывно об-
тирала поверхность цилиндра, подобно тому, какъ въ опытахъ РесІеЬ
(стр. 310). Внутренній цилиндръ наполненъ воздухомъ; отъ его крышки
идетъ трубка, два раза изогнутая подъ прямымъ угломъ (вверхъ, гори-
зонтально, внизъ) и погруженная нижнимъ концомъ въ ртуть, поднимаю-
щуюся вверхъ при постепенномъ охлажденіи воздуха. Наблюденія ско-
рости этого охлажденія даютъ возможность вычислить к для взятой жид-
кости. АѴ іпк еі т а п п пользовался тремя аппаратами, въ которыхъ тол-
щина (I жидкаго слоя равнялась 0.205 мм., 0,259 и 0,495 мм. Оказалось,
что значенія для к зависятъ отъ (1; для воды были получены числа
к = 0,001040, к = 0,001161 и к — 0,001416. Очевидно, что при этомъ спо-
собѣ теченія внутри жидкости не были вполнѣ устранены.
Эта работа вызвала полемику между АѴ іпкеішапп’омъ. Н.В.АѴе-
Ьег’омь и ОЪ егЪ ес к’омъ. Вееіг пользовался аналогичнымъ спосо-
бомъ ; но и эта работа вызвала довольно рѣзкую критику со стороны
Н. Р. АѴ е Ъ е г’а. Совершенно оригинальнымъ способомъ пользовался
Огаеіг. Жидкость, начальная температура которой протекаетъ че-
резъ длинную, тонкую металлическую трубку, погруженную въ воду, тем-
пература которой меньше іѵ, Измѣряется температура 4, до которой
жидкость охладилась, пройдя черезъ трубку. Сложная формула
а2
к 2ІГ, /
4 I
4 4 /
которую мы не выводимъ, даетъ искомое к. Въ этой формулѣ <5 плот-
ность, с теплоемкость жидкости. Ѵ7 объемъ жидкости, протекающей въ
секунду, / длина трубки въ см., р и р двѣ постоянныя, равныя ^ = 2,7043,
/7 = 0,81747. бгаеѣх изслѣдовалъ нѣкоторые растворы, глицеринъ, ал-
коголь, эфиръ, керосинъ, терпентинное масло и сѣроуглеродъ.
II. Слуги но въ указалъ на способъ опредѣленія отношенія вели-
чинъ к для даннаго вещества въ жидкомъ и твердомъ состояніяхъ.
Ѳ. Ѳ. Петрушевскій далъ способъ сравненія величинъ к для
жидкихъ и твердыхъ тѣлъ, основанный на наблюденіи увеличенія длины
стержня или объема жидкости, налитой въ стеклянный цилиндръ, если
стержень или жидкій столбъ нагрѣваются съ одного конца.
Въ заключеніе этой статьи упомянемъ, что а е е г пытался дать
кинетическую теорію теплопроводности жидкостей, аналогичную кинети-
ческой теоріи теплопроводности газовъ, созданной Сіаизіиз’омъ и упо-
мянутой ниже. Приведемъ одинъ изъ результатовъ теоріи Я а е е г’а.
Живую силу молекулы гдѣ т масса, ѵ скорость, можно написать,,
какъ функцію температуры въ видѣ
4 тѵ2 = у тд/02(1 + уі).
КУРСЪ ФИЗИКИ О ХВОЛЬСОНА. Т. Ш, изд. 3-е.
22
338
Теплопроводность.
Пусть і/ коеффиціентъ внутренняго тренія (т. П; теорія .Іае^ега
приводитъ къ формулѣ
Правая сторона можетъ имѣть весьма различныя значенія для раз-
личныхъ жидкостей, чѣмъ и объясняется отсутствіе простой связи между
к и ?/. Величина ГЦЛ равная увеличенію кинетической энергіи единицы
массы при нагрѣваніи на 1°, очевидно меньше теплоемкости с. ^Поэтому
мы должны имѣть для всѣхъ жидкостей
< с.
Л
Это соотношеніе подтверждается, какъ видно изъ слѣдующей таблички :
Вода . ... . 0,000124 0,0130 0,095 1,000
Алкоголь . . . 0,000487 0,0153 0,032 0,566
Эфиръ . . . . 0,000405 0,0026 0,156 0,520
Хлороформъ . . 0,000367 0.0065 0,056 0,233
Для нормальныхъ растворовъ въ водѣ Р г і Ь 2 КоМгаизсЬ нашелъ
к
КСІ.................0,00177
ССІ^СООН .... 0,00194
Н?ВО3...............0.00110.
Въ вид\ интереса, который пре вставляетъ теплопроводность воды,
мы сопоставимъ числа (въ С. О. 8. единицахъ), найденныя различными
учеными:
Ьипдциіві (1869) 0,00156 при 40,8°
АѴіпкеітапп (1874). . . . 0,00154 « 14°
Н. Г. ЛѴеЬег (1880) . . . . 0,00143 « 23,6°
— — — — — — 0,00124 « 4,1°
Сггаеіг (1885) п,00157 « 30°
СЬгее (1887) 0,00124 « 18°
Ьеев (1898) 0,00147 « 11°
Мііпег и СЬаіІоск (1899) . 0,00143 « 20»
В. \ѴеЬег (1903) 0,00131 « 20°
§ 8. Теплопроводность газовъ. Вопросъ о теплопроводности га-
зовъ былъ подвергнутъ не только экспериментальному, но и весьма глу-
бокому теоретическому изслѣдованію. Переходъ теплоты отъ болѣе теп-
гаго газоваго слоя къ сосѣднему съ нимъ, болѣе холодному, является ре-
зультатомъ перехода молекулъ, движущихся въ этихъ дв^хъ слояхъ съ
неодинаковою среднею живою силою, изъ одного слоя въ другой,
Газы.
339
вслѣдствіе чего средняя живая сила, а слѣд. и температура болѣе холод-
наго слоя должна возрастать, а болѣе теплаго — убывать. При устано-
вившемся стаціонарномъ тепловомъ состояніи убыль покрывается прито-
комъ энергіи изъ предыдущаго еще болѣе теплаго слоя, а притекшая энер-
гія передается слѣдующему слою, еще болѣе холодному. Теоретическій
разборъ вопроса, весьма сложный, принадлежитъ С1. МахлѵеІГу, Сіаи-
8іп8’у, ВоШшапп’у, ЗіеГап'у, Ѵоп Ьап^’у, О. Е. Меуег’у,
В и г Ь и г у и др.
Всѣ теоріи приводятъ къ том\ замѣчательному результату, что теп-
лопроводность газовъ не зависитъ отъ икъ упругости,
что слѣд. к не мѣняемся при разрѣженіи газовъ. На этотъ законъ намъ
уже приходилось указывать (стр. 278). Вамо собой разумѣется, что при
нѣкоторой, очень высокой степени разрѣженія этотъ законъ долженъ пере-
стать быть вѣрнымъ, какъ и аналогичные законы о независимости вну-
тренняго тренія и скорости звука въ газахъ отъ ихъ упругости (т. [ и
г. II). Теоретическіе выводы основаны на допущеніи, что число газо-
выхъ частицъ въ данномъ объемѣ весьма велико; это допущеніе даетъ
возможность пользоваться интегральнымъ исчисленіемъ. Вмѣстѣ съ этимъ
допущеніемъ перестаютъ быть вѣрными и основанные на немъ выводы.
Независимость теплопроводности к газовъ отъ ихъ упругости вы-
ясняется тѣмъ, что при уменьшенной въ п разъ упругости число частицъ,
переходящихъ изъ одного слоя въ сосѣдній, уменьшается въ п разъ; но
въ то же время средняя длина ихъ пути (т. I) увеличивается въ п разъ,
частицы проникаютъ въ п разъ глубже изъ одного слоя въ сосѣдній, а
потому полное количество перемѣстившейся энергіи остается такимъ же,
какимъ оно было до уменьшенія упругости. Любопытные опыты Сгоо-
к е 8’а подтверждаютъ этотъ результатъ теоріи. Шарикъ термометра, окру-
женный стеклянной оболочкой, изъ которой можно было выкачать воз-
духъ, имѣлъ температуру 25°. Онъ опускался въ воду, нагрѣтую до 65°;
затѣмъ опредѣлялось при различныхъ упругостяхъ р воздуха, остававша-
гося въ оболочкѣ, то время втеченіе котораго термометръ поднимался
до 60°. С г о о к е 8 нашелъ слѣдующія числа (Л] = одной миліонной
долѣ атмосферы):
Р і Р і
760 мм. 121 сек. 23 М. 227 сек.
1 » 150 » 12 » 252 >
620 Ѵ[. 161 » 5 » 322 »
117 » 183 » 2 » 412 »
59 » 203 »
При большихъ р играла роль конвекція. Подобные опыты произво-
дили Воііотіеу (азутіоііс ехретітепів) и, еще раньше, КипН и
ЛѴ а г Ь и г , которые прямому называютъ на наблюденіе скорости охла-
жденія термометра, какъ на весьма чувствительный способъ опредѣленія
степени разрѣженія газа. Теорія указываетъ далѣе на замѣчательную
22*
340
Теплопроводность.
связь между коэффиціентами к теплопроводности и // внутренняго тренія
газовъ. Эта связь выражается формулою
к = ѳі]Сѵ....................... (54)
гдѣ сѵ теплоемкость газа при постоянномъ объемѣ, е численный коеффи-
ціентъ, для котораго вышеназванные авторы выводятъ различныя зна-
ченія. С1 а и 8 і п 8 находитъ
8= 1,25 .........................(55)
Махмгеіі находитъ въ первой работѣ по этому предмету е = 1,5.
Позже Махлѵеіі создалъ другую теорію, допуская, что молекулы газа
отталкиваются съ силою, обратно пропорціона льнстю пятой степени ихъ
взаимнаго разстоянія; В о 11 г т а п п показалъ, что эта теорія приводитъ
КЪЧИСЛУ е = 2,5.......................(55, а)
О. Е. Меуег далъ для е очень сложное выраженіе, которое вычислили
Сопгаи и Иеи^еЬаиег; они нашли
е = 1,6027 .................. . (55,й)
Ниже мы увидимъ, къ какому значенію для е привели опытныя изслѣ-
дованія. Въ т. 1 была приведена формула
1
= птІЛІ.
3
Здѣсь п число молекулъ въ единицѣ объема, т масса одной моле-
кулы, А средняя длина пути и й средняя скорость движенія. Если это
выраженіе вставить въ (54), то получается
к = ЕптІЛіс.,.
3
Если бы к и е были точно извѣстны, то отсюда можно было бы вы-
числить среднюю длину пути А.
Зависимость теплопроводности к газовъ отъ температуры і также
опредѣляется формулою (54). Для тѣхъ газовъ, для которыхъ сѵ = Соп8І.,
т.-е. сѵ отъ і не зависитъ, мы должны имѣть одинаковую для к и за-
висимость отъ і. Теорія С1а8Іп.8’а показываетъ, что должно расти
пропорціонально корню изъ абсолютной температуры или корню изъ дву-
члена 1 аЛ гдѣ а = 0,00366. Итакъ для случая сѵ = Сопеѣ. мы должны
имѣть г______
к — к^Ѵ\.-\-аі.......................(5б)
или, если положить к — к^І + /?/").......................(57)
то @ = 0,00183 ......................... (58)
Теорія М а х лѵ е 1 Гя приводитъ къ совсѣмъ другому результату:
ѣ
к = ^,(1 + аі) = Т
273
а = 0,00365
(58,а)
Газы.
341
Отсюда слѣдуетъ, что для газовъ к должно быть пропор-
ціонально абсолютной температурѣ. Во всякомъ случаѣ
теплопроводность газовъ должна расти съ повышеніемъ температуры и
притомъ быстрѣе для газовъ, для которыхъ сѵ увеличивается съ темпе-
ратурой, чѣмъ для газовъ, для которыхъ сѵ отъ температуры не зависитъ.
Мы увидимъ ниже, насколько результаты опытныхъ изслѣдованій согласны
съ предсказаніями теоріи.
Переходимъ къ этимъ изслѣдованіямъ, вообще показавшимъ, что
газы принадлежатъ къ весьма дурнымъ проводникамъ теплоты.
Объ этомъ даетъ ясное представленіе слѣдующая сравнительная табличка
коеффиціентовъ к для нѣкоторыхъ тѣлъ (въ С. О. 5. единицахъ):
к
к
Серебро . . 1,00000
Ртуть. . . 0,02000
(/текло . 0,00170
Фланель. . 0,00004
к
Вода . . . 0,00130
Глицеринъ. 0,00066
, Алкоголь . 0,00049
] Эфиръ . . 0,00040
Водородъ .
Воздухъ . .
Пары |
(203°) |
0,00040
0,00005
0,000018
Итакъ, воздухъ
проводитъ въ 20000 разъ
хуже серебра, въ 400
разъ хуже ртути и въ 26 разъ хуже воды,
проводимость слоистыхъ веществъ, каковы
изготовленіе одежды, перья и т. под. Опытъ,
доказывающій неодинаковую теплопровод-
ность различныхъ газовъ, былъ сдѣланъ Ап-
сігелѵв’омъ, показавшимъ, что платиновая про-
волока сильнѣе накаливается отъ дѣйствія
электрическаго тока, когда она находится въ
кислородѣ, азотѣ и углекисломъ газѣ, чѣмъ
Этимъ объясняется дурная
мѣха, матерія, идущая на
Рис. 104.
когда она находится въ водородѣ. О г о ѵ е видоизмѣнилъ этотъ опытъ
слѣдующимъ образомъ. Токъ одной и той же баттареи послѣдовательно
проходитъ черезъ двѣ одинаковыя платиновыя проволоки, находящіяся
въ закрытыхъ стеклянныхъ цилиндрахъ, погруженныхъ въ воду, налитую
въ сосуды А п В (рис. 104). Термометры указываютъ измѣненіе темпе-
ратуры воды. Въ одной изъ трубокъ находится водородъ, въ другой
углекислота, кислородъ или азотъ. Оказывается, что если обозначить
черезъ 1 нагрѣваніе воды, въ которой находилась трубка съ водородомъ,
то нагрѣваніе воды, содержавшей трубку съ однимъ изъ названныхъ
342
Теплопроводность.
трехъ газовъ, равнялось соотвѣтственно 1,90—2,10 и 2.26. При этомъ
проволока въ азотѣ ярко накаливалась, а проволока въ водородѣ остава-
лась темною. Это явленіе объясняется тѣмъ, что водородъ, обладая боль-
шею теплопроводностью, быстро охлаждаетъ проволоку, не давая ей на-
калиться. Вслѣдствіе этого ея сопротивленіе не настолько возрастаетъ,
какъ сопротивленіе другой проволоки, а потому въ ней (см. т. IV) не
столько выдѣляется тепла, какъ въ послѣдней. Вѣроятно въ водородѣ не
только теплопроводность, но и конвекція больше, чѣмъ въ другихъ газахъ.
Ма^пиз сравнивала, по двумъ способамъ теплопроводность газовъ.
Во-первыхъ онъ погружалъ въ пары кипящей воды вертикальную сте-
клянную трубку, наполненную однимъ изъ сравниваемыхъ газовъ. Внутри
трубки находился резервуаръ термометра, служившаго для опредѣленія
скорости передачи тепла черезъ газъ. Оказалось, что для повышенія
температуры термометра отъ 20° до 80° требовалось въ воздухѣ 3,5 мпн.
въ Н 1,0 мин., въ СО2 — 4,25 мин. и въ амміакѣ — 3,5 мин. Ана-
логично X а г г наблюдалъ время охлажденія термометра въ сосудѣ, напол-
ненномъ однимъ изъ сравниваемыхъ газовъ; оказалось, что водородъ вы-
зываетъ въ 5,5 разъ болѣе быстрое охлажденіе, чѣмъ воздухъ.
Второй способъ Мар: пи 8’а будетъ понятенъ изъ разсмотрѣнія рпс.
105, представляющаго главную часть его прибора. Въ стеклянный со-
судъ А входятъ снизу двѣ трубки, служащія для наполненія его различ-
ными газами. Сбоку вставленъ термометръ, надъ резервуаромъ котораго
помѣщенъ щитъ изъ пробки или изъ двухъ мѣдныхъ пластинокъ, нахо-
дящихся на разстояніи 1 мм. другъ отъ друга. Сосудъ В наполненъ ки-
пящей водой, въ которую впускается непрерывная стр} я пара для под-
держанія кипѣнія. Весь приборъ помѣщенъ внутри большого стекляннаго
сосуда, окруженнаго водою при 15°. Оказалось, что черезъ нѣкоторое
время термометръ достигаетъ стаціонарнаго теплового состоянія, причемъ
наибольшее нагрѣваніе наблюдается въ водородѣ. ВиП замѣнилъ термо-
метръ термоэлектрической парой; но онъ заключилъ изъ своихъ опытовъ
объ отсутствіи теплопроводности у газовъ, что невѣрно.
Разсмотримъ теперЕ употребляемые нынѣ точные методы опредѣ-
ленія к для газовъ. Различаютъ собственно три метода, а именно:
Яіеіап'а или КипсІІ-ЛѴагЪ иг^’а, Сііг І8Ііап8 е п’а и Всіііеіег-
шасЬег’а. Первый былъ разработанъ особенно Ѵбіпкеі тапп’омъ.
Методъ СЬгІ8Ііап8еп’а трехъ мѣдныхъ пластинокъ уже былъ
нами разсмотрѣнъ выше при изученіи теплопроводности твердыхъ и жид-
кихъ тѣлъ. Методъ 81 е Г а п’а состоитъ въ слѣдующемъ: промежутокъ
между двумя цилиндрами былъ наполненъ испытуемымъ газомъ; внѣшній
цилиндръ погружался въ воду при 0°; внутренній служилъ воздушнымъ
термометромъ. Ширина б промежутка между двумя цилиндрами равня-
лась 2,346 мм. Предполагалось, что температура, указываемая воздуш-
нымъ термометромъ, въ каждый данный моментъ равна температурѣ і
внутренняго цилиндра. Если Р вѣсъ, с теплоемкость матеріала вну-
тренняго цилиндра, х время и х среднее изъ поверхностей [вухъ цилин-
Газы.
34^
дровъ, то очевидно к$ сіт — — РссМ, ибо внѣшній цилиндръ находится
при 0°. Отсюда
і - а = .
Рсд
Опредѣляя і для различныхъ г, можно было опредѣлить численное
значеніе а, а затѣмъ и абсолютное значеніе коеффиціента к. Опыты съ
воздухомъ при 7бО мм. и при 428 мм. дали одинаковое значеніе для к.
Среднее изъ всѣхъ наблюденій даетъ для воздуха к = 0,0000558 С. О 8.
Для другихъ газовъ 8 1 е Т а и нашелъ слѣдующія относительныя числа :
к
к
Воздухъ . 1
н,_ . 6.72
сн2. . . 1,37
О., . . . 1,02
СО .
СоЯ4
МО
со2.
0,98
0,75
0,66
0,64
8 1 е I а п приписывалъ весь переходъ тепла отъ одного цилиндра къ
другому теплопроводности газа, между тѣмъ какъ часть теплоты несом-
нѣнно переходила въ формѣ лучистой энергіи. Ріапск опредѣлилъ по
тому же способу к для нѣкоторыхъ газовъ; онъ нашелъ слѣдующія числа
(для воздуха к = 1):
І\Ю Л773 Свѣтильн. газъ,
/г =0,95 0,993 0,917 2,67
Почти одновременно со 8 1 е Е а п’омъ производили свои изслѣдо-
ванія Кип (11 и \ѴатЬпг§. Ихъ приборъ состоялъ изъ стекляннаго
полаго шара (радіусъ 2,972 см.) въ центрѣ котораго помѣщался резервуаръ
термометра. Шаръ можно было наполнить желаемымъ газомъ, а также
выкачать газъ до весьма высокой степени разрѣженія, нагрѣвая его до
200° и дѣйствуя въ то же время ртутнымъ насосомъ. Предварительно
нагрѣтый приборъ помѣщался въ смѣсь воды и льда, и наблюдалось
охлажденіе термометра, происходившее вслѣдствіе теплопроводности, кон-
векціи и лучеиспусканія. Чтобы отдѣлить эти три части другъ
отъ друга КипсИ и \ѴагЬпг^ поступали такъ. Конвекція зависитъ
отъ упругости р газа, уменьшаясь вмѣстѣ съ р, между тѣмъ какъ тепло-
проводность п лучеиспусканіе отъ р не зависятъ. При большихъ р замѣ-
чается, что скорость ѵ охлажденія уменьшается съ уменьшеніемъ р\ но
затѣмъ оказывается, что ѵ перестаетъ зависѣть отъ р между нѣкоторыми
предѣлами рх и р.>. Очевидно, что въ этихъ предѣлахъ конвекція уже ни-
какой роли не играетъ, такъ что дѣйствуютъ только теплопроводность и
лучеиспусканіе. Предѣлы рх и р> зависятъ отъ рода газа п отъ размѣ-
ровъ прибора. Чтобы отдѣлить лучеиспусканіе они довели газъ до весьма
высокой степени разрѣженія, при которой вліяніе теплопроводности ис-
чезало и скорость охлажденія дѣлалась независимой отъ газа, который
находился въ шарѣ и, что главное, отъ размѣровъ по с л ѣ д н я г о.
344
Теплопроводность.
Для разъясненія приводимъ нѣкоторыя числа. Число г секундъ, потреб-
ныхъ для охлажденія значенія: термометра отъ 59,3° до 19,6° имѣло слѣдующія
А. Водородъ. Давленіе. Приборъ I Приборъ II
760 мм. 60 сек. 25 сек.
154 » 66 » 25 »
8,8 » 68 » 30 »
В. В ѵ з д у х ъ. 760 мм. 171 сек. 114 сек
148 234 » 114 »
9,5 » 270 » 116 »
0.5 » 280 » 154 »
С. Крайнее достижимое разрѣженіе.
Газъ Приборъ Г. Приборъ II.
Водородъ ... 586 сек. 578 сек,
Воздухъ... 576 > 576 »
Углекисл. газъ . . 588 » 578 »
Въ оба прибора, различавшіеся размѣрами, вставлялся одинъ и тотъ
же термометръ. Такимъ образомъ можно было узнать, какая часть охла-
жденія вызывается лучеиспусканіемъ и опредѣлить скорость охлажденія,
вызванную одною теплопроводностью. Зная эту скорость и теплоемкость
охлаждающагося тѣла, можно опредѣлить количество тепла 7. теряемое
этимъ тѣломъ, а затѣмъ и коеффиціентъ к, который КипсІІ и АѴаг-
Ъпг^ принимали за функцію температуры вида к = &0(1 + /Ж $гаеІ2
вывелъ изъ опытовъ К ипсі Га и АѴ агЪиг&’а слѣдующія числа:
Воздухъ к = 0.0000492 С. О. 8. Водородъ к = 0,0003198 С. 0.8.
Углекисл. газъ к = 0,0000290 С. О. 8.
ѴѴіпкеІшапп произвелъ весьма большое число изслѣдованій, из-
ложенныхъ въ длинномъ рядѣ мемуаровъ. Совершенствуя свои спо-
собы, онъ получалъ отличавшіяся одно отъ другого числовыя значенія
для к и также для /?. Замѣтимъ, что послѣднія изъ его работъ дали :
(1893 г.) к -- 0,00005684 1
(1891 г.) /9 = 0,00190 | Воздухъ.
(1891 г.) к = 0,0000322 ]
/9 = 0,00401 і
Не вдаваясь въ подробное описаніе опытовъ АѴіпке 1ш а и п’а, огра-
Первыя наблюденія онъ произво-
лучеис-
(1891 г.) к - 0,0003829 I в
> ,? = 0.00175 I
Ъ глекпсл. газъ.
ничиваемся краткимъ ихъ обзоромъ.
дилъ по способу Зіеіап’а, стараясь однако исключить вліяніе
пусканія. Онъ достигъ этого, мѣняя толщину д газоваго слоя, заключен-
наго между двумя цилиндрами; ясно, что лучеиспусканіе отъ й не зави-
ситъ. Эти опыты дали для воздуха к—= 0,0000525 и @ = 0,00277. Для
другихъ газовъ и паровъ онъ нашелъ весьма большія Д какъ видно изъ
слѣдующей таблички:
Газы.
345
Г а з ы • р Пары: V
с2ні 0,005751 Н.О 0,004388
МО 0,004149 Алкоголь 0,006147
АЙ, 0,005128 Эфиръ 0,007012
СО, 0,004970 С52 0,005717.
Позднѣйшія опредѣленія по способу К ипйГа и ѴѴагЬиг^’а, а
также по способу С 11 г і 8 I і а п 8 е п’а (см. выше) дали для воздуха
/9 = 0,00208 и ,? = 0.00206. Чтобы опредѣлить /9, АѴ і п к е 1 т а и п
наблюдалъ сперва охлажденіе прибора отъ 18° до 8°, погружая его въ
смѣсь воды и льда, а затѣмъ охлажденіе отъ 117° до 107°, погружая при-
боръ, нагрѣтый до 125°, въ кипящую воду. Въ дальнѣйшихъ работахъ
онъ многократно мѣнялъ форму и матеріалъ прибора. Въ послѣдней
своей работѣ (1893) онъ пользовался металлическими шаровидными сосу-
дами, производя опредѣленія по нѣсколько измѣненному методу Йіеіап’а
С1ігІ8Ііап8еп нашелъ по своему способу для воздуха @ = 0,00153.
Методъ ЗсЫеіегшасііег’а заключается въ слѣдующемъ: плати-
новая проволока, которая въ позднѣйшихъ опытахъ была замѣнена про-
волокою изъ никкеля, длиною въ 320 мм. и толщиною въ 0,4 мм., на-
тянута вдоль оси стеклянной трубки ; эту трубку можно было наполнить
испытуемымъ газомъ и выкачать изъ нея газъ до весьма высокой сте-
пени разрѣженія. Трубка погружена въ воду, температура которой из-
вѣстна. Черезъ проволоку пропускается электрическій токъ извѣстной
силы /. Сопротивленіе проволоки измѣрялось, и когда оно переставало
мѣняться, то это указывало на достиженіе стаціонарнаго состоянія; когда
извѣстно, то извѣстна и температура і проволоки и количество д тепла,
которое она отдаетъ въ единицу времени. Если і выражено въ амперахъ,
чи въ омахъ, то д — 0,24/^ мал. калорій. Конвекція была устранена,
какъ въ способѣ Кппйѣ’а и АѴагЪпт^’а, достиженіемъ необходимаго
разрѣженія. Вліяніе лучеиспусканія опредѣлялось также по способу
Кипйі’а и АѴагЬпгц’а наблюденіями при крайней степени разрѣженія
газа въ трубкѣ; при этомъ опредѣлялась сила тока /0, при которой ге/, а
слѣд. и і имѣютъ прежнее значеніе. Тогда #0 = О,24/о2®> мал. кал. пере-
даются лучеиспусканіемъ, а слѣд.
д — д$ = 0.24(/2 — мал. кал-
переходятъ въ одну секунду отъ проволоки къ стѣнкамъ трубки вслѣдствіе
іеп.іопроводности газа. Формула (49) стр. 308, въ которой / длина, ра-
діусъ сѣченія проволоки, г2 радіусъ рѣченія трубки, — і2 = і, даетъ
для искомаго к :
к = У Г2 . . ...........(59)
2 лН гу
8 с 1і 1 е і е г ш а с 1і е г
Воздухъ.
/г0 - 0,0000556
Д — о,оѵ281
нашелъ при 0°
^2
0,000407
0,00275
СО.,
0,0000325 С. О. 8.
0,00548
346
Теплопроводность.
Для паровъ ртути при 203°:
к = 0,0000185 С. 0.8. /9 = 0.0074.
Чтобы опредѣлить /9 для воздуха. Н2 и СО2, бсіііёіегшасііег по-
гружалъ трубку сперва въ смѣсь воды и льда, а потомъ въ кипящую воду;
і въ (59) обозначаетъ во второмъ случаѣ избытокъ температуры прово-
локи надъ температурою трубки. Изъ числа изслѣдованій, не относящихся
къ послѣднему времени, упомянемъ слѣдующія: О г а е і г пользовался
способомъ Киікіі’а и ЛѴагЬиг^’а, наблюдая охлажденіе прибора выше
0° и выше 100°. Онъ находитъ:
Воздухъ. Н2 СО2
к(} = 0,0000484 0,000319 ’ 0,0000309
/9 = 0,00183 0.0016 0,0022.
ЕісйЬоіп находитъ по способу АѴ і п к е 1 ш а п п’а, полагая, что
для воздуха и для водорода р одинаковое:
Воздухъ и водородъ: СО2 С2Н±
в = 0,00199 0,00367 0,00445.
Н о е і к е г опредѣлилъ к для паровъ различныхъ органическихъ сое-
диненій, принимая для воздуха к = 1. Е^оп Мйііег (1896) подвергъ
методы Кппйі’а и ЛѴагЬиг^’а и АѴіпкеІтапп’а эксперимен-
тальному и критическому изслѣдованію и указалъ на нѣкоторые ихъ
недостатки.
Дальнѣйшія работы по вопросу о теплопроводности газовъ произво-
дили Раи 1і Ц 907), Тойй (1909), 8о(1(1у и Веггу (1910), Кписі-
8бп (1911), 8шо Іи сіюдѵ $кі (1911) и др.
Намъ остается разсмотрѣть еще одинъ рядъ работъ, относящихся къ
послѣднему времени. Главную цѣль этихъ работъ составляла провѣрка
двухъ законовъ, выраженныхъ формулами (54) и (56) — (58). Первая изъ
этихъ формулъ такова ,
А *• к = 8?]СѴ.........................(60)
Какъ мы видѣли, теоретическія изслѣдованія привели къ слѣдую-
щимъ значеніямъ для с:
Сіаизіиз......................8 = 1.25
МахАѵеІІ-ВоИгтапп . . . е = 2,5
0. Е. Меуег...................г = 1,6027
Е^оп Мйііег (1901), МеЫіз (1902) и ВсЬмагге (1902-3)
опредѣляли величину 8 для воздуха, аргона и гелія. Е § о п Мйііег из-
слѣдовалъ теплопроводность воздуха по способу КипсН-АѴагЬиг^’а
при 0° и при 100° (см. ниже). Онъ получилъ для г слѣдующія значенія:
0°................8= 1,94
100°............8 = 1,82
слѣд. ближе всего къ теоретическому значенію, найденному О. Е. Меу ег’омъ.
Разница между теоретическимъ значеніемъ и наблюденнымъ не можетъ
быть объяснена ошибками наблюденія. Меііііз (1902) изслѣдовалъ ар-
Газы.
347
го н ъ по способу АѴіпкеІшап п’а и нашелъ при 0° значеніе к = 0,000038.
8 с 11 и И 2 е (1901) нашелъ для аргона // === 0,0002104, а ЛіііепЪег-
^ег (1897) ср = 0,1233. Такъ какъ для аргона Ср * сѵ — 1,667, то по-
лучается _ .
г = 2,442.
Одновременно съ МеМіз’омъ Зсйѵгагіге изслѣдовалъ воздухъ,
аргонъ и гелій по способу ВсЫеіегтасііег’а. Онъ нашелъ для воз-
духа к = 0,0000569. Для аргона к — 0,00003894, а отсюда, какъ выше,
е = 2,501.
Въ высшей степени замѣчательно такое согласіе результатовъ, полу-
ченныхъ для аргона по двумъ совершенно различнымъ спо-
собамъ М е й 1 і з’омъ и 8 с Ь лѵ а г 2 е. Но еще замѣчательнѣе, что для
гелія 8сЬутагге нашелъ при 0°
к = 0,0003386
е = 2,49.
Для аргона и гелія получаются такимъ образомъ
одинаковыя значенія и притомъ такія, которыя вполнѣ
согласуются съ теоріей Махдѵ еИ-ВоИгшапп’а.
Итакъ очевидно, что для одноатомныхъ г а зовъ 8 = 2,5;
съ этимъ вполнѣ согласуется то, что ЛѴиеІІпег изъ наблюденій вы-
числилъ для одноатомныхъ паровъ ртути 8=3,15, тогда какъ для
другихъ не одноатомныхъ газовъ онъ получаетъ числа, близкія къ числу
О. Е. Меуег’а (1,6027).
Къ совершенно инымъ результатамъ приводятъ двѣ новыя работы надъ
многоатомными газами. 7іе§1ег (1904) изслѣдовалъ метанъ и
этанъ (С2/У6) по методу 8 с Ы е і е г т а с Ь е г’а: онъ получил ь слѣду-
ющія числа:
к 8
метанъ 0,0000746 1,593
этанъ. . . 0,0000496 1,946
Значенія 8 неодинаковы и число, получившееся для метана, лишь
случайно близко къ числу О. Е. Меуег’а. Наконецъ, въ 1906 году
появилась еще работа Р. Сг и п 111 е г’а , который изслѣдовалъ кислородъ,
азотъ и водородъ также по методу7 ЗсЫеіегш асііег’а. Онъ получилъ
слѣдующіе результаты:
0-2 н..
к (0°) 0,0000578 0,0000569 0,000387
1,921 1,959 1,907.
Замѣтимъ, что вышеприведенныя три теоретическія значенія для е
(Сіаиеіпз’а, МахѵѵеИ-Воіігтапп’а и О. Е. Меуег’а) были вы-
ведены въ предположеніи, что какъ энергія распространяющагося движе-
нія, такъ и интрамолекулярная энергія распространяются съ одинаковой
скоростью. Иная теорія, развитая также М а х лѵ еі Ромъ и В о И 2 -
348
Теплопроводность.
таи п’омъ, предполагаетъ, что интрамолекулярная энергія не принимаетъ
участія въ теплопроводности; эта теорія приводитъ къ формулѣ
е = 10 (СР _ й...................(60.а)
4 /
Она даетъ для различныхъ газовъ различныя значенія с. Для
сп
одноатомныхъ газовъ р = 1,666 и с = 2,5; для дву атомныхъ
Сѵ с
газовъ, для которыхъ приблизительно р = 1,4, получается с = 1,5. По-
слѣднее число однако не совпадаетъ съ величинами 8, найденными для
и Н2.
Второй изъ упомянутыхъ законовъ относится къ з а в и с и м ости
теплопроводности отъ температуры. По теоріи Сіаи 8Іи 8’а,
1
/ 9
к = к$ У 1 ’ф оЛ = 0 Т = к§ (1 ///) . . . (61)
273
/3 = 0,00183..................(62)
тогда какъ теорія М а х \ѵ е 1 Гя даетъ
ѣ
к = къ(1 + аЛ = 0 Т...............(63)
273
/3 = а = 0,00365 ...............(64)
Выше мы привели значенія для /?, данныя различными учеными.
Для воздуха
\Ѵіпке1шапп (1891) нашелъ » . . 0,00190
С И гІ8 (і ап 8 еп . . . 0,00153
бсЫеіегпіасЬег. . . . 0,00281
бггаеія........................0.00183
ЕісЬЬогп. .... .. 0.00199
Почти всѣ эти числа приближаются къ теоретическому = 0,00183.
То же самое относится къ /3 для паровъ ртути (Я с 1т 1 еіегпі ас Ьег) и
щя водорода (6 г а е 12, \Ѵ і п к е 1 пі а п п и Е і с Ь Ь о г п), какъ было ири-
ве іено выше. Для другихъ газовъ для /3 были найдены большія значе-
нія, которыя скорѣе говорили въ пользу теоріи МаххѵеІГя. Новѣй-
шія изслѣдованія привели къ важнымъ результатамъ также п въ отно-
шеніи второго закона. Ескетіеіп (1900) опредѣлялъ по способу^
\Ѵ і п к е 1 ш а п п’а к и ,3 для низкихъ температуръ (между 0°
и — 150°). Результаты его наблюденій видны изъ слѣдующей таблицы.
О» к
—500 —590 —73° | -150°
Воздухъ . . . 0,00004677 — 0.00003678 — 0,00002146 0,00362
Водородъ 0,0003186 — 0,00002393 — 0,0001175 •0.00422
Углекисл. . 0,00003434 0,00002824 — 0,00002546 — 0,00352
Газы.
349
Итакъ при этихъ низкихъ температурахъ три раз-
матриваемые газаслѣдуетъ закону МаххѵеП’я, а не Сіап-
зіиз’а. При болѣе высокихъ температурахъ, повидимому, оба закона не-
приложимы. С о ш р а и нашелъ для воздуха /? = 0,00130. Е о п М и 1 -
Іег (1901) даетъ число 000196
Онъ находитъ, что для воздуха к растетъ пропорціонально 0,57-ои
степени абсолютной температуры.
По формулѣ (60) к и г/ должны зависѣть въ одинаковой степени отъ
/, если сѵ можно считать постояннымъ. Зависимость отъ і была раз-
смотрѣна въ томѣ I. Все тамъ изложенное можетъ служить къ выясне-
нію только что приведенныхъ результатовъ. По Е^оп Мііііег’у, к
возрастаетъ съ температурой нѣсколько медленнѣе, чѣмъ //.
Найп показалъ, что лучи Еоепі^еп’а не вліяютъ на тепло-
проводность воздуха.
Г-жа Васильева изслѣдовала теоретически и экспериментально
теплопроводность газовыхъ смѣсей. Она показала теоретически, что
к не можетъ быть вычислено по правилу смѣшенія, если извѣстны кг и
&2 для составныхъ частей. Пусть рг и парціальныя давленія этихъ
частей, тогда
к= РіК Рі
. . (64, а)
Здѣсь А и В двѣ постоянныя, зависящія только отъ
зовъ, но незавпсятъ отъ процентнаго ихъ содержанія въ
даетъ выраженія:
А = _1_/ о \2 । "Ц + ^2
Ѵ2 \5 Г/ I т2
в — 1 [6 \2 ।
Ѣл2\52/ I
рода двухъ га-
смѣси. Теорія
(64,6)
Здѣсь т1 и т% массы одной молекулы газовъ; лд и 52 средніе діа-
метры молекулъ; о = - ($т $2). Для смѣси кислорода (т2) и водорода
1 2
(/т/і = /тг2), г-жа Васильева вычисляетъ, пользуясь числами для
коеффиціентовъ внутренняго тренія этихъ газовъ, величины А = 0,999 и
5=2,211. Отсюда слѣдуетъ, что к меньше числа, вычисляемаго по пра-
вилу смѣшенія (Д = В = 1). Этотъ результатъ былъ подтвержденъ измѣ-
мѣреніями ціо способу \Ѵіп ке 1т ап п’а), произведенными надъ 11 смѣ-
сями кислорода и водорода. Однако опыты дали числа, которыя оказа-
лись еще меньше вычисленныхъ по формуламъ (64,лО и (64,6). Чтобы
согласовать формулу (64,а) съ результатами опытовъ, пришлось бы при-
нять А = 1,379 и В = 3,064, т.-е. помножить числа, полученныя на осно-
ваніи формулъ (64,6), на 1.38. Г-жа Васильева показала, какимъ обра-
зомъ это отступленіе можетъ быть объяснено теоретически
350
Теплопроводность.
Опытное изслѣдованіе к для смѣсей (Лг, Не} произвелъ АѴ а с 11 8 -
гопі Ь (1908).
Весьма интересенъ вопросъ о теплопроводности газовъ, находя-
щихся въ состояніи диссоціаціи. М егп 8 і (1904) теоретически
вывелъ слѣдующую формулу, относящуюся, напримѣръ, къ случаю дис-
соціаціи И2О± = 2Л/О2.
’а — сі2
1 а
(64,0
Здѣсь к относится къ газу, въ которомъ имѣетъ мѣсто диссоціація,
— къ случаю полнаго отсутствія диссоціаціи, О есть коэффиціентъ диффу-
зіи И2О± относительно НО2, Р — давленіе, Т — абсолютная температура,
<2 теплота диссоціаціи, Р — газовая константа, а — степень дис-
соціаціи при Р = 1 атмосферѣ. е г п 81 провѣрилъ свою формулу, поль-
зуясь наблюденіями Ма^папіпі. который для теплопроводности диссо-
ціированной И2О± нашелъ необыкновенно высокую величину: совпаденіе
оказалось достаточно хорошимъ. Позже изслѣдованія Ееіісіапі относп-
сительно теплопроводности И2О± (1904) и РС/5 (1905) привели къ весьма
запутаннымъ результатамъ, не объяснимымъ теоріей І\тегп8І’а.
§ 9. Температурный скачекъ на границѣ двухъ тѣлъ. Весьма
интереснымъ п важнымъ является вопросъ о томъ, представляетъ ли со-
бои температура непрерывную функцію ня границѣ двухъ тѣлъ по на-
правленію нормали къ поверхности или же на границѣ происходитъ вне-
запный скачекъ температуры.
Р о і 8 8 о п допускаетъ возможность разрыва и дополняетъ формулу
(18,а) стр. 296, представляя ее въ видѣ:
1 (Иі 1 йі.-у , . х
^1 ., = ^2 ' = 4 Сі ~
ах ах
. (65)
гдѣ и і2 значенія и і2 у поверхности, д - - постоянная. Если положить
<1
(66)
то у, какъ сейчасъ будетъ видно, величина линеиная (размѣра А);
ее можно бы назвать коеффиціентомъ температурнаго скачка. Если скачка
нѣтъ, т.-е. = 4, то = -ю и 7 = 0. Во всякомъ случаѣ скачекъ мо-
жетъ имѣть мѣсто только тогда, когда существуетъ перпендикулярный къ
поверхности тепловой потокъ, такъ какъ отсутствіемъ такого потока, во
всякомъ случаѣ, исключается возможность скачка.
Было сдѣлано много попытокъ доказать существованіе температур-
наго скачка между твердыми или жидкими тѣлами. Оенргеіг (1871) из-
слѣдовалъ при помощи ряда горизонтальныхъ термометровъ теплопровод-
ность подогрѣваемаго сверху столба, состоявшаго изъ воды и нитрогли-
церина. Онъ нашелъ на пограничной поверхности температурный скачекъ
въ 2°- 3°; на границѣ мѣди и цинка скачекъ въ 1°,47. (т. АѴ іесіепіапп
Температурный скачекъ.
351
изслѣдовалъ рядъ металловъ и нашелъ, что на поверхности соприкосновенія
двухъ металловъ не происходитъ скачка, если соприкосновеніе металловъ
полное. Къ тому же результату пришелъ Ап^вігоет (1861).
На стр. 322 мы видѣли, что между температурами поверхности твер-
даго тѣла и жидкой струи, омывающей эту поверхность, можетъ суще-
ствовать значительная разница; эта разница вполнѣ объясняется суще-
ствованіемъ неподвижной жидкой пленки, которая образуется у поверх-
ности твердаго тѣла. Роговскій (1903) заключилъ изъ своихъ опы-
товъ о существованіи дѣйствительнаго температурнаго скачка. Онъ на-
тянулъ вдоль оси трубки проволоку, нагрѣваемую электрическимъ токомъ;
по трубкѣ протекала струя воды. Онъ нашелъ, что разница между тем-
пературой проволоки и воды могла доходить до 24°. Эту разницу, по
его мнѣнію, нельзя объяснить существованіемъ около проволоки водя-
ной пленки.
К о л о в р а т ъ - Ч е р в и н с к і и (1908) изучалъ вопросъ о темпе-
ратурномъ скачкѣ на границѣ двухъ жидкостей. Его приборъ, построен-
ный по моимъ указаніямъ, состоялъ изъ стекляннаго цилиндра, въ кото-
рый наливались испытуемыя жидкости, одна поверхъ другой. Этотъ ци-
линдръ окруженъ вторымъ, болѣе широкимъ, содержащимъ тѣ же жид-
кости, налитыя до тѣхъ же уровней, и образующія охранное кольцо. Дно
цилиндровъ образовала круглая латунная коробка, черезъ которую проте-
кала вода: крышкой служила подобная же коробка, наполненная масломъ
и нагрѣваемая электрическимъ токомъ. Температуры въ двухъ точкахъ,
недалекихъ отъ поверхности раздѣла, одна выше, другая ниже ея, измѣ-
рялись термоэлементами, которые могли бытъ перемѣщаемы въ вертикаль-
номъ направленіи, причемъ ихъ разстоянія отъ поверхности раздѣла из-
мѣрялись окулярнымъ микрометромъ зрительной трубы катетометра. Че-
резъ 4—5 часовъ послѣ начала пропусканія струи воды и электрическаго
тока устанавливалось стаціонарное тепловое состояніе. Оказалось, что
на границѣ р а з д ѣ л а между ртутью еі водою не с у щ е -
с т в у е т ъ температурнаго скачка, превышающаго погрѣшности
опыта, т.-е. 0,05°. Въ системѣ в о д а-в а з е л и но в о е масло оказался
слой масла, толщиною въ 1 мм., прилегающій къ водѣ, въ которомъ па-
деніе температуры было больше, чѣмъ въ маслѣ; и въ этомъ случаѣ ни-
какого скачка не замѣчалось. Промежуточный слой, вѣроятно, состоялъ
изъ нѣкотораго рода эмульсіи воды въ маслѣ.
Дѣйствительный температурный скачекъ имѣетъ мѣсто у поверх-
ности твердаго тѣла, окруженнаго сильно разрѣженнымъ
газомъ, когда между тѣломъ и газомъ происходитъ обмѣнъ теплоты.
Происхожденіе этого скачка слѣдующее: если, напр., тѣло теплѣе, чѣмъ
газъ, то молекулы, отскакивающія отъ поверхности тѣла, имѣютъ темпе-
ратуру, не превышающую температуры тѣла, тогда какъ молекулы, при-
текающія къ тѣлу изъ газа, обладаютъ болѣе низкой температурой. От-
сюда слѣдуетъ, что температура пограничнаго газоваго слоя ниже темпе-
ратуры поверхности тѣла. Пусть к и і относятся къ твердому тѣлу;
352
Теплопроводность.
пусть п направленіе нормали къ поверхности. # скачекъ температуры:
(65) и (66) даютъ
; * - в.
(ІП
Итакъ, у равняется толщинѣ {(іп) такого поверхност-
наго слоя твердаго тѣла, внутри котораго измѣненіе
температуры {(№) равно температурному скачку.
бтоіисйолѵвкі (1898) и Оейгске (1900) опытнымъ путемъ
опредѣляли величину у. Положимъ,
у = (±.........................(67)
гдѣ Ь средняя длина пути газ<>воп молекулы (т. Т). 8 ш о 1 и с Ъ о ѵѵ 8 кі нашелъ:
760
для воздуха...........у = 1,70/, = 0.0000171 см. “
для водорода..........у = 6,96/, = ЩСЮ0129 см. ~6°
Р
Здѣсь р обозначаетъ давленіе газа въ миллиметрахъ ртутнаго столба.
Подобныя значенія получаетъ О е й г с к е , а именно
для воздуха . . . у = 1,83/,
для водорода . . / = 5,701.
Зтоінсііо^'нкі разсматривалъ вопросъ о температурномъ скачкѣ
на основаніи кинетической теоріи газовъ и получилъ слѣдующій резуль-
татъ. Пусть // та часть молекулъ, которыя встрѣчаютъ поверхность твер-
даго тѣла, ею «поглощаются» и затѣмъ разсѣиваются равномѣрно во всѣ
стороны со скоростью, соотвѣтствующей температурѣ тѣла; другая часть
1 — отражается равномѣрно и безъ измѣненія скорости. Тео-
рія С1 а и я і и я’а (т. I) даетъ
по теоріи М а х ѵѵ е 1 Гя, получается
бтоіисйоѵѵякі показалъ, что существованіе температурнаго
скачка обнаруживается и въ болѣе раннихъ работахъ АѴ і п к е 1 т а в п’а .
К и п (1 і’а и АѴ а г Ь и г §*’а, В г и с й’а и Я с Ь. 1 е і е г т а с 11 е г’а.
Лазаревъ (1910) весьма тщательно изслѣдовалъ распредѣленіе тем-
пературъ въ слоѣ разрѣженнаго газа, соприкасающагося съ твердымъ тѣ-
ломъ ; онъ изслѣдовалъ воздухъ, углекислый газъ и водородъ. Онъ на-
шелъ, что [і въ значительной степени зависитъ отъ давленія газа и что
адсорбція газа у поверхности тѣла (т. I) должна играть большую роль,
такъ какъ образуется слой газа съ перемѣнною величиною теплопро-
водности.
Литература.
553
Кцисіяеп (1911) далъ новую теорію молекулярной теплопровод-
ности газовъ, въ которой онъ ввелъ понятіе о коеффиціентѣ аккомодаціи а.
Эта величина равна . .
.......................(68)
гдѣ і\ температура группы молекулъ, приближающихся къ твердой стѣнѣ,
температура удаляющихся отъ стѣны, и температура самой стѣны.
Величины с и а формулъ (67) и (68) связаны равенствомъ
гдѣ к для всѣхъ газовъ имѣетъ, повидимому, значеніе, близкое къ 1.9.
ЛИТЕР АТУР А.
Теорія теплопроводности.
Къ §§ 2 и 3.
Роигіег. ГЬёогіе апаіуіідие сіе Іа сЬаІепг. Рагів, 1822 (нѣм. перев. Ѵ&еіпзіеігіа.
1884) Мётоігв йе ГАкайётіе йев всіепсев. Т. IV и V, 1812.
РоІ88оп. ТЬёогіе таіЬётаіідпе йе Іа сЬаІепг. Рагів, 1835.
Піетапп. Рагііеііе ВіИегепііаІЩеісЬип.^еп. ВгаипвсЬгѵеі^, 1869; р. 114—184.
КігМго//. Ѵогіевип^еп йЬег йіе ТЬеогіе йег ХУатте. Ьеіргі^, 1894. стр. 1—51.
Ьатё. Ье^опв виг Іа іііёогіе апаіуіідие йе Іа сЬаІепг. Рагів, 1861.
Игопке. Еіпіеііип^ іп йіе апаІуіівсЬе Тііеогіе йег ХУагтегѵеЬгеііип^. Ьеіргі^, 1882.
Роіпсагё. ТЬёогіе апаіуіідпе йе Іа ргораіаііоп йе Іа сЬаІепг. Рагів, 1895.
Неіткоііх. Ѵогіев. ііЬег йіе ТЬеогіе йегЛУагше. Ьеіргі^, 1903, р. 23—147.
Ріетапп. Рагііеііе БіПегепііа^ІеісЬип^еп, II р. 77- 149, ВгаипвсЬуѵеі^, 1901.
НоЬ8Оп и. Піе88еІНог8І Епсукіор. сі. піаіЬ. \Уівв. 5, I р. 161- 231, 1903.
Н. Р. ѴРеЬег. \Ѵ. А. 10 р. 103, 1880.
Ризскі. ХѴіеп. Вег. 103 р. 809, 989, 1894.
ХХіейеЬикр. Апп. й. РЬув. (4), 1 р. 784, 1900.
()иеіеІеі. Мёт. йе ГАсай. йе Вгихеііев. 10, 1837; 13, 1841.
Теплопроводность твердыхъ тѣлъ.
Къ § 4.
А. С. Поповъ. Ж. Ф. X. О. 26 р. 331. 1894.
Ріскагх. МагЬиг&ег Вег., 25 Іюня 1902.
Не88. Дисс. МагЬиг^, 1906.
Роигіег. Апп. сЬ. еі рЬув. (2) 37 р. 291, 1828; Ро&^. Апп. 13 р. 327, 1828.
Рёсіеі. Апп. сЬ. еі рЬув. (3) 2 р. 107, 1841; Ро&§. Апп. 55 р. 167у 1842.
Саіѵегі апй йокпзоп. РЫ1. Тгапв. 148 р. 349, 1858; 149, 1859; Ргос. К. Яос. Ьоп-
йоп 9 р. 169, 1859; Ріііі. Ма&. (4) 16 р. 381, 1858; С. К. 47 р. 1069, 1858.
Іщ?еп1гои88 (или Іп^еп-Наизг). (Ігеп, йоигп. й. РЬувік 1; йопгп. йе рЬув. Т. 34
р. 68, 380, 1789.
Н. А. Гезехусъ. Извѣстія Технот Института, 1891 и 1892, р. 413.
Ѳ. Ѳ. Петрушевскій. Ж. Ф. X. О. 14 р. 154, 1882.
Віоі. Тгаііё йе рЬувідпе. 4 р. 669. Рагів. 1816.
» Пезргеіх. Апп. сЬ. еі рЬув. (2) 19 р. 99, 1821; 36, 1827; Ро^. Апп. 12 р. 281,
1828; 46 р. 340, 484, 1839; С. В. 35 р. 540, 1842.
Неітегзеп. Ро&&. Апп. 88 р. 461, 1853.
ЬащгЬег^. Ро&&. Апп. 66 р. 1, 1845.
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. III, изд. 3-е.
23
§54
Теплопроводность.
РоІ88оп. Ткёогіе таікётаіідпе сіе Іа скаіеиг. Рагіе, 1835, § 125 р. 254.
О. ѴМейетапп ипй Ргапг. Ро§рг. Апп. 89 р 497, 1853; ЬіеЪ. Апп. 88 р. 191, 1853;
Апп. ск. еі ркуз. (3) 41 р. 107, 1854; Ркіі. Ма&. (4) 7 р. 33, 1854.
О. ѴЕіейепгапп. Ро^. Апп. 95 р. 338, 1855; 108 р. 393, 1859; Апп. ск. еі рііуе.
(3) 58 р. 126, 1860; Ркіі. Ма^. (4) 19 р. 243, 1860.
СиШаий. Апп сЬ. еі рііуз (3) 48, 1856.
Еіііп^8Иаи8еп ипй Иегп8і. XV. А. 33 р. 487, 1888; ХѴіеп. Вег. 96, II р. 787, 1887-
Р. КоИІгаи8сИ. XV. А. 33 р. 678, 1888; Ріііі. Мар-. (5) 25 р. 448, 1888.
Ѵоц*і. XV. А. 64 р. 95, 18'18; Ооеіі. Ыаскг. 1897, Неіі 2.
Р А 8сИиІге. Апп. сі. Рііуз. (4) 9 р. 5 5, 1902.
Роске. XV. А. 67 р. 132, 1899.
Къ § 5.
ВиІоп§. Апп. ск еі рііуз. (2) 8 р. 113, 255, 1818.
РогЬе8. ЕбіпЬ. Тгапе. 23 р. 133, 1862; 24 р. 73, 1867; Ргос. ЕбіпЬ. 8ос. 8 р. 62,
1872—75.
Таіі. Тгапе. К. 8ос. ЕсІіпЪ. 1880 р. 717; Ріііі. Мар. (5) 12 р. 147, 1881.
Міісііеіі. Тгапе. Коу. 8ос. ЕбіпЬ. 1887 р. 535; 1890 р. 947; Ргос. ЕсІіпЪ. 8ос. 17
р. 300, 1889—90.
Вег&еі. Л. сіе ркузідие (2) 7 р. 503, 1888; 9 р. 135, 1890; С. К. 106 р. 287, 1888.
Р. Ыеитапп. Апп. ск. сі ркуе. (3) 66 р. 183, 1862; Ркіі Мар. (4) 25 р. 63, 1863.
Н. Р. ѴѴеЬег. Вегі. Вег. 1880 р. 457.
НесИі. Дисс. КбпірзЬегр, 1904; Апп. б. Рііуе. (4) 14 р. 1008, 1904.
Оіа^е. Дисс КбпірзЬегр, 1905; Апп сі. Рііуз. (4) 18 р. 904, 1905.
У. А. Ап&8ігоет. Рорр. Апп. 114 р. 513, 1861; 118 р. 423, 1863; 123 р. 628, 1864;
Ркіі Мар. (4) 25 р. 130, 1863; 26 р. 161, 1864; Оеіѵегз. аі. К. Акасі. Гбгкапбі. 8іоскко1т.
19 р. 21, 1862; Апп сіііт. еі рііуе. (3) 67 р. 379, 1863.
Рита8. Рорр. Апп. 129 р. 272, 393, 1866.
И. МеЬег. Рорр. Апп. 146 р. 257, 1872; Ркіі. Мар. (4) 44 р. 481, 1872.
Р. КоИІгаи8с1г. Вегі. Вег. 1899 р. 711 ; Апп. сі. Ркуз. (4) 1 р. 145, 1900.
йае^ек и Оіе88е11гог8і. Вегі. Вег. 1899 р. 719; ЛѴіев. АЬкапбІипреп (іег Ркуз.-Тѳскп.
Кеіскзапзіаіі 3 р. 269—424, 1900.
КігсШіо// ипй Нап8етапп. XV. А. 9 р. 1, 1880; 13 р. 406, 1881.
Р А. ЗсИиІге. XV. А. 66 р. 207, 1898.
ОгііпеІ8еп. Апп. б. Ркуе. (4) 3 р. 43, 1900; ХѴізз. АЪкапсІІ. 6. ркуе.-іескп. Кеіскз-
апеі. 4 р. 187, 1903.
8сИаи/еІЬег^ег. Апп. 6. Ркуе (4) 7 р. 589, 1902.
Ѵап АиЬеІ еі Раіііоі. б. бе ркуе. (3) 4 р. 522, 1895.
8ігапео. Кебіс. К. Асс. бі Ілпсеі (5) 7, 1 8ет. р. 197, 310, 1898.
Ь. Ьогепх. XV. А. 13 р. 422, 1*81.
О г ау. Ргос. К. 8ос. 56 р. 199, 1895.
Е. Наіі Ргос. Атег. Асаб. 31 р. 271, 1896.
Ве^Ип^ег. йізе. 2йгіск, 1896.
Сеіііег. Эізз. 2йгіск, 1896.
Р. Ленцъ. Вліяніе температуры на теплопроводность металловъ. С. П. 1869.
О8топй. Ркуе. Кеѵ. II. 218.
СИіѵоІ8ОП. Мёт. бе ГАс. б. 8і-РёіегзЬ. 37 № 12; Ехпег’е Верегі. 27 р. 1, 1891.
И. ѴЕеЬег. Вегі. Вег. 1880 р. 459
ОіеЬе. Ѵегіі. б. ркуе. Ѳее. 5 р 60, 1903; Віез. Вегііп, 1903.
Ріеі28сН. Апп. б. Ркуз. (4 3 р. 403, 1900.
НоІЬогп ипй ѴЛеп. 2ізск. (иг беиізске Іпрепіеиге 40 р. 45, 1896,
Дурные проводники.
Нег8сИеІ апй ЬеЬоиг. Кер. Вгіі. Азз. 1874 (2), 1877 (2), 1878 р. 133; 1879 р. 158.
Тупйаіі. Ріііі. Ма§. (4) 5, 1853 ; 6 р. 121, 1853.
Литература.
355
С. Ьап^. АѴагтеІеііип^ еіпі&ег Ваитаіегіаііеп, 1874.
Апсігеіив. Ргос. К. 8ос. 40 р. 544, 1881.
Норкіпв. РЫІ. Тгапз. 1857 р. 805.
Ье88. Ро^. Апп. Ег&ЪЗ. 8 р. 517, 1878.
Ьее8. РЫІ. Тгапз. 183 Ар. 481,1892 ; Ргос. К. 8ос 50 р. 421, 1892 ; 74 р. 337, 1904.
Ье88 апсі СНогІіоп. РЫІ. Ма&. (5) 41 р. 495, 1896.
СИгІ8ііап8еп. АѴ. А. 14 р. 23, 1881.
Оййопе. КепЗіс. К. Ас. Зеі Ьіпсеі (5) 6, 1 зет. р. 286, 1897.
Сга88І. Аііі Ізі. Хароіі (4) 5, 1892.
Ьой^е. РЫІ. Ма&. (5) 5 р. НО, 1878.
Неітегвеп. Ро§&. Апп. 88 р. 461, 1853.
ЬШго'ш. АѴіеп. Вег. 71, ІГ, 1875.
8тШі апй Кпоіі. Ргос. ЕЫпЪ. 8ос. 8 р. 123. 1874—75.
Р. Ыеитапп. Апп. сЫ еі рііуз. (3) 64 р. 66, 1862.
8іе/ап. АѴіеп. Вег. 74, II р. 438, 1876.
7?. Ѵ/еЬег. Хйгісіі. ѴіегІеЦаЬгззсЬгій 23 р. 209, 1878.
Уата^аіѵа. 3. о! іііе Ас. о! 8с. Ипіѵ. о! Зарап 2 р. 263, 1888.
8іасІІег. Везііттип^ 3. аЬз. АѴагтеІеііип^зѵегто^епз. Візз. Вегп. 1879.
Н. Меуег. \Ѵ. А. 34 р. 596, 1888.
Ьогсі Кеіѵіп апсі 3. Миггау. Ргос. Коу. 8ос. 58 р. 162, 1895.
Н]еІ8ігоет. РЫІ. Ма^. (5) 31р. 148, 1891 ; 3. 6. рііуз. (2) 10 р. 142, 1891.
РааІНогп. Візз. Зепа, 1894.
Ѵеп8ке. Осей. ХасЫ. 1891 р. 121.
Роске. АѴ. А. 67 р. 132, 1899.
ГЧѵеп. Ргос. К. 8ос. 76 р. 34, 1905.
ѴѴіпкеІтапп. АѴ. А. 67 р. 160, 794, 1899.
Георгіевскій. Ж. Ф. X. ’О. 35 р. 609, 1903.
Н]еІ8ігоет. ОІѵегз К. V. АкаЗ. Гоегіі. 1889, № 10 р. 668; РЫІ. Ма§. (5) 31
р. 148, 1891; 3. Зе рііуз. (2) 10 р. 142, 1891.
Чап88оп. біѵегз. К. V. АкаЗ. ЕоегЫ 58 р. 207, 1901.
Окайа. 3. оі’ ѣііе Меіеогоі. 8ос. о! Зарап, Февр. 1905; Меіеогоіо^. 7ізс1іг. 22
р. 330, 1904.
ІЛ8е Меііпег. АѴіеп. Вег. 115 р. 125, 1906.
Ьеев. (Смѣси). Ргос. К. 8ос. 62 р. 286, 1898,
Мигапо. (Камни). КепЗіс. К. Асс. Зеі Ьіпсеі (5) 7, II р. 61, 83, 1898.
Къ § 6.
Оикатеі. 3. Зе Гёсоіе Роіуіескп. 13 р. 356, 1832; 19 р. 155, 1848; С. К. 25
р. 842, 1842; 27 р. 129, 1848.
8іоке8. СатЬг. апЗ ВиЫіп Маііі. Зоигп. (2) 6 р. 215, 1851.
Ьатё. Ье^опз зиг Іа Тііёогіе апаі. Зе Іа скаіеиг. Рагіз, 1861.
8ёпагтопі. Апп. сЫ еі рііуз. (3) 21 р. 457, 1847 ; 22 р. 179, 1848; 23 р. 257, 1848;
С. К. 25 р. 459, 707, 1847; Ро^. Апп. 73 р. 191, 1848; 74 р. 190, 1848; 75 р. 50, 482,
1848; 76 р. 119, 1849; 80 р. 175, 1850.
А. М. Мауег. РЫІ. Ма&. (4) 44, 1872; 8і11. Зоигп. 1872.
Роепі^еп. Ро^. Апп. 151 р. 603, 1874; 152 р. 367, 1874.
V ѵ. ѣап@. АѴіеп. Вег. 53, II, 1866; Ро^К- Апп. 135 р. 29, 1868.
Чаппеіаг. Апп. сЫ еі рііуз. (4) 29, 1873; С. К. 95 р. 996, 1882; 114 р. 1352, 1892.
Тупйаіі. Аіііепаеит 1855 р. 1157.
Раре. АѴ. А. 1 р. 126, 1877.
Тисіізсіітій. ВеіЫ. 8 р. 490, 1884.
Ьеев. РЫІ. Тгапз. 183 А. р. 481, 1892.
Ьоитсіз. РЫІ. Ма§\ (6) 5 р. 152. 1903.
Реггоі. С. К. 136 р. 1246, 1903; АгсЫ зс. рііуз. еі паі. (4) 18 р. 445, 1905.
23*
35в
Теплопроводности.
}ае$ег, Агск. зс. ркуз. еі паі. (4) 22 р. 240, 1906.
ІГ. Ѵоі&. XV. А. 60 р. 350, 1897; 64 р. 94, 1898; 4. Ле рііуз. (3) 7 р. 85, 1898.
Ое Іа Кіѵе еі Песапйоііе. Ро^§. Апп. 14 р. 590; 1828; Апп. ск. еі рііуз. (2) 40, 1829.
Тупйаіі. Ркіі. Ма&. (4) 5 и 6, 1853. Апп. ск. еі рііуз. (3) 39 р. 348, 1853.
КпоЫаисІи Ро^&. Апп. 105 р. 623, 1858.
Ье88. Ро&&. Апп. Ег&ЪЛ. 8 р. 517, 1878.
Сгеі88. Ро^. Апп. 139 р.- 174, 1870.
ІГ. Ьоириіпіпе. Агск. 8с. рііуз. (4) 1 р. 9, 1896.
Теплопроводность жидкостей.
Къ § 7.
Рит/огй. Еззауя 2 р. 199, Я. бе рііуз. Ле Веіатеіііегіе 4; Л. оі‘Ыіскоізоп 14, 1806.
77г. ІНотзоп. Л. оі‘ Хіскоізоп 1 р. 81, 1802.
Міс1іоі8оп. Л. оі' Хіскоізоп 5 р. 197.
Миггау. 8узіет о! Скетізігу 3 еЛіі. 1 р. 305; Л. оі' Ыіскоізоп 1, 1802.
Ое8ргеіг. Апп. скіт. еі ркуз. 61 р. 206, 1839; Ро&&. Апп. 46 р. 340, 1839; 142
р. 618, 1868; С. К. 7 р. 933, 1838.
Рааігоіѵ. Ро&&. Апп. 134 р. 618, 1868.
Воііотіеу. Ркіі. Тгапз. Коу. 8ос. 1881, II р. 537; Ргос. Коу. 8ос. 28 р. 462, 1879;
31 р. 300, 1881.
СНгее. Ркіі. Ма&. $5) 24 р. 1, 1887; Ргос. К. 8ос. 42 р. 300, 1887; 43 р. 30, 1888.
Ап^вігоет. Ро^. Апп. 123 р. 638, 1864.
Ьип(ідиІ8і. Іірзаіа Епіѵегзііаеія АгззкгіГі 1869, р. 1.
Вег&еі. Л. Л. ркуз. (2) 7 р. 2, 1888; С. К. 105 р. 225, : 887 ; 106 р. 1152, 1888;
107 р. 171, 1888.
ѴѴас1г8тиі1і. XV. А. 48 р. 158, 1893; Бізз. Ьеіргі&, 1892.
ОиіИгіе. Ркіі. Тгапз. 159 р. 637, 1869; Ркіі. Ма§\ (4) 35 р. 283, 1868; 37 р. 468, 1869.
И. Г. ѴРеЬег. XV. А. 10 р. 103, 304, 472, 1880; Вегі. Вег. 1885, р. 809, СагГз Ке-
регі. 16 р. 389, 1880; Ехпегз Керегі. 22 р. 116, 1886.
V. АиЬеІ. Хізскг. Г. ркуз. Скеіпіе. 28 р. 336, 1899.
Ѵ^асіі8тиііі. Ркуз. Хізскг. 3 р. 79, 1901.
Ргііх КоШгаи8СІі. Дисс. Козіоск, 1904.
Мііпег ипй Сйаііоск. Ркіі. Ма§\ (5) 48 р. 46, 1899.
/?. ѴРеЬег. Апп. Л. Ркуз. (4). 11 р. 1047, 1903.
ЬогЬег^ XV. А. 14 р. 291, 1881.
Ое Нееп Виіі. Ас. Ве1&. (3) 18 р. 192, 1889.
СкгІ8ііап8еп. XV. А. 14 р. 23, 1881.
Ѵ^іпкеітапп. XV. А. 29 р. 1886.
В. В. Станкевичъ. Теплопроводность органическихъ жидкостей. Варшава, 1891.
НеппеЬег^. XV. А. 36 р. 146, 1889.
О. Зае^ег. ХѴіеп. Вег. 99 р. 245, 1890.
Вагиз. Ркіі. Ма§. (5) 33 р. 431, 1892.
Ѵ^іпкеітапп. Ро^. Апп. 153р. 481, 1874; XV. А. 10 р. 668, 1880. Полемика:
Н. Г. ѴУеЬег. XV. А. 11 р. 345, 1880; ОЬегЬеск. Ч\г. А. 7 р. 271, 1879; 11 р. 139, 1880.
Вееіг. XV. А. 8 р. 435, 1879.
Огаеіх. ЧС А. 18 р. 79, 1883; 25 р. 337, 1885.
Н. П. Слугиновъ. Ж. Ф. X. О. 23 р. 456, 1891.
Ѳ. Ѳ. Петрушевскій. Ж. Ф. X. О. 6 р. 56, 1874.
Заерег. ХѴіеп. Вег. 102 р. 253, 483, 1893.
Теплопроводность газовъ.
Къ § 8.
Мах^еіі. Ркіі. Ма§. (4) 20 р. 31 1860; 35 р. 214, 1868
СІаи8Іи8. Ро^. Апп. 115 р. 1, 1862.
Литература.
357
Воііхтапп. ХѴіеп. Вег. 66 II, р. 330, 1872; 72 II, р. 458, 1875; 94 I, р. 891, 1887.
8іе/ап (Теорія). ХѴіеп. Вег. 47 II, р. 81, 1863; 72 II, р. 74, 1875.
ѵ. Ьап%. Ро^. Апп. 145 р. 290, 1872; 148 р. 157, 1873; ХѴіеп. Вег. 64 II, р. 485,
1871; 65 II, р. 415, 1872.
О. Е. Меуег. Кіпеііеске Ткеогіе (Іег Саее, изд. І-ое (1877) стр. 331.
ВигЬигу. Ркіі. Ма#. (5) 30 р. 298, 1890.
Сгоокев. ЫаЬиге (англ.) 23 р. 234.
Воііотіеу. Тгапе. В. 8ос. 178 р. 447, 1887.
Апйгехѵв. Ргос. Коу. Ігіек. Асайету 1 р. 465, 1840.
Сгоѵе. Ркіі. Ма&. (3) 27 р. 445, 1845; Ро^. Апп. 71 р. 194, 1847; 78 р. 366, 1849.
Ма^тіз. Ро$&. Апп. 112 р. 160 351, 497, 1860; Ркіі. Ма&. (4) 22 р. 1, 1861.
Ыагг. Ро&р;. Апп. 142 р. 143, 1871.
Ви//. Ро^. Апп. 158 р. 177, 1876; Л. сі. ркуе. 5 р. 357, 1876.
8іе/ап. (Опыты). ХѴіеп. Вег. 65, II р. 45, 1872; 72, II р. 69, 1875 ; 74, II р. 438, 1876
СагГе Верегіог. 8 р. 64, 1872; 13 р. 290, 1877.
Ріапск. ХѴіеп. Вег. 72, II р. 269, 1875.
Кипйі ипй ѴГагЬигр. Ро§^. Апп. 156 р. 177, 1875; Вегі. Вег. 1875 р. 160.
Сгаеіх. XV. А. 14 р. 232, 511, 1881.
ѴѴіпкеІтапп. Ро$&. Апп. 156 р. 497, 1875; 157 р. 497, 1875; 159 р. 177. 1876;
XV. А. 1 р. 63, 1877; 19 р. 649, 1883; 29 р. 68, 1866; 44 р. 177,429, 1891; 48 р. 180, 1893.
СкгІ8ііап8еп. XV. А. 14 р. 23, 1881; 19 р. 282, 1883.
8скІеіеппаскег. XV. А. 34 р. 623, 1888; 36 р. 346, 1889.
Еіскот. XV. А. 40 р. 697, 1890.
Ное/кег. Віее. Лепа, 1892; ВеіЫ. 18 р. 742, 1894.
8тоІискохѵ8кі. XV. А. 64 р. 101, 1898.
Киііа. XV. А. 54 р. 104, 1895. Віее. Мйпскеп 1894.
Е&оп Миеііег. XV. А. 60 р. 82, 1897; Віее. Мйпскеп, 1896; Ркуе. Хіескг. 2 р. 161,
19о<>; Віее. Егіап^еп, 1901.
Ескегіеіп. Апп. й. Ркуе. (4) 3 р. 120. 1900; Рго^г. Ѳутп. 81. 81еркап іп Аи&е-
Ьиг^, 1902: Віее. Мйпскеп, 1900.
Коск. XV. А. 19 р. 857, 1883.
Сотрап. С. В. 133 р. 813, 1202, 1901.
МекІІ8. Віее. НаІІе, 1902.
Егіск Хіеріег. Дисс. НаІІе, 1904.
Р. Сііпікег. Дисс. НаІІе, 1906.
8ски'агхе. Ркуе. Хіескг. 3 р. 264, 1902; 4 р. 229, 1903; В. А. 11 р. 303, 1903.
Накп. Апп. й. Ркуе. (4) 12 р. 442, 1903.
Сопгаи и. МещтеЬаиег іп О. Е. Меуег. Кіпеііеске Ткеогіе йег Саее, 2-іѳ АиІІ.
Яиеаіге р. 128. Вгееіаи 1899.
\Ѵаск8тиік. Ркуе. Йіескг. 9 р. 235, 1908.
Г-жа Васильева. Ркуе. Хіескг. 5 р. 737, 1904.
Мегпві. ВоІІгтапп-Еееіескгііі р. 904, 1904.
Марпапіпі. Вепйіс. сі. Ьіпсеі 6, 1897; Сагг. сіііт. 30 р. 404, 1900.
Ееіісіапі. М. Сіт. (5) 7 р. 18, 1904; Ркуе. Еіескг. 6 р. 20, 1905.
Раиіі. Апп. й. Ркуе. (4) 23 р. 907, 1907.
Гоай. Ргос. В. 8ос. 83 р. 19, 1909.
8оййу а, Веггу. Ргос. В. 8ос. 83 р. 254, 576, 1910.
Кпий8еп. Апп. й. Рк. (4) 34 р. 593, 1911.
8тоІискои'8кі. Ркіі. Ма&. (6) 21 р. 11, 1911
Къ § 9.
Оезргеіх. Ро&§. Апп. 142 р. 626, 1871.
Ѵ^іейетапп, С. Ро^. Апп. 95 р. 337, 1855.
Ап^вігоепі. Ыоѵа Асіа 8ос. СТреа1а (3) 3 р. 51, 1861.
358
Термодинамика.
8тоІискоъі)8кі. №. А. 61 р. 101, 1898; ХѴіеп. Вег. 107 р. 304, 1898; 108 р. 5, 1899;
РЫІ. Ма^. (5) 46 р. 192, 1898; Оевіег. Сііет. 21^. 2 р. 385, 1899; Сііет. СепігаІЫ. 2
р. 353, 1899.
Секгске. Апп. д. Рііув. (4) 2 р. 102. 1900.
Роговскій. С. В. 137, 1903; 140 р. 1179, 1905; Ж. Ф. X. О. 35 р. 1244, 1903; 40
р. 213, 1908.
Вгизск. РЫІ. Ма&. 45 р. 31, 1898.
Роіззоп, см. Зтоіиско^зкі. XV. А. 64 р. 102, 1898.
Хвольсонъ. Ж. Ф. X. Общ. 40 р. 1, 1908.
Коловратъ-Червинскій. Ж. Ф. X. Общ. 40 р. 5, 1908.
Лазаревъ. Ж. Ф. X. Общ. 43 р. 69, 1911 ; Дисс. Москва, 1910.
Кпийзеп. Апп. <1. Рііуе. (4) 34 р. 593, 1911.
ГЛАВА ВОСЬМАЯ.
Основы термодинамики.
§ 1. Введеніе. Термодинамика представляетъ обширный и, по своему
характеру, разнообразію примѣненій и глубинѣ основныхъ мыслей и по-
ложеній, одинъ изъ важнѣйшихъ и интереснѣйшихъ отдѣловъ физики.
Чуждая гипотезъ, построенная на абсолютно достовѣрныхъ, хотя и
добытыхъ эмпирически основаніяхъ, она представляетъ единственный
отдѣлъ теоретической физики, выводы котораго не измѣнятся по суще-
ству при какомъ бы то ни было дальнѣйшемъ развитіи науки. Ея исход-
ными положеніями - опредѣляются основныя свойства окружающаго насъ
міра явленій, опредѣляются руководящія начала всего, что происходитъ
въ доступной нашему наблюденію вселенной, не исключая явленій жизни,
хотя и управляемыхъ еще другими, намъ неизвѣстными началами, но, во
всякомъ случаѣ, всегда и безусловно также подчиненныхъ началамъ тер-
модинамики. Раскрывая путь къ наиболѣе глубокому пониманію физи-
ческихъ явленій, термодинамика въ то же время несравненно обширнѣе
всякаго другого отдѣла физики рѣшаетъ основную задачу этой науки,
указывая на закономѣрныя связи между явленіями, и тѣмъ самымъ вы-
ясняя свойства веществъ, изъ которыхъ построенъ міръ. По досговѣрности
и реальности своихъ выводовъ она далеко оставляетъ за собою многіе отдѣлы
математической физики, которые, какъ напр. теорія теплопроводности,
построены на основаніяхъ весьма простыхъ, но не вполнѣ отвѣчающихъ
реальной дѣйствительности, и даже великое твореніе человѣческаго генія,
небесную механику, цѣликомъ основанную на одномъ эмпирическомъ
законѣ, обѣ половины котораго, можетъ быть, не абсолютно точны.
Термодинамика, въ обширномъ смыслѣ слова, есть наука объ энергіи
и ея свойствахъ, откуда уже явствуетъ, что она должна имѣть отношеніе
ко всѣмъ отдѣламъ физики и химіи, что она должна быть одинаково при-
ложима къ явленіямъ молекулярнымъ и къ явленіямъ, происходящимъ во
вселенной, къ матеріи и къ эфиру. Физика, химія и техника (паровая)
развиваются при ея помощи; придетъ время., когда н біологія пойметъ
ея міровое значеніе.
Введеніе.
359
Имѣя значеніе для всѣхъ отдѣловъ физики, термодинамика могла
бы быть разсматриваема, какъ самостоятельный, если угодно, какъ основ-
ной отдѣлъ физики, и тогда ее слѣдовало бы назвать энергетикой.
Термодинамику прежде называли, а иногда и теперь еще называ-
ютъ «механическою теоріею тепла».
Термодинамика построена на двухъ истинахъ, которыя принято на-
зывать началами. Одно изъ нихъ всегда обозначается, какъ «на-
чало первое», а другое, какъ «начало второе». Они представля-
ютъ истины, эмпирически найденныя, которыя не могутъ быть
выведены изъ другихъ еще болѣе основныхъ началъ, каковыми предста-
вляются напр. основные законы движенія; по крайней мѣрѣ такіе вы-
воды невозможны съ тою степенью общности, которою обладаютъ два
< начала» термодинамики. Но несмотря на эмпиризмъ пути, приведшаго
къ познанію этихъ началъ, ихъ справедливость абсолютно достовѣрна,
ибо всѣ наблюдаемыя нами явленія происходятъ согласно съ ними и, что
самое главное, въ весьма большомъ числѣ случаевъ удалось, исходя изъ
двухъ началъ термодинамики, предсказать новыя истины, предусмотрѣть
новыя закономѣрныя связи между явленіями, а слѣд. и новыя свойства
матеріи; и во всѣхъ этихъ случаяхъ предсказанія оправдывались опыт-
ными изслѣдованіями.
Мы увидимъ далѣе, что характеръ двухъ началъ весьма различный.
Первое начало весьма простое и различныя его формулировки относятся
между собою, какъ обобщеніе къ частному случаю, или какъ причина къ
очевидному слѣдствію. Второе начало менѣе просто и различныя его
формулировки, которыя дали Сагпоі, С 1 а и 8 і п 8, ЬогД Кеіѵіп,
НеІпгЬоИг, Ріанск, ВоИгшапп, Ріаипйіег, ОіЬЬз и др.,
съ перваго взгляда выражаютъ какъ бы совершенно различныя и между
собою ничѣмъ не связанныя истины. Необходимо глу бже вдуматься,
чтобы понять, что эти формулировки дѣйствительно выражаютъ одну и
ту же истину, какъ бы схваченную съ различныхъ сторонъ.
Первое начало было выяснено трудами ЕоЪегі Мауег’а (1842),
4ои1е’я (1843) и Неішйоііг’а (1847). Второе начало было впервые
высказано 8а<1і Сагпоі (1824), хотя въ формѣ, соотвѣтствовавшей воззрѣ-
ніямъ на теплоту, господствовавшимъ въ его время. С1аіі8Іи8 (1850)
преобразовалъ идеи СагпоЬ въ духѣ новаго ученія о теплотѣ, какъ о
формѣ энергіи; онъ и \Ѵ. ТЬошзоп (Ьогсі Кеіѵіп, 1851), выска-
завшій въ иной формѣ тѣ же истины, могутъ быть названы, рядомъ съ
Сагпоі, основателями термодинамики. Новый періодъ въ исторіи этой
науки беретъ евое начало въ концѣ семидесятыхъ годовъ истекшаго
XIX столѣтія. Работы Неітііоііг’а (1884) и ѲіЬЬз’а (1876, над-
лежащее вниманіе обращено на нихъ въ концѣ восьмидесятыхъ годовъ)
дали термодинамикѣ новое направленіе, во первыхъ введеніемъ понятій
о свободной энергіи и о родственномъ ей термодинамическомъ потенці-
алѣ, во вторыхъ развитіемъ ученія о т. наз. необратимыхъ процессахъ и,
наконецъ, въ третьихъ замѣчательными обобщеніями формулъ и выво-
360
Термодинамика.
довъ (СтіЬЪк), давшими возможность успѣшно прилагать термодинамику
къ такимъ явленіямъ, которыя до этого находились внѣ сферы ея из-
слѣдованій. На почвѣ термодинамики возникла и кинетическая теорія
газовъ (т. 1).
§ 2. Первое начало. Первое начало различно формулируется, смо-
тря по тому, съ какой точки зрѣнія мы смотримъ на ту науку, одинъ
изъ двухъ фундаментовъ которой оно составляетъ.
Для науки объ энергіи и ея свойствахъ первое начало есть
ни что иное, какъ принципъ сохраненія энергіи. Приборъ, дающій не-
прерывно работу безъ затраты энергіи, мы назовемъ теперь регреіпит
тоЬіІе перваго рода (для отличія отъ регреіпит тоЫІе второго
рода, съ которымъ мы познакомимся ниже). Мы видѣли въ т. I, какъ
тѣсно связаны между собою сохраненіе энергіи и невозможность регре-
і и и пі тоЫІе; поэтому первое начало можно формулировать и такъ:
Регреѣиит тоЬіІе перваго рода невозможно.
Вспомнимъ, что мы въ т. I высказывали, какъ принципъ первый,
что энергія тѣла есть функція его состоянія, т.-е. коли-
чественно вполнѣ этимъ состояніемъ опредѣляется.
Для термодинамики, въ которой ученію о теплотѣ дано осо-
бое значеніе, первое начало и заключается въ допущеніи, что теплота
есть форма энергіи, а потому она эквивалентна нѣкоторой работѣ.
Если теплоту д и работу г измѣрять опредѣленными единицами и если
эти двѣ величины эквивалентны, т.-е. одна изъ нихъ затрачивается при
полученіи другой, то между числами д и г всегда существуетъ соотношеніе
г = Ед 1
д = Аг /
(1)
гдѣ Е — механическій эквивалентъ тепла и А = 1 : Е термическій экви-
валентъ работы, постоянныя числа. Съ этой точки зрѣнія первое на-
чало еще называется началомъ (или принципомъ) экви-
валентности.
Можно было бы еще болѣе съузить первое начало. За первое
начало механической теоріи тепла можно было бы принять
положеніе, что теплота есть кинетическая энергія движе-
нія частицъ и атомовъ тѣлъ. Но этимъ мы ввели бы въ самое
начало элементъ гипотетическій и, можетъ быть, не абсолютно точный, ибо
мы не можемъ утверждать, чтобы всѣ движенія частицъ и атомовъ соот-
вѣтствовали только тепловой энергіи тѣла.
Приведенныя три формулировки перваго начала относятся другъ къ
другу, какъ общій случай къ частному, или какъ причина (теплота есть
кинетическая энергія) къ слѣдствію (теплота, эквивалентна работѣ).
Работы ученыхъ создавшихъ первое начало, какъ явствуетъ изъ
предъидущаго, распадаются на три категоріи, соотвѣтственно слѣдующимъ
тремъ достигнутымъ результатамъ:
1) Теплота не есть вещество, но опредѣляется движеніемъ частицъ.
Первое начало.
361
2) Энергія не создается и не теряется; всѣ формы энергіи эквива-
лентны другъ другу и работѣ.
3) Опредѣленіе численнаго значенія Е механическаго эквивалента
теплоты.
Теплота считалась до сороковыхъ годовъ прошлаго столѣтія за особаго
рода вещество, за «теплородъ», причемъ существовали весьма разно-
образные взгляды на отношеніе этого вещества къ флогистону химиковт,
и къ свѣтовому веществу приверженцевъ теоріи истеченія. Вопросъ о
вѣсомости теплорода долгое время занималъ физиковъ, пока опыты
Кит Іо г (Га, изложенные въ статьѣ «Ап Іпдиігу сопсегпіп^ Ше АѴеі^Ы
оі Неаі (1799). не доказали, что теплородъ долженъ быть отнесенъ къ
числу такъ называемыхъ < невѣсомыхъ». Скрытая теплота объяснялась
способностью теплорода соединяться съ матеріей и тѣмъ самымъ пере-
ставать быть свободнымъ и ощутительнымъ (В 1 а с к). Выдѣленіе тепла
при треніи объяснялось переходомъ вещества въ порошкообразное состоя-
ніе (опилки, стружки), причемъ предполагалось, что теплоемкость порошка
меньше теплоемкости сплошного тѣла, т.-е. что порошокъ содержитъ, при
одинаковой температурѣ, меньшій запасъ теплорода. Мнѣніе, что теплота
есть движеніе, а также болѣе или менѣе туманныя указанія на неуничто-
жаемость силы или иной, не всегда точно опредѣленной величины, встрѣ-
чаются у многихъ авторовъ.
ЬогсІ Васоп весьма опредѣленно высказалъ мнѣніе, что теплота
есть движеніе ; оно повторяется у В о у 1 е’я, X е лѵ I о п’а, Ь а ѵ о і $ і е г и др.
Огромное значеніе имѣли опыты ВишІогсГа (1798) и Нпшріігу
Оаху (1799). Графъ Китіогй (Веп?]апііп Тйотйоп, америка-
нецъ жившій въ Баваріи и получившій здѣсь титулъ графа Ни тіо г (Га)
опредѣлилъ нагрѣваніе, сопровождающее сверленіе пушекъ. Помѣстивъ
сверло и цилиндръ въ водѣ, онъ нашелъ, что 26,6 фунта воды черезъ
2г/2 часа нагрѣвались до кипѣнія. Онъ указываетъ, что вращеніе сверла
могло быть произведено одною лошадью. Отсюда является возможность
произвести грубое опредѣленіе механическаго эквивалента теплоты, если
допустить, что работа лошади равна 75 килогр.-метрамъ въ сек. Эта ра-
бота могла въ 2х/2 часа нагрѣть 26,6 ф. воды отъ 6° до 100°; отсюда
легко получить Е ±= 570.9, т.-е. что одна большая калорія эквивалентна
570,9 килогр.-метрамъ. Хотя это число довольно далеко отъ истин-
наго (427), но оно по крайней мѣрѣ одинаковаго съ нимъ порядка. Боль-
шое значеніе опытовъ Ни тіо г (Га заключалось въ томъ, что онъ непо-
средственными опытами доказалъ отсутствіе измѣненія тепло-
емкости при переходѣ сплошной массы въ порошко-
образные опилки. Этимъ уничтожалось приведенное выше объяс-
неніе цагрѣванія тѣлъ, сопровождающаго треніе. Указывая на неисчер-
паемость тренія, какъ источника теплоты, К и ш I о г сі рѣзко высказыва-
етъ мысль, что нѣчто, имѣющее такія свойства, какъ появляющаяся при
треніи теплота, можетъ быть только д в и ж е н і е м ъ.
Еще болѣе рѣшающее значеніе имѣли опыты Саѵу (1799 г.), ко-
362
Термодинамика.
торый подвергалъ взаимному тренію два куска льда, помѣщенные подъ
колоколомъ воздушнаго насоса, охлажденнаго ниже нуля. При этомъ оба
куска льда, температура которыхъ была около — 2°С (290/7), вполнѣ рас-
таяли; образовавшаяся вода имѣла температуру около -|-2()С(350/7). Те-
плоемкость воды вдвое больше теплоемкости льда, а слѣд. выдѣленіе тепла,
необходимаго для плавленія, сопровождалось въ этомъ опытѣ увеличені-
емъ, а не уменьшеніемъ теплоемкости вещества, подвергаемаго тренію.
Самъ Баѵу только въ 1812 г. вполнѣ убѣдился, что его опыты имѣютъ
рѣшающее значеніе и что «ійс іштесііаіе сате оі йеаі із тоііоп». Къ
взгляду КитіогсГа и Баѵу присоединились ТЬотаз Ѵоип$
(1807) и Атрёге (1821).
Какъ на предшественниковъ В. Мауег’а слѣдуетъ указать на
Мойг’а (1837), Зё^піп’а (1839) и Соісііп^’а (1842), а также на
8а(1і Сагпоі. Статья Мойг’а появилась въ 1837 г. въ весьма мало
распространенномъ журналѣ и самъ авторъ не зналъ объ ея напечатаніи.
Акіпе указалъ на нее въ 1864 г. и самъ Мойг вновь напечаталъ ее
въ 1868.г. 8ё^иіп напечаталъ свою статью въ 1839 г., подъ . заглаві-
емъ >0 вліяніи желѣзныхъ дорогъ и объ искусствѣ ихъ построить» ; на-
конецъ С о 1 (1 і п представилъ около 1842 г. датской Академіи рядъ ста-
тей, которыя однако были напечатаны только въ 1851 г. Въ указанныхъ
трехъ работахъ болѣе или менѣе ясно высказаны мысли объ эквивалент-
ности теплоты и работы, о сохраненіи или неуничтожаемое™ чего то,
помимо матеріи и т. под. Въ работѣ 8 ё § и і п’а встрѣчается даже вы-
численіе механическаго эквивалента тепла, приблизительно по методу
К. Мауег’а (см. ниже); онъ нашелъ ^ = 367. Наконецъ слѣдуетъ упо-
мянуть, что въ посмертномъ изданіи мелкихъ замѣтокъ 8 а (і і Сагпоѣ
(умеръ 1832) находятся ясныя указанія не только на первое начало, но
п на важнѣйшіе способы опредѣленія механическаго эквивалента теплоты.
Статья В. Мауег’а, въ которой впервые встрѣчается научно об-
основанное вычисленіе механическаго эквивалента теплоты, напечатана
въ 1842 г. <ТоиІе началъ свои экспериментальныя опредѣленія меха-
ническаго эквивалента тепла по цѣлому ряду разнообразныхъ способовъ
около 1840 г. Первая изъ этихъ работъ (читана 21 авг. 1843 въ собраніи
Британской Ассоціаціи въ Коркѣ) напечатана въ 1843 г. Знаменитые
опыты тренія жидкостей изложены въ 1847 г.; подробное ихъ описаніе
появилось въ 1850 г. Классическая работа НеІшйоІЬя’а «О сохране-
ніи силы» (ПеЬег діе Егйаііип^ йег КгаЙ), въ которой принципъ сохра-
ненія энергіи (какъ нынѣ принято говорить) распространенъ на всѣ
области физическихъ явленій, появилась въ 1847 г.
§ 3. Механическій эквивалентъ теплоты. Изъ равенства (1) стр. 360
г = Ед....................................................(2)
гдѣ г работа, д эквивалентное ей количество теплоты, ясно, что Е равно
числу единицъ работы, эквивалентныхъ одной единицѣ тепла; оно зави-
ситъ отъ выбора единицъ работы и тепла. На стр. 157 мы говорили объ
Механическій эквивалентъ теплоты.
363
единицахъ тепла и видѣли, что, вслѣдствіе зависимости теплоемкости воды
отъ температуры, необходимо при опредѣленіи калоріи указать, къ какой
температурѣ она относится.
Если работу измѣрять въ килограммометрахъ и подъ килограммомъ
разумѣть вѣсъ извѣстнаго эталона массы, то величина килограммометра,
а слѣд. и величина Д будетъ зависѣть отъ широты мѣста, точнѣе отъ
ускоренія Чѣмъ больше тѣмъ больше абсолютная величина кило-
граммометра и тѣмъ меньше Е, Если Е и § относятся къ одной точкѣ
на поверхности земли, Е' и къ другой, то мы имѣемъ
Килогр.-мѳтръ равенъ § . ІО7 эргамъ = § дж.улямъ, гдѣ § должно быть
выражено въ метрахъ и секундахъ. Если принять большую калорію рав-
ною 4200 . ІО7 эргамъ, то окажется, что большая калорія равна 4200 :
килограммометрамъ. Обобщая скажемъ: если въ системѣ малая
кало рія-эргъ
Ь = е 10? Эргъ = е Джуль .........................(О
мал. кал. мал. кал.
то въ системѣ большая калорія — к ил огр.-ме тръ
ЮООб?
ё
килогр.-метръ
болып. кал.
(5)
гдѣ § должно быть
метръ
выражено въ единицахъ і--------т.-е.я
ѵсек.)2
около 9,8. Величина е близка къ 4,2 и зависитъ только отъ
выбора температуры, къ которой отнесена малая кало-
рія. Принимая ^ = 4,2 и «§-=9,8, получаемъ во второй системѣ Е —
= 428,6; если г=4,189 и ^=9,81 то ^ = 427,0; ^ = 4,189 и ^=9,82
даютъ Е— 426,6. Если опредѣлять малую калорію среднею теплоемкостью
воды между 0° и 100°, то е, а слѣд. и Е еще болѣе уменьшаются.
Переходимъ къ методамъ опредѣленія величинъ е и Е,
Эти методы могутъ быть раздѣлены на методы теоретическіе п методы
экспериментальные, хотя они всѣ, въ сущности, основаны на сравненіи
нѣкоторой работы съ эквивалентнымъ ей количествомъ теплоты. Но въ
способахъ теоретическихъ это сравненіе какъ бы замаскировано тѣмъ, что
мы вычисляемъ 2? на основаніи готовой формулы, относящейся къ
какому-либо физическому явленію и содержащей, кромѣ Е, различныя фи-
зическія величины, численное значеніе которыхъ намъ уже извѣстно на
основаніи спеціальныхъ измѣреній. Въ экспериментальныхъ методахъ по-
лучаютъ Е путемъ возможно непосредственнаго сравненія величинъ г и «у,
т.-е. осуществляя на опытѣ одинъ изъ случаевъ превращенія работы въ
теплоту, или, въ рѣдкихъ случаяхъ, превращенія теплоты въ работу. Тео-
ретическихъ способовъ опредѣленія Е существуетъ два: способъ К. М а у е г’а
и способъ, основанный на свойствахъ насыщенныхъ паровъ.
364
Термодинамика.
I. Способъ К. М а у е г’а, Теплоемкость Ср газа при постоянномъ
давленіи больше теплоемкости сѵ- при постоянномъ объемѣ, такъ какъ
газъ, расширяясь, производитъ работу. Сравнивая эту работу съ
разностью ср — сѵ, мы вывели формулу (т. I)
гдѣ /? постоянная формулы К л а п е и р о н а рѵ == равная
/? = 29.27(5 1......................................................(7)
если за единицу длины принять метръ, за единицу вѣса килограммъ;
<5 есть плотность газа относительно воздуха. Ниже будетъ вновь выве-
дена формула Гб); она даетъ
= ......................(8)
Ср сѵ
Если ввести величину к = ср\ сѵ, которую мы подробно разсмотрѣли
на стр. 216—228, то получается:
Е—* “ .= ... (•)
К. Мауег, принявъ для величинъ, входящихъ въ эти формулы, не-
точныя числа, получилъ 25 = 367. Если въ (8) вставить для воздуха /? =
= 29,3, Ср = 0,2375 и сѵ = 0,1696, то получается
^=124............................(10)
Коіѵіапй находитъ 7; = 430,3, если принять к = 1,4053 (Воепі-
$еп), 25=436,6, если & = 1,397 (Ата^аі) и 25 = 429,6, если принять
число В е п а и 1С для скорости звука. Какъ среднее, наиболѣе вѣроятное,
Волѵіаікі находитъ для широты Балтиморы (39°18',9, ^- = 9,8005)
Е = 127,7........................(11)
Формула (6) относится къ идеальнымъ газамъ. Если вмѣсто урав-
ненія рѵ = РГ принять одно изъ другихъ предложенныхъ уравненій со-
стоянія, напр. уравненіе Ѵап (іег \Ѵ а а 1 ь’а или уравненіе С 1 а и -
8 іи 8’а, то формула (9) принимаетъ довольно сложный видъ. Если при-
нять формулу
рѵ । и
г = а 4-- Ь
РЫ V
+ сІ—
\ ѵ I I ѵ
которая по й о с Ь пі а п п’у выражаетъ наблюденія К е § и а и И надъ воз-
духомъ и углекислымъ газомъ, то вмѣсто (8) получается весьма сложное
выраженіе, которое, если вставить численныя значенія постоянныхъ (2,
с, /, т, п для воздуха даетъ 25 = 429.6. Числа, относящіяся къ СО2 даютъ
Е = 436,6.
Механическій эквивалентъ теплоты.
Збб
II. Способъ, основанный на свойствахъ насыщен-
ныхъ паровъ. Мы докажемъ впослѣдствіи слѣдующую важную формулу
{? = Тр (5 - О ....... (12)
Е аі
въ которой р скрытая теплота испаренія жидкости. Т абсолютная темпе-
ратура, при которой происходить испареніе, 5 удѣльный объемъ на-
сыщеннаго пара (число куб. метровъ, занимаемыхъ однимъ килограммомъ),
о удѣльный объемъ жидкости, р упругость насыщеннаго пара, которая
есть функція температуры і, производная этой функціи. Формула (12)
можетъ служить для опредѣленія величины Е. Регоі находитъ Е =
= 424,63, прилагая ее къ водѣ.
Переходимъ къ чисто экспериментальнымъ сравненіямъ ра-
боты г и экваивалентной ей теплоты д. Такихъ способовъ существуетъ
цѣлый рядъ.
III. Способъ тренія. Если внутри жидкости вращать ось, снаб-
женную лопастями, то приходится затратить нѣкоторую работу г, чтобы
преодолѣть треніе (сопротивленіе) жидкости; въ послѣдней при этомъ
выдѣляется нѣкоторое количество д теплоты. Опытъ долженъ быть по-
ставленъ такъ, чтобы можно было измѣрить д и г. Этимъ методомъ поль-
зовались З^иіе, Колѵіапд идр.
А. Опыты Яопіе’я. Приборъ, которымъ пользовался Яопіе,
изображенъ на рис. 106. Металлическій сосудъ 5, служащій калориме-
тромъ, установленъ на деревянной скамейкѣ, площадка которой состоитъ
изъ отдѣльныхъ деревянныхъ полосокъ. Черезъ этотъ сосудъ, изображен-
ный въ разрѣзѣ на рис. 107, проходитъ ось, снабженная боковыми крыль-
ями или лопастями. Эти крылья расположены по четыре въ одинъ рядъ,
причемъ два имѣютъ форму полосокъ и два форму, напоминающую ло-
пату (а). Такихъ рядовъ крыльевъ имѣется восемь; они расположены
въ вертикальныхъ плоскостяхъ, составляющихъ между собою равные углы
въ 45°. Къ боковой стѣнкѣ сосуда также прикрѣплены ряды пластинокъ
въ радіальномъ направленіи (Л); такихъ рядовъ четыре и они отстоятъ
другъ отъ друга на 90°. Ихъ форма такова, что онѣ не препятствуютъ
вращенію крыльевъ а, но зато онѣ не позволяютъ водѣ, налитой въ
сосудъ, вращаться цѣлою массою, вслѣдствіе чего вращеніе крыльевъ встрѣ-
чаетъ весьма большое сопротивленіе. Въ крышкѣ калориметра сдѣлано
боковое отверстіе для ввода термометра до и послѣ опыта. Деревянный
цилиндръ (1 разобщаетъ двѣ металлическія части оси, препятствуя потерѣ
тепла черезъ ось. Па верхнюю часть оси можетъ быть насаженъ дере-
вянный цилиндръ Л, вокругъ котораго навиты двѣ веревки въ одинако-
вомъ направленіи; онѣ оставляютъ поверхность цилиндра въ точкахъ,
другъ другу противоположныхъ, такъ что, если тянуть за обѣ веревки,
то онѣ одновременно сматываются съ цилиндра, который при этомъ вра-
щается. Концы веревокъ прикрѣплены къ неподвижнымъ блокамъ С и /?,
366
Термодинамика.
оси которыхъ для уменьшенія тренія лежатъ на окружностяхъ колеси-
ковъ. На болѣе толстыя части осей блоковъ С и О намотаны веревки,
къ концамъ которыхъ привѣшены свинцовые грузы Е и Е, Рядомъ по-
ставленныя линейки Н и С, снабженныя дѣленіями, опредѣляютъ высоту,
на которую подняты грузы Л и Е надъ поверхностью пола, до котораго
они могутъ опускаться.
Ходъ опыта таковъ: въ калориметръ, теплоемкость всѣхъ частей
котораго извѣстна, налита вода; вѣсъ и температура ея извѣстны. Гири
Рис. 106.
Рис. 107.
с
Е и Е приподняты, веревка намотана на цилиндръ А. Гири Е и Е за-
ставляютъ падать; онѣ вращаютъ блоки С и О, на которые наматываются ве-
ревки, вслѣдствіе чего вращается цилиндръ А, и съ нимъ ось и крылья
внутри калориметра В. Опытъ повторяется 20 разъ сряду, причемъ каж-
дый разъ гири Е и Е поднимаются на прежнюю высоту и веревки нама-
тываются на цилиндръ Л, предварительно снятый съ оси, чтобы это на-
матываніе не сопровождалось вращеніемъ оси и крыльевъ внутри В. Когда
опусканіе гирь было повторено 20 разъ, вновь измѣрялась' температура
воды калориметра. Повышеніе температуры составляло около 0°,5 Е.
Чтобы вычислить Е, необходимо было опредѣлить эквивалентныя
одна другой величины теплоты д, выдѣлившейся въ калориметрѣ вслѣдствіе
тренія, и работы г, затраченной на преодолѣваніе этого тренія. Теплота д
получалась, какъ произведеніе теплоемкости калориметра съ водою на по-
вышеніе его температуры, исправленное на потерю тепла вслѣдствіе луче-
испусканія.
Пусть Р вѣсъ одной изъ гирь, И высота, съ которой гири опуска-
лись ; въ такомъ случаѣ вся работа, произведенная при п поднятіяхъ
обѣихъ гирь (п = 20), равна 2пРИ. Однако не вся эта работа затрачива-
лась на преодолѣваніе тренія воды.
Во первыхъ гири достигаютъ пола, обладая нѣкоторою скоростью г/,
Механическій эквивалентъ теплоты.
367
1 Р 9
а слѣд. и энергіею ------ѵ, которая въ моментъ удара гирь переходитъ
2 Ѵ2
въ теплоту, но въ калориметръ не попадаетъ. Величина — Н1 есть вы-
сота, съ которой гири должны падать свободно, чтобы достигнуть пола
со скоростью ѵ; ясно, что работа 2пРК1 для калориметра пропадаетъ. Но
кромѣ того часть / работы тратится на преодолѣваніе тренія осей бло-
ковъ С и и на выпрямленіе и сгибаніе веревокъ. Съ другой стороны
натянутыя веревки укорачиваются послѣ того, какъ гири остановились, и
при этомъ производятъ работу г", идущую на вращеніе оси и крыльевъ.
Вся работа г, эквивалентная д, равна слѣдовательно
г = 2пРЦг — Лх) — / 4- г".
Не останавливаемся на деталяхъ опредѣленія поправокъ г' и г". Какъ
среднее изъ всѣхъ опытовъ, произведенныхъ съ водою, Лопіе нашелъ
килогр.-метр
= 424,30 —=----—-------
болыи. калор.
Лопіе производилъ также опыты надъ треніемъ ртути. Калори-
метръ и металлическія части внутри него сдѣланы изъ чугуна. Къ оси
придѣланы шесть вертикальныхъ большихъ крыльевъ, а къ стѣнкѣ кало-
риметра восемь неподвижныхъ перегородокъ. Малая теплоемкость ртути
имѣетъ ту выгоду, что получается большое повышеніе температуры; оно
доходило до 2,°4 Е. Два ряда опытовъ со ртутью дали
Е = 424,37
килогр.-метр.
б. калор.
^ = 425,77
килогр.-метр.
б. калор.
Далѣе Лопіе опредѣлилъ Е, производя въ калориметрѣ треніе чу-
гуна объ чугунъ. Приборъ, которымъ инъ при этомъ пользовался, изо-
браженъ на рис. 108 въ разрѣзѣ. На ось, вращающуюся внутри калори-
метра, наглухо насажена круглая пластинка Ь, имѣющая форму усѣченнаго
конуса. Вдоль той же оси свободно скользятъ два кольца, съ прикрѣп-
ленными къ нимъ рамкою с, трубкою е и круглою чугунною пластинкою
форма которой понятна изъ рисунка. Къ рамкѣ е прикрѣпленъ стержень
соединенный съ одноплечимъ рычагомъ /. Если на правый конецъ этого
рычага производить давленіе, то пластинка (1 надавливаетъ на вращающійся
кругъ Ь\ между ними происходитъ треніе, сопротивляющееся вращенію
оси, т.-е. спуску свинцовыхъ гирь. Потерянная энергія движенія гирь,
если ввести необходимыя поправки, появляется въ калориметрѣ, напол-
ненномъ водою, въ видѣ теплоты. Кромѣ поправокъ, упомянутыхъ выше,
Лопіе въ этихъ опытахъ ввелъ еще одну, стараясь опредѣлить, какая
часть работы гирь тратилась на сотрясеніе всего прибора и на получе-
ніе довольно сильнаго звука, сопровождавшаго треніе чугуна объ чугунъ.
Термодинамика.
Нагрѣваніе воды въ одномъ изъ рядовъ опытовъ доходило до 4°,3, въ дру-
гомъ до 1°,5. Среднее изъ всѣхъ вообще опытовъ Лбпіе’я даетъ
Е = 423,4
килогр.-метр.
б. калор.
причемъ б. калорія отнесена къ температурѣ воды между 13° и 15°.
3 о и 1 е повторилъ опредѣ-
леніе Е при помощи тренія
въ 1878 г. При этомъ онъ измѣ-
нилъ устройство прибора, слѣдуя
мысли, высказанной Н і г п’омъ
(ТЬёогіе Мёсапідие сіе Іа СЬа-
[епг, 3 изд. стр. 92). Калори-
метръ !г (рис. 109), наполнен-
ный водой и содержащій ось съ
крыльями и неподвижныя пере-
городки, почти вполнѣ свободно
виситъ въ воздухѣ, слегка опи-
раясь на три деревянныхъ стер-
женька, прикрѣпленные къ со-
суду -йу, плавающему въ водѣ, на-
литой въ другой сосудъ ѵ. Ось
Ь приводится во вращеніе отъ руки при помощи двухъ колесъ (I и ег
снабженныхъ рукоятками. На ось Ь насажено маховое колесо / и зубча-
тое колесо соединенное со счетчикомъ р.
Къ боковому краю верхней части калориметра прикрѣплены двѣ ве-
ревки, переброшенныя черезъ неподвижные блоки и снабженные чашеч-
ками АА, на которыя могутъ быть положены гири; пусть р вѣсъ одной
чашечки съ гирями. На рис. 110 показанъ горизонтальный разрѣзъ кало-
риметра (безъ оси) и направленіе двухъ силъ р, стремящихся повернуть
калориметръ въ опредѣленномъ направленіи, причемъ моментъ вращающей
пары равенъ 2од гдѣ р радіусъ сѣченія калориметра. Вращеніе оеи и
крыльевъ въ водѣ стремится повернуть калориметръ въ противоположномъ
направленіи; необходимо регулировать грузы р и скорость вращенія оси
такъ, чтобы калориметръ оставался неподвижнымъ. Въ этомъ случаѣ
треніе внутри калориметра въ каждый данный моментъ дѣйствуетъ, какъ
пара силъ, моментъ которой равенъ 2ор. При полномъ оборотѣ оси ра-
бота этой пары равна 2р . 2лг) = 4л/ю, а при и оборотахъ, произведен-
ныхъ во время опыта и сосчитанныхъ счетчикомъ вся работа г равна
г = клиру
(13)
Эквивалентное количество д теплоты измѣряется повышеніемъ тем-
пературы калориметра. Такимъ способомъ Лоиіе нашелъ 2: = 423.852.
Волѵ 1 ап(1 показалъ, что вычисленія Лои]ея нуждаются въ нѣко-
торыхъ исправленіяхъ (приведеніе температуръ къ воздушному термо-
Механическій эквивалентъ теплоты.
369
метру и др.), послѣ введенія которыхъ получается для широты Б а л -
тиморы и для калоріи, соотвѣтствующей 15°,7,
Е = 426,2.
В. Опыты К о аѵ 1 а п (Га, Місиіезси и другихъ. Опыты
Лопіе’я съ треніемъ были повторены Раѵге’омъ (1858, Е = 413,2) и
Нігп’омъ (Е между 400 и 450). Наи-
болѣе тщательное изслѣдованіе было
произведено К о лѵ Га п (Томъ (1879—80)
по способу, подобному только что опи-
санному. Приборъ Ко\ѵ1апсГа изо-
браженъ на рис. 111. Калориметръ ви-
ситъ на толстой проволокѣ, и составля-
етъ одно цѣлое съ колесомъ, на края
котораго дѣйствуютъ грузы у и р при
помощи двухъ веревокъ, перекинутыхъ
черезъ блоки п. Ось, снабженная сложною
системою крыльевъ, входитъ въ калориметръ снизу; она приводится во вра-
щеніе особымъ керосиновымъ двигателемъ. Безконечный винтъ на оси /е
дѣйствуетъ на хроноскопъ, записывающій число оборотовъ оси; на немъ
же отмѣчаются моменты, когда температура калориметра послѣдовательно
достигала опредѣленныхъ значеній. Съ величайшею тщательностью были
введены всѣ необходимыя поправки для перевода показаній термометра
къ абсолютной шкалѣ и др. Грузы р и о имѣли вѣсъ около 7,5 кгр.;
повышеніе температуры доходило до 35° и могло быть доведено до 45°
въ часъ. Обыкновенно наблюденіе продолжалось около 40 минутъ; на-
чальная температура воды бралась различною, иногда 0°, иногда 20°. Такъ
какъ отмѣчались моменты достиженія различныхъ температуръ, то можно
было опредѣлить Е, т.-е. работу, потребную для нагрѣванія 1 кгр. воды
на 1°. какъ функцію температуры, по своему ходу очевидно тождествен-
ную съ теплоемкостью воды, какъ функціи температуры. Оказалось, что
Е уменьшается отъ 5° до 30° и затѣмъ начинаетъ увеличиваться ; въ
этихъ опытахъ заключается весьма точное опредѣле-
ніе зависимости теплоемкости воды отъ температуры.
Мы не приводимъ тѣхъ чиселъ, которыя нашелъ Колѵіапй и ко-
КУРСЪ ФИЗИКИ О ХВОЛЬСОНА. Т. III, изд. 3-е. 24
370
Термодинамика.
торыя затѣмъ были исправлены различными учеными такъ какъ эти
числа уже были даны нами на стр. 160—163, равно какъ и результаты
опредѣленій СггіТТііІі 8*а, Саіепсіаг’а и Вагпев’а, а также 8сЬи-
біег’а и Огайоп’а. Мы видѣли, что калорія 17°—18° эквивалентна
Рис. іи.
4,184 джуля = 41,84 мегаэрга, и что она же равна средней калоріи
между 0° и 100°.
Приблизительно тѣмъ же способомъ, какъ Еоуѵіапсі, производилъ
свои измѣренія М і с п 1 е 8 с и. Для Парижа и для температуры между
10° и 13° онъ находитъ /1 = 426,84 КИЛОГР*
б. калор.
Волѵіапсі нашелъ для Балтиморы и при температурѣ 11°,5 число
428,2; поправка для Парижа равна — 0,4, такъ что для Парижа получа-
ется 427,8; это число отличается отъ найденнаго Міспіевси не бо-
лѣе, какъ на 0,25%.
Механическій эквивалентъ теплоты
371
Ріііи) построилъ приборъ, дающій возможность довольно быстро
опредѣлить величину Е. На маленькое колесо центробѣжной машины
(рис. 112) насажена ось, снабженная счетчикомъ. Къ оси прикрѣпленъ
сверху стальной конусовидный, сверху открытый сосудъ, въ который
вставляется такой же полый, но сверху закрытый сосудъ, наполненный
ртутью. Къ его крышкѣ придѣлана стрѣлка а черезъ отверстіе въ
крышкѣ проходитъ термометръ і. Отъ конца А и щтъ веревочка черезъ
блокъ г; она поддерживаетъ чашечку 5- Горизонтальная шкала подъ
концомъ И служитъ для наблюденія движеніи этого конца. При помощи
рукоятки вращаютъ большое колесо въ такомъ направленіи, чтобы со-
Рис. 112.
судъ к старался повернуть вставленный въ него сосудъ и полоску рк по
направленію, обратному направленію движенія часовой стрѣлки (если на
приборъ смотрѣть сверху). Въ чашку 5 кладется грузъ; скорость вра-
щенія оси и сосуда к регулируется такъ, чтобы конецъ Л полоски оста-
вался неподвижнымъ. Тогда работа г тренія опредѣляется формулою
Г = 2ШС/7О,
гдѣ п число оборотовъ оси. опредѣляемое счетчикомъ, р грузъ, дѣйству-
ющій на оконечность А стрѣлки, р разстояніе точки приложенія силы р
отъ оси вращенія. Тсчнѣе слѣдуетъ вмѣсто р взять р-\-р гдѣ р' ма-
лый грузъ, преодолѣвающій треніе оси колеса г. Эквивалентное количе-
ство д теплоты опредѣляется по повышенію температуры двухъ сталь-
ныхъ сосудиковъ и содержащейся въ однойъ изъ нихъ ртути, при-
чемъ необходимо ввести поправку на потерю теплоты лучеиспусканіемъ
и теплопроводностью. Риііц нашелъ съ такимъ приборомъ 2: = 426,6;
8 а 11111 к а съ приборомъ, нѣсколько измѣненнымъ, Е 426,26. Инте-
ресное видоизмѣненіе прибора Риііщ’а построилъ (ігітвеЬІ (1903).
Приборъ, удобный для опредѣленія Д построилъ также Н. 4. Смир-
новъ (1907).
IV. Способъ удара, опыты Нігп’а. Въ моментъ удара
24*
372
Термодинамика.
двухъ твердыхъ неупругихъ тѣлъ уничтожается почти вся ихъ живая
сила; взамѣнъ ея появляется количество теплоты, эквивалентное ей, а
слѣд. и той работѣ, которая была затрачена, когда тѣла были приведены
въ движеніе. На этомъ основанъ способъ Нігп’а, приборъ котораго изо-
браженъ на рис. 113. Къ деревянной двойной рамѣ привѣшена камен-
ная глыба /И, вѣсомъ въ 941 кгр., снабженная на концѣ В желѣзной
плиткой; далѣе желѣзный цилиндръ АА (вѣсъ 350 кгр.) и свинцовый ци-
линдръ 29, вдоль оси котораго имѣется каналъ, не проходящій насквозь,
такъ что вертикальномъ положеніи цилиндръ представляетъ толстостѣн-
Рис. 113.
ный сосудъ. Двѣ нити (см. рисунокъ) даютъ возможность^подвѣсить его
въ вертикальномъ положеніи. До опыта опредѣляютъ температуру ци-
линдра О при помощи термометра і, который потомъ вынимается. За-
тѣмъ отодвигаютъ цилиндръ АА направо, вслѣдствіе чего его^центръ тя-
жести поднимается на нѣкоторую высоту Л, что соотвѣтствуетъ затратѣ
работы рИ, если р вѣсъ цилиндра АА, Затѣмъ отпускаютъ цилиндръ АА ;
онъ ударяется о свинцовый цилиндръ О и отскакиваетъ немного назадъ,
причемъ онъ обратно поднимается на малую высоту к'; въ то же время
глыба 714, вѣсъ которой Р, немного перемѣщается налѣво, что соотвѣт-
ствуетъ нѣкоторому ея поднятію Л". Ясно, что работа г, превративша-
яся въ моментъ удара въ теплоту, равна
г - = р (И — /г') — Ріг".
Въ одномъ опытѣ, напр., было А = 1,166 м., И' = 87 мм., И" — 103 мм.,
р = 350 кгр., Р = 941 кгр. Вѣсъ свинцоваго цилиндрика равнялся
2,948 кгр. Тотчасъ послѣ удара онъ снимается, привѣшивается въ вер-
тикальномъ положеніи и въ его полость наливается вода, температура
которой опредѣляется термометромъ. Слѣдя достаточное время за темпе-
ратурой охлаждающагося цилиндра, можно вычислить, какова была его
температура вслѣдъ за ударомъ, а отсюда уже опредѣлить и количество
д теплоты, которое въ немъ выдѣлилось. Такими опытами Нігп нашелъ
Механическій эквивалентъ теплоты.
373
В = 425,2
кгр.-метр.
б. калор.
Котурницкій (1905) далъ тщательный теоретическій разборъ
этого метода.
V. Способъ сжатія газовъ. При изотермическомъ сжатіи
газа отъ объема ѵг до объема ѵ2 или отъ давленія рг до давленія р2 при
температурѣ I, причемъ ргѵг = р2ѵ2, производится, какъ мы видѣли (т. I)
работа
г = р2ѵ2\§?2.........................(14)
Рі
Если ѵ2 выразить въ куб. метрахъ, р2 въ килограммахъ на кв. метръ
поверхности, то г получится въ килогр.-метрахъ. Выводъ формулы (14)
будетъ повторенъ ниже. Результатомъ работы г сжатія газа является
эквивалентное ей количество д теплоты, выдѣляющейся въ самомъ газѣ.
3 о и 1 е воспользовался этимъ явленіемъ, чтобы опредѣлить Е, вычисляя г
и измѣряя д. Его приборъ изображенъ на рис. 114. Въ мѣдный цилин-
дрическій сосудъ С накачивается воздухъ при помощи нагнетательнаго
насоса, приводимаго въ движеніе рукояткою ЕРі. Воздухъ проходитъ
сперва черезъ высушивающій приборъ А и черезъ змѣевикъ В, погру-
женный въ сосудъ съ водою, темпе-
ратура которой измѣряется осо-
бымъ термометромъ. Цилиндръ С на-
ходится внутри калориметра съ во-
дою, температура которой также
опредѣляется термометромъ. При-
мѣрно 300 быстрыхъ качаній на-
соса было достаточно, чтобы до-
вести воздухъ въ С до давленія
приблизительно въ 22 атмосферы.
Тогда въ формулѣ (14) р2 =
= 22.10333 клгр. на 1 кв. метръ
поверхности; ѵ2 равно емкости со-
суда С, выраженной въ куб. ме-
трахъ. Въ опытахъ Я о и 1е я ѵ2 —
= 0,002232 ; слѣд. работа г вычис-
ляется по формулѣ
г =22.10333.0,0022321^22.
Эквивалентное этой работѣ количество теплоты получается по на-
блюденному повышенію температуры калориметра. Такимъ способомъ
Я о и 1 е нашелъ, какъ среднее изъ ряда наблюденій,
Е = 436,1 ™{’.-метр. _
б. калорія
Повышеніе температуры калориметра составляло долю градуса Фа-
374
Термодинамика.
ренгейта, а потому можно было сжатіе газа считать изотермическимъ и
пользоваться формулою (14). Яопіе производилъ также обратные опыты,
наблюдая пониженіе температуры калориметра въ случаѣ, когда воз-
духъ, предварительно сжатый въ цилиндрѣ С, былъ выпущенъ изъ него
въ свободный воздухъ. Тогда г представляетъ работу расширяющагося
газа, производимую насчетъ тепла, отнимаемаго отъ калориметра. Опыты
при различныхъ степеняхъ предварительнаго сгущенія газа, дали мало
между собою согласные результаты Е -449,8 — 446,5- 416,8.
VI. Способъ капилярныхъ трубокъ. Продавливаніе жид-
костей черезъ капилярныя трубки требуетъ затраты работы на преодолѣ-
ніе тренія внутри трубокъ, въ которыхъ выдѣляется эквивалентное коли-
чество тепла. 4 о и 1 е двигалъ внутри цилиндрическаго калориметра, на-
полненнаго водою, поршень вверхъ и внизъ; черезъ этотъ поршень про-
ходило множество вертикальныхъ капилярныхъ трубокъ. Измѣряя затра-
ченную работу и нагрѣваніе калориметра. 4 о и 1 е нашелъ
^=4246КИЛОГ?-меТр’
’ б. калор.
Подобные опыты Нігп’а дали 2: = 432,0.
ѴГІ. Способъ электродинамической индукціи. Если про-
водникъ электричества напр. металлическое тѣло, движется въ магнитномъ
полѣ, т.-е. въ пространствѣ, въ которомъ дѣйствуютъ магнитныя силы, то
въ этомъ тѣлѣ, вообще говоря, появляются электрическіе токи, предста-
вляющіе" особую форму энергіи, немедленно переходящую въ теплоту.
Источникомъ этой теплоты является работа, которую необходимо затра-
тить, чтобы, поддерживая движеніе проводника, преодолѣть т. наз. вза-
имодѣйствіе между возникающими (индуктируемыми) электрическими то-
ками и магнитнымъ полемъ; это взаимодѣйствіе является въ видѣ силы,
стремящейся придать проводнику движеніе, обратное тому, которое онъ
въ дѣйствительности имѣетъ. <Т о и 1 е вращалъ замкнутую проволочную
катушку, намотанную на желѣзное ядро, въ калориметрѣ, находившемся
между полюсами электромагнита. Работа измѣрялась, подобно тому какъ
въ опытахъ надъ треніемъ (стр. 366 рис. 106), опускающимися гирями, кото-
рыя приводили катушку во вращеніе. Вводя цѣлый рядъ поправокъ, о
которыхъ не распространяемся, Лоиіе нашелъ этимъ способомъ
Е = 459,62
б. калор.
Повидимому это число представляетъ результатъ перваго
экспериментальнаго опредѣленія величины Е (впервые
сообщено 21 августа 1843 г.). Впослѣдствіи Ѵіоііе пользовался тѣмъ
же способомъ; мѣдный дискъ вращался въ калориметрѣ между полюсами
электромагнита^ Онъ нашелъ для Е числа между 434,9 и 437,4. Недавніе
опыты (ГАгвопѵаГя дали числа, заключенныя между 421 и 427. Сюда
же относится методъ Ь. ХѴеЬег’а (1895), который измѣрялъ теплоту, вы-
Механическій эквивалентъ теплоты.
375
дѣлающуюся въ мѣдномъ цилиндрѣ, помѣщенномъ во вращающееся маг-
нитное поле. Подобный же методъ предложили ВаіПе и Гегу (1898).
ѴІП. Способъ нагрѣванія проводниковъ электриче-
скимъ токомъ. Если токъ, сила котораго /, проходитъ втеченіе і сек.
черезъ проводникъ, сопротивленіе котораго р, то электрическія силы произ-
водятъ въ этомъ проводникѣ работу г, равную
г = Роі джулямъ = і2оі . ІО7 эргамъ............(15)
если і выражено въ амперахъ, р — въ омахъ. Помѣщая въ калориметръ
проводникъ, сопротивленіе р котораго въ омахъ съ точностью извѣстно,
и пропуская черезъ него втеченіе извѣстнаго времени і токъ, сила кото-
раго измѣряется въ амперахъ, напр. при помощи тангенсъ-гальванометра
(т. IV), мы можемъ вычислить затраченную работу г. Калориметръ ука-
жетъ намъ эквивалентное ей количество теплоты, а это дастъ намъ воз-
можность вычислить Е. Первые опыты по этому способу были произве-
дены О и і п 1 и 8 Ісіііи8’омъ. они дали неточный результатъ (^=399,7),
такъ какъ величина ома въ то время (1857) не была извѣстна съ доста-
точною точностью. Йо иі е получилъ тѣмъ же способомъ Е = 429,4, поль-
зуясь ртутнымъ термометромъ, относя калорію къ 18°,6, и принимая для
ома значеніе, найденное Коммиссіей Британской Ассоціаціи. Вводя не-
обходимыя поправки, т.-е. переводя показанія ртутнаго термометра къ воз-
душному, и полагая, что омъ, принятый й о и 1 е’емъ, равенъ 0,9862 нынѣ
опредѣленнаго (сопротивленіе при 0° ртутнаго столба въ 1 кв. мм. попе-
речнаго сѣченія и длиною въ 1,063 метра), получаемъ исправленное число
йоиіе’я Е = 424,95 для 18°,6 и для широты Манчестера.
Подобные же опыты производили Н. Р. АѴеЬег, й а 11 п, Віеіе-
гісі, СггіПіійз и Всйизіег и Сі а п п о п. Число АѴ е Ь е г’а, испра-
вленное, согласно новому опредѣленію ома, равно 422,33; оно слишкомъ
мало. Число й а 11 п’а, также исправленное, равно 430,00 (калорія отне-
сена къ 16°).
Дальнѣйшее изслѣдованіе произвелъ Віеіегісі (1888, 1905), поль-
зуясь, какъ и й а й п, ледянымъ калориметромъ. Единицу теплоты онъ
опредѣляетъ по количеству льда, которое она при 0° переводитъ въ воду
при 0°. Онъ нашелъ для 11,5° — калоріи е = 4,1938 джуля и для 15° —
калоріи е = 4,1938 джуля.
Весьма тщательныя опредѣленія по этому способу произвели СгіИ-
I і і 118 (1893) и Всііизіег и Оаппоп (1895); работа СтгіПіѣІіе’а
продолжалась 5 лѣтъ. Относя калорію къ 15°, онъ находитъ для широты
Гринвича (^ = 981,17) Е = 427,88 Эти работы мы уже раз-
б. калор.
смотрѣли на стр. 161.
О г а е і ъ находитъ изъ наблюденій бе і П і 1118’а для 15° — калоріи
е = 4,1856 джуля. Какъ среднее изъ всѣхъ измѣреній, произведенныхъ
до 1906 г. онъ находитъ для 15° — калоріи е = 4,1861 джуля, причемъ
ошибка не превышаетъ 0,2%. Изслѣдованіе Вагпез’а (1909) дало
376
Термодинамика.
е = 4,1842 джуля; наконецъ, Сгётіеии Візраіі (1910) находятъ
е = 4,1851 джуля (15° — калорія).
Раѵге и ВіІЬеттапп получили Е = 444,2, сравнивая работу г,
получаемую по формулѣ Ц5) съ теплотою, соотвѣтствующей химическимъ
реакціямъ въ элементѣ. Этотъ способъ надежныхъ результатовъ дать не
можетъ.
IX. Способъ растяженія проволокъ. Если металличе-
скую проволоку подвергнуть внезапному растяженію, то она охлаждается.
Мы впослѣдствіи познакомимся съ теоріей этого явленія и выведемъ фор-
мулу, опредѣляющую величину охлажденія. Есііипсі произвелъ рядъ
опытовъ, представляющихъ замѣчательное подтвержденіе закона эквива-
лентности работы и теплоты. Для опредѣленія Е они менѣе пригодны,
хотя Е б 1 и и (1 вывелъ и численное значеніе величины Е изъ своихъ
опытовъ.
Приборъ Ейіипб’а изображенъ на рис. 115. Испытуемая прово-
лока натянута въ вертикальномъ шкапикѣ, дверцы С котораго изобра-
Рис. 115.
жены открытыми. Нижній ко-
нецъ Е проволоки прикрѣпленъ
къ рычагу РСН; конецъ Р ры-
чага находится нѣсколько выше
выступа, не дающаго ему упасть.
Вдоль рычага катится колесо Е,
поддерживающее грузъ О; прп
помощи двухъ веревочекъ можно
издали перекатывать грузъ отъ
нѣкотораго начальнаго, положе-
нія (около а"} къ концу Р ры-
чага и обратно. Ось вращенія
рычага находится въ О; когда
грузъ О находится въ началь-
номъ положеніи, то онъ уравно-
вѣшивается противовѣсомъ <2,
такъ что натяженіе проволоки
равно нулю. Проволока при-
крѣплена въ Е при помощи штиф-
тика къ рычагу; если вынуть
штифтикъ, то проволока дѣ-
лается свободною. Измѣненія
температуры проволоки измѣря-
лись термоэлементомъ, изобра-
женнымъ на рисункѣ; не опи-
сываемъ его устройства. Отъ него шли двѣ проволоки къ гальванометру,
отклоненіе котораго измѣрялось по способу трубы и шкалы. Мы можемъ
это отклоненіе принять за мѣру количества теплоты, выдѣлившейся или
исчезнувшей въ проволокѣ.
Механическій эквивалентъ теплоты.
377
Эквивалентность между работою и теплотою доказывается слѣдующими
опытами : 1) Грузъ О быстро перекатывается отъ а" къР; охлажденіе про-
волоки измѣряется отклоненіемъ и (въ дѣленіяхъ шкалы) гальванометра.
2) Грузъ О перекатывается отъ Р къ а"; получается нагрѣваніе, намѣряе-
мое отклоненіемъ и'. Теоретически и' = и; вслѣдствіе неизбѣжныхъ ошибокъ
наблюденій получаются не вполнѣ одинаковыя числа, и мы примемъ
4(«+ гг')замѣру н а г р ѣ в а н і я^проволоки, когда она укорачивается
вслѣдствіе перенесенія груза О отъ Р въ а". Приэтомъ проволока должна
произвести работу, равную произведенію вѣса р этого груза на удлиненіе Л
проволоки; итакъ г = рк Но удлиненіе Л пропорціонально грузу р,- а потому
г = ср2, гдѣ с множитель пропорціональности. 3) Грузъ О перемѣщается
къ концу Р\ когда проволока приняла температуру окружающаго воз-
духа, вынимаютъ штифтикъ въ Р, вслѣдствіе чего проволока внезапно
укорачивается, не производя никакой работы. Она сильнѣе на-
грѣвается, чѣмъ при второмъ опытѣ, и получается большее отклоненіе ГА
Разность 1} — + и') очевидно служитъ мѣрою теплоты, которая была
Затрачена на производство работы г— ср2. Отсюда слѣдуетъ, что при различ-
ныхъ р отношеніе величинъ I) — + «') и р2 должно быть постоян-
нымъ, что и подтвердилось опытами, какъ видно изъ слѣдующей таблички:
р и и' и ^~4("4
р2
11,848 46,5 46,0 96,5 0,66
6,665 29,3 27,1 41,6 0,67
8,393 33,9 33,2 54,5 0,61
10,242 42,2 42,2 74,0 0,68
10,758 56,0 54,7 116,0 0,70
Такимъ образомъ подтверждена эквивалентность между теплотою и
работою въ столь сложномъ явленіи. Въ позднѣйшей работѣ ЕсІІиікГу
удалось опредѣлить истинное измѣненіе температуры проволоки, а слѣд.
и количество теплоты, выдѣляющейся или исчезающей въ проволокѣ.
Зная ея удлиненіе Л, онъ опредѣлилъ работу г и могъ вычислить Е. Про-
волоки изъ различнаго матеріала дали: серебро — Е = 444; мѣдь — Е = 430;
кгр.-мет.
латунь — Е = 428 ^ГкалорГ Результатъ превосходный, если принять во
вниманіе трудность опредѣленія малыхъ измѣненій температуры проволоки.
X. Способъ затраты тепла на производство работы.
Нігп произвелъ замѣчательное изслѣдованіе той потери тепла, которая
сопровождаетъ производство работы въ цилиндрѣ паровой машины. Из-
слѣдуя машины въ 100 и болѣе паровыхъ силъ, Нігп измѣрялъ произ-
водимую ими работу г при помощи прибора, извѣстнаго подъ названіемъ
индикатора Уатта. Чтобы найти затраченную на эту работу теплоту
онъ опредѣлилъ количество <2 тепла, получаемое паромъ въ котлѣ, по-
терянное лучеиспусканіемъ и теплопроводностью, и д2 — переданное хо-
лодильнику. Въ такомъ случаѣ искомое д = О, — д± - д%. Столь слож-
378
Термодинамика.
ное изслѣдованіе не могло дать точныхъ результатовъ. Среднее изъ всѣхъ
его опредѣленій оказалось Е— 398, между тѣмъ какъ С1аи8Ііі8 нахо-
дитъ число Е = 413, какъ среднее изъ нѣкоторой части наблюденій
Нігп’а, которая была раньше опубликована. Опыты ЗсЬгоеіег’а до-
казали, что при нынѣшнихъ средствахъ наблюденій можно получить и
болѣе точное значеніе для Е, изслѣдуя холодильныя машины, въ
•которыхъ разность между теплотою (?, отданною конденсатору и тепло-
тою С}'. отнятой отъ охлаждаемаго тѣла (рефригераторъ), должна быть
эквивалентна затраченной работѣ.
§40 выраженіяхъ вида Хсіх + Уду, гдѣ X и У функціи отъ х и у.
Въ термодинамикѣ мы непрерывно встрѣчаемся съ особаго рода двучле-
нами или, въ общемъ случаѣ, многочленами. Правильное пониманіе смысла
и свойствъ этихъ выраженій можетъ представить нѣкоторыя затрудненія
для начинающихъ заниматься термодинамикой. Недоразумѣнія, могущія
вслѣдствіе этого возникнутъ и дѣйствительно возникавшія, заставили
Гіаивіив'а предпослать изданію своихъ статей особую главу, разъяс-
няющую свойства упомянутыхъ выраженій.
Положимъ, что х и у двѣ независимыя перемѣнныя, сіх и сіу ихъ
безконечно малыя приращенія, X и
У двѣ фу нкціи отъ х и у. Суще-
ствуютъ два рода выраженій вида
Хсіх + Уду. рѣзко другъ отъ друга
отличающіеся по смыслу и по
своимъ свойствамъ.
А. Дифференціалъ функ-
ціи двухъ перемѣнныхъ.
Положимъ, что нѣкоторая величина
г есть однозначная функція
двухъ независимыхъ перемѣнныхъ
хну; можно написать г = /(х,у).
Возьмемъ координатныя оси и при-
мемъ числа х и у за численныя
значенія координатъ точекъ. Каж-
дой точкѣ С (рис. 116) на плос-
кости соотвѣтствуютъ опредѣлен -
ныя х и у. а слѣд. также и опредѣленное значеніе г, такъ что можно
говорить о значеніяхъ величины г въ различныхъ точ-
кахъ плоскости. Полный дифференціалъ дх можно написать въ видѣ
дх Хсіх 4- Уду
гдѣ X и У двѣ функціи отъ х и у. удовлетворяющія условію
дХ _ дУ
ду дх
(16)
(16,а)
Вскякому безконечно малому перемѣщенію СС' въ плоскости соотвѣт-
ствуетъ опредѣленное значеніе дх. равное разности значеній величины х въ
точкахъ С и С Величина сіх зависитъ отъ четырехъ величинъ х. у. сіх
Выраженія вида Хсіх ѴЯу.
379
и (іу, изъ которыхъ первыя двѣ суть координаты начала линіи СС', а
другія двѣ — проекціи той-же линіи. Различно направленнымъ линіямъ
СО, СС“, СС'“ и т. д. соотвѣтствуютъ одинаковыя х и у, но различныя
(іх и (іу, а слѣд. и различныя (1г. Положимъ, что величина г имѣетъ
въ точкахъ А и В значенія гг и ; соединимъ эти точки кривою, кото-
рую мысленно разобьемъ на элементы. Каждому элементу соотвѣтствуетъ
опредѣленное значеніе величины сіг. Возьмемъ сумму этихъ величинъ (іг
для всѣхъ элементовъ кривой АВ и обозначимъ ее символически черезъ
В В
У = У йг = У {Х(1х +
А А
Какова бы ни была кривая АВ, величина этого интеграла всегда
равна
В в
& -- / йг = / (Хйх + УЛу) = г2 — гх =/(х2,у^ — • 07)
А А
т. е. она равна разности значеній величины г въ крайнихъ точкахъ В и А.
В
Значені е интеграла У (іг не зависитъ отъ пути, по ко-
А
уорому мы переходимъ отъ точки Л къ точкѣ В. .Это по-
нятно, такъ какъ сумма измѣненій (йг) величины г всегда равна пол-
ному измѣненію — гг. Чтобы для провѣрки вычислить интегралъ Ц
мы должны взять уравненіе у — (р(х) кривой АВ, вмѣсто у вставить <р(х)
въ % и К и кромѣ того (іу = у (х)сіх. Тогда І2 приметъ видъ
х2
®=/ Р(х)(іх =/(х2,у2) — Ж,я)=Ях2> —/[хх, . (18)
гдѣ хг и х2 координаты точекъ А и В. Итакъ 12 не зависитъ отъ вида
функціи ср(х), впрочемъ не вполнѣ произвольной, ибо кривая у — <р(х)
должна пройти черезъ точки А и В, такъ что <р(хА и <р(х2) имѣютъ
всегда одинаковое значеніе, равное ординатамъ точекъ А и В.
Изъ предыдущаго ясно, что
по замкнутому контуру § сіг § (Хсіх 4- Усіу) 0 . . <19)
В. Безконечно малая величина в и д а Хсіх Ц- У сіу. Возь-
мемъ двѣ совершенно произвольныя, однозначныя функціи X и У
двухъ независимыхъ перемѣнныхъ х и у, приращенія которыхъ суть (іх
и (іу. Составимъ двучленъ Хсіх 4- Усіу; онъ представитъ безконечно ма-
лую величину, которую мы символически обозначимъ черезъ сіг, такъ
что имѣемъ аналогично (16),
Лг -- Х&х +-Усіу..................(20)
380
Термодинамика.
Въ вида произвольности функцій X и V имѣемъ вообще
дХ . дѴ
ду дх
. (21)
Разница между (16) и (20) прежде всего та, что никакой вели-
чины г, какъ функціи отъ х и у, не существуетъ, ибо,
еслибы такая функція существовала, и выраженіе (20) представляло бы ея
дифференціалъ, то вмѣсто (21) мы непремѣнно имѣли бы равенство (16,а).
Если г не существуетъ, какъ функція отъ х и у, то и нельзя гово-
рить о значеніи г въ опредѣленной точкѣ плоскости,
имѣющей заданныя координаты х и у. Но зато всякой безконечно
короткой линіи СС', начертанной на плоскости, соот-
вѣтствуетъ опредѣленное значеніе безконечно малой
величины сіх, ибо, какъ .и прежде, координаты х и у начала линіи
СС' опредѣляютъ величины X и V, а проекціи линіи СС' равны сіх и сіу,
такъ что йх однозначно опредѣлено, если дано положеніе на плоскости,
направленіе и длина линіи СС. Кривую АВ, соединяющую двѣ точки
А и В, раздѣлимъ на элементы; каждому изъ нихъ соотвѣтствуетъ опредѣ-
ленное значеніе величины Лх. Сумма І2 этихъ значеній представитъ нѣ-
которую величину, которую мы можемъ обозначить черезъ х, такъ что
В В
і2-.= /аг = /(А<іх+ У ау) = г............(22)
А А
Чтобы вычислить х, мы, какъ и прежде, въ X и V вставимъ у — ср(х\
и вмѣсто г/у величину д>\х)(іх, гдѣд/ = др(х) уравненіе кривой АВ. Тогда
І2 приметъ видъ, аналогичный (18),
& =/ В(х)(іх — х....................(23)
Но важная разница заключается въ томъ, что значеніе этого
интеграла зависитъ отъ вида кривой, соединяющей
точкиЛиВ т.-е. отъ функціи у = <р(х). Отсюда ясно, что интегралъ 12,
взятый по замкнутому контуру, вообще имѣетъ нѣкоторое значеніе г0, не
равное нулю.
По замкнутому контуру
/аг=/ (хах + у ау) — .............(24)
Небезполезно иллюстрировать сказанное на частномъ примѣрѣ, поло-
живъ, напр. сперва х — ху2, (іх=у2(іх ^хусіу- Возьмемъ точки А и В
(рис. 117) съ координатами (— а,Ь) и (+ а,ІУ); въ нихъ х± = —' аЬ2,
г2=аЪ2, и потому для всякой кривой, ^соединяющей точки А и В, имѣ-
емъ іі—2аЬ2. Совѣтуемъ провѣрить это для прямой АВ(у=Ь, (іу=Ъ) и
для ломанной АОВ, которую слѣдуетъ разбить на двѣ части АО и ОВ,
уравненія которыхъ у = ± - х. Легко видѣть, что для всякой кривой
Функціи состоянія.
381
у = фіх), проходящей черезъ А и В, мы получимъ сіх =
такъ что 12 — %2 [ ф(х2)]2 — -*і[<Р(Лі)]2 = Х2У^ — хі Ѵі2 = 2.
Отбросимъ множитель 2 во
второмъ членѣ выраженія сіх;
мы получаемъ безконечно ма-
лую величину (іх =у2‘(іх + хуйу,
которая уже не представляется
дифференціаломъ какой - либо
функціи величинъ х и у. Легко
убѣдиться, что интегралъ І2, взя-
тый по прямой АВ, равенъ 2аЬ2,
между тѣмъ какъ интегралъ, взя-
тый по пути А ОВ, равенъ ^аЪ2,
такъ что интегралъ, взятый по
замкнутому контуру/ШОД
равенъ
Величины вида (20) постоянно встрѣчаются въ математикѣ и мы
лишь обобщали всѣмъ извѣстные примѣры, изъ которыхъ простѣйшій — вы-
раженіе т. наз. дифференціала площади сІ8=у(1х. Никакой величины 5,
какъ функціи отъ х и у не существуетъ и нѣтъ смысла говорить о зна-
ченіи 5 въ данной точкѣ. Зато всякой безконечно малой линіи СС'
(рис. 117) соотвѣтствуетъ опредѣленное (І8, имѣющее въ данномъ случаѣ
простое геометрическое значеніе; оно равно площади СС'О'О. Интегралъ
В
62 =^угіх = 8 равенъ площади АВОЕ (рис. 116); его величина зависитъ
А
отъ вида кривой, соединяющей точки А и В. Интегралъ по замкнутому
контуру не нуль; онъ равенъ площади фигуры, ограниченной этимъ кон-
туромъ. Совсѣмъ другой характеръ имѣетъ величина йх = у сіх хсіу ~
= ^(ху), дифференціалъ функціи х = ху. Каждой точкѣ соотвѣтствуетъ опре-
дѣленное х, имѣющее простое геометрическое значеніе. Въ А (рис. 116)
она равна хг = х1у1 = пл. А1АЕОА1; въ В она равна = Х2У% = пл-
В-^ВООВ^ Интегралъ
В в
62 сіх (усіххсіу) = пл. В^ЗОЕААіВ^
А А
независимо отъ вида кривой, вдоль которой мы перешли отъ А до В; ин-
тегралъ по замкнутой кривой равенъ нулю.
§ 5. Величины, опредѣляющія состояніе вещества. До СИЪЬз’а
разсматривали въ термодинамикѣ почти только химически однородныя
тѣла, которыя, однако, могли быть физически и неоднородными, т.-е. напр.
частью находиться въ твердомъ, частью въ жидкомъ видѣ, или частью
въ жидкомъ видѣ, частью въ парообразномъ и т. д. Огромное значеніе
работъ СгіЬЬз’а заключается въ примѣненіи термодинамическихъ мето-
довъ къ такимъ системамъ, которыя содержатъ въ себѣ и ^химически раз-
382
і ермо динамика.
нородныя части. Мы сперва будемъ разсматривать химически однород-
ное тѣло и, вообще, будемъ предполагать, что имѣемъ дѣло съ вѣсовою
единицею, напр. съ 1 кгр. какого-либо опредѣленнаго вещества.
Физическое состояніе такого «тѣла» опредѣляется двумя независи-
мыми другъ отъ друга величинами, которыя мы, въ общемъ случаѣ, обо-
значимъ черезъ х и у. Мы будемъ предполагать, что этими величинами
опредѣляется физическое состояніе тѣла въ обыденномъ смыслѣ слова,
т.-е. настолько, насколько оно опредѣляется напр. въ частномъ случаѣ ве-
личинами х = р и у — I (внѣшнимъ давленіемъ и температурою). Элек-
трическое и магнитное состояніе, присутствіе какихъ-либо особыхъ внѣш-
нихъ силъ, дѣйствующихъ на тѣло, внутреннія, хотя бы и стаціонарныя
движенія величинами х и у вообще не опредѣляются.
Всякую величину г, зависящую отъ состоянія тѣла, мы назвалц (т. I)
функціею состоянія. Она можетъ быть разсматриваема, какъ функ-
ція отъ хну. Когда мы пишемъ производную величины г
по одной изъ независимыхъ перемѣнныхъ, мы должны
ясно обозначить, какая величина взята за другую не-
зависимою перемѣнную. Положимъ, что въ одномъ случаѣ неза-
висимыя перемѣнныя суть х и у, въ другомъ х и Въ обоихъ случа-
яхъ имѣемъ производную -у ; но въ первомъ случаѣ аг есть измѣненіе
величины г, вызванное измѣненіемъ перемѣнной х при условіи у = Солзі;
во второмъ же случаѣ при условіи у = Сопзі. Для ясности мы во всѣхъ
случаяхъ, когда возможно недоразумѣніе, будемъ пользоваться символами
опуская указаніе на цругую независимую перемѣнную, остающуюся по-
стоянною, только въ томъ случаѣ, когда недоразумѣніе невозможно.
Особый интересъ представляетъ случай, когда независимыя пере-
мѣнныя суть какія-либо двѣ изъ трехъ величинъ
г», р, /.
гдѣ ѵ объемъ, р внѣшнее давленіе и і температура. Третья величина •
является въ этомъ случаѣ функціей состоянія, т.-е. функціей двухъ
остальныхъ.
Мы имѣемъ, такимъ образомъ, три функціи
^=/і(А і), Р)
которыя можно разсматривать, какъ различныя формы одного и того же
уравненія состоянія
Р(ѵ, р, і) = О.......................(25)
даннаго тѣла (т. I). Три функціи (25) даютъ шесть производныхъ:
Функціи состоянія.
383
Ати производныя попарно представляютъ величины другъ другу обрат-
ныя; такъ напр.
дѵ\ ___ /д/Л
др)і ~ ’
ибо въ обѣихъ дробяхъ мы имѣемъ дѣло съ одною и то же парою сопря-
женныхъ измѣненій (іѵ и (ір величинъ ѵ и р. имѣющихъ мѣсто при
і = Соп8І. Точно также вторая изъ шести производныхъ равна обратной
пятой, и четвертая — обратной шестой. Остаются три производныя само-
стоятельныя, и мы выберемъ какъ таковыя слѣдующія-’
ЛЛ !дѵ \ / др\
М)р 1^/»
Между ними существуетъ однако простая связь. Мы имѣемъ:
, л । дѵ} г. г др\ . . др\
аѵ = Н- ар -4- . I аі, ар = \ -^-\ аѵ \ -^т \ аі.
\др г 1 \ді ]р \дѵ д \ді)ѵ
Положимъ р = Соп8І; тогда (ір = 0 и эти два равенства даютъ:
Величины (іѵ и (іі въ обоихъ равенствахъ однѣ и тѣ же, соотвѣт-
ствующія случаю, когда р — Соп8і.. т.-е. когда ѵ и і мѣняются при по-
стоянномъ внѣшнемъ давленіи. Вставимъ (іѵ во второе равенство, со-
кратимъ на (іі и перенесемъ одинъ членъ въ другую сторону. Получаемъ
или
(27)
Формула, которую легко запомнить, и которая представилась бы
весьма странною, если бы отбросить скобки и подписанныя подъ ними
буквы. Вводя величины (26), получаемъ
(28)
Величины (26), связанныя равенствомъ (28), имѣютъ опредѣленное
физическое значеніе, а именно :
/Л? 1 \др) I = аг'о Р 1 = — (29)
1 др\
] | =7Ро V
384
Термодинамика.
гдѣ а коеффиціентъ теплового расширенія, см. (18) стр. 11,
//коеффиціентъ объемнаго сжатія (т. І)и у термическій
коеффиціентъ давленія, см (50) стр. 122. Вставляя (29) въ (28),
получаемъ
аг/0 = Р?ѵр0....................(30)
связь между тремя коеффиціентами а, /? и у для всѣхъ тѣлъ. Такъ напр.
для ртути при 0° (ѵ = т/0) и 760 мм. имѣемъ а = 0,00018, далѣе /? = 0,00003,
если за единицу давленія принять атмосферу. Формула (30) даетъ у = а: /? =
— 60; это значитъ, что если Нр нагрѣть отъ 0° до 1° при постоянномъ
объемѣ, то внѣшнее давленіе должно увеличиться на 60 атмосферъ.
Слѣдуетъ привыкнуть смотрѣть на всѣ встрѣчаю-
щіяся у насъ функціи состоянія и на ихъ производ-
ныя, именно какъ на функціи состоянія, т.-е. какъ на
функціи какихъ-либо двухъ величинъ, опредѣляющихъ
состояніе тѣла. Такъ напр. аѵ0 равно производной по і нѣкоторой
функціи отъ р и і\ слѣд. аг/0 непосредственно здѣсь представляется также,
какъ функція отъ р и Л Но такое представленіе слишкомъ узко; а есть
функція состоянія, какъ и всѣ величины, входящія въ уравненіе (30),
которое есть связь между шестью функціями состоянія, или шестью функ-
ціями двухъ перемѣнныхъ х и у.
До сихъ поръ мы предполагали, что имѣемъ дѣло съ однимъ одно-
роднымъ тѣломъ, выражаясь точнѣе, съ единицей вѣса химически и фи-
зически однороднаго вещества. Состояніе подобнаго тѣла, вообще говоря,
опредѣляется численными значеніями двухъ независимыхъ перемѣнныхъ
х и у. Назовемъ системой тѣлъ, или просто системой, совокуп-
ность нѣсколькихъ тѣлъ или веществъ, взятыхъ въ произвольныхъ коли-
чествахъ и могущихъ оказывать другъ на друга различныя физическія и
химическія воздѣйствія. Состояніе такой системы опредѣляется большимъ
числомъ независимыхъ перемѣнныхъ или, какъ ихъ иногда называютъ,
параметровъ.
§ 6. Обратимые и необратимые процессы. Переходъ тѣла или си-
стемы изъ нѣкотораго начальнаго состоянія въ новое состояніе называ-
ется процессомъ. Мы называемъ процессъ, или измѣненіе состоянія,
безконечно малымъ, если при этомъ процессѣ параметры измѣняются на
безконечно малыя величины, напр. для одного тѣла на сіх и сіу. Вся-
кій конечный процессъ можно разсматривать, какъ совокупность безко-
нечно большого числа послѣдовательныхъ безконечно малыхъ процессовъ ;
эти послѣдніе можно еще назвать элементарными процессами.
Чрезвычайно важную роль играетъ въ термодинамикѣ раздѣленіе про-
цессовъ на обратимые и необратимые. Однако весьма трудно
дать простую и вмѣстѣ съ тѣмъ достаточно общую характеристику этихъ
двухъ родовъ процессовъ. Можетъ быть только при дальнѣйшемъ разви-
тіи науки удастся найти окончательную формулировку для этой характе-
ристики. Изъ отсутствія такой формулировки вытекаетъ возможность вся-
ческихъ недоразумѣній, въ особенности у начинающихъ. Мы сперва раз-
Обратимые и необратимые процессы.
385
смотримъ нѣкоторые частные случаи обратимыхъ и необратимыхъ про-
цессовъ, а затѣмъ попытаемся обобщить полученные результаты
Процессъ называется обратимымъ, если онъ можетъ быть прой-
денъ въ обоихъ направленіяхъ, какъ отъ состоянія А къ состоянію В,
такъ и отъ состоянія В къ состоянію Л. Въ обоихъ случаяхъ прохо-
дятся одни и тѣ же промежуточныя состоянія, но только въ
обратномъ порядкѣ.
Окончательный результатъ двухъ обратимыхъ процессовъ, изъ кото-
рыхъ второй есть обращеніе перваго, долженъ быть нулемъ, т.-е. всѣ
тѣла, которыя принимали какое-либо участіе въ процессахъ и подверга-
лись при этомъ какимъ-либо измѣненіямъ состоянія, должны по истече-
ніи обоихъ процессовъ, въ точности вернуться въ тѣ первоначальныя со-
стоянія, въ которыхъ они находились до начала перваго процесса. Два
такіе взаимно противоположные процесса не произво-
дятъ никакого измѣненія во вселенной.
Для обратимости конечнаго процесса очевидно не-
обходимо, чтобы всѣ элементарные процессы, изъ
которыхъ онъ состоитъ, были бы обратимы. Конечный
процессъ необратимъ, если хоть одна произвольно малая часть его не-
обратима.
Разсмотримъ типичный примѣръ необратимаго процесса — внезап-
ное расширеніе газа въ сосѣднее пустое пространство.
Этотъ процессъ можетъ быть адіабатическимъ, если во время
расширенія газа не происходитъ обмѣна тепла между газомъ и окружа-
ющимъ пространствомъ. Вмѣстѣ съ тѣмъ это процессъ изотермиче-
скій, по крайней мѣрѣ для идеальнаго газа. Онъ очевидно необратимъ,
такъ какъ мы не можемъ вернуть газъ въ прежнее состояніе безъ участія
новыхъ тѣлъ, которыя частью сожмутъ газъ до прежняго объема, частью
отнимутъ отъ него выдѣляющуюся при сжатіи теплоту. Когда газъ вер-
нется въ первоначальное состояніе, все же останутся измѣненія въ дру-
гихъ тѣлахъ. Къ этому присоединяется еще слѣдующее важное обсто-
ятельство. Промежуточныя состоянія, проходимыя газомъ при сжатіи,
отнюдь не тождественны съ промежуточными состояніями, пройденными
газомъ при расширеніи въ пустоту. При расширеніи заполнялся почти
мгновенно весь увеличенный объемъ, причемъ давленіе въ разныхъ мѣ-
стахъ объема, занятаго газомъ, нѣкоторое время имѣло разныя значенія и
лишь постепенно уравнивалось. Это уравненіе давленія можетъ совер-
шаться даже довольно медленно, напр. при истеченіи газа изъ очень уз-
каго отверстія.
Послѣ этихъ общихъ соображеній и разбора одного примѣра пе-
рейдемъ къ разсмотрѣнію условій, опредѣляющихъ обратимость или не-
обратимость процесса. Прежде всего введемъ понятіе о физическомъ
равновѣсіи, которое можетъ осноситься къ любому процессу.
Понятіе о равновѣсіи, даваемое въ механикѣ, и относящееся къ про-
цессу движенія, представляетъ частный случай вводимаго нами понятія.
КУРСЪ ФИЗИКИ О. X в О Л Ь С О Н А. Т. Ш, изд. 3-е. 25
386
Термодинамика.
Представимъ себѣ какой-либо физическій процессъ, связанный съ измѣ-
неніемъ состоянія одного или нѣсколькихъ тѣлъ системы. Самое возник-
новеніе этого процесса должно вызываться опредѣленными причинами,
обусловленными состояніемъ тѣла или системы въ данный моментъ. Во-
обще говоря, состояніе тѣла или системы даетгь возможность указать эти
причины возникновенія процесса. Предположимъ, что состояніе тѣла та-
ково, что нѣтъ причинъ для возникновенія даннаго процесса. Тогда про-
цессъ и не возникнетъ, онъ невозможенъ, для него нѣтъ достаточнаго
основанія. Въ такомъ случаѣ говорятъ, что тѣло, или система, по
отношенію къ данному процессу, находится въ состоя-
ніи физическаго равновѣсія. Самый физическій процессъ можно
разсматривать, какъ послѣдовательное приближеніе къ состоянію равно-
вѣсія. Когда равновѣсіе достигнуто, мвцессъ прекращается.
Слѣдующая особенность отличаетъ физическія равновѣсія. Всякое
механическое равновѣсіе представляется намъ, поскольку мы можемъ
проникнуть во внутренній смыслъ механическихъ процессовъ, чисто ста-
тическимъ; физическое равновѣсіе, напротивъ, часто носитъ харак-
теръ динамическій. Такой характеръ имѣетъ равновѣсіе въ томъ
случаѣ, если наблюдаемый физическій процессъ есть результатъ двухъ про-
цессовъ, происходящихъ въ двухъ взаимно противоположныхъ направле-
ніяхъ и обладающихъ различной интенсивностью. Если интенсивности
двухъ процессовъ равны, то ихъ результатъ, т.-е. наблюдаемый физиче-
скій процессъ исчезаетъ и мы имѣемъ случай динамическаго рав-
но в ѣ с і я. Сюда относятся тепловое или температурное равновѣсіе сопри-
касающихся тѣлъ, равновѣсіе между жидкостью и ея паромъ и т. д.
Разсмотримъ сначала отдѣльное изолированное тѣло, напр.
одинъ килограммъ какого-либо опредѣленнаго вещества. Это можетъ быть
водородъ, ртуть, мѣдь или какое-либо другое химически однородное ве-
щество ; различныя части его могутъ однако быть въ различныхъ
физическихъ состояніяхъ, напр. ледъ и вода, жидкость и паръ,
или въ различныхъ аллотропическихъ состояніяхъ, напр. бѣлый
и красный фосфоръ. Часть вещества можетъ быть диссоціирована, что
происходитъ напр. съ парами іода; разсматриваемое тѣло можетъ быть
и растворомъ. Во всякомъ случаѣ, тѣло изолировано и, слѣ-
довательно, его запасъ энергіи не можетъ быть измѣненъ. Въ такомъ
тѣлѣ мыслимы различные физическіе процессы, напр. переносъ теп-
лоты, измѣненіе давленія въ разныхъ частяхъ, переходъ изъ одного со-
стоянія въ другое, аллотропическія превращенія, диссоціація, диффузія
и т. д. Однако каждый такой мыслимый физическій процессъ только
тогда произойдетъ въ дѣйствительности, если тѣло по отношенію
къ нему не находится въ равновѣсіи; при этомъ направленіе про-
цесса будетъ такимъ, что произойдетъ п р и б л и ж е н і е тѣла къ со-
стоянію равновѣсія. Въ обратномъ направленіи процессъ въ изолирован-
номъ тѣлѣ ни въ какомъ случаѣ произойти не можетъ. Врядъ ли нужно
пояснять эту мысль на примѣрахъ изъ числа разсмотрѣнныхъ выше про-
Обратимые и необратимые процессы.
387
цессовъ. Эти простыя соображенія приводятъ къ слѣдующему важному
результату: всѣ физическіе процессы, совершающіеся въ
изолированномъ тѣлѣ, необратимы (т.-е. не могутъ произойти въ обрат-
номъ направленіи при условіи изолированности даннаго тѣла). Собственно
говоря, слѣдуетъ исключить при этомъ тѣ процессы, въ которыхъ играетъ
роль нѣчто въ родѣ инерціи, т.-е. въ которыхъ тѣло переходитъ
черезъ состояніе равновѣсія, и затѣмъ происходитъ процессъ въ обрат-
номъ Направленіи. Однако высказанное положеніе можетъ быть обобщено
и на эти процессы, если они, какъ это обыкновенно бываетъ, постепенно
затухаютъ, т.-е. амплитуды послѣдовательныхъ, направленныхъ въ проти-
воположныя стороны процессовъ, постепенно уменьшаются. Если мы ис-
ключимъ чисто механическіе, совершающіеся безъ тренія, т.-е. въ при-
родѣ вовсе не встрѣчающіеся процессы, то высказанное положеніе спра-
ведливо безъ ограниченій.
Повидимому, всѣ необратимые процессы, совершающіеся въ изо-
лированномъ тѣлѣ, имѣютъ еще слѣдующій общій признакъ. Мы опредѣ-
ляли состояніе тѣла опредѣленными параметрами. Такими параметрами
могутъ быть температура, давленіе, концентрація и т. д. Если мы вы-
брали для опредѣленія состоянія тѣла его температуру /, то мы предпо-
лагаемъ, что эта температура въ каждый данный моментъ имѣетъ вполнѣ
опредѣленное значеніе. Но мы замѣчаемъ, что всякій разъ, когда въ
тѣлѣ совершается необратимый процессъ переноса теплоты, понятіе о тем-
пературѣ тѣла теряетъ смыслъ, такъ какъ при такомъ процессѣ мы имѣ-
емъ въ тѣлѣ безконечное множество различныхъ температуръ, относя-
щихся къ различнымъ его элементамъ. Равнымъ образомъ нельзя въ дан-
номъ тѣлѣ однозначно опредѣлить величину давленія втеченіе необрати-
маго процесса уравниванія давленія (расширеніе газа въ сосѣднее пустое
пространство). Состояніе раствора опредѣляется между прочимъ его кон-
центраціей. Во время необратимаго процесса диффузіи раствореннаго ве-
щества очевидно не можетъ быть рѣчи объ опредѣленной концентраціи
раствора. Итакъ, повидимому, при каждомъ необратимомъ процессѣ одинъ
параметръ становится неопредѣленнымъ и какъ характеристика состоянія
теряетъ смыслъ.
Перейдемъ теперь къ общему случаю вполнѣ произвольной
системы тѣлъ, въ которой возможны самые разнообразные физиче-
скіе процессы. Можетъ явиться мысль, что слѣдуетъ отдѣльно разобрать
случаи изолированной и случай неизолированной системы. Однако такое
заключеніе будетъ невѣрно, если мы хотимъ выяснить условія обратимости
физическихъ процессовъ, такъ какъ мы считаемъ процессъ только тогда
обратимымъ, если, по обращеніи его, всѣ тѣла, въ немъ участвовав-
шія, вернулись въ свое первоначальное состояніе. Поэтому, если напр.
данная система подвергается положительному или отрицательному притоку
теплоты, то тѣла, поглощающія или отдающія эту теплоту, должны быть
включены въ систему. Итакъ систему во всякомъ случаѣ слѣдуетъ счи-
тать изолированной, всякій обмѣнъ энергіи между ней и внѣшнимъ мі-
25*
388
Термодинамика.
ромъ, будь то въ видѣ энергіи свѣтовой, тепловой или электрической, —
слѣдуетъ считать невозможнымъ. Но съ другой стороны не ис-
ключаются чисто механическія взаимодѣйствія между
системой и внѣшнимъ міромъ. Если напр. система находится
подъ давленіемъ /?, то это давленіе должно уравновѣшиваться равнымъ
ему давленіемъ внѣшнихъ тѣлъ, напр. стѣнокъ сосуда (среди нихъ могутъ
быть и подвижныя части, напр. поршни). Мы можемъ, поэтому разсма-
тривать р, какъ давленіе, производимое на систему внѣшними, не при-
надлежащими къ системѣ, тѣлами. Это давленіе р можетъ быть
величиною перемѣнною.
Измѣненіе величины давленія возможно только при соотвѣтствен-
ныхъ измѣненіяхъ во внѣшнихъ тѣлахъ. Однако нѣтъ надобности при-
числять вслѣдствіе этого внѣшнія тѣла къ системѣ, такъ какъ разсматри-
ваемыя измѣненія могутъ быть кинематическаго характера
(измѣненія положенія) и уже во всякомъ случаѣ принадлежатъ къ числу
чисто механическихъ процессовъ. А чисто механическіе про-
цессы, которые одни только и возможны въ данномъ случаѣ, всегда мо-
гутъ быть произведены вполнѣ обратимымъ способомъ (см. ниже). Слѣ-
довательно ясно, что нѣтъ необходимости включать въ систему эти внѣш-
нія тѣла.
Примѣнимъ теперь къ случаю системы наши прежнія разсужденія.
Въ системѣ мыслимы самые разнообразные физическіе процессы. Если
система по отношенію къ одному изъ мыслимыхъ процессовъ находится въ
равновѣсіи, то этотъ процессъ не произойдетъ, такъ какъ нѣтъ достаточ-
наго основанія для его возникновенія. Если система по отношенію къ
данному процессу не находится въ равновѣсіи, то этотъ процессъ дол-
женъ возникнуть. При этомъ процессъ совершается въ томъ направле-
ніи, которое приближаетъ тѣло къ состоянію равновѣсія, и необра-
тимъ, т.-е. нельзя вернуть системы въ прежнее состояніе, не подвер-
гая ее никакимъ внѣшнимъ воздѣйствіямъ, кромѣ чисто механическихъ.
Слѣдуетъ отмѣтить, что мы разсматриваемъ только физическіе, а не чисто
механическіе процессы внутри нашей системы, такъ какъ чисто механи-
ческіе процессы всегда обратимы.
Всякій физическій процессъ, возникшій въ си-
стемѣ тѣлъ благодаря тому, что система по отноше-
нію къ нему, находится не въ состояніи равновѣсія,
необратимъ. Можно указать, какъ на общій признакъ такихъ процес-
совъ, на то, что они совершаются съ конечною скоростью.
При каждомъ физическомъ процессѣ мы должны
разсматривать всѣ тѣла, участвовавшія въ немъ. Въ та-
комъ случаѣ мы можемъ очевидно сказать, что каждый физическій про-
цессъ совершается въ изолированной системѣ. Процессъ, происхо-
дящій въ неизолированной системѣ, очевидно всегда можно раз-
сматривать, какъ часть полнаго физическаго процесса, происходящаго въ
изолированной системѣ, часть которой представляетъ данная система.
Обратимые и необратимые процессы.
389
Процессъ, происходящій въ неизолированной системѣ можно назвать пар-
ціальнымъ процессомъ. Мы можемъ теперь высказать слѣдующее
положеніе :
Если физическій процессъ необратимъ, то и всѣ
парціальные процессы, изъ которымъ онъ состоитъ,
также необратимы. Разумѣется, не слѣдуетъ смѣшивать парціаль-
ные процессы, происходящіе одновременно въ разныхъ частяхъ си-
стемы, съ происходящими послѣдовательно во времени частями
одного процесса.
Мы видѣли, что всѣ физическіе процессы, втеченіе которыхъ си-
стема находится на конечномъ разстояніи отъ состоянія равновѣсія, не-
обратимы. Отсюда слѣдуетъ, что процессъ только тогда обра-
тимъ, когда система постоянно находится въ состо-
яніи равновѣсія по отношенію къ данному процессу,
или, что въ предѣлѣ одно и то же, безконечно близка
къ состоянію равновѣсія.
Такъ какъ состояніе равновѣсія какъ разъ и есть то состояніе, при
которомъ процессъ н е происходитъ, то ясно, что обратимый процессъ
вообще произойдетъ только тогда, когда условія, опредѣляющія состояніе
системы, измѣнятся. Но благодаря этому измѣненію состояніе системы
не должно ни на одинъ моментъ отличаться на конечную величину отъ
состоянія равновѣсія. Отсюда слѣдуетъ, что самыя измѣненія должны
происходить б е з к о н е ч.н о медленно.
Физическій процессъ только тогда обратимъ, когда
онъ можетъ быть представленъ въ видѣ ряда послѣдо-
вательныхъ состояній, каждое изъ которыхъ безко-
нечномало отличается отъ состоянія равновѣсія по от-
ношенію къ данному процессу; обратимы й физическій
процессъ долженъ происходить безконечно медленно.
Если такой процессъ совершается системой въ обратномъ направле-
ніи, то послѣдовательныя состоянія, проходимыя системой въ прямопро-
тивоположномъ направленіи, также должны лишь безконечно мало отли-
чаться отъ состояніи равновѣсія. Изъ вышеизложеннаго видно, что об-
ратимый физическій процессъ представляетъ идеаль-
ный, предѣльный случай, который практически никогда
не осуществляется.
Покажемъ теперь на нѣсколькихъ примѣрахъ, какимъ образомъ можно
себѣ представить возникновеніе обратимыхъ процессовъ.
I. Какъ первый примѣръ разберемъ процессъ нагрѣванія или охла-
жденія нѣкотораго тѣла А отъ до вслѣдствіе притока или выдѣле-
нія теплоты. Если процессъ происходитъ вслѣдствіе соприкосновенія съ
нѣкоторымъ тѣломъ В или вслѣдствіе излученія послѣдняго, причемъ тем-
пература тѣла В отличается на конечную величину отъ температуры
тѣла Д, то система Д-|-“^ни на одинъ моментъ не находится въ тепловомъ
равновѣсіи, и процессъ очевидно необратимъ. Для того, чтобы обрати-
390
Термодинамика.
мымъ способомъ измѣнить температуру тѣла А отъ до 4° надо себѣ
мысленно представить безконечное множество тѣлъ В2, В3 . . . .
Вп . . . такихъ, чтобы температуры двухъ послѣдовательныхъ тѣлъ В от-
личались между собой лишь безконечно мало, и чтобы въ предѣльномъ
случаѣ послѣдовательный рядъ тѣлъ В обладалъ всѣми промежуточными
температурами отъ до 4°- Если мы приведемъ тѣло А послѣдовательно
въ соприкосновеніе со всѣми этими тѣлами В, то температура тѣла А из-
мѣнится отъ до 4°- Состояніе системы въ каждый данный моментъ
безконечно мало отличается отъ состоянія равновѣсія и весь процессъ
обратимъ: если мы снова приведемъ тѣло А въ соприкосновеніе съ тѣ-
лами В, но въ обратной послѣдовательности, то процессъ совершается въ
обратномъ направленіи. Результатъ совокупности двухъ процессовъ, въ
предѣльномъ случаѣ, есть нуль.
II. Какъ второй примѣръ разберемъ процессъ, возникающій при
измѣненіи давленія; для наглядности допустимъ, что наша си-
стема газообразна и пренебрежемъ дѣйствіемъ силы тяжести. Мы мо-
жемъ себѣ представить рядъ случаевъ, когда давленіе рг внезапно стано-
вится неравномѣрнымъ. Напр. можетъ быть внезапно удалена (разбита)
перегородка, отдѣляющая разсматриваемое пространство отъ сосѣдняго,
гдѣ давленіе имѣетъ другую величину р2 (напр. р% — 0, или же р2 > Рі) ’
или внутри самой системы можетъ произойти взрывъ. Во всѣхъ этихъ
случаяхъ въ теченіи процесса въ каждой точкѣ наблюдается опредѣлен-
ное, мѣняющееся со временемъ давленіе; но о давленіи, какъ о пара-
метрѣ, опредѣляющемъ состояніе системы, уже нельзя говорить. Это по-
нятіе утратило всякій смыслъ. Система находится на конечномъ разсто-
яніи отъ состоянія равновѣсія, и процессъ необратимъ.
Существенно то же самое получается, если внѣшнее давленіе ръ
производимое на систему, вдругъ мѣняется на конечную величину.
Пусть, напримѣръ, система въ какомъ-либо мѣстѣ ограничена подвижнымъ
поршнемъ, массой котораго можно пренебречь. Если внѣш-
нее давленіе вдругъ понизится съ р± до р*, то газъ расширится. Непо-
средственно подъ поршнемъ давленіе сразу понизится до _/л2. Внутрен-
нее давленіе дѣлается неопредѣленнымъ и процессъ необратимъ. Внѣш-
няя работа г равна
г==^-—^1),
гдѣ — первоначальный объемъ газа, — объемъ газа въ концѣ про-
цесса. Только въ темъ случаѣ, если давленіе непрерывно мѣ-
няется, т.-е. если система подвергается какъ бы дѣйствію безконечно
большого числа послѣдовательныхъ давленій, процессъ становится обра-
тимымъ. Такъ какъ давленія въ системѣ уравниваются, вообще, очень
быстро, гораздо быстрѣе, чѣмъ температуры, то процессъ въ дѣйствитель-
ности можетъ совершаться съ довольно большой скоростью.
Только при обратимомъ безконечно маломъ расши-
Обратимые и необратимые процессы.
391
реніи элементарная работа опредѣляется уравненіемъ
(1г — р&ѵ. При обратимомъ расширеніи состояніе системы въ каждый
данный моментъ безконечно мало отличается отъ состоянія равновѣсія.
III. Разсмотримъ теперь процессъ испаренія - жидкости. Си-
стема, состоящая изъ жидкости и пара, находится въ равновѣсіи, по от-
ношенію къ разбираемому процессу, если паръ насыщенъ, т.-е. облада-
етъ вполнѣ опредѣленной упругостью, которая для данной жидкости есть
функція температуры. Испареніе произойдетъ, напримѣръ, въ томъ слу-
чаѣ, если увеличится • объемъ ѵ системы. Процессъ обратимъ, если это
увеличеніе объема происходитъ безконечно медленно. Если оно проис-
ходитъ съ конечной скоростью, то система удаляется отъ состоянія рав-
новѣсія, въ особенности, если къ пару примѣшанъ какои-нибудь индиф-
ферентный газъ (напр. воздухъ); тогда процессъ испаренія становится
необратимымъ.
IV. Раствореніе твердаго тѣла въ жидкости, напр.
соли въ водѣ, только тогда является обратимымъ процессомъ, когда ра-
створъ въ каждый моментъ насыщенъ. Процессъ, обыкновенно понима-
емый подъ словомъ «раствореніе», необратимъ: онъ сопровождается са-
мостоятельнымъ и также необратимымъ процессомъ д и ф ф у з і и раство-
реннаго вещества въ растворѣ. При этомъ параметръ, характеризующій
растворъ, — концентрація, — становится неопредѣленнымъ подобно тому,
какъ въ прежнихъ примѣрахъ становились при необратимыхъ процессахъ
неопредѣленными температура или давленіе. Процессъ растворенія прои-
зойдетъ обратимымъ образомъ, если соблюсти напр. слѣдующія условія.
На днѣ высокаго цилиндрическаго сосуда, закрытаго подвижнымъ порш-
немъ, находится сухая соль. Пространство надъ солью занято парами воды,
упругость которыхъ равна той упругости, которую имѣетъ паръ надъ на-
сыщеннымъ растворомъ соли при температурѣ системы. Будемъ теперь
безконечно медленно опускать поршень и вмѣстѣ съ тѣмъ под-
держивать температуру постоянной. Образуется насыщенный растворъ.
Если теперь столь же медленно поднимать поршень, то система возвра-
тится въ свое первоначальное состояніе.
V. Необратимымъ представляется всякій процессъ, при кото-
ромъ мы имѣемъ движеніе тѣла, сопровождающееся тре-
ніемъ, слѣдовательно всякое движеніе на земной поверх-
ности. При всякомъ такомъ движеніи происходитъ превращеніе види-
маго движенія въ теплоту, а это процессъ необратимый. Если тѣло дви-
жется равномѣрно, то мы имѣемъ равновѣсіе между дѣйству-
ющими на тѣло внѣшними силами и силою тренія. Отсюда слѣдуетъ,
что равновѣсіе является хотя и необходимымъ, но не всегда достаточ-
нымъ условіемъ обратимости какого-либо процесса. Слѣдуетъ, впрочемъ,
замѣтить, что въ данномъ случаѣ мы имѣемъ только механическое, но не
тепловое равновѣсіе: температура тѣла становится неопредѣленной ве-
личиной. Легко видѣть, что въ случаѣ неравномѣрнаго движенія ско-
рость тѣла ѵ также становится неопредѣленной величиной благодаря тре-
392
Термодинамика.
нію, такъ какъ необходимъ нѣкоторый конечный промежутокъ времени,
чтобы измѣненіе ѵ у трущейся поверхности передалось другимъ ча-
стямъ тѣла.
Необратимы также всѣ процессы диффузіи въ твердыхъ,
жидкихъ и газообразныхъ тѣлахъ.
Повидимому, необратимы также и всѣ тѣ процессы, кото-
рые возникли благодаря нѣкоторому «освобождающему
дѣйствію». Такое дѣйствіе сопровождается весьма малой затратой
энергіи, не имѣющей никакой внутренней связи съ .собственно главнымъ
процессомъ и служащей только для устраненія какого-либо препятствія
для возникновенія главнаго процесса. Сюда относятся, напр. открытіе
крана, благодаря чему вода или газъ, находящіеся въ сосудѣ, могутъ на-
чать вытекать; разрядъ конденсатора (напр. лейденской банки), замыка-
ніе электрическаго тока, маленькая искра или сотрясеніе, вызывающія
взрывъ, зажиганіе горючаго матеріала и т. д. Во всѣхъ этихъ случаяхъ
возникшіе процессы необратимы.
Само собою ясно, что всѣ процессы, возникающіе ппи первоначально
неустойчивомъ равновѣсіи системы, необратимы. Сюда отно-
сится застываніе переохлажденныхъ жидкостей и пересыщенныхъ раство-
ровъ ; далѣе аллотропическое измѣненіе, происходящее не при темпера-
турѣ, характеризующей превращеніе; напримѣръ превращеніе обыкновен-
наго металлическаго олова при низкой температурѣ въ его сѣрое алло-
тропическое видоизмѣненіе. Послѣдній процессъ обратимъ, если онъ про-
сходитъ при температурѣ 20°.
Переходимъ къ одной изъ самыхъ интересныхъ и важныхъ сторонъ
разбираемаго нами вопроса. Мы уже замѣтили выше, что въ чистой
механикѣ, т.-е. въ ученіи о движеніи и о силахъ, мы встрѣча-
емся только съ обратимыми процессами. Дѣйствительно, не-
возможно на основаніи законовъ механики построить необратимый процессъ.
Возникаетъ, такимъ образомъ, дилемма. Съ одной стороны идеаломъ физики
является сведеніе причинъ всѣхъ физическихъ процессовъ на законы
механики, взглядъ на весь доступный наблюденію неорганизованный
міръ, какъ на механическую систему, въ которой дѣйствуютъ силы и
происходятъ движенія.
Съ другой стороны наблюденіе приводитъ насъ къ такому выводу:
въ то время, какъ всѣ механическіе процессы обра-
тимы, всѣ физическіе процессы на дѣлѣ необратимы,
такъ какъ выше разсмотрѣнные обратимые физическіе процессы пред-
ставляютъ только идеальные случаи, которые теоретически возможны, но
въ дѣйствительности неосуществимы.
Безсмертная заслуга Воікшапп’а заключается въ томъ, что онъ
устранилъ это недоразумѣніе и показалъ, въ чемъ заключается истинная
причина необратимости физическихъ процессовъ. Эта причина: моле-
кулярное строеніе матеріи, громадное число молекулъ, изъ ко-
торыхъ состоитъ каждое, даже очень маленькое, въ обычномъ смыслѣ
Обратимые и необратимые процессы.
393
слова, тѣло. Воіігтапп удачно примѣнилъ къ движенію молекулъ
законы теоріи вѣроятностей и объяснилъ кажущееся противо-
рѣчіе между законами наблюдаемыхъ физическихъ явленій и зако-
нами механики. Введенный имъ въ науку методъ называется теперь
статистическимъ методомъ.
Пояснимъ этотъ методъ на двухъ примѣрахъ.
I. Представимъ себѣ два замкнутыя пространства А и В, отдѣ-
ленныя другъ отъ друга перегородкой. Пространство В — совершенно
пусто; въ А находится одна молекула; она быстро движется, по-
стоянно мѣняетъ направленіе, ударяясь о стѣнки А и отражаясь, со-
гласно кинетической теоріи газовъ, какъ абсолютно упругое тѣло. Уда-
лимъ теперь перегородку, тогда очень скоро окажется, что молекула пе-
решла въ пространство В. Этотъ чисто механическій процессъ перехода
изъ А въ В очевидно вполнѣ обратимъ: черезъ нѣкоторое время мо-
лекула снова окажется въ А и, если въ этотъ моментъ задвинуть пере-
городку, то первоначальное состояніе (молекула въ А) возстановится.
Пусть теперь въ Л находятся двѣ молекулы, движущіяся незави-
симо одна отъ другой и, быть можетъ, время отъ времени сталкивающі-
яся. Если мы удалимъ перегородку, то снова произойдетъ обратимый
процессъ, такъ какъ навѣрное черезъ нѣкоторое время обѣ молекулы с л у -
ч а й н о окажутся въ А. Ждать этого случая придется вообще нѣсколько
дольше чѣмъ при одной молекулѣ. При трехъ молекулахъ ждать при-
дется еще дольше. При четырехъ, пяти, шести молекулахъ вѣроятность
того, что изъ всѣхъ возможныхъ случаевъ распредѣленія молекулъ между
объемами А и В осуществится какъ разъ тотъ, при которомъ всѣ моле-
кулы находятся въ- Д, становится все меньше и меньше, и придется
ждать все дольше и дольше, пока удастся въ дѣйствительности
наблюдать такой, теоретически, очевидно, вполнѣ возможный случай.
При десяти молекулахъ можетъ быть пройдетъ много часовъ, при
двадцати — много лѣтъ, а при ста — тысячелѣтія, пока случайно
всѣ молекулы въ одинъ и тотъ же моментъ окажутся въ А.
Пусть теперь въ А находится газъ, содержащій ІО20 молекулъ.
Если мы удалимъ перегородку, то весьма быстро установится динами-
ческое равновѣсіе, при которомъ отношеніе числа молекулъ въ А
къ числу молекулъ въ В приблизительно равно отношенію объе-
мовъ этихъ пространствъ. Въ данный промежутокъ времени прибли-
зительно столько же молекулъ летятъ отъ А къ В, какъ и отъ В
къ Д. Отношеніе чиселъ молекулъ въ А и В постоянно колеблется, не
удаляясь однако значительно отъ отношенія объемовъ. Теоретически
вполнѣ мыслимо, что при безпорядочномъ движеніи молекулъ случайно
всѣ ІО20 молекулъ въ какой-либо моментъ окажутся въ предѣлахъ про-
странства А. Но вѣроятность такого событія невообразимо мала, и
поэтому оно никогда не наблюдалось и не будетъ наблюдаться. Чрезвы-
чайно мала даже и вѣроятность того случая, чтобы отношеніе числа молекулъ
въ А къ числу молекулъ въ В настолько отличалось отъ отношенія объ-
394
Термодинамика.
емовъ, чтобы разность давленій стала бы доступной измѣренію. Даже
если бы ото произошло, то отношеніе давленій снова измѣнилось бы въ
столь короткое время, что, конечно, не удалось бы обнаружить зтой раз-
ности давленій.
Итакъ расширеніе газа изъ А въ пустоту В, какъ механическій про-
цессъ, обратимо. Но в ѣ р о я т н о с т ь обращенія такъ мала, что это обра-
щеніе не удается наблюдать; оно никогда не происходитъ. То, что ни-
когда не происходитъ, т.-е. не можетъ быть наблюдаемо, для насъ
является невозможнымъ процессомъ, и поэтому расширеніе
газа въ пустоту, какъ физическій процессъ, не-
обратимо.
II. Разсмотримъ движеніе тѣла А съ треніемъ на горизон-
тальной поверхности другого тѣла В, Начальная скорость тѣла А
пусть будетъ т.-е. вь началѣ движенія всѣ молекулы тѣла А имѣ-
ютъ составляющую скорости г/0, направленную въ сторону
движенія. Вслѣдствіе тренія движеніе молекулъ тѣлъ А и В мѣняется
такимъ образомъ, что скорость ѵ непрерывно уменьшается; въ то же
время истинная скорость неправильнаго движенія молекулъ возрастаетъ.
Наконецъ ѵ становится равнымъ 0 и тѣло А останавливается. Этотъ
чисто механическій процессъ несомнѣнно обратимъ. Тѣ же столкнове-
нія молекулъ, которыя уменьшили ѵ до нуля, могутъ случайно пове-
сти къ тому, что всѣ молекулы получатъ общую скорость ѵ, такъ что
спокойно лежащее тѣло начнетъ двигаться съ возрастающей скоростью,
въ слѣдствіи чего въ начальной точкѣ снова будетъ V = Ѵо. Но намъ ни-
когда не придется наблюдать подобнаго процесса, такъ какъ вѣроят-
н ость его невообразимо мала. Поэтому процессъ движенія тѣла съ тре-
ніемъ, какъ физическій процессъ, необратимъ.
Мы ограничимся этими двумя примѣрами; нетрудно примѣнить тѣ
же разсужденія и къ другимъ необратимымъ физическимъ процессамъ.
Теперь ясно, почему этотъ методъ разсмотрѣнія называется статисти-
ческимъ. Различные возможные результаты движенія даннаго числа
молекулъ распредѣляются сообразно тому, какъ часто они случа-
ются, какъ это дѣлается въ статистикѣ. Результаты движенія,
вполнѣ возможные механически, а слѣдовательно и математически, но
вмѣстѣ съ тѣмъ характеризующіеся невообразимо малой вѣроятностью,
соотвѣтствуютъ тѣмъ физическимъ процессамъ, которые никогда не на-
блюдаются, а слѣдовательно для насъ невозможны. Такимъ обра-
зомъ мы приходимъ къ слѣдующему результату:
Физическій процессъ необратимъ, если его обра-
щеніе представляетъ процессъ, статистически въ выс-
шей степени невѣроятный.
Существованіе необратимыхъ физическихъ процессовъ такимъ обра-
зомъ вовсе не противорѣчитъ механическому міровоззрѣнію. Молекуляр-
ная гипотеза въ связи съ исчисленіемъ вѣроятностей образуетъ мостъ,
связующій теоретически всегда обратимыя механическія
Круговые процессы.
395
явленія съ наблюдаемыми, не обратимыми физическими
явленіями.
§ 7. Круговые процессы, Графическія изображенія. Изъ числа
различныхъ процессовъ въ теоретическомъ отношеніи особенно важны
такъ называемые круговые процессы. Если въ тѣлѣ или въ системѣ
совершались различные физическіе процессы и въ концѣ концовъ тѣло
(или система) снова вернулось въ первоначальное состояніе, то мы гово-
римъ, что произошелъ круговой процессъ. Ие слѣдуетъ смѣши-
вать кругового процесса съ обратимымъ процессомъ, протекшимъ сначала
въ одномъ, потомъ въ обратномъ направленіи. Если мы обозначимъ на-
чальное состояніе тѣла или системы черезъ А, а черезъ В нѣкоторое
промежуточное состояніе тѣла или системы, возможно' болѣе отличаю-
щееся отъ Л, то при круговомъ процессѣ состояніе тѣла или системы по
нѣкоторому опредѣленному пути мѣняется отъ А до В, а затѣмъ по дру-
гому пути обратно отъ В до А.
Обратимый круговой процессъ долженъ состоять изъ ряда
обратимыхъ элементарныхъ процессовъ; круговой процессъ необратимъ,
если какая-либо часть его необратима. Легко понять, что изолиро-
ванная система не можетъ совершать кругового про-
цесса. Дѣйствительно мы видѣли, что въ изолированной системѣ фи-
зическіе процессы происходятъ въ томъ случаѣ, если система не нахо-
дится въ состояніи равновѣсія по отношенію къ данному процессу. Про-
цессъ въ данномъ случаѣ является не чѣмъ инымъ, какъ стремленіемъ
системы къ состоянію равновѣсія. Обратный процессъ, т.-е. удаленіе отъ
состоянія равновѣсія, возможенъ лишь при участіи внѣшнихъ тѣлъ.
Конечно, внутри системы возможны и обратимые процессы, но безъ
участія внѣшнихъ тѣлъ они не могутъ течь въ обратномъ направленіи,
какъ это видно изъ разсмотрѣннаго выше ряда примѣровъ. Если напр.
какое-либо тѣло системы пріобрѣло извѣстное количество теплоты тепло-
проводностью или лучеиспусканіемъ, то этотъ процессъ могъ быть обра-
тимымъ только въ томъ случаѣ, если въ системѣ заключается безконечно
большое число источниковъ теплоты. Обращеніе при этомъ возможно
только по тому же самому пути, а слѣдовательно кругового
процесса мы не получимъ. При нѣкоторыхъ другихъ обратимыхъ
процессахъ система непремѣнно подвергается дѣйствію внѣшнихъ силъ.
При двухъ различныхъ обратимыхъ процессахъ, ведущихъ отъ со-
стоянія А къ состоянію В, работа внѣшнихъ силъ должна быть различна.
Слѣдовательно при круговомъ процессѣ, когда тѣло или система по од-
ному пути переходитъ отъ Л къ В, а затѣмъ по другому пути
обратно отъ В къ Л, вся работа внѣшнихъ силъ не равна нулю. Слѣ-
довательно внѣ системы произошли измѣненія. Изъ этихъ разсуж-
деній непосредственно слѣдуетъ: въ изолированной системѣ
только какая-либо часть Мг можетъ совершать круго-
вой процессъ; при этомъ состояніе какой-либо другой
части М2 той же системы должно измѣняться. Слѣдо-
396
Термодинамика.
вательно, круговой процессъ всегда есть парціальный
процессъ. Если круговой процессъ обратимъ и вслѣдъ за тѣмъ
совершается въ обратномъ порядкѣ, то вся система возвращается въ
первоначальное состояніе; если круговой процессъ необратимъ, то
по окончаніи его въ другихъ частяхъ системы должны ока-
заться какія-либо измѣненія состоянія.
Важную роль играютъ въ термодинамикѣ графическія изображенія,
которыми впервые воспользовался Сіареугоп. Возьмемъ обыкно-
венныя координатныя оси и будемъ на осяхъ
Рис’ 118, откладывать величины х и у, опредѣляющія
У состояніе тѣла. Въ такомъ случаѣ точка на
/ плоскости является представителемъ опредѣ-
/ / леннаго состоянія тѣла. Понятно, что поло-
I женіе этой точки, при одномъ и томъ же со-
АѴ стояніи тѣла, будетъ весьма различное, смо-
тря по выбору независимыхъ перемѣнныхъ х
и у. Два различныя состоянія тѣла изо-
----------------------х бразятся двумя различными точками А и В
(рис. 118); переходъ тѣла отъ состоянія А къ
состоянію В изобразится нѣкоторою кривою АСВ, уравненіе которой выража-
етъ собою законъ перехода тѣла отъ начальнаго состоянія къ состоянію
окончательному.
Итакъ кривой АСВ соотвѣтствуетъ совершенно опредѣленный фи-
зическій процессъ, которому подвергнуто данное тѣло. Слѣдуетъ
обратить вниманіе на то чрезвычайно важное обстоятельство, что
только обратимые процессы могутъ быть пред-
ставлены графически. Это слѣдуетъ уже изъ того, что, какъ
выше указано, при необратимомъ процессѣ по крайней мѣрѣ одинъ изъ
параметровъ, опредѣляющихъ состояніе тѣла, становится неопредѣлен-
нымъ. Примѣры, ниже приведенные, послужатъ къ дальнѣйшему выяс-
ненію этой мысли.
Въ дальнѣйшемъ изложеніи каждый разъ, когда
физическій процессъ изображенъ графически, бу-
детъ предполагаться, что мы разсматриваемъ про-
цессъ обратимый.
Существуетъ безконечное множество различныхъ обратимыхъ про-
цессовъ, переводящихъ тѣло изъ начальнаго состоянія А въ новое состоя-
ніе В. Каждая кривая АСВ, соединяющая точки А и В, изображаетъ*
такой процессъ.
Одинъ и тотъ же физическій процессъ выражается весьма различ-
ными кривыми въ зависимости отъ того, какіе параметры х и у мы вы-
беремъ для опредѣленія состоянія тѣла.
Обратимый круговой процессъ изображается замкнутой
кривой, напр. АО ВС А. Двумъ направленіямъ, въ которыхъ этотъ про-
цессъ можетъ совершаться, въ графическомъ изображеніи соотвѣтству-
Круговые процессы.
397
ютъ направленія АОВСА и АСВОА, Разберемъ теперь подробнѣе нѣко-
торые особенно важные процессы.
Процессъ называется изотермическимъ, если онъ происхо-
дитъ при постоянной температурѣ, і = Сопзѣ Кривая, изображающая
этотъ процессъ, называется изотермою. Если за одну изъ независимыхъ
перемѣнныхъ х и у принята температура то изотерма есть прямая,
перпендикулярная къ оси і Если за независимыя перемѣнныя принять
ѵ и д то для идеальныхъ газовъ уравненіе изотермъ /тг/ = Соп8І;
это равностороннія гиперболы, ассимптоты которыхъ суть координатныя
оси. При необратимомъ изотермическомъ расширеніи газа невоз-
можно графически изобразить промежуточныя состоянія; напр. при рас-
ширеніи газа въ пустоту давленіе р представляется величиною неопре-
дѣленною. Для системы, состоящей изъ жидкости и ея насы-
щеннаго пара, изотерма есть прямая, параллельная оси ибо при
заданной температурѣ упругость р насыщеннаго пара отъ ѵ не зависитъ,
т.-е. уравненіе изотермы въ этомъ случаѣ р = Соп8І.
Каждой температурѣ і соотвѣтствуетъ опредѣленная изотерма, такъ
что всевозможныя изотермы представляютъ
кривыхъ линій, которыя, понятно, нигдѣ
не пересѣкаются. Черезъ каждую точку М
(рис. 119) на плоскости, въ которой рас-
положены координатныя оси х и у, можно
провести изотерму АМВ; ея точки опре-
дѣляютъ состоянія тѣла, при которыхъ
температура имѣетъ одно и то же значе-
ніе. Мы всегда можемъ себѣ представить,
что изотермическое измѣненіе состоянія
тѣла обусловлено тѣмъ, что тѣло нахо-
дится въ соприкосновеніи съ другимъ весьма
безпредѣльно большое число
большимъ тѣломъ (точнѣе — окружено такимъ тѣломъ), способнымъ под-
держивать въ немъ постоянную температуру. Тающій ледъ, пары кипя-
щей жидкости, большое количество движущейся воды и т. д. могутъ
служить такимъ тѣломъ. Если х~ѵ и у = р и мы имѣемъ дѣло съ идеаль-
нымъ газомъ, то кривая АМВ, какъ сказано, будетъ гипербола рѵ = Соп8І.
Процессъ вообще называется адіабатическимъ (т. I), когда
онъ происходитъ безъ теплового обмѣна между тѣломъ и остальнымъ мі-
ромъ. Кривая, изображающая такой процессъ, если онъ обратимъ,
называется адіабатою. Въ системѣ (у, р) уравненіе адіабаты для
идеальнаго газа рѵк = Соп8І. (т. I). Эта формула будетъ вновь выве-
дена ниже; въ ней к, — ср-.сѵ есть отношеніе теплоемкостей газа при
постоянномъ давленіи и при постоянномъ объемѣ. Черезъ каждую точку М
(рис. 119) можно провести адіабатическую линію СМО\ ея точки опре-
дѣляютъ тѣ послѣдовательныя состоянія тѣла, которыя получатся, если,
исходя изъ состоянія, опредѣляемаго точкою М, мы станемъ подвергать
тѣло адіабатическому процессу въ ту или другую сторону, т.-е. за-
398
Термодинамика.
ставимъ возрастать или убывать величину х, напр. объемъ. Уравненіе
рѵк = Сопзі. показываетъ, что въ системѣ (г/, р) и для идеальнаго
газа адіабата СМО болѣе круто спускается къ оси абсциссъ, чѣмъ изо-
терма АМВ.
На адіабатическомъ процессѣ особенно ясно обнаруживается, что
графическое изображеніе примѣнимо только къ обратимымъ процессамъ.
Напр., если газъ расширяется въ пустоту, то процессъ можетъ быть аді-
абатическимъ. Однако этотъ процессъ также и изотермическій; началь-
ное и конечное состояніе газа связаны между собой уравненіемъ рѵ =
= Соп8І, а не рѵк == Соп$і. По причинамъ, которыя выяснятся впо-
слѣдствіи, обратимый адіабатическій процессъ называется
также изентропическимъ.
Если процессъ протекаетъ при постоянномъ объемѣ, то кри-
выя, изображающія процессъ, называются изопикнами (у = Соп8І);
случаю р = Соп8І. соотвѣтствуютъ и з о б а р ы. Кривыя, изображающія
процессъ, въ теченіе котораго энергія имѣетъ постоянное значеніе, на-
зываются изэнергетами.
Въ книгѣ 2еипег’а «ТесйпіесЬе Тегтойупатік» (I, стр. 142)
можно найти изложеніе свойствъ группы кривыхъ, называемыхъ поли-
тропами. Эти кривыя имѣютъ важное практическое значеніе. Ихъ
уравненіе имѣетъ видъ
рѵп = С0П8І>
гдѣ п — нѣкоторое положительное число.
Въ частномъ случаѣ п = к — ср: сѵ мы имѣемъ адіабату идеальнаго газа.
§ 8. Теплота, получаемая тѣломъ. Измѣненія состоянія тѣла во
всѣхъ случаяхъ, кромѣ *тѣхъ, когда, они адіабатическія, сопровождаются
обмѣномъ тепла съ окружающими другими тѣлами. Эти послѣднія Мы
будемъ называть нагрѣвателями или охладителями, смотря по
тому, переходитъ ли теплота отъ нихъ къ разсматриваемому тѣлу или обратно.
Конечныя количества тепла, полученныя тѣломъ, будемъ обозна-
чить буквою ; весьма малыя количества черезъ безконечно ма-
лыя — черезъ Если тѣло отдаетъ теплоту охладителю, то мы бу-
демъ считать отрицательнымъ.
Теплота б/<3, полученная тѣломъ, распадается на три части. Нѣ-
которая часть б/Ц/ тратится на увеличеніе запаса внутренней кинети-
ческой энергіи тѣла, т.-е. живой силы движенія его частицъ; проще
говоря, б/Ц/ идетъ на повышеніе температуры тѣла. Вторая часть (1Р
тратится на внутреннюю работу, т.-е. на увеличеніе запаса по-
тенціальной энергіи частицъ тѣла. Наконецъ третья часть сІЬ рас-
ходуется на внѣшнюю работу, совершаемую тѣломъ при томъ без-
конечно маломъ измѣненіи состоянія, которое сопровождается поглоще-
ніемъ теплоты Если отрицательное, то теплота, отданная тѣ-
ломъ, образуется на счетъ кинетической и потенціальной энергіи частицъ
тѣла, и на счетъ работы, совершенной внѣшними силами надъ тѣломъ;
Теплота, получаемая тѣломъ.
399
Величина сР№ = 0, когда измѣненіе состоянія тѣла изотермическое. Ве-
личина (ІР повидимому всегда существуетъ; она играетъ главную роль,
когда измѣненіе состоянія сопровождается переходомъ тѣла изъ одного
«состоянія» (въ узкомъ смыслѣ слова) въ другое, т.-е. изъ твердаго въ
жидкое, изъ жидкаго въ газообразное или обратно; далѣе, когда проис-
ходитъ диссоціація (т. I) или превращеніе тѣла изъ одного состоянія въ
аллотропическое (т. I). Величина (ІР весьма мала для газовъ, свойства
которыхъ мало отличаются отъ свойствъ идеальныхъ газовъ (т. I;, для
которыхъ (ІР — 0.
Для (ІЬ имѣемъ выраженіе (ІЬ — Асіг, гдѣ А термическій коеффи-
ціентъ работы, (іг безконечно малая работа, совершенная тѣломъ; если (іг
отрицательное, то — (іг есть работа, совершенная внѣшними силами
надъ тѣломъ. Характеръ внѣшней работы (іг можетъ быть весьма раз-
личный; такая работа происходитъ напр. при измѣненіи формы тѣла
(раскручиваніе, укорачиваніе и т. под.), когда существуетъ внѣшняя со-
противляющаяся сила; далѣе сюда относится работа преодолѣванія тренія,
работа увеличенія поверхности жидкости (т. I) и т. д. Мы главнымъ
образомъ будемъ расматривать случаи, когда внѣшняя работа обусловли-
вается измѣненіемъ объема, причемъ вся поверхность подвержена вездѣ
одинаковому и къ ней нормальному давленію р. Въ этомъ случаѣ при
обратимомъ процессѣ (іг = рйѵ (т. I), и слѣд. сІЬ = Арйѵ.
Обозначимъ черезъ Іі весь запасъ энергіи, заключающійся въ тѣлѣ
и зависящій отъ равномѣрно-безпорядочныхъ движеній (стр. 3) частицъ,
энергія которыхъ ІУ, и отъ потенціальной энергіи Р частицъ. Въ вели-
чину 1} не входитъ энергія движенія тѣла, какъ цѣлаго. Для краткости
мы будемъ величину 1} называть энергіей тѣла. КігсЫіоИ да-
етъ этой величинѣ названіе « ѴѴіткип^ъіипсііоп» ; Т іі о ш 8 оп (Ьогсі Кеі-
ѵ і п) называетъ ее механическою энергіей тѣла. Энергія 1} тѣла есть не-
прерывная, однозначная и конечная функція его состоянія, такъ что
можно положить 1} = Р (х, у), гдѣ х и у независимыя перемѣнныя, опре-
дѣляющія состояніе тѣла; въ этомъ заключается принципъ I, высказан-
ный нами уже въ т. I, въ ученіи объ энергіи.
Мы имѣемъ и = ѴР Р\ С1аіі8Іи8 называетъ часть ѴР «ЛѴаг-
теіпЬаІЬ, а часть Р — «АѴегкіпІіак». Теплота, соотвѣтствующая вели-
чинѣ ѴР и поглащаемая вѣсовою единицею вещества при нагрѣваніи
на 1°, названа Сіапвіиз’омъ истинною теплоемкостью. Для
идеальныхъ газовъ она равна теплоемкости сѵ при постоянномъ объемѣ.
Если состояніе тѣла безконечно мало мѣняется, то энергія мѣняется на
величину (ІО = (ІѴР 4- <ІР- Но мы имѣли (10 — (ІѴР + <іР <ІР и
(ІЬ = Ар(іѵ, такъ что вообще
(іО = (Ш+(іЬ......................(31)
и при (ІЬ = Арйѵ
(10 = аи + Арйѵ..................(31,а)
Теплота отчасти тратится на измѣненіе запаса энергіи тѣла (по*
400
Термодинамика.
глощается тѣломъ), частью — на внѣшнюю работу.
Полагая
ди
ду
— С, имѣемъ
аи = вдх + сну
ди
с)х
В,
(32)
Величина (Ш есть полный
дифференціалъ функціи двухъ независи-
мыхъ перемѣнныхъ (стр. 378), а по-
тому, см. (16,бг),
дв - ос (33)
ду ~ дх ' ' ' 1 ’
Каждая точка на плоскости ко-
ординатныхъ осей х, у опредѣляетъ
состояніе тѣла и соотвѣтствующую
ему величину /7, такъ что можно го-
ворить о значеніи энергіи и въ раз-
личныхъ точкахъ плоскости. Поло-
жимъ, что измѣненіе состоянія тѣла
изображается кривой МЕЫ (рис. 120), и что въ /14 и въ 7Ѵ мы имѣемъ
и = и± и и = и>. Полное измѣненіе энергіи и при переходѣ изъ со-
стоянія М въ состояніе М равно
м
(34)
гдѣ предѣлы интеграла обозначены символически. Это количество не за-
виситъ отъ способа перехода тѣла изъ состоянія М въ состояніе 7Ѵ; въ
оно напр. одинаково для МОЫ и МЕЫ. Для кругового процесса
имѣемъ
...................(35)
Величина дѣ не есть дифференціалъ какой-либо функціи двухъ пе-
ремѣнныхъ х и у, опредѣляющихъ состояніе тѣла. Это особенно ясно для
случая, когда х = ѵ, у —р и (11,= Ардѵ. Полное количество теплоты,
расходуемой на внѣшнюю работу при процессѣ МОЫ, измѣряется пло-
щадью 5, ограниченной осью г/, крайними ординатами рг и р2 и кривою;
символически пишемъ
У 77 = АУ*рдѵ = А8 ....... (36, а)
м м
гдѣ 5 = СМОІІНО. Для процесса МЕЫ имѣемъ другое значеніе 5 =
СМЕЖНО. Для кругового процесса МОЫЕМ имѣемъ
77 — А Урдѵ = Ас..............(36, &)
гдѣ (У площадь, ограниченная кривой 1ИОМЕЛЕ Для произвольныхъ х и
у имѣемъ
Теплота, получаемая тѣломъ.
401
/V х2 х2
IсІЬ = А^рсіѵ — А^ Р(х)(1х,
М хг хг
гдѣ хг и х2 абсциссы точекъ М. и X. Чтобы преобразовать интегралъ,
мы должны вспомнить, что ѵ и р суть функціи отъ х и у, и что послѣд-
нія двѣ величины связаны нѣкоторымъ уравненіемъ вида у = др(х), урав-
неніемъ кривой МОЫ или МЕХ.
Выраженіе (31) показываетъ, что ао состоитъ изъ двухъ частей:
первая есть дифференціалъ функціи величинъ х и у, вторая же не пред-
ставляетъ такого дифференціала. Отсюда слѣдуетъ, что б/<2 не есть
дифференціалъ какой-либо функціи двухъ перемѣн-
ныхъ х и у, опредѣляющихъ состояніе тѣла. Если мы че-
резъ <2 обозначимъ полное количество тепла, поглощеннаго тѣломъ при
переходѣ изъ состоянія М въ состояніе X, то имѣемъ:
х2
= + А/рсіѵ. . . (37.а)
МММ хг
Если х = ѵ, у — р, то
0 = Ѵ^ — Ѵ^АЗ..................(37,6)
Площадь 5 зависитъ отъ вида кривой, соединяющей точки М и X;
отсюда слѣдуетъ, что количество (2 теплоты, поглощенной
тѣломъ при переходѣ отъ одного состоянія Л4 въ дру-
гое 7Ѵ, зависитъ отъ способа или пути перехода.
Обозначая полное количество теплоты, затраченной на внѣшнюю ра-
боту, черезъ Ь, имѣемъ
0^Ѵ2 — С^ + Ь................. (37, с)
Для кругового процесса, см. (35), 1)2 — 1}1 и слѣд.
<2 = А = Лг,
гдѣ г вся работа, совершенная тѣломъ при круговомъ процессѣ, или, точнѣе,
избытокъ положительной работы, совершенной тѣломъ, надъ той работой,
которую внѣшнія силы совершили надъ тѣломъ. Если х=ѵ и у=р> то
для кругового процесса, см. (36,6),
<2 = Ао....................(37, а)
Предположимъ, что безконечно малое измѣненіе состоянія, при ко-
торомъ тѣло поглощаетъ количество аО тепла, характеризуется измѣне-
ніемъ величинъ х и у на (1х и йу. Тогда мы можемъ положить
ао = хах 4- ѵау ....... (зв, а)
гдѣ X и V функціи отъ х и у, т.-е. функціи состоянія. Легко по-
нять значеніе этихъ величинъ. Если .у не мѣняется, то аО — Хах; если
х не мѣняется, то аО = Ѵйу. Отсюда ясно, что X и V характеризуютъ
количества теплоты, идущія на измѣненія отдѣльно одной изъ пере-
мѣнныхъ X и у.
КУРСЪ ФИЗИКИ О ХВОЛЬСОНА. Т. III, изд. 3-е. 26
402
Термодинамика
Особенный интересъ представляетъ частный случай, когда одна изъ
перемѣнныхъ есть температура, напр. если у=і. Въ этомъ случаѣ
введемъ обозначенія Хі и сх вмѣсто X и У, такъ что
б/р = Х^сіх схсІі.....................(38, Ь)
При і = Сопзѣ., имѣемъ г/С? = Х^х. Отсюда видно, что величина Хі
опредѣляетъ то количество теплоты, которое поглощается тѣломъ, когда
параметръ х при постоянной температурѣ увеличивается на единицу. От-
сюда слѣдуетъ, что Хі есть скрытая теплота измѣненія параметрах.
Если х — Соп8І., то для повышенія температуры тѣла на сіі требу-
ется количество теплоты сК± — сх(1і. Отсюда ясно, что свесть тепло-
емкость тѣла при постоянномъ^. Такимъ образомъ у насъ явля-
ется обобщенное представленіе- о теплоемкости. Фор-
мулы (31) и (38, Ь) даютъ легко
с
(38, с)
Въ частныхъ случаяхъ х — ѵ и х = р имѣемъ теплоемкости сѵ и ср,
давно намъ знакомыя.
Мы видѣли, что не есть дифференціалъ функціи перемѣнныхъ х
и у. опредѣляющихъ состояніе тѣла. Отсюда слѣдуетъ, что (і(і = Хсіх 4-
4- Ѵсіу представляетъ типичный примѣръ того рода безконечно малыхъ
величинъ, которыя нами были разсмотрѣны на стр. 379, подъ буквою В.
Величина (2=^сІ(2 зависитъ отъ пути; для замкнутаго пути, т.-е.
для кругового процесса §сіС} не равенъ нулю. Разность накрестъ взя-
тыхъ производныхъ не равна нулю, т.-е. мы имѣемъ важное неравен-
ство, см. (21) стр. 380,
дХ_ дУ
ду дх
(39)
Мы выведемъ ниже два общія и рядъ частныхъ выраженій для
разности этихъ двухъ производныхъ.
Для случая, когда независимыя перемѣнныя х и у суть двѣ изъ трехъ
величинъ ѵ. р, і, мы введемъ, вмѣсто (38, а) и (38, такія выраженія:
сІС} — ксіѵ 4~ Ідр....................(40, а)
сК) = асіѵ-\- сѵсіі . . ............(40, Ь)
сК± = есір 4~ срс1і...................(40, г)
Изъ предыдущаго ясно, что коеффиціенты при сіі въ двухъ послѣд-
нихъ формулахъ суть теплоемкости при постоянномъ объемѣ и при по-
стоянномъ давленіи. Формула (38, г) даетъ при х — ѵ
....................(40)бЛ
При х = р получается
ІдІЛ । л (дѵ\ . 1[дѵ\
Теплота, получаемая тѣломъ.
403
Функціи состоянія а и е представляютъ большой интересъ. Ими
опредѣляются тѣ количества теплоты, которыя тратятся на увеличеніе
объема (а) или упругости (^), когда измѣненіе состоянія тѣла изотер-
мическое (і = Соп8і.). Функцію а иногда называютъ скрытою те-
плотою расширенія. Функцію е можно, пожалуй, назвать скры-
тою теплотою измѣненія давленія. Легко сообразить, что во-
обще а > 0, е < 0, ибо изотермическое увеличеніе объема можетъ вообще
произойти только, когда тѣло производить работу > 0); изотермиче-
ское же увеличеніе упругости требуетъ затраты работы внѣшнихъ силъ,
причемъ эквивалентное количество теплоты должно выдѣлиться изъ тѣла.
Функціи а и е имѣютъ противоположные знаки. На теоретическую воз-
можность иного случая будетъ указано въ послѣдней главѣ этого отдѣла.
Нетрудно выяснить себѣ значеніе функцій к и I, полагая сперва /? = Соп8І.,
а потомъ ѵ = Соп8І.
Три выраженія для соотвѣтствуя одному и тому же измѣненію
состоянія тѣлъ, должны быть тождественно равны между собою; они
должны переходить одно въ другое при замѣнѣ одной пары независимыхъ
перемѣнныхъ другою. Это даетъ намъ связи между шестью функціями
6, /, а, е, сѵ и 4/: четыре изъ нихъ можно выразить черезъ остальныя
двѣ. При этомъ войдутъ производныя (26), которыя выражаются черезъ
коеффиціенты а, и у, связанные уравненіемъ (30). Такимъ образомъ
можно окончательно выразить &, /, а, е и у черезъ а, /?, сѵ и ср т.-е. че-
резъ величины наиболѣе намъ знакомыя. Введемъ въ (40, Ь} вмѣсто ѵ
и і. перемѣнныя р и іг тогда ѵ является функціей отъ р и Л и слѣд.
= адѵ -|- сѵ(іі = а
~дѵ
др
, । дѵ
4 СуСІІ.
Это выраженіе должно тождественно равняться = едр + ср(іі^ от-
куда получаются равенства
е = а ......... (41, а)
дѵ .
и ср = ад -\-сѵ, или
дѵ
с„ — с„ ...............(41, ЬУ
р ѵ ді
Формула (41, а) ясно показываетъ, что а и е разнаго знака, такъ
какъ ее можно написать въ видѣ е = — а$ѵ. Сравнивая (40, а) съ (40, &),
получаемъ двѣ формулы, изъ которыхъ при помощи (27) легко вывести:
ді
1~Сѵ др
ді ................<41’с>
к—а + сѵдѵ
Уравненія (41, а), (41,6), (41, с), (29) и (30) даютъ возможность вы-
разить величины у, к, I, а. е черезъ п, /?. сѵ. ср, т.-е. черезъ кбеффи-
ціенты расширенія и сжатія и черезъ двѣ теплоемкости:
26*
404
Термодинамика.
, _ ді____ ср
СР дѵ аѵ0
, ді №сѵ
‘^-др
а^о
аѵ*
7 ~ РрОѵ
Ср сѵ
а= р
(ср ~сѵ)рѵ
е =-----—
(41,/)
ат/0
(41,6/)
Если ввести к и I въ (40, а) то получается важная формула
а<^ = сР ддѵаѵ + Сѵ~драр..............................
§ 9. Формулы, основанныя на первомъ началѣ. Первое
(41,
начало
гласитъ, что теплота есть форма энергіи, что, слѣдовательно, нѣкото-
рое ея количество С? эквивалентно нѣкоторой работѣ г, и что теплота
тратится на производство работы. Оно выражается общимъ равен-
ствомъ <2 = Лг, или формулою (31), въ которой ясно изображено, что
часть теплоты тратится на внѣшнюю .работу. Сравненіе формулъ (31) и
(38, а) даетъ выраженіе для разности двухъ производныхъ, входящихъ въ
неравенство (39). Мы имѣемъ два выраженія
= АІ} Ардѵ и дХ) = Хдх + Уду.
Они должны сдѣлаться тождественно равными, если въ первое вставить
дѴ \ ді} , л дѵ , \ дѵ . т .
ао = ах + ау и аѵ=-^ах -у- ау. Такимъ образомъ получаются
ѵ ді} . л дѵ ді}. л дѵ ’
равенства X = + Ар и У — - + Ар . Дифференцируя имѣемъ:
дХ д21} і л др дѵ д д2ѵ
ду дудх ду дх ' дудх’
дѴ д2Ц др дѵ . д2ѵ
дх дхду ' дх ду ' ? дхду ’
Вычитая нижнее уравненіе изъ верхняго, и обозначая разность съ
правой стороны черезъ ЛД(х, у\ имѣемъ
дХ дУ АПГ Л
о(хѵ)-^др__дѵдр
^,у) дхду дудх
Это уравненіе мы назовемъ первымъ основнымъ уравне-
ніемъ. Оно можетъ быть разсматриваемо, какъ наиболѣе общее выра-
женіе связи, вытекающей, какъ слѣдствіе изъ перваго начала. Оно съ
особенною ясностью подтверждаетъ неравенство (39), показывающее, что
величина = Хдх Уду не есть дифференціалъ функціи двухъ пере-
мѣнныхъ х и у, но представляетъ величину того рода, которая была раз-
смотрѣна на стр. 379 подъ буквою В. Для трехъ частныхъ случаевъ (40)
получаемъ, вмѣсто (42), частныя формулы:
(42)
Круговой процессъ Карно.
405
. дѵ др ч дѵ др
1. х = ѵ, у=р-, — = -у =1; = = иоо ѵ ир независи-
мыя другъ отъ друга перемѣнныя ; О (у, р) = 1.
п , дѵ н др др дѵ дѵ „ „ , др
2, х = ѵ, у = і- =1; — = - — =0; слѣд. О(у, І) =
дх ду ді ’ ду ді ’ * ’ ді •
о 4. др „ дѵ дѵ др „ , .. дѵ
3. Х = р, у = - = 0; =^-; -С- == 1 ; слѣд. О (р,І) =----,т .
ду ду ді ’ дх 'Г’ ' ді
Такимъ образомъ получаются формулы, впервые выведенныя Сіаи-
8 і и 8гомъ, и выражающія связи между производными функцій к, I, а, е,
сѵ и Ср по р, г/, и і :
дк _дІ _ .
др дѵ~
да л-=АТ,=А^ = лгр . .
дѵ ді $ѵ
дср дѵ .
др ~~ АдТ~~А(ІЛ>0 ‘ • •
(42, а)
ді
де
ді
• • (42, Ь)
. • (42, с)
см. (29) ц (30).
Мы предложили, что дЬ = Ардѵ. Въ общемъ случаѣ
положить
мы должны
дѣ = Ьхдх -|- Ьуіу.
Тогда имѣемъ
Хдх + Уду =дд^дх-{- ду + Ьхдх 4- Ьуду.
Отсюда
_ №
~ дх
_ди
~ ду
и, слѣдовательно,
дХ_дѴ_д^х _дЬу
ду дх ду дх
(42, д}
Эта формула представляетъ собою обобщеніе формулы (42).
§ 10. Круговой процессъ Карно. Мы назвали круговымъ процес-
сомъ совокупность такихъ измѣненій состоянія тѣла, при окончаніи ко-
торыхъ это тѣло находится въ томъ же состояніи, въ которомъ оно на-
ходилось въ началѣ процесса, и мы назвали нагрѣвателями и охла-
дителями тѣ тѣла, отъ которыхъ тѣло получаетъ или которымъ оно
отдаетъ теплоту. Далѣе мы назвали процессъ обратимымъ, когда
тѣло можетъ его пройти въ одномъ направленіи и въ противоположномъ.
Въ обоихъ случаяхъ тѣло проходитъ черезъ одни и тѣ же состоянія; но
порядокъ, въ которомъ эти состоянія слѣдуютъ одно за другимъ, въ од-
номъ случаѣ одинъ, въ другомъ — противоположный.
Условія обратимости и необратимости процессовъ были нами по-
дробно разсмотрѣны.
406
Термодинамика.
цессовъ. мы видъли, что
Рис. 121.
Обратимся къ разсмотрѣнію нѣкоторыхъ свойствъ круговыхъ про-
вели обратимый процессъ совершается сперва
въ одномъ, а потомъ въ противоположномъ
направленіи, то окончательный результатъ
есть нуль», т.-е. совокупность обоихъ
процессовъ не вызываетъ никакихъ измѣ-
неній во вселенной. Тѣло, совершающее
эти два процесса, приходитъ въ прежнее
состояніе; нагрѣватели и охладители въ
первомъ процессѣ' соотвѣтственно служили
охладителями и нагрѣвателями во второмъ,
—х т.-е. они получили отданныя или отдали
полученныя количества теплоты. Отсюда
слѣдуетъ, что такую совокупность двухъ процессовъ мы можемъ приба-
вить къ даннымъ процессамъ, не мѣняя ихъ результата. На этомъ осно-
вана возможность дѣленія даннаго кругового обратимаго
процесса на нѣсколько процессовъ. Положимъ, что данъ круговой
процессъ АВСОА (рис. 121); проведемъ произвольную линію ВО и
прибавимъ два процесса ВО и ОВ. Ясно, что данный круговой про-
цессъ тождественъ съ совокупностью процессовъ АВОА и ВСОВ, По-
добнымъ же образомъ можно данный круговой процессъ раздѣлить и на
произвольно большое число отдѣльныхъ круговыхъ процессовъ.
Если тѣло совершаетъ круговой обратимый процессъ, то оно вгь нѣ-
которыхъ частяхъ этого процесса получаетъ теплоту отъ нагрѣвателей, въ
другихъ отдаетъ теплоту охладителямъ. Обозначимъ первое количество
черезъ второе черезъ ф2. Если > <32, то мы говоримъ, что кру-
говой процессъ былъ совершенъ въ прямомъ направленіи. Сі мы
называемъ затраченною теплотою, <Э2 перенесенною теплотою,
т.-е. перенесенною тѣломъ отъ нагрѣвателей къ охладителямъ. Разность
Сі — С2 = <7 затрачена на производство работы; мы назовемъ теплоту д
полезно затраченною. Итакъ, когда обратимый круго-
вой процессъ совершается въ прямомъ направленіи,
то затраченная теплота взятая отъ нагрѣвателей,
отчасти (<32) переходитъ на охладители, отчасти
(# = Сі — Сз) полезно затрачивается на производство
работы.
Когда круговой процессъ совершается въ обратномъ направленіи, то
тѣло получаетъ количество теплоты (?2 отъ охладителей, которые теперь
играютъ роль нагрѣвателей, дѣйствуя на тѣло въ такомъ порядкѣ, что
каждый слѣдующій имѣетъ температуру болѣе высокую, чѣмъ предыдущій.
Внѣшнія силы совершаютъ надъ тѣломъ работу, результатомъ которой
является эквивалентное ей количество теплоты д въ тѣлѣ. Наконецъ, тѣло
передаетъ нагрѣвателямъ, которые теперь играютъ роль охладителей, ко-
личество теплоты — <32 Я-
Все сказанное представляется особенно нагляднымъ, когда мы за не-
Круговой процессъ Карно.
407
зависимыя перемѣнныя примемъ ѵ и р, и когда д = Ли, см. (37,сі) и
рис. 120, такъ что <2Х С)2 + Аб, или
<22 = Аб ........ (43)
Отношеніе полезно затраченной теплоты д ко всей
затраченной теплотѣ <2Х называется экономическимъ
коеффиціентомъ кругового процесса, безразлично, будетъ
ли этотъ процессъ обратимый или необратимый. Обозначая этотъ коеф-
фиціентъ черезъ т), имѣемъ п п
= 41 - Ч2.............(44)
Чх Чі
Особенный интересъ представляетъ круговой процессъ, въ которомъ
тѣло получаетъ теплоту <2Х отъ одного только нагрѣвателя,
температура котораго 4? и передаетъ теплоту (?2 одному только
охладителю, температура котораго 4; полагаемъ 4 >> 4
Если такоі^ круговой процессъ совершается тѣломъ въ п р я м о м ъ
направленіи, то результатомъ его является переходъ теплоты
(<22) отъ болѣе теплаго тѣла къ болѣе, холодному и пе-
реходъ нѣкотораго количества теплоты (д) въ работу,
совершаемую самимъ тѣломъ (первая пара переходовъ).
Если такой круговой процессъ совершается тѣломъ въ обрат-
номъ направленіи, то въ результатѣ получается переходъ
тепла (<32) отъ болѣе холоднаго тѣла къ болѣе теплому
и переходъ нѣкотораго количества работы, совершае-
мой внѣшними силами надъ тѣломъ, въ теплоту (д) (вто-
рая пара переходовъ).
Переходы тепла отъ одного тѣла къ другому, а также переходъ
тепла въ работу и обратно мы будемъ называть превращеніями. Если
круговой процессъ обратимый, то возможны и первая и вторая пара пре-
вращеній; если онъ необратимый, то возможна только одна изъ нихъ.
Изъ круговыхъ обратимыхъ процессовъ имѣетъ особенное теоретиче-
ское и историческое значеніе круговой процессъ или циклъ
Карно (8 а й і Сагпоѣ, сынъ генерала С а г п о 1 временъ первой фран-
цузской революціи и дядя президента французской республики, умеръ въ
1832 году на 36-омъ году жизни). Этотъ процессъ, изображенный на
рис. 122, состоитъ изъ двухъ изотермическихъ и двухъ адіабатическихъ
процессовъ. Примемъ за независимыя перемѣнныя ѵ и р, и начнемъ
процессъ отъ состоянія, опредѣляемаго точкою А; пусть при этомъ объ-
емъ ѵх, упругость /?х и температура 4- Тѣло окружено нагрѣвателемъ,
температура котораго 4 и изотермически расширяется до объ-
ема ѵ2, причемъ давленіе дѣлается равнымъ р2. Этотъ процессъ изобра-
жается изотермою АВ.
Далѣе тѣло адіабатически расширяется до объема г>3, причемъ
упругость дѣлается равною р%. Температура тѣла понижается отъ 4
до 4- Затѣмъ тѣло окружается охладителемъ, температура котораго 4,
п сжимается до объема т/4 и упругости /?4, выбранныхъ такъ, чтобы че-
408
Термодинамика.
резъ конецъ О изотермы СО, изображающей этотъ процессъ, проходила
та адіабата, которая проходитъ черезъ точку А. Наконецъ тѣло адіаба-
тически сжимается до состоянія р±, причемъ и температура дѣлается
равною і±.
Вычислимъ экономическій коеффиціентъ кругового процесса Карно
для случая идеальнаго газа, пользуясь формулами, выведенными въ т. 1;
эти формулы, впрочемъ, бу-
дутъ вновь выведены въ
слѣдующей главѣ. Для ра-
боты г изотермиче-
скаго расширенія иде-
альнаго газа мы имѣли фор-
мулу (т. [)
г = . (45,а)
гдѣ А? постоянная формулы
Клапейрона рѵ = І^1,
Т абсолютная температура.
Для адіабатич е скихъ
измѣненій мы имѣли фор-
мулу Тѵк~~1 = Соп8І. Эта формула даетъ для адіабаты АО (рис. 122),
если положить 7\ = ^ + 273, Г2 = -|~ 273 :
= Т2ѵ±к~1,
а для адіабаты ВС
т^-1 = т^-1.
Эти двѣ формулы даютъ замѣчательное соотношеніе
(45.6)
Ѵ±
Формула (45,а) даетъ
И ^ = Аг.2 = АЦ7^
На основаніи (45,Ь) можемъ написать <32 = АЦТА% Ѵ'2. Вставивъ
и Р2 въ формулу (44) для и сокративъ общіе множители, получаемъ
выраженіе для экономическаго коеффиціента цикла Карно,
совершаемаго идеальнымъ газомъ:
0^-0, _ Л Л
1 ~ ~ Л
Онъ равенъ отношенію разности температуръ на-
грѣвателя и охладителя къ абсолютной температурѣ
нагрѣвателя. Если процессъ совершается между парами кипящей
воды и тающимъ льдомъ, то = 373, Г2 = 273 и
• • (46)
Круговой процессъ Карно. — Второе начало.
109
Ч = ~ = 0,268 .........................(46,а)
О і 6
или приближенно = А- Изъ формулы (46) можно вывести еще нѣ-
1 о
сколько интересныхъ соотношеній. Ее можно переписать такъ:
или
_ Л
О*
Количества теплоты, полученное отъ нагрѣвателя и погло-
щенное охладителемъ, относятся между собой, какъ абсолютныя тем-
пературы этихъ двухъ источниковъ теплоты. Послѣднюю формулу можно
написать такимъ образомъ:
<2і _ Оз 0
т\ т.2
Измѣнимъ теперь обозначенія. Пусть Рі и <32 означаютъ количе-
ства теплоты, полученныя отъ двухъ нашихъ источниковъ теплоты,
причемъ есть величина отрицательная (равная — при преж-
немъ обозначеніи). Тогда послѣднее уравненіе приметъ слѣдующую форму:
С1_|_^ = О....................(46,6)
/1 /2
Изъ перваго начала слѣдуетъ
+ > 0......................(*М
такъ какъ означаетъ всю теплоту, полученную тѣломъ при кру-
говомъ процессѣ и превращенную въ механическую работу.
Слѣдовательно, см. рис. 122,
<2і + <&> = А®-
Итакъ при обратимомъ круговомъ процессѣ Сагпоі
сумма количествъ теплоты, полученныхъ тѣломъ, эк-
вивалентна произведенной имъ работѣ, и слѣдова-
тельно не нуль, а сумма этихъ количествъ теплоты,
дѣленныхъ каждое на абсолютную температуру соот-
вѣтственнаго источника теплоты, равна нулю.
§ 11. Второе начало термодинамики; основанія работъ Сагпоі и
Сіаизіиз’а. Въ т. I, гл. третья, § 8 мы, подъ названіемъ принципа ПІ,
дали нѣкоторое понятіе о второмъ началѣ; общее указаніе на его харак-
теръ было нами дано въ § 1 этой главы. Разсмотримъ въ историческомъ
порядкѣ основныя работы, приведшія къ введенію въ науку второго
начала. При этомъ мы ограничиваемся главнѣйшими работами, далеко
410
Термодинамика.
не исчерпывая сложнаго и многосторонняго вопроса объ истинномъ зна-
ченіи второго начала.
Считая теплоту за неразрушимый агентъ и изучая условія, при ко-
торыхъ запасъ теплоты можетъ дать работу (напр. въ паровыхъ двигате-
ляхъ), Сагпоі пришелъ къ заключенію, что теплота можетъ произвести
работу только въ томъ случаѣ, когда она переходитъ отъ болѣе теплаго
тѣла къ болѣе холодному, иначе говоря, когда она падаетъ отъ болѣе вы-
сокой температуры къ болѣе низкой. Аналогія съ условіемъ, при кото-
ромъ вода можетъ давать работу, а именно паденіе отъ болѣе высокаго
уровня къ болѣе низкому, привела его къ представленію о паденіи те-
плоты (сішііе йе Іа сйаіепг), какъ объ источникѣ работы. Теплота С}.
взятая отъ нагрѣвателя (4), и цѣликомъ переходящая къ охладителю
(^) является, какъ полагалъ Сагпоі, при своемъ паденіи источникомъ
работы г. Отношеніе
ѵ = п............................(<М)
составляетъ экономическій коеффиціентъ кругового процесса, во время
котораго тѣло беретъ <2 отъ нагрѣвателя, передаетъ это охладителю и
совершаетъ работу г. При обратномъ процессѣ теплота <2 «поднимается >
съ температурнаго уровня 4 къ уровню і%, на что требуется затрата ра-
боты г внѣшними силами. Исходя изъ очерченныхъ здѣсь представленій,
Сагпоі доказалъ слѣдующую теорему.
Теорема Сагпоі. Экономическій коеффиціентъ кру-
гового обратимаго процесса, происходящаго между од-
нимъ нагрѣвателемъ и однимъ охладителемъ, т.-е. отно-
шеніе работы г къ количеству теплоты, перенесенной
отъ нагрѣвателя къ охладителю, не зависитъ отъ рода,
т.-е. отъ вещества тѣла, совершающаго этотъ процессъ.
Это значитъ, что если тѣла Р и Р' совершаютъ процессъ и перенесен-
ныя количества теплоты <2 для обоихъ тѣлъ одни и тѣ же, то и полу-
ченныя работы г и г' должны быть одинаковыми. Сагпоі. доказалъ
эту теорему на основаніи принципа невозможности регреішіт пюЬіІе,
т.-е. полученія работы безъ измѣненія чего-либо, изъ «ничего». Въ до-
стовѣрности этого принципа не сомнѣвались задолго до возникновенія
3 ченія объ энергіи и ея сохраненіи. Вотъ доказательство теоремы, дан-
ное самимъ Сагпоі. Положимъ, что совершимъ процессъ съ
тѣломъ Р въ прямомъ, съ тѣломъ Р' въ обратномъ направленіи. Резуль-
татъ будетъ такой: тѣла Р и Р' возвратятся къ прежнимъ состояніямъ;
теплота <2 перейдетъ отъ нагрѣвателя къ охладителю и обратно, такъ что
и въ этихъ послѣднихъ никакой перемѣны не произойдетъ. Далѣе въ
первомъ процессѣ получается работа г во второмъ тратится работа г'.
Окончательный результатъ заключается въ полученіи работы г—г' «изъ
ничего», что невозможно. Такимъ же путемъ Сагпоі доказалъ, что не
можетъ быть г < ги что, слѣдовательно, г = г'.
Это доказательство основано на неправильномъ представленіи о са-
Второе начало.
411
момъ круговомъ процессѣ. Мы знаемъ, что теплота, взятая отъ нагрѣвателя,
не переходитъ цѣликомъ къ охладителю, что нѣкоторая ея часть
является источникомъ работы г. Такимъ образомъ правильность самой
теоремы остается сомнительной. Великая заслуга Сагпоі заключается
однако въ указаніи на то. что возможность полученія работы насчетъ
имѣющагося запаса теплоты обусловлена переходомъ теплоты отъ болѣе
нагрѣтаго тѣла къ болѣе холодному. Его работа изложена въ статьѣ
«8пг Іа рнівзапсе шоігісе (Іи іеи >, вышедшей въ 1824 г. Втеченіе чет-
верти столѣтія <>на была почти забыта и только Сіареугоп развилъ
(1834) за это время идеи Сагпоі, сдѣлавъ ихъ болѣе понятными пу-
темъ введенія графическаго метода изображенія процессовъ. Сіаизіиз
и ѴѴ. Тііоиі8оп (Ь о г сі Кеіѵіп) почти одновременно (1850), п з м ѣ -
нивъ идеи СагпоЬ, положили прочное основаніе тому, что нынѣ
называется вторымъ началомъ термодинамики.
Когда возникло новое ученіе о теплотѣ, какъ о формѣ энергіи, и
выяснилось, что теплота тратится на производство работы, явилось
задачей отыскать въ изслѣдованіяхъ Сагпоі то, что дѣйствительно
вѣрно, перевести результаты этихъ изслѣдованій на языкъ новаго ученія.
Сіаивіив нашелъ, что теорема С а г п о I дѣйствительно вѣрна, если
только подъ экономическимъ коеффиціентомъ понимать отношеніе работы
или эквивалентной ей полезно затраченной теплоты д = ко
всей затраченной теплотѣ взятой отъ нагрѣвателя. Но доказательство
этой теоремы не можетъ быть основано на принципѣ невозможности рег-
реішіт тоЫІе; оно должно опираться на другой принципъ, составляю-
щій знаменитый постулатъ С1 а и 8 і и 8’а, на который можно смотрѣть,
какъ на выраженіе второго начала, хотя и съуженное, отнесенное къ
частному случаю. Мы покажемъ, какъ этотъ постулатъ обобщается.
Постулатъ Сіаивіиз’а (1850): Теплота не можетъ «сама
собою» перейти отъ брлѣе холоднаго тѣла къ бо-
лѣе теплому.
Слова сама собою» не выясняютъ, въ чемъ тутъ дѣло. Смыслъ по-
стулата будетъ понятенъ изъ такой его формулировки: единственнымъ
результатомъ какого бы то ни было сочетанія процес-
совъ, происходящихъ въ мертвой или въ живой при-
родѣ, не можетъ быть переходъ тепла отъ болѣе холод-
наго тѣла къ болѣе теплому. Такой переходъ (или, какъ гово-
рятъ, превращеніе) возможенъ, какъ результатъ нѣкоторыхъ процессовъ,
но не иначе, какъ въ сопровожденіи нѣкоторыхъ другихъ превращеній,
наличность которыхъ и является условіемъ его возможности.
Итакъ сущность постулата С1 а и 8 і и 8’а заключается въ томъ, что
переходъ теплоты отъ болѣе холоднаго тѣла къ болѣе теплому, хотя и
вполнѣ осуществимъ, но никогда не происходитъ одинъ: его необхо-
димо сопровождаетъ другой физическій процессъ. Такимъ вторымъ, со-
провождающимъ процессомъ, существованіе котораго опредѣляетъ самую
возможность разсматриваемаго перехода теплоты, можетъ оказаться пере-
412
Термодинамика.
ходъ теплоты отъ болѣе теплаго тѣла къ болѣе холодному, переходъ ра-
боты въ теплоту, диффузія двухъ газовъ (В о 112 ш апп) и т. п.
Постулатъ Сіаизіпз’а можетъ быть значительно обобщенъ слѣду-
ющимъ образомъ. Всѣ мыслимые процессы или, какъ мы ихъ условились
называть, превращенія могутъ быть раздѣлены на двѣ группы. Пре-
вращенія первой группы назовемъ положительными или есте-
ственными, превращенія второй группы — отрицательными
или неестественными.
Къ положительнымъ или естественнымъ превращеніямъ
относятся, напр.:
Переходъ теплоты отъ болѣе теплаго тѣла къ бо-
лѣе холодному.
Переходъ работы въ теплоту.
Взаимная диффузія двухъ газовъ.
Къ отрицательнымъ или неестественнымъ превращені-
ямъ относятся, напр.:
Переходъ теплоты отъ болѣе холоднаго тѣла къ бо-
лѣе теплому.
Переходъ теплоты въ работу.
Раздѣленіе двухъ газовъ, составляющихъ смѣсь.
Впослѣдствіи мы дадимъ болѣе точное опредѣленіе положитель-
ныхъ и отрицательныхъ превращеній.
Обобщенный постулатъ Сіаизіиз’а можетъ быть выра-
женъ въ видѣ слѣдующихъ положеній:
I. Положительныя превращенія могутъ происхо-
дить «сами собою».
П. Отрицательныя превращенія не могутъ происхо-
дить «сами собою», т.-е. никогда не могутъ являться единствен-
нымъ результатомъ какихъ-либо процессовъ.
ІП. Отрицательное превращеніе можетъ совер-
шаться только тогда, когда одновременно съ нимъ со-
вершается положительное превращеніе.
Изъ указанныхъ примѣровъ положительныхъ процессовъ непосред-
ственно видно, что они могутъ происходить «сами собою» и въ обыч-
номъ смыслѣ этого слова, т.-е. въ видѣ отдѣльныхъ, единичныхъ про-
цессовъ. Эго въ дѣйствительности постоянно и наблюдается. Что отри-
цательныя превращенія въ этомъ смыслѣ < сами собой» происходить не
могутъ, это для нѣкоторыхъ изъ нихъ непосредственно ясно. Положе-
ніе П гласитъ, что и комбинированіемъ какихъ-либо процессовъ точно
также невозможно получить отрицательное превращеніе, какъ един-
ственный результатъ всѣхъ произошедшихъ процессовъ. Изъ этого
не слѣдуетъ, что отрицательныя превращенія невозможны. Они могутъ
быть осуществлены, но не иначе, какъ одновременно съ положительнымъ
превращеніемъ. Это положительное превращеніе нельзя уничтожить, не
произведя въ какихъ-либо тѣлахъ системы новыхъ превращеній, такъ
Второе начало.
413
какъ положительное превращеніе уничтожается отрицательнымъ превра-
щеніемъ. а послѣднее необходимо должно сопровождаться новымъ поло-
жительнымъ превращеніемъ.
Легко пояснить высказанныя три положенія на нѣсколькихъ примѣ-
рахъ. При всякомъ ударѣ и при всякомъ треніи мы видимъ, что работа
сама собою переходитъ въ теплоту; теплопроводность и лучеиспусканіе
переносятъ теплоту отъ теплаго тѣла къ холодному. Въ прямомъ про-
цессѣ Карно переходъ теплоты въ работу сопровождается переходомъ те-
плоты отъ нагрѣвателя къ охладителю. Въ обратномъ процессѣ Карно
переходъ теплоты отъ охладителя къ нагрѣвателю сопровождается за-
тратою работы, результатомъ которой является эквивалентное количе-
ство теплоты.
Установивъ свой постулатъ, Сіаизіин доказалъ справедливость те-
оремы Сагпоі, нѣсколько измѣнивъ ея формулировку (см. стр. 410).
Теорема Сагпоі, измѣненная Сіа п зіпз’омъ: эконо-
мическій коеффиціентъ кругового обратимаго про-
цесса, происходящаго между однимъ нагрѣвателемъ и
однимъ охладителемъ, т.-е. отношеніе полезно затра-
ченной теплоты Я = К() всей затраченной те-
плотѣ взятой отъ нагрѣвателя, не зависитъ
отъ рода, т.-е. отъ вещества тѣла, совершающаго
этотъ процессъ.
Доказательство: допустимъ, что тѣла Р и Р' совершаютъ круговой
обратимый процессъ, причемъ количество теплоты полезно затрачен-
ной на производство работы г, для нихъ одинаковое, но перенесенныя
количества С?2 и С/2 различны, и пусть </2 > <32. Совершимъ съ тѣ-
ломъ Р круговой процессъ въ прямомъ, съ тѣломъ Р — въ обратномъ
направленіи. Въ результатѣ имѣемъ: 1) переходъ С?2 отъ нагрѣвателя
къ охладителю и затрата теплоты взятой отъ нагрѣвателя, на произ-
водство работы г; 2) переходъ рх2 отъ охладителя къ нагрѣвателю и
затрата работы г, переходящей въ теплоту, которая отдается нагрѣва-
телю. Окончательно тѣла Р и Р ’ возвратились въ начальныя состоянія,
работа г совершена тѣломъ и такая же работа совершена внѣшними си-
лами надъ тѣломъ; кромѣ того теплота С/2 — <32 перешла отъ болѣе холод-
наго тѣла къ болѣе теплому. Этотъ переходъ есть единственный ре-
зультатъ совокупности двухъ процессовъ, а слѣд. онъ невозможенъ; до-
пущеніе С?'2 >> <32 невозможно. Такимъ же образомъ докажемъ, что СГ2
не ф2. Итакъ <3'2 = ; отсюда слѣдуетъ, что + Я и
— <32 -р Я равны между собою; наконецъ и экономическіе коеффи-
ціенты я : С?! и я : Ф'і одинаковы, что и требовалось доказать. Ту же тео-
рему можно доказать, полагая, что но С22 не равно <32, а
слѣд. я и Я и работы г и г' неравны между собою. Доказательство бу-
детъ основано на невозможности полученія работы изъ теплоты, какъ
единственнаго результата совокупности двухъ процессовъ.
Прилагая теорему къ циклу Карно, ѵіы видимъ, что значе-
414
Термодинамика.
ніе экономическаго коеффиціента (46) стр. 408, выведенное для случая
идеальнаго газа, т.-е.
01 = 71 - т2
(21
(46,г)
представляетъ экономическій коеффиціентъ цикла Карно
для всякаго тѣла, которое этотъ циклъ совершаетъ.
Докажемъ, что экономическій коеффиціентъ ц цикла
Карно имѣемъ наибольшее возможное значеніе, т.-е. что
экономическій коеффиціентъ любого даннаго обратимаго или необра-
тимаго процесса, совершаемаго между тѣмъ же нагрѣвателемъ и тѣмъ же
охладителемъ, какъ и циклъ Карно, не можетъ быть больше і/. Поло-
жимъ, что въ обоихъ циклахъ <22 переносится отъ нагрѣвателя къ охла-
дителю, но что полезно затраченныя количества теплоты суть д въ циклѣ
Карно и д' > д въ данномъ циклѣ. Совершая данный циклъ въ прямомъ,
а циклъ Карно въ обратномъ направленіи, мы въ результатѣ получимъ,
какъ единственный результатъ, превращеніе теплоты д' — д въ работу,
что невозможно. Отсюда слѣдуетъ, что д : С?2 не можетъ быть больше,
чѣмъ д : <22, а отсюда, что т/ = Я •’ (С?2 "Ь не больше, чѣмъ г/ =
= Я : (С?2 + ЯУ
Также и для вполнѣ произвольнаго кругового процесса, при которомъ
Ту и Г2 суть крайнія температуры, можно показать, что V- При
этомъ число нагрѣвателей и охладителей можетъ быть произвольно велико,
для обратимаго процесса — безконечно велико. Не останавливаемся на
примѣрахъ, даваемыхъ различными авторами. Ѵаіепііпег показалъ,
какимъ условіямъ долженъ удовлетворять обратимый круговой процессъ,
чтобы т/ получило максимальное значеніе у.
Мы видѣли, что циклъ Карно даетъ между 100° и 0° величину
= 0,268 . .., т.-е. менѣе 27 % теплоты, взятой отъ нагрѣвателя, затра-
чивается полезно. Круговой процессъ, которому подвергается вода въ
паровыхъ машинахъ, весьма далекъ отъ идеальнаго цикла Карно. Онъ
сопровождается огромными побочными потерями тепла, а потому неуди-
вительно, что для него у составляетъ еще значительно меньшую дробь.
Отсюда ясно, что непосредственное полученіе работы насчетъ теплоты,
играющее столь большую роль въ современной техникѣ, представляется
не только практически, но и теоретически крайне неэкономичнымъ.
Мы видѣли, что отрицательное превращеніе возможно только въ со-
провожденіи положительнаго, о которомъ мы говоримъ, что оно компен-
сируетъ отрицательное превращеніе. Отрицательное превращеніе и
компенсирующее его положительное мы будемъ называть эквивалент-
ными другъ другу превращеніями.
Циклъ Карно указываетъ намъ на условіе эквивалентности
положительнаго и отрицательнаго превращеній. Понятіе объ эквивалент-
ности двухъ явленій неразрывно связано съ понятіемъ объ эквивалент-
ныхъ величинахъ, опредѣляемыхъ каждымъ изъ двухъ явленій. Оти во-
Второе начало.
415
личины должны быть равны по величинѣ, но могутъ быть и не равны
по знаку, когда явленія эквивалентны. Эквивалентъ щ превращенія те-
плоты д въ работу или обратно очевидно долженъ быть вида =+ ^/і(7^)
гдѣ Т температура тѣла, отдающаго теплоту или тѣла, которому те-
плота д передается. Знакъ (+) относится къ положительному превраще-
нію работы въ теплоту, знакъ (—) къ отрицательному обратному превра-
щенію. Эквивалентъ н2 перехода теплоты С? отъ теплаго тѣла темпера-
туры 1\ къ болѣе холодному тѣлу температуры Т2 или обратно, долженъ
быть вида #2 = +О/2(7ь 7^), причемъ знакъ (+) относится къ первому,
знакъ (—) ко второму переходу. Превращенія эквивалентны, когда ихъ
эквиваленты по абсолютной величинѣ равны между собою, т.-е. когда
^/і(7) = Р/2(Л, ^2), или когда
-«/і(Л+04(Л, Т2) = О..................(47, а)
Для опредѣленія вида функцій и /2 обратимся къ циклу Карно.
Въ этомъ циклѣ, какъ и во всякомъ обратимомъ круговомъ процессѣ,
сумма эквивалентовъ должна очевидно равняться нулю, ибо, еслибы она
была больше нуля, то мы для обратнаго процесса получили бы сумму,
меньшую нуля, что невозможно. Для кругового процесса Карно мы имѣли
формулу (46)
Фі— _ Л — і_^2_____і____.
Л~\ гг< ИЛИ Г 1 гг< ,
Чі Лі 4і
сокративъ на единицу, получаемъ легко
— 4-^ = 0......................(47,6)
11 7 2
Но = д + С?2, поэтому имѣемъ
— ~ =°.................(47’с)
Въ процессѣ Карно теплота д источника температуры 7) перехо-
дитъ въ работу, и теплота <22 переходитъ отъ І\ къ 72. Поэтому ра-
венство (47, а) принимаетъ для случая процесса Карно такой видъ
7'2) = 0.
Сравнивая это съ (47. с), мы видимъ, что (опускаемъ множитель про-
порціональности)
/і(П = у;/2(Л, = ..........(48)
Итакъ, эквивалентъ перехода теплоты д въ работу,
или обратно, равенъ + ; эквивалентъ перехода теплоты
отъ 7\ къ Т2 или обратно, равенъ + РIІ----------------^ ।, пРичемъ
у * 2 1 /
положительное превращеніе имѣетъ положительный эквивалентъ, а отри-
цательное превращеніе — отрицательный.
416
Термодинамика.
Разсмотримъ произвольный обратимый или необратимый
круговой процессъ, въ которомъ рядъ послѣдовательныхъ нагрѣва-
телей, температуры которыхъ Г/, Г/', Т^“ и т. д., отдаютъ количества
теплоты Оі', О/', Оі'" и т. д. Каждое такое количество распадается на
двѣ части: 0/ = д' -ф-02', 0/'= </" + Оа" и т. д., причемъ д', д" . . .
переходятъ въ работу, 02', 02" . . . передаются охладителямъ, темпера-
туры которыхъ Г2', Г2" и т. д. Ничто не мѣшаетъ сохранить эти обозна-
ченія и въ томъ случаѣ, когда 0/ — д', — д" и т. д. распадаются
каждое на нѣсколько частей, которыя передаются различнымъ охладите-
лямъ. Понятно, что вообще число охладителей можетъ не равняться числу
нагрѣвателей. Постулатъ въ только что формулированномъ видѣ даетъ
д . х-л 11 1
Л
О,
1
ИЛИ
или
2 і+Д-2 о,
71 7 2
20л ХГ1 О2 п
у 'г
1 1 1 2
Измѣнимъ наши обозначенія. Пусть 0 вообще обозначаетъ коли-
чество теплоты, полученное отъ какого бы то ни было источника, ко-
торый можетъ быть нагрѣвателемъ (0 0) или охладителемъ (ф<0), и
пусть Т абсолютная температура источника. Тогда мы должны по-
ложить — 0, = — С, Л = Т, Т2 = Т, и наше неравенство прини-
маетъ видъ
(2
(49)
Когда число нагрѣвателей и охладителей безконечно велико, то
вмѣсто (49) получаемъ
^^-<0....................(49, а)
Для обратимаго процесса долженъ имѣть мѣсто знакъ равенства.
Дѣйствительно, если бы для обратимаго процесса интегралъ былъ меньше
нуля, то онъ для того же процесса, пройденнаго въ обратномъ направле-
ніи, былъ бы ‘больше нуля, чего быть не можетъ. Такимъ образомъ мы
получаемъ з н*а м е ни ты й в ы в о д ъ С1 а и 8 і и з’а:
Во всякомъ обратимомъ круговомъ процессѣ
(60)
т.-е. сумма количествъ теплоты, полученныхъ тѣломъ
отъ источника, дѣленныхъ каждое на абсолютную тем-
пературу источника, или, что то же самое — на абсо-
Второе начало.
417
л ю т н у ю температуру тѣла (см. ниже), равна нулю. Для не-
обратимыхъ круговыхъ процессовъ всегда
< 0......................(50,а)
причемъ Т абсолютная температура источника, но не тѣла.
Для обратимыхъ круговыхъ процессовъ интегралъ несомнѣнно ра-
венъ нулю, но не существуетъ общаго строгаго доказательства того, что
для необратимыхъ круговыхъ процессовъ интегралъ всегда долженъ быть
отрицательнымъ. По этому вопросу существуетъ обширная литература,
изъ которой укажемъ здѣсь только интересную статью Сагѵаііо (1899).
Совершенно строго доказано, что интегралъ (50,а) не можетъ быть больше
нуля. Во многихъ сочиненіяхъ можно найти доказательства того, что
при необратимыхъ процессахъ этотъ интегралъ долженъ быть меньше
нуля; но эти доказательства не представляются убѣдительными. Мы здѣсь
имѣемъ дѣло съ частнымъ случаемъ гораздо болѣе общаго положенія, по
которому во всѣхъ термодинамическихъ формулахъ, въ которыхъ двѣ вели-
чины могутъ быть соединены только или знакомъ равенства или со-
вершенно опредѣленнымъ знакомъ неравенства, и въ которыхъ
при обратимыхъ процессахъ несомнѣнно возможенъ только знакъ равен-
ства, при необратимыхъ процессахъ непремѣнно долженъ быть постав-
ленъ соотвѣтственный знакъ неравенства.
Мы видѣли (стр. 387), что при необратимыхъ процессахъ параметры,
опредѣляющіе состояніе тѣла, становятся неопредѣленными. Если, напр.
температура нагрѣвателя или охладителя отличается на конечную величину
отъ температуры тѣла, совершающаго круговой процессъ, то во время на-
грѣванія или охлажденія этого тѣла его температура не имѣетъ опредѣ-
леннаго значенія. Этимъ подтверждается, что въ формулѣ (50,а) Т не мо-
жетъ быть температурой тѣла, какъ иногда ошибочно утверждаютъ; Т есть
температура источниковъ теплоты, которые мы представляемъ себѣ не-
исчерпаемыми.
Легко показать на примѣрахъ, что для необратимыхъ процессовъ
интегралъ (50,а} меньше, чѣмъ для обратимыхъ.
1. Пусть температура Т нагрѣвателя сдѣлается больше темпе-
ратуры тѣла на конечную величину; въ этомъ случаѣ положительные
элементы интеграла уменьшаются.
2. Пусть температура Т охладителя сдѣлается меньше темпера-
туры тѣла на конечную величину; въ этомъ случаѣ отрицательные эле-
менты интеграла увеличиваются.
3. Пусть внѣшнее давленіе на конечную величину меньше
давленія тѣла, и слѣд. тѣло, расширяясь, совершаетъ меньшую работу,
чѣмъ въ процессѣ обратимомъ, и меньше теплоты извлекаетъ изъ нагрѣ-
вателей для производства работы; въ этомъ случаѣ положительные эле-
менты уменьшаются.
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. ПІ. изд. 3-е.
27
418
Термодинамика.
4. Если внѣшнее давленіе на конечную величину больше
давленія тѣла, и слѣд. внѣшнія силы, сжимая тѣло, совершаютъ большую
работу, чѣмъ въ процессѣ обратимомъ, то эквивалентное количество тепла
выдѣляется въ тѣлѣ и переходитъ къ охладителямъ; въ этомъ случаѣ от-
рицательные элементы увеличиваются.
5. Въ случаѣ тренія или толчка выдѣляется избытокъ тепла
на охладителяхъ, или отъ нагрѣвателей берется меньше тепла; и въ этомъ
случаѣ нашъ интегралъ, понятно, также уменьшается.
Изъ формулы (50) вытекаетъ важное слѣдствіе, относящееся къ об-
ратимымъ процессамъ вообще:
если А иВ два состоянія тѣла, то для всѣхъ обра-
тимыхъ процессовъ, которые переводятъ тѣло изъ
состоянія А въ состояніе В,
в
^ = Соп8І...................(50,&)
А
т.-е. интегралъ имѣетъ одно и то же значеніе, ибо изъ
двухъ такихъ процессовъ можно составить обратимый круговой процессъ,
если однимъ процессомъ идти отъ А къ В, а другимъ отъ В къ А ; а для
кругового процесса интегралъ равенъ нулю. Полученный результатъ можно
еще обобщить. Положимъ, что МЫ (рис. 123) адіабата. Легко ви-
Рис. 123. Рис. 124.
дѣть, что для всѣхъ обратимыхъ процессовъ АВ, АВ', АВ", . . . значе-
ніе интеграла (50,6) также постоянно: вдоль МЫ элементы интеграла нули,
такъ какъ б/(? = 0.
Мы вывели формулу (50), вводя понятіе объ эквивалентахъ различ-
ныхъ превращеній. Однако (въ 1879 г.) Ріапск подвергнулъ критикѣ
ученіе Сіапвіиз’а объ эквивалентахъ и показалъ, что при болѣе стро-
гомъ разсмотрѣніи оно приводитъ къ другимъ выводамъ. Поэтому мы до-
кажемъ формулу (50) еще другимъ путемъ, хотя и не очень отличающимся
Второе начало.
419
3
отъ предыдущаго. Сперва докажемъ слѣдующее: пусть А и В (рис. 124)
два безконечно близкія другъ къ
другу состоянія тѣла, АСВ и АОВ
два обратимые процесса, и сІО"
количества теплоты, поглощаемыя тѣ-
ломъ при этихъ процессахъ; въ та-
комъ случаѣ б/р и б/ф" отличаются
другъ отъ друга на безконечно ма-
лую величину второго порядка. Для
доказательства примемъ ѵ и р за не-
зависимыя перемѣнныя. АСВОА пред-
ставляетъ обратимый круговой про-
цессъ, для котораго б/ф' = Ао,
см. (37,(1) стр. 401. Но о, какъ пло-
щадь, есть величина безконечно малая
должна быть и разность (ІС? — (10".
второго порядка, а слѣд. таковою
Изъ равенства (46,г) мы уже
вывели равенство (47,&). которое те-
перь напишемъ въ видѣ
Оі 0‘2 0
Л Г2
Если измѣнить обозначеніе и черезъ 02 обозначить теп-
лоту, полученную отъ охладителя (конечно отрицательную), то мы
получимъ
+ =0 ........................(50.С)
7 1 '2
Положимъ, что тѣло совершаетъ обратимый круговой процессъ АОНВА.
Проведемъ рядъ безконечно близкихъ адіабатъ ОВ, СО, ЕК и т. д. (рис. 125).
Онѣ раздѣляютъ данный процессъ на безконечное множество круговыхъ
процессовъ, ОСОБО, СЕКОС и т. д., см. стр. 406. Проведемъ изъ то-
чекъ О, С, У . . . , К, О, В . . . изотермы ОЕ, СЬ, КМ, ОЕ и т. д., и
разсмотримъ одинъ изъ процессовъ, напр., ОСОБО. Вдоль ОС поглоща-
ется теплота (ІОі отъ нагрѣвателя 7\; вдоль ОВ поглощается б/02 отъ
охладителя. На основаніи только что доказаннаго мы можемъ предполо-
жить, что б/0х было поглощено при переходѣ ОЕ, а сІОъ при пере-
ходѣ ОЕ,мбо вдоль СЕ и В/7имѣемъ б/0 = 0. Отсюда ясно, что процессъ
ОСОБО можно замѣнить безконечно малымъ процессомъ Карно ОЕОЕО.
и что вообще всякій обратимый круговой процессъ можно замѣнить без-
конечнымъ множествомъ безконечно малыхъ процессовъ Карно. Фор-
мула (50,с) даетъ
_п
Л “г т.2
Такія же равенства напишемъ и для остальныхъ процессовъ Карно
СЬКМС и т. д.; сложивъ всѣ эти равенства, получаемъ:
27*
420
Термодинамика.
2^ +^Ц
\ 1 * 2 I
Этимъ суммированіемъ мы исчерпываемъ всѣ количества сІС}. полу-
ченныя тѣломъ при круговомъ процессѣ, такъ что въ предѣлѣ мы вмѣсто
послѣдней суммы получаемъ
т ~ 0
т.-е. формулу (50).
§ 12. Второе начало термодинамики; работы ТЬотзоп’а, Воііг-
піапп’а и др.; регреіішт тоЬНе второго рода. Мы подробно остано-
вились на работахъ Сагпоі и Сіапвіпз’а, и лишь вкратцѣ ука-
жемъ на основныя черты работъ другихъ ученыхъ. \Ѵ. Т Ь о т 8 о п
(Ъ о г с! Кеіѵіп) положилъ въ основаніе своихъ разсужденій слѣдующій
постулатъ.
Постулатъ \Ѵ. ТЬошзоп’а (1851): невозможно получать при
помощи неодушевленной матеріи работу отъ какой либо
части матеріи, охлаждая ее ниже температуры наи-
болѣе холоднаго изъ окружающихъ тѣлъ. Иначе: теплота
наиболѣе холоднаго изъ данной системы тѣлъ не можетъ служить источ-
никомъ работы. Самъ ТЬош 8 о п призналъ, что этотъ постулатъ
лишь по формѣ отличается отъ постулата Сіапвіпв’а.
Постулату Т Ь о ш 8 о п’а можно дать иную, весьма интересную
формулировку. На стр. 360 мы назвали регреіпшп тоЬіІе перваго рода
машину, непрерывно дающую работу безъ затраты энергіи, и указали,
что первое начало, между прочимъ, можетъ быть формулируемо, какъ на-
чало невозможности регреішіш тоЫІе перваго рода.
Представимъ себѣ машину, которая непрерывно давала бы работу,
затрачивая энергію какого либо весьма обширнаго, практически неисчер-
паемаго источника тепла, температура котораго, однако, не выше тем-
пературы различныхъ тѣлъ, играющихъ роль при дѣйствіи машины. Если
бы такая машина была возможна, то мы могли бы пользоваться теплотою
океановъ, атмосферы или земной коры, какъ даровыхъ, неисчерпаемыхъ
источниковъ энергіи и эта машина принесла бы человѣчеству такую же
пользу, какъ и регреішіт тоЫІе перваго рода. Называя такую машину
регреіипт тоЫІе второго рода, мы можемъ формулировать
постулатъ АѴ. ТЬот8 оп’а такимъ образомъ:
Регреіипт тоЫІе второго рода невозможно.
Такимъ образомъ первое и второе начало термодина-
мики говорятъ, что невозможны регреіпиш тоЫІе ни
перваго, ни второго рода.
Нѣсколько позже (1852) \Ѵ. Тііотвоп далъ новую, также весьма
остроумную формулировку второго начала. Переходъ тепла отъ теплаго
тѣла къ холодному можно разсматривать, какъ стремленіе къ равномѣр-
ному распредѣленію теплоты, къ ея разсѣянію. Переходъ работы въ
Второе начало.
421
теплоту, т.-е. другихъ формъ энергіи, въ особенности энергіи видимаго
движенія тѣлъ въ энергію тепловую, которая затѣмъ разсѣивается, также
представляется какъ бы первымъ шагомъ къ разсѣянію имѣющагося за-
паса энергіи. Мы видѣли, что эти превращенія происходятъ въ природѣ
«сами собою», между тѣмъ какъ обратныя превращенія, которыя сопро-
вождаются сгущеніемъ энергіи, должны сопровождаться однимъ изъ пре-
вращеній, приводящихъ къ ея разсѣянію. Отсюда АѴ. Тйотноп вы-
велъ знаменитое положеніе, извѣстное подъ названіемъ постулата о
разсѣяніи энергіи (д.І88Іраііоп оі епег^у): энергія, имѣюща-
яся въ мірѣ, стремится къ разсѣянію т.-е. къ переходу
въ равномѣрно распредѣленную энергію тепловую.
Цѣнность энергіи заключается въ ея способности дать механи-
ческую работу; мы видѣли, однако, что неравномѣрное распредѣленіе те-
плоты, т.-е. наличность нагрѣвателя и охладителя, есть условіе возможности
полученія изъ нея работы. Стремленіе къ разсѣянію уменьшаетъ запасы
цѣнной энергіи. На этомъ основаніи Ріаипсііег высказалъ мысль о
стремленіи матеріи, какъ носителя энергіи, которая внѣ матеріи
не существуетъ, къ обезцѣненію (Епіхѵегкші^); энергія же стремится
къ вырожденію» (Епіагіші^).
На стр. 392—394 мы уже познакомились съ идеями ВоИгтапп’а по
вопросу объ обратимости физическихъ процессовъ. Далѣе мы указали на
стр. 2 и 3, что тепловая энергія есть энергія равномѣрно безпорядочнаго
движенія, и мы видѣли, что это движеніе есть наиболѣе вѣроятное.
Оно должно устанавливаться само собою и къ переходу въ это движеніе
должны стремиться всѣ другія, болѣе упорядоченныя и потому менѣе вѣ-
роятныя движенія. ВоН2шапп указываетъ, что всѣ положительныя
превращенія представляютъ переходы отъ менѣе вѣроятнаго къ болѣе вѣ-
роятному состоянію, и что поэтому второе начало должно быть
понимаемо, какъ стремленіе вселенной переходить отъ
менѣе вѣроятныхъ къ болѣе вѣроятнымъ состояніямъ.
Критическимъ разборомъ основъ второго начала занимались въ осо-
бенности Ріапск и С. 1\ е и т а п п; далѣе АѴаЫ, Ье СЬаіе-
Ііег. Рагкег, Реггіп, Масй. Вгуап, АѴгопвкі, Меуег-
Ь о И е г и др.
Весьма большой интересъ представляетъ вопросъ о границахъ обла-
сти дѣйствія второго начала. Вопросъ этотъ можетъ быть разсматри-
ваемъ съ различныхъ сторонъ. Такъ какъ, согласно вышесказанному,
второе начало должно быть разсматриваемо, какъ слѣдствіе, полученное
на основаніи теоріи вѣроятностей, то мы должны сказать, что подчиненіе
этому началу всѣхъ явленій природы является въ чрезвычайно высокой
степени вѣроятнымъ, но вмѣстѣ съ тѣмъ не являются абсолютно невоз-
можными и случаи не подчиненія этому началу. Примемъ, что вселенная,
въ которой совершаются процессы, аналогичные извѣстнымъ намъ про-
цессамъ, такъ велика, что весь доступный нашему наблюденію «астроно-
мическій > міръ относится къ ней, какъ атомъ относится къ тѣлу, имѣ-
422
Термодинамика.
ющему размѣры земли. Въ такомъ случаѣ возможно, что въ каждый
моментъ въ этой вселенной заключаются такія области, для которыхъ
случайно второй принципъ не имѣетъ силы. На иной точкѣ зрѣнія
стоитъ Аггііепіиз въ своемъ трудѣ Оаз Ѵ\егсІеп сіег ААеІІеп» (есть
русскій переводъ). Онъ развиваетъ космогенетическую теорію, приводя-
щую его къ заключенію, что въ поверхностныхъ слояхъ весьма обширной
космической туманности, имѣющей чрезвычайно малую плотность, господ-
ствуютъ такія условія, при которыхъ возможенъ переходъ тепла отъ бо-
лѣе холоднаго къ болѣе нагрѣтому тѣлу.
Въ послѣднее время неоднократно дѣлались попытки найти такіе
процессы, для которыхъ второе начало оказывается невѣрнымъ; болѣе
тщательный разборъ этихъ процессовъ показываетъ, что отступленія во
всѣхъ случаяхъ лишь кажущіяся. Сюда относится парадоксъ АѴ. АѴіеп’а
(1894), который показалъ, что при прохожденіи свѣта чрезъ двѣ Нико-
левы призмы (т. II), между которыми помѣщено тѣло, въ которомъ про-
исходитъ магнитное вращеніе плоскости поляризаціи (т. IV), второе на-
чало оказывается не имѣющимъ силы. Однако Вгіііоиіп (1898) и
Ріапск (1900) показали, что противорѣчіе со вторымъ началомъ исче-
заетъ, если точно изслѣдовать всѣ обстоятельства, въ особенности (Ріап с к)
отраженія свѣта въ призмахъ.
Другой примѣръ представляетъ собою придуманная СогЬіпо (1908)
комбинація зеркалъ и тѣлъ, испускающихъ свѣтъ въ магнитномъ полѣ
(явленіе Хеетапп’а, см. т. IV). Ьаие показалъ, что и въ этомъ слу-
чаѣ неприложимость второго начала является лишь кажущейся.
Совершенно иной характеръ имѣютъ многочисленныя попытки дока-
зательства противорѣчія между вторымъ началомъ и явленіемъ В г о ѵт п'ов-
скаго движенія. Англійскій ботаникъ Вгоаѵп въ 1827 году замѣтилъ,
что весьма малыя тѣльца, взвѣшенныя въ жидкости, находятся въ состо-
яніи непрерывнаго, неправильнаго движенія, имѣющаго характеръ какъ
бы дрожанія. Величина этихъ тѣлецъ не должна превосходить 4ц =
= 0,004 тт ; если она близка къ 0,01/ъ то наблюдается непрерывное
зигзагообразное движеніе, подобное тому, которое мы приписываемъ га-
зовымъ молекуламъ. Въ настоящее время общепринято, что эти видимыя
движенія вызываются ударами молекулъ жидкости и что, такимъ обра-
зомъ, явленіе Вголѵ п’овскаго движенія является подтвержденіемъ правиль-
ности современныхъ молекулярно-кинетическихъ гипотезъ. Мы не мо-
жемъ входить здѣсь въ подробности относительно многочисленныхъ ра-
ботъ, которыя, въ особенности за послѣдніе годы, были посвящены
В г о дѵ п’овскому движенію. Большинство этихъ работъ находится въ
связи съ изслѣдованіями коллоидовъ, при которыхъ большую роль сыгралъ
ультрамикроскопъ (т. II). Особенно важными являются теоретическія из-
слѣдованія Еіпзіеіп’а (1905), бтоіисйолѵбкі (1906) и Ьап^е-
ѵіп’а (1908), новѣйшія работы 8 ѵ е <1Ъ е г§’а, Ейгепііаіі’а, М о 1 і 8 сІѴа,
Хві^топйу, Аайп’а, Восіав/елѵзкі, ЗесЫі^’а и французскихъ
ученыхъ — Ргесіеу, Непгі, Впсіапх, ОаЬгоАѵеку, Ьап^е-
Абсолютная шкала температуръ.
423
ѵіп, Со(Iоп и Моиіоп, сіе Вго^ііе, СЬаидеваі^пев и, въ
особенности. Реггіп’а (1908, 1909).
бону (1888) первый обратилъ вниманіе на то обстоятельство, что
при В г о п’овскихъ движеніяхъ происходитъ переходъ теплоты (молеку-
лярныхъ движеній; въ работу безъ соотвѣтствующей компенсаціи. Тео-
ретически можно думать объ использованіи В г о лѵ п’овскаго движенія
для приведенія имъ въ движеніе особаго механизма и о добываніи дви-
женія такимъ путемъ. Подобныя идеи были высказаны также 8 ш о -
Іисііохѵзкі (1906) и Озілѵаі (і’омъ (1907). БѵесІЬег^ (1907) далъ
схематическое описаніе двухъ аппаратовъ, которые позволяютъ при по-
мощи В г о дѵ п’овскаго движенія осуществить непрерывный переходъ
теплоты отъ болѣе холоднаго тѣла къ болѣе нагрѣтому безъ соотвѣт-
ственной компенсаціи. Оказывается, что для чрезвычайно малыхъ об-
ластей возможны мѣстныя отклоненія отъ второго начала, но величина
этихъ отклоненій во всѣхъ случаяхъ всегда ничтожно мала. Неітйоііг
уже высказалъ мысль о томъ, что при извѣстныхъ молекулярныхъ про-
цессахъ въ ж и в о й клѣткѣ второе начало, можетъ быть, оказывается не
приложимымъ.
Мы будемъ говорить ниже (гл. ХШ) объ явленіяхъ опалесцен-
ціи, наблюдающихся въ жидкостяхъ вблизи критической темпера-
туры. йтоіисііолѵзѣі (1908) показалъ, что эти явленія можно объ-
яснить многочисленными малыми измѣненіями плотности, возникающими
внутри жидкости. К а ш пі е г 1 і п 11 - О п п е 8 (1904) изслѣдовалъ спектро-
скопически свѣтъ, испускаемый такими жидкостями при освѣщеніи, и пока-
залъ, что результаты, полученные имъ, согласуются съ теоріей 8шо-
1 и с 11 о дѵ 8 к і.
§ 13. Абсолютная шкала температуръ, предложенная XV. ТЬот-
зоп’омъ (Ьогй Кеіѵіп). Мы неоднократно указывали на абсолютную шкалу
температуръ XV. Тііотзоп’а и на то. что шкала водороднаго термо-
метра, въ которомъ измѣряется давленіе, а не объемъ газа, незамѣтно
мало отличается отъ шкалы Тііопібоп’а (см. стр. 7 и 15). Теперь
мы имѣемъ возможность познакомиться съ этою послѣднею. Она была
предложена въ 1848 г.: ея особенность и огромное преимущество заключа-
ются въ томъ, что она не зависитъ отъ физическихъ свойствъ какого-либо
опредѣленнаго вещества.
Возьмемъ какое-либо тѣло и заставимъ его изотермически измѣняться
при различныхъ температурахъ, которыя мы представляемъ себѣ опредѣ-
ленными, напр., какъ точки плавленія или кипѣнія различныхъ веществъ,
или о неизмѣнности которыхъ мы судимъ по постоянству показаній
какого-либо термометра, показанія и шкала котораго, однако, никакого
значенія не имѣютъ, такъ какъ у насъ раціональной шкалы еще нѣтъ, а
мы только намѣреваемся ее построить. Слѣдя за измѣненіями состоянія
тѣла, мы можемъ начертить рядъ изотермъ ДД, ВВ, СС и т. д. (рис. 126).
На изотермѣ ДД возьмемъ двѣ точки а и Л, и черезъ нихъ проведемъ
адіабаты ЛШ п точки которыхъ также опредѣляются изъ н а б л ю -
424
Термодинамика.
д е н і й надъ измѣненіями состоянія тѣла. Наконецъ опредѣлимъ ко-
личество С?! тепла, поглощаемаго тѣломъ при изотермическомъ измѣненіи аЬ.
Заставимъ тѣло со-
вершать круговые процес-
сы Карно аЬсіса, аЬ/еа
и т. д., и пусть ф2> (к и
т. д. количества тепла, пе-
реданныя охладителямъ въ
этихъ процессахъ. Каково
бы ни было взятое тѣло,
эти количества будутъ всег-
да одни и тѣ же, если
дано и изотермы однѣ и
тѣ же, т.-е. соотвѣтству-
ютъ однѣмъ и тѣмъ же
температурамъ, опредѣлен-
нымъ. какъ сказано выше.
Эти температуры обозна^
чимъ а л г е б р а и ч е с к и -
ми знаками 7], 7В и
т. д., и дадимъ одной изъ
нихъ, напр., температурѣ 7\
опредѣленное, отъ нашего выбора зависящее численное значеніе, н е
равное нулю и не отрицательное. Мы можемъ напр. изотермѣ,
соотвѣтствующей температурѣ тающаго льда, приписать численное зна-
ченіе 7^ = 273, или какое нибудь другое. Въ такомъ случаѣ численныя
значенія другихъ температуръ по шкалѣ Т Ь о ш 8 о п’а получаются изч>
пропорцій:
Л=<2і 7і.= ^
7"о (2-2 ^3 Оі
(51)
Для произвольныхъ двухъ промежуточныхъ температуръ Тп п Тт мы
очевидно имѣемъ т
1 п _
Фт
гдѣ С)п и (^т количества тепла, взятыя отъ нагрѣвателя и переданныя
охладителю въ циклѣ Ка рно, совершаемомъ между температурами Тп и Тт
Принимая источникъ 7\ за охладитель, мы получимъ такимъ же
образомъ численныя значенія по шкалѣ Т11 о т 8 о п’а для температуръ,
лежащихъ выше 7\.
Формула (46) стр. 408 показываетъ, что шкала газоваго тер-
мометра, содержащаго идеальный газъ, тождественна
съ абсолютною шкалою Тйотвоп’а. Свойства водорода, нагрѣ-
ваемаго при постоянномъ объемѣ, весьма мало отличаются отъ
свойствъ идеальнаго газа; теперь понятно, почему эта шкала принята
какъ основная.
Абсолютная
шкала температуръ.
425
Укажемъ на замѣчательное свойство абсолютной шкалы Т Ь о т -
8оп’а. Положимъ, что 7\, Г2, 73, . . . суть равн остоящія температуры,
напр. цѣлые градусы по этой шкалѣ, такъ что 1\ Т2 = Т2—Т3=Т3
— Т4= и т. д. Равенства (51) даютъ
_ 01-02.
К ~ ’
Га-73 _02-0з
т2 -
Д.
т
Раздѣливъ одну пропорцію на другую, получаемъ, такъ какъ 7\: Т> =
— (32 = (32 <з3 = <23 — = и т. д.,
или
Я1 = Я* = #з = и т. д.,
гдѣ, какъ прежде, дд, #2, #3 . .. количества тепла, превращенныя въ ра-
боту въ отдѣльныхъ процессахъ Карно, совершенныхъ между тѣми-же
двумя адіабатами МЫ и /?5 (рис. 126) и «равностоящими > (не геометри-
чески, конечно, а въ отношеніи температуръ) изотермами. Во всѣхъ
циклахъ Карно, совершаемыхъ между двумя данными
адіабатами и равностоящими изотермами, превраща-
ются въ работу одинаковыя количества тёпла. Если за
независимыя перемѣнныя принять ѵ и р (рис. 126), и если площади че-
тырехугольниковъ аЬсІс, ссі/е и т. д. обозначить черезъ од, . . . . , то
д2 — Аб2..., и т. д. (стр. 101). Равенство = д2 — Яз = • • • даетъ
од —- а2 —— о3 —....
т.-е. площади аЬсіс, ссі/е и т. д. равны между собою. Этотъ результатъ
можно обобщить. Отыщемъ на изотермѣ 1\ такую точку У, чтобы коли-
чество теплоты поглощенное тѣломъ на пути ЫУ, равнялось фр Че-
резъ Ь' проведемъ адіабату /7Ѵ, которая пересѣчетъ равноотстоящія изо-
термы въ точкахъ сі', /' и т. д. Если <2/, О/ . . . количества теплоты,
поглощенныя въ процессахъ сісГ, //' . . ., то изъ равенства С?і — оче-
видно слѣдуетъ ^2 = и т. д., см. (51). Адіабаты МЫ,
ЫѴ и т. д. мы назовемъ равностоящими.
Ясно, что а/ = б2 = . . . = ОД = Щ = . . . .
Если за независимыя перемѣнныя принять ѵ и р, то
площади четырехугольниковъ, образуемыхъ сѣтью рав-
ноотстоящихъ адіабатъ и изотермъ, равны между
собою.
Весьма любопытно, что если взять различныя тѣла, и сдѣлать
для нихъ <2 (рис. 126) одинаковыми, то ф3, и т. д., расположенныя на
произвольныхъ другихъ изотермахъ, также будутъ одинаковы для
всѣхъ тѣлъ. Нетрудно формулировать соотвѣтствующую теорему.
§ 14. Формулы, основанныя на второмъ началѣ. Малое количе-
ство теплоты поглощаемое тѣломъ, когда независимыя перемѣнныя
х и у получаютъ приращенія сіх и сіу. было нами выражено въ видѣ
(38,а) стр. 401, — ХЛх + Усіу. . . ^52^
426
Термодинамика.
гдѣ Л и У функціи отъ х и у Когда у = і, см. (38,6), мы пишемъ
б/р = Хі(іх-\-сх(іІ ... . . (52,а)
гдѣ сх одна изъ теплоемкостей тѣла. Въ частномъ случаѣ, когда х и у
двѣ изъ величинъ ѵ, р, і, мы ввели обозначенія 6, /, а, е, сѵ, и ср, ^м.
(40, а, 6, с) стр. Ю2. Связи между этими функціями выражены форму-
лами (41, а, 6, с, сі, /) стр. 403.
Первое начало дало намъ общую формулу (42) стр. 404. и частныя
формулы (42, а, Ь, с) стр. 405. Второе начало приводитъ къ новымъ вы-
раженіямъ для тои-же разности «накрестъ» взятыхъ производныхъ. Наи-
большій интересъ представляютъ, какъ мы увидимъ, соотношенія, выте-
кающія изъ комбинаціи формулъ, основанныхъ на первомъ и на второмъ
началѣ. Мы видѣли, что б/ф не есть полный дифференціалъ функціи пе-
ремѣнныхъ х и у, ибо накрестъ взятыя производныя не равны между
собою, сК) зависитъ отъ пути и для замкнутаго пути не равенъ нулю.
Формулы (50) и (50,6) показываютъ, что для обратимыхь процессовъ величина
5= у ......... (52,/>)
не зависитъ отъ пути и для замкнутаго пути равна нулю. Отсюда слѣ-
дуетъ, что для всякаго безконечно малаго обратимаго про-
цесса подинтегральная величина равна полному диф-
ференціалу нѣкоторой функціи величинъ х и у, которую
обозначимъ черезъ 5.
Впослѣдствіи мы ближе познакомимся съ этою функціею, которая
называется энтропіей. Мы имѣемъ
а^ = с18......................(53)
Т
л? л ѵ,
т. е. р есть полный дифференціалъ, и въ этомъ заключается
простѣйшая математическая формулировка второго начала. Изъ (53)
вытекаетъ формула для разности накрестъ взятыхъ производныхъ отъ ве-
личинъ X и У. Подставляя (52), мы видимъ, что
б/(? X . У
— 3= (Іх - р(1у
есть полный дифференціалъ, а потому для этой величины накрестъ взя-
тыя производныя должны быть равны:
Сокращаемъ знаменатель, переносимъ производныя отъ Хи К въ
одну сторону и дѣлимъ на Т. Тогда получается
Второе начало. Формулы.
427
дх_дУ_ 1 ( ХдТ- ѴдТ\
ду дх 7у ду дх у
Комбинируя эту формулу съ (42), получаемъ
„дТ Х7дТ лгггл , ч
X < —У——АТО (х, у)
ду дх
ч дѵ др дѵ др
Л(х, у) = ^— < —ѵ -г“
ѵ у дх Оу Оу дх
(54^
.................(55)
Это одна изъ самыхъ общихъ формулъ термодина-
мики, вытекающая изъ комбинаціи обоихъ ея началъ.
Разсмотримъ важный частный случай, когда одна изъ независимыхъ
перемѣнныхъ есть температура, т.-е. когда у = /, X — Хѣ У = сх
см. (52,я). Въ этомъ случаѣ ^—1,^ = 0, и (54) и (55) даютъ
ду дх
дХі дс^_Х(
ді дх Т
і —
дѵ др
ді дх
(56,а)
(56.0
или сокращенно
Хі=АТО{х. і)
(56,с)
(56,0 показываетъ, что если за одну изъ независимыхъ перемѣнныхъ при-
нята температура, то въ выраженіи для сі(^> коеффиціентъ при диффе-
ренціалѣ другой перемѣнной х вполнѣ опредѣляется. Первое начало
даетъ формулу, см. (42),
дХ{
ді
дсх
дх
(56,</)
— АО (х, 6.
Вставимъ (56,0 въ (56.</); получается
{дсЛ __ лтдО_^
\ дх ді
(56,г)
Всегда можетъ быть получена
производная
по х отъ
теплоемкости при постоянномъ х.
Перейдемъ къ тремъ частнымъ случаямъ, когда х и у суть двѣ изъ
трехъ величинъ ѵ, р, і. Къ этимъ случаямъ относятся формулы (40, а,
Ь. с) стр. 402, (41, а, Ь, с, д, стр. 403, и (42, &, Ь, с) стр. 405.
1. х=ѵ, у—р; Х=к, У=1; дО = к(іѵ + Ісір; О (ѵ, /?)=1,
см. стр. 405. Формула (54) даетъ
дк ді 1 / , ді . ді\
др дѵ Т\ др дѵ].....................
Изъ (42,а) или (55) получается
р ^—1ді =АТ
др дѵ
(57,^)
(57,М
428
Термодинамика.
Это весьма замѣчательная связь между функціями к и I.
2. х = ѵ, у = і; Х=а, Ѵ=сѵ\ (К^ = асіѵ-{-сѵ(1і\ О (ѵ, і}=$Ѵ
Одна изъ перемѣнныхъ — температура; (56,а} даетъ
да
ді
дсѵ а
дѵ Т
(58,а)
Комбинація этой формулы
съ (42,/»), стр. 405,
_ дс*> _ л дР
ді дѵ ді
или прямо (56,с) даетъ:
да
а = АТі>Р
ді
(58, с)
. . (58,Ь)
Эта замѣчательная формула извѣстна подъ названіемъ формулы
Т Ь о го 8 о п’а.
др
Вводя прежнее обозначеніе — = //?0, ц пользуясь формулою (41,б/),
ді
въ которой а и /9 коеффиціенты теплового расширенія и объемнаго сжатія,
мы можемъ (58,с) написать въ видѣ
а = АТ 0
,3ѵ
Вставляя (58,с) въ (58,6) или пользуясь прямо формулою (56,е), на-
ходимъ
(58,4/)
(58.4?)
Эта интересная формула связываетъ зависимость теплоемкости при
постоянномъ объемѣ отъ объема съ зависимостью давленія отъ темпе-
ратуры.
Если р есть линейная функція температуры, т.-е.
вида р = /?0(1 + или, иначе, если термическій коеф-
фиціентъ давленія ар не зависитъ отъ температуры, то
теплоемкость сѵ не зависитъ отъ объема.
дѵ
3. ѵ=р, у — і; А = е, V —ср; (10 = едр -ф срсІі; В(р, /) — — .
И здѣсь одна изъ перемѣнныхъ температура: (56,4г; даетъ
де дср _ е
ді др Т
Комбинируя эту формулу съ (42,с), стр. 105,
де дср дѵ
ді др ді
. . (59, а)
. . (59,/»)
или прямо на основаніи (56,с), получаемъ
Второе начало. Формулы.
429
е= АТ .......................(59.0
ді
дѵ
Эта формула аналогична формулѣ (58,с). Вводя — = аг/0, получа-
емъ еще проще
АТаѵ(}..................(59 А)
Вставляя (59,с*) въ (59,6), или пользуясь формулою (56,е), находимъ
(дСр ) = — А Т ...............(59,е)
\др )і дР Ѵ ’ 7
аналогично (58,^). Эта формула показываетъ, что если объемъ есть
линейная функція температуры, т.-е. если коеффиціентъ
расширенія не зависитъ отъ температуры,то теплоем-
кость Ср не зависитъ отъ давленія. (59,^) можно написать
еще въ такомъ видѣ:
(дсп \ да
р =- АТѵ0^ ....... (59,/)
ор )і 0 ді ѵ 7
Формулы (58,с) и (59,с) даютъ возможность написать новыя выра-
женія для д(3 вмѣсто (КЗ — адѵ Д- сѵді и б/ф — едр -ф- срсІі. Вставляя а и е,
получаемъ весьма важныя формулы
(1$ — сѵ(1і + АТ^-Лѵ
ді
д(3 = сраі — АТдѵ др
Если изъ (57,6) взять к или / и вставить
Шр) то легко получаются формулы
д(2 = (іаі+ АТдѵ)др
ді
ас?=(к(іі ±Атар)дѵ
(60,а)
въ выраженіе = ксіѵ +
(60,0
Выраженія для к и I были даны въ (41,с) и (41/), стр. 403. Для
(КЗ получается интересное выраженіе, если вставить для би/ значенія (41/):
= Ср Ц Лѵ + сѵ ~ др . ... . (60,с)
§ 15. Энергія тѣла. Формула КігсЫюГТ’а. Выводы предыдущаго
параграфа даютъ возможность составить формулу для энергіи 1} тѣла.
За независимыя перемѣнныя примемъ какую-либо величину х и темпе-
ратуру і. Въ этомъ случаѣ имѣемъ:
(КЗ = Х^х -ь схді
Хі = АТО(х, і)
(61, а)
430
Термодинамика.
см. (56,с); О(х, 0 дано въ (56,6). Пусть 67(х0, /0) = требуется найти
1]=1}(х, і). Значенія функцій сх ѵ, р при х = х0 обозначимъ черезъ
с0, ѵ0 и р0; это суть функціи отъ і, такъ что с0 = сх(х0, і), ѵ0 —
= ѵ(х0, і), р0 — р(х0, і). Имѣемъ :
АРаѵ=^+АРд^ах + + ар аі.
Множители при (Іх и ді должны равняться Х± и сх; вставляя вмѣсто
Хі его значеніе имѣемъ
...........
(ддт)х^с’~Ардя......................<в1*>
При х=ѵ и при х=р получаются соотвѣтственно
= АТ^—Ар = АТ*д№\
\дѵ { ді г ді \Т)
ІдІД
( ді ), ~ Сѵ
. . (61,д}
(бі.с)
Ради полноты добавимъ еще двѣ формулы:
Содержащаяся въ первой изъ формулъ (61,с?) величина
ОС/)
дР
ді
— Р
называется внутреннимъ давленіемъ, на основаніи слѣдующихъ
соображеній. Если при і = Сопві. объемъ ѵ увеличивается, то для этого
др
должно быть затрачено количество теплоты = адѵ = АІсм. (58. с).
Мы можемъ написать :
др
т
\дѵ + Ардѵ.
Второй членъ правой части этого равенства представляетъ собою количество
Энергія тѣла.
431
теплоты, затраченное на внѣшнюю работу. Первый же членъ, равный
очевидно, представляетъ собою количество теплоты, затраченное на
внутреннюю работу. Эта внутренняя работа равняется, слѣдовательно,
( тог,Д'а какъ внѣшняя работа равна рсіѵ. Аналогично внѣш-
нему давленію р множитель при (Іѵ въ выраженіи внутренней работы
и называютъ внутреннимъ давленіемъ. Аша^аі (1894—1909) изслѣ-
довалъ въ рядѣ работъ эту величину: въ послѣднее время ею занимался
такжр Ьейис (1909). Сравненіемъ съ результатами непосредствен-
ныхъ наблюденій Ашаі находитъ, что для реальныхъ газовъ вну-
треннее давленіе обратно пропорціонально квадрату объема.
о ™ -А дѵ др дѵ др
Вставляя ІЭ(х, і) — -3 ---,
ѵ дх ді дідх
легко преобразовать (61,6) и
представить въ видѣ:
(дІД = ЦрД— дѵ
\дх Д дх ді у 7) ді Эху 7)]’
Это равенство даетъ:
х
Ѵ(х, І) = ІДХ„, І) + АТ> Г|* * И
ѵ 7 \ о’ / । ) ]Эх VI дідх\Т]^
Если въ (бі.с) подставить х = х0, то получается
і) _г _Лп дѵ0
ді — со лРо ді-
Отсюда
/7(х0, 0 = ^(хо, У +
4)
Вставляя это выраженіе, имѣемъ:
і
.^с0-Ар0^°
*0
Ш-ЛГ2
Это формула Кіг сЫіоі Ра. Разсмотримъ два частные случая,
когда х — ѵ и когда х=р.
1.
дѵ
дх
1;^=о
ді
дѵо
ді
= 0; с0 равно значенію теплоемкости
X — ѵ;
при постоянномъ объемѣ ѵ = ѵ0. которую обозначимъ черезъ (сѵ)0; получается:
и(ѵ, і) = Ѵ(ѵ0, іп)+(с^і + АТ* I • (62,а)
^0 Ро
432
Термодинамика.
др
2. х =р : • = 0 : второй интегралъ легко упрощается; далѣе с0 есть
теплоемкость при постоянномъ давленіи р = р^ которую обозначимъ че-
резъ (Ср)0; давленіе р0 отъ і не зависитъ и потому
і
А I -~-'АРо№Ѵо’ ~ѵ(Ро, Ш
^0
Окончательно имѣемъ:
і
Щр, і) = и(р0,і0) + I (Ср)0М + Ар0\ѵ(р0,і)- г/(/?0Д0)] —
Р /
1 ................................(,,ад
Ро
Мы воспользуемся этими формулами въ слѣдующихъ главахъ.
§ 16. Энтропія и ея свойства. Положимъ, что А и В представля-
ютъ два состоянія даннаго тѣла, и допустимъ, что существуетъ хотя-бы
теоретическая возможность перейти отъ А къ В при помощи одного или
нѣсколькихъ различныхъ обратимыхъ процессовъ. Мы видѣли, что
въ этомъ случаѣ значеніе интеграла
В
I = СОП8І.,
А
т.-е. не зависитъ отъ того, которымъ изъ обратимыхъ процессовъ, веду-
щихъ отъ А къ В, мы воспользовались. Отсюда слѣдуетъ, какъ уже было
сказано (стр. 426), что : Т есть полный дифференціалъ нѣкоторой опре-
дѣленной функціи состоянія тѣла, т.-е. функція независимыхъ пере-
мѣнныхъ х и у, опредѣляющихъ состояніе тѣла. Эта функція называ-
ется энтропіей тѣла; мы ее обозначимъ черезъ 5. Тогда мы имѣ-
емъ» 5 = / (х, у), и далѣе
аЗ = ................. (63,а)
а<$ = таз ...... ... (бз,^)
в
^ = 3,-3, ........ (63,с)
е'
А
Здѣсь 5Х и 52 значенія функціи 5=/(х, у) въ состояніяхъ А и В.
Изъ сказаннаго явствуетъ, что энтропія тѣла, какъ и его энергія, опре-
дѣлены быть не могутъ, ибо мы не знаемъ состоянія тѣла, при которомъ
5 = 0. Можно говорить только о разности значеній энтропіи
въ двухъ состояніяхъ тѣла.
Энтропія.
433
Далѣе ясно, что такая разность только тогда имѣетъ смыслъ, когда
существуетъ обратимый путь отъ А къ В. Мы допускаемъ, что такой
путь дѣйствительно всегда существуетъ, и надо замѣтить, что предполо-
женіе о возможности обратимыхъ процессовъ щя всѣхъ происходящихъ
въ природѣ измѣненій до сихъ поръ не привело къ какимъ-либо про-
тиворѣчіямъ.
Если тѣло совершаетъ круговой процессъ, то въ концѣ процесса его
энтропія, какъ и его энергія, принимаетъ прежнее значеніе, ибо обѣ ве-
личины суть функціи состоянія.
Положимъ, что существуетъ необратимый процессъ, ведущій
отъ А къ В. Тогда мы составимъ круговой процессъ, идя отъ Л къ В
по пути необратимому и отъ В къ Л по пути обратимому, всегда суще-
ствующему. На основаніи формулы (50,а) стр. 417 имѣемъ
В А
/йО । ч / (10
+ (обр.) | < О,
> А В
или, см. (63,с), в
(необр.)— 52 < О,
А
В
(необр.) < 52 — .............(63,(і)
А
Для необратимаго процесса приращеніе энтропіи
в
Г
оольше интеграла I
А
Мы можемъ сказать, что при необратимомъ процессѣ прираще-
ніе энтропіи равно этому интегралу, взятому по любому обратимому
пути. Отсюда вытекаетъ важное слѣдствіе. Мы видѣли, что для обра-
тимаго безконечно малаго процесса = (111 -ф- Арсіѵ; для необратимаго
процесса это равенство перестаетъ имѣть мѣсто. Но для всякаго процесса
(18 = : Г, гдѣ (10 соотвѣтствуетъ обратимому процессу. Отсюда слѣ-
дуетъ, что, хотя для необратимаго процесса равенство = (111 +
А-Арйѵ не удовлетворено, однако, какъ для обратимаго, такъ
и для необратимаго процесса
</5=^+4^ ..............(вМ
Далѣе для обратимаго процесса
<18 = ^..................(63,/)
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. ПІ, изд. 3-е.
28
434
Термодинамика.
для необратимаго
<18 >-^
(ЬЗ^)
Назовемъ изентропическимъ такой процессъ, втеченіе кото-
раго энтропія не мѣняется. Для обратимаго адіабатическаго процесса
имѣемъ б/(2=О; (63,с) даетъ 52 = т.-е. 5 = Сопзѣ. Обратимый
адіабатическій процессъ есть процессъ изентропическій. Формула
(63//) даетъ, при б/<3 = 0, Необратимый адіабатиче-
скій процессъ не есть процессъ изентропическій; при
такомъ процессѣ энтропія растетъ.
Если тѣло поглощаетъ теплоту, то его энтропія всегда ра-
стетъ, см. (63,/) и (63,^). Если тѣло отдаетъ теплоту и процессъ
обратимъ, то энтропія тѣла убываетъ.
Для обратимыхъ изотермическихъ процессовъ Т = Сопзі. и
(63,с) даетъ о
...............(63,й)
Для одного изолированнаго тѣла имѣемъ б/<2 = 0; (63,6) и (63,^)
показываютъ, что энтропія изолированнаго тѣла можетъ
только расти или оставаться неизмѣнной; но ни въ ка-
комъ случаѣ энтропія изолированнаготѣла не можетъ
убывать.
Переходимъ къ вопросу объ энтропіи изолированной системы
тѣлъ, внутри которой могутъ происходить разнообразные физическіе и хи-
мическіе процессы.
Обобщая полученный результатъ, получаемъ: въ изолированной
системѣ энтропія не можетъ убывать; если въ системѣ происходятъ
обратимые процессы, то энтропія не мѣняется; она растетъ при необра-
тимыхъ процессахъ.
Выраженное въ этихъ словахъ положеніе нельзя строго доказать,
исходя изъ предыдущаго. Но оно подтверждается эмпирически тѣмъ, что
всѣ получаемые изъ него выводы оказываются вѣрными. Разсмотримъ
напр. случай системы, состоящей изъ двухъ тѣлъ. Здѣсь во-первыхъ
состояніе каждаго отдѣльнаго тѣла можетъ подвергаться измѣненіямъ, при-
чемъ его энтропія не можетъ убывать. Кромѣ того можетъ происходить
тепловой обмѣнъ между двумя тѣлами, температуры которыхъ обозначимъ
черезъ 7\ и Г2, причемъ Тг >> Т2. Если сІС? перейдетъ отъ перваго тѣла
ко второму, то энтропія системы измѣнится на величину
</8=^/*
\^2 ' 1 / 4*2
Если 7\ и Т2 безконечно мало отличаются другъ отъ друга, т.-е. пе-
реходъ теплоты представляетъ процессъ обратимый, то ^/5=0; если
7\ — Т2 величина конечная, то процессъ необратимъ и (18 > о. Этотъ
примѣръ подтверждаетъ, что энтропія 5 изолированной системы, состо-
ящей изъ двухъ тѣлъ, не можетъ уменьшаться.
Энтропія.
435
Разбирая другіе процессы, мы всегда приходимъ къ тому же резуль-
тату. V поэтому мы принимаемъ слѣдующую новую формулировку
второго начала термодинамики:
энтропія изолированнной системы тѣлъ не можетъ
убывать; она остается неизмѣнной при обратимыхъ, и
растетъ при необратимыхъ процессахъ, совершающихся
въ этой системѣ.
Мы приписываемъ каждому изъ тѣлъ, изъ которыхъ состоитъ си-
стема, опредѣленный составъ, опредѣленныя свойства и, въ каждый дан-
ный моментъ, опредѣленную температуру. Когда въ систему входятъ тѣла
неоднородныя или неравномѣрно нагрѣтыя, то мы ихъ мысленно
должны раздѣлить на надлежащее, въ крайнемъ случаѣ безконечно боль-
шое число частей, и подъ энтропіей тѣла подразумѣвать сумму энтропій
этихъ частей.
Паизіиз, обобщая теорему объ энтропіи изолированной системы,
говоритъ: энтропія вселенной стремится къ нѣкоторому
максимуму. Однако такое обобщеніе нельзя считать допустимымъ.
Энтропія 5 есть функція независимыхъ перемѣнныхъ х и у,
но она и сама можетъ быть принята за одну изъ незави-
симыхъ перемѣнныхъ, опредѣляющихъ состояніе тѣла.
Выведемъ нѣкоторыя замѣчательныя формулы, выражающія связи между
величинами <7, 5, р, ѵ, А Мы имѣли для всякаго процесса, обрати-
маго и необратимаго формулу (63,^), которая даетъ
а Тд8 = сіЫ + Ардѵ........... (64)
дЪ , \ ді} . , д17, . . [дѵ , . дѵ , \
т Лх + Эу=& + эу +Ар (<и * + У'ѵ)
Это даетъ дх дѴ. . дѵ — —н Ар — дх г дх (в4:,а)
дЗ ди , л дѵ
Т х- ду = з Ар — ду ду
Дифференцируемъ первое уравненіе по д/, второе по х и вычитаемъ.
Получаемъ замѣчательную формулу
Э5 дТ д8 дТ л (дѵ др дѵ др\ і ...
дх ду ду ох \дх ду ду дх )
Предоставляемъ читателю формулировать геометрическое зна-
ченіе этого равенства.
Переходимъ къ частнымъ случаямъ. Для ясности ставимъ производ-
ныя въ скобкахъ и внизу знакъ той величины, которая остается постоянною.
1. х=ѵ, у = і. Легко получается изъ (65)
— л (дР\
дѵ у ді
(бб.а)
28*
436
Термодинамика.
Этою формулою опредѣляется зависимость энтропіи отъ объема ѵ при
постоянной температурѣ і.
2. х=р, у =І. Получается зависимость энтропіи отъ давленія р
при постоянномъ і: 3. х = ѵ, у— 8. /дЗ' . /дѵ \ (ф \ ді )р Формула (65) даетъ . . . . (бб,6)
4 х = р, у — 3. /дѵ \ Получается (д8\ = А (?Р-\ /р 1 ді ]5 . . . (66,с) . . . (66у/)
5. х=ѵ, у—р даетъ интересную формулу
Э5 дТ дЗ дТ . , ч
дѵ др ор дѵ ...........................(66,0
Еще двѣ замѣчательныя формулы получаются, если въ (64,а) поло-
жить х — ѵ, у — 3;
дЗ дѵ дѵ дЗ
тогдаэх =0’ =1; полУчается:
/дѴ\ — т
\^)ѵ~
(66,/)
Первая формула показываетъ, что давленіе есть мѣра убы-
ванія энергіи, когда объемъ увеличивается изентропи-
чески; вторая говоритъ, что абсолютная температура есть
мѣра увеличенія энергіи, когда энтропія растетъ при
постоянномъ объемѣ.
Далѣе укажемъ на формулы, выражающія связь между энер-
гіей 1} и энтропіей 6 ; онѣ получаются, если въ (64,а) вставить сперва
. т дѵ дѵ
х = ѵ. у — і. Тогда - = 1, = О, такъ что получается
дх оу
Особенно замѣчательна вторая формула.
Если въ (64,а} вставить х = р, у I, то получается :
^67,6)
Энтропія.
437
Если во вторую формулу (67,6?) и во вторую (67,6) вставить значенія
производныхъ энергіи, данныя въ (61,б/) и (61,^) стр. 430, то получается:
= ?ѵ
\ ді]ѵ 7
Ід8\____Ср
\^/р“ Т
№,с)
На стр. 431 мы вывели формулу (62) КігсЫіоіГа для энергіи.
Выведемъ аналогичную формулу для э н т р о п і и въ зависимости отъ
х и А Мы имѣемъ:
Отсюда
Л) = Х^х + сх(11 = Тй8.
(68)
Формула (65) даетъ при у = і
д8 /др дѵ др сЫ _
дх \ ді дх дх ді/ ’
отсюда х
д \ді дх дх ді]
х0
Полагая въ (68) х = л0, имѣемъ
Э5(хОг С _ 0*)о
ді Т ’
и слѣдовательно,
5 (х0/) = 5 (х0, і0) + сіі.
А)
Окончательно
і х
5(х,0 = 5(хо,^)4- рс^°ді+А П^^-^\дх . (68,а)
і 1 1 С/Л С/Л С/ѵ і
Эту формулу также далъ К і г с к Ь. о И. Вводя величины (сѵ)0 и (Ср)0,
какъ на стр. 403, получаемъ частныя формулы :
1. х = ѵ.
$(р,і) = 8(р0, /0) +
438
Термодинамика
§ 17 Свободная энергія и термодинамическій потенціалъ. Бла-
годаря работамъ М а 8 8 і е и, Неітііоіі г’а, В и Іі е т’а, (3 і Ъ Ъ 8’а,
Ріапск’а, Каіапвоп’а, ѵап Ьааг’а и др. возникли обширные от-
дѣлы термодинамики, имѣющіе огромное практическое и теоретическое
значеніе. Въ Россіи занимались относящимися сюда вопросами въ осо-
бенности Умовъ, Шиллеръ, Голицынъ, Пиль чиковъ и др.
М а 8 8 і еи первый ввелъ двѣ функціи Н —Т8— С и Н'= Т8— и + Арѵ,
й показалъ ихъ значеніе, а именно первой для случая, когда независимыя
перемѣнныя х = ѵ и у = У, второй — для случая х = р, у — і. Черезъ каж-
дую изъ этихъ функцій просто выражаются энергія 67, энтропія 5, теплоем-
кости, коеффиціенты расширенія, сжатія и т. д. Онѣ, какъ мы увидимъ впо-
слѣдствіи на примѣрахъ, даютъ возможность свести вопросъ о рав-
новѣсіи системы къ простой минимумъ-задачѣ. Нѣ-
сколько позже НеІшЬоИг ввелъ понятіе о свободной энергіи,
которая только знакомъ отличается отъ функцій Н М а 8 8 і е п. Далѣе
ВиЬеш ввелъ названіе термодинамическаго потенціала для
— Н и — /У', и показалъ значеніе этихъ функцій для цѣлаго ряда во-
просовъ, относящихся къ явленіямъ диссоціаціи, растворимости, испаре-
нія и т. д. Сг і Ъ Ъ 8 въ высокой степени расширилъ и обобщилъ эту тео-
рію, играющую нынѣ важнѣйшую роль при разборѣ многихъ электриче-
скихъ и химическихъ явленій, которыхъ термодинамика до появленія ра-
ботъ названныхъ ученыхъ, въ особенности Н е 1 ш й оі 1 г’а, Сг і Ь Ь 8’а и
Р1 а и с к’а, не разсматривала. Въ послѣдующихъ главахъ мы встрѣтимся
съ многочисленными приложеніями той теоріи, которая здѣсь излагается.
Ввиду неустановившейся термйнологіи мы назовемъ величину
Р=1}—Т8...................(69)
свободною энергіей (Вийет называетъ эту величину термодина-
мическимъ потенціаломъ при постоянномъ объемѣ, Сг і Ь Ь 8 обозначаетъ ее
черезъ чр).
Волишку Ф = и- 75-Ь Аръ...................(ТО)
мы назовемъ термодинамическимъ потенціаломъ (П и й е ш
прибавляетъ «при постоянномъ давленіи»; Сг і Ъ Ь 8 обозначаетъ ее черезъ 0.
Покажемъ прежде всего, какимъ образомъ различныя физическія вели-
чины выражаются черезъ У7, когда х = ѵ, у = і, и черезъ Ф, когда х =
У = і-
I. Независимыя перемѣнныя ѵ -а і. Мы имѣли формулы
(61,О), (66, а) и (67,а):
ШАТ%-Ар
дѵ ді г
дЗ _ л дР
дѵ ’ ді
дѴ „д8
-ъ- = Т..=С„
(71, а)
Свободная энергія и термодинамическій потеіГціалъ.
439
Изъ
слѣдуетъ :
Р=Ѵ — Т8 . ... . . (71,6)
дР _дЦ___ т^__е ді ді ді . . . (71,0
дР^дІ^ д8 дѵ дѵ дѵ . <7і, а)
легко:
Формулы (71, а} и (71,6) даютъ отсюда
5=-^
ді
др
и=Р—Т^
ді
V Адѵ
— д*р
Сѵ~~ ді*
(72)
Нетрудно идти дальше, выражая черезъ Р величины а, ср,
у и т. д.
П. Независимыя перемѣнныя р и і. Воспользуемся
мулами (61, е), (66,6) и (67,6):
а, /9,
Изъ
получается
фор-
Р
— Ар ди__ др ~ д8_ = др ~ дѵ ді . „ дѵ . дѵ . ' АТ~ді Ар др ді ди ~ д8 л дѵ ді=тді Ар ді 1 (73, а)
Ф = и — Т8+Арѵ . . . ... . (73,6)
дФ ді 6Ф_ _дѴ_ ді _д^_ " др .гд8 о і . дѵ -тд-1^5 + АрТІ - Тд,5 +Лѵ + Ард" др др (73, С) (73,6?)
(73,о) и (73,6) даютъ отсюда легко:
с _ __6Ф
ді
дФ
6/ = Ф—
ді
1 6Ф
Ѵ ~ Адр
^д*Ф
СР ~ ~Т ді*
<м>
др
(74)
И здѣсь можно идти дальше, выражая и другія физическія вели-
чины черезъ Ф.
440
Термодинамика.
Замѣтимъ, что для системы тѣлъ, массы которыхъ имѣемъ:
ф = і
(74, а)
гдѣ /7 и Ф/ относятся къ единицамъ массы. Эти равенства непосред-
ственно вытекаютъ изъ аналогичныхъ выраженій для энергіи 1} и энтро-
піи 5 системы и изъ формулъ, опредѣляющихъ величины Р и Ф.
Перейдемъ къ разсмотрѣнію свойствъ свободной энергіи Р = 1}— 75,
причемъ выяснится и самый терминъ. Замѣтимъ, что НеІтІіоИг дѣ-
литъ всю энергію 1} системы на двѣ части, полагая и= Р О, причемъ
онъ О называетъ несвободною энергіею. Считаемъ нужнымъ уже
теперь указать, что оба термина имѣютъ смыслъ только для процессовъ
изотермическихъ, т.-е. когда температура системы не мѣняется.
Очевидно О = 75 и, далѣе,
сіР = сіи ТЛ8 — 8(іТ\
(10=778 + 877 (..............(7й)
Обозначимъ, какъ прежде (стр. 398), внѣшнюю работу, произведен-
ную системою, черезъ А; отрицательное I, т.-е. работ.у внѣшнихъ
силъ, произведенную надъ системою, удобнѣе будетъ обозначить особою
буквою /?. Кромѣ 7+2 = 717 7Ь, мы пишемъ еще <7(2 = (117 — <7/?.
Основное неравенсгво <7(2 778 даетъ
7У-778^771 1
аи— Т(і8^—(іь (.................(76)
(75) даетъ теперь
7Р^-7Ь 877 \
сІР^сІХ — 8(іТ ;..............(7',й)
(10^(1$+ 8ЛТ .............. (77, Ь)
Для изотермическихъ процессовъ
7Р^7Ь2.............. . (78, а)
7Р^7Ь...................
(ІО 7^ 7(2...............(78, с)
Знакъ равенства во всѣхъ формулахъ относятся къ случаю процес-
совъ обратимыхъ. Пусть Рк и <71 начальныя, Р2 и О2 измѣнившіяся
значенія Л и О. (78, а) и (78, 7) даютъ
Ло — %.................(78,
Л —........................(78, е)
О2-Оі^.....................(78,/)
Эти формулы показываютъ, что при изотермическихъ измѣненіяхъ
системы: .
1)Вся внѣшняя работа!, совершаемая системою, про-
изводится исключительно на счетъ запаса свободной
Общія условія равновѣсія системы.
441
энергіи. Эта работа наибольшая, когда измѣненіе си-
стемы (переходъ отъ /у къ представляетъ процессъ
обратимый.
2) Работа /? внѣшнихъ силъ только въ обратимомъ
процессѣ идетъ вся на увеличеніе запаса свободной
энергіи, слѣд. она при обратимомъ процессѣ наи-
меньшая.
3)Вся притекающая теплота идетъ на увеличеніе за-
паса несвободной энергіи.
(77,а} и (77,Ь) даютъ:
4) При всякомѣ повышеніи температуры часть 5У7
свободной энергіи переходитъ въ несвободную. Такимъ
образомъ энтропія 5 имѣетъ какъ бы характеръ теплоемкости несвобод-
ной энергіи.
Первыя три теоремы вполнѣ выясняютъ терминологію, введенную
Неі шЬ оііг’емъ; еще разъ замѣтимъ, что она имѣетъ смыслъ только
для изотермическихъ измѣненій. При адіабатическихъ измѣне-
ніяхъ (б/р = 0) работа сіѣ совершается отчасти насчетъ свободной энер-
гіи Л, отчасти насчетъ несвободной С, такъ какъ при охлажденіи, сопро-
вождающемъ это измѣненіе, количество теплоты 8(П переходитъ отъ
С къ Л.
§ 18. Система, состояніе которой опредѣляется многими перемѣнными;
условія равновѣсія системы. Одинъ изъ главныхъ результатовъ работъ
ОіЬЬз’а. НеІтЬоІіг’а, ВиЬет’а и Ріапск’а, наиболѣе характер-
ный для новой эры исторіи термодинамики, заключается въ распростра-
неніи методовъ этой науки на сложныя системы, состояніе которыхъ опре-
дѣляется многими перемѣнными, а не только двумя изъ трехъ, р, ѵ и і.
Ограничиваемся двумя примѣрами. Положимъ, что опредѣленное вѣсо-
вое количество Лі приведено въ парообразное состояніе, причемъ про-
исходитъ диссоціація, т.-е. часть молекулъ /// распадается по формулѣ
2Лі = Л + Н^. Количество разложенныхъ молекулъ представляетъ пе-
ремѣнную величину, характерную для даннаго состоянія вещества. Дру-
гой примѣръ представляетъ система, состоящая изъ нерастворенной соли
въ насыщенномъ растворѣ той же соли, и изъ пара растворителя надъ
растворомъ. Количества нерастворенной соли и пара суть перемѣнныя,
также характерныя для разсматриваемой системы. Для такой системы
мыслимы измѣненія этихъ перемѣнныхъ при заданныхъ ѵ и і или р и і.
Спрашивается, какого рода измѣненія въ .дѣйствительности возможны, и
какимъ условіямъ должны удовлетворять эти перемѣнныя, чтобы система
находилась въ устойчивомъ внутреннемъ равновѣсіи. Разберемъ сперва
первый вопросъ о возможныхъ измѣненіяхъ.
I случай. Даны і и ѵ, т.-е. измѣненія могутъ быть только изо-
термическія и безъ измѣненія объема (изохорическія).
Имѣемъ общую формулу (76):
ЛІ}—Тс18^(Ш................. (79)
442
Термодинамика.
При ѵ — Соп8І. имѣемъ = 0; 7 = Сопйі. даетъ
ащ—
т.-е.
....................(80, а)
Свободная энергія можетъ только оставаться неиз-
мѣнной или уменьшаться, когда /изданы. Увеличеніе сво-
бодной энергіи невозможно.
II случай. Даны і и р, т.-е. измѣненія системы могутъ быть
только изотермическія и при неизмѣнномъ давленіи (и з о -
піестическія. или изопикническія). Въ (79) слѣдуетъ положить
ЛР = — Ар(іѵ; при р и і постоянныхъ получаемъ
б/(6г—Г5 +Л^)<0.
т.-е.
г/Ф < 0...................(80. 6)
Термодинамическій потенціалъ можетъ только оста-
ваться неизмѣннымъ или уменьшаться, когда ^и р таны.
Возрастаніе этой величины невозможно.
Переходимъ къ фундаментальному вопросу объ условіяхъ равно-
вѣсія системы. Мы видѣли (стр. 386), что условіе обратимости без-
конечно малаго процесса заключается въ томъ, чтобы между даннымъ тѣ-
ломъ и окружающими его тѣлами имѣло мѣсто равновѣсіе, безконечно
мало нарушаемое. Соединяя данное и окружающія тѣла въ одну систему,
мы видимъ, что равновѣсіе есть условіе обратимости. Мы заключаемъ,
что и наоборотъ: обратимость возможныхъ процессовъ есть
условіе равновѣсія. II дѣйствительно, какой бы мы ни предста-
вили себѣ сличай равновѣсія системы, при безконечно маломъ нарушеніи
этого равновѣсія возможны безконечно малые процессы какъ въ одну,
такъ и въ другую сторону. Если напр. число разложенныхъ молекулъ
ЗН меньше числа, при которомъ система находится въ равновѣсіи, то это
число можетъ увеличиться, но не можетъ уменьшиться; если же насту-
пило равновѣсіе, то это число можно и увеличить и уменьшить, мѣняя
безконечно мало состояніе системы. Условіе обратимости опредѣляется
знаками равенства въ предыдущихъ формулахъ. Прилагая сказанное къ
двумъ случаямъ, къ которымъ относятся формулы (80, а) и (80, &). полу-
чаемъ важнѣйшія теоремы:
[. Когда даны і и ѵ. то система находится въ равно
вѣсіи при условіи
б/Г=О....................(81, а)
П. Когда даны і и р, то система находится въ равно-
вѣсіи при условіи
г/Ф = 0...................(81, Ь)
Здѣсь (ІЕ и б/Ф относятся къ измѣненіямъ системы, м ы с л и м ы м ъ
при заданныхъ условіяхъ (і и ѵ или і и р неизмѣнны) и согласнымъ съ
Заключеніе.
443
внутренними условіями, т.-е. съ тѣми связями, которыя существуютъ
между другими перемѣнными. Такъ напр. измѣненія количествъ .///, Л
и Н2 связаны условіями, что сумма массъ должна оставаться неизмѣнной,
и что число молекулъ Л должно равняться числу молекулъ Н.2. Въ дру-
гомъ изъ вышеприведенныхъ примѣровъ масса нерастворенной + масса
растворенной соли должна оставаться постоянной, и то же самое отно-
сится къ массѣ растворителя + масса пара.
Формулы (81, а) и (81,/?) можно вывести иначе. Система очевидно
будетъ находиться въ устойчивомъ равновѣсіи, когда всѣ мыслимыя из-
мѣненія невозможны, т.-е. даютъ б/Л>0 или сІФ > 0. Отсюда слѣ-
дуетъ, что система находится въ равновѣсіи, когда Е или
Ф минимумъ, а это и выражается формулами (81.6?) и (81,/>). Отсюда
ясно, что ^=0 или сІФ = 0 есть условіе достаточное для равно-
вѣсія ; но не видно, чтобы это было условіе необходимое. И дѣй-
ствительно, наблюдаются случаи равновѣсія, при которыхъ Е или Ф не
минимумъ, но это суть случаи равновѣсія неустойчиваго, легко на-
рушаемаго по направленію уменьшающихся Е или Ф.
§ 19. Заключеніе. Мы старались изложить въ этой главѣ основы
термодинамики, познакомить съ важнѣйшими величинами, встрѣчающи-
мися въ этой наукѣ и указать на соотношенія, существующія между ними.
Приложенія выведенныхъ формулъ будутъ разсмотрѣны во всѣхъ послѣ-
дующихъ главахъ. Мы, конечно, далеко не исчерпали теоретической сто-
роны теомодинамики, и между прочимъ вовсе не коснулись сложнаго во-
проса о механическомъ значеніи второ го начала. Ограничи-
ваемся, въ заключеніе, немногими словами по этому вопросу, литература
котораго подробно указана ниже.
Мы допускаемъ, что сущность теплоты заключается въ особаго рода,
можетъ быть очень сложныхъ механическихъ движеніяхъ частицъ. От-
сюда невольно является мысль о возможности вывода второго начала тер-
модинамики на основаніи принциповъ и формулъ теоретической меха-
ники. Этимъ вопросомъ занимались впервые ВоШтапп (1866 и 1877),
С Іа и 8 іи 8 (1870) и 8гі1у (1872), а затѣмъ ЬовсЬів ісіі, Кескпа-
§е1, В. А. Михельсонъ (въ Москвѣ), Оррепііеіш, й. й. Миеі-
Іег, Ьейіеи, Еіпвіеіп (1902) и др. Наконецъ, НеІтйоИг далъ
теорію, основанную на совершенно новыхъ началахъ, которыя И е г 12
впослѣдствіи развилъ въ своей системѣ механики.
Первый выводъ В о И 2 т а п п’а напоминаетъ выводъ принципа наи-
меньшаго дѣйствія въ механикѣ. Работа 8 2 і 1 у мало отличается отъ ра-
боты Воіігтапп’а; 8гі1у прилагаетъ принципъ НатіИоп’а къ те-
пловымъ движеніямъ и приходитъ къ заключенію, что второе начало пред-
ставляетъ въ термодинамикѣ то же самое, что принципъ НатіНоп’а
въ аналитической механикѣ.
Гораздо болѣе общимъ представляется путь, по которому шелъ С1 а и -
8ІН8, который исходить изъ предложенія, что вся механическая
работа, произведенная на счетъ теплоты при безко-
444
Термодинамика.
н е ч н о маломъ обратимомъ измѣненіи состоянія тѣла,
пропорціональна абсолютной температурѣ Т. Мы видѣли,
что (^ — (ІѴ7(ІР(стр. 398), гдѣ сІР и сік тратятся на внутрен-
нюю и на внѣшнюю работу и гдѣ (ІѴУ(ІР= (IV. Сіаизіиз вводитъ
новую величину X которую онъ называетъ дисгрегаціей, и которая
измѣряетъ собою степень раздробленности вещества; работу, произведен-
ную при увеличеніи дисгрегаціи на б/2, онъ и принимаетъ пропорціо-
нальной 7", т.-е. онъ пишетъ
(іР-уйЬ АкТйХ....................(82)
гдѣ к множитель пропорціональности.
Далѣе Сіаийіий вводитъ величину, которую онъ называетъ ви-
ріаломъ. Положимъ, что имѣется весьма большое число движущихся
частицъ, координаты которыхъ хп, уп, гп; скорости ѵп, массы тп, сла-
гаемыя дѣйствующихъ на нихъ силъ Хп, Уп, Въ такомъ случаѣ
живая сила равна
12 тпѵп~
п
Допустимъ, что движеніе стаціонарное, т.-е. каждая частица
не очень удаляется оть нѣкотораго средняго положенія, что скорость ея
остается въ нѣкоторыхъ предѣлахъ, и что послѣдовательные пути мало
отличаются другъ отъ друга. Сіаизіиз называетъ въ такомъ случаѣ
виріаломъ среднее значеніе, заданный промежутокъ времени, величины
-- 2 2 №пХп 4“ ^пУп 4“
п
и доказываетъ, что при стаціонарномъ движеніи системы средняя
живая сила системы, за данный промежутокъ времени,
равняется в и р і а л у системы. Принимая далѣе среднюю жи-
вую силу за мѣру абсолютной температуры, Сіаизіиз доказываетъ, что
= - (83)
п
гдѣ і время одного изъ періодически повторяющихся движеній, с множи-
тель пропорціональности. Формула (83) показываетъ, что величина, сто-
ящая съ лѣвой стороны, есть полный дифференціалъ: а въ
этомъ и заключается аналитическое выраженіе второго начала.
Въ позднѣйшей работѣ (1877) ВоНгтапп пользовался тѣмъ
статистическимъ методомъ, о которомъ было сказано на стр. 393. Въ
природѣ существуетъ тенденція отъ менѣе вѣроятнаго состоянія къ бо-
лѣе вѣроятному. В о 11 7 ш а п п показалъ, что логариѳмъ вѣ-
роятности опредѣленнаго состоянія лишь на постоянную величину
отличается отъ энтропіи.
НеІтІіоНя приложилъ къ тепловымъ движеніямъ свою теорію
циклическихъ движеній и вывелъ двѣ формулы, которыя могутъ
Литература.
445
быть разсматриваемы, какъ выраженія перваго и второго начала термо-
динамики.
Интересное обобщеніе формулъ термодинамики и приведеніе ихъ въ
весьма стройную систему можно найти въ обширной работѣ А.ѵ.ОеИ і п^ еп’а.
ЛИТЕРАТУРА.
Полный обзоръ литературы термодинамики до половины 1889 г. можно найти
въ книгѣ:
А. Тискегтапп. Іпсіех оі ІЬе Ьііегаіиге оі ТЬегтойупатъсе. АѴазЫп^Іоп, 1890.
(ЕтііЬеопіап тіесеііапеоие со11есііон8. Ѵоі. 34, агі. II). Въ первой части этой книги
статьи распредѣлены по содержанію на 58 отдѣловъ, и въ каждомъ отдѣлѣ въ хроно-
логическомъ порядкѣ; во второй части книги статьи распредѣлены по авторамъ въ
алфавитномъ поряднѣ. Всего указано свыше 1700 статей.
Подробный обзоръ литературы до 1870 года можно также найти въ книгѣ:
М. Ѵегйеі. ТЬёогіе тёсапідие сіе Іа сЬаІеиг. Рагіе 1868—72 (Оеиѵгее т. VII и VIII),
т. II, стр. 267—338.
Курсы термодинамики:
Окатовъ. Термодинамика. Спб. 1871.
Зиловъ. Элементарный курсъ механической теоріи тепла. Москва, 1882.
Нігп. ТЬёогіе шёсапідпе бе Іа сЬаІеиг. Рагіе 1875—76.
Ѵегйеі. ТІіёогіе тёсапідие сіе Іа сЬаІеиг. Рагіе 1868—72.
Моиііег. ЕІетепіе сіе іЬегтобупатідие. РагІ8 1872; есть русскій переводъ.
ВегігапсІ. ТЬегтосІупаіпідие. Рагіе 1887.
Ьірртапп. Соигв сіе ІЬегтобупатідие. Рагі8 1906.
Роіпсагё. ТЬегтосІупаітдие. Рагіе 1908.
2.еипег. Ѳгипсігй&е сіег тесЬапіесЬеп АѴагтеіЬеогіе. ЕгеіЪиг# 1860; 2-ое изд.,
Ьеір2І& 1866 и 1877.
Хеипег. ТесЬпіесЬе ТЬегтобупатік. Ьеіргі^ 1877, 2 части (техническія прило-
женія на первомъ планѣ).
Сіаивіив. АЪЬапсІІип^еп йЬег (ііе тесЬапіесЬе ЛѴагтеіЬеогіе. ВгаипесЬлѵеі^ 1864.
(Собраніе статей).
Сіаивіив. Віе тесЬапіесЬе АѴагтеіЬеогіе. ВгаипесЬхѵеі^ 1876—1879.
Риеігітапп. НапсІЬисІі (Іег тесЬапіесЬеп АѴагтеіІіеогіе. ВгаипесЬ\ѵеі§-, 1876—1885.
Сагі Ыеитапп. МесЬапіесЬе ТЬеогіе сіег АѴагте. Ьеіргщ, 1875.
Ріапск. Ѵогіееип^еп ііЬег ТЬегтобупатік. Ьеіргі^ 1911; есть русскій переводъ.
Махгѵеіі. ТЬеогу оі Ьеаі. Ьопсіоп, 1871.
ѴѴеіпвіеіп. ТЬегтосІупаітк, 1901—1908.
Ѵоі^і. ТЬегтосІупаітк, Ьеіргі^, 1903, 1904.
Реггіп. СЬітіе рЬуеідие. I Ьее ргіпсірее, Рагіе, 1903.
Неіт. Епег&еіік, Ьеіргі^ 1898.
Неітігоиг. Ѵогіееип^еп, ТЬеогіе сіег АѴагте р. 169—383, Ьеіргі^, 1903.
Н. А. Ьогепіх. АЬЬапсІІ. йЬег іЬеогеѣ РЬузік, I р. 202—298, 1907.
Вгуап. Епсукі. 4. таШ. ѴТее. 5 р. 71-—160, 1903.
Зскгйіег и РгапМ. Епсукі. 4. таіЬ. \Ѵіез. 5 р. 232—319, 1905.
Ѵап йег ѴѴааІв-КоІіпМатт. ЬеЬгЬ. 4. ТЬегтосІупатік, т. I, 1908.
Къ § 1.
8айі Сагпоі. Вёііехіопе еиг Іа риІ88апсе тоігісе (Іи іеи. Рагіе, 1824; новое
изданіе. (Рагіе, 1878) содержитъ замѣтки, найденныя послѣ смерти Сагпоі.
РоЬегі Мауег. Вешегкпп&еп йЬег (ііе Кгаііе йег шіЬеІеЫеп Ыаіиг. ЬіеЪ. Ап.
42 р. 1, 1842; Ѳееат. АЬЬапсІІ. ЕіиіЩагі, 1892.
446
Термодинамика.
}оиІе. Ргос. К. 8ос. 4 р. 280, 1837—1843 (аЬзігасіз); 5 р. 517, 1843—1850; РЫІ.
Ма&. (3) 25 р, 1, 1844; 26 р. 369, 1845; 27 р. 205, 1845; 28 р. 205, 1846; 31 р. 173, 1847;
35 р. 335, 1849; (4) 2 р. 263, 347, 435, 1851. Собраніе его статей вышло въ нѣмец-
комъ переводѣ Л 8ргепреГя подъ заглавіемъ „Ваз тесйапізсііе \Ѵагтеаециіѵа1епі“.
Вганпзсйхѵеі^, 1872.
Неітііоііх. ЁЬег (ііе ЕгЬаІіпп^ сіег Кгай. Вегііп 1847 и Ьеіргі^ 1862.
СІаіі8Іи8. Ро$&. Апп. 81 р. 168, 1850; 83 р. 118, 1851; 93 р. 481, 1854; 100 р.
353, 1857; 105 р. 239 1858 и др. Собраны въ АЪІіапсІІип^еп йЪег сііе тесІіапізсЫ АѴаг-
теіЬеогіе, ВгаппзсЫѵеі^, 1864.
ІГ. Пот8оп (Ьогсі Кеіѵіп). ЕсІіпЪ. Тгапз. 20 р. 261, 289, 1851; РЫІ. Ма$. (4)
4 р. 8, 105, 160, 304, 1852
ОіЬЬ8. Тгапз. Сопесіісиі Асасі. 2 р. 309, 382, 1873; 3 р. 108, 343, 1875—78; 8Ш.
Л. іб р. 441, 1878; на нѣмецкомъ языкѣ переводъ ОзіхѵаІсГа подъ заглавіемъ „Тііегто-
сІупапіі8С8е 8ішіірп“, Ьеіргі^, 1892; на французскомъ: Ье Сііаіеііег, ЕцшІіЬге сіе зуз-
іётез сЫтідиез, Рагіз, 1899; Роу, Віа^гаттез еі зигіасез іііегтосіупатідиез. Рагі8, 1903
(8сіепііа, рЬуз-таіЫ № 22).
НеІтИоІіх. Вегі. Вег. 1882 р. 23, 825; 1883 р. 647; Оез. АЫіапсІІ. 2 р. 958, 979:
3 р. 92.
Къ § 2.
Рит/огсі. Ап Іпдиігу сопсегпі^ іііе ХѴеі^Ьі о! Неаі. РЫІ. Тгапз. 1799; Сотріеіе
^Ѵогкз 2 р. 2.
Васоп. Ве іпіегргеіаііопе паіпгае. Егапсоіигіі, 1665; см. Рі8сНег, СезсЫсЫе сіег
Рііувік, 1 р. 213.
Воуіе. См. РІ8сНег, СезсЫсЫе сіег Рііузік, 2 р. 159.
Реъѵіоп. Оріісе. ЫЬ. III, диаезі. XVIII, р. 280, Ьаизаппе еі Оепеѵе 1740; см.
Н8СІіег. 1. с. 3 р. 215.
Віаск. Ьесіигез оп іііе Еіетепіз оі Сііетізігу, 1 р. 33.
Ьаѵоі8Іег еі Ьаріасе. Мётоіге зиг Іа скаіеиг. Мёт. сіе ГАсасІ. 1780
Нитркгу Рапу. СопігіЪиііопз іо рііузісаі аші тесіісаі кполѵіесі&е, соііесіесі Ьу
Ве(Шое8, Вгізіоі, 1799; Сотріеіе ХѴогкз 2 р. 11; Еіетепіз оі сііетісаі РЫІозорІіу, р. 94;
см. РІ8скег 1. с. 7 р. 588.
Рит/огсі. РЫІ. Тгапз. 1789 р. 286.
П. Уоип&. Ьесіигез оп паіига! рЫІозорЬу. Ьопсіоп 1807.
Атрёге. Апп. сЫт. еі рііуз. 58 р. 432, 1821.
Р. Мауег. ЬіеЬ. Апп. 42 р. 1, 1842.
Моііг. ЫеЪ. Апп. 24 р. 1, 1837; РЫІ. Ма§\ (5) 2 р. 110, 1876; АП^етеіпе Тііеогіе
сіег Вехѵе&ип^ и т. д. ВгаипзсЫѵеі^, 1868, р. 34 и 84.
Вё^иіп. Еішіез зиг ГіпПиепсе сіез сііешіпз <1е іег. Рагіз, 1839; см. Созтоз 26
р. 296, 1864.
Соісііщг. Ѵиіепзк. зеізк. ькгііі. КрЪепІіаѵп 2 р. 121, 167, 1851; РЫІ. Ма§. (4)
27 р. 56, 1864.
Къ § 3.
Р. Мауег. См. къ § 1.
Роъуіапсі. Ргос. Атег. Асасі. 15 (Ке\ѵ 8егіез 7) р. 75, 1879—80.
Регоі. С. К. 102 р. 1369, 1886; I бе рііуз. (2) 7 р. 129, 1888; Апп. сЫт. еі рііуз.
(6) 13 р. 145, 1888.
Зоиіе. (Способъ тренія). РЫІ. Ма$. (3)31 р. 173, 1847; РЫІ. Тгапз. 1850 р. 61,87 і
Ргос. К. 8ос. 27 р. 38, 1878, РЫІ. Тгапз. 1878 р. 365.
Роыіагиі. (Способъ тренія). См. выше.
Оау. РЫІ. Ма§. (5) 44 р. 169, 1897; 46 р. 1, 1898.
Раѵге. С. В. 46 р. 337, 1858.
Місиіезси. Л. сіе рііуз. (3) 1 р. 104, 1892; С. В. 112 р. 1308, 1891; Рііуз. Веѵие
1 р. 624, 1892.
Литература.
447
Риіщ. Ро^. Апп. 157 р. 437, 649, 1876.
8аііиІка. АѴ. А. 41 р. 748, 1890.
Н. А. Смирновъ. Ж. Ф. X. О. 39 р. 129, 1907.
Нігп. Весііегсііез еиг Гедиіѵаіепі шёсапідие сіе Іа скаіеиг, 1858 р. 20.
Вагпез. Ргос. К. 8ос. 82 р. 39, 1909.
Котурницкій. Ж. Ф. X. О. 37 р. 11, 1905.
Тоиіе. (Сжатіе газовъ). Ріііі. Ма$. (3) 26 р. 369, 1845. (Способъ капил. тру-
бокъ). РЫ1. Ма&. (3) 23 р. 38, 1843. (Способъ электродинам. индукціи). Ріііі. Ма§. (3)
23 р. 263, 343, 435, 1843. (Способъ нагрѣванія токомъ). Вер. Сотт. ЕІ. Ѵпіі. Ьоп-
сіоп, 1873 р. 175.
Ѵіоііе. Апп. сіііт. еі рііуе. (4) 22 р. 64, 1870.
И Агзопѵаі. Ьшпіёге ёіесігідпе, мартъ 1891.
Оиіпіиз Ісіііиз. Ро^§;. Апп. 101 р. 69, 1857.
Н. Р. ѴѴеЬег. Ріііі. Ма&. (5) 30, 1878.
Оіеіегісі. АѴ. А. 33 р. 409, 1888; Апп. сі. Рііуе. (4) 16 р. 611, 1905.
Еакп. АѴ. А. 25 р. 62, 1885; 37 р. 408, 1889.
Огі$Шіз. Ріііі. Тгапв. 184Ар. 361, 1893; Ргос. Воу. 8ос. 53 р. 6,1893, 55 р. 23,1894.
Всііизіег апй Оаппоп. Ріііі. Тгапз. 186А р, 415, 1895; Ргос. К. 8ос. 57 р. 25, 1895.
Раѵге еі 8іІЬегтапп. Апп. сіііт. еі рііуе. (3) 37, 1851.
Ейіипй. Р. Апп. 114 р. 13, 1861; 126 р. 539, 572, 1865; Апп. сіііт. еі рііуе.
(4) 8 р. 257, 1866.
Дальнѣйшая литература:
Вагіоіі. Мет. Ас. Ьіпсеі. (3) 8 р. 67, 1880; Ыиоѵо Сіт. (3) 8 р. 5, 1880.
Наца. АѴ. А. 15 р. 1, 1882.
ѴѴеЬзіег. Ргос. Атег. Асасі. (пелѵ еегіее) 12 р. 490, 1884—85 Ріііі. Ма&. (5) 20
р. 217, 1885.
Къ § 5.
Сіареугоп. 4. сіе ГЕсоІе роіуіесіт. 18 р. 170, 1834; Ро§&. Апп. 59 р. 446, 1843.
Къ § 6.
КігсНо//. Ро^. Апп. 103 р. 179, 1858.
№. ТНотзоп (Ьогй Кеіѵіп.) Ріііі. Ма§. (4) 9 р. 36, 523, 1855.
Сіаизіиз. АЫіапс11ип§еп (см. къ § 1) 1 р. 281.
Къ § 12.
Ріапск. \гег1і. 4. а. рііуе. Сее. 2 р. 206, 1900.
Еіпзіеіп. Аппаѣ й. Рііуе. (4) 17 р. 549, 1905; 19 р. 371, 1906.
8тоІисііоѵ)зкі. Аппаі. а. Рііуе. (4) 21 р. 756, 1906; 25 р. 205, 1908.
8ѵейЪег%. 7ібс1іг. Г. рііуе. Сііет. 59 р. 451, 1907; 67 р. 105, 1909.
ОаЪгогѵзкі. С. В. 149 р. 477, 1909.
Реггіп. С. В. 146 р. 967, 1908; 147 р. 475, 530, 1908; 4. сіе РЪуз. 1909 р. 609;
Апп. а. сіііт. еі рііуе. (8) 18 р. 5—114, 1909.
Къ § 13.
№. ТНотзоп (Ьогй Кеіѵіп). ЕаіпЬ. Тгапе. 16 р. 5, 541, 1849; Апп. сЪіт. еі рііуе.
(3) 35 р. 376, 1852.
Къ § 14.
КігсШіо#. Сее. АЪІіапаі. р. 454; Ро^. Апп. 103 р. 177, 1858.
Ата^аі. С. В. 142 р. 31, 1906; 148 р. 1135, 1359, 1909; 4 ае рііуз. (3) 3 р. 307,
1894; 8 р. 353, 1899; (4) 5 р. 499, 1906; 8 р. 617, 1909.
Къ §§ 17 и 18.
Маззіеи. С. В. 69 р. 858, 1057, 1869; 4. 4е рііуз. (1) 6 р. 216, 1877.
Неітігоііх. без. АЪІіапаі. 2 р. 968, 1883; Вегі. Вег. 1882 р. 23.
448
Приложенія термодинамики.
Оикет. Ье роіепііеі іііегтосіупатідие. Рагіе. 1886.
ОіЪЪз. См. къ § 1.
Ріапск. Г)І88. МйпсЪеп, 1879; \Ѵ. А. 19 р. 358, 1883; 30 р. 562, 1887; 31 р. 189,
1887; 32 р. 462, 1887; 46 р. 162, 1892; 2І8сЬг. 1. рЪуя. Сііет. 8 р. 647, 1891; Тііегтосіу-
патік. Ьеіргі^, 1897.
Умовъ. Ж. Ф. X. О. 21 р. 103, 1889; Виіі. сіе Іа 8ос. Ітрег. сіев Хаіигаі. де Моесои,
1894, № 1 и 2.
Шиллеръ. О. Ф. Н. О. Л. Е. 7 вып. 1 р. 22, 1894.
Пальчиковъ. Матеріалы къ вопросу о приложеніи термодинамическаго потен-
ціала. Одесса 1896.
Паіапзоп. \Ѵ. А. 42 р. 178, 1891; ХІ8(?йг. 1. рііуб. Сііет. 10 р. 733, 1892.
Голицынъ. Изв. Импер. Акад. Наукъ. 1894 № 4 стр. 387.
Г ѵоп Ьааг. йесіів Ѵогіга&е йЪег сіав НіегтодупатіясЬе Роіепііаі, 1906.
Къ § 19.
Воі/гтапп. ЛѴіеп. Вег. 53 р. 195, 1866; 63 р. 712, 1871; 76 р. 373, 1877; 78 р. 7,
1878; Ро^. Апп. 145 р. 211, 1872.
Сіаизіиз. Ро^. Апп. 141 р. 124, 1870; 142 р. 433, 1871; 144 р. 265, 1871; 146
р. 585, 1872.
$2ІІу. Ро§&. Апп. 145 р. 295, 1872; Ег^ЬсІ. 7 р. 74, 1876; 160 р. 435, 1877.
ЬозсИтісІі. ЛѴіеп. Вег. 59, II р. 395. 1869.
В. Михельсонъ. Простѣйшій выводъ второго закона термодинамики изъ началъ
аналитической механики. Москва, 1886; Матем. Сборникъ 13.
Рескпа§;еІ. Ро^. Апп. Ег&ЬсІ 6 р. 275, 1874.
ОррепИеіт. \Ѵ. А. 15 р. 495, 1882.
Г Е Мйііег. Ро&&. Апп. 152 р. 105, 1874.
ЬеЛіеи. С. К. 78 р. 221, 309, 1874.
Еіпзіеіп. В. А. 9 р. 417, 1902; 11 р. 170, 1903.
Неіткоііх. Вегі. Вег. 1884 р. 159, 318, 758; Сгеііе’б Эоигп. 97 р. 111, 317, 1884;
Сее. АЪЬ. III р. 119, 205.
А ѵ. ОеШп^еп. Мёт. Зе ГАсасІ. бее 8с. Зе 8і. РёіегеЪ. (7) 32 № 17, 1885.
ГЛАВА ДЕВЯТАЯ.
Приложенія термодинамики къ явленіямъ, нами уже
разсмотрѣннымъ.
§ 1. Идеальные газы. Ко многимъ вопросамъ, которые были раз-
смотрѣны въ т. I и въ предыдущихъ главахъ этого тома, могутъ быть
приложены формулы, выведенныя въ главѣ ЛТП. Такими приложеніями
мы теперь и займемся, оставляя однако вопросъ о приложеніи термоди-
намики къ явленіямъ, наблюдаемымъ въ растворахъ, до послѣдней главы
этого тома. Обращаемся, прежде всего, къ идеальнымъ газамъ;
выпишемъ нѣкоторыя изъ формулъ, которыя были выведены въ преды-
дущей главѣ. Мы имѣли:
(58.^) стр. 428. . . . ^Сѵ = АТ д ?........................
дѵ ді2
(59,е) стр. 429. . . . ^Ср — — АТ & .................(I,#)
др ді2
Идеальные газы.
449
ідІД л^др . . = — Ар . ... . (1,0
стр. 430. . . \ дѵ]і ді ІдІД КД = сѵ.......... \ ді] ІдІЛ л^дѵ л дѵ . - =—ЛГ — Ар . . . (1,0
(61,е) стр. 430 . . . \ ор)ѵ ді др (дІД л дѵ • \^\-Ср-Ар-^ (1,/) \ ді ]р ді
Мы въ дальнѣйшемъ будемъ имѣть дѣло съ тремя свойствами
идеальныхъ газовъ, которыя сперва укажемъ отдѣльно, а затѣмъ займемся
важнымъ вопросомъ объ ихъ взаимной связи. Эти три свойства суть:
1. Законъ Бойля-Маріотта, гласящій, что для даннаго ко-
личества даннаго газа рѵ = Сопві, если і = Сопзі. Эта формула даетъ
дР=-Р.............(2,а)
дѵ ѵ
2. Законъ Гей-Люссака, по которому всѣ газы имѣютъ одинъ
1
а = —
273
1
а = — .
273
ѵ
~~ Т
и тотъ же коеффиціентъ теплового расширенія
отъ состоянія газа; итакъ ѵ - ѵ0 (1 + аі), гдѣ
дѵ аѵ ѵ
— — аѵ0 =-----------= -
ді 1 + аі і -|- 1
даетъ
не зависящій
Эта формула
• • (2,0
(1, 6) указываетъ, что
Тогда
(2,с)
т. наз.
а
1 д2ѵ
гдѣ 7 = Д- — абсолютная температура. Далѣе имѣемъ — = 0.
*> = 0.....................
др
Теплоемкость ср не зависитъ отъ давленія р. Это
д2ѵ
законъ Ее^паиіі. Понятно, что и обратно (2,с) даетъ — 0, от-
куда ѵ = аТ + Ь. Допуская ѵ = 0 при Т — 0, получаемъ (2,6).
3. Законъ Яоиіе’я: энергія 1} идеальнаго газа есть
функція одной только темпе р ату ры, т.-е.
^ = /(0.......................(3)
Опыты, подтвержадающіе вѣрность этого закона, хотя бы въ тѣхъ
предѣлахъ, въ которыхъ справедливы первые два закона, будутъ разсмо-
трѣны ниже; теперь же укажемъ на слѣдствія, вытекающія изъ фор-
мулы (3). Эта формула показываетъ, что энергія остается постоянною,
когда объемъ или упругость мѣняются при постоянной температурѣ. Это
означаетъ, что притекающая теплота тратится только на нагрѣваніе и на
внѣшнюю работу. Поэтому законъ Л о и 1 е’я говоритъ, что въ идеаль-
ныхъ газахъ внутренняя работа равна нулю. Обратимся къ
формуламъ; изъ (3) слѣдуетъ, что
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. ІП, изд. 3-е.
29
450
Приложенія термодинамики.
Іди\_іди\_ іди\ (МЛ = ди
Д \др )(~ ’ у діД, у діІр ді
Формулы (1,сД/) даютъ, если написать д\(і) вмѣсто /'(і),
7'^=Р........................................................М
сѵ = УЯО............................(3,6)
. дѵ ,
ср сѵ — Ар .......................(3,с)
(3,6) показываетъ, что теплоемкость сѵ есть функція одной
температуры. Формула (3,а) даетъ
др -^ = 0
Р Т
откуда р = СІ\ гдѣ С можетъ зависѣть только отъ объема, такъ что мы
получаемъ
р = Т'іріѵ)
Изъ закона Л о и 1 е’я слѣдуетъ, что при постоянномъ объ-
емѣ давленіе газа растетъ пропорціонально абсолют-
ной температурѣ, т.-е. что
р = ро (1 -|- аі)............(3,е)
Мы предположили, что I}—/(і) и вывели сѵ = дд(/) и р =Ро (1 + «О;
легко показать, что три закона, которые выражаются этими формулами,
тождественны, ибо каждая изъ трехъ формулъ приводитъ къ остальнымъ
Двумъ.
д2р
етъ
ді2
имѣемъ
Дѣйствительно, положимъ, что дано сѵ = Фі(/). Тогда (1,а) да-
= 0, т.-е. р — а Т Ь. Но допуская, что р = 0 при Т — О,
др
6 = 0 и слѣд. р = аТ, или р =Ро (1 4- аі), Далѣе имѣемъ = а,
= 0. Наконецъ (1,^), которое на основаніи тож-
слѣд. (1,с) даетъ
дества (27) стр. 383 можно написать въ видѣ
/дѴ\ ___ дѵ Iлт др . \ ______ дѵ (дЦ\
у др Д др ( ді др ( дѵ ц ’
/д^\ Л • Ач *
даетъ I < | =0. Энергія есть функція только температуры.
\ &Р/і
Если считать даннымъ равенство р = ро (1 4" или р = аТ, то
тѣ же формулы (1,а), (1,с) и (1,ё) даютъ сѵ = ср-^і} и V = /(0.
Разсмотрѣвъ три закона Бойля-Маріот та, Гей-Люссака и
о и 1 е’я, мы теперь докажемъ, что каждый изъ этихъ трехъ
законовъ есть необходимое слѣдствіе двухъ дру-
гихъ. Для доказательства напишемъ формулы (2,а), (2,6) и (3,я) въ видѣ
др _________________ р дѵ __________ ѵ^^ ді Т
дѵ ѵ " ді Т ' др р '
Идеальные газы. 45 Г
Перемноживъ эти три формулы, мы получаемъ
др дѵ ді ___ і
дѵ ’ ді др ’
т.-е. тождество (27) стр. 383. Отсюда и вытекаетъ, что если какое-либо
вещество слѣдуетъ двумъ изъ трехъ законовъ, то оно слѣдуетъ и третьему.
Это доказательство принадлежитъ В а к к е г’у. Интересно однако раз-
смотрѣть ближе, къ какимъ еще слѣдствіямъ приводитъ допущеніе о вѣр-
ности какихъ-либо двухъ изъ этихъ трехъ законовъ.
А) Законы Бойль-Маріотта и Гей-Люссака. Они даютъ
рѵ = ... ...........(4,а)
Отсюда
дР _ # _ Р . дѵ _ $ _ . дР_ _ _Р_ и
ді ѵ Т ' ді р Т ' дѵ ѵ ’ ’ ’
Формулы (1,с) и (1,е) даютъ I/ = /(/); затѣмъ (1,е) даетъ сѵ = дг(і).
дѵ
Изъ и (1,/) получается ср - - Ар = сѵ, т.-е.
ср — сѵ = АК ....... . (4,с)
Это знакомая намъ формула (т. I). Но мы нашли сѵ = (рі(і); та-
кимъ образомъ получается еще
сР = 7^(0...................
В) Законы Бойль -Маріотта и Л о и 1 е’я. Первый даетърѵ =
— второй р — Тір(ѵ): отсюда
ѵТір(ѵ) = /1(Т).
Это возможно только, когда ѵ^(ѵ) — /і(Г) = /?, гдѣ /? посто-
янное число. Тогда обѣ формулы даютъ рѵ — ЦТ т.-е. законъ Гей-
Люссака, а слѣд. и формулу (4,б/).
С) Законы Гей-Люссака и Л о и 1 е’я. Первый даетъ ѵ =
= Тсо(р), второй р= Тц)(ѵ). Раздѣливъ одно равенство на другое, получаемъ
рсо(р) = ѵЩѵ); это показываетъ, что рс*Ар) = ѵгр(ѵ) — Ц, откуда опять
получается рѵ = ЦТ, т.-е. законъ Бойль-Маріотта, а затѣмъ и (4//).
Весьма важно замѣтить, что связь между тремя зако-
нами обнаруживается только на основаніи вто-
рого начала.
Любопытно, что всѣ три закона могутъ быть получены, какъ слѣд-
ствіе допущенія, что теплоемкости сѵ и ср суть функціи только темпера-
туры. Предоставляемъ читателю сдѣлать этотъ выводъ на основаніи
формулъ (1,а) и (1,й).
Полагая II = /(і\ мы имѣемъ :
29*
452
Приложенія термодинамики.
аи
аі ~
аи = сѵаі
($)
Обыкновенно допускаютъ, что для идеальныхъ газовъ теплоем-
кости сѵ и ср отъ і также не зависятъ, т.-е. что онѣ величины постоян-
ныя Тогда и—сѵТ-\-Ь\ полагая, что и = 0 при Г = О, получаемъ
и=сѵТ.......................(6)
Этою формулою мы пользовались въ т. I, разбирая вопросъ о вну-
тренней энергіи газа.
Опытныя изслѣдованія, относящіяся къ законамъ Бойля -Марі-
отта и Гей-Люссака, были разсмотрѣны въ т. I и въ т. [II.
Обратимся къ опытамъ, изъ которыхъ было выведено, что энергія га-
зовъ зависитъ только отъ температуры, или, что при расширеніи газа
Рис. 128.
внутренняя работа равна нулю, вслѣдствіе чего температура газа не
мѣняется, или онъ расширяется, не производя работы. Первыя из-
слѣдованія въ этомъ направленіи были произведены 3 о и 1 е’емъ. На
стр. 373 былъ изображенъ приборъ, которымъ Л о и 1 е пользовался
для опредѣленія механическаго эквивалента Е теплоты. Воздухъ нака-
чивался въ сосудъ С, помѣщенный въ калориметръ, причемъ сравнивалась
работа сжатія газа съ нагрѣваніемъ калориметра. Л о и 1 е произвелъ
кромѣ описанныхъ раньше, еще слѣдующіе опыты. Два металлическіе
сосуда /?' и фис., 127), соединенные трубками съ кранами И и Л".
помѣщены въ общій калориметръ СС. Въ одномъ сосудѣ воздухъ сжатъ
до 22 атмосферъ, въ другомъ по возможности разрѣженъ. Когда краны И
и И" были открыты, воздухъ расширялся, не производя работы; при
этомъ температура калориметра оставалась безъ замѣтнаго измѣненія,
откуда Лоиіе и заключилъ, что внутренняя работа расширенія газа
равна нулю. Въ другомъ опытѣ 3 о и 1 е помѣстилъ сосуды 7?' и въ
двухъ различныхъ калориметрахъ (рис. 128). Оказалось, что въ одномъ
изъ нихъ происходила такая же потеря теплоты, какая въ другомъ замѣ-
чалась прибыль. Въ первомъ сосудѣ газъ, расширяясь, производитъ ра-
боту, результатомъ которой является живая сила движенія газа въ сое-
Идеальные газы.
453
динительной трубкѣ. Во второмъ производится сжатіе уже перешедшаго
Рис. 129.
газа; живая сила переходящаго газа уничтожается, переходя въ теплоту.
Эти опыты Лопіе’я повторилъ впослѣдствіи Ве^папіі.
Нігп произвелъ опытъ съ приборомъ, изображеннымъ на рис. 129.
Трубка раздѣлена перегородкою, которая легко разбивалась шарикомъ к,
на двѣ части Л и В. Сперва
давленіе въ Л и В равно
1 атм., такъ что при откры-
томъ кранѣ И манометръ т
остается въ нормальномъ
положеніи, изображенномъ
на рисункѣ. Закрывъ кранъ
А, Нігп перегонялъ воз-
духъ, напр. изъ А въВ, такъ что въ В давленіе дѣлалось равнымъ атм.,
а въ Л равнымъ * атм. Затѣмъ онъ раздроблялъ стѣнку Ь, и тотчасъ
же открывалъ кранъ А. Манометръ оставался въ покоѣ, слѣд. измѣненіе
объема воздуха не сопровождалось замѣтнымъ измѣненіемъ его температуры.
%
в
_____
ъ
А
Допуская справедливость трехъ законовъ, разсмотрѣнныхъ выше, мы
имѣемъ основныя уравненія для идеальныхъ газовъ: рѵ — НТ и (І1}=сѵ(іі.
Вставляя второе выраженіе въ формулу б/С? = (11} + Арсіѵ, получаемъ
б/С? = сѵМ -|- Арйѵ............................................(7)
Сравнивая эту формулу съ г/С? = сѵсіі -|- асіѵ, см. (40,6) стр. 402, по-
лучаемъ для идеальныхъ газовъ
а = Ар....................., . . (7,я)
Тотъ же результатъ даетъ общая формула (58,с), если вставить =
р дѵ
— см. (4,6). Мы имѣли далѣе общую формулу ср— сѵ = а см. (41,6)
стр. 103; вставляя а = Ар и . получаемъ
Ср — сѵ — ......................
Эту же формулу получимъ, вводя въ (7), вмѣсто ѵ и Л новыя пере-
мѣнныя р и і. Тогда
, Оѵ , . дѵ ,, ѵ , । %,
(іѵ = -у— (ір + уу (іі =---(ір -4------(ІІ.
др ді р р
Вставляя (іѵ въ (7), получаемъ
б/С) = (сѵ + Л/?) (іі — Аѵйр....................(7 ,с)
Но при р = СопзС, т.-е. ф = 0, имѣемъ йО = ср(іі, слѣд. сѵ + Л/? =
= ср откуда и получается (7,6). Формула (7,с) даетъ
</(2 = ср(іі — Аѵйр......................(7,4/)
454
Приложенія термодинамики
Чтобы въ (7) вмѣсто ѵ и і ввести ѵ и /?, слѣдуетъ подставить
„ & л і , Р \ ѵ
ді — -• - дѵ 4- -<г- ар = Ѵг дѵ 4- -к Ф-
дѵ др Р /?
Если воспользоваться еще- формулою (7,/>) то получается
ѵдр + рдѵ ....................(8,а)
(7) и (7,б/) удобнѣе написать такъ* чтобы входили только двѣ перемѣн-
ныя величины. Равенство рѵ ЕТ даетъ
(Кі = сѵ(іі-^АЦТ~ . . (8,0
сК} = срсіі — АГІТ -р..................(8,с)
Если въ три послѣднія формулы подставить вмѣсто /? его значеніе
изъ' (7,й), то получается :
(К)=
Ср сѵ
Асѵ
_г Р<*ѵ + г~^г ѵЛр , . . . (9,«)
Ср сѵ
(1$ — сѵ(іі + <ср — сѵ) т —....... (»,Ь)
<К = ср(1і — (ср — Т ......................(9,0
Величины Ср и сѵ будемъ считать за постоянныя.
Чтобы нагрѣть газъ при постоянномъ объемѣ отъ і^ до /2°?
требуется количество теплоты = сѵ(і2— /Д а при постоянномъ давле-
ніи — количество (^ = ср (і2 — /г); внѣшняя работа г во второмъ слу-
чаѣ равна г = р(ѵ2 — = /?(/2 -г- /Д и на нее тратится количество
теплоты, равное Л/?(/2 — /Д
Изотермическое расширеніе газа мы уже разсматривали неод-
нократно ; оно опредѣляется равенствомъ б/(^ = Ардѵ = АЕТ^Ѵ . Отсюда
ѵ
<2 = АКП%^ = АКП$Р1 .
Формулы, относящіяся къ адіабатическимъ измѣненіямъ со-
стоянія, были выведены въ т. I. Онѣ легко получаются изъ (9,я, Ь, с),
если положить — 0, и ввести величину ср : сѵ^= к,; тогда получа-
ются уравненія
» дТ , др . дѵ , дѵ
= {к — 1) — — 0, - і) г = о, к------р и = 0.
' ѵ 7 Г ' р ' ѵ р
Идеальные газы.
155
Интегрируя, получаемъ уже знакомыя намь формулы
рѵк — Сопеі.
Тѵк~л = Соп8І.
Тк : рк~1 = Соп8і.
(10)
раѵ =
Работа г адіабатическаго расширенія равна
V V
к I _ Ро^о
і к - - 1
V
^0
Убыль энергіи газа равна Дг, ибо вся работа совершается на счетъ
энергіи газа. Та же формула даетъ работу сжатія газа отъ объема ѵ до ѵ$.
Предлагаемъ читателю сравнить измѣненіе упругости газа и затра-
ченную работу при одинаковыхъ изотермическомъ и адіабатическомъ
уменьшеніяхъ объема.
Энтропія газа получается изъ формулы (18 = С~ . причемъ ^<2
должно относиться къ обратимому процессу. Формулы (8,а, 6, с) даютъ,
если въ первую вмѣсто ѵ и р подставить ихъ значенія изъ равенства
рѵ = $Т.
СІр (ІѴ
аі> — сѴр - ср —
Л8 = сѵ~АЦ^
аз=срСІІ1, - л^ар
р Т р
. . (11)
Отсюда уже легко получается, если считать сѵ и ср постоянными,
5 = Сі + сѵ\%р + ср1§ѵ
3 = С2 + еѵ1ёТ-І-АЯІёѵ
5 = С3 + ср}ёТ — АП\%р
(12)
гдѣ Сь С2 и С3 постоянныя, причемъ напр. =- 50 — 5
аналогичныя выраженія получаются для С2 и С3.
Если газъ нагрѣвается при постоянномъ объемѣ, то его энтропія
растетъ на величину
5 - 50 = ~................... (12,а)
7 о
Если нагрѣваніе происходитъ при постоянномъ давленіи, то
имѣемъ: т
8-8„ = ср\^ т..........................(12.&)
При изотермическомъ расширеніи энтропія увеличива-
ется на величину
456
Приложенія термодинамики.
5 — 50 = Л/?!§• - = (<?„ — сѵ)\% .... (12,0
Ѵ0 И)
Если въ (12)
писать въ видѣ
вставить АР = ср — сѵ и ср
5 = Сі + сѵ\%(рѵк}
5 = а + сѵ\ё(Тѵк~1)
('гк \
рк—1)
: сѵ — к, то 5 можно на-
.................(13)
(10) показываетъ, что адіабатическія измѣненія суть въ то же время
изентропическія, если процессъ обратимый. Для необратимыхъ
л \ (ІС^ тт
процессовъ имѣемъ аѣ > . Положимъ напр., что газъ расширяется
въ пустоту, какъ въ опытѣ Яопіе’я (стр. 452). Такой процессъ не-
обратимый адіабатическій, но не изентропическій. Температура газа не
мѣняется, а потому мы найдемъ измѣненіе энтропіи, замѣняя этотъ
процессъ обратимымъ изотермическимъ процессомъ (см. стр. 432). Отсюда
слѣдуетъ, что хотя сЩ = 0, энтропія всетаки растетъ, и притомъ на ве-
личину, опредѣляемую формулою (12,г).
Свободная энергія Р газа и его термодинамическій
потенціалъ Ф опредѣляются изъ формулъ Р= 1}—Т8 иФ = {7—Г5 +
-)-Арѵ. Энергію напишемъ въ видѣ 17 = 17^-\-сѵ(Т—Т^)=Ѵ^сѵТ,
гдѣ V = С70— сѵТ0. Величину 5 возьмемъ изъ (12), написавъ С вмѣсто С2,
т.-е. 5 = С -|- сѵ\^Т 4- АР\^ѵ. Вставляя 1} и 5, получаемъ :
Р=(У— ТС)±сѵТ(1— І$Т) — АРТ1ёѵ .... (14)
ф = (Г—ГС) + ^Г(1—1^Г) + Л/?Г(1—1^). . . (14,бг)
Величина Р обратно пропорціональна плотности газа (т. 1).
Формула (14) даетъ
(ІР — — (С + сѵ\^Т 4~ АР\$ѵ)(іТ — Арсіѵ . . (14,6)
Отсюда ясно, что при изотермическомъ (сІТ = 0) расширеніи
газа вся работа производится насчетъ свободной энергіи Т7, которая не-
прерывно убываетъ, хотя вся энергія 17 остается постоянною. Вся при-
текающая теплота переходитъ въ энергію несвободную О. Когда ѵ сдѣ-
лается весьма велико (газъ очень разрѣженъ), то Р приближается къ
нулю; газъ теряетъ способность производить работу, хотя его энергія 17
осталась прежняя. Все это вполнѣ согласно съ тѣмъ, что было ска-
зано на стр. 441.
Изъ второй формулы (12) слѣдуетъ, что при изотермическомъ рас-
ширеніи газа его энтропія увеличивается. Отсюда вновь слѣ-
дуетъ, что если газъ расширяется въ пустоту, то это процессъ не-
обратимый.
Идеальные газы.
457
Разсмотримъ весьма интересный вопросъ о взаимной диф-
фузіи газовъ.
СііЬЬб доказалъ (см. Ріапск, Тйетіодупапіік, 3-ье изд. 1911
р. 214; русскій переводъ, Спб. 1900, стр. 186), что энтропія смѣси нѣ-
сколькихъ газовъ равна суммѣ энтропій отдѣльныхъ газовъ, занимающихъ
каждый весь объемъ ѵ смѣси. Отсюда слѣдуетъ, что взаимная
диффузія двухъ разнородныхъ газовъ (находящихся при оди-
наковомъ давленіи), причемъ ихъ объемы ѵх и ѵ2 увеличиваются до об-
щаго объема ѵ = + т?2, есть процессъ необратимый, ибо онъ со*
провождается увеличеніемъ энтропіи. Дѣйствительно, при диффузіи каж-
дый изъ газовъ расширяется изотермически, не входя ни въ какія тер-
мическія или механическія (работа) связи съ другими тѣлами, а потому
его энтропія увеличивается, откуда и слѣдуетъ, что энтропія смѣси, по-
лучаемой послѣ диффузіи, больше суммы энтропій газовъ до диффузіи.
Вычислимъ измѣненіе энтропіи, происходящее при взаимной
диффузіи газовъ. Положимъ, что мы имѣемъ произвольное число раз-
личныхъ газовъ, которые всѣ находятся при температурѣ Т и подъ да-
вленіемъ р\ обозначимъ черезъ щ число граммъ-молекулъ (т. I)
/-того газа и черезъ 5/ его энтропію до смѣшенія. Третья формула (12)
даетъ, если вмѣсто написать С[ и черезъ пі} обозначить молекуляр-
ный вѣсъ /-того газа:
= пі \тІСр\%Т — А^т^р .
Произведеніе А^пі} = Н не зависитъ отъ рода газа. Обозначивъ
еще теплоемкость при постоянномъ давленіи граммъ-молекулы
газа пііср черезъ получаемъ
5,- = пі Т — Н\^р + Ц .
Отсюда получается первоначальное значеніе 50 энтропіи всѣхъ га-
зовъ до ихъ смѣшенія
5о + ............(15)
Послѣ смѣшенія /-тый газъ будетъ находиться подъ парціаль-
нымъ давленіемъ рИ^ гдѣ Л/ = ^ : 2 пЬ 11 потому энтропія 5 смѣси будетъ
5 =2^/^/,^?П"“^1&(М/) + г/|..........................(15/0
Вычитая (15) изъ (15,а), получаемъ
5—50 = — Лг2/2Д§Л.............................(15,/?)
Всѣ суть правильныя дроби и потому 5 > 50, т.-е. энтропія при
смѣшеніи газовъ дѣйствительно возросла. Формула (15./?), очевидно мо-
жетъ относиться только къ случаю смѣшенія газовъ химически не-
однородныхъ. ибо для химически одинаковыхъ газовъ мы должны
имѣть 5 = 50. Такимъ образомъ увеличеніе энтропіи при диф-
458
Приложенія термодинамики.
фузіи есть признакъ химической неоднородности.
Это увеличеніе вовсе не зависитъ отъ рода газовъ, если только эти газы
химически неоднородны, напр. пары двухъ химически весьма близкихъ
другъ другу металловъ. Отсюда Ріапск остроумно заключаетъ, что
«химическая разница» двухъ газовъ не можетъ быть
представлена, какъ величина, непрерывно мѣняю-
щаяся и доходящая до нуля. Это величина разрывная, между
тѣмъ какъ «физическія разницы различныхъ тѣлъ всегда могутъ быть
представляемы, какъ величины, мѣняющіяся непрерывно ш.до нуля. Въ
этомъ заключается глубокое отличіе между физиче-
скими и химическими свойствами вещества.
§ 2. Реальные газы* Свойства газовъ, встрѣчаемыхъ въ природѣ,
отличаются отъ свойствъ идеальныхъ газовъ. Реальные газы не слѣду-
ютъ строго закону Бойль-Маріотта; отступленія ютъ него были
разсмотрѣны нами въ т. I. Мы видѣли, что формула рѵ = РТ была за-
мѣняема другими, а именно напр. формулами
Ке^папіі. . і ф- В — Лф-с(-°------------1
рѵ 1 I ѵ ) I ѵ
Ѵап Дер АѴааІз’а . . ф- — .
т , р 1 а
Сіаизіиза . . . =----г —
(16, а)
(ЗД
(16,с)
Дальнѣйшія формулы будутъ приведены въ 13-ой главѣ.
Въ т. III мы разсмотрѣли вопросъ объ отступленіяхъ газовъ отъ
закона Гей-Люссака. Въ немъ было показано, какихъ отступле-
Рис. 130.
А'
Р<
Р
ній слѣдуетъ ожидать на основаніи формулы Ѵап-сіег-
АѴааІз’а и были изложены опыты, подтвердившіе существо-
ваніе этихъ отступленій. Теперь намъ остается разсмотрѣть
классическіе опыты <1 о и 1 е’я и \Ѵ. Т Ь о т 8 о п’а (Ь о г (1
Кеіѵіп), показавшіе, что реальные газы не слѣдуютъ законѵ
Йо піе’я, что въ нихъ внутренняя работа не равна нулю, и что
они, слѣдовательно, обладаютъ не только кинетическою, но и
потенціальною энергіей. Чтобы понять идею этихъ опытовъ,
обратимся къ рис. 130. Длинная труба, поддерживаемая при
постоянной температурѣ, содержитъ перегородку съ малымъ от-
верстіемъ О. Газъ, находящійся при первоначальномъ давле-
ніи ръ притекаетъ со стороны ВВ и, пройдя черезъ отвер-
стіе О, расширяется, причемъ его давленіе дѣлается равнымъ
Ро < Рі- Положимъ, что мы въ А А еще имѣемъ давленіе рг.
а въ А'А' уже установилось давленіе р0, и пусть пі масса газа,
постоянно находящаяся между АА и АгАг, Такая же масса
занимаетъ объемъ = ВВАА, когда она вся находится при
давленіи ръ и объемъ = Л'Л'5'5', когда ея давленіе р^.
Газъ, занимающій въ нѣкоторый моментъ объемъ ВВА'А', зай-
Реальные газы.
459
метъ черезъ малый промежутокъ времени объемъ ААВ'В1. Работа
внѣшнихъ силъ при разсматриваемомъ перемѣщеніи равна АаХ
\АВ—р^'ХА'В^ гдѣ о площадь поперечнаго сѣченія трубы. Очевидно,
что ^У^ВА = ѵъ = такѣ что эта работа равна рхѵх - р^ѵ^
т.-е. она равнялась бы нулю, еслибы тазъ строго слѣдовалъ закону Бойль-
Маріотта. Газъ, расширяясь, тратитъ часть своей энергіи на произ-
водство внутренней работы* вслѣдствіе этого энергія 17 измѣняется на
нѣкоторую величину ЛС7 и температура газа понижается на 0°, если вну-
тренняя работа въ газѣ больше работы внѣшнихъ силъ. Если мы при-
мемъ іиассу газа т = 1, то охлажденіе газа соотвѣтствуетъ потерѣ коли-
чества теплоты, равной срѲ, и мы имѣемъ, очевидно.
ли= - срѲ I- А (р^ - роѴо)
(17)
т^е. измѣненіе энергіи равно замѣченной потерѣ тепла, сложенной съ те-
пловымъ эквивалентомъ работы внѣшнихъ силъ. Для идеальныхъ газовъ
Рі^і — Роѵо ‘ и внутренней работы нѣтъ; слѣдова-
тельно, Лі7=0 и # = 0. Опыты йопіе’я и Тііот-
8оп а показали, что Ѳ не нуль, что газъ охлаж-
дается и что при его расширеніи часть энергіи
тратится на внутреннюю работу, такъ что Л17 < 0.
Приборъ, которымъ пользовались Л о и I е и
Тйот8оп, изображенъ на рис. 131; въ немъ от-
верстіе въ перегородкѣ замѣнено пористой пробкою
изъ ваты или шелка, помѣщенной между двумя ме-
таллическими- сѣтками 5 и Трубка окружена бо-
лѣе широкой цинковой трубкой гг. заполненной ва-
той: весь приборъ окруженъ до уровня 55 водой.
Верхняя часть трубки стеклянная, черезъ ея стѣнку
наблюдаются показанія чувствительнаго термометра/.
Давленія рх и р0 указывались особенными мано-
Рис. 131.
метрами.
Опыты показали, что У пропорціонально разности (рх — р^), такъ
что можно положить
(9==^(А—Ро).......................(18)
гдѣ множитель /?, различный для различныхъ газовъ, указываетъ на по-
ниженіе температуры, когда давленіе мѣняется на 1 атм. Значеніе Д
оказалось (около 17°) для воздуха равнымъ 0°,262, для СО2 равнымъ 1°,225.
Для водорода было получено нагрѣваніе при расширеніи, т.-е./?< 0.
Далѣе оказалось, что ,9 обратно пропорціонально Г2, такъ что можно
положить
Для воздуха. л = 0,267.(273)2, для углекислоты п = 1,391 .(273)2.
460
Приложенія термодинамики.
Такимъ образомъ п равняется значенію /? при 0° или при Г0 = 273°.
Мы разсмотримъ теперь опыты, произведенные для опредѣленія вели-
чины Д послѣ Яоиіе’я и ТЬотвоп’а. Особенно интересенъ вопросъ
о зависимости величины отъ начальнаго давленія р. Первые опыты
Е. Каіапвоп’а (1887) съ СО2 при 20° привели къ заключенію, что д
медленно возрастаетъ съ увеличеніемъ давленія р по формулѣ
= 1,18° + 0.0126 р.
Къ противоположному результату пришелъ Кевіег (1905), кото-
рый также изслѣдовалъ СО2, измѣняя р въ предѣлахъ отъ 5 до 40 атмо-
сферъ; температуры онъ измѣрялъ термоэлектрическимъ путемъ. Онъ
нашелъ, что
/7 = 1,19° — 0,0015р,
т.-е. что охлажденіе убываетъ при возрастаніи давленія. Въ 1904 году
появились три работы— Е. Ѵо^еРя, Вгадіеу и Наіе’я и Віні^е’а.
Е. Ѵо е 1 изслѣдовалъ воздухъ приблизительно при 12°; давленіе
онъ выражалъ въ килограммахъ на квадр. сантиметръ. Мы будемъ въ
этомъ случаѣ обозначать давленіе чрезъ р\ а охлажденіе при измѣне-
ніи р' на единицу - чрезъ /?'. Ѵо^еі измѣнялъ давленіе р‘ отъ 1,08
до 153,0; при этомъ уменьшалось отъ 0,264° до 0,135°, такъ что
можно положивъ
Д' = 0,280° — 0,000932 р'.
Вгасііеу и Наіе изслѣдовали воздухъ при давленіяхър между 68
и 204 атм. и при температурахъ между -|-20° и —120°. Они нашли,
что /?, какъ функція р и Т, выражается лишь весьма запутанными фор-
мулами, которыя мы здѣсь не приводимъ. Мы ниже укажемъ только
на родъ зависимости /? отъ Т. Но предварительно разсмотримъ слѣд-
ствія, которыя могутъ быть получены термодинамическимъ путемъ изъ
формулы (17).
Выраженіе (17) можно написать въ видѣ
— срѲ = ли + А (роѵо — РіѴі)
(19, а}
Предположимъ, что измѣненіе давленія безконечно малое;
вмѣсто 0
йѲ , . ч
напишемъ ^ар, причемъ (19) даетъ
п
Т2
(20)
Далѣе имѣемъ АІ} = йр \ А^р^ѵ^ — рл) = Ай (рѵ) = Ар йр 4-
-[-Аѵйр. Такимъ образомъ, сокративъ еще на б/р, получаемъ вмѣсто (19* я)
06/ ді} у л дѵ . л .
— сп а = а ІАРа + Аѵ.........................(20,бі)
Р др др др
п ді} ,, ѵ . ді} - .
Сюда можно подставить ; при йі = 0 мы имѣемъ аЦ + ар -4-
Реальные газы.
161
дѵ
-4- Ар ' др. Съ другой стороны при ді = 0, см. формулу (60,а) стр. 429.
Р дѵ дід . дѵ лгдѵ
д(^— АТ д^др-, слѣдовательно -]-Лр =—АІ . Такимъ обра-
зомъ (20,а) принимаетъ видъ
СР др ~АІ ді л
Это весьма важное уравненіе было впервые выведено Т й о ш з о п’омъ.
Для идеальныхъ газовъ {рѵ — ПТ) правая сторона равна нулю,
тд
Если вмѣсто .
то получается
(21)
подставить эмпирически найденное выраженіе (19),
л дѵ л п
АТ ді Аѵ — ср
(22)
б//
Помножая обѣ стороны на мы получаемъ два полные дифференці-
ѵ
ала (слѣва дифференціалъ отъ А ; интегрируя, мы считаемъ ср постоян-
нымъ, что въ добавочномъ членѣ во всякомъ случаѣ допустимо. Получается:
V псп
— — - р 4- н
Т ЗАТ*^
Постоянную Н можно опредѣлить, допуская, что при очень боль-
V Р
шомъ Т газъ пріобрѣтаетъ свойства идеальнаго газа, для котораго -у = .
Пренебрегая при очень большомъ Т первымъ членомъ справа, находимъ
„ Я
п= — \ это даетъ уравненіе состоянія реальнаго газа на
основаніи опытовъ Л о и 1 е’я и Т Ь о ш 8 о п’а:
Р
(23)
ПС„
= з/~ 75
Н. Н. Шиллеръ далъ болѣе общее рѣшеніе уравненія (22), при-
нимая ср за функцію отъ Т и р. Онъ находитъ для ср общее рѣшеніе вида
Ср = ТЩТ* - *ПР),
гдѣ Р знакъ произвольной функціи.
дс (Рѵ
Пользуясь уравненіемъ ' см‘ СТ^' МЫ п0"
думаемъ изъ (23) уравненіе
дсѵ 2сѵп
др = ’
откуда
+ Сопві.
462
Приложенія термодинамики.
Если р весьма мало, то ср навѣрное отъ Т не зависитъ и равно
нѣкоторому отсюда получается легко
і і । Р
И- 2лг .
Наблюденія 4 6 и 1 е’я и Т 11 о т 8 о п’а даютъ возможность вычис-
лить отношеніе х внутренней работы ко внѣшней при изотермическомъ
расширеніи газа. Формулы (17) и (18) даютъ
467 = — ср$ — р^ — А (роѵо — руѵ^.
Эта потеря энергіи эквивалентна внутренней работѣ, между тѣмъ
какъ внѣшняя работа эквивалентна АрДѵ, если расширеніе весьма мало.
Формула В е § п а и 1 і (16,а) даетъ, если ограничиться однимъ доба-
вочнымъ членомъ,
Р№ _ х , в -~^і
' РіѴг
откуда /?о^о ” Ріѵі ~ ВРі (^о —‘ ^і), такъ чт0
467 = — Ср^ру — ро) — АВ (ѵ0 — ^).
Вычисленіе показываетъ, что отношеніе х внутренней работы къ
внѣшней при изотермическомъ расширеніи имѣетъ слѣдующія значенія,
если газъ расширяется отъ давленія, немного превышающаго атмосфер-
ное, до атмосфернаго
Воздухъ СО2
1 1
Х ~ 500 125
Эги числа быстро возрастаютъ, если начальная упругость рА значи-
тельно больше одной атмосферы, а р0 = 1 атмосф.
Наблюденія Яопіе’я и Тйотзоп’а хорошо согласуются съ вы-
водами изъ формулы Ѵа п - (1 е г - \Ѵа а 1 в’а
(р +^<Ѵ--Ь) = КГ ....... (24)
Здѣсь внутреннее давленіе газа, вызванное «сцѣпленіемъ» газо-
выхъ молекулъ (т. I); поэтому внутренняя работа при расширеніи равна
Пренебрегая членомъ, содержащимъ аЬ, мы изъ (24) легко получа-
емъ выраженіе для р0ѵ0 — р1ѵ1; если въ добавочныхъ членахъ. с<>-
Газовый термометръ. 403
держащихъ а и Ьу вставить и ѵ0 изъ равенствъ р1ѵ1 и роѵо =
= 7?Г0, то получается формула
РоѢ = ЖЛ — Л))+ фл— Ро) -
Такова внѣшняя работа расширенія; для внутренней мы находимъ
/ 1 1 \ а .
Вся работа эквивалента сѵ (7^ 70), такъ что имѣемъ сѵ(1\- Го) =
= — Л/?(7'1 — То) -|- А (/? ро). Но сѵ-\-АП = ср, слѣд.
(9/7 \
Ь\(р-ро).
Принимая атмосферу за единицу давленія, имѣемъ для воздуха а —
= 0.002312, Ь — 0,001970, ср = 0.2377. Тогда послѣдняя формула даетъ
7\ То = 0,265 (р± р0)9
что весьма близко къ числу 0,267, найденному Лопіе’емъ и Тйошеоп’омъ.
Особый интересъ представляетъ неоднократно за послѣдніе годы
поднимавшійся вопросъ относительно инверсіи, т.-е. измѣненія знака
величины /3 при опредѣленной температурѣ и относительно зависимости
этой температуры отъ начальнаго давленія р. Мы видѣли выше, что для
водорода при обычныхъ температурахъ величина @ отрицательна.
Еозе-Іппев показалъ, что наблюденія Лопіе’я и Тііотвоп’а
могутъ быть изображены также формулою вида
з а
^ = -^ — 7-
Для водорода а — 64,1, у = 0,331. Это даетъ /3 = 0 при 1 =—
— 79,3°. Ольшевскій (1901) подтвердилъ этотъ выводъ, заставляя во-
дородъ расширяться при низкихъ температурахъ. Онъ нашелъ, что при
I = — 80,5° измѣненіе температуры при расширеніи мѣняетъ знакъ. Для
воздуха перемѣна знака должна произойти при / = 360°, т.-е. при />>360°
воздухъ при расширеніи долженъ нагрѣваться.
§ 3. Газовый термометръ. Въ гл. II былъ разсмотрѣнъ способъ
измѣренія температуръ при помощи газоваго термометра. Показанія
этого прибора вполнѣ соотвѣтствовали бы шкалѣ абсолютныхъ темпера-
туръ ТЬошбОп’а, если бы газъ обладалъ свойствами идеальнаго газа.
Мы теперь можемъ рѣшить вопросъ о томъ, насколько шкала газо-
ваго термометра отличается отъ шкалы ТЬошвоп’а, и далѣе вопросъ о
температурѣ таянія льда по этой послѣдней шкалѣ. Обратимся вновь къ
опытамъ Л о и 1 е’я и Т11 о т 8 о п’а, въ которыхъ газъ, переходя отъ да-
вленія рх къ ръ, охлаждался на 0°. Предположимъ, что измѣненія давленія
464
Приложенія термодинамики.
безконечно малы, и что они вызываютъ измѣненіе температуры ді Фор-
мула (21) стр. 461 даетъ (дО — ді):
,, л I 'гдѵХ ,
— спді = А Іѵ Т <^.1 ар.
Р I дТ]
Предположимъ, что температура і измѣряется газовымъ термоме-
тромъ, и пусть а коеффиціентъ, полученный по формулѣ рѵ --- С(1 ~Ь а0.
откуда
дѵ__Со.
ді р '
„ , дѵ
Это выраженіе можно вставить вмѣсто — , и тогда получается, если
ввести и для ѵ его значеніе,
АС
-Срді=[1-а(Г-іУ]удр.
Интегрируя это уравненіе, причемъ Т—I можно считать постоян-
нымъ, и обозначая полное пониженіе температуры черезъ Ѳ, получаема^
СР0 = [1- а(7'-/)]ЛС18Ро,
Р Рі
откуда
АСа\%Р*
Ро
(25)
По этой формулѣ можно вычислить абсолютную температуру Т, со-
отвѣтствующую температурѣ і, указываемой газовымъ термометромъ, для
котораго 0° и 100° опредѣляются температурами тающаго льда и кипя-
щей воды при давленіи въ 760 мм.
Нѣсколько иное вычисленіе даетъ, если воспользоваться формулою
Я о с Ь ш а п п’а, выражающей результаты опытовъ Ее^папИ,
Т = 273,89 + 1,00026^—0,000026^,
гдѣ і температура по воздушному термометру, дѣйствующему при посто-
янномъ объемѣ. Указаніе на дальнѣйшія работы мы приводимъ въ об-
зорѣ литературы къ § 2.
§ 4. Поверхностное натяженіе. Мы видѣли, что увеличеніе по-
верхности 5 жидкости требуетъ затраты работы, равной
(іг =
см. т. I, гдѣ а поверхностное натяженіе. Это работа внѣшнихъ силъ,
дѣйствующихъ противъ внутреннихъ силъ сцѣпленія частицъ жидкости.
Отсюда слѣдуетъ, что
^(2 = (ІИ—Аасія.................(26, а)
Примемъ за независимыя перемѣнныя температуру і и 5, и положимъ
(10 = сМ -ф- Ь(І8 .................................. . (26, Ь)
Поверхностное натяженіе.
465
гдѣ с теплоемкость жидкости при постоянной поверх-
ности, Ь скрытая теплота увеличенія поверхности. Два
выраженія для даютъ
(11} — сді + (6 + Аа)(І8.
Эта величина должна быть полнымъ дифференціаломъ, т.-е.
дс__ дЬ । . да
д$ ~ ді' ді ’
или дс дЬ . да
дз — -ті = А ді ді
Второе начало даетъ
л 1 с\
Чп ' г дс ~ дЪ
дз ді или 1 -ѵ- д$ ^=т-~л+—ь, ді
т.-е. дс дЬ _ Ь
д$ ді т •
(27, а)
(27,6)
Сравнивая (27, а) съ (27,6) получаемъ
і да ,
Ь — — АТ^ ...... (28,а)
Вставивъ это выраженіе въ (27, а) и (26, 6), имѣемъ :
(28,6)
д$ ді*.ѵ ’ 7
ао, = сЛі—А Т СІ8 ....... (28, с)
Мы знаемъ, что поверхностное натяженіе жидкостей уменьша-
ется съ температурою; слѣд. (28,а) даетъ
6 > 0..................(28,О)
Для изслѣдованныхъ жидкостей а представляется въ видѣ
а = а0(1 — ^),
да о д2а
Т*”е’ > = ді2 ~ 0* Послѣднее равенство и (28, 6) показываютъ, что
тл да
с отъ 5 не зависитъ. Вводя, мы находимъ
Ь = АТа$.....................(29)
Для воды въ С. О. 5. системѣ а0 = 80(т. I), Л — 1 : 42 X ІО6
ѵ С.ЯТЧТ. 4/7 X Ч
эрговъ ; далѣе /9 = ; отсюда 6 = . Это показываетъ, что для
увеличенія поверхности воды на 1 кв. см. требуется
затрата одной милліонной доли малой калоріи. Прило-
КУРСЪ ФИЗИКИ О ХВОЛЬСОНА. Т. III, изд. 3-е. 30
466
Приложенія термодинамики.
женіемъ термодинамики къ явленіямъ капиллярности занимались О і Ь Ъ 8,
Ѵап йег АѴ а а 18, ОиЬет, В. НеІтЬоИг, \Ѵ а г Ь и г , біеіап,
ѵ. Ъап^, Еіпзіеіп, Ваккег, Ьелѵіз (1908), ѴѴ Ьіѣіа кег (1908),
Кіеетап (1909) и др. Большую роль при этихъ изслѣдованіяхъ игра-
етъ величина, которую можно назвать поверхностной энергіей;
мы будемъ обозначать ее черезъ (А. Мы имѣли выше формулу
(IV = сйі + (Ь -|- Аа)(1$.
Положимъ теперь Ь -|- Аа = Ѵ8 ; тогда формула (28, а) даетъ
Ѵ5=Аа — АТ^
ИЛИ
Аа = Ѵ8 4- 7'^4°^..................(29, а)
Эта формула напоминаетъ формулу (72) стр. 139
дГ
т=и+ т^~,
ді
гдѣ 1} означаетъ полную энергію, Л —свободную энергію. Такимъ обра-
зомъ, Аа представляетъ собою ту часть общей поверхностной энергіи 17з,
которая при изотермическихъ процессахъ можетъ переходить въ работу.
ЛѴІііИакег (1908) вычислилъ величину ІУз для эфира, метилфор-
міата, СС/4, бензола и хлоръ-бензола. Оказалось, что при критической
температурѣ Тс какъ энергія {7$, такъ и а равны нулю. При пониженіи
Т величина Ѵз возрастаетъ сначала очень быстро; когда Тс — Т равно
50—60°, Пз продолжаетъ возрастать, но медленно. Приблизительно при
Тс—7=180° Ыз становится постоянной и далѣе начинаетъ снова
уменьшаться. Чисто эмпирическимъ путемъ ЛѴйіѣѣакег находитъ
замѣчательное соотношеніе
Ѵз=КѴіТ.......................(29, Ь)
гдѣ означаетъ скрытую теплоту, идущую на внутреннюю работу
при испареніи, которую мы ближе разсмотримъ въ главѣ XI, § 5, К—по-
стоянная, имѣющая различныя значенія для различныхъ жидкостей.
Кіеетап (1909) вычислилъ зависимость величины К отъ свойствъ
жидкости, воспользовавшись формулой Еоіѵбз’а (т. I, гл. V § 11)
Лѣг/І3 = к\Тс- Т— аI
въ которой М обозначаетъ молекулярный вѣсъ, к и (1 — постоянныя,
приблизительно одинаковыя для всѣхъ жидкостей, причемъ, въ среднемъ,
& = 2,12 и б/ = 6. Кромѣ того Кіеетап воспользовался еще выше упо-
мянутой формулой для величины р/ и пришелъ къ выраженію
1 2
СЛ43д *
т~.........................(29,0
* г
Истинная теплоемкость.
467
въ которомъ Ьс означаетъ плотность при критической температурѣ Тс , а
С есть постоянная, одинаковая для всѣхъ жидкостей. При этомъ
С = 0,557.
§ 5. Энергія и энтропія твердыхъ и жидкмхъ тѣлъ. Принимая р
и I за независимыя перемѣнныя, мы вывели для энергіи и для эн-
тропіи формулы (62, Ь) стр. 432 и (68, с) стр. 437. Этими форму-
лами и выражаются О и 5 для жидкихъ и. твердыхъ тѣлъ. Ихъ можно
однако значительно упростить. Объемъ этихъ тѣлъ весьма мало мѣняется
съ измѣненіемъ давленія и температуры, вслѣдствіе чего въ (62, Ь) можно
пренебречь послѣдними двумя членами, а въ (68, с) послѣднимъ членомъ.
Далѣе ср мало мѣняется въ зависимости отъ давленія р, а потому можно
вмѣсто- (ср)ъ вставить Ср. Такимъ образомъ получается :
і
і) = Ѵ(р0, і0) СрЛі
I
<?(/>, О = $(а>Л)
^0
. (30)
Если еще пренебречь измѣненіемъ теплоемкосги ср въ зависимости
отъ температуры і, то получается:
о(р,і) = и{р0Л') + ср(і-і0\
5 (/?/) = 5 (р0, /0) + ср
(30, а)
Нетрудно затѣмъ написать и выраженіе для свободной энергіи Р =
= 11—8Т.
§ 6. Истинная теплоемкость по Сіапзіпз’у. Истинною теплоем-
костью Сіаизіи» называетъ то количество теплоты, которое тратится
только на увеличеніе кинетической энергіи Ѵ7 движенія частицъ тѣла,
когда это тѣло нагрѣвается на 1°. Наблюдаемая теплоемкость склады-
вается изъ истинной и изъ той части теплоты, которая тратится на внл -
треннюю и на внѣшнюю работу. На стр. 444 было указано, что С1 а и -
8іи8 пишетъ
(1^ = (І\)2-\-АкТс12 ....... (31, а)
гдѣ (12 приращеніе дисгрегаціи тѣла. Изъ (31, а) получается
СсІСІ Г(ІѴ7 .
Для обратимаго кругового процесса первый и третій интегралы
нули; слѣд.
) ~т
(31,6)
30*
468
Приложенія термодинамики.
Но кромѣ того, очевидно,
.................................................. (32)
Отсюда Сіаизіие выводитъ, что функція одной только
температуры и отъ состоянія тѣла не зависитъ. Дѣйствительно, пусть
ѴУ = /(і, х), гдѣ х какая-либо величина, опредѣляющая, вмѣстѣ съ і, со-
стояніе тѣла. Пусть д\Ѵ= МЛі -ф Шх-. формулы (32) и (31, Ь) даютъ
дМ_дЫ
дх ді
°\ТI Г) дМ д^
дх ді дх ді Т
Послѣднія два равенства даютъ М = 0, т.-е. Ѵ7 отъ х не за-
виситъ. Тогда и М — также отъ х не зависитъ. Но М и есть ис-
тинная теплоемкость, и такимъ образомъ положеніе Сіаизіиз’а дока-
зано. Измѣненіе теплоемкости въ зависимости отъ температуры вообще
не велико; Сіаизіиз приписываетъ это измѣненіе также внутренней
работѣ и считаетъ вообще истинную теплоемкость вещества
за величину постоянную, не зависящую отъ его состоя-
нія. Разница наблюдаемыхъ теплоемкостей тѣлъ въ твердомъ и жид-
комъ состояніяхъ является такимъ образомъ слѣдствіемъ неодинаковости
внутренней работы.
§ 7. Теплоемкости сѵ и ср для тѣлъ твердыхъ и жидкихъ. Мы
дѵ
имѣли формулы (41,6) стр. 403 и (58,с) стр. 428: ср—сѵ= а и а =
= Эти формулы даютъ
сѵ=Ср-АТдХ^(...................(32,а)
Но мы знаемъ, что
^дѵ ді ’ СМ* СТР‘ Такимъ обра-
зомъ имѣемъ
—@ѵ, получаемъ
(33, а)
дѵ дѵ
Вставляя сюда еще
с’ _с _
сѵ~- СР
Эту формулу можно написать въ видѣ
г -с а \2ѵ
сѵ — ср ^'І1+а,І р
(33, Ь)
(33, с)
Теплоемкости твердыхъ и жидкихъ тѣлъ.
469
Болѣе точное выраженіе получается, если въ равенствѣ ѵ = 77О(1 +
л дѵ I , , да\
считать а перемѣннымъ, и въ (33, а) вставить I а 4- 1. Тогда
формула (33. а) принимаетъ видъ
I да\2
сѵ ~ ср —А+ «0® Ѵ.......................('33,
Этою формулою можно воспользоваться, чтобы опредѣлить а за-
ср
тѣмъ и отношеніе к = — для твердыхъ и жидкихъ тѣлъ, для которыхъ
сѵ
коеффиціенты сжатія р и теплового расширенія а извѣстны. При этомъ
Р должно равняться относительному уменьшенію объема при возрастаніи
внѣшняго давленія на 1 клгр. на кв. м. Отсюда слѣдуетъ, что /? =
= /?0: 10333, гдѣ /?0 «табличный» коеффиціентъ, относимый къ давле-
нію въ 1 атмосферу. Вопросъ о сжатіи жидкихъ и твердыхъ тѣлъ
былъ разсмотрѣнъ нами въ т. I; вопросъ о тепловомъ расширеніи въ
т. III. Приводимъ результаты вычисленій, произведенныхъ по одной изъ
выведенныхъ формулъ; замѣтимъ, что для всѣхъ тѣлъ с р^>сѵ^ ибо
величина а, единственная изъ величинъ, входящихъ во второй членъ, ко-
торая можетъ быть отрицательною, возвышена въ квадратъ.
Вода. Принимая для ср числа В е а и к, для /? числа Ѳ г а 8 8 і
и для ѵ = /(/) числа К о р р’а, получаемъ слѣдующія значенія для сѵ и к:
і ср сѵ к=ср сѵ і ср сѵ сѵ
—10° 0,9997 0,9921 1,008 40° 1,0030 0,9774 1,026
0° 1,0000 0,9995 1,001 60° 1,0056 0,9567 1,051
4° 1,0002 1,0002 1,000 80° 1,0090 0,9330 1,081
20° 1,0012 0,9949 1,006 100° 1,0130 0,8891 1,139.
Понятно, что при 4° имѣемъ ср = = сѵ и к = 1, > ибо при 4° ѵ минимумъ и
слѣд. ^=0. Вагіоіі и Вігассіаіі (1894) а также Оіеіегісі
(1896) дали нѣсколько иныя числа.
Для ртути получается (ср по Ке^паиіі, /? по А піа^аі) при і = 0°:
ср = 0,0333, сѵ = ѵ,0290, к = 1,14. • 7
Алкоголь (этиловый) :
Рѵ к
7°,3 0,5643 0,4456 1,266
25° 0,613 0,518 1,183.
Э ф и р ъ (этиловый), по Г) г е с к е г’у:
/ Ср сѵ к
0° 0,5290 0,3583 1,476
14° 0,5373 0,3722' 1,443
470
Приложенія термодинамики
Сѣр оу г л еродъ 25° 0,244 0,160 1,525
Хлороформъ 25° 0,234 0,159 1,472.
Для
димъ двѣ
п е г’омъ.
металловъ вообще трудно опредѣлить величину к. Приво-
таблички; первая дана ВиеЫтапп’омъ, вторая ѴѴиеН-
і = 0° ' і = 20°
Си 1,012 Си 1,0222
Ре 1,008 Латунь 1,0261
1,016 Сталь 1,0154.
Стгііпеібеп (1908) нашелъ для к при 18° слѣдующія числа: —
- 1,067, М$— 1,035, АІ — 1,044, Л — 1,087, Ее — 1,014, М — 1,017,
Си- 1,026, —1,039, А/—1,021, 1,037, СЙ—1,052, 8п —1,039,
8Ь — 1,008, Рі— 1,019, Аи — 1,031, ТІ— 1,046, РЬ — 1,055, Ві— 1,012.
Ьиееапа (1910) нашелъ, что ср— сѵ для элементовъ съ повыше-
ніемъ температуры увеличивается, а для сплавовъ, вообще уменьшается.
Для сплава Ссі—Си оказалась, что ср — сѵ увеличивается съ возраста-
ніемъ давленія.
Обратимся къ другому вопросу. Формула (59, с) стр. 429
дСР — АТ^
др ~ д?
(34)
даетъ возможность найти зависимость теплоемкости ср отъ
давленія. Примемъ дср = Лср и др = Др—\ атм. Тогда
д^ѵ
Аср ~ АУ Ар.....................(35)
Выражая всѣ величины въ С. 0.6. единицахъ, мы должны положить:
А = 1 : 42.10~6 эрг.; Лр= 1 атмосф. = 1,014.106 динъ на кв. см. (т. I):
Т=213. Далѣе числа Корр’а даютъ при 0° для воды^ = 1,54.10~Л
Такимъ образомъ получаемъ, что теплоемкость воды мѣняется при 6°
на величину
Лср = — 1,025 . ІО-4
когда давленіе растетъ на 1 атмосферу.
§ 8. Адіабатическое измѣненіе состоянія жидкихъ и твердыхъ
тѣлъ. Разсмотримъ вліяніе внезапнаго измѣненія давленія на объемъ и
температуру твердыхъ и жидкихъ тѣлъ. Мы будемъ пользоваться бук-
вою 5 въ видѣ значка, чтобы отмѣтить, что величины относятся къ адіа-
батическимъ измѣненіямъ, при которыхъ энтропія 5 остается неизмѣн-
ною. Три выраженія (60, а} и (60, с) стр. 429 для даютъ при б/<2 = 0
сѵді8-]-АТ =0
срді ~ О
ді , . ді ,
СР 4" сѵ ^^Р8 — О
(36. а)
Адіабатическія измѣненія.
471
др др дѵ аѵ0
Отсюда, вставляя =— дѵдс = Зѵ ' П0ЛУчаемъ:
,, АТаѵ0,
аР =------7,- аѵ^
5 Су рѵ 4
АТ
<1і8 = а.ѵ0др5
СР
дѵ8 =—-г- Рѵдр8
К
Если изъ (36, а} опредѣлить
(36, Ь)
и принять во вни-
маніе формулу (32, я), стр. 4б«, ср— сѵ = АТ, то получаются за-
мѣчательныя формулы:
1
Если положить
дѵ\
др/8
дѵ
к— 1
1
к
к
к— 1
'ѵ
(36,с)
— @8ѵ, то а8 и Р8 можно на-
.. . = <4^
ді/8
звать адіабатическими коеффиціентами теплового расширенія (вѣрнѣе
сжатія) и объемнаго сжатія. Тогда (36,б/) даетъ:
и
і
а8— ~
1
а
к— 1
. (37)
1
к
Особенно замѣчательна вторая формула, показывающая, что адіа-
батическое сжатіе тѣлъ въ к разъ меньше сжатія изо-
термическаго.
Пусть Ѳ повышеніе температуры тѣла, происходящее, когда внѣшнее
давленіе внезапно увеличивается на Р атмосферъ. Мы можемъ при-
нять въ формулѣ (36,с) величины Т, ср и а за постоянныя и вмѣсто без-
конечно малыхъ измѣненій температуры и давленія подставить конеч-
ныя измѣненія температуры и объема Ѳ и Р, гакъ какъ Ѳ въ дѣйствитель-
ности всегда мало.
Т Ь о іи 8 о п’а
Такимъ образомъ мы приходимъ къ формулѣ
Ѳ = 10333 р
Ср
Если давленіе на тѣло внезапно уменьшится на Р, то его объ-
емъ возрастетъ на величину Дѵ5, а температура понизится на 0°: есіи
(38)
472
Приложенія термодинамики.
оно затѣмъ нагрѣется на 0°, то его объемъ увеличится еще на величину
аѲ
ѵ; полное увеличеніе объема очевидно будетъ равно и з о т е р -
1 4- аГ
мическому сжатію Дѵр Итакъ,
Дѵ8 4---ѵ =
1 4- аі
Раздѣлимъ всѣ члены на ѵР и положимъ Ѳ — РѲЪ гдѣ Ѳг опредѣляется
формулою (38). если положить въ ней Р = 1. Такъ какъ оба Дѵ суть
увеличенія объема, то Дѵ8=> Р8ѵР, Дѵ^— $ѵР, и мы получаемъ:
і 4~
ѲА= 10333
АТаѵ^
Ср
(39)
Эти формулы даютъ возможность опредѣлить^, измѣ-
ряя адіабатическій коеффиціентъ сжатія
В г е с к е г провѣрилъ эту формулу, наблюдая въ піезометрѣ вели-
чины /? и и вычисляя $ по формулѣ; онъ нашелъ прекрасное согла-
сіе наблюденій съ теоріей.
Формула (38) показываетъ, что если тѣло при нагрѣваніи
расширяется (а>0), то оно при сжиманіи нагрѣвается
(Ѳ >> 0); если же тѣло при нагрѣваніи сжимается (а < 0),
то оно при сжиманіи охлаждается (^<0).
4ои1е провѣрилъ формулу (38) для воды и для китоваго жира, при-
чемъ дѣйствительно обнаружилось охлажденіе воды при ея сжатіи, когда
і < 4°. Испытуемое вещество помѣщалось въ мѣдномъ сосудѣ, соеди-
ненномъ съ цилиндромъ, снабженнымъ поршнемъ, на который наклады-
вались грузы; измѣненія температуры измѣрялись при помощи термо-
электрическаго элемента, помѣщеннаго внутри сосуда. Не входя въ даль-
нѣйшія подробности приводимъ результаты наблюденій и рядомъ вели-
чины, вычисленныя по формулѣ (38) самимъ Лоиіе’емъ, а для воды
Лоиіе’емъ и затѣмъ ЛѴиеПп ег’омъ (ЬекгЪисЬ, 5-ое изд. ч. П стр. 599,
1896 г.). Въ нижеслѣдующихъ таблицахъ р обозначаетъ увеличеніе да-
вленія, выраженное въ клгр. на кв. см.: і начальная температура.
Р Р Вода. Ѳ набл. 0 вычисл. Ѳ вычисл.
26,19 1°,20 — 0°,0083 (Я о и 1 е) — 0°,0071 (АѴпеІІп ег). 0°,0069
26,19 5,00 4- 0,0014 + 0,0027 4- 0,0025
26,19 11,69 0,0205 0,0197 0,0193
26,19 30,00 0,0544 0,0563 0,0547
16,17 40,40 0,0450 0,0476 0,0434
Растяженіе твердыхъ тѣлъ.
473
Китовый жиръ.
р і° Ѳ набл. Ѳ вычисл.
8,19 16°,0 0°,0792 0,0886
29,17 16,27 0,2663 0,2837
Послѣ 4 о и 1 ея производили опытныя опредѣленія величины Ѳ
сперва Сгееігпапп и Сгоскеі (1884), а затѣмъ В и г і о п и М а г -
вЬаІІ (1891).
§ 9. Растяженіе твердыхъ тѣлъ. Положимъ, что проволока за-
крѣплена однимъ концомъ; на другой конецъ дѣйствуетъ растягивающая
сила р. Измѣненіе силы р вызываетъ измѣненія температуры проволоки,
которыя могутъ быть опредѣлены теоретически. Пусть I длина части
проволоки, масса которой единица; за независимыя перемѣнныя, опре-
дѣляющія состояніе стержня, примемъ I и р. Чтобы увеличить I на (11,
необходимо произвести работу рді противъ внутреннихъ силъ стержня,
и результатомъ этой работы является увеличеніе энергіи стержня. Поэтому
= (Ш — Арді....................(40, а}
Далѣе пишемъ въ видѣ:
Исір
. . (40,6)
гдѣ Ср теплоемкость при
раженія для сІО даютъ
постоянной нагрузкѣ. Два вы-
Отсюда
сп = Ар
рді
ді . ди л ді
ді др др
<^р' _дИ= _ Дді_
др Оі ді
л (ср'\ / Ь, \
Дг) Д77
Второе начало даетъ , откуда
дср‘ _ дИ _ _ А......................(40
др ді Т
Изъ (40,с) и (40Д) получается
слѣд. (40,А) даетъ
И----АТ ... .... (4О.е)
ді
Щ = ср'Аі АТд1^др ....... (41)
Подставляя (40,ё) въ (40,с), получаемъ
дср‘ , д21
др АТ ді2
(41.и)
474
Приложенія термодинамики.
Обозначая коэффиціентъ линейнаго расширенія при постоянной
нагрузкѣ р чрезъ имѣемъ
(4170
и, слѣдовательно, на основаніи (41л),
(41,с)
\ Р /і \ /р
Длина I есть функція і и р; при этомъ
М — 10 -р ~ (ір)
гдѣ Ь — модуль Юнга (т. I). Очевидно,
Р
или
(41X)
Формулы (41,с) и (41л) были выведены впервые Вепѣоп’омъ (1903).
Первая изъ нихъ указываетъ, что если коэффиціентъ линей-
наго расширенія проволоки при постоянномъ напря-
женіи возрастаетъ (убываетъ) съ повышеніемъ темпе-
ратуры, то теплоемкость ср' (при постоя н номъ напряже-
ніи) при изотермическомъ возрастаніи напряженія воз-
раста е т ъ (у б ы в а е т ъ). Вторая изъ этихъ формулъ даетъ слѣдующее по-
ложеніе : если коэффиціентъ линейнаго расширенія при
изотермическомъ возрастаніи напряженія возрастаетъ
(убываетъ), то модуль Юнга Е съ возрастаніемъ темпе-
ратуры убываетъ (возрастаетъ). Такъ какъ вообще у всѣхъ
металловъ Е съ возрастаніемъ температуры убываетъ, то, слѣдовательно,
коэффиціентъ линейнаго расширенія растянутыхъ металлическихъ про-
волокъ больше того-же коэффиціента проволокъ не растянутыхъ. Это
подтверждается опытами В аЫап сі ег’а (1872). К. ЛѴа^пег (1907) на-
шелъ, что для эбонитоваго стержня Е съ возрастаніемъ температуры
возрастаетъ и ц съ возрастаніемъ напряженія замѣтно умень-
шается. Даваемое (41,с) измѣненіе теплоемкости ср съ измѣне-
ніемъ напряженія весьма мало. Для Си, по вычисленію В е и 1 о п’а,
Аср = 2,89.10~6. когда Ар = 1 кгр. на 1 квадр. мм. Столь малое измѣ-
неніе А Ср не можетъ быть измѣрено на опытѣ.
Для адіабатическаго расширенія мы имѣемъ изъ (41) •
Ср^іл- АТ діаР = ^.......................(417)
или же, вт» силу (41.6),
Ср(іі -Д- АТІ^айр = 0..................(41.§)
Растяженіе твердыхъ тѣлъ.
475
Считая и ц за величины постоянныя, мы изъ (41,а) поллчаемъ
измѣненіе Ѳ температуры для слдчая, когда р внезапно увеличивается
на Р кгр.:
Ѳ = — А ГГ,1° Р .....................(42)
СР
Эта формула вполнѣ аналогична формулѣ (38) стр. 471. Знакъ ве-
тчины Ѳ зависитъ отъ знака ?/. Формула (42) показываетъ, что если
стержень при нагрѣваніи удлиняется, то онъ при ра-
стяженіи охлаждается; если онъ при нагрѣваніи уко-
рачивается, то онъ при растяженіи нагрѣвается.
Уже растянутая каучуковая лента при нагрѣваніи укорачивается:
такая лента при внезапномъ дальнѣйшемъ растяженіи дѣйствительно на-
грѣвается.
Измѣренія величины Ѳ произвелъ впервые Зоиіе (1859), но они не
отличались большою точностью и дали результаты, мало согласные съ
формулою (42). Болѣе точные опыты ЕсІІипсГа (1865) были произве-
дены по способу, изложенному на стр. 376, и съ приборомъ, изображен-
нымъ на рис. 115. Его числа также не согласуются съ формулою (42).
V е г (і е і и 81. К о Ь е г і полагали, что одна изъ причинъ несо-.
гласія заключается въ томъ, что коеффиціентъ расширенія р натянутой
проволоки не равенъ коеффиціенту расширенія проволоки ненатянутой,
опредѣляемому изъ наблюденій и взятому вмѣсто при вычисленіи. Од-
нако опыты Г) ай 1 ап й е г’а показали, что, хотя дѣйствительно зави-
ситъ отъ р, однако введеніе соотвѣтствующей поправки еще увеличиваетъ
разногласіе между наблюденіями ЕсІІипсГа и теоріей. Это разногласіе
вполнѣ исчезло, когда На§*а (1«82) опредѣлилъ всѣ величины, входящія
въ формулу (42), хля той самой проволоки, которая подвергалась растя-
женію. Приводимъ числа, найденныя этимъ наблюдателемъ:
Стальная проволока . . .
Нейзильберовая проволока .
Ѳ набл. О вычисл.
— О°.1О76 - 0°,1047
0°,1405 — 0°,1122
Согласіе можно считать полнымъ. Подобныя измѣренія были произ-
ведены Апс1ег8 8оп’омъ (1898), АѴ а с Й8 ш иі й’омъ (1888—1904),
ВеІГемъ (1905), К. АѴа^пег’омъ (1907) и др.
АѴ а § п е г нашелъ, что стержень изъ іодистаго серебра, имѣющій
отрицательный коеффиціентъ расширенія, нагрѣвается при растяженіи,
т.-е. обнаруживаетъ ту-же особенность, что и растянутый каучуковый
стержень. Дальнѣйшія теоретическія изслѣдованія относительно терми-
ческихъ вліяній не только растяженія, но также крученія и изгиба,
были произведены въ послѣднее время АѴа 8 8 пі иій’омъ, 81оііе(19О8)
и, въ весьма общемъ видѣ В гі] 1 о иі п’омъ (1909). 81 оііе нашелъ,
что крученіе вызываетъ охлажденіе; для цилиндрическаго желѣз-
наго стержня въ 1 м. длиною и въ 3,6 мм. толщиною это охлажденіе
равняется 0,0039° при крученіи на 90°.
I Іриложснія термодинамики.
476
Всѣ формулы, выводимыя здѣсь термодинамическимъ путемъ по-
нятно, имѣютъ силу лишь для обратимыхъ упругихъ процессовъ, т.-е. для
такихъ процессовъ, при которыхъ предѣлъ упругости остается не достиг-
нутымъ. Оказывается, что, какъ при растяженіи, такъ и при сжатіи пе-
реходъ за предѣлъ упругости сопровождается внезапнымъ весьма силь-
нымъ нагрѣва ніемъ стержня. Дп нникъ (1908) опредѣлилъ предѣлъ
упругости для различныхъ металлическихъ стержней, растягивая ихъ
постепенно возрастающимъ грузомъ и измѣряя ихъ температуру помощью
термоэлемента; первоначальное охлажденіе переходило внезапно въ силь-
ное нагрѣваніе. Такъ опредѣленные предѣлы упругости оказались вполнѣ
совпадающими съ полученными инымъ путемъ (приборомъ кн. Г а га-
ри н а , см. т. I).
§ 10. Давленіе лучистой энергіи и законъ Стефана. Представимъ
себѣ полость, т.-е. пространство, со всѣхъ сторонъ ограниченное твер-
дыми стѣнками, температура которыхъ Т; она свободна отъ матеріи; ея
объемъ обозначимъ черезъ ѵ. Внутри полости мыслимы всевозмож-
ныя лучистыя явленія, отличающіяся другъ отъ друга направленіемъ лу-
чей, направленіемъ и амплитудой колебаній и количественнымъ распре-
дѣленіемъ длинъ волнъ Л. Эти мыслимыя состоянія характеризуются
различною степенью существующаго въ пространствѣ порядка. Мы
имѣли бы полный порядокъ излученія, если бы существовали только
стоячія волны одного направленія; высокая степень порядка была бы и
въ случаѣ вполнѣ монохроматическихъ лучей, т.-е. вездѣ одинаковаго Л.
Мы видѣли, что при движеніи весьма большого числа молекулъ наи-
болѣе вѣроятнымъ оказывается вполнѣ безпорядочное движеніе. Оно
соотвѣтствуетъ тепловому движенію, и всякое другое, менѣе безпорядочное
движеніе имѣетъ тенденцію перейти во вполнѣ безпорядочное тепловое
движеніе. Эта тенденція къ наиболѣе вѣроятному состоянію и есть тен-
денція къ состоянію максимальной энтропіи.
Нѣчто вполнѣ аналогичное относится къ лучистому состоянію въ
пространствѣ ѵ. Каждое такое состояніе обладаетъ опредѣленною сте-
пенью вѣроятности и опредѣленною степенью порядка. Наибольшею вѣ-
роятностью обладаетъ состояніе вполнѣ безпорядочное и всякое другое
состояніе имѣетъ тенденцію перейти въ это послѣднее. Итакъ, суще-
ствуетъ вполнѣ опредѣленное «лучистое состояніе«
(Йіг аіііип^йяи йіапсі). которое само собою устанавли-
вается въ пространствѣ ѵ. Оно вполнѣ безпорядочное; всѣ
направленія распространенія лучей, а также колебаній въ пространствѣ
играютъ одинаковую роль. Оказывается возможнымъ опредѣлить нѣкото-
рую величину, энтропію излученія, которая въ этомъ состояніи имѣетъ
максимальное значеніе.
Лучистая энергія въ единицѣ о б ъ е м а является при этомъ
нѣкоторой функціей температуры гр (Т). Всѣ значенія Л встрѣчаются въ
этомъ излученіи; но энергія гр (Т) распредѣлена между различными Л по
Давленіе лучистой энергіи
477
вполнѣ опредѣленному закону, который и есть законъ абсолютно
чернаго излученія, разсмотрѣнный въ т. II.
Докажемъ, что лучистая энергія должна производить давленіе па
стѣнки полости г/, которую мы представимъ себѣ въ видѣ вертикально
поставленнаго цилиндра, закрытаго сверху абсолютно чернымъ тѣломъ А
температуры 71? а снизу такимъ же тѣломъ О температуры Т2 < 7]: бо-
ковыя стѣнки цилиндра вполнѣ отражаютъ всѣ лучи и теплоту не про-
пускаютъ. Внутри цилиндра находятся двѣ поперечныя пластинки В и
С, стороны которыхъ также вполнѣ зеркальны и теплоту не пропускаютъ.
Пластинки В и С могутъ быть выдвинуты черезъ боковыя поверхности
цилиндра; пластинка В находится близъ верхняго тѣла А; пластинка С
можетъ двигаться вдоль цилиндра, подобно поршню.
Сначала С вынута, В находится внутри цилиндра около А, такъ
что весь цилиндръ заполненъ энергіей гр (Т2). Вставляемъ С въ самомъ
низу, вынимаемъ В и поднимаемъ С почти до соприкосновенія съ А.
При этомъ вся энергія ѵ гр (Т2\ наполняющая цилиндръ, поглощается
чернымъ тѣломъ А. Затѣмъ мы вставляемъ В и вынимаемъ С, причемъ
возстанавливается первоначальное состояніе. Повторяя эту манипуляцію,
мы можемъ неограниченное число разъ брать теплоту отъ болѣе холод-
наго тѣла 7), превращать ее въ лучистую энергію ѵ гр (72) и переда-
вать въ видѣ теплоты болѣе теплому тѣлу А. По второму началу это
возможно только при наличности компенсирующаго положительнаго про-
цесса. Единственнымъ, при описанной манипуляціи, подобнымъ процессомъ
была бы затрата особой работы при поднятіи пластинки С. Такая работа
должна существовать, т.-е. пластинка С должна быть подвержена
большему давленію сверху, чѣмъ снизу. Отсюда слѣдуетъ, что лучи-
стая энергія, находящаяся ст> двухъ сторонъ отъ пла-
стинки С, про изв од итъ н а нее давленіе, и что это да-
вленіе возрастаетъ съ повышеніемъ температуры. Въ
т. II мы описали опыты П. Н. Лебедева, впервые доказавшаго пу-
темъ опыта существованіе этого давленія.
Электромагнитная теорія свѣта приводитъ къ результату, что, при
нормальномъ паденіи лучей на черную поверхность, это давленіе
на единицу поверхности равно гр(Т), т.-е. равно энергіи единицы объема.
Если поверхность вполнѣ зеркальна, то давленіе вдвое больше. При со-
вершенно безпорядочномъ состояніи - лучистой энергіи, лучи падаютъ подъ
всевозможными углами. Воіігтапп показалъ, что въ этомъ случаѣ да-
вленіе на абс. черную поверхность равно ^гр(Т); его выводъ подобенъ
выводу Сіапзіиз’а формулы для давленія газа (т. II).
Обращаемся къ выводу закона Стефана, который гласитъ, что ин-
тегральное лучеиспусканіе абс. чернаго тѣла пропорціонально четвертой
степени абсолютной температуры. Мы видѣли, что это испусканіе тож-
дественно съ тѣмъ, которое само собою устанавливается въ замкнутой
полости, и плотность энергіи котораго мы обозначили черезъ гр(Т).
478
Приложенія термодинамики.
Итакъ требуется доказать, что
чр(7) = СГ4 . . ..............(43)
Представимъ себѣ опять цилиндръ, въ которомъ находится подвиж-
ная пластинка (поршень); пусть ѵ объемъ между пластинкою и дномъ
цилиндра ; Т температура лучистой энергіи, наполняющей цилиндръ, т.-е.
температура чернаго тѣла, испускающаго совершенно такую же по со-
ставу (2) и напряженію лучистую энергію. Вся энергія въ объемѣ ѵ
равна и = гмр. Произведемъ безконечно малое измѣненіе состоянія, при-
чемъ пластинка передвигается и объемъ мѣняется на (1ѵ, Лучистая энер-
гія производитъ при этомъ работу = такъ какъ давленіе рав-
но з чр. Измѣряя теплоту и энергію въ механическихъ единицахъ,
мы получаемъ:
1 4
(К^ = (ШД-Лг = (Цуѵ) + о • • • (44)
3 3
Здѣсь ір функція температуры йотъ ѵ не зависитъ. Въ слу-
чаѣ изотермическаго расширенія отъ ѵ — до ѵ = гл2, имѣемъ, оче-
видно (й'Ц) = 0),
4
<3 = -у>(ѵ2 — .............(44, а)
О
При адіа батическомъ измѣненіи б/С) = 0 и мы получаемъ .
й'Ц) 4 (1ѵ_
4р 3" Ъ “
4
ЦУО 3 = СоП8І...............(45)
Этимъ замѣчательнымъ уравненіемъ опредѣляется
связь между давленіемъ и объемомъ запаса лучистой
энергіи при адіабатическомъ измѣненіи ея состоянія.
Согласно второму началу, величина : Т равна полному дифференціалу^
энтропіи 5*. Итакъ,
(15= 21 =Д- ^(іѵ................(46)
і I 31
Отсюда
л[ѵ\
44 4з4
дѵ д^
дТ дчр дТ
Это даетъ Т = 4у> или = 4 , т.-е.
у = СТ4 .......... (47)
Такимъ образомъ законъ Стефана доказанъ. Если под-
ставить (47) въ (45), то получается
і
Тѵ3= Сопеі.................(18)
Гипотеза Нернста.
479
Формулы (45) и (48) удивительно напоминаютъ формулы рѵк = Сопеѣ.
и Тѵк~г = Сопеі., которыя относятся къ адіабатическому измѣненію со-
стоянія и д е альныхъ газовъ, и въ которыхъ к = ср: сѵ . Въ (45) и
і _ 1
(48) имѣемъ - вмѣсто к. Изъ (47) слѣдуетъ Т=Ь^4 гдѣ Ь = С 4 но-
вая постоянная. Вставляя Т въ (4б) получаемъ
/ 4 —\ /4 \
(І8 = с1 ч СѵТа .
\іЬ ] /
Отсюда для энтропіи лучистой энергіи получаемъ:
4 -
5 = Соп8І. + ѵір4........................(49, а)
4
5 — Сопбі + — СѵТ3.......................(49, #)
<5
§ 11. Гипотеза Нернста. Въ 1906 г. появилась замѣчательная ра-
бота е г п 8 і’а о химическихъ равновѣсіяхъ, въ которой онъ высказалъ
нѣкоторую гипотезу относительно свойствъ вещества при температурахъ,
весьма близкихъ къ температурѣ абсолютнаго нуля. Эта гипотеза оказа-
лась въ высшей степени плодотворной въ самыхъ различныхъ областяхъ
физическихъ и физико-химическихъ явленій. Мы должны здѣсь ограни-
читься самымъ краткимъ изложеніемъ этой гипотезы, не входя въ даль-
нѣйшіе изъ нея выводы.
Мы имѣли въ гл. VIII, § 19 формулу вторую (72,^), или (78,^):
др
и=р ..................(50)
связывающую полный запасъ энергіи V со свободною энергіею Р. Если
V извѣстно, какъ функція температуры Г, то изъ (50) всетаки нельзя
опредѣлить Р, такъ какъ при интегрированіи получается неопредѣленная
постоянная, которую обозначимъ черезъ к и которая въ окончательномъ
результатѣ даетъ въ выраженіи Р членъ вида кТ. Это видно уже изъ
того, что если Р=/{Т) удовлетворяетъ уравненію (50), то Р=/(1)Д-к7
также ему удовлетворяетъ. Уравненіе (50) можно написать въ видѣ
о
др и /
— Р-\-Т -^ — — 1/, или Т2 — — и. откуда
Р — I А
г —— I -рг^сіі -ч— к т.-е.
/ е/
Р=—ТсІТ+кТ..........................(51)
Неопредѣленность въ выраженіи Р не даетъ возможности довести до
конца рѣшенія цѣлаго ряда разнообразныхъ проблемъ.
1*0
Проложенія термодинамики.
М е г п 8 Г замѣтилъ, что разность V — Е уменьшается съ пониже-
ніемъ температуры и онъ высказалъ прежде всего, гипо-
тезу, что при Т = 0 мы имѣемъ
Е—С..............................(52)
Ту же гипотезу принялъ, впрочемъ, еще раньше ѴапЧ Но И (1904).
дЕ
Равенство (52) возможно только вь случаѣ, когда въ (50) величина
конечная, т.-е. не безконечно большая; итакъ,
дЕ
= конечн. величинѣ.................(52, я)
ЭДегп8І останавливается, прежде всего, на случаяхъ химическихъ
реакцій, или физическихъ превращеній изъ одного состоянія въ другое.
Въ этомъ случаѣ
^2.....................(52. Ь)
гдѣ с± и теплоемкости системы до и послѣ реакціи. Для и можно при-
нять формулу вида
+ ..................................(б3)
Въ большинствѣ случаевъ можно ограничиться первыми тремя чле-
нами, но мы сохранимъ еще четвертый. Вставляя (53) въ (51), мы находимъ
Р—^ — аТ1%Т—0Т2-----------^-77'34-/:7' .... (54)
Далѣе мы имѣемъ
дЕ ч
—а—+ .... (54,а)
и і
Условіе (52,а) даетъ а = 0, т.-е.
..........................................................(55,а)
Р=У0- рТ2 — -і~?Р3 + кт .... (55,Р)
д^2^Т + 37Т2...........................(55,с)
-2?Т- 32 7Ті + к................(55Д)
^е^п8і предполагаетъ, что равенство Е=1) имѣетъ
мѣсто не только при 7—0, но и при весьма малыхъ Г,
т.-е. что
= М .................(56)
\ді/Т=О \дТ/Т=О
и въ этомъ заключается сущность его гипотезы. Изъ
(55,сі) слѣдуетъ теперь, что к = $ /Г)7\
Гипотеза Нернста. — Литература.
481
Это означаетъ, что Р и 67, какъ функціи отъ 7, изобра-
жаются кривыми, которыя при Т = 0 имѣютъ общую ка-
сательную, параллельную оси абсциссъ. Неопредѣленная по-
стоянная интегрированія /г, такимъ образомъ, опредѣлена, и мы имѣемъ:
^ = і/0-^П-4-77'3........(59,а)
Сі
Ар Ч
^=_2^_Ау72.............(59,*)
М е г и 8 і относитъ все изложенное къ «конденсированной» си-
стемѣ, состоящей исключительно изъ твердыхъ и жидкихъ ве-
ществъ ; къ газообразной системѣ гипотеза № е г п 8 і’а непосредственно
не прилагается.
Ріапск (1911) идетъ нѣсколько дальше, чѣмъ ЭДегпзі въ своей
первой работѣ. Онъ полагаетъ, что при 7=0 энтропія всякаго
твердаго или жидкаго тѣла равна нулю. Если принять для 17
выраженіе (55,а), а слѣд. для Р выраженіе (59,я), то первая изъ фор-
дР
мулъ (72) главы ѴШ, а именно, 5 = — дѣйствительно даетъ 7 = 0
при 7 = 0. Далѣе, Ріапск разсматриваетъ не свободную энергію Р, но
величину, равную Ф : Г, гдѣ Ф = 17 — Т8 -\-рѵ — термодинамическій потен-
ціалъ. Это приводитъ его къ результату, что при 7 = 0 теплоемкость ср = О
для всякаго твердаго или жидкаго тѣла, что и подтвержда-
ется изслѣдованіями И е г п 8 Ѵа и его учениковъ, о чемъ уже было ска-
зано на стр. 234.
Въ послѣдней работѣ ^е^п8І (1911) говоритъ, что вблизи 7=0
всѣ физическія величины дѣлаются независимыми отъ Т. Сюда отно-
сится 17. а потому Гр = г^=О; далѣе, объемъ, такъ что коеффиці-
ентъ расширенія дѣлается равнымъ нулю. Сжимаемость должна
при малыхъ Т оказаться независимой отъ 7, что подтверждается опытами
Стгііпе І8 еп’а (1911).
Мы здѣсь не можемъ входить въ дальнѣйшія подробности, относя-
щіяся къ интереснымтэ выводамъ изъ гипотезы е г п 8 Ра.
ЛИТЕРАТУРА.
Къ § 1.
Ваккег. 2І8СІ1Г. рііуе. Сііет. 14 р. 671. 1894; 17 р. 171, 1895; <1. 4е рЪуе. (3) 7
р. 152, 1898.
Зоиіе. РКП. Ма&. (3) 26 р. 369, 1845.
Не^паиіі. С. К. 36 р. 680, 1853.
Нігп. Тііёогіе тёсапідие 4е Іа сЬаІеиг, 2-ое изд., т. I, р. 52.
Хеипег. ТесѣпібсЪе ТЬегтойупатік. Ьеіргі^, 1887, т. I, р. 142.
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. III, изд. З-е.
31
482
Приложенія термодинамики.
Къ § 2.
Ткотзоп апсі Лшіе. РЫІ. Тгапз. 143 р. 357,1853 ; 144 р. 321, 1854 ; 152 р. 579, 1862.
Ыаіапзоп. АѴ. А. 31 р. 502, 1887.
8МИег. Ж Ф. X. О. 22 р. 110, 1890; АѴ. А. 40 р. 149, 1890.
ЗосНтапп. ЙсЫоѳшіІсІГз ЯЫсЫ. 1. РЬуз, и. МаШ. 5 р. 106, 109, 1860.
Дозе-Іппез. РЫІ. Ма^. (5) 45 р. 227, 1898; 50 р. 251, 1900; (6) 2 р. 130, 1901;
6 р. 353, 1903; 15 р. 301, 1908.
ОІ8?ехѵ8кі. Аппаі. 4. Рііуз. (4) 7 р. 818, 1902 ; РЫІ. Ма$. (6) 3 р. 535, 1902
Къ § 4.
СіЫэ8. ТЪегшосІупатібсІіе 8іийіеп, р. 258.
Ѵап сіег \ѴааІ8. ХізсЫ. рііуз. Сііет. 13 р. 657, 1894.
БиНет. С. В. 102 р. 1548, 1886.
Р. ѵ. НеШіоІіг. АѴ. А. 27 р. 508, 1886.
Ѵ/агЬиг^. АѴ. А. 28 р. 394, 1886.
8іе/ап. \Ѵ. А. 29 р. 655, 1886.
ѵ. Ьап& АѴіеп. Вег. 99, II,а р. 809, 1891.
Еіпзіеіп. П. А. 4 р. 513, 1901.
Кіеетапп. РЫІ. Ма^. (6) 18 р. 39, 1909.
Іешіз. РЫІ. Ма&. (6) 15 р 199, 1908; 17 р. 466, 1909.
Къ § 7.
Вагіоіі е 8ігассіаіі. Мііоѵо Сіт. (3) 36 р. 127, 1894.
Ріеіегісі. \Ѵ. А. 57 р. 333, 1896.
Оог8Іп& Апп. (1. Рііуз. (4) 25 р. 277, 1908.
Ьиззапа. К Сіт. (5) 19 р. 182, 1910.
Огііпеізеп. Апп. 6. Рііуз. (4) 26 р. 393, 1908.
Къ § 8.
Огескег. АѴ. А. 20 р. 870, 1883.
Зоиіе. РЫІ. Тгапз. 149 р. 133, 1859; РЫІ. Ма§. (4) 15 р. 17, 1858.
Сгееітапп апсі Сгоскеі. Ргос. В. 8ос. ЕйіпЪ. 13 р. 311, 1884.
Вигіоп апсі Магзкаіі. Ргос. В. 8ос. 50 р. 130, 1891.
Къ § 9.
Зоиіе. РЫІ. Тгапз. 149 р. 91, 1859.
Есііипй. Ро^. Апп. 126 р. 539, 1865.
Оакіапйег. Ро^. Апп. 145 р. 147, 1872.
На$а. АѴ. А. 15 р. 1, 1882.
ХѴаззтиік. АѴіеп. Вег. 98 р. 1393, 1889; 111 р. 1012, 1902; 112 р. 578, 1903;
И. А. 97 р. 52, 1888; 11 р. 146, 1903; 13 р. 182, 1904; ВоіЫтапп — ГезізсЫій, 1904 р. 555.
Данникъ. Ж. Ф. X. О. 40 р. 335, 1908.
Къ § 11.
Мегп8і. бюШп&ег ЫасЫ. 1906 р. 1; Вегі. Вег. 1906 р. 933; 1909 р. 247; 1911
р. 65; Арріісаііопз оі‘ Тііегтойупатіс іо Сііетізігу, Ьопйоп, 1907; ТІіеогеі. Сііетіе,
6-ое изд. р. 699—713, 732—736, 1910; йеіізсЫ. 1. ЕІекігосЬетіе 1909 р. 687; 1910 р. 96;
РЬуз. ХеіізсЫ. 12 р. 976, 1911; Д. Зе Рііуз. (4) 9 р. 721, 1910.
Лазаревъ. Ж. Ф. X. О. 40, (2) р. 79, 1908; 44, (2) р. 9, 1912.
Ріапск. Тііегтойупатік, 3 изд. р. 266, 1911.
8аскиг. Аппаі. 4. Рііуз. (4) 34 р. 455, 1911.
Вгоепзіесі. Хізсііг. 1. рііуз. Сііет. 56 р. 645, 1906.
Ѵагіі Но// Воіігтапп-Гезізсіігій р. 233, 1904.
Огипеізеп. Ѵегіі. сі. й. Рііуз. Сез. 1911 р. 426 (см. р. 501;.
Общія замѣчанія.
483
ГЛАВА ДЕСЯТАЯ.
Переходъ изъ твердаго состоянія въ жидкое и обратно. При-
ложеніе термодинамики къ общему случаю перехода вещества
изъ одного состоянія въ другое.
§ 1. Общія замѣчанія. Фаза. Въ предыдущихъ главахъ мы рас-
ширили обычное понятіе о состояніи вещества, опредѣляя это состояніе
совокупностью физическихъ свойствъ вещества и подразумѣвая подъ из-
мѣненіемъ состоянія измѣненіе хотя бы одной изъ величинъ, опредѣ-
ляющихъ эти физическія свойства, напр., температуры, объема и т. д.
Теперь мы для краткости будемъ говорить о перемѣнѣ состоянія
тѣла въ обычномъ смыслѣ, подразумѣвая переходъ тѣла изъ одного изъ
трехъ состояній, твердаго, жидкаго или газообразнаго, въ другое. Въ
этой главѣ мы разсмотримъ переходъ вещества изъ состоянія твердаго въ
жидкое и обратно, т.-е. такъ называемыя явленія плавленія и затвердѣ-
ванія, причемъ мы ограничиваемся тѣми случаями, когда переходы вы-
званы измѣненіями температуры или давленія. Интерес-
ный случай, когда переходъ вызванъ соприкосновеніемъ веществъ между
собою, т.-е. явленіе растворенія мы разсмотримъ отдѣльно въ по-
слѣдней главѣ.
Въ явленіяхъ перехода тѣлъ изъ одного состоянія въ другое мы,
впрочемъ, также имѣемъ дѣло съ соприкосновеніемъ тѣлъ физически раз-
нородныхъ, хотя и одинаковыхъ по химическому составу. Здѣсь будетъ
умѣстно познакомиться ближе съ терминомъ «фаза», который былъ вве-
денъ по предложенію б іЪЬз’а, и о которомъ уже было упомянуто выше.
Если мы имѣемъ нѣсколько соприкасающихся веществъ, или, какъ иногда
говорятъ, систему (или комплексъ) веществъ, то каждое вещество,
которое можетъ быть удалено изъ этой системы чисто
механическимъ способомъ, называется фазою. Если мы
имѣемъ ледъ, плавающій въ водѣ, то передъ нами двѣ фазы: твердая и
жидкая; если надъ ними находится еще паръ, то это третья фаза. Ра-
створъ одного вещества въ другомъ представляетъ одну фазу, ибо со-
ставныя части такого раствора не могутъ быть отдѣлены другъ отъ друга
механическимъ способомъ. Ненасыщенный растворъ и паръ надъ нимъ
представляютъ двѣ фазы. Насыщенный растворъ соли съ избыткомъ соли
нерастворенной и паръ надъ ними — это три фазы. При охлажденіи
раствора могутъ получиться четыре фазы: соль, ледъ, растворъ и паръ.
При нагрѣваніи многихъ твердыхъ тѣлъ замѣчается, что они при нѣ-
которой опредѣленной температурѣ переходятъ въ жидкое состояніе ; это
явленіе называется п’л а в л е н і е м ъ. Температура при которой оно со-
вершается, называется точкою плавленія. При этой же темпера-
турѣ происходитъ, вообще говоря, и обратный переходъ изъ жидкаго со-
стоянія въ твердое, если отъ жидкости отнимать теплоту; такимъ обра-
зомъ точка затвердѣванія (о водѣ говорятъ, что она замерзаетъ)
тождественна съ точкою плавленія. Весьма трудно нагрѣть твердое тѣло
31*
484
Плавленіе и затвердѣваніе.
выше точки плавленія, соотвѣтствующей его химическому составу и тѣмъ
внѣшнимъ физическимъ условіямъ, отъ которыхъ, какъ мы увидимъ нижеш
эта точка зависитъ, безъ того, чтобы тѣло расплавилось: жидкое же
тѣло при нѣкоторыхъ условіяхъ можетъ быть охлаждено значительно ниже
точки плавленія и затвердѣванія, не переходя при этомъ въ твердое со-
стояніе. Это явленіе переохлажденія жидкостей.
Температура плавленія і зависитъ отъ давленія р,
подъ которымъ вещество находится, такъ что можно писать
і = ^Р)................................(1)
или наоборотъ •
Р=/Ѵ)..................................(2)
Впрочемъ, эта зависимость не очень замѣтна въ обыденномъ смыслѣ
слова, т.-е. температура і мало мѣняется при значительныхъ измѣненіяхъ
давленія р.
Если къ твердому тѣлу непрерывно притекаетъ теплота, то его тем-
пература поднимается до точки плавленія, и затѣмъ остается постоянною
въ теченіи всего времени, пока происходитъ переходъ изъ твердаго состо-
янія въ жидкое. Этотъ переходъ никогда не происходитъ мгновенно, но
продолжается нѣкоторое время, зависящее отъ количества твердаго веще-
ства и отъ быстроты притока къ нему теплоты. Когда все вещество рас-
плавилось, вновь начинается повышеніе температуры массы, теперь уже
жидкой. Теплота, притекающая въ періодъ плавленія, и не вызывающая
поднятія температуры, тратится на внутреннюю работу, на увеличеніе
потенціальной энергіи вещества. При обратномъ переходѣ изъ
жидкаго состоянія въ твердое замѣчается обратное явленіе : охлажденіе
жидкости прекращается, когда достигается точка затвердѣванія и когда
дѣйствительно начинается затвердѣваніе, во время котораго температура
остается постоянною. Часть потенціальной энергіи жидкой массы пере-
ходитъ въ энергію тепловую, которая и пополняетъ собою убыль теплоты,
вызванную продолжающимся ея утекомъ. Пониженіе температуры вновь
начинается, когда вся масса перешла въ твердое состояніе. Теплота,
поглощаемая при плавленіи, или равная ей, выдѣля-
емая при затвердѣваніи, называется скрытою тепло-
тою плавленія или затвердѣванія; мы ее обозначимъ черезъ р.
Обыкновенно ее относятъ къ вѣсовой единицѣ вещества. Мы бу-
демъ ее относить къ одному килограмму и выражать въ большихъ кало-
ріяхъ. Скрытая теплота р зависитъ отъ температуры /, при которой проис-
ходитъ переходъ вещества изъ одного состоянія въ другое, или отъ того
давленія р, подъ которымъ вещество находится, такъ что можно написать
е = 9>(0............................................................(з)
ИЛИ х ч /
6 = 9>і(р) .............О)
Начальное, равномѣрное съ теченіемъ времени поднятіе температуры
твердаго тѣла, внезапное прекращеніе этого поднятія, полное постоянство
Точка плавленія.
485
температуры за все время плавленія и, наконецъ, внезапное возобновле-
ніе равномѣрнаго, хотя и съ другою скоростью, поднятія температуры —
все это представляетъ идеальную картину плавленія, наблюдаемую только
при плавленіи веществъ кристаллическихъ, напр. льда. Понятно,
что при этомъ предполагается равномѣрный притокъ теплоты. Для та-
кихъ кристаллическихъ тѣлъ величины і и д имѣютъ вполнѣ опредѣлен-
ное и ясное значеніе. При плавленіи тѣлъ некристаллическихъ, каковы
жиры, воскъ, стекло,желѣзо и т.д., картина мѣняется. Замѣчается прежде всего
замедленіе поднятія температуры до достиженія точки плавленія, ко-
торая однако достаточно рѣзко опредѣляется продолжительнымъ постоян-
ствомъ температуры во время плавленія. При этомъ замѣчается, что тѣло
до начала плавленія дѣлается мягкимъ и какъ бы постепенно пере-
ходитъ изъ твердаго состоянія въ жидкое. Для такихъ тѣлъ понятіе о
скрытой теплотѣ перестаетъ имѣть вполнѣ опредѣленное значеніе ; уве-
личеніе внутренней работы, а слѣд. и поглощеніе скрытой теплоты начи-
нается ранѣе замѣтнаго перехода въ жидкое'состояніе. Очевидно слѣдуетъ
причислить къ скрытой и ту теплоту, которая расходуется на размягче-
ніе твердаго тѣла. Для многихъ тѣлъ переходъ изъ твердаго состоянія
въ жидкое происходитъ такъ постепенно, что онъ отмѣчается только сперва
замедленнымъ, а затѣмъ вновь ускореннымъ нагрѣваніемъ. Опредѣленной
точки плавленія не существуетъ, если не принимать за таковую ту, при
которой измѣненіе температуры происходитъ наиболѣе медленно.
§ 2, Точка плавленія. Идеи Тамманна. Явленія, описанныя въ
предыдущемъ параграфѣ, привели Тамманна къ мысли, что только
кристаллическое состояніе вещества соотвѣтствуетъ тому особому
состоянію, которое можно назвать твердымъ (Тезѣ). Оно существенно
отличается отъ жидкаго и газообразнаго тѣмъ, что въ послѣднихъ двухъ
состояніяхъ распредѣленіе частицъ вполнѣ безпорядочное, а въ немъ оно
опредѣленнымъ образомъ упорядочено (т. I). Въ аморфныхъ тѣлахъ,
которыя могутъ быть тверды (Ііагі) въ обыденномъ смыслѣ слова, распре-
дѣленіе частицъ также вполнѣ безпорядочное.
Между состояніями газообразнымъ, жидкимъ и аморфнымъ возможны,
поэтому, непрерывные, т.-е. безъ скачковъ, переходы. При критической
температурѣ газъ и жидкость безъ перерыва переходятъ другъ въ друга,
т.-е. безъ измѣненія объема и безъ поглощенія скрытой теплоты. При
переохлажденіи жидкость можетъ непрерывно дѣлаться все гуще и нако-
нецъ становится твердой, какъ стекло, переходя въ аморфное «твердое» тѣло.
Но переходъ отъ жидкаго или отъ аморфнаго состоянія къ твердому
никогда не можетъ происходить непрерывно, и то же самое относится къ
переходу отъ одной кристаллической формы въ другую, когда существу-
етъ полиморфизмъ (т. I).
Тамманнъ разсматриваетъ всѣ аморфныя тѣла, какъ
переохлажденныя жидкости и считаетъ, что только
кристаллы находятся въ особомъ «твердомъ» состо-
яніи. Переходъ жидкое -- твердое никогда не можетъ происходить
486
Плавленіе и затвердѣваніе
непрерывно, а потому для этого перехода не существуетъ критической
температуры.
Для опредѣленія точки плавленія наблюдаютъ температуру посте-
пенно охлаждающагося расплавленнаго тѣла. Она сперва понижается за-
тѣмъ остается нѣкоторое время постоянною и наконецъ снова понижа-
ется. Ея значеніе во второмъ изъ этихъ трехъ періодовъ и даетъ иско-
мую точку плавленія, если только не происходитъ переохлажденія. Если
же жидкость переохлаждается, то ее можно охладить ниже точки плавле-
нія и однимъ изъ способовъ, указанныхъ ниже, заставить внезапно за-
твердѣть, причемъ ея температура мгновенно повышается до точки плав-
ленія, какъ мы увидимъ ниже.
Малыя количества вещества помѣщаются внутри капилярной трубки,
которая вмѣстѣ съ термометромъ помѣщается въ подходящую, постепенно
нагрѣваемую жидкость, напр. въ воду, сѣрную кислоту, масло, расплавлен-
ный параффинъ и т. д. Моментъ плавленія наблюдается непосредственно
по измѣненію вида вещества, а иногда и по тому, что вещество, дѣ-
лаясь жидкимъ, начинаетъ стекать внутри вертикально поставленной
трубки. Вопросомъ о точнѣйшемъ опредѣленіи точки плавленія занима-
лись Ьапсіоіі, Ріссагсі, ^гп81 и Невве, Апесііиеіг и
8 с Ь и 11 г , К о і Ь, Потылицинъ, Ѵісіог Меуег и друг.; лю-
бопытный электрическій способъ предложилъ Ь о е лѵ е (см. Ы е г и 8 1 и
Н е 8 8 е въ указаніи литературы).
Ее ТЬіеггу (1905) опредѣлялъ точки плавленія не-проводни-
ковъ электричества, помѣщая ихъ между двумя контактами такимъ обра-
зомъ, что при плавленіи токъ замыкался. Жуковъ и Курбатовь
(1907) пользовались короткой проволокой изъ изслѣдуемаго металла,
включая ее въ основную цѣпь батареи; при плавленіи проволоки основ-
ная цѣпь разрывалась, при чемъ въ побочной цѣпи начиналъ звонить
электрическій звонокъ.
Точка плавленія элементовъ мѣняется періодически, въ зависимости
отъ ихъ атомнаго вѣса. Эти періоды выражены не рѣзко, но все же ока-
зывается, что въ каждомъ изъ восьми рядовъ системы Менделѣева
замѣчается возрастаніе температуры плавленія съ возрастающимъ атом-
нымъ вѣсомъ.
Простые законы, которыми опредѣлялись бы точки плавленія, до
сихъ поръ не найдены. Были найдены лишь немногія правила, изъ ко-
торыхъ мы укажемъ одно, довольно любопытное. В а е у е г указалъ, что
въ гомологическихъ рядахъ четные и нечетные члены рѣзко отличаются
другъ отъ друга своими точками плавленія. Приводимъ точки плавленія
для ряда янтарной кислоты:
С4Я6О4 .... 180°
СбЯ8О4............... 970
• • 148°
С7//12С>4...........103°
С8//14О4 .... 140°
с9я16о4..............іобо
С1с/Ав^4 .... 127°
Сц^Ч*0^4.............108°.
Точка плавленія.
487
На другія правильности указали Т Ь. Реіегвеп, М ар ко в н и ко в ъ,
Ьепг, Солонина, РгапсЬітопі, МІ1І8 идр.
Нѣкоторыя тѣла затвердѣваютъ лишь при весьма низкихъ темпера-
турахъ. Такъ жидкій водородъ затвердѣваетъ при - 258°, жидкій азотъ
при - 214°, жидкій хлоръ при 102°; дальнѣйшіе примѣры мы приве-
демъ въ статьѣ объ ожиженіи газовъ. Изъ тѣлъ жидкихъ при обыкновен-
ныхъ температурахъ, упомянемъ: сѣрнистый углеродъ—113°, метиловый
алкоголь — 97,8°, этиловый алкоголь — 107,3°, хлористый этилъ— 141,6°.
Ртуть затвердѣваетъ при — 39°. Наоборотъ существуютъ тѣла, точки
плавленія которыхъ расположены очень высоко; они называются туго-
плавкими; нѣкоторыя тѣла, повидимому, до сихъ поръ вовсе не уда-
лось расплавить. Къ весьма тугоплавкимъ тѣламъ принадлежатъ нѣко-
торые металлы и ихъ окислы. 8аіпіе-С1аіге-Веѵі11е, одинъ изъ
первыхъ, расплавилъ платину и кремній ; Сг а и <1 і п первый воспользо-
вался для этой цѣли водороднымъ пламенемъ, въ которое вдувалась струя
кислорода. Ему удалось расплавить известь и кварцъ. В е р г е I г рас-
плавилъ кремній, боръ, титанъ и молибденъ, пользуясь электрическимъ
токомъ. Наиболѣе замѣчательные опыты были произведены въ этомъ на-
правленіи М о і 8 8 а п’омъ, построившимъ особаго рода электриче-
скую печь, въ которой при помощи сильныхъ электрическихъ то-
ковъ достигается въ небольшомъ пространствѣ весьма высокая темпера-
тура. Въ этой печи, повидимому, плавятся всѣ металлы и металлоиды,
причемъ образуются опредѣленныя химическія соединенія металловъ съ
кремніемъ, боромъ и въ особенности съ углеродомъ. По степени туго-
плавкости М о і 8 8 а п распредѣляетъ металлы въ такой рядъ : Рі, Сг, Мо,
Ѵг, Ѵ7о, Ѵа, причемъ Ѵа имѣетъ наиболѣе высокую точку плавленія.
Алмазъ въ электрической печи разбухаетъ и чернѣетъ. Въ послѣдніе
годы, въ особенности съ 1905, многочисленные изслѣдователи старались
опредѣлить съ возможно большей точностью точки плавленія ряда туго-
плавкихъ металловъ, преимущественно золота, мѣди, платины и
палладія. Главной цѣлью этихъ изслѣдованій являлось точное опредѣле-
ніе высокихъ постоянныхъ термометрическихъ точекъ, которыя могли-бы по-
служить для построенія точной шкалы, доходящей до высокихъ температуръ.
Для точнаго опредѣленія температуръ плавленія употреблялись раз-
нообразные методы, разсмотрѣнные нами въ главѣ, посвященной пироме-
тріи. За послѣдніе годы особенно часто примѣнялись методы оптической
пирометріи (гл. II § 13). Полученные такимъ путемъ результаты зави-
сятъ однако отъ численнаго значенія постоянныхъ, входящихъ въ фор-
мулы излученія, что дѣлаетъ эти результаты до нѣкоторой степени не
достовѣрными. Напримѣръ, при употребленіи формулы (47) стр. 65,
окончательный результатъ оказывается зависящимъ отъ посгоянной с,
которую мы приняли равной 14500, тогда какъ различные изслѣдователи
принимали ее равной инымъ немного отличнымъ числамъ
Мы приведемъ сперва результаты измѣреній, относящихся къ Аи,
Си, Рі и Ра.
488
Плавленіе и затвердѣваніе.
I. Золото. Старыя опредѣленія давали слѣдующія числа для
точки плавленія: НоІЪогп и АѴіеп (1895) 1072°, Неусоск и Ме-
ѵіііе 1061,7°, И. ВегіЬеІоі (1898) 1064°, СаІІепДаг (1899) 1061°,
ВоЪетіе Ливіей и Вове (1900) 1063°, НоІЪогп и Вау (1901)
1063,5° (въ СО2). Изъ этихъ изслѣдователей В. ВегіЪеІоі пользо-
вался особымъ оптическимъ методомъ, описаннымъ нами въ гл. П§ 11, IV
и въ началѣ § 13. НоІЪогп и Вау пользовались термоэлементомъ
(Рі—Рі-\-РК). Изъ новыхъ работъ упомянемъ прежде всего работу
Яасдпегой и Реггоі (1905), которые измѣряли температуру при по-
мощи газоваго термометра (воздухъ, Ы, О, СО, СО2). Приводя резуль-
таты, полученные В. Вегійеіоі и НоІЪогп и Вау’емъ къ абсо-
лютной шкалѣ температуръ Яасдиегосі и Реггоі даютъ слѣду-
ющія числа:
В. ВегіЪеІоі 1065,6°
НоІЪогп и Вау 1064,3°
Яасдпегосі и Реггоі 1067,4°
Среднее 1066°.
Новѣйшее изслѣдованіе было произведено Вау и Сіетепі’омъ
(1908); они пользовались термоэлементомъ, шкала котораго была опре-
дѣлена при помощи кислороднаго термометра. Они получили нѣсколько
меньшее число — 1059,3°.
П. Мѣдь. Интересно, что точки плавленія Си и Аи лежатъ другъ
къ другу настолько близко, что первоначально было трудно рѣшить, ко-
торая изъ нихъ лежитъ выше. Опредѣленія точки плавленія Си дали
слѣдующіе результаты:
НоІЪогп и АѴіеп 1082°
Неусоск и МеѵіПе 1080,5°
НоІЪогп и Вау 1084,1°
Вау и Сіегаепі 1081,0°
Эти числа относятся къ случаю плавленія безъ доступа воз-
духа; для плавленія на открытомъ воздухѣ НоІЪогп и Вау нашли
значительно болѣе низкое число — 1064,9°.
Ш. Платина и палладій. Изъ старыхъ опредѣленій приве-
демъ лишь нижеслѣдующія:
Рі Р4
НоІЪогп и АѴіеп 1780° 1587°
Ноітапп, Ьаигепсе и Вагг 1760° —
Въ послѣднее время были получены слѣдующіе результаты:
Рі РЛ
Нагкег (1905) 1710° —
НоІЪогп и Неппіп^ (1905) 1710°—1729° 1540°—1549°
Мегпні и АѴагіепЪег§' (1906) 1745° 1541°
Точка плавленія
189
РІ Р(І
НоІЬогп и Ѵаіепііпег (1906) 1789° 1575°
АѴаідпег и Впт^еев (1907) 1753° 1546°
МепдепЬаІІ и Іг^епвоіі (1907) — 1548° или 1576°
’ѴѴ’аісіпег и Впг^евв (1909) 1770° —
Критическое изслѣдованіе различныхъ методовъ опредѣленія точки
плавленія Рі произвели Еёгу и Сйёпеѵеап (1909); они указали на
большое вліяніе окружающаго газа.
Кегп8І и ЛѴагіепЪег^ пользовались оптическимъ пироме-
тромъ АѴаппег’а (гл. II § 13), который они подвергли тщательному из-
слѣдованію. Для постоянной с они приняли число 14600. НоІЬогп и
Ѵаіепііпег приняли с = 14200; въ этомъ предположеніи измѣренія
^гпвГа и АѴатІепЪет^’а даютъ слѣдующія числа:
Рі — 1775°; Р(І — 1563°.
Числа, найденныя Н о 1Ь о г п’омъ и Ѵаіепііпе г’омъ, лежатъ близко
къ этимъ. Мепсіе'пЬаІІ и Іп§ег8ОІ1 получили для Рсі два числа,
такъ какъ они исходили изъ температуры плавленія Рі и для послѣдней
принимали два вышеприведенныя числа 1745° и 1789°.
IV. Иныя тугоплавкія вещества. Изъ новыхъ работъ ни-
жеслѣдующія представляютъ большой интересъ.
АѴаійпег и Впт^е88 (1907), ВоИоп (1907) и АѴаіЧеп-
Ьег§ (1907) получили слѣдующіе результаты для вольфрама, тан-
тала и ніобія: ІГо 7а ыь
АѴаісІпег и Впг^еее 3080° 2910° —
АѴагіепЬег^ 2800°—2850° — —
ВоИоп — — 1950°
ДѴаіЧепЬегд’ пользовался оптическимъ пирометромъ ДѴ а п п ег’а.
ВоИоп также пользовался оптическимъ методомъ.
Мепсіепііаіі и Іп^етвоП нашли для точки плавленія стер-
женька лампы Кетп8І'а (т. IV) температуру 2380° и 2490° (см. выше).
Они-же получили для родія и иридія слѣдующія числа:
родій — 1907° или 1968°; иридій 2292° или 2388°.
Сгоойлѵіп и Маііеу (1907) нашли для чистой магнезіи (А/^О)
помощью пирометра АѴаппег’а температуру плавленія равной 1910°.
81еіп (1907) нашелъ, что чистая 8іО2 при 1600° становится вяз-
кой, а при 1750° текучей.
Углеродъ до сихъ поръ расплавить не удалось. Изслѣдованія
МоІ8 8ап’а привели къ заключенію, что углеродъ, почти всегда можетъ
плавиться только подъ высокимъ давленіемъ. Опыты Ьа Воза (1909)
привели однако къ заключенію, что при опредѣленныхъ условіяхъ и при
нормальномъ давленіи можетъ происходить расплавленіе углерода въ элек-
трической поющей вольтовой дугѣ (т. IV) и въ электрической искрѣ.
490
Плавленіе и затвердѣваніе
Нижеслѣдующія опредѣленія были сдѣланы за послѣдніе годы съ
высокою степенью точности Неусоск’омъ и Ыеѵіііе-’мъ (1895), Саі-
I е п д а г’омъ (1899). Н о 1 Ь о г п’омъ и Рау (1900), Б ау и Сіе -
т е п Сомъ:
Неусоск и Хеѵіііе Саііепсіаг НоІЬогп и Вау Вау и Сіетепі
Сй 320,7 321,7 —
РЬ 327,6 — 326,9 —
7.П 419,0 — 419,0 418,5
ЗЬ 629,5 — 630,6 —
АІ 654,5 — 657,0
А§ 960,7 961,5 958,3
Л^въ воздухѣ) 955,0 955,0 —
Ві 267,5 269,2 — —
Для 8гі Неусо ск и еѵ ііIе нашли 231,9°, Курнаковъ и Пу-
тинъ (1902) 231,5°.
Виг^ев8 опредѣлялъ температуры плавленія металловъ желѣзной
группы и получилъ слѣдующія данныя:
Ее Сг Со Ыі Мп
1505° 1489° 1464° 1435° 1207°
§ 3. Точка плавленія сплавовъ.. Сплавами мы называемъ однород-
ныя смѣси твердыхъ тѣлъ, полученныя «сплавленіемъ», т.-е. смѣшивані-
емъ составныхъ частеіі при достаточно высокой температурѣ, когда всѣ
эти части находятся въ жидкомъ состояніи Обыкновенно, говоря о спла-
вахъ, имѣютъ въ виду сплавы металлическіе; но могутъ быть также
сплавы, составленные изъ нѣсколькихъ кристалловъ, изъ жировъ или изъ
другихъ сплавляющихся веществъ. Строго говоря, сюда жо могутъ быть
отнесены и растворы, если только растворимое и растворитель, отдѣльно
взятые, имѣютъ опредѣленную точку затвердѣванія. И дѣйствительно
оказывается, что сплавы и растворы во многихъ отношеніяхъ облада-
ютъ вполнѣ аналогичными свойствами. Въ главѣ о растворахъ мы уви-
димъ, что точка затвердѣванія растворовъ лежитъ ниже точки затвер-
дѣванія растворителя, и мы познакомимся съ формулою ѵап ѴН о Г Га, опре-
дѣляющей величину пониженія этой точки. Впрочемъ, эта формула уже
была приведена въ т. I. Оказывается, что эта формула, хотя и въ огра-
ниченной степени, приложима и къ сплавамъ, какъ показали изслѣдо-
ванія Таттапп’аиНеусоск и Иеѵіііе’я.
Обращаемся прежде всего къ сплавамъ металловъ. Добавленіе не-
большого количества одного металла къ другому вообще понижаетъ
точку плавленія перваго, играющаго роль растворителя. Отложимъ на
оси Ох (рис. 132) процентное содержаніе металла В въ сплавѣ его съ
металломъ Л, такъ что точка О соотвѣтствуетъ чистому металлу А
(100 частей), и пусть точка Р соотвѣтствуетъ чистому металлу В. На
ординатахъ откладываемъ температуры плавленія сплавовъ, такъ что ОЕ —
Точка плавленія сплавовъ.
491
и РР— температуры плавленія металловъ А и В. Если къ металлу А
постепенно прибавлять металлъ В, то точки плавленія опредѣляются почти
прямой линіей ЕО; другая прямая РО получается, если къ металлу В
постепенно прибавлять металлъ А. Точка О соотвѣтствуетъ опредѣлен-
ному сплаву, который Сг и 1Ь г і е назвалъ
эвтектическимъ. При охлажденіи
одного изъ сплавовъ ОС затвердѣваютъ
сперва массы, болѣе богатыя металломъ А,
между тѣмъ какъ изъ сплавовъ СВ выдѣ-
ляются массы, болѣе богатыя металломъ В.
Если эти массы удалять, то отъ сплава
любого процентнаго содержанія всегда въ
концѣ концовъ останется сплавъ эвтекти-
ческій, затвердѣвающій при опредѣленной
температурѣ Ѳ = СО, какъ цѣлое. Мы уви-
димъниже,что эвтектическіе сплавы
X
вполнѣ аналогичны такъ назы-
ваемымъ кріогидратамъ, которые получаются изъ водныхъ ра-
створовъ. О а и і і е г нашелъ, что линія ЕОР замѣняется прямою ЕР,
когда металлы А и В изоморфны. Изображенный на рис. 132 простой
ходъ кривой плавленія» ЕОР въ весьма многихъ случаяхъ замѣ-
няется несравненно болѣе сложнымъ. Если существуетъ опредѣленное
химическое соединеніе между металлами, то линія ЕОР принимаетъ бо-
лѣе сложный видъ: на ней появляется максимумъ, соотвѣтствующій
этому соединенію, и два минимума, соотвѣтствующіе двумъ эвтектиче-
скимъ сплавамъ. Максимумъ можетъ даже лежать выше болѣе высокой
изъ точекъ плавленія двухъ составныхъ частей сплава. Сюда относится
открытый КоЬегів-Аизіеп’омъ сплавъ Аи и АІ пурпуроваго цвѣта,
соотвѣтствующій формулѣ АІ^Аи; его точка плавленія выше, а по но-
вѣйшимъ изслѣдованіямъ Неусоск и Меѵіііе’я какъ разъ равна
точкѣ плавленія чистаго золота. Другой примѣръ, а именно Ыа
и — К изслѣдовали впервые Мегг и ЛѴ еі 1Ь.
Какъ мы уже упоминали выше, начиная съ 1905 года появились
многочисленныя работы, посвященныя опредѣленію точекъ плавленія спла-
вовъ, произведенныя преимущественно въ Россіи, Германіи и Франціи.
Въ Россіи большая часть изслѣдованій была произведена Курнико-
вымъ и его учениками; эти изслѣдованія опубликованы въ Журналѣ
Русскаго Физико-Химическаго Общества и въ 2еіІ8сЬгіЙ Ійг Апог^а-
пібсЬе СЬетіе. Громадное число изслѣдованій было произведено Т а ш -
ш а п п’омъ и его учениками въ Геттингенѣ; эти работы почти всѣ опу-
бликованы въ 2еіІ8сЬгіЙ Гііг Апог^апівсЬе СЬетіе.
Таттапп (1908) опубликовалъ обзоръ работъ своихъ и своихъ
учениковъ. Въ весьма интересной таблицѣ онъ сопоставилъ около 120 не-
сомнѣнныхъ данныхъ для металлическихъ соединеній.
\Ѵгі^Ы, Сгаиііег и АиЬеІ изслѣдовали сплавъ 5Ь А/. Сплавъ
492
Плавленіе и затвердѣваніе.
формулы 8ЬАІ плавится при 1080е (8Ь при 630°, АІ при 660°); его
плотность 4,2176, между тѣмъ какъ она равнялась бы 5,2246, еслибы при
образованіи сплава не произошло большого увеличенія объема.
Курнаковъ, отчасти вмѣстѣ съ Лушинымъ, изслѣдовалъ мно-
жество сплавовъ. Изъ полученныхъ имъ результатовъ разсмотримъ два.
Ыа плавится при 97°, при — 39°. Если постепенно прибавлять
къ Ыа, то кривая плавленія сперва падаетъ до 21°,25 при 15 атомныхъ
процентахъ. Затѣмъ кривая поднимается, распадаясь на четыре дуги,
отдѣленныя другъ отъ друга перегибами; она доходитъ до 346° при
66,74°/0 что соотвѣтствуетъ формулѣ ; далѣе кривая опять
опускается. Не менѣе удивителенъ сплавъ Ыа— К (А/« плавится при 97°,
К при 62°,5). Сплавъ 1,497 : 1 плавится при 6°,88, а сплавъ
А/я : К—2 : 1 даже при — 12°,5.
Нѣкоторые сплавы отличаются необычайной низкой точкой плавле-
нія. Укажемъ на ихъ составъ по изслѣдованіямъ Маггоііо, который
нашелъ, что для нихъ точка плавленія не совпадаетъ съ точкою за-
твердѣванія ; въ скобкахъ указаны точки плавленія составныхъ частей.
Сплавъ Сплавъ Сплавъ Сплавъ
Вове. 0 а г с е Г. АѴ о о (Га. Ь ірр олѵі іг’а.
Ві (260°) 48,66% 49,21% 55,43% 50,66%
РЬ (325°) 24,00 » 32,55 » 25,84 » 24,97 »
8п (230°) 27,34 » 18,44 > 14,73 » 14,24 »
са (3200) — — 6,99 » 10,13 >
Точка плавленія: 96°,8 99°,2 75°,5 75°,5
Точка затвердѣванія: 95°,5 95°,0 67°,0 66°,8.
Въ послѣднее время найдены сплавы тѣхъ же четырехъ металловъ —
ВЦ 8Ь, 8п и РЬ, еще болѣе легкоплавкіе, нежели вышеуказанные. Два
сплава — 2ЬРЬ + 12,55л + ѢЪВі -ф 12,50/ и 12РЬ -ф 165л + 602?/+ \2Сй
плавятся уже при 55,5°.
Н а 11 о с к’у удалось получить жидкій сплавъ, нагрѣвая (при не-
большомъ сдавливаніи) до 100° смѣсь порошкообразныхъ составныхъ ча-
стей сплава Ѵѵ о о (Га.
Вопросомъ о плавленіи амальгамъ занимались ВсЬиеіг (1892)
и въ особенности Бахметьевъ и Въжаровъ. Работы послѣднихъ
содержатъ обстоятельный разборъ и литературу вопроса о плавленіи спла-
вовъ и амальгамъ.
Выше уже было указано, что неметаллическіе сплавы обладаютъ во
многихъ случаяхъ такими же свойствами, какъ и сплавы металлическіе.
Сюда относятся напр. сплавы солей. Такъ 8сЬаП^оІ8сЬ нашелъ,
что сплавъ изъ 54,3°/0 и 45,7% плавится при 226°, между
тѣмъ какъ точки плавленія составныхъ частей 338° и 313°. Подобныя
же изслѣдованія производилъ Сг и Нагіе. Вргіп^’у удалось расплавить
при 100° смѣсь солей К^'О^ и ІЧаСъНѵОс) (уксуснокислый натръ), кото-
рыя отдѣльно плавятся при температурахъ, лежащихъ выше 300°.
Переохлажденіе.
493
Неіпг, Ваіеііі и Раіагго, Ваіеііі и Магііиеііі,
Сапожниковъ и др. изслѣдовали сплавы органическихъ веществъ.
Приводимъ нѣкоторыя числа:
Нафталинъ. . 79°,3 Нафталинъ. . 79°,3 Нафталинъ 79°,3
Парафинъ . . 52°,4 Спермацетъ . 43°,9 Стеаринъ . . 54°,8
1 ч. нафтал. 1 3 ч. параф. ] 45°,2 1 ч. нафтал. 1 3,5 ч. спермац.] 36°,6 1 ч. нафтал. | 3 ч. стеарина| 46°,3
Здѣсь приведены эвтектическіе сплавы; другіе сплавы имѣютъ,
кромѣ указанной, еще одну болѣе высокую точку плавленія.
§ 4. Переохлажденіе. Мы упомянули (стр. 484). что при медлен-
номъ охлажденіи можно довести жидкость до температуры, лежащей зна-
чительно ниже температуры плавленія, или равной ей обычной темпера-
туры затвердѣванія. Такая жидкость немедленно затвердѣваетъ, если ее
подвергнуть сильному встряхиванію или перемѣшиванію, напр. стеклянною
палочкою, если въ нее вдувать струю воздуха, или если въ нее бросить
маленькій кусочекъ того твердаго вещества, плавленіемъ кото-
раго была получена жидкость. Прежде думали, что спокойное Рис. 133.
состояніе жидкости есть необходимое условіе возможности ея С
переохлажденія. Однако Везргеіг и Моиіі нашли, что
жидкость и во время сильнаго движенія можетъ достигнуть зна-
чительнаго переохлажденія. М о п і і охладилъ прокипяченую
воду до — 7°, подвергая ее все время сильному перемѣшива-
нію. Этимъ уничтожается гипотеза о неустойчивомъ распо-
ложеніи частицъ переохлажденной жидкости, которое будто
бы разрушается механическимъ дѣйствіемъ сотрясеній. ;іо
Первый, замѣтившій, что воду можно охладить ниже 0°,
былъ РаІігепІіеіЬ (1724); затѣмъ Сгау-Ьизеас показалъ, зо
что если покрыть воду слоемъ масла, то ее можно охладить
до — 12°. Везргеіг охлаждалъ воду въ термометренныхъ
трубкахъ даже до — 20°. Приборъ, изображенный на рис. 133 И
удобенъ для показанія переохлажденія воды. Онъ состоитъ и
изъ термометра, резервуаръ котораго окруженъ стекляннымъ
сосудомъ, содержащимъ воду. Если медленно охлаждать ниж-
нюю часть прибора, погрузивъ ее въ охлаждающую смѣсь, У
или окруживъ ее кисеею, которую обливаютъ эфиромъ, то не-
трудно охладить воду до —8°. Если затѣмъ встряхнуть приборъ, то вода
внезапно затвердѣваетъ, причемъ термометръ поднимается до 0°. Пере-
охлажденіе воды происходитъ и въ природѣ; такъ напр. морская вода
иногда переохлаждается. Когда она затѣмъ внезапно замерзаетъ, мо-
жетъ быть подъ вліяніемъ движенія, вызваннаго въ ней рыбой, то обра-
зуются въ огромномъ количествѣ отдѣльные куски льда — такъ назы-
ваемое сало.
Переохлажденіе легко удается съ жидкими каплями, плавающими
внутри другой жидкости (какъ въ извѣстныхъ опытахъ Р1 а I е а и, см. т. I).
494
Плавленіе и затвердѣваніе.
В и Г о и г охладилъ водяныя капли, плававшія внутри смѣси хлороформа
и миндальнаго масла, до — 20°. Капли сѣры въ растворѣ хлористаго
цинка удалось охладить до 20°, хотя точка плавленія сѣры 110°. Фос-
форъ, плавящійся при 44°, можно охладить подъ водою до 25° безъ того,
чтобы онъ затвердѣлъ. При этомъ любопытно, что малѣйшій кусочекъ
бѣлаго фосфора, попавшій въ переохлажденную жидкость, вызываетъ ея
затвердѣваніе, между тѣмъ какъ красный фосфоръ такого дѣйствія не
производитъ.
Сюда же можно отнести переохлажденіе расплавленныхъ солей, ка-
ковы глауберова соль (Ыа28О± + Ю/72О), сѣрноватистонатріевая соль
(7Ѵя253О3 + 5^0) и др. Однако здѣсь мы при нагрѣваніи получаемъ
растворы солей въ кристаллизаціонной водѣ, т.-е. переохлажденные ра-
створы. Если въ такую жидкость бросить малѣйшій кусочекъ той же
соли, то .кристаллизація немедленно начинается; черезъ нѣкоторое
время вся масса затвердѣваетъ, причемъ выдѣляется значительное коли-
чество теплоты.
Въ послѣднее время появился рядъ замѣчательныхъ изслѣдованій
Таттапп’а и его учениковъ по вопросу о переохлажденіи жидкостей.
Мы видѣли, что переохлажденная жидкость иногда, безъ перерыва, пере-
ходитъ въ аморфную, стекловидную массу. Въ другихъ случаяхъ
происходитъ кристаллизація, и притомъ либо сама собою, либо при вве-
деніи частицы твердаго вещества, Таттапп изслѣдовалъ 153 веще-
ства ; изъ нихъ 53 переходили въ аморфное, стекловидное состояніе.
Начавшаяся въ какой-либо точкѣ кристаллизація распространяется
въ переохлажденной жидкости съ нѣкоторою скоростью, которую обозна-
чимъ черезъ ѵ, Таттапп (1897) показалъ, что съ пониженіемъ тем-
пературы, т.-е. съ увеличеніемъ степени переохлажденія, скорость ѵ
сперва растетъ, потомъ остается постоянной, а затѣмъ быстро падаетъ,
дѣлаясь практически равной нулю для весьма сильно переохлажденной
жидкости. Далѣе Таттапп показалъ, что кромѣ скорости ѵ, слѣду-
етъ еще разсматривать способность къ кристаллизаціи,
которая измѣряется числомъ п ядеръ, или центровъ кристаллизаціи,
которые образуются въ данный промежутокъ времени въ единицѣ объема
переохлажденной жидкости. Это число также имѣетъ максимумъ при
опредѣленной степени переохлажденія, причемъ максимумъ п находится
при болѣе низкой температурѣ, чѣмъ максимумъ ѵ. Такъ напр. б е -
толъ (салициловый эфиръ — нафтола, С^Н^ОН)СОО. С10/77) пла-
вится при 95°. Скорость ѵ наибольшая около 75°; число п равно нулю
выше 30° и ниже —2°, его максимумъ при 30° и большія числа п на-
ходятся только между 20° и 10°. Чтобы опредѣлить п при низкой
температурѣ і, гдѣ ѵ = 0, слѣдуетъ держать жидкость нѣкоторое время
при /° и затѣмъ быстро нагрѣть до 75°. Образовавшіяся при ядра
при 75° быстро растутъ, дѣлаются видимыми и могутъ быть сосчитаны.
§ 5. Измѣненіе объема тѣлъ при плавленіи. Переходъ тѣлъ изъ
твердаго состоянія въ жидкое или обратно сопровождается иногда весьма
Измѣненіе объема при плавленіи.
495
значительнымъ измѣненіемъ объема, происходящимъ внезапно, или по
крайней мѣрѣ во время весьма малаго измѣненія температуры около точки
плавленія. Для большинства тѣлъ замѣчается увеличеніе объема при
плавленіи. Обратное явленіе т.-е. уменьшеніе объема при плавленіи
замѣчается на немногихъ тѣлахъ и составляетъ какъ бы исключеніе изъ
общаго правила. Нѣкоторыя тѣла обнаруживаютъ неправильныя
измѣненія объема вблизи точки плавленія, указывающія на из-
мѣненія внутренняго строенія вещества, предшествующія его переходу
изъ твердаго состоянія въ жидкое.
Наибольшій интересъ представляетъ уменьшеніе объема веще-
ства Н2О при переходѣ изъ твердаго состоянія въ жидкое, т.-е. при пе-
реходѣ льда въ воду. Егшапп первый (1827) точнѣе изслѣдовалъ это
явленіе, опредѣливъ плотности льда и воды около 0°. Онъ нашелъ, что
объемъ воды при 0° равенъ 0,9 объема воды при той же температурѣ.
Весьма тщательныя изслѣдованія объема льда и другихъ веществъ
въ моментъ плавленія произвелъ Корр (1855), пользуясь приборомъ,
изображеннымъ на рис. 134. Испытуемое вещество помѣщается внутри
стеклянной, открытой трубочки аа, которая находится внутри болѣе ши-
рокаго стекляннаго сосуда, наполненнаго водою, терпентиннымъ масломъ
или оливковымъ масломъ. Эта жидкость наполняетъ также часть капил-
лярной трубки, проходящей черезъ пробку, закрывающую сосудъ. Весь
приборъ помѣщается въ масло, которое постепенно подогрѣвается. Зная
тепловое расширеніе стекляннаго сосуда и наполняющей его
жидкости, можно опредѣлить измѣненіе объема вещества, нахо-
дящагося въ трубкѣ аа. Этотъ объемъ особенно тщательно
опредѣлялся для температуръ близкихъ къ точкѣ плавленія этого
вещества. Когда изслѣдовалась вода, приборъ наполнялся .
терпентиннымъ масломъ. Корр нашелъ, что 1 куб. см. воды
при 0° даетъ 1,102 куб. см. льда, или что одинъ объемъ льда |
даетъ 0,908 объема воды. Отсюда плотность <5 льда при 0°
равна (5 = 0,9073 сравнительно съ водою при 4°. Ріпескег
и Оеіввіег нашли (5 = 0,158; В гипп ег даетъ число (5 =
= 0,918; Випвеп нашелъ д = 0,91674, причемъ плотность
воды при 0° принята равною 0,99988. Виі’оиг опредѣлилъ
плотность смѣси масла и хлороформа, внутри которой ледъ
при 0° оставался въ покЛ, и нашелъ <5 = 0,9178; величину
расширенія онъ опредѣлилъ равною 0,0895, т.-е. около -1- .
2акг2елѵ8кі повторилъ опьіты Випзеп’аи нашелъ <5—0,91666.
Въ послѣднее ♦время Ы1 с Іі о 18, В а г н е 8, Ѵіпсені, Ьейис и
Во111 вновь опредѣлили плотность льда при 0°. Они нашли слѣдую-
щія числа:
Міскоів (1899) . . . (искусствен. ледъ).
I 0,9181 (рѣчной ледъ).
Вагпен (1901) . . . 0,9166 (рѣчной ледъ).
496
Плавленіе и затвердѣваніе.
Ѵілсепі (1902) . . . 0,9160 (искусствен. ледъ).
Ьесіис (1906) .... 0,9176 (искусствен. ледъ).
К о ѣ 11 (1908) .... 0,9168 (искусствен. ледъ).
Число 0,9170 можно нынѣ принять, какъ плотность чистаго льда
при 0°.
Реііегзоп изслѣдовалъ затвердѣваніе воды, уксусной кислоты и
муравьиной кислоты, пользуясь особеннымъ дилатометромъ. Далѣе изслѣ-
Рис. 135.
Рис. 136.
довали различныя органическія вещества Регсйе (бензолъ), ВаіеНіи
Раіагго (нафталинъ и др.) и НеуйлѵеШег (1897, бензолъ, фенолъ,
ментолъ, тимолъ, нафталинъ и стеариновая кислота).
Кромѣ воды уменьшаются въ объемѣ при плавленіи еще слѣ-
дующія вещества: висмутъ, сурьма, чугунъ, сплавы одной части Ві съ
4-мя частями 8Ь или съ 4 части кіа. А г о п 8 находитъ, что азотнокаліе-
вая соль также уменьшается въ объемѣ при плавленіи.
Е г пі а и и и въ особенности Корр изслѣдовали рядъ тѣлъ, расширяю-
щихся при плавленіи, или обнаруживающихъ неправильное расширеніе.
Приводимъ наиболѣе интересные, найденные ими результаты.
На рис. 135 абсциссы изображаютъ температуры, ординаты измѣне-
нія объема фосфора. До 44° фосфоръ расширяется правильно, при-
чемъ коеффиціентъ расширенія а = 0,000383. При 44° его объемъ вдругъ
увеличивается на 3,43 °/0, а затѣмъ жидкій фосфоръ опять правильно рас-
ширяется, причемъ а = 0,000506.
Рис. 136 показываетъ измѣненія объема сѣры. Между 78° и тем-
пературою плавленія 115° объемъ выражается формулою вида ѵ —
-(- Ы + сі2; при 115° происходитъ увеличеніе объема на 5°/0. Жидкая сѣра
расширяется затѣмъ правильно, причемъ а — 0,000460.
Весьма странно мѣняется объемъ стеарина, какъ видно на рис. 137.
Если его объемъ при 0° принять за единицу, то оказывается, что до 50°
объемъ растетъ правильно до 1,038. При 50° объемъ внезапно уменьша-
ется до 1,0076; затѣмъ онъ быстро растетъ, дѣлаясь при 60° равнымъ
1,0759. При 60° стеаринъ плавится и при этомъ его объемъ растетъ до
1,129; далѣе расплавленный стеаринъ расширяется правильно, достигая
Измѣненіе объема при плавленіи.
497
объема 1,150 при 80°. Объемъ воска не мѣняется въ моментъ плавле-
нія ; но зато онъ очень быстро растетъ между 35° и точкою плавленія,
которая равна 64 '.
Сплавъ Еозе (стр. 422) обнаруживаетъ весьма странную аномалію,
какъ видно на рис. 138, на которомъ линія ОВСЕЕ показываетъ законъ
измѣненія объема, іномалія, а именно значительное уменьшеніе объема
наблюдается между 44° и 98°. Сплавъ имѣетъ наибольшую плотность
при 69° когда объемъ значительно меньше, чѣмъ при 0°. Жидкій сплавъ
расширяется вполнѣ правильно, причемъ прямая ЕЕ является продолже-
ніемъ прямой ОВ,
Вопросомъ объ измѣненіи объема металловъ при плавленіи зани-
мались М і е 8 и УѴіпкеІтапп, Е. \ѴіесІетапп, Е о Ъ е г 18 и
\Ѵгі§йІ80п, Огиптасй, Ѵісепііпі и Отосіеіидр. Послѣд-
ніе названные ученые нашли для измѣненія Л объема при переходѣ ме-
талловъ изъ твердаго состоянія въ жидкое слѣдующія числа, выражаю-
щія это измѣненіе въ процентахъ самого объема.
Л°/о ІЬ 3,39 Сіі 4,72 5п 2,80 Ыа 2,5 Л°/о К 2,6 Р 3,5 3,67 Ві — 3,31 ^7о Вода. . . . — 9,1 (Випзеп) Муравьин. кисл. 12,3 (Реѣіегбзоп) Уксусн. кисл. . 12,6 ' »
Ваѣеіі і опредѣлилъ измѣненіе объема при плавленіи Цѣкоторыхъ
органическихъ веществъ. Объемъ одного грамма вещества увели-
чивается на ѵ - Нафталинъ . . Параффинъ. . — V куб. см. при точкѣ плавленія і*. ѵ'— ѵ № ѵ' — V 79,2 0,146 Спермацетъ . . 43,9 0,098 56,0 0,078 Нитронафталинъ 56,0 л0,078
Тоеріег (1894) опредѣлилъ измѣненіе объема при плавленіи раз-
личныхъ элементовъ. Онъ находитъ, что увеличеніе объема одного грамма
вещества есть періодическая функція атомнаго вѣса, убывающая въ каж-
дой изъ группъ системы Менделѣева съ возрастаніемъ атомнаго вѣса.
КУРСЪ ФИЗИКИ О. X В О Л ь С О Н А. Т. ПІ, изд. 3-е. 32
498
Плавленіе и затвердѣваніе.
Далѣе онъ подтвердилъ результатъ, найденный В і 11 е 1: объемъ іода уве-
личивается въ моментъ плавленія на 21%.
§ 6, Приложеніе термодинамики къ общему случаю перехода ве-
щества изъ одного состоянія въ другое. Формулы, которыя мы прежде
всего теперь выведемъ, одинаково относятся къ цѣлому ряду различныхъ
случаевъ перехода вещества изъ одного состоянія (въ узкомъ смыслѣ
слова) въ другое: къ переходу изъ твердаго состоянія въ жидкое, изъ
жидкаго въ газообразное, изъ твердаго въ газообразное, изъ одного алло-
тропическаго состоянія въ другое и т. д. Не останавливаясь пока на
опредѣленномъ случаѣ, мы предположимъ, что вещество переходитъ при
повышеніи температуры изъ нѣкотораго перваго состоянія (напр.
твердаго или жидкаго) въ нѣкоторое второе (напр. жидкое или газо-
образное). Предположимъ, что мы имѣемъ вѣсовую единицу вещества при
температурѣ /, и что нѣкоторая часть /х этого вещества находится во
второмъ состояніи (напр. расплавилась или испарилась), такъ что часть
1 — /х еще осталась въ первомъ состояніи. Величины і и р при-
мемъ за независимыя перемѣнныя, вполнѣ опредѣляю-
щія состояніе вещества. Давленіе р и температура і, при кото-
рой вещество находится, связаны во всѣхъ случаяхъ нѣкоторымъ урав-
неніемъ. такъ что можно положить:
Р=/(0............................(5)
Въ слѣдующемъ параграфѣ мы строго докажемъ, что такая зависи-
мость должна существовать во всѣхъ случаяхъ, къ которымъ относится
развиваемая здѣсь теорія. Для случая перехода изъ твердаго состоянія
въ жидкое наше вещество только и можетъ находиться при темпера-
турѣ плавленія і, соотвѣтствующей давленію р. На стр. 484 уже
было указано, что въ этомъ случаѣ і — Р(р\ откуда р = /(/). Для случая
перехода тѣлъ изъ жидкаго состоянія въ парообразное, причемъ пары
всегда насыщены, извѣстно изъ элементарнаго курса физики, что р есть
функція отъ і, т.-е. что упругость насыщеннаго пара даннаго вещества
есть функція одной только температуры. Обозначимъ далѣе черезъ 5 и
о удѣльные объемы вещества въ первомъ и во второмъ состояніяхъ. Тогда
весь объемъ занимаемый вѣсовой единицей вещества, равенъ
77 = (1-/1)5 /ХО =5 + р(в---5)..............(6)
Отсюда
Величины 5 и о суть функціи температуры. Если измѣнить
температуру на (іі и количество вещества, находящагося во второмъ состоя-
ніи на (ір, то это составитъ безконечно малое и несомнѣнно обрати-
мое измѣненіе состоянія вещества, къ которому приложимы оба начала
термодинамики. Количество теплоты поглощаемое веществомъ при
этомъ измѣненіи состоянія, напишется въ видѣ
(1$ = Хсір + У (іі.....................(8)
Переходъ вещества изъ одного состоянія въ другое.
199
Легко опредѣлить физическое значеніе величинъ X и У. Если і =
= Соп8І., то б/<2 = Хдр представляетъ количество теплоты, потребной
для перехода количества б/д вещества изъ перваго состоянія во второе,
безъ измѣненія температуры. Очевидно б/ф = рб/д, гдѣ о скрытая те-
плота перехода вѣсовой единицы вещества изъ перваго состоянія во
второе. Скрытая теплота р есть функція температуры
е = ф(0..............................О)
Сравнивая два выраженія для б/ф при / = Соп8І., мы видимъ, что
Х=о.............................. (10)
Если при д—Соп8І.. температура увеличивается на б//, то коли-
чество теплоты = У(іі идетъ только на нагрѣваніе всей вѣсовой еди-
ницы вещества на (іі градусовъ. Обозначимъ черезъ Сді и сМ количе-
ства теплоты, потребныя для нагрѣванія вѣсовыхъ единицъ вещества въ
первомъ и во второмъ состояніяхъ на йі при условіи д = СопеС,
т.-е. при томъ измѣненіи давленія, которое непремѣнно должно
сопровождать повышеніе температуры, чтобы послѣднее не вызвало пере-
хода вещества изъ одного состоянія въ другое.
Такимъ образомъ С и с теплоемкости вещества въ
двухъ состояніяхъ при условіи сохраненія двуфаз-
ности системы.
Было бы правильнѣе писать и с,, вмѣсто С и с, соотвѣтственно
общему обозначенію теплоемкости при постоянномъ х черезъ сх, см. стр.402.
Очевидно,
^ = (1—д) Ссіі 4 рсді = [С — д(С — б?)]б# . . (10, а)
Но мы имѣли при д — Соп8І. величину б/<2 = Уді. слѣд.
—д(С—б?)......................(11)
Такимъ образомъ физическое значеніе коеффиціентовъ X У въ (8)
обнаружено.
(8), (10) и (11) даютъ
б/ф = рб/д 4~ [ С— д(С—с)]сіі........(11,67)
Первое и второе начала термодинамики привели насъ къ слѣдую-
щимъ двумъ формуламъ, которыми мы теперь и воспользуемся:
оХ дУ д!дѵ др дѵ др\ .
ді др \дд ді ді др)................... '
дХ дУ_Х
ді др~ Т.............................( '
см. (42) стр. 404, и (54) стр. 427, гдѣ слѣдуетъ принять х = д, у = і,
такъ что во
перемѣнныя.
второй формулѣ
^=1
ду
др
ибо
Т и д независимыя
Легко понять, что (13) соотвѣтствуетъ формулѣ (5б,бі)
32*
500
Плавленіе и затвердѣваніе.
стр. 427,
мулу мы
Мы
, гдѣ вмѣсто X и У введены обозначенія X* и сх. Третью фор-
получаемъ, приравнивая правыя стороны формулъ (12) и (13).
д У
видѣли, что Х=д, см. (10); далѣе (11) даетъ г~=с— С. Въ
дѵ , др
должны вставить = с— з, см. (7), и ~=0, ибо р зависитъ
(12) МЫ дѵіиішіл г>ѵхсіогілг> — ---- ѵ/ о, ѵіи. \ 11 —
только отъ температуры. Такимъ образомъ (12) п (13) даютъ:
^+С-г = А(Я-5)^.....(14)
І+с-Н-............. <“)
е=АЛо (іо)
Этими основными формулами въ ученіи о переходѣ
вещества изъ одного состоянія въ другое мы будемъ поль-
зоваться и въ слѣдующихъ главахъ.
Выведемъ сперва для простое выраженіе. Формула (15) даетъ:
_ дд д _
Вставимъ это въ (11,а); получается
= СМ + рТ УУ- М-\- дсі^
или, какъ легко убѣдиться,
....... (16, я)
Здѣсь послѣдній членъ содержитъ полный дифференціалъ величины
, взятый по перемѣннымъ р и причемъ д зависитъ только отъ Л
Выведемъ интересныя формулы, связывающія теплоемкости С и с
съ теплоемкостями Ср и ср вещества въ двухъ состояніяхъ при томъ дав-
леніи р или той температурѣ і, при которыхъ происходитъ переходъ ве-
щества изъ одного состоянія въ другое. При этомъ мы, для избѣжанія
недоразумѣній, будемъ нѣкоторыя производныя ставить въ скобкахъ и
прибавлять снизу буквенное обозначеніе той величины, которая остается
постоянною. На необходимость пользоваться иногда этимъ способомъ обо-
значенія было указано на стр. 382. Величину , которая встрѣчается
/др\
въ (14) и (16), мы должны писать въ видѣ , ибо р и I мѣняются
М
при условіи р = Соп81., т.-е. при условіи, чтобы і оставалось тем-
Переходъ вещества изъ одного состоянія въ другое.
501
пературою перехода, и чтобы измѣненіе состоянія вещества не
сопровождалось переходомъ нѣкоторой части его изъ одной фазы въ дру-
,, І^Р\
гую. Эту величину І-.-? не слѣдуетъ смѣшивать съ величиною ко-
і (Л /.« С/4’
\
торая встрѣчалась во многихъ формулахъ главы III, и которую слѣдуетъ
писать въ видѣ 1^1 ,, такъ какъ тамъ объемъ ѵ предполагался постоян-
нымъ. Мы имѣли общую формулу (60, а) стр. 429
б/ф = СрМ— АТ
Въ нашемъ случаѣ р и і связаны равенствомъ р
при р> = Соп8І. получается
^ = спаг—Ат(~\ =
Р ХдііЛді].. ’
такъ что
ибо мы приняли при р, = Соп8І. равенство дС} = СМ; далѣе ѵ = 8, слѣд.
С = Ср —АТ
Аналогично имѣемъ
с = ср — АТ
(17, а)
(17,6)
Послѣдній множитель
одинъ и тотъ
же въ (17, а) и
(17,6);
предпослѣдніе множители
различны:
коеффиціенты расширенія
\иі ір \иЧР
при постоянномъ давленіи, 80 и б0 удѣльные
а и а
объемы въ первомъ и во второмъ состояніяхъ.
Замѣчательная формула получается, если вычесть (17,6) изъ (17, а)
и съ правой стороны замѣнить разность С — с выраженіемъ, взятымъ изъ
(15), а съ лѣвой стороны выраженіемъ, взятымъ изъ (16). Тогда
имѣемъ
, __д дд ! (дб\ ] д
р — СР~Т ді + )р] 0^5 •
(17. с)
Эта формула даетъ намъ возможность вычислить ср для насыщен-
наго пара.
др
Формула (16), стр. 500, даетъ намъ выраженіе для
С/ ь
др_ _____И _
ді АТ{о — 8).........................к ’
• Формулы (17,а) и (17,6) упрощаются, если вставить въ нихъ вы-
раженіе (18).
Съ самаго начала зтои главы мы допустили, что температура пере-
502
Плавленіе и затвердѣваніе.
хода і зависитъ отъ давленія р, и что слѣд. существуетъ связь вида і=
—/Хр) или Докажемъ теперь, что должно суще-
ствовать уравненіе, связывающее р и /, что слѣд. наше до-
пущеніе правильно. Пусть Ф3 и Ф2 термодинамическіе потенціалы вѣсо-
выхъ единицъ вещества въ двухъ его состояніяхъ; каждый изъ нихъ
есть функція отъ р и і. Если количество сір вещества переходитъ изъ
перваго состоянія во второе, то потенціалъ Ф всей смѣси измѣнится на
величину б/Ф = (Ф2 - - Ф3) сір. Система находится въ равновѣсіи, когда
б/ф = о, см. стр. 442, ибо р дано, а объемъ ѵ можетъ мѣняться при пе-
реходѣ изъ одного состоянія въ другое. Условіе йФ - - 0 даетъ Ф2 -
— Фх = 0, или яснѣе : Ф2Ср/) — = О- Уто и есть уравненіе, свя-
зывающее р и і и доказывающее, что наше допущеніе р = /(і) пра-
вильно. Интересно вывести (18) изъ равенства Ф2 — Фі = 0. Это ра-
венство даетъ
- ф,)_ л й(ф -ф,) а,
ді 1 др г
<7фі С^Фо
Формулы (74) стр. 439 даютъ = — У] и = — У2, гдѣ
и 52 энтропіи единицъ вѣса вещества въ двухъ его состояніяхъ. Слѣд.
первый членъ въ (19,&) равенъ — (У2— З^). Но У2 — есть прираще-
ніе энтропіи системы, которое имѣетъ мѣсто при переходѣ вѣсовой еди-
ницы вещества изъ перваго состоянія во второе. Изъ опредѣленія’ эн-
тропіи слѣдуетъ, что это приращеніе равно притекшей теплотѣ, дѣлен-
ной на Т. Притекшая теплота есть р, такъ что У2 — 5Х = ® и слѣд.
Далѣе третья изъ формулъ (74) стр. 439. въ которой ѵ удѣльный
объемъ (онъ теперь обозначенъ черезъ 5 и <т), даетъ:
л дФ.-> .
1 = Аз, , 4 Ап . .
др ' др
• • (19,с)
Подставляя (19,6) и (19,с) въ (19,а), и раздѣляя на ді, получаемъ
---4-^0—= о,
а это и есть равенство (18). Оно даетъ :
,, АТ(б — . ч
(іі = о сір . . . . . (20)
§ 7. Вліяніе давленія на точку плавленія. Приложимъ формулы,
выведенныя въ предыдущемъ параграфѣ, къ случаю перехода вещества
изъ твердаго состоянія въ жидкое. Тогда р есть давленіе, подъ кото-
рымъ находится вещество, отчасти твердое, отчасти жидкое: і есть тем-
Вліяніе давленія.
503
пера тура плавленія, соотвѣтствующая давленія» р; о есть скры-
тая теплота плавленія, 5 и б удѣльные объемы твердаго и жидкаго ве-
щества. Разность 5 — о вообще величина малая сравнительно съ 5 или б;
если принять за единицы вѣса килограммъ и кубическій метръ, то для
воды б 0,001, для льда 5 = 0,001091. Наконецъ, С и с суть теплоем-
кости льда и воды при условіи, чтобы измѣненіе температуры на 1° со-
провождалось необходимымъ измѣненіемъ давленія, соотвѣтственно связи,
выраженной формулою р - /(/).
Формула (16) или (20) даетъ возможность вычислить вліяніе да-
вленія на точку плавленія. Разность б — 8 величина малая, и
опытъ подтверждаетъ, что большія измѣненія давленія р вызываютъ срав-
нительно весьма малыя измѣненія температуры Л Поэтому мы въ ши-
рокихъ предѣлахъ измѣненія давленія можемъ считать (іі пропорціональнымъ
(ір, т.-е. считать формулу (20) вѣрною и для конечныхъ и даже для боль-
шихъ (ір. Пусть Ѳ измѣненіе температуры плавленія, вызванное измѣне-
ніемъ давленія на одну атмосферу, т.-е. въ 10333 килогр. на кв. м. по-
верхности. Тогда получаемъ
• ѳ = 10333 -...................(21)
Формулы (20) и (21) приводятъ немедленно къ важной теоремѣ. Ве-
личины А и Т по существу положительныя; скрытая теплота плавле-
нія д для всѣхъ изслѣдованныхъ тѣлъ положительная, а потому знакъ
величины Ѳ зависимъ отъ знака разности о — 8. Если б 8, то Ѳ 0;
если б < 8, то Ѳ < 0. Отсюда получается такая теорема:
Если плавленіе вещества сопровождается увели-
ченіемъ объема (б ^>8. случай обыкновенный), то при
увеличеніи давленія точка плавленія повышается; уже
расплавившееся вещество можетъ при увеличеніи да-
вленія вновь затвердѣть.
Если плавленіе вещества сопровождается
уменьшеніемъ объема (о <5, случай рѣдкій: вода, Ві, 8Ь
и т. д.), то при увеличеніи давленія точка плавле-
нія понижается; уже затвердѣвшее вещество
можетъ при увеличеніи давленія вновь сдѣлаться
ж и д к и м ъ.
Вообще можно сказать, что давленіе способствуетъ сохраненію того
состоянія вещества, которому соотвѣтствуетъ меньшій объемъ.
Итакъ для большинства тѣлъ точка плавленія повышается съ воз-
растающимъ давленіемъ. Обратное имѣетъ мѣсто для льда. При силь-
номъ давленіи ледъ плавится и мы при температурахъ ниже 0°
имѣемъ воду, а не ледъ. Такой результатъ вывели впервые *І а ш е 8
Т110Ш8 0И (1849) и С1аи8ІП8 (1850). Опытную повѣрку произвелъ
АѴ. Тйот8оп (Ьогй Кеіѵіп, 1850). Формула (21) даетъ возмож-
ность вычислить Ѳ. Для перехода льда въ воду имѣемъ: объемъ 1 клгр.
504
Плавленіе и затвердѣваніе.
воды равенъ б — 0,001 куб. метра, для льда 5 = 0,001091; далѣе имѣемъ
А = , Т — 273 и р = 80 (см. ниже). Вставивъ эти числа въ (21),
находимъ Ѳ = — 0,00753°.........................(22)
Отсюда слѣдуетъ, что точка плавленія льда понижается на 1°, когда
давленіе увеличивается на 132,8 атмосферъ.
ДѴ. Т Ь о ш 8 о и пользовался для повѣрки этого теоретическаго вы-
вода приборомъ, изображеннымъ на рис. 139 (отчасти схематически).
Стеклянный сосудъ наполненъ льдомъ и водою; въ немъ находится воз-
Рис. 139.
Рис. 140.
душный манометръ М и весьма чувствительный термометръ Т (эфирныи)
дающій возможность между — 0°,6 и 1°,1 опредѣлять температуру съ точ-
1 0
ностью до . Термометръ помѣщенъ внутри толстостѣнной оболочки,
1 Оѵ
предохраняющей его резервуаръ отъ вліянія давленія. Поршень Р служитъ
для увеличенія давленія, измѣряемаго манометромъ М. Для каждаго давле-
нія устанавливалась сама собою температура плавленія, т.-е. состояніе
равновѣсія, соотвѣтствующее данному давленію. Результаты наблюденій
приведены въ слѣдующей табличкѣ:
Давленіе. Аі 4/
наблюд. вычисл.
1 атмосф. 0°,00 0°,00
8,1 » 0,0575 - 0,0535
10,8 » — 0,1287 -0,1190.
506
Плавленіе и затвердѣваніе.
ревъ проволоку скрытую теплоту затвердѣванія тому льду, который плавится
подъ проволокою; здѣсь эта теплота играетъ роль скрытой теплоты пла-
вленія. Понятно, почему проволока должна состоять изъ хорошаго про-
водника теплоты, и почему опытъ не можетъ удасться, если металличе-
скую проволоку замѣнить напр. бичевкою. Температура льда должна
равняться 0°; если обсыпать ледъ поваренною солью, вслѣдствіе чего
происходитъ пониженіе его температуры, то опытъ не удается.
На разсмотрѣнномъ свойствѣ льда основана его пластичность,
которая есть не что иное, какъ текучесть (т. I) подъ сильнымъ да-
вленіемъ. Достаточно придавить рукою два куска льда другъ къ другу,
чтобы они «смерзлись», т.-е. соединились какъ бы въ одинъ’ кусокъ.
Объясняется это тѣмъ, что при сдавливаніи ледъ на поверхностяхъ со-
прикосновенія нѣсколько расплавляется, а образовавшаяся вода послѣ
прекращенія давленія вновь замерзаетъ. Подвергая кусочки льда силь-
ному давленію, можно получить одинъ кусокъ прозрачнаго льда любой
формы. Не останавливаемся на роли, которую приписываютъ этому свой-
Рис. 141.
ству льда для объясненія движеній глетчеровъ, тѣмъ болѣе, что вопросъ
объ этой роли представляется спорнымъ. Подробности можно найти въ
сочиненіяхъ и статьяхъ Т у п сі а 1 Гя, Г о г Ъ е 8’а, Напои М о 8 1 е у,
М’СоппеІ и Кій (Га, Вголѵпе’а, Коей и Кіоске, РГаипсІ-
Іег’а, РіаТГа, Невз’а и др.
катра (1902) нашелъ, что для растворовъ ЫаСІ и са-
хара въ водѣ величина Ѳ больше, чѣмъ для чистой воды.
Для большинства веществъ точка плавленія, какъ мы ви-
дѣли, повышается съ увеличеніемъ давленія; уже расплавив-
шееся вещество при достаточномъ давленіи вновь затвердѣва-
етъ. В и и 8 е и (1857) обнаружилъ это явленіе при помощи
прибора, изображеннаго на рис. 141. Толстостѣнная стеклян-
ная трубка асЬ, расширенная въ средней части и запаянная
съ двухъ концовъ, ( одержитъ въ Ь испытуемое вещество, подъ
нимъ ртуть, и въ са надъ ртутью воздухъ. Часть са калибри-
рована и служитъ манометромъ для опредѣленія давленія вну-
три прибора. Нижняя часть прибора погружалась до точки Ь
въ воду, температура которой была немного выше температуры
плавленія испытуемаго вещества, которое поэтому въ Ъ плави-
лось. Затѣмъ приборъ опускали глубже въ воду, вслѣдствіе чего
ртуть въ широкой части расширялась, поднималась въ трубкѣ са, и здѣсь
сжимала воздухъ, давленіе котораго передавалось черезъ ртуть къ испы-
туемому’ веществу. Послѣднее вновь дѣлалось твердымъ, хотя темпера-
тура была выше нормальной точки плавленія взятаго вещества. Мѣняя
давленіе р, которое измѣрялось манометромъ са, и температуру7 воды,
В и п 8 е п могъ опредѣлить температуры плавленія і при различныхъ да-
вленіяхъ р. Онъ производилъ опыты со спермацетомъ и съ парафиномъ,
и нашелъ слѣдующія числа:
Вліяніе давленія.
507
Спермацетъ.
Давленіе. Точка плавленія.
1 атмосф. 47°, 7
96 » 49,7
156 » 50.9
П а р а ф ф и н ъ.
Давленіе. Точка плавленія.
1 атмосф. 16°,3
85 » 48,9
100 » 49,9.
Подобные же опыты произвелъ Н о р к і п 8 ; найденныя имъ точки
плавленія указаны въ слѣдующей табличкѣ :
Давленіе. Спермацетъ. Воскъ. Стеаринъ. Сѣра.
1 атмосф. 51° 64°,5 72°,5 107°,О
519 » 60 74 ,5 73 .6 135 ,2
792 » 80,2 80 ,2 79 ,6 140 ,5.
Эти числа врядъ ли можно считать точными. Тѣмъ же вопросомъ
занимались В а ѣ е 11 і, А т а а 1, В а т і е п, V і 8 8 е г, I) е т е г 1 і а с ,
Вагие, НеуДлѵеіііег, ВегсЬе, Маск,Ьатра, Вышеслав-
цевъ и др., въ особенности же Таттапп. ВаіеПі изслѣдовалъ
рядъ органическихъ веществъ и сплавы ДѴ о о (Га и Ь і р р о лѵ і 1 г’а
(стр. 492). Опредѣляя для этихъ веществъ скрытую теплоту плавленія о
и измѣненіе о — 5 удѣльнаго объема въ моментъ плавленія, онъ могъ
сравнить наблюденныя величины Ѳ съ вычисленными по формулѣ (21)
стр. 503. Согласіе оказалось довольно удовлетворительнымъ, какъ видно
изъ слѣдующей таблички, относящейся къ наблюденіямъ при р - 8 атмосф.
Вещество. Ѳ Вещество. Ѳ
Набл. Вычисл. Набл. Вычисл.
Парафинъ. . . 0°,0280 0°,0300 Дифениламинъ . 0°,0231 0°,0221
Спермацетъ . . 0,0205 0,0185 Нафтиламинъ. . 0,0163 0,0143
Нафталинъ . . 0,0353 0,0341 Спл. Ьірродѵііг’а. 0,0039 0,0047
Питронафталинъ 0.0245 0,0237 (•плавъ ДѴоосГа . 0,0026 0,0029.
В а г и 8 нашелъ для нафталина температуры плавленія і при
давленіи въ р атмосферъ:
р 1 80 277 567 1435 атм.
/°= 79.2 83 90 100 130
Маск (1898) нашелъ для того же тѣла
р 150 675 1045 1500 1775 2140 атм.
& = 86,4 103,6 115,25 130,25 139,45 150,6
Весьма интересныя изслѣдованія произвелъ ІЭашіеп отчасти надъ
тѣми же тѣлами, какъ и ВаіеПі, доводя давленіе до 200 атмосферъ.
Онъ нашелъ, что Ѳ мѣняется въ зависимости отъ р по формулѣ вида
0 = а(р — 1) — Ь (р — I)2
(22,а)
Численныя значенія коеффиціентовъ а и Ь слѣдующія:
а Ь
Параффинъ . 0,029776 0,0000523
Нафталинъ . 0.035840 0.00Э0155
а Ь
Паратолу идинъ 0,014215 0,0000430
Дифениламинъ 0,024156 0,0000850.
508
Плавленіе и затвердѣваніе.
Второй членъ въ формулѣ (22,&) для этихъ веществъ отрицатель-
ный, а потому для нѣкотораго р = Р мы должны имѣть
0 = 0, а при р > Р повышеніе температуры должно за-
мѣниться пониженіемъ, т.-е. при р >> Р вещества пріобрѣтаютъ
свойства воды — они при плавленіи сжимаются. При давленіи р — Р
имѣемъ о = 5, т.-е. переходъ изъ твердаго состоянія въ
жидкое происходитъ безъ измѣненія объема. Зная а
и Ь, легко найти то р = Р. для котораго Ѳ = 0. Такъ напр. изъ опы-
товъ Оатпіепа получается для нитронафталина Р =175 атм., для па-
ратолуидина Р=166 атм., для нафтиламина Р = 83,5 атм. Непосред-
ственные опыты 1) а т і е п’а подтвердили, что точка плавленія послѣдняго
вещества при возрастающемъ давленіи сперва растетъ, а затѣмъ убываетъ,
и при р = 173 атм. она даже ниже нормальной точки плавленія при
р = 1 атм.
Въ 1898 г. появилась работа НеуйлѵеіНег’а, который, вполнѣ об-
ратно ІЭ а т і е п’у, находитъ, что Ѳ пропорціонально р даже при самыхъ
огромныхъ давленіяхъ.
Ь и 8 8 а п а нашелъ для фосфора
І = 44,24° + 0,0308/? — 0,0000007/Х2.
гдѣ р выражено въ атмосферахъ.
П у шинъ (1905) изслѣдовалъ Ссі(ЫО^^Н2О; онъ нашелъ
І = 58.7° + 0,00813/? 0,0000005/?2,
гдѣ р выражено въ килогр. на квадр. см. При р = 2900 получается
і = 78,іо.
Упомянемъ еще о наблюденіяхъ А т а $аі, которому удалось пре-
вратить при обыкновенной температурѣ въ твердое состояніе жидкій
четыреххлористыи углеродъ ССІ^ для точекъ плавленія кото-
раго онъ нашелъ слѣдующія температуры:
Давленіе: 210 620 900 1160 атм.
Точка плавленія: — 19°,5 0° Ч- 10° + 19°,5
Обращаемся къ разсмотрѣнію весьма интересныхъ работъ Т а ш -
іп а п п’а. Замѣтимъ, что онъ считаетъ результатъ изслѣдованій О а -
тіеп’а невѣрнымъ, хотя онъ самъ приходитъ къ тому выводу, что при
нѣкоторомъ, вообще весьма высокомъ давленіи Р, температура плавленія
I начинаетъ убывать; но давленія Р, найденныя В а т і е п’омъ, слиш-
комъ низки.
Мы уже указывали, что Татшапп считаетъ за «твердыя» тѣла только
кристаллы и разсматриваетъ аморфныя тѣла, какъ переохлажденныя жид-
кости. Онъ изслѣдовалъ теоретически и экспериментально кривую пла-
вленія р = /(/), которая въ плоскости ір, і) проходитъ черезъ всѣ воз-
можныя состоянія двуфазной системы, состоящей изъ твердаго и жид-
каго вещества. Онъ утверждаетъ, что к р и в а я и л а в л е н і я должна
быть замкнутою.
Вліяніе давленія.
509
ПустьАВ (рис. 142) представляетъ кривую насыщеннаго пара;
въ ея уравненіи р — с/ (/) величина р есть упругость насыщеннаго пара
при температурѣ і. Налѣво отъ АВ имѣемъ область ненасыщеннаго /
пара (газа), направо область жидкости.
Кривая АВ оканчивается въ критической точкѣ В При
болѣе высокомъ і разница между жидкостью и паромъ исчезаетъ. АС
представляетъ кривую плавленія; съ увеличеніемъ р растетъ температура
плавленія і.
Выше ЛСимѣемъ жидкость,
ниже АС тѣло твердое, т.-е. кри-
сталлъ.
Т а т ш а п п полагаетъ,что
кривая плавленія замкнута
(АСОЕЕА') т.-е. что область
кристаллическаго состо-
янія ограничена со
всѣхъ сторонъ.
Выше АСО имѣемъ жид-
кость, которая направо отъ СОЕ
переходитъ въ аморфный видъ,
а ниже ОЕЕ дѣлается стекло-
видной. Ни съ какой с то -
Рис. 142
роны невозможенъ непрерывный перехода, въ кристал-
лическое состояніе, т.-е. переходъ безъ измѣненія объема или
энергіи. Всѣ точки плоскости АСОЕЕА могутъ соотвѣтствовать также и
состоянію переохлажденной жидкости.
Уравненіе (16) даетъ
Лі АТАѵ •
сір р
(23)
гдѣ измѣненіе объема при плавленіи, т.-е. о — 5 обозначено черезъ Аѵ.
Кривая состоитъ по Таштапп’у изъ четырехъ частей. Въ АС
имѣемъ Аѵ >* 0 и 2> 0, а потому (іі: (1р >* 0. Въ С получаемъ Аѵ = 0,
но 2 >* О, М'. сір = 0. Далѣе кривая приближается къ оси абсциссъ, т.-е.,
съ повышеніемъ давленія, точка плавленія понижается; здѣсь Аѵ > ѵ.
Въ О имѣемъ р — 0, но Аѵ < 0 и сіі'.сір = гхэ. Въ ОЕ имѣемъ р р и
Аѵ < 0 ; въ Е уже Аѵ = 0, 2 0 и (іі: (ір = 0; наконецъ въ ЕЕ имѣемъ
Аѵ >> 0. 2 < 0. Итакъ р 0 въ АСО, р < 0 въ ОЕЕ, Аѵ > 0 въ АС и
ЕЕ, Аѵ < 0 въ СОЕ. Кривая ЕА есть кривая испаренія кристалла.
Опыты Ташіііапп’а надъ многими веществами показали, что і
всегда выражается формулою вида
і = с -|- ар — Ър2
(24)
т.-е. кривая всегда вогнута въ сторону оси давленій.
Экстраполированіемъ можно опредѣлить положеніе точки С.
510
Плавленіе и затвердѣваніе.
н Для глауберовой соли Таіутапп’у удалось дойти до
точки С и даже перейти ее. Для нея
Г = 32,6 + 0,000507/2 — 0,00000055/22.
Точка С лежитъ при р = 460 и і = 32°,7, т.-е. всего на 0,1° выше точки
плавленія при р = 1 кгр. Опыты показали, что і = 30°,0 при нѣкото-
ромъ /2, которое ниже 3000 кгр.
§ 8. Теплоемкости С и с твердыхъ и жидкихъ тѣлъ. Величины
С и с, встрѣчающіяся въ формулахъ (14) и (15) стр. 5оо, суть теплоем-
кости вещества въ твердомъ и жидкомъ состояніи при томъ перемѣн-
номъ давленіи, которое опредѣляется равенствомъ р = /(і), т.-е., при
условіи, чтобы измѣненіе температуры і на 1° сопровождалось измѣненіемъ
давленія до такого значенія его, при которомъ новая температура опять равна
температурѣ плавленія вещества. Для С и с мы вывели формулы (17,а)
гдѣ Ср и ср теплоемкости при постоянномъ давленіи твердаго тѣла и жид-
кости, 5 и о ихъ удѣльные объемы. Теперь мы можемъ вычислить С и с
для различныхъ тѣлъ, напр., для льда и для воды. Для воды имѣемъ
/р
= а'а0 = — 0,000062 X 0,001 = о,000000061,
гдѣ а' коеффиціентъ теплового расширенія воды при 0° и о0 удѣльный
объемъ, т.-е. число куб. м.. занимаемыхъ однимъ килограммомъ воды
при 0°. Для льда соотвѣтственно
аз0 = 0,000153 X 0,00109 = 0,000000167.
Далѣе для воды ср = 1, для льда Ср 0,48. Наконецъ мы видѣли,
что для перехода льда въ воду Аі = Ѳ = — 0°,00733, когда р мѣняется
на одну атмосферу. Измѣряя р въ килограммахъ на кв. метръ поверх-
0,00733
д/2\
10333
0,00733
Вставивъ эти числа въ формулу (25), находимъ
для воды:
для льда:
с = ср-- 0,055 = 0,945
с= Ср + 0,151 = 0,631
. . (25,а)
(25,6)
§ 9. Скрытая теплота плавленія. Мы въ самомъ началѣ этой главы
ввели понятіе о скрытой теплотѣ плавленія о, и эта величина вошла у
Скрытая теплота плавленія.
511
насъ во многія формулы. Разсмотримъ способы и нѣкоторые резуль-
таты ея опредѣленія.
Скрытая теплота опредѣляется. однимъ изъ калориметрическихъ спо-
собовъ, съ которыми мы познакомились въ главѣ объ опредѣленіи теп-
лоемкости. Обыкновенно примѣняютъ способъ смѣшенія (стр. 173) ;
но можно также пользоваться калориметромъ Випвеп'а (стр. 167), спо-
собомъ наблюденія охлажденія тѣла (стр. 185) и т. д. Послѣднимъ изъ
названныхъ способовъ пользовался напр. К и (1Ь е г §. Если примѣнять
способъ смѣшенія, то слѣдуетъ отличать два случая.
I. Когда температура плавленія ниже температуры жидкости
(обыкновенно, воды) въ калориметрѣ, то въ послѣдній вводятъ вѣсовое ко-
личество Р твердаго тѣла при температурѣ < і0. Пусть с± и с2
теплоемкости твердаго и жидкаго вещества при постоянномъ давленіи,
т.-е. Ср и ср предыдущаго параграфа; Ѳг начальная температура калори-
метра, Ѳ2 окончательная его температура, гдѣ Ѳ2 < Ѳг. Наконецъ, пусть
с сумма теплоемкостей всѣхъ частей калориметра вмѣстѣ съ содержа-
щейся въ немъ жидкостью. Искомая скрытая теплота р получается
изъ уравненія:
Рс^ — ^) + Ро + Рс2(Ѳ2 — /0) = — 02) = $ . . (26,а)
гдѣ <2 вообще количество теплоты, полученное калориметромъ, и не из-
мѣряемое выраженіемъ с(Ѳ1 — Ѳ2\ когда пользуются, напр.. калориме-
тромъ Випзеп’а.
II. Когда температура плавленія /0 выше начальной температуры
Ѳг калориметра, то въ послѣдній вводятъ жидкое вещество при темпера-
турѣ ; въ калориметрѣ это вещество затвердѣваетъ и охлаждается
до окончательной температуры Ѳ2. Искомое р получается изъ равенства
Рс2(іг — 4) Рр + Рс^ — 02) =- с(Ѳ2 — Ѳх) = . (26,Ь)
Само собой разумѣется, что слѣдуетъ ввести всѣ тѣ поправки и
пользоваться тѣми точными калориметрическими методами, которые были
указаны въ главѣ о теплоемкости тѣлъ. Когда калориметръ содержитъ
воду, и въ нее опускаютъ ледъ при 0° для опредѣленія его скрытой
теплоты плавленія, мы имѣемъ = 0 ; когда не требуется боль-
шой точности, то можно положить с2 = 1, такъ что (26,а) принимаетъ
болѣе простую форму
р 4- РѲ2 = с(^ - Р2)..................(26.с)
При точныхъ измѣреніяхъ слѣдуетъ для с, и с2 принимать сред-
нія теплоемкости веществъ для тѣхъ температурныхъ промежутковъ, между
которыми мѣняются ихъ температуры.
Скрытую теплоту плавленія р выражаютъ въ калоріяхъ, а потому
должно играть большую роль все то, что на стр. 158 до 166 было сказано
о малой опредѣленности калоріи. Смотря по тому, какую калорію мы
примемъ за единицу количества тепла, мы для р получимъ различныя
численныя значенія.
512
Плавленіе и затвердѣваніе.
Скрытая теплота плавленія или затвердѣванія должна зависѣть отъ
той температуры і0, при которой происходитъ переходъ вещества изъ
одного состоянія въ другое, причемъ внѣшнее давленіе р
предполагается всегда однимъ и тѣмъ же. Вспомнимъ,
что явленіе переохлажденія (стр. 484) указываетъ на возможность
измѣненія температуры затвердѣванія. Легко найти зависимость р
отъ /0. Положимъ, что вѣсовая единица жидкости, теплоемкость которой
с2, находится при температурѣ і2 и переходитъ въ твердое тѣло, темпе-
ратура котораго и теплоемкость сг. Допустимъ, что затвердѣваніе проис-
ходитъ одинъ разъ при температурѣ ^0, другой разъ при температурѣ /0 ,
п что скрытая теплота затвердѣванія въ первомъ случаѣ р, во второмъ о'.
Количества теплоты, потерянныя тѣломъ, должны въ обоихъ случаяхъ
быть одинаковыми; это даетъ равенство
— 4) Ч~ 9 “Ь ^і(^о — ^і) ~ “Ь "Ь — ^і)?
или « — о' = (с2 — сх)(/0 — Іо') ...... . (27)
Эта формула показываетъ, что если температура плавле-
нія уменьшается на 1°, то скрытая теплота плавле-
нія о уменьшается на (с2 — с2) калорій, причемъ для всѣхъ
изслѣдованныхъ веществъ с2 > с1? такъ что д всегда уменьшается съ по-
ниженіемъ температуры плавленія.
Формулу (27) очевидно можно написать въ видѣ
=С2 С1 • • • (27,а)
Буква р должна обозначать, что рѣчь идетъ объ измѣненіи р въ за-
висимости отъ і при постоянномъ давленіи р. между тѣмъ какъ
въ (15) величина дд\ді относится къ случаю того перемѣннаго давленія,
при которомъ система остается двуфазною и въ устойчивомъ равновѣсіи.
Реііегвоп подтвердилъ правильность формулы (27) для воды и
для фосфора, которые онъ вводилъ въ калориметръ въ переохлажденномъ
состояніи и заставлялъ затвердѣвать, вводя весьма маленькій кусочекъ льда
или фосфора. Для воды і0 — 0, с2 = 1, сг = 0,5, такъ что (27) даетъ
р = р — О,5Ло.
Наблюденія оказались вполнѣ согласными съ этой формулой; то же
самое относится къ опытамъ РеіЬегвоп’а съ фосфоромъ, для котораго
р уменьшается отъ 4,970 при 40°,05 до 4,744 при 27°,35.
Формула (27) показываетъ, что р' = 0 при нѣкоторой температурѣ г,
опредѣляемой равенствомъ
р = (с2 — — т)...................(28)
Т-е’ с (28,«)
с2
Вводя (28) въ (27), получаемъ
О- = (с2 - — т)...................(29)
Скрытая теплота плавленія.
513
гдѣ о' скрытая теплота при точкѣ затвердѣванія /0'. Для воды и льда
/0 = О, р — 80, с2= 1, сх = 0,5, такъ что (28,а) даетъ г — — 160 ; за-
тѣмъ (29) даетъ, если, отбросивъ значки, написать о вмѣсто р' и і вмѣсто
/,/, для скрытой теплоты затвердѣванія воды
Р = (с2 — с\)(і + 160)................(29,а)
Подобнымъ же образомъ р для всякаго тѣла выражается фор-
„улоюввда 9 й - <у)(( + „).......................(30)
гдѣ — п = г та температура, при которой о = 0; для воды мы нашли
/г = 160. Регзоп вывелъ изъ своихъ наблюденій, что для всѣхъ тѣлъ
п = 160, т.-е. что при температурѣ г = — 160° для всѣхъ тѣлъ @ = 0, и
что слѣд. формула(29,а), извѣстная подъ названіемъ формулы Р е г 8 оп’а,
даетъ д для всѣхъ тѣлъ, кромѣ, впрочемъ, металловъ, для которыхъ сямъ
Регвоп замѣтилъ неприложимость своей формулы. Эта формула под-
тверждается для Р, ЫаЫО^ СаС12; для воска и жировъ она
оказывается совершенно невѣрною. Опыты Г і 8 с й е г’а надъ бензоломъ,
Ваѣѣеііі надъ веществами, указанными на стр. 507, Тгепііпа^ііа
надъ сѣрноватистонатріевой солью, Рі скегіп^’а надъ Н28О^ Н28О± + ^40,
+ 4/72О и нафталиномъ окончательно показали, что формула
Регзоп’а не можетъ считаться правильною. Опыты Таштапп’а надъ
плавленіемъ льда также несогласны съ формулою Рег8оп’а. Для ме-
талловъ Регвоп предложилъ формулу
д = Ад | 1 + / — I,
і у » I
гдѣ А постоянное число, д коеффиціентъ упругости, 5 плотность металла.
Рогсгапй находитъ,- что для многихъ веществъ @ Рі = 30 Т,
гдѣ д и скрытыя теплоты плавленія и испаренія, Т абсолютная тем-
пература кипѣнія подъ атмосфернымъ давленіемъ.
Большой интересъ представляетъ скрытая теплота пла-
вленія льда. Для этой величины нашли: Ѵ^ііке 72, Ьаѵоівіег и
Ьаріасе 75, Эе іа Ргоѵобѣауе и Везаіпв 79,25, Ве^паиіі
79,23, Р ег8 о п 79,20, Н е 8 8 80,34, Випзеп 80,025. Новыя измѣренія
производили А. ЛѴ. 8тіИі (1903) и Б о го я в л е н с к і й (1904). Первый
находитъ д — 334,21 джуля = 79,896 среди, калоріи (между 0° и 100°) =
= 80 минимумъ калорій (37°). Богоявленскій находитъ д = 79,61
(15° калоріи) со среднею ошибкою въ 0,06 кал. Ьейис подвергъ всѣ
работы критическому разбору; онъ находитъ р = 79,2 (15° кал.). Сгпі-
иіапп (1907) ввелъ нѣкоторыя поправки въ вычисленія А. ЛѴ. Зтіій’а
и нашелъ д = 79,67 кал. (1 кал. = 4,1890 джуля). То же самое число
вывелъ К о і 11 (1908), какъ наиболѣе вѣроятное изъ всѣхъ произведен-
ныхъ измѣреній.
В егп іпі (1905) нашелъ для калія р = 13,61 и для натрія
2 = 17,75.
КУРСЪ ФИЗИКИ О. X В О Л Ь С О И А. Т. III, изд. 3-е.
33
514
Плавленіе и затвердѣваніе.
На стр. 485 было уже сказано, что для аморфныхъ тѣлъ, размягчаю-
щихся до достиженія точки плавленія, причемъ ихъ теплоемкость быстро
возрастаетъ съ температурою, понятіе о скрытой теплотѣ плавленія пред-
ставляется вообще неопредѣленнымъ.
Обращаемся къ интересному вопросу о вліяніи давленія на скрытую
теплоту плавленія. Формула (15) стр. 500 даетъ
....................<«>
Она показываетъ, что скрытая теплота о плавленія или затвердѣва-
нія зависитъ отъ температуры /, при которой происходитъ переходъ ве-
щества изъ одного состоянія въ другое. При этомъ предполагается, что
плавленіе и затвердѣваніе происходятъ при одной температурѣ Л соот-
вѣтствующей внѣшнему давленію р Воспользуемся формулою (31). чтобы
вычислить для воды и льда. Въ § 8 мы нашли для воды с = 0,945.
для льда С = 0,631; полагая далѣе у = 80 и Т = 273 получаемъ
|^0,945- 0,631 |° = 0,607 ............(32)
ѵ Ь Сі і о
Итакъ, если температура плавленія льда вслѣдствіе
увеличенія внѣшняго давленія понижается на 1°, то
скрытая теплота плавленія уменьши е тся н а 0,607 кало рій
На стр. 509 мы видѣли, какъ по теоріи Т а т т а п п’а о мѣняется
далѣе на кривой плавленія. Въ слѣдующемъ параграфѣ мы этотъ во-
просъ разсмотримъ точнѣе.
§ 10. Скрытая теплота аллотропическихъ или полиморфныхъ пре-
вращеній ; вліяніе давленія на температуру превращенія. Нѣкоторыя ве-
щества претерпѣваютъ при опредѣленной температурѣ измѣне-
ніе, превращаясь безъ измѣненія химическаго состава въ другую форму.
Для элементовъ такое измѣненіе называется аллотропическимъ (т. I); въ
общемъ случаѣ говорятъ о полиморфныхъ превращеніяхъ (т. I). При
температурѣ превращенія обѣ формы могутъ существовать рядомъ; ниже
этой температуры мы имѣемъ одну, выше — другую форму. Превраще-
ніе происходитъ съ поглощеніемъ или выдѣленіемъ опредѣленнаго коли-
чества 9 теплоты, которое можно назвать скрытою теплотою пре-
вращенія. Весь ходъ разсужденій, который привелъ насъ къ форму-
ламъ (14), (15) и (16) стр. 500, очевидно приложимъ и здѣсь, а потому
должна быть и здѣсь приложима формула
АТ
М— & (о — $)<1р....................(33)
которая и есть формула (16) стр. 500. Здѣсь о и 5 удѣльные объемы
двухъ формъ, причемъ о относится къ веществу, образующемуся при по-
вышеніи температуры съ поглощеніемъ количества теплоты о. Фор-
мула (33) опредѣляетъ измѣненіе температуры і превращенія въ зависи-
Аллотропическія измѣненія.
515
мости отъ измѣненія давленія р. Принимая сір равнымъ одной атмосферѣ,
мы получаемъ соотвѣтственное измѣненіе Ѳ температуры превращенія,
см. (21) стр. 503,
Ѳ — 10333 ?).....................(34)
У
Формула (34) была провѣрена для нѣсколькихъ веществъ.
Сѣра превращается при 95°,6 и давленіи въ 1 атм. изъ ромбиче-
ской формы въ моноклиномѣрную, причемъ поглощаются () — 2,52 болып.
кал.; далѣе измѣненіе объема одного килограмма вещества равно б—8 —
= 0,0000126 куб. метра, 7 = 273 -|- 95,6 — 368,6. Это даетъ
Ѳ = 0°,045.
В е і с Ь е г нашелъ путемъ опыта повышеніе температуры превраще-
нія сѣры, при увеличеніи внѣшняго давленія на 1 атм., равнымъ 0 = 0°,05.
Т а ш т а п п находитъ температуру превращенія при давленіи въ
1 атм. равною 94,6°.
Другой примѣръ представляетъ азотноамміачная соль, извѣст-
ная въ четырехъ формахъ. В е 11 а ѣ і и Е о ш а п е 8 і опредѣлили і и р
для всѣхъ трехъ, и о — 5 для двухъ превращеній. Вотъ найденныя
ими числа:
Первое превращеніе’
Второе «
Третье «
і о
31° 5,02
82°,5 5,33
124° 11,86
О---5
+ 0,00001964
— 0,00000854
По новѣйшимъ изслѣдованіямъ три превращенія происходятъ при
температурахъ: ромбическая при 32,4° въ моноклин., при 82,8° въ тетрагон.,
при 125,6° въ правильную.
Ьизаппа изслѣдовалъ вліяніе давленія на температуры і превра-
щенія и нашелъ слѣдующія числа, весьма согласныя съ вычисленными
для первыхъ двухъ превращеній.
1 Давленіе. Первое превращеніе. ЛІ Второе 1 превращеніе Аі Третье превращ. Лі
набл. ВЫЧИСЛ. ! набл. вычисл. набл.
100 атмосф. + 2°,98 4- 2°,94 1°,47 1°,40 4-1°,18
200 + 5,95 4- 5,88 2,82 - 2,80 + 2,33
250 « + 7,35 + 7,35 - 3,56 - 3.55 4- 3,07
Согласіе весьма хорошее.
Т а ш т а п п показалъ, что первыя двѣ кривыя превращенія пере-
сѣкаются при /7 = 930 кгр. на кв. см. и при температурѣ 64,16°. При
.этомъ давленіи и этой температурѣ могутъ одновременно и рядомъ суще-
ствовать три формы азотноамміачной соли.
О. ЬеЬтапп и АѴаІІегапЬ (1906/ сдѣлали замѣчательное откры-
зз*
516
Плавленіе и затвердѣваніе.
тіе: ромбическая разновидность при — 16° переходитъ вновь въ квадрат-
ную ; при этомъ превращеніи о - $ < О, гдѣ о относится къ ромбической,
5 — къ новой квадратной разновидности. ВеЬп (1908) изучилъ обѣ
квадратныя разновидности;‘какъ и ^Ѵаііегапі, онъ не нашелъ ника-
кого замѣтнаго различія въ кристаллографическомъ отношеніи между обѣ-
ими квадратными разновидностями.
Третій примѣръ представляетъ іодистая ртуть, для которой і —
— 127°, р = 1,15 (по 8 с йлѵ а г I г’у) и о—-5 = 0,0000013 (по В о сі лѵ е 1 Гу");
опыты Ьизаппа надъ этимъ веществомъ дали результаты, мало соглас-
ные съ формулою (32).
Іодистое серебро переходитъ при 145° изъ гексагональной
свѣтло-желтой формы въ красновато-желтую правильной системы, при-
чемъ Аѵ <0 и р = 6,8: по другимъ наблюденіямъ р — 6,25. Съ повышеніемъ
давленія температура плавленія должна понижаться. Таттапп про-
слѣдилъ ее до 110°,31 при /7 = 2237 кгр. на кв. см.
Таттапп показалъ, что полиморфизмъ есть весьма распростра-
ненное явленіе и онъ открылъ его во многихъ веществахъ, напр. въ фе-
нолѣ, іодистомъ метиленѣ (4 формы), твердой СО2 (двѣ формы при
р >2800 кгр. и і= — 7°,5) и т. д.
Наибольшій интересъ представляютъ изслѣдованія Т ат т ап п’а надъ
льдомъ. Онъ нашелъ, что кромѣ обыкновеннаго льда (ледъ I) существу-
ютъ еще двѣ модификаціи, которыя онъ называетъ ледъ II и ледъ III.
Температура плавленія льда I понижается до — 22°, когда давленіе
растетъ до /?=2200 кгр. на 1 кв. см. Здѣсь при увеличеніи давленія
образуется ледъ III, который плотнѣе воды (Аѵ > 0), вслѣдствіе чего
температура плавленія льда ІП съ увеличеніемъ давленія растетъ. Тат-
тапп прослѣдилъ кривую плавленія льда Ш до / = —17,3° и р =
= 3605 кгр. Экстраполированіе приводитъ къ тому результату, что при
р = 5040 кгр. и і — — 15,8° имѣется Аѵ — 0; при дальнѣйшемъ увели-
ченіи давленія р температура і должна опять понижаться.
Ледъ II получается, если ледъ I при - 80° подвергнуть давленію
около 2600—2900 кгр. При і = — 22,4° и р = 2230 могутъ одновременно
существовать ледъ I и ледъ II.
Въ 1909 году Таттапп’у удалось получить при нормальномъ
атмосферномъ давленіи ледъ III, при не очень низкихъ темпера-
турахъ устойчивый лишь при весьма большихъ давленіяхъ. Таттапп
охлаждалъ снѣгомъ углекислоты 5,5 куб. см. воды, находившейся подъ
давленіемъ въ 3060 кгр. При — 26° получался ледъ ІП, который охлаж-
дался въ жидкомъ воздухѣ до — 180°, причемъ давленіе падало до 2780 кгр.
Послѣ этого давленіе уменьшалось до 130 кгр., причемъ ледъ III не пе-
реходилъ въ обычный ледъ I. Это превращеніе совершалось лишь при
температурѣ между — 60° и — 10°, при чемъ давленіе возростало до
410 кгр. Дальнѣйшіе опыты показали, что при температурахъ ниже
— 120° ледъ III при давленіи въ 100 кгр. нѣкоторое время держится и, на-
конецъ, удалось получить ледъ III и подъ обычнымъ атмосфернымъ давле-
Литература.
517
ніемь. Съ этой цѣлью сосудъ, въ которомъ получался при температурѣ
жидкаго воздуха и подъ высокимъ давленіемъ ледъ III, чрезвычайно
быстро (въ 80 сек.) открывался и ледъ III погружался въ жидкій воз-
духъ, въ которомъ онъ тотчасъ тонулъ, тогда какъ ледъ I плаваетъ на
жидкомъ воздухѣ. Кусокъ льда III былъ вынутъ изъ жидкаго воздуха и
положенъ на столъ. Онъ тотчасъ началъ разбухать и распался въ бѣ-
лый порошокъ, кажущійся объемъ котораго въ 4—8 разъ превосходилъ
объемъ твердаго льда III.
Въ 1903 г. Таштапп и ЗаЬтеп построили самопишущій дила-
тографъ, чертящій кривую измѣненія объема тѣла при измѣненіи его тем-
пературы подъ постояннымъ давленіемъ (изобару). Внезапное измѣненіе
объема указываетъ на существованіе полиморфнаго превращенія. Этимъ
приборомъ были открыты превращенія для Ыа±Р2О7 (при 390° и 520°),
кварца (570°), /С2СО3 (400°), (200), плавиковаго шпата (300°) и т. д.
Конечно возможны превращенія и безъ измѣненія объема (Дѵ = 0 ), съ из-
мѣненіемъ, однако, напр. запаса энергіи (р не равно нулю).
ЛИТЕРАТУРА.
Къ § 2.
Таттапп. \Ѵ. А. 62 р. 280, 1897; 66 р. 473, 1898; 68 р. 553, 1899; О. А. 1 р.
275, 1900; 2 р. 1, 1900; 3 р. 161, 1900; 7 р. 198, 1902; 2ізсЬг. Г рЬуз. Сііет. 21 р. 17,
1896; 23 р. 326, 1897; 25 р. 441, 1898; 28 р. 17, 1899; 29 р. 51, 1899; Ж. Ф. X. Общ.
34 стр. 67 — 153, 1902 (обзоръ), книга: КгузіаШзіегеп иші ЗсЬтеІгеп, Ьеіргщ 1903.
См. УТ/еіпЬег^'. Вар. ргёзепіёз аи Соп^гёз іпіегпаі. 4е рЬуз. I р. 449, 1900.
Ьапбоіі. ХізсЬг. і рііуз. СЬет. 4 р. 349, 1888.
Рісагй. СЬет. Вег. 8 р. 687, 1875.
Кетзі ипд, Неззе. 8іе(іе- ипсі ВсЬтеІгрипсІ. ВгаипзсЬѵѵещ, 1893.
АпзсНиеіг ипй Всііиііх. СЬет. Вег. 10 р. 1800, 1877.
КоіН. СЬет. Вег. 19 р. 1970, 1886.
Потылицынъ. Ж. Ф. X. О. 24, Отд. Хим. р. 1, 1892.
Ѵісіог Меуег. СЬет. Вег. 27 р. 3129, 1894.
Ваеуег. СЬет. Вег. 10 р. 1286, 1877.
Жуковъ и Курбатовъ. Ж. Ф..-Хим. О. 39, Отд. хим. р. 1054, 1907.
Реіегзеп. СЬет. Вег. 7 р. 59, 1874.
Марковниковъ. ЫеЬ. Апп. 182 р. 340, 1876.
Ьепг. СЬет. Вег. 12 р. 582, 1879.
Солонина. Ж. Ф. X. О. 30 р. 819, 1898; СЬет. СепігаІЫ. 1 р. 327, 1899.
МШз. РЫ1. Ма$. (5) 17 р. 175, 1883.
РгапсНітопі. Вес. Тгаѵ. Рауз-Ваз, 16 р. 126, 1897.
8аіпі Сіаіге Оеѵіііе. Апп. сЫт. еі рЬуз. (3) 46 р. 182, 1856.
Оаибіп. С. В. 12 р. 947, 1841; 26 р. 94, 1848.
Оергеіх. С. В. 28 и 29, 1849.
Моіззап. С. В. 1893—1898; Апп. рЬуз. еі сЫт. (7) 4 р. 136, 1895.
Къ § 3.
Таттапп. ХізсЬг. Г. рЬуз. СЬет. 3 р. 441, 1889.
Неусоск апб Кеѵіііе Іоигп. СЬет. 8ос. 1889 р. 666 ; 1890 р. 376; 1895 р. 160, 1240.
ОиіНгіе. РЫ1. Ма§. (5) 17 р. 462, 1884.
Оаиііег. С. В. 123 р. 109, 1896.
РоЬегіз-Аизіеп. Ргос. В. 8ос. 59 р. 367, 1892.
518
Плавленіе и затвердѣваніе.
Мегг ипй Ѵ^еіііі. Сііет. Вег. 14 р. 1438, 1881.
РийЪег^. Ро&&. Апп. 18 р. 240, 1830.
Ѵап АиЪеІ. 4. де рііуз. (3) 7 р. 223, 1898; С. к. 132 р. 1266, 1901.
Курнаковъ. Ж. Ф. X. О. 31 р. 927, 1899; 2іесііг. і. апог&. Сііет. 23 р. 439, 1899.
Курнаковъ и Путинъ. Ж. Ф. X. О. 33 р. 565, 588, 1901; 21есііг. ѣ апог§. Сііет.
30 р. 86, 109, 1902.
Неусоск апй Кеѵіііе. РЫ1. Тгапе. 194 р. 201, 1900 (Аи— АІ); Ргос. К. 8ос. 68
р. 1, 1901 (Си — 8п).
Карр. Р. А. 6 р. 754, 1901.
Воийоиагй. С. В. 133 р. 1003, 1901; 134 р. 1431, 1902; 135 р. 794, 1902; 136
р. 1327, 1903; Виіі. 8ос. сіііт. 27/28 р. 5, 45, 1901 ; 29/30 р. 629, 1903.
8іоке8. Ргос. В. 8ос. 49 р. 174, 1891.
ѴѴгі^Пі. Ргос. В. 8ос. 52 р. 536, 1893.
РёІаЪоп. С. В. 137 р. 648, 920, 1903.
Е. ѴЧесІетапп. \Ѵ. А. 3 р. 237, 1878; 20 р. 228, 1883.
8ргіщ*. Виіі. де і’Асад. де Вгихеііее (3) 11 р.. 355, 1886.
Маггоііо. Аііі д. В. Асад, д. Тогіпо 17 р. 111, 1881.
Наііоск. 2іесііг. ѣ рііуе. Сііет. 2 р. 378, 1888.
8ска/^оі8СІг. Ро&&. Апп. 102 р. 293, 1857.
8скиеіг. \Ѵ. А. 46 р. 177, 1892.
Бахметьевъ и Въжаровъ. Ж. Ф. X. О. 25 р. 237, 1893.
8ргіщг (смѣсь солей). 2іесііг. і. рііуе. Сііет. 2 р. 536, 1888.
Нетія. Ро&8. Апп. 92 р. 588, 1854.
ВаііеІП е Раіагго. Киоѵо Сіт. (3) 17 р. 94, 1885.
ВаііеШ е МагііпеШ. АШ д. В. Асад. д. Тогіпо 20 р. 1.
Сапожниковъ, Гелъвихъ и Рдултовскій. Ж. Ф. X. О. 35 р. 1073, 1903.
Ѵап Ьааг. Ѵегеі. К. Акад. ХѴеі. 1902—03 р. 478, 576; 1903 р. 169.
Ваккиіз РоояеЬоот. 2іесііг. ѣ рііуе. Сііет. 30 р. 385, 1899.
Б. Маггоііо. Вепд. В. Іеі. ЬотЪ. (3) 18, 1884; ВеіЫ. 9 р. 664, 1885.
Ѵісепііпі е Отойеі. АШ В. Ас. Вота 3 р. 235, 294, 321, 1887.
8скгайег. 8іидіеп йЪег діе Вігисіиг дег Ье^ігип^еп. Рго^г. № 6, ІпеіегЬиг^
1889—1890.
КийЬег^. Ро§&. Апп. 71 р. 460, 1847.
МаШііевзеп. Ріііі. Тгапе. 1860 р. 177; Ро&&. Апп. 110 р. 21, 1860.
Іаттапп и его ученики. Около 80 работъ въ 2іесііг. і апог&. Сііетіе 1904—1905
Курнаковъ и его ученики. Много работъ въ Ж. Ф.-Х. О. и въ 2іесііг. I. апог&
Сііетіе.
Іаттапп (Обзоръ). Рііуе. 2іесііг. 10 р. 519, 1909.
Къ § 4.
Бевріеія. . С. В. 2, 1836; Ро^. Апп. 41 р. 492, 1837
Мопіі. АШ д. Асад. д. Тогіпо. 27 р. 94, 1891.
Еакгепкеіі. Ріііі. Тгапе. 38 р. 78, 1724.
Сау-Ьи88ас. Апп. сЫт. еі рііуе. (2) 63 р. 363, 1836.
Безргеіг. С. В. 5 р. 19, 1837.
Би/о’.г. Апп. сіііт. еі рііуе. (3) 68 р. 370, 1863.
Оегпег. С. В. 95 р. 1278, 1882; 3. де рііуе. (2) 2 р. 159, 1883.
Титіігг. ХѴіеп. Вег. 103 р. 268, 1894.
Мооге. 2І8СІ1Г. I. рііуе. Сііет. 12 р. 545, 1893.
Таттапп. См. § 2.
Бородовскій. Ж. Ф. X. О. 35 р. 128, 1903; Яіесііг. ѣ рііуе. Сііет. 43 р. 75. 1903.
Богоявленскій. 2іесііг. ѣ рііуе. Сііет. 27 р. 585, 1898.
Бахметьевъ. Ж. Ф. X. О. 32 р. 218, 1900; Мёт. Акад. де Уі.-РёіегеЪиг^, 10
№ 7, 1900.
Литература.
519
ОзііѵсМ. ХізсЫ. Т. рЬуз. СЬет. 23 р. 289, 1897.
ѴГіІзоп. РЫІ. Мад. (5) 50 р. 238, 1900.
Къ § 5.
Еттап. Ро^. Апп. 9 р. 557, 1827.
Корр. ЬіеЪ. Апп. 93 р. 129, 1855.
Ріиескег ипд. 0еІ88Іег. Р. Апп. 86 р. 238, 1852.
Вип8еп. Рор^. Апп. 141 р. 31, 1870.
Хакгхесѵвкі. XV. А. 47 р. 155, 1892.
Кіскоіз. РЬуз. Веѵ. 8 р. 21, 1899.
Вагпе8. РЬуз. Веѵ. 13 р. 55, 1901; Р1іу8. ХізсЬг. 3 р. 81, 1901—2.
Ѵіпсепі. РЬуз. Веѵ. 15 р. 129, 1902.
Огиптаск. . Р1іу8. 2ізсЬг. 3 р. 134, 1901—2.
Г-жа Соболева. Ж. Ф. X. О. 34 р. 714, 1902; ЕІзсЬг. 1. рііуе. СЬет. 42 р. 75, 1902.
Маііеі. Ргос. В. 8ос. 26 р. 77, 1877.
Агоп8. XV. А. 53 р. 107, 1894.
Реііегвоп. Допгп. рг. Сііет. (2) 24 р. 129. 293, 1881.
Еегске. XV. А. 44 р. 265, 1891.
ВаіеШ е Раіаххо. Мет. (1. В. Асс. Ьеі Ьіпсеі (4) 1 р. 1, 283, 1885.
Неусігѵеіііег. XV. А. 61 р. 526, 1897.
Кіе8 ипсі ѴГіпквІтапп. XV. А. 13 р. 43, 1881.
Е. МіесІетапп. XV. А. 20 р. 228, 1883.
КоЬегів апсі ѴЕгіукізоп. Хаіиге (англ.) 24 р. 470, 1881.
Ѵісепііпі е Отобеі. АШ (1. В. Асс. аі Тогіпо 22, 1887; ВеіЪІ. 11 р. 768, 1887.
ВаіеШ. АШ а. В. Ізі. Ѵеп (3) 3, 1886; ВеіЫ. 11 р. 233, 1887.
Тоеріег. \Ѵ. А. 53 р. 343, 1894.
ВШеі. ДаЬгзЬег. сі. СЬетіе, 1855 р. 46.
Къ § 7.
У 1кот8оп. РЫІ. Тгапз. ЕсІіпЬ. 16, 1845 ; РЫІ. Ма&. (3) 37, 1850.
ІГ' Ткотзоп. РЫІ. Ма§. (3) 37, 1850; Апп. сЫт. еГ рЬуз. (3) 35 р. 381, 1852.
СІаи8Іи8. Р. Апп. 81 р. 168, 1850; АЫіапсІІип^еп 1, 92.
Оеіѵаг. Ргос. В. 8ос. 30 р. 533, 1880.
Соо88еп8. АгсЬ. Хёегі. 20 р. 449, 1886.
Ата^аі. С. В. 117 р. 507, 1893.
Мои88оп. Ро&&. Апп. 105 р 161, 1858; Апп. сЫт. еі рЬуз. (3) 56 р. 252, 1859.
Воііотіеу. Ро^. Апп. 148 р. 192, 1873.
ЕогЬев. Ргос. В. 8ос. 10, 1860.
Мовіеу. РЫІ. Ма&. (4) 39 р. 1, 1870.
ЛТСоппеІ апсі КШб. Ргос. В. 8ос. 49 р. 323, 1891.
Коск ипсі Кіоске. XV. А. 8 р. 661, 1879.
Р/аипсІІег. ХѴіеп. Вег. 59, II р. 201, 1869.
Р/а//. Ро^. Апп. 155 р. 169, 1875.
Не88. Аппаі. б. Рііуе. (4) 36 р. 449, 1911.
Вип8еп. Ро&&. Апп. 81 р. 562, 1850.*
Норкіп8. АШепаеит 1854 р. 1207; Віп^іег’з ЛоигпаІ 134 р. 314, 1854.
ВаііеІІі. <1. Ье рЬуз. (2) 6 р. 90, 1887; АШ а. В. Ізі. Ѵеп. (3) 3, 1886.
йатіеп. С. В. 107 р. 1159, 1889; 112 р. 785, 1891.
Ата^аі. С. В. 105 р. 165, 1887.
Ое Ѵі88ег. Віеяегі. ІНгесЫ 1892; ЕЫсЬг. I. рЬуе. СЬет. 9 р. 767, 1892 ; Вес. дез
Тгаѵ. сЫт. ае Рауз-Вае. 12 р. 154, 1893; ВеіЫ. 18 р. 445, 1894.
Оетегііас. С. В. 122 р. 1117, 1896; 124 р. 75, 1897; Л ае рЬуз. (3) 6 р. 126, 1897.
Ваги.8. 8І11. «Іоигп. (3) 42 р. 125, 1891.
НеусЕіѵеіІІег. XV. А. 64 р. 725, 1898.
520
Испареніе и ожиженіе.
Таттапп, см. § 2.
РегсНе. \Ѵ. А. 44 р. 265, 1891.
Вгіііоиіп. Апп. сіііт. еі рііуе. (7) 13 р. 264, 1898
Маск. С. К. 127 р. 361, 1898.
Вышеславцевъ. Ж. Ф. X. О. 34 р. 41, 1902.
Ьатра. \Ѵіеп. Вег. 111 р. 316, 1902.
Къ § 9.
Реііегзоп. Зонгп. рг. Сііет. (2) 24 р. 151, 1881.
Регвоп. Апп. сЫт. еі рііуе. (3) 21 р. 312, 1847 ; 24 р. 265, 1848; 30 р. 73, 1850
Р-. Апп. 73 р. 469, 1848.
РІ8сНег. \Ѵ. А. 28 р. 429, 1886.
ВаііеІН. Аііі 3. В. Іеі. Ѵеп. (3) 3, 1886; ВеіЫ. 11 р. 233, 1887.
1 гепііпа^ііа. ХѴіеп. Вег. 72, 1875.
Ріскегіп^. Ргос. К. 8ос. 49 р. 20, 1891.
ѴѴіІке. См. Еіесііег, Сеесііісіііе Зег Рііуеік, 7 р. 364.
Ьаѵоівіег еі Ьаріасе. Мёт. Зе ГАсаЗ. Зее 8с. 1780.
Ое Іа Ргоѵо8іауе еі Оеваіпв. Апп. сіііт. еі рЬуе. (3) 8, 1843; Ро§&. Апп. 62
р. 30, 1844.
Ре^паиіі. Апп. сЫт. еі рііуе. (3) 8, 1843; Ро^. Апп. 62 р. 42, 1844.
Рег80п, Апп. сЫт. еі рііуе. (3) 30, 1850.
Не88. Меіап&ее рііуе. еі сЫт. (АсаЗ. Зе 8і.-РёіегеЪ.) 1.
Випзеп. Ро^. Апп. 141 р. 30, 1870.
Богоявленскій. Зап. Юрьевск. Общ. Ест. 13 р. 1, 1904.
Ьейис. С. К. 142 р. 46, 1906; Ж 3. Рііуе. (4) 5 р. 157, 1905.
Оиітапп. 3. рііуе. Сііет. 11 р. 279, 1907.
РоіН. ХіесЬг. Г. рііуе. Сііет. 63 р. 441, 1908.
Веігп. И. А. 1 р. 272, 1900.
Таттапп. ЛѴ. А. 67 р. 871, 1899.
А. ІГ. 8тіііі. Рііуе. Веѵ. 17 р. 193, 1903; 16 р. 383, 1903; 17 р. 193, 1903.
Къ § 10.
Реісііег. 2іес1іг. Г. рііуе. Сііет. 1 р. 221, 1888.
Веііаіі е Ротапеві. Аііі Зеі. Іеі Ѵеп. 1885.
Ьивваппа. Киоѵо Сітепіо (4) 1 р. 97, 1895.
Таттапп ипй 8актеп. И. А. 10 р. 879, 1903.
Таттапп. \Ѵ. А. 67 р. 871, 1899; 68 р. 640, 1899; см. также къ § 2.
ГЛАВА ОДИННАДЦАТАЯ.
Переходъ изъ жидкаго и твердаго состояній въ газообразное
и обратно.
§ 1. Испареніе и ожиженіе. Всякая жидкость, имѣющая свобод-
ную поверхность, т.-е. такую, вдоль которой она не соприкасается съ
твердымъ тѣломъ или съ другою жидкостью, непрерывно испаряется на
этой поверхности. Въ т. I уже было указано, какимъ образомъ мы дол-
жны себѣ представлять механизмъ испаренія, исходя изъ кинетической
теоріи строенія вещества. Частицы жидкости, принадлежащія ея поверх-
ностному слою и одаренныя въ данный моментъ большою скоростью по
направленію, составляющему достаточно большой уголъ съ самою поверх-
Испареніе и ожиженіе.
521
ностью, вылетаютъ изъ сферы вліянія сосѣднихъ частицъ, а слѣдова-
тельно и изъ самой жидкости. Совокупность частицъ, вылетѣвшихъ изъ
жидкости, составляетъ газообразное тѣло, называемое паромъ этой жид-
кости. Въ т. I было также указано, что испареніе должно сопровождаться
пониженіемъ температуры жидкости, такъ какъ вылетаютъ изъ нея ча-
стицы, обладающія наибольшею скоростью. Часть этой скорости теряется
однако вслѣдствіе противодѣйствія силъ сцѣпленія, и потому температура
пара всегда равна температурѣ самой жидкости.
Когда надъ жидкостью находится пустота, то испареніе происхо-
дитъ. по крайней мѣрѣ въ первый моментъ, съ весьма большою скоро-
стью. Когда же надъ поверхностью жидкости находится какой-либо газъ
или паръ другой жидкости, то многія изъ частицъ, вылетающихъ изъ
жидкости, встрѣчаются съ частицами газа или пара, и отбрасываются
ими обратно въ жидкость, вслѣдствіе чего испареніе происходитъ весьма
медленно.
Когда надъ жидкостью находится неограниченное пространство, въ
которомъ образующійся паръ можетъ въ такой мѣрѣ разсѣяться, что плот-
ность пара вблизи жидкости всегда остается малою, то испареніе про-
должается непрерывно, пока вся жидкость не испарится. Скорость испа-
ренія возрастаетъ вмѣстѣ съ температурою, что легко объясняется на ос-
нованіи той же кинетической теоріи строенія вещества. Съ повышеніемъ
температуры, вѣроятно, уменьшается дѣйствіе тѣхъ внутреннихъ причинъ,
которыя мы называемъ сцѣпленіемъ; въ то же время возрастаетъ сред-
няя скорость движенія частицъ, а тѣмъ самымъ для частицъ поверхност-
наго слоя жидкости не только облегчается удаленіе изъ этого слоя во
внѣшнее пространство, но и уменьшается вѣроятность обратнаго движе-
нія частицы въ жидкость вслѣдствіе удара объ идущую ей навстрѣчу ча-
стицу газа или пара, наполняющаго это пространство.
Когда испареніе происходитъ въ замкнутомъ пространствѣ,
то частицы, выдѣлившіяся изъ жидкости и образовавшія паръ, двигаясь
по всевозможнымъ направленіямъ, ударяются не только въ окружающую
стѣнку, но и въ поверхность жидкости, въ которой онѣ и удерживаются,
если попадаютъ въ сферу частичнаго дѣйствія. Чѣмъ гуще паръ надъ
жидкостью, тѣмъ больше число частицъ, попадающихъ въ данное время
обратно въ жидкость. Количество жидкости перестанетъ уменьшаться, и
испареніе какъ будто прекратится, когда паръ достигнетъ такой густоты,
что число частицъ, возвращающихся въ данное время въ жидкость, сдѣ-
лается равнымъ числу частицъ, вылетающихъ въ то же время изъ жид-
кости. Тогда устанавливается подвижное равновѣсіе (т. I): ко-
личество жидкости и пара остаются неизмѣнными. Плотность пара, а
слѣд. и его упругость достигли при этомъ нѣкотораго предѣльнаго значе-
нія, которое для данной жидкости и при данной температурѣ не
можетъ быть далѣе увеличено. Въ этомъ случаѣ говорятъ, что паръ
насыщенъ. Если надъ жидкостью сначала находилась пустота, то на-
сыщеніе достигается въ весьма малый промежутокъ времени. Если же
522
Испареніе и ожиженіе.
свободное пространство надъ жидкостью содержитъ газъ, то. какъ было
указано выше, испареніе вообще происходитъ медленно и насыщеніе до-
стигается лишь черезъ продолжительный промежутокъ времени. Съ по-
вышеніемъ температуры увеличивается скорость испаренія, равновѣсіе
прекращается и настаетъ вновь, когда упругость пара достигла новаго
увеличеннаго значенія. Упругость р насыщеннаго пара возрастаетъ съ
температурою I. Зависимость р отъ і мы изобразимъ въ видѣ
Р=/(«............................(1)
Видъ этой функціи зависитъ отъ рода жидкости.
Зависимость скорости ѵ испаренія отъ различныхъ обстоятельствъ
была впервые изслѣдована В а 1 і о п’омъ, который нашелъ, что ѵ пропор-
ціонально свободной поверхности 5 жидкости, и пропорціонально разно-
сти между упругостью Р насыщенныхъ паровъ при температурѣ
испаряющейся жидкости и упругостью р паровъ,уже находящихся
надъ жидкостью; кромѣ того онъ нашелъ, что эта скорость обратно про-
порціональна упругосіи Н посторонняго газа (напр. воздуха), находяща-
гося надъ жидкостью. При Н = 0, т.-е. при испареніи въ пустоту, ско-
рость ѵ безпредѣльно велика. Все сказанное даетъ намъ формулу
ѵ = (Р Р) . .............(І-а)
гдѣ С постоянный множитель. Однако эти законы не могутъ считаться
точными. Уже Ваііоп нашелъ, что число С зависитъ отъ скорости
движенія газа, т.-е. напр. отъ скорости вѣтра. Ьаѵаі нашелъ, что ѵ
обратно пропорціонально №, гдѣ п зависитъ отъ рода жидкости и отъ
окружающаго газа. Такъ напр. въ воздухѣ п = 1,18 для воды, п =
= 1,08 для алкоголя, п =0,66 для бензина и п =0,61 для эфира; въ во-
дородѣ п = 0,78 для воды, алкоголя и бензина, и іг = 0,49 для эфира.
Далѣе 81еіап показалъ, что скорость испаренія находится въ зависи-
мости отъ формы и размѣровъ свободной поверхности жидкости и въ нѣ-
которыхъ случаяхъ отъ формы сосуда. Испареніе происходитъ въ сред-
нихъ частяхъ поверхности иначе, чѣмъ вдоль ея края. Весьма интерес-
ныя теоретическія изслѣдованія привели 81 е 1 а п’а къ неожиданному ре-
зультату, что количество пара, образующагося въ данное время, во мно-
гихъ случаяхъ пропорціонально не самой величинѣ поверхности* жидко-
сти, какъ обыкновенно полагаютъ, но ея линейнымъ размѣрамъ. Если
напр. поверхность представляетъ кругъ, то скорость испаренія пропорці-
ональна діаметру, а не площади круга. АѴіпкеІтапп, Сре з нев-
скій и др. занимались опытною провѣркою этого закона. Далѣе 81 е 1 а п
изслѣдовалъ вопросъ о скорости испаренія жидкостей, помѣщенныхъ въ
вертикальныхъ трубкахъ, въ которыхъ надъ самою поверхностью жидко-
сти образуется слой насыщеннаго пара, медленно диффундирующаго къ
верхнему отверстію трубки, надъ которымъ плотность пара, разсѣиваю-
щагося во внѣшнемъ пространствѣ, можетъ приниматься равною нулю.
Испареніе и ожиженіе.
523
к? ѣ е Г а и показалъ, что при этихъ условіяхъ скорость испаренія обратно
пропорціональна разстоянію уровня жидкости отъ верхняго конца трубки.
При испареніи вѣсовой единицы жидкости расходуется нѣкоторое
количество р теплоты на внутреннюю работу разъединенія ча-
стицъ и на внѣшнюю работу расширенія, которая должна быть со-
вершена, когда испареніе происходитъ не въ пустоту, такъ какъ удѣльный
объемъ пара всегда больше удѣльнаго объема жидкости. Теплота $ на-
зывается скрытою теплотою испаренія. Она зависитъ отъ рода
жидкости и, для данной жидкости, отъ температуры /, при которой про-
исходитъ испареніе; мы введемъ обозначеніе
о = <р(Г)............................(2)
Если насыщенный паръ подвергать охлажденію или изотермическому
сжатію, то часть пара переходитъ въ жидкое состояніе, причемъ выдѣля-
ется скрытая теплота ожиженія, равная скрытой теплотѣ испаренія. Паръ,
весьма далекій отъ насыщенія, обладаетъ всѣми свойствами газовъ, т.-е.
онъ довольно точно слѣдуетъ законамъ Бойля-Маріотта и Гей-
Люссака, и внутренняя работа въ немъ весьма мала. По мѣрѣ при-
ближенія къ насыщенію, свойства пара все болѣе удаляются отъ свойствъ
идеальныхъ газовъ. Отсюда легко придти къ предположенію, что всѣ ве-
щества, которыя намъ извѣстны въ газообразномъ состояніи, суть пары
жидкостей, далекіе отъ насыщенія, и дѣйствительно въ настоящее время
(1898) удалось всѣ газы превратить въ жидкое состояніе. Такимъ обра-
зомъ, какъ бы исчезаетъ разница между паромъ и газомъ. Мы однако
продолжаемъ называть газомъ вещество, свойства котораго не очень отли-
чаются отъ свойствъ, которыя мы приписывали идеальнымъ газамъ, со-
храняя названіе пара для вещества, уже близкаго къ насыщенію, а слѣд.
и къ жидкому состоянію. Такое различіе1, понятно, весьма неопредѣ-
ленно и представляется мало научнымъ. Однако оно довольно удобно и
сохранилось на практикѣ.
Болѣе научное разграниченіи пара отъ газа могло бы быть полу-
чено, если обратиться къ явленіямъ, зависящимъ отъ критической
температуры, о которой уже было упомянуто въ т. I и которая ниже бу-
детъ разсмотрѣна подробно. Мы видѣли, что при температурѣ, которая
выше критической, газъ ни при какихъ давленіяхъ не сгущается въ жид-
кость, и что, слѣдовательно, охлажденіе ниже критической температуры
есть условіе возможности ожиженія газа. Мы могли бы поэтому назы-
вать вещество газомъ, если его температура выше, паромъ — если
она ниже критической. Но это на практикѣ неудобно, ибо заставило бы
насъ СО2 называть газомъ при 32° и паромъ при 30°, такъ какъ его кри-
тическая температура находится при 31°.
Свойства газовъ, а слѣд. и паровъ, находящихся далеко отъ насы-
щенія, были нами разсмотрѣны въ отдѣлѣ четвертомъ (т. I). Въ настоя-
щей главѣ мы разсмотримъ явленіе перехода вещества изъ жидкаго въ
парообразное состояніе и обратно. Слѣдующія главы будутъ посвящены
524
Испареніе и ожиженіе.
свойствамъ паровъ, насыщенныхъ и не насыщенныхъ;
въ послѣднемъ случаѣ предполагаемъ, что свойства пара далеки отъ
свойствъ идеальныхъ газовъ, т.-е. что паръ находится не очень далеко О'гъ
насыщенія.
§ 2. Кипѣніе. Если къ жидкости притекаетъ больше тепла, чѣмъ
необходимо, чтобы поддержать испареніе, происходящее у ея свободной
поверхности, то температура жидкости поднимается и испареніе увеличива-
ется, происходя сначала только у поверхности жидкости.
При нѣкоторой опредѣленной температурѣ начинается однако образованіе
пузырьковъ пара около стѣнокъ сосуда, въ которомъ жидкость помѣщена,
а также внутри жидкости. Эти пузырьки поднимаются въ жидкости и
лопаются на ея поверхности, причемъ содержащійся въ нихъ паръ осво-
бождается. Поверхность жидкости сильно волнуется, и внутри жидкости
происходятъ болѣе или менѣе бурныя и неправильныя движенія. Это
явленіе называется кипѣніемъ жидкости, и мы примемъ за его харак-
теристику именно появленіе пузырьковъ пара ниже уровня
жидкости. Когда началось кипѣніе, то вся теплота, притекающая извнѣ
къ жидкости, тратится на парообразованіе. Температура, которую мы
назовемъ точкою кипѣнія, остается постоянною во все время ки-
пѣнія. Ей соотвѣтствуетъ нѣкоторое значеніе величины р, которое мы
назовемъ скрытою теплотою кипѣнія.
Температура кипѣнія і зависитъ отъ давленія р,
подъ которымъ жидкость находится, ибо кипѣніе проис-
ходитъ тогда, когда упругость пара, заключающагося въ пузырькахъ
внутри жидкости, немного п р е в ы пі а е т ъ внѣшнее давленіе р.
Иногда говорятъ, что точка кипѣнія жидкости есть та температура, при
которой упругость насыщеннаго пара жидкости равняется внѣшнему да-
вленію. Однако это опредѣленіе не вполнѣ точно, ибо не только внутри
жидкости и въ пузырькахъ, но и около самой поверхности упругость пара
должна быть немного больше внѣшняго давленія; въ противномъ случаѣ
этотъ паръ не сталъ бы подниматься, перемѣщаясь отъ мѣстъ большаго
къ мѣстамъ меньшаго давленія. Говоря объ устройствѣ приборовъ, слу-
жащихъ для опредѣленія пли повѣрки верхней постоянной точки на
шкалѣ термометровъ, мы указали (стр. 29) на необходимость прибавить
къ этимъ приборамъ особый манометръ для опредѣленія разности между
барометрическимъ давленіемъ и упругостью пара.
При измѣненіи внѣшняго давленія р мѣняется точка кипѣнія въ
весьма широкихъ размѣрахъ, и въ этомъ заключается важное*, хотя и
лишь количественное различіе между плавленіемъ и кипѣніемъ. Подъ
колоколомъ воздушнаго насоса вода закипаетъ при температурахъ, близ-
кихъ къ 0°; въ замкнутомъ пространствѣ, находясь подъ давленіемъ соб-
ственныхъ паровъ, вода кипитъ при температурѣ, которая можетъ быть
значительно выше 100°; въ котлѣ Раріп’а, извѣстномъ изъ элементар-
наго курса физики, легко получаются температуры до 130°. Когда внѣш-
нее давленіе, которое можетъ быть произведено и выше лежащими сло"
Кипѣніе.
525
ями жидкости, уменьшается, то внезапное сильное кипѣніе можетъ при-
нять характеръ взрыва. На этомъ основано объясненіе происхожденія
гейзеровъ въ Исландіи и др. мѣстахъ, данное В и п 8 е п'омъ и Т у п -
д а 1 Г емъ: послѣдній построилъ приборъ, воспроизводящій явленія, на-
блюдаемыя въ гейзерахъ.
Мы обозначили черезъ р=](і) зависимость упругости насыщеннаго
пара отъ температуры; получающееся отсюда выраженіе вида
і = Р(р)...........................(3)
опредѣляетъ зависимость температуры кипѣнія і отъ внѣшняго давленія.
Для опредѣленія точекь кипѣнія жидкостей служатъ приборы, болѣе
или менѣе подобные прибору, изображенному на рис. 8 стр. 29, и слу-
жащему для опредѣленія или повѣрки верхней постоянной точки (100°) на
шкалѣ термометра. Различные сюда относящіеся приборы построили
Маіпе, Р а лѵ 1 е чѵ 8 к і, Н а п (і 1 и РгіЬгат, ѲагпеНеу и ЛѴіІ-
1 і а т 8 , Л о п е 8 идр. Резервуаръ термометра во всѣхъ этихъ прибо-
рахъ помѣщается надъ жидкостью, т.-е. въ парахъ, которые, поднявшись
по внутренней трубкѣ, сверху открытой, опускаются затѣмъ внизъ въ
пространствѣ между этой и наружной трубкой. Впрочемъ КаМЬаиш
видоизмѣнилъ устройство прибора, заставляя пары подниматься по на-
ружному пространству и опускаться по внутреннему, содержащему резер-
вуаръ термометра и соединенному съ холодильникомъ. Главная часть
этого прибора изображена на рис. 143. Въ послѣдней главѣ мы возвра-
Рис. 143.
тимся къ вопросу объ опредѣленіи точекъ
кипѣнія жидкостей.
Большой интересъ представляетъ опре-
дѣленіе плотности и молекуляр-
наго объема жидкости при тем-
пературѣ кипѣнія. Для этой цѣли
служитъ приборъ, изображенный на рис. 144.
Испытуемая жидкость помѣщается въ
колбѣ, и ею же наполняется пикнометръ б,
который подвѣшивается на проволокѣ у
внутри колбы; а термометръ, /? капилярная
трубка, черезъ которую вдувается слабая
струя воздуха, если жидкость кипитъ не-
правильно, т.-е. толчками (см. ниже).
Трубка а ведетъ къ холодильнику; трубка Ь
служитъ для того, чтобы сгустившаяся
холодная жидкость не попадала на термо-
метръ. Зная вѣсъ, емкость и коеффиціентъ
расширенія пикнометра и взвѣсивъ его
вмѣстѣ съ жидкостью, которая въ немъ
остается послѣ продолжительнаго его пре-
Рис. 144.
быванія въ парахъ той же жидкости, мы легко опредѣлимъ плотность сі
526
Испареніе и.ожиженіе.
жидкости при температурѣ кипѣнія: ея молекулярный объемъ ѵ
при той же температурѣ найдемъ по формулѣ ѵ = т : сі, гдѣ т ея мо-
лекулярный вѣсъ.
Говоря о точкѣ кипѣнія жидкости, имѣютъ въ виду ту температуру і,
при которой жидкость кипитъ, находясь подъ нормальнымъ да-
вленіемъ въ 760 мм. Такъ какъ во время опыта барометрическое
давленіе, вообще говоря, будетъ отличаться отъ нормальнаго, то для по-
лученія сравнимыхъ между собою результатовъ, необходимо ввести по-
правку, переходя отъ наблюденнаго і къ тому, которое соотвѣтствуетъ
нормальному давленіи). Мы увидимъ ниже, какъ слѣдуетъ вводить эту
поправку.
Точка кипѣнія жидкостей зависитъ отъ матеріала того со-
суда, въ которомъ кипѣніе совершается, и отъ степени его чистоты.
Важную роль при кипѣніи играетъ воздухъ или иной газъ, ра-
створенный въ жидкости или находящійся внутри жидкости или у стѣ-
нокъ сосуда, хотя бы и вгь самомъ ничтожномъ количествѣ.
Открытіе вліянія сосуда на точку кипѣнія обыкновенно приписыва-
ется Сгау-Ьи 8 8ас’у (1817); однако объ этомъ вліяніи, повидимому,
было извѣстно уже въ XVIII столѣтіи, такъ какъ въ 1777 г. появился
докладъ членовъ Воуаі 8 о с і е I у въ Лондонѣ, рекомендовавшій по-
мѣщать шарикъ термометра не въ кипящей жидкости, но въ ея парахъ.
Па вліяніе сосуда указалъ также А с Іі а г сі въ 1784 г. 6ау-Ьп88ас
нашелъ, что точка кипѣнія воды въ стеклянномъ сосудѣ выше, чѣмъ въ
металлическихъ; этотъ результатъ подтвердили Мипке иКисіЬег^
Позже М а г с е I тщательно изучилъ это явленіе. Онъ нашелъ, что точка
кипѣнія данной жидкости находится тѣмъ выше, чѣмъ лучше жидкость
смачиваетъ стѣнки сосуда, т.-е. чѣмъ больше сцѣпленіе между частицами
жидкости и частицами ‘ вещества, изъ котораго состоитъ внутренній по-
верхностный слой стѣнокъ сосуда. Въ стеклянномъ сосудѣ, тщательно
вычищенномъ сѣрною кислотою и затѣмъ промытомъ водою, получается
точка кипѣнія воды на 6° выше, чѣмъ въ сосудѣ металлическомъ. Подоб-
ный же результатъ нашелъ М а г с е і и для другихъ жидкостей.
Вліяніе раствореннаго воздуха на точку кипѣнія воды было открыто
Бе Ьис’омъ (1772), который высказалъ мнѣніе, что пузыри пара обра-
зуются внутри жидкости при ея кипѣніи вокругъ мельчайшихъ пузырь-
ковъ воздуха, служащихъ какъ бы ядромъ, около котораго путемъ вну-
тренняго испаренія возникаютъ пузыри пара. Онъ нашелъ, что вода, изъ
которой воздухъ удаленъ продолжительнымъ кипяченіемъ, можетъ быть
нагрѣта въ трубкѣ до 130°, безъ того, чтобы она начала кипѣть.
Этимъ вопросомъ занимались Боппу, Биіоиг, Оегпег, КгеЬ8,
Сггоѵе и др. Боппу показалъ, что чистая вода въ стеклянномъ, тща-
тельно вычищенномъ сосудѣ закипаетъ лишь при 137°, причемъ происхо-
дитъ какъ бы взрывъ перегрѣтой массы. Биіоиг наблюдалъ кипѣніе
нагрѣтой воды подъ колоколомъ воздушнаго насоса, послѣ того какъ весь
воздухъ былъ изъ нея изгнанъ. Оказалось, что температура кипѣнія
Кипѣніе.
527
иногда на 20° и болѣе превышала ту, которую слѣдовало ожидать соот-
вѣтственно имѣвшемуся давленію. К г е Ь б’у удалось нагрѣть воду, весьма
тщательно освобожденную отъ воздуха, почти до 200°, не вызывая кипѣ-
нія, а Сггоѵе даже высказалъ мысль, что абсолютно чистая вода вовсе
не можетъ быть доведена до кипѣнія.
Малѣйшій пузырекъ воздуха, введенный въ перегрѣтую воду, неме-
дленно вызываетъ сильное кипѣніе, причемъ всѣ пузыри пара образу-
ются одинъ за другимъ, въ томъ мѣстѣ, гдѣ находится пузырекъ воз-
духа, который самъ при этомъ, хотя и весьма медленно, уменьшается;
повидимому каждый пузырекъ пара увлекаетъ съ собою нѣкоторое коли-
чество воздуха, (т е г п е 2 показалъ, что 1 куб. мм. воздуха можетъ
поддерживать кипѣніе втеченіе 24 часовъ, причемъ около него или вѣр-
нѣе изъ него образуется до полумилліона пузырей пара, діаметромъ въ
5 мм. каждый.
Точка кипѣнія воды, повышенная вслѣдствіе вліянія сосуда или
вслѣдствіе отсутствія въ ней воздуха, немедленно дѣлается нормальною,
если въ жидкость ввести песокъ, опилки или вообще какое-либо твердое
тѣло, у поверхности котораго тотчасъ же и начинается 'образованіе пу-
зырьковъ пара. Это явленіе несомнѣнно вызывается тѣмъ слоемъ воз-
духа, который покрываетъ поверхность твердыхъ тѣлъ (т. I); оно ана-
логично одному изъ случаевъ выдѣленія растворенныхъ газовъ изъ жид-
костей (т. I): Когда слой воздуха истощится, то тѣло теряетъ способ-
ность вызывать кипѣніе. Тошііпвоп показалъ, что проволока, погру-
женная въ жидкость, близкую къ закипанію, вызываетъ кипѣніе, которое
однако черезъ нѣкоторое время прекращается ; проволока становится не-
дѣятельною. Проволока, предварительно прокаленная н затѣмъ охлаж-
денная въ парахъ самой жидкости, вообще недѣятельна. Проволока не-
дѣятельная вновь начинаетъ вызывать кипѣніе, если она нѣкоторое
время находилась въ воздухѣ. Впрочемъ Тошііпвоп приписываетъ
главную роль не самому воздуху, а содержащейся въ немъ пыли. Онъ
находитъ, что пузырекъ воздуха, совершенно лишенный пыли, не вызы-
ваетъ кипѣнія.
Итакъ температура кипѣнія зависитъ отъ сосуда и отъ содержанія
воздуха въ жидкости. Наблюденія ВисІЪег^’а и Магсеі показали,
однако, что температура паровъ кипящей жидкости отъ указан-
ныхъ обстоятельствъ не зависитъ ; она вполнѣ опредѣляется родомъ жид-
кости и внѣшнимъ давленіемъ.
Жидкости могутъ быть перегрѣты, если онѣ находятся внутри дру-
гой жидкости одинаковой съ ними плотности. В и і о и г нашелъ, что
капли воды, плавающія внутри смѣси льняного масла съ гвоздичнымъ
масломъ, могутъ быть нагрѣты до 178°, не переходя въ пары.
До сихъ поръ не удалось открыть простой зависи-
мости между точкою кипѣнія вещества и его химиче-
скимъ составомъ и строеніемъ. Однако открыты нѣкоторыя
правильности при сравненіи точекъ кипѣнія различныхъ веществъ. 06-
528
Испареніе и ожиженіе.
зоръ такихъ правильностей можно найти въ диссертаціи МагсклѵаІсГа
(1888), въ «ЪеЬгЬпсЬ йег аіі^етеіпеп СЬетіе» Озѣлѵаій’а (2-ое изд.
т. I), въ словарѣ ЕеЫіп^’а (НапйлѵогіегЬисЬ, статья Біейерипсі, 1893)
и особенно подробно въ книгѣ 6ггаЬат-ОНо, БеЬгЬпсЬ сіег СЬетіе I,
3 р. 535—564, 3-е изд., Брауншвейгъ 1898 (статья Магсклѵаій’а). Мы
укажемъ немногія изъ этихъ правильностей. Наиболѣе важное указаніе
дали Е а т 8 а у и V о и п §•, которые нашли, что отношеніе абсолют-
ныхъ температуръ кипѣнія Т± и Т2 при различныхъ давленіяхъ и р2
есть число одинаковое для веществъ химически родственныхъ. Отсюда
слѣдуетъ, что если ДТ есть измѣненіе абсолютной температуры кипѣнія Г,
вызванное измѣненіемъ давленія на 1 мм. вблизи нормальнаго давленія
ДТ
въ 760 мм., то величина а = есть величина, одинаковая для родствен-
ныхъ веществъ. На этомъ основано правило СгаИ’а для приведенія
точки кипѣнія, наблюденной при барометрическомъ давленіи Н, къ
нормальному давленію. Если наблюдалась точка кипѣнія Т\ то иско-
мая нормальная равна
Т = Г'+ «(760 —Я).......................(4)
Величины а вычислены для многихъ веществъ; вотъ нѣкоторые
примѣры:
а а
Вода . 0,000100 Бензолъ 0,000122
Этиловый алкоголь . 0,00009Ь Терпентинное масло . 0,000131
Анилинъ . 0,000113 Нафталинъ . . . . 0,000121
Сѣроуглеродъ . . . 0,000129 Ртуть 0,000122.
Чтобы для другого вещества опредѣлить Т по формулѣ (4), слѣдуетъ
для а взятъ значеніе, соотвѣтствующее веществу, которое химически
родственно веществу испытуемому.
Въ гомологическихъ рядахъ нормальныхъ алкоголей, кислотъ, слож-
ныхъ эфировъ, кетоновъ и нитриловъ замѣчается довольно правильное
повышеніе точки кипѣнія на 19 21°, при каждой замѣнѣ атома Н груп-
пою СН%. Для алдегидовъ повышеніе равно 26—27°. Замѣна атома Н
группою ОН вызываетъ повышеніе температуры кипѣнія, часто близкое
къ 100°. Введеніе перваго атома СІ въ метиловую группу вызываетъ по-
вышеніе точки кипѣнія приблизительно на 60°. Замѣна атома СІ ато-
момъ Вг или вызываетъ повышеніе точки кипѣнія приблизительно
на 24° и на 50°. Этими вопросами занимались Корр, ЛѴапкІуп,
ВсЬогІеттег, Ьіппетапп, 2іпке и РгапсЬітопі, \Ѵіп-
кеітапп, Ьоп^іпевси и др.
Вальденъ (1909) нашелъ весьма интересное соотношеніе между
абсолютной температурой кипѣнія Т не ассоціированной жид-
кости и ея капиллярной постоянной а? (т. I) при температурѣ Т.
Если выражено въ мм.2, то
Кипѣніе.
529
гдѣ М молекулярный вѣсъ жидкости. Произведеніе 7И&2 Вальденъ
называетъ молекулярнымъ сцѣпленіемъ. Для ассоціированныхъ
жидкостей дробь (4,а) имѣетъ величину, меньшую 1,16 и при томъ тѣмъ
меньшую, чѣмъ выше степень ассоціаціи. Если ввести поверхностное
натяженіе а (т. I), выражая его въ динахъ на см., то
9 «Іа5#
а =
2
л ™ , М
гдѣ а плотность жидкости. Обозначимъ молекулярный объемъ —-
чрезъ V; тогда изъ (4,а) имѣемъ:
Вальденъ провѣрилъ формулы (4.&1 и (4.&) для большого числа
органическихъ жидкостей *и нашелъ хорошее согласіе. Въ § 4 мы ещр
разъ возвратимся къ этимъ изслѣдованіямъ Вал ьдена.
Изъ числа опредѣленій температуръ кипѣнія, сдѣланныхъ за по-
слѣднее время, упомянемъ важную работу Еитогіороиіов’а (1908),
который нашелъ температуру кипѣнія сѣры равной 443,58°.
Большой интересъ представляютъ кипѣніе и протекающая совмѣстно
съ нимъ дестилляція металловъ. Это явленіе изслѣдовали К а Ы -
Ьапіп (1899—1902), ЗсйиПег (1903), Её ту (1903), КгаИ и Ветх-
іе Ій (1905), Моіззап (1905) и Сггееп^ѵоой (1909). Уже въ девя-
ностыхъ годахъ прошлаго вѣка 8с1іи11ег подвергъ дестилляціи легко-
плавкіе металлы. КаЫЬапш первый подвергъ дестилляціи въ пустотѣ
также и тугоплавкіе металлы, именно А/, 8Ь, АІ, М§, Са, 8г, Ва, 2лг,
Ссі, Та, РЬ, Ві, Си, А§, Аи, Ыі, Ре, Сг, 7лі и 8п. Онъ достигъ темпе-
ратуры въ 1440° и показалъ, что дестилляціей можно выдѣлять изъ метал-
лическихъ сплавовъ ихъ составныя части. Ему удалось помощью де-
стилляціи выдѣлить мѣдь изъ никкелевой монеты, содержавшей 25°/0 Си.
Г ё г у помощью оптическаго пирометра опредѣлилъ точки кипѣнія Си и 7.и.
Большое число изслѣдованій было произведено М о і 8 8 а п’омъ по-
мощью его электрической печи. Чистый металлъ или сплавъ помѣщался
въ небольшомъ тиглѣ и подвергался дѣйствію вольтовой дуги, которая
образовывалась внутри печи между двумя горизонтальными углями. Не-
много выше отверстія тигля помѣщалась горизонтальная мѣдная труба,
чрезъ которую съ большой быстротой протекала холодная вода. На эту
трубу осѣдали пары кипящаго металла. При многихъ опытахъ надъ тру-
бой помѣщался выступавшій изъ печи стеклянный колоколъ, въ кото-
ромъ конденсировались остатки металлическихъ паровъ. Такимъ путемъ
М о і 8 8 а п дестиллировалъ Си, Аи. Ыі. Ре, Мп, Сг, Мо. ѴР, V, Оз. Ри.
Рі, Рсі, ]г, РИ и сплавы Аи съ Си и 8п и А^ съ Си, РЬ и 8п. Металлы кон-
денсировались въ различныхъ формахъ, частью кристаллическихъ, частью
аморфныхъ. Въ этихъ опытахъ дестилляція происходила при обычномъ
атмосферномъ давленіи и при чрезвычайно высокихъ температурахъ, до-
курсъ ФИЗИКИ О. X В О Л ь С О Н А. Т. III, изд. 3-е. 34
530
Испареніе и ожиженіе.
ходившихъ до 3500°. 'При испареніи металловъ платиновой группы М о і 8 -
8ап употреблялъ токъ въ 500 амп. (для О^въ 700 амп.) и 110 вольтъ;
втеченіе 5 минутъ онъ получалъ отъ 9 С/г) до 29 (05) граммовъ дестил-
лированнаго металла. Въ желѣзной группѣ по трудности испаренія ме-
таллы расположились въ слѣдующій рядъ: Л4п, №, Сг, Ре. Еще труд-
нѣе достигается испареніе Мо и ѴС; послѣдній испарялся лишь ьчрезъ
20 минутъ при токѣ въ 700 амп. и 110 вольтъ, тогда какъ другіе ме-
таллы начинали испаряться уже чрезъ 5 минутъ.
Гёгу для температуръ кипѣнія Хи и Си нашелъ величины 1040°
и 2100°.
СггееплѵоосІ (1909) произвелъ первыя точныя опредѣленія темпе-
ратуръ кипѣнія металловъ (помощью пирометра УѴаппег’а). Онъ на-
шелъ слѣдующія числа :
АІ 1800° Си 2310° Мп 1900°
8Ь 1440° Ре 2450° 1955°
Ві 1420° РЬ 1525° 8п 2270°
Сг 2200° Мё 1120°
Вопросомъ о молекулярномъ объемѣ ѵ жидкостей при
температурахъ кипѣнія занимался Корр; данное имъ правило было
уже указано въ т. [. Изъ этого правила, которое говоритъ, что ѵ есть
аддитивное свойство и можетъ быть вычислено по извѣстному составу
вещества, слѣдуетъ, что изомеры должны имѣть одинъ и тотъ же моле-
кулярный объемъ ѵ при температурахъ кипѣнія, хотя эти температуры
далеко не одинаковы, какъ видно изъ слѣдующей таблички:
| Точка кипѣнія Молекулярный объемъ ѵ
Уксусная кислота . . с2н^о2 118°,0 63,8
Муравьинокислый этилъ « 32,5 62,7
Масляная кислота . . 162,5 108,2
Уксуснокислый метилъ « 77,5 106,2
Бутиловый этилъ . . ад0о 117 1 101,9
Метилпропиловый эфиръ « 38,9 105,1
Молекулярные объемы ѵ нормальныхъ алкоголеи увеличиваются при-
близительно на 21. а нормальныхъ жирныхъ кислотъ приблизительно на 22
при каждой замѣнѣ атома РІ группою СН^. Вопросомъ о молекулярныхъ
объемахъ при температурѣ к кипѣнія занимались еще Виіі, ТЬогре,
Ь о 8 8 е п , Н о г 81 ш а п п, 8 с Ь і 11, 2 а Ь п (1 е г и 8сЬгое(іег.
Вопросъ о кипѣніи растворовъ мы разсмотримъ въ послѣдней
главѣ этого тома.
§ 3. Сфероидальное состояніе. Если опустить нѣсколько капель
жидкости на горизонтальную поверхность твердаго тѣла, нагрѣтаго до
Сфероидальное состояніе.
531
температуры, которая значительно выше точки кипѣнія жидкости, то по-
слѣдняя. не закипая, принимаетъ форму, закругленную съ боковъ, а при
малыхъ количествахъ жидкости форму сплюснутаго шара или сфероида.
Въ этомъ случаѣ говорятъ, что жидкость приняла сфероидальное
состояніе. Оказывается, что при этомъ жидкость <вода, ртуть, эфиръ
и т. д) испаряется довольно медленно. Когда твердое тѣло охлаждается
и достигаетъ нѣкоторой температуры, лежащей однако еще значительно
выше точки кипѣнія жидкости, эта послѣдняя внезапно и со взрывомъ за-
кипаетъ, причемъ часть ея разбрасывается во всѣ стороны. Это явленіе
давно извѣстно; о немъ упоминаетъ ЕПет еще въ 1746 г. Первое
подробное его изслѣдованіе произвелъ Ь е і (1 е п Т г о 8 1 (1756), по имени
котораго оно иногда и называется. Далѣе имъ занимались ВитТогсІ,
ВоеЬегеіпег, Роиіііеі, Регкіпз, Мипке, ВиН, Ваисігі-
топѣ, Рег8оп, Агтвігоп^, Воиіі^пу , М агіас, сіе Ьиса,
8ийге, Вег^ег, Соііеу, Ро&^ еп Йо гТі, Тупйаіі, и др. Наи-
болѣе обстоятельное изслѣдованіе, разрѣшившее многіе спорные вопросы,
принадлежитъ Н. А. Гезехусу (1876). Въ послѣднее время занима-
лись этимъ явленіемъ въ особенности Кгізіепзеп (1889), Сгоззагі
(1895) и Зіагк (1898).
Спорными являлись вопросъ о температурѣ жидкости, находя-
щейся въ сфероидальномъ состояніи, вопросъ о томъ, соприкасается ли
жидкость съ нагрѣтою поверхностью и, наконецъ, вопросъ о причинахъ
самаго явленія. Названными выше учеными были высказываемы самыя
разнорѣчивыя мнѣнія по этимъ вопросамъ. Такъ напр. нѣкоторые наблю-
датели находили температуру водяной капли, находящейся въ сферо-
идальномъ состояніи, близкой къ |00°, между тѣмъ какъ другіе (Ваисі-
гі т о п і, сіе Ьиса) утверждали что она ниже 50° и даже доходитъ до 36°.
Для рѣшенія спорнаго вопроса о соприкасаніи сфероидальной капли
съ поверхностью твердаго тѣла можетъ служить электрическій токъ, если
одинъ электродъ соединить съ металлическимъ нагрѣтымъ тѣломъ, дра-
гой опустить въ жидкость. Вп И Г1832) полагалъ, что между каплей и
нагрѣтой поверхностью существуетъ прерывчатое соприкосновеніе, что
капля то поднимается, то опускается ; между тѣмъ ЫоеЬегеіпег еще
въ 1821 г. утверждалъ, что соприкосновенія вовсе нѣтъ.
Вий первый указалъ на то, что жидкость не смачиваетъ го-
рячей поверхности и потому, подобно каплямъ ртути на стеклѣ, мраморѣ
и т. под., принимаетъ сфероидальную форму. Самая капля поддержива-
ется упругостью слоя пара, образующагося подъ нею; вслѣдствіе своей
дурной теплопроводности этотъ паръ защищаетъ жидкость отъ непосред-
ственнаго дѣйствія теплоты. Этотъ паръ вырывается по сторонамъ на-
ружу, вслѣдствіе чего вдоль края капли образуются какъ бы впадины, и
нерѣдко вся капля принимаетъ звѣздообразную форму.
Опыты Н. А. Гезехуса показали, что когда сфероидъ спокойно
лежитъ на гладкой поверхности твердаго тѣла, то электрическій токъ, даже
при большой электродвижущей силѣ, не проходить отъ капли къ этому тѣлу.
34*
532
Испареніе и ожиженіе.
Когда поверхность неровная и сфероидъ сильно колеблется, то при не
очень высокихъ температурахъ замѣчается прохожденіе тока. Отсюда
слѣдуетъ, что сфероидъ вообще не касается горячей поверхности,
и что если происходятъ соприкосновенія, то они имѣютъ случайный ха-
рактеръ». Далѣе И. А. Гезехусъ нашелъ, что просвѣтъ между сферо-
идомъ и горячею поверхностью увеличивается съ повышеніемъ темпера-
туры твердаго тѣла. Жидкость несомнѣнно поддерживается паромъ; ея
температура, которая можетъ мѣняться въ довольно широкихъ предѣлахъ,
вообще говоря, не очень отличается отъ температуры кипѣнія жидкости.
8іагк (1898) включилъ телефонъ въ цѣпь электрическаго тока, въ
которую была введена сфероидальная капля, какъ въ опытахъ Н. А. Г е -
з е х у с а. Онъ показалъ, что капля производитъ быстрыя колебанія въ
вертикальномъ направленіи. Далѣе 8іагк указалъ, что на нижней сто-
ронѣ капли поверхностное натяженіе меньше, чѣмъ на верхней. Вслѣд-
ствіе этого жидкость на нижней поверхности капли радіально расходится,
по бокамъ поднимается, а на верхней поверхности радіально стремится
къ центру и во внутрь капли. Такимъ образомъ образуется кольце-
образное вихревое движеніе, которое и можетъ быть непосредственно на-
блюдаемо.
Эфиръ принимаетъ сфероидальное состояніе на поверхности горячей
воды. Воиіі^пу помѣстилъ жидкій 5О2, который кипитъ при — 10°
въ раскаленный платиновый тигель; нѣсколько капель воды, опущенныя
въ жидкость, немедленно замерзли. Е а г а (1 а у замѣнилъ жидкій 5О2
твердымъ СО2 и воду — ртутью: такимъ образомъ ему удалось заморозить
ртуть въ раскаленномъ платиновомъ тиглѣ.
Сфероидальнымъ состояніемъ объясняются различные опыты и явле-
нія Въ немъ заключается одна изъ вѣроятныхъ причинъ взрывовъ па-
ровыхъ котловъ. Сюда же относится извѣстный фактъ, что можно безъ
вреда опустить руку, немного влажную вслѣдствіе испарины, или смочен-
ную эфиромъ, въ расплавленный свинецъ и даже въ расплавленную бронзу.
§ 4. Скрытая теплота испаренія и кипѣнія. Разсматривая тепло-
выя явленія, сопровождающія переходъ тѣла изъ жидкаго состоянія въ
газообразное и обратно, приходится отличать нѣсколько различныхъ ве-
личинъ, на которыя мы прежде всего и укажемъ. Скрытою те-
плотою испаренія д (безъ всякихъ прибавленій) мы будемъ на-
зывать количество теплоты, поглощаемое вѣсовою единицею жидкости при
переходѣ ея въ паръ, насыщающій пространство. Иногда го-
ворятъ о скрытой теплотѣ кипѣнія; но такъ какъ кипѣніе въ зави-
симости отъ внѣшняго давленія можетъ происходить при всякой темпера-
турѣ, то ясно, что эта величина тождественна съ д. Если испаряется
граммъ-молекула, т.-е. т граммовъ, гдѣ т молекулярный вѣсъ вещества,
то поглощается молекулярная скрытая теплота испаре-
нія, равная тр, если д отнесено къ одному грамму. Величина р рас-
падается на двѣ части де и д;; первая расходуется на внѣшнюю ра-
боту расширенія вещества отъ удѣльнаго объема 5 жидкости до удѣль-
Скрытая теплота испаренія
533
наго объема и пара; вторая тратится на внутреннюю работу разъ-
единенія частицъ или, пользуясь терминомъ С1 а и 8 і и 8’а, на дисгрега-
цію (стр. 444) вещества. Величину ое можно назвать внѣшнею, а ве-
личину оі внутреннею скрытою теплотою испаренія; по-
слѣднюю иногда еще называютъ истинною скрытою теплотою испа-
ренія. Произведенія /пое и то; представляютъ тѣ же, но молеку-
лярныя величины.
Полною теплотою испаренія Л называется количество теп-
лоты, которое потребно, чтобы вѣсовую единицу жидкости нагрѣть отъ 0°
до данной температуры і, и при этой температурѣ превратить въ насы-
щенный паръ. Если черезъ д обозначить количество теплоты, расходуе-
мой при этомъ на нагрѣваніе жидкости, то
Л = д -|- р = д -|- оі -|- де , . . (5)
Если С теплоемкость жидкости при постоянномъ давленіи, то
і
д Ссіі..................................(6)
• 0
Элементарная внѣшняя работа расширенія равна рсіѵ, гдѣ р давленіе,
сіѵ приращеніе объема. Поэтому вся работа при испареніи, совершающемся
при постоянномъ давленіи р, равна р(б — 5); отсюда слѣдуетъ, что
Яе = АР(° — 5)......................(7)
гдѣ А термическій эквивалентъ работы. Объемъ 5 жидкости всегда очень
малъ сравнительно съ объемомъ б пара, гакъ что послѣднюю формулу
можно также написать въ видѣ
Ѳе = Аро .......... (8)
Вставляя (6) и (7) въ (5), получаемъ
і
= С(іі + оі + Ар(б — 8)...(9)
о
Сумма д Оі иногда называется теплотою насыщеннаго
пара; она опредѣляетъ избытокъ энергіи пара надъ энергіей, которою
обладала жидкость при 0°.
Величины р, о& Рь А и а суть функціи той температуры і, къ ко-
торой онѣ отнесены; С есть функція температуры, мѣняющейся отъ 0°
до і; величиною 5 и во всякомъ случаѣ ея зависимостью отъ і, какъ ска-
зано, можно вообще пренебречь.
Величина Ое несомнѣнно сперва растетъ, когда температура увели-
чивается. Но при критической температурѣ р^ = О, а нагому должна
существовать такая температура, при которой Ое имѣетъ наибольшее
значеніе. На это впервые указалъ Віеіегісі (1901). Затѣмъ Зіеіап
534
Испареніе и ожиженіе.
Рис. 145.
Меуег и К іііе г показали. что абсолютная температура, при которой
де максимумъ, равна 0,7 абсолютной критической температуры.
Переходимъ къ способамъ опредѣленія скрытой теп-
лоты испаренія и къ результатамъ этихъ опредѣленій. Первая по-
пытка опредѣленія р для воды принад-
лежитъ В1 а с к’у: онъ нашелъ о = 445.
Затѣмъ Ігѵіпе получилъ число 43о, за-
ставляя пары кипящей воды охлаждаться
въ калориметрѣ.
Существуютъ два главные ме-
тода опредѣленія о. Во-первыхъ,
можно пары кипящей жидкости ввести въ
калориметръ, заставляя ихъ охлаждаться
въ змѣевикѣ. Взвѣшивая образовавшуюся
жидкость, опредѣляя количество тепла, по-
лученнаго калориметромъ, и вводя необхо-
димыя поправки на лучеиспусканіе, можно
найти искомое р. Во-вторыхъ, можно
ввести въ самый* калориметръ опредѣлен-
ное количество испытуемой жидкости и измѣрить охлажденіе калориметра,
вызванное испареніемъ жидкости.
Иной способъ предложили Вголѵп и 8тііЬ (1903).
Первый способъ схематически иллюстрируется приборомъ, изо-
браженнымъ на рис. 145. Пары жидкости, кипящей въ ретортѣ С, про-
ходятъ по змѣевику 5, окруженному водою калориметра, и, сгустившись,
собираются въ резервуарѣ /?; образовавшаяся жидкость выпускается че-
резъ кранъ г и взвѣшивается. Трубка Т соединяетъ реторту и змѣевикъ
съ наружнымъ воздухомъ, такъ что пары образуются и сгущаются подъ
атмосфернымъ давленіемъ; і и V термометры, А мѣшалка, Р стѣнка,
ограждающая калориметръ отъ вліянія печи. Пусть Р вѣсъ образовав-
шейся жидкости, і ея температура кипѣнія, начальная, /2 окончательная
температура калориметра, С теплоемкость всѣхъ частей калориметра
вмѣстѣ съ водою, с теплоемкость испытуемой жидкости. Тогда о полу-
чается изъ равенства
+ Рс(і — 4) = С(/2 — У -н /?.............(10)
гдѣ Р количество теплоты, потерянной калориметромъ во время опыта
вслѣдствіе лучеиспусканія. Къ возможнымъ источникамъ погрѣшностей
относятся передача теплоты отъ очага къ калориметру черезъ паропровод-
ную трубку, и переходъ частицъ жидкости, увлеченныхъ парами, изъ С
въ калориметръ. Далѣе часть паровъ можетъ сгуститься, не дойдя до
калориметра: необходимо, чтобы образующаяся при этомъ жидкость сте-
кала обратно въ сосудъ, въ которомъ происходитъ кипѣніе. На это об-
стоятельство обратилъ особое вниманіе Вгіх.
Весьма удобный приборъ построилъ ВегіЬеІоі; онъ изображенъ
Скрытая теплота испаренія
535
на рис. 146. Жидкость РР нагрѣвается кольцевою газовою горѣлкою /,
расположенной подъ металлическою сѣткою т. Для защиты калориметра
служитъ деревянная крышка с' покрытая листомъ картона сс, и ме-
таллическая сѣтка п. Пары проходятъ черезъ ТТ въ змѣевикъ 55 и со-
бираются въ резервуарѣ /?.
соединенномъ трубкою і съ
наружнымъ воздухомъ.
КаЫепЬег^ (1901)
улучшилъ этотъ приборъ, за-
мѣнивъ горѣлку I платиновою
проволокою, помѣщенною въ
жидкость Р и нагрѣваемою
электрическимъ токомъ; этимъ
легко вызвать непрерывное и
ровное кипѣніе жидкости. До
классическихъ опытовъ Ке^-
п а и И (1845) производили
опредѣленія о для воды и для
другихъ жидкостей АѴ а 11,
С1 ё пі е п 1 и П е 8 о г т е ь,
Кит Го г (1, Ѵге, 8оиі-
Ьегп и Сгі^Ьіоп, Ое-
ргеІ2,Вгіх, А п сі г е лѵ $ и
другіе. АѴ а 11 вывелъ изъ
своихъ наблюденій, что для
воды величина
Рис. 146.
р = С0И8І.
Г11)
т.-е. что количество теплоты, потребной для того, чтобы воду при 0° пре-
вратить въ насыщенные пары при /°, не зависитъ отъ температуры Л
Такъ какъ для воды можно принять С= 1, то мы имѣли бы р + = Сопзі.,
т.-е. что скрытая теплота испаренія воды уменьшается на единицу при
повышеніи температуры на 1°. Этотъ такъ называемый законъ АѴаѣі’а,
однако, какъ мы увидимъ, невѣренъ. Точно также невѣренъ законъ
8 о и 1 Іі е г п’а и СгіцЫоп’а. по которому для воды р = Сопві., а именно
при всѣхъ температурахъ р = 523. Не приводимъ чиселъ, найденныхъ
всѣми вышеназванными учеными; ограничиваемся указаніемъ, что для
воды нашли: ВишГогсі 570, ХѴаіІ 533. Иге 593,4, Вгіх 540, Сіё-
шепі и Везотгоез 550, Везргеіг 540, Апсігечѵа 535,9. Любо-
пытно, что Вегіііеіоі со своимъ простымъ приборомъ нашелъ 536,2,
что весьма мало отличается отъ числа 536,5, даннаго Ке^паиіі.
Чтобы опредѣлить р п о второму способу (стр. 534), можно поль-
зоваться приборомъ, изображеннымъ на рис. 147. Испытуемая жидкость
536
Испареніе и ожиженіе
помѣщаетея въ колбочкѣ внутри воды калориметра; она соединена труб-
кою / съ воздушнымъ насосомъ; к трубочка, вытянутая въ капилярный
кончикъ. Термометръ служитъ для опредѣленія охлажденія калориметра.
Сюда же относится способъ і г I г’а (см. ниже), помѣстившаго испы-
туемую жидкость внутри парового калориметра (стр. 187).
Я. С. Вго\ѵп и А. С. 8ті11і одновременно (1903) предложили та-
кой способъ опредѣленія р, при которомъ вовсе не приходится пользо-
ваться калориметромъ. Въ жидкости помѣщается проволока, которая на-
грѣвается электрическимъ токомъ. Сперва жидкость доводится до кипѣнія,
а затѣмъ втеченіе нѣкотораго времени кипѣніе1 поддерживается. Испа-
Рис. 147.
рившееся количество жидкости опредѣляется взвѣшиваніемъ; количество
же1 поглощенной теплоты д вычисляется по формулѣ (5^ стр. 255
д = 0,24/^ мал. кал.
Здѣсь і время въ секундахъ, і сила тока въ амперахъ, е дѣйствующая на
проволоку электродвижущая сила въ вольтахъ.
Переходимъ къ знаменитымъ опытамъ Вед’паиіі, которому при-
надлежатъ первыя точныя опредѣленія зависимости скрытой теп-
лоты испаренія отъ температуры і. Приборъ, которымъ
пользовался Ке^паиИ, изображенъ на рис. 148.
Пары кипящей воды выходятъ изъ котла V, вмазаннаго въ печь,
черезъ трубку въ парораспредѣлитель г, устройство котораго будетъ ука-
зано ниже, и изъ него, по желанію наблюдателя, въ одинъ изъ калори-
метровъ О или /)', для наполненія которыхъ опредѣленнымъ количе-
ствомъ воды служитъ сосудъ У. Въ этотъ сосудъ наливалась вода до опре-
дѣленной черты, проведенной на стеклянной трубкѣ а, и затѣмъ она че-
резъ трубки е и е* впускалась сперва въ одинъ калориметръ, а затѣмъ въ
другой. Внутри каждаго калориметра находились два полые металличе-
скіе шара, соединенные между собою короткою вертикальною трубкою.
Паръ вступаетъ въ одинъ изъ верхнихъ шаровъ; нижніе шары соеди-
нены при помощи змѣевиковъ съ трубками с и с'. Кромѣ того нижніе
Скрытая теплота испаренія.
537
шары снабжены внизу трубками съ кранами для выпусканія образовав-
шейся воды въ сосудикъ увеличеніе вѣса котораго опредѣляло вѣсъ Р
сгустившихся паровъ. Шары соединены при помощи трубокъ с, с‘, р и
т огь ртутнымъ манометромъ пп' и съ резервуаромъ сгущеннаго воз-
духа Р. Этотъ резервуаръ окруженъ водою и соединенъ въ / съ нагнетатель-
нымъ насосомъ. Насосъ А служитъ для накачиванія ртути въ манометръ.
Мѣняя давленіе р, одинаковое во всѣхъ частяхъ прибора, т.-е. въ котлѣ
и въ калориметрахъ, можно было въ широкихъ предѣлахъ мѣнять темпе-
ратуру кипѣнія. Понятно, что р равнялось упругости насыщеннаго пара.
Устройство парораспредѣлителя г видно на рис. 149 и 150, изъ которыхъ
первый представляетъ разрѣзъ плоскостью, перпендикулярной, а
второй — плоскостью, параллельной плоскости рис. 148. Паръ проходитъ
черезъ трубку о, находящуюся на рис. 148 сзади г, и окруженную труб-
Рис. 148.
бывающему его конусу, черезъ коті
кою тп, также содержащею паръ,
вслѣдствіе4 чего уменьшена возмож-
ность сгущенія пара въ о. Изъ этой
трубки паръ входитъ въ металли-
ческую камеру (на рис. 150 мѣсто
входа обозначено пунктиромъ) содер-
жащую открытый снизу, полый ко-
нусъ е, снабженный круглымъ отвер-
стіемъ (г' на рис. 149) и плотно при-
легающій боковою стѣнкою къ обхва-
)ЫЙ проходятъ концы трубокъ с и с',
соединяющихъ парораспредѣлитель съ калориметрами. Поворачивая вну-
тренній конусъ при помощи рукоятки (рис. 148), можно его внутреннюю
полость соединить съ однимъ изъ калориметровъ или прекратить доступъ
пара къ послѣднимъ. Вода, образовавшаяся до вступленія пара въ кало-
риметръ, стекала въ сосудъ С, соединенный трубкою т' съ остальными
частями системы. Широкая трубка Г, черезъ которую непрерывно проте-
кала холодная вода, служила для охлажденія трубки т', въ которую
538
Испареніе и ожиженіе.
могли попадать пары изъ С въ началѣ опыта, когда парораспредѣлитель
еще не былъ соединенъ съ однимъ изъ калориметровъ. Температура па-
ровъ въ котлѣ V опредѣлялась нѣсколькими термометрами, помѣщенными
въ желѣзныхъ трубкахъ, вдѣланныхъ въ крышку котла V.
Е е п а и 11 опредѣлялъ изъ своихъ опытовъ ноли у ю т е п л о т у
испаренія 2 (стр. 533), т.-е. сумму
і
2 = ^ + е = + о...................... (12)
о
38 опредѣленій величины 2 для і = 100° дали въ среднемъ
2100 — 636.67 ......................(13)
причемъ крайнія числа были 635,6 и 638,4.
Замѣняя нагнетательный насосъ, сгущавшій воздухъ въ резервуарѣ
7? (рис. 148), насосомъ выкачивающимъ, Ее^паиіі могъ уменьшать
давленіе до 171 мм. Вообще въ его опытахъ р мѣнялось отъ 170,91 мм.
до 10354,84 мм., а температура кипѣнія отъ 63°,02 до 194°,4.
Нѣкоторыя изъ чиселъ, найденныхъ Ее^папИ для воды помѣщены
въ слѣдующей табличкѣ:
Давленіе Температура Полная теплота испаренія Скрытая теплота испаренія
Р /° 2 р = 2 — д = 2 — і
170,91 мм. 63,02 625,5 562,5
369,80 81,03 628,8 547,8
760,00 100,00 636,7 536,7
2285,26 134,4 649,0 514,6
3883,14 153,5 650,1 496,6
6127,67 171,6 655,5 483,9
10354,84 194,4 665,4 471,1
Числа послѣдняго столбца вычислены при допущеніи, что для воды
С = 1 и слѣд. д = і. В е §п а иіі далъ для величины 2 эмпирическую
формулу
2 =606,5-[-0,305/.....................(14)
Она даетъ при /=0° и /=100° числа 20 = 606,5 и 2юо = 637,0.
Она указываетъ на неправильность закона АѴаіі’а (стр. 535), полагав-
шаго, что для воды 2 = Соііні.. т.-е. не зависитъ отъ і. Принимая С — 1
и слѣд. д = I, получаемъ для скрытой т е и лоты испаренія в о д ы
о = 2 - /, т.-е.
о = 606,5 — 0,695/..........................................(15)
При / = 0° и /=100° имѣемъ о0 — 606.5 и
р1ш= 537,0..............................................(16)
Ее паи 11 принимаетъ для д болѣе точное выраженіе
д = I 0,00002/2 4- 0,0000003/3,
которое1 даетъ
о = 606.5 0,695/-- 0.00002/2 —0,0000003/3 . . . (16,а)
Скрытая теплота испаренія.
539
Послѣдняя формула даетъ рюо== 536,50, рі5о= 500,788 и р2оо = 464,300.
Чѣмъ выше температура воды, тѣмъ меньше скрытая теплота испаренія.
Чтобы отдѣлить другъ отъ друга внутреннюю скрытую теплоту р/ отъ
внѣшней де, необходимо знать удѣльный объемъ о насыщеннаго пара, ибо
можно положить де = Арб. см. (81 стр. 533. Мы увидимъ въ слѣдующемъ
параграфѣ, какъ можно вычислить а въ слѣдующей главѣ познако-
мимся съ методами экспериментальнаго опредѣленія этой величины.
Для воды, по Хенпег’у,
р^ = 31,10+ 0,096/ — 0,00002/2 + О,0ООО003/3 . . . (17)
С1ап8ІИ8 принимаетъ болѣе простыя формулы
о = 607- 0,708/ ]
р^ = 31,6+0,083/ С
Послѣдняя формула подтверждаетъ то, что выше было сказано о пер-
воначальномъ возрастаніи р^ съ температурою.
Для внутренней или истинной теплоты испаренія по-
лучается *
рг-= 575,4 —0,791/...................О9)
2е ип ег даетъ таблицы цѣлаго ряда величинъ, относящихся къ испа-
. ренію ; изъ этихъ таблицъ заимствуемъ нижеслѣдующія числа для воды:
/ 7 = / + $ >73 р мм. (ір (11 Л р 0/
- 20° 253° 0,927 0,0769 600,10 620,39 29,57 590,82
—10 263 2.093 0,1611 603,45 613,45 30,30 583,15
0 273 1,600 0,329 606,50 606,50 31,07 575,43
25 298 25,55 1,402 614,12 589,11 33,20 555,91
50 323 91,98 4,580 621,75 571,66 35,54 536,12
75 348 288,5 12,10 629,37 554,14 37,96 516,18
100 373 760,0 27,19 637,00 536,50 40,20 496,30
125 398 1743,9 53,79 644,62 518,73 12,25 476.48
150 423 3581,2 96,17 652,25 500,79 44,09- 456,70
175 148 6717,4 158,32 659,87 482,65 45,71 436,94
200 473 11689,0 243,44 667,50 464,30 47,13 417,17
Особый интересъ представляютъ два послѣдніе столбца, изъ кото-
рыхъ видно, сколько при испареніи тратится теплоты на внѣшнюю ра-
боту (р^), и сколько на внутреннюю. Величина $е растетъ съ темпера-
турою, между тѣмъ какъ р/ убываетъ, когда / растетъ. При нѣкоторой
температурѣ получается рг-=0; если допустить, что формула (19) вполнѣ
точна, то получается р/= 0 при /=-727°,5.
Формула (14), данная Ке^паиіі для л, подвергалась неоднократно
серьезной критикѣ. Такъ Неглѵіц’ показалъ, что для /<^50° эта фор-
мула несомнѣнно приводитъ къ слишкомъ малымъ числамъ. ХѴіпкеІ-
тапп высказалъ мнѣніе, что числа, найденныя Ве^паиИ изъ опы-
540
Испареніе и ожиженіе.
товъ, приводятъ къ болѣе сложной формулѣ вида Л = А + Ві ~\-Сі2 + Оі3;
АѴиеПпег пользуется трехчленною формулою и получаетъ выраженія:
Л = 589 + 0,6003/ — 0.001246/2 I
р —589 —0,3997/ —0,001246/2 | ..........'
При і = 0° имѣемъ Ло = р0 = 589, между тѣмъ какъ формула
Ке&паиіі даетъ 606,5. Разница довольно значительная. Оіеіегісі опре-
дѣлялъ непосредственно р0, пользуясь ледянымъ калориметромъ В и п 8 е п’а
(стр. 168) и заставляя воду во внутреннемъ сосудѣ медленно испаряться
при давленіи въ 3 мм. Какъ среднее изъ четырехъ рядовъ наблюденій
Оіеіегісі находитъ
р0—- 596,73 мал. кал.
На основаніи позднѣйшихъ изслѣдованій Оіеіегісі (1905) надъ
калориметромъ Випзеп’а и надъ величиною механическаго эквивалента
теплоты, А. АѴ. 8шііЬ (1907) нашелъ, что
Ро = 2497,9 джулей.
6ѵеп(І88оіі получилъ тѣмъ же способомъ р0 = 599,92 мал. кал.
Ке^папіі получилъ при /=100° изъ опытовъ р100 = 536,7 и,
какъ было сказано (стр. 535), почти то же самое число нашелъ Вег-
іііеіоі. Лугининъ, приборъ котораго будетъ описанъ ниже, также
нашелъ для 2 при точкѣ кипѣнія число, весьма мало отличающееся отъ
числа Ее^папіі (537). Негкег (1896) получилъ р100 = 540,4, но онъ
самъ полагаетъ, что число Е е § п а и 1 і заслуживаетъ большаго довѣрія.
6гГІіПі1і8 (1895) нашелъ р = 572,60 при 10°,15 и р — 578,70 при
30°,00. Сопоставляя свои числа съ результатами наблюденій Ве^паиіі
и Оіеіегісі, онъ приходитъ къ формулѣ
р = 596,63 — 0.6010/................(21)
НіагкхѵеаіЬег (1899) выводитъ изъ опытовъ Ее§паи11 двѣ
формулы :
выше 100° Л= 603,2+ 0,356/ —0,00021/2;
ниже 100° А = 598,9 + 0,4 12/ —0,00064/2.
При этомъ за единицу принята 15°-ная калорія. Апірн считаетъ за наи-
болѣе достовѣрныя слѣдующія числа:
Наблюдатель Температура О
ІЭіеѣегісі 0° 602,7
СгГІНШій 30° 579,25
« 40,15° 573,15
Ке^паиіі 99,88° 536,67.
Скрытая теплота испаренія другихъ ж и д к о с т е й была опредѣ-
ляема многими учеными.
Еер;пап1і пользовался при этихъ опредѣленіяхъ различными ме-
тодами. Чтобы найти р при температурѣ кипѣнія подъ нормаль-
Скрытая теплота испаренія.
541
нымъ барометрическимъ давленіемъ, онъ употреблялъ сравнительно про-
стой приборъ, описаніе котораго чы опускаемъ. АѴ і г 12 прикрѣпилъ
сосудикъ съ испытуемой жидкостью къ проволокѣ, опущенной въ ка-
меру парового калориметра ^стр. 187), и сравнивалъ количества осѣвшей
воды, когда сосудикъ содержалъ эту жидкость и когда онъ былъ пустой.
Полученная разность опредѣляла количество скрытой теплоты водяного
пара, израсходованное на испареніе жидкости. 8 с к і і I опредѣлилъ д для
многихъ органическихъ жидкостей. Сйарриія и М а 1 Ь і а 8 измѣ-
ряли о для ожиженныхъ газовъ; къ ихъ работамъ мы возвратимся въ
дченіи объ ожиженіи газовъ.
Любопытный способъ сравненія о для различныхъ жидкостей при
ихъ температурахъ кипѣнія предложилъ К а т 8 а у ; онъ пропускаетъ
одинъ и тотъ же электрическій токъ черезъ платиновыя проволоки, помѣ-
щенныя въ различныхъ жидкостяхъ, доводимыхъ нагрѣтою проволокою
до кипѣнія. Потеря вѣса сосудовъ опредѣляетъ количество испарившейся
жидкости, а поглощенная теплота легко вычисляется, когда извѣстны
сила тока и сопротивленія проволокъ. Чтобы перейти отъ относитель-
ныхъ чиселъ къ абсолютнымъ, Е а ш 8 ау и М і 8 8 М а г 8 й а 11 пользо-
вались значеніемъ о для бенз о л а, опредѣленнымъ по ихъ просьбѣ С г іі-
іііЬз’омъ. который нашелъ, что между 20° и 50° можно положить д ==
—107,05 — 0,158/" (въ калоріяхъ, отнесенныхъ къ 15°). Для точки кипѣ-
нія (80°,2) получается д = 94,37.
Ледянымъ калориметромъ В и п 8 е п’а пользовался 8ѵепсІ88оп для
опредѣленія значенія д для различныхъ жидкостей при 0°.
Возвращаемся къ изслѣдованіямъ Ее^паиіі для опредѣленія зави-
симости скрытой теплоты испаренія о отъ температуры у различныхъ
жидкостей. Онъ пользовался приборомъ, подобнымъ изображенному на
рис. 148, въ тѣхъ случаяхъ, когда температура кипѣнія была высокая или
когда опредѣлялось о для давленій выше барометрическаго. Для низкихъ
давленій, а также для жидкостей, кипящихъ при сравнительно низкой
температурѣ. Е е п а и 11 пользовался вторымъ изъ двухъ методовъ, ука-
занныхъ на стр. 534. Его приборъ изображенъ на рис. 151 и 152. На
первомъ изъ нихъ представленъ калориметръ, внутри котораго помѣщенъ
сосудъ А, содержащій испаряющуюся жидкость. Трубка тп, которая во
время опыта закрывается пробкою, служитъ для вливанія жидкое ги. Плос-
кіе сосуды В, С и О содержатъ спиральныя трубки, соединенныя между
собою и съ сосудомъ А при помощи короткихъ трубокъ Ь и с; труба
(1е соединена съ остальными частями прибора; Т термометръ, РШЬ мѣ-
шалка. Трубка сіе соединена съ пріемникомъ (рис. 152), помѣщеннымъ
въ охлаждающую смѣсь и соединеннымъ трубкою кі съ большимъ резер-
вуаромъ, въ которомъ воздухъ при помощи насоса можетъ быть разрѣ-
женъ до желаемой степени. Трубка г’ц соединена съ манометромъ.
Пусть с теплоемкость калориметра. іх и его начальная и оконча-
тельная температуры; тогда — ^) + А* есть количество теплоты, от-
данное калориметромъ, причемъ А* теплота, потерянная лучеиспусканіемъ.
542
Испареніе и ожиженіе.
Пусть дцдѣе Р начальный вѣсъ жидкости. Р вѣсъ жидкости, оставшейся
послѣ опыта въ калориметрѣ, и і ея температура кипѣнія, до которой
жидкость прежде всего охлаждается. Вся теплота, израсходованная
во время опыта, равна слѣдовательно с(іг — і2) + Р С(Р — Р) (і± I),
гдѣ С средняя теплоемкость жидкости между Р и ^°. На счетъ этой те-
плоты испарилось во-первыхъ количество жидкости Р — Р. на что потре-
Рис. 152.
бовалась теплота (Р—Р)д; во-вторыхъ оставшаяся жидкость къ концу
опыта вновь нагрѣлась до іР, что требуетъ количество теплоты Р'С'(і2 — і),
гдѣ С' средняя теплоемкость жидкости между Р и 4°: въ-третьихъ пары,
образовавшіеся при /°, проходя по трубкамъ внутри калориметра, нагрѣ-
вались до температуры послѣдняго, которую можно принять равною 2 (А+
причемъ они поглотили количество
гдѣ у теплоемкость паровъ.
теплоты у(Р — Р) — і
\
Такимъ образомъ получается уравненіе
р,)А-Р'с\і2-і)+7(р-р'^^ -/I (22)
служащее для опредѣленія р; если вся жидкость испарилась (Р = 0). то
для 2 = р 4" Сі получается
>="' -1,) + К+СІІ .... (23)
Вычтя Сі, гдѣ С средняя теплоемкость жидкости между 0° и і°,
Ве§паи1і получаетъ для скрытой теплоты испаренія (_>:
Сѣроуглеродъ . . . 90,0 —0,08922/—0,0004938/2.
Эфиръ.................о = 94,0 — 0,07901/ 0,0008514/2.
Хлороформъ. . . . 67,0 0,09485/—0,0000507/2.
Бензолъ...............р ='Ю9,0 0,13550/ — 0,0008515/2.
Скрытая теплота испаренія.
543
2еипег вычислилъ внѣшнюю скрытую теплоту и внутреннюю
р/, пользуясь формулами, которыя будутъ указаны въ слѣдующей главѣ.
Выписываемъ изъ его таблицъ немногія числа, относящіяся къ С32 :
Сѣроуглеродъ.
і Р 9 Ре Рі 1 р 0 Ре Рі
0° 127,9 90.0 7,21 82,8 100° 3325 76,1 8,81 67,3
50° 857,1 84,3 8,24 76,1 150° 9096 65.5 8,89 56,6
М. В. Лугининъ пользовался при опредѣленіяхъ Л для различ-
ныхъ жидкостей приборомъ, изображеннымъ на рис. 153. Пары жидкости
вступаютъ черезъ трубку ВВ въ камеру АА, въ которую выходятъ отвер-
стія трубокъ р и сс\ трубка сс. ведущая къ прибору въ которомъ пары
сгущаются, легко закрывается и открывается, если спустить или поднять
крышку (1; для этого служатъ винтъ и рукоятки дд. Въ началѣ опыта
трубка сс закрыта; р открыто и пары проходятъ черезъ р въ пріемникъ,
гдѣ они и сгущаются. Когда всѣ части прибора приняли постоянную
температуру, закрываютъ р и открываютъ сс. Пары проходятъ въ приз-
матическую трубу 2?, поперечное сѣченіе которой представляетъ шести-
конечную звѣзду; несгустившіеся пары проходятъ черезъ змѣевикъ
соединяющій верхній конецъ трубы Д съ полымъ шаромъ /, не имѣю-
щимъ непосредственнаго внутренняго соединенія съ трубою О. Нако-
нецъ трубка КК соединяетъ шаръ і съ наружнымъ воздухомъ; пп мѣ-
шалка. Въ калориметръ опущенъ термометръ, не изображенный на рис. 153.
Общее расположеніе всѣхъ частей прибора показано на рис. 154. Здѣсь
видны трубки Л, В и р. рукоятки дд и термометръ і. Мѣшалка приво-
дится въ движеніе при помощи небольшого электромагнитнаго двигателя.
Калориметръ установленъ на эбонитовыхгь ножкахъ внутри мѣднаго со-
суда, внутренняя поверхность котораго посеребрена; этотъ сосудъ съ
своей стороны установленъ внутри полости предохранительнаго сосуда
(система Вегіііеіоі), наполненнаго водою. Испытуемая жидкость ки-
питъ въ сосудѣ а; деревянная перегородка Т защищаетъ приборъ отъ
нагрѣванія со стороны сосуда а.
Опредѣленіемъ скрытой теплоты испаренія различныхъ жидкостей
занимались еще А п сі г е 8, Вегіііеіоі, ЛаВп. ЬіеЬеіапг, № е е -
8 е п и др.
Скрытую теплоту испаренія ожиженныхъ газовъ опредѣляли Еаѵге
и ЯіІЬегтапп (1853), Ве^паиН (1871), Гаѵге (1874), МаіЬіаз
и Саіііеіеі (1886), СЬарриіз (1888), Маійіае (1890), Вейп
(1900). А11 (1904, 1906), Езігеісйег (1904), Зйеагег (1905), Ееп-
пег и Вісйтеуег (1905) и Ветсаг (1905). Ве^паиН опредѣ-
лилъ съ большою тщательностью величину о для ССС, С2НЬСЦ
СН^СІ. ЗО2, ЗН2 и метиловаго эфира. Результаты, полученные для СО2
онъ опубликовалъ, начиная съ 1870 года, въ своихъ Ехрегіепсез»;
послѣ этого его аппараты и результаты наблюденій были при осадѣ Па-
рижа уничтожены; возстановить по сохранившимся замѣткамъ удалось
544
Испареніе и ожиженіе.
лишь результаты, полученные для А/773 и С2Н±СІ. результаты-же. относя-
щіеся къ 5О2, 5Л72, СН^СІ и метиловому эфиру, погибли. Для СО2 при
Рис. 153.
0° Ве^паиіі нашелъ о = 55,64, для С7/3 при 7,8° о = 294,21 и для
С2НЬСІ при 20,08° о = 87,73.
Г а ѵге нашелъ для СО.. (— 78°) д = 142,2, для Ы2О (— 89°) р=101,0
и для 8О2 (—10°) р=88,2.
Скрытая теплота испаренія.
545
Чрезвычайно остроумнымъ способомъ пользовался Майіаз: онъ
помѣщалъ сосудъ, содержавшій ожижжаемый газъ, въ калориметръ, въ ко-
торомъ вода поддерживалась при постоянной температурѣ подливаніемъ
капель сѣрной кислоты, вь то время, какъ жидкость испарялась. ІІредва-
Рис. 154.
рительное тщательное изученіе выдѣленія теплоты при смѣшеніи воды и
сѣрной кислоты позволило вычислить р. Маій іа 8 нашелъ для СО2(0°)
р = 56,47, для М2О (10°) р = 52,3 и для 50. (4°) р = 91,87. Для СО/онъ
довелъ измѣренія почти до критической температуры. Въ § 5 мы еще
возвратимся къ этой работѣ.
КУРСЪ ФИЗИКИ О. X В О Л Ь С О Н А. т. III, изд. 3-е.
35
546
Испареніе и ожиженіе.
СЬарриіз нашелъ слѣдующія числа, относящіяся къ испаренію
при 0°:
СО2 8О2 СН3СІ С2Ы2
р= 56,25 91,7 96,9 103,0.
ВеЬп находитъ для жидкаго воздуха р = 50,8.
А И опредѣлилъ р для жидкихъ О2 и ТѴ2 при различныхъ темпера-
турахъ. Укажемъ крайнія числа:
для жидкаго кислорода
— 183,0° — 201,5°
о = 52,09 59,10
для жидкаго азота
— 196,5° — 210,0°
р = 48,78 52,06.
Въ позднѣйшемъ большомъ изслѣдованіи АИ (1905) еще разъ опре-
дѣлилъ р для кислорода между- 182,98° и— 205° и для азота между
195,55° и — 210°. Между указанными температурами величины р из-
мѣнялись отъ 50,92 до 55,52 для кислорода и отъ 47,65 до 51,61 для азота.
Зависимости р отъ температуры оказались линейными слѣдующаго вида:
для кислорода р = 60,67 — 0,2080Г
для азота р = 68,85 — 0,2736Г.
Здѣсь Г = 273,04 — абсолютная температура. При темпера-
турѣ нормальнаго (при 760 мм. давленія) кипѣнія получилось:
для кислорода (при 182,93°) р = 50,92 ;
для азота (при — 195,55°) р = 47,65.
бііеагег уже ранѣе (1902) опредѣлилъ р для воздуха вышеопи-
саннымъ электрическимъ методомъ. Для воздуха, содержавшаго 21,8%
кислорода, онъ получилъ р = 44,2; при 56% и 72% кислорода получи-
лось соотвѣтственно р = 50,57 и р — 51,7. Позже (1903) для чистаго
кислорода онъ получилъ р = 61, для чистаго азота р = 49,73, для воз-
духа, содержавшаго 48% кислорода, р = 50,6, для воздуха, содержав-
шаго 90% кислорода, р = 59,0.
Геппег и КісЬітуег повторили опредѣленія при помощи ащ
парата 8 Ь е а г е г'а и для воздуха, содержащаго 20—95% кислорода,
получили для р почти постоянную величину, въ среднемъ равную р —51.
При 97,6% содержанія кислорода они получили р = 54,1.
Евігеісііег (1904) для кислорода нашелъ р = 57,8 и для
ЗО2 р = 95,9. Наконецъ, Велѵаг (1905) опредѣлилъ р для О2, ТѴ2 и//2,
погружая въ жидкость кусокъ свинца и ’ измѣряя испарявшееся количе-
ство жидкости. Онъ получилъ слѣдующія числа:
О2 Л/2 Н2
р = 51,15 50,4 123,1.
Скрытая теплота испаренія.
547
Курбатовъ (1902) находитъ для ртути при 358°
$ = 67,8.
Многіе ученые старались найти связь между скрытою те-
плотою испаренія и другими физическими величи-
нами, относящимися къ данному веществу.
Рісіеі (1876) и Тгоиіоп (1884) нашли замѣчательное соотно-
шеніе, которое извѣстно подъ названіемъ правила Тгопѣоп’а: мо-
лекулярная скрытая те п лота кипѣнія различныхъ ве-
ществъ при данномъ давленіи р пропорціональна аб-
солютной температурѣ кипѣнія. Если т молекулярный вѣсъ
и Т абсолютная температура кипѣнія, то по правилу Тгоиіоп’а
7=4.........................(24)
гдѣ к число, приблизительно одинаковое для различныхъ веществъ. При
р — 1 атм. это число колеблется около 21. Опредѣленія ЛѴ і г і г’а,
ЗсЬііГа, Сйаррпіб и Курбатова дѣйствительно подтверждаютъ
это правило; въ особенности, опредѣленія 8 с 11 і И’а даютъ для цѣлаго
ряда веществъ числа к, колеблющіяся между 19,8 и 21,0. Однако суще-
ствуетъ и цѣлый рядъ исключеній. Такъ для воды к = 25,8, для этило-
ваго алкоголя к = 24,0, для метиловаго 25,4. Для брома к = 22, для
сѣры 19,6, для ртути 20; при 0° получается для 5О2 к = 22,3, для ці-
ана 22,0 и для СО2 только 12,6; при температурѣ кипѣнія (—78°,2) СО2
дало бы вѣроятно к около 24. При различныхъ температурахъ получа-
ются для одного и того же вещества различныя значенія для к.
Лугининъ нашелъ, что для спиртовъ жирнаго ряда к довольно
постоянное число, равное приблизительно 26; для эфировъ жирнаго
ряда и для ароматическихъ углеводородовъ к близко къ 20—21; для
жирныхъ же кислотъ оно падаетъ до 13. Тѣмъ же вопросомъ] зани-
мались Ра&ііапі, О8ѣдѵа 1 сі, ЬіпеЪаг^ег, АиЬеІ, Вголѵп
и др. Курбатовъ (1902 —1903) много занимался вопросомъ о правилѣ
Тгоиѣоп’а; онъ составилъ списокъ 74-хъ веществъ, для которыхъ к
близко къ 21. Далѣе онъ показалъ, что отступленія могутъ быть объяс-
нены диссоціаціей или полимеризаціей частицъ пара. Для р т ути онъ
нашелъ к = 21,5, для анилина к = 22,3. Теоретическое значеніе пра-
вила Тгоиіоп’а мы разсмотримъ въ слѣдующемъ параграфѣ и въ главѣ
тринадцатой.
ЪіпеЬаг^ег находитъ, что если мѣнять давленіе р, то для раз-
личныхъ веществъ получается
гдѣ к' постоянная, близкая къ числу 40.
Курбатовъ (1902) показалъ, что формула ЬіпеЪаг^ег’а тео-
35*
548
Испареніе и ожиженіе.
ретически неправильна и на дѣлѣ не подтверждается. Другія формулы
дали Вогсгапсі, Ріпдіау и Краевичъ.
Замѣтимъ, что по ОЬасІГу р пропорціонально діэлектрической по-
стоянной вещества (см. т. IV и т. II), что однако по вычисленіямъ Ап-
ЬеГя далеко не точно.
№егп8І (1906) замѣнилъ формулу Тгоиіоп’а двумя слѣдующими:
=9,51^7' 0,007 Г;
ГПП о 1 ’Т'
? = 8,51^ Т.
Обѣ эти формулы даютъ хорошіе результаты. Віп^йат (1906) на-
ходитъ, что болѣе простая формула
= 17-1-0,011 Т
лучше согласуется съ опытными данными.
Приведемъ еще рядъ формулъ, дающихъ связь между теплотой ис-
паренія р и иными физическими величинами.
Бе Нееп (1883) далъ формулу
С — с = І.ЗЗЗар,
гдѣ С теплоемкость жидкости, с теплоемкость газа, а коеффиціентъ расши-
ренія жидкости.
Надеждинъ (1884) далъ формулу
р
= С0П8І.
ср
Въ ней с — теплоемкость жидкости, р — давленіе, подъ которымъ
происходитъ испареніе.
Тптіігг (1892) нашелъ зависимость
ѣ
Ѳ = 184,36 . (1 аі\
ср
гдѣ к = , сі — плотность газа, а — коеффиціентъ расширенія газа.
сѵ
МІ1І8 (1902—1906), исходя изъ предположенія, что взаимодѣйствія
молекулъ подчиняются закону М е лѵ 1 о п’а и не зависятъ отъ темпера-
туры, пришелъ къ формулѣ
з з
е/= — /а?),
гдѣ С — постоянная, О — плотность жидкости, сі — плотность газа.
Въ длинномъ рядѣ работъ онъ повѣрилъ приложимость этихъ формулъ
для различныхъ жидкостей.
Въ слѣдующей главѣ мы увидимъ, что упругость насыщеннаго пара
зависитъ отъ формы поверхности жидкости. Нопііеѵі^пе находитъ,
Скрытая теплота испаренія.
549
что и скрытая теплота испаренія зависитъ отъ формы поверх-
ности; онъ даетъ слѣдующую формулу для случая выпуклой поверх-
ности (напр. ртути въ капиллярной трубкѣ):
2а
е' ~ ~ Егд ’
гдѣ о' скрытая теплота испаренія на выпуклой, о на плоской поверхно-
сти, а капиллярная постоянная, <5 плотность жидкости, Е механическій эк-
вивалентъ теплоты, г радіусъ поверхности жидкости.
Въ т. I мы привели формулу 81 е Іа и’а
р = (6 — р) ѵ......................(24, а)
гдѣ к нормальное давленіе жидкости при плоской поверхности, р — да-
вленіе насыщеннаго пара и ѵ — .удѣльный объемъ жидкости.
Весьма интересныя новыя соотношенія нашелъ Таштапп (1909).
Мы приведемъ лишь нѣкоторыя изъ данныхъ имъ формулъ. Положимъ,
о1 есть капиллярная постоянная жидкости, выраженная въ
квадр. мм. и а — поверхностное натяженіе въ динахъ на см.
Для не-ассоціированныхъ жидкостей
е- = 17.9........................(24,0
а2
Для ассоціированныхъ жидкостей лѣвая часть меньше, чѣмъ
въ (24,6). Комбинируя (24,6) съ формулой Тгоиіоп’а, можно получить
формулу (4,а) стр. 528. Формула (24,6) дѣйствительна при температу-
рахъ отъ 34° для эфира (С2//5)О до 235° для анэтола С6/74. С3//б(ОСА/3).
Для болѣе широкихъ температурныхъ границъ имѣетъ силу формула
годная отъ — 196° (азотъ) до 235° (анэтолъ). Такъ какъ
9,81 . аЫ
гдѣ й плотность жидкости, то изъ (24,6) получается:
= 3,64 .....................(25)
ѵа
гдѣ т — молекулярный вѣсъ, ѵ — молекулярный объемъ.
На охлажденіи испаряющихся жидкостей и окружающихъ ихъ тѣлъ
основано устройство машинъ для добыванія льда, каковы машины С а г г ё,
Наггівон’а и др. Мы ихъ описывать не будемъ; замѣтимъ только, что
въ нѣкоторыхъ изъ нихъ ледъ образуется изъ самой испаряющейся воды,
въ другихъ-же охлажденіе вызывается испареніемъ эфира, жидкаго аммі-
ака и т. д.
550
Испареніе и ожиженіе.
§ 5, Приложеніе началъ термодинамики къ явленіямъ испаренія
жидкостей. Въ предыдущей главѣ мы вывели три формулы (14), (15)
и (16) стр. 500, относящіяся вообще къ переходу вещества изъ одного
состоянія (твердаго или жидкаго) въ другое (жидкое или газообразное),
или обратно, и мы примѣнили эти формулы къ явленію плавленія и за-
твердѣванія. Тѣ же формулы, а именно
& +С-, = Л(»-.5)|..........(25.»)
+ С-С = |..................(25, Ь)
Ѳ = ЛТ(о-8)^ .......... (25,с)
должны прилагаться и къ явленіямъ испаренія жидкостей и ожиженія
паровъ. Разсмотримъ значеніе и характеръ величинъ, входящихъ въ эти
формулы для этого случая.
Имѣется вѣсовая единица вещества, состоящаго изъ количества 1 — р
жидкости и изъ количества насыщеннаго пара надъ нею ; і и Т=
= /-(-273 температуры, р давленіе или упругость пара; А термическій
эквивалентъ работы. За независимыя перемѣнныя, опредѣляющія состо-
яніе «смѣси» жидкости и пара, принимаемъ і и /г. Давленіе р - /(/),
т.-е. оно зависитъ только отъ температуры; производная этой функціи
входитъ въ формулы (25). Въ нихъ о скрытая теплота испаренія, зави-
сящая отъ /, и мы пишемъ р = др(/); О состоитъ изъ двухъ частей (стр. 532)
е = 9р(0 = е^+ ѳі ’•.............................................(26>
5 и б удѣльные объемы жидкости и насыщеннаго пара; величина 5 всегда
весьма мала сравнительно съ о, такъ что ею можно пренебречь въ фор-
мулахъ (25, а, д, с). Величина о есть убывающая функція
температуры /, ибо чѣмъ больше /, тѣмъ плотнѣе насыщенный паръ
и слѣд. тѣмъ меньше объемъ, занимаемый вѣсовой единицей пара.
Для наглядности приводимъ значенія б для водяного пара, выражая
въ куб. метрахъ объемъ, занимаемый 1 килограммомъ пара.
1 б і б і б
— 20° 994,8 60° 12,05 125° 0,7556
0° 210,7 75° 4,103 150° 0.3839
25° 43,97 100° 1,650 200° 0,1257.
Удѣльный объемъ 5 воды весьма мало отличается отъ 0,001, откуда
и видно, что этою величиной можно пренебречь, сравнительно съ б.
С и с суть теплоемкости жидкости и пара при постоянномъ^,
и ихъ слѣдовало бы обозначить черезъ Ср и с^. Формулы (17,а) и (17,Л>)
стр. 501 даютъ связь между этими величинами и теплоемкостями Ср
и Ср при постоянномъ давленіи. Условія поглощенія количествъ теплоты
Приложеніе термодинамики.
С и с слѣдующія: температура і смѣси повышается на 1°, но количество
пара остается неизмѣннымъ, а потому паръ, который былъ насыщенъ при
/°, долженъ перейти въ паръ, насыщенный при (і -|- 1)°, причемъ его объемъ
[іб долженъ уменьшиться, а давленіе р должно увеличиться.
Итакъ поглощеніе теплотъ С и с должно сопровождаться увеличеніемъ
внѣшняго давленія и сжиманіемъ пара, т.-е. производствомъ ра-
боты внѣшними силами. Результатомъ этой работы является на вѣсовую
единицу пара нѣкоторое количество д теплоты, выдѣляющейся въ парѣ.
Къ этому д необходимо прибавить еще теплоту с, чтобы въ уменьшен-
номъ объемѣ помѣстилась вся вѣсовая единица пара и притомъ въ состо-
яніи насыщенія. Итакъ, чтобы перевести вѣсовую единицу насыщен-
наго пара при /° въ насыщенный паръ при (/+1)° необходимо
произвести сдавливаніе отъ первоначальнаго объема б до меньшаго б',
причемъ выдѣляется теплота д, и затѣмъ еще прибавить теплоту с, кото-
рая называется теплоемкостью насыщеннаго пара, причемъ
подразумѣваютъ слова «и остающагося насыщеннымъ*. Если
бы мы не произвели сдавливанія, то всякій притокъ тепла перевелъ бы
насыщенный паръ въ ненасыщенный, и мы имѣли бы совершенно другой
случай нагрѣванія при другихъ условіяхъ, напр. при ѵ = Сопеі. или при
р - Соп8І., а не при р = СопвС, каковое условіе мы имѣемъ здѣсь.
Относительно величины с слѣдуетъ отличать три случая. Очевидно
безразлично, будетъ ли сдавливаніе пара, сопровождающееся выдѣленіемъ
теплоты д, происходить одновременно съ притокомъ теплоты с, или послѣ
или до него. Представимъ себѣ, что мы сперва произведемъ сдавливаніе
пара, а затѣмъ уже прибавимъ недостающее количество теплоты с. Здѣсь
возможны три случая.
1. Сдавливаніе насыщеннаго пара отъ объема б до объема б' заста-
вило часть пара сгуститься въ жидкость; количества теплоты д недо-
статочно, чтобы нагрѣть весь паръ на 1°, его температура при объемѣ
о' равна / + г, гдѣ г правильная дробь. Необходимо прибавить теплоту с,
чтобы вѣсовая единица вещества превратилась въ паръ, насыщающій
пространство б' при температурѣ (^-|-1)0. Въ этомъ случаѣ с вели-
чина п о л о ж и т е л ь н а я.
2. Сдавливаніе1 пара можетъ его нагрѣть какъ разъ на 1°; тогда
одного сдавливанія достаточно, чтобы паръ, насыщающій простран-
ство б при температурѣ ^°, перевести въ паръ, насыщающій меньшее
пространство б' при температурѣ (/+1)°. Въ этомъ случаѣ никакого при-
тока теплоты не требуется, т.-е. с = 0.
3. Сдавливаніе пара выдѣлило столь значительное количество те-
плоты д, что температура пара при объемѣ оказалась больше (^+1)°.
Въ этомъ случаѣ паръ не насыщаетъ объема а', онъ «перегрѣтъ». Не-
обходимо отнять нѣкоторое количество теплоты, чтобы охладить его
до т.-е. вновь сдѣлать насыщеннымъ. Въ этомъ случаѣ с ве-
личина отрицательная.
Изъ всего сказаннаго ясно, что теплоемкость насыщеннаго пара
552
Испареніе и ожиженіе.
есть величина весьма интересная: она можетъ быть отрицательной и
мы увидимъ въ слѣдующей главѣ, что такіе случаи дѣйствительно быва-
ютъ, и что напр. для водяного пара с весьма большая отрицательная
величина. Мы видимъ далѣе, что знакъ теплоемкости с находится въ за-
висимости отъ дѣйствія давленія на насыщенный паръ. Формулируемъ
еще разъ эту связь, полагая, что знакъ величины с данъ.
Если теплоемкость насыщеннаго пара с>0, то этотъ
паръ при сдавливаніи отчасти сгущается въ жидкость,
при расширеніи дѣлается ненасыщеннымъ.
Если с = 0, то насыщенный паръ при сдавливаніи и
при расширеніи остается насыщеннымъ.
Если с<0, то насыщенный паръ при сдавливаніи
дѣлается ненасыщеннымъ или перегрѣтымъ: при рас-
ширеніи онъ отчасти сгущается в ъ, ж и д к о с т ь.
Само собою разумѣется, что сдавливаніе и расширеніе должны про-
исходить безъ притока или потери тепла, т.-е. адіабатически.
Величина с есть функція температуры и притомъ, какъ мы уви-
димъ, функція возрастающая. Мы положимъ
г = .......................(27)
Всего мы имѣемъ въ ученіи о насыщенныхъ парахъ дѣло съ че-
тырьмя функціями температуры: р=/(Су @ = о = и с=о(^).
связанными уравненіями (25, а, Ь, с\
С есть теплоемкость жидкости при ^ = Соп8і. т.-е. при непостоян-
номъ давленіи р. Но такъ какъ на практикѣ измѣненія давленія не мо-
гутъ быть очень велики, и теплоемкость жидкихъ тѣлъ весьма мало мѣ-
няется съ давленіемъ, то можно принять, что С есть теплоемкость
жидкости при постоянномъ давленіи, т.-е. обыкновенная
«табличная» теплоемкость.
Познакомившись съ характеромъ величинъ, входящихъ въ формулы
(25, а, с) для случая, когда онѣ относятся къ жидкости и къ насы-
щенному пару, сдѣлаемъ нѣкоторые выводы изъ этихъ формулъ. Для
объема ѵ жидкости и пара имѣемъ, см. (6) стр. 498,
г/ = (1 =5-]-^ (о 5)............(28)
Количество б/ф теплоты, соотвѣтствующее измѣненію I и на (іі
и равно, см. стр. 499,
(10 = \С + ..............(29)
На стр. 499 мы вывели формулу
</(? = СМ-}- Т(1 ................(30)
Мы назвали полною теплотою испаренія величину ^стр. 533)
Приложеніе термодинамики.
553
Отсюда
і
саі-у о............................
о
д/. _ г дд
ді ~ "* ді................................
Вставивъ это въ (25,6}, получаемъ
д/. д
ді Т................................
(34)
132)
(33)
Мы знаемъ, что д есть убывающая функція температуры: допу-
стимъ, что р есть линейная функція вида
о = а — Ы .......... (34)
Тогда (25.6) даетъ
„ , дд д „ , а Ы
С = С+А Т с “ 27.ІГ+/.........05)
Отсюда ясно, что с увеличивается съ возрастающей
температурой, ибо р дѣйствительно мало отличается отъ линейной
функціи, и если.мы имѣемъ формулу вида д-=а Ы-\-^і\ то вліяніе
третьяго члена на результатъ не велико.
Если въ выраженіи (25,с) пренебречь величиною 5 сравнительно съ о,
и разсматривать граммъ-молекулу вещества, т.-е. пг граммовъ, то для м о -
л е к у л я р н о й скрытой теплоты р получается выраженіе
тр = АТтодР = дтѵ
ді ді ’
гдѣ ѵ объемъ граммъ-молекулы пара. Допуская, въ видѣ приближенія,
что насыщенный паръ слѣдуетъ закону Бойля, имѣемъ рѵ — ЦТ,
см. т. I. Тогда получается приближенная формула:
тд = ДАТ* еЛ^Р..........................(36)
Перейдемъ къ разсмотрѣнію внѣшней и внутренней те-
плоты испаренія ре и р/. Для р^ мы имѣли выраженіе
р^ = Лдо ..................(36.67)
Если опять пренебречь величиною 5, взять граммъ - м о лекул у
вещества, и допустить приложимость закона Бойля, то получается
пг$е=#АТ.......... (36.&)
Это равенство показываетъ, что внѣшняя молекулярная
скрытая теплота испаренія есть величина при данной темпе-
ратурѣ приблизительно одинаковая для всѣхъ жидкостей; она пропорціо-
нальна абсолютной температурѣ, при которой происходитъ испареніе.
554
Испареніе и ожиженіе.
Для внутренней скрытой теплоты испаренія р/ имѣ-
ешь р/ о де. Вставляя (25,с) и (36,а), получаемъ
(др \
Т ді Ч ’
ИЛИ , ѵ
Для р/ можно вывести еще одно замѣчательное выраженіе, кото-
рымъ, какъ мы увидимъ въ слѣдующей главѣ, воспользовался Нетія для
опредѣленія вида функціи р = /(/). Оно относится къ случаю негустого
пара, свойства котораго мало отличаются отъ свойствъ идеальныхъ га-
зовъ. Допускаемъ, что запасъ энергіи пара зависитъ только отъ его тем-
пературы, но не зависитъ отъ его объема, т.-е. будетъ ли онъ насыщенъ
или ненасыщенъ. Пусть С теплоемкость жидкости, сѵ теплоемкость пара
при постоянномъ объемѣ. Переведемъ одинъ килограммъ жидкости при
0° въ паръ при температурѣ Г', заставляя жидкость одинъ разъ испа-
ряться при і", другой разъ при температурѣ і' < и нагрѣвая затѣмъ
паръ при постоянномъ объемѣ (безъ внѣшней работы) оіъ і' до і". Вну-
треннія скрытыя теплоты обозначимъ въ этихъ двухъ случаяхъ черезъ
и ое". Объемы пара въ обоихъ случаяхъ неодинаковы, но запасъ энер-
гіи одинъ и готъ же. Отсюда получается равенство пріобрѣтенныхъ ко-
личествъ энергіи:
С7" + о/' = Сі' -|- $і' Н" сѵУ" — О-
Отсюда = д., _~(С— Сѵ)(і" — і‘)............(38,а;
Положимъ і* = О, і" — /, р/' = и о/ = а; тогда имѣемъ
о,- = а — (С сѵ)і....................(39)
Эта формула показываете, что при повышеніи темпера-
туры на 1°, внутренняя скрытая теплота испаренія
уменьшается на величину, равную разности теплоем-
кости жидкости и теплоемкости пара пр и постоянномъ
объемѣ. Эта формула неприложима къ густымъ парамъ, потенціальной
энергіей которыхъ нельзя пренебречь.
Мы видѣли (стр. 547), что Тгоиіоп далъ правило, по которому
-у?, при данномъ давленіи р. величина одинаковая для всѣхъ веществъ
Бе Н е е п, а также В а ш 8 а у и У о и п вывели изъ своихъ измѣреній
другого рода соотношенія, а именно, что если различныя жидкости испа-
ряются при одномъ и томъ же давленіи (напр. если онѣ кипятъ при нор-
мальномъ атмосферномъ давленіи), то для нихъ
Т — Соп8і.........................(39,б/)
Приложеніе термодинамики.
555
Если формулу (36) написать въ видѣ
...........................................................(39 М
Т р ді
то дѣлается яснымъ что правило Тгоиіоп’а и формула (39.а) довольно
тѣсно между собою связаны, и формулы (39,а) и (25,с) даютъ р: (Н 5 ) =
= Соп8І. Если пренебречь объемомъ 5, то получается
о
= СОП8І.........................(39.С)
Вставляя сюда ѵ = ар, и рѵ = мы понятно опять получимъ правило
Тгопіоп’а. Формула (39,с) показываетъ, что для образованія единицы
объема насыщеннаго пара при данномъ давленіи р требуется одинаковое
для всѣхъ веществъ количество скрытой теплоты.
Мы видѣли выше (стр. 502), что
гдѣ 5) и 52 энтропіи вѣсовыхъ единицъ пара и жидкости. Правило
Тгоніоп’а даетъ:
* т(52 - 50 = к.....................(39,О)
Этимъ выражается правило ХѴеіп8Іеіп’а: измѣненіе молеку-
лярной энтропіи при испареніи есть одинаковая для
всѣхъ веществъ величина, если упругость р паровъ
одна и та же; при р — 1 атм. имѣемъ к = 21.
Энергія вѣсовой единицы смѣси жидкости и пара получаете^
если жидкость сперва при возрастающемъ давленіи нагрѣвать отъ началь-
ной температуры 4 до /°, и затѣмъ при постоянномъ р отчасти превра-
тить въ пары. Получается, см. (37),
і 1
+ + —5) . (40)
4 4
гдѣ І7О энергія вѣсовой единицы жидкости при температурѣ 4-
Для энтропіи 5 имѣемъ, на основаніи формулы (31),
аз = = Ст (Іі + сі ................(41,а}
Отсюда і
с , сСЛі №
5 + I -уѵ- + у................(41,6)
4
Здѣсь 50 энтропія вѣсовой единицы жидкости при температурѣ /0
Если считать С за величину постоянную, то получается
5.= 50-НС1^ + ^.......................(41, с)
556
Испареніе и ожиженіе.
Разсмотримъ различныя измѣненія состоянія нашей смѣси и опредѣ-
лимъ количество теплоты и работу г, которая соотвѣтствуетъ этимъ
измѣненіямъ.
1. Измѣненіе изотерми ческое, і = Сопзі. Количество пара
растетъ отъ а до а; давленіе р постоянное. Мы имѣемъ, очевидно,
0 = е(/і2 — Ді) | ..............0^
Г = — Р'іХ6 — 5) I
2. Постоянное количество пара: /і = Соп8і. Жидкость
и паръ нагрѣваются отъ до і2. Изъ предыдущаго (стр. 551) ясно, что
нагрѣваніе должно сопровождаться нѣкоторою работою г внѣшнихъ
силъ. При = Сопві. имѣемъ на основаніи (30 л). или проще, вста-
вляя (29,а; въ (29),
= си + аі
откуда Ч
= С(/2 - — 21) — ...........(43л)
4
гдѣ и о2 значенія величины о при температурахъ и і2. Работа г
внѣшнихъ силъ равна ,
12
г рдѵ.
4
Интегрируя по частямъ, имѣемъ
^2 ^2
г = . рѵ । — уѵдр.
Пусть р1? ѵг и р2, ѵ2 давленія и объемы при температурахъ и і2;
тогда первый членъ равенъ р2ѵ2— АА- Во второй членъ вставляемъ
ѵ = 5 + р{о — $), см. (28) стр. 552 ; тогда
І2 4
Г = р2Ѵ2 — РМ — 8 др М — р ^(о — 8) йі.
ІГ , ч , ч др о Ео г
Но (2эл) даетъ (а — 5) ~ гдѣ Е механическій эквива-
лентъ теплоты ; первый интегралъ равенъ р2 — р^ такъ что окончательно
І2
Г = р2Ѵ.2 - РіѴг — 8{р2 — р^ - ... (43.6)
Приложеніе термодинамики.
557
Такимъ образомъ въ (43,а) и (43,6) встрѣчается одинъ и тотъ-же
интегралъ. Въ частномъ случаѣ, когда @ имѣетъ видъ
$= — аі.....................(43, с)
этотъ интегралъ равенъ
4
/273--П^ = — ^) + ^° + 273а)18’• • (43,6/)
4
3. Адіаб атич е ск о е и змѣи е ні е состоянія смѣси жид-
кости и [пара; = 0. Требуется найти связь между /х и і при
адіабатическихъ измѣненіяхъ, а также работу г произведенную насыщен-
нымъ паромъ. Формула (31) даетъ
С -|— сі I I — 0...................(44,а)
Отсюда, принимая теплоемкость С жидкости постоянною, получаемъ
С\$Т + у = Соп8І....................(44,6)
Этою формулою и выражается связь между количествомъ р пара
и температурою Т при адіабатическихъ измѣненіяхъ состоянія смѣси.
Чтобы вычислить работу, вставимъ ѵ въ тождество рсіѵ — д{рѵ) — ѵЛр;
(28) даетъ, если считать 5 постояннымъ,
рсіѵ — СІ[рр(б -5)] — р(б — 5) (ІІ
Какъ п выше, (25,с) даетъ
рсіѵ = сі[рр\б — 5)] — СІ7.
Прилагая къ послѣднему члену тождество хсіу = <і(ху) —усіх, полу-
чаемъ на основаніи (44,а),
ат = Еа^) — ТЕа </ (^е) — еслі
Итакъ __ — Ецо\ЕСаі,
Отсюда искомая работа г равна
г = — Еп^I — — $0 — — ЕС(Т2 — Ту) (44,с)
Мы найдемъ связь между объемомъ ѵ смѣси и температурой
Т при адіабатическихъ измѣненіяхъ, если мы въ (44,6) вставимъ
изъ (25,с) и затѣмъ р (о — 5) замѣнимъ черезъ ѵ — 8, см. (28). Получается
С\%Т + А(у — 5) = Сопві................(45)
ѵ др _
гдѣ есть функція отъ і или Г
55Ь
Испареніе и ожиженіе.
Выведенныя соотношенія, а также и многія другія, которыя легко
получить, приводятъ къ различнымъ спеціальнымъ формуламъ, если для
одной изъ четырехъ функцій р, р, б и с принять опредѣленный видъ,
напр. если положить р = р0 — аі, или если для р подставить одну
изъ эмпирическихъ форму лъ, съ которыми мы * познакомимся въ слѣду-
ющей главѣ.
Въ основаніи всѣхъ теоретическихъ изслѣдованій должны лежать
формулы (25,бг, Ь, с\ дающія двѣ связи между четырмя функціями р, р,
о и с. Первая содержитъ всѣ четыре функціи, вторая двѣ функціи р и с,
третья три — р, б. Отсюда видно, что формулы (25,6) и (25,с) мо-
гутъ служить для опредѣленія б и с, если р и р извѣстны. Онѣ даютъ:
г = ..................(46)
(47)
Замѣтимъ, что формула.
реугоп’а или Сіаизіие’а
(25,с) иногда называется формулой С1 а -
или, наконецъ, (Яареуг оп-Сіаиеіие’а.
Рис. 155.
Рис. 156.
§ 6. Сгущеніе газовъ. На стр. 523 было упомянуто, что мы мо-
жемъ всѣ тѣла, газообразныя при обыкновенныхъ температурахъ, разсма-
тривать, какъ пары жидкостей, кипящихъ подъ атмосфернымъ давленіемъ
при низкихъ температурахъ. Поэтому должно быть возможнымъ сгустить
всѣ извѣстные намъ газы въ жидкое состояніе. И дѣйствительно, въ на-
стоящее время (1912) удалось всѣ извѣстные газы превратить въ жидкости
и, за исключеніемъ гелія, также и въ твердое состояніе. Непремѣннымъ
Сгущеніе газовъ.
550
условіемъ возможности сгущенія газа въ жидкость является пониженіе
его температуры ниже критической температуры (стр. 523).
Хотя подробности о критической температурѣ будутъ изложены ниже,
мы однако уже. здѣсь будемъ указывать на эту температуру для различ-
ныхъ газовъ.
Ѵап Магит первый сгустилъ газъ, сдавливая ИН. до 6 атмос-
феръ; затѣмъ Моп§е и Сіоиеі сгустили 8О2 въ трубкѣ, охлажденной
смѣсью снѣга и поваренной соли: далѣе Гоигстоу и Ѵаидиеііп,
а впослѣдствіи и О и у ѣ о п сіе Могѵеап превратили НН3 въ жид-
кость при атмосферномъ давленіи, пользуясь смѣсью снѣга съ хлори-
стымъ кальціемъ.
Въ 1823 г. появилась первая классическая работа Рага (іау я о сгу-
щеніи газовъ; вторую онъ опубликовалъ въ 1845 г. Рагасіау пользо-
вался двумя способами для превращенія газовъ въ жидкое состояніе. Пер-
вый способъ основанъ на сгущеніи газа, образующагося въ закрытой
стеклянной трубкѣ, подъ вліяніемъ своего собственнаго давленія. Распо-
ложеніе частей прибора понятно изъ рис. 155. АВ толстостѣнная стек-
лянная трубка, въ которую помѣщаютъ вещество Л, выдѣляющее при
нагрѣваніи испытуемый газъ. Конецъ В окруженъ охлаждающею смѣсью.
Помѣстивъ въ Л сухой гидратъ хлора (С/4~ 10//2О), Рагасіау полу-
чилъ впервые въ В жидкій хлоръ. Такимъ способомъ онъ сгустилъ да-
лѣе 802 (помѣстивъ въ трубку Н28О± + Н28 (изъ Ре8 - НСІ\
С02, Н20, С2Ы2 (изъ Н^С2Ы^), НН% и НСІ. Вскорѣ послѣ появленія первой
работы Катай ау’я Ви8 8у сгустилъ 802 въ большихъ количествахъ; онъ
нашелъ, что точка кипѣнія жидкаго 8О2 равна — 10° при нормальномъ
давленіи; при быстромъ испареніи жидкаго 8О2 онъ получилъ темпера-
туру — 68°-
Второй способъ Катайау’я (1845) заключался въ томъ, что онъ
при помощи двухъ нагнетательныхъ насосовъ сдавливалъ газъ до 40
атмосферъ, помѣщая стеклянный резервуаръ горизонтально въ охлажда-
ющей смѣси, или пользуясь изогнутымъ резервуаромъ СО (рис. 156),
внутри котораго находился маленькій воздушный манометръ О. Нижняя
часть вертикально поставленнаго резервуара окружалась охлаждающей
смѣсью, а именно смѣсью твердой С02 и эфира. Чтобы еще болѣе по-
низить температуру этой смѣси, Катай ау ускорялъ ея испареніе, по-
мѣстивъ весь приборъ подъ колоколъ воздушнаго насоса, какъ показано
на рисункѣ, причемъ температура понижалась до — 110°. Такимъ спо-
собомъ ему удалось сгустить въ жидкость, а отчасти перевести и въ
твердое состояніе С2Н±, РН%, 8іР12, ВРІ%, НЗ, Н20 и т. д. Остались не-
сгущенными 02, И2> Н2, СН4 (метанъ), окись азота (А/0) и окись угле-
рода (СО); эти шесть газовъ назывались поэтому п о с т о я н н ы м и.
Въ настоящее время лже ни одинъ изъ извѣстныхъ газовъ не заслу-
живаетъ этого названія.
Обширныя изслѣдованія надъ сгущеніемъ газовъ произвелъ X а і -
іегет; онъ доходилъ до давленій въ 1000 атм., но не могъ сгустить
560
Испареніе и ожиженіе.
многихъ газовъ такъ какъ онъ не охлаждалъ ихъ ниже критической
температуры.
Въ настоящее время нѣкоторые газы сгущаются заводскимъ спосо-
бомъ и разсылаются для продажи въ толстостѣнныхъ металлическихъ
сосудахъ.
Сгущеніе нѣкоторыхъ изъ газовъ, которые раньше назывались по-
стоянными, удалось п<>чти одновременно Саіііеіеі и Рісѣеі въ де-
кабрѣ 1877 г.; обѣ работы были доложены Парижской Академіи Наукъ въ
одинъ и тотъ же день, 24 декабря 1877 г. На рис. 157 изображенъ насосъ
Рис. 157.
Саіііеіеі, весьма удобный и для демонстрацій сгущенія газовъ. Онъ
представляетъ собою гидравлическій прессъ, дающій возможность достигать
давленій до 1000 атм. НасосъР приводится въ движеніе рычагомъ А; онъ
накачиваетъ воду въ трубку ТО. Вращая колесо И можно перемѣщать
поршень, находящійся въ цилиндрѣ Р, и тѣмъ самымъ медленно мѣ-
нять давленіе. Повернувъ колесо V' можно внезапно уменьшить да-
вленіе до атмосфернаго. Стеклянная трубка РТ содержитъ въ верхней
части испытуемый газъ, а подъ нимъ ртуть, отчасти наполняющую вну-
треннюю полость стального цилиндра В, въ которомъ надъ ртутью нахо-
дится вода, соединенная трубкою 777 съ насосомъ. Трубка Т окружена
водою или охладительною смѣсью и кромѣ того стекляннымъ колоколомъ.
Если дѣйствовать насосомъ, то вода вгоняется въ цилиндръ В, ртуть под-
нимается въ трубку Т и сжимаетъ газъ. Такимъ образомъ легко сгуститъ
СО2 при комнатной температурѣ. При внезапномъ уменьшеніи давленія
часть жидкой С0.2 затвердѣваетъ.
Сгущеніе газовъ.
561
Въ другихъ Приборахъ Саіііеіеі удлинилъ трубку Г, согнувъ ее
сперва горизонтально, а затѣмъ вертикально внизъ: эта вертикальная
часть и помѣщалась въ охлаждающую смѣсь. Далѣе Гаіііеіеі замѣ-
нилъ насосъ цилиндромъ, наполненнымъ водою, въ который при враще-
ніи большого колеса, снабженнаго рукоятками, медленно вдавливался пор-
шень. Величина давленія измѣрялась особенными манометрами.
Въ декабрѣ 1877 г. СаіПеіеі производилъ опыты съ СО и О2 при
— 30° и давленіи вь 300 атм.; газы не сгущались въ жидкость. Но при
Рис. 158.
внезапномъ уменьшеніи давленія въ трубкѣ Т образовывался туманъ и даже
замѣчались струйки жидкости на стѣнкахъ этой грубки. Далѣе С а і 11 е -
ѣ е ѣ замѣчалъ образованіе подобныхъ же тумановъ при опытахъ съ воз-
духомъ, съ А/> и сь Н2. Такимъ образомъ ему несомнѣнно удалось обна-
ружить переходъ этихъ газовъ въ жидкое состояніе, слѣды котораго од-
нако наблюдались лишь втеченіе весьма короткаго промежутка времени.
Въ 1882 г. Саіііеіеі окружилъ трубку, содержащую испытуемый газъ,
жидкимъ этиленомъ (С2//4), дающимъ температуру около — 102°. При
этомъ переходъ О2 въ жидкое состояніе сдѣлался уже весьма хорошо
замѣтнымъ.
Приборомъ СаіПеіеі пользовались 0^іег,ІІ08ѵау, Апвйеі],
НаиіеГеиіНе и С Іі а р р иі 8 и др. Изъ нихъ О § і е г сгустилъ водоро-
дистый кремній при —1° и 100 атм., —5° и 70 атм., и ври —11° и
50 атм. А П8сіе 11 изслѣдовалъ сгущеніе НСІ и ацетилена С>Н2. Нап-
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА Т. ІП, изд. 3-е. 36
562
Испареніе и ожиженіе.
іеГепіІІе и СЬарриіз сгущали смѣсь кислорода и озона при 125 атм.
и — 100°, пользуясь жидкимъ С2Л/2 для охлажденія. При этомъ озонъ
сгустился въ жидкую каплю синяго цвѣта. По 8 ѵ ау сгустилъ С08.
Рісіеі пользовался при своихъ первыхъ работахъ (1877) сложными
приборомъ, части котораго схематически изображены на рис. 158. Вь
сущности способъ Р і с і е і совпадаетъ съ первымъ способомъ Г а г а (і а у’я
Испытуемый газъ добывался въ толстостѣнномъ сосудѣ А, въ которомъ
нагрѣвалась бертолетова соль при опытахъ съ кислородомъ, и муравьино-
каліевая соль съ ѣдкимъ кали, когда производился опытъ сгущенія водо-
рода. Испытуемый газъ сдавливался въ трубкѣ /И самъ собою, вслѣд-
ствіе1 того, что изъ Ь продолжали притекать новыя количества газа. Сжа-
тіе сопровождали сильнымъ охлажденіемъ, которое вызывалось и поддер-
живалось двумя непрерывными круговыми процессами. Трубка М окру-
жена трубою, содержащею жидкій С0.2, непрерывно быстро испаряю-
щійся вслѣдствіе того, что насосъ Е выкачиваетъ газъ изъ М и вгоня-
етъ его въ Е, откуда насосъ дѣйствующій вмѣстѣ съ Е, нагнетаетъ
газъ въ трубку К, въ которой С0.2 дѣлается жидкимъ, и черезъ трубку к
обратно вгоняется въ Н. Для сгущенія С0.2 въ трубкѣ К производится
охлажденіе этой трубки при помощи жидкаго 8О2 въ трубѣ С, окружаю-
щей К Здѣсь повторяется надъ 8О2 та манипуляція, которая въ системѣ
КН производится надъ СО2. Насосъ А вытягиваетъ 8О2 изъ С (вслѣд-
ствіе чего жидкій 8О2 въ С быстро испаряется и охлаждается ) и перего-
няетъ его въ В, откуда насосъ нагнетаетъ его въ сосудъ /), въ кото-
ромъ онъ сгущается въ жидкость подъ вліяніемъ давленія и охлажденія
струею холодной воды, и черезъ трубку сі перегоняется обратно въ С.
Температура жидкаго 8О2 опускается въ С до - -70°; температура въ Н
доходитъ до —130°. Когда Рісіеі замѣнилъ углекислый газъ закисью
азота (Л2О\ температура въ Н понизилась до - 140°.
Открывая кранъ на лѣвомъ концѣ трубки Л4, Рісіеі выпускалъ на-
ружу сгущенный и охлажденный газъ. При этомъ Рісіеі наблюдалъ
струю жидкаго кислорода. Онъ утверждаетъ, что видѣлъ также1 синева-
тую струю жидкаго водорода, быстро исчезавшую, но производившую при
ударѣ объ полъ звукъ, напоминавшій удары металлическихъ предметовъ.
Однако нынѣ можно съ достовѣрностью сказать, что послѣднее наблюде-
ніе не могло имѣть мѣста при условіяхъ опытовъ Рісіеі.
Впослѣдствіи Рісіеі устроилъ въ Берлинѣ «лабораторію низкихъ
температуръ», въ которой сгущеніе газовъ производится въ большихъ раз-
мѣрахъ. Подобную же лабораторію устроилъ Каштегііп^ід-Оппез
въ Лейденѣ. Въ своей лабораторіи Рісіеі пользовался тѣмъ же спосо-
бомъ, который былъ описанъ выше, не) для охлажденія пріемниковъ онь
употребляетъ другіе газы. Первый круговой процессъ совершался не съ
жидкимъ 80^ но съ «жидкостью РісіеЬ, которая по указаніямъ самого
Рісіеі должна состоять изъ смѣси 64 вѣсовыхъ частей 8О2 и 44 ча-
стей СО2 и которую изслѣдовалъ Віиетске. 9та смѣсь сгущается го-
раздо легче, чѣмъ СО2. При 0° она сгущается при давленіи въ 1,76 атм.
Сгущеніе газовъ.
563
(8О2 при 1,51 атм., СО.) при 38.5 атм.). Пары жидкости Рісіеі охлаж-
даются холодною водою, сгущаются при 2 атм. въ жидкость и вгоняются
въ трубу, изъ которой ея пары непрерывно выкачиваются. При этомъ
.она охлаждается до —80°. Второй циклъ совершается закисью азота,
которая сгущается при — 80° и давленіи въ 10—12 атм., и сама
испаряясь, даетъ температуру — 135°. Третій циклъ совершается
жидкимъ воздухомъ, критическая температура котораго однако —140°,
такъ что ожиженіе воздуха этимъ способомъ представляется сомни-
тельныя ь.
К а т т е г 1 і п 11 - О п п е 8 пользовался въ своихгь первыхъ работахъ
тремя циклами: въ иервом ь циклѣ хлористый метилъ охлаждался быстрымъ
испареніемъ до — 70°; во второмъ сгущался этиленъ и охлаждался при испа-
реніи до —140°, при каковой температурѣ кислородъ уже могъ быть сгущенъ въ
жидкость. Позже К а ш ш е г 1 і в И - О п п е 8 въ своей кріогенетической лабо-
раторіи осуществилъ комбинацію пяти круговыхъ процессовъ, относительно
которых ь онъ сообщаете (1908) слѣдующія данныя. Испаряющійся хлоръ-
метилъ щетъ температуры отъ —23° до —90°; этиленъ даете тем-
пературы отъ 103° до — 165°. Третій круговой процессъ производился
съ кислородомъ, который при температурѣ испаренія этилена ожижа-
ется и кипитъ, охлаждаясь отъ —183° до —217°. Четвертый круговой
процессъ совершался съ жидкимъ воздухомъ, котораго добывалось
-болѣе 50 литровъ въ день. Пя-
тый процессъ производился съ
в о д о р’о д о м ъ, давая легко нѣ-
сколько ЛИТрОВЪ ЖИДКОСТИ, ТСМ-
цература которой за нѣсколько
часовъ ('два мѣнялась на 0,01°.
Въ 1883 г. появилась пер-
вая работа Вроб левскаго
(XV г о Ь1 е іѵ 8 к і) и Ольшев-
скаго (01 8 2 е \ѵ 8 к і), кото-
рые затѣмъ продолжали работать
независимо другъ отъ друга (Вро-
блевскій умеръ въ 1886 г.).
Приборъ, которымъ они пользо-
вались при первыхъ своихъ ра-
ботахъ, представляетъ видоиз-
мѣненіе прибора СаіІІеіеЬ,
причемъ охладителемъ служилъ
жидкій этиленъ, испаряющійся
при низкомъ давленіи. Этотъ
приборъ изображенъ на рис. 159.
Вт, немъ Ьсй верхняя часть
насоса СаіНеіеі; стеклянная
трубка д изогнута два раза
Рис. 159.
36*
564
Испареніе и ожиженіе*
подъ прямымъ угломъ; ея конецъ расположенъ внутри стекляннаго коло-
кола 5, помѣщеннаго въ стеклянномъ цилиндрѣ у, который содержитъ
хлористый кальцій, служащій для высушиванія въ немъ воздуха. Въ х
находится резервуаръ і водороднаго термометра; трубка аѵ соединяетъ 5
съ выкачивающимъ насосомъ. Черезъ пробку (1 проходитъ тонкая мѣдная
трубка кус, служащая для вливанія жидкаго этилена, который содер-
жится въ цилиндрѣ л, окруженномъ смѣсью снѣга или льда съ поварен-
ною солью. Если открыть кранъ а то жидкій этиленъ сперва про-
ходитъ по змѣевику окруженному смѣсью твердой СО2 съ эфиромъ, и
затѣмъ въ сосудъ х, въ которомъ онъ испаряется. Если давленіе въ 5 равно
25 мм., то его температура падаетъ до —136°; при давленіи въ 10 мм.
получалась температура —152°. Кислородъ легко сгущался въ жидкость
при температурѣ около — 130° и давленіи въ 20 атм. Онъ представлялъ
легкоподвижную, слабо синеватую жидкость; его критическая темпера-
тура — 118°, его плотность при —130° и 27 атм. около 0.9. Азотъ, воз-
духъ и СО не сгущались въ описанномъ приборѣ.
Тогда Вр об левскій пошелъ еще дальше, воспользовавшись кп-
п я іц и м ъ кислородомъ, какъ охладителемъ. Для этого онъ устроилъ
приборъ такимъ образомъ, что могъ понижать давленіе въ сосудѣ, въ ко-
торомъ былъ полученъ жидкій кислородъ только что описаннымъ спосо-
бомъ. Кислородъ кипитъ подъ атмосфернымъ давленіемъ при — 181°,5;
подъ давленіемъ въ 20 мм. температура понизилась до — 200°,4. 3 атв е р -
дѣванія кислорода не удалось наблюдать. Въ кипящемъ
кислородѣ удалось сгустить азотъ и окись углерода. Критическая темпе-
ратура азота —146°. окиси углерода —141°; азотъ кипитъ подъ давле-
ніемъ въ 740 мм. при— 195°, при 60 мм. точка кипѣнія — 204°. При этой
температурѣ азотъ з а т в е р д ѣ в а е т ъ (Вроблевскій); подъ давле-
ніемъ 40 мм. онъ охлаждается до—206°. Плотность жидкаго азота близъ
критической температуры около 0,4.
По О л ь ш е в с к о му, критическая температура метана (СТУ4) — 81°,8;
его точка кипѣнія —164°; при —185°,8 онъ затвердѣваетъ. Критиче-
ская температура окиси азота —93°,5 ; точка кипѣнія — 153°,6, точка
затвердѣванія —167°. Ольшевскій находитъ, что азотъ затвердѣва-
етъ не при —203°, какъ нашелъ Вробл е в скій, но при—214°. Ис-
паряясь при низкомъ давленіи въ 4 мм., азотъ, охлаждается до
— 225°. Для окиси углерода онъ находитъ точку затвердѣванія — 207°
подъ давленіемъ 100 мм. Кислородъ при —211° не затвердѣваетъ. Для
полученія большихъ количествъ жидкаго кислорода или воздуха, который
долженъ служить охладителемъ для другихъ газовъ, Ольшевскій поль-
зуется приборомъ, изображеннымъ на рис. 160. Кислородъ (или воздухъ)
находится въ резервуарѣ А подъ давленіемъ въ 100 атм.; отсюда онъ вы-
пускается въ желѣзную бутыль а, окруженную жидкимъ этиленомъ, на-
ходящимся въ сифоновидномъ сосудѣ /, окруженномъ смѣсью льда и по-
варенной соли. Этиленъ проходитъ изъ / сперва черезъ змѣевикъ, окру-
женный въ § смѣсью твердой углекислоты и эфира, находящеюся подъ
Сгущеніе газовъ.
565
низкимъ давленіемъ; трубка п ведетъ къ воздушному насосу. Жидкій
этиленъ кипитъ въ т подъ низкимъ давленіемъ, которое получается при
помощи насоса, выкачивающаго пары этилена черезъ трубку пі\ Ь и к
манометры. Жидкій кислородъ или воздухъ выпускается при помощи
крана (1 въ сосудъ е съ тройными стѣнками.
Рис. 160.
Сгущеніе водорода не удалось Вроблевскому, который ста-
рался теоретически опредѣлить критическую температуру этого газа. Для
этого онъ изслѣдовалъ объемъ и давленіе водорода при четырехъ темпе-
ратурахъ: 100°,0°,— 103°,5 (кипящій этиленъ) и—182°,45 (кипящій кис-
лородъ). Эги наблюденія (опубликованныя уже послѣ его смерти) дали
ему возможность опредѣлить критическую температуру водорода, оказав-
шуюся равной — 240°,4. Теоретическія изслѣдованія Ь. Ь1 а I а п 8 о п’а
привели къ критической температурѣ — 234° и точкѣ кипѣнія — 244°.
Почти одновременно (1895) Ольшевскому удалось опредѣлить эти тем-
пературы путемъ опыта. Онъ сгущалъ водородъ до 190 атм. и охлаждалъ
его щ — 211° въ кипящемъ кислородѣ. Уменьшая давленіе, онъ замѣтилъ
5Ьб
Испареніе и ожиженіе.
при 20 атмосферахъ кипѣніе во всей массѣ. Измѣряя температуру при
помощи платиновой проволоки, сопротивленіе которой служило мѣрой тем-
пературы, онъ нашелъ критическую температуру водорода
равною — 234°,5. Тѣмъ же способомъ онъ нашелъ точку кипѣнія водорода
подъ атмосфернымъ давленіемъ равною 243°,5. Оба числа близки къ
числамъ, предсказаннымъ 1» а I а п 8 о п’омъ. Опыты В е аѵ а г’а (1898) дали
нѣсколько болѣе высокія температуры.
Для аргона Ольшевскій (1895) нашелъ критическую темпера-
туру — 121°. Точка кипѣнія аргона - 186°,9; плотность около 1,5. При
давленіи ниже атмосфернаго и температурѣ — 189°,6, аргонъ затвер-
дѣваетъ. Для плотности жидкаго кислорода при точкѣ кипѣнія
(—181°,6) онъ находитъ 1,124, для азота (при 194°,4) 0,885.
МоІ88ап и Веѵѵаг получили (1897) жидкій фторъ, вводя этотъ
газъ въ стеклянный сосудъ, охлажденный жидкимъ кислородомъ. Около
— 185° фторъ превращается въ желтоватую жидкость: при столь низкихъ
температурахъ фторъ не дѣйствуетъ на стекло. М о і 8 8 а п и В е аѵ а г
показали (1903), что жидкій фторъ затвердѣваетъ при — 223°. Въ выс-
шей степенп замѣчательно, что твердый фторъ при —252,5° со взры-
вомъ соединяется съ жидкимъ водородомъ. Жидкій фторъ
реагируетъ при —187° съ сѣрой, фосфоромъ, селеномъ, мышьякомъ, ан-
траценомъ (С14//10), СаО и (со взрывомъ) съ твердымъ метаномъ.
Весною 1888 г. (10 мая) Вехѵаг’у впервые удалось получить зна-
чительныя количества жидкаго водорода. Онъ нашелъ, что жидкій водо-
родъ кипитъ подъ атмосфернымъ давленіемъ при — 252°. Плотность
жидкаго водорода оказалась равною 0.07, т.-е., въ 14 разъ
м е н ь ш е плотности воды. Ожиженіе водорода удалось путем ь
охлажденія его до 205° въ кипящемъ жидкомъ воздухѣ и сжатія до 180 атм.;
водородъ расширялся затѣмъ въ пространствѣ, предварительно охлажден-
номъ до —200°, причемъ и образовался жидкій водородъ. Уменьшая внѣш-
нее1 давленіе надъ жидкимъ Н2 до 30 мм., ЬеАѵат’у удалось получить и
т в е р д ы й в о д о р о д ъ, точка плавленія котораго равна — 257° (16° аЬн.).
Опыты Тгаѵеге’а и Лациего(1 (1903) дали — 258,9° (14,1° аЬз.). Твер-
дый водородъ представляетъ стекловидную, прозрачную массу, не пох< -
жую на металлъ.
Точку кипѣнія озона опредѣлили 018 2 е \ѵ 8 к і (1889) и Т г о о 8 і
(1898): первый нашелъ — 106°, второй - 119°. Жидкій ацетиленъ
кипитъ при — 83,8°; при —80° его можно сохранять въ закрытыхъ со-
судахъ, но при болѣе высокой температурѣ онъ легко взрывается. О жи-
же н іе гелія впервые удалось К ат т е гі іп ^11 -О пп е 8’у 10 іюля 1908 г.
Онъ еще раньше изслѣдовалъ изотермы гелія между + 100° и — 217°, и кромѣ
того при — 253° и — 259°; сравнивая ихъ съ изотермами водорода онъ,
і;а основаніи законовъ соотвѣтствующихъ состояній (гл. XIII, § 9) вы-
числилъ к р и т и ч е с к у ю т е м п е р а т у р у гелія равною 5,3° аЪз.
Ожиженіе удалось примѣненіемъ описаннаго выше метода многократныхъ
ыілловъ. Жидкій водородъ, кипящій подъ давленіемъ о см., охлаждалъ
Сгущеніе газовъ.
567
гелій, сдавленный до 100 атм., до 15° аЬ«. При расширеніи (см. ниж,ег
способъ Ьіпсіе) получался жидкій гелій. Его плотность равна
о,154, т.-е. онъ в ъ 7 разъ легче воды. Точка кипѣнія около 4,5° аЬн.;
критическая температура около 5° аЬ«., критическое давленіе (гл. ХШ)
около 2,3 атм. При давленіи въ 1 см. гелій не1 затвердѣваетъ. Въ 1909 г.
Категііп^іі-Оппез доводилъ внѣшнее давленіе до 2,2 мм., причемь
температура жидкаго гелія была ниже 2,5°, но затвердѣванія не замѣча-
лось; критическое давленіе оказалось равнымъ 2,75 атм. Въ 1911 г. тотъ
же ученый нашелъ, что точка кипѣнія 4,29° аіэз.; онъ достигъ т е м -
пературы 1,47° аЬ$. Повидимому, жидкій гелій имѣетъ мак-
симумъ плотности между 1,47° и 2,37° аЬн.
Изъ многочисленныхъ приборовъ, нынѣ служащихъ щя ожиже-
нія газовъ, мы разсмотримъ главнымъ образомъ одинъ. Онъ основанъ на
принципѣ, повидимому впервые примѣненномъ Ьіпсіе (опубликована
1895 8 с 41 г о е 1 е г’омъ), а затѣмъ и Беіѵаг’омъ. Въ приборѣ Ьіпсіе
охлажденіе газа происходитъ вслѣдствіе многократнаго прохожденія че-
резъ малое4 отверстіе отъ давленія въ 200 атм. до давленія въ 16 атм.
Опыты 4опіе’я и ТЬопізоп’а (стр. 458) показали, что газы при этомъ
охлаждаются, хотя при каждомъ прохожденіи пониженіе температуры не
велико. Важнѣйшую часть своего прибора Ьіпсіе называетъ <Оецеп-
віготаррагаг».; это двойной змѣевикъ состоящій изъ наружной и внутрен-
ней трубокъ.
На рис. 161 схематически изображены главнѣйшія части прибора
Ьіпсіе. Двойной насосъ С (компрессоръ) сжимаетъ воздухъ до 200 атм.
н вгоняетъ ею въ охладитель /?, въ которомъ осѣдаетъ большая часть во-
дяныхъ паровъ, а затѣмъ по внутренней изъ двухъ трубокъ 5 до отвер-
стія вь С, гдѣ воздухъ расширяется до
16 атм., причемъ онъ охлаждается. За-
тѣмъ воздухъ течетъ по наружной трубкѣ,
какъ указано стрѣлками на рисункѣ, и
вновь попадаетъ въ компрессоръ. Въ а
схематически показано мѣсто, гдѣ компрес-
соръ беретъ воздухъ изъ окружающаго про-
странства.
Воздухъ вступаетъ во внутреннюю
трубку при нѣкоторой температурѣ ; про- а
ходя по трубкѣ, онъ о х л а ж д а е т с я до
/2°- такъ какъ снаружи течетъ воздухъ бо-
лѣе4 холодный. Выходя изъ отверстія онь
охлаждается до и течетъ по наружной
і рубкѣ въ обратномъ направленіи. Легко
понять, что а слѣдовательно и 4 должны
і се болѣе4 и болѣе понижаться. Наконецъ 4 дѣлается ниже критической
температуры воздуха, а затѣмъ воздухъ, при давленіи въ 16 атм. начи-
наетъ переходить въ жидкое состояніе*.
568
Испареніе и ожиженіе.
Водородъ непосредственно не можетъ быть ожиженъ при помощи
прибора Ь і п (1 е, такъ какъ этотъ газъ при расширеніи (безъ внѣшней
работы) не охлаждается, но нагрѣвается (стр. 459), если его температура
выше —100°. Поэтому необходимо сперва охладить водородъ, напр. жид-
кимъ воздухомъ, ниже этой температуры, послѣ чего онъ можетъ быть
ожиженъ. Оізгеѵгзкі, Оелѵаг и др. строили приборы, спеціально
назначенные для ожиженія водорода.
Другіе приборы построили В е \ѵ а г , Т г і р 1 е г, Нагорной, 018 -
хелѵвкі, Вепесііскз; всѣ они основаны на примѣненіи охлажденія
газа, расширяющагося безъ внѣшней работы. Сіаисіе впервые въ 1902 г.
описалъ приборъ, въ которомъ газъ охлаждается въ слѣдствіи такого рас-
ширенія, которое сопровождается производствомъ в н ѣ ш н ей р а б о т ы.
Позже онъ значительно усовершенствовалъ этотъ аппаратъ и приспосо-
билъ его къ добыванію почти чистаго кислорода изъ атмосфернаго воз-
духа. Въ 1909 году онъ приспособилъ его къ опредѣленію содержанія
воздуха въ неонѣ, водородѣ и геліи. Полное описаніе своего аппарата
Сіаисіе помѣстилъ въ 19о6 и 1909 гг. въ Лоигпаі сіе РЬузіцие. Мы
ограничимся лишь нѣсколькими указаніями. Воздухъ при помощи ком-
прессора сжимается приблизительно до 4о атмосферъ. Расширяясь онъ
производитъ внѣшнюю работу, двигая поршень; эта работа соотвѣтству-
етъ 6—7 лошадинымъ силамъ. Поэтому изъ 30 лошадиныхъ силъ упо-
треблявшейся машины тратились лишь 23—24. При этомъ въ часъ по-
лучилось 20 литровъ жидкаго воздуха, т.-е. около 1 литра на часъ и
лошадиную силу. Отдѣленіе кислорода и азота основано на томъ, что
точка кипѣнія О2 лежитъ выше, чѣмъ у М, такъ что изъ жидкой
смѣси легче испаряется, а О2 наоборотъ, легче конденсируется изъ газо-
образной смѣси. Аппаратъ этотъ даетъ въ 24 часа до 1000 куб. метровъ
почти чистаго (до 98 °/0) кислорода. Охлажденіемъ получавшагося азота
до его ожиженія С1 а и (1 е получалъ смѣсь Не, Н и Не. Онъ нашелъ
(1904) что въ 1000000 частей воздуха содержатся 15 частей неона. 5 ча-
стей гелія п менѣе 1 части водоро щ.
Приводимъ обзоръ критическихъ температуръ и давленій (глава XIII),
точекъ кипѣнія подъ нормальнымъ давленіемъ въ 760 мм. и точекъ пла-
вленія по новѣйшимъ (1912 г.) даннымъ.
Вещество. Критич. темпер. Критич. давленіе (атмосферы). Темпер. кипѣнія. Темпер. плавленія.
Гелій . 268° (5° аЪз.) 2.75 4.29° аЬз. . —
Водородъ . . 242 20 252,6 258°(15°аІ)8.)
Воздухъ . . 140 39 ( 191)
Кислородъ - 118,8 50.8 182,8 227
Азотъ . - 146 35 195,6 210,5
Озонъ . . . -— — 1 19 —
Аргонъ 122.4 48,0 186,1 187,9
Криптона,. 62,5 54,3 152 169
Сгущеніе газовъ.
569
Вещество. Критич. темпер. Критич. давленіе (атмосферы). Темпер. кипѣнія. Темпер. плавленія.
Ксенонъ + 14,7 57,2 109 — 140
Неонъ . . 210 (?) 25 240 - 252,6 (?)
СО . . - 141 36 190 207
Фторъ . . . 120 (?) 40 (?) 187 223
- 92,9 64,6 150,2 160,6
Метанъ . . — 81,8 54,1 — 164 186,0
МО . . . — 38,8 77,5 — 89,8 — 102,3
Этиленъ + ю 51,7 102,5 -169
Ацетиленъ . 35.5 61.5 — 81.0 81,5 (?)
Фтористый
водородъ . — — — 92,3
Фосфористый
водородъ . 52.8 64 — 86,4 - 133
М ышьяковистый
водородъ . — — 55 119
Сюрмяной
водородъ . 4-138 91 18 91,5
8іН± . . . 3,5 17,8 — 116 191
(740 мм.)
... — -101,0 127,0
. — 1,5 50,0 65,0 — 77
(1810 мм.)
. + 138 91 41 68
ррл . . — — 95 160
рръ ... — — 75 82
РЕЛО . . . — 75 82
НО.,Р . . 63,5 139
Этанъ . . . 4-34 50,2 — 85.4 - 17 1,4
Пропанъ . . 97 44 45 —
на. . . . 51,3 «6 — 83,7 - 101,3
ИН:і . . . 130 1 15 33,5 77,7
Ціанъ . . . 128,3 59,6 21 34,4
Сѣроводородъ 100,2 92 - 60,2 - 83,0
5О2 . . . 155,4 78,9 10.1 76
Хлоръ . . 146.0 93,5 33,6 - 102
С0.2 . . 31 75 — 78 (— 65,0)
Сѣроуглеродъ 273,0 72,8 46 - 112,8
Алкоголь . . 244 62,7 78,1 — 112,3
Эфпръ . . . 197 35,8 34,9 117,6
Хлороформъ . 260 54 61 71
Толуолъ . . 321 — ну - 94,2
Эманація радія:
КиНіегіогсІ (1909) — — — 65 ' ••
570
Испареніе и ожиженіе.
Вещество. Критич. темпер. Критич. давленіе (атмосферы). Темпер. кипѣнія. Темпер, плавленія.
(тгау и Кашзау Вапкіпе (1910, — — — 62 — 71
вычисл.). . 4- 105 — — —
Точка кипѣнія жидкаго воздуха зависитъ отъ процентнаго содержа-
нія кислорода, увеличивающагося во время испаренія.
§ 7. Испареніе твердыхъ тізлъ. Твердыя тѣла могутъ переходить
въ газообразное состояніе такъ, что промежуточная жидкая фаза пли не-
замѣтна. или вовсе отсутствуетъ. Весьма возможно, что всѣ твердыя
тѣла постоянно испаряются, выдѣляя частицы хотя бы и въ минималь-
ныхъ количествахъ. Косвеннымъ доказательствомъ существованія пара,
окружающаго твердыя тѣла, можетъ служить тотъ запахъ, который ха-
рактеренъ для многихъ твердыхъ тѣлъ. Хеп^ЬеІіз (1904) показалъ,
что даже весьма тугоплавкіе окислы металловъ испаряются. Онъ подвѣ-
шивалъ листочки серебра въ замкнутыхъ сосудахъ надъ изслѣдуемыми
окислами, и нашелъ, что съ теченіемъ времени образуются на серебрѣ
пятна, какъ результатъ воздѣйствія паровъ окисловъ.
Въ послѣдующей работѣ (1907) 2еп^Ь.е1І8 изслѣдовалъ испареніе
элементовъ (металловъ и иныхъ), окисловъ, гидроксидовъ п многихъ со-
лей, которыя онъ употреблялъ въ порошкообразной формѣ. Отчетливое
дѣйствіе на (‘сребряные листки оказали РЬ, 7,п, 8Ь, Аг, 8, 8е, Те и
красный фосфоръ. Мо8 8 показалъ, что при обычныхъ температурахъ 5
испаряется. Онъ удерживалъ въ горизонтальномъ положеніи эвакуиро-
ванную стеклянную трубку, содержавшую на одномъ концѣ куски сѣры.
Черезъ 20 лѣтъ, впродолженіе которыхъ температура трубки не повы-
шалась выше 22°, на другомъ концѣ трубки оказались небольшіе ром-
бическіе кристаллы, которые еще черезъ 5 лѣтъ достигли 0.2 мм. въ
діаметрѣ. Упругость р1 пара, окружающаго твердыя тѣла, если о таковой
вообіце можно говорить, во всякомъ случаѣ для огромнѣйшаго числа тѣлъ
весьма мала.
Съ повышеніемъ температуры, когда тѣло близко къ переходу въ
жидкое1 состояніе, упругость пара можетъ сдѣлаться довольно значи-
тельной.
Капі8ау и Ѵоип&’у удалось изслѣдовать давленіе пара кам-
форы. Подобныя же измѣренія производили затѣмъ Агсіолѵ8кі, АНеп
(1900, камфора), біеігпег (1901, камфора, нафталинъ, Н§СІ, НрР
НрВг и др.) и ИІ е (1 ег8 сйиИе (1903, тѣ же вещества, антраценъ, бен-
зойная кислота и др.), Кйзіег (1905). Вагкег (1910), АѴе^ясІіеі-
(Іег (1910. ЫН±СІ) и др.
Для давленія паровъ нафталина гііеігпег находитъ при 35°
около 0,2 мм., при 55° около 1,2 мм. и при 75° около 5,4 мм.
АНеп даетъ слѣдующія числа:
І = 0° 20° 30° 40° 50° 60° 70° 75°
р 0,022 0,080 0.135 0.320 0.81 1,83 3,95 5.43 мм.
Испареніе твердыхъ тѣлъ.
571
Вагкег (1910) находитъ:
І - 0° 20° 30° 40°
р' = 0,023 0,0644 0,164 0,378 мм.
Воііа (начало 1910: работа не опубликована, но упомянута Ваг-
кег’омъ) находитъ для нафталина при 0° р' ~ 0,0088 мм. Си ер ан скі й
(1903) находитъ р' = 6.44 мм. при 80°.
Испареніе, твердыхъ тѣлъ можетъ быть наблюдаемо при температу-
рахъ. лежащихъ выше точки плавленія, если тѣло находится подъ весьма
малымъ внѣшнимъ давленіемъ, и если образующіеся пары быстро отво-
дятся. напр. если тѣло помѣщено подъ колоколъ непрерывно дѣйствую-
щаго воздушнаго насоса. СагпеПеу показалъ, что ледъ при такихь
условіяхъ быстро испаряется. Въ этомъ случаѣ жидкая фаза незамѣтна,
ибо каждая частичка льда, расплавившись, немедленно испаряется. По
и ниже 0° ледъ окруженъ паромъ, упругость котораго вполнѣ измѣрима ;
она при - 10° еще равна примѣрно 2 мм.
Общія формулы (14, 15. 16) стр. 500, которыя мы вывели для пере-
хода вещества изъ одного состоянія въ другое, очевидно приложимы и
къ случаю перехода изъ твердаго состоянія въ газообразное. Введемъ
слѣдующія обозначенія: д скрытая теплота испаренія жидкости. о* скры-
тая теплота плавленія, б удѣльный объемъ насыщеннаго пара надъ жидко-
стью. б( то же надъ твердымъ тѣломъ. 5 удѣльный объемъ жидкости.
5' твердаго тѣла, р упругость пара надъ жидкостью, р1 то же надъ
твердымъ тѣломъ. Скрытая теплота испаренія твердаго тѣла очевидно
равна р + (Л Допуская, что жидкость можетъ быть переохлаждена
(стр. 484), мы можемъ разсматривать давленія р и р' при одной и той
же температурѣ, Т. Формула (16) даетъ:
др
для испаренія жидкости о = АТ(о 8) ................ (48)
др*
для испаренія твердаго тѣла рД-р1—ДТХа' $') ................(48.а)
Въ виду малости 5 и 5' сравнительно съ б и о', мы можемъ прене-
бречь этими величинами, или по крайней мѣрѣ положить 8* = 5. Тогіа
дтя испаренія твердаго тѣла получаемъ
....................(49)
При температурѣ плавленія Т мы должны имѣть р -р' — и
б = о1 = о0, ибо при этой температурѣ всѣ три фазы су-
хи, е с т в у ю т ъ о д и о в р е м е н н о , т.-е. въ замкнутомъ, пространствѣ мо-
гу тъ находиться, соприкасаясь между собою, вещество твердое, жидкое4 и
парообразное, причемъ послѣднее одинаково принадлежитъ твердому тѣлу
и жидкости: его упругость и удѣльный объемъ суть р р' = и
б = б1 = б0.
Относительно температуры плавленія 70, при которой существують
572
Испареніе и ожиженіе.
одновременно всѣ три (разы, а упругости р и р\ и удѣльные объемы
б и б‘ дѣлаются равными, мы сдѣлаемъ весьма, важное замѣчаніе. Эта
температура, вполнѣ опредѣленная, не совпадающая съ обычною тем-
пературою плавленія, хотя и въ высшей степени мало отъ нея обличаю-
щаяся. Мы знаемъ, что температура плавленія зависитъ отъ внѣшняго
давленія. Обычная температура плавленія относится къ нормальному ба-
рометрическому давленію въ 760 мм.; температура же плавленія 7 о, при
которой одновременно рядомъ существуютъ всѣ три фазы, относится къ
тому спеціальному давленію р0, которое одинаково для паровъ надъ жид-
кимъ и для паровъ надъ твердымъ тѣломъ. Отсюда ясно, что напр. для
льда и воды температура точка плавленія при давленіи р0 = 4,6 мм.,
немного выше 0°. Для другихъ тѣлъ 70, вообще говоря, немного ниже
табличной точки плавленія, относящейся, какъ извѣстно, къ давленію въ
760 мм. Изъ сказаннаго видно, что всѣ три фазы могутъ одно-
в р е м е н и о суще с т в о в а ть (въ замкнутомъ пространствѣ и при от-
сутствіи другихъ тѣлъ, которыя увеличили бы число фазъ) только при
одной опредѣленной температурѣ 70 п при одномъ опре-
дѣленномъ давл (‘ніп /?0, т.-е. для нихъ существуетъ только одно
возможное состояніе, изображаемое на осяхъ р и і опредѣленною точкою.
Это знаменитая тройная точка, къ которой мы еще возвратимся въ по-
слѣдней главѣ.
Все изложенное основано на. предположеніи, что при температурахъ
иныхъ, чѣмъ 70, упругости р и р' различны.
Ке^паиіі. опредѣлявшій упругости пара надъ льдомъ п надъ
переохлажденной водой при одинаковыхъ температурахъ, не могъ замѣ-
тить разности между этими давленіями, и потому полагалъ, что они равны,
т.-е. что р —р'. Однако XV. Т11 о т 8 о п (1851), а позже КігсЫіоН (1858)
показали, что кривыя р' = /Д/) и р /(0 не могутъ совпадать, ибо ихъ
касательныя въ точкѣ Т Го, р = р* = р^ составляютъ между собою нѣ-
который уголъ. Дѣйствительно, при Т Тц имѣемъ б = б* = а0, и тогда
(48) и (49) даютъ, если ввести Е = * :
др' др _ о'Е
ді ді Т0(а ...............................1 ’
,, Ф' ()Р . лл
діы видимъ, что : это значитъ, что кривая р —
расположена ниже кривой р = /(/), ибо для первой тангенсъ угла каса-
тельной съ осью і больше, чѣмъ для второй. Отсюда слѣдуетъ, что кри-
вая р' - /Д/) упругости пара надъ твердымъ тѣломъ при Т < Го, и кри-
вая р = /(/) упругости пара надъ жидкостью при Т > Го, хотя и встрѣ-
чаются въ точкѣ Т = 70, но не имѣютъ въ этой точкѣ общей касатель-
Ч /-ГЧХ др1 др
нои. Формула (эО) даеть возможность вычислить разность
т.-е. разность приращеній давленій р* и р при температурѣ Го, при-
Испареніе твердыхъ тѣлъ.
573
че м ъ іі р ира ще пі я о г п осей ы к ь по в ы ш е н і ю т е м п ерат у р ы
на 1°. Для льда и воды имѣемъ р' — 79, Г = 273. б = 205; Е =
= 426. а потому (50) даетъ
* дР „ 0.59» .
оі о? кв.-метр.
Раздѣливъ это число па 13.596, получаемъ ту же разноегь въ мил-
лиметрахъ ртутнаго столба, такъ какъ давленіе одного миллиметра на кв.
метръ равно 13,596 кплогр., гдѣ 13.596 плотность ртути при 0°. Такимъ
образомъ имѣемъ
— 0.044 мм..................(5О.а)
ді ді ѵ
тт г « мм.
Правильнѣе было оы писать съ правой стороны символъ вмѣ-
сто мм. Катвау и Ѵоип§ (1884 и 1887, первая работа подверглась
критикѣ Н. Неітііоііг’а), Гізсііег (1886), йиЫііі и РегсЬе (1891)
• изслѣдовали давленія р и р' паровъ воды и бензола надъ жидкимъ и
надъ твердымъ веществомъ и нашли, что дѣйствительно р и р' не равны
между собою, но что они для воды и льда при 0°, для бензола при 5°,3
дѣлаются одинаковыми. Приводимъ числа ЗнЫіп’а для воды и льда:
1 р Надъ водой. Р Надъ льдомъ. Наблюд. Вычисл.
0° 4.6 мм. 4,6 мм. —
2» 3.995 3.916 3,918
4° 3.450 3,321 3.318
— 6° 2.973 2,808 2.804
- 8° 2,558 2.374 2,366
— 10° 2.191 1.997 1,993.
ТЬіеееп (1899) показалъ, что разность Р—Р* достигаетъ наи-
большаго значенія при 11,7°, причемъ р 1,873 мм., р' = 1,672 мм.
и слѣд. р р'= 0,201 мм. Коіасек и АѴпеПпег вывели формулу
для отношенія р'.р', основываясь на формулѣ Негіг’а, которая будетъ
разсмотрѣна въ слѣдующей главѣ. Формула. Коіасек’а имѣетъ видъ
Іи Д = а 18 1° + Ь т°- ............(51)
р‘ т ‘ Г - 7
гдѣ а и Ь постоянныя, зависящія отъ свойствъ вещества. Для воды и
льда а = 4.5342, Ь =— 1,8765; при помощи этихъ значеній найдены
числа послѣдняго столбца, которыя, какъ видно, прекрасно согласуются
съ числами, полученными изъ наблюденій.
Тйіезеп (1899) вывелъ для р и рі формулы для льда и для
воды. Первая имѣетъ видъ
Ія Рп - С1 ...... (51,о)
/'0 1
574
Испареніе и ожиженіе.
вторая —
Рп - 1т (а Ы-і-сГ-)
Ро 7
(51,6)
Здѣсь рв означаетъ давленіе1 пара при 0°. і — вычисленную темпе-
ратуру точки замерзанія, Т - I 273 — абсолютную температуру, С, а,
Ь. с, — постоянныя, !§ означаетъ Вгі^’овъ логарифмъ. Для р0 сюда
слѣдуетъ подставить величину (50,6). Всііееі (1903) показалъ, что фор-
мула Тіііезеп’а хорошо согласуется съ данными наблюденій. Въ позд-
нѣйшей работѣ (1905) 8с1іее1 пользовался формулами, получающи-
мися изъ формулы Н е г і г’а, именно:
18р = 28,58652 -5 ІІ?Г 2!М;.'4-’
]§•/?'= 11,4796 О,41д7’— 26(^’4-
(15,с)
Эти формулы очень хорошо согласуются съ результатами наблюде-
ній. Чрезвычайно тщательное изслѣдованіе опубликовали затѣмъ (1904)
ЗсЬееІ и Неизе. Для р0 они находятъ величину, равную 4,5788 мм.,
вполнѣ совпадающую съ (50,6). Далѣе они измѣрили р до 15,3° и р'
до —67,9°. Приведемъ нѣсколько чиселъ. Для воды:
і = 0° — 5° —10° — 15° —16°
р - 4,597 3,171 2.160 1,445 1,331 мм.
Для л ь д а :
Г = 0° —10° - 20° — 30° — 40° — 50° — 60° - 68°
р' = 4,579 1.963 0,784 0,288 0,096 0,0296 0.073 0,0008 мм.
Для разности (50,а) изъ этихъ чиселъ получается приблизительно
0,041 миллим.
ТЫе зеп (1909) показалъ, что результаты, полученные 8 с 11 ее Гемъ
и Неизе также хорошо согласуются съ формулой
18р; = 3'я9І2з2+(........................(“Л
или съ формулой
п1 /
= 9,632(1 0,00035/) ~.............(51д?)
Ро 7
Обѣ эти формулы сходны съ формулой (51.а). Наконецъ, Кегпзі
(1909) измѣрилъ величину р‘; изъ полученныхъ результатовъ онъ опу-
бликовалъ до сихъ поръ лишь три числа:
і= — 30° — 40° — 50°
р' = 0,291 0,0962 —0,301 мм.
Согласіе между этими числами и полученными 8 с Ь е е Гемъ и
Неизе удовлетворительное. Кегпзі даетъ общую формулу
Диссоціація. 575
1&Р 4-1,751^7' 0,002107'+ 6,5343. . . (51./)
Изслѣдованія Еегсііе дали для бензола при ^0 = 5°,6 общее да-
вленіе /70 - р р' = 35.5 мм., и далѣе
при /=5°,6. между тѣмъ какъ формула (50) даетъ 0,541.
Кпепеп и ВоЪзоп (1902) нашли, что при —60° давленіе па-
ровъ СО2 надъ жидкостью равно 4,30 атм., а надъ твердымъ веществомъ
3,97 атмосферъ.
§ 8. Диссоціація. Мы не имѣемъ возможности останавливаться на
всѣхъ возможныхъ случаяхъ диссоціаціи, разборъ которыхъ можно найти
въ книгахъ В и Іі е ш’а, И а с а л ь с к а г о, е г и 8 І’а и др. Ограничи-
ваемся краткимъ указаніемъ на случай д и с с о ц і а ц і и т в е р д а г о
тѣла, распадающагося па одно твердое тѣло и одно
г а з о о б р а з н о е. Сюда относится классическій примѣръ распаденія СаСО*
на СаО и СО2, впервые изученный Аітё (1837). а затѣмъ БеЬгау
(1867) и Ье Сііаіеііег (1886). Оказывается, что упругость р угле-
кислаго газа есть вполнѣ опредѣленная функція температуры і. Если на-
грѣть СаСО% до нѣкоторой температуры С то получается вполнѣ опредѣ-
ленная упругость СО2\ если до той же температуры і нагрѣть СаО.
окруженную углекислымъ газомъ, то послѣдній поглощается, пока давле-
ніе не сдѣлается равнымъ р. Общія формулы (14), (15) и (16) стр. 50н
приложимы и къ этом\ переходу отъ одного состоянія къ другому, такъ что
мы и здѣсь имѣемъ
2 = А Т( б — ....... (52)
7 Оі ѵ 7
гдѣ» о скрытая теплота диссоціаціи, которую мы отнесемъ къ одной граммъ-
молекулѣ вещества, о и 5 удѣльные объемы одной граммъ-молекулы газа
и твердаго вещества, или точнѣе п — 5 есть увеличеніе общаго объема
при диссоціаціи одной граммъ-молекулы вещества. Формулу (52) вывелъ
впервые Ногзітапп. Небезъинтересно вывести ее изъ теоріи термо-
динамическаго потенціала, подобно тому, какъ мы на стр. 502 вывели со-
отвѣтствующую формулу для случая плавленія. Пользуемся слѣдующими
обозначеніями. Пусть лх, п2 и пл число граммъ-молекулъ трехъ веществъ,
напр. СпСО3, СаО и СО2: 11 Уз потенціалы одной граммъ-моле-
кулы. такъ что потенціалъ Ф системы
ф = п1(р1 + п2д)2 + ..............(53)
Условіе равновѣсія системы 6?Ф = 0, т.-е.
ср^іц (р2сІп2 + = 0.
Числа сііц должны быть пропорціональны числамъ
показывающимъ, сколько молекулъ каждаго изъ веществъ образуется при
576
Испареніе и ожиженіе.
диссоціаціи; для случая СаСО% — СаО -р- СО2 имѣемъ напр. — 1,
ѵ2 = 1, ^з—1- имѣемъ, слѣдовательно, вообще
1 + ^2^2 + ^зФз = 0.
Если р и і безконечно мало измѣнятся, то эта сумма должна оста-
ваться равною нулю: это даетъ
(Офі . оср., . дср* \ , / дср± . да о , дср» \ ,,
7" + гз 74 аР + иі 7 + г2 -7- + ^=0.
1 др 2 др * 3 др ] г 1 \ 1 ді 1 2 ді 1 3 ді 1
дд); дср: г .
Но = Аѵ,п — 8Л ГДГЬ ооъемъ, 5/ энтропія одной граммъ-
дрі ді
молекулы вещества, см. (74) стр. 439. Итакъ
+ Ѵ^2 + Ѵ^др — + ^2 + ^35з)^= 0.
Но Ч- ѵ2ѵ2 4- равно измѣненію о* — 5 объема при диссоціаціи
одной граммъ-молекулы; -}- л2у2 + рз5з равно измѣненію энтропіи си-
стемы при тѣхъ же условіяхъ. Измѣненіе энтропіи равно поглощенной
теплотѣ р, дѣленной на абсолютную температуру Т. Такимъ образомъ
получаемъ
А(б — з}др = сіі,
а это и есть формула (52).
ЛИТЕРАТУРА.
Къ § 1.
Оаііоп. СіІЬ. Апп. 15, 1803.
Ьаѵаі. Мет. сіе Іа 8ос. Зез 8с. рііуз. еі паіиг. <1е] Воічіеаих (2) 5 р. 107, 1882 ;
Д. Зе рЬуз. (2) 1 р. 560, 1882.
8іерап. ХѴіеп. Вег. 68 р. 385, 1873; 83 р. 943, 1881.
Раіііск. ХѴіеп. Вег. 106, р. 384, 1897.
Ѵ^іпкеітапп, XV. А. 35 р. 401, 1888.
Срезневскій. Ж. Ф. X. О. 14 р. 420, 483, 1882; 15 р. 1, 1883.
Къ § 2.
Раріп. А пелѵ Зі^езіог, ЬопЗоп 1681 и 1687; Ьа тапіёге (ГатоПіг Іез оз, Ат-
зіегЗат 1681 и 1685.
Випзеп. Ро$8’. Апп. 72 р. 159, 1847.
Иа//2^. Сііет. Хелѵз. 75 р. 59, 1877.
Рашіенизкі. Сііет. Вег. 14 р. 88, 1881.
Напсіі ипй РііЬгат. ХѴіеп. Вег. 76, 1877.
Сагпеііеу апсі ѴѴіІІіатз. Доигп. СЬет. 8ос. 1878 р. 281; 1879 р. 1; 1880 р. 1.
Ропез. Сііет. ХТе\ѵз. 37 р. 88, 1878.
КаІіІЬаит. Сііет. Вег. 29 р. 71, 1896.
Весктапп. ХізсЬг. 1. рЬуз. Сііет. 40 р. 129, 1902; 44 р. 164, 1903; 63 р. 177,
1908; 78 р. 725, 1912.
Оау-Ьиззас. Апп. Зе сііітіе раг Сиуіоп Зе Могѵеаи. 82; Апп. сЫт. еі рііуз.
(2) 7, 1818.
Аскагй. Хоиѵ. Мёт. Зе ГАсаД. В. Зе Вегііп 1785 р. 2; Апп. сЫт. еі рЬуз. (1)
10 р. 49, 1791.
Мипке. СіІЬ. Апп. 57, 1817.
РиЛЬег^. Ро^. Апп. 40 р. 39, 562, 1837.
Литература.
577
Магсеі. Ро&". Апп. 57, р. 218, 1842; ВіЫіоІЪёдиѳ ипіѵегвеііе, 38 р. 388, 1842.
Ое Ьис. КесЪегскев виг Іев МосІШсаІіопв де ГАІшовркёге, Ѳепеѵе, 1772, 2-е изд.
т. 4 р. 209; (пігосіисііоп а ]а |рЪувідие Іеггевіге раг Іев Еіиідев ехрапвіЫев, Рагів,
1803, р. 93.
Ооппу. Апп. сЪіт. еі рЪув. (3) 16 р. 167, 1844.
Ои/оиг. Апп. сЪіт. еі рЬув. (3) 68 р. 370, 1863; Агск. вс. рЪув. 12 р. 210, -1861.
Сегпег. Апп. сЫт. еі рЪув. (4) 4 р. 335, 1875.
КгеЬз. Ро^? Апп. 133 р. 673, 1868; 136 р. 144, 1869; 138 р. 439, 1869.
Огоѵе. Совтов 22 р. 698, 1863.
Тотііпзоп. Ргос. К. 8ос. 17 р. 240, 1868—69; Ркіі. Ма$. (4) 37 р. 161, 1869; 38
р. 204, 1869.
Ратзау апй Уоипр. РЪіІ. Ма^?. (5) 20 р. 215, 1885; 21 р. 33, 135, 1886, 22 р. 32,
1886; ХІвсЪг. Г. рЪув. (Ліепъ 1 р. 249, 1887.
Магішаій. ВехіеЬип^еп гхѵівсЪеп біедерипсі ипсі сііет. Сопвіііиііоп. Вегііп, 1888.
Сга/І8. Сііет. Вег. 29 р. 709, 1887.
Корр. ЬіеЪ. Апп. 41 р. 86, 1842; 50 р. 142, 1844.; 96 р. 1, 1851.
ѴѴапкІуп. ЬіеЪ. Апп. 137 р. 83, 1863.
Еѵеггеіі. Ріііі. Ма$. (6) 4 р. 335, 1902.
8скогІеттег. ЬіеЪ. Апп. 161 р. 281, 1872.
Ыппетапп. ЬіеЪ. Апп. 182 р. 39, 1872.
Тлпке ипй ЕгапсЫтопі. ЬіеЪ. Апп. 164 р. 341, 1872.
УѴіпкеІтапп. \Ѵ. А. 1 р. 430, 1877.
Ьоп^іпезси. Апп. всіепііі. Даеву 1 р. 359, 1901.
ѴѴаІйеп. Хіескг. Г. рЪув. СЪет. 65 р. 183, 1909.
Огеетѵоой. Ргос. К. 8ос. 82 р. 396, 1909.
Къ § 3.
ЕІІег. Нівіоіге де ГАсадётіе <1е Вегііп, 1746 р. 42. .
Ьеійеп/гозі. Ве адиае соттипіе поппиііе диаІіІаІіЪие, ВиівЪиг^, 1756.
Рит/огй. ѲіІЪ. Апп. 17 р. 33, 1804.
ОоеЬегеіпег. ОіІЪ. Апп. 72 р. 211, 1822.
Роиіііеі. Апп. сЪіт. еі рЪуе. (2) 35 р. 5, 1827; Р. Апп. 11 р. 447, 1827.
Регкіпз. Апп. сЪіт. еі рЪув. (2) 36 р. 435, 1827; Ро&§. Апп. 12 р. 316, 1828.
Мипке. Ро(ц\ц-. Апп. 13 р. 232, 1828.
Ви$. Ро^§. Апп. 25 р. 591, 1832.
Ваийгітопі. Апп. сЪіт. еі рЪуе. (2) 61 р. 319, 1836.
Рег8оп. С. К. 15 р. 492, 1842; 31 р. 899, 1850; 32 р. 762, 1851.
Агтзігоп^. РЪіІ. Ма&. (3) 27 р. 257, 1845.
Воиіі^пу. С. К. 10 р. 397, 1840; 22 р. 300, 1851; 52 р. 91, 1861; 53 р. 1062, 1861;
Еіидев виг Іев согрв а Гёіаі вркёгоМаі, 3 изд. Рагів, 1857; Апп. сЫт. еі ркуе. (3) 9 р.
350, 1843; 11 р. 16, 1844; 27 р. 54, 1849; 28 р. 178, 1850.
Скигсіі. РЪіІ. Ма^. (4) 7 р. 275, 1854.
Магірпас. АгсЪ. вс. рЪув. 9 р. 72, 1860.
Ое киса. С. К. 51 р. 141, 1860; 53 р. 101, 1861; 55 р. 245, 1862.
8ийге. С. К. 51 р. 1092, 1860.
Вегрег. Ро^. Апп. 119 р. 594, 1863: 147 р» 472, 1872.
Соііеу. Ро^&. Апп. 143 р. 125, 1871.
Гезехусъ. Ж. Ф. X. О. 8 р. 310, 1876.
КгІ8іеп8еп. ТійвсЪгііІ іо г РЪуеік о(ц СЪетіѳ (2) 9 р. 161, 1888; ВеіЫ. 13 р. 155, 1889.
Ооззагі. Апп. сЫт. еі рЪув. (7) 4 р. 391, 1895.
Къ § 4.
Віеіегісі. В. А. 6 р. 869, 1901.
8іе{. Меуег. В. А. 7 р. 937, 1902.
КУРСЪ ФИЗИКИ О. X В О Л Ь С О Н А. Т. ПІ, изд. 3-е.
37
578
Испареніе и ожиженіе.
Кіііег. ХѴіеп. Вег. 111 р. 1046, 1902
Віаск. Ьесіигее оп Сііетіеігу. 1 р. 156. -
Ѵ7аіі. См. ВоЫпеоп: Мескапісаі Ркііоеорку 2, 1803.
Сіетепі еі Оезогтез. См. Ткёпагй, Тгаііё йе скітіе 1 р. 78, 1819; см. Ве&папіі,
Мёт. йе ГАсай. 21 р. 638, 1847.
Рит/огй. Хісоіеоп йоигпаі. 1812; Сгіік. Апп. 45, 1813.
[}ге. Ркіі. Тгапз. 1818 р. 385.
8оиікет апй Сгі^кіоп. См. ВоЫпеоп: МескапісаІ^Ркііоеорку 2 р. 160, 1803.
Оергеіх. Апп. скіт. еі рііуе. (2) 24 р. 323, 1823.
Вгіх. Ро&&. Апп. 55 р. 341, 1842.
Дпйгегш8. Роб'Е- Апп. 75 р. 501, 1848.
Вегікеіоі. С. К. 85 р. 647, 1877; й. йе ркуе. (1) 6 р. 337, 1877.
Ѵ/ігіх. А. 40 р. 438, 1890.
Рерріаиіі (вода). Вёіаііопе йе8 ехрёгіепсее 1 р. 635; Мёт. йе ГАсай. 21, 1847.
Негигі^. Ро^&. Апп. 137 р. 19, 592, 1869.
ѴЛпкеІтапп. XV. А. 9 р. 208, 358, 1880.
Неппіп& Аппаі. й. Рііуе. (4) 21 р. 849, 1905; 29 р. 441, 1909.
УѴиеІІпег. ЬекгЪиск йег Ехрегітепіаіркуеік. 2 р. 773, Ьеірхі^ 1896 (5-ое изданіе).
Оіеіегісі. XV. А. 37 р. 494, 1889; Аппаі. й. Рііуе. (4) 16 р. 593, 1905.
Лугининъ. Апп. скіт. еі рііуе. (7) 7 р. 251, 1896; 13 р. 289, 1898; Іпвіг. 16 р. 129,1896.
Нагкег. Мет. апй Ргосеей. Мапсііееіег Ріііі. 8ос. 10 р. 38, 1896; ВеіЫ. 20 р.
524, 1896.
Огі//іік8. Ргос. К. 8ос. 57 р. 212, 1895.
Виск'шаійі. Б. К&1. Вапеке Ѵійепек. паіигѵ. ор;. таііі. АІй. (6) 8 р. ЮЗ, 1896;
ВеіЫ. 22 р. 23, 1898.
8скі//. ЬіеЪ. Апп. 234 р. 300, 338, 1886.
Регзоп. С. В. 17 р. 495, 1843.
Рат8ау. РЫ1. Ма&. (5) 41 р. 38, 1896.
Рат8ау апй МІ88 Магзііаіі. Вер. Вгіі. Аее. Ірехѵісіі, 1895 р. 628; Ркіі. Ма&. (5)
41 р. 38, 1896.
Сгі//іік8 апй МІ88 Маг8ІіаІІ (бензолъ). Ркіі. Мар:. 41 р. 1, 1896.
Магзкаіі. Ркіі. Ма§. (5) 43 р. 27, 1897; С. К. 122 р. 1333, 1896.
8ѵеп88оп. Оеіѵегеі&і аі‘. К^І. Ак. Гоегіійі. 8іоскко1т. 52 р. 535, 1895.
Ре^паиіі (другія жидкост.і). Веі. йее ехрёг. 2 р. 97.
Апйгеъоз. См. выше.
Вегікеіоі. С. В. 82 р. 118, 1876; 85 р. 646, 1877; 88 р. 52, 1879; 89 р. 119, 1879;
90 р 1510, 1880; 93 р. 118, 1881; Апп. сЫт. еі ркуе. (5) 6 р. 145, 1875; 12 р. 529,1877.
йакп. Хіескг. к ркуе. Сііет. 11 р. 787, 1893.
ЫеЬеіапх. Віееегі. Вгееіаи, 1892; ВеіЫ. 17 р. 551, 1893
Ыеевеп. XV. А. 39 р. 131, 1896.
Ре^паиіі (ожиженные газы). Апп. скіт. еі ркуе. (4) 24 р. 375, 1871; Ехрёгіепсее
3 р. 925, 1870.
Раѵге еі 8іІЬегтапп. Апп. сЫт. еі ркуе. (3) 37 р. 470, 1853.
Раѵге. Апп. скіт. еі ркуе. (5) 1 р. 209, 1874.
Векп. О. А. 1 р. 272. 1900.
АИ. В. А. 13 р. 1010, 1904.
Курбатовъ. Ж. Ф. X. О. 34 р. 250, 659, 766, 1902; 35 р. 319,’ 1903; Хіескг. Г. ркуе.
Скет. 43 р. 104, 1903.
Теіскпег. В. А. 13 р. 611, 1904.
СкарриІ8. Апп. скіт. еі. ркуе. (6) 15 р. 498, 1888; С. В. 104 р. 897, 1887; 106
р. 1007, 1888.
Тгоиіоп. Ркіі. Ма^. (5) 18 р. 54, 1884.
Лугининъ. (правило Тгоиіоп а). С. В. 119 р. 601, 645, 1894; 120 р. 556, 1895.
Литература.
579
Ра&іапі. Кепйіс. К. Асс. йеі Ьіпсеі (5) 3 р. 69, 1894; Хиоѵо Сіт. (4) 2 р. 312,
1895; ВеіЫ. 18 р. 656, 901, 1894; 20 р. 360, 1896.
Овішаісі. ЬеІігЬ. а. аіі^. СЬетіе 1 р. 335, 1891 (2-ое изданіе).
ІЛпеЬаг^ег. 8І11. Лоигп. (3) 49 р. 380, 1895.
АиЬеІ. 3. сіе рііуз. (3) 5 р. 70, 1896.
Бачинскій. ХіесЬг. Г. рііуз. СЬет. 43 р. 369, 1903.
Ріпсііау. ХЫсЬг. Г. рЬуз. СЬет. 41 р. 35, 1902. •
Краевичъ. Ж. Ф. X. О. 21 р. 137, 1889.
ОЬасН. РЫІ. Ма&. (5) 32 р. 113, 1891.
Ноиііеѵірсіе. 3. бе рЬуз. (3) 5 р. 159, 18Й6.
ѴѴаІсіеп. ХізсЬг. Г. рЬуз. СЬет. 65 р. 228, 1909.
Маііііа8. С. К. 140 р. 1174, 1905; Л. бе РЬуз. (4) 4 р. 733, 1905; 7 р. 618, 1908.
Къ § 5.
Ратзау апсі Ѵоипр. ХЫсЬг. Г. рЬуз. СЬет. 1 р. 237, 1887.
Къ § 6.
ВИеагег. РЬуз. Кеѵ. 15 р. 243, 1902; полный обзоръ литературы вопроса о низ-
кихъ температурахъ (ожиженіе газовъ, измѣреніе температуръ, свойства веществъ)
за время отъ 1890 до 1902 года.
Ѵ/ігкпег. ѲезсЫсЫе шій ТЬеогіе йег Каііееггеи^ип^, НашЪиг^, 1897 (содержитъ
очеркъ и литературу вопроса объ ожиженіи газовъ).
Ѵап Магит. См. СЬарриіз еі Вег^еі. „Ъеропв йе рЬузідие &ёпёга!е“, Рагіз, 1891,
і. 1 р. 361.
Мощге еі Сіоиеі. То же.
Роигсгоу еі Ѵаидиеііп. Апп. сЫш. еі рЬуз. (1) 29. 1799.
Оиуіоп сіе Могѵеаи. „8иг Іез геігоійіззетепіз агіійсіеііез", Виііеі. 8ос. рііііотаі.
Ап. XII.
Рагасіау. РЫІ. Тгапз. 1823 р. 160 и 189; Апп. сЫт. еі рЬу$. (2) 22, 1823.
Ви$8у. Апп. сЫт. еі рЬуз/ (2) 26 р. 63, 1824; Ро^. Апп. 1 р. 237, 1824.
Рагасіау. РЫІ. Тгапз. 1845 р. 155; Апп. сЫт еі рЬуз. (3) 15, 1845.
КпіеІ8сН. ЬіеЬ. Апп. 259 р. 100, 1890.
Шіогіег. Апп. сЫт. еі рЬуз. (2) 60, 1835; Ъ’Іпзіііиі № 58 р. 197; 126 р. 327;
127 р. 331.
Ыаііегег. Ро^. Апп. 62 р. 132, 1844.
Ѵіііагсі еі Запу. Л. (1е рЬуз. (3) 4 р. 511, 1895.
Саіііеіеі. С. К. 85 р. 851, 1016, 1213, 1270, 1877; 86 р. 97, 1878, 94 р. 1224, 1882;
98 р. 1565, 1884; 99 р. 213, 1884; Апп. сЫт. еі рЬуз. (5) 15 р. 138, 1878; Л. сіе рЬуз.
(2) 4 р. 293, 1885; АгсЬ. зс. рЬуз. 66 р. 16, 1878.
Рісіеі. С. К. 85 р. 1214, 1220; 86 р. 106, 1878; АгсЬ. сіез зс. рЬуз. (2) 61 р. 16
1878; (3) 13 р. 212, 1885; Апп. сЫт. еі рЬуз. (5) 13, 1878.
О&ег. С. К. 88 р. 236, 1879.
ІІО8ѵау. Виіі. 8ос. сЫт. 37 р. 299, 1882; СЬет. Вег. 15 р. 1186, 1882.
Дп8(1еІІ. Ргос. К. 8ос. 29 р. 209, 1879; 34 р. 113, 1882; СЬет. Хе\ѵз 41 р. 75, 1880.
Наиіе/еиіііе еі СНарриІ8. С. К. 94 р. 1249, 1890.
АІі8сНиІ. ХізсЬг. I. Каііе-Іпсіизігіе 2 р. 201, 1895,
Віиетске. АѴ. А. 34 р. 10, 1888.
ипсі 0І82еси8кі. АѴ. А. 20 р. 243, 1883; Л. бе рЬуз. (2) 2 р. 485, 1883.
\ѴгоЫе^8кі. АѴ. А. 20 р. 860, 1883; 25 р. 371, 1885; 26 р. 134, 1885; АѴіеп. Вег.
97 р. 1321, 1885; С. К. 97 р. 166, 308, 1553, 1883; 98 р. 304, 982, 1884 ; 99 р. 136, 1884;
102 р. 1010, 1886; Керегіог. сі. РЬузік 20 р. 443, 1884; 25 р. 265, 329, 1889 (издано
послѣ смерти автора).
ОІ8гехѵ8кі. АѴ. А. 31 р. 58, 1883; 37 р. 337, 1889; 56 р. 133, 1895; РЫІ. Ма&. (5)
39 р. 188, 1895; 2І8сЫ. Ь рііуз. СЬет. 16 р. 380, 1895; С. К. 98 р. 365, 914, 1884;
37*
580
Испареніе и ожиженіе.
99 р. 133, 184, 706, 1884; 100 р. 350, 940, 1885; 101 р. 238, 1885; ХѴіеп. Вег. 94 р. 209,
1886; 95 р. 253, 1887.
Оізхегѵзкі (кипѣніе и крит. темп. Н2). XV. А. 56 р. 133, 1895; Аппаі. й. Рііуз. (4)
17 р. 986, 1905; Виіі. Сгас. 1912 р. 1; РЫІ. Ма&. (5) 40 р. 202, 1895; Аппаіее 6 сіііт.
еі рііуе. (8) 8 р. 193, 1906; (аргонъ) РЫІ. Тгапе. Ьопйоп 186 р. 253. 1895; Хіесііг. Г. рііуз.
Сііет. 16 р. 380, 1895.
Оізге'шзкі (гелій). XV. А. 59 р. 184, 1896; Апп. б. Рііуе. (4) 17 р. 994, 1905;
Аппаіее 6. сЫт. еі рііуе. (8) 8 р. 139, 1906.
Оізгеѵѵзкі. (обзоръ). Веѵие есіепііі. 1896 р. 414: Ж. Ф. X. О< 28, отд. хим., II
р. 102, 1896.
Моіззап еі Оемаг. С. К. 124 р. 1202, 1897; 125 р. 505, 1897; 136 р. 785, 1903.
Оеюаг. РЫІ. Ма§. (5) 18 р. 210, 1884; 34 р. 205, 326, 1892; 36 р. 328, 1893.
Оегѵаг (водородъ и гелій). С. В. 126 р. 1408, 1898; Ргос. К. 8ос. 63 р. 256, 1898;
Ргос. Сііет. 8ос. 1898, р. 146; Хаіиге (англ.) 58 р. 56, 1898; Апп. й. сіііт. еі рііуе. (7)
18 р. 145, 1899; 23 р. 417; 1901; 3. й. рііуе. 1901 р. 441; Ргос. В. 8ос. 85 р. 589, 1911.
Ьіпсіе Хіесііг. і. Каііе-Іпйиеігіе. 1894 р. 15; XV. А. 57 р. 328, 1896.
Зсіггоеіег. ХіесЫ. Ѵег. йеиіесіі. Іп^епіеиге 39 р. 1157, 1895.
Л’Агзопѵаі. С. В. 126 р. 1863, 1898 (описаніе прибора ІЛпсіе малыхъ размѣровъ).
Езігеіскег. Ріііі. Ма§. (5) 40 р. 454, 1895; Хіесіі. і. рііуе. Сііетіе 20 р. 609, 1896.
Ігаѵегз и Ладиеюсі. Хіесііг. і. рііуз. Сііет. 45 р. 416, 1903.
Оізгехѵзкі (новые приборы) Б. А. 10 р. 768, 1903; 12 р. 196, 1903; Апп. й. сЫт.
еі рііуе. (7) 29 р. 289, 1903.
Оехмаг еі Моіззап (фторъ) С. В. 136 р. 785, 1903.
Гольдгаммеръ. Воіігтапп йиЪеІЪапй р. 410, 1904.
СаиЬеі. Хіесііг. і. рііуе. Сііет. 40 р. 257, 1902; 49 р. 101, 1904.
Категііщгіг-Оппез. Многочисленныя статьи въ Соштипісаі. ігот Иіе рііуе. ІаЬог
оі іііе Рпіѵеге. оі Ьеійеп, начиная отъ 1899 г.
Категііп^іг-Оппез (гелій). С. В. 147 р. 421, 1908: Ѵегеі. К. Ак. ѵоп ХѴеі. іе
Атеіегйат 16 р. 495, 1907; р. 815, 819, 1908; Соттшііс. № 102, а и с, 105; подроб-
ное описаніе: Ѵегеі. к. Ак. ѵап ХѴеі. 17 р. 163, 1908; Ргос. оі іііе еесііоп оі Всіепсее
11, I р. 168, Век. 1908; Соттші. № 108; новыя работы: Ѵегеі. к. Акай, ѵап ХѴеі.
18 р. 168, 1909; 19 р. 1187, 1911; Соттипіс. № 112; Г.9, 122 Ь, 122 Ъ.
Сіаийе. С. В. 131 р. 500, 1900; 134 р. 1568, 1571, 1902; 141 р. 762, 823, 1.905;
142 р. 1333, 1906; 143 р. 583, 1906; 144 р. 1037, 1907; 148 р. 1454, 1909; 149 р. 915, 1909.
Эманація радія:
Киі1гег/ог(і. РЫІ. Ма^, (6) 17 р. 723, 1909.
Огау а. Катзау. Ргос. Сііет. 8ос. 26 р. 82, 1909. 3. сііет. 8ос. 95 р.
1073, 1909.
Еапкіпе, РЫІ. Ма&. (6) 21 р. 45, 1911.
Къ § 7.
Еатзау апй Уоип& РЫІ. Тгапе. 175 р. 37, 461, 1884; РЫІ. Ма&. (5) 23 р. 61, 1887.
Киепеп апй РоЬзоп. РЫІ. Ма&. (6) 3 р. 149, 1902.
ІЫезеп. XV. А. 67 р. 690, 1899.
Зіеіхпег. Віее. Егіап&еп 1901.
Хещ>1геІІ8. ХіесЫ. і. рііуе. Сііет. 50 р. 219, 1904; 57 р. 90, 1907.
Міейегзсіиіііе. Віее. Егіап^еп 1903.
Аітё (1837). Перепечатно: Лоигп. йе рііуе. 1899 р. 649.
Сагпеііеу. Каіиге (англ.) 42 р. 130, 1880; Сііет. Меіѵе 42 р. 313, 1880.
Ке§паиІі. Веі. йее Ехрёг. 2 р. 751; С. В. 39 р. 406, 1854; Ро^. Апп. 93 р. 575,1854.
Кігдіііо//. бее. АЫіапйІ. р. 482; Ро^ц. Апп. 103 р. 206, 1858.
ІГ. Потзоп. Тгапе. В. 8ос. ЕйіпЪ. 1851.
/?. НеІтПоІіх. XV. А. 27 р. 522, 1886.
Свойства насыщенныхъ паровъ.
581
ГізсНег. XV. А. 28 р. 400. 1886.
ЬиНІіп. Вйіап§ (1. 81оск1ю1ш Асагі. 17 АМ. 1 № 1, 1891—1892
РегсГіе, XV. А. 44 р. 265. 1891.
Коіасек. XV. А. 29 р. 347, 1886.
Ѵ^иеііпег. ЬеІігЬисІі 6. Ехрегішепіаірііубік 2 р. 825, Ьеіргі^ 1896 (5-ое изданіе).
Къ § 8.
Оиігет. Ье роіепііеі іііегшосіупаіпідие. Рагів, 1886.
Пасальскій. Равновѣсіе соприкасающихся массъ. Одесса, 1895.
Мегп8і, Тііеогеіівсііе Сііетіе, 8іЩЩагі 1893.
ОеЬгау. С. Е. 64 р. 603, 1867.
Ье Оіаіеііег. С. Е. 102 р. 1243, 1886.
^Ногзітапп. Сііет. Вег. 2 р. 137, 1869.
ГЛАВА ДВѢНАДЦАТАЯ.
Свойства насыщенныхъ паровъ. Гигрометрія.
§ 1. Введеніе. Мы обыкновенно называемъ паромъ всякое газо-
образное вещество, или находящееся въ состояніи насыщенія, т.-е. облада-
ющее наибольшею упругостью, возможною при данной температурѣ, или
недалекое отъ насыщенія, и по свойствамъ въ значительной степени от-
личающееся отъ идеальныхъ газовъ. Понятіе о насыщенномъ парѣ
вполнѣ опредѣленное; нельзя сказать того же самаго относительно поня-
тія о парѣ ненасыщенномъ, и нѣтъ возможности провести строго научной
грани между паромъ и газомъ, если не принять критической температуры
за такую грань, что однако практически весьма неудобно по причинамъ,
которыя были указаны выше. Изъ двухъ свойствъ пара : близости его
къ ожиженію и неслѣдованія законамъ Маріотта и Гей-Люссака,
мы должны большой вѣсъ придать первому. Дѣйствительно, съ одной
стороны мы въ т. I познакомились съ «отступленіями газовъ отъ закона
Маріотта^; мы видѣли, что эти отступленія, напр. даже для воздуха,
весьма замѣтны, и однако мы не сочли нужнымъ отнести соотвѣтствую-
щую главу къ ученію о парахъ. Съ другой стороны, мы можемъ принять,
что пары при нѣкоторыхъ условіяхъ вплоть до насыщенія слѣдуютъ двумъ
основнымъ законамъ идеальныхъ газовъ, а именно когда плотность этихъ
паровъ весьма невелика. Сюда можно напр. отнести пары воды прй 0°
или пары ртути при температурахъ ниже 100°. Мы видѣли (стр. 550),
что 1 кгр. насыщеннаго водяного пара занимаетъ при 0° объемъ, равный
210 куб. м.; его плотность въ 210000 разъ меньше плотности воды или
приблизительно въ 300 разъ меньше плотности воздуха.
Въ этой главѣ мы разсмотримъ свойства насыщенныхъ паровъ и
свойства ненасыщенныхъ паровъ для тѣхъ случаевъ, когда законы Марі-
отта и Гей-Люссака оказываются къ нимъ вовсе не приложимыми.
Пары ненасыщенные иногда еще называются перегрѣтыми, т.-е.
нагрѣтыми выше той температуры, при которой наличное количество ве-
щества насыщаетъ предоставленное ему пространство.
582
Насыщенные пары.
Вопросъ о свойствахъ паровъ, выдѣляющихся изъ растворовъ,
будетъ разсмотрѣнъ впослѣдствіи; смѣси жидкостей, смѣшивающихся во
всѣхъ пропорціяхъ, мы также относимъ къ растворамъ.
§ 2 Методы опредѣленія упругости насыщенныхъ паровъ. Упру-
гость насыщенныхъ паровъ даннаго вещества есть функція температуры;
эту функцію мы обозначимъ черезъ
р =
Если пространство, занимаемое паромъ, имѣетъ въ различныхъ мѣстахъ
неодинаковыя температуры і. напр. въ одной части (Л) і = въ другой
(5) I = /2, причемъ < 4, т0 упругость пара во всемъ пространствѣ
должна имѣть то значеніе ръ которое соотвѣтствуетъ болѣе низкой
температурѣ /х. Дѣйствительно, съ одной стороны упругость пара не
можетъ быть неодинаковой въ различныхъ частяхъ одного и того же
замкнутаго пространства, съ другой — упругость въ части А, гдѣ і = 4,
не можетъ быть больше рг. Въ этомъ случаѣ паръ въ В несасыщенъ и
если въ В находится жидкость, то она непрерывно испаряется, упругость
въ В дѣлается больше рг на весьма малую величину Дръ вслѣдствіе чего
паръ непрерывно переходитъ въ Л, гдѣ онъ тотчасъ сгущается. Такимъ
образомъ происходитъ перегонка жидкости отъ В къ Л; равновѣсіе тогда
установится, когда вся жидкость перейдетъ изъ В въ Л. Величина Лрг
во всякомъ случаѣ въ высшей степени малая, если только не требуется
большого давленія для перехода пара изъ В въ Л, т.-е. если Л и В не
соединены напр. длинными и тонкими трубками. Обычный методъ пере-
гонки жидкостей основанъ на изложенномъ принципѣ.
Кпийвеп (1910) показалъ, что равенство давленій въ двухъ сое-
диненныхъ между собою резервуарахъ, находящихся при различныхъ аб-
солютныхъ температурахъ 7\ и Т2. перестаетъ существовать въ томъ
случаѣ, если длина, соединительной трубки весьма мала по сравненію со
средней длиною пути молекулъ. Если рг и р2 суть давленія, то вмѣсто
А — А въ этомъ случаѣ имѣетъ мѣсто равенство
рг.р2 = ѴТ\ : ѴТ2.
Если паръ слѣдуетъ законамъ, справедливымъ для идеальнаго газа,
и <5Х и <52 суть плотности газа, то, вмѣсто равенства <5Х : <52 = : I Гх,
получается равенство
д^д^Т^.Т.,
Для дальнѣйшаго эти интересные результаты моглп-бы имѣть значе-
ніе лишь въ томъ случаѣ, если плотность пара весьма мала и соедини-
тельная трубка чрезвычайно узка. Практически такой случай невозмо-
женъ. Мы упоминаемъ здѣсь эту новую работу К п и (18 е п’а лишь въ виду
замѣчательнаго результата, содержащагося въ ней; она относится, соб-
ственно, къ I тому (кинетическая теорія газовъ).
Для опредѣленія зависимости упругости р насыщеннаго пара дан-
ной жидкости отъ температуры і было сдѣлано весьма большое число
Упругость насыщенныхъ паровъ.
583
экспериментальныхъ изслѣдованій. Непосредственные результаты пред-
ставляются въ видѣ рядовъ чиселъ р. соотвѣтствующихъ различнымъ і. На
основаніи этихъ чиселъ старались выразить зависимость р, оть I эмпи-
рическими формулами, на которыя мы и укажемъ ниже. Но кромѣ
того многіе ученые пытались вывести общій видъ- функціи р — /(Л на
основаніи какихъ-либо теоретическихъ соображеній; тогда
оставалось сравнить теоретически выведенную формулу съ тѣми числами,
которыя далъ опытъ. Съ нѣкоторыми изъ такихъ теоретическихъ формулъ
мы также познакомимся ниже.
Существуютъ три метода экспериментальнаго опредѣленія сопряжен-
ныхъ значеній давленія р и температуры это методы статическій, ди-
намическій и методъ изученія изотермъ.
Методъ статическій основанъ на измѣреніи давленія р на-
сыщенныхъ паровъ, соприкасающихся съ избыткомъ жидкости при опре
дѣленной температурѣ /, которая можетъ быть установлена по произволу.
Давленіе р измѣряется тѣмъ пониженіемъ ртутнаго
столба въ барометрической трубкѣ (рис. 162), которое
получается при введеніи жидкости въ такъ называемую
торричелліеву^ пустоту, и притомъ въ количествѣ, до-
статочномъ для того, чтобы пространство надъ ртутью
наполнилось насыщенными парами и еще осталось нѣ-
которое количество неиспарившейся жидкости. Давле-
ніе р измѣряется разностью высотъ ртутныхъ столбовъ
въ А и В, если положить, что А и В находятся при
одинаковой температурѣ і. Необходимо ввести по-
правку на давленіе столба жидкости, оставшейся въ Ву и
привести разность высотъ ртутныхъ столбовъ отъ къ 0°.
Рис. 162.
А. В
Методъ динамическій основанъ на измѣреніи температуры
Г кипѣнія жидкости, находящейся подъ опредѣленнымъ давленіемъ ко-
торое можетъ быть установлено по произволу. Мы знаемъ, что при тем-
пературѣ кипѣнія жидкости упругость ея насыщеннаго пара равна давле-
нію, подъ которымъ находится жидкость, а потому измѣреніе давленія р
и точки кипѣнія і даетъ* намъ пару сопряженныхъ значеній величинъ,
связанныхъ искомою функціей р = /(0.
Ве^паиІЬ показалъ, что оба метода даютъ совершенно одинаковые
результаты, если только жидкости взяты совершенно чистыя. Ма-
лѣйшая нечистота можетъ имѣть большое вліяніе, въ особенности на ре-
зультатъ, добытый по статическому методу, какъ показалъ между про-
чимъ Татшапп. Въ 1883 г. возникъ продолжительный споръ между
КаЫЬапт’омъ съ одной, и Ватзау и Тоип^’омъ съ другой сто-
роны ; первый утверждалъ, что статическій и динамическій методы даютъ
совершенно различныя числа, но въ концѣ концовъ долженъ былъ отка-
заться отъ этого мнѣнія.
Существуетъ третій методъ, дающій не только давленіе* р, но
и удѣльный объемъ о насыщеннаго пара. Этотъ сложный методъ, при-
584
Насыщенные пары.
водящій, особенно при высокихъ температурахъ, къ весьма точнымъ ре-
зультатамъ, можно назвать методомъ изученія изотермъ. Онъ за-
ключается въ изслѣдованіи зависимости между давленіемъ р и объемомъ
ѵ ненасыщеннаго пара про постоянной температурѣ. Эта зависи-
мость выражается нѣкоторой кривой, если принять ѵ и р за координаты.
Каждая кривая есть изотерма, соотвѣтствующая опредѣленной темпера-
турѣ і. При большихъ ѵ и малыхъ р изотерма мало отличается отъ ги-
перболы, ибо уравненіе ея мало отличается отъ уравненія рѵ = Сопзі.
По мѣрѣ уменьшенія объема ѵ и увеличенія давленія р, кривая начи-
наетъ все болѣе отличаться отъ гиперболы: въ нѣкоторой точкѣ опа
имѣетъ переломъ, превращаясь въ прямую, параллельную оси ѵ, т.-е.
ея уравненіе становится р — Сов8І.; давленіе уже не зависитъ отъ
объема, уменьшеніе когораго вызываетъ лишь сгущеніе части пара въ
жидкость. Координаты точки перелома кривой и суть р и п насыщен-
наго пара для той температуры, которая соотвѣтствуетъ разсматриваемой
изотермѣ. Этотъ способъ развили сперва А п (1 г е лѵ 8 . а затѣмъ въ осо-
бенности Аша^аі во Франціи, Еатзау и Тоипц въ Англіи и Ваі-
ѣ е 11 і въ Италіи.
§ 3. Измѣренія упругости насыщеннаго пара, произведенныя до
Кедпаиіі (1843). Изъ опытныхъ опредѣленій упругости р насыщеннаго
Рис. 163.
Рис. 164.
Рис. 165.
пара представляютъ особый интересъ, между прочимъ и для техники,
опредѣленія величины р для паровъ воды.
Первыя измѣренія этой величины производилъ въ 1759 г. Хіе^іег,
помѣщая въ котелъ Раріп’а сосудъ со ртутью, отъ котораго шла откры-
тая трубка М (рис. 163) черезъ крышку котла; высота ртути въ М и
термометръ 7 опредѣляли упругость р и температуру Л Тѣмъ же весьма
неточнымъ способомъ производили измѣренія Вёіапсоигі (1792) и XV а II
(1814). Послѣдній кромѣ того впервые вводилъ воду въ пространство
Упругость насыщенныхъ паровъ.
5 «5
надъ ртутнымъ столбомъ барометра В (рис. 164); онъ окружилъ верхнюю
часть А послѣдняго сосудомъ съ водою, температура которой измѣрялась
термометромъ. Тѣмъ же способомъ пользовался Вонійегп. Сюда же
можно отнести изслѣдованія Каетіг’а, который въ теченіе нѣсколькихъ
лѣтъ сравнивалъ показанія двухъ барометровъ, изъ которыхъ одинъ содержалъ
нѣкоторое количество воды надъ ртутью; температуры мѣнялись отъ
— 19° до 4- 26°.
Сг. С. 8 с 11 ш і (II придумалъ (1800) новый способъ : въ короткое колѣно
С (рис. 165) сифоннаго барометра помѣщается испытуемая жидкость,
кипяченіемъ которой изгоняется весь воздухъ изъ этого колѣна. Затѣмъ
Рис. 1(5*.
оно плотно закрывается пробкою А, черезъ которую проходитъ термо-
метръ Т. Тогда въ О остаются только пары, давленіе которыхъ измѣ-
ряется разностью высотъ ртутныхъ столбовъ въ В и О. Нѣсколько иначе
поступилъ С г’е (1818): онъ удлинилъ открытое колѣно В сифоннаго ба-
рометра (рис. 166) и помѣстилъ жидкость въ а окруживъ верхнюю часть
барометра сосудомъ В съ водою; приливая ртуть въ В можно было по-
стоянно удерживать ртуть въ другомъ колѣнѣ на одномъ уровнѣ а. Иско-
мое р равняется Н -|- А, гдѣ Н барометрическое давленіе, А разность
высотъ ртути въ открытомъ и закрытомъ колѣнахъ прибора: на рисункѣ
А отрицательное. АггЬег^ег и Сіігізііап производили чисто тех-
ническія измѣренія, опредѣляя нагрузку клапана, который пары могутъ
поднять при различныхъ температурахъ.
586
Насыщенные пары.
Ваііоп первый окружилъ два барометра во всю ихъ длину водою,
температура которой могла быть измѣняема нагрѣваніемъ. Его приборъ
изображенъ на рис. 167; Ь обыкновенный барометръ; а содержитъ надъ
ртутью нѣкоторое количество жидкости. Оба барометра окружены сте-
кляннымъ цилиндромъ, наполненнымъ водою. Весь приборъ подогрѣва-
ется снизу: ЕЕ'ЕЕ' мѣшалка. Недостатокъ этого метода заключается
въ невозможности поддерживать одну опредѣленную температуру во всей
длинѣ водяного столба.
Упругость паровъ для температуръ ниже 0° была впервые измѣрена
Сгау - Ь и 8 8 ас’омъ. который воспользовался разсмотрѣннымъ на стр. 582
Рис. 169.
свойствомъ паровъ принимать во всѣхъ частяхъ замкнутаго и неравно-
мѣрно нагрѣтаго пространства упругость, соотвѣтствующую наиболѣе низ-
кой изъ встрѣчающихся въ этомъ пространствѣ температуръ. Его при-
боръ изображенъ на рис. 168. АВ барометръ обыкновенный; СЕ второй
барометра», трубка котораго изогнута и оканчивается шаровиднымъ ре-
зервуаромъ Е, содержащимъ испытуемую жидкость и помѣщеннымъ въ
охладительную смѣсь изъ льда и поваренной соли; недостатокъ этой
смѣси заключается въ томъ, что ее неудобно перемѣшивать для дости-
женія однообразной температуры. Искомая упругость р опредѣляется
разностью высотъ А и С ртути въ двухъ барометрахъ.
Въ 1830 появилась работа Виіоп^’а и Ага^о, опредѣлявшихъ
по порученію французской Академіи Наукъ упругость водяного пара ю
5 пругость насыщенныхъ паровъ. 5^7
давленія въ 24 атм., т.-е. до температуры въ 224°. Распредѣленіе при-
боровъ I) и 1 о п ^'а и к г а о , которые пользовались методомъ наблю-
денія точекъ кипѣнія і воды при различныхъ давленіяхъ, показано на
рис. 169. Вода кипѣла въ котлѣ а\ черезъ крышку котла, снабженную
предохранительнымъ клапаномъ, нагрузку ЫУ котораго можно было мѣ-
нять, проходили желѣзныя трубки Ь и Р съ термометрами, измѣрявшими
температуру воды и пара. Далѣе отъ крышки котла шла трубка сі(Ѵсі"х
къ манометру /О; закрытая сверху трубка О содержала воздухъ, объемъ
Рис. 171.
Рис. 170.
котораго опредѣлялъ давленіе1 пара. Передатчикомъ этого давленія слу-
жила вода, наполнявшая всю трубку (ѴсѴ'х и пространство іі* надъ
ртутью въ /. Стеклянная трубка ро, соединенная трубкою ох съ дГх,
служила для опредѣленія уровня к ртути въ сосудѣ /. Вода въ верхней
части трубки охлаждалась непрерывнымъ потокомъ воды V. Изъ
описанія видно, что пары производили давленіе на воду въ и въ этомъ
заключается источникъ возможныхъ погрѣшностей, ибо температура въ сі1
была ниже, чѣмъ въ котлѣ, а потому и упругость пара вездѣ должна была
быть нѣсколько меньше той, которая соотвѣтствовала температурѣ воды и
паровъ въ самомъ котлѣ.
Коммиссія изъ американскихъ ученыхъ повторила (1830) опыты
588
Насыщенные пары.
1) и I о п д’а и А г а § о , но получила результаты, весьма замѣтно от-
личавшіеся отъ результатовъ, добытыхъ французскими учеными; такъ
напр. при 180° разность равнялась уже 0,65 атм., т.-е. около 500 мм.
ртутнаго столба.
Не останавливаемся на работахъ Вевргеіг (1821—1822) ц
Ріпескег’а (1854).
§ 4. Опредѣленія Ведпаиіі и ІИадпиз’а упругости насыщеннаго
пара. Въ 1843 г. были произведены, почти одновременно, классическія
изслѣдованія Ведпаиіі и Мадпив’омъ, причемъ Ведпаиіі измѣ-
рялъ р для водяныхъ паровъ отъ — 32° до + 230°, Мадпп8 отъ —20°
до ио°.
Ведпаиіі пользовался тремя различными методами.
1. Для температуръ ниже 0° Ведпаиіі употреблялъ ме-
тодъ Сгау-Ь и 8 8 а с’а (стр. 585, рис. 168) съ тою только разницею, что
онъ бралъ охлаждающую смѣсь изъ снѣга и хлористаго кальція, которая
удобно перемѣшивается, что въ данномъ случаѣ весьма важно.
2. Для температуръ между 0° и 50° Ведпаиіі пользо-
вался методомъ Раііоп’а (стр. 585, рпс. 167), значительно усовершен-
Рис. 173.
Рис. 172.
ствованнымъ. На рис. 170 изображенъ одинъ изъ приборовъ, построен-
ныхъ Ведпаиіі для этой цѣли; онъ, очевидно, не требуетъ объясненія.
Для нагрѣванія воды служитъ спиртовая лампочка, которая можетъ быть
приподнята или опущена, что и служитъ для измѣненія температуры
воды. Въ другой серіи опытовъ В е д п а и И воспользовался приборомъ,
•въ которомъ одна изъ трубокъ согнута и снабжена шаровиднымъ резер-
вуаромъ А (рис. 171). Въ этотъ резервуаръ помѣщается маленькій пузы-
рекъ, содержащій испытуемую жидкость, какъ показано на отдѣльномъ
рисункѣ 172. Между шаромъ А и трубкою барометра вставлена метал-
лическая оправа, отъ которой идетъ боковая трубка В черезъ сушильный
приборъ къ воздушному насосу. Сперва Ведпаиіі многократно вы-
качивалъ воздухъ изъ барометрической трубки, впуская каждый разъ
Измѣреніе упругости
589
сухой воздухъ: выкачавъ воздухъ до возможно большей степени разрѣ-
женія, онъ запаялъ соединительную трубку В и опредѣлилъ лпругость
воздуха, оставшагося въ резерву арѣ А. Затѣмъ подогрѣвался шаръ А
вслѣдствіе чего пузырекъ съ жидкостью лопался и часть жидкости ис-
парялась.
3. Для наблюденій при высокихъ температурахъ
Ее^панН пользовался динамическимъ способомъ. На рис. 173 изо-
браженъ приборъ, служившій для опредѣленій упругости насыщеннаго
Рис 174.
водяного пара при температурахъ между 42° и 150°. Вода наливалась
въ котелъ а. изображенный отдѣльно въ А въ разрѣзѣ. Небольшая печь
служила для поддержанія кипѣнія жидкости; температура послѣдней, а
также пара измѣрялась термометрами, которые были вставлены въ трубки,
вдѣланныя въ крышку котла. Котелъ соединенъ трубкой съ большимъ
шаромъ В, окруженнымъ водою для поддержанія въ немъ постоянной
температуры. Воздухъ, находящійся въ этомъ шарѣ, доведенъ до опре-
дѣленной упругости р при помощи нагнетательнаго или выкачивающаго
воздушнаго насоса, присоединеннаго къ трубкѣ V. Кранъ г закрывался,
когда въ В было достигнуто опредѣленное давленіе р\ для измѣренія
этого давленія служилъ открытый ртутный манометръ У, соединенный
съ В при помощи горизонтальной трубки, оканчивающейся нѣсколько
590
Насыщенные пары.
ниже г. Потокъ воды, протекающій черезъ трубку Г, сгущаетъ пары,
выходяшіе изъ котла а, въ которой обратно стекаетъ образовавшаяся
вода. Для температуръ выше 150° Ве^панИ пользовался подобнымъ
же приборомъ, болѣе крѣпкой конструкціи, снабженнымъ ртутнымъ мано-
метромъ въ 22 м. вышины, дававшимъ возможность измѣрять давленія
до 30 атм. Вмѣсто ртутныхъ термометровъ Ее^паиіі при нѣкото-
рыхъ измѣреніяхъ пользовался воздушнымъ термометромъ, резервуаръ ко-
тораго помѣщался внутри котла, въ которомъ кипѣла испытуемая жидкость.
Хеипег и Вгосй составили таблицы упругости р водяного пара
для различныхъ / на основаніи наблюденій К е а и 11
Приборъ Ма^пііб’а изображенъ на рис. 174. Главнѣйшую его
часть представляетъ широкая ^-образная трубка аесІЬ, отъ которой идетъ
горизонтальная трубка Ьс. Лѣвая вѣтвь еа, въ которой находятся изслѣ-
дуемые пары, въ верхней части а расширена, чтобы нѣсколько увеличить
пространство, предоставленное парамъ. Трубка есІЬ расположена, внутри
ящика, окруженнаго еще тремя ящиками, что даетъ возможность устано-
вить во внутреннемъ пространствѣ весьма постоянную температуру, на-
грѣваніемъ напр. наружнаго ящика втеченіе продолжительнаго времени
при помощи поставленныхъ подъ него лампъ. Окошечки въ стѣнкахъ
ящиковъ даютъ возможность видѣть снаружи уровни ртути въ двухъ ко-
лѣнахъ трубки аеМ. Для измѣренія температуры / внутренняго про-
странства служили ртутные термометры и, главнымъ образомъ, воздуш-
ный термометръ, двойной изогнутый резервуаръ котораго окружаетъ
трубку аесІЬ съ двухъ сторонъ; Т манометръ воздушнаго термометра
(стр. 18). Трубка Ьс присоединена въ с къ трубкѣ вѣтвь /і которой
ведетъ къ обыкновенному ртутномл манометру 7Ѵ; рядомъ съ этимъ ма-
нометромъ помѣщены барометръ и термометръ. Другая вѣтвь ведетъ
къ выкачивающему насосу, который при нѣкоторыхъ наблюденіяхъ замѣ-
нялся насосомъ нагнетательнымъ. Наблюденія производились слѣдую-
щимъ образомъ: закрытое колѣно аесі наполнялось ртутью, которая по-
двергалась кипяченію; затѣмъ вливалось черезъ трубку сЬ нѣкоторое
количество горячей и тщательно прокипяченой воды. Наклоняя трубку, можно
было помѣстить нѣкоторое количество воды въ а надъ ртутью, гдѣ она, по-
нятно, не могла испариться, находясь подъ давленіемъ, почти равнымъ атмо-
сферному. Размѣстивъ всѣ части прибора, какъ показано на рисункѣ, М а §• -
п и 8 выкачивалъ черезъ трубку воздухъ до тѣхъ поръ, пока въ а не начи-
нали образовываться пары воды, и пока наконецъ ртуть въ обоихъ ко-
лѣнахъ еа и М не устанавливалась приблизительно на одной высотѣ.
При низкихъ температурахъ і, когда давленіе паровъ невелико, прихо-
дилось въ (ІЬс производить весьма значительное разрѣженіе ; когда і близко
къ 100°, то давленіе въ (ІЬс было близко къ атмосферному, а при ^>100°
приходилось нягнетать воздухъ, такъ что ртуть въ правомъ колѣнѣ мано-
метра Ы стояла выше, чѣмъ въ лѣвомъ. Искомая упругость насыщен-
ныхъ паровъ р^Н—— Л2, гдѣ Н давленіе барометрическое, раз-
ность высотъ ртути въ манометрѣ и разность высотъ ртути въ ае и М,
Измѣреніе упругости.
591
причемъ и /г.2 положительныя, если въ лѣвыхъ колѣнахъ манометра и
трубки аеМ ртуть стоитъ выше, чѣмъ въ правыхъ. При опредѣленіи Л2
слѣдуетъ ввести поправку на давленіе воды, оставшейся надъ ртутью въ ае.
Результаты измѣреній упругости р паровъ воды, произведенныхъ
Ве^папіі и Ма^пиз’омъ, замѣчательно согласны между собою; для
доказательства приводимъ немногія числа изъ таблицъ, вычисленныхъ на
основаніи тѣхъ эмпирическихъ формулъ р = /(/"), которыя названными
учеными были предложены, и которыя будутъ указаны ниже:
і Ве^паиК. Ма^пиз. і Ве^паиіі. Ма^пиз.
Р Р Р Р
-20° 0,927 0,916 40° 54,906 54,969
-10 2,093 2,109 60 148,579 148,791
0 4,600 4,525 80 354,643 353,926
20 17,391 17,396 ПО 1075,370 1077,261.
К е $паи1і изслѣдовалъ, кромѣ воды, еще 28 другихъ веществъ,
измѣряя упругость р насыщенныхъ . паровъ въ различныхъ предѣлахъ
температуръ и давленій. Приводимъ списокъ нѣкоторыхъ изъ этихъ ве-
ществъ, прибавляя въ скобкахъ предѣлы температуръ, между которыми
каждое изъ этихъ вещеттвъ изслѣдовалось: алкоголь (—20° до 155°). эти-
ловый эфиръ (—20° до 120°), сѣроуглеродъ (—20° до 150°), хлороформъ
(+20° до 165°), бензолъ ( — 20° до 170°), че-
тыреххлористый углеродъ (—20° до 190°), ме-
тиловый алкоголь (— 30° до 150°), ацетонъ
(4-20° до 140°), хлористый кремній (—25° до
65°) терпентинное масло (0° до 200°), лимонное
масло (98° до 240°), ртуть (0° до 520°), сѣра (390°
до 570°), сѣрнистый газъ (—30° до 65°), амміакъ
(—30° до 100°), сѣроводородъ (—25° до 70°),
углекислый газъ (— 25° до 45°(?); послѣдняя
температура выше критической температуры,
равной 31°), закись азота (— 25° до + 40°).
§ 5. Измѣренія упругости насыщеннаго пара, произведенныя послѣ
Ведпаиіѣ Послѣ Ве^паиіі появилось и продолжаетъ появляться весьма
большое число изслѣдованій упругости насыщенныхъ паровъ различныхъ
веществъ; мы ограничимся указаніемъ на весьма немногія ихъ этихъ ра-
592
Насыщенные пары.
ботъ. Подробныя таблицы результатовъ и литературныя указанія можно
найти въ «Рйу8Іса1І8СІі-еІіетІ8СІіе ТаЬеІІеп» ЬаисІоІГа и Воегп-
81 еі п’а и въ «НапйЪисй сіег РЬуеік», ііегаи8§е§-еЬеп ѵоп А. V/і и к е Iіп а ип,
Т. II, АЬѢІіеіІ. 2, гдѣ изложены результаты опредѣленія упругости насы-
щенныхъ паровъ огромнаго числа различныхъ веществъ; здѣсь же при-
ведена и вся литература этого вопроса и даны также указанія на опре-
дѣленія удѣльнаго объема о насыщенныхъ паровъ, о чемъ будетъ
сказано ниже.
Три главные метода, которыми можно пользоваться для измѣренія
упругости р насыщенныхъ паровъ, были разсмотрѣны выше (стр. 582—
583). Особыя свойства жидкостей заставляютъ въ различныхъ случаяхъ
вводить разнообразныя измѣненія въ устройствѣ приборовъ. Такъ напр.
Ке^паиІЬ пользовался приборомъ, схематически изображеннымъ на
рис. І 75, чтобы опредѣлить упругость/? для веществъ, сгущающихся лишь
при большихъ давленіяхъ, каковы 5О2 и СО2. Два сообщающіеся сосуда
1 и В содержа™ ртуть. Въ А накачивается черезъ трубку Р испыту-
емое газообразное вещество, сгущающееся въ немъ въ жидкость ; В со-
единено трубкою Л4 съ манометромъ и съ нагнетательнымъ насосомъ, сгу-
щающимъ въ В воздухъ. Весь приборъ помѣщался въ воду или иную жид-
кость, или въ охлаждающую смѣсь для поддержанія въ немъ"' опредѣ-
ленной температуры. Разностью уровней ртути въ А и В можно было
пренебречь.
В а ш 8 а у и V о и п пользовались приборомъ, изображеннымъ на
рис. 176, чтобы изслѣдовать зависимость р —Щ) по динамическому ме-
тоду для жидкостей, имѣющихся въ небольшихъ количествахъ. Резер-
вуаръ термометра Т окруженъ пористымъ веществомъ Ь, напр. азбестомъ
или шерстью; испытуемое вещество находится въ воронкѣ 77, снабжен-
ной краномъ пг. Отъ него идетъ черезъ пробку, закрывающую стакан-
чикъ» 5, трубка, нижній конецъ которой, вытянутый въ капилярную трубку,
оканчивается у самой поверхности вещества Ь. окружающаго резервуаръ
термометра. Трубка г соединяетъ стаканчикъ А съ холодильникомъ, съ
манометромъ и съ большимъ сосудомъ, вь которомъ при помощи насоса
устанавливается желаемое давленіе /?, которое однако не можетъ быть
выше атмосфернаго. Стаканчикъ 5 помѣщаютъ въ воду7 или иную жид-
кость, температура которой выше искомой точки кипѣнія і жидкости.
Открывъ кранъ т, насыщаютъ сперва Ь жидкостью и затѣмъ оставляютъ
его настолько открытымъ, чтобы притекающая жидкость постоянно по-
полняла убыль, происходящую отъ ея кипѣнія и перехода паровъ черезъ
трубку г въ холодильникъ, гдѣ эти пары вновь сгущаются въ жидкость.
Термометръ Т показываетъ точку кипѣнія і, соотвѣтствующую давленію р.
Упругость насыщенныхъ паровъ воды опредѣляли послѣ Ведпаиіі
и М а §пи8’а сперва Саіііеіеі и Соіагдеаи, Капіз а у и Ѵоип
и, наконецъ, ВаііеИі; ихъ работы появились почти одновременно въ
1892 г. Изъ нихъ Оаіііеіеі и Соіагйеаи доходили до критической
температуры воды, т.-е. до 365° и до давленія, близкаго къ 200 атм.; из-
Измѣреніе упругости
593
мѣренія Вашвау’я и Уопп^’а простираются до 270° и давленія въ
41101 мм. Саіііеѣеѣ ц Соіатсіеаи нагрѣвали воду въ стальной
трубѣ, удерживая общій объемъ жидкости и пара постояннымъ, и измѣ-
ряя давленія при помощи водороднаго манометра. Кривыя по-
лучались, независимо оть количества взятой воды, одинаковымих до кри-
тической температуры, выше которой кривыя расходились (см. ниже
гл. XIV). Катзау и Уопп^ брали вмѣсто стальной трубы трубу
изъ зеленаго стекла, на которое вода и при высокой температурѣ не дѣй-
ствуетъ, и измѣряли давленіе воздушнымъ манометромъ. ВаНеІІі поль-
зовался способомъ изслѣдованія изотермъ ^стр. 583). Приводимъ нѣкото-
рыя изъ чиселъ, найденныхъ названными учеными для упругости
насыщенныхъ паровъ воды:
1 В е § п а и 1 1. В аі іеі Іі. Ватеау и С аіііеіеі и
Ѵо ип§. Соіатсіеаи.
100° 7бо мм. 760 мм. 760 мм. 1 атм.
150 3532 3578,36 3568 4,7
200 11360 11625 11625 15,1
230 20160 20775 20936 —
250 — 29951 29734 39,5
270 — 43368 41101 —
275 — — — 59,3
300 — 67620 — 86,2
320 — 88343 — —
325 — — — 121,1
350 — 126924 — 167,3
360 — 141865 — —
364,3 — 1 147990 = 1 = 194,61 атм. — —
365 — — — 200,5
Послѣднія два числа третьяго и пятаго столбцовъ относятся къ кри-
тической температурѣ, которую Саіііеіеі и Соіатсіеаи находятъ рав-
ной 365°, а Ваііеііі равной 364°,3.
Послѣ этихъ трехъ пзслѣдованій появились, начиная съ 1892 года,
работы ѴСіеЬе (1893, между 82° и 100°, динамическій методъ) Сйар-
риІ8 (1900, между 96° и 102°. динамическій методъ), Кпірр’а (1900,
между 180° и 359°, статическій методъ), Кп о Ы аи с ІГа, Ьіпйе и КІеЬе
(1905, между 100° и 180° динамическій методъ). Критическій обзоръ
всѣхъ изслѣдованій далъ Неппіп^ (1907), вычислившій вѣроятнѣйшія
значенія давленія р и величины между 0° и 200°.
Въ 1908 году появилась весьма тщательная работа НоІЬогп а и
Неппіп^’а, опредѣлявшихъ р между 50° и 200° по динамическому ме-
тоду, причемъ температуру они измѣряли платиновымъ термометромъ.
Погрѣшность окончательныхъ результатовъ даже при 200° не превосхо-
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. т. ІП, изд. 3-е. 38
594 Насыщенные пары.
✓
дить 0,02°, а вообще - 0,01°. Приводимъ нѣкоторыя изъ этихъ новѣй-
шихъ чиселъ:
І = 50° 70° 90° 100° 120° 140° 160° 180° 200°
р = 92,30 233,53 525,8 760,0 1488,9 2709,5 4633 7514 11647 мм.
Упругость р насыщенныхъ паровъ другихъ жидкостей опредѣ-
ляли, какъ сказано, весьма многіе ученые. Различныя органическія и не-
органическія вещества изслѣдовали, кромѣ Ве^панИ, еще Иассагі
и Ра^ііапі, Зіаейеі, ВсЬитапп, Уоип$, Ватзау иУоип^,
Вісііагйвоп, О. С. 8 сйшісІЛ, Ваііеііі, РегсЬе и др.
Ваги8 изслѣдовалъ сѣру, кадмій, цинкъ и висмутъ для да-
вленій р между7 нулемъ и 1 атмосф., пользуясь приборомъ, выдерживав-
шимъ высокія температуры. Приводимъ нѣкоторыя изъ чиселъ Вагиз’а:
Сѣра. Кадмій. Висмутъ. Цинкъ.
і Р І Р / р І Р
390° 272,3 мм. 549° 22 мм. 1199° 32 мм. 684° 28 мм.
420 472,1 « 620 75 < 1211 86 « 710 42 «
450 779,9 « 702 262 « 1260 97 < 758 99
480 1232,7 « 750 517 « 802 166
550 3086,6 « 760 624 « 863 368 «
570 3877,1 « 770 766 « 933 767
Зайончевскій и Надеждинъ опредѣлили р для нѣкоторыхъ
органическихъ жидкостей до критической температуры.
Давленіе паровъ натрія измѣряли йелѵеѣѣ (1902) и СгеЪЬагйі
(1905). Послѣдній даетъ слѣдующія числа:
і = 380° 400° 420° 440° 460° 480° 500° 520° 540° 560° 570°
р= 1,2 1,4 2,0 2,9 4,2 6,1 8,6 12,4 18,5 33,2 80 мм.
Давленіе паровъ сѣры опредѣляли также СаНепйаг и СггИ-
111118 (1891), Войепзѣеіп (1899) и, наконецъ, МаѣѣЬііез (1906) по
методу кипѣнія. Приводимъ нѣкоторыя числа Маіііііев’а:
і = 210,2° 230,6° 265,0° 306,5 341,7° 363,0° 379,4°
р= 1,35 4,48 2 20,5 53,5 105,3 133 250,1 мм.
Упругость насыщенныхъ паровъ ртути изслѣдовали Ве^паиіі,
Ватзау и Ѵоип$ (1881 и 1886), На^еп (1882), Н. Негіг (1882),
Мас-Ьеой (1883), Уоип§* (1891), РІаипйІ^ег (1897), ѵап йег
Р1ааІ8, Соіагйеаи и Віѵіёге (1900), МііІІег-ЕггЬасІі (1901),
йеѵѵеіі (1902), Могіеу (1904), ОеЫіагйі (1905), ЬаЪу (1908) и
КпиЙ8 еп (1909). Числа Ве^паиіі и На^еп’а несомнѣнно слиш-
комъ велики при низкихъ давленіяхъ, для которыхъ числа Н. Негѣг’а
заслуживаютъ наибольшаго довѣрія: основываясь на наблюденіяхъ, про-
изведенныхъ при болѣе высокихъ температурахъ, Негіг вычислилъ
упругости при низкихъ температурахъ, пользуясь формулой, которая бу-
Измѣреніе упругости, і 595
детъ указана ниже. Приводимъ числа, найденныя Негіг’омъ , сопоста-
вляя съ ними нѣкоторыя изъ чиселъ Ве^паи Н и Н а § е п’а •
і Ведпаиіі. И а § е п. Н е г 12. і Н е г 12.
0° 0,0200 мм. 0,015 мм. 0,00019 мм. 120 0,779 мм.
20 0,0372 « 0,021 « 0,0013 « . 140 1,93 «
40 0,0767 « • 0,033 « 0,0063 « 160 4,38
60 0,1643 0,055 « 0,026 180 9,23 «
80 0,3253 « 0,102 « 0,093 200 18,25 «
100 0,7455 « 0,210 « 0,285 « 220 34,90 «
Еатзау и Уоип^, а также Ріаипйіег нашли числа, хорошо
согласующіяся съ числами Негіг’а. На^еп находитъ при 15° упру-
гость 0,0195 мм. Негізг вычисляетъ 0,00082 мм.; между тѣмъ опыты
Ріаипсііег’а дали 0,0008] мм. Новѣйшія изслѣдованія Мог1еу(1904)
дали слѣдующіе результаты:
I = 16° 30° 40° 50° 60° 70°
р = 0,0010 0,0027 0,0052 0,0113 0,0214 0,0404 мм.
Для 0° Могіеу вычисляетъ отсюда /7 — 0,0004 мм. При болѣе высокихъ
температурахъ опредѣляли р для паровъ ртути Ведпаиіі и У о и п
(1891). Приводимъ нѣкоторыя числа:
і В е^паиіі. У о и п і Ве аиіі. То ип$.
180° 11,00 мм. 8,41 мм. 380 1139,65 мм. 1127,5 мм.
220 34,70 « 31,64 « 420 2177,53 « 2085,0
260 96,73 « 96,46 « 460 3888,14 « 3586,0
300 242,15 « 248,6 « 500 6520,25 —
340 548,43 « 559,1 «
СгеЪйагсіі (1905) даетъ слѣдующія числа (мы приводимъ лишь
нѣкоторыя):
І = 130° 160° 200° 230° 260° 300° 310°
р = 1,337 4,013 17,015 44,9 100,0 249,0 309,0 мм.
ЬаЬу (1908) выводитъ изъ наблюденій различныхъ изслѣдователей
слѣдующія формулы:
3623 932
\^р = 15,24431 — у' — 2,3672331^7 (между 15° и 270°) :
1§/7 = 10,04087 — 327^24-—0,7020537 (между 270° и 700°).
Здѣсь Т означаетъ абсолютную температуру. Кписізеп (1909)
опредѣлялъ р между 0° и 50,8°. При 0° онъ находитъ р — 0,0001846 мм
и вообще
= 10,5724 — —~’--6 0.847 .
38*
596
Насыщенные пары.
Хотя эта формула относится къ не высокимъ температурамъ она
похожа на вторую формулу ЬаЬу.
х Упругость паровъ сгущенныхъ газовъ опредѣляли Е а г а йау,
Вппвеп, Рісіеі, ,Саі11еіеі, Ѵіпсепі иСйарриіе, АѴгоЬ-
1 едѵ8кі, Оізгеѵгекі, Ата^аі, Скарриіз и Кіѵіёге, Ап8-
сіеіі, ЕзігеісЬег, Віиетске, КпіеіесЬ и др. Съ методами, ко-
торыми пользовались многіе изъ этихъ ученыхъ, мы познакомились въ
статьѣ о сгущеніи газовъ (стр. 558—570).
Мы разсмотрѣли способы опредѣленія упругости насыщеннаго пара
и привели численныя величины упругостей, найденныя нѣкоторыми на-
блюдателями. Съ различными попытками эмпирическаго или теоретиче-
скаго опредѣленія вида функціи р = /(і) мы познакомимся ниже.
Для полноты замѣтимъ еще, что упругость пара смѣси нѣсколь-
кихъ жидкостей, не растворяющихся одна въ другой,
равняется суммѣ упругостей паровъ отдѣльныхъ жидкостей, какъ
того требуетъ законъ В а И о п’а (т. I) Опыты К е а и 1 і надъ
смѣсями воды и сѣроуглерода, воды и четыреххлористаго углерода,
и наконецъ воды и бензола вполнѣ подтвердили это равенство. Во-
просъ объ упругости пара смѣсей жидкостей, растворяющихся одна
въ другой или смѣшивающихся во всѣхъ пропорціяхъ, будетъ разсмот-
рѣнъ ниже.
§ 6. Формулы для упругости насыщеннаго пара. До сихъ поръ
не удалось найти строго раціональной формы для вида функціи р — /(і),
т.-е. такой, выводъ которой былъ бы основанъ на началахъ термодина-
мики и на опредѣленныхъ гипотезахъ о строеніи вещества. Огромное
число существующихъ формулъ, которыми пользовались различные ученые,
большею частью совершенно эмпирическія; онѣ цѣнны тѣмъ,
что вкратцѣ и нерѣдко даже довольно точно выражаютъ большое число
наблюденныхъ чиселъ, замѣняя собою цѣлыя таблицы; далѣе онѣ даютъ
возможность находить значенія р для температуръ, промежуточныхъ между
тѣми, при которыхъ были дѣлаемы наблюденія. Онѣ такимъ образомъ
служатъ для интерполированія, но ими нельзя пользоваться для экстра-
полированія, т.-е. для опредѣленія р при такихъ і, которыя лежатъ внѣ
изслѣдованнаго промежутка температуръ.
Существуетъ далѣе не малое число формулъ теоретическихъ,
математически выведенныхъ. Но ихъ раціональными назвать нельзя, ибо
ихъ выводъ основанъ или на допущеніяхъ, завѣдомо лишь приблизительно
вѣрныхъ, или на эмпирическихъ выраженіяхъ какихъ-либо другихъ
величинъ, отъ которыхъ оказывается возможнымъ перейти къ величинѣ р.
Въ видѣ примѣра можно указать, что форма функціи р = і(I) опредѣля-
ется, если допустить, что пары до самаго насыщенія обладаютъ свой-
ствами идеальныхъ газовъ. Точно также видъ функціи р—/(і) опредѣ-
лится, если напр. принять, что величина ро : р, гдѣ р скрытая теплота
испаренія, о удѣльный объемъ паровъ, есть линейная функція темпера-
туры ; а это для многихъ веществъ приблизительно оправдывается. Оче-
Формулы для упругости паровъ. 597
видно, что видъ функціи выведенный на основаніи такого до-
пущенія, слѣдуетъ также считать эмпирическимъ.
Неоднократно старались отыскать такую связь между величинами р
для различныхъ жидкостей, которая дала бы возможность, из-
слѣдовавъ функцію р = /(/) для одной жидкости, опредѣлить ее для всѣхъ
другихъ. Первую попытку въ этомъ направленіи представляетъ такъ наз.
законъ Ва 1 ѣоп’а: упругости насыщенныхъ паровъ одинаковы для
всѣхъ жидкостей при температурахъ, одинаково отстоящихъ отъ нормаль-
ной точки кипѣнія. О г е и Ее^паиіі показали, что этотъ законъ
вообще не вѣренъ; но напр. позднѣйшія изслѣдованія Сг. С. 8 с И т і сИ’а
обнаружили, что для нѣкоторыхъ группъ веществъ этотъ законъ совер-
шенно строго вѣренъ. Такъ для шести кислотъ: муравьиной, уксусной,
пропіоновой, нормальной масляной, изомасляной и изовалеріановой рав-
нымъ измѣненіямъ давленія р соотвѣтствуютъ и совершенно равныя из-
мѣненія температуръ, хотя самыя эти температуры для нихъ различны,
ибо первая изъ названныхъ кислотъ кипитъ при іу = 100°,5, послѣдняя
при і2 = 174°,7. Эти температуры соотвѣтствуютъ /? = 760 мм. При
/>^=10 мм. имѣемъ іу * =— 2°,3 и 2^'= 70°,9. Эти числа даютъ іу— іу =
= 102,8 и 4—= 103,8, что вполнѣ согласно съ закономъ Баі-
і оп’а. Другой примѣръ указанъ Ь а п <1 о 1 Ь’омъ. Для алкоголей законъ
уже не подтверждается, какъ показалъ Сг. С. бсйтійі въ другой ра-
ботѣ, а для веществъ, химически совершенно не родственныхъ, этотъ за-
конъ оказывается вполнѣ невѣрнымъ. Достаточно напр. указать, что
ниже 80° упругость паровъ бензола больше, а выше 80° — меньше упру-
гости паровъ алкоголя.
Повидимому во многихъ случаяхъ гораздо ближе къ дѣйствитель-
ности законъ Биеіігіп^’а, выражающійся формулою
гдѣ іу и і2 температуры, при которыхъ давленія паровъ двухъ веществъ
равны р' = 760 мм., іу и і2 температуры, при которыхъ давленія имѣютъ
любое одинаковое значеніе р; наконецъ д величина постоянная для вся-
кой пары веществъ. По закону Б а 1 і о п’а д = 1 для всѣхъ паръ ве-
ществъ. Если всѣ веншства сравнивать съ водою, то і'2 — 100, и мы имѣемъ
ІОО” V9...........................(1’“)
Б и е 11 г і п § опредѣлилъ д для множества веществъ, сравнивая ихъ
съ водою (д = 1) и нашелъ числа отъ 0,522 (для СО2) до 2,292 (для сѣры).
В а пі 8 а у и V о и п § принимаютъ формулу
т{' = 7^ Г2)...................(2)
гдѣ Т\ и 7\ абсолютныя температуры для одного, Т2 и Т2 — для
другого вещества при давленіяхъ р и р'-, с множитель, вообще весьма ма-
598
Насыщенные пары.
лый. Если с = 0, то, какъ легко видѣть, (2) переходитъ въ (1). Изслѣ-
дованія ВісЬатйзо п’а вполнѣ подтвердили примѣнимость формулы (2).
Е ѵ е г е і 1 (1902) и Р о г 1 е г (1907) теоретически изслѣдовали формулу (2).
Мо8 8 (1903) далъ формулу
1 с
к=т^ь.........................<2-а)
гдѣ Тг и Г2 относятся къ одинаковому давленію р, с и Ъ — постоянныя,
т.-е. не зависятъ отъ р. Въ позднѣйшей работѣ онъ провѣрилъ фор-
мулу (2,(2) для воды и углекислоты и нашелъ, что она вполнѣ под-
тверждается.
Переходимъ къ обзору формулъ, предложенныхъ для выраженія за-
висимости р =/(/); число этихъ формулъ весьма велико, но между ними
можно указать шесть, которыя по разнымъ причинамъ представля-
ются особенно важными; эти формулы мы прежде всего и разсмотримъ.
1. Формула Уоліп§’а (1807); эта формула имѣетъ видъ
р = (а + Ы)ш.......................(3)
съ тремя постоянными а. Ь л т. Тгесі^оісі, Согіоііз, Биіоп^,
Меііеі, РатЪоиг и другіе, указанные Ед'еп’омъ въ обзорѣ, соста-
вленномъ въ 1833 г., пользовались формулой Ѵоип^’а.
2. Формула Косііе’а, предложенная также Аи^изі’омъ, имѣ-
етъ видъ
Р=Р^^СІ.........................(4)
гдѣ /70 упругость при і = О, Ь и с постоянныя числа.
Ведпаиіі также пользовался формулою В о с 11 е’а въ видѣ
1+тх ,л
р = а .а .......................,... (4/2)
гдѣ х=^ + 20. Сіареугоп, Ап^иві, АѴгеде и Ноігітапп
старались вывести формулу В осЬе’а теоретически, но эти выводы
нельзя назвать удачными. Сіаивіиз показалъ, что уравненіе В о с Ь е’а
можетъ быть выведено, если допустить, что пары до насыщенія слѣдуютъ
законамъ Маріотта и Гей-Люссака. Ма^пив выразилъ резуль-
таты своихъ изслѣдованій водяного пара формулою ВосЬе’а, на-
писавъ ее въ видѣ аі
р=р0 , 10Ь *....................(4.6)
гдѣ /?0 = 4,525 мм., а’= 7,4475, 6 = 234.69. Вообще формула Восйе’а
оказывается весьма пригодною; ею пользовались въ различныхъ видо-
измѣненіяхъ Вголѵп и Зайончевскій.
3. Формула Віоі. Въ 1801 г. Ваііоп вывелъ изъ своихъ на-
блюденій, что р растетъ въ геометрической прогрессіи, когда і растетъ
въ прогрессіи ариѳметической. Это приводитъ къ формулѣ р р^аі, от-
Формулы для упругости паровъ.
599
куда 1^/7 = Ь-\-сі. Віоѣ впервые предложилъ другую формулу для 1§7?,
а именно:
\^р = а + Ьа* 4-
. (5)
Этою формулою наиболѣе часто пользовались и пользуются до сихъ
поръ, причемъ весьма часто довольствуются двумя членами, т.-е. при-
Подъ знакомъ подразумѣвается обыкновенный бригговъ лога-
риѳмъ, для практики болѣе удобный, чѣмъ логариѳмъ натуральный. И а с -
сагі и Ра^ііані (1881) и Эсйптанл (1881) показали, что а имѣ-
етъ почти одинаковыя значенія для различныхъ жидкостей.
_Ве§наи11 воспользовался формулою Віоѣ, чтобы выразить ре-
зультаты своихъ многочисленныхъ изслѣдованій упругости паровъ воды
и другихъ жидкостей. Во многихъ случаяхъ Ке^наиіі писалъ фор-
мулу В і о I въ видѣ
\^р = а-\- Ьат . ..... (5,/Э
здѣсь г-~ гдѣ п нѣкоторое число; иначе говоря, г температура, счи-
таемая не отъ 0° шкалы Цельсія, но отъ нѣкоторой другой точки.
Для водяного пара Ве^папН даетъ три формулы:
а) Для і между 0° и 100°:
1§7? = а — Ьа* 4~ .................(6,я)
Числовыя значенія постоянныхъ, данныя Ве^паиіі, были вычи-
слены не вполнѣ вѣрно, какъ показалъ М о г і 1 г (въ Тифлисѣ).
Исправленныя значенія слѣдующія:
а = 4,7393707 = 0,996725536 — 1 = 0,006864937
= 0,611740767 = 0,131990711 — 2.
Ь) Для і между — 20° и 0°
р = а + + ....................(6,/>)
а = — 0,08038 = 0,6024724 — 1 = 0,0333980.
с) Для всѣхъ і отъ 20° до 4" 230°, въ особенности отъ 100° до 230°:
\рр = а — Ьо? + 20 — 20.......................(6,с)
а = 6,2640348 = 0,998343862 — 1 = 0,994049292 — 1
[1^ = 0,6924351
=0,1397743.
Ве^наиН замѣтилъ, что третій членъ формулы (5) большой роли
не играетъ, и что а для всѣхъ веществъ почти одинаковое, а именно въ
среднемъ а = 0,9932. Поэтому Ватѣоіі и Яігассіаіі приняли формулу
1^/7 = а 4“ #(0,9932)*...................(7,&)
600
Насыщенные пары.
которая, какъ оказалось, весьма хорошо выражаетъ результаты 156-ти
различныхъ рядовъ наблюденій.
Формулою Віоі пользовались весьма многіе ученые послѣ Ве&паиіі,
въ томъ числѣ Нате ау и Уоип§, Ваііеііі, 8. Уоип&, Кас-
сагі и Ра&ііапі, Сг. С. 8сЬті<1і, Сггаееі, Зсйптапп, Ьап-
йоіі. Ѵіпсепі и СЬарриіе и др.
Приводимъ еще два примѣра, представляющіе особый интересъ.
Ртуть. К а ш 8 а у и V о и п пишутъ формулу въ видѣ
— а + Ьа* ~ 160-
Въ ней 0 = 4.493745. Ь = - 3.890276, 1§а = 1,9980029.
Вода. Ваііеііі принимаетъ формулу
-- а 4 Ьа* -|-
и находитъ а Ь с ]$$?
отъ —10° до 100° 4,7325067 0,0137486 —4,101985 0,00701402 0,99670488-1
отъ 100» до 200» 6,2998803 —2,190434 —5,015341 0,98524460—1 0,99824205—1
отъ 200» до 364» 6,3210426 - 2,248200 —5,025107 0,98640132—1 0,99824089 1
4. Формула Вегігапй’а. Мы переходимъ къ формуламъ, ко-
торыя были теоретически выведены на основаніи нѣкоторыхъ допущеній
или на основаніи другихъ формулъ, однако, несомнѣнно эмпириче-
скаго характера. Сюда относятся формулы Вегѣгапй'а и формула
Виргё-НеНг’а, которая будетъ разсмотрѣна ниже. Всѣ выводы исхо-
дятъ изъ основной формулы (52) стр. 575, въ которой во всякомъ случаѣ
можно пренебречь величиной 5 сравнительно съ о. Итакъ, мы принимаемъ
» = АТ°Х
(8)
гдѣ 9 скрытая теплота испаренія, б удѣльный объемъ насыщеннаго пара;
способы опредѣленія послѣдней величины будутъ разсмотрѣны ниже. Вег-
ітап(1 даетъ четыре различныя формулы, которыя мы приведемъ, всего
ограничиваясь краткимъ указаніемъ на способъ ихъ вывода изъ формулы (8).
а) Ветітапй находитъ, что для водяныхъ паровъ можно положить
рб = Р(Т-^га) и ц — т пТ. Тогда (8) приводитъ къ выраженію
Для воды «=79,623, 3 = «8,578, #-=126,37 и І0&/< = 34,21083.
Ь) X е и пе г далъ для различныхъ веществъ таблицы величинъ др ^Р-,
&
Для нѣкоторыхъ веществъ д> не очень быстро мѣняется съ температурой.
Если принять д -- гдѣ п постоянное число, то (8) даетъ ігр -- - Т ^Р^
откуда р = КТп.......................(9,6)
ВегііапсІ даетъ значенія К и п для Нр. СО2 и алкоголя.
Формулы для упругости паровъ.
601
с) Для многихъ веществъ можно положить
Арб -г к
се = аТ — о.
9
Такъ напр. для воды д 0,000254758 Г — 0,019131. Формула (8) даетъ
гдѣ К. п и 7, ^ постоянныя числа. Формула (9.с) обыкновенно
и называется формулою В е г 1 г а п (Га Опредѣляя для различныхъ веществъ
п и 2, Вегігапсі замѣтилъ, что показатель п можно мѣнять въ ши-
рокихъ предѣлахъ и. подбирая каждый разъ соотвѣтствующее 2, полу-
чать формулы, почти одинаково хорошо согласующіяся съ результатами
наблюденій. Такъ напр. для водяныхъ паровъ можно принять:
/г=43 50 74 100
2 = 88,3 78,3 56.7 43.2
Понятно, что множитель К также мѣняется вмѣстѣ съ п и 2.
Вегігаікі принялъ для многихъ веществъ и - - 50, т.-е. положилъ
Тогда для 2 получились между прочимъ слѣдующія числа:
2 2 Л
Вода . . . . 78,3 Л7/3 46,728 80., 49,459
Алкоголь. . . 76 С52 54,784 СО., 35,00
Эфиръ . . . 55.4 ССІІ 61.667 8 134,89.
Для паровъ ртути Вегігапсі даетъ формулу
сі) Для нѣкоторыхъ веществъ оказалось, что формула вида (9,с) тѣмъ
лучше выражаетъ результаты измѣреній, чѣмъ больше принять п. По-
этому Вегігапсі принялъ п --зо, вслѣдствіе чего формула приводится
къ виду 2
р КЮ Т ........
Формулу, тождественную съ (9.с\ предложилъ также Неггшапп
(1879, т.-е. раньше ВегігаікГа).
5. Формула Б иргё-Негіг’а имѣетъ видъ
1^ = Л — іп1%Т П................(10)
гдѣ п и к. постоянныя числа. Ее можно привести къ виду
п
602
Насыщенные пары.
Существуетъ большое число выводовъ этой формулы, причемъ числа
т и п различно выражаются черезъ другія физическія величины; фор-
мулу (10) нерѣдко называютъ еще формулою Вапкіпе’а. Она получа-
ется, если предположить, что насыщенный паръ удовлетворяетъ законамъ
Маріотта и Гей-Люссака, и что скрытая теплота испаренія о есть
линейная функція температуры. Итакъ мы полагаемъ
рс> = /?7; д = а—^Т........................(Іі#)
гдѣ /? постоянная формулы Сіареугоп’а для идеальныхъ газовъ. Фор-
мула (8) даетъ, если подставить б и о,
АТ^РЛр а — р 1 — ,, р аі
или (ір а (іі @ (іі р^АРТ*~АР Т ’ Принимая /3 V АР с -с СР . ... . (11,6) а а п = . ~ = /4/? Ср сѵ
(для идеальныхъ газовъ АЦ=ср — сѵ, см. (4,с) стр. 451), получаемъ фор-
мулу (10), причемъ (11,«) и (11.6) указываютъ на физическое значеніе
величинъ т и п; к постоянное.
Негіг далъ другой выводъ этой формулы. Онъ исходитъ изъ вы-
раженія
Оі = Д(о— ...............(12)
для внутренней энергіи испаренія, см. стр. 533. Мы имѣли далѣе
формулу (38,а) стр. 554, которую можно написать въ видѣ
Оі = Оі — (С—сѵ ) (Г — ТА.......................(12,а)
гдѣ С теплоемкость жидкости, сѵ теплоемкость пара при постоянномъ
объемѣ. Пусть Т' температура нормальнаго кипѣнія (при р -
= 760 мм.); введемъ величину
А = р- + (С— сѵУГ...........................(12,6)
тогда (12,а) даетъ
... ... (12, с)
Вводя (12,с) въ (12), пренебрегая величиною 5, и вводя б изъ ра-
венства рб = получаемъ уравненіе, интегралъ котораго имѣетъ видъ
(10), причемъ
С С Ср
АЦ Ср сѵ
А Ь
АР ср сѵ
. (12,а)
Формулы для упругости паровъ.
603
Аналогичную формулу можно вывести для упругости р' пара твер-
даго вещества и затѣмъ найти отношеніе р: р'; такимъ способомъ най-
дены числа, приведенныя на стр. 573.
Пользуясь формулою (ДО), Н е г і 2 вычислилъ тѣ упругости р па-
ровъ ртут и, которыя были указаны на стр. 595. Другіе выводы фор-
мулы (10) дали СгіЬЪз, Л. Л. ТЬотзоп, Вегігапд, КігсййоП и
Краевичъ (1891).
Хотя выводъ формулы (10) основанъ на равенствѣ ро = /?Г, допу-
стимомъ только при малыхъ р, все же оказывается, что она весьма хо-
рошо выражаетъ результаты наблюденій, если на нее смотрѣть, какъ на
формулу эмпирически ю. т.-е. если опредѣлять постоянныя к, т и п
на основаніи результатовъ самыхъ наблюденій. На это было указано
СгиІсіЬ ег^’омъ, В егігапсГомъ, Вагпв’омъ и др. Ветігапсі пока-
залъ ея приложимость къ 16-ти парамъ, изслѣдованнымъ Ее^паиіі.
В а іи 8 выразилъ формулою (10) результаты своихъ наблюденій надъ упру-
гостою паровъ 5, О/, 7,п и Ві. Онъ нашелъ, что т для нихъ одинаковое.
ЛиИизЪиг^ег (1900) опредѣлилъ величины к, т и п для 109 ве-
ществъ и показалъ приложимость формулы (10) для многихъ изъ нихъ
до самой критической температуры, (дгаеія (1903) предложилъ замѣ-
нить (10) формулою’
аР^=к т\%Т . .... (12,о
въ которой а малая дробь. Онъ вывелъ эту формулу, замѣнивъ равен-
ство ро — РТ формулою Ѵап-Лег-ДѴааІб’а.
6. Формула X егп8І’а. Въ 1906 году появилась весьма важная работа
Хегпйі’а, въ которой, среди многихъ дрлгихъ результатовъ, дается также
общее выраженіе для р, имѣющее видъ
^ = -4^іг+1-’Я«7'-4ЖГ+6- '• •
Здѣсь Яо, е и С - постоянныя, имѣющія вполнѣ опредѣленное тео-
ретическое значеніе. Положимъ, Я есть теплота испаренія. Хегп8І
выводитъ формулу
2 = (204-3.5Г еР)
гдѣ л критическое давленіе; эта формула опредѣляетъ величины Я}
и е. С представляетъ собою постоянную интегрированія; мы ближе не
входимъ въ обсужденіе ея значенія. Формула (12,^) была приложена
Хегп8іомъ иЬеѵу (1909) къ/72О, Вгі1Гемъ(1906) къ Л773и Раіск’омъ
(1908) къ СІ.
Изъ множества другихъ формулъ упомянемъ немногія.
₽ г о п у . . р = ааі -|- Ьр* -|- г/ .
Ке88Іег . ,\^р = а—У.
604
Насыщенные пары.
О и 1 Ь+сі+<1і2 + еіі+/іі
В госіі . . . 1и=й4- г
' 1 +
(а =0,0036675).
В
А п 1 о і п е . . 1е?р = А
° і с
1956
Для воды . . 1§’р = 5,4310
Эта формула хорошо выражаетъ результаты наблюденій Саіііеіеі и
Соіагйеаи. Богаевскій показалъ, что формула Апіоіпе’а мо-
жетъ относиться только къ парамъ, которые до насыщенія слѣдуютъ за-
конамъ ЛІаріотта и Гей-Люссака.
1 с
Загоііпек. Т =а-\-Ьр4-\- .
I 5
Для воды . . . і — 8 Ц- 97р4 ? .
,т Іі #\4 ГЛ
При оолыпихъ р получается формула /? = І I, которую 14ир ег-
пау далъ для водяныхъ паровъ.
Тйіезеп (1899) вывелъ для во сы эмпирическую формулу
(/+ 273) = 5.409 а 100) 0,508 . ІО-31365 // 2654 (12./)
содержащую въ себѣ лишь двѣ постоянныя, такъ какъ 100° представляетъ
собою температуру кипѣнія при р — 760 мм., а 365° критическую темпе-
ратуру (265 = 365 —100). Неппіп^ (1907) показалъ, что эта формула
прекрасно согласуется съ наилучшими измѣреніями.
Дальнѣйшія формулы предложили сіе Нееп, ОегЬег, Бііішаг
и Еалѵвііі, Иплѵіп, Рісіеѣ, 8сЫепіпе11ег и др.
Нѣкоторые ученые предложили формулы, связывающія упругость
р и удѣльный объемъ о насыщенныхъ паровъ.
Вапкіпе предложилъ для водяныхъ паровъ формулу
17
іб
р(5 ,
X е и п е г:
р<У'= С,
гдѣ для водяныхъ паровъ /х = 1,0646, С = 1,7049.
Другія формулы дали Сіссопе, АѴіпкеІтапп и Апіоіпе.
Ріапск, Сіаивіиз и МахѵѵеП показали, что если для не-
насыщеннаго пара извѣстно уравненіе состоянія р = Р(ѵ, то можно
найти зависимость упругости насыщеннаго пара отъ температуры.
§ 7. Зависимость упругости насыщеннаго пара отъ формы по-
верхности жидкости и отъ внѣшнихъ силъ, дѣйствующихъ на эту по-
верхность. АѴ. ТІ10Ш8 0П (Ьогсі Кеіѵіп) показалъ въ 1870 г., что
упругость насыщеннаго пара должна зависѣть отъ формы поверхности
Упругость насыщенныхъ паровъ.
605
жидкости. Если при данной температурѣ упругость пара надъ плоской
поверхностью жидкости равна р, и надъ кривой равна ръ то
. <5а / 1 1 \ ,
А— Р + о <5ІД + /?2)......................(131
гдѣ О плотность жидкости, д плотность пара (относительно воды), а по-
верхностное натяженіе (т. I), и /?2 радіусы кривизны двухъ главныхъ
нормальныхъ сѣченій, считаемые положительными, если они направлены
во внутрь жидкости.
Формула (13) показываетъ, что у пру гость пара надъ выпук-
лою поверхностью больше, а надъ
вогнутою меньше, чѣмъ надъ по- Рис* 177'
верхностью плоскою.
Существуетъ больпюе число различныхъ
выводовъ формулы (13). Ограничиваемся про-
стѣйшимъ выводомъ. Вообразимъ себѣ подъ ко-
локоломъ, изъ подъ котораго выкачанъ воздухъ
(рис. 177), сосудъ съ жидкостью и въ ней вер-
тикально установленную капилярную трубку,
въ которой жидкость поднимается на высоту
А до горизонтальной плоскости АВ. Упру-
гость пара, которая равна р у самой поверх-
ности СІ), должна уменьшаться по мѣрѣ удаленія вверхъ отъ этой по-
верхности, подобно тому, какъ плотность воздуха уменьшается при уда-
леніи вверхъ отъ поверхности земли. Если р упругость пара на
уровнѣ АВ, то
р = р' 4- Ад.......................(14)
гдѣ <5 средняя плотность пара между СО и ДВ, и слѣд. А<5 вѣсъ столба
пара, давящаго на единицу поверхности. Упругость пара рг внутри
трубки надъ вогнутою поверхностью непремѣнно должна равняться р'. Въ
противномъ случаѣ были бы возможно регреілішп шоЬіІе. Дѣйствительно,
еслибы мы имѣли рг> р , напр. рг=р, то въ рг происходило бы непре-
рывное испареніе; паръ опускался бы внизъ и сгущался бы на поверх-
ности СІ), вдоль трубки мы имѣли бы непрерывное теченіе жидкости
снизу вверхъ, которое могло бы служить источникомъ работы. На это
можно возразить, что испареніе въ I и сгущеніе на СО вызвало бы охлаж-
деніе жидкости въ Е и выдѣленіе тепла въ СР, а это имѣло бы слѣд-
ствіемъ уменьшеніе рг и увеличеніе р, а слѣд. и р . Но такъ какъ СО
и Е соединены жидкимъ столбомъ, то въ результатѣ получилось бы тече-
ніе теплоты отъ СО къ С, и потому испареніе въ Е все-таки не могло
бы прекратиться, равновѣсіе было бы невозможно. По той же причинѣ
не можетъ быть рг < р'. Итакъ мы имѣемъ рг = р\ т.-е., см. (14),
&!= р Ид
(15, а)
Полное давленіе, испытываемое горизонтальною плоскостью СР,
606
Насыщенные пары.
должно быть одинаково внѣ и внутри трубки; въ этомъ заключается ги-
дростатическое условіе равновѣсія жидкости. Поверхностное давленіе Р
жидкостей опредѣляется формулою Ьаріасе’а (т. I.)
гдѣ К давленіе на плоской поверхности. Внѣ трубки имѣемъ слѣд. пол-
ное давленіе подъ поверхностью СО, равное р-\-К', внутри трубки оно
равно рг-\- НО Р, гдѣ О плотность жидкости. Приравнивая эти давле-
нія, вставляя Р, и сокращая на К, имѣемъ
Ру—р — НО ............. (15,/Л
Опредѣлимъ к изъ (15,а) и вставимъ въ (15,6); получается фор-
мула (13).
Въ данномъ случаѣ Р± и отрицательны, т.-е. направлены въ про-
странство надъ жидкостью, и слѣд. р{ <ір. Когда жидкость не смачива-
етъ стѣнокъ трубки, АВ расположено ниже СО, и поверхность жидкости
въ трубкѣ выпуклая; тогда имѣемъ рх > р.
Другіе выводы формулы (13) V/. Тііотзоп’а дали АѴагЬиг^,
Н. Неітііоііг (сынъ), Б. Б. Голицынъ, Еііг^егаісі, Зіеіап и
В и 11 е т. На поверхности жидкаго шарика, радіусъ котораго Р,
имѣемъ, пренебрегая въ знаменателѣ величиной д сравнительно съ
упругость пара
, 2ад
р<=р + ок
. (іад
Для водяного шарика а = 7,6 мгр. на 1 мм. (т. I); полагая 0 — 1,
имѣемъ при среднихъ температурахъ <5 = 0.000017. Это даетъ
Рі Р =
0.00026
Р
(15, (Р)
гдѣ Р должно быть выражено въ миллиметрахъ, а избытокъ давленія
рг— р получается въ миллиметрахъ водяного столба. Формула
(15,(Р) показываетъ, что при Р = 1 мм. избытокъ давленія пара у поверх-
ности шарика надъ давленіемъ у плоской поверхности равенъ примѣрно
0,0003 мм. воды или 0,00002 мм. ртути. Для капель, изъ которыхъ со-
стоятъ облака, можно положить примѣрно Р — 0,01 мм.; для нихъ р±
-/7 = 0,03 мм. воды. Если діаметръ капель равенъ длинѣ волны свѣто-
вого луча средней части спектра, то получается примѣрно рг—р—1 мм.
водяного столба. Изъ этихъ примѣровъ видно, что рг- р вообще вели-
чина весьма малая. Съ повышеніемъ температуры <5 увели-
чивается, но зато а уменьшается. При критической температурѣ
<5 = О; формула (13) показываетъ, что равновѣсіе возможно только при
а = 0 и р1= р, что и подтверждается опытомъ, какъ увидимъ ниже.
Упругость насыщенныхъ паровъ
607
Формулы (15л) и (15.6) даютъ при =/?2=— /?
(16)
, _ 2а
(О 6)7?
Въ т. I мы имѣли формулу, которая получается изъ (16) при 6=0.
Изъ формулы (13) вытекаетъ рядъ слѣдствій, показывающихъ, что замѣ-
чательный фактъ, открытый XV. Т Ь о т 8 о п’омъ, долженъ играть не мало-
важную роль въ нѣкоторыхъ явленіяхъ природы. Вообразимъ огромное число
весьма малыхъ жидкихъ капель различной величины, напр. облако, струю
водяного пара, жидкій налетъ при сгущеніи пара (напр., если дохнуть на
холодное стекло); чѣмъ меньше капля, тѣмъ больше упругость ея пара и
потому малыя капли должны поглощаться большими, должно
произойти уравниваніе величины капель. В. Неішііоііг указываетъ на
такой фактъ: если на стеклѣ образовался тонкій налетъ осѣвшаго пара
и между каплями есть нѣкоторыя размѣра большаго, чѣмъ остальныя, то
вокругъ нихъ образуется кольцо сухой поверхности: большая капля по-
глотила сосѣднія малыя капли.
Роль такого поглощенія наименьшихъ капель въ струѣ пара указали
1 1 Т Ьот8 оп и Воск, основываясь на интересныхъ наблюденіяхъ
В. Н е 1 ш Іі о 1 і г’а и Аііке п’а надъ видомъ струи пара. Я. Т Іі о т 8 о п
указалъ на роль пылинокъ при осажденіи пара, послѣ того какъ В. Неіш-
11 о 112 нашелъ, что при отсутствіи пылинокъ упругость пара можетъ во
много разъ (до 10-ти!) превысить предѣльную, безъ сгущенія пара въ
жидкость. Дѣло въ томъ, что зародыши капель не могутъ образоваться
изъ пара, ибо у нихъ упругость пара весьма велика. Около пыли-
нокъ же образуются сравнительно большія капли, для которыхъ упругость
пара мало отличается отъ нормальной. Сгущеніе пара пористыми гигро-
скопическими веществами объясняется тѣмъ, что упругость насыщеннаго
пара внутри тончайшихъ каналовъ, наполненныхъ жидкостью, меньше,
чѣмъ въ свободномъ воздухѣ.
Явленіе, открытое XV. Т Іі о ш 8 о п’омъ, должно играть важную роль
при кипѣніи жидкостей, разсмотрѣнномъ на стр. 524. Оно прекрасно объ-
ясняетъ роль введеннаго въ жидкость пузырька воздуха. Въ очень ма-
лыхъ пузырькахъ, т.-е. около сильно вогнутой жидкой поверхности,
упругость пара значительно уменьшена, а потому въ абсолютно чи-
стой жидкости зародыши пузырьковъ и вовсе образоваться не могутъ.
Віонсііоі и XV а г Ъ и г показали, что электрическое поле
должно вліять на упругость насыщеннаго пара. Положивъ, р есть упру-
гость пара внѣ электрическаго поля, р' — упругость на наэлектризован-
ной поверхности, о — электрическая плотность, Н — сила поля на по-
верхности, такъ что Н = — 4 зга (т. IV). Далѣе, пусть 6 — плотность
пара, О — плотность жидкости. Въ такомъ случаѣ, по Віопсііоѣ,
, 2ло26 Н2д
р-р = -~о =-
. . (16,6)
608 Насыщенные пары.
Такимъ образомъ р' <ір. Ооиу (1909) однако показалъ, что эта
формула должна быть замѣнена болѣе точною
Я2 / д \
р'~р = .............(1"'с)
Здѣсь К — (іі электрическая постоянная (т. IV) пара. Для многихъ паровъ
эта формула должна давать р'^> р\ въ ней К — 1 и <5 = О малыя дроби.
ВиЬеш (1890) и Ко епі^зЬег^ег (1898) показали, что упру-
гость пара магнитной жидкости уменьшается подъ вліяніемъ ма-
гнитнаго поля.
Проф. Н. Ы. Шиллеръ въ Кіевѣ обобщилъ результатъ, найден-
ный Тйопі вопомъ и Віопдіоі. Онъ показалъ, что всякая сила /,
дѣйствующая на поверхность раздѣла жидкости и пара, сверхъ давленія
К. существующаго при горизонтальной поверхности, должна вліять на
упругость пара р, дѣлая ее равной гдѣ вообще
Рі = р + д/..........................(17)
гдѣ, какъ выше, д плотность пара, О плотность жидкости. Для случая
кривой поверхности / есть положительное или отрицательное прпра-
/ 1 , 1 \
щеніе нормальнаго давленія, и равно а о т п Ь гакъ что (ДЗ) полу-
\Яі А?2/
чается, какъ частный случаи формулы (17) Шиллера. Своеобразный
выводъ этой формулы далъ К и с т я к о в с к і й.
Н. Н. (Пиллеръ указалъ на новый, весьма замѣчательный случай
примѣненія формулы (17), а именно, когда / есть парціальное давленіе
какого-либо газа, примѣшаннаго къ парамъ. Газъ, давящій на по-
верхность жидкости, долженъ увеличить упругость пара,
онъ долженъ какъ бы выдавливать паръ изъ жидкости. 11. 11. Шил-
леру удалось (1896) произвести рядъ опытовъ, доказывающихъ, что
испареніе жидкости ускоряется давленіемъ газа на ея поверхность. Ока-
залось, что при давленіи сжатаго до 115 атм. воздуха испарялось при
данной температурѣ и въ данномъ объемѣ почти въ 2,9 раза больше
эфира и почти въ 2,4 раза больше хлороформа, чѣмъ когда давленіе воз-
духа равнялось 1 атмосферѣ.
Интересные опыты И. II. Шиллера объясняютъ тѣ явленія ра-
створенія жидкостей и твердыхъ тѣлъ въ сжатыхъ газахъ, которыя наблю-
дали Наина у и Но^агіЬ (1880), Саіііеіеі (1880) и Ѵіііаг (1(1896).
§ 8. Вычисленіе удѣльнаго объема и плотности насыщенныхъ па-
ровъ. Удѣльный объемъ о и плотность д насыщенныхъ паровъ могутъ
быть измѣрены различными способами, съ которыми мы познакомимся
ниже. Кромѣ того о можетъ быть вычислено на основаніи формулы
Удѣльный объемъ и плотность паровъ.
609
ем. (25,с) стр. 550, въ которой Е механическій эквивалентъ теплоты, р
скрытая теплота испаренія, р упругость насыщеннаго пара, если послѣднія
двѣ величины для даннаго вещества хорошо изучены. З7дѣльнымъ объемомъ
5 жидкости можно пренебречь. Величина о представляетъ (стр. 550)
у б ы в а го щ у ю функцію температуры. Для водяныхъ паровъ р и р,
л йр ~ _
а слѣд. и хорошо извѣстны, и Сіаизтз вычислилъ значенія вели-
чинъ б для различныхъ температуръ между 58°,21 и 144°.74, для кото-
рыхъ б было опредѣлено опытами ЕаігЬаігп’а и Таіе’а.
Прежде (умали, что пары до насыщенія слѣдуютъ законамъ М а -
р і о т т а и Гей-Люссака, т.-е. что ихъ плотность Л относите* л ь и о
воздуха при одинаковыхъ съ нимъ давленіяхъ р и температурахъ і,
есть величина постоянная, равная той плотности 40, которая получается
для сильно перегрѣтыхъ паровъ однимъ изъ способовъ, разсмотрѣнныхъ
въ т. I. или на основаніи теоретической формулы
д — 28,88Л0,
гдѣ ц молекулярный вѣсъ пара. Для водяныхъ паровъ /х = 17,9, слѣд.
Д = 0,622.
Найдемъ выраженія для б и <5, предполагая, что пары до
насыщенія слѣдуютъ законамъ Маріотта и Гей-Люс-
сака, т.-е. что Л — Д. Такъ какъ общепринято подъ о подразумѣвать
объемъ въ куб. метрахъ, занимаемый однимъ килограм-
момъ пара, то мы должны принять 6 равнымъ числу килограммовъ,
которые вѣситъ куб. метръ пара. Если О число килограммовъ, которые вѣситъ
куб. метръ воздуха при давленіи р паровъ, насыщенныхъ при 1°, то. оче-
видно. <5 = /)Д. Но если = 1,293 есть число килогр., которые вѣситъ
куб. метръ воздуха при 0° и 760 мм., то
&оР
760(1 -|- аі)
1,293 X 273р
7607'
= 0,4645
Р
Т’
гдѣ Т абсолютная температура; отсюда
е килогр.
<5 = 0.4645 %° ................(19)
/ куб. метр.
Обратная величина равна
Т куб. метр.
0= 2,1528 . ..... (20)
рДо килогр.
Здѣсь р упругость пара, насыщеннаго при абсолютной температурѣ
Г, въ мм. ртути. Сравненіе величинъ о, найденныхъ по формулѣ (20),
съ найденными изъ опыта рѣшаетъ вопросъ о томъ, слѣдуютъ ли пары
до насыщенія законамъ М а р і о т т а и Гей-Люссака. Сдѣлаемъ та-
кое сравненіе. Для водяного пара Д= 0,622 и слѣд.
с р килогр.
й = 0.2889 .
Т куб. метр.
Т куб. метр.
6 = 3.4611
р килогр.
КУРСЪ ФИЗИКИ О ХВОЛЬСОНА. т. III, изд. 3-е.
39
610
Насыщенные пары.
Найдемъ о при /"=100°, т.-е. 7 = 373, /7 = 760. Подставляя, полу-
чаемъ б — 1,70. Итакъ, если бы водяной паръ при 100° слѣдовалъ закону
Маріотта до давленія въ 760 мм., т.-е. до насыщенія, то одинъ кгр.
занималъ бы объемъ б въ 1,70 куб. метра. Въ дѣйствительности однако
б меньше, а именно (по йеипег’у) б = 1,65. Отсюда слѣдуетъ, что
плотность Л относительно воздуха больше ^— 0,622, а именно
Л = К70 0,622=0,641.
1,65
С Іа и8іи8 даетъ такія значенія для плотности Д насыщеннаго во-
дяного пара относительно воздуха :
і = 0° 50° 100° 150° 200°
Д = 0,622 0,631 0,645 0,666 0,698.
Другіе наблюдатели находятъ менѣ^ быстрое возрастаніе величины
Д съ температурою, но во всякомъ случаѣ при всѣхъ температурахъ
не равно -Ло. При низкихъ температурахъ получается од-
нако плотность насыщеннаго пара, весьма мало отли-
чающаяся отъ теоретической плотности /10 пара, весьма
далекаго отъ насыщенія Отсюда слѣдуетъ, что при сравнительно
низкихъ температурахъ пары до насыщенія весьма мало отступа-
ютъ отъ законовъ Маріотта и Гей-Люссака. Непосредственные
опыты Оіеіегісі подтвердили, что при 0° пары воды до насыщенія
слѣдуютъ закону Маріотта. Изъ всего сказаннаго слѣдуетъ, что удѣль-
ный объемъ о насыщенныхъ паровъ можно лишь въ исключительныхъ
случаяхъ вычислять по формулѣ (20); гдѣ возможно, слѣдуетъ б вычи-
слять по формулѣ (18).
§ 9. Опытныя опредѣленія плотности и удѣльнаго объема насыщен-
ныхъ паровъ. Разсмотримъ важнѣйшіе способы измѣренія величинъ <5 и б.
1. Способъ ЕаігЬаігіГа и Таіеа (1861). Остроумный прин-
ципъ, на которомъ основанъ этотъ способъ, будетъ понятенъ изъ схема-
тическаго рис. 178. Два шара А и В соединены трубкой, содержащей
ртуть. Оба шара удерживаются при одинаковой температурѣ і, которая
медленно повышается. Шаръ А, объемъ V котораго извѣстенъ, содер-
житъ опредѣленное вѣсовое количество Р испытуемаго вещества; въ
шарѣ В заключается произвольное, но значительно большее количество
того же вещества. Упругость пара одинаковая въ обоихъ шарахъ, пока
пары насыщены. При нѣкоторой температурѣ і вся жидкость въ А испа-
рится, наполняя объемъ въ этотъ моментъ давленія р въ А и В еще
одинаковы. Но при самомъ маломъ дальнѣйшемъ повышеніи температуры
паръ въ В оказывается вновь насыщеннымъ, а паръ въ А ненасыщен-
нымъ (перегрѣтымъ), ибо въ В произошло новое испареніе, чего въ Л, гдѣ
уже нѣтъ жидкости, произойти не можетъ. Въ этотъ моментъ давленіе
въ В получаетъ перевѣсъ и столбъ ртути начинаетъ перемѣщаться отъ
В къ А. Опредѣляя температуру і въ тотъ моментъ, когда ртуть начи-
наетъ перемѣщаться, мы будемъ знать, что при /° вѣсовое количество Р
Удѣльный объемъ и плотность паровъ.
611
Насыщеннаго пара занимаетъ объемъ V. Выражая V въ куб. метрахъ,
Р въ килограммахъ, получаемъ пару сопряженныхъ значеній величинъ I и
V
б=р...............................(21)
Мѣняя количество Р жидкости въ А, мы получимъ различныя I и о.
ЕаігЬаігп и Таіе построили приборъ, въ которомъ сосудъ А
находился внутри сосуда В; этотъ приборъ изображенъ въ разрѣзѣ на
рис. 179. Къ металлическому сосуду В, снабженному манометромъ О и
термометромъ /, придѣлана длинная, внизу закрытая стеклянная трубка оо.
Внутри сосуда В находится стеклянный шаръ А, отъ котораго идетъ
внизъ стеклянная трубка, открытая снизу,
доходящая почти до нижняго конца труб-
ки оо. Обѣ трубки содержатъ нѣкоторое
количество ртути, уровни которой во вну-
тренней трубкѣ а, въ наружной Ь. Со-
судъ А содержитъ извѣстное вѣсовое ко-
личество Р, сосудъ В большое количество
воды, для паровъ которой РаігЪаігп
и Т а 1 е опредѣляли о. Трубка С содер-
житъ масло, сосудъ И песокъ. Для на-
грѣванія прибора служила горѣлка И и газовая труба съ отверстіями, три
раза спирально обходившая нижнюю часть сосуда В (см. рис. 180); каждое
отверстіе давало маленькое пламя, служившее для нагрѣванія. Уровень
а ртути наблюдался издали при помощи зрительной трубы; одновременно
наблюдалась и постепенно повышающаяся температура на термометрѣ і.
Остальное понятно изъ предыдущаго изложенія. Приходилось отмѣчать
температуру і для момента, когда ртуть въ а начинала подниматься и
когда слѣд. все количество Р воды наполняло объемъ V въ видѣ насы-
щеннаго пара.
Для температуръ ниже 100°, РаігЪаіп и Таіе пользо-
вались приборомъ, изображеннымъ на рис. 180 и основаннымъ на совер-
шенно другомъ началѣ. Трубка оо внизу открыта; она закрывается
каучуковой пробкой, черезъ которую проходитъ внутренняя трубка //, при-
паянная къ шару А; К сосудъ съ ртутью, въ которую опущены концы
обѣихъ трубокъ. Сосудъ А, объемъ котораго V, содержитъ вѣсовое ко-
личество Р воды, сосудъ В почти наполненъ водою, температура которой
измѣряется термометрами і и і4. Для нагрѣванія всего прибора служатъ
горѣлка И и спиральная горѣлка еее. Изъ описанія понятно, что Аи
представляетъ барометръ, въ пустоту котораго введено количество Р
воды. Если РІ барометрическое давленіе, й высота ртути въ оо надъ уро-
внемъ въ К, Іг4 давленіе (въ мм. ртутнаго столба) воды, находящейся въ
оо надъ ртутью, то упругость р насыщеннаго пара опредѣляется изъ ра-
венства р — Н И — И4. Упругость р насыщеннаго пара, какъ функція
температуры была извѣстна изъ опытовъ Не^паиіѣ Повышая посте-
39*
612
Насыщенные пары.
пенно температуру / и наблюдая непрерывно даввленіе парар, РаігЬаігп
и Таѣе получили рядъ чиселъ, совпадавшій съ числами Ке^паиіі до
нѣкотораго опредѣленнаго начиная отъ котораго упругости пара вне-
Рис. 1«о.
запно дѣлались меньше чиселъ, данныхъ Ве^паиН. Это показывало,
что выше этого і пары переставали быть насыщенными, и что при этомъ
і вѣсовое количество Р пара какъ разъ насыщало объемъ И ГаігЬаі гп
Удѣльный объемъ и плотность паровъ.
613
и Таіе нашли, что объемъ о килограмма пара въ куб. метрахъ, какъ
функція упругости р. выраженной въ мм. ртутнаго столба, равенъ
1257,605
а = 0,02562 + .................(22)
р + 18,29
Сопоставляемъ числа для б, найденныя ЕаігЬаігп’омъ и Та -
1 е’омъ, съ числами, которыя найдены С1 а и 8 і и 8’омъ на основаніи фор-
мулы (18), и съ числами, которыя получаются по формулѣ (20), основан-
ной на доп) іценіи. что пары до насыщенія слѣдуютъ законамъ М а р і о т т а
и Геи- Л ю с с а к а, т.-е. обладаютъ постоянною плотностью Л — Ло — 0,622
относительно воздуха.
і Р а і г Ъ а і г п и Таіе. Вычислено. 1 С1 а и 8 і и 8. Формула (18) Закины Маріотта и Гей-Люссака. Формула (20)
Набл. Формула (22)
58°,20 8,27 8,18 8,23 8,38
70,75 4,92 4,90 4,83 4,94
92,65 2,15 2,12 2.11 2.18
124,16 0,759 0,758 0,769 0,809
134,86 0,584 0,562 0,569 0,602
144,74 0,432 0,428 0,437 0.466.
Эти числа показываютъ, что
выражаетъ результаты наблюденіи.
формула (22) дѣйствительно хорошо
Далѣе видно замѣчательное согласіе
между величинами, теоретически
вычисленными на основаніи фор-
мулы (18), и наблюденными; на-
конецъ, послѣдній столбецъ пока-
зываетъ, что законы Маріотта
и Гей-Люссака къ насыщен-
нымъ парамъ не приложимы.
11. Способы Регоі. Въ
1888 г. появилась работа Регоі,
измѣрявшаго б двумя способами.
Способъ первый. Мѣд-
ный сосудъ Е (рис. 181) помѣ-
щается въ ванну, нагрѣваемую до
опредѣленной температуры. Че-
резъ трубку і выкачиваютъ изъ
него воздухъ. Внутри него помѣ-
щается стеклянный шаръ В съ
вытянутымъ горлышкомъ п запа-
янный стеклянный цилиндрикъ Л,
наполненный испытуемой жид-
Рис. 181.
костью. При нагрѣваніи прибора цилиндрикъ лопается и весь сосудъ,
а слѣд. и шаръ В наполняется насыщенными парами. Черезъ нѣкого- *
рое время запаиваютъ кончикъ а вытянутой трубки, пропуская силъ-
614
Насыщенные пары.
при температурѣ і объемъ V шара.
^ = 68°,2 88°,6 98°, 1
б = 5,744 2,531 1,782
ный электрическій токъ черезъ проволоку, окружающую этотъ кончикъ.
Взвѣшивая затѣмъ шаръ В, легко опредѣлить вѣсъ Р пара, насыщающаго
Способъ второй. Сосуды
В и А (рис. 182) соединены кра-
номъ /?; В содержитъ испытуемую
жидкость; сосудъ А можетъ быть
соединенъ съ воздушнымъ насосомъ.
Весь приборъ помѣщается въ про-
странство опредѣленной темпера-
туры /. Сперва /? закрыто ; че-
резъ 5 выкачиваютъ воздухъ. За-
тѣмъ закрываютъ 5 и открываютъ /?,
причемъ А наполняется парами. Да-
лѣе закрываютъ Р и черезъ 5 вытя-
гиваютъ пары, заставляя ихъ прохо-
дить черезъ сосудъ, наполненный
веществомъ, поглощающимъ пары.
Всю манипуляцію можно повторить
много разъ. Взвѣшивая сосудъ, по-
глотившій пары, можно найти вѣсъ
Р паровъ, насыщающихъ при /° объ-
емъ V сосуда А
Для водяныхъ паровъ Р е -
гоі находитъ:
99°,6 101°,6 124°,1
1,657 1,583 0,766.
Для паровъ э ф и р а:
^=28°,4 30°,0 31°,7 31°,9 57°,9 85°,5 110°,5
п = 0,4262 0,4000 0,3751 0,373 0,168 0,0778 0,0439.
Р е г о і воспользовался числами, найденными для о, чтобы на осно-
ваніи формулы (18) ’ вычислить механическій эквивалентъ те-
плоты; онъ получилъ Е — 424,63. Величины онъ измѣрялъ не-
посредственно весьма остроумнымъ способомъ, котораго мы не можемъ
разсматривать.
III. Способъ 8. Тоип^’а. Начиная съ 1891 г., стали поя-
вляться опредѣленія величины о для различныхъ жидкостей, произведен-
ныя 8. I о п п ^'омъ по новому способу; ограничиваемся схематиче-
скимъ указаніемъ на сущность этого способа. Стеклянная запаянная
трубка содержитъ жидкость и ея пары. Нижнюю часть вертикально уста-
новленной трубки удерживаютъ при нѣкоторой температурѣ і, верхнюю
часть, содержащую паръ и часть жидкости — при болѣе высокой темпе-
ратурѣ Т. Производятъ два наблюденія, при которыхъ различно великія
Удѣльный объемъ и плотность паровъ.
615
части жидкости находятся при температурѣ і. Напримѣръ, въ первомъ
опытѣ (іа (рис. 183) при /°, ас при Т>\ во второмъ (іа' при /°, а'с
при 7°. Уровни жидкости различны: въ первомъ опытѣ Ь, во вто-
ромъ — Ь'. Довольно сложная формула, которой мы не приводимъ, да-
етъ возможность найти отношеніе удѣльныхъ объемовъ о и 5 пара и
жидкости при Г0. У о и п § окружалъ нижнюю часть (іа или
(і'а трубою, черезъ которую протекала вода, а верхнюю ас или
а'с трубою, черезъ которую пропускались пары какой-либо ки-
пящей жидкости.
Въ многочисленныхъ новыхъ работахъ (1909, 1910)
8. У о и п д показалъ, что для многихъ паровъ вблизи нор-
мальной точки кипѣнія (р = 760 мм.) можно положить
о — а + ...........(22,а)
IV. Способъ СаіПеіеѣ и М а I Ь і а 8’а. Назван-
ные ученые опредѣляли плотность <5 относительно воды
при 4° насыщенныхъ паровъ закиси азота, этилена, углекис-
лаго газа и сѣрнистаго гава, сгущая газъ въ калибрирован-
ной трубкѣ въ жидкое состояніе. Уменьшая постепенно да-
вленіе, они отмѣчали моментъ, когда послѣдній слѣдъ жидкости
исчезалъ. Зная объемъ I/, занимаемый паромъ въ этотъ мо-
ментъ, и его вѣсъ Р, они могли найти д. Для опредѣленія
плотности (і жидкости они пользовались приборомъ, изображен-
нымъ на рис. 184. Сильнымъ охлажденіемъ они перегоняли
въ А столбъ жидкости; разность уровней ртути въ Л и В
давала возможность найти б/, когда <5 извѣстно. Они нашли для
азота между — 28° и -ф- 33°,9
Рис. 184.
закиси
б = 0,5099 — 0,00361/ — 0,0714 4 36,4 — /;
для этилена между — 30° и + 8°,9
д = 0,1929 — 0,00188/ — 0.0346 /9,2 — Г;
для СО2 между — 29°,8 и + 30°.2
д = 0,5668 — 0,00426/ — 0,084 V31 — /;
для 5О2 между -ф- 7°,3 и 154°,9
/° = 7,3 24,7 58,2 78,7 100,6 135,0 154,9
<5 = 0,00624 0,0112 0,0310 0,0464 0,0786 0,1888 0,4017.
V. Способъ Ваиег’а. Вайет опредѣлялъ (1895) плотность
насыщенныхъ паровъ, измѣряя п о т е р ю вѣса металлическаго полаго
шара, погруженнаго въ эти пары. Онъ изслѣдовалъ пары воды, эфира,
хлороформа, алкоголя, 8О2 и ССІ±. Для паровъ воды Вайет нахо-
дитъ слѣдующія плотности Л относительно воздуха (см. стр. 609) при
упругостяхъ р (въ мм. ртути):
р — 500 580 660 700 760
4 = 0,630 0,637 0,643 0,646 0,650.
616
Насыщенные пары.
VI, Способъ изслѣдованія изотермъ. Сущность этого
способа изложена на стр. 584, и тамъ же было указано, что онъ приво-
дитъ къ опредѣленію упругости р и удѣльнаго объема а насыщеннаго
пара при данной температурѣ. Сюда относятся изслѣдованія Нетлѵі^’а,
ХѴиеІІпег’а и Стгоігіап’а, Ваѣѣеііі, Ата^аі, 11 а т 8 а у и
Ѵоип^’а, 8сЬ.оор’а и др. Мы возвратимся къ нѣкоторымъ изъ этихъ
работъ, когда будемъ разсматривать свойства ненасыщенныхъ па-
ровъ, изслѣдованіе которыхъ составляло главный предметъ этихъ работъ.
Теперь укажемъ лишь на нѣкоторые результаты, относящіеся къ парамъ
насыщеннымъ.
Неглѵі^ вывелъ изъ своихъ наблюденій, что если р0 и ѵ0 упру-
гость и удѣльный объемъ пара, далекаго отъ насыщенія, и потому слѣ-
дующаго закону Маріотта, р и о тѣ же величины для пара насы-
щеннаго, Т та абсолютная температура, къ которой относятся вели-
чины Ръ и р и и, то
=0,0595 1 7’....................(22,а)
причемъ множитель 0.0595 одинъ и тотъ же для всѣхъ веществъ и для
всѣхъ изотермъ, т.-е. при всѣхъ Т.
Опыты АѴиеПпег’а и Сггоігіап’а, ВсЬоора и др. показали,
что формула Н е г і ^’а несправедлива. АѴ и е 11 п е г и Сггоігіап
нашли для паровъ воды, эфира и сѣроуглерода значенія о весьма близ-
кія къ тѣмъ, которыя вычисляются но формулѣ (18). Для паровъ воды
они нашли:
/0 = 80,1 90,1 99,8 110,39 119,50 134,58
о набл. = 3,400 2,352 1,666 1,207 0,885 0,580
о вычисл. = 3,380 2,343 1,655 1,197 0,883 0,577
0,6325 0,6388 0.6481 0,6437 0,6594 0,6605
Они находятъ, что до давленія 2-хъ атмосферъ можно принять
Л = Л^сѴТ.........................(23)
Но здѣсь с различно для различныхъ веществъ, а именно для хло-
роформа с — 0,0550, для эфира с — 0,0576, для сѣроуглерода с — о,0572,
для воды (только до 1 атм.) с = 0,0536. 8сНоор, наоборотъ, находитъ
с = 0,0595 для многихъ веществъ при нѣкоторыхъ Т. Когда Т растетъ,
коеффиціентъ с уменьшается. Регоі нашелъ, что формула Неглѵі^'а
справедлива для паровъ воды между 68°,2 и 110°,5. ВаііеПі даетъ
слѣдующія значенія и и А для водяного пара:
і = 14°,91 27,15 57,01 78,52 99,6о 130,32 182,90 231.41
о = 80,311 39,53 8,739 3,63 1,690 0,6615 0,1876 0,0724
Л = 0,6273 0,6286 0,6298 0,6302 0.6338 0,6376 0,6568 0,7056.
В а і і е 11 і находитъ, что формула Н е г і §’а должна быть за-
мѣнена формулою вида
Удѣльный объемъ и плотность паровъ.
617
РпѴ° = л V Т (аТЬ V
рб \ 1 Г-а ’
гдѣ Л, а, Ь и а постоянныя числа.
VII. Отчасти другими способами или измѣненіями разсмотрѣнныхъ
пользовались Аѵепагіиз, Б. Б. Голицынъ, Ногвітапп,
А п 8 б е 11 и др.
Б. Б. Голицынъ нагрѣвалъ данное вѣсовое количество Р жид-
кости въ запаянной трубкѣ и наблюдалъ температуру въ тотъ моментъ,
когда послѣдняя капля жидкости исчезаетъ. Зная объемъ V трубки,
легко найти б.
Большой интересъ представляютъ результаты измѣреніи АпзйеІГя
надъ НСІ, 8. Топика надъ 8пСІ±, ССЦ, С^Н^ Вашзау и Ѵоип^’а
и БаИеПі надъ эфиромъ (этиловымъ) и этиловымъ алкоголемъ. Уоищц’а
надъ метиловымъ алкоголемъ и т. д.
Исключительный интересъ представляютъ п а р ы у к с у с н о й к и с -
лоты, плотность которыхъ при низкихъ температурахъ и далеко отъ
насыщенія больше теоретической. Въ этомъ парѣ мы имѣемъ сложныя
молекулы, которыя при повышеніи температуры распадаются. Этимъ
объясняется, почему^ плотность 4‘ (относительно Н - 1) сперва убываетъ,
а потомъ растетъ. Приводимъ нѣкоторыя числа В а ш 8 а у и Уопп^’а
(1886) и Ѵоипя’а (1891):
і о А 1 б' Л'
20° 13,08 59,3 220° 0,0329 53,5
50 3,326 55,0 250 0,0193 56,5
100 0,546 50,95 280 — 67,1
150 0,142 ( 50,06 | (тіпітит) 300 0,00581 83,1
200 0,0487 51,06 321,65 (крит. темп.). 0,00246 137,7.
Въ заключеніе упомянемъ о такъ называемомъ з акон ѣ и а р а. -
болы, на который указалъ МаіЬіаз. Если за абсциссы принять тем-
пературы, а за ординаты плотности (і жидкости и б насыщеннаго пара, то
получаются двѣ кривыя АС и ВС (рис. 185), которыя встрѣчаются въ
нѣкоторой точкѣ С, соотвѣтствующей критической температурѣ (рисунокъ
относится къ СО2). Геометрическое мѣсто срединъ хордъ, параллельныхъ
оси ординатъ, есть прямая СО, нѣсколько наклоненная къ оси аб-
сциссъ. Вся линія АСВ повидимому мало отличается отъ параболы.
Зуйпеу То ип ц (1900) показалъ, что законъ параболы дѣйстви-
тельно подтверждается для многихъ веществъ; затѣмъ Бачинскій по-
казалъ. что этотъ законъ можетъ быть выведенъ и теоретически на осно-
ваніи формулы Ѵап сіег ѴѴааІй’а. Укажемъ на нѣкоторыя слѣдствія,
выведенныя изъ этого закона М аі Ііі а з’омъ. Положимъ у = ~ (б -[ сі)
есть ордината точки прямой ОС; соотвѣтствующая ей абсцисса пусть бу-
618
Насыщенные пары.
детъ Л Координаты С пусть будутъ О и А, т.-е. Л есть критическая
плотность. Абсолютныя температуры, которымъ соотвѣтствуютъ I и Ѳ
пусть будутъ Т и Тс. Уравненіе прямой ОС имѣетъ видъ:
у Л а{Тс — Т)........................(23, а)
Коеффиціентъ а, опредѣляющій наклонъ этой прямой къ оси аб-
сциссъ, всегда весьма малъ и для различныхъ веществъ, измѣняется въ
предѣлахъ между — 0.0005 и —0,0026. Изъ (23,а) слѣдуетъ:
у аТг I т\
л ............<2ЗД
Изъ ученія о соотвѣтственныхъ, состояніяхъ (гл. ХШ § 9) должно
слѣдовать, что величина.
имѣетъ одно и то же значеніе для всѣхъвеществъ.
Однако МаіЬіая показалъ, что число а для весьма многихъ ве-
ществъ близко къ 1, но для нѣкоторыхъ имѣетъ гораздо меньшія значе-
нія, именно, для трудно сжимаемыхъ газовъ. Такъ напримѣръ, для кис-
лорода а = 0,713, для азота а = 0,685, для водорода даже а = 0,236. Въ
новой работѣ Маійіаз (1905) находитъ, что величина
а
ь= Ѵ7С
(23, сі')
въ гораздо большей степени, нежели величина а, имѣетъ постоянное
значеніе для всѣхъ веществъ. МаіЬіаз предлагаетъ разбить всѣ ве-
Теплоемкость паровъ.
619
щестра на серіи (вещества съ приблизительно одинаковымъ значені-
емъ Ь) и на группы (вещества съ приблизительно одинаковымъ сі).
Въ послѣдней своей работѣ МаіЬіае (1909) находитъ для этилена
при температурахъ отъ - 23,75° до Д- 32,93° уравненіе діаметра у —
= 0,25431 — 0,00064/. Далѣе, а = 0,850, Ь 0,493. Для СО2 Ь = 0,489,
такъ что, очевидно, этиленъ и СО2 принадлежатъ къ одной серіи.
§ 10. Теплоемкость с насыщенныхъ паровъ. Мы имѣли (стр. 550)
двѣ основныя формулы (25,б?) и (25,6):
..............(24)
Й + с-- = 7.............................<*»
въ которыхъ о скрытая теплота испаренія, о и 5 удѣльные объемы на-
сыщеннаго пара и жидкости, р упругость насыщеннаго пара при темпе-
ратурѣ Т = I Д- 273, С теплоемкость жидкости и с теплоемкость
насыщеннаго п а р а, т.-е. количество теплоты, потребной. чт< >бы
1 кгр. пара, насыщеннаго при /° и занимающаго нѣкоторый объемъ о,
перевести въ паръ, н а с ы щепный при (/Д-1°), и занимающій м е н ь -
шій объемъ о'. При этомъ переходѣ паръ долженъ быть сжатъ внѣш-
ними силами, причемъ въ немъ выдѣляется нѣкоторое количество те-
плоты, нагрѣвающей его отъ до (^ Д- т°). Смотря по тому, имѣемъ ли
мы г < 1, г — 1 или г >> 1, получается с >> 0, с = 0, с < 0. Этотъ во-
просъ былъ подробно разсмотрѣнъ на стр. 551, когда мы ввели вели-
чину с. Итакъ, теплоемкость насыщенныхъ паровъ с мо-
жетъ быть величиною отрицательною. На стр. 552 мы ука-
зали на замѣчательныя слѣдствія:
Если с > 0, то насыщенный паръ при сдавливаніи отчасти сгуща-
ется въ жидкость; при расширеніи онъ дѣлается перегрѣтымъ.
Если с = 0, то паръ при сдавливаніи и при расширеніи остается на-
сыщеннымъ.
Если с<0, то паръ при сдавливаніи дѣлается перегрѣтымъ; при
расширеніи онъ отчасти сгущается въ жидкость.
Формулы (24) и (25) даютъ возможность вычислить с, что и было
сдѣлано Сіапві ііз’омъ и ііапкіпе’омъ (1850), открывшими, что те-
плоемкость насыщеннаго водяного пара есть вели-
чина отрицательная. Формула (25) даетъ
С-С+1-4..........................(26)
Если ввести полную теплоту испаренія, см. (12) стр. 538,
і
Х = )'сМ--\-о..................(27)
О
то получается _ <Гл ц /осЛ
620
Пас ыщонные пары
оолѣе точную формулу (16,а), вмѣсто которой
формулу о = 607 0,7082е, см. (18) стр. 539.
получаемъ:
к 6 0 7 - 0.7082е
с 0,305 — - , .
Для воды І{ епа и 11 далъ выраженіе 2= 606,5 Д- 0,305/ (стр. 539),
откуда ^ = 0.305. Для о мы имѣли (стр. 539): о = 606,5 0,695/ или
С1 а и 8 і и 8 предложила»
Вставляя о и 2 въ (28),
..................(29)
Это даетъ ”г *
І = 0° 40° 80° 100° 120° 160 200°
С = — 1,908 1,538 1,250 — 1,130 1,021 0.832 — 0.675.
Величины с не только отрицательныя, но и сравнительно весьма боль-
шія, ибо теплоемкости всѣхъ веществъ, кромѣ воды и водорода, меньше
единицы. Съ повышеніемъ температуры теплоемкость с у в е л и ч и в а -
ется, приближаясь къ нулю. Если бы можно было пользоваться фор-
мулою (29) и при большихъ /, то чы получили бы с = 0 при /= 520°.
Но такое заключеніе недопустимо, ибо изслѣдованія 1) п Ь е т’а и М а -
(Ьіаз’а показали, что при критической температурѣ слѣду-
етъ принять
с = эс ...........................(30)
Для воды критическая температура 365°, а потому значеніе с = 0
для водяныхъ паровъ врядъ-ли существуетъ.
Весьма важно, что формула (24) даетъ подобныя же отрицательныя
числа для с. Изъ нея получается
г . ду Л/ др
с С+л-Л0-ІІЛ.
или, если вставить 2 и пренебречь объемомъ 5.
дк я др
ді ді
др
Вставляя сюда изъ опытовъ КеоапИ. низъ опытовъ В а і г-
01 1 лз
. . , Г11 , л 1 ак
о а і г п а и 1 а I е а, А и = 0,305, получаемъ слѣдующія числа:
і - 55°, 21 77,49 92,65 117,17 131,77 144,74
с = 1,40 1.26 1,21 1,02 -0.90 0.81
ѴѴ и е 11 п е г выражаетъ результаты опредѣленій К е п а и 1 і вели-
чины 2 другою эмпирическою формулою и получаетъ для с
с=1— *'°Д4 — 0.001246Г
Эта формула не даетъ вовсе с>0: она даетъ максимальное значе-
ніе с— 0,736 при 697° и затѣмъ уменьшеніе с при і >697°.
Всѣ вычисленія с весьма недостовѣрны. Такъ Саііепйаг (1901)
Теплоемкость паровѣ
(>2І
получилъ для воды рядъ значеній с. изъ которыхъ мы приводимъ нѣ-
которыя :
1 = 00 20° 40° 60° 100° 140° —180° —200°
г = —1,680 —1,502 —1.351 — 1,223 1.028 0,895 — 0,801 - 0,750.
Эти числа значительно отличаются отъ вычисленныхъ С1 а и 8 і и з’омъ
и приведенныхъ выше. Если вычислять с для различныхъ веществъ,
пользуясь формулой (25). то оказывается, что всѣ изслѣдованныя веще-
ства можно раздѣлить на три гр} п пы. Для первой группы въ пре-
дѣлахъ температуръ, доступныхъ при опытахъ, с < 0, для второй с > 0.
для третьей с мѣняетъ знакъ, переходя отъ отрицательныхъ значеній къ
положительнымъ. Если выводъ Виііет’а и Маііііаб’а. см. (ЗОѢ вѣренъ,
то вещества третьей группы должны имѣть с - -- 0 при двухъ темпера-
турахъ, вещества второй группы по крайней мѣрѣ при одной температурѣ.
Первая группа: с < 0. Сюда относится, какъ мы видѣли, вода,
далѣе сѣроуглеродъ и ацетонъ.
Ведпаиіі даетъ для сѣроуглерода С = 0,23523 4- 0,0001630/,
2 = 90,00 4- 0,14601/ — 0.0004123/2. Отсюда :
/ 0° 40° 80°
100° 120° 150°
С= —0,183 0,160 0,143 0,140 0,137
0.132.
Для ацетона
С = 0,50643 4-0,000793/; 2 = 140,50 4-0,3664/ <».0о0516/2; эти фор-
мулы щютъ:
і= 0° ІО° 80° 100° 140°
с— 0.146 —0.100 0.065 - 0,051 0,040.
Около / = 20о° можно ожидать с- 0. А И (1903) находитъ, что
с <С 0 для насыщенныхъ паровъ кислорода и азота.
Вторая группа: с>0. Сюда относится этиловый эфиръ
(С4//10О), для котораго Ке^паиіі даетъ С — 0,52901 4~ 0,0005916/,
2 = 94,00 0,4500/— 0,0005556/2. Формула (25) даетъ
/= 0° 40° 80° 120°
С = 4-0,106 4-0,120 4-0.128 4-0,133.
При нѣкоторой низкой температурѣ (около 120°) можно ожи-
дать с - 0.
Третья группа: с мѣняетъ знакъ при легко достижимой тем-
пературѣ г. Сюда относятся бензолъ, ч е т ы р е х х л о р и с т ы й угле-
родъ, хлороформъ и, вѣроятно, а л к о г о л ь.
Для бензола:
/= 0° 40 80 112 120 160
С = —0 155 0,087 —0,040 0,000 4- 0,009 Д-0,052.
622
Насыщенные пары.
Для СС14:
1 = 0° 40 80 120 127 160
С-= -0,044 -0,026 0,012 0,002 0,000 + 0,006.
Для хлороформа:
і- 0“ 40 80 120 125 160
с = 0.108 0.065 0.031 0,003 0,000 4-0,020.
Всѣмъ этимъ числамъ большого значенія придавать нельзя, и ихъ
слѣдуетъ считать лишь приблизительно вѣрными.
Для алкоголя перемѣна знака величины с происходитъ около 135°.
Ѵап (Iег ЛѴааІз (1878), основываясь на своемъ уравненіи состо-
ср
янія, нашелъ, что с > 0, когда к = 1,07 и г<0, когда к >* 1,08.
сѵ
Ваііоп (1907) приходитъ къ иному заключенію. Если ко - ср\сѵ
для идеальнаго газоваго состоянія, то с < о для всѣхъ температуръ, если
к0> 1,202. Если-же к0> 1,202, то съ возрастаніемъ температуры сна-
чала 0, затѣмъ с^> 0 и наконецъ снова О Такимъ образомъ, величина
с мѣняетъ дважды знакъ. Полагая, что
выше приведенныя для Н2О, С82, эфира,
хлороформа, бензола и СС/4 числа вѣрны,
то мы можемъ сказать, что если на-
сыщенные пары воды или сѣ-
роуглерода внезапно сжать,
то они должны сдѣлаться не-
насыщенными или перегрѣ-
тыми; если же ихъ расширить, то часть паровъ должна
сгуститься въ жидкость.
Насыщенные пары эфира должны отчасти сгуститься при сжатіи
и сдѣлаться ненасыщенными при расширеніи. Пары хлороформа, бен-
зола и СС/4 должны обладать свойствами паровъ воды при темпера-
турахъ ниже 125°,’. 127° и 112°, а при болѣе высокихъ температурахъ,
должны обладать свойствами паровъ эфира.
Опыты Нігп’а и Саяіп’а вполнѣ подтвердили этотъ замѣчатель-
ный выводъ теоріи. Нігп наполнилъ цилиндръ, снабженный стеклянными
основаніями, парами воды при высокомъ давленіи; когда былъ открытъ
кранъ, выпускавшій паръ наружу, то внутри цилиндра замѣчался густой
туманъ: часть пара при расширеніи сгущалась. Далѣе Нігп изслѣдо-
валъ пары С82 и эфира, которые нагрѣвались въ колбѣ К (рис. 186) и
наполняли стеклянный цилиндръ Р, выгоняя воздухъ черезъ кранъ Л, ко-
торый затѣмъ закрывался. Когда поршень находился у праваго конца
цилиндра, Нігп быстро вдавливалъ поршень во внутрь цилиндра. При
этомъ пары С82 оставались прозрачными, пары эфира, наоборотъ, давали
туманъ, какъ того требуетъ теорія.
Сахіп наблюдалъ расширеніе паровъ при выпусканіи ихъ изъ ци-
Теплоемкость паровъ.
623
линдра, снабженнаго стеклянными основаніями, и кромѣ того сжатіе и рас-
ширеніе паровъ въ цилиндрѣ, соединенномъ съ другимъ цилиндромъ,
порптень котораго можно было быстро перемѣщать въ ту или другую сто-
рону. Эти опыты вполнѣ подтвердили результаты наблюденій Нігп’а
надъ парами воды и эфира. С а г і п изслѣдовалъ также пары бензола и
хлороформа и нашелъ, что при нѣкоторыхъ температурахъ образовывался
туманъ, когда пары расширялись, между тѣмъ какъ при сжатіи пары оста-
вались прозрачными. При болѣе высокихъ температурахъ наблюдалось
явленіе противоположное. Саяіп вывелъ изъ своихъ наблюденій, что
с 0 для хлороформа при 130° и для бензола при 120°, что мало отли-
чается отъ температуръ, вычисленныхъ на основаніи теоріи.
Водяной паръ, расширяясь въ цилиндрѣ паровой машины, отчасти
переходитъ въ жидкое состояніе.
Опредѣлимъ, какая часть [і вѣсовой единицы паровъ,
насыщенныхъ при абсолютной температурѣ Го, остается
въ видѣ пара, если произойдетъ адіабатическое рас-
ширеніе, понижающее температуру пара отъ Го до Т. Мы
имѣли формулу (44,Ь) на стр. 557 для случая адіабатическаго измѣненія
состоянія смѣси жидкости и пара:
= ....................(31)
гдѣ С теплоемкость жидкости, К постоянное число. При Т— Го имѣ-
емъ о — р0 и /х = 1, слѣд.
К=С18Т0 + ^..........................(32)
7 О
Такимъ образомъ извѣстно; затѣмъ (31) даетъ искомое /і.
Для воды С = 1, слѣд.
/< = 1ё70+ еА,
1 о
И 1^=0
у
Вставляя К, находимъ окончательно
= т )....................(33)
9\7 о Т)
Для другого пара получаемъ болѣе общую формулу
= ...................................(34)
Ро \ 1 о 1 /
Эта формула вполнѣ рѣшаетъ нашу задачу Приведемъ нѣсколько
примѣровъ, данныхъ В е г 1 г а п (Ромъ.
1) Водяной паръ насыщенъ при 150° (70 123), р0 = 500,78 ; найти /г
для различныхъ і до /=40°(7" -313).
(і-24
Насыщенные пары.
^=150° 130° 110° 90° 70° 50° 40°
= 1 0,9640 0,9283 0,8927 0,8571 0,8221 0,8041.
2) Водяной паръ насыщенъ при 200° ( Го = 473. д(}= 464,3);
найти /х для различныхъ і до /- 100° (Т= 373).
і -200° 180° 1600 140° 120° 100°
ц = I 0,9692 0,9387 0,9083 0,8780 0,8476.
3) Паръ эфира насыщенъ при 40° (70 —=313); найти для раз-
личныхъ температуръ / до /=120°, получающихся при сжатіи па-
р<)в ь. 1 Іолу чаются числа
/=40° 60° 80° 100° 120°
// = 1 0,8651 0,7109 0,5313 0,3169.
Формула (31) даетъ возможность рѣшить и многія другія задачи, от-
носящіяся къ случаю, когда въ начальномъ состояніи /х не равно еди-
ницѣ. Приведемъ еще одна изъ интересныхъ задачъ, рѣшенныхъ Вегі-
г а п (Томъ.
4) Дана вѣсовая единица воды при 200°; ей даютъ испариться,
вслѣдствіе чего она охлаждается. Найти /х при различныхъ температу-
рахъ смѣси. Въ этомъ случаѣ начальное значеніе /хо = О и слѣд. К
1§:Г0; (31) даетъ
гдѣ /’о = 173. Получаются числа :
/ = 2000 10(р 50о 0о
/х 0 0,0944 0,1651 0,2156 0,2474.
Вода охладится до 0°, прежде чѣмъ четверть ея испарится.
Намъ остается сказать о замѣчательныхъ работахъ МаіЬіаъ’а, ко-
торый впервые (1896) путемъ опыта показалъ, что с можетъ быть
величиною отрицательною. Ему удалось калориметрически измѣрить ко-
личество д тепла, потребнаго для нагрѣванія насыщеннаго пара 8О2 отъ
20° до /° при условіи сохраненія насыщенности. Очевидно
аі
Опыты дали для д отрицательныя значенія. Оказа-
лось, что с<0 при 20°; далѣе с растетъ и при 97°,5 получается с— -О;
при 106° с достигаетъ положительнаго максимума, затѣмъ с уменьшается
и при /=114° опять с = о. Выше 114° теплоемкость отрицательная и
по абсолютному значенію быстро возрастаетъ. При критической темпе-
ратурѣ (156°) должно, по мнѣнію Маійіаз’а, получиться с = ос,
какъ было сказано выше. Его изслѣдованія скрытой теплоты р
испаренія жидкихъ СО2, 80% и Л/2О привели его къ заключенію,
что при критической температурѣ і' не только р = О, но и^ =
Аі
Теплоемкость паровъ
625
= - - оо, т.-е. что кривая д = пересѣкаетъ ось і подъ прямымъ угломъ.
Отсюда, и на основаніи формулы (25), М а IИ і а 8 и заключаетъ, что при
/=/' должно быть с ——30.
§ И. Теплоемкость ср насыщенныхъ паровъ. Мы вывели фор-
мулу (17.с), стр. 501, которую можно написать въ видѣ
~ . до , д . б 8 / х
ср ~ср+ді~^®• • • • • (35)
Если приложить ее къ случаю испаренія, то ср есть теплоемкость на-
сыщеннаго пара, нагрѣваемаго при постоянномъ давленіи, при-
чемъ онъ перестаетъ быть насыщеннымъ; къ тому же слу-
чаю нагрѣванія относится величина дб, гдѣ б удѣльный объемъ насы-
щеннаго пара; Ср теплоемкость жидкости, @ скрытая теплота испаренія,
5 удѣльный объемъ жидкости. Приложимъ эту формулу къ насыщеннымъ
парамъ воды при 100°. Ріапск подставляетъ слѣдующія числа (при-
нимаемъ килограммъ и куб. метръ за единицы вѣса и объема): Т = 373,
6^ = 1,03, р = 536, Ст — — 0,708 (изъ чиселъ Ве^паиН для 100°), 5 =
= 0,001, =0,000001; далѣе онъ пользуется наблюденіемъ Н^ігп’а,
который нашелъ, что 1 килогр. насыщеннаго водяного пара занимаетъ
при 100° объемъ въ 1,6504 куб. метра и что при нагрѣваніи (при
/7 = Соп8І.) до 118°,5 объемъ возрастаетъ до 1,740 куб. м. Это даетъ б —
= 0,00484. Подставляя эти числа, по-
лучаемъ для насыщенныхъ паровъ воды при 100°
Ср = 0,47.
Непосредственныя измѣренія Ве^паиіі дали Ср = 0,48.
ТЬіевеп (1902) вычислилъ ср, а также ср для насыщенныхъ во-
дяныхъ паровъ, пользуясь формулою (35) и формулою (33,я) стр. 468.
Онъ находитъ: ср = 0,4655 при 0°; при 80° величина ср имѣетъ мини-
мумъ, равный 0,415; при 180° получается уже Ср = 0,51.
Кегпзі Ц909) вычислилъ сѵ совершенно'инымъ путемъ. Для сред-
ней молекулярной теплоемкости водяного пара между 0° и 80° онъ нахо-
дитъ число 8,19. Если это число раздѣлить на молекулярный вѣсъ воды (18),
то получается ^ = 0,455
для температуры, близкой къ 40°.
§ 12. Законъ ВаІІОП’а. Въ т. 1 мы познакомились съ закономъ
Ваііон’а, поскольку онъ относится къ смѣсямъ газовъ, химически не
дѣйствующихъ другъ на. друга. Въ примѣненіи къ насыщеннымъ парамъ
этотъ законъ гласить: упругость р насыщеннаго пара въ
пространствѣ, содержащемъ индифферентный, т.-е. хи-
мически на паръ недѣйствующій, газъ, такая же, какъ
КУРСЪ ФИЗИКИ О. X в О Л ь С О Н А. Т. III, изд. 3-е. 40
= 1,6504, И = 1.»0-М504
\ді ]р 18,5
626
Насыщенные пары.
въ пустотѣ. Разница въ томъ, что въ пустотѣ жидкость испаряется
и упругость р достигается мгновенно; въ пространствѣ же, содержащемъ
газъ, та же упругость достигается черезъ продолжительный промежутокъ
времени. Это легко объясняется медленностью диффузіи паровъ въ про-
странствѣ, содержащемъ газъ.
ВаНоп (1803) произвелъ рядъ опытовъ для подтвержденія этого
закона. Онъ оставлялъ нѣкоторое количество воздуха въ закрытомъ ко-
лѣнѣ сифоннаго барометра, устроеннаго на подобіе прибора ІІге (стр. 585,
рис. 166), п измѣрялъ его упругость; затѣмъ онъ вводилъ въ простран-
ство надъ ртутью нѣкоторое количество жидкости и измѣрялъ то наи-
большее значеніе упругости, котораго пары жидкости достигали черезъ
достаточно продолжительное время. Другіе опыты онъ производилъ съ
приборомъ, изображеннымъ на рис. 187. Черезъ крышку большого со-
суда проходятъ трубка сифоннаго барометра 7И, трубка воронки В, снаб-
женная краномъ и трубка С, соединенная съ воздушнымъ насосомъ. Весь
приборъ можетъ быть погруженъ въ теплую вод}.
Въ воронкѣ В находится испытуемая жидкость. Вы-
качавъ часть воздуха изъ большого сосуда, ВаНоп
открывалъ на короткое время кранъ В, причемъ нѣ-
которое количество жидкости падало на дно этого
сосуда. Давленіе паровъ измѣрялось увеличеніемъ
длины ртутнаго столба отъ М до А. Оно оказыва-
лось равнымъ тому давленію, которое устанавлива-
лось мгновенно, когда въ сосудѣ предварительно по
возможности былъ выкачанъ воздухъ.
Непгу (1804) и Оау-Еивзас (1815) по-
вторили опыты Ваііоп’а и подтвердили его за-
конъ. Приборъ, которымъ пользовался Сгау-Ьи8-
8 а с , былъ впослѣдствіи видоизмѣненъ М а
п и з’омъ, который придалъ ему форму, изображенную
жая, закрытая сверху, тщательно калибрированная
Рис. 187.
на рис. 188.
стеклянная трубка Т вдѣлана въ металлическую оправу, снабженную на
наружной поверхности винтовою нарѣзкою, при помощи которой она мо-
жетъ быть ввинчена въ доску небольшого треножника. Продолженіе оправы
снабжено краномъ г и подъ нимъ расширенною частью, въ которую плотно
вставляется стаканчикъ Сбоку припаяна къ Т длинная трубка 5.
Трубка Т наполовину наполняется ртутью, затѣмъ г закрывается и трубка
ввинчивается въ треножникъ. Приливая ртути въ 5, можно добиться
того, что уровни ртути въ 5 и Т будутъ одинаковые. Въ этомъ случаѣ
въ Т находится воздухъ подъ атмосфернымъ давленіемъ. Отмѣтивъ дѣ-
леніе, противъ котораго находится уровень ртути въ Т, вставляютъ въ
трубку подъ г стаканчикъ доверху наполненный испытуемой жидко-
стью. Если теперь на короткое время открыть кранъ г, то нѣсколько ка-
пель ртути попадаютъ изъ Т въ и въ то же время нѣсколько капель
жидкости поднимаются въ Т до пространства, содержащаго воздухъ, гдѣ
Законъ Паііопа.
627
часть ихъ мало-по-малу испаряется. Приливая ртути въ 5, доводятъ
ртуть въ Т до прежняго уровня; при этомъ уровень ртути въ 5 будетъ
выше, чѣмъ въ Г, на величину, измѣряющую упругость насыщенныхъ
паровъ въ воздухѣ.
Ведпаиіі весьма подробно изслѣдовалъ вопросъ о предѣлахъ точ-
ности закона Ваііоп’а. Онъ пользовался приборомъ, который былъ
описанъ на стр. 587 и изображенъ на рис. 171. Опредѣливъ упругость
насыщенныхъ паровъ въ пустотѣ, онъ повторилъ тѣ же измѣренія, оста-
вляя въ шарѣ различныя количества воздуха или другого газа. Кромѣ того
онъ непосредственно соединялъ шаръ А съ манометромъ, въ открытое колѣно
котораго онъ приливалъ ртуть, доводя объемъ газа и пара до той же величины,
которую имѣлъ одинъ объемъ газа ранѣе введенія въ него паровъ, т.-е. когда
трубочка съ жидкостью (см. рис. 172) еще была цѣла. Упругость паровъ измѣ-
рялась слѣд. въ сущности тѣмъ же способомъ, какъ въ приборѣ М а §• п и з’а
(рис. 188). В ера иИ нашелъ, что упругость насыщеннаго пара въ газѣ не-
много меньше, чѣмъ въ пустотѣ. Онъ полагалъ, что эту разность можно объя-
снить вліяніемъ гигроскопичности стѣнокъ трубки, на поверхности которыхъ
сгущается часть паровъ, прежде чѣмъ эти пары успѣли достичь максимальной
упругости. Образовавшаяся жидкость стекаетъ по стѣнкамъ трубки, а изъ
жидкости непрерывно выдѣляются новые пары, медленно диффундируя
черезъ газъ. Ведпаиіі измѣрялъ также количе-
ство паровъ въ газѣ, пропуская ихъ смѣсь черезъ со- Рис. 188.
суды, въ которыхъ происходило поглощеніе паровъ.
Онъ нашелъ, что равной упругости пара въ пустотѣ и
въ газѣ соотвѣтствуетъ и одинаковое его количество.
Объясненіе, данное Ведпаиіі, вполнѣ согласу-
ется съ наблюденіями Н е г лѵ і ^’а, медленно сжимав-
шаго ненасыщенные пары (въ пустотѣ) и замѣ-
тившаго налетъ осѣвшихъ паровъ на стѣнкахъ сосуда ра-
нѣе достиженія наибольшей упругости паровъ; упру-
гость при дальнѣйшемъ уменьшеніи пространства еще
продолжала немного расти.
Позднѣйшіе опыты Ведпаиіі съ этиловымъ
эфиромъ, сѣроуглеродомъ и бензоломъ показали, что въ
нѣкоторыхъ случаяхъ упругость паровъ въ газѣ можетъ
быть значительно меньше, чѣмъ въ пустотѣ. Такъ для
паровъ эфира при 29°,3 въ пустотѣ и въ воздухѣ эта
разность равнялась 36,2 мм., что составляетъ 5,8% всего давленія; упру-
гость сухого воздуха равнялась при этомъ 707 мм.
Малыя отступленія отъ закона Б а 11 о п’а нашли также К г о е п і
(1864), Тгоові и НапЬеіепіІІе (1876), Сгп^ііеіто и Миеіпа
(1887), Вгаип (1888) и др. Послѣдній нашелъ, что въ нѣкоторыхъ
слл чаяхъ давленіе смѣси газа и пара больше суммы давленій газа и
пара, насыщеннаго въ пустотѣ. Надо думать, что отступленія отъ за-
кона Ваііоп’а при не очень большихъ давленіяхъ
628
Насыщенные пары.
газа имѣютъ сложную причину. Помимо несомнѣннаго вліянія стѣнокъ,
сгущающихъ пары, является еще способность паровъ къ пересыще-
нію, обнаруженная многими наблюдателями, въ особенности АѴпеІІ-
пег’омъ и 6ггоігіап'омъ, Катзау и Топп^’омъ, КгеЪз’омъ и
В. НеІтЬоІіг’омъ, указавшимъ на возможность громаднаго пересыще-
нія паровъ въ пространствѣ, не содержащемъ пылинокъ, <> чемъ уже было
упомянуто на стр. 607.
Въ 1890 г. появилось обширное изслѣдованіе В. Б. Голицына о
законѣ I) а 11 о п’а и нѣкоторыхъ другихъ связанныхъ съ нимъ явленіяхъ.
Б. Б. Голицынъ пользовался двумя приборами. Первый представляетъ
длинную и узкую 77-образную трубку, оба конца которой запаяны. Трубка
содержала ртуть и надъ нею въ одномъ колѣнѣ столбикъ жидкости и
только пары послѣдней, а въ другомъ колѣнѣ кромѣ жидкости и ея па-
ровъ еще опредѣленное количество воздуха. Весь приборъ на-
грѣвался до опредѣленной температуры. Если законъ В а 1 і о п’а вѣ-
ренъ, то разность уровней ртути въ двухъ вѣтвяхъ трубки должна была
измѣрять упругость воздуха, которую можно было вычислить, зная коли-
чество воздуха и его температуру. Разность вычисленныхъ и наблюден-
ныхъ давленій указывала на отступленіе отъ закона О а И о п’а. Оказа-
лось, что въ этомъ приборѣ упругость паровъ въ газѣ всегда меньше,
чѣмъ въ пустотѣ. Такимъ образомъ эти наблюденія подтвердили резуль-
таты опытовъ Ке^папіі. Если объясненіе, данное Ве^паиІЬ,
вѣрно, то ясно, что въ длинной тонкой трубкѣ, въ которой диффузія па-
ровъ происходитъ медленно, кажущееся отступленіе отъ закона В а 1 -
іоп’а должно обнаружиться весьма рѣзко. Поэтому Б. Б. Голицынъ
производилъ дальнѣйшія изслѣдованія съ трубкою, изображенною на
рис. 189. Трубка аа имѣетъ длину 1 метръ, внутренній діаметръ 4,6 мм.,
длина трубки ЬЬ 40 см.; она оканчивается широкою частью А, длина ко-
торой 5 см., внутренній діаметръ 3,11 см. Обѣ вѣтви запаяны; онѣ со-
держатъ ртуть и надъ нею столбикъ испытуемой жидкости. Въ верхней
части трубки аа находятся только пары, въ А кромѣ того еще
Рис. 189. воздухъ. Въ этомъ приборѣ вліяніе стѣнокъ должно быть весьма
мало и диффузія паровъ черезъ газъ можетъ происходить быстро.
Опыты съ парами воды показали, что они въ воздухѣ
до 100° вполнѣ удовлетворяютъ закону В а 1 (о п’а. Дальнѣй-
а шія наблюденія надъ эфиромъ и надъ хлористымъ этиломъ, до-
веденныя до 100°, обнаружили нѣкоторое, хотя и не очень зна-
чительное отступленіе отъ закона В а И о п’а, и то при высокихъ
температурахъ. Результаты наблюденій ’ надъ эфиромъ помѣ-
!|д щены въ слѣдующей табличкѣ, въ которой /?0 упругость воз-
Ь духа, р упругость паровъ эфира въ пустотѣ, Д разность
между упругостью р и упругостью паровъ въ А: послѣдній
столбецъ содержитъ величину этой разности, выраженную въ
| Ъ процентахъ самой упругости р, т.-е. величину, опредѣляющую,
насколько паръ отступаетъ отъ закона В а 1 і о п’а.
Гигрометрія.
629
і Ро р 4 100 л р
63°,63 628 мм. 1920 мм. 2,6 мм. 0,1%
77°,97 647 » 2865 » 15,9 » 0,6
99°,80 684 » 4930 » 69.7 » 1,4.
Вліяніе стѣнокъ въ этихъ опытахъ не могло играть роли; отступле-
нія должны быть объяснены особою «задержкою» при испареніи.
Хотя при сравнительно небольшихъ упругостяхъ газа отступленія
отъ закона Ваііоп’а и невелики, но при очень большихъ давленіяхъ
пары, повидимому, вовсе не слѣдуютъ закону О а 11 о п’а. На это ука-
зываютъ замѣчательныя наблюденія Н. Н. Шиллера, о которыхъ
было сказано на стр. 608. Мы видѣли, что при сильномъ давленіи газа
упругость пара дѣлается значительно больше нормальной.
§ 13. Гигрометрія. Предметомъ гигрометріи служитъ, какъ из-
вѣстно, опредѣленіе количества водяныхъ паровъ, находящихся въ дан-
номъ мѣстѣ и въ данное время въ атмосферѣ, напр. въ одномъ куб. ме-
трѣ воздуха. Обыкновенно отличаютъ абсолютную и относительную влаж-
ность. Абсолютную влажность принято опредѣлять числомь
/ граммовъ водяныхъ паровъ, содержащихся въ одномъ куб. метрѣ
воздуха; она, очевидно, равна плотности паровъ относительно воды, по-
множенной на. милліонъ. Подъ относительной влажностью со подразумѣ-
ваютъ отношеніе числа / къ тому числу Р граммовъ пара, которое по-
требно, чтобы довести 1 куб. метръ воздуха при данной температурѣ і
до насыщенія: это отношеніе принято помножать на 100, такъ что от-
носительная влажность
со = 100 ....................(35,а)
показываетъ, сколько наличное количество паровъ составляетъ процен-
товъ отъ наибольшаго возможнаго при данной температурѣ і количества.
Пусть р упругость паровъ и Р наибольшая при /° возможная упру-
гость при насыщеніи; въ такомъ случаѣ можно положить
со =100^..........................(35,0
если допустить, что паръ до насыщенія слѣдуетъ закону Маріотта при
не очень высокихъ температурахъ, что приблизительно вѣрно. Связь
между / и р выражается формулою
х 0,622р 1,0582 .
/=1293 —гр. = ’ , 0 гр. . , . . (36)
7 760(1 + аі) 1 1 4- аіг г ѵ 7
гдѣ 1293 вѣсъ въ граммахъ одного куб. метра сухого воздуха при 0° и
760 мм.; 0,622 плотность водяныхъ паровъ относительно воздуха, р вы-
ражено въ мм. ртутнаго столба, а коеффиціентъ расширенія газовъ.
Формула (36) показываетъ, что числа / и р случайно мало отличаются
630
Насыщенные пары.
другъ отъ друга; при различныхъ і имѣемъ напр. для насыщен-
наго пара:
/О = — 20° —10° 0° 10° 15° 20° 25° 30°
Р мм. = 0,927 2,09 4,60 9,16 12,70 17,39 23,55 31,55
Р гр. = 1,2 2,5 4,8 9,3 12,6 17,0 22.7 30.1.
Около 14° имѣемъ численное равенство Р = Р. а т і п предло-
жилъ (1884) измѣрять влажность отношеніемъ вѣса паровъ къ вѣсу су-
хого воздуха: понятно, что въ этомъ случаѣ имѣемъ
со = 0,622 р Н-р (36, а)
гдѣ Н барометрическое давленіе, однако это предложеніе, повидимому,
не было принято.
Въ дальнѣйшемъ мы будемъ предполагать, что у насъ есть таблицы,
дающія упругость Р и вѣсъ Р для различныхъ температуръ і. Прихо-
дится сказать, что гигрометрія, занимающаяся однимъ изъ важнѣйшихъ
метеорологическихъ элементовъ, играющимъ важную роль также и при
многихъ физическихъ изслѣдованіяхъ, до сихъ поръ ни въ практическомъ,
ни въ теоретическомъ отношеніи не достигла желательной степени со-
вершенства. Если исключить весьма сложный, т. наз. химическій ме-
тодъ опредѣленія влажности, то оказывается, что всѣ другіе нынѣ упо-
требляемые методы не даютъ возможности опредѣлить влажность воздуха
со сколько-нибудь значительною точностью. Причина заключается отча-
сти въ несовершенствѣ приборовъ, отчасти въ недостаточной обоснован-
ности формулъ, служащихъ для вычисленія влажности по даннымъ, по-
лученнымъ изъ наблюденій.
Всѣхъ способовъ опредѣленія влажности или со) существуетъ че-
тыре, а именно: способъ химическій, способъ наблюденія точки росы,
способъ волосяного гигрометра и способъ психрометрическій. Къ разсмо-
трѣнію этихъ способовъ мы теперь и обратимся. Приборы, при помощи
которыхъ производятся измѣренія по первымъ тремъ способамъ, называ-
ются гигрометрами или гигроскопами, а по четвертому спо-
собу — психрометрами.
I. Способъ химическій. Этотъ способъ единственный, да-
ющій точные результаты; онъ основанъ на слѣдующемъ: при помощи
аспиратора заставляютъ нѣкоторый объемъ V наружнаго воздуха медленно
пройти черезъ трубку, содержащую вещество, поглощающее водяные
пары, напр. хлористый кальцій, фосфорный ангидридъ или пемзу, смочен-
ную сѣрною кислотою. Увеличеніе вѣса трубки, опредѣляемаго до и
послѣ опыта, даетъ вѣсъ ср паровъ, находящихся въ объемѣ V. Оче-
видно / — (р : V. Не разсматриваемъ устройства современныхъ двойныхъ
аспираторовъ, дающихъ возможность сколь угодно долго просасывать
воздухъ черезъ трубку. Покажемъ, какъ вычислить объемъ V наруж-
наго воздуха, прошедшаго черезъ трубку и обладавшаго температурой і
Гигрометрія.
631
и абсолютной влажностью /. соотвѣтствующей упругости р пара; баро-
метрическое давленіе обозначимъ черезъ Н. Пусть ѵ0 емкость аспира-
тора при 0°, к коеффиціентъ расширенія его стѣнокъ, и положимъ, что
онт> п разъ наполнился воздухомъ: его температуру обозначимъ черезъ
Въ такомъ случаѣ воздухъ, прошедшій черезъ трубку, занималъ въ аспи-
раторѣ объемъ ѵ = лг’0(1 + который будемъ считать извѣстными.
Этотъ воздухъ находится при температурѣ і'\ онъ въ аспираторѣ насы-
тился парами, максимальную упругость которыхъ при температурѣ і' обо-
значимъ черезъ Р. Упругость чистаго воздуха (безъ паровъ) внѣ аспи-
ратора равна Н — р, внутри аспиратора она равна Н — Р'. По извѣст-
ной формулѣ имѣемъ
Ѵ{Н—р} ѵ{Н- РЭ
1 —сс/ 1 —|— ос/
откуда
Если въ равенство /=#>: V подставить (36) и (37), то получается
1,0582 _ (р Н -р_ 1 -ф- аі’
1 аі ѵ ' Н — Р' 1 -ф- аі
или
= .................(38)
Отсюда получается р\ температуру і наружнаго воздуха знать не
нужно. Химическій способъ, которымъ впервые воспользовался Вгип-
пег (1841), даетъ весьма точные результаты; но онъ сложенъ и не го-
дится для текущихъ наблюденій. Удобный абсорбціонный гигрометръ съ
сѣрной кислотой построилъ Е. ѴѴеЬег въ 1898 г.
П. Способъ наблюденія точки росы. Если охлаждать
атмосферный воздухъ, температура котораго /, то при нѣкоторой темпе-
ратурѣ і' онъ окажется насыщеннымъ водяными парами. Эта темпера-
тура і' называется точкою росы, такъ какъ всякое дальнѣйшее ох-
лажденіе воздуха должно вызвать выдѣленіе росы на окружающихъ тѣ-
лахъ. Если Р и Р' наибольшія количества пара, соотвѣтствующія состо-
яніямъ насыщенія при температурахъ і и і', то относительная влаж-
ность со равна
со = 100 .......................(39)
Г
Сапіот теоретически изслѣдовалъ общій вопросъ объ осажденіи па-
ровъ при ихъ охлажденіи, приложивъ къ этому вопросу принципы термо-
динамики. Онъ нашелъ, что точка насыщенія и точка росы, полученная
изъ наблюденій, тогда только совпадаютъ, когда жидкость, образующаяся
при ожиженіи паровъ, смачиваетъ поверхность тѣла Л, на которой роса
должна появиться. Если же жидкость не смачиваетъ тѣла Л, то точка
632
Насыщенные пары.
росы получается ниже точки насыщенія (/'), которую ищутъ при гигрометри-
ческихъ изслѣдованіяхъ. Такъ при осажденіи водяныхъ паровъ на по-
верхности нефти получалась точка росы при 18°, тогда какъ і' равнялось
21°,2. Сапіог показалъ, что отсюда можетъ быть вычисленъ радіусъ г
сферьГ’частичнаго дѣйствія (т. I), и нашелъ для воды г = 6.5 . 10~5 мм.
Изъ теоріи Саи іо г’а вытекаетъ, что поверхность тѣла (стекла или ме-
талла) на которой наблюдается появленіе росы, должна быть весьма
тщательно вычищена.
Способъ наблюденія точки росы былъ впервые предложенъ Сйаг-
Іев Ье Воу (1771), который охлаждалъ воду въ стаканѣ, прибавляя къ
ней мелкіе кусочки льда, пока на наружной стѣнкѣ стакана не появля-
лась роса. Современное видоизмѣненіе этого .простого прибора предста-
вляетъ гигрометръ Б і п е 8’а.
Гигрометръ ЬапіеІГя, рис. 190, былъ построенъ въ 1827 г. Два
стеклянные полые шара А и В соединены трубкой; шаръ В окруженъ
кисеею, въ А находится шарикъ термометра. Прибо]
качанъ воздухъ, содержитъ эфиръ, который сперва
весь переливается въ А. На кисею наливается эфиръ,
который, испаряясь, охлаждаетъ шарикъ В; тогда въ
В сгущаются пары эфира и давленіе паровъ въ В
дѣлается меньше, чѣмъ въ А. Пары изъ А непре-
рывно переходятъ въ В, вслѣдствіе чего въ А эфиръ,
испаряясь, медленно охлаждается. Наблюдается по-
явленіе росы на наружной поверхности шарика Л,
иногда покрытой позолотой въ видѣ кольца. За I'
принимается температура термометра, находящагося
въ Л, и въ этомъ заключается источникъ большой
погрѣшности, такъ какъ температура внутри эфира,
не подвергаемаго перемѣшиванію, должна значительно
отличаться отъ температуры слоя наружнаго воздуха, прилегающаго къ
шарику А.
Лучшіе результаты долженъ давать гигрометръ Ве^паиіі, изобра-
женный на рис. 191. Онъ состоитъ изъ двухъ стеклянныхъ трубокъ О
и Е, закрытыхъ сверху пробками. Къ нижнимъ открытымъ концамъ при-
крѣплены тонкостѣнныя закрытыя снизу трубочки изъ полированнаго се-
ребра. Трубка Е пустая, въ ней находится только термометръ і. Въ О
находится эфиръ, температура котораго опредѣляется термометромъ Тру-
бочка А, открытая съ двухъ концовъ, оканчивается внизу у дна метал-
лическаго сосуда. Пространство надъ эфиромъ соединено при помощи
трубки В съ аспираторомъ, при дѣйствіи котораго непрерывная струя
воздуха медленно всасывается въ А, поднимается въ видѣ пузырьковъ
черезъ эфиръ и выходитъ черезъ В въ аспираторъ. Эфиръ подвергается
непрерывному перемѣшиванію и испаренію, вслѣдствіе чего температура въ Р
постепенно понижается. Появленіе росы на поверхности металлическаго
сосуда и температура і' наблюдаются издали при помощи зрительной
>, изъ котораго вы-
Рис. 190.
Гигрометрія.
633
трубы. Термометръ і служитъ только для опредѣленія температуры воз-
духа. Металлическіе сосудики оба сразу видны въ трубу, чѣмъ облегча-
ется опредѣленіе момента появленія росы на одномъ изъ нихъ. Дальнѣй-
шія усовершенствованія представляютъ гигрометры АПиагсГа и Сгоѵа.
Гигрометръ АПиагсГа изображенъ на рис. 192. Онъ состоитъ изъ
металлическаго четырехграннаго сосуда, содержащаго эфиръ, температура
Рис 191.
Рис. 192.
котораго измѣряется термометромъ і'. Передняя сторона А сосуда позо-
лочена и полирована; она окружена^пластинкою В, также позолоченной
и полированной, и отдѣленной отъ А узкимъ промежуткомъ. Черезъ
крышку сосуда проходятъ трубки С, О и Е; трубка С оканчивается внутри
сосуда близъ его дна; трубка же О оканчивается подъ самою крышкою
сосуда; Е служитъ для наливанія эфира. Конецъ Н остается откры-
тымъ , конецъ і соединяется каучуковою трубкою съ аспираторомъ. Краны
служатъ для регулированія быстроты теченія воздуха. Роса осаждается
на Л, но не осаждается на пластинкѣ В, которая, оставаясь блестящею,
облегчаетъ наблюдателю замѣтить появленіе росы на А. Пращевой тер-
мометръ і служитъ для опредѣленія температуры воздуха.
Гигрометръ Сгоѵа, рис. 193, состоитъ изъ тонкостѣнной мѣдной,
никкелированной трубки АI/, тщательно внутри полированной. Конецъ ея.
который обращаютъ къ свѣту, закрытъ пластинкой изъ матоваго стекла V;
на концѣ А находится длиннофокусная лупа, черезъ которую хорошо
видны пластинка V и кольцевое изображеніе этой пластинки во внутрен-
ней поверхности трубки. Черезъ трубку ЬѴ заставляютъ медленно про-
ходить воздухъ, влажность ш котораго желаютъ опредѣлить. Для этого
634
Насыщенные пары.
служитъ трубка Г, проведенная въ наружный воздухъ пли въ то пространство,
для котораго требуется найти со, и каучуковая всасывающая груша Р;
такимъ образомъ наблюдатель и приборъ могутъ оставаться внутри зда-
нія, когда опредѣляется влажность внѣшняго воздуха. Трубка ЬѴ помѣ-
щена внутри сосуда В, содержащаго сѣроуглеродъ или эфиръ; воздухъ
Рис. 193.
Рис. 194.
вдувается въ эту жидкость при помощи трубки К и выходитъ черезъ
трубку М; можно также 7И соединить съ аспираторомъ. При этомъ жид-
кость, а слѣд. и воздухъ въ ЬѴ охлаждаются; черезъ лупу Ь наблюда-
ютъ появленіе росы на той части внутренней поверхности трубки ЬѴ, въ
которой видно кольцевое изображеніе пластинки V. Термометръ і' даетъ
температуру, при которой роса появляется.
М 1 р р о 1 (1 устроилъ гигрометръ, въ которомъ роса осаждается на
блестящей поверхности ртути.
ПІ. Волосяной гигрометръ. Существуютъ различные ги-
гроскопы и гигрометры, основанные на измѣненіи формы или размѣровъ
нѣкоторыхъ гигроскопическихъ органическихъ тѣлъ изъ царства живот-
ныхъ и растеній въ зависимости отъ относительной влажности
со воздуха.
Этимъ свойствомъ, повидимому, впервые пользовался йапсіогіив
(умеръ 1636), судившій о влажности воздуха по длинѣ натянутой пенько-
вой веревки. Наибольшею извѣстностью пользуется волосяной гигро-
метръ 8аи8 8и г е’а, одна изъ формъ котораго изображена на рис. 194.
Человѣческій волосъ, вполнѣ, освобожденный отъ жирныхъ веществъ, при-
крѣпленъ однимъ концомъ въ онъ обернута, вокругъ колесика о и на-
Гигрометрія
635
тягивается грузикомъ р. Стрѣлка, прикрѣпленная къ колесику о, пере-
мѣщается по шкалѣ, когда длина волоса мѣняется. Заиззиге опредѣ-
лялъ точки 0 и 100, помѣщая приборъ сперва въ совершенно сухой, а
затѣмъ въ воздухъ, насыщенный водяными парами. Разстояніе между точ-
ками 0 и 100 онъ раздѣлилъ на 100 равныхъ частей. Изслѣдованія
В и 1 о п §’а, О а у -Ь и 8 8 а с’а, М е 11 о п і и въ особенности Ве^паиіѣ
показали, что эта шкала не даетъ относительной влажности со для сред-
нихъ значеній между 0 и 100, и что правильная шкала должна быть эм-
пирически опредѣлена для каждаго экземпляра гигрометра. Изъ ниже-
слѣдующаго примѣра, относящагося къ одному экземпляру, видно, какъ ве-
лика разница между правильною шкалою и шкалою 8 а и 8 8 и г е’а :
Шкала правильная 0 10 20 30 40 50 00 70 80 90 95 100
Шкала 8аи88ііге‘а 0 19,6 34,6 47,1 57,7 66,8 75,0 82.2 88,6 94,6 97,4 100
Ве^паиіі показалъ, что эти числа неодинаковы для различныхъ
экземпляровъ гигрометра. М о п п і е г устроилъ
волосяной гигрометръ, по формѣ похожій на
анероидный барометръ, а КісЬагй построилъ
волосяной гигрографъ.
IV. Психрометръ. Этотъ приборъ со-
стоитъ изъ двухъ термометровъ, сухого и влаж-
наго ; резервуаръ послѣдняго плотно обтянутъ
батистомъ, на который медленно притекаетъ
вода изъ нѣсколько выше расположеннаго со-
суда А (рис. 195); нынѣ чаще располагаютъ
открытый сосудъ съ водою нѣсколько ниже ре-
зервуара (и въ сторонѣ отъ него), причемъ сво-
бодный конецъ батиста опущенъ въ воду, ко-
торая и поднимается по нему къ резервуару,
Вслѣдствіе испаренія воды термометръ охлаж-
дается и показываетъ нѣкоторую температуру V.
которая ниже температуры і воздуха, показы-
ваемой сухимъ термометромъ. По наблюден-
нымъ температурамъ і и і' можно найти упру-
гость р водяныхъ паровъ въ атмосферѣ. Идея
психрометра принадлежитъ Я. Ьеяііе (1810);
въ Англіи введеніе этого прибора приписыва-
ется М а 8 о п’у; его изслѣдовали П а у - Ь и 8 -
Рис. 195.
зас (1822) и Ке^папіі (1845). Аи^и8І,по
имени котораго психрометръ теперь обыкновенно и называется, придалъ
ему (1825) форму, изображенную на рис. 195, и далъ формулу, которая
ниже будетъ выведена ; ту же формулу вывелъ Ар,і о И п. МахіѵеП
далъ болѣе полную теорію психрометра: новыя изслѣдованія психрометра
были даны Зворыкинымъ. Покажемъ, какимъ образомъ выводится
формула, дающая р по наблюденнымъ I и і'.
636
Насыщенные пары.
Пусть 5 поверхность влажнаго термометра, ѵ скорость испаренія, из-
мѣряемая количествомъ воды, которое испаряется въ единицу времени съ
его поверхности. Влажный термометръ перестанетъ охлаждаться, т.-е.
въ немъ устанавливается термическое равновѣсіе, когда онъ въ единицу
времени столько же получаетъ теплоты отъ окружающихъ его тѣлъ,
сколько онъ теряетъ вслѣдствіе испаренія воды на его поверхности. Пер-
вое количество принимаемъ пропорціональнымъ поверхности 5 и разности
температуръ і — 1' окружающей среды и самого термометра (законъ
Ньютона, стр. 276); второе количество пропорціонально скорости испа-
ренія ѵ. Мы имѣемъ слѣд. равенство
А3(і—і') = Вѵ...................(40,«)
гдѣ А и В постоянныя числа. Для скорости ѵ мы имѣли на стр. 522
формулу Ваііоп’а (1,«)
ѵ=^<Рг-р}.....................(40,6}
гдѣ С постоянный множитель, Н давленіе атмосферы, Р' давленіе насы-
щеннаго пара при температурѣ і' испаряющейся жидкости, р упругость
паровъ, дѣйствительно находящихся въ воздухѣ. Подставляя ѵ, получаемъ
Сокративъ на 5 и обозначивъ А: ВС черезъ а, получаемъ
р = рг—аН(і- -і')...................(41)
или, если считать Н постояннымъ и положить аН = &,
р = Р' — Ь(і— I') .................(42)
Формулы (41) или (42), которыми постоянно и пользуются, какъ
видно изъ этого вывода, далеко не строги, ибо какъ законъ Ньютона,
такъ и формула В а 11 о п’а лишь приблизительно вѣрны. Оказывается, что
коеффиціентъ а зависитъ отъ среды, въ которой помѣщенъ гигрометръ,
и отъ скорости вѣтра. Для пращевого психрометра, быстро вращае-
маго на свободномъ воздухѣ, можно принять а = 0,06069, между тѣмъ
какъ по Ве^папіі для неподвижнаго психрометра величина а коле-
блется между 0,00074 на свободномъ воздухѣ и 0,00128 въ небольшой
комнатѣ. Для психрометра, снабженнаго вентиляторомъ, Ап§оі нахо-
дитъ « = 0,00078. Обыкновенно принимаютъ « = 0,0008, когда ^ >> 0° и
а = 0,00069, когда і' < 0. Для удобства пользуются готовыми таблицами,
дающими величины р, со или /, если извѣстны і и разность і — при-
чемъ Н принято равнымъ 755 мм. Если Н значительно отличается отъ
этого числа, то приходится ввести нѣкоторую поправку къ числамъ, дан-
нымъ въ таблицахъ.
Баіѵіопі (1901) и Гезехусъ (1902) построили гигрометры, осно-
ванные на измѣреніи увеличенія упругости испытуемаго воздуха,
когда онъ вслѣдствіе испаренія въ немъ воды, доводится до насыщенія.
Литература.
637
Преимущество прибора Гезехуса заключается въ томъ, что измѣреніе
влажности производится имъ гораздо быстрѣе, чѣмъ приборомъ Раіѵіопі.
ЛИТЕРАТУРА.
Къ § 2.
КписКеп. Аппаі. а. РЬуз. (4) 31 р. 205, 633, 1910.
КаИІЬаит. СЬет. Вег. 16 р. 2476, 1883; 18 р. 2085. 3146, 1885; 19 р. 943, 3098,
1886 ; АгсЬ. 8с. рЬуз. (3) 24 р. 351, 1890.
Катзау апй Уоищ?. СЬет. Вег. 18 р. 2855, 1885; 19 р. 2107, 1886.
Къ § 3.
Хіеріег. Бе аі&езіоге Раріпі, р. 48, Вазеі, 1759.
Вёіапсоигі. Зоигп. Ье Гёсоіе роІуіесЬпідие 2, 1790; Мётоіге зиг Іа іогсе ехрап-
зіѵе бе Іа ѵареиг, Рагіз, 1792.
ѴЬаіі. МесЬапісаІ РЫІозорЬу оі КоЪізоп 2 р. 29, 1814 (изданіе Вге\ѵзіег’а).
ЗоиіНегп. МесЬапісаІ РЫІозорЬу оі КоЪізоп 2 р. 170, 1814.
Каетіх. Меіеогоіоё’іе 1 р. 290.
О. С. 8сИтШ. УаіигІеЬге 1 р. 296, 1801—1803; Ѳгеп’з Зоитаі 4 р. 151.
Ѵге. РЫІ. Тгапз. 1818.
АгхЬегрег. ЛаЬгезЬ. а. РоІуіесЬп. Іпзі. хи ХѴіеп 1, 1819.
СНгіізііап. Мёсапідие іпаизігіеііе 2 р. 225.
Оаііоп. Мёт. МапсЬезіег РЫІ. 8ос. 15 р. 409; (ІіІЬ. Апп. 15 р. 1, 1803.
Сау-Ьиззас. См. Віоі „Тгаііё ае РЬузічие" 1 р. 287.
Оиіопр еі Агаро. Мёт. ае ГАсаа. 10, 1830; Апп. сЫт. еі рЬуз. (2) 43 р. 74,
1830; Ро^. Апп. 17 р. 533, 1829; 18 р. 437, 1830.
Эезргеіг. Апп. сЫт. еі рЬуз. (2) 16, 1821; 21, 1822.
Ріиескег., Ро&&. Апп. 92 р. 193, 1854.
Коммиссія американскихъ ученыхъ (1830). См. Епсусі. Вгіі. 20 р. 588 (8іеат);
см. также Ре^паиіі, Кеі. аез Ехрёг. 1 р. 467.
Къ § 4.
Кеупаиіі. Мёт. ае Гіпзі. 21 р. 465, 1847; Кёі. аез Ехрёг. 1 и 2; Ро§&. Апп. Ег^Ъа.
2 р 119, 1848; Апп. сЫт. еі рЪуз. (3) 11 р. 273, 1814; 15 р. 179, 1845.
Марпи8. Ро$&. Апп. 61 р. 225, 1844; Апп. сЫт. еі рЬуз. (3) 12 р. 69, 1844.
ВгосН. Тгаѵ. еі Мёт. би Виг. іпіегпаі. а. Р. еі Мез. I А р. 33, 1881.
Хеипег. ТесЬпізсЬе ТЬегтоаіпатік 2, 1890.
Къ § 5.
Саіііеіеі еі Соіагйеаи (вода). Л. ае рЬуз. (2) 10 р. 333, 1891; Аппаіез а. сЫт. еі
рЬуз. (6) 25 р. 519, 1892.
Ваііеііі (вода) Мет. аеІГАсаа. аі Тогіпо (2) 41 р. 33, 1891 ; 43 р. 63, 1892. Аппа-
іез а. сЫт. еі рЬуз. (6) 26 р. 410, 1892; (7) 3 р. 408, 1894.
Катзау ап(і Уоип& (вода). РЫІ. Тгапз. 183 А, р. 107, 1892.
Катзау апсі Уоипр (различныя жидкости). РЫІ. Тгапз. 175 I р. 37, 1884 ; 175
II р. 461, 1884; 177, I р. 123, 1886; 178 А, р. 57, 1887; РЫІ. Ма&. (5) 20 р. 515, 1885;
Зоигп. сЬет. 8ос. 49 р. 37, 453, 790, 1886.
НоІЬогп и. Неппіпр. Аппаі. а. РЬуз. (4) 26 р. 833, 1908
ОеЫіапІі. Дисс. Егіап&еп 1904; ѴегЬ. а. а. рЬуз. Оез. 1905 р. 184.
Кассагі е РарКапі. Уиоѵо Сіт. (3) 10 р. 49, 1881; Аііі аі Тогіпо 16 р. 407, 1880.
8іаесіеІ. СЬет. Вег. 15 р. 2559, 1882; ВеіЫ. 7 р. 184, 1883.
8скитапп. АѴ. А. 12 р. 40, 1881.
Уоипр, Лоигп. СЬет. 8ос. 55 р. 483, 1889.
Кіс1гаг(І8оп. Зоигп. СЬет. 8ос. 49 р. 761, 1886; Візз. ЕгеіЪиг^, 1886.
638
Насыщенные пары.
О. С, 8с!гтійі. Хізсііг. Г. рііуз. СЪетіе 7 р. 434, 1891; 8 р. 628, 1891.
Еегске. \Ѵ. А. 44 р. 265, 1891.
Вагиз. РЫ1. Ма&. (5) 29 р. 141, 1890.
Зайончевскій. См. ВеіЫ. 3 р. 741, 1879.
Надеждинъ. Ж. Ф. X. О. 14 р. 157, 536, 1882; 15 р. 25, 1883.
Упругость паровъ ртути.
Аѵо^айго Ро&&. Апп. 27 р. 60, 1833.
Вепейіх. Ро&&. Апп. 92 р. 632, 1854.
Ре^паиіі. Веі без Ехрёг. 2 р. 506, 1862; Р. Апп. 111 р. 402, 1860.
На^еп. \Ѵ. А. 16 р. 610, 1882.
Ратзау апй Уоип^. Лонги. СЬет. 8ос. 49 р. 37, 1886.
Н. Негіх. \Ѵ. А. 17 р. 193, 1882.
Мас-Ьеой. Вер. Вгіі. Азз. 1883.
Могіеу. Ріііі. Ма&. (6) 7 р. 662, 1904; ХізсЬг. 1. рку©. Сііет. 49 р. 95, 1904.
Уоип& Тгапз. Сііет. 8ос. 59 р. 629, 1891.
Ѵап йег Ріааіз. Вес. ігаѵ. сЫт. 5 р. 49, 1886.
Р/аипйІег. \Ѵ. А. 63 р. 36, 1897.
ЬаЬу. РЫ1. Ма^. (6) 16 р. 789, 1908.
Кпийзеп. Аппаі. сі. Рііуз. (4) 29 р. 179, 1909.
Сгущенные газы.
Х^гоЫетѵзкі. А. 25 р. 371, 1885 (кислор., азотъ, СО, СО2).
Оізгеіѵзкі. С. В. 100 р. 351, 1885 (кислор.); р. 942 (ИО)\ р, 940 (С//4); \Ѵ. А
31, 74, 1887 (азотъ); Вніі. Асасі. Сгасоѵ. 1890 р. 57 (5//2) > РЬіІ. Ма&. (5) 39 р. 195
1895 (С2//4).
Езігеісііег. Ріііі. Ма&. (5) 40 р. 459, 1893 (кислор.).
Кпіеізсіі. ЫеЬ. Апп. 259 р. 100, 1890 (хлоръ).
Тгаѵегз, 8епіег шій йадиегой. 2ізс1іг. 1. рііуз. Сііет. 45 р. 416, 435, 1903.
Еізсііег ипй Аіі. Б. А. 9 р. 1176, 1902.
Ои Воіз ипй ѴѴіІІз. ѴегЬапсІІ. сіенізсіі. рііуз. без. 1 р. 168, 1899.
Ратзау апсі Уоип^. Лонгп. Сііет. 8ос. 49 р. 453, 1886 (бромъ, іодъ).
Еагайау. РЫ1. Тгапз. 1845 р. 155 (А773, НСІ, И2О, 8Н2, 8О2і СО2).
Ре^паиіі. Вёі. без ехрёг. 2 р. 596 (ИН3); р. 626, 646 (Н2О); р. 61 (8Н2); р. 581
(8О2)' 618 (СО2).
Віиетке. \Ѵ. А. 34 р. 19, 1888 (НСІ, 8О2).
Апзйеіі. Сііет. Ые\ѵз 41 р. 75, 1881 (НСІ).
Саіііеіеі. Агсіі. 8с. рііуз. 66 р. 16, 1878 (И2О, СО2); С. В. 94 р. 1824, 1880(С2//4)
йапззеп. Візз. Ьеусіеп. 1877 (А^О).
Апйгеіѵз. Ргос. В. 8ос. 24 р. 455, 1876 (СО2).
Ата^аі. С. В. 114 р. 1093, 1322, 1892 (СО2); Апп. сЫт. еі рііуз. (6) 29 р. 70
1893 (С2Я4).
Сііарриіз еі Ріѵіёге. С. В. 104 р. 1504, 1887 (С/Ѵ).
Къ § 6.
Оаііоп. См. къ § 3.
Сге. См. къ § 3.
Ре&іаиіі. С. В. 50, 1860; Ро^. Апп. 111 р. 402, 1860.
О. С. 8сктійі. Хізсііг. 1. рііуз. Сііетіе. 7 р. 434, 1891 ; 8 р. 645, 1891.
Ьапйоіі. ЬіеЪ. Апп. 8нрр1.-ВапЛ 6, 1868.
Оиекгіп^. ВаНопеІІе бгнпЛ^езеіге р. 20 Ьеіргі^, 1878; \Ѵ. А. 52 р. 556, 1894.
Ратзау апй Уоип& РЫ1. Ма&, (5) 21 р. 33, 1886; 22 р. 37, 1886.
Ріскагйзоп. Лонгп. Сііет. 8ос. 49 р. 761, 1886.
Уоип^. Ыаінгаі рііііозорііу 2 р. 400, 1807.
Е^еп. Ро^. Апп. 27 р. 9, 1833.
Литература.
639
Тгей^оШ. Тгаііе дез тасЫпез а ѵареиг р. 101, 1828.
Согіоііз. Би саісиі сіе ГеГГеі дез тасЫпез р. 58, 1829.
Оиіощу еі Агару). Мёт. де ГІпзі. 10 р. 230, 1830; Апп. сЫт. еі рііуз (2)
43 р. 74, 1830.
Коске. Мёт. (Іе ГІпзі. 10 р. 227, 1830.
Аиризі. Ро^. Апп. 13 р. 122, 1828; 18 р. 468, 1830; 27 р. 25, 1833.
Сіареугоп. Л. де Гёс. роіуіесіт. 14 р. 153, 1834.
УѴгейе. Ро&^. Апп. 53 р. 225, 1841.
Ноііхтапп. Ро&8- Апп. Ег^Ьд. 2 р. 183, 1847.
Марпиз. Ро^К Апп. 61 р. 225, 1844; Апп. сЫт. еі рііуз. (3) 12 р. 69, 1844.
Вгоъѵп. Ргос. К. 8ос. 26 р. 838, 1877.
Зайончевскій. См. ВеіЫ. 3 р. 741, 1879.
Гнузинъ. Труды Физ. Отд. О. Л. Е. 10 № 1, 1892.
ШіизЬигрег. Б. А. 3 р. 618, 1900.
Огаеіх. 2ІЗСІ1Г. Г. МаіЬ. и. Рііузік. 49 р. 289, 1903.
Віоі: Соппаіззапсе дез Тетрз, 1844.
Могііх. Виіі. Ас. де 8і. РеіегзЪ. 13 р. 43, 1869.
Ваііеііі. Апп. сіііт. еі рііуз. (7) 3 р. 409, 1894; 5 р. 256, 1895; 9 р. 409, 1896.
ВегігапД. Тііегтодупатідие р. 157, Рагіз, 1887.
Неггтапп. Сотрепдіит д. тесііап. АѴаегтеіЬеогіе р. 133, Вегііп, 1879.
Оиргё Тііёогіе тёсапідие де Іа сііаіеиг р. 96, Рагіз, 1869.
Негіх. АѴ. А. 17 р. 177, 1882.
ОіЪЪз. Тііегтодупатізсііе 8іидіеп. р. 181.
У. У. Ткотзоп Атѵепдип&еп дег Вупатік (переводъ) р. 190.
Вегігапй (формула Виргё). Тііегтодупатідие р. 91.
Кігскко//. АѴагте (лекціи) р. 95.
Краевичъ. Теоретическое изслѣдованіе упругости паровъ. Спб., 1891. -
СиІйЬегр. 2ізсЫ. д. Ѵег. деиізсіі. Іп&епіеиге 12 р. 676, 1868.
Ргопу. Л. де Гёс. роіуіесіт. 1847 № 2 р. 1.
Кеззіег. ЛаЪгезЪег. д. ОелѵегЪезсІшІд хи Восішт, 1880.
Вгоск. Мёт. ди Виг. іпіегп. дез Р. еі Мез. 1 А, р. 17, 1881.
Апіоіпе. С. В. 107 р. 681, 778, 836, 1888; 110 р. 632, 1890; 112, 284, 1891; 113
р. 328, 1892; 116 р. 170, 1893; Апп. сіііт. еі рііуз. (6) 22 р. 281, 1891.
Богаевскій. Ж. Ф. X. О. 29 р. 87, 1897.
Аагоііпек. АѴіепег Мопаізііеііе 4 р. 193, 1883; ВеіЫ. 7 р. 587, 1883.
Оирегпау. Апп. сіііт. еі рііуз. 23 р. 71, 1871.
Ое Нееп. Виіі. Ас. Веі^е (3) 11р. 165, 1886.
СегЬег. Ыоѵа асіа Ьеор. Сагоі. Ас. 52 № 3 р. 103, 1888; ВеіЫ. 12 р. 455, 1888.
Огшнп. РЫІ. Ма&. (5) 21 р. 299, 1881.
Рісіеі. С. В. 90 р. 1070, 1880.
Зскіетиеііег. АѴіеп. Вег. 106 р. 9, 1897.
Рапкіпе. ЕдіпЪ. Хе\ѵ. РЫІ. Лоигпаі, 1849.
Хеипег. ТесЫіізсІіе Тііегтодупатік 2 р. 36, 1890.
Сіссопе. Віѵ.-8с. Іпдизіг. 13 р. 170, 1881.
Ѵ/іпкеІтапп. АѴ. А. 9 р. 217, 1880.
Ріапск. АѴ. А. 13 р. 535, 1881.
Сіаизіиз. АѴ. А. 14 р. 279, 692, 1881.
Махъѵеіі. Хаіиге (англ.) 1875 (4 и 11 марта).
Къ § 7.
ІГ. Потзоп {Ьогй Кеіѵігі). РЫІ. Ма^. (4) 42 р. 448, 1871.
Ѵ/агЬигр. АѴ. А. 28 р. 394, 1886.
Р. Неіткоііх. АѴ. А. 27 р. 522, 1886.
Б. Б. Голицынъ. АѴ. А. 45 р. 200, 1888.
640
Насыщенные пары
Гііх^егаій. РЫІ. Ма§\ (5) 8 р. 382, 1889.
8іе{ап. АѴ. А. 29 р. 655, 1886.
Бикет. Апп. бе ГЕсоіе ногт. зирёг. (3) 2 р. 207, 1885.
7?. Неіткоііх (свойства струи пара). АѴ. А. 32 р. 1, 1887.
У. У. Ткотзоп. РЫІ. Ма^. (5) 36 р. 313, 1893.
Аіікеп. Ргос. В. 8ос. 51 р. 480, 1892.
Воск, Рго&. К. Веаізсітіе ВоіІіепЪиг^ о. Т. 1896; ВеіЫ. 20 р. 1861, 1896.
Віогкііоі. У. бе рйуе. (2) 3 р. 442, 1884.
Бикет. Апп. ёсоіе погтаіе (3) 7 р. 289, 1890.
Коепі^Ьег^ег. АѴ. А. 66 р. 709, 1898.
Н. Шиллеръ. О. Ф. Н. 06. Л. Е. 7, вып. 1 р. 31; вьт. 2 р. 7, 1895; Ж. Ф X. О.
29 р. 7, 1897; 30 р. 79, 159, 175, 1899; АѴ. А. 53 р. 396, 1894; 60 р. 755, 1897; 67 р 291,
1899; Кіевскія Унив. Извѣстія, 1897.
Соколовъ. Ж. Ф. X. О. 26 р. 319, 1894.
Кистяковскій. Ж. Ф. X. О. 29 р. 273, 1897; 30 р. 139, 1898.
Наппау агкі Но^агік. Ргос. К. 8ос. 30 р. 178, 1880.
Саіііеіеі. Л. бе рііуе. (1) 9 р. 193, 1880.
Ѵіііагй. Л. бе рііуз. (3) 5 р. 453, 1896.
Къ § 8.
Сіаизіив. Месііап. АѴагтеНіеогіе 1 р. 159.
Біеіегісі. АѴ. А. 38 р. 1, 1889.
Къ § 9.
ГаігЬаігп агкі Таіе. РЫІ. Ма&. (4) 21 р. 230, 1861 ; РЫІ. Тгапз. 1860 р. 185.
Регоі. Апп. сЫш. еі рііуе. (6) 13 р. 145, 1888; С. К. 102 р. 1369, 1886; Л. бе рііуз.
(2) 7 р. 129, 1888.
Ѵоип^. Тгапз. Сііет. 8ос. 59 р. 37, 1891.
Саіііеіеі еі Маікіав. С. К. 104 р. 1563, 1887; Л. бе рйу8. (2) 5 р. 549, 1886.
Ваиег. АѴ. А. 55 р. 184, 1895.
Негчѵір;. Ро&&. Апп. 137 р. 19; 1869.
ѴГиеІІпег игкі Сгоігіап, АѴ. А. 11 р. 545, 1880.
Ваііеііі. Меш. Асс. Тогіпо (2) 40, 41, 44, 1890—92; Ыиоѵ. Сіт. (3) 30 р. 235,
1891 ; Апп. сЫт. еі р1іу8. (6) 25 р. 38, 1892.
Ратвау апсі Уоип§. РЫІ. Тгапз. 176 р. 123, 1886; 177 р. 1, 1886; 178 р. 57,313,
1887; 180 р. 137, 1889; РЫІ. Ма§. (5) 23 р. 435, 1887; Ргос. К. 8ос. 54 р. 387, 1888.
Ата&аі. С. К. 114 р. 1093, 1322, 1892.
8скоор. ѴѴ. А. 12 р. 550, 1881.
Аѵепагіив. Виіі. бе ГАс. бе 8,-РёіегзІ). 22 р. 378, 1876; Мёі. рііуз. еі сЫт. 9 р.
647, 1876.
Апзаеіі. Ргос. В. 8ос. 30 р. 117, 1879.
Ног8ітапп. ЬіеЬ. Апп. 8ирр1. 6 р. 51, 1868.
Б. Голицынъ. АѴ. А. 47 р. 466, 1892.
\ѴгоЫег&8кі (кислородъ). АѴ. А. 25 р. 371, 1885.
Оівхеъжкі. С. К. 100 р. 351, 1885 (кислородъ). АѴ. А. 31 р. 73,1887 (азотъ, метанъ).
Маікіа8. С. В. 115 р. 35, 1890; 128 р. 1389, 1899; 139 р.359, 1904; 148 р. 1102,
1909. Л. бе рііуе. 1899 р. 407 ; 1905 р. 77.
8у(іпеу Уоип^. РЫІ. Мар;. (5) 50 р. 291, 1900.
Бачинскій. 2І8сЫ. Г. рііуз. Сііет. 41 р. 741, 1902.
Къ § 10.
С1аи8іи8. Ро&&. Апп. 79 р. 368, 500, 1850; АЫіапбЫп^еп 1 р. 73.
Рапкіпе. Тгап8. ЕбіпЪ. В. Яос. 20, 1849—1853.
Бикет. Л. бе рііуз. (3) 1 р. 470, 1892.
Литература.
641
МаШаз. <1. йе рііуе. (3) 5 р. 381, 1896; 7 р. 397, 626, 1898; С. В. 126 р. 1095,
1898; 148 р. 1102, 1909.
Сагіп. Апп. сіііт. еі рііуе. (4) 14 р. 374, 1868; С. В. 62 р. 56, 1866.
АИ. Оіее. Мііпскеп 1903
Нігп. Соетое 22 р. 413, 1863; Виіі. сіе Іа 8ос. іпйиеіг. Йе МиПіоиее 133 р. 137.
Вегігапй Тііегтосіупатідие р. 227, Рагіе, 1887.
Къ § 11.
Ріапск. Тііегтойупатік р. 138, Вегііп, 1897.
Шезеп. Б. А. 9 р. 80, 1902.
Оаііоп. Ріііі. Ма§. (6) 13 р. 536, 1907.
Иегп8і. Ѵегк. сі. й. рііуе. Сее. 1909 р. 320.
Къ § 12.
Оаііоп. Мапсіі. ріііі. 8ос. 5 р. 535, 1802; СИГЪ. Апп. 12 р. 385, 1802; 15 р. 21, 1803.
Непгу. Кіскоіёоп’е Й. 8 р. 297, 1804; (ИГЪ. Апп. 21 р. 393, 1805.
Оау-Ьи88ас. Апп. сіііт. еі рііуе. 95 р. 314, 1815; Віоі, Тгаііё йе рііуеідие 1 р. 298.
Ма&піі8. Ро&§. Апп. 38 р. 488, 1836.
Ре^паиіі. Апп. сіііт. еі рііуе. (3) 15 р. 129, 1845; (4) 26 р. 679, 1862; Мёт. сіе
ГАс. 26 р. 256, 722, 729, 1862; Ро^. Апп. 65 р. 135, 321, 1845.
Негищг. Ро^. Апп. 137, 592, 1869.
Кгоепірг. Ро&&. Апп. 123 р. 299, 1864.
Тгоо8і еі Наиіе/еиіііе. С. В. 83 р. 333, 975, 1871.
Оирііеіто е Ми8Іпа. Віѵ. ес. іпйиеіг. Рігепге 19 р. 185, 1887; ВеіЫ. 12 р.
464, 1888.
Вгаип. АѴ. А. 34 р. 943, 1888.
ХѴиеІІпег ипй Огоігіап. АѴ. А. 11 р. 607, 1888.
КгеЬ8. Ро^§. Апп. 133 р. 673, 1868; 136 р. 144, 1869.
/?. Неітііоііг. \Ѵ. А. 27 р. 508, 1886.
Б. Голицынъ. Вае Ваііопіесііе Ѳеееіг. Віее. 8гаееЪиг§, 1890; АѴ. А. 41 р. 588, 1890.
Къ § 13.-
йатіп. Й. сіе рііуе. (2) 3 р. 469, 1884.
Вгиппег. Апп. скіт. еі ркуе. (3) 3 р. 305, 1841.
7?. У/еЪег. Виіі. 8ос. №искаіе1. сіее ес. паіиг. 27 р. 55, 1898—99.
Сапіог. АѴ. А. 56 р. 492, 1895.
С1іаг1е8 Ье Роу. Мёіап^ее сіе Ркуеідие еі сіе Месіісіпе. МопіреШег 1771.
Оіпе8. См. Ргееіоп. Тііеогу оі Неаі, Ьопсіоп, 1894, р. 358.
Оапіеі. бгіІЪ. Апп. 65 р. 169, 1820; Меіеогоі. Еееауе апсі ОЬеегѵаііопе р. 139,
Ьопсіоп, 1827.
Ре&паиіі. Апп. скіт. еі ркуе. (3) 15 р. 129, 1845.
АІІиагй. Й. сіе ркуе. (1) 7 р. 328, 1878.
Сгоѵа. Й. сіе ркуе. (2) 2 р. 166, 437, 1883; 3 р. 390, 1884: С. В. 94 р. 1514, 1882.
ИірроШ. Меіеог. Хіескг. 1894 № 4.
8аи88иге. Ееваі еиг ГНу^готёігіе р. 1, Кеисііаіеі, 1783.
Оиіощ). См. Віоі. Рііуеідие 2 р. 207.
Оау-Ьи88ас. См. Віоі. Ркуеідие 2 р. 199.
Меііопі. Апп. скіт. еі ркуе. (2) 43 р. 39, 1830.
Рерріаиіі (волосяной гигрометръ). Апп. скіт. еі рііуе. (3) 15 р. 141, 1845.
Ьезііе. Кіскоіеоп’е йопгп. 3 р. 461.
Аи^и8і. Ро^. Апп. 5 р. 69, 1825.
Аріоііп. Тгапв. В. Ігівк. Асай. 17 р. 275, 1834.
Махіѵеіі. Хіескг. Г. Меіеогоі. 16 р. 177, 1881.
КУРСЪ ФИЗИКИ О. X В О Л Ь С О Н А. Т. III, ИЗД. 3-е.
41
642
Ненасыщенные пары.
Зворыкинъ. Опредѣленіе влажности посредствомъ психрометра. Прилож. къ
11 тому Записокъ Акад. Наукъ, 1881.
Ащ?оі. 4 (Іе рііун. (1) 10 р. 112, 1881.
Масё (іе Ьёріпау. 4 де рйуз. (1) 10 р. 17, 1881.
Заіѵіопі. АШ. К. Асс. Реіогііапа Мевзіпа 17, 1901; ВеіЫ. 1902 р. 369.
Гезехусъ. Ж. Ф. X. О. 1902 р. 331.
ГЛАВА ТРИНАДЦАТАЯ,
Ненасыщенные пары. Критическое состояніе. Ученіе о соот-
вѣтственныхъ состояніяхъ.
§ 1. Введеніе. Идеальные газы и насыщенные пары представля-
ютъ два крайніе члена въ непрерывномъ рядѣ возможныхъ состояній
вещества. Идеальные газы характеризуются произвольными двумя изъ
трехъ законовъ Бойля, Гей-Люссака и Джуля (стр. 450); на-
сыщенные пары — тѣмъ, что ихъ упругость есть функція только одной
температуры (для даннаго вещества), вслѣдствіе чего всякое изотермиче-
ское сжатіе и всякое охлажденіе при постоянномъ ѵ сопровождаются пе-
реходомъ части вещества изъ газообразнаго состоянія въ жидкое*. Реаль-
ные газы, уже не слѣдующіе* упомянутымъ законамъ, и пары, не слиш-
комъ удаленные отъ насыщенія, обладаютъ какъ бы промежуточными
свойствами. Никакой рѣзкой границы между реальными газами и па-
рами провести нельзя, а. потому мы ихъ соединяемъ подъ общимъ назва-
ніемъ ненасыщенныхъ паровъ. Важно замѣтить, что въ тѣхъ
случаяхъ, когда плотность и упругость насыщеннаго пара весьма малы,
мы можемъ допустить, что ненасыщенные пары вплоть до насыщенія
обладаютъ свойствами идеальныхъ газовъ. Такое допущеніе не приве-
детъ къ замѣтнымъ ошибкамъ напр. для паровъ ртути и даже* воды при 0°,
и мы имъ пользовались неоднократно, какъ для упрощенія точныхъ фор-
мулъ, такъ п для вывода новыхъ формулъ, хотя и не вполнѣ точныхъ.
Свойства насыщенныхъ паровъ были подробно разсмотрѣны въ предыду-
щей главѣ. Отступленія отъ законовъ Бойля, Гей-Люссака и
Джуля для «газовъ» въ обыденномъ смыслѣ слова, т.-е. для паровъ,
весьма далекихъ отъ насыщенія, были разсмотрѣны въ т. Е и въ этомъ
томѣ, стр. 128 и 458.
Въ этой главѣ мы прежде всего подробнѣе* разсмотримъ свойства не-
насыщенныхъ паровъ, обращая особенное вниманіе на состояніе ихъ,
уже недалекое отъ насыщенія. Сюда относятся напр. свойства
«паровъ различныхъ жидкостей», т.-е. веществъ, которыя при
обыкновенныхъ температурахъ и давленіяхъ находятся въ жидкомъ со-
стояніи. Такъ называемое ученіе о соотвѣтственныхъ состоя-
ніяхъ указываетъ на важную роль, которую слѣдуетъ приписать кри-
тическому состоянію вещества при изученіи свойствъ ненасыщен-
ныхъ паровъ. Вотъ почему мы соединили въ одной главѣ три какъ будто
Теплоемкость ненасыщенныхъ паровъ.
643
разнородные вопроса о ненасыщенныхъ парахъ, о критическомъ состоя-
ніи и о соотвѣтственныхъ состояніяхъ.
§ 2. Теплоемкость ненасыщенныхъ паровъ. На стр. 199—228 мы
разсмотрѣли теплоемкость газовъ, т.-е. ненасыщенныхъ паровъ, весьма
далекихъ отъ насыщенія. Далѣе мы показали (стр. 619), какъ вычисля-
ется та особаго рода теплоемкостью насыщенныхъ паровъ, которая,
какъ мы видѣли, можетъ быть величиною и отрицательною. Наконецъ
мы еще показали, какъ можно вычислить теплоемкость Ср насыщен-
ныхъ паровъ, которая есть не что иное, какъ предѣльное значеніе те-
плоемкости Ср ненасыщенныхъ паровъ, когда послѣдніе1 приближа-
ются къ состоянію насыщенія. Намъ остается разсмотрѣть вопросъ о
теплоемкости ненасыщенныхъ паровъ, не слишкомъ далекихъ отъ
насыщенія.
Первыя опредѣленія величины ср для паровъ были произведены
Ее^паиіі (1862) по способу, аналогичному тому, которымъ онъ поль-
зовался при опредѣленіи ср для газовъ и который былъ описанъ на стр. 203.
Разница та, что пары сгущались въ змѣевикѣ (внутри калориметра) въ
жидкость, причемъ выдѣлялась скрытая теплота испаренія. Пусть Р вѣ-
совое количество пара, і его температура при вступленіи въ калори-
метръ, температура ожижнія, с(=Ср) средняя теплоемкость пара
между /° и ^°, р скрытая теплота испаренія, Л и і" первоначальная и окон-
чательная температуры калориметра, С теплоемкость всего калориметра,
ю‘ средняя теплоемкость жидкости между температурами и Тогда
мы имѣемъ, очевидно,
РсЦ-і^ + Рд + Рс'^ = — і‘)^д -д' ... (1)
гдѣ д теплота, потерянная калориметромъ вслѣдствіе лучеиспусканія,
д' теплота, притекшая къ нему путемъ теплопроводности. Въ третьемъ
членѣ было бы точнѣе написать (/' + /н): 2, вмѣсто Первый членъ,
содержащій искомую величину ю, весьма малъ сравнительно со вторымъ
членомъ, а потому точное опредѣленіе с по формулѣ (1) невозможно. По-
этому Ве^папИ поступалъ слѣдующимъ образомъ: сперва онъ произ-
водилъ опытъ, нагрѣвая пары до температуры і, лежащей немного выше
температуры ожиженія ; затѣмъ онъ во второмъ опытѣ пропускалъ че-
резъ калориметръ то же вѣсовое количество Р пара, предварительно
нагрѣтаго до гораздо болѣе высокой температуры Г, причемъ калориметръ
нагрѣвался до температуры Т“ > і“. Такимъ образомъ получалось вто-
рое уравненіе
Рс(Т + Ро + РС& Т“) = С(Т"- п-і-д. дг‘.
Вычтя одно уравненіе изъ другого, онъ поллчилъ формулу, въ ко-
торой отсутствовала большая величина Ро; по этой формулѣ можно было
съ большею точностью вычислить среднюю теплоемкость с паровъ между
Т® и /°. Приводимъ нѣкоторыя изъ чиселъ В е § па и И:
и*
644
Ненасыщенные пары.
Т і с (паръ), с' (жидк.). с“ (тверд.).
Вода (Я2О) 220,9 128,1 0,4776 1 0.5
Эфиръ (С4//10О) 224,0 69.6 0,4796 0,53 —
Хлкоголь отиловыи (С>Л/6О) 220,1 107,5 0,4534 0,66 —
Сѣроуглеродъ (СХ2) .... 147 80 0,1534 0,23 —
Бензолъ (С6/76) 217,7 116 0,3754 0,44 —
Хлороформъ (СНСІ^ .... 238,4 117,4 0,1566 0,24 —
Бромъ 228,2 82,9 0,0555 0,11 0,08
Терпентинное масло (С10/716) . 249.0 179.1 0.5061 0.51 —
Теплоемкость паровъ меньше теплоемкости жидкостей и для воды
п брома приближается къ теплоемкости вещества въ твердомъ состояніи.
Величины с п с* вообще мѣняются въ одинаковомъ направленіи, при пе-
реходѣ отъ одного вещества къ другому.
Е. ЛѴіейетапп (1877) обошелъ указанное выше затрудненіе
тѣмъ, что онъ уменьшалъ давленіе р внутри калориметра, вслѣдствіе чего
пары сгущались не въ калориметрѣ, но послѣ выхода изъ него въ особомъ,
достаточно охлажденномъ сосудѣ. Мѣняя температуры, между которыми
происходило охлажденіе пара, онъ могъ опредѣлить зависимость с отъ
температуры. Пусть с с0 2а/^ теплоемкость при температурѣ /, такъ
что с0 -|- аі представляетъ среднюю теплоемкость между 0° и і°. Приво-
димъ нѣкоторыя изъ чиселъ Е. ЛѴіесІетапп’а, для с0 и 2а. п для с0‘
и 2а', относящихся къ жидкому состоянію вещества.
с0 2а Со* 2а*
Хлороформъ (СНСІ^.............. 0,1341 0,0001354 0,2223 0,0001014
Бензолъ (С6776)................ 0,2237 о,001023 0,3798 0,001440
Ацетонъ (С3Я6О)................ 0,2984 0,000774 0,5064 0,000793
Эфиръ (С4/У10О)................ 0,3725 0,000854 0,5290 0,000592.
Замѣчательно, что величины 2а и 2а' болѣе близки другъ къ другу,
чѣмъ величины и с0'.
Величину к = ср : сѵ <ддѣ ср тождественно съ только что разсмо-
трѣннымъ с) опредѣляли Р. А. Мйііег по цпособу Аззшапп’а (стр. 222)
и XV. Я а § ё г по способу измѣренія скорости звука. Приводимъ табличку, къ
которой прибавлены значенія к, вычисленныя по формулѣ ср —< ѵ = Л/?
(стр. 200), строго вѣрной только для идеальныхъ газовъ. Для ср вста-
влены числа, найденныя Ке^паиИ и Е. ЛѴіейетапп’омъ.
к (набл.). Мйііег к (набл.). За^ег к (вычисл.у. Ее&паиіі к (вычисл.). Е. ДѴіеЗетапп
Вода . . . . — 1,330 (95°) 1,306 (174°) —
Алкоголь . . — 1,133 (54°) 1,107 (164°) —
Эфиръ . . . . 1,029 (34°) 1,097 (20°) 1,060 (147°) 1,078 (0°)
. . . 1,189 (30°) — 1,208 (134°) —
» . . . . » — 1,248 (0°) —
Хлороформъ . . . 1,110 (30°) — 1,118 (178°) 1,139 (0°).
Зависимость теплоемкости отъ температуры показываетъ, что въ па-
Разныя свойства ненасыщенныхъ паровъ.
645
рахъ внутренняя, вѣроятно интрамолекулярная работа не равна нулю.
Молекулярная теплоемкость тсѵ гдѣ т молекулярный вѣсъ, а также сред-
няя атомная теплоемкость тсѵ : п, гдѣ п число атомовъ въ одной моле-
кулѣ, оказываются для различныхъ паровъ неодинаковыми; вторая вели-
чина равна напр. 2,81 для хлороформа, 2,67 для С52, 1,70 для эфира и
1,29 для бензола.
§ 3. Плотность, упругость и тепловое расширеніе ненасыщенныхъ
паровъ Для идеальныхъ газовъ мы имѣемъ рѵ — Гопзі. Разсматривая
Рис. 196-
отступленія отъ закона Бойля (т. 1), мы уже указали на обширныя
изслѣдованія А т а § а 1. Помѣщаемъ нѣкоторые рисунки, весьма наглядно
изображающіе результаты его изслѣдованій. На этихъ рисункахъ изобра-
жены изотермы, уравненіе которыхъ взято въ видѣ рѵ = /(р), т.-е. на
абсциссахъ отложены давленія р въ атмосферахъ, на ординатахъ произ-
веденія рѵ. Для идеальныхъ газовъ эти изотермы представляютъ прямыя,
параллельныя оси абсциссъ, ибо для такихъ газовъ уравненіе изотермъ
рѵ = Соп8І. Аша^аі изслѣдовалъ воздухъ О2, 7Ѵ2, СН± (метанъ). С2Н±
(этиленъ) и СО2, доводя давленіе въ нѣкоторыхъ опытахъ до 1000 атм. Для
646
Ненасыщенные пары.
Н2 изотермы оказались прямыми, наклоненными къ оси абсцисіъ, при-
чемъ рѵ росло вмѣстѣ съ р. Для Л/ѳ и СН± получились кривыя, причемъ
для СН± произведенія рѵ имѣли рѣзко выраженные минимумы при дав-
вленіяхъ около 120 атм. Изотермы для этилена изображены на
рис. 196. Съ повышеніемъ температуры минимумъ величины рѵ пере-
мѣщается въ сторону большихъ давленій. Для СО2 Аша^аі изслѣдо-
Рис. 197.
валъ изотермы отъ 0° до 258° и для давленіи до 1000 атм/; онѣ изобра-
жены на рис. 197; часть, относящаяся къ меньшимъ давленіямъ, изобра-
жена на рис. 198, причемъ масштабъ абсциссъ увеличенъ. Точки наи-
меньшихъ рѵ соединены пунктиромъ; ихъ геометрическое мѣсто напоми-
наетъ параболу. Изотермы 32° (критическая температура) и 35° на
обоихъ рисункахъ обозначены пунктиромъ. Кромѣ того на рис. 198
(съ лѣвой стороны внизу) обозначена пунктиромъ еще одна параболиче-
ск ая кривая, значеніе которой слѣдующее. При температурахъ ниже 32°
Разныя свойства ненасыщенныхъ паровъ.
647
углекислый газъ при нѣкоторомъ давленіи сгущается въ жидкость, при-
чемъ ѵ, а слѣд. и рѵ при р = Соп8І. уменьшается до значенія, соотвѣт-
ствующаго ожиженію всей массы. Вертикальныя части изотермъ соот-
вѣтствуютъ періоду ожиженія, такъ что продолженія (слѣва) изотермъ ниже
32° уже относятся къ жидкой СО2- Параболическая кривая соединяетъ
точки, соотвѣтствующія началу и окончанію ожиженія.
Изотермы различныхъ паровъ были изслѣдованы многими учеными,
изъ которыхъ назовемъ В і п е а и, Ногеітапп’а, СаЬоигя’а, Нігп’а,
Негѵѵч^’а, ѴѴиеІІпег’а и Ого Іг іа п’а, Всііоор’а, Віеіегісі,
Ата^аі, Ваііеііі, ЛѴгоЫелѵекі, Кат§ау и Ѵоип^’а. Мѣняя
внѣшнее давленіе при постоянной температурѣ, названные ученые наблю-
дали объемы ѵ пара, постепенно приближая состояніе послѣдняго до на-
сыщенія. Съ работами Н е г і ^’а и ЛѴ и е 11 п е г’а и Сг г о 1 г і а п’а
Рис. 1у8.
мы уже познакомились на стр. 616, поскольку онѣ относятся къ свой-
ствамъ ненасыщенныхъ паровъ; см. напр. формулу (21) Нёгхѵі^’а.
Віеіегісі изслѣдовалъ пары воды при 0° и нашелъ, что они до
насыщенія слѣдуютъ закону Бойля, какъ уже было упомянуто выше.
ВаѣѣеІІі изслѣдовалъ изотермы слѣдующихъ веществъ: С52, Н2О,
эфира и этиловаго алкоголя. Онъ находитъ, что уравненіе состоянія па-
ровъ можетъ быть выражено формулою
р +
тТ пТ
+ №
-V
(ѵ — Ь) = КТ.
648
Ненасыщенные пары.
гдѣ т, д, п, ѵ, Ь и 7? постоянныя величины. Выражая р въ мм. ртут-
наго столба и полагая, что ѵ объемъ одного грамма вещества. ВаѣѣеІІі
находитъ слѣдующія численныя значенія этихъ постоянныхъ:
7? Ь г? т р п V
С82 . . . 819,71 0.684 0,327 12868324 0,32021 95,877 1,9420
н2д. . 3430,92 0,742 1,137 57288567 0,22015 7711,6 0,12235
Эфиръ. . 832,01 1,098 0,764 8134004 0,19302 243,8 0,40101
Алкоголь 1343,80 0,941 0.851 432449000 0.71373 14.10-8 4.7151.
Катзау и Ѵоип^ даютъ въ своихъ обширныхъ таблицахъ зна-
ченія плотности 0 пара относительно водорода, находящагося
при томъ же давленіи и той же температурѣ, какъ и паръ. Если бы
пары обладали свойствами идеальныхъ газовъ, то д равнялось бы поло-
винѣ молекулярнаго вѣса 4, и было бы величиною постоянною. Приво-
димъ немногія характерныя числа изъ упомянутыхъ таблицъ. Давленіе
р выражено въ мм. ртутнаго столба; половину молекулярнаго вѣса обо-
значимъ черезъ Л.
1. Эфиръ, (С2/7б)2О; /1 = 37.
р мм. 900 4800 7° 50 100 д 38.96 44,46 р мм. 28000 42000 200 223 д 82,45 110,5.
Послѣднее число въ три раза больше теоретическаго А = 37.
2. Метиловы р мм. 7° й а л к о г о л ь д СН.^ОНг р мм. 16. V Л
2000 100 16,80 2000 230 16,01
10000 150 19,55 48000 — 31.60
28000 200 23,76 2000 240 16,00
44000 225 29.26 58000 — 40,00.
3. Этиловый р мм. алкоголь, д СМьОН- Л = р мм. 23. <5
993 90 23,47 3673 234 23,03
7353 150 26,92 40711 — 48,36
14725 180 30,33 3750 246 23,08
22015 200 33,68 44053 — 41,36.
5. Уксусная кислота, С2НдР2 ; Л — 30. Явленія, представляе-
мыя уксусной кислотой, усложняются тѣмъ, что при низкихъ температу-
рахъ паръ содержитъ молекулы состава (С2774О2)2, которыя при повы-
шеніи температуры диссоціируютъ. Приводимъ нѣкоторыя изъ чиселъ д
для различныхъ р и і.
р мм. 40° 70° 100° 140° 160° 200° 240° 260° 280°
20 54,22 43,55 35,63 31.32 — — — — —
100 — 51,21 41,81 33,72 32,10 — — — —
Разныя свойства ненасыщенныхъ паровъ.
649
р мм. 40° 70° 100° 140° 160° 200° 240° 260° 280°
300 — — 48,50 38,05 — — — — —
1000 — — — 46.81 41,82 — — — —
2000 — — — — 47,81 32,64 34,00 32,89 32,21
5000 — — — — — 47,90 38,79 36,39 34,66
10000 — — — — — — 47,60 42,80 39,10
16000 — — — — — — — 53,00 45,45
24000 — — — — — — •— — 60,70
За послѣдніе годы были произведены многочисленныя и плодотвор-
ныя изслѣдованія изотермъ кислорода, водорода и гелія Каттеіііп^іі
Оппез’омъ и его учениками бсііаік^ізк’омъ, Вгаак’омъ и НупсІ-
тапп’омъ въ Лейденѣ. Для кислорода мы приведемъ лишь крайнія
значенія, между которыми производились измѣренія. При 0° и 1 атм.
принято рѵ = 1.
і — 20,00° ^=16,60° І = 0,9°
р рѵ р рѵ р рѵ
23,713 1,0549 36,208 1,0303 22,401 0,9762
65,396 1,0362 51,464 1,0224 66,787 0,9477.
Для водорода впервые измѣрилъ изотермы при 20° 8с 11 а 1 кдѵі] к
въ Лейденѣ. Онъ нашелъ
рѵ = 1,07258 Д- 0,0006675 (І Д- 0,00000098^,
гдѣ б/= —плотность и р выражено въ атмосферахъ. Затѣмъ появился
рядъ изслѣдованій Каттегііп^іі Оппез’а, Вгаак’а и Нупсі-
тапп’а (1901—1907); мы здѣсь также приведемъ лишь крайнія значе-
нія произведенія рѵ при различныхъ температурахъ; рх — наименьшее,
р2 — наибольшее давленіе, ѵх и ѵ2 — соотвѣтственные объемы.
і — 200° 0° — 103,57° — 139,88° 182,81° - 204,70° - 212,82° — 217,41°
рх 47.837 44,996 28,447 25.406 20.406 16,749 15,416 14,633
р2 — 56,447 53,249 58,368 18,558 62,889 61,917 61,434 58,971
рхѵх = 1,1040 1,0293 0,63261 0,49459 0,32704 0,24036 0,20644 0,18738
р2ѵ2 = 1,1095 1,0346 0,64694 0,50232 0,33028 0,23009 0,18863 *0,16422.
мы не приводимъ.
Числа, относящіяся къ / = — 164,14° и — 195,27°
Чрезвычайно интересны изотермы гелія (1908):
і Рі = 100,35° 42,574 20,00° 27,539 0° 26,634 — 103,570 — 182,75° - 216,56° 9,564 1— 252,72° ' 53,948 258,82° 40,012
20,580 13,751
Р2 66,590 53,708 50,240 33,383 18,189 11,448 | 65,997 59,797
1,38725 1,08664 1,01392 0,63135 , 0,33787 0,21132 0,09120 0.06150
Р2Ѵ2~ 1,39929 1,009918 1,02521 0,63845 [ 0,34025 0,21219 0,09867 0,07531.
При і =— 258,82° и рх = 40,012 атм. рхѵх почти въ 16 разъ меньше
величины, соотвѣтствующей идеальному газовому состоянію !
Вопросомъ о тепловомъ расширеніи паровъ занимались С а Ь о и г 8 ,
Ногвѣшапп. Нігп, Ведпаиіі. Неглѵі^ и Агоа^аі. Приводимъ
650
Ненасыщенные пары.
нѣкоторыя изъ чиселъ, данныхъ С а Ь о и г 8’омъ для средняго коеффи-
ціента расширенія а между температурами и і.
Треххлористый фосфоръ. Уксусная кислота. Вода.
4) 182" 70 — 124° Іо - 107°
і а і а І а
190 0,00501 130 0,00854 110 0,00509
250 0,00874 160 0,01078 120 0,00615
300 0,00403 200 0,00762 150 0,00448
336 0,0305 336 0,00369 250. 0,00369.
Нігп нашелъ для водяныхъ паровъ слѣдующія значенія а между 0° и /°.
і = 118,5 162 200 246,5
а = 0,004187 0,004071 0,003938 0,003799.
Величина а приближается съ возрастающимъ і къ числу 0,00366,
относящемуся къ идеальнымъ газамъ. Неглѵі^ нашелъ для С52 число
а =0,0044 при і = 90° и давленіи въ 2500 мм., когда пары насыщены.
Ата^аі опредѣлялъ а для 5О2 и СО2 отъ 0° до 250° черезъ 1 гра-
дусъ. Онъ находитъ между 0° и 10° для перваго газа а 0,004130, для
второго газа а - - 0,003724; при 250° коеффиціенты расширенія равны
0,003685 и 0,003682, т.-е. почти равны между собою.
§ 4. Формула Ѵап-сІег-АѴааІз’а. Существуетъ весьма большое число
попытокъ выразить формулою вида /(у, р, /) = 0 уравненіе состоянія ве-
щества въ парообразномъ состояніи. Особый интересъ представляютъ тѣ
формулы, которыя должны сразу обнимать какъ парообразное, такъ и жид-
кое состояніе. Эти формулы играютъ важную роль въ ученіи о крити-
ческомъ состояніи, а потому необходимо прежде всего ознакомиться съ
важнѣйшими изъ этихъ формулъ. Наибольшею извѣстностью пользуется
знаменитая формула Ѵап-дег-АѴааІ8’а, на которую намъ уже не-
однократно приходилось указывать (напр. т. I) и даже ею пользоваться
(т. III, стр. 130). Эту формулу прежде всего и разсмотримъ. Она имѣ-
етъ видъ: / . а\ ,
+ Ь)= рт.......................(3)
гдѣ а, й, и 7? постоянныя числа. Укажемъ вкратцѣ на тѣ разсужденія,
которыя привели V а п - <1 е г - АѴ а а 18’а къ этому виду уравненія состо-
янія. Въ т. 1 мы вывели уравненіе рѵ = ЦТ на основаніи кинети-
ческой теоріи газовъ, не обращая вниманія на объемъ, занимаемый
молекулами газа, и на тѣ силы, которыя дѣйствуютъ между ними. Пусть
2г наименьшее разстояніе, до котораго могутъ сблизиться центры двухъ
молекулъ, такъ что г радіусъ молекулы (или, можетъ быть, сферы ея дѣй-
ствія) ; сумму объемовъ всѣхъ молекулъ, находящихся въ объемѣ ѵ, обо-
значимъ черезъ -ге/; свободный для движенія объемъ равенъ ѵ — ѵѵ. Умень-
шеніе свободнаго пространства должно уменьшить среднюю длину пути
молекулъ (т. I) на нѣкоторую величину, которую можно положить рав-
ной /г. Сокращеніе средняго пути должно увеличить число ударовъ мо-
лекулъ, т.-е. должно вліять, какъ фактическое уменьшеніе объема ѵ на
Формула Ѵап-НегАѴааІй’а.
651
нѣкоторую величину Ь.
Теорія, которой мы не развиваемъ, показываетъ,
что Ь зависитъ отъ у.
V а п - 4 е г - ААГ а а 1 8 находитъ, что
6 = 4^; 0. Е. М е у е г
полагаетъ, что у = и что Ь = 4
1
7= и что
1'2 а Мы
остановимся на первомъ выводѣ, т.-е. что Нравно учетверенному мо-
лекулярному объему тел Вліяніе силъ сцѣпленія, существующаго между
молекулами газа, должно обнаружиться присутствіемъ силъ, дѣйствующихъ
по направленію во внутрь газа на частицы, расположенныя на погранич-
ной поверхности газа. Вслѣдствіе этого наблюдаемое давленіе р должно быть
меньше того давленія р0, которое обнаружилъ бы идеальный газъ. Пусть
Р Ро Ра или А) = Р+Рі ; въ Формулу щя идеальныхъ газовъ р{& =
РТ мы должны вмѣсто Ро вставить р + рг. Величина силы рг должна
быть пропорціональна произведенію массы пограничнаго слоя газа на
массу остального газа; эти двѣ массы пропорціональны плотности, т.-е.
степени сгущенія даннаго газа, пли обратно пропорціональны объему ѵ.
занимаемому даннымъ количествомъ газа. Отсюда ясно, что рг обратно
пропорціонально ѵ2, и что въ формулѣ рѵ = РТ слѣдуетъ р замѣнить тѣмъ
двучленомъ, который находится въ формулѣ V ап - 4 ег - АѴ а аі 8’а. При-
веденныя здѣсь разсужденія неоднократно подвергались принципіальной
критикѣ; укажемъ, напр., на статьи Н. Я. Сонина и 4 а е е г’а.
Несомнѣнно, что уравненіе V а п - (1 е г - АѴ а а 1 в’а не исчерпываетъ
вопроса; оно точнѣе уравненія рѵ = РТ, но не съ абсолютною точ-
ностью совпадаеть съ истиннымъ уравненіемъ. Замѣтимъ, что по Ѵап-
4 е г - АѴ а а 18’у его уравненіе должно относиться какъ къ г а з о -
о б разному (къ пару), такъ и къ жидко му состоянію веще-
ства. Самъ Ѵап-4ег-АѴааІ8 указываетъ, что его уравненіе пере-
стаетъ быть вѣрнымъ, когда ѵ < 2й, что въ этомъ случаѣ величина й, сто-
ящая въ формулѣ, должна быть уменьшена. Сравненіе формулы Ѵап-4ег-
АѴ а а 18’а съ результатами опытныхъ изслѣдованій, разсмотрѣнныхъ въ
предыдущемъ параграфѣ, показало, что вообще а не есть число постоян-
ное, но что оно зависитъ отъ температуры.
Приложеніе формулы Ѵап-4ег-АѴааІ8’а къ вопросу о тепловомъ
расширеніи газовъ уже было разсмотрѣно на стр. 130; особенно важное
ея приложеніе къ вопросу о критическомъ состояніи будетъ разобрано
ниже. Теперь намъ остается сказать о нѣкоторыхъ слѣдствіяхъ, вытека-
ющихъ изъ этой формулы. Прежде всего укажемъ на нѣкоторыя ея пре-
образованія. Съ правой стороны положимъ РТ 7?^ + ^=7?71-|-а^),
гдѣ 7?' 7? : а. Если за единицу объема принять объемъ газа при і = 0°
и при единицѣ давленія (р = 1). то получается (1 + —Ь) •= И'. Под-
ставляя это значеніе для 7?', имѣемъ:
?+")(» = Ь)(1+а() . ... (4)
V6 /
652
Ненасыщенные пары.
Понятно, что и здѣсь число постоянныхъ, характерныхъ для даннаго
вещества, не два (а и 6), но три; третья скрыта въ величинѣ ѵ, измѣ-
ряемой для каждаго газа особой единицей, замѣняющей постоянную 7? въ
уравненіи (3). Послѣднее уравненіе можно написать еще въ такихъ формахъ:
КТ _ а
ѵ — Ь ѵ2 '
р
(5)
(6)
Если температура постоянна, то можно всю правую сторону уравне-
нія (4) обозначить одною буквою С и написать ото уравненіе въ видѣ
„ а , аЬ , , ,„ь
Рѵ с—ѵ + ~2+Ьр..........................(7)
При ^ = Соп8І. можно ур. (5) написать въ видѣ
р АТ—В........................
Это уравненіе показываетъ, что при координатахъ р и Т линіи по-
стояннаго" объема (изохоры) должны [быть прямыя. Съ этимъ вполнѣ
согласуются результаты, которые В а ш 8 а у и 8. У о и п нашли для СО2.
для паровъ эфира и для другихъ паровъ, а также Козе-Іппез и
8. Тои六 для пентана и изопентана. Приближенную формулу
можно получить, если въ (7) пренебречь членомъ, содержащимъ весьма ма-
лое произведеніе аЬ; если і = 0, или не очень отличается отъ нуля, то
величина С — й)(1+а/") мало отличается отъ единицы и по-
тому мы можемъ во второмъ членѣ справа вмѣсто 1: ѵ поставить р. Тогді
получается _
Л рѵ С (а — Ь)р..........................(9)
Эта формула показываетъ, что газъ, для котораго случайно
Ь = а, или эти постоянныя мало отличаются другъ отъ
друга, долженъ обладать свойствами идеальнаго газа.
Обратно, если газъ слѣдуетъ законамъ Бойля и Гей-Люссака, то
отсюда нельзя заключить, что молекулярный объемъ ѵѵ и внутреннее
сцѣпленіе ничтожны. Возможно что случайно для этого газа а и Ь
имѣютъ почти одинаковое значеніе. Нѣсколько болѣе точное выраженіе
получается, если сохранить въ (7) третій членъ справа, поставивъ и въ
немъ р вмѣсто 1 ; ѵ. Тогда получается
' рѵ С (а— Ь)р-\-аЬр2................... . (10)
Величина а можетъ быть опредѣлена для даннаго газа путемъ измѣ-
ренія термическаго коеффиціента давленія ар для котораго мы на стр. 131
вывели формулу (71):
I 1 “И і о I сс • • - (11)
р \ М) /
Формула Ѵап-сІегЛѴааІе’а.
653
Здѣсь а значеніе того же коеффиціента для идеальныхъ газовъ; мы
можемъ для него принять значеніе ар* найденное для водорода, т.-е. по-
ложить а - = 0,00366. Зная ар для другого газа или пара, мы найдемъ
число а. Общее уравненіе (3) даетъ затѣмъ число &, если извѣстны ве-
личины р, ѵ и Т. Впрочемъ мы увидимъ ниже, что наблюденія надъ
критическимъ состояніемъ вещества приводятъ къ непосредственному
опредѣленію величины Ь. Число а должно быть постоянное для даннаго
вещества. Однако, если вычислять а для различныхъ температуръ и при-
томъ для такихъ веществъ, какъ СО2, 5О2 и т. под., то оказывается, что
число а съ повышеніемъ температуры уменьшается. Такъ,
изъ опытовъ Апйгечѵз’а надъ СО2 получается а = 0,о0777 при 64° и
<2 = 0.00748 при 100°. Изъ опытовъ Аша^аі получаются для СО2 та-
кія числа: <2=0,00824 при 40°, <2 ^0,00795 при 70°, <2 = 0,00766 при
100° и <2 = 0,00742 при 258°.
биуе и ВгісІегісЬ вычислили значенія величинъ <2 и Ь для
83-хъ веществъ; способъ, которымъ они пользовались, мы разсмотримъ
въ ученіи о критическомъ состояніи (§ 6 этой главы).
Мы видѣли на стр. 64б, что произведеніе рѵ, разсматриваемое п р и
постоянной температурѣ, какъ функція отъ р, имѣетъ минимумъ,
и что геометрическое мѣсто минимумовъ на изотермахъ рѵ —/(р) пред-
ставляетъ кривую, напоминающую параболу. Съ этимъ ’ вполнѣ согласу-
ется формула Ѵап-(Іег- АѴ ааів’а, какъ это видно изъ приближенной
формулы (10) для газовъ, для которыхъ а^>Ь. Эта формула показыва-
етъ, что при малыхъ р произведеніе рѵ уменьшается, когда р растетъ;
при весьма большихъ р послѣдній членъ получаетъ перевѣсъ и рѵ опять
начинаетъ расти. Полный теоретическій разборъ этого вопроса принад-
лежитъ Л. Богаевскому; приводимъ вкратцѣ его выводъ. Если
изъ (7) вычислить д(рѵ) : др и въ выраженіе этой производной подста-
вить вмѣсто дѵ : др ея значеніе, взятое изъ (3), то получается
д( рѵ) _ аѵ(ѵ — Ь)2 — ПЬ Тѵ^
др 2а(ѵ - Ь)2 — /? Тѵ^ ‘
Приравнявъ это выраженіе нулю, получаемъ
а(ѵ— д)2— #дТѵ2 = О.....................(12)
Корень этого уравненія, который долженъ быть больше Ь равенъ
...........................................................
| а
Уравненіе (12) приводится, на основаніи (3), къ виду Ьрѵ2 аѵ-\-
-[-2<2&=0; вставивъ ѵ = ѵх, получаемъ р{ въ видѣ
= а(Ѵ1 — 2&).......................(12
Ьѵ±2
654
Ненасыщенные пары.
Изслѣдованіе второй производной показываетъ, что ѵ} и рх соотвѣт-
ствуютъ минимуму величины рѵ ~/(р} при данномъ Т. Формула (Г2,я)
показываетъ, что минимумъ существуетъ только при Т< Г е о м е -
представляетъ кривую, уравненіе
Уравненіе Ѵап-йет-АѴааІз’а
трическое мѣсто минимумовъ
которой вида р) = 0, гдѣ г — рѵ.
можно написать въ видѣ
а аЬ „
гр + 7р--
г #Т Ьр
V. . (Іг
У словіе ф = 0 даетъ
Ьг2 — аг + '2аЬр - о.
Это и есть искомое уравненіе ір(г,/7) = О. Мы видимъ, что эта кри-
вая есть парабола; вершина ея лежитъ на
динаты вершины суть гг
а
8Г2’
а
* = 2Ь-
ѵ 9 а
изотермѣ /1 = ^^5 коор-
Если уравненіе (3) написать въ видѣ
ЬРТ
ѵ— Ь
а
ѵ 1
то становится ясно, что на каждой изотермѣ имѣется точка, въ которой
она пересѣкается идеальной изотермой рѵ = ЯТ. Эту точк} Бачин-
скій (1906) называетъ орто метрической точкой. Если орто-
метрическій объемъ обозначить чрезъ ѵ\ то
Ь^Т = а
ѵг — Ь ѵг
(12, С)
Такимъ образомъ ортометрическая плотность является линейной функ-
ціей температуры. Для окиси этила Бачинскій находитъ, что урав-
неніе (12,г) подтверждается измѣреніями Аша^аі; въ этомъ случаѣ
-1- =0,7586 — 0,000923^.
ѵ‘
Перейдемъ къ важному вопросу о видѣ изотермъ ѵ =/(р\ по-
лучаемыхъ на основаніи формулы Ѵап-сІег-ЛѴааІз’а, если положить
Т= Сопві. Вспомнимъ, что для идеальныхъ газовъ изотермы рѵ =#Тпредста-
вляютъ равностороннія гиперболы. Если въ уравненіи (5) Ѵап-сіег-
\ѴааІ8’а Т очень большая величина, то послѣднимъ членомъ можно прене-
бречь и тогда уравненіе изотермы принимаетъ видъ р(у — Ь) — ЦТ; это та
же гипербола, сдвинутая на величину Ь въ сторону возрастающихъ ѵ. На
рис. 199 АВ представляетъ одну изъ изотермъ при большомъ Т. Общее
уравненіе (6) изотермы показываетъ, что даннымъ Г и р соотвѣтствуютъ три
Формула Ѵап-гіегЛѴааІв’а.
655
значенія ѵ2 и т/3 объема, изъ которыхъ должны быть вещественны одно
или всѣ три. При большихъ Т
изотермы имѣютъ видъ кривой
СО; прямая, параллельная оси
абсциссъ, пересѣкаетъ ее только
въ одной точкѣ, т.-е. изъ трехъ
корней одинъ только веществен-
ный, и даннымъ Т и р соот-
вѣтствуетъ только одинъ фи-
зически возможный объемъ, а
слѣд. и одно физически
возможное состояніе.При
нѣкоторомъ опредѣленномъ Т=
= 273 4- получается изотер-
ма/:/7, содержащая точку К, въ
которой касательная параллель-
на оси абсциссъ. Въ этой точкѣ
ѵ перегиба изотермы = 0и
дѣлаются вещественными
точки {обозначимъ черезъ
и Я. Корни уравненія (6)
всѣ три корня уравненія (6)
и равными между собою. Координаты этой
р = л и ѵ = д). Опредѣлимъ величины лг, д
должны удовлетворять условіямъ:
. , , , КТ
^і + ^ + ^з = * + — ,
^2 + ѴѴѴ3 4- ^3 =
аЬ
Подставивъ ѵѵ = ѵ2 = ѵ3 = у, р~л и 7'=^4-273, получаемъ
3<р = Ь + ^ + 273) 2 = а = аЬ
л лг л
Ъф* = —,
лг
откуда легко получается
<р = 3б
1 а
л=--—
27 [р
(13)
273
Тѣ же значенія мы получаемъ, рѣшая ур. (5) и два уравненія о и
д2р вѵ
—— = О относительно ѵ, р и Т.! Если ввести /? = а/?' = а(1 -|- а) (1 — 6),
дѵ2
гдѣ а = 1 : 273, то получается
8а
1 4- аг> =
276(1 4-а)(1— Ь)
(13,а) ,
Мы увидимъ ниже, какое физическое значеніе имѣетъ точка К
8 а
27 ЬР
656
Ненасыщенные пары.
При $ имѣемъ одинъ вещественный корень ; при і С # всѣ три
корня вещественны и изотерма имѣетъ видъ кривой СНЬМ. Однако,
если построить изотерму для такой температуры основываясь на опы-
тахъ, то оказывается слѣдующее: при большихъ ѵ и малыхъ р веще-
ство находится въ парообразномъ состояніи; при уменьшеніи ѵ получа-
ется часть МЬ кривой МЬНСц которую назовемъ теоретической
изотермой. Въ точкѣ Ь начинается о ж и ж е и і е : дальнѣйшее умень-
шеніе ѵ происходитъ при постоянномъ р, т.-е. изотерма есть прямая ли-
нія Ьса. Въ точкѣ а вся масса вещества перешла въ жидкое состояніе ; даль-
нѣйшее уменьшеніе объема происходитъ по изотермѣ аО. соотвѣтствующей
жидкому состоянію вещества. Физическая изотерма имѣетъ
видъ СаЬсМ. Первый Яатез ТЬотвоп (1871) указалъ (еще до
Ѵап-йег-ЛѴааІ 8’а), что если бы оказалось возможнымъ найти непре-
рывный переходъ вещества изъ газообразнаго состо-
янія въ жидкое, т.-е. такой изотермическій переходъ, при которомъ
вещество все время оставалось бы однороднымъ, то изотерма должна
была бы имѣть видъ кривой СН7М. Но такой переходъ до сихъ поръ
не оказался осуществимымъ; вѣтвь НЬ выражаетъ состояніе вещества,
при которомъ большему давленію соотвѣтствуетъ большій объемъ (при
Т = Соп8І.); такое состояніе можетъ быть только неустойчивымъ.
Махлѵеіі и Сіаизіив показали, черезъ какія двѣ точки а и Ь
теоретической изотермы должна пройти прямая асЬ. Ихъ разсужденіе
слѣдующее: если бы переходъ аНсЬЬ .былъ осуществимъ, то мы могли
бы произвести изотермическій обратимый круговой процессъ аНсЬЬса
для котораго О. Но Т = Соп8ѣ., слѣд. = 0; отсюда слѣду-
етъ, что и площадь, ограниченная кривой аНсЬЬса, равна нулю, или что
площади аНса и сЬЬс геометрически равны между собою. Отсюда слѣ-
дуетъ равенство площадей 8асЬ7 и ЗаНсЬЬТ. Но 0Ь = 8, ОТ -6, гдѣ,
какъ прежде, 5 и б удѣльные объемы жидкости и пара. Такимъ обра-
зомъ получается уравненіе Мах\ѵе11-С1ап8Іи8’а
б
о р(б — 8) = ^рсіѵ.................(14)
5
гдѣ интегрированіе должно производиться вдоль теоретической
изотермы. Ріапск далъ другой выводъ формулы (14).
Если въ (14) подставить р изъ уравненія Ѵап-(Іег-АѴааІв’а,
см. (5) стр. 652, то получается
р{в^5> .................................<15>
Такъ какъ точки а (8.р) и Ъ (б,р) лежатъ на теоретической изо-
термѣ (5), то мы должны имѣть:
Формула Ѵап-(кг-\ѴааІ8’а.
657
= /?Г
? б — Ь б2
КТ
8 — Ь 82
(16)
Три уравненія (15) и (16), рѣшить которыя при данныхъ /?, а и Ь до-
вольно трудно, даютъ упругость/? насыщеннаго пара и удѣль-
ные объемы 5 и ^жидкости и насыщеннаго пара, какъ
функціи температуры. Формула (25,с) стр. 550 даетъ тогда и
скрытую теплоту испаренія о, какъ функцію температуры. Итакъ
величины /?, 5, б и р могутъ быть вычислены для даннаго Т, если из-
вѣстно уравненіе состоянія вещества.
НІГ8СІ1 (1899) показалъ, что формулами (16) и (14) можно восполь-
зоваться для опредѣленія численныхъ значеній величинъ а и Ь. Оказа-
лось, что для толуола, ксилола и нѣкоторыхъ кислотъ съ повышеніемъ
температуры величина а увеличивается, а величина Ь уменьшается, т.-е.
что эти двѣ < постоянныя?, въ дѣйствительности, функціи температуры.
Ниже мы встрѣтимся съ нѣкоторыми попытками осуществить хотя
бы часть тѣхъ состояній вещества, которыя выражаются кривою аНсЬЬ.
Формула Ѵап-(1ег-ЛѴааІ8’а должна, какъ это видно изъ преды-
дущаго, одинаково относиться, какъ къ парообразному, такъ и къ жид-
кому состоянію вещества. Однако изслѣдованія Надеждина, Огі-
таЫі и др. показали, что уравненіе состоянія жидкости вообще не мо-
жетъ быть выражено формулою Ѵап-сІег-ЛѴ ааі8’а, которая, какъ было*
сказано, во всякомъ случаѣ перестаетъ быть вѣрною при ѵ < 2Ь. Д. П. Ко-
новаловъ показалъ, что если пренебречь работою внѣшняго давленія
при измѣненіи объема жидкости, то можно вывести изъ уравненія Vап-
сі ег-ЛѴ ааі 8’а формулу для теплового расширенія жидкостей, которая
была предложена Д. И. Менделѣевымъ (см. стр. 127). .
Уравненіе состоянія, связывающее три перемѣнныя, представляетъ,
вообще говоря, уравненіе нѣкоторой поверхности, называемой термо-
динамической поверхностью. 6іЬЬ8 первый указалъ на пре-
имущества такой поверхности въ случаѣ, если за перемѣнныя принять
объемъ г/, энергію е и энтропію ??. Д- А. Г о л ь д г а м м е р ъ обстоятельно
изслѣдовалъ эту поверхность для вещества Н2(Х т.-е. для воды и пара,
исходя изъ уравненія Vап-йег-АѴааІз’а, въ которое вмѣсто р и Т
были введены е и і].
V а п - а е г - \Ѵ а а 18 обобщилъ (1890) свою формулу для случая
с м ѣ с и нѣсколькихъ газовъ. Ограничиваемся указаніемъ, что К о г 1 е -
лѵ е §, Віиещске, К и е п е п, В ап. Вегіііеіоі занимались теорети-
ческимъ и экспериментальнымъ изслѣдованіемъ этой обобщенной формулы
Ѵап-а ег - ДѴааіз'а.
§ 5. Формула Сіаизінз’а и другія. Мы уже упомянули, что число а,
встрѣчающееся въ формулѣ V а п - а е г - ЛѴ а а 18’а повидимому уменьша-
ется. когда температура увеличивается. Сіаиніиз (1880) предположилъ,
КУРСЪ ФИЗИКИ О. X В О Л Ь С О Н А. т. III, изд. 3-е. 42
658
Ненасыщенные пары.
что оно обратно пропорціонально абсолютной температурѣ Т; вмѣстѣ съ
тѣмъ онъ ввелъ еще новую, четвертую постоянную, вводя ѵ-\-с вмѣсто
ѵ въ послѣднемъ членѣ формулы (5) стр. 652. Такимъ образомъ онъ по-
ла чилъ свою первую формулу
Р = —....................................<17)
ѵ — Ъ Т(ѵ + с)2 ѵ
Впослѣдствіи (1881) Сіаизіиз еще болѣе усложнила» это уравне-
ніе и остановился на второй формулѣ
_ АТ~п — В
$ ѵ — Ь (ѵ + с)2
содержащей пять постоянныхъ /?, Ь, А, В и с.
(18)
Эту формулу невозможно
обосновать теоретически и на нее
слѣдуетъ смотрѣть, какъ на формулу
эмпирическую.
Изотермы, уравненіе кото-
рыхъ получается, если въ (17) поло-
жить Т === Соп8І., имѣютъ вообще
тотъ же характеръ, какъ и изотермы
Ѵап-сіег- АѴааІб’а, разсмотрѣнныя
на стр. 655 (см. рис. 199). При
очень большихъ Т имѣемъ гиперболы
р(ѵ — = ПТ. При меньшихъ Т изо-
термы имѣютъ видъ кривой СО на
рис. 199. Принѣкоторомъ Г=$-|-273
получается изотерма вида ЕО съ
точкою /С, въ которой (і2р: (Іѵ2 — 0 и
Рис. 200.
касательная параллельна оси абсциссъ.
Координаты ѵ = д) и р = л; точки К,
а также величину $ мы получимъ тѣмъ же способомъ, которымъ мы поль-
зовались на стр. 655. Подставимъ для удобства ѵ Ц- с = V и Ь А- с = В
тогда первое уравненіе Сіапзіиз’а приводится къ виду
у3 [ватѵ—
Р ) рТ рТ
Обозначивъ корни этого уравненія черезъ Уь У2, и Г3, имѣемъ:
Ѵі+Ѵу-І-Уз — 5-1- ? ; УіУ> + У2Уі + ' ^^2^3—рТ
Полагая — У2 = У8 = у + с, Т — 0 273 и р = л получимъ легко
у = ЗЬ ~1~ 2С
2 _ _1
™ ~ 210 (Н-08
(19)
(273 + У>)‘2
8 а
27^ + с)
Уравненія состоянія.
659
__ /?($ + 273)
8(Ъ +>)
................. . . (19,а)
Иначе получимъ тѣ же значенія,
др п д2р
ненія = О и = і) подставимъ
если въ ур. (17), а также въ урав-
Т = 273, ѵ = д), р — л и рѣ-
шимъ эти три уравненія относительно $, у и л. Если то уравне-
ніе (17) имѣетъ три вещественные корня; теоретическая изотерма
(см. стр. 656) имѣетъ видь кривой РЕОСВАН (рис. 2оо), между тѣмъ
какъ физическая изотерма имѣетъ форму РЕСАН. Часть РЕ со-
отвѣтствуетъ жидкому состоянію, прямая ЕА испаренію, а часть АРІ
парообразному состоянію вещества. Въ Е объемъ ѵ — 8. въ А имѣемъ
ѵ = б. Площади ЕОСЕ и СВ АС должны быть равны, а слѣд. уравненіе
(14) МахлѵеП-СІаизіиз’а должно быть вѣрнымъ и здѣсь. Подставляя
подъ интеграломъ вмѣсто р его значеніе (17), получаемъ
/ ч п'гі — Ь а I 1 1 \ , .
р(а О = ЯЛд . . . (20)
О С/ I I О | С V Г С I
Прибавивъ, два уравненія
КТ _ а _ КТ а
? 8 Ь Т(8-\-с}2 б- Ь Т{б-\-С)2................
выражающія, что точки Е и А лежатъ на теоретической изотермѣ, мы
получаемъ три уравненія для опредѣленія упругости р и удѣльнаго объ-
ема б насыщеннаго пара и удѣльнаго объема 5 жидкости, а затѣмъ
на основаніи (25.с) стр. 550 и скрытую теплоту испаренія р, какъ функ-
ціи температуры. Сіаизіиз и Ріапск показали, какимъ образомъ
можно рѣшать уравненія (20) и (21).
Мы видѣли, что для всякаго даннаго Т произведеніе рѵ должно имѣть
минимумъ (стр. 646). Если (17) помножить на ѵ и приравнять производ-
ную по ѵ нулю, то получается уравненіе
ЬКТ2(ѵ + ^)3 = а(ѵ — с)(ѵ — 6)2,
вещественный корень котораго опредѣляетъ то значеніе объема ѵ, при ко-
торомъ на изотермѣ 7'=Соп8І. произведеніе рѵ имѣетъ наименьшее
значеніе.
Любопытно, что при большихъ ѵ получается уравненіе Лоиіе’я
и Т Ь о ш 8 о п’а, см. (23) стр. 461, изъ уравненія Г1 а и 8 і и 8’а, если ввести
нѣкоторыя упрощенія. Если въ (17) пренебречь величинами Ъ и с срав-
нительно съ ѵ и все уравненіе помножить на ѵ'. р. то получается
КТ а
Ѵ р ѵрТ *
Въ добавочномѣ членѣ можно подставить ѵр = КТ; тогда имѣемъ
рѵ = КТ -
ар
КТ2 ’
а это очевидно и есть уравненіе Лоиіе’я и Т1іот8оп’а.
42*
660
Ненасыщенные Пары.
С1аи8ІП8 полагалъ, что его первая формула (17) можетъ слу-
жить уравненіемъ состоянія углекислаго газа. Наблюденія А п -
сігелѵй’а, о которыхъ будетъ сказано ниже, привели его къ слѣдующимъ
значеніямъ величинъ /?. а, Ь и с (для СО2), которыя мы приводимъ въ
различныхъ единицахъ, не всегда указываемыхъ, когда эти числа приво-
дятся; вѣсъ газа 1 килогр.
1. р въ килогр. на кв. метръ, ѵ въ куб. метрахъ:
/? = 19,273 6= 0,000426 а = 5533 с= 0,000494.
2. р въ атмосферахъ, ѵ въ куб. метрахъ:
/?= 0,001865 6=0,000426 а = 0,535469 с = 0,000494.
3. р въ атмосферахъ, ѵ = 1 при 0° и р = 1 атмосф. :
/? = 0,003688 6 = 0,0оо843 «= 2,0935 с = 0.000977.
Значеніе /? одинаково для всѣхъ газовъ. Віиетске вычислилъ
таблицу для р при различныхъ *ѵ и Т на основаніи послѣднихъ чиселъ.
Столѣтовъ нашелъ въ ней нѣсколько ошибокъ и далъ новый рису-
нокъ теоретическихъ изотермъ для СО2 по Сіаивіиз’у. 8а г гаи вы-
числилъ на основаніи опытовъ Аша^аі величины Ь, а и с (третья си-
стема единицъ) для /72, 7Ѵ2, О2, СТУ4, С2Н± и СО2. Рііг§ега1(1 прило-
жилъ формулу С1 а и 8 іи8’а къ опытамъ К а т 8 ау и V оип ^’а надъ па-
рами алкоголя.
Къ парамъ эфира. воды и др. С1 а и 8 і и 8 приложилъ свою вто-
рую формулу (18); онъ находитъ слѣдующія числовыя значенія посто-
янныхъ (первая система единицъ):
6 А В с п
Эфиръ . 1,4318 0,001088 15,607 0,0044964 0,0006476 1,19233
Вода . 47,05 0,000754 45,17 0,00737 0,001815 1,24.
Мапаіга находитъ на основаніи опытовъ Ваѣѣеііі (стр. 647; для
водяныхъ паровъ: /?=47,05, 6 = 0,00084216, А = 34.38. В — 0,004465,
с= 0,00102134, /7=1,24962.
Мы довольно подробно разсмотрѣли уравненія состоянія, предложен-
ныя Vап-(іег-АѴааіб’омъ и СІ аизіив’омъ. Кромѣ этихъ уравне-
ній, существуетъ еще весьма большое число другихъ, предложенныхъ
различными учеными. Мы не будемъ указывать на пути, приведшіе къ
этимъ уравненіямъ и не будемъ заниматься разборомъ послѣднихъ; но мы
считаемъ не безполезнымъ составить списокъ этихъ формулъ, хотя бы и
неполный. Уравненій состоянія, которыя относятся только къ жидкостямъ,
мы не приводимъ.
Ѵап (1 ег ДѴааІ8 . . ^ + ^2^ -Ь)=#Т.......................(22)
(і я \
Р + — 6) — КТ . . . (23)
Уравненія состоянія.
661
I АТ~п В\
Сіаизіие, II . . . . -|—, (г1 --/>) =/?7. . . (24)
\ (г' + О2 /
Нігп, I . . • (р+а)(ѵ—Ь) — РТ.............(25)
Предложено еще до V ап-сіег-)Ѵа аіа'а.
Нігп, II и Оизіаѵ 8с1іті<Н рѵ = ВТ Сѵ—п (25,а)
Эта формула должна была относиться къ водянымъ парамъ
К ат тегіі пОппез^р ѵ) = РТ . . . . (26)
Ь
Здѣсь'ф(б.ѵ) есть функція, разложимая по степенямъ величины
.. ,. .о /?(1 аі) С(1-|-а() (ок/ті
Моиііп . . Р+-2= ..........(2ь’а}
Здѣсь /?, а, С, а — постоянныя. При/? = Сопві. Ь: ѵ — Ьо: ѵ^, гдѣ
Ьо и ѵ0 относятся къ 0°, а г имѣетъ одинаковое значеніе для всѣхъ р.
Если 7= Сопяѣ, то Ь-. ѵп = Ь{ : ѵрг. гдѣ Ь{ и относятся къ р=1 атм.,
а п зависитъ отъ I.
Н. \. Ь оге піи
I , а\ , Ь\
\р + -зІѵ~ ЯТ\ 1 + -1
\ ѵ2] \ ѵ /
(26,6)
Кеіп^апиш.
РТ
(2б,с)
Здѣсь А линейная функція Т Слѣдующее уравненіе представ-
ляетъ собою улучшенное уравненіе Н. А. Ьогепіи’а:
И Ь
8 ѵ
Ѵап Ьа а г
(26.с/)
(26, е)
1 2 V + 16 V2
Т и т 1 і г и
рѵ — ВТ ср . . . . (26,/)
КпоЫапсЬ, Ьіпііе и КІеЬе рѵ=ВТ р(\-\-сцА
(г/278\3
| ( Т )
(26,^)
А т а § а I
Ѵіоіі .
а)= д>(а)
М(р а)
-1 + ’ ’
2[ѵ(1 -- 6)(1 а?)]2]^1
(27І
(28)
Т
662
Ненасыщенные пары.
Таіі . . . ............(25)
Вапкіпе, ТЬотзоп и Я оиіе. рѵ — РТ ^ ... . (30)
Оиргё.......................Дг,-}-с) = /?7 ... (31)
Кеуе........................р\ѵ — (аТ+Р)] = ПТ (32)
Вескпадеі....................рѵ = РТ 1 — . (33)
Это уравненіе для СО2; М( упругость насыщеннаго пара при /°.
Ооиіііу и Ветігап а . (р+а)(ѵ-}-Ь)-[-сТ=О ... (34)
Вегігапа..........рѵ = #(Т-\- р)............(35)
йеипегиЬеаоих . . рѵ = ВТ—Срп...............(36)
Слѣдующія четыре уравненія представляютъ видоизмѣненія уравненія
Сіаиеіие’а:
„ НТ Са~Т
Заггаи . . . р =-------_............................./37)
ѵ — Ь (ѵ-\-сУ у ’
_а
РТ Ср ?
.’ае^ег . . . ................(38)
тТ ^А-пТ1' , ч
Ваііеііі . . . » = ---------------------- (За)
и ѵ — Ь (ѵ + № .........ѵ >
См. (2) стр. 647.
Шиллеръ. . . р + 7^^2-р^ —7Т’)=/?7 . . . . (40)
(1 +
—---И — ..............(41)
2/ Ѵ
Апіоіпе .... = .................(42)
Апагелѵб . . . . ѵ(1—рѵ) = А.................(43)
Здѣсь А зависитъ отъ Т; уравненіе относится къ СО2.
Віііег, .
для Н2О рѵ = ВТ —
рѵп
(44)
Уравненіе состоянія.
663
СгиеІсІЬег^ . . . рѵ — ВТ—Сра - Оѵ^.................(45)
Здѣсь $ = .
Эіеіегісі . . р(ѵ Ь) — КТе ^Іѵ ...... (45,о)
I С \ I
Вове-Іппез и 8. Уопіи рѵ = &Т\ 1-1---гтг- 4 , г. (45,Д)
& г I ѵ-\-к—рѵ 2] ѵ-]-к ѵ
Дальнѣйшія уравненія предложили Вгіііоиіп, 8 с й ш і <11, Т Ь. і е -
чеп (1885), Ьа^гап^е, ѵап Ьааг (1893), ОоеЬеІ (1904), Аша-
§-аІ, и др. Критическій разборъ различныхъ уравненій далъ ТЬіе-
ееп (1897).
Въ заключеніе этого обзора упомянемъ двѣ весьма важныя работы.
Ѵап йег ЛѴааІе приложилъ къ молекулярнымъ явленіямъ теорію
циклическихъ движеній и для дву атомныхъ газовъ получилъ формулу
указывающую на характеръ измѣненія Ь въ (22) при данной температурѣ
въ зависимости отъ ѵ. Значеніе Ь — Ьо соотвѣтствуетъ предѣльному зна-
ченію ѵ — оо, т.-е. наибольшему разрѣженію, а значеніе Ь = Ьг соотвѣт-
ствуетъ наибольшему уплотненію, когда также и ѵ — Ь±. Ѵап Ь а а г
(1904) провѣрилъ формулу (46) для водорода.
До сихъ поръ за уравненіе состоянія пара мы всегда принимали такое
уравненіе, которое связываетъ величины ѵ, р и і Ріапск (1908) ввелъ
иныя перемѣнныя, именно энтропію 5, энергію Е и объемъ V. Уравненіе,
выражающее 8, какъ функцію Е и И, онъ называетъ каноническимъ
уравненіемъ состоянія. Для одноатомнаго газа Ріапск получаетъ:
5 = + (47)
Здѣсь М число молекулъ въ объемѣ V, к универсальная по-
стоянная; именно,
16 эргъ
к = 1,346.10 градусъ..................(47,а)
Эта постоянная опредѣляется уравненіемъ
5 = йІ8ІГ-ЬСоп8к,
гдѣ IV — вѣроятность даннаго состоянія газа. Для граммъ-атома кЫ
равно /? = 8,31 . ІО7, т.-е. газовой постоянной: Д равняется восьмикрат-
ному объему атомной сферы, т.-е.
664
Ненасыщенные пары
$ = 2Ь
(47/)
гдѣ Ь — постоянная уравненія Ѵап-йег-\ѴааІ8’а (22). а и С— по-
стоянныя. Вводя р и Ріапск изъ (47) получаетъ уравненіе
а
ѵ2
- (47, с)
Интересно сравнить это уравненіе съ уравненіемъ Ѵап-сІегЛѴааІе’а
Р>Т _
ѵ — Ь ѵ2
(47.б/)
Если ввести р = 2/?, то
1
2Ь
4 Ь2
3 ѵ2
• • (47,е)
и
1 к і Ь і Ь2 і I
, = V { 1 р “Р " м ~Ь . • • • |
ѵ - Ь [ 1 ѵ ѵ*
(47/)
Такимъ образомъ, формула Ріапск’а весьма немного отлична отъ
формулы Ѵап-дег-АѴааІе'а, даже если принимать во вниманіе члены
второго порядка. Дальнѣйшее изслѣдованіе связи между обычнымъ и ка-
ноническимъ ураненіями состоянія опубликовалъ ЛѴа8ятиі1і (1909).
§ 6. Критическая температура и критическое состояніе. Намъ по
необходимости уже много разъ приходилось говорить о критической тем-
пературѣ, которую будемъ обозначатъ буквою д. Впервые мы на нее
указали еще въ т. I и многократно о ней упоминали въ этомъ томѣ. Мы
опредѣляли ее тѣмъ, что при всякой температурѣ і > $ вещество мо-
жетъ находиться только въ газообразномъ состояніи, изъ котораго оно ни
при какихъ давленіяхъ не переходитъ въ состояніе жидкое. Теперь мы
ближе познакомимся съ относящимися сюда опытными и теоретическими
изслѣдованіями.
Когда і &, то при и з о т е р м и ч е с к о м ъ сжатіи получается при
нѣкоторомъ давленіи р Р объемъ ѵ — а, т.-е. насыщенный паръ.
При дальнѣйшемъ уменьшеніи объема давленіе Р остается постояннымъ
и въ то же время часть вещества переходитъ въ жидкое состояніе.
Когда объемъ дойдетъ до ѵ - 5, мы имѣемъ только жидкость. Чѣмъ
выше тѣмъ больше давленіе Р и тѣмъ меньше объемъ о насыщен-
наго пара; объемъ-же 5 увеличивается съ увеличеніемъ і, несмотря на
увеличеніе давленія. Отсюда слѣдуетъ, что съ повышеніемъ і
уменьшается разность о — 5, т.-е. та прямолинейная часть фи-
зической изотермы, напр. вида р = /(^), которая соотвѣтствуетъ посте-
пенному переходу всей массы вещества изъ парообразнаго состоянія въ
жидкое. Когда I приближается къ разность о — 5 стремится къ нулю,
т.-е. объемъ о и 5 стремятся къ общему предѣльному значенію, которое
обозначимъ черезъ др; въ то же время давленіе Р стремится къ нѣкото-
Критическое состояніе.
665
рому опредѣленному значенію, которое обозначимъ черезъ лг. Это пока-
зываетъ, что на изотермѣ р = /{ѵ), которая относится къ значенію Т -
= #-|- 273, существуетъ особая точка, координаты которой ѵ = др и
р = л; она соотвѣтствуетъ такому состоянію вещества, въ которомъ
жидкое и парообразное состоянія какъ бы сливаются,
объемы о и 5 дѣлаются тождественными. При маломъ пониженіи темпе-
ратуры уже дѣлаются возможными и парообразное1 и жидкое состоянія.
Особое состояніе, опредѣляемое величинами і - -4), ѵ — д, р = л, назы-
вается критическимъ состояніемъ вещества; ср называется
критическимъ объемомъ, л — критическимъ давлені-
емъ. Весьма важно замѣтить, что когда вещество находится при крити-
ческой температурѣ то это еще вовсе не значитъ, что оно находится въ
критическомъ состояніи, которое характеризуется еще вполнѣ опредѣлен-
нымъ объемомъ ср и соотвѣтствующимъ температурѣ О и объему г/ да-
вленіемъ л. Изъ предыдущаго ясно, что критическое давленіе л есть
наибольшее давленіе, при которомъ можетъ находиться насыщенный паръ.
Обращаемся къ исторіи открытія критическаго состоянія.
Первыя сюда относящіяся изслѣдованія принадлежатъ С а п і а г (1
сіе Іа Тоиг’у (1822). Онъ нагрѣвалъ жидкости въ запаянныхъ стеклян-
ныхъ трубкахъ, причемъ сначала жидкость наполняла половину трубки,
а другая половина содержала только пары той же жидкости. Онъ замѣ-
тилъ, что при нѣкоторой температурѣ / жидкость исчезала, превращаясь
цѣликомъ въ паръ. Чтобы опредѣлить давленіе р пара въ этотъ моментъ,
онъ пользовался приборомъ, изображеннымъ на рис. 201. Трубка АВ со-
держала испытуемую жидкость, трубка ВСЕ и часть трубки ЕЕ напол-
нены ртутью, надъ которой находится воздухъ, такъ что трубка ЕЕ, за-
крытая сверху, служила манометромъ. Нагрѣвая весь приборъ, онъ могъ
опредѣлить температуру і и давленіе р, для эфира онъ нашелъ ^=175°,
р = 38 атм., для сѣроуглерода I = 254°, р = 71 атм., для алкоголя і- - 248°,
р 119 атм., и для воды і 362°. Подобныя же наблюденія произво-
дилъ Вгіоп (1859) для хлористаго этила С2Н§СІ (7=184°), сѣрнистаго
ангидрида (^ = 157-) и эфира С4//10О (^=190°,5). Еще раньше
Тйііогіег показалъ, что жидкая СО2 расширяется при нагрѣваніи отъ
0° до 30° въ четыре раза сильнѣе, чѣмъ въ тѣхъ же предѣлахъ темпера-
туръ расширяются газы. Первые, указавшіе на важное значеніе опы-
товъ Са^піагсі сіе Іа То и г’а, были Рагасіау (1848) и Д. И. Мен-
делѣевъ (1860), назвавшій температуру, при которой исчезала жидкость,
абсолютною температурою кипѣнія.
Истинный смыслъ явленія, открытаго Са^піагсі сіе Іа Той Ромъ,
былъ выясненъ знаменитыми опытами кпсігеуѵя’а (1869) надъ угольнымъ
ангидридомъ. Приборъ, которымъ пользовался Л п <1г е \ѵ 8, изображенъ на
рис. 202. Онъ состоялъ изъ двухъ толстостѣнныхъ мѣдныхъ трубъ
А А и ВВ, соединенныхъ трубкою аЬ ; всѣ три трубки наполнены водою.
Въ нихъ вставлены стеклянныя, сверху закрытыя, внизу расширяющіяся
трубки гг и 55; трубка гг содержала въ верхней части испытуемый газъ,
666
Ненасыщенные пары.
трубка 55 — воздухъ. Ртутные столбики / и § отдѣляли газы отъ воды.
Винты к и И служили для сжиманія воды, которая при этомъ поднима-
лась по трубкамъ г и 5. Трубка 5 служила манометромъ для опредѣленія
того общаго давленія, которое устанавливалось внутри прибора. Трубки
г и 5 были тщательно прокалибрированы, такъ что объемъ ѵ, занимаемый
веществомъ въ трубкѣ 5, могъ быть всегда опредѣленъ съ точностью.
Рис. 201.
Рис. 202.
Нагрѣвая врсь приборъ до опредѣленной температуры і. которая удержи-
валась неизмѣнной, Лп(1гелѵ8 постепенно измѣнялъ давленіе р, причемъ
измѣнялся и объемъ ѵ вещества въ трубкѣ 5. Опредѣляя величины р и
г/, \ п й г е лѵ 8 могъ построить изотермы , соотвѣтствующія различнымъ
температурамъ /, а именно / = 13°,1, 21°,5, 31°,1, 32°,5, 35°,5 и 48°,1.
Полученныя Апй г е 8’омъ изотермы для СО2 изображены на рис. 203,
на которомъ пунктиромъ обозначены также изотермы воздуха (равносто-
роннія гиперболы). Изотерма 48°, 1 щя СО2 по общему характеру напо-
минаетъ изотермы воздуха. Съ уменьшеніемъ і мѣняется характеръ изо-
термъ; при і = 13°,1 и ^ = 21°,5 изотермы содержатъ прямолинейные от-
рѣзки, соотвѣтствующіе, какъ уже сказано выше (стр. 656 и 659), періоду
Критическое состояніе.
667
постепеннаго перехода вещества изъ парообразнаго состоянія въ жидкое.
Прямолинейная часть уменьшается по мѣрѣ увеличенія на изотермѣ
31°,1 она, повидимому, уже исчезла. \н(1гек8 нашелъ, что она исче-
заетъ на изотермѣ 30°,92, каковую температуру й онъ и назвалъ кри-
тическою. Точка на этой изотермѣ, къ которой при повышеніи I
стремятся концы прямолинейныхъ частей изотермъ, опредѣляетъ крити-
ческое давленіе л; и объемъ и вообще критическое состояніе вещества.
Критическая температура можетъ служить для формулировки отличія
между газомъ и паромъ. Если температура I вещества выше критической д,
то его можно назвать газомъ (ни при какомъ давленіи не превра-
щающимся въ жидкость); если она ниже $ — паромъ.
Рис. 204.
На рис. 204 вновь изображены изотермы \пс1гелѵ8’а; линія ЕКЕ
соотвѣтствуетъ критической температурѣ $: при і < 0 ѵіы имѣемъ изо-
термы вида СаЬМ, прямолинейная часть аЬ которыхъ соотвѣтствуетъ
переходу изъ жидкаго состоянія въ парообразное, и обратно. Черезъ
концы прямолинейныхъ частей проведена кривая АКВ\ вѣтвь АК соот-
вѣтствуетъ объемамъ 5 жидкости, вѣтвь КВ — объемамъ о насыщеннаго
пара. Кривыя АКВ и ЕКЕ имѣютъ въ точкѣ К общую касательную, ко-
торая, какъ предѣлъ хордъ аЪ, должна быть параллельна оси аб-
сциссъ. Отсюда слѣдуетъ, что координаты $, ѵ - - у и р — л точки К, соот-
вѣтствующей критическому состоянію, должны удовлетворять уравненіямъ
/(/?, V, І) = О, = О, — о . . . . (48)
дѵ дѵ2 ѵ 7
668
Ненасыщенные пары.
гдѣ /(/?, ѵ, і) уравненіе состоянія вещества. Кромѣ того мы должны
имѣть въ точкѣ К
о — 5 = 0........................(48, а)
Весьма важно замѣтить, что уже для температуры /, которая не-
ного меньше такъ что 0 — і малая величина, получается значительная
разность между п и 5. Для СО2 можно положить $ = 31°. При і = 30°
имѣемъ 5 = 0,003714, о = 0,005513; отсюда а: 5 = 1,485, т.-е. а почтивъ
полтора раза больше 5. На это обстоятельство указалъ Н. Г. Сто лѣ-
то въ и мы къ нему возвратимся ниже.
Ученіе Ѵпсігехѵв’а о критическомъ состояніи показываетъ, что
между газообразнымъ и жидкимъ состояніями вещества нѣтъ рѣзкой гра-
ницы, такъ какъ отъ одного состоянія можно перейти къ другому такимъ
образомъ, что вся масса вещества все время остается одно-
родною, и . все же въ началѣ несомнѣнно будетъ газообразной, а въ
концѣ столь же несомнѣнно жидкой. Мы можемъ произвести такой не-
прерывный переходъ отъ газообразнаго состоянія въ
жидкое, если мы заставимъ газъ пройти рядъ состояній, изображаемыхъ
кривой, начало и конецъ которой находится напр. въ точкахъ (1 и /, и
которая сверху обходить точку К. совершенно минуя часть плоскости,
ограниченную кривой АКВ, т.-е. ту часть, точки которой соотвѣтствуютъ
неоднородному состоянію вещества. Несомнѣнно однородный газъ или
паръ (въ (Г) нагрѣваемъ при постоянномъ объемѣ до температуры, кото-
рая выше # (прямая йё), и затѣмъ охлаждаемы его при постоянномъ да-
вленіи ц> тѣхъ поръ, пока его объемъ сдѣлается меньше критическаго
объема </ (прямая с/); въ концѣ (точка /) мы имѣемъ несомнѣнно одно-
родную жидкость. Никакими наблюденіями нельзя при этомъ замѣтить
момента перехода вещества изъ одного состоянія въ другое. Такимъ
образомъ исчезаетъ возможность провести границу между жидкимъ состо-
яніемъ и газообразнымъ. Тіііевеп предлагаетъ поэтому считать веще-
ство находящимся въ жидкомъ или въ газообразномъ состояніи смотря по
тому, будетъ ли его плотность больше или меньше плотности въ крити-
ческомъ состояніи. При такомъ опредѣленіи однако уже нельзя сказать,
что газъ не можетъ быть ожиженъ при температурѣ, которая выше кри-
тической. Углекислый газъ при 35° и давленіи въ 3000 атм. слѣдовало
бы уже считать жидкимъ. Прямая, проходящая черезъ К (рис. 204) па-
раллельно оси ординатъ по направленію вверхъ, отдѣляла бы жидкое
состояніе ѵрлѣва), отъ газообразнаго (справа), что крайне неудобно.
Если за независимыя перемѣнныя принять объемъ ѵ и температуру Т,
то кривыя постояннаго давленія (и з о п і е с т ы) будутъ имѣть видъ С^А^а^
С2В2А2а2 и т. д. (рис. 205). Вѣтви С^, С2В2 и т. д. соотвѣтствуютъ
пару, изотермы-изопіесты ВГАЪ В2А2 и т. д. — смѣси пара и жидкости,
наконецъ вѣтви А^а^ А2а2 и т. д. — жидкости. Двѣ пограничныя
кривыя ОЕ и ВО сходятся въ одной точкѣ К, ордината которой равна
критической температурѣ а абсцисса — критическому объему <р; изо-
Критическое состояніе.
669
піеста р = я имѣетъ въ К общую съ пограничной кривой касательную,
параллельную оси абсциссъ.
Мы опредѣлили критическое состояніе теоретическими условіями (46)
и (47). М. П. Авенаріусъ (1870) исходилъ изъ другихъ теоретиче-
скихъ соображеній, полагая, что при критической температурѣ внутрен-
няя скрытая те п’л о т а испаренія ^-должна равняться
нулю. Къ этому результату легко приводитъ и условіе (47) на основа-
ніи выраженія
для всей скрытой теплоты испаренія; о — 5 = 0 даетъ
р = 0.
При критической температурѣ & скрытая теплота
испаренія равна нулю. На внѣшнюю работу тратится при испа-
реніи теплота — Ар(б — 1) = 0 (стр. 533): но д; = д — де; отсюда слѣ-
дуетъ, что при критической температурѣ д = де = щ = о. Этотъ резуль-
татъ теоріи былъ подтвержденъ МаіЬіаз’омъ (1890), измѣрявшимъ скры-
тую теплоту испаренія р жидкихъ СО2 и въ водяномъ калориметрѣ,
температура котораго удерживалась постоянною постепеннымъ прибавле-
ніемъ къ ней сѣрной кислоты, причемъ выдѣлялось количество теплоты, пред-
варительно тщательно измѣренное. Вотъ нѣкоторыя изъ его чиселъ для СО2 :
і = 0° 7°, 25 13°,69 16°,45 22°,4 28°,13 30°,59 ЗО«, 82
д = 56,25 50,26 42,02 39,92 31,80 19,35 7,26 3,72.
МаНііав даетъ эмпирическую формулу для СО2
р2 = 118,485(31 — 0 — 0,4707(31 — О2,
которая при I = & — 31° даетъ д = 0.
670
Ненасыщенные пары.
М а IИ і а 8 находитъ, что кривая д = /(і) встрѣчаетъ ось абсциссъ
(Ід
Аі~
при і — & подъ прямымъ угломъ, т.-е. что при
і — & мы имѣемъ
Ваккег (1897) показалъ, что такой результатъ предсказывается теоріей.
Замѣтимъ, что МаIЬіав изслѣдовалъ также теплоемкости Си
с жидкости и насыщеннаго пара при температурахъ, близкихъ къ
критической іі. Онъ находитъ для 8О2, что вблизи і — & теплоемкость
С жидкости растетъ съ температурой, причемъ она при і = О' повиди-
мому стремится къ предѣлу С = + оо. Для теплоемкости с насыщеннаго
пара (стр. 619) онъ получаетъ вблизи 1 = отрицательныя числа,
которыя при .1 = И повидимому стремятся къ предѣлу с = — оо. Мы
видѣли, что при температурахъ, далекихъ отъ критическихъ, с можетъ
быть и положительной и отрицательной величиной, которая однако ра-
стетъ съ повышеніемъ температуры. Результатъ, найденный М а
іЬіав’омъ, показываетъ, что для с должно при нѣкоторой температурѣ
существовать максимальное значеніе. Для 8О2 теплоемкость с < О
при низкихъ температурахъ; при 116° она равна нулю, выше дѣлается
положительной, достигаетъ максимума, затѣмъ уменьшается, при 1.32°,5
опять дѣлается равною нулю и при & = 156° стремится къ — оо.
Мы сперва опредѣлили критическую температуру & условіемъ
о — 5 = 0, а затѣмъ условіемъ р = 0. На третій способъ опредѣленія
указалъ еще въ 1835 г. Ргапкепііеіпі, а затѣмъ вновь Д. И. Мен-
делѣ е в ъ. Когда Ргапкепйеіт открылъ, что поднятіе жидкости въ
капилярныхъ трубкахъ, а слѣд. и капилярная постоянная а2 уменьша-
ются съ температурою, онъ высказалъ мысль, что вѣроятно существуетъ
такая температура, при которой а2 — 0. и что при этой температурѣ жид-
кость, какъ таковэя, должна перестать существовать, подобно тому, какъ это
наблюдалъ С а^пі а г д Де Іа Той г. Менделѣевъ первый опредѣ-
ленно высказалъ мысль, что при критической температурѣ & капилярная
постоянная а2 — О. Это вполнѣ подтверждается напр., для сѣрнаго эфира,
для котораго Вгипп ег нашелъ а2 — 5.3536 — 0,028102/. При і — 190°,5
имѣемъ а2 = о; эта температура весьма близка къ критической темпера-
турѣ & = 190°,0, найденной Зайончевскимъ. \Ѵ о И и В гі оп убѣ-
дились на опытѣ, что около этой температуры высота поднятія эфира въ
капилярной трубкѣ дѣлается равною нулю. О 8 і уѵ а 1 Д указываетъ еще
на 7 жидкостей, для которыхъ замѣчается подобное же согласіе между
вычисленнымъ и наблюденнымъ д\ ѴегвсІіаі'ІеН изслѣдовалъ под-
нятіе Л у жидкихъ СО2 и Л/2О въ капилярныхъ трубкахъ; для СО2 по-
лучается И = 0 около критической температуры (31°).
Въ ученіи о жидкостяхъ (т. I, гл. V § 11) мы познакомились съ фор-
мулой (44) К а пі 8 а у и 8 с й і е 1Д з’а
= к(т — О).
Здѣсь а поверхностное натяженіе въ динахъ на см., М —- моле-
кулярный вѣсъ, т = И ѵ удѣльный объемъ, к постоянная, при-
Критическое состояніе.
671
немъ для большинства жидкостей к = 2.12, (1 близко къ 6. Для нѣкото-
рыхъ веществъ к оказывается аномально малымъ, напр. для ацетона
к = 1,818, для пропіоновой кислоты к = 1,44 ; также для /7/, НВг, Н2В,
Н^Р и НСІ. Выше приведенное уравненіе можно написать въ видѣ
= к(& — і - 6)...............(48,6)
Если для двухъ температуръ і извѣстны значенія а и ѵ, то уравне-
ніе (48,Ь) даетъ величину к п критическую температуру 6.
Формула (48, Ь) пригодна лишь для не ассоціированныхъ жидкостей,
молекулы которыхъ соотвѣтствуютъ простымъ, не кратнымъ химическимъ
формуламъ. Для ассоціированной жидкости, какова, напримѣръ,
вода, молекула которой не есть Н2О, но (Л/2ОЪ, формула (48,6) не при-
годна, т.-е. к не является для нея постоянной и а (Мѵ/І* не предста-
вляетъ собою линейной функціи температуры. Для такихъ жидкостей
Ьіѵіп^віоп и Могдап (1909) даютъ формулу
а(Л4^)2/з = А + Ві + а2..............(48,с)
Здѣсь А равняется значенію а(Л4ѵ)2/з при і — 0°. Изъ (48,6) слѣ-
дуетъ, чт° дІа(Л4^] А р ,
1 Ц-, - — — к = Сопаі:
ді
изъ (48,с) слѣдуетъ, что
а[а(у8/3] _ в + 2СІ..................(48 а}
представляетъ собою линейную функцію/. Если постоянныя Д, В, С
опредѣлены эмпирически, то $ можетъ быть вычислена изъ соотношенія
А + Ві + СР = 0.....................(48, с)
въ которомъ положено і = $ — 6. Ьіѵіп^зІопиМог^ап полагаютъ
что при температурѣ і = — (Я - 6)
В 4- яСі = о....................(48,/)
Значеніе $, получаемое, какъ среднее, изъ (48,с) и (48,/) должно
наиболѣе приближаться къ дѣйствительному. Это хорошо подтвердилось
для ряда жидкостей. Для метиловаго алкоголя А = 282,66, В = — 0,7726,
С = — 0,0016864. Формула (48,с) даетъ 0 = 246,1°, формула (48,/) даетъ
$ = 235,1°. Среднее даетъ 0 = 240,6°, опыты-же даютъ $ = 24о°. Если
измѣренія производятся при температурахъ, не слишкомъ низкихъ по
сравненію съ $, то (48,/) должно давать удовлетворительные результаты.
Такъ напримѣръ, для воды (48,/) даетъ $ = 361°, тогда какъ непосред-
ственные опыты для & дали значенія 358,1°, 364,3° и 365°.
Сравнивая то, что въ § 4 и § 5 было сказано объ уравненіяхъ Ѵап
(Іег ДѴааІ8’а и Сіаивіие’а, съ тѣмъ, что здѣсь было изложено объ
опытахъ Апйгелѵв’а и о критическомъ состояніи вещества, въ особен-
ности сравнивая рис. 199, стр. 655 и рис. 204, стр. 667, мы видимъ, что
теоретическія изотермы Ѵап йег \Ѵ а а 18’а и С1 а и 8 і и 8’а по виду
672
Ненасыщенные пары.
вполнѣ совпадаюіъ съ физическими изотермами Апйгедѵз’а.
когда і больше температуры или равно ей. При # теоретическія
изотермы отличаются отъ физическихъ въ той части, которая ограни-
чена кривою АКВ (рис. 204) ; здѣсь физическія изотермы прямолинейны,
теоретическія имѣютъ форму, показанную на рис. 204 пунктиромъ а^сИЬ.
На стр. 656 было сказано, что Я. Т Іі о ш 8 о п еще до Ѵап йег АѴ а а 18’а
указалъ, что непрерывный и з о т е р м и ч е с к і й переходъ пара въ жидкость,
(Ч'ли бы онъ былъ осуществимъ, происходилъ бы именно по кривой вида
ЬНсйИ. Кривая ЕКР на рис. 199 соотвѣтствуетъ критической темпера-
турѣ, а точка К к р и т и ч е с к о м у с о стоянію, ибо мы опредѣлили
координаты этой точки (см. стр. 655) тѣмъ, что три корня ѵ2 и
уравненія ѵ = /(р) должны сдѣлаться равными между собою, или,
иначе, мы опредѣлили (стр. 667) величины д) и л;, рѣшая три уравненія
др д2р
/(р, /) = 0, = 0, = 0. По какъ разъ этими же условіями опре-
дѣляются критическіе температура объемъ д и давленіе лг.
Изъ сказаннаго слѣдуетъ, что величины (13) стр. 655 и (19) стр. 658
опредѣляютъ к р и т и ч е с к о е с о с т о я н і е вещества, и мы видимъ, что
(Ч'ли принять уравненіе Ѵап <1ег АѴааІв’а
= .............(49)
ТО
273 + <7 = . Ч — ЗЬ , . (49лг)
' 27 ЬР 7 27 & '
Вмѣсто первой формулы имѣемъ также, см. (13,о) стр. 655,
1 + 'І'/=27.(1-;А1- о...............(49Л)
Пользуясь этими формулами, Ітпуе и ЕгісІегісЬ вычислили а и Ь
для 83 веществъ, о чемъ уже было сказано на стр. 653.
Если же принять первое уравненіе С1аи8Іи8’а
Д+Т(гЬ)ф /"'-К7.......................<•»>
то ________ _______________________________
273 + '’ = | ’=3'’ + 23- ”=] 21И (СД (5І)
Формулы (49) и (51) могутъ служить для вычисленія
критическихъ величинъ, если уравненіе состоянія извѣстно, т.-е.
(‘ели величины а. Ь. К или а, Ь, с, К найдены.
Выражая р въ атмосферахъ и принимая ѵ = 1 при 0° и р = 1 атм.,
Ѵап (1 ег АѴааІв нашелъ для СО2 постоянныя а — 0,00874 и & = 0,0023.
Эти числа даютъ на основаніи формулъ (49): (>=32°,5, ф — 0,0069 и
л = 61 атм., между тѣмъ какъ А п сі г е лѵ 8 наблюдалъ $ = Зо°,9, др = о,ообб
и лг=70 атм. Если вспомнить, что Ѵап сіе г АѴ а а 1 8 опредѣлилъ посто-
Критическое состояніе
673
янныя а и Ь, основываясь на наблюденіяхъ сжимаемости СО2, то нельзя
не признать такое совпаденіе весьма удовлетворительнымъ и замѣчатель-
нымъ. На стр. 653 было сказано, что величина Ь можетъ быть опредѣ-
лена изъ наблюденій критическаго состоянія вещества. Дѣйствительно,
формулы (49) даютъ возможность вычислить а и Ь, если извѣстна
критическая температура $ и критическое давленіе тс.
Самъ Ѵап-(іег-ѴѴааІ8 воспользовался опредѣленіями величинъ д и тс
Лапвеп’омъ для І\?2О и своими собственными опредѣленіями (7 и тс
для С2Н±. чтобы вычислить постоянныя а и Ь для этихъ двухъ веществъ.
Исходя изъ уравненія С1аи8Іи8’а, мы также можемъ на основа-
ніи формулъ (51) вычислить критическія величины $, ср и тс. Принимая
щя /?, я, Ь, с числовыя величины, приведенныя на стр. 660 (третья
группа), получаемъ для СО2 критическія величины : $ — 30°,996, ср —
- 0,004483, тс =- 77,001.
Изъ формулъ (49) вытекаетъ интересное слѣдствіе, какъ показалъ
Ѳпуе. Выраженіе для $ можно приближенно написать въ видѣ 1 + ад—
X, ѵ а М 3 /. I (А тл
= —; далѣе мы имѣемъ лср = . Отсюда лд (1 аа). Если бы
вещество до критической температуры $ обладало свойствами идеальнаго
газа, то его объемъ и давленіе рг удовлетворяли бы равенству ррѵ± =
3
— 1 + сід. Отсюда слѣдуетъ лср = - ррѵъ т.-е. при критической тем-
о
пературѣ <7 вещество занимаетъ ' объема, которое оно заняло бы, слѣ-
дуя до этой температуры законамъ» Бойля и Гей-Люссака, или его
плотность Л въ к — 2,67 раза больше теоретической д. Н е і 1 Ь о г п ,
исходя изъ теоріи О. Е. Меуег’а (стр. 651), находитъ Л = $ У 2 <3
о
• = 3,77(5, что болѣе согласуется съ опредѣленіями 8. Тоип^’а плотно-
стей Л; это даетъ к — 3,77.
Ѵап Ьааг (1904) для водорода нашелъ к равнымъ 2,69. Для
нѣкоторыхъ веществъ к оказывается аномально большимъ, какъ мы ука-
зывали выше (Ѵо и п и Т Ь. о т а 8). Ѳпуе (1891) далъ эмпириче-
скую формулу7
к = к(1+ёТс).......................(52)
гдѣ к и § - - постоянныя, Тс — абсолютная критическая температура.
Для идеальнаго газа изъ рѵ ЦТ при г/ = Соп8І. получается
др
ді ѵ
Віеіегісі (1903)
температурѣ
вывелъ изъ наблюденій, что при критической
Ідр\ _ 2/?
]с~ 9
(52л)
КУРСЪ ФИЗИКИ О. ХВОЛЬСОНА. Т. III, изд. 3-е.
43
6?4
Ненасыщенные нары.
т.-е. имѣетъ удвоенное значеніе. Онъ обозначаетъ, далѣе, черезъ Е
отдачу испаренія (ейісіепсу по МахчѵеІГу), т.-е. величину
р(б — $)~ р
е
(52,0
см. гл. XI, § 5 формулы (25,с) и (36,а). Біеіегісі показалъ, что для
нормальныхъ веществъ при критической температурѣ получается
.................• ’ <52’<О
з
Формула. Ѵап-йег-АѴааІз’а даетъ въ (52,а} множителя вмѣсто 2 и
1
для Ес вмѣсто (52,с) величину Ѵап Бааг находитъ для водо-
рода Ес = - .
с 4,27
Обращаемся еще разъ къ теоретической изотермѣ арѵІіЬ, рис. 204,
стр. 667. Л. Богаевскій предположилъ, что физическая изотерма аЬс
пересѣкаетъ кривую арѵНЬ въ той точкѣ с, въ которой эта кривая имѣ-
етъ перегибъ.
Большой интересъ представляетъ вопросъ объ осуществленіи хотя
бы части кривой а^сІіЬ. Часть кривой получается легко, ибо
перегрѣтая жидкость, давленіе которой меньше давленія на-
сыщеннаго пара при той же температурѣ, находится въ состояніи, соот-
вѣтствующемъ точкамъ вѣтви ар;. На стр. 526 были упомянуты относя-
щіяся сюда наблюденія Воппу, В и іо и т’а и др. Часть Ыг изотермы
соотвѣтствуетъ пересыщенному пару. Многіе опыты указываютъ,
что состояніе пересыщенія дѣйствительно возможно. В. НеІтІіоІЬг
(сынъ) показалъ, что воздухъ, лишенный пыли и насыщенный парами
воды, при внезапномъ расширеніи охлаждается, причемъ пары не осаж-
даются, переходя въ состояніе пересыщенное. А. і і к е п указалъ на роль,
которую подобныя явленія могутъ играть въ природѣ, напр. при образо-
ваніи ливней, грозъ и т. д. Изслѣдованія АѴиеіІпег’а и (тіоігіап’а,
Вашзау и Ѵонп^’а, Ваііеііі и др. также указываютъ на воз-
можность пересыщеннаго состоянія паровъ. Часть рсН теоретической
изотермы, соотвѣтствующая неустойчивымъ состояніямъ вещества, врядъ-
ли окажется осуществимой. Попытка выяснить возможный характеръ ве-
щества на части рсИ изотермы была сдѣлана Ргезіоп’омъ; но мы на
ней не останавливаемся.
§ 7. Экспериментальное изслѣдованіе критическаго состоянія ве-
щества. Для опредѣленія критической температуры $ су-
ществуютъ четыре способа, которые мы прежде всего и разсмотримъ.
1. Способъ изученія изотермъ (способъ Ап (1 г е ѵг в’а).
При постоянной температурѣ і опредѣляется рядъ сопряженныхъ вели-
чинъ р и ѵ, на основаніи которыхъ можетъ быть начерчена изотерма. Та
Критическое состояніе.
6?5
изъ этихъ изотермъ, въ которой прямолинейная часть какъ разъ исчеза-
етъ, и соотвѣтствуетъ искомой температурѣ I = Этотъ способъ при-
мѣняли, кромѣ Лпдгелѵз’а, Кашзау и Тоип^, Ѵоип§, Ваѣѣеііі
и А ш а & а 1.
2. Способъ оптическій (способъ Са^ніагсі сіе Іа Тоиг’а).
Испытуемая жидкость помѣщается внутри стеклянной трубки, закрытой
съ обѣихъ сторонъ: свободная отъ жидкости часть трубки наполнена па-
рами той же жидкости и не должна содержать замѣтныхъ слѣдовъ воз-
духа, или иного посторонняго вещества; длина трубки обыкновенно
30—40 мм.. внутренній діаметръ около 3 мм., толщина стѣнокъ около
0,7 мм. Трубка помѣщается въ воздушную ванну, т.-е. внутри металли-
ческаго ящика съ двойными или тройными стѣнками, температуру кото-
раго можно медленно повышать или понижать. Особый термометръ даетъ воз-
можность слѣдить за температурой ; ящикъ
ками для наблюденія тру-
бочки издали при помощи
зрительной трубы. Жид-
кость ограничена сверху
ясно видимымъ менискомъ.
Когда температура і мед-
ленно растетъ, то жидкость
сперва расширяется; при
нѣкоторой температурѣ і =
= і\ менискъ исчеза-
етъ и вся трубка пред-
ставляется наполненной од-
нороднымъ веществомъ, па-
ромъ. При пониженіи за-
тѣмъ температуры наблю-
даются въ трубкѣ сперва
полосы, затѣмъ туманъ, въ
снабженъ стеклянными окошеч-
Рис. 206.
которомъ повидимому про-
исходятъ весьма бурныя
явленія, и наконецъ появляется въ нижней части трубки жидкій столбъ,
ограниченный сверху явственно замѣтнымъ менискомъ. Пусть і2 темпе-
ратура появленія мениска или первыхъ признаковъ разнородности ве-
ществъ. Допускаютъ, что $ = \ (^і 5 насколько это вѣрно, уви-
димъ ниже.
Оптическій способъ основанъ на тѣхъ представленіяхъ о сущности
критическихъ явленій, которыя были приведены выше ; они заставляютъ
насъ думать, что въ моментъ исчезновенія мениска вся трубка наполнена
веществомъ однороднымъ, обладающимъ вездѣ одинаковой плотностью.
Совершенно другой взглядъ развивали (1 е Н е е п, кн. Голицынъ,
Т г а и Ъ е и др., полагающіе, что послѣ исчезновенія мениска вещество
43*
676
Ненасыщенные пары.
еще не сдѣлалось однороднымъ. Эти работы вызвали большой рядъ по-
лемическихъ статей, разборомъ которыхъ мы здѣсь заняться не можемъ.
3. Способъ Н а д е ж д и н а. Безвременно умершій талантливый
ученый Надеждинъ пользовался приборомъ, изображеннымъ на рис. 206
и названнымъ имъ дифференціальнымъ дензиметромъ. Опредѣленіе тем-
пературы 'д при помощи этого прибора основано на томъ, что при этой
температурѣ плотности жидкости и пара дѣлаются одинаковыми, т.-е.
трубка оказывается наполненной однороднымъ веществомъ. Приборъ со-
стоитъ изъ трубки А А (рис. 206), вставленной въ оправу 5; эта оправа
снабжена трехгранною осью, на которой она, подобно коромыслу вѣсовъ,
качается внутри металлическаго подвѣса СС. Пустая трубка устанавли-
Рис. 207.
вается горизонтально при помощи гирьки Г. Когда^часть трубки напол-
нена жидкостью, а остальная часть насыщеннымъ паромъ, трубка прини-
маетъ наклонное положеніе. Весь приборъ помѣщается въ воздушную
ванну; когда температура послѣдней дѣлается равной трубка вновь
устанавливается горизонтально. Преимущество этого остроумнаго способа
заключается въ томъ, что онъ приложимъ къ случаямъ, когда испытуе-
мое вещество сильно окрашено (Вг, У), такъ что трудно видѣть менискъ,
или когда это вещество дѣйствуетъ на стекло (вода).
4. Способъ Саіііеіеі и Соіагйеаи. Помѣстимъ въ со-
судѣ, имѣющемъ объемъ т/, вѣсовое количество Р жидкости, занимающей
часть этого объема, причемъ другая часть содержитъ только пары этой
жидкости, и станемъ постепенно повышать температуру сосуда, опредѣ-
Критическое состояніе.
677
ляя давленіе р вь зависимости отъ і при постоянномъ объемѣ ѵ. Ста-
немъ мѣнять количество Р жидкости, которое однако всегда должно быть
бо іыпе того количества, вещества, которое наполняетъ объемъ ѵ при крити-
ческой температурѣ №\ иначе говоря, объемъ ѵ долженъ быть меньше
критическаго объема Р<$ взятаго количества жидкости. Пока мы имѣ-
емъ въ нашемъ сосудѣ жидкость и насыщенный парь, давленіе1 р кото-
раго не зависитъ отъ количества Р жидкости. Если на координатныхъ
осяхъ р и і чертить кривыя р /(і) для различныхъ Р, то всѣ эти кри-
выя должны совпадать, пока При температурѣ № вся жидкость
превращается въ паръ; при мы имѣемъ ненасыщенный паръ, или
газъ, давленіе р котораго очевидно должно зависѣть отъ коли-
чества вещества, находящагося при температурѣ і въ объ-
емѣ ѵ. Отсюда слѣдуетъ, что кривыя р — /(і), соотвѣтствующія различ-
нымъ Р, и совпадающія до і - должны при і > № вѣерообразно рас-
ходиться. Чѣмъ больше Р, тѣмъ больше для даннаго і и давленіе р.
Ѵбсцисса точки, въ которой начинается расхожденіе кривыхъ, и есть ис-
комая критическая температура />, а ордината — критическое давленіе л.
Какъ видно, этотъ способъ чрезвычайно напоминаетъ способъ Р а і г ~
Ь а і г п’а и Т а і е’а для опредѣленія плотности насыщеннаго пара
(стр. 611). Вся разница въ томъ, что въ опытахъ РаігЪаігп’а и Та-
іе’а объемъ ѵ былъ гораздо больше объема такъ что вся жид-
кость успѣвала испариться при температурѣ I < №.
Этимъ способомъ Саіііеіеі и Соіагсіеаи опредѣлили критиче-
скія величины воды = 365°, л = 200,5 атм.). Стгітаісіі изслѣдо-
валъ тѣмъ же способомъ СО.,, но получилъ неудовлетворительные ре-
зультаты.
Приборъ Саіііеіеі ц Соіагсіеаи изображенъ на рис. 207.
Испытуемая жидкость находится въ металлическомъ сосудѣ ЕО, помѣ-
щенномъ въ сосудѣ ѴѴ', и соединенномъ трубочкой АВСЕ съ труб-
кой ЕЬ. Часть ОАВСЕО наполнена ртутью, надъ которой находится
вода, заполняющая также трубку ЬР, соединенную съ водороднымъ ма-
нометромъ М и при посредствѣ трубки РК съ водянымъ насосомъ. Че-
резъ стѣнку трубки ЕТ проходятъ двѣ изолированныя проволочки 5 и 5'.
Изъ рисунка понятно, что звонокъ Н начинаетъ дѣйствовать, когда ртуть
въ трубкѣ ЕТ дойдетъ до уровня О. Накачивая воду въ приборъ, можно
такимъ способомъ всегда доводить ртуть въ ЕТ до одной и той же вы-
соты, а слѣд. объемъ ОЕ = ѵ надъ ртутью поддерживать постояннымъ.
Звонокъ Н начинаетъ дѣйствовать, когда ртуть въ ЕТ достигаетъ про-
волоки 5'; это служитъ предупрежденіемъ, указывая, что вещество въ ОЕ
заняло слишкомъ большой объемъ. Сосудъ ѴѴ наполняется ртутью,
точка кипѣнія которой выше критической температуры воды, пли смѣсью
равныхъ частей и которая плавится при 200° и еще не
разлагается при 400°. Термометры въ ѴѴ' и манометръ М опредѣляютъ
сопряженныя величины і ър
Критическое давленіе л; опредѣляется вмѣстѣ съ №, если
678
Ненасыщенные пары.
пользоваться методомъ изотермъ или методомъ Саіііеіеі и С о 1 а г -
(іеаи. Весьма важно замѣтить, что при критическомъ состо-
яніи вещества др: дѵ = 0 и д2р: дѵ2 = 0; отсюда слѣдуетъ, что на изо-
термѣ і= 'д величина р очень мало мѣняется около критической точки
(р — я, ѵ = и что достаточно измѣрить давленіе р вблизи крити-
ческаго состоянія на критической изотермѣ, чтобы получить искомое лг.
А1 1 8 с й и 1 построилъ простой приборъ для приблизительнаго опредѣле-
нія давленія лг.
Гораздо труднѣе опредѣленіе критическаго объема др. Наи-
болѣе, повидимому, надежный способъ указанъ М а і И і а в’омъ. Этотъ
способъ даетъ др, когда извѣстно $; онъ основанъ на законѣ па-
раболы, о которомъ было сказано на стр. 617, см. рис. 185. Опредѣли
ютъ для различныхъ температуръ і < д плотности д жидкости и <5 на-
сыщеннаго пара; тогда получаются точки на вѣтвяхъ АС и ВС пара-
болы, имѣющія попарно общія абсциссы. Раздѣляя хорды, соединяющія
сопряженныя точки, пополамъ, получаютъ прямую — діаметръ параболы.
Ордината точки С пересѣченія зтого діаметра съ прямой МЫ, гдѣ ОМ ~
= й, даетъ критическую плотность, величину обратную искомому крити-
ческому объему др.
Обращаемся къ способу второму, оптическому, основанному на
наблюденіи температуры исчезновенія мениска и температуры /2 по-
явленія мениска или первыхъ признаковъ неоднородности вещества
въ трубкѣ.
Большую важность представляютъ вопросы о пригодности этого спо-
соба, о томъ насколько и /2 могутъ служить для опредѣленія критиче-
ской температуры д, и въ связи съ ними общій вопросъ о состояніи ве-
щества вблизи критической точки и о правильности вышеизложенной тео-
ріи А п а г е ѵг 8’а. Этимъ вопросамъ были посвящены многочисленныя
работы цѣлаго ряда ученыхъ, вызвавшія продолжительную полемику. Раз-
бирать всѣ эти работы мы не будемъ, ограничиваясь литературными ука-
заніями; авторы ихъ были ДѴгоЫе ^ѵзкі, Латіп, Саіііеіеі и Со-
Іагаеаи, Ваііеііі, 7 а т Ь і а 8 і и Голицынъ. Сюда же можно
отнести работы Ре 11 аі, О о и у и ѴіНага’а. Многое, что утверждали
нѣкоторые изъ ученыхъ, въ особенности Саіііеіеі и Соіагйеаи,
основано на очевидныхъ недоразумѣніяхъ, а указанные ими опыты, на
которыхъ они основывали тѣ или другіе выводы — мало убѣдительны.
Въ видѣ примѣра укажемъ на слѣдующій опытъ СаіПеіеі и Соіаг-
йеаи: извѣстно, что іодъ растворяется въ жидкой, но не растворяется
въ газообразной СО2; названные ученые нашли, что если въ трубочку
налить растворъ іода въ жидкой СО2, то при критической температурѣ
получается однообразно окрашенное вещество, іодъ не выдѣляется, т.-е.
остается раствореннымъ. Отсюда СаіПеіеІ и Соіагйеаи заклю-
чили, что и выше критической температуры часть вещества находится
въ жидкомъ состояніи. Но этотъ опытъ неубѣдителенъ. Мы знаемъ, что
взаимная растворимость веществъ вообще увеличивается съ температу-
Критическое состояніе.
679
рою и нѣтъ ничего невозможнаго въ допущеніи, что выше критической
температуры газообразная С0.2 растворяетъ іодъ; такое допущеніе явля-
ется особенно естественнымъ послѣ опытовъ ѴіНагсГа, доказавшаго
возможность растворенія твердыхъ и жидкихъ тѣлъ въ газахъ.
Критическій разборъ указанныхъ выше работъ былъ сдѣланъ Сто-
лѣтовымъ (1892 и 1894) въ двухъ статьяхъ, которыя должно считать
классическими. Мы изложимъ только одна , наиболѣе важную часть раз-
сужденій Столѣтова, выясняющую значеніе количества жид-
кости, находящейся въ трубочкѣ. Пусть вѣсовое количество
жидкости равно Р, такъ что ея критическій объемъ Ру; объемъ трубки
около температуры и при внутреннемъ давленіи, близкомъ къ л, обо-
значимъ черезъ ѵ. На рис. 208 изображены въ увеличенномъ видѣ
часть АВ изотермы $, ближайшая къ критической точкѣ К, и часть СРЬНО
другой изотермы гдѣ і < $. Координатныя оси ѵОр показаны лишь
символически; истинное начало координатъ расположено гораздо ниже
и лѣвѣе.
Мы нагрѣваемъ вещество при постоянномъ объемѣ т/, а потому измѣ-
ненія его состоянія изображаются прямыми, параллельными оси Ор. Эти
прямыя достигаютъ критической изотермы АКБ въ какой-либо изъ
е я .т о ч е к ъ. пограничная кривая; внутри ея мы имѣемъ смѣсь
жидкости и насыщеннаго пара, направо отъ нея и надъ изотермою АКВ
имѣемъ только паръ или газъ, а налѣво, т.-е. въ области АКМ — только
жидкость. Представимъ себѣ первый (невѣроятный) случай, что объемъ
сосуда ѵ равенъ объему Ру вещества при его критическомъ состояніи,
т.-е. абсциссѣ точки К. Тогда измѣненіе вещества при его нагрѣваніи
происходитъ по прямой аЫС и въ моментъ достиженія критической тем-
пературы $ вещество будетъ какъ разъ находиться въ критическомъ со-
стояніи. Второй случай имѣемъ, когда Ру < ѵ, жидкости взято меньше,
чѣмъ въ первомъ случаѣ; тогда вещество, достигнувъ температуры бу-
детъ обладать объемомъ ѵ, который больше его критическаго объема;
ясно, что измѣненія вещества опредѣлятся прямой тпог. Въ точкѣ о
вся жидкость испарилась, и мы имѣемъ только паръ въ по-
слѣдній періодъ ог, раньше достиженія критической температуры. Тре-
тій случай имѣемъ, когда Ру>ѵ, когда жидкости взято больше, чѣмъ
въ первомъ. При температурѣ # объемъ ѵ меньше критическаго объ-
ема; измѣненіе состоянія опредѣляется прямой сІ/дИ. Въ точкѣ д вся
масса вещества превратилась вь жидкость и въ періодѣ діі вся трубка
наполнена жидкостью, незамѣтно переходящей въ газдобразное со-
стояніе при достиженіи изотермы $. Во второмъ и въ третьемъ случа-
яхъ вещество вовсе не проходитъ ч е р е з ъ критическое со-
стояніе. Исключая первый, весьма невѣроятный случай, мы видимъ,
что, смотря по взятому количеству жидкости, или вся жидкость должна
испариться, или она должна наполнить всю трубку, раньше, чѣмъ дости-
гается критическая температура. Отсюда слѣдуетъ, что менискъ, соста'
вляющій в и д и хМ у ю границу между жидкостью и паромъ, долженъ ис-
680
Ненасыщенные пары.
чезнуть или на нижнемъ концѣ трубки, когда вся жидкость испарится
(точка о), или на верхнемъ концѣ трубки, когда жидкость займетъ весь
объемъ ѵ (точка д), На дѣлѣ наблюдается совсѣмъ другое: менискъ ис-
чезаетъ гдѣ-нибудь посреди трубки, причемъ мѣсто исчезновенія зави-
ситъ отъ количества Р жидкости, которое можно мѣ ня т ь в ъ д о -
вольно широкихъ предѣлахъ. На этомъ и основывались раз-
наго рода догадки и выводы, и попытки опровергнуть ученіе А п (1 г е з’а
о критическомъ состояніи. Столѣтовъ вполнѣ выяснилъ кажущееся
противорѣчіе между этимъ ученіемъ и наблюденіями; приводимъ его раз-
сужденія. Присутствіе видимаго мениска показываетъ, что коеффп-
ціеиты преломленія жидкости и пара отличаются другъ отъ друга на-
столько, что поверхность ихъ раздѣла можетъ быть з а м ѣ ч е н а. Но чд в-
ствительность нашего глаза, имѣетъ предѣла,, каковъ бы ни былъ харак-
теръ наблюдаемаго оптическаго явленія, и потому м ы п е р е с т а е м ъ
видѣть менискъ, когда разность коэффиціентовъ преломленія жид-
кости и пара, или когда. разность ихъ плотностей достигаетъ нѣкоторой
опредѣленной, малой величины. Положимъ, что это происходитъ при тем-
пературѣ і и соотвѣтствующемъ давленіи р насыщеннаго пара, причемъ
ибо, при температурѣ О плотности и коэффиціенты преломленія
жидкости и пара должны, по ученію Апсігедѵз'а, сливаться. Пусть
СРНО та изотерма Л при достиженіи которой менискъ перестаетъ быть
замѣтнымъ, и пусть о и 5 удѣльные объемы насыщеннаго пара, и жид-
кости (подъ давленіемъ р пара). Положимъ, что Р$ ѵ < Рб, или что
вѣсъ Р находится между предѣлами, опредѣляемыми неравенствомъ
-<Р<Ѵ............................(52)
б 5 7
Объемы Р$ и Рб соотвѣтствуютъ точкамъ Р и /7; наше неравен-
ство показываетъ, что прямая, изображающая измѣненіе состоянія веще-
ства, пересѣкаетъ изотерму СРНО въ какой либо точкѣ прямолинейной
части РН, причемъ прямая можетъ быть расположена съ одной ши съ
Критическое состояніе.
681
другой стороны отъ аЬк, совпадая напр. съ сі/діі пли съ тпог. Менискъ
исчезаетъ, какъ только достигается изотерма РН, т.-е. напр. въ / или
въ п. Но въ этихъ точкахъ, лежащихъ на, прямолинейной части изо-
термы, мы несомнѣнно имѣемъ налицо и жидкость и паръ. Чѣмъ
больше Р при данномъ г/, тѣмъ лѣвѣе расположена точка / или точка и,
т.-е. тѣмъ большая часть вещества, находится въ жиДкомь состояніи и
тѣмъ выше въ трубкѣ наблюдается исчезновеніе ме-
н и с к а. Если Рз > ѵ, то прямая сі/діъ перемѣщается влѣво отъ Р; тогда
жидкость при нагрѣваніи заполняетъ всю трубку. Если Рб<^ѵ. то пря-
мая пгпог переходитъ вправо отъ РІ и вся жидкость испаряется раньше,
чѣмъ достигается изотерма СО. Въ обоихъ случаяхъ вовсе не происхо-
дитъ исчезновенія мениска, которое наблюдается при всѣхъ Р. удовле-
творяющихъ неравенству (52). Предѣлы для Р, опредѣляемые этимъ не-
равенствомъ, довольно широки, ибо. какъ мы видѣли на стр. 668, вели-
чины о и 5, одинаковыя въ точкѣ /<, значительно разнятся другъ оть
(руга при температурахъ і, немного отличающихся оть />. Такъ для СО2,
имѣемъ 31°; при ^=30° отношеніе б: 8 = 1,485. Если менискъ пе-
рестаетъ быть замѣтнымъ при ^ = 30°, то ясно, что Р можетъ колебаться
въ довольно широкихъ предѣлахъ при условіи, чтобы исчезновеніе ме-
ниска происходило гдѣ-нибудь между концами трубки. Когда измѣненіе*
состоянія опредѣляется прямой аЬК, то менискъ исчезаетъ (точка Ь) при-
близительно посерединѣ трубки.
Такимъ образомъ наблюдаемыя явленія вполнѣ объяснены, и мы ви-
димъ, что они вовсе не противорѣчатъ ученію АпеЗгелѵз’а. Все* ска-
занное объ исчезновеніи мениска относится и къ его появленію вновь,
хотя изотермы и 4 исчезновенія и появленія мениска могутъ быть и
не вполнѣ одинаковыя. Но ясно, что и оба меньше И. Чѣмъ
тщательнѣе производится наблюденіе, чѣмъ болѣе усовершенствованы ме-
тоды. тѣмъ ближе температуры п 4 должны оказываться другъ къ фугу
и къ температурѣ I). Столѣтовъ рекомендуетъ пользоваться методомъ
полосъ (т. II), для наблюденія мениска. Весьма интересныя и обстоятель-
ныя изслѣдованія Центнершвера вполнѣ подтвердили всѣ разсужде-
нія Столѣтова.
Разсмотрѣвъ способы опредѣленія критическаго состоянія намъ
остается вкратцѣ сказать о нѣкоторыхъ результатахъ экспериментальныхъ
работъ, и назвать имена русскихъ ученыхъ, которыя для насъ предста-
вляютъ особый интересъ. Авенаріусъ (въ Кіевѣ) и его ученики
почти первые начали спеціально заниматься опредѣленіемъ критическихъ
температуръ и успѣли, примѣрно за время отъ 1875 г. до 1887 г., со-
брать обширный числовой матеріалъ. Изъ учениковъ А в е и а р і у с а
назовемъ Зайонневскаго (котораго во всѣхъ иностранныхъ изданіяхъ
почему-то пишутъ 8 а о 18 с 11 е дѵ л к і), Павловскаго, Надеждина,
Страуса, Жука, Каннегисера и Дьячевскаго.
И а в л е в с к і й изслѣдовалъ больше »е число органическихъ жидко-
стей и нашелъ рядъ правилъ, изъ которыхъ приводимъ только одно: кри-
682
Ненасыщенные пары.
тпческія температуры гомологическпхъ соединеній отличаются на посто-
янную величину отъ температуръ кипѣнія ихъ при нормальномъ давле-
ніи. О другомъ правилѣ, относящемся къ смѣсямъ, будетъ сказано ниже.
Б у л а т о в ъ указалъ, что, вообще, критическая температура веще-
ства тѣмъ выше, чѣмъ сложнѣе составъ его молекулы.
Особый интересъ представ. гнетъ критическое состояніе с м ѣ -
с е и. Для смѣсей паровъ съ такими газами, критическая температура ко-
торыхъ весьма низка, опредѣляли & СаіПеіеі, А п й г е лѵ 8, СаіПеіег
пНаиіеіеиіІІе, Наннау и др. Вообще4 оказывается, что примѣсь
небольшого количества газа (водорода, азота, воздуха) немного понижа-
етъ $ и въ то же время сильно увеличиваетъ критическое давленіе лг.
Такъ напр. Наина у нашелъ для чистаго алкоголя г/= 235°,47 и л =
-67,07 атм.; для алкоголя съ примѣсью водорода $ = 230°,8 и л =
-- 163,5 атм. Рісіеі утверждаетъ, что опредѣленіемъ критической тем-
пературы можно пользоваться, какъ признакомъ чиетоты даннаго веще-
ства. Наиболѣе всестороннее изслѣдованіе критическаго состоянія смѣ-
сей произвелъ С а и Ь е I.
Температуру & смѣси двухъ жидкостей опредѣлялъ впервые
Страусъ (1880), который нашелъ правило, выражающееся формулой
= 0,^4-
+ а2
(53)
Здѣсь 'д, критическія температуры смѣси и двухъ ея состав-
ныхъ частей; и а2 процентное содержаніе этихъ частей. Этотъ за-
конъ былъ найденъ на основаніи наблюденій надъ смѣсями спирта и эфира.
Зная & и ^2, можно вычислить и такимъ образомъ Страусу уда-
лось предсказать критическую температуру воды на
основаніи наблюденій & для смѣсей спирта и воды (сообщено въ мартѣ
(1881 г.); онъ нашелъ # = 370° съ возможною ошибкою въ Н“50. Саіі-
Іеіеі и Соіагсіеаи нашли # = 365°. Правило Страуса было нѣсколько
позже найдено и Павловскимъ. Тѣмъ же вопросомъ занимались впо-
слѣдствіи Апвйеіі, Голицынъ, Оеѵѵаг и (}. 6г. ЗсЬтійІ; по-
слѣдній нашелъ, что правило Страуса подтверждается въ широкихъ
предкахъ, между прочимъ также для воздуха, какъ смѣси кислорода
(г\ =—118°) и азота (Л2 =— 146°); формула (53) даетъ і)=—140°,8,
наблюденія дали числа между — 140° и — 141°. Повидимому, можно го- )
ворить о законѣ Страуса.
Мы переходимъ теперь къ весьма интересному явленію, наблюдае-
мому, хотя и рѣдко, въ жидкостяхъ вблизи критической температуры. Го-
раздо чаще наблюдается оно вблизи критической температуры
растворенія, при которой двѣ жидкости, не смѣшивающіяся между
собою, но образующія два раздѣльные раствора, начинаютъ образовывать
однофазную, т.-е. гомогенную систему. Такъ какъ это явленіе наблюда-
ется и въ случаяхъ одной жидкости, то мы остановимся здѣсь на немъ
подробнѣе. Мы говоримъ объ явленіи опалесценціи.
Критическое состояніе.
683
Это явленіе впервые наблюдалъ Оиііігіе (1884), а затѣмъ ВоіЬ-
тип(1, О 81 лѵ а 1Й, бсЬтеіпетакегв (смѣсь трехъ жидкостей),
8. Тоип§ (1906) и др. По внѣшнему виду оно напоминаетъ явленіе,
которое обнаруживаютъ «мутныя» средины. Его подробно изслѣдовали
Ргіейіаепдег и затѣмъ Коноваловъ, который полагаетъ, что при-
чину опалесценціи слѣдуетъ искать въ частицахъ пыли, находящихся въ
жидкости и образующихъ, каждая, центръ, къ которому неодинаково
притягиваются составныя части смѣси. Работа раздѣленія смѣси, близь
критическаго состоянія, весьма мала; пылинки окружаются оболочкою,
составъ которой отличается отъ состава остальной жидкости и этого до-
статочно, чтобы вызвать явленіе опалесценціи.
Позже появились двѣ новыя теоріи В о п п а п'а и 8 т о 1 п с й о 8 к і.
Воппап (1904) объясняетъ опалесценцію слѣдующимъ образомъ. Ниже
критической температуры поверхностное натяженіе а на границѣ обѣихъ
фазъ положительно. При критической температурѣ оно становится рав-
нымъ нулю, если кривизна не слишкомъ велика. Для весьма малыхъ ка-
пель оно остается положительными^ даже при температурахъ, нѣсколько
превышающихъ критическую. Такимъ образомъ получается состояніе,
при которомъ одна фаза распредѣлена въ фугой въ видѣ маленькихъ ка-
пелекъ ; эти капельки и вызываютъ опалесценцію. Въ пользу этого
взгляда высказались ЛѴ е 8 е п й о п к (1908) иВоіктипй (1908). Послѣд-
ній изслѣдовалъ смѣси воды и масляной кислоты, къ которымъ онъ при-
мѣшивалъ еще различныя третьи вещества; онъ показалъ, что всѣ на-
блюденныя имъ явленія объясняются теоріей Воппап’а. На совершенно
иной, чисто кинетической основѣ базируется теорія 8пю1исйолѵ8кі
(1908). По кинетической теоріи распредѣленіе молекулъ въ данный мо-
ментъ изслѣдуется статистически. При этомъ оказывается, что вполнѣ воз-
можны небольшія мѣстныя отклоненія отъ абсолютной однородности;
они обладаютъ извѣстной степенью вѣроятности, зависящей отъ величины
отклоненія и отъ состоянія матеріи, бтоіисііолѵзкі показалъ, что
вблизи критическаго состоянія значительныя отклоненія отъ однородности
обладаютъ относительно большой степенью вѣроятности. Такимъ обра-
зомъ въ жидкости могутъ въ безчисленныхъ мѣстахъ возникнуть внутри
весьма малыхъ объемовъ конечныя измѣненія плотности — зерна раз-
рѣженій и уплотненій, вызывающія явленіе опалесценціи. Въ пользу
этой теоріи высказались Каілтегііп^іі-Оппее и Кеевот (1908),
изслѣдовавшіе жидкій этиленъ вблизи критической температуры и опре-
дѣлившіе количество свѣта опредѣленной длины волны, разсѣиваемаго
опалесцирующимъ слоемъ въ опредѣленномъ направленіи, какъ функцію
температуры і. Оказалось, что это количество свѣта пропорціонально
(і—/^)~1, что согласуется съ теоріей 8то1исііо\ѵ8кі, тогда какъ тео-
рія Воппап’а приводитъ къ зависимости вида (^ —$)~2.
Наппау и Но^агѣіі опредѣляли $ для растворовъ солей въ
различныхъ жидкостяхъ, а также для раствора 5 въ С52. Оказалось во-
первыхъ, что присутствіе растворенныхъ веществъ повышаетъ крити-
684
Ненасыщенные нары.
ческую температуру растворителя, и во-вторыхъ, что первыя не осажда-
ются, когда растворитель весь переходитъ въ парообразное состояніе, но
остаются растворенными въ этомъ парѣ.
Центнершверъ произвелъ обширное изслѣдованіе критической
температуры растворовъ въ жидкихъ амміакѣ и сѣрнистомъ ангидридѣ.
Онъ находитъ, что повышеніе критической температуры пропорціонально
концентраціи раствореннаго вещества, и что молекулярное повыше-
ніе этой температуры для даннаго растворителя не зависитъ отъ при-
роды раствореннаго вещества.
Вскорѣ послѣ появленія этой первой работы Центнершвера
ѴапЧ Но И иѴапЬааг изслѣдовали теоретически зависимость кри-
тическихъ величинъ отъ растворенныхъ веществъ. ѴапЧ Ноіі‘ (1903)
нашелъ, что молекулярное повышеніе критической температуры должно
быть пропорціонально молекулярному вѣсу растворителя. Если $ — кри-
тическая температура раствора, г>0 - чистаго растворителя и въ А грам-
махъ растворителя находятся 5 граммовъ вещества, то
$МТГ
11
(53, а)
гдѣ М молекулярный вѣсъ и Тс — абсолютная критическая темпе-
ратура растворителя, — молекулярный вѣсъ растворимаго вещества.
Коеффиціентъ пропорціональности к долженъ всегда равняться 3. ВіісЬ-
пег (1906) изслѣдовалъ жидкую СО2 и нашелъ для к значенія, близ-
кія къ 3. Центнершверъ и Накаляетъ (1906) изслѣдовали ра-
створы въ этиловомъ эѳирѣ, опредѣляя не только О, но также и крити-
ческое давленіе п. Оказалось, что
л; = лг0 -Ц к±С......................(53,&)
гдѣ лг0
ція.
относится къ чистому растворителю, с молекулярная концентра-
Такъ какъ (53,а) можно, очевидно, написать въ видѣ &= Ц- к2С, то
л= л0-|-—#0) . ... . . (53,с)
к
гдѣЛ= Для растворовъ трифеиилметана въ этиловомъ эѳирѣ А —
-0,37. Затѣмъ Центнершверъ и Калнинъ (1908) изслѣдовали
растворы въ пентанѣ и нашли для нихъ А — 0.33 : кх - = 455, к2 = 135,
какъ среднее для 7 изслѣдованныхъ веществъ. Незадолго до этого
Це нтн е р ш в е р ъ (1907) опубликовалъ изслѣдованіе растворовъ въ
метплхлоридѣ, этиловомъ эмирѣ и метиловомъ алкоголѣ. Онъ нашелъ,
что теоріи V а пЧ Н о П’а и V а п Ь а а г’а даютъ лишь приблизительно
вѣрныя значенія. Наконецъ, Центнершверъ (1909) изслѣдовалъ кри-
тическіе объемы и плотности многихъ растворовъ и нашелъ, что при
приближеніи къ критическому состоянію плотность возрастаетъ тѣмъ бы-
стрѣе, чѣмъ менѣе летуче растворенное вещество.
§ 8. Ученіе о соотвѣтственныхъ состояніяхъ. Сравнивая свойства
различныхъ веществъ, мы ихъ беремъ обыкновенно при одинаковыхъ
Соотвѣтственныя состоянія.
685
температурахъ і и давленіяхъ р\ или мы сравниваемъ вещества при
ихъ точкахъ кипѣнія, т.-е. когда упругости насыщенныхъ паровъ однѣ и
тѣ же. Спрашивается, раціональны ли подобные способы сравненія и не
слѣдуетъ ли сравнивать свойства веществъ, взявъ ихъ въ иныхъ, въ ка-
комъ либо смыслѣ «соотвѣтственныхъ» другъ другу состояніяхъ ? По-
пытки въ этомъ направленіи можно найти въ работахъ ВеіапсоигѴа
Оаііоп'а, Гагасіау’я, Сіаизіпй’а и ВиеЬгіпд’а.
Ученіе о соотвѣтственныхъ состояніяхъ, въ его современномъ видѣ,
принадлежитъ Ѵан-(1ег-\Ѵаа1 в’у. Исходною точкою его ученія слу-
житъ мысль, что критическія состоянія должны считаться дѣй-
ствительно одинаковыми или соотвѣтственными состояніями всѣхъ ве-
ществъ. Составимъ для каждаго вещества свою шкалу абсолютныхъ
температуръ, давленій и объемовъ, принявъ значенія этихъ величинъ при
критическихъ состояніяхъ 273 л и д за единицы. Если Г, р и ѵ
суть абсолютная температура, давленіе и объемъ при любомъ состояніи
даннаго вещества, то въ новыхъ шкалахъ абсолютная температура т.
давленіе е и объемъ п опредѣляются изъ равенствъ
_ 1 _р
т~ 273 + $’ е— л’
ѵ
п = —
9
• • (54)
Величины т, ь и п суть числовыя величины, уже не зависящія отъ
выбора какихъ бы то ни было единицъ. Онѣ называются приведен-
ными температурой, давленіемъ и объемомъ. Предположимъ,
что къ данному веществу приложимо уравненіе Ѵап-йег-АѴааІв’а
Ь) = Ь>Т.
(55)
Формулы
основаніи (49)
(54) даютъ
стр. 672,
_ Ъат
~ 27ЬР ’
7 =/тг(273 + $), р = ле. ѵ — пд, или, на
__ ьа
Р ~ 27 Ь2’
(56)
остается
(56) въ (55),
мы увидимъ, что
Вставляя
приведенное уравненіе
а, Ь и /? сократятся, и что
— 1) =
8/72
(57)
ѵ
— ЛпЬ . .
или
ът 3
8 = --
Зп — 1 п*
• (5а)
Въ это уравненіе входятъ только приведенныя температура т, да-
вленіе 8 и объемъ п, и не входятъ никакія величины, ха-
рактеризующія данное вещество и отличающія его отъ дру-
гихъ веществъ. Уравненіе (57) есть уравненіе состоянія всѣхъ ве-
щ е с т въ, къ которымъ приложима формула Ѵап-(1ег-\Ѵ ааі в’а. Мы
увидимъ, что многіе выводы, вытекающіе изъ этого уравненія и изъ дру-
686
Ненасыщенные пары
гихъ, получаемыхъ при введеніи величинъ т, е и п, оправдываются не
только для паровъ, но и для жидкостей. Теоретически мы, конечно, не
имѣемъ права ожидать, чтобы внѣ. предѣловъ примѣнимости формулы (55)
эти выводы оказались согласными съ результатами опытовъ.
Формула (57) показываетъ, что если двѣ изъ трехъ величинъ тп, е, п
даны, то третья имѣетъ для всѣхъ веществъ одно и то же значеніе, т.-е.
что напр. при одинаковыхъ приведенныхъ температу-
рахъ и давленіяхъ всѣ вещества занимаютъ и одина-
ковые приведенные объемы; количество взятаго вещества при
этомъ очевидно никакой роли не играетъ. Состоянія двухъ веществъ,
при которыхъ они имѣютъ одинаковые т, е и я, называются соотвѣт-
ственными состояніями. Ясно, что критическія состоянія
(т = 1, 6—1, п = 1) суть соотвѣтственныя состоянія. Изъ формулы (57)
вытекаетъ слѣдующій
Законъ I. Если на координатныхъ осяхъ отклады-
вать приведенные объемы др и давленія л;, то для
всѣхъ веществъ получаются одинаковыя изотермы, соот-
вѣтствующія одинаковымъ постояннымъ приведеннымъ температурамъ пг.
Обратимся къ формуламъ (15) и (16) стр. 656 и 657, опредѣляющимъ на
основаніи формулъ Ѵап-сіет-\ѴааІ8та и МахлѵеІІ-СІаивіие’а
упругость р насыщеннаго пара и удѣльные объемы о и 5 этого пара и
жидкости. Обозначимъ приведенную упругость насыщеннаго пара черезъ
приведенные объемы пара и жидкости черезъ и приведенную
температуру опять черезъ т. Тогда, см. (49) стр. 672,
Рл а
р = рѵл = а = щдр — зщй 5 —
21 о
Т=т(273 + #) =
Подставляя эти величины въ уравненія (15) и (16) стр. 56 и 657, по-
лучаемъ
Зщ — 1
35г — 1
. (59)
Въ этихъ уравненіяхъ также исчезли величины а, Ь и /?; они оди-
наковы для всѣхъ веществъ и могутъ служить для опредѣленія
Ръ аі и 5і по данной приведенной температурѣ т. С1аіі8Ііі8, Ріапск,
Зиловъ, Столѣтовъ и Кіііег показали, какъ при помощи нѣкото-
рыхъ вспомогательныхъ величинъ можно по данному т рѣшить уравне-
нія (59). Представимъ себѣ, что уравненія (59) рѣшены и получилось
А==/і(т), А=/2<», .... (60)
Соотвѣтственныя состоянія.
687
Эти три функціи одинаковы
а отсюда получается рядъ замѣчательныхъ
даетъ намъ
Законъ 11. При одинаковыхъ
для всѣхъ веществъ,
слѣдствій. Первое равенство
приведенныхъ темпе-
ратурахъ всѣ вещества обладаютъ одинаковою приве-
денною упругостью насыщеннаго пара. В а ш 8 а у и У о и п
называютъ кривую р± = /і(тп) ортометрическою кривою.
Равенство
Законъ
пературахъ
веденнымъ
Наконецъ,
ложимость нашихъ
Законъ IV. При одинаковыхъ приведенныхъ темпе-
ратурахъ всѣ
веденнымъ объемомъ жидкости.
Если исключить т изъ перваго и второго, а затѣмъ изъ перваго
и третьяго уравненій (60), то получается
<*1 = Л(Р1) , $1=РМ
аі = Л(^) даетъ
III. При одинаковыхъ приведенныхъ
всѣ вещества обладаютъ одинаковымъ при-
объемомъ насыщеннаго пара.
третье равенство зд = /3(т) даетъ, если допустить при-
выводовъ къ жидкостямъ,
тем -
вещества обладаютъ одинаковымъ при-
(61)
гдѣ /д и одинаковыя для всѣхъ веществъ функціи. Это даетъ намъ
Законъ V. Если на координатныхъ осяхъ отклады-
вать приведенные объемы и давленія, то для всѣхъ
веществъ получается одна и та же пограничная кри-
вая (АКВ на рис. 204).
Законъ П, который даетъ рг — /х(т), провѣряли V а п - сі е г -АѴ а а 18,
Надеждинъ, ^іапвоп, Сгпуеидр.
Такъ какъ критическое давленіе для многихъ веществъ имѣетъ
близкія другъ другу значенія, то изъ закона II слѣдуетъ, что о т н о ш е -
ніе И абсолютной температуры кипѣнія Т8 къ абсолют-
ной критической температурѣ Тс, т.-е.
= Л........................................(61, а)
* с
имѣетъ для многихъ веществъ одну и ту же числен-
ную величину. И дѣйствительно, И находится между о?56 для С82
и 0,73 для НСІ.
Курбатовъ (1908) нашелъ, что /і имѣетъ меньшую величину' для
тѣлъ съ малымъ молекулярнымъ вѣсомъ и для гомологическихъ рядовъ
правильно возрастаетъ вмѣстѣ съ молекулярнымъ вѣсомъ.
Вмѣсто р± = /і(^)? мы можемъ написать
Т\=,...........................(61,6;
I тг]
688
Ненасыщенные пары.
такъ какъ рх = р : л; и т = Т: Тс. Ѵап-(1ег-ЛѴааІ8 далъ для этой
функціи эмпирическую формулу
Т __ Т
.............(61,0
гдѣ / одинъ и тотъ же для всѣхъ веіцествъ множитель.
Если пользоваться натуральными логариѳмами, то, по Ѵап-
(Іег-АѴааІ 8’у (1904), должно быть приблизительно / = 7, тогда какъ въ
дѣйствительности / близко къ 7. Формулу (61,с) провѣряли многочисленные
изслѣдователи, давая ей различныя видоизмѣненія. Впервые это сдѣлали
Ка пі8 ау (1894) и бгиуе (1894). Послѣдній нашелъ, что / для раз-
личныхъ веществъ колеблется между 2,5 и 3,3 если пользоваться об ык-
новенными логариѳмами и что даже для опредѣленнаго вещества/не
постоянно, но зависитъ отъ температуры Т. Позже Сг и у е и Маііеі
(1902) нашли, что для многихъ веществъ / колеблется около средняго
значенія, равнаго 3,1. Это справедливо лишь для «нормальныхъ веществъ,
такъ какъ для «аномальныхъ», т.-е. полимеризованныхъ / имѣетъ
большія значенія. Нарреі (1904) также нашелъ, что / имѣетъ раз-
личныя значенія для различныхъ группъ тѣлъ. Такъ, онъ нашелъ для
аргона/=2,25, криптона/=2,39, ксенона /=2,38, тогда какъ для
бензола, эфира и подобныхъ веществъ / колеблется между 2,8 и 3,0. Такъ
какъ оказалось, что ртуть принадлежитъ къ группѣ аргона, то съ по-
мощью формулы (61,г) можно было вычислить критическія величины для
Нарреі нашелъ далѣе, что / есть функція приведенной темпе-
ратуры. Для аномальныхъ веществъ получаются значительно большія
значенія, напр. для воды /= 3,26, для уксусной кислоты /= 3,48, для
этиловаго алкоголя /=3,91, для изобутиловаго алкоголя /=4,17.
Кегіі8І вычислилъ, что для водорода, /= 1,83 для этиловаго алкоголя
/ = 4,05.
Изслѣдованіемъ формулы (61,с) занимались за послѣднее время пре-
имущественно ЭДегп8І, Лііріпег и Е и йогѣ
Въ первой своей работѣ Ліріпег (1906) находитъ, что / съ по-
вышеніемъ температуры сначала убываетъ, достигаетъ минимума и за-
тѣмъ вновь возрастаетъ. Положимъ, Ѳ есть приведенная температура
Т
- и Ѳх — значеніе Ѳ, при которомъ / имѣетъ минимальное значеніе /х;
обозначимъ / /і чрезъ А/. Если выразить графически функціональ-
ную зависимость А/ отъ Ѳ, то для Ѳ Ѳх получается прямая, для Ѳ >
— дуга круга. Возможно, что всѣ дуги при критической температурѣ
(Ѳ = 1) сходятся въ одной точкѣ, лежащей между А/ = 0,2 и А/ = 0,3
Для фтористаго бензола / = 2,89, Ѳх = 0,690; для /х = 2,25, Ѳх = 0,33 ;
для СО2 = 2,750 при Ѳх = 0,747. Въ слѣдующемъ изслѣдованіи
Зііріпѳг (1907) далъ формулу
/ — /о । ..............(61,б/)
Соотвѣтственныя состоянія.
689
Такъ, напримѣръ для Н§ 0 1 720 /== 2,2032 — 0,59746» + +—+ 1 О
для /У2 /= 1,1208 1,2251(9 + ѵ+г 1 — и
для Н,0 / = 3,4300 0,47276» + 1 — 0
При низкихъ температурахъ можно въ послѣднемъ членѣ положить
Ѳ = о; въ такомъ случаѣ получается формула
/=/о'~ аѲ,
гдѣ /0' =/0 + Ь. Вблизи критической температуры Тс (63,а) даетъ слиш-
комъ большія значенія. Лірѣпег (1908) объяснилъ это тѣмъ, что по
формулѣ (63) _
1^=/ — ѳ .
Вмѣстѣ съ (63,а) послѣдняя формула при Т = Тс т.-е. при Ѳ = 1
даетъ \%р = Ь, тогда какъ должно быть — \%р = 0. По-
этому онъ присоединилъ еще одинъ членъ, представивъ (63,а) въ видѣ
с(1 Ѳ) +1
• • (61, е)
Для фтористаго бензола (С§НЪР), С02 и ХНЪ отсюда получились
значенія / хорошо совпадающія съ наблюденными. ВиФогі въ двухъ
работахъ изслѣдовалъ свойства благородныхъ газовъ (Аг, Кг, Хе, Хе) и
далъ (1910) слѣдующія значенія /: Кг 2,371, Хе— 2,320.
Также и другіе изслѣдователи пытались видоизмѣнять формулу (63).
Могіяип (1900) по предложенію Биіоіі изслѣдовалъ формулу
Т_с--Т
Т
(61,/)
и нашелъ хорошее согласіе для 8Н2, КО, С&НЪР, СС14 и другихъ
веществъ.
Мегпеі (1906) далъ формулу
7\ (/ Тг \ і / т \ 1
Ідл ]др = 1,75І§ -(- а і I ~ — 11 1 — Т" ) і ' (®1,#)
Постоянная а здѣсь имѣетъ слѣдующія значенія:
Я2 Аг Л/2 О2 СО2 СНСІ^ ЫН3 НСІ Н2О (С2/7б)2О
а = 1,65 2,15 2,47 2,53 2,94 3,12 3,24 2,82 3,53 3,32
Віп^Ьат (1906) провѣрилъ формулу (63,(1) на свыше чѣмъ 100
веществахъ и получилъ хорошее согласіе.
Подставимъ въ равенство (60) = /$(т) величины т =
и
КУРСЪ ФИЗИКИ О.ХВОЛЬСОНА. Т. III, изд. 3-е.
1
273+ &
44
690
Ненасыщенные пары.
. Обозначимъ абсолютную критическую температуру для удобства
черезъ Тс = 273 а объемъ жидкости черезъ ѵ — 8. Тогда имѣемъ
/ (т\
ѵ = <р/»[т •
\1 с /
Это даетъ . у..
^=- .................(62>
Ѵ / Г\ Тс
IВ I 'Г' I
\ 1 с/
Отсюда получается
Законъ VI. Относительное увеличеніе объема жид-
костей при нагрѣваніи одинаково для всѣхъ жидкостей,
если нагрѣваніе начать при одинаковыхъ приведен-
ныхъ температурахъ и если нагрѣвать до одинаковыхъ
приведенныхъ температуръ. Дѣйствительно, Аѵ : ѵ одина-
ковы, если Т: Тс и ДТ . Тс, а слѣд. и (Т ф- АТ): Тс для всѣхъ веществъ
одинаковы.
Мы имѣли формулу, см. (25,с) стр. 550,
в = АТ(р — 8)
гдѣ р скрытая теплота испаренія, р упругость насыщеннаго пара. Вста-
вимъ Т = пгТс, п = <роѵ 5 = </51; др = лдръ ді = дТ = Тсдт ; тогда
получается:
Р Л , &Рі
Тс = тс &
Вставляя для л, д и Тс ихъ значенія (13) стр. 655, имѣемъ
— — Апг(а1 — $і) -=Р*
ТСЯ 8 ѵ 1 17 дш
Величина А? обратно пропорціональна молекулярному вѣсу /х, а по-
тому можно написать
гдѣ С постоянный коеффиціентъ. На основаніи законовъ 1, II и III,
вся правая сторона есть функція приведенной температуры, одинаковая
для всѣхъ веществъ, т. е.
~ = ф(/п).........................(63)
* С
Законъ VII. Произведеніе скрытой теплоты испа-
ренія на молекулярный вѣсъ, дѣленное на абсолют-
ную критическую температуру, есть вели чина, которая
при одинаковыхъ приведенныхъ температурахъ одна и
Соотвѣтственныя состоянія.
691
(63,а)
та же для всѣхъ веществъ. Величины и Тс постоянныя для
даннаго вещества, а потому мы можемъ написать р = СФ(пі), гдѣ С по-
стоянное, зависящее отъ рода тѣла.
Пусть Т8 — температура кипѣнія при нормальномъ давленіи и @
теплота испаренія при этой температурѣ. Мы можемъ (63) написать
въ видѣ: ~
т5 т/
Согласно формулѣ (61,я) стр. 687, Т8 : Тс имѣетъ для многихъ ве-
ществъ одинаковое значеніе (около 2/3); поэтому, приближенно,
т —
1 8
гдѣ к почти одинаковое число для различныхъ веществъ. Эта формула
въ сущности есть формула Т г о и 1 о п’а см. гл. XI, § 4 форм. (24); слѣ-
довательно, формула Т г о и I о п’а является частнымъ случаемъ формулы (63).
Законъ АПП. Скрытая теплота испаренія находится
въ одинаковой для всѣхъ веществъ зависимости отъ
приведенной температуры. Если при температурахъ т1 и т2
скрытыя теплоты испаренія для одного вещества рх и р2, для другого
вещества р/ и то мы имѣемъ : р2 = р/: .
Ѵап йег АѴааІв, Катпіег Іі п^й Оппез, Сигіе, Хаіап-
8 оп, Мезііп и Сонинъ обобщили ученіе о соотвѣтственныхъ состо-
яніяхъ, показавъ, что это ученіе можетъ быть основано не только на
уравненіи Ѵап сі о г АѴ а а 1 з’а, но и на другихъ уравненіяхъ гораздо
болѣе общаго вида.
Обращаемся къ вопросу о томъ, насколько выведенные здѣсь законы,
относящіеся къ ученію о соотвѣтственныхъ состояніяхъ, подтверждаются
на опытахъ.
Законъ I провѣрялъ Атад*а1 (1896), сравнивавшій между собою
приведенныя изотермы для различныхъ веществъ, а именно для СО2, воз-
духа и эфира, а затѣмъ для СО2 и С2Н±.
умнымъ оптическимъ способомъ сравненія
въ справедливости этого основного закона
состояніяхъ.
3 а к о н ъ II, рг = Л(т), гдѣ рг и пг
Пользуясь чрезвычайно остро-
изотермъ, Ат а^аі убѣдился
въ ученіи о соотвѣтственныхъ
приведенныя упругость насы-
щеннаго пара и температура, провѣрялъ, какъ уже было сказано, Ѵап
йег АѴааІв. Приведемъ нѣсколько примѣровъ. Для ЗО2 имѣемъ
Тс = 428°,4, лг = 78,9 атм.; для эфира Тс' = 463°, л7 = 36,9 атм. Далѣе
извѣстно, что при температурѣ Т =412°,9 давленіе паровъ 8О2 равно
р = 60 атм. При этомъ приведенное давленіе рг = 60 ; 78,9 = 0,7605, и
приведенная температура т — 412,9 : 428,4 = 0,964. Для эфира то же
самое приведенное давленіе р/= = 0,7605 соотвѣтствуетъ истинному
давленію р‘ = рхл' — 0,7605 X 36,9 = 28,4 атм. Такое давленіе паровъ
эфира имѣетъ мѣсто при температурѣ Г'= 445°,8, какъ это видно изъ
44*
692
Ненасыщенные пары.
таблицъ Зайончевскаго; приведенная температура т* = 445,8 :463 =
= 0,963. Итакъ, мы видимъ, что если р1'=р1, то и ігі =т.
3 а к о н ы Ш и IV провѣрялъ М а і Ь і а 8. Эти законы требуютъ,
чтобы приведенные объемы щ и насыщеннаго пара и жидкости были
одни и тѣ же для всѣхъ веществъ при одинаковыхъ приведенныхъ тем-
пературахъ т. Отсюда слѣдуетъ, что и приведенныя плотности и
т.-е. отношеніе плотностей б и сі пара и жидкости къ плотности О при
критической температурѣ, должно быть одно и то же для всѣхъ веществъ
при одинаковыхъ т, такъ что можно написать
ді = 75 = = р = .........(64)
Отсюда слѣдуетъ;
8 = ОР^пі); (1 = ОР2(ігі)...........(65)
Плотность <5 насыщеннаго пара и плотность (I жид-
кости выражаются для всѣхъ веществъ одинаковыми по
виду функціями приведенной температуры. Эти функціи,
взятыя для разныхъ веществъ, отличаются только множителемъ про-
порціональности, который самъ долженъ быть пропорціоналенъ критиче-
ской плотности. М а I й і а 8 принялъ для 8 и сі эмпирическія формулы вида
8 = /1(1 — пг — а\/1 — т й2)............(66)
сі = В(т — с 4- АVI пі).............. • (67)
гдѣ Л, а, Ь, В, с и й постоянныя, опредѣляемыя на основаніи наблюде-
ній. Для паровъ СО2, Н2О, 802, С2Н±, НСІ и эфира Маій іа 8 на-
шелъ дѣйствительно весьма близкія между собою значенія чиселъ а и Ь
и для б общую формулу
(5 = Д[1 —т — 1,13/1—т"+ (0,579)4 .... (68)
Для'жидкихъ СО2 и 8О2 величины с и И также почти одина-
ковы ; для нихъ
сі = В(т — 0,569 +-1,66 /Т^/тг)..........(69)
Законы II. III и IV провѣрялъ У о и п въ обширной работѣ и
для большого числа веществъ. Мы не приводимъ его чиселъ, ограничи-
ваясь указаніемъ, что упомянутые законы во многихъ случаяхъ подтверж-
дались, но что въ нѣкоторыхъ случаяхъ замѣчались и большія отступле-
нія, которыя однако есть поводъ объяснять неоднородностью изслѣдуе-
маго вещества (полимеризація, диссоціація). Вопросомъ о причинахъ
этихъ отступленій занимались Оиуе, V ап-сІег-ЛѴааІ8 и въ особен-
ности Бога евскі й (1897), посвятившій этому вопросу обширное из-
слѣдованіе, въ которомъ главнымъ образомъ разобрано вліяніе химиче-
скаго состава вещества на уклоненія отъ законовъ, къ которымъ приво-
дитъ ученіе о соотвѣтственныхъ состояніяхъ. Онъ находитъ, что вдали
отъ критической температуры вслѣдствіе полимеризаціи вещества эти за-
коны перестаютъ быть вѣрными.
Соотвѣтственныя состоянія.
693
Законъ V есть простое слѣдствіе предыдущихъ законовъ.
Законъ VI, относящійся къ расширенію жидкостей, даетъ возмож-
ность вычислить тепловую расширяемость одной жидкости, если извѣстны
расширяемость другой и критическія температуры обѣихъ жидкостей. По-
лагая, что для одной жидкости объемъ г>1= 1 4“ (ЦІ Ьгі2 сгі\ дЛЯ дру-
гой ѵ2 = 1 + а2і 4- Ь2& 4- с2і'\ можно вычислить и съ если из-
вѣстны а2, А2, с2 и критическія температуры обѣихъ жидкостей. V ап-
сіег-АѴааІз вычислилъ Ьг и сА для эфира, принявъ для а2, Ь2 и с2
числа, непосредственно опредѣленныя для шести различныхъ жидкостей
(С52, хлороформъ, хлористый этилъ и др.). Такимъ образомъ онъ полу-
чилъ по шести чиселъ для каждой изъ величинъ а1? Ь{ и с1. Числа для
аг оказались весьма близкими какъ другъ къ другу, такъ и къ числу, най-
денному непосредственно изъ наблюденій надъ расширеніемъ эфира.
Впрочемъ выше было указано, что мы не вправѣ ожидать точнаго опыт-
наго подтвержденія законовъ, относящихся къ жидкостямъ.
Законъ VII провѣрялъ Ѵап-сІег-\ѴааІ8, причемъ онъ полу-
чилъ слѣдующія числа:
Вода. Эфиръ. Ацетонъ. Хлороформъ. ссц С52
р = 7,5 1 1,41 1,49 1,57 2,03
0 = 489 90 126,5 60 15 82
№ Т ~ 7 г 1,35 1,31 1,44 1,35 1,34 1,15
с
Величины р суть скрытыя теплоты испаренія при одинаковыхъ при-
веденныхъ температурахъ т. а слѣд. различныхъ температурахъ і\ вмѣсто
послѣднихъ здѣсь показаны давленія р (въ атмосферахъ) насыщенныхъ
паровъ при этихъ температурахъ і.
Законъ VIII повидимому еще не былъ провѣряемъ. Чисто эмпи-
рическія формулы, которыми пользуются, чтобы выразить зависимость ве-
личины р отъ /, съ этимъ закономъ не согласуются.
Ваккег (1896) вывелъ еще рядъ другихъ законовъ, вытекающихъ
изъ ученія о соотвѣтственныхъ состояніяхъ и относящихся къ внутрен-
ней скрытой теплотѣ испаренія, къ теплоемкостямъ, энтропіи, энергіи,
свободной энергіи и къ скорости звука. Приводимъ два изъ этихъ зако-
новъ: въ соотвѣтственныхъ состояніяхъ теплоемкости обратно пропорціо-
нальны молекулярнымъ вѣсамъ; въ соотвѣтственныхъ состояніяхъ ско-
рости звука прямо пропорціональны критическимъ температурамъ и обратно
пропорціональны молекулярнымъ вѣсамъ.
Каттегііп^й Оппев (1894) показалъ, что для различныхъ ве-
ществъ въ соотвѣтственныхъ состояніяхъ должно быть
1/"—— = с
V мы с............
(70)
Здѣсь у — коеффиціентъ внутренняго тренія, М — молеку-
лярный вѣсъ. Постоянная С колеблется для нормальныхъ веществъ между
694
Ненасыщенные пары.
0,38 и 0,68 (при Т =0,58 7^). Сгпуе (1890) нашелъ слѣдующую связь:
п? — 1М ,Рс
/г2 -|- п.......................(?1)
Здѣсь п — показатель преломленія и вся лѣвая часть уравненія пред-
ставляетъ собою молекулярную преломляемость (т. II) веще-
ства. Для большинства веществъ к лежитъ между 1,8 и 2,0. Для ано-
мальныхъ веществъ к меньше (до 1,1). Ьесіис нашелъ, что всѣ газы
можно раздѣлить на три группы, причемъ въ соотвѣтственныхъ состоя-
ніяхъ всѣ газы одной группы обладаютъ одинаковымъ молекуляр-
нымъ объемомъ.
Теоріей соотвѣтственныхъ состояній занималась Кігйііпе Меуег
(урожд. В^еггит), Сгиуе и Маііеі, Нарреі, Віііег, Біеіе-
гісі и др.
Кігзііпе Меуег показала, что для двухъ веществъ за соотвѣт-
ственныя слѣдуетъ принять тѣ состоянія, для которыхъ величины
Тс — 1 п—р <р—ѵ
К ’ Р ’ ...............( ’
имѣютъ одинаковыя значенія. Здѣсь /С, Т7 и <2 — постоянныя, имѣющія
опредѣленныя значенія для каждаго вещества; ихъ можно разсматривать,
какъ видоизмѣненныя критическія величины, полагая К—Тс а Р —
= л;—6, <2 —ф— с. Вмѣсто величинъ т, е и я, см. (54), мы здѣсь за
характеристику соотвѣтственныхъ состояній принимаемъ величины
Оказалось, что для 25 изслѣдованныхъ веществъ 6 = 0; слѣдова-
тельно,
е' = 1 — ? = I — е ....................
ЗТ-
т.-е. новыя соотвѣтственныя давленія совпадаютъ съ прежними. Новыя
постоянныя а и с являются какъ-бы нулевыми точками температуры и
объема, имѣющими особыя значенія для каждаго вещества. К. Меуег
изслѣдовала 30 веществъ; для 25 веществъ изотермы Р= /(/г'), соотвѣт-
ствующія одинаковымъ т\ оказались идентичными. Для воды, уксус-
ной кислоты и трехъ алкоголей оказались отклоненія, вѣроятно, вслѣд-
ствіе возрастанія полимеризаціи при убываніи температуры. Въ новой
работѣ К. Меуег (1910) изслѣдовала еще нѣкоторыя вещества, въ осо-
бенности водородъ, и установила соотвѣтствующія нулевыя точки. Также
Сг и у е и М а 11 е 1 подтвердили полученные К. Меуег результаты.
Б. Вегійеіоі опубликовалъ рядъ изслѣдованій надъ соотвѣтствен-
ными состояніями. Онъ показалъ, что уравненіе состоянія, данное Ь о -
гепіг’омъ, приводитъ къ приведенному уравненію
Литература.
695
1
16 1
9 ’ пгп?
- । 32
п---=— т
4 / 9
4
(73, а)
а-І-^Ѵз/г—0,7 — 0,3т) = 8т...........................(73)
хорошо совпадающему съ данными наблюденіи. Въ другой работѣ онъ
далъ уравненіе
Онъ также ввелъ при этомъ, подобно К. М е у е г, въ качествѣ при-
веденныхъ температуры и объема, величины вида
т-тт ѵ-ѵт
Тс-Тт И Ѵс-Ѵт'
Здѣсь Тс и Ѵс = у относятся къ критическому состоянію, а Тщ и
Ѵт суть постоянныя.
ЛИТЕРАТУРА.
Къ § 2.
Рерпииіі. Мёт. де ІАсад. 26 р. 163, 1862 ; Кеі (Іѳе Ехрег. 2.
Е. Ѵ/іейетапп. \Ѵ. А. 2 р. 195, 1877.
Р. А. Миеііег. \Ѵ. А. 18 р. 94, 1883.
и?. йаерег. \Ѵ. А. 36 р. 165, 1889.
Къ § 3.
Атсцгаі. Апп. сіііт. еі рЬув. (4) 29 р. 246, 1873; 28 р. 456, 1883; (5) 22 р. 353
1881; (6) 29 р. 1, 1893; С. В. 73 р. 183, 1871 ; 75 р. 479, 1872; 99 р. 1153, 1884; 113 р.
450, 1891 ; 115 р. 638, 1892.
Ногзітапп, ѴѴиеІІпег ипй Сгоіпап, ЗсНоор, Оіеіегісі, Ваііеііі, Ратзау апй
Уоип§, ѴѴгоЫехѵзкі. См. литературу къ § 8 и § 9 главы XII, стр. 640.
Къ § 4.
Ѵап йег ѴѴааІз. Біе СопііпиіШ дев ^авібгті^еп иті Нйвві^еп гивіапдев. Пере-
водъ Роііг'ъ, Ьеір2І&. 1881.
О. Е. Меуег. Біе кіпеіівсііе ТЬеогіе дег Оаве р. 298, Вгевіаи, 1877.
Сонинъ. Проток. Отд. Физ. и Химіи Варш. О. Естеств. 1889 № 5 р. 10; № 6 р. 5.
йае&ег. \Ѵіеп. Вег. 101 р. 1520, 1892.
йатез ТИотзоп. Ргос. К. 8ос. 28, 1871.
Махчѵеіі. Хаіиге (англ.) 11 отъ 4 и 11 марта 1875.
Сіаизіиз. АѴ. А. 9 р. 337, 1880; 14 р. 279, 492, 1881 ; МесЬап. АѴагтеПіеогіе 2
р. 185, 203, 1891.
Ріапск. АѴ. А. 13 р. 535, 1881; Тііегтосіупапіік р. 145, Ьеірхі^, 1911.
Надеждинъ. Физ. изслѣдованія, Кіевъ, 1887, р. 116; Ехпег’в Керегі.23 р. 712, 1887.
Сгітаійі. Оагг. СЫт. Ііаі. 16 р. 63, 1886; ВеіЫ. 10 р. 562, 1886.
Д. Коноваловъ. Ж. Ф. X. О. 18, Отд. химич. р. 398, 1886.
ОіЬЬз. Тгапв. о! Ніе Соппесі. Асад. 2.
Гольдгаммеръ. Термодинамическая поверхность воды. Москва 1884 (изъ Учен.
Запис. Имп. Моск. Унив., отд. Физ.-Мат., вып. 6, 1884).
КоНеюер;. АгсЬ. пёегі. 24 р. 295, 1890.
Віиетске. 2івсЬг. Г. рЬув. СЪетіе 6 р. 153, 407, 1890; 8 р. 554, 1891; 9 р. 78,
722, 1892.
Киепеп. Вівв. Ьеудеп 1892; 2івсЬг. Т рЬув. СЬетіе 11 р. 38, 1893; ВеіЫ. 16 р.
521, 1892 ;_17 р. 21, 1893.
696
Ненасыщенные пары.
Нігзск. XV. А. 69 р. 469, 1899.
Ѵап-йег-УѴааІз. Біе Сопііпиііаі и т. д. Часть II, 1900; РЬуз. ЕізсЬг. 1 р.
608, 1900.
Оап. Вегікеіоі. боигп. (1е рЬуз. (3) 8 р. 521, 1899.
Къ § 5.
СІаіі8Іи8. XV. А. 9 р. 337, 1880; 14 р. 279, 692, 1881 ; Апп. сЫш. еі рЬуз. (5) 30
р. 433, 1883.
Ріапск. XV. А. 13 р. 535, 1881.
Віиетске. 2ізсЬг. Ѵег. <1. беиізсЬ. Іп&еп. 30 р. 110, 1886; Ьапбоіі, ТаЪеІІеп р. 83,
Вѳгііп 1894.
Столѣтовъ. О. Ф. Н. 06. Л. Е. 5 вып. 1 р. 3, 1892.
8аггаи. С. В. 94 р. 639, 718, 845, 1882; 110 р. 880, 1890.
Рііг^егаій. Ргос. В. 8ос. 42 р. 216, 1887.
Нігп. ТЬёогіе шёс. бе Іа сЬаІеиг. 1 р. 93, Рагіз 1865 (формула первая); Апп
сЫт. еі рЬуз. (4) 10 р. 365, 1867 (формула вторая).
Сизіаѵ 8скпМі. ХізсЬг. 6. Ѵег. беиізсЬ. Іп^еп. 11 р. 649, 771, 1867.
КаттегІіп^Н Оппез. К. Ак. ѵап ХѴеіепзсЬ. Атзіегбаш 1881; ВеіЫ. 5 р. 718, 1881.
Ата^аі. С. В. 94 р. 847, 1882.
Ѵіоіі. Вепб. Асс. Ьіпсеі 4 р. 285, 316, 462, 513, 1888.
Таіі. Ргос. ЕбіпЪ. 8ос. 16 р. 65, 1889; 18 р. 265, 1891; Хаіиге ^англ.) 45 р. 80,
152, 199, 1891.
Рапкіпе. РЫІ. Тгапз. 1854 р. 336.
Ткотзоп апй }оиІе. РЫІ. Тгапз. 1854 р. 321; 1862 р. 579.
Оиргё. Апп. сЫт. еі рііуз. (4) 1 р. 168, 185, 1864.
Реуе. Р“. Апп. 96 р. 424, 1855.
Рескпа^еі. Ро§&. Апп. Ег^Ъб. 5 р. 563, 1872.
Ооиіііу. С. В. 93 р. 1134, 1881.
Вегігапй. С. В. 105 р. 389, 1887.
Ьейоих. ТЬёогіе без тазсЫпез а Ггоіб. Рагіз (Бипоб) 1878
8аггаи. С. В. 110 р. 880, 1890.
}ае%ег. ХѴіеп. Вег. 101 р. 1675, 1892.
Ваііеііі. Апп. сЫт. еі рііуз. (7) 3 р. 409,1894; 5 р. 256, 1895; 9 р. 409, 1896.
Шиллеръ. XV. А. 40 р. 149, 1890.
8иікегІап(і. РЫІ. Ма^. (5) 35 р. 111, 1893.
Апіоіпе. С. В. 108 р. 896, 1889; 110 р. 1122, 1890.
АпАгеѵз. РЫІ. Ма§. (5) 1 р. 78, 1876; Ргос. В. 8ос. 24 р. 455, 1876.
Ріііег. XV. А. 3 р. 447, 1878.
ОиеІАЬег^. ХізсЬг. б. Ѵег. беиізсЬ. Іп^еп. 12 р. 673, 1868.
Вгіііоиіп. б. бе рііуз. (3) 2 р. 113, 1893.
О. 8скпМІ. АЬЬ. ЪбЬт. Ѳез. б. ХѴізз. 6, Рга&, 1867; XV. А. 11 р. 171, 1880.
Ткіезеп. XV. А. 24 р. 467, 1885; 63 р. 329, 1897.
Ьа^гапре. Виіі. Ас. Ве1§. 76 р. 171, 1883.
Хеипег. 2ізсЬг. б. Ѵег. беиізсЬег Іп^еп, 1866; ТесЬпізсЬе ТЬегтобупатік II
р. 227, 1890.
Оіеіегісі. XV. А. 69 р. 703, 1899.
Ѵап Ьааг. 2ізсЬг. I. рііуз. СЬет. 11 р. 433, 1893.
ОоеЪеІ. гізсЬг. Ь рЬуз. СЬет. 47 р. 471, 1904; 49 р. 129, 1904.
Реіщгапит. 2ізсЬг. Г. рЬуз. СЬет. 37 р. 237, 1901 ; Б. А. 6 р. 533, 549, 1901 ;
РЬуз. 2ізсЬг. 1 р. 176. 1900.
Ата^аі. С. В. 128 р. 538, 1899; боигп. бе рЬуз. 1899 р. 353.
Розе-Іппез и 8. Ѵоип§. РЫІ. Ма§. (5) 44 р. 80, 1897; 45 р. 107, 1898; 47 р. 353;
48 р. 213, 1899.
Литература.
697
Къ § 6.
Маііііав. Ье роіпі сгііідие сіея согрз ригз. Рагіз 1904; Варрогіь ргёз аи Соп^гёз,
іпіегпаі. де ркуз. 1 р. 615, Рагіз 1900.
Са^піагсі (іе Іа Тоиг. Аліи. скіт. еі рііуз. (2) 21 р. 127, 178, 1822; 22 р. 140,
1823; 23 р. 410, 1823.
Огіоп. Апп. сіііт. еі ркуз. (3) 56 р. 5, 1859.
Тііііогіег. Апп. скіт. еі рііуз. (2) 60 р. 427, 1835.
Гагайау. Ріііі. Тгапз. 1845, р. 155; Ро&8‘. Апп. Ег^Ьд. 2 р. 193, 1848.
Менделѣевъ. Хим. журн. Соколова и Энгельгардта 3 р. 81, 1860 ;Ро^. Апп. 141
р. 618, 1870.
АпЛге^в. Ріііі. Тгапз. 159 II, р. 583, 1869; 166 р. 421, 1876; 178 А, р. 45,1887;
Ро^. Апп. Ег$М. 5 р. 64, 1871.
ТИіезеп. Хізскг. Т. котргіт. и. Пііззще Оазе 1 р. 86,1897; ВеіЫ. 21 р. 953, 1897.
Авенаріусъ. Рор^. Апп. 151 р. 303, 1874; Виіі. Зе Мозсои 47 № 3, 1873.
МаіНіав. 3. Зе рііуз. (2) 9 р. 449, 1890; С. В. 119 р. 404, 849, 1894.
Ваккег. 3. Зе ркуз. (3) 6 р. 131, 1897.
РгапкепНеігн. Иіе Ьекге ѵоп сіег Соііаезіоп р. 86, 1836; 3. Г. ргасі. Скетіе 23
р. 401, 1841.
Зайончевскій. Изв. Кіевск. Унив. 1878 № 4 р. 21 ; №8 р. 29.
Озі'шаід. ЬеіігЬ. 3. а!1§. Скетіе, 2-ое изд. 1 р. 537, 1891.
ѴРоІ/. Апп. сЫт. еі рііуз. (3) 49 р. 272, 1857.
Огіоп. Апп. сЫт. еі рііуз. (3) 56 р. 221, 1859.
Оиуе. Агсіі. дез зс. ркуз. (3) 23 р. 197, 1890; С. К. 141, 1128, 1899; 3. де рііуз.
(2) 9 р. 312, 1890; Апп. сіііт. еі ркуз. (6) 21 р. 206, 1890.
НеіІЬогп. Агск. дез зс. ркуз. (3) 26 р. 9, 127, 1891.
}ап8веп. Іпаіщ. Біззегі. Ьеудеп 1877, р. 50; ВеіЫ. 2 р. 136, 1878.
Богаевскій. О различныхъ состояніяхъ вещества. Заи. Ими. Акад. Наукъ (7)
5 № 13, 1897.
/?. НеШіоІіх. \Ѵ. А. 27 р. 521, 1886.
Аіікеп. Хаіиге (англ.) 23 р. 195.
Рге8іоп. РЫІ. Ма&. (5) 42 р. 231, 1896.
Къ § 7.
Надеждинъ. Ж. Ф. X. О. 14 р. 157, 536, 1882; 15 р. 25, 1883; 16 р. 74, 222,
1884; Изв. Кіевск. Унив. 6 р. 32, 1885; Мёі. ркуз. еі скіт. іігёз ди Виіі. де бі.-РеіегзІ).
12 р. 299, 1885; Верегі. д. Ркуз. 23 р. 639, 708, 1887.
Саіііеіеі еі Соіагйеаи. 3. де ркуз. (2) 10 р. 333, 1891 ; С. В. 106 р. 1489, 1888;
112, р. 1170, 1891.
Огітаійі. Вепд. Асс. ді Вота (5) 1 р. 79, 1892.
МаШаз. С. В. 115 р. 35, 1890.
Аіівскиі. См.. Озіхѵаід, НііІізЬ. I. ркуз.-скет. Меззигщеп р. 139, Ьеіргщ, 1893.
Ѵ&гоЫе'Мвкі. \Ѵ. А. 19 р. 428, 1886.
^тіп. С. В. 96 р. 1448, 1883; 97 р. 10, 1883; 3. де ркуз. (2) 2 р. 391. 1883.
Ваііеііі. Ыиоѵо Сіт. (3) 33 р. 22, 57, 1893.
ХатЫаві. АШ В. Ас. деі Ьіпсеі 1 р. 423, 1892; 2 р. 21, 1893; 3. де ркуз. (3) 2
р. 274, 1893.
Б Голицынъ. Ж. Ф. X. О. 22 р. 265, 1890; О. Ф. И. Об. Л. Е. 4 вып. 2 р. 5
1891 ; 3. д. ркуз. (3) 1 р. 474, 192; \Ѵ. А. 50 р. 521. 1893.
Реііаі. 3. де ркуз. (3) 1 р. 228, 1892.
Ооиу. С. В. 115 р. 720, 1892; 116 р. 1289, 1893; 121 р. 201, 1895.
Ѵіііані. Апп. скіт. еі ркуз. (7) 10 р. 396, 1897; 3. де ркуз. (3) 5 р. 257, 453, 1896.
Столѣтовъ. Ж. Ф. X. О. 25 р. 303, 1893; 26 р. 26, 1894; О. Ф. Н. Об. Л. Е.
5 вып. 1 р. 1, 1892; Ркуз. Веѵие (нѣмецк.) 2 р. 44, 1892.
Авенаріусъ. Ро^. Апп. 151 р. 303, 1874; Виіі. де Мозсои 47 № 3 р. 117, 1873.
698
Ненасыщенные пары.
Зайончевскій. Изв. Кіевск. Унив. 1878 № 4 р. 21; № 8 р. 29.
Павлевскій. Сііет. Вег. 15 р. 2463, 1882; 16 р. 2633, 1883; 21 р. 2141, 1888.
Страусъ. Ж. Ф. X. О. 12 р. 207, 1880; 14 р. 511, 1882.
Коіігтипсі. Хіескг. 1. рііуе. Сііет. 26 р. 433, 1898; 63 р. 54, 1908.
5. Ѵоигцг. Сііет. Хелѵе 94 р. 149, 1906.
Коноваловъ. Аппаі. <1. Рііуе. (4) 10 р. 360, 1903; 12 р. 1160, 1903.
Бтоіисігоіѵзкі. Аппаі. сі. Рііуе. (4) 25 р. 205, 1908.
Каттегііп^іг Оппез и Кеезот. ѴегеІ. К. Акай, ѵап АѴеіепек. 16 р. 667, 1908;
Соттип. Рііуе. ЬаЬог. Ьеісіеп № 104,Ь.
Жукъ. Ж. Ф. X. О. 13 р. 239, 411, 1881; 14 р. 157, 1882; 16 р. 304, 1884;
Кіевск. Унив. Изв. 1884 (ноябрь).
Каннегисеръ. Ж. Ф. X. О. 16 р. 304, 1884 (статья Жука).
Дьячевскій Ж. Ф. X. О. 16 р. 304, 1884 (статья Жука).
Ата&аі. С. В, 114 р. 1093, 1322, 1892; й. йе рііуе. (3) 1 р. 288, 1892.
Каіапзоп. й. йе рііуе. (3) 4 р. 219, 1895; Виіі. Асай. Сгасоѵ. 1895 р. 93; ВеіЫ.
19 р. 618, 1895.
Оізхеъѵзкі. Сііет. Хе\ѵе. 71 р. 139, 1895; ВеіЫ. 19 р. 412, 1895; Ріііі. Ма&. (5)
40 р. 202, 1895.
Саіііеіеі. й. йе рііуе. (1) 9 р. 192, 1880; С. К, 90 р. 210, 1880.
Апйгеіѵз. Ріііі. Ма&, (5) 1 р. 78, 1876; Ріііі. Тгапе. 178 А, р. 45, 1887; Ргос. К.
8ос. 23 р. 514, 1876.
Саіііеіеі еі Н&иіе/еиіііе. С. К. 92 р. 901, 1881.
Наппау. Ргос. В. 8ос. 33 р. 294, 1882.
Центнершверъ. Критическая температура растворовъ. С. П. 1903; Ж. Р. Ф. X. О.
1903, Отд. Хим. р. 742, 897; Хіескг. 1. рііуе. Сііет. 46 р. 427, 1903; 19 р. 199, 1904;
54 р. 689, 1908; 61 р. 356, 1907; 69 р. 81, 1909.
Центнершверъ и Калънинъ. Хіескг. 1. ркуе. Сііет. 60 р. 441, 1907.
Булатовъ. Ж. Ф. X. О. 1899 р. 69.
СаиЬеі. Ьідиёіасііоп йее Мёіап&ее ^агеих. Рагіе 1901 ; Хіескг. Г. рііуе. Сііет. 40
р. 257, 1902; 49 р. 101, 1904.
Рісіеі. Хіесііг. Г. рііуе. Сііетіе 16 р. 26, 1895.
Апзйеіі. Ргос. В. 8ос. 34 р. 113, 1882.
Оегѵаг. Ргос. В. 8ос. 30 р. 538, 1880.
О. С. Бсіітійі. ЬіеЪ. Апп. 266 р. 266, 1891.
Наппау апй Но^агііг. Ргос. В. 8ос. 30 р, 178, 484, 1880.
НеіІЬогп. Хіесііг. Г. рііуе. Сііетіе 7 р. 601, 1891.
Къ § 8.
Сіаизіиз. Р. Апп. 82 р. 274, 1851.
Циекгіпр. Хеие Огипй^еееіхе хиг гаііопеііеп Ркуеік р. 73, 1878.
Ѵап-йег-ХѴааІз. Сопііпиііаі и т. д. р. 129.
Сіаизіиз. АѴ. А. 14 р. 279, 692, 1881.
Ріапск. АѴ. А. 13 р. 535, 1881.
Зиловъ. Ж. Ф. X. О. 14 р. 169, 1882 (статья Столѣтова).
Столѣтовъ. Ж. Ф. X. О. 14 р. 167, 1882.
Ціііег. АѴіеп. Вег. 111 р. 1046, 1902.
Ратзау апй Уоипр. Хіескг. 1. ркуе. Скешіе 1 р. 237, 433, 1387.
раттегІіпрк-Оппез. К. Ак. ѵоп АѴеіепеск. Ашеіегйат, 1881; ВеіЫ. 5 р. 718, 1881.
Сигіе. Агск. ес. ркуе. (3) 26 р. 13, 1893.
Мезііп. С. В. 116 р. 135, 1893.
Каіапзоп. С. В. 109 р. 855, 890, 1889; Агск. ес. ркуе. (3) 28 р. 1, 1892.
Сонинъ. Проток. Отд. Физ. и Химіи Варіи. О. Естеств. 1889 № 7 р. 1.
Курбатовъ. Ж Р. Ф.-Х. Общ., отд. Хим. 40 р. 813, 1908.
Введеніе.
699
Кіг8ііпе Меуег (урожд. Віеггит). 2І8с1іг. Г. рііуе. Сііет. 32 р. 1, 1900; 71
р. 325, 1910.
Ата^аі. С. В. 123 р. 30, 83, 547, 1896.
Маіійав. С. В. 112 р. 35, 1891 ; 3. сіе рііуз. (2) 7 р. 568, 1888; Рііуе. Веѵие (нѣ-
мецк.) 1 р. 678, 1892.
Оиуе. Агсіі. 8С. рііуе. (3) 31 р. 164, 463, 1894.
Ѵоип& РЫІ. Ма$. (5) 30 р. 423, 1890; 33 р. 153, 1892; 34 р. 507, 1892; Рііуз.
Веѵие (нѣмецк.) 1 р. 385, 1892.
Vап-сІег-^ааІ8 ]'г. К. АкаЗ. ѵ. УѴеіепасІі. АтзіегЗат. 1896—1897 р. 248.
Богаевскій. Зап. Имп. Ак. Наукъ (7) 5 № 13 р. 65.
Ваккег. 2І8сЬг. 1. рііуе. Сііетіе 21 р. 127, 507, 1896.
Кігвііпе Меуег. 2Цс1іг. I. рііуе. Сііет. 32 р. 1, 1900.
ВаізсНіпзкі 2І8СІ1Г. Г. рііуѳ. Сііет. 43 р. 369, 1903.
Нсрреі. Аппаі. (1. Рііуе. (4) 13 р. 340, 1904; 21 р. 342, 1906; 30 р. 175, 1909;
31 р. 841, 1910.
ГЛАВА ЧЕТЫРНАДЦАТАЯ.
Равновѣсіе соприкасающихся веществъ. Правило фазъ.
Растворы.
§ 1. Введеніе. Намъ остается разсмотрѣть группу весьма важныхъ
явленій. Нѣкоторыя изъ нихъ уже были подробно разобраны, другія были
лишь вкратцѣ упомянуты, и, наконецъ, третьихъ еще вовсе не приходилось
касаться въ предыдущихъ главахъ. Наиболѣе важною задачею предста-
вляется однако не пополненіе уже разсмотрѣннаго и не разборъ новыхъ
явленій, но объединеніе многочисленныхъ и разнообраз-
ныхъ группъ явленій, приведеніе ихъ къ одному весьма общему
началу и наконецъ выводъ свойствъ и законовъ этихъ явленій на осно-
ваніи нѣкотораго характернаго признака тѣхъ условій, при которыхъ всѣ
эти явленія происходятъ. Такимъ характернымъ признакомъ является
соприкосновеніе разнородныхъ веществъ, причемъ разно-
родность можетъ быть какъ химическая, такъ и физическая. Явленія, ко-
торыя наблюдаются въ растворахъ, представляютъ обширную и осо-
бенно интересную изъ относящихся сюда группъ явленій.
Разработка, главнымъ образомъ теоретическая, вопросовъ, съ кото-
рыми намъ предстоитъ ознакомиться, почти цѣликомъ принадлежитъ по-
слѣднимъ 10 и 15 годамъ, и ею занимались спеціалисты по термодина-
микѣ и химики. Можно сказать, что всѣ относящіеся сюда вопросы
принадлежатъ къ области той обширной и столь недавно возникшей на-
уки, которая называется физической химіей. Въ огромномъ боль-
шинствѣ даже обширныхъ учебниковъ физики многіе изъ этихъ вопро-
совъ до сихъ поръ вовсе не разсматриваются. И дѣйствительно, помѣ-
щеніе разбора этихъ вопросовъ въ учебникѣ физики встрѣчаетъ цѣлый
рядъ затрудненій, на которыя указать мы считаемъ не только возмож-
нымъ, но и необходимымъ, ибо эти указанія установить для читателя пра-
700
Равновѣсіе соприкасающихся веществъ.
вильную точку зрѣнія: они укажутъ намъ на необходимость сдѣлать
выборъ матеріала и объяснять отсутствіе многихъ вопросовъ тѣмъ, кто
ожидаетъ, что въ курсѣ физики можно исчерпать огромную область фи-
зико-химическихъ явленій. Главнѣйшія затрудненія заключаются въ
слѣдующемъ:
1. Многіе изъ относящихся сюда, тѣсно между собою сплетенныхъ
вопросовъ имѣютъ чисто химическій характеръ и требуютъ такихъ по-
знаній по химіи, что изложеніе ихъ въ курсѣ физики не представля-
ется удобнымъ и даже возможнымъ.
2. Нѣкоторыя, и притомъ важнѣйшія изъ относящихся сюда явле-
ній находятся въ тѣснѣйшей связи съ разнообразными электриче-
скими явленіями, каковы электропроводность растворовъ, явленія
электролиза, дѣйствіе гальваническихъ элементовъ и др. Эти явленія
должны быть отнесены къ другому отдѣлу физики, и потому намъ при-
дется въ т. IV еще разъ возвратиться къ нѣкоторымъ вопросамъ, кото-
рымъ посвящена эта глава.
3. Основатель ученія о соприкасающихся веществахъ ОіЪЬб, а
затѣмъ его послѣдователи КоогеЬоош, Ріапск, Кіеске, Мегпзі,
Ье С11 аIе 1 іег, Виііепі, а также параллельно съ нимъ работавшій
ѵ а пЧ Н о 11 изложили это ученіе въ столь сложной математической
формѣ, что повтореніе даннаго ими разбора наиболѣе общихъ случаевъ
соприкасанія веществъ заняло бы чрезмѣрно много мѣста и по своему
характеру не соотвѣтствовало бы нашему курсу. Отъ наиболѣе общихъ
выводовъ мы, такимъ образомъ, должны отказаться. Мы можемъ указать
на обширное сочиненіе II. Т. Посальскаго «Приложеніе термодина-
мики къ изысканію равновѣсія соприкасающихся массъ», Одесса 1895,
въ которомъ читатели найдутъ полный разборъ многихъ относящихся
сюда вопросовъ, и притомъ въ наиболѣе общей формѣ. Отказываясь по
необходимости отъ самыхъ общихъ выводовъ, мы встрѣчаемъ не мало за-
трудненій также и при разборѣ частныхъ случаевъ, или при доказатель-
ствѣ отдѣльныхъ къ нимъ относящихся теоремъ.
4. Ученіе о соприкасающихся веществахъ возникло, какъ уже было
сказано, сравнительно недавно, и намъ кажется, что накопившійся науч-
ный матеріалъ до сихъ поръ еще не былъ приведешь въ систему, доста-
точно ясную и полную, если, конечно, исключить упомянутые весьма
общіе выводы, въ особенности СгіЬЬв’а, Ріапск'а и ВиІіепГа. По-
мимо этихъ выводовъ мы находимъ большое число работъ различныхъ
ученыхъ, изъ которыхъ каждый имѣетъ свою точку зрѣнія и свои спо-
собъ разбора вопросовъ, что не мало затрудняетъ всякую попытку систе-
матически изложить эти вопросы.
До какой степени разнообразны относящіеся сюда вопросы можно
видѣть изъ слѣдующаго, далеко не полнаго ихъ перечня: переходт> ве-
щества изъ одного состоянія въ другое (плавленіе, испареніе), аллотро-
пическія измѣненія, диссоціація во всѣхъ ея формахъ, включая и іониза-
цію электролитовъ, растворимость, упругость пара растворовъ, кипѣніе
Кріогидраты.
701
растворовъ, затвердѣваніе растворовъ, осмотическое давленіе, тепловыя
явленія, сопровождающія раствореніе, а также разбавленіе растворовъ,
общая теорія растворовъ (Сіаизіив'а, Аггііепіиз’а и ѵапЧ НоіГа),
охлаждающія смѣси, кріогидраты, явленія диффузіи и т. д. Растворы
могутъ быть твердыхъ тѣлъ, жидкостей и газовъ, причемъ и раствори-
тели могутъ быть не только жидкими, но также и твердыми и газообраз-
ными. Самый характеръ раствора можетъ быть весьма различенъ, смотря
по роли, которую при раствореніи играютъ химическія явленія; достаточно
въ этомъ отношеніи мысленно сравнить раствореніе въ водѣ сахара, по-
варенной соли и сѣрной кислоты. Въ нашемъ обзорѣ вопросовъ со-
вершенно опущены вопросы чисто химическаго характера (химическое
равновѣсіе, скорость реакцій и др.), а также всѣ вопросы, относящіеся къ
области явленій электрическихъ и отчасти уже упомянутые нами выше.
Изъ перечисленныхъ вопросовъ мы разсмотримъ тѣ, которые пред-
ставляютъ глубокій интересъ для физики. Чтобы привести эти вопросы
въ необходимую систему и насколько возможно связать ихъ между со-
бою, мы считаемъ необходимымъ прежде всего разсмотрѣть знаменитое
правило фазъ СИЪЪв’а и теорію слабыхъ растворовъ, дан-
ную Р1 а и с к’омъ.
Выясненіе правила фазъ возможно только на рядѣ примѣровъ; при
этомъ намъ придется говорить о вліяніяхъ, отчасти извѣстныхъ изъ эле-
ментарнаго курса физики, отчасти разобранныхъ нами въ предыдущихъ
главахъ и въ т. I. Исключеніе составляютъ кріогидраты, о кото-
рыхъ намъ еще не приходилось говорить и о которыхъ придется упоми-
нать, приводя примѣры къ правилу фазъ. Поэтому мы предпосылаемъ
правилу фазъ статью о кріогидратахъ.
§ 2. Кріогидраты. Разсмотримъ, что происходитъ при охлажденіи
раствора какой либо соли въ водѣ. Возьмемч, координатныя реи Юс
(рис. 209) и примемъ за ординату температуру і, а за абсциссы — крѣ-
пость с раствора, напр. вѣсовое количество соли, растворенное въ 100 вѣ-
совыхъ частяхъ воды. При большомъ с растворъ, постепенно охлаждае-
мый, окажется насыщеннымъ солью при нѣкоторой сравнительно
высокой температурѣ /; величины с и і опредѣляютъ положеніе нѣкото-
рой точки О. Мы можемъ сказать, что въ О растворъ насыщенъ: при
дальнѣйшемъ его охлажденіи начинается выдѣленіе соли изъ ра-
створа. Если взять меньше соли, т.-е. меньше с, то насыщеніе и за-
тѣмъ выдѣленіе соли достигаются при болѣе низкой температурѣ; вмѣ-
сто О имѣемъ другую точку О ". Уменьшая постепенно г, мы получаемъ
точки, геометрическое мѣсто которыхъ представляетъ нѣкоторую кривую
линію ОО'ВВ', для простоты изображенную въ видѣ прямой. Линія ОВ
опредѣляетъ количество с соли, потребное для насыщенія 100 частей
воды при 0°. При еще меньшемъ с растворъ оказывается насыщеннымъ
при температурѣ ниже 0° (точки В'\ ОВ можно назвать линіей вы-
дѣленія соли или линіей насыщенія раствора солью.
Обратимся къ слабымъ растворамъ. Чистая вода выдѣляетъ ледъ при 0°
70^
Равновѣсіе соприкасающихся веществѣ.
(точка О); если слабый растворъ (с = Ок) охлаждать, то изъ иего начи-
наетъ выдѣляться ледъ при нѣкоторой температурѣ Нк < 0°: раз-
сматривая растворъ, какъ смѣсь ожиженнаго льда съ ожиженною солью,
мы по аналогіи можемъ сказать, что въ точкѣ Н растворъ насы-
щенъ льдомъ. При нѣсколько большемъ с получаемъ вмѣсто Н
точку Н', выдѣленіе льда начинается при болѣе низкой температурѣ.
Геометрическое мѣсто точекъ Н представляется въ видѣ нѣкоторой ли-
ніи ОН , которую можно назвать линіей выдѣленія льда или
линіей насыщенія раствора льдомъ.
Двѣ линіи ОВ' и ОН' пересѣкаются въ нѣкоторой точкѣ А, соот-
вѣтствующей опредѣленной крѣпости с' = ОЕ и опредѣленной темпера-
турѣ і = ЕА. Докажемъ прежде всего, что всякій растворъ при охлаж-
деніи долженъ дойти до точки Д, т.-е. до крѣпости с' и до температуры і'.
Дѣйствительно, положимъ сперва, что имѣемъ крѣпкій растворъ, который
при охлажденіи начинаетъ въ О выдѣлять соль. Тогда онъ дѣлается
менѣе крѣпкимъ (с уменьшается) и можетъ быть нѣсколько болѣе охлаж-
денъ, вслѣдствіе чего еще соль выдѣлится и т. д. Понятно, что состоя-
ніе раствора, непрерывно выдѣляющаго соль, будетъ мѣняться по линіи
ОО'ВВ', приближаясь къ точкѣ А. Положимъ теперь, что имѣемъ сла-
бый растворъ, для котораго с — Ок. Въ Н начинается выдѣленіе
льда, вслѣдствіе чего с увеличивается и температура дальнѣйшаго выдѣле-
нія льда понижается; ясно, что состояніе раствора, непрерывно выдѣляю-
щаго ледъ, должно мѣняться по линіи ОНН', также приближаясь къ
точкѣ Д, которая и будетъ достигнута въ обоихъ разсмотрѣнныхъ случа-
яхъ, когда с сдѣлается равнымъ с' и въ то же время і равнымъ і'.
Что же произойдетъ при дальнѣйшемъ охлажденіи раствора, состоя-
ніе котораго опредѣляется точкою А1 Такой растворъ будетъ за-
твердѣвать какъ цѣлое, т.-е. безъ измѣненія крѣпости
с'; изъ него будетъ выдѣляться смѣсь соли и льда въ постоян-
ной пропорціи г': 100, причемъ температура і останется постоян-
ною, пока не затвердѣетъ вся масса раствора. Отдѣльное выдѣленіе льда
или соли, или выдѣленіе смѣси льда и соли въ драгой пропорціи невоз-
кріогидраты.
703
можно, такъ какъ при такомъ выдѣленіи остался бы растворъ, въ кото-
ромъ с^>с или с<%; во такіе растворы не могутъ доходить до темпе-
ратуры Л. Опредѣленная по составу смѣсь, выдѣляющаяся при темпе-
ратурѣ і', называется кріогидратомъ, а сама температура і'
крі огидратной.
Величины сг и і' зависятъ отъ раствореннаго вещества и отъ раство-
рителя, роль котораго можетъ, кромѣ воды, играть и другая жидкость. При
данныхъ веществахъ составъ кріогидрата зависитъ еще отъ внѣшняго да-
вленія /?, но при данномъ давленіи составъ кріогидрата
(т.-е. с'} и кріогидратная температура/ вполнѣ опре-
дѣлены.
Проведемъ черезъ А прямую РО параллельно оси абсциссъ. Линія
ОАО и прямая РО раздѣляютъ всю площадь на четыре части: выше ли-
ніи ОАО, т.-е. въ области іОАО, мы имѣемъ ненасыщенные растворы,
если і не слишкомъ велико; ниже РАО имѣемъ смѣси твердой соли и
льда; области ОАР и ОАО соотвѣтствуютъ неустойчивымъ состоя-
ніямъ раствора, а именно ОАО — пересыщенному, ОАР переохлаж-
денному раствору.
Первый, изслѣдовавшій кріогидраты, былъ СгиіЬгіе (1875), счи-
тавшій ихъ за опредѣленныя химическія соединенія; онъ далъ и фор-
мулы для нѣкоторыхъ изъ нихъ, напр. 2ЫаСІ-\- 21Н2О(і' = — 23°), К№О% +
-|-89,2/72О и т. д. Первый Рі'аип(11ег выразилъ сомнѣніе въ хими-
ческомъ характерѣ кріогидратовъ; изслѣдованія О И е г’а вполнѣ подтвер-
дили, что кріогидраты представляютъ смѣси, а не химическія соединенія.
Наконецъ одновременныя работы Богородскаго (въ Казани) и Роп-
8 01, изслѣдовавшихъ кріогидраты при помощи микроскопа, окончательно
доказали несправедливость воззрѣній (л и 1 й г і е. Составъ кріогидратовъ,
какъ уже было упомянуто, зависитъ отъ внѣшняго давленія; эту зависи-
мость изслѣдовалъ Е о 1 о 11.
Кріогидраты (Р о п 8 о 1 предлагаетъ ихъ назвать сгуозеіз) могутъ
быть получены и изъ растворовъ жидкостей; такъ для раствора алкоголя
въ водѣ /' = - 34°, а составъ С^Н^О + ЗН2О, Понятіе о кріогидратахъ
можетъ быть обобщено; расплавленныя смѣси двухъ веществъ вообще
выдѣляютъ при охлажденіи или одну или другую изъ составныхъ частей
и лишь при опредѣленномъ составѣ смѣси послѣдняя затвердѣваетъ безъ
измѣненія состава. Такого рода смѣси называются эвтектическими.
Вотъ* нѣкоторые примѣры состава такихъ смѣсей и соотвѣтствующія тем-
пературы і' затвердѣванія: 53,14%А7ѴО3 + ^,^І^РЬ(ЫО^)2 . . . /' = 207°;
67,10%АЖ>3 + 32,90%МгЛЮ3 . . . /' = 215°; 97,64%АЖ>3 + 2,36%К25О4
. . . /' = 300°; 46,1%23/+ 53,9%57г . . . /'=133°. 59,2%5/+ 40,8%О/
. . . /'=144°; 62% стеариновой кислоты 4-38% пальмитиновой кислоты
. . . /' = 56°; 31% нафталина 4-69°/о паратолуидина . . . /' = 29°,1.
Въ заключеніе приводимъ рядъ чиселъ с и і' для нѣкоторыхъ кріо-
гидратовъ (растворитель вездѣ вода).
704
Равновѣсіе соприкасающихся веществъ.
СаО Ыа28О± Си80 '
с= 0,14 4,6 16,9 11,2
Л=-- 0°,15 — 0°,7 —2° 2°, 7
2п80±
30,8
—7°
Трости,
сахаръ
51,4
— 8°,5
ЫН^СІ
19,6
—15°
ЫаСІ
26,6
—23°
— 30°.
§ 3. Правило фазъ. По обширности значенія, по разнообразію
тѣхъ случаевъ, къ которымъ оно приложимо, правило фазъ занимаетъ со-
вершенно исключительное положеніе между закЛг&ми физики и химіи.
Оно было открыто 4. АѴіІІагй СгіЪЬз’омъ (1876), знаменитымъ амери-
канскимъ ученымъ. Въ Европѣ первый ВакЬиів ВоояеЪоот, а за
нимъ и другіе голландскіе ученые стали развивать ученіе СгіЪЪз’а, къ
которому затѣмъ примкнули Е и 11 е т во Франціи, Кіеске, Ріапск
и др. въ Германіи, МеуегІіоПег въ Австріи и т. д.; изъ голландскихъ
ученыхъ упомянемъ еще Зсіігеіпетакегз’а и Ѵгіепз’а.
Правилу фазъ посвящена обширная глава въ сочиненіи О 81 \ѵ а 1 (Га
ПеІігЬисй йег аіі^етеіпеп Сііетіе», изд. 2-ое, томъ 2, часть 2-ая, р. 124
и 301 (1897); спеціально этом) правилу посвящены брошюра Меуег-
ЬоПег’а (1893) и книга ВапсгоІСа (1897). На русскомъ языкѣ имѣ-
ется обстоятельное изложеніе правила фазъ въ статьѣ А. Горбова (1898).
Прежде всего установимъ терминологію.
Системою соприкасающихся тѣлъ или просто системою иі бу-
демъ называть совокупность тѣлъ твердыхъ, жидкихъ и газообразныхъ, за-
нимающихъ вмѣстѣ нѣкоторый объемъ ѵ и находящихся подъ общимъ
давленіемъ р и при общей температурѣ і. При этомъ совокупность тѣлъ
должна находиться въ равновѣсіи, т.-е. въ ней уже не должны
происходить количественныя или качественныя измѣненія, *напр раство-
реніе, диффузія, диссоціація и т. д. Эти тѣла могутъ быть химически
одинаковы и неодинаковы. Примѣрами системы могутъ служить: жид-
кость и надъ нею ея паръ; одно вещество, отчасти въ твердомъ состоя-
ніи, отчасти въ жидкомъ; то же, и кромѣ того еще паръ надъ жидкостью;
растворъ и паръ растворителя или растворителя и раствореннаго; насы-
щенный растворъ и избытокъ раствореннаго; растворъ, ледъ и паръ; на-
сыщенный растворъ, паръ и избытокъ раствореннаго ; то же, и кромѣ того
еще ледъ; нѣсколько жидкостей, нѣсколько растворенныхъ тѣлъ и пары
жидкостей; тѣло съ примѣсью продуктовъ его диссоціаціи и т. д.
Во всякой системѣ мы будемъ отличать фазы и вещества.
Понятіе о фазѣ уже было дано на стр. 483; мы назвали фазою
каждую изъ составныхъ частей системы, которую можно отдѣлить отъ
остальныхъ частей чисто механическимъ способомъ. Иначе говоря, фазы
суть тѣ однородныя части, на которыя раздѣляется система. Число твер-
дыхъ и жидкихъ фазъ можетъ быть неопредѣленно велико; газообраз-
ныхъ фазъ можётъ быть только одна, ибо два соприкасаю-
щихся газа не могутъ находиться въ равновѣсіи. Смѣсь газовъ, или про-
извольный растворъ представляютъ одну фазу. Жидкость и паръ, двѣ не
смѣшивающіяся жидкости, насыщенный растворъ и избытокъ растворен-
наго содержатъ двѣ фазы. Примѣрами системы, содержащей три фазы.
Правило фазъ.
705
могутъ служить: 1) вода, ледъ и паръ, 2) система СаСО% 4~ СаО + СО2,
3) насыщенный растворъ, избытокъ раствореннаго и паръ, 4) растворъ,
ледъ и паръ и т. д. Система, состоящая изъ насыщеннаго раствора двухъ
тѣлъ, избытковъ обоихъ тѣлъ и пара, или изъ насыщеннаго раствора од-
ного тѣла, избрітка послѣдняго, льда и пара содержитъ четыре фазы.
Кромѣ фазъ слѣдуетъ отличать во всякой системѣ еще «вещества^,
или, точнѣе, «независимыя вещества». По-нѣмецки ихъ назы-
ваютъ 81ойе или ипаЫіап^і^е ВезіапсШіеіІе; (тіЪЬн называетъ ихъ Ьо-
(Ііез, ВапсгоП- сотропепіб. Веществами (или компонентами) мы
называемъ тѣ химически разнородныя части системы, которыя, если онѣ
входятъ въ составъ фазы, могутъ быть количественно измѣнены въ этой
фазѣ, или «концентрація» которыхъ можетъ быть измѣнена по произ-
волу. Проф. Д. П. Коноваловъ любезно сообщилъ мнѣ болѣе ясное
опредѣленіе, которымъ онъ самъ пользуется: вещества или компоненты
суть тѣ составныя части системы, которыя могутъ переходить изъ одной
фазы въ другую путемъ обратимаго процесса. Замѣтимъ, что не такъ
важно указаніе на компоненты системы, какъ указаніе на ихъ число,
т.-е. на наименьшее число п составныхъ частей системы, количе-
ственно опредѣляющихъ собою остальныя части, если система должна быть
въ равновѣсіи при заданныхъ условіяхъ. МеуегііоПег, Ріапск,
Вапсгоіі и т. д. даютъ различныя опредѣленія понятія о числѣ неза-
висимыхъ веществъ, и разобраться въ этихъ опредѣленіяхъ не легко. По
къ счастью въ каждомъ частномъ случаѣ не трудно опредѣлить число п.
Если въ сис^рму входитъ химическое соединеніе и продукты его разло-
женія, то только послѣднія суть независимыя вещества, ибо ими вполнѣ
опредѣляется количество соединенія, могущее существовать въ системѣ
при заданныхъ условіяхъ. Приведемъ нѣкоторьія системы, содержащія
по одному веществу: вода, ледъ и паръ; смѣсь желтаго фосфора съ крас-
нымъ; смѣсь ромбической сѣры съ моноклиномѣрной. Всякій Растворъ
содержитъ по крайней мѣрѣ два вещества — растворитель и растворимое.
Если въ водномъ растворѣ находится также и гидратъ раствореннаго, то
этотъ гидратъ не есть отдѣльное независимое вещество, ибо при задан-
ныхъ условіяхъ его количество опредѣляется количествомъ воды и ра-
створеннаго вещества. Система, состоящая изъ СаСО^ СаО и СО2, со-
держитъ два вещества, ибо при заданной температурѣ количество СаСОл
вполнѣ опредѣляется количествами СаО и СО2- Если допустить, что въ
водномъ растворѣ ЫаСІ имѣются свободные юны ^а и С/, то все-таки
ЫаСЦ Ыа и СІ составляютъ одно вещество, такъ какъ іоны Ыа и СІ
отдѣльно не могутъ быть произвольно измѣняемы количественно и не пе-
реходятъ изъ одной фазы въ другую. Если въ растворѣ ЫаСІ еще ра-
створить хлоръ, то такой растворъ будетъ содержать три вещества: ра-
створитель, соль и хлоръ.
Мы поставили выше условіе, чтобы система находилась въ равно-
вѣсіи. чтобы въ ней не происходили никакія измѣненія. Характеръ
равновѣсія можетъ быть, однако, разнообразный и мы будемъ отли-
КУРСЪ ФИЗИКИ О ХВОЛЬСОНА. Т. III, изд. 3-е. 45
706
Равновѣсіе соприкасающихся веществъ.
чать нѣсколько родовъ устойчиваго равновѣсія. Пусть р и і давле-
ніе и температура системы.
Если самое существованіе системы, т.-е. наличность всѣхъ ея со-
ставныхъ частей (независимо отъ ихъ количественныхъ отношеній), обу-
словлено существованіемъ одной опредѣленной температуры 1‘ и одного
опредѣленнаго давленія р‘, такъ что при другихъ і или другихъ р си-
стема невозможна, то мы будемъ говорить, что равновѣсіе системы
абсолютное или что мы имѣемъ случай равновѣсія въ много-
кратной (тиИірІе) точкѣ. Смыслъ послѣдняго термина выяснится
ниже. Т г е ѵ о г предложилъ называть такую систему нонваріантною
(попѵагіапі зувіет).
Если при наличности составныхъ частей системы одна и только
одна изъ величинъ р или і можетъ быть выбрана произвольно, а другая
является вполнѣ опредѣленной функціей первой, то мы говоримъ, что си-
стема находится въ полномъ равновѣсіи (ѵо1І8Іап<1ще8 (діеісіі-
^ехѵісЫ). Тгеѵог называетъ такую систему моноваріантною.
Если при наличности составныхъ частей системы обѣ величины р
и і могутъ быть выбраны произвольно, то мы говоримъ, что система на-
ходится въ неполномъ равновѣсіи (ипѵо1І8Іап(1і^е8 СИеісй^е-
лѵісЫ). Тгеѵог называетъ такую систему диваріантною.
Послѣ всѣхъ этихъ подготовленій мы приступимъ къ выясненію
правила фазъ, которое можетъ быть высказано въ видѣ двухъ поло-
женій. Пусть іг число независимыхъ веществъ, число фазъ, входя-
щихъ въ составъ системы.
Положеніе I. Число Мфазъ не можетъ превышать числа
п независимыхъ веществъ болѣе, чѣмъ на два;
7Ѵ<л-|-2.
Ни при какихъ условіяхъ не можетъ образоваться система изъ
7Ѵ — з фазъ, или вообще изъ М фазъ, гдѣ 2Ѵ> п +
Положеніе И. Система находится:
при Л/ = л -|- 2 . . въ равновѣсіи абсолютномъ (равновѣ-
сіе въ многократной точкѣ; ри I вполнѣ
опредѣленныя; система неваріантная);
при М = л 1 • .въ равновѣсіи полномъ (р или і произ-
вольно; система м о н о в а р і а нт н ая);
при ^=п.........въ равновѣсіи неполномъ (р и і произ-
вольны; система ди варіантная).
Строгія, но весьма сложныя доказательства правила фазъ даны
ОіЬ Ьз’омъ Віеске и Ріапск’омъ ; простыя по виду, но не всегда убѣ-
дительныя доказательства дали Кегпві, МеуегкоПег, АѴіпсІ,
Каѵеап,Роп8оі, Реггіп, Вук, Мпеііег, ВоиІоисЬ (1909)
и др. Мы предпочитаемъ вовсе не приводить доказательства, ограничи-
ваясь введеніемъ въ курсъ физики этого важнаго начала; мы приведемъ
Правило фазъ.
707
«тройной» точкѣ. Одно вещество не можетъ
примѣры, на которыхъ оно подтверждается, и намъ кажется, что совокуп-
ность этихъ примѣровъ болѣе разъясняетъ сущность дѣла и даже убѣ-
дительнѣе доказываетъ вѣрность правила фазъ, чѣмъ упомянутыя слож-
ныя доказательства, вращающіяся въ сферѣ чрезмѣрно отвлеченныхъ
представленій. Мы раз-
смотримъ различныя ком-
бинаціи чиселъ п и ДА
I.Одно вещество:
п=1. Одно вещество въ
одной фазѣ (Ы— ] = гі) на-
ходится въ неполномъ рав-
новѣсіи ; и дѣйствительно,
имѣя отдѣльно взятое твер-
дое, жидкое или газообраз-
ное тѣло, мы можемъ про-
извольно мѣнять р и і; при
двухъ фазахъ (Ы = 2 = п +
-(- 1) мы должны имѣть пол-
ное равновѣсіе; при трехъ
фазахъ 3 — п-\-2) рав-
новѣсіе абсолютное или въ
составлять системы, находящейся въ равновѣсіи, въ болѣе чѣмъ трехъ
фазахъ. Приводимъ примѣры.
Л. Вещество Н2О. Возьмемъ координатныя оси (рис. 210) и
пусть абсциссы и ординаты суть температуры і и давленія р. Вещество
Н2О можетъ существовать въ трехъ фазахъ, какъ паръ, вода и ледъ,
но не болѣе. Для каждой отдѣльной фазы могдтъ мѣняться р и и каж-
дой такой отдѣльной фазѣ соотвѣтствуетъ на рис. 210 сплошная часть
плоскости или область; эти области обозначены черезъ п. (паръ), в. (вода)
л. (ледъ). Двѣ фазы даютъ полное равновѣсіе; изъ величинъ р и і
можетъ быть произвольно выбрана только одна. Такъ въ системѣ паръ
вода имѣемъ Р—/^\ уравненіе пограничной кривой АВ; система вода —
ледъ даетъ р — п кривую АС; наконецъ система ледъ — паръ да-
етъ р=/^і) и кривую Л/?, которая въ Л не имѣетъ общей касательной
сь АВ, какъ было показано на стр. 572. Всѣ три фазы могутъ одновре-
менно существовать только при одномъ опредѣленномъ давленіи р = р'
и одной опредѣленной температурѣ р' есть давленіе водяного пара
при температурѣ іг, которая немного выше 0°, и которая есть точка
плавленія льда при давленіи р'. Мы видѣли, что р' = 4,62 мм. ртути и
Г—4-0°,0074. Системѣ изъ всѣхь трехъ фазъ соотвѣтствуетъ трой-
ная точка Л, т.-е. точка, принадлежащая тремъ пограничнымъ кри-
вымъ. Итакъ, одной фазѣ соотвѣтствуетъ на нашемч^ рисункѣ область,
івумъ фазамъ — линія, тремъ — точка. Все это вполнѣ согласно съ пра-
виломъ фазъ. Понятно, что вмѣсто Н2О мы могли бы разсматривать и
другія вещества, которыя при повышеніи температуры плавятся и испа-
45*
708
Равновѣсіе соприкасающихся веществъ.
ряются. На рис. 210 проведена еще одна линія Аа (пунктиромъ). Пред-
ставляя продолженіе линіи ВА, она соотвѣтствуетъ неустойчивому
равновѣсію, въ которомъ находится система вода — паръ ниже о0,
когда мы имѣемъ дѣло съ переохлажденною водою. Мы видѣли (стр. 572).
Рис. 211.
о
что упругость паровъ
такой воды больше
упругости паровъ льда,
и что слѣд. Аа лежитъ
вышеЛР. Случаи не-
устойчиваго равновѣ-
сія играютъ вообще
очень важную роль, все
болѣе выясняющуюся
въ настоящее время.
Если одна изъ фазъ а
отъ прибавки малаго
количества вещества,
находящагося въ дру-
гой фазѣ /3, перехо-
дитъ въ эту фазу /?,
то мы говоримъ, что
•система находится въ
неустойчивомъ равно-
вѣсіи относитель-
но фазы/?. Такъ
кривая Аа (рис. 210)
соотвѣтствуетъ состо-
янію системы, неустойчивому относительно твердой фазы.
В, Вещество 5. Это вещество извѣсти о намъ в ъ четырехъ
фазахъ; паръ (я.), жидкая сѣра (ж.\ твердая сѣра ромбическая (/?.) и
твердая моноклиномѣрная (ж.). По правилу фазъ всѣ четыре фазы не
могутъ существовать одновременно, составляя систему соприкаса-
ющихся между собою тѣлъ. На рис. 211 буквы /г., ж.. р. и м. изобра-
жаютъ упомянутыя четыре фазы ; сплошныя линіи соотвѣтствуютъ устой-
чивымъ, пунктирныя — неустойчивымъ сочетаніямъ двухъ фазъ. Трой-
ныя точки Л, В, С и а соотвѣтствуютъ системамъ, содержащимъ три
фазы; изъ нихъ послѣдняя находится въ неустойчивомъ равновѣсіи. Ри-
сунокъ 211 совершенно схематическій и линіи для простоты проведены
прямыя. Температура і перехода ромбической сѣры въ моноклиномѣрную
зависитъ отъ давленія р, повышаясь, когда р растетъ. При /7=4 атм.
имѣемъ ^=95°,6; если /7=12 атм., то ^=96°,2. Линія ОА соотвѣт-
ствуетъ ромбической сѣрѣ Л- пары сѣры. Въ точкѣ Л происходитъ пере-
ходъ ромбической сѣры въ моноклиномѣрную, причемъ поглощается (ана-
логично плавленію) нѣкоторое количество скрытой теплоты (2,52 калоріи).
Если сѣра при этомъ находится подъ давленіемъ р' своихъ паровъ, то
Правило фазъ.
709
температура і' можетъ быть только одна опредѣленная и такимъ образомъ
мы имѣемъ первый изъ возможныхъ случаевъ абсолютнаго равновѣсія въ
точкѣ А (ромб. -|~ моноклин. 4" паръ). Линія АВ соотвѣтствуетъ системѣ
моноклин. сѣра + паръ; при 120° моноклин. сѣра плавится, находясь
подъ давленіемъ своихъ паровъ. Такъ какъ точка, плавленія
зависитъ отъ давленія, то ясно, что р и I въ В вполнѣ опредѣленныя;
наличность трехъ фазъ (монокл. сѣра + жидкая 4“ паръ) даетъ второй
случай абсолютнаго равновѣсія въ тройной точкѣ В. Линія ВС соотвѣт-
ствуетъ системѣ моноклин. сѣра + жидкая (при отсутствіи пара), для ко-
торой і есть опредѣленная функція отъ р. Линія АС выражаетъ систему
ромбич. сѣра-|- монокл. сѣра (при отсутствіи пара); координаты двухъ то-
чекъ этой линіи были приведены выше. Линіи ВС и АС пересѣкаются
вь тройной точкѣ С, въ которой имѣемъ абсолютно устойчивую систему
ромб. сѣра 4- монокл. сѣра -|- жидкость. Эту точку еще не удалось реалп-
зировать; ея координаты приблизительно 131° и 400 атм. Наконецъ,
линія СР соотвѣствуетъ системѣ ромб. сѣра -р жидкая сѣра; здѣсь да-
вленія очень велики, монокл. сѣра вовсе не образуется.
Всѣ разсмотрѣнныя системы (шесть съ двумя и три съ тремя фа-
зами) устойчивы. Переходимъ къ неустойчивымъ. Ромбическая сѣра
вовсе не переходитъ въ моноклиномѣрную, если не прибавить къ ней ма-
ленькаго кусочка послѣдней. Если такой кусочекъ не прибавленъ, то по-
лучается при ^^>95°,4 неустойчивая система: ромбическая сѣра + паръ
и линія Аа. продолженіе линіи АО. При 115° ромбическая сѣра пла-
вится. находясь подъ давленіемъ своихъ паровъ. Такимъ образомъ мы
получаемъ четвертую тройную точку а съ тремя фазами ромбич. сѣра 4~
4- жидкая 4- наръ. Если нагрѣваніе происходить при отсутствіи пара, то
точка плавленія ромбической сѣры зависитъ отъ давленія и мы имѣемъ не-
устойчивую систему ромбич. сѣра 4~ жидкая и линію аС, которая очевидно
должна проходить черезъ точку С и имѣть своимъ продолженіемъ линію СР.
Линія аВ соотвѣтствуетъ неустойчивой системѣ: расплавленная ромби-
ческая сѣра 4~ паръ. Наконецъ при охлажденіи монокл. сѣры, къ кото-
рой не примѣшанъ кусочекъ сѣры ромбической, и при і < 95°,4 получа-
ется неустойчивая система монокл. сѣра 4“ паръ и линія АЬ. прямое про-
долженіе линіи ВА.
Мы видимъ, что въ разобранномъ примѣрѣ всѣ возможныя комби-
націи вполнѣ согласуются съ правиломъ фазъ: каждая изъ системъ,
составленныхъ изъ двухъ фазъ, находится въ полномъ равновѣсіи (р и і
зависятъ другъ отъ друга); три фазы даютъ абсолютное равновѣсіе въ
одной изъ тройныхъ точекъ; система, содержащая четыре фазы, не-
возможна.
Подобно тому, какъ мы здѣсь разсмотрѣли сѣру, можно изслѣдовать
и другіе случаи аллотропическихъ и изомерныхъ превращеній, напр. мо-
дификаціи фосфора, ціанъ и параціанъ и др.
П. Два вещества; п — 2. Два вещества въ двухъ фазахъ
(А/—2 = я) находятся въ неполномъ равновѣсіи (р и і независимы другъ
710
Равновѣсіе соприкасающихся веществъ.
отъ друга); при трехъ фазахъ (Л/ = 3 = п-1- 1) имѣемъ полное равновѣ-
сіе (р и і связаны уравненіемъ); при четырехъ фазахъ ^=4 = /г-}-2)
получается абсолютное равновѣсіе въ четырехкратной точкѣ. Болѣе че-
тырехъ фазъ не можетъ содержать система, состоящая изъ двухъ веществъ.
Разборъ различныхъ сюда относящихся случаевъ представляется
иногда уже весьма сложнымъ и мы ограничиваемся немногими указані-
ями. Сюда относятся растворы, разные случаи диссоціаціи, напр. пе-
реходы высшихъ гидратовъ солей въ низшіе или въ безводныя соли.
При четырехъ фазахъ могутъ существовать четыре различныя системы,
содержащія каждая по три фазы, и шесть различныхъ системъ, состоящихъ
каждая изъ двухъ фазъ. Разсмотримъ сперва общій вопросъ объ обла-
стяхъ, занимаемыхъ этими системами. Обозначимъ четыре ф а з ы
символически черезъ а, Ь. с и сі. Четыре системы (аЬс). (аЬсі). (ассі) и
(ЬссГ) находятся въ полномъ равновѣсіи и имъ соотвѣтствуютъ четыре
функціи вида р=/(і). или въ системѣ рОі (рис. 212) четыре кривыя ли-
ніи АВ. АС. АО и АЕ. которыя сходятся въ четырехкратной точкѣ А
соотвѣтствующей системѣ (аЬссІ). Кривыя раздѣляютъ площадь на четыре
части, обозначенныя римскими числами. Каждыя двѣ сосѣднія кривыя
имѣютъ двѣ общія фазы; область системы состоящей изъ этихъ двухъ
фазъ, и есть часть площади, ограниченная этими линіями. Такимъ обра-
зомъ системы (аЬ). (асі). (ссГ) и (&?), находящіеся въ неполномъ равновѣ-
сіи. занимаютъ четыре области I, II, III и IV. Далѣе, противолежащія
линіи АВ и АО имѣютъ общія фазы а и с ; система (ас) занимаетъ слѣ-
довательно или І-|-ІІ пли Ш-рІѴ. Наконецъ линіи АС и АЕ имѣютъ
общія фазы Ь и 6?: система (Ы) занимаетъ части II + III или IV-рі.
Правило фазъ.
711
Какое бы изъ двухъ возможныхъ распредѣленій ни имѣло мѣсто, мы
всегда получимъ въ результатѣ (см. рисунокъ), что одна часть плоскости за-
нята одной системой (Ьс въ IV), противоположная ей — тремя систе-
мами (ай. ас п Ьй въ II), двѣ остальныя части — двумя системами каж-
дая (аЬ и ас въ I, сй и Ьй въ III).
Все сказанное даетъ намъ выводъ К о о ъ е Ьо о ш’а :
Два вещества въ четырехъ фазахъ даютъ шесть си-
стемъ, находящихся въ неполномъ равновѣсіи; изъ
нихъ четыре занимаютъ по одной, двѣ.— по двѣ части
площади, причемъ однако одна изъ четырехъ частей
площади занята одной системой,противоположная часть
— тремя,а остальныя двѣ части —каждая двумя систе-
мами. Четыре части площади разграничены четырьмя
линіями, соотвѣтствующими четыремъ системамъ, на-
ходящимся въ полномъ равновѣсіи и содержащимъ по
три фазы каждая.
Разсмотримъ нѣсколько примѣровъ.
А. Растворъ соли въ водѣ. Два вещества суть: соль
и Н2О. Четыре возможныя фазы: паръ (п.), растворъ (р.), ледъ (л.) и
твердая соль-(с.). Четыре системы (см. рис. 213): соль-|-ледъ + ра-
створъ (с. л. р.), ледъ -ф- растворъ + паръ (л. р. п.), соль -ф- растворъ +
+ паръ (с. р. п.) и соль 4- ледъ Д- паръ (с. л. и.), какъ того требуетъ пра-
вило фазъ, суть системы, находящіяся въ полномъ равновѣсіи,
ибо для каждой изъ этихъ системъ можно произвольно выбрать р и л и Л
Четыре линіи ДВ, ДС, АО и АЕ соотвѣтствуютъ этимъ четыремъ систе-
мамъ; четыре линіи пересѣкаются въ четырехкратной точкѣ Л, которой
712
Равновѣсіе соприкасающихся веществъ.
соотвѣтствуетъ система: паръ + растворъ + ледъ + соль. Это кріо-
гидратная точка, и мы видѣли въ § 2, что такая система дѣйстви-
тельно возможна только при одной опредѣленной температурѣ і' и одномъ
опредѣленномъ давленіи р'; р' и і' суть координаты точки А. Итакъ при
четырехъ фазахъ (Ы == п2) мы дѣйствительно имѣемъ абсолютное рав-
новѣсіе въ четырехкратной точкѣ. Системы, состоящія изъ двухъ фазъ,
находятся въ неполномъ. равновѣсіи; такъ напр. система растворъ +
+ паръ (р. п. въ II) обладаетъ при данномъ і различными р, смотря по
содержанію соли въ растворѣ; подобное относится и къ остальнымъ си-
стемамъ, содержащимъ двѣ фазы. Соотвѣтственно схемѣ, показанной на
рис. 212, и слѣдуя МеуегЬоіІег‘у, мы на рис. 213 показали области
всѣхъ шести системъ, содержащихъ по двѣ фазы. Но мнѣ кажется, что
въ данномъ случаѣ слѣдуетъ совершенно исключить систему ледъ + паръ
(л. п.), такъ какъ въ ней содержится только одно вещество. Для этой
системы М=я-|-і, а не М = она находится въ полномъ равновѣсіи:
см. линію АО на рис. 213.
В. Соль Мг25О4-|- 10/72О. Эта соль можетъ распадаться на без-
водную соль Ыа28О± и воду, такъ что мы имѣемъ два вещества І\Іа28О±
и Н2О. Если нагрѣвать гидратъ (г. — Ыа28О± -|- 10//2О) въ безвоздушномъ
пространствѣ, то изъ него выдѣляется паръ и образуется соль (с. =
— №28О±). Каждой температурѣ I соотвѣствуетъ опредѣленное давле-
ніе р, независимо отъ пространства, занимаемаго парами, а слѣд. и коли-
чества разложившагося гидрата. Такимъ образомъ система изъ трехъ
фазъ: гидратъ + соль -Д- паръ (г. с. п.) находится въ полномъ равновѣ-
сіи, и ей соотвѣтствуетъ нѣкоторая кривая ОА (рис. 214). Если при
тѣхъ же і увеличить давленіе и уменьшить объемъ, то часть Ыа28О4 Д-
Правило фазъ
713
4" ЮН2О переходитъ въ насыщенный растворъ безводной соли. Съ уве-
личеніемъ давленія р повышается температура і этого перехода.
Вторая система изъ трехъ с]()азъ: гидратъ 4~ растворъ 4~ паръ (г. р. и.)
также находится въ полномъ равновѣсіи; ей соотвѣтствуетъ линія ЕА.
Линіи ЕА и О А пересѣкаются въ точкѣ А, въ которой имѣемъ всѣ че-
тыре фазы гидратъ 4~ соль 4~ растворъ 4~ паръ; эта система (№ = п 4~ 2)
находится въ абсолютномъ равновѣсіи; температура /' = 32,38°. давле-
ніе р' пара вполнѣ опредѣленное (немного меньше давленія пара надъ
чистою водою при 33°). Точка А четырехкратная, ибо въ ней встрѣча-
ются еще двѣ линіи. Линія АС соотвѣтствуетъ системѣ: соль4~растворъ4~
-4 паръ (с. р. п.); гидратъ весь разложился. Наконецъ линія АВ соот-
вѣтствуетъ системѣ : гидратъ 4- растворъ 4" соль (г. р. с.): чѣмъ больше
давленіе, тѣмъ, какъ оказывается, выше температура распаденія гидрата
на растворъ и безводную соль. Системы изъ двухъ фазъ, находящіяся
вь неполномъ равновѣсіи (А/ = п\ и занимающія по одной изъ четырехъ
частей плоскости, суть растворъ4~ соль (р. с.), соль 4" паръ (с. п.), ги-
дратъ 4- паръ (г. п.) и гидратъ 4~ растворъ (г. р.). Системы: гидратъ 4“
4~ соль (г. с. въ ІП и IV) и растворъ 4~ паръ (р. п. въ IV и I) занима-
ютъ каждая по двѣ части плоскости.
С. Другіе примѣры. ВоогеЬоопі изслѣдовалъ еще цѣлый
рядъ системъ, состоящихъ изъ двухъ веществъ, могущихъ дать 4, 5 и
болѣе фазъ. Сюда относятся системы (Н2О, 5О2), (^4, ^4 О), ^4^)>
(НВг, Я2О), (ЯС/, Н>0\ (Ее2СІ^ Н2О\ (ыН±Вг~ 7ѴЯ3) и~др. Во всѣхъ
этихъ случаяхъ существуютъ и твердыя фазы ; въ послѣднемъ изъ при-
веденныхъ примѣровъ даже три различныя твердыя фазы, содержащія 1,
3 и 6 частицъ Чрезвычайно сложный случай системы (С/, У) изу-
чилъ біогіепЬескег.
Система (Н2О. 80^ даетъ пять фазъ, твердый гидратъ 5О24~
4- 1Н2О, растворъ 8О2 въ водѣ, растворъ воды въ жидкой 5О2, смѣсь
паровъ 8О2 и Н2О, ледъ. Всѣ пять фазъ одновременно не могутъ вхо-
дить въ составъ системы. Системы изъ четырехъ фазъ находятся въ
абсолютномъ равновѣсіи, и такихъ системъ извѣстно двѣ, соотвѣтствующія
двумъ различнымъ четырехкратнымъ точкамъ. Одной изъ этихъ системъ,
а именно: твердый гидратъ4“растворъ 8О2 въ водѣ растворъ воды въ
жидкой 5О24" смѣсь паровъ 8О2 и Н2О соотвѣтствуетъ точка р
= 177,3 см. ртути, /' — 12°,1. Другая система: ледъ + твердый ги-
дратъ 4-растворъ 8О2 въ Н2О \- смѣсь паровъ НО2 и 8О2 можетъ су-
ществовать только при /' — — 2°,6 и р' — 21,1 см. ртути.
Упомянемъ еще, что система СаСО^ СаО, СО2, которая состоитъ
изъ двухъ независимыхъ веществъ СаО и СО2 (ибо СаСО% представля-
етъ соединеніе этихъ двухъ), такъ что іг = 2, и содержитъ три фазы
(/V = 3 = п 4~ 1), должна, согласно правилу фазъ, находиться въ пол-
номъ равновѣсіи. И дѣйствительно, мы знаемъ, что въ этомъ классиче-
скомъ примѣрѣ диссоціаціи давленіе р есть опредѣленная функція темпе-
ратуры, пока кромѣ газа СО2 обѣ твердыя фазы находятся на лицо.
711
Равновѣсіе соприкасающихся веществъ
ПІ. Три и четыре вещества. Когда п = 3. то системы изъ
четырехъ фазъ находятся въ полномъ равновѣсіи; система изъ пяти
фазъ находится въ абсолютномъ равновѣсіи въ пятикратной точкѣ. Здѣсь
не мѣсто разсматривать столь сложные случаи и потому ограничиваемся
краткими указаніями. Сюда относятся напр. растворы двухъ солей А
и В въ водѣ, когда возможна двойная соль АВ. Подробно изслѣдована
система, состоящая изъ трехъ веществъ Л/я25О4, 7И^5О4 и Н2О. Си-
стема изъ пяти фазъ: Л/б?2Л4^5О4)2.4//2О (астраханитъ)4“Л/я25О4-|-
+ Мр80± Ц- растворъ-)- паръ находится въ абсолютномъ равновѣсіи, су-
ществуя только при і = 22° и р = 19,6 мм. ртути.
При п = 4 имѣемъ абсолютное равновѣсіе, если число фазъ М = 6.
Такъ напр. четыре вещества Иа28О^ КСІ. ЫаСІ, и Н2О могутъ дать си-
стему КСІЦ- На28О± . ЮН2О -|- ИаСІ 4- ИаК%(80^2 4- растворъ + паръ,
находящуюся въ абсолютномъ равновѣсіи при і' = 3°,5 въ шестикрат-
ной точкѣ.
Въ послѣднее время Всйгеіпетакегз (1907—1910) изслѣдо-
валъ цѣлый рядъ кватер парныхъ системъ {п = 4) и прежде
всего (1907) систему вода — этиловый алкоголь — сѣрнистый литій -
сѣрнистый аммоній, содержащую двѣ жидкія фазы; соотвѣтствующіе слои
различались процентнымъ содержаніемъ алкоголя и солей. Затѣмъ (1909)
онъ изслѣдовалъ теоретически вообще различные возможные случаи ква-
тернарныхъ системъ, а экспериментально — различные отдѣльные случаи,
напримѣръ, системы: Н2О— ЫаСІ ВаС12— СпС12, Н2О— этиловый ал-
коголь —А$І\Ю3 - Н2О СиС12 ВаС12 — ИН±СІ. Н2О Си80± -
Іл28О±— (Л/Л/4)25О4, Н2О этиловый алкоголь ИаСІ—Иа28О^ Н2О
~Иа2О ВаО НСІ. Н2О — Сп8О4 СпС12 {ИНХ\8О^ Н2О Ьі28О±—
Ре8О4~-(НН^)28О^ (1910).
Ограничиваемся этими примѣрами, въ достаточной мѣрѣ разъясняю-
щими правило фазъ и показывающими, какимъ образомъ можно руково-
диться этимъ правиломъ при разборѣ сложныхъ случаевъ соприкосно-
венія различныхъ веществъ, составляющихъ систему, находящуюся въ
равновѣсіи.
§ 4. Термодинамическая теорія слабыхъ растворовъ по Ріапск’у.
Подъ слабымъ растворомъ мы будемъ понимать газообразную, жидкую
или твердую фазу, въ составъ которой входитъ рядъ веществъ, причемъ
однако одно изъ веществъ количественно значительно преобладаетъ надъ
другими. Это вещество мы назовемъ растворителемъ, остальныя веще-
ства — растворенными. Пусть п0 число граммъ-молекулъ растворителя,
«і, п2. .... число граммъ-молекулъ растворенныхъ веществъ; мы
полагаемъ, что велико сравнительно съ остальными п. Величины
гдѣ і = 0,1,2,3 и т. д., мы назовемъ концентраціями; очевидно
близко къ единицѣ, остальныя Л малыя дроби. Изъ (1) слѣдуетъ
2 А/ = 1...................(2)
Теорія слабыхъ растворовъ.
715
Пусть энергія, г>0 объемъ одной граммъ-молекулы раствори-
теля. Допускаемъ, что энергія 17 и объемъ V раствора могутъ быть
представлены въ видѣ
17 = 4“ + • • • 1&іиі • • • • (3)
Ѵ=п^ѵ()-\-п1ѵ1-\-п2ѵ2 + . . . = .... (4)
Здѣсь и ѵі зависятъ отъ соотвѣтствующаго раствореннаго вещества
и отъ растворителя, но не зависятъ отъ остальныхъ ра-
створенныхъ веществъ. Послѣднее предположеніе допустимо толью >
для слабыхъ растворовъ. Если прибавить къ раствору граммъ-молекулу ра-
створителя, то вмѣсто будемъ имѣть я0 -}~ 1, а вмѣсто V и 17 получимъ
V и 17 + и0. Первое показываетъ, что дальнѣйшее разбавле-
ніе «слабаго» раствора происходитъ безъ сжатія и.іи расшире-
нія, а слѣд. и безъ производства внѣшней работы. Второе (17 + й0)
показываетъ, что и энергія пртг разбавленіи не мѣняется, т.-е. что и
внутренняя работа нуль. Отсюда ясно, что разбавленіе «слабаго»
раствора не сопровождается тепловыми эффектами. Если
разбавленіе вызываетъ измѣненіе объема или сопровождается тепловыми
эффектами, то это должно указывать на химическія преобразованія, проис-
ходящія между молекулами разбавленныхъ веществъ, т.-е. что мѣняются
числа пъ и т. д. Пусть I температура, р давленіе раствора. Тре-
буется опредѣлить условія равновѣсія раствора п р и
заданныхъ р и і, т.-е. условія, при которыхъ въ растворѣ
не происходятъ химическія и реобра.зованія, мѣняющія
ч и с л а П[ и л и й/. Проще говоря: т р е б у е т с я найти условія,
которымъ должны удовлетворять числа щ или концен-
траціи й/, чтобы при данныхъ ряі наступило химиче-
ское равновѣсіе въ слабомъ растворѣ. Мы знаемъ, что
условіе равновѣсія приводится къ виду </Ф = 0, гдѣ б/Ф измѣненіе термо-
динамическаго потенціала, вызванное такимъ измѣненіемъ системы (при
і — Соп8І. и р = СопзЬ.), которое совмѣстимо съ основными условіями,
связывающими величины Л/ между собою (см. ниже). Величина Ф= 17
Т8 + рѴ, гдѣ 17 энергія, V объемъ, Т абсолютная температура, 5 эн-
тропія раствора. Основная формула (63,ё) стр. 433 даетъ
с18 = + Раѵ _ ^П‘аиі + _ у, ЛЩ + Р^і
' «мая I
' Т
Такъ какъ послѣдняя сумма должна быть полнымъ дифференціа-
юмъ, то должны существовать функціи 5/ отъ і и р, дифференціалы ко-
торыхъ равны
4 ~Н Р^і
Г
(М)
Итакъ мы имѣемъ сІ8 — 2 Отсюда
716
Равновѣсіе соприкасающихся веществъ.
5 = 2 + &/).. . . (5)
гдѣ Ь[ отъ і и р не зависятъ, но могутъ зависѣть отъ Для опредѣ-
ленія величинъ Ріапск допускаетъ, что при достаточно высокомъ і
и маломъ р весь растворъ можетъ быть превращенъ въ смѣсь совершен-
ныхъ газовъ. Если практически такой переходъ невыполнимъ безъ из-
мѣненія чиселъ то это обстоятельство, по мнѣнію Ріапск’а, не должно
имѣть вліянія на вѣрность результатовъ нашего вывода. Для энтропіи
смѣси газовъ можно вывести формулу:
5=2«/(^ + ^у + . (6)
гдѣ Сі теплоемкость при постоянномъ объемѣ, Н постоянное для всѣхъ
газовъ число, равное коеффпціенту въ формулѣ рѵ = НТ, отнесенной къ
одной граммъ-молекулѣ газа; &і постоянныя, не зависящія отъ Я/. Части,
не зависящія отъ р и Т. должны быть одинаковы въ (5) п 6, откуда
— п№і такъ что для 5 получается
5=--2«^-+^ • • (а
Для термодинамическаго потенціала Ф — V Т8 Д- рѴ получаемъ
ф = 2 -Н V- + р 2 піѵі,
ф = т 2 щ - $і - кі + “ЦЛ') («)
Если мы введемъ обозначенія
II: 4- рѵ:
+ т = '/і...... (8, а)
ТО
Ф = 7'2 - - (рі) . •’ • (О
гдѣ ^і зависятъ оть р и Т. Положимъ, что одно изъ возможныхъ хими-
ческихъ превращеній (при Т = Сопеі. и р = Сопзі.) опредѣляется измѣ-
неніемъ величинъ щ на (іпі: тогда условіе б/Ф = 0 даетъ
2 ((ррдпі+Н 2 = о.
X - пі пі ѵп
Второй членъ равенъ нулю, ибо 2 Я/д1^й/ = 2 н0 /^. = 2 п ,
слѣд. второй членъ равенъ 2 пі • 2 ~ 2 2 — (Ѣ таіъ какъ
2 А/ = 1 и слѣд., д 2 = г1^кимъ образомъ остается
2(^Ш —= о........................(ад
Величины дпі не могутъ быть произвольными, такъ какъ химиче-
скія превращенія могутъ происходить только путемъ распаденія и обра-
Теорія слабыхъ растворовъ.
717
зованія цѣлыхъ молекулъ. Величины должны относиться другъ къ
другу, какъ цѣлыя ч и с л а /д, показывающія, сколько молекулъ даннаго
вещества образуется (уі > о) или распадается (ід < 0). Для случая дис-
соціаціи 2Лі = Н2 + Л имѣемъ ѵг - 2. ѵ2 = 1, г3 = 1; для случая
МО4 = 27ѴО2 очевидно щ = — 1, = 2, а для случая РС/% — РС18 -
-р С12 имѣемъ = — 1 ; ѵ2 = 1, Чз = 1- Замѣняя дп^ въ (9,а) пропор-
ціональными имъ цѣлыми числами получаемъ
1
= н АѵіЧ>і • (10)
Правая сторона не зависитъ отъ чиселъ Я/ или И; она функція отъ
р и і, которую мы обозначимъ черезъ і'} пли просто черезъ \%К.
Такимъ образомъ получаемъ окончательно условіе равновѣсія
слабаго раствора, т.-е. условіе отсутствія реакціи,
опредѣляемой числами ід.:
2 ѵ^ні = і&мр, о.............. . . (іп
ИІИ ................ц2)
Если возможны еще другія реакціи, то получается рядъ подобныхъ
условій равновѣсія, съ различными зд и различными функціями К, Усло-
віе (12) называется уравненіемъ Ріапск’а. ОііэЬз далъ уравненіе,
которое представляетъ частный случай уравненія Ріапск’а, а именно,
когда разсматриваемый растворъ газообразенъ. Но зато уравненіе СгіЪ Ья’а
относится не только къ «слабымъ растворамъ», но къ произвольной смѣси
газовъ; функція К(р, і) имѣетъ въ уравненіи СгіЬЬз’а вполнѣ опредѣ-
ленный видъ.
Съ измѣненіемъ р и I мѣняется и условіе равновѣсія. Выведемъ
общія выраженія для производныхъ отъ по р и і. Пусть 6 то уве-
личеніе объема, которое сопровождается реакціей, опредѣляемой
числами и пусть д то количество теплоты, которое погло-
щается при той же реакціи. Очевидно 5 = 2^/5 энергія увеличива-
ется на величину 2^п внѣшняя работа равна р8 = р 2^/- Выражая#
въ механическихъ единицахъ, получаемъ # = 2 ѵіиі
•-г Р 2 ѵРавенство \%К ѵурі даетъ
* д\$К 1 дрі д\$К д^і
дТ ~ Н ^Ѵі дТ ’ др ~ Н ѵі др <12-а)
Формула (8,а} даетъ
аііі рдѵі 4- ѵ^р иі 4 рѵі
(Рр і — ’ । у, 2 аТ,
ИЛИ, СМ. (4,0),
«,• 4- рѵі 'Ѵі
(1<!і = —р., дТ— .р др.
718
Равновѣсіе соприкасающихся веществъ.
Отсюда
Щ + рѵі
оТ =
д?і
др
Затѣмъ (12л) даетъ
д\%К
др
Т '
или
д\%к — я
дТ ~ НГ2
д\%К 8
др ' ~ НТ
(13)
(14)
Эти весьма замѣчательныя формулы показываютъ, что если ре-
акція происходитъ безъ тепловыхъ эффектовъ (# = О),
то условіе равновѣсія не зависитъ отъ температуры:
если реакція происходитъ безъ измѣненія объема
(5 = 0), то условіе равновѣсія не зависитъ отъ да-
вленія. Понятно, что подъ равновѣсіемъ слѣдуетъ понимать отсутствіе
именно той реакціи, къ которой относятся величины д и 5.
Выведенныя нами основныя формулы (11), (12), (13) и (14) отно-
сятся къ одному слабому раствору, т.-е. къ одной газообразной, жидкой
или твердой фазѣ. Перейдемъ къ случаю системы, состоящей изъ
произвольнаго числа фазъ, изъ которыхъ каждая представляетъ слабый
растворъ, т.-е. содержитъ одно вещество, количественно преобладающее
надъ другими, причемъ это вещество въ различныхъ фазахъ можетъ быть
и не. одно и то же. Въ газообразной фазѣ можетъ и не быть такого пре-
обладающаго вещества. Легко доказать, что формулы (11), (12), (13) и (14)
приложимы и къ такой системѣ. Дѣйствительно, для каждой фазы мы
имѣемъ для величины Ф выраженіе вида (9), а потому и для всей си-
стемы Ф выражается формулою (9), въ которой однако сумма содержитъ
ІЯп членовъ, гдѣ число фазъ и п число различныхъ веществъ или ро-
довъ молекулъ, встрѣчающихся въ системѣ. Символически напишемъ
Ф=2[«оЩ^о <Ро)- ср^-п^н}^- ср2) . . .] (14,а)
гдѣ знакъ суммы обозначаетъ суммированіе, распро-
страненное по фазамъ системы. Написавъ условіе б/Ф = О
и замѣнивъ величины дп пропорціональными имъ величинами с, мы
должны имѣть въ виду, что теперь измѣненіе можетъ сопровождаться пе-
реходомъ молекулъ или ихъ составныхъ частей изъ одной фазы въ дру-
гую. Разсужденія, вполнѣ аналогичныя предыдущимъ, даютъ вмѣсто (Ю),
(И) и (12)
2 Ы&ъ4- 2пч>і = (аО • • (15)
• • • =К{р,і)
(іо)
Растворимость.
719
Значеніе знака 2 то же? что и въ формулѣ (14,а). Въ формулѣ (16)
число множителей съ лѣвой стороны равно Ып, и изъ величинъ И по
крайней мѣрѣ 1 величина близка къ единицѣ, ибо въ системѣ мо-
жетъ быть только одна газообразная фаза, для которой величины И ни-
какимъ условіямъ не подвержены, а слѣд. въ системѣ содержатся Л7— 1
или 7Ѵ слабыхъ растворовъ, имѣющихъ каждый по одному А, близкому
къ единицѣ. Легко убѣдиться, что формулы (13) и (14)
д\$К _ д
дТ ~ НТ1
д\$К __ 8
др ~ НТ
(17)
(18)
остаются вѣрными и для разсматриваемой системы. Важныя слѣд-
ствія, которыя мы вывели изъ формулъ (13) и (14) стр. 718,
относятся очевидно и къ этой системѣ. Ріапск выводитъ
изъ формулы (15) еще одно слѣдствіе. Функція К конечная, а потому ни
одно И не можетъ равняться нулю. Это значитъ, что въ каждой
фазѣ должны встрѣчаться всѣ вообще возможные сорта
молекулъ, хотя бы въ минимальныхъ количествахъ.
Этимъ объясняется, почему газъ, жидкость или твердое тѣло никогда не
могутъ быть абсолютно освобождены отъ послѣднихт, слѣдовъ растворен-
ныхъ въ нихъ веществъ. Далѣе Ріапск заключаетъ напр., что между
соприкасающимися твердыми тѣлами всегда должна происходить диффу-
зія, хотя бы и въ высшей степени медленная.
Термодинамическая теорія не слабыхъ растворовъ еще не можетъ
считаться окончательно созданною. Къ ней относятся нѣкоторыя ра-
боты Неітіюіій’а, ВиЬет’а, Умова, Шиллера и др.
§ 5. Растворимость. Экспериментальныя данныя о растворахъ
твердыхъ, жидкихъ и газообразныхъ тѣлъ были изложены въ т. I. Въ
этомъ и въ нижеслѣдующихъ параграфахъ мы намѣреваемся разсмотрѣть
тѣ явленія, представляемыя растворами, которыя въ т. 1 или вовсе не
были затронуты, или разсмотрѣны вкратцѣ; при этомъ мы обратимъ
главное вниманіе на теоретическую сторону вопросовъ, въ осо-
бенности на приложеніе къ этимъ вопросамъ выводовъ термодинамики.
Раствореніе вообще сопровождается выдѣленіемъ или поглощеніемъ
нѣкотораго количества теплоты, которое назовемъ теплотою раство-
ренія. Эту теплоту будемъ считать положительною, когда она
выдѣляется при раствореніи; въ большинствѣ случаевъ теплота ра-
створенія отрицательная, т.-е. раствореніе сопровождается охлажденіемъ.
Изложеніе опытныхъ и теоретическихъ изслѣдованій, касающихся теплоты
растворенія, будетъ помѣщено въ § 7.
Сіаизіиз, Аггііепіиз и Ріапск основали ученіе о диссо-
ціаціи водныхъ растворовъ электролитовъ; основанія этого ученія уже
720
Равновѣсіе соприкасающихся веществъ
были изложены въ т. [. Мы къ нему возвратимся въ слѣдующемъ
параграфѣ.
Растворенныя вещества производятъ особаго рода давленіе на станки,
непроницаемыя для нихъ, но проницаемыя для растворителя. Это давле-
ніе, называемое осмотическимъ и впервые подробно изслѣдованное
РіеИег’омъ, уже было разсмотрѣно въ т. I. Дальнѣйшія подробности,
въ особенности связь между осмотическимъ давленіемъ и другими явле-
ніями, будутъ разсмотрѣны ниже.
V а пЧ Н о П, основываясь на опытахъ Р1 еП‘ е г’а, основалъ
знаменитое ученіе объ аналогіи между растворенными ве-
ществами и газами: осмотическое давленіе недиссоціированнаго
раствореннаго вещества равно давленію, которое это же вещество произ-
водило бы. занимая въ газообразномъ состояніи объемъ ѵ раствора и обла-
дай температурою Т послѣдняго. С л а б ы е растворы аналогичны разрѣ-
женнымъ газамъ, которые слѣдуютъ законамъ Бойля и Маріотта,
а потому къ такимъ растворамъ приложима формула
Рѵ = РТ............................ (19)
въ которой Р осмотическое давленіе, /? постоянная, обратно пропорціо-
нальная плотности или молекулярному вѣсу раствореннаго вещества, за-
нимающаго объемъ ѵ. Для водныхъ растворовъ электролитовъ имѣемъ,
вмѣсто (19)
Рѵ = іРТ............................(20)
гдѣ множитель і зависитъ отъ степени диссоціаціи. О теоріи Ѵап’і И оІГа
уже было сказано въ т. I.
Давленіе имѣетъ нѣкоторое вліяніе на растворимость веществъ
(см. т. I).
Растворимость вещества зависитъ какъ отъ рода этого ве-
щества, такъ п отъ растворителя. Никакихъ сколько нпбудь
общихъ законовъ или правильностей, которыя бы касались этой зависи-
мости, до сихъ поръ не удалось подмѣтить. Исключеніе представляютъ
правила, найденныя СагпеІІеу и А. ТЬотзо п’омъ. и относящіяся
къ изомерамъ:
1. Если группу изомерныхъ органическихъ соединеній распредѣ-
лить въ рядъ по степени ихъ растворимости и въ рядъ по ихъ темпера-
турѣ плавленія, то этц два ряда оказываются одинаковыми, причемъ
большей легкоплавкости соотвѣтствуетъ и большая растворимость. Изъ
1778 случаевъ, собранныхъ названными учеными, это правило подтвер-
дилось въ 1755 случаяхъ.
2. Для группы изомерныхъ кислотъ кромѣ того еще и ряды, полу-
чаемые для плавкости и растворимости солей этихъ кислотъ, совпадаютъ
съ рядомъ, полученнымъ для самихъ кислотъ. Изъ 143 случаевъ это пра-
вило подтвердилось 138 разъ.
3. Распредѣленіе изомеровъ въ указанномъ ряду не зависитъ отъ
рода растворителя. Изъ 666 случаевъ это правило подтвердилось во всѣхъ.
Растворимость.
721
4. Отношеніе растворимостей двухъ изомеровъ приблизительно оди-
наково для всѣхъ растворителей.
Вальденъ (1906) нашелъ, что растворяющая способность различ-
ныхъ жидкостей возрастаетъ вмѣстѣ съ ихъ діэлектрической постоянной А.
Въ новой работѣ (1908) онъ показалъ, что величина V р,, которую онъ
называетъ линейной растворимостью, пропорціональна к, Онъ
полагаетъ — 100/г: (п 7Ѵ), гдѣ п - - число молекулъ раствореннаго
вещества въ 7Ѵ молекулахъ жидкости. Онъ провѣрилъ это правило на
растворимости іодистаго тетраэтиламмонія въ 13 . жидкостяхъ.
Приводимъ только крайнія значенія (при 20 --25°):
з
л к й-.Ѵц
Вода . . . 3,318 76,0 50,5
Бромбензолъ 0,0037 7,5 48,9
з _
Въ среднемъ О: V р равняется 48 ; значеніе /г мѣняется въ сотни
разъ. Для іодистаго тетрапропиламмонія постоянная равняется 23.
Укажемъ еще на одну правильность, касающуюся растворимости го-
мологическихъ рядовъ, и найденную Ь. Непгу: въ ряду кислотъ типа
СпО^Н.2п_^ (щавелевая кислота С2О^Н^ малоновая янтарная
С±О±Нь глутаровая СЬО±Н% и т. д.) всѣ кислоты, для которыхъ п четное,
растворяются въ водѣ весьма мало, а кислоты, для которыхъ п нечетное,
весьма хорошо.
О вліяніи температуры на растворимость было достаточно
сказано въ т. I и мы считаемъ излишнимъ приводить дальнѣйшія
извлеченія изъ богатаго матеріала, собраннаго различными учеными —
Ра^^іаіе, АПиагсІ, Миійег, Кгетегв, Сорреі, ТЪіІсіеп
и бЬепеіопе (выше 100°), Еѣагсі, Могйеп8к]оЫ идр.
Обратимся къ попыткамъ теоретическаго изслѣдованія вопроса
о зависимости растворимости отъ температуры. Ье СЬаіе-
Ііег и Ѵап’і Но И почти одновременно (1885—86) дали слѣдующій вы-
водъ. Мы имѣли для перехода изъ жидкаго или твердаго состоянія въ
газообразное формулу
е = Л7(0 5)^.......................(21)
вь которой р скрытая теплота испаренія, а удѣльный объемъ пара,
5 удѣльный объемъ жидкаго или твердаго тѣла, А термическій эквива-
лентъ работы. Пренебрегая величиною 5 и замѣняя б буквою ѵ. имѣемъ
др _ о
дТ ~ АТѵ.................
(22)
Исходя изъ теоріи Ѵап’і НоІГа, на основаніи которой растворе-
ніе есть явленіе вполнѣ аналогичное испаренію, мы моліемъ приложить
формулу (22) и къ растворамъ, причемъ вмѣсто р слѣдуетъ вставить о с -
КУРСЪ ФИЗИКИ кО. X в О Л Ь С О Н А. т. III, изд. 3-е. 46
722
Равновѣсіе соприкасающихся веществъ.
м о т и ч е с к о е давленіе Р; 2 ^сть отрицательная теплота растворенія,
такъ что р >> О, если раствореніе сопровождается поглощеніемъ тепла.
Осмотическое давленіе Р очевидно можетъ служить мѣрою растворимости,
т.-е. количества вещества, распредѣленнаго въ единицѣ объема растворп-
дР
теля. Формула (22) показываетъ, что о и должны быть одного знака.
Отсюда слѣдуетъ, что растворимость должна расти вмѣстѣ
съ температурою, когда раствореніе сопровождается
поглощеніемъ тепла; растворимость должна умень-
шаться при возрастающей температурѣ, когда при
раствореніи выдѣляется теплота. Для большинства солей
имѣемъ первый случай; второй случай имѣемъ для извести, сѣрнокислой
соли церія и др.
Если взять ѵ изъ формулы (20) и подставить въ (22ц то получается
1 дР _ д\%Р о
РдТ~ дТ ~ іАРТ2
Для недиссоціированныхъ растворовъ имѣемъ
д\$Р__ о
дТ ~ АРГ2
(23)
(24)
Мы возвратимся ниже къ формулѣ (23). Бе Сйаіеііег восполь-
зовался ею (1888), чтобы теоретически опредѣлить зависимость раствори-
мости отъ температуры.
Большой интересъ представляетъ вопросъ о растворимости твердаго
вещества около или выше его точки плавленія. Въ нѣкоторыхъ
случаяхъ получается при точкѣ плавленія полная растворимость, т.-е. жид-
кое вещество и растворитель смѣшиваются во всѣхъ пропорціяхъ. Сюда
относится напр. растворимость котораго въ водѣ Еіагй изслѣ-
довалъ въ запаянныхъ трубкахъ при температурахъ значительно выше
100°. Онъ нашелъ для растворимости (число частей въ 100 частяхъ ра-
створа) выраженіе 81 0,1328/^, которое при 198° даетъ растворимость
100 ; но 198° есть какъ разъ температура плавленія азотносеребряной соли.
Въ другихъ случаяхъ жидкое вещество имѣетъ свою опредѣленную ра-
створимость. АѴ а 1 к е г вывелъ изъ (24) замѣчательную формулу
Л = — 1§а)......................(25)
Здѣсь л скрытая теплота плавленія вещества, 70 температура плав-
ленія. Значеніе а' и а слѣдующее: пусть Р и Р' осмотическія давленія
растворовъ твердаго и жидкаго вещества, или пропорціональныя имъ
растворимости; тогда ТѴ^Р и Т\%Р' оказываются линейными функціями
отъ Т и слѣд. выражаются прямыми линіями, если Т принять за абсциссы.
Двѣ прямыя пересѣкаются въ точкѣ Г(); а и а! суть углы между этими
прямыми и осью абсциссъ. Изслѣдуя растворимости, можно при помощи
(25) вычислить Л. АѴ а 1 к е г показалъ, что формула (25) удовлетвори-
тельно согласуется съ наблюденіями; для раствора воды въ эфирѣ полу-
Осмотическое давленіе.
723
чается л == 77 (вмѣсто 80), если допустить, что молекула воды имѣетъ
въ эфирѣ составъ Н±О2.
§ 6. Осмотическое давленіе и диффузія въ растворахъ. Опытная
сторона вопросовъ объ осмотическомъ давленіи и о диффузіи была въ
достаточной мѣрѣ разсмотрѣна въ т. I. Здѣсь мы изложимъ основы тео-
ріи этихъ явленій, а ниже связь между осмотическимъ давленіемъ и дру-
гими явленіями.
Покажемъ прежде всего, какимъ образомъ формула Рѵ=РТ для
осмотическаго давленія можетъ быть выведена изъ тео-
ріи Ріапск’а, изложенной въ § 4. Представимъ себѣ систему, состоя-
щую изъ двухъ жидкихъ фазъ: первая представляетъ слабый ра-
створъ. содержащій пѵ граммъ-молекулъ раствореннаго вещества и п0
граммъ-молекулъ растворителя; вторая фаза состоитъ изъ чистаго раство-
рителя. Обѣ фазы находятся при одной и той же температурѣ и отдѣ-
лены другъ отъ друга полупроницаемой стѣнкой, пропускающей только
растворитель. Концентраціи суть
Ло "° , = Л' = 1,
0 по+п^ ЛО + Я1
причемъ первыя двѣ относятся къ первой фазѣ, третья — ко второй. При
постоянныхъ р и I возможно только одно измѣненіе : переходъ одной мо-
лекулы растворителя изъ первой фазы во вторую; въ этомъ случаѣ
г0 = — 1 , = 0 , ѵ' = 4- 1.
Формула (15) даетъ
І^о = А ( 7-е ~Ь У1'),
гі
или
(/? \ 1
1 + „‘ =/7 (9> ...............(20
лг0/ п
ГГ 1 1 / Ч I \ у ^1 |\ /
При маломъ можно 1§* 1 -р замѣнить черезъ . Величины
и ф0. относящіяся къ растворителю въ двухъ фазахъ, суть функціи отъ
р и /; но такъ какъ температура і общая, то давленія въ двухъ фазахъ
должны быть различныя; обозначимъ ихъ черезъ и р'. Приближенно
можемъ принять, см. (8,л) стр. 716.
Ч' =Чо + <Р ~Ро)др = Ѵо — (Р Ро) -р ,
гдѣ ѵ0 объемъ граммъ-молекулы растворителя. Теперь имѣемъ, вмѣсто (26),
«0— Ро Р) НТ ’
Разность р^—р' и есть осмотическое давленіе Р, такъ что мы имѣемъ
нт
461
724
Равновѣсіе соприкасающихся веществъ.
лог/о весьма мало отличается отъ объема всего раствора, а потому 0 0
равно объему, занимаемому въ растворѣ одной граммъ-молекулой ра-
створеннаго вещества. Обозначая этотъ объемъ черезъ ѵ, получаемъ для
граммъ-молекулы раствореннаго вещества Рѵ = Н7\ а для вѣсо-
вой единицы
Рѵ=РТ,
а это и есть формула ѴапЧ Но Па. Теоріею осмотическаго давленія за-
нимались еще ВпЬет, Грузинцевъ, Р о у п 1 і п и др.
Теорія диффузіи растворенныхъ веществъ, основанная на ученіи
объ осмотическомъ давленіи, была дана егпзі’омъ. Мы можемъ изложить
здѣсь лишь малую часть этой теоріи, опуская все то, что относится къ
связи между диффузіей и электролизомъ (скорость іоновъ и т. под.); къ
этой связи мы возвратимся въ т. IV. Припомнимъ старую теорію диффу-
зіи, данную Р і с к’омъ (т. I). Положимъ, что растворъ занимаетъ цилин-
дрическій сосудъ, вдоль оси котораго мы считаемъ координату х; пусть
5 площадь поперечнаго сѣченія сосуда, Н концентрація въ одномъ изъ
сѣченій, т.-е. число граммъ-молекулъ вещества, приходящихся на единицу
объема раствора; очевидно И = /(х). Количество 5 раствореннаго вещества,
проходящаго во время т черезъ сѣченіе 5, равно
•5 =— .....................(27)
(іх
гдѣ к коеффиціентъ диффузіи и 5 выражено въ граммъ-молекулахъ. Чис-
ленно к равно количеству вещества, проходящаго въ единицу времени
черезъ единицу сѣченія, если на протяженіи единицы длины концентра-
ція мѣняется на единицу. За единицу времени принимаются обыкно-
венно с у т к и = 86400 сек. Въ видѣ примѣра укажемъ, что по наблю-
деніямъ ЗсйеНег’а для мочевины (СО^Л/4 = 60) к = 0,81 при 7°,5.
Перейдемъ къ теоріи № е г п 8 Ѵа. Пусть К сила, которая должна
дѣйствовать на граммъ-молекулу вещества, чтобы она въ растворѣ дви-
галась со скоростью 1 см. въ секунду. Въ поперечномъ слоѣ, тол-
щина котораго б/х, находятся Іізсіх граммъ-молекулъ вещества; это веще-
ство движется, такъ какъ на него дѣйствуетъ неодинаковое съ двухъ сто-
давленіе, а именно давленіе $Р съ одной, давленіе
ронъ осмотическое
ДРУГОЙ.
Дѣйствующая сила
равна — 5 ах
- гдѣ Ро
одну граммъ-молекулу дѣйствуетъ сила — $Р(
осмотическое давленіе при концентраціи Л=1. На
~ (1Н , , , Ро Ші
о . ах : Нзах = — / , ,
‘ - 0 (іх И (іх
подъ вліяніемъ которой она, т.-е. вообще вещество, находящееся въ слоѣ,
будетъ двигаться со скоростью —
Ро (ік
Кксіх
см. въ сек.
Въ одномъ см. длины
столба находится количество вещества 5Л, слѣд. въ одна секунду прой-
Осмотическое давленіе. — Теплота растворенія и разбавленія.
725
дутъ черезъ слой-------зИ =— о5 гр.-молекѵлъ вещества. Въ т
КН йх К (іх
сутокъ пройдетъ количество
$ = -86400-^-^.......................(28)
(IX
Сравнивая эту формулу съ (27), мы получаемъ
/С=8М00Р°.......................(29)
К
Ро равно давленію граммъ-молекулы газа, занимающей при данной тем-
пературѣ і единицу объема. Если к отнесено къ 1 кв. см. и если мы
желаемъ выразить К въ килограммахъ, то Ро должно равняться давленію
въ килограммахъ на кв. см. напр. 32 граммовъ кислорода, занимающихъ
1 куб. см. Мы знаемъ, что 32 грамма кислорода занимаютъ при 0° и да-
вленіи въ 1 атм. = 1,033 кгр. на кв. см. объемъ въ 22376 куб. см. От-
сюда Ро = 22376. 1,033(1 + аі). Вставляя это число въ (29), получаемъ
въ круглыхъ числахъ
„ 2 . 109(1 + аі)
К = --------------килогр................(30)
к
Эта замѣчательная формула даетъ возможность вычислить
силу, подъ вліяніемъ которой растворенное вещество
движ/ется внутри растворителя, если извѣстенъ коеф-
фиціентъ диффузіи к\ послѣдній долженъ быть отнесенъ къ 1 кв.
см. и жъ суткамъ, какъ единицамъ площади и времени. Мы упомянули,
что для мочевины = 60) & = 0,81 при ^= 7°,5. Это даетъ К—
= 2500 милліоновъ килогр. Такая сила потребна, чтобы въ водномъ ра-
створѣ перемѣщать 60 гр. мочевины со скоростью 1 см. въ сек. Громад-
ность этой силы объясняется тѣмъ, что вещество, находящееся въ ра-
створѣ, раздѣлено на весьма мелкія частицы, встрѣчающія огромное
сопротивленіе при своемъ движеніи. Достаточно вспомнить, какъ мед-
ленно въ воздухѣ падаютъ вещества, находящіяся въ состояніи мельчай-
шей пыли.
§ 7. Теплота растворенія и разбавленія. Раствореніе одного ве-
щества въ другомъ почти всегда сопровождается поглощеніемъ или выдѣ-
леніемъ нѣкотораго количества теплоты; выдѣляющуюся теплоту мы бу-
демъ считать положительною. Вникая въ разсматриваемое явленіе, мы
убѣждаемся, что слѣдуетъ отличать не менѣе шести различныхъ коли-
чествъ теплоты, отчасти связанныхъ между собою соотношеніями, кото-
рыя вывести не трудно. Количества теплоты, съ которыми здѣсь при-
ходится имѣть дѣло, суть слѣдующія (за растворитель примемъ воду).
1. Теплота растворенія <2, выдѣляющаяся, если 1 гр. ве-
щества растворить въ гр. воды.
2. Предѣльная теплота растворенія выдѣляющаяся, если 1 гр.
726
Равновѣсіе соприкасающихся веществъ.
вещества растворить въ сочень большомъ» количествѣ воды; по-
лучается изъ при Ц7 = ос.
3. Теплота насыщенія или интегральная теплота
растворенія ^0, выдѣляющаяся, если 1 гр. вещества растворить въ
такомъ количествѣ воды, чтобы получился насыщенный растворъ.
4. Теплота растворенія въ растворѣ Лу, выдѣляющаяся,
если вѣсовое количество сіл вещества растворить въ гр. воды, въ ко-
торыхъ уже растворено л гр. вещества. Понятно, что л<1, ибо при
л = 1 имѣемъ насыщенный растворъ.
5. Теплота растворенія въ насыщенномъ растворѣ б/дд,
выдѣляющаяся, если въ гр. воды, въ которыхъ уже разстворенъ почти
1 гр. вещества, прибавить количество сіл вещества, дѣлающее растворъ
насыщеннымъ.
6. Теплота разбавленія б/<2, выдѣляющаяся, если къ ра-
створу 1 гр. вещества въ чм гр. воды, прибавить количество Ле/ воды.
Легко видѣть, какимъ образомъ эти величины связаны между собою.
Прежде всего ясно, что величины (ід и должны быть вида
{.......................
ибо (ід зависитъ отъ количества л вещества, уже раствореннаго въ гр.
воды, а (10 зависитъ отъ количества воды, уже имѣющагося въ ра-
створѣ. содержащемъ 1 гр. вещества. Далѣе ясно, что
(ід1=/(1)сІл или ^=1ітВ\ ...........(32)
67 Л . 67 Л і
Я = 1 1
(^0 = {<ід = {/(п)сіп ...... (33)
і _ о о
Вмѣсто того, чтобы растворить 1 гр. вещества въ М7 гр. воды, мы
можемъ сперва растворить одинъ гр. вещества въ те/0 гр. воды, и полу-
ченный насыщенный растворъ разбавить, прибавляя (У7 те/0) гр. воды.
Это даетъ
е = <2о + + ..............(34)
оо
<2' = Р{1Ѵ)(І1Ѵ...................(35)
^0
(33) и (34) даютъ
1 Г
0. = ^/(л)т/л+ ....... (36)
О Щ)
Теплота растворенія и разбавленія
727
Путемъ опыта были опредѣляемы главнымъ образомъ величины
(1 гр. въ большомъ количествѣ воды)
1 __ //-14
представляетъ величина =/( 1):
атс
и 7? ~
ал
Большой интересъ
мы увидимъ, что она можетъ быть
опредѣлена теоретически. Большое число опредѣленій величины было
произведено сТ. ТЬотзеп’омъ (при 18°).
Дальнѣйшія опредѣленія отчасти величины <2', отчасти величины (2
(не очень большое количество воды) производили Л у г и н и н ъ , Хру-
щевъ, Вегійеіоі, Вегіііеіоі и •ѣоип^ПеізсІі. Раѵге и V а 1 -
8оіі, ЗаЬаііег, Могшее, Лоаппіз, Саібегоп, ѴапЧ НоН,
Еѵап, Реіегзеп, ВіѵаІ8, Э. Штаке.гьбергъ (1896, 1898) и др.
Нѣкоторыя изъ этихъ опредѣленій имѣютъ большое значеніе для термо-
химіи (см. глава V), напр. относящіяся къ растворенію кислотъ, основа-
ній, водныхъ и безводныхъ солей и т. д. Нѣкоторые изъ приведенныхъ
нами примѣровъ выясняютъ вліяніе кристаллизаціонной воды на тепло-
вые эффекты, сопровождающіе раствореніе. Гег8оп, АѴіпкеІшапп,
81апЬ и 8ско1г изслѣдовали зависимость величины (2 отъ Ѵ7, т.-е.
отъ количества воды, въ которой растворенъ 1 гр. вещества. Результаты
не представляютъ какихъ либо простыхъ соотношеній, и потому мы ихъ
не приводимъ. 8іаиЬ и 8сйо1г пользовались при своихъ измѣреніяхъ
(ЫаСІ и /СѴОВ) ледянымъ калориметромъ Виітп’а (стр. 167). Обшир-
ное изслѣдованіе Э. ІНтакельберга появилось въ 1898 г.
На поглощеніи теплоты при раствореніи и плавленіи основаны
охлаждающія смѣси. Если смѣшать три части снѣга или толче-
наго льда съ одною частью ЫаСІ при 0°, то температура понижается до
21°; двѣ части СаС12 и одна часть снѣга даетъ температуру —42°.
Это ничто иное, какъ кріогидратныя температуры соотвѣтственныхъ вод-
ныхъ растворовъ. Вопросомъ объ охлаждающихъ смѣсяхъ занимались
Ние<1огМ, Напашапп, Могііг (алкоголь и снѣгъ), РГаппйІег
(сѣрная кислота и снѣгъ), ТоПіп^ег и вода пли снѣгъ),
Наштегі (СаС12 .ЪН^О и вода или снѣгъ); весьма многостороннее из-
слѣдованіе принадлежитъ Хіѵгг§-ег’у, въ статьѣ котораго приведена и
литература (до 1881 г.).
Обращаемся къ теоретическимъ работамъ; относящимся къ те-
плотѣ растворенія, а именно прежде всего къ работамъ КігсІіЬоіГа
(1858), давшаго формулы для теплоты насыщенія ((?0) и для теплоты раз-
бавленія а слѣд. и для теплоты растворенія (ф). (см. 34). Къ вы-
воду этихъ формулъ мы теперь и приступимъ.
1. Формула КігсЫіоТГа для теплоты (?0 насыщенія, вы-
дѣляющейся при образованіи насыщеннаго раствора 1 гр. веще-
ства въ гр. воды. Пусть Р\ упругость и Оі удѣльный объемъ пара
при данной температурѣ I надъ насыщеннымъ растворомъ (см. § 8);
съ повышеніемъ температуры величина рѵ мѣняется, причемъ одновре-
менно мѣняется и степень концентраціи к раствора.
728
Равновѣсіе соприкасающихся веществъ.
Пусть далѣе р упругость и о удѣльный объемъ пара надъ чистой водой
при ; 5 и удѣльные объемы чистой воды и раствора. Для опредѣле-
нія (?0 вообразимъ нѣкоторый изотермическій круговой процессъ,
которому подвергаемъ вѣсовыхъ частей воды, содержащихся въ ра-
створѣ. Сумма количествъ теплоты, полученныхъ этою водою, должна
быть эквивалентна работѣ, которую она совершаетъ. Весь процессъ со-
стоитъ изъ четырехъ частей:
1. Увеличивая объемъ надъ растворомъ до величины заста-
вимъ всю воду перейти въ паръ. На основаніи (25,с) стр. 550 имѣемъ:
получ. тепл.: АТ(о1 — 8^ -ге/0 ; произв. раб.: А(°1 — 5і)^о-
2. Отдѣлимъ паръ отъ твердаго вещества и сожмемъ его до упру-
гости р; работу сжатія обозначимъ черезъ г:
получ. тепл.: - Аг: произв. раб.: - г.
3. Превратимъ парь въ воду, сжимая его:
получ.* тепл.: — АТ(о — 8} ^0; произв. раб.: р(о —
4. Растворяемъ вещество въ водѣ:
получ. тепл.: С?о
произв. раб.: нуль.
Произведенною работою здѣсь пренебрегаемъ.
Сумма полученныхъ» теплотъ должна равняться суммѣ произведен-
ныхъ работъ, помноженной на А. Пренебрегая вездѣ величинами 5 и
получаемъ
АТииЛо^?' о 1 — Аг — ф0 = - ро) Аг,
откуда
<?о = Ам0(ро — р^) АТчѵЛо^ — о
(37)
Ксли температура Т не высокая и упругость водяного пара не
велика, то можно принять, что паръ слѣдуетъ законамъ М а р і о т т а и
Гей-Люссака, т.-е. что ро рАс1 = Н1. Тогда первый членъ исче-
заетъ; вставляя во второмъ членѣ величины щ и о, получаемъ
<2о =
Рі ді
1 др
р ді
или
(38)
Это и есть формула КігсЬНоіГа для теплоты насы-
щенія, выдѣляющейся при образованіи насыщеннаго раствора
1 гр. вещества въ гр. воды.
Теплота растворенія и разбавленія .
729
II. Формула КігсйЬоіТа для теплоты разбавле-
нія, выдѣляющейся, если прибавить гр. воды къ раствору 1 гр.
вещества въ гр. воды. Пусть р' и о' упругость и удѣльный объемъ
пара надъ растворомъ 1 гр. вещества въ чю гр. воды. Это суть функціи
отъ і, причемъ съ измѣненіемъ і концентрація И не мѣняется;
з' и 5 удѣльный объемъ раствора и чистой воды. Совершаемъ опять
изотермическій круговой процессъ, состоящій изъ четырехъ частей :
1. Увеличиваемъ объемъ пара на величину о'бйе/, вслѣдствіе чего
количество воды испарится:
получ. тепл.: АТ(б‘ У) ^5
2. Отдѣлимъ вновь образовавшійся
гости р\ пусть сіг работа сжатія:
получ. тепл.: — Адг;
3. Превратимъ паръ въ воду :
получ. тепл.: — АТ(б — з) дтѵ;
произв. раб.: р'(б' — з'}(1тѵ.
паръ и сожмемъ его до упру-
произв. раб.: — (іг.
произв. раб.: р(б з](Ти).
4. Прильемъ эту воду къ раствору:
получ. тепл.: — б/ф: произв. раб.: нуль.
Складывая и пренебрегая величинами 5 и з\ имѣемъ
АТскы
б
И (
— А(р'б' — рб^сТіѵ — Асіг,
сіС^ = А(рб — ргб'\Тю 4- АТ б‘
(Тш .... (39)
о
Изъ этой болѣе точной формулы получается приближенная, если опять
положить рб = = р'б' = ТіТ; вставляя во второмъ членѣ о' и о. имѣемъ
-рр
ді
(Тш.
к
. . (40)
Эта формула КігсЫіоИ’а для теплоты разбавленія, вы-
дѣляющейся, если прибавить гр. воды къ раствору 1 гр. веще-
ства въ гр. воды. Формулы (40) и (38) очень похожи другъ на друга,
но между ними большая разница : въ (38) рг зависитъ только отъ і, ибо
/г, т.-е. концентрація насыщеннаго раствора сама зависитъ отъ і\
когда беремъ производную, то мы должны помнить, что вмѣстѣ съ і мѣ-
няется и /г. Въ (40) р‘ зависитъ отъ і и или отъ і и отъ концентраціи й,
независимыхъ другъ отъ друга, и производная по і относится къ случаю
И = Соп8І., что и выражено нами обычнымъ способомъ.
Шиллеръ ввелъ въ теорію КігсйіюІГа нѣкоторыя поправки.
730 •
Разновѣсіе соприкасающихся веществъ.
1
III. Ф о р м у л а, К і г с Ыі о I Га
(?, выдѣляющейся при раствореніи
мулы (34), (38) и (40) щютъ
<2 = АЯТ2
А
Р
ді
для теплоты растворенія
гр. вещества въ IV гр. во і,ы. Фор-
и .
Пд1ё_РР
' \ ді
(41)
' сі тѵ
п
Изъ этой общей формулы КігсЫіоГГа получается предѣльная
теплота растворенія С}', если положить ІѴ=ос.
Наиболѣе тщательное сравненіе результатовъ опытовъ сь формулой
(41) было произведено 8 с 1л оія’емъ: согласіе оказалось вообще удовле-
творительнымъ.
IV. Формула Ѵап’і Но Г Га для теплоты сІд{ растворе-
ренія въ насыщенномъ растворѣ. Разсматривая въ § 5 во-
просъ о растворимости, т.-е. о насыщенныхъ растворахъ, и прилагая
къ нимъ теорію ѴапЧ Но! Га (аналогія между растворенными веще-
ствами и газами), мы вывели формулу (23) стр. 722, которую напишемъ
въ видѣ»
е = іаят2 дХ^. .
О1
• • (42)
Здѣсь мы* о назвали отрицательной теплотой растворенія (т.-е. 2
поглощенная теплота) ; і коеффиціентъ, встрѣчающійся въ основной
формулѣ рѵ = /7? Г, и зависящій отъ диссоціаціи раствореннаго вещества
(электролита); Р осмотическое давленіе при насыщеніи. Легко сообра-
зить, которой пз ь величинъ, перечисленныхъ на стр.725 726, соотвѣтствуетъ
величина о въ (42). Выводя формулу (42), мы предположили, что раство-
реніе вещества совершается подъ осмотическимъ давленіемъ Р, ибо мы
исходили изъ формулы (21) для пара. Отсюда ясно, что о есть не что
иное, какъ теплота р а с т в о р е н і я въ насыщенномъ растворѣ,
отнесенная къ вѣсовой единицѣ раствореннаго вещества, и взятая съ
обратнымъ знакомъ, т.-е. р= сІдА : сія- -—/(1), см. (31) и (32). Такимъ
образомъ получаемъ .. р
= ІАРТ*
СІТГ
(43)
Для недпссоціированнаго вещества (/ = 1):
= арг* сія .
дТ
(44)
Покажемъ, какимъ образомъ формула (44) можетъ быть выведена
изъ теоріи Ріапск’а, изложенной въ § 4. Замѣтимъ, что формула (42)
не приложима къ веществамъ хорошо растворимымъ, такъ какъ при ея
выводѣ мы пользовались формулою (20), годною только для слабыхъ ра-
створовъ. Представимъ себѣ насыщенный, по "слабый растворъ какого
либо вещества вь водѣ, и въ той же водѣ нерастворенный избытокъ этого
Теплота растворенія и разбавленія.
731
вещества. Система состоитъ изъ двухъ фазъ, которыя обѣ слабые ра-
створы въ смыслѣ Р1 а п с к’а. Если мы имѣемъ п0 гр.-молекулъ воды, пг
гр.-молекулъ раствореннаго вещества и п* гр.-молекулъ избытка, то кон-
центраціи суть
= г > Аі ” г , й' = , = 1.
я0 + пі Ъ) + пі п'
Теоретически возможное измѣненіе (при р = Сопзі. и і — Сопбі.)
есть переходъ одной молекулы изъ твердой фазы въ жидкую. Въ
этомъ случаѣ»
^0 " = В = 1-
Формула (15) стр. 718 даетъ
1^1 == .... ... (45)
Эта формула показываетъ, что концентрація й, есть ф у н к ц і я
температуры и давленія. Формула (17) стр. 719 даетъ
•о....................(45,а)
гдѣ Н постоянная въ формулѣ рѵ — НТ отнесенная къ гр.-молекулѣ
газа, а д выраженное въ механическихъ единицахъ количество тепла,
поглощеннаго системою, когда происходитъ разсматриваемое измѣне-
ніе. т.-е. переходъ гр. молекулы изъ твердой фазы въ жидкую. Въ (45,
мы очевидно можемъ замѣнить величину Иг произвольною, ей пропорціо-
нальною величиною, напр. процентною концентраціей Л, или осмотиче-
скимъ давленіемъ Р, или вѣсовымъ количествомъ л вещества, растворен-
наго въ произвольномч» количествѣ воды. Справа мы должны написать
Р вмѣсто Н, если д отнесено къ одному грамму вещества. Если д вы-
ражено въ калоріяхъ, то правую сторону слѣдуетъ еще раздѣлить на А.
Ясно, что въ этомъ случаѣ д, количество тепла, поглощеннаго при пере-
ходѣ 1 гр. вещества въ уже насыщенный растворъ, ничто иное, какъ
сІдг : йл. Итакъ (45,а) даетъ
д\^Их __ д\%И __ сй^Р _ сй^тг _ 1 сідх
дТ - дТ ~ дТ ~ дТ ~ АЯТ* (іл
откуда
0^ = ахт^? = . (46)
01 дТ
а это и есть формула (44). Для одного грамма получаемъ теп-
лоту о растворенія въ насыщенномъ растворѣ
2 = д]^- = АХТ* дХ^- .... (47)
йл дТ дТ ѵ
Ѵап’і Ноіі воспользовался этою формулою для вычисленія вели-
чинъ р, поступая слѣдующимъ образомъ. Положимъ, что при температу-
рахъ и і.2 растворяются лх и л2 вѣсовыхъ единицъ вещества въ нѣко-
732
Равновѣсіе соприкасающихся веществъ.
торомъ количествѣ воды. Тогда можно (47) написать въ такомъ видѣ:
У = - АЦГ* ’^1.................(48)
го г
Формула VапЧ НоИ’а принимаетъ для растворовъ электроли-
товъ видь:
__ о
(И “ 2/Г2
(18,а)
такъ какъ Н близко къ числу 2.
ФОРЧЧ-
дТ
Однако, ѵап Ьааг (1894) далъ другую
о 2 — а
2Т2 * 2~ *
(48,6)
въ которой а «степень диссоціаціи», такъ что 1 а — і. Относительно
формулъ (48,а) и (48,6) возникъ продолжительный споръ.
Вальденъ (1907) въ двухъ весьма интересныхъ работахъ провѣрилъ
формулы V а п’і Н о П’а и Ѵап Ъ а а г’а для ряда органическихъ
растворителей - - метиловаго алкоголя, этиловаго алкоголя, ацетона, са-
лициловаго алдегида, ацетонитрила, пропіонитрила, нигрометана и воды;
раствореннымъ веществомъ служили и Л7. Величины
і или а = і 1 опредѣлялись изъ измѣреній электрической проводи-
мости (т. IV). Оказалось хорошее совпаденіе съ формулами (48,а) и
(48,б/), которыя практически даютъ одинаковыя величины. Теплота
растворенія к} въ различныхъ растворителяхъ имѣетъ различные знаки ;
температурный коеффиціентъ растворимости соотвѣтственно имѣетъ каж-
дый разъ обратный знакъ. И здѣсь также получилось хорошее совпа-
деніе съ формулами ѴапЧ И о (Ра и Ѵап Ьааг’а.
Съ повышеніемъ температуры теплота растворенія вообще
увеличивается; если она, какъ это бываетъ обыкновенно, отрицательна,
то она приближается къ нулю.
При выводѣ формулы (45) мы предположили, что растворенное тѣло,
находящееся въ избыткѣ, составляетъ твердую фазу. Очевидно, что этотъ
же выводъ приложимъ и къ случаю насыщеннаго раствора газа,
избытокъ котораго составляетъ вторую газообразную фазу. Для концен-
траціи к1 мы имѣемъ опять формулу
ш = ... - (49)
Формулы (13) и (14) стр. 718 даютъ
ЛкЛі дТ <1 " НГі • . . . (5О.а)
= др 5 НТ ’ ’ ’ .... (50,6)
Здѣсь д опять количество тепла, поглощеннаго при раствореніи гр.-
молеку лы газа въ насыщенномъ растворѣ; 5 измѣненіе объема, со-
провождающее это раствореніе. Для случая растворенія газа въ жид-
кости мы можемъ принять — 5 равнымъ объему7 гр.-молекулы газа. До-
Диссоціація и двойной обмѣнъ въ растворахъ.
733
пуская, что газъ слѣдуетъ законамъ М а р і о т т а и Гей-Люссака, мы
имѣемъ равенство р8—НТ, Тогда (50,6) даетъ д\%1ц = &? = д\$р. от-
куда = \^р + Сопві., или
Иг = Ср....................(51)
Растворимость газа пропорціональна давленію. Это
законъ Ренту (т. I), который такимъ образомъ выведенъ термодинами-
ческимъ путемъ. Величина С, могущая служить мѣрою растворимости
газа, зависитъ отъ температуры. Формулы (50,а) и (51) даютъ
НТ* дС
С дТ....................
Растворимость газовъ уменьшается съ температурою, такъ что можно
положить С = Со(1 — рі); отсюда слѣдуетъ, что д отрицательно, и что
слѣдовательно при раствореніи гр.-мол екулы газа выдѣляется теплота
При раствореніи одного грамма газа выдѣляется количество теплоты,
которое въ калоріяхъ можно положить равнымъ
С дт~~АК 1—&.......................' 3>
Эта формула указываетъ на связь между теплотою, выдѣляющеюся
при раствореніи газа и температурнымъ коеффиціентомъ растворимости
того же газа; зная & можно вычислить р.
Вопросомъ о тепловыхъ явленіяхъ, сопровождающихъ смѣшеніе
жидкостей, занимались Виріё, Ви88у и Виі^неі, Сгиііігіе,
и въ особенности ЬіпеЪаг^ег (1896). Смѣшенія, при которыхъ проис-
ходятъ сильныя химическія реакціи, напр. воды съ Н28О±, НСІ
и т. д., мы не разсматриваемъ.
§ 8. Диссоціація и двойной обмѣнъ въ растворахъ. Теорія
Р1 а п с к’а, изложенная въ § 4, даетъ возможность рѣшить вопросъ оба, усло-
віяхъ равновѣсія раствора, въ которомъ происходитъ диссоціація или бо-
лѣе сложное явленіе двойного обмѣна. Мы ограничиваемся разсмотрѣ-
ніемъ нѣкоторыхъ случаевъ.
I. Одно вещество (ЛЯ), отчасти распадающееся на,
составныя ч а с т и А и В. Этимъ веществомъ можетъ быть и самый
растворитель, въ которомъ его же составныя части остаются растворен-
ными. Положимъ, что п2 и гр.-молекулъ веществъ (ЛЯ), А и В на-
ходятся въ растворѣ; концентраціи суть И. — — , , йо = -3 •
я п ’ 3 п 1
здѣсь п — и0 -4- пл + п2 + я3, гдѣ число гр.-молекулъ растворителя. Оче-
видно п2=п% и й2 = й3. Возможнымъ измѣненіемъ является распаде-
ніе одной гр.-молекулы вещества {АВ) на составныя части А и В. Тогда
го = О, ^х= 1. ѵ2 = 1, = 1. Формула (12) стр. 717 даетъ, такъ
какъ Л2 —
А 2
^=К(Р' Т)....................(54 л)
734
Равновѣсіе соприкасающихся веществъ
Такъ какъ К не равно нулю, то и не можетъ равняться нулю,
а это значитъ, что если д и с с о ці аці я возможна, то она должна
имѣть мѣсто при всѣхъ температурахъ. Въ этомъ заклю-
чается термодинамическое подтвержденіе теоріи АггЬепіиз’а.
Если диссоціація весьма слабя, то можно положить 7^=1: тогда
(54,а) и (13) стр. 718 даютъ
2 —НТ2 ... (э4,й)
гдѣ д теплота диссоціаціи одной гр.-молекулы вещества.
КоЫгапзсЬ и И е у (1 лѵ е і 11 е г (1894) воспользовались измѣреніями
Л. ТІюшйеп'а, который нашелъ при 10,14°д = 14247 и при 24,6°</ =
= 13627 м. калорій на гр.-эквивалентъ, опредѣляя, по теоріи Аггііе-
піпз’а, теплоту нейтрализаціи одновалентныхъ сильныхъ кислотъ и осно-
ваній въ разведенныхъ растворахъ (гл. V § 4). Значенія д соотвѣтство-
вали эмпирическому уравненію
4045000
д = м. калоріи.
Если выражать д въ эргахъ (умножая на 41,9. ІО6) и Н въ С. О. А.
единицахъ (77 82,6 . ІО6), то получается :
, , 513000 ,
цу/г2 — — Соп8і,
или
_512300 _ 222500
И> = Се Г2 = С.1О 72 .... . (54,с)
Чтобы опредѣлить /?2 КоЫгаивсЬ и Неусілѵеіііег измѣрили
электрическую проводимость (т. IV) чистой воды при различныхъ тем-
пературахъ. По извѣстнымъ величинамъ подвижности іоновъ Н и ОН
(т. IV) опредѣляется = 14,3.10—1° при 18°. Отсюда получается С =
= 6,1 10~7. При 0° Л2=6,3 . 10 10 и при 50° Н2 — 14,7 . 10' 10; такимъ
образомъ, диссоціація возрастаетъ съ возрастаніемъ температуры. Число Д2
указываетъ, сколько граммовъ Н или сколько разъ 17 граммовъ НО со-
держатся въ 18 граммахъ воды. При 18° въ одномъ литрѣ заключаются
ш = 1000 И.2 : 18 = 0,8 . ІО 7 гр.-эквивалентовъН или ОН, т.-е. растворъ
гп = 0,8 . ІО-7 нормальный. Этотъ растворъ приблизительно въ 300
разъ болѣе разбавленъ, нежели насыщенный растворъ ВаЗО^ въ водѣ.
Однако въ кубическомъ миллиметрѣ его содержатся милліарды атомовъ Н
и гидроксильныхъ группъ НО. Въ нашемъ представленіи и въ микро-
скопѣ распредѣленіе 77 и 077 не отличается отъ непрерывнаго простран-
ственнаго распредѣленія, такъ какъ разстоянія между сосѣдними молеку-
лами имѣютъ величины порядка длины свѣтовыхъ волнъ. При 18° 1 гр.
77 и 17 гр. По содержатся въ 12500 куб. метрахъ воды. При 25° ра-
створъ /и = 1,07.10~7 нормаленъ.
II. Случай двойного обмѣна. Положимъ, что растворены
Упругость пара и точка кипѣнія растворовъ.
735
два вещества (АВ) и (СО), напр. КСІ и ЫаВг, или Ва8О± и К2СО2, при-
чемъ могутъ образоваться вещества (АО) и (ВС), напр. КВг и ЫаСІ, или
ВаСО2 и К28ОЛ. Требуется найти условія равновѣсія, которымъ должны
удовлетворять концентраціи й2, и Л4 веществъ (АВ), (СО), (АО) и
(ВС). Возможное измѣненіе есть распаденіе одной гр.-молекулы веществъ
(АВ) и (СО), и образованіе одной гр.-молекулы веществъ (АО) и (ВС).
Ясно, что ѵ±= I, ѵ2 — - 1, — 4- 1, ^4 = 4-1. Формула (12) стр. 717
даетъ
^1^2
или при данныхъ р и Т
Рі А
7;4 = Соіі8і....................(54, сі)
пгІг2 ѵ 7
Это знаменитая формула СгиЫЬег^’а и Ѵ^аая'е.
§ 9. Упругость пара и точка кипѣнія растворовъ. Разсматривая
пары какого либо раствора, мы должны отличать два случая: первый
случай — когда можно пренебречь упругостью пара раствореннаго
вещества, т.-е. когда газообразная фаза состоитъ только изъ паровъ ра-
створителя: сюда относятся вообще растворы твердыхъ тѣлъ, мало лету-
чихъ кислотъ (напр. Н28О± 4- пН2О) и т. д.; вт орой случай - когда
жидкая и газообразная фазы содержатъ оба вещества, т.-е. когда надъ
растворомъ находится смѣсь паровъ растворителя и раствореннаго ве-
щества ; сюда относятся растворы и смѣси жидкостей. Обращаемся прежде
всего къ первому случаю, когда надъ растворомъ находятся
пары только одного растворителя.
Упругость р' паровъ раствора меньше упругости р паровъ чистаго
растворителя. Въ связи съ вопросомъ о пониженіи» р р‘ упругости
паровъ раствора находится вопросъ о повышеніи і* - і температуры ки-
пѣнія раствора. При температурѣ і нормальнаго кипѣнія чистаго раство-
рителя упругость паровъ раствора меньше одной атмосферы, и потому
растворъ закипаетъ при болѣе высокой температурѣ В Этотъ фактъ
былъ давно извѣстенъ и имъ занимались еще Ра гай а у (1820), СггИ-
ПІІ18 (1824) и Ье^тапсі (1835).
Упругость паровъ растворовъ изучали впервые Сг ау - Ь іі8 8ас,
Ргіпнер и въ особенности ВаЪо (1847). Послѣдній вывелъ изъ сво-
ихъ наблюденій, произведенныхъ по способу В а 11 о п’а (стр. 586), законъ,
который можно выразить формулою
Р Р*
р = Сопзі........................(55)
относящейся къ какому либо данному раствору и выражающей такъ
называемый законъ В а Ь о : относительное пониженіе упру-
гости пара даннаго раствора не зависитъ отъ темпера-
туры. Изъ (55) получается, очевидно, что
р‘
- = Сопзі.....................(55, а)
736
Равновѣсіе соприкасающихся веществъ
т.-е. не зависитъ отъ Формула (40) стр. 729 даетъ въ этомъ слу-
чаѣ = 0. Это показываетъ, что законъ В а Ь о можетъ быть вѣренъ
только для такихъ слабыхъ растворовъ, въ которыхъ дальнѣйшее разба-
вленіе не вызываетъ никакихъ тепловыхъ эсрфектовъ.
Въ 1858 Ійбо г. появились результаты изслѣдованій ѴѴиеПпег’а,
произведенныхъ по способу, весьма близкому къ способу Марпа’а
(стр. 590), и дававшему возможность непосредственно измѣрить разность
р р' при различныхъ температурахъ. Его приборъ состоялъ изъ шести
вертикальныхъ, закрытыхъ сверху, широкихъ трубокъ, установленныхъ
двумя параллельными рядами, по три въ каждомъ, внутри большого ящика,
снабженнаго стеклянными стѣнками и наполненнаго водою, температуру
которой можно было мѣнять по произволу. Нижніе концы трубокъ сое-
динены при помощи трубочекъ какъ между собою, такъ и съ большимъ
грушевиднымъ резервуаромъ, установленнымъ внутри того же ящика.
Трубки наполнены ртутью, надъ которой помѣщены нѣкоторыя количества
испытуемыхъ растворовъ, а въ одной трубкѣ чистая вода. Выкачивая
воздухъ изъ резервуара, можно было заставить ртуть опуститься во всѣхъ
трубкахъ, причемъ надъ ртутью образовывались пары испытуемыхъ жид-
костей. Разность высотъ ртути въ различныхъ трубкахъ давала искомую
разность упругостей паровъ.
АѴ и е 11 п е г вывелъ изъ своихъ наблюденій, что пониженіе р р'
пропорціонально вѣсовому количеству т раствореннаго вещества, и что
для нѣкоторыхъ растворовъ относительное пониженіе (р р'): р не зави-
ситъ отъ і (законъ В а Ъ о), а для другихъ мѣняется съ температурою, или,
что то же самое - съ давленіемъ р. Эти выводы ѴѴиеПпег выражаетъ
формулою
р р* = т {ар + Ър*)......................(56)
въ которой а и Ь постоянныя, зависящія отъ рода раствореннаго вещества
(растворителемъ служила вода). ОяІлѵаЫ первый (1884) указалъ, что
если сравнивать величины р р‘ для растворовъ различныхъ веществъ,
содержащихъ одинаковое число граммъ-молекулъ этихъ веществъ (т про-
порціонально молекулярному вѣсу), то на основаніи чиселъ ЛѴиеІІ-
пет’а оказывается, что «молекулярныя пониженія» приблизи-
тельно одинаковыя для различныхъ растворенныхъ веществъ. Подобный
же результатъ вывелъ вслѣдъ затѣмъ (1885) Таттапп изъ своихъ
собственныхъ наблюденій для растворовъ химически подобныхъ солей.
Дальнѣйшія изслѣдованія произвели Раисйоп, Етйеп, 8Ь.ие11ег,
Мовег, Місоі. Віеіегісі, Вгетег, В. Неітііоііг, ѴѴаІкег
и др. Всѣ названные наблюдатели работали надъ водными раство-
рами; результаты ихъ наблюденій не выражаются простыми законами и
мы увидимъ ниже причину этой неудачи.
Каоиіі (1896) первый вывелъ изъ своихъ наблюденій опредѣлен-
ные, и притомъ весьма простые законы, которые выяснились благодаря
тому, что онъ растворителемъ взяль прежде всего не воду, но дру-
Упругость пара и точка кипѣнія растворовъ.
737
гія жидкости (напр. С52, эфиръ, бензолъ, хлороформъ, метиловый ал-
коголь и др.), и растворялъ въ нихъ, а затѣмъ также и въ водѣ, различныя
органическія вещества, но не соли и не кислоты, т.-е. не электро-
л и т ы. Для такихъ растворовъ В а о и Н вывелъ изъ своихъ наблюденій
слѣдующіе четыре закона:
р Р*
1. Для даннаго раствора дробь - —- не зависитъ отъ
температуры. $ і
2. Для даннаго растворяемаго вещества дробь^-^ —
пропорціональна концентраціи. Значеніе, которое принима-
етъ эта дробь, когда растворена одна гр.-молекула вещества, назовемъ от-
носительнымъ молекулярнымъ пониженіемъ.
3. Относительное молекулярное пониженіе не зави-
ситъ отъ природы раствореннаго вещества; это значитъ, что
одинаковое число гр.-молекулъ различныхъ веществъ, растворенныхъ въ
одинаковыхъ количествахъ одного и того же растворителя, вызываетъ
при данной температурѣ одинаковое пониженіе р — // упругости пара.
4. Въ различныхъ растворителяхъ получается оди-
наковое молекулярное пониженіе, если брать одина-
ковое число граммъ-молекулъ растворителя на одина-
ковыя количества растворенныхъ веществъ. Иначе говоря,
. Р—Р'
дробь - ? зависитъ только отъ отношенія числа гр.-молекулъ раство-
реннаго вещества къ числу гр.-молекулъ растворителя. Впослѣдствіи
В а о и И нѣсколько измѣнилъ четвертый законъ, формулировавъ его такъ :
р—/У
4,я. Относительное пониженіе - пропорцюналь-
’ *
но отношенію числа пх гр.-молекулъ раствореннаго ве-
щества къ суммѣ я0 + піч гДѣ я0 число гр.-молекулъ ра-
створителя.
Законы В а о и И’я выражаются формулою
г-г.' = с—а ...................(57>
Р »0 +
гдѣ постоянная сне зависитъ ни отъ температуры, ни
отъ рода растворителя, ни отъ рода раствореннаго ве-
щ е с т в а. Для слабыхъ растворовъ можно остаться при первоначаль-
ной формулировкѣ четвертаго закона, т.-е. можно написать
...................................(57, а)
Р «о
Что касается численнаго значенія коеффиціента въ формулѣ (57),
то оказалось, что с мало отличается отъ единицы, такъ что
можно положить
Р-Р . (58)
Р «о + «і
КУРСЪ ФИЗИКИ О. X В О Л Ь С О Н А. Т. ПІ, изд. 3-е.
47
738
Равновѣсіе соприкасающихся веществъ.
Это знаменитая формула ВаоиІѴя, которую для слабыхъ ра-
створовъ можно написать въ видѣ
Р- Р' = ^ ........ (58.а)
Р пп
Замѣтимъ, что (58) даетъ
Р'= _ по
Р «о + «і
(58,6)
Формула (58) можетъ быть выведена теоретически, какъ мы уви-
димъ ниже. Она даетъ возможность опредѣлить молеку-
лярный вѣсъ т раствореннаго вещества, если извѣстенъ
молекулярный вѣсъ М растворителя. Положимъ, что р граммовъ веще-
ства растворены въ О граммахъ растворителя. Тогда (58) даетъ
откуда
ё
р—р _ т
р О ё + ёМ'
М т
т=
и
Р'
р—р
(59)
Вескшаип, а также ЛѴі 11 иВгейі^ выработали практическіе
способы измѣренія р — р' для растворовъ испытуемаго вещества въ эфирѣ
и алкоголѣ. Слѣдуетъ однако замѣтить, что опредѣленіе т путемъ измѣ-
ренія упругости пара раствора представляетъ большія затрудненія. Го-
раздо удобнѣе, какъ мы увидимъ ниже, пользоваться динамическимъ спо-
собомъ, т.-е. измѣрять температуру кипѣнія раствора.
Законы КаопІѴя, а слѣд. и формулы (58) не приложимы къ ра-
створамъ электролитовъ въ водѣ, такъ какъ въ подобныхъ ра-
створахъ часть раствореннаго вещества диссоціирована, какъ уже было
многократно нами указано. Вмѣсто (58) имѣемъ теперь
Р—Р'^1 __п1._
Р +
<59, а)
гдѣ і вообще колеблется между 1 и 2 и зависить какъ отъ рода раство-
реннаго вещества, такъ и отъ концентраціи раствора. Таттапп (1887)
показалъ, какимъ образомъ можетъ быть опредѣлена степень диссоціаціи
по наблюденнымъ упругостямъ пара растворовъ.
Весьма любопытно, что растворы металловъ въ ртути, т.-е.
амальгамы, также слѣдуютъ законамъ В а о и 1 Ѵя, какъ показалъ В а ш 8 а у
(1889). Если при помощи формулы (59) вычислить молекулярные вѣса т
растворенныхъ металловъ, то они вообще оказываются близкими къ атом-
нымъ вѣсамъ [і этихъ металловъ. Это указываетъ на то, что молекулы
металловъ, растворенныхъ въ ртути, содержатъ вообще не болѣе одного
атома. Странное исключеніе представляютъ Ва и Са, для которыхъ вы-
численныя т около 0,5^, и К, для котораго т около 0.75^.
Упругость пара и точка кипѣнія растворовъ.
739
Мы уже упомянули, что пониженіе р—р' упругости пара раствора
находится въ тѣсной связи съ повышеніемъ і' -і точки кипѣ-
нія раствора. Это повышеніе измѣряли СггИПі1і8 (1824), Ье-
§гап(І (1835), Кгешегв (1856), СгегІасЬ (1887) идр. Приводимъ нѣ-
которыя изъ чиселъ О е г 1 а с Ь’а для температуры кипѣнія і' воднаг о
раствора, содержащаго 5 вѣсовыхъ частей раствореннаго вещества на
100 частей воды.
5 . і' 5 /' 5 і
87,1 114,8° ка 57,4 108,5 ЫаСІ 40,7 108,8
17000 230 кно 623,6 340 ЫаНО . ... . 22200 310
СаС12 305 178 кыо3 338,5 115 ЫсМО3 222 120
К2СО3 202,5 133,5 СаЗО^Н^О 240 104,2 Щавелев. кисл. 50000 125
КСЮ3 69,2 104.4 ЫСІ 151 168 Винная кисл. . 40000 169.
Температура паровъ, выдѣляющихся изъ этихъ ра-
створовъ при температурахъ і', также равна Л, какъ по-
казалъ М а § и и 8 непосредственнымъ опытомъ. Весьма распространенное
мнѣніе, что температура паровъ равна і (100° при 760 мм.), невѣрно.
Связь межд$ р—р' и і'— і легко опредѣлить. Растворъ кипитъ при
температурѣ причемъ онъ находится подъ нѣкоторымъ давленіемъ Н
(обыкновенно атмосфернымъ), которое и есть упругость р' = Н паровъ
раствора при температурѣ і*. Изъ таблицъ мы узнаемъ, что чистый ра-
створитель кипитъ при температурѣ когда онъ находится подъ нѣко-
торымъ давленіемъ р>р‘. Подъ давленіемъ Н=р' онъ кипитъ при нѣ-
которой температурѣ ^которая и есть точка кипѣнія растворителя. От-
сюда ясно, что і и і' > О суть точки кипѣнія раство-
рителя подъ давленіями р' и р (/?>/?')• Зная р и і и наблю-
дая мы изъ таблицъ узнаемъ р', и такимъ образомъ находимъ вели-
чину р—р\ которая можетъ служить для опредѣленія молекулярнаго
вѣса т раствореннаго вещества, см. (59) стр. 738. Такого рода измѣре-
нія составляютъ предметъ тонометріи.
Для случая слабыхъ растворивъ можно вывести особую формулу
для повышенія температуры кипѣнія — -і. Мы видѣли, что і‘ и і
суть точки кипѣнія растворителя при давленіяхъ р и р'. Безъ большой
погрѣшности мы можемъ положить
др _р—,р^р — р‘.
ді і‘ і Ді
Для слабыхъ растворовъ имѣемъ, см. (58,а),
ё_
. т лл
Р — Р=Р~^=Р_Мё
-- От ’
М
гдѣ т и М молекулярные вѣса раствореннаго вещества и растворителя.
740
Равновѣсіе соприкасающихся веществъ.
Р и О число граммовъ того и другого въ растворѣ. Послѣднія два урав-
ненія даютъ
М=Р — Р=меР
дР тПдР ...... (60)
ді ді
Но мы имѣемъ, см. (25,с) стр. 550, уравненіе р=Д7'(о—5)~ді’
скрытая теплота испаренія, о и 5 удѣльные объемы пара и жидкости.
Пренебрегая величиною 5 и допуская равенство ро — ЦТ, мы получаемъ
др о ро _ . ч
дта = А%Т~2' ^ставляя эту величину въ (60), получаемъ
.а.............(вад
/иі/р р п0
Величина МАР = 2 (точнѣе 1,987), ибо Р = 29,27 : <5, Д = -Г ,М=
4^0
= 28,88д. гдѣ б удѣльный вѣсъ пара относительно воздуха, см. (27,а)
и (33) стр. 200 и 201. Итакъ
.....................(.1)
піио
Обозначимъ черезъ Е повышеніе точки кипѣнія въ случаѣ, когда
1 гр.-молекула вещества (& = пі) растворена въЮО гр. ра-
створителя (0=100); (61) даетъ
0,02 Г
ІѢ =
р
(62)
Если § гр. вещества растворены въ 100 гр. раствори-
теля и повышеніе точки кипѣнія равно Аі, то (61) даетъ молекуляр-
ный вѣсъ т вещества равнымъ
т — Е ................... (63)
Аі
Величина Е можетъ быть опредѣлена или на основаніи (63) измѣре-
ніемъ повышенія точки кипѣнія Аі, если т считается извѣст-
нымъ, или-же прямо по формулѣ (62), если р извѣстно и выражено въ
малыхъ калоріяхъ на 1 гр. растворителя. Приводимъ нѣкоторыя числа,
полученныя по формулѣ (63), т.-е. эбулліоскопическимъ мето-
домъ, преимущественно Вальденомъ (1906):
Растворитель Е Растворитель Е
Бензолъ . 24,3 1 Нитроэтанъ . 26.0
Хлороформъ .... . 36,6 Метиловый алкоголь . . 8,4
Бромистый этилъ . . . 25,3 Этиловый алкоголь. . . 11,5
Бромистый этиленъ. . . 63.2 Четыреххлористый сѣро-
Этиловый эфиръ . . . . 21,1 углеродъ 48
Анилинъ . .32,2 Нитрометанъ 19,5
Упругость пара и точка кипѣнія растворовъ.
741
Растворитель. Е
Іодистый метилъ. . . . 41,9
Сѣроуглеродъ...........23.7
Уксусная кислота . . . 31,4
Пиридинъ...............27,1
Растворитель. Е
Муравьиная кислота . . 23,1
Фенолъ................30,4
Ацетонъ. . . . . . 16,7
Двуокись сѣры . . . 15
Вода..................5.2
Вескшапл (1907) нашелъ для уксусной кислоты 2: = 29,9, для
муравьиной кислоты 2: = 24,0. Вальденъ показалъ, что, по теоретиче-
ской формулѣ (62), значенія Е получаются всегда нѣсколько большими, въ
среднемъ на 8%. Опыты ВесктапіГа дали для жидкаго хлора Е=
= 16,5 и для брома 2: = 52. Изъ опытовъ Нипіег’а Тзакоіоіоз
(1907) вычислилъ, что для жидкаго кислорода 2: = 2,9. Если Е извѣстно,
то формула (63) можетъ служить для опредѣленія т.
Весктапп (1890) нашелъ этимъ способомъ для раствора въ
эфирѣ т = 251, что соотвѣтствуетъ молекулѣ /2; далѣе для раствора Р
въ сѣроуглеродѣ т = 124 = Р4; наконецъ для раствора 5 въ сѣроугле-
родѣ т колеблется въ зависимости отъ концентраціи между числами 245
и 318 (58 = 256).
Для растворовъ электролитовъ въ водѣ слѣдуетъ въ (61) прибавить
множитель / съ правой стороны; опредѣленіемъ этого множителя путемъ
сравненія наблюденнаго Аі съ вычисленнымъ по формулѣ (61) занимался
напр. Д. Турбаба.
Удобные приборы, служащіе для опредѣленія температуры кипѣнія
были построены КаопІГемъ и Ве с к іп а п п’омъ (1891); мы не оста-
навливаемся на ихъ описаніи.
Обращаемся къ теоретическому разбору вопроса объ
упругости пара растворовъ, а именно къ выводамъ Р1 а п с к’а, и
ѴапЧ Но! Га. Покажемъ сперва, какимъ образомъ формула (58,а)
стр. 738. данная ВаоиИ’емъ для слабыхъ растворовъ, можетъ быть вы-
ведена изъ общей теоріи Ріапск’а, изложенной въ § 4 (стр. 714). По-
ложимъ, что растворъ содержитъ гр.-молекулъ растворителя и пг гр.-
молекулъ раствореннаго вещества; въ газообразной фазѣ п2 гр.-молекулъ
пара. Концентраціи суть Ло = , ^і =—, Л2 = 1. Возмож-
но по + пі
ное измѣненіе есть переходъ молекулы растворителя изъ раствора въ
паръ. Въ этомъ случаѣ = — 1, ѵх = 0, ѵ2 = + 1. Формула (10) стр. 717
даетъ (пишемъ 9?' вмѣсто 9?)
1§7г0 = — — <р2')............... (64)
11
гдѣ Н постоянная формулы рѵ—НТ, отнесенной къ гр.-молекулѣ газа;
Фо' и двѣ функціи отъ р и Т. относящіяся къ гр.-молекулѣ -жидкаго
(Ф0Э и парообразнаго (ф2') растворителя. Общій видъ этихъ функцій по-
казанъ въ (8,&) стр. 716. Преобразуемъ (64);—1«7г0 = 1^(1 —)— —
Но н0
' 742
Равновѣсіе соприкасающихся веществъ.
при маломъ значеніи послѣдней дроби. Функціи др0' и <р2' относятся къ
давленію р\ подъ которымъ находятся паръ и растворъ. Для чистаго
растворителя давленіе пара равно р; пусть значеніе функцій для него
и для его пара ц0 и <р2. Формула (64) показываетъ, что <^0 = др2. При
небольшомъ р — р' можно положить
Фо' = Фо + , ,Р Р) И (р2 = Ѵ-2 - у (р р).
др ( др
Отсюда
. I дсро дсрі) \
То - Т2 = <Р - -р} у — .
\ др др /
Пусть о и 5 удѣльные объемы пара и жидкости; (8,&) стр. 716 даетъ
д(рп 5 дср? о
—— = — , ~ =-------, такъ что
др 1 др Т
о — 5
То 9>2 ={Р Р) ~
Уравненіе (64) принимаетъ видъ
я0
О — 5
НТ
(р -Р'\
Пренебрегая величиною 5
и допуская равенство ро — НТ, получаемъ
Р Р' _ «1
Р «о
(65)
Рис. 215.
Это и есть формула • К а о и 1 і’я для случая слабыхъ растворовъ :
она такимъ образомъ выведена изъ общихъ началъ термодинамики.
Другой выводъ болѣе общей формулы (58) далъ
V а п’ѣ Н о И. Этотъ выводъ указываетъ на связь между
осмотическимъ давленіемъ Р и пониженіемъ
р р упругости пара. Приводимъ выводъ въ той ин-
тересной формѣ, которую ему придалъ Аггйепіив.
Положимъ, что растворъ находится въ сосудѣ А (рис. 215),
отдѣленный полупроницаемою перегородкою отъ чистаго
растворителя Т7; остальное понятно изъ рисунка. Ра-
створъ поднимется по трубкѣ на нѣкоторую высоту
Ьа = И, согласно ученію объ осмотическомъ давленіи,
мы имѣемъ равенство
Р=ОИ.....................(66)
гдѣ О плотность раствора, которую можно принять рав-
ною плотности растворителя. Упругость пара въ Ь
равна р, въ а надъ растворомъ она равна р'. Очевидно, что и
внѣ трубки на высотѣ уровня а упругость пара должна равняться р .
Плотность д и упругость л; паровъ, находящихся надъ Р, мѣня-
Упругость пара и точка кипѣнія растворовъ.
743
югся въ зависимости отъ высоты х надъ уровнемъ Ь; при х = (»
и х = И имѣемъ я = р и я =р . Если х увеличивается на (Іх, то
упругость л уменьшается на величину, равную давленію слоя пара,
толщина котораго (іх. Итакъ (Іп = — дсіх; если М молекулярный вѣсъ
растворителя (и пара), то д = гдѣ ѵ объемъ гр.-молекулы пара,
п і-іт' (ізт /И .
Полагая л/ѵ~Н1, получаемъ = —^^ах\ интегрируя отъ х — о
до х — И,
т.-е. отъ л = р до м = р', получаемъ
р _ МИ
{7 ~~ НТ'
При малой разности р р можно написать ? = !§ 11 4~ г
— р Р \ Р
, такъ что мы имѣемъ
Р
р _ р р МИ
р ~ р нт
Положимъ, какъ прежде, что растворъ содержитъ гр.-молекулъ рас-
творителя и п± гр.-молекулъ раствореннаго вещества. Объемъ ѵ раствора
п^М
равенъ ѵ = & ; онъ занятъ пх гр.-молекулами раствореннаго веще-
л * тг
ства, слѣд. одна гр.-молекула занимаетъ объемъ = — п . По ученію
Ѵап’і НоИ’а объ аналогіи свойствъ газовъ и растворенныхъ веществъ
имѣемъ тѵР = НТ, или
П°™ Р ---ПТ
пхи
(66,6)
Вставляя (66) въ (Об,6), и сравнивая полученное равенство съ (ьо.а),
Р ~ Р'
получаемъ тотчасъ , = , откуда
Р ПО
Р—Р'
Р
.....................(66,г)
^о + ^1
Это и есть формула Каопіі’я для раствора произвольной концен-
траціи. Выведенныя формулы даютъ возможность найти связь между ос-
мотическимъ давленіемъ Р и упругостями р и р' паровъ растворителя и
раствора. Въ (66,6) замѣнимъ — черезъ ? ? , или, точнѣе,черезъ 7
п0 Р Р
Тогда получаемъ
о НТІЭ і Р
М Р
.Но Н\М равно значенію постоянной Р въ формулѣ рѵ — РТ, от-
744
Равновѣсіе соприкасающихся веществъ.
несенной къ 1 гр. пара растворителя; далѣе введемъ объемъ 5 одного
грамма жидкаго растворителя, равный 1:2?. Тогда получаемъ :
. р = кг ік Я, = кт. I /'......................(вт)
5 ° р 8 р Ѵ 7
Послѣднее выраженіе относится къ слабымъ растворамъ; въ знаме-
нателѣ послѣдней дроби можно поставить р вмѣсто р'. Для вычисленія
удобнѣе вновь ввести молекулярный вѣсъ М и плотность 2) = 1 :5 ра-
створителя. Когда за единицы объема и давленія приняты куб. метръ и
давленіе въ 1 клгр. на кв. м., то 2? = 29,27 : й, гдѣ й плотность газа от-
носительно воздуха (т. I); далѣе М= 28,88й; слѣд. 2? = 29,27 X 28,88 :
: М = 849 : 714. Если мы желаемъ вычислить осмотическое давленіе
Р въ килогр. на кв. метръ, то слѣдовало при 9нашемъ выводѣ вездѣ
брать килогр.-молекулы вмѣсто гр.-молекулы, и тогда 2) = ~ есть число
килограммовъ, которые вѣситъ 1 куб. метръ растворителя; очевидно 2? =
== 1ООО2)о, гдѣ 2)0 плотность растворителя относительно воды. Вставляя
2? и 5, имѣемъ
р__ 849Г. 1ООО2)о р — рг килогр. __ 849Г. 1ООО2)о р — р'
М Р кв. м. 10333714 Р
или, окончательно,
Р = 82.2 ? атмосф.............(67,бі)
714 Р
Здѣсь Р осмотическое давленіе, /)0 плотность ра-
створителя относительно воды, 714 молекулярный вѣсъ
растворителя, р и р упругости паровъ растворителя и
раствора при температурѣ Т. Такимъ образомъ измѣреніе Р
замѣняется измѣреніемъ р и р\ пли на практикѣ, какъ мы видѣли, из-
мѣреніемъ точекъ кипѣнія і и
Выразимъ осмотическое давленіе Р черезъ повышеніе Лі точки ки-
пѣнія раствора. Формулы (66,а) и (66,Ь) даютъ Р = Ж или, если
ввести 5 = 1:2),
Р= Ді .............................(67,Ь)
АТз
Полагая опять 1:5 = 2) = 1ооо2)0 и Л = * , получаемъ Р въ
420
килогр. на кв. метръ; раздѣляя правую сторону на ІоЗЗЗ, получаемъ
Р= —Ді атмосф. . ... (67.с)
Здѣсь Р осмотическое давленіе, 2)0 плотность ра-
створителя относительно воды, р скрытая теплота не-
Упругость пара и точка кипѣнія растворовъ.
715
паренія 1 гр. растворителя, выраженная въ малыхъ ка-
лоріяхъ, Т температура кипѣнія растворителя, Ді по-
вышеніе температуры кипѣнія раствора.
Для водныхъ растворовъ имѣемъ О0 — 1, М = 18, о- 536 и
въ (67,с) Т = 373 ; отсюда
Р ~4,Б7 7 ^ V атмосф. .... (67,б/)
Р
Р=Ь9,2Ді атмосф........................(67,^)
Хоуез и ЛЬЬоі ввели нѣкоторыя поправки въ формулу (67.бЛ.
Мы разсматривали до сихъ поръ тотъ случай, когда паръ раствора
состоитъ только изъ вещества растворителя. Обращаемся къ случаю,
когда растворенное вещество также испаряется, иначе говоря обращаемся
къ вопросу объ испареніи разнаго рода смѣс ей жидкостей.
Мы знаемъ (т. I), что при смѣшеніи двухъ жидкостей слѣдуетъ отличать
три случая:
1. Жидкости взаимно вовсе не растворяются, или. точнѣе, раство-
ряются въ весьма малыхъ количествахъ (вода и различныя масла).
2. Каждая изъ жидкостей растворяется въ другой и притомъ въ
опредѣленномъ количествѣ (вода и эфиръ). Послѣ взбалтыванія смѣси
получаются два слоя, представляющіе, каждый, насыщенный растворъ
одной изъ жидкостей въ другой.
3. Жидкости смѣшиваются во всѣхъ пропорціяхъ (вода и алкоголь,
хлороформъ и сѣроуглеродъ).
Замѣтимъ, что одинъ изъ первыхъ, занимавшихся вопросомъ о смѣ-
сяхъ жидкостей, былъ Адашевъ (въ Москвѣ, 1857), а затѣмъ особенно
много занимался этимъ вопросомъ Алексѣевъ.
Вопросомъ объ упругости паровъ смѣсей жидкостей зани-
мались до Коновалова (1881), которому принадлежитъ важнѣйшая
изъ относящихся сюда работъ, главнымъ образомъ М апи 8 , Е е ц -
паиіі, ѴѴиеІІпег; послѣ Коновалова — Ріапск, ѴГіпкеІ-
ш а п п, М е г п з 1, Віиетске п Сг е г Ь е г.
Ведпаиіі нашелъ, что для смѣсей перваго рода упругость пара
равна суммѣ упругостей паровъ двухъ не смѣшивающихся жидкостей;
онъ изслѣдовалъ смѣси РРО съ С52, Н2О съ СС/4 и Н2О съ бензоломъ.
Изъ смѣсей второго рода Ведпаиіі изслѣдовалъ только смѣсь воды съ
эфиромъ; оказалось, что упругость р пара смѣси мало отличается отъ
упругости паровъ эфира. Для смѣсей третьяго рода онъ нашелъ, что р
находится между упругостями рг и р2 паровъ составныхъ частей. Болѣе
сложныя отношенія нашелъ АѴ и е 1 1 п е г , показавшій, что р весьма
часто больше рА и больше /л2: а К о 8 с о е открылъ, что для смѣси воды*
съ муравьиной кислотой р, наоборотъ, меньше, чѣмъ р} и чѣмъ р2.
Коноваловъ (1881) изслѣдовалъ смѣси гомологическихъ кислотъ
746
Равновѣсіе соприкасающихся веществъ.
съ водою и гомологическихъ алкоголеи съ водою. Для смѣсей второго
рода (растворовъ) Коноваловъ находитъ, что упругость паровъ
двухъ насыщенныхъ растворовъ одинаковая, хотя составъ этихъ раство-
ровъ совершенно различный, напр. вода съ 10% эфира и эфиръ съ
3% воды. Что упругости паровъ обоихъ растворовъ должны быть равны,
можно показать слѣдующимъ образомъ. Вообразимъ трубку въ формѣ
Рис. 216.
кольца (рис. 216), содержащую два насыщенныхъ раствора въ а и Ъ.
Упругость паровъ въ с очевидно должна быть одинакова надъ а и надъ Ь,
въ противномъ случаѣ мы имѣли бы непрерывную перегонку и могли бы
построить регреіишп тпоЬіІе.
Результаты нѣкоторыхъ изслѣдованій Коновалова надъ смѣсями
третьяго рода изображены на рис. 217, 218 и 219. Они относятся къ
смѣсямъ трехъ поименованныхъ ниже веществъ съ водою. Ординаты
обозначаютъ упругости р пара смѣси при температурѣ, обозначенной у
каждой изъ кривыхъ; абсциссы обозначаютъ процентное содержаніе въ
смѣси вещества, смѣшаннаго съ водою, такъ что ордината лѣваго конца
кривой обозначаетъ упругость р± паровъ чистой воды, а праваго конца —
упругость р2 паровъ чистаго вещества, примѣшаннаго къ водѣ. Коно-
валовъ отличаетъ три типа кривыхъ.
А. Упругость р постоянно находится между рѵ и р2. Сюда отно-
сятся смѣси метиловаго алкоголя (рис. 217), этиловаго алкоголя, уксусной
кислоты и пропіоновой кислоты съ водою.
В. Упругость р больше р± и больше р2. Сюда относятся смѣси
пропиловаго алкоголя (рис. 218), изобутиловаго алкоголя и масляной ки-
слоты съ водою. Для нѣкоторой опредѣленной смѣси р максимальное.
С, Упругость р меньше рг и меньше р2- Единственный примѣръ
представляетъ смѣсь муравьиной кислоты съ водою (рис. 219). Для нѣко-
торой опредѣленной смѣси р минимальное.
Далѣе Коноваловъ нашелъ, что максимумъ или минимумъ р
Упругость пара и точка кипѣнія растворовъ.
747
соотвѣтствуетъ такой смѣси, для которой составъ пара одинаковъ съ со-
ставомъ самой смѣси; такая смѣсь перегоняется безъ измѣненія состава,
т.-е. кипитъ при постоянной температурѣ.
Памъ остается вывести интересную формулу Ріапск’а, относящу-
юся къ слабымъ растворамъ одной жидкости В въ другой А. Поло-
Рпс 218.
Рис 219.
жимъ, что въ растворѣ находятся /г0 гр.-молекулъ жидкости А и гр.-мо-
лекулъ жидкости 5, и что въ парѣ соотвѣтственныя числа и по-
лагаемъ. что пг и малы сравнительно съ п0 и п0'. Концентраціи суть
0 «о + Лі «0 + «1 «О + «1 по +«1
Возможныя измѣненія суть :
1) Переходъ гр.-молекулы вещества А изъ раствора въ паръ. Въ
этомъ случаѣ
Уо==—1, ^1 = 0, < = ѵ/ = 0.
Формула (11) стр. 717 даетъ
= №<(Р> Г).....................(Ь8)
Ао
2) Переходъ гр.-молекулы вещества В изъ раствора вгь паръ. Въ
этомъ случаѣ
г() =0, = 1, = о, — -|- 1;
это даетъ и •
1^7 =Ш(А Г).....................(68,
Йі
Обращаемся къ формулѣ (68). Имѣемъ
748
Равновѣсіе соприкасающихся веществъ
эта разность мало отличается отъ — Л/, такъ что можно написать
— /г/= Т) . ...........(68.Ь)
Пусть рѵ давленіе пара надъ чистою жидкостью А ; имѣемъ
К - /г/ = р, Г) = 1^( Г) + (р - - П •
Для Чистаго растворителя В очевидно /г1=й1' = О и р=р^\ слѣд.
]§К(р0, Г) = 0. Такимъ образомъ получаемъ
Формула (18) стр. 719 даетъ
Ах —А/= — (/?- Р0)т^ • • • (68’И
ГІ 1
гдѣ 5 измѣненіе объема, сопровождающее тотъ переходъ, къ которомд
относится разбираемая формула (68). Очевидно 5 можно принять рав-
нымъ объему гр.-молекулы пара жидкости А. Мы можемъ принять ра-
венство р08 = НТ, и тогда (68,с) даетъ
/?1 - . (69)
Ръ
Здѣсь и й/ концентраціи раствореннаго веще-
ства В въ слабомъ р а с т в о р ѣ и въ парѣ; /?0 у п р у г о с т ь
пара жидкости А и р упругость пара раствора. Замѣ-
чательная формула (6*9) показываетъ, что разности и р0— р
всегда одного знака, что нетрудно формулировать словами. \Ѵ і п к е 1 -
шапп (1890) изслѣдовалъ составъ паровъ смѣси пропиловаго алкоголя
съ водою нашелъ удовлетворительное согласіе съ формулою (69) Ріапск’а.
К е гп н і (1891) вывелъ нѣсколько иную формулу для величины ; Сг е г -
Ьег (1892) изслѣдовалъ составъ паровъ цѣлаго ряда смѣсей и сравни-
валъ результаты съ формулами Р1 а п с к’а и К е гп 8 і’а, которыя для
слабыхъ растворовъ не существенно отличаются другъ отъ друга.
§ ІО. Затвердѣваніе растворовъ. Растворенныя вещества понижа-
ютъ точка затвердѣванія растворителя. Основной законъ, которому слѣ-
дуетъ это явленіе, былъ открытъ еще В 1 а ц'сі е п’омъ (1788), показав-
шимъ, что пониженіе точки затвердѣванія пропор-
ціонально количеству гп раствореннаго вещества; если
два вещества растворены, то пониженіе равно суммѣ пониженій вы-
званныхъ каждымъ изъ этихъ двухъ веществъ въ отдѣльности. Впро-
чемъ въ нѣкоторыхъ случаяхъ В1 а § сі е п наблюдалъ отклоненія отъ за-
кона пропорціональности. Работа В 1 а ц (1 е п’а была забыта и только
въ 1871 г. Сорреі обратилъ на нее вниманіе ученыхъ, послѣ того,
какъ КиебогИ (1861), не знавшій о работѣ Віа^сіеп’а, вновь от-
крылъ законъ В1 а §• (1 е п’а о пропорціональности пониженія темпе-
ратуры количеству гп вещества. Виейогіі нашелъ далѣе, что при ра-
Затвердѣваніе растворовъ.
749
створеніи нѣкоторыхъ безводныхъ солей въ водѣ получается только въ
томъ случаѣ пропорціональность между Ді± и т, если допустить, что въ
растворѣ образуются опредѣленные гидраты (напр. СаСІ . и если
вычислять т, какъ число вѣсовыхъ единицъ водной соли, растворенныхъ
въ 100 вѣсовыхъ единицахъ воды, т.-е. если принимать во вниманіе, что
при дальнѣйшемъ прибавленіи безводной соли уменьшается количество
воды, играющей роль свободнаго растворителя, б’орреі (1871) под-
твердилъ главнѣйшіе выводы КиейогІГа; онъ первый ввелъ понятіе
о «молекулярномъ п о н и ж е н і и», сравнивая пониженія, вызванныя
различными веществами, взятыми не въ одинаковыхъ вѣсовыхъ количе-
ствахъ. но въ количествахъ, пропорціональныхъ молекулярнымъ вѣсамъ
этихъ веществъ. Онъ нашелъ, что молекулярное пониженіе, напр. отъ
1 гр.-молекулы на 100 частей воды, приблизительно одинаково для хими-
чески подобныхъ солей.
Каоиіі (1882—1884) пошелъ дальше своихъ предшественниковъ,
точнѣе выяснивъ законы разсматриваемаго явленія, подобно тому, какъ
онъ первый выяснилъ законы, касающіеся пониженія давленія пара, вы-
званнаго растворенными веществами. Онъ и здѣсь изслѣдовалъ прежде
всего не водные растворы, а изъ водныхъ — растворы неэлектролитовъ.
Прежде всего онъ подтвердилъ, что молекулярное пониженіе не зависитъ
отъ рода раствореннаго вещества, но различно для различныхъ раство-
рителей. Приводимъ числа, которыя онъ далъ для пониженій о, вызван-
ныхъ 1 гр.-молекулой вещества въ 100 гр. растворителя; для воды полу-
чаются два числа: около 18,5° для растворовъ алкоголя, глицерина, са-
хара, фенола, эфира, анилина, кислотъ муравьиной, щавелевой и винной
и т. д.: около 37° для электролитовъ, каковы ИаСІ, 1\!Н±СІ, КСІ, ИНО^
КС\, КН О, кислоты фосфорная и мышьяковая и т. д.
Растворитель
Вода...............
Муравьиная кисл. . .
Уксусная кисл.
о
37° и 18,5°
28°
39°
Р аств орител ь
Бензолъ..............
Нитробензолъ . . . .
Бромистый этиленъ
о
49°
70,5°
117°.
Понятно, что эти числа для практики имѣютъ лишь значеніе мно-
жителей въ формулѣ
ДІг=пб....................... (70)
гдѣ п число гр.-молекулъ растворенныхъ въ 100 гр. растворителя; /7 = 1
практически невозможно, по крайней мѣрѣ въ большинствѣ случаевъ.
("начала Е а о и 11 полагалъ, что для пониженія точки замерзанія суще-
ствуетъ подобная же зависимость отъ растворителя, какъ для по-
ниженія упругости пара, т.-е. что величины о обратно пропорціональны
молекулярнымъ вѣсамъ растворителей, и что слѣд. пониженіе Ді^ вы-
званное напр. одной гр.-молекулой раствореннаго вещества въ 100 гр.-
молекулахъ растворителя, есть величина, не зависящая ни отъ раствори-
теля, ни отъ раствореннаго вещества, и равная приблизительно 0°,62.
750
Равновѣсіе соприкасающихся веществъ.
Однако отъ этого вывода К а о и 1 і впослѣдствіи отказался, и мы уви-
димъ. что такой выводъ
несогласенъ съ результатами приложенія началъ
Рис. 220.
термодинамики къ вопросу о затвердѣваніи ра-
створовъ.
Законъ постоянства молекулярнаго пони-
женія для даннаго растворителя въ
нѣкоторыхъ случаяхъ не оправдывается. Такъ
напр. для раствора уксусной кислоты въ бен-
золѣ получается пониженіе, въ два раза мень-
шее, чѣмъ слѣдуетъ по упомянутому закону;
иначе говоря, пониженіе соотвѣтствуетъ не мо-
лекулярному вѣсу 60 но 120. Такое
отступленіе указываетъ на полимеризацію, на
удвоеніе частицъ уксусной кислоты, растворен-
ной въ бензолѣ. Отступленіе въ противопо-
ложную сторону представляютъ растворы элек-
тролитовъ въ водѣ, по ввергающихся, какъ мы
уже много разъ указывали, диссоціаціи. Къ
нимъ мы возвратимся ниже.
Приборы іля опредѣленія точки затвер-
дѣванія растворовъ построили К а о п И , Р о п-
801, НоПетапп, Аидѵегз, Еук-
тапп, ЕаЬіпуі, Клобуковъ, Веск-
т апп и др. Ограничиваемся описаніемъ прибора В е с к т ап п’а, изо-
браженнаго на рис. 220. Испытуемое вещество вливается въ сосудъ АА
черезъ боковую трубку А'. Сосудъ А содержитъ платиновую мѣшалку г
и весьма чувствительный термометръ О В е с к ш а п п’а, системы \Ѵ а 1 -
і е г (1 і п’а; устройство верхней части е этого термометра было показано
на рис. 17 стр. 16. Сосудъ А находится внутри болѣе широкаго сосуда В,
содержащаго воздухъ; наконецъ сосудъ В помѣщается внутри стакана С,
наполняемаго охлаждающею смѣсью, для перемѣшиванія которой служитъ
большая кольцевидная мѣшалка. Вопросъ о способѣ точнѣйшаго наблю-
денія момента, когда жидкость во внутреннемъ сосудѣ затвердѣваетъ, вы-
звалъ въ послѣднее время оживленный споръ, въ которомъ приняли уча-
стіе В а о и И, Р о п 8 о I и др.
Интереснымъ вопросомъ о затвердѣваніи водныхъ растворовъ сѣрной
кислоты занимались РТаипсПег и 8сііпе^^ (1875), Рісіеі (1894)
и И і 11т ау г (1898).
Обращаемся къ теоретическому разбору вопроса о связи между
составомъ раствора и пониженіемъ Аіг точки затвердѣванія,
а также между ЛІГ и осмотическимъ давленіемъ Р. Основная изъ отно-
сящихся сюда формулъ была выведена V а п’1 Н о 1 Гомъ, какъ результатъ
разбора нѣкотораго кругового процесса. Мы предпочитаемъ вывести фор-
мулу Ѵап’і И о П’а изъ общей теоріи Ріапск’а, изложенной въ § 4.
Представимъ себѣ систему, состоящую изъ раствора гр.-молекулъ
Затвердѣваніе растворовъ.
751
нѣкотораго вещества въ п0 гр.-молеку лахъ растворителя, и изъ твердаго
растворителя; температура Т системы есть температура затвердѣ-
ванія раствора. Концентраціи суть
Іг0 = -г° , /?х = 1 . /г., = 1.
«о + «Г «о + «і
Возможное при іанныхъ р и Т измѣненіе есть. переходъ молекулы
твердаго растворителя въ растворъ. Въ этомъ случаѣ
Ѵ0 = 1, ѵл = 0, 7'2 = 1.
Уравненія (10) и (11) стр. 717 даютъ
Ж = (фо Фз) = Т).....................................(71)
Но 1§7г0 = 1ц |1 -|- — |= Пі, такъ что
\ по/ по
21 = Ь (е/2 Фо)..............................(71,а)
п0 77
д2 и суть функціи давленія и температуры, относящіяся къ твердому
и къ жидкому растворителю, когда присутствуетъ растворенное вещество
и когда, вслѣдствіе этого, система находится при температурѣ Т.
Если = 0, то растворенное вещество отсутствуетъ, температура равна
температурѣ Го затвердѣванія чистаго растворителя, и вмѣсто Ф2 Фо
имѣемъ величину, которую обозначимъ черезъ (ф2 — Фо)о- При маломъ
Т Т(} = Ліг мы имѣемъ
фо - ф0 = (ф.2 - Фо)о + (Т- Го) . . (71,6)
Но (71,а) показываетъ, что (ф2 Фо)о — далѣе формула (71) и
формула (17) стр. 664 даютъ
Фо)о = н д\$К(р, Го) _ Нд _ ф
ді ді НТо2 Т2’
гдѣ д количество теплоты, притекающей къ системѣ при разсматривае-
момъ измѣненіи, и выраженной въ механическихъ единицахъ. Пусть (ц
скрытая теплота плавленія 1 грамма растворителя, выраженная въ ма-
лыхъ калоріяхъ. Тогда д = , гдѣ М молекулярный вѣсъ раствори-
теля и А термическій коеффиціентъ работы. Формулы (71,6) и (71,а)
даютъ теперь
Ф2 Фо ( ^0 Д р 2 ’
«і _
п , ~ АНТ2 ’
ибо Го — Т -- Ліх; отсюда
752
Равновѣсіе соприкасающихся веществъ.
= АНТ/ пх
1 ’ п0
(72)
Сг р*
Если вставить п0 = л, и пх = ; гдѣ и О число граммовъ ра-
/ИІ //4
створеннаго вещества и растворителя, т молекулярный вѣсъ растворен-
наго вещества, то получается
Лі
тОс^ отОрі
. (72)
ибо АН — 2 (стр. 740). Пусть Ех пониженіе точки затвердѣванія. когда
1 гр.-молекула вещества т) растворена въ 100 гр. растворителя
(О = 100) ; тогда .
0,02 702
6і
(73)
Ех.............................(74)
т
т = Е\^.................(75)
Послѣдняя формула можетъ служить для опредѣ-
ленія молекулярнаго вѣса т раствореннаго вещества
(^ граммовъ въ 100 гр. растворителя) путемъ наблюде-
нія пониженія Лі± точки затвердѣванія раствора. Фор-
мулы (73) и (75) и суть формулы, данныя Ѵап’і Но! Ромъ: онѣ вполнѣ
аналогичны (62) и (63) стр. 74о. Величины Ег вычисляются разъ на-
всегда ; приводимъ нѣкоторые примѣры:
Растворитель. Ег
Бензолъ............ . 53
Вода................ 18,6
Муравьиная кислота. . . . 28,4
Уксусная кислота..... 38,8
Растворитель. Ег
Нафталинъ............69,4
Фенолъ............... 76
Нитробензолъ.........69,5
Бромистый этиленъ . 119.
Формула (72) даетъ
пг М^Аі^ М^Аі^ М .
п0 АНТ^ 2Т^ 100^! 1
(7б)
Для водныхъ растворовъ (Л4=18, — 18,9) имѣемъ
/г0
Аіг
105
('И
Обратимся къ связи между пониженіемъ Ліх точки замерзанія и осмо-
тическимъ давленіемъ. Мы имѣли, см. (66,6) стр. 743,
НТОпх
М п0
(78)
Затвердѣваніе растворовъ.
753
Такъ какъ давленіе Р относится къ слабому раствору, точка затвер-
дѣванія Т котораго немного отличается отъ 7°, то мы въ (72) можемъ
вставить Т вмѣсто Т$. Формулы (72) и (78) даютъ, если ввести удѣль-
ный объемъ 5 растворителя (5 = 1: 79),
Р— ЛА
АТз
(79)
Полагая 1:5=2?= 1ООО/)о и А = —, получаемъ Р въ килогр.-ме-
426
трахъ; раздѣляя правую сторону еще на 10333, имѣемъ
Р= атмосф................(80)}
Здѣсь Р осмотическое давленіе, плотность ра-
створителя относительно воды, скрытая теплота
плавленія 1 гр. растворителя, выраженная въ малыхъ
калоріяхъ, Т температура затвердѣванія растворителя,
Аіг пониженіе температуры затвердѣванія раствора.
Для водныхъ растворовъ /Эо = 1, рх = 79, Т — 273
Р= 12,07А/х атмосф.
(81)
Формулы (79), (80) и (81) совершенно аналогичны формуламъ (67,/?),
(67,с) и (67,^) на стр. 744 и 745, которыя относились къ повышенію Аі точки,
кипѣнія. Формула (67) на стр. 744 и (79) даютъ
л, = . Р-Р-
Л4ох р
(32)
Этою формулою выражается связь между умень-
шеніемъ р — р' упругости паровъ и пониженіемъ Аіѵ
температуры Т затвердѣванія жидкости, молекуляр-
ный вѣсъ и скрытая теплота плавленія которой М и рх
когда въ ней растворяется какое либо вещество: по-
нятно, что р и р' также относятся къ температурѣ Т.
Для водныхъ растворовъ (Т = 273, М = 18, рх = 79) <иѣемъ
= 105
Р
(83)
Тотъ же результатъ получимъ, комбинируя (81) съ (67,б/), въ кото-
ромъ слѣдуетъ принять Т = 273. Съ этимъ также вполнѣ согласна ком-
бинація формулъ (65) стр. 742 и (77).
Опытною провѣркою формулъ ѴапТ НоіГа занимался кромѣ са-
мого V ап’і НоіГа, въ особенности Еуктапп; далѣе измѣряли вели-
чину Аі^ кромѣ ВаоиІѴя, еще Весктапп, Еатзау, Ропяоі.
АЪе^§, Яопез, Ьоотія, Мез‘ег ЛѴіІдегтапп и др. Непри-
водимъ результатовъ измѣреній, произведенныхъ названными учеными.
КУРСЪ ФИЗИКИ О. X В О Л ь С О Н А. т. III, изд. 3-е. 48
754
Равновѣсіе соприкасающихся веществъ
Оказалось весьма удовлетворительное согласіе между этими результатами
и формулою ѴапЧ Но!Га. Исключеніе представляютъ, какъ и слѣдо-
вало ожидать, водные растворы электролитовъ. Для нихъ пониженіе
въ і разъ больше того, когорое опредѣляется формулою ѴапЧ Но П’а.
АггЬепіий показалъ, какимъ образомъ і можетъ быть опредѣлено на
основаніи измѣренія электропроводности растворовъ (см. т. Л’). Вели-
чины /, опредѣленныя этимъ путемъ и изъ наблюденій надъ пониженіемъ
точки замерзанія (отношеніе наблюденнаго къ вычисленному), оказа-
лись весьма согласными между собою. Еще лучшее согласіе дали позд-
нѣйшія измѣренія М е ] е г АѴ і 1 (1 е г т а п п’а.
Таттапп (1889) и Неусоск и Хеѵіііе (1889—1890) опредѣ-
ляли пониженіе точки затвердѣванія растворовъ металловъ въ Н§(Е1 = 388),
^а(Е1 = 360) и 8п(Е1 =408). Въ и 8п металлы повидимому нахо-
дятся въ видѣ одноатомныхъ молекулъ; въ Ыа же молекулы растворен-
ныхъ металловъ содержатъ сложныя молекулы, вѣроятно четырехатомныя
(наблюденные Ех около 100 и меньше).
Выведенныя нами формулы не приложимы къ крѣпкимъ растворамъ,
аналогично тому, какъ законы Бойля и Гей-Люссака не прило-
жимы къ газамъ, не очень далекимъ отъ ожиженія. В г е сі і $ и X о у е 8
расширили теорію растворовъ, допустивъ, что осмотическое давленіе,
объемъ и температура раствора связаны уравненіемъ, тождественнымъ
съ уравненіемъ Vа п сіег АѴааІй’а. Эти теоретическія изслѣдованія
еще не могутъ считаться законченными.
ЛИТЕРАТУРА.
Къ § 1.
СіЬЬз. Тгапз. о! іЬе Соппесііспі Асабету 3 р. 152, 1876; ТІіегтобупатізсЬе
Віибіеп, перев. Озілѵаій’а. Ьеіргі^, 1892.
РоогеЪоот. Кесиеіі Тгаѵ. Рауз Ваз. 5 р. 335, 1886; 6 р. 266, 304, 1887; ХізсЬг.
Г. рЬуз. СЬет. 2, 1888; 8 р. 521, 1891.
Ріапск. АѴ. А. 13 р. 535, 1881 ; 19 р. 358, 1883; 30 р. 562; 31 р. 189; 32 р. 462
1887; 34 р. 139, 1888.
Ріеске. Хізсііг. Г. рііуз. СЬетіе 6 р. 268, 411, 1890; 7 р. 97, 115, 1891.
Негпзі. Хізсііг. Ь рЬуз. СЬетіе 8 р. ПО, 1891.
Ье Скаіеііег. С. К. 99 р. 786, 1884.
• Оиігет. Мёсапіцие р. 152.
Хіагіі Но//. 2ізсЬг. I. рііуз. СЬетіе 1 р. 481, 1887; Ѵогіезшщеп йЬег іЬеогеі. ипсі
рЬузісаІ. СЬетіе, ВгаипзсЫѵеі^, 1898.
Посалъскій. Равновѣсіе соприкасающихся массъ, Одесса, 1895.
Къ § 2 и § 3.
ОіМгіе. РЫІ. Ма^. (4) 49 р. 1, 206, 266, 1875; (5) 1 р. 49, 354, 446; 2 р. 211, 1876.
Р/ашиіІег. СЬет. Вегі. 20 р. 2223, 1877.
О//ег. АѴіеп Вег. 81 II, р. 1058, 1880.
Богородскій. Ж. Ф. X. О. 27, Отд. Хим. р. 516, 1895.
Ропзоі. Виіі. сіе Іа 8ос. СЫт. (3) 13, 1895; б. бе рііуз. (3) 4 р. 337, 1896; Апп.
<1е сЫт. еі рііуз. (7) 10 р. 79, 1897 ; ТЬёзе бе босіогаі, Рагіз 1897
Роіо//. ХізсЬг. Т. рЬуз. СЬетіе 17 р. 325, 1895.
Литература.
755
Меуегко//ег. Біе Рказепге^еі. Ьеіргі^, 1893.
Вапсго/і. Тке Рказе Виіе. Кѳ\ѵ-Ѵогк, 1897.
Горбовъ. Энцикл. Словарь Брокгаузъ-Эфрона 24 р. 852, С. П. 1898.
8скгеіпетакег8. 2ізскг. к ркуз. Скетіе 9 р. 74,1891; 10 р. 475, 1892, 11 р. 92, 1892.
Ѵгіепз. 2ізскг. Г. ркуз. Скетіе 7 р. 208, 1891.
Тгеѵог. См. Вапсго/і. Тке Рказе Виіе, р. 4.
Хетзі. Ткеогеіізске Скетіе р. 482.
Ріапск. Ткегтосіупатік р. 183.
Ѵіпсі. 2ізскг. Г. ркуз. Скет. 31 р. 390, 1899.
Раѵеаи. С. В. 138 р. 621, 1904.
Ропзоі. С. В. 138 р. 803, 1904.
Миеііег. С. В. 146 р. 866, 1908.
Воиіоиск. С. В. 149 р. 449, 1377, 1909.
Къ § 4 и § 5.
Ріапск. 2ізс1іг. Г. ркуз. Скетіе 1 р. 577, 1887; А. 34 р. 139, 1888; Ткегтоку-
патік, Ьеір'/Цг 1897, р. 210; Аскі. Ѵогіез. іік. ікеогеі. Ркузік, Ьеіргі§ 1910 р. 22—39. •
Неіткоііх. Ѳез. АЪкапкІ. 2 р. 987.
Иикет. Ье роіепііеі ікегтокупатідие, р. 32.
Умовъ. Ж. Ф. X. О. 21 р. 103, 1889.
Шиллеръ. Б. А. 5 р. 326, 1901.
Сіаивіив. Ро&§. Апп. 101 р. 338, 1857.
Аггкепіиз. 2ізскг. 1. ркуз. Скетіе 1 р. 631, 1887; 3 р. 115, 1889.
Ріапск. 2ізскг. к ркуз. Скетіе 1 р. 577, 1887.
Ѵап’і Но//. 2ізскг. Г. ркуз. Скетіе 1 р. 481, 1887.
Р/е//ег. Озтоіізске Ипіегзискип&еп. Ьеіргі^, 1877.
Сатеііеу апб А. Ткотзоп. Лоигп. Скет. 8ос. 1888 р. 782.
Вальденъ. 2ізскг. к ркуз. Скет. 55 р. 683, 1906; 61 р. 633, 1908.
Ь. Непгу. С. В. 99 р. 1157, 1884.
Ье Скаіеііег. С. В. 100 р. 441, 1885.
Ѵап’і Но//. Агсіі. пёегі. 20 р. 53, 1886.
Ье Скаіеііег. Веск. ехр. еі іііёог. зиг Іез ёдиіі. скіт. р. 138, Рагіз, 1888.
Ёіапі. С. В. 108 р. 176, 1889.
Ѵаікег. 2ізскг. Г. ркуз. Скетіе 5 р. 193, 1890.
Къ § 6.
Рикет. Л. бе ркуз. (2) 6 р. 397, 1887.
Грузинцевъ. Сообіц. Харьк. Мат. Общ. 4, 1884.
Роупііщг. ркіі. Мар:. (5) 42 р. 289, 1896.
Негпзі. 2ізскг. Г. ркуз. Скетіе. 2 р. 613, 1888.
8ске//ег. 2ізскг. к ркуз. Скетіе 2 р. 390, 1888.
Къ § 7.
Ткотзеп. Ткегтоскетізске Бпіегзискип^еп 3, Ьеіргі^, 1883.
Лугининъ. С. В. 86 р. 1393, 1878.
Хрущовъ. С. В. 89, 1879.
Вегікеіоі. С. В. 73 р. 672, 1871; 77 р. 26, 1873; 80 р. 512, 1875; 85 р. 9, 1877;
87 р. 574, 1878; 88 р. 716, 1879; 91 р. 1025, 1880; 93 р. 214, 1881; Апп. скіт. еі ркуз.
(5) 10 р. 389, 1877; Мёс. скіт. 1 р. 545, 1879.
Вегікеіоі еі Зоип^/Іеізск. С. В. 78 р. 711, 1874.
Раѵге еі Ѵаізоп. С. В. 74 р. 1156, 1872
8аЬаііег. С. В. 89 р. 43, 1879; 91 р. 42, 1880.
Могшее. С. В. 86 р. 1445, 1878.
Зоаппіз. С. В. 92 р. 1338, 1881.
48*
756
Равновѣсіе соприкасающихся веществъ.
Саібегоп. С. К. 85 р. 149, 1877. *
Ѵагіі Но//. Коп&І. 8ѵ. Ѵеі. Акай. Напді. 21 № 17 р. 13.
Еѵап. Хіескг. Г. ркуе. Скет. 14 р. 418, 1894.
Реіег8еп. Хіескг. 1. ркуе. Скет. 11р. 174, 1892.
РіѵаІ8. Хізскг. Г. ркуе. Скет. 24 р. 608, 1897.
Штакельбергъ. Хіескг. Г. ркуе. Скет. 20 р. 159, 1896; 26 р. 533, 1898.
Рег8оп. Апп. скіт. еі ркуз. (3) 33 р, 449, 1851.
ѴѴіпкеІтапп. Ро^ё- Апп. 149 р. 1, 1873.
8іаиЬ. Біее. 2іігіск. 1890.
8скоІг. АѴ. А. 45 р. 193, 1892.
Риебог/. Ро^. Апп. 122 р. 337, 1864; 136 р. 276, 1869; Апп. скіт. еі ркуе. (4)
3 р. 496, 1864.
Напатапп. Віп&І. «Іоигп. 173 р. 314, 1864.
Могііх. Скет. Хеііпп^ 6 II, р. 1374, 1882; Скет. Сепіг.-ВІаіі (3) 14 р. 95, 1883.
Р/аипбІег. АѴіеп. Вег. 71. II р. 509, 1875.
ТоШп^ег. АѴіеп. Вег. 72, II р. 535, 1875.
Наттегі. АѴіеп. Вег. 78, II р. 59, 1878.
Яшег^ег. Скег Каііетіескип&еп, Мипскеп, 1881.
КігсННо//. Роёё- Апп. 103 р. 177, 1858; 104 р. 612, 1858; Сее. Аккапді. р. 454.
Шиллеръ. Ж. Ф. X. О. 30 р. 160, 1898; 31 р. 93, 1899.
Валъденъ. Хіескг. I. ркуе. Скет. 58 р. 479, 1907; 59 р. 192, 1907.
Оиргё. Ргос. В. 8ос. 20 р. 336, 1872.
Ви88у еі Виі^пеі. Апп. скіт. еі ркуз. (4) 4 р. 5, 1865.
ОиіЪгіе. Ркіі. Ма^. (4) 18 р. 495, 1884.
ЫпёЬагрег. Ркуе. Кеѵ. 3 р. 418, 1896.
Къ § 8 и § 9.
ОиІбЬег^ ипб Ѵ^аа^е. «Іоигп. I. ргасі. Скет. (2) 19 р. 69, 1879; Еіидее еиг 1е&
айіпііёе скітідиее, Скіеііапіа, 1867.
Рагабау. Апп. скіт. еі ркуз. 20 р. 324, 1822.
Сгі//ИН8. Ро&&. Апп. 2 р. 227, 1824; Лоигп. оі 8сіепсе 78 р. 90.
Ье^гапб. Апп. скіт. еі ркуз. (2) 53 р. 423, 1833; 59 р. 423, 1835; «Іоигп. рг. Ск.
6 р. 56, 1835; Роёё- Апп. 37 р. 379, 1836.
ВаЬо. ЁЬег сііе 8раппкгаіі дез ЛѴаееегсІатрІее іп 8аІ2Ібзип^еп, РгеіЬиг^. 1847.
УХ/иеІІпег. Ро&&. Апп. 103 р. 529, 1858; 105 р. 85, 1858; 110 р. 564, 1860.
Таттапп. \Ѵ. А. 24 р. 523, 1885; 36 р. 692, 1889.
СШишІб. Ьекгкиск дег аіі^етеіпеп Сііетіе 1 р. 709, Ьеіргщ, 1891.
РаисИоп. С. К. 89 р. 752, 1879.
Етбеп. АѴ. А. 31 р. 145, 1887.
8с1гие11ег. Рго^г. <1. Каізег Кагі Ѳутпае. ги Аасііеп, 1890, 1891
Мо8ег. АѴ. А. 14 р. 72, 1881.
Иісоі. Ркіі. Ма&. (5) 22 р. 502, 1886.
Оіеіегісі. АѴ. А. 42 р. 513, 1891; 50 р. 47, 1892.
Вгетег. Кес. Тгаѵ. Рауе Ваз 6 р. 122, 1887.
Р. Неіткоііх. АѴ. А. 27 р. 568, 1886.
Ѵ/аІкег. Хіескг. I. ркуз. Сііетіе 2 р. 602, 1888.
Раоиіі. С. К. 103 р. 1125, 1886; 104 р. 976, 1430, 1887; 107 р. 442, 1888; Хіесііг.
Г. ркуе. Сііетіе 2 р. 353, 1888; Апп. скіт. еі рііуз. (6) 15 р. 375, 1888.
Весктапп. Хіескг. I. ркуз. Сііетіе 4 р. 532, 1889; 5 р. 76, 1890; 8 р. 223, 1891.
ЧРіІІ ипб Вгебі^. Скет. Вег. 22 р. 1084, 1889.
Таттапп. Мёт. сіе ГАсад. де 8і.-РеіегеЪ. 35 № 9, 1887.
Рат8ау. Лоигп. Скет. 8ос. 1889 р. 521
Кгетегз. Ро§^. Апп. 97 р. 19, 1856.
Ма%пи8. Роёё- Апп. 112 р. 404, 1861.
Литература.
757
ОегІасН. 2еіізсЬг. Г. апаіуі. СЬетіе 26 р. 413, 1887.
Турбаба. Отчетъ о засѣд. 06. Физ.-Хим. Наукъ при Харьк. Унив. 1895, № 6.
Ѵап'і Но//. 2ізсЬг. Г. рііуз. Сііешіе 1 р. 481. 1887.
Аггкепіиз. 2ізсЬг. Г. рііуз. Сііешіе 3 р. 115, 1889.
Иоуез ипб АЬЬоі. 2ізсЬг. Г. рііуз. СЬетіе 23 р. 56, 1897.
Адашевъ. КесЬегсІіез зиг Іа (Ііззоі. тиі. сіез ИфіЫез. Мозсои. 1857
Ма^пив. Ро&&. Апп. 38 р. 488, 1836.
Ке^паиіі. Кеі. сіез Ехрег. 2 р. 715; Ро§&. Апп. 93 р. 537, 1854.
Ѵкиеііпег. Ро&§. Апп. 129 р. 353, 1866.
Коноваловъ. Ж. Ф. X. О. 16. Отд. Хим. р. 10, 1884; АѴ. А. 14 р. 48, 219, 1881.
Ріапск. 2ізсЬг. Г. рііуз. СЬетіе 2 р. 405, 1888; АѴ. А. 32 р. 489, 1887.
ѴѴІпкеІтапп. АѴ. А. 39 р. 1, 1890.
Иетзі. 2ізс1іг. 1. рЬуз. СЬетіе 8 р. 1, 1891.
Віиетске. 2ізсЬг. Г. рЬуз. СЬетіе 6 р. 153, 1890.
СегЬег. 2изаттепзеігип§ сіез ВатрГез ѵоп Еіиззі^кеііз^етізсііеп. Візз. АѴоІіеп-
Ьиііеі, 1892.
Къ § 10.
Віа&іеп. РЫІ. Тгапз. 78 р. 143, 277, 311, 1788.
Сорреі. Апп. сЫт. еі рЬуз. (4) 23 р. 366, 1871 ; 25 р. 502, 1872; 26 р. 98, 1872.
Киесіог/. Ро^§\ Апп. 114 р. 63, 1861; 116 р. 55, 1862; 145 р. 599, 1871 ; Ап. сЫт.
еі рЬуз. (4) 17 р. 480, 1869.
Раоиіі. С. К. 94 р. 1517, 1882; 95 р. 10», 1030, 1882; 101 р. 1056, 1885; Апп.
сЫт. еі рЬуз. (5) 28 р. 137, 1883; (6) 2 р. 66, 1884; 4 р. 401, 1885, 8 р. 289, 1886;
9 р. 93, 1886; 2ізсЬг. Г. рЬуз. СЬетіе 2 р. 488, 1888; 9 р. 343, 1892; 20 р. 601, 1896.
Ропзоі. См. къ § 2.
Ноііетапп. СЬет. Вег. 21 р. 8б0, 1888.
Аиѵегз. СЬет. Вег. 21 р. 536, 701, 1888.
Еуктапп. 2ізсЬг. 1. рЬуз. СЬетіе 2 р. 964, 1888; 3 р. 203, 1889; 4 р. 517. 1889.
ЕаЫпуі. 2ізсЬг. Г. рііуз. СЬетіе 2 р. 964, 1888 ; 3 р. 38, 1889.
Клобуковъ. 2ІЗСІ1Г. Г. рЬуз. СЬетіе 4 р. 10, 1889.
Весктапп. 2ізсЬг. Г. рііуз. СЬетіе 2 р. 639, 1888.
Р/аипсНег ипб Всігпе^. АѴіеп. Вег. 71, 1875.
Рісіеі. С. К. 119 р. 642, 1894.
ННІтауг. АѴіеп. Вег. 106 р. 5, 1897.
Но//. 2ізсЬг. Г. рііуз. СЬетіе 1 р. 481, 1887.
Катвау. 2ізсЬг. Г. рЬуз. СЬетіе 5 р. 222, 1890.
АЬе&>. 2ізсЬг. Г. рЬуз. СЬетіе 15 р. 209, 1894; 20 р. 207, 1896; АѴ. А. 64
р. 486, 1898.
Ьоотіз. АѴ. А. 51 р. 500, 1894; 57 р. 495, 1896; 60 р. 523, 1897; РЬуз. Кеѵіелѵ 3
р. 270, 1896; 4 р. 274, 1897.
ѴѴШегтапп. 2еіізсЬг. Г. рііуз. СЬетіе 15 р. 337, 1894; 19 р. 63, 1896; РЫІ. Ма§.
(5) 44 р. 459, 1897.
Неусоск апсі Иеѵіііе. «Іоигп. СЬет. 8ос. 1889 р. 666; 1890 р. 376.
ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ.
Дбсолютная влажность 629, — темпера-
тура кипѣнія 665, — шкала температуръ
423.
Абсолютное равновѣсіе системы 706.
Адіабата 397.
Адіабатическій процессъ 397.
Адіабатическое измѣненіе состоянія тѣлъ
470, — жидкости и пара 557.
Акустическій термометръ 59.
Атомная теплоемкость 156.
Виріалъ 444.
Влажность 629.
Водяной эквивалентъ 156.
Вредное пространство (термометра) 20.
Второе начало термодинамики 359, 409,
420, 425, 435.
Вѣсовой дилатометръ 111, — термо-
метръ 47.
Газовый термометръ 18, 19, 21, 23, 463.
Гигрометрія 629.
Гигрометръ 630, — ИапіеІГя 632, —
Ке^паиИ 632, — АПиапГа 633, — Сгоѵа
633, — Заиззиге’а 634.
Гигроскопъ 630.
Градусъ 7.
Графическія изображенія 396.
Давленіе внутреннее 430, — лучистой
энергіи 477, — критическое 673, — при-
веденное 685.
Двойной обмѣнъ въ растворахъ 733.
Джу ль 157.
Диваріантная система 706.
Дилатографъ 517.
Дилатометръ 111, — Озідѵаіб’а 111.
Дисгрегація 414.
Диссоціація 575, — водныхъ растворовъ
электролитовъ 719.
Дифференціальный дензиметръ 676.
Диффузія газовъ 457, — слабыхъ ра-
створовъ 723
Единица количества теплоты механиче-
ская (теоретическая) 2, 12, 157, 165, —
практическая (калорія) 12, 13, 157, — тер-
мометрическая 165.
Законъ Авенаріуса (электродвижущая си-
ла) 49,—Ииіоп^’а и Реііі (теплоемкость) 227.
— Иеигпапп а (теплоемкость химическихъ
соединеній) 233, — Лоиіе’я и Корр’а (мо-
лекулярная теплоемкость) 235, — Незз’а
(термохимическій) 258, — термонейтраль-
ности соляныхъ растворовъ 268, — ВегіЬе-
Іоі (принципъ наибольшей работы) 271,—
Ньютона (охлажденіе) 276, — Ииіоп^’а и
Реііі (охлажденіе) 277, — преломленія изо-
термъ 298, — Бойль-Маріотта 449, — Гей-
Люссака 449, — Лоиіе’я 449, — ВиеЬгіп^’а
(упругость насыщенныхъ паровъ) 597, —
параболы (плотность насыщенныхъ паровъ)
617, — Иаііоп’а (упругость насыщенныхъ
паровъ) 625, — Страуса (критическая
температура) 682, — затвердѣваніе ра-
створовъ 748.
Законы соотвѣтственныхъ состояній
686—690.
Законы КаоиІГя 737.
Затвердѣваніе растворовъ 748.
Затраченная теплота 406.
Идеальные газы 448.
Изентропическій процессъ 348, 434
Измѣреніе температуры 6.
Изобара 398.
Изопикна 363.
Изопіеста 668.
Изотерма 247, 397, — физическая 656,
— теоретическая 656.
Изотермическій процессъ 397.
Предметный указатель.
75к>
Изотермическая поверхность 296.
Изотермическое измѣненіе состоянія
смѣси жидкости и пара 556.
Изохора 652.
Изэнергета 398.
Испареніе 520, — твердыхъ тѣлъ 570.
Истинная теплоемкость 156, 349, 467.
Источники теплоты 14, 248.
Калибрированіе термометровъ 26, 32,—
способы Сау-Ьиззас’а 33, — способъ Наіі-
8ІгоепГа 36.
Калориметрическая бомба 265.
Калориметрія 155.
Калориметръ 155. — Германа и Випзеп а
(ледяной) 167, — Раѵге’а и 8і1Ьегтапп’а
(ртутный) 171, — Ке^папіі 173, — Луги-
нина 175, — Гезехуса (воздушный) 177,
— Випзеп’а (паровой4 187.
Калорія большая 13, 157, — малая 13,
157.
Каноническое уравненіе состоянія 663.
Кипѣніе 524.
Коэффиціентъ температурный 9, — рас-
ширенія 11, 80, — внутренняго давленія
(въ термометрѣ) 39, — внѣшняго давленія
(въ термометрѣ) 39, — термическій дав-
ленія воды 112, — внѣшней теплопровод-
ности 276, — внутренней теплопровод-
ности 243, — экономическій кругового
процесса 407, — диффузіи 724.
Компараторъ 23.
Конвекція 274.
Концентрація 714.
Кривая плавленія 508.
Критическая температура 665. 671. 673.
Критическій объемъ 665, 678.
Критическое давленіе 665, 678.
Критическое состояніе 665, — смѣсей
682.
Кріогидратная температура 703.
Кріогидратная точка 712.
Кріогидраты 701.
Круговой процессъ 395, — Карно 407.
Линія выдѣленія соли (насыщенія ра-
створа солью) 701.
Мегаэргъ 157.
Мельдометръ 56.
Металлическій термометръ Вге^иеі 51. ,
Методы опредѣленія коэффиціентовъ
расширенія твердыхъ тѣлъ 82—90, —
кристалловъ 98—101, жидкостей 101—116,
— газовъ 135—145.
Методы опредѣленія механическаго эк-
вивалента теплоты 363—376.
Методы опредѣленія теплопроводности
твердыхъ тѣлъ 308—325, — жидкостей
331—337, — газовъ 339—345.
Методы опредѣленія упругости насы-
щенныхъ паровъ 583, 584.
Механическая теорія тепла 359.
Механическій эквивалентъ теплоты 160:
362.
Молекулярная теплоемкость 208.
Моноваріантная система 706.
Мраморный пирометръ 55.
Нагрѣватель 398.
Нонваріантная система 706.
Независимыя вещества 705.
Насыщенные пары 642.
Необратимый процессъ 384.
Несвободная энергія 440.
Обратимый процессъ 384, — круговой
395, — изотермическій 397, — адіабатиче-
скій (изентропическій) 398. 434.
Ожиженіе 520.
Опалесценція 682.
Оптическая пирометрія 59.
Ортометрическая точка 654.
Осмотическое давленіе 720, 723.
Относительная влажность 629.
Охладитель 398.
Охлажденіе 278, — твердыхъ тѣлъ въ
жидкостяхъ 285.
Паденіе температуры 292.
Параметръ 384.
Парціальный процессъ 389.
Первое начало термодинамики 360, 404.
Первое основное уравненіе термодина-
мики 404.
Перенесённая теплота 406.
Переохлажденіе 493.
Регрешит тоѣііе перваго рода 360, —
второго рода 420.
Пирометръ 52, — абсорбціонный 63, —
ртутный 52, — газовый 53, — платино-
вый 57, — термоэлектрическій 67.
Плавленіе 483.
Плотность насыщенныхъ паровъ 608,
610, — ненасыщенныхъ паровъ 645.
Поверхностное натяженіе 464.
Полезно затраченная теплота 406.
Политропа 398.
Поправка термометра 16.
Поправки ртутнаго термометра 35, 39,40.
Постулатъ Сіаизіиз’а 411, — \Ѵ. Тѣош-
зоп’а 420.
Правило фазъ 704.
Превращенія 407, — положительныя
760
Предметный указатель.
{естественныя) 412, — отрицательныя (не-
естественныя) 41’2.
Приведенная температура 9, 685.
Приведенное давленіе 685.
Приведенное уравненіе состоянія 685.
Приведенный объемъ 685.
Приниженіе основныхъ точекъ термо-
метра 38.
Психрометръ 630, 635, — Ап^изі а 635,
— пращевой 636.
Равновѣсіе системы 442, — физическое
385.
Радіометръ 251.
Разсѣяніе теплоты 420, — энергіи 421.
Растворимость 719.
Растяженіе твердыхъ тѣлъ 473.
Реальные газы 458.
Рекалесценція 275.
Реперы 6.
Ролэндъ 165.
Ртутные термометры 28.
Свободная энергія 438.
Сгущеніе газовъ 558.
Система тѣлъ 384, — диваріантная 706,
— моноваріантная 706, — кватернарная
714.
Скорость охлажденія 277, 286.
Скрытая теплота 402, — измѣненія да-
вленія 403, — расширенія 403, — пла-
вленія 510, — плавленія льда 513, — алло- ।
тропическаго превращенія 514, — испа-
ренія 523, 532, — кипѣнія 524.
Соотвѣтственныя состоянія 685.
Способы измѣренія температуры 49.
Способы опредѣленія влажности 630 —
—635, — плотности и удѣльнаго объема
насыщенныхъ паровъ 610—616, — скрытой
теплоты испаренія 534.
Способы опредѣленія критической тем-
пературы 674—676, — критическаго да-
вленія 677, — критическаго объема 678.
Способы опредѣленія теплоемкости твер-
дыхъ и жидкихъ тѣлъ 166—190.
Сплавъ 490, — КоЬегіз-Аизіеп’а 491. —
Козе 492, — Б’Агсеі 492, — ХѴоод’а 492,
— Ьіррохѵііг’а 492.
Средняя теплоемкость 13.
Статистическій методъ 393.
Сфероидальное состояніе 540.
Температура 5, — пустоты 8, — лучи-
стой энергіи 8, — приведенная 9, 685, —
черная 61, — критическая 665, 671, 673,
— кріогидратная 703.
Температурная шкала 6, 66.
Температурное состояніе тѣла 290.
Температурный коэффиціентъ 9.
Температурный скачокъ на границѣ двухъ
тѣлъ 350
Теорема Карно 410, 413.
Теорія слабыхъ растворовъ 714
Тепловая энергія 1.
Тепловое движеніе частицъ 3
Тепловой потокъ 295.
Теплоемкость 155, — атомная 156, —
молекулярная 156, — истинная 156, 467,
— воды 158, — твердыхъ и жидкихъ ве-
ществъ 190, 468, — сплавовъ 197, — ра-
створовъ 198, — газовъ 199, — газовъ
при постоянномъ давленіи 202, — газовъ
при постоянномъ объемѣ 211, - насы-
щенныхъ паровъ 619, 625, — ненасыщен-
ныхъ паровъ 643.
Теплопроводность 288, — внутренняя
289, — внѣшняя 295, — математическая
теорія 290. — твердыхъ тѣлъ 308, 317, —
анизотропныхъ тѣлъ 327, — жидкостей
331, — газовъ 338.
Теплота растворенія 719, 725—732, —
разбавленія 729.
Термическое послѣдѣйствіе 27.
Термографъ 52.
Термодинамика 358.
Термодинамическая поверхность 657.
Термодинамическій потенціалъ 438.
Термокалориметръ 187.
Термометрическая единица теплоты 165.
Термометрическая шкала 6.
Термо?»:етрія 15.
Термометръ 15, — нормальный 17, —
газовый 18, — газовый Ке^паиіі 19, —
газовый СЬарриіз 21, — дифференціаль-
ный 25, — съ жидкостями 25. — ртутный
28, — съ укороченною шкалою 44, —
ХѴайегсІіп’а 45, — максимумъ и минимумъ
46, — медицинскій 47, — вѣсовой 47, — ме-
таллическій Вге^иеГа 51,—акустическій 59.
Терморегуляторъ 72.
Термоскопъ 49—51.
Термостатъ 42, 72.
Термохимическія явленія 256
Термохимія 256.
Термъ 165.
Тонометрія 739.
Точка кипѣнія 524, — плавленія 485, —
плавленія сплавовъ 490.
Тройная точка 707.
Удѣльный объемъ насыщенныхъ паровъ
608, 610.
Предметный указатель.
761
Упругость назыщенныхъ паровъ 582,
584, 588, 591, 596, 604, — ненасыщенныхъ
паровъ, 645, — пара растворовъ 735—741,
— пара смѣсей жидкостей 745.
Уравненіе состоянія 382, 461, 657,
660—663.
Фаза 483, 704.
Функція состоянія 382.
Циклъ Карно 407.
Цѣнность энергіи 421.
Четырехкратная точка 710.
Чувствительность термометра 17.
Шкала температурная 7, — абсолютная
Томсоновская 7, — Цельсія 7
Эвтектическая смѣсь 703.
Эвтектическій сплавъ 491.
Эквивалентъ превращенія 415.
Экзотермическая реакція 258.
Экономическій коэффиціентъ кругового
процесса 407.
Эндотермическая реакція 258.
Энергетика 359.
Энергія 359, — кинетическая 1, 250,
— лучистая 1, 251,— поверхностная 466,
потенціальная 1, 253, — тепловая 1, 2, —
упруго измѣненнаго тѣла 1, — электри-
ческаго тока 252, — электрическаго за-
ряда 255, — молекулярная 255, — интра-
атомная 256, — свободная 438, — несвобод-
ная 440, — твердыхъ и жидкихъ тѣлъ
467, — смѣси жидкости и пара 555.
Энтропія 432, — газовъ 455, — твер-
дыхъ и жидкихъ тѣлъ 467, — смѣси жид-
кости и пара 555.
Эргъ 157.
УКАЗАТЕЛЬ РУССКИХЪ АВТОРОВЪ.
Абельсъ. Теплопроводность снѣга 326.
Авенаріусъ. Законъ 49, расширеніе жид-
костей 128, критическое состояніе 669, 681.
Адашевъ. Смѣси жидкостей 745.
Алексѣевъ. Смѣси жидкостей 745.
Андреевъ. Расширеніе ожиженныхъ га-
зовъ 125.
Бахметьевъ и Въжаровъ. Плавленіе
сплавовъ и амальгамъ 492.
Бачинскій. Ортометрическая точка 654.
Бекетовъ, Н. Н. Теплоемкость пал-
ладія 197.
Биронъ. Потеря тепла калориметромъ
184, теплоемкость 190, теплоемкость ра-
створовъ 198, 199.
Богаевскій. Упругость насыщенныхъ
паровъ 604, критическая температура 674,
соотвѣтственныя состоянія 682.
Богородскій. Кріогидраты 703.
Богоявленскій. Теплоемкость органи-
ческихъ веществъ 195, скрытая теплота
плавленія льда 513.
Булатовъ. Критическая температура 682.
Вальденъ.^ Кипѣніе 528, 529, раство-
римость 721, точка кипѣнія растворовъ 740.
Васильева. Теплопроводность газовыхъ
смѣсей 349.
Воейковъ. Теплопроводность снѣга 326.
Вревскій. Теплоемкость растворовъ 198.
Въжаровъ и Бахметьевъ. См. Бах-
метьевъ и Въжаровъ.
Гадолинъ. Удѣльная теплота 157.
Гезехусъ, Н. А. Воздушный калори-
метръ 177, сравненіе теплопроводности
(приборъ) 312, сфероидальное состояніе
531, 532, психрометръ 636.
Георгіевскій. Теплопроводность 325.
Германъ. Ледяной калориметръ 168.
Гнузинъ. Упругость водяныхъ паровъ
Голицынъ. Термостатъ 74, охлажденіе
тѣлъ 284, свободная энергія 438, упру-
гость насыщенныхъ паровъ 606, законъ
Ваііоп’а 628, критическая температура 675.
Гольдгаммеръ, Д. А. Термодинамиче-
ская поверхность 615, 657.
Горбовъ. Правило фазъ 704.
Грузинцевъ. Осмотическое давленіе 724.
Динникъ. Предѣлъ упругости метал-
ловъ 476.
Дьячевскій. Критическое состояніе 635.
Жуковъ и Курбатовъ. Точка плавле-
нія 486.
Жукъ. Критическое состояніе 681.
Зайончевскій. Упругость насыщенныхъ
паровъ 598, критическая температура 670.
Зворыкинъ. Теорія психрометра 635.
Зиловъ. Соотвѣтственныя состоянія
686.
Калнинъ и Центнершверъ. Критиче-
ское состояніе 684.
Каннегиссеръ. Критическое состояніе
681.
Кистяковскій. - Уупругость насыщен-
ныхъ паровъ 608.
Клобуковъ. Затвердѣваніе растворовъ
750.
Коловратъ-Червинскій. Термостатъ 74,
температурный скачокъ на границѣ жид-
костей 351.
Коноваловъ, Д. П. Теплоемкость 190,
теплоемкость растворовъ 198, формула
Ѵап бег \Ѵаа1з’а 657, опалесценція 683,
правило фазъ 705, смѣси жидкостей 745,
746.
Котовичъ. Теплоемкость газовыхь смѣ-
сей 230.
Указатель русскихъ авторовъ.
763
Краевичъ. Упругссгь насыщенныхъ па-
ровъ 603.
Красильникъ. Термостатъ 73.
Курбатовъ. Теплоемкость жидкостей 196,
скрытая теплота испаренія 547, правило
Тгопіоп’а, соотвѣтственныя состоянія 687.
Курбатовъ и Жуковъ. См. Жуковъ
и Курбатовъ.
Курнаковъ. Плавленіе сплавовъ 491.
Курнаковъ и Путинъ. Сплавы 492.
Курчинскій. Термостатъ 73.
Лазаревъ. Температурный скачекъ на
границѣ тѣлъ 352.
Ландезенъ. Расширеніе воды 119,122,
расширеніе растворовъ 121.
Лачиновъ. Опытъ ТупсіаІГя 167.
Лебедевъ, И. Водородный термо-
метръ 21.
Лебедевъ, П. Плотность каучука 93.
Ленцъ, Р. Наибольшая плотность воды
114, расширеніе растворовъ 115.
Ленцъ, Р. и Рѣзцовъ, Н. Расширеніе
морской воды 121.
Лермантовъ, В. В. Калибрированіе
термометровъ 36.
Лугининъ, В. Ф. Толуоловый термо-
метръ 46, ледяной калориметръ 171, кало-
риметръ 175, калориметрическая бомба 266,
расширеніе жидкостей 124, теплоемкость
171, теплопроводность дерева 331, скры-
тая теплота испаренія 540, 543, правило
Тгопіоп’а, теплота растворенія 727.
Лугининъ, В. Ф. и Щукаревъ, А. Н.
Калориметрія 155, теплота образованія
сплавовъ 268.
Марковниковъ. Точка плавленія 487.
Менделѣевъ, Д. И. Расширеніе воз-
духа 142, расширеніе жидкостей (формула)
127, расширеніе ртути 108, критическое
состояніе 665, 670.
Михельсонъ, В. А. Оптическая паро-
метрія 64.
Надеждинъ. Формула Ѵап йег ѴѴааІз’а
657, дифференціальный дензиметръ 676.
Огнянниковъ. Термостатъ 73.
Павлевскій. Точка кипѣнія 525, крити-
ческое состояніе 681.
- Пакалнетъ и Центнершверъ. Крити-
ческое состояніе 684.
Петрушевскій, Ѳ. Ѳ. Сравненіе теп-
лопроводностей 312, 337.
Пильчиковъ. Свободная энергія 438.
Писаржевскій и Танатаръ. Термохи-
мическія изслѣдованія 270.
Поповъ, А. С. Опытъ Тгеѵеііап’а 309.
Посальскій, Т. П. Диссоціація 575,
равновѣсіе соприкасающихся массъ 700.
Потылицынъ. Точка плавленія 486
Преображенскій, В. Дифференціаль-
ный воздушный калориметръ 178.
Путинъ. Сплавы 492, вліяніе давленія
на точку плавленія 508.
Путинъ и Курнаковъ. См. Курна-
ковъ и Путинъ.
Рихманъ. Способъ смѣшенія 173,
Роговскій. Температурный скачокъ на
границѣ тѣлъ 351.
Рѣзцовъ и Ленцъ см. Ленцъ и Рѣз-
цовъ.
Сапожниковъ. Сплавы органическихъ
веществъ 493.
Селивановъ. Расширеніе платины 56.
Слугиновъ, Н. Теплопроводность жид-
костей 337.
Солонина. Точка плавленія 487.
Сонинъ, Н. Я. Формула Ѵап сіег АѴааІз’а
621, соотвѣтственныя состоянія 691.
Срезневскій. Скорость испаренія 522.
Станкевичъ, В. В. Теплопроводность
органическихъ жидкостей 336.
Столѣтовъ. Уравненіе состоянія 660.
Критическое состояніе 679. Соотвѣтствен-
ныя состоянія 686.
Страусъ. Критическое состояніе 682.
Танатаръ и Писаржевскій. См. Пи-
саржевскій и Танатаръ.
Терешинъ, С. Я. Способъ охлажденія
187, охлажденіе тѣлъ 283.
Турбаба. Растворы 741.
Умовъ. Свободная энергія 438, сла-
бые растворы 719.
Федоровъ. Расширеніе кристалловъ
101.
Хвольсонъ, О. Д. Сравненіе теплопро-
водностей (приборъ) 312, зависимость те-
плопроводности отъ температуры 324.
Хрущевъ. Теплота растворенія 727.
Центнершверъ. Критическое состоя-
ніе 681, 684.
Центнершверъ и Калнинъ. См. Кал-
нинъ и Центнершверъ.
Центнершверъ и Пакалнетъ. См. Па-
калнетъ и Центнершверъ.
Цингеръ, А. и Щегляевъ, И. Тепло-
емкость твердыхъ тѣлъ 191.
Шиллеръ, Н. Н. Температура 6, сво-
бодная энергія 438, расширеніе газовъ 461,
764
Указатель иностранныхъ авторовъ
реальные газы 461, упругость насыщен-
ныхъ паровъ 608, уравненіе состоянія 662,
слабые растворы 719, теплота растворенія
и разбавленія 729.
Штакельбергъ, Э. Теплота растворе-
нія 727.
Щегляевъ и Цингеръ. См. Цингеръ
и Щегляевъ.
Щукаревъ. Паровой калориметръ 187.
Щукаревъ и Лугининъ. См. Лугининъ
и Щукаревъ.
УКАЗАТЕЛЬ ИНОСТРАННЫХЪ АВТОРОВЪ.
АЬЬе. Коэффиціентъ расширенія (при-
боръ) 89.
АЬЬе и Веной. Коэффиціентъ расши-
ренія 87.
АсЬагсі. Точка кипѣнія 526.
Абаш. Поправка на выступающій стол-
бикъ 41.
Агііег. Теплоемкость 194.
Асіуѵепіоѵѵзку. Коэффиціентъ расши-
ренія 143.
Аіте. Диссоціація газовъ 575.
Айкеп. Пересыщенные пары 674
АПеп. Испареніе камфоры 570.
АПеп и Бау. Пирометръ 70.
Аііиагсі. Гигрометръ 638.
АП. Скрытая теплота испаренія ожи-
женныхъ газовъ 546.
АЙ8сЬи1. Критическое давленіе 678.
Ата^аі. Расширеніе воды 122, 124,
расширеніе газовъ 147, 148, теплоемкость
газовъ 214, внутреннее давленіе 431, влія-
ніе давленія на точку плавленія 505, 508,
упругость насыщенныхъ паровъ 584, плот-
ность насыщенныхъ паровъ 616, ненасы-
щенные пары 645, 646, 649. 650, формула
Ѵап сіег АѴааІз’а 654, уравненіе состоянія
661, соотвѣтственныя состоянія 691.
Атаигу и Іатіп. Теплоемкость воды 159.
Ате$. Теплоемкость воды 161, 162,
скрытая теплота испаренія воды 540.
Апбгеае. Термостатъ 73.
Апсіге\ѵ8. Расширеніе газовъ 146, 147,
измѣреніе теплоты горѣнія 264, теплопро-
водность газовъ 341, теплоемкость жид-
костей 189, 190, скрытая теплота испаренія
535, упругость насыщенныхъ паровъ 684,
формула Ѵап бег ХѴааІз’а 553, уравненіе
состоянія 662, критическое состояніе 665,
критическая температура 674.
Ап§оі. Психрометръ 636.
Ап^БІгоеш. Методъ опредѣленія тепло-
проводности 321, теплопроводность 7/^332.
Ап$(1е11. Сгущеніе газовъ 561, упру-
гость насыщенныхъ паровъ 596.
Апіоіпе. Упругость насыщенныхъ па-
ровъ 604, уравненіе состоянія 662.
АріоЬп. Теорія психрометра 635.
Арріеуагсі. Платиновый термометръ 58.
Аррой. Термоскопъ 56.
Ага§о и Ои1оп&. Упругость насыщен-
ныхъ паровъ 586, 587.
Агсіоуѵзкі. Испареніе камфоры 570.
Агопб. Измѣненіе объема при плавле-
ніи 496.
АггЬепіиз. Космогенетическая теорія
422, диссоціація водныхъ растворовъ 719.
АгхЬег^ег. Упругость насыщенныхъ па-
ровъ 585.
А88шапп и Миеііег. Теплоемкость га-
зовъ 222.
АиЬеІ. Теплоемкость сплавовъ 197, пла-
вленіе сплавовъ 491, скрытая теплота
испаренія 547.
Аи§и8І. Психрометръ 635.
Аіі8ііп и НоіЬогп. Зависимость тепло-
емкости газовъ отъ температуры 208.
ВаЬо. Растворы (законъ) 735.
Васкег. Теплота образованія сплавовъ
268.
Ваеуег. Точка плавленія 486.
Ваккег. Соотвѣтственныя состоянія 693.
Ваіу и СЬогІеу. Измѣреніе высокихъ
температуръ 46.
Ваіу и Кат8ау. Расширеніе разрѣжен-
ныхъ газовъ 144.
Вапсгой. Правило фазъ 705.
Вагкег. Испареніе твердыхъ тѣлъ 570,
571.
Указатель иностранныхъ авторовъ.
7б5
Вагпе§. Теплоемкость воды 162, плот-
ность льда 495.
Вагпез и Саііепсіаг. Теплоемкость во-
ды 161, 163, 164.
Вагпез и Сооке. Теплоемкость воды
166, теплоемкость ртути 196.
Вагіоіі. Теплоемкость жидкостей 196.
Вагіоіі и Зігассіаіі. Теплоемкость воды
161,163, 166, теплоемкость ртути 196, упру-
гость насыщенныхъ паровъ (формула) 549.
Ваги$. Термоэлектрическая пирометрія
69, вліяніе давленія на точку плавленія
507, упругость насыщенныхъ паровъ 594.
Ваіеііі. Измѣненіе объема при плавле-
ніи 497, вліяніе давленія на точку плавле-
нія 507, скрытая теплота плавленія 513,
упругость насыщенныхъ паровъ 584, 592,
593, 594, (формула) 607, плотность и удѣль-
ный объемъ насыщенныхъ паровъ 616,
ненасыщенные пары 647, 648, уравненіе
состоянія 662, критическое состояніе 674.
Ваіеііі и Магііпеііі. Сплавы органи-
ческихъ веществъ 493.
Вагіеііі и Раіаххо. Сплавы органиче-
скихъ веществъ 493.
Вангіаіп. Термометръ 46
ВаіиІгітопі. Сфероидальное состояніе
531.
Ваиег. Плотность и удѣльный вѣсъ
насыщенныхъ паровъ (способъ) 615.
Ваитйагіеп. Расширеніе растворовъ 121.
Ваит^агіпег. Теплоемкость воды 159.
Вауег. Точка плавленія 486.
Весктапп. Термометръ 46, растворы
741, затвердѣваніе растворовъ 753.
ВесцнегеП. Фотометрическая пироме-
трія 59. термоэлектрическій пирометръ 68.
Вёйе. Теплоемкость металловъ 192.
Векп. Теплоемкость воды 165, тепло-
емкость при низкихъ температурахъ 229,
аллотропическія превращенія 516, скрытая
теплота испаренія 543.
Векп и КіеЬііх. Измѣреніе низкихъ
температуръ 72.
Веііаіі и Котапезі. Аллотропическія
превращенія 515.
Вепой. Расширеніе кристалловъ 100,
расширеніе твердыхъ тѣлъ 88.
Вепоіі и АЪЪе. См. АЪЪе и Веной.
Вепіоп. Растяженіе твердыхъ тѣлъ 474.
Вегагд и Веіагоске. Теплоемкость га-
зовъ при постоянномъ давленіи 202
Вег^еі. Теплопроводность (методъ) 319,
теплопроводность 332.
ВегкепЬизск. Температура пламени Бун-
зеновской горѣлки 270.
Вегніні. Скрытая теплота плавленія 513.
Вегікеіоі. Термохимическія изслѣдова-
нія 263, 264, теплоемкость 178, теплоем-
кость элементовъ 240, измѣреніе темпера-
туры горѣнія 265, калориметрическая бомба
265, законъ (принципъ наибольшей работы)
271, скрытая теплота испаренія 534, со-
отвѣтственныя состоянія 697.
Вегікеіоі, В. Оптическая пирометрія
59, оптическій термометръ 50, расширеніе
жидкостей 127.
Вегікеіоі и Ѵіеіііе. Теплоемкость га-
зовъ 214.
Вегігапд. Упруюсть насыщенныхъ па-
ровъ (формулы) 600, 601, теплоемкость
насыщенныхъ паровъ 623, уравненіе со-
стоянія 662.
Вегігапгі и Ооиіііу. Уравненіе состо-
янія 662.
Вёіапсоигі. Упругость насыщенныхъ
паровъ 584.
Віііеі. Измѣненіе объема при плавле-
ніи 498.
Віп^кат. Скрытая теплота испаренія
598, соотвѣтственныя состоянія 689.
Віоі. Теплопроводность (способъ) 312,
упругость водяныхъ паровъ (формула) 598.
В]‘егкеп. Расширеніе каучука 92.
Віаск. Скрытая теплота испаренія во-
ды 534.
Віаск и Ткотвеп. Теплоемкость жид-
костей способъ) 190.
Віа^деп. Затвердѣваніе растворовъ 748.
ВІопсІІоі и \ѴагЬиг§. Упругость насы-
щенныхъ паровъ 607.
ВІиетке. Сгущеніе газовъ 502, урав-
неніе состоянія 660.
Воск. Упругость насыщенныхъ паровъ
607.
Восіепзіеіп. Термостатъ 73.
Воеііскег. Приниженіе нуля 39.
Воіігтапп. Теплоемкость 241, статисти-
ческій методъ 392, теплопроводность га-
зовъ 340, второе начало термодинамики
421, вѣроятность и энтропія 444
Вопівскедѵ. Атомная теплоемкость 230.
Вогда. Коэффиціентъ расширенія (ме-
тодъ) 85.
Во88ска. Теплоемкость воды 159, рас-
ширеніе ртути 108.
Воііотіеу. Вліяніе давленія на точку
766
Указатель иностранныхъ авторовъ.
плавленія 505, методъ жидкаго столба
332, теплопроводность газовъ 339.
Воиззіпезд. Охлажденіе твердыхъ тѣлъ
въ жидкостяхъ 285, 286.
Воиіі^пу. Сфероидальное состояніе 532.
Воуіе и Магіоііе. Законъ 449.
Вгаак. Ненасыщенные пары 649.
Вгайіеу и Наіе. Расширеніе воздуха 460.
Вгаип. Сравненіе пирометровъ 58, за-
конъ Оаііоп’а 627.
Вге^иеі. Металлическій термометръ 51.
ВгіІІ.У пру гость насыщенныхъ паровъбОЗ.
Вгіх. Скрытая теплота испаренія 534.
ВгосЬ. Расширеніе ртути 108, 109, упру-
гость насыщенныхъ паровъ (формула) 604.
Вгогѵп. Движеніе взвѣшенныхъ въ жид-
кости частицъ 422, скрытая теплота испа-
ренія 547.
Вгохмп и 8тііЬ. Скрытая теплота испа-
ренія (способъ) 536.
Вгиппег. Плотность льда 495, гигро-
метръ 631, критическое состояніе 670.
ВиН. Сфероидальное состояніе 531.
Виі^пеі и Виззу. Теплоемкость смѣ-
сей жидкостей 198.
Випзеп. Ледяной калориметръ 168, па-
ровой калориметръ 187, вліяніе давленія
на температуру плавленія 506, скрытая
теплота плавленія льда 513. теплоемкость
и молекулярный вѣсъ 228, термохимиче-
скія изслѣдованія 270.
Виг^езз. Точка плавленія 490.
Виг^ез и \Ѵаійпег. Пирометрія 58.
Виззу. Сгущеніе газовъ 559.
Виззу и Виі^пеі. См. Виі^пеі и Виззу.
Вихгоіа и Еиззапа. Плотность раство-
ровъ 115.
Вузігоеш. Теплоемкость металловъ 192.
Са^піагй йе Еаіоиг. Измѣреніе высо-
кихъ температуръ 59, критическое состоя-
ніе 665, критическая температура 675.
СаЬоигз. Ненасыщенные пары 649.
Саіііеіеі. Сгущеніе газовъ 560, 561,
упругость насыщенныхъ паровъ 596.
Саіііеіеі и Соіагйеаи. Упругость на-
сыщенныхъ паровъ воды 592, критическое
состояніе 676, 677.
Саіііеіеі и МаіЬіаз. Плотность и удѣль-
ный объемъ насыщенныхъ паровъ 615.
Саііепсіаг. Измѣреніе высокихъ тем-
пературъ 57, теплоемкость насыщенныхъ
паровъ 621.
Саііепсіаг и Вагпезз. См. Вагпезз и
СаПепйаг.
Сапіопе и Сопііпо. Расширеніе кау-
чука 93.
Сапіог. Теорія гигрометра 631.
Сарзііск. Теплоемкость газовъ 225.
Сагсіапі и Тотазіпі. Теплоемкость во-
ды 166.
Сагпагхі. Расширеніе 127.
Сагпеііеу. Испареніе льда 571.
Сагпеііеу и А. ТЬопізоп. Растворы
(правило) 720.
Сагпеііеу и АѴіПіагпз. Точка кипѣнія 525
Сагпоі, 8. Первое начало термодина-
мики 362, круговой процессъ 407, тео-
рема 410, второе начало термодинамики
410.
СаиЬеі. Критическое состояніе 682.
Сахіп. Теплоемкость газовъ 221, теп-
лоемкость насыщенныхъ паровь 622, 623.
СеІІіег. Теплопроводность 325.
СЬапіагсі. Измѣреніе высокихъ темпе-
ратуръ 59.
СЬарриіз. Опредѣленіе верхней точки
на шкалЬ термометра (приборъ) 30, толу-
оловый термометръ 46, газовый термо-
метръ 21, изготовленіе термометра 30,
сравненіе шкалъ термометровъ 43, 44,
плотность воды 117, 118, расширеніе га-
зовъ 148, скрытая теплота испаренія
546, 547.
СЬарриіз и Нагкег. Измѣреніе высо-
кихъ температуръ 58.
СЬарриіз и Наиіеіеиіііе. Сгущеніе га-
зовъ 562.
СЬаіІоск и Мііпег. Методъ жидкой
пленки 336
СЬагІеу и Ваіу. См. Ваіу и СЬагІеу.
СЬгее. Методъ жидкаго столба 332.
СЬгізііап. Упругость насыщенныхъ па-
ровъ 585.
СЬгізііапзеп. Охлажденіе 284, тепло-
проводность 325, методъ жидкой пленки
335, теплопроводность газовъ 345.
Сіпеііі и Могеііо. Плотность воды 114.
Сіареугоп. Графическія изображенія
396, скрытая теплота испаренія 558.
Сіаийе. Сгущеніе газовъ 568.
Сіаизіиз. Истинная теплоемкость 156,
467, расширеніе СО2 148, уравненіе со-
стоянія 135, 657, 658, 659, 660, 661, по-
стулатъ 411, второе начало термодина-
мики 443, теплопроводность газовъ 339,
механическій эквивалентъ теплоты 378,
первое начало термодинамики (формулы)
405, энтропія 435, дисгрегація 444, ви-
Указатель иностранныхъ авторовъ.
767
ріалъ 444. вліяніе давленія на точку пла-
вленія 503, скрытая теплота испаренія
558, упругость насыщенныхъ паровъ 609,
удѣльный объемъ насыщенныхъ паровъ 609,
теплоемкость насыщенныхъ паровъ 619,
620, соотвѣтственныя состоянія 686, фор-
мула Ѵап йег ХѴааІз’а 656, диссоціація вод-
ныхъ растворовъ 719.
Сіетепі и Вау. Точка плавленія 488.
Сіетепі и Везогтез. Теплоемкость га-
зовъ 216, 220, скрытая теплота испаренія
воды 535.
Сіоиеі и Моп^е. Сгущеніе газовъ
559.
Соіагсіеаи и Саіііеіеі. См. Саіііеіеі
и Соіагсіеаи.
Соісііп^* Основы термодинамики 362.
Соіешап. Термоскопъ 651.
Сотрап. Теплопроводность газовъ 349.
Сопгаи и №и^еЬаиег. Теплопровод-
ность газовъ 340.
Сопііпо и Сапіопе. См. Сапіопе и
Сопііпо.
Сооке и Вагпез. См. Вагпез и Сооке.
Сорреі. Плотность воды 113, плот-
ность растворовъ 115, затвердѣваніе ра-
створовъ 749.
Согіоііз. Упругость водяныхъ паровъ
598.
СгаТі. Кипѣніе (правило) 528.
Сгаііз. Измѣреніе высокихъ темпера-
туръ 55, постоянныя точки термометра 45
Сгаѵѵіогсі. Измѣреніе теплотъ горѣнія
254.
Сгі^Ьі и 8оиі1іегп. Скрытая теплота
испаренія воды (законъ) 535.
Сгоокез. Радіометръ 251, теплопровод-
ность газовъ 339.
Сгоѵа. Фотометрическая пирометрія 60,
гигрометръ 633.
Сигіе. Соотвѣтственныя состоянія 691.
Сигіе и ЬаЬопІе. Интраатомная энер-
гія Ка 256.
• ВаЫапйег. Коэффиціентъ расширенія
92, растяженіе твердыхъ тѣлъ 475.
Ваііоп. Расширеніе газовъ 136, измѣ-
реніе теплоты горѣнія 264, скорость испа-
ренія 522, упругость насыщенныхъ паровъ
586, упругость насыщенныхъ паровъ (за-
конъ) 625, 626.
Ватіеп. Вліяніе давленія на точку
плавленія 507.
Вапіеіі. Гигрометръ 632.
В-Агсеѣ Сплавъ 492.
Ваѵу. Природы теплоты 361.
Вау и АПеп. См АПеп и Вау.
Вау и Сіешепі. См. Сіешепі и Вау.
Вау и НоІЬогп. Газовый пирометръ
54, пирометръ 70, коэффиціентъ расши-
ренія 91.
ВеЬгау. Диссоціація 575.
Ве Сапсіоііе и Ве Іа Кіѵе. Теплопро-
водность дерева 330.
Ве ЕогсгапсІ. Принципъ наибольшей
работы 272.
Ве Нееп. Теплоемкость при критиче-
ской температурѣ . 195, методъ жидкой
пленки 335, скрытая теплота испаренія
548, 554.
Ве Ьаппоу. Расширеніе растворовъ 121.
Ве Іа Ргоѵозіауе и Везаіпз. Охлаж-
деніе тѣлъ 282, скрытая теплота плавле-
нія льда 513.
Ве Іа Кіѵе и Ве Сапсіоііе. См. Ве
Сапсіоііе и Ве Іа Ніѵе.
Ве Іа Кіѵе и Магсеі. Теплоемкость
алмаза 191.
ВеІагосЬе и Вегагсі. См. Вегагсі и
Веіагосііе.
Ве Ьис. Коэффиціентъ расширенія 85,
теплоемкость воды 158, точка кипѣнія 526.
Ве Ьиса. Сфероидальное состояніе 531.
Ветегііас. Вліяніе давленія на точку
плавленія 507.
Везогшез и Сіётепі. См. Сіётепі и
Везогтез.
Везргеіх. Расширеніе растворовъ 114,
расширеніе воды 112, 113, теплопровод-
ность 314, методъ жидкаго столба 331,
температурный скачокъ на границѣ тѣлъ
350, переохлажденіе воды 493, точка пла-
вленія 487, скрытая теплота испаренія
воды 535.
Везаіпз и Ве Іа Ргоѵозіауе. См. Ве
Іа Ргоѵозіауе и Везаіпз.
Ве ТЬіеггу. Точка плавленія 480.
ВеѵіІІе и Тгоозі. Измѣреніе высокихъ
температуръ 54.
Веѵѵаг. Расширеніе тѣлъ при низкихъ
температурахъ 93, измѣреніе низкихъ тем-
пературъ 71,- калориметръ 179, теплоем-
кость при низкихъ температурахъ 193,
теплоемкость ожиженныхъ газовъ 196,
вліяніе давленія на температуру плавле-
нія 505, теплоемкость жидкаго водорода
196, сгущеніе газовъ 566, 568, скрытая
теплота испаренія 596.
768
Указатель иностранныхъ авторовъ.
Веѵѵаг и Оіасізіопе. Оптическая пи-
рометрія 60.
Оелѵаг и Моіззап. Сгущеніе газовъ 566.
Оіскзоп. Измѣреніе высокихъ темпе-
ратуръ 58.
Віскіпзоп и ѴѴаісіпег. Сравненіе тер-
мометровъ 44.
Віеззеікогзі и Лае^ег. Теплопровод-
ность 325.
Віеззеікогзі, 8скее1 и Тіезеп. Расши-
реніе воды 118.
Віеіегісі. Теплоемкость воды 161, 162,
механическій эквивалентъ теплоты 375,
скрытая теплота испаренія 533, 540, на-
сыщенные пары 610, ненасыщенные пары
647, уравненіе состоянія 663, критическое
состояніе 673, 674.
ВіПепЬег^ег. Теплопроводность аргона
347.
ВоеЪегеіпег. Сфероидальное состояніе
530. '
Воппап. Опалесценція 683.
Воппу. Точка кипѣнія 526.
Вогзеу. Коэффиціентъ расширенія ме-
талловъ 92.
Воиіе. Радіометръ 252.
Вгарег. Охлажденіе 283.
Вгескег. Теплоемкость эфира 469, коэф-
фиціентъ сжатія 472.
Вгезег. Теплоемкость газовъ 221.
Вгіоп. Расширеніе жидкой $О2 125,
критическое состояніе 165.
Виейгіп§. Упругость насыщенныхъ па-
ровъ (законъ) 597.
Виіоиг. Пирометръ 53, переохлажде-
ніе 494, плавленіе 495, кипѣніе 526, 527,
плотность льда 495.
ВиІіатеІ. Теплопроводность анизотроп-
ныхъ тѣлъ 327.
ВиЬет. Термидинамическій потенціалъ
438, диссоціація 575, упругость насыщен-
ныхъ паровъ 608, теплоемкость насыщен-
ныхъ наровъ 620, правило фазъ 704, сла-
бые растворы 719.
Ви1оп§. Теплоемкость газовъ 224, из-
мѣреніе теплотъ горѣнія 264, упругость
водяныхъ паровъ 598.
ВиІоп§ и Ага^о. См. Ага^о и Виіоп^.
Ви1оп§ и Реііі. Расширеніе 103,
коэффиціентъ расширенія 86, зависимость
теплоемкости отъ температуры 192, тепло-
емкость и атомный вѣсъ (законъ) 227,
охлажденіе (законъ) 277, расширеніе га-
зовъ 136.
Витаз. Теплоемкость сплавовъ 198,
Вирегпеу. Упругость водяныхъ па-
ровъ 604.
Виргё. Теплоемкость жидкихъ смѣсей
198, упругость насыщенныхъ паровъ 601,
уравненіе состоянія 662.
Виззу. Теплоемкость сѣры 191.
Ескегіеіп. Теплопроводность газовъ 348.
Едіег. Охлажденіе (формула) 284.
ЕсИипсІ. Механическій эквивалентъ теп-
лоты 370, растяженіе твердыхъ тѣлъ 475.
Еісккогп. Теплопроводность газовъ 346.
Еіпзіеіп. Атомная теплоемкость 232.
ЕПег. Сфероидальное состояніе 531.
Епідеп. Растворы 736.
Егшапп. Плавленіе 495.
Езітеіскег. Скрытая теплота испаренія
146, упругость насыщенныхъ паровъ 596.
Еіагсі. Растворимость 721.
Ешпогркороиіоз. Точка кипѣнія 5 529.
Ешпогркороиіоз и Патзау. Мельдо-
метръ 56.
Еѵегей. Упругость насыщенныхъ па-
ровъ ‘598.
Ехпег. Плотность воды 113.
Еукшапп. Затвердѣваніе растворовъ 753.
Ракгепкеіі. Переохлажденіе 493.
Гаігкаігп и Таіе. Плотность и удѣль-
ный объемъ насыщенныхъ паровъ (спо-
собъ) 610, 611, 612, 613.
Еаіск. Упругость насыщенныхъ паровъ
603.
Рагадау. Сфероидальное состояніе 532,
сгущеніе газовъ 559, упругость насыщен-
ныхъ паровъ 596.
Еаѵге. Механическій эквивалентъ теп-
лоты 369, скрытая теплота испаренія 544.
Еаѵге и 8іІЬегшапп. Калориметръ 172,
264, теплота горѣнія 264, механическій
эквивалентъ теплоты 376.
Регске. Измѣненіе объема при плав-
леніи 507, испареніе твердыхъ тѣлъ 573,
упругость насыщенныхъ паровъ 594.
Ееггеі. Охлажденіе 284.
Еегу. Абсорбціонный пирометръ 63, оп-
тическая пирометрія 66, точка кипѣнія 530
Ріск. Диффузія растворовъ 724.
Ріеѵех. Оптическая пирометрія 60.
РіпсІІау. Скрытая теплота испаренія 548.
Різскег. Теплоемкость газовъ 241, скры-
тая теплота плавленія 513, испареніе твер-
дыхъ тѣлъ 573
РИх^егаІсІ. Упругость насыщенныхъ
паровъ 606, формула Сіаизіиз’а 660.
Указатель иностранныхъ авторовъ.
769
Еіхеаи. Расширеніе алмаза 95, расши-
реніе мѣди 95, расширеніе кристалловъ
95, 100, расширеніе А&І 94, 101, коэффи-
ціентъ расширенія (способъ) 87.
Еіаи^ег^иез. Расширеніе воздуха 136,
теплоемкость воды 158.
ГогЬез. Теплопроводность (методъ) 317,
теплопроводность дерева 331.
ЕогсЬ. Расширеніе растворовъ 121.
Еогсгапсі. Скрытая теплота плавленія
513, скрытая теплота испаренія 548.
Еоигсгоу и Ѵаидиеііп. Сгущеніе га-
зовъ 539.
Роигіег. Математическая теорія тепло-
проводности 291, задачи на тепловое со-
стояніе тѣлъ 300.
ЕгапкепЬеіш. Критическое состояніе 670.
Егапх и ДѴіесІетапп. Теплопровод-
ность 315.
ЕгіесІІаепсІег. Опалесценція 683.
Ргіесіегісіі и Оиуе. Формула Ѵап-дег-
АѴааІз’а 653.
Егіесіегісіі и Маііеѣ Расширеніе жид-
костей (формула) 128.
Ейгзіепаи. Теплоемкость газовъ 226.
Еиезз. Коэффиціентъ расширенія (при-
боръ) 85.
баесіе. Теплоемкость 194.
баппоп и ЗсЪизіег. Механическій эк-
вивалентъ теплоты 162.
Оагпіег. Теплоемкость твердой воды 236.
баисііп. Точка плавленія 487.
ОаиіЪіег. Плавленіе сплавовъ 491.
ОаиіЪіег и Моіззап. Атомная теплоем-
кость 229
Оау-Ьиззас. Калибрированіе термоме-
тровъ 33, расширеніе газовъ 135, 136, за-
конъ 449, переохлажденіе 493, кипѣніе
526. упругость насыщенныхъ паровъ 586,
законъ Оаііоп’а 626.
Оау-Ьиззас и ДѴеІіег. Теплоемкость га-
зовъ 221.
ОеЬЪагді. Упругость насыщенныхъ па-
ровъ 594.
Оеіззіег и Ріиескег. Расширеніе льда 495
ОегЬег. Смѣси жидкостей 745.
Оегске. Теплопроводность 352.
Оегіасй. Расширеніе растворовъ 121.
Оегпех. Кипѣніе 527.
Оегоза. Теплоемкость воды 159, 160.
ОіЬЬз. Основы термодинамики 381. тер-
модинамическіе потенціалы 438, энтропія
смѣси газовъ 457, упругость насыщенныхъ
паровъ (формула) 603, термодинамическая
поверхность 657, правило фазъ 704.
ОіеЬе. Теплопроводность Ві 324.
(ЗІасШопе и Белѵаг. См. Велѵаг и
О1асІ8Іопе.
Оіауе. Теплопроводность 320, 324.
Оіаіхеі. Коэффиціентъ расширенія 85,
расширеніе металловъ 91.
Ооо88еп8. Вліяніе давленія на темпе-
ратуру плавленія 505.
6о88агі. Сфероидальное состояніе 531.
Ооиіііу. Уравненіе состоянія 662.
Ооиу. Вгохѵй’овское движеніе 423, упру-
гость насыщенныхъ паровъ 608.
Огаеіх. Охлажденіе 284, теплопровод-
ность жидкостей 337, механическій экви-
валентъ теплоты 375, теплопроводность га-
зовъ 346, 348, упругость насыщенныхъ
паровъ 603.
Огау и Катзау. Сгущеніе газовъ 570.
ОгеепАѴоод. Точка кипѣнія 530.
ОгеІ88. Теплопроводность дерева 330.
ОгіТТііЪз. Измѣреніе высокихъ темпе-
ратуръ 58, теплоемкость воды 161, 162, 165,
механическій эквивалентъ теплоты 163,
теплоемкость анилина 196, скрытая теплота
испаренія 540.
6гШШі8 и Лоіу. Теплоемкость воды 164.
Огітаійі. Уравненіе состоянія 657.
Огоігіап иДѴиеІІпег. Плотность и удѣль-
ный объемъ насыщенныхъ паровъ (спо-
собъ) 616.
Огоѵе. Теплопроводность газовъ 341,
кипѣніе 527.
Огйпеізеп. Расширеніе металловъ 92,
теплопроводность твердыхъ тѣлъ 322. 323.
ОгипшасЪ. Измѣненіе объема при пла-
вленіи 497.
ОиеШЬег^* Уравненіе состоянія 663.
Ои^ііеіто. Расширеніе жидкостей 118.
Ои^ііеішо иМизіпа. Законъ Иаііоп’а 627.
Оиіііаите. Поправки термометровъ 26,
изготовленіе термометра 37, приниженіе
нуля 38, поправка на выступающій стол-
бикъ 41, сравненіе термометровъ 73, рас-
ширеніе сплавсвъ 94.
Ои1(1Ьег§. Упругость насыщенныхъ па-
ровъ 613.
Ои1(1Ьег§ и ДѴаа^е. Двойной обмѣнъ
въ растворахъ 735.
ОйпіЪег. Теплопроводность газовъ 347.
Оиікгіе. Методъ жидкой пленки 334,
эвтектическіе сплавы 491, опалесценція 683,
кріогидраты 703.
КУРСЪ ФИЗИКИ О. X В О Л Ь С О Н А. Т. ІП, изд. 3-е.
49
770
Указатель иностранныхъ авторовъ.
биішапп. Скрытая теплота плавленія
льда 513.
Оиуе. Критическое состояніе 673, со-
отвѣтственныя состоянія 688.
Оиуе и РгіесІегісЬ. См. РгіегіегісИ и
Оиуе.
Оиуе и МаІІеі. Соотвѣтственныя со-
стоянія 688.
Охѵуег и Тгалѵегз. Сравненіе термо-
метровъ 58.
Нае^зігоеш. Теплопроводность 321.
На^а. Растяженіе твердыхъ тѣлъ 475.
На§еп. Упругость насыщенныхъ па-
ровъ 594.
НаЬп. Теплопроводность воздуха 349.
Наііоск. Сплавы 492.
На1І8Ітоет. Калибрированіе термоме-
тровъ 36, коэффиціентъ расширенія 90,
плотность воды 112.
На^еп и КиЬеп8. Испусканіе платины 62.
Накке и Зіешепэ. Пирометръ 70.
Нашшегі. Охлаждающія смѣси 727.
Натрзоп. Ожиженіе газовъ 568.
Напатапп. Охлаждающія смѣси 727.
НапШ и РгіЬгат. Точка кипѣнія 525.
Наппау. Критическое состояніе 682.
Наппау и Но^агіЬ. Критическая тем-
пература 683.
Напзетапп и КігсЬЬоН. Теплопровод-
ность твердыхъ тѣлъ 322.
Нарреі. Соотвѣтственныя состоянія 688.
Нагкег. Пирометръ 58, теплоемкость
Ее 193.
Нагітапп. Пирометръ 63.
Наиіеіеиіііе и СЬарриіэ. См. СЬарриІ8
и НаиіеГеиіПе.
Наиіеіеиіііе и Т^оозі. Законъ Баі-
іоп’а 627.
Неігіхѵеііег. Вліяніе давленія на точку
плавленія 507.
Неісіѵѵеііег и КоЫгаиэсІі. Диссоціація
воды 734.
НеіІЬогп. Расширеніе жидкостей 128,
критическая температура 673.
Неіпх. Сплавы органическихъ ве-
ществъ 493.
Неішегзеп. Теплопроводность 314.
Неіткоііх. Принципъ сохраненія энер-
гіи 362, свободная энергія 438, несвобод-
ная энергія 441.
Неішііоііг К. Упругость насыщенныхъ
паровъ 607, 629.
НеппеЬег^ Теплопроводность жидко-
стей 338.
Неппегѣ Калибрированіе термоме-
тровъ 34.
Неппіп§. Упругость насыщенныхъ па-
ровъ 593, 604.
Неппіп§ и НоІЬот. Испусканіе метал-
ловъ 62, расширеніе кварца 95, теплоем-
кость газовъ 207, упругость насыщенныхъ
паровъ 593.
НепгісЬзеп. Теплоемкость воды 160.
Непгісі. Расширеніе воды 117.
Непгу. Законъ ВаИоп’а 626, раствори-
мость (законъ) 721.
Негкег. Скрытая теплота испаренія
воды 540.
Неггиіапп. Упругость насыщенныхъ
паровъ 601.
Нег8с1іе11. Ледяной калориметръ 168.
Негіх. Теплоемкость газовъ 220, си-
стема механики 443, упругость насыщен-
ныхъ паровъ 594, упругость насыщен-
ныхъ паровъ (формула) 601, 602.
НегІ78ргип§. Температура солнца 64.
Нелѵі^. Скрытая теплота испаренія
воды 539, плотность и удгльный объемъ
насыщенныхъ паровъ 616, законъ ВаІ-
іоп’а 627, ненасыщенные пары 650.
Не88, Законъ 258, скрытая теплота
плавленія 513.
Непзе и ЗсЬееІ. Испареніе твердыхъ
тѣлъ 574.
Неусоск и Ыеѵіііе. Точка плавленія
сплавовъ 490,затвердѣваніе растворовъ 754.
Нігп. Расширеніе жидкостей 125, рас-
ширеніе воды 120, теплоемкость воды 159,
способъ охлажденія 186, теплоемкость жид-
костей 195, теплоемкость газовъ 221, ме-
ханическій эквивалентъ теплоты 373, 377,
идеальные газы 453, теплоемкость насы-
щенныхъ паровъ 622, 623, ненасыщенные
пары 650, уравненіе состоянія 661.
НІГ8СІ1. Уравненіе состоянія 657
Н]еІ8Ітоеш. Теплопроводность снѣга 325.
НоеГкег. Теплопроводность паровь ор-
ганическихъ соединеній 346.
НоНшапп. Термометръ ЗсЬоН’а 39, рас-
ширеніе воздуха 142.
Но^агіИ и Наппау. См. Наппау и Но-
§агік.
НоІЬогп. Измѣреніе высокихъ темпе-
ратуръ 58.
НоІЬогп и Аиэііп. См. Аизііп и НоІЬогп.
НоІЬогп и Ваисііп. См. Ваийіп и НоІ-
Ьогп.
НоІЬогп и Вау. См. Вау и НоІЬогп.
Указатель иностранныхъ авторовъ.
771
НоІЬо п и Неппіп§. См. Неппіп^ и
НоІЬогп.
НоІЬогп и КигІЬаиш. Пирометръ 65.
НоІЬогп и Ѵаіепііпег. Пирометрія 54.
НоІЬогп и ХѴіеп. Измѣреніе низкихъ
температуръ 72, пирометры 69, газовый
пирометръ 54.
Ноішап. Потеря тепла калориметромъ 184.
Ноігшапп. Поправка на выступающій
столбикъ 40.
Норе и ЯшпТопі. Температура наи-
большей плотности воды (способъ) 113.
Норкіпз. Вліяніе давленія на темпе-
ратуру плавленія 507.
НогІ8тапп. Диссоціація 575, ненасы-
щенные пары 649.
Ноиііеѵі^ие. Скрытая теплота испаре-
нія 548.
Позѵау. Сгущеніе газовъ 561.
Іп§епЬои§. Теплопроводность 311.
Іп§ег80І1 и МепйепЬаІІ. Точка плавле-
нія 482.
Ігѵіпе. Теплоемкость 157, скрытая те-
плота испаренія 534.
Лае§ег. Расширеніе жидкостей 128, те-
плопроводность 337, теплоемкость ненасы-
щенныхъ паровъ 644, уравненіе состоянія,
651, 662.
Лае^ег и Віе88е1Ьог8І. См. Віеззеі-
Ъог8І и Лае^ег.
Лае§ег и 8іеіпдѵеЬг. Теплоемкость 178,
калориметрическая бомба 267.
Лайп. Механическій эквивалентъ те-
плоты 375.
Латіп. Калориметръ 173, влажность 630.
Латіп и Атаигу. См. Атаигу и Латіп.
Латіп и КісЬагсі. Теплоемкость га-
зовъ 223.
Лапке. Теплоемкость воды 162.
Лаппеіаг. Теплопроводность кристал-
ловъ 328.
Лап88оп. Теплопроводность снѣга 326.
Лаедпетоі и Регоі. Расширеніе газовъ
149, точка плавленія 488.
ЛпедпегосІ и Тгаѵегз. Измѣреніе вы-
сокихъ температуръ 54, измѣреніе низкихъ
температуръ 71, расширеніе водорода 143,
сгущеніе газовъ 566.
Лагоііпек. Упругость насыщенныхъ па-
ровъ (формула) 604.
Леѵѵеіі. Упругость насыщенныхъ па-
ровъ 593, 594.
Лоскшапп. Газовый термометръ 464.
Лоііу. Мельдометръ 56, пирометръ 67,
паровой калориметръ 187, расширеніе га-
зовъ 192, теплоемкость газовъ 213.
Лоііу и бгШійіз. См. (ЗгШійіз и Лоііу.
Лоііу и ХѴЬііе. Сравненіе термомет-
ровъ 45.
Лопез. Точка кипѣнія 525.
Лопіе. Расширеніе каучука 92, механи-
ческій эквивалентъ теплоты 365, 373, 374,
375, законъ 449, адіабатическое сжатіе 472,
растяженіе твердыхъ тѣлъ 475, уравненіе
состоянія 662
Лопіе и Корр. Законъ 235
Лопіе и ТЬошзоп. Расширеніе газа въ
пустоту 458, 567.
ЛпЫіп. Испареніе твердыхъ тѣлъ 573.
ЛпІіпзЬпг^ег. Упругость насыщенныхъ
паровъ 603.
Лпп§к. Выдѣленіе теплоты при смѣши-
ваніи порошковъ съ жидкостями 256.
Лпріпег. Соотвѣтственныя состоянія
688, 689.
Каетіг. Упругость насыщенныхъ па-
ровъ 585.
КаЫЬапш. Кипѣніе 525, дестилляція
металловъ, 529, упругость насыщенныхъ
паровъ 583.
Как1епЬег§. Скрытая теплота испаре-
нія 535.
Каізег. Расширеніе газовъ 144, тепло-
емкость газовъ 224.
КаІеЬпе. Теплоемкость газовъ 225.
КатшегІіп^Ь Оппез. Измѣреніе низкихъ
температуръ 71, расширеніе водорода 143,
сгущеніе газовъ 562, 563, 567, ненасыщен-
ные пары 649, уравненіе состоянія 661, со-
отвѣтственныя состоянія 693.
Каиітег1іп§Ь Оппез и Кеезот. Опа-
лесценція 683.
Карр. Газовый термометръ 21.
Кеезош и КашшегІіп^Ь Оппе8. См.
КашшегІіп^Ь Оппез и Кеезот.
Ке88Іег. Упругость насыщенныхъ па-
ровъ 603.
КіеЫГг и Векп. См. Векп и КіеЬііх.
КігсЬЬоТТ. Законъ 61, формула 431,
испареніе твердыхъ тѣлъ 572, упругость
насыщенныхъ паровъ (формула) 603, те-
плота растворенія 727.
КігсЬЬоН и Напзетапп. См. Нап8е-
піапп и Кігсккой.
КІеЬе. Уравненіе состоянія 661.
КІеЬе и Ьіпсіе. Упругость насыщенныхъ
паровъ 593.
Кіеешапп. Поверхностное натяженіе 466.
49*
772
Указатель
иностранныхъ авторовъ.
КпіеізсЪ. Упругость насыщенныхъ па-
ровъ 596.
Кпірр. Упругость насыщенныхъ па-
ровъ 543.
КпоЫаисЪ. Теплопроводность дерева
330, упругость насыщенныхъ паровъ 593,
уравненіе состоянія 661
Кписізеп. Теплопроводность газовъ 353,
насыщенные пары 582, упругость насы-
щенныхъ паровъ 594.
Коей. Теплоемкость газовъ 226.
Коепі§§Ьег§ег. Упругость насыщен-
ныхъ паровъ 608
КоЫгаизсІі. Изготовленіе термометра
46* расширеніе эбонита 94, теплоемкость
газовъ 222, теплопроводность (методъ) 321,
теплопроводность жидкостей 336.
КоЫгаизсІі и НеШлѵеіІег. См. НеШ-
лѵеііег и КоЫгаизсЬ.
Коіасек. Испареніе твердыхъ тѣлъ 573.
Корр. Плотность воды 114, расшире-
ніе воды 116, коэффиціентъ расширенія
87, калориметръ 177, теплоемкость газо-
выхъ смѣсей 230, атомная теплоемкость
235, плавленіе 495, молекулярный объемъ
жидкости при температурѣ кипѣнія 530.
Корр и МаШііезеп. Коэффиціентъ рас-
ширенія 87.
КгеЬз. Кипѣніе 527.
КгеШііщ. Расширеніе воды 117, рас-
ширеніе растворовъ 121.
Кгетегз. Расширеніе растворовъ 121.
Кгіэіепэеп. Сфероидальное состояніе 531.
Кгеѵѵіп^. Законъ ОаЙоп’а 627.
Кгие^еі и ЬасІепЬиг^. Измѣреніе низ-
кихъ температуръ 72.
Киепеп и КоЬ§оп. Испареніе твердыхъ
тѣлъ 575.
Кйэіег. Испареніе твердыхъ тѣлъ 570.
КипсІЬ Расширеніе каучука 93.
Кшісіі и ХѴагЬиг^. Теплоемкость га-
зовъ 224, теплопроводность газовъ 343.
Кипя. Теплоемкость угля 195.
КигІЬашп. Оптическая пирометрія 66.
КигІЬашп и НоІЬогп. См. НоІЬогп и
КигІЬашп.
ЬаЬу. Упругость насыщенныхъ па-
ровъ 594.
ЬаЬогсІе. Теплоемкость сплавовъ 197.
ЬасІепЬиг^ и Кгие^еі. См. Кгие^еі и
Ьас1епЬиг§.
Ьаештеі. Атомная теплоемкость 233.
Ьашё. Теплопроводность анизотропныхъ
тѣлъ 327.
Ьашра. Вліяніе давленія на точку пла-
вленія 506.
Ьашу. Мраморный пирометръ 55.
Ьап§Ьег§. Сравненіе теплопроводно-
стей 314.
Ьаріасе. Поверхностное давленіе 606.
Ьаріасе и Ьаѵоі8Іег. Коэффиціентъ
расширенія твердыхъ тѣлъ 82, теплоем-
кость твердыхъ тѣлъ (способъ) 160, скры-
тая теплота плавленія льда 513.
Ьа Роза. Плавленіе С 489.
Ьаѵаі. Испареніе 522.
Ьаѵоіэіег и Ьаріасе. См. Ьаріасе и
Ьаѵоі§іег.
Ье СЬаІеІіег. Пирометрія 68, 69, 70,
коэффиціентъ расширенія 91, расширеніе
сплавовъ 93, теплоемкость газовъ 211, те-
плоемкость С 229, диссоціація 575, раство-
римость 721, 722.
Ье СЬаіеІіег и Маііагсі. Теплоемкость
газовъ 215.
ЬесЬег. Теплоемкость металловъ 193.
Ьесіоих. Уравненіе состоянія 662.
Ьесіис. Расширеніе газовъ 143, скры-
тая теплота плавленія льда 513
Ьее$. Охлажденіе 285, теплопроводность
при низкихъ температурахъ 326, тепло-
проводность кристалловъ 329, теплопро-
водность деревъ 331, теплопроводность
жидкостей 334.
ЬеЬтапп и ШаІІегапЬ Аллотропиче-
скія превращенія 515. •
ЬеШепГгоэЬ Сфероидальное состоя-
ніе 531.
Ьёшегау. Коэффиціентъ расширенія 91.
Ьетке. Сравненіе термометровъ 43.
Ье Коу. Точка росы 632.
Ьепх. Теплопроводность 324.
Ье§1іе. Психрометръ 635.
Ьеѵу. Расширеніе 107.
Ьеѵу и ЫегпзЬ Упругость насыщенныхъ
паровъ 603.
ЬіеЬі^. Теплоемкость воды 160.
Ьіпсіе. Теплоемкость воздуха 215, сгу-
щеніе газовъ 567, уравненіе состоянія 661.
Ьіпсіе и КІеЬе. См. КІеЬе и Ьіпсіе.
Ьіпсіеск и Коіке. Психрометръ 30.
Ьіпсіетапп и №гп8І. Калориметръ 178,
атомная теплоемкость 232.
ЬішІпег. Ледяной калориметръ 171,
теплоемкость минераловъ 195.
ЬіпеЬаг^ег. Скрытая теплота испаре-
нія 547, теплота растворенія 733.
Ьірроѵѵііх. Сплавы 492.
Указатель иностранныхъ авторовъ.
773
Ьіѵіп§8Іопе и Мог^ап. Критическое
состояніе 671.
Ьосі^е. Теплопроводность (методъ) 325.
ЬогЬег^. Теплопроводность жидко-
стей 334.
Ьогепх. Теплоемкость и молекулярный
вѣсъ 228, охлажденіе (формула) 285, Те-
плопроводность твердыхъ тѣлъ 323, урав-
неніе состоянія 661.
Ьо\ѵпсІ8. Теплопроводность кристал-
ловъ 329.
Ілісііп. Теплоемкость воды 161.
Ешпшег. Оптическая пирометрія 64.
Ьиттег и Ргіп§8Ъеіт. Оптическая
пирометрія 64, 66, теплоемкость газовъ 222,
охлажденіе 284.
Ьипс1диІ8І. Теплопроводность жидкостей
332, 338.
Ьіі8аппа. Плотность воды 114, плот-
ность растворовъ 116, теплоемкость га-
зовъ 210, вліяніе давленія на точку пла-
вленія 508, аллотропическія превращенія
515, 516.
Ьи88аппа и Виххоіа. См. Виххоіа и
Ьи88аппа.
Мас Регіапе. Охлажденіе 286.
МасЬ. Температура 6, калориметръ 155.
МасИе. Теплоемкость жидкостей 237.
Маск. Вліяніе давленія на температуру
плавленія 507.
Мас Ьеосі. Упругость насыщенныхъ
паровъ 594.
Ма^іе. Теплоемкость растворовъ 199.
Ма&пн8. Расширеніе газовъ 136, 137,
атомная теплоемкость 232, теплопровод-
ность газовъ 342, упругость насыщенныхъ
паровъ 588, 590, 591, 598, законъ Паііоп’а
626, точка кипѣнія растворовъ 739.
МаЫег. Калориметрическая бомба 267.
МаЫке. Ртутный пирометръ 53, по-
правка на выступающій столбикъ 41.
Маіпе. Точка кипѣнія 525.
Макохѵег. Теплоемкость газовъ 223.
Маііагд и Ье Сйаіеііег. См. Ье Сйа-
іеііег и МаПагсі.
Маііеі и РгіейегісЬ. См. Ргіесіегісіі и
Маііеі.
Маііогу и \ѴаШпег. Сравненіе термо-
метровъ 58, механическій эквивалентъ те-
плоты 161.
Мапаіга. Формула Сіаизіиз’а 660.
Мапеиѵгіег. Теплоемкость газовъ 226.
Магсеі. Точка кипѣнія 526, 527.
Магсеі и Ве Іа Ріѵе. См. Ве Іа Кіѵе
и Магсеі.
МагсЪІ8. Перемѣщеніе основныхъ то-
чекъ термометра 36, термометръ 46.
Магскѵѵаісі. Кипѣніе 528.
Магек. Расширеніе воды 117.
- Магі^пас. Расширеніе растворовъ 121,
теплоемкость жидкостей 185, 191.
Магк и ШсЬагсІ8. Расширеніе га-
зовъ 141. -
Магііпеііі. Теплоемкость воды 166.
Магііпеііі и Ваііеііі. См. ВаіеШ и
Магііпеііі.
Магііпі. Выдѣленіе тепла при смѣши-
ваніи порошковъ съ жидкостями 256.
Ма8оп. Психрометръ 635.
Ма88Іеи. Термодинамическіе потенці-
алы 438.
Ма88оп. Теплоемкость газовъ 221.
Маійіа8. Теплоемкость растворовъ 198,
скрытая теплота испаренія 545, законъ
параболы 617, 618, 619, теплоемкость на-
сыщенныхъ паровъ 624, 625, критическое
состояніе 669, 670, соотвѣтственныя со-
стоянія 693
МаііЫе8. Упругость насыщенныхъ па-
ровъ 594.
МаііЬіезеп. Плотность воды 112, рас-
ширеніе воды (формула) 119, расширеніе
сплавовъ 93. расширеніе металловъ 91,
коэффиціентъ расширенія 86.
Маіійіевеп и Корр. См. Корр и Маі-
Шіезеп.
Махдѵеіі. Единица теплоты 157, тепло-
проводность газовъ 339, 340, 348, 349,
упругость насыщенныхъ паровъ 604, тео-
рія психрометра 635, уравненіе состоя-
нія 656.
Мауег К. Первое начало термодина-
мики 362, механическій эквивалентъ те-
плоты 364
Мауег Т. Методъ охлажденія 187
Мауег V. Пирометрія ,55.
Маххоііо. Теплоемкость сплавовъ 197,
точка плавленія сплавовь 492.
МеЫІ8. Теплопроводность Аг 346, 347.
Меіііпк. Измѣреніе низкихъ темпера-
туръ 72.
Меіапдег. Расширеніе газовъ 144.
МепдепИаІІ и Іп^ег8о11. См Іп§ег80І1
и Мепдепііаіі.
Мегх и АѴеііИ. Сплавъ 491.
Мезііп. Термоскопъ 50, соотвѣтствен-
ныя состоянія 691
774
Указатель иностранныхъ авторовъ.
Меуег. Теплопроводность кристалловъ
328, уравненіе состоянія 651.
Меуег А. М. Измѣреніе высокихъ тем-
пературъ 59.
Меуег Е. Теплопроводность воздуха
346, теплопроводность газовъ 349.
Меуег К. (урожд. В]еггиш). Соотвѣт-
ственныя состоянія 694.
Меуег О. Е. Теплопроводность га-
зовъ 339.
Меуег 8. Молекулярная теплопровод-
ность 235, скрытая теплота испаренія 534.
Місиіезси. Механическій эквивалентъ
теплоты 370.
МіІИхег. Расширеніе Н& 104.
МІІІ8. Скрытая теплота испаренія 548.
Мііпег и СЬаіІоск. См. СИаНоск и
Мііпег.
МіІіЬаІег. Теплоемкость Н& 196.
МіІіЬаІег и №ссагі. Теплоемкость
Н% 196.
Міізсйеі. Теплопроводность 319.
МіІБсЬегІісЬ. Расширеніе кристалловъ
95, 98.
Мойг. Основы термодинамики 362.
Моіззап. Плавленіе металловъ 487, де-
стилляція металловъ 529, 530.
Моіззап и баиійіег. См. баиійіег и
Моіззап.
Моп^е и СІоиеі. См. Сіоиеі и Моп§е.
Моппіег. Гигрометръ 635.
Мопіі. Переохлажденіе 493.
МоогЬу и Кеупоійз. Теплоемкость
воды 164.
Могеііо и Сіпеііі. См. Сіпеііі иМогейо.
Мог^ап и Ьіѵіп^зіопе. См. Ьіѵіп^зіопе
и Мог&ап.
Мог^ез. Теплота растворенія 727.
Могііг. Упругость насыщенныхъ па-
ровъ 599, охлаждающія смѣси 727.
Могіеу. Упругость насыщенныхъ па-
ровъ Н% 594.
Могіеу и Ко^егз. Расширеніе метал-
ловъ 90.
Могіхип. Соотвѣтственныя состоянія 689.
Мозег. Растворы 736.
Мозз. Упругость насыщенныхъ па-
ровъ. 598.
Моиііп. Уравненіе состоянія 661.
Моиззоп. Вліяніе давленія на точку
плавленія 505.
Мйііег. Теплоемкость газовъ 222, те-
плоемкость насыщенныхъ паровъ 644.
Мйііег Е. Теплопроводность газовъ 349
Мйііег - ЕггЬасй. Тепловой эффектъ
химическихъ реакцій 263, упругость насы-
щенныхъ паровъ 594.
Миепсййаизеп. Теплоемкость воды
159, 160.
Мипке. Точка кипѣнія 526.
Мизіпа и 6и§1іеЪпо. См. Ои^ііеішо
и Мизіпа.
№ссагі и МіКйаІег. См. Мііійаіег и
№ссагі.
№ссагі п Ра§1іапі. Упругость насы-
щенныхъ паровъ 594, 599.
Каіапзоп Е. Расширеніе СО% 460.
№а1апзоп Ь. Сгущеніе газовъ 565.
№йегег. Сгущеніе газовъ 559.
Каишапп. Теплоемкость газовъ 241.
№§геапо. Теплоемкость жидкостей 189.
№гпз1. Оптическая пирометрія 65, те-
плопроводность диссаціированнныхъ га-
зовъ 350, гипотеза 479, скрытая теплота
испаренія 548, испареніе твердыхъ тѣлъ
574г упругость насыщенныхъ паровъ (фор-
мула) 603, теплоемкость насыщенныхъ па-
ровъ 625, соотвѣтственныя состоянія 689,
диффузія 724.
ІЧегпзі и Ьеѵу. См. Ьеѵу и Кегпзі.
Кегпзі и Еішіетапп. См. Еіпдетапп
и №гпзГ.
Кеи^еЬаиег и Сопгаи. См. Сопгаи и
ІЧеи^ейаиег.
Шеитапп Р. Теплоемкость воды 158,
нагрѣватель 177, теплоемкость сплавовъ
(законъ) 177, теплоемкость и молеку-
лярный вѣсъ (законъ) 233, теплопровод-
ность 320.
Мехѵіііе и Неусоск. См. Неусоск и
ІЧеѵіІІе.
№\ѵіоп. Лучеиспусканіе (законъ) 276.
Ыісоі. Растворы 36.
Міейегзсйиііе. Испареніе твердыхъ
тѣлъ 570.
ТЧіейІз. Ртутный пирометръ 53.
ІЧіррокІ. Гигрометръ 634
Міѵеп. Теплопроводность 326.
Г4огѣ Плотность воды 114.
ОЬасй. Скрытая теплота испаренія 548.
ОЬегЬеск. Охлажденіе въ потокѣ воз-
духа 285.
Ойегйойег. Теплоемкость Ре 193.
ОНег. Кріогидраты 703.
О^іег. Сгущеніе газовъ 561.
Окагіа. Теплопроводность снѣга 322.
Оізхеѵѵзкі. Сравненіе газовыхъ термо-
метровъ 24, измѣреніе низкихъ темпера-
Указатель
иностранныхъ авторовъ.
775
туръ 71, сгущеніе газовъ 563, 564, 565,
566, 568, упругость насыщенныхъ па-
ровъ 596.
Отойеі и Ѵісепііпі. Измѣненіе объема
при плавленіи 499.
Озтопсі. Теплопроводность 324.
ОзйѵаШ. Дилатометръ 111, единица
количества теплоты 257, правило Тгоиіоп’а
547, правило фазъ 704, упругость пара
растворовъ 736.
Ра§е. Теплоемкость смѣсей жидкостей 198.
Ра^ііапі. Правило Тгоиіоп’а 597
Ра^ііапі и Иассагі. См. Ыассагі и
Ра^ііапі.
Раіііоі и Ѵап АиЬеІ. Теплопровод-
ность 325.
Раіаххо и Ваіеііі. См. Ваіеііі и Раіаххо.
Раітег. Термометръ 50.
Раре. Теплопроводность кристалловъ 328.
Радиеі. Теплоемкость воздуха 222.
Рагкз. Выдѣленіе тепла при смѣшива-
ніи порошковъ съ жидкостями 256.
Рёсіеі. Теплопроводность 310.
Реііаі. Измѣреніе низкихъ темпера-
туръ 72.
Регкіпз. Сфероидальное состояніе 531.
Реггоі. Удѣльный объемъ и плотность
насыщенныхъ паровъ 611, 613, механиче-
скій эквивалентъ теплоты 614.
Реггоі. Теплопроводность 329.
Регвоп. Ртутный пирометръ 52, скры-
тая теплота плавленія (формула) 513.
Реііі и Ви1оп§. См. Ви1оп§ и Реііі.
Реііегзоп. Теплоемкость 196, пла-
вленіе 496, скрытая теплота плавленія 512.
Ріай. Расширеніе кристалловъ 99.
Ріашісііег. Теплоемкость 180, 183, 184,
теплоемкость жидкостей 189, теплота смѣ-
шенія и Н2О 268, второе начало
термодинамики 421, упругость насыщен-
ныхъ паровъ 594, кріогидраты 703,
охлаждающія смѣси 727.
РТашкПег и Ріаііпег. Теплоемкость
воды 159.
Ріаипйіег и Ре^паиіі. Теплоемкость
(формула) 183.
Ріскегіщг. Скрытая теплота плавле-
нія 513.
Рісіеі. Расширеніе жидкаго ацетилена
125, правило Тгоиіоп’а 527, сгущеніе га-
зовъ 560, 562, упругость насыщенныхъ
паровъ 596, критическое состояніе 682.
Ріегге. Сравненіе термометровъ 43, пере-
охлажденіе воды 120
РіопсЬоп. Измѣреніе высокихъ темпе-
ратуръ 56, теплоемкость металловъ 193,
теплоемкость кварца 194
Ріапск. Температура лучистой энер-
гіи 8, теплопроводность газовъ 343, экви-
валенты превращеній 418, расширеніе ги-
потезы Мегпзі’а 481, теплоемкость насы-
щенныхъ паровъ 625, уравненіе состоянія
656, 663, упругость насыщенныхъ паровъ
604, теорія слабыхъ растворовъ 714, те-
плота растворенія 730, 731, соотвѣтствен-
ныя состоянія 686, правило фазъ 704, осмо-
тическое давленіе 723, смѣси жидкостей 741.
Ріаііпег и РіаипсІІег. См. РіаипсІІег
и Ріаііпег.
Ріиескег. Упругость насыщенныхъ па-
ровъ 588.
Ріиескег и Оеіззіег. См. беіззіег и
Ріиескег.
Роіззоп. Формула 201, математическая
теорія теплопроводности 291, задачи на
тепловое состояніе тѣлъ 300, температур-
ный скачокъ на границѣ тѣлъ 350.
Ропзоі. Кріогидраты 703, правило
фазъ 706.
Рогіег. Упругость насыщенныхъ па-
ровъ 598.
Роиіііеі. Газовый термометръ 53, из-
мѣреніе высокихъ температуръ 56, элек-
трическій пирометръ 67, теплоемкость Рі
192, охлажденіе 282.
Ргезіоп. Критическое состояніе 674.
РгіЬгат и Напді. См. НапШ и РгіЬгат.
Ргіп^зііеіт и Ьшптег. См Ьшптег
и Ргіп^зЬеіт.
Ргіпзер. Измѣреніе высокихъ темпе-
ратуръ 56.
Ргопу. Упругость насыщенныхъ па-
ровъ (формула) 603.
РиІігісЬ. Коэффиціентъ расширенія 89.
Риіи]. Механическій эквивалентъ те-
плоты 371.
Оиіпке. Акустическій термометръ 59.
Оиіпіиз Ісіііиз. Механическій эквива-
лентъ теплоты 375.
Ратзау. Скрытая теплота испаренія
541, растворы 753.
Ратзау и Ваіу. См. Ваіу и Ратзау.
Ратзау и ЕитогрЬороиІоз. См. Еи-
тогрЬороиІоз и Ратзау.
Ратзау и бгау. См. бгау и Ратзау.
Ратзау и тізз Магзѣаіі. Скрытая те-
плота испаренія 541.
Ратзау и Ѵоип§. Кипѣніе 528, испа-
776
Указатель иностранныхъ авторовъ
реніе твердыхъ тѣлъ 570, 573у упругость
насыщенныхъ паровъ 583, 584, 592, 593,
594, (формула) 597, 600, плотность и удѣль-
ный объемъ насыщенныхъ паровъ 617, те-
плоемкость ненасыщенныхъ паровъ 648,
законъ Каопіі’я 738
Катвдеп. Коэффиціентъ расширеній
(методъ) 184.
Капсіаіі. Расширеніе кварца 95, 100.
Папкіпе. Расширеніе жидкостей 128,
сгущеніе газовъ 570, упругость насыщен-
ныхъ паровъ 602, (формула) 604, тепло-
емкость насыщенныхъ паровъ 619, урав-
неніе состоянія 662.
Каоиіі. Упругость пара растворовъ
(законъ) 736, 737, 743, затвердѣваніе ра-
створовъ 749.
Кескпа^еі. Сравненіе термометровъ 43,
расширеніе 108, расширеніе воздуха
143, уравненіе состоянія 662.
Кееск. Теплоемкость газовъ (фор-
мула) 227.
Ке^паиК. Газовый термометръ 19, срав-
неніе шкалъ термометровъ 23, 43, воздуш-
ный пирометръ 53, пирометрія 55, расши-
реніе 104, расширеніе газовъ 137, 139,
141, 144, 145, 147, теплоемкость воды 158,
150, калориметръ 173, 175, потеря тепла
калориметромъ 187, теплоемкость С 191,
теплоемкость сплавовъ 197, теплоемкость
газовъ 203, 210, теплоемкость СО* 209,
скрытая теплота плавленія льда 513, скры-
тая теплота испаренія 536, 538, 540, 541,
543, 544, испареніе твердыхъ тѣлъ 572,
насыщенные пары 583, упругость насы-
щенныхъ паровъ 588, 589, 591, 593, 594,
596, законъ Паііоп’а 597, 598, 599, 627, те-
плоемкость насыщенныхъ паровъ 621, 625,
гигрометръ 632, 635, психрометръ 636,
теплоемкость ненасыщенныхъ паровъ 643,
смѣси жидкостей 795
Не^паиіі и РТаипдІег. См. РТаипйІег
и Не^паиН.
НеісѴіег. Аллотропическія превращенія
5 515.
ПеІп^апит. Уравненіе состоянія 661.
Кеі8. Моллекулярная теплоемкость 236.
Кеуе. Уравненіе состоянія 662.
Реіпоі(І8. Радіометръ 252.
ЯеупоІ€І8 и МоогЬу. См. МоогЬу и
РеупоШз.
КісѣагсІ. Гигрографъ 135.
НісЬагсІ и Лагпіп. См. Лагпіп и Кіскагд.
ПісЬагсІэ. Теплоемкость и молекуляр-
ный вѣсъ 228, термическій эффектъ хи-
мическихъ реакцій 263.
КісЬаг(І8 и Магк. См. Магк и КіскапЕ.
ШскагсІ8Оп. Упругость насыщенныхъ
паровъ 594, 598.
Піскагіх. Теплоемкость 195, теплоем-
кость газовыхъ смѣсей 230, атомная те-
плоемкость 231.
Яіеске. Правило фазъ 704, 706.
Кіеіэск. Теплопроводность 324.
КПіег. Скрытая теплота испаренія 534,
уравненіе состоянія 662, соотвѣтственныя
состоянія 694.
КоЬегІ8-Аи8Іеп. Сплавъ 491.
РоЬ8оп и Киепеп См. Киепеп и КоЬ8оп.
Косѣе. Упругость насыщенныхъ паровъ
(формула) 598.
Ко(1\ѵе11. Расширеніе 95.
Ноепі^еп. Теплоемкость газовъ 222,
теплопроводность кристалловъ 328.
Ко§ег8 и Могіеу. См. Могіеу и Ко§ег8.
Коііа. Испареніе твердыхъ тѣлъ 571.
КоІоТТ. Кріогидраты 703.
КоохеЬоот. Правило фазъ 704, 711.
Ко8е. Сплавъ 492.
Ко8е-Іппе8. Уравненіе состоянія 663.
Козеііі. Расширеніе воды 117, 119,
плотность растворовъ 115, охлажденіе (фор-
мула) 284.
Коік. Скрытая теплота плавленія льда 513.
Ноіке. Измѣреніе низкихъ темпера-
туръ 72.
Похѵіапй. Механическій эквивалентъ
теплоты 160, 364, 368, 369, теплоемкость
воды 163, 164.
Ноу. Коэффиціентъ расширенія.
КшіЬег^. Расширеніе газовъ 136, точки
кипѣнія 527.
КиесіогТ. Соотвѣтственныя состоянія
689, охлаждающія смѣси 727.
Пиеітапп. Теплоемкость металловъ 470
КишТогб. Потеря тепла калориметромъ
179, измѣреніе теплотъ горѣнія 264, ме-
тодъ жидкаго столба 331, природа тепло-
рода 361, скрытая теплота испаренія 535.
КшпТогсІ и Норе. См. Норе и ПитГогсІ.
Щі88пег. Расширеніе каучука 93, рас-
ширеніе гуттаперчи 94.
Киікегіогй. Максимальный и минималь-
ный термометръ 461, сгущеніе газовъ 569.
8акшеп и Таттап. Дилатографъ 517.
Закиіка. Механическій эквивалентъ те-
плоты 371.
8аіпіе СіаігеВеѵіііе. Точка плавленія 487
Указатель иностранныхъ авторовъ.
777
Заіпіе Сіаіге Оеѵіііе и Тгоозі. Измѣ-
реніе высокихъ температуръ 53.
Заіѵіопі. Гигрометръ 636.
Запсіогіиз. Гигрометръ 634.
Заггаи. Уравненіе состоянія 135, 662.
Заиззиге. Гигрометръ 634.
8сЬай§оізс1і. Сплавы 492.
ЗсЬаІкшцк. Изотермы водорода 649.
ЗсЬаиІеІЬег^ег. Теплопроводность твер-
дыхъ тѣлъ 323.
ЗсЬеНег. Диффузія растворовъ 724.
ЗсЬееІ. Коэффиціентъ расширенія 91,
расширеніе кварца 95, плотность воды 117.
испареніе твердыхъ тѣлъ 574
ЗсЬееІ и Неизе. См. Неизе и ЗсЬееІ.
ЗсЬееІ, Зеіі и ТЬіезеп. Сравненіе тер-
мометровъ 43, расширеніе 109.
ЗсЬеигег и Кезіпег. Термометръ АѴаІ-
іегбіп’а 45.
8сЬій. Теплоемкость жидкостей 195,
зависимость теплоемкости отъ темпера-
туры 236, скрытая теплота испаренія 541,
правило Тгоиіопа 547.
Зсѣіпх. Пирометръ 68.
ЗсЫеіегшасЬег. Теплопроводность га-
зовъ 345.
ЗсЬшісК. Упругость насыщенныхъ па-
ровъ 585, 594, законъ Паііоп’а 597, урав-
неніе состоянія 661.
ЗсЬоепУез. Пирометръ 70.
ЗсЪоІх. Теплота растворенія 730.
8сЬо1х и ЗіаиЬ. Теплота растворенія 730.
ЗсЬоор. Плотность и удѣльный объемъ
насыщенныхъ растворовъ 616, ненасыщен-
ные пары 647.
ЗсЬоЙ. Термометръ 32, расширеніе
стекла 93.
ЗсИой и ХѴіпкеІтапп. Расширеніе сте-
колъ 93.
ЗсЬгеіпетакегз. Кватернарныя си-
стемы 714.
ЗсЬйІІег. Теплоемкость смѣсей жид-
костей 195, теплоемкость растворовъ 198,
растворы 736.
ЗсЬиІх. Теплоемкость сплавовъ 197, те-
плоемкость и молекулярный вѣсъ 228,
плавленіе амальгамъ 492.
Зсііиіхе. Теплопроводность сплавовъ 316.
Зсѣйііег. Дестилляція металловъ 529.
ЗсЪйІІег и ХѴагіЬа. Единица теплоты
157, ледяной калориметръ 171, измѣреніе
теплотъ горѣнія 205.
Зсйшпапп. Упругость насыщенныхъ
паровъ 594, 599.
ЗсНизіег. Температура солнца 64.
Зсііизіег и Оаппоп. См. баппоп и
ЗсЪизіег.
ЗсІпѵаІЬе. Выдѣленіе тепла при смѣ-
шеніи порошковъ съ жидкостями 256.
Зсйхѵагіг. Аллотропическія превраще-
нія 516.
Зсііхѵагіге. Теплопроводность газовъ 349.
8е§иіп. Эквивалентность теплоты и ра-
боты 362.
Зёпагтопі. Теплопроводность кристал-
ловъ 328.
ЗЪеагег. Измѣреніе низкихъ темпера-
туръ 72, скрытая теплота испаренія 546.
Зіетепз. Пирометръ 57.
Зіетепз и Наізке. См. Наізке и Зіетепз.
ЗіеІЬегтапп и Еаѵге. См. Раѵге и
ЗіеІЬегтапп.
Зіоііе. Коэффиціентъ расширенія 92.
Зтіік. Скрытая теплота плавленія льда
513, скрытая теплота испаренія воды 540.
ЗтоІисЬолѵзкі. Температурный скачокъ
на границѣ тѣлъ 352, теорія опалесцен-
ціи 683.
ЗоЪпске. Измѣненіе теплоемкости съ
температурой 240.
Зоиійегп. Упругость насыщенныхъ па-
ровъ 585.
Зоиіііет и Сгі^Ыоп. См. Сгі^Ніоп и
Зоийіегп.
ЗоиПіегІапсі. Расширеніе воды 112
8ргіп§. Сплавы 492.
8іасШіа§еп. Расширеніе сплавовъ 94.
Зіаесіеі. Упругость насыщенныхъ па-
ровъ 594.
Зіаі^тиеІІег. Теплоемкость 241.
Зіагк. Сфероидальное состояніе 532
Зіагкхѵеаікег. Скрытая теплота испа-
ренія воды 540.
ЗіаиЬ и Зскоіх. См. Зсііоіх и ЗіаиЬ.
Зіеіап. Законъ лучеиспусканія 60, 477,
охлажденіе тѣлъ 283, 284, теплопровод-
ность газовъ 342, испареніе 522, скрытая
теплота испаренія 549.
Зіеіп. Точка плавленія 489.
ЗіеіплѵеЪг и Лае^ег. См. Лае^ег и Зіеіп-
лѵеНг.
Зіеіхпег. Испареніе твердыхъ тѣлъ 570.
Зіеѵепз. Теплоемкость газовъ 235.
ЗіеАѵагі. Оптическая пирометрія 65.
Зіойтапп. Измѣреніе теплотъ горѣнія
265, теплота образованія 271.
Зіокез. Теплопроводность анизотроп-
ныхъ тѣлъ 327
778
Указатель иностранныхъ авторовъ
8іогіепЬескег. Правило фазъ 713.
8ігассіаіі и Вагіоіі. См. Вагіоіі и
8ігассіа1і.
8ігескег. Теплоемкость газовъ 224.
8иіЬег1ап<і. Уравненіе состоянія 662.
8ѵе(1Ьег§. ВгоАѴп’овское движеніе 423.
Зѵесіеііиь. Расширеніе Ре 94.
$ѵепс188оп. Скрытая теплота испаренія
540, 541.
8хі1у. Второе начало термодинамики 443.
Таіі. Теплопроводность 318, уравненіе
состоянія 662.
Таштап. Твердое состояніе 485, пла-
вленіе сплавовъ 491, переохлажденіе 494,
вліяніе давленія на точку плавленія 508,
скрытая теплота плавленія 513, аллотропи-
ческія превращенія 515, 516, скрытая те-
плота испаренія 549, упругость насыщен-
ныхъ паровъ 583, твердые растворы 754.
Таштап и Заіітеп. См. 8аЪтеп и
Таттап.
Таіе и РаігЬаігп. См. ЕаігЬаігп и Таіе.
ТЬап. Ледяной калориметръ 171.
ТЬіевеп. Отставаніе показаній термо-
метра 37, расширеніе металловъ 92, расши-
реніе воды 118, испареніе твердыхъ тѣлъ
573, упругость насыщенныхъ паровъ (фор-
мула) 604, теплоемкость насыщенныхъ па-
ровъ 625, уравненіе состоянія 663, крити-
ческое состояніе 668.
ТЪіІогіег. Расширеніе жидкой СО2 125,
критическое состояніе 665.
ТЪотзеп Л. Теплоемкость 190, калори-
метръ 263, теплота горѣнія 270, теплота
растворенія 727, диссоціація 734
ТЬотзеп Ь. Измѣреніе теплотъ горѣ-
нія 265
ТЬот8оп Лате8. Уравненіе состоя-
нія 656.
ТІЮПІ8ОП Л. Л. Упругость насыщенныхъ
паровъ 603, 607. ,
ТЬотзоп АѴ. (Ьопі Кеіѵіп). Абсолют-
ная шкала температуръ 7, 423, постулатъ
420, второе начало термодинамики 420,
вліяніе давленія на температуру плавле-
нія 504, испареніе твердыхъ тѣлъ 572,
упругость насыщенныхъ паровъ 604, урав-
неніе состоянія 662.
ТіІсІеп. Теплоемкость при низкихъ тем-
пературахъ 194.
Тоеріег. Плавленіе 497.
ТоЫіп^ег. Охлаждающія смѣси 727
То1ѵег-Рге8Іоп 8. Акустическое измѣре-
ніе температуръ 59.
Тот1іп8оп. Кипѣніе 527.
Тотшазіпі и Сагсіапі. См. Сапіапі и
Тотта8Іпі.
Тгаѵегз и Охѵуег. См. Охѵуег и Тгаѵегв.
Тгаѵег8 и Лациегосі. См. Ладиегод и
Тгаѵегъ.
Тгесі^оід. Упругость насыщенныхъ па-
ровъ 598.
Тгеііх. Теплоемкость газовъ 226
Тгепііпа^ііа. Скрытая теплота плавле-
нія 513.
Тгеѵеііап. Теплопроводность (опытъ) 308.
Тгеѵог. Правило фазъ 706.
Тгіріег. Сгущеніе газовъ 568.
Тгоо8І. Сгущеніе газовъ 566.
1 гоо8І и НаиіеГеиіІІе. См. Наиіеіеиіііе
И ТГОО8І.
Тгоо8і и 8аіпі Сіаіге Веѵіііе. См.
8аіпіе Сіаіге Веѵіііе и Тгооьі.
Тгоиіоп. Скрытая теплота кипѣнія (пра-
вило) 547.
Твакоіоіоз. Точка кипѣнія раство-
ровъ 741.
ТисЬ8сЪті(1і. Теплопроводность кри-
сталловъ 324.
Титіігх. Плотность растворовъ 115,
теплоемкость водяного пара 208, скрытая
теплота испаренія 548, уравненіе состоя-
нія 661.
Тиііоп. Коэффиціентъ расширенія 90
ТушІаІІ. Теплоемкость (опытъ) 167, те-
плопроводность кристалловъ 328, кипѣ-
ніе 525.
Ііге. Теплоемкость воды 158, скрытая
теплота испаренія воды 535, законъ Иаі-
іоп’а 597.
Ѵаіепііпег. Теплоемкость газовъ 225.
Ѵап АиЬеІ. Молекулярная теплоемкость
235, теплоемкость жидкостей 335.
Ѵап АиЬеІ и РаіІІоі. См. Раіііоі и
Ѵап АиЬеІ.
Ѵап сіег Р1ааі8. Упругость насыщен-
ныхъ паровъ 594.
Ѵап сіег \ѴааІ8. Уравненіе состоянія
130, 650, 651, 654, 657, 660, 663, расши-
реніе ЗО2 148, теплоемкость насыщен-
ныхъ паровъ 622, соотвѣтственныя состоя-
нія 685
Ѵап Ьааг. Расширеніе воды 112, урав-
неніе состоянія 661, 663, критическое со-
стояніе 684. теплота растворенія 732.
Ѵап Магит. Сгущеніе газовъ 559.
Ѵап’і НоП. Теплоемкость жидкостей 199,
критическое состояніе 684, растворимость
Указатель иностранныхъ авторовъ.
779
720, 721, теплота растворенія 730, 731,
точка кипѣнія растворовъ 742.
Ѵаидиеііп и Еоигсгоу. См. Еоигсгоу
и Ѵаидиеііп.
Ѵеііеп. Теплоемкость воды 159, 160.
ѴегсІеѣ Растяженіе твердыхъ тѣлъ 475.
ѴегзсѣаТТеІі. Критическое состояніе 670.
Ѵісепііпі и Отогіеі. См. Отогіеі и
Ѵісепііпі.
Ѵіеіііе и Вегіііеіоі. См. Вегіѣеіоі и
Ѵіеіііе.
Ѵіііагд. Критическая температура 678.
ѴіІІагд и Лаггу. См. Лаггу и Ѵіііагд.
Ѵіііагі. Расширеніе дерева 101.
Ѵіпсепі. Плотность льда 496.
Ѵіоіі. Уравненіе состоянія 661.
Ѵіоііе. Оптическая пирометрія 60, те-
плоемкость платины 192, теплоемкость ал-
маза 195, охлажденіе 284, механическій
эквивалентъ теплоты 374.
Ѵіззег. Вліяніе давленія на точку пла-
вленія 507.
Ѵо§е1. Расширеніе воздуха 460
Ѵоі§і. Теплопроводность 316, 326, те-
плопроводность кристалловъ 330.
Ѵоп Ьап§. Теплопроводность кристал-
ловъ 328.
АѴаа^е и Си1(1Ьег§. См. 6и1(1Ьег§ и
АѴаа^е.
АѴасІіэтиіІі. Теплопроводность жидко-
стей 336.
АѴа^пег. Охлажденіе 285, растяженіе
твердыхъ тѣлъ 475.
АѴаідпег и Виг§е88. См. Виг§е88 и
ХѴаідпег.
ХѴаігіпег и Оіскіпзоп. См. Оіскіпэоп
и АѴаідпег.
АѴаідпег и Маііогу. См. Маііогу и
АѴаідпег.
АѴаИепІіп. Термометръ 45.
ѴѴаІкег. Растворимость 722.
АѴаппег. Пирометръ 68.
\ѴагЬиг§. Единица теплоты 162, упру-
гость насыщенныхъ паровъ 606.
АѴагЬиг§ и ВІопсіІоЕ См. Віопдіоі и
АѴагЬиг§.
АѴагіІіа и 8с1іи11ег. См. 8с1іи11ег и
АѴаНІіа.
АѴаээтиіІі. Растяженіе твердыхъ тѣлъ
475, уравненіе состоянія 664
АѴаіегшап. Воздушный калориметръ 178.
АѴаіегэіоп. Расширеніе воды 120.
ѴѴаІІ. Скрытая теплота испаренія воды
(законъ) 535, упругость насыщенныхъ па
ровъ 584.
АѴеЬег. Расширеніе воды 113, тепло-
емкость твердыхъ тѣлъ 194. 229, охлажде-
ніе 284, теплопроводность твердыхъ тѣлъ
321, теплопроводность жидкостей 334.
АѴеЬег Ь. Механическій эквивалентъ
теплоты 374.
АѴеЬег Н. Теплопроводность жидкостей
336, абсорбціонный гигрометръ 631.
\ѴесІ§\ѵоосІ. Пирометръ 56.
\Ѵе§8СІіеі(1ег. Испареніе твердыхъ
тѣлъ 570.
АѴеідпег. Переохлажденіе воды 120.
АѴеіпІіоІд. Теплоемкость Рі 192.
АѴейЫеіп. Энтропія (правило) 555.
ѴѴеіВі и Мегг. См. Мегг и ѴѴеіІН.
АѴеІіег и 6ау-1лі88ас. См. Сау-Ьиээас
и АѴеМег.
АѴІііііакег. Поверхностная энергія 466.
АѴіеЬе. Сравненіе термометровъ 43,
измѣреніе высокихъ температуръ 46, упру-
гость насыщенныхъ паровъ 593.
АѴіегіетапп. Температура пустоты 8,
теплоемкость газовъ 206, зависимость те-
плоемкости отъ температуры 209, теплоем-
кость паровъ 240, теплопроводность 316,
теплоемкость насыщенныхъ паровъ 644.
АѴіегіетапп и Егапг. См. Егапг и \Ѵіе-
детапп.
\Ѵіе§апсІ. Теплоемкость элементовъ 195.
АѴіеп. Лучеиспусканіе (законы) 60, (фор-
мула) 60, парадоксъ 422.
АѴіІбегтапп. Затвердѣваніе раство-
ровъ 754.
АѴіІке. Скрытая теплота плавленія 513.
АѴіПіашэ и Сагпеііеу. См. Сагпеііеу
и АѴіІІіатэ.
АѴіпкеІтапп. Теплоемкость 196,
теплоемкость стеколъ 236, теплопровод-
ность жидкостей 351, теплопроводность
газовъ 344, скрытая теплота испаренія
воды 539.
АѴігіг. Скрытая теплота испаренія 541,
правило Тгоиіоп’а 547.
АѴііко\ѵ8кі. Измѣреніе низкихъ темпе-
ратуръ 71, расширеніе воздуха 148, тепло-
емкость воздуха 208. 214, теплоемкость
газовъ 225.
АѴоИ. Критическая температура 670.
\ѴгоЫе\ѵ8ку. Измѣреніе низкихъ тем-
пературъ 70, сгущеніе газовъ 563, 564,
565, упругость насыщенныхъ паровъ 596
АѴиеІІпег. Поправка на выступающій
78Ѳ
Указатель иностранныхъ авторовъ
столбикъ 40, расширеніе ртути 108, рас-
ширеніе жидкостей (формула) 128, тепло-
емкость С 191, теплоемкость газовъ 224,
скрытая теплота испаренія воды 540, испа-
реніе твердыхъ тѣлъ 573, теплоемкость
насыщенныхъ паровъ 620, упругость пара
растворовъ 736.
АѴиеІІпег и бгоігіап. См. бгоігіап и
АѴиеІІпег.
Ѵоип§. Упругость насыщенныхъ па-
ровъ 594, (формула) 598, удѣльный объ-
емъ и плотность насыщенныхъ паровъ 614,
615, 616, 617, уравненіе состоянія 663, со-
* отвѣтственныя состоянія 692.
Ѵоип§ и Кашзау. См. Кашзау и
Ѵоип§.
Хакгхехѵзку. Плотность льда 495.
7еп§Ье1І8. Испареніе твердыхъ тѣлъ 570.
7іе§1ег. Теплопроводность газовъ 347,
упругость насыщенныхъ паровъ 584.
Хеипег. Политропы 398, скрытая те-
плота испаренія воды 539, упругость на-
сыщенныхъ паровъ (формула) 600, 603,
уравненіе состоянія 662.
Хоеііпег. Радіометръ 252.
7\ѵег§ег. Охлаждающія смѣси 727.
Изданія К. Л. РИККЕРА, въ Петроградѣ, Морская 17
Основаніе термохиміи и ея значеніе для теоретической химіи. Г. Яна. Пере-
водъ съ 2 нѣмецк. изданія Н. С. Дрентельна. 1893. Цѣна 2 руб.
Физическая химія какъ основаніе аналитической химіи проф. В. Герца. Пер.
съ разрѣш. и доп. автора съ нѣм. лаборанта Д. Д. Гарднера подъ ред. проф. А. А. Яков-
кина, ѴІ4-124 стр. съ 13 черт. 1911. Цѣна 1 руб.
Краткій учебникъ аналитической химіи для практич. занятій въ лабораторіи
провизора Э. К. Леценіуса. 1905. Цѣна 30 коп.
Качественнь’й химическій анализъ. Проф. Ф. П. Тредъуэлла. Переводъ съ
3 нѣм. изд. Л. Ю. Явейна. Съ 14 рис. и 1 спектр. табл. 1904. Цѣна 3 руб. 20 коп.,
въ перепл. 3 руб. 70 коп.
Руководство къ качественному химическому анализу. Штэделеръ-Кольбе.
Вновь обработано Пг. Н. АЬе1]апх, профессоромъ химіи Цюрихскаго университета. Пер.
съ 10-го нѣм. изд. подъ ред. проф. А. А Яковкина. 1889. Цѣна 70 коп.
Руководство къ приготовленію химическихъ неорганическихъ препаратовъ.
Прив.-доц. д-ра К. Рюста. Перев. подъ ред. прив.-доц. Л. Явейна. Съ 15 рис. 1903.
Цѣна 70 коп.
О теоріи растворовъ. Чтеніе въ Обществѣ естественной исторіи и медицины
4 марта 1892 г., проф. А* Горстмана. Перев. съ нѣм. Н. С. Дрентельна. 1893. Ц. 40 к.
Задачи химіи нашего времени. Проф. В. Майера. Перев. съ нѣм. Н. С. Дрен-
те чьна. 1890. Цѣна 50 коп.
Физическая кристаллографія и введеніе къ изученію кристаллографическихъ
свойствъ важнѣйшихъ соединеній П. Грота. Переводъ съ 3 перераб. нѣм. изданія
подъ редакціею и съ добавлен. проф. Ф. Левинсонъ-Лессинга. ХІІІ-(-850 стр. съ 707 рис.
и 3 хромолит. табл. 1897. Ц. 10 р.
Учебникъ кристаллографіи. Проф. Ф. Ю. Левинсонъ-Лессинга. Часть I. Гео-
метрическая кристаллографія. 159 стр. съ 251 рис. 1911. Ц. 1 р. 60 коп.
Введеніе въ кристаллооптику. Состав. И. А. Преображенскій. 50 стр. съ 71 рис.
1913. Цѣна 80 коп.
Популярныя рѣчи профессора Г. Гельмгольца. Перев. съ нѣмецк. подъ редакц.
О. Д. Хвольсона и С. Я. Терешина. 2-е пересмотр. и исправл. изд. Ч. I. Съ 19 рис.
и 1 портретомъ. 1898. Цѣна 1 руб. Ч. II. Съ 30 рис. 1899. Цѣна 1 руб.
Содержаніе: I часть: О взаимодѣйствіи силъ природы. — О сохраненіи силы. —
О цѣли и объ успѣхахъ естестврзнанія. — Современное развитіе взглядовъ Фарадея на
электричество. II часть: О зрѣніи человѣка. — Новѣйшіе успѣхи теоріи зрѣнія. —
Вихревыя бури и грозы. — Возникновеніе планетной системы.
Начальное руководство къ самостоятельному изученію высшей математики
и механики. Сост. проф. Н. Б. Делоне. 2 просм. и доп. изд. Съ 321 фигурой въ текстѣ.
1912. Ц. 4 р. 20 к. въ изящн. переп. 5 р.
Дифференціальное и интегральное исчисленія съ приложеніями къ анализу и
геометріи. Составилъ А. Пароменскій. 3-е испр. и доп. статьею объ интегрированіи
дифференц. уравненій изданіе. VIII—|—500 стр. Съ 56 рис. 1908. Цѣна 4 р. 50 к.
Начальный курсъ высшаго математическаго анализа. Курсъ старшаго класса
Николаевск. инж. училища, проф. А. Саткевича. Съ 39 фиг. 1905. Ц. 3 р.
Высшая математика въ примѣненіи къ вопросамъ естествознанія проф. А. Фур-
мана. Перев. съ нѣмецк. подъ редакц. проф. Н. А. Гезехуса. Съ 101 черт. 1903. Ц. 3 р.
20 к., въ перепл. 3 руб. 70 коп.
Въ Инженерномъ журналѣ 1893 г. проф. К. Л. Кирпичевъ помѣстилъ отзывъ о
1 нѣмецк. изданіи этого сочиненія, изъ котораго мы приводимъ: Съ особеннымъ удо-
вольствіемъ рекомендуемъ эту книгу начинающимъ заниматься дифференц. исчисленіемъ;
она смѣло поддержитъ ту цѣль, которую поставилъ себѣ авторъ въ предисловіи: она
навѣрное внушитъ любовь къ занятіямъ, возбудитъ интересъ читателя и доставитъ пол-
ное удовлетвореніе и радость въ работѣ. Пожелаемъ возможно большаго распростра-
неніе этой драгоцѣнной книіѣ.
Начала дифференціальнаго и интегральнаго исчисленій и ихъ приложенія
къ описанію явленій природы проф. Г. Буркхардта. Перев. съ нѣм. А. Я. Билибина
и В. А. Крогіуса. ХП4-232 сір. Съ 39 рис. 1909. Цѣна 2 руб. 40 коп.
Бесѣдя о механикѣ, заслуж. проф. В. Л. Кирпичева. ІХЦ-371 стр. съ 227 фи-
гурами. 1907. Цѣна 2 руб. 80 коп., въ перепл. 3 руб. 30 коп.
Основанія теоретической механики. Проф. П. О. Сомова. Съ 276 фигур. и
700 упражненіями и задачами. 1904. Ц. 5 руб., въ перепл. 5 руб. 80 коп.
Изданія К. Л. РИККЕРА, въ Петроградѣ, Морская 17.
Основы механики. Курсъ Николаевой. Инженернаго Училища С. Балдина. Съ
184 черт. и 258 задачами. 1906. Ц 3 р. 40 к., въ пер. 3 р. 90 к.
Механика для техническихъ и ремесленныхъ училищъ, а также для самообученія*
сост. Ф. Губеръ. Перев. съ 4-го нѣмецк. изданія, 3-е русск. изд подъ редакц. и съ
доп. проф. М. Н. Демьянова. Съ 522 чертеж. 1902. Ц. 3 р., въ пер. 3 р. 80 к.
Существеннымъ отличіемъ по содержанію этого изданія отъ прежнихъ является
глава VII, введенная редакторомъ, гдѣ популярно и вмѣстѣ съ тѣмъ сжато изложены
основы графической старики. Съ введеніемъ этой главы „Механика" Губера пріобрѣла
надлежащую стройность и законченность. Богатое содержаніе книги, отвѣчающее вполнѣ
современ. состоянію техническ. познаній, популярное изложеніе при строго научной тер-
минологіи, побуждаютъ насъ горячо рекомендовать эту книгу русскимъ техникамъ.
„Желѣзнодорожная недѣля", 1902, № 44.
Курсъ теоретическойгвдеханики для техниковъ и инженеровъ. Сост проф. Н. Б.
Делоне. 2-ое исправл. изд. лѴЦ-416 стр. съ 163 фиг. въ текстѣ. 1913. Ц. 3 р. 50 к.
Лекціи по практической механикѣ, читанныя въ Варш. Полит. Инст., орд. про-
фесс. Н. Б. Делоне. Съ 214 фиг 1901. Ц. 2 р., въ пер. 2 р. 50 к.
Механика, Р. Лауэнштейна. Перев. съ 7 нѣм. обработаннаго К. Аренсомъ изд.
М. П. Новгородскаго. Съ 218 рис. 1908. Ц. 1 р. 60 к.
Электротехника. Соч. Л. Свенторжецкаго, преподават. Николаевской Инженер-
ной Академіи. Основные законы. — Техническія измѣренія — Аккумуляторы, динамо-
машины и электродвигатели постояннаго тока. 2-е знач. дополн. и перераб. изданіе.
Текстъ съ отдѣльн. атласомъ черт. въ 65 табл. 1901. Ц. 7 р., въ изящн. перепл. ц. 9 р.
Авторъ задался цѣлью составить руководство не только для учащихся, но и вообще
для всякаго инженера, интересующагося вопросами электротехники и надо отдать спра-
ведливость, — исполнилъ свою задачу блестяще; въ его руководство можно добавить
пояснительныхъ подробностей, не нужныхъ для вполнѣ внимательнаго читателя, но
убавить ничего нельзя. „^Московскія Вѣдомости" 1902, № 135.
Электротехника перемѣннаго, однофазнаго и трехфазнаго тока. Соч. Л. Свен-
торжецкаго. Основные законы, техническія измѣренія, динамо-машины, трансформаторы
и электродвигатели. Съ 191 фиг. въ текстѣ и 3 табл. черт. 1902. Ц. 3 р. 60 к., въ пер. 4 р. 16 к.
Практическое руководство къ примѣненію электричества въ промышленности.
Единицы и измѣренія. Источники электричества. — Электрическое освѣщеніе. — Элек-
трическая передача работы. — Гальванопластика и электрометаллургія. - Телефонія.
Составили Е. Кадіа и Л. Дюбостъ. Съ 291 черт. въ текстѣ. Перев. съ 6-го франц.
изданія ииж. Д. Головъ. Русское изданіе 4-е. Съ 291 черт. 1903. Ц. 5 р., въ пер. 5 р. 80 к.
Теоретическій и практическій курсъ электротехники. Сост. П. Войнаровскій,
преподаватель Электротехническаго института. Часть I. Основныя свѣдѣнія изъ высшей
математики необходимыя электротехнику. Съ 31 рис. 1897. Въ изящн. пер. 1 р. 50 к.
Часть II. Основы теоріи электрическихъ и магнитныхъ явленій. Съ 94 рис. 1899. Въ
перепл. ц. 1 руб. 80 коп. Часть III. Теорія явленій перемѣнныхъ токовъ въ однофаз-
ныхъ и многофазныхъ цѣпяхъ. Съ 102 рис. 1902. Въ перепл. цѣна 1 руб. 60 коп.
Электрическіе источники свѣта, способы ихъ изслѣдованія и примѣненія.
Сост. инж.-электр. А. А. Кузнецовъ. Съ 325 рис. 1904. Ц. 4 р. 50 к., въ перепл. 5 р.
Настоящій трудъ раздѣленъ на шесть главъ, изъ которыхъ три первыя посвящены
разсмотрѣнію фотометровъ, фотометрическихъ эталоновъ, методовъ фотометрическихъ
измѣреній и общихъ свойствъ источниковъ св1'.а. Въ четвертой и пятой главахъ разо-
браны свойства дуговыхъ лампъ и лампъ накаливанія; въ прибавленіи къ четвертой главѣ
разсмотрѣны лампы съ разрѣженными газами и парами. Въ шестой главѣ изложены спо-
собы примѣненія электрическихъ источниковъ свѣта. Книга составлена въ объемѣ куріа
лекцій по фотометріи и электрическимъ источникамъ свѣта, читаемыхъ авторомъ студен-
тамъ Электротехническаго Института Императора Александра III.
Электрическія измѣренія. Пособіе для производства практическихъ работъ въ
электротехническихъ лабораторіяхъ. В. Закржевскаго, завѣд. Электротехн. лабор. Военно-
Электротехнической школы. 2-е исправл и дополн. изданіе. Съ 179 чертеж. '901.
Цѣна 2 р. 40 к., въ перепл. 2 р. 90 к.
Содержаніе книги вполнѣ соотвѣтствуетъ назначенію и благодаря обилію мате-
ріала и весьма цѣнныхъ практическихъ свѣдѣній является въ современн. электротехн.
литературѣ единственнымъ полнымъ и толковымъ практическ. руководствомъ. Въ виду
этого настоящая книга можетъ быть весьма полезна студентамъ, техникамъ и, вообще,
всѣмъ кому только приходится имѣть дѣла съ разнообразными электрическими и техни-
ческими измѣреніями. „Электротехникъ" 1901. Іюль.
Типографія Э. Ф. Мексъ. Петроградъ, Забалканскій пр. № 22.